Данное изобретение относится к модифицированному белку, связывающему фактор Н (fHbp) и его применению для индукции иммунного ответа против патогенной инфекции или колонизации, например, против Neisseria meningitidis или Neisseria gonorrhoeae.
Менингококк Neisseria meningitidis (Nm) остается ведущей причиной сепсиса и бактериального менингита у детей и молодых совершеннолетних детей. Начало заболевания может быть чрезвычайно быстрым, с показателем смертности около 10% для септицемического заболевания1, при этом те, кто выжил, могут испытывать значительную утрату трудоспособности, включая утрату конечностей и неврологические дефициты1. Поэтому профилактическая иммунизация является лучшим способом защиты индивидуумов от менингококковой инфекции. Доступны вакцины на основе бактериальной капсулы2, но имеются только частично эффективные вакцины, пригодные для эндемической инфекции серогруппы В, которая является причиной более 80% случаев в Великобритании в настоящее время3; полисахарид капсулы Nm серогруппы В является слабо иммуногененным, так как он идентичен по структуре с человеческим гликопротеином в нервной ткани и может индуцировать аутоиммунитет в случае использования в качестве вакцины4. Таким образом, существует острая потребность в создании новых вакцин, и прилагаются значительные усилия в науке и промышленности для достижения этой важной цели.
Главной мишенью иммунного ответа, вызванного против менингококковых везикул наружной мембраны (OMV), является PorA16,17,18, интегральный белок наружной мембраны (ОМР) в менингококке19. Однако последовательность этого белка является разнообразной, и распространенность конкретных вариантов отличается по географическому региону, и вакцины OMV являются в значительной степени PorA-специфическими. Варианты PorA идентифицированы по последовательностям в вариабельных областях (VR) белка, которые локализованы в экспонированных на поверхности петлях белка и являются мишенью иммунных ответов17. PorA имеет семь внеклеточных петель; четвертая петля представляет собой вариабельную область 2 (VR2) и является мишенью наибольшей бактерицидной активности сыворотки (SBA), генерированной PorA после природной инфекции и после иммунизации OMV16,18. Бактерицидная активность сыворотки (SBA) является известным коррелятом защиты против менингококкового заболевания. Несмотря на разнообразие последовательностей, около 70% изолятов в Великобритании будет покрыто вакцинами, содержащими шесть белков PorA (http://pubmlst.org/neisseria/PorA).
Основным препятствием для разработки бактериальных вакцин является трудность в получении некоторых количеств интегральных белков наружной мембраны (ОМР), таких как PorA, в их нативной конформации. Это обусловлено тем, что белки наружной мембраны (ОМР) содержат гидрофобные домены, которые пересекают мембрану и не сворачиваются правильно, когда экспрессируются в виде растворимых рекомбинантных белков. Правильное сворачивание является критическим для PorA, так как бактерицидная активность сыворотки (SBA) индуцируется конформационными, а не линейными эпитопами белка20. Предыдущие попытки использовать пептиды PorA в качестве вакцин оказались неудачными, так как они не были достаточно иммуногенными и не презентировали иммуногенную часть PorA в ее правильной конформации. Таким образом, единственными вакцинами на основе PorA, находящимися на стадии разработки, являются везикулы наружной мембраны (OMV), которые обладают ограниченной эффективностью у грудных детей2, являются реактогенными21 и плохо определяемыми, вызывая вопросы нормативно-правового регулирования. Везикулы наружной мембраны (OMV) в качестве иммуногенов не являются подходящими, поскольку устойчивость и токсичность могут вызывать проблемы во время изготовления. Например, везикулы наружной мембраны (OMV) могут содержать токсичный липополисахарид (LPS).
Менингококковый белок, связывающий фактор Н (fHbp) представляет собой экспонированный на поверхности липопротеин, который состоит из двух β-цилиндров5 (фигура 1А). N-Концевой β-цилиндр fHbp имеет относительно открытую структуру, тогда как С-концевой β-цилиндр стабилизирован за счет обширного водородного связывания между семью β-цепями, которые образуют этот цилиндр5.
Важно, что fHbp является ключевым антигеном в вакцинах против Nm серогруппы В, находящихся на стадии разработки фармацевтическими компаниями, такими как Pfizer, GSK и другие, и включен в вакцины6,7,8 OMV следующего поколения. Вакцина компании Pfizer состоит из двух fHbp, тогда как вакцина компании GSK имеет один fHbp в коктейле других антигенов, который включает везикулы наружной мембраны (OMV). fHbp связывает человеческий, но не мышиный, фактор Н (fH)9,10, наиболее представленный в плазме белок, который понижающе регулирует систему комплемента11, важный аспект иммунитета против Nm12. Иммунизация подростков и взрослых fHbp вызывает SBA13.
fHbp подразделяли на различные схемы на основе его предсказанной аминокислотной последовательности. В настоящей заявке распознаны три группы вариантов (v1, v2 и v37) и число пептидов (www.mlst.org). Важно, что сыворотка, созданная против v1 fHbp, не опосредует бактерицидную активность сыворотки (SBA) против Nm, экспрессирующего белки v2 и v3, и наоборот. Вакцина компании GSK содержит один белок v1 (v1.1), тогда как состав компании Pfizer включает v1 и v3 fHbp1314. Таким образом, ни одна из существующих в настоящее время вакцин не включает v2 fHbp, даже несмотря на то, что значительная доля заболевания в Великобритании в настоящее время вызвана штаммами, экспрессирующими fHbp из этой группы вариантов315.
В патентной заявке WO 2011024072 описано применение fHbp, который выбран или сконструирован таким образом, что он имеет последовательность, которая может вызывать продукцию бактерицидных антименингококковых антител широкого спектра после введения хозяину-животному. В этом документе указывается, что дополнительные менингококковые антигены могут быть обеспечены с помощью сконструированного fHbp в форме N- или С-концевого слитого белка. Однако такое предложение вряд ли будет обеспечивать белок, который будет представлять иммуногенную часть многих менингококковых антигенов, таких как PorA, в правильной конформации, и они не будут достаточно иммуногенными.
Целью настоящего изобретения является обеспечение альтернативных и улучшенных иммуногенных молекул для вакцинации против патогенных организмов, в частности, для предупреждения или уменьшения менингококковой или гонококковой инфекции или колонизации.
Согласно первому аспекту изобретения предлагается модифицированный белок, связывающий фактор Н (fHbp), представляющий собой fHbp или его вариант, который действует в качестве молекулярного каркаса для модификации путем добавления по меньшей мере одной петли экзогенного пептида из другого антигена.
В настоящем документе было показано, что иммуногенные пептиды, такие как пептиды из PorA, могут быть введены в белок, связывающий фактор Н (fHbp), который действует в качестве молекулярного каркаса. Пептиды, вводимые в fHbp, презентированы иммунной системе и способны вызывать защитные ответы, такие как SBA. Предпочтительно молекула fHbp обеспечивает идеальный молекулярный каркас для стабильного включения пептидных петель для дисплея эпитопов, в частности, эпитопов, которые трудно стабилизировать и отображать в их нативной конформации, например, петель из интегральных белков наружной мембраны (ОМР), таких как PorA. Это противоречит решениям, например, описанным в WO 2011024072, где простые N- или слитые С-концы fHbp и дополнительного антигена не решат трудности, связанные с внутренней стабильностью и растворимостью некоторых антигенов. В частности, многие белки наружной мембраны (ОМР), такие как PorA, трудно экспрессировать из-за нерастворимости их пересекающих мембрану доменов. PorA имеет структуру 16-бета-цепочечного цилиндра с экспонированными на поверхности петлями между цепями 1 и 2 (петля 1), цепями 7 и 8 (петля 4), цепями 9 и 10 (петля 5) и цепями 11 и 12 (петля 7), которые, как это было продемонстрировано, являются наиболее эффективными антигенами. fHbp содержит два бета-цилиндра, поэтому последовательности пептидных петель из белков наружной мембраны (ОМР) могут быть встроены в концы петель между бета-цепями fHbp для презентирования фрагментов внеклеточных петель из интегральных белков наружной мембраны (ОМР) в их нативных конформациях для иммунизации. Таким образом, каркасную молекулу модифицированного fHbp согласно изобретению можно применять в качестве профилактической или терапевтической вакцины, направленной на Nm или гонококк, в которой один белок презентирует ключевые эпитопы из двух различных антигенов.
В одном варианте осуществления fHbp представляет собой менингококковый fHbp. В другом варианте осуществления fHbp представляет собой гонококковый fHbp. fHbp может содержать любой из вариантов v1, v2 и v3. В одном варианте осуществления fHbp может содержать v1 fHbp. В другом варианте осуществления fHbp может содержать v2 fHbp. В другом варианте осуществления fHbp может содержать v3 fHbp.
В одном варианте осуществления вариант v1 fHbp может представлять собой вариант v1.1, v1.13, v1.14, v1.15, v1.4 или v1.55. В одном варианте осуществления вариант v1 fHbp может не быть представлять собой v1.1. В одном варианте осуществления вариант v1 fHbp может не представлять собой v1.55. В одном варианте осуществления вариант v1 fHbp может не представлять собой v1.1 или v1.55. В одном варианте осуществления вариант v2 fHbp может представлять собой вариант v2.16, v2.19, v2.22 или v2.25. В одном варианте осуществления вариант v3 fHbp может представлять собой вариант v3.45. В одном варианте осуществления fHbp содержит любой из вариантов v1.4, v2.25 или v3.45 fHbp.
Вариант fHbp может содержать ортолог fHbp. Например, вариант fHbp может содержать Ghfp, гонококковый гомолог fHbp. Ghfp является нефункциональным и тесно связан с V3 fHbp (>95% идентичности аминокислотной последовательности, константа диссоциации KD>100 мкМ с фактором Н).
В одном варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности 
В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

В другом варианте осуществления fHbp, который должен быть в дальнейшем модифицирован по меньшей мере одной петлей экзогенного пептида, может содержать или состоять из последовательности

Вариант fHbp может содержать одну или несколько мутаций аминокислотных остатков, включая добавления, делеции или замены, относительно fHbp дикого типа в дополнение к петле(петлям) экзогенного пептида, обеспеченной на модифицированном fHbp. Например, fHbp может действовать в качестве каркаса, на котором обеспечены петли экзогенного пептида, и варианты относительно дикого типа могут содержать аминокислотные мутации в каркасном участке в областях снаружи точек прикрепления петли(петель) экзогенного пептида. Ссылка на fHbp дикого типа может относиться к любому из вариантов fHbp, обсуждаемых в настоящем документе, например, любой из SEQ ID NO: 1-13.
Вариант fHbp может содержать по меньшей мере одну аминокислотную замену по сравнению с аминокислотой в белке дикого типа. Вариант fHbp может содержать не более одной аминокислотной замены по сравнению с белком дикого типа. Вариант fHbp может содержать не более трех аминокислотных замен по сравнению с белком дикого типа. Вариант fHbp может содержать не более четырех аминокислотных замен по сравнению с белком дикого типа. Вариант fHbp может содержать не более пяти аминокислотных замен по сравнению с белком дикого типа. Вариант fHbp может содержать не более шести аминокислотных замен по сравнению с белком дикого типа. В одном варианте осуществления предлагается вариант fHbp, который содержит шесть аминокислотных мутаций по сравнению с белком дикого типа.
Аминокислотные замены могут представлять собой консервативные замены. Например, мутированный остаток может обладать по существу такими же свойствами, как замещенный остаток дикого типа. Например, замещенный остаток может содержать по существу аналогичный или такой же заряд или гидрофобность, как замещенный остаток дикого типа. Например, замещенный остаток может содержать по существу аналогичную молекулярную массу или стерический объем, как замещенный остаток дикого типа.
В одном варианте осуществления вариант fHbp может иметь по меньшей мере 75% идентичности с диким типом. В другом варианте осуществления вариант fHbp может иметь по меньшей мере 80% идентичности с диким типом. В другом варианте осуществления вариант fHbp может иметь по меньшей мере 85% идентичности с диким типом. В другом варианте осуществления вариант fHbp может иметь по меньшей мере 90% идентичности с диким типом. В другом варианте осуществления вариант fHbp может иметь по меньшей мере 95% идентичности с диким типом. В другом варианте осуществления вариант fHbp может иметь по меньшей мере 98% идентичности с диким типом. В другом варианте осуществления вариант fHbp может иметь по меньшей мере 99% идентичности с диким типом. В другом варианте осуществления вариант fHbp может иметь по меньшей мере 99,5% идентичности с диким типом. Вышеуказанное процентное изменение не предназначено для включения изменения процента идентичности при добавлении петли(петель) экзогенного пептида (т.е. это процент идентичности только компонента fHbp по сравнению с диким типом), и не включает делецию последовательности fHbp в участке встраивания петель из других белков.
Модифицированный fHbp может быть модифицирован таким образом, чтобы он не был способен связывать фактор Н, или по меньшей мере обладал пониженной активностью связывания фактора Н. Модифицированный fHbp может быть нефункциональным относительно функции fHbp дикого типа. В одном варианте осуществления модифицированный fHbp обладает нарушенной способностью связываться с фактором комплемента Н (CFH) с константой диссоциации (KD), которая на >2 порядков выше по сравнению с белком дикого типа. Нефункциональные fHbp могут быть обеспечены путем мутации последовательности fHbp. В одном варианте осуществления нефункциональные fHbp могут быть обеспечены с помощью одной или нескольких петель экзогенных пептидов, предотвращая связывание фактора Н.
Мутация(и) аминокислотного остатка может предотвращать или уменьшать связывание модифицированным fHbp фактора комплемента Н. В другом варианте осуществления мутация(и) аминокислотного остатка может существенно не влиять на функцию fHbp. В одном варианте осуществления мутация(и) аминокислотного остатка в fHbp или его вариантах может быть выбрана из группы, состоящей из аминокислоты в положении 85, 133, 134, 135, 136, 204, 206, 211, 212, 213, 222, 225, 227, 231 и 252 на v1.1 fHbp или соответствующем положении в других fHbp.
В одном варианте осуществления мутация(и) аминокислотного остатка может содержать или состоять из замены на аланин вместо остатка дикого типа. В одном варианте осуществления замена(ы) аминокислотного остатка может содержать или состоять из замены на любую другую аминокислоту вместо остатка дикого типа.
Предпочтительно обеспечение нефункционального fHbp (т.е. отсутствие связывания или меньшее связывание фактора Н) может устранять или уменьшать любые отрицательные эффекты рекрутинга фактора Н на успех вакцины.
В одном варианте осуществления мутация(и) аминокислотных остатков может повысить стабильность модифицированного fHbp, в частности, в варианте осуществления, где обеспечен V2 fHbp, при этом V2 fHbp может быть стабилизирован мутациями в последовательности V2 fHbp. Подробную информацию, касающуюся мутаций для стабильности V2, можно найти в патенте WO 2014030003, который включен в настоящий документе путем ссылки. Например, аминокислотная замена для стабилизации может находиться в одной или более аминокислотах в положении 35, 36, 42, 43, 46, 107, 112, 114, 137 и 138 в V2 fHbp. Замена для стабилизации может быть произведена в одном или нескольких из Ser35, Leu36, Asp42, Glu43, Arg46, Asp107, Val112, Leu114, Ser137 и Gly138.
В одном варианте осуществления петля(и) экзогенного пептида является иммуногенной. Петля(и) экзогенного пептида может происходить из белка, экспонированного на наружной мембране/поверхности.
Петля(и) экзогенного пептида может быть прокариотической по происхождению. Петля(и) экзогенного пептида может происходить из белка на бактерии, такого как белок наружной мембраны (ОМР) патогена. Белок наружной мембраны (ОМР) может представлять собой интегральный ОМР или липопротеин. Петля(и) экзогенного пептида может происходить из менингококкового белка, такого как менингококковый белок наружной мембраны. Петля(и) экзогенного пептида может происходить из белка наружной мембраны другого патогена, такого как N. gonorrhoeae.
Петля экзогенного пептида может содержать фрагмент трансмембранного бета-цилиндрического белка. Петля экзогенного пептида может содержать фрагмент бета-цилиндрического белка порина. Петля экзогенного пептида может содержать фрагмент PorA. В другом варианте осуществления петля экзогенного пептида может содержать фрагмент FetA.
Петля(и) экзогенного пептида, такая как фрагменты PorA, может иметь длину 16 аминокислот. В одном варианте осуществления петля(и) экзогенного пептида, такая как фрагменты PorA, может иметь длину от 8 до 20 аминокислот. В другом варианте осуществления петля(и) экзогенного пептида, такая как фрагменты PorA, может иметь длину от 8 до 16 аминокислот. В другом варианте осуществления петля(и) экзогенного пептида, такая как фрагменты PorA, может иметь длину от 10 до 16 аминокислот. В другом варианте осуществления петля(и) экзогенного пептида, такая как фрагменты PorA, может иметь длину от 12 до 16 аминокислот. В другом варианте осуществления петля(и) экзогенного пептида, такая как фрагменты PorA, может иметь длину от 14 до 18 аминокислот. В другом варианте осуществления петля(и) экзогенного пептида, такая как фрагмент PorA, может иметь длину, достаточную для обеспечения иммуногенного эпитопа. В другом варианте осуществления петля(и) экзогенного пептида, такая как фрагменты PorA, может иметь любую длину, достаточную для обеспечения иммуногенного эпитопа и поддержания нативной конформации относительно фрагмента в диком типе.
Петля(и) экзогенного пептида может быть выбрана из любой из петель 1-7 PorA или их фрагментов; и/или их комбинаций. Петля(и) экзогенного пептида может быть выбрана из любой из петель PorA, включающих петлю 1 (между бета-цепями 1 и 2), петлю 4 (между бета-цепями 7 и 8), петлю 5 (между бета-цепями 9 и 10) и петлю 7 (между бета-цепями 11-12); или их фрагментов; и/или их комбинаций.
Петля экзогенного пептида может содержать любой пептид, выбранный из петли 1 PorA (между бета-цепями 1 и 2); петли 4 (между бета-цепями 7 и 8); и петли 5 (между бета-цепями 9 и 10); или их фрагментов; и/или их комбинаций.
Петля экзогенного пептида может содержать петлю 1 PorA (между бета-цепями 1 и 2) или ее фрагмент. Петля экзогенного пептида может содержать петлю 4 PorA (между бета-цепями 7 и 8) или ее фрагмент. Петля экзогенного пептида может содержать петлю 5 PorA (между бета-цепями 9 и 10) или ее фрагмент.
Специалисту в данной области будет понятно, что последовательности вариантов петель PorA могут быть обеспечены незначительными мутациями относительно дикого типа и могут все же функционировать в качестве эпитопа. Таким образом, петля(и) экзогенного пептида может содержать варианты петли PorA. Варианты могут включать одно или несколько аминокислотных добавлений, делеций или замен относительно последовательности дикого типа. В другом варианте осуществления варианты могут включать не более чем одно аминокислотное добавление, делецию или замену относительно последовательности дикого типа. В другом варианте осуществления варианты могут включать не более 2, 3, 4 или 5 аминокислотных добавлений, делеций или замен относительно последовательности дикого типа. Замены могут представлять собой консервативные замены. Например, обеспечение альтернативного аминокислотного остатка, обладающего по существу аналогичными свойствами, такими как заряд, гидрофобность, стерический размер или молекулярная масса. Варианты могут включать последовательности, имеющие по меньшей мере 85% идентичности последовательности с последовательностью петли PorA дикого типа. В другом варианте осуществления варианты могут включать последовательности, имеющие по меньшей мере 90%, 95%, 98%, 99% или 99,5% идентичности последовательности с последовательностью петли PorA дикого типа.
В одном варианте осуществления модифицированный fHbp может содержать две или более петли экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать три или более петли экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать от 1 до 7 петель экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать от 1 до 5 петель экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать от 1 до 3 петель экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать от 2 до 7 петель экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать от 3 до 7 петель экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать от 2 до 5 петель экзогенного пептида. В одном варианте осуществления модифицированный fHbp может содержать от 3 до 5 петель экзогенного пептида. Модифицированный fHbp или его варианты могут быть модифицированы петлей экзогенного пептида по меньшей мере в одном положении. Модифицированный fHbp или его вариант может быть модифицирован петлей экзогенного пептида по меньшей мере в двух положениях. Модифицированный fHbp или его вариант может быть модифицирован петлей экзогенного пептида по меньшей мере в трех положениях. Модифицированный fHbp или его вариант может быть модифицирован петлей экзогенного пептида по меньшей мере в четырех положениях. Модифицированный fHbp или его вариант может быть модифицирован петлей экзогенного пептида по меньшей мере в пяти положениях. Модифицированный fHbp или его вариант может быть модифицирован петлей экзогенного пептида по меньшей мере в шести положениях. Модифицированный fHbp или его вариант может быть модифицирован петлей экзогенного пептида по меньшей мере в семи положениях.
Петля пептида может быть обеспечена (например, используя fHbp в качестве каркаса) между двумя бета-листами белка, связывающего фактор Н. Петля пептида может быть встроена в fHbp или его вариант в одном или нескольких аминокислотных положениях, выбранных из положений, куда могут быть встроены петли экзогенного пептида, такие как петли PorA (в диапазон включены все остатки в петле), между аминокислотами 49-54, 83-88, 114-124, 199-206, 227-233 и 240-246 v1.1 fHbp, или в соответствующих положениях в других fHbp.
По меньшей мере одна петля экзогенного пептида может быть обеспечена в виде слитых N- или С-конца.
Последовательности fHbp, в которые может быть встроена петля(и) экзогенного пептида, могут находиться в любом из положений, подчеркнутых в контексте первичной аминокислотной последовательности V1.1 fHbp, представленной ниже. В варианте осуществления, в котором используется альтернативный вариант fHbp, сайты встраивания могут находиться в эквивалентных положениях.
Положение 1 в fHbp (P1), остатки 83-88
Р2, остатки 199-206
Р3, остатки 227-233
Р4, остатки 49-54
Р5, остатки 114-124
Р7, остатки 240-246
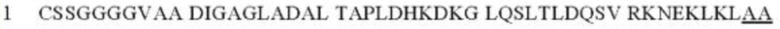

В одном варианте осуществления сайт встраивания петли экзогенного пептида может находиться в положении 1 в fHbp (P1), остатках 83-88 (последовательность EVDGQL (SEQ ID NO: 15)). В другом варианте осуществления сайт встраивания петли экзогенного пептида может находиться в положении Р2, остатках 199-206 (последовательность KPDGKRHA (SEQ ID NO: 16)). В другом варианте осуществления сайт встраивания петли экзогенного пептида может находиться в положении Р3, остатках 227-233 (последовательность FGGKAQE (SEQ ID NO: 17)). В другом варианте осуществления сайт встраивания петли экзогенного пептида может находиться в положении Р4, остатках 49-54 (последовательность AAQGAE (SEQ ID NO: 18)). В другом варианте осуществления сайт встраивания петли экзогенного пептида может находиться в положении Р5, остатках 114-124 (последовательность IQDSEHSGKM (SEQ ID NO: 19)). В другом варианте осуществления сайт встраивания петли экзогенного пептида может находиться в положении Р7, остатках 240-246 (последовательность KTVNGI (SEQ ID NO: 20)).
Сайт встраивания петли экзогенного пептида в любом заданном положении 1-7 может находиться между любыми остатками, идентифицированными в положениях 1-7 fHbp. Альтернативно, сайт встраивания петли экзогенного пептида в любом заданном положении 1-7 может находиться до первого остатка или после последнего остатка, идентифицированного в положениях 1-7 fHbp. Например, если петля экзогенного пептида встроена в положении 4, вставка может представлять собой * AAQGAE (SEQ ID NO: 21), A*AQGAE (SEQ ID NO: 22), AA*QGAE (SEQ ID NO: 23), AAQ*GAE (SEQ ID NO: 24), AAQG*AE (SEQ ID NO: 25), AAQGA*E (SEQ ID NO: 26) или AAQGAE* (SEQ ID NO: 27), где * обозначает сайт встраивания.
В другом варианте осуществления специалисту в данной области будет понятно, что сайт встраивания петли экзогенного пептида может быть вариабельным, таким образом, что от 1 до 5 остатков в области сайта встраивания могут быть удалены из fHbp (например, заменены петлей) без значительного влияния на структуру fHbp. В одном варианте осуществления один или несколько аминокислотных остатков в идентифицированных положениях заменены/замещены петлей экзогенного пептида. В альтернативном варианте осуществления два, три, четыре, пять или более аминокислотных остатков в идентифицированных положениях заменены/замещены петлей экзогенного пептида. В другом варианте осуществления сайт встраивания петли экзогенного пептида может быть вариабельным, таким образом, что от 1 до 3 остатков в области сайта встраивания могут быть удалены из fHbp (например, заменены петлей) без значительного влияния на структуру fHbp. В другом варианте осуществления сайт встраивания петли экзогенного пептида может быть вариабельным, таким образом, что от 1 до 2 остатков в области сайта встраивания могут быть удалены из fHbp (например, заменены петлей) без значительного влияния на структуру fHbp. В другом варианте осуществления сайт встраивания петли экзогенного пептида может быть вариабельным, таким образом, что 1 остаток в области сайта встраивания может быть удален из fHbp (например, заменен петлей) без значительного влияния на структуру fHbp. Например, когда сайт встраивания представляет собой аминокислотный остаток 86 на одном конце петли и остаток 87 на другом конце петли, вариант может включать замену 5, 4, 3, 2 или 1 остатка петлей в области указанного сайта встраивания. В альтернативном варианте осуществления шесть или более аминокислотных остатков в идентифицированных положениях заменены/замещены петлей экзогенного пептида. В альтернативном варианте осуществления семь или более (где это применимо) аминокислотных остатков в идентифицированных положениях заменены/замещены петлей экзогенного пептида. В альтернативном варианте осуществления восемь или более (где это применимо) аминокислотных остатков в идентифицированных положениях заменены/замещены петлей экзогенного пептида. В альтернативном варианте осуществления девять или более (где это применимо) аминокислотных остатков в идентифицированных положениях заменены/замещены петлей экзогенного пептида. Все аминокислотные остатки любого из положений встраивания 1-7 могут быть заменены петлей экзогенного пептида.
Например, если петля экзогенного пептида встроена в положении 4 и заменяет один или более остатков, вставка может представлять собой A*QGAE (SEQ ID NO: 28), AA*GAE (SEQ ID NO: 29), AA*AE (SEQ ID NO: 30), AA*E (SEQ ID NO: 31), AA*, A*GAE (SEQ ID NO: 32), A*AE (SEQ ID NO: 33), AA*E (SEQ ID NO: 34), A*E, A*, *AQGAE (SEQ ID NO: 35), *QGAE (SEQ ID NO: 36), *GAE (SEQ ID NO: 37), *AE, *E, AAQ* AE (SEQ ID NO: 38), AAQ*E (SEQ ID NO: 39), AAQ* (SEQ ID NO: 40), AAQG*E (SEQ ID NO: 41), AAQG* (SEQ ID NO: 42), AAQGA* (SEQ ID NO: 43), где * обозначает сайт встраивания, и один или более остатков удалены из исходной последовательности.
Специалист в данной области поймет, что эквивалентные комбинации сайтов встраивания и/или замен петлей экзогенного пептида могут быть сделаны с альтернативными последовательностями других идентифицированных положений встраивания 1-7.
В одном варианте осуществления область сайта встраивания может быть смещена на +/-5 остатков выше или ниже любого из положений 1-7. Альтернативно, область сайта встраивания может быть смещена на +/-4 остатка выше или ниже любого из положений 1-7. Альтернативно, область сайта встраивания может быть смещена на +/-3 остатка выше или ниже любого из положений 1-7. Альтернативно, область сайта встраивания может быть смещена на+1-2 остатка выше или ниже любого из положений 1-7. Альтернативно, область сайта встраивания может быть смещена н а+/-1 остаток выше или ниже любого из положений 1-7.
Дополнительно или альтернативно, петля(и) пептида может быть обеспечена в положении, которое стерически предотвращает взаимодействие fHbp:CFH. Это включает в себя петлю экзогенного пептида, встроенную в любой один или более сайтов между остатками 114-124, 199-206 или 240-246 (например, положения 2, 5 и 7), подчеркнутыми на первичной последовательности VI ниже:

В одном варианте осуществления изобретения модифицированный fHbp является иммуногенным. Модифицированный fHbp может представлять собой рекомбинантный белок. Модифицированный fHbp может представлять собой слитый белок, такой как рекомбинантный слитый белок. Модифицированный fHbp может представлять собой изолированную молекулу модифицированного fHbp. Молекула модифицированного fHbp согласно изобретению может быть описана как единичный белок, мультивалентная вакцина. Модифицированный fHbp может быть включен в OMV-вакцину.
В вариантах осуществления, в которых более одной петли экзогенного пептида встроено в fHbp или его варианты, петли экзогенного пептида могут быть одинаковыми, например, иметь одинаковые последовательности или по существу аналогичные. Например, некоторые эпитопы, такие как эпитопы PorA, могут не вызывать достаточных функциональных ответов, когда они представлены в отдельности на fHbp. В этом случае настоящее изобретение может быть использовано для обеспечения такого же эпитопа на множестве сайтах на этой же модифицированной молекуле fHbp, тем самым усиливая иммуногенное распознавание эпитопа.
Альтернативно, петли экзогенного пептида отличаться друг от друга. Например, когда петли экзогенного пептида происходят из одного белка, такого как PorA, различные петли экзогенного пептида могут происходить из различных областей белка, такого как PorA. В одном варианте осуществления различные петли экзогенного пептида могут быть получены в результате перекрывания и из различных областей белка, такого как PorA.
В вариантах осуществления, в которых более одной петли экзогенного пептида встроено в fHbp или его варианты, петли экзогенного пептида могут происходить из различных видов или штаммов. Например, когда мультивалентная вакцина требуется для множества различных антигенов, включая различные организмы.
Последовательность петли пептида PorA может быть выбрана из любой из последовательностей, представленных в Таблице 1 (например, любой из SEQ ID NO: 45-79). Комбинации различных последовательностей PorA из Таблицы 1 могут быть обеспечены (одна петля на сайт) в любом из сайтов встраивания Р1-Р7, описанных в настоящем документе. Дополнительно или альтернативно, две или более таких же последовательностей PorA из Таблицы 1 могут быть обеспечены (одна петля на сайт) в любом из сайтов встраивания Р1-Р7, описанных в настоящем документе.
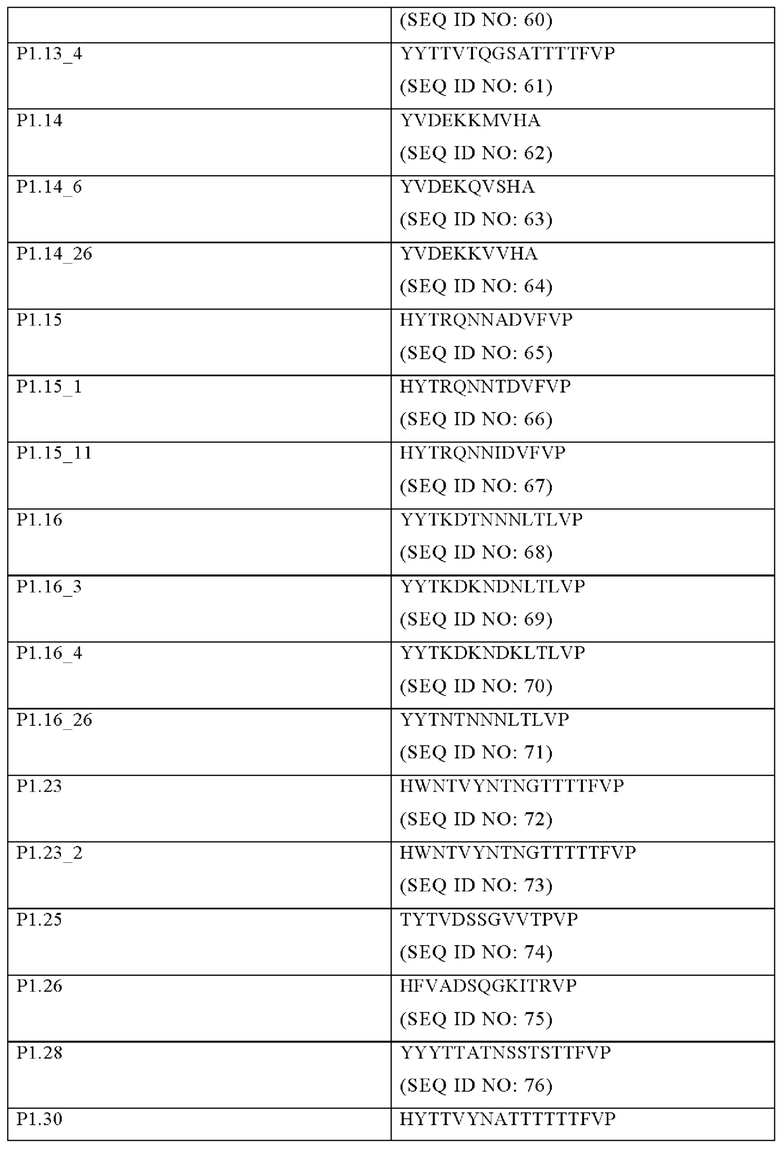
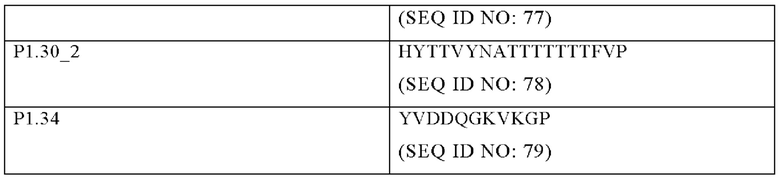
Специалисту будет понятно, что варианты, включающие одну или две, или более аминокислотных замен, добавлений или делеций, могут быть обеспечены для последовательностей PorA из Таблицы 1 без значительного удаления иммуногенной функции. Замены могут быть сделаны для сходных аминокислотных остатков, например, имеющих сходную молекулярную массу, заряд, гидрофобность или фрагменты, или синтетических аналогов. Специалист, кроме того, поймет, что варианты могут представлять собой усечения последовательностей PorA из Таблицы 1, при этом усеченные варианты обеспечивают достаточные аминокислотные остатки для образования узнаваемого эпитопа. В одном варианте осуществления последовательность PorA имеет по меньшей мере 80% идентичности с любой одной из последовательностей в Таблице 1. В другом варианте осуществления последовательность PorA имеет по меньшей мере 85% идентичности с любой одной из последовательностей в Таблице 1. В другом варианте осуществления последовательность PorA имеет по меньшей мере 90% идентичности с любой одной из последовательностей в Таблице 1. В другом варианте осуществления последовательность PorA имеет по меньшей мере 95% идентичности с любой одной из последовательностей в Таблице 1. В другом варианте осуществления последовательность PorA имеет по меньшей мере 98% идентичности с любой одной из последовательностей в Таблице 1.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:

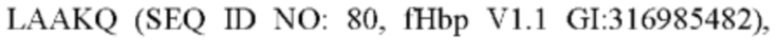 при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенные рамкой.
при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенные рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:

(SEQ ID NO: 81, fHbp V1.4 GL989557230), при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:

(SEQ ID NO: 82, fHbp VI. 13 GI:752774533), при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:
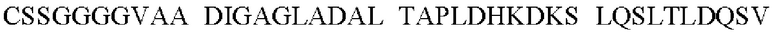
 при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:
 при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:
 при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:

(SEQ ID NO: 86, fHbp V2.16 GL488155511), при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:

(SEQ ID NO: 87, fHbp V2.19 GL488148626), при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:

(SEQ ID NO: 88, fHbp V2.22 GI: 120865922), при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:

(SEQ ID NO: 89, fHbp 2.25 GP488158712), при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:
 при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамко й.
при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамко й.
В одном варианте осуществления fHbp, который в дальнейшем будет модифицирован петлей экзогенного пептида, может содержать или состоять из последовательности:
 при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
при этом последовательность любой петли VR2 PorA в Таблице 1 может заменить любую аминокислоту или группы аминокислот, выделенных рамкой.
Модифицированный fHbp может содержать последовательность, представленную в любой из SEQ ID NO: 92-109.
Модифицированный fHbp может содержать последовательность, представленную в SEQ ID NO: 92-109, при этом последовательность 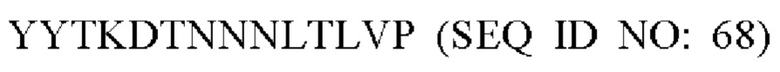 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли VR2, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли VR2, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:
 (SEQ ID NO: 92, fHbp V1.1 GL316985482, PorA VR2 P1.16 в P1), или такой же последовательности, при этом последовательность
(SEQ ID NO: 92, fHbp V1.1 GL316985482, PorA VR2 P1.16 в P1), или такой же последовательности, при этом последовательность 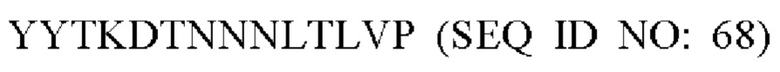 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 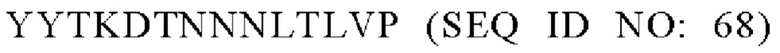 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

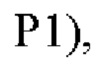 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 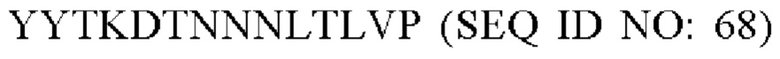 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

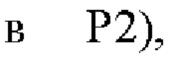 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность  заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

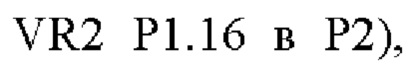 или такой же последовательности, при этом последовательность YYTKDTNNNLTLVP (SEQ ID NO: 68) заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
или такой же последовательности, при этом последовательность YYTKDTNNNLTLVP (SEQ ID NO: 68) заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

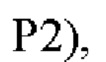 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 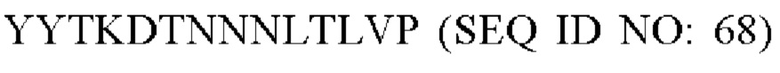 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

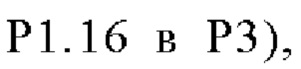 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 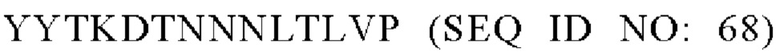 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

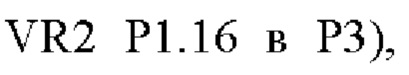 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 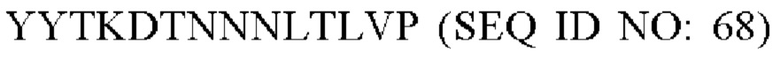 заменена последовательностью любой петли VR2 PorA, например, любой последовательностью петли PorA, обеспеченной в Таблице 1.
заменена последовательностью любой петли VR2 PorA, например, любой последовательностью петли PorA, обеспеченной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

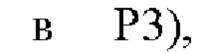 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность  заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

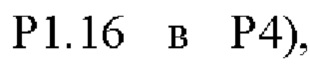 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность  заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

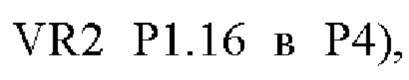 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 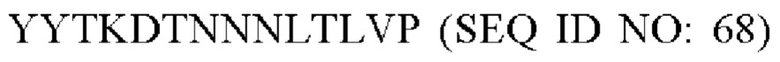 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

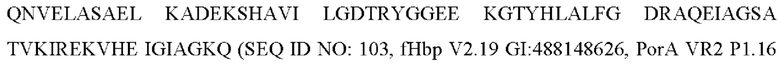
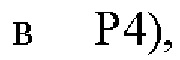 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 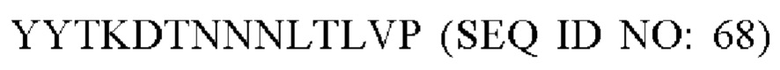 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

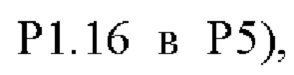 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 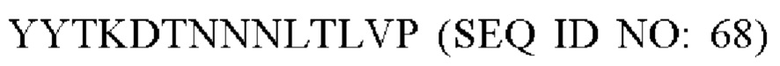 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

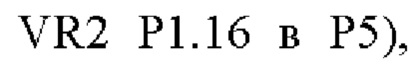 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность  заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:


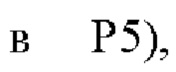 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность  заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, обеспеченной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, обеспеченной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

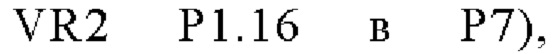 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность  заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

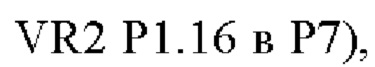 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 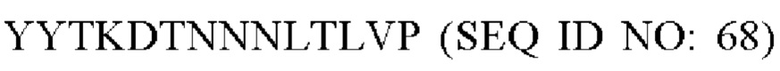 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
В одном варианте осуществления модифицированный fHbp может содержать или состоять из последовательности:

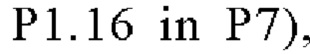 или такой же последовательности, при этом последовательность
или такой же последовательности, при этом последовательность 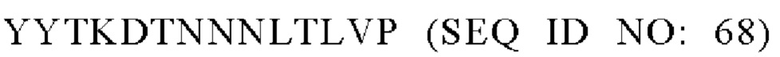 заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
заменена любой последовательностью петли VR2 PorA, например, любой последовательностью петли PorA, представленной в Таблице 1.
Специалисту будет понятно, что одна, две, три или четыре, или более аминокислотных замен, делеций или добавлений может быть сделано в модифицированном fHbp согласно изобретению в настоящем документе без значительного удаления его иммуногенной функции или нарушения стабильности. Замены могут быть сделаны для сходных аминокислотных остатков, например, имеющих сходную молекулярную массу, заряд, гидрофобность или фрагменты, или синтетических аналогов. Такие модификации рассматриваются как часть изобретения. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 75% идентичности с любым модифицированным fHbp, описанным в настоящем документе. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 80% идентичности с любым модифицированным fHbp, описанным в настоящем документе. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 85% идентичности с любым модифицированным fHbp, описанным в настоящем документе. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 90% идентичности с любым модифицированным fHbp, описанным в настоящем документе. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 95% идентичности с любым модифицированным fHbp, описанным в настоящем документе. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 98% идентичности с любым модифицированным fHbp, описанным в настоящем документе. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 99% идентичности с любым модифицированным fHbp, описанным в настоящем документе. В одном варианте осуществления модифицированный fHbp может иметь по меньшей мере 99,5% идентичности с любым модифицированным fHbp, описанным в настоящем документе.
В соответствии с другим аспектом изобретения обеспечена нуклеиновая кислота, кодирующая в основном или по меньшей мере модифицированный fHbp в соответствии с изобретением в настоящем документе.
Нуклеиновая кислота может содержаться в векторе, таком как вирусный вектор.
Согласно другом аспекту изобретения обеспечена композиция, содержащая модифицированный fHbp в соответствии с изобретением в настоящем документе.
Композиция может содержать две или более различных молекулы модифицированного fHbp (например, его различные формы/виды) в соответствии с изобретением в настоящем документе. Например, композиция может содержать два или более различных вариантов модифицированного fHbp в соответствии с изобретением. Например, композиция может содержать варианты v1 и v2 fHbp. Композиция может содержать варианты v2 и v3 fHbp. В другом варианте осуществления композиция содержит по меньшей мере вариант v2 fHbp.
Согласно другому аспекту изобретения предлагается композиция, содержащая нуклеиновую кислоту в соответствии с изобретением в настоящем документе.
Композиция может содержать фармацевтически приемлемый носитель. Композиция может, кроме того, содержать адъювант.
Согласно следующему аспекту изобретения предлагается модифицированный fHbp, нуклеиновая кислота или композиция в соответствии с изобретением для применения в качестве лекарственного средства.
Согласно следующему аспекту изобретения предлагается модифицированный fHbp, нуклеиновая кислота или композиция в соответствии с изобретением для применения в лечении или предупреждении патогенной инфекции или колонизации у субъекта.
Согласно следующему аспекту изобретения предлагается способ лечения или предупреждения возникновения патогенной инфекции или колонизации у субъекта, включающий введение субъекту модифицированного fHbp, нуклеиновой кислоты или композиции в соответствии с изобретением.
Согласно следующему аспекту изобретения предлагается способ вакцинации, включающий введение субъекту модифицированного fHbp, нуклеиновой кислоты или композиции в соответствии с изобретением.
Введение может быть осуществлено в терапевтически эффективном количестве. Специалист сможет определить подходящую дозировку и частоту введения.
Субъект может представлять собой млекопитающее, например, человека.
Инфекция может представлять собой бактериальную инфекцию. Например, инфекция может представлять собой менингит, такой как Neisseria meningitidis или Neisseria gonorrhoeae.
Согласно следующему аспекту изобретения предлагается единичный белок, мультивалентная вакцина, содержащая модифицированный белок, связывающий фактор Н (fHbp) в соответствии с изобретением.
Вакцину можно применять в качестве профилактической или терапевтической вакцины, направленной на. Nm.
Применение можно осуществлять с фармацевтически приемлемым носителем. Дополнительно или альтернативно, применение можно осуществлять с адъювантом. Подходящие фармацевтически приемлемые носители и адъюванты хорошо известны специалисту в данной области.
Согласно следующему аспекту изобретения предлагается комбинация модифицированного fHbp в соответствии с изобретением и по меньшей мере одной другой профилактически или терапевтически активной молекулы.
По меньшей мере одна другая профилактически или терапевтически активная молекула может содержать вакцину или антиген, отличный от модифицированного fHbp в соответствии с изобретением в настоящем документе. Комбинацию можно применять в комбинированной вакцине или терапии. Например, комбинацию можно применять в комбинированной вакцине или терапии, где используется другой менингококковый антиген.
В одном варианте осуществления по меньшей мере одна другая профилактически или терапевтически активная молекула представляет собой моновалентную вакцину, содержащую конъюгат белок : капсульный полисахарид. Моновалентная вакцина, содержащая конъюгат белок : капсульный полисахарид, может содержать любую капсулу серогруппы С или А с обезвреженными бактериальными токсинами, бивалентные вакцины (с капсульным полисахаридом серогруппы С и А, конъюгированным с обезвреженными бактериальными токсинами), квадри-(серогруппы А, С, Y, W) или пента- (А, С, Y, W, X) валентные конъюгированные вакцины.
Альтернативно, по меньшей мере одна другая профилактически или терапевтически активная молекула может представлять собой конъюгированную вакцину, при этом антиген(ы), содержащий каркас fHbp, несущий петли экзогенного пептида (такие как петли PorA), может быть включен в качестве молекулы белка-носителя в конъюгированную вакцину. Конъюгированная вакцина может содержать капсульные полисахариды любой серогруппы из штаммов А, С, Y, W или X индивидуально или в комбинации.
Согласно другому аспекту изобретения предлагается применение белка, связывающего фактор Н (fHbp) в качестве каркаса для дисплея эпитопа.
Применение в качестве каркаса для дисплея эпитопа может включать применение белка, связывающего фактор Н (fHbp), содержащего любую из модификаций, описанных в настоящем документе.
В дополнение к их потенциальному применению в качестве вакцин, композиции или модифицированные fHbp согласно изобретению могут быть полезными в качестве диагностических реагентов и в качестве показателя иммунной компетентности вакцины.
Термин «иммуногенный» означает, что молекула способна вызывать иммунный ответ в организме человека или животного. Иммунный ответ может быть защитным.
Иммунный ответ, вызванный модифицированным fHbp согласно изобретению, может влиять на способность Neisseria meningitidis (Nm) инфицировать субъекта, иммунизированного модифицированным fHbp согласно изобретению. Предпочтительно способность Nm инфицировать субъекта, иммунизированного модифицированным fHbp согласно изобретению, затруднена или предотвращена. Индуцируемый иммунный ответ может узнавать и разрушать Nm. Альтернативно или дополнительно, индуцированный иммунный ответ может затруднять или предотвращать репликацию Nm. Альтернативно или дополнительно, индуцированный иммунный ответ может затруднять или предупреждать вызывание Nm заболевания у человека или животного, не относящегося к человеку.
Термин «петля пептида», используемый в настоящем документе, понимается как последовательность одноцепочечного полипептида, заякоренная на обоих концах (например, заякоренная на каркас, такой как fHbp). Термин «петля» не подразумевает или не требует какой-либо конкретной вторичной структуры, принятой полипептидом.
Термин «экзогенный», используемый в контексте «петли экзогенного пептида», означает, что петля пептида происходит из другого источника по сравнению с белком fHbp (то есть не является fHbp или его фрагментом). Однако она может происходить от такого же организма, что и fHbp. Например, модифицированный fHbp может включать fHbp N. meningitidis, модифицированный (экзогенной) пептидной петлей(петлями), происходящими из PorA N. meningitidis.
Термин «слитый белок», используемый в настоящем документе, означает полипептид, содержащий комбинацию последовательностей из различных генных продуктов или источников.
Термин «слитый белок» может быть использован взаимозаменяемо с термином «химерная молекула».
Ссылка на «идентичность» последовательности, используемую в настоящем документе, может относиться к проценту идентичности между двумя выровненными последовательностями с использованием стандартных параметров NCBI BLASTp (http://blast.ncbi.nlm.nih.gov).
Термин «выделенный», в случае применения к модифицированному fHbp согласно настоящему изобретению, означает белок: (i) кодируемый нуклеиновыми кислотами с использованием способов рекомбинантной ДНК или вирусного вектора; или (ii) синтезированный, например, способами химического синтеза; или (iii) отделенный от биологических материалов, а затем очищенный. Выделенный полипептид согласно изобретению включает белок, экспрессированный из нуклеотидной последовательности, кодирующей белок, или из рекомбинантного вектора, содержащего нуклеотидную последовательность, кодирующую белок.
Термин «защитный» означает предупреждение заболевания, уменьшенный риск возникновения, передачи и/или прогрессирования инфекционного заболевания, снижение тяжести заболевания, излечение состояния или заболевания, облегчение симптомов или снижение тяжести заболевания или симптомов заболевания.
Термин «профилактика» означает предупреждение или профилактическое лечение заболевания. Профилактика может включать уменьшенный риск возникновения, передачи и/или прогрессирования инфекции, или уменьшенную тяжесть заболевания.
Термин «лечение» означает излечение состояния или заболевания, облегчение симптомов или уменьшение тяжести заболевания или симптомов заболевания.
Специалисты в данной области поймут, что необязательные признаки одного варианта осуществления или аспекта изобретения могут быть применимы, где это уместно, к другим вариантам осуществления или аспектам изобретения.
Варианты осуществления изобретения теперь будут описаны более подробно, исключительно в качестве примера, со ссылкой на прилагаемые чертежи.
Фигура 1. Дизайн химерного fHbp:PorAs
(A) Схематическое изображение поверхности N. meningitidis, показывающее главные признаки наружной мембраны, липоолигосахарид и пили 4 типа, а также важные антигены, fHbp и PorA. Петля иммуногенного VR2 PorA выделена цветом и fHbp показан взаимодействующим с доменами 6 и 7 человеческого CFH.
(B) Структура V1 fHbp с доменами 6-7 CFH, показывающая шесть положений (Р1-5 и Р7), используемых для создания химерного fHbp:PorAs, в который встроены петли PorA. Примечание: положение 5 находится на границе между fHbp:CFH.
Фигура 2: Применение fHbp в качестве молекулярного каркаса
А) Белковая структура V1.1 fHbp (серый, ленточное представление) с шестью положениями (Р1-5 и Р7), используемыми для создания химерной fHbp:PorAs. В) Вторичная структура V1.1 fHbp (серый, стрелки представляют β-листы, прямоугольники представляют α-спирали). Локализации сайтов встраивания VR2 Р1.16 PorA указаны сплошными черными линиями, числа указывают диапазон остатков, куда могут быть встроены петли VR2 PorA (соответствуют номерам остатков в 1D). С) Анализ очищенного fHbp:PorAs с петлей VR2 Р1.16 PorA в положениях 1-5 или 7 fHbp, дикого типа (V1.1 WT) с помощью SDS-PAGE и Вестерн-блоттинга. Блоты зондировали α-V1 fHbp pAb и α-P1.16 mAb. D) Первичная последовательность (SEQ ID NO: 1) V1.1 fHbp, указывающая локализации (подчеркнуто) положений 1-5 и 7, в которые могут быть встроены петли из других белков.
Фигура 3. Характеристика химерного fHbp: Рог As
(A) Структура fHbp:PorAs, перекрывающаяся с петлей Р1.16 (черный, PDBID: 2 тра) с Fab α-Р1.16 mAb, и fHbp:PorA с петлей в положении 1, положении 3 и положении 7, демонстрирующая, что эпитоп находится в конформации, распознаваемой бактерицидным антителом.
(B) Стабильность N-концевых (NT) и С-концевых (СТ) бета-цилиндров fHbp с помощью анализа методом дифференциальной сканирующей калориметрии, выполненного с использованием температурного градиента 20-120°С. Температура плавления показана для N-концевых (NTTM) и С-концевых (СТТМ) цилиндров fHbp. Связывание fHbp:PorAs с фактором комплемента Н (CFH) и анализ SPR с использованием mAbs (моноклональных антител) fHbp и химерного fHbp:PorAs, связанных с чипом СМ5 BIAcore. CFH (fH67) протекал над поверхностью при разбавлении в интервале 0,5-32 нМ, и рассчитывали константу диссоциации (KD); константы диссоциации (KD) для fHbp:PorAs подтверждают отсутствие CFH-связывания fHbp с петлей в положении 5, которая сталкивается с границей раздела fHbp:CFH (фигура 2A). NB=отсутствие связывания.
Фигура 4. Репертуар антигенов, выбранных для химерного fHbp:PorAs (А, В) Частота вариантов fHbp и подтипов VR2 PorA, соответственно, в изолятах N. meningitidis в Великобритании между 2010-2015 годами из библиотеки Meningitis Research Foundation Genome Library (http://www.meningitis.org/research/genome) показана в виде круговых диаграмм (выше) и в таблицах (ниже) с частотой специфических fHbps и Рог As.
Примечание: На долю V2 fHbp приходится 38,9% изолятов.
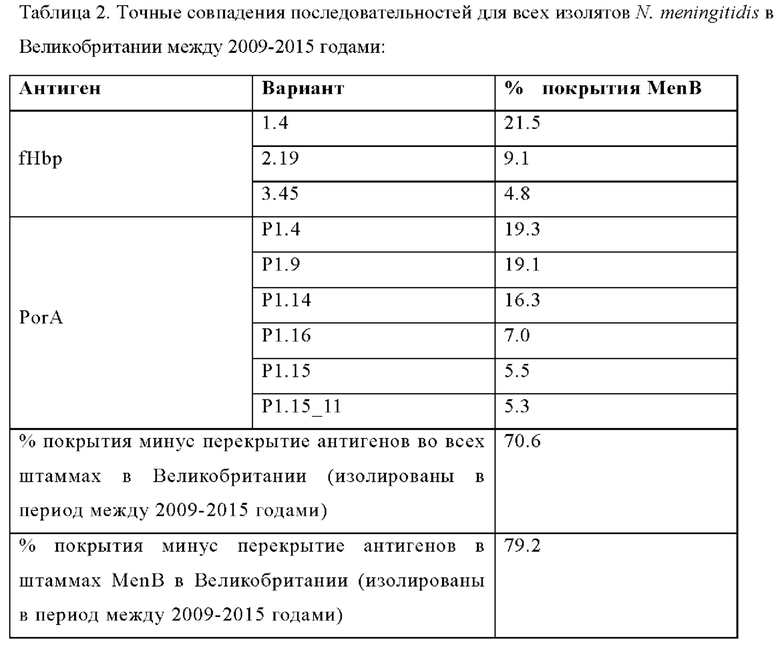
Точные совпадения последовательностей для:
- Вакцины Pfizer, 3,02%
- Bexsero fHbp (V1.1) или PorA (P1. 16), 15,86%
Химерного fHbp: Рог As, fHbp или PorA, 72%
(23,5% с fHbp и PorA)
Фигура 5. Распознавание антигенов Neisseria Meningitidis fHbp (А) и PorA (В) мышиной иммунной сывороткой. Лизаты целых клеток из штаммов Н44/76 (WT), Н44/67 ΔfHbp и Н44/67 ΔPorA Neisseria Meningitidis разделяли с помощью SDS-PAGE, переносили на PVDF-мембрану и зондировали с использованием мышиной иммунной сыворотки. Мышиную иммунную сыворотку получали путем иммунизации мышей BalbC три раза 20 мкг очищенных химер fHbp-PorA с петлями VR2 в Р1, Р2, Р4, Р5 или Р7.
Фигура 6. Стабилизация V2 fHbp: конструирование и иммуногенность fHbp:PorAs
(A) Стабилизация V2.22 и V2.25 V2 fHbp шестью (Мб) или двумя (М2) аминокислотными заменами. Анализ методом DSC проводили с 20 мкМ белка, используя температурный градиент 20-120°С. Температуру плавления регистрировали для N-концевых (NTtm) и С-концевых цилиндров fHbp.
(B) Петли PorA химерного fHbp:PorAs распознаются соответствующими моноклональными антителами (mAb). Петли VR2 PorA из Р1.2, Р1.4, Р1.9, Р1.14 и Р1.15 встраивали в положение 1 V2,25 fHbp. SDS-PAGE и Вестерн-блот-анализ очищенного V2.25 fHbp дикого типа и химерного V3.45 fHbp-PorA. Вестерн-блоты зондировали pAbs V2.25 fHbp и специфичными для петли mAbs PorA (NIBSC). Связывание CFH детектировали с помощью Вестерн-блот-анализа с нормальной человеческой сывороткой и pAbs CFH.
Фигура 7. Химерный fHbp:PorAs вызывает защитный иммунитет. Мышей иммунизировали химерным fHbp:PorA, то есть Р(1)(1)(13), Р(2)(1)(13) и Р(3)(1)(13) трижды, и измеряли бактерицидную активность сыворотки (SBA) против указанных штаммов; показатель SBA>8 считается защитным. Отсутствие PorA-направленной SBA (то есть SBA 0, против мутанта fHbp) с петлей VR2 в положении 3, то есть Р(3)(1)(13), по-видимому, обусловлено тем, что петля не выступает из цилиндра fHbp так далеко, как в положении 1.
Фигура 8. Частота вариантов VR2 PorA (А) и fHbp (В) в штаммах N. meningitidis серогруппы В (n=243), выделенных в 2016 году в Великобритании. Данные загружены из Meningococcal Research Foundation, 27 июня 2017 года. Прочее: остальные аллели, которые встречаются в <4 изолятах. (С) Анализ рекомбинантных химерных антигенов с помощью SDS-PAGE и Вестерн-блоттинга. Иммуноблоты зондировали mAbs VR2 α-PorA: P1.4, P1.9, P1.14 и P1.15. (D) Детекция PorA в панели изолятов N. meningitidis серогруппы В с помощью мышиной поликлональной антисыворотки из химерных антигенов fHbpV1.4:PorA151/P1.1.10_1, fHbpV1.4:PorA151/P1.14 и fHbpV1.4:PorA151/P1.15, fHbpV3.45:Por158/P1.4 и fHbpV3.45:PorA158/P1.9.
Пример 1
Было показано, что иммуногенные пептиды могут быть введены в белок, связывающий фактор Н (fHbp), и пептиды презентированы иммунной системе и способны вызывать защитные ответы (Фиг. 5 и 7). Пептиды использовали из интегрального мембранного белка PorA для подтверждения в принципе этого подхода. PorA трудно экспрессировать из-за нерастворимости его трансмембранных доменов. Иммуногенные части молекулы расположены во внеклеточных петлях, которые подвергаются воздействию иммунной системы. Однако эффективные иммунные ответы генерируются только против петель, находящихся в их правильной конформации; линейные пептидные последовательности не вызывают функциональных иммунных ответов. Зная структуру fHbp, можно ввести петли PorA в fHbp и генерировать соответствующие ответы против PorA. Это приводит к образованию химерной молекулы, основанной на последовательностях fHbp и PorA в определенных сайтах для создания химерной молекулы. Этот подход может быть использован для любого другого иммуногенного интегрального белка наружной мембраны.
Было показано, что вероятной причиной исключения v2 fHbp из вакцин является внутренняя нестабильность его N-концевого β-цилиндра: i) было невозможно определить атомную структуру этой части v2 fHbp10, ii) v2 fHbp является чувствительным к расщеплению протеазой (масс-спектрометрия показывает, что расщепленные участки расположены в N-концевом β-цилиндре, не показано), и iii) дифференциальная сканирующая калориметрия подтверждает, что нестабильность лежит в этой области v2 fHbp10.
Были успешно генерированы стабильные v2 fHbps. Был проведен мутагенез, воздействующий на N-концевой цилиндр, с заменой аминокислот (a.a.s) по отдельности или в комбинации. Замена шести аминокислот в М6 fHbp стабилизирует v2 fHbp (т.е. 6 замен в 130 аминокислотах этого β-цилиндра, <0,5%) (см. WO 2014030003 для подробной информации, касающейся мутаций). Это следует из дифференциальной сканирующей калориметрии (DSC) и чувствительности к расщеплению протеазой (см. WO 2014030003 для получения подробной информации). Боковые цепи измененных остатков способствуют взаимодействиям между β-листами N-концевого цилиндра, так как они ориентированы по направлению к центру молекулы; изменения не влияют на иммуногенность белка, как ожидалось (отсутствует различие в SBA, или уровнях IgG α-fHbp, не показано).
Химерный v1.1 fHbp создавали путем введения VR2 длиной 13 аминокислот из Р1.16 PorA, который вызывает SBA у реципиентов OMV-вакцин16. В то время как интегральные мембранные белки содержат гидрофобные (то есть нерастворимые) β-цилиндры, fHbp содержит два цилиндра, которые могут быть экспрессированы и очищены до высоких степеней очистки. Последовательность VR2 вводили в шесть различных положений fHbp (Фиг. 2 В); эти сайты выбирали на основе сходного расстояния между фланкирующими β-листами в PorA22 и fHbp для уменьшения вероятности того, что встраивание будет разрушать всю структуру fHbp (Фиг. 2 В для предсказанного эффекта вставок). Оценивали иммуногенность трех fHbp со вставкой VR2 в другой fHbp (Фиг. 2 В). Все белки вызывали ответы антител, направленных против fHbp и PorA (Фиг. 5 и 7), и важным является то, что оба белка, которые были протестированы (с VR2 в сайте 1 или 2), независимо индуцируют SBA против fHbp и PorA (SBA для Nm Н44/76, 512; и для Nm H44/76αfHbp, 256 для обоих fHbps). Это обеспечивает доказательство в принципе этого подхода.
FHbp в качестве каркаса для мультивалентных вакцин
Нефункциональные fHbp в качестве вакцин. Функция fHbp не была известна, когда начинали клинические испытания fHbp-содержащих вакцин; fHbp демонстрирует высокоаффинные взаимодействия с fH (константа диссоциации <5 нМ) независимо от группы вариантов, при этом fH занимает большую область fHbp5. Это взаимодействие может ухудшить применение fHbp в качестве вакцины путем i) блокирования иммуногенных эпитопов и препятствования образованию антител, которые могут конкурировать с fH, и ii) снижения активации комплемента (посредством рекрутинга fH) и, следовательно, активации В-клеток на участке индукции иммунного ответа. Использование нефункциональных fHbps решает эти проблемы. Были идентифицированы ключевые аминокислоты v1, 2 и 3 fHbps, которые необходимы для взаимодействий10 с fH, и было показано, что модификация отдельных аминокислот v1, v2 и v3 fHbps, которые предотвращают связывание fH, сохраняет или даже повышает иммуногенность этого важного вакцинного антигена10,23.
Для создания и оценки монобелковых, мультивалентных вакцин-кандидатов:
Защитные эпитопы PorA из преобладающих сероподтипов (которые определяются их последовательностью PorA) Nm15 вводили в белки v1, стабильный v2 и v3; определяли их стабильность и узнавание mAbs PorA и fHbp. Последовательности PorA выбирали таким образом, чтобы охватить разнообразие изолятов в Великобритании, но могут быть использованы данные из любой коллекции менингококковых штаммов.
Способы исследования
Генерирование и характеристика вакцин-кандидатов. Рекомбинантные fHbps конструировали и экспрессировали в Е coli, используя стандартные плазмидные векторы; белки очищали путем аффинной очистки с использованием полигистидиновой метки в белке, анионного обмена и гель-фильтрации10 химерных v1, V2 и V3 fHbps, так как они либо присутствуют в существующих вакцинах (v1.1 и 3.45), либо в связи с опытом с белком (v2), или из-за их распространенности в штаммах Nm. Петли PorA вводили в fHbp стандартными способами, и было показано, что слитые белки связываются с моноклональными антителами (mAb) против общих сероподтипов PorA. Эту стратегию использовали для сравнения нативных и сконструированных последовательностей, и выполнения тонкого картирования антигенных и fH-связывающих кандидатов. DSC проводили с использованием VP Capillary DSC (GEHealthcare), и SPR с помощью Biacore 3000 (GE Healthcare) или ProteOn XPR36 (BioRad), как описано ранее10.
Список использованной литературы включен в настоящий документ путем ссылки.
Пример 2 - Химерные антигены, содержащие расширенный диапазон петель VR2 PorA, генерируют иммунные ответы
Для тестирования возможности адаптировать химерные антигены fHbp:PorA генерировали несколько химерных антигенов, состоящих из различных комбинаций fHbp и VR2 PorA. Полные данные по геному менингококка, имеющиеся для выделенных в Великобритании штаммов (библиотека Meningitis Research Foundation Meningococcus Genome Library, разработанная Public health England, the Wellcome Trust Sanger Institute и University of Oxford в качестве совместной работы), позволяют сконструировать химерные антигены, имеющие точные совпадения последовательностей с наиболее распространенными антигенами в заданном регионе. В 2016 году наиболее распространенными VR2 PorA в изолятах N. meningitidis серогруппы В являлись Р1.4 (15,2%), Р1.14 (15,2%), Р1.9 (12,8%), Р1.16 (11,1%) и Р1.15 (5,8%, Фигура 8 В). P1.10_1 VR2 присутствовал в 1,6% изолятов серогруппы В. Наиболее распространенными fHbp варианта 1, варианта 2 и варианта 3 являлись V1.4, V2.19 и V3.45, присутствующие в 21,8%, 5,3% и 4,9% изолятов N. meningitidis серогруппы В, соответственно (Фигура 8С). Было сконструировано пять различных химерных антигенов, в которых VR2 PorA был встроен в положение 151 (V1.4) или положение 158 (V3.45, Фигура 8А). После экспрессии и очистки химерного антигена Вестерн-блот-анализы подтвердили, что все эти химерные антигены удерживали эпитопы, распознаваемые их родственными α-VR2 mAb и α-fHbp pAbs (Фигура 8D). Термическую стабильность V1.1, V1.4 и V3.45 fHbps дикого типа и химерных антигенов определяли методом дифференциальной сканирующей калориметрии (DSC, Таблица 3).
Для изучения способности этих химерных антигенов fHbp:PorA вызывать иммунные ответы, группы мышей CD1 иммунизировали каждым химерным антигеном/алюминий-содержащим адъювантом; антисыворотку, полученную после иммунизации, объединяли. Для оценки полученных иммунных ответов PorA проводили вестерн-блоттинг с использованием объединенной антисыворотки и панели изолятов N. meningitidis серогруппы В. На Фигуре 8Е показано, что все химерные антигены вызывали образование антител α-PorA, которые распознавали их родственный VR2 PorA. Для оценки ответов SBA α-PorA проводили сывороточный бактерицидный анализ с использованием объединенной антисыворотки, содержащей химерный антиген/алюминий - содержащий адъювант, и штаммов N. meningitidis серогруппы В с несовпадающими вариантами fHbp для устранения перекрестной защиты fHbp. Титры изменялись в диапазоне от >20 до >1280 и в >8 раз превышали пороговое значение для принятой корреляции защитного иммунитета против N. meningitidis (Andrews, N. et al. Clin Diagn Lab Immunol 10, 780-786 (2003)) (Таблица 4).


Температура плавления, Tm
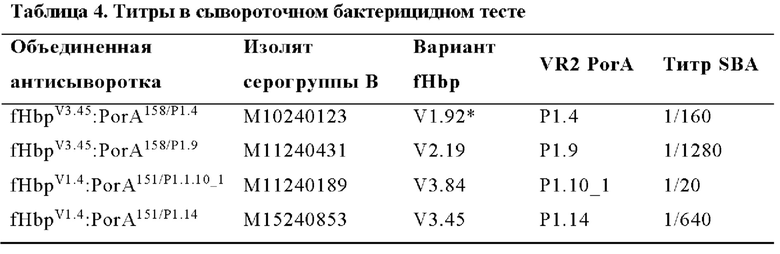
Титры SBA α-PorA генерировали с использованием объединенной антисыворотки, содержащей химерный антиген/алюминий - содержащий адъювант, и изолятов N. meningitidis серогруппы В с несовпадающими вариантами fHbp.* fHbp усеченный в остатке 242.
fHbpv1,4:PorA151/P115 не тестировали, так как он требовался для создания штаммов ΔfHbp, так как fHbp в штаммах с Р1.15 VR2 PorA не является несовпадающим.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ОКСФОРД ЮНИВЕРСИТИ ИННОВЭЙШН ЛИМИТЕД
<120> Модифицированный белок, связывающий фактор Н
<130> JA69120P.WOP
<150> GB1614687.0
<151> 2016-08-31
<160> 109
<170> PatentIn version 3.5
<210> 1
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 1
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu
100 105 110
Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Lys Thr Val Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 2
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 2
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Leu Gln Thr Glu
100 105 110
Gln Val Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Ser Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly His Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ser Asp Ile Lys Pro Asp Lys Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Gln Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Glu Thr Ala Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 3
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 3
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Lys Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Leu Gln Thr Glu
100 105 110
Gln Val Gln Asp Ser Glu Asp Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Lys Gly Gly Ser Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly His Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Glu
180 185 190
Leu Ala Thr Ala Tyr Ile Lys Pro Asp Glu Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Asp Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Gln Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Glu Thr Ala Asn Gly Ile His His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 4
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 4
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Leu Gln Thr Glu
100 105 110
Gln Glu Gln Asp Pro Glu His Ser Gly Lys Met Val Ala Lys Arg Arg
115 120 125
Phe Lys Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Lys Asp Val Met Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly His Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Glu
180 185 190
Leu Ala Thr Ala Tyr Ile Lys Pro Asp Glu Lys His His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Asp Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Gln Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Glu Thr Ala Asn Gly Ile His His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 5
<211> 263
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 5
Cys Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Val Ala Ala Asp
1 5 10 15
Ile Gly Ala Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys
20 25 30
Asp Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn
35 40 45
Gly Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Arg Thr Phe Lys Ala
50 55 60
Gly Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys
65 70 75 80
Ile Ser Arg Phe Asp Phe Ile Arg Gln Ile Glu Val Asp Gly Gln Leu
85 90 95
Ile Thr Leu Glu Ser Gly Glu Phe Gln Val Tyr Lys Gln Ser His Ser
100 105 110
Ala Leu Thr Ala Leu Gln Thr Glu Gln Val Gln Asp Ser Glu His Ser
115 120 125
Gly Lys Met Val Ala Lys Arg Gln Phe Arg Ile Gly Asp Ile Val Gly
130 135 140
Glu His Thr Ser Phe Gly Lys Leu Pro Lys Asp Val Met Ala Thr Tyr
145 150 155 160
Arg Gly Thr Ala Phe Gly Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr
165 170 175
Thr Ile Asp Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu
180 185 190
Lys Ser Pro Glu Leu Asn Val Asp Leu Ala Ala Ala Asp Ile Lys Pro
195 200 205
Asp Glu Lys His His Ala Val Ile Ser Gly Ser Val Leu Tyr Asn Gln
210 215 220
Ala Glu Lys Gly Ser Tyr Ser Leu Gly Ile Phe Gly Gly Gln Ala Gln
225 230 235 240
Glu Val Ala Gly Ser Ala Glu Val Glu Thr Ala Asn Gly Ile Arg His
245 250 255
Ile Gly Leu Ala Ala Lys Gln
260
<210> 6
<211> 260
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 6
Cys Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Val Thr Ala Asp
1 5 10 15
Ile Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys
20 25 30
Asp Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn
35 40 45
Gly Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn
50 55 60
Gly Asp Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg
65 70 75 80
Phe Asp Phe Ile Arg Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu
85 90 95
Glu Ser Gly Glu Phe Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr
100 105 110
Ala Leu Gln Thr Glu Gln Glu Gln Asp Pro Glu His Ser Glu Lys Met
115 120 125
Val Ala Lys Arg Arg Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr
130 135 140
Ser Phe Asp Lys Leu Pro Lys Asp Val Met Ala Thr Tyr Arg Gly Thr
145 150 155 160
Ala Phe Gly Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp
165 170 175
Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Ser Pro
180 185 190
Glu Leu Asn Val Asp Leu Ala Val Ala Tyr Ile Lys Pro Asp Glu Lys
195 200 205
His His Ala Val Ile Ser Gly Ser Val Leu Tyr Asn Gln Asp Glu Lys
210 215 220
Gly Ser Tyr Ser Leu Gly Ile Phe Gly Glu Lys Ala Gln Glu Val Ala
225 230 235 240
Gly Ser Ala Glu Val Glu Thr Ala Asn Gly Ile His His Ile Gly Leu
245 250 255
Ala Ala Lys Gln
260
<210> 7
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 7
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Asp Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly
165 170 175
His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ala Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Gly Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 8
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 8
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly
165 170 175
His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 9
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 9
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Pro Asn Gly Arg Leu His Tyr Ser Ile Asp Phe Thr Lys Lys Gln Gly
165 170 175
Tyr Gly Arg Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 10
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 10
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Thr Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Thr Ile Thr Leu Ala Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asn His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Asp Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Pro Asn Gly Arg Leu His Tyr Ser Ile Asp Phe Thr Lys Lys Gln Gly
165 170 175
Tyr Gly Arg Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 11
<211> 261
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 11
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly
50 55 60
Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile
65 70 75 80
Ser Arg Phe Asp Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile
85 90 95
Thr Leu Ala Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala
100 105 110
Val Val Ala Leu Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp
115 120 125
Ser Leu Ile Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu
130 135 140
His Thr Ala Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly
145 150 155 160
Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile
165 170 175
Asp Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr
180 185 190
Pro Glu Gln Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Glu
195 200 205
Lys Ser His Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu
210 215 220
Lys Gly Thr Tyr His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile
225 230 235 240
Ala Gly Ser Ala Thr Val Lys Ile Arg Glu Lys Val His Glu Ile Gly
245 250 255
Ile Ala Gly Lys Gln
260
<210> 12
<211> 257
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 12
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Lys
20 25 30
Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly Thr Leu Thr Leu
35 40 45
Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly Asp Lys Asp Asn
50 55 60
Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile Ser Arg Phe Asp
65 70 75 80
Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile Thr Leu Ala Ser
85 90 95
Gly Glu Phe Gln Ile Tyr Lys Gln Asn His Ser Ala Val Val Ala Leu
100 105 110
Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn
115 120 125
Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe
130 135 140
Asn Gln Leu Pro Gly Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser
145 150 155 160
Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala
165 170 175
Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn
180 185 190
Val Glu Leu Ala Ala Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala
195 200 205
Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr Tyr
210 215 220
His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala
225 230 235 240
Thr Val Lys Ile Gly Glu Lys Val His Glu Ile Ser Ile Ala Gly Lys
245 250 255
Gln
<210> 13
<211> 285
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 13
Met Thr Arg Ser Lys Pro Val Asn Arg Thr Thr Phe Cys Cys Leu Ser
1 5 10 15
Leu Thr Ala Gly Pro Asp Ser Asp Arg Leu Gln Gln Arg Arg Gly Gly
20 25 30
Gly Gly Gly Val Ala Ala Asp Ile Gly Thr Gly Leu Ala Asp Ala Leu
35 40 45
Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Lys Ser Leu Thr Leu
50 55 60
Glu Ala Ser Ile Pro Gln Asn Gly Thr Leu Thr Leu Ser Ala Gln Gly
65 70 75 80
Ala Glu Lys Thr Phe Lys Ala Gly Gly Lys Asp Asn Ser Leu Asn Thr
85 90 95
Gly Lys Leu Lys Asn Asp Lys Ile Ser Arg Phe Asp Phe Val Gln Lys
100 105 110
Ile Glu Val Asp Gly Gln Thr Ile Thr Leu Ala Ser Gly Glu Phe Gln
115 120 125
Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Arg Ile Glu Lys
130 135 140
Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser Phe
145 150 155 160
Leu Val Ser Asp Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu Pro
165 170 175
Asp Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp Ala
180 185 190
Asp Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly His
195 200 205
Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu Ala
210 215 220
Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu Gly
225 230 235 240
Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr Arg Leu Ala Leu
245 250 255
Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys Ile
260 265 270
Gly Glu Lys Val His Glu Ile Gly Ile Ala Asp Lys Gln
275 280 285
<210> 14
<211> 256
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 14
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Pro Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu
50 55 60
Asn Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile
65 70 75 80
Arg Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu
85 90 95
Phe Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr
100 105 110
Glu Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg
115 120 125
Gln Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys
130 135 140
Leu Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser
145 150 155 160
Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys
165 170 175
Gln Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val
180 185 190
Asp Leu Ala Ala Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val
195 200 205
Ile Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser
210 215 220
Leu Gly Ile Phe Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu
225 230 235 240
Val Lys Thr Val Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 15
<211> 6
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 15
Glu Val Asp Gly Gln Leu
1 5
<210> 16
<211> 8
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 16
Lys Pro Asp Gly Lys Arg His Ala
1 5
<210> 17
<211> 7
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 17
Phe Gly Gly Lys Ala Gln Glu
1 5
<210> 18
<211> 6
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 18
Ala Ala Gln Gly Ala Glu
1 5
<210> 19
<211> 10
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 19
Ile Gln Asp Ser Glu His Ser Gly Lys Met
1 5 10
<210> 20
<211> 6
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 20
Lys Thr Val Asn Gly Ile
1 5
<210> 21
<211> 7
<212> БЕЛОК
<213> Neisseria meningitidis
<220>
<221> Xaa
<222> (1)..(1)
<223> exogenous loop insert
<400> 21
Xaa Ala Ala Gln Gly Ala Glu
1 5
<210> 22
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (2)..(2)
<223> Exogenous loop insert
<400> 22
Ala Xaa Ala Gln Gly Ala Glu
1 5
<210> 23
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (3)..(3)
<223> Exogenous loop insert
<400> 23
Ala Ala Xaa Gln Gly Ala Glu
1 5
<210> 24
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (4)..(4)
<223> Exogenous loop insert
<400> 24
Ala Ala Gln Xaa Gly Ala Glu
1 5
<210> 25
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (5)..(5)
<223> Exogenous loop insert
<400> 25
Ala Ala Gln Gly Xaa Ala Glu
1 5
<210> 26
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (6)..(6)
<223> Exogenous loop insert
<400> 26
Ala Ala Gln Gly Ala Xaa Glu
1 5
<210> 27
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
19
<220>
<221> Xaa
<222> (7)..(7)
<223> Exogenous loop insert
<400> 27
Ala Ala Gln Gly Ala Glu Xaa
1 5
<210> 28
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (2)..(2)
<223> Exogenous loop insert
<400> 28
Ala Xaa Gln Gly Ala Glu
1 5
<210> 29
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (3)..(3)
<223> Exogenous loop insert
<400> 29
Ala Ala Xaa Gly Ala Glu
1 5
<210> 30
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (3)..(3)
<223> Exogenous loop insertion
<400> 30
Ala Ala Xaa Ala Glu
1 5
<210> 31
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa can be any naturally occurring amino acid
<400> 31
Ala Ala Xaa Glu
1
<210> 32
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Modified polypepitide
<220>
<221> Xaa
<222> (2)..(2)
<223> Exogenous loop insertion
<400> 32
Ala Xaa Gly Ala Glu
1 5
<210> 33
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (2)..(2)
<223> Exogenous loop insertion
<400> 33
Ala Xaa Ala Glu
1
<210> 34
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (3)..(3)
<223> Exogenous loop insertion
<400> 34
Ala Ala Xaa Glu
1
<210> 35
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (1)..(1)
<223> Exogenous loop insertion
<400> 35
Xaa Ala Gln Gly Ala Glu
1 5
<210> 36
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (1)..(1)
<223> Exogenous loop insertion
<400> 36
Xaa Gln Gly Ala Glu
1 5
<210> 37
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (1)..(1)
<223> Exogenous loop insertion
<400> 37
Xaa Gly Ala Glu
1
<210> 38
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (4)..(4)
<223> Exogenous loop insertion
<400> 38
Ala Ala Gln Xaa Ala Glu
1 5
<210> 39
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (4)..(4)
<223> Exogenous loop insertion
<400> 39
Ala Ala Gln Xaa Glu
1 5
<210> 40
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (4)..(4)
<223> Exogenous loop insertion
<400> 40
Ala Ala Gln Xaa
1
<210> 41
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (5)..(5)
<223> Exogenous loop insertion
<400> 41
Ala Ala Gln Gly Xaa Glu
1 5
<210> 42
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (5)..(5)
<223> Exogenous loop insertion
<400> 42
Ala Ala Gln Gly Xaa
1 5
<210> 43
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<220>
<221> Xaa
<222> (6)..(6)
<223> Exogenous loop insertion
<400> 43
Ala Ala Gln Gly Ala Xaa
1 5
<210> 44
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 44
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu
100 105 110
Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Lys Thr Val Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 45
<211> 13
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 45
Tyr Val Ala Val Glu Asn Gly Val Ala Lys Lys Val Ala
1 5 10
<210> 46
<211> 15
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 46
His Phe Val Gln Gln Thr Pro Lys Ser Gln Pro Thr Leu Val Pro
1 5 10 15
<210> 47
<211> 15
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 47
His Phe Val Gln Gln Thr Pro Gln Ser Gln Pro Thr Leu Val Pro
1 5 10 15
<210> 48
<211> 14
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 48
Thr Leu Ala Asn Gly Ala Asn Asn Thr Ile Ile Arg Val Pro
1 5 10
<210> 49
<211> 14
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 49
Thr Leu Ala Lys Gly Ala Asn Asn Thr Ile Ile Arg Val Pro
1 5 10
<210> 50
<211> 13
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 50
His Val Val Val Asn Asn Lys Val Ala Thr His Val Pro
1 5 10
<210> 51
<211> 10
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 51
Tyr Val Asp Glu Gln Ser Lys Tyr His Ala
1 5 10
<210> 52
<211> 15
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 52
His Phe Val Gln Asn Lys Gln Asn Gln Arg Pro Thr Leu Val Pro
1 5 10 15
<210> 53
<211> 15
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 53
His Phe Val Gln Asn Lys Gln Asn Gln Pro Pro Thr Leu Val Pro
1 5 10 15
<210> 54
<211> 15
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 54
His Phe Val Gln Asp Lys Lys Gly Gln Pro Pro Thr Leu Val Pro
1 5 10 15
<210> 55
<211> 18
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 55
His Phe Val Gln Asn Lys Gln Asn Gln Gln Asn Gln Pro Pro Thr Leu
1 5 10 15
Val Pro
<210> 56
<211> 18
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 56
His Phe Val Gln Asn Lys Gln Asn Lys Gln Asn Gln Pro Pro Thr Leu
1 5 10 15
Val Pro
<210> 57
<211> 15
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 57
His Phe Val Gln Asn Lys Gln Asn Lys Pro Pro Thr Leu Val Pro
1 5 10 15
<210> 58
<211> 18
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 58
Tyr Trp Thr Thr Val Asn Thr Gly Ser Ala Thr Thr Thr Thr Thr Phe
1 5 10 15
Val Pro
<210> 59
<211> 17
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 59
Tyr Trp Thr Thr Val Asn Thr Gly Ser Ala Thr Thr Thr Thr Phe Val
1 5 10 15
Pro
<210> 60
<211> 16
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 60
Tyr Trp Thr Thr Val Asn Thr Gly Ser Ala Thr Thr Thr Phe Val Pro
1 5 10 15
<210> 61
<211> 17
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 61
Tyr Tyr Thr Thr Val Thr Gln Gly Ser Ala Thr Thr Thr Thr Phe Val
1 5 10 15
Pro
<210> 62
<211> 10
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 62
Tyr Val Asp Glu Lys Lys Met Val His Ala
1 5 10
<210> 63
<211> 10
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 63
Tyr Val Asp Glu Lys Gln Val Ser His Ala
1 5 10
<210> 64
<211> 10
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 64
Tyr Val Asp Glu Lys Lys Val Val His Ala
1 5 10
<210> 65
<211> 13
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 65
His Tyr Thr Arg Gln Asn Asn Ala Asp Val Phe Val Pro
1 5 10
<210> 66
<211> 13
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 66
His Tyr Thr Arg Gln Asn Asn Thr Asp Val Phe Val Pro
1 5 10
<210> 67
<211> 13
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 67
His Tyr Thr Arg Gln Asn Asn Ile Asp Val Phe Val Pro
1 5 10
<210> 68
<211> 14
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 68
Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu Val Pro
1 5 10
<210> 69
<211> 14
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 69
Tyr Tyr Thr Lys Asp Lys Asn Asp Asn Leu Thr Leu Val Pro
1 5 10
<210> 70
<211> 14
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 70
Tyr Tyr Thr Lys Asp Lys Asn Asp Lys Leu Thr Leu Val Pro
1 5 10
<210> 71
<211> 13
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 71
Tyr Tyr Thr Asn Thr Asn Asn Asn Leu Thr Leu Val Pro
1 5 10
<210> 72
<211> 17
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 72
His Trp Asn Thr Val Tyr Asn Thr Asn Gly Thr Thr Thr Thr Phe Val
1 5 10 15
Pro
<210> 73
<211> 18
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 73
His Trp Asn Thr Val Tyr Asn Thr Asn Gly Thr Thr Thr Thr Thr Phe
1 5 10 15
Val Pro
<210> 74
<211> 14
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 74
Thr Tyr Thr Val Asp Ser Ser Gly Val Val Thr Pro Val Pro
1 5 10
<210> 75
<211> 14
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 75
His Phe Val Ala Asp Ser Gln Gly Lys Ile Thr Arg Val Pro
1 5 10
<210> 76
<211> 17
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 76
Tyr Tyr Tyr Thr Thr Ala Thr Asn Ser Ser Thr Ser Thr Thr Phe Val
1 5 10 15
Pro
<210> 77
<211> 17
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 77
His Tyr Thr Thr Val Tyr Asn Ala Thr Thr Thr Thr Thr Thr Phe Val
1 5 10 15
Pro
<210> 78
<211> 18
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 78
His Tyr Thr Thr Val Tyr Asn Ala Thr Thr Thr Thr Thr Thr Thr Phe
1 5 10 15
Val Pro
<210> 79
<211> 11
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 79
Tyr Val Asp Asp Gln Gly Lys Val Lys Gly Pro
1 5 10
<210> 80
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 80
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu
100 105 110
Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Lys Thr Val Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 81
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 81
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Leu Gln Thr Glu
100 105 110
Gln Val Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Ser Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly His Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ser Asp Ile Lys Pro Asp Lys Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Gln Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Glu Thr Ala Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 82
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 82
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Lys Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Leu Gln Thr Glu
100 105 110
Gln Val Gln Asp Ser Glu Asp Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Lys Gly Gly Ser Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly His Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Glu
180 185 190
Leu Ala Thr Ala Tyr Ile Lys Pro Asp Glu Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Asp Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Gln Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Glu Thr Ala Asn Gly Ile His His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 83
<211> 255
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 83
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Leu Gln Thr Glu
100 105 110
Gln Glu Gln Asp Pro Glu His Ser Gly Lys Met Val Ala Lys Arg Arg
115 120 125
Phe Lys Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Lys Asp Val Met Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly His Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Glu
180 185 190
Leu Ala Thr Ala Tyr Ile Lys Pro Asp Glu Lys His His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Asp Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Gln Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Glu Thr Ala Asn Gly Ile His His Ile Gly Leu Ala Ala Lys Gln
245 250 255
<210> 84
<211> 263
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 84
Cys Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Val Ala Ala Asp
1 5 10 15
Ile Gly Ala Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys
20 25 30
Asp Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn
35 40 45
Gly Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Arg Thr Phe Lys Ala
50 55 60
Gly Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys
65 70 75 80
Ile Ser Arg Phe Asp Phe Ile Arg Gln Ile Glu Val Asp Gly Gln Leu
85 90 95
Ile Thr Leu Glu Ser Gly Glu Phe Gln Val Tyr Lys Gln Ser His Ser
100 105 110
Ala Leu Thr Ala Leu Gln Thr Glu Gln Val Gln Asp Ser Glu His Ser
115 120 125
Gly Lys Met Val Ala Lys Arg Gln Phe Arg Ile Gly Asp Ile Val Gly
130 135 140
Glu His Thr Ser Phe Gly Lys Leu Pro Lys Asp Val Met Ala Thr Tyr
145 150 155 160
Arg Gly Thr Ala Phe Gly Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr
165 170 175
Thr Ile Asp Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu
180 185 190
Lys Ser Pro Glu Leu Asn Val Asp Leu Ala Ala Ala Asp Ile Lys Pro
195 200 205
Asp Glu Lys His His Ala Val Ile Ser Gly Ser Val Leu Tyr Asn Gln
210 215 220
Ala Glu Lys Gly Ser Tyr Ser Leu Gly Ile Phe Gly Gly Gln Ala Gln
225 230 235 240
Glu Val Ala Gly Ser Ala Glu Val Glu Thr Ala Asn Gly Ile Arg His
245 250 255
Ile Gly Leu Ala Ala Lys Gln
260
<210> 85
<211> 260
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 85
Cys Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Val Thr Ala Asp
1 5 10 15
Ile Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys
20 25 30
Asp Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn
35 40 45
Gly Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn
50 55 60
Gly Asp Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg
65 70 75 80
Phe Asp Phe Ile Arg Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu
85 90 95
Glu Ser Gly Glu Phe Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr
100 105 110
Ala Leu Gln Thr Glu Gln Glu Gln Asp Pro Glu His Ser Glu Lys Met
115 120 125
Val Ala Lys Arg Arg Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr
130 135 140
Ser Phe Asp Lys Leu Pro Lys Asp Val Met Ala Thr Tyr Arg Gly Thr
145 150 155 160
Ala Phe Gly Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp
165 170 175
Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Ser Pro
180 185 190
Glu Leu Asn Val Asp Leu Ala Val Ala Tyr Ile Lys Pro Asp Glu Lys
195 200 205
His His Ala Val Ile Ser Gly Ser Val Leu Tyr Asn Gln Asp Glu Lys
210 215 220
Gly Ser Tyr Ser Leu Gly Ile Phe Gly Glu Lys Ala Gln Glu Val Ala
225 230 235 240
Gly Ser Ala Glu Val Glu Thr Ala Asn Gly Ile His His Ile Gly Leu
245 250 255
Ala Ala Lys Gln
260
<210> 86
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 86
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Asp Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly
165 170 175
His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ala Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Gly Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 87
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 87
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly
165 170 175
His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 88
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 88
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Pro Asn Gly Arg Leu His Tyr Ser Ile Asp Phe Thr Lys Lys Gln Gly
165 170 175
Tyr Gly Arg Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 89
<211> 254
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 89
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Thr Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Thr Ile Thr Leu Ala Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asn His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Asp Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Pro Asn Gly Arg Leu His Tyr Ser Ile Asp Phe Thr Lys Lys Gln Gly
165 170 175
Tyr Gly Arg Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
245 250
<210> 90
<211> 261
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 90
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly
50 55 60
Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile
65 70 75 80
Ser Arg Phe Asp Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile
85 90 95
Thr Leu Ala Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala
100 105 110
Val Val Ala Leu Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp
115 120 125
Ser Leu Ile Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu
130 135 140
His Thr Ala Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly
145 150 155 160
Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile
165 170 175
Asp Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr
180 185 190
Pro Glu Gln Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Glu
195 200 205
Lys Ser His Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu
210 215 220
Lys Gly Thr Tyr His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile
225 230 235 240
Ala Gly Ser Ala Thr Val Lys Ile Arg Glu Lys Val His Glu Ile Gly
245 250 255
Ile Ala Gly Lys Gln
260
<210> 91
<211> 257
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 91
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Lys
20 25 30
Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly Thr Leu Thr Leu
35 40 45
Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly Asp Lys Asp Asn
50 55 60
Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile Ser Arg Phe Asp
65 70 75 80
Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile Thr Leu Ala Ser
85 90 95
Gly Glu Phe Gln Ile Tyr Lys Gln Asn His Ser Ala Val Val Ala Leu
100 105 110
Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn
115 120 125
Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe
130 135 140
Asn Gln Leu Pro Gly Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser
145 150 155 160
Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala
165 170 175
Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn
180 185 190
Val Glu Leu Ala Ala Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala
195 200 205
Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr Tyr
210 215 220
His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala
225 230 235 240
Thr Val Lys Ile Gly Glu Lys Val His Glu Ile Ser Ile Ala Gly Lys
245 250 255
Gln
<210> 92
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 92
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr
85 90 95
Leu Val Pro Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe Gln Val Tyr
100 105 110
Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu Gln Ile Gln
115 120 125
Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln Phe Arg Ile
130 135 140
Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu Pro Glu Gly
145 150 155 160
Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp Asp Ala Gly
165 170 175
Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly Asn Gly
180 185 190
Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp Leu Ala Ala
195 200 205
Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile Ser Gly Ser
210 215 220
Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu Gly Ile Phe
225 230 235 240
Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val Lys Thr Val
245 250 255
Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
260 265
<210> 93
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 93
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly
50 55 60
Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile
65 70 75 80
Ser Arg Phe Asp Phe Val Gln Lys Ile Glu Val Asp Tyr Tyr Thr Lys
85 90 95
Asp Thr Asn Asn Asn Leu Thr Leu Val Pro Gln Thr Ile Thr Leu Ala
100 105 110
Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala
115 120 125
Leu Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile
130 135 140
Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala
145 150 155 160
Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe
165 170 175
Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala
180 185 190
Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln
195 200 205
Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His
210 215 220
Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr
225 230 235 240
Tyr His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser
245 250 255
Ala Thr Val Lys Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly
260 265 270
Lys Gln
<210> 94
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 94
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr
85 90 95
Leu Val Pro Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe Gln Ile Tyr
100 105 110
Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu Lys Ile Asn
115 120 125
Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser Phe Leu Val
130 135 140
Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu Pro Ser Gly
145 150 155 160
Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly
165 170 175
Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly His Gly Lys
180 185 190
Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu Ala Ser Ala
195 200 205
Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu Gly Asp Thr
210 215 220
Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala Leu Phe Gly
225 230 235 240
Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys Ile Arg Glu
245 250 255
Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
260 265
<210> 95
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 95
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu
100 105 110
Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ala Asp Ile Lys Pro Asp Tyr Tyr Thr Lys Asp Thr Asn
195 200 205
Asn Asn Leu Thr Leu Val Pro Lys Arg His Ala Val Ile Ser Gly Ser
210 215 220
Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu Gly Ile Phe
225 230 235 240
Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val Lys Thr Val
245 250 255
Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
260 265
<210> 96
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 96
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly
50 55 60
Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile
65 70 75 80
Ser Arg Phe Asp Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile
85 90 95
Thr Leu Ala Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala
100 105 110
Val Val Ala Leu Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp
115 120 125
Ser Leu Ile Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu
130 135 140
His Thr Ala Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly
145 150 155 160
Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile
165 170 175
Asp Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr
180 185 190
Pro Glu Gln Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Tyr
195 200 205
Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu Val Pro Lys Ser His
210 215 220
Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr
225 230 235 240
Tyr His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser
245 250 255
Ala Thr Val Lys Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly
260 265 270
Lys Gln
<210> 97
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 97
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly
165 170 175
His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Tyr Tyr Thr Lys Asp Thr Asn Asn
195 200 205
Asn Leu Thr Leu Val Pro Lys Ser His Ala Val Ile Leu Gly Asp Thr
210 215 220
Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala Leu Phe Gly
225 230 235 240
Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys Ile Arg Glu
245 250 255
Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
260 265
<210> 98
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 98
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu
100 105 110
Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu
225 230 235 240
Val Pro Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val Lys Thr Val
245 250 255
Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
260 265
<210> 99
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 99
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly
50 55 60
Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile
65 70 75 80
Ser Arg Phe Asp Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile
85 90 95
Thr Leu Ala Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala
100 105 110
Val Val Ala Leu Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp
115 120 125
Ser Leu Ile Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu
130 135 140
His Thr Ala Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly
145 150 155 160
Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile
165 170 175
Asp Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr
180 185 190
Pro Glu Gln Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Glu
195 200 205
Lys Ser His Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu
210 215 220
Lys Gly Thr Tyr His Leu Ala Leu Phe Gly Tyr Tyr Thr Lys Asp Thr
225 230 235 240
Asn Asn Asn Leu Thr Leu Val Pro Arg Ala Gln Glu Ile Ala Gly Ser
245 250 255
Ala Thr Val Lys Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly
260 265 270
Lys Gln
<210> 100
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 100
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly
165 170 175
His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu Val
225 230 235 240
Pro Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys Ile Arg Glu
245 250 255
Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
260 265
<210> 101
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 101
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu Val
50 55 60
Pro Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn Thr Gly Lys
65 70 75 80
Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg Gln Ile Glu
85 90 95
Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe Gln Val Tyr
100 105 110
Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu Gln Ile Gln
115 120 125
Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln Phe Arg Ile
130 135 140
Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu Pro Glu Gly
145 150 155 160
Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp Asp Ala Gly
165 170 175
Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly Asn Gly
180 185 190
Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp Leu Ala Ala
195 200 205
Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile Ser Gly Ser
210 215 220
Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu Gly Ile Phe
225 230 235 240
Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val Lys Thr Val
245 250 255
Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
260 265
<210> 102
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 102
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Tyr Tyr Thr Lys Asp Thr Asn Asn Asn
50 55 60
Leu Thr Leu Val Pro Ala Glu Lys Thr Phe Lys Val Gly Asp Lys Asp
65 70 75 80
Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile Ser Arg Phe
85 90 95
Asp Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile Thr Leu Ala
100 105 110
Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala
115 120 125
Leu Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile
130 135 140
Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala
145 150 155 160
Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe
165 170 175
Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala
180 185 190
Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln
195 200 205
Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His
210 215 220
Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr
225 230 235 240
Tyr His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser
245 250 255
Ala Thr Val Lys Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly
260 265 270
Lys Gln
<210> 103
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 103
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu Val
50 55 60
Pro Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn Thr Gly Lys
65 70 75 80
Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg Gln Ile Glu
85 90 95
Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe Gln Ile Tyr
100 105 110
Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu Lys Ile Asn
115 120 125
Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser Phe Leu Val
130 135 140
Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu Pro Ser Gly
145 150 155 160
Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly
165 170 175
Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly His Gly Lys
180 185 190
Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu Ala Ser Ala
195 200 205
Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu Gly Asp Thr
210 215 220
Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala Leu Phe Gly
225 230 235 240
Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys Ile Arg Glu
245 250 255
Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
260 265
<210> 104
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 104
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu
100 105 110
Gln Ile Gln Asp Ser Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr
115 120 125
Leu Val Pro His Ser Gly Lys Met Val Ala Lys Arg Gln Phe Arg Ile
130 135 140
Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu Pro Glu Gly
145 150 155 160
Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp Asp Ala Gly
165 170 175
Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly Asn Gly
180 185 190
Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp Leu Ala Ala
195 200 205
Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile Ser Gly Ser
210 215 220
Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu Gly Ile Phe
225 230 235 240
Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val Lys Thr Val
245 250 255
Asn Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
260 265
<210> 105
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 105
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly
50 55 60
Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile
65 70 75 80
Ser Arg Phe Asp Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile
85 90 95
Thr Leu Ala Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala
100 105 110
Val Val Ala Leu Gln Ile Glu Lys Ile Asn Asn Pro Tyr Tyr Thr Lys
115 120 125
Asp Thr Asn Asn Asn Leu Thr Leu Val Pro Lys Ile Asp Ser Leu Ile
130 135 140
Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala
145 150 155 160
Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe
165 170 175
Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala
180 185 190
Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln
195 200 205
Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His
210 215 220
Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu Lys Gly Thr
225 230 235 240
Tyr His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser
245 250 255
Ala Thr Val Lys Ile Arg Glu Lys Val His Glu Ile Gly Ile Ala Gly
260 265 270
Lys Gln
<210> 106
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 106
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr
115 120 125
Leu Val Pro Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser Phe Leu Val
130 135 140
Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu Pro Ser Gly
145 150 155 160
Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly
165 170 175
Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly His Gly Lys
180 185 190
Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu Ala Ser Ala
195 200 205
Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu Gly Asp Thr
210 215 220
Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala Leu Phe Gly
225 230 235 240
Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys Ile Arg Glu
245 250 255
Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
260 265
<210> 107
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 107
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Gly Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe Gln Thr Glu
100 105 110
Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala Lys Arg Gln
115 120 125
Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe Asp Lys Leu
130 135 140
Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe Gly Ser Asp
145 150 155 160
Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln
165 170 175
Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu Asn Val Asp
180 185 190
Leu Ala Ala Ala Asp Ile Lys Pro Asp Gly Lys Arg His Ala Val Ile
195 200 205
Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser Tyr Ser Leu
210 215 220
Gly Ile Phe Gly Gly Lys Ala Gln Glu Val Ala Gly Ser Ala Glu Val
225 230 235 240
Lys Thr Val Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu Val
245 250 255
Pro Gly Ile Arg His Ile Gly Leu Ala Ala Lys Gln
260 265
<210> 108
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 108
Cys Ser Ser Gly Ser Gly Ser Gly Gly Gly Gly Val Ala Ala Asp Ile
1 5 10 15
Gly Thr Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp
20 25 30
Lys Gly Leu Lys Ser Leu Thr Leu Glu Asp Ser Ile Ser Gln Asn Gly
35 40 45
Thr Leu Thr Leu Ser Ala Gln Gly Ala Glu Lys Thr Phe Lys Val Gly
50 55 60
Asp Lys Asp Asn Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Ile
65 70 75 80
Ser Arg Phe Asp Phe Val Gln Lys Ile Glu Val Asp Gly Gln Thr Ile
85 90 95
Thr Leu Ala Ser Gly Glu Phe Gln Ile Tyr Lys Gln Asp His Ser Ala
100 105 110
Val Val Ala Leu Gln Ile Glu Lys Ile Asn Asn Pro Asp Lys Ile Asp
115 120 125
Ser Leu Ile Asn Gln Arg Ser Phe Leu Val Ser Gly Leu Gly Gly Glu
130 135 140
His Thr Ala Phe Asn Gln Leu Pro Ser Gly Lys Ala Glu Tyr His Gly
145 150 155 160
Lys Ala Phe Ser Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile
165 170 175
Asp Phe Ala Ala Lys Gln Gly His Gly Lys Ile Glu His Leu Lys Thr
180 185 190
Pro Glu Gln Asn Val Glu Leu Ala Ser Ala Glu Leu Lys Ala Asp Glu
195 200 205
Lys Ser His Ala Val Ile Leu Gly Asp Thr Arg Tyr Gly Ser Glu Glu
210 215 220
Lys Gly Thr Tyr His Leu Ala Leu Phe Gly Asp Arg Ala Gln Glu Ile
225 230 235 240
Ala Gly Ser Ala Thr Val Lys Ile Arg Tyr Tyr Thr Lys Asp Thr Asn
245 250 255
Asn Asn Leu Thr Leu Val Pro Lys Val His Glu Ile Gly Ile Ala Gly
260 265 270
Lys Gln
<210> 109
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный полипептид
<400> 109
Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly Ala Gly Leu
1 5 10 15
Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys Ser Leu Gln
20 25 30
Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys Leu Lys Leu
35 40 45
Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp Ser Leu Asn
50 55 60
Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp Phe Ile Arg
65 70 75 80
Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser Gly Glu Phe
85 90 95
Gln Ile Tyr Lys Gln Asp His Ser Ala Val Val Ala Leu Gln Ile Glu
100 105 110
Lys Ile Asn Asn Pro Asp Lys Ile Asp Ser Leu Ile Asn Gln Arg Ser
115 120 125
Phe Leu Val Ser Gly Leu Gly Gly Glu His Thr Ala Phe Asn Gln Leu
130 135 140
Pro Ser Gly Lys Ala Glu Tyr His Gly Lys Ala Phe Ser Ser Asp Asp
145 150 155 160
Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala Ala Lys Gln Gly
165 170 175
His Gly Lys Ile Glu His Leu Lys Thr Pro Glu Gln Asn Val Glu Leu
180 185 190
Ala Ser Ala Glu Leu Lys Ala Asp Glu Lys Ser His Ala Val Ile Leu
195 200 205
Gly Asp Thr Arg Tyr Gly Gly Glu Glu Lys Gly Thr Tyr His Leu Ala
210 215 220
Leu Phe Gly Asp Arg Ala Gln Glu Ile Ala Gly Ser Ala Thr Val Lys
225 230 235 240
Ile Arg Tyr Tyr Thr Lys Asp Thr Asn Asn Asn Leu Thr Leu Val Pro
245 250 255
Lys Val His Glu Ile Gly Ile Ala Gly Lys Gln
260 265
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАРИАНТЫ ФАКТОР H-СВЯЗЫВАЮЩЕГО БЕЛКА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2811942C2 |
| ВАРИАНТЫ ФАКТОР Н-СВЯЗЫВАЮЩЕГО БЕЛКА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2714248C2 |
| Композиции с Neisseria meningitidis и способы их применения | 2020 |
|
RU2839906C1 |
| КОМПОЗИЦИИ NEISSERIA MENINGITIDIS И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2739504C2 |
| КОМПОЗИЦИИ NEISSERIA MENINGITIDIS И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2723045C2 |
| ИСКУССТВЕННЫЕ АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2763798C1 |
| Конструкции для направленного редактирования генов и способы с их применением | 2020 |
|
RU2832109C2 |
| КОМПОЗИЦИИ ГЕМАГГЛЮТИНИНА ГРИППА С ГЕТЕРОЛОГИЧНЫМИ ЭПИТОПАМИ И/ИЛИ ИЗМЕНЕННЫМИ САЙТАМИ РАСЩЕПЛЕНИЯ ПРИ СОЗРЕВАНИИ | 2017 |
|
RU2769406C2 |
| СПОСОБ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ БЕЛКОВОГО/ПЕПТИДНОГО АНТИГЕНА | 2021 |
|
RU2830627C1 |
| ГЕНЕТИЧЕСКИ СКОНСТРУИРОВАННЫЕ КЛЕТКИ, ЧУВСТВИТЕЛЬНЫЕ К КЛОСТРИДИАЛЬНЫМ НЕЙРОТОКСИНАМ | 2020 |
|
RU2824389C2 |
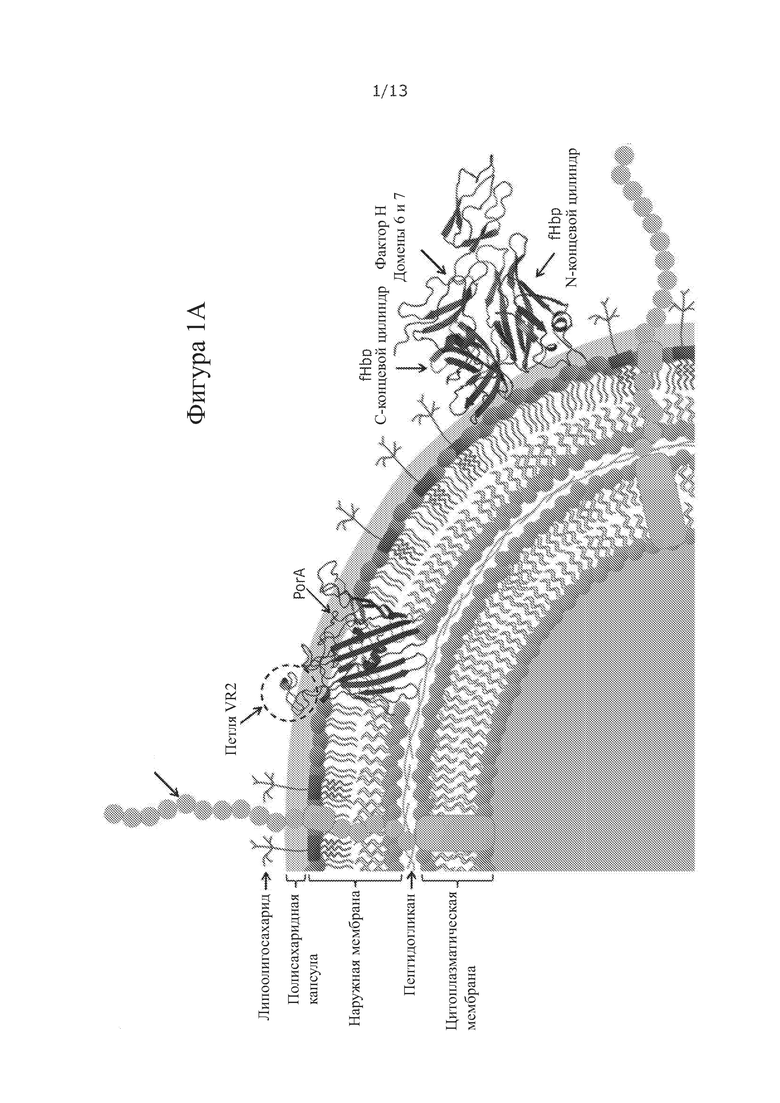
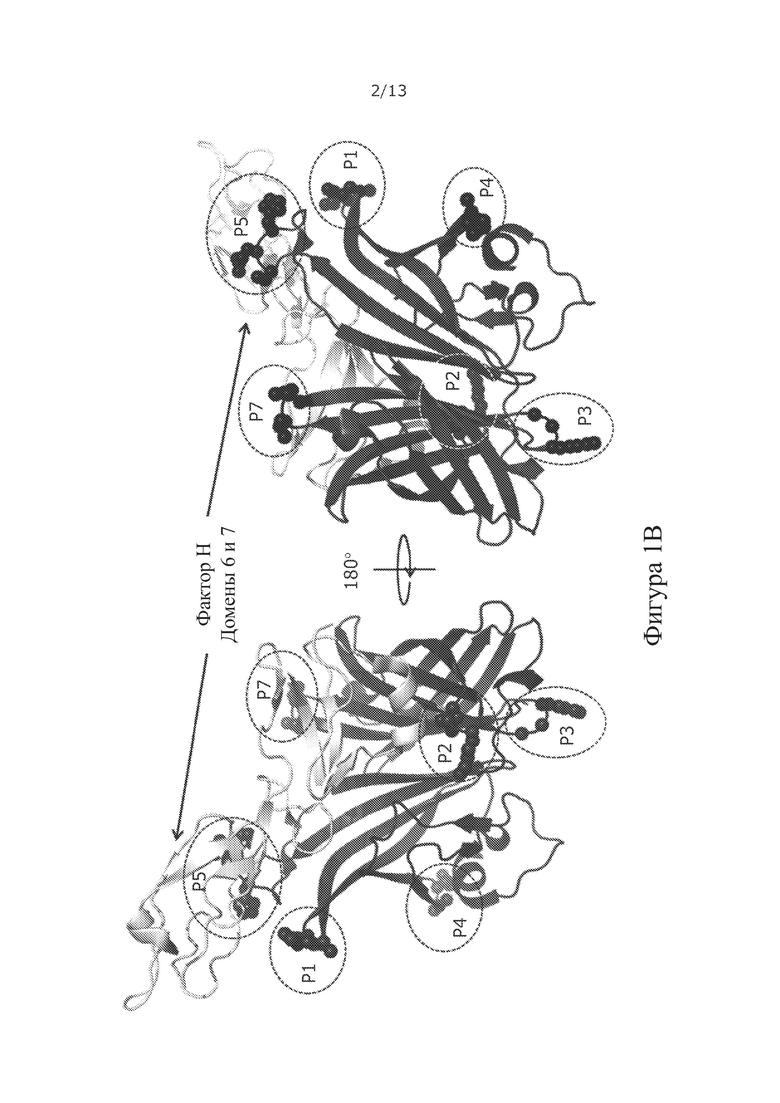
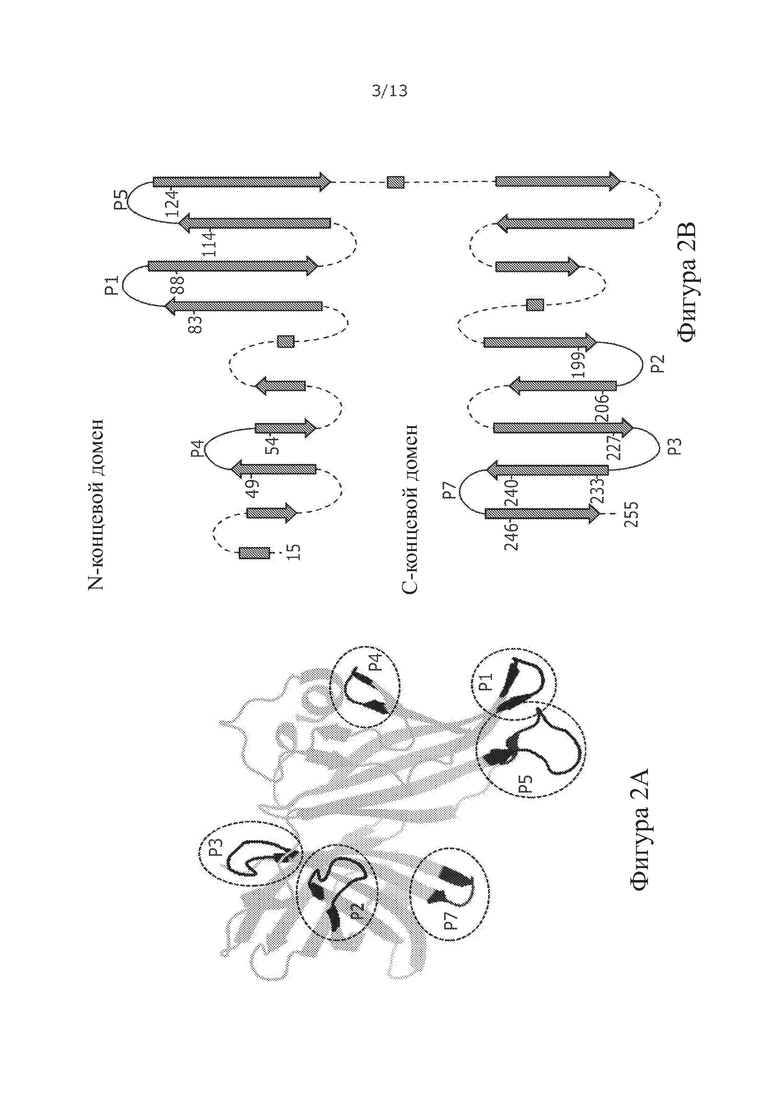
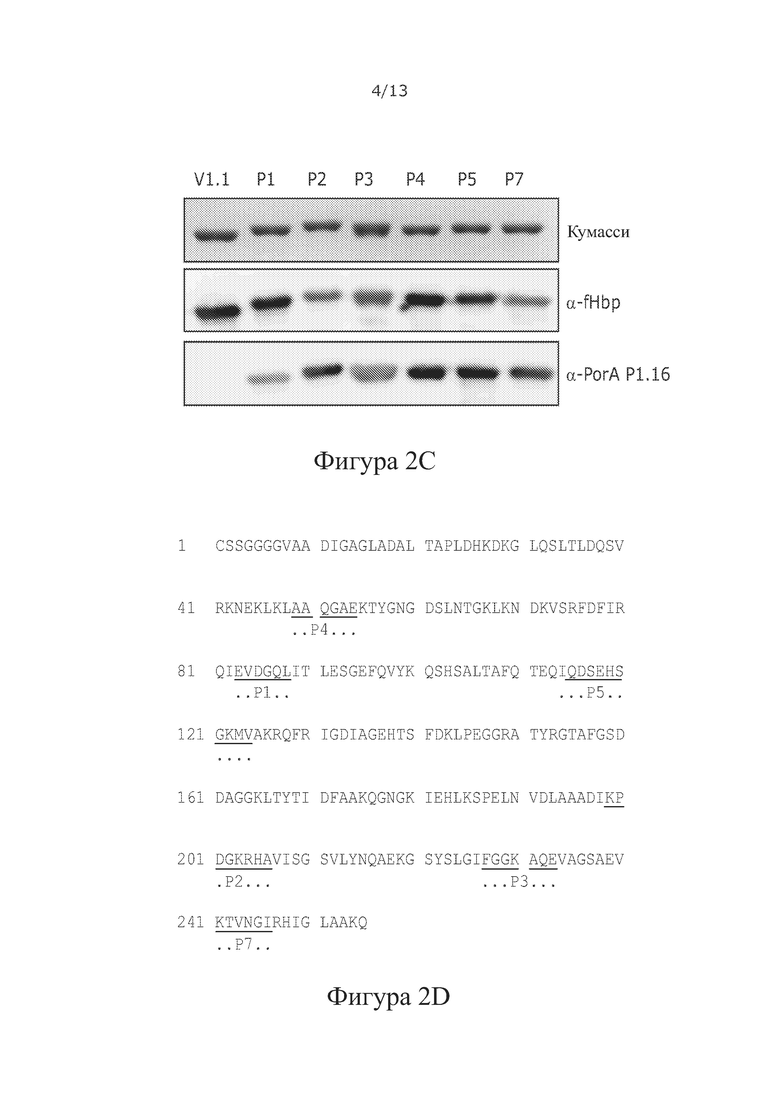

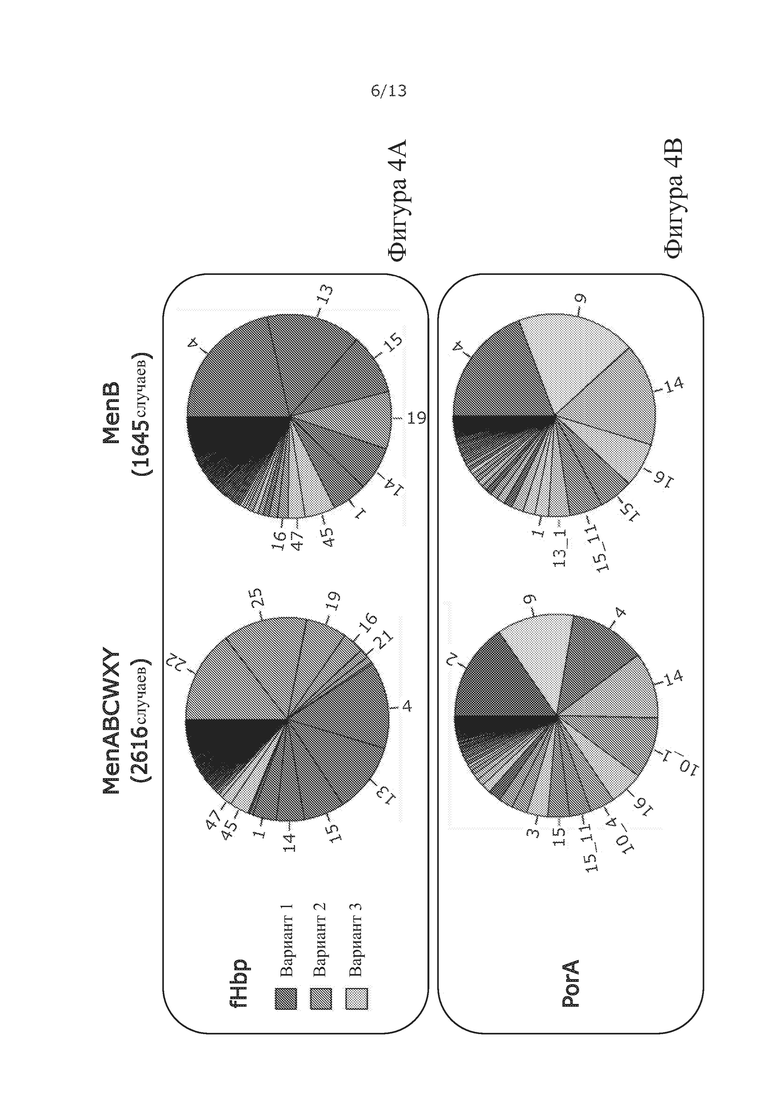
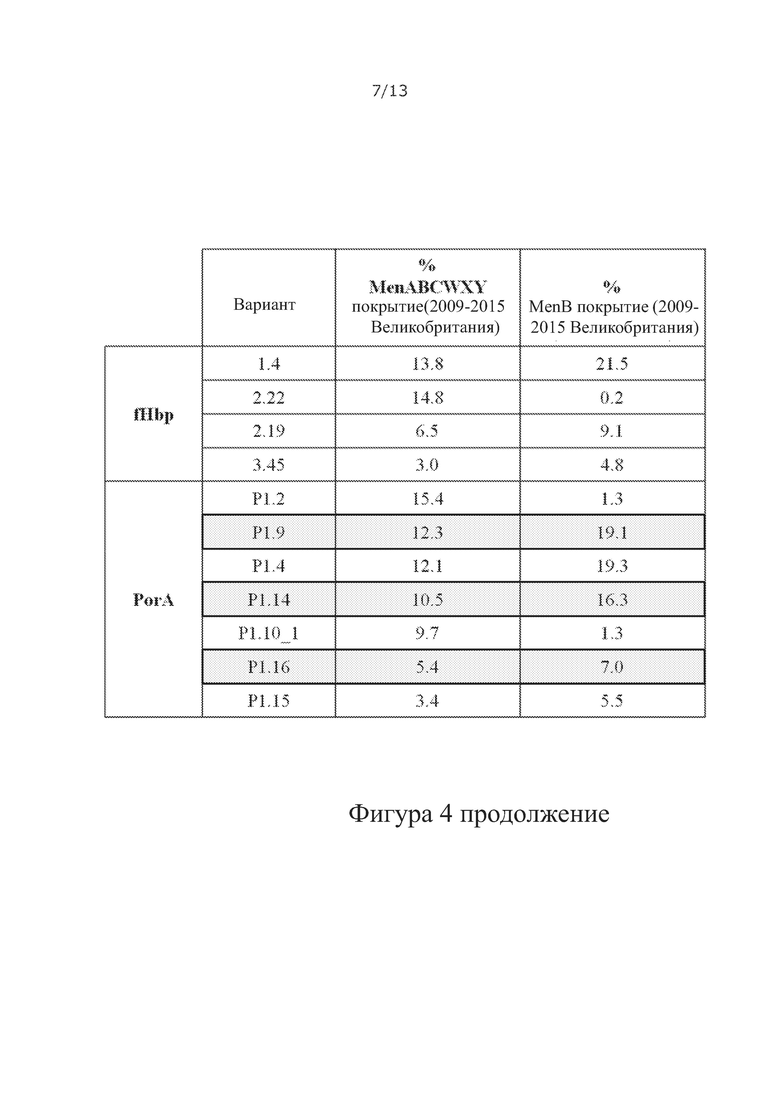
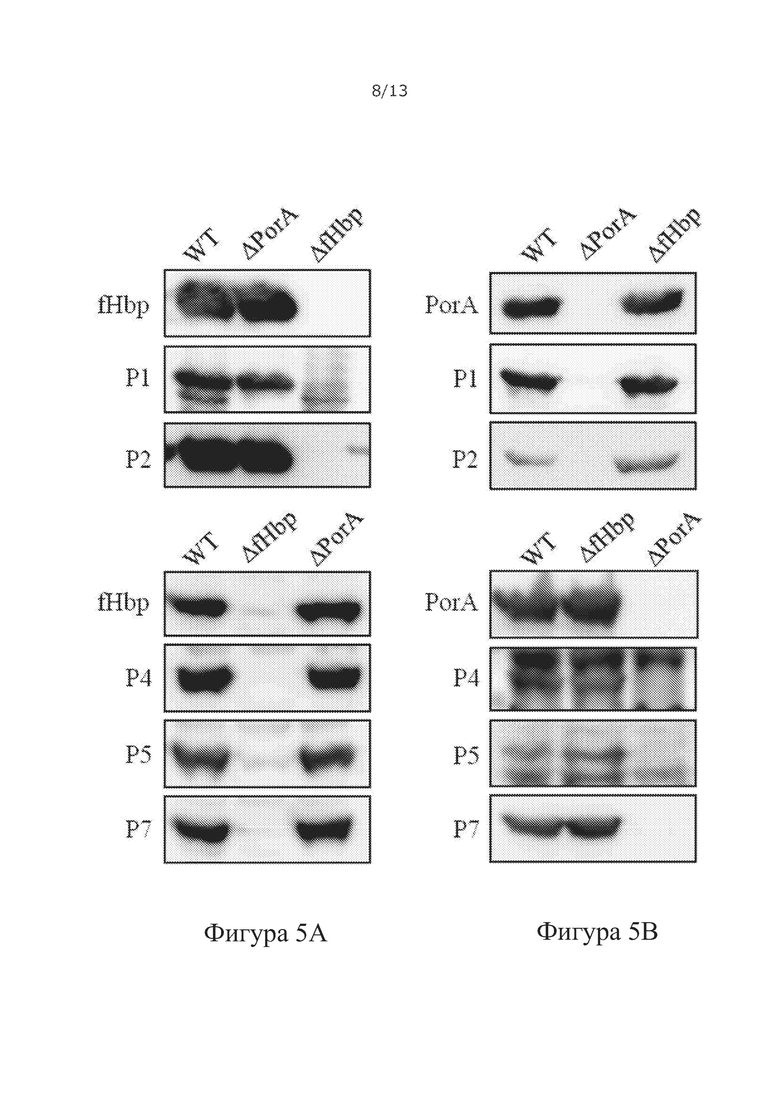
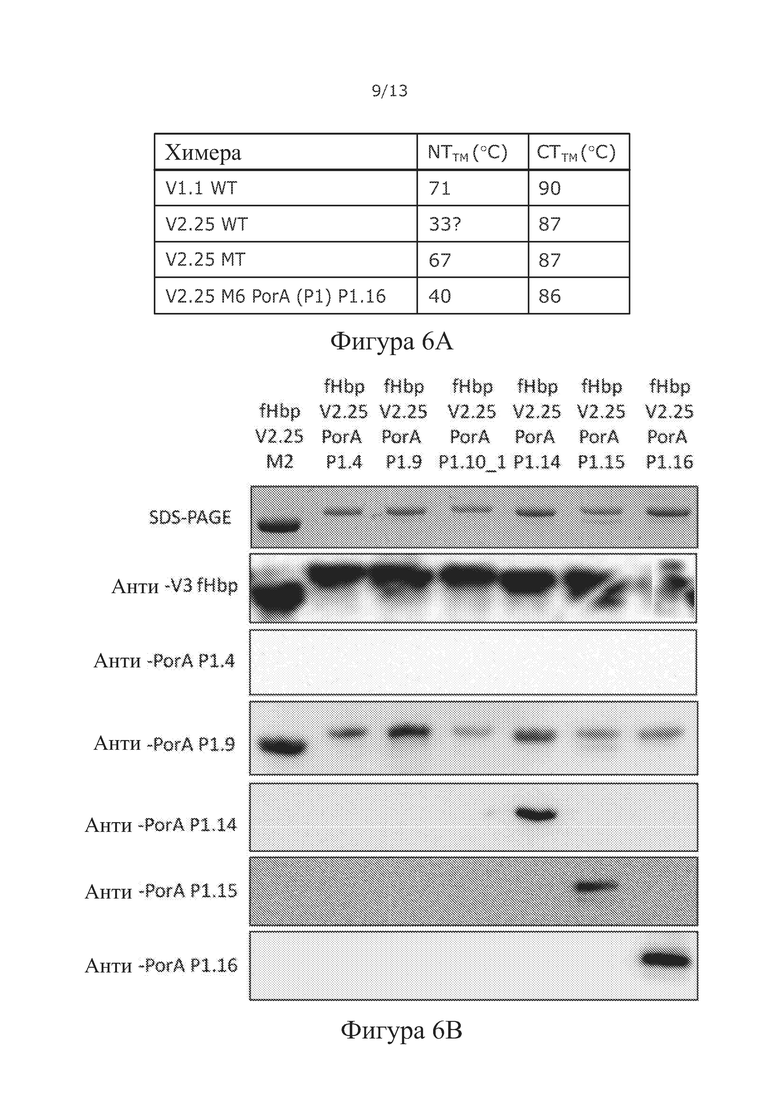
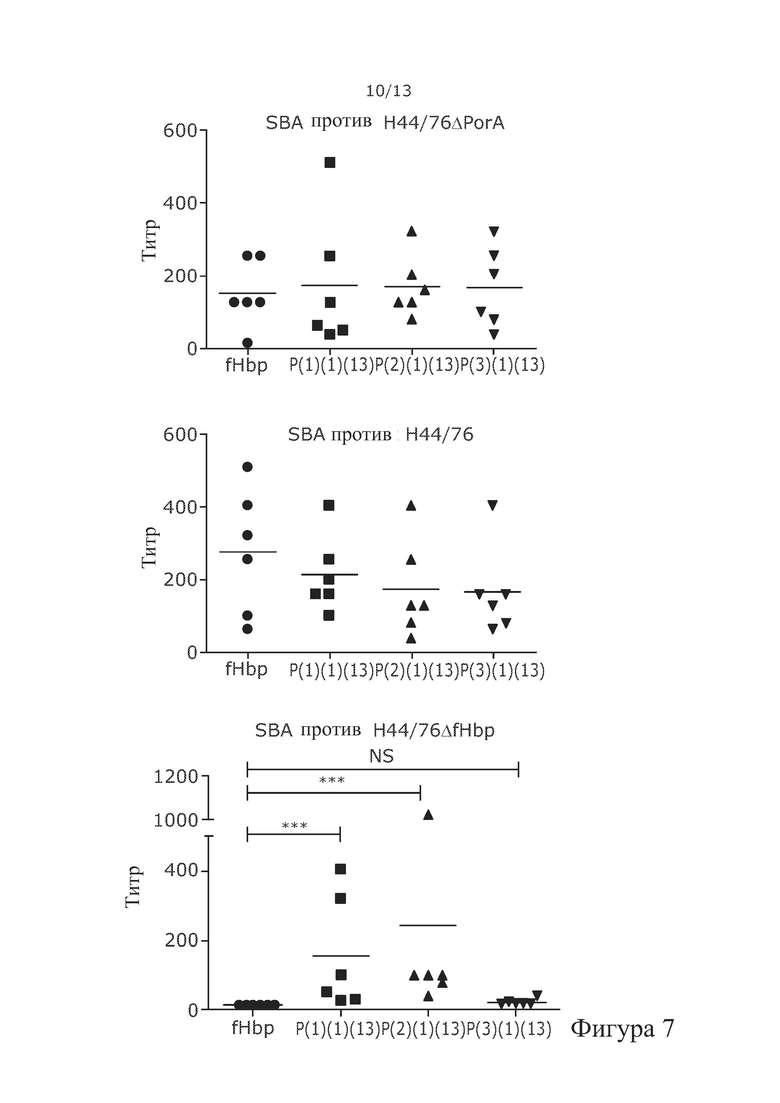
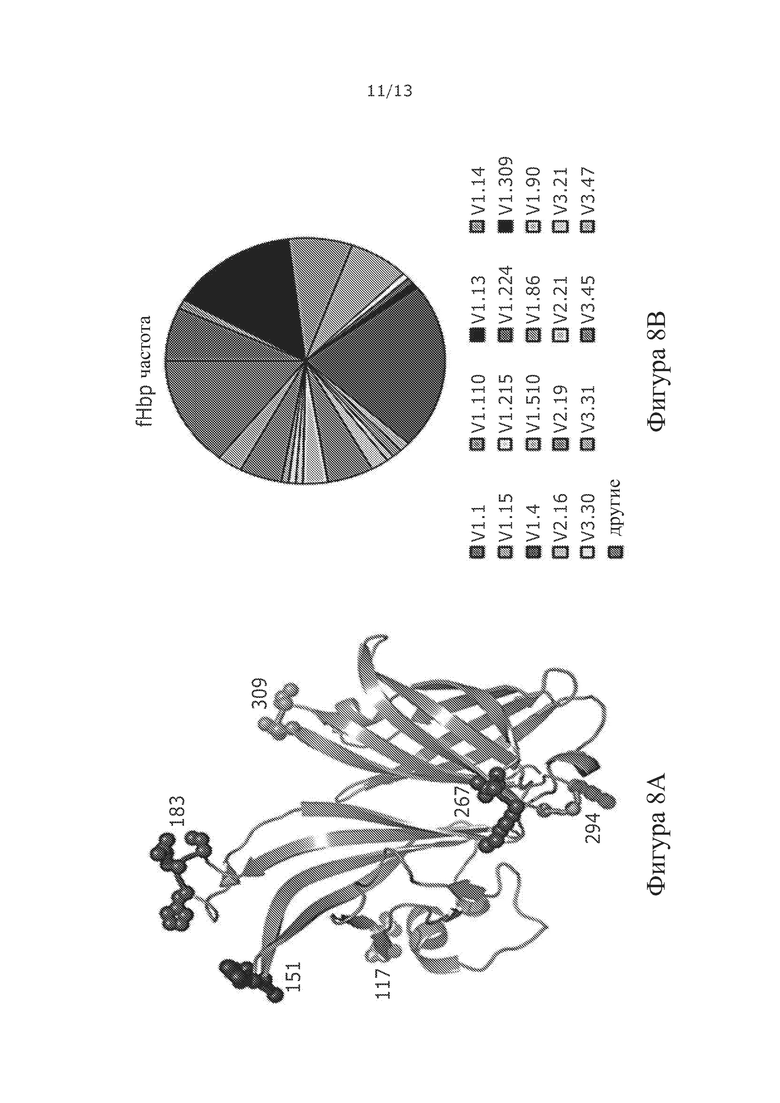
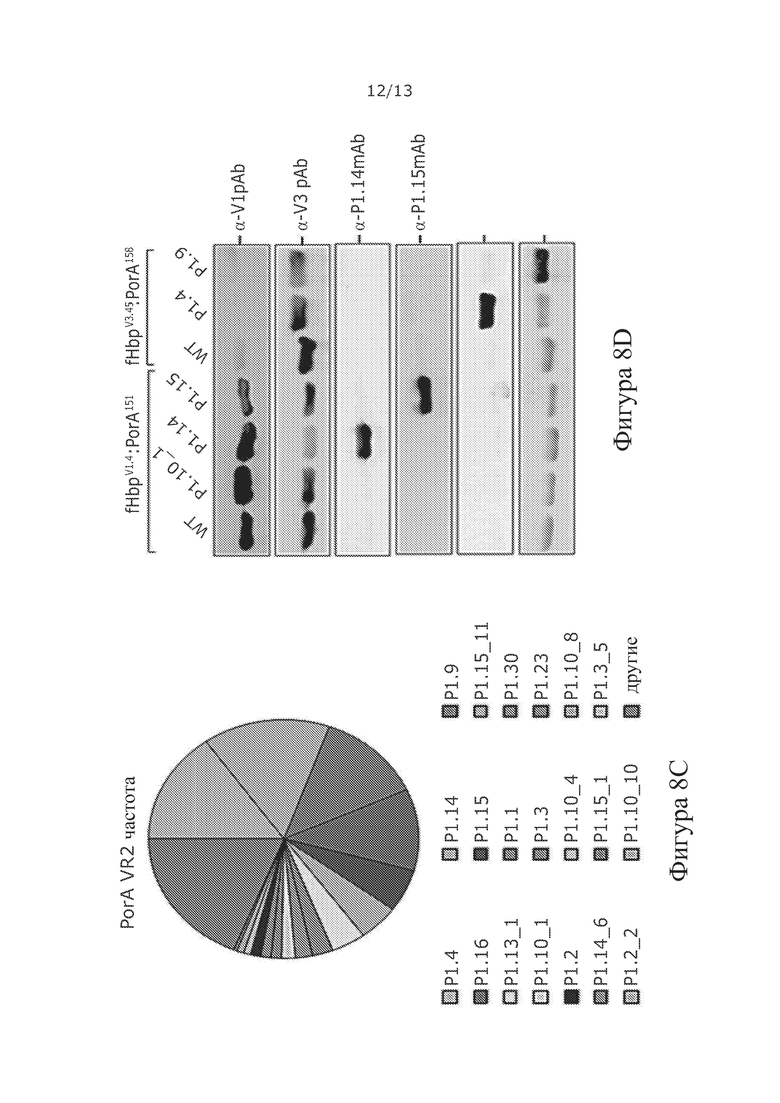
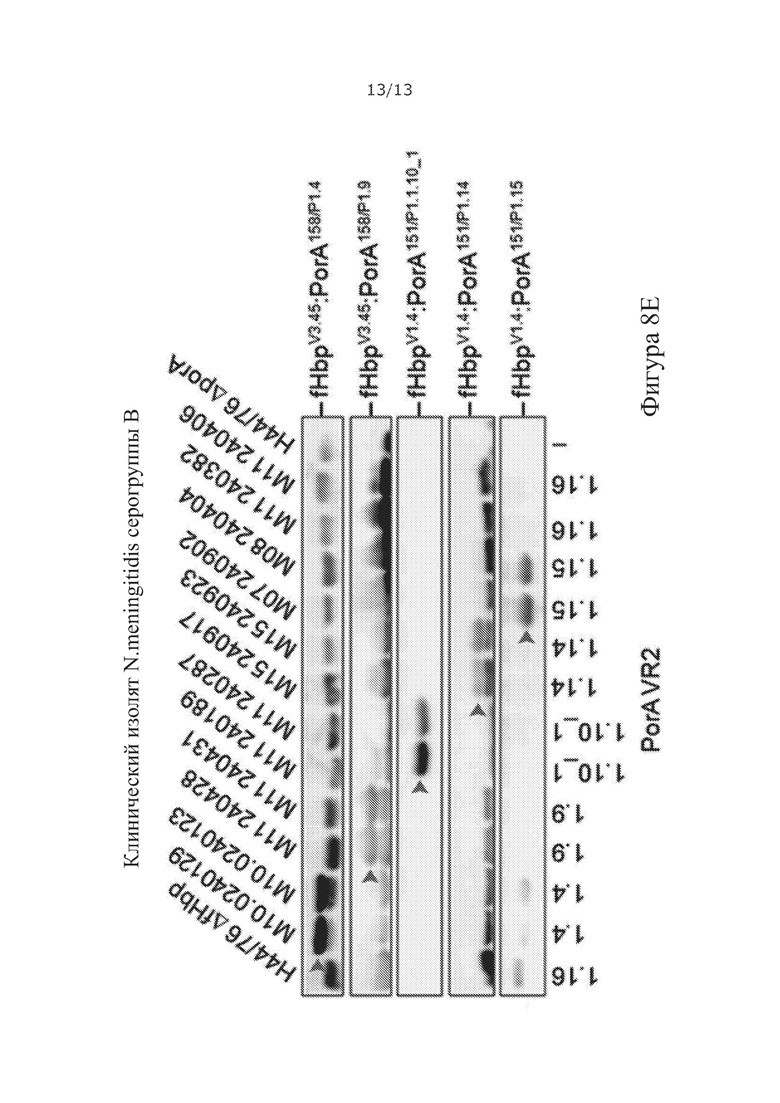
Изобретение относится к модифицированному белку, связывающему фактор Н (fHbp), представляющему собой fHbp, или его вариант, модифицированному путем добавления по меньшей мере одной петли экзогенного пептида; и связанной нуклеиновой кислоте, композициям и применению. Модифицированный белок, связывающий фактор Н (fHbp), может быть использован для лечения или предупреждения возникновения патогенной инфекции или колонизации у субъекта. 5 н. и 12 з.п. ф-лы, 8 ил., 4 табл., 2 пр.
1. Модифицированный белок, связывающий фактор H (fHbp), содержащий fHbp дикого типа или гонококковый ортолог дикого типа fHbp (Ghfp), или их вариант, имеющий по меньшей мере 75% идентичности с любой из последовательностей, представленных в SEQ ID NO: 1-13, который дополнительно модифицирован путем добавления петли экзогенного пептида, отличающийся тем, что петля экзогенного пептида имеет длину 8-20 аминокислот и при этом петля экзогенного пептида встроена в аминокислотном положении, которое соответствует любому из аминокислотных остатков с номерами 49-54, 83-88, 114-124, 199-206, 227-233 и 240-246 в SEQ ID NO: 1 или эквивалентных остатков в любой из SEQ ID NO: 2-13; и при этом экзогенная петля содержит последовательность, выбранную из любой из SEQ ID NO: 45-79.
2. Модифицированный белок, связывающий фактор Н, по п. 1, отличающийся тем, что модифицированный fHbp модифицирован таким образом, что он не способен связывать фактор Н, или по меньшей мере обладает пониженной активностью в отношении связывания фактора Н.
3. Модифицированный белок, связывающий фактор Н, по п. 1 или 2, отличающийся тем, что петля(и) экзогенного пептида имеет последовательность интегрального белка наружной мембраны.
4. Модифицированный белок, связывающий фактор H, по любому из пп. 1-3, отличающийся тем, что петля(и) экзогенного пептида имеет последовательность прокариотического полипептида.
5. Модифицированный белок, связывающий фактор H, по п. 4, отличающийся тем, что петля(и) экзогенного пептида представляет собой менингококковый белок.
6. Модифицированный белок, связывающий фактор H, по п. 4, отличающийся тем, что петля(и) экзогенного пептида представляет собой гонококковый белок.
7. Модифицированный белок, связывающий фактор H, по любому из пп. 1-6, отличающийся тем, что петля(и) экзогенного пептида содержит фрагмент PorA.
8. Модифицированный белок, связывающий фактор H, по любому из пп. 1-7, отличающийся тем, что петля(и) экзогенного пептида выбрана из любой из петель 1-7 PorA или их вариантов, включающих не более 1, 2, 3, 4 или 5 аминокислотных добавлений, делеций или замен; и их комбинаций; или отличающийся тем, что петля(и) экзогенного пептида выбрана из любой из петель PorA, содержащих последовательность в соответствии с любой из SEQ ID NO: 45-79, или их вариантов, включающих не более 1, 2, 3, 4 или 5 аминокислотных добавлений, делеций или замен.
9. Модифицированный белок, связывающий фактор H, по любому из пп. 1-8, отличающийся тем, что модифицированный fHbp содержит последовательность, представленную в любой из SEQ ID NO: 1-13; или ее вариант, имеющий по меньшей мере 75% идентичности с любой из последовательностей, представленных в SEQ ID NO: 1-13, при этом по меньшей мере одна петля экзогенного пептида представляет собой дополнительную вставку в пределах последовательности, представленной в любой из SEQ ID NО: 1-13, или ее варианта, имеющего по меньшей мере 75% идентичности с любой из последовательностей, представленных в SEQ ID NO: 1-13.
10. Нуклеиновая кислота, кодирующая модифицированный fHbp, по любому из пп. 1-9.
11. Нуклеиновая кислота по п. 10, отличающаяся тем, что нуклеиновая кислота представляет собой вектор, дополнительно необязательно вирусный вектор.
12. Композиция, содержащая терапевтически эффективное количество модифицированного fHbp, по любому из пп. 1-9 или нуклеиновую кислоту по пп. 10-11, и фармацевтически приемлемый носитель, причем композиция предназначена для индукции иммунного ответа против петли экзогенного пептида.
13. Композиция по п. 12, отличающаяся тем, что композиция содержит две или более различных молекулы модифицированного fHbp.
14. Композиция по любому из пп. 12, 13, отличающаяся тем, что композиция, кроме того, содержит адъювант.
15. Композиция по любому из пп. 12-14, отличающаяся тем, что композиция, кроме того, содержит по меньшей мере одну другую профилактически или терапевтически активную молекулу; и необязательно при этом, что по меньшей мере одна другая профилактически или терапевтически активная молекула представляет собой: моновалентную вакцину, содержащую конъюгат белок: капсульный полисахарид;
или конъюгированную вакцину, при этом антиген(ы), содержащий каркас fHbp, несущий петли экзогенного пептида, вводят в качестве молекулы белка-носителя в конъюгированную вакцину.
16. Применение модифицированного fHbp по любому из пп. 1-9, нуклеиновой кислоты по п. 10 или 11 или композиции по любому из пп. 12-15 для лечения или предупреждения возникновения менингококковой инфекции или колонизации у субъекта.
17. Применение белка, связывающего фактор H (fHbp), по любому из пп. 1-9 в качестве каркаса дисплея эпитопа.
| ДОМЕНЫ И ЭПИТОПЫ МЕНИНГОКОККОВОГО БЕЛКА NMB1870 | 2005 |
|
RU2375374C2 |
| WO 2007060548 A2, 31.05.2007 | |||
| WO 2009114485 A2, 17.09.2009 | |||
| WO 2011024072 A2, 03.03.2011 | |||
| SCARSELLI MARIA ET AL, "Rational design of a meningococcal antigen inducing broad protective immunity", SCIENCE TRANSLATIONAL MEDI, AAAS - AMERICAN ASSOCIATION FOR THE ADVANCEMENT OF SCIENCE, US, 20110, vol | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Огнетушитель | 0 |
|
SU91A1 |
Авторы
Даты
2022-06-06—Публикация
2017-08-31—Подача