Изобретение относится к медицине, в частности к фармакогенетике.
Послеоперационный болевой синдром является важнейшим фактором, влияющим на процесс ранней реабилитации и длительности послеоперационного пребывания пациента в стационаре. (Мазитова М., и др. 2012, Pomposelli J.J. et al., 1988, Kehlet H., 1988.) Для 88% пациентов отсутствие болевого синдрома сопряжено с высокой степенью удовлетворенности лечением и качеством жизни. (Berkowitz R, et al. 2019.)
Реакция организма на послеоперационный стресс, который усугубляется наличием болевого синдрома, проявляется дисфункцией легочной, сердечнососудистой систем, желудочно-кишечного тракта, а также нейроэндокринными и метаболическими нарушениями, что особенно губительно сказывается на пациентах с тяжелой сопутствующей патологией. (Liu S, et al. 1995., Scull T, et al., 1998).
Помимо нестероидных противовоспалительных препаратов (НПВП), к препаратам, широко применяемым в качестве послеоперационной аналгезии, относятся опиоиды, в частности трамадол, который традиционно рассматривается среди опиоидных анальгетиков, строго говоря, к ним не относится. Правильнее называть его анальгетиком центрального действия, механизм которого частично обусловлен воздействием на опиатные рецепторы. (Овечкин A.M., и др. 2019).
Согласно национальным клиническим рекомендациям по послеоперационному обезболиванию (Овечкин A.M., и др. 2019), трамадол входит в перечень препаратов, применяемых в качестве послеоперационного обезболивания в составе мультимодальной аналгезии (ММА). Выбор конкретной схемы ММА зависит от травматичности хирургического вмешательства. Выраженность болевого синдрома принято оценивать по визуальной аналоговой шкале (ВАШ), в которой 0 соответствует отсутствию боли, 10 - боли максимальной интенсивности. ВОЗ и Международная ассоциация по изучению боли (IASP) считают адекватным послеоперационное обезболивание при показателях ВАШ в покое менее 3, а при движении менее 4. Существует мнение, что в начале XXI века качество обезболивания хирургических больных практически не изменилось (Correll D.J. et al. 2014).
В современной концепции послеоперационного обезболивания, отраженной в национальных клинических рекомендациях, не представлено данных о применении обезболивающих препаратов в зависимости от генетических особенностей конкретного пациента.
Доказано, что индивидуальная анальгетическая эффективность и профиль неблагоприятных побочных реакций значительно зависят от генетических особенностей человека, обусловленных либо унаследованными вариантами (например, генетическими вариантами зародышевой линии), либо приобретенными вариантами (т.е. соматической мутацией) (Ladak S. S. J., et al. 2007). Генетические особенности пациента могут играть значительную роль в ответе на проводимое лечение, в том числе в неэффективности терапии, нежелательных реакций на терапию. Аллельные варианты генов, представляющие собой полиморфные участки генов, в той или иной степени влияют на фармакокинетику и фармакодинамику лекарственных средств (Кукес В.Г., и др. 2007).
В настоящее время отсутствует алгоритм выбора схемы послеоперационного обезболивания у пациентов после видеолапароскопической холецистэктомии с учетом данных фармакогенетического тестирования.
В качестве прототипа текущего алгоритма персонализации выбран инструмент GeneSight. Текущий прототип на основе выявления полиморфизмов генов CYP2D6, CYP2C19, CYP3A4, CYP2C9 позволяет получить практический результат для врача в виде следующей интерпретации: 1) «Применять лекарственный препарат без опасений», 2) «Применять лекарственный препарат с осторожностью» и 3) «Применять лекарственный препарат с большой осторожностью и частым мониторингом состояния». Однако ограничением клинического применения данного прототипа является его валидность для принятия решения о применении психотропных препаратов. Данный алгоритм не применим для трамадола и нестероидных противовоспалительных препаратов и выбора метода послеоперационного обезболивания.
Задачей текущего изобретения является разработка способа, позволяющего прогнозировать отсутствие ожидаемой эффективности обезболивания трамадолом у пациентов после хирургических вмешательств, в частности после видеолапароскопической холецистэктомии, и определить необходимость комбинированной схемы послеоперационного обезболивания.
Сущность изобретения заключается в предоперационном генотипировании пациентов, с определением носительства полиморфного маркера CYP2D6. В зависимости от наличия либо отсутствия данного полиморфного маркера будет определяться схема послеоперационного обезболивания (монотерапия трамадолом либо применение мультимодальной аналгезии с включением одного или нескольких препаратов других групп).
Геном - кандидатом, участвующим в биотрансформации трамадола, является CYP2D6. Выбор данного полиморфного маркера основан на результатах зарубежных и собственного клинического исследования.
В клиническом исследовании доказано, что наличие полиморфного маркера CYP2D6*4 (rs3892097) определяет невозможность применения монотерапии трамадолом в качестве послеоперационного обезболивания после видеолапароскопической холецистэктомии.
Материалом для фармакогенетического тестирования может служить кровь или буккальный эпителий. После получения результатов генотипирования можно сделать вывод о том, стоит ли назначать трамадол в режиме монотерапии для обезболивания или необходимо применять комбинацию анальгетиков различных групп для анальгезии у пациентов после видеолапароскопической холецистэктомии.
При наличии полиморфной аллели CYP2D6*4 (генотип GA или АА) невозможно применение трамадола для послеоперационного обезболивания в рамках монотерапии, так как применение в максимальной суточной дозе сопровождается высокой интенсивностью болевого синдрома (более 5 баллов). При наличии генотипа GA и АА по аллельному варианту CYP2D6*4 необходимо включение в схему обезболивания анальгетиков других групп (кеторолак, парацетамол и другие), так как ограничения режимов дозирования согласно инструкции по медицинскому применению не позволяют увеличить максимальную суточную дозу трамадола для достижения адекватной аналгезии и снижения интенсивности болевого синдрома (менее 4 баллов по визуально-аналоговой шкале). Анальгетики других групп (кеторолак, парацетамол), представленные в клинических рекомендациях по послеоперационному обезболиванию, не метаболизируются изоферментом CYP2D6, генетический полиморфизм которого не оказывает существенного влияния на их метаболизм. Таким образом, при выявлении в ходе фармакогенетического тестирования генотипа GA и АА по аллельному варианту CYP2D6*4 необходимо включение в схему обезболивания как минимум одного анальгетика - кеторолака, парацетамола. Изобретение позволяет на основе результатов фармакогенетического тестирования повысить эффективность послеоперационного обезболивания, тем самым ускоряя раннюю активизацию больного в послеоперационном периоде и минимизируя негативные последствия боли за счет оптимизации стартовой схемы послеоперационного обезболивания.
Реализация заявляемого изобретения продемонстрирована следующими примерами.
Было проведено проспективное исследование, в которое включено 107 пациентов с неосложненным острым калькулезным холециститом, которым выполнялась видеолапароскопическая холецистэктомия. Всем включенным пациентам с целью послеоперационного обезболивания назначался трамадол 100 мг × 4 раза в сутки (максимальная суточная доза согласно инструкции по медицинскому применению). В качестве критерия эффективности послеоперационного обезболивания в течение раннего послеоперационного периоде (первые 5 суток с момента оперативного вмешательства) выполнялась оценка интенсивности боли с помощью визуальной аналоговой шкалы (ВАШ) через 2, 6, 12, 24, 36, 48 часов (Таблица 1).
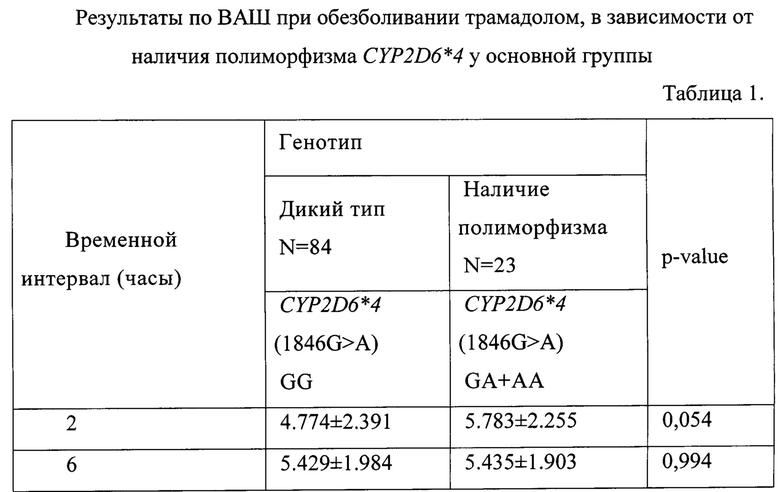
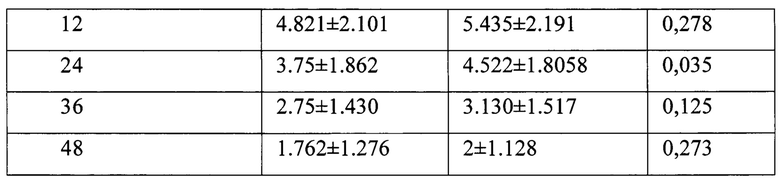
В результате было установлено, что у гомозигот и гетерозигот по полиморфной аллели CYP2D6*4 (GA и АА) интенсивность болевого синдрома по данным ВАШ была выше во все исследуемые временные промежутки в среднем более чем на 1 балл, при этом через 24 часа различия являются статистически значимыми (р<0,05).
Полученные результаты свидетельствуют о том, что носительство полиморфной аллели CYP2D6*4 (генотипы GA и АА) приводит к недостаточной эффективности монотерапии трамадолом в максимальной суточной дозе, что требует включения в стартовую схему анальгезии лекарственных препаратов других групп из перечня клинических рекомендаций: кеторолак, парацетамол. Напротив, отсутствие данной полиморфной аллели (генотип GG) повышает эффективность монотерапии трамадолом в максимальной дозе при послеоперационном обезболивании после видеолапароскопической холецистэктомии.
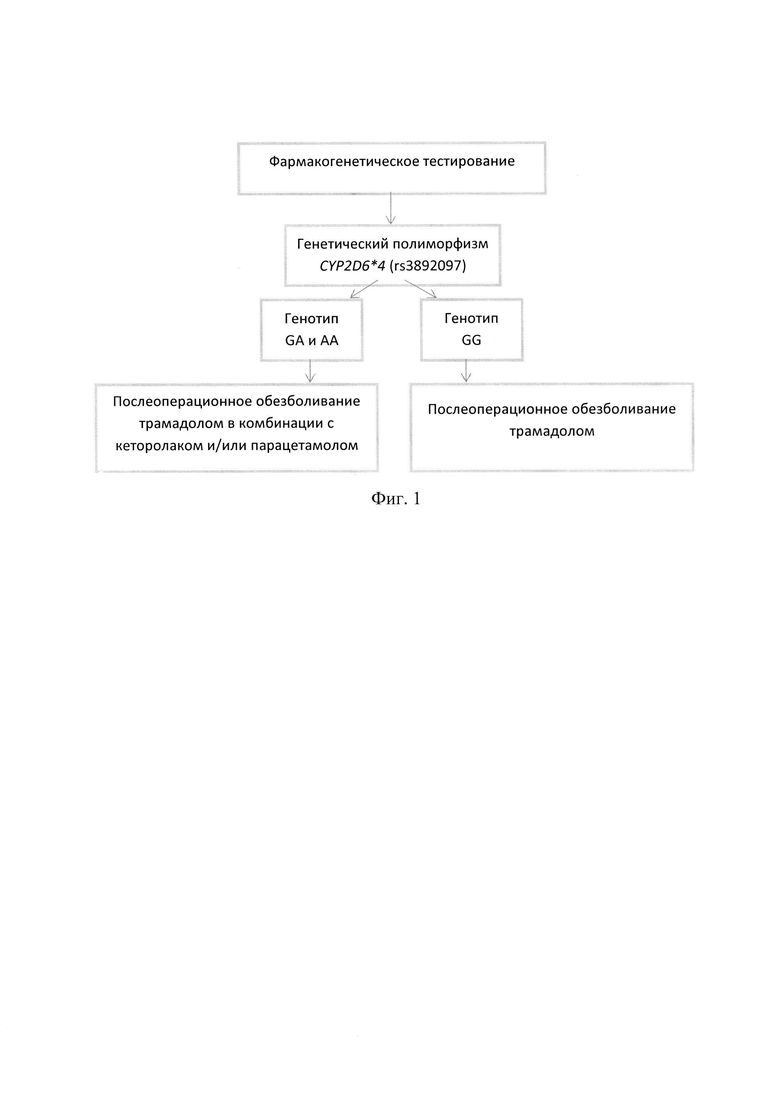
На Фиг. 1 - алгоритм назначения стартовой схемы послеоперационного обезболивания на основе определения генетического полиморфизма CYP2D64 rs3892097.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выбора стартовых обезболивающих лекарственных препаратов в послеоперационном периоде после кардиохирургических вмешательств | 2021 |
|
RU2774227C1 |
| СПОСОБ ПОВЫШЕНИЯ БЕЗОПАСНОСТИ ПРИМЕНЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРИ ЛЕЧЕНИИ ПАЦИЕНТОВ С СИНДРОМОМ ОТМЕНЫ АЛКОГОЛЯ | 2018 |
|
RU2690522C1 |
| Способ дифференцированного выбора фармакотерапии боли в спине на фоне дорсопатии у лиц операторских профессий | 2024 |
|
RU2840447C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОЦЕНКИ ЭФФЕКТИВНОСТИ ТЕРАПИИ ГАЛОПЕРИДОЛОМ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СОПРОВОЖДАЮЩИХСЯ РАЗВИТИЕМ ПСИХОТИЧЕСКОЙ СИМПТОМАТИКИ | 2017 |
|
RU2643944C1 |
| СПОСОБ ПРОГНОЗИРОВАНИИ ОЦЕНКИ ЭФФЕКТИВНОСТИ ТЕРАПИИ ЛЕВОМЕПРОМАЗИНОМ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СОПРОВОЖДАЮЩИХСЯ РАЗВИТИЕМ ПСИХОТИЧЕСКОЙ СИМПТОМАТИКИ | 2018 |
|
RU2695657C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИНТЕНСИВНОСТИ И РЕЗИСТЕНТНОСТИ БОЛЕВОГО СИНДРОМА ПОСЛЕ ОПЕРАЦИИ ВИДЕОЛАПАРОСКОПИЧЕСКОЙ ХОЛЕЦИСТЭКТОМИИ У БОЛЬНЫХ ХРОНИЧЕСКИМ КАЛЬКУЛЕЗНЫМ ХОЛЕЦИСТИТОМ | 2011 |
|
RU2461830C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОЦЕНКИ ЭФФЕКТИВНОСТИ ТЕРАПИИ ПРОМАЗИНОМ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СОПРОВОЖДАЮЩИХСЯ РАЗВИТИЕМ ПСИХОТИЧЕСКОЙ СИМПТОМАТИКИ | 2018 |
|
RU2695659C1 |
| СПОСОБ ПОСЛЕОПЕРАЦИОННОГО ОБЕЗБОЛИВАНИЯ БОЛЬНЫХ, ОПЕРИРОВАННЫХ ПОД СПИНАЛЬНОЙ АНЕСТЕЗИЕЙ | 2010 |
|
RU2459640C2 |
| СПОСОБ ВЫБОРА ДОЗИРОВКИ ПЕРИНДОПРИЛА У ПАЦИЕНТОВ С ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА НА ФОНЕ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 2016 |
|
RU2642284C1 |
| СПОСОБ ВЫБОРА СТАРТОВОЙ АНТИГИПЕРТЕНЗИВНОЙ ТЕРАПИИ БЛОКАТОРАМИ РЕЦЕПТОРОВ АНГИОТЕНЗИНА II У ПАЦИЕНТОВ С ВПЕРВЫЕ ВЫЯВЛЕННОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ 1-2 СТЕПЕНИ | 2024 |
|
RU2838951C1 |
Изобретение относится к области медицины, в частности к фармакогенетике. Определяют полиморфизм rs3892097 гена CYP2D6. При выявлении генотипа GA и АА по аллельному варианту CYP2D6*4 для послеоперационного обезболивания используют трамадол 400 мг/сут в сочетании с кеторолаком 90 мг/сут или трамадол 400 мг/сут в сочетании с парацетамолом 4 г/сут. В случае выявления генотипа GG по аллельному варианту CYP2D6*4 используют монотерапию трамадолом 400 мг/сут. Изобретение позволяет на основе результатов фармакогенетического тестирования повысить эффективность послеоперационного обезболивания, тем самым ускоряя раннюю активизацию больного в послеоперационном периоде и минимизируя негативные последствия боли за счет оптимизации стартовой схемы послеоперационного обезболивания. 1 ил., 1 табл., 1 пр.
Способ выбора стартовой схемы послеоперационного обезболивания у пациентов после видеолапароскопической холецистэктомии, отличающийся тем, что определяют полиморфизм rs3892097 гена CYP2D6, и при выявлении генотипа GA и АА по аллельному варианту CYP2D6*4 для послеоперационного обезболивания используют трамадол 400 мг/сут в сочетании с кеторолаком 90 мг/сут или трамадол 400 мг/сут в сочетании с парацетамолом 4 г/сут; в случае выявления генотипа GG по аллельному варианту CYP2D6*4 используют монотерапию трамадолом 400 мг/сут.
| Способ выбора анестезиологического обеспечения при оперативных вмешательствах | 1988 |
|
SU1572650A1 |
| EP 0002973131 A4, 15.03.2017 | |||
| МУРАДЯН А.А | |||
| Персонализированный подход к ускоренной реабилитации в хирургии неосложненного острого калькулезного холецистита | |||
| Дисс | |||
| канд | |||
| мед | |||
| наук | |||
| Москва, 2020, 149 c | |||
| МУРАДЯН А.А | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2022-08-30—Публикация
2021-11-26—Подача