Изобретение относится к медицине, в частности к фармакогенетике, и может быть использовано для выбора лекарственных препаратов при послеоперационном обезболивании пациентов после кардиохирургических вмешательств.
Несмотря на существование множества методов обезболивания согласно данным зарубежной литературы более 40% пациентов страдают послеоперационным болевым синдромом в течение 3 месяцев с момента выполнения кардиохирургических операций ( М, et al. 2014). Неадекватно купируемый болевой синдром может являться причиной ряда инфекционных осложнений в раннем послеоперационном периоде, повышения артериального давления, тромбоэмболических осложнений ввиду ограничения подвижности пациента и активации симпатоадреналовой вегетативной системы. Адекватное купирование послеоперационного болевого синдрома необходимо для ранней активизации пациента и минимизации ряда послеоперационных осложнений.
М, et al. 2014). Неадекватно купируемый болевой синдром может являться причиной ряда инфекционных осложнений в раннем послеоперационном периоде, повышения артериального давления, тромбоэмболических осложнений ввиду ограничения подвижности пациента и активации симпатоадреналовой вегетативной системы. Адекватное купирование послеоперационного болевого синдрома необходимо для ранней активизации пациента и минимизации ряда послеоперационных осложнений.
Нестероидные противовоспалительные препараты являются одной из наиболее известных и часто применяемых групп лекарственных препаратов с целью обезболивания. Согласно международным клиническим рекомендациям нестероидные противовоспалительные препараты входят в перечень средств, рекомендуемых с целью послеоперационного обезболивания у пациентов после кардиохирургических операций (Sousa-Uva M. et al. 2017).
На сегодняшний день согласно российским клиническим рекомендациям (Овечкин, А.М и др. 2019) по послеоперационному обезболиванию рекомендуемые схемы после кардиохирургических операций включают комбинацию лекарственных препаратов: кетопрофен +/- парацетамол +/- опиоидный анальгетик (промедол, трамадол, морфин и др.), назначение или неназначение лекарственных препаратов в составе которой должно опираться на интенсивность болевого синдрома у конкретного пациента. При этом рекомендуемая интенсивность болевого синдрома не должна превышать 4 баллов по визуально-аналоговой шкале или цифровой рейтинговой шкале в течение раннего послеоперационного периода. Однако, в действующих клинических рекомендациях не представлено данных о количестве применяемых в рамках данного варианта комбинированного обезболивания лекарственных препаратов в зависимости от генетических особенностей конкретного пациента.
Известно, что персонализированный подход к послеоперационному обезболиванию на основе генотипирования и выявления однонуклеотидных полиморфизмов генов CYP1A2, CYP2C19, CYP2C9, CYP2D6, CYP3A4, CYP3A5, СОМТ, OPRM1, и АВСВ1 позволяет снизить интенсивность послеоперационной боли, а также сопровождается уменьшением потребности в назначении наркотических анальгетиков, применение которых зачастую сопряжено с рядом неблагоприятных побочный реакций, прежде всего в виде угнетения дыхания (Senagore AJ, 2017).
На сегодняшний день не существует алгоритма выбора схемы послеоперационного обезболивания у пациентов кардиохирургического профиля на основе выявления генетических полиморфизмов.
Известен способ персонализации нестероидных противовоспалительных препаратов в виде изменения режима дозирования с зависимости от генетического полиморфизма гена CYP2C9 (Theken и др. 2020 г). К недостаткам данного способа стоит отнести отсутствие алгоритма выбора схемы послеоперационного обезболивания зависимости от генетического полиморфизма гена CYP2C9.
В качестве прототипа текущего алгоритма персонализации выбран инструмент GeneSight. Текущий прототип на основе выявления полиморфизмов генов CYP2D6, CYP2C19, CYP3A4, CYP2C9 позволяет получить практический результат для врача в виде следующей интерпретации: 1) «Применять лекарственный препарат без опасений», 2) «Применять лекарственный препарат с осторожностью» и 3) «Применять лекарственный препарат с большой осторожностью и частым мониторингом состояния». Однако, ограничением клинического применения данного прототипа является его валидность для принятия решения о применении психотропных препаратов. Данный алгоритм не применим для нестероидных противовоспалительных препаратов и выбора метода послеоперационного обезболивания.
Задачей текущего изобретения является разработка способа, позволяющего прогнозировать отсутствие ожидаемой эффективности обезболивания кетопрофеном у пациентов кардиохирургического профиля и определить необходимость комбинированной схемы послеоперационного обезболивания.
Сущность изобретения заключается в определении генетического полиморфизма гена CYP2C9 в зависимости от которого определяется необходимость включения или невключения нескольких лекарственных препаратов в стартовую схему послеоперационного обезболивания.
Проводится фармакогенетическое тестирование по полиморфизму CYP2C9*3 rs1057910. Выбор данного полиморфизма основан на результатах собственных экспериментальных и клинических исследований. Установлено, что цитохром CYP2C9 является одним из наиболее значимых для метаболизма ряда нестероидных противовоспалительных препаратов в печени человека, что говорит о необходимости его изучения в исследованиях эффективности и безопасности у пациентов различных групп. В клиническом исследовании данный полиморфизм подтвердил свою значимость как прогностический фактор эффективности послеоперационного обезболивания кетопрофеном.
Материалом для фармакогенетического тестирования может служить кровь или буккальный эпителий. После получения результатов генотипирования можно сделать вывод о том, стоит ли назначать кетопрофен в режиме монотерапии для обезболивания или необходимо применять комбинацию анальгетиков различных групп для анальгезии у пациентов после кардиохирургических вмешательств.
При наличии полиморфной аллели CYP2C9*3 (генотип АС или СС) возможно применение кетопрофена для послеоперационного обезболивания в рамках монотерапии, так как применение в максимальной суточной дозе сопровождается невысокой интенсивностью болевого синдрома (не более 6 баллов) и не сопряжено с неблагоприятными побочными реакциями. При наличии генотипа АА по аллельному варианту CYP2C9*3 необходимо включение в схему обезболивания анальгетиков других групп (трамадол, парацетамол и другие), так как ограничения режимов дозирования согласно инструкции по медицинскому применению не позволяют увеличить максимальную суточную дозу кетопрофена для достижения адекватной интенсивности болевого синдрома (менее 4 баллов по визуально-аналоговой шкале). Анальгетики других групп (трамадол, парацетамол), представленные в клинических рекомендациях по послеоперационному обезболиванию, не метаболизируются изоферментом CYP2C9, генетический полиморфизм которого не оказывает существенного влияния на их метаболизм. Таким образом, при выявлении в ходе фармакогенетического тестирования генотипа АА по аллельному варианту CYP2C9*3 необходимо включение в схему обезболивания как минимум одного анальгетика - трамадола или парацетамола.
Изобретение позволяет на основе результатов фармакогенетического тестирования повысить эффективность послеоперационного обезболивания, тем самым ускоряя раннюю активизацию больного в послеоперационном периоде и минимизируя негативные последствия боли за счет оптимизации стартовой схемы послеоперационного обезболивания.
Реализация заявляемого изобретения продемонстрирована следующими примерами.
Было проведено проспективное исследование, в которое включено 90 пациентов. У всех пациентов выполнялось кардиохирургическое оперативное вмешательство по соответствующим показаниям. Всем включенным пациентам с целью послеоперационного обезболивания назначался кетопрофен в дозе 100 мг в/м 2 раза в сутки (максимальная суточная доза согласна инструкции по медицинскому применению). В качестве критерия эффективности послеоперационного обезболивания в течение раннего послеоперационного периоде (первые 5 суток с момента оперативного вмешательства) выполнялась оценка интенсивности боли с помощью цифровой рейтинговой шкале, согласно которой были выделены следующие группы больных: 1) пациенты с высокой интенсивностью болевого синдрома на фоне обезболивания кетопрофеном (нон-респондеры, более 6 баллов по цифровой рейтинговой шкале в течение раннего послеоперационного периода); 2) пациенты с невысокой интенсивностью болевого синдрома (респондеры, менее 6 баллов по цифровой рейтинговой шкале в течение раннего послеоперационного периода) (таблица 1).
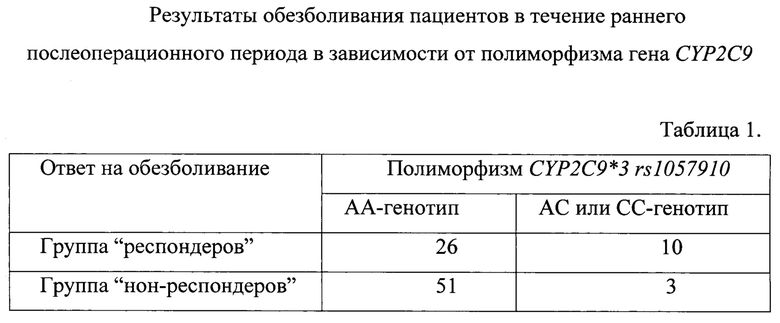
В результате было установлено, что в общей выборке пациентов генотип CYP2C9*3 АА повышал риск неэффективности послеоперационного обезболивания (нон-респондеры): (чувствительность - 66,2%, специфичность - 23%; OR - 6,5 (95% CI 1,6-25,8); р - 0,0053). При этом частота острого почечного повреждения и выраженность диспепсии, как наиболее частые неблагоприятные побочные реакции на фоне применения кетопрофена, статистически значимо не различались у больных с генотипами АА и АС-СС (р>0,05).
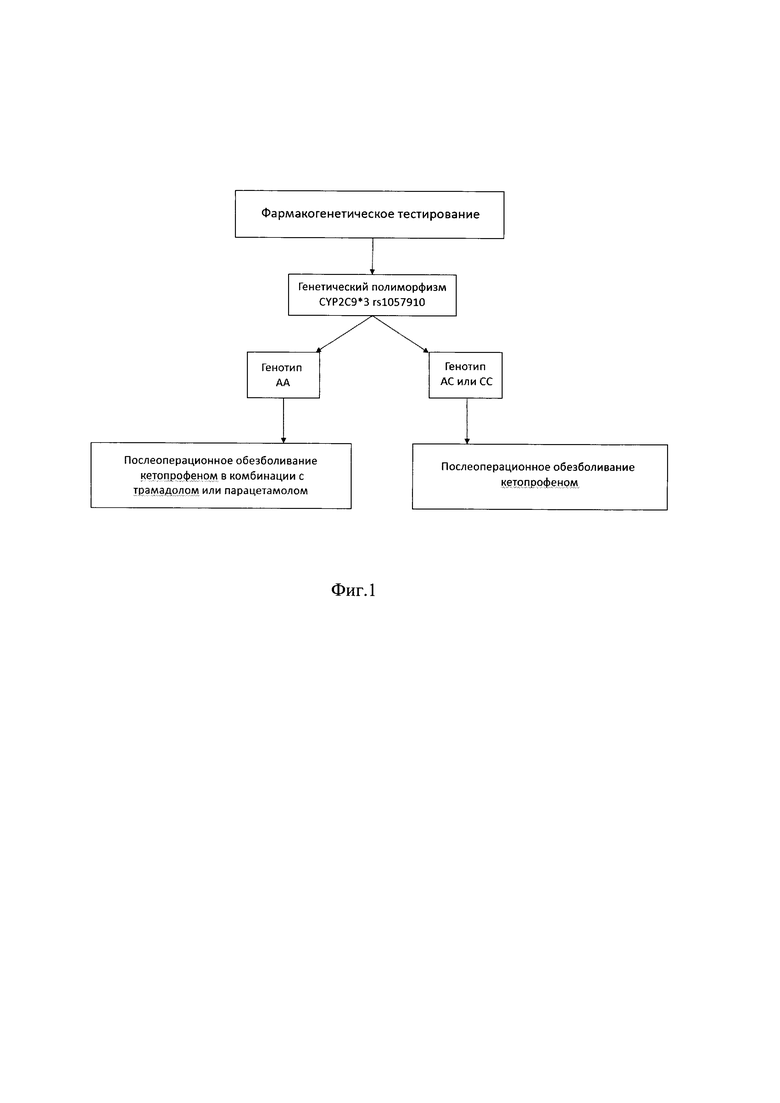
Данный результат свидетельствует о недостаточной эффективности монотерапии кетопрофеном в максимальной дозе при послеоперационном обезболивании после кардиохирургических вмешательств, что требует включения в стартовую схему анальгезии лекарственных препаратов других групп из перечня клинических рекомендаций: трамадол и/или парацетамол. На Фиг. 1 представлен алгоритм назначения стартовой схемы послеоперационного обезболивания на основе определения генетического полиморфизма CYP2C9*3 rs1057910.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выбора стартовой схемы послеоперационного обезболивания у пациентов после видеолапароскопической холецистэктомии | 2021 |
|
RU2779003C1 |
| Способ дифференцированного выбора фармакотерапии боли в спине на фоне дорсопатии у лиц операторских профессий | 2024 |
|
RU2840447C1 |
| СПОСОБ ПОВЫШЕНИЯ БЕЗОПАСНОСТИ ПРИМЕНЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРИ ЛЕЧЕНИИ ПАЦИЕНТОВ С СИНДРОМОМ ОТМЕНЫ АЛКОГОЛЯ | 2018 |
|
RU2690522C1 |
| СПОСОБ ВЫБОРА СТАРТОВОЙ АНТИГИПЕРТЕНЗИВНОЙ ТЕРАПИИ БЛОКАТОРАМИ РЕЦЕПТОРОВ АНГИОТЕНЗИНА II У ПАЦИЕНТОВ С ВПЕРВЫЕ ВЫЯВЛЕННОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ 1-2 СТЕПЕНИ | 2024 |
|
RU2838951C1 |
| Способ дифференцированного выбора фармакотерапии артериальной гипертензии на фоне дорсопатии у лиц операторских профессий | 2024 |
|
RU2826094C1 |
| СПОСОБ ПОСЛЕОПЕРАЦИОННОГО ОБЕЗБОЛИВАНИЯ БОЛЬНЫХ, ОПЕРИРОВАННЫХ ПОД СПИНАЛЬНОЙ АНЕСТЕЗИЕЙ | 2010 |
|
RU2459640C2 |
| СПОСОБ ПРЕМЕДИКАЦИИ ПЕРЕД ОПЕРАТИВНЫМИ ГИНЕКОЛОГИЧЕСКИМИ ВМЕШАТЕЛЬСТВАМИ, ВЫПОЛНЯЕМЫМИ В УСЛОВИЯХ ОБЩЕЙ АНЕСТЕЗИИ | 2014 |
|
RU2549474C1 |
| СПОСОБ КУПИРОВАНИЯ БОЛЕВЫХ СИНДРОМОВ, ОБУСЛОВЛЕННЫХ ЗЛОКАЧЕСТВЕННЫМИ НОВООБРАЗОВАНИЯМИ | 2018 |
|
RU2695350C2 |
| Способ послеоперационного обезболивания онкологических больных с хроническим болевым синдромом при выполнении декомпрессивно-стабилизирующих операций на позвоночнике | 2023 |
|
RU2811259C2 |
| СПОСОБ ЛИМФОТРОПНОГО НЕНАРКОТИЧЕСКОГО ОБЕЗБОЛИВАНИЯ ОНКОЛОГИЧЕСКИХ ПАЦИЕНТОВ | 2019 |
|
RU2720108C1 |
Изобретение относится к области медицины, в частности к фармакогенетике, и предназначено для выбора стартовых обезболивающих лекарственных препаратов в послеоперационном периоде после кардиохирургических вмешательств. Определяют полиморфизм rs1057910 гена CYP2C9. При выявлении генотипа АС или СС CYP2C9*3 для послеоперационного обезболивания используют монотерапию кетопрофеном 200 мг/сут. В случае выявления генотипа АА CYP2C9*3 для послеоперационного обезболивания используют кетопрофен 200 мг/сут в сочетании с трамадолом 100 мг/сут или кетопрофен 200 мг/сут в сочетании с парацетамолом 4 г/сут. Изобретение обеспечивает повышение эффективности послеоперационного обезболивания. 1 ил., 1 табл., 1 пр.
Способ выбора стартовых обезболивающих лекарственных препаратов в послеоперационном периоде после кардиохирургических вмешательств, отличающийся тем, что определяют полиморфизм rs1057910 гена CYP2C9, и при выявлении генотипа АС или СС по аллельному варианту CYP2C9*3 для послеоперационного обезболивания используют монотерапию кетопрофеном 200 мг/сут; в случае выявления генотипа АА по аллельному варианту CYP2C9*3 для послеоперационного обезболивания используют кетопрофен 200 мг/сут в сочетании с трамадолом 100 мг/сут или кетопрофен 200 мг/сут в сочетании с парацетамолом 4 г/сут.
| СПОСОБ ПОСЛЕОПЕРАЦИОННОГО ОБЕЗБОЛИВАНИЯ БОЛЬНЫХ, ОПЕРИРОВАННЫХ ПОД СПИНАЛЬНОЙ АНЕСТЕЗИЕЙ | 2010 |
|
RU2459640C2 |
| THEKEN K.N | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Clinical Pharmacology & Therapeutics | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| CALVO A.M | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2022-06-16—Публикация
2021-06-17—Подача