Изобретение относится к области медицины, в частности к клинической фармакогенетике, и предназначено для выбора стартовой антигипертензивной терапии блокаторами рецепторов ангиотензина II у пациентов с артериальной гипертензией 1-2 степени.
Несмотря на доступность и достаточный выбор антигипертензивных препаратов (далее - АП), адекватный контроль артериального давления (далее - АД) наблюдается лишь у 53% больных артериальной гипертензией (далее - АГ) [Rysz J, et al. 2020]. Высокая распространенность не диагностированных случаев АГ и неконтролируемой гипертонии связана с частым отсутствием специфических клинических проявлений повышенного АД, значительной вариабельностью эффективности антигипертензивной терапии и низкой приверженности к терапии, в том числе из-за опасений развития нежелательных лекарственных реакций (НЛР). Генетический полиморфизм является причиной 20-95% всех неблагоприятных ответов (неэффективность и/или НЛР) организма человека на лекарственные препараты. Отличительной чертой генетических особенностей является их постоянство в течение всей жизни. Выявление этих генетических особенностей у больных позволяет прогнозировать фармакологический ответ, а значит повысить эффективность и безопасность применения АП [Сычёв Д.А. и др. 2006].
Согласно клиническим рекомендациям «Российского кардиологического общества» и «Российского научного медицинского общества терапевтов» по АГ у взрослых 2024 года [РКО. 2024] всем пациентам с АГ (кроме пациентов низкого риска с АД<150/90 мм рт.ст., пациентов 80 лет и старше, пациентов с синдромом старческой астении) в качестве стартовой терапии рекомендована комбинация антигипертензивных препаратов, предпочтительно фиксированная, для улучшения приверженности к терапии. Предпочтительные комбинации должны включать блокатор РААС (ингибитор АПФ или БРА) и дигидропиридиновые антогонисты или диуретик.
Ирбесартан, одобренный для применения в 1997 г. [Fischer J, et al. 2006], по сравнению с другими БРА, обладает наибольшей биодоступностью при приеме внутрь и длительным периодом полувыведения, позволяющим принимать его один раз в сутки. Большая часть препарата выводится через желудочно-кишечный тракт (98%), метаболизируясь в печени с помощью системы CYP2C9 c образованием неактивного метаболита, что повышает безопасность применения его у пациентов с умеренными нарушениями функции почек [https://grls.rosminzdrav.ru]. Более того, по аффинности к рецептору ангиотензина II 1 типа (АТ1) ирбесартан превосходит олмесартан, кандесартан, эпросартан, телмисартан, валсартан, лозартан и его активный метаболит [Miura S, et al. 2011].
На сегодняшний день не существует алгоритма выбора стартовой ангигипертензивной терапии блокаторами рецепторов ангиотензина II на основе выявления генетических полиморфизмов.
Из уровня техники известен «Способ прогнозирования риска развития гипертонической болезни у мужчин по результатам генетического тестирования» [Патент РФ 2809912C1]. Изобретение относится к медицине, а именно к кардиологии, биотехнологии и медицинской генетике, и может быть использовано для прогнозирования риска развития гипертонической болезни у мужчин по результатам генетического тестирования. Из периферической венозной крови выделяют ДНК. Проводят анализ полиморфных локусов BAG6, AC026703.1 и OBFC1. При выявлении комбинации генотипов rs805303 GG BAG6 × rs1173771 AA AC026703.1 × rs4387287 AA OBFC1 прогнозируют высокий риск развития гипертонической болезни у мужчин. Способ обеспечивает получение новых критериев оценки риска развития гипертонической болезни у мужчин русской национальности, являющихся уроженцами Центрального Черноземья РФ и не имеющих родства между собой, на основе данных о полиморфных локусах BAG6, AC026703.1 и OBFC1.
Недостатком данного способа является то, что он позволяет оценить риск развития АГ, но не предлагает алгоритм выбора антигипертензивной терапии.
Известен «Способ прогнозирования риска развития гипертонической болезни с учетом генетических и средовых факторов» [Патент РФ 2678441C1]. Изобретение относится к области медицины, а именно к прогнозированию риска развития гипертонической болезни у индивидуумов русской национальности, являющихся жителями Центрального Черноземья. Для этого проводят выделение ДНК из периферической венозной крови. Анализ полиморфизмов генов, отличающийся тем, что анализируют полиморфизмы генов факторов роста rs6214 IGF-1 и rs2981582 FGFR2. Устанавливают наличие у респондента средовых факторов риска развития гипертонической болезни, а именно определяют статус курения. Прогнозируют высокий риск развития гипертонической болезни при выявлении сочетания генотипа GG rs6214 IGF-1, генотипа ТТ rs2981582 FGFR2 и положительного статуса курения. Изобретение обеспечивает получение критериев оценки риска развития гипертонической болезни у указанной категории пациентов с учетом сочетания генетических и средовых факторов. Однако, данный способ также позволяет оценить риск развития АГ у жителей Центрального Черноземья, но не предлагает алгоритм выбора антигипертензивной терапии.
Наиболее близким к заявляемому является «Способ терапии артериальной гипертензии у детей с ожирением на основании исследования патологических аллелей генов» [Патент РФ 2787390C1]. Изобретение относится к биотехнологии, в частности, к педиатрии и детской эндокринологии, может быть применено для оценки показания к медикаментозной терапии артериальной гипертензии у детей с ожирением. Проводят исследование панели генов, ассоциированных с развитием артериальной гипертензии, которое позволит подобрать персонализированную патогенетическую терапию и предотвратить поражение органов-мишеней. Способ обеспечивает стабилизацию артериального давления и предотвращение поражения органов-мишеней в результате антигипертензивной терапии, подобранной с учетом фармакогенетического тестирования, замедляет прогрессирование заболевания и формирование осложнений, уменьшает частоту госпитализаций и повышает качество жизни пациентов. Однако, способ позволяет провести персонализацию терапии БРА среди пациентов детского возраста с ожирением, а в панель исследуемых генов включены гены, ответственные за фармакодинамику БРА, тогда, как гены ответственные за метаболизм БРА, способны оказывать влияние на уровень концентрации ЛС и скорость ее достижения, что определяет эффективность и безопасность фармакотерапии.
Раскрытие изобретения
Задачей предлагаемого изобретения является персонализация антигипертензивной терапии у пациентов с впервые выявленной артериальной гипертензией 1-2 степени и разработка способа, позволяющего прогнозировать риск развития нежелательной лекарственной реакции на фоне терапии ирбесартаном.
Техническим результатом, на достижение которого направлено предлагаемое изобретение, является повышение эффективности и безопасности стартовой антигипертензивной терапии у пациентов с впервые диагностированной АГ 1-2 степени на основе результатов фармакогенетического тестирования, тем самым повышая контроль цифр АД и приверженность пациентов к лечению.
Технический результат достигается тем, что способ выбора стартовой антигипертензивной терапии блокаторами рецепторов ангиотензина II у пациентов с артериальной гипертензией 1-2 степени, отличающийся тем, что определяют генетические полиморфизмы гена CYP2C9 (CYP2C9*2 (Arg144Cys) и CYP2C9*3 (Ile359Leu)), и при выявлении генотипа С/С по аллельному варианту CYP2C9*2 и А/А по аллельному варианту CYP2C9*3 для стартовой терапии артериальной гипертензии 1-2 степени используют терапию ирбесартаном 150 мг/сут в режиме монотерапии или комбинированной терапии в зависимости от группы риска АГ; в случае выявления генотипов С/Т или Т/Т по аллельному варианту CYP2C9*2 и/или генотипов А/С и С/С по аллельному варианту CYP2C9*3 для стартовой терапии артериальной гипертензии 1-2 степени используют терапию валсартаном 80 мг/сут в режиме монотерапии или комбинированной терапии в зависимости от группы риска АГ.
Проводится фармакогенетическое тестирование по полиморфизмам CYP2C9*2 (Arg144Cys) и CYP2C9*3 (Ile359Leu). Выбор данных полиморфизмов основан на результатах собственных экспериментальных и клинических исследованиях. Установлено, что цитохром CYP2C9 является одним из наиболее значимых для метаболизма ирбесартана, что говорит о необходимости изучения его генетических полиморфизмов в исследованиях эффективности и безопасности у пациентов различных групп. В то время, как валсартан не подвергается метаболизму в печени. В клиническом исследовании данные полиморфизмы подтвердили свою значимость как прогностический фактор эффективной и безопасной антигипертензивной терапии ирбесартаном.
Материалом для фармакогенетического тестирования может служить кровь или буккальный эпителий. После получения результатов генотипирования можно сделать вывод о целесообразности назначения ирбесартана (в режиме монотерапии или в комбинации с гидрохлортиазидом в зависимости от группы риска АГ) в качестве стартовой терапии артериальной гипертензии 1-2 степени, или необходимо применять валсартан (в режиме монотерапии или в комбинации с гидрохлортиазидом в зависимости от группы риска АГ).
При наличии полиморфной аллели CYP2C9*2 (генотип С/Т или Т/Т) и/или CYP2C9*3 (генотип А/С или С/С) целесообразно применение валсартана (в режиме монотерапии или в комбинации с гидрохлортиазидом в зависимости от группы риска АГ) в качестве стартовой терапии артериальной гипертензии 1-2 степени с целью повышения безопасности терапии, так как валсартан не подвергается метаболизму в печение. При наличии генотипа С/С по аллельному варианту CYP2C9*2 и А/А по CYP2C9*3 целесообразно включение в схему стартовой антигипертензивной терапии у пациентов с АГ 1-2 степени ирбесартана (в режиме монотерапии или в комбинации с гидрохлортиазидом в зависимости от группы риска АГ) с целью повышения эффективности фармакотерапии.
Краткое описание чертежей
Изобретение поясняется таблицей, чертежами, схемами.
В таблице 1 представлены результаты корреляционного анализа изменений САД, ДАД через 3 недели терапии БРА и минимальной равновесной концентрации препарата (ирбесартана, валсартана).
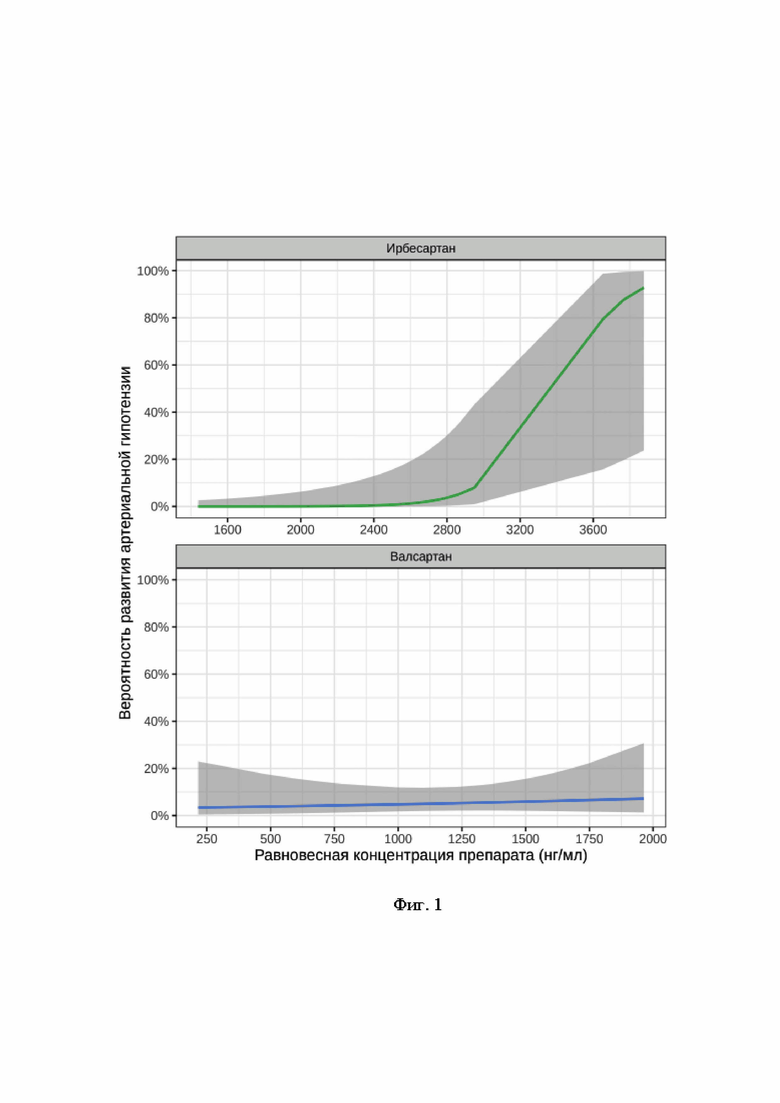
На фиг. 1 представлена вероятность развития артериальной гипотензии в зависимости от минимальной равновесной концентрации препаратов.
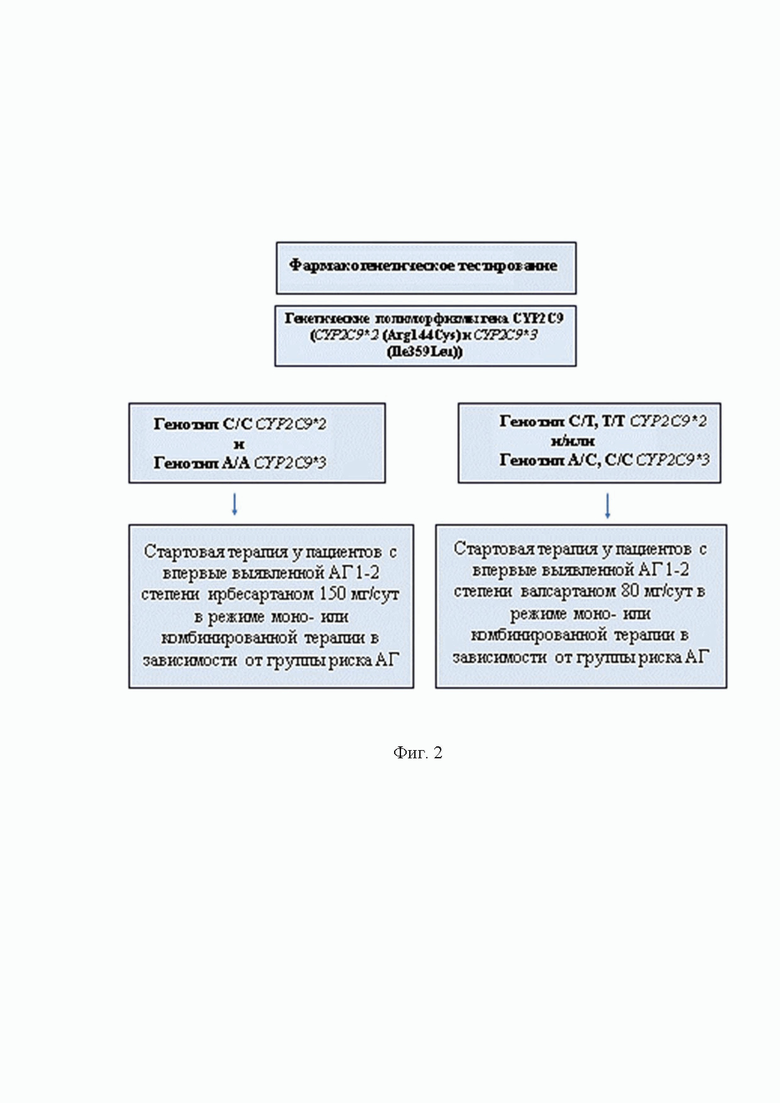
На фиг. 2 представлена схема способа выбора стартовой антигипертензивной терапии блокаторами рецепторов ангиотензина II у пациентов с впервые выявленной артериальной гипертензией 1-2 степени.
Изобретение подтверждается клиническими примерами.
Проведено проспективное исследование, в которое включено 179 пациентов с впервые выявленной АГ 1-2 степени низкого и умеренного риска. Все пациенты были случайным образом распределены по группам применения ирбесартана или валсартана методом простой рандомизации (метод конвертов). Участники исследования получали БРА (ирбесартан и валсартан) в монотерапии или в комбинации с гидрохлортиазидом в течение 3 месяцев. Так 83 пациента, включенных в исследование получали ирбесартан 150 мг 1 раз в сутки, 32 из них находились на монотерапии ирбесартаном, а 51 пациент получали комбинированную терапию ирбесартан 150 мг+гидрохлортиазид 12,5 мг. 96 пациентам был назначен валсартан, 8 из них получали монотерапию валсартаном 80 мг 1 раз в сутки, а 88 пациентам была назначена комбинированная терапия валсартан 80 мг+гидрохлортиазид 12,5 мг. При достижении целевых цифр АД через 3 недели терапии (<140/90 мм рт.ст., при хорошей переносимости <130/80 мм рт.ст., но не <120/70 мм рт.ст.) пациенты продолжали соблюдать свой режим дозирования препаратов в течение 3 месяцев лечения. При недостаточном контроле цифр АД проводили интенсификацию терапии путём увеличения дозы ирбесартана или валсартана в два раза в составе моно- или комбинированной терапии. Через 3 недели всем пациентам проводили фармакогенетическое тестирование на наличие полиморфной аллели CYP2C9*2 (генотип С/Т или Т/Т) и CYP2C9*3 (генотип А/С или С/С), и определяли минимальную равновесную концентрацию ирбесартана/валсартана методом высокоэффективной жидкостной хроматографии в соответствии с требованиями ГФ РФ, ОФС.1.2.1.2.0005.15 «Высокоэффективная жидкостная хроматография».
В результате было установлено, что у пациентов, принимавших ирбесартан было выявлено статистически значимо более выраженное снижение офисного САД и ДАД (в среднем на 1,26 [95% ДИ: -1,51; -1] мм рт. ст. и на 0,86 [95% ДИ: -1,16; -0,55] мм рт. ст. соответственно, при увеличении концентрации на каждые 100 нг/мл) через 3 недели назначенной фармакотерапии, при этом статистически значимой ассоциации данных показателей с концентрацией валсартана установлено не было (табл. 1).
Среди пациентов, получавших ирбесартан, была установлена статистически значимая связь минимальной равновесной концентрации с увеличением шансов развития артериальной гипотонии (ОШ=1,72 [95% ДИ: 1,15; 2,56], p=0,008), при применении валсартана ассоциация не была статистически значимой (ОШ=1,05 [95% ДИ: 0,86; 1,27], p=0,651) (фиг. 1).
Установлено, что генотип по аллельному варианту CYP2C9*2 (Arg144Cys) и CYP2C9*3 (Ile359Leu) является значимым предиктором эффекта.
Носительство полиморфного аллеля CYP2C9*2 у пациентов, получавших ирбесартан, было статистически значимо ассоциировано с более выраженным снижением офисного САД через 3 недели терапии в среднем на 8,3 [95% ДИ: -12,7; -3,8] мм рт. ст., в то время как у пациентов, получавших валсартан, носительство данного аллеля было ассоциировано с менее выраженным эффектом препарата (средняя разница - 7,4 [95% ДИ: 1,6; 13,2] мм рт.ст.). Эффект ирбесартана на снижение офисного САД через 3 недели терапии был на 89,8% [95% ДИ: 43,4; 100] опосредован значением минимальной равновесной концентрации препарата (p<0,001), в то время как у пациентов, получавших валсартан, данный показатель не являлся статистически значимым медиатором эффекта препарата (p=0,79).
Носительство полиморфного аллеля CYP2C9*3 у пациентов, получавших ирбесартан, было статистически значимо ассоциировано с более выраженным снижением офисного САД через 3 недели терапии в среднем на 11,8 [95% ДИ: -16,6; -7] мм рт. ст., у пациентов, получавших валсартан, носительство данного аллеля было ассоциировано с более выраженным эффектом препарата в среднем на 10,5 [95% ДИ: -16,2; -4,9] мм рт.ст.. Эффект ирбесартана на снижение офисного САД через 3 недели терапии был на 100% [95% ДИ: 65,5; 100] опосредован значением минимальной равновесной концентрации препарата (p=0,002), в то время как у пациентов, получавших валсартан, данный показатель не являлся статистически значимым медиатором эффекта препарата (p=0,97).
Данные результаты свидетельствуют о выраженном фармакодинамическом концентрационно зависимом эффекте ирбесартана, а также риске развития артериальной гипотензии у носителей полиморфных аллелей CYP2C9*2 и CYP2C9*3. На фиг. 2 представлен алгоритм назначения стартовой антигипертензивной терапии блокаторами рецепторов ангиотензина II у пациентов с впервые выявленной артериальной гипертензией 1-2 степени на основе определения генетических полиморфизмов гена CYP2C9 (CYP2C9*2 (Arg144Cys) и CYP2C9*3 (Ile359Leu)).
Таблица 1
Результаты корреляционного анализа изменений САД, ДАД через 3 недели терапии и минимальной равновесной концентрации препарата
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ дифференцированного выбора фармакотерапии артериальной гипертензии на фоне дорсопатии у лиц операторских профессий | 2024 |
|
RU2826094C1 |
| СПОСОБ ВЫБОРА ДОЗИРОВКИ ПЕРИНДОПРИЛА У ПАЦИЕНТОВ С ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА НА ФОНЕ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 2016 |
|
RU2642284C1 |
| БИОМАРКЕРЫ ДЛЯ ОЦЕНКИ ЭФФЕКТИВНОСТИ АЛИСКИРЕНА В КАЧЕСТВЕ ГИПЕРТЕНЗИВНОГО АГЕНТА | 2006 |
|
RU2408363C2 |
| СПОСОБ ТЕРАПИИ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ У ДЕТЕЙ С ОЖИРЕНИЕМ НА ОСНОВАНИИ ИССЛЕДОВАНИЯ ПАТОЛОГИЧЕСКИХ АЛЛЕЛЕЙ ГЕНОВ | 2022 |
|
RU2787390C1 |
| Способ прогнозирования риска развития преэклампсии у женщин с хронической артериальной гипертензией | 2018 |
|
RU2699974C1 |
| Способ выбора стартовых обезболивающих лекарственных препаратов в послеоперационном периоде после кардиохирургических вмешательств | 2021 |
|
RU2774227C1 |
| Способ прогнозирования развития коморбидной формы артериальной гипертензии и хронической обструктивной болезни легких | 2016 |
|
RU2620566C1 |
| Способ выбора стартовой схемы послеоперационного обезболивания у пациентов после видеолапароскопической холецистэктомии | 2021 |
|
RU2779003C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ЭНАЛАПРИЛА ПРИ ЛЕЧЕНИИ БОЛЬНЫХ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ В РОССИЙСКОЙ ПОПУЛЯЦИИ | 2006 |
|
RU2305837C1 |
| Способ прогнозирования развития коморбидной формы артериальной гипертензии при хронической обструктивной болезни легких | 2024 |
|
RU2833137C1 |
Изобретение относится к медицине, а именно к клинической фармакогенетике, и может быть использовано для выбора стартовой антигипертензивной терапии блокаторами рецепторов ангиотензина II у пациентов с артериальной гипертензией 1-2 степени. Определяют полиморфизмы CYP2C9*2 (Arg144Cys) и CYP2C9*3 (Ile359Leu) гена CYP2C9. При выявлении генотипа С/С CYP2C9*2 и А/А CYP2C9*3 для стартовой терапии используют терапию ирбесартаном 150 мг/сут. В случае выявления генотипов С/Т, или Т/Т CYP2C9*2, и/или генотипов А/С и С/С CYP2C9*3 для стартовой терапии используют терапию валсартаном 80 мг/сут. Способ обеспечивает повышение эффективности и безопасности стартовой антигипертензивной терапии у пациентов с впервые диагностированной артериальной гипертензией 1-2 степени за счет выбора препарата на основе результатов фармакогенетического тестирования. 2 ил., 1 табл.
Способ выбора стартовой антигипертензивной терапии блокаторами рецепторов ангиотензина II у пациентов с артериальной гипертензией 1-2 степени, отличающийся тем, что определяют полиморфизмы CYP2C9*2 (Arg144Cys) и CYP2C9*3 (Ile359Leu) гена CYP2C9 и при выявлении генотипа С/С по аллельному варианту CYP2C9*2 и А/А по аллельному варианту CYP2C9*3 для стартовой терапии артериальной гипертензии 1-2 степени используют терапию ирбесартаном 150 мг/сут; в случае выявления генотипов С/Т или Т/Т по аллельному варианту CYP2C9*2 и/или генотипов А/С и С/С по аллельному варианту CYP2C9*3 для стартовой терапии артериальной гипертензии 1-2 степени используют терапию валсартаном 80 мг/сут.
| Способ дифференцированного выбора фармакотерапии артериальной гипертензии на фоне дорсопатии у лиц операторских профессий | 2024 |
|
RU2826094C1 |
| US 20050181386 A1, 18.08.2005 | |||
| РЕБРОВА Е.В | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Москвы у пациентов с АГ I-II степени, получающих фармакотерапию ирбесартаном | |||
| Фармакогенетика и фармакогеномика | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| СИНИЦИНА И.И | |||
| и др | |||
| Клиническая фармакогенетика блокаторов рецепторов | |||
Авторы
Даты
2025-04-24—Публикация
2024-11-18—Подача