Изобретение относится к области медицины, конкретно, к онкологии, касается способов предсказания инвазии опухоли в капсулу щитовидной железы у больных с папиллярным раком.
Папиллярная карцинома является наиболее частой злокачественной опухолью щитовидной железы (до 90% всех случаев злокачественных патологий данной локализации), рецидивы заболевания встречаются у 25-35% пациентов [1, 2]. Развитие злокачественных опухолей щитовидной железы ассоциировано с возникновением ряда генетических нарушений, что способствует вовлечению в механизмы опухолей прогрессии МАРК (mitogen-activated protein kinase) и AKT/m-TOR сигнальных каскадов [3]. Известно, что половина случаев папиллярного рака щитовидной железы связана с активацией гена BRAF [2, 4].
Активация AKT/mTOR сигнального пути, связанная с повышением продукции транскрипционных, ростовых факторов, является ключевым механизмом опухолевой трансформации клеток [5]. Его составляющими являются протеинкиназы: АКТ, c-Raf, GSK-3, PDK1, а также m-TOR, ее субстраты p70-S64 и Е-ВР1, онкосупрессор PTEN. Показана высокая экспрессия киназ m-TOR, АКТ в опухолях щитовидной железы, сопряженная с риском прогрессирования заболевания [6].
К значимым молекулярным параметрам онкогенеза относят также транскрипционные и ростовые факторы: ядерный фактор NF-κВ, HIF, VEGF и карбоангидразы IX (CAIX) [7]. Имеются экспериментальные данные о значимости транскрипционных факторов HIF-1, NF-κВ в обеспечении инвазивного роста и в формировании метастатического потенциала папиллярного рака щитовидной железы [8, 9].
Известен факт того, что наибольшая активность AKT/m-TOR сигнального каскада наблюдается у пациентов с наличием мутации гена BRAF [3]. Полагают, что его гиперактивация является причиной развития резистентности к проводимому лечению у больных раком щитовидной железы [10, 11], в том числе и таргетной терапии ингибиторами BRAF [12].
Сложность и многокомпонентность молекулярных механизмов развития и прогрессирования опухоли является причиной отсутствия до настоящего времени значимых и клинически апробированных молекулярных прогностических факторов развития заболевания. Показано, что наличие соматической мутации BRAF-V600E не может определять исход заболевания. В работе Jing F.J. и соавторов (2013) отмечен факт того, что появление спорадической мутации гена не является признаком агрессивного поведения опухоли и не может быть использовано в качестве предсказательного маркера относительно риска развития отдаленных метастазов [13].
В последние годы частота обнаружения агрессивных форм данного морфологического варианта рака значительно возросла, в том числе ввиду широкого внедрения скрининга и доступности ультразвукового исследования шеи [14]. Основные медицинские проблемы данного заболевания составляют безболезненное течение, затрудняющее диагностику, и возникновение рецидивов после первичного хирургического вмешательства [15]. Существующие на данный момент времени морфологические и клинические параметры, связанные с прогнозированием возникновения рецидивов заболевания недостаточно точны [16]. Наличие прорастания капсулы щитовидной железы [17] без учета биологических особенностей опухоли не позволяют оценить агрессивность течения заболевания, риск прогрессирования заболевания.
Наиболее близким к предлагаемому способу является метод, основанный на изучении молекулярных особенностей опухоли путем изучения экспрессии генов :SFXN1, SLC12A4, SLC35A1, SLC35E1 и SLCO1C1 [18]. Однако, способ является малодоступным ввиду сложности метода. Существенный недостатком данного способа также является отсутствие связи с клиническими и морфологическими параметрами опухоли.
Новый технический результат - повышение точности и информативности способа.
Для достижения нового технического результата в способе прогнозирования инвазии опухоли в капсулу при папиллярном раке щитовидной железы проводят исследование опухолевых биологических маркеров в ткани пациента, выделяют РНК и определяют экспрессию 4Е-ВР1, учитывают данные о размере опухоли и данные о метастатическом поражении регионарных лимфатических узлов до гистологического исследования, далее рассчитывают регрессионную функцию F по формуле:
F=-1.350367+-0,00972X1+1,007675X2-0,35654X3-0,033X4,
где:
-1,350367 - значение коэффициента регрессии свободного члена;
X1 - возраст пациента на момент хирургического лечения, лет;
-0,00972 - значение коэффициента регрессии этого признака
Х2 - размер опухоли, при этом, при размере опухоли до 1 см в наибольшем измерении, ограниченной тканью щитовидной железы Х2=1;
при размере опухоли от 1 до 4 см в наибольшем измерении, ограниченной тканью щитовидной железы Х2=2;
при размере опухоли более 4 см в наибольшем измерении, ограниченной тканью щитовидной железы Х2=3;
при опухоли любого размера, распространяющаяся за пределы капсулы щитовидной железы Х2=4;
1,007675 - значение коэффициента регрессии этого признака;
Х3 - распространенность процесса, при этом, при отсутствии признаков метастатического поражения регионарных лимфатических узлов Х3=0;
при наличии поражения метастазами регионарных лимфатических узлов Х3=1;
0,35654 - значение коэффициента регрессии этого признака;
Х4 - экспрессия 4Е-ВР1, усл. ед.
0,033 - значение коэффициента регрессии этого признака;
затем рассчитывают вероятность прорастания опухоли в капсулу щитовидной железы Р по формуле:
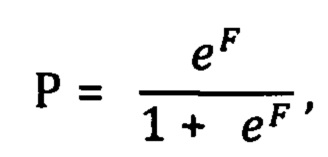
где е = 2,718,
и при Р менее 0,04 оценивают низкий, а при Р более 0,041 оценивают высокий риск прорастания капсулы.
Способ осуществляю следующим способом: для прогнозирования инвазии опухоли в капсулу щитовидной железы в ткани опухоли, полученной после тиреоидэктомии, выделяют РНК и определяют экспрессию 4Е-ВР1. С учетом клинических данных (стадии Т и N) до гистологического исследования опухоли определяют регрессионную функцию (F) и вероятность прорастания опухоли в капсулу щитовидной железы (р) с целью определения сроков динамического наблюдения.
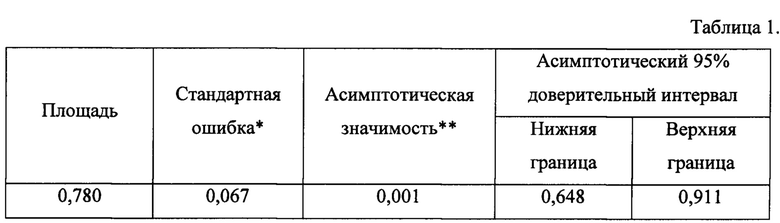
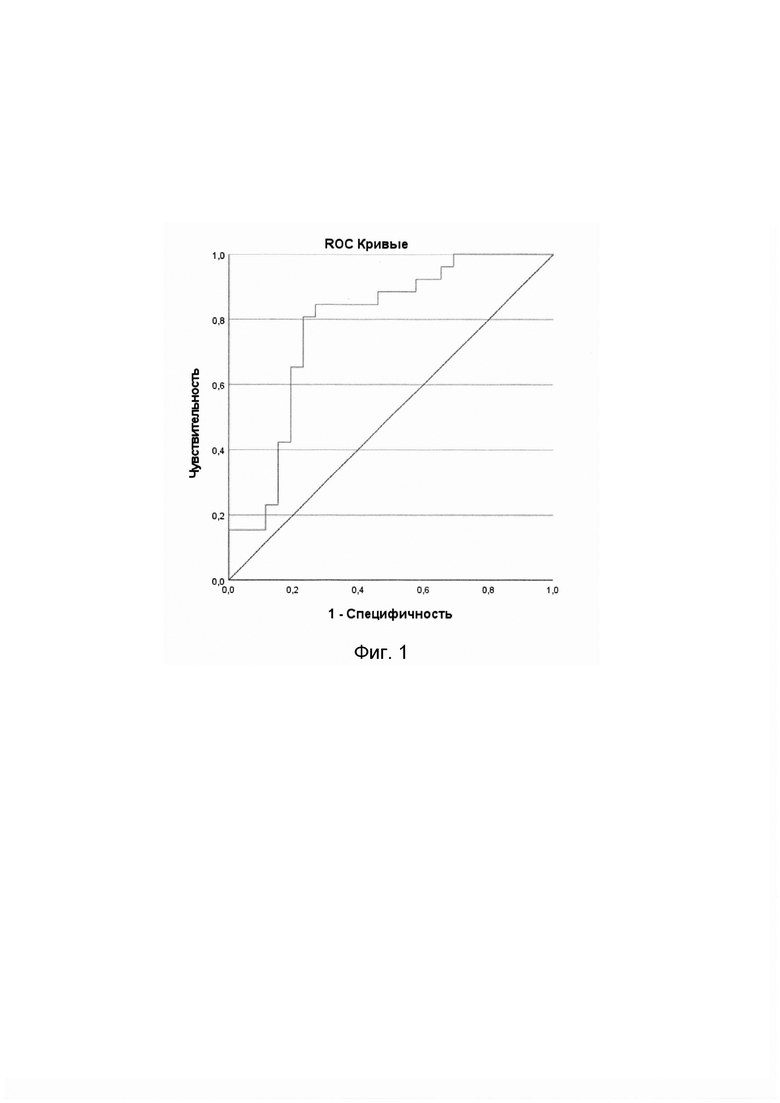
Определение эффективности математической модели проводилось при помощи ROC - анализа (Receiver Operating Characteristic). Чувствительность модели для прогнозирования у пациентов риска прорастания капсулы составила 80,77%, специфичность - 73,08%. Для оценки качества построенной математической модели использовалась характеристика площади под ROC-кривой - AUC (Area Under Curve), результаты представлены в таблице 1 Приложения.
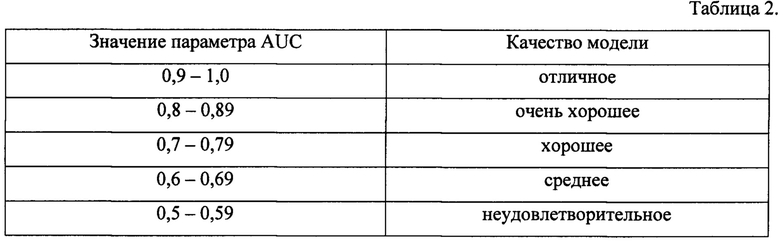
Значение параметра AUC для данной модели составило 0,780, что позволяет характеризовать ее как хорошую согласно общепринятым критериям, представленным в таблице 2 Приложения.
В качестве оптимального порога отсечения, позволяющего отнести полученные результаты к одному из двух классов, выбрано требование максимальной суммарной чувствительности и специфичности модели:
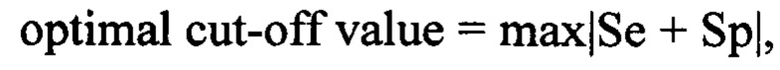
где Se - чувствительность модели, Sp - специфичность модели.
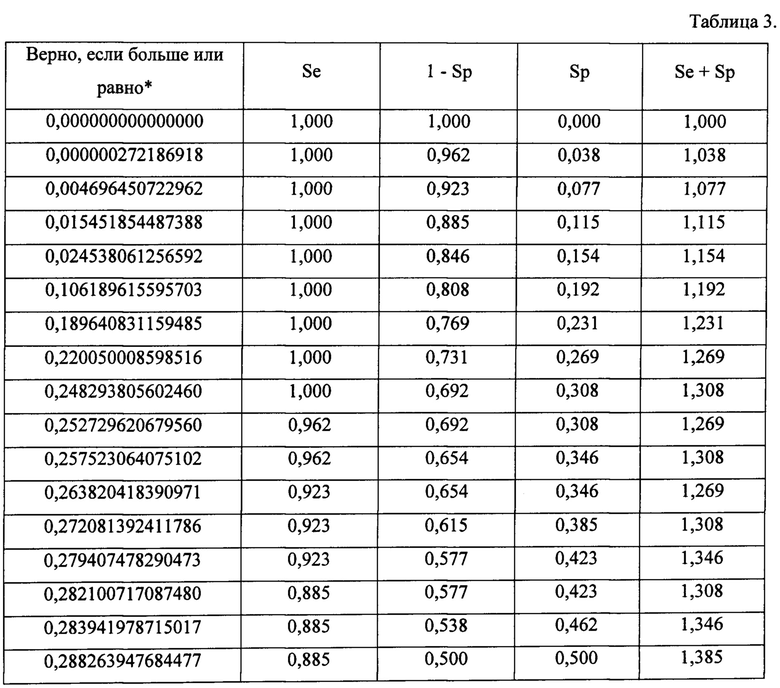
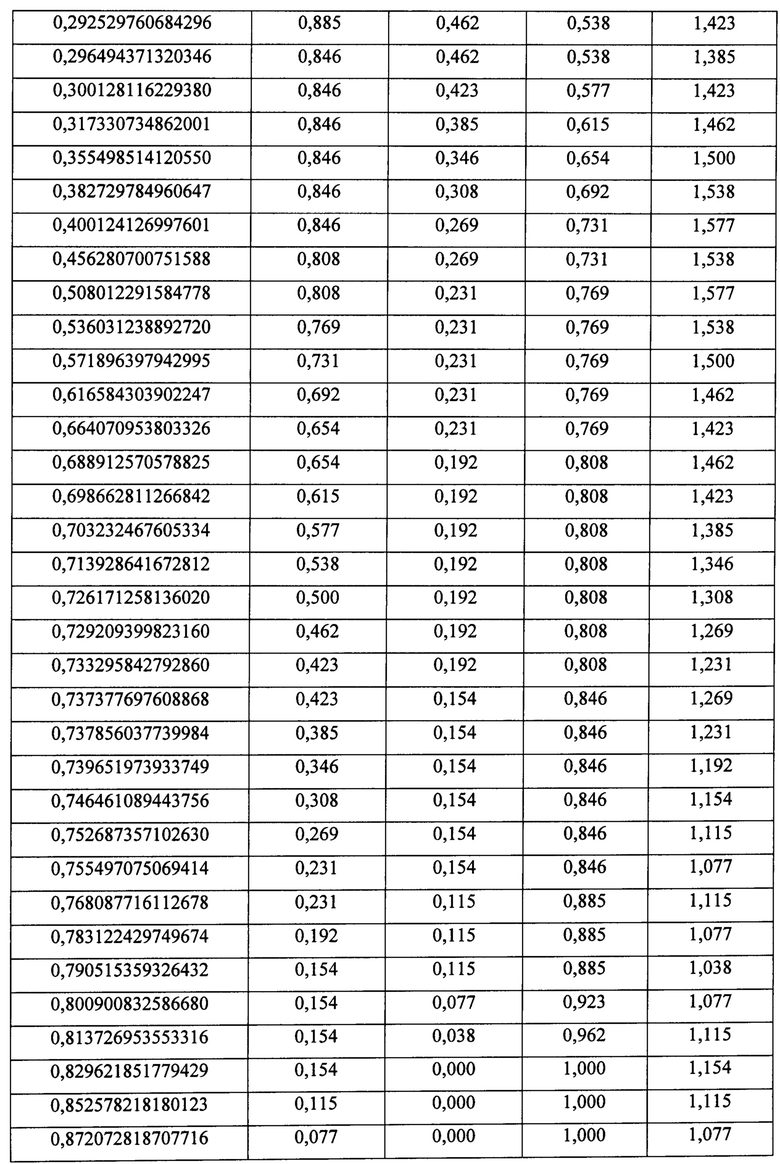
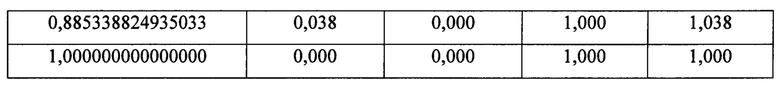
Значение пороговой величины было определено на основании результатов вычислений координат ROC-кривой, представленных в таблице 3 Приложения.
Максимальное суммарное значение чувствительности и специфичности составило 1,577, что соответствует порогу отсечения, равному 0,4.
Результаты построения ROC-кривой для данной модели отображены на Фиг 1. Приложения, где ROC-кривая для модели, определяющей вероятность экстратиреоидной инвазии опухоли в капсулу щитовидной железы.
Способ основан на результатах анализа данных лабораторных и клинических исследований. Информативность отобранных критериев подтверждена наличием связи экспрессии молекулярных показателей с клинико-морфологическими параметрами опухоли.
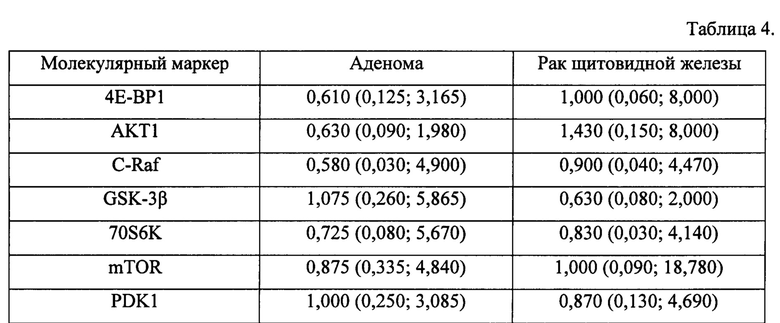
Значимых различий уровней компонентов PI3K/AKT/mTOR - сигнального пути, МАРК - сигнального пути, между злокачественной и доброкачественной патологией не выявлено (таблица 4 Приложения)
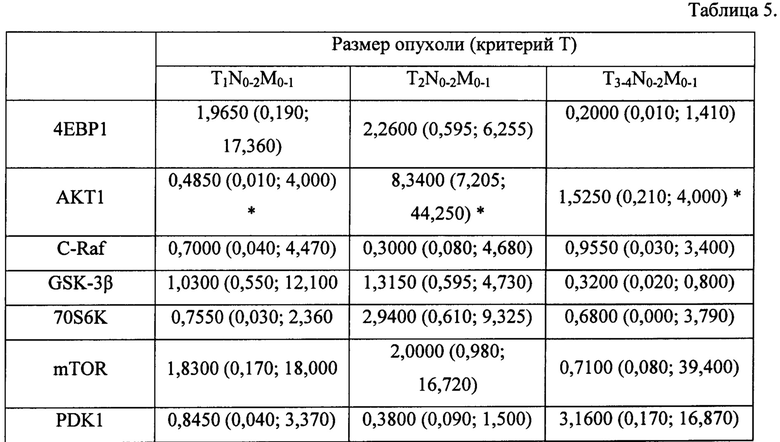
Несмотря на отсутствие изменения уровня мРНК компонентов PI3K/AKT/mTOR -сигнального пути в злокачественной опухоли щитовидной железы по сравнению с тканью аденомы, у больных с размером опухоли T1N0-2M0-1, T2N0-2M0-1 и T3-4N0-2M0-1, в исследовании продемонстрирован рост экспрессии серин-треониновой протеинкиназы АКТ1 (р=0,0127) с увеличением стадии заболевания Т (таблица 5 Приложения).
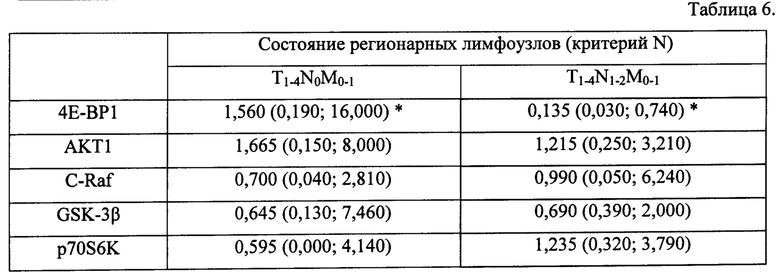
Также в исследовании продемонстрировано снижение уровня экспрессии ингибитора трансляции 4ЕВР1 в 11,6 раз (р=0,0197) и рост фосфоинозитид-зависимой киназы PDK1 в 5,5 раза (р=0,029) по мере появления метастатических поражений регионарных лимфоузлов (таблица 6 Приложения).
Принимая во внимание значимость этих показателей, все они были включены в статистическую модель с расчетом дискриминационных функций. Информативность полученных функций оценивали у 12 пациентов, не включенных в основную выборку. Чувствительность и специфичность полученной модели составила, соответственно, 73,1% и 80,7%, диагностическая точность -95,6%.
Таким образом, выявлена прогностическая модель, позволяющая прогнозировать прорастание капсулы при папиллярном раке щитовидной железы опухоли. Выявленные факты позволяют рассматривать эти параметры в качестве дополнительных информативных маркеров, позволяющих прогнозировать прогрессирование заболевания. Клинический пример 1.
Больная П., 47 лет, проходила лечение в клиниках НИИ онкологии Томского НИМЦ, отделение опухолей головы и шеи с диагнозом: «папиллярный рак щитовидной железы, T3N0M0» и проведено хирургическое лечение (18.05. 2016 г. - тиреоидэктомия).
Для прогнозирования прорастания капсулы при папиллярном раке щитовидной железы была применен предлагаемый способ, было рассчитано значение регрессионной функции F по формуле:
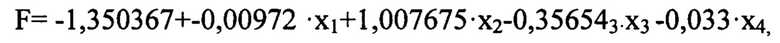
где коэффициенты регрессионной функции:
x1 - возраст пациента на момент хирургического лечения, лет (47 лет);
x2 - величина опухолевого узла (х2=3);
х3 - показатель метастазирования в лимфоузлы(х3=0);
x4 - экспрессия 4Е-ВР1, усл. ед.
В последующем, используя значение регрессионной функции и основание натурального логарифма (е), рассчитывается математическая модель в виде формулы для определения у больных риска прорастания капсулы при папиллярном раке щитовидной железы Р.
Общий вид математической модели:
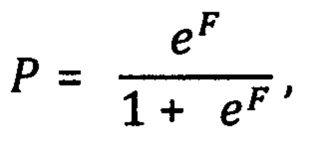
где е=2,718,
4Е-ВР1 составила 51,98 Усл. Ед.. Значение регрессионной функции, F равно -0,4988 и вероятность прорастания опухоли в капсулу щитовидной железы, Р=0,37757. Выявлен низкий риск экстратиреодиной инвазии и прорастания опухоли в капсулу щитовидной железы.
Риск прорастания опухоли в капсулу определен как низкий в соответствии с уровнем порога отсечения, что согласуется с проведенным гистологическим исследованием, не выявившим признаки прорастания капсулы щитовидной железы. Данные гистологического исследования: папиллярный рак щитовидной железы без инвазии в капсулу и сосуды. Отмечено, что у больной не наблюдалось признаков рецидива заболевания в течение 47 месяцев после хирургического вмешательства.
Клинический пример 2.
Больной П., 42 года, проходил лечение в клиниках НИИ онкологии Томского НИМЦ в отделении опухолей головы и шеи с диагнозом «папиллярный рак щитовидной железы, T4N0M0» и проведено хирургическое лечение (13.10. 2016 г. - гемитиреоидэктомия).
Для прогнозирования экстратиреоидной инвазии опухоли была применена математическая модель согласно предлагаемому способу и рассчитано значение регрессионной функции F по формуле:
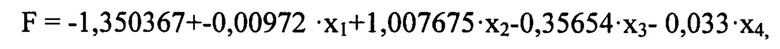
где коэффициенты регрессионной функции:
x1 - возраст пациента на момент хирургического лечения, лет(42);
x2 - величина опухолевого узла (х2=4);
х3 - показатель метастазирования в лимфоузлы (х3=0);
x4 - экспрессия 4Е-ВР1, Усл. Ед.
В последующем, используя значение регрессионной функции и основание натурального логарифма (е), рассчитывается математическая модель в виде формулы для определения у больных риска прорастания капсулы при папиллярном раке щитовидной железы.
Общий вид математической модели:
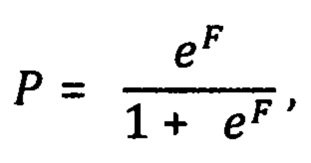
е=2,718
Экспрессия 4ЕВР1 была равна 0,93 Усл. Ед. Значение регрессионной функции, F=0,22593,) и вероятность прорастания опухоли в капсулу щитовидной железы, Р=0,55624. Выявлен высокий риск экстратиреодиной инвазии и прорастания опухоли в капсулу щитовидной железы
Полученные результаты соответствовали заключению гистологического исследования, подтверждающего факт наличия признаков прорастания капсулы щитовидной железы. Результаты гистологического исследования: Папиллярный рак щитовидной железы с инвазией в капсулу щитовидной железы на фоне хронического аутоиммунного тиреоидита. Период наблюдение за больным составил 26 месяцев.
Таким образом, предлагаемый способ позволяет предсказать неблагоприятный прогноз заболевания, а именно риск развитии рецидивов опухоли после проведенного лечения, в ранние сроки после тиреоидэктомии, до гистологической верификации диагноза. Введение дополнительных молекулярных критериев предсказания инвазии опухоли в капсулу щитовидной железы позволит модифицировать тактику динамического наблюдения за пациентами и своевременно проводить диагностику рецидивов заболевания.
Источники информации
1. Злокачественные новообразования в России в 2016 году (заболеваемость и смертность). / Под ред. Каприна А.Д., Старинского В.В., Петровой Г.В. - М.: МНИОИ им. П.А. Герцена, 2018.
2. Kim WW, На ТК, Bae SK. Clinical implications of the BRAF mutation in papillary thyroid carcinoma and chronic lymphocytic thyroiditis. // J Otolaryngol Head Neck Surg. -2018 - V. 47(1). - P. 4. Published 2018 Jan 9. doi:10.1186/s40463-017-0247-6.
3. Faustino A, Couto JP, Pópulo H, Rocha AS, Pardal F, Cameselle-Teijeiro JM, Lopes JM, Sobrinho-Simões M, Soares P. mTOR pathway overactivation in BRAF mutated papillary thyroid carcinoma. // J Clin Endocrinol Metab. - 2012. - V.97(7). - P.1139-49. doi: 10.1210/jc.2011-2748.
4. Margalef P, Colomer C, Villanueva A., Montagut C, Iglesias M, Bellosillo B, Salazar R, Martinez-Iniesta M, Bigas A, Espinosa L. BRAF-induced tumorigenesis is IKKα-dependent but NF-κB-independent. // Sci Signal. - 2015. - V. 8(373). - P. 38. doi: 10.1126/scisignal.2005886.
5. Tanaka TN, Alloju SK, Oh DK, Cohen EW. Thyroid cancer: molecular pathogenesis, tyrosine kinase inhibitors, and other new therapies. // The American journal of hematology/oncology. -2015.-V.11(4).-P. 5-9.
6. Tavares C, Eloy C, Melo M, Gaspar da Rocha A, Pestana A, Batista R, Bueno Ferreira L, Rios E, Sobrinho Simões M, Soares P. mTOR Pathway in Papillary Thyroid Carcinoma: Different Contributions of mTORCl and mTORC2 Complexes for Tumor Behavior and SLC5A5 mRNA Expression. // Int J Mol Sci. - 2018. -V.19(5). P.1448. doi:10.3390/ijmsl9051448.
7. Marotta V, Sciammarella C, Capasso M, Testori A, Pivonello C, Chiofalo MG, Pivonello R, Pezzullo L, Botti G, Colao A, Faggiano A. Erratum to: Preliminary data of VEGF-A and VEGFR-2 polymorphisms as predictive factors of radiological response and clinical outcome in iodine-refractory differentiated thyroid cancer treated with sorafenib. Endocrine. - 2017. -V.57(3). - P.544. doi: 10.1007/s12020-017-1269-6.
8. Burrows N, Babur M, Resch J, Ridsdale S, Mejin M, Rowling EJ, Brabant G, Williams KJ. GDC-0941 inhibits metastatic characteristics of thyroid carcinomas by targeting both the phosphoinositide-3 kinase (PI3K) and hypoxia-inducible factor-1α (HIF-1α) pathways. // J Clin Endocrinol Metab. -2011. - V.96(12). -P.1934-43. doi: 10.1210/jc.2011-1426.
9. Ma Y, Wang Q, Liu F, Ma X, Wu L, Guo F, Zhao S, Huang F, Qin G. KLF5 promotes the tumorigenesis and metastatic potential of thyroid cancer cells through the NF-κВ signaling pathway. // Oncol Rep.- 2018. - V.40(5). - P.2608-2618. doi: 10.3892/or.2018.6687.
10. Xing M. Genetic alterations in the phosphatidylinositol-3 kinase/Akt pathway in thyroid cancer. // Thyroid. - 2010. - V.20(7). P. 697-706. doi: 10.1089/thy.2010.1646.
11. Mondragón-Teran P, López-Hernández LB, Gutiérrez-Salinas J, Suárez-Cuenca JA, Luna-Ceballos RJ, Erazo Valle-Soh's A.Intracellular signalling mechanisms in thyroid cancer. // Cirugia у Cirujano. - 2016. - V.84(5). - P.434-443.
12. Byeon HK, Na HJ, Yang YJ, Kwon HJ, Chang JW, Ban MJ, Kim WS, Shin DY, Lee EJ, Koh YW, Yoon JH, Choi EC. c-Met-mediated reactivation of PI3K/AKT signaling contributes to insensitivity of BRAF(V600E) mutant thyroid cancer to BRAF inhibition. // Mol Carcinog.-2016.-V.55(11).-P.1678-1687. doi: 10.1002/mc.22418. Epub 2015 Oct 12.
13. Jing FJ, Liang J, Liang ZY, Meng C, Long W, Li XY, Lin YS. BRAF(V600E) mutation is not a positive predictor for distant metastasis in sporadic papillary thyroid carcinoma. // Chin Med J (Engl). - 2013.- V.126(16). P.3013-8.
14. Coca-Pelaz A, Shah JP, Hernandez-Prera JC, Ghossein RA, Rodrigo JP, Hartl DM, Olsen KD, Shaha AR, Zafereo M, Suarez C, Nixon IJ, Randolph GW, Makitie AA, Kowalski LP, Vander Poorten V, Sanabria A, Guntinas-Lichius O, Simo R, Zbaren P, Angelos P, Khafif A, Rinaldo A, Ferlito A. Papillary Thyroid Cancer-Aggressive Variants and Impact on Management: A Narrative Review. Adv Ther. 2020 Jul;37(7):3112-3128. doi: 10.1007/sl2325-020-01391-l. Epub 2020 Jun 1. PMID: 32488657; PMCID: PMC7467416.
15. Lin B, Ma H, Ma M, Zhang Z, Sun Z, Hsieh IY, Okenwa O, Guan H, Li J, Lv W. The incidence and survival analysis for anaplastic thyroid cancer: a SEER database analysis. Am J Transl Res. 2019 Sep 15;ll(9):5888-5896. PMID: 31632557; PMCID: PMC6789224.
16. Xia BY, Abuduwaili M, Fei Y, Xing ZC, Liu Y, Zhang LY, Su AP, Zhu JQ. Analysis of correlation factors of contralateral central lymph node metastasis in unilateral papillary thyroid carcinoma with lateral cervical lymph node metastasis. Zhonghua Wai Ke Za Zhi. 2021 Jun l;59(6):502-506. Chinese, doi: 10.3760/cma.j.cnl 12139-20200706-00541. PMID: 34102735.
17. Huang J, Shi H, Song M, Liang J, Zhang Z, Chen X, Liu Y, Wang S, Wu Z. Surgical Outcome and Malignant Risk Factors in Patients With Thyroid Nodule Classified as Bethesda Category III. Front Endocrinol (Lausanne). 2021 Sep 14;12:686849. doi: 10.3389/fendo.2021.686849. PMID: 34594299; PMCID: PMC8477748.
18. Han R, Sun W, Zhang H. Identification of a Signature Comprising 5 Soluble Carrier Family Genes to Predict the Recurrence of Papillary Thyroid Carcinoma. Technol Cancer Res Treat.
2021 Jan-Dec; 20:15330338211036314. doi: 10.1177/15330338211036314. PMID: 34590520; PMCID: PMC8489750.
Приложение
Таблица 1. Данные ROC анализа Примечание
* - в соответствии с непараметрическим предположением;
** - Н0: действительная площадь=0,5.
Таблица 2. Связь параметра AUC с качеством модели
Таблица 3. Чувствительность и специфичность полученной модели
Примечание:
* - наименьшее пороговое значение - минимальное наблюдаемое проверяемое значение минус 1, а наибольшее пороговое значение - максимальное наблюдаемое проверяемое значение плюс 1. Все остальные пороговые значения - средние двух последовательных упорядоченных наблюдаемых проверяемых значений.
Таблица 4 Экспрессия молекулярных маркеров в ткани доброкачественной и злокачественной патологии щитовидной железы, Me(Q1; Q3).
Примечание: * - значимость различий между доброкачественной и злокачественной патологией щитовидной железы, р<0,05;
Таблица 5 Экспрессия молекулярных маркеров рака щитовидной железы в зависимости от размера опухоли, Me(Q1; Q3
Примечание: * - значимость различий между группами в зависимости от размера опухоли, р<0,05;
Таблица 6. Экспрессии молекулярных маркеров рака щитовидной железы в зависимости от наличия регионарных метастазов, Me(Q1; Q3).
Примечание: * - значимость различий между группами в зависимости от состояния регионарных лимфатических узлов, р<0,05;
Фиг 1. ROC-кривая для модели, определяющей вероятность инвазии опухоли в капсулу щитовидной железы.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования развития рецидивов опухоли при папиллярном раке щитовидной железы | 2022 |
|
RU2795086C1 |
| СПОСОБ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2023 |
|
RU2820815C1 |
| СПОСОБ ДООПЕРАЦИОННОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ДОБРОКАЧЕСТВЕННЫХ И ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2614700C1 |
| Способ комплексной дооперационной дифференциальной диагностики доброкачественных и злокачественных узловых образований щитовидной железы | 2022 |
|
RU2805941C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ МЕСТНЫХ РЕЦИДИВОВ В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ У БОЛЬНЫХ МЕСТНО-РАСПРОСТРАНЕННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2020 |
|
RU2734719C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ЧЕЛОВЕКА | 2014 |
|
RU2569154C1 |
| СПОСОБ ДООПЕРАЦИОННОГО ОПРЕДЕЛЕНИЯ ОБЪЕМА ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВЫСОКОДИФФЕРЕНЦИРОВАННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2548783C1 |
| Способ прогнозирования риска развития отдаленных метастазов у больных операбельными формами рака молочной железы с метастазами в регионарные лимфоузлы | 2020 |
|
RU2733697C1 |
| СПОСОБ ОЦЕНКИ РИСКА НАЛИЧИЯ РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ У ПАЦИЕНТА С УЗЛОВЫМИ ОБРАЗОВАНИЯМИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2019 |
|
RU2725749C1 |
| Способ прогнозирования высокого риска регионарного метастазирования при раке молочной железы | 2023 |
|
RU2816441C1 |
Изобретение относится к области медицины, а именно к онкологии, и может быть использовано для прогнозирования инвазии опухоли в капсулу при папиллярном раке щитовидной железы. Способ включает проведение исследования опухолевых биологических маркеров в ткани пациента. Выделяют РНК из ткани опухоли и определяют экспрессию 4Е-ВР1, учитывают данные о размере опухоли и данные о метастатическом поражении регионарных лимфатических узлов до гистологического исследования и рассчитывают вероятность прорастания опухоли в капсулу щитовидной железы. Использование изобретения позволяет предсказать неблагоприятный прогноз заболевания, а именно риск развитии рецидивов опухоли после проведенного лечения, в ранние сроки после тиреоидэктомии, до гистологической верификации диагноза. 1 ил., 6 табл., 2 пр.
Способ прогнозирования инвазии опухоли в капсулу при папиллярном раке щитовидной железы путем проведения исследования опухолевых биологических маркеров в ткани пациента, характеризующийся тем, что выделяют РНК и определяют экспрессию 4Е-ВР1, учитывают данные о размере опухоли и данные о метастатическом поражении регионарных лимфатических узлов до гистологического исследования, далее рассчитывают регрессионную функцию F по формуле
F=-1,350367+-0,00972X1+1,007675X2-0,35654X3-0,033X4,
где:
-1,350367 - значение коэффициента регрессии свободного члена;
X1 - возраст пациента на момент хирургического лечения, лет;
-0,00972 - значение коэффициента регрессии этого признака;
Х2 - размер опухоли, при этом, при размере опухоли до 1 см в наибольшем измерении, ограниченной тканью щитовидной железы Х2=1;
при размере опухоли от 1 до 4 см в наибольшем измерении, ограниченной тканью щитовидной железы Х2=2;
при размере опухоли более 4 см в наибольшем измерении, ограниченной тканью щитовидной железы Х2=3;
при опухоли любого размера, распространяющейся за пределы капсулы щитовидной железы Х2=4;
1,007675 - значение коэффициента регрессии этого признака;
Х3 - распространенность процесса, при этом, при отсутствии признаков метастатического поражения регионарных лимфатических узлов Х3=0;
при наличии поражения метастазами регионарных лимфатических узлов Х3=1;
0,35654 - значение коэффициента регрессии этого признака;
Х4 - экспрессия 4Е-ВР1, усл. ед.;
0,033 - значение коэффициента регрессии этого признака;
затем рассчитывают вероятность прорастания опухоли в капсулу щитовидной железы Р по формуле
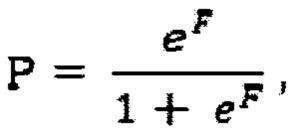
где е = 2,718,
и при Р менее 0,04 оценивают низкий, а при Р более 0,041 высокий риск прорастания капсулы.
| СПОСОБ ДООПЕРАЦИОННОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ДОБРОКАЧЕСТВЕННЫХ И ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2614700C1 |
| СПОСОБ ДИАГНОСТИКИ ВЫСОКОДИФФЕРЕНЦИРОВАННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2546011C1 |
| Прибор для очинки карандашей | 1927 |
|
SU8194A1 |
| БУТОЛИНА К.М | |||
| и др | |||
| Иммуногистохимическая оценка риска лимфогенного метастазирования папиллярного рака щитовидной железы// Журнал Гродненского государственного медицинского университета, 2018, Т.16 (6), С | |||
| Приспособление в лесопильной раме для автоматического изменения подачи с изменением толщины бревна | 1923 |
|
SU661A1 |
| HAN R | |||
| et al | |||
| Identification of a Signature | |||
Авторы
Даты
2022-10-04—Публикация
2022-01-19—Подача