Изобретение относится к области аналитической химии и касается способа определения содержания клавулановой кислоты в мышечных тканях животного происхождения: мышечных тканях крупного рогатого скота (КРС). Сущность способа заключается в извлечении анализируемого соединения из объекта исследования раствором ацетонитрила в деионизованной воде, подкисленным муравьиной кислотой, с последующей очисткой экстрактов на обращеннофазном сорбенте со слабыми анионообменными свойствами, фильтрацией и дальнейшим определением содержания клавулановой кислоты методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией (ВЭЖХ-МС/МС). Использование данного способа позволяет с высокой точностью количественно определить содержание клавулановой кислоты в мышечных тканях животного происхождения.
Изобретение относится к области аналитической химии и может быть использовано для контроля содержания остаточных количеств клавулановой кислоты в продукции животноводства.
Клавулановая кислота представляет собой бета-лактамное соединение, структурно родственное пенициллинам, на фиг. 1. Клавулановая кислота проявляет очень слабую антибактериальную активность, и поэтому не может использоваться в качестве самостоятельного антибиотика. Однако, она является мощным ингибитором β-лактамазы S. aureus и β-лактамаз, опосредованных плазмидами, вырабатываемых грамм-отрицательными бактериями [1].
В ветеринарии применяют клавулановую кислоту в сочетании с амоксициллином или ампициллином, относя данные комбинированные препараты к отдельному классу антибиотиков - аминопенициллины и бета-лактамазный ингибитор [2]. В последнее десятилетие проводятся успешные доклинические исследования совместного применения клавулановой кислоты с мециллинамом [3].
В РФ и РБ зарегистрировано 11 ветеринарных препаратов: комбинаций амоксициллина и клавулановой кислоты [4, 5]. К факторам бесконтрольного применения на территории Российской Федерации препарата типа «амоксиклав» относится то, что данная комбинация веществ зарегистрирована в реестре ветеринарных препаратов как препараты свободного отпуска: не подлежащие ограничению в применении через надзор ветеринарных врачей [4]. Пенициллиновые антибиотики и входящий в них класс «аминопенициллины и бета-лактамазный ингибитор» являются критически важными ветеринарными препаратами. Расчетный расход пенициллиновых антибиотиков на производство биомассы сельскохозяйственных животных на 2007 год в странах ЕС составил 20 мг/кг. Данное значение в общей доли потребления антибиотиков странами ЕС соответствует доли от 10% до 80% [6]. Максимально допустимые уровни остаточного содержания клавулановой кислоты в продукции животноводства следующие: мясо, жир - не более 0,1 мг/кг, печень, почки, молоко - не более 0,2/0,4/0,2 мг/кг, соответственно.
Описаны способы определения клавулановой кислоты в различных объектах исследования. Разделение и формирование хроматографического пика в них осуществляют на хроматографических колонках с обращенно-фазным сорбентом С8 и С18. Встречаются исследования с применением спектрометрического детектора в ультрафиолетовой области [7], в том числе и в молоке [8]. Масс-спектрометрическому детектированию посвящены работы последних 15 лет [9-16].
Наиболее близкий по назначению, является способ определения клавулановой кислоты в тканях свинины методом жидкостной хроматографии с тандемной масс-спектрометрией [17], Извлечение клавулановой кислоты проводят в течение 15 с. в ходе гомогенизации 1 г образца с 7 см3 фосфатного буфера и последующей экстракцией на встряхивателе, в течение 20 мин. Слои разделяют центрифугированием, а аликвоту супернатанта отбирают для стадии очистки ультрафильтрацией, с отсечением молекул с массой больше 30 кДа. После стадии ультрафильтрации, фильтрат пропускают через насадочный фильтр с порами 0,2 мкм в флакон для хроматографа и анализируют методом ВЭЖХ-МС/МС.
1. Недостаток способа-прототипа состоит в том, что извлечение клавулановой кислоты из объекта исследования проводят с помощью фосфатного буфера, без применения дополнительной стадии очистки от его компонентов, что может приводить к загрязнению источника ионов масс-спектрометра.
2. Недостатком способа-прототипа является применение узкоспециализированных устройств ультрафильтрации (Amicon Microcon® YM-30), граница отсечения которых (30 кДа) является недостаточной для получения чистых фильтратов, и приводит к нарастающему снижению чувствительности средства измерения.
3. Недостатком способа-прототипа является отсутствие описания работоспособности подхода на образцах говядины и других представителей КРС.
Настоящее изобретение направлено на устранение недостатков прототипа, а именно, на замену вида экстрагента и введение стадии твердофазной очистки (ТФО) с селективным к клавулановой кислоте сорбентом с анионообменными свойствами, взамен ультрафильтрации, предусмотрены возможности работы с образцами говядины.
Патентуемый способ количественного определения клавулановой кислоты в мышечных тканях животного происхождения включает: извлечение анализируемого соединения из образца смесью деионизованной воды, ацетонитрила, подкисленной муравьиной кислотой; стадию твердофазной очистки на обращеннофазном сорбенте со слабыми анионо-обменными свойствами, с последующей фильтрацией сквозь насадочный фильтр в флакон хроматографа и анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией.
Способ отличается от прототипа следующими признаками. В качестве экстрагента клавулановой кислоты, применяют смесь деионизованной воды, ацетонитрила и муравьиной кислоты, в соотношении 90/9,5/0,5. Проводят процедуру ТФО, на картридже с обращеннофазным сорбентом со слабыми анионо-обменными свойствами марки Oasis WAX Waters (60 мг, 3 см3), пропусканием экстракта сквозь слой сорбента и последующей промывкой 1 см3 смеси ацетонитрила и деионизованной воды, в соотношении 1/1, элюированием клавулановой кислоты в новую пробирку с помощью 1 см3 смеси ацетонитрила с деонизованной водой и муравьиной кислотой в соотношении 49,75/49,75/0,5, соответсвенно, с последующей фильтрацией и анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией.
Технический результат изобретения - возможность количественного определения клавулановой кислоты без применения узкоспециализированных расходных материалов для процедуры ультрафильтрации, повышение относительной интенсивности сигнала средства измерения за счет снижения шумов от применения этапа ТФО.
Патентуемый способ позволяет, увеличить извлечение определяемого соединения из объектов исследования относительно прототипа, увеличить аналитический отклик сигнала детектора масс-спектрометра по клавулановой кислоте, а также получать экстракты, дополнительно очищенные от примесей буфера.
Заявленный технический результат достигается за счет того, что при осуществлении способа в качестве экстрагента применяют смесь деионизованной воды, ацетонитрила и муравьиной кислоты, в соотношении 90/9,5/0,5, а процедуру тфердофазной очистки, проводят на картридже с обращеннофазным сорбентом марки Oasis WAX Waters (60 мг, 3 см3), с дополнительной стадией промывки 1 см3 смеси ацетонитрила и деионизованной воды, в соотношении 1/1, и элюированием клавулановой кислоты с помощью 1 см3 смеси ацетонитрила с деонизованной водой и муравьиной кислотой в соотношении 49,75/49,75/0,5, с последующей фильтрацией перед анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией.
Рекомендуемые режимы выполнения способа подобраны в результате экспериментов, проведенных заявителем: исследована зависимость полноты извлечения определяемого соединения и относительной интенсивности сигнала на детекторе масс-спектрометра от типа экстрагента; исследована возможность перехода от стадии ультрафильтрации к стадии ТФО, при различных условиях проведения ТФО на различных типах сорбентов.
Перед проведением экспериментов, в гомогенаты мышечной ткани КРС, вводили эквивалентное количество клавулановой кислоты. Процедура подготовки образцов к анализу, при оценке зависимости полноты извлечения определяемых соединений и относительной интенсивности сигнала на детекторе масс-спектрометра от типа экстрагента, соответствовала прототипу. В эксперименте варьировался тип экстрагента. За эталон принимали холостой образец, прошедший процедуру пробоподготовки согласно прототипу, с введением в него определяемого компонента перед анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией.
Было установлено, что в результате смены экстрагента, увеличивается полнота извлечения компонента на 23,4% из образцов мышечной ткани. Зависимость степени извлечения от типа экстрагента отображена графически на фиг. 2 и в табл. 1.
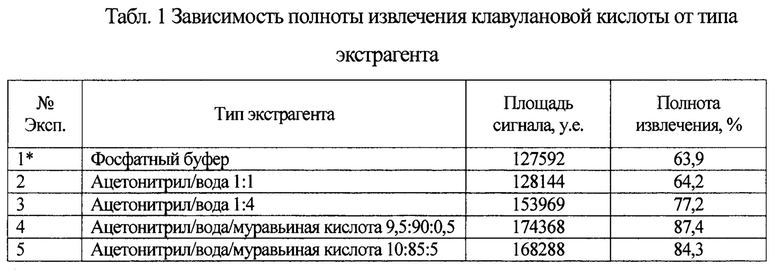

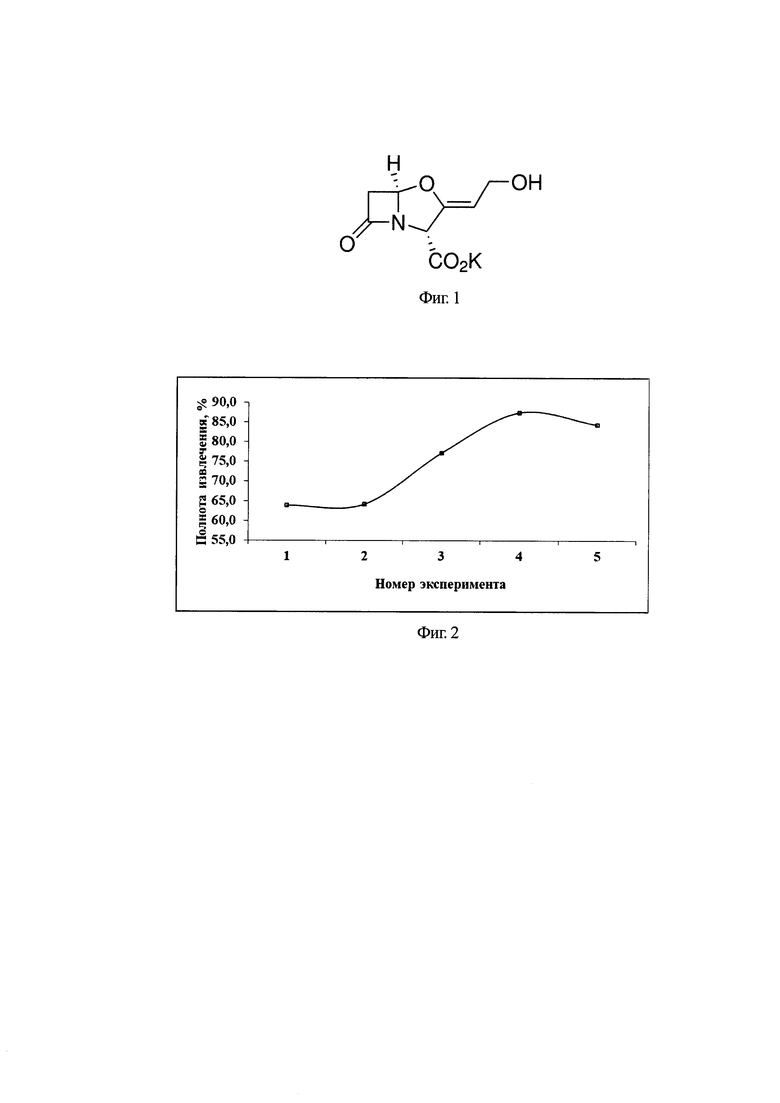
Согласно полученным данным можно заключить, что оптимальным экстрагентом является смесь Ацетонитрил/вода/муравьиная кислота в соотношении 9,5:90:0,5, соответственно. Что соответствует опыту №4 (Табл. 1). Сравнение масс-хроматограммы клавулановой кислоты полученной по прототипу с масс-хроматограммой, полученной в результате эксперимента №4, представлено на фиг. 3.
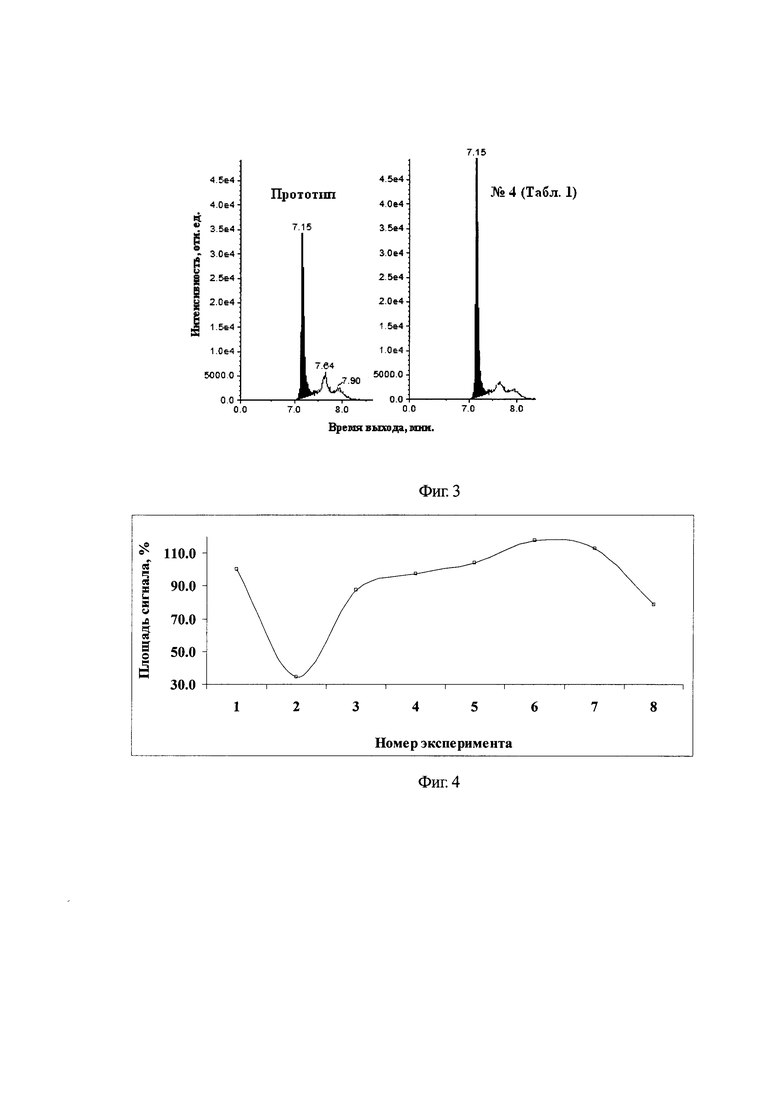
Было установлено, что при замене процедуры очистки экстракта, с улырафилырафии (Amicon Microcon® YM-30) на ТФО с обращеннофазным сорбентом со слабыми анионо-обменными свойствами марки Oasis WAX Waters (60 мг, 3 см3), увеличивается относительный отклик сигнала детектора по клавулановой кислоте до 17-18%, относительно прототипа. Зависимость отклика сигнала детектора от способа очистки экстракта выражена в % от прототипа и отображена графически в табл. 2 и на фиг. 4.
При проведении экспериментов, варьировали, способ очистки экстрактов (ультрафильтрация/ТФО) и способы промывки экстрактов на стадии ТФО. Эксперименты проводили на экстрактах гомогенатов мышечной ткани, полученных по опыту №4 (Табл. 1) в которые вводили эквивалентное количество клавулановой кислоты, перед стадией очистки. За промывочный объем стадии ТФО принимали 1 см3 раствора, указанного в табл. 2. После стадии промывки, анализируемый компонент элюировали в приемный флакон 1 см3 смеси ацетонитрила с деонизованной водой и муравьиной кислотой в соотношении 49,75/49,75/0,5 и анализировали. За эталонное значение принимали результат, полученный с применение стадии ультрафилырации на Amicon Microcon® YM-30.

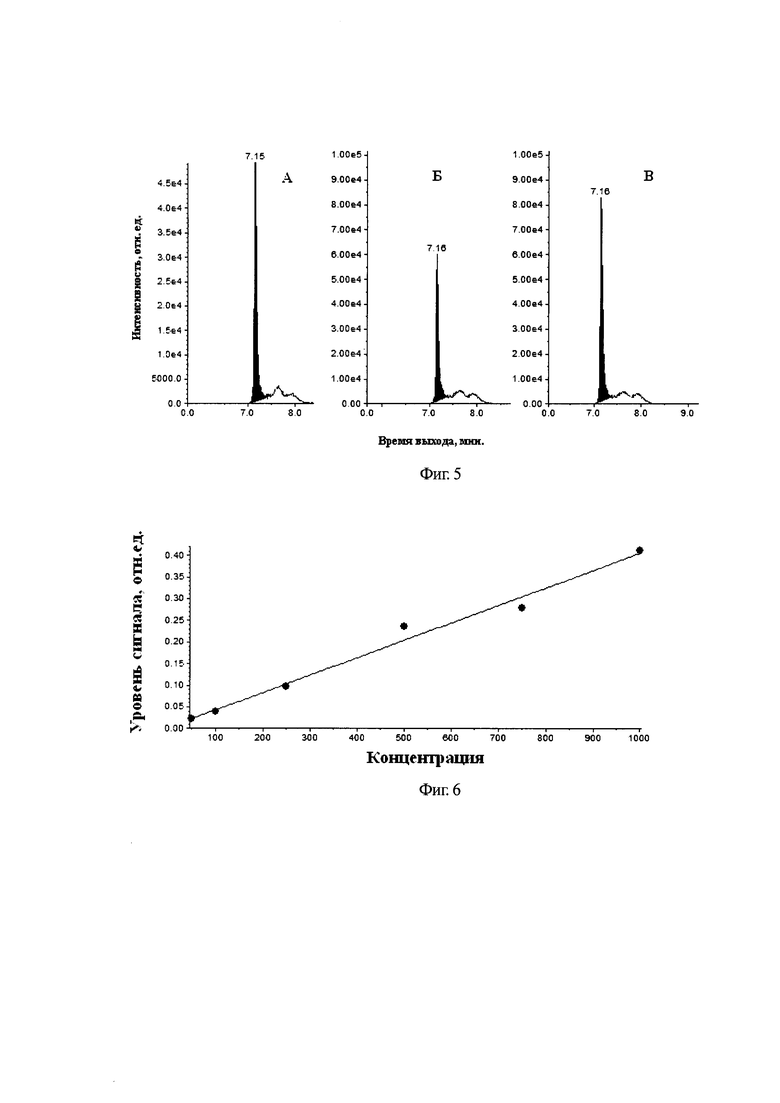
Согласно полученным данным, можно заключить, что оптимальным способом очистки, является ТФО, а протоколом ее проведения - дополнительная промывка смесью ацетонитрил/деионизованная вода в соотношении 1:1, что соответствует опыту №6 (Табл. 2). Введение дополнительной очистки позволяет добиться значительного увеличения сигнала детектора масс-спектрометра. На Фиг. 5 изображена разница относительных интенсивностей сигналов детектора масс-спектрометра между клавулановой кислотой, прошедшей ультрафильтрацию - «А», ТФО на Oasis WAX Waters (60 мг, 3 см3) с минимальным протоколом очистки - «Б», ТФО на Oasis WAX Waters (60 мг, 3 см3) с расширенным протоколом очистки - «В».
Было установлено, что при применении новых протоколов экстракции и ТФО на Oasis WAX Waters (60 мг, 3 см3) с расширенным протоколом очистки значительно повышает аналитический отклик детектора масс-спектрометра при определении клавулановой кислоты в мышечных тканях КРС и позволяет проводить полноценный количественный анализ данного соединения. Пример градуировочной зависимости клавулановой кислоты, полученный в соответствии с патентуемым способом представлен на фиг. 6.
Список литературы
1. Clavulanic acid - Режим доступа: https://www.chemicalbook.com/ChemicalProductProperty_EN_CB9722501.htm
2. OIE list of antimicrobial agents of veterinary importance - Режим доступа: https://www.oie.int/fileadmin/Home/eng/Our_scientific_expertise/docs/pdf/AMR/ A_OIE_List_antimicrobials_May2018.pdf
3. Birgy A. et al. //Journal of Antimicrobial Chemotherapy. 2017. V. 72, I. 7. P. 1911-1914.
4. Реестр ветеринарных препаратов Российской Федерации. - Режим доступа: https://galen.vetrf.ru/#/registry/pharm/registry?page=l&f_chemicalName=%D0%BA%D0%BB%D0%B0%D0%B2%D1%83%D0%BB%D0%B0%D0%BD%D0%BE%D0%B2%D0%B0%D1%8F%20%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D 1%82%D0%B0
5. Реестр ветеринарных препаратов Республики Беларусь. - Режим доступа: http://www.dvpn.gov.by/uploads/download/vp%2020_10.htm
6. Всемирная организация здравоохранения. Европейское региональное бюро. 2011. Борьба с устойчивостью к антибиотикам с позиций безопасности пищевых продуктов в Европе. - Режим доступа: https://www.euro.who.int/__data/assets/pdf_file/0011/144695/e94889R.pdf
7. Foroutan S.M. at al. // Journal of Pharmaceutical and Biomedical Analysis. 2007. V. 45. Issue 3. P. 531-534.
8. Guo P. et al. // Food Additives & Contaminants. 2017. DOI: 10.1080/19440049.2016.1277271.
9. Baldzsi J. et al. // Studia Universitatis Babes-Bolyai Chemia. 2017. DOI: 10.24193/subbchem.2017.2.12.
10. Yoona R.-H. et al. //Journal of Chromatography B. 2004. 813. P. 121-127
11. Parijatha B. et al. // World journal of pharmacy and pharmaceutical sciences. 2017. V. 6, Issue 1, P. 1540-1554.
12. DubalaA. et al. //Journal of Chromatographic Science. 2015. 53. P. 694-701.
13. Bhandarkar, D. et al. //ASMS. 2015. TP 280. Shimadzu Analytical (India) Pvt.Ltd.
14. Ramanatham V.S., Venkateswarlu, P.A. // Indo American Journal of Pharmaceutical Research. 2017:7(12).
15. Chaitanya Krishna, A. et al. // International Journal of Pharmacy and Pharmaceutical Sciences. 2012. V. 4. Suppl. 3.
16. Ciric, B. et al. // Vojnosanit Pregl. 2010. 67(11). P. 887-892.
17. Reyns, T. et al. //Analytica Chimica Acta 597. 2007. P. 282-289
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГЛИФОСАТА, ЕГО МЕТАБОЛИТА И ГЛЮФОСИНАТА В ПРОДУКЦИИ ЖИВОТНОВОДСТВА | 2021 |
|
RU2783283C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСТАТОЧНЫХ КОЛИЧЕСТВ ТРИФЕНИЛМЕТАНОВЫХ КРАСИТЕЛЕЙ В МЫШЕЧНОЙ ТКАНИ РЫБ | 2015 |
|
RU2578974C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСТАТОЧНЫХ КОЛИЧЕСТВ АВИЛАМИЦИНА В БИОЛОГИЧЕСКИХ ТКАНЯХ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ | 2021 |
|
RU2783284C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ДИМЕТИЛТЕРЕФТАЛАТА В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2010 |
|
RU2425380C1 |
| Способ подготовки пробы мочи для определения монометилфталата, моноэтилфталата, монобутилфталата, монобензилфталата, моноэтилгексилфталата методом высокоэффективной жидкостной хроматографии/масс-спектрометрии | 2019 |
|
RU2687738C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ Н-БУТИЛОВОГО ЭФИРА 2-[4-(5-ТРИФТОРМЕТИЛПИРИДИЛ-2-ОКСИ)ФЕНОКСИ]ПРОПИОНОВОЙ КИСЛОТЫ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2005 |
|
RU2287812C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2011 |
|
RU2466406C1 |
| Способ определения суммарного содержания оловоорганических соединений в природных водах | 2022 |
|
RU2791423C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФТАЛЕВОЙ КИСЛОТЫ В СЫВОРОТКЕ КРОВИ | 2006 |
|
RU2324185C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСТАТОЧНЫХ КОЛИЧЕСТВ ПИПЕРАЗИНА В БИОЛОГИЧЕСКИХ ТКАНЯХ И ОБЪЕКТАХ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ | 2024 |
|
RU2837303C1 |
Изобретение относится к области аналитической химии и может быть использовано для контроля содержания остаточных количеств клавулановой кислоты в продукции животноводства. Способ количественного определения содержания клавулановой кислоты в мышечных тканях животного происхождения (в частности, в мышечных тканях крупного рогатого скота) включает извлечение анализируемого соединения из образца раствором ацетонитрила в деионизованной воде, подкисленной муравьиной кислотой, с последующей стадией твердофазной очистки (ТФО) на обращенно-фазном сорбенте со слабыми анионо-обменными свойствами и последующей фильтрацией перед анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией. При этом извлечение анализируемого соединения из образца осуществляют смесью деионизованной воды и ацетонитрила, подкисленной муравьиной кислотой, в соотношении 90/9,5/0,5. Процедуру ТФО проводят на картридже с обращенно-фазным сорбентом марки Oasis WAX Waters (60 мг, 3 см3), с дополнительной стадией промывки 1 см3 смеси ацетонитрила и деионизованной воды, в соотношении 1/1, и элюированием клавулановой кислоты с помощью 1 см3 смеси ацетонитрила с деонизованной водой и муравьиной кислотой в соотношении 49,75/49,75/0,5, с последующей фильтрацией перед анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией. Использование способа позволяет увеличить извлечение определяемого соединения из объектов исследования, обеспечивает повышение относительной интенсивности сигнала средства измерения за счет снижения шумов при применении этапа ТФО, что значительно повышает аналитический отклик детектора масс-спектрометра при определении клавулановой кислоты в мышечных тканях животного происхождения и позволяет проводить полноценный количественный анализ данного соединения. 2 табл., 6 ил.
Способ количественного определения клавулановой кислоты в мышечных тканях животного происхождения, включающий извлечение анализируемого соединения из образца раствором ацетонитрила в деионизованной воде, подкисленной муравьиной кислотой, с последующей стадией твердофазной очистки на обращенно-фазном сорбенте со слабыми анионо-обменными свойствами и последующей фильтрацией перед анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией, отличающийся тем, что в качестве экстрагента применяют смесь деионизованной воды, ацетонитрила и муравьиной кислоты, в соотношении 90/9,5/0,5, а процедуру твердофазной очистки проводят на картридже с обращенно-фазным сорбентом марки Oasis WAX Waters (60 мг, 3 см3), с дополнительной стадией промывки 1 см3 смеси ацетонитрила и деионизованной воды, в соотношении 1/1, и элюированием клавулановой кислоты с помощью 1 см3 смеси ацетонитрила с деонизованной водой и муравьиной кислотой в соотношении 49,75/49,75/0,5, с последующей фильтрацией перед анализом методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией.
| REYNS T | |||
| et al | |||
| Quantitative analysis of clavulanic acid in porcine tissues by liquid chromatography combined with electrospray ionization tandem mass spectrometry | |||
| Analytica Chimica Acta, 2007, V | |||
| ПРИБОР ДЛЯ КОНТРОЛЯ ВРЕМЕНИ ПРИХОДА И УХОДА НА РАБОТУ | 1921 |
|
SU597A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ПОРШНЕВОЙ ДВИГАТЕЛЬ | 1916 |
|
SU282A1 |
| Найдено в PubMed PMID: 17683740, doi:10.1016/j.aca.2007.06.056 | |||
| ПАРОПЕРЕГРЕВАТЕЛЬ ДЛЯ ЛОКОМОБИЛЬНЫХ КОТЛОВ | 1912 |
|
SU277A1 |
| RU | |||
Авторы
Даты
2022-10-12—Публикация
2021-12-20—Подача