ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает преимущество по предварительной заявке на патент США № 62/677850, поданной 30 мая 2018 г., содержание которой включено в данный документ посредством ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ
В настоящем изобретении предусмотрены антитела или их антигенсвязывающие фрагменты, например, моноклональные антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эктоферментом эктонуклеозидтрифосфатдифосфогидролазой 2 (ENTPD2), и способы применения этих антител или антигенсвязывающих фрагментов.
Настоящее изобретение также относится к видам комбинированной терапии, предусматривающим антитело к ENTPD2 человека или его антигенсвязывающий фрагмент и по меньшей мере одно дополнительное терапевтическое средство.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и включен в данный документ посредством ссылки во всей своей полноте. Указанная копия в формате ASCII, созданная 5 апреля 2019 г., имеет название PAT058145-WO-PCT_SL.txt, и ее размер составляет 635873 байта.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Клеточный стресс и апоптоз инициируют высвобождение ATP во внеклеточное пространство. Увеличение концентрации ATP содействует быстрому развитию воспаления, что приводит к усилению передачи сигнала в T-клетках, ингибированию регуляторных T-клеток (Treg) и содействию активации инфламмасом в дендритных клетках и макрофагах. Эктофермент эктонуклеозидтрифосфатдифосфогидролаза 2 (ENTPD2) является членом семейства эктонуклеозидаз, которые гидролизуют 5'-трифосфаты, и представляет собой интегральный мембранный белок, который участвует в пуринергической передаче сигнала. ENTPD2 катализирует превращение аденозинтрифосфата (ATP) в аденозиндифосфат (ADP) и аденозинмонофосфат (AMP). В свою очередь, превращение AMP в аденозин катализируется кластером дифференцировки 73 (CD73), также известным как экто-5'-нуклеотидаза (экто-5'-NT). Молекула AMP взаимодействует с несколькими рецепторами, в том числе аденозиновыми рецепторами A1, A2A, A2B и A3. Рецептор A2A получил особое внимание ввиду его обширной экспрессии на иммунных клетках. AMP характеризуется плейотропными эффектами в микроокружении опухоли, включающими размножение регуляторных Т-клеток (Treg), ингибирование ответов с участием эффекторных Т-клеток (Teff), опосредованных интерфероном (IFN)-γ, и размножение супрессорных клеток миелоидного происхождения (MDSC). См., например, Allard B, et al., Curr Opin Pharmacol 29:7-16 (2016) и Allard D, et al., Immunotherapy 8:145-163 (2016).
В мышиной модели гепатоцеллюлярной карциномы было показано, что ENTPD2 обеспечивает превращение внеклеточного ATP в AMP, который предотвращает дифференцировку моноцитарных супрессорных клеток миелоидного происхождения (MDSC) в дендритные клетки, содействуя таким образом поддержанию численности MDSC in vitro и in vivo (Chiu et al., Nat Commun. 8:517-28 (2017).
ENTPD2 экспрессируется на раковых клетках, как описано в данном документе. Новые композиции и способы для регуляции активности ENTPD2 и соответствующие терапевтические средства являются весьма желательными.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе предусмотрены антитела или их антигенсвязывающие фрагменты, например, моноклональные антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эктоферментом эктонуклеозидтрифосфатдифосфогидролазой 2 (ENTPD2). Антитела к ENTPD2 или их антигенсвязывающие фрагменты применимы для лечения заболеваний, ассоциированных с ENTPD2, таких как рак.
В одном аспекте в данном документе предусмотрены антитела или их антигенсвязывающие фрагменты, которые специфично связываются с белком ENTPD2 человека, где антитело или его антигенсвязывающий фрагмент содержат область 1, определяющую комплементарность, тяжелой цепи (HCDR1), область 2, определяющую комплементарность, тяжелой цепи (HCDR2), область 3, определяющую комплементарность, тяжелой цепи (HCDR3), область 1, определяющую комплементарность, легкой цепи (LCDR1), область 2, определяющую комплементарность, легкой цепи (LCDR2) и область 3, определяющую комплементарность, легкой цепи (LCDR3) из любого антитела или антигенсвязывающего фрагмента, приведенных в таблице 1. В некоторых вариантах осуществления HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3 из таких антител или антигенсвязывающих фрагментов выбраны из последовательностей HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, приведенных в таблице 1. В некоторых вариантах осуществления такие антитела или антигенсвязывающие фрагменты содержат вариабельную область тяжелой цепи (VH), приведенную в таблице 1. В некоторых вариантах осуществления такие антитела или антигенсвязывающие фрагменты содержат вариабельную область легкой цепи (VL), приведенную в таблице 1.
В другом аспекте в данном документе предусмотрены антитела или антигенсвязывающие фрагменты, выбранные из любого из следующих:
1) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 1,
последовательность HCDR2, содержащую SEQ ID NO: 2,
последовательность HCDR3, содержащую SEQ ID NO: 3,
последовательность LCDR1, содержащую SEQ ID NO: 14,
последовательность LCDR2, содержащую SEQ ID NO: 15, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
2) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 4,
последовательность HCDR2, содержащую SEQ ID NO: 5,
последовательность HCDR3, содержащую SEQ ID NO: 3,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 19;
3) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 7,
последовательность HCDR2, содержащую SEQ ID NO: 8,
последовательность HCDR3, содержащую SEQ ID NO: 9,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
4) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 38,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 50,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
5) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 41,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 53,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
6) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 44,
последовательность HCDR3, содержащую SEQ ID NO: 45,
последовательность LCDR1, содержащую SEQ ID NO: 56,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
7) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 38,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 61,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
8) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 41,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 62,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
9) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 44,
последовательность HCDR3, содержащую SEQ ID NO: 45,
последовательность LCDR1, содержащую SEQ ID NO: 63,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
10) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 38,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 50,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
11) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 41,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 53,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
12) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 44,
последовательность HCDR3, содержащую SEQ ID NO: 69,
последовательность LCDR1, содержащую SEQ ID NO: 56,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
13) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 82,
последовательность HCDR2, содержащую SEQ ID NO: 83,
последовательность HCDR3, содержащую SEQ ID NO: 84,
последовательность LCDR1, содержащую SEQ ID NO: 95,
последовательность LCDR2, содержащую SEQ ID NO: 96, и
последовательность LCDR3, содержащую SEQ ID NO: 97;
14) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 85,
последовательность HCDR2, содержащую SEQ ID NO: 86,
последовательность HCDR3, содержащую SEQ ID NO: 84,
последовательность LCDR1, содержащую SEQ ID NO: 98,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 100;
15) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 88,
последовательность HCDR2, содержащую SEQ ID NO: 89,
последовательность HCDR3, содержащую SEQ ID NO: 90,
последовательность LCDR1, содержащую SEQ ID NO: 101,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 97;
16) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 106,
последовательность HCDR2, содержащую SEQ ID NO: 107,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 119,
последовательность LCDR2, содержащую SEQ ID NO: 120, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
17) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 109,
последовательность HCDR2, содержащую SEQ ID NO: 110,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 122,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 123;
18) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 112,
последовательность HCDR2, содержащую SEQ ID NO: 113,
последовательность HCDR3, содержащую SEQ ID NO: 114,
последовательность LCDR1, содержащую SEQ ID NO: 124,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
19) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 106,
последовательность HCDR2, содержащую SEQ ID NO: 129,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 119,
последовательность LCDR2, содержащую SEQ ID NO: 120, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
20) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 109,
последовательность HCDR2, содержащую SEQ ID NO: 130,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 122,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 123;
21) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 112,
последовательность HCDR2, содержащую SEQ ID NO: 131,
последовательность HCDR3, содержащую SEQ ID NO: 114,
последовательность LCDR1, содержащую SEQ ID NO: 124,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
22) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 136,
последовательность HCDR2, содержащую SEQ ID NO: 137,
последовательность HCDR3, содержащую SEQ ID NO: 138,
последовательность LCDR1, содержащую SEQ ID NO: 149,
последовательность LCDR2, содержащую SEQ ID NO: 150, и
последовательность LCDR3, содержащую SEQ ID NO: 151;
23) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 139,
последовательность HCDR2, содержащую SEQ ID NO: 140,
последовательность HCDR3, содержащую SEQ ID NO: 138,
последовательность LCDR1, содержащую SEQ ID NO: 152,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 154;
24) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 142,
последовательность HCDR2, содержащую SEQ ID NO: 143,
последовательность HCDR3, содержащую SEQ ID NO: 144,
последовательность LCDR1, содержащую SEQ ID NO: 155,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 151;
25) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 160,
последовательность HCDR2, содержащую SEQ ID NO: 161,
последовательность HCDR3, содержащую SEQ ID NO: 162,
последовательность LCDR1, содержащую SEQ ID NO: 173,
последовательность LCDR2, содержащую SEQ ID NO: 150, и
последовательность LCDR3, содержащую SEQ ID NO: 174;
26) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 163,
последовательность HCDR2, содержащую SEQ ID NO: 164,
последовательность HCDR3, содержащую SEQ ID NO: 162,
последовательность LCDR1, содержащую SEQ ID NO: 175,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 176;
27) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 166,
последовательность HCDR2, содержащую SEQ ID NO: 167,
последовательность HCDR3, содержащую SEQ ID NO: 168,
последовательность LCDR1, содержащую SEQ ID NO: 177,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 174;
28) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 220,
последовательность HCDR3, содержащую SEQ ID NO: 221,
последовательность LCDR1, содержащую SEQ ID NO: 61,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
29) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 222,
последовательность HCDR3, содержащую SEQ ID NO: 221,
последовательность LCDR1, содержащую SEQ ID NO: 62,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
30) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 223,
последовательность HCDR3, содержащую SEQ ID NO: 224,
последовательность LCDR1, содержащую SEQ ID NO: 63,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
31) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 220,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 61,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
32) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 222,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 62,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
33) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 223,
последовательность HCDR3, содержащую SEQ ID NO: 69,
последовательность LCDR1, содержащую SEQ ID NO: 63,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
34) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 1,
последовательность HCDR2, содержащую SEQ ID NO: 245,
последовательность HCDR3, содержащую SEQ ID NO: 246,
последовательность LCDR1, содержащую SEQ ID NO: 254,
последовательность LCDR2, содержащую SEQ ID NO: 15, и
последовательность LCDR3, содержащую SEQ ID NO: 255;
35) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 4,
последовательность HCDR2, содержащую SEQ ID NO: 247,
последовательность HCDR3, содержащую SEQ ID NO: 246,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 256;
36) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 7,
последовательность HCDR2, содержащую SEQ ID NO: 248,
последовательность HCDR3, содержащую SEQ ID NO: 249,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 255;
37) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 1,
последовательность HCDR2, содержащую SEQ ID NO: 261,
последовательность HCDR3, содержащую SEQ ID NO: 262,
последовательность LCDR1, содержащую SEQ ID NO: 254,
последовательность LCDR2, содержащую SEQ ID NO: 15, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
38) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 4,
последовательность HCDR2, содержащую SEQ ID NO: 247,
последовательность HCDR3, содержащую SEQ ID NO: 262,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 19;
39) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 7,
последовательность HCDR2, содержащую SEQ ID NO: 248,
последовательность HCDR3, содержащую SEQ ID NO: 263,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
40) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 272,
последовательность HCDR2, содержащую SEQ ID NO: 273,
последовательность HCDR3, содержащую SEQ ID NO: 274,
последовательность LCDR1, содержащую SEQ ID NO: 254,
последовательность LCDR2, содержащую SEQ ID NO: 285, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
41) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 275,
последовательность HCDR2, содержащую SEQ ID NO: 276,
последовательность HCDR3, содержащую SEQ ID NO: 274,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 286, и
последовательность LCDR3, содержащую SEQ ID NO: 19;
42) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 278,
последовательность HCDR2, содержащую SEQ ID NO: 279,
последовательность HCDR3, содержащую SEQ ID NO: 280,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 286, и
последовательность LCDR3, содержащую SEQ ID NO: 16.
В другом аспекте в данном документе предусмотрены антитела или антигенсвязывающие фрагменты, выбранные из любого из следующих:
1) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 10 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 21 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
2) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 25 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 29 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
3) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 33 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 29 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
4) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 46 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 57 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
5) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 46 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 64 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
6) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 70 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 74 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
7) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 25 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 78 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
8) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 91 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 102 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
9) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 115 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 125 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
10) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 132 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 125 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
11) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 145 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 156 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
12) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 169 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 178 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
13) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 225 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 229 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
14) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 233 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 237 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
15) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 241 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 229 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
16) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 250 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 257 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
17) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 264 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 268 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей; или
18) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 281 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 287 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей.
В другом аспекте в данном документе предусмотрены антитела или антигенсвязывающие фрагменты, выбранные из любого из следующих:
1) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 12 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 23 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
2) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 27 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 31 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
3) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 35 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 31 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
4) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 48 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 59 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
5) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 48 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 66 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
6) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 72 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 76 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
7) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 27 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 80 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
8) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 93 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 104 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
9) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 117 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 127 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
10) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 134 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 127 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
11) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 147 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 158 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
12) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 171 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 180 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
13) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 227 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 231 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
14) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 235 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 239 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
15) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 243 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 231 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
16) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 252 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 259 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
17) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 266 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 270 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей; или
18) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 283 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 289 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей.
В данном документе также предусмотрены антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эпитопом в ENTPD2 человека, где эпитоп содержит по меньшей мере один (например, по меньшей мере два, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять, по меньшей мере шесть, по меньшей мере семь, по меньшей мере восемь, по меньшей мере девять, по меньшей мере десять, по меньшей мере одиннадцать, по меньшей мере двенадцать, по меньшей мере тринадцать, по меньшей мере четырнадцать, по меньшей мере пятнадцать, по меньшей мере двадцать) из следующих остатков: His50, Asp76, Pro78, Gly79, Gly80, Tyr85, Asp87, Asn88, Gly91, Gln94, Ser95, Gly98, Glu101, Gln102, Gln105, Asp106, Arg245, Thr272, Gln273, Leu275, Asp278, Arg298, Ala347, Ala350, Thr351, Arg392, Ala393, Arg394 или Tyr398.
В данном документе также предусмотрены антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эпитопом в ENTPD2 человека, где эпитоп содержит по меньшей мере один (например, по меньшей мере два, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять, по меньшей мере шесть, по меньшей мере семь, по меньшей мере восемь, по меньшей мере девять, по меньшей мере десять, по меньшей мере одиннадцать, по меньшей мере двенадцать, по меньшей мере тринадцать, по меньшей мере четырнадцать, по меньшей мере пятнадцать, по меньшей мере двадцать) из следующих остатков: Gly79, Gln250, Leu253, Trp266, Arg268, Gly269, Phe270, Ser271, Thr272, Gln273, Val274, Leu275, Asp278, Arg298, Ser300, Ser302, Gly303, Thr380, Trp381, Ala382, Gly390, Gln391, Arg392, Ala393, Arg394 или Asp397.
В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, относятся к изотипу IgG1, IgG2, IgG3 или IgG4. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, относятся к изотипу IgG1. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, содержат Fc-область, выбранную из Fc-области IgG1, Fc-области IgG2, Fc-области IgG4 или гибридной Fc-области IgG2/IgG4 . В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, содержат Fc-область, выбранную из Fc-области IgG1. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, содержат модифицированную Fc-область. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, содержат модифицированную Fc-область, характеризующуюся сниженной активностью антителозависимой клеточной цитотоксичности (ADCC) или комплементзависимой цитотоксичности (CDC) по сравнению с исходным антителом.
В другом аспекте в данном документе предусмотрены антитела или их антигенсвязывающие фрагменты, которые конкурируют с любым антителом или антигенсвязывающим фрагментом, приведенными в таблице 1, за связывание с белком ENTPD2 человека.
В другом аспекте в данном документе предусмотрены антитела или их антигенсвязывающие фрагменты, которые связываются по сути с тем же эпитопом ENTPD2, что и любое антитело или антигенсвязывающий фрагмент, приведенные в таблице 1.
В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, связываются с белком ENTPD2 человека с константой диссоциации (KD), составляющей менее 10 нМ, например, с KD, составляющей менее 5 нМ, или с KD, составляющей менее 3 нМ, например, согласно измерению с помощью Biacore. В некоторых вариантах осуществления константу диссоциации антител или их антигенсвязывающих фрагментов, описанных в данном документе, для ENTPD2 человека измеряют с помощью Biacore при 25ºC.
В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, ингибируют ферментативную активность ENTPD2 человека на по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90%. В некоторых вариантах осуществления ферментативную активность ENTPD2 человека измеряют с помощью анализа FRET in vitro, в котором измеряется гидролиз ATP до ADP под действием рекомбинантного ENTPD2 либо ENTPD2, экспрессирующегося на поверхности клеток.
В некоторых вариантах осуществления антитела к ENTPD2 человека или их антигенсвязывающие фрагменты, описанные в данном документе, ингибируют способность ENTPD2 к гидролизу аденозинтрифосфата (ATP). В некоторых вариантах осуществления способность ENTPD2 к гидролизу ATP измеряют с помощью анализа FRET in vitro, в котором измеряется гидролиз ATP до ADP под действием рекомбинантного ENTPD2 либо ENTPD2, экспрессирующегося на поверхности клеток.
В некоторых вариантах осуществления антитела к ENTPD2 человека или их антигенсвязывающие фрагменты, описанные в данном документе, препятствуют связыванию ATP с ENTPD2 или удерживают ATP в каталитическом домене ENTPD2. В некоторых вариантах осуществления способность ENTPD2 к гидролизу ATP измеряют с помощью анализа FRET in vitro, в котором измеряется гидролиз ATP до ADP под действием рекомбинантного ENTPD2 либо ENTPD2, экспрессирующегося на поверхности клеток.
В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, описанные в данном документе, представляют собой человеческие или гуманизированные антитела или их фрагменты.
В другом аспекте в данном документе предусмотрены нуклеиновые кислоты, кодирующие антитело к ENTPD2 человека или его антигенсвязывающий фрагмент, описанные в данном документе. Такие нуклеиновые кислоты могут кодировать полипептиды, содержащие сегменты или домены антител к ENTPD2 или их антигенсвязывающих фрагментов, описанных в данном документе.
Также предусмотрены векторы, содержащие такие нуклеиновые кислоты, кодирующие антитело к ENTPD2 человека или его антигенсвязывающий фрагмент, описанные в данном документе. В некоторых вариантах осуществления вектор выбран из ДНК-вектора, РНК-вектора, плазмиды, космиды или вирусного вектора. В некоторых вариантах осуществления вектор представляет собой вирусный вектор на основе любого из следующих вирусов: лентивируса, аденовируса, аденоассоциированного вируса (AAV), вируса простого герпеса (HSV), парвовируса, ретровируса, вируса осповакцины, вируса Синдбис, вируса гриппа, реовируса, вируса ньюкаслской болезни (NDV), вируса кори, вируса везикулярного стоматита (VSV), полиовируса, поксвируса, вируса Сенека-Валли, вируса Коксаки, энтеровируса, вируса миксомы или вируса Мараба. В некоторых вариантах осуществления вектор представляет собой вектор на основе AAV. В некоторых вариантах осуществления вектор представляет собой лентивирусный вектор. В некоторых вариантах осуществления вектор дополнительно содержит промотор, например, тканеспецифичный промотор. В некоторых вариантах осуществления вектор дополнительно содержит выявляемый маркер.
Также в данном документе предусмотрены клетки, содержащие нуклеиновую кислоту или набор нуклеиновых кислот, кодирующие антитело к ENTPD2 человека или его антигенсвязывающий фрагмент, описанные в данном документе, или вектор, содержащий такие нуклеиновую кислоту или набор нуклеиновых кислот.
В другом аспекте в данном документе предусмотрены фармацевтические композиции, содержащие антитело к ENTPD2 человека или его антигенсвязывающий фрагмент, описанные в данном документе, нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, вектор, содержащий такие нуклеиновую кислоту или набор нуклеиновых кислот, или клетку, содержащую нуклеиновую кислоту или наборы нуклеиновых кислот или вектор, описанные в данном документе, и фармацевтически приемлемый носитель.
В другом аспекте в данном документе предусмотрены способы получения антитела к ENTPD2 человека или его антигенсвязывающего фрагмента путем культивирования клетки, содержащей нуклеиновую кислоту или наборы нуклеиновых кислот, кодирующие антитело к ENTPD2 человека или его антигенсвязывающий фрагмент, или вектор, содержащий такие нуклеиновую кислоту или наборы нуклеиновых кислот, и сбор антитела или его антигенсвязывающего фрагмента из культуральной среды.
В другом аспекте в данном документе предусмотрены способы лечения рака у субъекта, нуждающегося в этом, путем введения субъекту терапевтически эффективного количества антитела к ENTPD2 человека или антигенсвязывающего фрагмента, описанного в данном документе, нуклеиновой кислоты или наборов нуклеиновых кислот, кодирующих такие антитело или антигенсвязывающий фрагмент, вектора, содержащего нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, клетки, содержащей такие нуклеиновую кислоту или наборы нуклеиновых кислот или вектор, или фармацевтической композиции, содержащей такие антитело или антигенсвязывающий фрагмент, нуклеиновую кислоту или наборы нуклеиновых кислот, вектор или клетку. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, нуклеиновую кислоту или наборы нуклеиновых кислот, вектор, клетку или фармацевтическую композицию вводят субъекту посредством внутривенного, внутриопухолевого или подкожного путей.
В другом аспекте в данном документе предусмотрены способы стимуляции иммунного ответа у субъекта путем введения субъекту антитела к ENTPD2 человека или антигенсвязывающего фрагмента, описанного в данном документе, нуклеиновой кислоты или наборов нуклеиновых кислот, кодирующих такие антитело или антигенсвязывающий фрагмент, вектора, содержащего нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, клетки, содержащей такие нуклеиновую кислоту или наборы нуклеиновых кислот или вектор, или фармацевтической композиции, содержащей такие антитело или антигенсвязывающий фрагмент, нуклеиновую кислоту или наборы нуклеиновых кислот, вектор или клетку, в количестве, эффективном для стимуляции иммунного ответа.
В некоторых вариантах осуществления такие способы могут дополнительно включать введение субъекту по меньшей мере одного дополнительного терапевтического средства.
В некоторых вариантах осуществления такие способы могут дополнительно включать введение субъекту по меньшей мере двух дополнительных терапевтических средств.
В другом аспекте в данном документе предусмотрены антитело или его антигенсвязывающий фрагмент, описанные в данном документе, нуклеиновая кислота или набор нуклеиновых кислот, кодирующие такие антитело или его антигенсвязывающий фрагмент, вектор или клетка, содержащие такие нуклеиновую кислоту или набор нуклеиновых кислот, или фармацевтическая композиция, содержащая такие антитело или его антигенсвязывающий фрагмент, нуклеиновую кислоту или набор нуклеиновых кислот, вектор или клетку, для применения в качестве лекарственного препарата.
В другом аспекте в данном документе предусмотрены антитело или его антигенсвязывающий фрагмент, описанные в данном документе, нуклеиновая кислота, кодирующая такие антитело или его антигенсвязывающий фрагмент, вектор или клетка, содержащие такие нуклеиновую кислоту или набор нуклеиновых кислот, или фармацевтическая композиция, содержащая такие антитело или его антигенсвязывающий фрагмент, нуклеиновую кислоту или набор нуклеиновых кислот, вектор или клетку, для применения в лечении рака.
В другом аспекте в данном документе предусмотрены фармацевтическая композиция, содержащая антитело или его антигенсвязывающий фрагмент, описанные в данном документе, и по меньшей мере одно дополнительное терапевтическое средство или процедура.
В некоторых вариантах осуществления по меньшей мере одно дополнительное терапевтическое средство или процедура выбраны из одного или нескольких из химиотерапии, таргетной противораковой терапии, онколитического лекарственного средства, цитотоксического средства, иммунотерапии, цитокина, хирургической процедуры, процедуры облучения, активатора костимулирующей молекулы, ингибитора ингибирующей молекулы, вакцины или клеточной терапии.
В некоторых вариантах осуществления по меньшей мере одно дополнительное терапевтическое средство является ингибитором PD-1, например, антителом к PD-1. В некоторых вариантах осуществления ингибитор PD-1 выбран из PDR001, ниволумаба, пембролизумаба, пидилизумаба, MEDI0680, REGN2810, TSR-042, PF-06801591 или AMP-224.
В некоторых вариантах осуществления по меньшей мере одно дополнительное терапевтическое средство является ингибитором PD-L1, например, антителом к PD-L1. В некоторых вариантах осуществления ингибитор PD-L1 выбран из FAZ053, атезолизумаба, авелумаба, дурвалумаба или BMS-936559.
В некоторых вариантах осуществления по меньшей мере одно дополнительное терапевтическое средство является антагонистом A2AR. В некоторых вариантах осуществления антагонист A2AR выбран из:
i. молекулы антитела к CD73 или ее антигенсвязывающего фрагмента, где антитело к CD73 необязательно выбрано из:
a. молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 295, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 296, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 295 или 296;
b. молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 299, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 300, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 299 или 300;
c. молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 302, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 303, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 302 или 303;
d. молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 304, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 305, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 304 или 305;
e. молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 306, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 307, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 306 или 307; или
f. молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 308, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 309, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 308 или 309; или
ii. PBF509/NIR178, CPI444/V81444, AZD4635/HTL-1071, випаденанта, GBV-2034, AB928, теофиллина, истрадефиллина, тозаденанта/SYN-115, KW-6356, ST-4206 и преладенанта/SCH-420814; или
iii. 5-бром-2,6-ди-(1H-пиразол-1-ил)пиримидин-4-амина или его фармацевтически приемлемой соли; (S)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амина или его фармацевтически приемлемой соли; (R)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амина, или его рацемата, или его фармацевтически приемлемой соли; 7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амина или его фармацевтически приемлемой соли и 6-(2-хлор-6-метилпиридин-4-ил)-5-(4-фторфенил)-1,2,4-триазин-3-амина или его фармацевтически приемлемой соли.
В некоторых вариантах осуществления по меньшей мере одно дополнительное терапевтическое средство выбрано из:
i. ингибитора CTLA-4, где ингибитор CTLA-4 необязательно выбран из ипилимумаба или тремелимумаба;
ii. ингибитора TIM-3, где ингибитор TIM-3 необязательно выбран из MBG453, TSR-022 или LY3321367;
iii. ингибитора LAG-3, где ингибитор LAG-3 необязательно выбран из LAG525, BMS-986016, TSR-033, MK-4280 или REGN3767;
iv. агониста GITR, где агонист GITR необязательно выбран из GWN323, BMS-986156, MK-4166, MK-1248, TRX518, INCAGN1876, AMG 228 или INBRX-110;
v. молекулы полиспецифического антитела к CD3, где молекула полиспецифического антитела к CD3 необязательно представляет собой молекулу биспецифического антитела к CD3 и CD123 (например, XENP14045) или молекулу биспецифического антитела к CD3 и CD20 (например, XENP13676);
vi. молекулы цитокина, где молекула цитокина необязательно представляет собой IL-15 в комплексе с растворимой формой альфа-субъединицы рецептора IL-15 (IL-15Ra);
vii. ингибитора макрофагального колониестимулирующего фактора (M-CSF), где ингибитор M-CSF необязательно представляет собой MCS110;
viii. ингибитора CSF-1R, где ингибитор CSF-1R необязательно представляет собой BLZ945;
ix. ингибитора индоламин-2,3-диоксигеназы (IDO) и/или триптофан-2,3-диоксигеназы (TDO);
x. ингибитора TGF-β;
xi. онколитического вируса;
xii. средства терапии на основе T-клеток с химерным антигенным рецептором (CAR).
В некоторых вариантах осуществления по меньшей мере одно дополнительное терапевтическое средство выбрано из: 1) ингибитора протеинкиназы C (PKC); 2) ингибитора белка теплового шока 90 (HSP90); 3) ингибитора фосфоинозитид-3-киназы (PI3K) и/или мишени рапамицина (mTOR); 4) ингибитора цитохрома P450 (например, ингибитора CYP17 или ингибитора 17-альфа-гидроксилазы/C17-20-лиазы); 5) железохелатирующего средства; 6) ингибитора ароматазы; 7) ингибитора р53, например, ингибитора взаимодействия р53/Mdm2; 8) индуктора апоптоза; 9) ингибитора ангиогенеза; 10) ингибитора альдостеронсинтазы; 11) ингибитора рецептора Smoothened (SMO); 12) ингибитора рецептора пролактина (PRLR); 13) ингибитора сигнального пути Wnt; 14) ингибитора CDK4/6; 15) ингибитора рецептора 2 фактора роста фибробластов (FGFR2)/рецептора 4 фактора роста фибробластов (FGFR4); 16) ингибитора макрофагального колониестимулирующего фактора (M-CSF); 17) ингибитора одного или нескольких из c-KIT, высвобождения гистамина, Flt3 (например, FLK2/STK1) или PKC; 18) ингибитора одного или нескольких из VEGFR-2 (например, FLK-1/KDR), PDGFR-бета, c-KIT или Raf-киназы C; 19) агониста соматостатина и/или ингибитора высвобождения гормона роста; 20) ингибитора киназы анапластической лимфомы (ALK); 21) ингибитора рецептора инсулиноподобного фактора роста 1 (IGF-1R); 22) ингибитора P-гликопротеина 1; 23) ингибитора рецептора фактора роста эндотелия сосудов (VEGFR); 24) ингибитора киназы BCR-ABL; 25) ингибитора FGFR; 26) ингибитора CYP11B2; 27) ингибитора HDM2, например, ингибитора взаимодействия HDM2-p53; 28) ингибитора тирозинкиназы; 29) ингибитора c-MET; 30) ингибитора JAK; 31) ингибитора DAC; 32) ингибитора 11β-гидроксилазы; 33) ингибитора IAP; 34) ингибитора PIM-киназы; 35) ингибитора поркупина; 36) ингибитора BRAF, например, BRAF V600E или BRAF дикого типа; 37) ингибитора HER3; 38) ингибитора MEK; 39) ингибитора липидкиназы или одного или нескольких средств, приведенных в таблице 16.
В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент, нуклеиновую кислоту или набор нуклеиновых кислот, вектор, клетку или фармацевтическую композицию вводят параллельно с по меньшей мере одним дополнительным терапевтическим средством, до него или после него.
В некоторых вариантах осуществления введение антитела или антигенсвязывающего фрагмента, нуклеиновой кислоты или набора нуклеиновых кислот, вектора, клетки или фармацевтической композиции обеспечивает один или несколько из следующих эффектов:
(a) увеличение количества CD45+ CD4- CD8+ CD69+ CD25+ клеток в очаге опухоли или поражения у субъекта;
(b) увеличение количества CD45+ CD8- CD4+ FOXP3- CD69+ CD25+ клеток в очаге опухоли или поражения у субъекта;
(c) уменьшение уровня MCP1 или IL-1β в плазме крови субъекта или
(d) увеличение уровня MCP1 в очаге опухоли или поражения у субъекта.
В другом аспекте в данном документе предусмотрено применение антитела или его антигенсвязывающего фрагмента, описанных в данном документе, нуклеиновой кислоты, кодирующей такие антитело или его антигенсвязывающий фрагмент, вектора или клетки, содержащих такую нуклеиновую кислоту, или фармацевтической композиции, содержащей такие антитело или его антигенсвязывающий фрагмент, нуклеиновую кислоту, вектор или клетку, в изготовлении лекарственного препарата для лечения рака.
В другом аспекте в данном документе предусмотрены способы лечения рака у субъекта, нуждающегося в этом, при этом такой способ включает введение субъекту терапевтически эффективного количества антитела к ENTPD2 человека или антигенсвязывающего фрагмента, описанных в данном документе, в комбинации со вторым терапевтическим средством, выбранным из ингибитора PD-1 или ингибитора PD-L1.
В другом аспекте в данном документе предусмотрены способы стимуляции иммунного ответа у субъекта, при этом такой способ включает введение субъекту терапевтически эффективного количества антитела к ENTPD2 человека или антигенсвязывающего фрагмента, описанных в данном документе, в комбинации со вторым терапевтическим средством, выбранным из ингибитора PD-1 или ингибитора PD-L1.
В другом аспекте в данном документе предусмотрены композиции, содержащие антитело к ENTPD2 человека или антигенсвязывающий фрагмент, описанные в данном документе, для применения в комбинации со вторым терапевтическим средством, выбранным из ингибитора PD-1 или ингибитора PD-L1, в лечении рака у субъекта.
В другом аспекте в данном документе предусмотрены композиции, содержащие антитело к ENTPD2 человека или антигенсвязывающий фрагмент, описанные в данном документе, в комбинации со вторым терапевтическим средством, выбранным из ингибитора PD-1 или ингибитора PD-L1, для применения в лечении рака у субъекта.
В некоторых вариантах осуществления ингибитор PD-1 представляет собой антитело к PD-1. В некоторых вариантах осуществления ингибитор PD-1 выбран из PDR001, ниволумаба, пембролизумаба, пидилизумаба, MEDI0680, REGN2810, TSR-042, PF-06801591 или AMP-224.
В некоторых вариантах осуществления ингибитор PD-L1 представляет собой антитело к PD-L1. В некоторых вариантах осуществления ингибитор PD-L1 выбран из FAZ053, атезолизумаба, авелумаба, дурвалумаба или BMS-936559.
В некоторых вариантах осуществления рак представляет собой ENTPD2+ рак. В некоторых вариантах осуществления рак представляет собой рак ободочной и прямой кишки (CRC), рак желудка (например, аденокарциному желудка, карциному желудка), рак пищевода (например, плоскоклеточную карциному пищевода (ESCC)), рак легкого (например, мелкоклеточный рак легкого), рак молочной железы (например, аденокарциному молочной железы) или рак яичника.
Все публикации, патенты и номера доступа, упомянутые в данном документе, включены в данный документ посредством ссылки во всей своей полноте, как если бы каждая отдельная публикация или патент были конкретно и отдельно указаны как включенные посредством ссылки.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На фиг. 1A изображена экспрессия ENTPD2 в иллюстративных линиях раковых клеток, определенная с помощью проточной цитометрии. Фиг. 1B представляет собой таблицу (таблицу 20), в которой показана плотность рецепторов ENTPD2 в иллюстративных линиях раковых клеток.
На фиг. 2 изображены иллюстративные изображения IHC-окрашивания на ENTPD2 в фиксированных в формалине и залитых в парафин тканях первичных опухолей ободочной и прямой кишки, пищевода и яичника.
На фиг. 3A показаны аминокислотные последовательности тяжелой цепи (SEQ ID NO: 330) и легкой цепи (SEQ ID NO: 334) FAb22 антитела к ENTPD2 человека, при этом CDR подчеркнуты (согласно определению по Kabat), и остатки, расположенные в области контакта антитела и антигена, отмечены в каждом Fab как (*). На фиг. 3B показаны аминокислотные последовательности тяжелой цепи (SEQ ID NO: 336) и легкой цепи (SEQ ID NO: 239) FAb23 антитела к ENTPD2 человека, при этом CDR подчеркнуты (согласно определению по Kabat), и остатки, расположенные в области контакта антитела и антигена, отмечены как (*). На фиг. 3C показаны аминокислотные последовательности тяжелой цепи (SEQ ID NO: 338) и легкой цепи (SEQ ID NO: 340) FAb24 антитела к ENTPD2 мыши, при этом CDR подчеркнуты (согласно определению по Kabat), и остатки, расположенные в области контакта антитела и антигена, отмечены как (*).
На фиг. 4A показана аминокислотная последовательность рекомбинантного ENTPD2 человека (остатки 29-462, с мутацией Y350A), используемого в кристаллографических исследованиях (SEQ ID NO: 1014), при этом элементы вторичной структуры показаны ниже аминокислотной последовательности. Прямоугольниками представлены α-спирали, а стрелками представлены β-тяжи. Неотмеченные стрелки и прямоугольники, соответствующие разрывам при форматировании последовательности, являются смежными с предшествующими отмеченными структурными элементами. Неструктурированные области не указаны. Растворимый внеклеточный домен ENTPD2 человека охватывает остатки 29-462. В конструкции используются N-концевой пептид GP67, являющийся сигналом секреции (первые 38 остатков выделены серым цветом), с сайтом отщепления сигнального пептида после последнего остатка и C-концевая гексагистидиновая (SEQ ID NO: 1010) металлоаффинная метка для облегчения очистки. Asn129, Asn294, Asn378 и Asn443 представляют собой предсказанные сайты N-связанного гликозилирования, для которых наблюдается гликозилирование в кристаллических структурах и которые показаны курсивом. Asn64 также представляет собой предсказанный сайт N-связанного гликозилирования, не наблюдаемый в этих кристаллических структурах. Остатки, расположенные в области контакта антигена и Fab в комплексах FAb22 и FAb23, указаны соответственно символами (*) и (:) ниже аминокислотной последовательности. На фиг. 4B показана аминокислотная последовательность рекомбинантного ENTPD2 мыши (остатки 29-462), используемого в кристаллографических исследованиях (SEQ ID NO: 1015), при этом элементы вторичной структуры показаны ниже аминокислотной последовательности. Прямоугольниками представлены α-спирали, а стрелками представлены β-тяжи. Неотмеченные стрелки и прямоугольники, соответствующие разрывам строки, являются смежными с предшествующими отмеченными структурными элементами. Неструктурированные области не указаны. Зрелый ENTPD2 мыши начинается с Thr29. В конструкции используются N-концевой пептид GP67, являющийся сигналом секреции (остатки 1-38), с сайтом отщепления сигнального пептида после остатка 38 и C-концевая гексагистидиновая (SEQ ID NO: 1010) металлоаффинная метка для облегчения очистки. Asn129, Asn294, Asn378 и Asn443 представляют собой потенциальные сайты N-связанного гликозилирования, показанные курсивом. Остатки, расположенные в области контакта антигена и FAb24, указаны символом (#) под аминокислотной последовательностью.
На фиг. 5A показано графическое изображение кристаллической структуры апо-формы эктодомена ENTPD2 человека с показанными остатками 33-453. Две проекции повернуты друг к другу под углом в 90 градусов. Отмечены последовательные элементы вторичной структуры. Дисульфидные связи показаны квадратными скобками. Амино- и карбокси-концы отмечены как NT и CT соответственно. Мембранопроксимальная доля содержит как N-, так и C-конец (субдомен 1: Pro36-Ser161 и Lys427-Phe461) и заштрихована более темным цветом, чем мембранодистальная доля (субдомен 2: Gly162-Gln426). ATP-субстрат прочно связывается в междолевой щели. Местоположение ATP-связывающего участка проиллюстрировано на фиг. 5B. Показан аналог ATP AMP-PNP, наложенный на активный центр ENTPD2 человека, из коструктуры ENTPD2 крысы (PDB 3CJA).
На фиг. 6 проиллюстрирован общий вид FAb22 антитела к ENTPD2 человека в комплексе с ENTPD2 человека. Две проекции показаны на расстоянии в 90 градусов друг от друга. AMP-PNP смоделирован в активном центре ENTPD2 на основе наложения из коструктуры ENTPD2 крысы PDB 3CJA. Тяжелая цепь Fab заштрихована более темным цветом.
На фиг. 7 проиллюстрирован общий вид FAb23 антитела к ENTPD2 человека в комплексе с ENTPD2 человека. Две проекции показаны на расстоянии в 90 градусов друг от друга. AMP-PNP смоделирован в активном центре ENTPD2 на основе наложения из коструктуры ENTPD2 крысы PDB 3CJA. Тяжелая цепь Fab заштрихована более темным цветом.
На фиг. 8 проиллюстрирован общий вид FAb24 антитела к ENTPD2 мыши в комплексе с ENTPD2 мыши. AMP-PNP смоделирован в активном центре ENTPD2 на основе наложения из коструктуры ENTPD2 крысы PDB 3CJA. Тяжелая цепь Fab заштрихована более темным цветом.
Фиг. 9 представляет собой диаграмму, иллюстрирующую долговременную эффективность антитела mAb13 к ENTPD2 мыши в комбинации с Ab к PD-1 в сингенной модели опухоли из клеток B16LM3.
Фиг. 10A-10C представляют собой графики, иллюстрирующие эффективность антитела mAb13 к ENTPD2 мыши в комбинации с Ab к PD-1 в сингенной модели опухоли B16F10, связанную с увеличенным притоком активированных CD8+ и CD4+ T-клеток-хелперов в очаг опухоли в день 8 после обработки.
На фиг. 11A-11B изображено определение характеристик модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека, в которой иллюстрируется экспрессия ENTPD2 человека с помощью FACS in vitro и устойчивость экспрессии ENTPD2 человека в опухолях in vivo с помощью IHC с использованием Ab к CD39L1 человека от Novus (в разведении 1:40).
Фиг. 12A-12B представляют собой графики, иллюстрирующие дозозависимую эффективность антител mAb1 и mAb6 к ENTPD2 человека в комбинации с Ab к PD-1 в модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека.
Фиг. 13A-13B представляют собой точечные диаграммы, на которых показаны уровни IL-1b (фиг. 13A) и MCP-1 (фиг. 13B) в плазме крови после обработки с помощью антитела mAb1 к ENTPD2 человека или изотипического контроля в ксенотрансплантатной модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека, на мышах C57BL/6. Фиг. 13C-13D представляют собой точечные диаграммы, на которых показаны уровни IL-1β (фиг. 13C) и MCP-1 (фиг. 13D) в опухоли после обработки с помощью антитела mAb1 к ENTPD2 человека или изотипического контроля в ксенотрансплантатной модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека, на мышах C57BL/6.
Фиг. 14 представляет собой график, на котором показана эффективность антитела mAb1 к ENTPD2 в комбинации с антагонистом A2AR NIR178 in vivo в ксенотрансплантатной модели из клеток B16LM3, сконструированной для экспрессии ENTPD2 человека, на мышах C57BL/6.
Фиг. 15 представляет собой график, на котором показана иллюстративная активность Ab к ENTPD2 в биохимическом функциональном анализе ENTPD2 человека. Антитела mAb1, mAb17, mAb19 и mAb21 к ENTPD2 человека сильно ингибируют каталитическую активность рекомбинантного ENTPD2 человека.
На фиг. 16A-16B изображена иллюстративная активность Ab к ENTPD2 человека в функциональном анализе с использованием клеток NIH/3T3 или RKO, экспрессирующих ENTPD2 человека или макака-крабоеда.
На фиг. 17 изображен график, иллюстрирующий функциональную активность антител mAb13, mAb14, mAb15 к ENTPD2 мыши in vitro в функциональном анализе с использованием клеток NIH/3T3, экспрессирующих ENTPD2 мыши.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе предусмотрены антитела или их антигенсвязывающие фрагменты, например, моноклональные антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эктоферментом эктонуклеозидтрифосфатдифосфогидролазой 2 (например, белком ENTPD2 человека). Антитела к ENTPD2 или их антигенсвязывающие фрагменты применимы для лечения заболеваний, ассоциированных с ENTPD2, таких как рак.
Определения
Используемая в описании и формуле изобретения форма единственного числа включает ссылки на форму множественного числа, если контекст явно не указывает на иное. Например, термин "клетка" включает множество клеток, в том числе их смеси.
Во всем данном описании и нижеследующей формуле изобретения, если контекст не требует иного, слово "содержать" и его варианты, такие как "содержит" и "содержащий", используются в данном документе в их открытом и неограничивающем смысле, если не указано иное.
При использовании в данном документе "состоящий из" исключает любые элемент, стадию или ингредиент, не указанные в аспекте, варианте осуществления и/или элементе формулы изобретения. При использовании в данном документе "состоящий по сути из" не исключает материалы или стадии, которые существенно не влияют на основные и новые характеристики аспекта, варианта осуществления и/или пункта формулы изобретения.
В каждом случае в данном документе любой из терминов "содержащий", "состоящий по сути из" и "состоящий из" может быть заменен любым из других двух терминов.
Все числовые обозначения, например, pH, температура, время, концентрация и молекулярная масса, в том числе диапазоны, являются приближенными значениями, которые варьируются в сторону (+) или (-) с шагом 0,1. Следует понимать, хотя это не всегда указано в явной форме, что всем числовым обозначениям предшествует термин "приблизительно". Также следует понимать, хотя это не всегда указано в явной форме, что реагенты, описанные в данном документе, представляют собой лишь примеры и что соответствующие им эквиваленты известны из уровня техники.
Как используется в данном документе, эктонуклеозидтрифосфатдифосфогидролаза 2 (ENTPD2) (также известная как белок 1, подобный антигену CD39, CD39-подобный белок 1, CD39L1, экто-ATP-дифосфогидролаза 2, экто-ATPаза, экто-ATPаза 2, экто-ATPDаза 2, NTPDаза-2, NTPDаза 2) относится к ферменту типа 2 из семейства эктонуклеозидтрифосфатдифосфогидролаз (E-NTPDаз), которое представляет собой семейство эктонуклеозидаз, гидролизующих 5'-трифосфаты. Фермент ENTPD2 кодируется геном ENTPD2. Ген ENTPD2 человека картирован на хромосоме в местоположении 9q34.3, и геномную последовательность гена ENTPD2 человека можно найти в GenBank под номером NC_000009.12. Последовательности мРНК и белка для вариантов транскриптов ENTPD2 человека можно найти в GenBank под следующими №№ доступа:
Изоформа 1: NM_203468.2 (мРНК) → NP_982293.1 (белок с 495 аминокислотами)
Изоформа 2: NM_001246.3 (мРНК) → NP_001237.1 (белок с 472 аминокислотами)
Эктонуклеозидтрифосфатдифосфогидролаза 2, изоформа 1 [Homo sapiens, NP_982293.1]
MAGKVRSLLPPLLLAAAGLAGLLLLCVPTRDVREPPALKYGIVLDAGSSH TSMFIYKWPADKENDTGIVGQHSSCDVPGGGISSYADNPSGASQSLVGCL EQALQDVPKERHAGTPLYLGATAGMRLLNLTNPEASTSVLMAVTHTLTQY PFDFRGARILSGQEEGVFGWVTANYLLENFIKYGWVGRWFRPRKGTLGAM DLGGASTQITFETTSPAEDRASEVQLHLYGQHYRVYTHSFLCYGRDQVLQ RLLASALQTHGFHPCWPRGFSTQVLLGDVYQSPCTMAQRPQNFNSSARVS LSGSSDPHLCRDLVSGLFSFSSCPFSRCSFNGVFQPPVAGNFVAFSAFFY TVDFLRTSMGLPVATLQQLEAAAVNVCNQTWAQLQARVPGQRARLADYCA GAMFVQQLLSRGYGFDERAFGGVIFQKKAADTAVGWALGYMLNLTNLIPA DPPGLRKGTDFSSWVVLLLLFASALLAALVLLLRQVHSAKLPSTI (SEQ ID NO: 291)
Эктонуклеозидтрифосфатдифосфогидролаза 2 Homo sapiens (ENTPD2), вариант транскрипта 1, мРНК [NM_203468.2]
1 ggctccccgc actctccggg tccacgcatc gtcctcccgc gcgcccgccc gcccatggcc
61 gggaaggtgc ggtcactgct gccgccgctg ctgctggccg ccgcgggcct cgccggcctc
121 ctactgctgt gcgtccccac ccgcgacgtc cgggagccgc ccgccctcaa gtatggcatc
181 gtcctggacg ctggttcttc acacacgtcc atgtttatct acaagtggcc ggcagacaag
241 gagaacgaca caggcattgt gggccagcac agctcctgtg atgttccagg tgggggcatc
301 tccagctatg cagacaaccc ttctggggcc agccagagtc ttgttggatg cctcgaacag
361 gcgcttcagg atgtgcccaa agagagacac gcgggcacac ccctctacct gggagccaca
421 gcgggtatgc gcctgctcaa cctgaccaat ccagaggcct cgaccagtgt gctcatggca
481 gtgactcaca cactgaccca gtaccccttt gacttccggg gtgcacgcat cctctcgggc
541 caggaagagg gggtgtttgg ctgggtgact gccaactacc tgctggagaa cttcatcaag
601 tacggctggg tgggccggtg gttccggcca cggaagggga cactgggggc catggacctg
661 gggggtgcct ctacccagat cacttttgag acaaccagtc cagctgagga cagagccagc
721 gaggtccagc tgcatctcta cggccagcac taccgagtct acacccacag cttcctctgc
781 tatggccgtg accaggtcct ccagaggctg ctggccagcg ccctccagac ccacggcttc
841 cacccctgct ggccgagggg cttttccacc caagtgctgc tcggggatgt gtaccagtca
901 ccatgcacca tggcccagcg gccccagaac ttcaacagca gtgccagggt cagcctgtca
961 gggagcagtg acccccacct ctgccgagat ctggtttctg ggctcttcag cttctcctcc
1021 tgccccttct cccgatgctc tttcaatggg gtcttccagc ccccagtggc tgggaacttt
1081 gtggccttct ctgccttctt ctacactgtg gactttttgc ggacttcgat ggggctgccc
1141 gtggccaccc tgcagcagct ggaggcagcc gcagtgaatg tctgcaacca gacctgggct
1201 cagctgcaag ctcgggtgcc agggcaacgg gcccgcctgg ccgactactg cgccggggcc
1261 atgttcgtgc agcagctgct gagtcgcggc tacggcttcg acgagcgcgc cttcggcggc
1321 gtgatcttcc agaagaaggc cgcggacact gcagtgggct gggcgctcgg ctacatgctg
1381 aacctgacca acctgatccc cgccgacccg ccggggctgc gcaagggcac agacttcagc
1441 tcctgggtcg tcctcctgct gctcttcgcc tccgcgctcc tggctgcgct tgtcctgctg
1501 ctgcgtcagg tgcactccgc caagctgcca agcaccattt aggggccgac gggggcagct
1561 gccccatccc tcccccaacc cctgtatccc caccccgtac tcccacccct cccacaaccc
1621 ctgtacctcc cacccctgta tccccacccc tccacccacc cctctcccaa cctctctccc
1681 cgcccctgta tcctgcattc ctccacccac cctctatccc ccaccgctcc accccaccac
1741 tgtcttctcc atccttccac cccaccctca gcgtctctgc ccctaaggca gcccaggaaa
1801 taggaactga gactctggta cccacaggag cctgggtggg caaagagcgc tcaatccagc
1861 tccttgaacc cctccagccc gcttcagcct gggcatcact gcaggccccg tgctcctcct
1921 cctcctcctc agggctgggt ctccagagag tggggccttg gtcctgagaa tcagccctta
1981 gaggctcctt ctgtgtagtc tgggtctgta ctggggaggg tcacagccca cgggctggca
2041 gccagcccag cacctacttg taaaaatttt gtaataaaaa gtttttccta gagacgtgaa
2101 aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaa (SEQ ID NO: 292)
Эктонуклеозидтрифосфатдифосфогидролаза 2, изоформа 2 [Homo sapiens, NP_001237.1]
MAGKVRSLLPPLLLAAAGLAGLLLLCVPTRDVREPPALKYGIVLDAGSSH TSMFIYKWPADKENDTGIVGQHSSCDVPGGGISSYADNPSGASQSLVGCL EQALQDVPKERHAGTPLYLGATAGMRLLNLTNPEASTSVLMAVTHTLTQY PFDFRGARILSGQEEGVFGWVTANYLLENFIKYGWVGRWFRPRKGTLGAM DLGGASTQITFETTSPAEDRASEVQLHLYGQHYRVYTHSFLCYGRDQVLQ RLLASALQTHGFHPCWPRGFSTQVLLGDVYQSPCTMAQRPQNFNSSARVS LSGSSDPHLCRDLVSGLFSFSSCPFSRCSFNGVFQPPVAGNFVAFSAFFY TVDFLRTSMGLPVATLQQLEAAAVNVCNQTWAQQLLSRGYGFDERAFGGV IFQKKAADTAVGWALGYMLNLTNLIPADPPGLRKGTDFSSWVVLLLLFAS ALLAALVLLLRQVHSAKLPSTI (SEQ ID NO: 293)
Эктонуклеозидтрифосфатдифосфогидролаза 2 Homo sapiens (ENTPD2), вариант транскрипта 2, мРНК [NM_001246.3]
1 ggctccccgc actctccggg tccacgcatc gtcctcccgc gcgcccgccc gcccatggcc
61 gggaaggtgc ggtcactgct gccgccgctg ctgctggccg ccgcgggcct cgccggcctc
121 ctactgctgt gcgtccccac ccgcgacgtc cgggagccgc ccgccctcaa gtatggcatc
181 gtcctggacg ctggttcttc acacacgtcc atgtttatct acaagtggcc ggcagacaag
241 gagaacgaca caggcattgt gggccagcac agctcctgtg atgttccagg tgggggcatc
301 tccagctatg cagacaaccc ttctggggcc agccagagtc ttgttggatg cctcgaacag
361 gcgcttcagg atgtgcccaa agagagacac gcgggcacac ccctctacct gggagccaca
421 gcgggtatgc gcctgctcaa cctgaccaat ccagaggcct cgaccagtgt gctcatggca
481 gtgactcaca cactgaccca gtaccccttt gacttccggg gtgcacgcat cctctcgggc
541 caggaagagg gggtgtttgg ctgggtgact gccaactacc tgctggagaa cttcatcaag
601 tacggctggg tgggccggtg gttccggcca cggaagggga cactgggggc catggacctg
661 gggggtgcct ctacccagat cacttttgag acaaccagtc cagctgagga cagagccagc
721 gaggtccagc tgcatctcta cggccagcac taccgagtct acacccacag cttcctctgc
781 tatggccgtg accaggtcct ccagaggctg ctggccagcg ccctccagac ccacggcttc
841 cacccctgct ggccgagggg cttttccacc caagtgctgc tcggggatgt gtaccagtca
901 ccatgcacca tggcccagcg gccccagaac ttcaacagca gtgccagggt cagcctgtca
961 gggagcagtg acccccacct ctgccgagat ctggtttctg ggctcttcag cttctcctcc
1021 tgccccttct cccgatgctc tttcaatggg gtcttccagc ccccagtggc tgggaacttt
1081 gtggccttct ctgccttctt ctacactgtg gactttttgc ggacttcgat ggggctgccc
1141 gtggccaccc tgcagcagct ggaggcagcc gcagtgaatg tctgcaacca gacctgggct
1201 cagcagctgc tgagtcgcgg ctacggcttc gacgagcgcg ccttcggcgg cgtgatcttc
1261 cagaagaagg ccgcggacac tgcagtgggc tgggcgctcg gctacatgct gaacctgacc
1321 aacctgatcc ccgccgaccc gccggggctg cgcaagggca cagacttcag ctcctgggtc
1381 gtcctcctgc tgctcttcgc ctccgcgctc ctggctgcgc ttgtcctgct gctgcgtcag
1441 gtgcactccg ccaagctgcc aagcaccatt taggggccga cgggggcagc tgccccatcc
1501 ctcccccaac ccctgtatcc ccaccccgta ctcccacccc tcccacaacc cctgtacctc
1561 ccacccctgt atccccaccc ctccacccac ccctctccca acctctctcc ccgcccctgt
1621 atcctgcatt cctccaccca ccctctatcc cccaccgctc caccccacca ctgtcttctc
1681 catccttcca ccccaccctc agcgtctctg cccctaaggc agcccaggaa ataggaactg
1741 agactctggt acccacagga gcctgggtgg gcaaagagcg ctcaatccag ctccttgaac
1801 ccctccagcc cgcttcagcc tgggcatcac tgcaggcccc gtgctcctcc tcctcctcct
1861 cagggctggg tctccagaga gtggggcctt ggtcctgaga atcagccctt agaggctcct
1921 tctgtgtagt ctgggtctgt actggggagg gtcacagccc acgggctggc agccagccca
1981 gcacctactt gtaaaaattt tgtaataaaa agtttttcct agagacgtga aaaaaaaaaa
2041 aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaa (SEQ ID NO: 294)
Как используется в данном документе, белок ENTPD2 человека также охватывает белки, которые по всей своей длине характеризуются по меньшей мере приблизительно 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности с любой из изоформ ENTPD2. Последовательности белков ENTPD2 мыши, макака-крабоеда и других животных известны из уровня техники.
Используемый в данном документе термин "антитело" относится к последовательности белка или полипептида, полученной из молекулы иммуноглобулина, которая специфично связывается с антигеном. Антитела могут являться поликлональными или моноклональными, многоцепочечными или одноцепочечными или интактными иммуноглобулинами и могут быть получены из природных источников или из рекомбинантных источников. Например, встречающееся в природе антитело IgG может представлять собой гликопротеин, содержащий по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, соединенные между собой посредством дисульфидных связей. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенно обозначаемой в данном документе как VH) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов - CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно обозначаемой в данном документе как VL) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена - CL. VH- и VL-области могут быть дополнительно подразделены на области гипервариабельности, называемые областями, определяющими комплементарность (CDR), которые чередуются с более консервативными областями, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от амино-конца к карбоксильному концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, в том числе с различными клетками иммунной системы (например, эффекторными клетками) и первым компонентом (C1q) классического пути активации системы комплемента. Антитело может представлять собой моноклональное антитело, человеческое антитело, гуманизированное антитело, камелизированное антитело или химерное антитело. Антитела могут относиться к любому изотипу (например, IgG, IgE, IgM, IgD, IgA и IgY), классу (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подклассу.
Термин "фрагмент антитела" или "антигенсвязывающий фрагмент" относится к по меньшей мере одной части антитела, которая сохраняет способность специфично взаимодействовать (например, посредством связывания, стерического несоответствия, стабилизации/дестабилизации, пространственного распределения) с эпитопом антигена. Примеры фрагментов антител включают без ограничения Fab-, Fab'-, F(ab')2-, Fv-фрагменты, scFv-фрагменты антител, Fv, стабилизированные дисульфидными связями (sdFv), Fd-фрагмент, состоящий из VH- и CH1-доменов, линейные антитела, однодоменные антитела, такие как sdAb (либо VL, либо VH), VHH-домены верблюдовых, полиспецифические антитела, образованные из фрагментов антител, таких как бивалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области, и выделенную CDR или другие эпитопсвязывающие фрагменты антитела. Антигенсвязывающий фрагмент также может быть включен в состав однодоменных антител, максиантител, миниантител, нанотел, интрател, диател, триател, тетрател, v-NAR и бис-scFv (см., например, Hollinger and Hudson, Nature Biotechnology 23:1126-1136, 2005). Антигенсвязывающие фрагменты также могут быть привиты на остовы на основе полипептидов, таких как фибронектин III типа (Fn3) (см. патент США № 6703199, в котором описаны миниантитела на основе полипептида фибронектина). Термин "scFv" относится к слитому белку, который содержит по меньшей мере один фрагмент антитела, содержащий вариабельную область легкой цепи, и по меньшей мере один фрагмент антитела, содержащий вариабельную область тяжелой цепи, где вариабельные области легкой и тяжелой цепей непрерывно связаны друг с другом, например, посредством синтетического линкера, например, короткого гибкого полипептидного линкера, и способны экспрессироваться в виде одноцепочечного полипептида, и где scFv сохраняет специфичность интактного антитела, из которого он получен. Если не указано иное, то используемый в данном документе scFv может иметь вариабельные VL- и VH-области в любом порядке, например, относительно N-конца и С-конца полипептида scFv может содержать VL-линкер-VH или может содержать VH-линкер-VL.
Используемые в данном документе термины "область, определяющая комплементарность" или "CDR" относятся к последовательностям аминокислот в пределах вариабельных областей антитела, которые придают специфичность к антигену и аффинность связывания. Например, как правило, три CDR находятся в каждой вариабельной области тяжелой цепи (например, HCDR1, HCDR2 и HCDR3), и три CDR находятся в каждой вариабельной области легкой цепи (например, LCDR1, LCDR2 и LCDR3). Точные границы аминокислотной последовательности указанной CDR можно определить с помощью любой из ряда широко известных схем, в том числе описанных в Kabat et al. (1991), "Sequences of Proteins of Immunological Interest," 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (схема нумерации "по Kabat"), Al-Lazikani et al., (1997) JMB 273, 927-948 (схема нумерации "по Chothia") или их комбинации и схемы нумерации ImMunoGenTics (IMGT) (Lefranc, M.-P., The Immunologist, 7, 132-136 (1999); Lefranc, M.-P. et al., Dev. Comp. Immunol., 27, 55-77 (2003) (схема нумерации "IMGT"). Согласно комбинированной схеме нумерации по Kabat и Chothia для указанной CDR-области (например, CDR1 HC, CDR2 HC, CDR3 HC, CDR1 LC, CDR2 LC или CDR3 LC) в некоторых вариантах осуществления CDR соответствуют аминокислотным остаткам, которые определены как часть CDR по Kabat, вместе с аминокислотными остатками, которые определены как часть CDR по Chothia. Как используется в данном документе, CDR, определенные в соответствии со схемой нумерации "по Chothia", также иногда называют "гипервариабельными петлями".
Например, согласно Kabat аминокислотные остатки CDR в вариабельном домене тяжелой цепи (VH) нумеруются как 31-35 (HCDR1) (например, со вставкой(вставками) после положения 35), 50-65 (HCDR2) и 95-102 (HCDR3); и аминокислотные остатки CDR в вариабельном домене легкой цепи (VL) нумеруются как 24-34 (LCDR1) (например, со вставкой(вставками) после положения 27), 50-56 (LCDR2) и 89-97 (LCDR3). В качестве другого примера, согласно Chothia аминокислоты CDR в VH нумеруются как 26-32 (HCDR1) (например, со вставкой(вставками) после положения 31), 52-56 (HCDR2) и 95-102 (HCDR3); и аминокислотные остатки в VL нумеруются как 26-32 (LCDR1) (например, со вставкой(вставками) после положения 30), 50-52 (LCDR2) и 91-96 (LCDR3). При объединении определений CDR по Kabat и Chothia CDR содержат, например, аминокислотные остатки 26-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3) в человеческой VH и аминокислотные остатки 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3) в человеческой VL или состоят из них. Согласно IMGT аминокислотные остатки CDR в VH нумеруются как примерно 26-35 (CDR1), 51-57 (CDR2) и 93-102 (CDR3), и аминокислотные остатки CDR в VL нумеруются как примерно 27-32 (CDR1), 50-52 (CDR2) и 89-97 (CDR3) (нумерация "в соответствии с Kabat"). Согласно IMGT CDR-области антитела можно определять с помощью программы IMGT/DomainGap Align. Как правило, если конкретно не указано иное, молекулы антител могут содержать любую комбинацию из одной или нескольких CDR по Kabat и/или CDR по Chothia.
Термин "эпитоп" включает любую белковую детерминанту, способную специфично связываться с иммуноглобулином или иным образом взаимодействовать с молекулой. Эпитопные детерминанты обычно состоят из химически активных поверхностных групп молекул, таких как аминокислоты или углеводные или сахарные боковые цепи, и могут обладать специфическими характеристиками трехмерной структуры, а также специфическими характеристиками заряда. Эпитоп может быть "линейным" или "конформационным". Конформационные и линейные эпитопы отличаются тем, что связывание с первым, но не с последним, утрачивается в присутствии денатурирующих растворителей.
Термин "одновалентное антитело", используемый в данном документе, относится к антителу, которое связывается с одним эпитопом в молекуле-мишени.
Термин "двухвалентное антитело", используемый в данном документе, относится к антителу, которое связывается с двумя эпитопами в по меньшей мере двух идентичных молекулах-мишенях. Двухвалентное антитело может также перекрестно связывать молекулы-мишени друг с другом. "Двухвалентное антитело" также относится к антителу, которое связывается с двумя разными эпитопами в по меньшей мере двух идентичных молекулах-мишенях.
Термин "поливалентное антитело" относится к отдельной связывающей молекуле с "валентностью", превышающей единицу, где "валентность" описывается как количество антигенсвязывающих компонентов на молекулу конструкции антитела. Таким образом, отдельная связывающая молекула может связываться с более чем одним связывающим участком в молекуле-мишени. Примеры поливалентных антител включают без ограничения двухвалентные антитела, трехвалентные антитела, четырехвалентные антитела, пятивалентные антитела и т. п., равно как и биспецифические антитела и бипаратопные антитела. Например, в случае с ENTPD2 поливалентное антитело (например, бипаратопное антитело к ENTPD2) имеет связывающий компонент для двух доменов ENTPD2 соответственно.
Термин "поливалентное антитело" также относится к отдельной связывающей молекуле, которая имеет более одного антигенсвязывающего компонента для двух отдельных молекул-мишеней. Например, это относится к антителу, которое связывается с ENTPD2 (например, белком ENTPD2 человека) и второй молекулой-мишенью, отличной от ENTPD2. В одном варианте осуществления поливалентное антитело представляет собой четырехвалентное антитело, которое имеет четыре эпитопсвязывающих домена. Четырехвалентная молекула может быть биспецифической и двухвалентной для каждого связывающего участка в данной молекуле-мишени.
Термин "биспецифическое антитело", используемый в данном документе, относится к антителу, которое связывается с двумя или более разными эпитопами. В некоторых вариантах осуществления биспецифическое антитело связывается с двумя разными мишенями. В некоторых вариантах осуществления биспецифическое антитело связывается с двумя разными эпитопами в одной молекуле-мишени. Антитело, которое связывается с двумя разными эпитопами в одной молекуле-мишени, также известно как "бипаратопное антитело".
Фразы "моноклональное антитело" или "композиция на основе моноклональных антител", используемые в данном документе, относятся к полипептидам, в том числе антителам, биспецифическим антителам и т. д., которые имеют по существу идентичную аминокислотную последовательность или получены из одного и того же генетического источника. Данный термин также охватывает препараты на основе молекул антител одного молекулярного состава. Композиция на основе моноклональных антител проявляет один тип специфичности и аффинности связывания в отношении конкретного эпитопа.
Используемая в данном документе фраза "человеческое антитело" охватывает антитела, имеющие вариабельные области, в которых как каркасные области, так и CDR-области получены из последовательностей человеческого происхождения. Кроме того, если антитело содержит константную область, то константная область также получена из таких человеческих последовательностей, например, человеческих последовательностей зародышевого типа, или мутантных вариантов человеческих последовательностей зародышевого типа, или антитела, содержащего консенсусные последовательности каркасных областей, полученные в результате анализа последовательностей человеческих каркасных областей, например, как описано в Knappik, et al. (2000. J Mol Biol 296, 57-86). Структуры и местоположения вариабельных доменов иммуноглобулина, например, CDR, можно определить с помощью хорошо известных схем нумерации, например, схемы нумерации по Kabat, схемы нумерации по Chothia или комбинации схем нумерации по Kabat и Chothia и схемы нумерации ImMunoGenTics (IMGT) (см., например, Sequences of Proteins of Immunological Interest, U.S. Department of Health and Human Services (1991), eds. Kabat et al.; Al Lazikani et al., (1997) J. Mol. Bio. 273:927-948; Kabat et al., (1991) Sequences of Proteins of Immunological Interest, 5th edit., NIH Publication no. 91-3242 U.S. Department of Health and Human Services; Chothia et al., (1987) J. Mol. Biol. 196:901-917; Chothia et al., (1989) Nature 342:877-883; Al-Lazikani et al., (1997) J. Mal. Biol. 273:927-948 и Lefranc, M.-P., The Immunologist, 7, 132-136 (1999); Lefranc, M.-P. et al., Dev. Comp. Immunol., 27, 55-77 (2003)).
Человеческие антитела по настоящему изобретению могут содержать аминокислотные остатки, которые не закодированы в человеческих последовательностях (например, мутации, введенные посредством случайного или сайт-специфического мутагенеза in vitro или благодаря соматическим мутациям in vivo, или консервативную замену, которая содействует стабильности или изготовлению). Однако подразумевается, что используемый в данном документе термин "человеческое антитело" не включает антитела, в которых последовательности CDR, полученные из последовательностей зародышевого типа от другого вида млекопитающего, такого как мышь, были привиты на последовательности человеческих каркасных областей.
Фраза "рекомбинантное человеческое антитело", используемая в данном документе, включает все человеческие антитела, полученные, экспрессированные, созданные или выделенные посредством рекомбинантных способов, такие как антитела, выделенные из животного (например, мыши), которое является трансгенным или трансхромосомным по генам человеческих иммуноглобулинов, или гибридомы, полученной из него, антитела, выделенные из клетки-хозяина, трансформированной для экспрессии человеческого антитела, например, из трансфектомы, антитела, выделенные из рекомбинантной комбинаторной библиотеки человеческих антител, и антитела, полученные, экспрессированные, созданные или выделенные с помощью любых других способов, которые включают сплайсинг всех последовательностей гена человеческого иммуноглобулина или их части с получением других последовательностей ДНК. Такие рекомбинантные человеческие антитела имеют вариабельные области, в которых каркасные области и CDR-области получены из последовательностей человеческого иммуноглобулина зародышевого типа. Однако в определенных вариантах осуществления такие рекомбинантные человеческие антитела могут быть подвергнуты мутагенезу in vitro (или, в случае использования животного, трансгенного по последовательностям человеческого Ig, соматическому мутагенезу in vivo), и, таким образом, аминокислотные последовательности VH- и VL-областей рекомбинантных антител представляют собой последовательности, которые, хотя и получены из человеческих последовательностей VH и VL зародышевого типа и являются родственными им, могут не существовать в естественных условиях в репертуаре человеческих антител зародышевого типа in vivo.
Термин "Fc-область", используемый в данном документе, относится к полипептиду, содержащему CH3, CH2 и по меньшей мере часть шарнирной области константного домена антитела. Fc-область может необязательно содержать CH4-домен, присутствующий в некоторых классах антител. Fc-область может содержать всю шарнирную область константного домена антитела. В одном варианте осуществления в настоящем изобретении предусмотрены Fc-область и CH1-область антитела. В одном варианте осуществления в настоящем изобретении предусмотрена CH3-область Fc-области антитела. В другом варианте осуществления в настоящем изобретении предусмотрены Fc-область, CH1-область и C-каппа/лямбда-область константного домена антитела. В одном варианте осуществления связывающая молекула по настоящему изобретению содержит константную область, например, константную область тяжелой цепи. В одном варианте осуществления такая константная область является модифицированной по сравнению с константной областью дикого типа. Иными словами, полипептиды по настоящему изобретению, раскрытые в данном документе, могут содержать изменения или модификации одного или нескольких из трех константных доменов тяжелой цепи (CH1, CH2 или CH3) и/или домена константной области легкой цепи (CL). Примеры модификаций включают добавления, делеции или замены одной или нескольких аминокислот в одном или нескольких доменах. Такие изменения могут быть включены с целью оптимизации эффекторной функции, периода полужизни и т. д.
Используемый в данном документе термин "аффинность" относится к силе взаимодействия между антителом и антигеном в отдельных антигенных сайтах. В пределах каждого антигенного сайта вариабельная область "плеча" антитела взаимодействует с антигеном посредством слабых сил нековалентного взаимодействия во многих сайтах; при этом чем больше взаимодействий, тем сильнее аффинность. Используемый в данном документе термин "высокая аффинность" в отношении антитела IgG или его фрагмента (например, Fab-фрагмента) относится к антителу, характеризующемуся нокдауном антигена-мишени, составляющим 10-8 M или меньше, 10-9 M или меньше, или 10-10 M, или 10-11 M или меньше, или 10-12 M или меньше, или 10-13 M или меньше. Однако, высокоаффинное связывание может варьироваться в случае с другими изотипами антител. Например, высокоаффинное связывание для изотипа IgM относится к антителу, которое характеризуется нокдауном, составляющим 10-7 M или меньше или 10-8 M или меньше.
Используемый в данном документе термин "авидность" относится к информативной мере общей стабильности или прочности комплекса антитело-антиген. Она контролируется тремя основными факторами: аффинностью антитела к эпитопу; валентностью как антигена, так и антитела; а также структурным расположением взаимодействующих частей. В конечном итоге данные факторы определяют специфичность антитела, другими словами, вероятность того, что конкретное антитело свяжется с определенным антигенным эпитопом.
Термин "специфичность связывания", используемый в данном документе, относится к способности отдельного антигенсвязывающего центра антитела вступать в реакцию с одной антигенной детерминантой, а не с другой антигенной детерминантой. Антигенсвязывающий центр антитела располагается в Fab-части молекулы и сформирован из гипервариабельных областей тяжелой и легкой цепей. Аффинность связывания антитела представляет собой силу реакции между одной антигенной детерминантой и одним антигенсвязывающим центром антитела. Она представляет собой сумму сил притяжения и отталкивания, действующих между антигенной детерминантой и антигенсвязывающим центром антитела.
Термин "лечить" или "лечение" относится как к терапевтическому лечению, так и к профилактическим или предупредительным мерам, где целью является предупреждение или замедление нежелательного физиологического изменения или нарушения. Для целей настоящего изобретения благоприятные или необходимые клинические результаты включают без ограничения выявляемое или невыявляемое ослабление симптомов, уменьшение степени выраженности заболевания, стабилизацию (т. е. отсутствие ухудшения) состояния заболевания, задержку или замедление прогрессирования заболевания, облегчение или смягчение болезненного состояния и ремиссию (частичную либо полную). "Лечение" может также означать продление выживаемости по сравнению с ожидаемой выживаемостью при отсутствии получения лечения. В других вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к ингибированию прогрессирования пролиферативного нарушения физическим путем, например, посредством стабилизации различимого симптома, физиологическим путем, например, посредством стабилизации физического параметра, либо ими обоими. В других вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к снижению или стабилизации размера опухоли или количества раковых клеток.
Термин "субъект" относится к животному, являющемуся человеком или отличному от человека, для которого проводят лечение в соответствии со способами по настоящему изобретению. Предусматриваются ветеринарные и неветеринарные пути применения. Данный термин включает без ограничения млекопитающих, например, людей, других приматов, свиней, грызунов, таких как мыши и крысы, кроликов, морских свинок, хомяков, коров, лошадей, кошек, собак, овец и коз. Типичные субъекты включают людей, сельскохозяйственных животных и домашних питомцев, таких как кошки и собаки. В некоторых вариантах осуществления субъектом является человек.
"Эффективное количество" относится к количеству, достаточному для достижения благоприятных или необходимых результатов. Например, терапевтическое количество представляет собой такое количество, при котором достигается необходимый терапевтический эффект. Данное количество может быть таким же, как и профилактически эффективное количество, которое представляет собой количество, необходимое для предупреждения начала проявления заболевания или симптомов заболевания, или отличным от него. Эффективное количество можно вводить посредством одного или нескольких введений, применений или доз. "Терапевтически эффективное количество" терапевтического соединения (т. е. эффективная доза) зависит от выбранных терапевтических соединений. Композиции можно вводить с частотой от одного или нескольких раз в день до одного или нескольких раз в неделю. Специалист в данной области поймет, что на дозу и временные рамки, требуемые для эффективного лечения субъекта, могут влиять определенные факторы, в том числе без ограничения тяжесть заболевания или нарушения, предыдущие виды лечения, общее состояние здоровья и/или возраст субъекта и наличие других заболеваний. Более того, лечение субъекта терапевтически эффективным количеством терапевтических соединений, описанных в данном документе, может включать одну процедуру лечения или курс лечения.
Термин "нуклеиновая кислота" или "полинуклеотид" относится к дезоксирибонуклеиновым кислотам (ДНК) или рибонуклеиновым кислотам (РНК) и их полимерам в однонитевой или двухнитевой форме. Термин "набор нуклеиновых кислот" может, например, включать отдельные выделенные нуклеиновые кислоты, кодирующие легкую цепь и тяжелую цепь антитела или домены биспецифического или полиспецифического антитела. Если конкретно не ограничено, термин охватывает нуклеиновые кислоты, содержащие известные аналоги природных нуклеотидов, которые имеют свойства связывания, подобные свойствам эталонной нуклеиновой кислоты, и метаболизируются способом, подобным способу для встречающихся в природе нуклеотидов. Если не указано иное, конкретная последовательность нуклеиновой кислоты также в неявной форме охватывает ее варианты с консервативными модификациями (например, с заменами кодонов вырожденными кодонами), аллели, ортологи, SNP и комплементарные последовательности, а также указанную в явной форме последовательность. В частности, замены вырожденными кодонами можно осуществлять посредством создания последовательностей, в которых в третьем положении одного или нескольких выбранных (или всех) кодонов произведена замена любым из канонических оснований и/или дезоксиинозиновыми остатками (Batzer et al., Nucleic Acid Res. 19:5081 (1991); Ohtsuka et al., J. Biol. Chem. 260:2605-2608 (1985); и Rossolini et al., Mol. Cell. Probes 8:91-98 (1994)).
Термины "пептид", "полипептид" и "белок" используются взаимозаменяемо и относятся к соединению, состоящему из аминокислотных остатков, ковалентно связанных пептидными связями. Белок или пептид должен содержать по меньшей мере две аминокислоты, и не установлено ограничение на максимальное количество аминокислот, которые может содержать последовательность белка или пептида. Полипептиды включают любой пептид или белок, содержащий две или более аминокислоты, соединенные друг с другом пептидными связями. Используемый в данном документе термин относится как к коротким цепям, которые также, как правило, называются в данной области техники, например, пептидами, олигопептидами и олигомерами, так и к более длинным цепям, которые обычно называются в данной области техники белками, которых существует множество типов. "Полипептиды" включают, например, среди прочего, биологически активные фрагменты, по существу гомологичные полипептиды, олигопептиды, гомодимеры, гетеродимеры, варианты полипептидов, модифицированные полипептиды, производные, аналоги, слитые белки. Полипептид включает природный пептид, рекомбинантный пептид или их комбинацию.
Термин "консервативные модификации последовательности" относится к аминокислотным модификациям, которые не оказывают значительного влияния на характеристики связывания антитела или фрагмента антитела, содержащих данную аминокислотную последовательность, или значительно не изменяют их. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации могут быть введены в антитело или фрагмент антитела по настоящему изобретению с помощью стандартных методик, известных из уровня техники, таких как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены представляют собой замены, при которых аминокислотный остаток заменяется аминокислотным остатком, имеющим сходную боковую цепь. Семейства аминокислотных остатков, имеющих сходные боковые цепи, были определены в уровне техники. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин).
Термины "гомологичный" или "идентичность" относятся к идентичности последовательностей субъединиц двух полимерных молекул, например, двух молекул нуклеиновой кислоты, таких как две молекулы ДНК или две молекулы РНК, или двух молекул полипептидов. Если положение субъединицы в обеих из двух молекул занимает одна и та же мономерная субъединица, например, если положение в каждой из двух молекул ДНК занято аденином, то они являются гомологичными или идентичными по данному положению. Гомология между двумя последовательностями находится в прямой зависимости от количества совпадающих или гомологичных положений; например, если половина (например, пять положений в полимере длиной десять субъединиц) положений в двух последовательностях являются гомологичными, то эти две последовательности являются гомологичными на 50%; если 90% положений (например, 9 из 10) являются совпадающими или гомологичными, то эти две последовательности являются гомологичными на 90%. Процент "идентичности последовательностей" можно определить путем сравнения двух оптимально выровненных последовательностей в пределах окна сравнения, при этом для оптимального выравнивания этих двух последовательностей фрагмент аминокислотной последовательности в окне сравнения может содержать добавления или делеции (например, гэпы или выступы) по сравнению с эталонной последовательностью (которая не содержит добавлений или делеций). Процент можно рассчитать путем определения количества положений, в которых в обеих последовательностях встречается идентичный аминокислотный остаток, с получением количества совпадающих положений, деления количества совпадающих положений на общее количество положений в окне сравнения и умножения результата на 100 с получением процента идентичности последовательностей. Результатом является процент идентичности рассматриваемой последовательности относительно запрашиваемой последовательности.
Термин "выделенный" означает измененный относительно природного состояния или извлеченный из него. Например, нуклеиновая кислота или пептид, в естественных условиях присутствующие в живом животном, не являются "выделенными", однако те же нуклеиновая кислота или пептид, частично или полностью отделенные от материалов, сопутствующих им в их природном состоянии, являются "выделенными". Выделенные нуклеиновая кислота или белок могут находиться в по существу очищенной форме или могут находиться в ненативной среде, такой как, например, клетка-хозяин. Выделенное антитело по существу не содержит других антител, имеющих другие типы антигенной специфичности (например, выделенное антитело, которое специфично связывается с ENTPD2, по существу не содержит антител, которые специфично связываются с антигенами, отличными от ENTPD2). Выделенное антитело, которое специфично связывается с молекулой-мишенью, может, однако, характеризоваться перекрестной реактивностью с теми же антигенами из других видов, например, выделенное антитело, которое специфично связывается с ENTPD2, может связываться с молекулами ENTPD2 из других видов. Более того, выделенное антитело может по существу не содержать других клеточного материала и/или химических веществ.
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понятно специалисту обычной квалификации в области техники, к которой относится настоящее изобретение. Хотя при осуществлении на практике настоящего изобретения можно применять способы и материалы, подобные или эквивалентные тем, которые описаны в данном документе, ниже описаны подходящие способы и материалы. Все публикации, заявки на патент, патенты и другие литературные источники, упомянутые в данном документе, включены посредством ссылки во всей своей полноте. В случае противоречия настоящее описание, включая определения, будет иметь преимущественную силу. Кроме того, материалы, способы и примеры являются исключительно иллюстративными и не предполагаются как ограничивающие.
Подробности одного или нескольких вариантов осуществления настоящего изобретения изложены в прилагаемых графических материалах и описании ниже. Другие признаки, цели и преимущества настоящего изобретения будут очевидны из описания и графических материалов, а также из формулы изобретения.
Антитела и их антигенсвязывающие фрагменты, которые специфично связываются с ENTPD2 человека
В одном аспекте в данном документе предусмотрены антитела или их антигенсвязывающие фрагменты, например, моноклональные антитела или их антигенсвязывающие фрагменты, которые специфично связываются с белком ENTPD2 ("антитела к ENTPD2 или антигенсвязывающие фрагменты" или "антитела против ENTPD2 или антигенсвязывающие фрагменты"). В некоторых вариантах осуществления в данном документе предусмотрены антитела или их антигенсвязывающие фрагменты, например, моноклональные антитела или их антигенсвязывающие фрагменты, которые специфично связываются с белком ENTPD2 человека ("человеческие антитела к ENTPD2 или антигенсвязывающие фрагменты" или "антитела к ENTPD2 человека или антигенсвязывающие фрагменты").
В некоторых вариантах осуществления антитела к ENTPD2 или их антигенсвязывающие фрагменты (например, антитела к ENTPD2 человека или антигенсвязывающие фрагменты), предусмотренные в данном документе, содержат CDR1 тяжелой цепи (HCDR1), CDR2 тяжелой цепи (HCDR2), CDR3 тяжелой цепи (HCDR3), а также CDR1 легкой цепи (LCDR1), CDR2 легкой цепи (LCDR2) и CDR3 легкой цепи (LCDR3). В некоторых вариантах осуществления антитела к ENTPD2 или антигенсвязывающие фрагменты (например, антитела к ENTPD2 человека или антигенсвязывающие фрагменты), предусмотренные в данном документе, содержат вариабельную область тяжелой цепи (VH), содержащую CDR1, CDR2 и CDR3, и вариабельную область легкой цепи (VL), содержащую CDR1, CDR2 и CDR3. В некоторых вариантах осуществления антитела к ENTPD2 или их антигенсвязывающие фрагменты (например, антитела к ENTPD2 человека или антигенсвязывающие фрагменты), предусмотренные в данном документе, содержат последовательность полноразмерной тяжелой цепи (HC) и последовательность полноразмерной легкой цепи (LC).
В таблице 1 перечислены последовательности иллюстративных антител к ENTPD2 или их антигенсвязывающих фрагментов, которые специфично связываются с белком ENTPD2 человека.
Таблица 1. Последовательности иллюстративных моноклональных антител (MAB) и фрагментов антител (FAB), которые связываются с ENTPD2 человека
В некоторых вариантах осуществления антитело или фрагмент антитела (например, антигенсвязывающий фрагмент) к ENTPD2 человека содержат VH-домен, имеющий аминокислотную последовательность любого VH-домена, описанного в таблице 1. Другие подходящие антитела или фрагменты антител (например, антигенсвязывающие фрагменты) к ENTPD2 человека могут содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью в VH-домене с VH-областями, показанными в последовательностях, описанных в таблице 1. В определенных вариантах осуществления в настоящем изобретении также предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 человека, где антитела или фрагменты антител (например, антигенсвязывающие фрагменты) содержат CDR VH, имеющую аминокислотную последовательность любой из CDR VH, перечисленных в таблице 1. В конкретных вариантах осуществления в настоящем изобретении предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 человека, содержащие одну, две, три, четыре, пять или больше CDR VH, имеющих аминокислотную последовательность любой из CDR VH, перечисленных в таблице 1 (или, в качестве альтернативы, состоящие из них).
В некоторых вариантах осуществления антитело или фрагмент антитела (например, антигенсвязывающий фрагмент) к ENTPD2 человека содержат VL-домен, имеющий аминокислотную последовательность любого VL-домена, описанного в таблице 1. Другие подходящие антитела или фрагменты антител (например, антигенсвязывающие фрагменты) к ENTPD2 человека могут содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью в VL-домене с VL-областями, показанными в последовательностях, описанных в таблице 1. В настоящем изобретении также предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 человека, при этом антитела или фрагменты антител (например, антигенсвязывающие фрагменты) содержат CDR VL, имеющую аминокислотную последовательность любой из CDR VL, перечисленных в таблице 1. В частности, в настоящем изобретении предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 человека, содержащие одну, две, три или больше CDR VL, имеющих аминокислотную последовательность любой из CDR VL, перечисленных в таблице 1 (или, в качестве альтернативы, состоящие из них).
Другие антитела или фрагменты антител (например, антигенсвязывающий фрагмент) к ENTPD2 человека, раскрытые в данном документе, содержат аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью в CDR-областях с CDR-областями, показанными в последовательностях, описанных в таблице 1. В некоторых вариантах осуществления они содержат мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в CDR-областях по сравнению с CDR-областями, показанными в последовательности, описанной в таблице 1.
В данном документе также предусмотрены последовательности нуклеиновых кислот, которые кодируют VH, VL, полноразмерную тяжелую цепь и полноразмерную легкую цепь антител и их антигенсвязывающих фрагментов, которые специфично связываются с ENTPD2 человека, например, последовательности нуклеиновых кислот из таблицы 1. Такие последовательности нуклеиновых кислот могут быть оптимизированы для экспрессии в клетках млекопитающих.
Другие антитела к ENTPD2 человека, раскрытые в данном документе, включают антитела, в которых аминокислоты или нуклеиновые кислоты, кодирующие аминокислоты, были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью с последовательностями, описанными в таблице 1. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты содержат мутантные аминокислотные последовательности, где не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в вариабельных областях по сравнению с вариабельными областями, показанными в последовательности, описанной в таблице 1, при этом они сохраняют по существу такую же терапевтическую активность.
Поскольку каждое предусмотренное антитело связывается с ENTPD2 человека, последовательности (аминокислотные последовательности и нуклеотидные последовательности, кодирующие аминокислотные последовательности) VH, VL, полноразмерной легкой цепи и полноразмерной тяжелой цепи можно подвергать "смешиванию и подбору" для создания других ENTPD2-связывающих антител, раскрытых в данном документе. Такие подвергнутые "смешиванию и подбору" ENTPD2-связывающие антитела можно тестировать с помощью анализов связывания, известных из уровня техники (например, разновидностей ELISA, анализов, описанных в иллюстративных примерах). В случае, когда цепи подвергают смешиванию и подбору, последовательность VH из конкретной пары VH/VL следует заменить структурно сходной последовательностью VH. Последовательность полноразмерной тяжелой цепи из конкретной пары полноразмерная тяжелая цепь/полноразмерная легкая цепь следует заменить структурно сходной последовательностью полноразмерной тяжелой цепи. Последовательность VL из конкретной пары VH/VL следует заменить структурно сходной последовательностью VL. Последовательность полноразмерной легкой цепи из конкретной пары полноразмерная тяжелая цепь/полноразмерная легкая цепь следует заменить структурно сходной последовательностью полноразмерной легкой цепи.
Соответственно, в одном варианте осуществления в настоящем изобретении предусмотрены выделенное моноклональное антитело или его антигенсвязывающий фрагмент, имеющие вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 10, 25, 33, 46, 70, 91, 115, 132, 145, 169, 225, 233, 241, 250, 264, 281, 328; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 21, 29, 57, 64, 74, 78, 102, 125, 156, 178, 229, 237, 257, 268, 287, 332; где антитело специфично связывается с ENTPD2 человека.
В другом варианте осуществления в настоящем изобретении предусмотрены (i) выделенное моноклональное антитело, имеющее полноразмерную тяжелую цепь (HC), содержащую аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 12, 27, 35, 48, 72, 93, 117, 134, 147, 171, 227, 235, 243, 252, 266, 283, 330; и полноразмерную легкую цепь (LC), содержащую аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 23, 31, 59, 66, 76, 80, 104, 127, 158, 180, 231, 239, 259, 270, 289, 334; или (ii) функциональный белок, содержащий его антигенсвязывающую часть.
В другом варианте осуществления в настоящем изобретении предусмотрены антитела, связывающиеся с ENTPD2 человека, или их фрагменты антител, которые содержат CDR1, CDR2 и CDR3 тяжелой цепи и CDR1, CDR2 и CDR3 легкой цепи, описанные в таблице 1, или их комбинации. Аминокислотные последовательности CDR1 VH антител показаны под SEQ ID NOs: 1, 4, 6, 7, 37, 40, 42, 43, 82, 85, 87, 88, 106, 109, 111, 112, 136, 139, 141, 142, 160, 163, 165, 166, 185, 187, 188, 206, 207, 208, 213, 214, 215, 272, 275, 277. Аминокислотные последовательности CDR2 VH антител показаны под SEQ ID NOs: 2, 5, 8, 38, 41, 44, 83, 86, 89, 107, 110, 113, 129, 130, 131, 137, 140, 143, 161, 164, 167, 186, 189, 220, 222, 223, 245, 247, 248, 261, 273, 276, 279. Аминокислотные последовательности CDR3 VH антител показаны под SEQ ID NO: 3, 39, 68, 84, 108, 138, 162, 221, 246, 262, 277, 274, 9, 45, 69, 90, 114, 144, 168, 190, 224, 249, 263, 274, 280. Аминокислотные последовательности CDR1 VL антител показаны под SEQ ID NOs: 14, 17, 20, 50, 53, 56, 61, 62, 63, 95, 98, 101, 119, 122, 124, 149, 152, 155, 173, 175, 177, 198, 201, 254. Аминокислотные последовательности CDR2 VL антител показаны под SEQ ID NOs: 15, 18, 51, 54, 96, 99, 120, 150, 153, 199, 285, 286. Аминокислотные последовательности CDR3 VL антител показаны под SEQ ID NOs: 16, 19, 52, 55, 97, 100, 121, 123, 151, 154, 174, 176, 200, 255, 256.
С учетом того, что каждое из антител связывается с ENTPD2 человека и что специфичность связывания с антигеном обеспечивается преимущественно CDR1-, CDR2- и CDR3-областями, последовательности CDR1, CDR2 и CDR3 VH и последовательности CDR1, CDR2 и CDR3 VL можно подвергнуть "смешиванию и подбору" (т. е. CDR из различных антител можно подвергнуть смешиванию и подбору), при том что каждое антитело должно содержать CDR1, CDR2 и CDR3 VH и CDR1, CDR2 и CDR3 VL, для создания других антител, связывающихся с ENTPD2 человека, раскрытых в данном документе. Такие "подвергнутые смешиванию и подбору" ENTPD2-связывающие антитела можно тестировать с помощью анализов связывания, известных из уровня техники и описанных в разделе "Примеры" (например, разновидностей ELISA). В случае, когда последовательности CDR VH подвергают смешиванию и подбору, последовательность CDR1, CDR2 и/или CDR3 из конкретной последовательности VH следует заменить структурно сходной(сходными) последовательностью(последовательностями) CDR. Аналогичным образом, в случае, когда последовательности CDR VL подвергают смешиванию и подбору, последовательность CDR1, CDR2 и/или CDR3 из конкретной последовательности VL следует заменить структурно сходной(сходными) последовательностью(последовательностями) CDR. Специалисту обычной квалификации в данной области будет совершенно очевидно, что новые последовательности VH и VL можно создавать путем замены одной или нескольких последовательностей CDR-областей VH и/или VL структурно сходными последовательностями из последовательностей CDR, показанных в данном документе для моноклональных антител по настоящему изобретению.
Соответственно, в настоящем изобретении предусмотрены выделенное моноклональное антитело или его антигенсвязывающая область, содержащие CDR1 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 1, 4, 6, 7, 37, 40, 42, 43, 82, 85, 87, 88, 106, 109, 111, 112, 136, 139, 141, 142, 160, 163, 165, 166, 182, 187, 188, 206, 207, 208, 213, 214, 215, 272, 275, 277; CDR2 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 2, 5, 8, 38, 41, 44, 83, 86, 89, 107, 110, 113, 129, 130, 131, 137, 140, 143, 161, 164, 167, 183, 189, 220, 222, 223, 245, 247, 248, 261, 273, 276; CDR3 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3, 39, 68, 84, 108, 138, 162, 221, 246, 262, 277, 274, 9, 45, 69, 90, 114, 144, 168, 190, 224, 249, 263, 274, 280; CDR1 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 14, 17, 20, 50, 53, 56, 61, 62, 63, 95, 98, 101, 119, 122, 124, 149, 152, 155, 173, 175, 177, 195, 201, 254; CDR2 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 15, 18, 51, 54, 96, 99, 120, 150, 153, 196, 285, 286; и CDR3 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 16, 19, 52, 55, 97, 100, 121, 123, 151, 154, 174, 176, 197, 255, 256; где антитело специфично связывается с ENTPD2 человека.
В определенных вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, представляет собой антитело или фрагмент антитела (например, антигенсвязывающий фрагмент), которые описаны в таблице 1.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат область 1, определяющую комплементарность, тяжелой цепи (HCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 1, 4, 6 или 7; область 2, определяющую комплементарность, тяжелой цепи (HCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 2, 5 или 8; область 3, определяющую комплементарность, тяжелой цепи (HCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 3 или 9; область 1, определяющую комплементарность, легкой цепи (LCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 14, 17 или 20; область 2, определяющую комплементарность, легкой цепи (LCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18; и область 3, определяющую комплементарность, легкой цепи (LCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 16 или 19.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 1; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 2; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 3; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 14; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 4; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 5; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 3; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 17; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 19.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 6; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 2; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 3; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 14; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 7; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 8; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 9; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 20; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37, 40, 42 или 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38, 41 или 44; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39 или 45; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 50, 53 или 56; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51 или 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52 или 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 50; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 40; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 41; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 53; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 42; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 50; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 44; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 45; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 56; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37, 40, 42 или 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38, 41 или 44; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39 или 45; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61, 62 или 63; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51 или 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52 или 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 40; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 41; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 62; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 42; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 39; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 44; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 45; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 63; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37, 40, 42 или 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38, 41 или 44; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68 или 69; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 50, 53 или 56; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51 или 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52 или 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 50; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 40; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 41; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 53; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 42; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 38; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 50; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 44; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 69; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 56; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 82, 85, 87 или 88; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 83, 86 или 89; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 84 или 90; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 95, 98 или 101; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 96 или 99; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 97 или 100.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 82; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 83; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 84; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 95; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 96; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 97.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 85; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 86; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 84; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 98; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 100.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 87; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 83; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 84; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 95; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 96; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 97.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 88; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 89; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 90; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 101; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 97.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 106, 109, 111 или 112; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 107, 110 или 113; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108 или 114; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 119, 122 или 124; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99 или 120; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 121 или 123.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 106; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 107; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 119; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 120; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 121.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 109; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 110; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 122; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 123.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 111; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 107; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 119; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 120; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 121; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 112; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 113; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 114; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 124; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 121.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 106, 109, 111 или 112; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 129, 130 или 131; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108 или 114; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 119, 122 или 124; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99 или 120; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 121 или 123.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 106; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 129; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 119; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 120; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 121.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 109; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 130; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 122; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 123.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 111; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 129; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 108; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 119; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 120; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 121.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 112; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 131; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 114; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 124; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 99; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 121.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 136, 139, 141 или 142; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 137, 140 или 143; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 138 или 144; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 149, 152 или 155; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 150 или 153; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 151 или 154.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 136; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 137; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 138; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 149; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 150; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 151.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 139; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 140; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 138; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 152; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 153; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 154.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 141; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 137; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 138; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 149; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 150; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 151.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 142; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 143; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 144; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 155; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 153; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 151.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 160, 163, 165 или 166; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 161, 164 или 167; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 162 или 168; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 173, 175 или 177; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 150 или 153; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 174 или 176.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 160; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 161; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 162; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 173; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 150; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 174.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 163; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 164; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 162; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 175; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 153; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 176.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 165; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 161; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 162; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 173; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 150; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 174.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 166; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 167; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 168; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 177; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 153; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 174.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37, 40, 42 или 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 220, 222 или 223; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 221 или 224; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61, 62 или 63; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51 или 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52 или 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 220; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 221; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 40; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 222; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 221; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 62; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 42; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 220; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 221; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 223; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 224; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 63; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37, 40, 42 или 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 220, 222 или 223; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68 или 69; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61, 62 или 63; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51 или 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52 или 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 37; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 220; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 40; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 222; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 62; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 55.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 42; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 220; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 68; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 61; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 51; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 43; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 223; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 69; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 63; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 54; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 52.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 1, 4, 6 или 7; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 245, 247 или 248; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 246 или 249; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 17, 20 или 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 255 или 256.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 1; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 245; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 246; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 255.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 4; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 247; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 246; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 17; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 256.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 6; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 254; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 246; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 255.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 7; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 248; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 249; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 20; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 255.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 1, 4, 6 или 7; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 247, 248 или 261; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 262 или 263; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 17, 20 или 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16 или 19.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 1; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 261; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 262; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 4; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 247; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 262; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 17; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 19.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 6; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 261; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 262; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 15; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 7; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 248; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 263; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 20; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 18; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 272, 275 или 278; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 273, 276 или 279; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 274, 277 или 280; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 17, 20 или 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 285 или 286; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16 или 19.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 272; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 273; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 274; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 285; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 275; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 276; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 274; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 17; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 286; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 19.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 277; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 273; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 274; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 254; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 285; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 278; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 279; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 280; LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 20; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 286; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 16.
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 10 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 21 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 25 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 29 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 33 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 29 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 46 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 57 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 46 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 64 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 70 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 74 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 25 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 78 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 91 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 102 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 115 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 125 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 132 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 125 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 145 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 156 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 169 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 178 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 225 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 229 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 233 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 237 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 241 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 229 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 250 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 257 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 264 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 268 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело или его антигенсвязывающая область, которые специфично связываются с ENTPD2 человека, содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 281 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 287 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 12 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 23 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 27 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 31 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 35 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 31 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 48 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 59 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 48 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 66 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 72 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 76 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 27 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 80 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 93 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 104 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 117 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 127 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 134 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 127 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 147 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 158 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 171 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую SEQ ID NO: 180 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 227 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 231 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 235 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 239 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 243 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 231 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 252 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 259 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 266 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 270 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления антитело, которое специфично связывается с ENTPD2 человека, содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 283 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации), и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 289 (или последовательность, на по меньшей мере приблизительно 90%, 95%, 99% или больше идентичную ей и/или имеющую одну, две, три или более замены, вставки, делеции или модификации).
В некоторых вариантах осуществления в настоящем изобретении предусмотрены антитело или его антигенсвязывающий фрагмент, которые связываются с белком ENTPD2 человека с константой диссоциации (KD), составляющей менее 10 нМ, например, с KD, составляющей менее 9 нМ, менее 8 нМ, менее 7 нМ, менее 6 нМ, менее 5 нМ, менее 4 нМ, менее 3 нМ, менее 2 нМ, менее 1 нМ, например, согласно измерению с помощью Biacore. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, предусмотренные в данном документе, связываются с белком ENTPD2 человека с константой диссоциации (KD), составляющей менее 5 нМ, например, согласно измерению с помощью Biacore. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, предусмотренные в данном документе, связываются с белком ENTPD2 человека с константой диссоциации (KD), составляющей менее 3 нМ, например, согласно измерению с помощью Biacore. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, предусмотренные в данном документе, связываются с белком ENTPD2 человека с константой диссоциации (KD), составляющей менее 1 нМ, например, согласно измерению с помощью Biacore. В некоторых вариантах осуществления константу диссоциации антител или их антигенсвязывающих фрагментов, описанных в данном документе, для ENTPD2 человека измеряют с помощью Biacore при 25ºC.
В данном документе также предусмотрены антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эпитопом в ENTPD2 человека, где эпитоп содержит по меньшей мере один (например, по меньшей мере два, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять, по меньшей мере шесть, по меньшей мере семь, по меньшей мере восемь, по меньшей мере девять, по меньшей мере десять, по меньшей мере одиннадцать, по меньшей мере двенадцать, по меньшей мере тринадцать, по меньшей мере четырнадцать, по меньшей мере пятнадцать, по меньшей мере двадцать) из следующих остатков: His50, Asp76, Pro78, Gly79, Gly80, Tyr85, Asp87, Asn88, Gly91, Gln94, Ser95, Gly98, Glu101, Gln102, Gln105, Asp106, Arg245, Thr272, Gln273, Leu275, Asp278, Arg298, Ala347, Ala350, Thr351, Arg392, Ala393, Arg394 или Tyr398. В некоторых вариантах осуществления такие антитела или антигенсвязывающие фрагменты включают без ограничения MAb1, MAb2, MAb3, MAb7, MAb17, MAb19, MAb20, MAb21 и Fab23, раскрытые в таблице 1.
В данном документе также предусмотрены антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эпитопом в ENTPD2 человека, где эпитоп содержит по меньшей мере один (например, по меньшей мере два, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять, по меньшей мере шесть, по меньшей мере семь, по меньшей мере восемь, по меньшей мере девять, по меньшей мере десять, по меньшей мере одиннадцать, по меньшей мере двенадцать, по меньшей мере тринадцать, по меньшей мере четырнадцать, по меньшей мере пятнадцать, по меньшей мере двадцать) из следующих остатков: Gly79, Gln250, Leu253, Trp266, Arg268, Gly269, Phe270, Ser271, Thr272, Gln273, Val274, Leu275, Asp278, Arg298, Ser300, Ser302, Gly303, Thr380, Trp381, Ala382, Gly390, Gln391, Arg392, Ala393, Arg394 или Asp397. В некоторых вариантах осуществления такие антитела или антигенсвязывающие фрагменты включают без ограничения MAb4, MAb5, MAb6, MAb16, MAb18 и Fab22, раскрытые в таблице 1.
После определения необходимого эпитопа в антигене можно создавать антитела к этому эпитопу, например, с помощью методик, описанных в настоящем изобретении. В качестве альтернативы в ходе процесса разработки при создании антител и определения их характеристик может выясняться информация о необходимых эпитопах. На основании этой информации можно затем провести конкурентный скрининг антител в отношении связывания с одним и тем же эпитопом. Подход к достижению этого заключается в проведении исследований перекрестной конкуренции с целью обнаружения антител, которые конкурентно связываются друг с другом, например, антител, конкурирующих за связывание с антигеном. Высокопроизводительный способ "сортировки" антител на основании их перекрестной конкуренции описан в международной заявке на патент № WO 2003/48731. Как будет понятно специалисту в данной области, практически все, с чем может специфично связываться антитело, может представлять собой эпитоп. Эпитоп может содержать те остатки, с которыми связывается антитело.
В целом, антитела, специфичные в отношении конкретного антигена-мишени, будут преимущественно распознавать эпитоп в антигене-мишени в сложной смеси белков и/или макромолекул.
Области данного полипептида, которые содержат эпитоп, могут быть идентифицированы с помощью множества методик картирования эпитопов, хорошо известных из уровня техники. См., например, Epitope Mapping Protocols in Methods in Molecular Biology, Vol. 66 (Glenn E. Morris, Ed., 1996, Humana Press, Totowa, N.J). Например, линейные эпитопы могут быть определены, например, посредством параллельного синтеза большого количества пептидов на твердых подложках, при этом пептиды соответствуют частям молекулы белка, и осуществления реакции пептидов с антителами, когда пептиды все еще прикреплены к подложкам. Такие методики известны из уровня техники и описаны, например, в патенте США. № 4708871; Geysen et al., (1984) Proc. Natl. Acad. Sci. USA 8:3998-4002; Geysen et al., (1985) Proc. Natl. Acad. Sci. USA 82:78-182; Geysen et al., (1986) Mol. Immunol. 23:709-715. Аналогичным образом, конформационные эпитопы без труда идентифицируют путем определения пространственной конформации аминокислот, как, например, с помощью рентгеновской кристаллографии и двумерного ядерного магнитного резонанса. См., например, Epitope Mapping Protocols выше. Антигенные области белков также могут быть идентифицированы с помощью стандартных графиков антигенности и гидропатичности, таких как графики, построенные с помощью, например, программы из системы программного обеспечения Omiga версии 1.0, доступной от Oxford Molecular Group. В этой компьютерной программе используются способ Хоппа-Вудса, Hopp et al., (1981) Proc. Natl. Acad. Sci USA 78:3824-3828; для определения профилей антигенности и методика Кайта-Дулиттла, Kyte et al., (1982) J. Mol. Biol. 157:105-132; для построения графиков гидропатичности.
Молекула антитела может представлять собой поликлональное или моноклональное антитело. Моноклональное антитело может быть получено с помощью гибридомной технологии или с помощью способов, в которых не используется гибридомная технология (например, рекомбинантных способов). В некоторых вариантах осуществления антитело может быть получено рекомбинантным путем, например, может быть получено с помощью фагового дисплея или с помощью комбинаторных способов.
Фаговый дисплей и комбинаторные способы для создания антител известны из уровня техники (как описано, например, в Ladner et al., патент США № 5223409; Kang et al., международная публикация № WO 92/18619; Dower et al., международная публикация № WO 91/17271; Winter et al., международная публикация WO 92/20791; Markland et al., международная публикация № WO 92/15679; Breitling et al., международная публикация WO 93/01288; McCafferty et al., международная публикация № WO 92/01047; Garrard et al., международная публикация № WO 92/09690; Ladner et al., международная публикация № WO 90/02809; Fuchs et al. (1991) Bio/Technology 9:1370-1372; Hay et al. (1992) Hum Antibod Hybridomas 3:81-85; Huse et al. (1989) Science 246:1275-1281; Griffiths et al. (1993) EMBO J 12:725-734; Hawkins et al. (1992) J Mol Biol 226:889-896; Clackson et al. (1991) Nature 352:624-628; Gram et al. (1992) PNAS 89:3576-3580; Garrard et al. (1991) Bio/Technology 9:1373-1377; Hoogenboom et al. (1991) Nuc Acid Res 19:4133-4137 и Barbas et al. (1991) PNAS 88:7978-7982).
В одном варианте осуществления антитело представляет собой полностью человеческое антитело (например, антитело, полученное в организме мыши, которая была модифицирована методами генной инженерии для продуцирования антитела из последовательности человеческого иммуноглобулина) или антитело, не являющееся человеческим, например, антитело грызуна (мыши или крысы), козы, примата (например, обезьяны), верблюда.
Антитело может представлять собой антитело, в котором вариабельная область или ее часть, например, CDR, получены в организме, отличном от человеческого, например, в организме крысы или мыши. Химерные антитела, антитела с привитыми CDR и гуманизированные антитела находятся в пределах объема настоящего изобретения. Антитела, полученные в организме, отличном от человеческого, например, в организме крысы или мыши, и затем подвергнутые модификации, например, в каркасной части вариабельной области или константной области, для уменьшения антигенности у человека, находятся в пределах объема настоящего изобретения.
Химерные и/или гуманизированные антитела могут быть сконструированы для минимизации иммунного ответа пациента-человека на антитела, продуцируемые у субъектов, отличных от человека, или полученные в результате экспрессии генов, кодирующих антитела, отличные от человеческих. Химерные антитела содержат вариабельную область антитела животного, отличного от человека, и константную область человеческого антитела. Такие антитела сохраняют специфичность связывания с эпитопом исходного моноклонального антитела, но могут быть менее иммуногенными при введении людям и, следовательно, с большей вероятностью будут переносимыми для пациента. Например, каждая из одной или всех (например, одной, двух или трех) вариабельных областей легкой(легких) цепи(цепей) и/или одной или всех (например, одной, двух или трех) вариабельных областей тяжелой(тяжелых) цепи(цепей) антитела мыши (например, моноклонального антитела мыши) могут быть соединены с человеческой константной областью, такой как без ограничения человеческая константная область IgG1. Химерные моноклональные антитела могут быть получены с помощью методик рекомбинантных ДНК, известных из уровня техники. Например, ген, кодирующий константную область молекулы антитела, отличного от человеческого, может быть заменен геном, кодирующим человеческую константную область (см. Robinson et al., PCT-публикация заявки на патент PCT/US86/02269; Akira, et al., заявка на европейский патент 184187; или Taniguchi, M., заявка на европейский патент 171496). Кроме того, другие подходящие методики, которые можно применять для получения химерных антител, описаны, например, в патентах США №№ 4816567; 4,978,775; 4975369 и 4816397.
Химерное антитело может быть дополнительно "гуманизировано" путем замены частей вариабельной области, не участвующих в связывании с антигеном, эквивалентными частями из человеческих вариабельных областей. Гуманизированные антитела содержат в вариабельной области тяжелой и/или легкой цепи одну или несколько человеческих каркасных областей вместе с областями, определяющими комплементарность (CDR), отличными от человеческих (например, из мыши, крысы или хомяка). В некоторых вариантах осуществления гуманизированное антитело содержит последовательности, являющиеся полностью человеческими, за исключением CDR-областей. Гуманизированные антитела, как правило, являются менее иммуногенными для людей по сравнению с негуманизированными антителами и, таким образом, обеспечивают благоприятные терапевтические эффекты в определенных ситуациях. Гуманизированные антитела к ENTPD2 могут быть получены с помощью способов, известных из уровня техники. См., например, Hwang et al., Methods 36:35, 2005; Queen et al., Proc. Natl. Acad. Sci. U.S.A. 86:10029-10033, 1989; Jones et al., Nature 321:522-25, 1986; Riechmann et al., Nature 332:323-27, 1988; Verhoeyen et al., Science 239:1534-36, 1988; Orlandi et al., Proc. Natl. Acad. Sci. U.S.A. 86:3833-3837, 1989; патенты США №№ 5225539; 5530101; 5585089; 5693761; 5693762 и 6180370; а также WO 90/07861.
Человеческие антитела к ENTPD2 могут быть получены с помощью способов, известных из уровня техники. Например, технологию "гуманиринга" применяют для превращения антител, отличных от человеческих, в сконструированные человеческие антитела. В публикации заявки на патент США № 20050008625 описан осуществляемый in vivo способ замены вариабельной области антитела, отличного от человеческого, человеческой вариабельной областью в антителе с сохранением тех же или обеспечением лучших характеристик связывания по сравнению с таковыми у антитела, отличного от человеческого. Способ основывается на определяемой эпитопом замене вариабельных областей эталонного антитела, отличного от человеческого, таковыми из полностью человеческого антитела. Полученное в результате человеческое антитело в целом является структурно неродственным эталонному антителу, отличному от человеческого, но связывается с тем же эпитопом в том же антигене, что и эталонное антитело. Вкратце, подход с последовательной определяемой эпитопом комплементарной заменой обеспечивается благодаря созданию в клетках конкуренции между "конкурентом" и библиотекой разнообразных гибридных форм эталонного антитела ("тестируемых антител") за связывание с антигеном, находящимся в ограниченных количествах, в присутствии репортерной системы, которая реагирует на связывание тестируемого антитела с антигеном. Конкурентом может быть эталонное антитело или его производное, такое как одноцепочечный Fv-фрагмент. Конкурентом также может быть природный или искусственный лиганд антигена, который связывается с тем же эпитопом, что и эталонное антитело. Единственные требования к конкуренту заключаются в том, чтобы он связывался с тем же эпитопом, что и эталонное антитело, и чтобы он конкурировал с эталонным антителом за связывание с антигеном. Тестируемые антитела имеют одну общую антигенсвязывающую V-область из эталонного антитела, отличного от человеческого, и другую V-область, отобранную случайным образом из иного источника, такого как репертуарная библиотека человеческих антител. Общая V-область из эталонного антитела служит в качестве указателя, располагая тестируемые антитела на одном и том же эпитопе в антигене и в одной и той же ориентации для того, чтобы отбор склонялся в сторону наиболее высокого качества связывания с антигеном относительно эталонного антитела.
Много типов репортерных систем можно применять для выявления необходимых взаимодействий между тестируемыми антителами и антигеном. Например, дополняющие друг друга репортерные фрагменты могут быть связаны соответственно с антигеном и тестируемым антителом для того, чтобы активация репортера при дополнении фрагментов происходила только тогда, когда тестируемое антитело связывается с антигеном. Если продукты слияния антитело-репортерный фрагмент и антиген-репортерный фрагмент экспрессируются совместно с конкурентом, то активация репортера становится зависимой от способности тестируемого антитела конкурировать с конкурентом, которая является пропорциональной аффинности тестируемого антитела в отношении антигена. Другие репортерные системы, которые можно применять, включают реактиватор самоингибируемой системы реактивации репортера (RAIR), раскрытый в заявке на патент США с регистрационным № 10/208730 (публикация № 20030198971), или систему конкурентной активации, раскрытую в заявке на патент США с регистрационным № 10/076845 (публикация № 20030157579).
При использовании системы последовательной определяемой эпитопом комплементарной замены проводят отбор для идентификации клеток, экспрессирующих одно тестируемое антитело вместе с конкурентом, антигеном и компонентами репортера. В этих клетках каждое тестируемое антитело конкурирует индивидуально с конкурентом за связывание с антигеном, находящимся в ограниченном количестве. Активность репортера является пропорциональной количеству антигена, связавшегося с тестируемым антителом, которое, в свою очередь, является пропорциональным аффинности тестируемого антитела в отношении антигена и стабильности тестируемого антитела. Тестируемые антитела изначально отбирают на основании их активности по сравнению с активностью эталонного антитела при экспрессии в качестве тестируемого антитела. Результатом первого цикла отбора является набор "гибридных" антител, каждое из которых состоит из одной и той же V-области, отличной от человеческой, из эталонного антитела и человеческой V-области из библиотеки, и каждое из которых связывается с тем же эпитопом в антигене, что и эталонное антитело. Одно или несколько гибридных антител, отобранных в первом цикле, будут характеризоваться аффинностью в отношении антигена, сравнимой с таковой у эталонного антитела или превышающей ее.
На второй стадии замены V-области человеческие V-области, отобранные на первой стадии, используют в качестве указателя для отбора человеческих заменяющих фрагментов для остальной части V-области эталонного антитела, отличного от человеческого, с использованием разнообразной библиотеки когнатных человеческих V-областей. Гибридные антитела, отобранные в первом цикле, также можно применять в качестве конкурентов для второго цикла отбора. Результатом второго цикла отбора является набор полностью человеческих антител, которые структурно отличаются от эталонного антитела, но которые конкурируют с эталонным антителом за связывание с одним и тем же антигеном. Некоторые из отобранных человеческих антител связываются с тем же эпитопом в том же антигене, что и эталонное антитело. Среди этих отобранных человеческих антител одно или несколько связываются с одним и тем же эпитопом с аффинностью, которая является сравнимой с таковой у эталонного антитела или превышает ее.
При использовании мышиного или химерного антитела к ENTPD2 можно получить человеческие антитела, которые связываются с ENTPD2 человека с такой же специфичностью связывания и такой же или лучшей аффинностью связывания. Кроме того, такие человеческие антитела к ENTPD2 также могут быть получены коммерческим путем от компаний, которые обычно производят человеческие антитела, например, KaloBios, Inc. (Маунтин-Вью, Калифорния).
В некоторых вариантах осуществления в настоящем изобретении предусмотрены антитело или его антигенсвязывающий фрагмент, которые связываются с белком ENTPD2 человека и модулируют одну или несколько форм активности/функций ENTPD2, например, ингибируют формы ферментативной активности ENTPD2 человека, например, на по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90%. В некоторых вариантах осуществления ферментативную активность ENTPD2 человека измеряют с помощью анализа FRET in vitro, в котором измеряется гидролиз ATP до ADP под действием рекомбинантного ENTPD2 либо ENTPD2, экспрессирующегося на поверхности клеток.
В некоторых вариантах осуществления антитела к ENTPD2 человека или их антигенсвязывающие фрагменты, описанные в данном документе, ингибируют способность ENTPD2 к гидролизу аденозинтрифосфата (ATP). В некоторых вариантах осуществления способность ENTPD2 к гидролизу ATP измеряют с помощью анализа FRET in vitro, в котором измеряется гидролиз ATP до ADP под действием рекомбинантного ENTPD2 либо ENTPD2, экспрессирующегося на поверхности клеток.
В некоторых вариантах осуществления антитела к ENTPD2 человека или их антигенсвязывающие фрагменты, описанные в данном документе, препятствуют связыванию ATP с ENTPD2 или удерживают ATP в каталитическом домене ENTPD2. В некоторых вариантах осуществления препятствование связыванию ATP с ENTPD2 или удерживание ATP в каталитическом домене ENTPD2 измеряют с помощью анализа FRET in vitro, в котором измеряется гидролиз ATP до ADP под действием рекомбинантного ENTPD2 либо ENTPD2, экспрессирующегося на поверхности клеток.
Антитела и их антигенсвязывающие фрагменты, которые специфично связываются с ENTPD2 мыши
В данном документе также предусмотрены антитела или их антигенсвязывающие фрагменты, например, моноклональные антитела или их антигенсвязывающие фрагменты, которые специфично связываются с белком ENTPD2 мыши. В таблице 26 перечислены последовательности иллюстративных антител к ENTPD2 или их антигенсвязывающих фрагментов, которые специфично связываются с белком ENTPD2 мыши.
Таблица 26. Последовательности иллюстративных моноклональных антител (MAB) и фрагментов антител (FAB), которые связываются с ENTPD2 мыши
В некоторых вариантах осуществления антитело или фрагмент антитела (например, антигенсвязывающий фрагмент) к ENTPD2 мыши содержат VH-домен, имеющий аминокислотную последовательность любого VH-домена, описанного в таблице 26. Другие подходящие антитела или фрагменты антител (например, антигенсвязывающие фрагменты) к ENTPD2 мыши могут содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью в VH-домене с VH-областями, показанными в последовательностях, описанных в таблице 26. В определенных вариантах осуществления в настоящем изобретении также предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 мыши, где антитела или фрагменты антител (например, антигенсвязывающие фрагменты) содержат CDR VH, имеющую аминокислотную последовательность любой из CDR VH, перечисленных в таблице 26. В конкретных вариантах осуществления в настоящем изобретении предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 мыши, содержащие одну, две, три, четыре, пять или больше CDR VH, имеющих аминокислотную последовательность любой из CDR VH, перечисленных в таблице 26 (или, в качестве альтернативы, состоящие из них).
В некоторых вариантах осуществления антитело или фрагмент антитела (например, антигенсвязывающий фрагмент) к ENTPD2 мыши содержат VL-домен, имеющий аминокислотную последовательность любого VL-домена, описанного в таблице 26. Другие подходящие антитела или фрагменты антител (например, антигенсвязывающие фрагменты) к ENTPD2 мыши могут содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью в VL-домене с VL-областями, показанными в последовательностях, описанных в таблице 26. В настоящем изобретении также предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 мыши, при этом антитела или фрагменты антител (например, антигенсвязывающие фрагменты) содержат CDR VL, имеющую аминокислотную последовательность любой из CDR VL, перечисленных в таблице 26. В частности, в настоящем изобретении предусмотрены антитела или фрагменты антител (например, антигенсвязывающие фрагменты), которые специфично связываются с ENTPD2 мыши, содержащие одну, две, три или больше CDR VL, имеющих аминокислотную последовательность любой из CDR VL, перечисленных в таблице 26 (или, в качестве альтернативы, состоящие из них).
Другие антитела или фрагменты антител (например, антигенсвязывающий фрагмент) к ENTPD2 мыши, раскрытые в данном документе, содержат аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью в CDR-областях с CDR-областями, показанными в последовательностях, описанных в таблице 26. В некоторых вариантах осуществления они содержат мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в областях CDR при сравнении с областями CDR, показанными в последовательности, описанной в таблице 26.
В данном документе также предусмотрены последовательности нуклеиновых кислот, которые кодируют VH, VL, полноразмерную тяжелую цепь и полноразмерную легкую цепь антител и их антигенсвязывающих фрагментов, которые специфично связываются с ENTPD2 мыши, например, последовательности нуклеиновых кислот из таблицы 26. Такие последовательности нуклеиновых кислот могут быть оптимизированы для экспрессии в клетках млекопитающих.
В данном документе также предусмотрены антитела или их антигенсвязывающие фрагменты, которые специфично связываются с эпитопом в ENTPD2 мыши, где эпитоп содержит по меньшей мере один (например, по меньшей мере два, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять, по меньшей мере шесть, по меньшей мере семь, по меньшей мере восемь, по меньшей мере девять, по меньшей мере десять, по меньшей мере одиннадцать, по меньшей мере двенадцать, по меньшей мере тринадцать, по меньшей мере четырнадцать, по меньшей мере пятнадцать, по меньшей мере двадцать) из следующих остатков: Ser74, Cys75, Asp76, Tyr349, Tyr350, Asp353, Phe354, Thr357, Val358, Gly360, Gln385, Ala386, Arg387, Val388, Pro389, Gly390, Gln391, Thr393, Arg394 или Tyr398.
Каркасные области и сконструированные или модифицированные антитела
Антитело по настоящему изобретению также можно получить при использовании антитела, имеющего одну или несколько из последовательностей VH и/или VL, в качестве исходного материала для конструирования модифицированного антитела, при этом данное модифицированное антитело может иметь измененные свойства по сравнению с исходным антителом. Антитело может быть сконструировано посредством модификации одного или нескольких остатков в пределах одной или обеих вариабельных областей (т. е. VH и/или VL), например, в пределах одной или нескольких CDR-областей и/или в пределах одной или нескольких каркасных областей. Дополнительно или в качестве альтернативы, антитело может быть сконструировано посредством модификации остатков в пределах константной(константных) области(областей), например, для изменения эффекторной (эффекторных) функции (функций) антитела.
Один тип конструирования вариабельной области, который можно осуществлять, представляет собой прививание CDR. Антитела взаимодействуют с антигенами-мишенями преимущественно посредством аминокислотных остатков, которые расположены в шести областях, определяющих комплементарность (CDR), тяжелой и легкой цепей. По этой причине аминокислотные последовательности в пределах CDR являются более разнообразными среди отдельных антител, чем последовательности за пределами CDR. Поскольку последовательности CDR отвечают за большинство взаимодействий антитело-антиген, можно экспрессировать рекомбинантные антитела, которые имитируют свойства конкретных встречающихся в природе антител, посредством конструирования векторов экспрессии, которые содержат последовательности CDR из конкретного встречающегося в природе антитела, привитые на последовательности каркасных областей из другого антитела с другими свойствами (см., например, Riechmann, L. et al., 1998 Nature 332:323-327; Jones, P. et al., 1986 Nature 321:522-525; Queen, C. et al., 1989 Proc. Natl. Acad., U.S.A. 86:10029-10033; патент США № 5225539 авторства Winter и патенты США №№ 5530101; 5585089; 5693762 и 6180370 авторства Queen et al.).
Такие последовательности каркасных областей можно получить из общедоступных баз данных ДНК или опубликованных литературных источников, которые содержат последовательности генов антител зародышевого типа или перегруппированные последовательности антител. Например, последовательности ДНК зародышевого типа для генов вариабельной области человеческих тяжелой и легкой цепей можно найти в базе данных человеческих последовательностей зародышевого типа "VBase" (доступной в Интернете по адресу www.mrc-cpe.cam.ac.uk/vbase), а также в Kabat, E. A., et al., 1991 Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242; Tomlinson, I. M., et al., 1992 J. Mol. Biol. 227:776-798; и Cox, J. P. L. et al., 1994 Eur. J Immunol. 24:827-836. Например, последовательности ДНК зародышевого типа для генов вариабельной области человеческих тяжелой и легкой цепей и перегруппированные последовательности антител можно найти в базе данных "IMGT" (доступной в Интернете по адресу www.imgt.org; см. Lefranc, M.P. et al., 1999 Nucleic Acids Res. 27:209-212).
Примером последовательностей каркасных областей для применения в антителах и их антигенсвязывающих фрагментах по настоящему изобретению являются последовательности, которые являются структурно сходными с последовательностями каркасных областей, применяемыми в отобранных антителах и их антигенсвязывающих фрагментах по настоящему изобретению, например, консенсусные последовательности и/или последовательности каркасных областей, применяемые в моноклональных антителах по настоящему изобретению. Последовательности CDR1, 2 и 3 VH и последовательности CDR1, 2 и 3 VL могут быть привиты на каркасные области, которые имеют последовательность, идентичную той, что обнаруживается в гене иммуноглобулина зародышевого типа, из которого получена последовательность каркасной области, или последовательности CDR могут быть привиты на каркасные области, которые содержат одну или несколько мутаций по сравнению с последовательностями зародышевого типа. Например, было обнаружено, что в определенных случаях благоприятной является мутация остатков в пределах каркасных областей для сохранения или повышения способности антитела к связыванию с антигеном (см., например, патенты США №№ 5530101; 5585089; 5693762 и 6180370 авторства Queen et al.).
Другой тип модификации вариабельной области заключается в мутации аминокислотных остатков в пределах CDR1-, CDR2- и/или CDR3-областей VH и/или VL с улучшением таким образом одного или нескольких свойств связывания (например, аффинности) антитела, представляющего интерес, что известно как "созревание аффинности". Для введения мутации(мутаций) можно осуществлять сайт-направленный мутагенез или ПЦР-опосредованный мутагенез, и эффект в отношении связывания антитела или другого функционального свойства, представляющего интерес, можно оценивать в анализах in vitro или in vivo, описанных в данном документе и приведенных в разделе "Примеры". Можно вводить консервативные модификации (которые обсуждались выше). Мутации могут представлять собой аминокислотные замены, добавления или делеции. Более того, как правило, изменяют не более одного, двух, трех, четырех или пяти остатков в пределах CDR-области.
Можно использовать широкий спектр каркасных структур или остовов антител/иммуноглобулинов при условии, что полученный в результате полипептид содержит по меньшей мере одну связывающую область, которая специфично связывается с ENTPD2 (например, белком ENTPD2 человека). Такие каркасные структуры или остовы включают 5 основных идиотипов человеческих иммуноглобулинов, их антигенсвязывающих фрагментов и включают иммуноглобулины других видов животных, предпочтительно имеющие гуманизированные составляющие. Антитела с одной тяжелой цепью, такие как идентифицированные у верблюдовых, представляют особый интерес в этом отношении. Специалисты в данной области продолжают обнаруживать и разрабатывать новые каркасные структуры, остовы и фрагменты.
В одном аспекте настоящее изобретение относится к способу получения неиммуноглобулиновых антител с использованием неиммуноглобулиновых остовов, на которые можно привить CDR по настоящему изобретению. Можно использовать известные или будущие неиммуноглобулиновые каркасные структуры и остовы, при условии, что они содержат связывающую область, специфичную в отношении белка-мишени ENTPD2. Известные неиммуноглобулиновые каркасные структуры или остовы включают без ограничения фибронектин (Compound Therapeutics, Inc., Уолтем, Массачусетс), анкирин (Molecular Partners AG, Цюрих, Швейцария), доменные антитела (Domantis, Ltd., Кембридж, Массачусетс и Ablynx NV, Звейнарде, Бельгия), липокалин (Pieris Proteolab AG, Фрайзинг, Германия), небольшие модульные иммунофармацевтические средства (Trubion Pharmaceuticals Inc., Сиэтл, Вашингтон), максиантитела (Avidia, Inc., Маунтин-Вью, Калифорния), белок A (Affibody AG, Швеция) и аффилин (гамма-кристаллин или убиквитин) (Scil Proteins GmbH, Галле, Германия).
Фибронектиновые остовы имеют в своей основе домен фибронектина III типа (например, десятый модуль фибронектина III типа (10 домен Fn3)). Домен фибронектина III типа имеет 7 или 8 бета-тяжей, которые распределены между двумя бета-складчатыми слоями, которые сами упакованы внахлест друг с другом с образованием сердцевины белка и при этом дополнительно содержат петли (аналогичные CDR), которые соединяют бета-тяжи друг с другом и являются доступными для растворителя. По меньшей мере три такие петли присутствуют на каждом краю сэндвича из бета-складчатых слоев, где край представляет собой границу белка, перпендикулярную направлению бета-тяжей (см. патент США № 6818418). Эти остовы на основе фибронектина не относятся к иммуноглобулинам, хотя их общая укладка близко сходна с таковой у наименьшего функционального фрагмента антитела - вариабельной области тяжелой цепи, которая содержит полную антигенраспознающую единицу в IgG верблюда и ламы. Благодаря этой структуре неиммуноглобулиновое антитело имитирует свойства связывания с антигеном, которые являются сходными по своей природе и аффинности со свойствами антител. Эти остовы можно применять в стратегии случайного выбора и перетасовки петель in vitro, которая является сходной с процессом созревания аффинности антител in vivo. Эти молекулы на основе фибронектина можно применять в качестве остовов, при этом петлевые области молекулы могут быть заменены на CDR по настоящему изобретению с помощью стандартных методик клонирования.
Анкириновая технология основана на применении белков с модулями с анкириновыми повторами в качестве остовов для переноса вариабельных областей, которые можно применять для связывания с различными мишенями. Модуль с анкириновым повтором представляет собой полипептид из 33 аминокислот, состоящий из двух антипараллельных альфа-спиралей и бета-изгиба. Связывание вариабельных областей оптимизируют главным образом путем применения рибосомного дисплея.
Авимеры получают из природного белка, содержащего A-домен, такого как LRP-1. Эти домены используются по своей природе для белок-белковых взаимодействий, и у человека более 250 белков имеют в основе своей структуры A-домены. Авимеры состоят из ряда различных мономерных (2-10) "A-доменов", связанных посредством аминокислотных линкеров. Авимеры, которые могут связываться с антигеном-мишенью, можно создавать с помощью методики, описанной, например, в публикациях заявок на патент США №№ 20040175756; 20050053973; 20050048512 и 20060008844.
Аффинные лиганды-аффитела представляют собой небольшие простые белки, состоящие из трехспирального пучка на основе остова из одного из IgG-связывающих доменов белка A. Белок A представляет собой поверхностный белок бактерии Staphylococcus aureus. Этот доменный остов состоит из 58 аминокислот, 13 из которых выбраны случайным образом для создания библиотек аффител с большим количеством вариантов лигандов (см., например, патент США № 5831012). Молекулы аффител имитируют антитела, они имеют молекулярную массу 6 кДа в сравнении с молекулярной массой антител, которая составляет 150 кДа. Несмотря на свой небольшой размер, связывающий участок в молекулах аффител является сходным с таковым у антитела.
Антикалины представляют собой продукты, разработанные компанией Pieris ProteoLab AG. Их получают из липокалинов - широко распространенной группы небольших и устойчивых белков, которые обычно участвуют в физиологическом транспорте или запасании химически чувствительных или нерастворимых соединений. Несколько природных липокалинов встречаются в тканях или биологических жидкостях человека. Архитектура белков напоминает иммуноглобулины с гипервариабельными петлями поверх жесткого каркаса. Тем не менее, в противоположность антителам или их рекомбинантным фрагментам липокалины состоят из одной полипептидной цепи со 160-180 аминокислотными остатками, при этом они лишь незначительно превышают по размеру один домен иммуноглобулина. Набор из четырех петель, которые образуют связывающий карман, проявляет выраженную структурную пластичность и допускает наличие ряда боковых цепей. Таким образом, связывающий участок можно видоизменить с помощью фирменного способа для того, чтобы распознавать заданные молекулы-мишени различной формы с высокой аффинностью и специфичностью. Один белок из семейства липокалинов - билин-связывающий белок (BBP) из Pieris brassicae - применяли для разработки антикалинов посредством осуществления мутагенеза набора из четырех петель. Одним примером заявки на патент, в которой описываются антикалины, является PCT-публикация № WO 199916873.
Молекулы аффилинов представляют собой небольшие белки, отличные от иммуноглобулинов, которые разработаны с конкретными видами аффинности в отношении белков и малых молекул. Новые молекулы аффилинов можно очень быстро отобрать из двух библиотек, каждая из которых имеет в своей основе отличный от других каркасный белок человеческого происхождения. Молекулы аффилинов не проявляют какой-либо структурной гомологии с белками, представляющими собой иммуноглобулины. В настоящее время используется два аффилиновых остова, один из которых представляет собой гамма-кристаллин, являющийся структурным белком хрусталика глаза человека, а другой представляет собой белок из суперсемейства "убиквитинов". Оба человеческих остова являются весьма небольшими, проявляют стабильность при высоких температурах и являются наиболее устойчивыми к изменениям pH и денатурирующим средствам. Эта высокая стабильность в основном обусловлена развернутой бета-складчатой структурой белков. Примеры белков, полученных из гамма-кристаллина, описаны в WO 200104144, а примеры "убиквитиноподобных" белков описаны в WO 2004106368.
Миметики эпитопов белков (PEM) представляют собой циклические пептидоподобные молекулы среднего размера (MW 1-2 кДа), имитирующие бета-шпилечные вторичные структуры белков - основную вторичную структуру, участвующую в белок-белковых взаимодействиях.
Сконструированные антитела и их антигенсвязывающие фрагменты по настоящему изобретению включают те, в которых были осуществлены модификации в остатках каркасных областей в пределах VH и/или VL, например, для улучшения свойств антитела. Как правило, такие модификации каркасных областей осуществляют для уменьшения иммуногенности антитела. Например, один подход заключается в осуществлении "обратной мутации" одного или нескольких остатков каркасных областей с восстановлением соответствующей последовательности зародышевого типа. Более конкретно, антитело, которое подверглось соматической мутации, может содержать остатки каркасных областей, которые отличаются от последовательности зародышевого типа, из которой получено антитело. Такие остатки могут быть идентифицированы посредством сравнения последовательностей каркасных областей антитела с последовательностями зародышевого типа, из которых получено антитело. Для возвращения последовательностей каркасных областей к их конфигурации зародышевого типа можно осуществлять "обратные" соматические мутации с восстановлением последовательности зародышевого типа посредством, например, сайт-направленного мутагенеза. Также предполагается, что такие "подвергнутые обратной мутации" антитела охватываются настоящим изобретением.
Другой тип модификации каркасной области предусматривает мутацию одного или нескольких остатков в пределах каркасной области или даже в пределах одной или нескольких CDR-областей для удаления T-клеточных эпитопов со снижением таким образом потенциальной иммуногенности антитела. Данный подход также называется "деиммунизацией" и более подробно описан в публикации заявки на патент США № 20030153043 авторства Carr et al.
В качестве дополнения или альтернативы модификациям, осуществляемым в пределах каркасных или CDR-областей, антитела по настоящему изобретению можно конструировать таким образом, чтобы они содержали модификации в пределах Fc-области, как правило, для изменения одного или нескольких функциональных свойств антитела, таких как период полужизни в сыворотке крови, фиксация комплемента, связывание с Fc-рецептором и/или антигензависимая клеточная цитотоксичность. Кроме того, антитело по настоящему изобретению может быть химически модифицировано (например, к антителу могут быть присоединены один или несколько химических компонентов), или оно может быть модифицировано с изменением характера его гликозилирования, опять-таки для изменения одного или нескольких функциональных свойств антитела. Каждый из этих вариантов осуществления более подробно описан ниже. Нумерация остатков в Fc-области производится согласно EU-индексу по Kabat.
В одном варианте осуществления шарнирную область CH1 модифицируют таким образом, что изменяется число цистеиновых остатков в шарнирной области, например, увеличивается или уменьшается. Этот подход дополнительно описан в патенте США № 5677425 авторства Bodmer et al. Число цистеиновых остатков в шарнирной области CH1 изменяют, например, с целью облегчения сборки легких и тяжелых цепей или с целью увеличения или уменьшения стабильности антитела.
В другом варианте осуществления фрагмент Fc-шарнирная область антитела подвергают мутации для уменьшения биологического периода полужизни антитела. Более конкретно, одну или несколько аминокислотных мутаций вводят в область контакта между доменами CH2-CH3 фрагмента Fc-шарнирная область, вследствие чего антитело характеризуется нарушенным связыванием с белком A стафилококка (SpA) по сравнению со связыванием нативного домена Fc-шарнирная область с SpA. Этот подход описан более подробно в патенте США № 6165745 авторства Ward et al.
В другом варианте осуществления антитело модифицируют для увеличения его биологического периода полужизни. Возможны различные подходы. Например, можно вводить одну или несколько из следующих мутаций: T252L, T254S, T256F, как описано в патенте США № 6277375 авторства Ward. В качестве альтернативы для увеличения биологического периода полужизни антитело можно изменить в пределах CH1- или CL-области таким образом, чтобы оно содержало эпитоп связывания рецептора реутилизации, образованный двумя петлями CH2-домена Fc-области IgG, как описано в патентах США №№ 5869046 и 6121022 авторства Presta et al.
В одном варианте осуществления Fc-область изменяют посредством замены по меньшей мере одного аминокислотного остатка другим аминокислотным остатком с целью изменения эффекторных функций антитела. Например, одну или несколько аминокислот можно заменить другим аминокислотным остатком таким образом, чтобы антитело характеризовалось измененной аффинностью в отношении эффекторного лиганда, но сохраняло способность к связыванию с антигеном исходного антитела. Эффекторный лиганд, аффинность в отношении которого изменяют, может представлять собой, например, Fc-рецептор или компонент C1 системы комплемента. Этот подход описан более подробно в патентах США №№ 5624821 и 5648260, оба авторства Winter et al.
В другом варианте осуществления одну или несколько аминокислот, выбранных из аминокислотных остатков, можно заменить другим аминокислотным остатком таким образом, чтобы антитело характеризовалось измененным связыванием с C1q и/или сниженной или устраненной комплементзависимой цитотоксичностью (CDC). Этот подход описан более подробно в патенте США № 6194551 авторства Idusogie et al.
В другом варианте осуществления один или несколько аминокислотных остатков изменяют, чтобы таким образом изменить способность антитела к фиксации комплемента. Этот подход дополнительно описан в PCT-публикации WO 94/29351 авторства Bodmer et al.
В некоторых вариантах осуществления ENTPD2-связывающие антитела или их антигенсвязывающие фрагменты содержат константную область IgG1 человека. В некоторых вариантах осуществления константная область IgG1 человека включает в себя Fc-область.
В некоторых вариантах осуществления Fc-область ENTPD2-связывающих антител или их антигенсвязывающих фрагментов содержит одну или несколько мутаций, опосредующих сниженную или отсутствующую антителозависимую клеточную цитотоксичность (ADCC) или комплементзависимую цитотоксичность (CDC). В некоторых вариантах осуществления аминокислотные остатки L234 и L235 в константной области IgG1 заменены на A234 и A235. В некоторых вариантах осуществления аминокислотный остаток N267 в константной области IgG1 заменен на A267. В некоторых вариантах осуществления аминокислотные остатки D265 и P329 в константной области IgG1 заменены на A265 и A329. В определенных вариантах осуществления Fc-область необязательно содержит мутацию или комбинацию мутаций, придающие сниженную эффекторную функцию, выбранные из любой из D265A, P329A, P329G, N297A, D265A/P329A, D265A/N297A, L234/L235A, P329A/L234A/L235A, и P329G/L234A/L235A. В некоторых вариантах осуществления Fc-область содержит мутацию или комбинацию мутаций, придающие сниженную эффекторную функцию, выбранные из любой из D265A, P329A, P329G, N297A, D265A/P329A, D265A/N297A, L234/L235A, P329A/L234A/L235A, и P329G/L234A/L235A (все положения указаны согласно нумерации EU).
В еще одном варианте осуществления Fc-область модифицируют для увеличения способности антитела опосредовать антителозависимую клеточную цитотоксичность (ADCC) и/или для увеличения аффинности антитела в отношении Fc-гамма-рецептора посредством модификации одной или нескольких аминокислот. Этот подход дополнительно описан в PCT-публикации WO 00/42072 авторства Presta. Более того, связывающие участки в IgG1 человека для Fc-гамма RI, Fc-гамма RII, Fc-гамма RIII и FcRn были картированы, и были описаны варианты с улучшенным связыванием (см. Shields, R. L. et al., 2001 J. Biol. Chem. 276:6591-6604). Например, Fc-область может содержать мутацию или комбинацию мутаций, придающие увеличенную эффекторную функцию, выбранные из любой из S239D, I332E, A330L, S298A, E333A, E333S, K334A, K236A, K236W, F243L, P247I, D280H, K290S, R292P, S298D, S298V, Y300L, V305I, A339D, A339Q, A339T, P396L (все положения указаны согласно нумерации EU).
В еще одном варианте осуществления модифицируют характер гликозилирования антитела. Например, может быть получено агликозилированное антитело (т. е. антитело без гликозилирования). Характер гликозилирования можно изменять, например, для увеличения аффинности антитела в отношении антигена. Такие модификации углеводов можно осуществлять, например, посредством изменения одного или нескольких сайтов гликозилирования в пределах последовательности антитела. Например, можно произвести одну или несколько аминокислотных замен, которые приводят к устранению одного или нескольких сайтов гликозилирования в каркасной части вариабельной области, устраняя таким образом гликозилирование в этом сайте. Такое агликозилирование может увеличивать аффинность антитела в отношении антигена. Такой подход описан более подробно в патентах США №№ 5714350 и 6350861 авторства Co et al.
Дополнительно или в качестве альтернативы может быть получено антитело, которое характеризуется измененным типом гликозилирования, как, например, гипофукозилированное антитело, имеющее уменьшенные количества фукозильных остатков, или антитело, имеющее увеличенное содержание структур с остатком GlcNAc в точке ветвления. Было продемонстрировано, что такие измененные паттерны гликозилирования увеличивают способность антител к ADCC. Такие модификации углеводов можно осуществлять, например, посредством экспрессии антитела в клетке-хозяине с измененным механизмом гликозилирования. Клетки с измененным механизмом гликозилирования были описаны в уровне техники, и их можно использовать в качестве клеток-хозяев, в которых экспрессируются рекомбинантные антитела по настоящему изобретению, с получением таким образом антитела с измененным характером гликозилирования. Например, в EP 1176195 авторства Hang et al. описывается линия клеток с функциональным нарушением гена FUT8, который кодирует фукозилтрансферазу, вследствие чего антитела, экспрессирующиеся в такой линии клеток, демонстрируют гипофукозилирование. В PCT-публикации WO 03/035835 авторства Presta описывается вариант линии клеток CHO - клетки Lecl3 с пониженной способностью к присоединению фукозы к углеводам, связанным с Asn(297), что также приводит к гипофукозилированию антител, экспрессирующихся в такой клетке-хозяине (см. также Shields, R. L. et al., 2002 J. Biol. Chem. 277:26733-26740). В PCT-публикации WO 99/54342 авторства Umana et al. описываются линии клеток, сконструированные для экспрессии гликозилтрансфераз, модифицирующих гликопротеины (например, бета-(1,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII)), благодаря чему антитела, экспрессирующиеся в сконструированных линиях клеток, демонстрируют увеличенное содержание структур с остатком GlcNAc в точке ветвления, что приводит к увеличению активности ADCC у антител (см. также Umana et al., 1999 Nat. Biotech. 17:176-180).
В некоторых вариантах осуществления антитело к ENTPD2 относится к изотипу IgG1 с одной или несколькими мутациями (например, по сравнению с Fc-областью дикого типа того же изотипа). В некоторых вариантах осуществления одна или несколько мутаций выбраны из N297A, N297Q (Bolt S et al. (1993) Eur J Immunol 23:403-411), D265A, L234A, L235A (McEarchern et al., (2007) Blood, 109:1185-1192), C226S, C229S (McEarchern et al., (2007) Blood, 109:1185-1192), P238S (Davis et al., (2007) J Rheumatol, 34:2204-2210), E233P, L234V (McEarchern et al., (2007) Blood, 109:1185-1192), P238A, A327Q, A327G, P329A (Shields RL. et al., (2001) J Biol Chem. 276(9):6591-604), K322A, L234F, L235E (Hezareh et al., (2001) J Viral 75, 12161-12168; Oganesyan et al., (2008). Acta Crystallographica 64, 700-704), P331S (Oganesyan et al., (2008) Acta Crystallographica 64, 700-704), T394D (Wilkinson et al. (2013) MAbs 5(3): 406-417), A330L, M252Y, S254T и/или T256E, где положение аминокислоты указано в соответствии с системой нумерации EU или Kabat. В определенных вариантах осуществления Fc-область дополнительно содержит аминокислотную делецию в положении, соответствующем глицину 236 в соответствии с системой нумерации EU или Kabat.
В некоторых вариантах осуществления антитело относится к изотипу IgG1 и имеет константную область тяжелой цепи, которая содержит мутацию C220S в соответствии с системой нумерации EU или Kabat.
В некоторых вариантах осуществления Fc-область содержит одну или несколько мутаций, выбранных из L234F, L235E, P331S, D265A и/или N297Q, в соответствии с системой нумерации EU или Kabat. В некоторых вариантах осуществления Fc-область содержит одну или несколько мутаций, выбранных из L234A, L235A, D265A, P329A, N297A, N297Q в соответствии с системой нумерации EU или Kabat.
В определенных вариантах осуществления антитело относится к изотипу IgG2. В некоторых вариантах осуществления антитело содержит константную область IgG2 человека. В некоторых вариантах осуществления константная область IgG2 человека включает в себя Fc-область. В некоторых вариантах осуществления Fc-область содержит одну или несколько модификаций. Например, в некоторых вариантах осуществления Fc-область содержит одну или несколько мутаций (например, по сравнению с Fc-областью дикого типа того же изотипа). В некоторых вариантах осуществления одна или несколько мутаций выбраны из V234A, G237A, P238S, H268A, H268E, H268Q, V309L, N297A, N297Q, V309L, A330S, P331S, C232S, C233S, M252Y, S254T, и/или T256E, где положение аминокислоты указано в соответствии с системой нумерации EU или Kabat.
В определенных вариантах осуществления антитело относится к изотипу IgG4. В некоторых вариантах осуществления антитело содержит константную область IgG4 человека. В некоторых вариантах осуществления константная область IgG4 человека включает в себя Fc-область. В некоторых вариантах осуществления Fc-область содержит одну или несколько модификаций. Например, в некоторых вариантах осуществления Fc-область содержит одну или несколько мутаций (например, по сравнению с Fc-областью дикого типа того же изотипа). В некоторых вариантах осуществления одна или несколько мутаций выбраны из E233P, F234V, L234A, L235A, G237A, E318A (Hutchins et al. (1995) Proc Natl Acad Sci USA, 92:11980-11984), S228P, L236E, S241P, L248E (Reddy et al., (2000) J Immunol,164:1925-1933; Angal et al., (1993) Mol Immunol. 30(1):105-8; US 8614299 B2), T394D, M252Y, S254T, T256E, N297A и/или N297Q, где положение аминокислоты указано в соответствии с системой нумерации EU или Kabat.
В некоторых вариантах осуществления Fc-область дополнительно содержит одну или несколько дополнительных мутаций, выбранных из M252Y, S254T и/или T256E, где положение аминокислоты указано в соответствии с системой нумерации EU или Kabat.
В некоторых вариантах осуществления один или несколько вариантов IgG1, описанных в данном документе, можно использовать в комбинации с мутацией A330L (Lazar et al., (2006) Proc Natl Acad Sci USA, 103:4005-4010) или одной или несколькими из мутаций L234F, L235E и/или P331S (Sazinsky et al., (2008) Proc Natl Acad Sci USA, 105:20167-20172), где положение аминокислоты указано в соответствии с системой нумерации EU или Kabat, для устранения активации комплемента. В некоторых вариантах осуществления варианты IgG, описанные в данном документе, можно использовать в комбинации с одной или несколькими мутациями для улучшения периода полужизни антитела в сыворотке крови человека (например, мутациями M252Y, S254T, T256E в соответствии с системой нумерации EU или Kabat) (Dall'Acqua et al., (2006) J Biol Chem, 281:23514-23524; и Strohl et al., (2009) Current Opinion in Biotechnology, 20:685-691).
В некоторых вариантах осуществления вариант IgG4 по настоящему изобретению можно использовать в комбинации с мутацией S228P в соответствии с системой нумерации EU или Kabat (Angal et al., (1993) Mol Immunol, 30:105-108) и/или с одной или несколькими мутациями, описанными в Peters et al., (2012) J Biol Chem. 13;287(29):24525-33) для улучшения стабилизации антитела.
В некоторых вариантах осуществления антитело имеет Fc-область, выбранную из Fc-области IgG2, Fc-области IgG4 или гибридной Fc-области IgG2/IgG4.
Антитела верблюдовых
У белков, представляющих собой антитела, полученные из представителей семейства, к которому относятся двугорбые верблюды и одногорбые верблюды (Camelus bactrianus и Camelus dromaderius), в том числе представителей из Нового Света, таких как виды лам (Lama pacos, Lama glama и Lama vicugna), были определены характеристики размера, сложности структуры и антигенности у субъектов-людей. В определенных антителах IgG из этого семейства млекопитающих, которые обнаруживаются в природе, отсутствуют легкие цепи, и, следовательно, они по своей структуре отличаются от типичной четырехцепочечной четвертичной структуры, имеющей две тяжелые и две легкие цепи, в антителах от других животных. См. PCT/EP93/02214 (WO 94/04678, опубликованная 3 марта 1994 г.).
Область антитела верблюдовых, которая представляет собой небольшой отдельный вариабельный домен, идентифицированный как VHH, можно получить с помощью генной инженерии с получением небольшого белка, характеризующегося высокой аффинностью в отношении мишени, что дает в результате полученный из антитела низкомолекулярный белок, известный как "нанотело верблюдовых". См. патент США № 5759808, выданный 2 июня 1998 г.; см. также Stijlemans, B. et al., 2004 J Biol Chem 279: 1256-1261; Dumoulin, M. et al., 2003 Nature 424: 783-788; Pleschberger, M. et al. 2003 Bioconjugate Chem 14: 440-448; Cortez-Retamozo, V. et al. 2002 Int J Cancer 89: 456-62; и Lauwereys, M. et al. 1998 EMBO J 17: 3512-3520. Сконструированные библиотеки антител и фрагментов антител верблюдовых являются коммерчески доступными, например, от Ablynx, Гент, Бельгия. Как и в случае с другими антителами и их антигенсвязывающими фрагментами, происходящими из организма, отличного от человека, аминокислотную последовательность антитела верблюдовых можно изменить рекомбинантным путем с получением последовательности, которая более близко напоминает человеческую последовательность, т. е. нанотело можно "гуманизировать". Таким образом можно дополнительно снижать природную низкую антигенность антител верблюдовых у людей.
Нанотело верблюдовых имеет молекулярную массу, составляющую примерно одну десятую от массы молекулы IgG человека, и данный белок имеет физический диаметр, составляющий лишь несколько нанометров. Одним следствием небольшого размера является способность нанотел верблюдовых связываться с антигенными сайтами, которые являются функционально невидимыми для белков, представляющих собой антитела, большего размера, т. е. нанотела верблюдовых являются применимыми в качестве реагентов для выявления антигенов, которые в ином случае являются скрытыми при использовании классических иммунологических методик, и в качестве возможных терапевтических средств. Таким образом, еще одним следствием небольшого размера является то, что нанотело верблюдовых может осуществлять ингибирование в результате связывания с конкретным сайтом в бороздке или узкой щели белка-мишени и, следовательно, может служить в роли, которая более близко напоминает функцию классического низкомолекулярного лекарственного средства, чем таковую у классического антитела.
Низкая молекулярная масса и компактный размер дополнительно приводят к тому, что нанотела верблюдовых являются чрезвычайно термостабильными, стабильными к экстремальным значениям pH и к протеолитическому расщеплению и характеризуются слабой антигенностью. Другим следствием является то, что нанотела верблюдовых легко перемещаются из кровеносной системы в ткани и даже пересекают гематоэнцефалический барьер и могут обеспечивать лечение нарушений, которые поражают нервную ткань. Нанотела могут дополнительно способствовать транспорту лекарственных средств через гематоэнцефалический барьер. См. заявку на патент США 20040161738, опубликованную 19 августа 2004 г. Эти признаки в сочетании с низкой антигенностью у людей указывают на большой терапевтический потенциал. Кроме того, эти молекулы могут полностью экспрессироваться в прокариотических клетках, таких как E. coli, и они экспрессируются в виде слитых белков с белками бактериофага и являются функциональными.
Соответственно, признаком настоящего изобретения является антитело или нанотело верблюдовых, характеризующееся высокой аффинностью в отношении ENTPD2. В одном варианте осуществления в данном документе антитело или нанотело верблюдовых продуцируется в естественных условиях у животного из семейства верблюдовых, т. е. оно продуцируется верблюдовыми после иммунизации с помощью ENTPD2 или его пептидного фрагмента с применением методик, описанных в данном документе для других антител. В качестве альтернативы ENTPD2-связывающее нанотело верблюдовых конструируют, т. е. получают посредством отбора, например, из фаговой библиотеки, в которой отображены подвергнутые соответствующему мутагенезу белки, представляющие собой нанотела верблюдовых, с применением процедур пэннинга с ENTPD2 в качестве мишени, как описано в примерах в данном документе. Сконструированные нанотела можно дополнительно адаптировать к конкретным требованиям с помощью генной инженерии так, чтобы они имели период полужизни у получающего их субъекта, составляющий от 45 минут до двух недель. В конкретном варианте осуществления антитело или нанотело верблюдовых получают посредством прививания последовательностей CDR тяжелой или легкой цепей человеческих антител по настоящему изобретению на последовательности каркасных областей нанотела или однодоменного антитела, как описано, например, в PCT/EP93/02214.
Биспецифические молекулы и поливалентные антитела
В другом аспекте настоящее изобретение относится к биспецифическим или полиспецифическим молекулам, содержащим ENTPD2-связывающее антитело или его фрагмент по настоящему изобретению. Антитело по настоящему изобретению или его антигенсвязывающие области можно дериватизировать или связать с другой функциональной молекулой, например, с другим пептидом или белком (например, другим антителом или лигандом рецептора) с получением биспецифической молекулы, которая связывается с по меньшей мере двумя различными связывающими участками или молекулами-мишенями. Антитело по настоящему изобретению фактически можно дериватизировать или связать с более чем одной другой функциональной молекулой с получением полиспецифических молекул, которые связываются с более чем двумя различными связывающими участками и/или молекулами-мишенями; также предполагается, что такие полиспецифические молекулы охватываются используемым в данном документе термином "биспецифическая молекула". Для создания биспецифической молекулы по настоящему изобретению антитело по настоящему изобретению можно функционально связать (например, посредством химического связывания, генетического слияния, нековалентной ассоциации или иным образом) с одной или несколькими другими связывающими молекулами, такими как другое антитело, фрагмент антитела, пептид или связывающий миметик, в результате чего получают биспецифическую молекулу.
Соответственно, настоящее изобретение включает биспецифические молекулы, содержащие по меньшей мере один первый элемент, обеспечивающий специфичность связывания с ENTPD2, и второй элемент, обеспечивающий специфичность связывания со вторым эпитопом-мишенью. Например, второй эпитоп-мишень представляет собой другой эпитоп ENTPD2, отличающийся от первого эпитопа-мишени.
Кроме того, в настоящем изобретении, в котором биспецифическая молекула является полиспецифической, молекула может дополнительно содержать третий элемент, обеспечивающий специфичность связывания, в дополнение к таковым для первого и второго эпитопов-мишеней.
В одном варианте осуществления биспецифические молекулы по настоящему изобретению содержат в качестве элемента, обеспечивающего специфичность связывания, по меньшей мере одно антитело или его фрагмент антитела, в том числе, например, Fab, Fab', F(ab')2, Fv или одноцепочечный Fv. Антитело также может представлять собой димер легких цепей или тяжелых цепей или любой их минимальный фрагмент, такой как Fv или одноцепочечная конструкция, которая описана в Ladner et al., патент США № 4946778.
Диатела представляют собой двухвалентные биспецифические молекулы, в которых VH- и VL-домены экспрессируются в одной полипептидной цепи и соединены линкером, который является слишком коротким, чтобы обеспечивать возможность спаривания между двумя доменами в одной и той же цепи. VH- и VL-домены спариваются с комплементарными доменами другой цепи, создавая таким образом два антигенсвязывающих участка (см., например, Holliger et al., 1993 Proc. Natl. Acad. Sci. USA 90:6444-6448; Poljak et al., 1994 Structure 2:1121-1123). Диатела можно получать посредством экспрессии двух полипептидных цепей со структурой VHA-VLB и VHB-VLA (конфигурация VH-VL) либо VLA-VHB и VLB-VHA (конфигурация VL-VH) в одной и той же клетке. Большинство из них могут экспрессироваться в растворимой форме у бактерий. Одноцепочечные диатела (scDb) получают путем соединения двух полипептидных цепей, образующих диатело, с линкером размером примерно 15 аминокислотных остатков (см. Holliger and Winter, 1997 Cancer Immunol. Immunother., 45 (3-4):128-30; Wu et al., 1996 Immunotechnology, 2 (1):21-36). scDb могут экспрессироваться у бактерий в растворимой активной мономерной форме (см. Holliger and Winter, 1997 Cancer Immunol. Immunother., 45 (34): 128-30; Wu et al., 1996 Immunotechnology, 2 (1):21-36; Pluckthun and Pack, 1997 Immunotechnology, 3 (2): 83-105; Ridgway et al., 1996 Protein Eng., 9 (7):617-21). Диатело можно сливать с Fc с получением "дидиатела" (см. Lu et al., 2004 J. Biol. Chem., 279 (4):2856-65).
Другие антитела, которые могут использоваться в биспецифических молекулах по настоящему изобретению, представляют собой мышиные, химерные и гуманизированные моноклональные антитела.
Биспецифические молекулы по настоящему изобретению можно получить посредством конъюгирования составляющих элементов, обеспечивающих специфичность связывания, с помощью способов, известных из уровня техники. Например, каждый элемент, обеспечивающий специфичность связывания, в биспецифической молекуле можно получить отдельно, а затем конъюгировать с другими. Если элементы, обеспечивающие специфичность связывания, представляют собой белки или пептиды, то для ковалентного конъюгирования можно применять ряд связывающих или сшивающих средств. Примеры сшивающих средств включают белок A, карбодиимид, N-сукцинимидил-5-ацетилтиоацетат (SATA), 5,5'-дитиобис(2-нитробензойную кислоту) (DTNB), о-фенилендималеимид (oPDM), N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) и сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-SMCC) (см., например, Karpovsky et al., 1984 J. Exp. Med. 160:1686; Liu, M A et al., 1985 Proc. Natl. Acad. Sci. USA 82:8648). Другие способы включают способы, описанные в Paulus, 1985 Behring Ins. Mitt. No. 78, 118-132; Brennan et al., 1985 Science 229:81-83, и Glennie et al., 1987 J. Immunol. 139: 2367-2375. Конъюгирующие средства представляют собой SATA и сульфо-SMCC, оба из которых доступны от Pierce Chemical Co. (Рокфорд, Иллинойс).
Если элементы, обеспечивающие специфичность связывания, представляют собой антитела, их можно конъюгировать посредством образования связей между сульфгидрильными группами C-концевых шарнирных областей двух тяжелых цепей. В конкретном варианте осуществления шарнирную область модифицируют таким образом, чтобы она содержала нечетное количество остатков с сульфгидрильной группой, например, один, перед конъюгированием.
В качестве альтернативы оба элемента, обеспечивающие специфичность связывания, могут быть закодированы в одном и том же векторе и могут экспрессироваться и собираться в одной и той же клетке-хозяине. Этот способ является особенно применимым в случае, когда биспецифическая молекула представляет собой слитый белок mAb X mAb, mAb X Fab, Fab X F(ab')2 или лиганд X Fab. Биспецифическая молекула по настоящему изобретению может представлять собой одноцепочечную молекулу, содержащую одно одноцепочечное антитело и детерминанту связывания, или одноцепочечную биспецифическую молекулу, содержащую две детерминанты связывания. Биспецифические молекулы могут содержать по меньшей мере две одноцепочечные молекулы. Способы получения биспецифических молекул описаны, например, в патенте США № 5260203; патенте США № 5455030; патенте США № 4881175; патенте США № 5132405; патенте США № 5091513; патенте США № 5476786; патенте США № 5013653; патенте США № 5258498 и патенте США № 5482858.
Связывание биспецифических молекул со своими специфическими мишенями можно подтвердить, например, с помощью твердофазного иммуноферментного анализа (ELISA), радиоиммунологического анализа (REA), FACS-анализа, биологического анализа (например, ингибирования роста) или вестерн-блот-анализа. В каждом из этих анализов обычно выявляют наличие комплексов белок-антитело, представляющих особый интерес, путем использования меченого реагента (например, антитела), специфичного в отношении комплекса, представляющего интерес.
В другом аспекте в настоящем изобретении предусмотрены поливалентные соединения, содержащие по меньшей мере две идентичные или отличающиеся антигенсвязывающие части антител и их антигенсвязывающих фрагментов по настоящему изобретению, связывающиеся с ENTPD2. Антигенсвязывающие части могут быть связаны друг с другом посредством слияния белков или ковалентной или нековалентной связи. В качестве альтернативы способы связывания были описаны для биспецифических молекул. Четырехвалентные соединения можно получить, например, путем сшивания антител и их антигенсвязывающих фрагментов по настоящему изобретению с антителом или антигенсвязывающим фрагментом, которые связываются с константными областями антител и их антигенсвязывающих фрагментов по настоящему изобретению, например, Fc или шарнирной областью.
Тримеризующий домен описан, например, в патенте EP 1012280B1, принадлежащем Borean. Пентамеризующие модули описаны, например, в PCT/EP97/05897.
В некоторых вариантах осуществления ENTPD2-связывающие антитела или их антигенсвязывающие фрагменты представляют собой биспецифические антитела, которые распознают первый антиген и второй антиген. В некоторых вариантах осуществления первый антиген представляет собой ENTPD2 человека или его встречающийся в природе вариант. В некоторых вариантах осуществления второй антиген может представлять собой белок, липид, полисахарид или гликолипид, экспрессирующийся на одной или нескольких опухолевых клетках.
Антитела с удлиненным периодом полужизни
В настоящем изобретении предусмотрены антитела, которые специфично связываются с ENTPD2 (например, белком ENTPD2 человека) и характеризуются удлиненным периодом полужизни in vivo.
Многие факторы могут влиять на период полужизни белка in vivo. Например, к ним относятся фильтрация в почках, метаболизм в печени, разрушение посредством протеолитических ферментов (протеаз) и иммунные ответы (например, нейтрализация белка посредством антител и поглощение макрофагами и дендритными клетками). Для продления периода полужизни антител и их антигенсвязывающих фрагментов по настоящему изобретению можно применять ряд стратегий. Например, это можно осуществлять посредством химического связывания с полиэтиленгликолем (PEG), PEG ReCODE, остовом антитела, полисиаловой кислотой (PSA), гидроксиэтилкрахмалом (HES), альбуминсвязывающими лигандами и углеводными защитными фрагментами; посредством генетического слияния с белками, связывающимися с белками сыворотки крови, такими как альбумин, IgG, FcRn и трансферрин; посредством связывания (генетического или химического) с другими связывающими компонентами, которые связываются с белками сыворотки крови, такими как нанотела, Fab, дарпины, авимеры, аффитела и антикалины; посредством генетического слияния с rPEG, альбумином, доменом альбумина, альбуминсвязывающими белками и Fc; или посредством включения в наноносители, составы с медленным высвобождением или медицинские устройства.
Для продления циркуляции антител в сыворотке крови in vivo молекулы инертного полимера, такого как высокомолекулярный PEG, могут быть присоединены к антителам или их фрагментам с использованием или без использования линкера с несколькими функциональными группами посредством сайт-специфического конъюгирования PEG с N- или С-концом антител либо посредством эпсилон-аминогрупп, присутствующих в лизиновых остатках. Для пегилирования антитела, как правило, осуществляют реакцию антитела, его антигенсвязывающего фрагмента с полиэтиленгликолем (PEG), таким как реакционноспособный сложный эфир или альдегидное производное PEG, в условиях, при которых одна или несколько групп PEG присоединяются к антителу или фрагменту антитела. Пегилирование можно осуществлять посредством реакции ацилирования или реакции алкилирования с реакционноспособной молекулой PEG (или аналогичным реакционноспособным водорастворимым полимером). Предполагается, что используемый в данном документе термин "полиэтиленгликоль" охватывает любую из форм PEG, которые применялись для дериватизации других белков, как, например, моно(C1-C10)алкокси- или арилоксиполиэтиленгликоль или полиэтиленгликоль-малеимид. В одном варианте осуществления антитело, которое должно быть пегилировано, представляет собой агликозилированное антитело. Будет применяться дериватизация с помощью линейного или разветвленного полимера, которая приводит к минимальной потере биологической активности. Степень конъюгирования можно тщательно контролировать посредством SDS-PAGE и масс-спектрометрии для обеспечения надлежащего конъюгирования молекул PEG с антителами. Непрореагировавший PEG можно отделить от конъюгатов антитело-PEG посредством эксклюзионной или ионообменной хроматографии. PEG-дериватизированные антитела можно тестировать в отношении активности связывания, а также в отношении эффективности in vivo с применением способов, хорошо известных специалистам в данной области, например, посредством иммунологических анализов, описанных в данном документе. Способы пегилирования белков известны из уровня техники и могут применяться по отношению к антителам и их антигенсвязывающим фрагментам по настоящему изобретению. См., например, EP 0154316 авторства Nishimura et al. и EP 0401384 авторства Ishikawa et al.
Другие модифицированные технологии пегилирования включают преобразующую технологию химически ортогонального направленного конструирования (PEG ReCODE), при которой химически определенные боковые цепи включаются в состав биосинтетических белков посредством преобразующей системы, которая содержит тРНК-синтетазу и тРНК. Данная технология позволяет включать более чем 30 новых аминокислот в состав биосинтетических белков в клетках E. coli, дрожжей и млекопитающих. тРНК включает стандартную аминокислоту в любом месте, где расположен янтарный стоп-кодон, преобразовывая янтарный стоп-кодон в кодон, который сигнализирует о включении химически определенной аминокислоты.
Технология рекомбинантного пегилирования (rPEG) также может применяться для удлинения периода полужизни в сыворотке крови. Данная технология предусматривает генетическое слияние неструктурированного белкового хвоста из 300-600 аминокислот с существующим фармацевтическим белком. Поскольку кажущаяся молекулярная масса такой неструктурированной белковой цепи в приблизительно 15 раз превышает ее фактическую молекулярную массу, период полужизни белка в сыворотке крови значительно увеличивается. В отличие от традиционного пегилирования, для которого требуется химическое конъюгирование и повторная очистка, способ изготовления значительно упрощается, и продукт является однородным.
Полисиалирование представляет собой другую технологию, в которой используется природный полимер полисиаловая кислота (PSA) для продления периода активности и улучшения стабильности терапевтических пептидов и белков. PSA представляет собой полимер сиаловой кислоты (сахара). При применении для доставки лекарственных средств на основе белков и терапевтических пептидов полисиаловая кислота обеспечивает защитную микросреду при конъюгировании. Это увеличивает период активности терапевтического белка в кровотоке и предотвращает его распознавание иммунной системой. Полимер PSA в естественных условиях обнаруживается в организме человека. Его начали использовать некоторые бактерии, которые эволюционировали на протяжении миллионов лет, для покрытия им своих клеточных стенок. Эти полисиалированные в естественных условиях бактерии вследствие этого были способны благодаря молекулярной мимикрии противодействовать защитной системе организма. PSA можно с легкостью получить из таких бактерий в больших количествах и с заданными физическими характеристиками. Бактериальная PSA является полностью неиммуногенной, даже в случае, когда она связана с белками, так как она является химически идентичной PSA в организме человека.
Другая технология предусматривает применение производных гидроксиэтилкрахмала ("HES"), связанных с антителами. HES представляет собой модифицированный природный полимер, полученный из крахмала восковидной кукурузы, и может метаболизироваться посредством ферментов организма. Растворы HES обычно вводят для восполнения недостающего объема крови и улучшения реологических свойств крови. Модификация антитела с помощью HES позволяет продлить период полужизни в кровотоке благодаря увеличению стабильности молекулы, а также благодаря снижению почечного клиренса, что приводит к увеличению биологической активности. Изменяя различные параметры, такие как молекулярная масса HES, можно адаптировать к конкретным требованиям широкий спектр конъюгатов HES-антитело.
Антитела, характеризующиеся увеличенным периодом полужизни in vivo, также можно получать путем введения одной или нескольких аминокислотных модификаций (т. е. замен, вставок или делеций) в константный домен IgG или его FcRn-связывающий фрагмент (предпочтительно Fc или фрагмент домена шарнирная область-Fc). См., например, международную публикацию № WO 98/23289; международную публикацию № WO 97/34631 и патент США № 6277375.
Кроме того, антитела можно конъюгировать с альбумином, чтобы сделать антитело или фрагмент антитела более стабильными in vivo или чтобы они характеризовались более длительным периодом полужизни in vivo. Методики являются хорошо известными из уровня техники, см., например, международные публикации №№ WO 93/15199, WO 93/15200 и WO 01/77137 и европейский патент № EP 413622.
Стратегии по увеличению периода полужизни являются особенно применимыми для нанотел, связывающих средств на основе фибронектина и других антител или белков, для которых необходим увеличенный период полужизни in vivo.
Конъюгаты антител
В настоящем изобретении предусмотрены антитела или их антигенсвязывающие фрагменты, которые специфично связываются с внеклеточным доменом ENTPD2 (например, белка ENTPD2 человека), рекомбинантно слитые или химически конъюгированные (в том числе посредством как ковалентного, так и нековалентного конъюгирования) с гетерологичным белком или полипептидом (или его антигенсвязывающим фрагментом, предпочтительно с полипептидом размером по меньшей мере 10, по меньшей мере 20, по меньшей мере 30, по меньшей мере 40, по меньшей мере 50, по меньшей мере 60, по меньшей мере 70, по меньшей мере 80, по меньшей мере 90 или по меньшей мере 100 аминокислот) с получением слитых белков. В частности, в настоящем изобретении предусмотрены слитые белки, содержащие антигенсвязывающий фрагмент антитела, описанного в данном документе (например, Fab-фрагмент, Fd-фрагмент, Fv-фрагмент, F(ab)2-фрагмент, VH-домен, CDR VH, VL-домен или CDR VL) и гетерологичный белок, полипептид или пептид. Способы слияния или конъюгирования белков, полипептидов или пептидов с антителом или фрагментом антитела известны из уровня техники. См., например, патенты США №№ 5336603, 5622929, 5359046, 5349053, 5447851 и 5112946; европейские патенты №№ EP 307434 и EP 367166; международные публикации №№ WO 96/04388 и WO 91/06570; Ashkenazi et al., 1991, Proc. Natl. Acad. Sci. USA 88: 10535-10539; Zheng et al., 1995, J. Immunol. 154:5590-5600; и Vil et al., 1992, Proc. Natl. Acad. Sci. USA 89:11337-11341.
Дополнительные слитые белки можно получать посредством методик перетасовки генов, перетасовки мотивов, перетасовки экзонов и/или перетасовки кодонов (в совокупности называемых "перетасовкой ДНК"). Перетасовку ДНК можно использовать для изменения форм активности антител и их антигенсвязывающих фрагментов по настоящему изобретению (например, для получения антител и их антигенсвязывающих фрагментов с более высокими значениями аффинности и более низкими значениями скорости диссоциации). См. в целом патенты США №№ 5605793, 5811238, 5830721, 5834252 и 5837458; Patten et al., 1997, Curr. Opinion Biotechnol. 8:724-33; Harayama, 1998, Trends Biotechnol. 16(2):76-82; Hansson, et al., 1999, J. Mol. Biol. 287:265-76; и Lorenzo and Blasco, 1998, Biotechniques 24(2):308-313. Антитела и их антигенсвязывающие фрагменты или кодируемые антитела и их антигенсвязывающие фрагменты можно изменять посредством воздействия на них случайного мутагенеза с помощью ПЦР с внесением ошибок, случайной вставки нуклеотидов или других способов перед рекомбинацией. Полинуклеотид, кодирующий антитело, его антигенсвязывающий фрагмент, которые специфично связываются с ENTPD2 (например, белком ENTPD2 человека), может быть подвергнут рекомбинации с одним или несколькими компонентами, мотивами, секциями, частями, доменами, фрагментами и т. д. одной или нескольких гетерологичных молекул.
Более того, антитела и их антигенсвязывающие фрагменты можно слить с маркерными последовательностями, такими как пептид, для облегчения очистки. В одном варианте осуществления маркерная аминокислотная последовательность представляет собой гексагистидиновый пептид (SEQ ID NO: 1010), такой как метка, представленная в векторе pQE (QIAGEN, Inc., 9259 Eton Avenue, Чатсворт, Калифорния, 91311), среди прочих, многие из которых являются коммерчески доступными. Например, как описано в Gentz et al., 1989, Proc. Natl. Acad. Sci. USA 86:821-824, гексагистидин (SEQ ID NO: 1010) обеспечивает удобную очистку слитого белка. Другие пептидные метки, применимые для очистки, включают без ограничения гемагглютининовую ("HA") метку, которая соответствует эпитопу, полученному из белка гемагглютинина вируса гриппа (Wilson et al., 1984, Cell 37:767), и "FLAG"-метку.
В одном варианте осуществления антитела и их антигенсвязывающие фрагменты по настоящему изобретению конъюгированы с диагностическим или выявляемым средством. Такие антитела могут быть применимыми для контроля или прогнозирования начала проявления, развития, прогрессирования и/или степени тяжести заболевания или нарушения в рамках процедуры клинического тестирования, такой как определение эффективности конкретной терапии. Такую диагностику и выявление можно осуществлять посредством связывания антитела с выявляемыми веществами, в том числе без ограничения с различными ферментами, такими как без ограничения пероксидаза хрена, щелочная фосфатаза, бета-галактозидаза или ацетилхолинэстераза; простетическими группами, такими как без ограничения стрептавидин/биотин и авидин/биотин; флуоресцентными материалами, такими как без ограничения умбеллиферон, флуоресцеин, флуоресцеинизотиоцианат, родамин, дихлортриазиниламинофлуоресценин, дансилхлорид или фикоэритрин; люминесцентными материалами, такими как без ограничения люминол; биолюминесцентными материалами, такими как без ограничения люцифераза, люциферин и экворин; радиоактивными материалами, такими как без ограничения йод (131I, 125I, 123I и 121I), углерод (14C), сера (35S), тритий (3H), индий (115In, 113In, 112In и 111In), технеций (99Tc), таллий (201Ti), галлий (68Ga, 67Ga), палладий (103Pd), молибден (99Mo), ксенон (133Xe), фтор (18F), 153Sm, 177Lu, 159Gd, 149Pm, 140La, 175Yb, 166Ho, 90Y, 47Sc, 186Re, 188Re, 142Pr, 105Rh, 97Ru, 68Ge, 57Co, 65Zn, 85Sr, 32P, 153Gd, 169Yb, 51Cr, 54Mn, 75Se, 113Sn и олово-117; и позитронно-активными металлами, применяющимися в различных методах позитронно-эмиссионной томографии, а также ионами нерадиоактивных парамагнитных металлов.
Кроме того, антитело, его антигенсвязывающий фрагмент могут быть конъюгированы с терапевтическим компонентом или компонентом, представляющим собой лекарственное средство. Терапевтические компоненты или компоненты, представляющие собой лекарственные средства, не следует рассматривать как ограниченные классическими химическими терапевтическими средствами. Например, компонент, представляющий собой лекарственное средство, может представлять собой белок, пептид или полипептид, обладающие необходимой биологической активностью. Такие белки могут включать, например, токсин, такой как абрин, рицин A, экзотоксин синегнойной палочки, холерный токсин или дифтерийный токсин; белок, такой как фактор некроза опухоли, интерферон альфа, интерферон бета, фактор роста нервов, фактор роста тромбоцитов, тканевой активатор плазминогена, проапоптотическое средство, антиангиогенное средство или модификатор биологического ответа, такой как, например, лимфокин.
Более того, антитело можно конъюгировать с терапевтическими компонентами, такими как ион радиоактивного металла, как, например, излучатель альфа-частиц, такой как 213Bi, или с макроциклическими хелаторами, применимыми для конъюгирования ионов радиоактивных металлов, в том числе без ограничения 131In, 131Lu, 131Y, 131Ho, 131Sm, с полипептидами. В одном варианте осуществления макроциклический хелатор представляет собой 1,4,7,10-тетраазациклододекан-N, N',N'',N'''-тетрауксусную кислоту (DOTA), которая может быть присоединена к антителу посредством линкерной молекулы. Такие линкерные молекулы являются широко известными из уровня техники и описаны в Denardo et al., 1998, Clin Cancer Res. 4 (10):2483-90; Peterson et al., 1999, Bioconjug. Chem. 10 (4):553-7; и Zimmerman et al., 1999, Nucl. Med. Biol. 26 (8):943-50, каждая из которых включена посредством ссылки во всей своей полноте.
Методики конъюгирования терапевтических компонентов с антителами являются хорошо известными, см., например, Amon et al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy", в Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. (eds.), pp. 243-56 (Alan R. Liss, Inc. 1985); Hellstrom et al., "Antibodies For Drug Delivery", в Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), pp. 623-53 (Marcel Dekker, Inc. 1987); Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", в Monoclonal Antibodies 84: Biological And Clinical Applications, Pinchera et al. (eds.), pp. 475-506 (1985); "Analysis, Results, And Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy", в Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), pp. 303-16 (Academic Press 1985), и Thorpe et al., 1982, Immunol. Rev. 62:119-58.
Антитела также могут быть прикреплены к твердым подложкам, которые являются особенно применимыми для иммунологических анализов или очистки антигена-мишени. Такие твердые подложки включают без ограничения стекло, целлюлозу, полиакриламид, нейлон, полистирол, поливинилхлорид или полипропилен.
Нуклеиновые кислоты, кодирующие антитела, векторы и клетки-хозяева
Также в данном документе предусмотрены нуклеиновые кислоты, кодирующие антитело или его антигенсвязывающий фрагмент, описанные в данном документе. Такие нуклеиновые кислоты могут кодировать полипептиды, содержащие сегменты или домены антител к ENTPD2 или их антигенсвязывающих фрагментов, описанных выше. Такие нуклеиновые кислоты или полинуклеотиды могут кодировать по меньшей мере одну CDR-область и обычно все три CDR-области из тяжелой или легкой цепи антител к ENTPD2, описанных в данном документе. Такие нуклеиновые кислоты или полинуклеотиды также могут кодировать всю или по существу всю последовательность вариабельной области тяжелой цепи и/или легкой цепи антител к ENTPD2, описанных в данном документе. Такие нуклеиновые кислоты или полинуклеотиды также могут кодировать как вариабельную область, так и константную область антитела. Вследствие вырожденности генетического кода каждая из аминокислотных последовательностей иммуноглобулинов будет кодироваться рядом последовательностей нуклеиновых кислот. Например, настоящее изобретение относится к первой и второй нуклеиновым кислотам, кодирующим соответственно вариабельные области тяжелой и легкой цепей молекулы антитела к ENTPD2 человека, выбранной из одной или нескольких молекул антител, раскрытых в данном документе. Нуклеиновая кислота может содержать нуклеотидную последовательность, представленную в таблице 1, или последовательность, по существу идентичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90%, 95% или 99% идентичностью последовательности по отношению к ней или которая отличается на не более чем 3, 6, 15, 30 или 45 нуклеотидов от последовательностей, показанных в таблице 1).
В определенных вариантах осуществления нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере одну, две или три CDR или гипервариабельные петли из вариабельной области тяжелой цепи, имеющей аминокислотную последовательность, представленную в таблице 1, или последовательность, по существу гомологичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90%, 95% или 99% идентичностью последовательности по отношению к ней и/или которая имеет одну или несколько замен, например, консервативных замен). В других вариантах осуществления нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере одну, две или три CDR или гипервариабельные петли из вариабельной области легкой цепи, имеющей аминокислотную последовательность, представленную в таблице 1, или последовательность, по существу гомологичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90%, 95% или 99% идентичностью последовательности по отношению к ней и/или которая имеет одну или несколько замен, например, консервативных замен). В еще одном другом варианте осуществления нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере одну, две, три, четыре, пять или шесть CDR или гипервариабельных петель из вариабельных областей тяжелой и легкой цепей, имеющих аминокислотную последовательность, представленную в таблице 1, или последовательность, по существу гомологичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90%, 95% или 99% идентичностью последовательности по отношению к ней и/или которая имеет одну или несколько замен, например, консервативных замен).
В определенных вариантах осуществления нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере одну, две или три CDR или гипервариабельные петли из вариабельной области тяжелой цепи, имеющую нуклеотидную последовательность, представленную в таблице 1, или последовательность, по существу гомологичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90%, 95% или 99% идентичностью последовательности по отношению к ней). В другом варианте осуществления нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере одну, две или три CDR или гипервариабельные петли из вариабельной области легкой цепи, имеющую нуклеотидную последовательность, представленную в таблице 1, или последовательность, по существу гомологичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90%, 95% или 99% идентичностью последовательности по отношению к ней). В еще одном варианте осуществления нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере одну, две, три, четыре, пять или шесть CDR или гипервариабельных петель из вариабельных областей тяжелой и легкой цепей, имеющую нуклеотидную последовательность, представленную в таблице 1, или последовательность, по существу гомологичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90%, 95% или 99% идентичностью последовательности по отношению к ней).
Полинуклеотидные последовательности можно получать с помощью твердофазного синтеза ДНК de novo или с помощью ПЦР-мутагенеза существующей последовательности, кодирующей ENTPD2-связывающее антитело или его связывающий фрагмент. Прямой химический синтез нуклеиновых кислот можно осуществлять с помощью способов, известных из уровня техники, таких как фосфотриэфирный способ из Narang et al., 1979, Meth. Enzymol. 68:90; фосфодиэфирный способ из Brown et al., Meth. Enzymol. 68:109, 1979; диэтилфосфорамидитный способ из Beaucage et al., Tetra Lett., 22:1859, 1981; и способ с использованием твердой подложки из патента США № 4458066. Введение мутаций в полинуклеотидную последовательность с помощью ПЦР можно осуществлять, как описано, например, в PCR Technology: Principles and Applications for DNA Amplification, H. A. Erlich (Ed.), Freeman Press, NY, N.Y., 1992; PCR Protocols: A Guide to Methods and Applications, Innis et al. (Ed.), Academic Press, San Diego, Calif., 1990; Mattila et al., Nucleic Acids Res. 19:967, 1991; и Eckert et al., PCR Methods and Applications 1:17, 1991.
Также в данном документе предусмотрены векторы (например, векторы экспрессии), содержащие нуклеиновую кислоту, кодирующую полипептид, содержащий сегмент или домен антител к ENTPD2 или их антигенсвязывающих фрагментов, описанных в данном документе. Такие векторы можно использовать для экспрессии и/или получения ENTPD2-связывающих антител или их антигенсвязывающих фрагментов. Термин "вектор экспрессии" относится к молекуле нуклеиновой кислоты-переносчика, в которую может быть вставлена необходимая кодирующая последовательность для введения в клетку, где она может экспрессироваться. Вектор может представлять собой ДНК-вектор, РНК-вектор, плазмиду, космиду, или вирусный вектор, или искусственные хромосомы (см., например, Harrington et al., Nat Genet 15:345, 1997). Например, невирусные векторы, применимые для экспрессии ENTPD2-связывающих антител или их антигенсвязывающих фрагментов в клетках млекопитающих (например, человека), включают pThioHis A, B и C, pcDNA3.1/His, pEBVHis A, B и C (Invitrogen, Сан-Диего, Калифорния), векторы на основе MPSV и многочисленные другие векторы, известные из уровня техники, для экспрессии белков. Например, в одном классе векторов используются ДНК-элементы, которые получены из вирусов животных, таких как, например, вирус папилломы крупного рогатого скота, вирус полиомы, аденовирус, вирус осповакцины, бакуловирус, ретровирусы (вирус саркомы Рауса, MMTV или MOMLV) или вирус SV40. В другом классе векторов используются РНК-элементы, полученные из РНК-содержащих вирусов, таких как вирус леса Семлики, вирус восточного энцефалита лошадей и флавивирусы.
Применимые вирусные векторы включают векторы на основе любых из следующих вирусов: ретровирусов, лентивирусов, аденовирусов, аденоассоциированных вирусов, вирусов герпеса (например, вируса простого герпеса (HSV)), векторов на основе SV40, вируса папилломы, вируса Эпштейна-Барр HBP, вируса осповакцины, вируса Синдбис, вируса гриппа, реовируса, вируса ньюкаслской болезни (NDV), вируса кори, вируса везикулярного стоматита (VSV), парвовируса, полиовируса, поксвируса, вируса Сенека-Валли, вируса Коксаки, энтеровируса, вируса миксомы, вируса Мараба или вируса леса Семлики (SFV). См. Brent et al., выше; Smith, Annu. Rev. Microbiol. 49:807, 1995; и Rosenfeld et al., Cell 68:143, 1992.
В некоторых вариантах осуществления вектор представляет собой лентивирусный вектор. Векторы, полученные из ретровирусов, таких как лентивирус, являются подходящими инструментами для осуществления долговременного переноса генов, поскольку они обеспечивают долговременную стабильную интеграцию трансгена и его размножение в дочерних клетках. Лентивирусные векторы обладают дополнительным преимуществом по сравнению с векторами, полученными из онкоретровирусов, таких как вирусы лейкоза мышей, заключающимся в том, что ими можно трансдуцировать непролиферирующие клетки, такие как гепатоциты. Они также обладают дополнительным преимуществом, заключающимся в низкой иммуногенности. Ретровирусный вектор также может представлять собой, например, гамма-ретровирусный вектор. Гамма-ретровирусный вектор может содержать, например, промотор, сигнал упаковки (ψ), сайт связывания праймера (PBS), один или несколько (например, два) длинных концевых повторов (LTR) и трансген, представляющий интерес, например, ген, кодирующий CAR. В гамма-ретровирусном векторе могут отсутствовать структурные гены вирусов, такие как gag, pol и env. Иллюстративные гамма-ретровирусные векторы включают вирус лейкоза мышей (MLV), вирус некроза селезенки (SFFV) и вирус миелопролиферативной саркомы (MPSV), а также векторы, полученные из них. Другие гамма-ретровирусные векторы описаны, например, в Tobias Maetzig et al., "Gammaretroviral Vectors: Biology, Technology and Application" Viruses. 2011 Jun; 3(6): 677-713.
В некоторых вариантах осуществления вектор представляет собой вектор на основе аденоассоциированного вируса (AAV), например, вектор на основе рекомбинантного AAV (rAAV). "AAV" представляет собой аббревиатуру для аденоассоциированного вируса и может применяться в отношении самого вируса или его производных. Термин охватывает все подтипы как встречающихся в природе, так и рекомбинантных форм, за исключением случаев, когда требуется иное. Аббревиатура "rAAV" относится к рекомбинантному аденоассоциированному вирусу, также называемому вектором на основе рекомбинантного AAV (или "вектором на основе rAAV"). Термин "AAV" включает, например, AAV 1 типа (AAV1), AAV 2 типа (AAV2), AAV 3 типа (AAV3), AAV 4 типа (AAV4), AAV 5 типа (AAV5), AAV 6 типа (AAV6), AAV 7 типа (AAV7), AAV 8 типа (AAV8), AAV 9 типа (AAV9), AAV 10 типа (AAV10, в том числе AAVrh10), AAV 12 типа (AAV12), AAV птиц, AAV крупного рогатого скота, AAV собак, AAV лошадей, AAV приматов, AAV млекопитающих, отличных от приматов, и AAV овец. "AAV приматов" относится к AAV, который инфицирует приматов, "AAV млекопитающих, отличных от приматов" относится к AAV, который инфицирует млекопитающих, отличных от приматов, "AAV крупного рогатого скота" относится к AAV, который инфицирует млекопитающих, относящихся к крупному рогатому скоту, и т. д.
Геномные последовательности различных серотипов AAV, а также последовательности нативных инвертированных концевых повторов (ITR), белков Rep и субъединиц капсида известны из уровня техники. Такие последовательности можно найти в литературе или в общедоступных базах данных, таких как GenBank. См., например, №№ доступа в GenBank NC-002077 (AAV1), AF063497 (AAV1), NC-001401 (AAV2), AF043303 (AAV2), NC-001729 (AAV3), NC-001829 (AAV4), U89790 (AAV4), NC-006152 (AAV5), AF513851 (AAV7), AF513852 (AAV8) и NC-006261 (AAV8) или в публикациях, таких как WO2005033321 (AAV1-9), раскрытия которых включены в данный документ посредством ссылки. См. также, например, Srivastava et al. (1983) J. Virology 45:555; Chiorini et al. (1998) J. Virology 71:6823; Chiorini et al. (1999) J. Virology 73: 1309; Bantel-Schaal et al. (1999) J. Virology 73:939; Xiao et al. (1999) J. Virology 73:3994; Muramatsu et al. (1996) Virology 221:208; Shade et al. (1986) J. Virol. 58:921; Gao et al. (2002) Proc. Nat. Acad. Sci. USA 99: 11854; Moris et al. (2004) Virology 33:375-383; публикации международных заявок на патент WO 00/28061, WO 99/61601, WO 98/11244 и патент США № 6156303.
Используемый в данном документе термин "вектор на основе rAAV" относится к вектору на основе AAV, содержащему полинуклеотидную последовательность, происходящую не от AAV (т. е. полинуклеотид, гетерологичный по отношению к AAV), как правило, последовательность, представляющую интерес для генетической трансформации клетки. В некоторых вариантах осуществления гетерологичный полинуклеотид может быть фланкирован по меньшей мере одной и иногда двумя последовательностями инвертированных концевых повторов (ITR) AAV. Термин "вектор на основе rAAV" охватывает как векторные частицы на основе rAAV, так и векторные плазмиды на основе rAAV. Вектор на основе rAAV может быть однонитевым (ssAAV) либо самокомплементарным (scAAV). "Вирус AAV", или "вирусная частица AAV", или "векторная частица на основе rAAV" относится к вирусной частице, состоящей из по меньшей мере одного капсидного белка AAV (как правило, из всех капсидных белков AAV дикого типа) и заключенного в капсид полинуклеотидного вектора на основе rAAV. Если частица содержит гетерологичный полинуклеотид (т. е. полинуклеотид, отличный от генома AAV дикого типа, такой как трансген, который должен быть доставлен в клетку млекопитающего), она, как правило, называется "векторной частицей на основе rAAV" или просто "вектором на основе rAAV". Таким образом, получение частицы rAAV обязательно включает получение вектора на основе rAAV, такого как вектор, содержащийся в частице rAAV.
В некоторых вариантах осуществления вектор может представлять собой рекомбинантную молекулу ДНК, содержащую нуклеиновую кислоту, кодирующую антитело, которое связывается с белком ENTPD2 человека. Используемый в данном документе термин "рекомбинантный" означает, что вектор, полинуклеотид, полипептид или клетка представляют собой продукт различных комбинаций стадий клонирования, рестрикции или лигирования (например, в отношении полинуклеотида или полипептида, содержащегося в них) и/или других процедур, которые приводят к получению конструкции, отличающейся от продукта, обнаруживаемого в природе. Рекомбинантный вирус или вектор представляет собой вирусную частицу, содержащую рекомбинантный полинуклеотид. Данные термины соответственно включают продукты репликации исходной полинуклеотидной конструкции и дочерние продукты исходной вирусной конструкции.
Рекомбинантный вектор, как правило, содержит одну или несколько регуляторных последовательностей, функционально связанных с последовательностью нуклеиновой кислоты, которая должна экспрессироваться. Термин "регуляторная последовательность" включает промоторы, энхансеры и другие элементы, контролирующие экспрессию (например, сигналы полиаденилирования). Регуляторные последовательности включают последовательности, которые управляют конститутивной экспрессией нуклеотидной последовательности, а также тканеспецифичные регуляторные и/или индуцируемые последовательности. Векторы экспрессии могут также содержать элементы, предназначенные для оптимизации стабильности матричной РНК и ее способности к трансляции в клетках-хозяевах, и/или маркеры для отбора по чувствительности к лекарственному средству для создания постоянных стабильных клеточных клонов, экспрессирующих антитело, которое связывается с белком ENTPD2 человека. Конструкция вектора экспрессии может зависеть от таких факторов, как выбор клетки-хозяина, которая должна быть трансформирована, необходимый уровень экспрессии белка и т. п. Общие способы создания таких рекомбинантных векторов экспрессии можно найти в Sambrook and Russell eds. (2001) Molecular Cloning: A Laboratory Manual, 3rd edition; сериях Ausubel et al. eds. (2007 г., с дополнениями и исправлениями до 2010 г.) Current Protocols in Molecular Biology, среди других, известных из уровня техники.
"Промотор" представляет собой контролирующую последовательность, которая представляет собой область последовательности нуклеиновой кислоты, с помощью которой контролируются инициация и скорость транскрипции. Он может содержать генетические элементы, с которыми могут связываться регуляторные белки и молекулы, такие как РНК-полимераза, и другие факторы транскрипции. Фразы "функционально расположенный", "функционально связанный", "под контролем" и "под транскрипционным контролем" означают, что промотор находится в надлежащих функциональных местоположении и/или ориентации по отношению к последовательности нуклеиновой кислоты для контроля инициации транскрипции и/или экспрессии этой последовательности. Промотор можно использовать или не использовать в сочетании с "энхансером", который относится к цис-действующей регуляторной последовательности, участвующей в активации транскрипции последовательности нуклеиновой кислоты.
Промотор может быть естественным образом связан с геном или последовательностью, а также может быть получен посредством выделения 5'-некодирующих последовательностей, расположенных выше кодирующего сегмента и/или экзона. Такой промотор может называться "эндогенным". Аналогичным образом, энхансер может быть естественным образом связан с последовательностью нуклеиновой кислоты и быть расположенным ниже или выше данной последовательности. В качестве альтернативы, определенные преимущества будут достигнуты посредством расположения кодирующего сегмента нуклеиновой кислоты под контролем рекомбинантного или гетерологичного промотора, который относится к промотору, обычно не связанному с последовательностью нуклеиновой кислоты в своей естественной среде. Рекомбинантный или гетерологичный энхансер также относится к энхансеру, обычно не связанному с последовательностью нуклеиновой кислоты в своей естественной среде. Такие промоторы или энхансеры могут включать промоторы или энхансеры из других генов, а также промоторы или энхансеры, выделенные из любой другой прокариотической клетки, вируса или эукариотической клетки, и промоторы или энхансеры, "не встречающиеся в природе", т. е. содержащие другие элементы других областей регуляции транскрипции и/или мутации, которые изменяют экспрессию. В дополнение к получению последовательностей нуклеиновых кислот промоторов и энхансеров синтетическим путем, последовательности можно получать с помощью технологии рекомбинантного клонирования и/или амплификации нуклеиновых кислот, например, ПЦР, совместно с композициями, раскрытыми в данном документе (см. US 4683202, US 5928906). Кроме того, предусматривается, что также можно использовать контролирующие последовательности, которые управляют транскрипцией и/или экспрессией последовательностей в неядерных органеллах, таких как митохондрии, хлоропласты и т. п.
Используемые промоторы могут быть конститутивными, индуцируемыми, синтетическими, ткане- или клеточноспецифичными и/или применимыми в подходящих условиях для управления экспрессией введенного сегмента ДНК на высоком уровне, что является преимущественным при крупномасштабном получении рекомбинантных белков и/или пептидов. Кроме того, также могут быть включены другие регуляторные элементы для улучшения экспрессии нуклеиновой кислоты, кодирующей антитело, которое связывается с белком ENTPD2 человека, например, энхансеры, сайт связывания рибосомы, последовательности терминации транскрипции и т. п.
В некоторых вариантах осуществления используется конститутивный промотор для обеспечения постоянной экспрессии антитела к ENTPD2 человека. Примеры конститутивного промотора включают без ограничения немедленно-ранний промотор цитомегаловируса (CMV), ранний промотор вируса обезьян 40 (SV40), промотор вируса опухоли молочной железы мышей (MMTV), промотор длинного концевого повтора (LTR) вируса иммунодефицита человека (HIV), промотор MoMuLV, промотор вируса лейкоза птиц, немедленно-ранний промотор вируса Эпштейна-Барр, промотор вируса саркомы Рауса, а также промоторы человеческих генов, такие как без ограничения промотор гена актина, промотор гена миозина, промотор гена фактора элонгации 1α, промотор гена гемоглобина и промотор гена креатинкиназы.
Индуцируемые промоторы также предусматриваются как часть настоящего изобретения. Использование индуцируемого промотора обеспечивает наличие молекулярного переключателя, способного включать экспрессию полинуклеотидной последовательности, с которой он функционально связан, если такая экспрессия требуется, или отключать экспрессию, если экспрессия не требуется. Примеры индуцируемых промоторов включают без ограничения металлотионеин-индуцируемый промотор, глюкокортикоид-индуцируемый промотор, прогестерон-индуцируемый промотор и тетрациклин-индуцируемый промотор.
В некоторых вариантах осуществления используется ткане- или клеточноспецифичный промотор для обеспечения экспрессии антитела к ENTPD2 человека только в конкретных тканях или клетках. Характерные особенности ткане- или клеточноспецифичных промоторов или элементов, а также анализы для определения характеристик их форм активности хорошо известны специалистам в данной области. Примеры включают промотор гена LIMK2 человека (Nomoto et al. 1999, Gene, 236(2):259-271), гена рецептора соматостатина 2 типа (Kraus et al., 1998, FEES Lett., 428(3): 165-170), гена эпидидимального белка, связывающего ретиноевую кислоту, мыши (Lareyre et al., 1999, J. Biol. Chem., 274(12):8282-8290), гена CD4 человека (Zhao-Emonet et al., 1998, Biochim. Biophys. Acta, 1442(2-3): 109-119), гена альфа-2-цепи коллагена (XI типа) мыши (Tsumaki, et al., 1998, J. Biol. Chem., 273(36):22861-22864), гена дофаминового рецептора D1A (Lee, et al., 1997, J. Auton. Nerv. Syst., 74(2-3):86-90), гена инсулиноподобного фактора роста II (Wu et al., 1997, Biochem. Biophys. Res. Commun., 233(1):221-226), гена тромбоцитарно-эндотелиальной молекулы 1 клеточной адгезии человека (Almendro et al., 1996, J. Immunol., 157(12):5411-5421), гена мышечной креатинкиназы (MCK) (Wang et al., Gene Ther. 2008 Nov;15(22):1489-99).
В некоторых вариантах осуществления используется синтетический промотор для обеспечения экспрессии антитела к ENTPD2 человека. Синтетические промоторы могут значительно превосходить природные промоторы по активности транскрипции. Например, можно выбрать синтетические промоторы, активность которых не отключается или не снижается под действием эндогенных клеточных механизмов или факторов. Другие элементы, в том числе сайты связывания транс-действующих факторов и энхансеры, могут быть вставлены в синтетический промотор для улучшения эффективности транскрипции. Синтетические промоторы можно рационально разработать и синтезировать химическим путем с объединением лучших признаков как синтетических, так и биологических промоторов. Синтетические олигонуклеотиды отжигают и лигируют посредством нескольких способов для создания полноразмерного химически синтезированного промотора. Синтетические промоторы могут представлять собой индуцируемые промоторы или промоторы, специфичные для типа клеток.
Для эффективной трансляции кодирующих последовательностей также может требоваться специфический сигнал инициации. Такие сигналы включают инициирующий кодон ATG или смежные последовательности. Может быть необходимым обеспечение наличия экзогенных сигналов контроля трансляции, в том числе инициирующего кодона ATG. Специалист обычной квалификации в данной области легко сможет определить это и обеспечить наличие необходимых сигналов. Хорошо известно, что инициирующий кодон должен быть "внутрирамочным" по отношению к рамке считывания необходимой кодирующей последовательности для обеспечения трансляции всей вставки. Экзогенные сигналы контроля трансляции и инициирующие кодоны могут быть природными либо синтетическими. Эффективность экспрессии можно усилить посредством включения подходящих элементов, представляющих собой энхансеры транскрипции.
Для экспрессии можно использовать любые подходящие клетки-хозяева, известные из уровня техники, например, клетки-хозяева, являющиеся клетками млекопитающих, бактериальные клетки-хозяева, дрожжевые клетки-хозяева, клетки-хозяева, являющиеся клетками насекомых, и т. д. Как прокариотические, так и эукариотические системы экспрессии являются широко доступными. В некоторых вариантах осуществления система экспрессии представляет собой систему экспрессии в клетках млекопитающих, такую как система экспрессии в клетках CHO. В некоторых вариантах осуществления нуклеиновая кислота может быть кодон-оптимизированной для облегчения экспрессии в необходимой клетке-хозяине. Будет важно использовать промотор и/или энхансер, который эффективно управляет экспрессией сегмента ДНК в типе клеток, органелле и организме, выбранных для экспрессии. Специалисты в области молекулярной биологии обычно знают об использовании комбинаций промоторов, энхансеров и типов клеток для экспрессии белков, например, см. Sambrook et al. (2001).
Большинство транскрибируемых эукариотических молекул РНК будут подвергаться сплайсингу РНК для удаления интронов из первичных транскриптов. При использовании векторов, содержащих геномные эукариотические последовательности, могут требоваться донорные и/или акцепторные сайты сплайсинга для обеспечения надлежащего процессинга транскрипта для экспрессии белка (см. Chandler et al., 1997, Proc. Natl. Acad. Sci. USA, 94(8):3596-601).
Векторы или конструкции по настоящему изобретению обычно будут содержать по меньшей мере один сигнал терминации. "Сигнал терминации" или "терминатор" состоит из последовательностей ДНК, участвующих в специфической терминации РНК-транскрипта РНК-полимеразой. Таким образом, в определенных вариантах осуществления предусматривается сигнал терминации, который завершает продуцирование РНК-транскрипта. Терминатор может быть необходим in vivo для достижения необходимых уровней первичного транскрипта. В эукариотических системах терминаторная область может также содержать специфические последовательности ДНК, которые позволяют осуществлять сайт-специфическое расщепление нового транскрипта таким образом, чтобы сделать доступным сайт полиаденилирования. Данные сигналы необходимы специализированной эндогенной полимеразе для добавления фрагмента из приблизительно 200 остатков A (поли-A) к 3'-концу транскрипта. Молекулы РНК, модифицированные с помощью данного поли-A-хвоста, по-видимому, являются более стабильными и транслируются более эффективно. Таким образом, в других вариантах осуществления, предусматривающих эукариот, предпочтительно, чтобы терминатор содержал сигнал для расщепления РНК, и более предпочтительно, чтобы сигнал терминатора способствовал полиаденилированию первичного транскрипта. Элементы терминатора и/или сайта полиаденилирования могут служить для повышения уровней первичного транскрипта и/или для сведения к минимуму сквозного прочитывания с переходом от кассеты к другим последовательностям. Терминаторы, предусмотренные для применения в настоящем изобретении, включают любой известный терминатор транскрипции, описанный в данном документе или известный специалисту обычной квалификации в данной области, в том числе без ограничения, например, терминирующие последовательности генов, такие как, например, терминатор гена гормона роста крупного рогатого скота или вирусные терминирующие последовательности, такие как, например, терминатор SV40. В определенных вариантах осуществления сигналом терминации может являться отсутствие транскрибируемой или транслируемой последовательности, например, вследствие усечения последовательности.
При экспрессии, в частности при эукариотической экспрессии, как правило, будет включен сигнал полиаденилирования для осуществления надлежащего полиаденилирования транскрипта. Считается, что природа сигнала полиаденилирования не имеет решающего значения для успешного осуществления настоящего изобретения на практике, и/или можно использовать любую такую последовательность. Предпочтительные варианты осуществления включают сигнал полиаденилирования SV40 и/или сигнал полиаденилирования гена гормона роста крупного рогатого скота, удобные и/или известные как хорошо функционирующие в различных клетках-мишенях. Полиаденилирование может увеличивать стабильность транскрипта или может облегчать цитоплазматический транспорт.
Для размножения вектора в клетке-хозяине он может содержать одну или несколько точек начала репликации (часто называемых "ori"), которые представляют собой специфическую последовательность нуклеиновой кислоты, в которой инициируется репликация. В качестве альтернативы можно использовать автономно реплицирующуюся последовательность (ARS), если клетка-хозяин представляет собой дрожжевую клетку.
В определенных вариантах осуществления настоящего изобретения клетки, содержащие конструкцию нуклеиновой кислоты по настоящему изобретению, можно идентифицировать in vitro или in vivo посредством включения маркера в вектор экспрессии. Такие маркеры будут придавать клетке идентифицируемое изменение, позволяющее легко идентифицировать клетки, содержащие вектор экспрессии. Обычно селектируемый маркер представляет собой маркер, который придает свойство, которое обеспечивает возможность отбора. Положительный селектируемый маркер представляет собой такой маркер, при котором наличие маркера обеспечивает возможность его отбора, тогда как отрицательный селектируемый маркер представляет собой такой маркер, при котором его наличие предотвращает его отбор. Пример положительного селектируемого маркера представляет собой маркер устойчивости к лекарственному средству.
Обычно включение селектируемого маркера для отбора по чувствительности к лекарственному средству способствует клонированию и идентификации трансформантов, например, гены, которые придают устойчивость к неомицину, пуромицину, гигромицину, DHFR, GPT, зеоцину и гистидинолу, являются применимыми селектируемыми маркерами. В дополнение к маркерам, придающим фенотип, который обеспечивает возможность установления различий между трансформантами на основе реализации условий, также предусматриваются другие типы маркеров, в том числе маркеры для скрининга, такие как GFP, применение которых основано на колориметрическом анализе. В качестве альтернативы можно использовать ферменты для скрининга, такие как тимидинкиназа вируса простого герпеса (HSV-tk) или хлорамфениколацетилтрансфераза (CAT). Специалист в данной области также будет знать, как использовать иммунологические маркеры, возможно в сочетании с FACS-анализом. Считается, что используемый маркер не важен при условии, что он способен экспрессироваться одновременно с нуклеиновой кислотой, кодирующей продукт гена. Дополнительные примеры селектируемых маркеров и маркеров для скрининга хорошо известны специалисту в данной области.
В векторах экспрессии также может быть предусмотрено положение последовательности сигнала секреции для образования слитого белка с полипептидами, кодируемыми вставленными последовательностями ENTPD2-связывающего антитела. Вставляемые последовательности ENTPD2-связывающего антитела чаще связывают с сигнальными последовательностями до включения в вектор. Векторы, которые должны использоваться для получения последовательностей, кодирующих вариабельные домены легкой и тяжелой цепей ENTPD2-связывающего антитела, иногда также кодируют константные области или их части. Такие векторы обеспечивают возможность экспрессии вариабельных областей в виде слитых белков с константными областями, что таким образом приводит к продуцированию интактных антител и их антигенсвязывающих фрагментов. Как правило, такие константные области являются человеческими.
При создании вектора экспрессии можно использовать вектор, содержащий сайт множественного клонирования (MCS), который представляет собой область нуклеиновой кислоты, содержащую несколько сайтов для рестрикционных ферментов, любой из которых можно использовать в сочетании со стандартной рекомбинантной технологией для расщепления вектора. См. Carbonelli et al., 1999, Levenson et al., 1998, и Cocea, 1997. "Расщепление рестрикционным ферментом" относится к каталитическому расщеплению молекулы нуклеиновой кислоты с помощью фермента, который функционирует только в конкретных местоположениях молекулы нуклеиновой кислоты. Множество таких рестрикционных ферментов являются коммерчески доступными. Применение таких ферментов широко известно специалистам в данной области. Часто вектор линеаризуют или фрагментируют с помощью рестрикционного фермента, который производит разрез в пределах MCS, для обеспечения лигирования экзогенных последовательностей с вектором. "Лигирование" относится к способу образования фосфодиэфирных связей между двумя фрагментами нуклеиновой кислоты, которые могут быть или не быть смежными друг с другом. Методики, предусматривающие рестрикционные ферменты и реакции лигирования, хорошо известны специалистам в области рекомбинантной технологии.
Способы введения векторов экспрессии, содержащих полинуклеотидные последовательности, представляющие интерес, варьируются в зависимости от типа клетки-хозяина. Например, трансфекцию с использованием хлорида кальция обычно используют для прокариотических клеток, тогда как обработку фосфатом кальция или электропорацию можно применять для других клеток-хозяев (см. в общих чертах Sambrook et al., выше). Другие способы включают, например, электропорацию, обработку фосфатом кальция, трансформацию, опосредованную липосомами, инъекцию и микроинъекцию, баллистические способы/генную пушку, виросомы, иммунолипосомы, конъюгаты поликатион:нуклеиновая кислота, "голую" ДНК, искусственные вирионы, слияние со структурным белком VP22 вируса герпеса, усиленное средством поглощение ДНК, трансдукцию ex vivo, слияние протопластов, ретровирусную трансдукцию, вирусную трансфекцию, липидную трансфекцию или другие традиционные методики. В случае слияния протопластов клетки выращивают в среде и подвергают скринингу в отношении соответствующей активности. Для долговременного получения рекомбинантных белков с высоким выходом зачастую будет необходима стабильная экспрессия. Например, линии клеток, которые стабильно экспрессируют полипептиды, можно получать с помощью векторов экспрессии, которые содержат вирусные точки начала репликации или эндогенные экспрессионные элементы и ген селектируемого маркера. После введения вектора клеткам можно предоставлять возможность роста в течение 1-2 дней в обогащенной среде перед их переносом в селективную среду. Задачей селектируемого маркера является придание устойчивости к факторам отбора, и его присутствие обеспечивает возможность роста клеток, которые успешно экспрессируют введенные последовательности, в селективной среде. Пролиферацию устойчивых стабильно трансфицированных клеток можно обеспечивать с применением методик культивирования тканей, соответствующих типу клеток. Способы и условия культивирования полученных в результате трансфицированных клеток и извлечения полученной молекулы антитела известны специалистам в данной области и могут быть изменены или оптимизированы в зависимости от конкретных используемых вектора экспрессии и клетки-хозяина, являющейся клеткой млекопитающего, исходя из настоящего описания.
Также в данном документе предусмотрены клетки, которые содержат любой из векторов экспрессии, описанных в данном документе. В некоторых вариантах осуществления настоящее изобретение относится к клетке-хозяину, которая содержит молекулу нуклеиновой кислоты, описанную в данном документе. Такие клетки могут представлять собой клетку-хозяина или терапевтическую клетку. Термины "клетка-хозяин" и "рекомбинантная клетка-хозяин" используются в данном документе взаимозаменяемо и относятся не только к конкретной рассматриваемой клетке, но и к потомству или потенциальному потомству такой клетки. Поскольку в последующих поколениях могут происходить определенные модификации из-за мутаций либо из-за влияний окружающей среды, такое потомство может в действительности не быть идентичным родительской клетке, но по-прежнему включаться в объем термина, используемого в данном документе.
В одном варианте осуществления клетки-хозяева модифицированы методами генной инженерии таким образом, что они содержат нуклеиновые кислоты, кодирующие молекулу антитела. В одном варианте осуществления клетки-хозяева модифицированы методами генной инженерии путем применения кассеты экспрессии. Фраза "кассета экспрессии" относится к нуклеотидным последовательностям, которые способны осуществлять экспрессию гена у хозяев, совместимых с такими последовательностями. Такие кассеты могут содержать промотор, открытую рамку считывания с интронами или без них и сигнал терминации. Также можно применять дополнительные факторы, необходимые или полезные при осуществлении экспрессии, такие как, например, индуцируемый промотор.
Клетки-хозяева, которые должны нести и экспрессировать цепи ENTPD2-связывающего антитела, могут представлять собой без ограничения эукариотическую клетку или прокариотическую клетку, такую как бактериальная клетка, клетка насекомого или клетка человека. E. coli является одним прокариотическим хозяином, применимым для клонирования и экспрессии полинуклеотидов по настоящему изобретению. Другие подходящие для применения микробные хозяева включают бацилл, таких как Bacillus subtilis, и других энтеробактерий, таких как Salmonella, Serratia и различные виды Pseudomonas. Для этих прокариотических хозяев также можно создать векторы экспрессии, которые, как правило, содержат последовательности, контролирующие экспрессию, совместимые с клеткой-хозяином (например, точку начала репликации). Кроме того, будет присутствовать любое количество разнообразных хорошо известных промоторов, как, например, лактозная промоторная система, триптофановая (trp) промоторная система, бета-лактамазная промоторная система или промоторная система из фага лямбда. Как правило, промоторы контролируют экспрессию, необязательно с помощью операторной последовательности, и имеют последовательности сайта связывания рибосомы и т. п. для инициации и завершения транскрипции и трансляции. Для экспрессии ENTPD2-связывающих полипептидов по настоящему изобретению также можно использовать другие микроорганизмы, такие как дрожжи. Также можно использовать клетки насекомых в комбинации с бакуловирусными векторами. Подходящие клетки насекомых включают без ограничения клетки Sf9.
В одном варианте осуществления клетки-хозяева, являющиеся клетками млекопитающих, используют для экспрессии и получения ENTPD2-связывающих антител по настоящему изобретению. Например, они могут представлять собой гибридомную линию клеток, экспрессирующих эндогенные гены иммуноглобулинов (например, клетку гибридомы из миеломы 1D6.C9), либо линию клеток млекопитающих, несущих экзогенный вектор экспрессии (например, клетку миеломы SP2/0). Они включают любую нормальную мортальную или нормальную или аномальную иммортальную клетку животного или человека. Например, был разработан ряд подходящих линий клеток-хозяев, способных секретировать интактные иммуноглобулины, в том числе линии клеток CHO, различные линии клеток Cos, клетки HeLa, линии клеток миеломы, трансформированные B-клетки и гибридомы. Применение тканевой культуры клеток млекопитающих для экспрессии полипептидов в общих чертах обсуждается, например, в Winnacker, From Genes to Clones, VCH Publishers, N.Y., N.Y., 1987. Векторы экспрессии для клеток-хозяев, являющихся клетками млекопитающих, могут содержать последовательности, контролирующие экспрессию, такие как точка начала репликации, промотор и энхансер (см., например, Queen, et al., Immunol. Rev. 89:49-68, 1986), а также необходимые сайты процессинга информации, такие как сайты связывания рибосомы, сайты сплайсинга РНК, сайты полиаденилирования и последовательности терминаторов транскрипции. Эти векторы экспрессии обычно содержат промоторы, полученные из генов млекопитающих или из вирусов млекопитающих. Подходящие промоторы могут быть конститутивными, специфичными для типа клеток, специфичными для стадии развития и/или модулируемыми или регулируемыми. Применимые промоторы включают без ограничения промотор гена металлотионеина, конститутивный большой поздний промотор аденовируса, дексаметазон-индуцируемый промотор MMTV, промотор SV40, промотор pol III MRP, конститутивный промотор MPSV, тетрациклин-индуцируемый промотор CMV (такой как немедленно-ранний промотор CMV человека), конститутивный промотор CMV и комбинации промотор-энхансер, известные из уровня техники.
Клетка-хозяин может использоваться для получения или экспрессии антитела, которое связывается с белком ENTPD2 человека. Соответственно, настоящее изобретение также относится к способам получения антитела, которое связывается с белком ENTPD2 человека, с помощью клетки-хозяина. В одном варианте осуществления способ включает культивирование клетки-хозяина (в которую был введен рекомбинантный вектор экспрессии, кодирующий антитело) в подходящей среде таким образом, чтобы продуцировалось антитело, которое связывается с белком ENTPD2 человека. В другом варианте осуществления способ дополнительно включает выделение антитела из среды или клетки-хозяина. Подходящие эукариотические клетки включают без ограничения клетки Vero, клетки HeLa, клетки COS, клетки CHO, клетки HEK293, клетки BHK и клетки MDCKII.
Получение моноклональных антител
Моноклональные антитела (mAb) можно получать с помощью ряда методик, в том числе традиционного способа получения моноклональных антител, например, стандартной методики гибридизации соматических клеток по Kohler and Milstein, 1975 Nature 256: 495. Можно использовать множество методик получения моноклонального антитела, например, вирусную или онкогенную трансформацию B-лимфоцитов.
Животная система для получения гибридом представляет собой мышиную систему. Получение гибридомы в организме мыши является хорошо отработанной процедурой. Протоколы иммунизации и методики выделения иммунизированных спленоцитов для слияния известны из уровня техники. Партнеры по слиянию (например, клетки миеломы мыши) и процедуры слияния также являются известными.
В некоторых вариантах осуществления антитела по настоящему изобретению представляют собой гуманизированные моноклональные антитела. Химерные или гуманизированные антитела и их антигенсвязывающие фрагменты по настоящему изобретению можно получить, исходя из последовательности моноклонального антитела мыши, полученного согласно описанному выше. ДНК, кодирующую тяжелую и легкую цепи иммуноглобулинов, можно получить из мышиной гибридомы, представляющей интерес, и сконструировать таким образом, чтобы она содержала последовательности иммуноглобулинов, отличные от мышиных (например, человеческие), с применением стандартных методик молекулярной биологии. Например, для создания химерного антитела мышиные вариабельные области можно связать с человеческими константными областями с применением способов, известных из уровня техники (см., например, патент США № 4816567 авторства Cabilly et al.). Для создания гуманизированного антитела мышиные CDR-области мыши можно вставить в человеческую каркасную область с применением способов, известных из уровня техники. См., например, патент США № 5225539 авторства Winter и патенты США №№ 5530101; 5585089; 5693762 и 6180370 авторства Queen et al.
В некоторых вариантах осуществления антитела по настоящему изобретению представляют собой человеческие моноклональные антитела. Такие человеческие моноклональные антитела, направленные против ENTPD2, можно получать с использованием трансгенных или трансхромосомных мышей, несущих части человеческой иммунной системы вместо мышиной системы. Эти трансгенные и трансхромосомные мыши включают мышей, называемых в данном документе соответственно мышами HuMAb и мышами KM, и они в совокупности называются в данном документе "мышами с человеческим Ig".
Мышь HuMAb® (Medarex, Inc.) содержит минилокусы генов человеческих иммуноглобулинов, которые кодируют не подвергшиеся перегруппировке последовательности тяжелых цепей (мю и гамма) и каппа-легкой цепи иммуноглобулина человека, вместе с целенаправленными мутациями, которые инактивируют эндогенные локусы мю- и каппа-цепей (см., например, Lonberg, et al., 1994 Nature 368 (6474): 856-859). Соответственно, мыши проявляют сниженную экспрессию IgM или K мыши, и в ответ на иммунизацию введенные трансгены, кодирующие человеческие тяжелые и легкие цепи, подвергаются переключению класса и соматической мутации с получением высокоаффинного моноклонального IgG-каппа человека (Lonberg, N. et al., 1994, выше; обзор в Lonberg, N., 1994 Handbook of Experimental Pharmacology 113:49-101; Lonberg, N. and Huszar, D., 1995 Intern. Rev. Immunol. 13: 65-93, и Harding, F. and Lonberg, N., 1995 Ann. N.Y. Acad. Sci. 764:536-546). Получение и использование мышей HuMAb, а также геномные модификации, которые несут такие мыши, дополнительно описываются в Taylor, L. et al., 1992 Nucleic Acids Research 20:6287-6295; Chen, J. et al., 1993 International Immunology 5: 647-656; Tuaillon et al., 1993 Proc. Natl. Acad. Sci. USA 94:3720-3724; Choi et al., 1993 Nature Genetics 4:117-123; Chen, J. et al., 1993 EMBO J. 12: 821-830; Tuaillon et al., 1994 J. Immunol. 152:2912-2920; Taylor, L. et al., 1994 International Immunology 579-591; и Fishwild, D. et al., 1996 Nature Biotechnology 14: 845-851. См. также патенты США №№ 5545806; 5569825; 5625126; 5633425; 5789650; 5877397; 5661016; 5814318; 5874299 и 5770429; все авторства Lonberg и Kay; патент США № 5545807 авторства Surani et al.; PCT-публикации №№ WO 92103918, WO 93/12227, WO 94/25585, WO 97113852, WO 98/24884 и WO 99/45962, все авторства Lonberg и Kay; и PCT-публикацию № WO 01/14424 авторства Korman et al.
В некоторых вариантах осуществления продуцирование человеческих антител по настоящему изобретению можно осуществлять с использованием мыши, которая несет последовательности человеческих иммуноглобулинов в трансгенах и трансхромосомах, как, например, мыши, которая несет трансген, кодирующий человеческую тяжелую цепь, и трансхромосому, кодирующую человеческую легкую цепь. Такие мыши, называемые в данном документе "мышами KM", подробно описаны в PCT-публикации WO 02/43478 авторства Ishida et al.
Более того, альтернативные трансгенные животные системы, экспрессирующие гены человеческих иммуноглобулинов, являются доступными из уровня техники, и их можно использовать для продуцирования ENTPD2-связывающих антител и их антигенсвязывающих фрагментов. Например, можно использовать альтернативную трансгенную систему, называемую Xenomouse (Abgenix, Inc.). Такие мыши описаны, например, в патентах США №№ 5939598; 6075181; 6114598; 6150584 и 6162963 авторства Kucherlapati et al.
Более того, альтернативные трансхромосомные животные системы, экспрессирующие гены человеческих иммуноглобулинов, являются доступными из уровня техники, и их можно использовать для продуцирования ENTPD2-связывающих антител по настоящему изобретению. Например, можно использовать мышей, несущих как трансхромосому, кодирующую человеческую тяжелую цепь, так и трансхромосому, кодирующую человеческую легкую цепь, называемых "мышами TC"; такие мыши описаны в Tomizuka et al., 2000 Proc. Natl. Acad. Sci. USA 97:722-727. Кроме того, в уровне техники были описаны коровы, несущие трансхромосомы, кодирующие человеческие тяжелые и легкие цепи (Kuroiwa et al., 2002 Nature Biotechnology 20:889-894), и их можно использовать для продуцирования ENTPD2-связывающих антител по настоящему изобретению.
Человеческие моноклональные антитела также можно получать с применением способов фагового дисплея для скрининга библиотек генов человеческих иммуноглобулинов. Такие способы фагового дисплея для выделения человеческих антител определены в уровне техники или описаны в примерах ниже. См., например, патенты США №№ 5223409; 5403484 и 5571698 авторства Ladner et al; патенты США №№ 5427908 и 5580717 авторства Dower et al; патенты США №№ 5969108 и 6172197 авторства McCafferty et al. и патенты США №№ 5885793; 6521404; 6544731; 6555313; 6582915 и 6593081 авторства Griffiths et al.
Человеческие моноклональные антитела по настоящему изобретению также можно получать с использованием мышей SCID, которым были перенесены человеческие иммунные клетки таким образом, что после иммунизации может формироваться ответ с образованием человеческих антител. Такие мыши описаны, например, в патентах США №№ 5476996 и 5698767 авторства Wilson et al.
Способы конструирования модифицированных антител
Как обсуждается выше, ENTPD2-связывающие антитела, имеющие последовательности VH и VL или последовательности полноразмерной тяжелой и легкой цепей, показанные в данном документе, можно использовать для создания новых ENTPD2-связывающих антител путем модификации последовательностей полноразмерной тяжелой цепи и/или легкой цепи, последовательностей VH и/или VL или константной(константных) области(областей), присоединенной(присоединенных) к ним. Таким образом, в другом аспекте настоящего изобретения структурные признаки ENTPD2-связывающего антитела по настоящему изобретению используются для создания структурно родственных ENTPD2-связывающих антител, которые сохраняют по меньшей мере одно функциональное свойство антител и их антигенсвязывающих фрагментов по настоящему изобретению, как, например, связывание с ENTPD2 человека и его ингибирование.
Например, одну или несколько CDR-областей антител и их антигенсвязывающих фрагментов по настоящему изобретению или их мутантных вариантов можно объединить рекомбинантным путем с известными каркасными областями и/или другими CDR с созданием дополнительных сконструированных рекомбинантным путем ENTPD2-связывающих антител и их антигенсвязывающих фрагментов по настоящему изобретению, как обсуждается выше. Другие типы модификаций включают модификации, описанные в предыдущем разделе. Исходным материалом для способа конструирования является одна или несколько из последовательностей VH и/или VL, предусмотренных в данном документе, или одна или несколько их CDR-областей. Для создания сконструированного антитела не обязательно фактически получать (т. е. экспрессировать в виде белка) антитело, имеющее одну или несколько последовательностей VH и/или VL, предусмотренных в данном документе, или одну или несколько их CDR-областей. Вместо этого информацию, содержащуюся в последовательности(последовательностях), используют в качестве исходного материала для получения последовательности(последовательностей) "второго поколения", полученной(полученных) из исходной(исходных) последовательности(последовательностей), а затем последовательность(последовательности) "второго поколения" получают и экспрессируют в виде белка.
Измененную последовательность антитела также можно получить посредством скрининга библиотек антител, имеющих фиксированные последовательности CDR3 или минимальные необходимые детерминанты связывания, которые описаны в US20050255552, и разнообразные последовательности CDR1 и CDR2. Скрининг можно осуществлять согласно любой технологии скрининга, подходящей для скрининга антител из библиотек антител, как, например, технологии фагового дисплея.
Стандартные методики молекулярной биологии можно применять для получения и экспрессии измененной последовательности антитела. Антитело, кодируемое измененной(измененными) последовательностью(последовательностями) антитела, представляет собой антитело, которое сохраняет одно, некоторые или все из функциональных свойств ENTPD2-связывающих антител, описанных в данном документе, при этом данные функциональные свойства включают без ограничения специфичное связывание с белком ENTPD2 человека и его стабилизацию.
Функциональные свойства измененных антител можно оценить с помощью стандартных анализов, доступных из уровня техники и/или описанных в данном документе, таких как анализы, изложенные в разделе "Примеры" (например, разновидности ELISA).
В некоторых вариантах осуществления способов конструирования антител и их антигенсвязывающих фрагментов по настоящему изобретению мутации можно вводить произвольным или избирательным образом по всей последовательности, кодирующей ENTPD2-связывающее антитело, или ее части, и полученные модифицированные ENTPD2-связывающие антитела можно подвергнуть скринингу в отношении активности связывания и/или других функциональных свойств, описанных в данном документе. Способы введения мутаций были описаны в уровне техники. Например, в PCT-публикации WO 02/092780 описываются способы создания и скрининга мутантных вариантов антител с применением насыщающего мутагенеза, сборки с лигированием синтезированных фрагментов или их комбинации. В качестве альтернативы в PCT-публикации WO 03/074679 описываются способы применения способов вычислительного скрининга для оптимизации физико-химических свойств антител.
Определение характеристик антител
Характеристики антител и их антигенсвязывающих фрагментов по настоящему изобретению могут быть определены с помощью различных функциональных анализов. Например, их характеристики могут быть определены по их способности к связыванию с белком ENTPD2 (например, белком ENTPD2 человека).
Способность антитела к связыванию с ENTPD2 (например, белком ENTPD2 человека) можно выявить прямым способом посредством мечения антитела, представляющего интерес, или антитело может быть немеченым, и связывание выявляют непрямым способом с применением различных форматов сэндвич-анализов, известных из уровня техники.
В некоторых вариантах осуществления ENTPD2-связывающие антитела и их антигенсвязывающие фрагменты по настоящему изобретению блокируют связывание эталонного ENTPD2-связывающего антитела с белком ENTPD2 (например, белком ENTPD2 человека) или конкурируют с ним за это связывание. Они могут представлять собой полностью человеческие или гуманизированные ENTPD2-связывающие антитела, описанные выше. Они также могут представлять собой другие человеческие, мышиные, химерные или гуманизированные ENTPD2-связывающие антитела, которые связываются с тем же эпитопом, что и эталонное антитело. Способность к блокированию связывания эталонного антитела или конкуренции с ним за это связывание указывает на то, что тестируемое ENTPD2-связывающее антитело связывается с тем же или сходным эпитопом по сравнению с эпитопом, определяемым эталонным антителом, или с эпитопом, который расположен достаточно близко к эпитопу, с которым связывается эталонное ENTPD2-связывающее антитело. Особенно вероятно, что такие антитела обладают преимущественными свойствами, идентифицированными для эталонного антитела. Способность к блокированию эталонного антитела или конкуренции с ним можно определить, например, с помощью конкурентного анализа связывания. В конкурентном анализе связывания тестируемое антитело исследуют в отношении способности к ингибированию специфичного связывания эталонного антитела с общим антигеном, таким как белок ENTPD2 (например, белок ENTPD2 человека). Тестируемое антитело конкурирует с эталонным антителом за специфичное связывание с антигеном, если избыток тестируемого антитела осуществляет значительное ингибирование связывания эталонного антитела. Значительное ингибирование означает, что тестируемое антитело обычно снижает специфичное связывание эталонного антитела на по меньшей мере 10%, 25%, 50%, 75% или 90%.
Существует ряд известных конкурентных анализов связывания, которые можно применять для оценки конкуренции антитела с эталонным антителом за связывание с конкретным белком, в данном случае с ENTPD2 (например, белком ENTPD2 человека). Они включают, например, твердофазный прямой или непрямой радиоиммунологический анализ (RIA), твердофазный прямой или непрямой иммуноферментный анализ (EIA), конкурентный сэндвич-анализ (см. Stahli et al., Methods in Enzymology 9:242-253, 1983); твердофазный прямой EIA с использованием комплекса биотин-авидин (см. Kirkland et al., J. Immunol. 137:3614-3619, 1986); твердофазный анализ с прямым мечением, твердофазный сэндвич-анализ с прямым мечением (см. Harlow & Lane, выше); твердофазный RIA с прямым мечением с использованием метки I-125 (см. Morel et al., Molec. Immunol. 25:7-15, 1988); твердофазный прямой EIA с использованием комплекса биотин-авидин (Cheung et al., Virology 176:546-552, 1990) и RIA с прямым мечением (Moldenhauer et al., Scand. J. Immunol. 32:77-82, 1990). Как правило, такой анализ включает применение очищенного антигена, связанного с твердой поверхностью, или клеток, несущих любой из них, немеченого тестируемого ENTPD2-связывающего антитела и меченого эталонного антитела. Конкурентное ингибирование измеряют путем определения количества метки, связавшейся с твердой поверхностью или клетками в присутствии тестируемого антитела. Обычно тестируемое антитело присутствует в избытке. Антитела, идентифицируемые с помощью конкурентного анализа (конкурирующие антитела), включают в себя антитела, связывающиеся с тем же эпитопом, что и эталонное антитело, и антитела, связывающиеся со смежным эпитопом, который расположен достаточно близко к эпитопу, с которым связывается эталонное антитело, чтобы имело место стерическое несоответствие.
Для определения того, связываются ли выбранные ENTPD2-связывающие моноклональные антитела с уникальными эпитопами, каждое антитело можно биотинилировать с помощью коммерчески доступных реагентов (например, реагентов от Pierce, Рокфорд, Иллинойс). Конкурентные исследования с использованием немеченых моноклональных антител и биотинилированных моноклональных антител можно осуществлять с использованием планшетов для ELISA, покрытых белком ENTPD2. Связывание биотинилированного MAb можно выявить с помощью зонда на основе конъюгата стрептавидина и щелочной фосфатазы. Для определения изотипа очищенного ENTPD2-связывающего антитела можно выполнять ELISA с определением изотипа. Например, лунки титрационных микропланшетов можно покрывать 1 мкг/мл антитела к IgG человека в течение ночи при 4°C. После блокирования с помощью 1% BSA в планшетах осуществляют реакцию с моноклональным ENTPD2-связывающим антителом в концентрации 1 мкг/мл или меньше или очищенными изотипическими контролями при температуре окружающей среды в течение одного-двух часов. Затем содержимое лунок можно приводить в реакцию со специфическими в отношении IgG1 человека либо IgM человека зондами, конъюгированными со щелочной фосфатазой. Планшеты затем проявляют и анализируют таким образом, чтобы можно было определить изотип очищенного антитела.
Для демонстрации связывания моноклональных ENTPD2-связывающих антител с живыми клетками, экспрессирующими белок ENTPD2 (например, белок ENTPD2 человека), можно применять проточную цитометрию. Вкратце, линии клеток, экспрессирующих ENTPD2 (выращиваемые при стандартных условиях роста), можно смешивать с различными концентрациями ENTPD2-связывающего антитела в PBS, содержащем 0,1% BSA и 10% фетальную телячью сыворотку крови, и инкубировать при 37°C в течение 1 часа. После промывания осуществляют реакцию клеток с антителом к IgG человека, меченным флуоресцеином, при тех же самых условиях, что и при окрашивании первичным антителом. Образцы можно анализировать с помощью прибора FACScan с использованием свойств светорассеяния и бокового рассеяния в целях гейтирования по отдельным клеткам. Можно применять альтернативный анализ с использованием флуоресцентной микроскопии (в дополнение к анализу или вместо анализа) методом проточной цитометрии. Клетки можно окрашивать точно так же, как описано выше, и исследовать с помощью флуоресцентной микроскопии. Этот способ позволяет визуализировать отдельные клетки, однако может характеризоваться сниженной чувствительностью в зависимости от плотности антигена.
ENTPD2-связывающие антитела и их антигенсвязывающие фрагменты по настоящему изобретению можно дополнительно тестировать в отношении реактивности с белком ENTPD2 (например, белком ENTPD2 человека) или антигенным фрагментом с помощью вестерн-блоттинга. Вкратце, очищенный белок ENTPD2 (например, белок ENTPD2 человека) или слитые белки на его основе или клеточные экстракты из клеток, экспрессирующих ENTPD2, можно получить и подвергнуть электрофорезу в полиакриламидном геле в присутствии додецилсульфата натрия. После электрофореза разделенные антигены переносят на нитроцеллюлозные мембраны, блокированные 10% фетальной телячьей сывороткой крови, и зондируют с помощью моноклональных антител, подлежащих тестированию. Связывание с IgG человека можно выявить с помощью антитела к IgG человека, конъюгированного с щелочной фосфатазой, и проявить с помощью субстрата BCIP/NBT в виде таблеток (Sigma Chem. Co., Сент-Луис, Миссури).
ENTPD2-связывающие антитела и их антигенсвязывающие фрагменты по настоящему изобретению можно дополнительно тестировать в отношении их способностей к модулированию одной или нескольких форм активности/функций ENTPD2.
ENTPD2-связывающие антитела и их антигенсвязывающие фрагменты по настоящему изобретению также можно тестировать с помощью любого из способов или анализов, описанных в разделе "Примеры".
Способы лечения и терапевтическое применение
Антитела по настоящему изобретению имеют многочисленные диагностические и терапевтические полезные свойства in vitro и in vivo, которые включают диагностику и лечение нарушений с ENTPD2-зависимыми патофизиологическими особенностями. Например, эти молекулы можно вводить в клетки в культуре in vitro или ex vivo или субъектам-людям, например, in vivo, для лечения, предупреждения и диагностики ряда нарушений с ENTPD2-зависимыми патофизиологическими особенностями. Соответственно, в одном аспекте в данном документе предусмотрены способы лечения рака у субъекта, нуждающегося в этом, путем введения субъекту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента, описанного в данном документе, нуклеиновой кислоты, кодирующей такие антитело или антигенсвязывающий фрагмент, вектора, содержащего нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, клетки, содержащей такие нуклеиновую кислоту или вектор, или фармацевтической композиции, содержащей такие антитело или антигенсвязывающий фрагмент, нуклеиновую кислоту, вектор или клетку. В одном аспекте в настоящем изобретении предусмотрен способ ингибирования или снижения интенсивности роста опухолевых клеток у субъекта, включающий введение субъекту терапевтически эффективного количества антитела к ENTPD2 человека, раскрытого в данном документе.
В другом аспекте предусмотрен способ лечения субъекта, например, снижения интенсивности или облегчения гиперпролиферативного состояния или нарушения (например, рака), например, солидной опухоли, гематологического рака, опухоли мягких тканей или метастатического поражения у субъекта.
Соответственно, в одном варианте осуществления в настоящем изобретении предусмотрен способ ингибирования роста опухолевых клеток у субъекта, включающий введение субъекту терапевтически эффективного количества одной или нескольких молекул антитела к ENTPD2 человека или их функциональных фрагментов, описанных в данном документе, в отдельности или в комбинации с другими средствами, например, терапевтическими средствами, или терапевтическими методами.
В некоторых вариантах осуществления такие способы могут дополнительно включать стадию анализа уровней экспрессии ENTPD2 в образце, полученном от субъекта, например, в биоптате ткани субъекта.
Термин "рак" подразумевается как включающий все типы раковых образований или онкогенных процессов, метастатических тканей или злокачественно трансформированных клеток, тканей или органов независимо от гистопатологического типа или стадии инвазивности. Примеры раковых нарушений включают без ограничения солидные опухоли, опухоли мягких тканей и метастатические поражения. Примеры солидных опухолей включают злокачественные новообразования, например, формы саркомы, формы аденокарциномы и формы карциномы различных систем органов, как, например, те, которые поражают печень, легкое, молочную железу, лимфоидную ткань, желудочно-кишечный тракт (например, толстую кишку), мочеполовой тракт (например, клетки почки, уротелиальные клетки), предстательную железу и глотку. Формы аденокарциномы включают такие злокачественные новообразования, как большинство форм рака толстой кишки, рак прямой кишки, почечноклеточную карциному, рак печени (гепатокарциному, например, гепатокарциному на поздней стадии при наличии или отсутствии вирусной инфекции, например, хронического вирусного гепатита), немелкоклеточную карциному легкого, рак тонкой кишки и рак пищевода. Формы плоскоклеточной карциномы включают злокачественные новообразования, например, в легком, пищеводе, коже, области головы и шеи, полости рта, заднем проходе и шейке матки.
Метастатические поражения при вышеупомянутых формах рака также можно лечить или предупреждать с помощью способов и композиций по настоящему изобретению.
Иллюстративные формы рака, рост которых можно ингибировать с помощью молекул антител, раскрытых в данном документе, включают формы рака, как правило, отвечающие на иммунотерапию. Неограничивающие примеры предпочтительных форм рака для лечения включают рак желудочно-кишечного тракта (например, рак желудка (желудочный рак), рак ободочной и прямой кишки (CRC)), рак пищевода (например, плоскоклеточную карциному пищевода (ESCC)), рак поджелудочной железы и холангиокарциному. Кроме того, рефрактерные или рецидивирующие злокачественные новообразования можно лечить с помощью молекул антител, описанных в данном документе.
Примеры других форм рака, которые можно лечить, включают рак легкого (например, немелкоклеточный рак легкого (NSCLC) (например, NSCLC плоскоклеточного и/или неплоскоклеточного гистологического подтипа или NSCLC в форме аденокарциномы)), меланому (например, меланому на поздней стадии), рак почки (например, почечноклеточную карциному, например, светлоклеточную почечноклеточную карциному), рак печени, миелому (например, множественную миелому), рак предстательной железы, рак молочной железы (например, рак молочной железы, который не характеризуется экспрессией одного, двух или всех из эстрогенового рецептора, прогестеронового рецептора или Her2/neu, например, трижды негативный рак молочной железы), рак поджелудочной железы, рак головы и шеи (например, плоскоклеточную карциному головы и шеи (HNSCC)), рак анального канала, рак желудка и пищевода, рак щитовидной железы, рак шейки матки, лимфопролиферативное заболевание (например, посттрансплантационное лимфопролиферативное заболевание) или гематологический рак, T-клеточную лимфому, неходжкинскую лимфому или лейкоз (например, миелоидный лейкоз), рак костей, рак поджелудочной железы, рак кожи, рак головы и шеи, злокачественную меланому кожи или внутриглазную злокачественную меланому, рак матки, рак яичника, рак прямой кишки, рак анального канала, рак желудка и пищевода, рак желудка, рак яичка, рак матки, карциному фаллопиевых труб, карциному эндометрия, карциному шейки матки, карциному влагалища, карциному вульвы, болезнь Ходжкина, неходжкинскую лимфому, миелому (например, множественную миелому), рак пищевода, рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечника, саркому мягких тканей, рак уретры, рак полового члена, хронические или острые формы лейкоза, в том числе острый миелоидный лейкоз, хронический миелоидный лейкоз, острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз, солидные опухоли детского возраста, лимфоцитарную лимфому, рак мочевого пузыря, рак почки (например, почечный рак, например, почечноклеточную карциному (RCC) (например, метастатическую RCC или светлоклеточную почечноклеточную карциному)), рак мочеточника, карциному почечной лоханки, неоплазию центральной нервной системы (CNS), первичную лимфому CNS, ангиогенез в опухоли, опухоль оси позвоночника, глиому ствола головного мозга, аденому гипофиза, саркому Капоши, эпидермоидный рак, плоскоклеточный рак, T-клеточную лимфому, формы рака, индуцированные факторами окружающей среды, в том числе индуцированные асбестом, и комбинации указанных форм рака.
В некоторых вариантах осуществления средства терапии, представленные в данном документе, можно применять для лечения пациента, у которого имеется (или который идентифицирован как имеющий) рак, ассоциированный с инфекцией, например, вирусной или бактериальной инфекцией. Иллюстративные формы рака включают рак шейки матки, рак анального канала, HPV-ассоциированный плоскоклеточный рак головы и шеи, HPV-ассоциированные формы папилломы пищевода, HHV6-ассоциированные формы лимфомы, EBV-ассоциированные формы лимфомы (в том числе лимфома Беркитта), MALT-лимфому желудка, другие формы MALT-лимфомы, ассоциированные с инфекцией, HCC и саркому Капоши.
В других вариантах осуществления рак представляет собой гематологическое злокачественное новообразование или рак, включающий без ограничения лейкоз или лимфому. Например, молекулу антитела к ENTPD2 человека или ее антигенсвязывающий фрагмент в отдельности или в комбинации с другими средствами, например, терапевтическими средствами, можно применять для лечения форм рака и злокачественных новообразований, в том числе без ограничения, например, форм острого лейкоза, в том числе без ограничения, например, B-клеточного острого лимфоидного лейкоза ("BALL"), T-клеточного острого лимфоидного лейкоза ("TALL"), острого лимфоидного лейкоза (ALL); одной или нескольких форм хронического лейкоза, в том числе без ограничения, например, хронического миелогенного лейкоза (CML), хронического лимфоцитарного лейкоза (CLL); дополнительных форм гематологического рака или гематологических состояний, в том числе без ограничения, например, B-клеточного пролимфоцитарного лейкоза, бластной плазмоцитоидной дендритноклеточной неоплазии, лимфомы Беркитта, диффузной крупноклеточной B-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной или крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, MALT-лимфомы, мантийноклеточной лимфомы, лимфомы из клеток маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, плазмобластной лимфомы, плазмоцитоидной дендритноклеточной неоплазии, макроглобулинемии Вальденстрема и "предлейкоза", который представляет собой разнообразную группу гематологических состояний, объединенных неэффективным образованием (или дисплазией) миелоидных клеток крови, и т. п.
В одном варианте осуществления рак выбран из рака ободочной кишки (например, рака ободочной и прямой кишки (CRC) или аденокарциномы ободочной и прямой кишки), рака желудка (например, аденокарциномы желудка, карциномы желудка), рака пищевода (например, плоскоклеточной карциномы пищевода (ESCC)), рака легкого (например, мелкоклеточного рака легкого), рака молочной железы (например, аденокарциномы молочной железы) или рака яичника.
В одном варианте осуществления рак представляет собой рак ободочной и прямой кишки (CRC) или аденокарциному ободочной и прямой кишки.
В другом варианте осуществления рак представляет собой рак желудка.
В еще одном варианте осуществления рак представляет собой плоскоклеточную карциному пищевода (ESCC).
В еще одном варианте осуществления рак характеризуется сверхэкспрессией ENTPD2 (является ENTPD2-положительным/ENTPD2+), как, например, ENTPD2+ CRC, ENTPD2+ рак желудка (например, ENTPD2-положительный рак желудка), ENTPD2+ плоскоклеточная карцинома пищевода (ENTPD2+ ESCC).
Антитело или его антигенсвязывающий фрагмент, описанные в данном документе, нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, или вектор или клетку, содержащие нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, или фармацевтическую композицию, содержащую такие антитело или антигенсвязывающий фрагмент, нуклеиновую кислоту, вектор или клетку, можно вводить субъекту посредством внутривенного, внутриопухолевого или подкожного путей. В некоторых вариантах осуществления такие антитело или его фрагмент, нуклеиновую кислоту, вектор, клетку или фармацевтическую композицию вводят внутривенно.
Также предусмотрены антитело или его антигенсвязывающий фрагмент, описанные в данном документе, фармацевтическая композиция, содержащая такие антитело или антигенсвязывающий фрагмент, нуклеиновая кислота, кодирующая такие антитело или антигенсвязывающий фрагмент, или вектор, содержащий нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, для применения в лечении рака.
В настоящем изобретении также предусмотрены пути применения антитела или его антигенсвязывающего фрагмента, описанных в данном документе, фармацевтической композиции, содержащей такие антитело или антигенсвязывающий фрагмент, нуклеиновой кислоты, кодирующей такие антитело или антигенсвязывающий фрагмент, или вектора, содержащего нуклеиновую кислоту, кодирующую такие антитело или антигенсвязывающий фрагмент, в изготовлении лекарственного препарата для лечения рака.
Виды комбинированной терапии
Различные средства лечения, описанные выше, можно применять в комбинации с другим средством лечения. Настоящее изобретение также относится к фармацевтической композиции, содержащей комбинацию в соответствии с настоящим изобретением, описанную в данном документе, в частности, вместе с инструкциями по одновременному, раздельному или последовательному ее применению (особенно в случае совместной активности) в лечении рака. Например, антитела к ENTPD2 или их антигенсвязывающие фрагменты, описанные в данном документе, можно применять в комбинации с одним или несколькими средствами лечения, представляющими собой стандарт оказания медицинской помощи (например, при раке), другой молекулой антитела, иммуномодулятором (например, активатором костимулирующей молекулы или ингибитором коингибирующей молекулы); вакциной, например, терапевтической противораковой вакциной; или другими формами клеточной терапии, описанными ниже.
Соответственно, способы лечения рака, описанные в данном документе, могут дополнительно включать введение по меньшей мере одного дополнительного терапевтического средства субъекту, нуждающемуся в лечении. Также в данном документе предусмотрены способы лечения рака, включающие введение по меньшей мере двух дополнительных терапевтических средств субъекту, нуждающемуся в лечении.
Термин "комбинация" относится к фиксированной комбинации в одной единичной лекарственной форме либо к комбинированному введению, где соединение по настоящему изобретению и по меньшей мере одного партнера по комбинации (например, по меньшей мере одно другое лекарственное средство, которое поясняется ниже, также называемое "терапевтическим(терапевтическими) средством(средствами)" или "совместно применяемым(применяемыми) средством(средствами)") можно вводить независимо в одно и то же время или по отдельности в пределах временных промежутков, особенно если эти временные промежутки обеспечивают партнерам по комбинации возможность проявления кооперативного, например, синергического, эффекта. Отдельные компоненты могут быть упакованы в набор или предоставлены по отдельности. Один или оба компонента (например, порошки или жидкости) могут быть восстановлены или разбавлены до необходимой дозы перед введением. Термины "совместное введение" или "комбинированное введение" или им подобные, используемые в данном документе, подразумеваются как охватывающие введение выбранного партнера по комбинации одному субъекту, нуждающемуся в этом (например, пациенту), и предполагают включение режимов лечения, в которых средства не обязательно вводят одним и тем же путем введения или в одно и то же время. Термин "фармацевтическая комбинация", используемый в данном документе, означает продукт, полученный в результате смешивания или комбинирования более чем одного терапевтического средства, который включает как фиксированные, так и нефиксированные комбинации терапевтических средств. Термин "фиксированная комбинация" означает, что оба терапевтические средства, например, соединение по настоящему изобретению и партнера по комбинации, вводят пациенту одновременно в виде единого объекта или дозы. Термин "нефиксированная комбинация" означает, что терапевтические средства, например, соединение по настоящему изобретению и по меньшей мере одного партнера по комбинации, вводят пациенту в виде отдельных объектов одновременно, параллельно либо последовательно без конкретных временных ограничений, при этом такое введение обеспечивает терапевтически эффективные уровни по меньшей мере двух соединений в организме пациента. Последнее также применимо в отношении "коктейльной терапии", например, при введении трех или более терапевтических средств.
Используемый в данном документе термин "фармацевтическая комбинация" относится к фиксированной комбинации в одной единичной лекарственной форме либо нефиксированной комбинации или набору из частей для комбинированного введения, где два или более терапевтических средства можно вводить независимо в одно и то же время или по отдельности в пределах временных промежутков, особенно если эти временные промежутки обеспечивают партнерам по комбинации возможность проявления кооперативного, например, синергического, эффекта.
Термин "комбинированная терапия" относится к введению двух или более терапевтических средств для лечения терапевтического состояния или нарушения, описанного в настоящем изобретении. Такое введение охватывает совместное введение данных терапевтических средств по существу одновременно, как, например, в одной капсуле, имеющей фиксированное соотношение активных ингредиентов. В качестве альтернативы такое введение охватывает совместное введение в нескольких или в отдельных контейнерах (например, таблетках, капсулах, порошках и жидкостях) для каждого активного ингредиента. Порошки и/или жидкости могут быть восстановлены или разбавлены до требуемой дозы перед введением. Кроме того, такое введение также охватывает применение каждого типа терапевтического средства последовательно примерно в одно и то же время либо в разное время. В любом случае режим лечения будет обеспечивать благоприятные эффекты комбинации лекарственных средств при лечении состояний или нарушений, описанных в данном документе.
Молекулы антител к ENTPD2 можно применять в комбинации с другими средствами терапии. Например, комбинированная терапия может включать композицию по настоящему изобретению, совместно составленную и/или вводимую вместе с одним или несколькими дополнительными терапевтическими средствами, например, одним или несколькими противораковыми средствами, цитотоксическими или цитостатическими средствами, гормональными средствами лечения, вакцинами и/или другими средствами иммунотерапии. В других вариантах осуществления молекулы антител вводят в комбинации с другими методами терапевтического лечения, включающими хирургическое вмешательство, облучение, криохирургию и/или термотерапию. В таких видах комбинированной терапии можно преимущественно использовать более низкие дозы вводимых терапевтических средств, избегая таким образом возможных токсических эффектов или осложнений, связанных с различными видами монотерапии.
Термин "в комбинации с" не предполагает обозначение того, что вид терапии или терапевтические средства должны вводиться в одно и то же время и/или быть составлены для совместной доставки, хотя данные способы доставки находятся в пределах объема, описанного в данном документе.
Молекулы антител к ENTPD2 человека можно вводить параллельно с по меньшей мере одним или несколькими дополнительными видами терапии или терапевтическими средствами, до них или после них. Молекулу антитела к ENTPD2 человека и другое по меньшей мере одно средство или терапевтический протокол можно применять в любом порядке. Как правило, каждое средство будет вводиться в дозе и/или по временному графику, которые определены для данного средства. Также следует понимать, что по меньшей мере одно дополнительное терапевтическое средство, используемое в данной комбинации, можно вводить совместно в одной композиции или вводить по отдельности в разных композициях. В целом, ожидается, что дополнительные терапевтические средства, используемые в комбинации, будут использоваться на уровнях, которые не превышают уровни, на которых они используются по отдельности. В некоторых вариантах осуществления уровни, используемые в комбинации, будут ниже уровней при использовании по отдельности.
Настоящее изобретение, таким образом, помимо прочего, относится к комбинированному продукту для одновременного, раздельного или последовательного применения, такому как комбинированный препарат или фиксированная фармацевтическая комбинация, или к комбинации такого препарата и комбинации.
Иллюстративные антагонисты аденозинового рецептора A2A
В определенных вариантах осуществления молекулы антител к ENTPD2 человека, описанные в данном документе, вводят в комбинации с по меньшей мере одним антагонистом аденозинового рецептора A2A (A2AR). В определенных вариантах осуществления молекулы антител к ENTPD2 человека, описанные в данном документе, вводят в комбинации с по меньшей мере двумя антагонистами аденозинового рецептора A2A (A2AR). Иллюстративные антагонисты A2AR включают без ограничения, например, PBF509/NIR178 (Palobiofarma/Novartis), CPI444/V81444 (Corvus/Genentech), AZD4635/HTL-1071 (AstraZeneca/Heptares), випаденант (Redox/Juno), GBV-2034 (Globavir), AB928 (Arcus Biosciences), теофиллин, истрадефиллин (Kyowa Hakko Kogyo), тозаденант/SYN-115 (Acorda), KW-6356 (Kyowa Hakko Kogyo), ST-4206 (Leadiant Biosciences) и преладенант/SCH 420814 (Merck/Schering).
В определенных вариантах осуществления антагонист A2AR представляет собой PBF509/NIR178. PBF509/NIR178 и другие антагонисты A2AR раскрыты в US 8796284 и WO 2017/025918, включенных в данный документ посредством ссылки во всей своей полноте. В определенных вариантах осуществления антагонист A2AR представляет собой 5-бром-2,6-ди-(1H-пиразол-1-ил)пиримидин-4-амин или его фармацевтически приемлемую соль. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
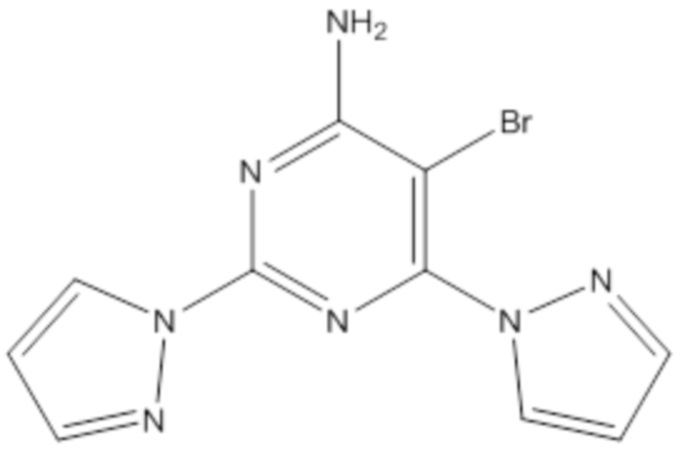 или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
В определенных вариантах осуществления антагонист A2AR представляет собой CPI444/V81444. CPI-444 и другие антагонисты A2AR раскрыты в WO 2009/156737, включенной в данный документ посредством ссылки во всей своей полноте. В определенных вариантах осуществления антагонист A2AR представляет собой (S)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амин или его фармацевтически приемлемую соль. В определенных вариантах осуществления антагонист A2AR представляет собой (R)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амин, или его рацемат, или его фармацевтически приемлемую соль. В определенных вариантах осуществления антагонист A2AR представляет собой 7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амин или его фармацевтически приемлемую соль. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
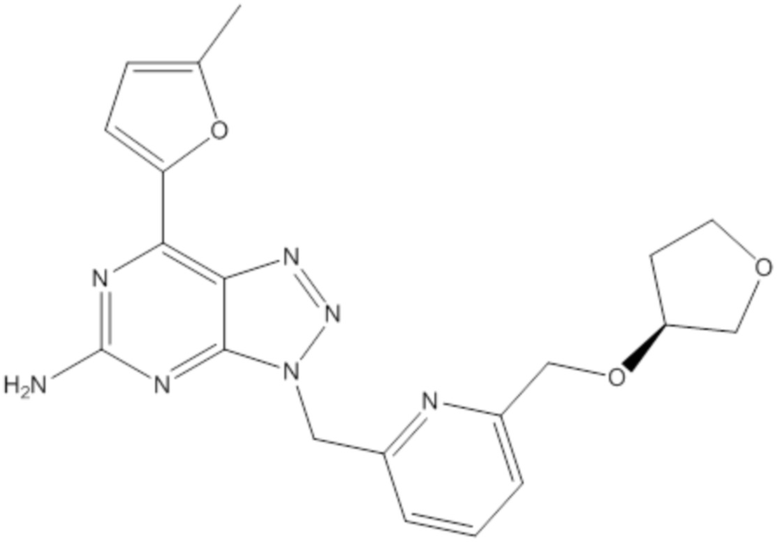 или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
В определенных вариантах осуществления антагонист A2AR представляет собой AZD4635/HTL-1071. Антагонисты A2AR раскрыты в WO 2011/095625, включенной в данный документ посредством ссылки во всей своей полноте. В определенных вариантах осуществления антагонист A2AR представляет собой 6-(2-хлор-6-метилпиридин-4-ил)-5-(4-фторфенил)-1,2,4-триазин-3-амин или его фармацевтически приемлемую соль. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
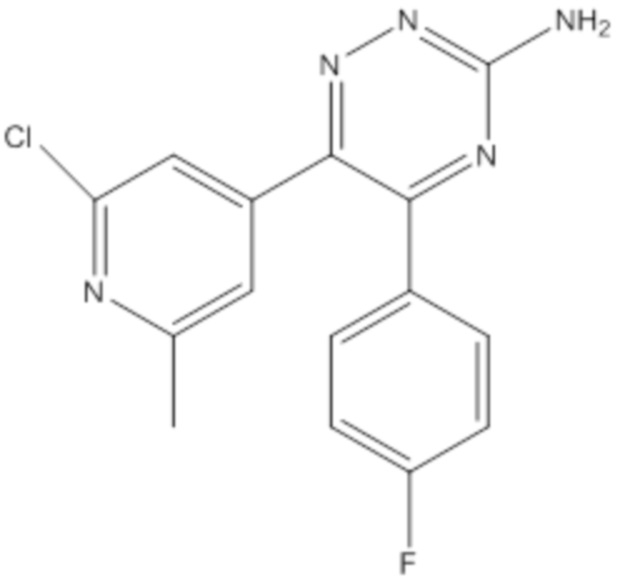 или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
В определенных вариантах осуществления антагонист A2AR представляет собой ST-4206 (Leadiant Biosciences). В определенных вариантах осуществления антагонист A2AR является антагонистом A2AR, описанным в US 9133197, включенном в данный документ посредством ссылки во всей своей полноте. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
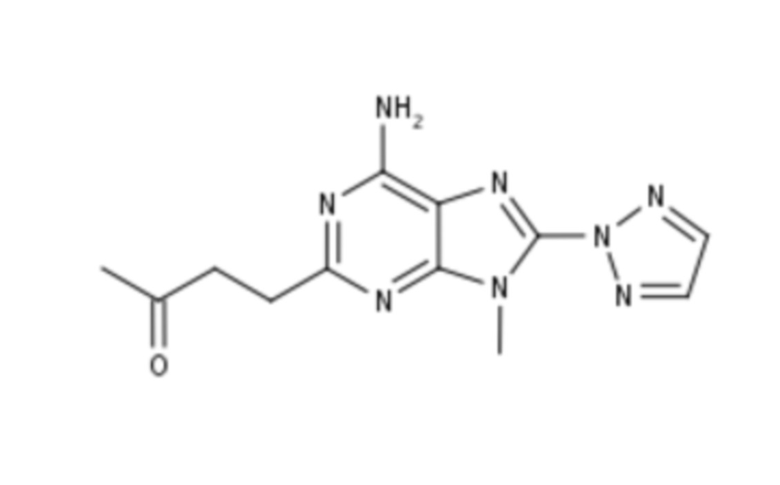 или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
В определенных вариантах осуществления антагонист A2AR является антагонистом A2AR, описанным в US8114845, US9029393, US20170015758 или US20160129108, включенных в данный документ посредством ссылки во всей своей полноте.
В определенных вариантах осуществления антагонист A2AR представляет собой истрадефиллин (регистрационный номер CAS: 155270-99-8). Истрадефиллин также известен как KW-6002 или 8-[(E)-2-(3,4-диметоксифенил)винил]-1,3-диэтил-7-метил-3,7-дигидро-1H-пурин-2,6-дион. Истрадефиллин раскрыт, например, в LeWitt et al. (2008) Annals of Neurology 63 (3): 295-302.
В определенных вариантах осуществления антагонист A2AR представляет собой тозаденант (Biotie). Тозаденант также известен как SYN115 или 4-гидрокси-N-(4-метокси-7-морфолин-4-ил-1,3-бензотиазол-2-ил)-4-метилпиперидин-1-карбоксамид. Тозаденант блокирует эффект эндогенного аденозина в отношении рецепторов А2А, что приводит к усилению эффекта дофамина в отношении рецептора D2 и ингибированию эффекта глутамата в отношении рецептора mGluR5. В некоторых вариантах осуществления антагонист A2AR представляет собой преладенант (регистрационный номер CAS: 377727-87-2). Преладенант также известен как SCH 420814 или 2-(2-фуранил)-7-[2-[4-[4-(2-метоксиэтокси)фенил]-1-пиперазинил]этил]7H-пиразоло[4,3-е][1,2,4]триазоло[1,5-с]пиримидин-5-амин. Преладенант был разработан как лекарственное средство, действующее в качестве сильного и избирательного антагониста аденозинового рецептора А2А.
В определенных вариантах осуществления антагонист A2AR представляет собой випаденант. Випаденант также известен как BIIB014, V2006 или 3-[(4-амино-3-метилфенил)метил]-7-(фуран-2-ил)триазоло[4,5-d]пиримидин-5-амин.
Другие иллюстративные антагонисты A2AR включают, например, ATL-444, MSX-3, SCH-58261, SCH-412348, SCH-442416, VER-6623, VER-6947, VER-7835, CGS-15943 или ZM-241385.
В некоторых вариантах осуществления антагонист A2AR является антагонистом сигнального пути A2AR, например, ингибитором CD-73, например, антителом к CD73. Целенаправленное воздействие на внеклеточное продуцирование аденозина под действием CD73 может ослаблять иммуносупрессивные эффекты аденозина. Антитела к CD73 характеризуются рядом форм активности, например, ингибированием активности эктонуклеотидазы CD73, ослаблением АМР-опосредованной супрессии лимфоцитов и ингибированием роста сингенных опухолей. Антитела к CD73 могут управлять изменениями как в миелоидных, так и лимфоидных популяциях инфильтрирующих лейкоцитов в микроокружении опухоли. Эти изменения включают, например, увеличение количества CD8+ эффекторных клеток и активированных макрофагов, а также снижение доли супрессорных клеток миелоидного происхождения (MDSC) и регуляторных Т-лимфоцитов. В одном варианте осуществления молекула антитела к CD73 представляет собой полную молекулу антитела или ее антигенсвязывающий фрагмент. В некоторых вариантах осуществления молекула антитела к CD73 выбрана из любой из молекул антител, перечисленных в таблице 2. В других вариантах осуществления молекула антитела к CD73 содержит последовательность вариабельного домена тяжелой цепи, последовательность вариабельного домена легкой цепи или их обе, раскрытые в таблице 2. В определенных вариантах осуществления молекула антитела к CD73 связывается с белком CD73 и снижает активность CD73, например, CD73 человека, например, ингибирует ее или оказывает на нее антагонистическое действие.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2016/075099, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 представляет собой MEDI 9447, например, раскрытый в WO 2016/075099. Альтернативные названия MEDI 9447 включают клон 10.3 или 73combo3. MEDI 9447 представляет собой антитело IgG1, которое ингибирует активность CD73, например, оказывает на нее антагонистическое действие. MEDI 9447 и другие молекулы антител к CD73 также раскрыты в WO 2016/075176 и US2016/0129108, полное содержание которых включено в данный документ посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из MEDI 9477. Аминокислотная последовательность вариабельного домена тяжелой цепи MEDI 9477 раскрыта под SEQ ID NO: 295 (см. таблицу 2). Аминокислотная последовательность вариабельного домена легкой цепи MEDI 9477 раскрыта под SEQ ID NO: 296 (см. таблицу 2).
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2016/081748, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 представляет собой 11F11, например, раскрытый в WO 2016/081748. 11F11 представляет собой антитело IgG2, которое ингибирует активность CD73, например, оказывает на нее антагонистическое действие. Антитела, полученные из 11F11, например, CD73.4 и CD73.10; клоны 11F11, например, 11F11-1 и 11F11-2; и другие молекулы антител к CD73 раскрыты в WO 2016/081748 и US 9605080, полное содержание которых включено в данный документ посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из 11F11-1 или 11F11-2. Аминокислотная последовательность вариабельного домена тяжелой цепи 11F11-1 раскрыта под SEQ ID NO: 302 (см. таблицу 2). Аминокислотная последовательность вариабельного домена легкой цепи 11F11-1 раскрыта под SEQ ID NO: 303 (см. таблицу 2). Аминокислотная последовательность вариабельного домена тяжелой цепи 11F11-2 раскрыта под SEQ ID NO: 299 (см. таблицу 2). Аминокислотная последовательность вариабельного домена легкой цепи 11F11-2 раскрыта под SEQ ID NO: 300 (см. таблицу 2). В одном варианте осуществления молекула антитела к CD73 содержит тяжелую цепь, легкую цепь или их обе из 11F11-1 или 11F11-2. Аминокислотные последовательности тяжелой и легкой цепей 11F11-1 раскрыты соответственно под SEQ ID NO: 297 и SEQ ID NO: 301 (см. таблицу 2). Аминокислотные последовательности тяжелой и легкой цепей 11F11-2 раскрыты соответственно под SEQ ID NO: 294 и SEQ ID NO: 298 (см. таблицу 2).
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое, например, в US 9605080, включенном в данный документ посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к CD73 представляет собой CD73.4, например, раскрытый в US 9605080. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из CD73.4. Аминокислотная последовательность вариабельного домена тяжелой цепи CD73.4 раскрыта под SEQ ID NO: 304 (см. таблицу 2). Аминокислотная последовательность вариабельного домена легкой цепи 11F11-2 раскрыта под SEQ ID NO: 305 (см. таблицу 2).
В одном варианте осуществления молекула антитела к CD73 представляет собой CD73.10, например, раскрытый в US 9605080. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из CD73.10. Аминокислотная последовательность вариабельного домена тяжелой цепи CD73.10 раскрыта под SEQ ID NO: 306 (см. таблицу 2). Аминокислотная последовательность вариабельного домена легкой цепи CD73.10 раскрыта под SEQ ID NO: 307 (см. таблицу 2).
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2009/0203538, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 представляет собой 067-213, например, раскрытый в WO 2009/0203538.
В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из 067-213. Аминокислотная последовательность вариабельного домена тяжелой цепи 067-213 раскрыта под SEQ ID NO: 308 (см. таблицу 2). Аминокислотная последовательность вариабельного домена легкой цепи 067-213 раскрыта под SEQ ID NO: 309 (см. таблицу 2).
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US 9090697, включенном в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 представляет собой TY/23, например, раскрытый в US 9090697. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из TY/23.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2016/055609, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO 2016/055609.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2016/146818, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO 2016/146818.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2004/079013, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO 2004/079013.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2012/125850, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO 2012/125850.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2015/004400, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO 2015/004400.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO 2007/146968, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO 2007146968.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US2007/0042392, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в US2007/0042392.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US2009/0138977, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в US2009/0138977.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое во Flocke et al., Eur J Cell Biol. 1992 Jun;58(1):62-70, включенной в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого во Flocke et al., Eur J Cell Biol. 1992 Jun;58(1):62-70.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в Stagg et al., PNAS. 2010 Jan 107(4): 1547-1552, включенной в данный документ посредством ссылки во всей своей полноте. В некоторых вариантах осуществления молекула антитела к CD73 представляет собой TY/23 или TY11.8, раскрытый у Stagg et al. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого у Stagg et al.
В одном варианте осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с молекулой антитела к CD73, например, описанной в данном документе, и антагонистом A2AR, необязательно выбранным из группы, содержащей PBF509/NIR178, CPI444/V81444, AZD4635/HTL-1071, випаденант, GBV-2034, AB928, теофиллин, истрадефиллин, тозаденант/SYN-115, KW-6356, ST-4206 и преладенант/SCH 420814.
Таблица 2. Последовательности иллюстративных молекул антител к CD73
MEDI 9447
11F11-2
11F11-1
CD73.4
CD73.10
067-213
Молекулы антител к CD73, применяемые в видах комбинированной терапии, раскрытых в данном документе, могут содержать любую из последовательностей VH/VL, раскрытых в таблице 2, или аминокислотную последовательность, по существу идентичную ей (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную ей). Иллюстративные последовательности антител к CD73 включают:
(i) аминокислотные последовательности VH и VL из MEDI 9447, SEQ ID NO: 295-296 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 295-296);
(ii) аминокислотные последовательности HC и LC из 11F11-2, SEQ ID NO: 297-298 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 297-298);
(iii) аминокислотные последовательности VH и VL из 11F11-2, SEQ ID NO: 299-300 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 299-300);
(iv) аминокислотные последовательности HC и LC из 11F11-1, SEQ ID NO: 297 и 301 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 297 и 301);
(v) аминокислотные последовательности VH и VL из 11F11-1, SEQ ID NO: 302-303 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 302-303);
(vi) аминокислотные последовательности VH и VL из CD73.4, SEQ ID NO: 304-305 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 304-305);
(vii) аминокислотные последовательности VH и VL из CD73.10, SEQ ID NO: 306-307 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 306-307); или
(viii) аминокислотные последовательности VH и VL из 067-213, SEQ ID NO: 308-309 соответственно, или аминокислотную последовательность, по существу идентичную им (например, на по меньшей мере 80%, 85%, 90%, 95%, 99% или больше идентичную по отношению к SEQ ID NO: 308-309).
Антитело к ENTPD2 человека, описанное в данном документе, можно применять в комбинации с ингибитором коингибирующей молекулы (например, ингибитором PD-1 (например, молекулой антитела к PD-1), ингибитором PD-L1 (например, молекулой антитела к PD-L1), ингибитором PD-L2 (например, молекулой антитела к PD-L2), ингибитором LAG-3 (например, молекулой антитела к LAG-3), ингибитором TIM-3 (например, молекулой антитела к TIM-3)), активатором костимулирующей молекулы (например, агонистом GITR (например, молекулой антитела к GITR)), цитокином (например, IL-15 в комплексе с растворимой формой альфа-субъединицы рецептора IL-15 (IL-15Ra)) или любой их комбинацией.
Ингибиторы PD-1
В определенных вариантах осуществления антитело к ENTPD2, описанное в данном документе, вводят в комбинации с ингибитором PD-1. В некоторых вариантах осуществления ингибитор PD-1 выбран из PDR001 (Novartis), ниволумаба (Bristol-Myers Squibb), пембролизумаба (Merck & Co), пидилизумаба (CureTech), MEDI0680 (Medimmune), REGN2810 (Regeneron), TSR-042 (Tesaro), PF-06801591 (Pfizer), BGB-A317 (Beigene), BGB-108 (Beigene), INCSHR1210 (Incyte) или AMP-224 (Amplimmune).
Иллюстративные ингибиторы PD-1
В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1. В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1, описанную в US 2015/0210769, опубликованной 30 июля 2015 г. под названием "Antibody Molecules to PD-1 and Uses Thereof", включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-1 содержит по меньшей мере одну, две, три, четыре, пять или шесть областей, определяющих комплементарность (CDR) (или в совокупности все CDR), из вариабельной области тяжелой и легкой цепей, содержащей аминокислотную последовательность, показанную в таблице 3 (например, из последовательностей вариабельной области тяжелой и легкой цепей BAP049 клона E или BAP049 клона B, раскрытых в таблице 3), или кодируемой нуклеотидной последовательностью, показанной в таблице 3. В некоторых вариантах осуществления CDR указаны согласно определению по Kabat (например, как изложено в таблице 3). В некоторых вариантах осуществления CDR указаны согласно определению по Chothia (например, как изложено в таблице 3). В некоторых вариантах осуществления CDR указаны согласно комбинации определений CDR как по Kabat, так и по Chothia (например, как изложено в таблице 3). В одном варианте осуществления CDR1 VH согласно комбинации определений CDR по Kabat и Chothia содержит аминокислотную последовательность GYTFTTYWMH (SEQ ID NO: 541). В одном варианте осуществления одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или больше изменений, например, аминокислотных замен (например, консервативных аминокислотных замен) или делеций, по сравнению с аминокислотной последовательностью, показанной в таблице 3 или кодируемой нуклеотидной последовательностью, показанной в таблице 3.
В одном варианте осуществления молекула антитела к PD-1 содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 под SEQ ID NO: 501, аминокислотную последовательность VHCDR2 под SEQ ID NO: 502 и аминокислотную последовательность VHCDR3 под SEQ ID NO: 503; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 под SEQ ID NO: 510, аминокислотную последовательность VLCDR2 под SEQ ID NO: 511 и аминокислотную последовательность VLCDR3 под SEQ ID NO: 512, каждая из которых раскрыта в таблице 3.
В одном варианте осуществления молекула антитела содержит VH, содержащую VHCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 524, VHCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 525, и VHCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 526; и VL, содержащую VLCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 529, VLCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 530, и VLCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 531, каждая из которых раскрыта в таблице 3.
В одном варианте осуществления молекула антитела к PD-1 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 506 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 506. В одном варианте осуществления молекула антитела к PD-1 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 520 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 520. В одном варианте осуществления молекула антитела к PD-1 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 516 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 516. В одном варианте осуществления молекула антитела к PD-1 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 506, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 520. В одном варианте осуществления молекула антитела к PD-1 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 506, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 516.
В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 507 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 507. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 521 или 517 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 521 или 517. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 507, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 521 или 517.
В одном варианте осуществления молекула антитела к PD-1 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 508 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 508. В одном варианте осуществления молекула антитела к PD-1 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 522 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 522. В одном варианте осуществления молекула антитела к PD-1 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 518 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 518. В одном варианте осуществления молекула антитела к PD-1 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 508, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 522. В одном варианте осуществления молекула антитела к PD-1 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 508, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 518.
В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 509 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 509. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 523 или 519 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 523 или 519. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 509, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 523 или 519.
Молекулы антител, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в US 2015/0210769, включенной посредством ссылки во всей своей полноте.
Таблица 3. Аминокислотные и нуклеотидные последовательности иллюстративных молекул антител к PD-1
Другие иллюстративные ингибиторы PD-1
В одном варианте осуществления молекула антитела к PD-1 представляет собой ниволумаб (Bristol-Myers Squibb), также известный как MDX-1106, MDX-1106-04, ONO-4538, BMS-936558 или OPDIVO®. Ниволумаб (клон 5C4) и другие антитела к PD-1 раскрыты в US 8008449 и WO 2006/121168, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи ниволумаба, например, раскрытые в таблице 4.
В одном варианте осуществления молекула антитела к PD-1 представляет собой пембролизумаб (Merck & Co), также известный как ламбролизумаб, MK-3475, MK03475, SCH-900475 или KEYTRUDA®. Пембролизумаб и другие антитела к PD-1 раскрыты в Hamid, O. et al. (2013) New England Journal of Medicine 369 (2): 134-44, US 8354509 и WO 2009/114335, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи пембролизумаба, например, раскрытые в таблице 4.
В одном варианте осуществления молекула антитела к PD-1 представляет собой пидилизумаб (CureTech), также известный как CT-011. Пидилизумаб и другие антитела к PD-1 раскрыты в Rosenblatt, J. et al. (2011) J Immunotherapy 34(5): 409-18, US 7695715, US 7332582 и US 8686119, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи пидилизумаба, например, раскрытые в таблице 4.
В одном варианте осуществления молекула антитела к PD-1 представляет собой MEDI0680 (Medimmune), также известный как AMP-514. MEDI0680 и другие антитела к PD-1 раскрыты в US 9205148 и WO 2012/145493, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи MEDI0680.
В одном варианте осуществления молекула антитела к PD-1 представляет собой REGN2810 (Regeneron). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи REGN2810.
В одном варианте осуществления молекула антитела к PD-1 представляет собой PF-06801591 (Pfizer). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи PF-06801591.
В одном варианте осуществления молекула антитела к PD-1 представляет собой BGB-A317 или BGB-108 (Beigene). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BGB-A317 или BGB-108.
В одном варианте осуществления молекула антитела к PD-1 представляет собой INCSHR1210 (Incyte), также известный как INCSHR01210 или SHR-1210. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INCSHR1210.
В одном варианте осуществления молекула антитела к PD-1 представляет собой TSR-042 (Tesaro), также известный как ANB011. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-042.
Дополнительные известные антитела к PD-1 включают антитела, описанные, например, в WO 2015/112800, WO 2016/092419, WO 2015/085847, WO 2014/179664, WO 2014/194302, WO 2014/209804, WO 2015/200119, US 8735553, US 7488802, US 8927697, US 8993731 и US 9102727, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к PD-1 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в PD-1, что и одно из антител к PD-1, описанных в данном документе.
В одном варианте осуществления ингибитор PD-1 представляет собой пептид, который ингибирует сигнальный путь PD-1, например, как описано в US 8907053, включенном посредством ссылки во всей своей полноте. В одном варианте осуществления ингибитор PD-1 представляет собой иммуноадгезин (например, иммуноадгезин, который содержит внеклеточную или PD-1-связывающую часть PD-L1 или PD-L2, слитую с константной областью (например, Fc-областью последовательности иммуноглобулина)). В одном варианте осуществления ингибитор PD-1 представляет собой AMP-224 (B7-DCIg (Amplimmune), например, раскрытый в WO 2010/027827 и WO 2011/066342, включенных посредством ссылки во всей своей полноте).
Таблица 4. Аминокислотные последовательности других иллюстративных молекул антител к PD-1
В одном варианте осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с по меньшей мере одним ингибитором PD-1, описанным в данном документе, и по меньшей мере одним антагонистом рецептора A2A, описанным в данном документе.
Ингибиторы PD-L1
В определенных вариантах осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с ингибитором PD-L1. Ингибитор PD-L1 может представлять собой антитело, его антигенсвязывающий фрагмент, иммуноадгезин, слитый белок или олигопептид. В некоторых вариантах осуществления ингибитор PD-L1 выбран из FAZ053 (Novartis), атезолизумаба, также известного как Tecentriq® (Genentech/Roche), авелумаба, также известного как Bavencio® (Merck Serono и Pfizer), дурвалумаба, также известного как Imfinzi® (MedImmune/AstraZeneca) или BMS-936559 (Bristol-Myers Squibb).
Иллюстративные ингибиторы PD-L1
В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1. В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1, раскрытую в US 2016/0108123, опубликованной 21 апреля 2016 г. под названием "Antibody Molecules to PD-L1 and Uses Thereof", включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-L1 содержит по меньшей мере одну, две, три, четыре, пять или шесть областей, определяющих комплементарность (CDR) (или в совокупности все CDR), из вариабельной области тяжелой и легкой цепей, содержащей аминокислотную последовательность, показанную в таблице 5 (например, из последовательностей вариабельной области тяжелой и легкой цепей BAP058 клона O или BAP058 клона N, раскрытых в таблице 5), или кодируемой нуклеотидной последовательностью, показанной в таблице 5. В некоторых вариантах осуществления CDR указаны согласно определению по Kabat (например, как изложено в таблице 5). В некоторых вариантах осуществления CDR указаны согласно определению по Chothia (например, как изложено в таблице 5). В некоторых вариантах осуществления CDR указаны согласно комбинации определений CDR как по Kabat, так и по Chothia (например, как изложено в таблице 5). В одном варианте осуществления CDR1 VH согласно комбинации определений CDR по Kabat и Chothia содержит аминокислотную последовательность GYTFTSYWMY (SEQ ID NO: 647). В одном варианте осуществления одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или больше изменений, например, аминокислотных замен (например, консервативных аминокислотных замен) или делеций, по сравнению с аминокислотной последовательностью, показанной в таблице 5 или кодируемой нуклеотидной последовательностью, показанной в таблице 5.
В одном варианте осуществления молекула антитела к PD-L1 содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 под SEQ ID NO: 601, аминокислотную последовательность VHCDR2 под SEQ ID NO: 602 и аминокислотную последовательность VHCDR3 под SEQ ID NO: 603; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 под SEQ ID NO: 609, аминокислотную последовательность VLCDR2 под SEQ ID NO: 610 и аминокислотную последовательность VLCDR3 под SEQ ID NO: 611, каждая из которых раскрыта в таблице 5.
В одном варианте осуществления молекула антитела к PD-L1 содержит VH, содержащую VHCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 628, VHCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 629, и VHCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 630; и VL, содержащую VLCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 633, VLCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 634, и VLCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 635, каждая из которых раскрыта в таблице 5.
В одном варианте осуществления молекула антитела к PD-L1 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 606 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 606. В одном варианте осуществления молекула антитела к PD-L1 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 616 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 616. В одном варианте осуществления молекула антитела к PD-L1 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 620 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 620. В одном варианте осуществления молекула антитела к PD-L1 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 624 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 624. В одном варианте осуществления молекула антитела к PD-L1 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 606, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 616. В одном варианте осуществления молекула антитела к PD-L1 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 620, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 624.
В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 607 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 607. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 617 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 617. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 621 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 621. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 625 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 625. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 607, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 617. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 621, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 625.
В одном варианте осуществления молекула антитела к PD-L1 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 608 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 608. В одном варианте осуществления молекула антитела к PD-L1 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 618 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 618. В одном варианте осуществления молекула антитела к PD-L1 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 622 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 622. В одном варианте осуществления молекула антитела к PD-L1 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 626 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 626. В одном варианте осуществления молекула антитела к PD-L1 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 608, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 618. В одном варианте осуществления молекула антитела к PD-L1 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 622, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 626.
В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 615 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 615. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 619 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 619. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 623 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 623. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 627 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 627. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 615, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 619. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 623, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 627.
Молекулы антител, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в US 2016/0108123, включенной посредством ссылки во всей своей полноте.
Таблица 5. Аминокислотные и нуклеотидные последовательности иллюстративных молекул антител к PD-L1
Другие иллюстративные ингибиторы PD-L1
В одном варианте осуществления молекула антитела к PD-L1 представляет собой атезолизумаб (Genentech/Roche), также известный как MPDL3280A, RG7446, RO5541267, YW243.55.S70 или TECENTRIQ™. Атезолизумаб и другие антитела к PD-L1 раскрыты в US 8217149, включенном посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи атезолизумаба, например, раскрытые в таблице 6.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой авелумаб (Merck Serono и Pfizer), также известный как MSB0010718C или Bavencio®. Авелумаб и другие антитела к PD-L1 раскрыты в WO 2013/079174, включенной посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи авелумаба, например, раскрытые в таблице 6.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой дурвалумаб (MedImmune/AstraZeneca), также известный как MEDI4736 или Imfinzi®. Дурвалумаб и другие антитела к PD-L1 раскрыты в US 8779108, включенном посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи дурвалумаба, например, раскрытые в таблице 6.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой BMS-936559 (Bristol-Myers Squibb), также известный как MDX-1105 или 12A4. BMS-936559 и другие антитела к PD-L1 раскрыты в US 7943743 и WO 2015/081158, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-936559, например, раскрытые в таблице 6.
Дополнительные известные антитела к PD-L1 включают антитела, описанные, например, в WO 2015/181342, WO 2014/100079, WO 2016/000619, WO 2014/022758, WO 2014/055897, WO 2015/061668, WO 2013/079174, WO 2012/145493, WO 2015/112805, WO 2015/109124, WO 2015/195163, US 8168179, US 8552154, US 8460927 и US 9175082, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к PD-L1 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в PD-L1, что и одно из антител к PD-L1, описанных в данном документе.
Таблица 6. Аминокислотные последовательности других иллюстративных молекул антител к PD-L1
В одном варианте осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с по меньшей мере одним ингибитором PD-L1, описанным в данном документе, и по меньшей мере одним антагонистом рецептора A2A, описанным в данном документе.
Ингибиторы LAG-3
В определенных вариантах осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с ингибитором LAG-3. Ингибитор LAG-3 может представлять собой антитело, его антигенсвязывающий фрагмент, иммуноадгезин, слитый белок или олигопептид. В некоторых вариантах осуществления ингибитор LAG-3 выбран из LAG525 (Novartis), BMS-986016 (Bristol-Myers Squibb), TSR-033 (Tesaro), MK-4280 (Merck & Co) или REGN3767 (Regeneron).
Иллюстративные ингибиторы LAG-3
В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3. В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3, раскрытую в US 2015/0259420, опубликованной 17 сентября 2015 г. под названием "Antibody Molecules to LAG-3 and Uses Thereof", включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к LAG-3 содержит по меньшей мере одну, две, три, четыре, пять или шесть областей, определяющих комплементарность (CDR) (или в совокупности все CDR), из вариабельной области тяжелой и легкой цепей, содержащей аминокислотную последовательность, показанную в таблице 7 (например, из последовательностей вариабельной области тяжелой и легкой цепей BAP050 клона I или BAP050 клона J, раскрытых в таблице 7), или кодируемой нуклеотидной последовательностью, показанной в таблице 7. В некоторых вариантах осуществления CDR указаны согласно определению по Kabat (например, как изложено в таблице 7). В некоторых вариантах осуществления CDR указаны согласно определению по Chothia (например, как изложено в таблице 7). В некоторых вариантах осуществления CDR указаны согласно комбинации определений CDR как по Kabat, так и по Chothia (например, как изложено в таблице 7). В одном варианте осуществления CDR1 VH согласно комбинированной схеме нумерации CDR по Kabat и Chothia содержит аминокислотную последовательность GFTLTNYGMN (SEQ ID NO: 766). В одном варианте осуществления одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или больше изменений, например, аминокислотных замен (например, консервативных аминокислотных замен) или делеций, по сравнению с аминокислотной последовательностью, показанной в таблице 7 или кодируемой нуклеотидной последовательностью, показанной в таблице 7.
В одном варианте осуществления молекула антитела к LAG-3 содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 под SEQ ID NO: 701, аминокислотную последовательность VHCDR2 под SEQ ID NO: 702 и аминокислотную последовательность VHCDR3 под SEQ ID NO: 703; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 под SEQ ID NO: 710, аминокислотную последовательность VLCDR2 под SEQ ID NO: 711 и аминокислотную последовательность VLCDR3 под SEQ ID NO: 712, каждая из которых раскрыта в таблице 7.
В одном варианте осуществления молекула антитела к LAG-3 содержит VH, содержащую VHCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 736 или 737, VHCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 738 или 739, и VHCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 740 или 741; и VL, содержащую VLCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 746 или 747, VLCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 748 или 749, и VLCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 750 или 751, каждая из которых раскрыта в таблице 7. В одном варианте осуществления молекула антитела к LAG-3 содержит VH, содержащую VHCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 758 или 737, VHCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 759 или 739, и VHCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 760 или 741; и VL, содержащую VLCDR1, кодируемую нуклеотидной последовательностью под SEQ ID NO: 746 или 747, VLCDR2, кодируемую нуклеотидной последовательностью под SEQ ID NO: 748 или 749, и VLCDR3, кодируемую нуклеотидной последовательностью под SEQ ID NO: 750 или 751, каждая из которых раскрыта в таблице 7.
В одном варианте осуществления молекула антитела к LAG-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 706 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 706. В одном варианте осуществления молекула антитела к LAG-3 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 718 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 718. В одном варианте осуществления молекула антитела к LAG-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 724 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 724. В одном варианте осуществления молекула антитела к LAG-3 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 730 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 730. В одном варианте осуществления молекула антитела к LAG-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 706, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 718. В одном варианте осуществления молекула антитела к LAG-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 724, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 730.
В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 707 или 708 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 707 или 708. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 719 или 720 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 719 или 720. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 725 или 726 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 725 или 726. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 731 или 732 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 731 или 732. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 707 или 708, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 719 или 720. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 725 или 726, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 731 или 732.
В одном варианте осуществления молекула антитела к LAG-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 709 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 709. В одном варианте осуществления молекула антитела к LAG-3 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 721 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 721. В одном варианте осуществления молекула антитела к LAG-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 727 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 727. В одном варианте осуществления молекула антитела к LAG-3 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 733 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 733. В одном варианте осуществления молекула антитела к LAG-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 709, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 721. В одном варианте осуществления молекула антитела к LAG-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 727, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 733.
В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 716 или 717 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 716 или 717. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 722 или 723 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 722 или 723. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 728 или 729 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 728 или 729. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 734 или 735 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 734 или 735. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 716 или 717, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 722 или 723. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 728 или 729, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 734 или 735.
Молекулы антител, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в US 2015/0259420, включенной посредством ссылки во всей своей полноте.
Таблица 7. Аминокислотные и нуклеотидные последовательности иллюстративных молекул антител к LAG-3
Другие иллюстративные ингибиторы LAG-3
В одном варианте осуществления молекула антитела к LAG-3 представляет собой BMS-986016 (Bristol-Myers Squibb), также известный как BMS986016. BMS-986016 и другие антитела к LAG-3 раскрыты в WO 2015/116539 и US 9505839, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-986016, например, раскрытые в таблице 8.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой TSR-033 (Tesaro). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-033.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой MK-4280 (Merck & Co). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи MK-4280.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой REGN3767 (Regeneron). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи REGN3767.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой IMP731 или GSK2831781 (GSK и Prima BioMed). IMP731 и другие антитела к LAG-3 раскрыты в WO 2008/132601 и US 9244059, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи IMP731, например, раскрытые в таблице 8. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи GSK2831781.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой IMP761 (Prima BioMed). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи IMP761.
Дополнительные известные антитела к LAG-3 включают антитела, описанные, например, в WO 2008/132601, WO 2010/019570, WO 2014/140180, WO 2015/116539, WO 2015/200119, WO 2016/028672, US 9244059, US 9505839, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к LAG-3 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в LAG-3, что и одно из антител к LAG-3, описанных в данном документе.
В одном варианте осуществления ингибитор LAG-3 представляет собой растворимый белок LAG-3, например, IMP321 (Prima BioMed), например, раскрытый в WO 2009/044273, включенной посредством ссылки во всей своей полноте.
Таблица 8. Аминокислотные последовательности других иллюстративных молекул антител к LAG-3
Ингибиторы TIM-3
В определенных вариантах осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с ингибитором TIM-3. Ингибитор TIM-3 может представлять собой антитело, его антигенсвязывающий фрагмент, иммуноадгезин, слитый белок или олигопептид. В некоторых вариантах осуществления ингибитор TIM-3 выбран из MBG453 (Novartis), TSR-022 (Tesaro) или LY3321367 (Eli Lilly).
Иллюстративные ингибиторы TIM-3
В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3. В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3, раскрытую в US 2015/0218274, опубликованной 6 августа 2015 г. под названием "Antibody Molecules to TIM-3 and Uses Thereof", включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к TIM-3 содержит по меньшей мере одну, две, три, четыре, пять или шесть областей, определяющих комплементарность (CDR) (или в совокупности все CDR), из вариабельной области тяжелой и легкой цепей, содержащей аминокислотную последовательность, показанную в таблице 9 (например, из последовательностей вариабельной области тяжелой и легкой цепей ABTIM3-hum11 или ABTIM3-hum03, раскрытых в таблице 9), или кодируемой нуклеотидной последовательностью, показанной в таблице 9. В некоторых вариантах осуществления CDR указаны согласно определению по Kabat (например, как изложено в таблице 9). В некоторых вариантах осуществления CDR указаны согласно определению по Chothia (например, как изложено в таблице 9). В одном варианте осуществления одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или больше изменений, например, аминокислотных замен (например, консервативных аминокислотных замен) или делеций, по сравнению с аминокислотной последовательностью, показанной в таблице 9 или кодируемой нуклеотидной последовательностью, показанной в таблице 9.
В одном варианте осуществления молекула антитела к TIM-3 содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 под SEQ ID NO: 801, аминокислотную последовательность VHCDR2 под SEQ ID NO: 802 и аминокислотную последовательность VHCDR3 под SEQ ID NO: 803; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 под SEQ ID NO: 810, аминокислотную последовательность VLCDR2 под SEQ ID NO: 811 и аминокислотную последовательность VLCDR3 под SEQ ID NO: 812, каждая из которых раскрыта в таблице 9. В одном варианте осуществления молекула антитела к TIM-3 содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 под SEQ ID NO: 801, аминокислотную последовательность VHCDR2 под SEQ ID NO: 820 и аминокислотную последовательность VHCDR3 под SEQ ID NO: 803; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 под SEQ ID NO: 810, аминокислотную последовательность VLCDR2 под SEQ ID NO: 811 и аминокислотную последовательность VLCDR3 под SEQ ID NO: 812, каждая из которых раскрыта в таблице 9.
В одном варианте осуществления молекула антитела к TIM-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 806 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 806. В одном варианте осуществления молекула антитела к TIM-3 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 816 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 816. В одном варианте осуществления молекула антитела к TIM-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 822 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 822. В одном варианте осуществления молекула антитела к TIM-3 содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 826 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 826. В одном варианте осуществления молекула антитела к TIM-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 806, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 816. В одном варианте осуществления молекула антитела к TIM-3 содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 822, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 826.
В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 807 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 807. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 817 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 817. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 823 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 823. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 827 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 827. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 807, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 817. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 823, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 827.
В одном варианте осуществления молекула антитела к TIM-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 808 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 808. В одном варианте осуществления молекула антитела к TIM-3 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 818 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 818. В одном варианте осуществления молекула антитела к TIM-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 824 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 824. В одном варианте осуществления молекула антитела к TIM-3 содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 828 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 828. В одном варианте осуществления молекула антитела к TIM-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 808, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 818. В одном варианте осуществления молекула антитела к TIM-3 содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 824, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 828.
В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 809 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 809. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 819 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 819. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 825 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 825. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 829 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 829. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 809, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 819. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 825, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 829.
Молекулы антител, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в US 2015/0218274, включенной посредством ссылки во всей своей полноте.
Таблица 9. Аминокислотные и нуклеотидные последовательности иллюстративных молекул антител к TIM-3
Другие иллюстративные ингибиторы TIM-3
В одном варианте осуществления молекула антитела к TIM-3 представляет собой TSR-022 (AnaptysBio/Tesaro). В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-022. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи APE5137 или APE5121, например, раскрытые в таблице 10. APE5137, APE5121 и другие антитела к TIM-3 раскрыты в WO 2016/161270, включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к TIM-3 представляет собой LY3321367 (Eli Lilly). В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи LY3321367.
В одном варианте осуществления молекула антитела к TIM-3 представляет собой антитело клона F38-2E2. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи F38-2E2.
Дополнительные известные антитела к TIM-3 включают антитела, описанные, например, в WO 2016/111947, WO 2016/071448, WO 2016/144803, US 8552156, US 8841418 и US 9163087, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к TIM-3 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в TIM-3, что и одно из антител к TIM-3, описанных в данном документе.
Таблица 10. Аминокислотные последовательности других иллюстративных молекул антител к TIM-3
Ингибиторы CTLA-4
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором CTLA-4. Ингибитор CTLA-4 может представлять собой антитело, его антигенсвязывающий фрагмент, иммуноадгезин, слитый белок или олигопептид. В некоторых вариантах осуществления ингибитор CTLA-4 представляет собой ипилимумаб (Yervoy®, Bristol-Myers Squibb) или тремелимумаб (Pfizer). Антитело ипилимумаб и другие антитела к CTLA-4 раскрыты в US 6984720, включенном в данный документ посредством ссылки. Антитело тремелимумаб и другие антитела к CTLA-4 раскрыты в US 7411057, включенном в данный документ посредством ссылки.
Агонисты GITR
В определенных вариантах осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с агонистом GITR. Агонист GITR может представлять собой антитело, его антигенсвязывающий фрагмент, иммуноадгезин, слитый белок или олигопептид. В некоторых вариантах осуществления агонист GITR представляет собой GWN323 (Novartis), BMS-986156 (BMS), MK-4166 или MK-1248 (Merck), TRX518 (Leap Therapeutics), INCAGN1876 (Incyte/Agenus), AMG 228 (Amgen) или INBRX-110 (Inhibrx).
Иллюстративные молекулы антител к GITR
В одном варианте осуществления агонист GITR представляет собой молекулу антитела к GITR. В одном варианте осуществления агонист GITR представляет собой молекулу антитела к GITR, описанную в WO 2016/057846, опубликованной 14 апреля 2016 г. под названием "Compositions and Methods of Use for Augmented Immune Response and Cancer Therapy", включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к GITR содержит по меньшей мере одну, две, три, четыре, пять или шесть областей, определяющих комплементарность (CDR) (или в совокупности все CDR), из вариабельной области тяжелой и легкой цепей, содержащей аминокислотную последовательность, показанную в таблице 11 (например, из последовательностей вариабельной области тяжелой и легкой цепей MAB7, раскрытых в таблице 11), или кодируемой нуклеотидной последовательностью, показанной в таблице 11. В некоторых вариантах осуществления CDR указаны согласно определению по Kabat (например, как изложено в таблице 11). В некоторых вариантах осуществления CDR указаны согласно определению по Chothia (например, как изложено в таблице 11). В одном варианте осуществления одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или больше изменений, например, аминокислотных замен (например, консервативных аминокислотных замен) или делеций, по сравнению с аминокислотной последовательностью, показанной в таблице 11 или кодируемой нуклеотидной последовательностью, показанной в таблице 11.
В одном варианте осуществления молекула антитела к GITR содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 под SEQ ID NO: 909, аминокислотную последовательность VHCDR2 под SEQ ID NO: 911 и аминокислотную последовательность VHCDR3 под SEQ ID NO: 913; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 под SEQ ID NO: 914, аминокислотную последовательность VLCDR2 под SEQ ID NO: 916 и аминокислотную последовательность VLCDR3 под SEQ ID NO: 918, каждая из которых раскрыта в таблице 11.
В одном варианте осуществления молекула антитела к GITR содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 901 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 901. В одном варианте осуществления молекула антитела к GITR содержит VL, содержащую аминокислотную последовательность под SEQ ID NO: 902 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 902. В одном варианте осуществления молекула антитела к GITR содержит VH, содержащую аминокислотную последовательность под SEQ ID NO: 901, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 902.
В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 905 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 905. В одном варианте осуществления молекула антитела содержит VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 906 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 906. В одном варианте осуществления молекула антитела содержит VH, кодируемую нуклеотидной последовательностью под SEQ ID NO: 905, и VL, кодируемую нуклеотидной последовательностью под SEQ ID NO: 906.
В одном варианте осуществления молекула антитела к GITR содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 903 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 903. В одном варианте осуществления молекула антитела к GITR содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 904 или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичную по отношению к SEQ ID NO: 904. В одном варианте осуществления молекула антитела к GITR содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 903, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 904.
В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 907 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 907. В одном варианте осуществления молекула антитела содержит легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 908 или нуклеотидной последовательностью, на по меньшей мере 85%, 90%, 95% или 99% или больше идентичной по отношению к SEQ ID NO: 908. В одном варианте осуществления молекула антитела содержит тяжелую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 907, и легкую цепь, кодируемую нуклеотидной последовательностью под SEQ ID NO: 908.
Молекулы антител, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в WO 2016/057846, включенной посредством ссылки во всей своей полноте.
Таблица 11. Аминокислотные и нуклеотидные последовательности иллюстративной молекулы антитела к GITR
Другие иллюстративные антитела к GITR и агонисты GITR
В одном варианте осуществления молекула антитела к GITR представляет собой BMS-986156 (Bristol-Myers Squibb), также известный как BMS 986156 или BMS986156. BMS-986156 и другие антитела к GITR раскрыты, например, в US 9228016 и WO 2016/196792, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-986156, например, раскрытые в таблице 12.
В одном варианте осуществления молекула антитела к GITR представляет собой MK-4166 или MK-1248 (Merck). MK-4166, MK-1248 и другие антитела к GITR раскрыты, например, в US 8709424, WO 2011/028683, WO 2015/026684 и Mahne et al. Cancer Res. 2017; 77(5):1108-1118, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи MK-4166 или MK-1248.
В одном варианте осуществления молекула антитела к GITR представляет собой TRX518 (Leap Therapeutics). TRX518 и другие антитела к GITR раскрыты, например, в US 7812135, US 8388967, US 9028823, WO 2006/105021 и Ponte J et al. (2010) Clinical Immunology; 135:S96, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TRX518.
В одном варианте осуществления молекула антитела к GITR представляет собой INCAGN1876 (Incyte/Agenus). INCAGN1876 и другие антитела к GITR раскрыты, например, в US 2015/0368349 и WO 2015/184099, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INCAGN1876.
В одном варианте осуществления молекула антитела к GITR представляет собой AMG 228 (Amgen). AMG 228 и другие антитела к GITR раскрыты, например, в US 9464139 и WO 2015/031667, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи AMG 228.
В одном варианте осуществления молекула антитела к GITR представляет собой INBRX-110 (Inhibrx). INBRX-110 и другие антитела к GITR раскрыты, например, в US 2017/0022284 и WO 2017/015623, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления агонист GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INBRX-110.
В одном варианте осуществления агонист GITR (например, слитый белок) представляет собой MEDI 1873 (MedImmune), также известный как MEDI1873. MEDI 1873 и другие агонисты GITR раскрыты, например, в US 2017/0073386, WO 2017/025610 и Ross et al. Cancer Res 2016; 76(14 Suppl): Abstract № 561, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления агонист GITR содержит один или несколько из Fc-домена IgG, функционального мультимеризационного домена и рецепторсвязывающего домена лиганда глюкокортикоид-индуцируемого рецептора TNF (GITRL) в MEDI 1873.
Дополнительные известные агонисты GITR (например, антитела к GITR) включают агонисты, описанные, например, в WO 2016/054638, включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к GITR представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в GITR, что и одно из антител к GITR, описанных в данном документе.
В одном варианте осуществления агонист GITR представляет собой пептид, который активирует сигнальный путь GITR. В одном варианте осуществления агонист GITR представляет собой связывающий фрагмент иммуноадгезина (например, связывающий фрагмент иммуноадгезина, содержащий внеклеточную или GITR-связывающую часть GITRL), слитый с константной областью (например, Fc-областью последовательности иммуноглобулина).
Таблица 12. Аминокислотные последовательности других иллюстративных молекул антител к GITR
Иллюстративные молекулы полиспецифических антител к CD3
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с молекулой полиспецифического антитела к CD3 (например, молекулой биспецифического антитела к CD3). В одном варианте осуществления молекула полиспецифического антитела к CD3 связывается с CD3 и опухолевым антигеном-мишенью (TTA). В одном варианте осуществления TTA выбран из CD19, CD20, CD38 или CD123. В одном варианте осуществления молекула полиспецифического антитела к CD3 представлена в формате, раскрытом на фиг. 1А, 1В, 1С и 125 в WO 2016/182751, включенной в данный документ посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула полиспецифического антитела к CD3 представляет собой молекулу биспецифического антитела к CD3 x CD123, например, XENP14045 (например, как изложено в таблице 15), или молекулу биспецифического антитела к CD3 x CD123, раскрытую в WO 2016/086189 или WO 2016/182751, включенных в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула биспецифического антитела к CD3 x CD123 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи XENP14045 или аминокислотную последовательность, по существу идентичную им (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90% или 95% идентичностью последовательности по отношению к ним).
В одном варианте осуществления полиспецифическое антитело к CD3 представляет собой молекулу биспецифического антитела к CD3 x CD20, например, XENP13676 (например, как изложено в таблице 13) или молекулу биспецифического антитела к CD3 x CD20, раскрытую в WO 2016/086189 или WO 2016/182751, включенных в данный документ посредством ссылки во всей своей полноте. В одном варианте осуществления молекула биспецифического антитела к CD3 x CD20 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи XENP13676 или аминокислотную последовательность, по существу идентичную им (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90% или 95% идентичностью последовательности по отношению к ним).
Таблица 13. Аминокислотные последовательности иллюстративных молекул биспецифических антител к CD3
Комплексы IL15/IL-15Ra
В определенных вариантах осуществления антитело к ENTPD2 человека, описанное в данном документе, вводят в комбинации с комплексом IL-15/IL-15Ra. В некоторых вариантах осуществления комплекс IL-15/IL-15Ra выбран из NIZ985 (Novartis), ATL-803 (Altor) или CYP0150 (Cytune).
Иллюстративные комплексы IL-15/IL-15Ra
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит IL-15 человека в комплексе с растворимой формой IL-15Ra человека. Комплекс может содержать IL-15, ковалентно или нековалентно связанный с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека нековалентно связан с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека в композиции содержит аминокислотную последовательность под SEQ ID NO: 1001 из таблицы 14, а растворимая форма IL-15Ra человека содержит аминокислотную последовательность под SEQ ID NO: 1002 из таблицы 14, описанные в WO 2014/066527, включенной посредством ссылки во всей своей полноте. Молекулы, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в WO 2007/084342, включенной посредством ссылки во всей своей полноте.
Таблица 14. Аминокислотные и нуклеотидные последовательности иллюстративных комплексов IL-15/IL-15Ra
Другие иллюстративные комплексы IL-15/IL-15Ra
В одном варианте осуществления комплекс IL-15/IL-15Ra представляет собой ALT-803 - слитый белок на основе IL-15/IL-15Ra и Fc (растворимый комплекс IL-15N72D:IL-15RaSu/Fc). ALT-803 раскрыт в WO 2008/143794, включенной посредством ссылки во всей своей полноте. В одном варианте осуществления слитый белок на основе IL-15/IL-15Ra и Fc содержит последовательности, раскрытые в таблице 15.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит IL-15, слитый с доменом Sushi IL-15Ra (CYP0150, Cytune). Домен Sushi IL-15Ra относится к домену, начинающемуся с первого цистеинового остатка после сигнального пептида IL-15Ra и заканчивающемуся четвертым цистеиновым остатком после указанного сигнального пептида. Комплекс IL-15, слитого с доменом Sushi IL-15Ra, раскрыт в WO 2007/04606 и WO 2012/175222, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления слитый белок IL-15/домен Sushi IL-15Ra содержит последовательности, раскрытые в таблице 15.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит слитый белок на основе IL-15 и IL-15Ra, который может дополнительно содержать линкер, в частности глицин-сериновый линкер, соединяющий IL-15 и IL-15Ra, как раскрыто в WO 2014/186469 (Попечительский совет Системы университетов штата Техас), включенной посредством ссылки во всей своей полноте. В одном варианте осуществления слитый белок IL-15/IL-15Ra содержит последовательности, раскрытые в таблице 15.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит слитый белок на основе домена Sushi IL-15Ra и IL-15, связанных глицин-сериновым линкером, как раскрыто в WO 2015/109124 (Kadmon Corp.), включенной посредством ссылки во всей своей полноте. В одном варианте осуществления слитый белок IL-15/IL-15Ra содержит последовательности, раскрытые в таблице 15.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит слитый белок на основе IL-15, IL-15Ra, Fc-домена и RGD-пептида, предпочтительно в конфигурации полипептид RGD/Fc-домен/полипептид IL-15/полипептид IL-15Ra, как раскрыто в WO 2017/000913 (Numab Biopharmaceuticals), включенной посредством ссылки во всей своей полноте. В одном варианте осуществления слитый белок RGD/Fc/IL-15/IL-15Ra содержит последовательность, раскрытую в таблице 15.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит гетеродимерный белок, содержащий IL-15, связанный с первым Fc-доменом, и IL-15Ra, связанный со вторым Fc-доменом. IL-15 представляет собой зрелую форму IL-15 человека, а IL-15Ra представляет собой внеклеточный домен IL-15Ra человека или его усеченный вариант, такой как IL-15Ra-Sushi. Два Fc-домена могут содержать мутации, обеспечивающие образование гетеродимера посредством взаимодействий по типу "выступ во впадину", и иллюстративные конструкции раскрыты в WO 2015/103928 (Jiangsu Hendrui Medicine Co), включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит комбинацию из IL-15, содержащего аминокислотную мутацию по типу замены на Cys, и IL-15Ra (его внеклеточный домен или домен Sushi), содержащего мутацию по типу замены на Cys, способствующую образованию внутримолекулярных дисульфидных связей между полипептидами. Последовательности IL-15 и IL-15Ra с комбинациями мутаций раскрыты в WO 2016/095642 (Jiangsu Hendrui Medicine Co), включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит гетеродимерный белок, содержащий IL-15, связанный с первым Fc-доменом, и IL-15Ra, связанный со вторым Fc-доменом. Первый и второй Fc-домены могут иметь набор перечисленных аминокислотных замен: S267K/L368D/K370S: S267K/LS364K/E357Q; S364K/E357Q: L36HD/K370S; L36HD/K370S; S364K; L36HE/K370S: S364K; T411T/E360E/Q362E: D401K; L368D/K370S: S364K/E357L и K370S: S364K/E357Q в соответствии с нумерацией EU и, кроме того, могут содержать дополнительные аминокислотные замены и замены для устранения связывания с Fc-гамма-рецептором, как раскрыто в WO 2018/071919 (Xencor, Inc.), включенной посредством ссылки во всей своей полноте.
Таблица 15. Аминокислотные последовательности других иллюстративных комплексов IL-15/IL-15Ra
Где X представляет собой E или K
LTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGKGGGGSPPPMSVEHADIWVKSYSLYSRERYICNSGFKRKAGTSSLTECVLNKATNVAHWTTPSLKCIRDPALVHQRPAPPSTVSGGSGGGGSGGGSGGGGSLQNWVNVISDLKKIEDLIQSMHIDATLYTESDVHPSCKVTAMKCFLLELQVISLESGDASIHDTVENLIILANNSLSSNGNVTESGCKECEELEEKNIKEFLQSFVHIVQMFINTS
Иллюстративные средства, связывающие CSF-1/1R
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации со средством, связывающим CSF-1/1R.
В некоторых вариантах осуществления средство, связывающее CSF-1/1R, является ингибитором макрофагального колониестимулирующего фактора (M-CSF). M-CSF также иногда известен как CSF-1.
В другом варианте осуществления средство, связывающее CSF-1/1R, представляет собой 4-((2-(((1R,2R)-2-гидроксициклогексил)амино)бензо[d]тиазол-6-ил)окси)-N-метилпиколинамид (соединение A15) или соединение, раскрытое в РСТ-публикации № WO 2005/073224, которые являются ингибиторами тирозинкиназы CSF-1R. В некоторых вариантах осуществления средство, связывающее CSF-1/1R, представляет собой соединение A33 или средство, связывающее CSF-1, раскрытое в PCT-публикации № WO 2004/045532 или PCT-публикации № WO 2005/068503, в том числе RX1 или 5H4, которые являются ингибиторами M-CSF (например, молекулу или Fab-фрагмент антитела к M-CSF).
В некоторых вариантах осуществления средство, связывающее CSF-1/1R, является ингибитором CSF1R или 4-(2-((1R,2R)-2-гидроксициклогексиламино)бензотиазол-6-илокси)-N-метилпиколинамидом. 4-(2-((1R,2R)-2-гидроксициклогексиламино)бензотиазол-6-илокси)-N-метилпиколинамид раскрыт как пример 157 на странице 117 РСТ-публикации № WO 2007/121484.
В некоторых вариантах осуществления средство, связывающее CSF-1/1R, представляет собой пексидартиниб (регистрационный номер CAS 1029044-16-3). Пексидартиниб также известен как PLX3397 или 5-((5-хлор-1Н-пирроло[2,3-b]пиридин-3-ил)метил)-N-((6-(трифторметил)пиридин-3-ил)метил)пиридин-2-амин. Пексидартиниб является низкомолекулярным ингибитором рецепторных тирозинкиназ (RTK) KIT, CSF1R и FLT3.
В некоторых вариантах осуществления средство, связывающее CSF-1/1R, представляет собой эмактузумаб. Эмактузумаб также известен как RG7155 или RO5509554. Эмактузумаб представляет собой гуманизированное антитело mAb IgG1, нацеливающееся на CSF1R.
В некоторых вариантах осуществления средство, связывающее CSF-1/1R, представляет собой FPA008. FPA008 представляет собой гуманизированное антитело mAb, которое ингибирует CSF1R.
Иллюстративные ингибиторы IDO/TDO
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором индоламин-2,3-диоксигеназы (IDO) и/или триптофан-2,3-диоксигеназы (TDO).
В некоторых вариантах осуществления ингибитор IDO/TDO выбран из (4E)-4-[(3-хлор-4-фторанилино)-нитрозометилиден]-1,2,5-оксадиазол-3-амина (также известного как INCB24360 или эпакадостат; регистрационный номер CAS: 1204669-58-8 (Incyte)), индоксимода (1-метил-D-триптофана), α-циклогексил-5H-имидазо[5,1-a]изоиндол-5-этанола (также известного как NLG919) или BMS-986205 (также известного как F001287 или ONO-7701).
В некоторых вариантах осуществления ингибитор IDO/TDO представляет собой эпакадостат. Он является сильным и избирательным ингибитором индоламин-2,3-диоксигеназы (IDO1) с IC50, составляющей 10 нМ. Эпакадостат является высокоизбирательным по сравнению с другими родственными ферментами, такими как IDO2 или триптофан-2,3-диоксигеназа (TDO).
В некоторых вариантах осуществления ингибитор IDO/TDO представляет собой индоксимод (NewLink Genetics). Индоксимод, который представляет собой D-изомер 1-метилтриптофана, является перорально вводимым низкомолекулярным ингибитором метаболического пути индоламин-2,3-диоксигеназы (IDO), который нарушает механизмы, благодаря которым опухоли избегают иммуноопосредованного разрушения. NLG919 является сильным ингибитором метаболического пути IDO с Ki/EC50, составляющей соответственно 7 нМ/75 нМ в бесклеточных анализах.
В некоторых вариантах осуществления ингибитор IDO/TDO представляет собой BMS-986205 (также известный как F001287 или ONO-7701) (Flexus/BMS). BMS-986205 является низкомолекулярным ингибитором индоламин-2,3-диоксигеназы 1 (IDO1).
Иллюстративные ингибиторы TGF-β
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором трансформирующего фактора роста бета (TGF-β). Ингибитор TGF-β может представлять собой антитело, его антигенсвязывающий фрагмент, иммуноадгезин, слитый белок или олигопептид. В некоторых вариантах осуществления ингибитор TGF-β выбран из фрезолимумаба и XOMA 089 (Xoma).
TGF-β принадлежит к большому семейству структурно родственных цитокинов, включающему, например, костные морфогенетические белки (BMP), факторы роста и дифференцировки, активины и ингибины. В некоторых вариантах осуществления ингибиторы TGF-β, описанные в данном документе, могут связывать и/или ингибировать одну или несколько изоформ TGF-β (например, одну, две или все из TGF-β1, TGF-β2 или TGF-β3).
В некоторых вариантах осуществления ингибитор TGF-β представляет собой фрезолимумаб (регистрационный номер CAS: 948564-73-6). Фрезолимумаб также известен как GC1008. Фрезолимумаб представляет собой человеческое моноклональное антитело, которое связывается с изоформами 1, 2 и 3 TGF-бета и ингибирует их. Фрезолимумаб раскрыт, например, в WO 2006/086469, US 8383780 и US 8591901.
Тяжелая цепь фрезолимумаба имеет следующую аминокислотную последовательность: QVQLVQSGAEVKKPGSSVKVSCKASGYTFSSNVISWVRQAPGQGLEWMGGVIPIVDIANYAQRFKGRVTITADESTSTTYMELSSLRSEDTAVYYCASTLGLVLDAMDYWGQGTLVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPSCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK (SEQ ID NO: 1012).
Легкая цепь фрезолимумаба имеет следующую аминокислотную последовательность: ETVLTQSPGTLSLSPGERATLSCRASQSLGSSYLAWYQQKPGQAPRLLIYGASSRAPGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYADSPITFGQGTRLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO: 1013).
В некоторых вариантах осуществления ингибитор TGF-β представляет собой XOMA 089. XOMA 089 также известен как XPA.42.089. XOMA 089 представляет собой полностью человеческое моноклональное антитело, которое связывает и нейтрализует лиганды TGF-бета 1 и 2, не взаимодействуя при этом с TGF-бета 3.
Вариабельная область тяжелой цепи XOMA 089 имеет следующую аминокислотную последовательность: QVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARGLWEVRALPSVYWGQGTLVTVSS (SEQ ID NO: 310) (раскрытую под SEQ ID NO: 6 в WO 2012/167143).
Вариабельная область легкой цепи XOMA 089 имеет следующую аминокислотную последовательность: SYELTQPPSVSVAPGQTARITCGANDIGSKSVHWYQQKAGQAPVLVVSEDIIRPSGIPERISGSNSGNTATLTISRVEAGDEADYYCQVWDRDSDQYVFGTGTKVTVLG (SEQ ID NO: 311) (раскрытую под SEQ ID NO: 8 в WO 2012/167143).
Иллюстративные ингибиторы VEGFR
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором рецептора фактора роста эндотелия сосудов (VEGF) (например, ингибитором одного или нескольких из VEGFR (например, VEGFR-1, VEGFR-2 или VEGFR-3) или VEGF).
В некоторых вариантах осуществления ингибитор VEGFR представляет собой сукцинат ваталаниба (соединение A47) или соединение, раскрытое в EP 296122.
В некоторых вариантах осуществления ингибитор VEGFR представляет собой 1-метил-5-((2-(5-(трифторметил)-1H-имидазол-2-ил)пиридин-4-ил)окси)-N-(4-(трифторметил)фенил)-1H-бензо[d]имидазол-2-амин (соединение A37) или соединение, раскрытое в РСТ-публикации № WO 2007/030377, которые являются ингибиторами одного или нескольких из VEGFR-2, PDGFR-бета, KIT или Raf-киназы C.
Другие иллюстративные ингибиторы сигнального пути VEGFR, которые можно применять в комбинациях, раскрытых в данном документе, включают, например, бевацизумаб (AVASTIN®), акситиниб (INLYTA®); аланинат бриваниба (BMS-582664, (S)-((R)-1-(4-(4-фтор-2-метил-1Н-индол-5-илокси)-5-метилпирроло[2,1-f][1,2,4]триазин-6-илокси)пропан-2-ил)2-аминопропаноат); сорафениб (NEXAVAR®); пазопаниб (VOTRIENT®); малат сунитиниба (SUTENT®); цедираниб (AZD2171, CAS 288383-20-1); варгатеф (BIBF1120, CAS 928326-83-4); форетиниб (GSK1363089); телатиниб (BAY57-9352, CAS 332012-40-5); апатиниб (YN968D1, CAS 811803-05-1); иматиниб (GLEEVEC®); понатиниб (AP24534, CAS 943319-70-8); тивозаниб (AV951, CAS 475108-18-0); регорафениб (BAY73-4506, CAS 755037-03-7); дигидрохлорид ваталаниба (PTK787, CAS 212141-51-0); бриваниб (BMS-540215, CAS 649735-46-6); вандетаниб (CAPRELSA® или AZD6474); мотезаниба дифосфат (AMG706, CAS 857876-30-3, N-(2,3-дигидро-3,3-диметил-1Н-индол-6-ил)-2-[(4-пиридинилметил)амино]-3-пиридинкарбоксамид, описанный в РСТ-публикации № WO 02/066470; линфаниб (ABT869, CAS 796967-16-3); кабозантиниб (XL184, CAS 849217-68-1); лестауртиниб (CAS 111358-88-4); N-[5-[[[5-(1,1-диметилэтил)-2-оксазолил]метил]тио]-2-тиазолил]-4-пиперидинкарбоксамид (BMS38703, CAS 345627-80-7); (3R,4R)-4-амино-1-((4-((3-метоксифенил)амино)пирроло[2,1-f][1,2,4]триазин-5-ил)метил)пиперидин-3-ол (BMS690514); N-(3,4-дихлор-2-фторфенил)-6-метокси-7-[[(3aα,5β,6aα)-октагидро-2-метилциклопента[c]пиррол-5-ил]метокси]-4-хиназолинамин (XL647, CAS 781613-23-8); 4-метил-3-[[1-метил-6-(3-пиридинил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]амино]-N-[3-(трифторметил)фенил]-бензамид (BHG712, CAS 940310-85-0); афлиберцепт (EYLEA®) и эндостатин (ENDOSTAR®).
Иллюстративные антитела к VEGF, которые можно применять в комбинациях, раскрытых в данном документе, включают, например, моноклональное антитело, которое связывается с тем же эпитопом, что и моноклональное антитело A4.6.1 к VEGF, полученное из гибридомы ATCC HB 10709; рекомбинантное гуманизированное моноклональное антитело к VEGF, полученное в соответствии с Presta et al. (1997) Cancer Res. 57:4593-4599. В одном варианте осуществления антитело к VEGF представляет собой бевацизумаб (BV), также известный как rhuMAb-VEGF или AVASTIN®. Он содержит мутантные каркасные области IgG1 человека и антигенсвязывающие области, определяющие комплементарность, из мышиного моноклонального антитела A.4.6.1 к hVEGF, которое блокирует связывание VEGF человека с его рецепторами. Бевацизумаб и другие гуманизированные антитела к VEGF дополнительно описаны в патенте США № 6884879, выданном 26 февраля 2005 г. Дополнительные антитела включают антитела серии G6 или B20 (например, G6-31, B20-4.1), описанные в PCT-публикации № WO 2005/012359, PCT-публикации № WO 2005/044853. В отношении дополнительных антител см. патенты США №№ 7060269, 6582959, 6703020, 6054297, WO98/45332, WO 96/30046, WO94/10202, EP 0666868B1, публикации заявок на патент США №№ 2006/009360, 2005/0186208, 2003/0206899, 2003/0190317, 2003/0203409 и 2005/0112126; а также Popkov et al, Journal of Immunological Methods 288: 149-164 (2004). Другие антитела включают антитела, которые связываются с функциональным эпитопом в VEGF человека, содержащим остатки F17, M18, D19, Y21, Y25, Q89, I91, K101, E103 и C104 или, в качестве альтернативы, содержащим остатки F17, Y21, Q22, Y25, D63, 183 и Q89.
Иллюстративные ингибиторы EGFR
В некоторых вариантах осуществления молекулу антитела к ENTPD2 человека, например, молекулу антитела к ENTPD2, описанную в данном документе, применяют в комбинации с ингибитором тирозинкиназы (например, ингибитором рецепторной тирозинкиназы (RTK)). Иллюстративные ингибиторы тирозинкиназ включают без ограничения ингибитор сигнального пути эпидермального фактора роста (EGF) (например, ингибитор рецептора эпидермального фактора роста (EGFR)), ингибитор сигнального пути фактора роста эндотелия сосудов (VEGF) (например, ингибитор рецептора фактора роста эндотелия сосудов (VEGFR) (например, ингибитор VEGFR-1, ингибитор VEGFR-2, ингибитор VEGFR-3)), ингибитор сигнального пути фактора роста тромбоцитов (PDGF) (например, ингибитор рецептора фактора роста тромбоцитов (PDGFR) (например, ингибитор PDGFR-β)), ингибитор RAF-1, ингибитор KIT и ингибитор RET. В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором рецептора эпидермального фактора роста (EGFR).
В некоторых вариантах осуществления ингибитор EGFR представляет собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757.
В некоторых вариантах осуществления ингибитор EGFR выбран из одного или нескольких из эрлотиниба (Tarceva®), гефитиниба (Iressa®), цетуксимаба (Erbitux®), панитумумаба (Vectibix®), нецитумумаба (Portrazza®), дакомитиниба, нимотузумаба, имгатузумаба, афатиниба или осимертиниба (Tagrisso).
Другие противораковые средства, например, ингибиторы сигнальных путей тирозинкиназ, которые можно применять в комбинациях, раскрытых в данном документе, включают без ограничения выбранные ингибиторы тирозинкиназ, выбранные из сунитиниба (Sutent®) или сорафениба (Nexavar®).
В некоторых вариантах осуществления противораковое средство, применяемое в комбинации с ингибитором Hedgehog, выбрано из группы, состоящей из акситиниба (AG013736), босутиниба (SKI-606), цедираниба (RECENTINTM, AZD2171), дазатиниба (SPRYCEL®, BMS-354825), эрлотиниба (TARCEVA®), гефитиниба (IRESSA®), иматиниба (Gleevec®, CGP57148B, STI-571), лестауртиниба (CEP-701), нератиниба (HKI-272), нилотиниба (TASIGNA®), семаксаниба (семаксиниба, SU5416), сунитиниба (SUTENT®, SU11248), тоцераниба (PALLADIA®), вандетаниба (ZACTIMA®, ZD6474), ваталаниба (PTK787, PTK/ZK), трастузумаба (HERCEPTIN®), бевацизумаба (AVASTIN®), ритуксимаба (RITUXAN®), цетуксимаба (ERBITUX®), панитумумаба (VECTIBIX®), ранибизумаба (Lucentis®), нилотиниба (TASIGNA®), сорафениба (NEXAVAR®), алемтузумаба (CAMPATH®), конъюгата гемтузумаб-озогамицин (MYLOTARG®), ENMD-2076, PCI-32765, AC220, BIBW 2992 (TOVOKTM), SGX523, PF-04217903, PF-02341066, PF-299804, BMS-777607, ABT-869, MP470, BIBF 1120 (VARGATEF®), AP24534, JNJ-26483327, MGCD265, DCC-2036, BMS-690154, CEP-11981, тивозаниба (AV-951), OSI-930, MM-121, XL-184, XL-647, XL228, AEE788, AG-490, AST-6, BMS-599626, CUDC-101, PD153035, пелитиниба (EKB-569), вандетаниба (Zactima), WZ3146, WZ4002, WZ8040, ABT-869 (линифаниба), AEE788, AP24534 (понатиниба), AV-951 (тивозаниба), акситиниба, BAY 73-4506 (регорафениба), аланината бриваниба (BMS-582664), бриваниба (BMS-540215), цедираниба (AZD2171), CP 673451, CYC116, E7080, Ki8751, маситиниба (AB1010), MGCD-265, дифосфата мотезаниба (AMG-706), MP-470, OSI-930, гидрохлорида пазопаниба, PD173074, тозилата сорафениба (Bay 43-9006), SU 5402, TSU-68 (SU6668), ваталаниба, XL880 (GSK1363089, EXEL-2880).
Иллюстративные ингибиторы c-MET
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором c-MET.
В некоторых вариантах осуществления ингибитор c-MET представляет собой соединение A17 или соединение, описанное в патентах США №№ 7767675 и 8420645.
В некоторых вариантах осуществления ингибитор c-MET представляет собой JNJ-38877605. JNJ-38877605 является низкомолекулярным ингибитором c-MET, характеризующимся доступностью при пероральном применении. JNJ-38877605 избирательно связывается с c-MET, таким образом ингибируя фосфорилирование c-MET и нарушая пути передачи сигнала, опосредованной c-MET.
В некоторых вариантах осуществления ингибитор c-MET представляет собой AMG 208. AMG 208 является избирательным низкомолекулярным ингибитором c-MET. AMG 208 ингибирует лигандзависимую и лиганднезависимую активацию c-MET, ингибируя его тирозинкиназную активность, что может приводить к ингибированию роста клеток в опухолях, которые сверхэкспрессируют c-MET.
В некоторых вариантах осуществления ингибитор c-MET представляет собой AMG 337. AMG 337 является ингибитором c-MET, характеризующимся биодоступностью при пероральном применении. AMG 337 избирательно связывается с c-MET, таким образом нарушая пути передачи сигнала, опосредованной c-MET.
В некоторых вариантах осуществления ингибитор c-MET представляет собой LY2801653. LY2801653 является низкомолекулярным ингибитором c-MET, характеризующимся доступностью при пероральном применении. LY2801653 избирательно связывается с c-MET, таким образом ингибируя фосфорилирование c-MET и нарушая пути передачи сигнала, опосредованной c-MET.
В некоторых вариантах осуществления ингибитор c-MET представляет собой MSC2156119J. MSC2156119J является ингибитором c-MET, характеризующимся биодоступностью при пероральном применении. MSC2156119J избирательно связывается с c-MET, в результате чего происходит ингибирование фосфорилирования c-MET и нарушение путей передачи сигнала, опосредованной c-MET.
В некоторых вариантах осуществления ингибитор c-MET представляет собой капматиниб. Капматиниб также известен как INCB028060. Капматиниб является ингибитором c-MET, характеризующимся биодоступностью при пероральном применении. Капматиниб избирательно связывается с c-MET, таким образом ингибируя фосфорилирование c-MET и нарушая пути передачи сигнала, опосредованной c-MET.
В некоторых вариантах осуществления ингибитор c-MET представляет собой кризотиниб. Кризотиниб также известен как PF-02341066. Кризотиниб является аминопиридиновым ингибитором рецепторной тирозинкиназы, являющейся киназой анапластической лимфомы (ALK), и c-MET/рецептора фактора роста гепатоцитов (HGFR), характеризующимся доступностью при пероральном применении. Кризотиниб ATP-конкурентным образом связывается с ALK-киназой и слитыми белками на основе ALK и ингибирует их. Кроме того, кризотиниб ингибирует киназу c-MET и нарушает сигнальный путь c-MET. В целом это средство подавляет рост опухолевых клеток.
В некоторых вариантах осуществления ингибитор c-MET представляет собой голватиниб. Голватиниб является двойным ингибитором киназ c-MET и VEGFR-2 с потенциальной противоопухолевой активностью, характеризующимся биодоступностью при пероральном применении. Голватиниб связывается как с c-MET, так и с VEGFR-2 и ингибирует их активность, в результате чего может ингибироваться рост опухолевых клеток и выживание опухолевых клеток, которые сверхэкспрессируют эти рецепторные тирозинкиназы.
В некоторых вариантах осуществления ингибитор c-MET представляет собой тивантиниб. Тивантиниб также известен как ARQ 197. Тивантиниб является низкомолекулярным ингибитором c-MET, характеризующимся биодоступностью при пероральном применении. Тивантиниб связывается с белком c-MET и нарушает пути передачи сигнала, опосредованной c-MET, что может индуцировать клеточную гибель опухолевых клеток, сверхэкспрессирующих белок c-MET или экспрессирующих конститутивно активированный белок c-MET.
Иллюстративные ингибиторы IAP
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором ингибитора белка апоптоза (IAP).
В некоторых вариантах осуществления ингибитор IAP представляет собой (S)-N-((S)-1-циклогексил-2-((S)-2-(4-(4-фторбензоил)тиазол-2-ил)пирролидин-1-ил)-2-оксоэтил)-2-(метиламино)пропанамид (соединение A21) или соединение, раскрытое в патенте США № 8552003.
Иллюстративные ингибиторы mTOR
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором мишени рапамицина у млекопитающих (mTOR).
В некоторых вариантах осуществления ингибитор mTOR представляет собой 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он (соединение А41).
В некоторых вариантах осуществления ингибитор mTOR представляет собой эверолимус (также известный как RAD001 или AFINITOR®; соединение A36) или соединение, впервые раскрытое в РСТ-публикации № WO 94/09010.
В некоторых вариантах осуществления ингибитор mTOR выбран из одного или нескольких из темсиролимуса (TORISEL®), PF-4691502, GDC0980, OSI-027, GSK1059615, KU-0063794, WYE-354, паломида 529 (P529), PF-04691502, гедатолисиба (PF-05212384, PKI-587), ридафоролимуса (официально известного как деферолимус, (1R,2R,4S)-4-[(2R)-2[(1R,9S,12S,15R,16E,18R,19R,21R,23S,24E,26E,28Z,30S,32S,35R)-1,18-дигидрокси-19,30-диметокси-15,17,21,23,29,35-гексаметил-2,3,10,14,20-пентаоксо-11,36-диокса-4-азатрицикло[30.3.1.04,9]гексатриаконта-16,24,26,28-тетраен-12-ил]пропил]-2-метоксициклогексилдиметилфосфинат, также известного как AP23573 и MK8669 и описанного в РСТ-публикации № WO 03/064383); рапамицина (AY22989, SIROLIMUS®); симапимода (регистрационный номер CAS: 164301-51-3); (5-{2,4-бис[(3S)-3-метилморфолин-4-ил]пиридо[2,3-d]пиримидин-7-ил}-2-метоксифенил)метанола (AZD8055); 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метилпиридо[2,3-d]пиримидин-7(8Н)-она (PF04691502, регистрационный номер CAS: 1013101-36-4); N2-[1,4-диоксо-4-[[4-(4-оксо-8-фенил-4H-1-бензoпиран-2-ил)морфолиний-4-ил]метокси]бутил]-L-аргинилглицил-L-α-аспартил-L-серина в форме внутренней соли (SF1126, регистрационный номер CAS: 936487-67-1) (SEQ ID NO: 1011) или XL765 (SAR245409).
Иллюстративные ингибиторы PI3K-γ, -δ
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором фосфатидилинозитол-4,5-бисфосфат-3-киназы (PI3K), например, гамма- и/или дельта-изоформы фосфатидилинозитол-4,5-бисфосфат-3-киназы (PI3K-γ,δ).
В некоторых вариантах осуществления ингибитор PI3K является ингибитором дельта- и гамма-изоформ PI3K. Иллюстративные ингибиторы PI3K, которые можно применять в комбинации, описаны, например, в WO 2010/036380, WO 2010/006086, WO 09/114870, WO 05/113556. В некоторых вариантах осуществления ингибитор PI3K выбран из одного или нескольких из GSK 2126458, GDC-0980, GDC-0941, Sanofi XL147, XL756, XL147, PF-46915032, CAL-101, CAL 263, SF1126, PX-886 и двойного ингибитора PI3K.
В некоторых вариантах осуществления ингибитор PI3K-γ,δ представляет собой иделалисиб (регистрационный номер CAS: 870281-82-6). Иделалисиб также известен как ZYDELIG®, GS-1101, CAL-101 или 5-фтор-3-фенил-2-[(1S)-1-(7H-пурин-6-иламино)пропил]-4(3H)-хиназолинон. Иделалисиб блокирует P110δ, дельта-изоформу PI3K. Иделалисиб раскрыт, например, в Wu et al. Journal of Hematology & Oncology (2013) 6: 36.
В некоторых вариантах осуществления ингибитор PI3K-γ,δ представляет собой 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он (соединение А41).
Другие иллюстративные ингибиторы PI3K-γ,δ, которые можно применять в комбинации, включают, например, пиктилисиб (GDC-0941), LY294002, пиларалисиб (XL147), PI-3065, PI-103, VS-5584 (SB2343), CZC24832, дувелисиб (IPI-145, INK1197), TG100-115, CAY10505, GSK1059615, PF-04691502, AS-605240, воксталисиб (SAR245409, XL765), IC-87114, омипалисиб (GSK2126458, GSK458), TG100713, гедатолисиб (PF-05212384, PKI-587), аналог PKI-402, XL147, PIK-90, PIK-293, PIK-294, 3-метиладенин (3-MA), AS-252424, AS-604850 или апитолисиб (GDC-0980, RG7422).
В некоторых вариантах осуществления ингибитор PI3K представляет собой соединение A8 или соединение, раскрытое в РСТ-публикации № WO 2010/029082.
В некоторых вариантах осуществления ингибитор PI3K представляет собой (4S,5R)-3-(2'-амино-2-морфолино-4'-(трифторметил)-[4,5'-бипиримидин]-6-ил)-4-(гидроксиметил)-5-метилоксазолидин-2-он (соединение A13) или соединение, раскрытое в РСТ-публикации № WO 2013/124826, которые являются панспецифичными ингибиторами PI3K.
Иллюстративные ингибиторы PI3K-γ,-δ включают без ограничения дувелисиб и иделалисиб. Иделалисиб (также называемый GS-1101 или CAL-101; Gilead) представляет собой малую молекулу, которая блокирует дельта-изоформу PI3K. Структура иделалисиба (5-фтор-3-фенил-2-[(1S)-1-(7H-пурин-6-иламино)пропил]-4(3H)-хиназолинона) показана ниже.
Дувелисиб (также называемый IPI-145; Infinity Pharmaceuticals и AbbVie) представляет собой малую молекулу, которая блокирует PI3K-δ,γ. Структура дувелисиба (8-хлор-2-фенил-3-[(1S)-1-(9H-пурин-6-иламино)этил]-1(2H)-изохинолинона) показана ниже.
В одном варианте осуществления ингибитор является двойным ингибитором фосфатидилинозитол-3-киназы (PI3K) и mTOR, выбранным из 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метилпиридо[2,3-d]пиримидин-7(8H)-она (PF-04691502); N-[4-[[4-(диметиламино)-1-пиперидинил]карбонил]фенил]-N'-[4-(4,6-ди-4-морфолинил-1,3,5-триазин-2-ил)фенил]мочевины (PF-05212384, PKI-587); апитолисиба (GDC-0980, RG7422); 2,4-дифтор-N-{2-(метилокси)-5-[4-(4-пиридазинил)-6-хинолинил]-3-пиридинил}бензолсульфонамида (GSK2126458); 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-(пиперазин-1-ил)-3-(трифтометил)фенил)-1H-имидазо[4,5-c]хинолин-2(3H)-она в форме соли малеиновой кислоты (NVP-BGT226); 3-[4-(4-морфолинилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-2-ил)]фенола (PI-103); 5-(9-изопропил-8-метил-2-морфолино-9H-пурин-6-ил)пиримидин-2-амина (VS-5584, SB2343) или N-[2-[(3,5-диметоксифенил)амино]хиноксалин-3-ил]-4-[(4-метил-3-метоксифенил)карбонил]аминофенилсульфонамида (XL765).
Иллюстративные ингибиторы JAK
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, описанную в данном документе, вводят в комбинации с ингибитором янус-киназ (JAK).
В некоторых вариантах осуществления ингибитор JAK представляет собой 2-фтор-N-метил-4-(7-(хинолин-6-илметил)имидазо[1,2-b][1,2,4]триазин-2-ил)бензамид (соединение A17) или его дигидрохлоридную соль или соединение, раскрытое в РСТ-публикации № WO 2007/070514.
В некоторых вариантах осуществления ингибитор JAK представляет собой фосфат руксолитиниба (также известный как JAKAFI; соединение A18) или соединение, раскрытое в РСТ-публикации № WO 2007/070514.
В определенных вариантах осуществления любая из комбинаций, раскрытых в данном документе, в качестве альтернативы или в комбинации дополнительно включает в себя одно или несколько из средств, описанных в таблице 16.
Таблица 16. Выбранные терапевтические средства, которые можно вводить в комбинации с молекулами антител к ENTPD2 человека, например, в качестве средства монотерапии или в комбинации с другими иммуномодуляторами, описанными в данном документе. Каждая публикация, перечисленная в этой таблице, включена в данный документ посредством ссылки во всей своей полноте, включая все структурные формулы в ней.
Торговое наименование
US 2007/142401
WO 2005/039549
TASIGNA®
HCl • H20
US 7169791 
US 2010/0105667
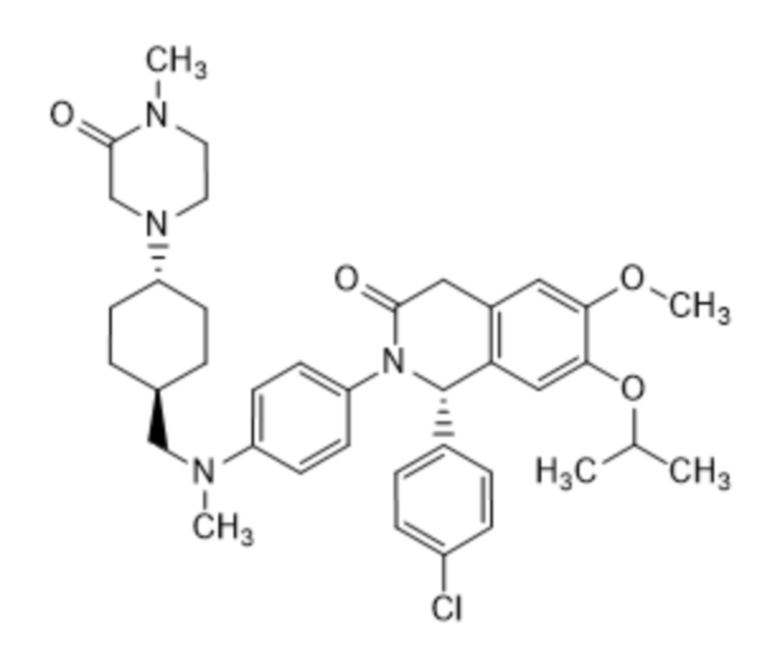
EXJADE®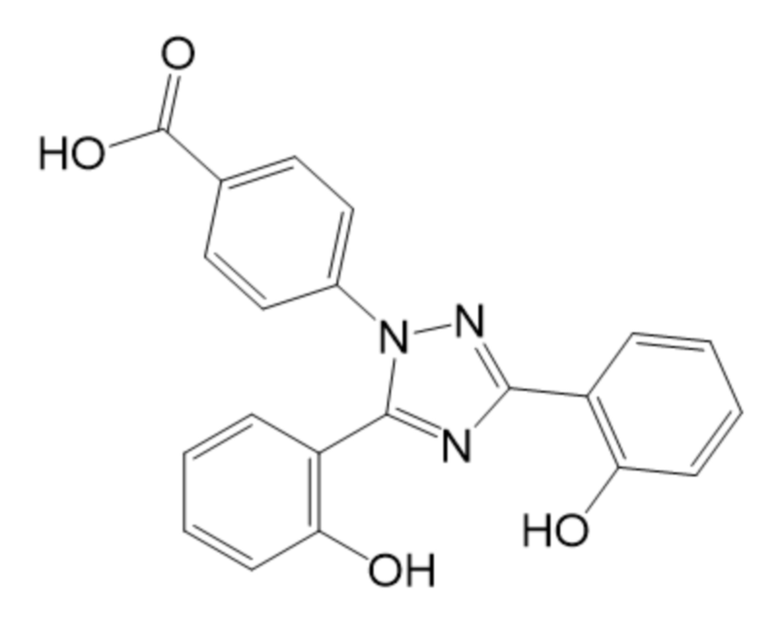
FEMARA®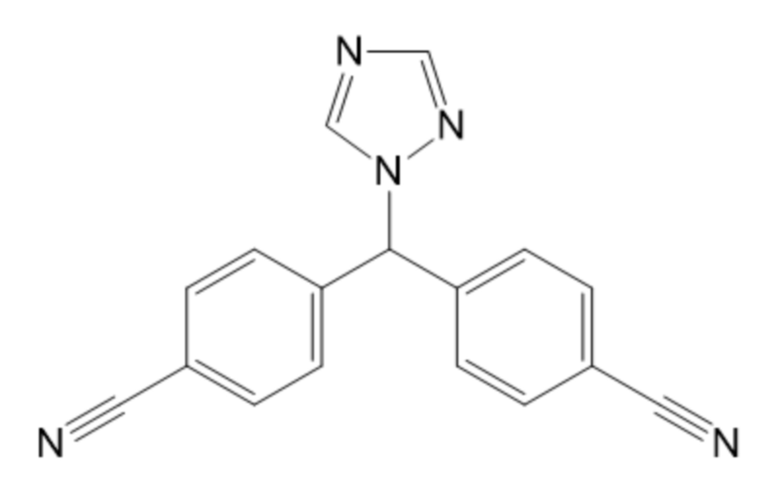
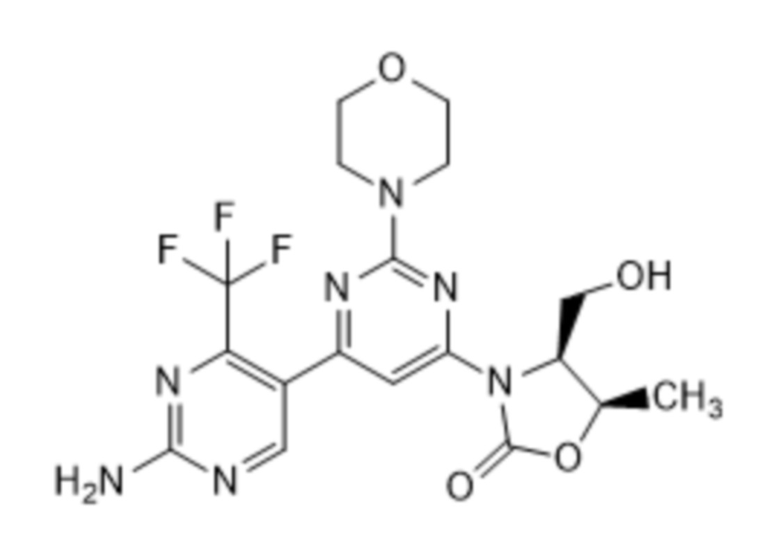
GLEEVEC®
Мезилат
Дигидрохлоридная соль
US 7767675
US 8420645 H3PO4
H3PO4
WO 2002/022577
EP 1870399
ZYKADIA™ 
KISQALI®
US 8685980 
WO 2008/106692
US 8735551
Линкер: SMCC (см. абзац [00117])
Полезная нагрузка: DM1 (см. абзац [00111])
См. также пункт 29 формулы изобретения 
US 2012/252785
WO 2014/085318 
SIGNIFOR®
US 7473761 
US 8519129 
AMDRAY™ 
сукцинат
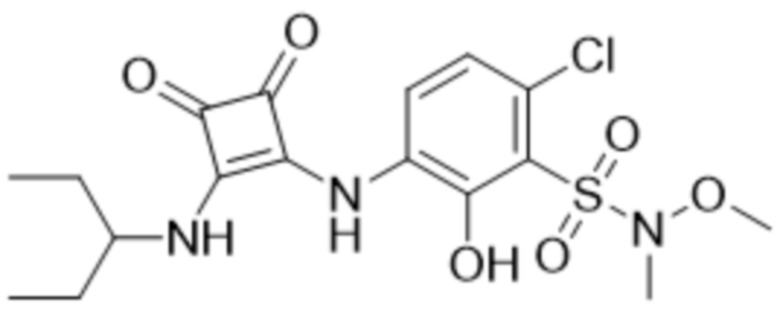
или его холиновая соль
US 7989497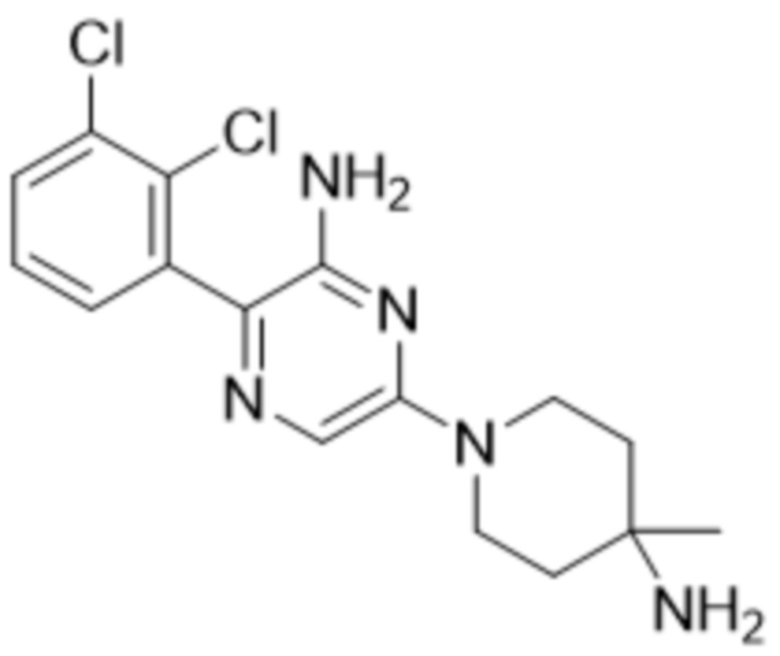
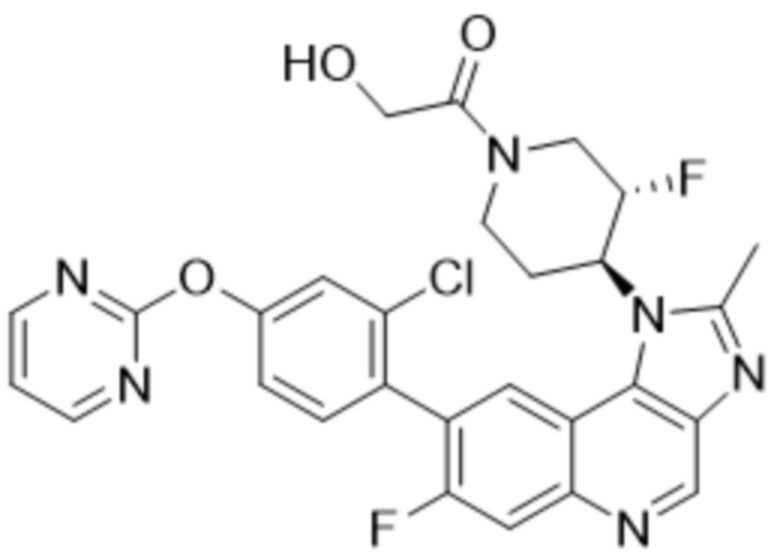
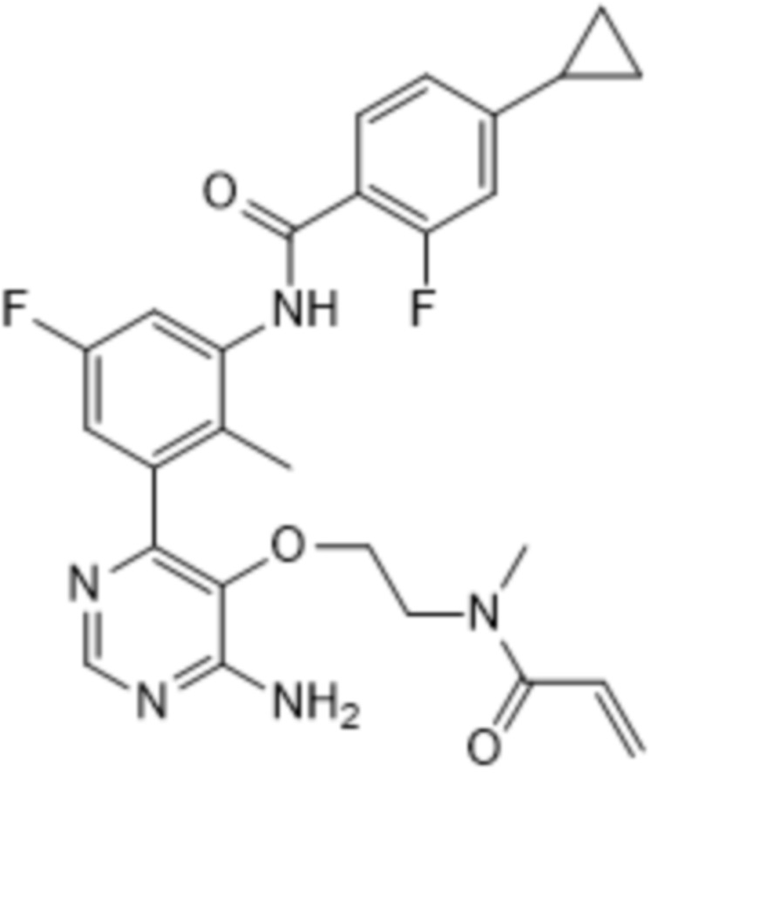
WO 2015/079417
US 7378423
US 7994185
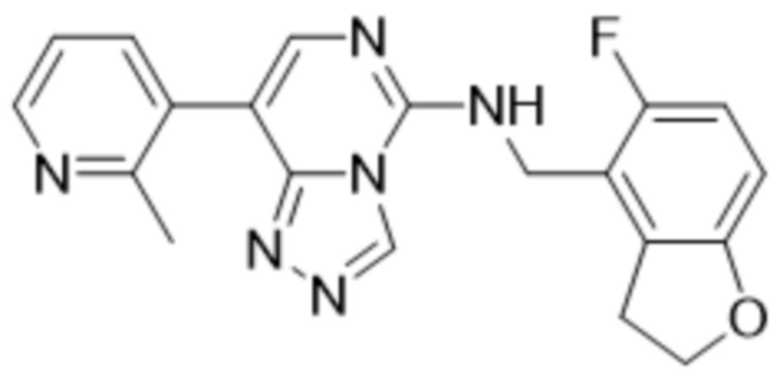
US 9580437
EP 3237418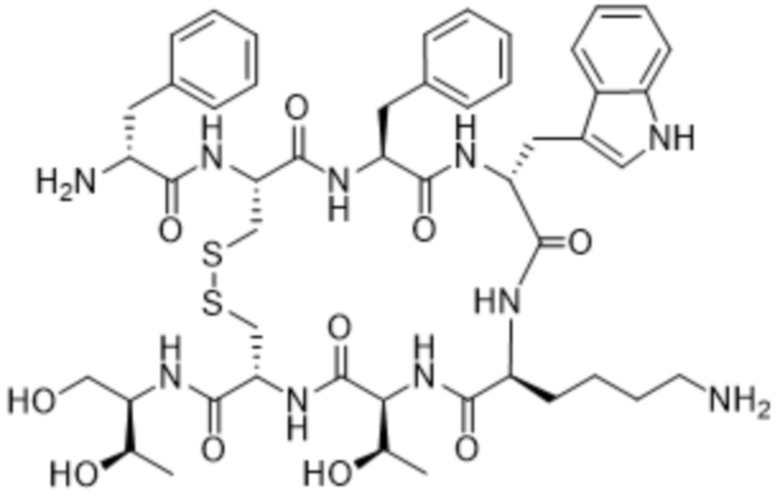
EP 0029579
Молекулы антител к ENTPD2 человека, описанные в данном документе, можно вводить в комбинации с дополнительным терапевтическим средством. В некоторых вариантах осуществления дополнительное терапевтическое средство выбрано из одного или нескольких из: 1) ингибитора протеинкиназы C (PKC); 2) ингибитора белка теплового шока 90 (HSP90); 3) ингибитора фосфоинозитид-3-киназы (PI3K) и/или мишени рапамицина (mTOR); 4) ингибитора цитохрома P450 (например, ингибитора CYP17 или ингибитора 17-альфа-гидроксилазы/C17-20-лиазы); 5) железохелатирующего средства; 6) ингибитора ароматазы; 7) ингибитора р53, например, ингибитора взаимодействия р53/Mdm2; 8) индуктора апоптоза; 9) ингибитора ангиогенеза; 10) ингибитора альдостеронсинтазы; 11) ингибитора рецептора Smoothened (SMO); 12) ингибитора рецептора пролактина (PRLR); 13) ингибитора сигнального пути Wnt; 14) ингибитора CDK4/6; 15) ингибитора рецептора 2 фактора роста фибробластов (FGFR2)/рецептора 4 фактора роста фибробластов (FGFR4); 16) ингибитора макрофагального колониестимулирующего фактора (M-CSF); 17) ингибитора одного или нескольких из высвобождения гистамина, Flt3 (например, FLK2/STK1) или PKC; 18) ингибитора одного или нескольких из VEGFR-2 (например, FLK-1/KDR), PDGFR-бета, c-KIT или Raf-киназы C; 19) агониста соматостатина и/или ингибитора высвобождения гормона роста; 20) ингибитора киназы анапластической лимфомы (ALK); 21) ингибитора рецептора инсулиноподобного фактора роста 1 (IGF-1R); 22) ингибитора P-гликопротеина 1; 23) ингибитора рецептора фактора роста эндотелия сосудов (VEGFR); 24) ингибитора киназы BCR-ABL; 25) ингибитора FGFR; 26) ингибитора CYP11B2; 27) ингибитора HDM2, например, ингибитора взаимодействия HDM2-p53; 28) ингибитора тирозинкиназы; 29) ингибитора c-MET; 30) ингибитора JAK; 31) ингибитора DAC; 32) ингибитора 11β-гидроксилазы; 33) ингибитора IAP; 34) ингибитора PIM-киназы; 35) ингибитора поркупина; 36) ингибитора BRAF, например, BRAF V600E или BRAF дикого типа; 37) ингибитора HER3; 38) ингибитора MEK или 39) ингибитора липидкиназы, например, описанного в данном документе и в таблице 1.
В одном варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя сотрастаурин (соединение A1) или соединение, раскрытое в РСТ-публикации № WO 2005/039549, которые являются ингибиторами PKC, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор PKC представляет собой сотрастаурин (соединение A1) или соединение, раскрытое в РСТ-публикации № WO 2005/039549.
В одном варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя нилотиниб (соединение A2, Tasigna®) или соединение, раскрытое в РСТ-публикации № WO 2004/005281, которые являются ингибиторами BCR-ABL, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор BCR-ABL представляет собой нилотиниб или соединение, раскрытое в РСТ-публикации № WO 2004/005281.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя ингибитор HSP90 или применяется в комбинации с ним для лечения нарушения, например, нарушения, описанного в данном документе, например, рака.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, применяется в комбинации с 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-оном (соединением A41), который является ингибитором PI3K и/или mTOR, для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор PI3K и/или mTOR представляет собой 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он (соединение А41).
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 3-(2,6-дихлор-3,5-диметоксифенил)-1-(6-((4-(4-этилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-1-метилмочевину (соединение A5) или соединение, раскрытое в патенте США № 8552002, которые являются ингибиторами FGFR, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор FGFR представляет собой 3-(2,6-дихлор-3,5-диметоксифенил)-1-(6-((4-(4-этилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-1-метилмочевину (соединение А5) или соединение, раскрытое в патенте США № 8552002. Соединение А5 имеет следующую структуру:
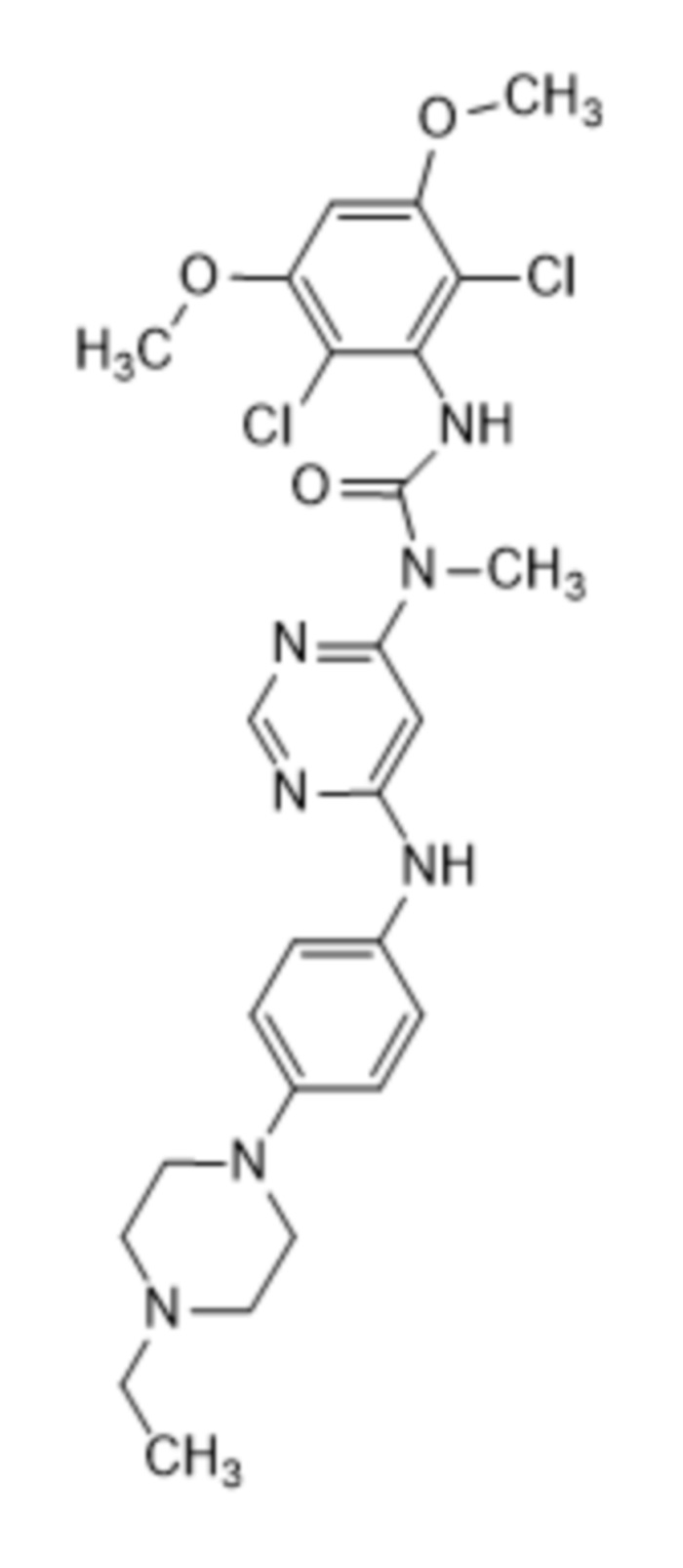
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя бупарлизиб (соединение A6) или соединение, раскрытое в РСТ-публикации № WO 2007/084786, которые являются ингибиторами PI3K, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор PI3K представляет собой бупарлизиб (соединение A6) или соединение, раскрытое в РСТ-публикации № WO 2007/084786. Соединение А6 имеет следующую структуру:
a. 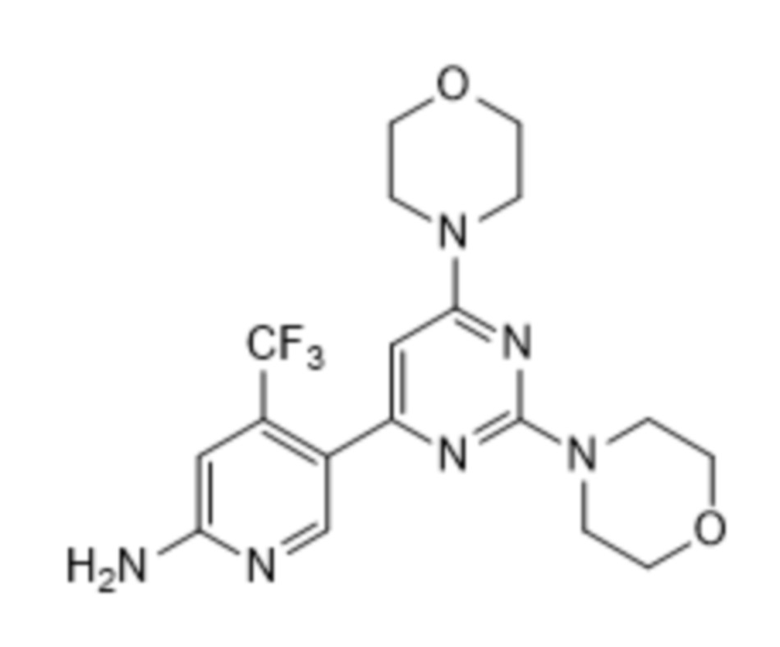
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 8-(2,6-дифтор-3,5-диметоксифенил)-N-(4-((диметиламино)метил)-1Н-имидазол-2-ил)хиноксалин-5-карбоксамид (соединение А7) или соединение, раскрытое в РСТ-публикации № WO 2009/141386, которые являются ингибиторами FGFR, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор FGFR представляет собой 8-(2,6-дифтор-3,5-диметоксифенил)-N-(4-((диметиламино)метил)-1H-имидазол-2-ил)хиноксалин-5-карбоксамид (соединение A7) или соединение, раскрытое в РСТ-публикации № WO 2009/141386.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя (S)-N1-(4-метил-5-(2-(1,1,1-трифтор-2-метилпропан-2-ил)пиридин-4-ил)тиазол-2-ил)пирролидин-1,2-дикарбоксамид (соединение A8) или соединение, раскрытое в PCT-публикации № WO 2010/029082, которые являются ингибиторами PI3K, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор PI3K представляет собой (S)-N1-(4-метил-5-(2-(1,1,1-трифтор-2-метилпропан-2-ил)пиридин-4-ил)тиазол-2-ил)пирролидин-1,2-дикарбоксамид (соединение A8) или соединение, раскрытое в РСТ-публикации № WO 2010/029082.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя ингибитор цитохрома P450 (например, ингибитор CYP17) или соединение, раскрытое в РСТ-публикации № WO 2010/149755, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор цитохрома P450 (например, ингибитор CYP17) представляет собой соединение, раскрытое в РСТ-публикации № WO 2010/149755, US 8263635 B2 или EP 2445903 B1.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя (S)-1-(4-хлорфенил)-7-изопропокси-6-метокси-2-(4-(метил(((1r,4S)-4-(4-метил-3-оксопиперазин-1-ил)циклогексил)метил)амино)фенил)-1,2-дигидроизохинолин-3(4H)-он (соединение A10) или соединение, раскрытое в РСТ-публикации № WO 2011/076786, которые являются ингибиторами HDM2, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор HDM2 представляет собой (S)-1-(4-хлорфенил)-7-изопропокси-6-метокси-2-(4-(метил(((1r,4S)-4-(4-метил-3-оксопиперазин-1-ил)циклогексил)метил)амино)фенил)-1,2-дигидроизохинолин-3(4H)-он (соединение A10) или соединение, раскрытое в РСТ-публикации № WO 2011/076786.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя деферазирокс (также известный как EXJADE; соединение A11) или соединение, раскрытое в РСТ-публикации № WO 1997/049395, которые являются железохелатирующими средствами, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления железохелатирующее средство представляет собой деферазирокс или соединение, раскрытое в РСТ-публикации № WO 1997/049395. В одном варианте осуществления железохелатирующее средство представляет собой деферазирокс (соединение A11).
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя летрозол (также известный как FEMARA; соединение A12) или соединение, раскрытое в US 4978672, которые являются ингибиторами ароматазы, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор ароматазы представляет собой летрозол (соединение A12) или соединение, раскрытое в патенте США 4978672.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя (4S,5R)-3-(2'-амино-2-морфолино-4'-(трифторметил)-[4,5'-бипиримидин]-6-ил)-4-(гидроксиметил)-5-метилоксазолидин-2-он (соединение A13) или соединение, раскрытое в РСТ-публикации № WO 2013/124826, которые являются ингибиторами PI3K, например, панспецифичными ингибиторами PI3K, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор PI3K представляет собой (4S,5R)-3-(2'-амино-2-морфолино-4'-(трифторметил)-[4,5'-бипиримидин]-6-ил)-4-(гидроксиметил)-5-метилоксазолидин-2-он (соединение A13) или соединение, раскрытое в РСТ-публикации № WO 2013/124826.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя (S)-5-(5-хлор-1-метил-2-оксо-1,2-дигидропиридин-3-ил)-6-(4-хлорфенил)-2-(2,4-диметоксипиримидин-5-ил)-1-изопропил-5,6-дигидропирроло[3,4-d]имидазол-4(1H)-он (соединение A14) или соединение, раскрытое в РСТ-публикации № WO 2013/111105, которые являются ингибиторами p53 и/или взаимодействия p53/Mdm2, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор p53 и/или взаимодействия p53/Mdm2 представляет собой (S)-5-(5-хлор-1-метил-2-оксо-1,2-дигидропиридин-3-ил)-6-(4-хлорфенил)-2-(2,4-диметоксипиримидин-5-ил)-1-изопропил-5,6-дигидропирроло[3,4-d]имидазол-4(1H)-он (соединение A14) или соединение, раскрытое в РСТ-публикации № WO 2013/111105.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 4-((2-(((1R,2R)-2-гидроксициклогексил)амино)бензо[d]тиазол-6-ил)окси)-N-метилпиколинамид (соединение А15) или соединение, раскрытое в РСТ-публикации № WO 2005/073224, которые являются ингибиторами тирозинкиназы CSF-1R, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор тирозинкиназы CSF-1R представляет собой 4-((2-(((1R,2R)-2-гидроксициклогексил)амино)бензо[d]тиазол-6-ил)окси)-N-метилпиколинамид (соединение A15) или соединение, раскрытое в РСТ-публикации № WO 2005/073224.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя индуктор апоптоза и/или ингибитор ангиогенеза, такой как мезилат иматиниба (также известный как GLEEVEC®; соединение А16) или соединение, раскрытое в РСТ-публикации № WO 1999/003854, или применяется в комбинации с ними для лечения нарушения, например, описанного нарушения. В одном варианте осуществления индуктор апоптоза и/или ингибитор ангиогенеза представляет собой мезилат иматиниба (соединение A16) или соединение, раскрытое в РСТ-публикации № WO 1999/003854.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 2-фтор-N-метил-4-(7-(хинолин-6-илметил)имидазо[1,2-b][1,2,4]триазин-2-ил)бензамид (соединение A17) или его дигидрохлоридную соль или соединение, раскрытое в PCT-публикации № WO 2007/070514, которые являются ингибиторами JAK, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор JAK представляет собой 2-фтор-N-метил-4-(7-(хинолин-6-илметил)имидазо[1,2-b][1,2,4]триазин-2-ил)бензамид (соединение A17) или его дигидрохлоридную соль или соединение, раскрытое в РСТ-публикации № WO 2007/070514.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя фосфат руксолитиниба (также известный как JAKAFI; соединение A18) или соединение, раскрытое в РСТ-публикации № WO 2007/070514, которые являются ингибиторами JAK, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор JAK представляет собой фосфат руксолитиниба (соединение A18) или соединение, раскрытое в РСТ-публикации № WO 2007/070514.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя панобиностат (соединение A19) или соединение, раскрытое в РСТ-публикации № WO 2014/072493, которые являются ингибиторами деацетилаз (DAC), или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор DAC представляет собой панобиностат (соединение A19) или соединение, раскрытое в РСТ-публикации № WO 2014/072493.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя осилодростат (соединение A20) или соединение, раскрытое в РСТ-публикации № WO 2007/024945, которые являются ингибиторами одного или нескольких из цитохрома P450 (например, 11B2), альдостерона или ангиогенеза, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя (S)-N-((S)-1-циклогексил-2-((S)-2-(4-(4-фторбензоил)тиазол-2-ил)пирролидин-1-ил)-2-оксоэтил)-2-(метиламино)пропанамид (соединение A21) или соединение, раскрытое в US 8552003, которые являются ингибиторами IAP, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор IAP представляет собой (S)-N-((S)-1-циклогексил-2-((S)-2-(4-(4-фторбензоил)тиазол-2-ил)пирролидин-1-ил)-2-оксоэтил)-2-(метиламино)пропанамид (соединение A21) или соединение, раскрытое в патенте США 8552003.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя (R)-2-(5-(4-(6-бензил-4,5-диметилпиридазин-3-ил)-2-метилпиперазин-1-ил)пиразин-2-ил)пропан-2-ол (соединение A25) или соединение, раскрытое в РСТ-публикации № WO 2010/007120, которые являются ингибиторами Smoothened (SMO), или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор SMO представляет собой (R)-2-(5-(4-(6-бензил-4,5-диметилпиридазин-3-ил)-2-метилпиперазин-1-ил)пиразин-2-ил)пропан-2-ол (соединение A25) или соединение, раскрытое в PCT-публикации № WO 2010/007120.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя церитиниб (также известный как ZYKADIA; соединение A23), который является ингибитором ALK, или применяется в комбинации с ним для лечения нарушения, например, нарушения, описанного в данном документе.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 7-циклопентил-N, N-диметил-2-((5-(пиперазин-1-ил)пиридин-2-ил)амино)-7H-пирроло[2,3-d]пиримидин-6-карбоксамид (соединение A24) или соединение, раскрытое в патенте США 8415355 или патенте США 8685980, которые являются ингибиторами JAK и/или CDK4/6, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор JAK и/или CDK4/6 представляет собой 7-циклопентил-N, N-диметил-2-((5-(пиперазин-1-ил)пиридин-2-ил)амино)-7H-пирроло[2,3-d]пиримидин-6-карбоксамид (соединение A24) или соединение, раскрытое в патенте США 8415355 или патенте США 8685980.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя молекулу человеческого моноклонального антитела (соединение A26), раскрытую в патенте США № 7867493, которая является ингибитором рецептора пролактина (PRLR), или применяется в комбинации с ней для лечения нарушения, например, нарушения, описанного в данном документе.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя N-(4-((1R,3S,5S)-3-амино-5-метилциклогексил)пиридин-3-ил)-6-(2,6-дифторфенил)-5-фторпиколинамид (соединение A27) или соединение, раскрытое в РСТ-публикации № WO 2010/026124, которые являются ингибиторами PIM-киназ, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор PIM-киназ представляет собой N-(4-((1R,3S,5S)-3-амино-5-метилциклогексил)пиридин-3-ил)-6-(2,6-дифторфенил)-5-фторпиколинамид (соединение A27) или соединение, раскрытое в РСТ-публикации № WO 2010/026124.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 2-(2',3-диметил-[2,4'-бипиридин]-5-ил)-N-(5-(пиразин-2-ил)пиридин-2-ил)ацетамид (соединение А28) или соединение, раскрытое в РСТ-публикации № WO 2010/101849, которые являются ингибиторами сигнального пути Wnt, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор сигнального пути Wnt представляет собой 2-(2',3-диметил-[2,4'-бипиридин]-5-ил)-N-(5-(пиразин-2-ил)пиридин-2-ил)ацетамид (соединение A28) или соединение, раскрытое в РСТ-публикации № WO 2010/101849. В одном варианте осуществления ингибитор сигнального пути Wnt представляет собой 2-(2',3-диметил-[2,4'-бипиридин]-5-ил)-N-(5-(пиразин-2-ил)пиридин-2-ил)ацетамид (соединение A28).
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя ингибитор BRAF или применяется в комбинации с ним для лечения нарушения, например, нарушения, описанного в данном документе, например, рака.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 7-циклопентил-N, N-диметил-2-((5-((1R,6S)-9-метил-4-оксо-3,9-диазабицикло[4.2.1]нонан-3-ил)пиридин-2-ил)амино)-7Н-пирроло[2,3-d]пиримидин-6-карбоксамид (соединение A30) или соединение, раскрытое в РСТ-публикации № WO 2011/101409, которые являются ингибиторами CDK4/6, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор CDK4/6 представляет собой 7-циклопентил-N, N-диметил-2-((5-((1R,6S)-9-метил-4-оксо-3,9-диазабицикло[4.2.1]нонан-3-ил)пиридин-2-ил)амино)-7H-пирроло[2,3-d]пиримидин-6-карбоксамид (соединение A30) или соединение, раскрытое в РСТ-публикации № WO 2011/101409.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя соединение A31 или соединение, раскрытое в РСТ-публикации № WO 2012/022814, которые являются ингибиторами HER3, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор HER3 представляет собой соединение A31 или соединение, раскрытое в РСТ-публикации WO 2012/022814.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя соединение A32 или соединение, раскрытое в РСТ-публикации № WO 2014/160160, которые являются ингибиторами FGFR2 и/или FGFR4 (например, конъюгат молекулы антитела к FGFR2 и/или FGFR4 и лекарственного средства, например, mAb 12425), или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В некоторых вариантах осуществления соединение A32 представляет собой конъюгат молекулы антитела к FGFR2 и/или FGFR4 и лекарственного средства, например, mAb 12425.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя соединение A33 или соединение, раскрытое в РСТ-публикации № WO 2004/045532, которые являются ингибиторами M-CSF (например, молекулу или Fab-фрагмент антитела к M-CSF), или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя ингибитор MEK или применяется в комбинации с ним для лечения нарушения, например, рака, описанного в данном документе.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя мидостаурин (соединение А35) или соединение, раскрытое в РСТ-публикации № WO 2003/037347, которые являются ингибиторами одного или нескольких из c-KIT, высвобождения гистамина, Flt3 (например, FLK2/STK1) или PKC, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор представляет собой мидостаурин (соединение A35) или соединение, раскрытое в РСТ-публикации № WO 2003/037347.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 1-метил-5-((2-(5-(трифторметил)-1H-имидазол-2-ил)пиридин-4-ил)окси)-N-(4-(трифторметил)фенил)-1H-бензо[d]имидазол-2-амин (соединение A37) или соединение, раскрытое в РСТ-публикации № WO 2007/030377, которые являются ингибиторами одного или нескольких из VEGFR-2, PDGFR-бета, KIT или Raf-киназы C, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор одного или нескольких из VEGFR-2, PDGFR-бета, KIT или Raf-киназы C представляет собой 1-метил-5-((2-(5-(трифторметил)-1H-имидазол-2-ил)пиридин-4-ил)окси)-N-(4-(трифторметил)фенил)-1H-бензо[d]имидазол-2-амин (соединение A37) или соединение, раскрытое в РСТ-публикации № WO 2007/030377.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя диаспартат пасиреотида (также известный как SIGNIFOR; соединение A38), или соединение, раскрытое в РСТ-публикации № WO 2002/010192 или патенте США № 7473761, которые являются агонистами соматостатина и/или ингибиторами высвобождения гормона роста, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления агонист соматостатина и/или ингибитор высвобождения гормона роста представляет собой диаспартат пасиреотида (соединение A38) или соединение, раскрытое в РСТ-публикации № WO 2002/010192 или патенте США № 7473761.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя модулятор передачи сигнала и/или ингибитор ангиогенеза или применяется в комбинации с ними, например, для лечения нарушения, такого как рак, описанный в данном документе.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1Н-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в PCT-публикации № WO 2013/184757, которые являются ингибиторами EGFR, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор EGFR представляет собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757. В одном варианте осуществления молекула антитела к ENTPD2 человека применяется в комбинации с (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамидом (соединением A40) или соединением, раскрытым в РСТ-публикации № WO 2013/184757, для лечения нарушения, такого как рак.
В некоторых вариантах осуществления (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в PCT-публикации № WO 2013/184757, которые являются ингибиторами EGFR, вводят в комбинации с ингибитором ENTPD2 (например, молекулой антитела к ENTPD2 человека) для лечения рака.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя N6-(2-изопропокси-5-метил-4-(1-метилпиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)-1H-пиразоло[3,4-d]пиримидин-4,6-диамин (соединение A42) или соединение, раскрытое в РСТ-публикации № WO 2008/073687, которые являются ингибиторами ALK, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор ALK представляет собой N6-(2-изопропокси-5-метил-4-(1-метилпиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)-1H-пиразоло[3,4-d]пиримидин-4,6-диамин (соединение A42) или соединение, раскрытое в РСТ-публикации № WO 2008/073687.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя 3-(4-(4-((5-хлор-4-((5-метил-1H-пиразол-3-ил)амино)пиримидин-2-ил)амино)-5-фтор-2-метилфенил)пиперидин-1-ил)тиетан-1,1-диоксид (соединение A43), 5-хлор-N2-(2-фтор-5-метил-4-(1-(тетрагидро-2H-пиран-4-ил)пиперидин-4-ил)фенил)-N4-(5-метил-1H-пиразол-3-ил)пиримидин-2,4-диамин (соединение A44), или 5-хлор-N2-(4-(1-этилпиперидин-4-ил)-2-фтор-5-метилфенил)-N4-(5-метил-1H-пиразол-3-ил)пиримидин-2,4-диамин (соединение A45), или соединение, раскрытое в РСТ-публикации № WO 2010/002655, которые являются ингибиторами IGF-1R, или применяется в комбинации с ними для лечения нарушения, например, описанного нарушения. В одном варианте осуществления ингибитор IGF-1R представляет собой 3-(4-(4-((5-хлор-4-((5-метил-1H-пиразол-3-ил)амино)пиримидин-2-ил)амино)-5-фтор-2-метилфенил)пиперидин-1-ил)тиетан-1,1-диоксид (соединение A43), 5-хлор-N2-(2-фтор-5-метил-4-(1-(тетрагидро-2H-пиран-4-ил)пиперидин-4-ил)фенил)-N4-(5-метил-1H-пиразол-3-ил)пиримидин-2,4-диамин (соединение A44), 5-хлор-N2-(4-(1-этилпиперидин-4-ил)-2-фтор-5-метилфенил)-N4-(5-метил-1H-пиразол-3-ил)пиримидин-2,4-диамин (соединение A45) или соединение, раскрытое в РСТ-публикации № WO 2010/002655.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя валсподар (также известный как AMDRAY; соединение A46) или соединение, раскрытое в EP 296122, которые являются ингибиторами P-гликопротеина 1, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор P-гликопротеина 1 представляет собой валсподар (соединение A46) или соединение, раскрытое в EP 296122.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя одно или несколько из сукцината ваталаниба (соединения A47) или соединения, раскрытого в EP 296122, которые являются ингибиторами VEGFR, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор VEGFR представляет собой сукцинат ваталаниба (соединение A47) или соединение, раскрытое в EP 296122.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя ингибитор IDH или соединение, раскрытое в WO 2014/141104, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор IDH представляет собой соединение, раскрытое в РСТ-публикации № WO 2014/141104.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя ингибитор BCL-ABL или соединение, раскрытое в РСТ-публикациях №№ WO 2013/171639, WO 2013/171640, WO 2013/171641 или WO 2013/171642, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор BCL-ABL представляет собой соединение, раскрытое в РСТ-публикациях №№ WO 2013/171639, WO 2013/171640, WO 2013/171641 или WO 2013/171642.
В другом варианте осуществления комбинация, например, комбинация, содержащая молекулу антитела к ENTPD2 человека, описанную в данном документе, включает в себя ингибитор c-RAF или соединение, раскрытое в РСТ-публикации № WO 2014/151616, или применяется в комбинации с ними для лечения нарушения, например, нарушения, описанного в данном документе. В одном варианте осуществления ингибитор c-RAF представляет собой соединение A50 или соединение, раскрытое в РСТ-публикации № WO 2014/151616. В некоторых вариантах осуществления ингибитор c-RAF или соединение A50 представляет собой соединение формулы (I):
b. 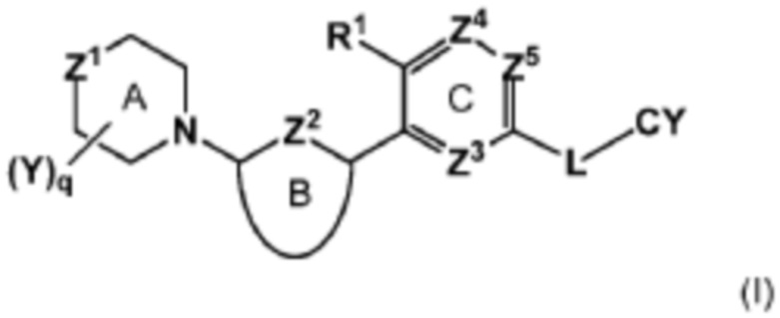
c. или его фармацевтически приемлемую соль, где:
d. Z1 представляет собой O, S, S(=O) или SO2;
e. Z2 представляет собой N, S или CRa, где Ra представляет собой H, галоген, C1-4-алкил или C1-4-галогеналкил;
f. R1 представляет собой CN, галоген, OH, C1-4-алкокси или C1-4-алкил, который необязательно замещен группами в количестве от одной до трех, выбранными из галогена, C1-4-алкокси, CN и гидроксила;
g. кольцо B выбрано из фенила, пиридина, пиримидина, пиразина, пиридазина, пиридона, пиримидона, пиразинона, пиридазинона и тиазола, каждый из которых необязательно замещен группами в количестве до двух, выбранными из галогена, OH, CN, C1-4-алкила, C2-4-алкенила, -O-(C1-4-алкила), NH2, NH-(C1-4-алкила), -N(C1-4-алкил)2, -SO2R2, NHSO2R2, NHC(O)R2, NHCO2R2, C3-6-циклоалкила, 5-6-членного гетероарила, -O-C3-6-циклоалкила, -O-(5-6-членный гетероарил), C4-8-гетероциклоалкила и -O-(4-8-членный гетероциклоалкил), где каждый гетероциклоалкил и гетероарил содержит гетероатомы в количестве до трех, выбранные из N, O и S, в качестве членов кольца,
i. где каждый C1-4-алкил, C2-4-алкенил, C3-6-циклоалкил, 5-6-членный гетероарил и 4-8-членный гетероциклоалкил необязательно замещен группами в количестве до трех, выбранными из оксо, гидроксила, галогена, C1-4-алкила, C1-4-галогеналкила, C1-4-алкокси и -(CH2)1-2Q, где Q представляет собой OH, C1-4-алкокси, -CN, NH2, -NHR3, -N(R3)2, -SO2R3, NHSO2R3, NHC(O)OR3 или NHC(O)R3; при этом каждый R2 и R3 независимо представляет собой C1-4-алкил; и
ii. кольцо B необязательно конденсировано с 5-6-членным ароматическим или неароматическим кольцом, содержащим гетероатомы в количестве до двух, выбранные из N, O и S, при этом 5-6-членное кольцо может быть замещено галогеном, C1-4-алкилом, C1-4-галогеналкилом или C1-4-алкокси, и в случае, если конденсированное кольцо не является ароматическим, варианты заместителя могут дополнительно включать оксо;
h. каждый Y независимо выбран из C1-4-алкила, C1-4-алкокси, CN, галогена, оксо, -(CH2)POR4, -(CH2)pN(R4)2, -(CH2)pNHC(O)R4, -(CH2)pNHCOO(C1-4-алкила) и имидазола,
i. или две группы Y в кольце A необязательно взяты вместе с образованием кольца, конденсированного или соединенного мостиком с кольцом А, где указанное конденсированное или соединенное мостиком кольцо необязательно содержит гетероатом, выбранный из N, O и S, в качестве члена кольца, и необязательно замещено группами в количестве до двух, выбранными из C1-4-алкила, C1-4-алкокси, CN, галогена, оксо, -(CH2)pOR4, -(CH2)PN(R4)2, -(CH2)pNHC(O)R4 и -(CH2)pNHCOO(C1-4-алкил);
j. каждый R4 независимо представляет собой H или C1-4-алкил;
k. каждое p независимо равняется 0, 1 или 2;
l. q равняется 0, 1 или 2;
m. Z3, Z4 и Z5 независимо выбраны из CH и N и необязательно NO;
n. L представляет собой -C(=O)-NR4-[CY] или -NR4-C(=O)-[CY], где [CY] указывает на то, какой атом L присоединен к CY; и
o. CY представляет собой ароматическое кольцо, выбранное из фенила, пиридина, пиримидина, пиразина, пиридазина, пиридона, тиазола, изотиазола, оксазола, пиразола и изоксазола, при этом кольцо необязательно конденсировано с тиофеновым, имидазольным, оксазолоновым или пиррольным кольцом;
p. и CY замещен группами в количестве до двух, выбранными из галогена, CN, R5, OR5, SO2R5, -S(=NH)(=O)R5, OH, NH2, NHR5 и -N(R5)2,
i. где каждый R5 независимо представляет собой C1-4-алкил, C2-4-алкенил, C2-6-гетероциклил, 5-членный гетероарил, содержащий гетероатомы в количестве до трех, выбранные из N, O и S, в качестве членов кольца, или C3-8-циклоалкил, и R5 необязательно замещен группами в количестве до четырех, выбранными из оксо, галогена, CN, R6, OH, OR6, SO2R6, NH2, NHR6, N(R6)2, NHSO2R6, NHCOOR6, NHC(=O)R6, -CH2OR7, -CH2N(R7)2, где каждый
q. R6 независимо представляет собой C1-4-алкил, и каждый R7 независимо представляет собой H или C1-4-алкил;
r. и два R4, R5, R6 или R7 при одном и том же атоме азота могут быть взяты вместе с образованием 5-6-членного гетероциклического кольца, необязательно содержащего дополнительный N, O или S в качестве члена кольца и необязательно замещенного группами в количестве до двух, выбранными из C1-4-алкила, оксо, галогена, ОН и C1-4-алкокси.
Иллюстративные средства клеточной терапии
Молекулы антител к ENTPD2 человека также можно применять в комбинации со средством клеточной терапии, например, средством терапии с использованием химерных антигенных рецепторов (CAR), средством терапии на основе T-клеток, средством терапии на основе естественных клеток-киллеров (NK) или средством терапии на основе дендритных клеток.
Комбинации со средствами CAR-терапии
Молекулы антител к ENTPD2 человека, описанные в данном документе, можно вводить в комбинации со вторым терапевтическим средством, например, клеткой, содержащей химерный антигенный рецептор (CAR). CAR может содержать i) внеклеточный антигенсвязывающий домен, ii) трансмембранный домен и iii) внутриклеточный сигнальный домен (который может содержать один или оба из первичного сигнального домена и костимулирующего домена). CAR может дополнительно содержать лидерную последовательность и/или последовательность шарнирной области. В конкретных вариантах осуществления CAR-конструкция содержит scFv-домен, где перед scFv может располагаться необязательная лидерная последовательность, а за ним могут располагаться необязательная последовательность шарнирной области, трансмембранная область и внутриклеточный сигнальный домен, например, где домены являются смежными и находятся в одной и той же рамке считывания с образованием единого слитого белка.
В некоторых вариантах осуществления молекула CAR предусматривает молекулу CAR для CD19, описанную в данном документе, например, молекулу CAR для CD19, описанную в US 2015/0283178, например, CTL019. В вариантах осуществления CAR для CD19 содержит аминокислотную или имеет нуклеотидную последовательность, показанную в US 2015/0283178, включенном в данный документ посредством ссылки во все своей полноте, или последовательность, по существу идентичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90% или 95% идентичностью последовательности по отношению к ней).
В одном варианте осуществления CAR-Т-клетка, которая связывается с CD19, имеет обозначение согласно USAN тисагенлеклейсел-T. CTL019 получают посредством генной модификации T-клеток, опосредованной стабильной вставкой путем трансдукции с помощью самоинактивирующегося лентивирусного (LV) вектора, дефектного по репликации, содержащего трансген CTL019 под контролем промотора гена EF-1-альфа. CTL019 может представлять собой смесь положительных и отрицательных по трансгену Т-клеток, которые доставляются субъекту из расчета процентного количества положительных по трансгену Т-клеток.
В одном варианте осуществления CAR для CD19 содержит аминокислотную последовательность, представленную под SEQ ID NO: 12 в PCT-публикации WO 2012/079000. В варианте осуществления аминокислотная последовательность представляет собой
MALPVTALLLPLALLLHAARPdiqmtqttsslsaslgdrvtiscrasqdiskylnwyqqkpdgtvklliyhtsrlhsgvpsrfsgsgsgtdysltisnleqediatyfcqqgntlpytfgggtkleitggggsggggsggggsevklqesgpglvapsqslsvtctvsgvslpdygvswirqpprkglewlgviwgsettyynsalksrltiikdnsksqvflkmnslqtddtaiyycakhyyyggsyamdywgqgtsvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO: 312),
или последовательность, по существу идентичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90% или 95% идентичностью последовательности по отношению к ней), с последовательностью сигнального пептида, которая указана заглавными буквами, или без нее.
В одном варианте осуществления аминокислотная последовательность представляет собой
diqmtqttsslsaslgdrvtiscrasqdiskylnwyqqkpdgtvklliyhtsrlhsgvpsrfsgsgsgtdysltisnleqediatyfcqqgntlpytfgggtkleitggggsggggsggggsevklqesgpglvapsqslsvtctvsgvslpdygvswirqpprkglewlgviwgsettyynsalksrltiikdnsksqvflkmnslqtddtaiyycakhyyyggsyamdywgqgtsvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO: 313),
или последовательность, по существу гомологичную ей (например, последовательность, которая характеризуется по меньшей мере приблизительно 85%, 90% или 95% идентичностью последовательности по отношению к ней).
Антигенсвязывающий домен химерного антигенного рецептора (CAR)
Антигенсвязывающий домен может представлять собой любой домен, который связывается с антигеном, в том числе без ограничения моноклональное антитело, поликлональное антитело, рекомбинантное антитело, человеческое антитело, гуманизированное антитело и их функциональный фрагмент, в том числе без ограничения однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен (VHH) нанотела верблюдовых, а также альтернативный остов, который, как известно из уровня техники, функционирует в качестве антигенсвязывающего домена, такой как рекомбинантный домен фибронектина, T-клеточный рецептор (TCR) или его фрагмент, например, одноцепочечный TCR, и т. п. В некоторых случаях целесообразно, чтобы антигенсвязывающий домен был получен от того же вида, у которого в конечном итоге будут применять CAR. Например, для применения у человека может быть целесообразно, чтобы антигенсвязывающий домен CAR содержал в антигенсвязывающем домене антитела или фрагмента антитела человеческие или гуманизированные остатки.
В некоторых вариантах осуществления антигенсвязывающий домен CAR представляет собой scFv-фрагмент антитела, который является гуманизированным по сравнению с мышиной последовательностью scFv, из которого он получен.
В некоторых вариантах осуществления антигенсвязывающий домен связывается с опухолевым антигеном, описанным в данном документе. В вариантах осуществления опухолевый антиген выбран из CD19; CD123; CD22; CD30; CD171; CS-1 (также называемого белком 1 подгруппы CD2, CRACC, SLAMF7, CD319 и 19A24); молекулы 1, подобной лектинам С-типа (CLL-1 или CLECL1); CD33; варианта III рецептора эпидермального фактора роста (EGFRvIII); ганглиозида G2 (GD2); ганглиозида GD3 (aNeu5Ac(2-8)aNeu5Ac(2-3)bDGalp(1-4)bDGlcp(1-1)Cer); антигена созревания В-клеток (BCMA), являющегося представителем семейства рецепторов TNF; Tn-антигена ((Ag Tn) или (GalNAcα-Ser/Thr)); простатического специфического мембранного антигена (PSMA); орфанного рецептора 1, подобного рецепторной тирозинкиназе (ROR1); Fms-подобной тирозинкиназы 3 (FLT3); опухолеассоциированного гликопротеина 72 (TAG72); CD38; CD44v6; раково-эмбрионального антигена (СЕА); молекулы адгезии эпителиальных клеток (ЕРСАМ); В7Н3 (CD276); KIT (CD117); альфа-2-субъединицы рецептора интерлейкина-13 (IL-13Ra2 или CD213A2); мезотелина; альфа-субъединицы рецептора интерлейкина 11 (IL-11Ra); антигена стволовых клеток предстательной железы (PSCA); сериновой протеазы 21 (тестизина или PRSS21); рецептора 2 фактора роста эндотелия сосудов (VEGFR2); антигена системы Льюис (Y); CD24; рецептора фактора роста тромбоцитов бета-типа (PDGFR-бета); стадиеспецифического эмбрионального антигена 4 (SSEA-4); CD20; рецептора фолиевой кислоты альфа; рецепторной тирозинпротеинкиназы ERBB2 (Her2/neu); муцина 1, ассоциированного с клеточной поверхностью (MUC1); рецептора эпидермального фактора роста (EGFR); молекулы адгезии нервных клеток (NCAM); простазы; простатической кислой фосфатазы (РАР); мутантного фактора элонгации 2 (ELF2M); эфрина В2; белка активации фибробластов альфа (FAP); рецептора инсулиноподобного фактора роста 1 (рецептора IGF-I), карбоангидразы IX (CAIX); субъединицы бета-типа 9 протеасомы (просомы, мультикаталитической протеазы) (LMP2); гликопротеина 100 (gp100); онкогенного слитого белка, состоящего из кластерного региона точечных разрывов (BCR) и гомолога 1 онкогена вируса лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназы; рецептора 2 эфрина А-типа (EphA2); фукозил-GM1; молекулы адгезии, представляющей собой сиалилированный антиген системы Льюис (sLe); ганглиозида GM3 (aNeu5Ac(2-3)bDGalp(1-4)bDGlcp(1-1)Cer); трансглутаминазы 5 (TGS5); высокомолекулярного антигена, ассоциированного с меланомой (HMWMAA); ганглиозида о-ацетил-GD2 (OAcGD2); рецептора фолиевой кислоты бета; опухолевого эндотелиального маркера 1 (TEM1/CD248); белка, родственного опухолевому эндотелиальному маркеру 7 (TEM7R); клаудина 6 (CLDN6); рецептора тиреотропного гормона (TSHR); представителя D группы 5 класса С рецепторов, сопряженных с G-белками (GPRC5D); белка, кодируемого открытой рамкой считывания 61 X-хромосомы (CXORF61); CD97; CD179a; киназы анапластической лимфомы (ALK); полисиаловой кислоты; плацентоспецифического белка 1 (PLAC1); гексасахаридной части гликоцерамида globoH (GloboH); дифференцировочного антигена молочной железы (NY-BR-1); уроплакина 2 (UPK2); клеточного рецептора 1 вируса гепатита A (HAVCR1); бета-3-адренорецептора (ADRB3); паннексина 3 (PANX3); рецептора 20, сопряженного с G-белком (GPR20); антигена локуса K9 комплекса лимфоцитарных антигенов 6 (LY6K); обонятельного рецептора 51Е2 (OR51E2); белка, кодируемого альтернативной рамкой считывания гена TCR-гамма (TARP); белка опухоли Вильмса (WT1); раково-тестикулярного антигена 1 (NY-ESO-1); раково-тестикулярного антигена 2 (LAGE-1a); антигена 1, ассоциированного с меланомой (MAGE-A1); белка, кодируемого транслокационным вариантом 6 гена ETS, локализованным в р-плече 12 хромосомы (ETV6-AML); белка сперматозоидов 17 (SPA17); представителя 1А семейства X-антигенов (XAGE1); ангиопоэтин-связывающего рецептора клеточной поверхности 2 (TIE-2); раково-тестикулярного антигена меланомы 1 (MAD-CT-1); раково-тестикулярного антигена меланомы 2 (MAD-CT-2); Fos-родственного антигена 1; опухолевого белка р53 (р53); мутантного р53; простеина; сурвивина; теломеразы; опухолевого антигена 1 карциномы предстательной железы (РСТА-1 или галектина 8), антигена меланомы 1, распознаваемого Т-клетками (MelanA или MART1); мутантного антигена саркомы крыс (Ras); теломеразной обратной транскриптазы человека (hTERT); антигена саркомы с точечными разрывами при транслокации; меланомного ингибитора апоптоза (ML-IAP); ERG (продукта слитого гена трансмембранной сериновой протеазы 2 (TMPRSS2) и ETS); N-ацетилглюкозаминилтрансферазы V (NA17); белка с парным box-доменом Рах-3 (РАХ3); андрогенового рецептора; циклина В1; нейробластомного гомолога онкогена вируса миелоцитоматоза птиц v-myc (MYCN); представителя С семейства гомологов Ras (RhoC); белка 2, родственного тирозиназе (TRP-2); цитохрома Р450 1В1 (CYP1B1); белка, подобного CCCTC-связывающему фактору (белку с "цинковыми пальцами") (BORIS или "брата регулятора импринтированных сайтов"), антигена плоскоклеточной карциномы 3, распознаваемого Т-клетками (SART3); белка с парным box-доменом Рах-5 (РАХ5); проакрозин-связывающего белка sp32 (OY-TES1); лимфоцитоспецифической протеинтирозинкиназы (LCK); якорного белка 4 киназы A (AKAP-4); антигена 2 синовиальной саркомы с точечным разрывом в X-хромосоме (SSX2); рецептора конечных продуктов гликирования (RAGE-1); почечного убиквитарного белка 1 (RU1); почечного убиквитарного белка 2 (RU2); легумаина; Е6 вируса папилломы человека (Е6 HPV); Е7 вируса папилломы человека (Е7 HPV); кишечной карбоксилэстеразы; мутантного белка теплового шока 70-2 (mut-hsp70-2); CD79a; CD79b; CD72; иммуноглобулиноподобного рецептора 1, ассоциированного с лейкоцитами (LAIR1); рецептора Fc-фрагмента IgA (FCAR или CD89); представителя 2 подсемейства А лейкоцитарных иммуноглобулиноподобных рецепторов (LILRA2); представителя f семейства белков, подобных молекулам CD300 (CD300LF); представителя А семейства 12 лектиновых доменов С-типа (CLEC12A); антигена 2 стромальных клеток костного мозга (BST2); белка 2, подобного муциноподобному рецептору гормона, содержащему EGF-подобный модуль (EMR2); лимфоцитарного антигена 75 (LY75); глипикана-3 (GPC3); антигена 5, подобного Fc-рецептору (FCRL5); и полипептида 1, подобного иммуноглобулину лямбда (IGLL1).
В одном варианте осуществления молекула CAR предусматривает молекулу CAR для BCMA, например, CAR для BCMA, описанную в US 2016/0046724 или WO 2016/014565, включенных в данный документ посредством ссылки. В вариантах осуществления CAR для BCMA содержит аминокислотную или имеет нуклеотидную последовательность молекулы CAR или антигенсвязывающего домена в соответствии с US 2016/0046724 или таблицей 1 или 16, SEQ ID NO: 271 или SEQ ID NO: 273 из WO 2016/014565, включенной в данный документ посредством ссылки, или последовательность, по существу идентичную любой из вышеупомянутых последовательностей (например, которая характеризуется по меньшей мере приблизительно 85%, 90% или 95% идентичностью последовательности по отношению к любой из вышеупомянутых последовательностей CAR для BCMA). Аминокислотные последовательности молекул CAR для BCMA и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia) и нуклеотидные последовательности, кодирующие их, указаны в WO 2016/014565.
Трансмембранный домен химерного антигенного рецептора (CAR)
Что касается трансмембранного домена, в различных вариантах осуществления CAR можно разработать так, чтобы он содержал трансмембранный домен, присоединенный к внеклеточному домену CAR.
Трансмембранный домен может быть получен из природного либо из рекомбинантного источника. Если источник является природным, то домен может быть получен из любого мембраносвязанного или трансмембранного белка. В одном аспекте трансмембранный домен способен передавать сигнал внутриклеточному(внутриклеточным) домену(доменам) всякий раз, когда CAR связался с мишенью. Трансмембранный домен может содержать по меньшей мере трансмембранную(трансмембранные) область(области), например, альфа-, бета- или дзета-цепи T-клеточного рецептора, CD28, CD27, CD3-эпсилон, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, CD154. В некоторых вариантах осуществления трансмембранный домен может содержать по меньшей мере трансмембранную(трансмембранные) область(области), например, KIRDS2, OX40, CD2, CD27, LFA-1 (CD11a, CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD40, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, IL2R-бета, IL2R-гамма, IL7R-α, ITGA1, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, TNFR2, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, PAG/Cbp, NKG2D, или NKG2C.
В некоторых случаях трансмембранный домен может быть присоединен к внеклеточной области CAR, например, антигенсвязывающему домену CAR, посредством шарнирной области, например, шарнирной области из человеческого белка. Например, в одном варианте осуществления шарнирная область может представлять собой шарнирную область человеческого Ig (иммуноглобулина) (например, шарнирную область IgG4, шарнирную область IgD), линкер GS (например, линкер GS, описанный в данном документе), шарнирную область KIR2DS2 или шарнирную область CD8a.
Внутриклеточный сигнальный домен химерного антигенного рецептора (CAR)
Цитоплазматические домен или область CAR содержат внутриклеточный сигнальный домен. Внутриклеточный сигнальный домен обычно отвечает за активацию по меньшей мере одной из нормальных эффекторных функций иммунной клетки, в которую был введен CAR.
Примеры внутриклеточных сигнальных доменов для применения в CAR включают цитоплазматические последовательности Т-клеточного рецептора (TCR) и корецепторов, которые действуют совместно, инициируя передачу сигнала после вступления в контакт с антигенным рецептором, а также любое производное или вариант этих последовательностей и любую рекомбинантную последовательность, которая обладает такими же функциональными возможностями.
Первичный сигнальный домен регулирует первичную активацию комплекса TCR стимулирующим образом либо ингибирующим образом. Первичные внутриклеточные сигнальные домены, которые действуют стимулирующим образом, могут содержать сигнальные мотивы, известные как иммунорецепторные тирозиновые активирующие мотивы или ITAM.
Примеры первичных внутриклеточных сигнальных доменов, содержащих ITAM, включают домены CD3-дзета, общей гамма-цепи FcR (FCER1G), Fc-гамма RIIa, FcR-бета (Fc-эпсилон R1b), CD3-гамма, CD3-дельта, CD3-эпсилон, CD79a, CD79b, DAP10 и DAP12. В одном варианте осуществления CAR содержит внутриклеточный сигнальный домен, например, первичный сигнальный домен CD3-дзета.
Внутриклеточный сигнальный домен CAR может содержать сигнальный домен CD3-дзета в отдельности или в комбинации с любым(любыми) другим(другими) необходимым(необходимыми) внутриклеточным(внутриклеточными) сигнальным(сигнальными) доменом(доменами), применимым(применимыми) в качестве составной части CAR по настоящему изобретению. Например, внутриклеточный сигнальный домен CAR может содержать часть дзета-цепи CD3 и костимулирующий сигнальный домен. Костимулирующий сигнальный домен относится к части CAR, содержащей внутриклеточный домен костимулирующей молекулы. Костимулирующая молекула представляет собой молекулу клеточной поверхности, отличную от антигенного рецептора или его лигандов, которая требуется для эффективного ответа лимфоцитов на антиген. Примеры таких молекул включают CD27, CD28, 4-1BB (CD137), OX40, CD30, CD40, PD-1, ICOS, лимфоцитарный функционально-ассоциированный антиген 1 (LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3 и лиганд, который связывается с CD83, и т. п. Например, было продемонстрировано, что костимуляция с помощью CD27 усиливает размножение, эффекторную функцию и выживание человеческих CART-клеток in vitro и увеличивает персистенцию и противоопухолевую активность человеческих T-клеток in vivo (Song et al. Blood. 2012; 119(3):696-706). Дополнительные примеры таких костимулирующих молекул включают CDS, ICAM-1, GITR, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, CD4, CD8-альфа, CD8-бета, IL2R-бета, IL2R-гамма, IL7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), NKG2D, CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, и CD19a.
Активация и размножение иммунных эффекторных клеток (например, T-клеток)
Иммунные эффекторные клетки, такие как Т-клетки, можно активировать и размножать, как правило, с применением способов, описанных, например, в патентах США 6352694; 6534055; 6905680; 6692964; 5858358; 6887466; 6905681; 7144575; 7067318; 7172869; 7232566; 7175843; 5883223; 6905874; 6797514; 6867041 и публикации заявки на патент США № 2006/0121005, включенных в данный документ посредством ссылки.
Примеры иммунных эффекторных клеток включают Т-клетки, например, альфа/бета-Т-клетки и гамма/дельта-Т-клетки, В-клетки, естественные клетки-киллеры (NK), естественные T-клетки-киллеры (NKT), тучные клетки и фагоциты миелоидного происхождения.
Способы получения клеток, экспрессирующих CAR, описаны, например, в US 2016/0185861, включенном в данный документ посредством ссылки.
Иллюстративные противораковые вакцины
Молекулы антител к ENTPD2 человека можно применять в комбинации с иммуногенным средством, таким как раковые клетки, очищенные опухолевые антигены (в том числе рекомбинантные белки, пептиды и молекулы углеводов), клетки и клетки, трансфицированные генами, кодирующими иммуностимулирующие цитокины (He et al. (2004) J. Immunol. 173:4919-28). Неограничивающие примеры противоопухолевых вакцин, которые можно применять, включают пептиды антигенов меланомы, такие как пептиды gp100, антигены MAGE, Trp-2, MART1 и/или тирозиназу, опухолевые клетки, трансфицированные для экспрессии цитокина GM-CSF, вакцины на основе ДНК, вакцины на основе РНК и вакцины на основе трансдуцирующих вирусов. Противораковая вакцина может быть профилактической или терапевтической.
Блокаду ENTPD2 можно применять в сочетании с совокупностью рекомбинантных белков и/или пептидов, экспрессирующихся в опухоли, для выработки иммунного ответа на эти белки.
Другие противоопухолевые вакцины могут содержать белки из вирусов, участвующих в развитии форм рака человека, таких как вирусы папилломы человека (HPV), вирусы гепатита (HBV и HCV), вирус герпеса, ассоциированный с саркомой Капоши (KHSV), и вирус Эпштейна-Барр (EBV). Другой формой опухолеспецифичного антигена, который можно применять в сочетании с блокадой ENTPD2, являются очищенные белки теплового шока (HSP), выделенные из самой опухолевой ткани. Такие белки теплового шока содержат фрагменты белков из опухолевых клеток, и эти HSP являются весьма эффективными при доставке в антигенпрезентирующие клетки для вызывания противоопухолевого иммунитета (Suot, R & Srivastava, P (1995) Science 269:1585-1588; Tamura, Y. et al. (1997) Science 278:117-120).
Дендритные клетки (DC) являются активными антигенпрезентирующими клетками, которые можно применять для инициирования антигенспецифических ответов. DC могут быть получены ex vivo и нагружены различными белковыми и пептидными антигенами, а также экстрактами опухолевых клеток (Nestle, F. et al. (1998) Nature Medicine 4: 328-332). DC также могут быть трансдуцированы генетическим путем, чтобы они также экспрессировали эти опухолевые антигены. Также проводили прямое слияние DC с опухолевыми клетками в целях иммунизации (Kugler, A. et al. (2000) Nature Medicine 6:332-336). В качестве способа вакцинации иммунизацию с помощью DC можно эффективно применять в комбинации с блокадой CD73 для активации более сильных противоопухолевых ответов.
Иллюстративные онколитические вирусы
Молекулы антител к ENTPD2 человека можно вводить в комбинации с онколитическими вирусами. В ряде вариантов осуществления онколитические вирусы способны избирательно реплицироваться в раковой клетке и запускать ее гибель или замедлять ее рост. В некоторых случаях онколитические вирусы не обеспечивают эффект или обеспечивают минимальный эффект в отношении нераковых клеток. В некоторых вариантах осуществления комбинацию применяют для лечения рака, например, рака, описанного в данном документе. Онколитический вирус включает без ограничения онколитический аденовирус, онколитические вирусы простого герпеса, онколитический ретровирус, онколитический парвовирус, онколитический вирус осповакцины, онколитический вирус Синдбис, онколитический вирус гриппа или онколитический РНК-содержащий вирус (например, онколитический реовирус, онколитический вирус ньюкаслской болезни (NDV), онколитический вирус кори или онколитический вирус везикулярного стоматита (VSV)).
Иллюстративные онколитические вирусы включают без ограничения следующие:
онколитический аденовирус группы B (ColoAd1) (PsiOxus Therapeutics Ltd.) (см., например, клиническое испытание с идентификационным номером NCT02053220);
ONCOS-102 (ранее называемый CGTG-102), который представляет собой аденовирус, содержащий гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) (Oncos Therapeutics) (см., например, клиническое испытание с идентификационным номером NCT01598129);
VCN-01, который представляет собой генетически модифицированный онколитический аденовирус человека, кодирующий гиалуронидазу PH20 человека (VCN Biosciences, S.L.) (см., например, клинические испытания с идентификационными номерами NCT02045602 и NCT02045589);
условно-репликативный аденовирус ICOVIR-5, который представляет собой вирус, полученный из аденовируса человека дикого типа серотипа 5 (Had5), который был модифицирован для избирательной репликации в раковых клетках с нарушенной регуляцией сигнального пути белок ретинобластомы/E2F (Каталонский институт онкологии) (см., например, клиническое испытание с идентификационным номером NCT01864759);
Celyvir, который содержит аутологичные мезенхимальные стволовые клетки, полученные из костного мозга (MSC), инфицированные онколитическим аденовирусом ICOVIR5 (Университетская детская больница Ниньо Хесус, Мадрид, Испания/Ramon Alemany) (см., например, клиническое испытание с идентификационным номером NCT01844661);
CG0070, который представляет собой условно-репликативный онколитический аденовирус серотипа 5 (Ad5), в котором промотор E2F-1 человека управляет экспрессией существенно важных генов вируса E1a, за счет чего обеспечивается ограничение вирусной репликации и цитотоксичности опухолевыми клетками, дефектными по сигнальному пути Rb (Cold Genesys, Inc.) (см., например, клиническое испытание с идентификационным номером NCT02143804); или
DNX-2401 (ранее называемый Delta-24-RGD), который представляет собой аденовирус, который был сконструирован для избирательной репликации в клетках, дефектных по сигнальному пути белка ретинобластомы (Rb), и для более эффективного инфицирования клеток, которые экспрессируют определенные интегрины, связывающиеся с RGD (Клиника Наваррского университета, Наваррский университет/DNAtrix, Inc.) (см., например, клиническое испытание с идентификационным номером NCT01956734).
В некоторых вариантах осуществления онколитический вирус, описанный в данном документе, вводят с помощью инъекции, например, подкожной, внутриартериальной, внутривенной, внутримышечной, интратекальной или внутрибрюшинной инъекции. В ряде вариантов осуществления онколитический вирус, описанный в данном документе, вводят внутриопухолевым, чрескожным, чресслизистым, пероральным, интраназальным путем или посредством легочного введения.
Дополнительные иллюстративные виды терапии рака
Иллюстративные комбинации молекул антител к ENTPD2 человека (по отдельности или в комбинации с другими стимулирующими средствами) и стандарта оказания медицинской помощи при раке включают по меньшей мере следующее. В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, например, молекулу антитела к ENTPD2 человека, описанную в данном документе, применяют в комбинации с химиотерапевтическим средством, представляющим собой стандарт оказания медицинской помощи при раке, включающим без ограничения анастрозол (Arimidex®), бикалутамид (Casodex®), сульфат блеомицина (Blenoxane®), бусульфан (Myleran®), бусульфан для инъекций (Busulfex®), капецитабин (Xeloda®), N4-пентоксикарбонил-5-дезокси-5-фторцитидин, карбоплатин (Paraplatin®), кармустин (BiCNU®), хлорамбуцил (Leukeran®), цисплатин (Platinol®), кладрибин (Leustatin®), циклофосфамид (Cytoxan® или Neosar®), цитарабин, арабинозид цитозина (Cytosar-U®), липосомальный цитарабин для инъекций (DepoCyt®), дакарбазин (DTIC-Dome®), дактиномицин (актиномицин D, Cosmegan), гидрохлорид даунорубицина (Cerubidine®), липосомальный цитрат даунорубицина для инъекций (DaunoXome®), дексаметазон, доцетаксел (Taxotere®), гидрохлорид доксорубицина (Adriamycin®, Rubex®), этопозид (Vepesid®), фосфат флударабина (Fludara®), 5-фторурацил (Adrucil®, Efudex®), флутамид (Eulexin®), тезацитибин, гемцитабин (дифтордезоксицитидин), гидроксимочевину (Hydrea®), идарубицин (Idamycin®), ифосфамид (IFEX®), иринотекан (Camptosar®), L-аспарагиназу (ELSPAR®), лейковорин кальция, мелфалан (Alkeran®), 6-меркаптопурин (Purinethol®), метотрексат (Folex®), митоксантрон (Novantrone®), милотарг, паклитаксел (Taxol®), феникс (иттрий-90/MX-DTPA), пентостатин, имплантат с полифепрозаном 20 и кармустином (Gliadel®), цитрат тамоксифена (Nolvadex®), тенипозид (Vumon®), 6-тиогуанин, тиотепу, тирапазамин (Tirazone®), гидрохлорид топотекана для инъекций (Hycamptin®), винбластин (Velban®), винкристин (Oncovin®), винорелбин (Navelbine®), ибрутиниб, иделализиб и конъюгат брентуксимаб-ведотин.
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, например, молекулу антитела к ENTPD2 человека, описанную в данном документе, применяют в комбинации с алкилирующим средством, включающим без ограничения азотистые иприты, производные этиленимина, алкилсульфонаты, нитрозомочевины и триазены; урациловый иприт (Aminouracil Mustard®, Chlorethaminacil®, Demethyldopan®, Desmethyldopan®, Haemanthamine®, Nordopan®, Uracil nitrogen mustard®, Uracillost®, Uracilmostaza®, Uramustin®, Uramustine®), хлорметин (Mustargen®), циклофосфамид (Cytoxan®, Neosar®, Clafen®, Endoxan®, Procytox®, RevimmuneTM), ифосфамид (Mitoxana®), мелфалан (Alkeran®), хлорамбуцил (Leukeran®), пипоброман (Amedel®, Vercyte®), триэтиленмеламин (Hemel®, Hexalen®, Hexastat®), триэтилентиофосфорамин, темозоломид (Temodar®), тиотепу (Thioplex®), бусульфан (Busilvex®, Myleran®), кармустин (BiCNU®), ломустин (CeeNU®), стрептозоцин (Zanosar®) и дакарбазин (DTIC-Dome®). Дополнительные иллюстративные алкилирующие средства включают без ограничения оксалиплатин (Eloxatin®); темозоломид (Temodar® и Temodal®); дактиномицин (также известный как актиномицин-D, Cosmegen®); мелфалан (также известный как L-PAM, L-сарколизин и фенилаланиновый иприт, Alkeran®); алтретамин (также известный как гексаметилмеламин (HMM), Hexalen®); кармустин (BiCNU®); бендамустин (Treanda®); бусульфан (Busulfex® и Myleran®); карбоплатин (Paraplatin®); ломустин (также известный как CCNU, CeeNU®); цисплатин (также известный как CDDP, Platinol® и Platinol®-AQ); хлорамбуцил (Leukeran®); циклофосфамид (Cytoxan® и Neosar®); дакарбазин (также известный как DTIC, DIC и имидазолкарбоксамид, DTIC-Dome®); алтретамин (также известный как гексаметилмеламин (HMM), Hexalen®); ифосфамид (Ifex®); преднумустин; прокарбазин (Matulane®); мехлорэтамин (также известный как азотистый иприт, мустин и гидрохлорид мехлорэтамина, Mustargen®); стрептозоцин (Zanosar®); тиотепу (также известную как тиофосфамид, TESPA и TSPA, Thioplex®); циклофосфамид (Endoxan®, Cytoxan®, Neosar®, Procytox®, Revimmune®) и бендамустин-HCl (Treanda®).
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека, например, молекулу антитела к ENTPD2 человека, описанную в данном документе, применяют в комбинации с антрациклинами, включающими без ограничения, например, доксорубицин (Adriamycin® и Rubex®); блеомицин (Lenoxane®); даунорубицин (гидрохлорид даунорубицина, дауномицин и гидрохлорид рубидомицина, Cerubidine®); липосомальный даунорубицин (липосомальный цитрат даунорубицина, DaunoXome®); митоксантрон (DHAD, Novantrone®); эпирубицин (Ellence™); идарубицин (Idamycin®, Idamycin PFS®); митомицин C (Mutamycin®); гелданамицин; гербимицин; равидомицин и дезацетилравидомицин. Иллюстративные алкалоиды барвинка, которые можно применять в комбинации с молекулами антител к ENTPD2 человека, включают без ограничения тартрат винорелбина (Navelbine®), винкристин (Oncovin®) и виндезин (Eldisine®); винбластин (также известный как сульфат винбластина, винкалейкобластин и VLB, Alkaban-AQ® и Velban®) и винорелбин (Navelbine®).
Иллюстративные ингибиторы протеасом, которые можно применять в комбинации с антителом к ENTPD2 человека, описанным в данном документе, включают без ограничения бортезомиб (Velcade®); карфилзомиб (PX-171-007, (S)-4-метил-N-((S)-1-(((S)-4-метил-1-((R)-2-метилоксиран-2-ил)-1-оксопентан-2-ил)амино)-1-оксо-3-фенилпропан-2-ил)-2-((S)-2-(2-морфолиноацетамидо)-4-фенилбутанамидо)-пентанамид; маризомиб (NPI-0052); цитрат иксазомиба (MLN-9708); деланзомиб (CEP-18770) и O-метил-N-[(2-метил-5-тиазолил)карбонил]-L-серил-O-метил-N-[(1S)-2-[(2R)-2-метил-2-оксиранил]-2-оксо-1-(фенилметил)этил]-L-серинамид (ONX-0912).
В определенных вариантах осуществления молекулу антитела к ENTPD2 человека вводят в комбинации с лучевой терапией. Лучевую терапию можно осуществлять с помощью одного из нескольких способов или комбинации способов, в том числе без ограничения дистанционной лучевой терапии, внутренней лучевой терапии, имплантации источника излучения, стереотаксической радиохирургии, системной лучевой терапии, радиотерапии и постоянной или временной интерстициальной брахитерапии. Термин "брахитерапия" относится к лучевой терапии, осуществляемой с помощью пространственно ограниченного радиоактивного материала, введенного в организм в очаг опухоли или в другой очаг пролиферативного заболевания ткани или рядом с ним. Данный термин предполагает без ограничения включение воздействия радиоактивных изотопов (например, At-211, I-131, I-125, Y-90, Re-186, Re-188, Sm-153, Bi-212, P-32 и радиоактивных изотопов Lu). Подходящие источники излучения для применения в качестве средства для кондиционирования клеток по настоящему изобретению включают как твердые вещества, так и жидкости. В качестве неограничивающего примера, источник излучения может представлять собой радионуклид, такой как I-125, I-131, Yb-169, Ir-192 в качестве твердого источника, I-125 в качестве твердого источника или другие радионуклиды, которые испускают фотоны, бета-частицы, гамма-излучение или другие терапевтические лучи. Радиоактивный материал также может представлять собой жидкость, полученную из любого раствора радионуклида(радионуклидов), например, раствора I-125 или I-131, или радиоактивную жидкость можно получить с использованием взвеси в подходящей жидкости, содержащей мелкие частицы твердых радионуклидов, таких как Au-198, Y-90.
Блокаду ENTPD2 также можно эффективно применять в комбинации с химиотерапевтическими режимами. В этих случаях возможно снизить дозу вводимого химиотерапевтического реагента.
Иллюстративные цитотоксические средства, которые можно вводить в комбинации с молекулой антитела к ENTPD2 человека, включают средства, ингибирующие образование микротрубочек, ингибиторы топоизомераз, антиметаболиты, ингибиторы митоза, алкилирующие средства, антрациклины, алкалоиды барвинка, интеркалирующие средства, средства, способные препятствовать пути передачи сигнала, средства, которые стимулируют апоптоз, ингибиторы протеасом и излучение (например, при местном или общем облучении тела).
Получение образцов
Образцы, используемые в способах, описанных в данном документе, можно получать от субъекта с применением любого из способов, известных из уровня техники, например, с помощью биопсии или хирургического вмешательства. Образец можно подвергнуть мгновенной заморозке и хранить при -80°C для последующего применения. Образец также можно фиксировать с помощью фиксирующего средства, такого как формальдегид, параформальдегид или смесь уксусная кислота/этанол. РНК или белок можно экстрагировать из свежего, замороженного или фиксированного образца для анализа.
Фармацевтические композиции, дозы и способы введения
Также в данном документе предусмотрены композиции, например, фармацевтические композиции, для применения в лечении ENTPD2-ассоциированного заболевания, например, рака, описанного в данном документе. Такие композиции содержат одно или несколько антител или антигенсвязывающих фрагментов, описанных в данном документе, нуклеиновых кислот, кодирующих такие антитела или антигенсвязывающие фрагменты, или векторов, содержащих нуклеиновую кислоту, кодирующую такие антитела или антигенсвязывающие фрагменты. Такие композиции могут дополнительно содержать другое средство, например, современный стандарт оказания медицинской помощи при заболевании, которое подлежит лечению.
Фармацевтические композиции, как правило, содержат фармацевтически приемлемый носитель. Используемая в данном документе формулировка "фармацевтически приемлемый носитель" включает солевой раствор, растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые средства, изотонические средства и средства, замедляющие всасывание, и т. п., совместимые с фармацевтическим введением. Фармацевтические композиции, как правило составляют таким образом, чтобы они были совместимы с предполагаемым путем их введения. Примеры путей введения включают парентеральное (например, внутривенное, внутриартериальное, внутрибрюшинное), внутричерепное, интратекальное или интраназальное (например, ингаляционное), внутрикожное, подкожное или внутриопухолевое введение.
Фраза "фармацевтически приемлемый" используется в данном документе для обозначения тех соединений, материалов, композиций и/или лекарственных форм, которые с медицинской точки зрения подходят для применения в контакте с тканями людей и животных без чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения в соответствии с разумным соотношением польза/риск.
В некоторых вариантах осуществления фармацевтические композиции содержат один или несколько фармацевтически приемлемых носителей, включающих, например, ионообменные материалы, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как человеческий сывороточный альбумин, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протаминсульфат, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натрий-карбоксиметилцеллюлозу, полиакрилаты, воски, блок-сополимеры полиэтилена и полиоксипропилена, полиэтиленгликоль и ланолин.
Способы составления подходящих фармацевтических композиций известны из уровня техники, см., например, Remington: The Science and Practice of Pharmacy. 21st ed., 2005; и книги серии Drugs and the Pharmaceutical Sciences: a Series of Textbooks and Monographs (Dekker, NY). Например, растворы или суспензии, используемые для парентерального или подкожного применения, могут содержать следующие компоненты: стерильный разбавитель, такой как вода для инъекций, солевой раствор, нелетучие масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители; антибактериальные средства, такие как бензиловый спирт или метилпарабены; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатирующие средства, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты, и средства для регулирования тоничности, такие как хлорид натрия или декстроза. Значение pH можно корректировать с помощью кислот или оснований, таких как хлористоводородная кислота или гидроксид натрия. Препарат может быть заключен в ампулы, одноразовые шприцы или многодозовые флаконы, изготовленные из стекла или пластика.
Фармацевтические композиции, подходящие для инъекционного применения, могут включать стерильные водные растворы (в случае растворимости в воде) или дисперсии и стерильные порошки для получения стерильных инъекционных растворов или дисперсии для немедленного приема. Подходящие носители для внутривенного введения включают физиологический раствор, бактериостатическую воду, Cremophor EL™ (BASF, Парсиппани, Нью-Джерси) или фосфатно-солевой буферный раствор (PBS). Во всех случаях композиция должна быть стерильной и должна быть текучей до такой степени, чтобы ее можно было легко вводить через шприц. Она должна быть стабильной в условиях изготовления и хранения и должна быть защищена от загрязняющего действия микроорганизмов, таких как бактерии и грибы. Носитель может представлять собой растворитель или дисперсионную среду, содержащие, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т. п.) и их подходящие смеси. Надлежащую текучесть можно поддерживать, например, посредством применения покрытия, такого как лецитин, посредством поддержания требуемого размера частиц в случае дисперсии и посредством применения поверхностно-активных веществ. Предотвращения действия микроорганизмов можно достичь с помощью различных антибактериальных и противогрибковых средств, например, парабенов, хлорбутанола, фенола, аскорбиновой кислоты, тимеросала и т. п. Во многих случаях предпочтительным будет включение в композицию изотонических средств, например, сахаров, полиспиртов, таких как маннит, сорбит, или хлорида натрия. Длительное всасывание инъекционных композиций можно обеспечить посредством включения в композицию средства, которое замедляет всасывание, например, моностеарата алюминия и желатина.
Стерильные инъекционные растворы можно получать посредством включения активного соединения в требуемом количестве в подходящий растворитель с одним ингредиентом или комбинацией ингредиентов, перечисленных выше, при необходимости с последующей стерилизующей фильтрацией.
Обычно дисперсии получают посредством включения активного соединения в стерильную среду-носитель, которая содержит основную дисперсионную среду и другие требуемые ингредиенты из тех, которые перечислены выше. В случае стерильных порошков для получения стерильных инъекционных растворов предпочтительными способами получения являются вакуумная сушка и сублимационная сушка, которые позволяют получить порошкообразный активный ингредиент с любым дополнительным необходимым ингредиентом из их раствора, предварительно подвергнутого стерилизующей фильтрации.
Составы для парентерального введения могут представлять собой однократную болюсную дозу, инфузионную форму или нагрузочную болюсную дозу с последующей поддерживающей дозой. Такие композиции можно вводить с определенными фиксированными или варьирующимися промежутками, например, один раз в день или "при необходимости".
Подходящие фармацевтические композиции для инъекций могут содержать буфер (например, ацетатный, фосфатный или цитратный буфер), поверхностно-активное вещество (например, полисорбат), необязательно стабилизирующее средство (например, человеческий альбумин) и т. д. Препараты для периферического введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и инъекционные органические сложные эфиры, такие как этилолеат. Водные носители включают, например, воду, спиртовые/водные растворы, эмульсии или суспензии, в том числе солевой раствор и буферные среды. В некоторых вариантах осуществления фармацевтическая композиция содержит 0,01-0,1 M фосфатный буфер или 0,8% солевой раствор. Другие распространенные среды-носители для парентерального введения включают растворы фосфата натрия, раствор Рингера с декстрозой, декстрозу и хлорид натрия, раствор Рингера с лактатом или нелетучие масла. Среды-носители для внутривенного введения включают средства для восполнения жидкости и питательных веществ, средства для восполнения электролитов, такие как средства на основе раствора Рингера с декстрозой, и т. п. Также могут присутствовать консерванты и другие добавки, такие как, например, противомикробные средства, антиоксиданты, хелатирующие средства и инертные газы и т. п.
В одном варианте осуществления терапевтические соединения получают с носителями, которые будут защищать терапевтические соединения от быстрого выведения из организма, как, например, в составе с контролируемым высвобождением, в том числе в имплантатах и микроинкапсулированных системах доставки.
Фармацевтические композиции можно включать в контейнер, упаковку или дозатор вместе с инструкциями по введению.
Дозу, токсичность и терапевтическую эффективность терапевтических соединений можно определять с помощью стандартных фармацевтических процедур в культурах клеток или у экспериментальных животных, например, для определения LD50 (дозы, смертельной для 50% особей в популяции) и ED50 (дозы, терапевтически эффективной для 50% особей в популяции). Соотношение доз между токсичным и терапевтическим эффектами представляет собой терапевтический индекс и может быть выражено как соотношение LD50/ED50. Соединения, которые демонстрируют высокие терапевтические индексы, являются предпочтительными. Хотя соединения, которые демонстрируют токсичные побочные эффекты, можно применять, но следует позаботиться о разработке системы доставки, которая направляет такие соединения в очаг поражения ткани, с целью сведения к минимуму потенциального повреждения неинфицированных клеток и снижения таким образом побочных эффектов.
Данные, полученные из анализов культур клеток и исследований на животных, можно использовать для составления диапазона доз для применения у людей. Доза таких соединений предпочтительно находится в пределах диапазона циркулирующих концентраций, который включает ED50 с небольшой или отсутствующей токсичностью. Доза может варьироваться в пределах данного диапазона в зависимости от используемой лекарственной формы и используемого пути введения. Для любого соединения, применяемого в способе по настоящему изобретению, терапевтически эффективную дозу можно вначале оценить с помощью анализов культур клеток. Дозу можно составлять в животных моделях с достижением диапазона циркулирующих концентраций в плазме крови, который включает IC50 (т. е. концентрацию тестируемого соединения, при которой достигается полумаксимальное ингибирование симптомов), определенную в культуре клеток. Такую информацию можно использовать для более точного определения применимых доз у людей. Уровни в плазме крови можно измерить, например, с помощью высокоэффективной жидкостной хроматографии.
Наборы
Также в данном документе предусмотрены наборы, содержащие одно или несколько из композиций, предусмотренных в данном документе, и инструкций по применению. Инструкции по применению могут включать инструкции по диагностике или лечению ENTPD2-ассоциированного заболевания, например, рака, описанного в данном документе. Наборы, предусмотренные в данном документе, можно применять в соответствии с любым из способов, описанных в данном документе. Специалистам в данной области будут известны другие подходящие пути применения наборов, предусмотренных в данном документе, и они смогут использовать эти наборы для таких путей применения. Наборы, предусмотренные в данном документе, также могут содержать оболочку почтового отправления (например, конверт с предварительно оплаченным почтовым сбором или почтовую упаковку), которая может использоваться для возвращения образца для анализа, например, в лабораторию. Набор может содержать один или несколько контейнеров для образца, или образец может находиться в стандартном флаконе для сбора крови. Набор также может содержать одно или несколько из формы информированного согласия, формы заявки на тестирование и инструкций по применению набора в способе, описанном в данном документе. Способы применения таких наборов также включены в данный документ. Одна или несколько из форм (например, форма заявки на тестирование) и контейнер, содержащий образец, могут быть закодированы, например, штрих-кодом для идентификации субъекта, который предоставил образец.
Специалисту в данной области будут понятны многие способы и материалы, подобные или эквивалентные описанным в данном документе, которые можно применять при осуществлении на практике настоящего изобретения. Следует отметить, что настоящее изобретение никоим образом не ограничено описанными способами и материалами.
ПРИМЕРЫ
Хотя были обсуждены конкретные варианты осуществления рассматриваемого изобретения, приведенное выше описание является иллюстративным, а не ограничивающим. Многие видоизменения настоящего изобретения станут очевидными для специалистов в данной области после ознакомления с настоящим описанием и нижеприведенной формулой изобретения. Полный объем настоящего изобретения должен определяться посредством ссылки на пункты формулы изобретения наряду с полным объемом их эквивалентов, а также на описание наряду с такими видоизменениями. Настоящее изобретение дополнительно описано в следующих примерах, которые не ограничивают объем настоящего изобретения, описанный в формуле изобретения.
Пример 1. Экспрессия ENTPD2 при раке
Эктонуклеозидтрифосфатдифосфогидролаза 2 (также называемая ENTPD2, NTPDазой 2, NTPDазой-2, экто-ATPазой 2, экто-ATPDазой 2, белком 1, подобным антигену CD39, CD39L1, экто-ATP-дифосфогидролазой 2) принадлежит к семейству внеклеточных ATP-гидролаз, которые регулируют пуринергическую передачу сигнала, в частности, опосредованную ATP, UTP, а также ADP и UDP, во внеклеточном пространстве (в отношении обзора см. Robson et al Purinergic Signaling 2:409-430 (2006)). 5'-AMP, являющийся конечным продуктом гидролиза ATP/ADP, затем дефосфорилируется до аденозина под действием экто-5'-нуклеотидазы (также известной как экто-5'NTаза или CD73).
Функциональная роль ENTPD2 при раке не была хорошо описана. В ранних сообщениях внимание было сосредоточено на сверхэкспрессии ENTPD2 в крысиной модели глиомы, которая приводила к усиленному росту опухоли in vivo посредством ADP-опосредованного модулирования тромбоцитов и микроокружения опухоли, а также способствовала воспалительному состоянию, усиливающему распространение опухоли (Braganhol et al Cancer Sci 100(8): 1434-42 (2009); Braganhol et al Purinergic Signal 8(2):235-43 (2012)). В последнее время сообщалось о повышенной экспрессии ENTPD2 в гепатоцеллюлярной карциноме, где его экспрессия была ассоциирована с неблагоприятным прогнозом ввиду повышенного накопления/поддержания супрессорных клеток миелоидного происхождения (Chiu et al Nature Communications 8(1): 517 (2017)).
Хотя находящиеся в открытом доступе данные об определении функциональных характеристик ENTPD2 при раке ограничены, было показано, что медиаторы пуринергической передачи сигнала, высвобождающиеся во внеклеточное пространство, такие как ATP и аденозин, играют важную роль в иммунитете и воспалении. ATP, высвобождающийся из подвергнутых стрессу, поврежденных или апоптотических клеток, запускает быстрое воспаление посредством активации рецепторов P2RX и P2RY, которые повышают привлечение иммунных клеток, усиливают передачу сигнала от TCR в T-клетках и способствуют активации дендритных клеток и макрофагов. С другой стороны, передача сигнала, опосредованная аденозином, приводит к образованию иммуносупрессивной ниши посредством ингибирования эффекторных T-клеток, а также нарушения регуляции функции мононуклеарных клеток-фагоцитов (в отношении обзора см. Cekic et al Nature Reviews Immunology 16: 177-192 (2016), Antonioli et al Nature Reviews Cancer 13: 842-857 (2013)). В доклинических исследованиях было продемонстрировано, что блокада передачи сигнала, опосредованной аденозином, или восстановление уровней внеклеточного ATP в очаге опухоли индуцирует привлечение лимфоцитов и противоопухолевые ответы (Michaud et al Science 334(6062): 1573-7 (2011); Allard et al Clinical Cancer Research 19(20): 5626-35 (2013)).
Повышенная экспрессия ENTPD2 в раковых клетках потенциально может привести к существенному изменению баланса пуринергической передачи сигналов в микроокружении опухоли, смещая его в сторону более иммуносупрессивного состояния. Целенаправленное ингибирование каталитической функции ENTPD2 может, следовательно, обеспечивать возможность сдвига баланса в сторону ATP-управляемого провоспалительного состояния Th-1-подобного типа, усиливая противоопухолевый иммунный ответ.
Экспрессия ENTPD2 в различных подтипах опухолей тщательно не изучалась. Антитело mAb1 к ENTPD2 человека применяли для оценки экспрессии ENTPD2 в разных линиях раковых клеток при различных показаниях. Клетки окрашивали с помощью антитела mAb1 к ENTPD2 человека при 5 мкг/мл в течение 45 мин. на льду с последующим инкубированием с Fcγ-специфичным вторичным Ab козы к IgG человека, конъюгированным с Alexa Fluor 647 или APC (разведение 1:400; Jackson ImmunoResearch Laboratories, Вест-Гроув, Пенсильвания). Все процедуры инкубирования и промывания проводили в буфере для FACS, состоящем из 1x фосфатно-солевого буферного раствора HyClone (GE Healthcare, Питтсбург, Пенсильвания), 1% фетальной бычьей сыворотки крови HyClone (GE Healthcare, Питтсбург, Пенсильвания), 2 мМ EDTA (ThermoFisher, Уолтем, Массачусетс).
Повышенная экспрессия ENTPD2 наблюдалась в иллюстративных линиях раковых клеток при показаниях рака ободочной и прямой кишки, пищевода, желудка, молочной железы и легкого, как показано на фиг. 1A. Плотность рецепторов ENTPD2 определяли количественно с помощью Quantum Simply Cellular с антителом к IgG человека от Bangs Laboratories (Фишерс, Индиана) согласно указаниям производителя (таблица 20, фиг. 1B).
Таблица 20. Плотность экспрессии ENTPD2 в различных иллюстративных линиях раковых клеток.
С целью оценки экспрессии белка ENTPD2 в тканях первичных опухолей фиксированные в формалине и залитые в парафин микроматрицы опухолевых тканей с соответствующими соседними нормальными тканями получали от Cureline (Брисбен, Калифорния). IHC-окрашивание проводили с помощью Ab к CD39L1/ENTPD2 для IHC (NBP1-85752, Novus, Литлтон, Колорадо) с использованием автоматизированного протокола Ventana со стандартным методом демаскирования антигена CC1 при высоком pH и 95°C и с последующими инкубированиями с конъюгированным с HRP вторичным Ab к Rb Ventana DISCOVERY® OmniMap и набором на основе DAB Ventana DISCOVERY® ChromoMap (Ventana, Тусон, Аризона).
Повышенная экспрессия ENTPD2, локализованного на клеточной мембране, наблюдалась в подгруппах образцов опухолей ободочной и прямой кишки, пищевода и яичника. В срезах соответствующих нормальных тканей не были выявлены или были выявлены очень низкие фоновые уровни экспрессии ENTPD2 (фиг. 2).
Пример 2. Получение гуманизированных моноклональных антител, которые связываются с ENTPD2 человека
Получение конструкций для экспрессии ENTPD2 человека, крысы, мыши и макака-крабоеда
Нуклеотидные последовательности, кодирующие полноразмерный ENTPD2 человека, макака-крабоеда (Cyno), крысы и мыши, а также ENTPD1 (CD39) человека и мыши, синтезировали на основе информации об аминокислотных последовательностях из баз данных GenBank® или UniProtKB (см. таблицу 24). Все синтезированные фрагменты ДНК клонировали в соответствующие векторы экспрессии.
Таблица 24. Последовательности реагентов, используемых для получения антитела к ENTPD2
Экспрессия и очистка рекомбинантных ENTPD1 мыши и ENTPD2 мыши и крысы из культур HEK
Рекомбинантные мономерные ENTPD2 мыши или крысы, а также ENTPD1 мыши получали следующим образом. Клетки FreeStyle™ 293-F (Thermo Fisher Scientific) культивировали в среде для экспрессии Gibco™ FreeStyle™ 293 и транзиентно трансфицировали плазмидой, содержащей промотор CMV, сигнальный пептид IgK мыши, остатки 29-462 (внеклеточный домен) ENTPD2 мыши или крысы или остатки 38-478 ENTPD1 мыши и полигистидиновую (His6) метку (SEQ ID NO: 1010). Через четыре дня после трансфекции клетки из культуры объемом 1 л осаждали при 2600 × g в течение 10 минут, и надосадочную жидкость осветляли путем фильтрации через фильтр с размером пор 0,22 мкм. Надосадочную жидкость дополняли с помощью 20 мМ Трис-HCl, pH 8,0, и 20 мМ имидазола и загружали в колонку, предварительно упакованную с помощью 6 мл агарозы Ni-NTA (Qiagen). Колонку промывали 10 объемами колонки промывочного буфера [20 мМ Трис (pH 8,0), 150 мМ NaCl, 20 мМ имидазола] и элюировали 5 объемами колонки элюирующего буфера [20 мМ Трис (pH 8,0), 150 мМ NaCl, 250 мМ имидазола]. Белок подвергали замене буфера на TBS, pH 7,4, с использованием колонки для обессоливания PD-10 (GE Healthcare) и замораживали для хранения.
Экспрессия и очистка ENTPD1 человека и ENTPD2 человека и макака-крабоеда из клеток насекомых
Бакуловирусную систему экспрессии Bac-to-Bac® (Thermo Fisher Scientific) использовали для экспрессии рекомбинантных белков ENTPD1 человека и ENTPD2 человека и макака-крабоеда. Остатки 38-478 ENTPD1 человека или остатки 29-462 ENTPD2 человека или макака-крабоеда клонировали в вектор экспрессии pFastBac™1 (Thermo Fisher Scientific) с сигнальным пептидом GP67 и C-концевой меткой Avi-His6 (SEQ ID NO: 1010). Клонированные векторы вводили путем трансформации в компетентные клетки DH10Bac™ Escherichia coli (Thermo Fisher Scientific) с получением рекомбинантных бакмид. Рекомбинантные бакмиды затем экстрагировали с помощью набора PureLink® HiPure Plasmid Miniprep (Thermo Fisher Scientific) и вводили путем трансфекции в клетки Sf9 (Spodoptera frugiperda) с помощью FuGene® HD (Promega) с получением рекомбинантного бакуловируса (BV). После одного цикла амплификации полученный в результате BV использовали для инфицирования клеток High Five™ (Trichoplusia ni) (Thermo Fisher Scientific) в 1 л суспензионной культуры при плотности 2 × 106 клеток/мл и при множественности инфицирования (MOI), составляющей 10. Через 72 ч. после инфицирования клетки осаждали путем центрифугирования при 2600 × g в течение 10 мин., и собирали среду, содержащую секретированный гликозилированный рекомбинантный белок. Надосадочную жидкость затем дополняли с помощью 50 мМ Трис, pH 8,0, 1 мМ NiCl2, 5 мМ CaCl2, а затем центрифугировали при 2600 × g в течение 30 мин. Надосадочную жидкость подвергали фильтрации через фильтр с размером пор 0,22 мкм и загружали в колонку, упакованную с помощью 6 мл агарозы Ni-NTA (Qiagen). Колонку промывали 10 объемами колонки промывочного буфера, описанного выше, и элюировали элюирующим буфером (также описанным выше). Белок подвергали замене буфера на TBS (20 мМ Трис, pH 7,4, 150 мМ NaCl) с использованием колонки для обессоливания PD-10 (GE Healthcare) и замораживали для хранения.
Получение линий клеток, стабильно экспрессирующих ENTPD1 или ENTPD2
Стабильные линии клеток, экспрессирующих ENTPD1 или ENTPD2, получали с помощью ретровирусной трансдукции. Для получения ретровируса клетки 293T совместно трансфицировали ретровирусным вектором экспрессии, экспрессирующим ENTPD1 или ENTPD2, и пакующим вектором pCL-Eco или pCL-10A1 (Novus Biologicals, № по кат. NBP2-29540 или NBP2-2952) с использованием реагента для трансфекции FuGene® 6 (Promega, № по кат. E2692) согласно рекомендациям производителя. Клетки поддерживали в инкубаторе с увлажнением при 37oC и 5% CO2, и образцы надосадочной жидкости культуры клеток, содержащие вирус, собирали через 48 часов после трансфекции. Клетки NIH/3T3 и 300.19 (ATCC®) выращивали до почти полной конфлюэнтности в 6-луночном планшете. Среду для выращивания удаляли от клеток, и добавляли надосадочную жидкость, содержащую вирус, в присутствии 8 мкг/мл полибрена (конечная концентрация) (EMD Millipore, № по кат. TR-1003-G). После инкубирования в течение 3-6 часов при 37oC добавляли свежую среду. Затем клетки культивировали в соответствующих условиях отбора с получением стабильных линий клеток, экспрессирующих ENTPD1 или ENTPD2.
Получение, экспрессия и очистка вирусоподобных частиц (VLP)
Клетки 300.19 поддерживали в DMEM с 10% FBS. Для получения VLP клетки подвергали замене среды на DMEM с 4% FBS, затем совместно трансфицировали плазмидой для экспрессии ENTPD2 человека и плазмидой для экспрессии ретровирусного Gag при соотношении 3:2 в мкг. Через сорок восемь часов после трансфекции надосадочную жидкость культуры клеток собирали и осветляли путем центрифугирования при 2500 × g в течение 5 мин. в настольной центрифуге и выдерживали на льду. VLP очищали путем ультрацентрифугирования при 100000 × g через 20% сахарозную подушку в центрифужных пробирках Ultra-Clear™ объемом 38,5 мл (Beckman Coulter®, № по каталогу 344058) на роторе Beckman Coulter® SW 32 Ti в ультрацентрифуге Sorvall™ RC 6 Plus. Полученные осадки ресуспендировали в 300 мкл холодного стерильного PBS и подвергали количественной оценке с помощью анализа с BCA Pierce (Thermo Fisher Scientific, № по каталогу 23225).
Получение гибридом
Мышей, трансгенных по Bcl-2 (линии C57BL/6-Tgn(bcl-2)22WEHI), иммунизировали антигеном с помощью процедуры, называемой "повторной иммунизацией в нескольких участках" (RIMMS) (K.E. Kilpatrick et al. Hybridoma 1997). Вкратце, мышам инъецировали 22,5 мкг His6-меченного ECD 29-462 белка ENTPD2 человека ("His6" раскрыт под SEQ ID NO: 1010) в 8 конкретных участков вблизи периферических лимфатических узлов (PLN). Данную процедуру повторяли 8 раз в течение 20-дневного периода. В день 18 собирали тестируемые образцы крови, и титр сывороточных антител анализировали с помощью FACS и ELISA. В некоторых случаях мышей BALB/c иммунизировали с помощью 50 мкг His6-меченного ECD 29-462 белка ENTPD2 человека ("His6" раскрыт под SEQ ID NO: 1010) в полном адъюванте Фрейнда от Sigma Adjuvant System® или неполном адъюванте Фрейнда, 50 мкг VLP, экспрессирующих ENTPD2 человека, в PBS или 5 × 10e6 клеток 300.19, стабильно сверхэкспрессирующих ENTPD2 человека (SEQ ID NO: 291), в PBS. Животным дважды делали подкожную или внутрибрюшинную инъекцию с интервалом в две недели с последующей внутривенной бустерной инъекцией примерно две недели спустя, вводя им 50 мкг VLP, экспрессирующих ENTPD2 человека, или His6-меченного ECD 29-462 белка ENTPD2 человека в PBS ("His6" раскрыт под SEQ ID NO: 1010). Через десять дней после второй иммунизации собирали тестируемые образцы крови, и титр сывороточных антител анализировали с помощью FACS и ELISA. У мышей с высоким титром удаляли селезенки и объединенные периферические лимфатические узлы (PLN). Для сбора лимфоцитов селезенки и PLN промывали один раз с помощью PBS, а затем диссоциировали путем пропускания через сито с размером ячеек 70 микрон (Falcon, № 352350). Полученные лимфоциты промывали еще 2 раза перед проведением слияния в среде Cytofusion® (среда для электропорации BTXpress Cytofusion®, № по кат. 47001).
Для проведения слияния клетки миеломы F0 смешивали с лимфоцитами в соотношении 1:4. Смесь клеток центрифугировали, суспендировали в среде Cytofusion® и затем вносили в камеру для электрослияния (камера с коаксиальными электродами 9ML от Harvard Apparatus, № 470020). Электрослияние осуществляли в соответствии с инструкциями производителя с использованием системы для получения гибридом Hybrimune CEEF-50B (Cyto Pulse Sciences, Inc). Слитым клеткам предоставляли возможность восстановления в течение 5 минут в камере, их разбавляли 1:10 в среде без гипоксантина, аминоптерина и тимидина (HAT) [DMEM+20% FBS, 1% смесь пенициллин/стрептомицин/глутамин (PSG), 1X заменимые аминокислоты (NEAA), 0,5X добавка для слияния и клонирования гибридом (Roche; HFCS)] и оставляли при 37oC и 5% CO2 на один час. Затем добавляли 4X среду HAT (DMEM+20% FBS, 1% PSG, 1X NEAA, 4X HAT, 0,5X HFCS) для доведения концентрации HAT до 1X, и плотность корректировали, доводя до 66000 клеток/мл. Клетки высевали в 384-луночные планшеты из расчета 60 мкл/лунка.
FACS-скрининг
Через десять дней после слияния планшеты с гибридомами подвергали скринингу на наличие ENTPD2-специфичных антител с помощью проточной цитометрии для подтверждения специфичного связывания антител-кандидатов с ENTPD2 человека, экспрессирующимся на клеточной поверхности, с использованием трех линий клеток: исходных клеток NIH/3T3, клеток NIH/3T3, стабильно сверхэкспрессирующих ENTPD2 человека, и клеток RKO (ATCC®), которые экспрессируют эндогенный ENTPD2 человека. Клетки тщательно ополаскивали с помощью PBS, обрабатывали аккутазой (Millipore, № SCR005) для отделения их от планшетов для выращивания и ресуспендировали в холодном PBS. Клетки биотинилировали и метили флуоресцентным красителем согласно инструкциям производителя (набор для биотинилирования белков клеточной поверхности FluoReporter™, Thermo Fisher Scientific, № по кат. F-20650; PE-Cy7-стрептавидин, ThermoFisher Scientific, № по кат. SA1012). Клетки ресуспендировали из расчета примерно 1 × 106 клеток/мл в буфере для FACS (PBS с 2% FBS+0,1% NaN3). В 384-луночный планшет предварительно вносили 20 мкл надосадочной жидкости гибридомы и добавляли 20 мкл суспензии клеток. Клетки инкубировали в течение 1 часа при 4oC, дважды промывали с помощью холодного буфера для FACS и ресуспендировали в 20 мкл буфера для FACS, содержащего вторичное антитело в разведении 1:400 (Fcγ-специфичный F(ab')2 антитела козы к IgG мыши, конъюгированный с аллофикоцианином; Jackson ImmunoResearch, № по кат. 115-136-071). После дополнительного инкубирования в течение 45 мин. при 4oC клетки дважды промывали с помощью буфера для FACS и ресуспендировали в 20 мкл буфера для FACS с 2 мкг/мл йодида пропидия (Sigma Aldrich, № по кат. P4864). Среднее геометрическое значение интенсивности флуоресценции рассчитывали в отдельных живых клетках с помощью программного обеспечения FlowJo™.
Хиты из этого первичного проточно-цитометрического скрининга с использованием клеток подтверждали при вторичном проточно-цитометрическом скрининге. Гибридомы, экспрессирующие антитела, которые связывались как с клетками NIH/3T3-hENTPD2, так и с клетками RKO, размножали до получения 45 мл культур, продуцирующих белок, в бессывороточной среде для культивирования гибридом с добавкой для среды HT (50×) Hybri-Max™ (Sigma, № по кат. H0137) в колбах CellStar® Autoflask™ (Greiner Bio-One). Культуры поддерживали во встряхивателе-инкубаторе при 37°C и 5% CO2 в течение примерно 8 дней, а затем клетки осаждали, и образцы надосадочной жидкости отбирали посредством очистки на смоле с белком G. Белки затем подвергали замене буфера на PBS с использованием колонок NAP-10™ (GE Healthcare).
Получение рекомбинантных антител
mAb, полученные из гибридом, подвергали скринингу в клеточном анализе на ингибирование гидролиза ATP под действием ENTPD2. В этом анализе идентифицировали два лидерных ингибирующих mAb: mAb17 и mAb16.
Получали химерные антитела, состоящие из мышиных вариабельных областей и человеческих константных областей. Из гибридом получали последовательности ДНК вариабельных областей (VH и VL) для клонирования и оптимизации антител (гуманизации, удаления потенциальных посттрансляционных модификаций и т. д.). ДНК вариабельной области из мышиных моноклональных антител амплифицировали с помощью 5'-RACE из РНК, полученной из каждой отобранной гибридомной линии клеток, с применением стандартных способов. Полипептидные последовательности каждой из мышиных вариабельных областей тяжелой/легкой цепи показаны в таблице 1 для mAb17 и mAb16 соответственно. Соответствующие нуклеотидные последовательности вариабельных областей тяжелой/легкой цепей для каждой из гибридом показаны под SEQ ID NO: 234/SEQ ID NO: 238 и SEQ ID NO: 226/SEQ ID NO: 230. Для получения химерных антител последовательности ДНК, кодирующие VL и VH из гибридомы, амплифицированные с помощью 5'-RACE-PCR, клонировали в векторы экспрессии, содержащие соответствующие последовательности константных областей человеческой тяжелой цепи дикого типа и человеческой легкой цепи (IgG1, каппа-цепь). Эти векторы выделяли в минимальном количестве с помощью набора QIAprep Spin Miniprep (QIAGEN, № по кат. 27106) и вводили путем нуклеофекции в фирменную линию клеток CHO с помощью Amaxa™ 4D-Nucleofector™ (Lonza). Трансфицированные клетки помещали в селективную среду для получения стабильных пулов, и полученные в результате пулы подвергали 14-дневному процессу получения белка с периодической подпиткой. Образцы надосадочной жидкости культуры клеток, содержащие белок, осветляли путем центрифугирования при 3000 × g в течение 15 минут и фильтрации через фильтр с размером пор 0,22 мкм. Белки очищали с помощью смолы MabSelect SuRe™ (GE Healthcare) на очистительном устройстве ÄKTA™ Pure или ÄKTA™ и элюировали с помощью элюирующего буфера для IgG Pierce™ (Thermo Fisher Scientific, № 21004), затем подвергали замене буфера на PBS путем диализа или с использованием колонки для обессоливания HiPrep (GE Healthcare). В случаях, когда полученный в результате белок был на < 95% димерным согласно данным аналитической эксклюзионной хроматографии (AnSEC) с использованием Superdex® 200 Increase, белок подвергали препаративной SEC с использованием колонки HiLoad® Superdex® 200 (GE Healthcare) с использованием PBS в качестве подвижной фазы.
Гуманизация
Конструкции вариабельных областей также разрабатывали для гуманизации и оптимизации последовательностей (например, удаления потенциальных сайтов посттрансляционных модификаций) с помощью программы из системы программного обеспечения для внутреннего пользования. Для каждой мышиной VH и VL были выбраны одна или несколько человеческих каркасных областей с обратными мутациями в "верньерных" зонах (Foote and Winter 1992, Journal of Molecular Biology; 224 (2):487-499) для поддержания аффинности и необходимой функциональной активности. Как mAb17, так и mAb16 также гуманизировали с использованием разработки на основе трехмерной кристаллической структуры. Вкратце, кристаллическую структуру загружали в Molecular Operating Environment (MOE™) (Chemical Computing Group ULC) и получали с помощью стандартной методики получения структур с использованием силового поля Amber10EHT. Fab затем сравнивали по структуре с библиотекой гуманизированных Fab собственной разработки с помощью специально созданного скрипта под названием "cdr_grafter SVL". Скрипт сравнивает по структуре вводимую структуру мышиного Fab со структурами человеческих Fab в базе данных для внутреннего пользования и выводит перечень детализированных параметров, касающихся структурных сходств между мышиными (донорными) и человеческими (акцепторными) Fab. Эти параметры включают сравнение величин RMSD для каркасных и "стволовых" областей и длины для CDR. На основании этих параметров были отобраны четыре акцепторных Fab-кандидата для прививания донорных CDR из mAb17 и были отобраны три акцепторных Fab-кандидата для прививания донорных CDR из mAb16. Гуманизация mAb17 приводила к получению mAb1, mAb2, mAb3 и mAb7. Гуманизация и оптимизация mAb16 приводила к получению mAb4, mAb5 и mAb6.
Последовательности ДНК, кодирующие разработанные гуманизированные домены VL и VH в обеих стратегиях гуманизации, заказывали в GeneArt (Life Technologies Inc., Регенсбург, Германия) с оптимизацией кодонов для Cricetulus griseus. Эти вариабельные области субклонировали в векторы экспрессии, содержащие соответствующие последовательности константных областей человеческой тяжелой цепи дикого типа и человеческой легкой цепи (IgG1, каппа-цепь), с применением стандартных способов.
Рекомбинантные антитела получали посредством введения векторов, кодирующих тяжелую и легкую цепи, в клетки FreeStyle™ 293-F (Thermo Fisher Scientific) путем совместной трансфекции. Трансфицированные клетки поддерживали в среде для экспрессии Gibco® FreeStyle™ 293 (Thermo Fisher Scientific, № 12338018) в колбах CellStar® Autoflask™ (Greiner Bio-One), помещенных во встряхиватель-инкубатор, при 37°C и 5% CO2 в течение примерно 5 дней, и затем клетки осаждали, а образцы надосадочной жидкости, содержащие белок, отбирали посредством очистки на смоле MabSelect SuRe™ (GE Healthcare). Белки затем подвергали замене буфера на PBS с использованием колонок NAP-10™ (GE Healthcare).
Пример 3. Получение человеческих антител к ENTPD2 человека и их Fab-фрагментов с помощью фагового дисплея
Fab, которые специфично связываются с ENTPD2 человека (SEQ ID NO: 291), получали с помощью технологии фагового дисплея HuCAL PLATINUM® от MorphoSys. Фагмидная библиотека основана на концепции HuCAL® (Knappik et al., 2000, J Mol Biol 296, 57-86), и в ней используется технология CysDisplayTM для отображения Fab на поверхности фага (Lohning, WO 2001/05950).
Проводили четыре типа пэннинга: твердофазный пэннинг против непосредственно нанесенного в качестве покрытия рекомбинантного ENTPD2 человека (hENTPD2), пэннинг в растворе против ENTPD2, пэннинг с использованием цельных клеток и пэннинг для созревания аффинности.
Пэннинг с использованием гранул
Перед пэннингом с использованием гранул антиген иммобилизировали на магнитных гранулах, покрытых карбоновой кислотой (Dynabeads™ M-270 с карбоновой кислотой, Thermo Fisher Scientific, № по кат. 14306D). 1 × 107 гранул, покрытых антигеном, на пул фагов блокировали с помощью 1x ChemiBlocker (EMD Millipore). Параллельно с этим соответствующее количество антител на фаге блокировали с помощью 50% человеческой сыворотки крови/0,33x ChemiBlocker/0,05% Tween 20. Для предотвращения отбора фага, связывающегося с гранулами, блокированные фаговые частицы предварительно инкубировали с использованием гранул с иммобилизованным нерелевантным белком. Блокированные гранулы, покрытые антигеном, добавляли к предварительно адсорбированным и блокированным фаговым частицам, и антителам на фаге предоставляли возможность связывания с гранулами, покрытыми антигеном. Фаговые частицы, связавшиеся с гранулами, покрытыми антигеном, собирали путем магнитной сепарации. Несколько стадий промывания обеспечивали удаление неспецифично связавшегося фага. Наконец, специфично связавшийся фаг элюировали с гранул, покрытых антигеном. Элюат переносили в 14 мл культуры E. coli TG1 и инкубировали для инфицирования фагом.
После центрифугирования инфицированные бактерии осаждали и ресуспендировали в 2x среде YT, высевали на чашки с агаром LB/хлорамфениколом и инкубировали в течение ночи. Колонии соскабливали с чашек и использовали для "спасения" фага, поликлональной амплификации отобранных клонов и получения фага. При наличии очищенного фага начинали следующий цикл пэннинга. Второй и третий циклы твердофазного пэннинга проводили с использованием того же протокола, что и для первого цикла, за исключением того, что использовали меньшее количество антигена и более жесткие условия промывания.
Пэннинг в растворе
Блокировали подходящее количество гранул со стрептавидином (Dynabeads™ M-280 со стрептавидином, Thermo Fisher Scientific, № по кат. 11206D). Параллельно с этим блокировали подходящее количество антител на фаге. Для удаления фага, связывающегося со стрептавидином или гранулами, проводили предварительную адсорбцию блокированных фаговых частиц с использованием блокированных гранул со стрептавидином, покрытых нерелевантным биотинилированным белком. Затем биотинилированный ENTPD2 добавляли к предварительно адсорбированным и блокированным фаговым частицам, и антителам на фаге предоставляли возможность связывания с антигеном в растворе. Комплексы фаг-антиген захватывали с помощью блокированных гранул со стрептавидином, и фаговые частицы, связавшиеся с гранулами со стрептавидином, собирали с помощью магнитного сепаратора. Неспецифично связавшийся фаг смывали с помощью нескольких стадий промывания. Специфично связавшийся фаг элюировали с гранул со стрептавидином. Элюат переносили в 14 мл культуры E. coli TG1 и инкубировали для инфицирования фагом. Последующее инфицирование фагом и получение фага проводили в соответствии с протоколом пэннинга с использованием гранул, и начинали следующий цикл пэннинга. Второй и третий циклы пэннинга с использованием гранул в растворе проводили с использованием того же протокола, что и для первого цикла пэннинга, за исключением того, что применяли условия промывания повышенной жесткости.
Пэннинг с использованием цельных клеток
Для каждой процедуры пэннинга блокировали подходящее количество антител на фаге. Параллельно с этим для каждого пула фагов блокировали подходящее количество клеток-мишеней, экспрессирующих ENTPD2, и подходящее количество адсорбированных клеток без экспрессии антигена ENTPD2. Блокированные клетки-мишени осаждали путем центрифугирования, ресуспендировали в растворе предварительно блокированных фаговых частиц, и антителам на фаге предоставляли возможность связывания с антигеном, представленным на клетке. Комплексы фаг-клетка промывали несколько раз. Специфично связавшийся фаг элюировали с клеток-мишеней. После центрифугирования надосадочную жидкость (элюат) наносили на антиген-отрицательные адсорбированные клетки для удаления фага, связывающегося с молекулами клеточной поверхности, отличными от антигена-мишени (после адсорбции). Конечную надосадочную жидкость переносили в культуру E. coli TG1 для инфицирования фагом. Второй и третий цикл пэннинга с использованием цельных клеток проводили с использованием того же протокола, что и для первого цикла пэннинга.
Пэннинг для созревания аффинности
Создание библиотек для созревания аффинности HuCAL PLATINUM®
Для созревания аффинности были отобраны четыре Fab-кандидата. Для увеличения аффинности и биологической активности отобранных антител области CDR-L3 и CDR-H2 оптимизировали путем кассетного мутагенеза с применением тринуклеотид-направленного мутагенеза, оставляя при этом неизменными каркасные области (Virnekäs et al. 1994, Nucleic Acids Research 22 (25), pp. 5600-5607). Для оптимизации CDR-L3 фрагмент ДНК размером ~ 400 п. о., кодирующий CDR-L3, каркасную область 4, а также константную область легкой цепи, удаляли из последовательности, кодирующей исходные антитела, путем рестрикционного расщепления и заменяли репертуаром фрагментов ДНК, кодирующих диверсифицированные области CDR-L3 вместе с каркасной областью 4 и константным доменом. Во втором библиотечном наборе была диверсифицирована последовательность, кодирующая CDR-H2, при этом соединительные каркасные области оставались неизменными. С целью снижения влияния генетического окружения исходной недиверсифицированной последовательности фрагмент ДНК размером ~ 150 п. о., содержащий исходные последовательности CDR-H2 и каркасной области 3, заменяли имитационной последовательностью размером ~ 590 п. о. посредством рестрикционного расщепления и лигирования перед тем, как диверсифицированную кассету CDR-H2 (включая каркасную область 3) вставляли также посредством рестрикционного расщепления и лигирования. Электропорацию смесей для лигирования проводили в клетках MC1061F´ с получением примерно 108-109 в > 5 × 106 независимых колоний. Амплификацию библиотеки проводили, как описано ранее (Rauchenberger et al. 2003, J Biol Chem 278 (40), pp. 38194-38205). Для контроля качества примерно 10-20 отдельных клонов на библиотеку произвольным образом отбирали и секвенировали.
Для отбора кандидатов с улучшенной аффинностью фаги, полученные из библиотек для созревания аффинности, подвергали двум-трем циклам пэннинга для созревания аффинности. Жесткость пэннинга повышали путем снижения концентрации антигена в каждом цикле пэннинга (Low et al. 1996, J.Mol.Biol. 260, pp. 359-368). В дополнение к снижению количества антигена проводили отбор по скорости диссоциации (Hawkins et al. 1992, J.Mol.Biol. 226 (3), pp. 889-896). Эти стратегии использовали в комбинации с длительными стадиями промывания.
Экспрессия
Субклонирование из дисплейного вектора в вектор для экспрессии Fab у E. coli
Для обеспечения быстрой экспрессии растворимого Fab вставки, кодирующие Fab, в отобранном фаге HuCAL PLATINUM® субклонировали из дисплейного вектора pMORPH®30 в вектор экспрессии pMORPH®x11, представляющий собой pMORPH®x11_FH. После трансформации E. coli TG1 F- экспрессию отдельных клонов и получение периплазматических экстрактов, содержащих Fab-фрагменты HuCAL®, проводили, как описано ранее (Rauchenberger et al., 2003, J Biol Chem 278: 38194-38205).
Микромасштабное получение His-меченных Fab-фрагментов
Экспрессию Fab-фрагментов, кодируемых бактериальным вектором экспрессии, в клетках E. coli TG1 F- осуществляли в пробирках Falcon объемом 50 мл с использованием 25 мл 2x среды YT, дополненной 0,1% глюкозой, 34 мкг/мл хлорамфеникола и 1 мМ IPTG (изопропил-ß-D-тиогалактопиранозида). Культуры встряхивали при 30°C в течение 18 ч. Клетки собирали и разрушали с помощью комбинации лизоцима и реагента для экстракции белков BugBuster® (Merck, Германия). His6-меченные Fab-фрагменты ("His6" раскрыт под SEQ ID NO: 1010) выделяли посредством IMAC (GE Healthcare, Германия) и элюировали с помощью имидазола. Замену буфера на 1X PBS Дульбекко (pH 7,2) проводили с использованием планшетов "PD MultiTrap™ G-25" (GE Healthcare, Германия). Концентрации белков определяли с помощью UV-спектрофотометрии. Чистоту иллюстративных отобранных образцов анализировали в 15% геле для SDS-PAGE в денатурирующих невосстанавливающих условиях.
Субклонирование в вектор для экспрессии IgG и FabCys и экспрессия в клетках HKB11
Для экспрессии полноразмерного IgG в клетках HKB11 отобранные кандидаты или пулы кандидатов клонировали в вектор pMORPH®4_IgG1f. Субклонирование проводили в качестве двухстадийного способа для удобного и эффективного преобразования большого количества клонов Fab с уникальными последовательностями в формат IgG.
Эукариотические клетки HKB11 трансфицировали ДНК-вектором экспрессии в клетках млекопитающих, кодирующим как тяжелую, так и легкую цепи IgG. Образцы надосадочной жидкости культуры клеток собирали в день 3 или 6 после трансфекции и подвергали стандартной аффинной хроматографии с белком A (MabSelect™ SuRe™, GE Healthcare). Если не указано иное, проводили замену буфера на 1x PBS Дульбекко (pH 7,2, Invitrogen), и образцы подвергали стерилизующей фильтрации (размер пор 0,2 мкм).
Концентрации белков определяли с помощью UV-спектрофотометрии, и показатели чистоты IgG анализировали в денатурирующих, восстанавливающих и невосстанавливающих условиях с использованием CE-SDS (LabChip GXII, Perkin Elmer, США). Для анализа препаратов IgG в нативном состоянии проводили HP-SEC.
Сводные данные об антителах
В таблице 1 представлена информация о последовательностях антител к ENTPD2 человека, полученных из мышиных гибридом и фагового дисплея.
Пример 4. Определение биохимических характеристик антител к ENTPD2 человека
Антитела к ENTPD2 человека оценивали в следующих анализах.
FACS-скрининг. Специфичное связывание антител-кандидатов с эндогенно экспрессирующимся ENTPD2 оценивали с помощью проточной цитометрии. Клетки тщательно ополаскивали с помощью 1x PBS и обрабатывали аккутазой (Millipore, № SCR005) для отделения от планшетов для выращивания и ресуспендировали из расчета примерно 1 × 105 клеток/90 мкл в 1x буфере для FACS (2% FBS+0,1% NaN3 в PBS). В 96-луночный планшет с U-образным дном предварительно вносили 10 мкл 10x раствора антитела в буфере для FACS и добавляли 90 мкл суспензии клеток. Клетки инкубировали в течение 30 минут при 4oC, промывали 1x с помощью холодного PBS и ресуспендировали в 100 мкл вторичного антитела, разведенного 1:500 в 1x буфере для FACS (Fcγ-специфичный F(ab')2 антитела козы к IgG человека, конъюгированный с аллофикоцианином; Jackson ImmunoResearch, № по кат. 109-136-098). После дополнительного инкубирования в течение 15 мин. при 4oC клетки дважды промывали с помощью PBS и ресуспендировали в 100 мкл 1x буфера для FACS с 4 мкг/мл йодида пропидия (Life Technologies, № по кат. P3566). Среднее геометрическое значение интенсивности флуоресценции рассчитывали в отдельных живых клетках с помощью программного обеспечения FlowJo.
ELISA-скрининг на антигене, непосредственно нанесенном в качестве покрытия. 384-луночные планшеты MaxiSorp™ (Thermo Nunc) покрывали с помощью 2 мкг/мл рекомбинантного ENTPD2, разведенного в PBS. После блокирования с помощью 2% BSA (бычьего сывороточного альбумина) в PBS в течение 1 ч. при комнатной температуре, 3-кратного промывания планшетов с помощью TBST (0,05% Tween 20 в TBS, Sigma, № по кат. T9039) добавляли первичные антитела в TBST и 2% BSA в серийном разведении и инкубировали в течение 1 ч. при комнатной температуре. Планшеты промывали вновь, и связавшиеся антитела выявляли путем инкубирования с антителом к hFc-гамма, конъюгированным с пероксидазой хрена (HRP; Jackson ImmunoResearch, № по кат. 115-035-098, в разведении 1:5000 в 1x TBST+2% BSA), в течение 1 ч. при комнатной температуре с последующим промыванием с помощью TBST и добавлением после этого субстрата пероксидазы SureBlue (KPL, № 52-00-03). Спустя 15 мин регистрировали поглощение при 650 нм и анализировали в GraphPad Prism6.
Скрининг на Biacore. Аффинность измеряли путем определения кинетических констант скоростей с помощью поверхностного плазмонного резонанса (SPR) на приборе Biacore T200 или T100 с комплектом для повышения чувствительности T200 (Biacore, GE Healthcare). Антитела захватывали на сенсорных чипах CM5 (Biacore, GE Healthcare), полученных с использованием антитела мыши к Fc-домену IgG человека (ThermoFisher, № по каталогу 05-4200), связанного с поверхностью посредством аминогруппы. Связывание с ECD ENTPD2 человека и макака-крабоеда (Cyno) при 25°C выявляли при концентрациях в диапазоне от 0,78 нМ до 500 нМ в зависимости от аффинности антитела. Аналитам ENTPD2 предоставляли возможность ассоциации в течение 180 с и диссоциации в течение не более 1800 с в зависимости от скорости диссоциации антитела при скорости потока 30 мкл/мин. Подвижный буфер представлял собой PBS, pH 7,2 (полученный из 10X исходного раствора Corning, № по кат. 46-013-CM) + 0,05% Tween 20. Регенерацию осуществляли посредством 30-секундных операций введения 3 M или 4 M MgCl2 для полного удаления захваченного антитела и оставшегося комплекса с поверхности, после чего захватывали новое антитело. Необработанные данные анализировали с помощью программного обеспечения для оценки Biacore T200 версии 1.0 и аппроксимировали моделью связывания 1:1, при этом все параметры были установлены для глобальной аппроксимации, за исключением RI, который был установлен для локальной аппроксимации.
Для mAb1 - mAb10 подтверждали специфичность антитела. Все клоны демонстрировали значительное связывание с ENTPD2 человека в диапазоне от наномолярного до субнаномолярного. Антитела mAb8, mAb9 и mAb10 демонстрировали слабую аффинность в отношении ENTPD2 мыши. Ни одно из отобранных антител не связывается с ENTPD2 крысы. См. таблицу 21 и таблицу 22.
Таблица 21. Константы диссоциации (KD) для отдельных антител к ENTPD2 человека
KD (нМ)
KD (нМ)
KD (нМ)
Таблица 22. Связывание отдельных антител к ENTPD2 человека с клетками, экспрессирующими ENTPD2
Перекрестная реактивность. Клетки NIH/3T3, экспрессирующие ENTPD1 человека (NP_001767), получали с использованием подхода ретровирусной трансдукции. Через 72 ч. после трансдукции сконструированные клетки окрашивали с помощью антитела к CD39/ENTPD1 человека, конъюгированного с APC (R&D Systems, Миннеаполис, Миннесота), и живые клетки, экспрессирующие ENTPD1 человека, отделяли от остальной части популяции посредством сортировки клеток с активированной флуоресценцией. Стабильную экспрессию ENTPD1 периодически повторно подтверждали с помощью FACS с использованием вышеописанного антитела к CD39/ENTPD1 человека, конъюгированного с APC (1:100).
Клетки H520 идентифицировали в качестве линии раковых клеток, экспрессирующих ENTPD3 (Ct 25) и ENTPD8 (Ct 26), с помощью Taqman и использовали для скрининга на избирательность.
При использовании любого из тестируемых Ab к ENTPD2 человека не наблюдалось значительное связывание с какой-либо из контрольных линий клеток (таблица 25).
Таблица 25. Перекрестная реактивность mAb к ENTPD2 человека
Эпитоп-специфическая сортировка с помощью системы Octet Red96
Эпитоп-специфическую сортировку антител к ENTPD2 человека проводили с помощью системы Octet Red96 (ForteBio, США), которая проводит измерения методом биослойной интерферометрии (BLI). Белок ENTPD2 человека-Avi-His6 ("His6" раскрыт под SEQ ID NO: 1010) биотинилировали с помощью AviTag™ с использованием биотинлигазы BirA согласно рекомендациям производителя (Avidity LLC, США, № по кат. BirA500). Биотинилированный иммуногенный остов загружали из расчета 0,5 мкг/мл на предварительно уравновешенные стрептавидиновые сенсоры (ForteBio, США). Затем сенсоры переносили в раствор, содержащий 100 нМ антитела A в 1X буфере для кинетического анализа (ForteBio, США). Сенсоры быстро промывали в 1X буфере для кинетического анализа и переносили во второй раствор, содержащий 100 нМ конкурирующего антитела. Кинетические характеристики связывания определяли на основании необработанных данных с помощью аналитического программного обеспечения для системы Octet Red96 (версия 9.0, ForteBio, США). Антитела тестировали во всех парных комбинациях в качестве как первого (блокирующего) антитела, связывающегося с hENTPD2, так и второго (конкурирующего) антитела. Все антитела демонстрировали значительное перекрестное блокирование в этом анализе, что указывает на то, что антитела mAb1-10 могут иметь сходные эпитопы.
Пример 5. Кристаллографическое исследование и картирование эпитопов для FAb22 антитела к ENTPD2 человека
В этом примере FAb22 антитела к ENTPD2 человека кристаллизовали в комплексе с эктодоменом ENTPD2 человека (с мутацией Y350A), и определяли соответствующую структуру. Анализ связывания FAb22 антитела к ENTPD2 человека с ENTPD2 человека на основе рентгенографических данных позволяет получить подробную информацию о вступлении в контакт с антигеном на молекулярном уровне и понять природу выявленных паратопов Fab и антигенных эпитопов.
Материалы и способы
Экспрессия и очистка Fab-фрагментов
Последовательности ДНК, кодирующие идентифицированные VH- и VL-домены, субклонировали в векторы экспрессии в клетках млекопитающих, содержащие соответствующие последовательности человеческого CH1 дикого типа и человеческой константной области легкой каппа-цепи. Рекомбинантные человеческие Fab получали посредством введения векторов в клетки путем транзиентной совместной трансфекции с использованием реагента для трансфекции. После трансфекции клетки культивировали в течение 5-6 дней, и осуществляли очистку антител. Клетки осаждали путем центрифугирования (2600 × g в течение 10 минут), и образцы надосадочной жидкости культуры клеток, содержащие антитело, осветляли путем фильтрации через фильтр с размером пор 0,22 мкм. Fab очищали на колонках с белком G (GE Healthcare Life Sciences) и элюировали с использованием кислых условий элюирующего буфера.
Получение комплекса ENTPD2 человека и FAb22 антитела к ENTPD2 человека
Для получения комплекса ENTPD2-FAb22 1,3-кратный молярный избыток FAb22 объединяли с hENTPD2 Y350A в 20 мМ Трис, pH 7,5, со 150 мМ NaCl с получением конечной концентрации 5,65 мг/мл. Образец комплекса инкубировали на льду в течение 2 часов и передавали для постановки скрининга кристаллизации.
Кристаллизация и сбор рентгенографических данных
Кристаллы выращивали в 96-луночных планшетах (планшетах Crystalquick Plus от Greiner Bio-One) методом диффузии паров в сидячей капле. Подробно, 0,2 мкл исходного раствора белка смешивали с 0,2 мкл резервуарного раствора, и каплю уравновешивали против 50 мкл того же резервуарного раствора при 20°C. Эксперименты ставили с использованием роботизированной системы Phoenix (Art Robbins Instruments), и образцы хранили в специально сконструированном устройстве для визуализации кристаллов на опорной раме собственной разработки (Novartis GNF, системы для внутреннего пользования).
Для сбора рентгенографических данных один кристалл устанавливали непосредственно на криопетлю и подвергали мгновенному охлаждению в жидком азоте. Рентгенографические данные собирали в Advanced Light Source, BL5.03, с помощью CCD-детектора Quantum Q315 с использованием рентгеновского излучения с длиной волны 0,9765 Å. 180 изображений с углом поворота в 1,0° для каждого регистрировали на расстоянии от кристалла до детектора, составляющем 350 мм, и обрабатывали с помощью HKL2000 (Z. Otwinowski and W. Minor, "Processing of X-ray Diffraction Data Collected in Oscillation Mode", Methods in Enzymology, Volume 276: Macromolecular Crystallography, part A, p.307-326, 1997, C.W. Carter, Jr. & R. M. Sweet, Eds., Academic Press (New York).
Определение и анализ структуры
Структуру комплекса FAb22-ENTPD2 определяли посредством молекулярного замещения с помощью программы Phaser (McCoy et al., 2007, J Appl Crystallogr 40:658-674) с использованием уточненных структур ENTPD2 человека, ранее определенных в собственной лаборатории, и координат Fab антитела к RSV клона B21m (код PDB 3QRG) в качестве независимых поисковых моделей. Структуру уточняли с помощью итерационных циклов построения модели с последующим автоматическим кристаллографическим уточнением с помощью программ Coot 0.8.0 ("набор кристаллографических объектно-ориентированных инструментов"; Emsley et al., 2010, Acta Crystallogr Sect D: Biol Crystallogr; 66:486-501) и AutoBuster 2.11.5 (Bricogne et al., 2011, BUSTER версии 2.11.2. Кембридж, Великобритания: Global Phasing Ltd.).
Визуальный осмотр кристаллических структур осуществляли с помощью программ Coot (Emsley et al., 2010, Acta Crystallogr Sect D: Biol Crystallogr; 66:486-501) и PyMOL (молекулярно-графическая система; DeLano Scientific: Пало-Альто, Калифорния). Качество конечных уточненных моделей оценивали с помощью программ Coot и PROCHECK v3.3 (Laskowski et al., 1992, J Appl Crystallogr; 26:283-291). Остатки ENTPD2 человека, которые становятся менее доступными для растворителя при связывании с FAb22 антитела к ENTPD2 человека, идентифицировали с помощью программы AREAIMOL из пакета программ CCP4 ("совместный вычислительный проект номер 4", 1994). Межмолекулярные контакты определяли с использованием расстояния отсечения 4,0 Å и идентифицировали с помощью программы NCONT CCP4.
Результаты
Кристаллическая структура FAb22 антитела к hENTPD2 в комплексе с ENTPD2 человека
FAb22 антитела к hENTPD2 в комплексе с ENTPD2 человека с мутацией Y350A кристаллизовали в 96-луночных планшетах с помощью способа диффузии паров в сидячих каплях при 20°C. Кристаллы выращивали в 0,1 M HEPES, pH 7,5, 20% полиэтиленгликоле 3350, 0,2 M хлорида магния. Кристаллы появлялись спустя примерно 6 недель и вырастали до полного размера в течение нескольких дней.
Кристалл комплекса FAb22-ENTPD2 находился в пространственной группе C2 моноклинной сингонии с одним комплексом на асимметричную единицу. Полный набор дифракционных данных собирали для комплекса с разрешением до 2,75 ангстрема.
Определение структуры посредством молекулярного замещения проводили с использованием ранее определенных координат ENTPD2 человека и координат Fab согласно коду PDB 3QRG. Уточнение с помощью AutoBuster приводило к хорошим статистическим показателям уточнения и общим геометрическим параметрам. Два остатка FAb22 Ala55L и Tyr33H, а также четыре остатка ENTPD2 Gly120, Thr122, Tyr229 и Ala430 были полными маргинальными остатками по карте Рамачандрана в структуре комплекса FAb22-ENTPD2. Остатки ENTPD2 Gly120 и Thr122 в дополнение к остаткам Fab Ala55L и Tyr33H четко определены с точки зрения электронной плотности и по всей вероятности являются подлинными полными маргинальными остатками по геометрическому критерию. Примечательно, что Tyr33H представляет собой остаток CDR, участвующий в связывании с ENTPD2, как описано ниже. Остатки ENTPD2 Tyr229 и Ala430 неточно моделировались с точки зрения электронной плотности.
Аминокислотные последовательности тяжелой цепи и легкой цепи FAb22 антитела к ENTPD2 человека приведены на фиг. 3A с подчеркнутыми CDR (согласно определению по Kabat, 1991, Sequences of proteins of immunological interest, NIH Publication No. 91-3242) и остатками, расположенными в области контакта Fab и антигена, отмеченными как *. Общий вид трехмерной структуры комплекса FAb22 антитела к ENTPD2 человека/ENTPD2 Y350A изображен на фиг. 6.
Аминокислотная последовательность рекомбинантного ENTPD2 человека, применяемого в данном примере (SEQ ID NO: 291), приведена на фиг. 4A. Растворимый внеклеточный домен ENTPD2 человека охватывает остатки 29-462. Сконструированная мутация Y350A присутствовала в конструкции и выделена серым цветом и курсивом. В конструкции, применяемой в данном случае, использовались N-концевой пептид GP67, являющийся сигналом секреции (первые 38 остатков), и C-концевая 6x-гистидиновая метка (SEQ ID NO: 1010). Asn64, Asn129, Asn294, Asn378 и Asn443 представляют собой предсказанные сайты N-связанного гликозилирования, из которых только те, в которых наблюдалось гликозилирование в кристаллической структуре, выделены серым цветом и курсивом. Элементы вторичной структуры показаны ниже аминокислотной последовательности, при этом прямоугольниками представлены α-спирали, а стрелками представлены β-тяжи. Остатки, для которых не отмечены элементы вторичной структуры, представляют неструктурированные сегменты, являющиеся петлями и изгибами.
Аминокислотная последовательность ENTPD2 человека обладает высокой гомологией последовательности с соответствующими последовательностями из видов грызунов и других млекопитающих, а структура характеризуется общей укладкой, практически идентичной по отношению к описанной для ENTPD2 крысы (т. е. с кодом PDB 3CJA, Zebisch, M., Strater, N. (2008) Proc.Natl.Acad.Sci.Usa 105: 6882-6887). Инвариантные и консервативные спаривания с помощью дисульфидных связей наблюдаются для Cys75/Cys99, Cys242/Cys284, Cys265/Cys310, Cys323/Cys328 и Cys377/Cys399. RMSD (среднеквадратическое отклонение) для 388 α-атомов углерода C между структурами ENTPD2 человека и крысы составляет примерно 0,365 Å.
Конечная модель комплекса FAb22/ENTPD2 содержала остатки 37-448 ENTPD2. Активный центр для гидролиза ATP находится между двумя субдоменами (субдомен 1: Pro36-Ser161 и Lys427-Phe461; субдомен 2: Gly162-Gln426). Остатки ENTPD2, не включенные в конечную модель, включают в себя остатки 29-36 на N-конце и остатки 60-65, соответствующие остаткам петли, соединяющей тяжи β2 и β3, остатки 179-193, соответствующие петле, взаимодействующей с мембраной (MIL), и C-концевые остатки после Ile448. В конечную уточненную модель были включены все остатки тяжелой и легкой цепей Fab, за исключением концевых цистеиновых остатков (Cys228 в тяжелой цепи/Cys218 в легкой цепи).
FAb22 связывается с антигеном ENTPD2 преимущественно благодаря вступлению в контакт с предсказанной мембранодистальной долей посредством взаимодействий, в которых участвуют все 6 CDR вариабельных доменов тяжелой и легкой цепей. Остатки CDR FAb22, по-видимому, в значительной степени не проникают в щель активного центра ENTPD2 и не влияют на связывание с ATP-субстратом. Остатки CDR3 и CDR2 тяжелой цепи секвестрируют остатки, включающие в себя и фланкирующие антипараллельный 2-тяжевой β-складчатый слой, состоящий из тяжей β10/β11. Концевые остатки CDR3 тяжелой цепи вступают в дополнительные связывающие контакты с остатками на N-конце спирали α14, а также спиралей α8 и α13. В связывающих взаимодействиях вариабельного домена легкой цепи с ENTPD2 участвуют главным образом остатки CDR1 и CDR3, которые преимущественно связываются с N-концом спирали α14. При образовании комплекса FAb22/ENTPD2 вглубь погружается примерно 16700 Å2 общей совокупной поверхности, доступной для растворителя, при практически равных вкладах тяжелой и легкой цепей Fab. Остатки эпитопа и паратопа, участвующие в непосредственных межмолекулярных контактах, рассчитанных в пределах расстояния отсечения 4,0 Å, перечислены в таблице 17 и отмечены на фиг. 3A и 4A. В непосредственных межмолекулярных контактах участвуют в общей сложности 25 остатков Fab и 26 остатков ENTPD2, при этом CDR тяжелой цепи предоставляют больше связывающихся остатков, чем CDR легкой цепи. Среди этих остатков паратопа Fab тирозиновые остатки CDR вносят вклад в большое количество контактов с ENTPD2, в которых участвуют 10 из 14 остатков Tyr CDR. Остатки CDR тяжелой цепи, участвующие в межмолекулярных контактах, включают в себя остатки CDR1 Ser31, Gly32, Tyr33 и Tyr34; остатки CDR2 Tyr54, Asp55, Asp57; а также остатки CDR3 Tyr100, Tyr101, Arg102, Tyr103, Ser106, Tyr107, Asp112, Tyr113. Tyr27 из FR1 тяжелой цепи также вступает в контакт с антигеном ENTPD2. В связывании с ENTPD2 участвуют остатки CDR1 легкой цепи, включающие в себя Tyr31, Asp32, Gly33 и Tyr36, а также остатки CDR2 легкой цепи Glu59, Ser60 и остатки CDR3 Ser95, Asn96 и Asp98. Glu1, боковая цепь которого является неупорядоченной и не смоделирована в структуре комплекса, в дополнение к Gly61 в FR3 находятся в пределах расстояния контакта от сайта N-связанного гликозилирования, наблюдаемого для Asn294 в антигене ENTPD2 и выделенного на фиг. 3A.
Таблица 17. Остатки эпитопа и паратопа в FAb22/hENTPD2
Tyr54H, Asp55H
H-CDR2
Tyr101H, Tyr107H
H-CDR3
Tyr54H, Tyr101H
H-CDR2, H-CDR3
Tyr100H, Tyr101H, Tyr113H
H-CDR3
Glu59L, Ser60L
L-CDR2
Tyr54H
H-CDR2
Ser95L, Asn96L, Asp98L
L-CDR3
Tyr31L, Tyr36L
L-CDR1
Пример 6. Кристаллографическое исследование и картирование эпитопов для FAb23 антитела к ENTPD2 человека
В этом примере FAb23 антитела к ENTPD2 человека кристаллизовали в комплексе с эктодоменом ENTPD2 человека (с мутацией Y350A), и определяли соответствующую структуру. Анализ связывания FAb23 антитела к ENTPD2 человека с ENTPD2 человека на основе рентгенографических данных позволяет получить подробную информацию о вступлении в контакт с антигеном на молекулярном уровне и понять природу выявленных паратопов Fab и антигенных эпитопов.
Материалы и способы
Получение комплекса ENTPD2 человека и FAb23 антитела к ENTPD2 человека
Для получения комплекса ENTPD2-FAb23 1,6-кратный молярный избыток ENTPD2 объединяли с FAb23 в 20 мМ Трис, pH 7,5, со 100 мМ NaCl и концентрировали до 9,08 мг/мл путем ультрафильтрации, инкубировали на льду в течение 10 минут и передавали для постановки испытаний по кристаллизации.
Кристаллизация и сбор рентгенографических данных
FAb23 антитела к hENTPD2 в комплексе с ENTPD2 человека с мутацией Y350A кристаллизовали в 96-луночных планшетах (Greiner Bio-One) с помощью способа диффузии паров в сидячих каплях при 20°C. Подробно, 0,2 мкл исходного раствора белка смешивали с 0,2 мкл резервуарного раствора, и каплю уравновешивали против 50 мкл того же резервуарного раствора при 20°C. Эксперименты ставили с использованием роботизированной системы Phoenix (Art Robbins Instruments), и образцы хранили в специально сконструированном устройстве для визуализации кристаллов на опорной раме собственной разработки (Novartis GNF, системы для внутреннего пользования).
Для сбора рентгенографических данных один кристалл устанавливали непосредственно на криопетлю и подвергали мгновенному охлаждению в жидком азоте. Наборы рентгенографических данных собирали в Advanced Light Source, BL5.03, с помощью CCD-детектора Quantum Q315r с использованием рентгеновского излучения с длиной волны 0,9765 Å. 140 изображений с углом поворота в 1,0° для каждого регистрировали на расстоянии от кристалла до детектора, составляющем 300 мм, и обрабатывали с помощью HKL2000 (Z. Otwinowski and W. Minor, "Processing of X-ray Diffraction Data Collected in Oscillation Mode", Methods in Enzymology, Volume 276: Macromolecular Crystallography, part A, p.307-326, 1997, C.W. Carter, Jr. & R. M. Sweet, Eds., Academic Press (New York).
Определение и анализ структуры
Структуру комплекса FAb23-ENTPD2 определяли посредством молекулярного замещения с помощью программы Phaser (McCoy et al., 2007, J Appl Crystallogr 40:658-674) с использованием уточненных координат ENTPD2 человека, ранее определенных в собственной лаборатории, и гомологичной модели FAb23, созданной с помощью инструмента для моделирования антител в программном обеспечении MOE (Molecular Operating Environment (MOE), 2013.08; Chemical Computing Group ULC, 1010 Sherbooke St. West, Suite № 910, Монреаль, Квебек, Канада, H3A 2R7, 2018), которая продемонстрировала высокое сходство последовательности с Fab-фрагментом ICSM 18, представляющего собой антитело к PRP (код PDB 4W9D), в качестве независимых поисковых моделей. Структуру уточняли с помощью итерационных циклов построения модели с последующим автоматическим кристаллографическим уточнением с помощью программ Coot 0.8.0 ("набор кристаллографических объектно-ориентированных инструментов"; Emsley et al., 2010, Acta Crystallogr Sect D: Biol Crystallogr; 66:486-501) и AutoBuster 2.11.5 (Bricogne et al., 2011, BUSTER версии 2.11.2. Кембридж, Великобритания: Global Phasing Ltd.).
Визуальный осмотр кристаллической структуры осуществляли с помощью программ Coot (Emsley et al., 2010, Acta Crystallogr Sect D: Biol Crystallogr; 66:486-501) и PyMOL (молекулярно-графическая система; DeLano Scientific: Пало-Альто, Калифорния). Качество конечных уточненных моделей оценивали с помощью программ Coot и PROCHECK v3.3 (Laskowski et al., 1992, J Appl Crystallogr; 26:283-291). Остатки ENTPD2 человека, которые становятся менее доступными для растворителя при связывании с Fab MAB17 антитела к ENTPD2 человека, идентифицировали с помощью программы AREAIMOL из пакета программ CCP4 ("совместный вычислительный проект номер 4", 1994). Межмолекулярные контакты определяли с использованием расстояния отсечения 4,0 Å и идентифицировали с помощью программы NCONT CCP4.
Результаты
Кристаллическая структура комплекса FAb23 антитела к hENTPD2/ENTPD2
FAb23 антитела к hENTPD2 в комплексе с ENTPD2 человека с мутацией Y350A кристаллизовали в 96-луночных планшетах с помощью способа диффузии паров в сидячих каплях при 20°C. Кристаллы выращивали в 0,08 M Бис-Трис-пропана, pH 8,8, 0,02 M лимонной кислоты, 16% PEG 3350. Кристаллы появлялись спустя примерно 6 недель и вырастали до полного размера в течение нескольких дней.
Кристалл комплекса FAb23-ENTPD2 находился в пространственной группе P21 моноклинной сингонии с одним комплексом на асимметричную единицу. Полный набор дифракционных данных собирали для комплекса с разрешением до 2,0 ангстрема. Конечную модель FAb23 в комплексе с ENTPD2 уточняли с помощью AutoBuster с хорошими статистическими показателями уточнения и общими геометрическими параметрами. В конечной модели присутствовали в общей сложности четыре полных маргинальных остатка по карте Рамачандрана, при этом два остатка были из легкой цепи FAb23 (Ser39 и Thr50) и два из ENTPD2 (Thr122 и Ala430). Для Ser39 в легкой цепи Fab электронная плотность была недостаточной, и его моделировали по приблизительным расчетам. Все другие остатки были надлежащим образом определены с точки зрения электронной плотности и по всей вероятности являются подлинными полными маргинальными остатками по карте Рамачандрана. Остатки ENTPD2, не включенные в конечную модель, включают в себя остатки 29-34 на N-конце и остатки после 448 на C-конце. Остатки 139-144 в константной области цепи FAb23 и концевой цистеин (Cys227) также не были включены в конечную модель. Последние два остатка в легкой цепи FAb23 (Glu212 и Cys213) также отсутствовали в конечной модели ввиду неупорядоченности.
Аминокислотные последовательности тяжелой цепи и легкой цепи FAb23 антитела к ENTPD2 человека приведены на фиг. 3B с подчеркнутыми CDR (согласно определению по Kabat, 1991, Sequences of proteins of immunological interest, NIH Publication No. 91-3242) и остатками, расположенными в области контакта Fab и антигена, отмеченными как *. Общий вид трехмерной структуры комплекса FAb23/ENTPD2 Y350A изображен на фиг. 7.
В отличие от FAb22, связывание FAb23 с ENTPD2 предусматривает значительный контакт вариабельных доменов как тяжелой, так и легкой цепей как с мембранопроксимальной, так и с мембранодистальной долями. Вариабельная область тяжелой цепи образует CDR2- и CDR3-петли, участвующие в связывании с ENTPD2, при отсутствии вклада со стороны CDR1. В связывании с ENTPD2 участвуют остатки из всех трех 3 CDR вариабельной области легкой цепи. Контакты с мембранодистальной долей ENTPD2 обеспечиваются главным образом остатками из CDR3 тяжелой цепи, CDR2 легкой цепи и остатками из FR3 легкой цепи, связывающимися с остатками из петлевой области ENTPD2 между α13 и α14, а также взаимодействиями FR3 с антипараллельными тяжами β10/β11 и спиралью α9. Остатки CDR3 легкой цепи и CDR2 тяжелой цепи обеспечивают обширное связывание со спиралью α2 и остатками петли, соединяющей β3 и α1 мембранопроксимальной доли ENTPD2. Концевые остатки CDR3 тяжелой цепи Tyr104, Tyr105 и Gly106 выступают в щель активного центра ENTPD2 между N-концами спиралей α8, α11 и α14 мембранодистальной доли. Наложение аналога ATP AMP-PNP из связанной кристаллической структуры ENTPD2 крысы PDB 3CJA позволяет предположить, что Tyr105 располагается там, где согласно предсказанию будет связываться адениновое кольцо ATP, что потенциально обуславливает стерическое затруднение связывания с субстратом. Tyr105 и Tyr104 на конце CDR3 тяжелой цепи также могут вносить возмущение в остатки активного центра ENTPD2, в том числе Tyr350 и Arg394, необходимые для π-π- и катион-π-стэкинг-взаимодействий с адениновым кольцом ATP-субстрата. При связывании FAb23 с ENTPD2 вглубь погружается примерно 17500 Å2 совокупной поверхности, доступной для растворителя. Остатки эпитопа и паратопа, участвующие в непосредственных межмолекулярных контактах, рассчитанных в пределах расстояния отсечения 4,0 Å, перечислены в таблице 18 и отмечены на фиг. 3B и 4A. В непосредственных межмолекулярных контактах участвуют 25 остатков Fab и 29 остатков ENTPD2. Остатки тяжелой цепи Tyr55, Ile57, Thr59, Gln62 из CDR2, а также Phe102, Tyr105, Ile107, Tyr110 из CDR3 вносят вклад в связывание с ENTPD2 при отсутствии вклада со стороны остатков из CDR1. Остатки легкой цепи, которые вносят вклад в связывание с ENTPD2, включают в себя Ser27 и Tyr31 из CDR1, Ser49 и Asn52 из CDR2, а также Trp90, Ser91, Ser92, Tyr93 и Trp95 из CDR3. Остатки легкой цепи, не относящиеся к CDR, которые вносят вклад в связывание с ENTPD2, включают в себя Glu1, который наблюдается и моделируется в кристаллической структуре как пироглутамат, Thr22 из FR1, а также Ser64, Gly65, Ser66, Gly67, Thr68 и Phe69 из FR3.
Таблица 18. Остатки эпитопа и паратопа в FAb23/ENTPD2 человека
Пример 7. Кристаллографическое исследование и картирование эпитопов для FAb24 антитела к ENTPD2 мыши
В этом примере Fab антитела MAB13 к ENTPD2 мыши кристаллизовали в комплексе с эктодоменом ENTPD2 мыши, и определяли соответствующую структуру. Анализ связывания FAb24 антитела к ENTPD2 мыши с ENTPD2 мыши на основе рентгенографических данных позволяет получить подробную информацию о вступлении в контакт с антигеном на молекулярном уровне и понять природу выявленных паратопов Fab и антигенных эпитопов.
Материалы и способы
Получение комплекса ENTPD2 мыши и FAb24 антитела к ENTPD2 мыши
Для получения комплекса ENTPD2 мыши и FAb24 очищенный ENTPD2 мыши и FAb24 в 20 мМ Трис, pH 7,5, со 100 мМ NaCl объединяли в молярном соотношении 1:1, инкубировали на льду при 4 градусах Цельсия в течение ночи. На следующее утро образец концентрировали до 9,88 мг/мл путем ультрафильтрации и передавали для постановки испытаний по кристаллизации.
Кристаллизация и сбор рентгенографических данных
FAb24 антитела к ENTPD2 мыши в комплексе с ENTPD2 с мутацией Y350A кристаллизовали в 96-луночных планшетах (Greiner Bio-One) с помощью способа диффузии паров в сидячих каплях при 20°C. Подробно, 0,2 мкл исходного раствора белка смешивали с 0,2 мкл резервуарного раствора, и каплю уравновешивали против 50 мкл того же резервуарного раствора при 20°C. Эксперименты ставили с использованием роботизированной системы Phoenix (Art Robbins Instruments), и образцы хранили в специально сконструированном устройстве для визуализации кристаллов на опорной раме собственной разработки (Novartis GNF, системы для внутреннего пользования).
Для сбора рентгенографических данных один кристалл устанавливали непосредственно на криопетлю и подвергали мгновенному охлаждению в жидком азоте. Наборы рентгенографических данных собирали в SSRL в канале синхротронного излучения 7-1, оснащенном CCD-детектором ADSC Quantum 315r, с использованием рентгеновского излучения с длиной волны 1,1808 Å. 340 изображений с углом поворота в 0,5° для каждого регистрировали на расстоянии от кристалла до детектора, составляющем 400 мм, и обрабатывали с помощью HKL2000 (Z. Otwinowski and W. Minor, "Processing of X-ray Diffraction Data Collected in Oscillation Mode", Methods in Enzymology, Volume 276: Macromolecular Crystallography, part A, p.307-326, 1997, C.W. Carter, Jr. & R. M. Sweet, Eds., Academic Press (New York).
Определение и анализ структуры
Структуру комплекса FAb24-ENTPD2 мыши определяли посредством молекулярного замещения с помощью программы Phaser (McCoy et al., 2007, J Appl Crystallogr 40:658-674) с использованием уточненных структур ENTPD2 мыши и FAb24, ранее определенных в собственной лаборатории, в качестве независимых поисковых моделей. Структуру уточняли с помощью итерационных циклов построения модели с последующим автоматическим кристаллографическим уточнением с помощью программ Coot 0.8.0 ("набор кристаллографических объектно-ориентированных инструментов"; Emsley et al., 2010, Acta Crystallogr Sect D: Biol Crystallogr; 66:486-501) и AutoBuster 2.11.5 (Bricogne et al., 2011, BUSTER версии 2.11.2. Кембридж, Великобритания: Global Phasing Ltd.).
Визуальный осмотр кристаллической структуры осуществляли с помощью программ Coot (Emsley et al., 2010, Acta Crystallogr Sect D: Biol Crystallogr; 66:486-501) и PyMOL (молекулярно-графическая система; DeLano Scientific: Пало-Альто, Калифорния). Качество конечных уточненных моделей оценивали с помощью программ Coot и PROCHECK v3.3 (Laskowski et al., 1992, J Appl Crystallogr; 26:283-291). Остатки ENTPD2 мыши, которые становятся менее доступными для растворителя при связывании с FAb24 антитела к ENTPD2 мыши, идентифицировали с помощью программы AREAIMOL из пакета программ CCP4 ("совместный вычислительный проект номер 4", 1994). Межмолекулярные контакты определяли с использованием расстояния отсечения 4,0 Å и идентифицировали с помощью программы NCONT CCP4.
Структуру комплекса FAb24-ENTPD2 мыши определяли посредством молекулярного замещения с помощью программы Phaser (McCoy et al., 2007, J Appl Crystallogr 40:658-674) с использованием уточненных структур ENTPD2 мыши и FAb24, ранее определенных в собственной лаборатории, в качестве независимых поисковых моделей. Структуру уточняли с помощью итерационных циклов построения модели с последующим автоматическим кристаллографическим уточнением с помощью программ Coot 0.8.0 ("набор кристаллографических объектно-ориентированных инструментов"; Emsley et al., 2010, Acta Crystallogr Sect D: Biol Crystallogr; 66:486-501) и AutoBuster 2.11.5 (Bricogne et al., 2011, BUSTER версии 2.11.2. Кембридж, Великобритания: Global Phasing Ltd.).
Результаты
Кристаллическая структура комплекса FAb24 антитела к ENTPD2 мыши/ENTPD2 мыши
FAb24 антитела к ENTPD2 мыши в комплексе с ENTPD2 мыши кристаллизовали в 96-луночных планшетах с помощью способа диффузии паров в сидячих каплях при 20°C. Кристаллы выращивали в 0,2 M цитрата триаммония, pH 7,0, 20% PEG 3350. Кристаллы появлялись спустя примерно 1 месяц и вырастали до полного размера в течение нескольких дней.
Кристалл комплекса FAb24-ENTPD2 мыши находился в пространственной группе P21 моноклинной сингонии с одним комплексом на асимметричную единицу. Полный набор дифракционных данных собирали для комплекса с разрешением до 3,0 ангстрема. Конечную модель FAb24 в комплексе с ENTPD2 мыши уточняли с помощью AutoBuster с хорошими статистическими показателями уточнения и общими геометрическими параметрами. В конечной модели присутствовали два полных маргинальных остатка по карте Рамачандрана - Thr122 в ENTPD2 мыши и Ala57 в FAb24, оба из которых были четко определены с точки зрения электронной плотности. Asn129 и Asn378 были единственными остатками, в которых наблюдалось N-связанное гликозилирование. Glu1 в тяжелой цепи FAb24 наблюдался и моделировался как пироглутамат. Остатки ENTPD2 мыши, не включенные в конечную модель, включают в себя остатки 29-35 на N-конце, остатки 61-66, соответствующие остаткам петли, соединяющей тяжи β2 и β3, остатки 182-194, соответствующие петле, взаимодействующей с мембраной (MIL), остатки петли 290-293 между α9 и β11 и C-концевые остатки после Ala450. В конечную уточненную модель были включены все остатки тяжелой и легкой цепей FAb24, за исключением концевого цистеина Cys225 в тяжелой цепи.
Аминокислотные последовательности тяжелой и легкой цепей FAb24 антитела к ENTPD2 мыши приведены на фиг. 3C с подчеркнутыми CDR (согласно определению по Kabat, 1991, Sequences of proteins of immunological interest, NIH Publication No. 91-3242) и остатками, расположенными в области контакта Fab и антигена, отмеченными как *. Общий вид трехмерной структуры комплекса FAb24/mENTPD2 изображен на фиг. 8.
FAb24 антитела к ENTPD2 мыши вступает в контакт преимущественно с предполагаемой мембранодистальной долей (остатками G162-E426) антигена ENTPD2. Для остатков CDR вариабельных доменов тяжелой цепи и легкой цепи наблюдается равный вклад в связывание с ENTPD2.
По сравнению с FAb22 и FAb23, связывающимися с ENTPD2 человека, FAb24 вступает в контакт с ENTPD2 мыши в совершенно другом направлении, перпендикулярном наблюдаемому в комплексах FAb22 и FAb23 с hENTPD2. FAb24 связывается преимущественно с мембранодистальной долей ENTPD2 мыши посредством обширных взаимодействий CDR тяжелой цепи и относительно немногочисленных взаимодействий CDR легкой цепи. Остатки CDR1 и CDR3 тяжелой цепи совместно с остатками CDR1 и CDR2 легкой цепи связываются со спиралями α11 и α13 в mENTPD2. Остатки CDR2 тяжелой цепи вступают во взаимодействия с остатками взаимосоединяющей петли между α13 и α14. CDR3 тяжелой цепи наблюдается в конформации, при которой она изогнута под углом почти в 90 градусов и содержит короткий мотив в виде β-изгиба на своем конце. В единственные контакты с проксимальной долей ENTPD2 мыши вступают два остатка FR3 тяжелой цепи посредством взаимодействий с β3 5-тяжевого антипараллельного складчатого слоя. В антителе MAB13 не наблюдаются CDR, проходящие в активный центр ENTPD2 достаточно далеко, чтобы влиять на активность гидролиза ATP посредством прямого затруднения функции субстратсвязывающего центра. При связывании FAb24 с ENTPD2 мыши вглубь погружается примерно 16300 Å2 общей совокупной поверхности, доступной для растворителя. Остатки эпитопа и паратопа, участвующие в непосредственных межмолекулярных контактах, рассчитанных в пределах расстояния отсечения 4,0 Å, перечислены в таблице 19 и отмечены на фиг. 3C и 4B. В непосредственных межмолекулярных контактах участвуют 22 остатка Fab и 18 остатков ENTPD2 мыши, которые образуют паратоп и эпитоп, наблюдаемые при вступлении в контакт Fab и ENTPD2. Остатки CDR тяжелой цепи включают в себя Thr28, Thr30, His31, Tyr32 и Gly33 в CDR1; Trp50, Asn52, Thr53, а также Asp54, Thr55 в CDR2; Tyr99, Gly100, Thr101, Leu102, Tyr103 и Phe110 в CDR3. Два остатка Thr74 и Ser75 из FR3 тяжелой цепи также вносят вклад в связывание. Остатки CDR легкой цепи, которые вносят вклад в связывание, включают в себя Thr34 и Lys36 из CDR1, Tyr56 из CDR2, а также Trp97 из CDR3.
Таблица 19. Остатки эпитопа и паратопа в FAB24/ENTPD2 мыши
Thr101H, Leu102H, Tyr103H
H-CDR3
Thr101H, Tyr103H
H-CDR3
Lys36L
Tyr56L
L-CDR1
L-CDR2
Trp97L
L-CDR3
Trp50H, Asn52H, Thr53H, Asp54H
H-CDR2
Пример 8. Ингибирование роста опухоли с помощью антитела MAB13 к ENTPD2 в комбинации с Ab к PD-1 в сингенной модели опухоли из клеток B16LM3
Модель из клеток B16LM3 формировали у самок мышей C57BL/6 посредством подкожной инъекции 0,5 × 106 клеток в правый бок каждой мыши. Через день после имплантации мышей рандомизировали в группы обработки (n=10 на группу). Мыши получали обработку с помощью антитела mAb13 к ENTPD2 мыши либо неспецифичного изотипического контроля mIgG2a (клон MOPC-173, BioLegend, Сан-Диего, Калифорния) в конечной дозе 15 мг/кг в дни 1, 5, 8, 12, 15.
Ab к PD-1 (клон RMP1-14, Bio X Cell, Вест-Лебанон, Нью-Гэмпшир) или неспецифичный изотипический контроль rIgG2a (клон RTK2758, BioLegend, Сан-Диего, Калифорния) доставлялся i.p. в конечной дозе 10 мг/кг в дни 1, 5, 8, 12, 15. Все дозы корректировали в соответствии с индивидуальной массой тела мышей.
Все тестируемые средства хорошо переносились на протяжении исследования, и выраженные клинические симптомы токсичности или потери массы тела не наблюдались ни в одной из групп обработки. Комбинация обработки с помощью антитела mAb13 к ENTPD2 мыши и Ab к PD-1 значимо продлевала выживаемость мышей по сравнению с отсутствием обработки (p < 0,005), изотипическим контролем (p < 0,05) или Ab к PD-1 (p < 0,01) (для определения того, значимо ли различались кривые выживаемости, использовали логарифмический ранговый критерий (Кокса-Мантеля)) (фиг. 9).
Пример 9. Комбинированная обработка с помощью антитела mAb13 к ENTPD2 и Ab к PD-1 в сингенной модели опухоли B16F10 индуцирует приток активированных T-клеток в опухоль
Модель B16F10 формировали у самок мышей C57BL/6 посредством подкожной инъекции 0,5 × 106 клеток в правый бок каждой мыши. В день 7, после того как опухоли достигали примерно 30 мм3, мышей рандомизировали в соответствии с объемом опухоли в группы обработки (n=10 на группу). Мыши получали обработку с помощью антитела mAb13 к ENTPD2 мыши в конечной дозе 15 мг/кг, Ab к PD-1 (клон RMP1-14, Bio X Cell, Вест-Лебанон, Нью-Гэмпшир) i.p. в конечной дозе 10 мг/кг либо комбинацию обоих видов обработки в дни 1, 5 и 8. Все дозы корректировали в соответствии с индивидуальной массой тела мышей.
После обработки с помощью антитела mAb13 к ENTPD2 мыши или Ab к PD-1 в отдельности не наблюдалась значимая противоопухолевая эффективность, однако в группе, получавшей комбинацию антитела mAb13 к ENTPD2 мыши и Ab к PD-1, наблюдалось значимое снижение интенсивности роста опухоли по сравнению с контролем без обработки (p < 0,05, однофакторный ANOVA/критерий Тьюки для множественных сравнений) (фиг. 10A-10B).
Для того, чтобы понять влияние видов обработки на микроокружение опухоли, мышей подвергали эвтаназии в день 8, и опухоли диссоциировали в среде HyClone RPMI1640 (GE Healthcare, Питтсбург, Пенсильвания) с использованием пробирок gentleMACS C (Miltenyi Biotec, Оберн, Калифорния) на диссоциаторе gentleMACS Octo (Miltenyi Biotec, Оберн, Калифорния). Примерно 2 × 106 диссоциированных опухолевых клеток блокировали с помощью Ab крысы к CD16/CD32 мыши (Biolegend, Сан-Диего, Калифорния) для снижения неспецифичного связывания с FcγRIII/II и затем окрашивали с помощью следующего коктейля Ab: антитело крысы к CD45 мыши, конъюгированное с BUV395 (клон 30-F11) (BD Biosciences, Сан-Хосе, Калифорния), антитело крысы к CD8a мыши, конъюгированное с BUV737 (клон 53-6.7) (BD Biosciences, Сан-Хосе, Калифорния), антитело крысы к CD4 мыши, конъюгированное с BV510 (клон RM4-5) (BD Bioscience, Сан-Хосе, Калифорния), антитело к CD69 мыши, конъюгированное с PercPCy5.5 (клон H1-2F3) (Biolegend, Сан-Диего, Калифорния), и антитело крысы к CD25 мыши, конъюгированное с eFluor450 (клон eBio3C7) (eBioscience, Сан-Диего, Калифорния), в разведениях согласно рекомендациям производителя. Все процедуры инкубирования и промывания проводили в буфере для FACS, состоящем из 1x фосфатно-солевого буферного раствора HyClone (GE Healthcare, Питтсбург, Пенсильвания), 1% фетальной бычьей сыворотки крови HyClone (GE Healthcare, Питтсбург, Пенсильвания), 2 мМ EDTA (ThermoFisher, Уолтем, Массачусетс). После окрашивания с помощью коктейля антител к антигенам клеточной поверхности диссоциированные опухолевые клетки промывали в буфере для FACS, фиксировали и пермеабилизировали с помощью набора буферов для окрашивания Foxp3/факторов транскрипции eBioscience (ThermoFisher, Уолтем, Массачусетс) для обеспечения возможности внутриклеточного окрашивания с помощью антитела мыши к FOXP3 мыши, конъюгированного с eFluor660 (клон 150D/E4) (eBioscience, Сан-Диего, Калифорния).
При использовании комбинированной обработки с помощью антитела mAb13 к ENTPD2 мыши и Ab к PD-1 наблюдался значительный приток активированных CD4+ T-клеток-хелперов (определенных как CD45+ CD8- CD4+ FOXP3- CD69+ CD25+) (7,0-кратное увеличение по сравнению с отсутствием обработки, p < 0,0001, однофакторный ANOVA/критерий Тьюки для множественных сравнений) и CD8+ T-клеток (определенных как CD45+ CD4- CD8+ CD69+ CD25+) (5,8-кратное изменение по сравнению с отсутствием обработки, p < 0,05, однофакторный ANOVA/критерий Тьюки для множественных сравнений) по сравнению со всеми другими группами обработки (фиг. 10C).
Пример 10. Дозозависимая эффективность антител mAb1 и mAb6 к ENTPD2 человека в комбинации с Ab к PD-1 in vivo в ксенотрансплантатной модели из клеток B16LM3, сконструированной для экспрессии ENTPD2 человека, на мышах C57BL/6
Чтобы продемонстрировать целенаправленную противоопухолевую активность Ab к ENTPD2 человека in vivo, была разработана модель из клеток B16LM3 клона 5, сконструированная для экспрессии ENTPD2 человека. Эта модель была получена из модели меланомы из клеток B16LM3, где был осуществлен нокаут эндогенной экспрессии ENTPD2 мыши посредством введения белка CAS9 с последовательностями направляющей РНК CRISPR, направленных на ENTPD2 мыши, путем транзиентной электропорации, а сверхэкспрессия белка ENTPD2 человека обеспечивалась с помощью подхода ретровирусной трансдукции. Экспрессию ENTPD2 человека в модели подтверждали in vitro с помощью FACS с использованием антитела mAb17 к ENTPD2 человека, избирательно воздействующего на ENTPD2 человека. Для демонстрации полного нокаута эндогенного ENTPD2 мыши использовали антитело mAb13 к ENTPD2 мыши, избирательно воздействующее на ENTPD2 мыши (фиг. 11A). Модель из клеток B16LM3 клона B5 демонстрировала кинетические характеристики роста, сравнимые с исходной линией, и устойчивую экспрессию ENTPD2 человека у сингенного хозяина (фиг. 11B).
Модель из клеток B16LM3 клона B5, сконструированную для экспрессии ENTPD2 человека, формировали у самок мышей C57BL/6 посредством подкожной инъекции 0,5 × 106 клеток в правый бок каждой мыши. После того как опухоли достигали примерно 35-50 мм3, мышей рандомизировали в соответствии с объемом опухоли в группы обработки (n=8 на группу). Мыши получали обработку путем i.v. введения антитела mAb1 или mAb6 к ENTPD2 человека в конечной дозе 0,1, 1 или 10 мг/кг либо неспецифичного изотипического контроля IgG1 человека из расчета 10 мг/кг в день 1 исследования. Дозы Ab к PD-1 (клон RMP1-14, Bio X Cell, Вест-Лебанон, Нью-Гэмпшир) вводили i.p. при конечной дозе 10 мг/кг в D1 и D5. Все дозы корректировали в соответствии с индивидуальной массой тела мышей. Все тестируемые средства хорошо переносились на протяжении исследования, и выраженные клинические симптомы токсичности или потери массы тела не наблюдались ни в одной из групп обработки (таблица 23).
После обработки с помощью антитела mAb1 или mAb6 к ENTPD2 человека в качестве средств монотерапии или комбинации неспецифичного изотипического контроля и Ab к PD-1 не наблюдалась значимая противоопухолевая эффективность. Комбинированный режим применения антитела mAb1 к ENTPD2 человека и Ab к PD-1 (в фиксированной дозе 10 мг/кг) демонстрировал дозозависимый противоопухолевый эффект со значением ∆T/∆C, составляющим 18,4% (10 мг/кг), 35,7% (1 мг/кг) и 33,4% (0,1 мг/кг). Аналогичным образом, комбинированный режим применения антитела mAb6 к ENTPD2 человека и Ab к PD-1 (в фиксированной дозе 10 мг/кг) также демонстрировал дозозависимый противоопухолевый эффект со значением ∆T/∆C, составляющим 29,2% (10 мг/кг), 27,3% (1 мг/кг) и 41,0% (0,1 мг/кг) (таблица 23 и фиг. 12A-12B).
Таблица 23. Дозозависимая эффективность Ab к ENTPD2 человека в ксенотрансплантатной модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека, в день 7 обработки
при введении дозы в D1
при введении дозы в D1 и D5
при введении дозы в D1
при введении дозы в D1 и D5
при введении дозы в D1
при введении дозы в D1 и D5
при введении дозы в D1
при введении дозы в D1 и D5
при введении дозы в D1
при введении дозы в D1 и D5
при введении дозы в D1
при введении дозы в D1 и D5
при введении дозы в D1
при введении дозы в D1 и D5
при введении дозы в D1
при введении дозы в D1
Пример 11. Активность mAb к ENTPD2 человека в ксенотрансплантатной модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека, на мышах C57BL/6
Для того, чтобы понять непосредственное влияние блокады ENTPD2 с точки зрения задействования иммунных путей, у мышей C57BL/6 собирали плазму крови и опухоли из клеток B16LM3 клона B5 (средний объем опухоли ~ 170 мм3) через 24 ч. после обработки с помощью антитела mAb1 к ENTPD2 человека или изотипического контроля из расчета 10 мг/кг. Антитело mAb1 к ENTPD2 человека не характеризуется перекрестной реактивностью с ENTPD2 мыши, поэтому любое модулирование уровней цитокинов в периферических отделах будет отражать изменения в микроокружении опухоли.
Вкратце, плазму крови выделяли посредством сбора крови в пробирку с литий-гепарином для сбора крови и получения плазмы крови Microvette MV-H-300 (SAI Infusion Technologies, Лейк-Вилла, Иллинойс) и ее осаждения путем центрифугирования при 1000-2000 × g в течение 10 мин. Образцы плазмы крови хранили при -80°C до применения. Образцы опухолей иссекали хирургическим путем и подвергали мгновенной заморозке в жидком азоте. Опухолевую ткань затем гомогенизировали в реагенте для экстракции белков из тканей T-PER (ThermoFisher, Уолтем, Массачусетс) с помощью прибора TissueLyser (Qiagen, Германия). Образцы лизатов опухолей осаждали путем центрифугирования при 11000 об./мин в течение 15 мин, и образцы надосадочной жидкости собирали для анализа концентрации белков с помощью набора для анализа белков с BCA Pierce (ThermoFisher, Уолтем, Массачусетс). 200 мкг белка или 25 мкл неразбавленной плазмы крови использовали для анализа цитокинов с помощью набора для 29-плексного анализа мышиных цитокинов V-PLEX (MSD, Роквилл, Мэриленд) согласно рекомендациям производителя.
При использовании обработки с помощью антитела mAb1 к ENTPD2 человека наблюдалось значительное уменьшение уровня MCP1 в плазме крови (p < 0,05, непарный t-критерий), сопровождающееся примерно 2-кратным увеличением уровня MCP1 в очаге опухоли (фиг. 13B и 13D), что потенциально отражает задействование миелоидных клеток и привлечение их в очаг опухоли. Кроме того, наблюдались примерно 2-кратное уменьшение уровня IL-1β в плазме крови от животных, обработанных антителом mAb1 к ENTPD2 человека (p=0,05, непарный t-критерий) и тенденция, позволяющая предположить параллельное снижение в очаге опухоли (фиг. 13A и 13C).
Пример 12. Активность mAb к ENTPD2 человека в комбинации с антагонистом A2AR в ксенотрансплантатной модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека, на мышах C57BL/6
Модель из клеток B16LM3 клона B5, сконструированную для экспрессии ENTPD2 человека, формировали у самок мышей C57BL/6 посредством подкожной инъекции 0,5 × 106 клеток в правый бок каждой мыши. После того как опухоли достигали примерно 50 мм3, мышей рандомизировали в соответствии с объемом опухоли в группы обработки (n=8 на группу). Мыши получали обработку путем внутривенного (i.v.) введения антитела mAb1 к ENTPD2 в конечной дозе 10 мг/кг либо неспецифичного изотипического контроля IgG1 человека из расчета 10 мг/кг в день 1 исследования. NIR178 вводили перорально (p.o.) с 4 днями приема и 3 днями без приема, начиная в начале исследования из расчета 50 мг/кг либо 200 мг/кг. Все дозы корректировали в соответствии с индивидуальной массой тела мышей. Исследование осуществляли в течение тринадцати дней после начала лечения, и объемы опухолей оценивали один раз в два дня для оценки эффективности. Все тестируемые средства хорошо переносились на протяжении исследования, и выраженные клинические симптомы токсичности или потери массы тела не наблюдались ни в одной из групп обработки (таблица 27).
Таблица 27. Эффективность Ab к ENTPD2 человека и антагониста A2AR in vivo в ксенотрансплантатной модели из клеток B16LM3 клона B5, сконструированной для экспрессии ENTPD2 человека, в день 13 обработки
при введении дозы в D1
при введении дозы в D1
4 дня приема/3 дня без приема
при введении дозы в D1
4 дня приема/3 дня без приема
при введении дозы в D1
4 дня приема/3 дня без приема
После обработки с помощью комбинации неспецифичного изотипического контроля и антагониста A2AR NIR178 из расчета 50 либо 200 мг/кг не наблюдалась значимая противоопухолевая эффективность. Комбинированный режим применения антитела mAb1 к ENTPD2 (10 мг/кг) и NIR178 (50 мг/кг) демонстрировал противоопухолевый эффект со значением ∆T/∆C, составляющим 61,6% (таблица 27 и фиг. 14). Эти данные позволяют предположить, что при блокировании нескольких узлов аденозинового сигнального пути имеет место повышенная противоопухолевая эффективность.
Пример 13. Оценка Ab к ENTPD2 в биохимических и клеточных функциональных анализах
Биохимические и клеточные функциональные анализы разрабатывали в собственной лаборатории, чтобы понять функциональное влияние Ab к ENTPD2, направленного на очищенный внеклеточный домен ENTPD2 (остатки 29-462), а также на полностью интактный белок в случае с нативной клеточной конформацией. ENTPD2 гидролизует ATP до ADP, который затем можно выявить с помощью анализа ADP2 Transcreener методом TR-FRET HTRF в красной области спектра (BellBrook Labs, Мэдисон, Висконсин), где ADP, продуцируемый под действием ENTPD2, будет конкурировать с ADP, меченным радиоактивным изотопом, за связывание с антителом к ADP, конъюгированным с Tb. Образующийся в результате сигнал обратно пропорционален концентрации ADP в образце.
Для оценивания активности Ab к ENTPD2 в биохимическом анализе ENTPD2 Ab к ENTPD2 и рекомбинантный ENTPD2 (остатки 29-462) разбавляли в реакционном буфере (50 мМ HEPES, pH 7,1, 10 мМ MgCl2, 0,01% BSA) до необходимой концентрации. 4 мкл на лунку раствора ENTPD2 и 2 мкл на лунку раствора Ab к ENTPD2 переносили в ProxiPlate (PerkinElmer, Уолтем, Массачусетс) и инкубировали в течение 30 мин при комнатной температуре. Затем инициировали реакцию посредством добавления 2 мкл ATP (конечная концентрация в анализе 1 мкМ), и образец инкубировали в течение 25 мин при комнатной температуре. Реакцию гасили с помощью 200 мМ EDTA/200 мМ EGTA (5 мкл на лунку), и в лунки добавляли реагенты для выявления (5 мкл на лунку) при конечной концентрации 4 нМ антитела ADP2 и 4 нМ ADP, меченного радиоактивным изотопом, в лунке (BellBrook Labs, Мэдисон, Висконсин). Планшет затем инкубировали при комнатной температуре в течение 60 мин перед измерением сигнала HTRF.
Для осуществления клеточных функциональных анализов клетки NIH/3T3, сконструированные для экспрессии ENTPD2 человека/макака-крабоеда/мыши, или раковые клетки ободочной и прямой кишки RKO (ATCC, Манассас, Виргиния) с эндогенной экспрессией ENTPD2 высевали в течение ночи из расчета 150, 200 и 250 клеток на лунку для линий NIH/3T3, экспрессирующих соответственно ENTPD2 мыши, макака-крабоеда и человека, или 1000 клеток на лунку для RKO в 384-луночный планшет для культивирования тканей в 30 мкл на лунку (Perkin Elmer, Уолтем, Массачусетс). На следующий день клетки предварительно инкубировали с Ab к ENTPD2 дозозависимым образом в течение 60 мин при 37ºC, 5% CO2 (10 мкл 5X дозы антитела на лунку) и затем стимулировали с помощью ATP в конечной концентрации 10 мкМ (Teknova, Холлистер, Калифорния) в течение 20 минут при комнатной температуре (10 мкл 5X (50 мкМ) ATP на лунку). Реакции гасили с помощью 40 мМ EDTA/40 мМ EGTA по 25 мкл на лунку, и 15 мкл погашенной среды переносили в малообъемные планшеты ProxiPlate (PerkinElmer, Уолтем, Массачусетс) для выявления ADP. Продуцирование ADP выявляли с помощью анализа ADP2 Transcreener методом TR-FRET в красной области спектра (BellBrook Labs, Мэдисон, Висконсин) при конечной концентрации 4 нМ антитела ADP2 и 13,4 нМ ADP, меченного радиоактивным изотопом, в лунках (получали 4X раствор, и к погашенной кондиционированной среде добавляли 5 мкл "смеси реагентов для выявления"). Планшеты инкубировали с реагентами для выявления в течение 1 часа при комнатной температуре перед прочитыванием планшетов в режиме HTRF.
Сигнал HTRF (испускание при 620 нм и 665 нм) оценивали в обоих анализах с использованием планшет-ридера Envision в режиме HTRF (Perkin Elmer, Уолтем, Массачусетс). Коэффициент HTRF определяли с помощью следующей формулы: Коэффициент HTRF=R=испускание при 665 нм/испускание при 620 нм × 10000. Затем определяли % остаточной активности и % ингибирования следующим образом: 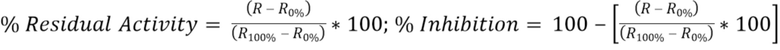 .
.
При этом R0% представляет собой коэффициент HTRF для отрицательного контроля (0% активность фермента), а R100% представляет собой коэффициент HTRF для положительного контроля (100% активность фермента). Данные анализировали в Microsoft Excel и представляли на графике с помощью программного обеспечения GraphPad Prism 7.0, и значения IC50 получали с помощью (четырехпараметрического) анализа зависимости ответа от log (концентрации агониста) методом нелинейной регрессии с переменным угловым коэффициентом.
Иллюстративная активность Ab к ENTPD2 в биохимическом функциональном анализе ENTPD2 человека
Ab к ENTPD2, полученные в рамках мероприятий по гибридомной и фаг-дисплейной технологии, сортировали по функциональной активности в биохимическом анализе ENTPD2 человека. Иллюстративная активность Ab к ENTPD2 и их IC50 показаны на фиг. 15 и в таблице 28. Для ряда Ab наблюдался определенный спектр форм активности, при этом некоторые из них проявляли весьма сильную активность в анализе с субнаномолярной IC50 и полное ингибирование мишени, хотя другие при этом демонстрировали намного более слабую активность и лишь частичное ингибирование фермента (данные не показаны).
Таблица 28. Профили активности Ab к ENTPD2 в биохимическом функциональном анализе ENTPD2 человека in vitro
IC50 (нМ)
Активность Ab к ENTPD2 в клеточных функциональных анализах ENTPD2 человека и макака-крабоеда
При первоначальном профилировании Ab в биохимическом анализе ENPTD2 был идентифицирован ряд активных хитов с сильной ингибирующей активностью в отношении рекомбинантного внеклеточного домена ENTPD2, однако для подгруппы Ab наблюдались неодинаковые профили поведения в биохимических и клеточных функциональных анализах, что позволяет предположить, что между очищенным рекомбинантным белком и нативной клеточной конформацией могут существовать конформационные отличия (данные не показаны). С целью подтверждения сильной активности Ab в отношении нативного ENTPD2 Ab к ENTPD2 профилировали по ингибирующей активности с использованием клеток NIH/3T3, сконструированных для экспрессии ENTPD2 человека или макака-крабоеда, или линии клеток RKO с эндогенной экспрессией ENTPD2. Сводные данные профилей активности Ab к ENTPD2 в различных анализах с использованием клеток NIH/3T3, экспрессирующих ENTPD2 человека или макака-крабоеда, или клеток RKO зафиксированы в таблице 29. Иллюстративные графики, на которых изображена сильная активность для подгруппы Ab к ENTPD2 во всех трех функциональных анализах, показаны на фиг. 16.
Таблица 29. Профили активности Ab, избирательно воздействующих на ENTPD2, в анализах с использованием клеток NIH/3T3, экспрессирующих ENTPD2 человека или макака-крабоеда, или клеток RKO in vitro
Пример 14. Структурно-управляемая инженерия позволила идентифицировать более активные суррогатные Ab к ENTPD2 мыши
Антитело mAb13 к ENTPD2 идентифицировали в качестве Ab, избирательно воздействующего на ENTPD2 мыши (EC50 составляет 3-4 нМ согласно FACS) при отсутствии связывания с ENTPD2 человека или макака-крабоеда. Активность антитела mAb13 к ENTPD2 оценивали с использованием линии клеток NIH3T3, сконструированной для экспрессии ENTPD2 мыши, где антитело mAb13 к ENTPD2 проявляло активность в качестве частичного ингибитора фермента с IC50, составляющей 2,8 нМ, и максимальным ингибированием мишени, составляющим 44%. При изучении кристаллической структуры комплекса Fab антитела mAb13 к ENTPD2/mENTPD2 и наложения аналога ATP-субстрата из rENTPD2 с кодом PDB 3CJA в активном центре mENTPD2 был выявлен T30 в CDR1 HC антитела mAb13 к ENTPD2 в качестве оптимального сайта, в котором согласно предсказанию замена более крупной аминокислотой будет приводить к стерическому блокированию связывания с ATP. Была сконструирована подгруппа конструкций с заменами в положении T30 CDR1 антитела mAb13 к ENTPD2, включающая антитела mAb14 и mAb15 к ENTPD2. Оценивание сконструированных вариантов антител mAb14 и mAb15 к ENTPD2 в функциональном анализе ENTPD2 мыши с использованием клеток NIH/3T3 продемонстрировало значительное улучшение ингибирования мишени по сравнению с исходным антителом mAb13 к ENTPD2 с достижением примерно 76-79% ингибирования ENTPD2 мыши при IC50, составляющей 5-6 нМ (таблица 30, фиг. 17).
Таблица 30. Профили активности Ab, избирательно воздействующих на ENTPD2 мыши, в клеточном функциональном анализе ENTPD2 мыши in vitro
при 100 нМ (± среднеквадратическая ошибка)
Если не указано иное, то технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понятно специалисту, хорошо знакомому с областью техники, к которой относится настоящее изобретение.
Если не указано иное, все способы, стадии, методики и манипуляции, которые конкретно не описаны подробно, могут выполняться и выполняются широко известным способом, как будет ясно специалисту в данной области. Например, вновь делается ссылка на стандартные руководства и общий уровень техники, упоминаемый в данном документе, и на дополнительные литературные источники, цитируемые в данном документе. Если не указано иное, каждый из литературных источников, цитируемых в данном документе, включен во всей своей полноте посредством ссылки.
Пункты формулы изобретения являются неограничивающими и приведены ниже.
Хотя конкретные аспекты и пункты формулы изобретения были подробно раскрыты в данном документе, это было выполнено в качестве примера лишь в целях иллюстрации и не предназначено для ограничений с точки зрения объема прилагаемой формулы изобретения или объема объекта формулы изобретения с любым соответствующим будущим применением. В частности, авторами настоящего изобретения предполагается, что различные замены, изменения и модификации могут быть выполнены по отношению к настоящему изобретению без отступления от сущности и объема настоящего изобретения, определенного формулой изобретения. Считается, что выбор исходного материала в виде нуклеиновой кислоты, клона, представляющего интерес, или типа библиотеки является привычным вопросом для специалиста обычной квалификации в данной области со знанием аспектов, описанных в данном документе. Считается, что другие аспекты, преимущества и модификации находятся в пределах объема нижеследующей формулы изобретения. Специалистам в данной области будут понятны многие эквиваленты конкретных аспектов настоящего изобретения, описанного в данном документе, или с помощью проведения только лишь обычных экспериментов они будут способны установить такие эквиваленты. Предполагается, что такие эквиваленты охватываются нижеследующей формулой изобретения. Изменение формулировки объема пункта формулы изобретения в позднее поданных соответствующих заявках может быть связано с ограничениями патентных законов различных стран и не должно пониматься как отказ от объекта формулы изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NOVARTIS AG
<120> АНТИТЕЛА К ENTPD2, ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ И СПОСОБЫ ПРИМЕНЕНИЯ
АНТИТЕЛ И ВИДОВ КОМБИНИРОВАННОЙ ТЕРАПИИ
<130> PAT058145-WO-PCT
<140>
<141>
<150> 62/677,850
<151> 2018-05-30
<160> 1015
<170> PatentIn версия 3.5
<210> 1
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1
Asp Tyr Asn Met Asp
1 5
<210> 2
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 2
Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe Lys
1 5 10 15
Gly
<210> 3
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 3
Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe Asp Val
1 5 10 15
<210> 4
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 4
Gly Tyr Thr Phe Thr Asp Tyr
1 5
<210> 5
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 5
Asn Pro Lys Tyr Asp Ile
1 5
<210> 6
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 6
Gly Tyr Thr Phe Thr Asp Tyr Asn Met Asp
1 5 10
<210> 7
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 7
Gly Tyr Thr Phe Thr Asp Tyr Asn
1 5
<210> 8
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 8
Ile Asn Pro Lys Tyr Asp Ile Ser
1 5
<210> 9
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 9
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
1 5 10 15
Asp Val
<210> 10
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 10
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Arg Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 11
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 11
gaagtgcagc tggtgcagtc tggcgccgaa gtgaagaagc ctggcgagtc cctgaagatc 60
tcctgcaagg cctccggcta caccttcacc gactacaaca tggactgggt gcgacagatg 120
cccggcaagg gcctggaatg gatgggcgac atcaacccta agtacgacat ctccacctac 180
aaccagcagt tcaagggcca agtgaccatc tccgccgaca agtccatccg gaccgcctac 240
ctgcagtggt cctccctgaa ggcctctgac accgccatgt actactgcgc cagacggggc 300
ttcttcctgt actacggcat caactactac tacttcgacg tgtggggcca gggcaccctc 360
gtgacagtgt catct 375
<210> 12
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 12
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Arg Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 13
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 13
gaagtgcagc tggtgcagtc tggcgccgaa gtgaagaagc ctggcgagtc cctgaagatc 60
tcctgcaagg cctccggcta caccttcacc gactacaaca tggactgggt gcgacagatg 120
cccggcaagg gcctggaatg gatgggcgac atcaacccta agtacgacat ctccacctac 180
aaccagcagt tcaagggcca agtgaccatc tccgccgaca agtccatccg gaccgcctac 240
ctgcagtggt cctccctgaa ggcctctgac accgccatgt actactgcgc cagacggggc 300
ttcttcctgt actacggcat caactactac tacttcgacg tgtggggcca gggcaccctc 360
gtgacagtgt catctgctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgcgacaag acccacacct gccccccctg cccagctcca 720
gaactgctgg gagggccttc cgtgttcctg ttccccccca agcccaagga caccctgatg 780
atcagcagga cccccgaggt gacctgcgtg gtggtggacg tgtcccacga ggacccagag 840
gtgaagttca actggtacgt ggacggcgtg gaggtgcaca acgccaagac caagcccaga 900
gaggagcagt acaacagcac ctacagggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagaata caagtgcaaa gtctccaaca aggccctgcc agccccaatc 1020
gaaaagacaa tcagcaaggc caagggccag ccacgggagc cccaggtgta caccctgccc 1080
cccagccggg aggagatgac caagaaccag gtgtccctga cctgtctggt gaagggcttc 1140
taccccagcg atatcgccgt ggagtgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc cagtgctgga cagcgacggc agcttcttcc tgtacagcaa gctgaccgtg 1260
gacaagtcca ggtggcagca gggcaacgtg ttcagctgca gcgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gcaag 1365
<210> 14
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 14
Ser Ala Ser Ser Ser Val Ser Tyr Ile His
1 5 10
<210> 15
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 15
Ser Thr Ser Asn Leu Ala Ser
1 5
<210> 16
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 16
His Gln Trp Ser Ser Tyr Pro Trp Thr
1 5
<210> 17
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 17
Ser Ser Ser Val Ser Tyr
1 5
<210> 18
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 18
Ser Thr Ser
1
<210> 19
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 19
Trp Ser Ser Tyr Pro Trp
1 5
<210> 20
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 20
Ser Ser Val Ser Tyr
1 5
<210> 21
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 21
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 22
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 22
gatatccagc tgacccagtc cccttccagc ctgtctgcct ctgtgggcga cagagtgaca 60
attacctgct ccgcctcctc ctccgtgtcc tacatccact ggttccagca gaagcccggc 120
aaggccccca agctgctgat ctactccacc tccaacctgg cctccggcgt gccctctaga 180
ttctccggct ctggctctgg cacctttttt accctgacca tctccagcct gcagcccgag 240
gacttcgcca cctacttttg ccaccagtgg tccagctacc cctggacctt tggccagggc 300
accaaggtgg aaatcaag 318
<210> 23
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 23
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 24
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 24
gatatccagc tgacccagtc cccttccagc ctgtctgcct ctgtgggcga cagagtgaca 60
attacctgct ccgcctcctc ctccgtgtcc tacatccact ggttccagca gaagcccggc 120
aaggccccca agctgctgat ctactccacc tccaacctgg cctccggcgt gccctctaga 180
ttctccggct ctggctctgg cacctttttt accctgacca tctccagcct gcagcccgag 240
gacttcgcca cctacttttg ccaccagtgg tccagctacc cctggacctt tggccagggc 300
accaaggtgg aaatcaagcg tacggtggcc gctcccagcg tgttcatctt cccccccagc 360
gacgagcagc tgaagagtgg caccgccagc gtggtgtgcc tgctgaacaa cttctacccc 420
cgggaggcca aggtgcagtg gaaggtggac aacgccctgc agagcggcaa cagccaggag 480
agcgtcaccg agcaggacag caaggactcc acctacagcc tgagcagcac cctgaccctg 540
agcaaggccg actacgagaa gcataaggtg tacgcctgcg aggtgaccca ccagggcctg 600
tccagccccg tgaccaagag cttcaacagg ggcgagtgc 639
<210> 25
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 25
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Lys Ala Thr Ile Thr Val Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 26
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 26
caggtgcagc tggtgcagtc tggcgccgag gtggtgaaac ctggcgcctc cgtgaagatc 60
tcctgcaagg cctccggcta caccttcacc gactacaaca tggactgggt gaaacaggcc 120
cctggccagc ggctggaatg gatcggcgac atcaacccta agtacgacat ctccacctac 180
aaccagcagt tcaagggcaa ggccaccatc accgtggaca agtccgcctc caccgcctac 240
atggaactgt cctccctgcg gagcgaggac accgccgtgt actactgcgc cagacggggc 300
ttcttcctgt actacggcat caactactac tacttcgacg tgtggggcca gggcaccctg 360
gtgacagtgt cctcc 375
<210> 27
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 27
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Lys Ala Thr Ile Thr Val Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 28
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 28
caggtgcagc tggtgcagtc tggcgccgag gtggtgaaac ctggcgcctc cgtgaagatc 60
tcctgcaagg cctccggcta caccttcacc gactacaaca tggactgggt gaaacaggcc 120
cctggccagc ggctggaatg gatcggcgac atcaacccta agtacgacat ctccacctac 180
aaccagcagt tcaagggcaa ggccaccatc accgtggaca agtccgcctc caccgcctac 240
atggaactgt cctccctgcg gagcgaggac accgccgtgt actactgcgc cagacggggc 300
ttcttcctgt actacggcat caactactac tacttcgacg tgtggggcca gggcaccctg 360
gtgacagtgt cctccgctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgcgacaag acccacacct gccccccctg cccagctcca 720
gaactgctgg gagggccttc cgtgttcctg ttccccccca agcccaagga caccctgatg 780
atcagcagga cccccgaggt gacctgcgtg gtggtggacg tgtcccacga ggacccagag 840
gtgaagttca actggtacgt ggacggcgtg gaggtgcaca acgccaagac caagcccaga 900
gaggagcagt acaacagcac ctacagggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagaata caagtgcaaa gtctccaaca aggccctgcc agccccaatc 1020
gaaaagacaa tcagcaaggc caagggccag ccacgggagc cccaggtgta caccctgccc 1080
cccagccggg aggagatgac caagaaccag gtgtccctga cctgtctggt gaagggcttc 1140
taccccagcg atatcgccgt ggagtgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc cagtgctgga cagcgacggc agcttcttcc tgtacagcaa gctgaccgtg 1260
gacaagtcca ggtggcagca gggcaacgtg ttcagctgca gcgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gcaag 1365
<210> 29
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 29
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Arg Ile Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Thr Leu Thr Ile Ser Ser Val Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 30
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 30
gagatcgtgc tgacccagtc ccctgccacc ctgtctgcca gccctggcga gcggatcacc 60
ctgtcctgct ccgcctcctc ctccgtgtcc tacatccact ggtatcagca gaagcccggc 120
caggcccctc ggctgctgat ctactccacc tccaacctgg cctccggcat ccctgccaga 180
ttctccggct ctggctccgg caccttttac accctgacca tctccagcgt ggaacccgag 240
gacgccgccg tgtactactg ccaccagtgg tccagctacc cctggacctt cggcggaggc 300
accaagctgg aaatcaag 318
<210> 31
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 31
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Arg Ile Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Thr Leu Thr Ile Ser Ser Val Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 32
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 32
gagatcgtgc tgacccagtc ccctgccacc ctgtctgcca gccctggcga gcggatcacc 60
ctgtcctgct ccgcctcctc ctccgtgtcc tacatccact ggtatcagca gaagcccggc 120
caggcccctc ggctgctgat ctactccacc tccaacctgg cctccggcat ccctgccaga 180
ttctccggct ctggctccgg caccttttac accctgacca tctccagcgt ggaacccgag 240
gacgccgccg tgtactactg ccaccagtgg tccagctacc cctggacctt cggcggaggc 300
accaagctgg aaatcaagcg tacggtggcc gctcccagcg tgttcatctt cccccccagc 360
gacgagcagc tgaagagtgg caccgccagc gtggtgtgcc tgctgaacaa cttctacccc 420
cgggaggcca aggtgcagtg gaaggtggac aacgccctgc agagcggcaa cagccaggag 480
agcgtcaccg agcaggacag caaggactcc acctacagcc tgagcagcac cctgaccctg 540
agcaaggccg actacgagaa gcataaggtg tacgcctgcg aggtgaccca ccagggcctg 600
tccagccccg tgaccaagag cttcaacagg ggcgagtgc 639
<210> 33
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 33
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Lys Ala Thr Ile Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 34
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 34
caggtgcagc tggtgcagtc tggcgccgag gtggtgaaac ctggcgcctc cgtgaagatc 60
tcctgcaagg cctccggcta caccttcacc gactacaaca tggactgggt gaaacaggcc 120
cctggccagc ggctggaatg gatcggcgac atcaacccta agtacgacat ctccacctac 180
aaccagcagt tcaagggcaa ggccaccatc accgtggaca cctccgcctc caccgcctac 240
atggaactgt cctccctgcg gagcgaggac accgccgtgt actactgcgc cagacggggc 300
ttcttcctgt actacggcat caactactac tacttcgacg tgtggggcca gggcaccctg 360
gtgacagtgt cctcc 375
<210> 35
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 35
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Lys Ala Thr Ile Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 36
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 36
caggtgcagc tggtgcagtc tggcgccgag gtggtgaaac ctggcgcctc cgtgaagatc 60
tcctgcaagg cctccggcta caccttcacc gactacaaca tggactgggt gaaacaggcc 120
cctggccagc ggctggaatg gatcggcgac atcaacccta agtacgacat ctccacctac 180
aaccagcagt tcaagggcaa ggccaccatc accgtggaca cctccgcctc caccgcctac 240
atggaactgt cctccctgcg gagcgaggac accgccgtgt actactgcgc cagacggggc 300
ttcttcctgt actacggcat caactactac tacttcgacg tgtggggcca gggcaccctg 360
gtgacagtgt cctccgctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgcgacaag acccacacct gccccccctg cccagctcca 720
gaactgctgg gagggccttc cgtgttcctg ttccccccca agcccaagga caccctgatg 780
atcagcagga cccccgaggt gacctgcgtg gtggtggacg tgtcccacga ggacccagag 840
gtgaagttca actggtacgt ggacggcgtg gaggtgcaca acgccaagac caagcccaga 900
gaggagcagt acaacagcac ctacagggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagaata caagtgcaaa gtctccaaca aggccctgcc agccccaatc 1020
gaaaagacaa tcagcaaggc caagggccag ccacgggagc cccaggtgta caccctgccc 1080
cccagccggg aggagatgac caagaaccag gtgtccctga cctgtctggt gaagggcttc 1140
taccccagcg atatcgccgt ggagtgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc cagtgctgga cagcgacggc agcttcttcc tgtacagcaa gctgaccgtg 1260
gacaagtcca ggtggcagca gggcaacgtg ttcagctgca gcgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gcaag 1365
<210> 37
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 37
Ser Gly Tyr Tyr Trp Asn
1 5
<210> 38
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 38
Tyr Ile Ser Tyr Asp Ala Asp Asn Asn Tyr Asn Pro Ser Leu Lys Asn
1 5 10 15
<210> 39
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 39
Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Arg Gly Ser Tyr Tyr Tyr
1 5 10 15
Val Met Asp Tyr
20
<210> 40
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 40
Gly Tyr Ser Ile Thr Ser Gly Tyr
1 5
<210> 41
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 41
Ser Tyr Asp Ala Asp
1 5
<210> 42
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 42
Gly Tyr Ser Ile Thr Ser Gly Tyr Tyr Trp Asn
1 5 10
<210> 43
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 43
Gly Tyr Ser Ile Thr Ser Gly Tyr Tyr
1 5
<210> 44
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 44
Ile Ser Tyr Asp Ala Asp Asn
1 5
<210> 45
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 45
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Arg Gly Ser Tyr
1 5 10 15
Tyr Tyr Val Met Asp Tyr
20
<210> 46
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 46
Gln Ile Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Asp Ala Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Arg Gly Ser Tyr
100 105 110
Tyr Tyr Val Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser
<210> 47
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 47
cagatccagc tgcaggaatc tggccctggc ctggtgaaac cctcccagac cctgtccctg 60
acctgcaccg tgtccggcta ctccatcacc tccggctact actggaactg gatccggcag 120
caccccggca agggcctgga atggatcggc tacatctcct acgacgctga caacaactac 180
aaccccagcc tgaagaacag agtgaccatc tcccgggaca cctccaagaa ccagttctcc 240
ctgaagctgt cctccgtgac cgccgctgac accgccgtgt actactgcgc tggcggctac 300
tacagatacg gcctgggctc ctaccggggc tcctactact acgtgatgga ctactggggc 360
cagggcacca ccgtgaccgt gtcctct 387
<210> 48
<211> 459
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 48
Gln Ile Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Asp Ala Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Arg Gly Ser Tyr
100 105 110
Tyr Tyr Val Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
130 135 140
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
145 150 155 160
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
165 170 175
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
180 185 190
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
195 200 205
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
210 215 220
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
225 230 235 240
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
245 250 255
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
260 265 270
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
275 280 285
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
290 295 300
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
305 310 315 320
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
325 330 335
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
340 345 350
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
355 360 365
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
370 375 380
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
385 390 395 400
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
405 410 415
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
420 425 430
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
435 440 445
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 49
<211> 1377
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 49
cagatccagc tgcaggaatc tggccctggc ctggtgaaac cctcccagac cctgtccctg 60
acctgcaccg tgtccggcta ctccatcacc tccggctact actggaactg gatccggcag 120
caccccggca agggcctgga atggatcggc tacatctcct acgacgctga caacaactac 180
aaccccagcc tgaagaacag agtgaccatc tcccgggaca cctccaagaa ccagttctcc 240
ctgaagctgt cctccgtgac cgccgctgac accgccgtgt actactgcgc tggcggctac 300
tacagatacg gcctgggctc ctaccggggc tcctactact acgtgatgga ctactggggc 360
cagggcacca ccgtgaccgt gtcctctgct agcaccaagg gcccaagtgt gtttcccctg 420
gcccccagca gcaagtctac ttccggcgga actgctgccc tgggttgcct ggtgaaggac 480
tacttccccg agcccgtgac agtgtcctgg aactctgggg ctctgacttc cggcgtgcac 540
accttccccg ccgtgctgca gagcagcggc ctgtacagcc tgagcagcgt ggtgacagtg 600
ccctccagct ctctgggaac ccagacctat atctgcaacg tgaaccacaa gcccagcaac 660
accaaggtgg acaagagagt ggagcccaag agctgcgaca agacccacac ctgccccccc 720
tgcccagctc cagaactgct gggagggcct tccgtgttcc tgttcccccc caagcccaag 780
gacaccctga tgatcagcag gacccccgag gtgacctgcg tggtggtgga cgtgtcccac 840
gaggacccag aggtgaagtt caactggtac gtggacggcg tggaggtgca caacgccaag 900
accaagccca gagaggagca gtacaacagc acctacaggg tggtgtccgt gctgaccgtg 960
ctgcaccagg actggctgaa cggcaaagaa tacaagtgca aagtctccaa caaggccctg 1020
ccagccccaa tcgaaaagac aatcagcaag gccaagggcc agccacggga gccccaggtg 1080
tacaccctgc cccccagccg ggaggagatg accaagaacc aggtgtccct gacctgtctg 1140
gtgaagggct tctaccccag cgatatcgcc gtggagtggg agagcaacgg ccagcccgag 1200
aacaactaca agaccacccc cccagtgctg gacagcgacg gcagcttctt cctgtacagc 1260
aagctgaccg tggacaagtc caggtggcag cagggcaacg tgttcagctg cagcgtgatg 1320
cacgaggccc tgcacaacca ctacacccag aagtccctga gcctgagccc cggcaag 1377
<210> 50
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 50
Lys Ala Ser Gln Ser Val Asp Tyr Glu Gly His Ser Tyr Met Asn
1 5 10 15
<210> 51
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 51
Ala Ala Ser Asn Leu Glu Ser
1 5
<210> 52
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 52
Gln Gln Ser Asn Glu Asp Pro Pro Thr
1 5
<210> 53
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 53
Ser Gln Ser Val Asp Tyr Glu Gly His Ser Tyr
1 5 10
<210> 54
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 54
Ala Ala Ser
1
<210> 55
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 55
Ser Asn Glu Asp Pro Pro
1 5
<210> 56
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 56
Gln Ser Val Asp Tyr Glu Gly His Ser Tyr
1 5 10
<210> 57
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 57
Glu Thr Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly His Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Val Glu Pro Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 58
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 58
gagacagtgc tgacccagtc ccctgccacc ctgtccgtgt ctcccggcga gagagccacc 60
atcagctgca aggcctccca gtccgtggac tacgaaggcc attcctacat gaactggtat 120
cagcagaagc ccggccaggc ccctcggctg ctgatctacg ccgcctccaa cctggaatcc 180
ggcatccctg cccggttctc cggctctggc tctggcaccg acttcaccct gaccatctcc 240
agcgtggaac ccgaggacgc cgccacctac tactgccagc agtccaacga ggaccccccc 300
accttcggcg gaggcaccaa gctggaaatc aag 333
<210> 59
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 59
Glu Thr Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly His Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Val Glu Pro Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 60
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 60
gagacagtgc tgacccagtc ccctgccacc ctgtccgtgt ctcccggcga gagagccacc 60
atcagctgca aggcctccca gtccgtggac tacgaaggcc attcctacat gaactggtat 120
cagcagaagc ccggccaggc ccctcggctg ctgatctacg ccgcctccaa cctggaatcc 180
ggcatccctg cccggttctc cggctctggc tctggcaccg acttcaccct gaccatctcc 240
agcgtggaac ccgaggacgc cgccacctac tactgccagc agtccaacga ggaccccccc 300
accttcggcg gaggcaccaa gctggaaatc aagcgtacgg tggccgctcc cagcgtgttc 360
atcttccccc ccagcgacga gcagctgaag agtggcaccg ccagcgtggt gtgcctgctg 420
aacaacttct acccccggga ggccaaggtg cagtggaagg tggacaacgc cctgcagagc 480
ggcaacagcc aggagagcgt caccgagcag gacagcaagg actccaccta cagcctgagc 540
agcaccctga ccctgagcaa ggccgactac gagaagcata aggtgtacgc ctgcgaggtg 600
acccaccagg gcctgtccag ccccgtgacc aagagcttca acaggggcga gtgc 654
<210> 61
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 61
Lys Ala Ser Gln Ser Val Asp Tyr Asp Gly Asn Ser Tyr Met Asn
1 5 10 15
<210> 62
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 62
Ser Gln Ser Val Asp Tyr Asp Gly Asn Ser Tyr
1 5 10
<210> 63
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 63
Gln Ser Val Asp Tyr Asp Gly Asn Ser Tyr
1 5 10
<210> 64
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 64
Glu Thr Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asn Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Val Glu Pro Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 65
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 65
gagacagtgc tgacccagtc ccctgccacc ctgtccgtgt ctcccggcga gagagccacc 60
atcagctgca aggcctccca gtccgtggac tacgacggca actcctacat gaactggtat 120
cagcagaagc ccggccaggc ccctcggctg ctgatctacg ccgcctccaa cctggaatcc 180
ggcatccctg cccggttctc cggctctggc tctggcaccg acttcaccct gaccatctcc 240
agcgtggaac ccgaggacgc cgccacctac tactgccagc agtccaacga ggaccccccc 300
accttcggcg gaggcaccaa gctggaaatc aag 333
<210> 66
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 66
Glu Thr Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asn Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Val Glu Pro Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 67
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 67
gagacagtgc tgacccagtc ccctgccacc ctgtccgtgt ctcccggcga gagagccacc 60
atcagctgca aggcctccca gtccgtggac tacgacggca actcctacat gaactggtat 120
cagcagaagc ccggccaggc ccctcggctg ctgatctacg ccgcctccaa cctggaatcc 180
ggcatccctg cccggttctc cggctctggc tctggcaccg acttcaccct gaccatctcc 240
agcgtggaac ccgaggacgc cgccacctac tactgccagc agtccaacga ggaccccccc 300
accttcggcg gaggcaccaa gctggaaatc aagcgtacgg tggccgctcc cagcgtgttc 360
atcttccccc ccagcgacga gcagctgaag agtggcaccg ccagcgtggt gtgcctgctg 420
aacaacttct acccccggga ggccaaggtg cagtggaagg tggacaacgc cctgcagagc 480
ggcaacagcc aggagagcgt caccgagcag gacagcaagg actccaccta cagcctgagc 540
agcaccctga ccctgagcaa ggccgactac gagaagcata aggtgtacgc ctgcgaggtg 600
acccaccagg gcctgtccag ccccgtgacc aagagcttca acaggggcga gtgc 654
<210> 68
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 68
Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Ser Gly Ser Tyr Tyr Tyr
1 5 10 15
Val Met Asp Tyr
20
<210> 69
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 69
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Ser Gly Ser Tyr
1 5 10 15
Tyr Tyr Val Met Asp Tyr
20
<210> 70
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 70
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Tyr Asp Ala Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Ser Gly Ser Tyr
100 105 110
Tyr Tyr Val Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser
<210> 71
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 71
caggtgcagc tgcaggaatc tggccctggc ctggtgaaac cctcccagac cctgtccctg 60
acctgcaccg tgtccggcta ctccatcacc tccggctact actggaactg gatccggcag 120
caccccggca agggcctgga atggatgggc tacatctcct acgacgctga caacaactac 180
aaccccagcc tgaagaacag aatcaccatc tcccgggaca cctccaagaa ccagttctcc 240
ctgaagctgt cctccgtgac cgccgctgac accgccgtgt actactgcgc tggcggctac 300
tacagatacg gcctgggctc ctactccggc tcctactact acgtgatgga ctactggggc 360
cagggcacca ccgtgaccgt gtcctct 387
<210> 72
<211> 459
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 72
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Tyr Asp Ala Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Ser Gly Ser Tyr
100 105 110
Tyr Tyr Val Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
130 135 140
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
145 150 155 160
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
165 170 175
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
180 185 190
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
195 200 205
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
210 215 220
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
225 230 235 240
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
245 250 255
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
260 265 270
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
275 280 285
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
290 295 300
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
305 310 315 320
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
325 330 335
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
340 345 350
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
355 360 365
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
370 375 380
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
385 390 395 400
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
405 410 415
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
420 425 430
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
435 440 445
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 73
<211> 1377
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 73
caggtgcagc tgcaggaatc tggccctggc ctggtgaaac cctcccagac cctgtccctg 60
acctgcaccg tgtccggcta ctccatcacc tccggctact actggaactg gatccggcag 120
caccccggca agggcctgga atggatgggc tacatctcct acgacgctga caacaactac 180
aaccccagcc tgaagaacag aatcaccatc tcccgggaca cctccaagaa ccagttctcc 240
ctgaagctgt cctccgtgac cgccgctgac accgccgtgt actactgcgc tggcggctac 300
tacagatacg gcctgggctc ctactccggc tcctactact acgtgatgga ctactggggc 360
cagggcacca ccgtgaccgt gtcctctgct agcaccaagg gcccaagtgt gtttcccctg 420
gcccccagca gcaagtctac ttccggcgga actgctgccc tgggttgcct ggtgaaggac 480
tacttccccg agcccgtgac agtgtcctgg aactctgggg ctctgacttc cggcgtgcac 540
accttccccg ccgtgctgca gagcagcggc ctgtacagcc tgagcagcgt ggtgacagtg 600
ccctccagct ctctgggaac ccagacctat atctgcaacg tgaaccacaa gcccagcaac 660
accaaggtgg acaagagagt ggagcccaag agctgcgaca agacccacac ctgccccccc 720
tgcccagctc cagaactgct gggagggcct tccgtgttcc tgttcccccc caagcccaag 780
gacaccctga tgatcagcag gacccccgag gtgacctgcg tggtggtgga cgtgtcccac 840
gaggacccag aggtgaagtt caactggtac gtggacggcg tggaggtgca caacgccaag 900
accaagccca gagaggagca gtacaacagc acctacaggg tggtgtccgt gctgaccgtg 960
ctgcaccagg actggctgaa cggcaaagaa tacaagtgca aagtctccaa caaggccctg 1020
ccagccccaa tcgaaaagac aatcagcaag gccaagggcc agccacggga gccccaggtg 1080
tacaccctgc cccccagccg ggaggagatg accaagaacc aggtgtccct gacctgtctg 1140
gtgaagggct tctaccccag cgatatcgcc gtggagtggg agagcaacgg ccagcccgag 1200
aacaactaca agaccacccc cccagtgctg gacagcgacg gcagcttctt cctgtacagc 1260
aagctgaccg tggacaagtc caggtggcag cagggcaacg tgttcagctg cagcgtgatg 1320
cacgaggccc tgcacaacca ctacacccag aagtccctga gcctgagccc cggcaag 1377
<210> 74
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 74
Asp Thr Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Arg Ala Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly His Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Val Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 75
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 75
gacacccaga tgacccagtc cccctcctcc ctgtccgtgt ccgtgggcga cagagccacc 60
atcacatgca aggcctccca gtccgtggac tacgaaggcc attcctacat gaactggtat 120
cagcagaagc ccggcaaggc ccccaagctg ctgatctacg ccgcctccaa cctggaatcc 180
ggcgtgccct ccagattctc cggctccggc tctggcaccg acttcaccct gaccatctcc 240
agcgtgcagc ccgaggactt cgccacctac tactgccagc agtccaacga ggaccccccc 300
accttcggcg gaggcaccaa gctggaaatc aag 333
<210> 76
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 76
Asp Thr Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Arg Ala Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly His Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Val Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 77
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 77
gacacccaga tgacccagtc cccctcctcc ctgtccgtgt ccgtgggcga cagagccacc 60
atcacatgca aggcctccca gtccgtggac tacgaaggcc attcctacat gaactggtat 120
cagcagaagc ccggcaaggc ccccaagctg ctgatctacg ccgcctccaa cctggaatcc 180
ggcgtgccct ccagattctc cggctccggc tctggcaccg acttcaccct gaccatctcc 240
agcgtgcagc ccgaggactt cgccacctac tactgccagc agtccaacga ggaccccccc 300
accttcggcg gaggcaccaa gctggaaatc aagcgtacgg tggccgctcc cagcgtgttc 360
atcttccccc ccagcgacga gcagctgaag agtggcaccg ccagcgtggt gtgcctgctg 420
aacaacttct acccccggga ggccaaggtg cagtggaagg tggacaacgc cctgcagagc 480
ggcaacagcc aggagagcgt caccgagcag gacagcaagg actccaccta cagcctgagc 540
agcaccctga ccctgagcaa ggccgactac gagaagcata aggtgtacgc ctgcgaggtg 600
acccaccagg gcctgtccag ccccgtgacc aagagcttca acaggggcga gtgc 654
<210> 78
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 78
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Glu Ile Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Thr Leu Thr Ile Ser Ser Val Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 79
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 79
gagatcgtgc tgacccagtc ccctgccacc ctgtctgcca gccctggcga ggagatcacc 60
ctgtcctgct ccgcctcctc ctccgtgtcc tacatccact ggtatcagca gaagcccggc 120
caggcccctc ggctgctgat ctactccacc tccaacctgg cctccggcat ccctgccaga 180
ttctccggct ctggctccgg caccttttac accctgacca tctccagcgt ggaacccgag 240
gacgccgccg tgtactactg ccaccagtgg tccagctacc cctggacctt cggcggaggc 300
accaagctgg aaatcaag 318
<210> 80
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 80
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Glu Ile Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Thr Leu Thr Ile Ser Ser Val Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 81
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 81
gagatcgtgc tgacccagtc ccctgccacc ctgtctgcca gccctggcga ggagatcacc 60
ctgtcctgct ccgcctcctc ctccgtgtcc tacatccact ggtatcagca gaagcccggc 120
caggcccctc ggctgctgat ctactccacc tccaacctgg cctccggcat ccctgccaga 180
ttctccggct ctggctccgg caccttttac accctgacca tctccagcgt ggaacccgag 240
gacgccgccg tgtactactg ccaccagtgg tccagctacc cctggacctt cggcggaggc 300
accaagctgg aaatcaagcg tacggtggcc gctcccagcg tgttcatctt cccccccagc 360
gacgagcagc tgaagagtgg caccgccagc gtggtgtgcc tgctgaacaa cttctacccc 420
cgggaggcca aggtgcagtg gaaggtggac aacgccctgc agagcggcaa cagccaggag 480
agcgtcaccg agcaggacag caaggactcc acctacagcc tgagcagcac cctgaccctg 540
agcaaggccg actacgagaa gcataaggtg tacgcctgcg aggtgaccca ccagggcctg 600
tccagccccg tgaccaagag cttcaacagg ggcgagtgc 639
<210> 82
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 82
Ser Ser Ser Ala Ala Trp Asn
1 5
<210> 83
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 83
Arg Ile Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala Val Ser Val
1 5 10 15
Lys Ser
<210> 84
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 84
Gly Ser Tyr Val Thr Ser Ser Tyr Glu Gly Phe Asp Tyr
1 5 10
<210> 85
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 85
Gly Asp Ser Val Ser Ser Ser Ser Ala
1 5
<210> 86
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 86
Tyr Tyr Arg Ser Lys Trp Tyr
1 5
<210> 87
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 87
Gly Asp Ser Val Ser Ser Ser Ser Ala Ala Trp Asn
1 5 10
<210> 88
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 88
Gly Asp Ser Val Ser Ser Ser Ser Ala Ala
1 5 10
<210> 89
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 89
Ile Tyr Tyr Arg Ser Lys Trp Tyr Asn
1 5
<210> 90
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 90
Ala Arg Gly Ser Tyr Val Thr Ser Ser Tyr Glu Gly Phe Asp Tyr
1 5 10 15
<210> 91
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 91
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Ser
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Ile Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Gly Ser Tyr Val Thr Ser Ser Tyr Glu Gly Phe
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 92
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 92
caggtgcaat tgcagcagag cggtccgggc ctggtgaaac cgagccagac cctgagcctg 60
acctgcgcga tttccggaga tagcgtgagc tctagctctg ctgcttggaa ctggattcgt 120
cagagcccga gccgtggcct cgagtggctg ggccgtatct actaccgtag caaatggtac 180
aacgactatg ccgtgagcgt gaaaagccgc attaccatta acccggatac ttcgaaaaac 240
cagtttagcc tgcaactgaa cagcgtgacc ccggaagata cggccgtgta ttattgcgcg 300
cgtggttctt acgttacttc ttcttacgaa ggtttcgatt actggggcca aggcaccctg 360
gtgactgtta gctca 375
<210> 93
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 93
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Ser
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Ile Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Gly Ser Tyr Val Thr Ser Ser Tyr Glu Gly Phe
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 94
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 94
caggtgcaat tgcagcagag cggtccgggc ctggtgaaac cgagccagac cctgagcctg 60
acctgcgcga tttccggaga tagcgtgagc tctagctctg ctgcttggaa ctggattcgt 120
cagagcccga gccgtggcct cgagtggctg ggccgtatct actaccgtag caaatggtac 180
aacgactatg ccgtgagcgt gaaaagccgc attaccatta acccggatac ttcgaaaaac 240
cagtttagcc tgcaactgaa cagcgtgacc ccggaagata cggccgtgta ttattgcgcg 300
cgtggttctt acgttacttc ttcttacgaa ggtttcgatt actggggcca aggcaccctg 360
gtgactgtta gctcagcctc caccaagggt ccatcggtct tccccctggc accctcctcc 420
aagagcacct ctgggggcac agcggccctg ggctgcctgg tcaaggacta cttccccgaa 480
ccggtgacgg tgtcgtggaa ctcaggcgcc ctgaccagcg gcgtgcacac cttcccggct 540
gtcctacagt cctcaggact ctactccctc agcagcgtgg tgaccgtgcc ctccagcagc 600
ttgggcaccc agacctacat ctgcaacgtg aatcacaagc ccagcaacac caaggtggac 660
aagagagttg agcccaaatc ttgtgacaaa actcacacat gcccaccgtg cccagcacct 720
gaactcctgg ggggaccgtc agtcttcctc ttccccccaa aacccaagga caccctcatg 780
atctcccgga cccctgaggt cacatgcgtg gtggtggacg tgagccacga agaccctgag 840
gtcaagttca actggtacgt ggacggcgtg gaggtgcata atgccaagac aaagccgcgg 900
gaggagcagt acaacagcac gtaccgggtg gtcagcgtcc tcaccgtcct gcaccaggac 960
tggctgaatg gcaaggagta caagtgcaag gtctccaaca aagccctccc agcccccatc 1020
gagaaaacca tctccaaagc caaagggcag ccccgagaac cacaggtgta caccctgccc 1080
ccatcccggg aggagatgac caagaaccag gtcagcctga cctgcctggt caaaggcttc 1140
tatcccagcg acatcgccgt ggagtgggag agcaatgggc agccggagaa caactacaag 1200
accacgcctc ccgtgctgga ctccgacggc tccttcttcc tctacagcaa gctcaccgtg 1260
gacaagagca ggtggcagca ggggaacgtc ttctcatgct ccgtgatgca tgaggctctg 1320
cacaaccact acacgcagaa gagcctctcc ctgtctccgg gtaaa 1365
<210> 95
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 95
Ser Gly Asp Asn Leu Pro Glu Lys Tyr Ala Tyr
1 5 10
<210> 96
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 96
Asp Asp Asn Lys Arg Pro Ser
1 5
<210> 97
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 97
Gln Ser Tyr Gly Lys Trp Gly Trp Thr Trp Val
1 5 10
<210> 98
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 98
Asp Asn Leu Pro Glu Lys Tyr
1 5
<210> 99
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 99
Asp Asp Asn
1
<210> 100
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 100
Tyr Gly Lys Trp Gly Trp Thr Trp
1 5
<210> 101
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 101
Asn Leu Pro Glu Lys Tyr
1 5
<210> 102
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 102
Ser Tyr Glu Leu Thr Gln Pro Leu Ser Val Ser Val Ala Leu Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Ser Gly Asp Asn Leu Pro Glu Lys Tyr Ala
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Asp Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Ala Gln Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Gly Lys Trp Gly Trp Thr
85 90 95
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 103
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 103
agctacgaac tgacccagcc gctgtccgtg agcgtggctc tgggccagac cgcgcggatt 60
acctgtagcg gcgataacct gccggaaaaa tacgcttact ggtaccagca gaaaccgggc 120
caggcgccgg tgctggtgat ctacgacgac aacaaacgtc cgagcggcat cccggaacgt 180
tttagcggat ccaacagcgg caacaccgcg accctgacca ttagccgcgc ccaggcggga 240
gacgaagcgg attattactg ccagtcttac ggtaaatggg gttggacttg ggtgtttggc 300
ggcggcacga agttaaccgt ccta 324
<210> 104
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 104
Ser Tyr Glu Leu Thr Gln Pro Leu Ser Val Ser Val Ala Leu Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Ser Gly Asp Asn Leu Pro Glu Lys Tyr Ala
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Asp Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Ala Gln Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Gly Lys Trp Gly Trp Thr
85 90 95
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln Pro Lys
100 105 110
Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu Gln
115 120 125
Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro Gly
130 135 140
Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys Ala Gly
145 150 155 160
Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala Ala
165 170 175
Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg Ser
180 185 190
Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys Thr Val
195 200 205
Ala Pro Thr Glu Cys Ser
210
<210> 105
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 105
agctacgaac tgacccagcc gctgtccgtg agcgtggctc tgggccagac cgcgcggatt 60
acctgtagcg gcgataacct gccggaaaaa tacgcttact ggtaccagca gaaaccgggc 120
caggcgccgg tgctggtgat ctacgacgac aacaaacgtc cgagcggcat cccggaacgt 180
tttagcggat ccaacagcgg caacaccgcg accctgacca ttagccgcgc ccaggcggga 240
gacgaagcgg attattactg ccagtcttac ggtaaatggg gttggacttg ggtgtttggc 300
ggcggcacga agttaaccgt cctaggtcag cccaaggctg ccccctcggt cactctgttc 360
ccgccctcct ctgaggagct tcaagccaac aaggccacac tggtgtgtct cataagtgac 420
ttctacccgg gagccgtgac agtggcctgg aaggcagata gcagccccgt caaggcggga 480
gtggagacca ccacaccctc caaacaaagc aacaacaagt acgcggccag cagctatctg 540
agcctgacgc ctgagcagtg gaagtcccac agaagctaca gctgccaggt cacgcatgaa 600
gggagcaccg tggagaagac agtggcccct acagaatgtt ca 642
<210> 106
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 106
Ser Tyr Ala Val Ser
1 5
<210> 107
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 107
Arg Ile Val Pro Trp Leu Gly His Thr Gln Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 108
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 108
Glu Ser Pro Gly Tyr Arg Tyr Ser Phe Asp Val
1 5 10
<210> 109
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 109
Gly Gly Thr Phe Asp Ser Tyr
1 5
<210> 110
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 110
Val Pro Trp Leu Gly His
1 5
<210> 111
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 111
Gly Gly Thr Phe Asp Ser Tyr Ala Val Ser
1 5 10
<210> 112
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 112
Gly Gly Thr Phe Asp Ser Tyr Ala
1 5
<210> 113
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 113
Ile Val Pro Trp Leu Gly His Thr
1 5
<210> 114
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 114
Ala Arg Glu Ser Pro Gly Tyr Arg Tyr Ser Phe Asp Val
1 5 10
<210> 115
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 115
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asp Ser Tyr
20 25 30
Ala Val Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Val Pro Trp Leu Gly His Thr Gln Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Pro Gly Tyr Arg Tyr Ser Phe Asp Val Trp Asp Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 116
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 116
caggtgcaat tggtgcagag cggtgccgaa gtgaaaaaac cgggcagcag cgtgaaagtt 60
agctgcaaag catccggagg gacgtttgac tcttacgctg tttcttgggt gcgccaggcc 120
ccgggccagg gcctcgagtg gatgggccgt atcgttccgt ggctgggcca tactcagtac 180
gcccagaaat ttcagggccg ggtgaccatt accgccgatg aaagcaccag caccgcctat 240
atggaactga gcagcctgcg cagcgaagat acggccgtgt attattgcgc gcgtgaatct 300
ccgggttacc gttactcttt cgatgtttgg gaccaaggca ccctggtgac tgttagctca 360
<210> 117
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 117
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asp Ser Tyr
20 25 30
Ala Val Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Val Pro Trp Leu Gly His Thr Gln Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Pro Gly Tyr Arg Tyr Ser Phe Asp Val Trp Asp Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 118
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 118
caggtgcaat tggtgcagag cggtgccgaa gtgaaaaaac cgggcagcag cgtgaaagtt 60
agctgcaaag catccggagg gacgtttgac tcttacgctg tttcttgggt gcgccaggcc 120
ccgggccagg gcctcgagtg gatgggccgt atcgttccgt ggctgggcca tactcagtac 180
gcccagaaat ttcagggccg ggtgaccatt accgccgatg aaagcaccag caccgcctat 240
atggaactga gcagcctgcg cagcgaagat acggccgtgt attattgcgc gcgtgaatct 300
ccgggttacc gttactcttt cgatgtttgg gaccaaggca ccctggtgac tgttagctca 360
gcctccacca agggtccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 420
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 480
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 540
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 600
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagag agttgagccc 660
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 720
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 780
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 840
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 900
agcacgtacc gggtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 960
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 1020
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggaggag 1080
atgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 1140
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 1200
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 1260
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 1320
cagaagagcc tctccctgtc tccgggtaaa 1350
<210> 119
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 119
Ser Gly Asp Ala Ile Gly Glu Lys Tyr Val Tyr
1 5 10
<210> 120
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 120
Asp Asp Asn Asn Arg Pro Ser
1 5
<210> 121
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 121
Ala Ser Tyr Asp Leu Gln Gln Ala Arg Trp Val
1 5 10
<210> 122
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 122
Asp Ala Ile Gly Glu Lys Tyr
1 5
<210> 123
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 123
Tyr Asp Leu Gln Gln Ala Arg Trp
1 5
<210> 124
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 124
Ala Ile Gly Glu Lys Tyr
1 5
<210> 125
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 125
Ser Tyr Glu Leu Thr Gln Pro Leu Ser Val Ser Val Ala Leu Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Ser Gly Asp Ala Ile Gly Glu Lys Tyr Val
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Asp Asp Asn Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Ala Gln Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ala Ser Tyr Asp Leu Gln Gln Ala Arg
85 90 95
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 126
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 126
agctacgaac tgacccagcc gctgtccgtg agcgtggctc tgggccagac cgcgcggatt 60
acctgtagcg gcgatgctat cggtgaaaaa tacgtttact ggtaccagca gaaaccgggc 120
caggcgccgg tgctggtgat ctacgacgac aacaaccgtc cgagcggcat cccggaacgt 180
tttagcggat ccaacagcgg caacaccgcg accctgacca ttagccgcgc ccaggcggga 240
gacgaagcgg attattactg cgcttcttac gacctgcagc aggctcgttg ggtgtttggc 300
ggcggcacga agttaaccgt ccta 324
<210> 127
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 127
Ser Tyr Glu Leu Thr Gln Pro Leu Ser Val Ser Val Ala Leu Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Ser Gly Asp Ala Ile Gly Glu Lys Tyr Val
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Asp Asp Asn Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Ala Gln Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ala Ser Tyr Asp Leu Gln Gln Ala Arg
85 90 95
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln Pro Lys
100 105 110
Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu Gln
115 120 125
Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro Gly
130 135 140
Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys Ala Gly
145 150 155 160
Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala Ala
165 170 175
Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg Ser
180 185 190
Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys Thr Val
195 200 205
Ala Pro Thr Glu Cys Ser
210
<210> 128
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 128
agctacgaac tgacccagcc gctgtccgtg agcgtggctc tgggccagac cgcgcggatt 60
acctgtagcg gcgatgctat cggtgaaaaa tacgtttact ggtaccagca gaaaccgggc 120
caggcgccgg tgctggtgat ctacgacgac aacaaccgtc cgagcggcat cccggaacgt 180
tttagcggat ccaacagcgg caacaccgcg accctgacca ttagccgcgc ccaggcggga 240
gacgaagcgg attattactg cgcttcttac gacctgcagc aggctcgttg ggtgtttggc 300
ggcggcacga agttaaccgt cctaggtcag cccaaggctg ccccctcggt cactctgttc 360
ccgccctcct ctgaggagct tcaagccaac aaggccacac tggtgtgtct cataagtgac 420
ttctacccgg gagccgtgac agtggcctgg aaggcagata gcagccccgt caaggcggga 480
gtggagacca ccacaccctc caaacaaagc aacaacaagt acgcggccag cagctatctg 540
agcctgacgc ctgagcagtg gaagtcccac agaagctaca gctgccaggt cacgcatgaa 600
gggagcaccg tggagaagac agtggcccct acagaatgtt ca 642
<210> 129
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 129
Arg Ile Val Pro Trp Leu Gly Phe Thr Arg Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 130
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 130
Val Pro Trp Leu Gly Phe
1 5
<210> 131
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 131
Ile Val Pro Trp Leu Gly Phe Thr
1 5
<210> 132
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 132
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asp Ser Tyr
20 25 30
Ala Val Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Val Pro Trp Leu Gly Phe Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Pro Gly Tyr Arg Tyr Ser Phe Asp Val Trp Asp Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 133
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 133
caggtgcaat tggtgcagag cggtgccgaa gtgaaaaaac cgggcagcag cgtgaaagtt 60
agctgcaaag catccggagg gacgtttgac tcttacgctg tttcttgggt gcgccaggcc 120
ccgggccagg gcctcgagtg gatgggccgt atcgttccgt ggctgggctt cactcgttac 180
gcccagaaat ttcagggccg ggtgaccatt accgccgatg aaagcaccag caccgcctat 240
atggaactga gcagcctgcg cagcgaagat acggccgtgt attattgcgc gcgtgaatct 300
ccgggttacc gttactcttt cgatgtttgg gaccaaggca ccctggtgac tgttagctca 360
<210> 134
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 134
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asp Ser Tyr
20 25 30
Ala Val Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Val Pro Trp Leu Gly Phe Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Pro Gly Tyr Arg Tyr Ser Phe Asp Val Trp Asp Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 135
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 135
caggtgcaat tggtgcagag cggtgccgaa gtgaaaaaac cgggcagcag cgtgaaagtt 60
agctgcaaag catccggagg gacgtttgac tcttacgctg tttcttgggt gcgccaggcc 120
ccgggccagg gcctcgagtg gatgggccgt atcgttccgt ggctgggctt cactcgttac 180
gcccagaaat ttcagggccg ggtgaccatt accgccgatg aaagcaccag caccgcctat 240
atggaactga gcagcctgcg cagcgaagat acggccgtgt attattgcgc gcgtgaatct 300
ccgggttacc gttactcttt cgatgtttgg gaccaaggca ccctggtgac tgttagctca 360
gcctccacca agggtccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 420
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 480
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 540
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 600
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagag agttgagccc 660
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 720
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 780
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 840
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 900
agcacgtacc gggtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 960
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 1020
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggaggag 1080
atgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 1140
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 1200
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 1260
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 1320
cagaagagcc tctccctgtc tccgggtaaa 1350
<210> 136
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 136
Ser Tyr Ala Met Ser
1 5
<210> 137
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 137
Val Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 138
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 138
Gly Asp Asp Tyr Gly Asp Asp Tyr Tyr Tyr Tyr Gly Met Asp Val
1 5 10 15
<210> 139
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 139
Gly Phe Thr Phe Ser Ser Tyr
1 5
<210> 140
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 140
Ser Gly Ser Gly Gly Ser
1 5
<210> 141
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 141
Gly Phe Thr Phe Ser Ser Tyr Ala Met Ser
1 5 10
<210> 142
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 142
Gly Phe Thr Phe Ser Ser Tyr Ala
1 5
<210> 143
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 143
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 144
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 144
Ala Arg Gly Asp Asp Tyr Gly Asp Asp Tyr Tyr Tyr Tyr Gly Met Asp
1 5 10 15
Val
<210> 145
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 145
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asp Asp Tyr Gly Asp Asp Tyr Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 146
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 146
gaggtgcagc tgttggagtc tgggggaggc ttggtacagt ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttagc agctatgcca tgagctgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtctcagtt attagtggta gtggtggtag cacatactac 180
gcagactccg tgaagggccg gttcaccatc tccagagaca attccaagaa cacgctgtat 240
ctgcaaatga acagcctgag agccgaggac acggccgtat attactgtgc gagaggggat 300
gactacggtg acgactacta ctactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 147
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 147
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asp Asp Tyr Gly Asp Asp Tyr Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 148
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 148
gaggtgcagc tgttggagtc tgggggaggc ttggtacagt ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttagc agctatgcca tgagctgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtctcagtt attagtggta gtggtggtag cacatactac 180
gcagactccg tgaagggccg gttcaccatc tccagagaca attccaagaa cacgctgtat 240
ctgcaaatga acagcctgag agccgaggac acggccgtat attactgtgc gagaggggat 300
gactacggtg acgactacta ctactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct cagctagcac caagggccca agtgtgtttc ccctggcccc cagcagcaag 420
tctacttccg gcggaactgc tgccctgggt tgcctggtga aggactactt ccccgagccc 480
gtgacagtgt cctggaactc tggggctctg acttccggcg tgcacacctt ccccgccgtg 540
ctgcagagca gcggcctgta cagcctgagc agcgtggtga cagtgccctc cagctctctg 600
ggaacccaga cctatatctg caacgtgaac cacaagccca gcaacaccaa ggtggacaag 660
agagtggagc ccaagagctg cgacaagacc cacacctgcc ccccctgccc agctccagaa 720
ctgctgggag ggccttccgt gttcctgttc ccccccaagc ccaaggacac cctgatgatc 780
agcaggaccc ccgaggtgac ctgcgtggtg gtggacgtgt cccacgagga cccagaggtg 840
aagttcaact ggtacgtgga cggcgtggag gtgcacaacg ccaagaccaa gcccagagag 900
gagcagtaca acagcaccta cagggtggtg tccgtgctga ccgtgctgca ccaggactgg 960
ctgaacggca aagaatacaa gtgcaaagtc tccaacaagg ccctgccagc cccaatcgaa 1020
aagacaatca gcaaggccaa gggccagcca cgggagcccc aggtgtacac cctgcccccc 1080
agccgggagg agatgaccaa gaaccaggtg tccctgacct gtctggtgaa gggcttctac 1140
cccagcgata tcgccgtgga gtgggagagc aacggccagc ccgagaacaa ctacaagacc 1200
acccccccag tgctggacag cgacggcagc ttcttcctgt acagcaagct gaccgtggac 1260
aagtccaggt ggcagcaggg caacgtgttc agctgcagcg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgagcctg agccccggca ag 1362
<210> 149
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 149
Arg Ser Ser Gln Ser Leu Leu His Gly Asn Arg Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 150
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 150
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 151
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 151
Met Gln Ala Leu Gln Thr Pro Pro Thr
1 5
<210> 152
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 152
Ser Gln Ser Leu Leu His Gly Asn Arg Tyr Asn Tyr
1 5 10
<210> 153
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 153
Leu Gly Ser
1
<210> 154
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 154
Ala Leu Gln Thr Pro Pro
1 5
<210> 155
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 155
Gln Ser Leu Leu His Gly Asn Arg Tyr Asn Tyr
1 5 10
<210> 156
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 156
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Gly
20 25 30
Asn Arg Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 157
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 157
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catggtaatc gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactcct 300
ccgacgttcg gccaagggac caaggtggaa atcaaa 336
<210> 158
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 158
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Gly
20 25 30
Asn Arg Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 159
<211> 657
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 159
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catggtaatc gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactcct 300
ccgacgttcg gccaagggac caaggtggaa atcaaacgaa ctgtggctgc accaagcgtg 360
ttcatcttcc cccccagcga cgagcagctg aagagtggca ccgccagcgt ggtgtgcctg 420
ctgaacaact tctacccccg ggaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
agcggcaaca gccaggagag cgtcaccgag caggacagca aggactccac ctacagcctg 540
agcagcaccc tgaccctgag caaggccgac tacgagaagc ataaggtgta cgcctgcgag 600
gtgacccacc agggcctgtc cagccccgtg accaagagct tcaacagggg cgagtgc 657
<210> 160
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 160
Ser Cys Ser Met Asn
1 5
<210> 161
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 161
Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 162
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 162
Asp Gln Gly Asn Trp Asn Tyr Asp Asp Tyr Tyr Asn Gly Leu Asp Val
1 5 10 15
<210> 163
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 163
Gly Phe Thr Phe Asn Ser Cys
1 5
<210> 164
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 164
Ser Ser Ser Ser Ser Thr
1 5
<210> 165
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 165
Gly Phe Thr Phe Asn Ser Cys Ser Met Asn
1 5 10
<210> 166
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 166
Gly Phe Thr Phe Asn Ser Cys Ser
1 5
<210> 167
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 167
Ile Ser Ser Ser Ser Ser Thr Ile
1 5
<210> 168
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 168
Ala Arg Asp Gln Gly Asn Trp Asn Tyr Asp Asp Tyr Tyr Asn Gly Leu
1 5 10 15
Asp Val
<210> 169
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 169
Glu Val Leu Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Ser Cys
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Gly Asn Trp Asn Tyr Asp Asp Tyr Tyr Asn Gly Leu
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 170
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 170
gaggtgctgc tggtggagtc tgggggaggc ttggtacagc ctggggggtc cctgagactc 60
tcctgtgcag cctctgggtt caccttcaat agctgtagca tgaactgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtttcatac attagtagta gtagtagtac catttactac 180
gcagactctg tgaagggccg attcaccatc tccagagaca atgccaagaa ctcactgtat 240
ctgcaaatga acagcctgaa agacgaggac acggctgtgt attactgtgc gagagatcag 300
ggtaactgga actacgacga ctactacaac ggtttggacg tctggggcca agggaccacg 360
gtcaccgtct cctca 375
<210> 171
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 171
Glu Val Leu Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Ser Cys
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Gly Asn Trp Asn Tyr Asp Asp Tyr Tyr Asn Gly Leu
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 172
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 172
gaggtgctgc tggtggagtc tgggggaggc ttggtacagc ctggggggtc cctgagactc 60
tcctgtgcag cctctgggtt caccttcaat agctgtagca tgaactgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtttcatac attagtagta gtagtagtac catttactac 180
gcagactctg tgaagggccg attcaccatc tccagagaca atgccaagaa ctcactgtat 240
ctgcaaatga acagcctgaa agacgaggac acggctgtgt attactgtgc gagagatcag 300
ggtaactgga actacgacga ctactacaac ggtttggacg tctggggcca agggaccacg 360
gtcaccgtct cctcagctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgcgacaag acccacacct gccccccctg cccagctcca 720
gaactgctgg gagggccttc cgtgttcctg ttccccccca agcccaagga caccctgatg 780
atcagcagga cccccgaggt gacctgcgtg gtggtggacg tgtcccacga ggacccagag 840
gtgaagttca actggtacgt ggacggcgtg gaggtgcaca acgccaagac caagcccaga 900
gaggagcagt acaacagcac ctacagggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagaata caagtgcaaa gtctccaaca aggccctgcc agccccaatc 1020
gaaaagacaa tcagcaaggc caagggccag ccacgggagc cccaggtgta caccctgccc 1080
cccagccggg aggagatgac caagaaccag gtgtccctga cctgtctggt gaagggcttc 1140
taccccagcg atatcgccgt ggagtgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc cagtgctgga cagcgacggc agcttcttcc tgtacagcaa gctgaccgtg 1260
gacaagtcca ggtggcagca gggcaacgtg ttcagctgca gcgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gcaag 1365
<210> 173
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 173
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 174
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 174
Met Gln Ala Leu Gln Thr Pro Leu Thr
1 5
<210> 175
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 175
Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
1 5 10
<210> 176
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 176
Ala Leu Gln Thr Pro Leu
1 5
<210> 177
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 177
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
1 5 10
<210> 178
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 178
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 179
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 179
gatattgtga tgactcagtc tccactctcc ctgcccgtca ctcctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactcct 300
ctcactttcg gcggagggac caaggtggag atcaaa 336
<210> 180
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 180
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 181
<211> 657
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 181
gatattgtga tgactcagtc tccactctcc ctgcccgtca ctcctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactcct 300
ctcactttcg gcggagggac caaggtggag atcaaacgta cggtggccgc tcccagcgtg 360
ttcatcttcc cccccagcga cgagcagctg aagagtggca ccgccagcgt ggtgtgcctg 420
ctgaacaact tctacccccg ggaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
agcggcaaca gccaggagag cgtcaccgag caggacagca aggactccac ctacagcctg 540
agcagcaccc tgaccctgag caaggccgac tacgagaagc ataaggtgta cgcctgcgag 600
gtgacccacc agggcctgtc cagccccgtg accaagagct tcaacagggg cgagtgc 657
<210> 182
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 182
His Tyr Gly Met Asn
1 5
<210> 183
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 183
Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe Lys
1 5 10 15
Gly
<210> 184
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 184
Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
1 5 10
<210> 185
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 185
Gly Tyr Thr Phe Thr His Tyr
1 5
<210> 186
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 186
Asn Thr Asp Thr Gly Asn
1 5
<210> 187
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 187
Gly Tyr Thr Phe Thr His Tyr Gly Met Asn
1 5 10
<210> 188
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 188
Gly Tyr Thr Phe Thr His Tyr Gly
1 5
<210> 189
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 189
Ile Asn Thr Asp Thr Gly Asn Pro
1 5
<210> 190
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 190
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
1 5 10 15
<210> 191
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 191
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Gln Pro Gly Gln
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 192
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 192
caggtccagc tggtgcagtc aggagctgag ctgaagcagc ctggacagtc ggtgaagatc 60
tcctgcaagg cttcagggta caccttcaca cactatggga tgaactgggt gaagcaggca 120
ccaggacagg gtctaaagtg gatgggctgg atcaacactg acactgggaa tccaacatat 180
gctgatgact tcaaaggacg gtttgtcttc tccttggaca cctctgtcag cactgcatat 240
ctgcagatca gcaacctcaa gaatgaagac acggccacgt attactgtgt gagatatgga 300
accctatata gcggatatgg gttttttttt gattcctggg gccaagggac cctggtcacc 360
gtctcctca 369
<210> 193
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 193
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Gln Pro Gly Gln
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Lys Thr Thr Ala
115 120 125
Pro Ser Val Tyr Pro Leu Ala Pro Val Cys Gly Asp Thr Thr Gly Ser
130 135 140
Ser Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Leu Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr
180 185 190
Val Thr Ser Ser Thr Trp Pro Ser Gln Ser Ile Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Glu Pro Arg Gly
210 215 220
Pro Thr Ile Lys Pro Cys Pro Pro Cys Lys Cys Pro Ala Pro Asn Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Ile Lys Asp Val
245 250 255
Leu Met Ile Ser Leu Ser Pro Ile Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Glu Asp Asp Pro Asp Val Gln Ile Ser Trp Phe Val Asn Asn Val
275 280 285
Glu Val His Thr Ala Gln Thr Gln Thr His Arg Glu Asp Tyr Asn Ser
290 295 300
Thr Leu Arg Val Val Ser Ala Leu Pro Ile Gln His Gln Asp Trp Met
305 310 315 320
Ser Gly Lys Glu Phe Lys Cys Lys Val Asn Asn Lys Asp Leu Pro Ala
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Pro Lys Gly Ser Val Arg Ala Pro
340 345 350
Gln Val Tyr Val Leu Pro Pro Pro Glu Glu Glu Met Thr Lys Lys Gln
355 360 365
Val Thr Leu Thr Cys Met Val Thr Asp Phe Met Pro Glu Asp Ile Tyr
370 375 380
Val Glu Trp Thr Asn Asn Gly Lys Thr Glu Leu Asn Tyr Lys Asn Thr
385 390 395 400
Glu Pro Val Leu Asp Ser Asp Gly Ser Tyr Phe Met Tyr Ser Lys Leu
405 410 415
Arg Val Glu Lys Lys Asn Trp Val Glu Arg Asn Ser Tyr Ser Cys Ser
420 425 430
Val Val His Glu Gly Leu His Asn His His Thr Thr Lys Ser Phe Ser
435 440 445
Arg Thr Pro Gly Lys
450
<210> 194
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 194
caggtccagc tggtgcagtc aggagctgag ctgaagcagc ctggacagtc ggtgaagatc 60
tcctgcaagg cttcagggta caccttcaca cactatggga tgaactgggt gaagcaggca 120
ccaggacagg gtctaaagtg gatgggctgg atcaacactg acactgggaa tccaacatat 180
gctgatgact tcaaaggacg gtttgtcttc tccttggaca cctctgtcag cactgcatat 240
ctgcagatca gcaacctcaa gaatgaagac acggccacgt attactgtgt gagatatgga 300
accctatata gcggatatgg gttttttttt gattcctggg gccaagggac cctggtcacc 360
gtctcctcag ccaagaccac cgcccccagc gtgtaccccc tggcccccgt gtgcggcgat 420
accaccggca gcagcgtgac cctgggctgc ctggtgaagg gctacttccc cgagcccgtg 480
accctgacct ggaacagcgg ctccctgagc agcggcgtgc acaccttccc cgccgtgctg 540
cagagcgacc tgtacaccct gtccagctcc gtgaccgtga caagcagcac ctggcccagc 600
cagagcatca cctgcaacgt ggcccacccc gccagcagca ccaaggtgga caagaagatc 660
gagcccaggg gccccaccat caagccctgc cccccctgca agtgcccagc ccccaacctg 720
ctgggcggac ccagcgtgtt catcttcccc cccaagatca aggacgtgct gatgatcagc 780
ctgagcccca tcgtgacctg cgtggtggtg gacgtgagcg aggacgaccc cgacgtgcag 840
atcagctggt tcgtgaacaa cgtggaggtg cacaccgccc agacccagac ccaccgggag 900
gactacaaca gcaccctgcg cgtcgtgtcc gccctgccca tccagcacca ggactggatg 960
agcggcaaag aattcaagtg caaggtgaac aacaaggacc tgcctgcccc catcgagcgg 1020
accatcagca agcccaaggg cagcgtgaga gccccccagg tgtacgtgct gccccctccc 1080
gaggaagaga tgaccaagaa acaggtgaca ctgacctgca tggtgaccga cttcatgccc 1140
gaggacatct acgtggagtg gaccaacaac ggcaagaccg agctgaacta caagaacacc 1200
gagcctgtgc tggacagcga cggcagctac ttcatgtaca gcaagctgcg ggtggagaag 1260
aaaaactggg tggagcggaa cagctacagc tgcagcgtgg tgcacgaggg cctgcacaac 1320
caccacacca ccaagagctt cagccggacc cccggcaag 1359
<210> 195
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 195
Lys Ser Ser Gln Ser Leu Phe Asn Ser Asn Thr Asn Lys Asn Tyr Leu
1 5 10 15
Asn
<210> 196
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 196
Tyr Ala Ser Thr Arg His Thr
1 5
<210> 197
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 197
Gln Gln Trp Tyr Ser Tyr Pro Trp Thr
1 5
<210> 198
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 198
Ser Gln Ser Leu Phe Asn Ser Asn Thr Asn Lys Asn Tyr
1 5 10
<210> 199
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 199
Tyr Ala Ser
1
<210> 200
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 200
Trp Tyr Ser Tyr Pro Trp
1 5
<210> 201
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 201
Gln Ser Leu Phe Asn Ser Asn Thr Asn Lys Asn Tyr
1 5 10
<210> 202
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 202
Asp Ile Met Met Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ala Gly
1 5 10 15
Glu Lys Ala Thr Ile Thr Cys Lys Ser Ser Gln Ser Leu Phe Asn Ser
20 25 30
Asn Thr Asn Lys Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Phe Tyr Tyr Ala Ser Thr Arg His Thr Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Thr Ser Val Gln Asp Glu Asp Leu Ala Asp Tyr Tyr Cys Gln Gln
85 90 95
Trp Tyr Ser Tyr Pro Trp Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 203
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 203
gacatcatga tgacccagtc tccatcatcc ctgagtgtgt cagcaggaga gaaagccact 60
atcacctgca agtccagtca gagtcttttc aacagtaaca ccaacaagaa ctacttgaac 120
tggtacctgc agaaaccagg gcagtctcct aaactgctgt tctattatgc atccactagg 180
catactgggg tccctgatcg cttcataggc agtggatctg ggacagattt cactctcacc 240
atcaccagtg tccaggatga agacctggca gattattact gtcagcagtg gtatagctac 300
ccgtggacgt tcggacctgg caccaagctg gaaatcaaa 339
<210> 204
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 204
Asp Ile Met Met Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ala Gly
1 5 10 15
Glu Lys Ala Thr Ile Thr Cys Lys Ser Ser Gln Ser Leu Phe Asn Ser
20 25 30
Asn Thr Asn Lys Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Phe Tyr Tyr Ala Ser Thr Arg His Thr Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Thr Ser Val Gln Asp Glu Asp Leu Ala Asp Tyr Tyr Cys Gln Gln
85 90 95
Trp Tyr Ser Tyr Pro Trp Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser
115 120 125
Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn
130 135 140
Phe Tyr Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp Gly Ser Glu
145 150 155 160
Arg Gln Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr
180 185 190
Glu Arg His Asn Ser Tyr Thr Cys Glu Ala Thr His Lys Thr Ser Thr
195 200 205
Ser Pro Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
210 215 220
<210> 205
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 205
gacatcatga tgacccagtc tccatcatcc ctgagtgtgt cagcaggaga gaaagccact 60
atcacctgca agtccagtca gagtcttttc aacagtaaca ccaacaagaa ctacttgaac 120
tggtacctgc agaaaccagg gcagtctcct aaactgctgt tctattatgc atccactagg 180
catactgggg tccctgatcg cttcataggc agtggatctg ggacagattt cactctcacc 240
atcaccagtg tccaggatga agacctggca gattattact gtcagcagtg gtatagctac 300
ccgtggacgt tcggacctgg caccaagctg gaaatcaaac gcgctgatgc cgcccctacc 360
gtgagcatct tcccccccag cagcgagcag ctgaccagcg gcggagccag cgtggtgtgc 420
ttcctgaaca acttctaccc caaggacatc aacgtgaagt ggaagatcga cggcagcgag 480
cggcagaacg gcgtgctgaa cagctggacc gaccaggaca gcaaggactc cacctacagc 540
atgagcagca ccctgaccct gaccaaggac gagtacgagc ggcacaacag ctacacctgc 600
gaggccaccc acaagaccag caccagcccc atcgtgaaga gcttcaaccg gaacgagtgc 660
<210> 206
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 206
Gly Tyr Thr Phe Trp His Tyr
1 5
<210> 207
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 207
Gly Tyr Thr Phe Trp His Tyr Gly Met Asn
1 5 10
<210> 208
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 208
Gly Tyr Thr Phe Trp His Tyr Gly
1 5
<210> 209
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 209
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Gln Pro Gly Gln
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Trp His Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 210
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 210
caggtccagc tggtgcagtc aggagctgag ctgaagcagc ctggacagtc ggtgaagatc 60
tcctgcaagg cttcagggta caccttctgg cactatggga tgaactgggt gaagcaggca 120
ccaggacagg gtctaaagtg gatgggctgg atcaacactg acactgggaa tccaacatat 180
gctgatgact tcaaaggacg gtttgtcttc tccttggaca cctctgtcag cactgcatat 240
ctgcagatca gcaacctcaa gaatgaagac acggccacgt attactgtgt gagatatgga 300
accctatata gcggatatgg gttttttttt gattcctggg gccaagggac cctggtcacc 360
gtctcctca 369
<210> 211
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 211
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Gln Pro Gly Gln
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Trp His Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Lys Thr Thr Ala
115 120 125
Pro Ser Val Tyr Pro Leu Ala Pro Val Cys Gly Asp Thr Thr Gly Ser
130 135 140
Ser Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Leu Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr
180 185 190
Val Thr Ser Ser Thr Trp Pro Ser Gln Ser Ile Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Glu Pro Arg Gly
210 215 220
Pro Thr Ile Lys Pro Cys Pro Pro Cys Lys Cys Pro Ala Pro Asn Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Ile Lys Asp Val
245 250 255
Leu Met Ile Ser Leu Ser Pro Ile Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Glu Asp Asp Pro Asp Val Gln Ile Ser Trp Phe Val Asn Asn Val
275 280 285
Glu Val His Thr Ala Gln Thr Gln Thr His Arg Glu Asp Tyr Asn Ser
290 295 300
Thr Leu Arg Val Val Ser Ala Leu Pro Ile Gln His Gln Asp Trp Met
305 310 315 320
Ser Gly Lys Glu Phe Lys Cys Lys Val Asn Asn Lys Asp Leu Pro Ala
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Pro Lys Gly Ser Val Arg Ala Pro
340 345 350
Gln Val Tyr Val Leu Pro Pro Pro Glu Glu Glu Met Thr Lys Lys Gln
355 360 365
Val Thr Leu Thr Cys Met Val Thr Asp Phe Met Pro Glu Asp Ile Tyr
370 375 380
Val Glu Trp Thr Asn Asn Gly Lys Thr Glu Leu Asn Tyr Lys Asn Thr
385 390 395 400
Glu Pro Val Leu Asp Ser Asp Gly Ser Tyr Phe Met Tyr Ser Lys Leu
405 410 415
Arg Val Glu Lys Lys Asn Trp Val Glu Arg Asn Ser Tyr Ser Cys Ser
420 425 430
Val Val His Glu Gly Leu His Asn His His Thr Thr Lys Ser Phe Ser
435 440 445
Arg Thr Pro Gly Lys
450
<210> 212
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 212
caggtccagc tggtgcagtc aggagctgag ctgaagcagc ctggacagtc ggtgaagatc 60
tcctgcaagg cttcagggta caccttctgg cactatggga tgaactgggt gaagcaggca 120
ccaggacagg gtctaaagtg gatgggctgg atcaacactg acactgggaa tccaacatat 180
gctgatgact tcaaaggacg gtttgtcttc tccttggaca cctctgtcag cactgcatat 240
ctgcagatca gcaacctcaa gaatgaagac acggccacgt attactgtgt gagatatgga 300
accctatata gcggatatgg gttttttttt gattcctggg gccaagggac cctggtcacc 360
gtctcctcag ccaagaccac cgcccccagc gtgtaccccc tggcccccgt gtgcggcgat 420
accaccggca gcagcgtgac cctgggctgc ctggtgaagg gctacttccc cgagcccgtg 480
accctgacct ggaacagcgg ctccctgagc agcggcgtgc acaccttccc cgccgtgctg 540
cagagcgacc tgtacaccct gtccagctcc gtgaccgtga caagcagcac ctggcccagc 600
cagagcatca cctgcaacgt ggcccacccc gccagcagca ccaaggtgga caagaagatc 660
gagcccaggg gccccaccat caagccctgc cccccctgca agtgcccagc ccccaacctg 720
ctgggcggac ccagcgtgtt catcttcccc cccaagatca aggacgtgct gatgatcagc 780
ctgagcccca tcgtgacctg cgtggtggtg gacgtgagcg aggacgaccc cgacgtgcag 840
atcagctggt tcgtgaacaa cgtggaggtg cacaccgccc agacccagac ccaccgggag 900
gactacaaca gcaccctgcg cgtcgtgtcc gccctgccca tccagcacca ggactggatg 960
agcggcaaag aattcaagtg caaggtgaac aacaaggacc tgcctgcccc catcgagcgg 1020
accatcagca agcccaaggg cagcgtgaga gccccccagg tgtacgtgct gccccctccc 1080
gaggaagaga tgaccaagaa acaggtgaca ctgacctgca tggtgaccga cttcatgccc 1140
gaggacatct acgtggagtg gaccaacaac ggcaagaccg agctgaacta caagaacacc 1200
gagcctgtgc tggacagcga cggcagctac ttcatgtaca gcaagctgcg ggtggagaag 1260
aaaaactggg tggagcggaa cagctacagc tgcagcgtgg tgcacgaggg cctgcacaac 1320
caccacacca ccaagagctt cagccggacc cccggcaag 1359
<210> 213
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 213
Gly Tyr Thr Phe His His Tyr
1 5
<210> 214
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 214
Gly Tyr Thr Phe His His Tyr Gly Met Asn
1 5 10
<210> 215
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 215
Gly Tyr Thr Phe His His Tyr Gly
1 5
<210> 216
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 216
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Gln Pro Gly Gln
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe His His Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 217
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 217
caggtccagc tggtgcagtc aggagctgag ctgaagcagc ctggacagtc ggtgaagatc 60
tcctgcaagg cttcagggta caccttccac cactatggga tgaactgggt gaagcaggca 120
ccaggacagg gtctaaagtg gatgggctgg atcaacactg acactgggaa tccaacatat 180
gctgatgact tcaaaggacg gtttgtcttc tccttggaca cctctgtcag cactgcatat 240
ctgcagatca gcaacctcaa gaatgaagac acggccacgt attactgtgt gagatatgga 300
accctatata gcggatatgg gttttttttt gattcctggg gccaagggac cctggtcacc 360
gtctcctca 369
<210> 218
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 218
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Gln Pro Gly Gln
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe His His Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Lys Thr Thr Ala
115 120 125
Pro Ser Val Tyr Pro Leu Ala Pro Val Cys Gly Asp Thr Thr Gly Ser
130 135 140
Ser Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Leu Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr
180 185 190
Val Thr Ser Ser Thr Trp Pro Ser Gln Ser Ile Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Glu Pro Arg Gly
210 215 220
Pro Thr Ile Lys Pro Cys Pro Pro Cys Lys Cys Pro Ala Pro Asn Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Ile Lys Asp Val
245 250 255
Leu Met Ile Ser Leu Ser Pro Ile Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Glu Asp Asp Pro Asp Val Gln Ile Ser Trp Phe Val Asn Asn Val
275 280 285
Glu Val His Thr Ala Gln Thr Gln Thr His Arg Glu Asp Tyr Asn Ser
290 295 300
Thr Leu Arg Val Val Ser Ala Leu Pro Ile Gln His Gln Asp Trp Met
305 310 315 320
Ser Gly Lys Glu Phe Lys Cys Lys Val Asn Asn Lys Asp Leu Pro Ala
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Pro Lys Gly Ser Val Arg Ala Pro
340 345 350
Gln Val Tyr Val Leu Pro Pro Pro Glu Glu Glu Met Thr Lys Lys Gln
355 360 365
Val Thr Leu Thr Cys Met Val Thr Asp Phe Met Pro Glu Asp Ile Tyr
370 375 380
Val Glu Trp Thr Asn Asn Gly Lys Thr Glu Leu Asn Tyr Lys Asn Thr
385 390 395 400
Glu Pro Val Leu Asp Ser Asp Gly Ser Tyr Phe Met Tyr Ser Lys Leu
405 410 415
Arg Val Glu Lys Lys Asn Trp Val Glu Arg Asn Ser Tyr Ser Cys Ser
420 425 430
Val Val His Glu Gly Leu His Asn His His Thr Thr Lys Ser Phe Ser
435 440 445
Arg Thr Pro Gly Lys
450
<210> 219
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 219
caggtccagc tggtgcagtc aggagctgag ctgaagcagc ctggacagtc ggtgaagatc 60
tcctgcaagg cttcagggta caccttccac cactatggga tgaactgggt gaagcaggca 120
ccaggacagg gtctaaagtg gatgggctgg atcaacactg acactgggaa tccaacatat 180
gctgatgact tcaaaggacg gtttgtcttc tccttggaca cctctgtcag cactgcatat 240
ctgcagatca gcaacctcaa gaatgaagac acggccacgt attactgtgt gagatatgga 300
accctatata gcggatatgg gttttttttt gattcctggg gccaagggac cctggtcacc 360
gtctcctcag ccaagaccac cgcccccagc gtgtaccccc tggcccccgt gtgcggcgat 420
accaccggca gcagcgtgac cctgggctgc ctggtgaagg gctacttccc cgagcccgtg 480
accctgacct ggaacagcgg ctccctgagc agcggcgtgc acaccttccc cgccgtgctg 540
cagagcgacc tgtacaccct gtccagctcc gtgaccgtga caagcagcac ctggcccagc 600
cagagcatca cctgcaacgt ggcccacccc gccagcagca ccaaggtgga caagaagatc 660
gagcccaggg gccccaccat caagccctgc cccccctgca agtgcccagc ccccaacctg 720
ctgggcggac ccagcgtgtt catcttcccc cccaagatca aggacgtgct gatgatcagc 780
ctgagcccca tcgtgacctg cgtggtggtg gacgtgagcg aggacgaccc cgacgtgcag 840
atcagctggt tcgtgaacaa cgtggaggtg cacaccgccc agacccagac ccaccgggag 900
gactacaaca gcaccctgcg cgtcgtgtcc gccctgccca tccagcacca ggactggatg 960
agcggcaaag aattcaagtg caaggtgaac aacaaggacc tgcctgcccc catcgagcgg 1020
accatcagca agcccaaggg cagcgtgaga gccccccagg tgtacgtgct gccccctccc 1080
gaggaagaga tgaccaagaa acaggtgaca ctgacctgca tggtgaccga cttcatgccc 1140
gaggacatct acgtggagtg gaccaacaac ggcaagaccg agctgaacta caagaacacc 1200
gagcctgtgc tggacagcga cggcagctac ttcatgtaca gcaagctgcg ggtggagaag 1260
aaaaactggg tggagcggaa cagctacagc tgcagcgtgg tgcacgaggg cctgcacaac 1320
caccacacca ccaagagctt cagccggacc cccggcaag 1359
<210> 220
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 220
Tyr Ile Ser Tyr Asp Gly Asp Asn Asn Tyr Asn Pro Ser Leu Lys Asn
1 5 10 15
<210> 221
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 221
Gly Tyr Tyr Arg Tyr Gly Leu Ser Tyr Tyr Tyr Val Met Asp Tyr
1 5 10 15
<210> 222
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 222
Ser Tyr Asp Gly Asp
1 5
<210> 223
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 223
Ile Ser Tyr Asp Gly Asp Asn
1 5
<210> 224
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 224
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Ser Tyr Tyr Tyr Val Met Asp
1 5 10 15
Tyr
<210> 225
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 225
Asp Ile Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Tyr Asp Gly Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Ser Tyr Tyr Tyr Val Met Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 226
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 226
gatatacagc ttcaggagtc aggacctggc ctcgtgaaac cttctcagtc tctgtctctc 60
acctgctctg tcactggcta ctccatcacc agtggttatt actggaactg gatccggcag 120
tttccaggaa acaaactgga atggatgggc tacataagct acgacggtga caataactac 180
aacccatctc tcaaaaatcg aatctccatc actcgtgaca catctaagaa ccagtttttc 240
ctgaagttga gttctgtgac tactgaggac acagctacat attactgtgc aggaggctac 300
tataggtacg gcctgtcgta ttactatgtt atggactact ggggtcaagg aacctcagtc 360
accgtctcct ca 372
<210> 227
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 227
Asp Ile Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Tyr Asp Gly Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Ser Tyr Tyr Tyr Val Met Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 228
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 228
gatatacagc ttcaggagtc aggacctggc ctcgtgaaac cttctcagtc tctgtctctc 60
acctgctctg tcactggcta ctccatcacc agtggttatt actggaactg gatccggcag 120
tttccaggaa acaaactgga atggatgggc tacataagct acgacggtga caataactac 180
aacccatctc tcaaaaatcg aatctccatc actcgtgaca catctaagaa ccagtttttc 240
ctgaagttga gttctgtgac tactgaggac acagctacat attactgtgc aggaggctac 300
tataggtacg gcctgtcgta ttactatgtt atggactact ggggtcaagg aacctcagtc 360
accgtctcct cagctagcac caagggccca agtgtgtttc ccctggcccc cagcagcaag 420
tctacttccg gcggaactgc tgccctgggt tgcctggtga aggactactt ccccgagccc 480
gtgacagtgt cctggaactc tggggctctg acttccggcg tgcacacctt ccccgccgtg 540
ctgcagagca gcggcctgta cagcctgagc agcgtggtga cagtgccctc cagctctctg 600
ggaacccaga cctatatctg caacgtgaac cacaagccca gcaacaccaa ggtggacaag 660
agagtggagc ccaagagctg cgacaagacc cacacctgcc ccccctgccc agctccagaa 720
ctgctgggag ggccttccgt gttcctgttc ccccccaagc ccaaggacac cctgatgatc 780
agcaggaccc ccgaggtgac ctgcgtggtg gtggacgtgt cccacgagga cccagaggtg 840
aagttcaact ggtacgtgga cggcgtggag gtgcacaacg ccaagaccaa gcccagagag 900
gagcagtaca acagcaccta cagggtggtg tccgtgctga ccgtgctgca ccaggactgg 960
ctgaacggca aagaatacaa gtgcaaagtc tccaacaagg ccctgccagc cccaatcgaa 1020
aagacaatca gcaaggccaa gggccagcca cgggagcccc aggtgtacac cctgcccccc 1080
agccgggagg agatgaccaa gaaccaggtg tccctgacct gtctggtgaa gggcttctac 1140
cccagcgata tcgccgtgga gtgggagagc aacggccagc ccgagaacaa ctacaagacc 1200
acccccccag tgctggacag cgacggcagc ttcttcctgt acagcaagct gaccgtggac 1260
aagtccaggt ggcagcaggg caacgtgttc agctgcagcg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgagcctg agccccggca ag 1362
<210> 229
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 229
Asp Thr Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asn Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 230
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 230
gacactgtgc tgacccaatc tccagcctct ttggctgtgt ctctagggca gagggccacc 60
atctcctgca aggccagcca aagtgttgat tatgatggta atagttatat gaactggtac 120
caacagaaac caggacagcc acccaaactc ctcatctatg ctgcatccaa tctagaatct 180
gggatcccag ccaggtttag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatgc tgcaacctat tactgtcagc aaagtaatga ggatcctccg 300
acgttcggtg gaggcaccaa gctggaaatc aaa 333
<210> 231
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 231
Asp Thr Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asn Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 232
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 232
gacactgtgc tgacccaatc tccagcctct ttggctgtgt ctctagggca gagggccacc 60
atctcctgca aggccagcca aagtgttgat tatgatggta atagttatat gaactggtac 120
caacagaaac caggacagcc acccaaactc ctcatctatg ctgcatccaa tctagaatct 180
gggatcccag ccaggtttag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatgc tgcaacctat tactgtcagc aaagtaatga ggatcctccg 300
acgttcggtg gaggcaccaa gctggaaatc aaacgtacgg tggccgctcc cagcgtgttc 360
atcttccccc ccagcgacga gcagctgaag agtggcaccg ccagcgtggt gtgcctgctg 420
aacaacttct acccccggga ggccaaggtg cagtggaagg tggacaacgc cctgcagagc 480
ggcaacagcc aggagagcgt caccgagcag gacagcaagg actccaccta cagcctgagc 540
agcaccctga ccctgagcaa ggccgactac gagaagcata aggtgtacgc ctgcgaggtg 600
acccaccagg gcctgtccag ccccgtgacc aagagcttca acaggggcga gtgc 654
<210> 233
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 233
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 234
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 234
gaggtccaac tgcaacagtt tggagctgaa ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaagg cttctggcta cacattcact gactacaaca tggactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggagat attaatccta agtatgatat ttctacctac 180
aatcagcaat tcaagggaaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggagctcc gcagcctgac atctgaggac actgcagtct attattgtgc aagaagaggc 300
ttttttcttt actacggtat taactactat tacttcgatg tctggggcgc agggaccacg 360
gtcaccgtct cctca 375
<210> 235
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 235
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 236
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 236
gaggtccaac tgcaacagtt tggagctgaa ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaagg cttctggcta cacattcact gactacaaca tggactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggagat attaatccta agtatgatat ttctacctac 180
aatcagcaat tcaagggaaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggagctcc gcagcctgac atctgaggac actgcagtct attattgtgc aagaagaggc 300
ttttttcttt actacggtat taactactat tacttcgatg tctggggcgc agggaccacg 360
gtcaccgtct cctcagctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgcgacaag acccacacct gccccccctg cccagctcca 720
gaactgctgg gagggccttc cgtgttcctg ttccccccca agcccaagga caccctgatg 780
atcagcagga cccccgaggt gacctgcgtg gtggtggacg tgtcccacga ggacccagag 840
gtgaagttca actggtacgt ggacggcgtg gaggtgcaca acgccaagac caagcccaga 900
gaggagcagt acaacagcac ctacagggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagaata caagtgcaaa gtctccaaca aggccctgcc agccccaatc 1020
gaaaagacaa tcagcaaggc caagggccag ccacgggagc cccaggtgta caccctgccc 1080
cccagccggg aggagatgac caagaaccag gtgtccctga cctgtctggt gaagggcttc 1140
taccccagcg atatcgccgt ggagtgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc cagtgctgga cagcgacggc agcttcttcc tgtacagcaa gctgaccgtg 1260
gacaagtcca ggtggcagca gggcaacgtg ttcagctgca gcgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gcaag 1365
<210> 237
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 237
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Thr Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 238
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 238
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctctagggga ggagatcacc 60
ctaacctgca gtgccagctc gagtgtaagt tacatacact ggtaccagca gaagtcaggc 120
acttctccca cactcttgat ttatagcaca tccaatctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtagttatc catggacgtt cggtggaggc 300
accaagctgg aaatcaaa 318
<210> 239
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 239
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Thr Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 240
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 240
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctctagggga ggagatcacc 60
ctaacctgca gtgccagctc gagtgtaagt tacatacact ggtaccagca gaagtcaggc 120
acttctccca cactcttgat ttatagcaca tccaatctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtagttatc catggacgtt cggtggaggc 300
accaagctgg aaatcaaacg tacggtggcc gctcccagcg tgttcatctt cccccccagc 360
gacgagcagc tgaagagtgg caccgccagc gtggtgtgcc tgctgaacaa cttctacccc 420
cgggaggcca aggtgcagtg gaaggtggac aacgccctgc agagcggcaa cagccaggag 480
agcgtcaccg agcaggacag caaggactcc acctacagcc tgagcagcac cctgaccctg 540
agcaaggccg actacgagaa gcataaggtg tacgcctgcg aggtgaccca ccagggcctg 600
tccagccccg tgaccaagag cttcaacagg ggcgagtgc 639
<210> 241
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 241
Asp Ile Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Tyr Asp Gly Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Ser Gly Ser Tyr
100 105 110
Tyr Tyr Val Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser
115 120 125
Ser
<210> 242
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 242
gatatacagc ttcaggagtc aggacctggc ctcgtgaaac cttctcagtc tctgtctctc 60
acctgctctg tcactggcta ctccatcacc agtggttatt actggaactg gatccggcag 120
tttccaggaa acaaactgga atggatgggc tacataagct acgacggtga caataactac 180
aacccatctc tcaaaaatcg aatctccatc actcgtgaca catctaagaa ccagtttttc 240
ctgaagttga gttctgtgac tactgaggac acagctacat attactgtgc aggaggctac 300
tataggtacg gcctgggctc ctactccggc tcgtattact atgttatgga ctactggggt 360
caaggaacct cagtcaccgt ctcctca 387
<210> 243
<211> 459
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 243
Asp Ile Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Tyr Asp Gly Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Gly Ser Tyr Ser Gly Ser Tyr
100 105 110
Tyr Tyr Val Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser
115 120 125
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
130 135 140
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
145 150 155 160
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
165 170 175
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
180 185 190
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
195 200 205
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
210 215 220
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
225 230 235 240
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
245 250 255
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
260 265 270
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
275 280 285
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
290 295 300
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
305 310 315 320
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
325 330 335
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
340 345 350
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
355 360 365
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
370 375 380
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
385 390 395 400
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
405 410 415
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
420 425 430
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
435 440 445
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 244
<211> 1377
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 244
gatatacagc ttcaggagtc aggacctggc ctcgtgaaac cttctcagtc tctgtctctc 60
acctgctctg tcactggcta ctccatcacc agtggttatt actggaactg gatccggcag 120
tttccaggaa acaaactgga atggatgggc tacataagct acgacggtga caataactac 180
aacccatctc tcaaaaatcg aatctccatc actcgtgaca catctaagaa ccagtttttc 240
ctgaagttga gttctgtgac tactgaggac acagctacat attactgtgc aggaggctac 300
tataggtacg gcctgggctc ctactccggc tcgtattact atgttatgga ctactggggt 360
caaggaacct cagtcaccgt ctcctcagct agcaccaagg gcccaagtgt gtttcccctg 420
gcccccagca gcaagtctac ttccggcgga actgctgccc tgggttgcct ggtgaaggac 480
tacttccccg agcccgtgac agtgtcctgg aactctgggg ctctgacttc cggcgtgcac 540
accttccccg ccgtgctgca gagcagcggc ctgtacagcc tgagcagcgt ggtgacagtg 600
ccctccagct ctctgggaac ccagacctat atctgcaacg tgaaccacaa gcccagcaac 660
accaaggtgg acaagagagt ggagcccaag agctgcgaca agacccacac ctgccccccc 720
tgcccagctc cagaactgct gggagggcct tccgtgttcc tgttcccccc caagcccaag 780
gacaccctga tgatcagcag gacccccgag gtgacctgcg tggtggtgga cgtgtcccac 840
gaggacccag aggtgaagtt caactggtac gtggacggcg tggaggtgca caacgccaag 900
accaagccca gagaggagca gtacaacagc acctacaggg tggtgtccgt gctgaccgtg 960
ctgcaccagg actggctgaa cggcaaagaa tacaagtgca aagtctccaa caaggccctg 1020
ccagccccaa tcgaaaagac aatcagcaag gccaagggcc agccacggga gccccaggtg 1080
tacaccctgc cccccagccg ggaggagatg accaagaacc aggtgtccct gacctgtctg 1140
gtgaagggct tctaccccag cgatatcgcc gtggagtggg agagcaacgg ccagcccgag 1200
aacaactaca agaccacccc cccagtgctg gacagcgacg gcagcttctt cctgtacagc 1260
aagctgaccg tggacaagtc caggtggcag cagggcaacg tgttcagctg cagcgtgatg 1320
cacgaggccc tgcacaacca ctacacccag aagtccctga gcctgagccc cggcaag 1377
<210> 245
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 245
Asp Ile Asn Pro Asn Tyr Asp Ile Thr Thr Tyr Asn Gln Arg Phe Lys
1 5 10 15
Gly
<210> 246
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 246
Arg Gly Phe Phe Pro Tyr Tyr Gly Asn Ser Tyr Tyr Tyr Phe Asp Val
1 5 10 15
<210> 247
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 247
Asn Pro Asn Tyr Asp Ile
1 5
<210> 248
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 248
Ile Asn Pro Asn Tyr Asp Ile Thr
1 5
<210> 249
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 249
Ala Arg Arg Gly Phe Phe Pro Tyr Tyr Gly Asn Ser Tyr Tyr Tyr Phe
1 5 10 15
Asp Val
<210> 250
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 250
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Tyr Asp Ile Thr Thr Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Pro Tyr Tyr Gly Asn Ser Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 251
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 251
gaggtccagc tgcaacagtt tggagctgag ctggtgaagc ctgggacttc agtgaagata 60
tcctgcaagg cttctggcta cacattcact gactacaaca tggactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggagat attaatccta actatgatat tactacctac 180
aaccagaggt tcaagggaaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggagctcc gcagcctgac atctgaggac actgcagtct attactgtgc aagaagagga 300
ttttttcctt attacggtaa tagctactat tacttcgatg tctggggcgc agggaccacg 360
gtcaccgtct cctca 375
<210> 252
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 252
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Tyr Asp Ile Thr Thr Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Pro Tyr Tyr Gly Asn Ser Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 253
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 253
gaggtccagc tgcaacagtt tggagctgag ctggtgaagc ctgggacttc agtgaagata 60
tcctgcaagg cttctggcta cacattcact gactacaaca tggactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggagat attaatccta actatgatat tactacctac 180
aaccagaggt tcaagggaaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggagctcc gcagcctgac atctgaggac actgcagtct attactgtgc aagaagagga 300
ttttttcctt attacggtaa tagctactat tacttcgatg tctggggcgc agggaccacg 360
gtcaccgtct cctcagctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgcgacaag acccacacct gccccccctg cccagctcca 720
gaactgctgg gagggccttc cgtgttcctg ttccccccca agcccaagga caccctgatg 780
atcagcagga cccccgaggt gacctgcgtg gtggtggacg tgtcccacga ggacccagag 840
gtgaagttca actggtacgt ggacggcgtg gaggtgcaca acgccaagac caagcccaga 900
gaggagcagt acaacagcac ctacagggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagaata caagtgcaaa gtctccaaca aggccctgcc agccccaatc 1020
gaaaagacaa tcagcaaggc caagggccag ccacgggagc cccaggtgta caccctgccc 1080
cccagccggg aggagatgac caagaaccag gtgtccctga cctgtctggt gaagggcttc 1140
taccccagcg atatcgccgt ggagtgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc cagtgctgga cagcgacggc agcttcttcc tgtacagcaa gctgaccgtg 1260
gacaagtcca ggtggcagca gggcaacgtg ttcagctgca gcgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gcaag 1365
<210> 254
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 254
Ser Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 255
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 255
His Gln Trp Ser Asn Tyr Pro Trp Thr
1 5
<210> 256
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 256
Trp Ser Asn Tyr Pro Trp
1 5
<210> 257
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 257
Gln Ile Val Leu Thr Gln Ser Pro Thr Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Asn Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 258
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 258
caaattgttc tcacccagtc tccaacaatc atgtctgcat ctctagggga ggagatcacc 60
cttacctgca gtgccagctc gagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acttctccca aactcttgat ttatagcaca tccaacctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtaattatc catggacgtt cggtggaggc 300
accaagctgg aaatcaaa 318
<210> 259
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 259
Gln Ile Val Leu Thr Gln Ser Pro Thr Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Asn Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 260
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 260
caaattgttc tcacccagtc tccaacaatc atgtctgcat ctctagggga ggagatcacc 60
cttacctgca gtgccagctc gagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acttctccca aactcttgat ttatagcaca tccaacctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtaattatc catggacgtt cggtggaggc 300
accaagctgg aaatcaaacg tacggtggcc gctcccagcg tgttcatctt cccccccagc 360
gacgagcagc tgaagagtgg caccgccagc gtggtgtgcc tgctgaacaa cttctacccc 420
cgggaggcca aggtgcagtg gaaggtggac aacgccctgc agagcggcaa cagccaggag 480
agcgtcaccg agcaggacag caaggactcc acctacagcc tgagcagcac cctgaccctg 540
agcaaggccg actacgagaa gcataaggtg tacgcctgcg aggtgaccca ccagggcctg 600
tccagccccg tgaccaagag cttcaacagg ggcgagtgc 639
<210> 261
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 261
Asp Ile Asn Pro Asn Tyr Asp Ile Thr Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 262
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 262
Arg Gly Phe Phe Leu Tyr Tyr Gly Ser Ser Tyr Tyr Tyr Phe Asp Val
1 5 10 15
<210> 263
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 263
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ser Ser Tyr Tyr Tyr Phe
1 5 10 15
Asp Val
<210> 264
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 264
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Tyr Asp Ile Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ser Ser Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 265
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 265
gaggtccagc tgcaacagtt tggagctgag ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaagg cttctggcta cacattcact gactacaaca tggactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggagat attaatccta actatgatat tactagctac 180
aaccagaagt tcaagggaaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggagctcc gcagcctgac atctgaggac actgcagtct attactgtgc aagaagaggg 300
ttttttcttt actacggtag tagctactat tacttcgatg tctggggcgc agggaccacg 360
gtcaccgtct cctca 375
<210> 266
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 266
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Tyr Asp Ile Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ser Ser Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 267
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 267
gaggtccagc tgcaacagtt tggagctgag ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaagg cttctggcta cacattcact gactacaaca tggactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggagat attaatccta actatgatat tactagctac 180
aaccagaagt tcaagggaaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggagctcc gcagcctgac atctgaggac actgcagtct attactgtgc aagaagaggg 300
ttttttcttt actacggtag tagctactat tacttcgatg tctggggcgc agggaccacg 360
gtcaccgtct cctcagctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgcgacaag acccacacct gccccccctg cccagctcca 720
gaactgctgg gagggccttc cgtgttcctg ttccccccca agcccaagga caccctgatg 780
atcagcagga cccccgaggt gacctgcgtg gtggtggacg tgtcccacga ggacccagag 840
gtgaagttca actggtacgt ggacggcgtg gaggtgcaca acgccaagac caagcccaga 900
gaggagcagt acaacagcac ctacagggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagaata caagtgcaaa gtctccaaca aggccctgcc agccccaatc 1020
gaaaagacaa tcagcaaggc caagggccag ccacgggagc cccaggtgta caccctgccc 1080
cccagccggg aggagatgac caagaaccag gtgtccctga cctgtctggt gaagggcttc 1140
taccccagcg atatcgccgt ggagtgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc cagtgctgga cagcgacggc agcttcttcc tgtacagcaa gctgaccgtg 1260
gacaagtcca ggtggcagca gggcaacgtg ttcagctgca gcgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gcaag 1365
<210> 268
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 268
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 269
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 269
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctctagggga ggagatcacc 60
ctaacctgca gtgccagctc gagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acttctccca aactcttgat ttatagcaca tccaacctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtagttatc catggacgtt cggtggaggc 300
accaagctgg aaatcaaa 318
<210> 270
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 270
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr
35 40 45
Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 271
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 271
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctctagggga ggagatcacc 60
ctaacctgca gtgccagctc gagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acttctccca aactcttgat ttatagcaca tccaacctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtagttatc catggacgtt cggtggaggc 300
accaagctgg aaatcaaacg tacggtggcc gctcccagcg tgttcatctt cccccccagc 360
gacgagcagc tgaagagtgg caccgccagc gtggtgtgcc tgctgaacaa cttctacccc 420
cgggaggcca aggtgcagtg gaaggtggac aacgccctgc agagcggcaa cagccaggag 480
agcgtcaccg agcaggacag caaggactcc acctacagcc tgagcagcac cctgaccctg 540
agcaaggccg actacgagaa gcataaggtg tacgcctgcg aggtgaccca ccagggcctg 600
tccagccccg tgaccaagag cttcaacagg ggcgagtgc 639
<210> 272
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 272
Glu Tyr Thr Met His
1 5
<210> 273
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 273
Gly Ile Asn Pro Asn Asn Gly Ile Thr Thr Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 274
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 274
Arg Gly Phe Pro Ile Tyr Tyr Tyr Gly Thr Ser Leu Tyr Tyr Phe Asp
1 5 10 15
Tyr
<210> 275
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 275
Gly Tyr Thr Phe Thr Glu Tyr
1 5
<210> 276
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 276
Asn Pro Asn Asn Gly Ile
1 5
<210> 277
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 277
Gly Tyr Thr Phe Thr Glu Tyr Thr Met His
1 5 10
<210> 278
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 278
Gly Tyr Thr Phe Thr Glu Tyr Thr
1 5
<210> 279
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 279
Ile Asn Pro Asn Asn Gly Ile Thr
1 5
<210> 280
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 280
Ala Arg Arg Gly Phe Pro Ile Tyr Tyr Tyr Gly Thr Ser Leu Tyr Tyr
1 5 10 15
Phe Asp Tyr
<210> 281
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 281
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Gly Ile Asn Pro Asn Asn Gly Ile Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Arg Ser Leu Thr Ser Glu Gly Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Pro Ile Tyr Tyr Tyr Gly Thr Ser Leu Tyr Tyr
100 105 110
Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
115 120 125
<210> 282
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 282
gaggtccagc tgcaacagtc tggacctgag ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaaga cttctggata cacattcact gaatacacca tgcactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggaggt attaatccta acaatggtat tactacttac 180
aaccagaagt tcaagggcaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggacctcc gcagcctgac atctgagggt tctgcagtct attactgtgc aagaagggga 300
ttccctattt attactacgg tactagcctc tactactttg actactgggg ccaaggcacc 360
actctcacag tctcctca 378
<210> 283
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 283
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Gly Ile Asn Pro Asn Asn Gly Ile Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Arg Ser Leu Thr Ser Glu Gly Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Pro Ile Tyr Tyr Tyr Gly Thr Ser Leu Tyr Tyr
100 105 110
Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 284
<211> 1368
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 284
gaggtccagc tgcaacagtc tggacctgag ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaaga cttctggata cacattcact gaatacacca tgcactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggaggt attaatccta acaatggtat tactacttac 180
aaccagaagt tcaagggcaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggacctcc gcagcctgac atctgagggt tctgcagtct attactgtgc aagaagggga 300
ttccctattt attactacgg tactagcctc tactactttg actactgggg ccaaggcacc 360
actctcacag tctcctcagc tagcaccaag ggcccaagtg tgtttcccct ggcccccagc 420
agcaagtcta cttccggcgg aactgctgcc ctgggttgcc tggtgaagga ctacttcccc 480
gagcccgtga cagtgtcctg gaactctggg gctctgactt ccggcgtgca caccttcccc 540
gccgtgctgc agagcagcgg cctgtacagc ctgagcagcg tggtgacagt gccctccagc 600
tctctgggaa cccagaccta tatctgcaac gtgaaccaca agcccagcaa caccaaggtg 660
gacaagagag tggagcccaa gagctgcgac aagacccaca cctgcccccc ctgcccagct 720
ccagaactgc tgggagggcc ttccgtgttc ctgttccccc ccaagcccaa ggacaccctg 780
atgatcagca ggacccccga ggtgacctgc gtggtggtgg acgtgtccca cgaggaccca 840
gaggtgaagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 900
agagaggagc agtacaacag cacctacagg gtggtgtccg tgctgaccgt gctgcaccag 960
gactggctga acggcaaaga atacaagtgc aaagtctcca acaaggccct gccagcccca 1020
atcgaaaaga caatcagcaa ggccaagggc cagccacggg agccccaggt gtacaccctg 1080
ccccccagcc gggaggagat gaccaagaac caggtgtccc tgacctgtct ggtgaagggc 1140
ttctacccca gcgatatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1200
aagaccaccc ccccagtgct ggacagcgac ggcagcttct tcctgtacag caagctgacc 1260
gtggacaagt ccaggtggca gcagggcaac gtgttcagct gcagcgtgat gcacgaggcc 1320
ctgcacaacc actacaccca gaagtccctg agcctgagcc ccggcaag 1368
<210> 285
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 285
Thr Thr Ser Asn Leu Ala Ser
1 5
<210> 286
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 286
Thr Thr Ser
1
<210> 287
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 287
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Arg Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr
35 40 45
Thr Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 288
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 288
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctctagggga ggagatcacc 60
ctaacctgca gtgccagctc gagtgtaagt tacatgcact ggtaccagca gaggtcaggc 120
acttctccca aactcttgat ttataccaca tccaacctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtagttatc cgtggacgtt cggtggaggc 300
accaagctgg aaatcaaa 318
<210> 289
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 289
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Arg Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr
35 40 45
Thr Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 290
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 290
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctctagggga ggagatcacc 60
ctaacctgca gtgccagctc gagtgtaagt tacatgcact ggtaccagca gaggtcaggc 120
acttctccca aactcttgat ttataccaca tccaacctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctctcacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtagttatc cgtggacgtt cggtggaggc 300
accaagctgg aaatcaaacg tacggtggcc gctcccagcg tgttcatctt cccccccagc 360
gacgagcagc tgaagagtgg caccgccagc gtggtgtgcc tgctgaacaa cttctacccc 420
cgggaggcca aggtgcagtg gaaggtggac aacgccctgc agagcggcaa cagccaggag 480
agcgtcaccg agcaggacag caaggactcc acctacagcc tgagcagcac cctgaccctg 540
agcaaggccg actacgagaa gcataaggtg tacgcctgcg aggtgaccca ccagggcctg 600
tccagccccg tgaccaagag cttcaacagg ggcgagtgc 639
<210> 291
<211> 495
<212> БЕЛОК
<213> Homo sapiens
<400> 291
Met Ala Gly Lys Val Arg Ser Leu Leu Pro Pro Leu Leu Leu Ala Ala
1 5 10 15
Ala Gly Leu Ala Gly Leu Leu Leu Leu Cys Val Pro Thr Arg Asp Val
20 25 30
Arg Glu Pro Pro Ala Leu Lys Tyr Gly Ile Val Leu Asp Ala Gly Ser
35 40 45
Ser His Thr Ser Met Phe Ile Tyr Lys Trp Pro Ala Asp Lys Glu Asn
50 55 60
Asp Thr Gly Ile Val Gly Gln His Ser Ser Cys Asp Val Pro Gly Gly
65 70 75 80
Gly Ile Ser Ser Tyr Ala Asp Asn Pro Ser Gly Ala Ser Gln Ser Leu
85 90 95
Val Gly Cys Leu Glu Gln Ala Leu Gln Asp Val Pro Lys Glu Arg His
100 105 110
Ala Gly Thr Pro Leu Tyr Leu Gly Ala Thr Ala Gly Met Arg Leu Leu
115 120 125
Asn Leu Thr Asn Pro Glu Ala Ser Thr Ser Val Leu Met Ala Val Thr
130 135 140
His Thr Leu Thr Gln Tyr Pro Phe Asp Phe Arg Gly Ala Arg Ile Leu
145 150 155 160
Ser Gly Gln Glu Glu Gly Val Phe Gly Trp Val Thr Ala Asn Tyr Leu
165 170 175
Leu Glu Asn Phe Ile Lys Tyr Gly Trp Val Gly Arg Trp Phe Arg Pro
180 185 190
Arg Lys Gly Thr Leu Gly Ala Met Asp Leu Gly Gly Ala Ser Thr Gln
195 200 205
Ile Thr Phe Glu Thr Thr Ser Pro Ala Glu Asp Arg Ala Ser Glu Val
210 215 220
Gln Leu His Leu Tyr Gly Gln His Tyr Arg Val Tyr Thr His Ser Phe
225 230 235 240
Leu Cys Tyr Gly Arg Asp Gln Val Leu Gln Arg Leu Leu Ala Ser Ala
245 250 255
Leu Gln Thr His Gly Phe His Pro Cys Trp Pro Arg Gly Phe Ser Thr
260 265 270
Gln Val Leu Leu Gly Asp Val Tyr Gln Ser Pro Cys Thr Met Ala Gln
275 280 285
Arg Pro Gln Asn Phe Asn Ser Ser Ala Arg Val Ser Leu Ser Gly Ser
290 295 300
Ser Asp Pro His Leu Cys Arg Asp Leu Val Ser Gly Leu Phe Ser Phe
305 310 315 320
Ser Ser Cys Pro Phe Ser Arg Cys Ser Phe Asn Gly Val Phe Gln Pro
325 330 335
Pro Val Ala Gly Asn Phe Val Ala Phe Ser Ala Phe Phe Tyr Thr Val
340 345 350
Asp Phe Leu Arg Thr Ser Met Gly Leu Pro Val Ala Thr Leu Gln Gln
355 360 365
Leu Glu Ala Ala Ala Val Asn Val Cys Asn Gln Thr Trp Ala Gln Leu
370 375 380
Gln Ala Arg Val Pro Gly Gln Arg Ala Arg Leu Ala Asp Tyr Cys Ala
385 390 395 400
Gly Ala Met Phe Val Gln Gln Leu Leu Ser Arg Gly Tyr Gly Phe Asp
405 410 415
Glu Arg Ala Phe Gly Gly Val Ile Phe Gln Lys Lys Ala Ala Asp Thr
420 425 430
Ala Val Gly Trp Ala Leu Gly Tyr Met Leu Asn Leu Thr Asn Leu Ile
435 440 445
Pro Ala Asp Pro Pro Gly Leu Arg Lys Gly Thr Asp Phe Ser Ser Trp
450 455 460
Val Val Leu Leu Leu Leu Phe Ala Ser Ala Leu Leu Ala Ala Leu Val
465 470 475 480
Leu Leu Leu Arg Gln Val His Ser Ala Lys Leu Pro Ser Thr Ile
485 490 495
<210> 292
<211> 2156
<212> ДНК
<213> Homo sapiens
<400> 292
ggctccccgc actctccggg tccacgcatc gtcctcccgc gcgcccgccc gcccatggcc 60
gggaaggtgc ggtcactgct gccgccgctg ctgctggccg ccgcgggcct cgccggcctc 120
ctactgctgt gcgtccccac ccgcgacgtc cgggagccgc ccgccctcaa gtatggcatc 180
gtcctggacg ctggttcttc acacacgtcc atgtttatct acaagtggcc ggcagacaag 240
gagaacgaca caggcattgt gggccagcac agctcctgtg atgttccagg tgggggcatc 300
tccagctatg cagacaaccc ttctggggcc agccagagtc ttgttggatg cctcgaacag 360
gcgcttcagg atgtgcccaa agagagacac gcgggcacac ccctctacct gggagccaca 420
gcgggtatgc gcctgctcaa cctgaccaat ccagaggcct cgaccagtgt gctcatggca 480
gtgactcaca cactgaccca gtaccccttt gacttccggg gtgcacgcat cctctcgggc 540
caggaagagg gggtgtttgg ctgggtgact gccaactacc tgctggagaa cttcatcaag 600
tacggctggg tgggccggtg gttccggcca cggaagggga cactgggggc catggacctg 660
gggggtgcct ctacccagat cacttttgag acaaccagtc cagctgagga cagagccagc 720
gaggtccagc tgcatctcta cggccagcac taccgagtct acacccacag cttcctctgc 780
tatggccgtg accaggtcct ccagaggctg ctggccagcg ccctccagac ccacggcttc 840
cacccctgct ggccgagggg cttttccacc caagtgctgc tcggggatgt gtaccagtca 900
ccatgcacca tggcccagcg gccccagaac ttcaacagca gtgccagggt cagcctgtca 960
gggagcagtg acccccacct ctgccgagat ctggtttctg ggctcttcag cttctcctcc 1020
tgccccttct cccgatgctc tttcaatggg gtcttccagc ccccagtggc tgggaacttt 1080
gtggccttct ctgccttctt ctacactgtg gactttttgc ggacttcgat ggggctgccc 1140
gtggccaccc tgcagcagct ggaggcagcc gcagtgaatg tctgcaacca gacctgggct 1200
cagctgcaag ctcgggtgcc agggcaacgg gcccgcctgg ccgactactg cgccggggcc 1260
atgttcgtgc agcagctgct gagtcgcggc tacggcttcg acgagcgcgc cttcggcggc 1320
gtgatcttcc agaagaaggc cgcggacact gcagtgggct gggcgctcgg ctacatgctg 1380
aacctgacca acctgatccc cgccgacccg ccggggctgc gcaagggcac agacttcagc 1440
tcctgggtcg tcctcctgct gctcttcgcc tccgcgctcc tggctgcgct tgtcctgctg 1500
ctgcgtcagg tgcactccgc caagctgcca agcaccattt aggggccgac gggggcagct 1560
gccccatccc tcccccaacc cctgtatccc caccccgtac tcccacccct cccacaaccc 1620
ctgtacctcc cacccctgta tccccacccc tccacccacc cctctcccaa cctctctccc 1680
cgcccctgta tcctgcattc ctccacccac cctctatccc ccaccgctcc accccaccac 1740
tgtcttctcc atccttccac cccaccctca gcgtctctgc ccctaaggca gcccaggaaa 1800
taggaactga gactctggta cccacaggag cctgggtggg caaagagcgc tcaatccagc 1860
tccttgaacc cctccagccc gcttcagcct gggcatcact gcaggccccg tgctcctcct 1920
cctcctcctc agggctgggt ctccagagag tggggccttg gtcctgagaa tcagccctta 1980
gaggctcctt ctgtgtagtc tgggtctgta ctggggaggg tcacagccca cgggctggca 2040
gccagcccag cacctacttg taaaaatttt gtaataaaaa gtttttccta gagacgtgaa 2100
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaa 2156
<210> 293
<211> 472
<212> БЕЛОК
<213> Homo sapiens
<400> 293
Met Ala Gly Lys Val Arg Ser Leu Leu Pro Pro Leu Leu Leu Ala Ala
1 5 10 15
Ala Gly Leu Ala Gly Leu Leu Leu Leu Cys Val Pro Thr Arg Asp Val
20 25 30
Arg Glu Pro Pro Ala Leu Lys Tyr Gly Ile Val Leu Asp Ala Gly Ser
35 40 45
Ser His Thr Ser Met Phe Ile Tyr Lys Trp Pro Ala Asp Lys Glu Asn
50 55 60
Asp Thr Gly Ile Val Gly Gln His Ser Ser Cys Asp Val Pro Gly Gly
65 70 75 80
Gly Ile Ser Ser Tyr Ala Asp Asn Pro Ser Gly Ala Ser Gln Ser Leu
85 90 95
Val Gly Cys Leu Glu Gln Ala Leu Gln Asp Val Pro Lys Glu Arg His
100 105 110
Ala Gly Thr Pro Leu Tyr Leu Gly Ala Thr Ala Gly Met Arg Leu Leu
115 120 125
Asn Leu Thr Asn Pro Glu Ala Ser Thr Ser Val Leu Met Ala Val Thr
130 135 140
His Thr Leu Thr Gln Tyr Pro Phe Asp Phe Arg Gly Ala Arg Ile Leu
145 150 155 160
Ser Gly Gln Glu Glu Gly Val Phe Gly Trp Val Thr Ala Asn Tyr Leu
165 170 175
Leu Glu Asn Phe Ile Lys Tyr Gly Trp Val Gly Arg Trp Phe Arg Pro
180 185 190
Arg Lys Gly Thr Leu Gly Ala Met Asp Leu Gly Gly Ala Ser Thr Gln
195 200 205
Ile Thr Phe Glu Thr Thr Ser Pro Ala Glu Asp Arg Ala Ser Glu Val
210 215 220
Gln Leu His Leu Tyr Gly Gln His Tyr Arg Val Tyr Thr His Ser Phe
225 230 235 240
Leu Cys Tyr Gly Arg Asp Gln Val Leu Gln Arg Leu Leu Ala Ser Ala
245 250 255
Leu Gln Thr His Gly Phe His Pro Cys Trp Pro Arg Gly Phe Ser Thr
260 265 270
Gln Val Leu Leu Gly Asp Val Tyr Gln Ser Pro Cys Thr Met Ala Gln
275 280 285
Arg Pro Gln Asn Phe Asn Ser Ser Ala Arg Val Ser Leu Ser Gly Ser
290 295 300
Ser Asp Pro His Leu Cys Arg Asp Leu Val Ser Gly Leu Phe Ser Phe
305 310 315 320
Ser Ser Cys Pro Phe Ser Arg Cys Ser Phe Asn Gly Val Phe Gln Pro
325 330 335
Pro Val Ala Gly Asn Phe Val Ala Phe Ser Ala Phe Phe Tyr Thr Val
340 345 350
Asp Phe Leu Arg Thr Ser Met Gly Leu Pro Val Ala Thr Leu Gln Gln
355 360 365
Leu Glu Ala Ala Ala Val Asn Val Cys Asn Gln Thr Trp Ala Gln Gln
370 375 380
Leu Leu Ser Arg Gly Tyr Gly Phe Asp Glu Arg Ala Phe Gly Gly Val
385 390 395 400
Ile Phe Gln Lys Lys Ala Ala Asp Thr Ala Val Gly Trp Ala Leu Gly
405 410 415
Tyr Met Leu Asn Leu Thr Asn Leu Ile Pro Ala Asp Pro Pro Gly Leu
420 425 430
Arg Lys Gly Thr Asp Phe Ser Ser Trp Val Val Leu Leu Leu Leu Phe
435 440 445
Ala Ser Ala Leu Leu Ala Ala Leu Val Leu Leu Leu Arg Gln Val His
450 455 460
Ser Ala Lys Leu Pro Ser Thr Ile
465 470
<210> 294
<211> 2087
<212> ДНК
<213> Homo sapiens
<400> 294
ggctccccgc actctccggg tccacgcatc gtcctcccgc gcgcccgccc gcccatggcc 60
gggaaggtgc ggtcactgct gccgccgctg ctgctggccg ccgcgggcct cgccggcctc 120
ctactgctgt gcgtccccac ccgcgacgtc cgggagccgc ccgccctcaa gtatggcatc 180
gtcctggacg ctggttcttc acacacgtcc atgtttatct acaagtggcc ggcagacaag 240
gagaacgaca caggcattgt gggccagcac agctcctgtg atgttccagg tgggggcatc 300
tccagctatg cagacaaccc ttctggggcc agccagagtc ttgttggatg cctcgaacag 360
gcgcttcagg atgtgcccaa agagagacac gcgggcacac ccctctacct gggagccaca 420
gcgggtatgc gcctgctcaa cctgaccaat ccagaggcct cgaccagtgt gctcatggca 480
gtgactcaca cactgaccca gtaccccttt gacttccggg gtgcacgcat cctctcgggc 540
caggaagagg gggtgtttgg ctgggtgact gccaactacc tgctggagaa cttcatcaag 600
tacggctggg tgggccggtg gttccggcca cggaagggga cactgggggc catggacctg 660
gggggtgcct ctacccagat cacttttgag acaaccagtc cagctgagga cagagccagc 720
gaggtccagc tgcatctcta cggccagcac taccgagtct acacccacag cttcctctgc 780
tatggccgtg accaggtcct ccagaggctg ctggccagcg ccctccagac ccacggcttc 840
cacccctgct ggccgagggg cttttccacc caagtgctgc tcggggatgt gtaccagtca 900
ccatgcacca tggcccagcg gccccagaac ttcaacagca gtgccagggt cagcctgtca 960
gggagcagtg acccccacct ctgccgagat ctggtttctg ggctcttcag cttctcctcc 1020
tgccccttct cccgatgctc tttcaatggg gtcttccagc ccccagtggc tgggaacttt 1080
gtggccttct ctgccttctt ctacactgtg gactttttgc ggacttcgat ggggctgccc 1140
gtggccaccc tgcagcagct ggaggcagcc gcagtgaatg tctgcaacca gacctgggct 1200
cagcagctgc tgagtcgcgg ctacggcttc gacgagcgcg ccttcggcgg cgtgatcttc 1260
cagaagaagg ccgcggacac tgcagtgggc tgggcgctcg gctacatgct gaacctgacc 1320
aacctgatcc ccgccgaccc gccggggctg cgcaagggca cagacttcag ctcctgggtc 1380
gtcctcctgc tgctcttcgc ctccgcgctc ctggctgcgc ttgtcctgct gctgcgtcag 1440
gtgcactccg ccaagctgcc aagcaccatt taggggccga cgggggcagc tgccccatcc 1500
ctcccccaac ccctgtatcc ccaccccgta ctcccacccc tcccacaacc cctgtacctc 1560
ccacccctgt atccccaccc ctccacccac ccctctccca acctctctcc ccgcccctgt 1620
atcctgcatt cctccaccca ccctctatcc cccaccgctc caccccacca ctgtcttctc 1680
catccttcca ccccaccctc agcgtctctg cccctaaggc agcccaggaa ataggaactg 1740
agactctggt acccacagga gcctgggtgg gcaaagagcg ctcaatccag ctccttgaac 1800
ccctccagcc cgcttcagcc tgggcatcac tgcaggcccc gtgctcctcc tcctcctcct 1860
cagggctggg tctccagaga gtggggcctt ggtcctgaga atcagccctt agaggctcct 1920
tctgtgtagt ctgggtctgt actggggagg gtcacagccc acgggctggc agccagccca 1980
gcacctactt gtaaaaattt tgtaataaaa agtttttcct agagacgtga aaaaaaaaaa 2040
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaa 2087
<210> 295
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 295
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Tyr Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Arg Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Gly Tyr Gly Arg Val Asp Glu Trp Gly Arg Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 296
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 296
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Leu Ser Asn Ile Gly Arg Asn
20 25 30
Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Leu Asp Asn Leu Arg Leu Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Trp Asp Asp Ser His
85 90 95
Pro Gly Trp Thr Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 297
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 297
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Leu Tyr Asp Gly Ser Asn Lys Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Ser Trp Tyr Pro Asp Ser Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Asn Phe Gly Thr Gln Thr Tyr Thr Cys Asn Val Asp His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Thr Val Glu Arg Lys Cys Cys
210 215 220
Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser
290 295 300
Val Leu Thr Val Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 298
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 298
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 299
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 299
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Leu Tyr Asp Gly Ser Asn Lys Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Ser Trp Tyr Pro Asp Ser Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 300
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 300
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 301
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 301
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Gly Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Pro Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp His Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 302
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 302
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Leu Tyr Asp Gly Ser Asn Lys Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Ser Trp Tyr Pro Asp Ser Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 303
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 303
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Gly Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Pro Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp His Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 304
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 304
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Leu Tyr Asp Gly Ser Asn Lys Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Ser Trp Tyr Pro Asp Ser Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 305
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 305
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 306
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 306
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Glu Ser Asn Lys Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Ser Trp Tyr Pro Asp Ser Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 307
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 307
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 308
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 308
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Arg Ser Gly Ser Tyr Asn Tyr Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Arg
115 120
<210> 309
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 309
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 310
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 310
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Leu Trp Glu Val Arg Ala Leu Pro Ser Val Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 311
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 311
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Ala Asn Asp Ile Gly Ser Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Ala Gly Gln Ala Pro Val Leu Val Val Ser
35 40 45
Glu Asp Ile Ile Arg Pro Ser Gly Ile Pro Glu Arg Ile Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Arg Asp Ser Asp Gln
85 90 95
Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105
<210> 312
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 312
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 313
<211> 465
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 313
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Lys Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser Val Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu Thr Ile Ile
180 185 190
Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln
195 200 205
Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
225 230 235 240
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
245 250 255
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
260 265 270
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
275 280 285
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
290 295 300
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
305 310 315 320
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
325 330 335
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
340 345 350
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
355 360 365
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
370 375 380
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
385 390 395 400
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
405 410 415
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
420 425 430
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
435 440 445
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
450 455 460
Arg
465
<210> 314
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 314
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Met
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 315
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 315
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Glu Pro
245 250 255
Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro
260 265 270
Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
275 280 285
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
290 295 300
Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
305 310 315 320
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
325 330 335
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
340 345 350
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
355 360 365
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
370 375 380
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln
385 390 395 400
Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
405 410 415
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
420 425 430
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
435 440 445
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
450 455 460
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
465 470 475 480
Leu Ser Pro Gly Lys
485
<210> 316
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 316
Asp Phe Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Thr
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 317
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 317
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Tyr Tyr Gly Gly Asp Trp Tyr Phe Asn Val Trp Gly
100 105 110
Ala Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 318
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 318
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Glu Pro
245 250 255
Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro
260 265 270
Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
275 280 285
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
290 295 300
Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
305 310 315 320
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
325 330 335
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
340 345 350
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
355 360 365
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
370 375 380
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln
385 390 395 400
Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
405 410 415
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
420 425 430
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
435 440 445
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
450 455 460
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
465 470 475 480
Leu Ser Pro Gly Lys
485
<210> 319
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 319
Gln Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Pro Leu Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Val Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Thr Ser Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 320
<400> 320
000
<210> 321
<400> 321
000
<210> 322
<400> 322
000
<210> 323
<400> 323
000
<210> 324
<400> 324
000
<210> 325
<400> 325
000
<210> 326
<400> 326
000
<210> 327
<400> 327
000
<210> 328
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 328
Glu Val Lys Leu Glu Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Ser Tyr Ile Ser Tyr Asp Gly Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Ser Tyr Tyr Tyr Val Met Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ala
115 120
<210> 329
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 329
gaagtgaagc tggagcagtc aggacctggc ctcgtgaaac cttctcagtc tctgtctctc 60
acctgctctg tcactggcta ctccatcacc agtggttatt actggaactg gatccggcag 120
tttccaggaa acaaactgga atggatgagc tacataagct acgacggtga caataactac 180
aacccatctc tcaaaaatcg aatctccatc actcgtgaca catctaagaa ccagtttttc 240
ctgaagttga gttctgtgac tactgaggac acagctacat attactgtgc aggaggctac 300
tataggtacg gcctgtcgta ttactatgtt atggactact ggggtcaagg aacctcagtc 360
acagtctccg ca 372
<210> 330
<211> 227
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 330
Glu Val Lys Leu Glu Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Ser Tyr Ile Ser Tyr Asp Gly Asp Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Gly Gly Tyr Tyr Arg Tyr Gly Leu Ser Tyr Tyr Tyr Val Met Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ala Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
210 215 220
Lys Ser Cys
225
<210> 331
<211> 681
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 331
gaagtgaagc tggagcagtc aggacctggc ctcgtgaaac cttctcagtc tctgtctctc 60
acctgctctg tcactggcta ctccatcacc agtggttatt actggaactg gatccggcag 120
tttccaggaa acaaactgga atggatgagc tacataagct acgacggtga caataactac 180
aacccatctc tcaaaaatcg aatctccatc actcgtgaca catctaagaa ccagtttttc 240
ctgaagttga gttctgtgac tactgaggac acagctacat attactgtgc aggaggctac 300
tataggtacg gcctgtcgta ttactatgtt atggactact ggggtcaagg aacctcagtc 360
acagtctccg cagctagcac caagggccca agtgtgtttc ccctggcccc cagcagcaag 420
tctacttccg gcggaactgc tgccctgggt tgcctggtga aggactactt ccccgagccc 480
gtgacagtgt cctggaactc tggggctctg acttccggcg tgcacacctt ccccgccgtg 540
ctgcagagca gcggcctgta cagcctgagc agcgtggtga cagtgccctc cagctctctg 600
ggaacccaga cctatatctg caacgtgaac cacaagccca gcaacaccaa ggtggacaag 660
agagtggagc ccaagagctg c 681
<210> 332
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 332
Asp Ile Lys Met Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asn Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 333
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 333
gatattaaga tgacccaatc tccagcctct ttggctgtgt ctctagggca gagggccacc 60
atctcctgca aggccagcca aagtgttgat tatgatggta atagttatat gaactggtac 120
caacagaaac caggacagcc acccaaactc ctcatctatg ctgcatccaa tctagaatct 180
gggatcccag ccaggtttag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatgc tgcaacctat tactgtcagc aaagtaatga ggatcctccg 300
acgttcggtg gaggcaccaa gctggaactc aaa 333
<210> 334
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 334
Asp Ile Lys Met Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asn Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 335
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 335
gatattaaga tgacccaatc tccagcctct ttggctgtgt ctctagggca gagggccacc 60
atctcctgca aggccagcca aagtgttgat tatgatggta atagttatat gaactggtac 120
caacagaaac caggacagcc acccaaactc ctcatctatg ctgcatccaa tctagaatct 180
gggatcccag ccaggtttag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatgc tgcaacctat tactgtcagc aaagtaatga ggatcctccg 300
acgttcggtg gaggcaccaa gctggaactc aaacgtacgg tggccgctcc cagcgtgttc 360
atcttccccc ccagcgacga gcagctgaag agtggcaccg ccagcgtggt gtgcctgctg 420
aacaacttct acccccggga ggccaaggtg cagtggaagg tggacaacgc cctgcagagc 480
ggcaacagcc aggagagcgt caccgagcag gacagcaagg actccaccta cagcctgagc 540
agcaccctga ccctgagcaa ggccgactac gagaagcata aggtgtacgc ctgcgaggtg 600
acccaccagg gcctgtccag ccccgtgacc aagagcttca acaggggcga gtgc 654
<210> 336
<211> 228
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 336
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Lys Tyr Asp Ile Ser Thr Tyr Asn Gln Gln Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Phe Phe Leu Tyr Tyr Gly Ile Asn Tyr Tyr Tyr Phe
100 105 110
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys
225
<210> 337
<211> 684
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 337
gaggtccaac tgcaacagtt tggagctgaa ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaagg cttctggcta cacattcact gactacaaca tggactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggagat attaatccta agtatgatat ttctacctac 180
aatcagcaat tcaagggaaa ggccacattg actgtagaca agtcctccag cacagcctac 240
atggagctcc gcagcctgac atctgaggac actgcagtct attattgtgc aagaagaggc 300
ttttttcttt actacggtat taactactat tacttcgatg tctggggcgc agggaccacg 360
gtcaccgtct cctcagctag caccaagggc ccaagtgtgt ttcccctggc ccccagcagc 420
aagtctactt ccggcggaac tgctgccctg ggttgcctgg tgaaggacta cttccccgag 480
cccgtgacag tgtcctggaa ctctggggct ctgacttccg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgacagtgcc ctccagctct 600
ctgggaaccc agacctatat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagagagtgg agcccaagag ctgc 684
<210> 338
<211> 226
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 338
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Gln Pro Gly Gln
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Asn Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Tyr Gly Thr Leu Tyr Ser Gly Tyr Gly Phe Phe Phe Asp Ser
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
210 215 220
Ser Cys
225
<210> 339
<211> 678
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 339
caggtccagc tggtgcagtc aggagctgag ctgaagcagc ctggacagtc ggtgaagatc 60
tcctgcaagg cttcagggta caccttcaca cactatggga tgaactgggt gaagcaggca 120
ccaggacagg gtctaaagtg gatgggctgg atcaacactg acactgggaa tccaacatat 180
gctgatgact tcaaaggacg gtttgtcttc tccttggaca cctctgtcag cactgcatat 240
ctgcagatca gcaacctcaa gaatgaagac acggccacgt attactgtgt gagatatgga 300
accctatata gcggatatgg gttttttttt gattcctggg gccaagggac cctggtcacc 360
gtctcctcag ctagcaccaa gggcccaagt gtgtttcccc tggcccccag cagcaagtct 420
acttccggcg gaactgctgc cctgggttgc ctggtgaagg actacttccc cgagcccgtg 480
acagtgtcct ggaactctgg ggctctgact tccggcgtgc acaccttccc cgccgtgctg 540
cagagcagcg gcctgtacag cctgagcagc gtggtgacag tgccctccag ctctctggga 600
acccagacct atatctgcaa cgtgaaccac aagcccagca acaccaaggt ggacaagaga 660
gtggagccca agagctgc 678
<210> 340
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 340
Asp Ile Met Met Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ala Gly
1 5 10 15
Glu Lys Ala Thr Ile Thr Cys Lys Ser Ser Gln Ser Leu Phe Asn Ser
20 25 30
Asn Thr Asn Lys Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Phe Tyr Tyr Ala Ser Thr Arg His Thr Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Thr Ser Val Gln Asp Glu Asp Leu Ala Asp Tyr Tyr Cys Gln Gln
85 90 95
Trp Tyr Ser Tyr Pro Trp Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 341
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 341
gacatcatga tgacccagtc tccatcatcc ctgagtgtgt cagcaggaga gaaagccact 60
atcacctgca agtccagtca gagtcttttc aacagtaaca ccaacaagaa ctacttgaac 120
tggtacctgc agaaaccagg gcagtctcct aaactgctgt tctattatgc atccactagg 180
catactgggg tccctgatcg cttcataggc agtggatctg ggacagattt cactctcacc 240
atcaccagtg tccaggatga agacctggca gattattact gtcagcagtg gtatagctac 300
ccgtggacgt tcggacctgg caccaagctg gaaatcaaac gtacggtggc cgctcccagc 360
gtgttcatct tcccccccag cgacgagcag ctgaagagtg gcaccgccag cgtggtgtgc 420
ctgctgaaca acttctaccc ccgggaggcc aaggtgcagt ggaaggtgga caacgccctg 480
cagagcggca acagccagga gagcgtcacc gagcaggaca gcaaggactc cacctacagc 540
ctgagcagca ccctgaccct gagcaaggcc gactacgaga agcataaggt gtacgcctgc 600
gaggtgaccc accagggcct gtccagcccc gtgaccaaga gcttcaacag gggcgagtgc 660
<210> 342
<211> 1485
<212> ДНК
<213> Homo sapiens
<400> 342
atggccggga aggtgcggtc actgctgccg ccgctgctgc tggccgccgc gggcctcgcc 60
ggcctcctac tgctgtgcgt ccccacccgc gacgtccggg agccgcccgc cctcaagtat 120
ggcatcgtcc tggacgctgg ttcttcacac acgtccatgt ttatctacaa gtggccggca 180
gacaaggaga acgacacagg cattgtgggc cagcacagct cctgtgatgt tccaggtggg 240
ggcatctcca gctatgcaga caacccttct ggggccagcc agagtcttgt tggatgcctc 300
gaacaggcgc ttcaggatgt gcccaaagag agacacgcgg gcacacccct ctacctggga 360
gccacagcgg gtatgcgcct gctcaacctg accaatccag aggcctcgac cagtgtgctc 420
atggcagtga ctcacacact gacccagtac ccctttgact tccggggtgc acgcatcctc 480
tcgggccagg aagagggggt gtttggctgg gtgactgcca actacctgct ggagaacttc 540
atcaagtacg gctgggtggg ccggtggttc cggccacgga aggggacact gggggccatg 600
gacctggggg gtgcctctac ccagatcact tttgagacaa ccagtccagc tgaggacaga 660
gccagcgagg tccagctgca tctctacggc cagcactacc gagtctacac ccacagcttc 720
ctctgctatg gccgtgacca ggtcctccag aggctgctgg ccagcgccct ccagacccac 780
ggcttccacc cctgctggcc gaggggcttt tccacccaag tgctgctcgg ggatgtgtac 840
cagtcaccat gcaccatggc ccagcggccc cagaacttca acagcagtgc cagggtcagc 900
ctgtcaggga gcagtgaccc ccacctctgc cgagatctgg tttctgggct cttcagcttc 960
tcctcctgcc ccttctcccg atgctctttc aatggggtct tccagccccc agtggctggg 1020
aactttgtgg ccttctctgc cttcttctac actgtggact ttttgcggac ttcgatgggg 1080
ctgcccgtgg ccaccctgca gcagctggag gcagccgcag tgaatgtctg caaccagacc 1140
tgggctcagc tgcaagctcg ggtgccaggg caacgggccc gcctggccga ctactgcgcc 1200
ggggccatgt tcgtgcagca gctgctgagt cgcggctacg gcttcgacga gcgcgccttc 1260
ggcggcgtga tcttccagaa gaaggccgcg gacactgcag tgggctgggc gctcggctac 1320
atgctgaacc tgaccaacct gatccccgcc gacccgccgg ggctgcgcaa gggcacagac 1380
ttcagctcct gggtcgtcct cctgctgctc ttcgcctccg cgctcctggc tgcgcttgtc 1440
ctgctgctgc gtcaggtgca ctccgccaag ctgccaagca ccatt 1485
<210> 343
<211> 495
<212> БЕЛОК
<213> Macaca fascicularis
<400> 343
Met Ala Gly Lys Val Arg Ser Leu Leu Pro Pro Leu Leu Leu Ala Ala
1 5 10 15
Ala Gly Leu Ala Gly Leu Leu Leu Leu Cys Val Pro Thr Arg Asp Ile
20 25 30
Arg Glu Pro Pro Ala Leu Lys Tyr Gly Ile Val Leu Asp Ala Gly Ser
35 40 45
Ser His Thr Ser Met Phe Ile Tyr Lys Trp Pro Ala Asp Lys Glu Asn
50 55 60
Asp Thr Gly Ile Val Gly Gln His Ser Ser Cys Asp Val Pro Gly Gly
65 70 75 80
Gly Ile Ser Ser Tyr Ala Asp Asn Pro Ser Gly Ala Gly Gln Ser Leu
85 90 95
Val Gly Cys Leu Glu Gln Ala Leu Arg Asp Val Pro Lys Glu Arg His
100 105 110
Ala Gly Thr Pro Leu Tyr Leu Gly Ala Thr Ala Gly Met Arg Leu Leu
115 120 125
Asn Leu Thr Asn Pro Glu Ala Ser Thr Ser Val Leu Thr Ala Val Thr
130 135 140
His Thr Leu Thr Gln Tyr Pro Phe Asp Phe Arg Gly Ala Arg Ile Leu
145 150 155 160
Ser Gly Gln Glu Glu Gly Val Phe Gly Trp Val Thr Ala Asn Tyr Leu
165 170 175
Leu Glu Asn Phe Ile Lys Tyr Gly Trp Val Gly Arg Trp Phe Arg Pro
180 185 190
Arg Lys Gly Thr Leu Gly Ala Met Asp Leu Gly Gly Ala Ser Thr Gln
195 200 205
Ile Thr Phe Glu Thr Thr Ser Pro Ala Glu Asp Arg Ala Ser Glu Val
210 215 220
Gln Leu Arg Leu Tyr Gly Gln His Tyr Arg Val Tyr Thr His Ser Phe
225 230 235 240
Leu Cys Tyr Gly Arg Asp Gln Val Leu Gln Arg Leu Leu Ala Ser Ala
245 250 255
Leu Gln Thr His Ser Phe His Pro Cys Trp Pro Arg Gly Phe Ser Thr
260 265 270
His Val Leu Leu Gly Asp Val Tyr Gln Ser Pro Cys Thr Val Ala Gln
275 280 285
Arg Pro Gln Thr Phe Asn Ser Ser Ala Arg Val Ser Leu Ser Gly Ser
290 295 300
Ser Asp Pro His Leu Cys Arg Asp Leu Val Ser Gly Leu Phe Ser Phe
305 310 315 320
Ser Ser Cys Pro Phe Ser Arg Cys Ser Phe Asn Gly Val Phe Gln Pro
325 330 335
Pro Val Ala Gly Asn Phe Ile Ala Phe Ser Ala Phe Phe Tyr Thr Val
340 345 350
Asn Phe Leu Arg Thr Ser Met Gly Leu Pro Val Ala Thr Leu Gln Gln
355 360 365
Leu Glu Ala Ala Ala Val Asn Val Cys Asn Gln Thr Trp Ala Gln Leu
370 375 380
Gln Ala Arg Val Pro Gly Gln Gln Ala His Leu Ala Asp Tyr Cys Ala
385 390 395 400
Gly Ala Met Phe Val Gln Gln Leu Leu Ser Arg Gly Tyr Gly Phe Asp
405 410 415
Glu Arg Ala Phe Gly Gly Val Ile Phe Gln Lys Lys Ala Ala Asp Thr
420 425 430
Ala Val Gly Trp Ala Leu Gly Tyr Met Leu Asn Leu Thr Asn Leu Ile
435 440 445
Pro Ala Asp Pro Pro Gly Leu Arg Lys Gly Thr Asp Phe Ser Ser Trp
450 455 460
Val Val Leu Leu Leu Leu Phe Ala Ser Ala Leu Leu Ala Ala Leu Val
465 470 475 480
Leu Leu Leu His Gln Val His Ser Ala Lys Leu Pro Ser Thr Ile
485 490 495
<210> 344
<211> 1485
<212> ДНК
<213> Macaca fascicularis
<400> 344
atggccggga aggtgcggtc actgctgccg ccgctgctgc tggccgccgc gggcctcgcc 60
ggcctcctac tgctgtgcgt gcccaccagg gacattaggg agcctcccgc tctgaaatac 120
ggcatcgtgc tggacgccgg aagcagccac acctccatgt tcatctacaa gtggcccgcc 180
gacaaggaga acgacacagg catcgtgggc cagcatagct cctgcgacgt gcctggaggc 240
ggcatctcca gctacgccga caatccttcc ggcgctggac agtccctggt gggatgtctg 300
gagcaggccc tgagggacgt gcctaaggag agacacgccg gcacccctct gtacctggga 360
gccacagccg gcatgagact cctgaatctg accaaccctg aggcctccac ctccgtcctg 420
acagccgtga cacataccct gacccagtac cccttcgatt tcaggggagc cagaatactg 480
agcggccagg aagaaggcgt gttcggatgg gtgaccgcca actacctcct ggagaacttc 540
atcaagtacg gctgggtggg caggtggttt agacccagga agggcaccct gggagctatg 600
gatctgggcg gagcttccac acagatcacc ttcgagacca cctcccccgc tgaggacaga 660
gcctccgagg tgcagctgag gctgtacggc cagcattaca gggtgtatac acacagcttc 720
ctgtgctacg gcagggacca ggtcctgcag agactgctcg cttccgccct gcagacccac 780
tccttccacc cttgctggcc taggggcttt agcacccatg tgctcctggg agatgtgtac 840
cagagcccct gcaccgtggc ccaaagaccc cagaccttta actcctccgc tagagtgagc 900
ctgagcggca gctccgatcc ccacctgtgt agggacctgg tcagcggact gttcagcttc 960
agcagctgcc ctttcagcag gtgcagcttc aatggcgtgt tccagcctcc cgtggccggc 1020
aacttcatcg ctttctccgc cttcttctac accgtcaact ttctgaggac aagcatggga 1080
ctgcccgtgg ctaccctcca acaactggag gccgccgccg tgaacgtgtg caaccagaca 1140
tgggcccaac tgcaggctag ggtgcccggc caacaggccc atctggctga ctactgtgcc 1200
ggcgccatgt tcgtgcagca gctgctgagc aggggctatg gattcgacga gagggccttc 1260
ggcggcgtca tcttccaaaa gaaggccgcc gatacagccg tgggctgggc tctgggctac 1320
atgctgaacc tgacaaacct gatccccgct gacccccccg gactgaggaa gggaaccgat 1380
ttcagcagct gggtcgtgct cctgctgctg tttgctagcg ccctgctcgc cgctctggtg 1440
ctgctgctgc accaggtgca ctccgccaag ctgcccagca ccatt 1485
<210> 345
<211> 495
<212> БЕЛОК
<213> Mus musculus
<400> 345
Met Ala Gly Lys Leu Val Ser Leu Val Pro Pro Leu Leu Leu Ala Ala
1 5 10 15
Val Gly Leu Ala Gly Leu Leu Leu Leu Cys Val Pro Thr Gln Asp Val
20 25 30
Arg Glu Pro Pro Ala Leu Lys Tyr Gly Ile Val Leu Asp Ala Gly Ser
35 40 45
Ser His Thr Ser Met Phe Val Tyr Lys Trp Pro Ala Asp Lys Glu Asn
50 55 60
Asp Thr Gly Ile Val Gly Gln His Ser Ser Cys Asp Val Arg Gly Gly
65 70 75 80
Gly Ile Ser Ser Tyr Ala Asn Asp Pro Ser Arg Ala Gly Gln Ser Leu
85 90 95
Val Glu Cys Leu Glu Gln Ala Leu Arg Asp Val Pro Lys Asp Arg Tyr
100 105 110
Ala Ser Thr Pro Leu Tyr Leu Gly Ala Thr Ala Gly Met Arg Leu Leu
115 120 125
Asn Leu Thr Ser Pro Glu Ala Thr Ala Lys Val Leu Glu Ala Val Thr
130 135 140
Gln Thr Leu Thr Arg Tyr Pro Phe Asp Phe Arg Gly Ala Arg Ile Leu
145 150 155 160
Ser Gly Gln Asp Glu Gly Val Phe Gly Trp Val Thr Ala Asn Tyr Leu
165 170 175
Leu Glu Asn Phe Ile Lys Tyr Gly Trp Val Gly Arg Trp Ile Arg Pro
180 185 190
Arg Lys Gly Thr Leu Gly Ala Met Asp Leu Gly Gly Ala Ser Thr Gln
195 200 205
Ile Thr Phe Glu Thr Thr Ser Pro Ser Glu Asp Pro Asp Asn Glu Val
210 215 220
His Leu Arg Leu Tyr Gly Gln His Tyr Arg Val Tyr Thr His Ser Phe
225 230 235 240
Leu Cys Tyr Gly Arg Asp Gln Val Leu Gln Arg Leu Leu Ala Ser Ala
245 250 255
Leu Gln Ile His Arg Phe His Pro Cys Trp Pro Lys Gly Tyr Ser Thr
260 265 270
Gln Val Leu Leu Arg Glu Val Tyr Gln Ser Pro Cys Thr Met Gly Gln
275 280 285
Arg Pro Gln Thr Phe Asn Ser Ser Ala Thr Val Ser Leu Ser Gly Thr
290 295 300
Ser Asn Ala Ala Leu Cys Arg Asp Leu Val Ser Gly Leu Phe Asn Ile
305 310 315 320
Ser Ser Cys Pro Phe Ser Gln Cys Ser Phe Asn Gly Val Phe Gln Pro
325 330 335
Pro Val Ala Gly Asn Phe Ile Ala Phe Ser Ala Phe Tyr Tyr Thr Val
340 345 350
Asp Phe Leu Lys Thr Val Met Gly Leu Pro Val Gly Thr Leu Lys Gln
355 360 365
Leu Glu Asp Ala Thr Glu Thr Thr Cys Asn Gln Thr Trp Ala Glu Leu
370 375 380
Gln Ala Arg Val Pro Gly Gln Gln Thr Arg Leu Pro Asp Tyr Cys Ala
385 390 395 400
Val Ala Met Phe Ile His Gln Leu Leu Ser Arg Gly Tyr Arg Phe Asp
405 410 415
Glu Arg Ser Phe Arg Gly Val Val Phe Glu Lys Lys Ala Ala Asp Thr
420 425 430
Ala Val Gly Trp Ala Leu Gly Tyr Met Leu Asn Leu Thr Asn Leu Ile
435 440 445
Pro Ala Asp Leu Pro Gly Leu Arg Lys Gly Thr His Phe Ser Ser Trp
450 455 460
Val Ala Leu Leu Leu Leu Phe Thr Val Leu Ile Leu Ala Ala Leu Val
465 470 475 480
Leu Leu Leu Arg Gln Val Arg Ser Ala Lys Ser Pro Gly Ala Leu
485 490 495
<210> 346
<211> 1485
<212> ДНК
<213> Mus musculus
<400> 346
atggctggaa agttggtgtc actggtgcca cccctgctgc tggctgccgt gggcctcgcc 60
ggcctcctgc tactgtgcgt ccctacccaa gacgtccggg agccgcccgc cctcaagtat 120
ggcatcgttc tggatgctgg ctcttcacac acatccatgt ttgtctacaa gtggccagcg 180
gacaaggaaa atgacacagg tatcgtgggc cagcacagct cttgcgatgt tcgaggtggt 240
ggcatctcca gctacgcaaa tgacccttct agggcaggcc agagtctggt tgaatgtctt 300
gaacaggcac ttcgggatgt gcccaaagac agatatgcca gcactccact ctacctggga 360
gctacagcag gcatgcgcct actcaacctg accagcccag aggccacagc caaggtgctg 420
gaggcagtga cacagacgct cacacggtac ccctttgact tccgtggtgc ccgcatcctc 480
tcgggacagg atgaaggggt gtttggctgg gtgactgcca actacctgct ggagaacttc 540
atcaagtatg gctgggtagg ccggtggata cggccaagga agggaactct gggggccatg 600
gaccttgggg gtgcctcaac acagatcacc tttgagacaa ccagtccatc tgaagatcca 660
gataatgagg tccatttgcg gctctatggc cagcattacc gtgtctacac ccatagcttc 720
ctctgctatg gccgggacca ggttctccag aggcttctgg ccagtgccct ccagatccat 780
cgcttccacc cctgctggcc aaagggctac tccacccaag tgctgctccg ggaagtctac 840
cagtctccat gcactatggg tcagcgtccc cagaccttca acagcagtgc cactgtcagc 900
ctgtcaggga ccagcaacgc tgccctctgt cgtgacctcg tctctgggct cttcaatatc 960
tcctcctgtc ccttttccca atgctccttc aatggggttt tccagcctcc cgtggctggg 1020
aacttcatag ccttttctgc tttctactat actgtagact tcctgaagac agtgatgggg 1080
ctgcctgtgg gaaccctgaa gcagctggag gatgccacag agaccacctg caaccagacc 1140
tgggctgagc ttcaggcccg agtacccgga cagcagaccc gcctgcctga ctactgcgct 1200
gtagccatgt tcatacatca gctattgagc cgcggttatc gcttcgacga gcgctctttc 1260
cgtggagtgg tcttcgaaaa gaaggcggca gacacggctg tcggctgggc gctgggctac 1320
atgctgaatt tgaccaacct gattcccgct gacctcccgg gactacgtaa gggcacccac 1380
ttcagctcct gggttgctct cctgctgctc ttcacagtcc tgatcttggc ggctttggtc 1440
ctgctcttgc gccaggtgcg ctctgccaag tccccaggcg ccctc 1485
<210> 347
<211> 495
<212> БЕЛОК
<213> Rattus norvegicus
<400> 347
Met Ala Gly Lys Leu Val Ser Leu Val Pro Pro Leu Leu Leu Ala Ala
1 5 10 15
Ala Gly Leu Ala Gly Leu Leu Leu Leu Cys Val Pro Thr Gln Asp Val
20 25 30
Arg Glu Pro Pro Ala Leu Lys Tyr Gly Ile Val Leu Asp Ala Gly Ser
35 40 45
Ser His Thr Ser Met Phe Val Tyr Lys Trp Pro Ala Asp Lys Glu Asn
50 55 60
Asp Thr Gly Ile Val Gly Gln His Ser Ser Cys Asp Val Gln Gly Gly
65 70 75 80
Gly Ile Ser Ser Tyr Ala Asn Asp Pro Ser Lys Ala Gly Gln Ser Leu
85 90 95
Val Arg Cys Leu Glu Gln Ala Leu Arg Asp Val Pro Arg Asp Arg His
100 105 110
Ala Ser Thr Pro Leu Tyr Leu Gly Ala Thr Ala Gly Met Arg Leu Leu
115 120 125
Asn Leu Thr Ser Pro Glu Ala Thr Ala Arg Val Leu Glu Ala Val Thr
130 135 140
Gln Thr Leu Thr Gln Tyr Pro Phe Asp Phe Arg Gly Ala Arg Ile Leu
145 150 155 160
Ser Gly Gln Asp Glu Gly Val Phe Gly Trp Val Thr Ala Asn Tyr Leu
165 170 175
Leu Glu Asn Phe Ile Lys Tyr Gly Trp Val Gly Arg Trp Ile Arg Pro
180 185 190
Arg Lys Gly Thr Leu Gly Ala Met Asp Leu Gly Gly Ala Ser Thr Gln
195 200 205
Ile Thr Phe Glu Thr Thr Ser Pro Ser Glu Asp Pro Gly Asn Glu Val
210 215 220
His Leu Arg Leu Tyr Gly Gln His Tyr Arg Val Tyr Thr His Ser Phe
225 230 235 240
Leu Cys Tyr Gly Arg Asp Gln Ile Leu Leu Arg Leu Leu Ala Ser Ala
245 250 255
Leu Gln Ile His Arg Phe His Pro Cys Trp Pro Lys Gly Tyr Ser Thr
260 265 270
Gln Val Leu Leu Gln Glu Val Tyr Gln Ser Pro Cys Thr Met Gly Gln
275 280 285
Arg Pro Arg Ala Phe Asn Gly Ser Ala Ile Val Ser Leu Ser Gly Thr
290 295 300
Ser Asn Ala Thr Leu Cys Arg Asp Leu Val Ser Arg Leu Phe Asn Ile
305 310 315 320
Ser Ser Cys Pro Phe Ser Gln Cys Ser Phe Asn Gly Val Phe Gln Pro
325 330 335
Pro Val Thr Gly Asn Phe Ile Ala Phe Ser Ala Phe Tyr Tyr Thr Val
340 345 350
Asp Phe Leu Thr Thr Val Met Gly Leu Pro Val Gly Thr Leu Lys Gln
355 360 365
Leu Glu Glu Ala Thr Glu Ile Thr Cys Asn Gln Thr Trp Thr Glu Leu
370 375 380
Gln Ala Arg Val Pro Gly Gln Lys Thr Arg Leu Ala Asp Tyr Cys Ala
385 390 395 400
Val Ala Met Phe Ile His Gln Leu Leu Ser Arg Gly Tyr His Phe Asp
405 410 415
Glu Arg Ser Phe Arg Glu Val Val Phe Gln Lys Lys Ala Ala Asp Thr
420 425 430
Ala Val Gly Trp Ala Leu Gly Tyr Met Leu Asn Phe Thr Asn Leu Ile
435 440 445
Pro Ala Asp Leu Pro Gly Leu Arg Lys Gly Thr His Phe Ser Ser Trp
450 455 460
Val Ala Leu Leu Leu Leu Phe Thr Val Leu Ile Leu Ala Ala Leu Val
465 470 475 480
Leu Leu Leu Arg Gln Val Arg Ser Ala Lys Ser Pro Gly Ala Leu
485 490 495
<210> 348
<211> 1485
<212> ДНК
<213> Rattus norvegicus
<400> 348
atggctggaa agttggtgtc actggtgcca cccctgctgc tggctgccgc gggcctcgcc 60
ggcctcctgc tactgtgcgt ccctacccaa gacgtccggg agccgcccgc cctcaagtat 120
ggcatcgttc tggatgctgg ctcttcacac acatccatgt ttgtctacaa gtggccagcg 180
gacaaggaaa atgacacagg tatcgtgggc cagcacagct cctgcgatgt gcagggcggc 240
ggcatttcca gctatgccaa cgacccctcc aaagccggac agtccctggt caggtgcctg 300
gagcaggccc tgagagacgt ccccagagac agacacgcga gcacccctct gtatctcggc 360
gccacagccg gcatgaggct gctgaacctg acctcccctg aggccacagc cagagtcctg 420
gaggctgtca cccagaccct gacacagtac cccttcgact ttaggggcgc cagaatactg 480
tccggccagg atgaaggcgt gttcggctgg gtgacagcca actacctgct ggagaacttt 540
attaagtacg gctgggtggg cagatggatc aggcccagga agggcaccct gggagccatg 600
gatctcggcg gagcctccac ccagatcacc tttgagacca ccagcccctc cgaagacccg 660
ggcaatgagg tccacctgag gctgtacggc cagcactata gagtctacac ccacagcttc 720
ctgtgctacg gcagagatca aatcctgctg agactgctcg cttccgccct gcagattcat 780
aggtttcacc cctgctggcc caaaggctac agcacccagg tgctgctcca agaggtgtac 840
cagagccctt gcaccatggg acagagaccc agggctttca acggaagcgc catcgtgtcc 900
ctcagcggca ccagcaacgc caccctgtgt agggacctcg tgagcagact gttcaacatc 960
tcctcctgcc ctttcagcca gtgttccttc aatggcgtgt ttcagccccc tgtgacaggc 1020
aacttcatcg ccttcagcgc tttctactac accgtggact ttctcacaac cgtcatgggc 1080
ctgcccgtgg gaaccctgaa gcaactggag gaagccaccg agatcacctg caaccagacc 1140
tggaccgaac tgcaagccag ggtgcccggc cagaagacca gactggccga ctactgtgct 1200
gtcgccatgt tcattcacca actgctgagc aggggctacc acttcgatga aaggagcttc 1260
agggaggtgg tgttccagaa gaaggccgcc gataccgctg tgggctgggc tctgggctac 1320
atgctcaact tcaccaacct gatccccgcc gatctccccg gactgaggaa gggaacccac 1380
ttcagctcct gggttgctct cctgctgctc ttcacagtcc tgatcttggc ggctttggtc 1440
ctgctcttgc gccaggtgcg ctctgccaag tccccaggcg ccctc 1485
<210> 349
<211> 510
<212> БЕЛОК
<213> Homo sapiens
<400> 349
Met Glu Asp Thr Lys Glu Ser Asn Val Lys Thr Phe Cys Ser Lys Asn
1 5 10 15
Ile Leu Ala Ile Leu Gly Phe Ser Ser Ile Ile Ala Val Ile Ala Leu
20 25 30
Leu Ala Val Gly Leu Thr Gln Asn Lys Ala Leu Pro Glu Asn Val Lys
35 40 45
Tyr Gly Ile Val Leu Asp Ala Gly Ser Ser His Thr Ser Leu Tyr Ile
50 55 60
Tyr Lys Trp Pro Ala Glu Lys Glu Asn Asp Thr Gly Val Val His Gln
65 70 75 80
Val Glu Glu Cys Arg Val Lys Gly Pro Gly Ile Ser Lys Phe Val Gln
85 90 95
Lys Val Asn Glu Ile Gly Ile Tyr Leu Thr Asp Cys Met Glu Arg Ala
100 105 110
Arg Glu Val Ile Pro Arg Ser Gln His Gln Glu Thr Pro Val Tyr Leu
115 120 125
Gly Ala Thr Ala Gly Met Arg Leu Leu Arg Met Glu Ser Glu Glu Leu
130 135 140
Ala Asp Arg Val Leu Asp Val Val Glu Arg Ser Leu Ser Asn Tyr Pro
145 150 155 160
Phe Asp Phe Gln Gly Ala Arg Ile Ile Thr Gly Gln Glu Glu Gly Ala
165 170 175
Tyr Gly Trp Ile Thr Ile Asn Tyr Leu Leu Gly Lys Phe Ser Gln Lys
180 185 190
Thr Arg Trp Phe Ser Ile Val Pro Tyr Glu Thr Asn Asn Gln Glu Thr
195 200 205
Phe Gly Ala Leu Asp Leu Gly Gly Ala Ser Thr Gln Val Thr Phe Val
210 215 220
Pro Gln Asn Gln Thr Ile Glu Ser Pro Asp Asn Ala Leu Gln Phe Arg
225 230 235 240
Leu Tyr Gly Lys Asp Tyr Asn Val Tyr Thr His Ser Phe Leu Cys Tyr
245 250 255
Gly Lys Asp Gln Ala Leu Trp Gln Lys Leu Ala Lys Asp Ile Gln Val
260 265 270
Ala Ser Asn Glu Ile Leu Arg Asp Pro Cys Phe His Pro Gly Tyr Lys
275 280 285
Lys Val Val Asn Val Ser Asp Leu Tyr Lys Thr Pro Cys Thr Lys Arg
290 295 300
Phe Glu Met Thr Leu Pro Phe Gln Gln Phe Glu Ile Gln Gly Ile Gly
305 310 315 320
Asn Tyr Gln Gln Cys His Gln Ser Ile Leu Glu Leu Phe Asn Thr Ser
325 330 335
Tyr Cys Pro Tyr Ser Gln Cys Ala Phe Asn Gly Ile Phe Leu Pro Pro
340 345 350
Leu Gln Gly Asp Phe Gly Ala Phe Ser Ala Phe Tyr Phe Val Met Lys
355 360 365
Phe Leu Asn Leu Thr Ser Glu Lys Val Ser Gln Glu Lys Val Thr Glu
370 375 380
Met Met Lys Lys Phe Cys Ala Gln Pro Trp Glu Glu Ile Lys Thr Ser
385 390 395 400
Tyr Ala Gly Val Lys Glu Lys Tyr Leu Ser Glu Tyr Cys Phe Ser Gly
405 410 415
Thr Tyr Ile Leu Ser Leu Leu Leu Gln Gly Tyr His Phe Thr Ala Asp
420 425 430
Ser Trp Glu His Ile His Phe Ile Gly Lys Ile Gln Gly Ser Asp Ala
435 440 445
Gly Trp Thr Leu Gly Tyr Met Leu Asn Leu Thr Asn Met Ile Pro Ala
450 455 460
Glu Gln Pro Leu Ser Thr Pro Leu Ser His Ser Thr Tyr Val Phe Leu
465 470 475 480
Met Val Leu Phe Ser Leu Val Leu Phe Thr Val Ala Ile Ile Gly Leu
485 490 495
Leu Ile Phe His Lys Pro Ser Tyr Phe Trp Lys Asp Met Val
500 505 510
<210> 350
<211> 1530
<212> ДНК
<213> Homo sapiens
<400> 350
atggaagata caaaggagtc taacgtgaag acattttgct ccaagaatat cctagccatc 60
cttggcttct cctctatcat agctgtgata gctttgcttg ctgtggggtt gacccagaac 120
aaagcattgc cagaaaacgt taagtatggg attgtgctgg atgcgggttc ttctcacaca 180
agtttataca tctataagtg gccagcagaa aaggagaatg acacaggcgt ggtgcatcaa 240
gtagaagaat gcagggttaa aggtcctgga atctcaaaat ttgttcagaa agtaaatgaa 300
ataggcattt acctgactga ttgcatggaa agagctaggg aagtgattcc aaggtcccag 360
caccaagaga cacccgttta cctgggagcc acggcaggca tgcggttgct caggatggaa 420
agtgaagagt tggcagacag ggttctggat gtggtggaga ggagcctcag caactacccc 480
tttgacttcc agggtgccag gatcattact ggccaagagg aaggtgccta tggctggatt 540
actatcaact atctgctggg caaattcagt cagaaaacaa ggtggttcag catagtccca 600
tatgaaacca ataatcagga aacctttgga gctttggacc ttgggggagc ctctacacaa 660
gtcacttttg taccccaaaa ccagactatc gagtccccag ataatgctct gcaatttcgc 720
ctctatggca aggactacaa tgtctacaca catagcttct tgtgctatgg gaaggatcag 780
gcactctggc agaaactggc caaggacatt caggttgcaa gtaatgaaat tctcagggac 840
ccatgctttc atcctggata taagaaggta gtgaacgtaa gtgaccttta caagaccccc 900
tgcaccaaga gatttgagat gactcttcca ttccagcagt ttgaaatcca gggtattgga 960
aactatcaac aatgccatca aagcatcctg gagctcttca acaccagtta ctgcccttac 1020
tcccagtgtg ccttcaatgg gattttcttg ccaccactcc agggggattt tggggcattt 1080
tcagcttttt actttgtgat gaagttttta aacttgacat cagagaaagt ctctcaggaa 1140
aaggtgactg agatgatgaa aaagttctgt gctcagcctt gggaggagat aaaaacatct 1200
tacgctggag taaaggagaa gtacctgagt gaatactgct tttctggtac ctacattctc 1260
tccctccttc tgcaaggcta tcatttcaca gctgattcct gggagcacat ccatttcatt 1320
ggcaagatcc agggcagcga cgccggctgg actttgggct acatgctgaa cctgaccaac 1380
atgatcccag ctgagcaacc attgtccaca cctctctccc actccaccta tgtcttcctc 1440
atggttctat tctccctggt ccttttcaca gtggccatca taggcttgct tatctttcac 1500
aagccttcat atttctggaa agatatggta 1530
<210> 351
<211> 510
<212> БЕЛОК
<213> Mus musculus
<400> 351
Met Glu Asp Ile Lys Asp Ser Lys Val Lys Arg Phe Cys Ser Lys Asn
1 5 10 15
Ile Leu Ile Ile Leu Gly Phe Thr Ser Ile Leu Ala Val Ile Ala Leu
20 25 30
Ile Ala Val Gly Leu Thr Gln Asn Lys Pro Leu Pro Glu Asn Val Lys
35 40 45
Tyr Gly Ile Val Leu Asp Ala Gly Ser Ser His Thr Asn Leu Tyr Ile
50 55 60
Tyr Lys Trp Pro Ala Glu Lys Glu Asn Asp Thr Gly Val Val Gln Gln
65 70 75 80
Leu Glu Glu Cys Gln Val Lys Gly Pro Gly Ile Ser Lys Tyr Ala Gln
85 90 95
Lys Thr Asp Glu Ile Gly Ala Tyr Leu Ala Glu Cys Met Glu Leu Ser
100 105 110
Thr Glu Leu Ile Pro Thr Ser Lys His His Gln Thr Pro Val Tyr Leu
115 120 125
Gly Ala Thr Ala Gly Met Arg Leu Leu Arg Met Glu Ser Glu Gln Ser
130 135 140
Ala Asp Glu Val Leu Ala Ala Val Ser Thr Ser Leu Lys Ser Tyr Pro
145 150 155 160
Phe Asp Phe Gln Gly Ala Lys Ile Ile Thr Gly Gln Glu Glu Gly Ala
165 170 175
Tyr Gly Trp Ile Thr Ile Asn Tyr Leu Leu Gly Arg Phe Thr Gln Glu
180 185 190
Gln Ser Trp Leu Ser Leu Ile Ser Asp Ser Gln Lys Gln Glu Thr Phe
195 200 205
Gly Ala Leu Asp Leu Gly Gly Ala Ser Thr Gln Ile Thr Phe Val Pro
210 215 220
Gln Asn Ser Thr Ile Glu Ser Pro Glu Asn Ser Leu Gln Phe Arg Leu
225 230 235 240
Tyr Gly Glu Asp Tyr Thr Val Tyr Thr His Ser Phe Leu Cys Tyr Gly
245 250 255
Lys Asp Gln Ala Leu Trp Gln Lys Leu Ala Lys Asp Ile Gln Val Ser
260 265 270
Ser Gly Gly Val Leu Lys Asp Pro Cys Phe Asn Pro Gly Tyr Glu Lys
275 280 285
Val Val Asn Val Ser Glu Leu Tyr Gly Thr Pro Cys Thr Lys Arg Phe
290 295 300
Glu Lys Lys Leu Pro Phe Asp Gln Phe Arg Ile Gln Gly Thr Gly Asp
305 310 315 320
Tyr Glu Gln Cys His Gln Ser Ile Leu Glu Leu Phe Asn Asn Ser His
325 330 335
Cys Pro Tyr Ser Gln Cys Ala Phe Asn Gly Val Phe Leu Pro Pro Leu
340 345 350
His Gly Ser Phe Gly Ala Phe Ser Ala Phe Tyr Phe Val Met Asp Phe
355 360 365
Phe Lys Lys Val Ala Lys Asn Ser Val Ile Ser Gln Glu Lys Met Thr
370 375 380
Glu Ile Thr Lys Asn Phe Cys Ser Lys Ser Trp Glu Glu Thr Lys Thr
385 390 395 400
Ser Tyr Pro Ser Val Lys Glu Lys Tyr Leu Ser Glu Tyr Cys Phe Ser
405 410 415
Gly Ala Tyr Ile Leu Ser Leu Leu Gln Gly Tyr Asn Phe Thr Asp Ser
420 425 430
Ser Trp Glu Gln Ile His Phe Met Gly Lys Ile Lys Asp Ser Asn Ala
435 440 445
Gly Trp Thr Leu Gly Tyr Met Leu Asn Leu Thr Asn Met Ile Pro Ala
450 455 460
Glu Gln Pro Leu Ser Pro Pro Leu Pro His Ser Thr Tyr Ile Gly Leu
465 470 475 480
Met Val Leu Phe Ser Leu Leu Leu Val Ala Val Ala Ile Thr Gly Leu
485 490 495
Phe Ile Tyr Ser Lys Pro Ser Tyr Phe Trp Lys Glu Ala Val
500 505 510
<210> 352
<211> 1530
<212> ДНК
<213> Mus musculus
<400> 352
atggaagata taaaggattc taaggtgaag agattttgct ccaaaaatat tctgatcatc 60
cttggtttca cctctatctt ggctgtgata gctttgattg ctgtgggact gacccagaac 120
aaacctttgc cagaaaatgt taagtatggg attgtgttgg atgcggggtc atctcacacc 180
aacctgtaca tctacaagtg gccggccgag aaggagaatg acacaggggt ggtgcagcag 240
ttagaggaat gccaagtgaa aggtcctgga atctcaaaat atgctcagaa aacagatgaa 300
atcggtgcgt acctggccga atgcatggaa ctgtccaccg aactgatacc aacatccaag 360
catcaccaga ctcctgtcta cctgggagcc acagcaggca tgcgcttgct tagaatggaa 420
agcgaacaat cggcagacga ggtcctggct gcagtgtcaa caagccttaa gagctacccc 480
tttgacttcc agggtgccaa gatcatcact ggacaagagg aaggtgccta tgggtggatt 540
actattaact atctgctggg cagattcact caggaacaga gttggctaag cctcatctca 600
gacagtcaga aacaggaaac ctttggcgct ttggatctcg gcggagcctc cacacagatc 660
accttcgtgc cccaaaacag cactatagag tccccagaaa actctctgca attccgtctc 720
tatggcgagg actatactgt gtacacacac agcttcctgt gctatgggaa ggatcaggct 780
ctctggcaga aactggccaa ggacattcag gtttcaagtg gtggcgtcct taaggaccca 840
tgctttaacc caggatacga gaaggttgtg aatgtaagtg agctctatgg cactccctgc 900
accaaaagat tcgaaaagaa gctaccattt gatcagtttc gaatccaggg cactggagac 960
tacgaacagt gccaccagag catccttgag ctcttcaaca acagccactg cccttactcc 1020
cagtgtgcct tcaatggcgt cttcctgcca cctctccatg ggagttttgg ggcgttttct 1080
gctttctact ttgtgatgga tttttttaag aaggtagcga aaaacagtgt catctctcag 1140
gagaaaatga ccgagataac aaaaaatttt tgctcaaaat cttgggaaga gacaaagaca 1200
tcttatcctt cagtaaagga gaagtacctg agtgagtact gcttctcggg cgcctacatc 1260
ctctctctcc tgcaaggcta taacttcaca gacagctcct gggaacagat tcattttatg 1320
ggcaagatca aagacagcaa cgcggggtgg actttgggct acatgctgaa cttgaccaac 1380
atgatcccag ctgaacagcc gttgtccccg cctctccctc actccaccta catcggcctc 1440
atggttctct tctccctgct cttggttgct gtggccatca caggcctgtt catctatagc 1500
aagccttcat atttctggaa agaggcagta 1530
<210> 353
<400> 353
000
<210> 354
<400> 354
000
<210> 355
<400> 355
000
<210> 356
<400> 356
000
<210> 357
<400> 357
000
<210> 358
<400> 358
000
<210> 359
<400> 359
000
<210> 360
<400> 360
000
<210> 361
<400> 361
000
<210> 362
<400> 362
000
<210> 363
<400> 363
000
<210> 364
<400> 364
000
<210> 365
<400> 365
000
<210> 366
<400> 366
000
<210> 367
<400> 367
000
<210> 368
<400> 368
000
<210> 369
<400> 369
000
<210> 370
<400> 370
000
<210> 371
<400> 371
000
<210> 372
<400> 372
000
<210> 373
<400> 373
000
<210> 374
<400> 374
000
<210> 375
<400> 375
000
<210> 376
<400> 376
000
<210> 377
<400> 377
000
<210> 378
<400> 378
000
<210> 379
<400> 379
000
<210> 380
<400> 380
000
<210> 381
<400> 381
000
<210> 382
<400> 382
000
<210> 383
<400> 383
000
<210> 384
<400> 384
000
<210> 385
<400> 385
000
<210> 386
<400> 386
000
<210> 387
<400> 387
000
<210> 388
<400> 388
000
<210> 389
<400> 389
000
<210> 390
<400> 390
000
<210> 391
<400> 391
000
<210> 392
<400> 392
000
<210> 393
<400> 393
000
<210> 394
<400> 394
000
<210> 395
<400> 395
000
<210> 396
<400> 396
000
<210> 397
<400> 397
000
<210> 398
<400> 398
000
<210> 399
<400> 399
000
<210> 400
<400> 400
000
<210> 401
<400> 401
000
<210> 402
<400> 402
000
<210> 403
<400> 403
000
<210> 404
<400> 404
000
<210> 405
<400> 405
000
<210> 406
<400> 406
000
<210> 407
<400> 407
000
<210> 408
<400> 408
000
<210> 409
<400> 409
000
<210> 410
<400> 410
000
<210> 411
<400> 411
000
<210> 412
<400> 412
000
<210> 413
<400> 413
000
<210> 414
<400> 414
000
<210> 415
<400> 415
000
<210> 416
<400> 416
000
<210> 417
<400> 417
000
<210> 418
<400> 418
000
<210> 419
<400> 419
000
<210> 420
<400> 420
000
<210> 421
<400> 421
000
<210> 422
<400> 422
000
<210> 423
<400> 423
000
<210> 424
<400> 424
000
<210> 425
<400> 425
000
<210> 426
<400> 426
000
<210> 427
<400> 427
000
<210> 428
<400> 428
000
<210> 429
<400> 429
000
<210> 430
<400> 430
000
<210> 431
<400> 431
000
<210> 432
<400> 432
000
<210> 433
<400> 433
000
<210> 434
<400> 434
000
<210> 435
<400> 435
000
<210> 436
<400> 436
000
<210> 437
<400> 437
000
<210> 438
<400> 438
000
<210> 439
<400> 439
000
<210> 440
<400> 440
000
<210> 441
<400> 441
000
<210> 442
<400> 442
000
<210> 443
<400> 443
000
<210> 444
<400> 444
000
<210> 445
<400> 445
000
<210> 446
<400> 446
000
<210> 447
<400> 447
000
<210> 448
<400> 448
000
<210> 449
<400> 449
000
<210> 450
<400> 450
000
<210> 451
<400> 451
000
<210> 452
<400> 452
000
<210> 453
<400> 453
000
<210> 454
<400> 454
000
<210> 455
<400> 455
000
<210> 456
<400> 456
000
<210> 457
<400> 457
000
<210> 458
<400> 458
000
<210> 459
<400> 459
000
<210> 460
<400> 460
000
<210> 461
<400> 461
000
<210> 462
<400> 462
000
<210> 463
<400> 463
000
<210> 464
<400> 464
000
<210> 465
<400> 465
000
<210> 466
<400> 466
000
<210> 467
<400> 467
000
<210> 468
<400> 468
000
<210> 469
<400> 469
000
<210> 470
<400> 470
000
<210> 471
<400> 471
000
<210> 472
<400> 472
000
<210> 473
<400> 473
000
<210> 474
<400> 474
000
<210> 475
<400> 475
000
<210> 476
<400> 476
000
<210> 477
<400> 477
000
<210> 478
<400> 478
000
<210> 479
<400> 479
000
<210> 480
<400> 480
000
<210> 481
<400> 481
000
<210> 482
<400> 482
000
<210> 483
<400> 483
000
<210> 484
<400> 484
000
<210> 485
<400> 485
000
<210> 486
<400> 486
000
<210> 487
<400> 487
000
<210> 488
<400> 488
000
<210> 489
<400> 489
000
<210> 490
<400> 490
000
<210> 491
<400> 491
000
<210> 492
<400> 492
000
<210> 493
<400> 493
000
<210> 494
<400> 494
000
<210> 495
<400> 495
000
<210> 496
<400> 496
000
<210> 497
<400> 497
000
<210> 498
<400> 498
000
<210> 499
<400> 499
000
<210> 500
<400> 500
000
<210> 501
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 501
Thr Tyr Trp Met His
1 5
<210> 502
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 502
Asn Ile Tyr Pro Gly Thr Gly Gly Ser Asn Phe Asp Glu Lys Phe Lys
1 5 10 15
Asn
<210> 503
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 503
Trp Thr Thr Gly Thr Gly Ala Tyr
1 5
<210> 504
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 504
Gly Tyr Thr Phe Thr Thr Tyr
1 5
<210> 505
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 505
Tyr Pro Gly Thr Gly Gly
1 5
<210> 506
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 506
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Thr Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Tyr Pro Gly Thr Gly Gly Ser Asn Phe Asp Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Trp Thr Thr Gly Thr Gly Ala Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 507
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 507
gaggtgcagc tggtgcagtc aggcgccgaa gtgaagaagc ccggcgagtc actgagaatt 60
agctgtaaag gttcaggcta caccttcact acctactgga tgcactgggt ccgccaggct 120
accggtcaag gcctcgagtg gatgggtaat atctaccccg gcaccggcgg ctctaacttc 180
gacgagaagt ttaagaatag agtgactatc accgccgata agtctactag caccgcctat 240
atggaactgt ctagcctgag atcagaggac accgccgtct actactgcac taggtggact 300
accggcacag gcgcctactg gggtcaaggc actaccgtga ccgtgtctag c 351
<210> 508
<211> 443
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 508
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Thr Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Tyr Pro Gly Thr Gly Gly Ser Asn Phe Asp Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Trp Thr Thr Gly Thr Gly Ala Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 509
<211> 1329
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 509
gaggtgcagc tggtgcagtc aggcgccgaa gtgaagaagc ccggcgagtc actgagaatt 60
agctgtaaag gttcaggcta caccttcact acctactgga tgcactgggt ccgccaggct 120
accggtcaag gcctcgagtg gatgggtaat atctaccccg gcaccggcgg ctctaacttc 180
gacgagaagt ttaagaatag agtgactatc accgccgata agtctactag caccgcctat 240
atggaactgt ctagcctgag atcagaggac accgccgtct actactgcac taggtggact 300
accggcacag gcgcctactg gggtcaaggc actaccgtga ccgtgtctag cgctagcact 360
aagggcccgt ccgtgttccc cctggcacct tgtagccgga gcactagcga atccaccgct 420
gccctcggct gcctggtcaa ggattacttc ccggagcccg tgaccgtgtc ctggaacagc 480
ggagccctga cctccggagt gcacaccttc cccgctgtgc tgcagagctc cgggctgtac 540
tcgctgtcgt cggtggtcac ggtgccttca tctagcctgg gtaccaagac ctacacttgc 600
aacgtggacc acaagccttc caacactaag gtggacaagc gcgtcgaatc gaagtacggc 660
ccaccgtgcc cgccttgtcc cgcgccggag ttcctcggcg gtccctcggt ctttctgttc 720
ccaccgaagc ccaaggacac tttgatgatt tcccgcaccc ctgaagtgac atgcgtggtc 780
gtggacgtgt cacaggaaga tccggaggtg cagttcaatt ggtacgtgga tggcgtcgag 840
gtgcacaacg ccaaaaccaa gccgagggag gagcagttca actccactta ccgcgtcgtg 900
tccgtgctga cggtgctgca tcaggactgg ctgaacggga aggagtacaa gtgcaaagtg 960
tccaacaagg gacttcctag ctcaatcgaa aagaccatct cgaaagccaa gggacagccc 1020
cgggaacccc aagtgtatac cctgccaccg agccaggaag aaatgactaa gaaccaagtc 1080
tcattgactt gccttgtgaa gggcttctac ccatcggata tcgccgtgga atgggagtcc 1140
aacggccagc cggaaaacaa ctacaagacc acccctccgg tgctggactc agacggatcc 1200
ttcttcctct actcgcggct gaccgtggat aagagcagat ggcaggaggg aaatgtgttc 1260
agctgttctg tgatgcatga agccctgcac aaccactaca ctcagaagtc cctgtccctc 1320
tccctggga 1329
<210> 510
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 510
Lys Ser Ser Gln Ser Leu Leu Asp Ser Gly Asn Gln Lys Asn Phe Leu
1 5 10 15
Thr
<210> 511
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 511
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 512
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 512
Gln Asn Asp Tyr Ser Tyr Pro Tyr Thr
1 5
<210> 513
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 513
Ser Gln Ser Leu Leu Asp Ser Gly Asn Gln Lys Asn Phe
1 5 10
<210> 514
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 514
Trp Ala Ser
1
<210> 515
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 515
Asp Tyr Ser Tyr Pro Tyr
1 5
<210> 516
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 516
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Gly Asn Gln Lys Asn Phe Leu Thr Trp Tyr Gln Gln Lys Pro Gly Lys
35 40 45
Ala Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr
65 70 75 80
Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 517
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 517
gagatcgtcc tgactcagtc acccgctacc ctgagcctga gccctggcga gcgggctaca 60
ctgagctgta aatctagtca gtcactgctg gatagcggta atcagaagaa cttcctgacc 120
tggtatcagc agaagcccgg taaagcccct aagctgctga tctactgggc ctctactaga 180
gaatcaggcg tgccctctag gtttagcggt agcggtagtg gcaccgactt caccttcact 240
atctctagcc tgcagcccga ggatatcgct acctactact gtcagaacga ctatagctac 300
ccctacacct tcggtcaagg cactaaggtc gagattaag 339
<210> 518
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 518
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Gly Asn Gln Lys Asn Phe Leu Thr Trp Tyr Gln Gln Lys Pro Gly Lys
35 40 45
Ala Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr
65 70 75 80
Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 519
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 519
gagatcgtcc tgactcagtc acccgctacc ctgagcctga gccctggcga gcgggctaca 60
ctgagctgta aatctagtca gtcactgctg gatagcggta atcagaagaa cttcctgacc 120
tggtatcagc agaagcccgg taaagcccct aagctgctga tctactgggc ctctactaga 180
gaatcaggcg tgccctctag gtttagcggt agcggtagtg gcaccgactt caccttcact 240
atctctagcc tgcagcccga ggatatcgct acctactact gtcagaacga ctatagctac 300
ccctacacct tcggtcaagg cactaaggtc gagattaagc gtacggtggc cgctcccagc 360
gtgttcatct tcccccccag cgacgagcag ctgaagagcg gcaccgccag cgtggtgtgc 420
ctgctgaaca acttctaccc ccgggaggcc aaggtgcagt ggaaggtgga caacgccctg 480
cagagcggca acagccagga gagcgtcacc gagcaggaca gcaaggactc cacctacagc 540
ctgagcagca ccctgaccct gagcaaggcc gactacgaga agcataaggt gtacgcctgc 600
gaggtgaccc accagggcct gtccagcccc gtgaccaaga gcttcaacag gggcgagtgc 660
<210> 520
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 520
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Gly Asn Gln Lys Asn Phe Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ala Pro Arg Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr
65 70 75 80
Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 521
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 521
gagatcgtcc tgactcagtc acccgctacc ctgagcctga gccctggcga gcgggctaca 60
ctgagctgta aatctagtca gtcactgctg gatagcggta atcagaagaa cttcctgacc 120
tggtatcagc agaagcccgg tcaagcccct agactgctga tctactgggc ctctactaga 180
gaatcaggcg tgccctctag gtttagcggt agcggtagtg gcaccgactt caccttcact 240
atctctagcc tggaagccga ggacgccgct acctactact gtcagaacga ctatagctac 300
ccctacacct tcggtcaagg cactaaggtc gagattaag 339
<210> 522
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 522
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Gly Asn Gln Lys Asn Phe Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ala Pro Arg Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr
65 70 75 80
Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 523
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 523
gagatcgtcc tgactcagtc acccgctacc ctgagcctga gccctggcga gcgggctaca 60
ctgagctgta aatctagtca gtcactgctg gatagcggta atcagaagaa cttcctgacc 120
tggtatcagc agaagcccgg tcaagcccct agactgctga tctactgggc ctctactaga 180
gaatcaggcg tgccctctag gtttagcggt agcggtagtg gcaccgactt caccttcact 240
atctctagcc tggaagccga ggacgccgct acctactact gtcagaacga ctatagctac 300
ccctacacct tcggtcaagg cactaaggtc gagattaagc gtacggtggc cgctcccagc 360
gtgttcatct tcccccccag cgacgagcag ctgaagagcg gcaccgccag cgtggtgtgc 420
ctgctgaaca acttctaccc ccgggaggcc aaggtgcagt ggaaggtgga caacgccctg 480
cagagcggca acagccagga gagcgtcacc gagcaggaca gcaaggactc cacctacagc 540
ctgagcagca ccctgaccct gagcaaggcc gactacgaga agcataaggt gtacgcctgc 600
gaggtgaccc accagggcct gtccagcccc gtgaccaaga gcttcaacag gggcgagtgc 660
<210> 524
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 524
acctactgga tgcac 15
<210> 525
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 525
aatatctacc ccggcaccgg cggctctaac ttcgacgaga agtttaagaa t 51
<210> 526
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 526
tggactaccg gcacaggcgc ctac 24
<210> 527
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 527
ggctacacct tcactaccta c 21
<210> 528
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 528
taccccggca ccggcggc 18
<210> 529
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 529
aaatctagtc agtcactgct ggatagcggt aatcagaaga acttcctgac c 51
<210> 530
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 530
tgggcctcta ctagagaatc a 21
<210> 531
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 531
cagaacgact atagctaccc ctacacc 27
<210> 532
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 532
agtcagtcac tgctggatag cggtaatcag aagaacttc 39
<210> 533
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 533
tgggcctct 9
<210> 534
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 534
gactatagct acccctac 18
<210> 535
<211> 440
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 535
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser
115 120 125
Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys
180 185 190
Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala
210 215 220
Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
225 230 235 240
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
245 250 255
Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
260 265 270
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
275 280 285
Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
290 295 300
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
305 310 315 320
Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
325 330 335
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr
340 345 350
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
355 360 365
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
370 375 380
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
385 390 395 400
Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe
405 410 415
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
420 425 430
Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 536
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 536
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 537
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 537
Gln Val Gln Leu Val Gln Ser Gly Val Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Leu Thr Thr Asp Ser Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Lys Ser Leu Gln Phe Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 538
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 538
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 539
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 539
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Gln Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Ser Gly Glu Ser Thr Tyr Ala Glu Glu Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Asn Thr Ala Tyr
65 70 75 80
Leu Gln Ile Thr Ser Leu Thr Ala Glu Asp Thr Gly Met Tyr Phe Cys
85 90 95
Val Arg Val Gly Tyr Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His
210 215 220
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 540
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 540
Glu Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Arg Ser Ser Val Ser Tyr Met
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp Ile Tyr
35 40 45
Arg Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Cys Leu Thr Ile Asn Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Ser Ser Phe Pro Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 541
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 541
Gly Tyr Thr Phe Thr Thr Tyr Trp Met His
1 5 10
<210> 542
<400> 542
000
<210> 543
<400> 543
000
<210> 544
<400> 544
000
<210> 545
<400> 545
000
<210> 546
<400> 546
000
<210> 547
<400> 547
000
<210> 548
<400> 548
000
<210> 549
<400> 549
000
<210> 550
<400> 550
000
<210> 551
<400> 551
000
<210> 552
<400> 552
000
<210> 553
<400> 553
000
<210> 554
<400> 554
000
<210> 555
<400> 555
000
<210> 556
<400> 556
000
<210> 557
<400> 557
000
<210> 558
<400> 558
000
<210> 559
<400> 559
000
<210> 560
<400> 560
000
<210> 561
<400> 561
000
<210> 562
<400> 562
000
<210> 563
<400> 563
000
<210> 564
<400> 564
000
<210> 565
<400> 565
000
<210> 566
<400> 566
000
<210> 567
<400> 567
000
<210> 568
<400> 568
000
<210> 569
<400> 569
000
<210> 570
<400> 570
000
<210> 571
<400> 571
000
<210> 572
<400> 572
000
<210> 573
<400> 573
000
<210> 574
<400> 574
000
<210> 575
<400> 575
000
<210> 576
<400> 576
000
<210> 577
<400> 577
000
<210> 578
<400> 578
000
<210> 579
<400> 579
000
<210> 580
<400> 580
000
<210> 581
<400> 581
000
<210> 582
<400> 582
000
<210> 583
<400> 583
000
<210> 584
<400> 584
000
<210> 585
<400> 585
000
<210> 586
<400> 586
000
<210> 587
<400> 587
000
<210> 588
<400> 588
000
<210> 589
<400> 589
000
<210> 590
<400> 590
000
<210> 591
<400> 591
000
<210> 592
<400> 592
000
<210> 593
<400> 593
000
<210> 594
<400> 594
000
<210> 595
<400> 595
000
<210> 596
<400> 596
000
<210> 597
<400> 597
000
<210> 598
<400> 598
000
<210> 599
<400> 599
000
<210> 600
<400> 600
000
<210> 601
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 601
Ser Tyr Trp Met Tyr
1 5
<210> 602
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 602
Arg Ile Asp Pro Asn Ser Gly Ser Thr Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Asn
<210> 603
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 603
Asp Tyr Arg Lys Gly Leu Tyr Ala Met Asp Tyr
1 5 10
<210> 604
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 604
Gly Tyr Thr Phe Thr Ser Tyr
1 5
<210> 605
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 605
Asp Pro Asn Ser Gly Ser
1 5
<210> 606
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 606
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Arg Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Asn Ser Gly Ser Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Asn Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Arg Lys Gly Leu Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 607
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 607
gaagtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctac cgtgaagatt 60
agctgtaaag tctcaggcta caccttcact agctactgga tgtactgggt ccgacaggct 120
agagggcaaa gactggagtg gatcggtaga atcgacccta atagcggctc tactaagtat 180
aacgagaagt ttaagaatag gttcactatt agtagggata actctaagaa caccctgtac 240
ctgcagatga atagcctgag agccgaggac accgccgtct actactgcgc tagagactat 300
agaaagggcc tgtacgctat ggactactgg ggtcaaggca ctaccgtgac cgtgtcttca 360
<210> 608
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 608
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Arg Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Asn Ser Gly Ser Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Asn Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Arg Lys Gly Leu Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 609
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 609
Lys Ala Ser Gln Asp Val Gly Thr Ala Val Ala
1 5 10
<210> 610
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 610
Trp Ala Ser Thr Arg His Thr
1 5
<210> 611
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 611
Gln Gln Tyr Asn Ser Tyr Pro Leu Thr
1 5
<210> 612
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 612
Ser Gln Asp Val Gly Thr Ala
1 5
<210> 613
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 613
Trp Ala Ser
1
<210> 614
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 614
Tyr Asn Ser Tyr Pro Leu
1 5
<210> 615
<211> 1338
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 615
gaagtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctac cgtgaagatt 60
agctgtaaag tctcaggcta caccttcact agctactgga tgtactgggt ccgacaggct 120
agagggcaaa gactggagtg gatcggtaga atcgacccta atagcggctc tactaagtat 180
aacgagaagt ttaagaatag gttcactatt agtagggata actctaagaa caccctgtac 240
ctgcagatga atagcctgag agccgaggac accgccgtct actactgcgc tagagactat 300
agaaagggcc tgtacgctat ggactactgg ggtcaaggca ctaccgtgac cgtgtcttca 360
gctagcacta agggcccgtc cgtgttcccc ctggcacctt gtagccggag cactagcgaa 420
tccaccgctg ccctcggctg cctggtcaag gattacttcc cggagcccgt gaccgtgtcc 480
tggaacagcg gagccctgac ctccggagtg cacaccttcc ccgctgtgct gcagagctcc 540
gggctgtact cgctgtcgtc ggtggtcacg gtgccttcat ctagcctggg taccaagacc 600
tacacttgca acgtggacca caagccttcc aacactaagg tggacaagcg cgtcgaatcg 660
aagtacggcc caccgtgccc gccttgtccc gcgccggagt tcctcggcgg tccctcggtc 720
tttctgttcc caccgaagcc caaggacact ttgatgattt cccgcacccc tgaagtgaca 780
tgcgtggtcg tggacgtgtc acaggaagat ccggaggtgc agttcaattg gtacgtggat 840
ggcgtcgagg tgcacaacgc caaaaccaag ccgagggagg agcagttcaa ctccacttac 900
cgcgtcgtgt ccgtgctgac ggtgctgcat caggactggc tgaacgggaa ggagtacaag 960
tgcaaagtgt ccaacaaggg acttcctagc tcaatcgaaa agaccatctc gaaagccaag 1020
ggacagcccc gggaacccca agtgtatacc ctgccaccga gccaggaaga aatgactaag 1080
aaccaagtct cattgacttg ccttgtgaag ggcttctacc catcggatat cgccgtggaa 1140
tgggagtcca acggccagcc ggaaaacaac tacaagacca cccctccggt gctggactca 1200
gacggatcct tcttcctcta ctcgcggctg accgtggata agagcagatg gcaggaggga 1260
aatgtgttca gctgttctgt gatgcatgaa gccctgcaca accactacac tcagaagtcc 1320
ctgtccctct ccctggga 1338
<210> 616
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 616
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Gly Thr Ala
20 25 30
Val Ala Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Trp Ala Ser Thr Arg His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 617
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 617
gctattcagc tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta aagcctctca ggacgtgggc accgccgtgg cctggtatct gcagaagcct 120
ggtcaatcac ctcagctgct gatctactgg gcctctacta gacacaccgg cgtgccctct 180
aggtttagcg gtagcggtag tggcaccgac ttcaccttca ctatctcttc actggaagcc 240
gaggacgccg ctacctacta ctgtcagcag tataatagct accccctgac cttcggtcaa 300
ggcactaagg tcgagattaa g 321
<210> 618
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 618
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Gly Thr Ala
20 25 30
Val Ala Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Trp Ala Ser Thr Arg His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 619
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 619
gctattcagc tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta aagcctctca ggacgtgggc accgccgtgg cctggtatct gcagaagcct 120
ggtcaatcac ctcagctgct gatctactgg gcctctacta gacacaccgg cgtgccctct 180
aggtttagcg gtagcggtag tggcaccgac ttcaccttca ctatctcttc actggaagcc 240
gaggacgccg ctacctacta ctgtcagcag tataatagct accccctgac cttcggtcaa 300
ggcactaagg tcgagattaa gcgtacggtg gccgctccca gcgtgttcat cttccccccc 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac 420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 620
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 620
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Thr Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Asn Ser Gly Ser Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Arg Lys Gly Leu Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 621
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 621
gaagtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctac cgtgaagatt 60
agctgtaaag tctcaggcta caccttcact agctactgga tgtactgggt ccgacaggct 120
accggtcaag gcctggagtg gatgggtaga atcgacccta atagcggctc tactaagtat 180
aacgagaagt ttaagaatag agtgactatc accgccgata agtctactag caccgcctat 240
atggaactgt ctagcctgag atcagaggac accgccgtct actactgcgc tagagactat 300
agaaagggcc tgtacgctat ggactactgg ggtcaaggca ctaccgtgac cgtgtcttca 360
<210> 622
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 622
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Thr Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Asn Ser Gly Ser Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Arg Lys Gly Leu Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 623
<211> 1338
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 623
gaagtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctac cgtgaagatt 60
agctgtaaag tctcaggcta caccttcact agctactgga tgtactgggt ccgacaggct 120
accggtcaag gcctggagtg gatgggtaga atcgacccta atagcggctc tactaagtat 180
aacgagaagt ttaagaatag agtgactatc accgccgata agtctactag caccgcctat 240
atggaactgt ctagcctgag atcagaggac accgccgtct actactgcgc tagagactat 300
agaaagggcc tgtacgctat ggactactgg ggtcaaggca ctaccgtgac cgtgtcttca 360
gctagcacta agggcccgtc cgtgttcccc ctggcacctt gtagccggag cactagcgaa 420
tccaccgctg ccctcggctg cctggtcaag gattacttcc cggagcccgt gaccgtgtcc 480
tggaacagcg gagccctgac ctccggagtg cacaccttcc ccgctgtgct gcagagctcc 540
gggctgtact cgctgtcgtc ggtggtcacg gtgccttcat ctagcctggg taccaagacc 600
tacacttgca acgtggacca caagccttcc aacactaagg tggacaagcg cgtcgaatcg 660
aagtacggcc caccgtgccc gccttgtccc gcgccggagt tcctcggcgg tccctcggtc 720
tttctgttcc caccgaagcc caaggacact ttgatgattt cccgcacccc tgaagtgaca 780
tgcgtggtcg tggacgtgtc acaggaagat ccggaggtgc agttcaattg gtacgtggat 840
ggcgtcgagg tgcacaacgc caaaaccaag ccgagggagg agcagttcaa ctccacttac 900
cgcgtcgtgt ccgtgctgac ggtgctgcat caggactggc tgaacgggaa ggagtacaag 960
tgcaaagtgt ccaacaaggg acttcctagc tcaatcgaaa agaccatctc gaaagccaag 1020
ggacagcccc gggaacccca agtgtatacc ctgccaccga gccaggaaga aatgactaag 1080
aaccaagtct cattgacttg ccttgtgaag ggcttctacc catcggatat cgccgtggaa 1140
tgggagtcca acggccagcc ggaaaacaac tacaagacca cccctccggt gctggactca 1200
gacggatcct tcttcctcta ctcgcggctg accgtggata agagcagatg gcaggaggga 1260
aatgtgttca gctgttctgt gatgcatgaa gccctgcaca accactacac tcagaagtcc 1320
ctgtccctct ccctggga 1338
<210> 624
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 624
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ala Ser Gln Asp Val Gly Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Trp Ala Ser Thr Arg His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 625
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 625
gacgtcgtga tgactcagtc acccctgagc ctgcccgtga ccctggggca gcccgcctct 60
attagctgta aagcctctca ggacgtgggc accgccgtgg cctggtatca gcagaagcca 120
gggcaagccc ctagactgct gatctactgg gcctctacta gacacaccgg cgtgccctct 180
aggtttagcg gtagcggtag tggcaccgag ttcaccctga ctatctcttc actgcagccc 240
gacgacttcg ctacctacta ctgtcagcag tataatagct accccctgac cttcggtcaa 300
ggcactaagg tcgagattaa g 321
<210> 626
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 626
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ala Ser Gln Asp Val Gly Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Trp Ala Ser Thr Arg His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 627
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 627
gacgtcgtga tgactcagtc acccctgagc ctgcccgtga ccctggggca gcccgcctct 60
attagctgta aagcctctca ggacgtgggc accgccgtgg cctggtatca gcagaagcca 120
gggcaagccc ctagactgct gatctactgg gcctctacta gacacaccgg cgtgccctct 180
aggtttagcg gtagcggtag tggcaccgag ttcaccctga ctatctcttc actgcagccc 240
gacgacttcg ctacctacta ctgtcagcag tataatagct accccctgac cttcggtcaa 300
ggcactaagg tcgagattaa gcgtacggtg gccgctccca gcgtgttcat cttccccccc 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac 420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 628
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 628
agctactgga tgtac 15
<210> 629
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 629
agaatcgacc ctaatagcgg ctctactaag tataacgaga agtttaagaa t 51
<210> 630
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 630
gactatagaa agggcctgta cgctatggac tac 33
<210> 631
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 631
ggctacacct tcactagcta c 21
<210> 632
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 632
gaccctaata gcggctct 18
<210> 633
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 633
aaagcctctc aggacgtggg caccgccgtg gcc 33
<210> 634
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 634
tgggcctcta ctagacacac c 21
<210> 635
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 635
cagcagtata atagctaccc cctgacc 27
<210> 636
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 636
tctcaggacg tgggcaccgc c 21
<210> 637
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 637
tgggcctct 9
<210> 638
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 638
tataatagct accccctg 18
<210> 639
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 639
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 640
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 640
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Tyr His Pro Ala
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 641
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 641
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ile Met Met Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Pro Ser Gly Gly Ile Thr Phe Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ile Lys Leu Gly Thr Val Thr Thr Val Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 642
<211> 216
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 642
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Arg Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly Gln
100 105 110
Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser Glu Glu
115 120 125
Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr
130 135 140
Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro Val Lys
145 150 155 160
Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn Lys Tyr
165 170 175
Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His
180 185 190
Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys
195 200 205
Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 643
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 643
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly Trp Phe Gly Glu Leu Ala Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Ser Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 644
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 644
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Leu Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 645
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 645
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Asp Thr Phe Ser Thr Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Lys Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Phe His Phe Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 646
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 646
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 647
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 647
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Tyr
1 5 10
<210> 648
<400> 648
000
<210> 649
<400> 649
000
<210> 650
<400> 650
000
<210> 651
<400> 651
000
<210> 652
<400> 652
000
<210> 653
<400> 653
000
<210> 654
<400> 654
000
<210> 655
<400> 655
000
<210> 656
<400> 656
000
<210> 657
<400> 657
000
<210> 658
<400> 658
000
<210> 659
<400> 659
000
<210> 660
<400> 660
000
<210> 661
<400> 661
000
<210> 662
<400> 662
000
<210> 663
<400> 663
000
<210> 664
<400> 664
000
<210> 665
<400> 665
000
<210> 666
<400> 666
000
<210> 667
<400> 667
000
<210> 668
<400> 668
000
<210> 669
<400> 669
000
<210> 670
<400> 670
000
<210> 671
<400> 671
000
<210> 672
<400> 672
000
<210> 673
<400> 673
000
<210> 674
<400> 674
000
<210> 675
<400> 675
000
<210> 676
<400> 676
000
<210> 677
<400> 677
000
<210> 678
<400> 678
000
<210> 679
<400> 679
000
<210> 680
<400> 680
000
<210> 681
<400> 681
000
<210> 682
<400> 682
000
<210> 683
<400> 683
000
<210> 684
<400> 684
000
<210> 685
<400> 685
000
<210> 686
<400> 686
000
<210> 687
<400> 687
000
<210> 688
<400> 688
000
<210> 689
<400> 689
000
<210> 690
<400> 690
000
<210> 691
<400> 691
000
<210> 692
<400> 692
000
<210> 693
<400> 693
000
<210> 694
<400> 694
000
<210> 695
<400> 695
000
<210> 696
<400> 696
000
<210> 697
<400> 697
000
<210> 698
<400> 698
000
<210> 699
<400> 699
000
<210> 700
<400> 700
000
<210> 701
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 701
Asn Tyr Gly Met Asn
1 5
<210> 702
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 702
Trp Ile Asn Thr Asp Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe Lys
1 5 10 15
Gly
<210> 703
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 703
Asn Pro Pro Tyr Tyr Tyr Gly Thr Asn Asn Ala Glu Ala Met Asp Tyr
1 5 10 15
<210> 704
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 704
Gly Phe Thr Leu Thr Asn Tyr
1 5
<210> 705
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 705
Asn Thr Asp Thr Gly Glu
1 5
<210> 706
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 706
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Leu Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Arg Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Pro Pro Tyr Tyr Tyr Gly Thr Asn Asn Ala Glu Ala Met
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 707
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 707
caagtgcagc tggtgcagtc gggagccgaa gtgaagaagc ctggagcctc ggtgaaggtg 60
tcgtgcaagg catccggatt caccctcacc aattacggga tgaactgggt cagacaggcc 120
cggggtcaac ggctggagtg gatcggatgg attaacaccg acaccgggga gcctacctac 180
gcggacgatt tcaagggacg gttcgtgttc tccctcgaca cctccgtgtc caccgcctac 240
ctccaaatct cctcactgaa agcggaggac accgccgtgt actattgcgc gaggaacccg 300
ccctactact acggaaccaa caacgccgaa gccatggact actggggcca gggcaccact 360
gtgactgtgt ccagc 375
<210> 708
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 708
caggtgcagc tggtgcagtc tggcgccgaa gtgaagaaac ctggcgcctc cgtgaaggtg 60
tcctgcaagg cctctggctt caccctgacc aactacggca tgaactgggt gcgacaggcc 120
aggggccagc ggctggaatg gatcggctgg atcaacaccg acaccggcga gcctacctac 180
gccgacgact tcaagggcag attcgtgttc tccctggaca cctccgtgtc caccgcctac 240
ctgcagatct ccagcctgaa ggccgaggat accgccgtgt actactgcgc ccggaacccc 300
ccttactact acggcaccaa caacgccgag gccatggact attggggcca gggcaccacc 360
gtgaccgtgt cctct 375
<210> 709
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 709
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Leu Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Arg Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Pro Pro Tyr Tyr Tyr Gly Thr Asn Asn Ala Glu Ala Met
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly
450
<210> 710
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 710
Ser Ser Ser Gln Asp Ile Ser Asn Tyr Leu Asn
1 5 10
<210> 711
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 711
Tyr Thr Ser Thr Leu His Leu
1 5
<210> 712
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 712
Gln Gln Tyr Tyr Asn Leu Pro Trp Thr
1 5
<210> 713
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 713
Ser Gln Asp Ile Ser Asn Tyr
1 5
<210> 714
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 714
Tyr Thr Ser
1
<210> 715
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 715
Tyr Tyr Asn Leu Pro Trp
1 5
<210> 716
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 716
caagtgcagc tggtgcagtc gggagccgaa gtgaagaagc ctggagcctc ggtgaaggtg 60
tcgtgcaagg catccggatt caccctcacc aattacggga tgaactgggt cagacaggcc 120
cggggtcaac ggctggagtg gatcggatgg attaacaccg acaccgggga gcctacctac 180
gcggacgatt tcaagggacg gttcgtgttc tccctcgaca cctccgtgtc caccgcctac 240
ctccaaatct cctcactgaa agcggaggac accgccgtgt actattgcgc gaggaacccg 300
ccctactact acggaaccaa caacgccgaa gccatggact actggggcca gggcaccact 360
gtgactgtgt ccagcgcgtc cactaagggc ccgtccgtgt tccccctggc accttgtagc 420
cggagcacta gcgaatccac cgctgccctc ggctgcctgg tcaaggatta cttcccggag 480
cccgtgaccg tgtcctggaa cagcggagcc ctgacctccg gagtgcacac cttccccgct 540
gtgctgcaga gctccgggct gtactcgctg tcgtcggtgg tcacggtgcc ttcatctagc 600
ctgggtacca agacctacac ttgcaacgtg gaccacaagc cttccaacac taaggtggac 660
aagcgcgtcg aatcgaagta cggcccaccg tgcccgcctt gtcccgcgcc ggagttcctc 720
ggcggtccct cggtctttct gttcccaccg aagcccaagg acactttgat gatttcccgc 780
acccctgaag tgacatgcgt ggtcgtggac gtgtcacagg aagatccgga ggtgcagttc 840
aattggtacg tggatggcgt cgaggtgcac aacgccaaaa ccaagccgag ggaggagcag 900
ttcaactcca cttaccgcgt cgtgtccgtg ctgacggtgc tgcatcagga ctggctgaac 960
gggaaggagt acaagtgcaa agtgtccaac aagggacttc ctagctcaat cgaaaagacc 1020
atctcgaaag ccaagggaca gccccgggaa ccccaagtgt ataccctgcc accgagccag 1080
gaagaaatga ctaagaacca agtctcattg acttgccttg tgaagggctt ctacccatcg 1140
gatatcgccg tggaatggga gtccaacggc cagccggaaa acaactacaa gaccacccct 1200
ccggtgctgg actcagacgg atccttcttc ctctactcgc ggctgaccgt ggataagagc 1260
agatggcagg agggaaatgt gttcagctgt tctgtgatgc atgaagccct gcacaaccac 1320
tacactcaga agtccctgtc cctctccctg gga 1353
<210> 717
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 717
caggtgcagc tggtgcagtc tggcgccgaa gtgaagaaac ctggcgcctc cgtgaaggtg 60
tcctgcaagg cctctggctt caccctgacc aactacggca tgaactgggt gcgacaggcc 120
aggggccagc ggctggaatg gatcggctgg atcaacaccg acaccggcga gcctacctac 180
gccgacgact tcaagggcag attcgtgttc tccctggaca cctccgtgtc caccgcctac 240
ctgcagatct ccagcctgaa ggccgaggat accgccgtgt actactgcgc ccggaacccc 300
ccttactact acggcaccaa caacgccgag gccatggact attggggcca gggcaccacc 360
gtgaccgtgt cctctgcttc taccaagggg cccagcgtgt tccccctggc cccctgctcc 420
agaagcacca gcgagagcac agccgccctg ggctgcctgg tgaaggacta cttccccgag 480
cccgtgaccg tgtcctggaa cagcggagcc ctgaccagcg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgaccgtgcc cagcagcagc 600
ctgggcacca agacctacac ctgtaacgtg gaccacaagc ccagcaacac caaggtggac 660
aagagggtgg agagcaagta cggcccaccc tgccccccct gcccagcccc cgagttcctg 720
ggcggaccca gcgtgttcct gttccccccc aagcccaagg acaccctgat gatcagcaga 780
acccccgagg tgacctgtgt ggtggtggac gtgtcccagg aggaccccga ggtccagttc 840
aactggtacg tggacggcgt ggaggtgcac aacgccaaga ccaagcccag agaggagcag 900
tttaacagca cctaccgggt ggtgtccgtg ctgaccgtgc tgcaccagga ctggctgaac 960
ggcaaagagt acaagtgtaa ggtctccaac aagggcctgc caagcagcat cgaaaagacc 1020
atcagcaagg ccaagggcca gcctagagag ccccaggtct acaccctgcc acccagccaa 1080
gaggagatga ccaagaacca ggtgtccctg acctgtctgg tgaagggctt ctacccaagc 1140
gacatcgccg tggagtggga gagcaacggc cagcccgaga acaactacaa gaccaccccc 1200
ccagtgctgg acagcgacgg cagcttcttc ctgtacagca ggctgaccgt ggacaagtcc 1260
agatggcagg agggcaacgt ctttagctgc tccgtgatgc acgaggccct gcacaaccac 1320
tacacccaga agagcctgag cctgtccctg ggc 1353
<210> 718
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 718
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ser Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Thr Leu His Leu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 719
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 719
gatattcaga tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta gctctagtca ggatatctct aactacctga actggtatct gcagaagccc 120
ggtcaatcac ctcagctgct gatctactac actagcaccc tgcacctggg cgtgccctct 180
aggtttagcg gtagcggtag tggcaccgag ttcaccctga ctatctctag cctgcagccc 240
gacgacttcg ctacctacta ctgtcagcag tactataacc tgccctggac cttcggtcaa 300
ggcactaagg tcgagattaa g 321
<210> 720
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 720
gacatccaga tgacccagtc cccctccagc ctgtctgctt ccgtgggcga cagagtgacc 60
atcacctgtt cctccagcca ggacatctcc aactacctga actggtatct gcagaagccc 120
ggccagtccc ctcagctgct gatctactac acctccaccc tgcacctggg cgtgccctcc 180
agattttccg gctctggctc tggcaccgag tttaccctga ccatcagctc cctgcagccc 240
gacgacttcg ccacctacta ctgccagcag tactacaacc tgccctggac cttcggccag 300
ggcaccaagg tggaaatcaa g 321
<210> 721
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 721
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ser Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Thr Leu His Leu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 722
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 722
gatattcaga tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta gctctagtca ggatatctct aactacctga actggtatct gcagaagccc 120
ggtcaatcac ctcagctgct gatctactac actagcaccc tgcacctggg cgtgccctct 180
aggtttagcg gtagcggtag tggcaccgag ttcaccctga ctatctctag cctgcagccc 240
gacgacttcg ctacctacta ctgtcagcag tactataacc tgccctggac cttcggtcaa 300
ggcactaagg tcgagattaa gcgtacggtg gccgctccca gcgtgttcat cttccccccc 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac 420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 723
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 723
gacatccaga tgacccagtc cccctccagc ctgtctgctt ccgtgggcga cagagtgacc 60
atcacctgtt cctccagcca ggacatctcc aactacctga actggtatct gcagaagccc 120
ggccagtccc ctcagctgct gatctactac acctccaccc tgcacctggg cgtgccctcc 180
agattttccg gctctggctc tggcaccgag tttaccctga ccatcagctc cctgcagccc 240
gacgacttcg ccacctacta ctgccagcag tactacaacc tgccctggac cttcggccag 300
ggcaccaagg tggaaatcaa gcgtacggtg gccgctccca gcgtgttcat cttcccccca 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gtctgctgaa caacttctac 420
cccagggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcacaag gtgtacgcct gtgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 724
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 724
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Leu Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Pro Pro Tyr Tyr Tyr Gly Thr Asn Asn Ala Glu Ala Met
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 725
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 725
caggtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctag tgtgaaagtc 60
agctgtaaag ctagtggctt caccctgact aactacggga tgaactgggt ccgccaggcc 120
ccaggtcaag gcctcgagtg gatgggctgg attaacaccg acaccggcga gcctacctac 180
gccgacgact ttaagggcag attcgtgttt agcctggaca ctagtgtgtc taccgcctac 240
ctgcagatct ctagcctgaa ggccgaggac accgccgtct actactgcgc tagaaacccc 300
ccctactact acggcactaa caacgccgag gctatggact actggggtca aggcactacc 360
gtgaccgtgt ctagc 375
<210> 726
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 726
caggtgcagc tggtgcagtc tggcgccgaa gtgaagaaac ctggcgcctc cgtgaaggtg 60
tcctgcaagg cctctggctt caccctgacc aactacggca tgaactgggt gcgacaggcc 120
cctggacagg gcctggaatg gatgggctgg atcaacaccg acaccggcga gcctacctac 180
gccgacgact tcaagggcag attcgtgttc tccctggaca cctccgtgtc caccgcctac 240
ctgcagatct ccagcctgaa ggccgaggat accgccgtgt actactgcgc ccggaacccc 300
ccttactact acggcaccaa caacgccgag gccatggact attggggcca gggcaccacc 360
gtgaccgtgt cctct 375
<210> 727
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 727
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Leu Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Thr Asp Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Pro Pro Tyr Tyr Tyr Gly Thr Asn Asn Ala Glu Ala Met
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly
450
<210> 728
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 728
caggtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctag tgtgaaagtc 60
agctgtaaag ctagtggctt caccctgact aactacggga tgaactgggt ccgccaggcc 120
ccaggtcaag gcctcgagtg gatgggctgg attaacaccg acaccggcga gcctacctac 180
gccgacgact ttaagggcag attcgtgttt agcctggaca ctagtgtgtc taccgcctac 240
ctgcagatct ctagcctgaa ggccgaggac accgccgtct actactgcgc tagaaacccc 300
ccctactact acggcactaa caacgccgag gctatggact actggggtca aggcactacc 360
gtgaccgtgt ctagcgctag cactaagggc ccgtccgtgt tccccctggc accttgtagc 420
cggagcacta gcgaatccac cgctgccctc ggctgcctgg tcaaggatta cttcccggag 480
cccgtgaccg tgtcctggaa cagcggagcc ctgacctccg gagtgcacac cttccccgct 540
gtgctgcaga gctccgggct gtactcgctg tcgtcggtgg tcacggtgcc ttcatctagc 600
ctgggtacca agacctacac ttgcaacgtg gaccacaagc cttccaacac taaggtggac 660
aagcgcgtcg aatcgaagta cggcccaccg tgcccgcctt gtcccgcgcc ggagttcctc 720
ggcggtccct cggtctttct gttcccaccg aagcccaagg acactttgat gatttcccgc 780
acccctgaag tgacatgcgt ggtcgtggac gtgtcacagg aagatccgga ggtgcagttc 840
aattggtacg tggatggcgt cgaggtgcac aacgccaaaa ccaagccgag ggaggagcag 900
ttcaactcca cttaccgcgt cgtgtccgtg ctgacggtgc tgcatcagga ctggctgaac 960
gggaaggagt acaagtgcaa agtgtccaac aagggacttc ctagctcaat cgaaaagacc 1020
atctcgaaag ccaagggaca gccccgggaa ccccaagtgt ataccctgcc accgagccag 1080
gaagaaatga ctaagaacca agtctcattg acttgccttg tgaagggctt ctacccatcg 1140
gatatcgccg tggaatggga gtccaacggc cagccggaaa acaactacaa gaccacccct 1200
ccggtgctgg actcagacgg atccttcttc ctctactcgc ggctgaccgt ggataagagc 1260
agatggcagg agggaaatgt gttcagctgt tctgtgatgc atgaagccct gcacaaccac 1320
tacactcaga agtccctgtc cctctccctg gga 1353
<210> 729
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 729
caggtgcagc tggtgcagtc tggcgccgaa gtgaagaaac ctggcgcctc cgtgaaggtg 60
tcctgcaagg cctctggctt caccctgacc aactacggca tgaactgggt gcgacaggcc 120
cctggacagg gcctggaatg gatgggctgg atcaacaccg acaccggcga gcctacctac 180
gccgacgact tcaagggcag attcgtgttc tccctggaca cctccgtgtc caccgcctac 240
ctgcagatct ccagcctgaa ggccgaggat accgccgtgt actactgcgc ccggaacccc 300
ccttactact acggcaccaa caacgccgag gccatggact attggggcca gggcaccacc 360
gtgaccgtgt cctctgcttc taccaagggg cccagcgtgt tccccctggc cccctgctcc 420
agaagcacca gcgagagcac agccgccctg ggctgcctgg tgaaggacta cttccccgag 480
cccgtgaccg tgtcctggaa cagcggagcc ctgaccagcg gcgtgcacac cttccccgcc 540
gtgctgcaga gcagcggcct gtacagcctg agcagcgtgg tgaccgtgcc cagcagcagc 600
ctgggcacca agacctacac ctgtaacgtg gaccacaagc ccagcaacac caaggtggac 660
aagagggtgg agagcaagta cggcccaccc tgccccccct gcccagcccc cgagttcctg 720
ggcggaccca gcgtgttcct gttccccccc aagcccaagg acaccctgat gatcagcaga 780
acccccgagg tgacctgtgt ggtggtggac gtgtcccagg aggaccccga ggtccagttc 840
aactggtacg tggacggcgt ggaggtgcac aacgccaaga ccaagcccag agaggagcag 900
tttaacagca cctaccgggt ggtgtccgtg ctgaccgtgc tgcaccagga ctggctgaac 960
ggcaaagagt acaagtgtaa ggtctccaac aagggcctgc caagcagcat cgaaaagacc 1020
atcagcaagg ccaagggcca gcctagagag ccccaggtct acaccctgcc acccagccaa 1080
gaggagatga ccaagaacca ggtgtccctg acctgtctgg tgaagggctt ctacccaagc 1140
gacatcgccg tggagtggga gagcaacggc cagcccgaga acaactacaa gaccaccccc 1200
ccagtgctgg acagcgacgg cagcttcttc ctgtacagca ggctgaccgt ggacaagtcc 1260
agatggcagg agggcaacgt ctttagctgc tccgtgatgc acgaggccct gcacaaccac 1320
tacacccaga agagcctgag cctgtccctg ggc 1353
<210> 730
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 730
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ser Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Thr Leu His Leu Gly Ile Pro Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Gln Gln Tyr Tyr Asn Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 731
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 731
gatattcaga tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta gctctagtca ggatatctct aactacctga actggtatca gcagaagccc 120
ggtaaagccc ctaagctgct gatctactac actagcaccc tgcacctggg aatcccccct 180
aggtttagcg gtagcggcta cggcaccgac ttcaccctga ctattaacaa tatcgagtca 240
gaggacgccg cctactactt ctgtcagcag tactataacc tgccctggac cttcggtcaa 300
ggcactaagg tcgagattaa g 321
<210> 732
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 732
gacatccaga tgacccagtc cccctccagc ctgtctgctt ccgtgggcga cagagtgacc 60
atcacctgtt cctccagcca ggacatctcc aactacctga actggtatca gcagaagccc 120
ggcaaggccc ccaagctgct gatctactac acctccaccc tgcacctggg catcccccct 180
agattctccg gctctggcta cggcaccgac ttcaccctga ccatcaacaa catcgagtcc 240
gaggacgccg cctactactt ctgccagcag tactacaacc tgccctggac cttcggccag 300
ggcaccaagg tggaaatcaa g 321
<210> 733
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 733
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ser Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Thr Leu His Leu Gly Ile Pro Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Gln Gln Tyr Tyr Asn Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 734
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 734
gatattcaga tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta gctctagtca ggatatctct aactacctga actggtatca gcagaagccc 120
ggtaaagccc ctaagctgct gatctactac actagcaccc tgcacctggg aatcccccct 180
aggtttagcg gtagcggcta cggcaccgac ttcaccctga ctattaacaa tatcgagtca 240
gaggacgccg cctactactt ctgtcagcag tactataacc tgccctggac cttcggtcaa 300
ggcactaagg tcgagattaa gcgtacggtg gccgctccca gcgtgttcat cttccccccc 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac 420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 735
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 735
gacatccaga tgacccagtc cccctccagc ctgtctgctt ccgtgggcga cagagtgacc 60
atcacctgtt cctccagcca ggacatctcc aactacctga actggtatca gcagaagccc 120
ggcaaggccc ccaagctgct gatctactac acctccaccc tgcacctggg catcccccct 180
agattctccg gctctggcta cggcaccgac ttcaccctga ccatcaacaa catcgagtcc 240
gaggacgccg cctactactt ctgccagcag tactacaacc tgccctggac cttcggccag 300
ggcaccaagg tggaaatcaa gcgtacggtg gccgctccca gcgtgttcat cttcccccca 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gtctgctgaa caacttctac 420
cccagggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcacaag gtgtacgcct gtgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 736
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 736
aattacggga tgaac 15
<210> 737
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 737
aactacggca tgaac 15
<210> 738
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 738
tggattaaca ccgacaccgg ggagcctacc tacgcggacg atttcaaggg a 51
<210> 739
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 739
tggatcaaca ccgacaccgg cgagcctacc tacgccgacg acttcaaggg c 51
<210> 740
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 740
aacccgccct actactacgg aaccaacaac gccgaagcca tggactac 48
<210> 741
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 741
aacccccctt actactacgg caccaacaac gccgaggcca tggactat 48
<210> 742
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 742
ggattcaccc tcaccaatta c 21
<210> 743
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 743
ggcttcaccc tgaccaacta c 21
<210> 744
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 744
aacaccgaca ccggggag 18
<210> 745
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 745
aacaccgaca ccggcgag 18
<210> 746
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 746
agctctagtc aggatatctc taactacctg aac 33
<210> 747
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 747
tcctccagcc aggacatctc caactacctg aac 33
<210> 748
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 748
tacactagca ccctgcacct g 21
<210> 749
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 749
tacacctcca ccctgcacct g 21
<210> 750
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 750
cagcagtact ataacctgcc ctggacc 27
<210> 751
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 751
cagcagtact acaacctgcc ctggacc 27
<210> 752
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 752
agtcaggata tctctaacta c 21
<210> 753
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 753
agccaggaca tctccaacta c 21
<210> 754
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 754
tacactagc 9
<210> 755
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 755
tacacctcc 9
<210> 756
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 756
tactataacc tgccctgg 18
<210> 757
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 757
tactacaacc tgccctgg 18
<210> 758
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 758
aactacggga tgaac 15
<210> 759
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 759
tggattaaca ccgacaccgg cgagcctacc tacgccgacg actttaaggg c 51
<210> 760
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 760
aaccccccct actactacgg cactaacaac gccgaggcta tggactac 48
<210> 761
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 761
ggcttcaccc tgactaacta c 21
<210> 762
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 762
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Asp Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Ser Thr Asn Ser Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Leu Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Phe Gly Tyr Ser Asp Tyr Glu Tyr Asn Trp Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 763
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 763
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Asn Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 764
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 764
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ala Tyr
20 25 30
Gly Val Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Asp Asp Gly Ser Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Arg Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Asp Val Ala Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 765
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 765
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Val Gly
1 5 10 15
Gln Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Gly
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Val Tyr Phe Ala Ser Thr Arg Asp Ser Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Asp Tyr Phe Cys Leu Gln
85 90 95
His Phe Gly Thr Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 766
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 766
Gly Phe Thr Leu Thr Asn Tyr Gly Met Asn
1 5 10
<210> 767
<400> 767
000
<210> 768
<400> 768
000
<210> 769
<400> 769
000
<210> 770
<400> 770
000
<210> 771
<400> 771
000
<210> 772
<400> 772
000
<210> 773
<400> 773
000
<210> 774
<400> 774
000
<210> 775
<400> 775
000
<210> 776
<400> 776
000
<210> 777
<400> 777
000
<210> 778
<400> 778
000
<210> 779
<400> 779
000
<210> 780
<400> 780
000
<210> 781
<400> 781
000
<210> 782
<400> 782
000
<210> 783
<400> 783
000
<210> 784
<400> 784
000
<210> 785
<400> 785
000
<210> 786
<400> 786
000
<210> 787
<400> 787
000
<210> 788
<400> 788
000
<210> 789
<400> 789
000
<210> 790
<400> 790
000
<210> 791
<400> 791
000
<210> 792
<400> 792
000
<210> 793
<400> 793
000
<210> 794
<400> 794
000
<210> 795
<400> 795
000
<210> 796
<400> 796
000
<210> 797
<400> 797
000
<210> 798
<400> 798
000
<210> 799
<400> 799
000
<210> 800
<400> 800
000
<210> 801
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 801
Ser Tyr Asn Met His
1 5
<210> 802
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 802
Asp Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 803
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 803
Val Gly Gly Ala Phe Pro Met Asp Tyr
1 5
<210> 804
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 804
Gly Tyr Thr Phe Thr Ser Tyr
1 5
<210> 805
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 805
Tyr Pro Gly Asn Gly Asp
1 5
<210> 806
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 806
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Gly Ala Phe Pro Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 807
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 807
caggtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggctctag cgtgaaagtt 60
tcttgtaaag ctagtggcta caccttcact agctataata tgcactgggt tcgccaggcc 120
ccagggcaag gcctcgagtg gatgggcgat atctaccccg ggaacggcga cactagttat 180
aatcagaagt ttaagggtag agtcactatc accgccgata agtctactag caccgtctat 240
atggaactga gttccctgag gtctgaggac accgccgtct actactgcgc tagagtgggc 300
ggagccttcc ctatggacta ctggggtcaa ggcactaccg tgaccgtgtc tagc 354
<210> 808
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 808
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Gly Ala Phe Pro Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 809
<211> 1332
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 809
caggtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggctctag cgtgaaagtt 60
tcttgtaaag ctagtggcta caccttcact agctataata tgcactgggt tcgccaggcc 120
ccagggcaag gcctcgagtg gatgggcgat atctaccccg ggaacggcga cactagttat 180
aatcagaagt ttaagggtag agtcactatc accgccgata agtctactag caccgtctat 240
atggaactga gttccctgag gtctgaggac accgccgtct actactgcgc tagagtgggc 300
ggagccttcc ctatggacta ctggggtcaa ggcactaccg tgaccgtgtc tagcgctagc 360
actaagggcc cgtccgtgtt ccccctggca ccttgtagcc ggagcactag cgaatccacc 420
gctgccctcg gctgcctggt caaggattac ttcccggagc ccgtgaccgt gtcctggaac 480
agcggagccc tgacctccgg agtgcacacc ttccccgctg tgctgcagag ctccgggctg 540
tactcgctgt cgtcggtggt cacggtgcct tcatctagcc tgggtaccaa gacctacact 600
tgcaacgtgg accacaagcc ttccaacact aaggtggaca agcgcgtcga atcgaagtac 660
ggcccaccgt gcccgccttg tcccgcgccg gagttcctcg gcggtccctc ggtctttctg 720
ttcccaccga agcccaagga cactttgatg atttcccgca cccctgaagt gacatgcgtg 780
gtcgtggacg tgtcacagga agatccggag gtgcagttca attggtacgt ggatggcgtc 840
gaggtgcaca acgccaaaac caagccgagg gaggagcagt tcaactccac ttaccgcgtc 900
gtgtccgtgc tgacggtgct gcatcaggac tggctgaacg ggaaggagta caagtgcaaa 960
gtgtccaaca agggacttcc tagctcaatc gaaaagacca tctcgaaagc caagggacag 1020
ccccgggaac cccaagtgta taccctgcca ccgagccagg aagaaatgac taagaaccaa 1080
gtctcattga cttgccttgt gaagggcttc tacccatcgg atatcgccgt ggaatgggag 1140
tccaacggcc agccggaaaa caactacaag accacccctc cggtgctgga ctcagacgga 1200
tccttcttcc tctactcgcg gctgaccgtg gataagagca gatggcagga gggaaatgtg 1260
ttcagctgtt ctgtgatgca tgaagccctg cacaaccact acactcagaa gtccctgtcc 1320
ctctccctgg ga 1332
<210> 810
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 810
Arg Ala Ser Glu Ser Val Glu Tyr Tyr Gly Thr Ser Leu Met Gln
1 5 10 15
<210> 811
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 811
Ala Ala Ser Asn Val Glu Ser
1 5
<210> 812
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 812
Gln Gln Ser Arg Lys Asp Pro Ser Thr
1 5
<210> 813
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 813
Ser Glu Ser Val Glu Tyr Tyr Gly Thr Ser Leu
1 5 10
<210> 814
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 814
Ala Ala Ser
1
<210> 815
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 815
Ser Arg Lys Asp Pro Ser
1 5
<210> 816
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 816
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Met Gln Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Val Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Ser Arg
85 90 95
Lys Asp Pro Ser Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 817
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 817
gctattcagc tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta gagctagtga atcagtcgag tactacggca ctagcctgat gcagtggtat 120
cagcagaagc ccgggaaagc ccctaagctg ctgatctacg ccgcctctaa cgtggaatca 180
ggcgtgccct ctaggtttag cggtagcggt agtggcaccg acttcaccct gactatctct 240
agcctgcagc ccgaggactt cgctacctac ttctgtcagc agtctaggaa ggaccctagc 300
accttcggcg gaggcactaa ggtcgagatt aag 333
<210> 818
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 818
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Met Gln Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Val Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Ser Arg
85 90 95
Lys Asp Pro Ser Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 819
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 819
gctattcagc tgactcagtc acctagtagc ctgagcgcta gtgtgggcga tagagtgact 60
atcacctgta gagctagtga atcagtcgag tactacggca ctagcctgat gcagtggtat 120
cagcagaagc ccgggaaagc ccctaagctg ctgatctacg ccgcctctaa cgtggaatca 180
ggcgtgccct ctaggtttag cggtagcggt agtggcaccg acttcaccct gactatctct 240
agcctgcagc ccgaggactt cgctacctac ttctgtcagc agtctaggaa ggaccctagc 300
accttcggcg gaggcactaa ggtcgagatt aagcgtacgg tggccgctcc cagcgtgttc 360
atcttccccc ccagcgacga gcagctgaag agcggcaccg ccagcgtggt gtgcctgctg 420
aacaacttct acccccggga ggccaaggtg cagtggaagg tggacaacgc cctgcagagc 480
ggcaacagcc aggagagcgt caccgagcag gacagcaagg actccaccta cagcctgagc 540
agcaccctga ccctgagcaa ggccgactac gagaagcata aggtgtacgc ctgcgaggtg 600
acccaccagg gcctgtccag ccccgtgacc aagagcttca acaggggcga gtgc 654
<210> 820
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 820
Asp Ile Tyr Pro Gly Gln Gly Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 821
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 821
Tyr Pro Gly Gln Gly Asp
1 5
<210> 822
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 822
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asp Ile Tyr Pro Gly Gln Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Gly Ala Phe Pro Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 823
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 823
caggtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctag tgtgaaagtt 60
agctgtaaag ctagtggcta tactttcact tcttataata tgcactgggt ccgccaggcc 120
ccaggtcaag gcctcgagtg gatcggcgat atctaccccg gtcaaggcga cacttcctat 180
aatcagaagt ttaagggtag agctactatg accgccgata agtctacttc taccgtctat 240
atggaactga gttccctgag gtctgaggac accgccgtct actactgcgc tagagtgggc 300
ggagccttcc caatggacta ctggggtcaa ggcaccctgg tcaccgtgtc tagc 354
<210> 824
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 824
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asp Ile Tyr Pro Gly Gln Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Gly Ala Phe Pro Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 825
<211> 1332
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 825
caggtgcagc tggtgcagtc aggcgccgaa gtgaagaaac ccggcgctag tgtgaaagtt 60
agctgtaaag ctagtggcta tactttcact tcttataata tgcactgggt ccgccaggcc 120
ccaggtcaag gcctcgagtg gatcggcgat atctaccccg gtcaaggcga cacttcctat 180
aatcagaagt ttaagggtag agctactatg accgccgata agtctacttc taccgtctat 240
atggaactga gttccctgag gtctgaggac accgccgtct actactgcgc tagagtgggc 300
ggagccttcc caatggacta ctggggtcaa ggcaccctgg tcaccgtgtc tagcgctagc 360
actaagggcc cgtccgtgtt ccccctggca ccttgtagcc ggagcactag cgaatccacc 420
gctgccctcg gctgcctggt caaggattac ttcccggagc ccgtgaccgt gtcctggaac 480
agcggagccc tgacctccgg agtgcacacc ttccccgctg tgctgcagag ctccgggctg 540
tactcgctgt cgtcggtggt cacggtgcct tcatctagcc tgggtaccaa gacctacact 600
tgcaacgtgg accacaagcc ttccaacact aaggtggaca agcgcgtcga atcgaagtac 660
ggcccaccgt gcccgccttg tcccgcgccg gagttcctcg gcggtccctc ggtctttctg 720
ttcccaccga agcccaagga cactttgatg atttcccgca cccctgaagt gacatgcgtg 780
gtcgtggacg tgtcacagga agatccggag gtgcagttca attggtacgt ggatggcgtc 840
gaggtgcaca acgccaaaac caagccgagg gaggagcagt tcaactccac ttaccgcgtc 900
gtgtccgtgc tgacggtgct gcatcaggac tggctgaacg ggaaggagta caagtgcaaa 960
gtgtccaaca agggacttcc tagctcaatc gaaaagacca tctcgaaagc caagggacag 1020
ccccgggaac cccaagtgta taccctgcca ccgagccagg aagaaatgac taagaaccaa 1080
gtctcattga cttgccttgt gaagggcttc tacccatcgg atatcgccgt ggaatgggag 1140
tccaacggcc agccggaaaa caactacaag accacccctc cggtgctgga ctcagacgga 1200
tccttcttcc tctactcgcg gctgaccgtg gataagagca gatggcagga gggaaatgtg 1260
ttcagctgtt ctgtgatgca tgaagccctg cacaaccact acactcagaa gtccctgtcc 1320
ctctccctgg ga 1332
<210> 826
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 826
Asp Ile Val Leu Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Met Gln Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Val Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Lys Asp Pro Ser Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 827
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 827
gatatcgtcc tgactcagtc acccgatagc ctggccgtca gcctgggcga gcgggctact 60
attaactgta gagctagtga atcagtcgag tactacggca ctagcctgat gcagtggtat 120
cagcagaagc ccggtcaacc ccctaagctg ctgatctacg ccgcctctaa cgtggaatca 180
ggcgtgcccg ataggtttag cggtagcggt agtggcaccg acttcaccct gactattagt 240
agcctgcagg ccgaggacgt ggccgtctac tactgtcagc agtctaggaa ggaccctagc 300
accttcggcg gaggcactaa ggtcgagatt aag 333
<210> 828
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 828
Asp Ile Val Leu Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Met Gln Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Val Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Lys Asp Pro Ser Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 829
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 829
gatatcgtcc tgactcagtc acccgatagc ctggccgtca gcctgggcga gcgggctact 60
attaactgta gagctagtga atcagtcgag tactacggca ctagcctgat gcagtggtat 120
cagcagaagc ccggtcaacc ccctaagctg ctgatctacg ccgcctctaa cgtggaatca 180
ggcgtgcccg ataggtttag cggtagcggt agtggcaccg acttcaccct gactattagt 240
agcctgcagg ccgaggacgt ggccgtctac tactgtcagc agtctaggaa ggaccctagc 300
accttcggcg gaggcactaa ggtcgagatt aagcgtacgg tggccgctcc cagcgtgttc 360
atcttccccc ccagcgacga gcagctgaag agcggcaccg ccagcgtggt gtgcctgctg 420
aacaacttct acccccggga ggccaaggtg cagtggaagg tggacaacgc cctgcagagc 480
ggcaacagcc aggagagcgt caccgagcag gacagcaagg actccaccta cagcctgagc 540
agcaccctga ccctgagcaa ggccgactac gagaagcata aggtgtacgc ctgcgaggtg 600
acccaccagg gcctgtccag ccccgtgacc aagagcttca acaggggcga gtgc 654
<210> 830
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 830
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ala Ser Gly Phe Thr Phe Ser Ser
20 25 30
Tyr Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Asp Trp
35 40 45
Val Ser Thr Ile Ser Gly Gly Gly Thr Tyr Thr Tyr Tyr Gln Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ser Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
100 105 110
Ser Ala
<210> 831
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 831
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Arg Arg Tyr
20 25 30
Leu Asn Trp Tyr His Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser His Ser Ala Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 832
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 832
Glu Val Gln Val Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Tyr Cys Val Ala Ser Gly Phe Thr Phe Ser Gly Ser
20 25 30
Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Lys Lys Tyr Tyr Val Gly Pro Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly
115 120
<210> 833
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 833
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln His Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Ser Pro Leu Thr Phe Gly Gly Gly Thr Lys Ile Glu Val
100 105 110
Lys
<210> 834
<400> 834
000
<210> 835
<400> 835
000
<210> 836
<400> 836
000
<210> 837
<400> 837
000
<210> 838
<400> 838
000
<210> 839
<400> 839
000
<210> 840
<400> 840
000
<210> 841
<400> 841
000
<210> 842
<400> 842
000
<210> 843
<400> 843
000
<210> 844
<400> 844
000
<210> 845
<400> 845
000
<210> 846
<400> 846
000
<210> 847
<400> 847
000
<210> 848
<400> 848
000
<210> 849
<400> 849
000
<210> 850
<400> 850
000
<210> 851
<400> 851
000
<210> 852
<400> 852
000
<210> 853
<400> 853
000
<210> 854
<400> 854
000
<210> 855
<400> 855
000
<210> 856
<400> 856
000
<210> 857
<400> 857
000
<210> 858
<400> 858
000
<210> 859
<400> 859
000
<210> 860
<400> 860
000
<210> 861
<400> 861
000
<210> 862
<400> 862
000
<210> 863
<400> 863
000
<210> 864
<400> 864
000
<210> 865
<400> 865
000
<210> 866
<400> 866
000
<210> 867
<400> 867
000
<210> 868
<400> 868
000
<210> 869
<400> 869
000
<210> 870
<400> 870
000
<210> 871
<400> 871
000
<210> 872
<400> 872
000
<210> 873
<400> 873
000
<210> 874
<400> 874
000
<210> 875
<400> 875
000
<210> 876
<400> 876
000
<210> 877
<400> 877
000
<210> 878
<400> 878
000
<210> 879
<400> 879
000
<210> 880
<400> 880
000
<210> 881
<400> 881
000
<210> 882
<400> 882
000
<210> 883
<400> 883
000
<210> 884
<400> 884
000
<210> 885
<400> 885
000
<210> 886
<400> 886
000
<210> 887
<400> 887
000
<210> 888
<400> 888
000
<210> 889
<400> 889
000
<210> 890
<400> 890
000
<210> 891
<400> 891
000
<210> 892
<400> 892
000
<210> 893
<400> 893
000
<210> 894
<400> 894
000
<210> 895
<400> 895
000
<210> 896
<400> 896
000
<210> 897
<400> 897
000
<210> 898
<400> 898
000
<210> 899
<400> 899
000
<210> 900
<400> 900
000
<210> 901
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 901
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
Gly Val Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Val Ile Trp Gly Gly Gly Gly Thr Tyr Tyr Ala Ser Ser Leu Met
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Ala Tyr Gly His Asp Gly Gly Phe Ala Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 902
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 902
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Ser Ser Asn
20 25 30
Val Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gly Gln Ser Tyr Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 903
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 903
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
Gly Val Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Val Ile Trp Gly Gly Gly Gly Thr Tyr Tyr Ala Ser Ser Leu Met
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Ala Tyr Gly His Asp Gly Gly Phe Ala Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 904
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 904
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Ser Ser Asn
20 25 30
Val Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gly Gln Ser Tyr Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 905
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 905
gaggtgcagc tggtggaatc tggcggcgga ctggtgcagt ccggcggctc tctgagactg 60
tcttgcgctg cctccggctt ctccctgtcc tcttacggcg tggactgggt gcgacaggcc 120
cctggcaagg gcctggaatg ggtgggagtg atctggggcg gaggcggcac ctactacgcc 180
tcttccctga tgggccggtt caccatctcc cgggacaact ccaagaacac cctgtacctg 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact actgcgccag acacgcctac 300
ggccacgacg gcggcttcgc catggattat tggggccagg gcaccctggt gacagtgtcc 360
tcc 363
<210> 906
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 906
gagatcgtga tgacccagtc ccccgccacc ctgtctgtgt ctcccggcga gagagccacc 60
ctgagctgca gagcctccga gtccgtgtcc tccaacgtgg cctggtatca gcagagacct 120
ggtcaggccc ctcggctgct gatctacggc gcctctaacc gggccaccgg catccctgcc 180
agattctccg gctccggcag cggcaccgac ttcaccctga ccatctcccg gctggaaccc 240
gaggacttcg ccgtgtacta ctgcggccag tcctactcat accccttcac cttcggccag 300
ggcaccaagc tggaaatcaa g 321
<210> 907
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 907
gaggtgcagc tggtggaatc tggcggcgga ctggtgcagt ccggcggctc tctgagactg 60
tcttgcgctg cctccggctt ctccctgtcc tcttacggcg tggactgggt gcgacaggcc 120
cctggcaagg gcctggaatg ggtgggagtg atctggggcg gaggcggcac ctactacgcc 180
tcttccctga tgggccggtt caccatctcc cgggacaact ccaagaacac cctgtacctg 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact actgcgccag acacgcctac 300
ggccacgacg gcggcttcgc catggattat tggggccagg gcaccctggt gacagtgtcc 360
tccgctagca ccaagggccc aagtgtgttt cccctggccc ccagcagcaa gtctacttcc 420
ggcggaactg ctgccctggg ttgcctggtg aaggactact tccccgagcc cgtgacagtg 480
tcctggaact ctggggctct gacttccggc gtgcacacct tccccgccgt gctgcagagc 540
agcggcctgt acagcctgag cagcgtggtg acagtgccct ccagctctct gggaacccag 600
acctatatct gcaacgtgaa ccacaagccc agcaacacca aggtggacaa gagagtggag 660
cccaagagct gcgacaagac ccacacctgc cccccctgcc cagctccaga actgctggga 720
gggccttccg tgttcctgtt cccccccaag cccaaggaca ccctgatgat cagcaggacc 780
cccgaggtga cctgcgtggt ggtggacgtg tcccacgagg acccagaggt gaagttcaac 840
tggtacgtgg acggcgtgga ggtgcacaac gccaagacca agcccagaga ggagcagtac 900
aacagcacct acagggtggt gtccgtgctg accgtgctgc accaggactg gctgaacggc 960
aaagaataca agtgcaaagt ctccaacaag gccctgccag ccccaatcga aaagacaatc 1020
agcaaggcca agggccagcc acgggagccc caggtgtaca ccctgccccc cagccgggag 1080
gagatgacca agaaccaggt gtccctgacc tgtctggtga agggcttcta ccccagcgat 1140
atcgccgtgg agtgggagag caacggccag cccgagaaca actacaagac caccccccca 1200
gtgctggaca gcgacggcag cttcttcctg tacagcaagc tgaccgtgga caagtccagg 1260
tggcagcagg gcaacgtgtt cagctgcagc gtgatgcacg aggccctgca caaccactac 1320
acccagaagt ccctgagcct gagccccggc aag 1353
<210> 908
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 908
gagatcgtga tgacccagtc ccccgccacc ctgtctgtgt ctcccggcga gagagccacc 60
ctgagctgca gagcctccga gtccgtgtcc tccaacgtgg cctggtatca gcagagacct 120
ggtcaggccc ctcggctgct gatctacggc gcctctaacc gggccaccgg catccctgcc 180
agattctccg gctccggcag cggcaccgac ttcaccctga ccatctcccg gctggaaccc 240
gaggacttcg ccgtgtacta ctgcggccag tcctactcat accccttcac cttcggccag 300
ggcaccaagc tggaaatcaa gcgtacggtg gccgctccca gcgtgttcat cttccccccc 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac 420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 909
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 909
Ser Tyr Gly Val Asp
1 5
<210> 910
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 910
Gly Phe Ser Leu Ser Ser Tyr
1 5
<210> 911
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 911
Val Ile Trp Gly Gly Gly Gly Thr Tyr Tyr Ala Ser Ser Leu Met Gly
1 5 10 15
<210> 912
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 912
Trp Gly Gly Gly Gly
1 5
<210> 913
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 913
His Ala Tyr Gly His Asp Gly Gly Phe Ala Met Asp Tyr
1 5 10
<210> 914
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 914
Arg Ala Ser Glu Ser Val Ser Ser Asn Val Ala
1 5 10
<210> 915
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 915
Ser Glu Ser Val Ser Ser Asn
1 5
<210> 916
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 916
Gly Ala Ser Asn Arg Ala Thr
1 5
<210> 917
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 917
Gly Ala Ser
1
<210> 918
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 918
Gly Gln Ser Tyr Ser Tyr Pro Phe Thr
1 5
<210> 919
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 919
Ser Tyr Ser Tyr Pro Phe
1 5
<210> 920
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 920
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Glu Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Met Val Arg Gly Asp Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 921
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 921
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Ala
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Asn Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 922
<400> 922
000
<210> 923
<400> 923
000
<210> 924
<400> 924
000
<210> 925
<400> 925
000
<210> 926
<400> 926
000
<210> 927
<400> 927
000
<210> 928
<400> 928
000
<210> 929
<400> 929
000
<210> 930
<400> 930
000
<210> 931
<400> 931
000
<210> 932
<400> 932
000
<210> 933
<400> 933
000
<210> 934
<400> 934
000
<210> 935
<400> 935
000
<210> 936
<400> 936
000
<210> 937
<400> 937
000
<210> 938
<400> 938
000
<210> 939
<400> 939
000
<210> 940
<400> 940
000
<210> 941
<400> 941
000
<210> 942
<400> 942
000
<210> 943
<400> 943
000
<210> 944
<400> 944
000
<210> 945
<400> 945
000
<210> 946
<400> 946
000
<210> 947
<400> 947
000
<210> 948
<400> 948
000
<210> 949
<400> 949
000
<210> 950
<400> 950
000
<210> 951
<400> 951
000
<210> 952
<400> 952
000
<210> 953
<400> 953
000
<210> 954
<400> 954
000
<210> 955
<400> 955
000
<210> 956
<400> 956
000
<210> 957
<400> 957
000
<210> 958
<400> 958
000
<210> 959
<400> 959
000
<210> 960
<400> 960
000
<210> 961
<400> 961
000
<210> 962
<400> 962
000
<210> 963
<400> 963
000
<210> 964
<400> 964
000
<210> 965
<400> 965
000
<210> 966
<400> 966
000
<210> 967
<400> 967
000
<210> 968
<400> 968
000
<210> 969
<400> 969
000
<210> 970
<400> 970
000
<210> 971
<400> 971
000
<210> 972
<400> 972
000
<210> 973
<400> 973
000
<210> 974
<400> 974
000
<210> 975
<400> 975
000
<210> 976
<400> 976
000
<210> 977
<400> 977
000
<210> 978
<400> 978
000
<210> 979
<400> 979
000
<210> 980
<400> 980
000
<210> 981
<400> 981
000
<210> 982
<400> 982
000
<210> 983
<400> 983
000
<210> 984
<400> 984
000
<210> 985
<400> 985
000
<210> 986
<400> 986
000
<210> 987
<400> 987
000
<210> 988
<400> 988
000
<210> 989
<400> 989
000
<210> 990
<400> 990
000
<210> 991
<400> 991
000
<210> 992
<400> 992
000
<210> 993
<400> 993
000
<210> 994
<400> 994
000
<210> 995
<400> 995
000
<210> 996
<400> 996
000
<210> 997
<400> 997
000
<210> 998
<400> 998
000
<210> 999
<400> 999
000
<210> 1000
<400> 1000
000
<210> 1001
<211> 114
<212> БЕЛОК
<213> Homo sapiens
<400> 1001
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 1002
<211> 170
<212> БЕЛОК
<213> Homo sapiens
<400> 1002
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val
65 70 75 80
Thr Thr Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly
85 90 95
Lys Glu Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr
100 105 110
Thr Ala Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro
115 120 125
Ser Thr Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr
130 135 140
Pro Ser Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser
145 150 155 160
His Gln Pro Pro Gly Val Tyr Pro Gln Gly
165 170
<210> 1003
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1003
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asp Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 1004
<211> 297
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1004
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
65 70 75 80
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
85 90 95
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
100 105 110
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
115 120 125
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
130 135 140
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
145 150 155 160
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
165 170 175
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
180 185 190
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
195 200 205
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
210 215 220
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
225 230 235 240
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
245 250 255
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
260 265 270
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
275 280 285
Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295
<210> 1005
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (93)..(93)
<223> /замена="Lys"
<220>
<221> Сайт
<222> (1)..(114)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов"
<400> 1005
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 1006
<211> 77
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1006
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro
65 70 75
<210> 1007
<211> 422
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1007
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp
20 25 30
Leu Ile Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp
35 40 45
Val His Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu
50 55 60
Leu Gln Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr
65 70 75 80
Val Glu Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly
85 90 95
Asn Val Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys
100 105 110
Asn Ile Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe
115 120 125
Ile Asn Thr Ser Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Leu Gln Ile Thr
145 150 155 160
Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val Lys Ser
165 170 175
Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly Phe Lys
180 185 190
Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn Lys Ala
195 200 205
Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile Arg Asp
210 215 220
Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val Thr Thr
225 230 235 240
Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly Lys Glu
245 250 255
Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr Thr Ala
260 265 270
Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro Ser Thr
275 280 285
Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr Pro Ser
290 295 300
Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser His Gln
305 310 315 320
Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr Val Ala Ile
325 330 335
Ser Thr Ser Thr Val Leu Leu Cys Gly Leu Ser Ala Val Ser Leu Leu
340 345 350
Ala Cys Tyr Leu Lys Ser Arg Gln Thr Pro Pro Leu Ala Ser Val Glu
355 360 365
Met Glu Ala Met Glu Ala Leu Pro Val Thr Trp Gly Thr Ser Ser Arg
370 375 380
Asp Glu Asp Leu Glu Asn Cys Ser His His Leu Ser Arg Met Asp Tyr
385 390 395 400
Lys Asp Asp Asp Asp Lys Asp Tyr Lys Asp Asp Asp Asp Lys Asp Tyr
405 410 415
Lys Asp Asp Asp Asp Lys
420
<210> 1008
<211> 209
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1008
Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val Lys Ser
1 5 10 15
Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly Phe Lys
20 25 30
Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn Lys Ala
35 40 45
Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile Arg Asp
50 55 60
Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Gly Gly Ser Gly
65 70 75 80
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser Leu Gln Asn
85 90 95
Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln
100 105 110
Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro
115 120 125
Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val
130 135 140
Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu Asn
145 150 155 160
Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr
165 170 175
Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys
180 185 190
Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn Thr
195 200 205
Ser
<210> 1009
<211> 459
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1009
Ala Cys Asp Cys Arg Gly Asp Cys Phe Cys Gly Gly Gly Gly Gly Ser
1 5 10 15
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
20 25 30
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
35 40 45
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
50 55 60
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
65 70 75 80
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
85 90 95
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
100 105 110
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
115 120 125
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
130 135 140
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
145 150 155 160
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
165 170 175
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
180 185 190
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
195 200 205
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
210 215 220
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
225 230 235 240
Pro Gly Lys Gly Gly Gly Gly Ser Pro Pro Pro Met Ser Val Glu His
245 250 255
Ala Asp Ile Trp Val Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr
260 265 270
Ile Cys Asn Ser Gly Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr
275 280 285
Glu Cys Val Leu Asn Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro
290 295 300
Ser Leu Lys Cys Ile Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala
305 310 315 320
Pro Pro Ser Thr Val Ser Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
325 330 335
Gly Ser Gly Gly Gly Gly Ser Leu Gln Asn Trp Val Asn Val Ile Ser
340 345 350
Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp Ala
355 360 365
Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr Ala
370 375 380
Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser Gly
385 390 395 400
Asp Ala Ser Ile His Asp Thr Val Glu Asn Leu Ile Ile Leu Ala Asn
405 410 415
Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys Glu
420 425 430
Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser Phe
435 440 445
Val His Ile Val Gln Met Phe Ile Asn Thr Ser
450 455
<210> 1010
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетическая 6xHis метка"
<400> 1010
His His His His His His
1 5
<210> 1011
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1011
Arg Gly Asp Ser
1
<210> 1012
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1012
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Asn
20 25 30
Val Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Val Ile Pro Ile Val Asp Ile Ala Asn Tyr Ala Gln Arg Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Thr Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Thr Leu Gly Leu Val Leu Asp Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Ser Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 1013
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1013
Glu Thr Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala Asp Ser Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 1014
<211> 478
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1014
Met Leu Leu Val Asn Gln Ser His Gln Gly Phe Asn Lys Glu His Thr
1 5 10 15
Ser Lys Met Val Ser Ala Ile Val Leu Tyr Val Leu Leu Ala Ala Ala
20 25 30
Ala His Ser Ala Phe Ala Thr Arg Asp Val Arg Glu Pro Pro Ala Leu
35 40 45
Lys Tyr Gly Ile Val Leu Asp Ala Gly Ser Ser His Thr Ser Met Phe
50 55 60
Ile Tyr Lys Trp Pro Ala Asp Lys Glu Asn Asp Thr Gly Ile Val Gly
65 70 75 80
Gln His Ser Ser Cys Asp Val Pro Gly Gly Gly Ile Ser Ser Tyr Ala
85 90 95
Asp Asn Pro Ser Gly Ala Ser Gln Ser Leu Val Gly Cys Leu Glu Gln
100 105 110
Ala Leu Gln Asp Val Pro Lys Glu Arg His Ala Gly Thr Pro Leu Tyr
115 120 125
Leu Gly Ala Thr Ala Gly Met Arg Leu Leu Asn Leu Thr Asn Pro Glu
130 135 140
Ala Ser Thr Ser Val Leu Met Ala Val Thr His Thr Leu Thr Gln Tyr
145 150 155 160
Pro Phe Asp Phe Arg Gly Ala Arg Ile Leu Ser Gly Gln Glu Glu Gly
165 170 175
Val Phe Gly Trp Val Thr Ala Asn Tyr Leu Leu Glu Asn Phe Ile Lys
180 185 190
Tyr Gly Trp Val Gly Arg Trp Phe Arg Pro Arg Lys Gly Thr Leu Gly
195 200 205
Ala Met Asp Leu Gly Gly Ala Ser Thr Gln Ile Thr Phe Glu Thr Thr
210 215 220
Ser Pro Ala Glu Asp Arg Ala Ser Glu Val Gln Leu His Leu Tyr Gly
225 230 235 240
Gln His Tyr Arg Val Tyr Thr His Ser Phe Leu Cys Tyr Gly Arg Asp
245 250 255
Gln Val Leu Gln Arg Leu Leu Ala Ser Ala Leu Gln Thr His Gly Phe
260 265 270
His Pro Cys Trp Pro Arg Gly Phe Ser Thr Gln Val Leu Leu Gly Asp
275 280 285
Val Tyr Gln Ser Pro Cys Thr Met Ala Gln Arg Pro Gln Asn Phe Asn
290 295 300
Ser Ser Ala Arg Val Ser Leu Ser Gly Ser Ser Asp Pro His Leu Cys
305 310 315 320
Arg Asp Leu Val Ser Gly Leu Phe Ser Phe Ser Ser Cys Pro Phe Ser
325 330 335
Arg Cys Ser Phe Asn Gly Val Phe Gln Pro Pro Val Ala Gly Asn Phe
340 345 350
Val Ala Phe Ser Ala Phe Phe Ala Thr Val Asp Phe Leu Arg Thr Ser
355 360 365
Met Gly Leu Pro Val Ala Thr Leu Gln Gln Leu Glu Ala Ala Ala Val
370 375 380
Asn Val Cys Asn Gln Thr Trp Ala Gln Leu Gln Ala Arg Val Pro Gly
385 390 395 400
Gln Arg Ala Arg Leu Ala Asp Tyr Cys Ala Gly Ala Met Phe Val Gln
405 410 415
Gln Leu Leu Ser Arg Gly Tyr Gly Phe Asp Glu Arg Ala Phe Gly Gly
420 425 430
Val Ile Phe Gln Lys Lys Ala Ala Asp Thr Ala Val Gly Trp Ala Leu
435 440 445
Gly Tyr Met Leu Asn Leu Thr Asn Leu Ile Pro Ala Asp Pro Pro Gly
450 455 460
Leu Arg Lys Gly Thr Asp Phe Ser His His His His His His
465 470 475
<210> 1015
<211> 478
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1015
Met Leu Leu Val Asn Gln Ser His Gln Gly Phe Asn Lys Glu His Thr
1 5 10 15
Ser Lys Met Val Ser Ala Ile Val Leu Tyr Val Leu Leu Ala Ala Ala
20 25 30
Ala His Ser Ala Phe Ala Thr Gln Asp Val Arg Glu Pro Pro Ala Leu
35 40 45
Lys Tyr Gly Ile Val Leu Asp Ala Gly Ser Ser His Thr Ser Met Phe
50 55 60
Val Tyr Lys Trp Pro Ala Asp Lys Glu Asn Asp Thr Gly Ile Val Gly
65 70 75 80
Gln His Ser Ser Cys Asp Val Arg Gly Gly Gly Ile Ser Ser Tyr Ala
85 90 95
Asn Asp Pro Ser Arg Ala Gly Gln Ser Leu Val Glu Cys Leu Glu Gln
100 105 110
Ala Leu Arg Asp Val Pro Lys Asp Arg Tyr Ala Ser Thr Pro Leu Tyr
115 120 125
Leu Gly Ala Thr Ala Gly Met Arg Leu Leu Asn Leu Thr Ser Pro Glu
130 135 140
Ala Thr Ala Lys Val Leu Glu Ala Val Thr Gln Thr Leu Thr Arg Tyr
145 150 155 160
Pro Phe Asp Phe Arg Gly Ala Arg Ile Leu Ser Gly Gln Asp Glu Gly
165 170 175
Val Phe Gly Trp Val Thr Ala Asn Tyr Leu Leu Glu Asn Phe Ile Lys
180 185 190
Tyr Gly Trp Val Gly Arg Trp Ile Arg Pro Arg Lys Gly Thr Leu Gly
195 200 205
Ala Met Asp Leu Gly Gly Ala Ser Thr Gln Ile Thr Phe Glu Thr Thr
210 215 220
Ser Pro Ser Glu Asp Pro Asp Asn Glu Val His Leu Arg Leu Tyr Gly
225 230 235 240
Gln His Tyr Arg Val Tyr Thr His Ser Phe Leu Cys Tyr Gly Arg Asp
245 250 255
Gln Val Leu Gln Arg Leu Leu Ala Ser Ala Leu Gln Ile His Arg Phe
260 265 270
His Pro Cys Trp Pro Lys Gly Tyr Ser Thr Gln Val Leu Leu Arg Glu
275 280 285
Val Tyr Gln Ser Pro Cys Thr Met Gly Gln Arg Pro Gln Thr Phe Asn
290 295 300
Ser Ser Ala Thr Val Ser Leu Ser Gly Thr Ser Asn Ala Ala Leu Cys
305 310 315 320
Arg Asp Leu Val Ser Gly Leu Phe Asn Ile Ser Ser Cys Pro Phe Ser
325 330 335
Gln Cys Ser Phe Asn Gly Val Phe Gln Pro Pro Val Ala Gly Asn Phe
340 345 350
Ile Ala Phe Ser Ala Phe Tyr Tyr Thr Val Asp Phe Leu Lys Thr Val
355 360 365
Met Gly Leu Pro Val Gly Thr Leu Lys Gln Leu Glu Asp Ala Thr Glu
370 375 380
Thr Thr Cys Asn Gln Thr Trp Ala Glu Leu Gln Ala Arg Val Pro Gly
385 390 395 400
Gln Gln Thr Arg Leu Pro Asp Tyr Cys Ala Val Ala Met Phe Ile His
405 410 415
Gln Leu Leu Ser Arg Gly Tyr Arg Phe Asp Glu Arg Ser Phe Arg Gly
420 425 430
Val Val Phe Glu Lys Lys Ala Ala Asp Thr Ala Val Gly Trp Ala Leu
435 440 445
Gly Tyr Met Leu Asn Leu Thr Asn Leu Ile Pro Ala Asp Leu Pro Gly
450 455 460
Leu Arg Lys Gly Thr His Phe Ser His His His His His His
465 470 475
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ИЗ АНТИТЕЛА К ПРОГАСТРИНУ И ИММУНОТЕРАПИИ ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2784604C2 |
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНЫХ АНТИГЕННЫХ РЕЦЕПТОРОВ И ИНГИБИТОРОВ PD-1 | 2017 |
|
RU2809160C2 |
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ РАКА, НАЦЕЛИВАЮЩИЕСЯ НА CD38 И TGF-БЕТА | 2019 |
|
RU2808632C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТИТЕЛ ПРОТИВ КЛАУДИНА 18.2 ДЛЯ ЛЕЧЕНИЯ РАКА | 2014 |
|
RU2792932C2 |
| АНТИТЕЛА К МЕЗОТЕЛИНУ | 2019 |
|
RU2837574C2 |
| КОМБИНАЦИИ АНТИТЕЛ К STAPHYLOCOCCUS AUREUS | 2019 |
|
RU2804815C2 |
| ПРОКОАГУЛЯНТНЫЕ АНТИТЕЛА | 2018 |
|
RU2810094C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО | 2021 |
|
RU2840407C1 |
| МОНОВАЛЕНТНЫЕ АНТИТЕЛА К ПРОПЕРДИНУ И ФРАГМЕНТЫ АНТИТЕЛ | 2018 |
|
RU2790103C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
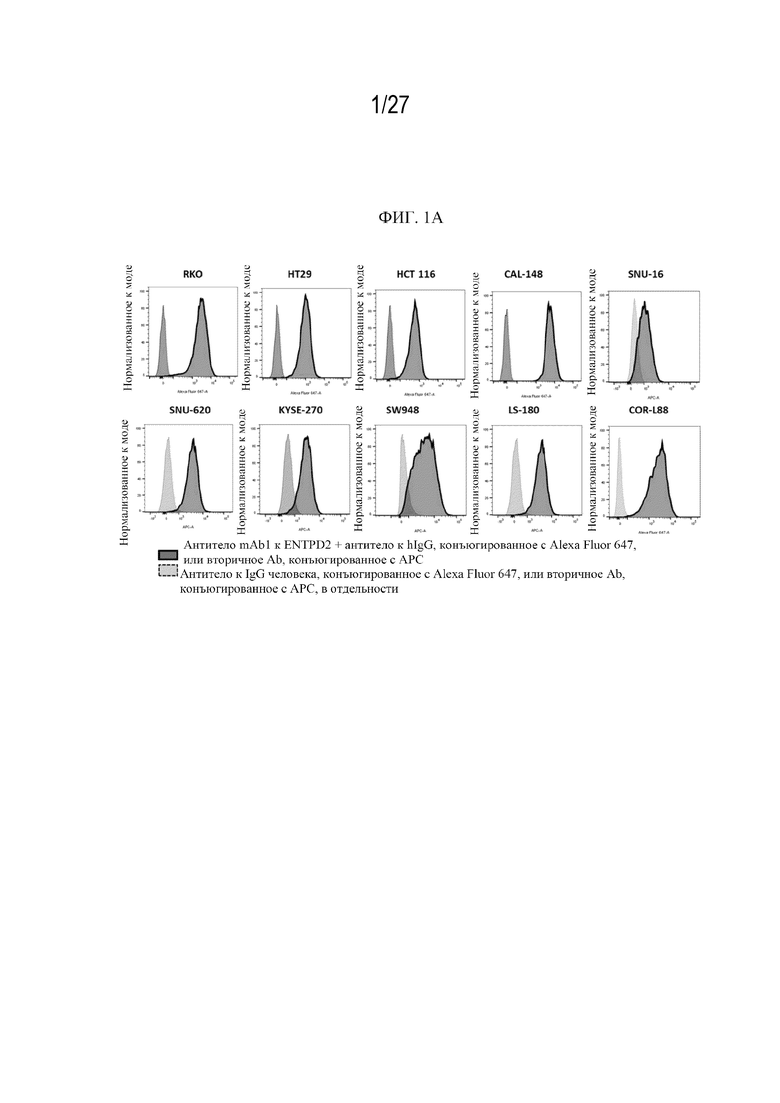
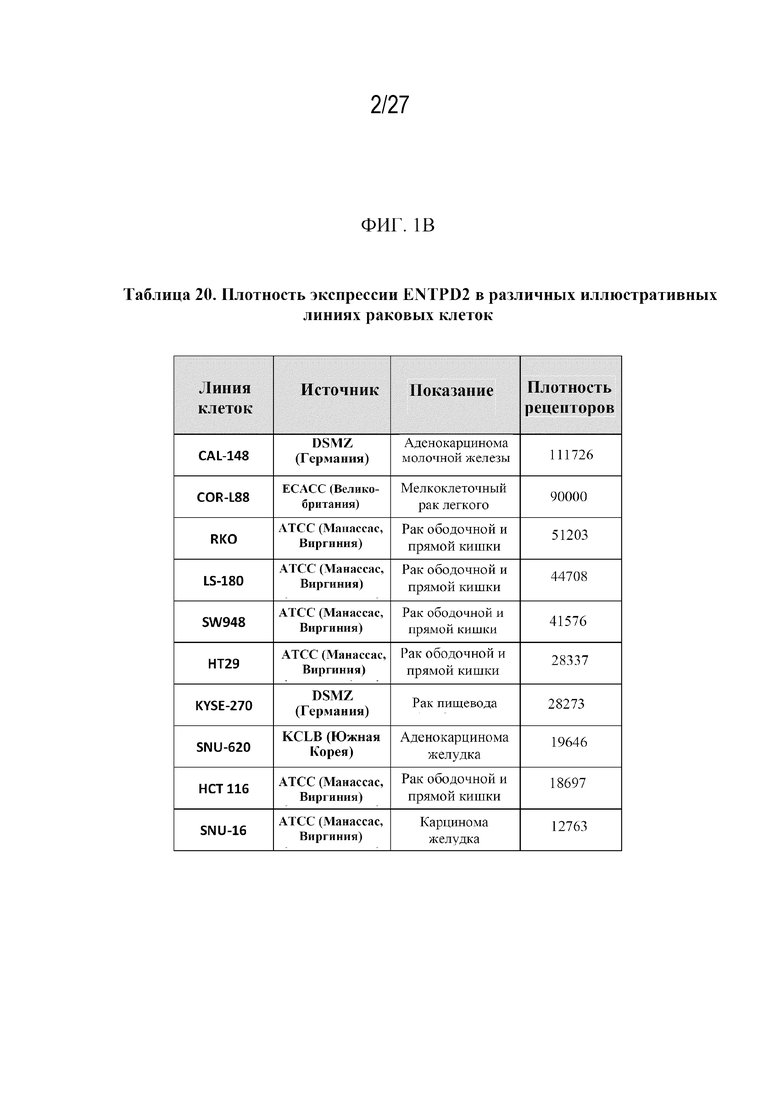
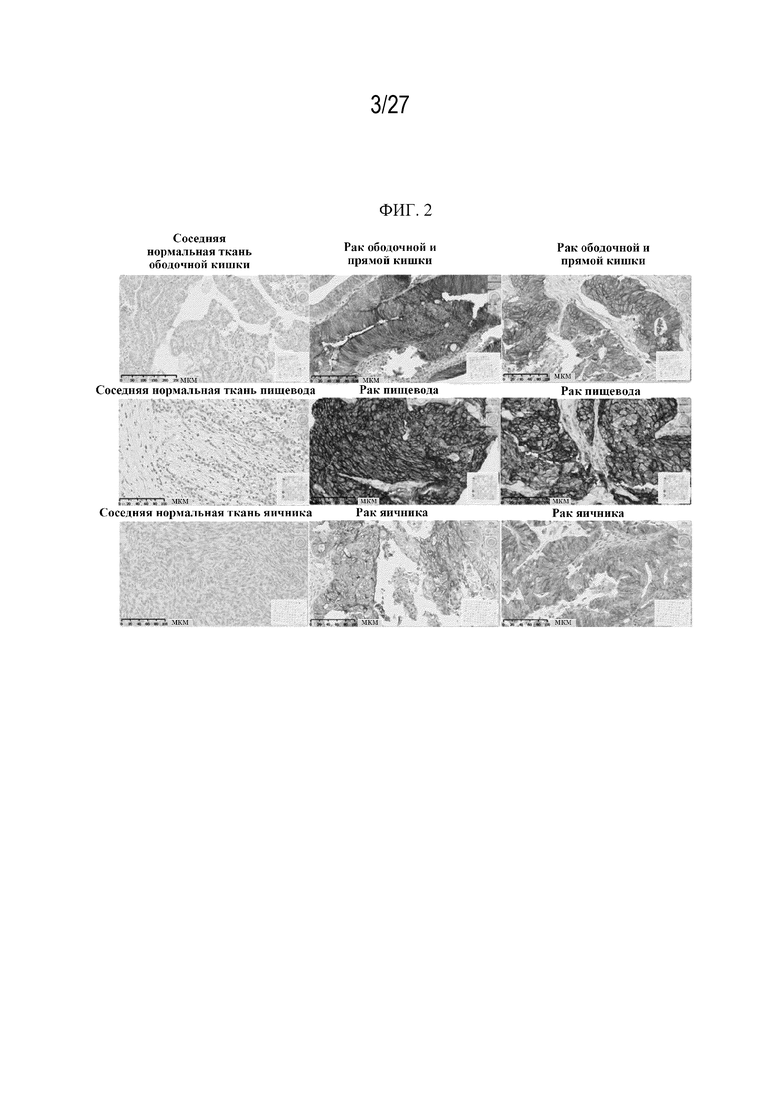





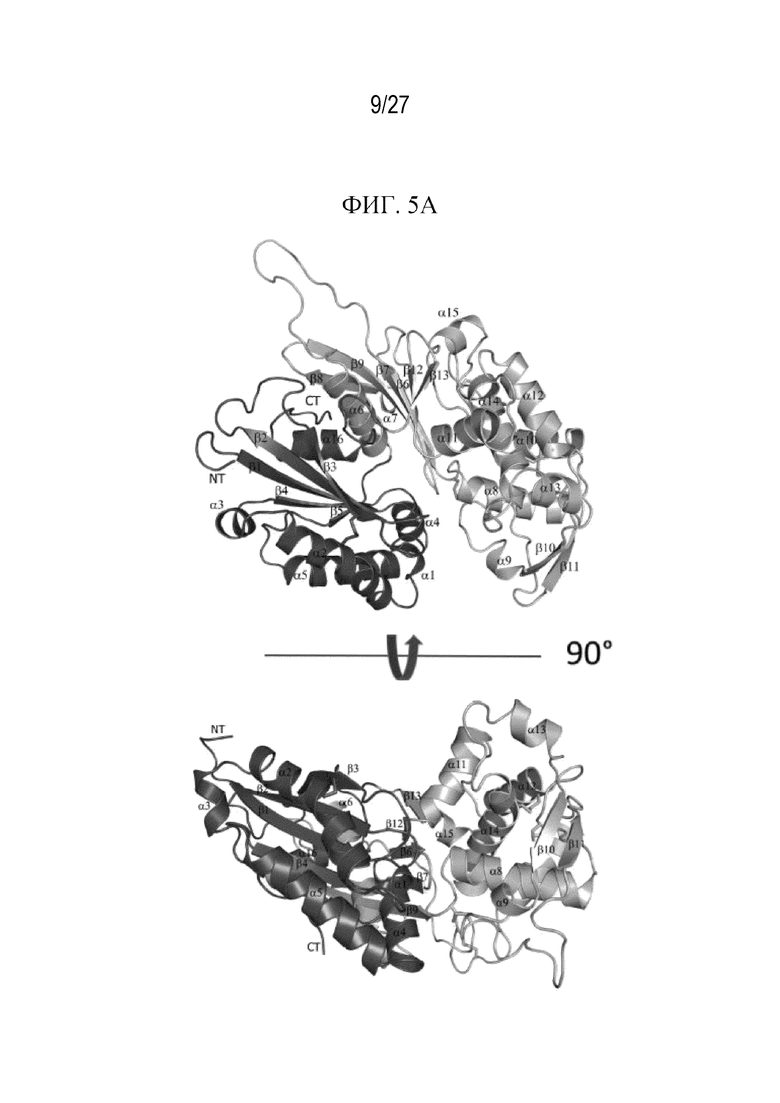
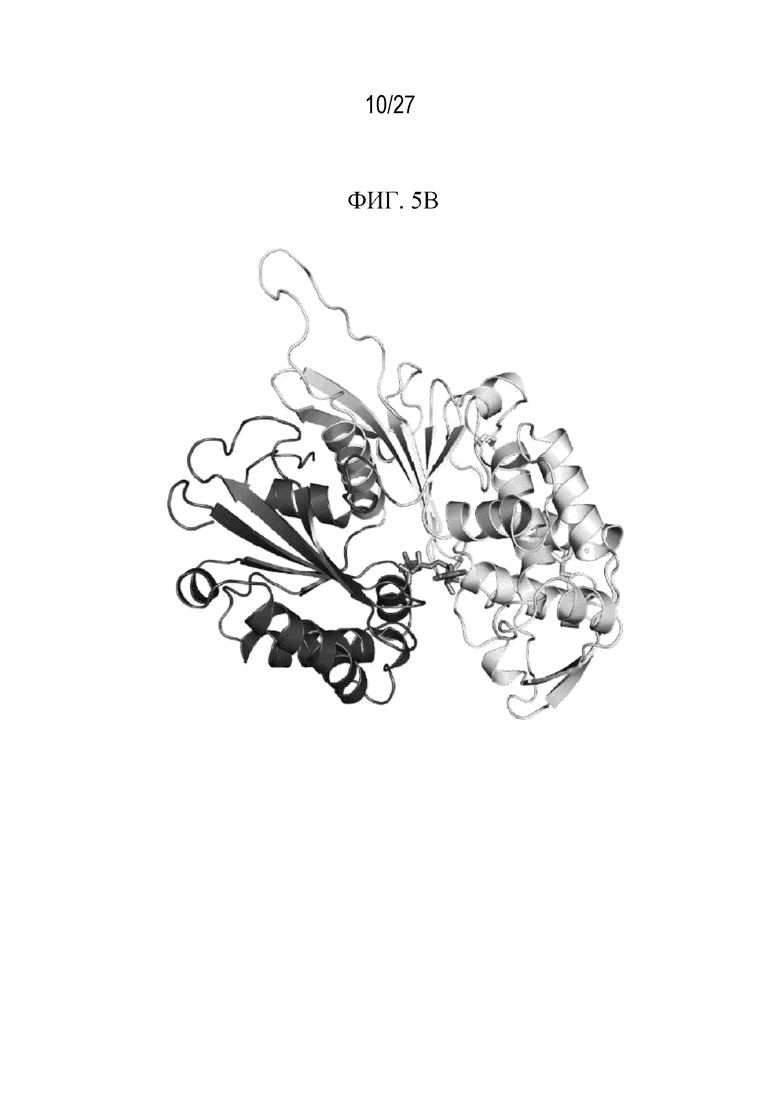
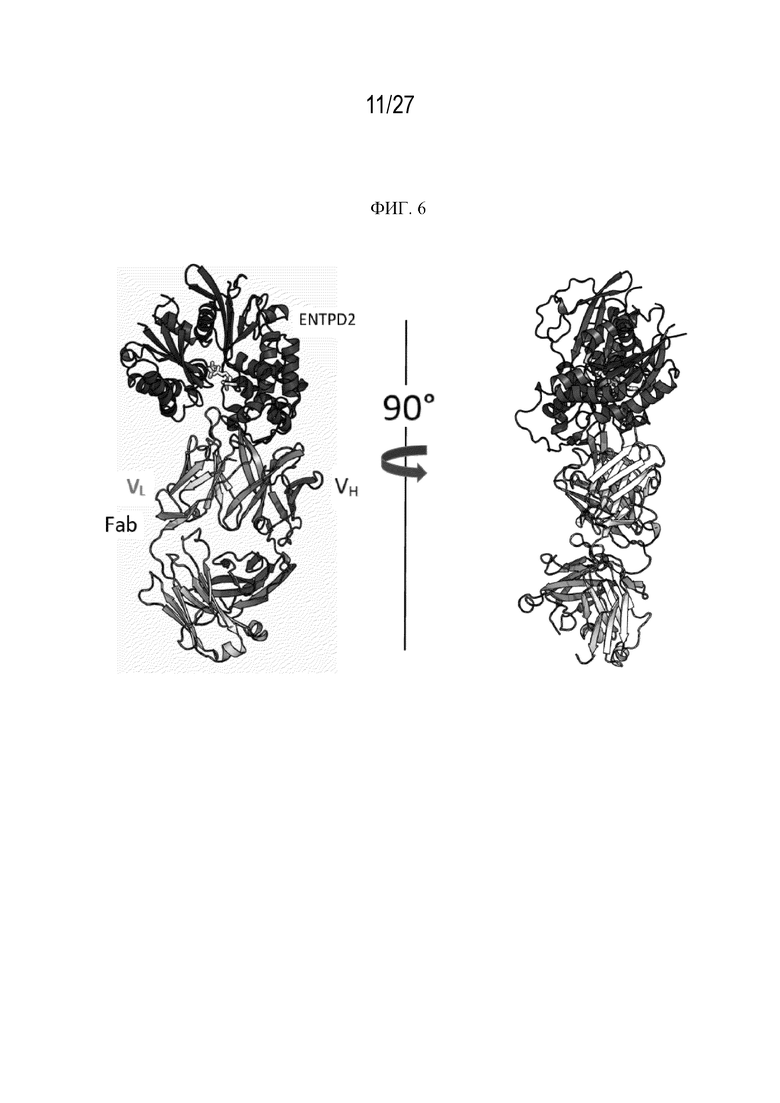
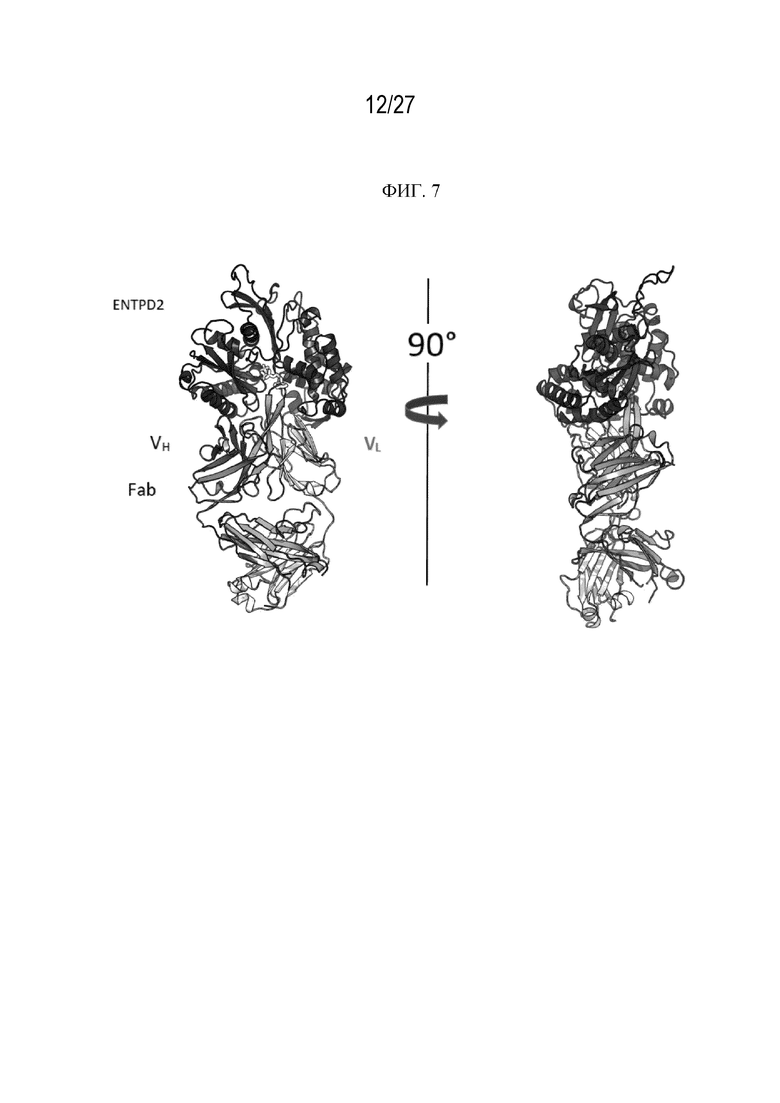
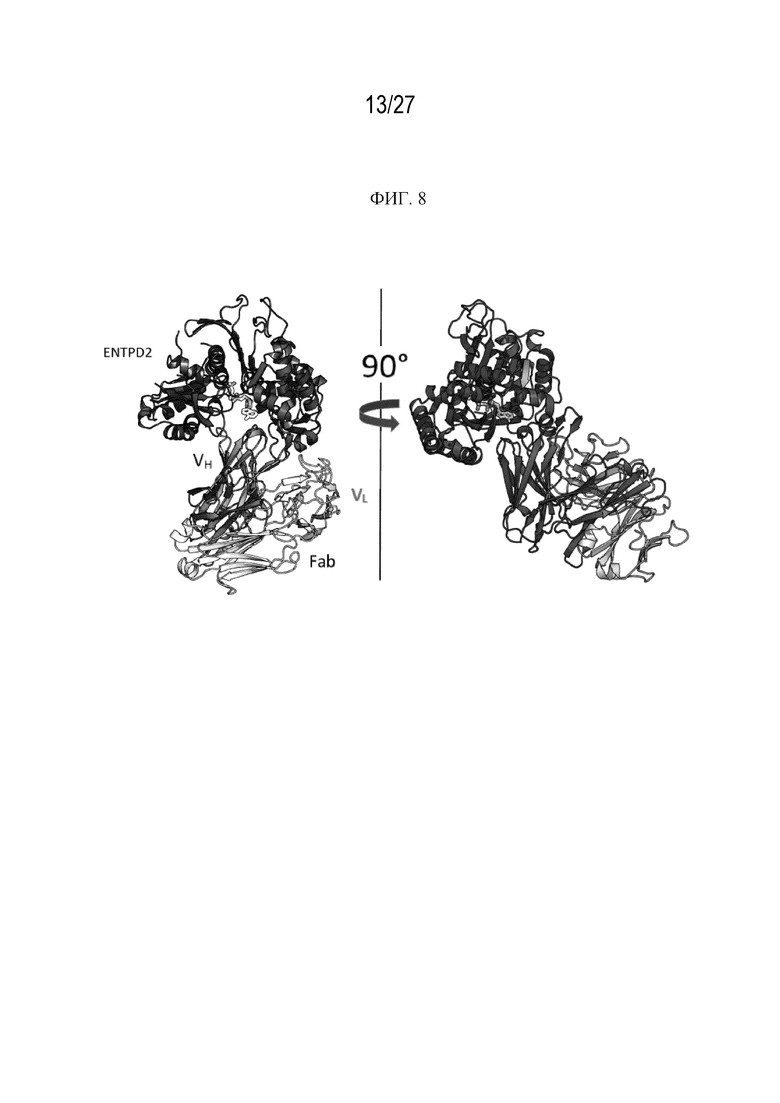
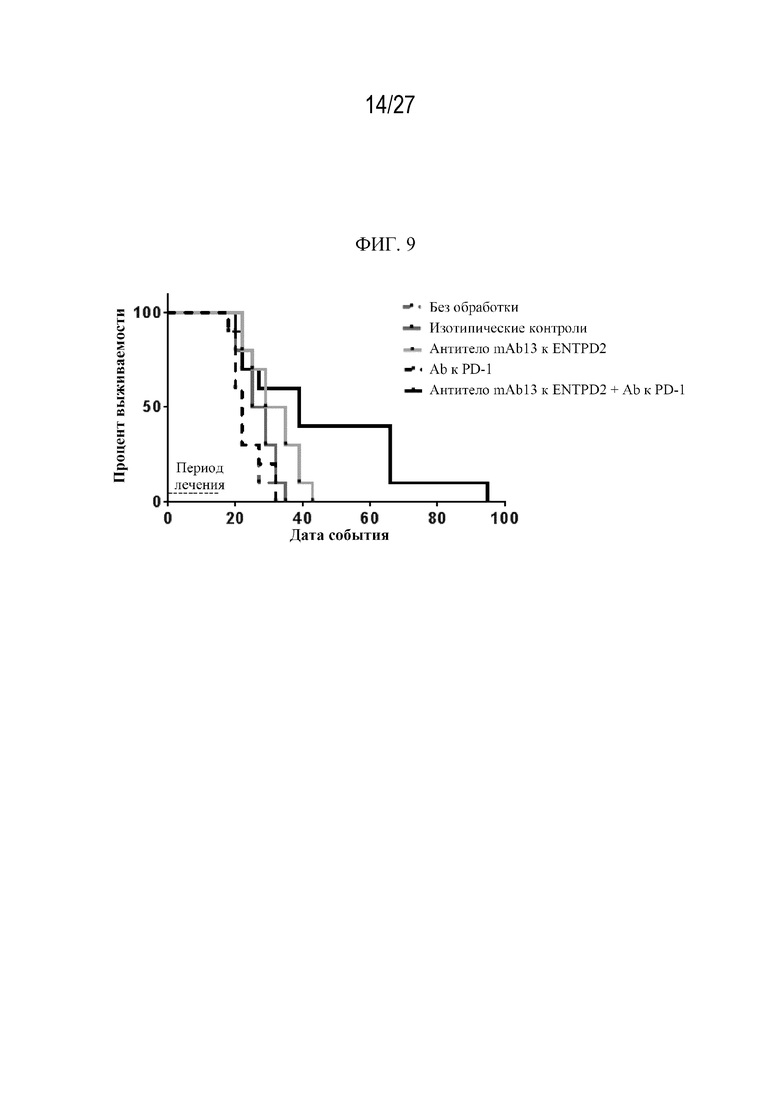
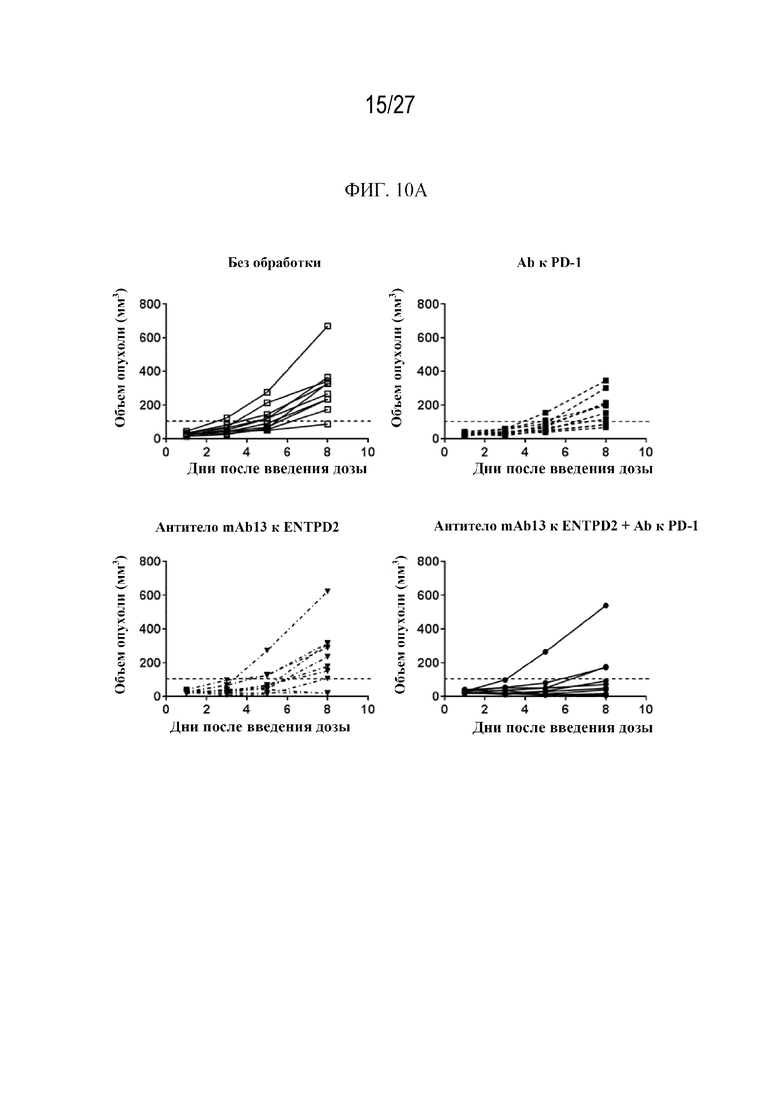
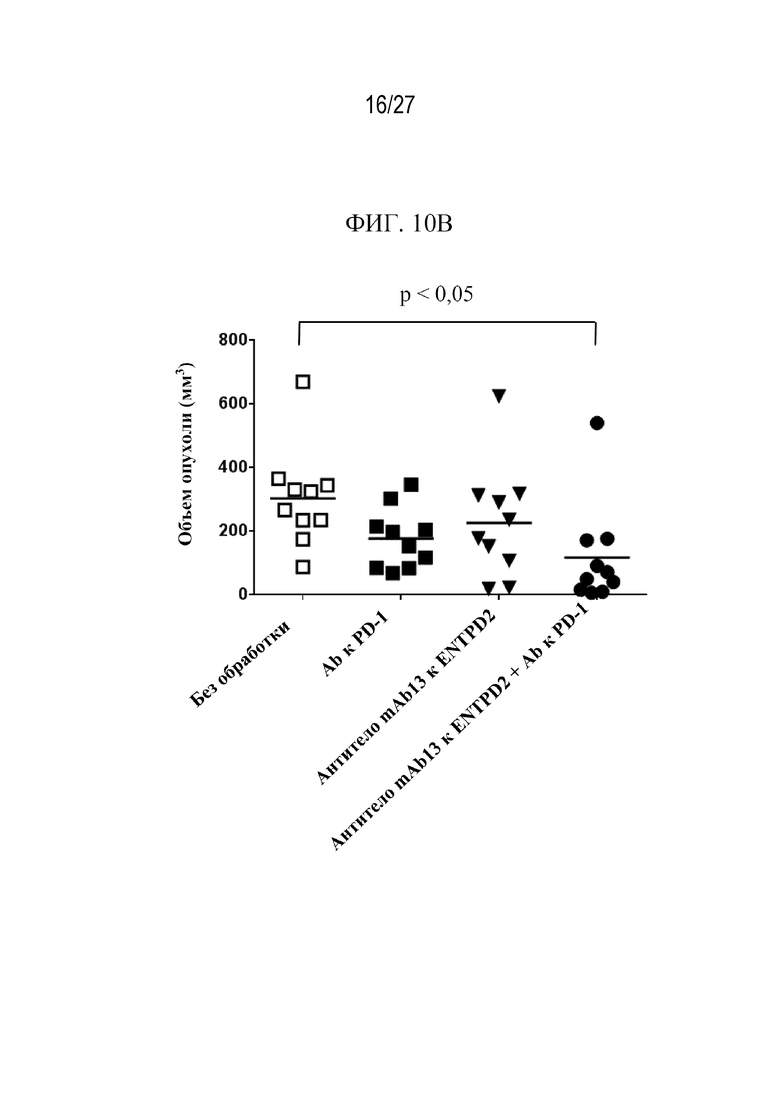
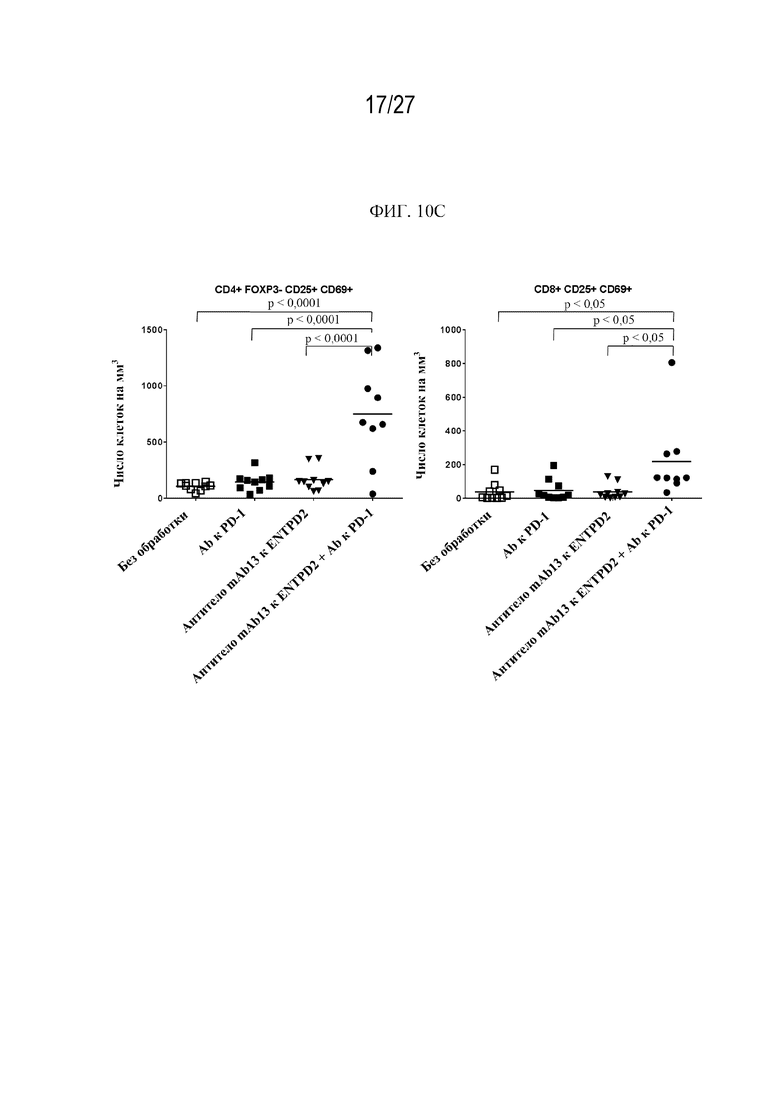
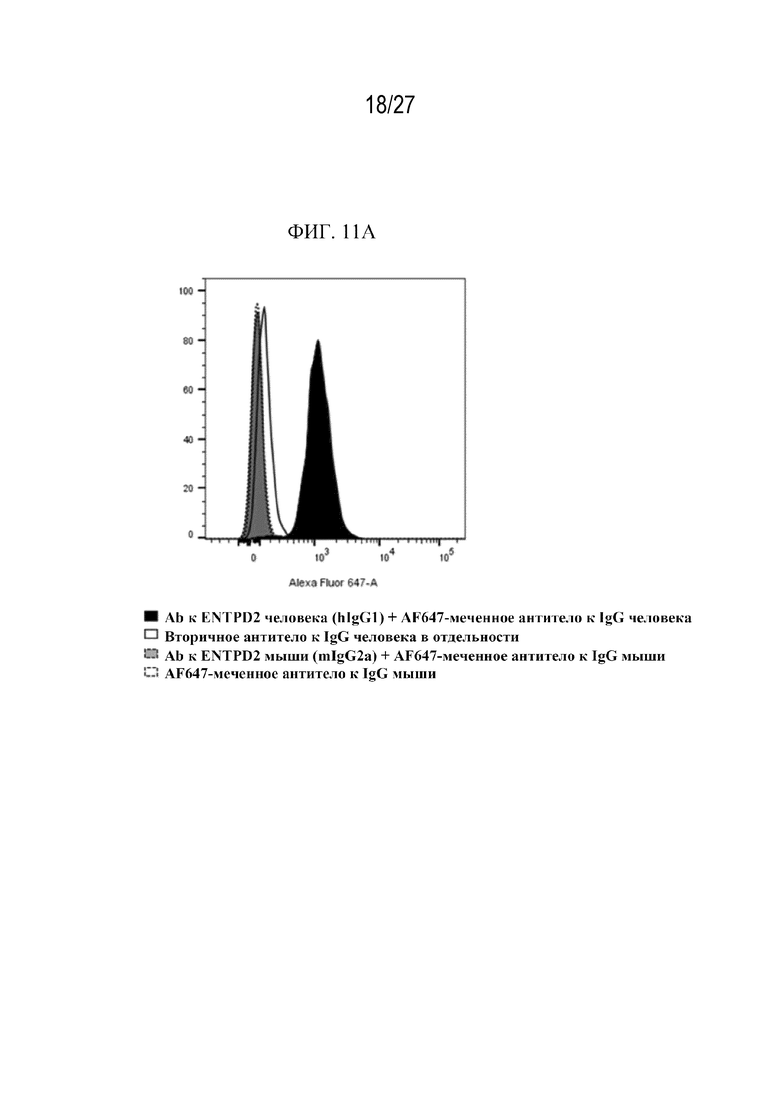


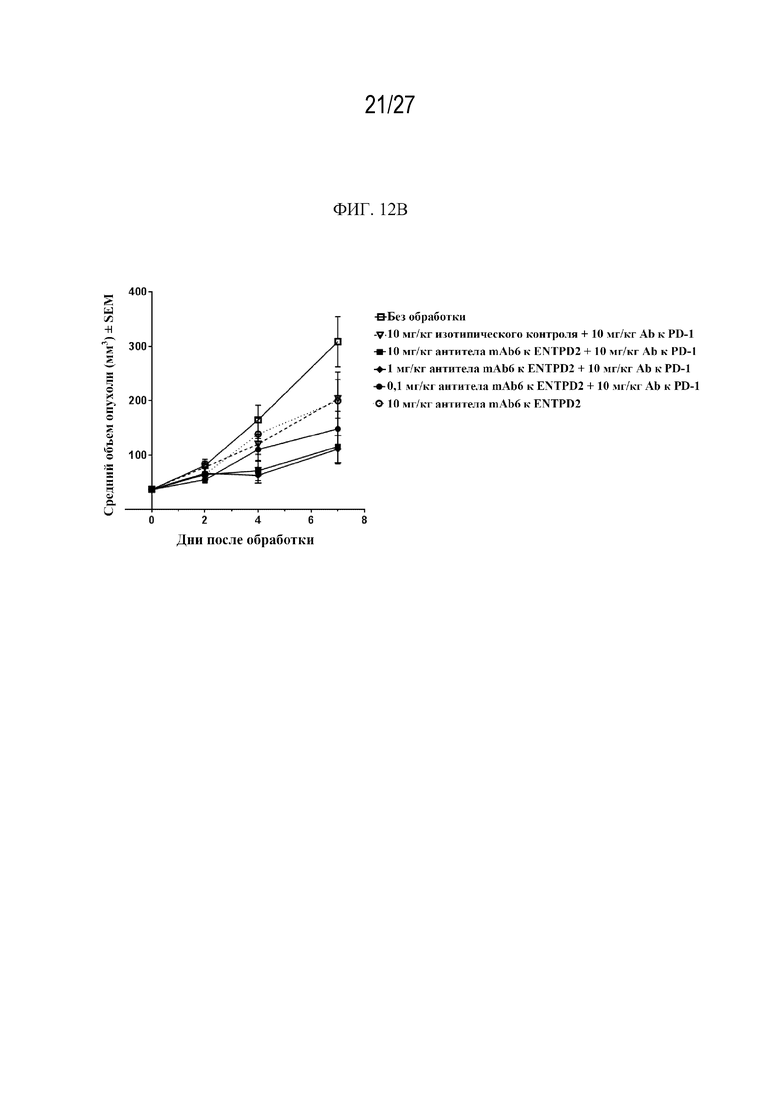
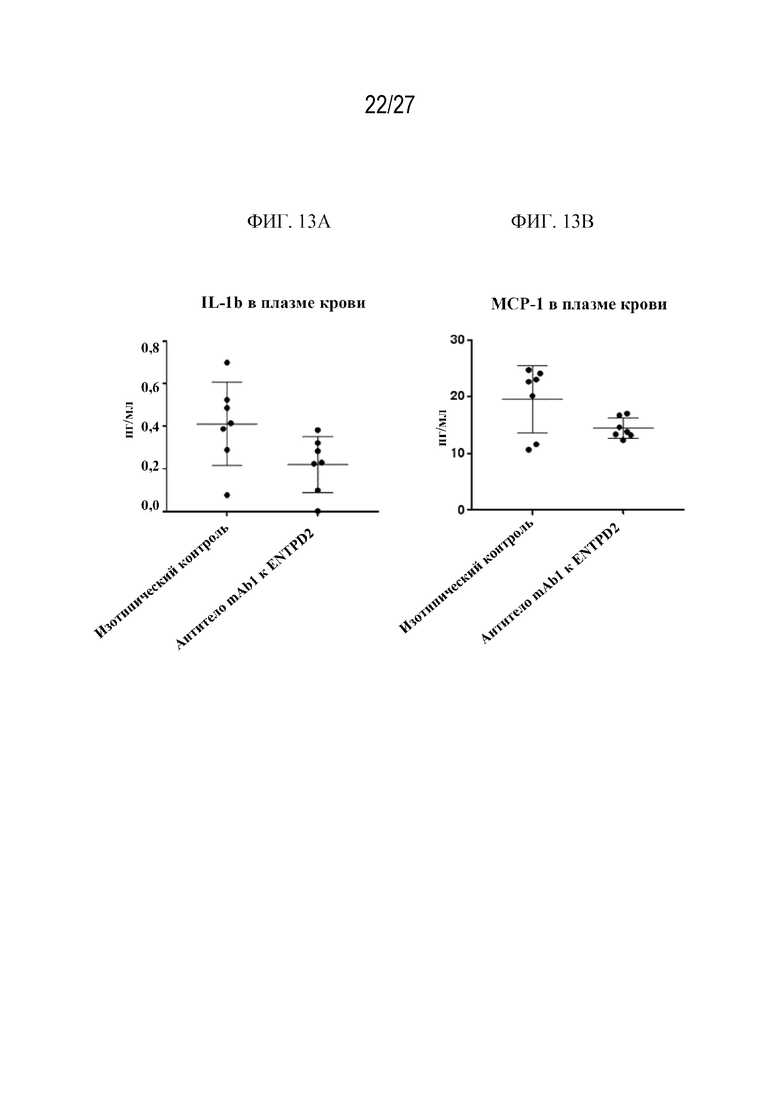
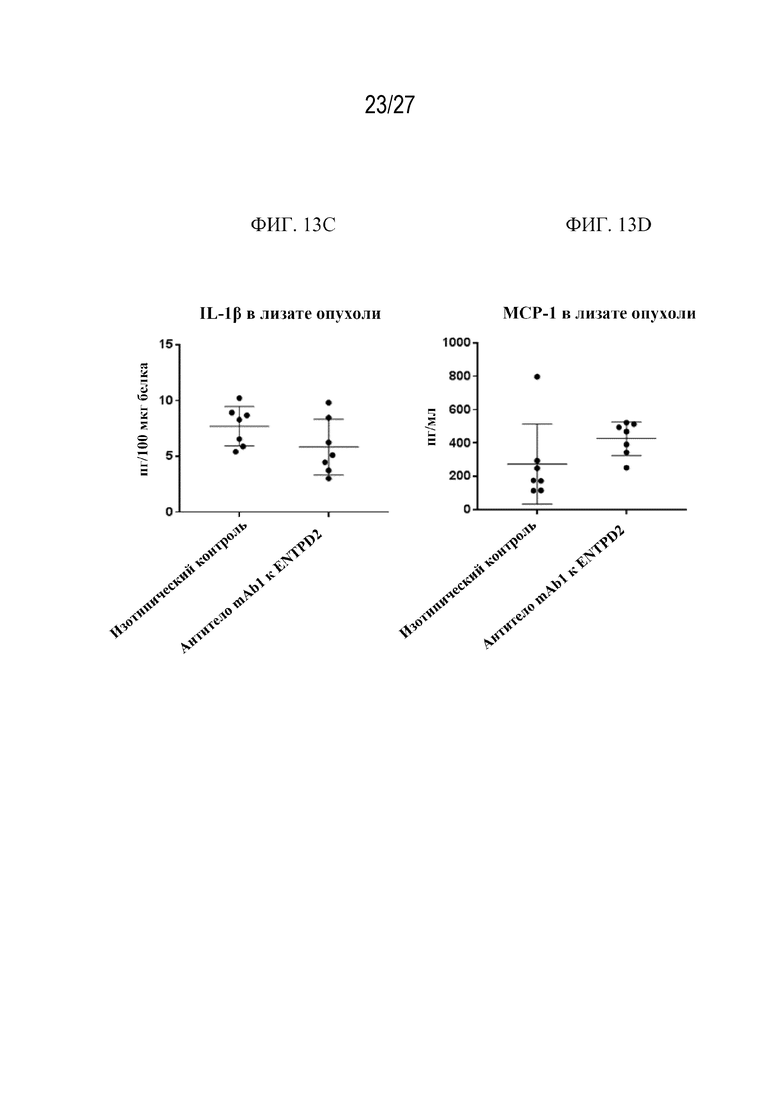
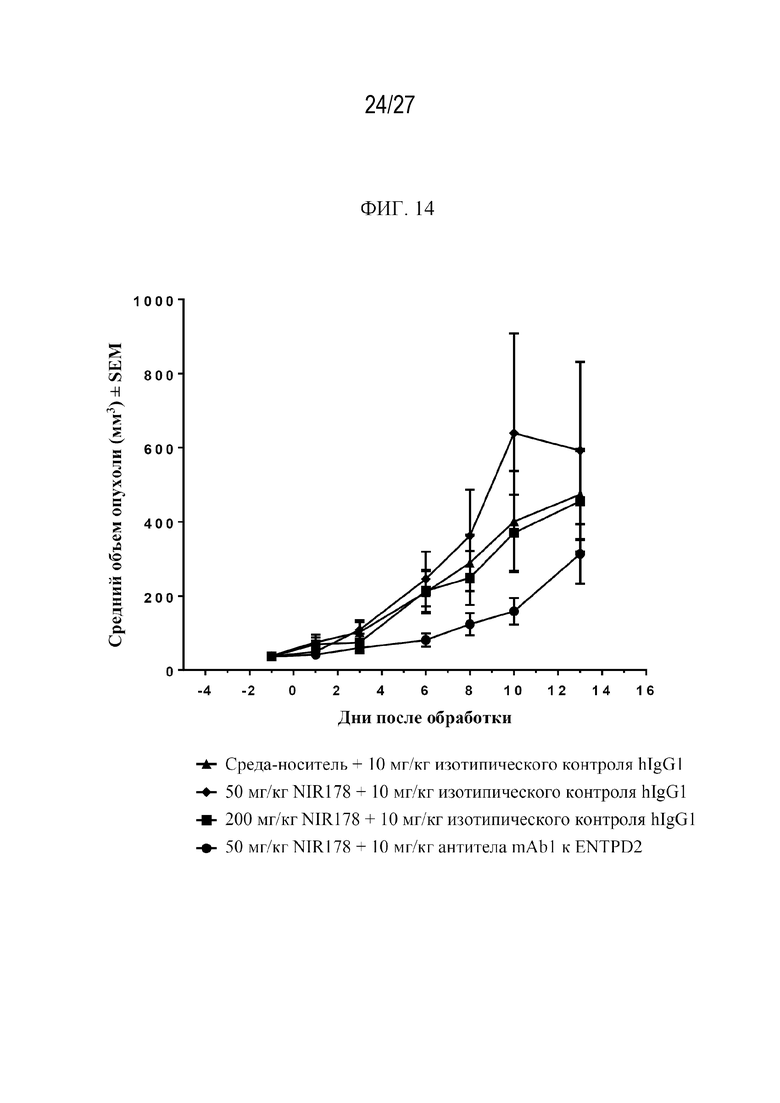
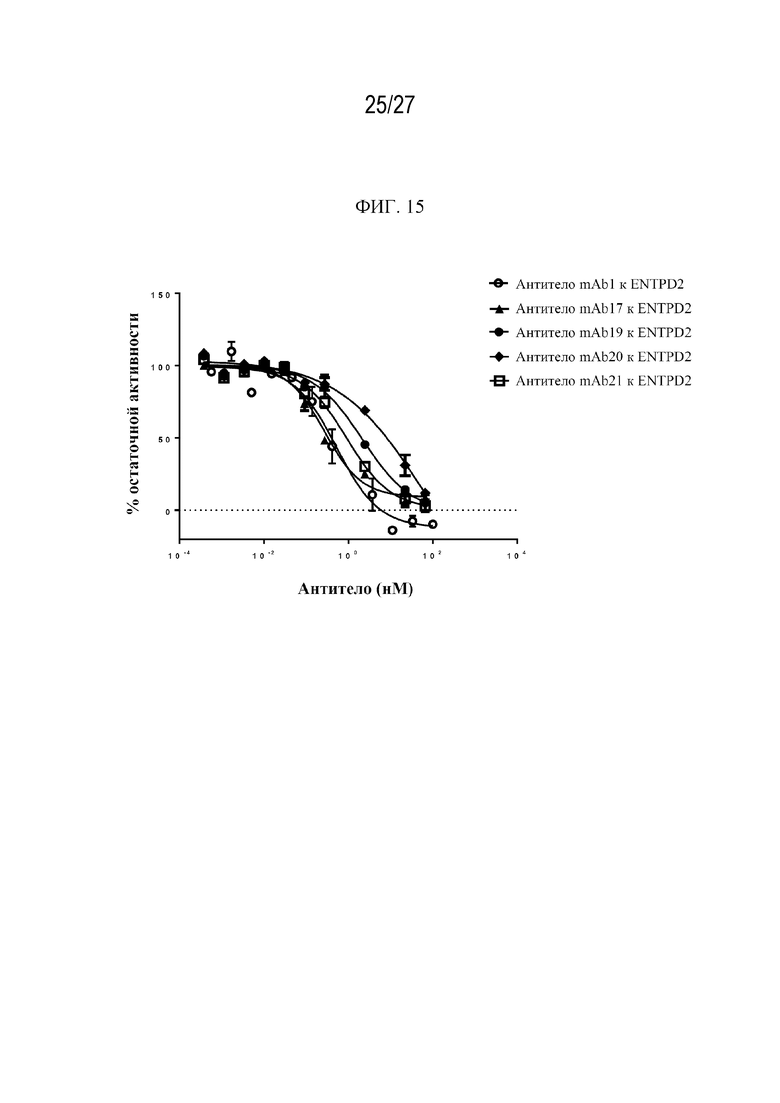
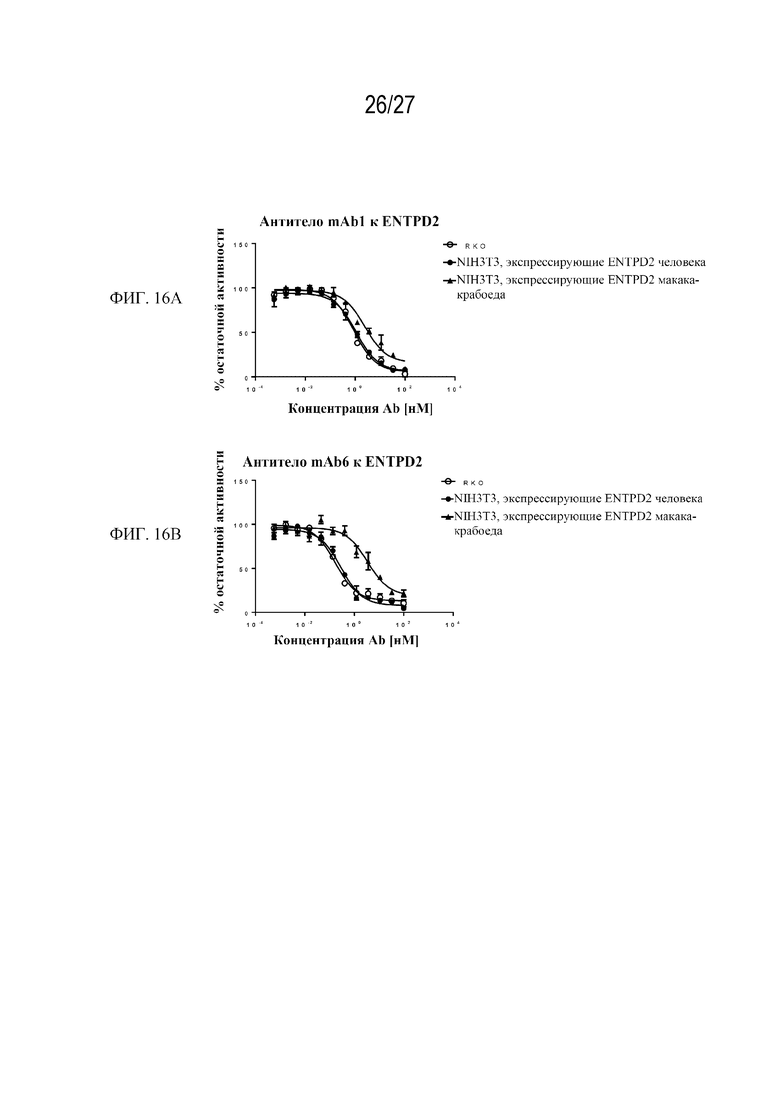
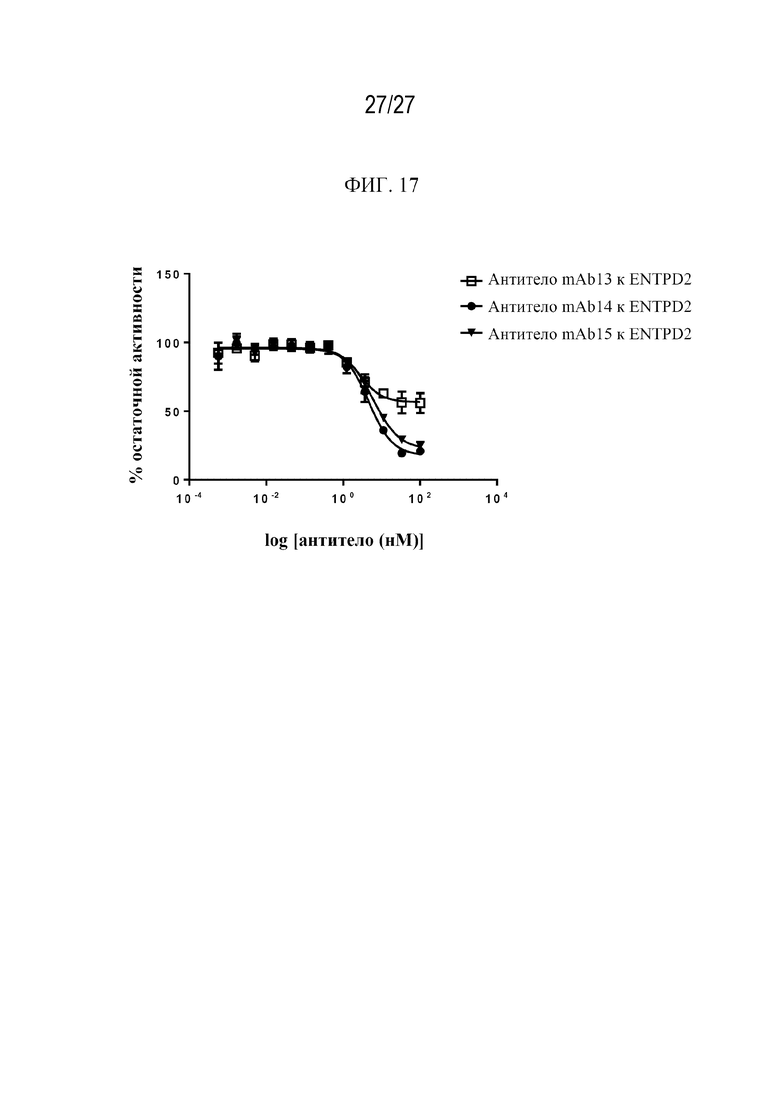
Изобретение относится к биотехнологии. Предложены антитело или его антигенсвязывающий фрагмент, которые специфично связываются с белком эктонуклеозидтрифосфатдифосфогидролазой 2 (ENTPD2) человека. Также предложены нуклеиновая кислота, кодирующая указанное антитело или его антигенсвязывающий фрагмент, вектор экспрессии, содержащий указанную нуклеиновую кислоту, клетка, содержащая нуклеиновую кислоту или вектор экспрессии. Также предложена фармацевтическая композиция для лечения рака, характеризующегося сверхэкспрессией ENTPD2, содержащая антитело или его антигенсвязывающий фрагмент, нуклеиновую кислоту, вектор или клетку. Также предложены способ лечения рака, характеризующегося сверхэкспрессией ENTPD2, у субъекта и способ стимуляции иммунного ответа у субъекта, предусматривающие введение субъекту указанных антитела или антигенсвязывающего фрагмента, нуклеиновой кислоты, вектора, клетки или фармацевтической композиции. Изобретение может быть использовано в терапии рака, характеризующегося сверхэкспрессией ENTPD2. 12 н. и 27 з.п. ф-лы, 17 ил., 30 табл., 14 пр.
1. Антитело или его антигенсвязывающий фрагмент, которые специфично связываются с белком эктонуклеозидтрифосфатдифосфогидролазой 2 (ENTPD2) человека, где антитело или его антигенсвязывающий фрагмент содержат область 1, определяющую комплементарность, тяжелой цепи (HCDR1), область 2, определяющую комплементарность, тяжелой цепи (HCDR2), область 3, определяющую комплементарность, тяжелой цепи (HCDR3), область 1, определяющую комплементарность, легкой цепи (LCDR1), область 2, определяющую комплементарность, легкой цепи (LCDR2) и область 3, определяющую комплементарность, легкой цепи (LCDR3), где антитело или его антигенсвязывающий фрагмент выбраны из любого из следующих:
1) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 1,
последовательность HCDR2, содержащую SEQ ID NO: 2,
последовательность HCDR3, содержащую SEQ ID NO: 3,
последовательность LCDR1, содержащую SEQ ID NO: 14,
последовательность LCDR2, содержащую SEQ ID NO: 15, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
2) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 4,
последовательность HCDR2, содержащую SEQ ID NO: 5,
последовательность HCDR3, содержащую SEQ ID NO: 3,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 19;
3) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 7,
последовательность HCDR2, содержащую SEQ ID NO: 8,
последовательность HCDR3, содержащую SEQ ID NO: 9,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
4) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 38,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 50,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
5) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 41,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 53,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
6) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 44,
последовательность HCDR3, содержащую SEQ ID NO: 45,
последовательность LCDR1, содержащую SEQ ID NO: 56,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
7) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 38,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 61,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
8) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 41,
последовательность HCDR3, содержащую SEQ ID NO: 39,
последовательность LCDR1, содержащую SEQ ID NO: 62,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
9) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 44,
последовательность HCDR3, содержащую SEQ ID NO: 45,
последовательность LCDR1, содержащую SEQ ID NO: 63,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
10) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 38,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 50,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
11) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 41,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 53,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
12) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 44,
последовательность HCDR3, содержащую SEQ ID NO: 69,
последовательность LCDR1, содержащую SEQ ID NO: 56,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
13) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 82,
последовательность HCDR2, содержащую SEQ ID NO: 83,
последовательность HCDR3, содержащую SEQ ID NO: 84,
последовательность LCDR1, содержащую SEQ ID NO: 95,
последовательность LCDR2, содержащую SEQ ID NO: 96, и
последовательность LCDR3, содержащую SEQ ID NO: 97;
14) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 85,
последовательность HCDR2, содержащую SEQ ID NO: 86,
последовательность HCDR3, содержащую SEQ ID NO: 84,
последовательность LCDR1, содержащую SEQ ID NO: 98,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 100;
15) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 88,
последовательность HCDR2, содержащую SEQ ID NO: 89,
последовательность HCDR3, содержащую SEQ ID NO: 90,
последовательность LCDR1, содержащую SEQ ID NO: 101,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 97;
16) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 106,
последовательность HCDR2, содержащую SEQ ID NO: 107,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 119,
последовательность LCDR2, содержащую SEQ ID NO: 120, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
17) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 109,
последовательность HCDR2, содержащую SEQ ID NO: 110,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 122,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 123;
18) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 112,
последовательность HCDR2, содержащую SEQ ID NO: 113,
последовательность HCDR3, содержащую SEQ ID NO: 114,
последовательность LCDR1, содержащую SEQ ID NO: 124,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
19) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 106,
последовательность HCDR2, содержащую SEQ ID NO: 129,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 119,
последовательность LCDR2, содержащую SEQ ID NO: 120, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
20) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 109,
последовательность HCDR2, содержащую SEQ ID NO: 130,
последовательность HCDR3, содержащую SEQ ID NO: 108,
последовательность LCDR1, содержащую SEQ ID NO: 122,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 123;
21) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 112,
последовательность HCDR2, содержащую SEQ ID NO: 131,
последовательность HCDR3, содержащую SEQ ID NO: 114,
последовательность LCDR1, содержащую SEQ ID NO: 124,
последовательность LCDR2, содержащую SEQ ID NO: 99, и
последовательность LCDR3, содержащую SEQ ID NO: 121;
22) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 136,
последовательность HCDR2, содержащую SEQ ID NO: 137,
последовательность HCDR3, содержащую SEQ ID NO: 138,
последовательность LCDR1, содержащую SEQ ID NO: 149,
последовательность LCDR2, содержащую SEQ ID NO: 150, и
последовательность LCDR3, содержащую SEQ ID NO: 151;
23) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 139,
последовательность HCDR2, содержащую SEQ ID NO: 140,
последовательность HCDR3, содержащую SEQ ID NO: 138,
последовательность LCDR1, содержащую SEQ ID NO: 152,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 154;
24) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 142,
последовательность HCDR2, содержащую SEQ ID NO: 143,
последовательность HCDR3, содержащую SEQ ID NO: 144,
последовательность LCDR1, содержащую SEQ ID NO: 155,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 151;
25) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 160,
последовательность HCDR2, содержащую SEQ ID NO: 161,
последовательность HCDR3, содержащую SEQ ID NO: 162,
последовательность LCDR1, содержащую SEQ ID NO: 173,
последовательность LCDR2, содержащую SEQ ID NO: 150, и
последовательность LCDR3, содержащую SEQ ID NO: 174;
26) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 163,
последовательность HCDR2, содержащую SEQ ID NO: 164,
последовательность HCDR3, содержащую SEQ ID NO: 162,
последовательность LCDR1, содержащую SEQ ID NO: 175,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 176;
27) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 166,
последовательность HCDR2, содержащую SEQ ID NO: 167,
последовательность HCDR3, содержащую SEQ ID NO: 168,
последовательность LCDR1, содержащую SEQ ID NO: 177,
последовательность LCDR2, содержащую SEQ ID NO: 153, и
последовательность LCDR3, содержащую SEQ ID NO: 174;
28) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 220,
последовательность HCDR3, содержащую SEQ ID NO: 221,
последовательность LCDR1, содержащую SEQ ID NO: 61,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
29) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 222,
последовательность HCDR3, содержащую SEQ ID NO: 221,
последовательность LCDR1, содержащую SEQ ID NO: 62,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
30) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 223,
последовательность HCDR3, содержащую SEQ ID NO: 224,
последовательность LCDR1, содержащую SEQ ID NO: 63,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
31) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 37,
последовательность HCDR2, содержащую SEQ ID NO: 220,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 61,
последовательность LCDR2, содержащую SEQ ID NO: 51, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
32) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 40,
последовательность HCDR2, содержащую SEQ ID NO: 222,
последовательность HCDR3, содержащую SEQ ID NO: 68,
последовательность LCDR1, содержащую SEQ ID NO: 62,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 55;
33) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 43,
последовательность HCDR2, содержащую SEQ ID NO: 223,
последовательность HCDR3, содержащую SEQ ID NO: 69,
последовательность LCDR1, содержащую SEQ ID NO: 63,
последовательность LCDR2, содержащую SEQ ID NO: 54, и
последовательность LCDR3, содержащую SEQ ID NO: 52;
34) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 1,
последовательность HCDR2, содержащую SEQ ID NO: 245,
последовательность HCDR3, содержащую SEQ ID NO: 246,
последовательность LCDR1, содержащую SEQ ID NO: 254,
последовательность LCDR2, содержащую SEQ ID NO: 15, и
последовательность LCDR3, содержащую SEQ ID NO: 255;
35) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 4,
последовательность HCDR2, содержащую SEQ ID NO: 247,
последовательность HCDR3, содержащую SEQ ID NO: 246,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 256;
36) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 7,
последовательность HCDR2, содержащую SEQ ID NO: 248,
последовательность HCDR3, содержащую SEQ ID NO: 249,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 255;
37) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 1,
последовательность HCDR2, содержащую SEQ ID NO: 261,
последовательность HCDR3, содержащую SEQ ID NO: 262,
последовательность LCDR1, содержащую SEQ ID NO: 254,
последовательность LCDR2, содержащую SEQ ID NO: 15, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
38) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 4,
последовательность HCDR2, содержащую SEQ ID NO: 247,
последовательность HCDR3, содержащую SEQ ID NO: 262,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 19;
39) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 7,
последовательность HCDR2, содержащую SEQ ID NO: 248,
последовательность HCDR3, содержащую SEQ ID NO: 263,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
40) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 272,
последовательность HCDR2, содержащую SEQ ID NO: 273,
последовательность HCDR3, содержащую SEQ ID NO: 274,
последовательность LCDR1, содержащую SEQ ID NO: 254,
последовательность LCDR2, содержащую SEQ ID NO: 285, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
41) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 275,
последовательность HCDR2, содержащую SEQ ID NO: 276,
последовательность HCDR3, содержащую SEQ ID NO: 274,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 286, и
последовательность LCDR3, содержащую SEQ ID NO: 19;
42) антитела или его антигенсвязывающего фрагмента, содержащих:
последовательность HCDR1, содержащую SEQ ID NO: 278,
последовательность HCDR2, содержащую SEQ ID NO: 279,
последовательность HCDR3, содержащую SEQ ID NO: 280,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 286, и
последовательность LCDR3, содержащую SEQ ID NO: 16.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, где антитело или его антигенсвязывающий фрагмент выбраны из любого из следующих:
1) антитела или его антигенсвязывающего фрагмента, содержащих вариабельную область тяжелой цепи (VH), содержащую SEQ ID NO: 10 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и вариабельную область легкой цепи (VL), содержащую SEQ ID NO: 21 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
2) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 25 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 29 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
3) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 33 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 29 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
4) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 46 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 57 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
5) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 46 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 64 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
6) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 70 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 74 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
7) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 25 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 78 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
8) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 91 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 102 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
9) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 115 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 125 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
10) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 132 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 125 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
11) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 145 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 156 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
12) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 169 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 178 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
13) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 225 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 229 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
14) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 233 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 237 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
15) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 241 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 229 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
16) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 250 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 257 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
17) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 264 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 268 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей; или
18) антитела или его антигенсвязывающего фрагмента, содержащих VH, содержащую SEQ ID NO: 281 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и VL, содержащую SEQ ID NO: 287 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей.
3. Антитело или его антигенсвязывающий фрагмент по п. 1 или 2, где антитело или его антигенсвязывающий фрагмент выбраны из любого из следующих:
1) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 12 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 23 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
2) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 27 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 31 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
3) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 35 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 31 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
4) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 48 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 59 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
5) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 48 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 66 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
6) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 72 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 76 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
7) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 27 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 80 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
8) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 93 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 104 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
9) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 117 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 127 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
10) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 134 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 127 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
11) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 147 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 158 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
12) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 171 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 180 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
13) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 227 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 231 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
14) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 235 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 239 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
15) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 243 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 231 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
16) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 252 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 259 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей;
17) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 266 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 270 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей; или
18) антитела, содержащего тяжелую цепь, содержащую SEQ ID NO: 283 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей, и легкую цепь, содержащую SEQ ID NO: 289 или последовательность, на по меньшей мере приблизительно 95% или больше идентичную ей.
4. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент включают:
1) антитело или его антигенсвязывающий фрагмент, содержащие:
последовательность HCDR1, содержащую SEQ ID NO: 1,
последовательность HCDR2, содержащую SEQ ID NO: 2,
последовательность HCDR3, содержащую SEQ ID NO: 3,
последовательность LCDR1, содержащую SEQ ID NO: 14,
последовательность LCDR2, содержащую SEQ ID NO: 15, и
последовательность LCDR3, содержащую SEQ ID NO: 16;
2) антитело или его антигенсвязывающий фрагмент, содержащие:
последовательность HCDR1, содержащую SEQ ID NO: 4,
последовательность HCDR2, содержащую SEQ ID NO: 5,
последовательность HCDR3, содержащую SEQ ID NO: 3,
последовательность LCDR1, содержащую SEQ ID NO: 17,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 19; или
3) антитело или его антигенсвязывающий фрагмент, содержащие:
последовательность HCDR1, содержащую SEQ ID NO: 7,
последовательность HCDR2, содержащую SEQ ID NO: 8,
последовательность HCDR3, содержащую SEQ ID NO: 9,
последовательность LCDR1, содержащую SEQ ID NO: 20,
последовательность LCDR2, содержащую SEQ ID NO: 18, и
последовательность LCDR3, содержащую SEQ ID NO: 16.
5. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4, где антитело или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи (VH), содержащую SEQ ID NO: 10 или последовательность, по меньшей мере приблизительно на 95% или более идентичную ей, и вариабельную область легкой цепи (VL), содержащую SEQ ID NO: 21 или последовательность, по меньшей мере приблизительно на 95% или более идентичную ей.
6. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-5, где антитело или его антигенсвязывающий фрагмент содержат SEQ ID NO: 12 или последовательность, по меньшей мере приблизительно на 95% или более идентичную ей, и легкую цепь, содержащую SEQ ID NO: 23 или последовательность, по меньшей мере приблизительно на 95% или более идентичную ей.
7. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-6, где антитело или его антигенсвязывающий фрагмент связываются с белком ENTPD2 человека с константой диссоциации (KD), составляющей менее 10 нМ или менее 3 нМ согласно измерению с помощью Biacore.
8. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-7, где антитело или его антигенсвязывающий фрагмент ингибируют ферментативную активность ENTPD2 человека на по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90%.
9. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-8, где антитело или его антигенсвязывающий фрагмент ингибируют способность ENTPD2 к гидролизу аденозинтрифосфата (ATP).
10. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-9, где антитело или его антигенсвязывающий фрагмент препятствуют связыванию ATP с ENTPD2 или удерживают ATP в каталитическом домене ENTPD2.
11. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-10, где антитело или его антигенсвязывающий фрагмент представляют собой человеческое или гуманизированное антитело или его фрагмент.
12. Нуклеиновая кислота, кодирующая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-11.
13. Вектор экспрессии, содержащий нуклеиновую кислоту по п. 12.
14. Вектор экспрессии по п. 13, где вектор выбран из ДНК-вектора, РНК-вектора, плазмиды, космиды или вирусного вектора.
15. Вектор экспрессии по п. 14, где вектор представляет собой вирусный вектор на основе любого из следующих вирусов: лентивируса, аденовируса, аденоассоциированного вируса (AAV), вируса простого герпеса (HSV), парвовируса, ретровируса, вируса осповакцины, вируса Синдбис, вируса гриппа, реовируса, вируса ньюкаслской болезни (NDV), вируса кори, вируса везикулярного стоматита (VSV), полиовируса, поксвируса, вируса Сенека-Валли, вируса Коксаки, энтеровируса, вируса миксомы или вируса Мараба.
16. Вектор экспрессии по любому из пп. 13-15, дополнительно содержащий промотор или выявляемый маркер.
17. Клетка для получения антитела или его антигенсвязывающего фрагмента по любому из пп. 1-11, содержащая нуклеиновую кислоту по п. 12 или вектор экспрессии по любому из пп. 13-16.
18. Способ получения антитела или его антигенсвязывающего фрагмента, при этом способ включает культивирование клетки по п. 17 и сбор антитела или его антигенсвязывающего фрагмента из культуральной среды.
19. Фармацевтическая композиция для лечения рака, характеризующегося сверхэкспрессией ENTPD2, содержащая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-11, нуклеиновую кислоту по п. 12, вектор по любому из пп. 13-16 или клетку по п. 17 и фармацевтически приемлемый носитель.
20. Применение антитела или его антигенсвязывающего фрагмента по любому из пп. 1-11, нуклеиновой кислоты по п. 12, вектора по любому из пп. 13-16, клетки по п. 17 или фармацевтической композиции по п. 18 в изготовлении лекарственного препарата для лечения рака, характеризующегося сверхэкспрессией ENTPD2.
21. Применение по п.20, где рак представляет собой рак ободочной и прямой кишки (CRC), рак желудка (необязательно, аденокарциному желудка, карциному желудка), рак пищевода (необязательно, плоскоклеточную карциному пищевода (ESCC)), рак легкого (необязательно, мелкоклеточный рак легкого), рак молочной железы (необязательно, аденокарциному молочной железы) или рак яичника.
22. Способ лечения рака, характеризующегося сверхэкспрессией ENTPD2, у субъекта, нуждающегося в этом, при этом способ включает введение субъекту терапевтически эффективного количества антитела или антигенсвязывающего фрагмента по любому из пп. 1-11, нуклеиновой кислоты по п. 12, вектора по любому из пп. 13-16, клетки по п. 17 или фармацевтической композиции по п. 18.
23. Способ по п. 22, где рак представляет собой рак ободочной и прямой кишки (CRC), рак желудка (необязательно, аденокарциному желудка, карциному желудка), рак пищевода (необязательно, плоскоклеточную карциному пищевода (ESCC)), рак легкого (необязательно, мелкоклеточный рак легкого), рак молочной железы (необязательно, аденокарциному молочной железы) или рак яичника.
24. Способ по любому из пп. 22, 23, где антитело или его антигенсвязывающий фрагмент, нуклеиновую кислоту, вектор экспрессии, клетку или фармацевтическую композицию вводят субъекту посредством внутривенного, внутриопухолевого или подкожного путей.
25. Способ стимуляции иммунного ответа у субъекта, при этом способ включает введение субъекту антитела или антигенсвязывающего фрагмента по любому из пп. 1-11, нуклеиновой кислоты по п. 12, вектора по любому из пп. 13-16, клетки по п. 17 или фармацевтической композиции по п. 18 в количестве, эффективном для стимуляции иммунного ответа.
26. Способ по любому из пп. 22-25, дополнительно включающий применение в отношении субъекта по меньшей мере одного дополнительного терапевтического средства или процедуры.
27. Способ по п. 26, где по меньшей мере одно дополнительное терапевтическое средство или процедура выбраны из одного или нескольких из химиотерапии, таргетной противораковой терапии, онколитического лекарственного средства, цитотоксического средства, иммунотерапии, цитокина, хирургической процедуры, процедуры облучения, активатора костимулирующей молекулы, ингибитора ингибирующей молекулы, вакцины или клеточной терапии.
28. Способ по п. 27, где по меньшей мере одно дополнительное терапевтическое средство является ингибитором PD-1, необязательно, где ингибитор PD-1 выбран из PDR001, ниволумаба, пембролизумаба, пидилизумаба, MEDI0680, REGN2810, TSR-042, PF-06801591 или AMP-224.
29. Способ по п. 27, где по меньшей мере одно дополнительное терапевтическое средство является ингибитором PD-L1, необязательно, где ингибитор PD-L1 выбран из FAZ053, атезолизумаба, авелумаба, дурвалумаба или BMS-936559.
30. Способ по п. 27, где по меньшей мере одно дополнительное терапевтическое средство является антагонистом A2AR, где антагонист A2AR выбран из:
(i) молекулы антитела к CD73 или ее антигенсвязывающего фрагмента, где антитело к CD73 необязательно выбрано из:
a) молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 295, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 296, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 295 или 296;
b) молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 299, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 300, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 299 или 300;
c) молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 302, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 303, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 302 или 303;
d) молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 304, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 305, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 304 или 305;
e) молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 306, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 307, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 306 или 307; или
f) молекулы антитела к CD73, содержащей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 308, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 309, или аминокислотную последовательность, на по меньшей мере 85%, 90%, 95% или больше идентичную по отношению к SEQ ID NO: 308 или 309; или
(ii) PBF509/NIR178, CPI444/V81444, AZD4635/HTL-1071, випаденанта, GBV-2034, AB928, теофиллина, истрадефиллина, тозаденанта/SYN-115, KW-6356, ST-4206 и преладенанта/SCH-420814; или
(iii) 5-бром-2,6-ди-(1H-пиразол-1-ил)пиримидин-4-амина или его фармацевтически приемлемой соли; (S)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амина или его фармацевтически приемлемой соли; (R)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амина, или его рацемата, или его фармацевтически приемлемой соли; 7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-5-амина или его фармацевтически приемлемой соли и 6-(2-хлор-6-метилпиридин-4-ил)-5-(4-фторфенил)-1,2,4-триазин-3-амина или его фармацевтически приемлемой соли.
31. Способ по п. 27, где по меньшей мере одно дополнительное терапевтическое средство выбрано из:
i) ингибитора CTLA-4, где ингибитор CTLA-4 необязательно выбран из ипилимумаба или тремелимумаба;
ii) ингибитора TIM-3, где ингибитор TIM-3 необязательно выбран из MBG453, TSR-022 или LY3321367;
iii) ингибитора LAG-3, где ингибитор LAG-3 необязательно выбран из LAG525, BMS-986016, TSR-033, MK-4280 или REGN3767;
iv) агониста GITR, где агонист GITR необязательно выбран из GWN323, BMS-986156, MK-4166, MK-1248, TRX518, INCAGN1876, AMG 228 или INBRX-110;
v) молекулы полиспецифического антитела к CD3, где молекула полиспецифического антитела к CD3 необязательно представляет собой молекулу биспецифического антитела к CD3 и CD123 (необязательно, XENP14045) или молекулу биспецифического антитела к CD3 и CD20 (необязательно, XENP13676);
vi) молекулы цитокина, где молекула цитокина необязательно представляет собой IL-15 в комплексе с растворимой формой альфа-субъединицы рецептора IL-15 (IL-15Ra);
vii) ингибитора макрофагального колониестимулирующего фактора (M-CSF), где ингибитор M-CSF необязательно представляет собой MCS110;
viii) ингибитора CSF-1R, где ингибитор CSF-1R необязательно представляет собой BLZ945;
ix) ингибитора индоламин-2,3-диоксигеназы (IDO) и/или триптофан-2,3-диоксигеназы (TDO);
x) ингибитора TGF-β;
xi) онколитического вируса;
xii) средства терапии на основе T-клеток с химерным антигенным рецептором (CAR).
32. Способ по п. 27, где по меньшей мере одно дополнительное терапевтическое средство выбрано из: 1) ингибитора протеинкиназы C (PKC); 2) ингибитора белка теплового шока 90 (HSP90); 3) ингибитора фосфоинозитид-3-киназы (PI3K) и/или мишени рапамицина (mTOR); 4) ингибитора цитохрома P450 (например, ингибитора CYP17 или ингибитора 17-альфа-гидроксилазы/C17-20-лиазы); 5) железохелатирующего средства; 6) ингибитора ароматазы; 7) ингибитора р53, необязательно, ингибитора взаимодействия р53/Mdm2; 8) индуктора апоптоза; 9) ингибитора ангиогенеза; 10) ингибитора альдостеронсинтазы; 11) ингибитора рецептора Smoothened (SMO); 12) ингибитора рецептора пролактина (PRLR); 13) ингибитора сигнального пути Wnt; 14) ингибитора CDK4/6; 15) ингибитора рецептора 2 фактора роста фибробластов (FGFR2)/рецептора 4 фактора роста фибробластов (FGFR4); 16) ингибитора макрофагального колониестимулирующего фактора (M-CSF); 17) ингибитора одного или нескольких из c-KIT, высвобождения гистамина, Flt3 (необязательно, FLK2/STK1) или PKC; 18) ингибитора одного или нескольких из VEGFR-2 (необязательно, FLK-1/KDR), PDGFR-бета, c-KIT или Raf-киназы C; 19) агониста соматостатина и/или ингибитора высвобождения гормона роста; 20) ингибитора киназы анапластической лимфомы (ALK); 21) ингибитора рецептора инсулиноподобного фактора роста 1 (IGF-1R); 22) ингибитора P-гликопротеина 1; 23) ингибитора рецептора фактора роста эндотелия сосудов (VEGFR); 24) ингибитора киназы BCR-ABL; 25) ингибитора FGFR; 26) ингибитора CYP11B2; 27) ингибитора HDM2, например, ингибитора взаимодействия HDM2-p53; 28) ингибитора тирозинкиназы; 29) ингибитора c-MET; 30) ингибитора JAK; 31) ингибитора DAC; 32) ингибитора 11β-гидроксилазы; 33) ингибитора IAP; 34) ингибитора PIM-киназы; 35) ингибитора поркупина; 36) ингибитора BRAF, необязательно, BRAF V600E или BRAF дикого типа; 37) ингибитора HER3; 38) ингибитора MEK; 39) ингибитора липидкиназы или 40) одного или нескольких соединений, обозначенных А1-А6.
33. Способ по п. 27, где антитело или антигенсвязывающий фрагмент по любому из пп. 1-11, нуклеиновую кислоту по п. 12, вектор экспрессии по любому из пп. 13-16, клетку по п. 17 или фармацевтическую композицию по п. 18 вводят параллельно с по меньшей мере одним дополнительным терапевтическим средством, до него или после него.
34. Способ лечения рака, характеризующегося сверхэкспрессией ENTPD2, у субъекта, нуждающегося в этом, при этом способ включает введение субъекту терапевтически эффективного количества антитела или антигенсвязывающего фрагмента по любому из пп. 1-11 в комбинации со вторым терапевтическим средством, выбранным из ингибитора PD-1 или ингибитора PD-L1.
35. Способ стимуляции иммунного ответа у субъекта, при этом способ включает введение субъекту антитела или антигенсвязывающего фрагмента по любому из пп. 1-11 в комбинации со вторым терапевтическим средством, выбранным из ингибитора PD-1 или ингибитора PD-L1.
36. Применение композиции, содержащей антитело или антигенсвязывающий фрагмент по любому из пп. 1-11, в комбинации со вторым терапевтическим средством, выбранным из ингибитора PD-1 или ингибитора PD-L1, в лечении рака, характеризующегося сверхэкспрессией ENTPD2, у субъекта.
37. Способ по п. 34 или 35 или применение по п. 36, где ингибитор PD-1 выбран из PDR001, ниволумаба, пембролизумаба, пидилизумаба, MEDI0680, REGN2810, TSR-042, PF-06801591 или AMP-224.
38. Способ по п. 34 или 35 или применение по п. 36, где ингибитор PD-L1 выбран из FAZ053, атезолизумаба, авелумаба, дурвалумаба или BMS-936559.
39. Способ по п. 34 или применение по п. 36, где рак представляет собой рак ободочной и прямой кишки (CRC), рак желудка (необязательно, аденокарциному желудка, карциному желудка), рак пищевода (необязательно, плоскоклеточную карциному пищевода (ESCC)), рак легкого (необязательно, мелкоклеточный рак легкого), рак молочной железы (необязательно, аденокарциному молочной железы) или рак яичника.
| CHIU D.K.C | |||
| ET AL | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| BRAGANHOL E | |||
| ET AL | |||
| Selective | |||
Авторы
Даты
2023-03-01—Публикация
2019-05-29—Подача