ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящая заявка относится к соединению, которое ингибирует некроз клеток и/или рецептор-взаимодействующую протеинкиназу 1 (RIP1), а также к способу его получения и применения. Соединение согласно настоящей заявке и включающая его композиция могут применяться в способах предупреждения и/или лечения заболеваний, включающих некроз клеток и/или воспаление.
УРОВЕНЬ ТЕХНИКИ
[0002] Программируемая некротическая гибель клеток, также известная как программируемый некроз, является новым путем гибели клеток, открытым в последние годы. Программируемый некроз представляет собой характеризующуюся сильным воспалением форму гибели клеток и рассматривается как важный патологический фактор при многих дегенеративных и воспалительных заболеваниях, которые включают нейродегенеративные заболевания, инсульт, ишемическую болезнь сердца, инфаркт миокарда, дегенеративные заболевания сетчатки, воспалительное заболевание кишечника, заболевание почек, заболевание печени и многие другие связанные заболевания.
[0003] Активация ядерного фактора каппа В (NF-kB), индуцируемая фактором некроза опухоли альфа (ФНО-α), играет важную роль в иммунной системе и воспалительной реакции. RIP1 является многофункциональным переносчиком сигнала, участвующим в опосредовании активации NF-kB, апоптоза и некроза клеток, и является переходной точкой, которая определяет гибель клетки, тем самым, играя важную роль в таких процессах, как выживание и апоптоз клеток или программируемый некроз и т.п. Участие активности киназы RIP1 крайне важно при опосредовании программируемого некроза клеток - пути некротической гибели клеток, независимого от каспазы.
[0004] Исследования показывают, что Некростатин-1 (Nec-1), ингибитор киназы RIP1, известный в уровне техники, демонстрирует эффективные терапевтические эффекты при различных воспалительных заболеваниях. Позднее в данной области были открыты некоторые ингибиторы киназы RIP1 с различными структурами. Однако существующие ингибиторы киназы RIP1 имеют недостатки в различных аспектах, такие как неудовлетворительную активность, плохие фармакокинетические свойства или низкую биодоступность при приеме внутрь и т.д., причем некоторые из них не могут проходить через гематоэнцефалический барьер, чтобы проникнуть в центральную нервную систему. Все эти недостатки препятствуют их дальнейшему исследованию и клиническому применению.
[0005] Таким образом, в уровне техники сохраняется потребность в предоставлении обладающих клиническим значением высокоэффективных и селективных низкомолекулярных ингибиторов киназы RIP1, блокирующих RIPl-зависимый программируемый некроз клеток, а также в предупреждении и лечении заболеваний или нарушений, опосредованных киназой RIP1, или заболеваний или нарушений, вызванных программируемым некрозом клетки.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0006] В настоящей заявке предложен новый ингибитор киназы RIP1, который может применяться для предупреждения и лечения заболеваний или нарушений, опосредованных киназой RIP1, или заболеваний или нарушений, вызванных программируемым некрозом клеток.
[0007] В одном аспекте настоящей заявки предложено соединение Формулы (I):
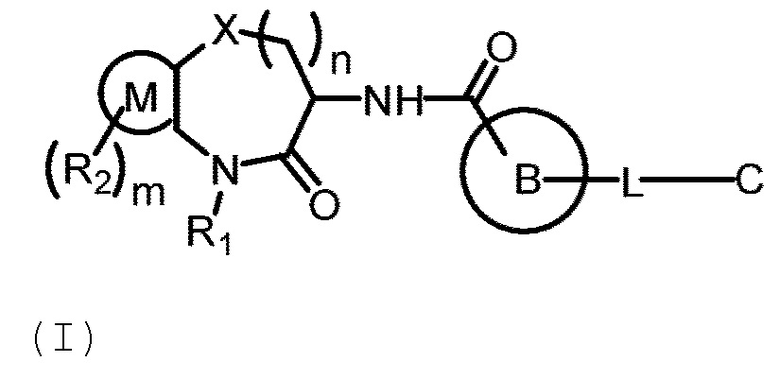
или его фармацевтически приемлемая соль, где: X представляет собой О, S или СН2;
кольцо М имеет структуру 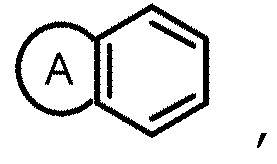 где кольцо А выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила;
где кольцо А выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила;
кольцо В выбрано из группы, состоящей из замещенного или незамещенного 5-12-членного арила, замещенного или незамещенного 5-12-членного гетероарила и замещенного или незамещенного 5-12-членного гетероциклила;
С выбрано из группы, состоящей из замещенного или незамещенного (C3-C12) циклоалкила, замещенного или незамещенного 5-12-членного арила, замещенного или незамещенного 5-12-членного гетероарила и замещенного или незамещенного 5-12-членного гетероциклила;
L выбрано из группы, состоящей из О, S, NH, N(CH3), замещенного или незамещенного C1-C6 алкилен-О-, замещенного или незамещенного C1-C6 алкилен-NH-, (замещенного или незамещенного C1-C6 алкилен)2-N-, замещенного или незамещенного C1-C6 алкилена, замещенного или незамещенного С3-С6 алкенилена, замещенного или незамещенного или С3-С6 алкенилен-О-;
R1 выбран из группы, состоящей из Н и замещенного или незамещенного C1-C6 алкила;
R2 выбран из группы, состоящей из Н, галогена, гидроксила, екеиоксо, бензила, замещенного или незамещенного C1-C6 алкила, замещенного или незамещенного C1-C6 алкокси и C1-C6 ацила;
m равно 0, 1, 2 или 3;
n равно 1, 2 или 3;
где "замещенный" относится к замещению одного или более атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена, циано, алкила, ацила, сульфонила, гидроксила, амино, бензила, екеиоксо, (C1-C4) алкила, галоген (C1-C4) алкила, (С1-С4) алкокси, галоген (С1-С4) алкокси, нитро и (C1-C4) алкилС(О)-.
[0008] В другом аспекте настоящей заявки предложен способ получения соединения Формулы (I):
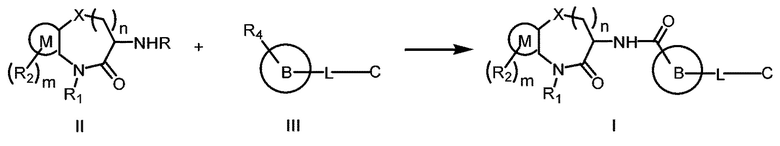
где R4 представляет собой -СООН или -COO-G+, где G+ является ионом щелочного металла;
когда R представляет собой Н, способ включает: реакцию соединения Формулы (II) с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I); и
когда R представляет собой защитную группу аминогруппы, способ включает: удаление R из соединения Формулы (II) в кислотных условиях и затем реакцию соединения Формулы (II), из которого удалено R, с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I).
[0009] В еще одном аспекте настоящей заявки предложена фармацевтическая композиция, включающая терапевтически эффективное количество соединения Формулы (I) или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
[0010] В другом аспекте настоящей заявки предложено применение соединения Формулы (I) или его фармацевтически приемлемой соли или фармацевтической композиции, включающей его, в производстве лекарственных средств для лечения или предупреждения заболеваний или нарушений, опосредованных киназой RIP1, или заболеваний или нарушений, вызванных программируемым некрозом клеток.
[0011] В другом аспекте настоящей заявки предложен способ ингибирования киназы RIP1 у субъекта, включающий введение субъекту эффективного количества соединения Формулы (I) или его фармацевтически приемлемой соли или фармацевтической композиции, включающей их.
[0012] В еще одном аспекте настоящей заявки предложена комбинация лекарственных средств, включающая: (а) соединение Формулы (I) или его фармацевтически приемлемую соль; и (b) по меньшей мере одно дополнительное действующее вещество.
[0013] В другом аспекте настоящей заявки предложено промежуточное соединение Формулы (II):
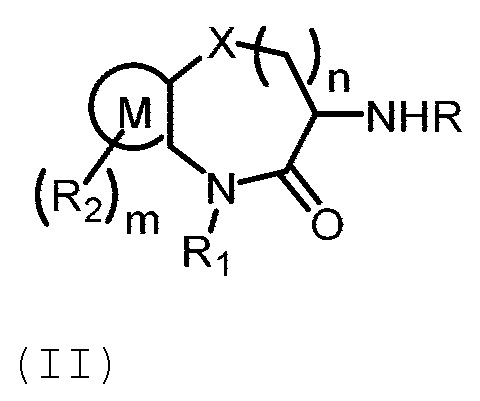
где:
R представляет собой Н или защитную группу аминогруппы; X представляет собой О, S или СН2;
R1 выбран из группы, состоящей из Н и замещенного или незамещенного C1-C6 алкила;
R2 выбран из группы, состоящей из Н, галогена, гидроксила, оксиоксо, бензила, замещенного или незамещенного C1-C6 алкила, замещенного или незамещенного C1-C6алкокси и C1-C6 ацила;
m равно 0, 1, 2 или 3; и
n равно 1, 2 или 3;
где "замещенный" относится к замещению одного или более атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена, циано, алкила, ацила, сульфонила, гидроксила, амино, бензила, оксо, (C1-C4) алкила, галоген (C1-C4) алкила, (С1-С4) алкокси, галоген (С1-С4) алкокси, нитро и (C1-C4) алкилС(О)-.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0014] На Фиг. 1 показана температура тела мышей в зависимости от времени после введения разных доз (10 мг/кг, 20 мг/кг и 30 мг/кг) RIP1-034 в модели ФНО-α-индуцированного летального шока у мышей.
[0015] На Фиг. 2 показана концентрация в плазме крови каждой мыши в зависимости от времени после однократного перорального введения (10 мг/кг) Соединения RIP1-034 согласно настоящей заявке.
[0016] На Фиг. 3 показана средняя концентрация в плазме крови мышей в зависимости от времени после однократного перорального введения (10 мг/кг) соединения RIP1-034 согласно настоящей заявке.
ПОДРОБНОЕ ОПИСАНИЕ
[0017] Далее будет приведена подробная ссылка на определенные варианты осуществления изобретения, примеры которых проиллюстрированы в сопровождающих структурах и формулах. Хотя изобретение будет описано в сочетании с пронумерованными вариантами осуществления, следует понимать, что изобретение не должно ограничиваться этими вариантами осуществления. Напротив, предполагается, что изобретение охватывает все альтернативы, модификации и эквиваленты, которые могут быть включены в объем настоящего изобретения, определяемый формулой изобретения. Специалист в данной области сумеет определить множество способов и материалов, подобных или эквивалентных описанным в настоящем документе, которые могут использоваться при практическом осуществлении настоящего изобретения. Настоящее изобретение никоим образом не ограничивается описанными способами и материалами. В случае если один или больше включенных литературных источников и подобных материалов отличаются от приведенных в данной заявке или противоречат ей, включая, без ограничения, определенные термины, использование терминов, описанные методики и т.п., настоящая заявка имеет преимущественную силу.
[0018] Следует понимать, что некоторые признаки настоящего изобретения, которые для ясности описаны в контексте отдельных вариантов осуществления, также могут быть представлены в комбинации в одном варианте осуществления. С другой стороны, различные признаки настоящего изобретения, которые для краткости описаны в контексте одного варианта осуществления, также могут быть представлены отдельно или в любой подходящей подкомбинации.
[0019] Определения
[0020] При использовании в настоящем документе, если не указано иное, используются следующие определения. В рамках данной заявки химические элементы идентифицированы в соответствии с Периодической таблицей химических элементов, версии CAS, Handbook of Chemistry and Physics, 75-е изд. Кроме того, общие принципы органической химии и определенные функциональные группы и реакционная способность описаны в публикациях "Organic Chemistry", Thomas Sorrell, University Science Books, Sausalito, 1999 и "March's Advanced Organic Chemistry", 5th Edition, Smith, M.B. and March, J., John Wiley & Sons, New York: 2 001, которые включены в настоящий документ посредством отсылки во всей своей полноте.
[0021] в настоящем документе описаны связывающие заместители. Если структура явно требует присутствия связывающей группы, переменные Маркуша, перечисленные для этой группы, считаются связывающими группами. Например, если структура требует присутствия связывающей группы, и определение группы Маркуша для этой переменной включает "алкил", то подразумевается, что "алкил" представляет собой связывающую алкиленовую группу.
[0022] При использовании в настоящем документе термин "замещенный", независимо от того, предшествует ли ему термин "необязательно", означает, что в химической группе один или более атомов водорода удалены и заменены подходящими заместителями. Если не указано иное, "необязательно замещенная" группа может иметь подходящий заместитель в каждом замещаемом положении группы, и, когда больше одного положения в любой данной структуре может быть замещено больше чем одним заместителем, выбранным из определенных групп, заместители могут быть одинаковыми или разными в каждом положении. Комбинации заместителей, предусмотренные в настоящей заявке, предпочтительно являются такими комбинациями, которые приводят к образованию стабильных или химически возможных соединений. Термин "стабильный" при использовании в настоящем документе, относится к соединению, которое остается по существу неизменным, когда оно подвергается воздействию условий, которые обеспечивают возможность его получения, обнаружения и, в некоторых вариантах осуществления, выделения и очистки, и когда оно используется для одной или больше целей, описанных в настоящем документе. Если химическая группа специально не указана как "незамещенная", следует понимать, что описанная в настоящем документе химическая группа включает заместитель. Например, при указании "арила" он включает замещенный арил и незамещенный арил.
[0023] Если показано, что связь с заместителем пересекает связь, связывающую два атома в кольце, то тогда такой заместитель может быть связан с любым атомом в кольце. При перечислении заместителя без указания атома, через который такой заместитель связан с остальной частью соединения данной формулы, такой заместитель может быть связан через любой атом в такой формуле. Комбинации заместителей и/или переменных допустимы, но только в том случае, если такие комбинации приводят к стабильным соединениям.
[0024] В случае, когда какая-либо переменная (такая как Ri) присутствует больше одного раза в любой составляющей или формуле соединения, ее определение при каждом появлении является независимым друг от друга. Таким образом, например, если показано, что группа замещена 0-2 группами Ri, то тогда группа необязательно может быть замещена не больше чем двумя группами Ri, причем каждая Ri при каждом появлении независимо выбрана из определения Ri.
[0025] Термин "Ci-j" при использовании в настоящем документе указывает диапазон чисел атомов углерода, где i и j являются целыми числами, причем j больше, чем i, и диапазон чисел атомов углерода включает граничные значения (т.е. i и j) и каждое целое число между граничными значениями. Например, C1-6 обозначает диапазон 1-6 атомов углерода, включая 1 атом углерода, 2 атома углерода, 3 атома углерода, 4 атома углерода, 5 атомов углерода и 6 атомов углерода. В некоторых вариантах осуществления термин "C1-12" обозначает от 1 до 12, в частности 1-10, в частности 1-8, в частности 1-6, в частности 1-5, в частности 1-4, в частности 1-3, или, в частности, 1-2 атома углерода.
[0026] При использовании в настоящем документе термин "углеводород" относится к группе, присоединенной через атом углерода, имеющий =O или =S заместитель, который обычно содержит по меньшей мере одну углерод-водородную связь и основной углеродный скелет и может, необязательно, содержать гетероатом (гетероатомы). Таким образом, углеводородная группа может включать, без ограничения перечисленными, алкил, алкенил, алкинил, арил, гетероарил, циклоалкил, гетероциклил и т.п.
[0027] При использовании в настоящем документе, термин "алкил", либо в качестве части другого термина, либо используемый независимо, относится к насыщенной нормальной или разветвленной углеводородной группе. Термин "Ci-j алкил" относится к алкилу, содержащему i-j атомов углерода. В некоторых вариантах осуществления алкильная группа содержит 1-12 атомов углерода. В некоторых вариантах осуществления алкильная группа содержит 1-11 атомов углерода, 1-10 атомов углерода, 1-9 атомов углерода, 1-8 атомов углерода, 1-7 атомов углерода, 1-6 атомов углерода, 1-5 атомов углерода, 1-4 атома углерода, 1-3 атома углерода или 1-2 атома углерода. Примеры алкила включают, без ограничения перечисленными, метил, этил, 1-пропил (н-пропил), 2-пропил (изопропил), 1-бутил (н-бутил), 2-метил-1-пропил (изобутил), 2-бутил (необутил), 2-метил-2-пропил (трет-бутил), 1-пентил (н-пентил), 2-пентил, 3-пентил, 2-метил-2-бутил, 3-метил-2-бутил, 3-метил-1-бутил, 2-метил-1-бутил, 1-гексил, 2-гексил, 3-гексил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 3-метил-3-пентил, 2-метил-3-пентил, 2,3-диметил-2-бутил, 3,3-диметил-2-бутил, 1-гептил, 1-октил и т.п.Примеры "C1-12 алкила" включают, без ограничения перечисленными, метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, недецил и додецил. Примеры "C1-6 алкила" включают, без ограничения перечисленными, метил, этил, н-пропил, изопропил, н-бутил, изобутил, необутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, 2-метил-2-бутил, 3-метил-2-бутил, 3-метил-1-бутил, 2-метил-1-бутил, 1-гексил, 2-гексил, 3-гексил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 3-метил-3-пентил, 2-метил-3-пентил, 2,3-диметил-2-бутил, 3,3-диметил-2-бутил и т.п.
[0028] Термин "галоген" при использовании в настоящем документе относится к F, Cl, Br или I.
[0029] Термин "циано" при использовании в настоящем документе относится к -CN.
[0030] Термин "гидроксил" при использовании в настоящем документе относится к -ОН.
[0031] Термин "амино" при использовании в настоящем документе относится к -NH2.
[0032] Термин "нитро" при использовании в настоящем документе относится к -NO2.
[0033] Термин "окси", при использовании в настоящем документе относится к атому кислорода с двойной связи с другим атомом (таким как углерод или сера). Например, если он непосредственно связан с атомом углерода, образуется карбонильная группа (С=O).
[0034] Термин "ацил" при использовании в настоящем документе относится к функциональной группе, содержащей карбонильную группу, такой как -C(=O)R', где R' представляет собой водород или углеводородную группу. В некоторых вариантах осуществления ацил является группой, представленной формулой алкилС(О)-.
[0035] Термин "сульфонил" при использовании в настоящем документе относится к группе -S(O)2-R', где R' представляет собой углеводородную группу.
[0036] Термин "галогеналкил" при использовании в настоящем документе относится к алкильной группе, которая замещена одним или более атомами галогена, где один или более атомов галогена независимо замещают один или более атомов водорода на одном или более атомах углерода алкильной группы. Например, термин "C1-6 галогеналкил" включает C1-6 алкил, содержащий 1-7, 1-6, 1-5, 1-4, 1-3 или 1-2 атома галогена, и примеры включают, без ограничения перечисленными, хлорметил, дифторметил, трихлорметил, трифторметил, 2-бромэтил, 2,2,2-трифторэтил, тетрафторэтил, пентафторэтил, 2,2-дифторпропил, 2,2,2-трифторпропил, 4,4,4-трифторбутил, 5,5,5-трифторпентил и 6,6,6-трифторгексил, и т.д.
[0037] Термин "алкенил" при использовании в настоящем документе, используемый либо в качестве части другого термина, либо используемый независимо, относится к нормальной или разветвленной углеводородной группе, содержащей по меньшей мере одну углерод-углеродную двойную связь, которая необязательно может быть независимо замещена одним или более заместителями, описанными в настоящем документе, и включает радикалы, имеющие "цис" и "транс" ориентации, или "Е" и "Z" ориентации. В некоторых вариантах осуществления алкенильная группа содержит 2-12 атомов углерода. В некоторых вариантах осуществления алкенильная группа содержит 2-11 атомов углерода. В некоторых вариантах осуществления алкенильная группа содержит 2-10 атомов углерода, 2-9 атомов углерода, 2-8 атомов углерода, 2-7 атомов углерода, 2-6 атомов углерода, 2-5 атомов углерода, 2-4 атома углерода или 2-3 атома углерода. В некоторых вариантах осуществления алкенильная группа содержит 2 атома углерода. Примеры алкенильных групп включают, без ограничения перечисленными, винил, пропенил, бутенил, пентенил, 1-метил-2-бутен-1-ил, 5-гексенил и т.п.
[0038] Термин "алкинил" при использовании в настоящем документе, используемый либо в качестве части другого термина, либо используемый независимо, относится к нормальной или разветвленной углеводородной группе, содержащей по меньшей мере одну углерод-углеродную тройную связь, которая необязательно может быть независимо замещена одним или более заместителями, описанными в настоящем документе. В некоторых вариантах осуществления алкинильная группа содержит 2-12 атомов углерода. В некоторых вариантах осуществления алкинильная группа содержит 2-11 атомов углерода. В некоторых вариантах осуществления алкинильная группа содержит 2-10 атомов углерода, 2-9 атомов углерода, 2-8 атомов углерода, 2-7 атомов углерода, 2-6 атомов углерода, 2-5 атомов углерода, 2-4 атома углерода или 2-3 атома углерода. В некоторых вариантах осуществления алкинильная группа содержит 2 атома углерода. Примеры алкинильных групп включают, без ограничения перечисленными, этинил, 1-пропинил, 2-пропинил и т.п.
[0039] Термин "алкилен" при использовании в настоящем документе относится к двухвалентной алкильной группе, термин "алкенилен" при использовании в настоящем документе относится к двухвалентной алкенильной группе, и термин "алкинилен" при использовании в настоящем документе относится к двухвалентной алкинильной группе.
[0040] При использовании в настоящем документе термин "алкокси", используемый либо в качестве части другого термина, либо используемый независимо, относится к алкильной группе, как определено выше, присоединенной к первичной молекуле через атом кислорода. Термин "Ci-j алкокси" относится к алкильной группе алкоксигруппы, содержащей i-j атомов углерода. В некоторых вариантах осуществления алкоксигруппа содержит 1-12 атомов углерода. В некоторых вариантах осуществления алкоксигруппа содержит 1-11 атомов углерода. В некоторых вариантах осуществления алкоксигруппа содержит 1-10 атомов углерода, 1-9 атомов углерода, 1-8 атомов углерода, 1-7 атомов углерода, 1-6 атомов углерода, 1-5 атомов углерода, 1-4 атома углерода, 1-3 атома углерода или 1-2 атома углерода. Примеры "С1-12 алкокси группы" включают, без ограничения перечисленными, метокси, этокси, пропокси (например, н-пропокси и изопропокси), трет-бутокси, неопентилокси и н-гексилокси, и т.п.
[0041] Термин "галогеналкокси" при использовании в настоящем документе относится к алкоксигруппе, замещенной одним или более атомами галогена, где один или более атомов галогена независимо замещают один или более атомов водорода на одном или более атомах углерода алкоксигруппы. Например, термин "C1-6 галогеналкокси" включает С1-6 алкоксигруппы, содержащие 1-7, 1-6, 1-5, 1-4, 1-3 или 1-2 атома галогена.
[0042] При использовании в настоящем документе термин "арил", используемый либо в качестве части другого термина, либо используемый независимо, относится к моноциклической или полициклической кольцевой системе, содержащей в общей сложности 5-20 членов колец, где по меньшей мере одно кольцо в кольцевой системе является ароматическим, при этом каждое кольцо в кольцевой системе содержит 3-12 членов кольца. Примеры "арила" включают, без ограничения перечисленными, фенил, бифенил, нафтил, антрацил и т.п., которые могут нести один или более заместителей. Также в рамки термина "арил", при его использовании в настоящем документе, включена группа, в которой ароматическое кольцо конденсировано с одним или более дополнительными кольцами. В случае полициклической кольцевой системы только одно из колец должно быть ароматическим (например, 2,3-дигидроиндол), хотя ароматическими могут быть все кольца (например, хинолин). Второе кольцо может быть конденсированным или содержать мостик. Примеры полициклических арильных групп включают, без ограничения перечисленными, бензофуранил, инданил, фталимидил, нафтимидил, фенантридинил, тетрагидронафтил и т.п. Арильная группа необязательно может быть замещена в одном или более положениях в кольце одним или более заместителями, описанными в настоящем документе.
[0043] Термин "бензил" при использовании в настоящем документе относится к -СН2-фенилу.
[0044] При использовании в настоящем документе термины "циклоалкил", "карбоциклил" и "карбоциклическое кольцо" являются взаимозаменяемыми и используются либо в качестве части другого термина, либо независимо, для обозначения насыщенных, частично ненасыщенных или полностью ненасыщенных (то есть ароматических) моноциклических и полициклических кольцевых систем, где все атомы колец представляют собой углерод, и которые содержат по меньшей мере 3 кольцеобразующих атома углерода. В некоторых вариантах осуществления циклоалкильная группа может содержать 3-12 кольцеобразующих атомов углерода, 3-11 кольцеобразующих атомов углерода, 3-10 кольцеобразующих атомов углерода, 3-9 кольцеобразующих атомов углерода, 3-8 атомов углерода кольца, 3-7 атомов углерода кольца, 3-6 атомов углерода кольца, 3-5 атомов углерода кольца, 4-12 атомов углерода кольца, 4-11 атомов углерода кольца, 4-10 кольцеобразующих атомов углерода, 4-9 кольцеобразующих атомов углерода, 4-8 кольцеобразующих атомов углерода, 4-7 кольцеобразующих атомов углерода, 4-6 кольцеобразующих атомов углерода или 4-5 кольцеобразующих атомов углерода. Циклоалкильная группа необязательно может быть замещена в одном или более положениях кольца одним или более заместителями, описанными в настоящем документе. Циклоалкил может быть насыщенным, частично ненасыщенным или полностью ненасыщенным. В некоторых вариантах осуществления циклоалкил может быть насыщенной циклической алкильной группой. В некоторых вариантах осуществления циклоалкил может быть ненасыщенной циклической алкильной группой, содержащей по меньшей мере одну двойную связь или тройную связь в кольцевой системе.
[0045] В некоторых вариантах осуществления циклоалкил может быть насыщенной или ненасыщенной моноциклической карбоциклической кольцевой системой, примеры которой включают, без ограничения перечисленными, циклопропил, циклобутил, циклопентил, 1 циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил, циклогексадиенил, циклогептил, циклооктил, циклононил, циклодецил, циклоундецил, циклододецил и т.п.
[0046] В некоторых вариантах осуществления циклоалкил может быть насыщенной или ненасыщенной полициклической (например, бициклической и трициклической) карбоциклической кольцевой системой, которая может быть конденсированной, спиро или мостиковой кольцевой системой. При использовании в настоящем документе термин "конденсированное кольцо" относится к кольцевой системе, в которой два кольца имеют два общих соседних атома, термин "спирокольцо" относится к кольцевой системе, в которой два кольца соединены через один общий атом, и термин "кольцо с мостиком" относится к кольцевой системе, в которой два кольца имеют три или более общих атомов. Примеры конденсированных карбоциклических групп включают, без ограничения перечисленными, нафтил, бензопиренил, антраценил, аценафтенил, флуоренил и т.п. Примеры спирокарбоциклила включают, без ограничения перечисленными, спиро[5.5]ундецил, спиро-пентадиенил, спиро[3.6] -децил и т.п. Примеры карбоциклила с мостиком включают, без ограничения перечисленными, бицикло[1,1,1]пентенил, бицикло[2,2,1]гептенил, бицикло[2.2.1]гептанил, бицикло[2.2.2]-октанил, бицикло[3.3.1]нонанил, бицикло[3.3.3]ундеканил и т.п.
[0047] Термин "гетероатом" при использовании в настоящем документе относится к азоту, кислороду, сере или фосфору и включает любую окисленную форму азота или серы и любую кватернизированную форму основного азота.
[0048] Термин "гетероарил" при использовании в настоящем документе, используемый либо в качестве части другого термина, либо используемый независимо, относится к арильной группе, содержащей один или более гетероатомов в дополнение к атомам углерода, которые необязательно могут быть независимо замещены одним или более заместителями, описанными в настоящем документе. Примеры гетероарильных групп включают, без ограничения перечисленными, тиенил, фуранил, пирролил, имидазолил, пиразолил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиазолил, изотиазолил, тиадиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, индолизинил, пуринил, нафтиридинил, бензофуранил и птеридинил, и т.д. Гетероарильная группа также включает группы, в которых гетероароматическое кольцо конденсировано с одним или более арильным, циклоалкильным или гетероциклильным кольцами. Неограничивающие примеры включают индолил, изоиндолил, бензотиенил, бензофуранил, дибензофуранил, индазолил, бензимидазолил, бензотиазолил, хинолинил, изохинолинил, циннолинил, фталазинил, хиназолинил, хиноксалинил, 4Н-хиназинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил, тетрагидрохинолинил, тетрагидроизохинолинил, пиридо[2,3-b](4Н)-1,4-оксазин-3-он. В некоторых вариантах осуществления термин "5-10-членный гетероарил" относится к 5-6-членному гетероарильному кольцу, содержащему 1-3 гетероатома, независимо выбранных из азота, кислорода, серы или фосфора, или 8-10-членной бициклической гетероарильной группе, содержащей 1-4 гетероатома, независимо выбранных из азота, кислорода, серы или фосфора.
[0049] Термин "гетероцикл" или "гетероциклил" при использовании в настоящем документе относится к насыщенной, частично ненасыщенной или полностью ненасыщенной карбоциклической группе, в которой один или более атомов кольца являются гетероатомами, независимо выбранными из азота, кислорода, серы или фосфора, а остальные атомы кольца являются углеродом, где один или более атомов кольца могут быть необязательно независимо замещены одним или более заместителями. В некоторых вариантах осуществления гетероциклил является насыщенным гетероциклилом. В некоторых вариантах осуществления гетероциклил является ненасыщенным гетероциклилом, содержащим одну или более двойных связей в кольцевой системе. В некоторых вариантах осуществления гетероциклил может включать углерод, азот, серу или фосфор в любой окисленной форме и основной азот в любой кватернизированной форме. "Гетероциклил" также включает радикалы, где гетероциклильные радикалы конденсированы с насыщенным, частично ненасыщенным или полностью ненасыщенным (т.е. ароматическим) карбоциклическим или гетероциклическим кольцом. Гетероциклил может быть присоединен через углерод или азот. В некоторых вариантах осуществления гетероциклил присоединен через углерод. В некоторых вариантах осуществления гетероциклил присоединен через азот. Например, группа, полученная из пиррола, может представлять собой пиррол-1-ил (азот-связанный) или пиррол-3-ил (углерод-связанный). Кроме того, группа, полученная из имидазола, может представлять собой имидазол-1-ил (азот-связанный) или имидазол-3-ил (углерод-связанный).
[0050] В некоторых вариантах осуществления термин "3-12-членный гетероциклил" относится к 3-12 членной насыщенной или частично ненасыщенной моноциклической или полициклической гетероциклической кольцевой системе, содержащей 1-3 гетероатома, независимо выбранных из азота, кислорода, серы или фосфора. Конденсированные, спиро и мостиковые кольцевые системы также включены в указанное выше определение. Примеры моноциклических гетероциклических групп включают, без ограничения перечисленными, оксетанил, 1,1-диоксидотиетанил, пирролидинил, тетрагидрофурил, тетрагидротиенил, пирролил, фурил, тиенил, пиразолил, имидазолил, тиазолил, оксазолил, пиперидинил, пиперазинил, морфолинил, пиридинил, пиразинил, пиримидинил, пиридазинил, триазинил, пиридонил, пиримидинонил, пиразинонил, пиридазинонил, пирролидинил и триазинонил и т.д. Примеры конденсированных гетероциклических групп включают, без ограничения перечисленными, фенил-конденсированное кольцо или пиридил-конденсированное кольцо, такое как хинолил, изохинолил, хиноксалинил, хиназинил, хиназолинил, азаиндолизинил, птеридинил, бензопиранил, изобензопиранил, индолил, изоиндолил, индазинил, индазолил, пуринил, бензофурил, изобензофурил, бензимидазолил, бензотиенил, бензотиазолил, карбазолил, феназинил, фенотиазинил, фенантридинил, имидазо[1,2-а]пиридил, [1,2,4]триазоло[4,3-а]пиридил и [1,2,3]триазоло[4,3-а]пиридил, и т.д. Примеры спирогетероциклической группы включают, без ограничения перечисленными, спиропиранил и спирооксазинил, и т.д. Примеры мостиковых гетероциклических групп включают, без ограничения перечисленными, морфолинил, гексаметилентетрамин, 3-аза-бицикло[3.1.0]гексан, 8-аза-бицикло[3.2.1]октан, 1-аза-бицикло[2.2.2]октан и 1,4-диазабицикло[2.2.2]октан (DABCO), и т.д.
[0051] Подходящие моновалентные заместители на замещаемых атомах углерода "необязательно замещенных" групп независимо представляют собой галоген; -(CH2)0-4R°; - (СН2)0-4OR°; -О (СН2)0-4Ro; -О-(СН2)0-4С(О)OR°; -(СН2)0-4СН(OR°)2; -(СН2)0-4SR°; -(CH2)0-4Ph, который может быть замещен R°; -(СН2)0-4О(СН2)0-1Ph, который может быть замещен R°; -CH=CHPh, который может быть замещен R°;
(СН2)0-4О(СН2)0-1-пиридил, который может быть замещен R°; -NO2; CN; -N3; -(CH2)0-4N(R°)2; -(CH2)0-4N(R°)С(О)R°; -N(R°)С(S)R°; -(CH2)0-4N(R°)С(О)NR°2; -N(R°)С(S)NR°2; -(CH2)0-4N(R°)С(О)OR°; N(R°)N(R°)С(О)R°; -N(R°)N(R°)С(О)NR°2; -N(R°)N(R°)C(O)OR°; (CH2)0-4C(O)R°; -C(S)R°; -(CH2)0-4C(O)OR°; -(CH2)0-4C(O) SR°; -(CH2)0-4C(O)OSiR°3; -(CH2)0-4OC(O)R°; -OC(O)(CH2)0-4SR°-; -(CH2)0-4SC(O)R°; -(CH2)0-4C(O)NR°2; -C(S)NR°2; -C(S)SR°; -SC(S)SR°; -(CH2)0-4OC(O)NR°2; -С(O)N(OR°)R°; -С(O)С(O)R°; -С(О)CH2C(O)R°; -C(NOR°)R°; -(CH2)0-4SSR°; -(CH2)0-4S(O)2R°; -(CH2)0-4S(O)2OR°; -(CH2)0-4OS(O)2R°; -S(O)2NR°2; -(CH2)0-4S(O)R°; -N(R°)S(O)2NR°2; -N(R°)S(O)2R°; -N(OR°)R°; -C(NH)NR°2; -P(O)2R°; -P(O)R°2; OP(O)R°2; -OP(O)(OR°)2; SiR°3; -(C1-4 нормальный или разветвленный алкилен)O-N(R°)2; или -(C1-4 нормальный или разветвленный алкилен)С(О)O-N(R°)2, где каждый R° может быть замещен, как определено ниже, и независимо представляет собой водород, C1-6 алифатическую группу, -CH2Ph, -О(СН2)0-1Ph, -СН2-(5-6-членное гетероарильное кольцо) или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы; или, несмотря на представленное выше определение, два независимо присутствующих R° образуют, вместе с их атомом, присутствующим между ними, 3-12 членное насыщенное, частично ненасыщенное или полностью ненасыщенное моноциклическое или бициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, и может быть замещено, как определено ниже.
[0052] Подходящий моновалентный заместитель на R° (или в кольце, образованном двумя независимо присутствующими R° вместе атомом между ними) независимо представляет собой галоген,
(CH2)0-2R•, -(галогенR•), -(СН2)0-2ОН, -(СН2)0-2OR•, -(СН2)0-2СН(OR•)2, -О(галогенR•), -CN, -N3, -(СН2)0-2С(О)R•, -(СН2)0-2С(О)ОН, -(СН2)0-2C(O)OR•, -(СН2)0-2SR•, -(CH2)0-2SH, -(СН2)0-2NH2, -(СН2)0-2NHR•, -(СН2)0-2NR•2, -NO2, -SiR•3, -OSiR•3, -C(O)SR•, -(C1-4 нормальный или разветвленный алкилен) С(О)OR• или -SSR•, где каждый R• не замещен или замещен только одним или более галогенами, в случае присутствия префикса "галоген", и независимо выбран из C1-4 алифатической группы, -CH2Ph, -O(CH2)0-1Ph или 5-6-членного насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы. Подходящий двухвалентный заместитель на насыщенном атоме углерода в R° включает =O и =S.
[0053] Подходящий двухвалентный заместитель на насыщенном атоме углерода "необязательно замещенной группы" включает: =O, =S, =NNR*2, =NNHC(O)R*, =NNHC(O)OR*, =NNHS(O)2R*, =NR*, =NOR*, -O(C(R*2))2-3-O- или -S(C(R*2))2-3-S-, где R* при каждом появлении выбран из водорода, C1-6 алифатической группы, которая может быть замещена, как определено ниже, или незамещенного 5-6-членного насыщенного, частично ненасыщенного или арильного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы. Подходящий двухвалентный заместитель, связанный с замещаемым углеродом в орто-положении "необязательно замещенной группы" включает -О(CR*2)2-3-O-, где R* при каждом появлении выбран из водорода, C1-6 алифатической группы, которая может быть замещена, как определено ниже, или незамещенного 5-6 членного насыщенного, частично ненасыщенного или полностью ненасыщенного кольца, содержащего 0-4 гетероатома, независимо выбранных из азота, кислорода или серы.
[0054] Подходящий заместитель на алифатической группе R* включает галоген, -R•, (галогенR•), -ОН, -OR•, -О(галогенR)•, -CN, -С(О)ОН, -С(О)OR•, -NH2, -NHR•, -NR2• или -NO2, где каждый R• не замещен или замещен только одним или более галогенами, в случае присутствия префикса "галоген", и независимо представляет собой C1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или полностью ненасыщенное кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы.
[0055] Подходящий заместитель на замещаемом атоме азота "необязательно замещенной группы" включает -R†, -NR†2, -C(O)R†, -C(O)OR†, -C(O)C(O)R†, -С(О)CH2C(О)R†, S(O)2R†, S(O)2NR†2, -C(S)NR†2, -C(NH)NR†2 или -N(R†)S(O)2R†, где каждый R† независимо представляет собой водород, C1-6 алифатическую группу, которая может быть замещенной, как определено ниже, незамещенной -OPh или незамещенным 5-6-членным насыщенным, частично ненасыщенным или полностью ненасыщенным кольцом, содержащим 0-4 гетероатома, независимо выбранных из азота, кислорода или серы; или несмотря на представленное выше определение, два независимо присутствующих R† образуют, вместе с атомом между ними, незамещенное 3-12-членное насыщенное, частично ненасыщенное или полностью ненасыщенное моноциклическое или бициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы.
[0056] Подходящий заместитель на алифатической группе R† независимо представляет собой галоген, -R•, (галогенR•), -ОН, OR•, -О(галогенR•), -CN, -С(О)ОН, -С(О)OR•, -NH2, -NHR•, -NR2• или -NO2, где каждый R• не замещен или замещен только одним или более галогенами, в случае присутствия префикса "галоген", и независимо представляет собой C1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы.
[0057] Термин "защищенная группа" при использовании в настоящем документе относится к группе атомов, которая блокирует, уменьшает или препятствует реакционной способности функциональной группы в случае присоединения к реакционноспособной функциональной группе в молекуле. Например, "защитная группа аминогруппы" является заместителем, присоединенным к аминогруппе, который блокирует или защищает функциональную аминогруппу в соединении. Подходящие защитные группы аминогруппы включают, без ограничения перечисленными, ацетил, трифторацетил, трифенилметил, аллилоксикарбонил, триметилсилил (TMS), трет-бутоксикарбонил (Boc), бензилоксикарбонил (CBZ) и 9-флуоренилметиленоксикарбонил (Fmoc) и т.д. Аналогичным образом, "защитная группа гидроксила" относится к заместителю гидроксильной группы, который блокирует или защищает гидроксильную функциональную группу. Подходящие защитные группы включают ацетил и силил. "Защитная группа карбоксигруппы" относится к заместителю карбоксильной группы, который блокирует или защищает карбоксильную функциональную группу. Обычные защитные группы карбоксила включают фенилсульфонилэтил, цианоэтил, 2-(триметилсилил)этил, 2-(триметилсилил)этоксиметил, 2-(п-толуолсульфонил)этил, 2-(п-нитрофенилсульфинил)этил, 2-(дифенилфосфино)-этил и нитроэтил и т.д. Общее описание защитных групп и их применения см. в публикации P. G. М. Wuts and Т. W. Greene, Greene's Protective Groups in Organic Synthesis, 4th Edition, Wiley-Interscience, New York, 2006.
[0058] Соединения
[0059] В одном аспекте настоящей заявки предложено соединение Формулы (I):
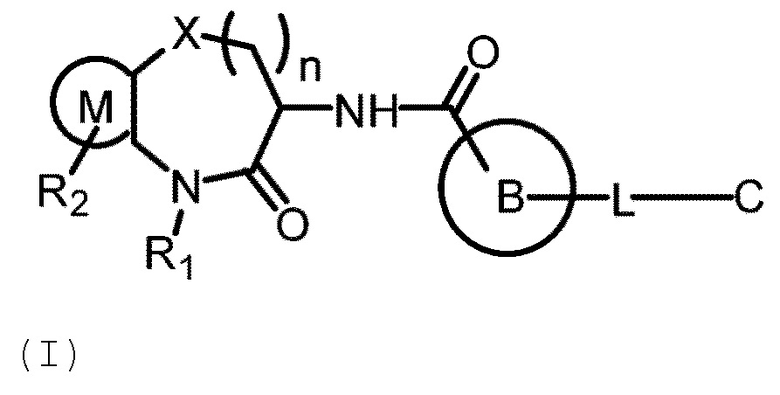
или его фармацевтически приемлемая соль, где: X представляет собой О, S или СН2;
кольцо М имеет структуру 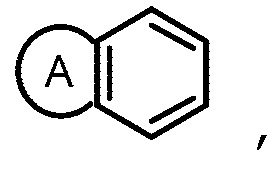 где кольцо А выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила;
где кольцо А выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила;
кольцо В выбрано из группы, состоящей из замещенного или незамещенного 5-12-членного арила, замещенного или незамещенного 5-12-членного гетероарила и замещенного или незамещенного 5-12-членного гетероциклила;
С выбрано из группы, состоящей из замещенного или незамещенного (C3-C12) циклоалкила, замещенного или незамещенного 5-12-членного арила, замещенного или незамещенного 5-12-членного гетероарила и замещенного или незамещенного 5-12-членного гетероциклила;
L выбрано из группы, состоящей из О, S, NH, N(CH3), замещенного или незамещенного - C1-C6 алкилен-О-, замещенного или незамещенного C1-C6 алкилен-NH-, (замещенного или незамещенного C1-С6 алкилен)2-N-, замещенного или незамещенного C1-C6 алкилена, замещенного или незамещенного С3-С6 алкенилена, замещенного или незамещенного С3-С6 алкенилен-О-;
R1 выбран из группы, состоящей из Н и замещенного или незамещенного C1-C6 алкила;
R2 выбран из группы, состоящей из Н, галогена, гидроксила, циано, оксо, бензила, замещенного или незамещенного амино, замещенного или незамещенного C1-C6 алкила, замещенного или незамещенного C1-C6 алкокси и C1-C6 ацила; и
n равно 1, 2 или 3;
где "замещенный" относится к замещению одного или более атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена, циано, алкила, ацила, сульфонила, гидроксила, амино, бензила, вкеиоксо, (C1-C4) алкила, галоген(C1-С4) алкила, (C1-C4) алкокси, галоген (С1-С4) алкокси, нитро и (C1-С4) алкилС(О)-.
[0060] В некоторых вариантах осуществления X представляет собой О или S.
[0061] В некоторых вариантах осуществления X представляет собой О.
[0062] В некоторых вариантах осуществления X представляет собой S.
[0063] В некоторых вариантах осуществления кольцо А представляет собой замещенный или незамещенный 5-членный гетероарил или замещенный или незамещенный 5-членный гетероциклил. В некоторых вариантах осуществления кольцо А представляет собой замещенный или незамещенный 5-членный гетероарил или замещенный или незамещенный 5-членный гетероциклил, где 5-членный гетероарил и 5-членный гетероциклил содержат один или более гетероатомов, выбранных из N или О.
[0064] В некоторых вариантах осуществления кольцо А представляет собой замещенный или незамещенный 6-членный гетероарил или замещенный или незамещенный 6-членный гетероциклил. В некоторых вариантах осуществления кольцо А представляет собой замещенный или незамещенный 6-членный гетероарил или замещенный или незамещенный 6-членный гетероциклил, где 6-членный гетероарил и 6-членный гетероциклил содержат один или более гетероатомов, выбранных из N или О.
[0065] В некоторых вариантах осуществления кольцо В представляет собой замещенный или незамещенный 5-12-членный арил, замещенный или незамещенный 5-6-членный гетероарил или замещенный или незамещенный 5-6-членный гетероциклил.
[0066] В некоторых вариантах осуществления кольцо В представляет собой замещенный или незамещенный 5-10-членный арил. В некоторых вариантах осуществления кольцо В представляет собой замещенный или незамещенный 5-6-членный арил. В некоторых вариантах осуществления кольцо В представляет собой замещенный или незамещенный фенил.
[0067] В некоторых вариантах осуществления кольцо В представляет собой замещенный или незамещенный 5-6-членный гетероарил или замещенный или незамещенный 5-6-членный гетероциклил. В некоторых вариантах осуществления кольцо В представляет собой замещенный или незамещенный 5-6-членный гетероарил или замещенный или незамещенный 5-6-членный гетероциклил, где 5-6-членный гетероарил и 5-6-членный гетероциклил содержат один или более гетероатомов, выбранных из N или О.
[0068] В некоторых вариантах осуществления кольцо В представляет собой группу, выбранную из группы, состоящей из:
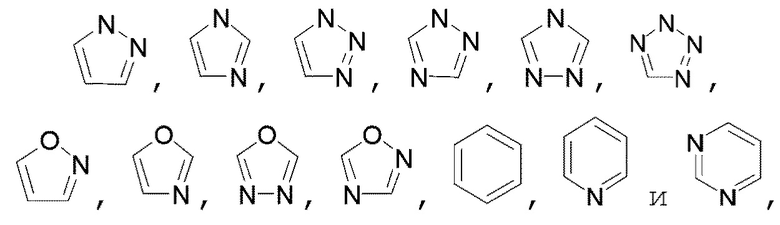
каждый из которых необязательно замещен одним или более заместителями, описанными в настоящем документе.
[0069] В некоторых вариантах осуществления С представляет собой замещенный или незамещенный 5-12-членный арил. В некоторых вариантах осуществления С представляет собой замещенный или незамещенный 5-10-членный арил. В некоторых вариантах осуществления С представляет собой замещенный или незамещенный 5-6-членный арил. В некоторых вариантах осуществления С представляет собой замещенный или незамещенный 6-членный арил. В некоторых вариантах осуществления С представляет собой замещенный или незамещенный фенил. В некоторых вариантах осуществления С замещено одной или более группами, выбранными из группы, состоящей из галогена, циано, гидроксила, амино, нитро, алкила, галогеналкила, алкокси и галогеналкокси. В некоторых вариантах осуществления С замещено одной или более группами, выбранными из группы, состоящей из галогена, циано, гидроксила, амино, нитро и алкила. В некоторых вариантах осуществления С замещено одной или более группами, выбранными из группы, состоящей из галогена и алкила.
[0070] В некоторых вариантах осуществления L представляет собой О, NH или замещенный или незамещенный C1-C6 алкилен. В некоторых вариантах осуществления L представляет собой О, NH или незамещенный C1-C6 алкилен. В некоторых вариантах осуществления L представляет собой О. В некоторых вариантах осуществления L представляет собой NH. В некоторых вариантах осуществления L представляет собой метилен.
[0071] В некоторых вариантах осуществления R1 представляет собой Н. В некоторых вариантах осуществления R1 представляет собой замещенный или незамещенный C1-C6 алкил. В некоторых вариантах осуществления R1 представляет собой незамещенный C1-C6 алкил. В некоторых вариантах осуществления R1 представляет собой метил, этил или пропил. В некоторых вариантах осуществления R1 представляет собой метил.
[0072] В некоторых вариантах осуществления R2 выбран из группы, состоящей из Н, галогена, гидроксила, оксо, бензила, замещенного или незамещенного C1-C6 алкила, замещенного или незамещенного С1-С6алкокси и C1-C6 ацила. В некоторых вариантах осуществления R2 представляет собой Н, галоген, гидроксил, оксо, бензил, метил, трифторметил, метокси или ацетил.
[0073] В некоторых вариантах осуществления m равно 0 или 1. В некоторых вариантах осуществления m равно 0. В некоторых вариантах осуществления m равно 1.
[0074] В некоторых вариантах осуществления n равно 1 или 2. В некоторых вариантах осуществления n равно 1.
[0075] В некоторых вариантах осуществления в настоящей заявке предложено соединение Формулы (Ia):
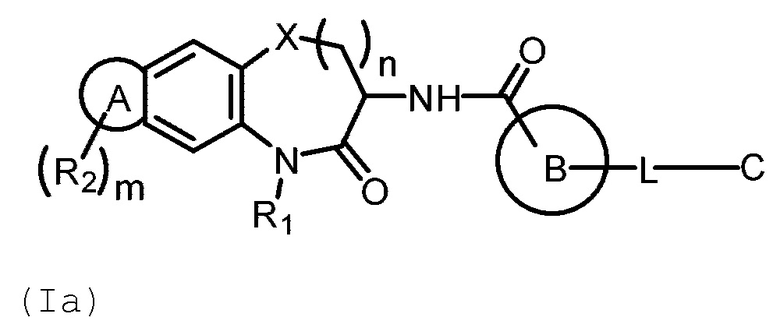
или его фармацевтически приемлемая соль, где кольцо А, кольцо В, С, L, R1, R2, m и n имеют определенное выше значение.
[0076] В некоторых вариантах осуществления в настоящей заявке предложено соединение Формулы (Ib):
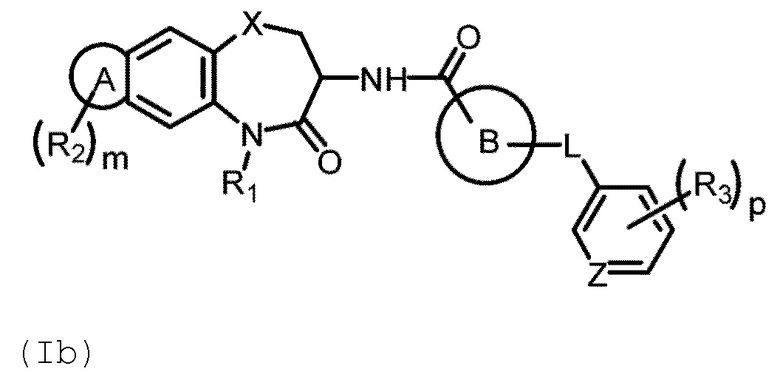
или его фармацевтически приемлемая соль, где кольцо А, кольцо В, R1, R2, и m имеют определенное выше значение, L представляет собой О или СН2, Z представляет собой N или СН, R3 выбран из галогена или замещенного или незамещенного С1-С6 алкила, и р равно 0, 1, 2 или 3.
[0077] В некоторых вариантах осуществления, в соединениях Формулы (Ia) и (Ib), структурная группа, представленная формулой
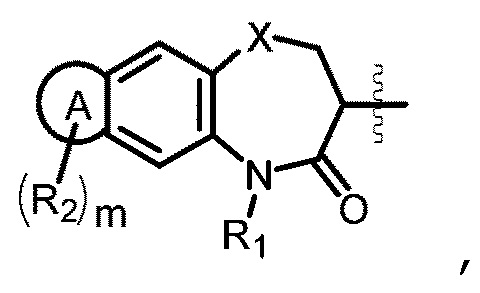
выбрана из группы, состоящей из:
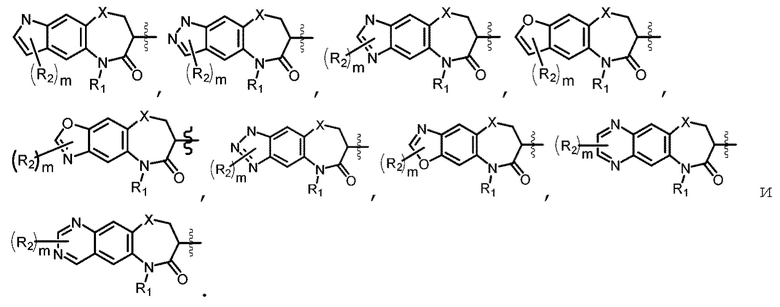
[0078] В некоторых вариантах осуществления R2 выбран из группы, состоящей из Н, галогена, гидроксила, оксо, бензила, замещенного или незамещенного C1-C6 алкила, замещенного или незамещенного C1-C6 алкокси и C1-C6 ацила. В некоторых вариантах осуществления R2 представляет собой Н, Cl, гидроксил, оксо, бензил, метил, трифторметил, метокси или ацетил.
[0079] В некоторых вариантах осуществления m равно 0 или 1. В некоторых вариантах осуществления m равно 0. В некоторых вариантах осуществления m равно 1.
[0080] В некоторых вариантах осуществления в настоящей заявке предложено соединение Формулы (Ic):
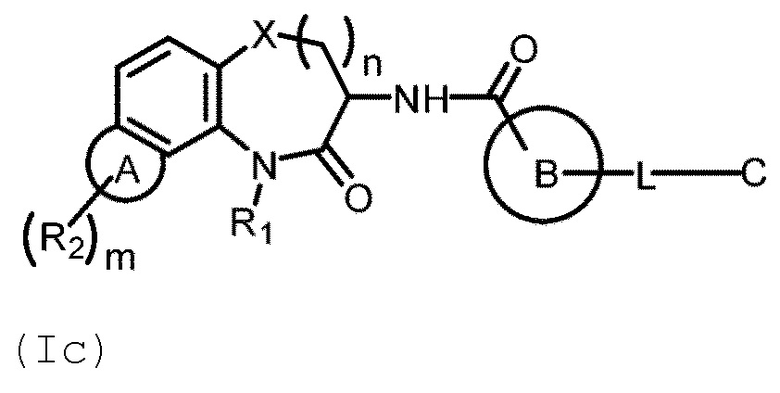
или его фармацевтически приемлемая соль, где кольцо А представляет собой замещенный или незамещенный 6-членный гетероарил или замещенный или незамещенный 6-членный гетероциклил, и кольцо В, С, L, R1, R2, m и n имеют определенное выше значение.
[0081] В некоторых вариантах осуществления в настоящей заявке предложено соединение Формулы (Id):
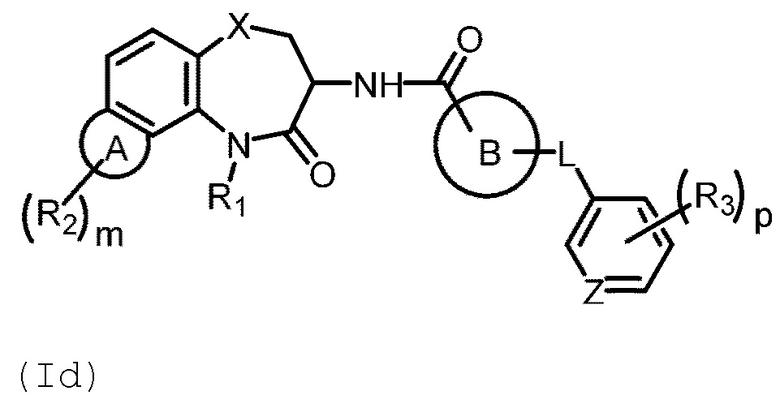
или его фармацевтически приемлемая соль, где кольцо А представляет собой замещенный или незамещенный 6-членный гетероарил или замещенный или незамещенный 6-членный гетероциклил, L представляет собой О или СН2, Z представляет собой N или СН, R3 представляет собой галоген и замещенный или незамещенный С1-С6 алкил, р равно 0, 1, 2 или 3, и кольцо В, R1, R2 и m имеют определенное выше значение.
[0082] В некоторых вариантах осуществления, в соединениях Формулы (Ic) и (Id), структурная группа, представленная формулой
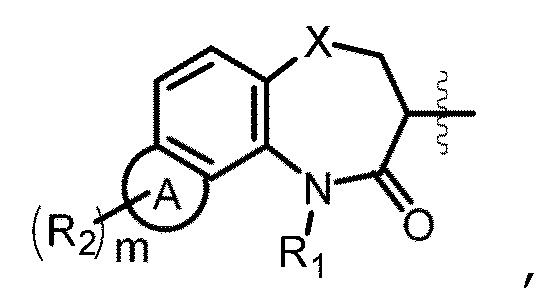
выбрана из группы, состоящей из:
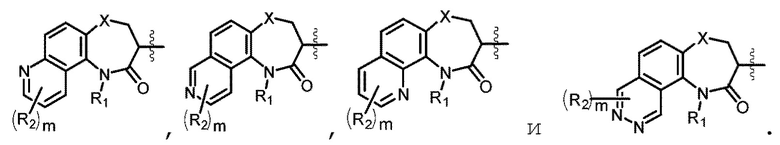
[0083] В некоторых вариантах осуществления R2 выбран из группы, состоящей из Н, галогена, гидроксила, оксо, бензила, замещенного или незамещенного C1-C6 алкила, замещенного или незамещенного С1-С6алкокси и C1-C6 ацила. В некоторых вариантах осуществления R2 представляет собой Н.
[0084] В некоторых вариантах осуществления m равно 0 или 1. В некоторых вариантах осуществления m равно 0. В некоторых вариантах осуществления m равно 1.
[0085] В некоторых вариантах осуществления в настоящей заявке предложено соединение Формулы (I), выбранное из группы, состоящей из следующего:
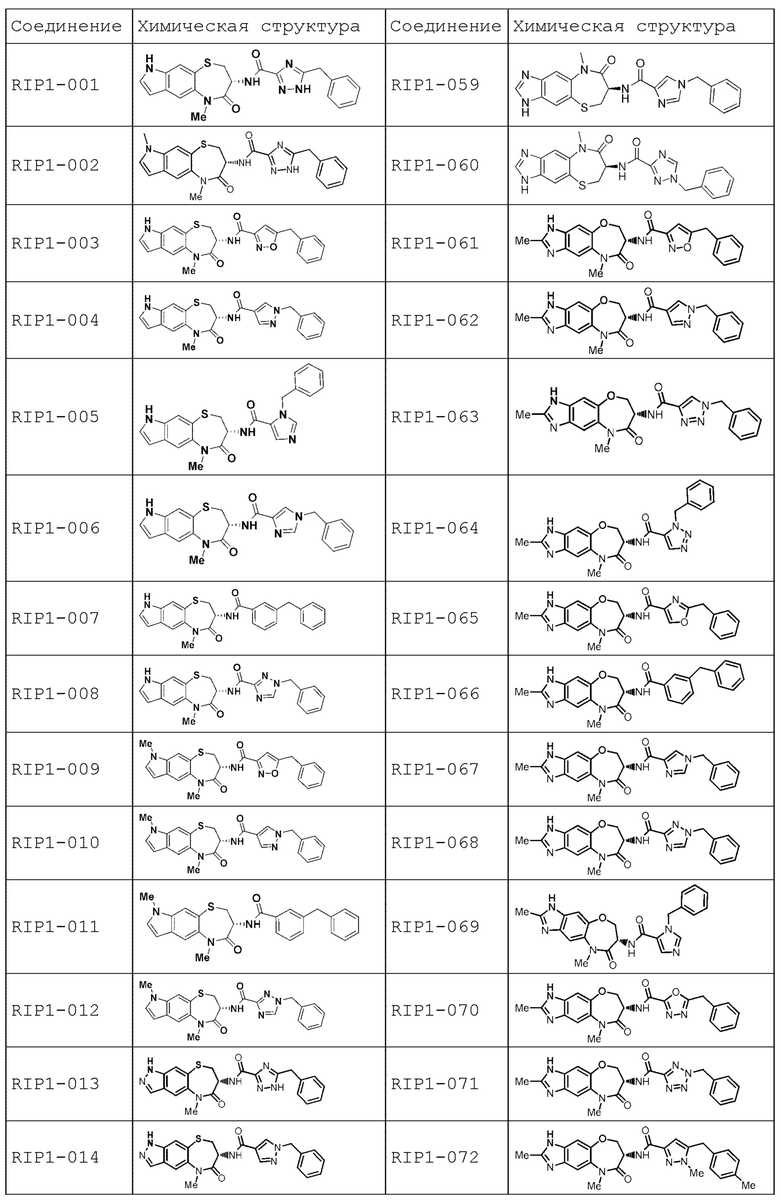
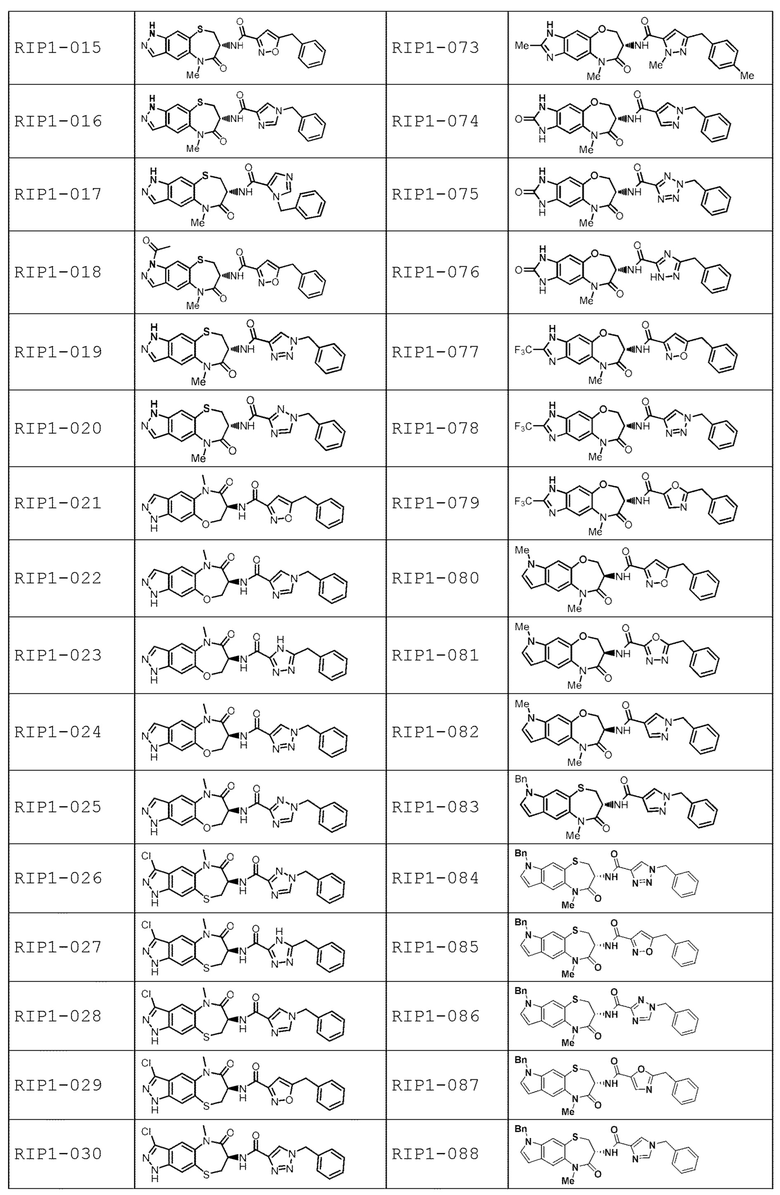
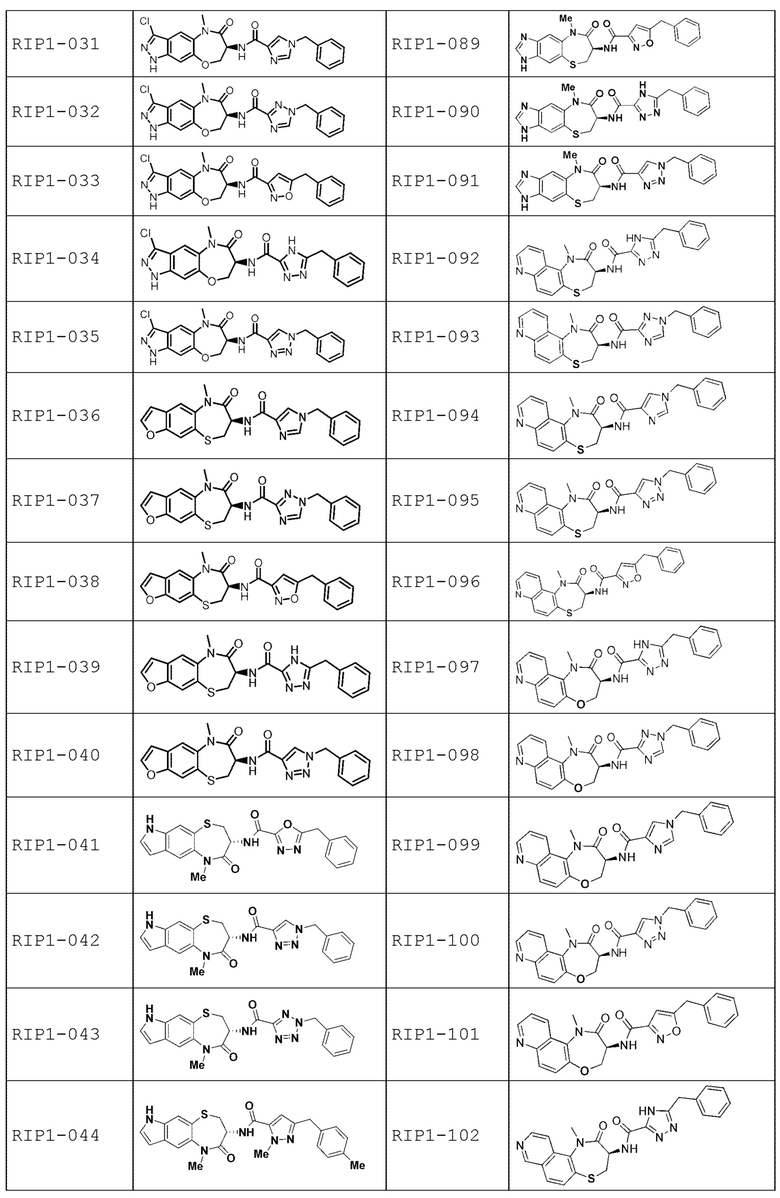
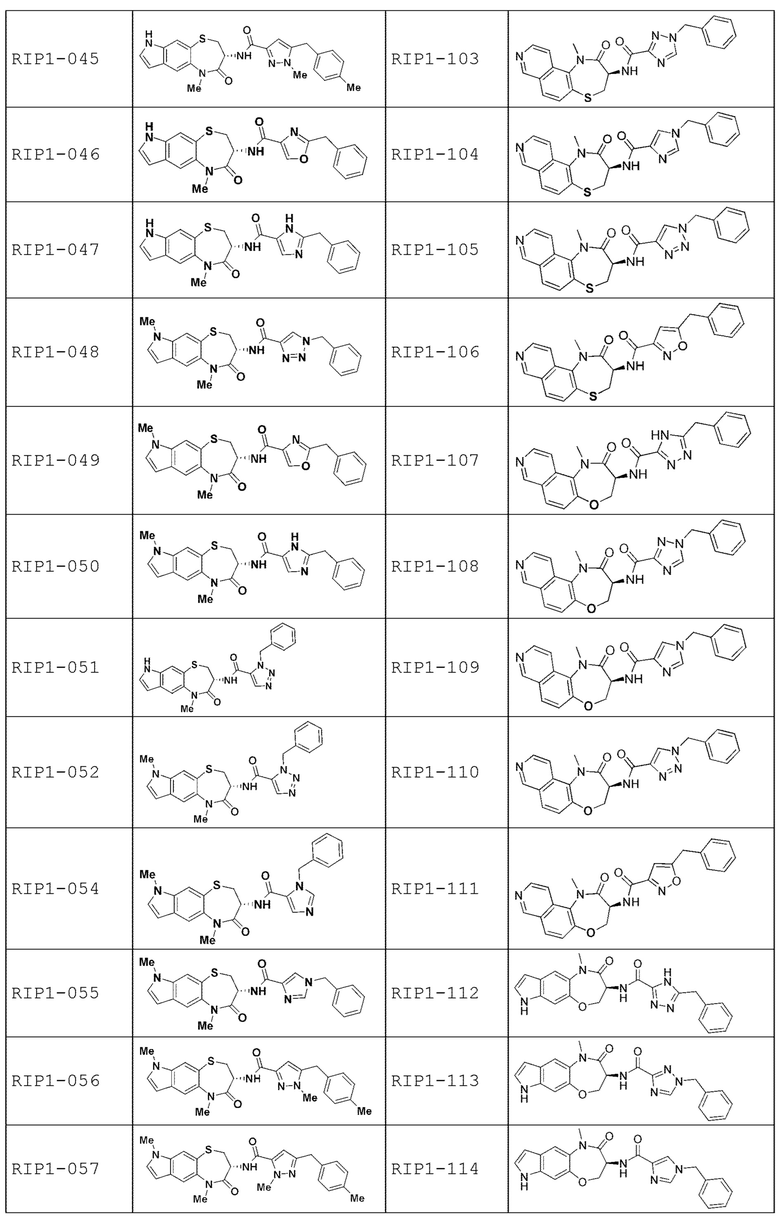
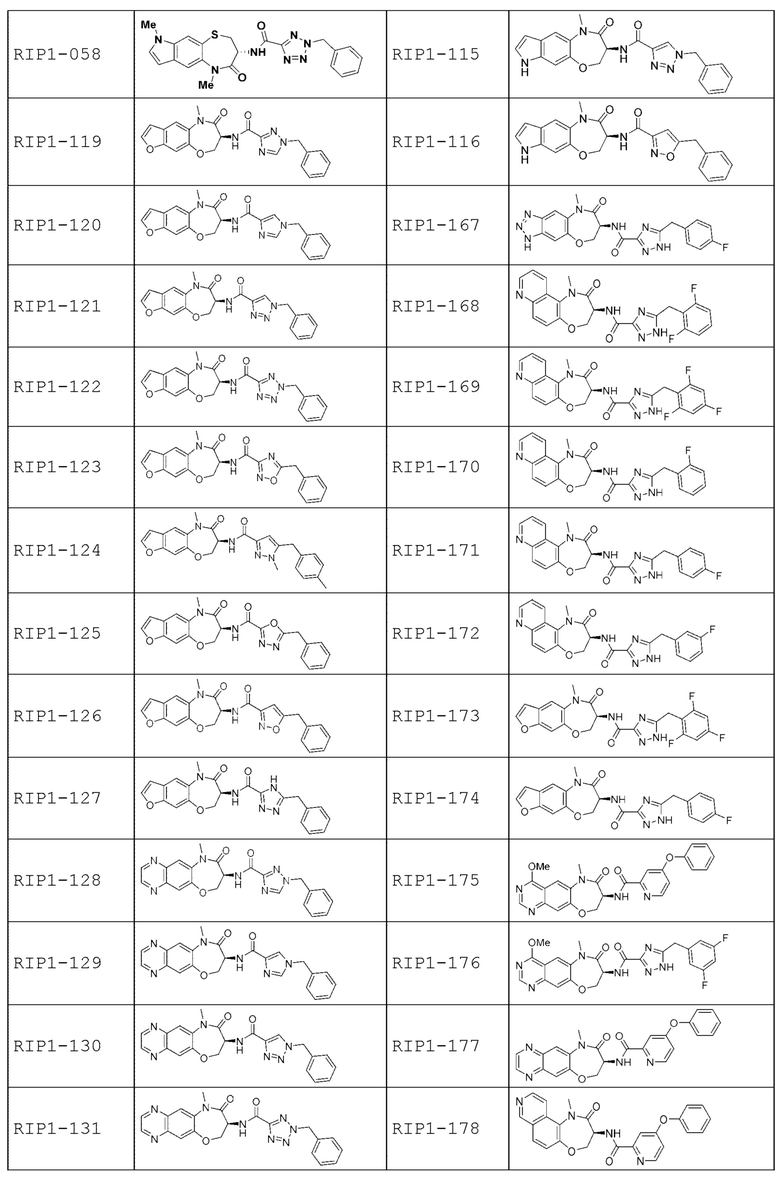
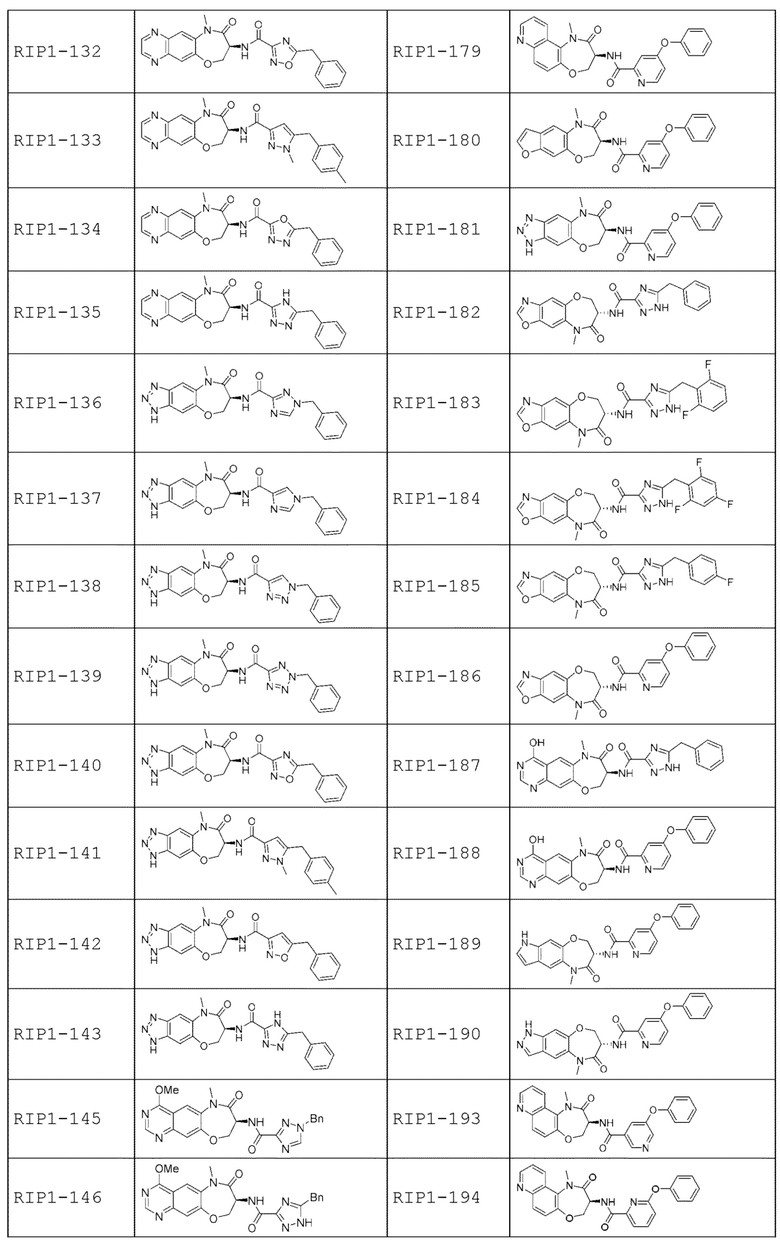
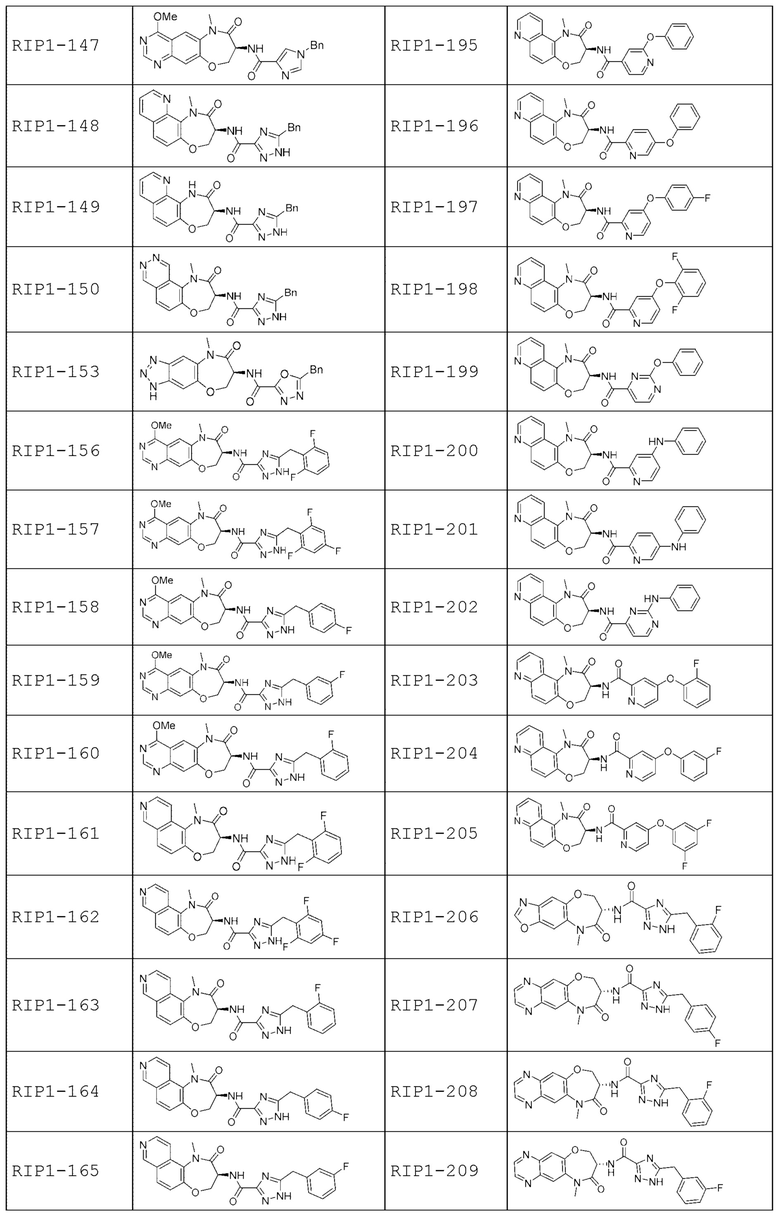
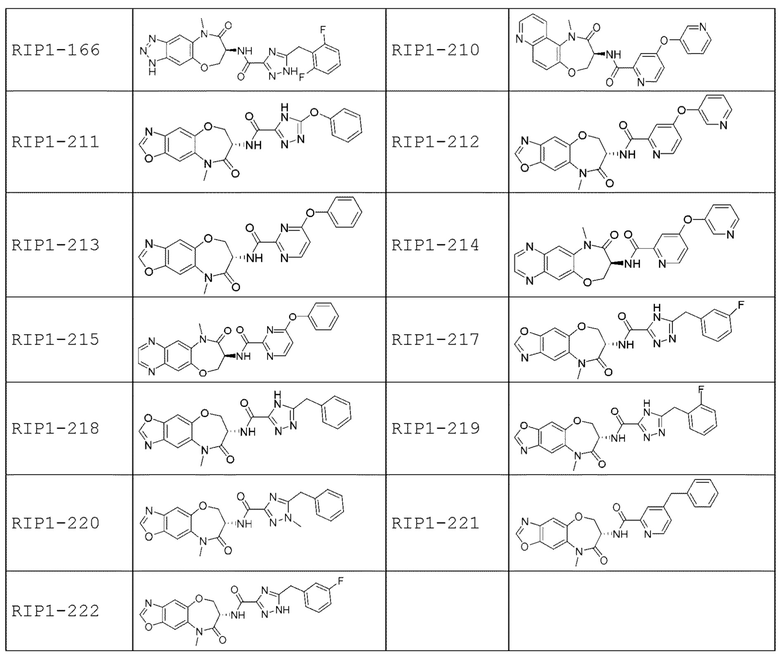
[0086] Соединение, предложенное в настоящем документе, может существовать в виде ряда различных форм или производных, которые включены в рамки настоящей заявки. Такие формы или производные включают, например, таутомеры, стереоизомеры, рацемические смеси, региоизомеры, соли, пролекарства, сольватированные формы, различные кристаллические формы или полиморфные модификации и активные метаболиты.
[0087] Соединение, предложенное в настоящем документе, может включать один или более центров асимметрии и, таким образом, могут существовать в различных стереоизомерных формах, таких как энантиомеры и/или диастереомеры. Таким образом, соединение и его композиция, предложенные в настоящем документе, могут находиться в форме отдельного энантиомера, диастереомера или геометрического изомера или могут находиться в форме смеси стереоизомеров. В некоторых вариантах осуществления соединения, предложенные в настоящем документе, представляют собой энантиомерно чистые соединения. В некоторых вариантах осуществления предложены смеси энантиомеров или диастереомеров.
[0088] Термин "энантиомер" при использовании в настоящем документе относится к двум стереоизомерам соединения, которые являются несовпадающими при наложении зеркальными отображениями друг друга. Термин "диастереомер" при использовании в настоящем документе относится к паре оптических изомеров, которые не являются зеркальными отображениями друг друга. Диастереомеры обладают разными физическими свойствами, такими как точки плавления, точки кипения, спектральные свойства и реакционные способности.
[0089] Кроме того, если не указано иное, некоторые соединения, предложенные в настоящем документе, могут иметь одну или более двойных связей, которые могут существовать в виде Z или Е изомера. Настоящая заявка дополнительно охватывает такие соединения, как отдельные изомеры, по существу не содержащие других изомеров и, альтернативно, в виде смесей разных изомеров, например, рацемических смесей энантиомеров. В дополнение к вышеупомянутым соединениям, по сути, настоящая заявка также охватывает композиции, включающие одно или более соединений.
[0090] Термин "изомер" при использовании в настоящем документе включает любые возможные геометрические изомеры и стереоизомеры. Например, "изомеры" включают цис- и транс-изомеры, Е- и Z-изомеры, R- и S-энантиомеры, диастереомеры, D-изомеры, L-изомеры, их рацемические смеси а также другие их смеси. Например, в некоторых вариантах осуществления стереоизомер может быть предоставлен в форме, которая по существу не содержит одного или более соответствующих энантиомеров, которые могут называться "стереохимически обогащенными".
[0091] Если предпочтителен конкретный энантиомер, соединение согласно настоящей заявке может быть представлено в виде энантиомера, который по существу не содержит противоположного энантиомера и может называться "оптически обогащенным". При использовании в настоящем документе термин "оптически обогащенный" означает, что соединение состоит из значительно большей части одного энантиомера. В некоторых вариантах осуществления соединение состоит по меньшей мере из приблизительно 90 вес.% предпочтительного энантиомера. В некоторых вариантах осуществления соединение состоит по меньшей мере из приблизительно 95, 98 или 99 вес.% предпочтительного энантиомера. Предпочтительные энантиомеры могут быть выделены из рацемических смесей любым способом, известным в данной области, включая хиральную высокоэффективную жидкостную хроматографию (ВЭЖХ), образование и кристаллизацию хиральных солей, или получены с помощью асимметричного синтеза. См., например, Jacques et al., Enantiomers, Racemates and Resolutions (Wiley Interscience, New York, 1981); Wilen, S.H. et al., Tetrahedron 33:2725 (1977); Eliel, E.L. Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); и Wilen, S.H. Tables of Resolving Agents and Optical Resolutions p.268 (E.L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972).
[0092] Соединение, предложенное в настоящем документе, также может существовать в разных таутомерных формах, и все такие формы включены в объем настоящей заявки. Термин "таутомер" или "таутомерная форма" относится к структурным изомерам с разными энергиями, которые способны к взаимному превращению через низкий энергетический барьер. Например, протоновые таутомеры (также известные как протонные таутомеры) включают взаимное превращение посредством миграции протона, такие как кето-енольная, амид-имидокислотная, лактам-лактимная, енамин-иминовая изомеризация, и кольцевые формы, в которых протон может занимать два или более положений гетероциклической системы, такой как 1Н- и 3Н-имидазол, 1Н-, 2Н- и 4Н-1,2,4-триазол, 1Н- и 2Н-изоиндол и 1Н- и 2Н-пиразол. Валентные таутомеры включают взаимные превращения путем реорганизации некоторых связывающих электронов. Таутомерные формы могут находиться в равновесии или могут быть стерически заблокированы в одной форме при соответствующем замещении. Если не указано иное, предусмотрено, что соединения согласно настоящей заявке, идентифицированные по названию или структуре как одна конкретная таутомерная форма, включают другие таутомерные формы.
[0093] В некоторых вариантах осуществления соединение согласно настоящей заявке является S-энантиомером. В некоторых вариантах осуществления соединение настоящей заявки является R-энантиомером.
[0094] Соединения согласно настоящей заявке также включают пролекарства, активные метаболические производные (активные метаболиты), активные промежуточные соединения и их фармацевтически приемлемые соли.
[0095] Термин "пролекарство" при использовании в настоящем документе относится к соединению или его фармацевтически приемлемой соли, которые при метаболизации при физиологических условиях или при превращении в ходе сольволиза дают требуемое активное соединение. Пролекарства включают, без ограничения, сложные эфиры, амиды, карбаматы, карбонаты, уреиды, сольваты или гидраты активного соединения. Обычно пролекарство неактивно или менее активно, чем активное соединение, но может обеспечивать один или несколько преимуществ, таких как улучшенные технологические свойства, удобство при введении и/или улучшенные метаболические свойства. Например, некоторые Пролекарства являются сложными эфирами активного соединения; во время метаболического гидролиза сложноэфирная группа отщепляется с образованием действующего лекарственного средства. Кроме того, некоторые Пролекарства активируются ферментативно с получением активного соединения или соединений, которые в ходе последующей химической реакции дают активное соединение. Пролекарства могут переходить из формы Пролекарства в активную форму в одну стадию или могут иметь одну или более промежуточных форм, которые сами могут обладать активностью или могут быть неактивными. Получение и применение пролекарств описано в публикациях Т. Higuchi and V. Stella, "Pro-drugs as Novel Delivery Systems", Vol.14 of the A.C.S. Symposium Series, и Bioreversible Carriers in Drug Design, Edward B. edited by Roche, American Pharmaceutical Association and Pergamon Press, 1987.
[0096] Термин "метаболит" при использовании в настоящем документе, такой как активный метаболит, перекрывается с пролекарствами, как описано выше. Следовательно, такие метаболиты являются фармакологически активными соединениями или соединениями, которые впоследствии метаболизируются до фармакологически активных соединений, которые являются производными, образующимися в результате метаболического процесса в организме субъекта. Например, такие метаболиты могут образовываться в результате окисления, восстановления, гидролиза, амидирования, дезамидирования, этерификации, деэтерификации, ферментативного расщепления и т.п. вводимого соединения, соли или Пролекарства. Из них активные метаболиты представляют собой фармакологически активные производные соединения. В случае пролекарств соединение-пролекарство обычно неактивно или обладает более низкой активностью, чем продукт метаболизма. В случае активных метаболитов исходное соединение может быть либо активным соединением, либо неактивным пролекарством.
[0097] Пролекарства и активные метаболиты могут быть идентифицированы с помощью стандартных методик, известных в данной области. См., например, Bertolini et al., 1997, J Med Chem 40: 2011-2016; Shan et al., J Pharm Sci 86: 756-757; и Bagshawe, 1995, DrugDev Res 34: 220-230.
[0098] Термин "активное промежуточное соединение" при использовании в настоящем документе относится к промежуточному соединению в процессе синтеза, которое проявляет такую же или по существу такую же биологическую активность, что и конечное синтезируемое соединение.
[0099] Соединения согласно настоящей заявке могут быть включены в составы или могут быть в форме фармацевтически приемлемых солей. Если не указано иное, соединение, предложенное в настоящем документе, включает фармацевтически приемлемые соли такого соединения.
[0100] Термин "фармацевтически приемлемый" при использовании в настоящем документе означает, что вещество или композиция совместимы химически и/или токсикологически с другими компонентами, входящими в состав, и/или субъектами, которых подвергают лечению с их применением.
[0101] Если не указано иное, термин "фармацевтически приемлемая соль" при использовании в настоящем документе включает соль, которая сохраняет биологическую эффективность свободных кислот и свободных оснований указанного соединения и не является нежелательной с биологической точки зрения. Предусмотренные фармацевтически приемлемые формы солей включают, без ограничения перечисленными, моно, бис, трис, тетракис и т.д. Фармацевтически приемлемые соли являются нетоксичными в количествах и концентрациях, в которых их вводят. Получение таких солей может облегчать фармакологическое применение благодаря изменению физических свойств соединения, которое не препятствует проявлению его физиологического эффекта. Полезные изменения физических свойств включают снижение температуры плавления для облегчения чересслизистого введения и повышение растворимости для облегчения введения более высоких концентраций лекарственных средств.
[0102] Фармацевтически приемлемые соли могут включать соли присоединения кислоты, такие как соли, включающие сульфат, хлорид, гидрохлорид, фумарат, малеат, фосфат, сульфамат, ацетат, цитрат, лактат, тартрат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат, циклогексилсульфонат и хинат. Фармацевтически приемлемые соли могут быть получены из кислот, таких как серная кислота, соляная кислота, фумаровая кислота, малеиновая кислота, фосфорная кислота, сульфаминовая кислота, уксусная кислота, лимонная кислота, молочная кислота, винная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, циклогексилсульфоновая кислота и хинная кислота.
[0103] Фармацевтически приемлемые соли также могут включать соли присоединения основания, такие как соли, включающие бензатин, хлорпрокаин, холин, диэтаноламин, этаноламин, трет-бутиламин, этилендиамин, меглумин, прокаин, алюминий, кальций, литий, магний, калий, натрий, аммоний, цинк и алкиламины в случае присутствия кислотных функциональных групп, таких как карбоксильные группы, или фенола. См., например. Remington's Pharmaceutical Sciences, 19th Edition, Mack Publishing Co., Easton, PA, Volume 2, Page 1457, 1995; "Handbook of Pharmaceutical Salts: Properties, Selection, and Use", Stahl and Wermuth, Wiley-VCH, Weinheim, Germany, 2002. Такие соли могут быть получены с использованием подходящих соответствующих оснований.
[0104] Фармацевтически приемлемые соли могут быть получены стандартными методами. Например, соединение в форме свободного основания можно растворять в подходящем растворителе, таком как водный или водно-спиртовой раствор, содержащий подходящую кислоту, а затем выделять при выпаривании раствора. Таким образом, если конкретное соединение является основанием, требуемая фармацевтически приемлемая соль могут быть получена любым подходящим способом, доступным в данной области, например, при обработке свободного основания неорганической кислотой (такой как соляная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.д.) или органической кислотой (такой как уксусная кислота, малеиновая кислота, янтарная кислота, миндальная кислота, фумаровая кислота, малоновая кислота, пировиноградная кислота, щавелевая кислота, гликолевая кислота, салициловая кислота, пиранозиловые кислоты, такие как глюкуроновая кислота или галактуроновая кислота, α-оксикислоты, такие как лимонная кислота или винная кислота, аминокислоты, такие как аспарагиновая кислота или глутаминовая кислота, ароматические кислоты, такие как бензойная кислота или коричная кислота, и сульфоновые кислоты, такие как п-толуолсульфоновая кислота или этансульфоновая кислота).
[0105] Аналогичным образом, если конкретное соединение является кислотой, требуемая фармацевтически приемлемая соль может быть получена любым подходящим способом, например, при обработке свободной кислоты неорганическим или органическим основанием, таким как амин (первичный, вторичный или третичный), гидроксид щелочного металла или гидроксид щелочноземельного металла и т.д. Иллюстративные примеры подходящих солей включают органические соли, полученные из аминокислот (таких как L-глицин, L-лизин и L-аргинин), аммиака, первичных аминов, вторичных аминов, третичных аминов, циклических аминов (таких как гидроксиэтилпирролидин, пиперидин, морфолин или пиперазин), и неорганические соли, полученные из натрия, кальция, калия, магния, марганца, железа, меди, цинка, алюминия и лития.
[0106] Также следует понимать, что соединение согласно настоящей заявке может существовать в несольватированной форме, сольватированной форме (например, гидратированной форме) и в твердой форме (например, кристаллической или полиморфной форме), при этом предполагается, что настоящая заявка охватывает все подобные формы.
[0107] Термин "сольват" или "сольватированная форма" при использовании в настоящем документе относится к форме присоединения растворителя, содержащей стехиометрическое или нестехиометрическое количество растворителя. Некоторые соединения имеют тенденцию захватывать фиксированные молярные отношения молекул растворителя в кристаллическом твердом состоянии, образуя, таким образом, сольват. Если растворителем является вода, образующийся сольват является гидратом; а если растворителем является спирт, образующийся сольват является алкоголятом. Примеры растворителей, образующих сольваты, включают, без ограничения перечисленными, воду, изопропанол, метанол, этанол, ДМСО, этилацетат, уксусную кислоту, этаноламин, ацетон и эфир и т.д.
[0108] Термины "кристаллическая форма", "полиморфная форма" и "полиморфная модификация" при использовании в настоящем документе могут использоваться попеременно и относятся к кристаллической структуре, в которой соединение (или его соль или сольват) кристаллизовано в различных конфигурациях упаковки кристалла, которые имеют одинаковый элементный состав. Различные кристаллические формы обычно имеют разные рентгеновские дифрактограммы, инфракрасные спектры, температуры плавления, плотность, твердость, кристаллическую форму, оптические и электрические свойства, стабильность и растворимость, и т.д. Растворитель для перекристаллизации, скорость кристаллизации, температура хранения и другие факторы могут приводить к преобладанию одной кристаллической формы. Полиморфные модификации соединения могут быть получены при кристаллизации в разных условиях.
[0109] Настоящая заявка также предусматривает включение всех изотопов атомов в соединении. Изотопы атома включают атомы, имеющие одинаковый атомный номер, но разные массовые числа. Например, если не указано иное, водород, углерод, азот, кислород, фосфор, сера, фтор, хлор, бром или иод в соединении согласно настоящей заявке также включают их изотопы, например, без ограничения перечисленными, 1H, 2H, 3H, 11С, 12С, 13С, 14С, 14N, 15N, 16O, 17О, 18О, 31P, 32Р, 32S, 33S, 34S, 36S, 17F, 19F, 35Cl, 37Cl, 79Br, 81Br, 127I и 131I. В некоторых вариантах осуществления водород включает протий, дейтерий, тритий или их комбинацию. В некоторых вариантах осуществления углерод включает 12С, 13С или их комбинацию. В некоторых вариантах осуществления содержание различных изотопных атомов определенного элемента может соответствовать состоянию, в котором элемент обычно встречается в природе, или состоянию, в котором определенный изотоп обогащен.
[0110] Синтез соединений
[0111] Синтез соединений (включая их фармацевтически приемлемые соли) согласно настоящей заявке показан на схеме синтеза в примерах ниже. Соединение согласно настоящей заявке может быть получено с использованием любых известных методов органического синтеза и может быть синтезировано согласно любым возможным путям синтеза. Таким образом, схемы, представленные в настоящем документе, являются лишь примерными и не должны рассматриваться как ограничение других возможных методов, которые могут использоваться для получения соединения согласно настоящей заявке.
[0112] Реакции, используемые для получения соединений согласно настоящей заявке, могут проводить в подходящих растворителях. Подходящие растворители могут практически не реагировать с исходными материалами (реагентами), промежуточными соединениями или продуктами при температурах, при которых проводят реакции (например, при температурах, которые могут изменяться от точки замерзания растворителя до точки кипения растворителя). Данную реакцию могут проводить в одном растворителе или в смеси больше чем одного растворителя. В зависимости от конкретной стадии реакции подходящие растворители для конкретной стадии реакции могут быть подобраны специалистами в данной области.
[0113] Получение соединений согласно настоящей заявке может включать защиту и снятие защиты различных химических групп. Потребность в защите и снятии защиты и выбор подходящих защитных групп могут быть определены специалистами в данной области. Химию защитных групп можно найти, например, в Т. W. Greene and Р. G. M. Wuts, Protective Groups in Organic Synthesis, 3rd edition, Wiley & Sons, Inc., New York (1999).
[0114] Реакции можно контролировать с помощью любого подходящего метода, известного в данной области. Например, образование продукта можно контролировать при использовании спектральных методов, таких как спектроскопия ядерного магнитного резонанса (такая как 1H или 13С-ЯМР), инфракрасная спектроскопия, спектрофотометрия (такая как УФ-вид), масс-спектрометрия, или с помощью хроматографического метода, такого как высокоэффективная жидкостная хроматография (ВЭЖХ), жидкостная хроматография-масс-спектроскопия (ЖХ-МС) или тонкослойная хроматография (ТСХ). Соединения могут быть очищены разными способами, включая ВЭЖХ и нормально-фазовую хроматографию на силикагеле.
[0115] В иллюстративных целях общий путь синтеза для получения соединений согласно настоящей заявке, а также промежуточных соединений показан ниже.
[0116] В одном аспекте настоящей заявки предложен способ получения соединения Формулы (I) согласно настоящей заявке, как показано ниже:
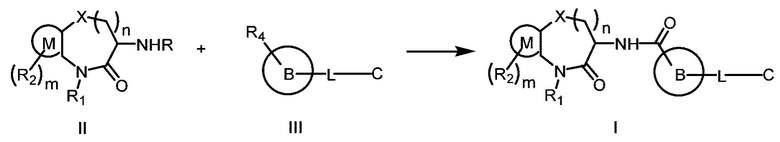
где R4 представляет собой -СООН или -COO-G+, где G+ является ионом щелочного металла;
когда R представляет собой Н, способ включает реакцию соединения Формулы (II) с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I); и
когда R представляет собой защитную группу аминогруппы, способ включает удаление R из соединения Формулы (II) в кислотных условиях и затем реакцию соединения Формулы (II), из которого удален R, с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I).
[0117] В некоторых вариантах осуществления G+ представляет собой Li+, Na+ или K+.
[0118] В некоторых вариантах осуществления соединение Формулы (I) согласно настоящей заявке может быть получено по схеме, выбранной из группы, состоящей из следующего:
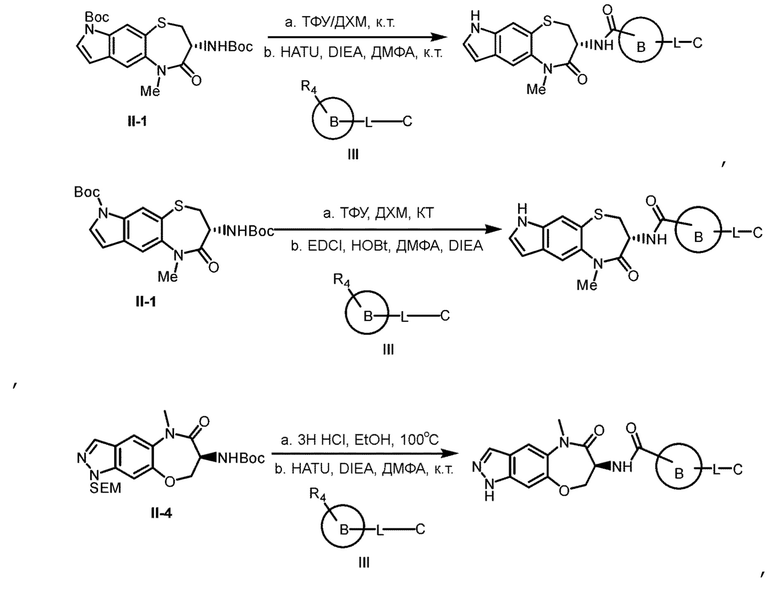
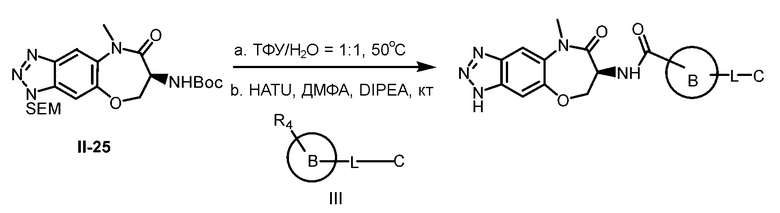
и
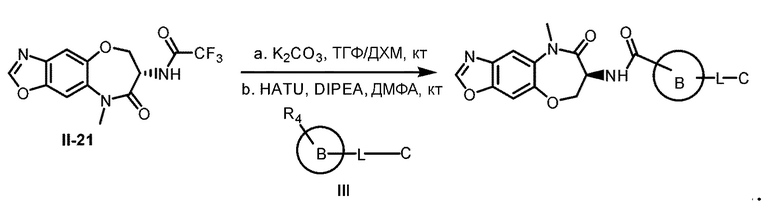
[0119] В некоторых вариантах осуществления R представляет собой Н, и соединение Формулы (II) реагирует с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I).
[0120] В некоторых вариантах осуществления инертный растворитель выбран из ДМФА, ДМСО, ацетонитрила, ТГФ, ДХМ или их комбинации.
[0121] В некоторых вариантах осуществления конденсирующий реагент выбран из HATU, DCC, HOBt, HBTU, HCTU, TBTU, TSTU, TNTU, EDCI, CDI, РуВОР или их комбинации.
[0122] В некоторых вариантах осуществления основание выбрано из DIEA (диизопропилэтиламина), триэтиламина, DMAP, пиридина или их комбинации.
[0123] В некоторых вариантах осуществления R представляет собой защитную группу аминогруппы, и R удаляют из соединения Формулы (II) в кислотных условиях, а затем соединение Формулы (II), из которой удален R, подвергают реакции с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I).
[0124] В некоторых вариантах осуществления кислотные условия означают, что реакционная система содержит соляную кислоту или трифторметансульфоновую кислоту.
[0125] В некоторых вариантах осуществления инертный растворитель выбран из ДМФА, ДМСО, ацетонитрила, ТГФ, ДХМ или их комбинации.
[0126] В некоторых вариантах осуществления конденсирующий реагент выбран из HATU, DCC, HOBt, HBTU, HCTU, TBTU, TSTU, TNTU, EDCI, CDI, РуВОР или их комбинации.
[0127] В некоторых вариантах осуществления основание выбрано из DIEA, триэтиламина, DMAP, пиридина или их комбинации.
[0128] В некоторых вариантах осуществления функциональная группа, включающая, без ограничения перечисленными, ацил и алкил, и т.д., может быть дополнительно введена в соединение Формулы (I) стандартным способом, например, как показано на схеме ниже:
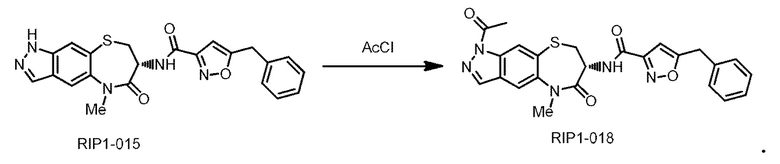
[0129] В еще одном аспекте настоящей заявки предложено промежуточное соединение Формулы (II) для получения соединения Формулы (I):
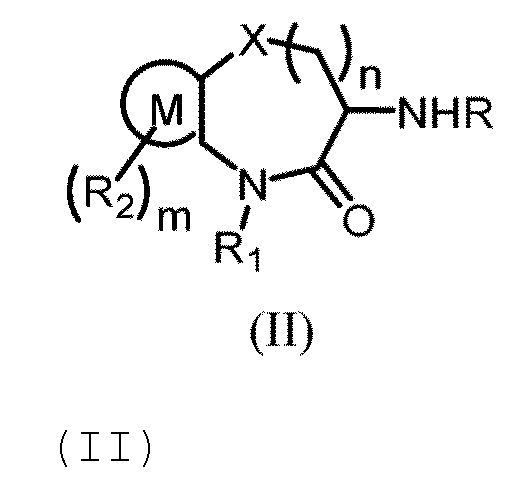
где:
R представляет собой Н или защитную группу аминогруппы;
Х представляет собой О, S или СН2;
R1 выбрано из группы, состоящей из Н и замещенного или незамещенного C1-C6 алкила;
r2 выбран из группы, состоящей из Н, галогена, гидроксила, оксо, бензила, замещенного или незамещенного C1-C6 алкила, замещенного или незамещенного C1-С6алкокси и C1-C6 ацила;
m равно 0, 1, 2 или 3; и
n равно 1, 2 или 3;
где "замещенный" относится к замещению одного или более атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена, циано, алкила, ацила, сульфонила, гидроксила, амино, бензила, оксо, (C1-C4) алкила, галоген(C1-С4) алкила, (C1-C4) алкокси, галоген (C1-C4) алкокси, нитро и (C1-C4) алкил С (О)-.
[0130] В некоторых вариантах осуществления промежуточное соединение Формулы (II) выбрано из группы, состоящей из:
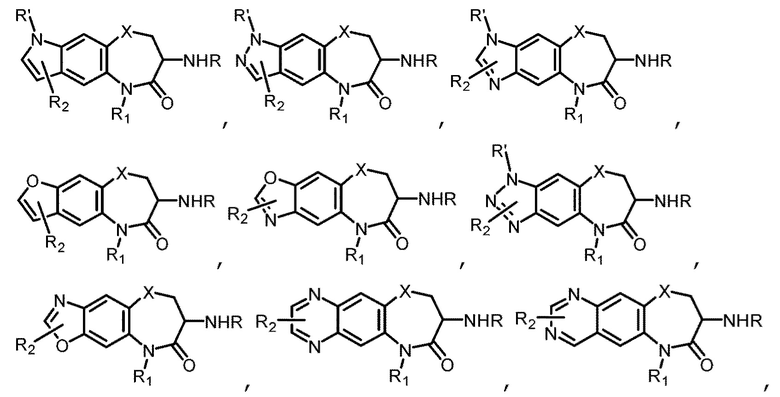
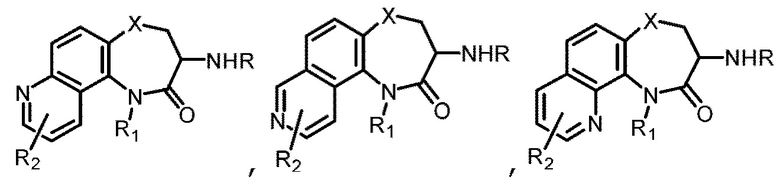 и
и 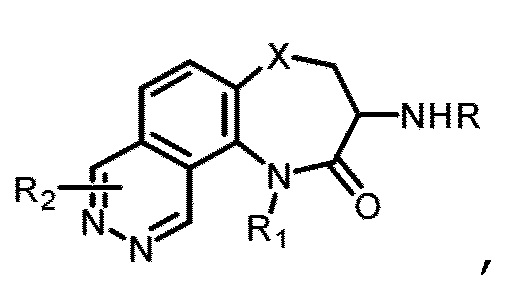
где R' выбран из Н, Boc, SEM, (C1-C4) алкила и бензила.
[0131] В некоторых вариантах осуществления промежуточное соединение Формулы (II) выбрано из группы, состоящей из:
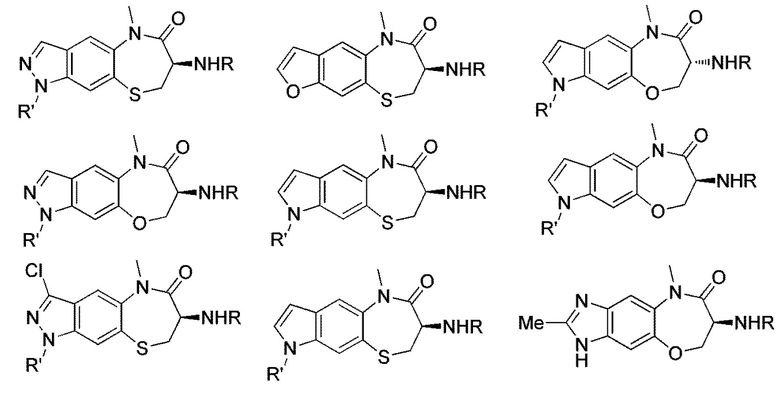
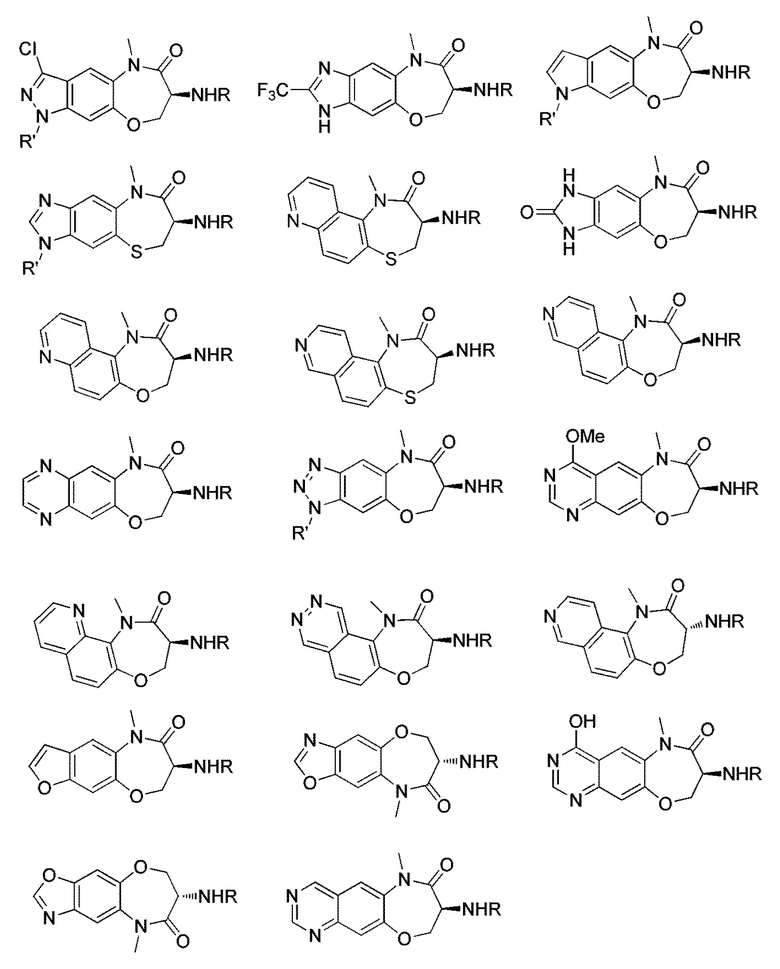
где R является Н, Boc или ТФУ, и R' выбран из Н, Boc или SEM.
[0132] В некоторых вариантах осуществления соединение Формулы (II) согласно настоящей заявке может быть получено по схеме, показанной ниже:
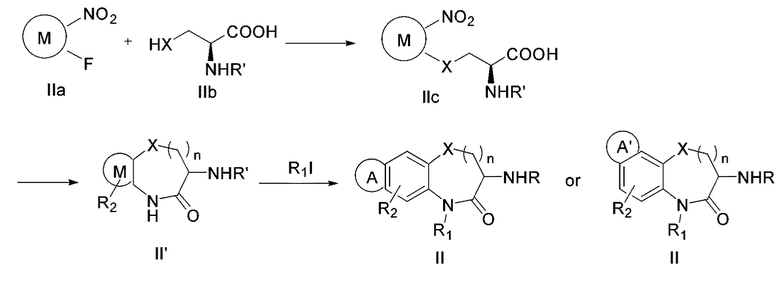
которая включает:
(a) реакцию соединения Формулы IIa с соединением Формулы IIb в инертном растворителе в присутствии основания с получением соединения Формулы IIc;
(b) восстановление нитрогруппы в соединении Формулы IIc в спиртовом растворителе под атмосферой водорода и/или в присутствии металлического катализатора с последующей циклизацией в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы II'; и
(c) реакцию соединения Формулы II' с R1I в присутствии основания с получением соединения Формулы II.
[0133] В некоторых вариантах осуществления основание в Стадии (а) выбрано из карбоната цезия, карбоната калия, NaOH, NaH, н-BuLi, KHMDS или их комбинации.
[0134] В некоторых вариантах осуществления инертный растворитель в Стадиях (а) и (b) выбран из ДМФА, ДМСО, ацетонитрила, ТГФ или их комбинации.
[0135] В некоторых вариантах осуществления Стадию (а) проводят при температуре от -20°С до 100°С.
[0136] В некоторых вариантах осуществления спиртовой растворитель в Стадии (b) выбран из метанола, этанола, изопропанола, н-пропанола, н-бутанола, изобутанола или их комбинации.
[0137] В некоторых вариантах осуществления металлический катализатор в Стадии (b) представляет собой Pd/C.
[0138] В некоторых вариантах осуществления конденсирующий реагент в Стадии (b) выбран из группы, состоящей из HATU, DCC, HOBt, HBTU, HCTU, TBTU, TSTU, TNTU, EDCI, CDI, РуВОР или их комбинации.
[0139] В некоторых вариантах осуществления основание в Стадии (с) выбрано из DIEA, триэтиламина, DMAP, пиридина или их комбинации.
[0140] В некоторых вариантах осуществления соединение Формулы (II) согласно настоящей заявке может быть получено по схеме, показанной ниже:
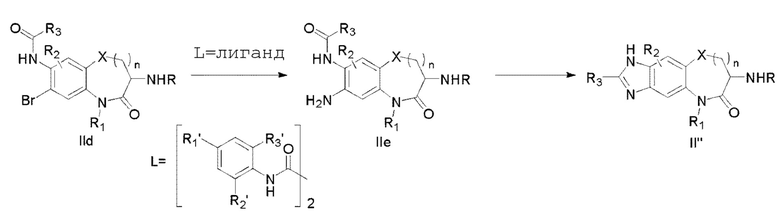
которая включает
(a) подвергание соединения Формулы IId реакции сочетания с водным аммиаком в инертном растворителе в присутствии медного катализатора и лиганда L с получением соединения Формулы IIe; и
(b) подвергание соединения Формулы IIe дегидратированию и реакции замыкания цикла в кислотных или основных условиях с получением соединения Формулы II''.
[0141] В некоторых вариантах осуществления R3 представляет собой метил или трифторметил, R1', R2' и R3' могут быть Н, метилом, метокси, фенилом, бензилом, фенокси, нафтилом и т.д., и другие группы имеют определенное выше значение.
[0142] В некоторых вариантах осуществления лиганд L в Стадии (а) выбран из группы, состоящей из:
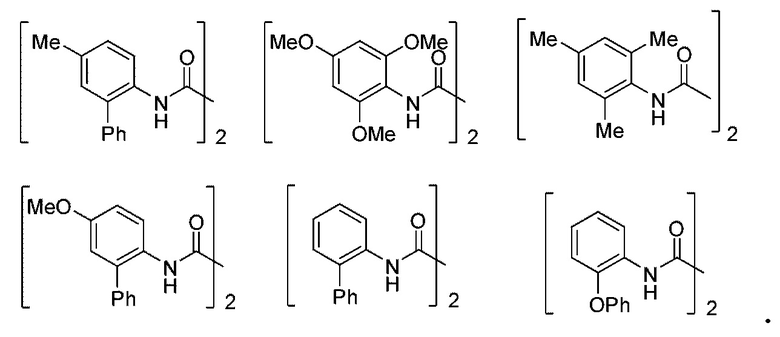
[0143] В некоторых вариантах осуществления инертный растворитель в Стадии (а) выбран из ДМСО, ДМФА, 1,4-диоксана или их комбинации.
[0144] В некоторых вариантах осуществления медный катализатор в Стадии (а) выбран из CuI, CuCN, CuBr, CuCl, Cu2O или их комбинации.
[0145] В некоторых вариантах осуществления весовое отношение водного аммиака к инертному растворителю в Стадии (а) составляет от 1:10 до 1:1.
[0146] В некоторых вариантах осуществления количество медного катализатора в Стадии (а) составляет 0,5-20 мол.% относительно соединения Формулы IId.
[0147] В некоторых вариантах осуществления количество лиганда L в Стадии (а) составляет 0,5-30 мол.% относительно соединения Формулы IId.
[0148] В некоторых вариантах осуществления Стадию (а) проводят при температуре от 40°С до 150°С.
[0149] В некоторых вариантах осуществления кислотные условия в Стадии (b) означают, что реакционная система содержит кислоту, выбранную из группы, состоящей из уксусной кислоты, 15% серной кислоты или их комбинации.
[0150] В некоторых вариантах осуществления основные условия в Стадии (b) означают, что реакционная система содержит основание, выбранное из группы, состоящей из карбоната натрия, карбоната калия, карбоната цезия, карбоната кальция, фосфата калия или их комбинации.
[0151] В некоторых вариантах осуществления Стадию (b) проводят при температуре от комнатной температуры (10°С-40°С) до 80°С, например, от 10°С до 80°С, от 15°С до 80°С, от 20°С до 80°С, от 25°С до 80°С, от 30°С до 80°С, от 35°С до 80°С или от 40°С до 80°С.
[0152] Примерное соединение Формулы (II) может быть получено согласно схеме, показанной ниже:
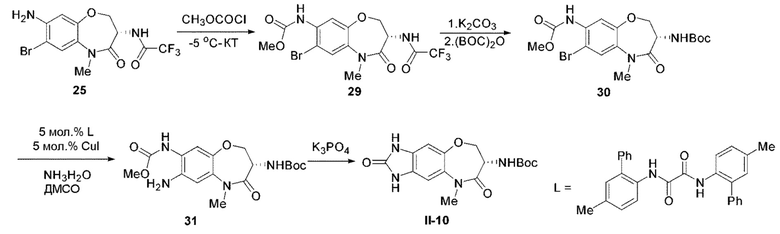
где Соединение 25 подвергают реакции с метиломхлорформиатом в дихлорметане в основных условиях при температуре от -5°С до комнатной температуры с получением Промежуточного соединения 29. Трифторацетильную защитную группу Промежуточного соединения 29 удаляют в основных условиях, а затем первичную аминогруппу защищают Вос-группой путем реакции с Boc ангидридом, получая, таким образом. Соединение 30. Затем в инертном растворителе, в присутствии медного катализатора и лиганда L, Соединение 30 подвергают реакции сочетания с водным аммиаком с получением Соединения 31. После этого проводят реакцию дегидратирования и циклизации при нагревании в основных условиях с получением соединения Формулы II-10.
[0153] Применение соединения
[0154] В одном аспекте настоящей заявки предложено соединение Формулы (I) или его фармацевтически приемлемая соль, способные ингибировать активность киназы RIP1.
[0155] Таким образом, в другом аспекте настоящей заявки предложен способ ингибирования киназы RIP1 у субъекта, включающий введение субъекту эффективного количества соединения согласно настоящей заявке или его фармацевтически приемлемой соли.
[0156] В некоторых вариантах осуществления соединение согласно настоящей заявке может ингибировать активность киназы RIP1 со значением IC50 0,1 нМ-1000 мкМ, 1 нМ-500 мкМ, 0,1 нМ-100 мкМ, 0,1 нМ-80 мкМ, 0,1 нМ-50 мкМ, 0,1 нМ-40 мкМ, 0,1 нМ-30 мкМ, 0,1 нМ-20 мкМ, 0,1 нМ-10 мкМ, 0,1 нМ-5 мкМ, 0,1 нМ-1 мкМ, 0,1 нМ-0,5 мкМ, 0,1 нМ-0,1 мкМ, 0,1 нМ-0,05 мкМ, 0,1 нМ-40 нМ, 0,1 нМ-30 нМ, 0,1 нМ-20 нМ, 0,1 нМ-10 нМ, 0,1 нМ-5 нМ, 0,1 нМ-4 нМ, 0,1 нМ-3 нМ, 0,1 нМ-2 нМ, 0,1 нМ-1 нМ и 0,1 нМ-0,5 нМ.
[0157] Таким образом, в другом аспекте соединение согласно настоящей заявке или его фармацевтически приемлемая соль может применяться в производстве лекарственного средства для ингибирования активности киназы RIP1.
[0158] В еще одном аспекте соединение согласно настоящей заявке или его фармацевтически приемлемая соль может применяться в производстве лекарственного средства для предупреждения или лечения заболеваний, связанных с киназой RIP1.
[0159] В еще одном аспекте соединение согласно настоящей заявке или его фармацевтически приемлемая соль может применяться в производстве лекарственного средства для предупреждения или лечения заболеваний или нарушений, вызванных программируемым некрозом клеток.
[0160] Фармацевтическая композиция
[0161] В одном аспекте настоящей заявки предложена фармацевтическая композиция, включающая соединение согласно настоящей заявке или его фармацевтически приемлемую соль.
[0162] В некоторых вариантах осуществления фармацевтическая композиция согласно настоящей заявке включает больше одного соединения согласно настоящей заявке или его фармацевтически приемлемой соли.
[0163] В некоторых вариантах осуществления фармацевтическая композиция согласно настоящей заявке включает одно или более соединений согласно настоящей заявке или их фармацевтически приемлемых солей и фармацевтически приемлемый носитель.
[0164] Фармацевтически приемлемые носители являются стандартными фармацевтическими носителями в данной области и могут быть получены способами, известными в области фармацевтики. В некоторых вариантах осуществления соединения согласно настоящей заявке или их фармацевтически приемлемых соли могут быть смешаны с фармацевтически приемлемыми носителями для получения фармацевтических композиций.
[0165] Термин "фармацевтически приемлемый" при использовании в настоящем документе означает, что соединение, материал, композиция и/или лекарственная форма являются пригодными для контакта с тканями человека или животных и при этом не вызывают чрезмерные токсические эффекты, раздражение, аллергические реакции, другие проблемы или осложнения и демонстрируют разумное отношение выгоды/риска. В некоторых вариантах осуществления фармацевтически приемлемые соединения, материалы, композиции и/или лекарственные формы одобрены регулирующими органами (например. Управление по контролю качества пищевых продуктов и лекарственных средств США, Национальное управление по контролю качества медицинской продукции Китая и Европейское агентство по контролю качества лекарственных средств) или перечислены в сертифицированных справочниках фармакопеи (например. Фармакопее США, Китайской фармакопее и Европейской фармакопее) для применения у животных, в особенности человека.
[0166] Термин "фармацевтически приемлемый носитель" при использовании в настоящем документе относится к фармацевтически приемлемому материалу, композиции или носителю, такому как жидкий или твердый наполнитель, разбавитель, вспомогательное вещество, растворитель или упаковочный материал, применяемому в переноса или доставки соединения согласно настоящей заявке или его фармацевтически приемлемой соли из одного положения, физиологической жидкости, ткани, органа (внутреннего или наружного) или части тела в другое положение, физиологическую жидкость, ткань, орган или часть тела. Фармацевтически приемлемый носитель может быть растворителем, разбавителем, вспомогательным веществом или другими материалами, которые могут использоваться в контакте с тканями животных без чрезмерной токсичности или нежелательных реакций. Примеры фармацевтически приемлемых носителей включают, без ограничения перечисленными, углеводы, крахмал, целлюлозу, солод, трагакант, желатин, раствор Рингера, альгиновую кислоту, изотонический раствор хлорида натрия и буферы, и т.д. Фармацевтически приемлемые носители, которые могут применяться в настоящей заявке, включают носители, известные в данной области, такие как раскрытые в "Remington Pharmaceutical Sciences" Mack Pub. Co., New Jersey (1991).
[0167] Фармацевтическая композиция также может содержать фармацевтически приемлемые добавки, необходимые для приближенного воспроизведения физиологических условий, включающие, без ограничения перечисленными, например, фармацевтически приемлемую жидкость, гель или твердые носители, водные среды (например, хлорид натрия для инъекций, раствор Рингера для инъекций, изотонический раствор декстрозы для инъекций, стерильную воду для инъекций или раствор декстрозы и лактатированный раствор Рингера для инъекций), неводную среду (например, жирное масло растительного происхождения, хлопковое масло, кукурузное масло, кунжутное масло или арахисовое масло), противомикробные вещества, изотонические вещества (такие как хлорид натрия или глюкозу), буферы (например, фосфатный или цитратный буферы), антиоксиданты (например, бисульфат натрия), анестетики (например, прокаина гидрохлорид), суспендирующие вещества/дисперсанты (например, карбоксиметилцеллюлозу натрия, гидроксипропилметилцеллюлозу или поливинилпирролидон), хелатообразователи (например, ЭДТА (этилендиаминтетрауксусную кислоту) или ЭГТА (этиленгликоль бис(2-аминоэтиловый эфир) тетрауксусной кислоты)), эмульгаторы (например, полисорбат 80 (Tween-80)), разбавители, ароматизаторы, вкусовые добавки, подсластители, адъюванты, вспомогательные добавки или нетоксичные вспомогательные вещества, другие компоненты, известные в данной области, или различные комбинации вышеперечисленного. Подходящие компоненты могут включать, например, наполнители, связующие вещества, разрыхлители, буферы, консерванты, смазывающие вещества, вкусовые добавки, загустители, красители или эмульгаторы.
[0168] Форма фармацевтической композиции зависит от множества факторов, включая, например, путь введения, тяжесть заболевания или водимую дозу и т.д.
[0169] В некоторых вариантах осуществления фармацевтическая композиция может быть изготовлена для введения субъекту подходящим путем, включая, помимо прочего, пероральный путь, инъекцию (такую как внутривенная инъекция, внутримышечная инъекция, подкожная инъекция, внутрикожная инъекция, внутрисердечная инъекция, интратекальная инъекция, внутриплевральная инъекция и внутрибрюшинная инъекция и т.д.), пути чресслизистого введения (такие как интраназальное введение, внутриротовое введение и т.д.), подъязычный путь, ректальный путь, трансдермальный путь, внутриглазной путь и легочный путь введения. В зависимости от требуемого способа введения фармацевтическая композиция может быть изготовлена в виде таблеток, капсул, пилюль, драже, порошков, гранул, облаток, таблеток для рассасывания, суппозиториев, суспензий, эмульсий, сиропов, аэрозолей (в твердом виде или в жидкой среде), спреев, мазей, паст, пластырей, кремов, лосьонов, гелей и средств для ингаляции и т.д.
[0170] В некоторых вариантах осуществления фармацевтическая композиция является препаратом для перорального введения. Препарат для перорального введения включает, без ограничения, капсулы, саше, пилюли, таблетки, таблетки для рассасывания (основой для добавления вкусовых добавок часто служит сахароза, гуммиарабик или трагакант), порошки, гранулы, водные или неводные растворы или суспензии, эмульсии типа вода в масле или масло в воде, настойки или сиропы, пастилки (где подходящие инертные основы включают, например, желатин и глицерин, или сахарозу или гуммиарабик) и/или ополаскиватели для полости рта или их аналоги.
[0171] Твердый препарат для перорального введения (такой как капсулы, таблетки, пилюли, драже, порошки и гранулы, и т.д.) включает действующее вещество и одну или более фармацевтически приемлемые вспомогательных добавок, таких как цитрат натрия или фосфат дикальция, и/или следующие вещества: (1) наполнители или добавки, такие как крахмал, лактозу, сахарозу, глюкозу, маннит и/или кремниевую кислоту; (2) связующие вещества, такие как карбоксиметилцеллюлозу, альгинат, желатин, поливинилпирролидон, сахарозу и/или гуммиарабик; (3) смачивающие вещества, такие как глицерин; (4) разрыхлители, такие как агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновую кислоту, некоторые силикаты и/или карбонат натрия; (5) растворы замедлителей всасывания, таких как парафин; (6) ускорители всасывания, такие как четвертичные соединения аммония; (7) смазывающие вещества, такие как ацетол и глицерилмоностеарат; (8) абсорбенты, такие как каолин и бентонит; (9) скользящие вещества, такие как тальк, стеарат кальция, стеарат магния, твердый полиэтиленгликоль, додецилсульфат натрия и их смеси; и (10) красители.
[0172] Жидкий препарат для перорального введения включает фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и настойки. В дополнение к действующему веществу жидкая лекарственная форма также может содержать обычно используемый инертный разбавитель, например, воду или другие растворители, солюбилизаторы и эмульгаторы, такие как этанол, изопропанол, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутандиол, масла (в частности, хлопковое масло, арахисовое масло, кукурузное масло, оливковое масло, касторовое масло и кунжутное масло), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоль и сложный эфир сорбита и жирной кислоты или смесь двух или более из них. В дополнение к инертному разбавителю в жидкий препарат для перорального введения также могут быть добавлены адъюванты, такие как смачивающие вещества, эмульгирующие и суспендирующие вещества, подсластители, ароматизаторы, пигменты, отдушки и консерванты.
[0173] В некоторых вариантах осуществления фармацевтическая композиция является препаратом для инъекций. Препарат для инъекций включает стерильные водные растворы, дисперсии, суспензии или эмульсии. В любых возможных случаях препарат для инъекций должен быть стерильным и находиться в жидком состоянии для облегчения инъекции, должен оставаться стабильным в условиях производства и хранения и должен быть устойчивым к контаминации микроорганизмами (например, бактериями и грибами). Носитель может быть растворителем или дисперсионной средой, включающими, например, воду, этанол, полигидроксисоединения (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль и т.д.) и их подходящие смеси и/или растительные масла. Препарат для инъекций должен обладать надлежащей текучестью, которую можно поддерживать различными способами, например, при использовании покрытий, таких как лецитин, с помощью поверхностно-активных веществ и т.д. Устойчивость к контаминации микроорганизмами может достигаться путем добавления различных антибактериальных и противогрибковых средств (например, парабена, хлорбутанола, фенола, сорбиновой кислоты, тимеросала и т.д.).
[0174] В некоторых вариантах осуществления фармацевтическая композиция является препаратом в форме спрея для перорального введения или препаратом в форме назального спрея. Препараты в форме спрея включают, без ограничения перечисленными, водные аэрозоли, неводные суспензии, липосомные препараты или препараты твердых частиц и т.д. Водные аэрозоли получают путем приготовления водного раствора или суспензии действующего вещества с обычным фармацевтически приемлемым наполнителем и стабилизатором. Носитель и стабилизатор могут быть различными в зависимости от потребностей конкретного соединения и обычно включают неионогенные поверхностно-активные вещества (серии Tween или полиэтиленгликоль), олеиновую кислоту, лецитин, аминокислоты, такие как глицин, буферы, соли, сахар или сахароспирты. Аэрозоли обычно изготавливают из изотонических растворов и могут доставлять с помощью небулайзера.
[0175] Фармацевтическая композиция может быть изготовлена для обеспечения быстрого высвобождения, замедленного высвобождения или отсроченного высвобождения активного ингредиента после введения субъекту. В некоторых вариантах осуществления фармацевтическая композиция может быть изготовлена в форме с замедленным высвобождением. При использовании в настоящем документе термин "форма с замедленным высвобождением" означает, что действующее вещество высвобождается из фармацевтической композиции в течение более длительного периода времени (пролонгированное высвобождение) или в определенном участке (контролируемое высвобождение), в результате чего оно биологически всасывается в организме субъекта (например, в желудочно-кишечном тракте субъекта). В некоторых вариантах осуществления более длительный период времени может составлять от 1 до 24 часов, от 2 до 12 часов, от 3 до 8 часов, от 4 до 6 часов, от 1 до 2 дней или больше. В некоторых вариантах осуществления более длительный период времени может составлять по меньшей мере приблизительно 4 часа, по меньшей мере приблизительно 8 часов, по меньшей мере приблизительно 12 часов или по меньшей мере приблизительно 24 часа. В некоторых вариантах осуществления фармацевтическая композиция может быть изготовлена в форме таблетки. Например, скорость высвобождения действующего вещества можно регулировать не только действующим веществом, которое растворяется в желудочно-кишечном соке независимо от рН, и затем диффундирует из таблетки или пилюли, но также зависит от физического процесса распада и растворения таблетки. В некоторых вариантах осуществления полимерные материалы, раскрытые в "Medical Applications of Controlled Release", Langer and Wise eds, CRC Pres., Boca Raton, Florida (1974), "Controlled Drug Bioavailability", Drug Product Design and Performance, Smolen and Ball eds, Wiley, New York (1984), Ranger and Peppas, 1983, J Macromol. Sci. Rev. Macromol Chem. 23:61, Levy et al., 1985, Science 228:190, During et al., 1989, Ann. Neurol. 25:351, и Howard et al., 1989, J. Neurosurg. 71:105, могут использоваться для замедленного высвобождения.
[0176] В некоторых вариантах осуществления фармацевтическая композиция включает 1-99% по весу соединения Формулы I или его фармацевтически приемлемой соли. В некоторых вариантах осуществления фармацевтическая композиция включает 5-99% по весу, 10-99% по весу, 15-99% по весу, 20-99% по весу, 25-99% по весу, 30-99% по весу, 35-99% по весу, 40-99% по весу, 45-99% по весу, 50-99% по весу, 55-99% по весу, 60-99% по весу или 65-99% по весу соединения Формулы I или его фармацевтически приемлемой соли.
[0177] В некоторых вариантах осуществления фармацевтическая композиция может быть изготовлена в виде стандартной лекарственной формы, которая содержит 0,01-1000 мг, 0,01-900 мг, 0,01-800 мг, 0,01-700 мг, 0,01-600 мг, 0,01-500 мг, 0,01-400 мг, 0,01-300 мг, 0,01-200 мг, 0,01-100 мг, 0,01-50 мг, 0,05-900 мг, 0,05-800 мг, 0,05-700 мг, 0,05-600 мг, 0,05-500 мг, 0,05-400 мг, 0,05-300 мг, 0,05-200 мг, 0,05-100 мг, 0,05-50 мг, 0,1-1000 мг, 0,1-900 мг, 0,1-800 мг, 0,1-700 мг, 0,1-600 мг, 0,1-500 мг, 0,1-400 мг, 0,1-300 мг, 0,1-200 мг, 0,1-100 мг или 0,1-50 мг соединения Формулы I или его фармацевтически приемлемой соли. Термин "стандартная лекарственная форма" при использовании в настоящем документе относится к физически дискретной единице, подходящей в качестве единицы дозы, при этом каждая такая единица содержит заданное количество активного ингредиента, вычисленное так, чтобы производить требуемый терапевтический эффект, в сочетании с подходящим фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включая таблетки с риской или оболочкой), капсулы, пилюли, порошки, облатки, суппозитории, растворы или суспензии для инъекций и подобные лекарственные формы и их разделенная многодозовая форма. Конечно, суточная доза соединения согласно настоящей заявке будет изменяться в зависимости от используемого соединения, способа введения, требуемого лечения и конкретного заболевания, подвергаемого лечению. В некоторых вариантах осуществления суточная доза соединения согласно настоящей заявке составляет 0,01-200 мг/кг массы тела, вводимые однократно, или 0,01-100 мг/кг мг/кг массы тела, вводимые отдельно. Независимо от способа введения оптимальная доза для человека зависит от определенного лечения. Обычно, начиная с малой дозы, дозу постепенно повышают, пока не будет определена наиболее подходящая доза.
[0178] Комбинация лекарственных средств
[0179] В одном аспекте настоящей заявки предложена комбинация лекарственных средств, включающая соединение согласно настоящей заявке или его фармацевтически приемлемую соль и по меньшей мере одно дополнительное действующее вещество.
[0180] В некоторых вариантах осуществления комбинация лекарственных средств применяется для лечения или предупреждения опосредованных киназой RIP1 заболеваний или нарушений или заболеваний или нарушений, вызванных программируемым некрозом клеток.
[0181] В некоторых вариантах осуществления по меньшей мере одно дополнительное действующее вещество включает, без ограничения перечисленными, тромболитическое средство, тканевой активатор плазминогена, антикоагулянт, ингибитор агрегации тромбоцитов, противомикробное средство (антибиотики, антибиотики широкого спектра действия, β-лактам, противомикобактериальные средства, бактерицидные антибиотики и терапия против MRSA), бета-агонист длительного действия, комбинацию ингаляционного кортикостероида и бета-агониста длительного действия, бета-агонист кратковременного действия, модулятор лейкотриенов, антитела против IgE, метилксантиновый бронходилататор, ингибитор тучных клеток, ингибитор протеинтирозинкиназы, антагонист рецепторов простагландина CRTH2/D-типа, аэрозоль адреналина для ингаляции, ингибитор фосфодиэстеразы, комбинацию ингибитора фосфодиэстеразы-3 и ингибитора фосфодиэстеразы-4, ингаляционное антихолинергическое средство длительного действия, антагонист мускариновых рецепторов, антагонист мускариновых рецепторов длительного действия, низкие дозы стероидов, ингаляционный кортикостероид, пероральный кортикостероид, кортикостероид для наружного применения, антитимоцитарный глобулин, талидомид, хлорамбуцил, блокатор кальциевых каналов, увлажняющее средство для наружного применения, ингибитор АПФ, ингибитор обратного захвата серотонина, ингибиторы рецепторов эндотелина-1, противофиброзное средство, ингибитор протонной помпы, регулятор трансмембранной проводимости при муковисцидозе, муколитики, панкреатин, бронходилататор, интравитреальную инъекцию, ингибитор против фактора роста эндотелия сосудов, цилиарный нейротрофический фактор роста, трехвалентную инактивированную вакцину против гриппа (IIV3), четырехвалентную инактивированную вакцину против гриппа (IIV4), трехвалентную рекомбинантную вакцину против гриппа, четырехвалентную живую аттенуированную вакцину против гриппа, противовирусное средство, инактивированную вакцину против гриппа, цилиарный нейротрофический фактор роста, агент переноса гена, иммуномодулятор, ингибитор кальциневрина, интерферон γ, антигистаминное средство, ингибитор PD-1, ингибитор PD-L1, моноклональное антитело, поликлональное антитело против Т-клеток, лошадиное антитело против тимоцитарного гамма-глобулина, кроличье антитело против тимоцитарного глобулина, антагонист против CD40, ингибитор JAK и мышиное мАт против TCR.
[0182] В некоторых вариантах осуществления соединение согласно настоящей заявке или его фармацевтически приемлемую соль и по меньшей мере одно дополнительное действующее вещество вводят отдельно, одновременно или последовательно, в любом порядке.
[0183] Способы лечения и показания
[0184] Соединение согласно настоящей заявке или его фармацевтически приемлемая соль способны ингибировать активность киназы RIP1. Таким образом, в одном аспекте настоящей заявки предложен способ лечения или предупреждения опосредованных киназой RIP1 заболеваний или нарушений или заболеваний или нарушений, вызванных программируемым некрозом клеток, включающий введение субъекту эффективного количества соединения согласно настоящей заявке или его фармацевтически приемлемой соли, или фармацевтической композиции, или комбинации лекарственных средств согласно настоящей заявке.
[0185] Термин "субъект" при использовании в настоящем документе относится к организму, ткани или клетке. Субъекты могут включать субъектов-людей для медицинских целей (например, диагностики и/или лечения существующих состояний или заболеваний или профилактического лечения с целью предотвращения возникновения состояний или заболеваний) или субъектов-животных для медицинских или ветеринарных целей или целей разработки. Субъекты также включают образцы из культуры тканей, культуры клеток, воссоздания органов и получения стволовых клеток, и т.д. Подходящие субъекты-животные включают млекопитающих и птиц. Термин "млекопитающее" при использовании в настоящем документе включает, без ограничения, приматов (таких как люди, обезьяны и человекообразные обезьяны, и т.д.), бычьих (такие как быки и т.д.), овец (таких как овцы, козы и т.д.), свиней, лошадей, кошек, собак, кроликов, грызунов (например, мышей, крыс и т.д.) и т.п. Термин "птицы" при использовании в настоящем документе включает, без ограничения, куриц, уток, гусей, перепелок, индеек и фазанов, и т.д. В некоторых вариантах осуществления субъект является млекопитающим или клеткой млекопитающего. В некоторых вариантах осуществления субъект является человеком или клеткой человека. Субъекты-люди включают, без ограничения перечисленными, плод, новорожденного, грудного ребенка, подростка и взрослых субъектов. Кроме того, "субъект" может включать пациентов, страдающих или подозреваемых на наличие определенного состояния или заболевания. Таким образом, в настоящем документе термины "субъект" и "пациент" используются попеременно. Субъект также может относиться к клеткам в лаборатории или биотехнологической среде в тестах.
[0186] Термин "эффективное количество" при использовании в настоящем документе относится к количеству лекарственного средства или фармацевтического средства, которое вызывает биологическую или медицинскую реакцию, например требуемую исследователю или клиническому врачу, в ткани, системе, у животного или человека. Кроме того, термин "терапевтически эффективное количество" означает любое количество, которое приводит к улучшенному лечению, заживлению, предотвращению или облегчению заболевания, нарушения или побочного эффекта, или уменьшению развития заболевания или нарушения, по сравнению с соответствующим субъектом, который не получает такое количество. Термин также включает, в рамках своего объема, количество, эффективное для улучшения нормальных физиологических функций. Терапевтически эффективное количество одного или более соединений согласно настоящей заявке известно специалисту или может быть легко определено стандартными методами, известными в данной области.
[0187] В некоторых вариантах осуществления опосредованные киназой RIP1 заболевания или нарушения или заболевания или нарушения, вызванные программируемым некрозом клеток, выбраны из группы, состоящей из воспалительного заболевания кишечника, болезни Крона, язвенного колита, псориаза, дегенеративного заболевания сетчатки, отслоения сетчатки, пигментного ретинита, макулодистрофии, панкреатита, атопического дерматита, ревматоидного артрита, спондилоартрита, подагры, SoJIA, системной красной волчанки, синдрома Шегрена, системной склеродермии, антифосфолипидного синдрома, васкулита, остеоартроза, неалкогольного стеатогепатита, алкогольного стеатогепатита, аутоиммунного гепатита, гепатита В, гепатита С, аутоиммунного гепатобилиарного заболевания, первичного склерозирующего холангита, отравления ацетаминофеном, гепатотоксичности, нефрита, целиакии, аутоиммунной ИТП, отторжения трансплантата, ишемического-реперфузионного повреждения паренхиматозных органов, сепсиса, синдрома системного воспалительного ответа, нарушения мозгового кровообращения, инфаркта миокарда, болезни Хантингтона, болезни Альцгеймера, болезни Паркинсона, аллергического заболевания, астмы, атопического дерматита, рассеянного склероза, диабета I типа, гранулемы Вегенера, легочного саркоидоза, болезни Бехчета, синдрома лихорадки, связанной с интерлейкин-1-превращающим ферментом, хронической обструктивной болезни легких, периодического синдрома, связанного с рецептором фактора некроза опухоли, периодонтита, инсульта, ожогов, ожогового шока, черепно-мозговой травмы, атеросклероза, повреждения почек, вызванного цисплатином, острого повреждения почек, панкреатита, хронического заболевания почек, острого респираторного дистресс-синдрома, хронической обструктивной болезни легких, болезни Гоше, болезни Нимана-Пика, острой печеночной недостаточности, онкологических заболеваний (например, рака поджелудочной железы), бактериальной инфекции, повреждения, вызванного курением, кистозного фиброза, мутации ключевого регуляторного гена NF-κВ, дефицита гемм-окисленной убиквитин-лигазы-1 IRP2, синдрома дефицита комплекса сборки линейных цепей убиквитина, гемобластных злокачественных новообразований, злокачественных новообразований солидных органов, гриппа, стафилококковых инфекций, микобактериальных инфекций, лизосомных болезней накопления, GM2 ганглиозидоза, а-маннозидоза, аспартилглюкозаминурии, болезни накопления эфиров холестерина, хронической недостаточности гексозаминидазы А, цистиноза, болезни Данона, болезни Фабри, болезни Фарбера, фукозидоза, галактосиалидоза, GM1 ганглиозидоза, накопления муколипидов, детской болезни накопления свободной сиаловой кислоты, ювенильной недостаточности гексозаминидазы А, болезни Краббе, дефицита лизосомной кислой липазы, метахроматической лейкодистрофии, мукополисахаридоза, множественной сульфатазной недостаточности, нейронального цероидного липофусциноза, болезни Помпе, пикнодизостоза, болезни Сандхоффа, болезни Шиндлера, болезни Салла, болезни Тея-Сакса, болезни Вольмана, синдрома Стивенса-Джонсона и токсического эпидермального некролиза.
[0188] Настоящая заявка также включает, без ограничения, следующие варианты осуществления:
[0189] Пункт 1. Соединение Формулы (I) или его оптический изомер, таутомер или фармацевтически приемлемая соль:
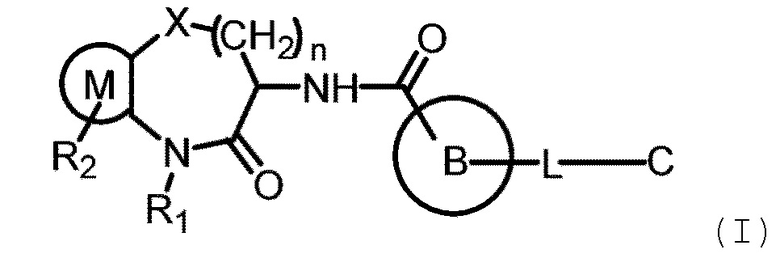
где
X представляет собой О, S или СН2;
кольцо М имеет структуру 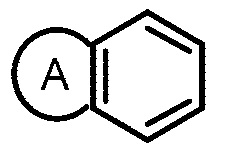 , где кольцо А выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила, где кольцевой скелет гетероарильной группы или гетероциклильной группы содержит один или более гетероатомов, выбранных из N, О или S;
, где кольцо А выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила, где кольцевой скелет гетероарильной группы или гетероциклильной группы содержит один или более гетероатомов, выбранных из N, О или S;
n выбрано из 1, 2 или 3;
В выбрано из группы, состоящей из замещенного или незамещенного фенила, замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила;
L выбрано из группы, состоящей из О, S, NH, N(СН3), замещенного или незамещенного C1-C6 алкилена, замещенного или незамещенного C1-C6 алкилен-O-, замещенного или незамещенного C1-С6 алкилен-NH-, (замещенного или незамещенного C1-C6 алкилен)2-N-, замещенного или незамещенного С3-С6 алкенилена и замещенного или незамещенного С3-С6 алкенилен-O-;
С выбрано из группы, состоящей из Н, замещенного или незамещенного (С3-С6) циклоалкила, замещенного или незамещенного фенила, замещенного или незамещенного 5-6-членного гетероарила и замещенного или незамещенного 5-6-членного гетероциклила;
r1 выбран из Н или замещенного или незамещенного C1-C6 алкила;
R2 представляет любой один или более заместителей в фенильном кольце, выбранных из группы, состоящей из Н, галогена, замещенного галогеном или незамещенного C1-C6 алкила и C1-C6 ацила;
где, если не указано иное, "замещенный" относится к замещению одного или более атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена, циано, алкила, ацила, сульфонила, гидроксила, амино, бензила, оксо (=O), (C1-C4) алкила, галоген (C1-C4) алкила, (C1-C4) алкокси, галоген(C1-C4)алкокси, нитро и (C1-C4) алкил С (O)-; и
конфигурация каждого хирального центра независимо является R-конфигурацией или S-конфигурацией.
[0190] Пункт 2. Соединение согласно Пункту 1, где С представляет собой замещенный или незамещенный фенил или замещенный или незамещенный 5-6-членный гетероарил.
[0191] Пункт 3. Соединение согласно Пункту 1, где L представляет собой замещенный или незамещенный C1-C6 алкилен.
[0192] Пункт 4. Соединение согласно Пункту 1, где кольцо А представляет собой 5-членное кольцо, содержащее один или более атомов N на циклическом скелете.
[0193] Пункт 5. Способ получения соединения согласно Пункту 1, включающий Стадию (а) или (b):
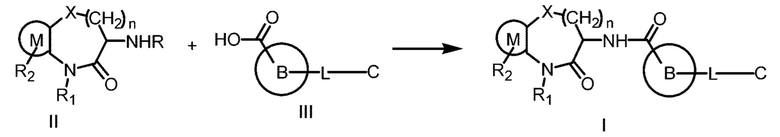
(а) реакции соединения Формулы II с соединением Формулы III в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы I, где R представляет собой Н; или
(b) удаления защитной группы аминогруппы из соединения Формулы II в кислотных условиях и затем реакции с соединением Формулы III в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы I, где R представляет собой защитную группу аминогруппы (предпочтительно Boc), и другие группы имеют значение, определенное в Пункте 1.
[0194] Пункт 6. Фармацевтическая композиция, включающая: (а) терапевтически эффективное количество соединения Формулы I или его оптического изомера, таутомера или фармацевтически приемлемой соли или их комбинации; и (b) фармацевтически приемлемый носитель.
[0195] Пункт 7. Применение соединения Формулы I согласно Пункту 1 или его фармацевтически приемлемой соли, рацемата, R-изомера, S-изомера или их смеси в производстве фармацевтической композиции для лечения или предупреждения опосредованных киназой RIP1 заболеваний или нарушений; или в производстве фармацевтической композиции для лечения или предупреждения заболеваний или нарушений, вызванных программируемым некрозом клеток.
[0196] Пункт 8. Применение согласно Пункту 7, где заболевания или нарушения выбраны из группы, состоящей из воспалительного заболевания кишечника, болезни Крона, неспецифического язвенного колита, псориаза, отслоения сетчатки, пигментного ретинита, макулодистрофии, панкреатита, атопического дерматита, ревматоидного артрита, спондилоартрита, подагры, SoJIA, системной красной волчанки, синдрома Шегрена, системной склеродермии, антифосфолипидного синдрома, васкулита, остеоартроза, неалкогольного стеатогепатита, алкогольного стеатогепатита, аутоиммунного гепатита, аутоиммунного гепатобилиарного заболевания, первичного склерозирующего холангита, отравления ацетаминофеном, гепатотоксичности, нефрита, целиакии, аутоиммунной ИТП, отторжения трансплантата, ишемического-реперфузионного повреждения паренхиматозных органов, сепсиса, синдрома системного воспалительного ответа, нарушения мозгового кровообращения, инфаркта миокарда, болезни Хантингтона, болезни Альцгеймера, болезни Паркинсона, аллергического заболевания, астмы, атопического дерматита, рассеянного склероза, диабета I типа, гранулемы Вегенера, легочного саркоидоза, болезни Бехчета, синдрома лихорадки, связанной с интерлейкин-1-превращающим ферментом, хронической обструктивной болезни легких, периодического синдрома, связанного с рецептором фактора некроза опухоли и периодонтита.
[0197] Пункт 9. Промежуточное соединение Формулы II ниже:
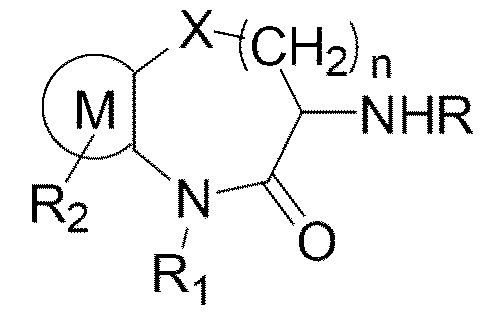
где R выбран из группы, состоящей из Н и защитной группы аминогруппы (предпочтительно Boc); и другие группы имеют значение, определенное в пункте 1.
[0198] Пункт 10. Промежуточное соединение согласно Пункту 9, выбранное из группы, состоящей из:
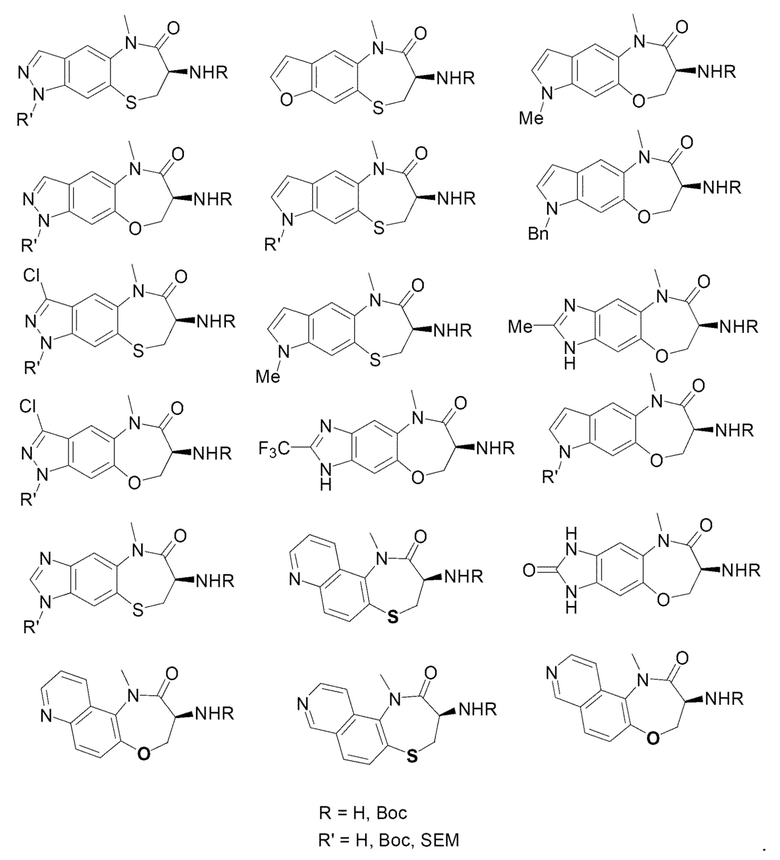
[0199] В настоящей заявке предложен новый класс соединений, ингибирующих активность киназы RIP1. По сравнению с существующими соединениями соединение настоящей заявки обладает лучшим ингибирующим действием против программируемого некроза клеток и улучшенной селективностью и фармакокинетикой.
[0200] Примеры
[0201] Настоящая заявка дополнительно описана ниже в сочетании с конкретными примерами. Следует понимать, что эти примеры являются лишь иллюстрацией настоящей заявки и не предназначены для ограничения объема настоящей заявки. В экспериментальных способах, в которых не указаны конкретные условия в следующих примерах, используются обычные условия или условия, рекомендованные производителем. Если не указано иное, проценты и части являются массовыми процентами.
[0202] Пример 1:. Синтез примерных Соединений RIP1-001, RIP1-003, RIP1-023, RIP1-136 и RIP1-182
[0203] Способ 1:
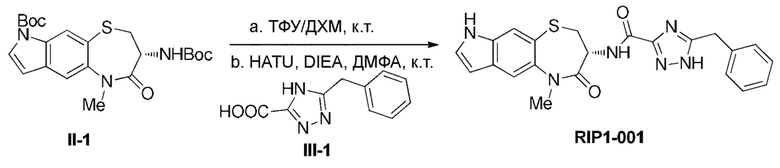
[0204] Соединение II-1 (27,8 мг, 0,08 ммоль) помещали в одногорлую колбу объемом 25 мл, затем добавляли ТФУ (1 мл) и ДХМ (4 мл) и проводили реакцию при комнатной температуре в течение 30 мин до полного завершения реакции, как было показано ТСХ. Растворитель удаляли при пониженном давлении, а остаток сушили в вакууме и повторно растворяли в ДМФА (4 мл). HATU (38 мг, 0,1 ммоль), DIEA (51,7 мг, 0,4 ммоль) и добавляли 5-бензил-4Н-1,2,4-триазол-3-карбоновую кислоту III-1 (20,3 мг, 0,1 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью обращенно-фазовой колоночной хроматографии и лиофилизировали с получением RIP1-001: белое твердое вещество, 14,0 мг (40,4%).
[0205] При изменении соединения Формулы II и соединения Формулы III, Соединения RIP1-002, RIP1-013 - RIP1-020, RIP1-026 - RIP1-030, RIP1-036 - RIP1-040, RIP1-092 - RIP1-135, RIP1-145 -RIP1-150, RIP1-156 - RIP1-165, RIP1-168 - RIP1-180, RIP1-187 -RIP1-189, RIP1-193 - RIP1-205, RIP1-207 - RIP1-210 и RIP1-214 -RIP1-215 также могут быть получены Способом 1.
[0206] Способ 2:
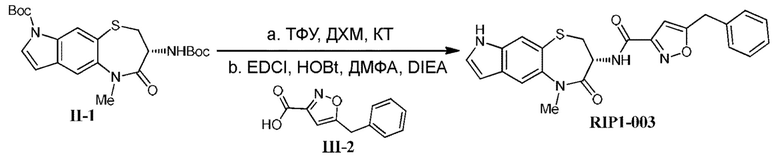
[0207] II-1 (30,0 мг) растворяли в дихлорметане (1 мл), затем добавляли ТФУ (0,3 мл) и перемешивали при комнатной температуре в течение 3 ч. Дихлорметан и ТФУ удаляли при выпаривании на роторном испарителе с получением Вос-незащищенного аминотрифторацетата.
[0208] Промежуточное Вос-незащищенное соединение, полученное в предыдущей стадии (17,7 мг), растворяли в ДМФА (1 мл), затем последовательно добавляли DIEA (43,3 мг), EDCI (19,3 мг) и HOBt (13,6 мг), перемешивали при нормальной температуре в течение 1 ч и затем охлаждали до 0°С. Трифторацетат, полученный в предыдущей стадии, растворяли в ДМФА (1 мл) и затем медленно, по каплям добавляли в реакционный раствор. Реакционный раствор переносили в комнатную температуру и оставляли реагировать на ночь. После завершения реакции медленно добавляли воду (10 мл), перемешивали в течение 0,5 ч и экстрагировали этилацетатом (10 мл). Этилацетатный слой собирали, сушили, выпаривали на роторном испарителе досуха и разделяли остаток с помощью колоночной хроматографии на силикагеле (элюент : петролейный эфир : этилацетат = 3:1) с получением RIP1-003 (19,0 мг, выход 66%).
[0209] При изменении соединения Формулы II и соединения Формулы III, Соединения RIP1-004 - RIP1-012, RIP1-041 - RIP1-058 и RIP1-061 - RIP1-088 также могут быть получены Способом 2.
[0210] Способ 3:
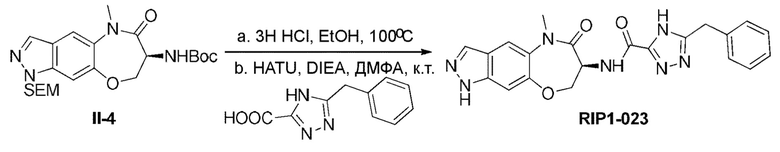
[0211] Соединение 11-4 (27,8 мг, 0,06 ммоль) помещали в герметично закрывающуюся пробирку объемом 15 мл, затем добавляли 3Н HCl (1 мл) и EtOH (0,5 мл) и проводили реакцию при 100°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Растворитель удаляли при пониженном давлении, а остаток сушили в вакууме и повторно растворяли в ДМФА (4 мл). Добавляли HATU (28,5 мг, 0,075 ммоль), DIEA (38,8 мг, 0,3 ммоль) и 5-бензил-4Н-1,2,4-триазол-3-карбоновую кислоту (15,2 мг, 0,075 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl, и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью обращенно-фазовой колоночной хроматографии и лиофилизировали с получением RIP1-023: белое твердое вещество, 10 мг (40%).
[0212] При изменении соединения Формулы II и соединения Формулы III, Соединения RIP1-021 - RIP1-025, RIP1-031 - RIP1-035, RIP1-059 - RIP1-060, RIP1-089 - RIP1-091 и RIP1-190 также могут быть получены Способом 3.
[0213] Способ 4:
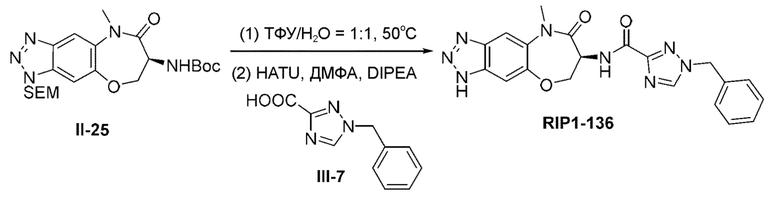
[0214] Соединение II-25 (1,0 экв.) помещали в одногорлую колбу, затем добавляли смешанный растворитель ТФУ/H2O (1:1) и проводили реакцию при 50°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Растворитель удаляли при пониженном давлении, а остаток сушили в вакууме и повторно растворяли в безводном ДМФА. Добавляли HATU (1,2 экв.), DIPEA (5 экв.) и неочищенный продукт, полученный после соединения Стадии 1) (1,1 экв.) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали деионизированной водой и насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью обращенно-фазовой колоночной хроматографии и лиофилизировали с получением Соединения RIP1-136.
[0215] При изменении соединения Формулы II и соединения Формулы III, Соединения RIP1-137 - RIP1-143, RIP1-153, RIP1-166 - RIP1-167 и RIP1-181 также могут быть получены Способом 4.
[0216] Способ 5:
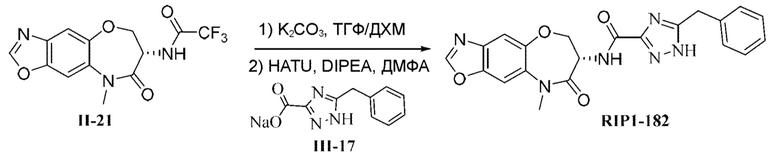
[0217] II-21 (60 мг, 0,1823 ммоль) и K2CO3 (51 мг, 0,3646 ммоль) добавляли в реакционную колбу объемом 50 мл, затем добавляли ТГФ (3 мл) и H2O (3 мл) и проводили реакцию в течение ночи при комнатной температуре. После завершения реакции растворитель удаляли при выпаривании на роторном испарителе. Добавляли HATU (84 мг, 0,2187 ммоль), III-1 (43 мг, 0,1914 ммоль) и DIPEA (150 мкл, 0,9118 ммоль), и затем в качестве растворителя добавляли ДМФА (4 мл). Реакцию продолжали при комнатной температуре в течение 1 ч. После завершения реакции, обращенно-фазовая колоночная хроматография давала RIP1-182 (28 мг, выход 36,8%).
[0218] При изменении соединения Формулы II и соединения Формулы III, Соединения RIP1-183 - RIP1-186, RIP1-206, RIP1-211 - RIP1-213 и RIP1-217 - RIP1-222 также могут быть получены Способом 5.
[0219] Способ синтеза, промежуточные соединения и выход соединения Формулы (I) согласно настоящей заявке представлены ниже:
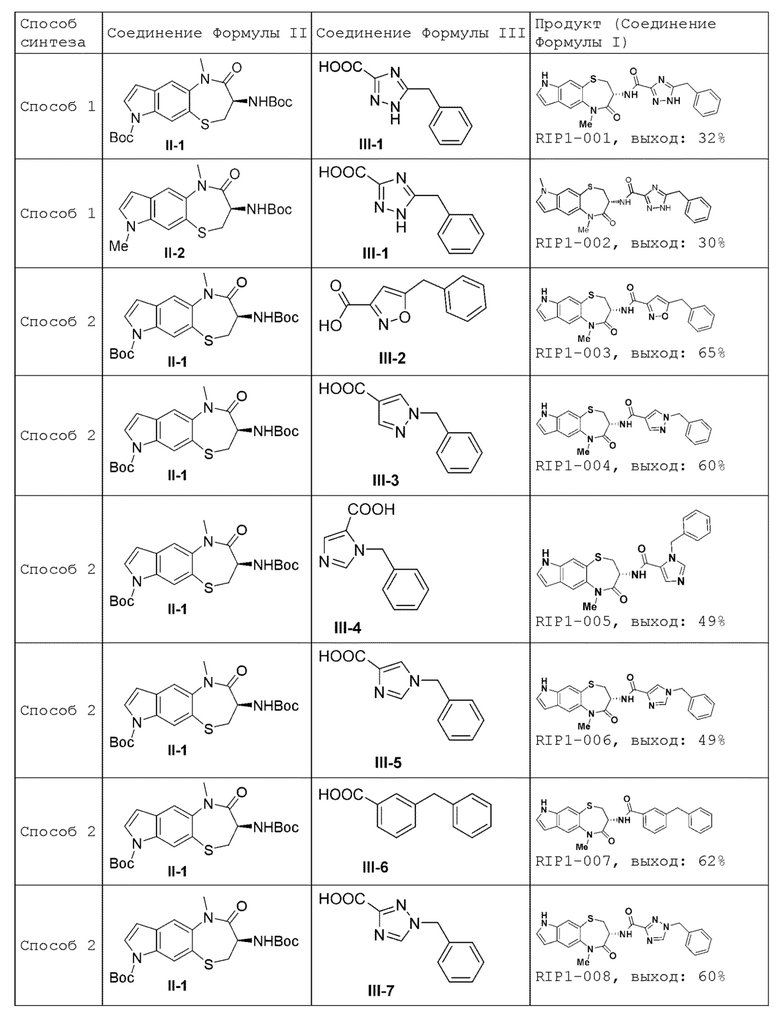
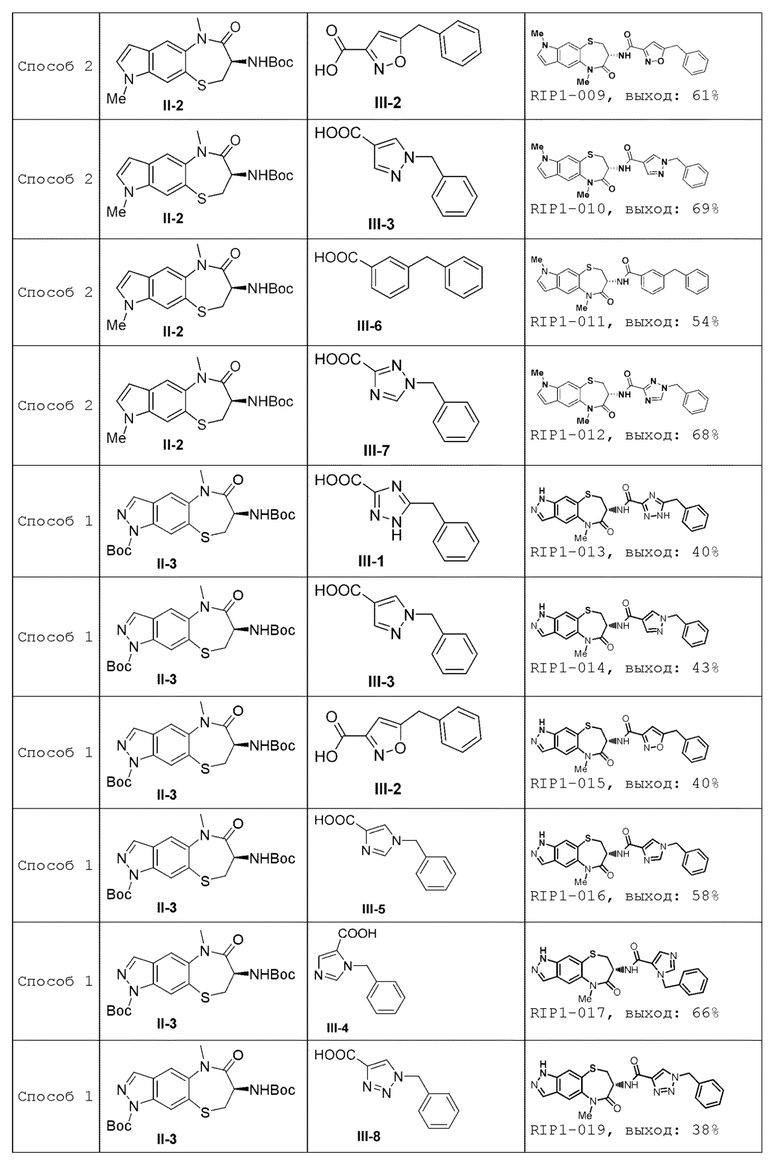
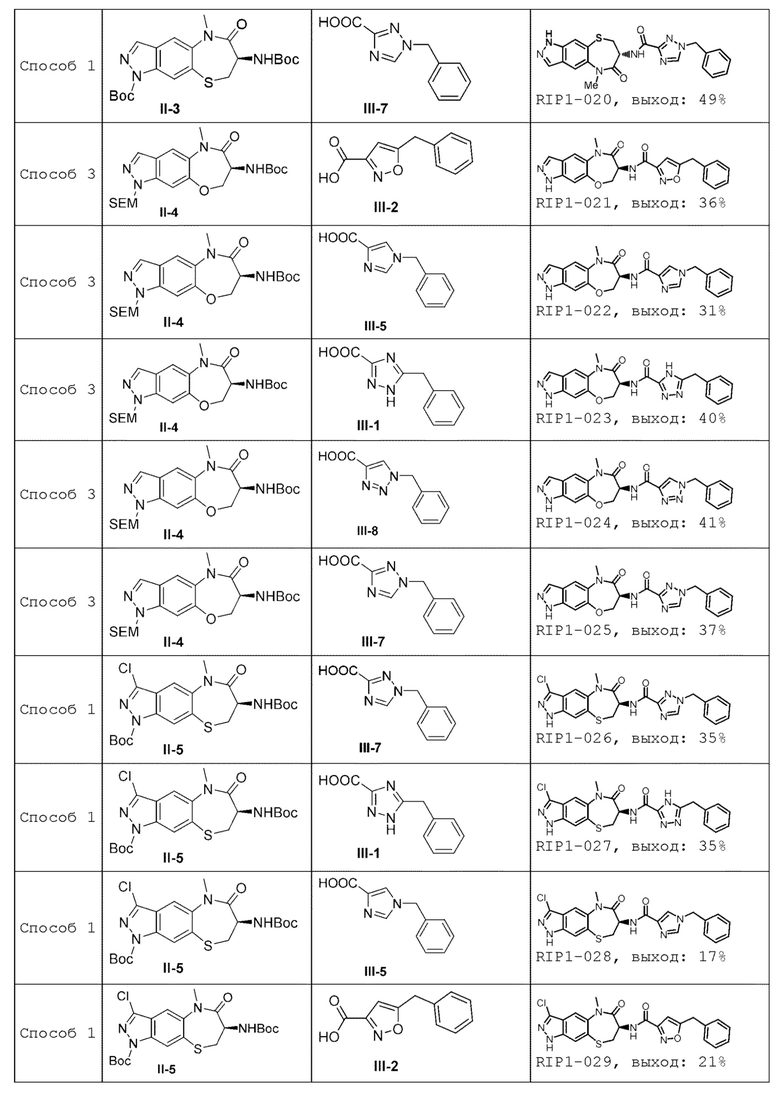
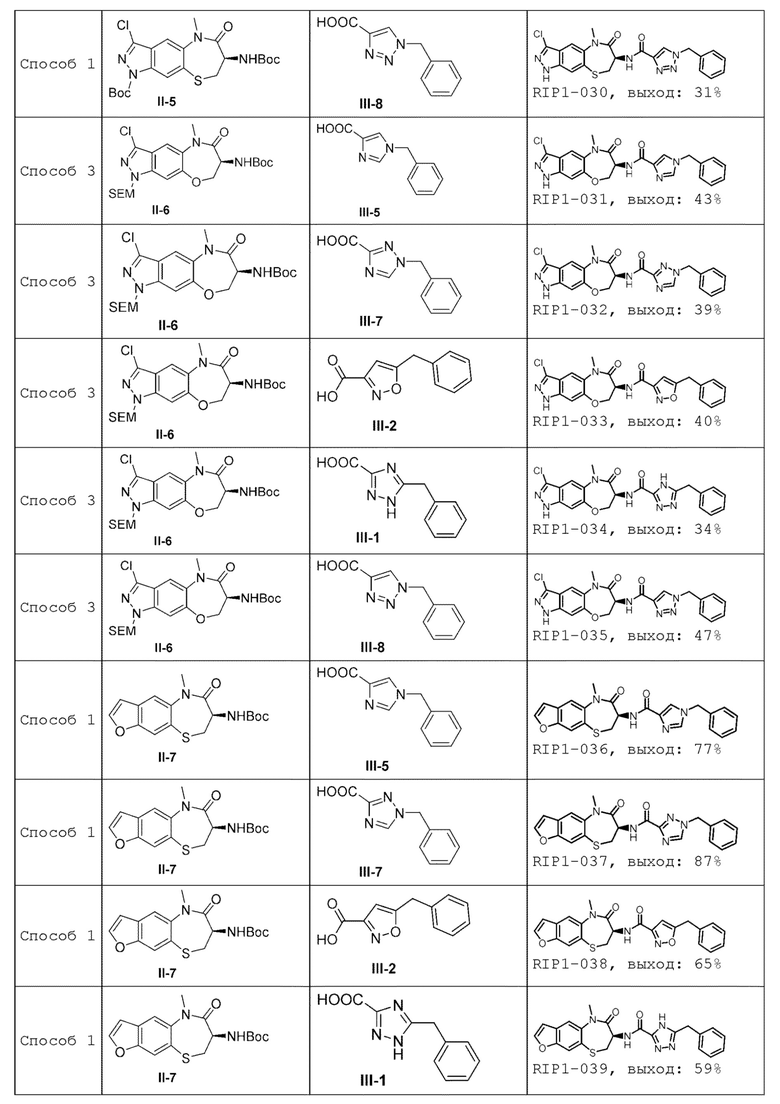
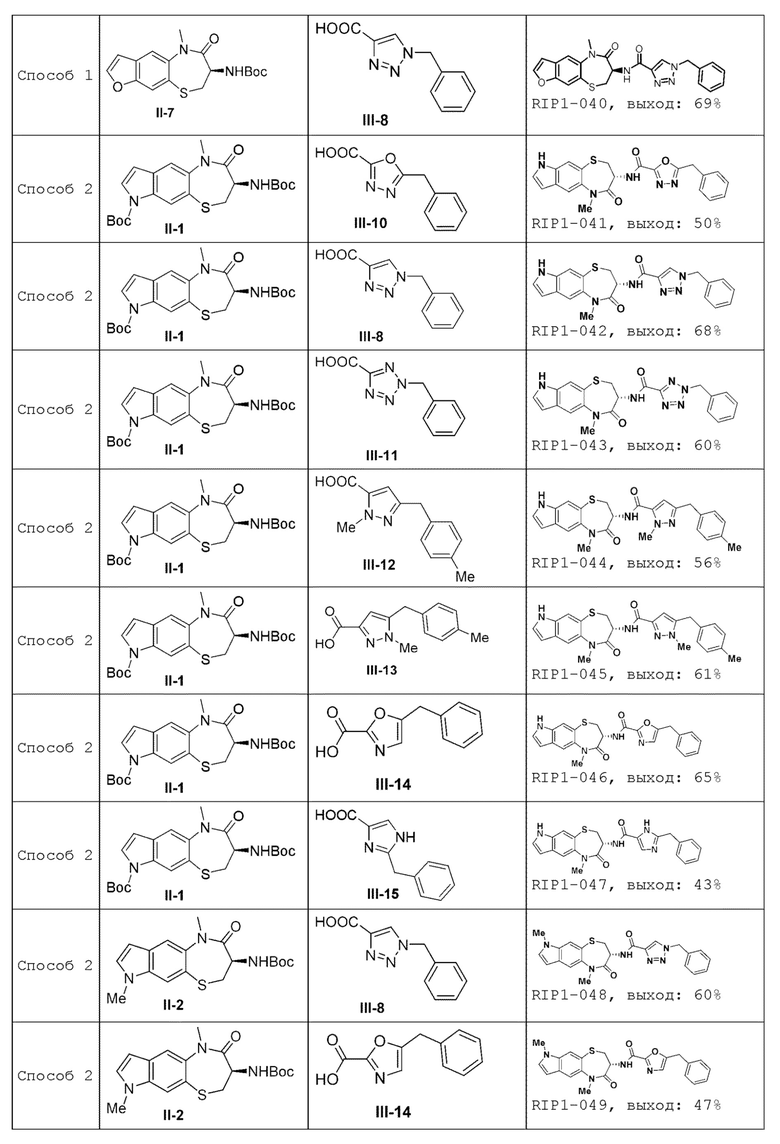
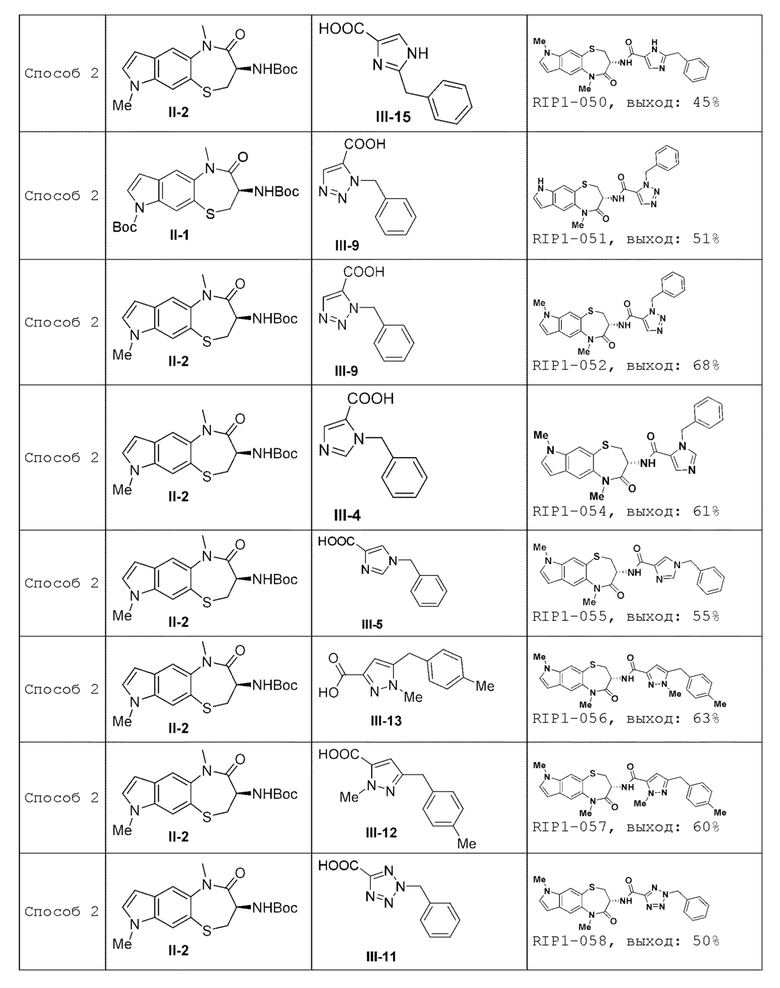
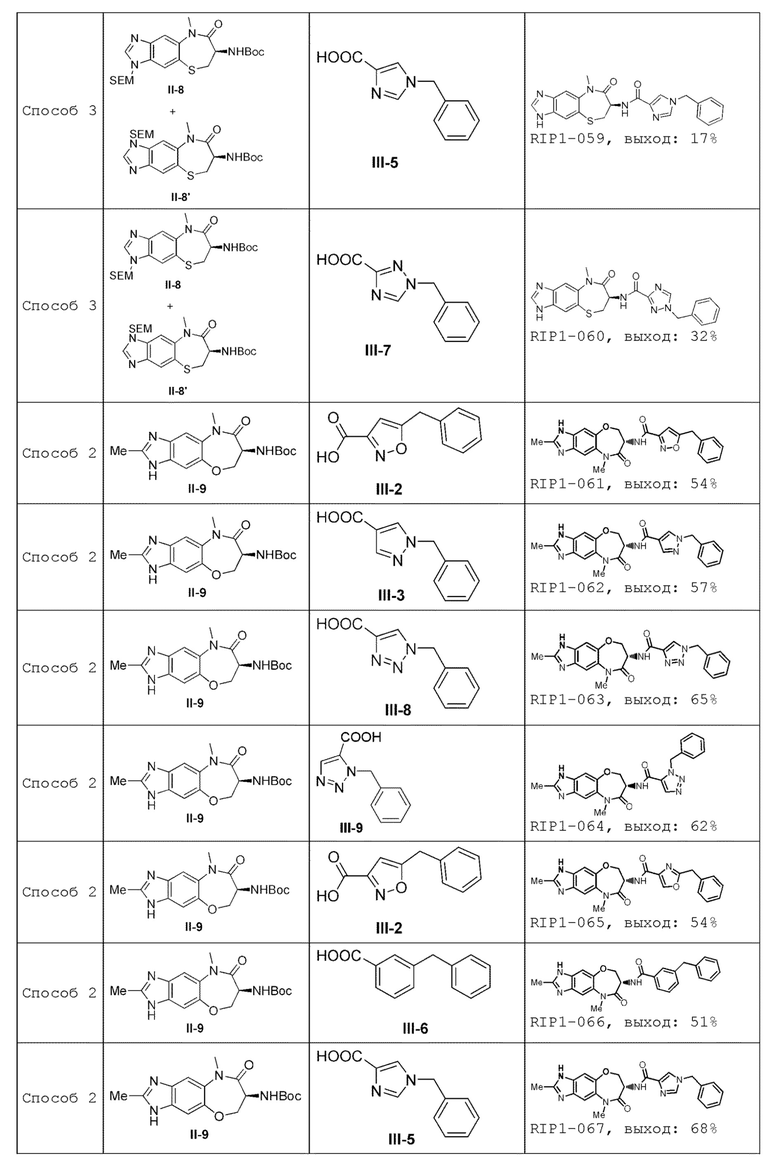
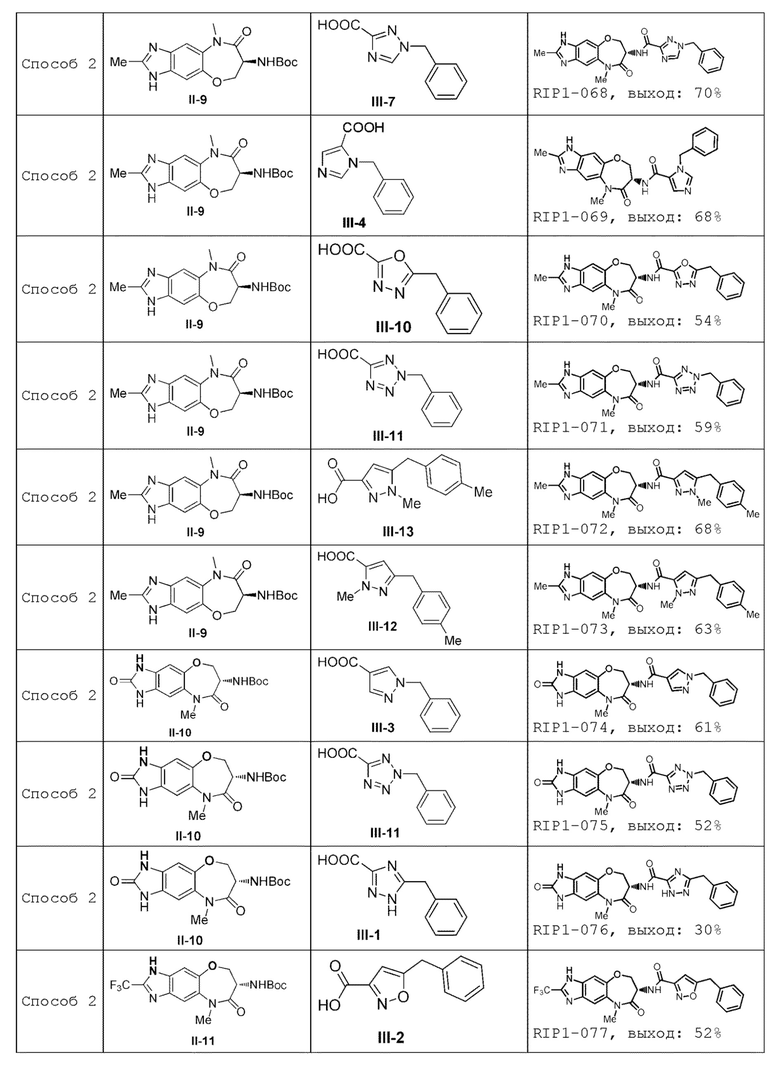
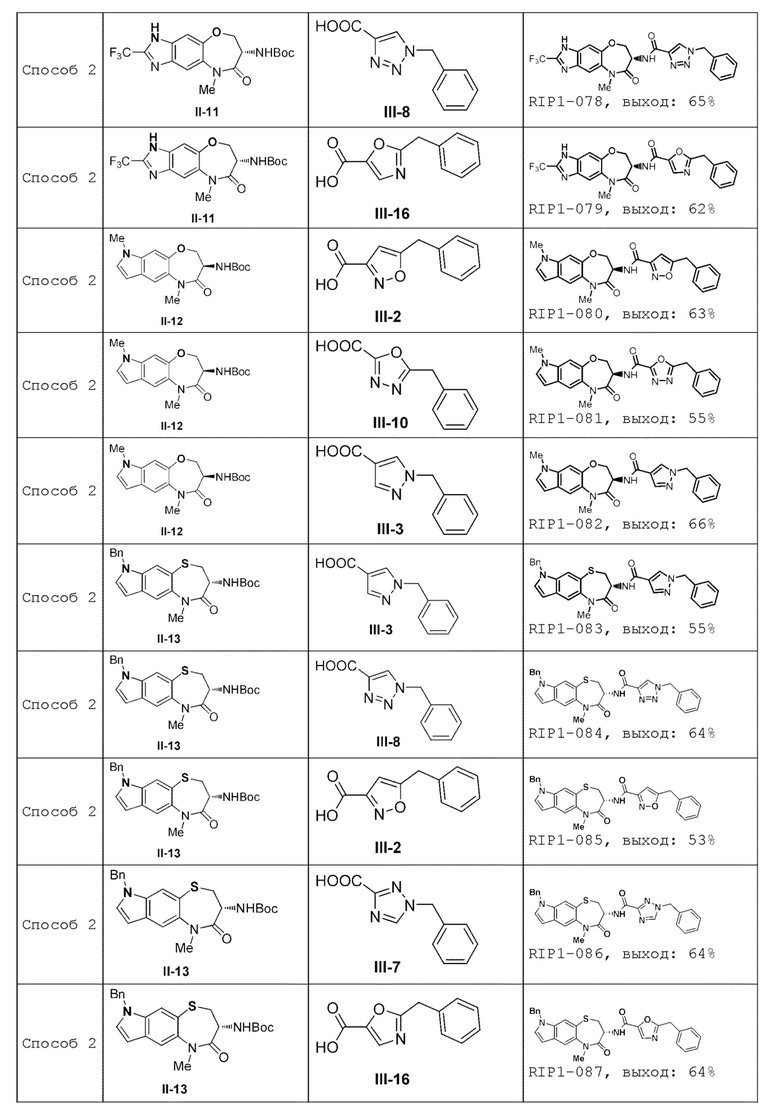
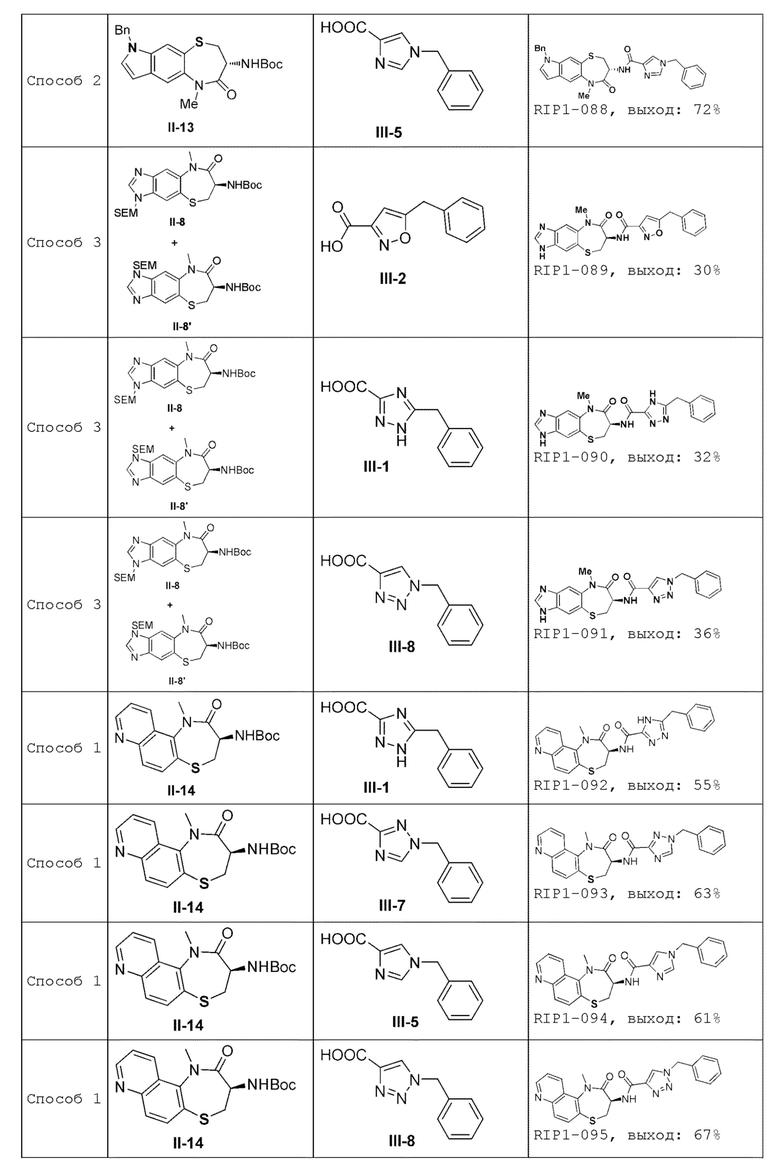
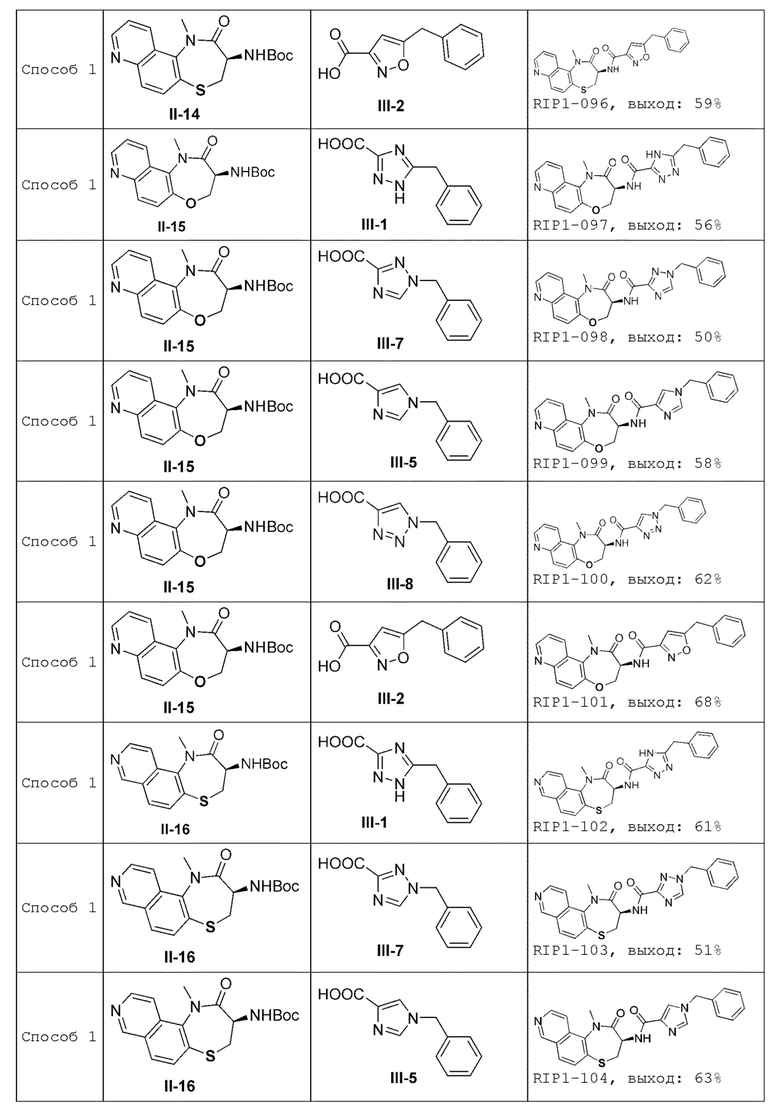
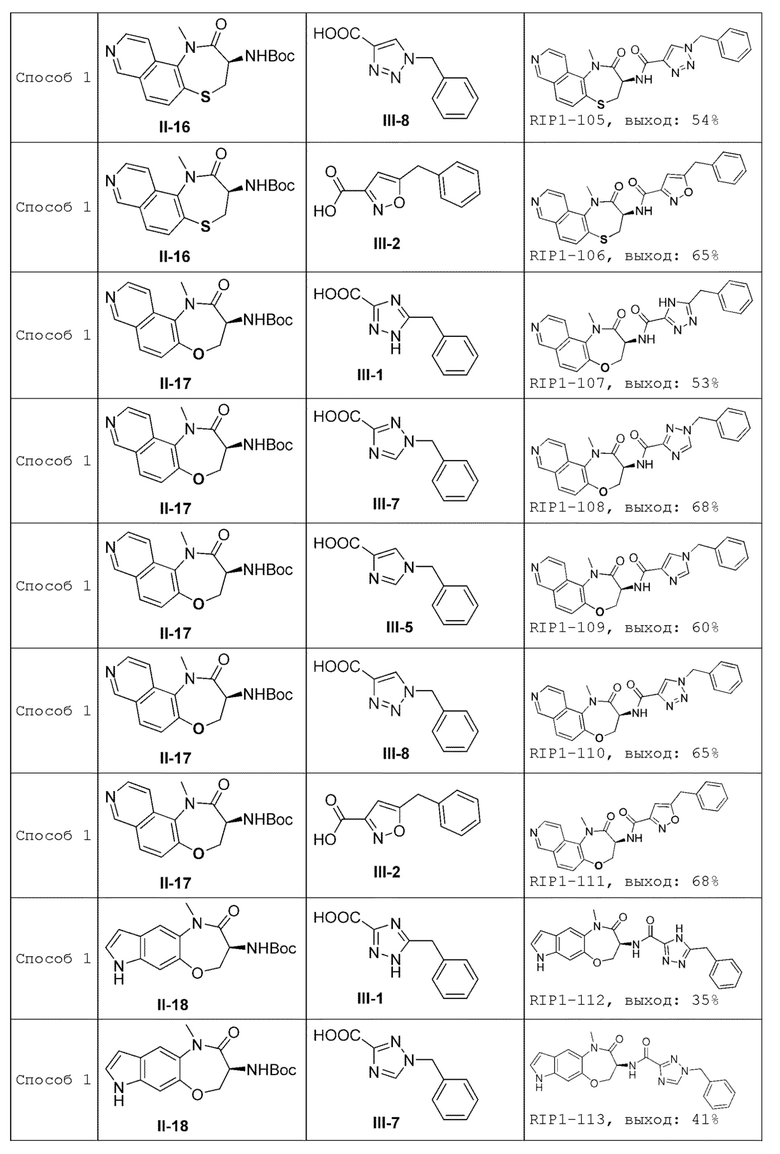
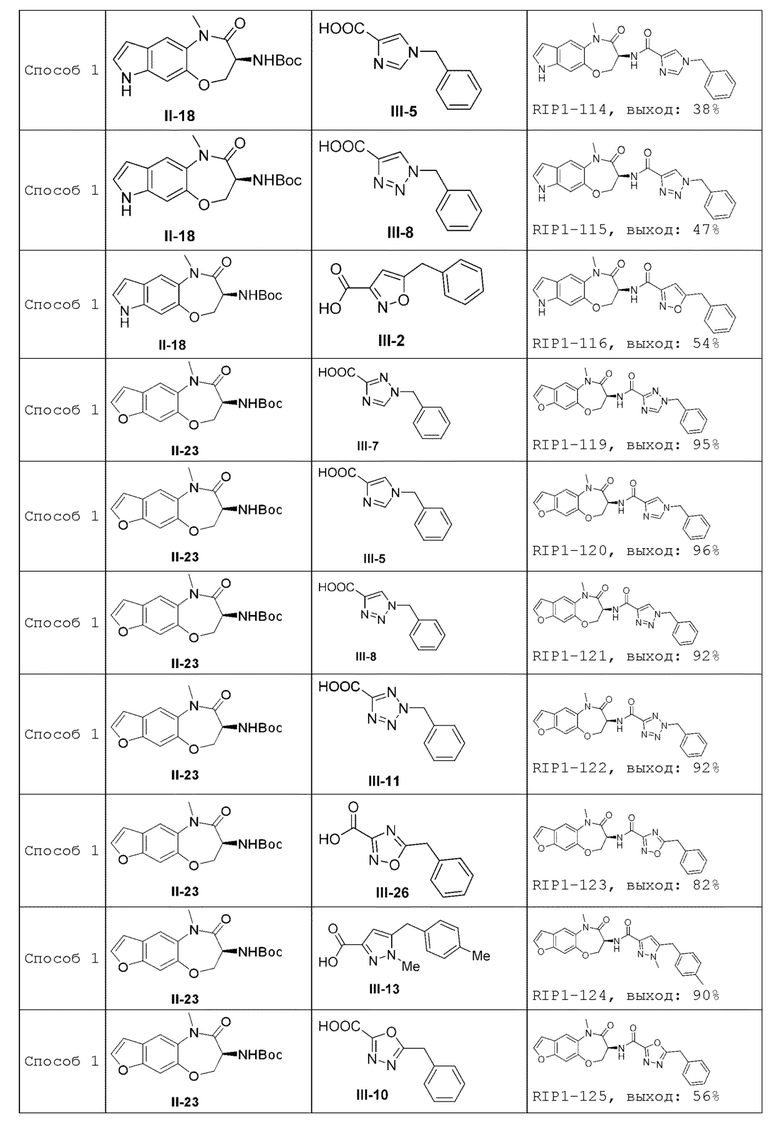
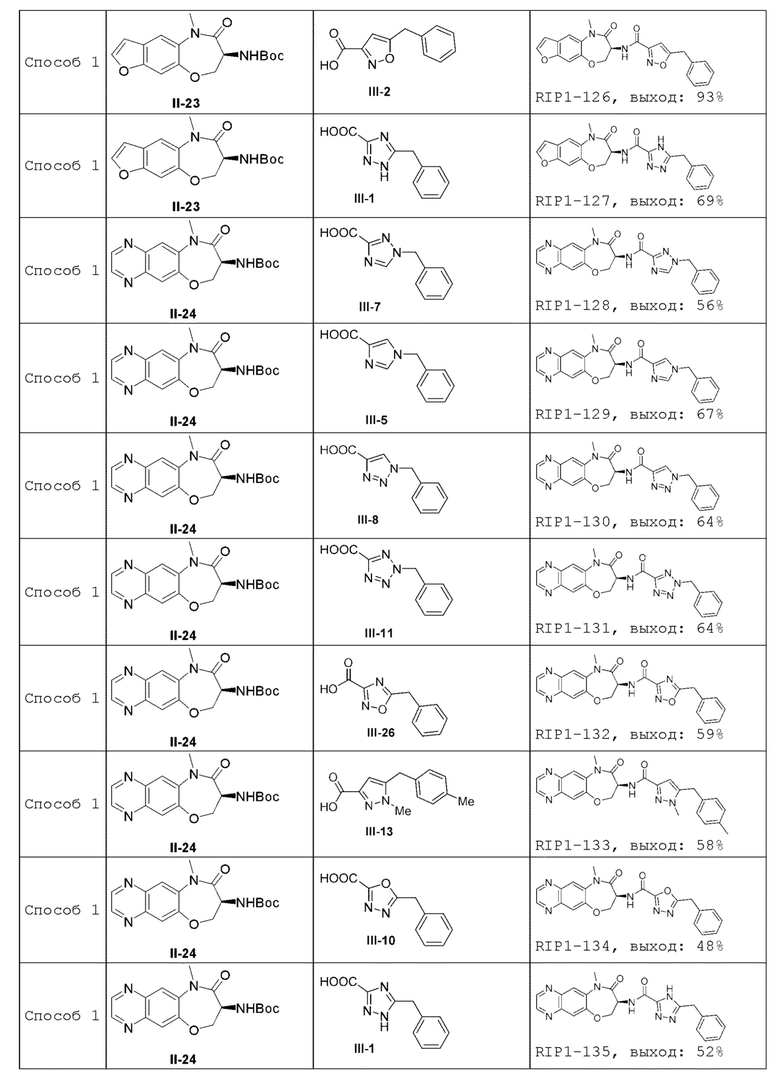
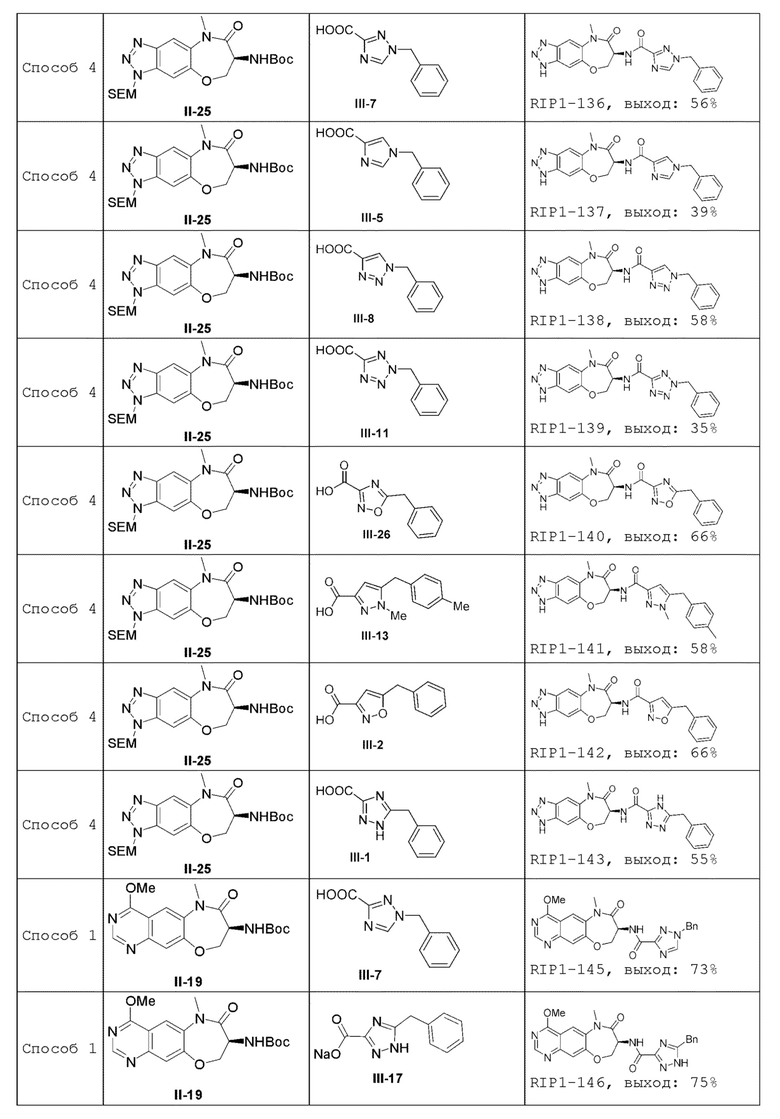
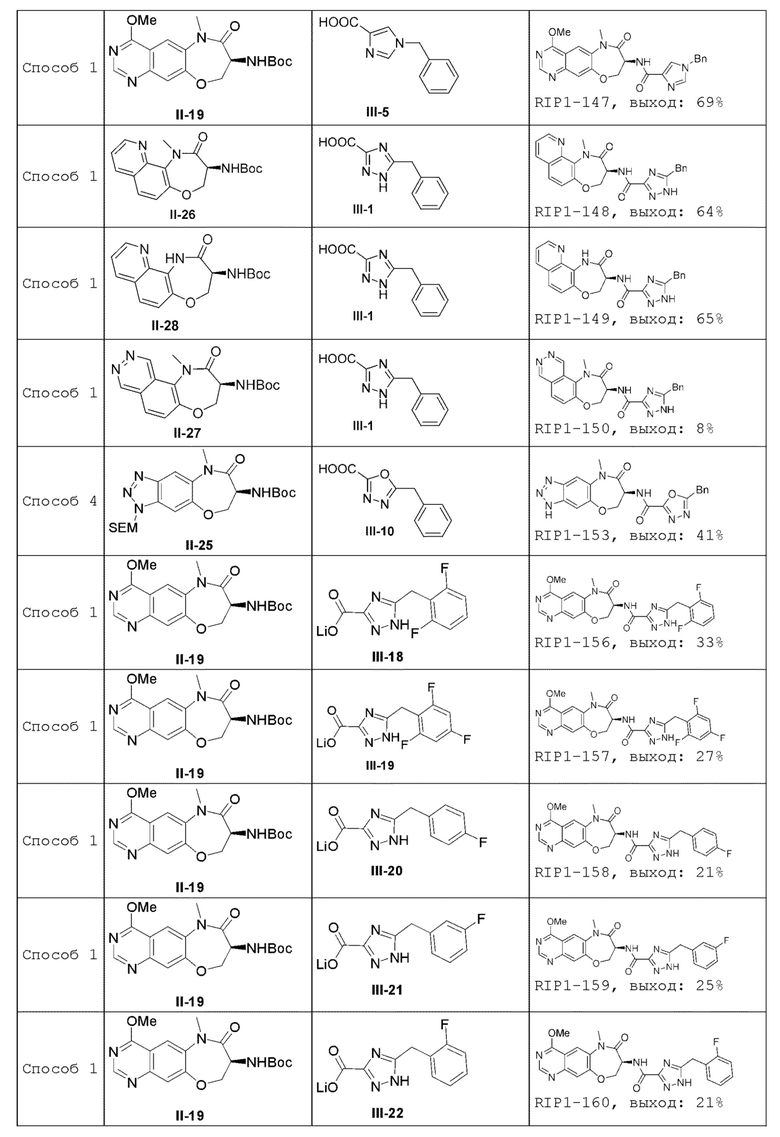
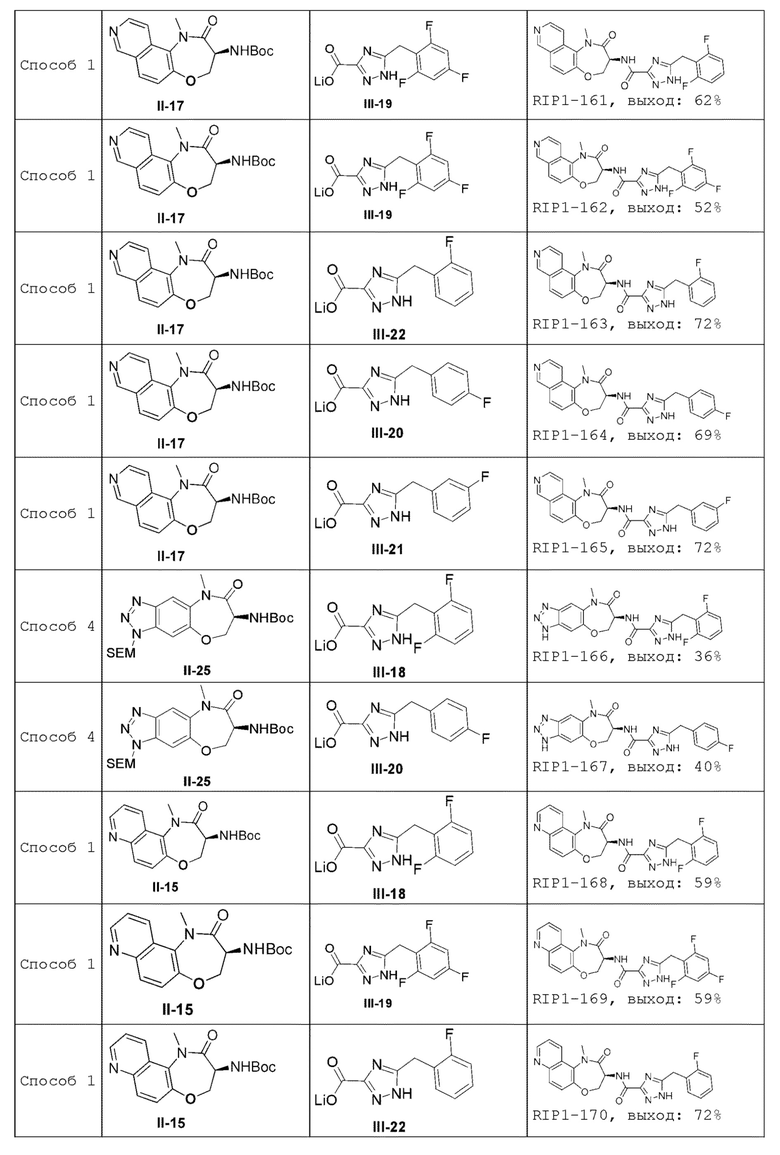
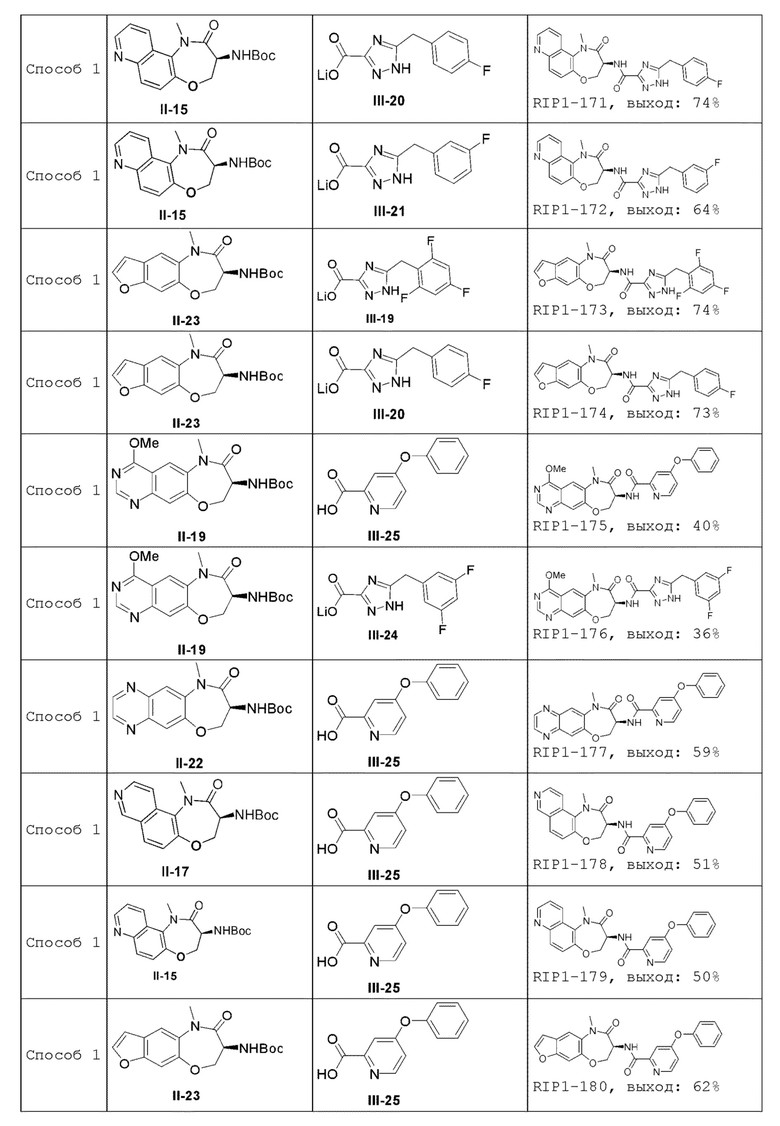
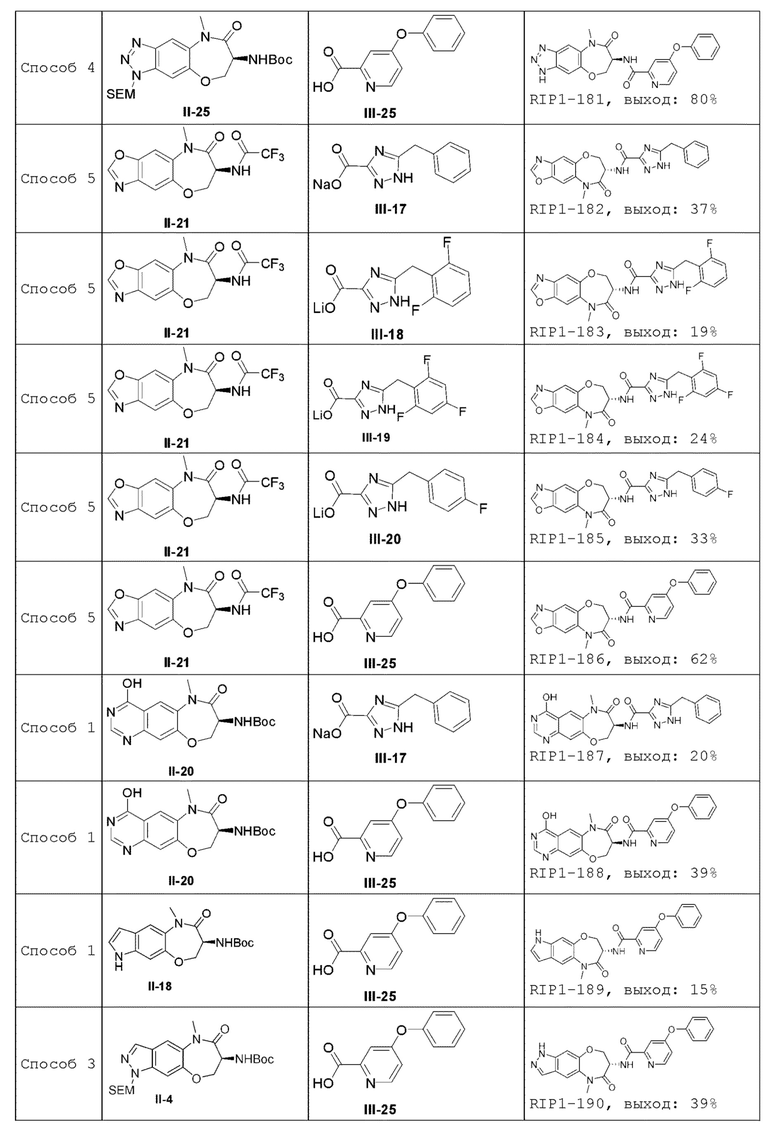
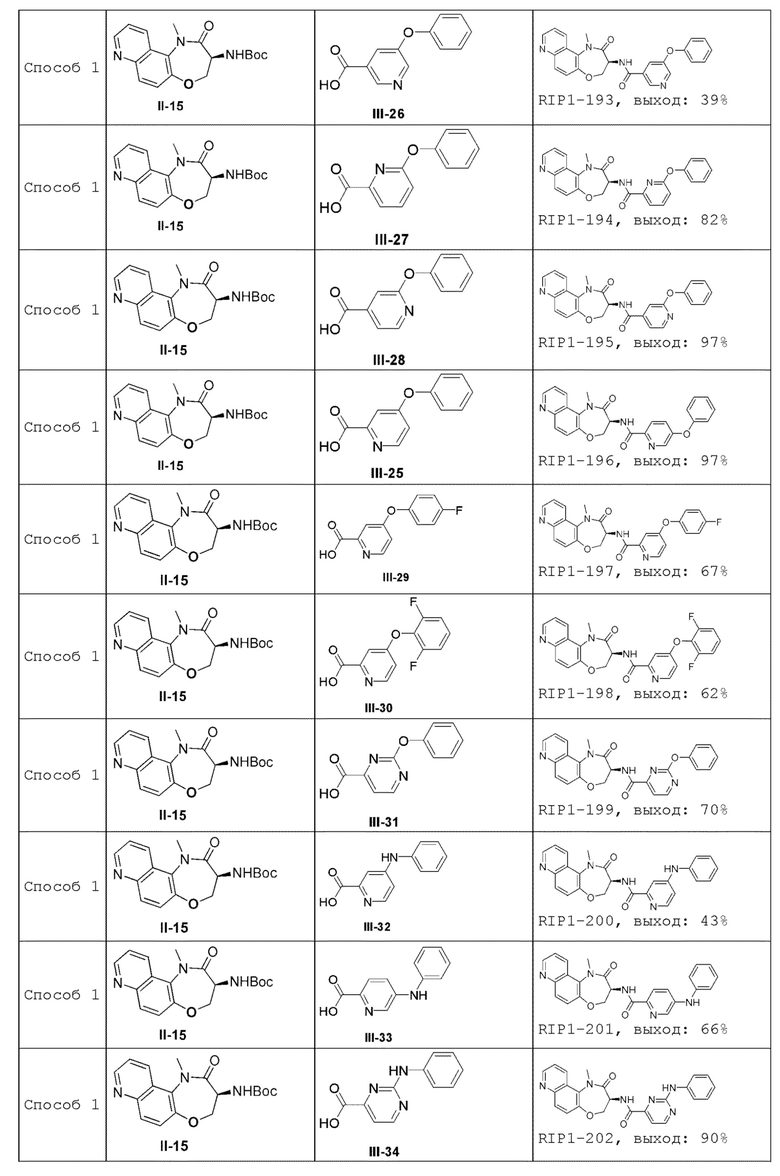
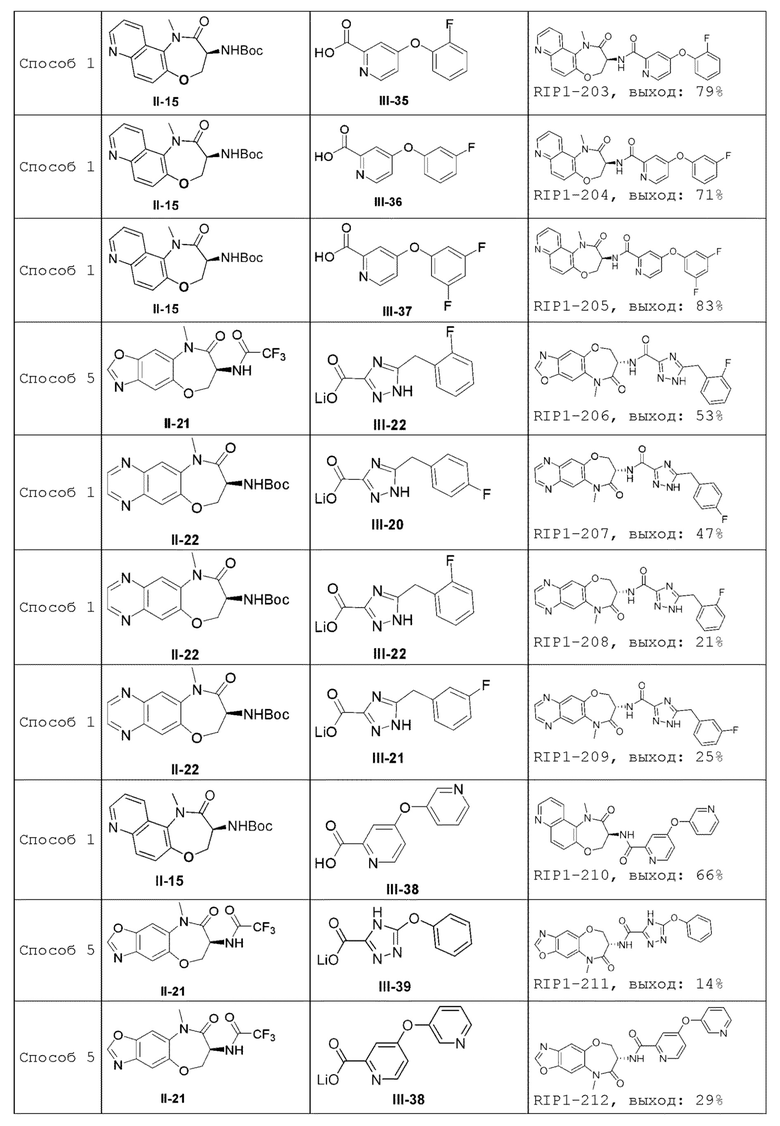
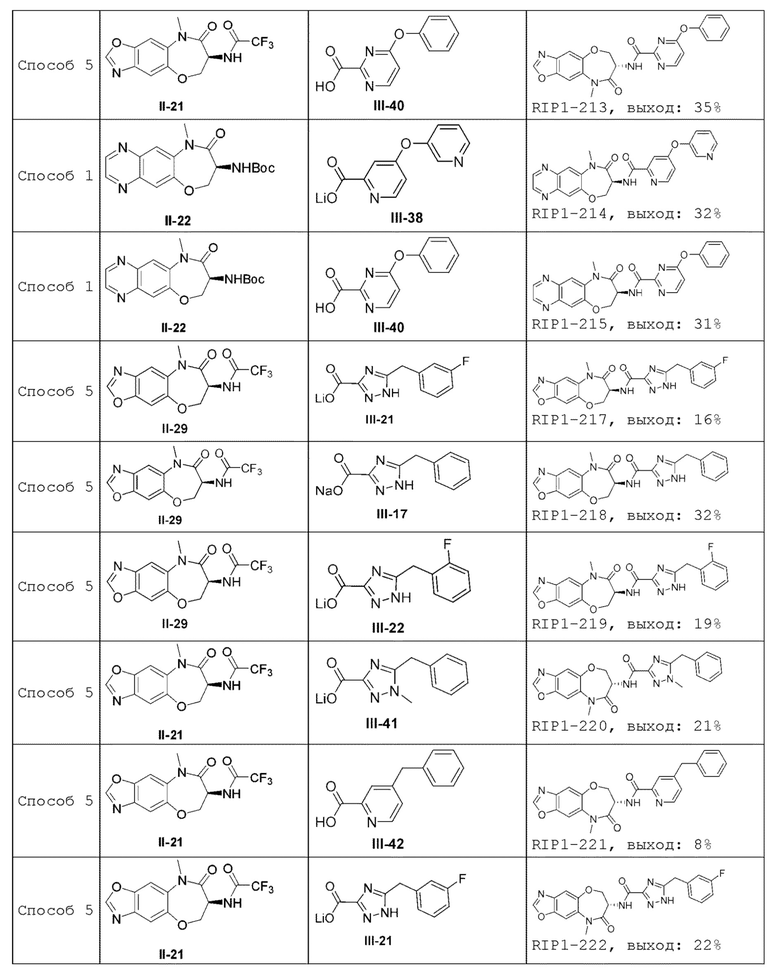
[0220] Данные анализа каждого соединения показаны ниже.
[0221] RIP1-001
[0222] 1H-ЯМР (500 МГц, CDCl3) δ=8,86 (с, 1Н), 8,31 (д, J=7,8, 1Н), 7,63 (с, 1Н), 7,49 (с, 1Н), 7,31-7,26 (м, 2Н), 7,25-7,17 (м, 5Н), 6,50 (с, 1Н), 4,83-4,76 (м, 1Н), 4,08 (с, 2Н), 3,76 (дд, J=11,1, 6,9, 1Н), 3,46 (с, 3Н), 2,83 (т, J=11,2, 1Н); МС-ЭРИ m/z 433,4 (М+Н)+.
[0223] RIP1-002
[0224] 1Н-ЯМР (400 МГц, CDCl3) δ (м.д.): 2,79 (т, J=11,2 Гц, 1Н), 3,45 (с, 3Н), 3,75 (с, 3Н), 3,76-3,80 (м, 1Н), 4,06 (с, 2Н), 4,66-4,73 (м, 1Н), 6,41 (с, 1Н), 7,04-7,08 (м, 1Н), 7,19-7,30 (м, 5Н), 7,45 (с, 1Н), 7,56 (с, 1Н), 8,16 (ш, 1Н); МС-ЭРИ (М+Н)+=447.1.
[0225] RIP1-003
[0226] 1Н-ЯМР (500 МГц, CDCl3) δ=8,49 (с, 1Н), 7,84 (д, J=7,4, 1Н), 7,71 (с, 1Н), 7,54 (с, 1Н), 7,34-7,29 (м, 3Н), 7,28-7,24 (м, 1Н), 7,21 (д, J=7,1, 2Н), 6,56-6,54 (м, 1Н), 6,26 (с, 1Н), 4,78-4,73 (м, 1Н), 4,09 (с, 2Н), 3,82 (дд, J=11,2, 6,9, 1Н), 3,48 (с, 3Н), 2,84 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 173,86, 169,89, 158,15, 158,01, 137,99, 135,24, 129,36, 128,88, 128,74, 127,31, 126,83, 119,90, 117,90, 116,81, 103,06, 101,54, 49,68, 38,12, 37,19, 33,16; МС-ЭРИ: 433,3 (М+Н)+.
[0227] RIP1-004
[0228] 1Н-ЯМР (500 МГц, CDCl3) δ=8,73 (с, 1Н), 7,83 (д, J=0,4, 1Н), 7,76 (с, 1Н), 7,68 (с, 1Н), 7,52 (с, 1Н), 7,37-7,31 (м, 3Н), 7, 28-7, 26 (м, 1Н), 7,21 (дд, J=7,7, 1,5, 2Н), 7,03 (д, J=7,3, 1Н), 6,53-6,50 (м, 1Н), 5,27 (с, 2Н), 4,81-4,75 (м, 1Н), 3,85 (дд, J=11,2, 6,9, 1Н), 3,47 (с, 3Н), 2,80 (т J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 171,01, 161,45, 138,86, 137,98, 135,42, 134,74, 130,83, 129,45, 129,14, 128,63, 128,12, 126,99, 119,95, 118,52, 118,03, 116,86, 103,08, 56,63, 49,78, 38,65, 37,33; МС-ЭРИ: 432,4 (М+Н)+.
[0229] RIP1-005
[0230] 1Н-ЯМР (500 МГц, CDCl3) δ=8,75 (с, 1Н), 7,66 (с, 1Н), 7,59 (д, J=0,6, 1Н), 7,55 (с, 1Н), 7,53 (с, 1Н), 7,30-7,23 (м, 4Н), 7,19 (д, J=7,3, 1Н), 7,08 (д, J=1,7, 1Н), 7,06 (с, 1Н), 6,53-6,51 (м, 1Н), 5,44 (с, 2Н), 4,75-4,69 (м, 1Н), 3,77 (дд, J=11,2, 6,8, 1Н), 3,48 (с, 3Н), 2,76 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,55, 159,08, 141,63, 137,96, 136,58, 134,72, 132,64, 129,46, 128,94, 128,08, 127,32, 127,02, 125,32, 119,90, 117,97, 116,92, 103,08, 50,02, 49,66, 38,47, 37,33, 1,16; МС-ЭРИ: 432,4 (М+Н)+.
[0231] RIP1-006
[0232] 1Н-ЯМР (500 МГц, CDCl3) δ=9,01 (с, 1Н), 8,07 (д, J=8,0, 1Н), 7,65 (с, 1Н), 7,48 (с, 1Н), 7,47 (д, J=1,2, 1Н), 7,44 (д, J=1,3, 1Н), 7,36-7,31 (м, 3Н), 7,23-7,22 (м, 1Н), 7,13 (дд, J=7,6, 1,7, 2Н), 6, 48-6, 45 (м, 1Н), 5,08 (с, 2Н), 4,83 (ддд, J=11,2, 7,8, 7,0, 1Н), 3,80 (дд, J=11,1, 6,8, 1H), 3,47 (с, 3Н), 2,88 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,79, 161,75, 138,15, 137,17, 137,13, 135,27, 134,70, 129,39, 129,27, 128,74, 127,60, 126,93, 122,47, 119,90, 117,99, 116,74, 102,86, 51.44, 49,37, 38,68, 37,27; МС-ЭРИ: 432,4 (М+Н)+.
[0233] RIP1-007
[0234] 1Н-ЯМР (500 МГц, CDCl3) δ=8,84 (с, 1Н), 7,71 (с, 1Н), 7,64 (с, 1Н), 7,61 (дт, J=7,1, 1,6, 1Н), 7,54 (с, 1Н), 7,42 (д, J=7,2, 1Н), 7,35-7,25 (м, 5Н), 7,19 (т, J=7,4, 1Н), 7,15 (д, J=7,1, 2Н), 6,53-6,51 (м, 1Н), 4,88-4,81 (м, 1Н), 4,00 (с, 2Н), 3,94 (дд, J=11,1, 6,8, 1Н), 3,50 (с, 3Н), 2,85 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,95, 166,48, 141,85, 140,53, 137,95, 134,79, 134,04, 132,55, 129,46, 129,01, 128,86, 128,70, 127,82, 127,07, 126,42, 124,99, 119,89, 118,08, 116,86, 103,00, 50,35, 41,87, 38,55, 37,32; МС-ЭРИ: 442,4 (М+Н)+.
[0235] RIP1-008
[0236] 1Н-ЯМР (500 МГц, CDCl3) δ=9,03 (с, 1Н), 8,22 (д, J=7,6, 1Н), 8,02 (с, 1Н), 7,70 (с, 1Н), 7,50 (с, 1Н), 7,39-7,34 (м, 3Н), 7, 29-7, 27 (м, 2Н), 7,25 (д, J=1,8, 1Н), 6,49 (с, 1Н), 5,36 (с, 2Н), 4,87-4,81 (м, 1Н), 3,92 (дд, J=11,2, 6,9, 1Н), 3,49 (с, 3Н), 2,85 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,36, 158,12, 157,01, 144,07, 137,82, 134,82, 133,91, 129,47, 129,31, 129,08, 128,37, 127,17, 119,62, 118,30, 116,78, 102,83, 54,45, 49,89, 38,52, 37,36; МС-ЭРИ: 433,4 (М+Н)+.
[0237] RIP1-009
[0238] 1Н-ЯМР (500 МГц, CDCl3) δ=7,84 (д, J=7,4, 1Н), 7,65 (с, 1Н), 7,52 (с, 1Н), 7,32 (т, J=7,3, 2Н), 7,28 (с, 1Н), 7,21 (д, J=7,1, 2Н), 7,15 (д, J=3,1, 1Н), 6,48 (д, J=3,0, 1Н), 6,26 (с, 1Н), 4,77-4,70 (м, 1Н), 4,08 (с, 2Н), 3,85-3,80 (м, 4Н), 3,48 (с, 3Н), 2,84 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 173,96, 170,03, 158,33, 158,12, 137,72, 135,63, 135,41, 131,53, 129,95, 129,02, 128,89, 127,46, 119,55, 117,07, 116,41, 101,70, 101,57, 49,83, 38,33, 37,31, 33,31, 31,77; МС-ЭРИ: 447,4 (М+Н)+.
[0239] RIP1-010
[0240] 1Н-ЯМР (500 МГц, CDCl3) δ=7,82 (с, 1Н), 7,75 (с, 1Н), 7,64 (с, 1Н), 7,51 (с, 1Н), 7,37-7,31 (м, 3Н), 7,23-7,20 (м, 2Н), 7,14 (д, J=3,1, 1Н), 6,96 (д, J=7,3, 1Н), 6,47 (д, J=3,0, 1Н), 5,27 (с, 2Н), 4,77-4,71 (м, 1Н), 3,87-3,82 (м, 4Н), 3,47 (с, 3Н), 2,78 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 171,00, 161,31, 138,80, 137,66, 135,66, 135,46, 131,49, 130,81, 129,91, 129,13, 128,61, 128,12, 119,63, 118,60, 117,04, 116,41, 101,55, 56,62, 49,75, 38,71, 37,30, 33,30; МС-ЭРИ: 446,4 (М+Н)+.
[0241] RIP1-011
[0242] 1Н-ЯМР (500 МГц, CDCl3) δ=7,66 (с, 1Н), 7,63 (с, 1Н), 7,59 (д, J=7,3, 1Н), 7,53 (с, 1Н), 7,35 (д, J=7,1, 1Н), 7,34-7,25 (м, 4Н), 7,19 (т, J=7,4, 1Н), 7,16 (д, J=1,2, 1Н), 7,15 (д, J=3,0, 2Н), 6,48 (д, J=3,7, 1Н), 4,83-4,77 (м, 1Н), 4,00 (с, 2Н), 3,91 (дд, J=11,1, 6,8, 1Н), 3,84 (с, 3Н), 3,50 (с, 3Н), 2,82 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,97, 166,28, 141,78, 140,56, 137,68, 135,67, 134,16, 132,43, 131,50, 129,92, 129,01, 128,81, 128,69, 127,81, 126,40, 124,97, 119,63, 117,06, 116,42, 101,56, 50,29, 41,87, 38,60, 37,27, 33,29; МС-ЭРИ: 456,4 (М+Н)+.
[0243] RIP1-012
[0244] 1Н-ЯМР (500 МГц, CDCl3) δ=8,18 (д, J=7,5, 1Н), 7,99 (с, 1Н), 7,65 (с, 1Н), 7,51 (с, 1Н), 7,39-7,34 (м, 3Н), 7,27 (д, J=2,5, 1Н), 7,26 (д, J=2,0, 1Н), 7,15 (д, J=3,1, 1Н), 6,47 (дд, J=3,1, 0,7, 1Н), 5,35 (с, 2Н), 4,83-4,77 (м, 1Н), 3,91 (дд, J=11,2, 6,9, 1Н), 3,84 (с, 3Н), 3,48 (с, 3Н), 2,83 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,36, 157,94, 157,08, 143,97, 137,67, 135,65, 133,95, 131,49, 129,94, 129,30, 129,06, 128,36, 119,55, 117,06, 116,53, 101,51, 54,42, 49,80, 38,53, 37,32, 33,29; МС-ЭРИ: 447,4 (М+Н)+.
[0245] RIP1-013
[0246] 1Н-ЯМР (400 МГц, CDCl3) δ 8,03 (с, 1Н), 7,89 (с, 1Н), 7,68 (с, 1Н), 7,37-7,21 (м, 5Н), 4,87-4,74 (м, 1Н), 4,13 (с, 2Н), 3,87-3,74 (м, 1Н), 3,50 (с, 3Н), 2,99-2,87 (м, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,0, 158,2, 138,8, 138,6, 135,9, 134,2, 128,8, 127,2, 126,1, 123,8, 117,5, 116,8, 49,5, 37,5, 37,3, 33,2. МС-ЭРИ: m/z 434,1 (М+Н)+.
[0247] RIP1-014
[0248] 1Н-ЯМР (400 МГц, CDCl3) δ 11,82 (с, 1Н), 7,92 (с, 1Н), 7,87 (с, 1Н), 7,81 (с, 1Н), 7,66 (с, 1Н), 7,60-7,54 (м, 2Н), 7,38-7,31 (м, 3Н), 7,24-7,19 (м, 2Н), 5,25 (с, 2Н), 4,90 (дт, J=11,4, 7,4 Гц, 1Н), 3,79 (дд, J=11,3, 6,8 Гц, 1Н), 3,43 (с, 3Н), 2,93 (т, J=11,4 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 171,0, 162,1, 139,1, 138,6, 138,5, 135,3, 134,7, 131,1, 129,1, 128,6, 128,2, 126,0, 123,9, 118,0, 116,8, 116,8, 56,6, 49,6, 37,7, 37,6. МС-ЭРИ: m/z 433,1 (М+Н)+.
[0249] RIP1-015
[0250] 1Н-ЯМР (400 МГц, CDCl3) δ 10,97 (с, 1Н), 8,01 (с, 1Н), 7,92 (д, J=7,1 Гц, 1Н), 7,80 (с, 1Н), 7,63 (с, 1Н), 7,36-7,15 (м, 5Н), 6,27 (с, 1Н), 4,88-4,72 (м, 1Н), 4,07 (с, 2Н), 3,80 (дд, J=11,0, 6,7 Гц, 1Н), 3,47 (с, 3Н), 2,89 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 174,2, 169,7, 158,5, 158,1, 138,9, 138,7, 135,3, 135,0, 129,0, 128,9, 127,5, 126,5, 124,2, 117,0, 116,9, 101,7, 49,6, 37,6, 37,5, 33,3. МС-ЭРИ: m/z 434,1 (М+Н)+.
[0251] RIP1-016
[0252] 1Н-ЯМР (400 МГц, CDCl3) δ 11,94 (с, 1Н), 8,17 (д, J=8,2 Гц, 1Н), 7,88 (д, J=0,7 Гц, 1Н), 7,68 (с, 1Н), 7,52 (с, 1Н), 7,49 (с, 1Н), 7,48 (с, 1Н), 7,35-7,29 (м, 3Н), 7,15-7,10 (м, 2Н), 5,08 (с, 2Н), 4,91 (ддд, J=11,4, 8,0, 7,0 Гц, 1Н), 3,79 (дд, J=11,1, 6,7 Гц, 1Н), 3,43 (с, 3Н), 2,96 (т, J=11,3 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,3, 162,2, 138,7, 138,6, 137,3, 136,7, 135,2, 134,5, 129,3, 128,7, 127,6, 126,0, 123,8, 122,8, 116,7, 116,6, 51,4, 49,1, 37,8, 37,4. МС-ЭРИ: m/z 433,1 (М+Н)+.
[0253] RIP1-017
[0254] 1Н-ЯМР (400 МГц, CDCl3) δ 11,61 (шс, 1Н), 8,00 (с, 1Н), 7,80-7,46 (м, 5Н), 7,26-7,13 (м, 3Н), 7,12-6,97 (м, 2Н), 5,44 (к, J=15,0 Гц, 2Н), 4,77 (с, 1Н), 3,79-3,66 (м, 1Н), 3,48 (с, ЗН), 2,86 (т, J=11,0 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,5, 159,4, 141,8, 138,7, 136,5, 134,8, 133,0, 128,9, 128,1, 127,3, 126,3, 125,1, 124,0, 117,0, 116,9, 53,6, 50,2, 49,4, 37,6. МС-ЭРИ: m/z 433,1 (М+Н)+.
[0255] RIP1-019
[0256] 1Н-ЯМР (400 МГц, CDCl3+CD3OD) δ 7,99 (с, 1Н), 7,92 (с, 1Н), 7,81 (с, 1Н), 7,64 (с, 1Н), 7,38-7,30 (м, 3Н), 7,25-7,19 (м, 2Н), 5,58-5,45 (м, 2Н), 4,78 (дд, J=11,3, 6,7 Гц, 1Н), 3,75 (дд, J=11,1, 6,8 Гц, 1Н), 3,46 (с, 3Н), 2,91 (т, J=11,3 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3+CD3OD) δ 170,0, 159,4, 142,8, 138,9, 138,7, 134,5, 133,8, 129,3, 129,2, 128,3, 126,4, 125,7, 124,0, 117,1, 116,9, 54,6, 49,2, 37,51, 37,49. МС-ЭРИ: m/z 434,1 (М+Н)+.
[0257] RIP1-020
[0258] 1Н-ЯМР (400 МГц, CDCl3+CD3OD) δ 8,07 (с, 1Н), 8,02 (с, 1Н), 7,89 (с, 1Н), 7,66 (с, 1Н), 7,40-7,33 (м, 3Н), 7,29-7,26 (м, 2Н), 5,37 (с, 2Н), 4,82 (дд, J=11,2, 6,8 Гц, 1Н), 3,86 (дд, J=11,1, 6,8 Гц, 1Н), 3,49 (с, 3Н), 2,88 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3+CD3OD) δ 170,1, 158,1, 156,6, 144,2, 138,8, 138,6, 134,4, 133,8, 129,3, 129,1, 128,3, 126,1, 123,9, 117,5, 116,8, 54,4, 49,6, 49,5, 37,52, 37,47. МС-ЭРИ: m/z 434,1 (М+Н)+.
[0259] RIP1-021
[0260] 1Н-ЯМР (400 МГц, CDCl3) δ 10,49 (с, 1Н), 8,05 (с, 1Н), 7,80 (д, J=6,3 Гц, 1Н), 7,60 (с, 1Н), 7,35-7,27 (м, 4Н), 7,24-7,19 (м, 2Н), 6,29 (с, 1Н), 5,07-4,98 (м, 1Н), 4,69 (дд, J=9,8, 7,4 Гц, 1Н), 4,24 (дд, J=11,1, 9,9 Гц, 1Н), 4,10 (с, 2Н), 3,51 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 174,3, 168,4, 158,8, 158,0, 150,0, 138,6, 135,3, 135,2, 131,7, 129,1, 128,9, 127,5, 120.6, 115,4, 103,2, 101,7, 76,6, 49,2, 36,7, 33,3. МС-ЭРИ: m/z 418.0 (М+Н)+.
[0261] RIP1-022
[0262] 1Н-ЯМР (400 МГц, CDCl3) δ 11,00 (шс, 1Н), 8,07-7,96 (м, 2Н), 7,53 (с, 1Н), 7,51-7,46 (м, 2Н), 7,38-7,30 (м, 3Н), 7,19-7,11 (м, 2Н), 5,15-5,04 (м, 3Н), 4,70-4,63 (м, 1Н), 4,31-4,22 (м, 1Н), 3,48 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 169,1, 162,4, 150,0, 137,3, 136,8, 135,2, 134,9, 131,8, 129,3, 128,8, 127,7, 122,7, 115,1, 103,0, 77,0, 51,5, 48,7, 36,5. МС-ЭРИ: m/z 417.1 (М+Н)+.
[0263] RIP1-023
[0264] 1Н-ЯМР (400 МГц, CDCl3) δ 8,00 (с, 1Н), 7,56 (с, 1Н), 7,31-7,27 (м, 2Н), 7,26-7,17 (м, 4Н), 5,01 (дд, J=11,2, 7,4 Гц, 1Н), 4,67-4,58 (м, 1Н), 4,26-4,17 (м, 1Н), 4,10 (с, 2Н), 3,47 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,6, 158,7, 154,5, 149,7, 138,7, 135,9, 134,3, 131,4, 128,9, 127,3, 120,3, 115,2, 103,6, 76,4, 49,0, 36,6, 33,3. МС-ЭРИ: m/z 418,1 (М+Н)+.
[0265] RIP1-024
[0266] 1Н-ЯМР (400 МГц, CDCl3) δ 10,93 (шс, 1Н), 8,03 (д, J=6,8 Гц, 1Н), 7,91 (с, 1Н), 7,84 (с, 1Н), 7,47 (с, 1Н), 7,26 (с, 2Н), 7,17 (с, 3Н), 5,53-5,36 (м, 2Н), 5,07-4,91 (м, 1Н), 4,56 (т, J=8,5 Гц, 1Н), 4,19 (т, J=10,4 Гц, 1Н), 3,41 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,6, 159,9, 149,9, 142,8, 138,6, 134,9, 133,8, 131,7, 129,4, 129,2, 128,4, 125,7, 120,5, 115,2, 103,1, 76,7, 54,7, 48,9, 36,6. МС-ЭРИ: m/z 418,1 (М+Н)+.
[0267] RIP1-025
[0268] 1Н-ЯМР (400 МГц, CDCl3) δ 11,54 (шс, 1Н), 8,17-7,86 (м, 3Н), 7,47 (с, 1Н), 7,33-7,26 (м, 3Н), 7,23-7,16 (м, 2Н), 5,30 (с, 2Н), 5,09-4,96 (м, 1Н), 4,71 (т, J=8,2 Гц, 1Н), 4,18 (т, J=10,3 Гц, 1Н), 3,43 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,6, 158,8, 156,7, 149,6, 144,3, 138,8, 134,6, 133,8, 131,3, 129,3, 129,1, 128,5, 120,5, 115,0, 103,7, 76,7, 54,5, 49,4, 36,6. МС-ЭРИ: m/z 418,1 (М+Н)+.
[0269] RIP1-026
[0270] 1Н-ЯМР (400 МГц, CDCl3) δ 11,81 (с, 1Н), 8,24 (с, 1Н), 8,08 (с, 1Н), 7,81 (с, 1Н), 7,51 (с, 1Н), 7,41-7,34 (м, 3Н), 7,33-7,27 (м, 2Н), 5,38 (с, 2Н), 4,88-4,75 (м, 1Н), 3,96 (дд, J=10,7, 6,7 Гц, 1Н), 3,51 (с, 3Н), 2,92 (т, J=11,1 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 169,7, 158,5, 156,7, 144,3, 139,9, 139,2, 134,8, 133,7, 129,4, 129,2, 128,5, 127,4, 121,3, 118,3, 115,2, 54,6, 49,8, 37,6, 37,4. МС-ЭРИ: m/z 468, 0 (М+Н)+.
[0271] RIP1-027
[0272] 1Н-ЯМР (400 МГц, CDCl3) δ 8,23 (шс, 1Н), 7,81 (с, 1Н), 7,54 (с, 1Н), 7,29-7,26 (м, 1Н), 7,25-7,20 (м, 4Н), 4,70 (дд, J=11,2, 6,8 Гц, 1Н), 4,10 (с, 2Н), 3,72 (дд, J=11,0, 6,8 Гц, 1Н), 3,47 (с, 3Н), 2,86 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 169,8, 158,4, 139,9, 139,4, 135,8, 134,6, 129,0, 128,9, 127,9, 127,3, 121,2, 118,4, 115,3, 49,5, 37,6, 37,2, 33,2. МС-ЭРИ: m/z 466, 0 (М-Н)-.
[0273] RIP1-028
[0274] 1Н-ЯМР (400 МГц, CDCl3) δ 11,69 (с, 1Н), 8,16 (д, J=7,9 Гц, 1Н), 7,68 (с, 1Н), 7,51-7,44 (м, 3Н), 7,37-7,31 (м, 3Н), 7,17-7,10 (м, 2Н), 5,12 (д, J=16,7 Гц, 2Н), 4,87 (дт, J=11,5, 7,2 Гц, 1Н), 3,82 (дд, J=11,0, 6,6 Гц, 1Н), 3,47 (с, 3Н), 2,97 (т, J=11,3 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,1, 162,3, 139,7, 139,6, 137,4, 136,6, 135,1, 135,0, 129,3, 128,8, 127,9, 127,7, 122,9, 121,2, 117,3, 115,3, 51,5, 49,1, 37,7, 37,5. МС-ЭРИ: m/z 467,0 (М+Н)+.
[0275] RIP1-029
[0276] 1Н-ЯМР (400 МГц, CDCl3) δ 10,90 (шс, 1Н), 7,91 (с, 1Н), 7,78 (с, 1Н), 7,56 (с, 1Н), 7,37-7,27 (м, 3Н), 7,24-7,19 (м, 2Н), 6,28 (с, 1Н), 4,78 (дд, J=11,2, 6,7 Гц, 1Н), 4,09 (с, 2Н), 3,81 (дд, J=11,1, 6,7 Гц, 1Н), 3,50 (с, 3Н), 2,92 (т, J=11,3 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 174,3, 169,5, 158,6, 158,0, 139,7, 139,7, 135,5, 135,3, 129,1, 128,9, 128,2, 127,5, 121,5, 117,5, 115,6, 101,7, 49,5, 37,6, 37,3, 33,3. МС-ЭРИ: m/z 4 68, 0 (М+Н)+.
[0277] RIP1-030
[0278] 1Н-ЯМР (400 МГц, CDCl3+CD3OD) δ 11,85 (шс, 1Н), 8,19 (д, J=7,1 Гц, 1Н), 7,91 (с, 1Н), 7,80 (с, 1Н), 7,57 (с, 1Н), 7,41-7,31 (м, 3Н), 7,26-7,19 (м, 2Н), 5,57-5,46 (м, 2Н), 4,84-4,68 (м, 1Н), 3,76 (дд, J=10,7, 6,7 Гц, 1Н), 3,45 (д, J=29,4 Гц, 3Н), 2,92 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3+CD3OD) δ 169,9, 159,4, 142,8, 139,7, 139,6, 134,9, 133,8, 129,4, 129,2, 128,3, 128,1, 125,7, 121,3, 117,7, 115,5, 54,6, 49,2, 37,6, 37,4. МС-ЭРИ: m/z 468,1 (М+Н)+.
[0279] RIP1-031
[0280] 1Н-ЯМР (400 МГц, CDCl3) δ 11,05 (с, 1Н), 8,03 (д, J=7,3 Гц, 1Н), 7,53-7,46 (м, 2Н), 7,43 (с, 1Н), 7,39-7,30 (м, 3Н), 7,18 (с, 1Н), 7,17-7,11 (м, 2Н), 5,21-5,04 (м, 3Н), 4,72-4,63 (м, 1Н), 4,29 (дд, J=11,3, 9,9 Гц, 1Н), 3,51 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,8, 162,8, 150,7, 139,7, 137,4, 136,4, 135,1, 134,7, 132,3, 129,3, 128,8, 127,7, 122,9, 117,6, 113,6, 103,5, 76,8, 51,5, 48,7, 36,5. МС-ЭРИ: m/z 451,1 (М+Н)+.
[0281] RIP1-032
[0282] 1Н-ЯМР (400 МГц, CDCl3) δ 11,53 (с, 1Н), 8,15 (д, J=6,4 Гц, 1Н), 8,08 (с, 1Н), 7,46 (с, 1Н), 7,40-7,28 (м, 5Н), 5,37 (с, 2Н), 5,07 (дт, J=11,1, 6,9 Гц, 1Н), 4,85 (дд, J=9,6, 7,4 Гц, 1Н), 4,35-4,25 (м, 1Н), 3,52 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,4, 159,0, 156,5, 150,3, 144,4, 139,9, 134,4, 133,7 131,8, 129,3, 129,2, 128,5, 117,7, 113,5, 104,6, 76,6, 54,6, 49,5, 36,6. МС-ЭРИ: m/z 452, 1 (М+Н)+.
[0283] RIP1-033
[0284] 1Н-ЯМР (400 МГц, CDCl3) δ 11,38 (шс, 1Н), 7,83 (шс, 1Н), 7,40 (с, 1Н), 7,30-7,11 (м, 6Н), 6,24 (с, 1Н), 5,07-4,93 (м, 1Н), 4,67-4,55 (м, 1Н), 4,21 (т, J=10,5 Гц, 1Н), 4,02 (с, 2Н), 3,45 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 174,4, 168,2, 159,1, 157,8, 150,8, 139,7, 135,2, 135,1, 132,3, 129,0, 128,9, 127,5, 117,8, 114,0, 103,8, 101,7, 76,4, 49,1, 36,7, 33,3. МС-ЭРИ: m/z 452, 1 (М+Н)+.
[0285] RIP1-034
[0286] 1Н-ЯМР (400 МГц, CDCl3+CD3OD) δ 7,45 (с, 1Н), 7,32-7,12 (м, 6Н), 5,05-4,92 (м, 1Н), 4,61 (т, J=8,4 Гц, 1Н), 4,22 (т, J=10,4 Гц, 1Н), 4,08 (с, 2Н), 3,46 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3+CD3OD) δ 168,5, 158,8, 150,5, 139,9, 135,7, 134,3, 132,0, 128,84, 128,80, 127,2, 117,6, 113,7, 104,2, 76,3, 49,0, 36,6, 33,1. МС-ЭРИ: m/z 452,1 (М+Н)+.
[0287] RIP1-035
[0288] 1Н-ЯМР (400 МГц, CDCl3) δ 7,92 (с, 1Н), 7,49 (с, 1Н), 7,36-7,32 (м, 2Н), 7,29-7,18 (м, 5Н), 5,51 (с, 2Н), 5,07-4,95 (м, 1Н), 4,61 (дд, J=9,7, 7,4 Гц, 1Н), 4,29-4,20 (м, 1Н), 3,49 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,6, 159,8, 150,6, 142,3, 139,8, 134,3, 133,8, 132,1, 129,2, 129,0, 128,1, 125,8, 117,5, 113,8, 103,9, 76,3, 54,4, 48,6, 36,5. МС-ЭРИ: m/z 452, 1 (М+Н)+.
[0289] RIP1-036
[0290] 1Н-ЯМР (400 МГц, CDCl3) δ 8,01 (д, J=7,7 Гц, 1Н), 7,81 (с, 1Н), 7,69 (д, J=1,8 Гц, 1Н), 7,50 (с, 1Н), 7,44 (д, J=7,7 Гц, 2Н), 7,38-7,29 (м, 3Н), 7,17-7,07 (м, 2Н), 6,76 (с, 1Н), 5,08 (с, 2Н), 4,77 (дт, J=11,1, 7,5 Гц, 1Н), 3,79 (дд, J=11,0, 6,8 Гц, 1Н), 3,45 (с, 3Н), 2,89 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,6, 161,6, 153,1, 147,4, 141,4, 137,1, 135,3, 129,6, 129,2, 128,7, 127,6, 123,3, 122,4, 118,3, 117,3, 106,8, 51,4, 49,1, 38,7, 37,1. МС-ЭРИ: m/z 433,1 (М+Н)+.
[0291] RIP1-037
[0292] 1Н-ЯМР (400 МГц, CDCl3) δ 8,15 (д, J=7,7 Гц, 1Н), 8,02 (с, 1Н), 7,82 (с, 1Н), 7,70 (д, J=2,2 Гц, 1Н), 7,50 (с, 1Н), 7,38-7,32 (м, 3Н), 7,27-7,22 (м, 2Н), 6,77 (дд, J=2,1, 0,9 Гц, 1Н), 5,35 (с, 2Н), 4,80 (дт, J=11,1, 7,2 Гц, 1Н), 3,89 (дд, J=11,2, 6,9 Гц, 1Н), 3,45 (с, 3Н), 2,87 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,2, 157,9, 156,9, 153,1, 147,5, 144,0, 141,0, 133,9, 129,6, 129,2, 129,0, 128,3, 123,0, 118,4, 117,3, 106,7, 54,3, 49,5, 38,5, 37,2. МС-ЭРИ: m/z 434,1 (М+Н)+.
[0293] RIP1-038
[0294] 1Н-ЯМР (400 МГц, CDCl3) δ 7,87-7,79 (м, 2Н), 7,71 (д, J=2,1 Гц, 1Н), 7,52 (с, 1Н), 7,35-7,19 (м, 5Н), 6,79 (д, J=1,3 Гц, 1Н), 6,27 (с, 1Н), 4,74 (дт, J=11,2, 7,2 Гц, 1Н), 4,08 (с, 2Н), 3,83 (дд, J=11,1, 6,9 Гц, 1Н), 3,46 (с, 3Н), 2,88 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 174,0, 169,9, 158,2, 158,1, 153,1, 147,5, 141,1, 135,3, 129,7, 129,0, 128,9, 127,4, 123,1, 118,4, 117,4, 106,8, 101,7, 49,6, 38,3, 37,2, 33,3. МС-ЭРИ: m/z 434, 1 (М+Н)+.
[0295] RIP1-039
[0296] 1Н-ЯМР (400 МГц, CDCl3) δ 8,25 (д, J=7,9 Гц, 1Н), 7,80 (с, 1Н), 7,70 (д, J=2,1 Гц, 1Н), 7,46 (с, 1Н), 7,15 (с, 5Н), 6,76 (д, J=1,3 Гц, 1Н), 4,77 (дт, J=11,3, 7,4 Гц, 1Н), 4,06 (с, 2Н), 3,74 (дд, J=11,2, 6,9 Гц, 1Н), 3,42 (с, 3Н), 2,87 (т, J=11,3 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,4, 158,7, 153,1, 147,5, 141,1, 136,1, 129,8, 128,9, 128,7, 127,0, 123,0, 118,3, 117,4, 106,8, 49,6, 38,3, 37,3, 32,9. МС-ЭРИ: m/z 434,1 (М+Н)+.
[0297] RIP1-040
[0298] 1Н-ЯМР (400 МГц, CDCl3) δ 8,11 (д, J=7,5 Гц, 1Н), 7,87 (с, 1Н), 7,82 (с, 1Н), 7,70 (д, J=1,7 Гц, 1Н), 7,51 (с, 1Н), 7,39-7,31 (м, 3Н), 7,26-7,20 (м, 2Н), 6,78 (с, 1Н), 5,59-5,45 (м, 2Н), 4,77 (дт, J=11,1, 7,3 Гц, 1Н), 3,81 (дд, J=11,1, 6,9 Гц, 1Н), 3,46 (с, 3Н), 2,91 (т, J=11,2 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,2, 159,1, 153,1, 147,5, 143,1, 141,3, 133,9, 129,7, 129,4, 129,2, 128,3, 125,4, 123,2, 118,3, 117,3, 106,8, 54,6, 49,3, 38,5, 37,2. МС-ЭРИ: m/z 434,1 (М+Н)+.
[0299] RIP1-041
[0300] 1Н-ЯМР (500 МГц, CDCl3) δ=8,59 (с, 1Н), 8,12 (ш, 1Н), 7,72 (с, 1Н), 7,55 (с, 1Н), 7,34-7,27 (м, 6Н), 6,56 (с, 1Н), 4,77-4,70 (м, 1Н), 4,23 (с, 2Н), 3,84 (дд, J=11,2, 6,9, 1Н), 3,49 (с, 3Н), 2,84 (т, J=11,1, 1Н). МС-ЭРИ: 434,1 (М+Н)+.
[0301] RIP1-042
[0302] 1Н-ЯМР (500 МГц, CDCl3) δ=8,83 (с, 1Н), 8,16 (д, J=7,8, 1Н), 7,86 (с, 1Н), 7,67 (с, 1Н), 7,51 (с, 1Н), 7,37-7,33 (м, 3Н), 7,26-7,21 (м, 3Н), 6,50 (с, 1Н), 5,51 (д, J=7,1, 2Н), 4,85-4,79 (м, 1Н), 3,81 (дд, J=11,2, 6,9, 1Н), 3,48 (с, 3Н), 2.88 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,33, 159,19, 143,19, 138,10, 134,68, 133,93, 129,45, 129,37, 129,17, 128,31, 127,00, 125,44, 119,89, 118,01, 116,83, 102,98, 54,59, 49,56, 38,48, 37,33; МС-ЭРИ: 433,2 (М+Н)+.
[0303] RIP1-043
[0304] 1Н-ЯМР (500 МГц, CDCl3) δ=8,83 (с, 1Н), 8,19 (д, J=7,4, 1Н), 7,72 (с, 1Н), 7,53 (с, 1Н), 7,39-7,34 (м, 5Н), 7,31-7,29 (м, 1Н), 6,54-6,52 (м, 1Н), 5,79 (с, 2Н), 4,86-4,81 (м, 1Н), 3,92 (дд, J=11,2, 6,9, 1Н), 3,49 (с, 3Н), 2,85 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 169,94, 159,74, 155,64, 137,78, 134,80, 132,51, 129,54, 129,43, 129,26, 128,73, 127,21, 119,64, 118,26, 116,88, 103,00, 57,59, 50,07, 38,32, 37,40; МС-ЭРИ: 434, 1 (М+Н)+.
[0305] RIP1-044
[0306] 1Н-ЯМР (400 МГц, CDCl3) δ=9,17 (с, 1Н), 7,89 (д, J=7,8, 1Н), 7,66 (с, 1Н), 7,49 (с, 1Н), 7,23 (т, J=2,7, 1Н), 7,08 (д, J=7,8, 2Н), 6,98 (д, J=7,9, 2Н), 6,46 (с, 1Н), 6,46 (с, 1Н), 4,88-4,80 (м, 1Н), 3,91 (с, 2Н), 3,86 (дд, J=11,1, 6,8, 1Н), 3,69 (с, 3Н), 3,48 (с, 3Н), 2,87 (т, J=11,2, 1Н), 2,30 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,84, 161,46, 144,46, 143,36, 137,92, 136,61, 134,74, 133,66, 129,58, 129,36, 128,34, 127,05, 119,66, 118,07, 116,69, 106,81, 102,72, 77,48, 77,16, 76,84, 49,50, 38,65, 37,27, 37,12, 31,56, 21,12; МС-ЭРИ: 460,2 (М+Н)+.
[0307] RIP1-045
[0308] 1Н-ЯМР (500 МГц, CDCl3) δ=8,68 (с, 1Н), 7,69 (с, 1Н), 7,54 (с, 1Н), 7,28 (с, 1Н), 7,14-7,07 (м, 5Н), 6,54 (с, 1Н), 6,30 (с, 1Н), 4,75-4,68 (м, 1Н), 4,01 (с, 3Н), 3,89 (с, 2Н), 3,81 (дд, J=11,0, 6,8, 1Н), 3,47 (с, 3Н), 2,78 (т, J=11,1, 1Н), 2,33 (с, 3Н); МС-ЭРИ: 460,15 (М+Н)+.
[0309] RIP1-046
[0310] 1Н-ЯМР (500 МГц, CDCl3) δ=8,85 (с, 1Н), 8,00 (с, 1Н), 7,99 (д, J=8,4, 1Н), 7,68 (с, 1Н), 7,52 (с, 1Н), 7,35-7,31 (м, 2Н), 7,30-7,25 (м, 3Н), 6,50 (с, 1Н), 4,83-4,77 (м, 1Н), 4,10 (с, 2Н), 3,83 (дд, J=11,1, 6,8, 1Н), 3,49 (с, 3Н), 2,87 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,31, 162,98, 159,70, 141,31, 137,89, 135,78, 134,64, 134,58, 129,33, 128,80, 128,80, 127,31, 126,89, 119,70, 117,90, 116,70, 102,85, 49,36, 38,37, 37,16, 34,49; МС-ЭРИ: 433,1 (М+Н)+.
[0311] RIP1-047
[0312] 1Н-ЯМР (500 МГц, CD3OD) δ=7,74 (с, 1Н), 7,69 (с, 1Н), 7,59 (с, 1Н), 7,40 (д, J=3,1, 1Н), 7,34-7,29 (м, 2Н), 7,26-7,21 (м, 3Н), 6,55 (дд, J=3,1, 0,7, 1Н), 4,10 (с, 2Н), 3,94-3,90 (м, 1Н), 3,64 (дд, J=11,2, 6,9, 1Н), 3,45 (с, 3Н), 2,95 (т, J=11,4, 1Н); МС-ЭРИ: 432,1 (М+Н)+.
[0313] RIP1-048
[0314] 1Н-ЯМР (500 МГц, CDCl3) δ=8,15 (д, J=7,5, 1Н), 7,86 (с, 1Н), 7,64 (с, 1Н), 7,52 (с, 1Н), 7,38-7,34 (м, 3Н), 7,26-7,22 (м, 2Н), 7,14 (д, J=2,8, 1Н), 6,47 (д, J=3,0, 1Н), 5,52 (д, J=7,6, 2Н), 4,81-1,74 (м, 1Н), 3,82 (с, 3Н), 3,80 (дд, J=7,0, 4,2, 1Н), 3,48 (с, 3Н), 2,87 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,30, 159,10, 143,24, 137,88, 135,60, 133,96, 131,45, 129,92, 129,38, 129,18, 128,32, 125,43, 119,69, 117,06, 116,37, 101,54, 54,60, 49,56, 38,52, 37,30, 33,29; МС-ЭРИ: 447,4 (М+Н)+.
[0315] RIP1-049
[0316] 1Н-ЯМР (500 МГц, CDCl3) δ=8,00 (с, 1Н), 7,95 (д, J=7,6, 1Н), 7,65 (с, 1Н), 7,53 (с, 1Н), 7,37-7,32 (м, 2Н), 7,31-7,27 (м, 3Н), 7,15 (д, J=3,0, 1Н), 6,48 (д, J=3,0, 1Н), 4,79-4,73 (м, 1Н), 4,11 (с, 2Н), 3,85-3,81 (м, 4Н), 2,86 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,47, 163,01, 159,70, 141,36, 137,83, 136,05, 135,63, 134,85, 131,47, 129,94, 128,94, 127,44, 119,65, 119,54, 117,06, 116,40, 101,55, 49,45, 38,56, 37,26, 34,65, 33,30; МС-ЭРИ: 447,4 (М+Н)+.
[0317] RIP1-050
[0318] 1Н-ЯМР (500 МГц, CDCl3) δ=8,85 (ш, 1Н), 7,60 (с, 1Н), 7,50 (с, 1Н), 7,34 (д, J=7,0, 2Н), 7,23 (т, J=7,3, 2Н), 7,20-7,16 (м, 2Н), 7,14 (д, J=3,0, 1Н), 7,02 (д, J=5,9, 1Н), 6,47 (д, J=3,1, 1Н), 5,29 (с, 2Н), 4,72-4,67 (м, 1Н), 3,80 (с, 3Н), 3,68 (дд, J=11,4, 7,0, 1Н), 3,41 (с, 3Н), 3,17 (т, J=11,4, 1Н); 13С-ЯМР (126 МГц, CDCl3) δ 171,54, 159,75, 148,15, 137,59, 135,62, 131,65, 129,99, 129,25, 129,17, 128,78, 128,60, 127,73, 119,59, 117,19, 116,18, 101,75, 101,54, 53,56, 50,53, 49,68, 37,71, 33,29; МС-ЭРИ: 447,3 (М+Н)+.
[0319] RIP1-051
[0320] 1Н-ЯМР (500 МГц, CDCl3) δ=8,64 (с, 1Н), 8,06 (с, 1Н), 7,69 (с, 1Н), 7,65 (д, J=7,3, 1Н), 7,56 (с, 1Н), 7,32-7,30 (м, 1Н), 7,25-7,19 (м, 5Н), 6,57-6,55 (м, 1Н), 5,82 (д, J=3,1, 2Н), 4, 76-4,70 (м, 1Н), 3,75 (дд, J=11,3, 7,0, 1Н), 3,48 (с, 3Н), 2,79 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,38, 156,74, 137,78, 135,46, 134,75, 134,24, 129,92, 129,57, 128,78, 128,31, 128,05, 127,16, 119,75, 118,03, 117,03, 103,24, 53,28, 50,04, 38,17, 37,49 МС-ЭРИ: 433,1 (М+Н)+.
[0321] RIP1-052
[0322] 1Н-ЯМР (500 МГц, CDCl3) δ=8,02 (с, 1Н), 7,64 (с, 1Н), 7,54 (с, 1Н), 7,41 (д, J=7,2, 1Н), 7,26-7,20 (м, 5Н), 7,17 (д, J=3,0, 1Н), 6,50 (д, J=3,0, 1Н), 5,82 (с, 2Н), 4,71-4,65 (м, 1Н), 3,84 (с, 3Н), 3,77 (дд, J=11,2, 6,9, 1Н), 3,48 (с, 3Н), 2,75 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,15, 156,66, 137,40, 135,98, 135,69, 135,45, 134,14, 131,69, 130,00, 128,78, 128,34, 128,11, 119,33, 117,14, 116,43, 101,64, 53,24, 50,03, 38,26, 37,39, 33,32; МС-ЭРИ: 447,3 (М+Н)+.
[0323] RIP1-054
[0324] 1Н-ЯМР (500 МГц, CDCl3) δ=7,62 (с, 1Н), 7,57 (с, 1Н), 7,53 (с, 1Н), 7,52 (с, 1Н), 7,27 (с, 1Н), 7,26-7,23 (м, 2Н), 7,16 (д, J=7,1, 1Н), 7,14 (д, J=2,9, 1Н), 7,07 (д, J=7,0, 2Н), 6,47 (д, J=3,0, 1Н), 5,44 (с, 2Н), 4,71-4,65 (м, 1Н), 3,81 (с, 3Н), 3,77 (дд, J=11,1, 6,7, 1Н), 3,47 (с, 1Н), 2,75 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,53, 159,00, 141,58, 137,61, 136,60, 135,62, 132,56, 131,51, 129,90, 128,91, 128,06, 127,35, 127,27, 119,52, 117,06, 116,35, 101,55, 49,97, 49,63, 38,50, 37,26, 33,25; МС-ЭРИ: 446,4 (М+Н)+.
[0325] RIP1-055
[0326] 1Н-ЯМР (500 МГц, CDCl3) δ=8,03 (д, J=7,7, 1Н), 7,63 (с, 1Н), 7,50 (с, 1Н), 7,45 (с, 1Н), 7,43 (с, 1Н), 7,35-7,30 (м, 3Н), 7,13 (д, J=3,5, 3Н), 6,46 (д, J=3,0, 1Н), 5,07 (с, 2Н), 4,80-4,75 (м, 1Н), 3,82-3,78 (м, 4Н), 3,47 (с, 3Н), 2,86 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,77, 161,55, 138,01, 137,24, 137,06, 135,56, 135,31, 131,33, 129,86, 129,23, 128,69, 127,57, 122,37, 119,81, 117,00, 116,33, 101,48, 51,40, 49,30, 38,69, 37,21, 33,25; МС-ЭРИ: 446,4 (М+Н)+.
[0327] RIP1-056
[0328] 1H-ЯМР (500 МГц, CDCl3) δ=7,84 (д, J=7,6, 1Н), 7,64 (с, 1Н), 7,51 (с, 1Н), 7,14 (д, J=2,9, 1Н), 7,08 (д, J=7,8, 2Н), 6,98 (д, J=7,8, 2Н), 6,47 (д, J=3,0, 1Н), 6,45 (с, 1Н), 4,81-4,75 (м, 1Н), 3,90 (с, 2Н), 3,86-3,82 (м, 4Н), 3,69 (с, 3Н), 3,48 (с, 3Н), 2,84 (т, J=11,1, 1Н), 2,31 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,86, 161,24, 144,67, 143,21, 137,91, 136,60, 135,60, 133,73, 131,38, 129,89, 129,58, 128,34, 119,76, 117,01, 116,39, 106,82, 101,50, 49,46, 38,69, 37,22, 37,09, 33,27, 31,58, 21,12; МС-ЭРИ: 474,4 (М+Н)+.
[0329] RIP1-057
[0330] 1Н-ЯМР (500 МГц, CDCl3) δ=7,63 (с, 1Н), 7,52 (с, 1Н), 7,14 (д, J=3,0, 1Н), 7,13-7,09 (м, 4Н), 7,07 (д, J=7,3, 1Н), 6,47 (д, J=3,0, 1Н), 6,29 (с, 1Н), 4,72-4,66 (м, 1Н), 4,01 (с, 3Н), 3,89 (с, 2Н), 3,83-3,78 (м, 4Н), 3,47 (с, 3Н), 2,77 (т, J=11,1, 1Н), 2,33 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,44, 158,73, 150,97, 137,56, 136,44, 136,02, 135,64, 135,30, 131,55, 129,94, 129,42, 128,74, 119,42, 117,01, 116,37, 105,91, 101,57, 49,71, 39,07, 38,45, 37,18, 34,20, 33,26, 21,17; МС-ЭРИ: 474,4 (М+Н)+.
[0331] RIP1-058
[0332] 1Н-ЯМР (500 МГц, CDCl3) δ=8,32 (с, 1Н), 8,12 (д, J=7,4, 1Н), 7,65 (с, 1Н), 7,53 (с, 1Н), 7,36-7,29 (м, 4Н), 7,16 (д, J=3,0, 1Н), 6,49 (д, J=3,0, 1Н), 4,74-4,68 (м, 1Н), 4,23 (с, 2Н), 3,86-3,81 (м, 4Н), 3,48 (с, 3Н), 2,85 (т, J=11,1, 1Н); МС-ЭРИ: 448,4 (М+Н)+.
[0333] RIP1-059
[0334] 1Н-ЯМР (400 МГц, Метанол-d4) δ 8,31 (с, 1Н), 7,97 (с, 1Н), 7,81 (дд, J=9,0, 1,4 Гц, 1Н), 7,79-7,73 (м, 2Н), 7,61 (д, J=1,3 Гц, 1Н), 7,39-7,24 (м, 6Н), 5,26 (с, 1Н), 5,22 (с, 2Н), 4,69 (дд, J=11,5, 6,9 Гц, 1Н), 3,68 (дд, J=11,3, 6,9 Гц, 1Н), 3,46 (с, 3Н), 2,98 (т, J=11,4 Гц, 1Н); ЭРИ: m/z 433,1 (М+Н)+.
[0335] RIP1-060
[0336] 1Н-ЯМР (400 МГц, Метанол-d4) δ 8,55 (с, 1Н), 8,32 (с, 1Н), 7,97 (с, 1Н), 7,76 (с, 1Н), 7,36-7,34 (м, 4Н), 7,33 (д, J=3,5 Гц, 5Н), 5,44 (с, 2Н), 5,42 (с, 1Н), 4,71 (дд, J=11,6, 6,9 Гц, 1Н), 3,68 (дд, J=11,4, 6,9 Гц, 1Н), 3,45 (с, 2Н), 3,15-2,95 (м, 1Н); ЭРИ: m/z 434,1 (М+Н)+.
[0337] RIP1-061
[0338] 1Н-ЯМР (500 МГц, CDCl3) δ=7,82 (д, J=7,0, 1Н), 7,38 (ш, 1Н), 7,35-7,24 (м, 5Н), 7,21 (д, J=7,3, 2Н), 6,27 (с, 1Н), 4,99-4,93 (м, 1Н), 4,66 (дд, J=9,4, 7,9, 1Н), 4,22 (т, J=10,5, 1Н), 4,09 (с, 2Н), 3,42 (с, 3Н), 2,61 (с, 3Н); МС-ЭРИ: 432,1 (М+Н)+; МСВР (ESI) Вычисл. для C23H22O4N5 (М+Н)+: 432,1666, найдено: 432,1662.
[0339] RIP1-062
[0340] 1Н-ЯМР (500 МГц, CDCl3) δ=7,87 (с, 1Н), 7,79 (с, 1Н), 7,37-7,27 (м, 4Н), 7,24-7,20 (м, 3Н), 7,17 (д, J=6,8, 1Н), 5,27 (с, 2Н), 5,00-4,94 (м, 1Н), 4,66 (дд, J=9,6, 7,6, 1Н), 4,21 (т, J=10,5, 1Н), 3,40 (с, 3Н), 2,57 (с, 3Н); МС-ЭРИ: 431,4 (М+Н)+; МСВР (ESI) Вычисл. для C23H23O3N6 (М+Н)+: 431,1826, найдено: 431,1827.
[0341] RIP1-063
[0342] 1Н-ЯМР (500 МГц, CDCl3) δ=8,09 (д, J=7,3, 1Н), 7,91 (с, 1Н), 7,36-7,31 (м, 3Н), 7,29 (с, 1Н), 7,25-7,20 (м, 3Н), 5,51 (д, J=3,9, 2Н), 5,03-4,97 (м, 1Н), 4,62 (дд, J=9,3, 7,8, 1Н), 4,24 (т, J=0,5, 1Н), 3,39 (с, 3Н), 2,56 (с, 3Н); МС-ЭРИ: 432,3 (М+Н)+; МСВР (ESI) Вычисл. для C22H22O3N7 (М+Н)+: 432,1779, найдено: 432,1778.
[0343] RIP1-064
[0344] 1Н-ЯМР (500 МГц, CDCl3) δ=8,10 (с, 1Н), 7,74 (д, J=7,0, 1Н), 7,37 (с, 1Н), 7,30 (с, 1Н), 7,26-7,18 (м, 5Н), 5,80 (с, 2Н), 5,05-4,97 (м, 1Н), 4,65-4,53 (м, 1Н), 4,20 (т, J=10,4, 1Н), 3,44 (с, 3Н), 2,62 (с, 3Н); МС-ЭРИ: 432,4 (М+Н)+; МСВР (ESI) Вычисл. для C22H22O3N7 (М+Н)+: 432,1779, найдено: 432,1779.
[0345] RIP1-065
[0346] 1Н-ЯМР (500 МГц, CDCl3) δ=8,04 (с, 1Н), 7,94 (д, J=7,3, 1Н), 7,35-7,26 (м, 6Н), 7,24 (с, 1Н), 5,00-4,94 (м, 1Н), 4,64 (дд, J=9,6, 7,6, 1Н), 4,24 (т, J=10,5, 1Н), 4,11 (с, 2Н), 3,41 (с, 3Н), 2,58 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 168,70, 163,42, 160,70, 153,52, 146,05, 141,68, 136,01, 135,52, 134,61, 131,65, 128,96, 128,92, 128,67, 127,51, 109,29, 107,33, 77,16, 49,14, 36,31, 34,60, 14,95; МС-ЭРИ: 432,3 (М+Н)+; МСВР (ESI) Вычисл. для C23H22O4N5 (М+Н)+: 432,1666, найдено: 432,1668.
[0347] RIP1-066
[0348] 1Н-ЯМР (500 МГц, CDCl3) δ=7,68-7,62 (м, 2Н), 7,48 (д, J=6,5, 1Н), 7,39-7,27 (м, 4Н), 7,24 (д, J=6,5, 2Н), 7,18 (т, J=7,3, 1Н), 7,15 (д, J=7,6, 2Н), 5,07-4,96 (м, 1Н), 4,77 (дд, J=9,5, 7,6, 1H), 4,25 (т, J=10,4, 1H), 4,00 (с, 2H), 3,44 (с, 3Н), 2,55 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 169,13, 167,46, 153,51, 146,01, 142,09, 140,34, 133,42, 132,99, 131,31, 129,02, 128,96, 128,72, 127,82, 126,49, 125,02, 109,75, 109,71, 106,91, 106,87, 77,41, 50,00, 41,83, 36,38, 14,96; МС-ЭРИ: 431,3 (М+Н)+; МСВР (ESI) Вычисл. для C26H25O3N4 (М+Н)+: 431,1921, найдено: 432,1922.
[0349] RIP1-067
[0350] 1Н-ЯМР (500 МГц, CD3OD) δ=7,76 (с, 1Н), 7,63 (с, 1Н), 7,51 (с, 1Н), 7,36-7,27 (м, 4Н), 7,24 (д, J=7,7, 2Н), 5,21 (с, 2Н), 5,00-4,94 (м, 1Н), 4,53 (дд, J=9,7, 7,8, 1Н), 4,29 (т, J=10,6, 1Н), 3,43 (с, 3Н), 2,58 (с, 3Н); 13С-ЯМР (125 МГц, CD3OD) δ 171,00, 164,12, 155,23, 147,60, 139,43, 137,54, 136,79, 133,32, 130,05, 129,42, 128,86, 124,35, 110,26, 110,25, 108,27, 108,24, 78,21, 52,01, 50,22, 36,48, 14,35; МС-ЭРИ: 431,4 (М+Н)+; МСВР (ESI) Вычисл. для C23H23O3N6 (М+Н)+: 431,1826, найдено: 431,1829.
[0351] RIP1-068
[0352] 1Н-ЯМР (500 МГц, CDCl3) δ=8,18 (д, J=6,8, 1Н), 8,10 (с, 1Н), 7,38-7,32 (м, 4Н), 7,26-7,22 (м, 3Н), 5,36 (с, 2Н), 5,03-4,97 (м, 1Н), 4,77 (дд, J=9,2, 7,9, 1Н), 4,25 (т, J=10,4, 1Н), 3,42 (с, 3Н), 2,56 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 168,59, 159,01, 156,58, 153,60, 145,85, 144,35, 133,69, 131,17, 129,35, 129,17, 128,33, 109,89, 109,84, 107,10, 107,05, 77,36, 54,54, 49,69, 36,35, 14,92; МС-ЭРИ: 432,4 (М+Н)+; МСВР (ESI) Вычисл. для C22H22O3N7 (М+Н)+: 432,1779, найдено: 432,1777.
[0353] RIP1-069
[0354] 1Н-ЯМР (500 МГц, CDCl3) δ=7,65 (с, 1Н), 7,56 (с, 1Н), 7,30-7,26 (м, 2Н), 7,26-7,19 (м, 4Н), 7,07 (д, J=1,3, 1Н), 7,06 (с, 1Н), 5,44 (с, 2Н), 4,98-4,91 (м, 1Н), 4,60 (дд, J=9,7, 7,6, 1Н), 4,23-4,09 (м, 1Н), 3,41 (с, 3Н), 2,57 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 169,19, 159,69, 153,28, 146,06, 141,71, 136,46, 132,94, 131,44, 128,97, 128,16, 127,25, 125,03, 109,68, 109,66, 107,23, 107,22, 77,36, 50,14, 49,18, 36,39, 15,06; МС-ЭРИ: 431,4 (М+Н)+; МСВР (ESI) Вычисл. для C23H23O6N3 (М+Н)+: 431,1826, найдено: 431,1829.
[0355] RIP1-070
[0356] 1Н-ЯМР (500 МГц, CDCl3) δ=8,11 (Д, J=6,9, 1H), 7,41 (с, 1H), 7,34-7,26 (м, 6Н), 4,99-4,93 (м, 1Н), 4,68 (дд, J=9,6, 7,8, 1Н), 4,26-4,20 (м, 4Н), 3,43 (с, 3Н), 2,61 (с, 3Н); МС-ЭРИ: 433,4 (М+Н)+; МСВР (ESI) Вычисл. для C22H21O4N6 (М+Н)+: 433,1619, найдено: 433,1613.
[0357] RIP1-071
[0358] 1Н-ЯМР (500 МГц, CDCl3) δ=8,16 (д, J=6,7, 1Н), 7,40 (с, 1Н), 7,39-7,33 (м, 5Н), 7,29 (с, 1Н), 5,80 (с, 2Н), 5,06-5,00 (м, 1Н), 4,77 (дд, J=9,6, 7,7, 1Н), 4,25 (т, J=10,4, 1Н), 3,44 (с, 3Н), 2,60 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 168,24, 159,37, 156,51, 153,65, 146,04, 132,32, 131,31, 129,55, 129,32, 128,76, 110,18, 110,14, 107,06, 107,01, 77,04, 57,75, 49,82, 36,42, 14,96; МС-ЭРИ: 433,3 (М+Н)+; МСВР (ESI) Вычисл. для C21H21O3N8 (М+Н)+: 433,1731, найдено: 433,1733.
[0359] RIP1-072
[0360] 1Н-ЯМР (500 МГц, CDCl3) δ=7,86 (д, J=7,1, 1Н), 7,28 (с, 1Н), 7,24 (с, 1Н), 7,08 (д, J=7,8, 2H), 6,98 (д, J=7,7, 2H), 6,45 (с, 1Н), 5,02-4,93 (м, 1Н), 4,68 (т, J=8,6, 1Н), 4,24 (т, J=10,4, 1Н), 3,91 (с, 2Н), 3,72 (с, 3Н), 3,40 (с, 3Н), 2,57 (с, 3Н), 2,30 (с, 3Н); 13С-ЯМР (125 МГц, CDCl3) δ 168,97, 162,35, 153,60, 145,99, 143,87, 143,82, 136,74, 133,46, 131,58, 129,62, 128,35, 109,21, 109,16, 107,33, 107,25, 106,77, 77,36, 49,22, 37,21, 36,26, 31,58, 21,10, 14,93; МС-ЭРИ: 459,4 (М+Н)+; МСВР (ESI) Вычисл. для C25H27O3N6 (М+Н)+: 459,2139, найдено: 59,2141.
[0361] RIP1-073
[0362] 1Н-ЯМР (500 МГц, CDCl3) δ=7,37 (с, 1Н), 7,26 (с, 1Н), 7,13-7,08 (м, 5Н), 6,36 (с, 1Н), 4,96-4,89 (м, 1Н), 4,64 (дд, J=9,6, 7,6, 1Н), 4,16 (т, J=10,5, 1Н), 4,01 (с, 3Н), 3,89 (с, 2Н), 3,42 (с, 3Н), 2,61 (с, 3Н), 2,31 (с, 3Н); 13С-ЯМР (126 МГц, CDCl3) δ 168,86, 159,53, 153,46, 151,15, 146,25, 136,27, 136,10, 134,95, 131,73, 129,43, 128,71, 107,19, 107,17, 107,13, 107,13, 106,33, 77,29, 49,32, 39,10, 36,34, 34,14, 21,14, 15,01; МС-ЭРИ: 459,4 (М+Н)+; МСВР (ESI) Вычисл. для C25H27O3N6 (М+Н)+: 459,2139, найдено: 459,2140.
[0363] RIP 1-074
[0364] 1Н-ЯМР (500 МГц, CD3OD) δ=8,18 (с, 1Н), 7,98 (с, 1Н), 7,40-7,33 (м, 3Н), 7,31-7,28 (м, 2Н), 7,11 (с, 1Н), 6,93 (с, 1Н), 5,38 (с, 2Н), 5,08-5,03 (м, 1Н), 4,48 (дд, J=9,8, 7,8, 1Н), 4,41 (дд, J=11,5, 9,9, 1Н), 3,41 (с, 3Н); МС-ЭРИ m/z 433,0 (М+Н)+.
[0365] RIP 1-075
[0366] 1Н-ЯМР (500 МГц, CD3OD) δ=7,46-7,43 (м, 1Н), 7,43-7,38 (м, 2Н), 7,11 (с, 1Н), 6,95 (с, 1Н), 5,96 (с, 1Н), 5,38-5,35 (м, 1Н), 5,07 (дд, J=11,4, 7,7, 1Н), 4,46 (дд, J=11,3, 10,0, 1Н), 3,42 (с, 2Н); МС-ЭРИ m/z 435,3 (М+Н)+.
[0367] RIP 1-076
[0368] 1Н-ЯМР (500 МГц, CD3OD) δ=7,35-7,28 (м, 5Н), 7,10 (с, 1Н), 6,95 (с, 1Н), 5,03 (дд, J=11,2, 7,5, 1Н), 4,37 (дд, J=11,1, 10,1, 1Н), 4,18 (с, 2Н), 4,09-4,03 (м, 1Н), 3,42 (с, 3Н); МС-ЭРИ m/z 434,4 (М+Н)+.
[0369] RIP1-077
[0370] 1Н-ЯМР (400 МГц, CDCl3) δ=7,86 (д, J=8,3, 1Н), 7,67 (с, 1Н), 7,51-7,41 (м, 1Н), 7,33-7,25 (м, 3Н), 7,21 (д, J=7,0, 2Н), 6,27 (с, 1Н), 5,02-4,86 (м, 1Н), 4,73 (дд, J=11,6, 5,7, 1Н), 4,27 (т, J=10,5, 1Н), 4,09 (с, 2Н), 3,47 (с, 3Н), МСВР (ESI) Вычисл. для C23H18F3N5O4 (М+Н)+: 486,1389, найдено: 486,1392.
[0371] RIP1-078
[0372] 1Н-ЯМР (500 МГц, CDCl3) δ=12,22 (с, 1Н), 8,23 (с, 2Н), 7,90 (с, 1Н), 7,65 (с, 1Н), 7,40-7,34 (м, 4Н), 7,27 (д, J=3,3, 2Н), 5,54 (с, 2Н), 5,06-4,98 (м, 1Н), 4,33 (т, J=10,5, 1Н), 3,67-3,33 (м, 4Н); МСВР (ESI) Вычисл. для C22H18F3N7O3Na (M+Na)+: 508,1321, найдено: 508,1315.
[0373] RIP1-079
[0374] 1Н-ЯМР (500 МГц, CDCl3) δ 12,15 (с, 1Н), 8,13 (д, J=6,5 Гц, 1Н), 8,05 (с, 1Н), 7,70 (с, 1Н), 7,35 (д, J=7,2 Гц, 2Н), 7,33-7,30 (м, 4Н), 5,04-4,97 (м, 1Н), 4,85-4,80 (м, 1Н), 4,36 (т, J=10,4 Гц, 1Н), 4,14 (с, 3Н), 3,54 (с, 2Н); МСВР (ESI) Вычисл. для C23H18F3N5O4 (М+Н)+: 486,1389, найдено: 486,1390.
[0375] RIP1-080
[0376] 1Н-ЯМР (500 МГц, CDCl3) δ=7,84 (д, J=7,3, 1Н), 7,64 (с, 1Н), 7,52 (с, 1Н), 7,35-7,27 (м, 3Н), 7,21 (д, J=7,5, 2Н), 7,15 (д, J=2,7, 1Н), 6,48 (д, J=2,9, 1Н), 6,26 (с, 1Н), 4,77-4,70 (м, 1Н), 4,08 (с, 2Н), 3,86-3,77 (м, 4Н), 3,47 (с, 3Н), 2,84 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 173,97, 170,04, 158,30, 158,11, 137,68, 135,62, 135,39, 131,53, 129,94, 129,01, 128,88, 127,45, 119,51, 117,06, 116,39, 101,69, 101,55, 49,82, 38,31, 37,30, 33,29, 29,45; МС-ЭРИ: 447,3 (М+Н)+.
[0377] RIP1-081
[0378] 1Н-ЯМР (500 МГц, CDCl3) δ=8,12 (д, J=7,2, 1Н), 7,65 (с, 1Н), 7,53 (с, 1Н), 7,34-7,27 (м, 5Н), 7,16 (д, J=3,0, 1Н), 6,49 (д, J=3,1, 1H), 4,74-4,68 (м, 1H), 4,23 (с, 2Н), 3,86-3,81 (м, 4Н), 3,48 (с, 3Н), 2,85 (т, J=11,1, 1H); 13С-ЯМР (125 МГц, CDCl3) δ 169,44, 167,63, 158,80, 152,21, 137,46, 135,66, 133,05, 131,67, 130,02, 129,14, 129,00, 127,92, 119,28, 117,11, 116,47, 101,61, 50,24, 38,13, 37,39, 33,32, 31,96;; МС-ЭРИ: 448,4 (М+Н)+.
[0379] RIP1-082
[0380] 1Н-ЯМР (500 МГц, CDCl3) δ=7,82 (с, 1Н), 7,77 (с, 1Н), 7,64 (с, 1Н), 7,52 (с, 1Н), 7,36-7,29 (м, 3Н), 7,21 (д, J=7,3, 2Н), 7,14 (д, J=2,4, 1Н), 7,07 (д, J=7,2, 1Н), 6,47 (д, J=3,0, 1Н), 5,25 (с, 2Н), 4,78-4,72 (м, 1Н), 3,85-3,80 (м, 4Н), 3,46 (с, 3Н), 2,79 (т, J=11,1, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 171,11, 161,37, 138,86, 137,65, 135,64, 135,46, 131,49, 130,83, 129,90, 129,09, 128,57, 128,10, 119,60, 118,55, 117,04, 116,38, 101,54, 56,57, 49,73, 38,66, 37,31, 33,27; МС-ЭРИ: 446,4 (М+Н)+.
[0381] RIP1-083
[0382] 1Н-ЯМР (500 МГц, CDCl3) δ=7,83 (с, 1Н), 7,78 (с, 1Н), 7,61 (с, 1Н), 7,54 (с, 1Н), 7,37-7,28 (м, 7Н), 7,22 (д, J=1,5, 1Н), 7,21 (д, J=3,1, 2Н), 7,16 (д, J=0,7, 1Н), 7,15 (с, 1Н), 6,54 (д, J=3,1, 1Н), 5,32 (с, 2Н), 5,25 (с, 2Н), 4,82-4,75 (м, 1Н), 3,78 (дд, J=11,2, 6,9, 1Н), 3,45 (с, 3Н), 2,78 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 171,18, 161,43, 138,92, 137,87, 136,76, 135,45, 135,23, 130,86, 130,83, 130,12, 129,09, 129,07, 129,04, 128,54, 128,09, 126,97, 119,92, 118,49, 117,19, 116,52, 102,27, 56,53, 50,44, 49,70, 38,59, 37,36, 1,14; МС-ЭРИ: 522,4 (М+Н)+.
[0383] RIP1-084
[0384] 1Н-ЯМР (500 МГц, CDCl3) δ=8,15 (д, J=7,9, 1Н), 7,88 (с, 1Н), 7,61 (с, 1Н), 7,53 (с, 1Н), 7,36-7,33 (м, 5Н), 7,26-7,22 (м, 3Н), 7,20 (д, J=3,0, 1Н), 7,15 (д, J=7,3, 2Н), 6,53 (д, J=3,1, 1Н), 5,51 (д, J=6,4, 2Н), 5,32 (с, 2Н), 4,83-4,76 (м, 1Н), 3,78 (дд, J=11,2, 6,8, 1Н), 3,47 (с, 3Н), 2,85 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,31, 159,09, 143,19, 138,04, 136,77, 135,15, 133,95, 130,82, 130,10, 129,32, 129,10, 129,06, 128,26, 128,06, 126,96, 125,43, 119,94, 117,17, 116,48, 102,23, 54,53, 50,42, 49,49, 38,45, 37,32;; МС-ЭРИ: 523,4 (М+Н)+.
[0385] RIP1-085
[0386] 1Н-ЯМР (500 МГц, CDCl3) δ=7,85 (д, J=7,7, 1Н), 7,61 (с, 1Н), 7,54 (д, J=1,1, 1Н), 7,37-7,30 (м, 6Н), 7,23-7,20 (м, 3Н), 7,16 (д, J=7,6, 2Н), 6,55 (с, 1Н), 6,27 (с, 1Н), 5,33 (с, 2Н), 4,79-4,73 (м, 1Н), 4,08 (с, 2Н), 3,79 (дд, J=11,3, 6,5, 1Н), 3,47 (с, 3Н), 2,81 (т, J=11,1, 1H); 13С-ЯМР (125 МГц, CDCl3) δ 173,96, 170,04, 158,28, 158,11, 137,89, 136,75, 135,36, 135,20, 130,91, 130,15, 129,10, 128,99, 128,86, 128,10, 127,43, 126,98, 119,82, 117,20, 116,54, 102,27, 101,67, 50,45, 49,79, 38,26, 37,34, 33,26;; МС-ЭРИ: 523,4 (М+Н)+.
[0387] RIP1-086
[0388] 1Н-ЯМР (500 МГц, CDCl3) δ=8,18 (д, J=7,6, 1Н), 8,01 (с, 1Н), 7,62 (с, 1Н), 7,53 (с, 1Н), 7,37-7,33 (м, 5Н), 7,30 (д, J=7,0, 1Н), 7,26 (т, J=3,7, 2Н), 7,21 (д, J=3,1, 1H), 7,17 (д, J=7,4, 2H), 6,54 (д, J=3,1, 1H), 5,35 (с, 2H), 5,33 (с, 2Н), 4,86-4,80 (м, 1Н), 3,87 (дд, J=11,1, 7,0, 1Н), 3,47 (с, 3Н), 2,81 (т, J=11,1, 1H); 13С-ЯМР (125 МГц, CDCl3) δ 170,34, 157,91, 156,99, 144,00, 137,84, 136,77, 135,22, 133,92, 130,85, 130,11, 129,25, 129,08, 129,00, 128,31, 128,07, 127,00, 119,84, 117,19, 116,62, 102,23, 54,37, 50,43, 49,74, 38,48, 37,36; МС-ЭРИ: 523,5 (М+Н)+.
[0389] RIP1-087
[0390] 1Н-ЯМР (500 МГц, CDCl3) δ=8,00 (с, 1Н), 7,95 (д, J=7,7, 1Н), 7,62 (с, 1Н), 7,54 (с, 1Н), 7,36-7,33 (м, 4Н), 7,32 (с, 1Н), 7,30-7,28 (м, 3Н), 7,21 (д, J=3,1, 1Н), 7,16 (д, J=7,2, 2Н), 6,54 (д, J=3,1, 1Н), 5,33 (с, 2Н), 4,81-4,75 (м, 1Н), 4,10 (с, 2Н), 3,79 (дд, J=11,0, 6,9, 1Н), 3,48 (с, 3Н), 2,83 (т, J=11,1, 1Н); 13С-ЯМР (126 МГц, CDCl3) δ 170,45, 163,02, 159,69, 141,37, 138,01, 136,78, 135,99, 135,20, 134,80, 130,84, 130,13, 129,10, 128,91, 128,09, 127,90, 127,41, 126,97, 119,94, 117,18, 116,53, 102,26, 50,45, 49,41, 38,50, 37,29, 34,61; МС-ЭРИ: 523,4 (М+Н)+.
[0391] RIP1-088
[0392] 1Н-ЯМР (500 МГц, CDCl3) δ=8,04 (д, J=7,9, 1Н), 7,60 (с, 1Н), 7,52 (с, 1Н), 7,47 (с, 1Н), 7,44 (с, 1Н), 7,36-7,31 (м, 6Н), 7,19 (д, J=2,2, 1Н), 7,15 (д, J=7,8, 2Н), 7,13 (д, J=7,0, 2Н), 6,53 (д, J=2,9, 1Н), 5,32 (с, 2Н), 5,07 (с, 2Н), 4,83-4,77 (м, 1Н), 3,76 (дд, J=11,0, 6,8, 1Н), 3,45 (с, 3Н), 2,84 (т, J=11,2, 1Н); 13С-ЯМР (125 МГц, CDCl3) δ 170,77, 161,52, 138,16, 137,13, 137,02, 136,80, 135,23, 135,12, 130,71, 130,05, 129,20, 129,04, 128,66, 128,02, 127,56, 126,95, 122,43, 120,07, 117,13, 116,45, 102,20, 51,38, 50,39, 49,29, 38,59, 37,25; МС-ЭРИ: 522,3 (М+Н)+.
[0393] RIP1-089
[0394] 1Н-ЯМР (400 МГц, CD3OD_SPE) δ 8,30 (с, 1Н), 8,00 (д, J=18,6 Гц, 1H), 7,75 (с, 1Н), 7,26 (дд, J=18,8, 6,7 Гц, 5H), 6,33 (с, 1Н), 4,66 (дд, J=11,7, 7,0 Гц, 1H), 4,11 (с, 2Н), 3,69-3,51 (м, 1Н), 3,43 (с, 3Н), 3,30 (дт, J=3,3, 1,6 Гц, 2Н), 3,05 (т, J=11,5 Гц, 1Н), 13С-ЯМР (101 МГц, CD3OD_SPE) δ 174,48 (с), 170,74 (с), 159,07 (с), 157,90 (с), 143,94 (с), 141,00 (с), 135,77 (с), 128,47 (с), 128,45 (с), 126,85 (с), 121,08 (с), 49,89 (с), 36,95 (с), 36,10 (с), 32,22 (с). ЭРИ: m/z 434,1 (М+Н)+.
[0395] RIP1-090
[0396] 1Н-ЯМР (400 МГц, CD3OD_SPE) δ 8,30 (с, 1Н), 7,94 (с, 1Н), 7,74 (с, 1Н), 7,25 (дд, J=14,0, 6,9 Гц, 5Н), 4,70 (дд, J=11,6, 6,9 Гц, 1Н), 4,12 (с, 2Н), 3,66 (дт, J=16,1, 8,1 Гц, 1Н), 3,44 (с, 3Н), 3,05-2,96 (м, 1Н). ЭРИ: m/z 434,1 (М+Н)+.
[0397] RIP1-091
[0398] 1Н-ЯМР (400 МГц, CDCl3) δ 8,14 (с, 1Н), 7,98 (д, J=2,0 Гц, 1Н), 7,95 (с, 1Н), 7,62 (с, 1Н), 7,32 (дт, J=28,9, 5,7 Гц, 5Н), 5,54 (с, 2Н), 4,81-4,71 (м, 1Н), 3,76 (дд, J=10,9, 7,1 Гц, 1Н), 3,48 (с, 3Н), 2,93 (т, J=11,3 Гц, 1Н), 13С-ЯМР (101 МГц, CDCl3) δ 170,35 (с), 159,33 (с), 159,26 (с), 143,32 (с), 142,62 (с), 142,59 (с), 140,73 (с), 139,38 (с), 136,30 (с), 133,76 (с), 129,19 (с), 129,01 (с), 128,12 (с), 125,65 (с), 121,87 (с), 121,19 (с), 112,26 (с), 63,44 (с), 54,43 (с), 38,09 (с), 37,12 (с). ЭРИ: m/z 434,1 (М+Н)+.
[0399] RIP1-092
[0400] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,2, 1,5 Гц, 1Н), 8,13 (д, J=8,4 Гц, 1Н), 8,08 (д, J=8,8 Гц, 1Н), 7,90 (д, J=8,8 Гц, 1Н), 7,47 (дд, J=8,6, 4,2 Гц, 1Н), 7,24-7,15 (м, 5Н), 4,77 (дд, J=10,5, 7,4 Гц, 1Н), 4,09 (с, 2Н), 3,87 (дд, J=11,4, 7,2 Гц, 1Н), 3,46 (с, 2Н), 3,38 (с, 3Н), 3,03 (т, J=11,2 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 172,01, 158,15, 151,46, 149,38, 141,76, 135,89, 135,02, 131,82, 130,26, 128,87, 128,80, 127,13, 127,06, 124,16, 122,32, 60,46, 50,79, 49,72, 39,25, 36,93, 33,20, МС (ЭРИ): m/z 445,1 (М+Н)+.
[0401] RIP1-093
[0402] 1Н-ЯМР (400 МГц, CDCl3) δ 9,00 (дд, J=4,2, 1,6 Гц, 1Н), 8,19-8,13 (м, 2Н), 8,10 (дд, J=8,8, 0,5 Гц, 1Н), 8,03 (с, 1Н), 7,93 (д, J=8,7 Гц, 1Н), 7,51 (дд, J=8,6, 4,2 Гц, 1Н), 7,39-7,34 (м, 3Н), 7,29-7,25 (м, 2Н), 5,37 (с, 2Н), 4,84 (дт, J=10,7, 7,4 Гц, 1Н), 4,01 (дд, J=11,4, 7,2 Гц, 1Н), 3,42 (с, 3Н), 3,03 (т, J=11,1 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 171,94, 158,02, 156,69, 151,46, 149,52, 143,95, 141,71, 135,07, 133,77, 131,71, 130,33, 129,20, 128,98, 128,24, 127,10, 124,19, 122,23, 54,34, 49,68, 39,52, 36,90, МС (ЭРИ): m/z 445,1 (М+Н)+.
[0403] RIP1-094
[0404] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,1, 1,5 Гц, 1Н), 8,15 (д, J=8,5 Гц, 1Н), 8,05 (д, J=8,8 Гц, 1Н), 7,99 (д, J=7,9 Гц, 1Н), 7,90 (д, J=8,7 Гц, 1Н), 7,51-7,41 (м, 3Н), 7,36-7,28 (м, 3Н), 7,15-7,09 (м, 2Н), 5,07 (с, 2Н), 4,77 (дт, J=10,9, 7,5 Гц, 1Н), 3,87 (дд, J=11,3, 7,1 Гц, 1Н), 3,38 (с, 3Н), 3,04 (т, J=11,1 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 172,38, 161,63, 151,35, 149,45, 142,03, 137,07, 136,74, 135,08, 135,07, 131,86, 130,06, 129,16, 128,66, 127,50, 127,19, 124,23, 122,54, 122,20, 51,35, 49,27, 39,62, 36,80, МС (ЭРИ): m/z 444,1 (М+Н)+.
[0405] RIP1-095
[0406] 1Н-ЯМР (400 МГц, CDCl3) δ 8,99 (дд, J=4,2, 1,6 Гц, 1Н), 8,18 (дд, J=8,5, 0,6 Гц, 1Н), 8,13-8,05 (м, 2Н), 7,93 (д, J=8,7 Гц, 1Н), 7,87 (с, 1Н), 7,51 (дд, J=8,6, 4,2 Гц, 1Н), 7,38-7,34 (м, 3Н), 7,27-7,22 (м, 2Н), 5,53 (д, J=1,3 Гц, 2Н), 4,79 (дт, J=10,9, 7,4 Гц, 1Н), 3,42 (с, 3Н), 3,07 (т, J=11,1 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 171,86, 159,14, 151,44, 149,50, 142,86, 141,91, 135,03, 133,75, 131,77, 130,22, 129,28, 129,11, 128,22, 127,10, 125,42, 124,21, 122,25, 54,52, 49,45, 39,45, 36,86, МС (ЭРИ): m/z 445,1 (М+Н)+.
[0407] RIP1-096
[0408] 1Н-ЯМР (400 МГц, CDCl3) δ 9,00 (дд, J=4,1, 1,5 Гц, 1Н), 8,17 (д, J=8,1 Гц, 1Н), 8,10 (д, J=8,8 Гц, 1Н), 7,93 (д, J=8,7 Гц, 1Н), 7,81 (д, J=7,4 Гц, 1Н), 7,52 (дд, J=8,6, 4,2 Гц, 1Н), 7,35-7,18 (м, 5Н), 6,26 (с, 1Н), 4,75 (дт, J=10,7, 7,3 Гц, 1Н), 4,09 (с, 2Н), 3,93 (дд, J=11,3, 7,1 Гц, 1Н), 3,42 (с, 3Н), 3,03 (т, J=11,1 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 174,10, 171,58, 158,19, 157,97, 151,51, 149,51, 141,74, 135,18, 135,01, 131,70, 130,36, 128,93, 128,75, 127,39, 127,03, 124,18, 122,30, 101,58, 49,72, 39,27, 36,88, 33,18, МС (ЭРИ): m/z 445,1 (М+Н)+.
[0409] RIP1-097
[0410] 1Н-ЯМР (400 МГц, MeOD) δ 8,80 (д, J=3,5 Гц, 1Н), 8,30 (д, J=8,3 Гц, 1Н), 7,97 (д, J=9,0 Гц, 1Н), 7,61-7,51 (м, 2Н), 7,25-7,07 (м, 5Н), 4,95 (д, J=7,7 Гц, 1Н), 4,63-4,52 (м, 1Н), 4,45 (т, J=9,9 Гц, 1Н), 4,14-3,97 (м, 2Н), 3,32 (с, 3Н), 13С-ЯМР (100 МГц, MeOD) δ 171,13, 149,77, 149,28, 145,94, 132,31, 130,26, 129,57, 128,49, 128,36, 126,82, 125,23, 124,19, 121,90, 77,28, 49,09, 36,43, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0411] RIP1-098
[0412] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,2, 1,6 Гц, 1Н), 8,17-8,06 (м, 3Н), 8,02 (с, 1Н), 7,59 (д, J=9,0 Гц, 1H), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,41-7,36 (м, 3Н), 7,29 (дд, J=7,1, 2,4 Гц, 2Н), 5,38 (с, 2Н), 5,17 (дт, J=10,9, 7,5 Гц, 1Н), 4,85 (дд, J=9,9, 7,6 Гц, 1Н), 4,41-4,34 (м, 1Н), 3,47 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,89, 158,47, 156,57, 150,04, 149,22, 146,78, 143,98, 133,72, 131,10, 131,08, 129,57, 129,22, 129,01, 128,27, 125,30, 124,07, 121,71, 78,16, 54,39, 48,95, 37,41, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0413] RIP1-099
[0414] 1Н-ЯМР (400 МГц, CDCl3) δ 8,94 (дд, J=4,1, 1,5 Гц, 1Н), 8,12 (дд, J=20,9, 8,5 Гц, 2Н), 7,94 (д, J=7,5 Гц, 1Н), 7,58 (д, J=9,0 Гц, 1Н), 7,52-7,44 (м, 3Н), 7,39-7,32 (м, 3Н), 7,15 (дд, J=7,3, 1,9 Гц, 2Н), 5,16-5,06 (м, 3Н), 4,76 (дд, J=9,9, 7,6 Гц, 1Н), 4,44-4,34 (м, 1Н), 3,46 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 171,28, 162,04, 149,96, 149,25, 146,77, 137,07, 135,05, 131,19, 130,96, 130,87, 130,27, 129,88, 129,19, 128,70, 127,52, 126,58, 125,30, 124,43, 124,15, 123,92, 122,51, 121,61, 78,41, 51,39, 48,52, 37,33, МС (ЭРИ): m/z 428,1 (М+Н)+.
[0415] RIP1-100
[0416] 1Н-ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=4,2, 1,6 Гц, 1Н), 8,19-8,13 (м, 1Н), 8,11 (д, J=9,1 Гц, 1Н), 8,05 (д, J=7,4 Гц, 1Н), 7,89 (с, 1Н), 7,58 (д, J=9,1 Гц, 1Н), 7,49 (дд, J=8,6, 4,2 Гц, 1Н), 7,40-7,34 (м, 3Н), 7,29-7,24 (м, 3Н), 5,54 (д, J=4,1 Гц, 2Н), 5,11 (дт, J=10,9, 7,5 Гц, 1Н), 4,78 (дд, J=9,9, 7,6 Гц, 1Н), 4,40 (дд, J=10,8, 10,1 Гц, 1Н), 3,47 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,80, 159,56, 150,04, 149,20, 146,78, 142,75, 133,71, 131,14, 131,00, 129,74, 129,31, 129,14, 128,26, 125,45, 125,24, 124,10, 121,70, 78,13, 54,55, 48,74, 37,40, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0417] RIP1-101
[0418] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,2, 1,6 Гц, 1Н), 8,15 (д, J=7,9 Гц, 1Н), 8,12 (д, J=9,4 Гц, 1Н), 7,75 (д, J=7,1 Гц, 1Н), 7,59 (д, J=9,1 Гц, 1Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,36-7,27 (м, 3Н), 7,25-7,20 (м, 2Н), 6,28 (с, 1Н), 5,07 (дт, J=10,9, 7,4 Гц, 1Н), 4,79 (дд, J=9,9, 7,6 Гц, 1Н), 4,45-4,32 (м, 1Н), 4,10 (с, 2Н), 3,47 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 174,17, 170,51, 158,63, 157,86, 150,10, 149,17, 146,79, 135,16, 131,14, 131,06, 129,57, 128,94, 128,77, 127,40, 125,19, 124,05, 121,75, 101,59, 49,03, 37,41, 33,20, 29,33, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0419] RIP1-102
[0420] 1Н-ЯМР (400 МГц, CDCl3) δ 9,30 (с, 1Н), 8,59 (д, J=6,0 Гц, 1H), 8,22 (д, J=7,7 Гц, 1Н), 7,94 (д, J=8,4 Гц, 1H), 7,83 (д, J=8,4 Гц, 1Н), 7,59 (д, J=5,9 Гц, 1H), 7,25-7,18 (м, 5Н), 4,77 (дт, J=10,8, 7,5 Гц, 1Н), 4,11 (с, 2Н), 3,90 (дд, J=11,3, 7,1 Гц, 1Н), 3,40 (с, 3Н), 3,07 (т, J=11,1 Гц, 1Н), 13С-ЯМР (101 МГц, CDCl3) δ 171,58, 153,09, 144,48, 140,90, 135,87, 133,17, 131,66, 131,47, 129,76, 128,89, 128,83, 128,29, 127,17, 116,00, 100,00, 77,25, 49,55, 39,17, 36,59, 33,25, МС (ЭРИ): m/z 445,0 (М+Н)+.
[0421] RIP1-103
[0422] 1Н-ЯМР (400 МГц, CDCl3) δ 9,34 (с, 1Н), 8,64 (д, J=5,9 Гц, 1Н), 8,18 (д, J=7,5 Гц, 1Н), 8,04 (с, 1Н), 7,97 (д, J=8,4 Гц, 1Н), 7,85 (д, J=8,4 Гц, 1Н), 7,60 (д, J=5,9 Гц, 1Н), 7,41-7,33 (м, 3Н), 7,27 (д, J=5,2 Гц, 2Н), 5,37 (с, 2Н), 4,91-4,78 (м, 1Н), 4,02 (дд, J=11,3, 7,1 Гц, 1Н), 3,43 (с, 3Н), 3,06 (т, J=11,1 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 171,60, 158,03, 156,64, 153,19, 144,62, 143,97, 140,85, 133,73, 133,21, 131,64, 131,47, 129,79, 129,21, 129,00, 128,24, 128,23, 115,91, 54,36, 49,55, 39,37, 36,56, МС (ЭРИ): m/z 445,0 (М+Н)+.
[0423] RIP1-104
[0424] 1Н-ЯМР (400 МГц, CDCl3) δ 9,33 (с, 1Н), 8,62 (д, J=5,9 Гц, 1Н), 8,02 (д, J=7,8 Гц, 1Н), 7,94 (д, J=8,4 Гц, 1Н), 7,84 (д, J=8,4 Гц, 1Н), 7,61 (д, J=5,9 Гц, 1Н), 7,46 (д, J=13,1 Гц, 2Н), 7,39-7,30 (м, 3Н), 7,18-7,09 (м, 2Н), 5,09 (с, 2Н), 4,79 (дт, J=10,9, 7,4 Гц, 1Н), 3,91 (дд, J=11,2, 7,0 Гц, 1Н), 3,41 (с, 3Н), 3,09 (т, J=11,1 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 172,03, 161,63, 153,10, 144,56, 141,18, 137,06, 136,75, 135,05, 133,20, 131,72, 131,53, 129,77, 129,18, 128,69, 128,00, 127,49, 122,53, 116,02, 51,37, 49,12, 39,52, 36,45, МС (ЭРИ): m/z 444,1 (М+Н)+.
[0425] RIP1-105
[0426] 1Н-ЯМР (400 МГц, CDCl3) δ 9,33 (с, 1Н), 8,63 (д, J=6,0 Гц, 1Н), 8,13 (д, J=7,7 Гц, 1Н), 7,95 (д, J=8,4 Гц, 1Н), 7,89-7,81 (м, 2Н), 7,61 (д, J=6,0 Гц, 1Н), 7,40-7,33 (м, 3Н), 7,27-7,22 (м, 2Н), 5,53 (д, J=1,8 Гц, 2Н), 4,79 (дт, J=10,9, 7,3 Гц, 1Н), 3,92 (дд, J=11,3, 7,0 Гц, 1H), 3,43 (с, 3Н), 3,10 (т, J=11,1 Гц, 1H), 13С-ЯМР (100 МГц, CDCl3) δ 171,53, 159,16, 153,16, 144,66, 142,83, 141,07, 133,73, 133,16, 131,61, 131,50, 129,78, 129,30, 129,13, 128,22, 128,11, 125,42, 115,95, 54,54, 49,29, 39,33, 36,52, МС (ЭРИ): m/z 445,1 (М+Н)+.
[0427] RIP1-106
[0428] 1Н-ЯМР (400 МГц, CDCl3) δ 9,34 (с, 1Н), 8,65 (д, J=6,0 Гц, 1Н), 7,98-7,94 (м, 1Н), 7,87-7,80 (м, 2Н), 7,61 (д, J=6,0 Гц, 1Н), 7,35-7,27 (м, 3Н), 7,24-7,19 (м, 2Н), 6,26 (с, 1Н), 4,75 (дт, J=10,9, 7,3 Гц, 1Н), 4,09 (с, 2Н), 3,94 (дд, J=11,3, 7,1 Гц, 1Н), 3,42 (с, 3Н), 3,06 (т, J=11,1 Гц, 1Н), 13С-ЯМР (100 МГц, CDCl3) δ 174,13, 171,24, 158,20, 157,94, 153,21, 144,73, 140,90, 135,17, 133,13, 131,53, 131,45, 129,78, 128,93, 128,76, 128,23, 127,40, 115,88, 101,57, 49,56, 39,14, 36,54, 33,18, МС (ЭРИ): m/z 445,0 (М+Н)+.
[0429] RIP1-107
[0430] 1Н-ЯМР (400 МГц, CDCl3) δ 9,25 (с, 1Н), 8,56 (д, J=6,0 Гц, 1Н), 8,11 (д, J=5,3 Гц, 1Н), 7,96 (д, J=8,8 Гц, 1Н), 7,58 (д, J=6,0 Гц, 1Н), 7,43 (д, J=8,7 Гц, 1Н), 7,25-7,16 (м, 5Н), 5,06 (с, 1Н), 4,75 (дд, J=9,7, 7,7 Гц, 1Н), 4,40 (т, J=10,5 Гц, 1Н), 4,12 (с, 2Н), 3,45 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,42, 158,63, 152,90, 152,36, 143,92, 135,85, 132,00, 129,55, 129,07, 128,89, 128,83, 127,20, 127,18, 123,58, 115,79, 77,93, 48,81, 37,08, 33,24, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0431] RIP1-108
[0432] 1Н-ЯМР (400 МГц, CDCl3) δ 9,31 (с, 1Н), 8,61 (д, J=6,0 Гц, 1Н), 8,10 (д, J=7,2 Гц, 1Н), 8,03 (с, 1Н), 8,00 (д, J=8,7 Гц, 1Н), 7,60 (д, J=6,0 Гц, 1Н), 7,48 (д, J=8,7 Гц, 1Н), 7,43-7,34 (м, 3Н), 7,32-7,27 (м, 2Н), 5,38 (с, 2Н), 5,14 (дт, J=10,9, 7,4 Гц, 1Н), 4,86 (дд, J=9,9, 7,5 Гц, 1Н), 4,45-4,37 (м, 1Н), 3,48 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,55, 158,49, 156,55, 153,04, 152,36, 144,16, 143,97, 133,69, 131,99, 129,46, 129,24, 129,06, 129,04, 128,28, 127,25, 123,64, 115,67, 78,14, 54,42, 48,83, 37,05, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0433] RIP1-109
[0434] 1Н-ЯМР (400 МГц, CDCl3) δ 9,22 (с, 1Н), 8,52 (д, J=6,0 Гц, 1Н), 7,89 (м, 2Н), 7,53 (д, J=5,9 Гц, 1Н), 7,40 (дд, J=9,4, 6,4 Гц, 3Н), 7,28-7,22 (м, J=8,8 Гц, 3Н), 7,12-7,05 (м, 2Н), 5,10-4,98 (м, 2Н), 4,70 (дд, J=9,8, 7,5 Гц, 1Н), 4,34 (т, J=10,5 Гц, 1Н), 3,39 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,95, 162,06, 152,96, 152,39, 144,04, 137,10, 136,67, 135,04, 132,06, 129,35, 129,25, 129,19, 128,70, 127,52, 127,21, 123,61, 122,56, 115,78, 78,39, 51,39, 48,38, 36,97, МС (ЭРИ): m/z 428,0 (М+Н)+.
[0435] RIP1-110
[0436] 1Н-ЯМР (400 МГц, CDCl3) δ 9,29 (с, 1Н), 8,60 (д, J=5,9 Гц, 1Н), 8,07 (д, J=7,1 Гц, 1Н), 7,98 (д, J=8,7 Гц, 1Н), 7,89 (с, 1Н), 7,61 (д, J=5,9 Гц, 1Н), 7,47 (д, J=8,7 Гц, 1Н), 7,42-7,33 (м, 3Н), 7,29-7,22 (м, 2Н), 5,65-5,46 (м, 2Н), 5,10 (дт, J=10,9, 7,4 Гц, 1Н), 4,78 (дд, J=9,6, 7,7 Гц, 1Н), 4,43 (т, J=10,5 Гц, 1Н), 3,48 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,47, 159,59, 153,00, 152,33, 144,13, 142,70, 133,71, 132,02, 129,37, 129,31, 129,23, 129,15, 128,25, 127,22, 125,47, 123,55, 115,73, 78,10, 54,56, 48,60, 37,04, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0437] RIP1-111
[0438] 1Н-ЯМР (400 МГц, CDCl3) δ 9,30 (с, 1Н), 8,61 (д, J=6,0 Гц, 1Н), 7,99 (д, J=8,7 Гц, 1Н), 7,77 (д, J=7,0 Гц, 1Н), 7,60 (д, J=6,0 Гц, 1Н), 7,47 (д, J=8,7 Гц, 1Н), 7,36-7,28 (м, 3Н), 7,25-7,20 (м, 2Н), 6,28 (с, 1Н), 5,05 (дт, J=11,0, 7,3 Гц, 1Н), 4,80 (дд, J=9,9, 7,4 Гц, 1Н), 4,40 (дд, J=10,8, 10,1 Гц, 1Н), 4,10 (с, 2Н), 3,48 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 174,21, 170,18, 158,65, 157,82, 153,04, 152,30, 144,20, 135,15, 131,97, 129,50, 129,07, 128,95, 128,78, 127,41, 127,23, 123,51, 115,67, 101,57, 77,88, 48,89, 37,05, 33,20, МС (ЭРИ): m/z 429,1 (М+Н)+.
[0439] RIP1-112
[0440] 1Н-ЯМР (400 МГц, ДМСО) δ 11,10 (с, 1Н), 8,29 (с, 1Н), 7,43-7,01 (м, 9Н), 6,27 (с, 1Н), 4,79 (д, J=9,3 Гц, 1Н), 4,49-4,16 (м, 2Н), 4,05 (с, 2Н), 3,44 (с, 3Н), МС (ЭРИ): m/z 417,1 (М+Н)+. МС (ЭРИ): m/z 417,1 (М+Н)+.
[0441] RIP1-113
[0442] 1Н-ЯМР (400 МГц, CDCl3) δ 9,04 (д, J=91,0 Гц, 1Н), 8,08 (д, J=17,6 Гц, 4Н), 7,44-7,35 (м, 5Н), 6,94 (с, 1Н), 6,46 (с, 1Н), 5,36 (с, 2Н), 4,72 (с, 2Н), 4,19 (с, 1Н), 3,37 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 168,92, 168,71, 158,53, 156,72, 150,46, 150,11, 146,25, 135,34, 133,81, 129,20, 128,96, 128,28, 125,99, 119,43, 105,15, 103,10, 57,00, 54,33, 49,26, 36,36, МС (ЭРИ): m/z 417,1 (М+Н)+.МС (ЭРИ): m/z 417,1 (М+Н)+.
[0443] RIP1-114
[0444] 1Н-ЯМР (400 МГц, CDCl3) δ 8,27 (с, 1Н), 7,89 (д, J=7,2 Гц, 1Н), 7,42-7,37 (м, 3Н), 7,31-7,25 (м, 3Н), 7,19-7,16 (м, 1H), 7,14 (с, 1Н), 7,08 (дд, J=7,3, 1,9 Гц, 2Н), 6,47-6,44 (м, 1Н), 5,02 (с, 2Н), 4,99 (дд, J=7,5, 3,6 Гц, 1Н), 4,59 (дд, J=9,7, 7,5 Гц, 1H), 4,15 (дд, J=11,0, 9,8 Гц, 1Н), 3,43 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 174,49, 168,24, 160,97, 145,31, 135,99, 134,09, 133,06, 129,08, 128,90, 128,14, 127,62, 126,49, 124,60, 124,15, 121,32, 113,94, 103,45, 101,71, 50,32, 47,74, 35,24, 34,91, МС (ЭРИ): m/z 416,1 (М+Н)+. МС (ЭРИ): m/z 416,1 (М+Н)+.
[0445] RIP1-115
[0446] 1Н-ЯМР (400 МГц, CDCl3) δ 8,44 (с, 1Н), 8,15-8,01 (м, 2Н), 7,96-7,82 (м, 2Н), 7,45-7,31 (м, 5Н), 6,96 (д, J=6,5 Гц, 1Н), 6,45 (с, 1Н), 5,26 (с, 1Н), 5,08 (дд, J=16,4, 8,7 Гц, 2Н), 4,65 (с, 2Н), 3,37 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 168,88, 159,57, 150,15, 146,56, 142,94, 135,17, 133,78, 129,29, 129,10, 128,25, 125,36, 119,51, 118,72, 104,95, 102,90, 99,99, 57,17, 54,51, 49,02, 36,52, МС (ЭРИ): m/z 417,1 (М+Н)+. МС (ЭРИ): m/z 417,1 (М+Н)+.
[0447] RIP1-116
[0448] 1Н-ЯМР (400 МГц, CDCl3) δ 8,37 (с, 1Н), 7,77 (д, J=6,4 Гц, 2Н), 7,38-7,29 (м, 5Н), 6,96 (д, J=6,4 Гц, 1Н), 6,46 (д, J=4,3 Гц, 1Н), 6,31 (д, J=5,0 Гц, 1Н), 6,28 (д, J=3,0 Гц, 1Н), 5,13-4,97 (м, 2Н), 4,31 (т, J=6,7 Гц, 1Н), 4,09 (с, 2Н), 3,38 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 174,04, 168,59, 158,61, 150,13, 146,45, 135,23, 130,95, 128,93, 128,79, 127,38, 126,20, 122,97, 119,48, 118,68, 114,00, 104,97, 101,55, 65,61, 57,20, 49,22, 33,19, МС (ЭРИ): m/z 417,1 (М+Н)+. МС (ЭРИ): m/z 417,1 (М+Н)+.
[0449] RIP1-119
[0450] 1Н-ЯМР (400 МГц, CDCl3) δ 8,08 (д, J=7,2 Гц, 1Н), 8,03 (с, 1Н), 7,68 (д, J=2,2 Гц, 1Н), 7,43 (с, 1Н), 7,40-7,34 (м, 4Н), 7,31-7,27 (м, 2Н), 6,77 (дд, J=2,2, 0,8 Гц, 1Н), 5,37 (с, 2Н), 5,10 (дт, J=11,1, 7,4 Гц, 1Н), 4,77 (дд, J=9,8, 7,5 Гц, 1Н), 4,25 (дд, J=11,0, 9,9 Гц, 1Н), 3,49 (с, 3Н); МС-ЭРИ: m/z 418,0 (М+Н)+.
[0451] RIP1-120
[0452] 1Н-ЯМР (400 МГц, CDCl3) δ 7,93 (д, J=7,3 Гц, 1Н), 7,66 (д, J=1,7 Гц, 1Н), 7,47 (д, J=4,2 Гц, 2Н), 7,41 (с, 1Н), 7,38-7,28 (м, 4Н), 7,14 (д, J=5,8 Гц, 2Н), 6,75 (с, 1Н), 5,09 (с, 2Н), 5,07-4,98 (м, 1Н), 4,71-4,63 (м, 1Н), 4,25 (т, J=10,5 Гц, 1Н), 3,47 (с, 3Н); МС-ЭРИ: m/z 417,0 (М+Н)+.
[0453] RIP1-121
[0454] 1Н-ЯМР (400 МГц, CDCl3) δ 8,04 (д, J=7,2 Гц, 1H), 7,89 (с, 1Н), 7,67 (д, J=2,2 Гц, 1H), 7,43 (с, 1Н), 7,41-7,33 (м, 4Н), 7,28-7,24 (м, 2Н), 6,77 (дд, J=2,1, 0,8 Гц, 1Н), 5,54 (д, J=3,3 Гц, 2Н), 5,06 (дт, J=11,1, 7,4 Гц, 1Н), 4,69 (дд, J=9,7, 7,5 Гц, 1Н), 4,27 (дд, J=11,1, 9,9 Гц, 1Н), 3,49 (с, 3Н); МС-ЭРИ: m/z 418,1 (М+Н)+.
[0455] RIP1-122
[0456] 1Н-ЯМР (400 МГц, CDCl3) δ 8,07 (д, J=6,9 Гц, 1Н), 7,69 (д, J=2,2 Гц, 1Н), 7,44 (с, 1Н), 7,42-7,34 (м, 6Н), 6,77 (дд, J=2,2, 0,9 Гц, 1Н), 5,81 (с, 2Н), 5,09 (дт, J=11,0, 7,3 Гц, 1Н), 4,78 (дд, J=9,8, 7,5 Гц, 1Н), 4,26 (дд, J=11,0, 9,9 Гц, 1Н), 3,50 (с, 3Н); МС-ЭРИ: m/z 419,1 (М+Н)+.
[0457] RIP1-123
[0458] 1Н-ЯМР (400 МГц, CDCl3) δ 8,00 (д, J=6,8 Гц, 1Н), 7,69 (д, J=2,2 Гц, 1Н), 7,44 (с, 1Н), 7,39-7,29 (м, 6Н), 6,77 (дд, J=2,2, 0,9 Гц, 1Н), 5,05 (дт, J=11,0, 7,3 Гц, 1Н), 4,77 (дд, J=9,8, 7,5 Гц, 1Н), 4,28 (с, 2Н), 4,24 (дд, J=11,0, 9,9 Гц, 1Н), 3,50 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 207,1, 179,5, 168,2, 163,1, 155,7, 153,0, 147,6, 146,8, 132,6, 132,1, 129,1, 129,0, 128,0, 125,1, 115,3, 106,4, 106,0, 49,4, 36,4, 33,0, 31,0; МС-ЭРИ: m/z 419,1 (М+Н)+.
[0459] RIP1-124
[0460] 1Н-ЯМР (400 МГц, CDCl3) δ 7,74 (д, J=7,2 Гц, 1Н), 7,67 (д, J=2,2 Гц, 1Н), 7,43 (с, 1Н), 7,36 (д, J=0,5 Гц, 1Н), 7,10 (д, J=7,8 Гц, 2Н), 6,99 (д, J=8,0 Гц, 2Н), 6,76 (дд, J=2,2, 0,9 Гц, 1Н), 6,48 (с, 1Н), 5,06 (дт, J=11,1, 7,4 Гц, 1Н), 4,72 (дд, J=9,7, 7,5 Гц, 1Н), 4,24 (дд, J=11,1, 9,8 Гц, 1Н), 3,92 (с, 2Н), 3,71 (с, 3Н), 3,48 (с, 3Н), 2,31 (с, 3Н); МС-ЭРИ: m/z 445,1 (М+Н)+.
[0461] RIP1-125
[0462] 1Н-ЯМР (400 МГц, CDCl3) δ 8,04 (с, 1Н), 7,69 (д, J=2,2 Гц, 1Н), 7,45 (с, 1Н), 7,40-7,36 (м, 1Н), 7,35-7,28 (м, 5Н), 6,78 (д, J=1,3 Гц, 1Н), 4,99 (т, J=8,9 Гц, 1Н), 4,73 (дд, J=9,8, 7,5 Гц, 1Н), 4,31-4,21 (м, 3Н), 3,49 (с, 3Н); МС-ЭРИ: m/z 419,1 (М+Н)+.
[0463] RIP1-126
[0464] 1Н-ЯМР (400 МГц, CDCl3) δ 7,76 (д, J=6,9 Гц, 1Н), 7,68 (д, J=2,2 Гц, 1Н), 7,43 (с, 1Н), 7,38-7,27 (м, 4Н), 7,23 (д, J=6,9 Гц, 2Н), 6,77 (д, J=1,4 Гц, 1Н), 6,29 (с, 1Н), 5,01 (дт, J=11,1, 7,2 Гц, 1Н), 4,71 (дд, J=9,7, 7,5 Гц, 1H), 4,24 (дд, J=10,9, 10,0 Гц, 1Н), 4,10 (с, 2Н), 3,48 (с, 3Н); МС-ЭРИ: m/z 419,0 (М+Н)+.
[0465] RIP1-127
[0466] 1Н-ЯМР (400 МГц, CDCl3) δ 8,17 (д, J=7,2 Гц, 1Н), 7,73 (д, J=2,2 Гц, 1Н), 7,48 (д, J=9,5 Гц, 1Н), 7,39 (с, 1Н), 7,31 (с, 1Н), 7,29-7,21 (м, 4Н), 6,82 (дд, J=2,1, 0,8 Гц, 1Н), 5,10 (дт, J=10,9, 7,3 Гц, 1Н), 4,71 (дд, J=9,7, 7,6 Гц, 1Н), 4,35-4,25 (м, 1Н), 4,17 (с, 2Н), 3,51 (с, 3Н); МС-ЭРИ: m/z 418,0 (М+Н)+.
[0467] RIP1-128
[0468] 1Н-ЯМР (400 МГц, CDCl3) δ 8,87 (д, J=1,8 Гц, 1Н), 8,84 (д, J=1,8 Гц, 1Н), 8,08 (д, J=7,1 Гц, 1Н), 8,03 (с, 1Н), 7,95 (с, 1Н), 7,92 (с, 1Н), 7,42-7,36 (м, 3Н), 7,31-7,27 (м, 2Н), 5,39 (с, 2Н), 5,18 (дт, J=11,3, 7,3 Гц, 1Н), 4,84 (дд, J=9,8, 7,4 Гц, 1Н), 4,35 (дд, J=11,2, 9,9 Гц, 1Н), 3,61 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,5, 158,5, 156,5, 151,4, 145,4, 145,2, 144,0, 142,0, 141,0, 140,0, 133,7, 129,3, 129,1, 128,3, 122,6, 121,6, 76,4, 54,4, 49,1, 36,3; МС-ЭРИ: m/z 430,0 (М+Н)+.
[0469] RIP1-129
[0470] 1Н-ЯМР (400 МГц, ДМСО) δ 8,94 (дд, J=5,1, 1,8 Гц, 2Н), 8,19 (с, 1Н), 8,13 (д, J=7,9 Гц, 1Н), 7,98 (д, J=1,1 Гц, 1Н), 7,92 (с, 2Н), 7,89 (с, 1Н), 7,76 (с, 1Н), 7,40-7,27 (м, 3Н), 5,26 (с, 2Н), 4,98-4,87 (м, 1Н), 4,66-4,56 (м, 1Н), 4,51 (дд, J=9,8, 7,6 Гц, 1Н), 3,72 (с, 3Н); 13С-ЯМР (100 МГц, ДМСО) δ 169,3, 163,1, 162,0, 151,6, 146,2, 146,2, 141,4, 140,8, 140,7, 139,4, 138,3, 137,6, 137,5, 136,1, 132,8, 129,3, 129,2, 128,5, 128,4, 128,2, 128,2, 126,8, 123,4, 122,7, 120,8, 76,0, 51,5, 50,3, 36,0; МС-ЭРИ: m/z 429,0 (М+Н)+.
[0471] RIP1-130
[0472] 1Н-ЯМР (400 МГц, CDCl3) δ 8,84 (д, J=5,5 Гц, 2Н), 8,05 (д, J=6,9 Гц, 1Н), 8,00-7,85 (м, 3Н), 7,43-7,23 (м, 5Н), 5,54 (с, 2Н), 5,14 (дт, J=11,2, 7,2 Гц, 1Н), 4,82-4,70 (м, 1Н), 4,38 (т, J=10,6 Гц, 1Н), 3,60 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,4, 159,6, 151,5, 145,4, 145,1, 142,7, 141,9, 141,0, 140,2, 133,7, 129,3, 129,2, 128,3, 125,5, 122,5, 121,4, 76,4, 54,6, 48,9, 36,3; МС-ЭРИ: m/z 430,0 (М+Н)+.
[0473] RIP1-131
[0474] 1Н-ЯМР (400 МГц, CDCl3) δ 8,88 (д, J=7,4 Гц, 2Н), 8,11 (д, J=6,6 Гц, 1Н), 7,94 (д, J=16,3 Гц, 2Н), 7,43-7,34 (м, 5Н), 5,81 (с, 2Н), 5,18 (дт, J=11,3, 7,2 Гц, 1Н), 4,88-4,79 (м, 1Н), 4,37 (т, J=10,6 Гц, 1Н), 3,61 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,1, 159,3, 156,1, 151,3, 145,5, 145,2, 142,0, 141,0, 139,8, 132,3, 129,4, 129,2, 128,7, 122,7, 121,6, 76,1, 57,6, 49,3, 36,3; МС-ЭРИ: m/z 431,0 (М+Н)+.
[0475] RIP1-132
[0476] 1Н-ЯМР (400 МГц, CDCl3) δ 8,85 (д, J=7,3 Гц, 2Н), 8,00 (д, J=6,9 Гц, 1Н), 7,93 (д, J=16,7 Гц, 2Н), 7,39-7,28 (м, 5Н), 5,12 (дт, J=11,3, 7,2 Гц, 1Н), 4,82 (дд, J=9,8, 7,4 Гц, 1Н), 4,34 (дд, J=11,1, 10,1 Гц, 1Н), 4,28 (с, 2Н), 3,60 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 179,7, 167,9, 162,9, 155,8, 151,3, 145,6, 145,3, 142,0, 141,0, 139,7, 132,6, 129,1, 129,0, 128,0, 122,8, 121,6, 76,0, 49,4, 36,3, 33,0; МС-ЭРИ: m/z 431,1 (М+Н)+.
[0477] RIP1-133
[0478] 1Н-ЯМР (400 МГц, CDCl3) δ 8,83 (д, J=6,8 Гц, 2Н), 7,91 (д, J=16,9 Гц, 2Н), 7,74 (д, J=7,1 Гц, 1Н), 7,09 (д, J=7,7 Гц, 2Н), 6,98 (д, J=7,8 Гц, 2Н), 6,47 (с, 1Н), 5,13 (дт, J=11,3, 7,2 Гц, 1Н), 4,77 (дд, J=9,4, 7,5 Гц, 1Н), 4,33 (т, J=10,6 Гц, 1Н), 3,91 (с, 2Н), 3,71 (с, 3Н), 3,59 (с, 3Н), 2,30 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 169,0, 161,7, 151,6, 145,3, 145,1, 144,0, 143,4, 141,9, 141,0, 140,3, 136,6, 133,5, 129,5, 128,3, 122,5, 121,4, 106,9, 80,1, 65,6, 48,8, 37,1, 36,2, 31,5, 21,0; МС-ЭРИ: m/z 457,1 (М+Н)+.
[0479] RIP1-134
[0480] 1Н-ЯМР (400 МГц, CDCl3) δ 8,86 (д, J=6,4 Гц, 2Н), 8,06 (д, J=6,7 Гц, 1Н), 7,94 (д, J=16,9 Гц, 2Н), 7,39-7,27 (м, 5Н), 5,07 (дт, J=11,3, 7,1 Гц, 1Н), 4,83-4,74 (м, 1Н), 4,37 (т, J=10,6 Гц, 1Н), 4,26 (с, 2Н), 3,61 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 167,8, 167,5, 158,4, 152,7, 151,2, 145,6, 145,3, 142,0, 141,0, 139,7, 132,8, 129,1, 128,9, 127,9, 122,8, 121,6, 75,8, 49,5, 36,4, 31,9; МС-ЭРИ: m/z 431,1 (М+Н)+.
[0481] RIP1-135
[0482] 1Н-ЯМР (400 МГц, CDCl3) δ 8,82 (д, J=6,8 Гц, 2Н), 8,13 (д, J=7,3 Гц, 1Н), 7,93 (с, 1Н), 7,87 (с, 1Н), 7,19 (д, J=13,4 Гц, 5Н), 5,09 (дт, J=11,3, 7,4 Гц, 1Н), 4,75-4,66 (м, 1Н), 4,40-4,30 (м, 1Н), 4,11 (с, 2Н), 3,56 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,4, 162,7, 158,7, 151,4, 145,4, 145,2, 141,9, 140,9, 140,0, 135,8, 128,8, 128,8, 127,1, 122,6, 121,4, 76,2, 49,1, 36,3, 33,1; МС-ЭРИ: m/z 430,1 (М+Н)+.
[0483] RIP1-136
[0484] 1Н-ЯМР (400 МГц, CDCl3) δ 8,21 (с, 1Н), 8,18 (д, J=6,2 Гц, 1H), 7,81 (с, 1Н), 7,61 (с, 1Н), 7,41-7,35 (м, 3Н), 7,34-7,28 (м, 2Н), 5,42 (с, 2Н), 5,10-4,96 (м, 1Н), 4,86 (с, 1Н), 4,32 (т, J=10,4 Гц, 1Н), 3,52 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 168,3, 158,8, 156,3, 144,5, 133,4, 129,3, 128,4, 76,4, 54,6, 49,6, 36,5; МС-ЭРИ: m/z 419,0 (М+Н)+.
[0485] RIP1-137
[0486] 1Н-ЯМР (400 МГц, CDCl3) δ 8,05 (д, J=7,5 Гц, 1Н), 7,65 (с, 1Н), 7,58-7,47 (м, 3Н), 7,40-7,31 (м, 3Н), 7,20-7,13 (м, 2Н), 5,12 (с, 2Н), 5,07-4,97 (м, 1Н), 4,73 (дд, J=9,8, 7,5 Гц, 1Н), 4,35-4,26 (м, 1Н), 3,50 (с, 3Н); МС-ЭРИ: m/z 418,1 (М+Н)+.
[0487] RIP1-138
[0488] 1Н-ЯМР (400 МГц, CDCl3) δ 8,15 (д, J=7,1 Гц, 1Н), 7,96 (с, 1Н), 7,72 (с, 1Н), 7,57 (с, 1Н), 7,43-7,32 (м, 3Н), 7,31-7,27 (м, 2Н), 5,55 (с, 2Н), 5,05 (дт, J=14,7, 7,3 Гц, 1Н), 4,76-4,67 (м, 1Н), 4,31 (т, J=10,5 Гц, 1Н), 3,51 (с, 3Н); МС-ЭРИ: m/z 419,1 (М+Н)+.
[0489] RIP1-139
[0490] 1Н-ЯМР (400 МГц, CDCl3) δ 8,19 (д, J=6,6 Гц, 1Н), 7,82 (с, 1Н), 7,63 (с, 1Н), 7,45-7,32 (м, 5Н), 5,83 (с, 2Н), 5,08 (дт, J=11,1, 7,1 Гц, 1Н), 4,86-4,75 (м, 1Н), 4,30 (т, J=10,5 Гц, 1Н), 3,53 (с, 3Н); МС-ЭРИ: m/z 420,0 (М+Н)+.
[0491] RIP1-140
[0492] 1Н-ЯМР (400 МГц, CDCl3) δ 8,08 (с, 1Н), 7,81 (с, 1Н), 7,61 (с, 1Н), 7,41-7,28 (м, 5Н), 5,03 (с, 1Н), 4,85-4,67 (м, 1Н), 4,31 (с, 2Н), 4,30-4,25 (м, 1Н), 3,54 (с, 3Н); МС-ЭРИ: m/z 420,0 (М+Н)+.
[0493] RIP1-141
[0494] 1Н-ЯМР (400 МГц, CDCl3) δ 7,89 (д, J=7,1 Гц, 1Н), 7,75-7,45 (д, J=47,5 Гц, 2Н), 7,10 (д, J=7,9 Гц, 2Н), 7,00 (д, J=7,9 Гц, 2Н), 6,52 (с, 1Н), 5,01 (дт, J=14,3, 7,2 Гц, 1Н), 4,80 (дд, J=9,7, 7,4 Гц, 1Н), 4,34-4,24 (м, 1Н), 3,94 (с, 2Н), 3,75 (с, 3Н), 3,50 (с, 3Н), 2,31 (с, 3Н); МС-ЭРИ: m/z 446,1 (М+Н)+.
[0495] RIP1-142
[0496] 1Н-ЯМР (400 МГц, CDCl3) δ 7,84 (д, J=7,0 Гц, 1Н), 7,77 (с, 1Н), 7,60 (с, 1Н), 7,36-7,27 (м, 3Н), 7,25-7,19 (м, 2Н), 6,31 (с, 1Н), 5,02 (дт, J=11,2, 7,2 Гц, 1Н), 4,73 (дд, J=9,7, 7,5 Гц, 1Н), 4,34-4,23 (м, 1Н), 4,11 (с, 2Н), 3,53 (с, 3Н); МС-ЭРИ: m/z 419,0 (М+Н)+.
[0497] RIP1-143
[0498] 1Н-ЯМР (400 МГц, ДМСО) δ 8,50 (с, 1Н), 8,13-7,56 (м, 2Н), 7,37-7,10 (м, 6Н), 4,86 (д, J=9,8 Гц, 1Н), 4,63-4,29 (м, 2Н), 4,13 (с, 2Н), 3,39 (с, 3Н); МС-ЭРИ: m/z 419,0 (М+Н)+.
[0499] RIP1-145
[0500] 26,9 мг, выход 73%, 1Н-ЯМР (400 МГц, ДМСО) δ 8,90 (с, 1Н), 8,59 (ш, 1Н), 8,44 (с, 1Н), 8,18 (с, 1Н), 7,52 (с, 1Н), 7,48-7,25 (м, 5Н), 5,54 (с, 2Н), 5,05-4,84 (м, 1Н), 4,80-4,64 (м, 1Н), 4,63-4,44 (м, 1Н), 3,56 (с, 3Н), 3,45 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 168,48, 160,64, 158,47, 156,53, 154,79, 147,83, 147,60, 143,99, 136,34, 133,73, 129,22, 129,01, 128,27, 121,13, 120,88, 119,66, 77,27, 54,39, 48,96, 36,14, 34,24, МС-ЭРИ m/z 460,1 (М+Н)+.
[0501] RIP1-146
[0502] 27,6 мг, выход 75%, 1H-ЯМР (400 МГц, CDCl3) δ 8,12-8,00 (м, 2Н), 7,97 (с, 1Н), 7,39 (с, 1Н), 7,17-7,03 (м, 5Н), 5,03-4,85 (м, 1Н), 4,68-4,52 (м, 1Н), 4,32-4,20 (м, 1Н), 4,04 (с, 2Н), 3,52 (с, 3Н), 3,41 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 168,34, 160,62, 158,75, 154,74, 147,71, 147,67, 136,33, 135,91, 128,83, 128,73, 127,05, 120,91, 120,87, 119,61, 76,51, 48,97, 36,14, 34,30, 33,04, МС-ЭРИ m/z 460,1 (М+Н)+.
[0503] RIP1-147
[0504] 25,3 мг, выход 69%, 1H-ЯМР (400 МГц, CDCl3) δ 8,13 (с, 1Н), 8,05 (с, 1Н), 7,93 (ш, J=7,2 Гц, 1Н), 7,51-7,44 (м, 3Н), 7,39-7,32 (м, 3Н), 7,18-7,10 (м, 2Н), 5,10 (с, 2Н), 5,09-5,01 (м, 1Н), 4,76-4,68 (м, 1Н), 4,39-4,30 (м, 1Н), 3,61 (с, 3Н), 3,51 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 168,88, 162,02, 160,69, 154,95, 147,69, 147,44, 137,08, 136,72, 136,68, 135,06, 129,19, 128,70, 127,53, 122,53, 120,97, 120,74, 119,56, 51,38, 48,52, 36,03, 34,23, МС-ЭРИ m/z 459,1 (М+Н)+.
[0505] RIP1-148
[0506] МС-ЭРИ: m/z 429,1 (М+Н)+.
[0507] RIP1-149
[0508] 1Н-ЯМР (400 МГц, CDCl3+CD3OD) δ 8,76 (дд, J=4,2, 1,6 Гц, 1Н), 8,08 (дд, J=8,2, 1,6 Гц, 1Н), 7,46 (д, J=9,1 Гц, 1Н), 7,36 (дд, J=8,2, 4,3 Гц, 1Н), 7,29-7,18 (м, 6Н), 4,98 (дд, J=8,5, 2,4 Гц, 1Н), 4,70 (дд, J=11,2, 2,4 Гц, 1Н), 4,30 (дд, J=11,2, 8,7 Гц, 1Н), 4,09 (с, 2Н); МС-ЭРИ: m/z 415,1 (М+Н)+.
[0509] RIP1-150
[0510] МС-ЭРИ: m/z 430,0 (М+Н)+.
[0511] RIP1-153
[0512] 1H-ЯМР (400 МГц, ДМСО) δ 8,12 (с, 1Н), 7,75 (с, 1Н), 7,42-7,23 (м, 5Н), 4,90-4,80 (м, 1Н), 4,65 (т, J=10,7 Гц, 1Н), 4,48-4,40 (м, 1Н), 4,37 (с, 2Н), 3,42 (с, 3Н); 13С-ЯМР (100 МГц, ДМСО) δ 168,3, 167,9, 158,8, 153,5, 148,6, 136,0, 134,4, 129,4, 129,3, 127,8, 110,3, 107,4, 75,1, 49,7, 36,4, 31,2; МС-ЭРИ: m/z 420,0 (М+Н)+.
[0513] RIP1-156
[0514] 13,1 мг, выход 33%, 1H-ЯМР (400 МГц, ДМСО) δ 8,40 (с, 1Н), 8,13 (с, 1Н), 7,48 (с, 1Н), 7,45-7,31 (м, 1Н), 7,17-7,03 (м, 2Н), 4,88 (дт, J=11,6, 7,7 Гц, 1Н), 4,70 (т, J=10,7 Гц, 1Н), 4,48 (дд, J=9,7, 7,6 Гц, 1Н), 4,14 (с, 2Н), 3,50 (с, 3Н), 3,40 (с, 3Н), МС-ЭРИ m/z 496,0 (М+Н)+.
[0515] RIP1-157
[0516] 11,0 мг, выход 27%, 1Н-ЯМР (400 МГц, ДМСО) δ 8,57 (с, 1Н), 8,40 (с, 1Н), 8,13 (с, 1Н), 7,48 (с, 1Н), 7,23 (т, J=8,5 Гц, 2Н), 4,89 (дт, J=11,4, 7,6 Гц, 1Н), 4,70 (т, J=10,7 Гц, 1Н), 4,49 (дд, J=9,5, 7,7 Гц, 1Н), 4,11 (с, 2Н), 3,51 (с, 3Н), 3,40 (с, 3Н), МС-ЭРИ m/z 514,0 (М+Н)+.
[0517] RIP1-158
[0518] 5,4 мг, выход 21%, 1Н-ЯМР (400 МГц, ДМСО) δ 8,46 (с, 1Н), 8,20 (с, 1Н), 7,54 (с, 1Н), 7,37 (дд, J=8,2, 5,7 Гц, 2Н), 7,22 (т, J=8,7 Гц, 2Н), 4,96 (дт, J=11,5, 7,7 Гц, 1Н), 4,76 (т, J=10,7 Гц, 1Н), 4,56 (дд, J=9,5, 7,7 Гц, 1Н), 4,18 (с, 2Н), 3,57 (с, 3Н), 3,46 (с, 3Н), 13С-ЯМР (100 МГц, ДМСО) δ 168,75, 160,43, 154,61, 149,50, 147,72, 136,72, 131,04, 130,95, 120,69, 120,44, 119,66, 115,89, 115,68, 75,91, 49,05, 35,86, 34,13, МС-ЭРИ m/z 478,1 (М+Н)+.
[0519] RIP1-159
[0520] 6,4 мг, выход 25%, 1Н-ЯМР (400 МГц, ДМСО) δ 8,64 (с, 1Н), 8,46 (с, 1Н), 8,19 (с, 1Н), 7,54 (с, 1Н), 7,43 (дд, J=14,3, 7,6 Гц, 1Н), 7,23-7,09 (м, 3Н), 4,97 (дт, J=11,4, 7,7 Гц, 1Н), 4,76 (т, J=10,7 Гц, 1Н), 4,56 (дд, J=9,5, 7,8 Гц, 1Н), 4,22 (с, 2Н), 3,57 (с, 3Н), 3,47 (с, 3Н), 13С-ЯМР (100 МГц, ДМСО) δ 168,75, 163,85, 161,43, 160,42, 154,61, 149,49, 147,72, 136,71, 131,01, 130,92, 130,12, 125,28, 125,25, 120,68, 120,43, 119,65, 116,08, 115,86, 114,13, 113,93, 99,99, 75,91, 49,06, 35,86, 34,13, МС-ЭРИ m/z 478,1 (М+Н)+.
[0521] RIP1-160
[0522] 8,0 мг, выход 21%, 1Н-ЯМР (400 МГц, ДМСО) δ 8,56 (с, 1Н), 8,40 (с, 1Н), 8,13 (с, 1Н), 7,48 (с, 1Н), 7,38-7,27 (м, 2Н), 7,24-7,13 (м, 2Н), 4,90 (дт, J=11,5, 7,7 Гц, 1Н), 4,70 (т, J=10,7 Гц, 1Н), 4,49 (дд, J=9,7, 7,6 Гц, 1H), 4,15 (с, 2Н), 3,51 (с, 3Н), 3,40 (с, 3Н), 13С-ЯМР (100 МГц, ДМСО) δ 168,74, 161,97, 160,42, 159,54, 154,60, 149,48, 147,71, 136,71, 131,75, 131,71, 129,58, 129,50, 125,06, 125,02, 120,67, 120,43, 119,65, 115,92, 115,70, 75,90, 49,05, 35,85, 34,13, МС-ЭРИ m/z 478,0 (М+Н)+.
[0523] RIP1-161
[0524] 1Н-ЯМР (400 МГц, CDCl3) δ 9,29 (с, 1Н), 8,59 (д, J=6,0 Гц, 1Н), 8,08 (д, J=5,8 Гц, 1Н), 7,98 (д, J=8,7 Гц, 1Н), 7,60 (д, J=6,0 Гц, 1Н), 7,46 (д, J=8,8 Гц, 1Н), 7,22 (тд, J=8,3, 4,1 Гц, 1Н), 6,95-6,82 (м, 2Н), 5,13-5,01 (м, 1Н), 4,78 (дд, J=9,8, 7,5 Гц, 1Н), 4,48-4,37 (м, 1Н), 4,21 (с, 2Н), 3,46 (с, 3Н); МС-ЭРИ: m/z 465,0 (М+Н)+.
[0525] RIP1-162
[0526] 1Н-ЯМР (400 МГц, CDCl3) δ 9,31 (с, 1Н), 8,61 (д, J=6,0 Гц, 1Н), 7,99 (д, J=8,8 Гц, 1Н), 7,60 (д, J=6,0 Гц, 1Н), 7,47 (д, J=8,8 Гц, 1Н), 6,73-6,64 (м, 2Н), 5,06 (дд, J=10,9, 7,5 Гц, 1Н), 4,78 (дд, J=9,9, 7,5 Гц, 1Н), 4,46-4,37 (м, 1Н), 4,15 (с, 2Н), 3,47 (с, 3Н); МС-ЭРИ: m/z 483,0 (М+Н)+.
[0527] RIP1-163
[0528] 1Н-ЯМР (400 МГц, CDCl3) δ 9,29 (с, 1Н), 8,59 (д, J=6,0 Гц, 1Н), 8,10 (с, 1Н), 7,99 (д, J=8,8 Гц, 1Н), 7,60 (д, J=6,0 Гц, 1Н), 7,47 (д, J=8,7 Гц, 1Н), 7,29-7,18 (м, 2Н), 7,06 (т, J=7,3 Гц, 1Н), 7,00 (т, J=9,1 Гц, 1Н), 5,14-5,02 (м, 1Н), 4,79 (дд, J=9,9, 7,5 Гц, 1Н), 4,46-4,37 (м, 1Н), 4,19 (с, 2Н), 3,47 (с, 3Н); МС-ЭРИ: m/z 447,0 (М+Н)+.
[0529] RIP1-164
[0530] 1Н-ЯМР (400 МГц, CDCl3) δ 9,30 (с, 1Н), 8,59 (д, J=6,0 Гц, 1Н), 8,11 (д, J=7,3 Гц, 1Н), 7,99 (д, J=8,7 Гц, 1Н), 7,60 (д, J=6,0 Гц, 1Н), 7,46 (д, J=8,8 Гц, 1Н), 7,22 (дд, J=8,3, 5,4 Гц, 2Н), 6,94 (т, J=8,6 Гц, 2Н), 5,06 (дт, J=11,0, 7,4 Гц, 1Н), 4,77 (дд, J=9,9, 7,5 Гц, 1Н), 4,45-4,38 (м, 1Н), 4,11 (с, 2Н), 3,46 (с, 3Н); МС-ЭРИ: m/z 447,0 (М+Н)+.
[0531] RIP1-165
[0532] 1Н-ЯМР (400 МГц, CDCl3) δ 9,30 (с, 1Н), 8,60 (д, J=6,0 Гц, 1Н), 8,12 (с, 1Н), 7,99 (д, J=8,8 Гц, 1Н), 7,60 (д, J=6,0 Гц, 1Н), 7,47 (д, J=8,7 Гц, 1Н), 7,25-7,21 (м, 1Н), 7,05 (д, J=7,5 Гц, 1Н), 7,01-6,89 (м, 2Н), 5,13-5,01 (м, 1Н), 4,79 (дд, J=9,8, 7,6 Гц, 1Н), 4,43 (т, J=10,5 Гц, 1Н), 4,15 (с, 2Н), 3,48 (с, 3Н); МС-ЭРИ: m/z 447,0 (М+Н)+.
[0533] RIP1-166
[0534] 1Н-ЯМР (400 МГц, ДМСО) δ 8,53 (с, 1Н), 8,10 (с, 1Н), 7,75 (с, 1Н), 7,46-7,32 (м, 1Н), 7,19-7,02 (м, 2Н), 4,85 (дт, J=11,1, 7,6 Гц, 1Н), 4,65-4,57 (м, 1Н), 4,41 (дд, J=9,8, 7,8 Гц, 1Н), 4,14 (с, 2Н), 3,42 (с, 3Н); МС-ЭРИ: m/z 455,0 (М+Н)+.
[0535] RIP1-167
[0536] 1Н-ЯМР (400 МГц, ДМСО) δ 8,53 (д, J=6,4 Гц, 1Н), 8,10 (д, J=13,8 Гц, 1Н), 7,74 (с, 1Н), 7,35-7,27 (дд, J=8,6, 5,6 Гц, 3Н), 7,21-7,10 (м, 3Н), 4,86 (дд, J=10,8, 6,8 Гц, 1Н), 4,64-4,54 (м, 1Н), 4,42 (дд, J=9,8, 7,8 Гц, 1Н), 4,30 (дд, J=14,2, 7,1 Гц, 1Н), 4,12 (с, 2Н), 3,42 (с, 3Н); МС-ЭРИ: m/z 437,0 (М+Н)+.
[0537] RIP1-168
[0538] 1Н-ЯМР (400 МГц, CDCl3) δ 8,99-8,91 (м, 1Н), 8,28-7,99 (м, 3Н), 7,57 (д, J=9,0 Гц, 1Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,21 (тд, J=8,2, 4,1 Гц, 1Н), 6,88 (т, J=7,7 Гц, 2Н), 5,15-5,03 (м, 1Н), 4,76 (дд, J=9,8, 7,8 Гц, 1Н), 4,40 (т, J=10,4 Гц, 1Н), 4,20 (с, 2Н), 3,45 (с, 3Н); МС-ЭРИ: m/z 465,0 (М+Н)+.
[0539] RIP1-169
[0540] 1Н-ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=4,2, 1,5 Гц, 1Н), 8,22-8,02 (м, 3Н), 7,57 (д, J=9,0 Гц, 1Н), 7,50 (дд, J=8,5, 4,2 Гц, 1Н), 6,65 (т, J=8,0 Гц, 2Н), 5,07 (дд, J=10,8, 7,7 Гц, 1Н), 4,76 (дд, J=9,9, 7,6 Гц, 1Н), 4,39 (т, J=10,4 Гц, 1Н), 4,13 (с, 2Н), 3,46 (с, 3Н); МС-ЭРИ: m/z 483,0 (М+Н)+.
[0541] RIP1-170
[0542] 1Н-ЯМР (400 МГц, CDCl3) δ 8,93 (дд, J=4,2, 1,5 Гц, 1Н), 8,26-8,00 (м, 3Н), 7,57 (д, J=9,1 Гц, 1Н), 7,49 (дд, J=8,6, 4,2 Гц, 1Н), 7,25-7,12 (м, 2Н), 7,04-6,98 (м, 1Н), 6,97-6,91 (т, 1Н), 5,17-5,04 (м, 1Н), 4,76-4,70 (м, 1Н), 4,39 (т, J=10,5 Гц, 1Н), 4,15 (с, 2Н), 3,45 (с, 3Н); МС-ЭРИ: m/z 447,0 (М+Н)+.
[0543] RIP1-171
[0544] 1Н-ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=4,2, 1,6 Гц, 1Н), 8,13 (т, J=9,2 Гц, 3Н), 7,58 (д, J=9,0 Гц, 1Н), 7,50 (дд, J=8,5, 4,3 Гц, 1Н), 7,24-7,18 (м, 2Н), 6,98-6,91 (м, 2Н), 5,09 (дд, J=10,6, 7,7 Гц, 1Н), 4,77 (дд, J=9,9, 7,6 Гц, 1Н), 4,43-4,36 (м, 1Н), 4,11 (с, 2Н), 3,46 (с, 3Н); МС-ЭРИ: m/z 447,0 (М+Н)+.
[0545] RIP1-172
[0546] 1Н-ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=4,2, 1,6 Гц, 1Н), 8,13 (т, J=9,7 Гц, 3Н), 7,58 (д, J=9,0 Гц, 1Н), 7,50 (дд, J=8,5, 4,2 Гц, 1H), 7,22 (тд, J=7,9, 6,1 Гц, 1Н), 7,04-7,00 (м, 1Н), 6,98-6,87 (м, 2Н), 5,09 (дд, J=10,8, 7,7 Гц, 1H), 4,77 (дд, J=9,9, 7,6 Гц, 1Н), 4,43-4,36 (м, 1Н), 4,13 (с, 2Н), 3,46 (с, 3Н); МС-ЭРИ: m/z 447,0 (М+Н)+.
[0547] RIP1-173
[0548] 1Н-ЯМР (400 МГц, CDCl3) δ 8,07 (с, 1Н), 7,69 (д, J=2,2 Гц, 1Н), 7,44 (с, 1Н), 7,38 (д, J=9,0 Гц, 1Н), 6,77 (дд, J=2,2, 0,8 Гц, 1Н), 6,74-6,65 (м, 2Н), 5,07-4,97 (м, 1Н), 4,70 (дд, J=9,8, 7,5 Гц, 1Н), 4,27 (дд, J=11,0, 9,9 Гц, 1Н), 4,14 (с, 2Н), 3,49 (с, 3Н); МС-ЭРИ: m/z 470,1 (М-Н)-,
[0549] RIP1-174
[0550] 1Н-ЯМР (400 МГц, CDCl3) δ 8,11 (с, 1Н), 7,69 (д, J=2,2 Гц, 1Н), 7,44 (с, 1Н), 7,36 (с, 1Н), 7,22 (дд, J=8,4, 5,4 Гц, 2Н), 6,94 (т, J=8,7 Гц, 2Н), 6,80-6,75 (м, 1Н), 5,04 (дд, J=10,7, 7,8 Гц, 1Н), 4,68 (дд, J=9,7, 7,6 Гц, 1Н), 4,31-4,22 (м, 1Н), 4,10 (с, 2Н), 3,48 (с, 3Н); МС-ЭРИ: m/z 436,0 (М+Н)+.
[0551] RIP1-175
[0552] 15,1 мг, выход 40%, 1Н-ЯМР (400 МГц, CDCl3) δ 8,83 (д, J=6,8 Гц, 1Н), 8,37 (д, J=5,4 Гц, 1Н), 8,08 (с, 1Н), 7,99 (с, 1Н), 7,53 (с, 1Н), 7,43 (с, 1Н), 7,34 (т, J=7,5 Гц, 2Н), 7,17 (д, J=7,1 Гц, 1Н), 7,00 (д, J=7,7 Гц, 2Н), 6,88 (д, J=3,1 Гц, 1Н), 5,05-4,91 (м, 1Н), 4,73-4,65 (м, 1Н), 4,30 (т, J=10,6 Гц, 1Н), 3,55 (с, 3Н), 3,46 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 168,69, 166,13, 163,72, 160,66, 154,87, 153,72, 151,23, 150,15, 147,76, 147,53, 136,56, 130,35, 125,76, 120,95, 120,79, 119,62, 114,53, 110,66, 76,79, 49,21, 36,05, 34,24, МС-ЭРИ m/z 472,0 (М+Н)+.
[0553] RIP1-176
[0554] МС-ЭРИ: m/z 496,0 (М+Н)+.
[0555] RIP1-177
[0556] 1Н-ЯМР (400 МГц, CDCl3) δ 8,84 (д, J=7,2 Гц, 1Н), 8,80-8,70 (м, 2Н), 8,38 (д, J=5,6 Гц, 1Н), 7,87 (с, 1Н), 7,83 (с, 1Н), 7,52 (д, J=2,4 Гц, 1Н), 7,34 (т, J=7,9 Гц, 2Н), 7,16 (д, J=7,4 Гц, 1Н), 6,99 (д, J=7,8 Гц, 2Н), 6,88 (дд, J=5,6, 2,5 Гц, 1Н), 5,06 (дт, J=11,4, 7,3 Гц, 1Н), 4,71 (дд, J=9,7, 7,4 Гц, 1Н), 4,37-4,25 (м, 1Н), 3,54 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 167,68, 165,10, 162,70, 152,68, 150,50, 150,17, 149,11, 144,33, 144,08, 140,90, 139,98, 139,17, 129,31, 124,72, 121,43, 120,34, 119,74, 113,51, 109,64, 75,37, 48,31, 35,13, МС-ЭРИ m/z 442,1 (М+Н)+.
[0557] RIP1-178
[0558] 1Н-ЯМР (400 МГц, CDCl3) δ 9,22 (с, 1Н), 8,84 (д, J=7,3 Гц, 1Н), 8,52 (д, J=6,0 Гц, 1H), 8,38 (д, J=5,6 Гц, 1Н), 7,91 (д, J=8,7 Гц, 1Н), 7,53 (д, J=6,0 Гц, 1Н), 7,50 (д, J=2,5 Гц, 1Н), 7,40 (д, J=8,7 Гц, 1Н), 7,33 (т, J=7,9 Гц, 2Н), 7,16 (т, J=7,4 Гц, 1Н), 6,98 (д, J=7,7 Гц, 2Н), 6,88 (дд, J=5,6, 2,5 Гц, 1Н), 5,01 (дт, J=11,0, 7,4 Гц, 1Н), 4,73 (дд, J=9,8, 7,5 Гц, 1Н), 4,40-4,32 (м, 1Н), 3,41 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,73, 166,11, 163,76, 153,70, 153,01, 152,34, 151,23, 150,16, 144,12, 132,01, 130,34, 129,38, 129,28, 127,21, 125,76, 123,52, 120,77, 115,73, 114,50, 110,64, 78,13, 49,03, 36,98, МС-ЭРИ m/z 441,0 (М+Н)+.
[0559] RIP1-179
[0560] 1Н-ЯМР (400 МГц, CDCl3) δ 8,87 (д, J=2,9 Гц, 1Н), 8,82 (д, J=7,4 Гц, 1Н), 8,38 (д, J=5,6 Гц, 1Н), 8,06 (дд, J=17,3, 8,8 Гц, 2Н), 7,51 (д, J=8,8 Гц, 2Н), 7,42 (дд, J=8,5, 4,2 Гц, 1Н), 7,33 (т, J=7,8 Гц, 2Н), 7,16 (т, J=7,4 Гц, 1Н), 6,98 (д, J=7,8 Гц, 2Н), 6,88 (дд, J=5,5, 2,4 Гц, 1Н), 5,03 (дт, J=10,8, 7,6 Гц, 1Н), 4,72 (дд, J=9,7, 7,7 Гц, 1Н), 4,34 (т, J=10,4 Гц, 1Н), 3,40 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 170,03, 165,07, 162,70, 152,66, 150,24, 149,10, 148,99, 148,16, 145,72, 130,09, 129,96, 129,30, 128,75, 124,71, 124,16, 123,05, 120,65, 119,73, 113,46, 109,59, 77,11, 48,13, 36,30, МС-ЭРИ m/z 441,1 (М+Н)+.
[0561] RIP1-180
[0562] 1Н-ЯМР (400 МГц, CDCl3) δ 8,89 (д, J=7,4 Гц, 1Н), 8,45 (д, J=5,6 Гц, 1Н), 7,68 (д, J=2,2 Гц, 1Н), 7,60 (д, J=2,5 Гц, 1Н), 7,46-7,35 (м, 4Н), 7,25-7,21 (м, 1Н), 7,10-7,04 (м, 2Н), 6,94 (дд, J=5,6, 2,5 Гц, 1Н), 6,77 (дд, J=2,2, 0,8 Гц, 1Н), 5,05 (дт, J=11,1, 7,4 Гц, 1Н), 4,72 (дд, J=9,7, 7,5 Гц, 1Н), 4,28 (дд, J=11,1, 9,8 Гц, 1Н), 3,50 (с, 3Н); МС-ЭРИ: m/z 430,0 (М+Н)+.
[0563] RIP1-181
[0564] 1Н-ЯМР (400 МГц, ДМСО) δ 8,96-8,76 (м, 1Н), 8,52 (д, J=5,4 Гц, 1Н), 7,99 (с, 1Н), 7,66 (с, 1Н), 7,44 (т, J=7,7 Гц, 2Н), 7,30-7,20 (м, 2Н), 7,15 (д, J=7,9 Гц, 2Н), 4,87-4,69 (м, 1Н), 4,54-4,24 (м, 2Н); МС-ЭРИ: m/z 431,0 (М+Н)+.
[0565] RIP1-182
[0566] 1Н-ЯМР (400 МГц, CDCl3) δ 8,08 (с, 1Н), 8,05 (ш, J=7,4 Гц, 1Н), 7,51 (с, 1Н), 7,38 (с, 1Н), 7,16-7,01 (м, 5Н), 4,97 (дд, J=17,4, 7,3 Гц, 1Н), 4,62-4,52 (м, 1Н), 4,24-4,15 (м, 1Н), 4,01 (с, 2Н), 3,39 (с, 3Н), МС-ЭРИ m/z 419,1 (М+Н)+.
[0567] RIP1-183
[0568] 1Н-ЯМР (400 МГц, CDCl3) δ 8,16 (с, 1Н), 8,08 (ш, J=6,7 Гц, 1Н), 7,62 (с, 1Н), 7,49 (с, 1Н), 7,22 (дд, J=14,7, 7,4 Гц, 1Н), 6,89 (т, J=7,6 Гц, 2Н), 5,05 (дд, J=18,0, 7,5 Гц, 1Н), 4,73-4,65 (м, 1Н), 4,33-4,25 (м, 1Н), 4,20 (с, 2Н), 3,49 (с, 3Н), МС-ЭРИ m/z 455,1 (М+Н)+.
[0569] RIP1-184
[0570] 1Н-ЯМР (400 МГц, CDCl3) δ 8,17 (с, 1Н), 8,11 (ш, J=7,2 Гц, 1Н), 7,61 (с, 1Н), 7,49 (с, 1Н), 6,63 (т, J=7,8 Гц, 2Н), 5,10-4,97 (м, 1Н), 4,71-4,60 (м, 1Н), 4,36-4,25 (м, 1Н), 4,11 (с, 2Н), 3,48 (с, 3Н), МС-ЭРИ m/z 473,1 (М+Н)+.
[0571] RIP1-185
[0572] 1Н-ЯМР (400 МГц, CDCl3) δ 8,09 (с, 1Н), 8,06 (ш, J=6,1 Гц, 1Н), 7,53 (с, 1Н), 7,41 (с, 1Н), 7,13-7,00 (м, 2Н), 6,86-6,73 (м, 2Н), 5,02-4,88 (м, 1Н), 4,65-4,50 (м, 1Н), 4,28-4,14 (м, 1Н), 3,99 (с, 2Н), 3,40 (с, 3Н), МС-ЭРИ m/z 437,1 (М+Н)+.
[0573] RIP1-186
[0574] 1Н-ЯМР (400 МГц, CDCl3) δ 8,87 (д, J=7,4 Гц, 1Н), 8,44 (д, J=5,6 Гц, 1Н), 8,16 (с, 1Н), 7,63 (с, 1Н), 7,60 (д, J=2,4 Гц, 1Н), 7,49 (с, 1Н), 7,41 (т, J=7,9 Гц, 2Н), 7,25 (т, J=7,5 Гц, 1Н), 7,07 (д, J=7,8 Гц, 2Н), 6,95 (дд, J=5,6, 2,5 Гц, 1Н), 5,06 (дт, J=11,2, 7,5 Гц, 1Н), 4,73 (дд, J=9,7, 7,6 Гц, 1Н), 4,36-4,25 (м, 1Н), 3,51 (с, 3Н), 13С-ЯМР (100 МГц, CDCl3) δ 169,10, 166,13, 163,72, 154,11, 153,71, 151,29, 150,13, 147,81, 147,17, 138,69, 135,07, 130,35, 125,76, 120,79, 114,50, 114,15, 110,66, 105,77, 77,46, 49,32, 36,15, МС-ЭРИ m/z 431,1 (М+Н)+.
[0575] RIP1-187
[0576] МС-ЭРИ m/z 446,1 (М+Н)+.
[0577] RIP1-188
[0578] МС-ЭРИ m/z 458,1 (М+Н)+.
[0579] RIP1-189
[0580] 1Н-ЯМР (500 МГц, CDCl3) δ 8,92 (д, J=7,2 Гц, 1Н), 8,44 (д, J=5,6 Гц, 1Н), 8,32 (с, 1Н), 7,59 (д, J=2,5 Гц, 1Н), 7,46 (с, 1Н), 7,40 (т, J=7,9 Гц, 2Н), 7,26-7,23 (м, 2Н), 7,22 (с, 1Н), 7,06 (д, J=7,6 Гц, 2Н), 6,94 (дд, J=5,6, 2,5 Гц, 1Н), 6,54 (с, 1Н), 5,09-5,03 (м, 1Н), 4,71 (дд, J=9,6, 7,5 Гц, 1Н), 4,24 (дд, J=11,0, 9,8 Гц, 1Н), 3,51 (с, 3Н); МС-ЭРИ: 429,45 [М+Н]+,
[0581] RIP1-190
[0582] 1Н-ЯМР (500 МГц, CDCl3) δ 8,92 (д, J=7,2 Гц, 1Н), 8,45 (д, J=5,6 Гц, 1H), 7,60 (с, 2Н), 7,41 (т, J=7,9 Гц, 2H), 7,31 (с, 1Н), 7,26-7,22 (м, 1Н), 7,06 (д, J=7,9 Гц, 2Н), 6,95 (дд, J=5,3, 2,2 Гц, 1Н), 5,10-5,03 (м, 1Н), 4,69 (дд, J=9,6, 7,5 Гц, 1Н), 4,32-4,26 (м, 1Н), 3,52 (с, 3Н); МС-ЭРИ: 430, 40 [М+Н]+,
[0583] RIP1-193
[0584] 1Н-ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=4,2, 1,5 Гц, 1Н), 8,72 (д, J=1,3 Гц, 1Н), 8,48 (д, J=2,6 Гц, 1Н), 8,13 (дд, J=13,3, 8,7 Гц, 2Н), 7,65-7,62 (м, 1Н), 7,59 (д, J=9,0 Гц, 1Н), 7,53-7,44 (м, 2Н), 7,40-7,33 (м, 2Н), 7,17 (т, J=7,4 Гц, 1Н), 7,01 (д, J=7,7 Гц, 2Н), 5,11 (дт, J=10,8, 7,3 Гц, 1Н), 4,82 (дд, J=9,9, 7,6 Гц, 1Н), 4,43-4,35 (м, 1Н), 3,47 (с, 3Н); МС-ЭРИ: m/z 441,1 (М+Н)+.
[0585] RIP1-194
[0586] 1Н-ЯМР (400 МГц, CDCl3) δ 8,94 (д, J=2,9 Гц, 1Н), 8,37 (д, J=7,5 Гц, 1Н), 8,16-8,05 (м, 2Н), 7,83-7,73 (м, 2Н), 7,61-7,45 (м, 4Н), 7,32 (т, J=7,4 Гц, 1Н), 7,26-7,22 (м, 2Н), 7,03 (дд, J=7,7, 1,3 Гц, 1Н), 5,05 (дт, J=11,0, 7,6 Гц, 1Н), 4,72 (дд, J=9,8, 7,6 Гц, 1Н), 4,29 (дд, J=10,9, 10,0 Гц, 1Н), 3,44 (с, 3Н); МС-ЭРИ: m/z 441,0 (М+Н)+.
[0587] RIP1-195
[0588] 1Н-ЯМР (400 МГц, CDCl3) δ 9,00-8,94 (м, 1Н), 8,28 (д, J=5,2 Гц, 1Н), 8,15 (т, J=8,8 Гц, 2Н), 7,61 (д, J=9,0 Гц, 1Н), 7,52 (дд, J=8,6, 4,2 Гц, 1Н), 7,46-7,34 (м, 3Н), 7,28 (дд, J=5,2, 1,3 Гц, 1Н), 7,26-7,20 (т, J=7,4 Гц, 2Н), 7,13 (д, J=7,6 Гц, 2Н), 5,10 (дт, J=10,8, 7,2 Гц, 1Н), 4,88 (дд, J=9,9, 7,6 Гц, 1Н), 4,42-4,33 (м, 1Н), 3,50 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 171,0, 164,6, 164,5, 153,6, 150,2, 149,2, 148,7, 146,8, 144,2, 131,3, 131,0, 129,8, 129,4, 125,2, 124,0, 121,8, 121,3, 115,6, 109,6, 78,1, 49,6, 37,5; МС-ЭРИ: m/z 441,0 (М+Н)+.
[0589] RIP1-196
[0590] 1Н-ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=4,1, 1,5 Гц, 1Н), 8,74 (д, J=7,5 Гц, 1Н), 8,35 (д, J=2,5 Гц, 1Н), 8,19-8,08 (м, 2Н), 8,00 (д, J=8,6 Гц, 1Н), 7,59 (д, J=9,1 Гц, 1Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,44-7,37 (м, 2Н), 7,28 (дд, J=8,6, 2,8 Гц, 1Н), 7,25-7,19 (м, 1Н), 7,09-7,03 (м, 2Н), 5,13 (дт, J=11,0, 7,6 Гц, 1Н), 4,80 (дд, J=9,9, 7,6 Гц, 1Н), 4,41 (дд, J=10,9, 10,0 Гц, 1Н), 3,48 (с, 3Н); МС-ЭРИ: m/z 441,0 (М+Н)+.
[0591] RIP1-197
[0592] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (д, J=3,0 Гц, 1Н), 8,89 (д, J=7,4 Гц, 1Н), 8,47 (д, J=5,6 Гц, 1Н), 8,14 (дд, J=15,2, 8,8 Гц, 2Н), 7,59 (д, J=9,1 Гц, 1Н), 7,54 (д, J=2,5 Гц, 1Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,14-7,07 (м, 2Н), 7,07-7,00 (м, 2Н), 6,94 (дд, J=5,6, 2,5 Гц, 1Н), 5,10 (дт, J=10,9, 7,5 Гц, 1Н), 4,79 (дд, J=9,8, 7,6 Гц, 1Н), 4,47-4,37 (м, 1Н), 3,48 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 171,1, 166,2, 163,7, 158,9, 151,4, 150,2, 150,1, 149,5, 149,2, 146,8, 131,1, 131,0, 129,8, 125,2, 124,1, 122,4, 122,3, 121,7, 117,2, 116,9, 114,3, 110,3, 78,2, 49,2, 37,4; МС-ЭРИ: m/z 459,1 (М+Н)+.
[0593] RIP1-198
[0594] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (д, J=2,8 Гц, 1Н), 8,90 (д, J=7,5 Гц, 1Н), 8,51 (д, J=5,6 Гц, 1Н), 8,14 (дд, J=17,1, 8,8 Гц, 2Н), 7,59 (д, J=9,1 Гц, 1Н), 7,54 (д, J=2,5 Гц, 1Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,24-7,18 (ддд, J=14,4, 7,0, 4,4 Гц, 1Н), 7,07-6,99 (м, 3Н), 5,10 (дт, J=11,0, 7,5 Гц, 1Н), 4,79 (дд, J=9,9, 7,6 Гц, 1Н), 4,41 (дд, J=10,8, 10,0 Гц, 1Н), 3,48 (с, 3Н); МС-ЭРИ: m/z 477,0 (М+Н)+.
[0595] RIP1-199
[0596] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,1, 1,4 Гц, 1Н), 8,72 (д, J=4,8 Гц, 1Н), 8,60 (д, J=7,4 Гц, 1Н), 8,18-8,09 (м, 2Н), 7,69 (д, J=4,8 Гц, 1Н), 7,59 (д, J=9,0 Гц, 1Н), 7,54-7,48 (м, 3Н), 7,37-7,32 (м, 1Н), 7,28-7,24 (м, 2Н), 5,08 (дт, J=10,9, 7,5 Гц, 1Н), 4,77 (дд, J=9,9, 7,6 Гц, 1Н), 4,37 (дд, J=10,8, 10,0 Гц, 1Н), 3,47 (с, 3Н); МС-ЭРИ: m/z 442,0 (М+Н)+.
[0597] RIP1-200
[0598] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (д, J=2,9 Гц, 1Н), 8,91 (д, J=7,5 Гц, 1Н), 8,27 (д, J=5,6 Гц, 1Н), 8,14 (дд, J=19,8, 8,8 Гц, 2Н), 7,59 (д, J=9,1 Гц, 1Н), 7,54 (д, J=2,0 Гц, 1Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,35 (т, J=7,8 Гц, 2Н), 7,21-7,11 (м, 3Н), 6,92 (дд, J=5,6, 2,3 Гц, 1Н), 6,24 (с, 1Н), 5,12 (дт, J=11,0, 7,6 Гц, 1Н), 4,82-4,75 (м, 1Н), 4,46-4,38 (м, 1Н), 3,48 (с, 3Н); МС-ЭРИ: m/z 440,0 (М+Н)+.
[0599] RIP1-201
[0600] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,1, 1,4 Гц, 1Н), 8,79 (д, J=7,4 Гц, 1Н), 8,68 (т, J=1,4 Гц, 1Н), 8,20-8,09 (м, 2Н), 7,95 (д, J=1,5 Гц, 2Н), 7,60 (д, J=9,0 Гц, 1Н), 7,51 (дд, J=8,6, 4,2 Гц, 1Н), 7,42-7,30 (м, 2Н), 7,18-7,10 (м, 3Н), 5,12 (дт, J=10,9, 7,5 Гц, 1Н), 4,87-4,76 (м, 1Н), 4,41 (дд, J=10,8, 10,0 Гц, 1Н), 3,49 (с, 3Н); МС-ЭРИ: m/z 440,0 (М+Н)+.
[0601] RIP1-202
[0602] 1Н-ЯМР (400 МГц, CDCl3) δ 8,97 (дд, J=4,2, 1,5 Гц, 1Н), 8,81 (д, J=7,1 Гц, 1Н), 8,61 (д, J=4,8 Гц, 1Н), 8,19-8,10 (м, 2Н), 7,68 (д, J=7,7 Гц, 2Н), 7,61 (д, J=9,0 Гц, 1Н), 7,51 (дд, J=8,6, 4,2 Гц, 1Н), 7,46 (т, J=7,9 Гц, 2Н), 7,37 (д, J=4,8 Гц, 1Н), 7,34 (с, 1Н), 7,14 (т, J=7,4 Гц, 1Н), 5,08 (дт, J=10,9, 7,4 Гц, 1Н), 4,84 (дд, J=9,9, 7,6 Гц, 1Н), 4,45-4,34 (м, 1Н), 3,51 (с, 3Н); МС-ЭРИ: m/z 441,0 (М+Н)+.
[0603] RIP1-203
[0604] 1Н-ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=4,2, 1,6 Гц, 1Н), 8,90 (д, J=7,5 Гц, 1Н), 8,48 (д, J=5,6 Гц, 1Н), 8,19-8,14 (м, 1Н), 8,12 (д, J=9,1 Гц, 1Н), 7,59 (д, J=9,1 Гц, 1Н), 7,55 (д, J=2,5 Гц, 1Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,26-7,13 (м, 4Н), 6,97 (дд, J=5,6, 2,5 Гц, 1Н), 5,10 (дт, J=11,0, 7,5 Гц, 1Н), 4,79 (дд, J=9,9, 7,6 Гц, 1Н), 4,41 (дд, J=10,9, 10,0 Гц, 1Н), 3,48 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 171,1, 165,6, 163,6, 151,4, 150,2, 150,1, 149,2, 146,8, 131,1, 131,0, 129,8, 127,3, 127,2, 125,3, 125,27, 124,1, 123,5, 121,7, 117,7, 117,5, 113,8, 109,7, 78,2, 49,2, 37,4; МС-ЭРИ: m/z 459,0 (М+Н)+.
[0605] RIP1-204
[0606] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,2, 1,6 Гц, 1Н), 8,90 (д, J=7,5 Гц, 1Н), 8,50 (д, J=5,6 Гц, 1Н), 8,18-8,14 (м, 1Н), 8,12 (д, J=9,1 Гц, 1Н), 7,60 (дд, J=5,7, 3,3 Гц, 2Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,37 (тд, J=8,3, 6,6 Гц, 1Н), 7,01-6,93 (ддд, J=10,0, 6,9, 2,1 Гц, 2Н), 6,86 (дд, J=8,2, 2,1 Гц, 1Н), 6,80 (дт, J=9,4, 2,3 Гц, 1Н), 5,11 (дт, J=11,0, 7,6 Гц, 1Н), 4,80 (дд, J=9,9, 7,6 Гц, 1Н), 4,42 (дд, J=10,8, 10,0 Гц, 1Н), 3,48 (с, 3Н); МС-ЭРИ: m/z 459,0 (М+Н)+.
[0607] RIP1-205
[0608] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,2, 1,6 Гц, 1Н), 8,91 (д, J=7,5 Гц, 1Н), 8,54 (д, J=5,6 Гц, 1Н), 8,19-8,15 (м, 1Н), 8,12 (д, J=9,1 Гц, 1Н), 7,61 (дд, J=9,0, 5,8 Гц, 2Н), 7,50 (дд, J=8,6, 4,2 Гц, 1Н), 7,04 (дд, J=5,6, 2,5 Гц, 1Н), 6,71 (tt, J=8,8, 2,3 Гц, 1Н), 6,65-6,57 (м, 2Н), 5,11 (дт, J=10,9, 7,5 Гц, 1Н), 4,81 (дд, J=9,9, 7,6 Гц, 1Н), 4,42 (дд, J=10,8, 10,0 Гц, 1Н), 3,49 (с, 3Н); МС-ЭРИ: m/z 477,0 (М+Н)+.
[0609] RIP1-206
[0610] 1Н-ЯМР (400 МГц, CDCl3) δ 8,16 (с, 1Н), 8,07 (с, 1Н), 7,63 (с, 1Н), 7,49 (с, 1Н), 7,32-7,21 (м, 2Н), 7,12-7,01 (м, 2Н), 5,1-5,02 (м, 1Н), 4,71 (дд, J=9,8, 7,7 Гц, 1Н), 4,33-4,25 (м, 1Н), 4,19 (с, 2Н), 3,50 (с, 3Н); МС-ЭРИ: m/z 437,0 (М+Н)+.
[0611] RIP1-207
[0612] 1Н-ЯМР (400 МГц, CDCl3) δ 8,78 (д, J=5,5 Гц, 2Н), 8,04 (с, 1Н), 7,88 (с, 1Н), 7,83 (с, 1Н), 7,35-7,22 (м, 1Н), 7,15 (с, 1Н), 6,94-6,84 (м, 2Н), 5,10-4,97 (м, 1Н), 4,75-4,64 (м, 1Н), 4,33-4,26 (м, 1Н), 4,04 (с, 2Н), 3,52 (с, 3Н); МС-ЭРИ: m/z 448,0 (М+Н)+.
[0613] RIP1-208
[0614] 1Н-ЯМР (400 МГц, CDCl3) δ 8,81-8,72 (м, 2Н), 7,88 (с, 1Н), 7,82 (с, 1Н), 7,17-7,06 (м, 2Н), 6,92 (дт, J=18,1, 8,1 Гц, 2Н), 5,09-4,97 (м, 1Н), 4,72-4,58 (м, 1Н), 4,33-4,22 (м, 1Н), 4,09 (с, 2Н), 3,51 (с, 3Н), МС-ЭРИ m/z 448,1 (М+Н)+.
[0615] RIP1-209
[0616] 1Н-ЯМР (400 МГц, CDCl3) δ 8,91-8,78 (м, 2Н), 7,95 (с, 1Н), 7,89 (с, 1Н), 7,19 (дд, J=13,9, 7,5 Гц, 1Н), 7,06-6,79 (м, 3Н), 5,17-5,01 (м, 1Н), 4,78-4,67 (м, 1Н), 4,43-4,30 (м, 1Н), 4,12 (с, 2Н), 3,59 (с, 3Н), МС-ЭРИ m/z 448,1 (М+Н)+.
[0617] RIP1-210
[0618] 1Н-ЯМР (400 МГц, CDCl3) δ 8,96 (дд, J=4,2, 1,5 Гц, 1Н), 8,91 (д, J=7,5 Гц, 1Н), 8,52 (т, J=3,9 Гц, 2Н), 8,46 (д, J=2,4 Гц, 1Н), 8,20-8,07 (м, 2Н), 7,64-7,56 (м, 2Н), 7,54-7,47 (м, 1Н), 7,46-7,34 (м, 2Н), 7,00 (дд, J=5,6, 2,6 Гц, 1Н), 5,11 (дт, J=10,9, 7,5 Гц, 1Н), 4,80 (дд, J=9,9, 7,6 Гц, 1Н), 4,42 (дд, J=10,8, 10,1 Гц, 1Н), 3,48 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 171,0, 165,4, 163,4, 151,6, 150,5, 150,5, 150,1, 149,2, 146,9, 146,8, 143,1, 131,1, 131,0, 129,7, 128,1, 125,2, 124,6, 124,1, 121,7, 114,6, 110,5, 78,1, 49,2, 37,4; МС-ЭРИ: m/z 442,0 (М+Н)+.
0619] RIP1-211
[0620] 1Н-ЯМР (400 МГц, CDCl3) δ 8,11 (с, 1Н), 7,90 (д, J=8,0 Гц, 2Н), 7,82 (ш, J=6,9 Гц, 1Н), 7,60 (с, 1Н), 7,44 (с, 1Н), 7,37 (т, J=7,9 Гц, 2Н), 7,22 (д, J=7,5 Гц, 1Н), 4,99-4,88 (м, 1Н), 4,74-4,65 (м, 1Н), 4,29-4,18 (м, 1Н), 3,46 (с, 3Н), МС-ЭРИ m/z 421,0 (М+Н)+.
[0621] RIP1-212
[0622] 1Н-ЯМР (400 МГц, CDCl3) δ 8,88 (ш, J=7,4 Гц, 1Н), 8,65-8,47 (м, 3Н), 8,17 (с, 1Н), 7,64 (с, 1Н), 7,62 (д, J=2,4 Гц, 1Н), 7,61-7,52 (м, 2Н), 7,50 (с, 1Н), 7,04 (дд, J=5,5, 2,5 Гц, 1Н), 5,06 (дт, J=11,1, 7,5 Гц, 1Н), 4,74 (дд, J=9,8, 7,6 Гц, 1Н), 4,36-4,27 (м, 1H), 3,52 (с, 3Н), МС-ЭРИ m/z 432,0 (M+Н)+.
[0623] RIP1-213
[0624] 1Н-ЯМР (400 МГц, CDCl3) δ 8,77 (д, J=7,3 Гц, 1Н), 8,74 (с, 1Н), 8,10 (с, 1Н), 7,58 (с, 1Н), 7,49 (с, 1Н), 7,43 (с, 1Н), 7,38 (т, J=7,9 Гц, 2Н), 7,23 (т, J=7,5 Гц, 1H), 7,07 (д, J=7,9 Гц, 2Н), 4,99 (дт, J=11,1, 7,5 Гц, 1Н), 4,69 (дд, J=9,7, 7,7 Гц, 1Н), 4,29-4,18 (м, 1Н), 3,45 (с, 3Н), МС-ЭРИ m/z 432,0 (М+Н)+.
[0625] RIP1-214
[0626] 1Н-ЯМР (400 МГц, CDCl3) δ 8,91 (д, J=7,2 Гц, 1Н), 8,88-8,82 (м, 2Н), 8,57-8,43 (м, 3Н), 7,95 (с, 1Н), 7,91 (с, 1Н), 7,61 (д, J=2,4 Гц, 1Н), 7,48-7,33 (м, 2Н), 7,01 (дд, J=5,5, 2,5 Гц, 1Н), 5,13 (дт, J=11,4, 7,3 Гц, 1Н), 4,79 (дд, J=9,7, 7,4 Гц, 1Н), 4,39 (дд, J=11,2, 10,0 Гц, 1Н), 3,62 (с, 3Н), МС-ЭРИ m/z 443,0 (М+Н)+.
[0627] RIP1-215
[0628] 1Н-ЯМР (400 МГц, CDCl3) δ 8,81 (с, 1Н), 8,81-8,76 (м, 2Н), 8,75 (с, 1Н), 7,89 (с, 1Н), 7,86 (с, 1Н), 7,49 (с, 1Н), 7,38 (т, J=7,8 Гц, 2Н), 7,23 (т, J=7,5 Гц, 1Н), 7,07 (д, J=7,9 Гц, 2Н), 5,06 (дт, J=11,4, 7,2 Гц, 1Н), 4,74 (дд, J=9,6, 7,4 Гц, 1Н), 4,39-4,23 (м, 1Н), 3,55 (с, 3Н), МС-ЭРИ m/z 443,0 (М+Н)+.
[0629] RIP1-217
[0630] 1Н-ЯМР (400 МГц, CDCl3) δ 8,16 (с, 1Н), 8,14 (с, 1Н), 7,66 (с, 1Н), 7,43 (с, 1Н), 7,18 (дд, J=14,0, 7,6 Гц, 1Н), 7,03-6,83 (м, 3Н), 5,02 (дд, J=18,1, 7,4 Гц, 1Н), 4,74-4,62 (м, 1Н), 4,36-4,24 (м, 1Н), 4,12 (с, 2Н), 3,49 (с, 3Н), МС-ЭРИ m/z 437,1 (М+Н)+.
[0631] RIP1-218
[0632] 1Н-ЯМР (400 МГц, CDCl3) δ 8,09 (с, 1Н), 8,04 (д, J=6,9 Гц, 1Н), 7,59 (с, 1Н), 7,38 (с, 1Н), 7,28-7,19 (м, 5Н), 5,03-4,92 (м, 1Н), 4,70-4,60 (м, 1Н), 4,26-4,18 (м, 1Н), 4,09 (с, 2Н), 3,42 (с, 3Н), МС-ЭРИ m/z 419,0 (М+Н)+.
[0633] RIP1-219
[0634] 1Н-ЯМР (400 МГц, CDCl3) δ 8,09 (с, 1Н), 8,04 (д, J=7,1 Гц, 1Н), 7,59 (с, 1Н), 7,37 (с, 1Н), 7,18-7,10 (м, 2Н), 7,03-6,86 (м, 2Н), 4,97 (дт, J=11,0, 7,5 Гц, 1Н), 4,70-4,57 (м, 1Н), 4,28-4,17 (м, 1Н), 4,10 (с, 2Н), 3,42 (с, 3Н), МС-ЭРИ m/z 437,0 (М+Н)+.
[0635] RIP1-220
[0636] 1Н-ЯМР (400 МГц, CDCl3) δ 8,12-8,04 (м, 2Н), 7,56 (с, 1Н), 7,42 (с, 1Н), 7,29-7,13 (м, 5Н), 4,92 (дт, J=11,0, 7,4 Гц, 1Н), 4,65-4,55 (м, 1Н), 4,28-4,19 (м, 1Н), 4,03 (с, 3Н), 3,96 (с, 2Н), 3,43 (с, 3Н), МС-ЭРИ m/z 433,0 (М+Н)+.
[0637] RIP1-221
[0638] 1Н-ЯМР (400 МГц, CDCl3) δ 8,80 (д, J=7,5 Гц, 1Н), 8,41 (д, J=5,0 Гц, 1H), 8,08 (с, 1Н), 7,86 (с, 1Н), 7,57 (с, 1Н), 7,42 (с, 1Н), 7,25-7,20 (м, 2Н), 7,15 (дд, J=8,2, 4,4 Гц, 2Н), 7,10-7,03 (м, 2Н), 5,02 (дт, J=11,2, 7,6 Гц, 1Н), 4,67 (дд, J=9,7, 7,6 Гц, 1Н), 4,29-4,18 (м, 1Н), 3,94 (с, 2Н), 3,42 (с, 3Н), МС-ЭРИ m/z 429,1 (М+Н)+.
[0639] RIP1-222
[0640] 1Н-ЯМР (400 МГц, CDCl3) δ 8,09 (с, 1Н), 8,06 (д, J=7,3 Гц, 1Н), 7,54 (с, 1Н), 7,41 (с, 1Н), 7,13 (дд, J=14,1, 7,5 Гц, 1Н), 6,97-6,77 (м, 3Н), 4,97 (дд, J=18,3, 7,7 Гц, 1Н), 4,68-4,52 (м, 1Н), 4,23 (т, J=10,5 Гц, 1Н), 4,05 (с, 2Н), 3,41 (с, 3Н), МС-ЭРИ m/z 437,1 (М+Н)+.
[0641] Пример 2: Синтез Соединения RIP1-018
[0642]
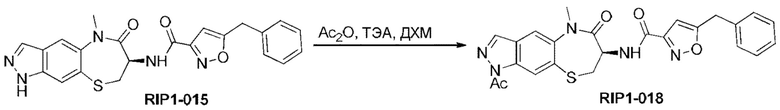
[0643] Соединение RIP1-015 (13 мг, 0,03 ммоль) помещали в одногорлую колбу объемом 25 мл, затем добавляли ДХМ (5 мл), одну каплю уксусного ангидрида и две капли ТЭА и проводили реакцию при комнатной температуре в течение 30 мин до полного завершения реакции, как было показано ТСХ. Растворитель удаляли при пониженном давлении и экстрагировали остаток ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью обращенно-фазовой колоночной хроматографии и лиофилизировали с получением RIP1-018: белое твердое вещество, 10 мг (70,7%).
[0644] RIP1-018: 1Н-ЯМР (400 МГц, CDCl3) δ 8,87 (с, 1Н), 8,17 (с, 1Н), 7,86 (д, J=7,5 Гц, 1Н), 7,70 (с, 1Н), 7,38-7,29 (м, 3Н), 7,27-7,23 (м, 2Н), 6,32 (с, 1Н), 4,82-4,72 (м, 1Н), 4,12 (с, 2Н), 3,86 (дд, J=11,1, 6,8 Гц, 1Н), 3,51 (с, 3Н), 3,01-2,94 (м, 1Н), 2,85 (с, 3Н); 13С-ЯМР (100 МГц, CDCl3) δ 174,1, 171,0, 169,7, 158,2, 158,1, 142,3, 139,1, 137,4, 135,3, 129,8, 129,0, 128,9, 127,5, 127,5, 122,5, 116,7, 101,7, 49,5, 37,7, 37,4, 33,3, 23,0, МС-ЭРИ: m/z 476,1 (М+Н)+.
[0645] Пример 3: Синтез соединения II-1
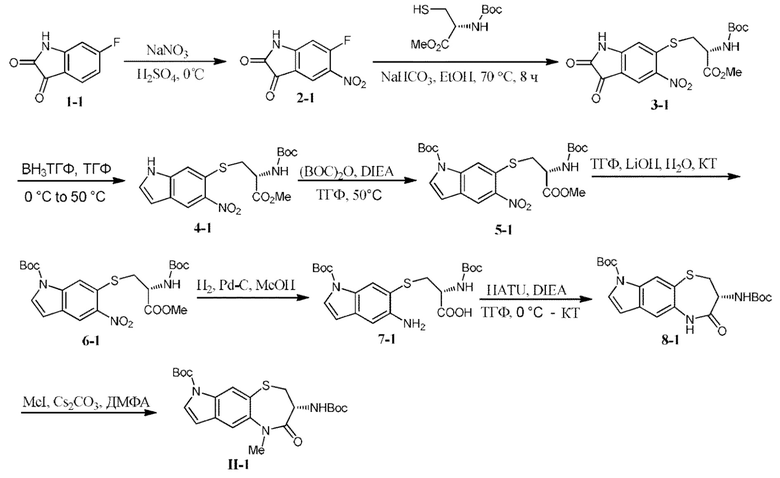
[0646] NaNO3 (11,33 г) и H2SO4 (100 мл) добавляли в реакционную колбу объемом 500 мл, перемешивали и охлаждали до 0°С в ледяной бане. Соединение 1-1 (20,00 г) растворяли в H2SO4 (120 мл) и раствор 1-1 в H2SO4 медленно, по каплям добавляли в реакционную колбу. После завершения добавления реакцию продолжали при 0°С в течение 1 ч, и затем реакционный раствор вливали в воду со льдом (1 л), перемешивали в течение 0,5 ч и фильтровали. Осадок на фильтре промывали водой до нейтральной реакции. Осадок на фильтре суспендировали, промывали EtOH/H2O (7:3) (80 мл) в течение 0,5 ч и фильтровали. Осадок на фильтре сушили с получением неочищенного продукта 2-1 (18,83 г, выход 74%).
[0647] 2-1 (9,10 г), N-Boc-L-цистеин (13,24 г) и NaHCO3 (5,67 г) последовательно добавляли в реакционную колбу, затем добавляли EtOH (200 мл) и проводили реакцию при 70°С в течение 8 ч. После завершения реакции реакционный раствор охлаждали при перемешивании, при этом образовывалось большое количество осадка. Добавляли H2O (100 мл) и перемешивали еще в течение 0,5 ч до полного выпадения осадка. После фильтрации осадок на фильтре суспендировали, промывали H2O (500 мл) в течение 0,5 ч и фильтровали. Осадок на фильтре сушили с получением неочищенного продукта 3-1 (17,5 г, выход 95%). 1H-ЯМР (500 МГц, ДМСО-d6) δ=11,60 (с, 1Н), 8,27 (с, 1Н), 7,56 (д, J=8,4, 1H), 6,96 (с, 1H), 4,34-4,28 (м, 1H), 3,70 (с, 3Н), 3,58 (дд, J=13,0, 3,8, 1Н), 3,31 (дд, J=12,8, 10,8, 1Н), 1,37 (с, 9Н); 13С-ЯМР (125 МГц, ДМСО-d6) δ 181,47, 170,82, 160,37, 155,35, 153,15, 149,16, 139,90, 122,60, 114,61, 107,90, 78,81, 52,43, 51,51, 33,36, 28,04; МС-ЭРИ m/z 424,1 (М-Н)-.
[0648] 3-1 (10,00 г) помещали в реакционную колбу объемом 250 мл, затем добавляли ТГФ (80 мл) и перемешивали до полного растворения. Затем раствор охлаждали до -10°С и к реакционному раствору медленно добавляли раствор ВН3 в ТГФ (1 моль/л, 40 мл). После завершения добавления реакционный раствор нагревали до комнатной температуры и проводили реакцию в течение 2 ч, а затем переносили на 50°С и проводили реакцию в течение 15 мин. После охлаждения до 0°С реакцию останавливали путем медленного добавления H2O (10 мл), перемешивали в течение 0,5 ч и выпаривали на роторном испарителе с удалением большей части ТГФ. Остаток растворяли в этилацетате и экстрагировали водой. Этилацетатный слой сушили и выпаривали на роторном испарителе досуха с получением неочищенного продукта, который разделяли с помощью колоночной хроматографии на силикагеле (элюент: этилацетат : петролейный эфир = 1:5) с получением 4-1 (6,6 г, выход 71%). 1Н-ЯМР (500 МГц, CD3OD) δ=8,40 (с, 1Н), 7,59 (с, 1Н), 7,43 (д, J=3,2, 1Н), 6,63 (д, J=3,1, 1Н), 4,39 (дд, J=8,3, 5,0, 1Н), 3,68 (с, 3Н), 3,49 (дд, J=13,8, 5,0, 1Н), 3,26 (дд, J=13,8, 8,5, 1Н), 1,39 (с, 9Н); 13С-ЯМР (125 МГц, CD3OD) δ 172,95, 157,70, 143,95, 140,05, 129,85, 127,13, 125,92, 120,12, 113,10, 104,46, 80,86, 61,53, 52,89, 28,61, 14,46; МС-ЭРИ m/z 394,1, 433,4 (М-Н)-.
[0649] 4-1 (3,00 г) помещали в реакционную колбу объемом 100 мл и добавляли ТГФ (30 мл) до полного растворения. DIEA (1,27 г) и Вое ангидрид (2,07 г) последовательно добавляли с перемешиванием. Реакционный раствор нагревали до 50°С и проводили реакцию в течение ночи. После завершения реакции реакционный раствор охлаждали до комнатной температуры, выпаривали на роторном испарителе досуха и экстрагировали этилацетатом и водой. Этилацетатную фазу собирали, сушили и выпаривали досуха на роторном испарителе. Остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: этилацетат : петролейный эфир = 1:8) с получением Соединения 5-1 (3,57 г, выход 95%). МС-ЭРИ m/z 496,3 (М+Н)+.
[0650] 5-1 (3,50 г) помещали в реакционную колбу объемом 100 мл и добавляли ТГФ (20 мл) до полного растворения. Добавляли моногидрат гидроксида лития (0,89 г) и H2O (10 мл) и перемешивали при комнатной температуре в течение 24 ч. После завершения реакции реакционный раствор доводили до рН 4-5 при использовании 1 моль/л HCl в ледяной бане, выпаривали на роторном испарителе с удалением большей части ТГФ и экстрагировали этилацетатом и водой. Органическую фазу собирали, сушили и выпаривали досуха на роторном испарителе с получением неочищенного продукта 6-1.
[0651] К неочищенному продукту 6-1 добавляли метанол (30 мл) до полного растворения и три раза барботировали аргоном. Под атмосферой аргона добавляли Pd-C (0,75 г), а затем при перемешивании добавляли водород и проводили реакцию при 25°С в течение 24 ч. После завершения реакции реакционный раствор фильтровали через диатомит для удаления Pd-C и досуха выпаривали фильтрат на роторном испарителе с получением неочищенного продукта 7-1.
[0652] К неочищенному продукту 7-1 добавляли безводный ТГФ (200 мл) до полного растворения. Добавляли DIEA (2,01 г) и охлаждали до 0°С с перемешиванием. Медленно добавляли HATU (5,37 г) и после завершения добавления реакционный раствор нагревали до комнатной температуры и проводили реакцию в течение ночи. Добавляли H2O (10 мл) и перемешивали в течение 0,5 ч, и большую часть ТГФ удаляли при выпаривании на роторном испарителе. Остаток экстрагировали этилацетатом и водой. Этилацетатный слой собирали, сушили и досуха выпаривали на роторном испарителе. Остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир : этилацетат = 6:1) с получением 8-1 (1,85 г, общий выход в трех стадиях 60%).
[0653] 8-1 (1,80 г) помещали в реакционную колбу объемом 100 мл и добавляли ДМФА (15 мл) до полного растворения. Добавляли карбонат цезия (1,76 г) и охлаждали до -5°С с перемешиванием. Затем медленно добавляли иодметан (0,68 г). После завершения добавления реакционный раствор нагревали до комнатной температуры и проводили реакцию в течение 3 ч при комнатной температуре. После окончания реакции к реакционному раствору медленно добавляли H2O (60 мл), при этом образовывалось большое количество осадка. После завершения добавления реакционный раствор перемешивали в течение 0,5 ч и фильтровали. Осадок на фильтре собирали и сушили с получением 1,63 г (1,63 г, выход 88%).1Н-ЯМР (500 МГц, CDCl3) δ=8,42 (с, 1Н), 8,31 (с, 1Н), 7,64 (д, J=3,5, 1Н), 7,32 (с, 1Н), 6,51 (д, J=3,6, 1Н), 5,65 (д, J=7,7, 1Н), 4,47-4,41 (м, 1Н), 3,81 (дд, J=11,0, 6,7, 1Н), 2,87 (т, J=11,4, 1Н), 1,69 (с, 9Н), 1,38 (с, 9Н); 13С-ЯМР (125 МГц, CDCl3) δ 172,51, 154,70, 149,32, 134,71, 133,57, 132,01, 128,14, 122,58, 122,02, 116,02, 106,92, 80,16, 50,40, 39,06, 38,74, 28,39, 28,26; МС-ЭРИ m/z 448,2 (М+Н)+.
[0654] Пример 4: Синтез соединения II-2
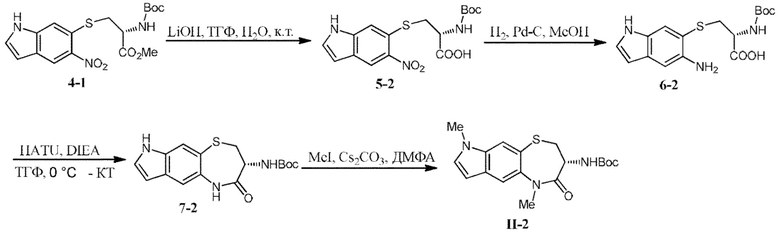
[0655] 4-1 (3 г) помещали в реакционную колбу объемом 100 мл и добавляли ТГФ (20 мл) до полного растворения. Добавляли моногидрат гидроксида лития (0,96 г) и H2O (10 мл) и перемешивали при комнатной температуре в течение 24 ч. После окончания реакции реакционный раствор доводили до рН 4-5 при использовании 1 моль/л HCl в ледяной бане, выпаривали на роторном испарителе с удалением большей части ТГФ и экстрагировали этилацетатом и водой. Органическую фазу собирали, сушили и досуха выпаривали на роторном испарителе с получением неочищенного продукта 5-2. МС-ЭРИ: Вычисл. для C16H19N3O6S (M): 381,1, найдено МС-ЭРИ m/z 380,0433.4 (М-Н)-.
[0656] К неочищенному продукту 5-2 добавляли метанол (30 мл) до полного растворения и три раза барботировали аргоном. Под атмосферой аргона добавляли Pd-C (0,81 г), затем добавляли водород при перемешивании и проводили реакцию при 25°С в течение 24 ч. После окончания реакции реакционный раствор фильтровали через диатомит для удаления Pd-C и досуха выпаривали фильтрат на роторном испарителе с получением неочищенного продукта 6-2. МС-ЭРИ m/z 352,1 (М+Н)+.
[0657] К неочищенному продукту 6-2 добавляли безводный ТГФ (200 мл) до полного растворения. Добавляли DIEA (2,15 г) и охлаждали до 0°С при перемешивании. Медленно добавляли HATU (5,77 г), нагревали до комнатной температуры и проводили реакцию в течение ночи. Добавляли H2O (10 мл) и перемешивали в течение 0,5 ч, и большую часть ТГФ удаляли при выпаривании на роторном испарителе. Остаток экстрагировали этилацетатом и водой. Этилацетатный слой собирали, сушили и выпаривали на роторном испарителе досуха. Остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 6:1) с получением 7-2 (1,43 г, общий выход в трех стадиях 57%). МС-ЭРИ m/z 334,1 (М+Н)+.
[0658] 7-2 (1,40 г) помещали в реакционную колбу объемом 100 мл и добавляли ДМФА (15 мл) до полного растворения. Добавляли карбонат цезия (1,78 г) и затем охлаждали до -5°С при перемешивании. Затем медленно добавляли иодметан (0,69 г), нагревали до комнатной температуры и проводили реакцию в течение 3 ч при комнатной температуре. После окончания реакции в реакционный раствор медленно добавляли H2O (60 мл), при этом образовывалось большое количество осадка. После завершения добавления реакционный раствор перемешивали в течение 0,5 ч и фильтровали. Осадок на фильтре собирали и сушили с получением II-2 (1,25 г, выход 86%). 1Н-ЯМР (500 МГц, CDCl3) δ=7,59 (с, 1Н), 7,51 (с, 1Н), 7,12 (д, J=2,9, 1Н), 6,46 (д, J=2,6, 1Н), 5,61 (д, J=7,6, 1Н), 4,41-4,32 (м, 1Н), 3,79 (с, 3H), 3,68 (дд, J=11,0, 6,7, 1Н), 3,45 (с, 3H), 2,75 (т, J=11,2, 1Н), 1,36 (с, 9Н); 13С-ЯМР (125 МГц, CDCl3) δ 171,13, 154,65, 137,94, 135,56, 131,37, 129,84, 119,70, 117,06, 116,16, 101,52, 79,92, 50,78, 39,01, 37,11, 33,22, 28,40; МС-ЭРИ m/z 362,1 (М+Н)+.
[0659] Пример 5: Синтез соединения II-3
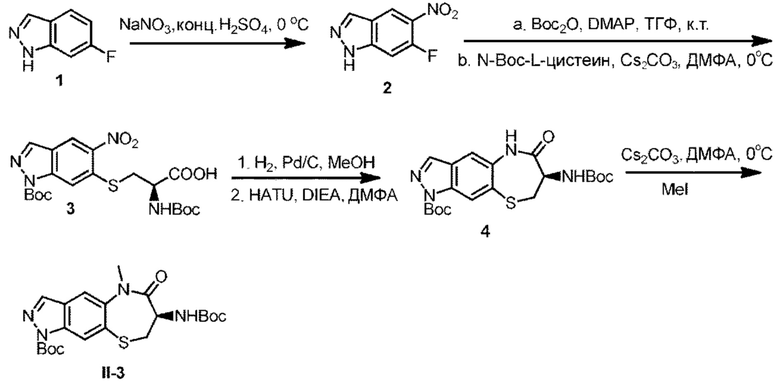
[0660] NaNO3 (5100 мг, 60 ммоль) помещали в реакционную колбу объемом 500 мл, а затем по каплям добавляли концентрированную серную кислоту (60 мл) при 0°С. 6-Фториндазол 1 (8167 мг, 60 ммоль) растворяли в концентрированной серной кислоте (60 мл), и затем полученный раствор медленно, по каплям добавляли к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 2,5 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в смесь воды со льдом (500 мл) и фильтровали через фильтровальную бумагу на вакуумном фильтре. Фильтрат экстрагировали ЕА. Органическую фазу объединяли с твердой фазой, полученной в результате вакуумного фильтрования, промывали насыщенным NaHCO3 и насыщенным NaCl, сушили над Na2SO4, выпаривали, а остаток разделяли с помощью колоночной хроматографии (ДХМ) с получением 2: бледно-желтое твердое вещество (3300 мг, 30,3%).
[0661] Соединение 2 (144 9 мг, 8 ммоль) помещали в реакционную колбу объемом 250 мл, и затем добавляли Boc2O (2095 мг, 9,6 ммоль), DMAP (195 мг, 1,6 ммоль) и ТГФ (100 мл), и проводили реакцию при комнатной температуре в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. После удаления растворителя при пониженном давлении получали Вос-защищенное промежуточное соединение. Промежуточное соединение использовали непосредственно в следующей стадии без очистки. N-Boc-L-цистеин (2655 мг, 12 ммоль) и Cs2CO3 (7819 мг, 24 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли ДМФА (80 мл) при 0°С и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли раствор Вос-защищенного промежуточного соединения, полученного после Реакции в ДМФА (20 мл), и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 3: бледно-желтое твердое вещество 2400 мг (62,2%).
[0662] Соединение 3 (2310 мг, 4,8 ммоль) помещали в трехгорлую колбу объемом 250 мл и три раза барботировали аргоном. Под атмосферой аргона добавляли Pd/C (4000 мг, 10% веса) и МеОН (150 мл), три раза барботировали водородом и проводили реакцию в течение 8 ч под атмосферой водорода при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит на вакуумном фильтре. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (40 мл). К раствору добавляли HATU (1825 мг, 4,8 ммоль) и DIEA (1240 мг, 9,6 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА:РЕ=1:2) с получением 4: грязно-желтое твердое вещество (800 мг, 38%).
[0663] 4 (434,5 мг, 1 ммоль) помещали в реакционную колбу, а затем добавляли Cs2CO3 (407,3 мг, 1,25 ммоль) и ДМФА (40 мл) и проводили реакцию при 0°С в течение 10 мин. К раствору по каплям медленно добавляли иодметан (177,4 мг, 1,2 5 ммоль) и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:2) с получением II-3: бледно-желтое твердое вещество (417 мг, 93%).
[0664] II-3: 1Н-ЯМР (400 МГц, CDCl3) δ 8,51 (с, 1Н), 8,15 (с, 1Н), 7,64 (с, 1Н), 5,57 (д, J=7,9 Гц, 1Н), 4,34 (дт, J=11,5, 7,3 Гц, 1Н), 3,69 (дд, J=11,0, 6,6 Гц, 1Н), 3,45 (с, 3H), 2,82 (т, J=11,3 Гц, 1Н), 1,73 (с, 9Н), 1,35 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,7, 154,6, 148,7, 141,8, 139,0, 138,0, 129,4, 126,9, 121,6, 116,8, 85,9, 80,2, 50,6, 38,4, 37,2, 28,4, 28,2, МС-ЭРИ: m/z 471,1 (М+Н)+.
[0665] Соединение II-5 может быть получено согласно такому же способу синтеза из 2 до II-3 в этом примере при использовании Соединения 8 в качестве исходного вещества. Синтез 8 был таким же, как описано в Примере 7.
[0666] II-5
[0667] 1Н-ЯМР (400 МГц, CDCl3) δ 8,49 (с, 1Н), 7,58 (с, 1Н), 5,57 (д, J=7,9 Гц, 1Н), 4,33 (дт, J=11,6, 7,3 Гц, 1Н), 3,68 (дт, J=14,1, 7,1 Гц, 1Н), 3,47 (с, 3H), 2,84 (т, J=11,3 Гц, 1Н), 1,72 (с, 9Н), 1,36 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,6, 154,6, 148,0, 142,5, 140,5, 138,8, 131,1, 124,6, 122,0, 115,6, 80,3, 50,5, 38,3, 37,2, 28,4, 28,2, МС-ЭРИ: m/z 505,1 (M+Na)+.
[0668] Пример 6: Синтез соединения II-4
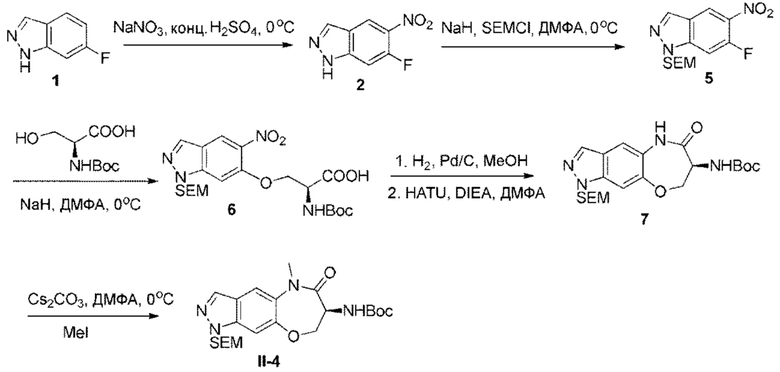
[0669] NaNO3 (5100 мг, 60 ммоль) помещали в реакционную колбу объемом 500 мл, а затем при 0°С по каплям добавляли концентрированную серную кислоту (60 мл). 6-Фториндазол 1 (8167 мг, 60 ммоль) растворяли в концентрированной серной кислоте (60 мл), и затем полученный раствор по каплям медленно добавляли к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 2,5 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в смесь воды со льдом (500 мл) и фильтровали через фильтровальную бумагу на вакуумном фильтре. Фильтрат экстрагировали ЕА. Органическую фазу объединяли с твердой фазой, полученной после вакуумной фильтрации, промывали насыщенным NaHCO3 и насыщенным NaCl, сушили над Na2SO4, выпаривали, а остаток разделяли с помощью колоночной хроматографии (ДХМ) с получением 2: бледно-желтое твердое вещество (3300 мг, 30,3%).
[0670] Соединение 2 (1086,8 мг, 6 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли Cs2CO3 (2443 мг, 7,5 ммоль), а затем добавляли ДМФА (40 мл) при 0°С и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли SEMC1 (1,33 мл, 7,5 ммоль), и проводили реакцию в течение 4 ч при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:8) с получением 5: бледно-желтое твердое вещество (900 мг, 48,2%). 1Н-ЯМР (400 МГц, CDCl3) δ 8, 59 (д, J=6, 9 Гц, 1Н), 8,18 (с, 1Н), 7,42 (д, J=10,7 Гц, 1Н), 5,72 (с, 2Н), 3,62-3,51 (м, 2Н), 0,93-0,86 (м, 2Н), -0,06 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 154,8 (д, J=262,1 Гц), 140,8 (д, J=11,5 Гц), 134,0 (д, J=10,9 Гц), 136,3, 121,0, 120,0, 98,3 (д, J=26,1 Гц), 78,5, 67,2, 17,8, -1,4.
[0671] N-Boc-L-серин (1026,1 мг, 5 ммоль) и NaH (400 мг, 10 ммоль, 60% по весу) помещали в реакционную колбу объемом 250 мл и три раза барботировали аргоном. Под атмосферой аргона при 0°С добавляли ДМФА (50 мл) и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли раствор 5 (778,5 мг, 2,5 ммоль) в ДМФА (10 мл) и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, затем экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 6: бледно-желтое твердое вещество (473 мг, 38,1%). 1Н-ЯМР (400 МГц, CDCl3) δ 7,95 (с, 1Н), 7,53 (с, 1Н), 7,33 (с, 1Н), 5, 73-5,60 (м, 2Н), 5,58-5,47 (м, 1Н), 4,70-4,59 (м, 1Н), 4, 58-4,49 (м, 1Н), 4,17-4,09 (м, 1Н), 3,60-3,48 (м, 2Н), 3,45 (с, 3H), 0,96-0,85 (м, 2Н), -0,08 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 169,4, 155,1, 150,0, 138,2, 134,0, 132,2, 121,9, 115,3, 103,1, 80,3, 78,0, 66,6, 49,9, 36,4, 28,3, 17,7, -1,4.
[0672] Соединение 6 (450 мг, 0,9062 ммоль) помещали в трехгорлую колбу объемом 100 мл и три раза барботировали аргоном. Под атмосферой аргона добавляли Pd/C (600 мг, 10% по весу) и МеОН (30 мл), три раза барботировали водородом и проводили реакцию в течение 4 ч под атмосферой водорода при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит на вакуумном фильтре. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (20 мл). К раствору добавляли HATU (380,2 мг, 1 ммоль) и DIEA (234 мг, 1,81 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА:РЕ=1:2) с получением коричневого твердого вещества 7 (260 мг, 64%).
[0673] Cs2CO3 (226, 6 мг, 0, 6955 ммоль) и ДМФА (20 мл) добавляли к 7 и проводили реакцию при 0°С в течение 10 мин. Иодметан (98,7 мг, 0,6955 ммоль) по каплям медленно добавляли к раствору и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:2) с получением II-4: коричневое твердое вещество (202 мг, 7 5,3%).
[0674] II-4: 1Н-ЯМР (400 МГц, CDCl3) δ 7, 95 (с, 1Н), 7,53 (с, 1Н), 7,33 (с, 1Н), 5,72-5,62 (м, 2Н), 5,54 (д, J=7,2 Гц, 1Н), 4,65 (дт, J=11,2, 7,3 Гц, 1Н), 4,53 (дд, J=9,5, 7,4 Гц, 1Н), 4,18-4,08 (м, 1Н), 3,57-3,49 (м, 2Н), 3,45 (с, 3H), 1,36 (с, 9Н), 0,95-0,86 (м, 2Н), -0,06 (с, 9Н); 13С-ЯМР (101 МГц, CDCl3) δ 169, 4, 155,1, 150,0, 138,2, 133,96, 132,2, 121,9, 115,3, 103,1, 80,3, 78,0, 66,6, 49,9, 36,4, 28,3, 17,7, -1,4.
[0675] Соединение II-6 может быть получено согласно такому же способу синтеза из 2 до II-4 в данном примере при использовании Соединения 8 в качестве исходного вещества. Синтез 8 проводили, как описано в Примере 7.
[0676] II-6
[0677] 1Н-ЯМР (400 МГц, CDCl3) δ 7,48 (с, 1Н), 7,32 (с, 1Н), 5, 65-5, 58 (м, 2Н), 5,50 (д, J=7,1 Гц, 1Н), 4,65 (дт, J=11,3, 7,2 Гц, 1Н), 4,55 (дд, J=9,5, 7,3 Гц, 1Н), 4,21-4,12 (м, 1Н), 3,62-3,54 (м, 2Н), 3,49 (с, 3H), 1,38 (с, 9Н), 0, 97-0, 88 (м, 2Н), -0,02 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 169,2, 155,1, 151,0, 139,3, 134,1, 133,1, 119,1, 114,0, 103,6, 80,2, 78,1, 77,3, 66,9, 49,8, 36,3, 28,2, 17,7, -1,4.
[0678] Пример 7: Синтез Соединения 8
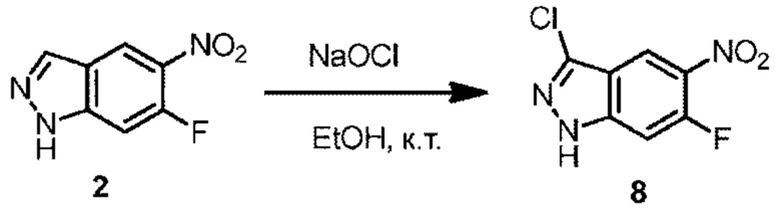
[0679] Соединение 2 (2000 мг, 11 ммоль) помещали в реакционную колбу объемом 250 мл, а затем добавляли EtOH (50 мл) и NaOCl (20 мл, 55 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакцию подкисляли 1Н HCl, экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:4) с получением 8: бледно-желтое твердое вещество (2000 мг, 84,3%).
[0680] 8: 1Н-ЯМР (400 МГц, CD3OD_SPE) δ 8,41 (д, J=6, 9 Гц, 1Н), 7,42 (д, J=11,1 Гц, 1Н); 13С-ЯМР (101 МГц, CD3OD_SPE) δ 156,2 (д, J=260,0 Гц), 143,4 (д, J=12,2 Гц), 137,7, 135,2 (д, J=11,6 Гц), 120, 2, 116, 8, 99, 8 (д, J=26,4 Гц).
[0681] Пример 8: Синтез Соединения II-7
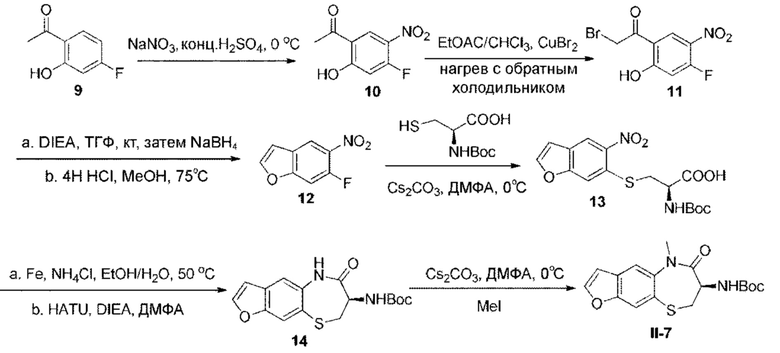
[0 682] NaNO3 (5100 мг, 60 ммоль) помещали в реакционную колбу объемом 500 мл, а затем по каплям добавляли концентрированную серную кислоту (60 мл) при 0°С. 4-Фтор-2-гидроксиацетофенон 9 (9248 мг, 60 ммоль) растворяли в концентрированной серной кислоте (60 мл), а затем полученный раствор по каплям медленно добавляли к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 2,5 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в смесь воды со льдом (500 мл) и фильтровали через фильтровальную бумагу на вакуумном фильтре. Фильтрат экстрагировали ЕА. Органическую фазу объединяли с твердой фазой, полученной при вакуумной фильтрации, промывали насыщенным NaHCO3 и насыщенным NaCl, сушили над Na2SO4, выпаривали, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:20) с получением 10: бледно-желтое твердое вещество (4570 мг, 38,2%). 1H-ЯМР (400 МГц, CDCl3) δ 13,02 (с, 1Н), 8,65 (д, J=8,3 Гц, 1Н), 6,83 (д, J=12,2 Гц, 1Н), 2,72 (с, 3H); 13С-ЯМР (100 МГц, CDCl3) δ 203,2, 168,5 (д, J=14,5 Гц), 161,9, 159,2, 130,6, 116,0 (д, J=2,5 Гц), 107,6 (д, J=23,0 Гц), 26,9.
[0683] CuBR2 (1898 мг, 8,5 ммоль) помещали в реакционную колбу объемом 250 мл, затем добавляли этилацетат (50 мл) и нагревали с обратным холодильником. К реакционному раствору добавляли раствор 10 (995,7 мг, 5 ммоль) в хлороформе (50 мл) и проводили реакцию при нагревании с обратным холодильником в течение 2 4 ч. Зеленый цвет жидкости реакции уходил, при этом образовывалось твердое вещество цвета извести. Прореагировала большая часть 10, как показала ТСХ. Твердое вещество отфильтровывали через диатомит на вакуумном фильтре. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:20-1:10) с получением 11: коричневое твердое вещество (833 мг, 60%). 1Н-ЯМР (400 МГц, CDCl3) δ 8, 37 (д, J=7,3 Гц, 1Н), 7,77 (д, J=2,3 Гц, 1Н), 7,41 (д, J=10,6 Гц, 1Н), 6,90 (дд, J=2,2, 0,7 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 156,8 (д, J=12,4 Гц), 155,3, 152,7, 148,6 (д, J=3,7 Гц), 123,6 (д, J=2,1 Гц), 119,2 (д, J=1,8 Гц), 107,3 (д, J=1,2 Гц), 101,5 (д, J=25,8 Гц).
[0684] Соединение 11 (5004 мг, 18 ммоль) помещали в реакционную колбу объемом 500 мл, добавляли ТГФ (180 мл), а затем медленно добавляли DIEA (3 мл, 18 ммоль) и проводили реакцию в течение 4 5 мин при комнатной температуре до полного завершения реакции, как было показано ТСХ. К раствору добавляли NaBH4 (2723 мг, 72 ммоль) и проводили реакцию в течение 8 ч при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакцию останавливали путем медленного добавления метанола. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в МеОН (50 мл). Затем добавляли 4Н HCl (25 мл) и нагревали до 75°С в течение 3 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:10) с получением 12: желтое твердое вещество (1200 мг, 36, 8%).
[0685] N-Boc-L-цистеин (2660 мг, 12 ммоль) и Cs2CO3 (7819 мг, 24 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли ДМФА (40 мл) при 0°С и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли раствор 12 (1086 мг, 6 ммоль) в ДМФА (10 мл) и проводили реакцию при 0°С в течение 24 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 13: бледно-желтое твердое вещество 2780 мг (колич.). 1H-ЯМР (400 МГц, CDCl3) δ 8,30 (с, 1Н), 7,64 (д, J=2,0 Гц, 1Н), 7,54 (с, 1Н), 6,75 (д, J=1,9 Гц, 1Н), 5,70 (с, 1Н), 4,50 (с, 1Н), 3,60-3, 49 (м, 1Н), 3,35 (с, 1Н), 1,35 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 175,1, 157,2, 155,9, 147,8, 143,5, 132,4, 124,9, 119,7, 110,4, 107,1, 80,5, 53,5, 36,1, 28,4, МС-ЭРИ: m/z 383,1 (М+Н)+.
[0686] Соединение 13 (956 мг, 2,5 ммоль) помещали в реакционную колбу объемом 100 мл и добавляли Fe (698 мг, 12,5 ммоль) и NH4Cl (267 мг, 5 ммоль). Затем добавляли EtOH (24 мл) и H2O (6 мл) и проводили реакцию при 50°С в течение 4 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (60 мл). К раствору добавляли HATU (950 мг, 2,5 ммоль) и DIE (0,83 мл, 5 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА:РЕ=1:3) с получением желтовато-коричневого твердого вещества 14 (500 мг, 59,8%).
[0687] 14 (1500 мг, 4,5 ммоль) помещали в реакционную колбу, а затем добавляли Cs2CO3 (1759 мг, 5,4 ммоль) и ДМФА (60 мл) и проводили реакцию при 0°С в течение 10 мин. Иодметан (7 66,5 мг, 5,4 ммоль) по каплям медленно добавляли к раствору и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:4) с получением II-7: белое твердое вещество 1320 мг (84,2%).
[0688] II-7: 1Н-ЯМР (400 МГц, CDCl3) δ 7,78 (с, 1Н), 7,69 (д, J=2,1 Гц, 1Н), 7,52 (с, 1Н), 6,77 (д, J=1,3 Гц, 1Н), 5,58 (д, J=7,8 Гц, 1Н), 4,37 (дт, J=11,3, 7,5 Гц, 1Н), 3,70 (дд, J=11,1, 6,7 Гц, 1Н), 3,44 (с, 3H), 2,79 (т, J=11,2 Гц, 1Н), 1,37 (с, 9Н); 13С-ЯМР (101 МГц, CDCl3) δ 171,0, 154,6, 153,1, 147,4, 141,4, 129,6, 123,3, 118,1, 117,4, 106,7, 80,0, 50,7, 39,0, 37,0, 28,4.
[0689] Пример 9: Синтез Соединения II-8
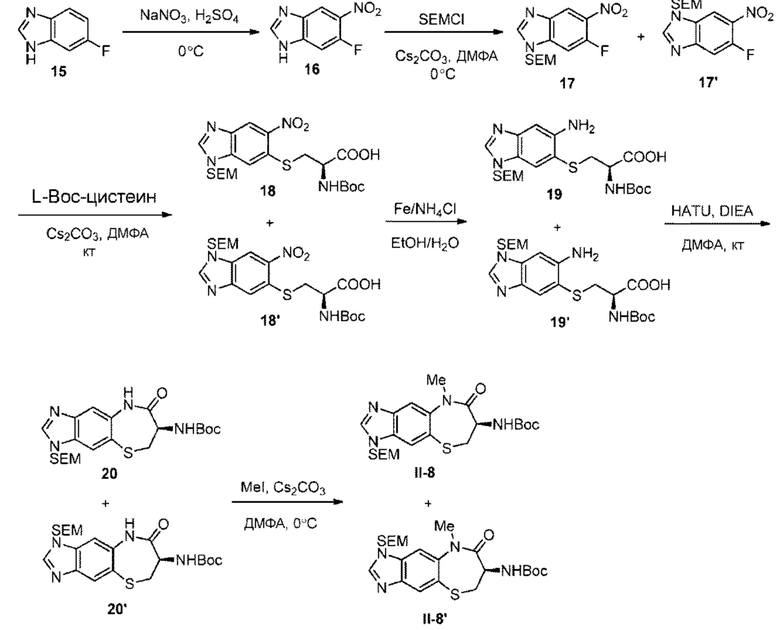
[0690] NaNO3 (2520 мг, 30 ммоль) помещали в реакционную колбу объемом 500 мл, а затем по каплям добавляли концентрированную серную кислоту (30 мл) при 0°С. 6-Фторбензимидазол 15 (29 мг, 30 ммоль) растворяли в концентрированной серной кислоте (30 мл), а затем полученный раствор по каплям медленно добавляли к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 2,5 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в смесь воды со льдом (500 мл) и доводили до основного рН насыщенным растворм NaCO3. Реакционный раствор экстрагировали ЕА и сушили над Na2SO4. После удаления растворителя при пониженном давлении получали коричневый твердый порошок, который использовали непосредственно в следующей реакции без очистки с помощью колоночной хроматографии.
[0691] Соединение 16 (2300 мг, 12,7 ммоль) помещали в реакционную колбу объемом 50 мл, добавляли Cs2CO3 (5200 мг, 15,9 ммоль), а затем добавляли ДМФА (20 мл) при 0°С и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли SEMCl (2,8 мл, 15,9 ммоль) и проводили реакцию в течение 4 ч при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:8) с получением пары изомеров 17 и 17' в соотношении приблизительно 1:1, которые нельзя было разделить с помощью колоночной хроматографии: бледно-желтое твердое вещество (900 мг).
[0692] N-Boc-L-цистеин (284 мг, 1,3 ммоль) и Cs2CO3 (837 мг, 2,6 ммоль) помещали в реакционную колбу объемом 50 мл, а затем добавляли ДМФА (10 мл) при комнатной температуре и проводили реакцию в течение 15 мин. Затем медленно добавляли раствор смешанных 17 и 17' в ДМФА (2 мл) по каплям и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=10:1) с получением пары изомеров Соединений 18 и 18': бледно-желтое твердое вещество (140,6 мг, 86%).
[0693] Соединения 18 и 18' (330 мг, 0,64 ммоль) помещали в трехгорлую колбу объемом 250 мл и три раза барботировали аргоном. Под атмосферой аргона добавляли порошок Fe (180 мг, 3,2 ммоль), NH4Cl (172,2 мг, 3,2 ммоль), этанол (12,5 мл) и деионизированную воду (10 мл) и проводили реакцию при нагревании с обратным холодильником в течение 3 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит на вакуумном фильтре и сушили над безводным Na2SO4. После удаления растворителя при пониженном давлении получали неочищенный продукт в виде пары изомеров 19 и 19'.
[0694] К раствору Соединений 19 и 19' в ДМФА добавляли HATU (2 93 мг, 0,8 ммоль) и DIEA (181 мг, 1,4 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой, а затем насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА:РЕ=1:2) с получением пары изомеров 20 и 20': грязно-желтое твердое вещество (240 мг, 38%).
[0695] Соединения 20 и 20' (240 мг, 0,52 ммоль) помещали в реакционную колбу, а затем добавляли Cs2CO3 (202 мг, 0,62 ммоль) и ДМФА (10 мл) и проводили реакцию при 0°С в течение 10 мин. Иодметан (88 мг, 0,62 ммоль) по каплям медленно добавляли к раствору и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:2) с получением пары изомеров II-8 и II-8': бледно-желтое твердое вещество (120 мг, 93%). Затем после удаления защитной группы из промежуточных соединений, общее промежуточное соединение получали для конечной реакции конденсации.
[0696] Данные для II-8+II-8': ЭРИ: m/z 479,2 (М+Н)+.
[0697] Пример 10: Синтез Соединения II-9
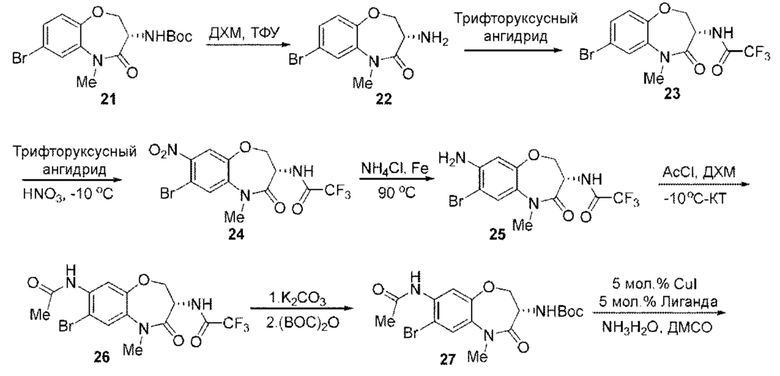
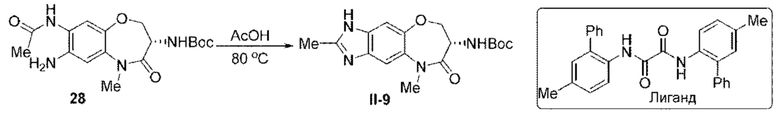
[0698] Соединение 21 (8 г) добавляли в одногорлую колбу объемом 250 мл, оборудованную мешалкой, и добавляли дихлорметан (50 мл) до полного растворения. При перемешивании добавляли трифторуксусную кислоту (12 мл) и реакционный раствор перемешивали при комнатной температуре в течение 1 ч с последующим выпариванием на роторном испарителе для удаления дихлорметана и трифторуксусной кислоты. Остаток экстрагировали водой (80 мл), доводили до рН 8-9, а затем экстрагировали этилацетатом. Органическую фазу собирали, экстрагировали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали на вакуумном фильтре и выпаривали досуха на роторном испарителе с получением Соединения 22 в виде коричневого твердого вещества (5,8 г). МС-ЭРИ т/z (79 Br) 271,0 и (81Br) 273,0 (М+Н)+.
[0699] Соединение 22 (5,5 г), N, N-диизопропилэтиламин (3,93 г) и трифторуксусный ангидрид (5,75 г) последовательно добавляли в одногорлую колбу объемом 250 мл, оборудованную мешалкой, затем добавляли дихлорметан (50 мл) до полного растворения и перемешивали при комнатной температуре в течение 8 ч. После окончания реакции реакционный раствор экстрагировали водой (50 мл). Дихлорметановый слой собирали, экстрагировали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали для удаления безводного сульфата натрия, выпаривали досуха на роторном испарителе, а остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат =7:1) с получением Соединения 23 (7,30 г, выход 98%). МС-ЭРИ m/z (79Br) 367, 1 и (81Br) 369,1 (М+Н)+.
[0700] Трифторуксусный ангидрид (60 мл) добавляли в двугорлую колбу объемом 250 мл, оборудованную термометром и мешалкой, и охлаждали до -30°С. Добавляли Соединение 23 (7 г) и растворяли при перемешивании. Концентрированную азотную кислоту (1,4 г) медленно добавляли по каплям, и затем реакцию продолжали в течение 4 ч, при этом температуру поддерживали при -10°С или ниже. После окончания реакции реакционный раствор вливали в воду со льдом (300 мл) и тщательно перемешивали. Образовывалось большое количество твердого вещества, которое отфильтровывали на вакуумном фильтре. Осадок на фильтре промывали водой до нейтральной реакции, собирали и сушили с получением Соединения 24 в виде желтого твердого вещества (7,70 г, выход 96%). МС-ЭРИ m/z (79Br) 411 и (81Br) 413 (М)+.
[0701] Соединение 24 (7 г), порошок железа (7,6 г), насыщенный водный раствор хлорида аммония (100 мл) и этанол (100 мл) последовательно добавляли в одногорлую колбу объемом 250 мл, оборудованную мешалкой, нагревали до 90°С и проводили реакцию в течение 5 ч. После окончания реакции реакционный раствор фильтровали через диатомит, и осадок на фильтре три раза промывали дихлорметаном (150 мл). Фильтрат собирали и выпаривали на роторном испарителе для удаления большей части этанола и дихлорметана. Оставшуюся жидкость доводили до рН 8-9 насыщенным карбонатом натрия и три раза экстрагировали дихлорметаном (300 мл). Органическую фазу собирали, один раз, соответственно, промывали насыщенным раствором бикарбонатом натрия и насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали, выпаривали досуха на роторном испарителе, а остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат =8:1) с получением Соединения 25 (4,02 г) в виде белого твердого вещества. Выход 62%; МС-ЭРИ m/z (79Br) 382,1 и (81Br) 384,0 (М+Н)+.
[0702] Соединение 25 (4 г) и N,N-диизопропилэтиламин (1,83 г) последовательно добавляли в двугорлую колбу объемом 250 мл, снабженную термометром и мешалкой, и при перемешивании добавляли дихлорметан (40 мл) до полного растворения. Затем реакционный раствор охлаждали до -10°С. Ацетилхлорид (1,06 г) растворяли в дихлорметане (10 мл). Раствор ацетилхлорида в дихлорметане по каплям медленно добавляли к вышеуказанному реакционному раствору таким образом, чтобы температура реакционного раствора во время добавления оставалась на уровне -5°С или ниже. Затем реакционный раствор медленно нагревали до комнатной температуры и оставляли реакцию на ночь. После окончания реакции в реакционный раствор вливали воду (50 мл) и экстрагировали. Органическую фазу собирали, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали, выпаривали на роторном испарителе досуха и отделяли и очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат =4:1) с получением Соединения 26 в виде белого твердого вещества (3,19 г). Выход 72%. 1H-ЯМР (500 МГц, CDCl3) δ=8,34 (с, 1Н), 7,62 (с, 1Н), 7,55 (д, J=6,3, 1Н), 7,39 (с, 1Н), 4,88-4, 82 (м, 1Н), 4,70 (дд, J=9,8, 7,4, 1Н), 4,22 (дд, J=10,9, 10,1, 1Н), 3,39 (с, 3H), 2,26 (с, 3H); 13С-ЯМР (125 МГц, CDCl3) δ 168,38, 167,73, 156,74 (к, J=38,4), 149,71, 135,40, 131,81, 126,45, 115,78, 115,57 (к, J=287,6), 108,53, 77,41, 77,16, 76 91, 76 35, 49 75, 35 76, 25 04; МС-ЭРИ m/z 424, 1 (79Br) и 426,1 (81Br) (М+Н)+.
[0703] Соединение 26 (3 г) и безводный карбонат калия (3 г) последовательно добавляли в одногорлую колбу объемом 100 мл, снабженную перемешивающим элементом, и добавляли тетрагидрофуран (15 мл) и воду (15 мл) до полного растворения. Реакционный раствор перемешивали в течение ночи при комнатной температуре. После окончания реакции к реакционному раствору добавляли Вое ангидрид (2,31 г) и перемешивали при комнатной температуре в течение 5 ч. Реакционный раствор экстрагировали водой (30 мл) и дихлорметаном (30 мл). Органическую фазу собирали, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали и выпаривали на роторном испарителе досуха с получением Соединения 27 в виде белого твердого вещества (3 г, выход 99%). МС-ЭРИ m/z (79Br) 428, 0 и (81Br) 429, 9 (М+Н)+.
[0704] CuI (19,0 мг, 0,1 ммоль), N1, N2-бис (5-метил-[1,1'-бифенил]-2-ил)оксамид (42,0 мг, 0,1 ммоль), Соединение 27 (0,856 г, 2 ммоль) и K3PO4 (0,424 г, 2 ммоль) последовательно добавляли к пробирку Шленка объемом 10 мл, снабженную мешалкой. Затем 25% водный аммиак (0,28 г) и ДМСО (2 мл) последовательно добавляли шприцем в пробирку Шленка под атмосферой аргона и пробирку Шленка закрывали. Реакционный раствор нагревали до 60°С и проводили реакцию в течение 2 4 ч. После окончания реакции реакционный раствор охлаждали до комнатной температуры, разбавляли этилацетатом (30 мл) и фильтровали через диатомит. Осадок на фильтре промывали этилацетатом и перегоняли фильтрат при пониженном давлении. Оставшийся остаток очищали и разделяли с помощью колоночной хроматографии на силикагеле (проявляющий реагент: дихлорметан:метанол =30:1) с получением Соединения 28 в виде коричневого твердого вещества (0,59 г, выход 81%). МС-ЭРИ: Вычисл. для C17H24N4O5 (М): 364,1, найдено МС-ЭРИ m/z 365,1 (М+Н)+.
[0705] Соединение 28 (1 г) добавляли в одногорлую колбу объемом 50 мл, снабженную перемешивающим элементом, затем добавляли уксусную кислоту (15 мл), нагревали до 80°С и проводили реакцию в течение 1 ч. После окончания реакции реакционный раствор нагревали до комнатной температуры, добавляли воду (50 мл) и экстрагировали этилацетатом. Органическую фазу собирали, промывали насыщенным раствором бикарбоната натрия и насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали и выпаривали досуха на роторном испарителе. Остаток разделяли и очищали с помощью колоночной хроматографии на силикагеле (проявляющий реагент: дихлорметан:метанол =25:1) с получением Промежуточного соединения II-9 в виде бледно-желтого твердого вещества (0,74 г, выход 78%). 1H-ЯМР (400 МГц, CDCl3) δ=7,29 (с, 1Н), 7,21 (с, 1Н), 5,62 (д, J=7,3, 1Н), 4,65-4,56 (м, 1Н), 4,51 (дд, J=9,4, 7,5, 1Н), 4,14 (т, J=10,4, 1Н), 3,38 (с, 3H), 2,55 (с, 3H), 1,38 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 169,49, 155,56, 153,52, 149,54, 146,13, 136,19, 131,83, 109,50, 107,07, 80,67, 77,84, 50,25, 36,20, 28,34, 14,94; МС-ЭРИ m/z 347,0 (М+Н)+; ЭРИ-МСВР Вычисл. для C17H23O4N4 (М+Н)+: 347, 1714, найдено: 347, 1717.
[0706] Пример 11: Синтез Соединения II-10
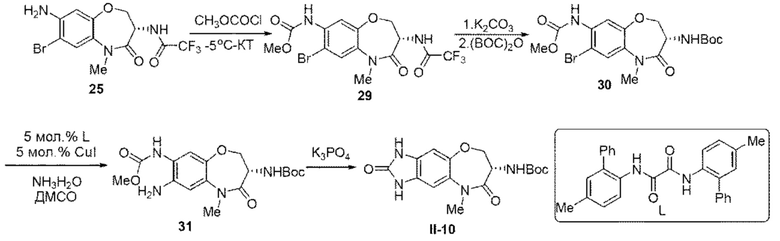
[0707] Соединение 25 (4 г) и N,N-диизопропилэтиламин (1,83 г) последовательно добавляли в двугорлую колбу объемом 250 мл, снабженную термометром и мешалкой, а затем при перемешивании добавляли дихлорметан (40 мл) до полного растворения. Реакционный раствор охлаждали до -5°С. Ацетилхлорид (1,29 г) растворяли в дихлорметане (10 мл). Раствор ацетилхлорида в дихлорметане по каплям медленно добавляли к вышеуказанному реакционному раствору таким образом, чтобы температура реакционного раствора оставалась на уровне 0°С или ниже во время добавления. Затем реакционный раствор медленно нагревали до комнатной температуры и проводили реакцию в течение ночи. После окончания реакции в реакционный раствор вливали воду (50 мл) и проводили экстракцию. Органическую фазу собирали, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали, выпаривали досуха на роторном испарителе и разделяли и очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат =4:1) с получением Соединения 29 в виде белого твердого вещества (3,19 г, выход 67%), МС-ЭРИ m/z 440, 2 (79Br) и 442, 2 (81Br) (М+Н)+.
[0708] Соединение 29 (3 г) и безводный карбонат калия (3 г) последовательно добавляли в одногорлую колбу объемом 100 мл, снабженную перемешивающим элементом, и добавляли тетрагидрофуран (15 мл) и воду (15 мл) до полного растворения. Реакционный раствор перемешивали в течение ночи при комнатной температуре. После окончания реакции в реакционный раствор добавляли Вое ангидрид (2,30 г) и перемешивали при комнатной температуре в течение 5 ч. Реакционный раствор экстрагировали водой (30 мл) и дихлорметаном (30 мл). Органическую фазу собирали, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали и выпаривали досуха на роторном испарителе с получением Соединения 30 в виде белого твердого вещества (3 г, выход 99%). МС-ЭРИ m/z 465, 8 (79Br) и 467, 8 (81Br) (M+Na)+.
[0709] CuI (19,0 мг, 0,1 ммоль), N1,N2-бис (5-метил- [1,1'-бифенил]-2-ил)оксамид (42,0 мг, 0,1 ммоль), Соединение 30 (0,888 г, 2 ммоль) и K3PO4 (0,424 г, 2 ммоль) последовательно добавляли в пробирку Шленка объемом 10 мл, снабженную мешалкой. Затем 2 5% водный аммиак (0,28 г) и ДМСО (2 мл) последовательно добавляли шприцем в пробирку Шленка под атмосферой аргона и пробирку Шленка закрывали. Реакционный раствор нагревали до 70°С и проводили реакцию в течение 24 ч. После окончания реакции реакционный раствор охлаждали до комнатной температуры, разбавляли этилацетатом (30 мл) и фильтровали через диатомит. Осадок на фильтре промывали этилацетатом, а фильтрат перегоняли при пониженном давлении. Остаток очищали и разделяли с помощью колоночной хроматографии на силикагеле (проявляющий реагент: дихлорметан:метанол =30:1) с получением Соединения 31 в виде коричневого твердого вещества (0,40 г, выход 53%). МС-ЭРИ m/z 381,1 (М+Н)+.
[0710] Соединение 31 (1 г) добавляли в одногорлую колбу объемом 2 5 мл, снабженную перемешивающим элементом, а затем добавляли ДМСО (10 мл) и фосфат калия (1,67 г), нагревали до 100°С и проводили реакцию в течение 5 ч. После окончания реакции реакционный раствор охлаждали до комнатной температуры, добавляли воду (50 мл) и экстрагировали этилацетатом. Органическую фазу собирали, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали и выпаривали досуха на роторном испарителе. Остаток разделяли и очищали с помощью колоночной хроматографии на силикагеле (проявляющий реагент: дихлорметан:метанол =20:1) с получением Соединения II-10 в виде бледно-желтого твердого вещества (0,69 г, выход 78%). 1H-ЯМР (500 МГц, CDCl3) δ=10,58 (с, 1Н), 10,46 (с, 1Н), 6,88 (с, 1Н), 6,62 (с, 1Н), 5,72 (д, J=7,1, 1Н), 4,64-4,59 (м, 1Н), 4,58-4,50 (м, 1Н), 4,21-4,09 (м, 1Н), 3,32 (с, 3H), 1,44 (с, 9Н); МС-ЭРИ m/z 371,1.
[0711] Пример 12: Синтез Соединения II-11
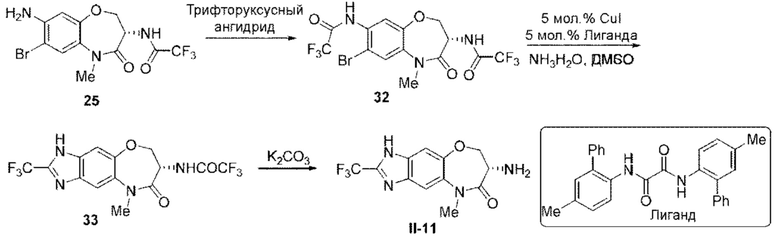
[0712] Соединение 25 (4 г) и N,N-диизопропилэтиламин (1,83 г) последовательно добавляли в двугорлую колбу объемом 250 мл, снабженную термометром и мешалкой, и добавляли дихлорметан (40 мл) до полного растворения при перемешивании. Затем реакционный раствор охлаждали до -20°С. Трифторуксусный ангидрид (2,9 г) растворяли в дихлорметане (10 мл). Раствор трифторуксусного ангидрида в дихлорметане по каплям медленно добавляли к вышеуказанному реакционному раствору таким образом, чтобы температура реакционного раствора оставалась на уровне -10°С или ниже во время добавления. Затем реакционный раствор медленно нагревали до комнатной температуры и проводили реакцию в течение ночи. После окончания реакции в реакционный раствор вливали воду (50 мл) и проводили экстракцию. Органическую фазу собирали, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, фильтровали, выпаривали досуха на роторном испарителе и разделяли и очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат =4:1) с получением Соединения 32 в виде белого твердого вещества (4,20 г). Выход 84%. МС-ЭРИ m/z 475,8 (79Br) и 477, 8 (81Br) (M-H)-.
[0713] CuI (19,0 мг, 0,1 ммоль), N1,N2-бис(5-метил-[1,1'-бифенил]-2-ил)оксамид (42,0 мг, 0,1 ммоль), Соединение 32 (0,956 г, 2 ммоль) и K3PO4 (0,424 г, 2 ммоль) последовательно добавляли в пробирку Шленка объемом 10 мл, снабженную мешалкой. Затем 25% водный аммиак (0,28 г) и ДМСО (2 мл) последовательно добавляли шприцем в пробирку Шленка под атмосферой аргона и пробирку Шленка закрывали. Реакцию продолжали при комнатной температуре в течение 24 ч. После окончания реакции добавляли уксусную кислоту (5 мл) и перемешивали еще в течение 8 ч. Реакционный раствор разбавляли этилацетатом (40 мл) и фильтровали через диатомит. Осадок на фильтре промывали этилацетатом и перегоняли фильтрат при пониженном давлении. Остаток очищали и разделяли с помощью колоночной хроматографии на силикагеле (проявляющий реагент: дихлорметан:метанол =30:1) с получением Соединения 33 в виде коричневого твердого вещества (0,40 г, выход 51%). 1Н-ЯМР (500 МГц, CDCl3) δ=10,39 (с, 1Н), 7,75 (с, 1Н), 7,59 (с, 1Н), 7,39 (с, 1Н), 4,87-4,79 (м, 1Н), 4,79-4, 72 (м, 1Н), 4,24 (т, J=9,0, 1Н), 3,53 (с, 3H); МС-ЭРИ m/z 397,0 (М+Н)+.
[0714] Соединение 33 (0,4 г) добавляли в одногорлую колбу, снабженную мешалкой, и при перемешивании добавляли тетрагидрофуран (4 мл) до полного растворения. Затем добавляли безводный K2CO3 (0,42 г) и H2O (4 мл) и перемешивали в течение ночи при комнатной температуре. После окончания реакции реакционный раствор экстрагировали этилацетатом (15 мл) и H2O (15 мл). Органическую фазу собирали, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и выпаривали досуха на роторном испарителе с получением Соединения II-11 (0,3 г, выход 99%). 1Н-ЯМР (400 МГц, ДМСО-d6) δ=7,74 (с, 1Н), 7,45 (с, 1Н), 4,28 (дд, J=9,9, 7,6, 1Н), 3,99 (дд, J=11,4, 10,1, 1Н), 3,68 (дд, J=11,5, 7,6, 1Н), 3,37 (с, 3H); МС-ЭРИ m/z 301,3 (М+Н)+.
[0715] Пример 13: Синтез Соединения II-14
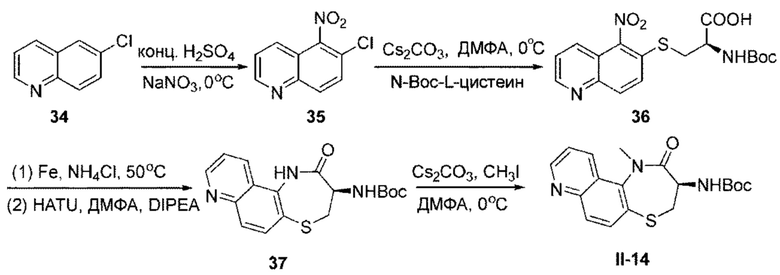
[0716] NaNO3 (5,2 г, 61,1 ммоль) помещали в реакционную колбу объемом 500 мл, а затем при 0°С по каплям добавляли концентрированную серную кислоту (60 мл). 6-Хлорхинолин (10,0 г, 61,1 ммоль) растворяли в концентрированной серной кислоте (60 мл), а затем полученный раствор по каплям медленно добавляли к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в смесь воды со льдом (500 мл) и фильтровали через фильтровальную бумагу на вакуумном фильтре. Фильтрат экстрагировали ЕА. Органическую фазу объединяли с твердой фазой, полученной после вакуумной фильтрации, промывали насыщенным NaHCO3 и насыщенным NaCl, сушили над Na2SO4, выпаривали, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:8) с получением 35: бледно-желтое твердое вещество (11,2 г, 88%). 1Н-ЯМР (400 МГц, CDCl3) δ 9,01 (дд, J=4,2, 1,5 Гц, 1Н), 8,19 (д, J=9,1 Гц, 1Н), 8,04 (д, J=8,6 Гц, 1Н), 7,75 (д, J=9,1 Гц, 1Н), 7,59 (дд, J=8,7, 4,2 Гц, 1Н).
[0717] N-Boc-L-цистеин (3,5 г, 15,8 ммоль) и Cs2CO3 (10,3 г, 31,6 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли ДМФА (40 мл) и проводили реакцию в течение 15 мин при 0°С. Затем раствор Соединения 35 (2,2 г, 10,5 ммоль) в ДМФА (20 мл) медленно добавляли по каплям и проводили реакцию при 0°С в течение 24 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 36: бледно-желтое твердое вещество (4,2 г, колич.). 1Н-ЯМР (400 МГц, CDCl3) δ 8,83-8,67 (м, 1Н), 8,05 (д, J=9,1 Гц, 1Н), 7,88 (д, J=8,5 Гц, 1Н), 7,74 (д, J=9,1 Гц, 1Н), 7,34 (дд, J=8,7, 4,5 Гц, 1Н), 5,74 (д, J=6,8 Гц, 1Н), 4,74 (дд, J=6,3, 3,1 Гц, 1Н), 3,99 (дд, J=15,0, 2,5 Гц, 1Н), 3,60 (дд, J=15,0, 3,6 Гц, 1Н), 1,48 (с, 9Н).
[0718] Соединение 36 (2,0 г, 5,09 ммоль) помещали в реакционную колбу объемом 100 мл и добавляли Fe (1,42 г, 25,4 ммоль) и NH4Cl (0,43 г, 8,14 ммоль). Затем добавляли EtOH (40 мл) и H2O (10 мл) и проводили реакцию при 50°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (80 мл). К раствору добавляли HATU (2,3 г, 6,11 ммоль) и DIEA (1,77 мл, 10,2 ммоль) и проводили реакцию при комнатной температуре в течение 3 0 мин до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью быстрой колоночной хроматографии (ЕА:РЕ=1:3) с получением 37 в виде бледно-желтого твердого вещества (1,2 г, выход в 2 стадиях: 68%).
[0719] Соединение 37 (1,0 г, 2,9 ммоль) помещали в реакционную колбу, а затем добавляли Cs2CO3 (1,1 г, 3,48 ммоль) и ДМФА (60 мл) и проводили реакцию при 0°С в течение 10 мин. Иодметан (4 94 мг, 3,4 8 ммоль) по каплям медленно добавляли к раствору и проводили реакцию при 0°С в течение 3 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:4) с получением Соединения II-14: белое твердое вещество (0,95 г, 91%). 1ЯМР (400 МГц, CDCl3) δ 8, 98 (дд, J=4,2, 1,6 Гц, 1Н), 8,18 (д, J=8,5 Гц, 1Н), 8,05 (д, J=8,7 Гц, 1Н), 7,88 (д, J=8,7 Гц, 1Н), 7,52 (дд, J=8,6, 4,2 Гц, 1Н), 5,59 (д, J=7,8 Гц, 1Н), 4,38 (дт, J=10,6, 7,6 Гц, 1Н), 3,82 (дд, J=11,2, 7,0 Гц, 1Н), 3,39 (с, 3H), 2,91 (дд, J=19,8, 8,7 Гц, 1Н), 1,36 (с, 9Н). 13С-ЯМР (100 МГц, CDCl3 δ 172,66, 154,45, 151,37, 149,42, 141,92, 134,89, 131,82, 130,13, 127,13, 124,21, 122,23, 80,18, 50,78, 39,98, 36,76, 28,26.
[0720] Пример 14: Синтез Соединения II-15
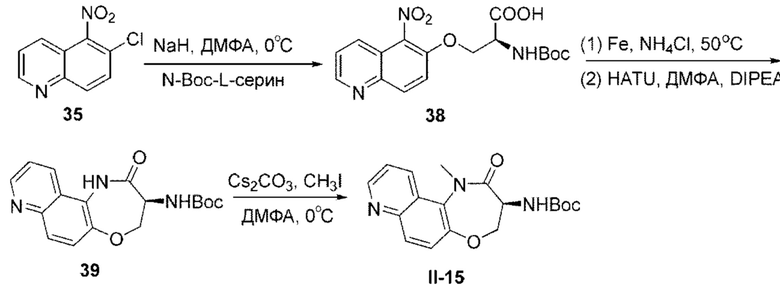
[0721] N-Boc-L-серин (3,25 г, 15,8 ммоль) и NaH (0,76 г, 31,65 ммоль, 60% веса) помещали в реакционную колбу объемом 250 мл и три раза барботировали аргоном. Под атмосферой аргона добавляли ДМФА (50 мл) ghb 0°С и проводили реакцию в течение 30 мин. Затем раствор 35 (2,2 г, 10,55 ммоль) в ДМФА (10 мл) медленно добавляли по каплям и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М НС1, экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 38: бледно-желтое твердое вещество 2,1 г (53%). 1Н-ЯМР (400 МГц, MeOD) δ 8,89 (м, 1Н), 8,26 (д, J=9,1 Гц, 1Н), 8,17 (д, J=8,1 Гц, 1Н), 7,89 (д, J=9,0 Гц, 1Н), 7,69 (м, 1Н), 4,68 (с, 2Н), 4,60 (с, 1Н), 1,46 (с, 9Н).
[0722] Соединение 38 (1,92 г, 5,09 ммоль) помещали в реакционную колбу объемом 100 мл и добавляли Fe (1,42 г, 25,4 ммоль) и NH4Cl (0,43 г, 8,14 ммоль). Затем добавляли EtOH (40 мл) и H2O (10 мл) и проводили реакцию при 50°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (80 мл). В раствор добавляли HATU (2,3 г, 6,11 ммоль) и DIEA (1,77 мл, 10,2 ммоль) и проводили реакцию при комнатной температуре в течение 3 0 мин до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью быстрой колоночной хроматографии (ЕА:РЕ=1:3) с получением 37 виде бледно-желтого твердого вещества (1,1 г, выход в 2 стадиях: 6 6%).
[0723] Соединение 39 (1,0 г, 3,04 ммоль) помещали в реакционную колбу, а затем добавляли Cs2CO3 (1,48 г, 4,56 ммоль) и ДМФА (60 мл) и проводили реакцию при 0°С в течение 10 мин. Иодметан (518 мг, 3,65 ммоль) по каплям медленно добавляли к раствору и проводили реакцию при 0°С в течение 3 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:4) с получением Соединения II-15: белое твердое вещество (0,96 г, 92%). 1Н-ЯМР (400 МГц, CDCl3) δ 8, 90 (дд, J=4,1, 1,4 Гц, 1Н), 8,12 (д, J=8,4 Гц, 1Н), 8,04 (д, J=9,1 Гц, 1Н), 7,51 (д, J=9,1 Гц, 1Н), 7,46 (дд, J=8,6, 4,2 Гц, 1Н), 5,54 (д, J=6,7 Гц, 1Н), 4, 73-4,59 (м, 2Н), 4,31-4,20 (м, 1Н), 3,41 (с, 3H), 1,35 (с, 9Н). 13С-ЯМР (100 МГц, CDCl3) δ 171,59, 154,95, 149,94, 149,15, 146,67, 131,16, 130,89, 129,73, 125,11, 124,08, 121,63, 80,30, 78,72, 49,94, 37,26, 28,21.
[072 4] Пример 15: Синтез Соединения II-16
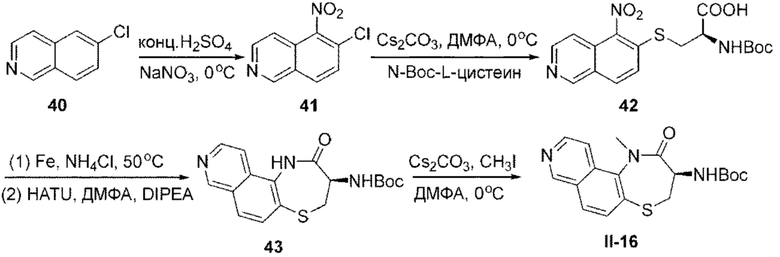
[0725] NaNO3 (5,2 г, 61,1 ммоль) помещали в реакционную колбу объемом 500 мл, а затем по каплям при 0°С добавляли концентрированную серную кислоту (60 мл). 6-Хлоризохинолин 40 (10,0 г, 61,1 ммоль) растворяли в концентрированной серной кислоте (60 мл), по каплям медленно добавляли полученный раствор к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в смесь воды со льдом (500 мл) и фильтровали через фильтровальную бумагу на вакуумном фильтре. Фильтрат экстрагировали ЕА. Органическую фазу объединяли с твердой фазой, полученной после вакуумной фильтрации, промывали насыщенным NaHCO3 и насыщенным NaCl, сушили над Na2SO4, выпаривали, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:8) с получением 41: бледно-желтое твердое вещество (11,2 г, 88%). 1Н-ЯМР (400 МГц, CDCl3) δ 9, 36 (с, 1Н), 8,73 (д, J=6,0 Гц, 1Н), 8,11 (д, J=8,8 Гц, 1Н), 7,70 (д, J=8,8 Гц, 1Н), 7,56 (д, J=6,0 Гц, 1Н).
[0726] N-Boc-L-цистеин (3,5 г, 15,8 ммоль) и Cs2CO3 (10,3 г, 31,6 ммоль) помещали в реакционную колбу объемом 250 мл, добавили с ДМФА (40 мл) и проводили реакцию в течение 15 мин при 0°С. Затем по каплям медленно добавляли раствор Соединения 41 (2,2 г, 10,5 ммоль) в ДМФА (20 мл) и проводили реакцию при 0°С в течение 24 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 42: бледно-желтое твердое вещество (4,2 г, колич.). 1Н-ЯМР (400 МГц, CDCl3) δ 8,52 (с, 1Н), 8,32 (д, J=6,3 Гц, 1Н), 7,94 (д, J=8,8 Гц, 1Н), 7,77 (д, J=8,8 Гц, 1Н), 7,44 (д, J=6,3 Гц, 1Н), 5,69 (д, J=6, 9 Гц, 1Н), 4,68 (м, 1Н), 3,97 (д, J=14,7 Гц, 1Н), 3,55 (дд, J=15,0, 4,4 Гц, 1Н), 1,47 (с, 9Н).
[0727] Соединение 42 (2,0 г, 5,09 ммоль) помещали в реакционную колбу объемом 100 мл и добавляли Fe (1,42 г, 25,4 ммоль) и NH4Cl (0,43 г, 8,14 ммоль). Затем добавляли EtOH (40 мл) и H2O (10 мл) и проводили реакцию при 50°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (80 мл). К раствору добавляли HATU (2,3 г, 6,11 ммоль) и DIEA (1,77 мл, 10,2 ммоль) и проводили реакцию при комнатной температуре в течение 3 0 мин до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА:РЕ=1:3) с получением 43 в виде бледно-желтого твердого вещества (1,2 г, выход в 2 стадиях: 68%).
[0728] Соединение 43 (1,0 г, 2,9 ммоль) помещали в реакционную колбу, затем добавляли Cs2CO3 (1,1 г, 3,48 ммоль) и ДМФА (60 мл) и проводили реакцию при 0°С в течение 10 мин. Иодметан (4 94 мг, 3,4 8 ммоль) по каплям медленно добавляли к раствору и проводили реакцию при 0°С в течение 3 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:4) с получением Соединения II-16: белое твердое вещество (0,95 г, 91%). 1Н-ЯМР (400 МГц, CDCl3) δ 9,31 (с, 1Н), 8,64 (д, J=6,0 Гц, 1Н), 7,91 (д, J=8,4 Гц, 1Н), 7,78 (д, J=8,4 Гц, 1Н), 7,62 (д, J=6,0 Гц, 1Н), 5,63 (д, J=7,7 Гц, 1Н), 4,37 (м, 1Н), 3,82 (дд, J=11,1, 7,0 Гц, 1Н), 3,39 (с, 3H), 2,95 (дд, J=12,5, 9,7 Гц, 1Н), 1,35 (с, 9Н). 13С-ЯМР (100 МГц, CDCl3) δ 172,29, 154,43, 153,10, 144,60, 141,08, 133,02, 131,67, 131,49, 129,73, 128,01, 116,00, 80,25, 50,62, 39,84, 36,41, 28,26.
[0729] Пример 16: Синтез Соединения II-17
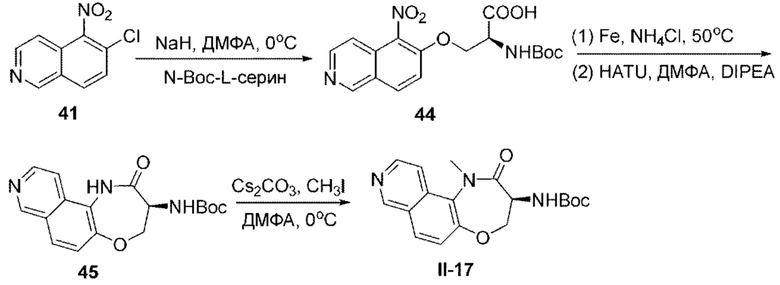
[0730] N-Boc-L-серин (3,25 г, 15,8 ммоль) и NaH (0,76 г, 31,65 ммоль, 60% по весу) помещали в реакционную колбу объемом 250 мл и три раза барботировали аргоном. Под атмосферой аргона добавляли ДМФА (50 мл) при 0°С и проводили реакцию в течение 30 мин. Затем по каплям медленно добавляли раствор 41 (2,2 г, 10,55 ммоль) в ДМФА (10 мл) и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М НС1, затем экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 44: бледно-желтое твердое вещество (2,1 г, 53%).
[0731] Соединение 44 (1,92 г, 5,09 ммоль) помещали в реакционную колбу объемом 100 мл и добавляли Fe (1,42 г, 25,4 ммоль) и NH4Cl (0,43 г, 8,14 ммоль). Затем добавляли EtOH (40 мл) и H2O (10 мл) и проводили реакцию при 50°С в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (80 мл). К раствору добавляли HATU (2,3 г, 6,11 ммоль) и DIEA (1,77 мл, 10,2 ммоль) и проводили реакцию при комнатной температуре в течение 3 0 мин до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью быстрой колоночной хроматографии (ЕА:РЕ=1:3) с получением 45 в виде бледно-желтого твердого вещества (1,1 г, выходв в 2 стадиях: 66%).
[0732] Соединение 45 (1,0 г, 3,04 ммоль) помещали в реакционную колбу, а затем добавляли Cs2CO3 (1,48 г, 4,56 ммоль) и ДМФА (60 мл) и проводили реакцию при 0°С в течение 10 мин. Иодметан (518 мг, 3,65 ммоль) медленно добавляли по каплям к раствору и проводили реакцию в течение 3 ч при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:4) с получением Соединения II-17: белое твердое вещество (0,96 г, 92%). 1Н-ЯМР (400 МГц, CDCl3) δ 9,27 (с, 1Н), 8,60 (д, J=6,0 Гц, 1Н), 7,94 (д, J=8,8 Гц, 1Н), 7,60 (д, J=6, 0 Гц, 1Н), 7,42 (д, J=8,7 Гц, 1Н), 5,53 (д, J=6,2 Гц, 1Н), 4,76-4,60 (м, 2Н), 4, 36-4, 25 (м, 1Н), 3,44 (с, 3H), 1,38 (с, 9Н). 13С-ЯМР (100 МГц, CDCl3) δ 171,24, 154,94, 152,95, 152,31, 144,12, 132,01, 129,26, 129,21, 127,13, 123,44, 115,74, 80,40, 78,75, 49,79, 36,92, 28,23.
[0733] Пример 17: Синтез Соединения II-18
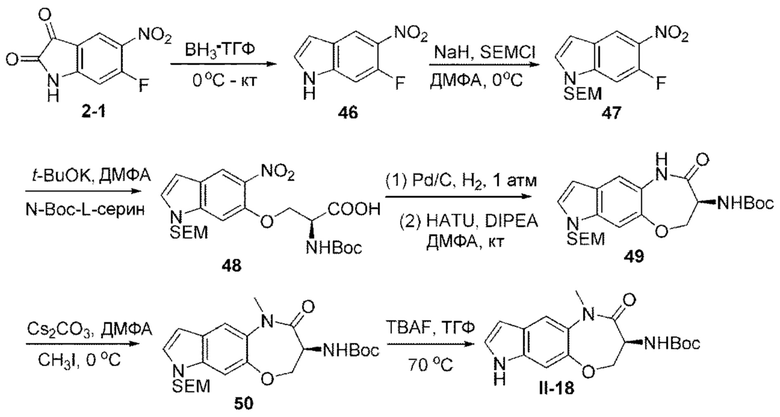
[0734] Соединение 2-1 (9,48 г, 45,12 ммоль) растворяли в ТГФ (90 мл) и добавляли ВН3 (135,6 мл, 1 M в ТГФ) при 0°С под атмосферой аргона. Реакционный раствор нагревали до комнатной температуры, и проводили реакцию в течение 2 ч до полного завершения реакции, как было показано ТСХ. Добавляли 1 М HCl, чтобы остановить реакцию, после чего реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, а остаток разделяли с помощью колоночной хроматографии (ЕА/РЕ=1:3) с получением Соединения 46 (6,0 г, выход 74%).
[0735] Соединение 46 (6,0 г, 33,3 ммоль) и NaH (1,68 г, 41,64 ммоль) смешивали, растворяли в ДМФА (120 мл) при 0°С и поддерживали эту температуру в ходе реакции в течение 30 мин. Затем добавляли SEMC1 (8,82 мл, 49,98 ммоль) и проводили реакцию в течение ночи до полного завершения реакции, как было показано ТСХ. Добавляли 1 М HCl для остановки реакции, затем реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и разделяли остаток с помощью колоночной хроматографии (ЕА/РЕ=1:8) с получением Соединения 47 (8,22 г, выход 80%). 1H-ЯМР (400 МГц, CDCl3) δ 8, 46 (д, J=7,2 Гц, 1Н), 7, 48-7, 20 (м, 2Н), 6,71 (дд, J=3,4, 0,7 Гц, 1Н), 5,50 (с, 2Н), 3,52 (дд, J=8,6, 7,7 Гц, 2Н), 0, 97-0, 92 (м, 2Н), -0,00 (с, 9Н). 13С-ЯМР (100 МГц, CDCl3) δ 155,46, 152,91, 140,01, 139,90, 132,89, 132,86, 125,77, 121,15, 121,14, 105,86, 100,31, 100,05, 77,66, 67,93, 19,17, 0,00.
[0736] N-Boc-L-серин (4,96 г, 24,15 ммоль) и t-BuOK (7,23 г, 64,5 ммоль) помещали в реакционную колбу объемом 250 мл и три раза барботировали азотом. Под атмосферой аргона при 0°С добавляли ДМФА (50 мл) и проводили реакцию в течение 30 мин. Затем по каплям медленно добавляли раствор 47 (5,0 г, 16,1 ммоль) в ДМФА (30 мл) и проводили реакцию в течение ночи при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, затем экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 48: бледно-желтое твердое вещество (1, 67 г, 21%).
[0737] Соединение 48 (1,67 г) растворяли в метаноле (40 мл), а затем добавляли Pd/C (167 мг). Реакцию продолжали в течение 3 ч при комнатной температуре под содержащей водород атмосферой до полного завершения реакции, как было показано ТСХ. Pd/C удаляли путем фильтрации через диатомит и удаляли растворитель путем перегонки при пониженном давлении. Полученный неочищенный продукт растворяли в ДМФА (40 мл), а затем добавляли DIPEA и HATU и проводили реакцию при комнатной температуре в течение 1 ч до полного завершения реакции, как было показано ТСХ. Затем добавляли воду и экстрагировали систему этилацетатом, выпаривали, очищали с помощью колоночной флеш-хроматографии (ЕА/РЕ=1:3) с получением Соединения 49 (1,0 г, выход в двух стадиях: 66%).
[0738] Соединение 49 (1,0 г, 2,23 ммоль) помещали в реакционную колбу и затем добавляли Cs2CO3 (1,09 г, 3,36 ммоль) и ДМФА (20 мл) и проводили реакцию при 0°С в течение 10 мин. К раствору по каплям медленно добавляли иодметан (380 мг, 2,68 ммоль) и проводили реакцию при 0°С в течение 3 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали ЕА, промывали деионизированной водой и насыщенным NaCl и сушили над Na2SO4. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА:РЕ=1:8) с получением Соединения 50: белое твердое вещество (0,96 г, 93%). 1Н-ЯМР (400 МГц, CDCl3) δ 7,44 (с, 1Н), 7,29 (с, 1Н), 7,21 (д, J=3,2 Гц, 1Н), 6,50 (д, J=3,1 Гц, 1Н), 5,57 (д, J=6,8 Гц, 1Н), 5,50-5,39 (м, 2Н), 4,70 (дт, J=11,0, 7,3 Гц, 1Н), 4,59 (дд, J=9,5, 7,5 Гц, 1Н), 4,15 (дд, J=10,9, 9,8 Гц, 1Н), 3,54-3, 47 (м, 5Н), 1,41 (с, 9Н), 1,00-0,91 (м, 2Н), 0,00 (с, 9Н). 13С-ЯМР (100 Гц, CDCl3) δ 171,03, 156,49, 147,69, 136,09, 131,71, 130,81, 127,63, 116,59, 105,00, 103,74, 81,39, 79,21, 77,27, 67,38, 51,47, 37,56, 29,65, 19,06, 0,00.
[0739] Под атмосферой аргона Соединение 50 (0,9 г, 1,95 ммоль) растворяли в безводном ТГФ (15 мл), а затем добавляли раствор TBAF (13,65 мл, 1 M в ТГФ) и проводили реакцию при 70°С в течение 4 ч. После завершения реакции удаляли ТГФ и добавляли воду. Реакционный раствор 3 раза экстрагировали этилацетатом. Органические фазы объединяли, сушили над безводным сульфатом натрия, выпаривали, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА/РЕ=1:3) с получением Соединения II-18 (210 мг, выход 33%). МС-ЭРИ m/z 330,1 (М-Н)-.
[0740] Пример 18: Синтез Соединения II-23
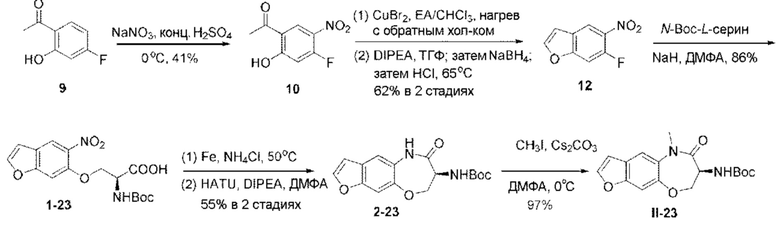
[0741] NaNO3 (5,1 г, 60 ммоль) помещали в реакционную колбу объемом 500 мл, и затем по каплям при 0°С добавляли концентрированную серную кислоту (60 мл). 4-Фтор-2-гидроксиацетофенон 9 (9,25 г, 60 ммоль) растворяли в концентрированной серной кислоте (60 мл), и затем полученный раствор по каплям медленно добавляли к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 2,5 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в смесь воды со льдом (500 мл) и фильтровали через фильтровальную бумагу на вакуумном фильтре. Фильтрат экстрагировали этилацетатом. Органическую фазу смешивали с твердой фазой, полученной после вакуумной фильтрации, последовательно промывали насыщенным бикарбонатом натрия и насыщенным солевым раствором, сушили над безводным сульфатом натрия, выпаривали, а остаток разделяли с помощью колоночной хроматографии (ЕА/РЕ=1:20) с получением 10: бледно-желтое твердое вещество (4,9 г, 41%). Соединение 10: 1Н-ЯМР (400 МГц, CDCl3) δ 13,02 (с, 1Н), 8,65 (д, J=8,3 Гц, 1Н), 6,83 (д, J=12,2 Гц, 1Н), 2,72 (с, 3H); 13С-ЯМР (100 МГц, CDCl3) δ 203,1, 168,4, 168,3, 161,8, 159,1, 130,5, 115,9, 115,9, 107,6, 107,4, 26,8; МС-ЭРИ: m/z 200,0 (М+Н)+.
[0742] CuBr2 (1,9 г, 8,5 ммоль) помещали в реакционную колбу объемом 250 мл, а затем добавляли этилацетат (50 мл) и нагревали с обратным холодильником. В реакционный раствор добавляли раствор 10 (1,0 г, 5 ммоль) в хлороформе (50 мл) и проводили реакцию при нагревании с обратным холодильником в течение 24 ч. Зеленый цвет реакционной жидкости исчезал, и при этом образовывалось твердое вещество цвета извести. После превращения большей части 10, как показала ТСХ, реакционный раствор фильтровали через диатомит на вакуумном фильтре. Растворитель удаляли при пониженном давлении и растворяли полученный неочищенный продукт в ТГФ (180 мл). Медленно добавляли DIPEA (3,0 мл, 18 ммоль) и проводили реакцию при комнатной температуре в течение 4 5 мин до полного завершения реакции, как было показано ТСХ. К системе добавляли NaBH4 и проводили реакцию при комнатной температуре в течение 2 ч. После завершения реакции реакцию останавливали путем медленного добавления метанола, и затем добавляли 4Н HCl и проводили реакцию в течение ночи при 65°С. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Разделение с помощью колоночной хроматографии (ЕА/РЕ=1:10) давало 12: желтое твердое вещество (0,56 г, выход в двух стадиях 62%). Соединение 12: 1Н-ЯМР (400 МГц, CDCl3) δ 8,37 (д, J=7,3 Гц, 1Н), 7,78 (д, J=2,3 Гц, 1Н), 7,42 (д, J=10,6 Гц, 1Н), 6,91 (дд, J=2,2, 0,7 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 156,8, 156,7, 155,2, 152,6, 148,5, 148,4, 123,5, 123,5, 119,1, 119,1, 107,2, 107,2, 101,6, 101,3; МС-ЭРИ: m/z 182,0 (М+Н)+.
[0743] N-Boc-L-серин (453 мг, 2,2 ммоль) и NaH (105,6 мг, 4,4 ммоль) помещали в реакционную колбу объемом 50 мл, добавляли ДМФА (8 мл) при 0°С и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли раствор 12 (200 мг, 1,1 ммоль) в ДМФА (2 мл) и проводили реакцию в течение 4,5 ч при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 1-23:350 мг, выход 86%.
[0744] Соединение 1-23 (800 мг, 2,18 ммоль) помещали в реакционную колбу объемом 100 мл и добавляли порошок Fe (610 мг, 10,9 ммоль) и NH4Cl (233 мг, 4,36 ммоль). Затем добавляли EtOH (24 мл) и H2O (6 мл) и проводили реакцию при 50°С в течение 4 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (30 мл). К раствору добавляли HATU (995 мг, 2,62 ммоль) и DIPEA (1,52 мл, 8,72 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА:РЕ=1:3) с получением Соединения 2-23 (380 мг, выход в 2 стадиях: 55%).
[0745] Соединение 2-23 (380 мг, 1,2 ммоль) растворяли в ДМФА (10 мл) и добавляли Cs2CO3 (584 мг, 1,8 ммоль). Иодметан (203 мг, 1,43 ммоль) по каплям медленно добавляли к раствору и проводили реакцию при комнатной температуре в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА/РЕ=1:4) с получением II-23: белое твердое вещество, 385 мг, выход 97%. 1H-ЯМР (400 МГц, CDCl3) δ 7,66 (д, J=2,2 Гц, 1Н), 7,41 (с, 1Н), 7,31 (с, 1Н), 6,74 (д, J=1,4 Гц, 1Н), 5,51 (д, J=7,0 Гц, 1Н), 4,65 (дт, J=11,0, 7,3 Гц, 1Н), 4,57 (дд, J=9,5, 7,4 Гц, 1Н), 4,15 (дд, J=10,9, 9,7 Гц, 1Н), 3,46 (с, 3H), 1,39 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 169, 5, 155, 1, 152, 9, 147, 7, 146, 6, 132, 7, 124,7, 115,2, 106,4, 105,7, 80,2, 77,9, 50,0, 36,1, 28,2; МС-ЭРИ: m/z 333, 0 (М+Н)+.
[074 6] Пример 19: Синтез Соединения II-24
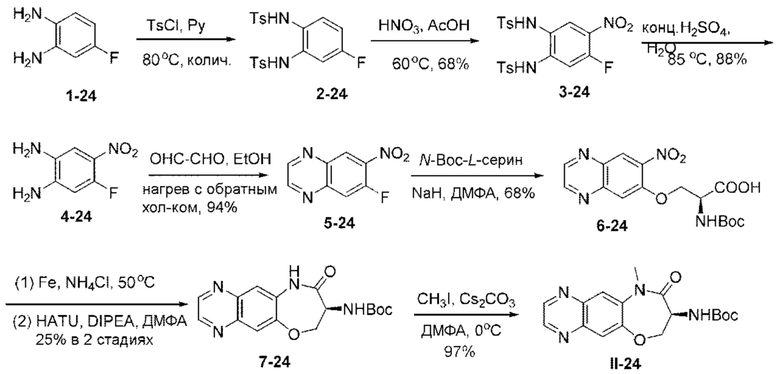
[0747] Соединение 1-24 (5,04 г, 40 ммоль) растворяли в пиридине (10 мл), а затем по каплям медленно добавляли TsCl (15,25 г, 80 ммоль), растворенный в пиридине (25 мл), нагревали до 80°С и проводили реакцию в течение ночи до полного завершения реакции, как было показано ТСХ. Реакционный раствор охлаждали до комнатной температуры и добавляли 3Н соляную кислоту (150 мл) в ледяной бане. Образовывалось большое количество осадка, который перемешивали в течение 0,5 ч и затем фильтровали. Осадок на фильтре представлял собой коричневатое твердое вещество. Получали продукт 2-24 (17,4 г, выход: количественный).
[0748] Соединение 2-24 (20 г, 46,08 ммоль) растворяли в уксусной кислоте (80 мл) и добавляли дымящую азотную кислоту (4,8 мл), нагревали до 60°С и проводили реакцию в течение 2 ч. После завершения реакции реакционный раствор фильтровали, а затем промывали этанолом (40 мл). Получали Соединение 3-24 в виде белого твердого вещества (15 г, выход 68%).
[0749] Соединение 3-24 (13,4 г, 28 ммоль) добавляли к смешанной системе концентрированной серной кислоты (30 мл) и воды (3 мл), нагревали до 85°С и проводили реакцию в течение 1 ч. После охлаждения систему медленно вливали в воду со льдом (300 мл), при этом образовывалось твердое вещество. Твердое вещество растворяли при медленном нагревании, доводили до рН 9 водным раствором аммиака и фильтровали. Осадок на фильтре промывали водой и в результате получали Соединение 4-24 в виде твердого вещества (4,2 г, выход 88%).
[0750] Соединение 4-24 (4,2 г, 24,5 ммоль) растворяли в этаноле (120 мл) и добавляли оксальдегид (40% в воде, 5,67 мл).
Систему нагревали до 90°С и проводили реакцию в течение 1 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор перегоняли при пониженном давлении для удаления этанола, экстрагировали этилацетатом, сушили над безводным сульфатом натрия, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА/РЕ=1:2) с получением Соединения 5-24 в виде белого твердого вещества (4,46 г, выход 94%). 1Н-ЯМР (400 МГц, CDCl3) δ 9,02-8,97 (м, 2Н), 8,86 (д, J=7,5 Гц, 1Н), 7,99 (д, J=10,8 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 155,5, 152,9, 148,4, 146,7, 146,6, 145,3, 145,2, 138,71, 138,69, 128,4, 116,9, 116,7; МС-ЭРИ: m/z 194,0 (М+Н)+.
[0751] N-Boc-L-серин (3,18 г, 15,54 ммоль) и NaH (0,93 г, 23,31 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли ДМФА (40 мл) при 0°С и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли раствор Соединения 5-24 (1,5 г, 7,7 7 ммоль) в ДМФА (20 мл) и проводили реакцию в течение 3 ч при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН=20:1) с получением 6-24 (2,0 г, выход 68%).
[0752] Соединение 6-24 (2,43 г, 6,43 ммоль) помещали в реакционную колбу объемом 250 мл и добавляли порошок Fe (1,79 г, 32,14 ммоль) и NH4Cl (0,69 г, 12,86 ммоль). Затем добавляли EtOH (80 мл) и H2O (20 мл) и проводили реакцию при 50°С в течение 4 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор фильтровали через диатомит. Растворитель удаляли при пониженном давлении, а остаток повторно растворяли в ДМФА (30 мл). К раствору добавляли HATU (2,93 г, 7,72 ммоль) и DIPEA (3,32 г, 25,75 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА:РЕ=1:3) с получением Соединения 7-24 (540 мг, выход в 2 стадиях: 2 5%).
[0753] Соединение 7-24 (340 мг, 1,03 ммоль) растворяли в ДМФА (10 мл) и добавляли Cs2CO3 (503 мг, 1,55 ммоль). К раствору по каплям медленно добавляли иодметан (175 мг, 1,2 4 ммоль) и проводили реакцию при комнатной температуре в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА/РЕ=1:4) с получением 11-24: белое твердое вещество, 345 мг, выход 97%. 1H-ЯМР (400 МГц, CDCl3) δ 8,84 (д, J=1,8 Гц, 1Н), 8,82 (д, J=1,8 Гц, 1Н), 7,92 (с, 1Н), 7,85 (с, 1Н), 4,73 (дт, J=11,3, 7,2 Гц, 1Н), 4,65 (дд, J=9,5, 7,2 Гц, 1Н), 4,26 (дд, J=11,2, 9,7 Гц, 1Н), 3,58 (с, 3H); 13С-ЯМР (100 МГц, CDCl3) δ 169,3, 155,0, 151,5, 145,3, 145,1, 141,9, 140,9, 140,2, 122,5, 121,2, 80,5, 50,1, 36,1, 28,2; МС-ЭРИ: m/z 345,0 (М+Н)+.
[07 54] Пример 20: Синтез Соединения II-25
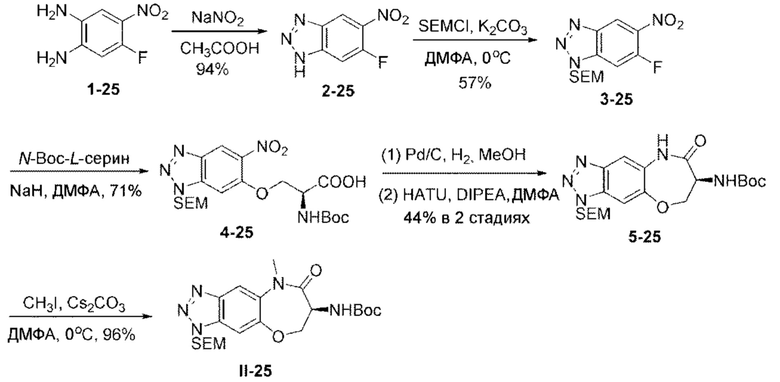
[0755] Промежуточное Соединение 1-25 (4,4 г, 25,71 ммоль) растворяли в уксусной кислоте (100 мл), а затем при 5°С добавляли нитрит натрия (3,85 г, 55,79 ммоль). Температуру поддерживали в ходе реакции в течение 10 мин, при этом превращение прошло полностью. Реакционный раствор выпаривали на роторном испарителе для удаления уксусной кислоты, экстрагировали этилацетатом и выпаривали с получением Соединения 2-25 в виде твердого вещества (4,37 г, выход 94%).
[0756] Соединение 2-25 (4,0 г, 21,98 ммоль) растворяли в уксусной кислоте (80 мл), а затем при 0°С добавляли K2CO3 (6.07 г, 44 ммоль) и SEMCl (5,5 г, 33 ммоль). Реакцию поддерживали при 0°С в течение 2 ч, при этом превращение прошло полностью. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия, выпаривали и очищали с помощью колоночной хроматографии (ЕА/РЕ=1:6) с получением Соединения 3-25 (3,9 г, выход 57%).
[0757] N-Boc-L-серин (5,11 г, 25 ммоль) и NaH (1,5 г, 37,5 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли ДМФА (60 мл) при 0°С и проводили реакцию в течение 15 мин. Затем раствор Соединения 3-25 (3,9 г, 12,5 ммоль) в ДМФА (20 мл) медленно добавляли по каплям и проводили реакцию в течение 2 ч при 0°С до полного завершения реакции, как было показано ТСХ. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН = 20:1) с получением Соединения 4-25 в виде желтого твердого порошка (4,4 г, выход 71%).
[0758] Соединение 4-25 (4,3 г, 8,65 ммоль) растворяли в метаноле (80 мл), и затем добавляли 10% Pd/C (2,15 г). Под атмосферой водорода реакцию продолжали в течение 4 ч при нормальной температуре под нормальным давлением до полного превращения неочищенного продукта. Реакционный раствор фильтровали через диатомит для удаления Pd/C и выпаривали для удаления метанола. Полученный неочищенный продукт растворяли в ДМФА (30 мл), а затем добавляли DIPEA (2,24 г, 17,3 ммоль) и HATU (3,95 г, 10,38 ммоль) и проводили реакцию в течение 1 ч с перемешиванием при комнатной температуре, пока реакция не была завершена. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА/РЕ=1:3) с получением Соединения 5-25 (1/7 г, выход в 2 стадиях: 44%).
[0759] Соединение 5-25 (1/7 г, 3,79 ммоль) растворяли в ДМФА (40 мл) и добавляли Cs2CO3 (1/85 г/ 5/68 ммоль). К раствору по каплям медленно добавляли иодметан (0/59 г/ 4/17 ммоль) и проводили реакцию при комнатной температуре в течение 2 ч до полного завершения реакции/ как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом/ промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении и разделяли с помощью быстрой колоночной хроматографии (ЕА/РЕ=1:4) с получением 11-25: белое твердое вещество 1,69 г, выход 96%. 1H-ЯМР (400 МГц, CDCl3) δ 7,93 (с, 1Н), 7,49 (с, 1Н), 5,98 (с, 2Н), 5,60 (д, J=7,0 Гц, 1Н), 4,69 (дт, J=11,2, 7,2 Гц, 1Н), 4,60 (ддд, J=11,2, 7,4, 3,8 Гц, 1Н), 4,22 (дд, J=11,1, 9,7 Гц, 1Н), 3,66-3,57 (м, 2Н), 3,54 (с, 3Н), 1,41 (с, 9Н), 1,02-0,94 (м, 2Н), 0,00 (с, 9Н); 13С-ЯМР (100 МГц, CDCl3) δ 170,6, 156,5, 152,2, 144,8, 136,6, 132,7, 115,5, 104,8, 81,8, 68,8, 51,3, 37,9, 29,7, 19,1, 0,0; МС-ЭРИ: m/z 464,1 (M+H)+.
[0760] Пример 21: Синтез Соединения 11-19
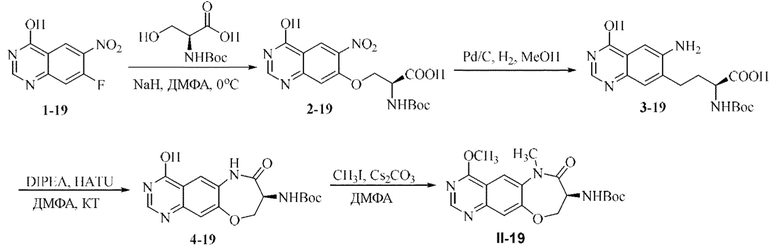
[0761] N-Boc-L-Серин (9,80 г, 47,80 ммоль) и NaH (3,80 г, 95,60 ммоль) добавляли в реакционную колбу объемом 500 мл, затем добавляли ДМФА (120 мл) и проводили реакцию при 0°С в течение 30 мин. 1-19 (5,00 г, 23,9 ммоль) растворяли в ДМФА (100 мл), затем по каплям медленно добавляли к реакционному раствору и проводили реакцию при 0°С в течение 3,5 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали досуха на роторном испарителе, а остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: дихлорметан:метанол = 10:1) с получением 2-19 (4,99 г, выход 53%). МС-ЭРИ m/z 393,0 (М-Н)-.
[0762] 2-19 (900 мг, 2,28 ммоль) и Pd/C (900 мг) добавляли в реакционную колбу объемом 100 мл, а затем добавляли метанол (20 мл) до полного растворения. Реакцию продолжали в течение 5 ч при комнатной температуре под атмосферой водорода. После окончания реакции реакционный раствор фильтровали через диатомит для удаления Pd/C и выпаривали досуха на роторном испарителе для удаления растворителя с получением неочищенного 3-19. МС-ЭРИ m/z 363,1 (М-Н)-.
[0763] Неочищенное 3-19, HATU (1,04 г, 2,74 ммоль) и DIPEA (755 мкл, 4,57 ммоль) добавляли в реакционную колбу объемом 100 мл, а затем добавляли ДМФА (20 мл) для их растворения. Реакцию продолжали в течение ночи при 75°С. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха и разделяли с помощью колоночной хроматографии на силикагеле (элюент: дихлорметан:метанол = 10:1) с получением 4-19 (155 мг, выход 19,6%). МС-ЭРИ m/z 347,0 (М+Н)+.
[0764] 4-19 (400 мг, 1,16 ммоль) и карбонат цезия (791 мг, 2,43 ммоль) добавляли в реакционную колбу объемом 100 мл, а затем добавляли ДМФА (15 мл). После реакции при 0°С в течение 10 мин, по каплям медленно добавляли иодметан (152 мкл, 2,43 ммоль) и проводили реакцию при 0°С в течение 1 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха и разделяли с помощью колоночной хроматографии на силикагеле (элюент: дихлорметан:метанол = 40:1) с получением конечного продукта 11-19 (275 мг, выход 64%). МС-ЭРИ m/z 375,1 (М+Н)+.
[0765] Пример 22: Синтез Соединения 11-26
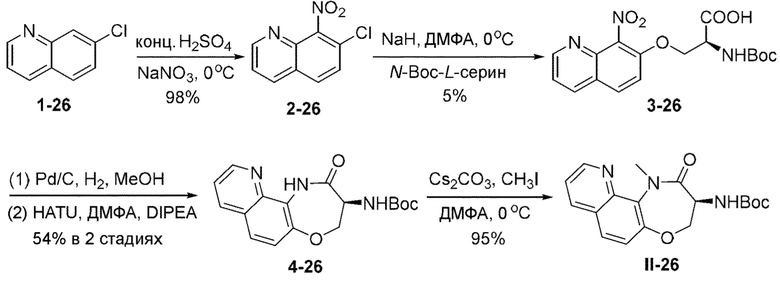
[0766] NaNO3 (2,73 г, 32,1 ммоль) помещали в реакционную колбу объемом 100 мл, а затем по каплям при 0°С добавляли концентрированную серную кислоту (15 мл). Соединение 1-26 (5,0 г, 30,6 ммоль) растворяли в концентрированной серной кислоте (15 мл), и затем полученный раствор по каплям медленно добавляли к раствору NaNO3 в концентрированной серной кислоте и проводили реакцию при 0°С в течение 3 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор вливали в воду со льдом (150 мл), при этом образовывалось большое количество белого осадка. Реакционный раствор фильтровали через фильтровальную бумагу и 3 раза промывали осадок на фильтре водой со льдом и сушили с получением Соединения 2-36 в виде белого твердого порошка (6,25 г, выход 98%). Соединение 2-26: 1H-ЯМР (400 МГц, CDCl3) δ 9,01 (дд, J=4,3, 1,6 Гц, 1Н), 8,25 (дд, J=8,4, 1,6 Гц, 1Н), 7,92 (д, J=8,9 Гц, 1Н), 7,61 (д, J=8,9 Гц, 1Н), 7,56 (дд, J=8,4, 4,3 Гц, 1Н); 13С-ЯМР (100 МГц, CDCl3) δ 153,1, 140,2, 135,9, 130,2, 127,4, 127,2, 125,8, 123,0; МС-ЭРИ: m/z 209,0 (M+H)+.
[0767] N-Boc-L-серин (5,9 г, 28,8 ммоль) и NaH (1,73 г, 43,1 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли ДМФА (40 мл) при 0°С и проводили реакцию в течение 15 мин. Затем раствор Соединения 2-26 (3,0 г, 14,4 ммоль) в ДМФА (30 мл) медленно добавляли по каплям и проводили реакцию в течение ночи при 0°С. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН = 20:1) с получением 3-26 в виде желтого твердого порошка: 0,27 г, выход 5%.
[0768] Соединение 3-26 (200 мг, 0,53 ммоль) растворяли в метаноле (2 мл), и затем добавляли 10% Pd/C (100 мг). Под атмосферой водорода реакцию продолжали в течение 2 ч при нормальной температуре под нормальным давлением до полного превращения неочищенного продукта. Реакционный раствор фильтровали через диатомит для удаления Pd/C и выпаривали для удаления метанола. Полученный неочищенный продукт растворяли в ДМФА (3 мл), затем добавляли DIPEA (274,2 мг, 2,12 ммоль) и HATU (3,95 г, 0,64 ммоль) и проводили реакцию в течение 1 ч с перемешиванием при комнатной температуре, пока реакция не была завершена. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА/РЕ=1:3) с получением Соединения 4-26 (95 мг, выход в 2 стадиях: 54%). МС-ЭРИ: m/z 330,0 (М+Н)+.
[0769] Соединение 4-26 (40 мг, 0,12 ммоль) растворяли в ДМФА (5 мл) и добавляли Cs2CO3 (76 мг, 0,23 ммоль). Иодметан (24,8 мг, 0,18 ммоль) медленно добавляли по каплям к раствору и проводили реакцию при комнатной температуре в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении и разделяли с помощью колоночной флеш-хроматографии (ЕА/РЕ=1:4) с получением 11-26: белое твердое вещество, 40 мг, выход 95%. МС-ЭРИ: m/z 344,0 (М+Н)+.
[0770] Пример 23: Синтез Соединения 11-27
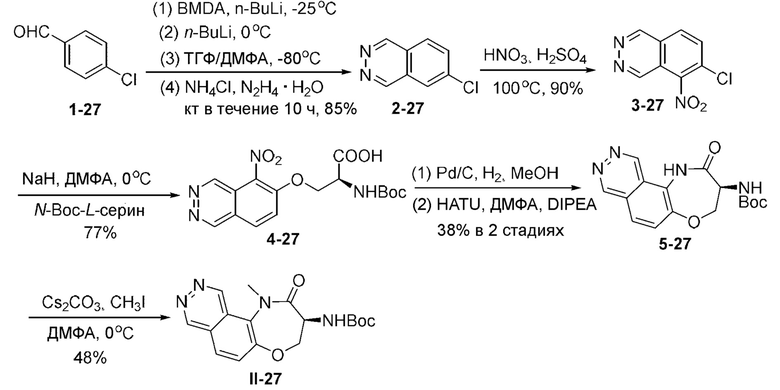
[0771] BMDA (5,27 г, 39,6 ммоль) растворяли в смеси растворителей ТГФ (15 мл) и н-гексана (60 мл) и затем добавляли н-BuLi (24 мл, 1 М в гексане) при -25°С. Температуру поддерживали в ходе реакции в течение 30 мин. Добавляли Соединение 1-27 (5,06 г, 36,0 ммоль) и проводили реакцию при -25°С в течение 30 мин, добавляли н-BuLi (33,6 мл, 1 М в гексане) и проводили реакцию при 0°С в течение 2 ч. Затем систему охлаждали до -80°С, и затем добавляли ДМФА (8,4 мл, 118,8 ммоль) и проводили реакцию при -80°С в течение 10 мин, а затем при 0°С в течение 2 ч. Добавляли NH4Cl (5,76 г, 118,8 ммоль) и N2H4⋅H2O (4,2 мл, 68,36 ммоль) и проводили реакцию в течение ночи при комнатной температуре до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ЕА/РЕ=2:1) с получением Соединения 2-27 (5,0 г, выход 85%).
[0772] Соединение 2-27 (2 г, 12,15 ммоль) растворяли в концентрированной серной кислоте (40 мл), и затем добавляли дымящую азотную кислоту (3,83 г, 60,75 ммоль), нагревали до 90°С и проводили реакцию в течение 2 ч до полного превращения неочищенного продукта. Реакционный раствор охлаждали до комнатной температуры, вливали в воду со льдом (150 мл) и доводили до нейтрального рН водным раствором аммиака. Реакционный раствор экстрагировали этилацетатом, выпаривали, а остаток разделяли с помощью колоночной флеш-хроматографии (ЕА/РЕ=2:1) с получением Соединения 3-27 (2,28 г). 1H-ЯМР (400 МГц, CDCl3) δ 9,66 (д, J=1,3 Гц, 1Н), 9,55 (д, J=1,3 Гц, 1Н), 8,15 (д, J=8,7 Гц, 1Н), 8,05 (д, J=8,7 Гц, 1Н); МС-ЭРИ: m/z 209,0 (М+Н)+.
[0773] N-Boc-L-серин (2,94 г, 14,35 ммоль) и NaH (1,15 г, 28,71 ммоль) помещали в реакционную колбу объемом 250 мл, добавляли ДМФА (30 мл) при 0°С и проводили реакцию в течение 15 мин. Затем по каплям медленно добавляли раствор Соединения 3-27 (2,0 г, 9,57 ммоль) в ДМФА (20 мл) и проводили реакцию в течение 5 ч при 0°С. Реакционный раствор подкисляли 0,2 М HCl, экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ:МеОН = 10:1) с получением Соединения 4-27 в виде желтого твердого порошка (2,8 г, выход 77%).
[0774] Соединение 4-27 (1,1 г, 3,18 ммоль) растворяли в метаноле (20 мл), и затем добавляли 10% Pd/C (1,1 г). Под атмосферой водорода реакцию продолжали в течение 2 ч при нормальной температуре под нормальным давлением до полного превращения неочищенного продукта. Реакционный раствор фильтровали через диатомит для удаления Pd/C и выпаривали для удаления метанола. Полученный неочищенный продукт растворяли в ДМФА (20 мл), и затем добавляли DIPEA (1,23 г, 9,52 ммоль) и HATU (1,45 г, 3,82 ммоль) и проводили реакцию в течение 1 ч с перемешиванием при комнатной температуре, пока реакция не была завершена. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной хроматографии (ДХМ/МеОН = 20:1) с получением Соединения 5-27 (390 мг, выход в 2 стадиях: 38%). МС-ЭРИ: m/z 331,0 (М+Н)+.
[0775] Соединение 5-27 (240 мг, 0,73 ммоль) растворяли в ДМФА (8 мл) и добавляли Cs2CO3 (355 мг, 1,09 ммоль). Иодметан (123 мг, 0,87 ммоль) медленно добавляли по каплям к раствору и проводили реакцию при комнатной температуре в течение 2 ч до полного завершения реакции, как было показано ТСХ. Реакционный раствор экстрагировали этилацетатом, промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, а остаток разделяли с помощью колоночной флеш-хроматографии (ДХМ/МеОН = 1:20) с получением 11-27: белое твердое вещество, 120 мг, выход 48%. МС-ЭРИ: m/z 345,0 (М+Н)+.
[0776] Пример 24: Синтез Соединения 11-21
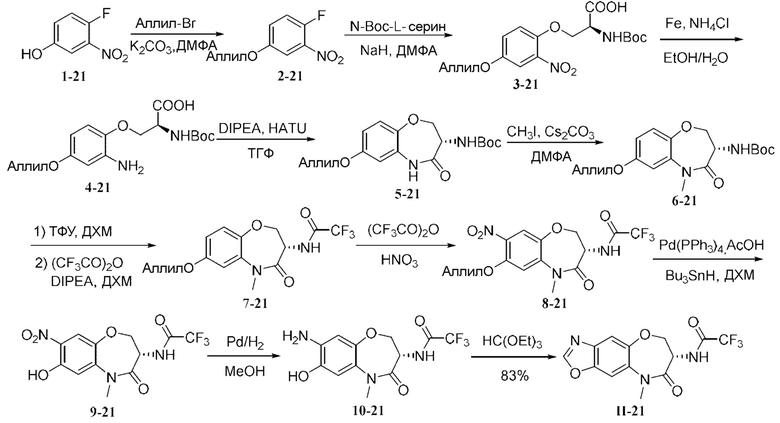
[0777] 1-21 (10 г, 63,65 ммоль) и карбонат калия (26,39 г, 190,96 ммоль) добавляли в реакционную колбу объемом 500 мл, а затем добавляли ДМФА (300 мл). Аллилбромид (17 мл, 190,96 ммоль) добавляли по каплям и проводили реакцию при комнатной температуре в течение 3 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха, а остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 5:1) с получением 2-21 (12,41 г, выход 99%). МС-ЭРИ m/z 198,0 (М+Н)+.
[0778] N-Boc-L-Серин (7,80 г, 38,06 ммоль) и NaH (3,6 г, 88,81 ммоль) добавляли в реакционную колбу объемом 250 мл, и затем добавляли ДМФА (100 мл) в качестве растворителя. Реакцию продолжали при 0°С в течение 30 мин. 2-21 (5,00 г, 25,37 ммоль) растворяли в ДМФА (50 мл), затем по каплям медленно добавляли в реакционный раствор и проводили реакцию при 0°С в течение 1 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха с получением неочищенного 3-21 (4,99 г, выход 53%). МС-ЭРИ m/z 381,1 (М-Н)-.
[0779] Весь неочищенный продукт 3-21, восстановленный порошок железа (7,1 г, 126,87 ммоль) и хлорид аммония (2,2 г, 40,6 ммоль) добавляли в реакционную колбу объемом 250 мл, и затем добавляли этанол/воду (120 мл/30 мл). Реакцию проводили при нагревании с обратным холодильником при 70°С в течение 1 ч. После окончания реакции реакционный раствор фильтровали через диатомит для удаления порошка железа и выпаривали фильтрат на роторном испарителе досуха с получением неочищенного 4-21. МС-ЭРИ m/z 351,1 (М+Н)+.
[0780] Весь неочищенный 4-21, HATU (11,6 г, 30,44 ммоль) и DIPEA (17 мл, 101,48 ммоль) добавляли в реакционную колбу объемом 250 мл, а затем ТГФ (200 мл) добавляли в качестве растворителя. Реакцию продолжали при комнатной температуре в течение 1 ч. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления ТГФ, промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха, а остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 8:1) с получением 5-21 (4,00 г, выход 23,6%). МС-ЭРИ m/z 333,1 (М-Н)-.
[0781] 5-21 (2,85 г, 8,50 ммоль) и карбонат цезия (4,14 г, 12,7 ммоль) добавляли в реакционную колбу объемом 250 мл, и затем добавляли ДМФА (85 мл). Реакцию проводили при 0°С в течение 30 мин, и затем по каплям медленно добавляли иодметан (635 мкл, 10,2 ммоль) и проводили реакцию при 0°С в течение 1 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали на роторном испарителе досуха. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 10:1) с получением Соединения 6-21 (2,90 г, выход 98%). МС-ЭРИ m/z 347,2 (М-Н)-.
[0782] 6-21 (2,90 г, 8,30 ммоль) добавляли в реакционную колбу объемом 250 мл, и затем добавляли дихлорметан (64 мл) и ТФУ (16 мл). Реакцию продолжали при комнатной температуре в течение 1 ч. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления растворителя, добавляли воду (100 мл), доводили до рН 8-9 насыщенным бикарбонатом натрия и экстрагировали этилацетатом. Органическую фазу выпаривали досуха на роторном испарителе, добавляли трифторуксусный ангидрид (1,70 мл, 11,6 ммоль) и DIPEA (2,1 мл, 12,4 ммоль) и в качестве растворителя добавляли ДХМ (85 мл). Реакцию продолжали в течение ночи при комнатной температуре. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления растворителя, промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали досуха на роторном испарителе. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 10:1) с получением 7-21 (2,65 г, выход 92,7%). МС-ЭРИ m/z 345,0 (М+Н)+.
[0783] 7-21 (2,65 г, 7,70 ммоль) и трифторуксусный ангидрид (80 мл) добавляли в реакционную колбу объемом 250 мл и охлаждали до -30°С. Концентрированную азотную кислоту (560 мкл, 8,4 ммоль) медленно добавляли по каплям с последующей реакцией в течение 1 ч при температуре, регулируемой на уровне -10°С или ниже. После окончания реакции реакционный раствор промывали водой (100 мл), экстрагировали этилацетатом и выпаривали досуха на роторном испарителе. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 6:1) с получением Соединения 8-21 (2,70 г, выход 90,2%). МС-ЭРИ m/z 390,0 (М+Н)+.
[0784] 8-21 (2,70 г, 6,90 ммоль), тетракис(трифенилфосфин)-палладий (3,1 г, 2,7 ммоль), гидрид три-н-бутилолова (5,6 мл, 20,8 ммоль) и уксусную кислоту (2,5 мл, 41,6 ммоль) добавляли в реакционную колбу объемом 250 мл, а затем ДХМ (70 мл) добавляли в качестве растворителя. Реакцию продолжали в течение 1 ч при комнатной температуре. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления растворителя, промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали досуха на роторном испарителе. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 3:1) с получением Соединения 9-21 (1,10 г, выход 45,7%) и побочного продукта 10-21 (849 мг, выход 38,6%). МС-ЭРИ m/z 350,0 (М+Н)+.
[0785] 9-21 (1,10 г, 3,10 ммоль) и Pd/C (1,1 г) добавляли в реакционную колбу объемом 100 мл, и затем добавляли метанол (35 мл). Реакцию продолжали в течение 1 ч при комнатной температуре под атмосферой водорода. После окончания реакции реакционный раствор фильтровали через диатомит для удаления Pd/C. Фильтрат выпаривали досуха на роторном испарителе с получением 10-21 (860 мг, выход 87%). МС-ЭРИ m/z 320,1 (М+Н)+.
[0786] 10-21 (1,71 г, 5,36 ммоль) и триэтилортоформиат (100 мл) добавляли в реакционную колбу объемом 250 мл и проводили реакцию в течение 3 ч при нагревании с обратным холодильником при 130°С.После окончания реакции в реакционный раствор добавляли воду (100 мл) и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали на роторном испарителе досуха. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 1:1) с получением 11-21 (1,70 г, выход 98%). МС-ЭРИ m/z 330,1 (М+Н)+.
[0787] Пример 25: Синтез Соединения 11-29
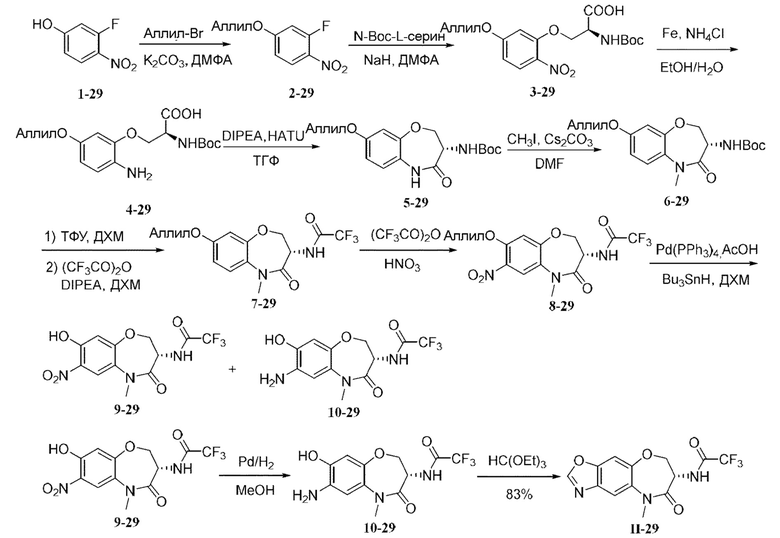
[0788] 1-29 (10 г, 63,65 ммоль) и карбонат калия (26,39 г, 190,96 ммоль) добавляли в реакционную колбу объемом 500 мл, а затем добавляли ДМФА (300 мл). Аллилбромид (17 мл, 190,96 ммоль) добавляли по каплям и проводили реакцию при комнатной температуре в течение 3 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха, а остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 5:1) с получением 2-29 (12,30 г, выход 98%). МС-ЭРИ m/z 198,0 (М+Н)+.
[0789] N-Boc-L-Серин (7,80 г, 38,06 ммоль) и NaH (3,6 г, 88,81 ммоль) добавляли в реакционную колбу объемом 250 мл, а затем добавляли ДМФА (100 мл) в качестве растворителя. Реакцию продолжали при 0°С в течение 30 мин. 2-29 (5,00 г, 25,37 ммоль) растворяли в ДМФА (50 мл), затем медленно добавляли по каплям в реакционный раствор и проводили реакцию при 0°С в течение 1 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха с получением неочищенного 3-29 (4,99 г, выход 53%). МС-ЭРИ m/z 381,1 (М-Н)-.
[0790] Весь неочищенный продукт 3-29, восстановленный порошок железа (7,1 г, 126,87 ммоль) и хлорид аммония (2,2 г, 40,6 ммоль) добавляли в реакционную колбу объемом 250 мл, а затем добавляли этанол/воду (120 мл/30 мл). Реакцию проводили при нагревании с обратным холодильником при 70°С в течение 1 ч. После окончания реакции реакционный раствор фильтровали через диатомит для удаления порошка железа и выпаривали фильтрат досуха на роторном испарителе с получением неочищенного 4-29. МС-ЭРИ m/z 353,1 (М+Н)+.
[0791] Весь неочищенный 4-29, HATU (11,6 г, 30,44 ммоль) и DIPEA (17 мл, 101,48 ммоль) добавляли в реакционную колбу объемом 250 мл, и затем добавляли ТГФ (200 мл) в качестве растворителя. Реакцию продолжали при комнатной температуре в течение 1 ч. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления ТГФ, промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия, выпаривали на роторном испарителе досуха, а остаток разделяли с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир: этилацетат = 8:1) с получением 5-29 (1,50 г, выход 17,7%). МС-ЭРИ m/z 333,2 (М-Н)-.
[0792] 5-29 (1,97 г, 5,84 ммоль) и карбонат цезия (2,85 г, 8,75 ммоль) добавляли в реакционную колбу объемом 250 мл, а затем добавляли ДМФА (50 мл). После реакции при 0°С в течение 30 мин, иодметан (438 мкл, 7,03 ммоль) медленно добавляли по каплям и проводили реакцию при 0°С в течение 1 ч. После окончания реакции реакционный раствор промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали досуха на роторном испарителе. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 10:1) с получением Соединения 6-29 (1,65 г, выход 81%). МС-ЭРИ m/z 293,1 (М+Н)+.
[0793] 6-29 (1,65 г, 4,70 ммоль) добавляли в реакционную колбу объемом 250 мл, а затем добавляли дихлорметан (40 мл) и ТФУ (10 мл). Реакцию продолжали при комнатной температуре в течение 1 ч. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления растворителя, добавляли воду (100 мл), доводили до рН 8-9 насыщенным бикарбонатом натрия и экстрагировали этилацетатом. Органическую фазу выпаривали досуха на роторном испарителе, добавляли трифторуксусный ангидрид (905 мкл, 6,5 ммоль) и DIPEA (1,17 мл, 7,10 ммоль) и в качестве растворителя добавляли ДХМ (50 мл). Реакцию продолжали в течение ночи при комнатной температуре. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления растворителя, промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали досуха на роторном испарителе. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 10:1) с получением 7-29 (1,60 г, выход 98,8%). МС-ЭРИ m/z 345,0 (М+Н)+.
[0794] 7-29 (1,50 г, 4,30 ммоль) и трифторуксусный ангидрид (45 мл) добавляли в реакционную колбу объемом 250 мл и охлаждали до -30°С.Концентрированную азотную кислоту (320 мкл, 4,70 ммоль) медленно добавляли по каплям и проводили реакцию в течение 1 ч при температуре, регулируемой на уровне -10°С или ниже. После окончания реакции реакционный раствор промывали водой (100 мл), экстрагировали этилацетатом и выпаривали на роторном испарителе досуха. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 6:1) с получением Соединения 8-29 (1,43 г, выход 85,6%). МС-ЭРИ m/z 390,0 (М+Н)+.
[0795] 8-29 (1,33 г, 3,4 ммоль), тетракис(трифенилфосфин)-палладий (1,16 г, 1,0 ммоль), гидрид три-н-бутилолова (2,74 мл, 10,2 ммоль) и уксусную кислоту (1,22 мл, 20,5 ммоль) добавляли в реакционную колбу объемом 250 мл, а затем ДХМ (35 мл) добавляли в качестве растворителя. Реакцию продолжали в течение 1 ч при комнатной температуре. После окончания реакции реакционный раствор выпаривали на роторном испарителе для удаления растворителя, промывали насыщенным раствором NaCl и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали досуха на роторном испарителе. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 3:1) с получением 9-29 (800 мг, выход 67,4%) и продукта 10-29 (312 мг, 27,0%). МС-ЭРИ m/z 349,9 (М+Н)+.
[0796] 9-29 (0,80 г, 2,20 ммоль) и Pd/C (0,80 г) добавляли в реакционную колбу объемом 100 мл, а затем добавляли метанол (25 мл). Реакцию продолжали в течение 1 ч при комнатной температуре под атмосферой водорода. После окончания реакции реакционный раствор фильтровали через диатомит для удаления Pd/C. Фильтрат выпаривали досуха на роторном испарителе с получением 10-29 (636 мг, выход 90,6%). МС-ЭРИ m/z 320,0 (М+Н)+.
[0797] 10-29 (0,948 г, 2,97 ммоль) и триэтилортоформиат (50 мл) добавляли в реакционную колбу объемом 250 мл и проводили реакцию в течение 3 ч при нагревании с обратным холодильником при 130°С.После окончания реакции в реакционный раствор добавляли воду (100 мл) и экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором NaCl, сушили над безводным сульфатом натрия и выпаривали досуха на роторном испарителе. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: петролейный эфир:этилацетат = 1:1) с получением 11-29 (0.900 г, выход 92,1%). МС-ЭРИ m/z 330,0 (М+Н)+.
[0798] Пример 26: Тест ингибирования ФНО-индуцированного программируемого некроза клеток Jurkat (FADD-/-) (IC50)
[0799] Среду RPMI-1640 (содержащую сыворотку, 50 мкл на лунку) добавляли в белый 96-луночный планшет для культур клеток, и затем по 0,5 мкл раствора лекарственного средства соответствующей концентрации, включающего соединение согласно настоящей заявке или контрольное соединение 7-Cl-O-Nec-l или GSK2982772 (7-Cl-O-Nec-l и GSK2982772 являются известными ингибиторами киназы RIP1), или 0,5 мкл 100% ДМСО добавляли в каждую лунку. По две повторности лунок были установлены для каждой концентрации каждого соединения.
[0800] Клетки Jurkat (FADD-/-) (линию клеток Т-клеточного лейкоза из периферической крови человека, с нокаутом гена FADD) культивировали in vitro. После роста до логарифмической фазы роста клетки собирали и центрифугировали при 1000 об/мин в течение 5 мин. Супернатант отбрасывали, клетки ресуспендировали в свежей среде и доводили до плотности 5×105/мл. Суспензию клеток добавляли в культуральный планшет, содержащий лекарственное средство (40 мкл на лунку). В группах лечения в каждую лунку добавляли по 10 мкл ФНО (фактора некроза опухоли, конечная концентрация 10 нг/мл), разведенного в среде для культивирования клеток, и инкубировали в течение 20 часов в инкубаторе для клеток (37°С, 5% CO2). Затем в каждую лунку добавляли по 50 мкл раствора Cell Titer-Glo и инкубировали при комнатной температуре в течение 10 мин. Затем люминесценцию регистрировали на планшетном анализаторе BioTek для измерения внутриклеточного уровня АТФ. Эффект тестируемых соединений на ингибирование ФНО-индуцированного некроза клеток вычисляли относительно лунки с полной активностью и фоновой лунки (при использовании контрольной необработанной лунки с ДМСО в качестве 100% жизнеспособности клеток), и полумаксимальную ингибирующую концентрацию (IC50) соединения вычисляли с помощью статистической программы Graphpad Prism. Результат показан в Таблице 1 ниже.
[0801] Пример 27: Тест ингибирования активности ADP-Glo™ RIP1 киназы (Ki)
[0802] Ген RIP1 человека трансдуцировали в клетки насекомых Sf-9, и белок RIP1 очищали с помощью Ni+ аффинной хроматографии, а затем при использовании молекулярного сита S-200 для удаления мультимеров белка. Полученный белок RIP1 хранили при -70°С, и активность белка RIP1 при катализе аутофосфорилирования определяли при использовании набора для анализа киназной активности ADP-Glo™ (Promega) и определяли ингибирующую активность лекарственного средства против киназы RIP1.
[0803] Лекарственное средство (соединения согласно настоящей заявке и контрольные соединения 7-Cl-O-Nec-l и GSK2982772) растворяли в 100% ДМСО и последовательно разводили 3-кратно с получением в общей сложности 11 градиентов концентрации, и приготавливали 100× раствор. 100 нл соединения переносили в 384-луночный аналитический планшет. Две повторности лунок были установлены для каждой концентрации каждого лекарственного средства.
[0804] Раствор фермента RIP1 и раствор АТФ приготавливали в буфере для анализа (содержащем 50 мМ HEPES, рН 7,5, 30 мМ MgCl2, 50 мМ NaCl, 1 мМ DTT, 0,02% CHAPS и 0,5 мг/мл BSA). Затем 5 мкл раствора фермента RIP1 (конечная концентрация 50 нМ) добавляли в аналитический планшет и инкубировали при комнатной температуре в течение 1 ч. 5 мкл раствора АТФ (конечная концентрация 10 мкМ) добавляли в аналитический планшет и инкубировали при комнатной температуре в течение 4 ч. Затем 5 мкл реагента ADP-Glo добавляли в аналитический планшет и инкубировали при комнатной температуре в течение 60 мин. 5 мкл раствора для анализа киназы добавляли в аналитический планшет и инкубировали при комнатной температуре в течение 30 мин. После считывания данных на Envision, степень ингибирования в каждой лунке вычисляли относительно лунки с полной активностью и фоновой лунки, и Ki соединения вычисляли при использовании программы GraphPad Prism 7 (с использованием уравнения Моррисона для аппроксимации кривой и расчета Ki). Результаты представлены в Таблице 1.
[0805]
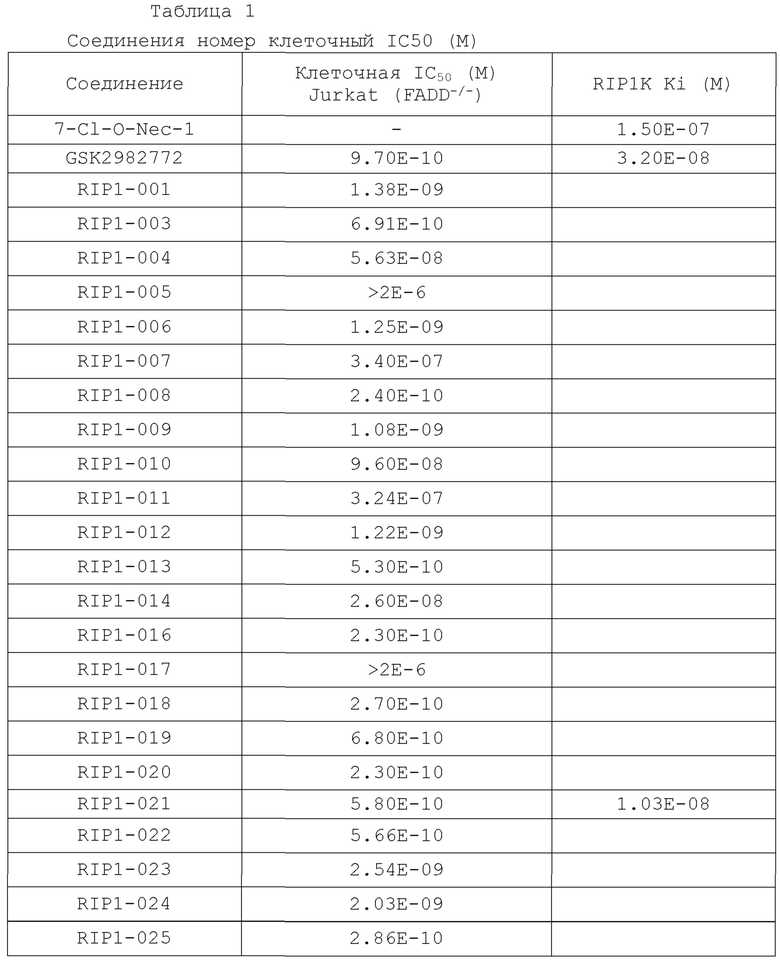
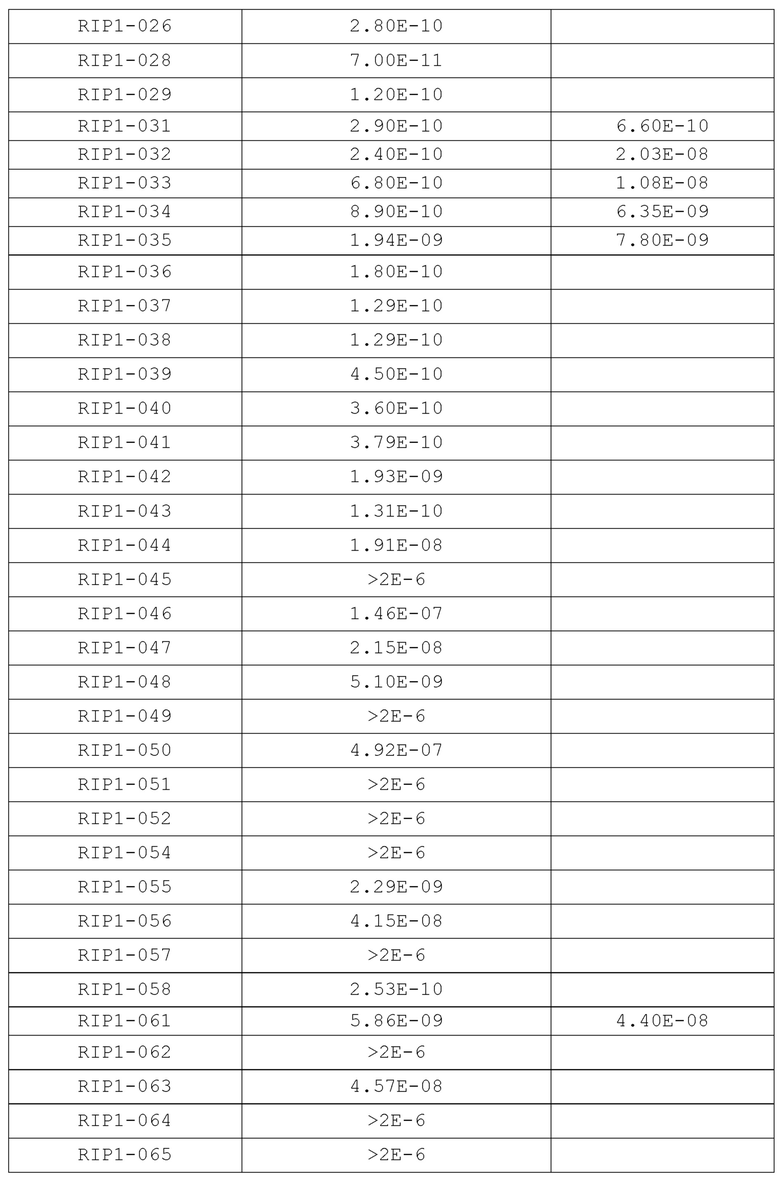
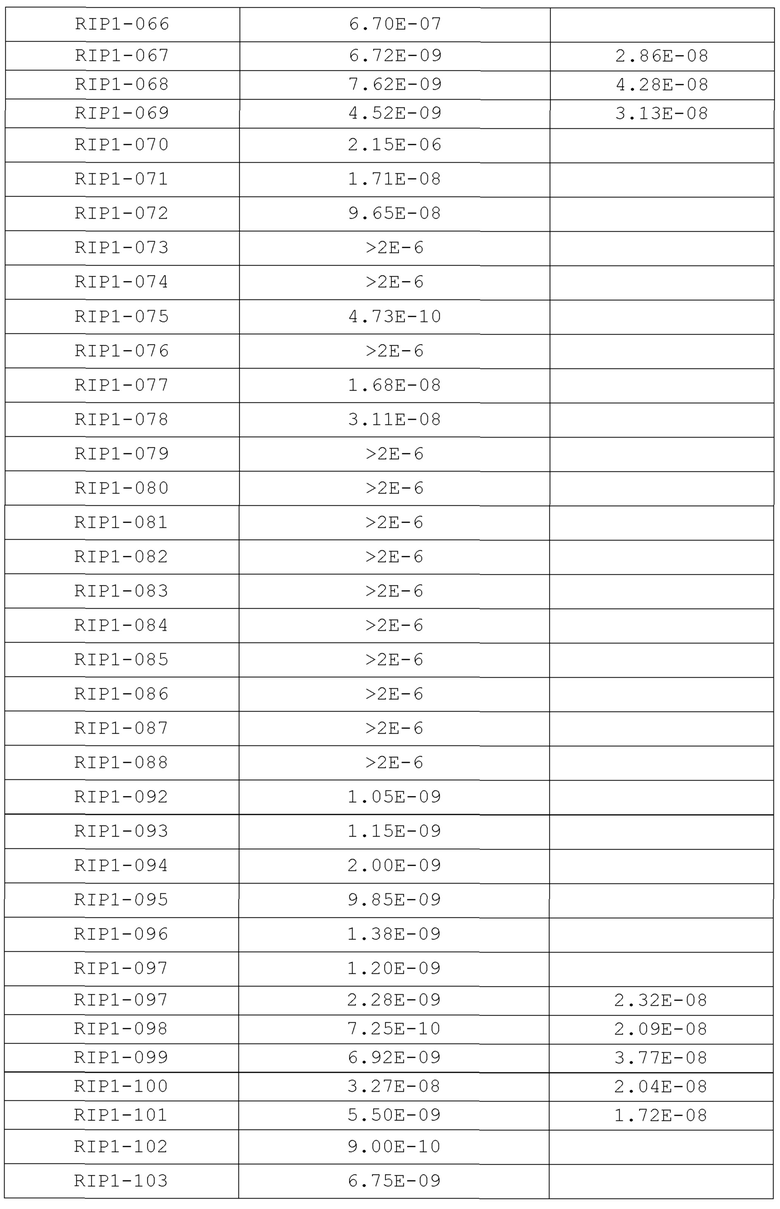
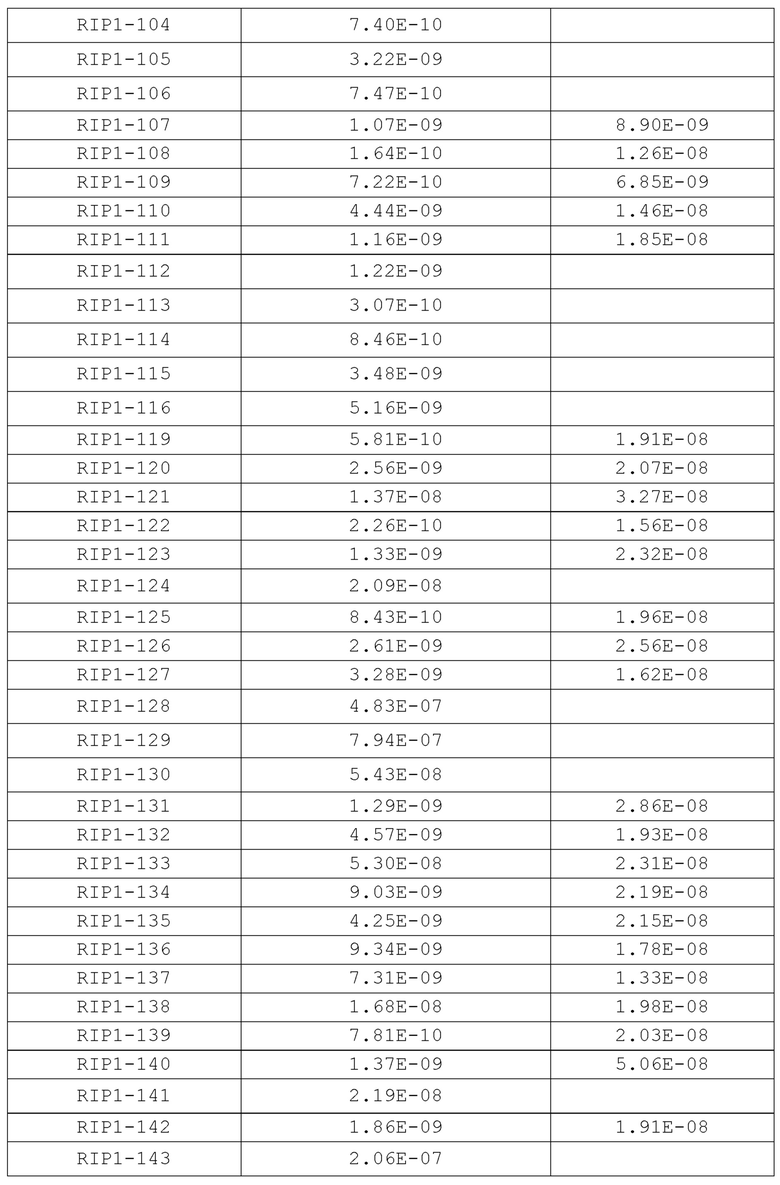
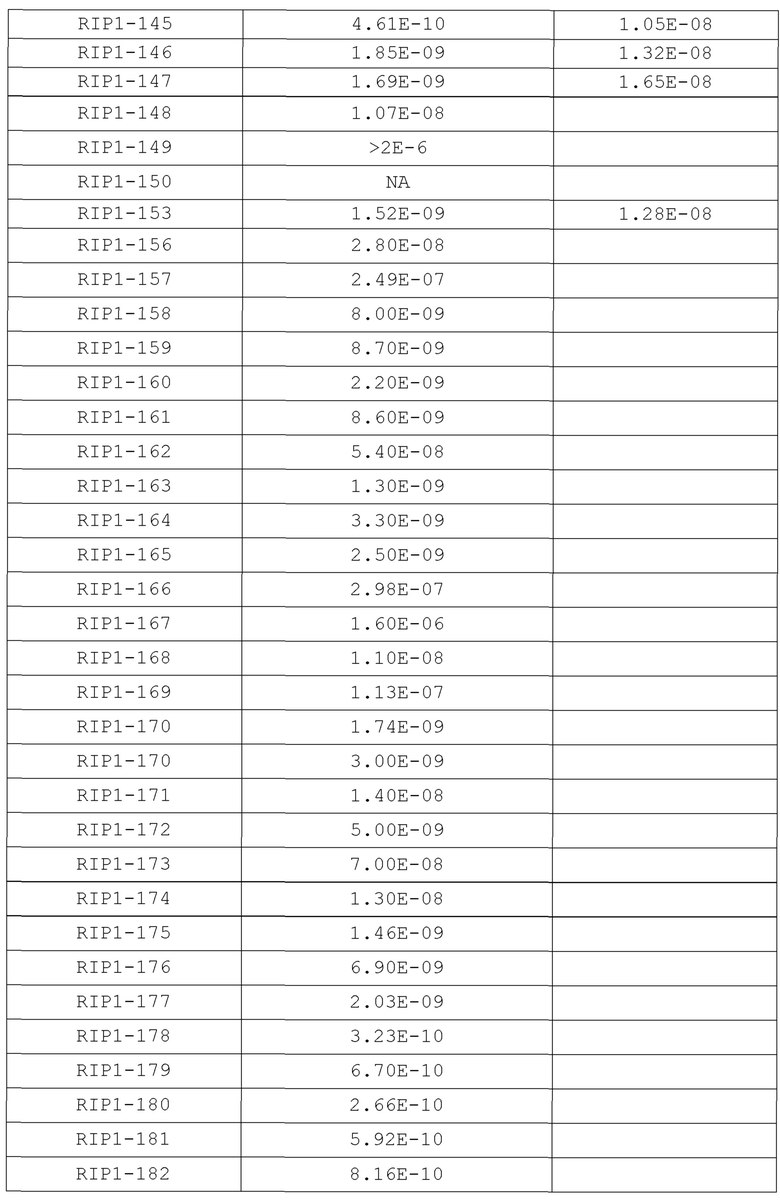
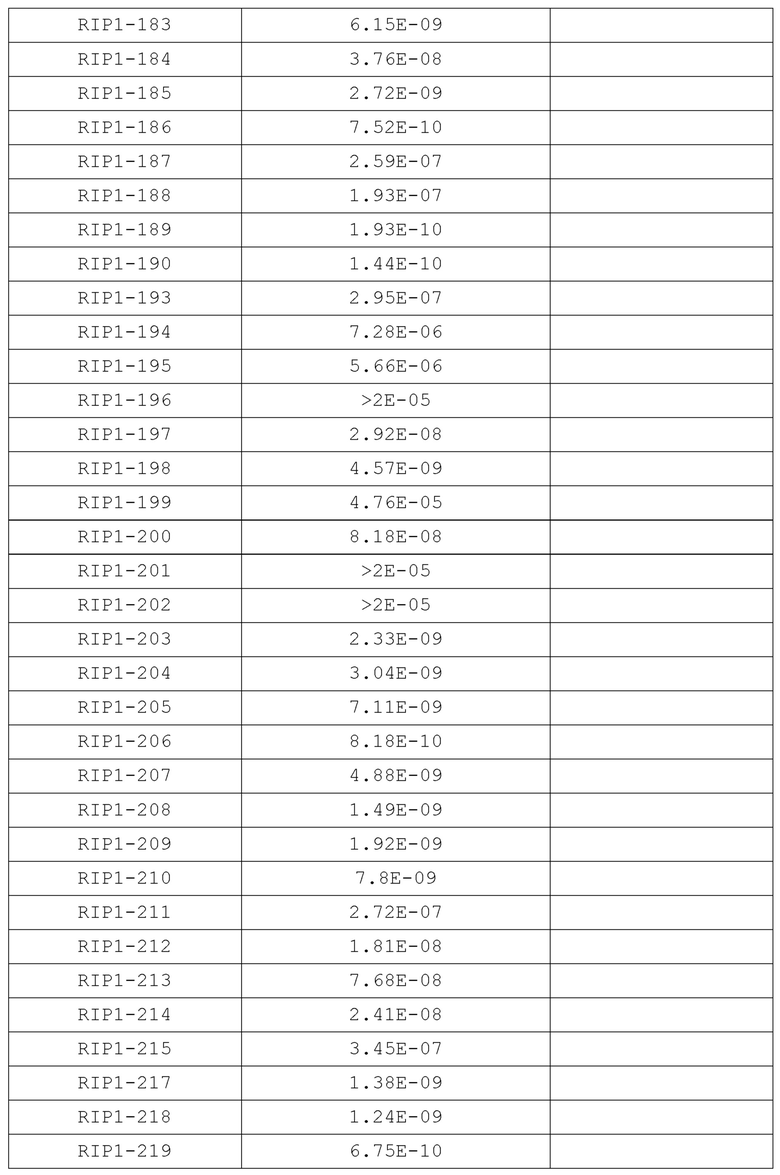

[0806] Как видно из Таблицы 1, соединения согласно настоящей заявке могут эффективно ингибировать активность киназы RIP1.
[0807] Пример 28: Эффективность in vivo в тесте ФНО-α-индуцированного шока у мышей
[0808] Мышей C57BL/6 специально стерилизовали и распределяли животных случайным образом в группы в соответствии с их массой тела. Приготавливали 0,15 мг/мл ФНО-α. Каждой мыши вводили по 200 мкл ФНО-альфа (30 мкг на мышь) в хвостовую вену. За 15 мин до индукции ФНО-α лекарственное средство вводили в соответствии с массой тела. В 0 ч, 1 ч, 2 ч, 4 ч и 6 ч температуру тела мыши определяли с помощью термометром для мелких животных и записывали, при этом во время теста наблюдали за состоянием животного. Через 6 ч мышей умерщвляли CO2. Экспериментальные данные были нанесены на график при использовании Graph Pad Prism 7 и выражены как среднее значение ± стандартная ошибка (Среднее ± SEM). Площадь под кривой клинической оценки анализировали при использовании однофакторного дисперсионного анализа. Значение р<0,05 считали значимым различием по сравнению с контрольной группой.
[0809] На Фиг. 1 показана температура тела мышей в зависимости от времени после введения мышам Соединения RIP1-034 согласно настоящей заявке в разных дозах (10 мг/кг, 20 мг/кг и 30 мг/кг). Тест показывает, что введение Соединения RIP1-034 эффективно ингибирует снижение температуры тела из-за системного воспалительного ответа, вызванного ФНО-α.
[0810] Пример 29: Измерение концентрации в плазме крови мышей после однократного перорального введения
[0811] Раствор для перорального введения, содержащий соединение RIP1-034 согласно настоящей заявке, приготавливали в день введения с водным раствором, содержащим 0,5% МС/0,25% Tween 80. Всем животным не давали корм в течение ночи перед введением, и через 4 часа после введения им давали возможность свободно принимать пищу. Каждая группа включала по три мыши, и каждой мыши перорально вводили однократную дозу 10 мг/кг в день эксперимента. Примерно 30 мкл цельной крови забирали из дорсальной вены задней конечности через 0,25, 0,5, 1, 2, 4, 6, 8 и 24 часа после введения, переносили в антикоагуляционную пробирку, содержащую гепарин натрия, и несколько раз тщательно перемешивали путем переворачивания. Собранный образец крови центрифугировали при 4°С и 4000 г в течение 5 мин для сбора плазмы, и образец плазмы переносили в чистые полиэтиленовые микроцентрифужные пробирки, а затем хранили в морозильной камере при -75±15°С до анализа. Фактический вводимый объем вычисляли на основе массы тела животного. Все образцы исследовали с помощью ЖХ-МС/МС, и концентрацию исследуемого лекарственного средства в образцах определяли методом стандартной кривой. Концентрация в плазме крови каждой мыши в каждой точке времени измерения после однократного перорального введения показана на Фиг. 2. Средняя концентрация в плазме в группе из трех мышей в каждую точку времени измерения после однократного перорального введения показана на Фиг. 3.
[0812] Этот тест показывает, что Соединение RIP1-034 может достигать требуемой концентрации в плазме после перорального введения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЭСТЕИНАСЦИДИНА, СОЕДИНЕНИЯ, ПРОМЕЖУТОЧНЫЙ ПРОДУКТ | 1997 |
|
RU2194709C2 |
| СПОСОБ СИНТЕЗА ФТАЛАСЦИДИНА И ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2001 |
|
RU2267492C2 |
| СУЛЬФОНИЛМОЧЕВИНЫ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2739356C2 |
| СУЛЬФОНИЛМОЧЕВИНЫ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2795512C2 |
| Производное индола, используемое в качестве ингибитора CRTH2 | 2017 |
|
RU2756270C2 |
| ПРОИЗВОДНЫЕ 1,3,4-ОКСАДИАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРА ГИСТОНДЕАЦЕТИЛАЗЫ 6 И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2021 |
|
RU2822624C1 |
| СИНТЕЗ ГАЛИХОНДРИНОВ | 2018 |
|
RU2794176C2 |
| ИНГИБИТОРЫ НУКЛЕОЗИДФОСФОРИЛАЗ И НУКЛЕОЗИДАЗ | 2003 |
|
RU2330042C2 |
| ОБЩИЙ СИНТЕЗ МИРИАПОРОНОВ | 2003 |
|
RU2328492C2 |
| НОВОЕ ПРОИЗВОДНОЕ ПИПЕРИДИНА И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГИБИРОВАНИЯ АУТОТАКСИНА | 2022 |
|
RU2834850C2 |
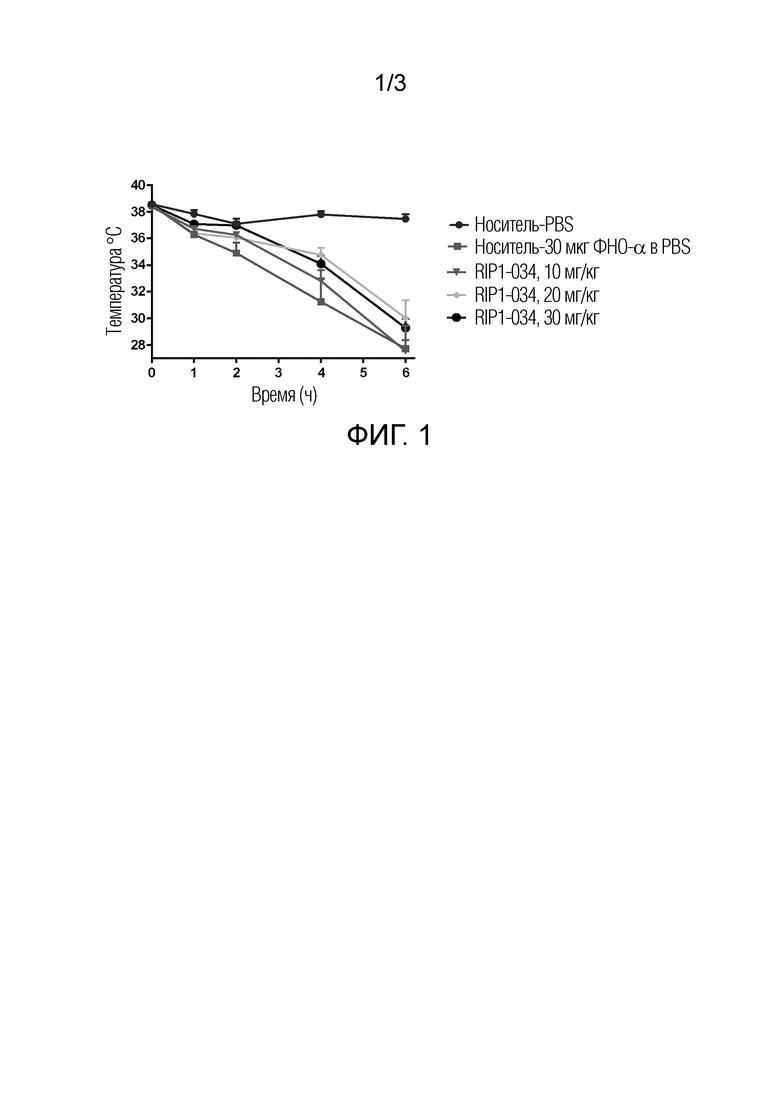
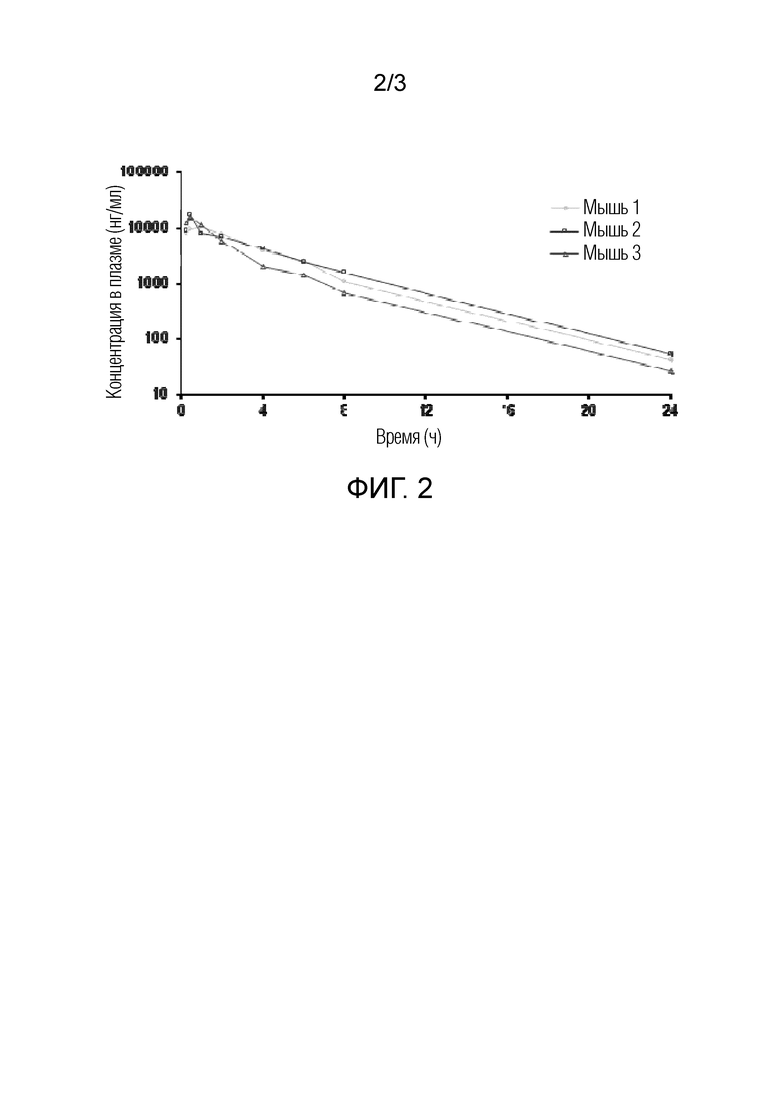
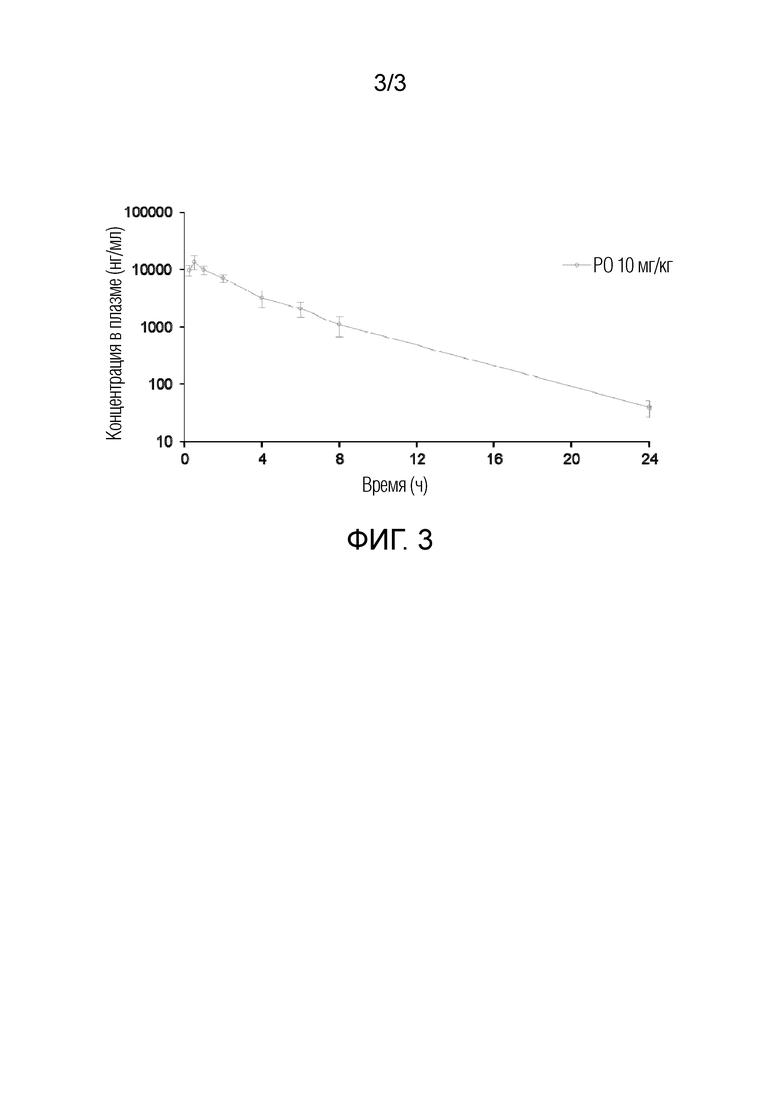
Изобретение относится к области органической химии, а именно к соединению формулы (I) или его фармацевтически приемлемой соли, где X представляет собой O или S; кольцо M имеет структуру 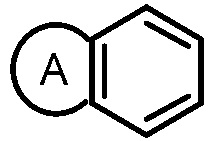 , где кольцо A выбрано из группы, состоящей из 5-6-членного гетероарила, содержащего 1-3 гетероатома, независимо выбранных из азота и кислорода, и 5-членного гетероциклила, содержащего 2 гетероатома азота; кольцо B выбрано из группы, состоящей из замещенного или незамещенного 6-членного арила и замещенного или незамещенного 5-6-членного гетероарила, содержащего 1-4 гетероатома, независимо выбранных из азота и кислорода; где “замещенный” относится к замещению 1 атома водорода в группе заместителем, выбранным из C1-C6 алкила; C выбрано из группы, состоящей из замещенного или незамещенного 6-членного арила, замещенного или незамещенного 6-членного гетероарила, содержащего 1 гетероатом азота; где “замещенный” относится к замещению 1-3 атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена и C1-C6 алкила; L выбрано из группы, состоящей из O, NH, C1-C6 алкилена; R1 выбран из группы, состоящей из H и C1-C6 алкила; R2 выбран из группы, состоящей из галогена, гидроксила, оксо, бензила, C1-C6 алкила, C1-C6 галогеналкила, C1-C6алкокси и C1-C6 aцила; и m равно 0 или 1; n равно 1. Также изобретение относится к способу получения соединения формулы (I), фармацевтической композиции на основе соединения формулы (I), применению соединения формулы (I), способу ингибирования киназы RIP1 у субъекта и промежуточному соединению формулы (II). Технический результат: лечение или предупреждение заболеваний, опосредованных киназой RIP1, обеспечиваемое соединением формулы (I). 6 н. и 18 з.п. ф-лы, 3 ил., 1 табл., 29 пр.
, где кольцо A выбрано из группы, состоящей из 5-6-членного гетероарила, содержащего 1-3 гетероатома, независимо выбранных из азота и кислорода, и 5-членного гетероциклила, содержащего 2 гетероатома азота; кольцо B выбрано из группы, состоящей из замещенного или незамещенного 6-членного арила и замещенного или незамещенного 5-6-членного гетероарила, содержащего 1-4 гетероатома, независимо выбранных из азота и кислорода; где “замещенный” относится к замещению 1 атома водорода в группе заместителем, выбранным из C1-C6 алкила; C выбрано из группы, состоящей из замещенного или незамещенного 6-членного арила, замещенного или незамещенного 6-членного гетероарила, содержащего 1 гетероатом азота; где “замещенный” относится к замещению 1-3 атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена и C1-C6 алкила; L выбрано из группы, состоящей из O, NH, C1-C6 алкилена; R1 выбран из группы, состоящей из H и C1-C6 алкила; R2 выбран из группы, состоящей из галогена, гидроксила, оксо, бензила, C1-C6 алкила, C1-C6 галогеналкила, C1-C6алкокси и C1-C6 aцила; и m равно 0 или 1; n равно 1. Также изобретение относится к способу получения соединения формулы (I), фармацевтической композиции на основе соединения формулы (I), применению соединения формулы (I), способу ингибирования киназы RIP1 у субъекта и промежуточному соединению формулы (II). Технический результат: лечение или предупреждение заболеваний, опосредованных киназой RIP1, обеспечиваемое соединением формулы (I). 6 н. и 18 з.п. ф-лы, 3 ил., 1 табл., 29 пр.
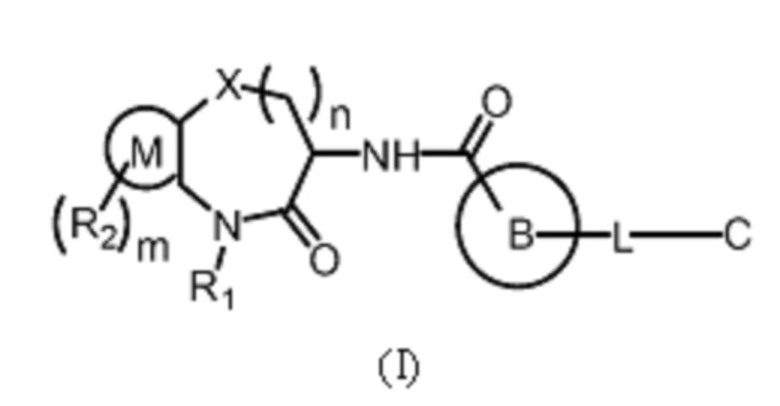 ,
, 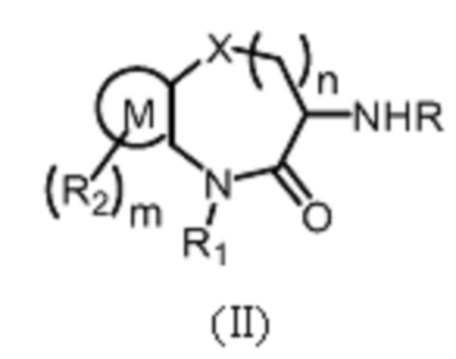
1. Соединение Формулы (I):
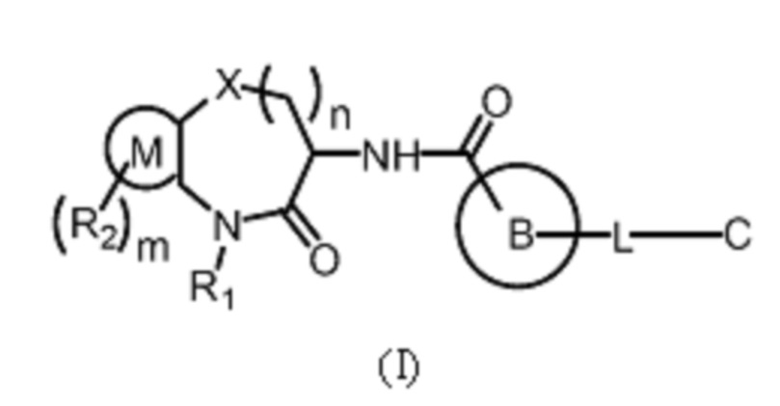
или его фармацевтически приемлемая соль, где:
X представляет собой O или S;
кольцо M имеет структуру 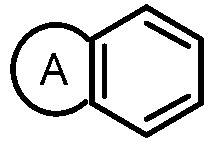 , где кольцо A выбрано из группы, состоящей из 5-6-членного гетероарила, содержащего 1-3 гетероатома, независимо выбранных из азота и кислорода, и 5-членного гетероциклила, содержащего 2 гетероатома азота;
, где кольцо A выбрано из группы, состоящей из 5-6-членного гетероарила, содержащего 1-3 гетероатома, независимо выбранных из азота и кислорода, и 5-членного гетероциклила, содержащего 2 гетероатома азота;
кольцо B выбрано из группы, состоящей из замещенного или незамещенного 6-членного арила и замещенного или незамещенного 5-6-членного гетероарила, содержащего 1-4 гетероатома, независимо выбранных из азота и кислорода; где “замещенный” относится к замещению 1 атома водорода в группе заместителем, выбранным из C1-C6 алкила;
C выбрано из группы, состоящей из замещенного или незамещенного 6-членного арила, замещенного или незамещенного 6-членного гетероарила, содержащего 1 гетероатом азота; где “замещенный” относится к замещению 1-3 атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена и C1-C6 алкила;
L выбрано из группы, состоящей из O, NH, C1-C6 алкилена;
R1 выбран из группы, состоящей из H и C1-C6 алкила;
R2 выбран из группы, состоящей из галогена, гидроксила, оксо, бензила, C1-C6 алкила, C1-C6 галогеналкила, C1-C6алкокси и C1-C6 aцила; и
m равно 0 или 1;
n равно 1.
2. Соединение или его фармацевтически приемлемая соль по п.1, где X представляет собой O или S.
3. Соединение или его фармацевтически приемлемая соль по п.1, где кольцо A представляет собой 5-членный гетероарил, содержащий 1-3 гетероатома, независимо выбранных из азота и кислорода, или 5-членный гетероциклил, содержащий 2 гетероатома азота.
4. Соединение или его фармацевтически приемлемая соль по п.1, где кольцо A представляет собой 6-членный гетероарил, содержащий 1 или 2 гетероатома азота.
5. Соединение или его фармацевтически приемлемая соль по п.1, где кольцо B представляет собой замещенный или незамещенный 6-членный арил, замещенный или незамещенный 5-6-членный гетероарил, содержащий 1-4 гетероатома, независимо выбранных из азота и кислорода; где “замещенный” относится к замещению 1 атома водорода в группе заместителем, выбранным из C1-C6 алкила.
6. Соединение или его фармацевтически приемлемая соль по п.1, где C представляет собой замещенный или незамещенный 6-членный арил или замещенный или незамещенный 6-членный гетероарил, содержащий 1 гетероатом азота; где “замещенный” относится к замещению 1-3 атомов водорода в группе заместителем, выбранным из группы, состоящей из галогена и C1-C6 алкила.
7. Соединение или его фармацевтически приемлемая соль по п.1, где L представляет собой O, NH или C1-C6 алкилен.
8. Соединение или его фармацевтически приемлемая соль по п.1, где R1 представляет собой H.
9. Соединение или его фармацевтически приемлемая соль по п.1, где R1 представляет собой незамещенный C1-C6 алкил.
10. Соединение или его фармацевтически приемлемая соль по п.1, где соединение имеет Формулу (Ia):
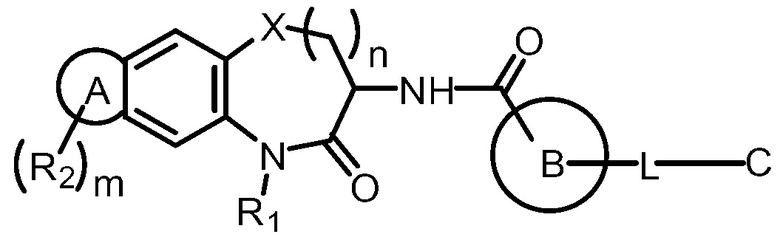
(Ia).
11. Соединение или его фармацевтически приемлемая соль по п.1, где соединение имеет Формулу (Ib):
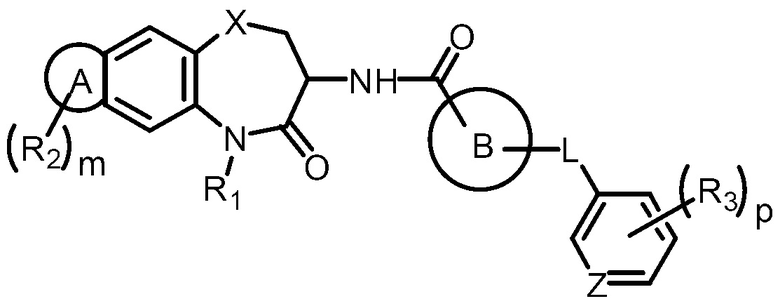
(Ib)
где
L представляет собой O или CH2;
Z представляет собой N или CH;
R3 выбран из галогена и C1-C6 алкила; и
p равно 0, 1, 2 или 3.
12. Соединение или его фармацевтически приемлемая соль по п.10 или 11, где структурная группа, представленная формулой 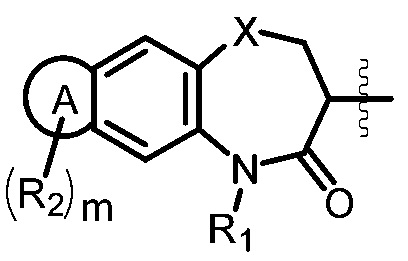 , выбрана из группы, состоящей из:
, выбрана из группы, состоящей из:
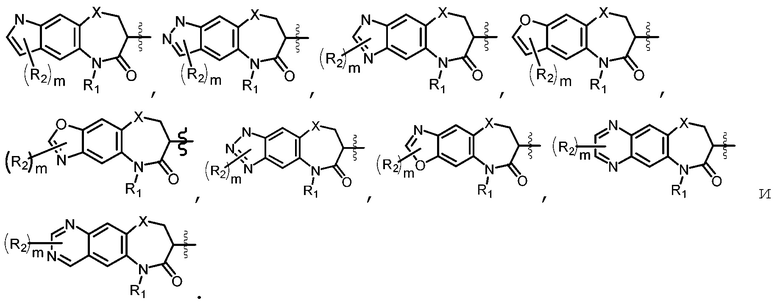
13. Соединение или его фармацевтически приемлемая соль по п.1, где соединение имеет Формулу (Ic):
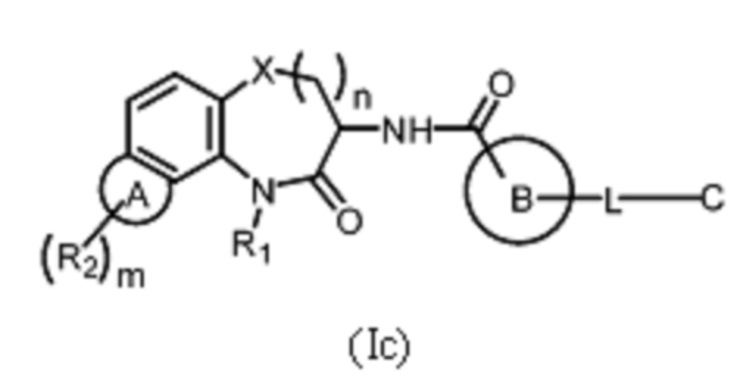
где кольцо A представляет собой 6-членный гетероарил, содержащий 1-2 гетероатома азота.
14. Соединение или его фармацевтически приемлемая соль по п.1, где соединение имеет Формулу (Id):
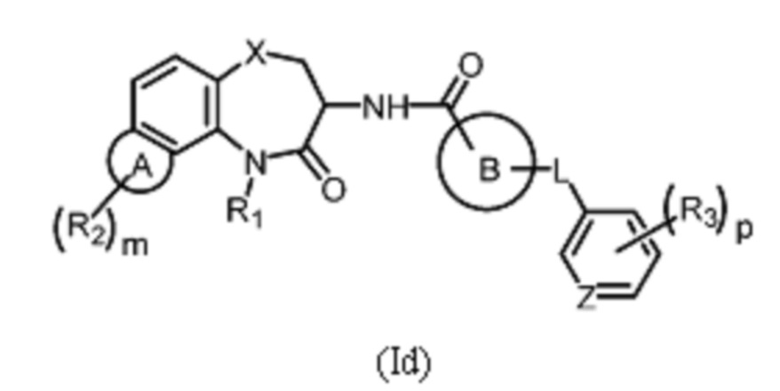
где
кольцо A представляет собой незамещенный 6-членный гетероарил, содержащий 1-2 гетероатома азота;
L представляет собой O или CH2;
Z представляет собой N или CH;
R3 выбран из группы, состоящей из галогена и незамещенного C1-C6 алкила; и
p равно 0, 1, 2 или 3.
15. Соединение или его фармацевтически приемлемая соль по п.13 или 14, где структурная группа, представленная формулой 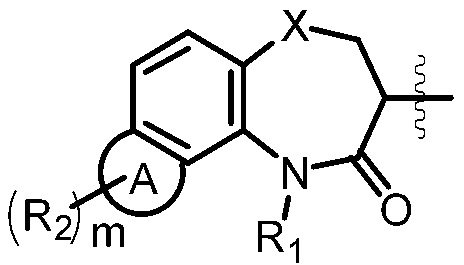 , выбрана из группы, состоящей из:
, выбрана из группы, состоящей из:
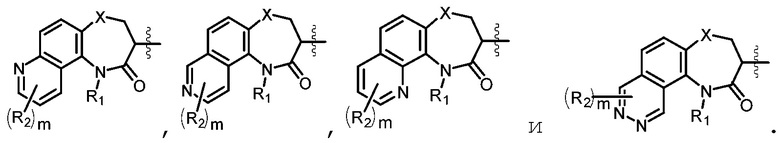
16. Соединение или его фармацевтически приемлемая соль по любому из предыдущих пунктов, где кольцо B является группой, выбранной из группы, состоящей из:
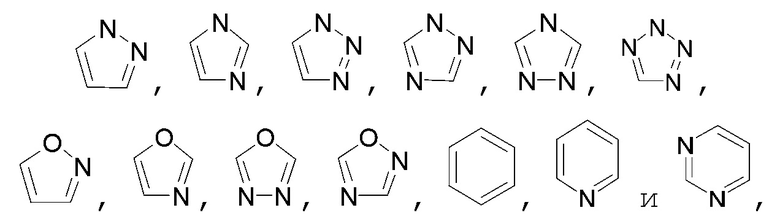 .
.
17. Соединение или его фармацевтически приемлемая соль по п.1, где соединение выбрано из группы, состоящей из:
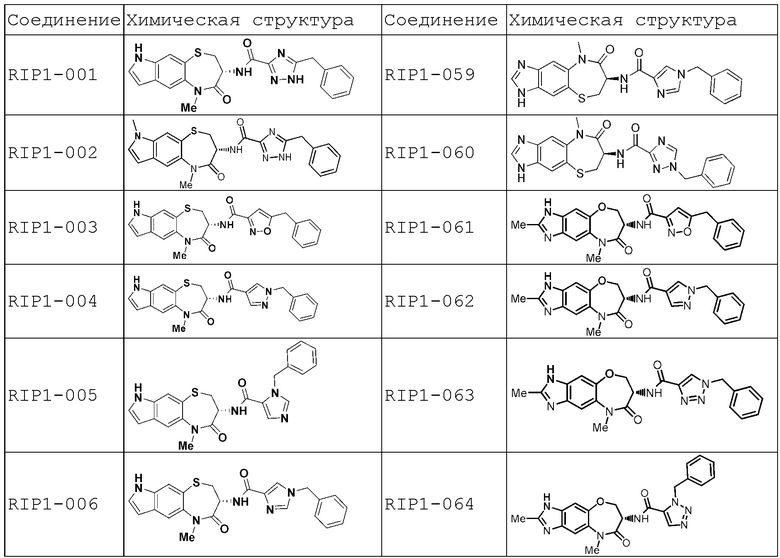
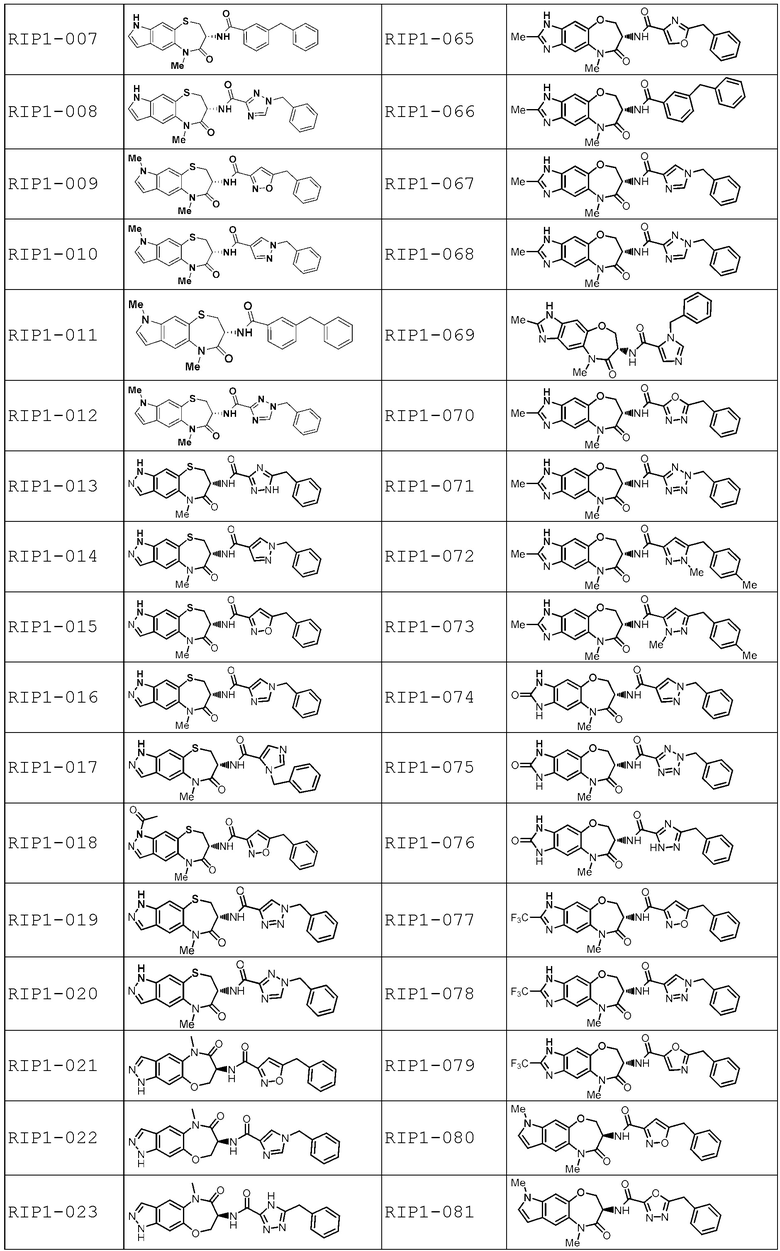
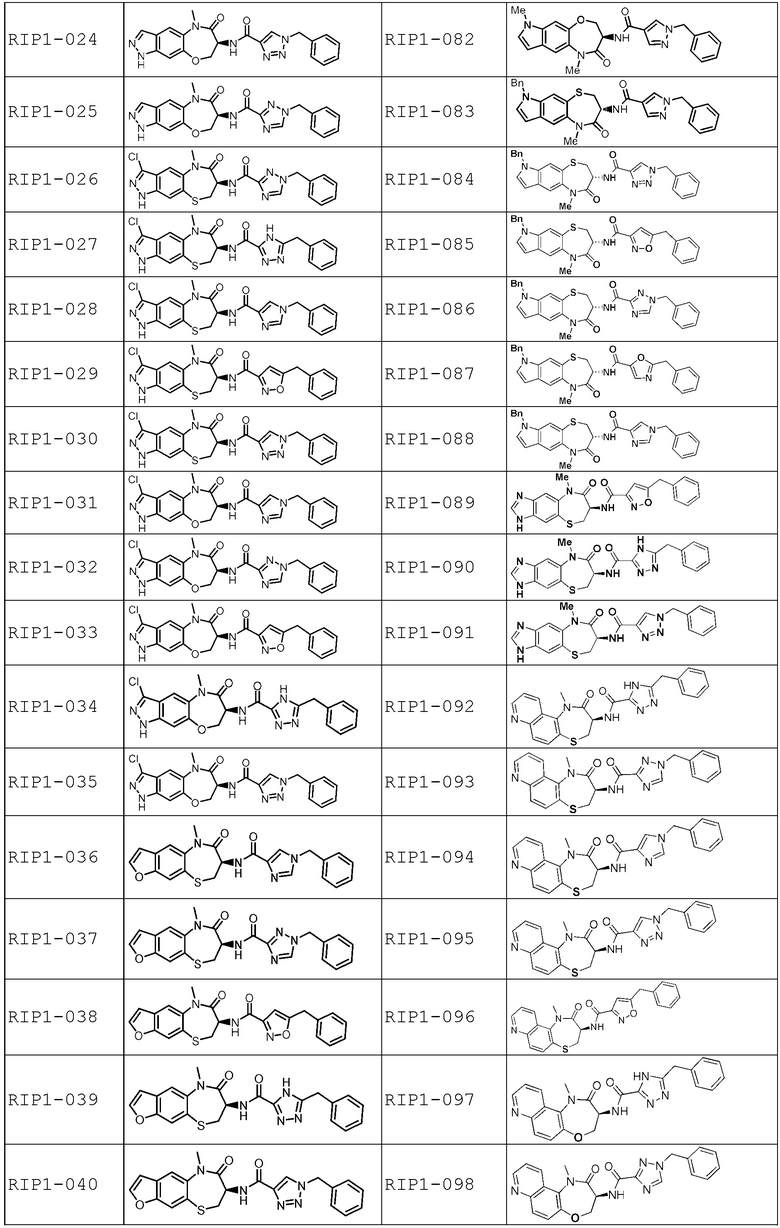
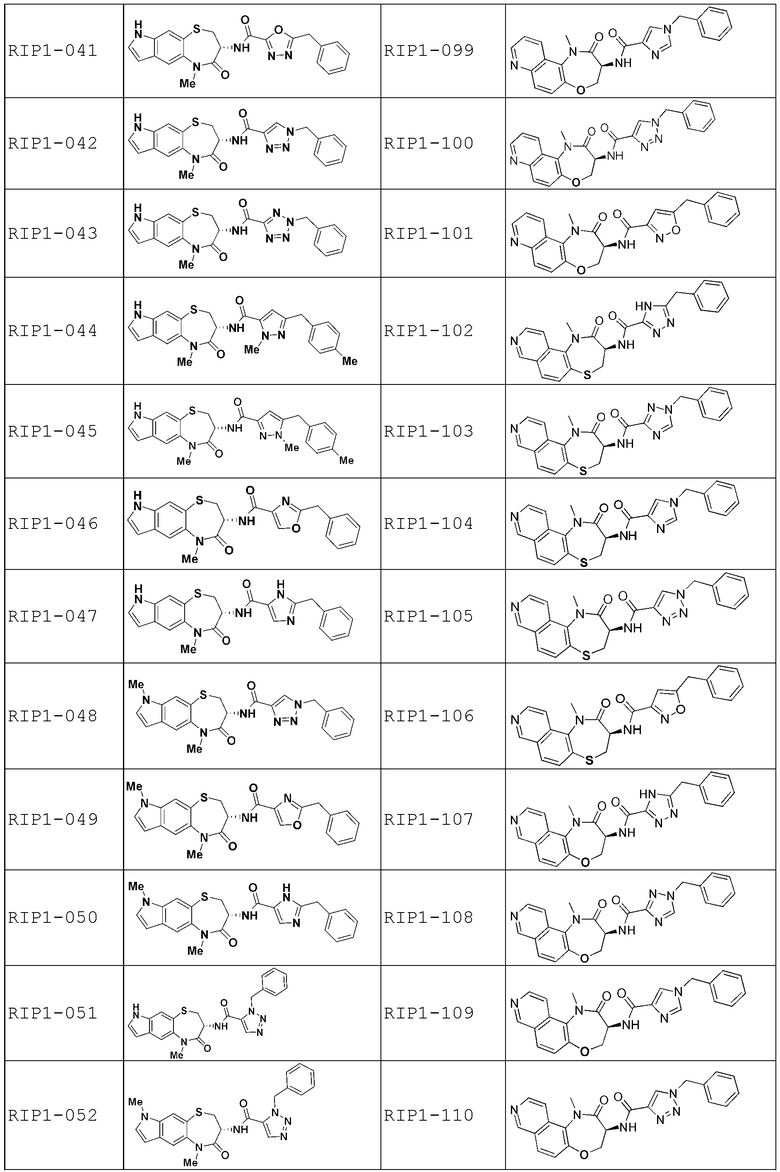
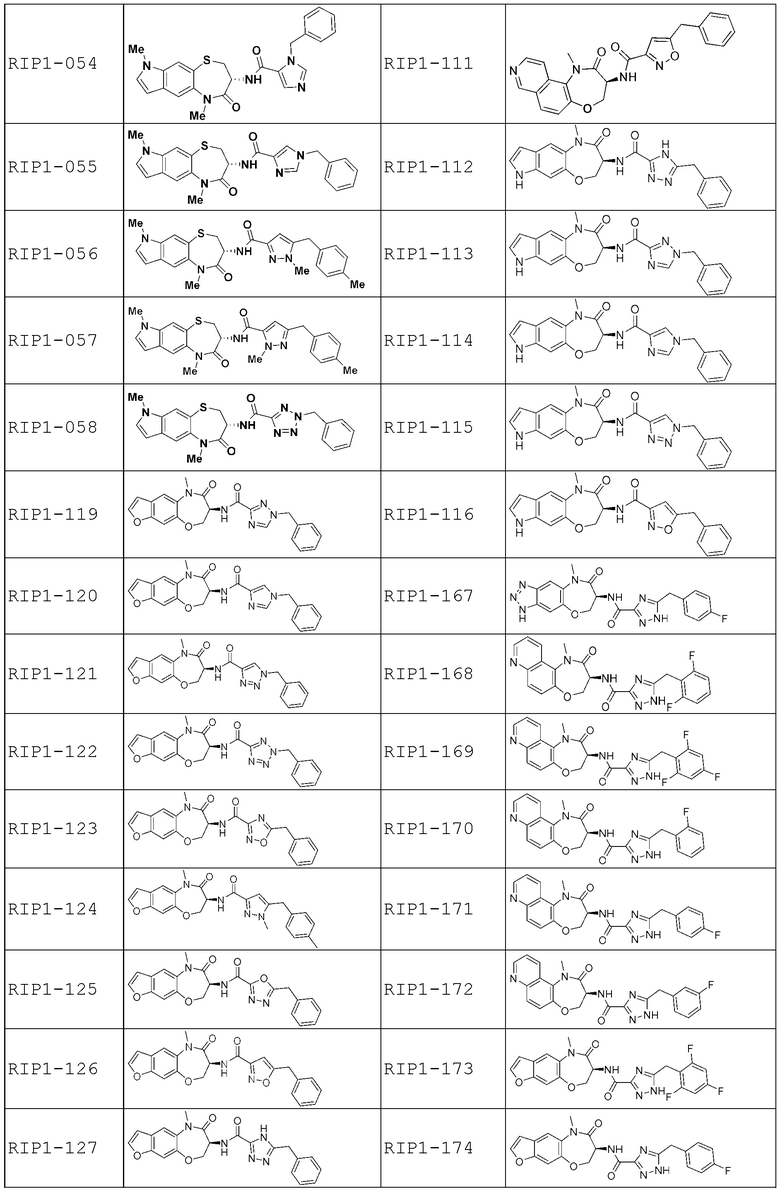
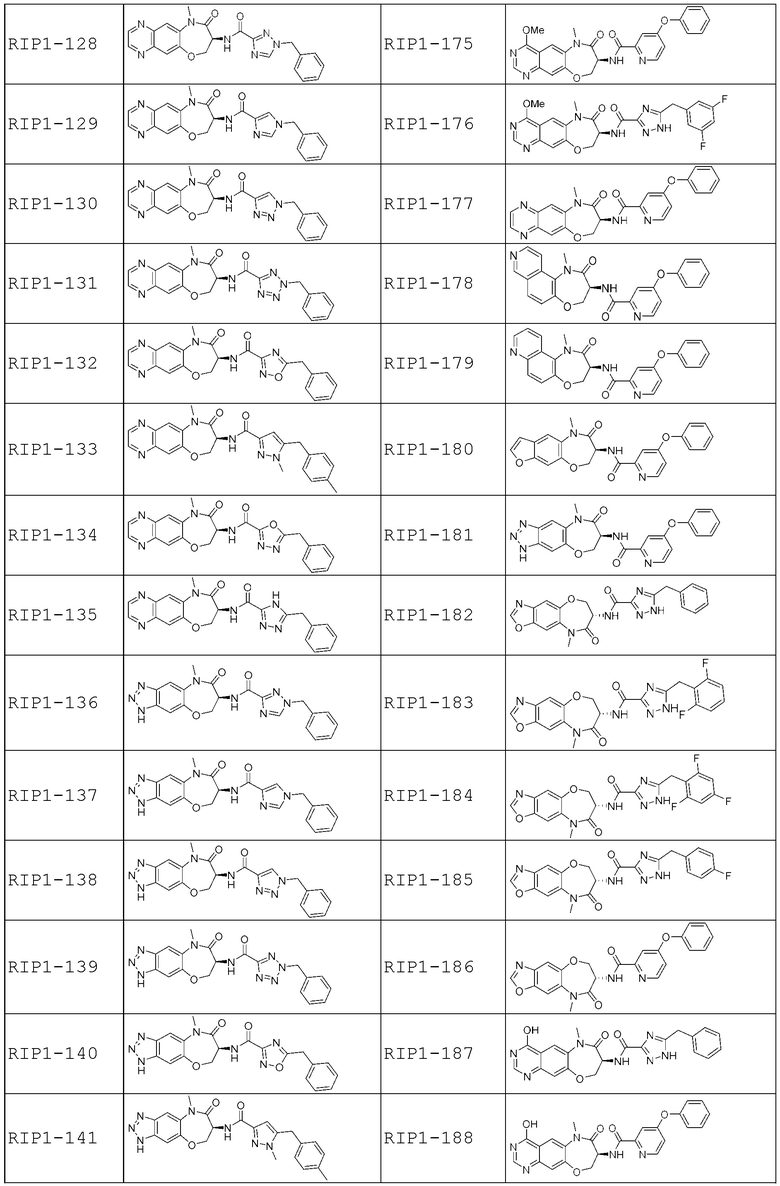
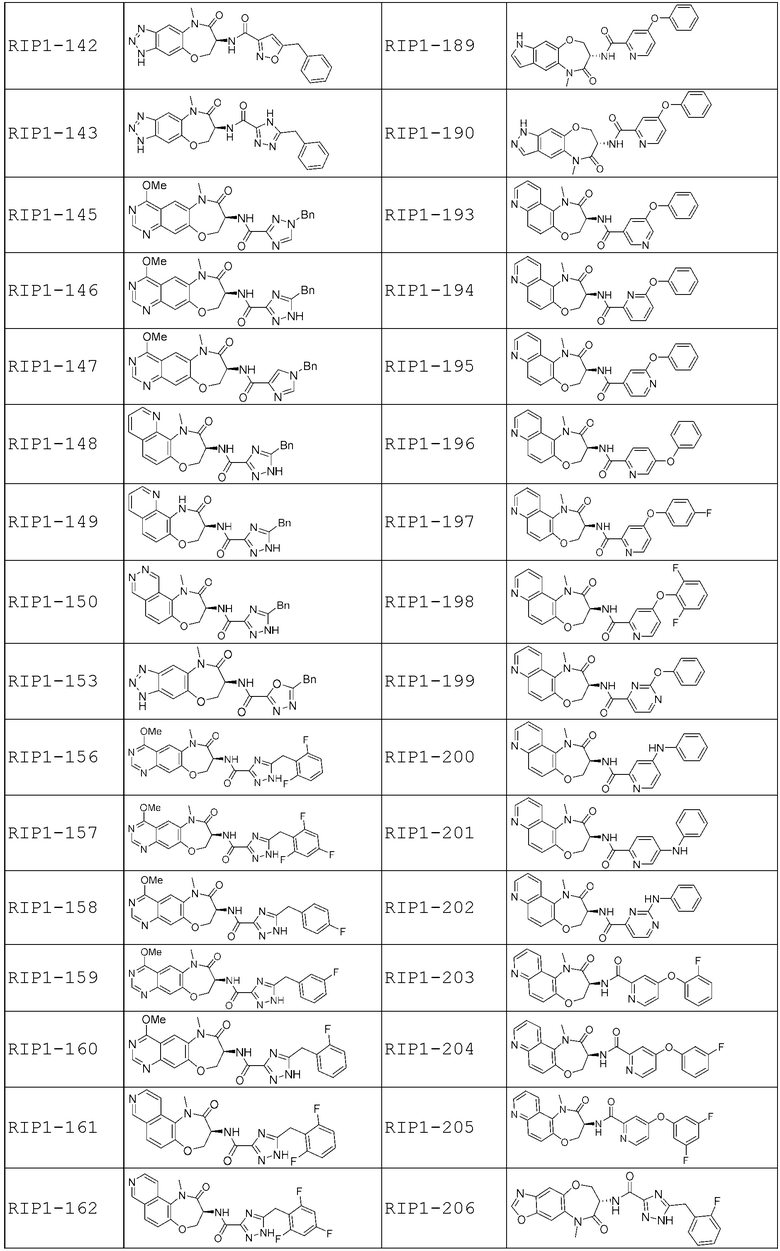
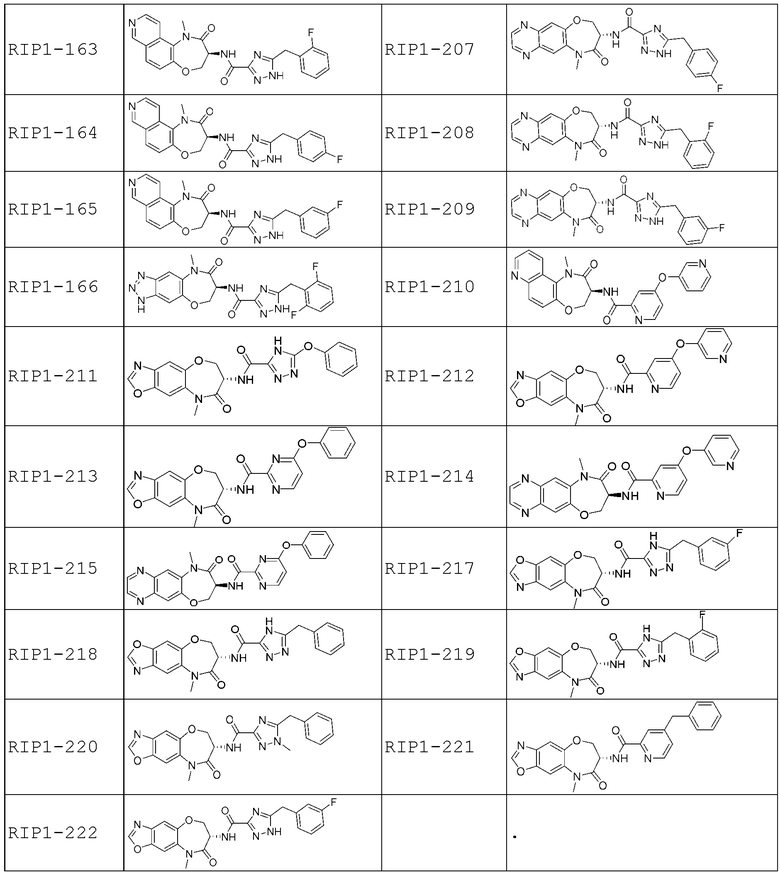
18. Способ получения соединения по п.1,
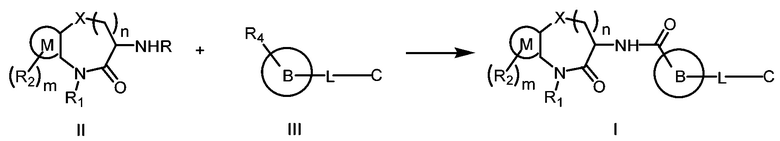
где R4 представляет собой -COOH или -COO-G+, где G+ является ионом щелочного металла;
когда R представляет собой H, способ включает: реакцию соединения Формулы (II) с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I) по п.1; и
когда R представляет собой защитную группу аминогруппы, выбранную из трифторацетила и трет-бутоксикарбонила (Boc), способ включает: удаление R из соединения Формулы (II) в кислотных условиях и затем реакцию соединения Формулы (II), из которой удален R, с соединением Формулы (III) в инертном растворителе в присутствии конденсирующего реагента и основания с получением соединения Формулы (I) по п.1.
19. Фармацевтическая композиция для лечения или предупреждения заболеваний или нарушений, опосредованных киназой RIP1, включающая терапевтически эффективное количество соединения Формулы (I) или его фармацевтически приемлемой соли по любому из пп.1-17 и фармацевтически приемлемый носитель.
20. Применение соединения или его фармацевтически приемлемой соли по любому из пп.1-17 или фармацевтической композиции по п.19 в производстве лекарственного средства для лечения или предупреждения заболеваний или нарушений, опосредованных киназой RIP1.
21. Применение по п.20, где опосредованные киназой RIP1 заболевания или нарушения выбраны из группы, состоящей из воспалительного заболевания кишечника, болезни Крона, язвенного колита, псориаза, дегенеративного заболевания сетчатки, отслоения сетчатки, пигментного ретинита, макулодистрофии, панкреатита, атопического дерматита, ревматоидного артрита, спондилоартрита, подагры, SoJIA, системной красной волчанки, синдрома Шегрена, системной склеродермии, антифосфолипидного синдрома, васкулита, остеоартроза, неалкогольного стеатогепатита, алкогольного стеатогепатита, аутоиммунного гепатита, гепатита B, гепатита C, аутоиммунного гепатобилиарного заболевания, первичного склерозирующего холангита, отравления ацетаминофеном, гепатотоксичности, нефрита, целиакии, аутоиммунной ИТП, отторжения трансплантата, ишемического-реперфузионного повреждения паренхиматозных органов, сепсиса, синдрома системного воспалительного ответа, нарушения мозгового кровообращения, инфаркта миокарда, болезни Хантингтона, болезни Альцгеймера, болезни Паркинсона, аллергического заболевания, астмы, атопического дерматита, рассеянного склероза, диабета I типа, гранулемы Вегенера, легочного саркоидоза, болезни Бехчета, синдрома лихорадки, связанной с интерлейкин-1-превращающим ферментом, хронической обструктивной болезни легких, периодического синдрома, связанного с рецептором фактора некроза опухоли, периодонтита, инсульта, ожогов, ожогового шока, черепно-мозговой травмы, атеросклероза, повреждения почек, вызванного цисплатином, острого повреждения почек, панкреатита, хронического заболевания почек, острого респираторного дистресс-синдрома, хронической обструктивной болезни легких, болезни Гоше, болезни Нимана-Пика, острой печеночной недостаточности, онкологических заболеваний (например, рака поджелудочной железы), бактериальной инфекции, повреждения, вызванного курением, кистозного фиброза, мутации ключевого регуляторного гена NF-κB, дефицита гемм-окисленной убиквитин-лигазы-1 IRP2, синдрома дефицита комплекса сборки линейных цепей убиквитина, гемобластных злокачественных новообразований, злокачественных новообразований солидных органов, гриппа, стафилококковых инфекций, микобактериальных инфекций, лизосомных болезней накопления, GM2 ганглиозидоза, α-маннозидоза, аспартилглюкозаминурии, болезни накопления эфиров холестерина, хронической недостаточности гексозаминидазы A, цистиноза, болезни Данона, болезни Фабри, болезни Фарбера, фукозидоза, галактосиалидоза, GM1 ганглиозидоза, накопления муколипидов, детской болезни накопления свободной сиаловой кислоты, ювенильной недостаточности гексозаминидазы A, болезни Краббе, дефицита лизосомной кислой липазы, метахроматической лейкодистрофии, мукополисахаридоза, множественной сульфатазной недостаточности, нейронального цероидного липофусциноза, болезни Помпе, пикнодизостоза, болезни Сандхоффа, болезни Шиндлера, болезни Салла, болезни Тея-Сакса, болезни Вольмана, синдрома Стивенса-Джонсона и токсического эпидермального некролиза.
22. Способ ингибирования киназы RIP1 у субъекта, включающий введение субъекту эффективного количества соединения или его фармацевтически приемлемой соли по п.1 или фармацевтической композиции по п.19.
23. Промежуточное соединение Формулы (II):
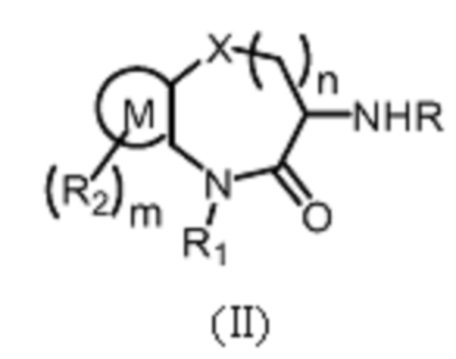
где:
R представляет собой H или защитную группу аминогруппы, выбранную из трифторацетила, трет-бутоксикарбонила (Boc), бензилоксикарбонила (CBZ) и 9-флуоренилметиленоксикарбонила (Fmoc);
X представляет собой O или S;
кольцо M имеет структуру  , где кольцо A выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила, содержащего 1-3 гетероатома, независимо выбранных из азота и кислорода, и 5-членного гетероциклила, содержащего 2 гетероатома азота;
, где кольцо A выбрано из группы, состоящей из замещенного или незамещенного 5-6-членного гетероарила, содержащего 1-3 гетероатома, независимо выбранных из азота и кислорода, и 5-членного гетероциклила, содержащего 2 гетероатома азота;
где указанный 5-членный гетероарил необязательно замещен по гетероатому азота при помощи R', выбранного из группы, состоящей из H, Boc, (C1-C6) алкила и бензила;
R1 выбран из группы, состоящей из H и C1-C6 алкила;
R2 выбран из группы, состоящей из галогена, гидроксила, оксо, бензила, C1-C6 алкила, C1-C6 галогеналкила, C1-C6 алкокси и C1-C6 ацила;
m равно 0 или 1; и
n равно 1.
24. Промежуточное соединение по п.23, выбранное из группы, состоящей из:
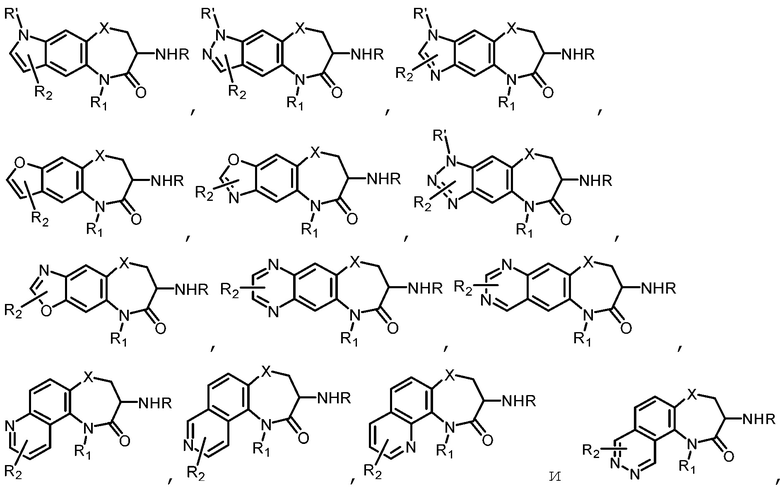
где R' выбран из группы, состоящей из H, Boc, (C1-C4) алкила и бензила.
| CN 105121432 B, 03.08.2018 | |||
| WO 2017109724 A1, 29.06.2017 | |||
| WO 2016027253 A1, 25.02.2016 | |||
| WO 2018073193 A1, 26.04.2018 | |||
| Мотовило | 1929 |
|
SU19507A1 |
| Двигатель внутреннего горения | 1928 |
|
SU26152A1 |
Авторы
Даты
2023-04-10—Публикация
2019-06-25—Подача