Изобретение относится к области получения оксида графена, который может быть использован в области нанотехнологии и химической промышленности в качестве сырья для получения создания материалов суперсорбентов нового поколения, селективных мембран, производства носимой электроники, биосенсоров, биомедицинских приложений, высокоэнергоемких химических источников тока (суперконденсаторы и батареи) и различных композиционных материалов.
Оксид графена (ранее имел другое название «оксид графита» или графитовой кислотой) представляет собой двумерный материал - производное графена с присоединенными по краям или внутри углеродной сетки кислородсодержащими функциональными группами и/или молекулами. Номенклатура этих групп обширна: гидроксильные, фенольные, карбонильные, карбоксильные, арильные, эфирные, фосфорсодержащие и т.п. Разновидностью являются оксиды графена, модифицированные полимерами, такими как полиэтиленгликоль, полиэфиры, поливинилы, полиакрилы и т.д. Еще одну группу оксидов графена составляют допированные соединения. В частности, известны оксиды графена, содержащие в своей структуре один или несколько атомов бора, азота, алюминия, фосфора, кремния, серы или же группы на их основе, например меламин, фосфин, силан, полисилоксан, сульфиды и т.д. [Hummers W.S., Offeman R.E.. Preparation of Graphitic Oxide // Journal of American Chemical Society.- 1958.- V. 80, N. 6, P. 1339.; Sadri R., Kamali K. Z., Hosseini M., etс.Experimental study on thermo-physical and rheological properties of stable and green reduced graphene oxide nanofluids: Hydrothermal assisted technique // Journal of Dispersion Science and Technology-2017. - V.38, N.9. - P.1302-1310].
По сорбционной емкости оксид графена значительно превосходят ионообменные смолы на полимерной основе и другие традиционные сорбенты. Использование уникальных сорбционных свойств оксидов графена могут реализовываться несколькими путями, например абсорбцией; физической адсорбцией; хемосорбцией; ионным обменом; с установлением Ван-дер-ваальсовых взаимодействий, водородных, ковалентных или нековалентных связей. Все это и составляет суть интереса к оксидам графена для создания материалов супер-сорбентов нового поколения, селективных мембран, производства носимой электроники, биосенсоров, биомедицинских приложений, высокоэнергоемких химических источников тока (суперконденсаторы и батареи). [Jirickova A., Jankovsky O., Sofer Z., Sedmidubsky D. Synthesis and applications of graphene oxide. // Materials - 2022. - V.15. - P.920].
Известны четыре основных метода получения оксида графена. Все они используют окисление кусочков графита в водной среде сильных кислот (например, концентрированной серной кислоты) в присутствии высокоактивных окислителей. За этими методами закрепились названия: Хаммерса, Хофмана, Штауденмайера и Броди.
Известен способ неорганического синтеза оксида графена, описанный ранее в 1958 году в работах Хаммерса и Оффемана [Hummers W.S., Offeman R.E.. Preparation of graphitic oxide // Journal of American Chemical Society. - 1958.- V. 80, N.6. -P. 1339.], путем окисления природного графита перманганатом калия с добавкой нитрата натрия в концентрированной (95-98%) серной кислоте. Полученную реакционной смесь очищают от остатков электролитов (солей), путем промывания водой и ионообменными смолами. В настоящее время существует различные вариации использования данного метода [S.Shamaila, A.K.L. Sajjad, I. Anum. Modifications in development of grapheme oxide synthetic routes // Chemical Engineering Journal. - 2016. - V.294 - P. 458-477.], касающиеся подготовки исходных веществ, соотношения их количеств, технологических режимов и методов очистки конечного продукта. Однако, несмотря на многочисленные попытки усовершенствовать способ синтеза оксида графена по Хаммерса-Оффемана. Данный способ имеет следующие недостатки:
- не высокая степень окисления конечного продукта, т.е. полученный оксид графена, содержит значительную примесь недоокисленного графита;
- сложности контроля технологических режимов и невысокая времени скорость окисления;
- многостадийность особенно для очистки конечного продукта;
- в результате реакции с графита со смесью нитрата натрия и концентрированной серной кислоте образуются побочные продукты - токсичные окислы азота и серы.
Для устранения указанных выше недостатков в различных работах были предприняты попытки усовершенствования метода Хаммерса-Оффемана. Авторы изобретения [Patent US9428394B2 at 2016-08-30. Highly oxidized graphene oxide and methods for production thereof. / Inventor: Tour J.M., Kosynkin, D.V. - Application US13/321,623. Priority date 2009-05-22 - 23 p.] для обеспечения полноты окисления графита и исключения применение нитрата, проводили процесс в смеси
серной и фосфорной кислот с увеличенным количеством перманганата калия по отношению к графиту. Недостатки данного способа: большой
расходу перманганата калия, что соответственно приводит к затратам на очистку или регенерацию токсичных отходов.
Известен способ получения оксида графена, описанный в работе [Kovtyukhova N. I., Ollivier P.J., Martin B.R., Mallouk T.E., Chizhik S.A. etc. Layer-by-layer assembly of ultrathin composite films from micronsized graphite oxide sheets and polycations // Chemistry of Materials. - 1999. - V. 11, N. 3, - P. 771-778.]. Данный способ включает 6 стадий: 1) Обработка графита перекисным реагентом в серной кислоте, включающий окислительное интеркалирование графита персульфатом калия в растворе серной кислоты с пятиокисью фосфора; 2) Обработка графита в условиях, вызывающих эксфолиацию графита; 3) Обработка предварительно эксфолиированного графита, суспендированного в концентрированной серной кислоте, перманганатом калия; 4) Разбавление реакционной смеси водой; 5) Добавление к разбавленной реакционной смеси пероксида водорода для
восстановления соединений марганца высших степеней окисления до сульфата двухвалентного марганца; 6) Промывка продукта раствором кислоты и диализ.
Недостатки данного способа являются:
- процесс подготовки графита является многостадийным и требует для своего осуществления дополнительного оборудования;
- появляются дополнительные токсичные отходы, что влечет дополнительные затраты на их обезвреживание или утилизацию;
- использование нитрат натрия также влечет появлению трудноулавливаемых отходов производства, связанные с появлением токсичных паров азотной кислоты и диоксида азота.
Все это достаточно усложняет технологию получения оксида графена.
В работе авторов [Patent US9815701B1 at 2017-11-14. Synthesis of reduced graphene oxide nanoparticles / Inventor: Gasme M.A., Awad l., Hendi A.A., etc. Current Assignee: King Saud University - Application US15/442,606. Priority date 2017-02-24 - 13 р.] описан способ получения восстановленного оксида графена, включающий стадии: смешивание углеродной сажи с кислотой и постепенного добавления в этот раствор первого окислителя для получения суспензии окисленной формы углерода; затем проводят перемешивание суспензии при температуре 35°C с последовательным повышением температуры до 60°С и добавление к полученному раствору (суспензии) воды и второго окислителя. При перемешивании суспензии образуются наночастицы восстановленного оксида графена. В качестве кислоты применяют серную кислоту с добавкой фосфорной кислоты. В качестве первого и второго окислителя применяют соответственно перманганат калия и перекись водорода.
Недостатками известного способа являются следующие: -применение углеродной сажи вместо графита не позволяет получить качественный оксид графена; углеродная сажа не интеркалируется и и не способна разделяться на слои окисленного графена; полученный продукт является смесью малоупорядоченного аморфного углеродного материала (сажи) и оксидом графена.
Известен способ получения оксида графена [Патент РФ №2709594(13) C1 от 18.12.2019 Способ получения оксида графена / Авторы - Ткачев А. Г., Мележик А.В., Осипов А.А. Ткачев М. А. -Заявка: №2018134006 от 26.09.2018 г.- Бюл. №35. -14 c.] включающий стадии обработки углеродного материала первым окислителем (перманганатомкалия) в среде концентрированной серной кислоты, разбавление реакционной смеси водой, затем обработку вторым окислителем (перекисью водорода) и промывку полученного углеродсодержащего продукта окисления раствором кислоты, затем водой, в заявляемом способе в качестве углеродного материала используют графит, а перед обработкой перманганатом калия графит дополнительно обрабатывают раствором перекиси водорода в серной кислоте, причем количество перекиси водорода берут от 0,15 до 0,30 масс.ч. на 1 масс.ч. графита в пересчете на 100%-ную перекись водорода. В результате реакции концентрированной серной кислоты и перексида водорода образуется надсерная кислота (кислота Каро):
H2O2+H2SO4=H2SO5+H2O.
После этого в реакционную смесь добавляют воду и затем смешивают с перманганатом калия при сохранении концентрации свободной воды до 2%.
Недостатком данного изобретения являются: использование концентрированных растворов перекиси водорода (до 60% масс.) требует использования специальных мер по безопасности и управлению технологического процесса; использование агрессивных жидкостей, серная кислоты (100% мас.) и олеум и сильных окислителей (пероксид водорода, кислота Каро и перманганат калия) требует дорогостоящего металлоемкого оборудования, устойчивым к коррозии; использование перманганата калия также создает дополнительные сложности в очистке конечного продукта; отсутствуют данные для оценки степени превращения графита в оксид графена, что ставит под вопрос масштабируемости технологии.
В изобретении [Патент РФ №2720780 C2 от 20.01.2020. Способ синтеза оксида графена /Авторы: Архипов М.А., Арсанукаев М. М., Мотчаный А.И, Ковалев С.С., Шицле В. Ф. Заявка: 2018126661, 19.07.2018 г.- Бюл. №2 -8 c.] предложен химический способ синтеза оксида графена из графита, в котором сначала готовят смесь серной кислоты с сухим льдом в достаточном для отвердевания смеси количестве и смесь по меньшей мере одного окислителя, например калия перманганата, с сухим льдом, при этом по меньшей мере одна из указанных смесей содержит измельченный графит.Полученные смеси загружают в автоклав высокого давления и перемешивают, например, посредством вращения и встряхивания автоклава. Стадию интеркалирования графита посредством его окисления проводят в автоклаве в среде сверхкритического флюида, нагревая внешнюю стенку автоклава до 35-50°С. Оксид графена диспергируют в воде и отмывают в растворах кислот и воде. В изобретении также указывается о получении оксида графена высокого качества с относительно низкими временными затратами при значительном снижении расхода серной кислоты. Недостатком данного изобретения являются: использование концентрированных растворов серной кислоты, специального оборудования (автоклава), высоких давлений (до 74 бар).
Известно изобретение [Patent CN106564891A at 2017-04-19. Preparing method of oxidized graphene and high-conductivity graphene. / Inventor: Liu H., Zhang Z., Zhang C., Hu X. Current Assignee: Shandong Oubo New Material Co Ltd - Application CN201610979110.6A. Priority date at 2016-11-07 - 19 p.], в котором предложен химический способ получения окисленного графена из графита, включающий несколько стадий: сначала в условиях герметизации защитного газа графит, интеркалятор и окислитель после смешивания подвергают низкотемпературной реакции и получают реакционную смесь; затем реакционную смесь, полученную на вышеуказанной стадии, разделяют, после чего получают продукт реакции и наконец, продукт реакции, полученный на вышеуказанной стадии, десорбируют в диспергаторе, и получают диспергирующую жидкость на основе окисленного графена. За счет принятия низкотемпературного режима количество дефектов, очевидно, снижается, под действием давления интеркалятор вставляется между слоями графенового листа, действующая сила между слоями уменьшается, а расстояние между слоями увеличивается; затем окислитель поступает в участки между слоями графенового листа, происходит окислительная реакция, в результате чего образуется окисленный графен; и из-за влияния давления интеркалятор и окислитель быстрее попадают в участки между слоями графенового листа, реакция способствует более полному завершению за короткое время, достигается одностадийная интеркаляция в графен, а затем графен получен и приготовлен порошок с низким процентом брака и высоким качеством. Недостатком данного изобретения являются: использование различных химических добавок (восстановителей, окислителей, растворителей и модифицирующих агентов), требует применения инертной среды, высоких давлений (10-100 атм.) и температур (1200-1800°С), что ограничивает его промышленное применение.
В изобретении [Patent CN106353390B at 25.06.2019. The method that electron beam irradiation prepares graphite oxide alkenyl enzyme-free glucose sensor / Inventor: Cheng L., Wang R., Jiang X., Hu Y. Current Assignee: University of Shanghai for Science and Technology - Application CN201610847831.1A. Priority date at 2016-09-24. - 8 p.] также предложен традиционный способ получения Оксид графен, путем окисления графита в смеси пероксидисульфата калия (K2S2O8) и пятиокиси фосфора (P2O5) в концентрированной серной кислоте до 80°С. Далее смесь охлаждают до комнатной температуре в течение 4,5 часа. Окисленный графит разбавляют, помещают в деионизированную воду на ночь, после фильтруют, промывают, полученный осадок сушат при 60°С в вакууме. К остатку после высушивания медленно добавляют к перманганат калия (KMnO4) в концентрированной серной кислоте в условиях: охлаждение в ледяной бани и перемешивание в течение 2 часов при температуре 35°С. Затем используется разбавление деионизированной водой и медленно добавляется 30% перекись водорода (H2O2).Также в этом изобретении предложен метод определения глюкозы путем ее окисления электронно-лучевым облучением без использования ферментов, в качестве датчика служит оксида графена / полианилина.
В изобретение [Patent CN102569736B at 29.04.2015. Carbon-coated graphene oxide composite material as well as preparation method and application thereof / Inventor: Zhou M., Pan J., Wang Y. Current Assignee: Oceans King Lighting Science and Technology Co Ltd etc. - Application CN201010616270.7A Priority date at 2010-12-30 - 10 p.] предложен композитный материал на основе оксида графена с углеродным покрытием, а также способ получения и применение композитного материала на основе оксида графена с углеродным покрытием. В качестве органического источника углерода может служить соединения сахарозы, полэтиленгликоля и глюкозного органического вещества. В этом изобретении получение оксида графена также включает этапы смешивания графитовый порошка, пероксидисульфата калия и пятиокись фосфора в концентрированной серной кислоте при 80°С. Затем охлаждение более 6 часов, повторное фильтрование, промывка до нейтрального pH и сушка. В высушенный образец при 0°С добавляют смесь концентрированной серной кислоте и перманганата калия и поддерживают температуру менее 20°C, затем, выдержав 2 часа на масляной бане при 35°C, медленно добавляют мл деионизированной воды, через 15 минут продолжайте добавлять 2,8 л деионизированной воды (где 50 мл содержат перекись водорода с концентрацией 30%), смесь приобретает цвет затем стекловидно-желтый цвет, вакуумная фильтрация в горячем состоянии. Композитный материал на основе оксида графена с покрытием из углерода, получают путем смешивания оксида графена и сахарозы, а затем нагревание смеси до пастообразного состояния; далее полученную пасту подвергают пиролиза составляет 300~600°С, а время 3~10 ч.
Как видно, в изобретении Patent CN102569736B дублируются технологические приемы, как и в Patent CN106353390B. Недостатком изобретений [Patent CN106353390B at 25.06.2019. The method that Electron Beam Irradiation prepares graphite oxide alkenyl enzyme-free glucose sensor / Inventor: Cheng L., Wang R., Jiang X., Hu Y. Current Assignee: University of Shanghai for Science and Technology - Application CN201610847831.1A. Priority date at 2016-09-24. - 8 p.; Patent CN102569736B at 29.04.2015. Carbon-coated graphene oxide composite material as well as preparation method and application thereof / Inventor: Zhou M., Pan J., Wang Y. Current Assignee: Oceans King Lighting Science and Technology Co Ltd etc. - Application CN201010616270.7A Priority date at 2010-12-30 - 10 p.] состоит в том, что: для получение твердого оксида графена требуется проведения дополнительных стадий фильтрования, промывания, вакуумная сушки продукта, использование сильных окислителей на основе 30% перекись водорода (H2O2), пероксидисульфата калия (K2S2O8) и перманганат калия (KMnO4), в концентрированной серной кислоты требует специальных мер предосторожностей.
Наиболее близким способом по технике является двухстадийный метод получения оксида графена [И.И. Кулакова, Г.В. Лисичкин. Химическое модифицирование графена // Журнал общей химии. - 2020. - Т. 90, №10. С.1601-1626.] без использования сильных окислителей - путем анодного окисления графита смесью серной и азотной кислот с микроволновым активированием процесса. С ростом напряжения выход окисленного продукта уменьшается, тогда как повышение плотности тока увеличивает массу конечного продукта продуктов. В то же время с повышением концентрации H2SO4 количество окисленного продукта и его выход в дисперсию увеличиваются, при этом сохраняется тенденция к снижению выхода с ростом напряжения. Использование высокого напряжения и плотности указывает, что основным окислителем в процессе получения оксида графена из графита является надсерная кислота (кислота Каро).
Недостатками данного способа являются:
- использование микроволнового активирования требует применения специального и дорогостоящего оборудования;
- побочные продукты возникающие в результате применения азотной кислоты, создает дополнительные сложности в очистке конечного продукта;
- отсутствие технологических данных для оценки степени электрохимической конверсии графита в оксид графена ставит под вопрос о масштабируемости технологии.
Прототипом является способ получения структур нанолистов оксида графена и/или оксида графита толщиной менее 100 нм в электрохимической ячейке. Причем способ включает стадию пропускания тока через ячейку с целью интеркаляции анионов в графитовый положительный электрод для отшелушивания графитового положительного электрода [Патент РФ №2691365C1 от 11.06.2019 г.Получение оксида графена // Абделькадер А., Кинлок И., Драйф Р. Заявка: RU2016118529A от 20.11.2014 -Бюл. №17. -59 с.] в результате чего электрохимическая интеркаляции, отшелушивание и окисление графита до оксида графена на положительном электроде происходит не в столь сильно коррозионных и/или окислительных условиях, как в обычных способах, а с электролитами, которые обеспечивают сравнительно менее коррозионную и/или окисляющую среду на графитовом аноде. Для проведения электрохимического процесса используется в смеси электролита, включающих различные органические и неорганические (цитрат, ацетат, нитрат, сульфат) анионы и катионы (Na+, Fe2+,, Fe3+, Al3+,Sn2+и Li+). Предпочтительная, чтобы плотность тока была в пределах 300 мА / см2. Авторами изобретения также обнаружено, что: при поддержании желаемых уровней окисления и использовании органических анионов (например, цитрат-/ацетат-ионов) для интеркаляции и отшелушивания анода можно получить оксид графена с подходящей толщиной (например, возможно получение оксида графена в один, два и/или несколько слоев; электрическое отшелушивание графитового анода с использованием органических анионов обеспечивает более постепенное и однородное вспучивание графита. Это, как полагают, является результатом менее агрессивной интеркаляции углеродсодержащих анионов в положительный электрод, вызванной положительным электродным потенциалом. Согласно наблюдениям авторов изобретения, такое менее агрессивное поведение означает, что структурные дефекты графита подвергаются менее энергичному воздействию интеркалирующих анионов, поэтому существует незначительная тенденция к разделению изолированных участков в графите с непропорциональной скоростью по сравнению с соседними анодными участками. Это, в свою очередь, означает, что существует менее локализованное механическое и/или окислительное напряжение, поэтому большие куски графита менее склонны отрываться от электрода прежде, чем может произойти более обширная интеркаляция/окисление/вспучивание анода в целом. Кроме того, полагают, что органические анионы (такие как цитрат) стабилизируют листы оксида графена после их формирования. Недостатками данного способа являются:
- необходимость проведения дополнительный стадий очистки для удаления различного сорта анионов и катионов, входящих в сложный состав смеси электролита. Особенно, сложно удалить полученного оксида графена - органические анионы и катионы (Fe2+,Fe3+, Al3+и Sn2+).
- использование сложного состава электролита достаточно удораживает технологию.
- электрохимический процесс протекает длительное время в течение 6-10 ч в расчете на несколько грамм (без учета времени на стадии очистки и промывки продукта), что ставит под вопрос его дальнейшее лабораторного и промышленного применения.
Задачей данного изобретение является разработка доступного для лабораторного и промышленного применения способа получения оксида графена из глюкозы, без использования токсичного перманганата калия, азотной кислоты и сильных неорганических окислителей.
Техническим результатом при осуществлении данного изобретения является разработка технологии получения оксида графена из глюкозы с использование двух стадий - химической и электрохимической. Указанный технический результат достигается тем, что процесс синтеза оксида графена осуществляется, путем химического и электрохимического окисления глюкозы в смеси пентаоксида фосфора (V), позволяющий проводить графитизацию и отшелушивания конечного продукта без дополнительного оборудования и применения токсичных и сильных неорганических окислителей, увеличить выход и снизить число стадий, требующихся для выделения и очистки конечного продукта.
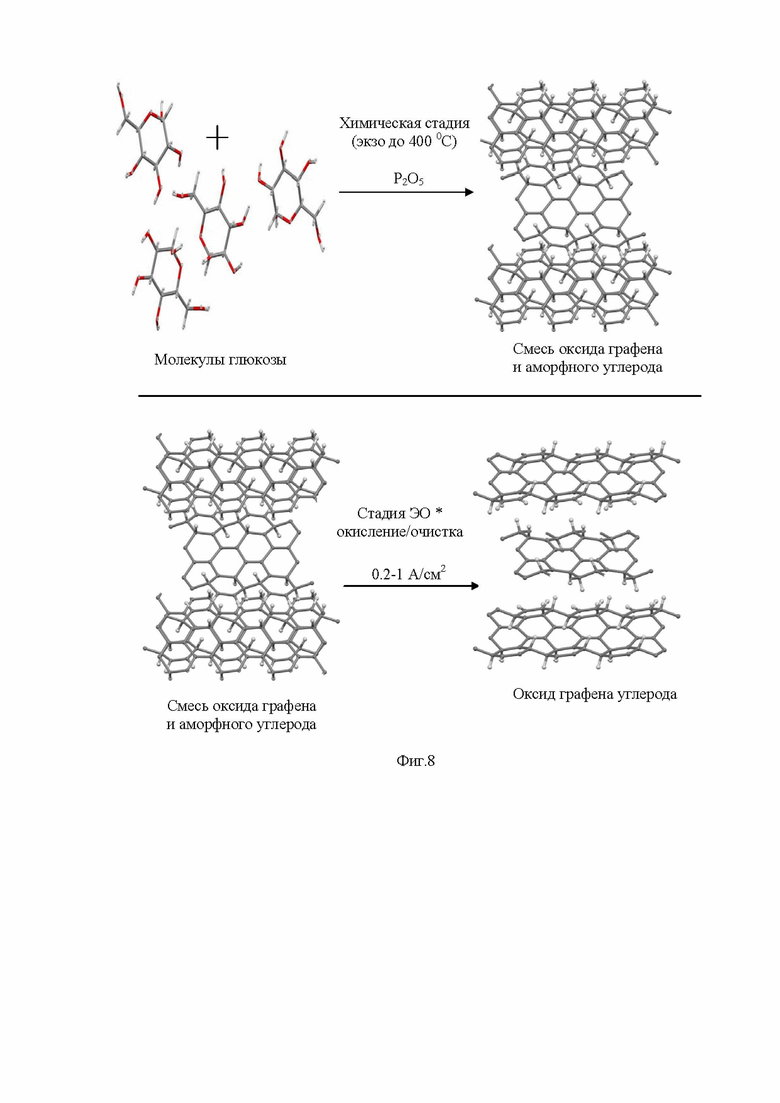
Сущность способа получения оксида графена из глюкозы состоит в том, что процесс их синтез осуществляется в две технологические стадии: вначале проводят процесс химическое окисления сырья в смеси пентаоксида фосфора (V) в экзотермическом режиме при температуре (до 450°С), в котором одновременно происходит происходит графитизация, окисление и отшелушивания чешуек оксида графена, затем в диафрагменном электролизере проводят электрохимическую стадию дополнительного окисления и очистки конечного продукта - оксида графена.
Сущность получения оксида графена из глюкозы поясняется примерами.
Пример 1. Процесс получения оксида графена проводили в две стадии - химического и электрохимического окисления из глюкозы. Для этого в колбу объемом 1,0 л вводили D-глюкозу (C6H12O6) и пентаоксида фосфора (V) (P2O5), где их смешивали в мольном соотношении 0,5÷0,5. Затем к полученной смеси добавляли 1% пероксида димезилата ((CH3S(O)2O)2). В результате добавления инициатора реакции - пероксида димезилата самопроизвольно протекала экзотермическая реакция графитизации, отшелушивания и химического окисления глюкозы. Температура реакции поднималась до 400°С. Отходящие газы в виде CO2 и сублимированного P2O5 пропускали и нейтрализовали в водном растворе хлорида кальция.
После охлаждения, полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера. Катодом служила стальная пластина или графит. В качестве электролита использовали 10,0 М водный раствор метансульфокислоты в котором проводили электролиз при плотности анодного тока 0,2 А/см2. Температуру электролиза поддерживали при 40-50°С, с перемешиванием на магнитной мешалки (400-600 об. мин) в течение 2-3 часов. По окончании электролиза продукт выделяли и помещали на керамический фильтр, затем его многократно промывали бидистилированной водой и сушили при температуре 80°С вначале при комнатной (30 мин), затем в вакуумном шакфу при низком давлении 10-15 кПа.
Выход оксида графена составил 64% масс.
Пример 2. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозу, где ее смешивали пентаоксида фосфора (V) при соотношении 0,6÷0,4 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,2 А/см2. Выделенный продукт выделяли, промывали и сушили по примеру 1.
Выход оксида графена составил 62% масс.
Пример 3. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозу, где ее смешивали пентаоксида фосфора (V) соотношении 0,7÷0,3 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,2 А/см2. Выделенный продукт выделяли, промывали и сушили по примеру 1.
Выход оксида графена составил 58% масс.
Пример 4. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозу, где ее смешивали пентаоксида фосфора (V) соотношении 0,8÷0,2 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,2 А/см2. Выделенный продукт выделяли, промывали и сушили по примеру 1.
Выход оксида графена составил 54% масс.
Пример 5. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозу, где ее смешивали пентаоксида фосфора (V) соотношении 4÷1 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,2 А/см2. Выделенный продукт промывали и сушили по примеру 1.
Выход оксида графена составил 48% масс.
Пример 6. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозы, где ее смешивали пентаоксида фосфора (V) соотношении 0,5÷0,5 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,5 А/см2. Выделенный продукт промывали и сушили по примеру 1.
Выход оксида графена составил 70% масс.
Пример 7. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозы, где ее смешивали пентаоксида фосфора (V) P2O5 соотношении 0,4÷0,6 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,5 А/см2. Выделенный продукт промывали и сушили по примеру 1.
Выход оксида графена составил 76% масс.
Пример 7. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозы, где ее смешивали пентаоксида фосфора (V) соотношении 0,3÷0,7 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,5 А/см2. Выделенный продукт промывали и сушили по примеру 1.
Выход оксида графена составил 88% масс.
Пример 8. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозы, где ее смешивали пентаоксида фосфора (V) соотношении 0,2÷0,8 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,5 А/см2. Выделенный продукт промывали и сушили по примеру 1.
Выход оксида графена составил 92% масс.
Пример 9. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозы, где ее смешивали пентаоксида фосфора (V) соотношении 0,1÷0,9 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 0,5 А/см2. Выделенный продукт промывали и сушили по примеру 1.
Выход оксида графена составил 91% масс.
Пример 10. Получение оксида графена проводили по примеру 1. Для этого в колбу объемом 1,0 л помещали D-глюкозы, где ее смешивали пентаоксида фосфора (V) соотношении 0,1÷0,9 и добавляли к полученной смеси до 1% пероксида димезилата. Затем полученную смесь высушивали и формовали в виде пластин, которые помещали в анодное отделение диафрагменного электролизера и проводили процесс аналогично примеру 1 при плотности анодного тока 1,0 А/см2. Выделенный продукт промывали и сушили по примеру 1.
Выход оксида графена составил 92% масс.
Количественное определение оксида графена проводилось методом центрифугирования. Для этого 1,0 г высушенный продукта после электролиза растворяли в 100,0 мл воды и помещали в цетрифужную пробирку. Далее процесс центрифугирования проводили при 15000 оборотах в течение 30 минут. По окончанию раствор разделяли на 2 части: вначале выделяли на бумажном фильтре углеродные частицы, которые были в виде дисперсии и плавали в водном растворе пробирки (оксид графена), затем выделяли и высушивали остаток углеродных частиц осевших на дно центрифужной пробирки (аморфный углерод). Полученные углеродные частицы взвешивали на аналитических весах.
Результаты выходов оксида графена представлены в таблице 1.
Из табл. 1 видно, что выход оксида графена с увеличением мольного соотношения C6H12O6 падает, а с увеличением плотности анодного тока растет.
Данные выходов оксида графена.
A/ cm2
Образование оксида графена подтверждено методами сканирующей электронной микроскопии, определение удельной поверхности по методу БЭТ, рентгеновской дифрактометрии, колебательной спектроскопии (комбинационного рассеивания света (КРС) и инфракрасной (ИК) Фурье спектроскопии).
На фиг. 1 представлены изображения оксида графена, снятые на сканирующем электронном микроскопе LEO- 1450 с микрозондовым анализатором ISYS с системой EDX (Carl-Zeiss SMT AG, Германия) при разрешениях: 30 мкм (фиг. 1.a), 10 мкм (фиг. 1.b), 1 мкм (фиг. 1.c) и 10 нм (фиг. 1.d). Морфология виде слоистых нанолистов представленная на фиг. 1 a и b характерна для полученного оксида графена. Структуры нанолистов полученного оксида графена имеют толщину менее 100 нм (фиг. 1.c и d).
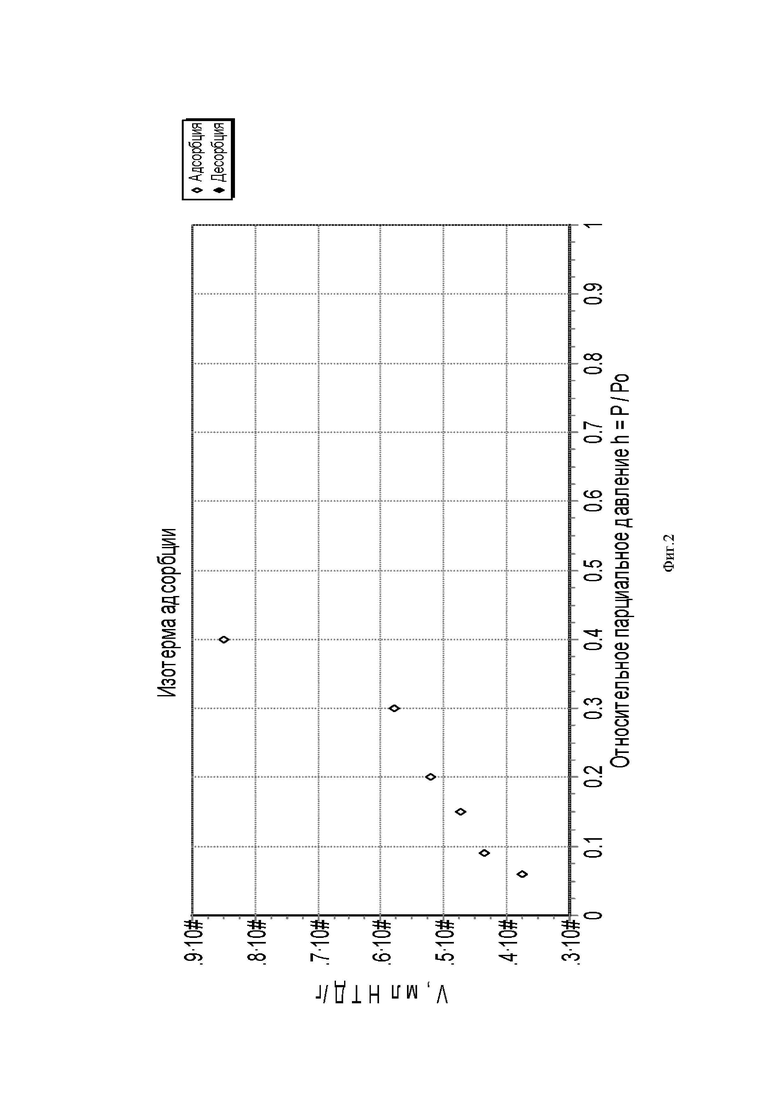
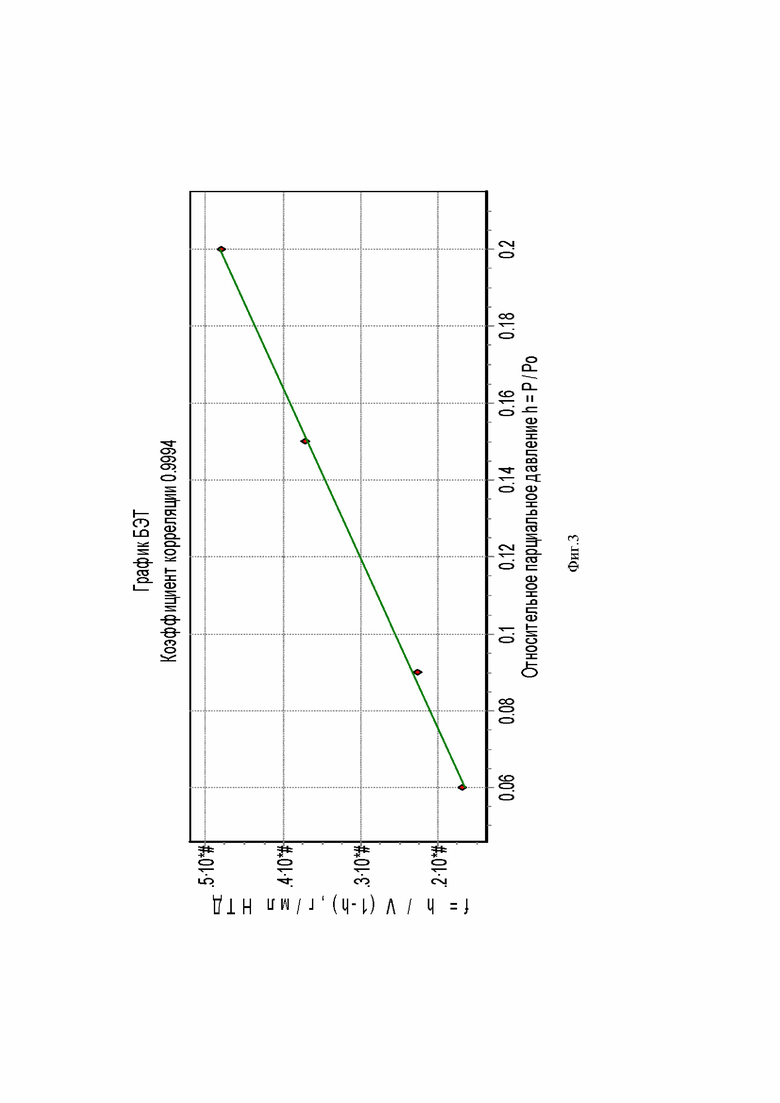
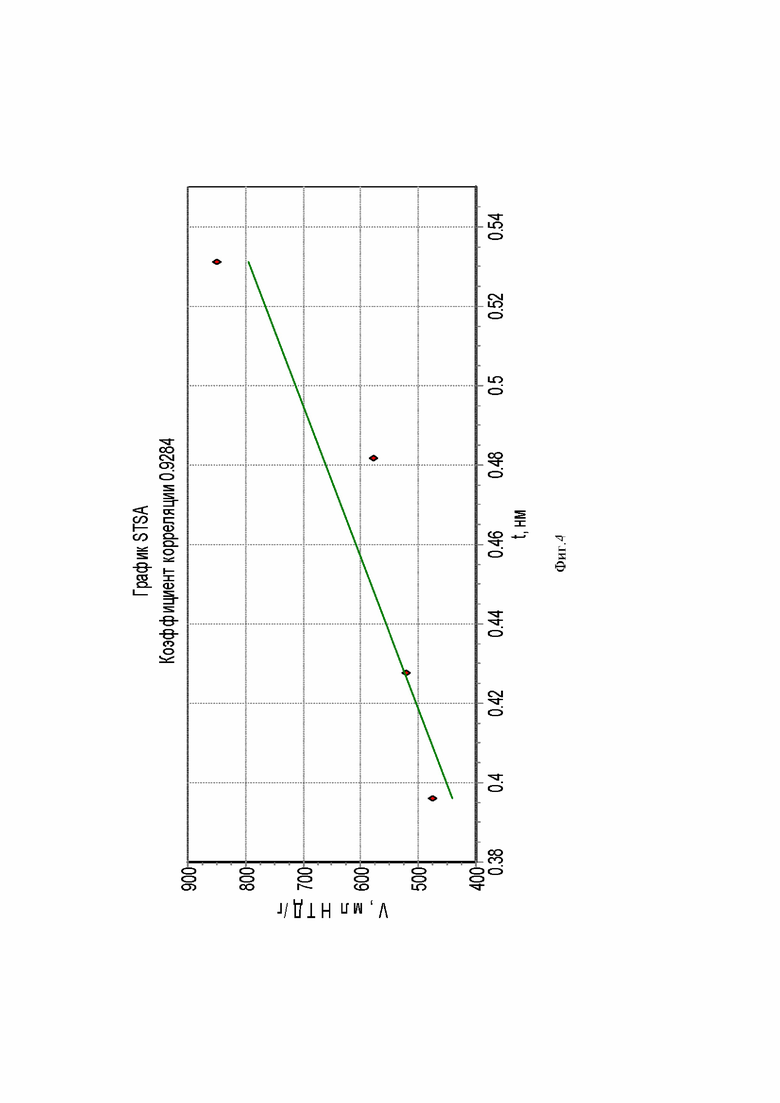
На фиг. 2 - фиг. 4 представлены зависимости изотермы адсорбции и график БЭТ, использованный для определения величина удельной поверхности (метод БЭТ) и удельная поверхность мезопор (метод STSA)
Удельная поверхность оксида графена (по методу БЭТ)
Удельная поверхность мезопор оксида графена (метод STSA)
Как видно из таблиц 2 и 3 полученный оксид графена имеет высокое значение удельной поверхности (1907.8±39.5 м2/г и удельная поверхности мезопор (4055.7±937.0 м2/г), что позволит использовать его для создания перспективных сорбционных (очистка и разделения веществ) и электродных материалов (для химических источников тока).
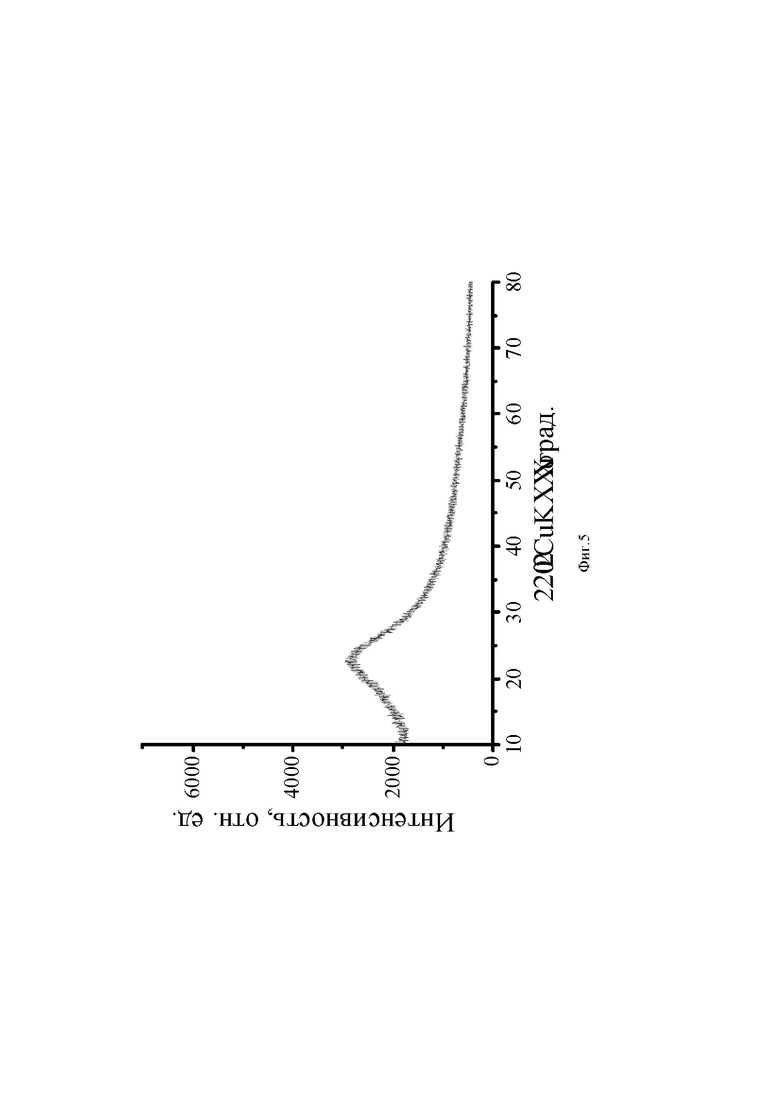
Представленное гало на порошковая дифрактограмме (фиг. 5), указывает, что исследуемый материал - двумерный с аморфной структурой, характерный для оксида графена.
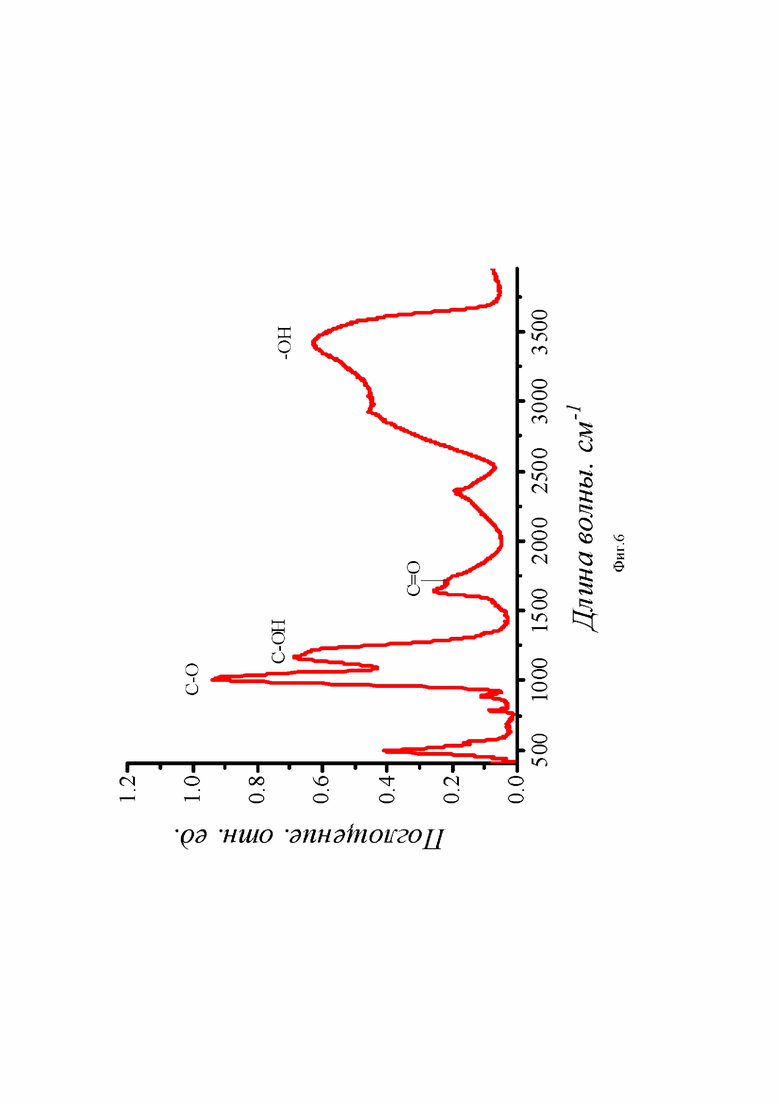
На фиг. 6 приведен ИК-Фурье спектр синтезированного оксида графена из глюкозы. Графитизация молекул глюкозы подтверждается появлением пика ИК-поглощения при 1610 см-1, соответствующего плоскостному колебанию С=O связи, характерному для sp2 -графитовых материалов. Кроме того, ИК-Фурье спектры показывают наличие кислородных функциональных групп в графитовой структуре, о чем свидетельствуют пики при 3300, 1700, 1200 и 1022 см-1, которые приписываются валентному колебанию интеркалированных свободных молекул H2O, С=O карбоксильных групп, эпокси С-О-С и алкокси С-О соответственно. О наличии связанных молекул Н2О также свидетельствуют пики при 1500, 1360 и 1295 см-1, обусловленные деформационными колебаниями -ОН-функциональные группы [Adel M., El-Maghraby A., El-Shazly O., El-Wahidy E.-W. F., Mohamed M.A.A. Synthesis of few-layer graphene-like nanosheets from glucose: New facile approach for graphene-like nanosheets large-scale production // Journal of Materials Research. - 2016. - V.31(04). P.455-467.].
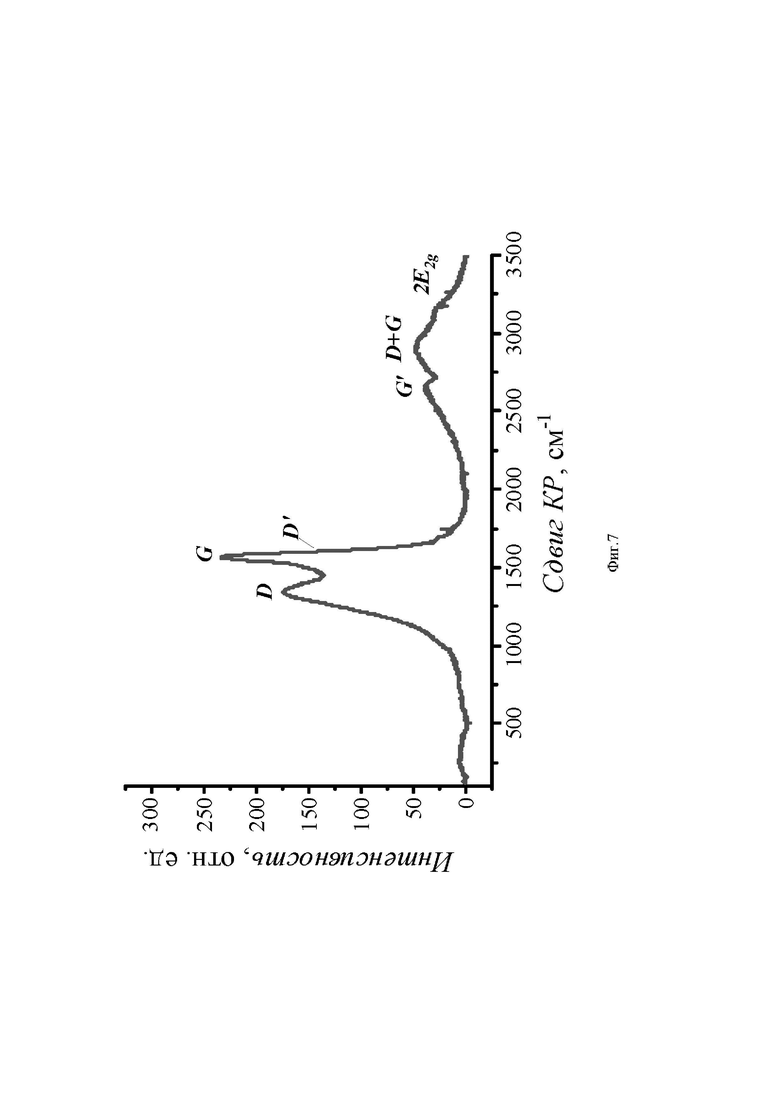
На фиг. 7 представлен КРС спектр углеродной системы. В спектрах КР УНТ обычно присутствуют три характерные полосы: G-мода тангенциального растяжения (1500-1600 см-1), D-мода (-1350 см-1) и моды радиального дыхания (RBMs) (100-400 см-1), в зависимости от (в зависимости от длины волны источника возбуждения). Однако в большинстве случаев более крупные МУНТ не показывают сигналов комбинационного рассеяния RBM.[Lehman J.H., Terrones M., Mansfield E., Hurst K. E., Meunier V. Evaluating the characteristics of multiwall carbon nanotubes //Carbon. - 2011. - V. 49(8). - P. 2581-2602.]. Положение их полосы G близко к положению графита (-1580 см-1). G-полоса характеризует углеродные связи в плоскости колебательной моды sp2 - данный параметр отображает степень кристаллизации материала. Полоса D представляет собой моду комбинационного рассеяния с двойным резонансом, которую можно понимать, как мера структурного беспорядка, возникающего из-за аморфного углерода и любых дефектов [Bokobza L., Bruneel J.-L., Couzi M. Raman spectroscopy as a tool for the analysis of carbon-based materials (highly oriented pyrolitic graphite, multilayer graphene and multiwall carbon nanotubes) and of some of their elastomeric composites // Vibrational Spectroscopy - 2014. - V. 74. - P.57-63]. Из фиг.7 также видно, что спектры первого порядка состоят из двух широких полос с центром при 1580 см-1 (включая неразрешенные полосы G и D’) и 1337 см-1. Подобно полосе D, D’ представляет собой колебательную моду двойного резонанса, вызванную беспорядком, дефектами или ионным интеркалированием между графитовыми стенками [Rao A.M., Richter E., Bandow S., Chase B., etc. Diameter-selective Raman scattering from vibrational modes in carbon nanotube // Science. - 1997. - V.275. - P.187-91.]. КР спектры второго порядка представляют 3 основные широкие полосы, из которых определяются (2D, D+G и 2D2). В частности, 2D-полоса теперь появляется как синглет из-за наличия некоторых дефектов ориентации и упаковки, приводящих к уширенной «дираковской» одиночной 2D-полосе [Pawlyta M., Rouzaud J.N., Duber S. Raman microspectroscopy characterization of carbon black: Spectral analysis and structural information // Carbon - 2015. - V. 84. - P.479-490.]. Комбинации D+G [Osswald S, Havel M, Gogotsi Y. Monitoring oxidation of multiwalled carbon nanotubes by Raman spectroscopy // J Raman Spectrosc. - 2007. - V.38(6). - P.728-36.], соответствует индуцированному дефектом процессу двойного резонанса «междолинного» рассеяния. Из рисунка (B) можно заметить, что положение линий D и G функционализированных нанотрубок смещено в сторону более высоких волновых чисел(~+9 cm-1). Кроме того, полосы G и D’ демонстрируют четкое разделение c ростом времени выдержки (времени функционализации).
На основании полученных данных физико-химического анализа предположен механизм образования оксида графена представлен на фиг. 8.
Таким образом, представленные выше данные физико-химического анализа подтверждают, что конечным продуктом в процессе двух стадийного -химического и электрохимического окисления из глюкозы в смеси пентаоксида фосфора является оксид графена.
Предложенный способ получения оксида графена путем двух стадий - химического и электрохимического окисления глюкозы в смеси пентаоксида фосфора обладает рядом преимуществ:
- используемые исходные вещества являются легко доступными для лабораторного и промышленного производства оксида графена;
- полученный оксид графена имеет высокую развитую удельную поверхность более 1000 см2 /г и толщину нанолистов менее 100 нм;
- повышение производительности и снижении многостадийности процесса происходит за счет отсутствия использования неорганических окислителей;
- высокая скорость окисления на первой химической стадии (1-5 мин) и второй электрохимической стадии (2-3 часа)
- отсутствие необходимости подвода тепла и других технологических приемов для получения продукта, за счет протекания экзотермической реакции.
- процесс получения может быть легко автоматизирован
- побочные продукты: ортофосфорная и метансульфокислота могут быть легко утилизированы, путем регенерации или использованы повторно в рецикл;
- способ является экологически безопасным за счет отсутствия токсичных и вредных веществ;
- относительно небольшие энергозатраты, за счет возможности получения конечного продукта при меньших плотностях тока (0,2-1,0 A/cм2).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ГРАФЕНА | 2018 |
|
RU2709594C1 |
| Способ масштабирования синтеза оксида графена | 2021 |
|
RU2783099C2 |
| ДИМЕТИЛДИСУЛЬФОПЕРОКСИД (ПЕРОКСИД ДИМЕЗИЛАТА) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2694545C1 |
| Способ получения электропроводящего гидрофильного аэрогеля на основе композита из графена и углеродных нанотрубок | 2017 |
|
RU2662484C2 |
| Способ получения наноструктурированного порошкового композита на основе графена и диоксида циркония с использованием уротропина | 2023 |
|
RU2812131C1 |
| Способ получения платинового композита на носителе из термически обработанного оксида графена | 2024 |
|
RU2827645C1 |
| Способ получения композита MnO/C | 2022 |
|
RU2792622C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГРАФЕНА | 2016 |
|
RU2657504C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГРАФЕНОСОДЕРЖАЩИХ МАТЕРИАЛОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2016 |
|
RU2648892C2 |
| Способ электрохимического получения наноразмерных частиц графита | 2024 |
|
RU2823291C1 |

Изобретение относится к получению оксида графена, который может быть использован в нанотехнологии и химической промышленности. Способ получения оксида графена из глюкозы включает две технологические стадии. Сначала проводят процесс химического синтеза оксида графена из смеси глюкозы с пентаоксидом фосфора (V) в экзотермическом режиме при температуре до 450°С, который включает графитизацию, окисление и отшелушивание чешуек. Затем осуществляют электрохимическую стадию окисления и очистки конечного продукта – оксида графена в диафрагменном электролизере при плотностях тока 0,2-1 А/см2. Смесь после первой стадии формуют в виде пластин и помещают в анодное отделение диафрагменного электролизера. В качестве катода используют стальную пластину или графит, а в качестве электролита – 10 М водный раствор метансульфокислоты. Температуру при электролизе поддерживают в диапазоне 40-50°С. Изобретение позволяет получить оксид графена из глюкозы без использования токсичного перманганата калия, азотной кислоты и сильных неорганических окислителей. 8 ил., 3 табл., 10 пр.
Способ получения оксида графена из глюкозы, включающий две технологические стадии: процесс химического синтеза оксида графена из смеси глюкозы с пентаоксидом фосфора (V) в экзотермическом режиме при температуре до 450°С, включающий графитизацию, окисление и отшелушивание чешуек, и электрохимическую стадию окисления и очистки конечного продукта - оксида графена в диафрагменном электролизере при плотностях тока 0,2-1 А/см2, при этом смесь после первой стадии формуют в виде пластин и помещают в анодное отделение диафрагменного электролизера, в качестве катода используют стальную пластину или графит, а в качестве электролита - 10 М водный раствор метансульфокислоты, температуру при электролизе поддерживают 40-50°С.
| ПОЛУЧЕНИЕ ОКСИДА ГРАФЕНА | 2014 |
|
RU2691365C1 |
| СПОСОБ СИНТЕЗА ОКСИДА ГРАФЕНА | 2018 |
|
RU2720780C2 |
| CN 106564891 A, 19.04.2017 | |||
| CN 106353390 B, 25.06.2019 | |||
| CN 102569736 B, 29.04.2015. | |||
Авторы
Даты
2023-05-29—Публикация
2022-07-19—Подача