Изобретение относится к химической промышленности, а именно, к способу разделения смеси замещенного бисфталоцианината лантанида и свободного фталоцианиного лиганда, конкретно, бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина.
Из литературы известно, что часто в процессе синтеза бисфталоцианинатов в качестве побочного продукта может образовываться свободный фталоцианин. Разделить данную смесь является достаточно затруднительным процессом и требует применение различных растворителей в качестве элюентов [Tikhomirova T., Nalimova K., Kerner A., Vashurin A., Znoyko S. Er (III) and Lu (III) complexes of 2(3), 9(10), 16(17), 23(24)-tetrakis-and 2,3,9,10,16, 17,23,24-octakis-[4-(1-methyl-1-phenylethyl)phenoxy]phthalocyaninato. Synthesis and spectroscopic properties // Porphyrin science by women: in 3 volumes. - 2019. - P. 613-621].
Известен способ разделения [Tran-Thi T. H., Mattioli T. A., Chabach D., De Cian A., Weiss R. Hole localization or delocalization? An optical, Raman, and redox study of lanthanide porphyrin-phthalocyanine sandwich-type heterocomplexes //The Journal of Physical Chemistry. - 1994. - V. 98. - №. 34. - P. 8279-8288] двухкомпонентной смеси, содержащей бисфталоцианинат гадолиния(III) и протонированную форму бисфталоцианината гадолиния(III). Данную систему невозможно разделить методом колоночной хроматографии. Для разделения предлагается использовать добавление к смеси гидразин-гидрата, позволяя перевести бисфталоцианиновый комплекс в восстановленную форму. Затем путем повторного окисления данной восстановленной формы с помощью перхлората железа(III) получают только бисфталоцианинат гадолиния(III). Подобная процедура позволяет исключить протонированный компонент, поэтому данный способ обеспечивает формирование в реакционной массе чистого бисфталоцианината гадолиния(III).
Недостатком данного способа является то, что с помощью него нельзя разделить смесь бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина, полученные в процессе синтеза.
Задачей изобретения является возможность эффективного разделения смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина колоночной хроматографией с применением одного растворителя, являющегося одновременно элюентом, что удешевляет и упрощает данный процесс.
Задача решена тем, что способ разделения смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина колоночной хроматографией характеризуется применением последовательного внесения восстановителя и окислителя в хроматографическую колонку, при этом перед началом проведения колоночной хроматографии на силикагеле с использованием хлороформа в качестве элюента в раствор смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина в хлороформе добавляют гидразин-гидрат в качестве восстановителя для перехода нейтрально-радикальной формы бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) в восстановленную форму, что также наглядно фиксируется путем изменения цвета с зеленого на сине-голубой, упрощая визуальный контроль процесса:
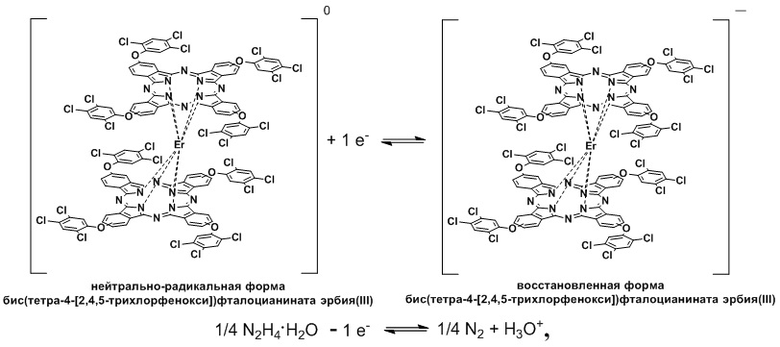
Полученный сине-голубой раствор вносят в хроматографическую колонку,
элюированием хлороформом легко выделяют тетра-4-(2,4,5-трихлорфенокси)фталоцианин в виде раствора в хлороформе, далее растворитель отгоняют, получая твердый тетра-4-(2,4,5-трихлорфенокси)фталоцианин, при этом остающийся на старте бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III) находится в восстановленной форме. Далее в хроматографическую колонку вносят раствор ацетилацетоната железа(III) в хлороформе для взаимодействия с бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинатом эрбия(III), образуя нейтрально-радикальную форму, что также наглядно фиксируют путем изменения цвета с сине-голубого на зеленый, упрощая визуальный контроль процесса:
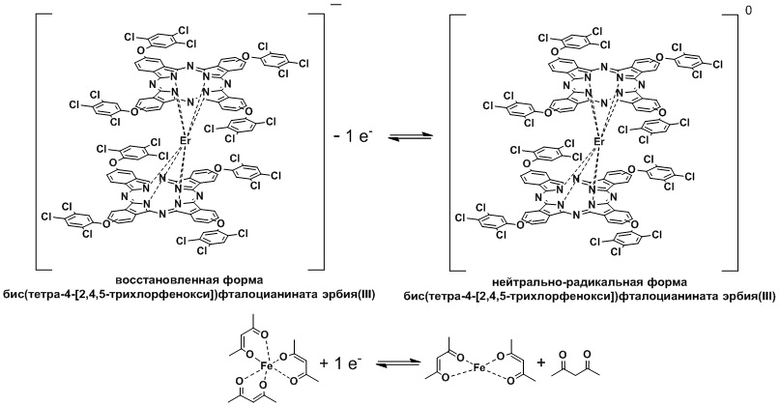
Элюированием хлороформом легко выделяют бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III) в виде раствора в хлороформе, далее растворитель отгоняют, получая твердый бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III). Таким образом достигают разделения смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина.
Изобретение позволяет получить следующие преимущества:
1) разделить бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианин.
2) применить один растворитель, являющийся одновременно элюентом, а именно хлороформ, что упрощает и удешевляет процесс.
3) визуализировать контроль процесса ввиду характерного окрашивания форм соединений.
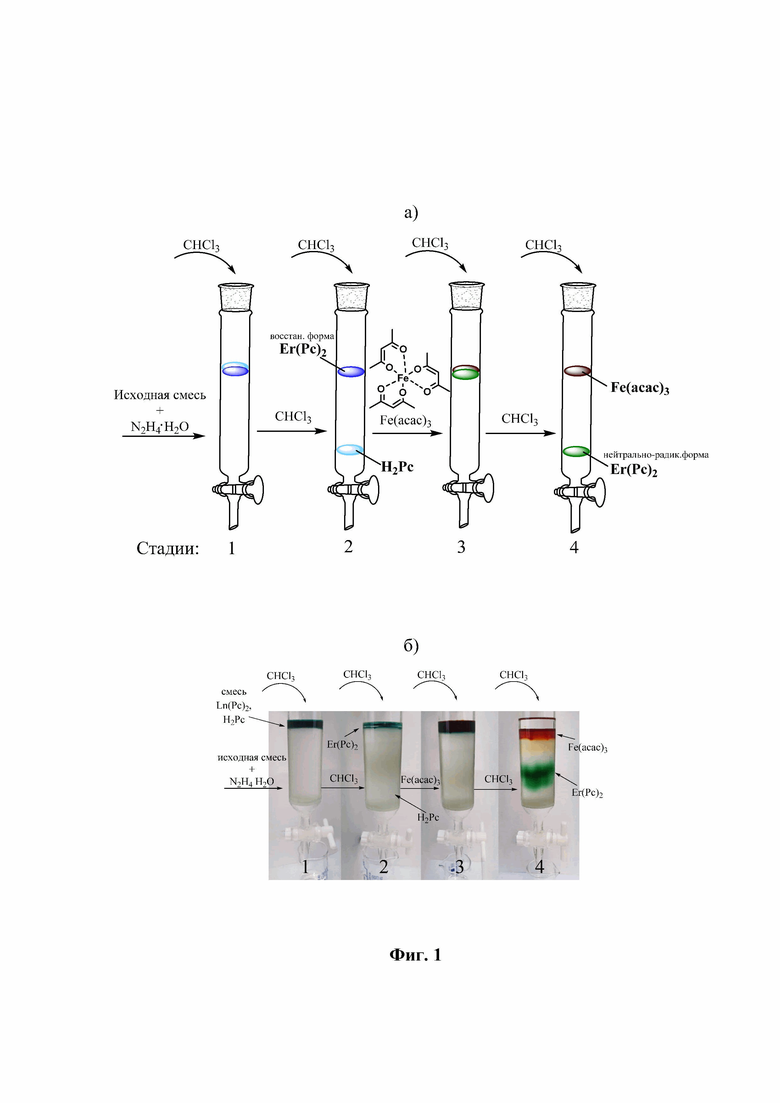
Изобретение поясняется чертежами. На фиг.1 изображена схема процесса колоночной хроматографии для разделения смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) (Er(Pc)2) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина (H2Pc): 1 - внесение исходной смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина с добавлением гидразин-гидрата в хроматографическую колонку, 2 - выделение из хроматографической колонки тетра-4-(2,4,5-трихлорфенокси)фталоцианина, элюируя хлороформом, 3 - внесение раствора ацетилацетоната железа(III) (Fe(acac)3) в хлороформе в хроматографическую колонку, 4 - выделение из хроматографической нейтрально-радикальной формы бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) (Er(Pc)2), элюируя хлороформом. На фиг.1б представлены реальные фотографии данного процесса. На фиг.2 - электронный спектр поглощения в хлороформе бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III); на фиг.3 - электронный спектр поглощения в хлороформе тетра-4-(2,4,5-трихлорфенокси)фталоцианина; на фиг.4 - MALDI-TOF масс-спектр бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III); на фиг.5 - MALDI-TOF масс-спектр тетра-4-(2,4,5-трихлорфенокси)фталоцианина; на фиг.6 - ИК-спектр бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III); на фиг.7 - ИК-спектр тетра-4-(2,4,5-трихлорфенокси)фталоцианина. На фиг.8 представлены электронный спектр поглощения (а) смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина в хлороформе и масс-спектр (б) смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина.
Для разделения смеси используют следующие вещества:
- хлороформ - ТУ 2631-066-44493179-01;
- гидразин-гидрат - ГОСТ 19503-88;
- силикагель - MachereyNagel M60;
- ацетилацетанат железа(III) - ТУ 6-09-4715-79.
Для получения смеси используются следующие вещества:
- 1,8-Диазабицикло[5.4.0]ундец-7-ен (Sigma-Aldrich, 98%)
- ацетилацетонат эрбия(III) (Sigma-Aldrich, 97%)
- изо-амиловой спирт (ТУ 2632-181-44493179-2014);
- этанол (ГОСТ Р 54267-2010)
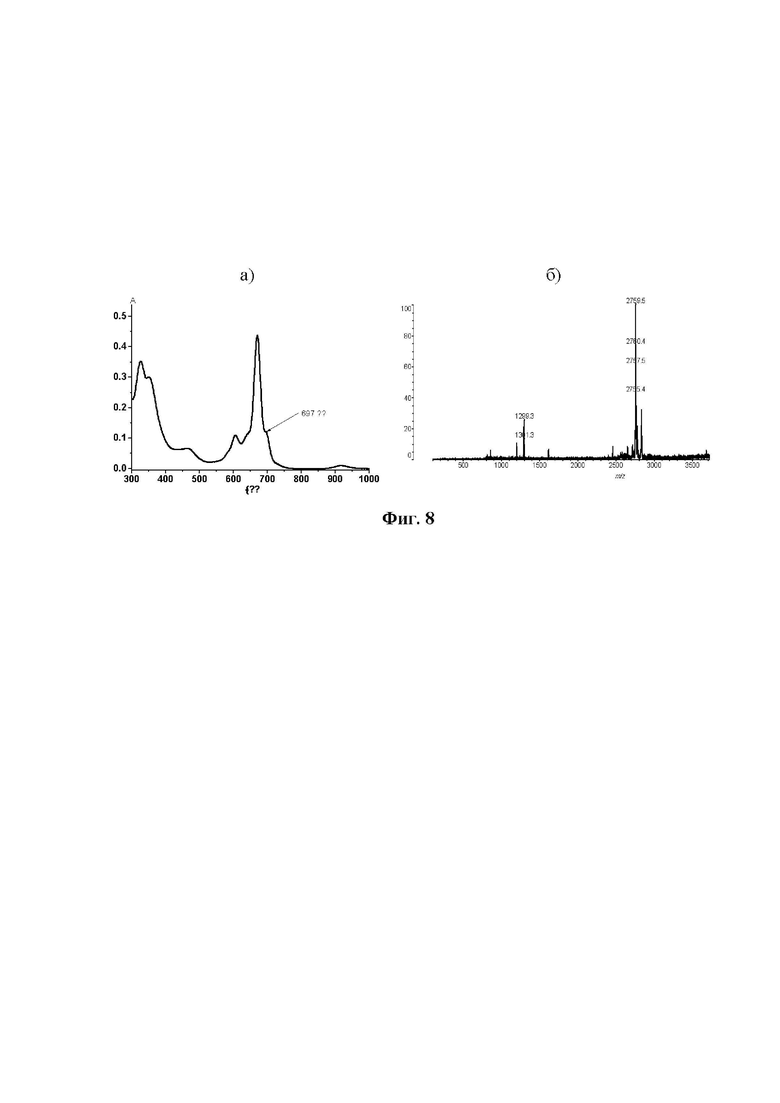
Получение бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) сопровождается примесью тетра-4-(2,4,5-трихлорфенокси)фталоцианина, что подтверждается электронным спектром поглощения (фиг.8а), что обусловлено наличием уширения в спектре при 697 нм, и масс-спектром (фиг.8б), что обусловлено наличием сигнала как бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) [M+H]+, а именно 2759,5, так и сигнала тетра-4-(2,4,5-трихлорфенокси)фталоцианина [M+3H]3+, а именно 1299,3.
Получение смеси проводят по следующей методике. Смесь 1.6 ммоль 2,4,5-трихлорфеноксифталонитрила, полученного согласно методике [Botnar A., Tikhomirova T., Nalimova K., Erzunov D., Razumov M., Vashurin A. Novel d-and f-metal phthalocyaninates based on 4-(2, 4, 5-trichlorophenoxy) phthalonitrile. Synthesis, spectroscopic and fluorescent properties //Journal of Molecular Structure. - 2020. - Т. 1205. - С.127626.], 0.8 ммоль ацетилацетоната эрбия(III), 1.3 ммоль 1,8-диазабицикло[5.4.0]ундец-7-ена и 10 мл изо-амилового спирта кипятят 12 ч, охлаждают и заливают смесью этанол:вода (4:1). Образовавшийся осадок отфильтровывают и промывают смесью этанол: вода (4:1) до прозрачных фильтратов. Целевой продукт экстрагируют хлороформом. Первичную очистку осуществляют колоночной хроматографией на силикагеле M60 с использованием хлороформа в качестве элюента.
Заявляемый способ разделения осуществляют следующим образом.
Пример 1.
В приготовленный раствор смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина, массой 0,001 г и 2,7 мл хлороформа, добавляют гидразин-гидрат объемом 50 мкл. При этом цвет раствора изменятся с зеленого на сине-голубой. Раствор выдерживают не менее 30 мин для того, чтобы полностью перевести нейтрально-радикальную форму бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) в восстановленную. В хроматографическую колонку диаметром 3 см вносят раствор силикагеля в хлороформе, при этом высота столба силикагеля составила 7,5 см. В колонку вносят сине-голубой раствор смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина. Элюируя хлороформ, выделяют тетра-4-(2,4,5-трихлорфенокси)фталоцианин в виде раствора в хлороформе, который отгоняют, получая твердый тетра-4-(2,4,5-трихлорфенокси)фталоцианин. Далее в колонку вносят приготовленный раствор ацетилацетоната железа(III), содержащий 0,1 г ацетилацетоната железа(III) и 2,7 мл хлороформа. В результате окислительно-восстановительной реакции восстановленная форма бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) переходит в нейтрально-радикальную форму. Элюируя хлороформом, выделяют нейтрально-радикальную форму бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) в виде раствора в хлороформе, который отгоняют, получая твердый бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III).
Разделенные с помощью предложенного способа соединения идентифицировали с помощью элементного анализа, спектроскопии поглощения, масс-спектрометрии, ИК-спектроскопии:
Бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III)
Выход: 92%.
Найдено, %: C 48.80; H 1.49, N 7.99.
Вычислено, %: C 48.82; H 1.46; N 8.13. C112H40Cl24ErN16О8.
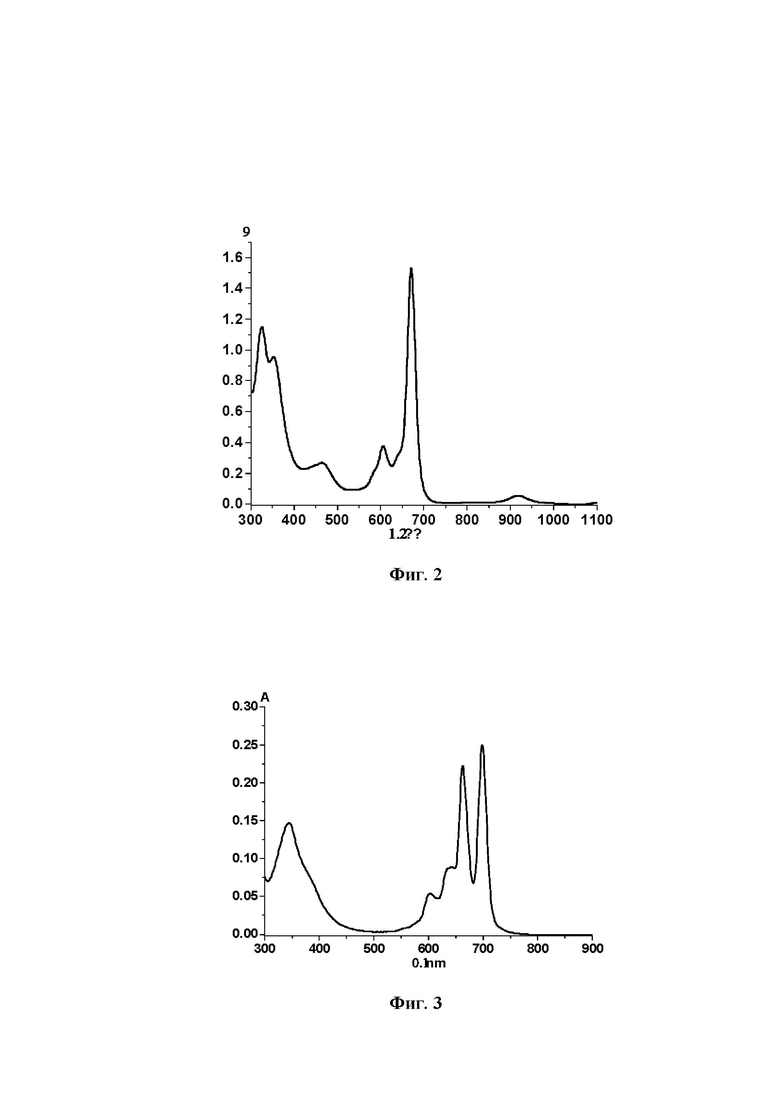
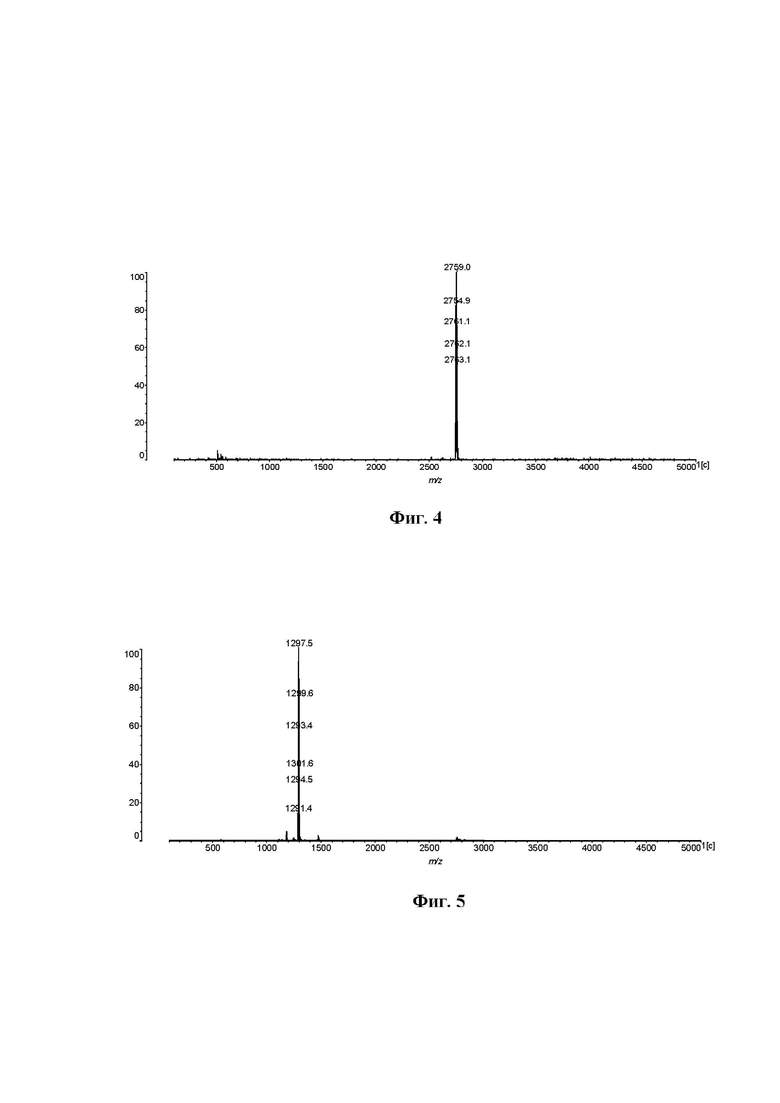
ЭСП в хлороформе, λmax, нм, 326, 353, 465, 606, 671, 918 (фиг.2). Масс-спектр (MALDI-TOF), m/z: 2759.0 [M+3Н]3+(фиг.4).
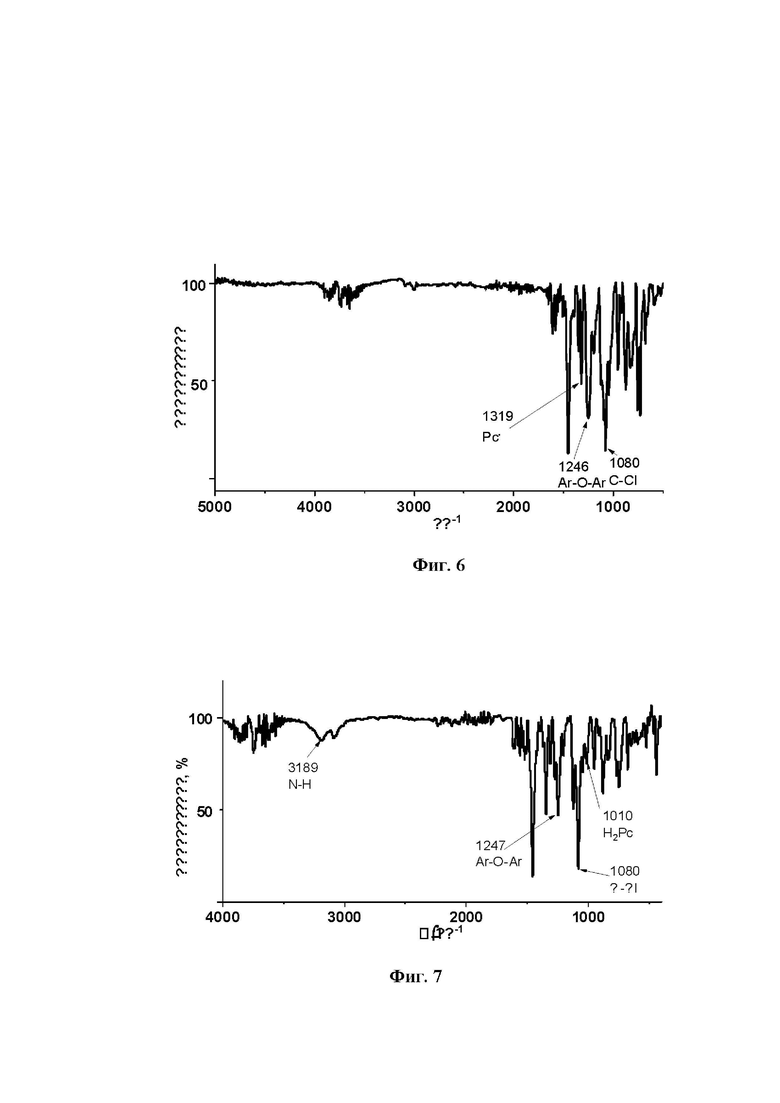
ИК-спектр, ν, см-1: 1080 (C-Cl), 1246 (Ar-O-Ar), 1319 (радикал Рс∙) (фиг.6).
Тетра-4-(2,4,5-трихлорфенокси)фталоцианин.
Выход: 8%.
Найдено, %: C 51.86; H 1.74, N 8.62.
Вычислено, %: C 51.89; H 1.71; N 8.64. C56H22Cl12N8О4.
ЭСП в хлороформе, λmax, нм, 344, 603, 663, 698 (фиг.3).
Масс-спектр (MALDI-TOF), m/z: 1297.5 [M+1Н]+(фиг.5).
ИК-спектр, ν, см-1: 1010 (H2Pc), 1080 (C-Cl), 1247 (Ar-O-Ar), 3189 (N-H) (фиг.7).
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕТРА-4-[4-(2,4,5-ТРИХЛОРФЕНОКСИ)]ФТАЛОЦИАНИН МЕДИ | 2017 |
|
RU2667915C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-(2,4,5-ТРИХЛОРФЕНОКСИ)ФТАЛОНИТРИЛА | 2017 |
|
RU2684113C1 |
| ТЕТРА-4-[4-(2,4,5-ТРИХЛОР-3,6-ДИСУЛЬФОФЕНОКСИ)]-ФТАЛОЦИАНИНЫ МЕДИ И КОБАЛЬТА | 2017 |
|
RU2659224C1 |
| ТЕТРА-4-[4'-(4''-МЕТИЛФЕНИЛАЗО)ФЕНОКСИ]ФТАЛОЦИАНИН | 2011 |
|
RU2454418C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ТЕТРА-(4-ТРЕТ-БУТИЛ-5-НИТРО)ФТАЛОЦИАНИНА | 2012 |
|
RU2507229C1 |
| ТЕТРА-4-(1-БЕНЗОТРИАЗОЛИЛ)ТЕТРА-5-[1(2)НАФТОКСИ]-ФТАЛОЦИАНИНЫ КОБАЛЬТА | 2015 |
|
RU2574064C1 |
| ТЕТРА-4-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]ТЕТРА-5-НИТРОФТАЛОЦИАНИНЫ КОБАЛЬТА И НИКЕЛЯ | 2016 |
|
RU2620270C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ТЕТРА-4-[(4'-КАРБОКСИ)ФЕНИЛАМИНО]ФТАЛОЦИАНИНА | 2011 |
|
RU2463324C1 |
| ГОМОГЕННЫЕ КАТАЛИЗАТОРЫ ОКИСЛЕНИЯ ДИАЛКИЛДИТИОКАРБАМАТОВ НА ОСНОВЕ ТЕТРА-4-(1-БЕНЗОТРИАЗОЛИЛ)-ТЕТРА-5-(СУЛЬФОНАФТОКСИ)ФТАЛОЦИАНИНОВ КОБАЛЬТА | 2015 |
|
RU2580323C1 |
| ТЕТРА-4-({4`-[(4"-ОКТИЛОКСИБЕНЗОИЛ)ОКСИ]БЕНЗОИЛ}ОКСИ)ФТАЛОЦИАНИН МЕДИ | 2006 |
|
RU2313545C1 |
Изобретение относится к химической промышленности, конкретно к способу разделения смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина. Способ характеризуется последовательным внесением восстановителя и окислителя в хроматографическую колонку, при этом перед началом проведения колоночной хроматографии на силикагеле с использованием хлороформа в качестве элюента в раствор смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина в хлороформе добавляют гидразин-гидрат в качестве восстановителя для перехода нейтрально-радикальной формы бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) в восстановленную форму и выдерживают не менее 30 минут. Восстановление нейтрально-радикальной формы наглядно фиксируется изменением цвета с зеленого на сине-голубой, упрощая визуальный контроль процесса. Полученный сине-голубой раствор вносят в хроматографическую колонку, элюированием хлороформом выделяют тетра-4-(2,4,5-трихлорфенокси)фталоцианин в виде раствора в хлороформе, далее растворитель отгоняют, получая твердый тетра-4-(2,4,5-трихлорфенокси)фталоцианин, при этом остающийся на старте бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III) находится в восстановленной форме. В хроматографическую колонку вносят раствор ацетилацетоната железа(III) в хлороформе для взаимодействия с бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинатом эрбия(III), образуя нейтрально-радикальную форму, что наглядно фиксируют путем изменения цвета с сине-голубого на зеленый. Элюированием хлороформом выделяют бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III) в виде раствора, далее растворитель отгоняют, получая твердый бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III). Техническим результатом изобретения является предоставление способа упрощенного и эффективного разделения смеси бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина колоночной хроматографией с применением одного растворителя, являющегося одновременно элюентом. 8 ил., 1 пр.
Способ разделения смеси бис(тетра-4-[2,4,5-трихлорфенокси]) фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина колоночной хроматографией, характеризующийся тем, что восстановитель и окислитель вносят поочередно, при этом перед началом проведения колоночной хроматографии на силикагеле с использованием хлороформа в качестве элюента в раствор смеси бис(тетра-4-[2,4,5-трихлорфенокси]) фталоцианината эрбия(III) и тетра-4-(2,4,5-трихлорфенокси)фталоцианина в хлороформе добавляют гидразин-гидрат в качестве восстановителя для перевода нейтрально-радикальной формы бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) в восстановленную форму, при этом раствор выдерживают не менее 30 мин для полного перехода нейтрально-радикальной в восстановленную форму:
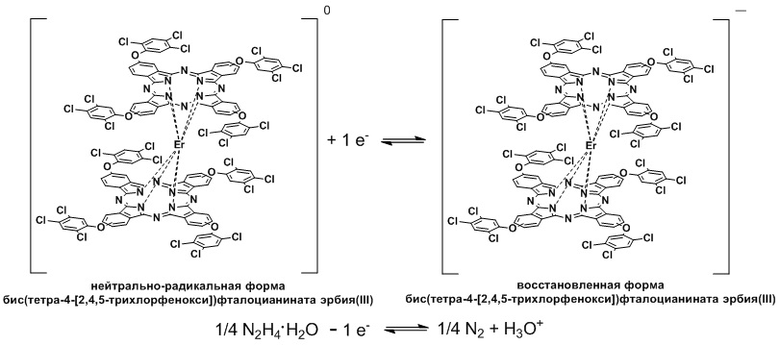
затем полученный сине-голубой раствор вносят в хроматографическую колонку, элюированием хлороформом из хроматографической колонки выделяют тетра-4-(2,4,5-трихлорфенокси)фталоцианин в виде раствора в хлороформе, далее растворитель отгоняют, получая твердый тетра-4-(2,4,5-трихлорфенокси)фталоцианин, при этом остающийся на старте бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III) находится в восстановленной форме, далее в хроматографическую колонку вносят раствор ацетилацетоната железа(III) в хлороформе, в качестве аниона используют ацетилацетонат для растворения в хлороформе и взаимодействия с бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинатом эрбия(III), и образования достаточно подвижной нейтрально-радикальной формы бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианината эрбия(III) зеленого цвета:
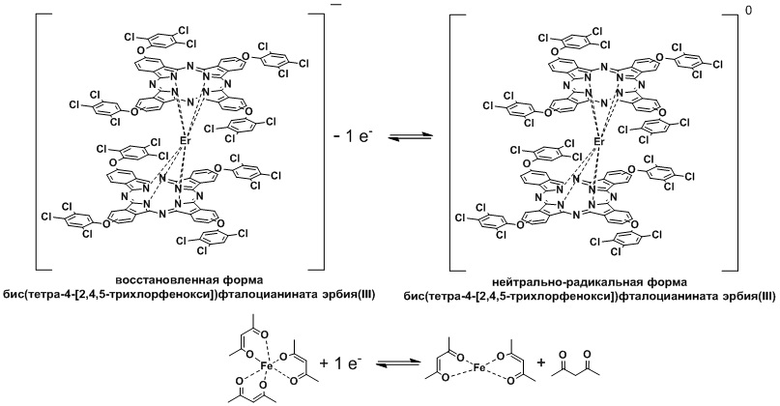
которую из хроматографической колонки элюированием хлороформом легко выделяют в виде раствора в хлороформе, далее растворитель отгоняют, получая твердый бис(тетра-4-[2,4,5-трихлорфенокси])фталоцианинат эрбия(III).
| Tran-Thi T | |||
| H., Mattioli T | |||
| A., Chabach D., De Cian A., Weiss R | |||
| Hole localization or delocalization? An optical, Raman, and redox study of lanthanide porphyrin-phthalocyanine sandwich-type heterocomplexes //The Journal of Physical Chemistry,1994, p | |||
| Химический огнетушитель | 1925 |
|
SU8279A1 |
| Tikhomirova T., Nalimova K., Kerner A., Vashurin A., Znoyko S | |||
| Er (III) and Lu (III) | |||
Авторы
Даты
2023-05-29—Публикация
2022-11-07—Подача