Изобретение относится к способу получения солей олова (IV) и может быть использовано в технологии материалов и изделий из керамики при получении простых и сложных оксидных соединений, в научных исследованиях и аналитическом контроле. В настоящее время водорастворимые соли олова (IV) находят все более широкое применение в качестве прекурсоров для синтеза методами «мокрой» химии наноразмерных порошков диоксида олова SnO2 и его сложных оксидных соединений - ортостаннатов, применяемых в технологии электропроводящей керамики различного назначения (Иванов В.В., Сидорак И.А., Шубин А.А., Денисова Л.Т. Получение порошков SnO2 разложением термически нестабильных соединений // Journal of Siberian Federal University. Engineering & Technologies. 2010. № 3. С. 189-213; Анисимов В.В., Сапрыкин А.В., Артемкина И.М., Макаров Н.А. Влияние анионного состава исходных солей на получение ортостанната цинка золь-гель методом // Стекло и керамика. 2021. № 4. С. 20-25). Описано использование SnCl4 для получения тонких пленок диоксида олова SnO2 (Gordillo G. et al. Preparation and characterization of SnO2 thin films deposited by spray pyrolysis from SnCl2 and SnCl4 precursors // Thin Solid Films. 1994. V. 252. №. 1. P. 61-66), который применяют в качестве просвечивающего и проводящего слоя в электронных приборах. Использование тонких пленок диоксида олова в качестве проводящего элемента при производстве устройств фотовольтаики приводит к повышению эффективности солнечного элемента.
Для промышленного применения, особенно в области получения керамических материалов, важно применять ресурсоэффективные способы их получения, обеспечивающие максимально достижимый выход целевого продукта, не требующие специальных условий реализации и не влекущие за собой применения в технологическом процессе реагентов либо образования побочных соединений, способных оказать негативное воздействие на здоровье человека или окружающую среду. Известные способы получения солей олова (IV) в основном заключаются в окислении металлического олова газообразным хлором до тетрахлорида олова и его дальнейшей химической переработке.
Известен способ получения тетрахлорида олова из металлического олова и газообразного хлора (Брауэр Г. Руководство по неорганическому синтезу. М.: Мир. 1985. С. 820-821). Через металлические гранулы олова пропускают газообразный хлор, отбирают полученный тетрахлорид олова в отдельный приемник. Авторами предложена установка из трех сосудов, один из которых следует опускать в воду для охлаждения. Основным недостатком данного способа является применение в качестве исходного реагента газообразного хлора. Помимо этого, получаемый данным способом тетрахлорид олова является безводным и требует дополнительной переработки для его применения в методах «мокрой» химии (золь-гель процесс, гетерофазное (со)осаждение и пр.).
Известен способ получения тетрахлорида олова из металлического гранулированного олова и газообразного хлора (Ключников Н.Г. Неорганический синтез. М.: Просвещение. 1988. 240 с.) в четырехколенной трубке при температуре 250-280°С. Недостатком метода является то, что он относится к лабораторным способам синтеза тетрахлорида олова, его масштабирование до промышленного использования затруднительно. Помимо этого, данный способ предполагает использование газообразного хлора и его нагрев, что влечет за собой использование реактора в коррозионно-стойком исполнении и котлонадзорного оборудования.
Известен способ получения тетрахлорида олова высокой чистоты, по которому металлическое олово подвергают взаимодействию с хлором при атмосферном давлении и 80-110°С в установке с обратным холодильником. Затем продукт очищают с отбором фракции чистого тетрахлорида олова высокотемпературной ректификацией. Синтез и очистку тетрахлорида олова выполняют в токе высокочистого аргона в оборудовании из высокочистого кварца. Недостатком данного метода, помимо использования газообразного хлора и его нагрева, является необходимость использования инертного благородного газа (аргона) для создания защитной среды.
Известен способ получения нитрата олова с химической формулой Sn(NO3)4 по реакции хлорида олова (IV) и пентаоксида азота (Коттон Ф., Уилкинсон Дж. Основы неоганической химии. М: Мир, 1979, 678 с.). Недостатками данного способа является то, что обозначенный метод не оформлен как технологический процесс с конкретным указанием диапазонов варьирования условий проведения, а также нет определенных сведений, в каком виде накапливается целевой продукт и как его можно выделить из получаемых реакционных смесей.
Известен способ получения нитрата олова (IV) RU 2655142 C1, который заключается в прямом взаимодействии оксида олова (IV) с азотной кислотой в растворе этилцеллозольва в бисерной мельнице со стеклянным бисером в качестве перетирающего агента при комнатной температуре. Основным недостатком предлагаемого способа является использование в качестве исходного вещества диоксида олова SnO2.
Известен способ получения ацетата олова (IV), по которому к раствору ацетата олова (II) в ледяной уксусной кислоте добавляют избыток пероксида водорода (Шапошник А.В., Сизаск Е.А., Корчагина С.Н., Звягин А.А., Рябцев С.В., Назаренко И.Н. Сенсорные свойства наноматериалов на основе диоксида олова по отношению к сероводороду // Сорбционные и хроматографические процессы. 2014. Т. 14. Вып. 4. С. 674-677.). Недостатками данного способа является то, что он не определен как способ ни с точки зрения реагентов, ни в плане получаемого продукта, ни по условиям проведения и аппаратурного оформления, а также то, что для его реализации требуется использование вещества, оборот которого в Российской Федерации ограничен и в отношении которого устанавливаются меры контроля.
Известен способ получения соли олова (IV) с анионами азотной и бензойной кислот RU2735433C1 путем окисления соответствующих солей олова (II) пероксидом водорода. В качестве исходного сырья для получения соли олова (IV) формулой Sn(NO3)2(OCOC6H5)2 выбран бензоат или нитрат олова (II), которые окисляют пероксидом водорода в присутствии азотной или соответственно бензойной кислоты при комнатной температуре в бисерной мельнице в присутствии перетирающего агента стеклянного бисера в уайт-спирите как базовом растворителе объемной фазы. Недостатками данного способа являются использование большого количества легколетучего легковоспламеняющегося растворителя и необходимость дополнительной технологической стадии по разделению водной и органической фаз реакционной смеси.
Наиболее близким к предлагаемому техническому решению является способ получения нитрата олова (IV) патент RU №2717810 C1 (прототип), который заключается в окислении нитрата олова (II) Sn(NO3)2 пероксидом водорода в присутствии азотной кислоты. Пероксид водорода используют в форме водного раствора с концентрацией 8-15%, который дозируют с избытком в отношении оловосодержащего восстановителя - нитрата олова (II). Азотную кислоту берут в виде 54%-ного водного раствора в мольном соотношении с восстановителем (2,05-2,40):1. Процесс проводят при комнатной температуре в бисерной мельнице со стеклянным бисером в качестве перетирающего агента в присутствии уайт-спирита как базового компонента объемной фазы.
Недостатками этого способа являются:
1. Необходимость отделения органической фазы после окончания технологического процесса.
2. Применение легколетучего легко воспламеняющегося органического растворителя - уайт-спирита, что требует дополнительных мер безопасности при проведении окислительно-восстановительной реакции.
3. Необходимость постоянного контроля за накоплением соли олова (IV) и расходованием соли олова (II).
Технической задачей предлагаемого изобретения является получение соли олова (IV) в форме устойчивого к гидролизу водного раствора в результате прямого взаимодействия соли олова (II) с окислителем в водной среде.
Поставленная задача решается путем разработки способа получения солей олова (IV) из солей олова (II), где в качестве исходного сырья для получения соли олова (IV) формулой SnX4 (X=Cl-, NO3-, CH3COO-) или Sn(SO4)2 выбрана соответствующая соль олова (II), которую подвергают прямому взаимодействию с окислителем в присутствии соответствующей кислоты (соляной или азотной или серной или уксусной) в установке с обратным холодильником, оборудованной перемешивающим устройством и дозатором для подачи окислителя, при этом соль олова (II) загружают в требуемом для дальнейшего использования количестве, а кислоту берут в форме водного раствора в мольном соотношении 2,5-2,8 относительно безводной загружаемой соли олова.
Полученные результаты подтверждаются примерами. При других условиях реализации способа технический результат не достигается.
Пример 1.
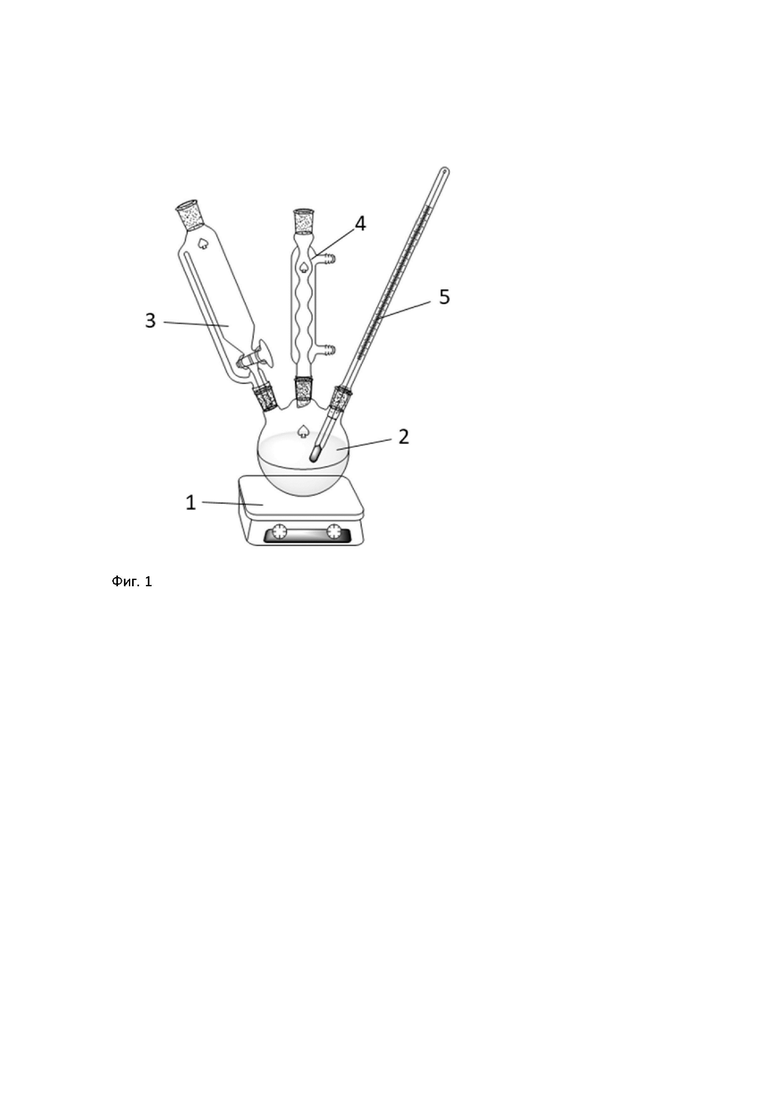
В реактор 2 загружают 100 мл водного раствора соляной кислоты (ч, ГОСТ 3118-77), подключают обратный холодильник 4 и при постоянном перемешивании перемешивающим устройством 1 вносят предварительно измельченный ручным или механическим способом олова (II) хлорид 2-водный (ч, ГОСТ 36-78) в количестве 100 г. Перемешивание ведут на холоду до полного растворения хлорида олова. Допускается подогрев реакционной смеси до 40-50°С для интенсификации процесса растворения, в этом случае после полного растворения хлорида олова нагрев выключают и охлаждают реакционную смесь до комнатной температуры. Контроль температуры реакционной смеси ведут термометром 4. Далее отмеряют 50 мл 37%-ного водного раствора пероксида водорода (ч, ГОСТ 177-88), который подают в реактор 2 дозатором 3 при постоянном перемешивании. Завершение реакции отслеживают по скачкообразному изменению окраски раствора.
По ходу процесса без прекращения перемешивания отбирают пробы реакционной смеси, которые сразу же анализируют на содержание соли олова (IV). Данные обозначенного текущего контроля позволяют получить временную зависимость достижения выхода соли олова (IV), приведенную в таблице 1.
Пример 2.
По примеру 1, отличающийся тем, что в качестве исходной соли олова (II) использовали специально приготовленный олова (II) нитрат.
Пример 3.
По примеру 1, отличающийся тем, что в качестве исходной соли олова (II) использовали олова (II) сульфат (ч, ТУ 2623-033-00205067-2003).
Пример 4
По примеру 1, отличающийся тем, что в качестве исходной соли олова (II) использовали олова (II) ацетат (95 %, Alfa Aesar, рег. номер CAS 638-39-1).
Пример 5
По примеру 1, отличающийся тем, что в качестве окислителя использовали смесь водных растворов азотной HNO3 (ГОСТ 4461-77) и соляной HCl (ГОСТ 3118-77) кислот, взятых в соотношении 1:3 по объему.
Данные обозначенного текущего контроля позволяют получить временную зависимость достижения выхода соли олова (IV), приведенную в таблице 2.
Положительный эффект предлагаемого решения состоит в том, что:
1. Предлагаемый процесс имеет высокие балансовые характеристики и обеспечивает практически полное расходование оловосодержащего реагента с достижением высокого процента перехода масс исходных реагентов в массу целевого продукта. При этом средние соли олова (II) гораздо более доступны в качестве реагентов для получения солей олова (IV).
2. Предлагаемый способ прост в исполнении и легко контролируется по ходу протекания, не требует специальных условий проведения и не сопровождается применением в технологическом процессе реагентов либо образованием побочных соединений, способных оказать негативное воздействие на здоровье человека или окружающую среду.
3. Конечный продукт образуется в виде устойчивого к гидролизу водного раствора соли олова (IV) заданной концентрации, пригодного для дальнейшей переработки методами «мокрой» химии (золь-гель процесс, гетерофазное (со)осаждение и пр.).
4. В предлагаемом решении ни природа аниона исходной соли олова (II), ни природа окислителя не имеет принципиального значения точки зрения аппаратурного оформления.
5. Процесс не осложнен применением реагентов, оборот которых в Российской Федерации ограничен и в отношении которых устанавливаются меры контроля.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения нитрата олова (IV) путем окисления нитрата олова (II) | 2019 |
|
RU2717810C1 |
| Способ получения соли олова (IV) с анионами азотной и бензойной кислот | 2020 |
|
RU2735433C1 |
| Способ получения хлорида олова (II) путем окисления металла | 2019 |
|
RU2717528C1 |
| Способ получения нитрата олова (II) при окислении металла | 2020 |
|
RU2744006C1 |
| Способ получения нитрата олова (IV) | 2017 |
|
RU2655142C1 |
| СПОСОБ ЭКСТРАКЦИОННОГО ВЫДЕЛЕНИЯ РАДИОНУКЛИДОВ ОЛОВА ИЗ РАСТВОРОВ МИНЕРАЛЬНЫХ И ОРГАНИЧЕСКИХ КИСЛОТ, А ТАКЖЕ ИХ СОЛЕЙ | 2008 |
|
RU2412907C2 |
| Способ получения основного нитрата олова (IV) Sn(OH)(NO) | 2017 |
|
RU2680065C1 |
| Двухстадийный способ получения карбоксилатов олова (II) из металла | 2017 |
|
RU2678092C1 |
| Способ получения бензоата и замещенных бензоатов олова (IV) из вторичного сырья | 2017 |
|
RU2673470C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОГО ХЛОРИДА ИЛИ НИТРАТА МЕДИ (II) | 2011 |
|
RU2476380C1 |
Изобретение относится к химической промышленности и может быть использовано в производстве керамических материалов и изделий, в научных исследованиях, в аналитической химии, при изготовлении электронных приборов, устройств фотовольтаики и солнечных элементов. Соль олова (II) окисляют в водной среде без применения органического растворителя прямым взаимодействием со смесью 65-68%-ной азотной HNO3 и 32-35%-ной соляной HCl кислот в объёмном соотношении 1:3 или 37%-ным водным раствором пероксида водорода в присутствии соляной HCl, или азотной HNO3, или серной H2SO4, или уксусной CH3COOH кислот. Изобретение позволяет упростить процесс получения соли олова (IV) в виде устойчивого к гидролизу водного раствора и обеспечить практически полный переход массы исходного реагента в массу целевого продукта. 1 ил., 2 табл., 5 пр.
Способ получения соли олова (IV) из солей олова (II), отличающийся тем, что окисление соли олова (II) проводят в водной среде без применения органического растворителя прямым взаимодействием со смесью 65-68%-ной азотной HNO3 и 32-35%-ной соляной HCl кислот в объёмном соотношении 1:3 или 37%-ным водным раствором пероксида водорода в присутствии соляной HCl, или азотной HNO3, или серной H2SO4, или уксусной CH3COOH кислот.
| Способ получения нитрата олова (IV) путем окисления нитрата олова (II) | 2019 |
|
RU2717810C1 |
| Способ получения нитрата олова (IV) | 2017 |
|
RU2655142C1 |
| Способ получения хлорида олова (II) путем окисления металла | 2019 |
|
RU2717528C1 |
| Способ получения соли олова (IV) с анионами азотной и бензойной кислот | 2020 |
|
RU2735433C1 |
| Способ получения нитрата олова (II) при окислении металла | 2020 |
|
RU2744006C1 |
| CN 102849789 A, 02.01.2013 | |||
| ЛАЗАРЕВ А.И | |||
| и др., Справочник химика-аналитика, Москва, Металлургия, 1976, с.с | |||
| Топливник с глухим подом | 1918 |
|
SU141A1 |
Авторы
Даты
2023-05-31—Публикация
2022-11-02—Подача