Родственные заявки
[0001] Данная заявка испрашивает приоритет по предварительной заявке США № 62/471937, поданной 15 марта 2017 года; и 62/475140, поданной 22 марта 2017 года; полное содержание каждой из которых включено в данный документ посредством ссылки.
Включение перечня последовательностей посредством ссылки
[0002] Данная заявка была подана вместе с перечнем последовательностей в электронном формате. Перечень последовательностей представлен в виде файла под названием «MRNA032001WO SequenceListing.txt», созданного 26 февраля 2018 года, размер которого составляет 715 байт. Информация в электронном формате перечня последовательностей полностью включена в данное описание посредством ссылки.
Область изобретения
[0003] Данное описание обеспечивает новые соединения, композиции, содержащие такие соединения, и способы, включающие применение композиций липидных наночастиц, для доставки одного или более терапевтических и/или профилактических средств для и/или продукции полипептидов в клетках или органах млекопитающих. В дополнение к новому липиду композиции липидных наночастиц по данному изобретению могут включать в себя один или более катионных и/или ионизируемых липидов, фосфолипидов, включая полиненасыщенные липиды, ПЭГ-липиды, структурные липиды и/или терапевтические и/или профилактические средства в определенных фракциях.
Уровень техники
[0004] Эффективная целевая доставка биологически активных веществ, таких как низкомолекулярные лекарственные средства, белки и нуклеиновые кислоты, представляет собой постоянную медицинскую проблему. В частности, доставка нуклеиновых кислот в клетки затруднена из-за относительной нестабильности и низкой проницаемости клеток таких частиц. Таким образом, существует необходимость в разработке способов и композиций для облегчения доставки терапевтических и/или профилактических средств, таких как нуклеиновые кислоты, в клетки.
[0005] Липидсодержащие композиции наночастиц, липосомы и липоплексы доказали свою эффективность в качестве транспортных средств в клетки и/или внутриклеточные компартменты для биологически активных веществ, таких как низкомолекулярные лекарственные средства, белки и нуклеиновые кислоты. Такие композиции обычно включают один или более «катионных» и/или амино (ионизируемых) липидов, фосфолипидов, включая полиненасыщенные липиды, структурные липиды (например, стерины) и/или липиды, содержащие полиэтиленгликоль (ПЭГ-липиды). Катионные и/или ионизируемые липиды включают, например, аминсодержащие липиды, которые могут быть легко протонированы. Хотя было продемонстрировано множество таких композиций липидсодержащих наночастиц, улучшения в области безопасности, эффективности и специфичности по-прежнему отсутствуют.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0006] В данном изобретении предложены новые соединения и композиции и способы, включающие их.
[0007] Первый аспект описания относится к соединениям формулы (I):

или их N-оксиду,
или их соли, или их таутомеру, где:
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ,
-CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из карбоцикла, гетероцикла, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -N(R)2, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и -C(R)N(R)2C(O)OR, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'', (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и
C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и
C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13.
[0008] Другой аспект данного изобретения относится к соединениям формулы (III):
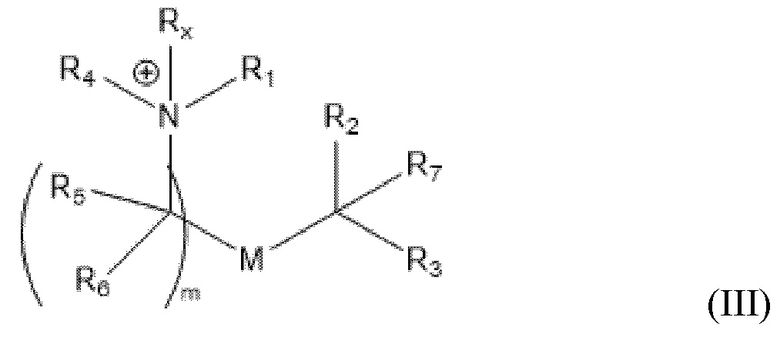
или их N-оксиду,
или их соли, или их таутомеру, где:
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ,
-CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из карбоцикла, гетероцикла, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -N(R)2, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и -C(R)N(R)2C(O)OR, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и
C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и
C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13.
[0009] В некоторых вариантах осуществления подмножество соединений формулы (I) включает соединения, в которых когда R4 представляет собой -(CH2)nQ, -(CH2)nCHQR, -CHQR, или CQ(R)2, тогда (i) Q не представляет собой -N(R)2, когда n равно 1, 2, 3, 4 или 5, или (ii) Q не представляет собой 5, 6 или 7-членный гетероциклоалкил, когда n равно 1 или 2.
[0010] Например, когда R4 представляет собо -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR или CQ(R)2, тогда (i) Q не представляет собой -N(R)2, когда n равно 1, 2, 3, 4 или 5, или (ii) Q не представляет собой 5, 6 или 7-членный гетероциклоалкил, когда n равно 1 или 2.
[0011] В других вариантах осуществления другое подмножество соединений формулы (I) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероарила, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -CRN(R)2C(O)OR, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и 5-14-членного гетероциклоалкила, имеющего один или более гетероатомов, выбранных из N, O и S, который замещен одним или более заместителями, выбранными из оксо (=O), OH, амино, моно- или ди-алкиламино и C1-3 алкила, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0012] В еще одних вариантах осуществления другое подмножество соединений формулы (I) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероцикла, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -CRN(R)2C(O)OR, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR, и -C(=NR9)N(R)2, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5; и когда Q представляет собой 5-14-членный гетероцикл и (i) R4 представляет собой -(CH2)nQ, в которой n равно 1 или 2, или (ii) R4 представляет собой -(CH2)nCHQR, в которой n равно 1, или (iii) R4 представляет собой CHQR и -CQ(R)2, тогда Q представляет собой как 5-14-членный гетероарил, так и 8-14-членный гетероциклоалкил;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0013] В еще одних вариантах реализации изобретения другое подмножество соединений формулы (I) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероарила, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -CRN(R)2C(O)OR, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR, причем каждый o независимо выбирают из 1, 2, 3 и 4 и -C(=NR9)N(R)2 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила,
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0014] В еще одних вариантах реализации изобретения другое подмножество соединений формулы (I) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ,
-CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из карбоцикла, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и -C(R)N(R)2C(O)OR, причем каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'', (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и
C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и
C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13.
[0015] В еще одних вариантах осуществления другое подмножество соединений формулы (I) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C2-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 представляет собой -(CH2)nQ или -(CH2)nCHQR, где Q представляет собой -N(R)2 и n выбирают из 3, 4 и 5;
каждый R5 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C1-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0016] В еще одних вариантах реализации изобретения другое подмножество соединений формулы (I) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из -(CH2)nQ, -(CH2)nCHQR, -CHQR и -CQ(R)2, где Q представляет собой -N(R)2 и n выбирают из 1, 2, 3, 4 и 5;
каждый R5 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C1-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0017] В некоторых вариантах осуществления подмножество соединений формулы (III) включает те, в которых, когда R4 представляет собой -(CH2)nQ, -(CH2)nCHQR, -CHQR, или CQ(R)2, тогда (i) Q не представляет собой -N(R)2 когда n равно 1, 2, 3, 4 или 5, или (ii) Q не представляет собой 5, 6 или 7-членный гетероциклоалкил, когда n равно 1 или 2.
[0018] В других вариантах осуществления другое подмножество соединений формулы (III) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероарила, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -CRN(R)2C(O)OR, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и 5-14-членного гетероциклоалкила, имеющего один или более гетероатомов, выбранных из N, O и S, который замещен одним или более заместителями, выбранными из оксо (=O), OH, амино, моно- или ди-алкиламино и C1-3 алкила, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0019] В еще одних вариантах осуществления другое подмножество соединений формулы (III) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероцикла, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -CRN(R)2C(O)OR, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR, и -C(=NR9)N(R)2, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5; и когда Q представляет собой 5-14-членный гетероцикл и (i) R4 представляет собой -(CH2)nQ, в которой n равно 1 или 2, или (ii) R4 представляет собой -(CH2)nCHQR, в которой n равно 1, или (iii) R4 представляет собой CHQR и -CQ(R)2, тогда Q представляет собой как 5-14-членный гетероарил, так и 8-14-членный гетероциклоалкил;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0020] В еще одних вариантах реализации изобретения другое подмножество соединений формулы (III) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероарила, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -CRN(R)2C(O)OR, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR, каждый o независимо выбирают из 1, 2, 3 и 4 и -C(=NR9)N(R)2, каждый o независимо выбирают из 1, 2, 3 и 4, и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0021] В еще одних вариантах реализации изобретения другое подмножество соединений формулы (III) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ,
-CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из карбоцикла, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и -C(R)N(R)2C(O)OR, причем каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'', (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и
C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и
C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13.
[0022] В еще одних вариантах осуществления другое подмножество соединений формулы (III) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C2-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 представляет собой -(CH2)nQ или -(CH2)nCHQR, где Q представляет собой -N(R)2 и n выбирают из 3, 4 и 5;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C1-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0023] В еще одних вариантах реализации изобретения другое подмножество соединений формулы (III) включает соединения, в которых
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из -(CH2)nQ, -(CH2)nCHQR, -CHQR и -CQ(R)2, где Q представляет собой -N(R)2 и n выбирают из 1, 2, 3, 4 и 5;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и C1-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13,
или их N-оксиды, или их соли, или их изомеры.
[0024] В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (IA):
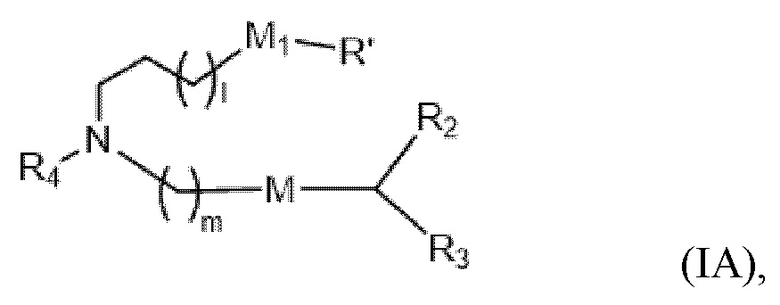
или их N-оксид, или их соль, или их изомер, где l выбирают из 1, 2, 3, 4 и 5; m выбирают из 5, 6, 7, 8 и 9; M1 представляет собой связь или M'; R4 представляет собой водород, незамещенный C1-3 алкил, -(CH2)oC(R10)2(CH2)n-oQ или -(CH2)nQ, в которой Q представляет собой OH, -NHC(S)N(R)2, -NHC(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)R8, -NHC(=NR9)N(R)2, -NHC(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR,
гетероарил или гетероциклоалкил; M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -P(O)(OR')O-, -S-S-, арильной группы и гетероарильной группы; и R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила и C2-14 алкенила. Например, m равно 5, 7 или 9. Например, Q представляет собой OH, -NHC(S)N(R)2 или -NHC(O)N(R)2. Например, Q представляет собой -N(R)C(O)R или -N(R)S(O)2R.
[0025] В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (IB):
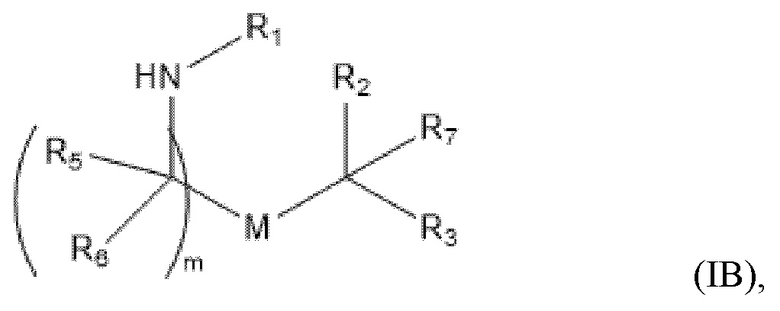
или их N-оксид, или их соль, или их изомер, в которых все переменные имеют значения, определенные в данном документе. Например, m выбирают из 5, 6, 7, 8 и 9; M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -P(O)(OR')O-, -S-S-, арильной группы и гетероарильной группы; и R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила и C2-14 алкенила. Например, m равно 5, 7 или 9.
[0026] В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (II):
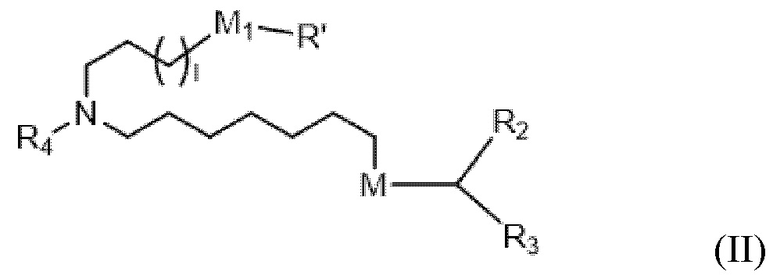
или их N-оксид, или их соль, или их изомер, причем l выбирают из 1, 2, 3, 4 и 5; M1 представляет собой связь или M'; R4 представляет собой водород, незамещенный C1-3 алкил, -(CH2)oC(R10)2(CH2)n-oQ или -(CH2)nQ, в которой n равно 2, 3 или 4 и Q представляет собой OH, -NHC(S)N(R)2, -NHC(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)R8, -NHC(=NR9)N(R)2, -NHC(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, гетероарил или гетероциклоалкил; M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -P(O)(OR')O-, -S-S-, арильной группы и гетероарильной группы; и R2 и R3 независимо выбирают из группы, состоящей из H, C1-1 алкила и C2-14 алкенила.
[0027] В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (IIa), (IIb), (IIc) или (IIe):
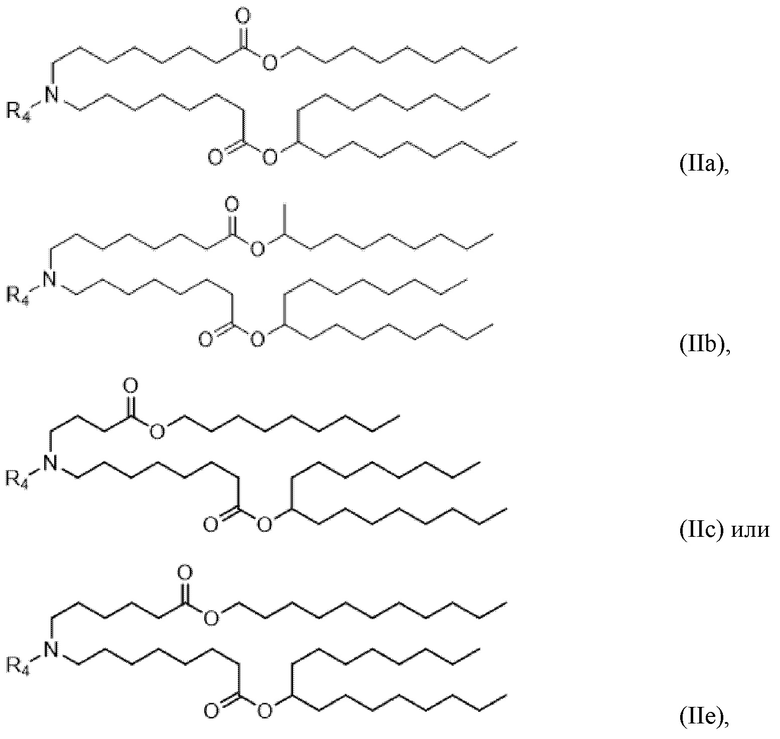
или их N-оксид, или их соль, или их изомер, где R4 соответствует описанию в данном документе.
[0028] В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (IId):

или их N-оксид, или их соль, или их изомер, где n равно, 2, 3 или 4; и m, R', R'' и от R2 до R6 описаны в данном документе. Например, каждый из R2 и R3 могут быть независимо выбраны из группы, состоящей из C5-14 алкила и C5-14 алкенила.
[0029] В другом варианте осуществления подмножество соединений формулы (I) включает соединения формулы (IIf):

или их N-оксид, или их соль, или их изомер, где n равно, 2, 3 или 4; и m, M, M'', R', R'' и от R2 до R6 описаны в данном документе. Например, каждый из R2 и R3 может незвисимо быть выбран из группы, состоящей из C5-14 алкила и C5-14 алкенила и n выбирают из 2, 3 и 4.
[0030] В другом варианте осуществления подмножество соединений формулы (I) включает соединения формулы (IIg):
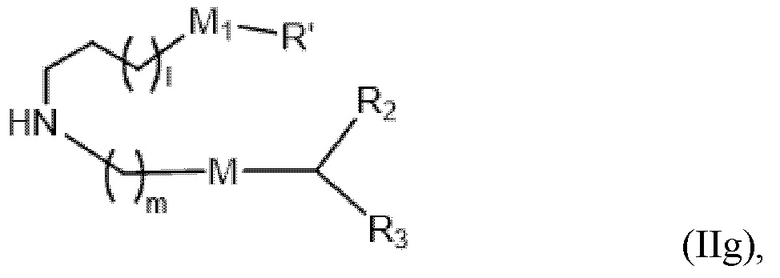
[0031] или их N-оксид, или их соль, или их изомер, где l, m, M, M1, R', R2 и R3 описаны в данном документе. Например, каждый из R2 и R3 может независимо быть выбран из группы, состоящей из C5-14 алкила и C5-14 алкенила, l выбирают из 1, 2, 3, 4 и 5 и m выбирают из 5, 6, 7, 8 и 9. В другом аспекте описание относится к композиции наночастиц, включающей липидный компонент, содержащей соединение, как описано в данном документе (например, соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III)).
[0032] В еще одном аспекте описание относится к фармацевтической композиции, содержащей композицию наночастиц в соответствии с предшествующими аспектами, и фармацевтически приемлемый носитель. Например, фармацевтическая композицию охлаждают или замораживают для хранения и/или отправки (например, хранится при температуре 4°C или ниже, например, при температуре около -150°C и между около 0°C или между около -80°C и около -20°C (например, около -5°C, -10°C, -15°C, -20°C, -25°C, -30°C, -40°C, -50°C, -60°C, -70°C, -80°C, -90°C, -130°C или -150°C). Например, фармацевтическая композиция представляет собой раствор, который держат в холодильнике для хранения и/или отправки, например, при около -20° C, -30°C, -40°C, -50°C, -60°C, -70°C, или -80°C.
[0033] В другом аспекте данное изобретение относится к способу доставки терапевтического и/или профилактического средства (например, мРНК) в клетку (например, клетку млекопитающего). Данный способ включает стадию введения субъекту (например, млекопитающему, такому как человек) композиции наночастиц, содержащих (i) липидный компонент, содержащий фосфолипид (такой как полиненасыщенный липид), ПЭГ-липид, структурный липид и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и (ii) терапевтическое и/или профилактическое средство, при котором введение включает в себя приведение в контакт клетки с композицией наночастиц, посредством чего терапевтическое и/или профилактическое средство доставляется в клетку.
[0034] В другом аспекте данное изобретение относится к способу получения интересующего полипептида в клетке (например, клетке млекопитающего). Способ включает стадию приведения в контакт клетки с композицией наночастиц, содержащей (i) липидный компонент, содержащий фосфолипид (такой как полиненасыщенный липид), ПЭГ-липид, структурный липид и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и (ii) мРНК, кодирующую интересующий полипептид, благодаря чему мРНК способна транслироваться в клетке с образованием полипептида.
[0035] В другом аспекте данное изобретение относится к способу лечения заболевания или расстройства у млекопитающего (например, человека), нуждающегося в этом. Способ включает стадию введения млекопитающему терапевтически эффективного количества композиции наночастиц, содержащей (i) липидный компонент, содержащий фосфолипид (такой как полиненасыщенный липид), ПЭГ-липид, структурный липид и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и (ii) терапевтическое и/или профилактическое средство (например, мРНК). В некоторых вариантах осуществления заболевание или расстройство характеризуется дисфункциональной или аберрантной активностью белка или полипептида. Например, заболевание или расстройство выбирают из группы, состоящей из редких заболеваний, инфекционных заболеваний, рака и пролиферативных заболеваний, генетических заболеваний (например, муковисцидоза), аутоиммунных заболеваний, диабета, нейродегенеративных заболеваний, сердечно-сосудистых и реноваскулярных заболеваний и заболеваний обмена веществ.
[0036] В другом аспекте данное изобретение относится к композиции наночастиц для применения при лечении заболевания или расстройства у млекопитающего (например, человека), нуждающегося в этом. Композиция наночастиц содержит (i) липидный компонент, содержащий фосфолипид (такой как полиненасыщенный липид), ПЭГ-липид, структурный липид и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и (ii) терапевтическое и/или профилактическое средство (например, мРНК). В некоторых вариантах осуществления заболевание или расстройство характеризуется дисфункциональной или аберрантной активностью белка или полипептида. Например, заболевание или расстройство выбирают из группы, состоящей из редких заболеваний, инфекционных заболеваний, рака и пролиферативных заболеваний, генетических заболеваний (например, муковисцидоза), аутоиммунных заболеваний, диабета, нейродегенеративных заболеваний, сердечно-сосудистых и реноваскулярных заболеваний и заболеваний обмена веществ.
[0037] В другом аспекте данное изобретение относится к композиции наночастиц для применения в изготовлении лекарственного средства при лечении заболевания или расстройства у млекопитающего (например, человека), нуждающегося в этом. Композиция наночастиц содержит (i) липидный компонент, содержащий фосфолипид (такой как полиненасыщенный липид), ПЭГ-липид, структурный липид и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и (ii) терапевтическое и/или профилактическое средство (например, мРНК). В некоторых вариантах осуществления заболевание или расстройство характеризуется дисфункциональной или аберрантной активностью белка или полипептида. Например, заболевание или расстройство выбирают из группы, состоящей из редких заболеваний, инфекционных заболеваний, рака и пролиферативных заболеваний, генетических заболеваний (например, муковисцидоза), аутоиммунных заболеваний, диабета, нейродегенеративных заболеваний, сердечно-сосудистых и реноваскулярных заболеваний и заболеваний обмена веществ.
[0038] В другом аспекте в данном изобретении предложена композиция наночастиц для применения в изготовлении лекарственного средства при лечении заболевания или расстройства у млекопитающего (например, человека), нуждающегося в этом. Композиция наночастиц содержит (i) липидный компонент, содержащий фосфолипид (такой как полиненасыщенный липид), ПЭГ-липид, структурный липид и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и (ii) терапевтическое и/или профилактическое средство (например, мРНК). В некоторых вариантах осуществления заболевание или расстройство характеризуется дисфункциональной или аберрантной активностью белка или полипептида. Например, заболевание или расстройство выбирают из группы, состоящей из редких заболеваний, инфекционных заболеваний, рака и пролиферативных заболеваний, генетических заболеваний (например, муковисцидоза), аутоиммунных заболеваний, диабета, нейродегенеративных заболеваний, сердечно-сосудистых и реноваскулярных заболеваний и заболеваний обмена веществ.
[0039] В другом аспекте данное изобретение относится к способу доставки (например, специфической доставки) терапевтического и/или профилактического средства в орган млекопитающего (например, в печень, селезенку, легкое или бедренную кость). Данный способ включает стадию введения субъекту (например, млекопитающему) композиции наночастиц, содержащую (i) липидный компонент, содержащий фосфолипид, ПЭГ-липид, структурный липид и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и (ii) терапевтическое и/или профилактическое средство (например, мРНК), при котором введение включает приведение в контакт клетки с композицией наночастиц, посредством чего терапевтическое и/или профилактическое средство доставляется в орган-мишень (например, печень, селезенку, легкое или бедренную кость).
[0040] В другом аспекте данное изобретение относится к способу улучшенной доставки терапевтического и/или профилактического средства (например, мРНК) в ткань-мишень (например, печень, селезенку, легкое или бедренную кость). Данный способ включает введение субъекту (например, млекопитающему) композиции наночастиц, причем данная композиция содержит (i) липидный компонент, содержащий соединение Формула(I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), фосфолипид, структурный липид и ПЭГ-липид; и (ii) терапевтическое и/или профилактическое средство, причем введение включает в себя приведение в контакт ткани-мишени с композицией наночастиц, посредством чего терапевтическое и/или профилактическое средство доставляется в ткань-мишень.
[0041] В еще одном аспекте данное изобретение относится к способу снижения иммуногенности, включающему введение композиции наночастиц по данному изобретению в клетки, причем композиция наночастиц уменьшает индукцию клеточного иммунного ответа клеток на композицию наночастиц по сравнению с индукцией клеточного иммунного ответа в клетках, вызванного контрольной композицией, которая содержит контрольный липид вместо соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III). Например, клеточный иммунный ответ представляет собой врожденный иммунный ответ, адаптивный иммунный ответ или их оба.
[0042] Данное описание также включает способы синтеза соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) и способы получения композиции наночастиц, включающих липидный компонент, содержащий соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III).
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0043] На Фиг. 1 представлены результаты предварительного лечения приматов, не являющихся человеком, метотрексатом или дексаметазоном до введения композиции наночастиц, содержащих MC3.
[0044] На Фиг. 2 продемонстрирована экспрессия мРНК hEPO, измеренная после внутривенного введения различных композиций наночастиц в дозе 0,01 мг/кг при 60-минутной инфузии наивным яванским макакам.
[0045] На Фиг. 3-6 продемонстрированы, соответственно, результаты экспрессии hEPO, измеренные при внутривенном введении крысам в различных дозах различных композиций наночастиц, содержащих соединения 26, 18, 25 и MC3.
[0046] На Фиг. 7 продемонстрирована площадь под кривой (AUC) для композиций наночастиц, содержащих соединения 18, 25 и 26 и MC3, в различных дозах от 0,005 мг/кг до 2 мг/кг.
[0047] На Фиг. 8 продемонстрированы результаты экспрессии люциферазы, измеренные при внутримышечном введении мышам различных композиций наночастиц, содержащих MC3, соединения 168-170 и 173-175 в дозе 0,01 мг/кг в различные временные точки: 3 часа (левый блок), 6 часов (средний блок) и 24 часа (правый блок). Числа 1-7 на этой фигуре соответствуют MC3, соединениям 168-170 и 173-175 соответственно.
[0048] На Фиг. 9 продемонстрированы результаты экспрессии hEPO, измеренные при внутримышечном введении мышам различных композиций наночастиц, содержащих MC3, соединения 18, 25, 30, 108-112, 60 и 122 в дозе 0,01 мг/кг в различные временные точки: 3 часа (левый блок), 6 часов (средний блок) и 24 часа (правый блок). Числа 1-11 на этой фигуре соответствуют MC3, соединениям 18, 25, 30, 108-112, 60 и 122 соответственно.
[0049] На Фиг. 10 продемонстрированы результаты экспрессии люциферазы (общий поток), измеренные при внутривенном введении различных композиций наночастиц, содержащих MC3 или различные соединения, раскрытые в данном документе. Числа 1-12 на этой фигуре соответствуют соединению 18, МС3, соединениям 48-50, 54, 111, 60, 75, 68, 66, 128, 65, 130, 133-135, 147, 96 и 151 соответственно.
[0050] На Фиг. 11А и 11В продемонстрированы результаты экспрессии антитела против НА (антитело против гемагглютинина), измеренные после внутривенного введения различных композиций наночастиц, содержащих МС3 и соединение 18, в дозе 0,1 мг/кг (Фиг. 11А) или 0,3 мг/кг (Фиг. 11В) посредством 60 минутной инфузии наивным яванским макакам.
[0051] Фиг. 12А-12С представляют собой серию графиков, демонстрирующих уровни экспрессии люциферазы через 3ч (Фиг. 12А), 6ч (Фиг. 12В) и 24 ч (Фиг. 12С) после внутривенного введения мышам композиций наночастиц, содержащих соединения по изобретению. Значения общего потока были получены с помощью люминесцентной визуализации тела (BLI). На этих фигурах числа 1-14 относятся к композициям, содержащим соединения 160, 98, 161-165, 171, 172, 183-186 и MC3 соответственно.
[0052] Фиг. 13А-13С представляют собой серию графиков, демонстрирующих уровни экспрессии люциферазы через 3ч (Фиг. 13А), 6ч (Фиг. 13В) и 24 ч (Фиг. 13С) после внутривенного введения мышам композиций наночастиц, содержащих соединения по изобретению. Значения общего потока были получены с помощью люминесцентной визуализации тела (BLI). PBS (натрий-фосфатный буфер) использовали в качестве контроля. Результаты представлены на логарифмической шкале. На этих фигурах числа 1-15 относятся к композициям, содержащим MC3, соединения 18, 111, 168-170, 174, 175, 178, 179, 181, 182, 218, 198 и PBS соответственно.
[0053] Фиг. 14А-14С представляют собой серию графиков, демонстрирующих уровни экспрессии люциферазы в печени (Фиг. 14А) селезенке (Фиг. 14В) и почке (Фиг. 14С), ex vivo, через 6 ч после внутривенного введения мышам композиций наночастиц, содержащих соединения по изобретению. Значения общего потока были получены с помощью люминесцентной визуализации тела (BLI). PBS (натрий-фосфатный буфер) использовали в качестве контроля. На этих фигурах числа 1-15 относятся к композициям, содержащим MC3, соединения 18, 111, 168-170, 174, 175, 178, 179, 181, 182, 218, 198 и PBS соответственно.
[0054] Фиг. 15А и 15В представляют собой пару графиков, демонстрирующих частоты активированных В-клеток в селезенке мышей CD-1, которым вводили соединения по изобретению, по сравнению с МС3 и по сравнению с мышами, не получавшими никакого лечения (наивный испытуемый субъект). PBS использовали в качестве контроля. На Фиг. 15А показан процент клеток CD19+. На Фиг. 15B показан процент клеток CD19+ CD69+ CD86+. Числа 1-16, относящиеся к композициям, содержащим мРНК, экспрессирующую люциферазу, являются следующими: 1: MC3, 2: Соединение 18, 3: Соединение 111, 4: Соединение 168, 5: Соединение 169, 6: Соединение 170, 7: Соединение 174, 8: Соединение 175, 9: Соединение 178, 10: Соединение 179, 11: Соединение 181, 12: Соединение 182, 13: Соединение 218, 14: Соединение 198, 15: PBS, 16: лечение наивного субъекта.
[0055] Фиг. 16А и 16В представляют собой пару графиков, демонстрирующих частоты активированных В-клеток в селезенке мышей CD-1, которым вводили соединения по изобретению, по сравнению с МС3 и по сравнению с мышами, не получавшими никакого лечения (наивный испытуемый субъект). PBS использовали в качестве контроля. На Фиг. 16А показан процент клеток CD19+. На Фиг. 16B показан процент клеток CD19+ CD69+ CD86+. Числа 1-14, относящиеся к композициям, содержащим мРНК, экспрессирующую люциферазу и являются следующими: 1: Соединение 147, 2: Соединение 184, 3: Соединение 232, 4: Соединение 189, 5: Соединение 200, 6: Соединение 233, 7: Соединение 234, 8: Соединение 235, 9: Соединение 237, 10: Соединение 239, 11: Соединение 243, 12: MC3; 13: PBS, 14: лечение наивного субъекта.
[0056] Фиг. 17 представляет собой график, демонстрирующий экспрессию мРНК hEPO у мышей CD1, измеренную через 3 часа (левый блок), 6 часов (средний блок) и 24 часа (правый блок) после внутривенного введения различных композиций наночастиц. Числа 1-13, относящиеся к композициям, содержащим мРНК, экспрессирующую hEPO и являются следующими: 1: Соединение 147, 2: Соединение 184, 3: Соединение 232, 4: Соединение 189, 5: Соединение 200, 6: Соединение 233, 7: Соединение 234, 8: Соединение 235, 9: Соединение 237, 10: Соединение 239, 11: Соединение 243, 12: MC3; 13: PBS.
[0057] На Фиг. 18А и 18В продемонстрированы результаты экспрессии люциферазы, измеренные при внутримышечном введении различных композиций наночастиц мышам CD-1 в дозе 0,01 мг/кг. Фиг. 18А представляет собой гистограмму, демонстрирующую общий поток через 6 часов после введения. Числа над каждым столбцом обозначают уровень экспрессии относительно MC3. Фиг. 18B демонстрирует значения общего потока через 3 ч, 6 ч и 24 ч после введения. Числа 1-11 на фигурах обозначают композиции, содержащие следующее: 1: MC3, 2: Соединение 143, 3: Соединение 49, 4: Соединение 113, 5: Соединение 61, 6: Соединение 72, 7: Соединение 75, 8: Соединение 71, 9: Соединение 128, 10: Соединение 156, 11: Соединение 157.
[0058] На Фиг. 19А и 19В продемонстрированы результаты экспрессии люциферазы, измеренные при подкожном введении различных композиций наночастиц мышам CD-1 в дозе 0,05 мг/кг. Фиг. 19А представляет собой гистограмму, демонстрирующую общий поток через 6 часов после введения. Числа над каждым столбцом обозначают уровень экспрессии относительно MC3. Фиг. 19B демонстрирует значения общего потока через 3 ч, 6 ч и 24 ч после введения. Числа 1-12 на фигурах обозначают композиции, содержащие следующее: 1: PBS, 2: MC3, 3: Соединение 25, 4: Соединение 30, 5: Соединение 20, 6: Соединение 110, 7: Соединение 112, 8: Соединение 113, 9: Соединение 72, 10: Соединение 75, 11: Соединение 122, 12: Соединение 24.
[0059] Фиг. 20А-20С представляют собой серию графиков, демонстрирующих уровни экспрессии люциферазы в печени (Фиг. 20А) селезенке (Фиг. 20В) и (Фиг. 20С) в месте инъекции ex vivo, через 24 часа после введения CD-1 мышам композиций наночастиц, содержащих соединения по данному изобретению. Значения общего потока были получены с помощью люминесцентной визуализации тела (BLI). PBS (натрий-фосфатный буфер) использовали в качестве контроля. Числа 1-12 на фигурах обозначают композиции, содержащие следующее: 1: PBS, 2: MC3, 3: Соединение 25, 4: Соединение 30, 5: Соединение 20, 6: Соединение 110, 7: Соединение 112, 8: Соединение 113, 9: Соединение 72, 10: Соединение 75, 11: Соединение 122, 12: Соединение 24.
[0060] Фиг. 21A-21J представляет собой серию графиков, демонстрирующих экспрессию цитокинов, индуцированную композициями, содержащими липиды по данному раскрытию. Фиг. 21A: G-CSF (12); Фиг. 21B: ИФН-гамма (38); Фиг. 21C: MCP-1 (51); Фиг. 21D: ИФН-альфа (30); Фиг. 21E: IL-6 (28); Фиг. 21F: IL-12p70 (39); Фиг. 21G: IL-10 (22); Фиг. 21H: MIP-1 бета (72); Фиг. 21I: ФНО-альфа (45); Фиг. 21J: RANTES (44). Числа 1-12 на фигурах обозначают композиции, содержащие следующее: 1: PBS, 2: MC3, 3: Соединение 25, 4: Соединение 30, 5: Соединение 20, 6: Соединение 110, 7: Соединение 112, 8: Соединение 113, 9: Соединение 72, 10: Соединение 75, 11: Соединение 122, 12: Соединение 24.
[0061] Фиг. 22А-22С представляют собой серию графиков, демонстрирующих уровни экспрессии люциферазы через 3ч (Фиг. 22А), 6ч (Фиг. 22В) и 24 ч (Фиг. 22С) после подкожного введения мышам композиций наночастиц, содержащих соединения по изобретению. Значения общего потока были получены с помощью люминесцентной визуализации тела (BLI). PBS (натрий-фосфатный буфер) использовали в качестве контроля. Числа 1-12 на фигурах обозначают композиции, содержащие следующее: 1: PBS, 2: MC3, 3: Соединение 168, 4: Соединение 23, 5: Соединение 19, 6: Соединение 108, 7: Соединение 109, 8: Соединение 111, 9: Соединение 60, 10: Соединение 61, 11: Соединение 69, 12: Соединение 128.
[0062] На Фиг. 23 продемонстрированы результаты экспрессии hEPO, измеренные при подкожном введении мышам различных композиций наночастиц, содержащих соединения по раскрытию в дозе 0,05 мг/кг в различные временные точки: 3 часа (левый блок), 6 часов (средний блок) и 24 часа (правый блок). Числа 1-11 на этой фигуре соответствуют MC3, PBS и соединениям 18, 25, 48, 49, 111, 60, 168, 207 и 233 соответственно.
[0063] На Фиг. 24 продемонстрированы результаты экспрессии люциферазы, измеренные при внутримышечном введении мышам различных композиций наночастиц, содержащих соединения по раскрытию в дозе 0,01 мг/кг в различные временные точки: 3 часа (левый блок), 6 часов (средний блок) и 24 часа (правый блок). Числа 1-9 на этой фигуре соответствуют MC3 и соединениям 178, 181, 182, 218, 198, 200, 233 и 239 соответственно.
[0064] На Фиг. 25 представлены результаты экспрессии hEPO, измеренные через 3 ч, 6 ч и через 24 часа после введения, при внутривенном введении мышам CD-1 композиций наночастиц, содержащих соединение 18 или МС3, и модифицированные мРНК, в которых каждый уридин был заменен N1-метил псевдоуридином или в которых каждый уридин был заменен 5-метоксиуридином, в дозе 0,5 мг/кг. Числа 1-4 на фигуре обозначают композиции, содержащие следующее: 1: Модифицированные мРНК, в которых каждый уридин заменен 5-метоксиуридином, и MC3; 2: Модифицированные мРНК, в которых каждый уридин заменен N1-метил псевдоуридином, и MC3; 3: Модифицированные мРНК, в которых каждый уридин заменен 5-метоксиуридином, и соединение 18; 4: Модифицированные мРНК, в которых каждый уридин заменен N1-метил псевдоуридином, и соединение 18.
[0065] Фиг. 26 представляет собой график, на котором представлена активация В-клеток в спленоцитах мыши, которым вводили композиции наночастиц, содержащие соединение 18 или МС3, и модифицированные мРНК, в которых каждый уридин был заменен N1-метил псевдоуридином или в которых каждый уридин был заменен 5-метоксиуридином. PBS использовали в качестве контроля. Числа 1-5 на фигуре обозначают композиции, содержащие следующее: 1: Модифицированные мРНК, в которых каждый уридин заменен 5-метоксиуридином, и MC3; 2: Модифицированные мРНК, в которых каждый уридин заменен N1-метил псевдоуридином, и MC3; 3: Модифицированные мРНК, в которых каждый уридин заменен 5-метоксиуридином, и соединение 18; 4: Модифицированные мРНК, в которых каждый уридин заменен N1-метил псевдоуридином, и соединение 18; 5: PBS.
[0066] Фиг. 27 представляет собой график, демонстрирующий экспрессию мРНК hEPO у мышей CD1, измеренную через 3 часа (левый блок), 6 часов (средний блок) и 24 часа (правый блок) после подкожного введения различных композиций наночастиц в дозе 0,5 мг/кг. Числа 1-9, относящиеся к композициям, содержащим мРНК, экспрессирующую hEPO и являются следующими: 1: PBS, 2: Соединение 18, 3: Соединение 30, 4: Соединение 96, 5: Соединение 151, 6: Соединение 98, 7: Соединение 163, 8: Соединение 164, 9: Соединение 165.
[0067] Фиг. 28A-28J представляет собой серию графиков, демонстрирующих экспрессию цитокинов, индуцированную композициями, содержащими липиды по данному раскрытию и модифицированную мРНК, экспрессирующую hEPO, в которой каждый уридин был заменен N1-метил псевдоуридином, измеренные через 6 ч после подкожного введения мышам CD-1. Фиг. 28A: G-CSF; Фиг. 28B: ИФН-гамма; Фиг. 28C: ИФН-альфа; Фиг. 28D: IL-12p70; Фиг. 28E: IP-10; F: IL-6; Фиг. 28G: MCP-1; Фиг. 28H: MIP-1 бета; Фиг. 28I: RANTES; Фиг. 28J: ФНО-альфа. Числа 1-9 на фигуре обозначают композиции, содержащие следующее: 1: PBS, 2: Соединение 18, 3: Соединение 30, 4: Соединение 96, 5: Соединение 151, 6: Соединение 98, 7: Соединение 163, 8: Соединение 164, 9: Соединение 165.
[0068] Фиг. 29А - 29С представляют собой серию графиков, иллюстрирующих оптимизацию эффективности и клиренса аминолипидов. На Фиг. 29А продемонстрирована биолюминесценция люциферазы всего тела новых LNP в сравнении с LNP MC3, измеренная у мышей CD-1 (n=6), через 6 часов после внутривенного введения мРНК hEPO 0,5 мг/кг в липид. На графике продемонстрированы концентрации hEPO в сыворотке; столбики ошибок указывают стандартное отклонение отношения экспрессии нового липида к экспрессии MC3. * p < 0,05, ** p < 0,01, ***p < 0,001, н.з. = не является статистически значимым. Числа 1-9, относящиеся к композициям, содержащим: 1: Соединение 281, 2: Соединение 138, 3: Соединение 136, 4: Соединение 6, 5: Соединение 18, 6: Соединение 29, 7: Соединение 14, 8: Соединение 25 и 9: Соединение 26. На Фиг. 29B приведены уровни соединения 18 и соединения 25 по сравнению с MC3, измеренные в ткани печени крыс Спрег-Доули (n=3 в каждый момент времени), которым вводили дозу 0,2 мг/кг LNP, содержащую мРНК hEPO. р <0,05 для AUC соединения 18 и соединения 25 относительно MC3. Фиг. 29С представляет собой график, демонстрирующий экспрессию hEPO у крыс Спрег-Доули. Концентрации hEPO в сыворотке измеряли после внутривенного введения дозы 1 мг/кг LNP, содержащей соединение 18, соединение 25, соединение 26 или MC3 и мРНК hEPO (n=3).
[0069] Фиг. 30А-30С представляют собой серию графиков, демонстрирующих фармакокинетический профиль и профиль экспрессии соединения 18 после многократных доз. На Фиг. 30А представлено сравнение тканевого распределения МС3 и соединения 18 после внутривенного введения трех болюсных доз, содержащих мРНК 0,05 мг/кг, мышам CD-1 (n=3 в каждый момент времени), вводимых еженедельно. На Фиг. 30B продемонстрирована концентрация hEPO в сыворотке через 6 ч после внутривенного введения болюсных доз, содержащих 0,5 мг/кг LNP, содержащих мРНК hEPO, мышам CD-1 (n=8), вводимых еженедельно. На Фиг. 30C проиллюстрирован клиренс из ткани печени соединения 18 и его основного метаболита, соединения 166, после введения мышам CD-1 доз, содержащих 0,25 мг/кг мРНК, (n=3 в момент времени), вводимых еженедельно.
[0070] Фиг. 31А-31С представляют собой серию графиков, на которых продемонстрирован профиль экспрессии для липидных наночастиц по изобретению в исследовании на яванском макаке. На Фиг. 31А представлены концентрации hEPO в сыворотке после доставки мРНК hEPO 0,01 мг/кг в MC3 или соединении 18. Жидкие наночастицы вводили внутривенно посредством инфузии в течении 60 мин (n=3). р <0,05 для AUC соединения 18 относительно MC3. На Фиг. 31В продемонстрированы концентрации антитела IgG человека против гриппа А в сыворотке после доставки 0,3 мг/кг в LNP мРНК антитела МС3 или соединения 18, вводимых внутривенно, посредством инфузии в течение 60 минут (n=3), р <0,05 для AUC соединения 18 относительно MC3. На Фиг. 31C продемонстрированы концентрации hEPO в сыворотке после доставки в LNP мРНК hEPO 0,2 мг/кг соединения 18, еженедельное дозирование, вводимое внутривенно, посредством инфузии в течение 60 минут (n=4).
[0071] Фиг. 32А-32С представляют собой серию графиков, демонстрирующих результаты токсикологической оценки в течение одного месяца у крыс и приматов, не являющихся человеком. PBS (натрий-фосфатный буфер) использовали в качестве контроля. На Фиг. 32A представлены уровни аланинаминотрансферазы в сыворотке у крыс Спрег-Доули, вводимой внутривенно посредством инфузии в течение 10 минут, вводимой еженедельно в течение 5 недель. Уровни в сыворотке измеряли через 24 часа после пятой дозы (n=10). Статистической разницы между PBS и каждым уровнем дозы не наблюдалось. На Фиг. 32B представлены уровни аспартатаминотрансферазы в сыворотке у крыс Спрег-Доули, вводимой внутривенно посредством инфузии в течение 10 минут, еженедельное введение в течение 5 недель. Уровни в сыворотке измеряли через 24 ч после пятой дозы (n=10). * p < 0,05, статистической разницы между PBS и дозами 0,05, и 2,0 мг/кг не наблюдалось. На Фиг. 32C продемонстрированы уровни аланинаминотрансферазы в сыворотке у яванских макак, которым вводили мРНК 1 мг/кг внутривенно посредством инфузии в течение 60 минут, вводимой еженедельно. Уровни в сыворотке измеряли через 24 ч после пятой дозы (n=4). Не наблюдалось статистической разницы между уровнями PBS и соединения 18 до введения дозы и на 30 сутки. На Фиг. 32D продемонстрированы уровни аспартатаминотрансферазы в сыворотке у яванских макак, которым вводили мРНК 1 мг/кг внутривенно посредством инфузии в течение 60 минут, вводимой еженедельно. Уровни в сыворотке измеряли через 24 ч после пятой дозы (n=4). Не наблюдалось статистической разницы между уровнями PBS и соединения 18 до введения дозы и на 30 сутки.
[0072] Фиг. 33А та 33B представляют собой пару графиков, демонстрирующих результаты токсикологической оценки в течение одного месяца у крыс и приматов, не являющихся человеком. На Фиг. 33A продемонстрирована концентрация C5b9 в сыворотке у яванских макаков, которым вводили мРНК 1 мг/кг, на 1-е и 29-е сутки (n=4). Не было обнаружено статистической разницы между PBS и соединением 18 во все временные точки. На Фиг. 33B продемонстрирована концентрация MCP-1 в сыворотке у яванских макаков, которым вводили мРНК 1 мг/кг, на 1-е и 29-е сутки. n=4, * p < 0,05, статистическая разница между PBS и соединением 18 не наблюдалась в любой другой временной точке.
[0073] Фиг. 34А-34С представляют собой серию изображений эффективности эндосомального выхода липидных наночастиц по данному изобретению в фиксированных клетках. Клетки HeLa трансфицировали LNP MC3 и соединения 18, инкапсулирующими мРНК люциферазы, которые были мечены родамином и обрабатывали для одномолекулярной FISH (флуоресцентная гибридизация in situ) (smFISH, красный) после 4-часовой инкубации вместе с клетками, электропорированными несформированной мРНК. Молекулы мРНК, которые выделяют эндоцитарные органеллы в цитозоль, продемонстрированы зеленым цветом (оверлей анализа изображения). Эффективность эндосомального выхода оценивали путем вычисления отношения между количеством цитозольной мРНК и количеством интернализованных LNP на клетку. Фиг. 34А представляет собой изображение, на котором продемонстрированы электропорированные клетки HeLa. Фиг. 34В представляет собой изображение, на котором продемонстрированы клетки HeLa, обработанные МС3. Фиг. 34В представляет собой изображение, на котором продемонстрированы клетки HeLa, обработанные соединением 18.
[0074] Фиг. 35А и 35В представляют собой пару графиков, сравнивающих распределение МС3 и соединения 18 в тканях. На Фиг. 35A показано распределение MC3 и соединения 18 в тканях после трех внутривенных инъекций 0,05 мг/кг мРНК, введенных мышам CD-1 (n=3 в каждой временной точке). На Фиг. 35B показано распределение MC3 и соединения 18 в ткани через 12 ч после введения мРНК 0,2 мг/кг яванским макакам (n=2).
[0075] Фиг. 36 представляет собой график, иллюстрирующий экспрессию IgG человека у яванского макака, которому вводили 0,1 мг/кг мРНК IgG человека в композиции, содержащей MC3 или соединение 18, внутривенно посредством инфузии в течение 60 минут (n=3).
[0076] Фиг. 37 представляет собой серию графиков, иллюстрирующих некроз единичных клеток MC3 в печени крысы и фермент печени. Верхний ряд представляет собой пару изображений печени крыс, которым вводили 0,3 мг/кг жидкой наночастицы (LNP), не содержащей мРНК (справа) и PBS (натрий-фосфатный буфер) в качестве контроля (слева). Нижний ряд представляет собой пару графиков, на которых продемонстрирована экспрессию ALT (слева) и AST (справа) в печени после введения 0,3 мг/кг LNP на основе MC3, содержащего мРНК. ALT и AST были повышены, и патология показала признаки некроза.
[0077] Фиг. 38 представляет собой график, на котором продемонстрированы уровни мРНК в NHP после повторного введения дозы в течение 29 суток.
[0078] Фиг. 39А и 39В представляют собой пару графиков, на которых продемонстрирована экспрессия hEPO у мышей, нокаутированных по ApoE, и мышей, нокаутированных по LDLr, которым вводили LNP на основе соединения 18. На Фиг. 39A продемонстрирована экспрессия hEPO у мышей, нокаутированных по ApoE. На Фиг. 39B продемонстрирована экспрессия hEPO у мышей, нокаутированных по LDLr.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0079] Данное изобретение относится к новым композициям липидов и наночастиц липидов, включая новый липид. В данном изобретении также предложены способы доставки терапевтического и/или профилактического средства в клетку млекопитающего, в частности доставка терапевтического и/или профилактического средства в орган млекопитающего, продуцирование представляющего интерес полипептида в клетке млекопитающего и лечение заболевания или расстройства у млекопитающего, нуждающегося в этом. Например, способ получения представляющего интерес полипептида в клетке включает приведение в контакт композиции наночастиц, содержащей мРНК, с клеткой млекопитающего, посредством чего мРНК может самостоятельно транслироваться с получением представляющего интерес полипептида. Способ доставки терапевтического и/или профилактического средства в клетку или орган млекопитающего может включать введение композиции наночастиц, включающей терапевтическое и/или профилактическое средство, субъекту, при котором введение включает в себя приведение в контакт клетки или органа с композицией, посредством чего терапевтическое и/или профилактическое средство доставляется в клетку или орган.
Липиды
[0080] Данное изобретение относится к липидам, содержащим центральный аминный фрагмент и по меньшей мере одну биоразлагаемую группу. Описанные в данном документе липиды могут преимущественно применять в композициях липидных наночастиц для доставки терапевтических и/или профилактических средств в клетки или органы млекопитающих. Например, липиды, описанные в данном документе, имеют небольшую иммуногенность или не имеют ее вообще. Например, соединение липида любой формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) имеет более низкую иммуногенность по сравнению с эталонным липидом (например, MC3, KC2 или DLinDMA). Например, композиция, содержащая липид, описанный в данном документе, и терапевтический или профилактический агент, имеет повышенный терапевтический индекс по сравнению с соответствующей композицией, которая содержит эталонный липид (например, MC3, KC2 или DLinDMA) и тот же терапевтический или профилактический агент.
[0081] В первом аспекте данного изобретения соединения, описанные в данном документе, имеют формулу (I):
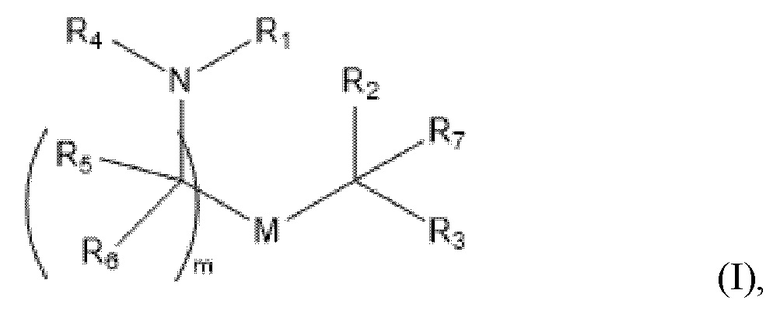
или их N-оксид, или их соль, или их изомер, где
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ,
-CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из карбоцикла, гетероцикла, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -N(R)2, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и -C(R)N(R)2C(O)OR, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-,
-N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и
C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и
C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13; и при этом когда R4 представляет собой -(CH2)nQ, -(CH2)nCHQR, -CHQR или CQ(R)2, тогда (i) Q не представляет собой -N(R)2, когда n равно 1, 2, 3, 4 или 5, или (ii) Q не представляет собой 5, 6 или 7-членный гетероциклоалкил, когда n равно 1 или 2.
[0082] Другой аспект данного изобретения относится к соединениям формулы (III):

или его N-оксиду,
или его соли, или его таутомеру, где:
или его соли, или его таутомеру, где:
R1 выбирают из группы, состоящей из C5-30 алкила, C5-20 алкенила, -R*YR'', -YR'' и -R''M'R';
R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл;
R4 выбирают из группы, состоящей из водорода, C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ,
-CHQR, -CQ(R)2 и незамещенного C1-6 алкила, где Q выбирают из карбоцикла, гетероцикла, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -N(R)2, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2, -N(OR)C(=CHR9)N(R)2, -C(=NR9)N(R)2, -C(=NR9)R, -C(O)N(R)OR и -C(R)N(R)2C(O)OR, каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5;
Rx выбирают из группы, состоящей из C1-6 алкила, C2-6 алкенила, -(CH2)rOH и -(CH2)rNR2,
где r выбирают из 1, 2, 3, 4, 5 и 6;
каждый R5 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
каждый R6 независимо выбирают из группы, состоящей из OH, C1-3 алкила, C2-3 алкенила и H;
M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-, -C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, -S-S-, арильной группы и гетероарильной группы, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил;
R7 выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила и H;
R8 выбирают из группы, состоящей из C3-6 карбоцикла и гетероцикла;
R9 выбирают из группы, состоящей из H, CN, NO2, C1-6 алкила, -OR, -S(O)2R, -S(O)2N(R)2, C2-6 алкенила, C3-6 карбоцикла и гетероцикла;
R10 выбирают из группы, состоящей из H, OH, C1-3 алкила и C2-3 алкенила;
каждый R независимо выбирают из группы, состоящей из C1-3 алкила, C2-3 алкенила, (CH2)qOR* и H,
и каждый q независимо выбирают из 1, 2 и 3;
каждый R' независимо выбирают из группы, состоящей из C1-18 алкила, C2-18 алкенила, -R*YR'', -YR'' и H;
каждый R'' независимо выбирают из группы, состоящей из C3-15 алкила и
C3-15 алкенила;
каждый R* независимо выбирают из группы, состоящей из C1-12 алкила и
C2-12 алкенила;
каждый Y независимо представляет собой C3-6 карбоцикл;
каждый X независимо выбирают из группы, состоящей из F, Cl, Br и I; и
m выбирают из 5, 6, 7, 8, 9, 10, 11, 12 и 13.
[0083] В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (IA):
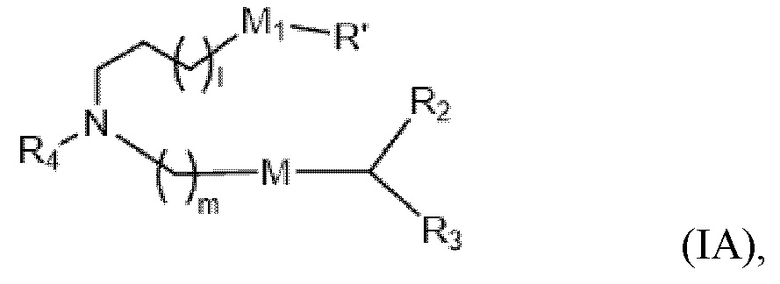
или их N-оксид, или их соль, или их изомер, где l выбирают из 1, 2, 3, 4 и 5; m выбирают из 5, 6, 7, 8 и 9; M1 представляет собой связь или M'; R4 представляет собой водород, незамещенный C1-3 алкил, -(CH2)oC(R10)2(CH2)n-oQ или -(CH2)nQ, в которой Q представляет собой OH, -NHC(S)N(R)2, -NHC(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)R8, -NHC(=NR9)N(R)2, -NHC(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR,
гетероарил или гетероциклоалкил; M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -P(O)(OR')O-, -S-S-, арильной группы и гетероарильной группы,; и R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила и C2-14 алкенила. Например, m равно 5, 7 или 9. Например, Q представляет собой OH, -NHC(S)N(R)2 или -NHC(O)N(R)2. Например, Q представляет собой -N(R)C(O)R или -N(R)S(O)2R.
[0084] В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (IB):

или его N-оксид, или его соль, или изомер, в которых все переменные имеют значения, определенные в данном документе. Например, m выбирают из 5, 6, 7, 8 и 9; M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -P(O)(OR')O-, -S-S-, арильной группы и гетероарильной группы; и R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила и C2-14 алкенила. Например, m равно 5, 7 или 9. В конкретных вариантах осуществления подмножество соединений формулы (I) включает соединения формулы (II):

или его N-оксид, или его соль, или его изомер, где l выбирают из 1, 2, 3, 4 и 5; M1 представляет собой связь или M'; R4 представляет собой водород, незамещенный C1-3 алкил, -(CH2)oC(R10)2(CH2)n-oQ или -(CH2)nQ, в которой n равно 2, 3 или 4 и Q представляет собой OH, -NHC(S)N(R)2, -NHC(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)R8, -NHC(=NR9)N(R)2, -NHC(=CHR9)N(R)2, -OC(O)N(R)2, -N(R)C(O)OR,
гетероарил или гетероциклоалкил; M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -P(O)(OR')O-, -S-S-, арильной группы и гетероарильной группы; и R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила и C2-14 алкенила.
[0085] Соединения любой формулы (I) или (IA)включают один или более из следующих признаков, если применимо.
[0086] В некоторых вариантах осуществления M1 представляют собой M'.
[0087] В некоторых вариантах осуществления M и M' независимо представляют собой C(O)O- или -OC(O)-.
[0088] В некоторых вариантах осуществления по меньшей мере один из M и M' представляет собой C(O)O- или -OC(O)-.
[0089] В конкретных вариантах осуществления по меньшей мере один из M и M' представляет собой -OC(O)-.
[0090] В конкретных вариантах осуществления M представляет собой -OC(O)- и M' представляет собой -C(O)O-. В некоторых вариантах осуществления M представляет собой -C(O)O- и M' представляет собой -OC(O)-. В конкретных вариантах осуществления M и M', каждый, представляют собой -OC(O)-. В некоторых вариантах осуществления, M и M', каждый, представляют собой -C(O)O-.
[0091] В конкретных вариантах осуществления по меньшей мере один из M и M' представляет собой -OC(O)-M''-C(O)O-.
[0092] В некоторых вариантах осуществления, M и M' независимо представляют собой -S-S-.
[0093] В некоторых вариантах осуществления, по меньшей мере один из M и M' представляет собой -S-S.
[0094] В некоторых вариантах осуществления один из M и M' представляет собой C(O)O- или -OC(O)-, а другой представляют собой -S-S-. Например, M представляет собой C(O)O- или -OC(O)- и M' представляет собой -S-S- или M' представляет собой C(O)O- или -OC(O)- и M представляет собой -S-S-
[0095] В некоторых вариантах осуществления один из M и M' представляет собой -OC(O)-M''-C(O)O-, в которых M'' представляет собой связь, C1-13 алкил или C2-13 алкенил. В других вариантах осуществления M'' представляет собой C1-6 алкил или C2-6 алкенил. В конкретных вариантах осуществления M'' представляет собой C1-4 алкил или C2-4 алкенил.
[0096] В некоторых вариантах осуществления m равно 1, 3 или 5.
[0097] В некоторых вариантах реализации изобретения R4 представляет собой водород.
[0098] В некоторых вариантах реализации изобретения R4 представляет собой водород.
[0099] В некоторых вариантах осуществления R4 представляет собой незамещенный метил или -(CH2)nQ, в которой Q представляет собой OH, -NHC(S)N(R)2, -NHC(O)N(R)2, -N(R)C(O)R или -N(R)S(O)2R.
[00100] В некоторых вариантах осуществления Q представляет собой OH.
[00101] В некоторых вариантах осуществления Q представляет собой -NHC(S)N(R)2.
[00102] В некоторых вариантах осуществления Q представляет собой -NHC(O)N(R)2.
[00103] В некоторых вариантах осуществления Q представляет собой -N(R)C(O)R.
[00104] В некоторых вариантах осуществления Q представляет собой -N(R)S(O)2R.
[00105] В некоторых вариантах осуществления Q представляет собой -O(CH2)nN(R)2.
[00106] В некоторых вариантах осуществления Q представляет собой -O(CH2)nOR.
[00107] В некоторых вариантах осуществления Q представляет собой -N(R)R8.
[00108] В некоторых вариантах осуществления Q представляет собой -NHC(=NR9)N(R)2.
[00109] В некоторых вариантах осуществления Q представляет собой -NHC(=CHR9)N(R)2.
[00110] В некоторых вариантах осуществления Q представляет собой -OC(O)N(R)2.
[00111] В некоторых вариантах осуществления Q представляет собой -N(R)C(O)OR.
[00112] В некоторых вариантах реализации n равно 2.
[00113] В некоторых вариантах реализации n равно 3.
[00114] В некоторых вариантах реализации n равно 4.
[00115] В некоторых вариантах реализации M1 отсутствует.
[00116] В некоторых вариантах осуществления по меньшей мере R5 представляет собой гидроксил. Например, один R5 представляет собой гидроксил.
[00117] В некоторых вариантах осуществления по меньшей мере R6 представляет собой гидроксил. Например, один R6 представляет собой гидроксил.
[00118] В некоторых вариантах осуществления один из R5 и R6 представляет собой гидроксил. Например, один R5 представляет собой гидроксил и каждый R6 представляет собой водород. Например, один R6 представляет собой гидроксил и каждый R5 представляет собой водород.
[00119] В некоторых вариантах осуществления Rx представляет собой C1-6 алкил. В некоторых вариантах осуществления Rx представляет собой C1-3 алкил. Например, Rx представляет собой метил. Например, Rx представляет собой этил. Например, Rx представляет собой пропил.
[00120] В некоторых вариантах осуществления Rx представляет собой -(CH2)rOH и, r равно 1, 2 или 3. Например, Rx представляет собой метанoил. Например, Rx представляет собой этаноил. Например, Rx представляет собой пропаноил.
[00121] В некоторых вариантах осуществления, Rx представляет собой -(CH2)rNR2, r равно 1, 2 или 3 и каждый R представляет собой H или метил. Например, Rx представляет собой метанамино, метилметанамино или диметилметанамино. Например, Rx представляет собой аминометанил, метиламинометанил или диметиламинометанил. Например, Rx представляет собой аминоэтанил, метиламиноэтанил или диметиламиноэтанил. Например, Rx представляет собой аминопропанил, метиламинопропанил или диметиламинопропанил.
[00122] В некоторых вариантах осуществления, R' представляет собой C1-18 алкил, C2-18 алкенил, -R*YR'' или -YR''.
[00123] В некоторых вариантах осуществления, R2 и R3 независимо представляют собой C3-14 алкил или C3-14 алкенил.
[00124] В одном варианте осуществления соединения формулы (I) имеют формулу (IIa),
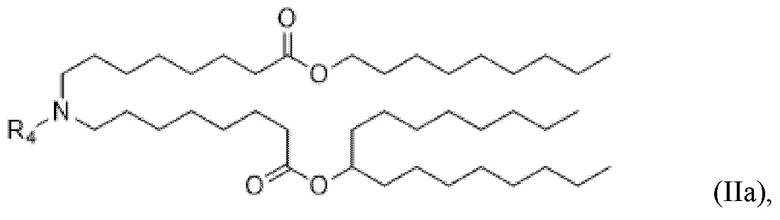
или их N-оксиды, или их соли, или их изомеры, где R4 соответствует описанию в данном документе.
[00125] В другом варианте осуществления соединения формулы (I) имеют формулу (IIb),
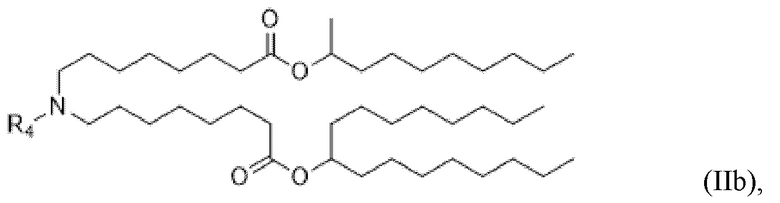
или их N-оксиды, или их соли, или их изомеры, где R4 соответствует описанию в данном документе.
[00126] В другом варианте осуществления соединения формулы (I) имеют формулу (IIc) или (IIe):

или их N-оксиды, или их соли, или их изомеры, где R4 соответствует описанию в данном документе.
[00127] В другом варианте осуществления соединения формулы (I) имеют формулу (IIf):
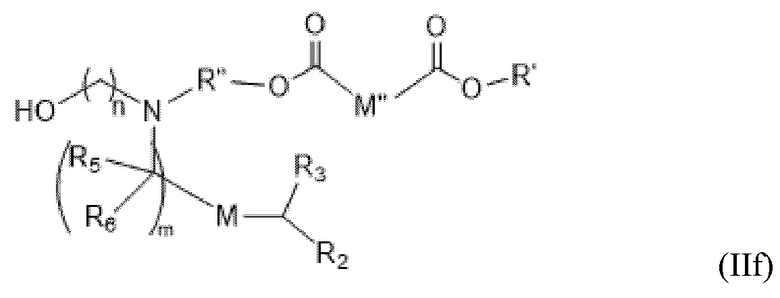
или их N-оксиды, или их соли, или их изомеры.
где M представляет собой -C(O)O- или -OC(O)-, M'' представляет собой C1-6 алкил или C2-6 алкенил, R2 и R3 независимо выбирают из группы, состоящей из C5-14 алкила и C5-14 алкенила, и n выбирают из 2, 3 и 4.
[00128] В дополнительном варианте осуществления соединения формулы (I) имеют формулу (IId),
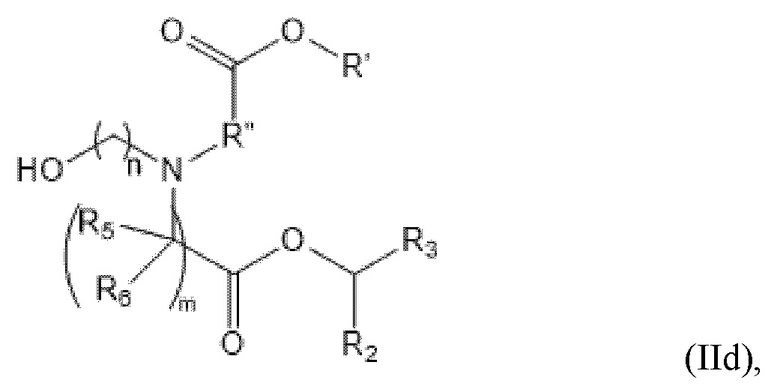
или их N-оксиды, или их соли, или их изомеры, где n равно 2, 3 или 4; и m, R', R'' и от R2 до R6 описаны в данном документе. Например, каждый из R2 и R3 могут быть независимо выбраны из группы, состоящей из C5-14 алкила и C5-14 алкенила.
[00129] В дополнительном варианте осуществления соединения формулы (I) имеют формулу (IIg),
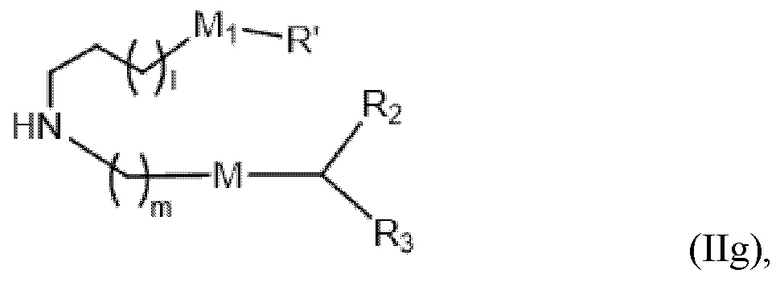
или их N-оксиды, или их соли, или их изомеры, где l выбирают из 1, 2, 3, 4 и 5; m выбирают из 5, 6, 7, 8 и 9; M1 представляет собой связь или M'; M и M' независимо выбирают из -C(O)O-, -OC(O)-, -OC(O)-M''-C(O)O-, -C(O)N(R')-, -P(O)(OR')O-, -S-S-, арильной группы и гетероарильной группы; и R2 и R3 независимо выбирают из группы, состоящей из H, C1-14 алкила и C2-14 алкенила. Например, M'' представляет собой C1-6 алкил (например, C1-4 алкил) или C2-6 алкенил (например, C2-4 алкенил). Например, R2 и R3 независимо выбирают из группы, состоящей из C5-14 алкила и C5-14 алкенила.
[00130] Соединения любой из формул (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) и (III) включают один или более из следующих признаков, если применимо.
[00131] В некоторых вариантах осуществления, R4 выбирают из группы, состоящей из C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR и -CQ(R)2, где Q выбирают из
C3-6 карбоцикла, 5-14-членного ароматического или неароматического гетероцикла, имеющего один или более
гетероатомов, выбранных из N, O, S и P, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3,
-CX2H, -CXH2, -CN, -N(R)2, -N(R)S(O)2R8, -C(O)N(R)2, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2,
-N(R)C(S)N(R)2 и -C(R)N(R)2C(O)OR, причем каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5.
[00132] В другом варианте осуществления R4 выбирают из группы, состоящей из C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR и -CQ(R)2, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероарила, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)S(O)2R8, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -C(R)N(R)2C(O)OR, и 5-14-членного гетероциклоалкила, имеющего один или более гетероатомов, выбранных из N, O и S, которые замещены одним или более заместителями, выбранными из оксо (=O), OH, амино и C1-3 алкила, причем каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5.
[00133] В другом варианте осуществления R4 выбирают из группы, состоящей из C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR и -CQ(R)2, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероцикла, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)S(O)2R8, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -C(R)N(R)2C(O)OR, причем каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5; и когда Q представляет собой 5-14-членный гетероцикл и (i) R4 представляет собой -(CH2)nQ, в которой n равно 1 или 2, или (ii) R4 представляет собой -(CH2)nCHQR, в которой n равно 1, или (iii) R4 представляет собой CHQR и -CQ(R)2, тогда Q представляет собой как 5- 14-членный гетероарил или 8-14-членный гетероциклоалкил.
[00134] В другом варианте осуществления R4 выбирают из группы, состоящей из C3-6 карбоцикла, -(CH2)nQ, -(CH2)nCHQR, -(CH2)oC(R10)2(CH2)n-oQ, -CHQR и -CQ(R)2, где Q выбирают из C3-6 карбоцикла, 5-14-членного гетероарила, имеющего один или более гетероатомов, выбранных из N, O и S, -OR, -O(CH2)nN(R)2, -C(O)OR, -OC(O)R, -CX3, -CX2H, -CXH2, -CN, -C(O)N(R)2, -N(R)S(O)2R8, -N(R)C(O)R, -N(R)S(O)2R, -N(R)C(O)N(R)2, -N(R)C(S)N(R)2, -C(R)N(R)2C(O)OR, причем каждый o независимо выбирают из 1, 2, 3 и 4 и каждый n независимо выбирают из 1, 2, 3, 4 и 5.
[00135] В другом варианте осуществления, R4 представляет собой -(CH2)nQ, где Q представляет собой -N(R)S(O)2R8 и n выбирают из 1, 2, 3, 4 и 5. В дополнительном варианте осуществления, R4 представляет собой -(CH2)nQ, где Q представляет собой -N(R)S(O)2R8, в которой R8 представляет собой C3-6 карбоцикл, такой как C3-6 циклоалкил и n выбирают из 1, 2, 3, 4 и 5. Например, R4 представляет собой -(CH2)3NHS(O)2R8 и R8 представляет собой циклопропил.
[00136] В другом варианте осуществления, R4 представляет собой -(CH2)oC(R10)2(CH2)n-oQ, где Q представляет собой -N(R)C(O)R, причем n выбирают из 1, 2, 3, 4 и 5 и o выбирают из 1, 2, 3 и 4. В дополнительном варианте осуществления, R4 представляет собой -(CH2)oC(R10)2(CH2)n-oQ, где Q представляет собой -N(R)C(O)R, где R представляет собой C1-C3 алкил и n выбирают из 1, 2, 3, 4 и 5 и o выбирают из 1, 2, 3 и 4. В другом варианте осуществления R4 представляет собой -(CH2)oC(R10)2(CH2)n-oQ, где Q представляет собой -N(R)C(O)R, где R представляет собой C1-C3 алкил, причем n равно 3 и o равно 1. В некоторых вариантах осуществления, R10 представляет собой H, OH, C1-3 алкил или C2-3 алкенил. Например, R4 представляет собой 3-ацетамидо-2,2-диметилпропил.
[00137] В некоторых вариантах осуществления, один R10 представляет собой H и один R10 представляет собой C1-3 алкил или C2-3 алкенил. В другом варианте осуществления каждый R10 представляет собой C1-3 алкил или C2-3 алкенил. В другом варианте осуществления каждый R10 представляет собой представляет собой C1-3 алкил (например, метил, этил или пропил). Например, один R10 представляет собой метил и один R10 представляет собой этил или пропил. Например, один R10 представляет собой этил и один R10 представляет собой метил или пропил. Например, один R10 представляет собой пропил и один R10 представляет собой метил или этил. Например, каждый R10 представляет собой метил. Например, каждый R10 представляет собой этил. Например, каждый R10 представляет собой пропил.
[00138] В некоторых вариантах осуществления один R10 представляет собой H и один R10 представляет собой OH. В другом варианте осуществления каждый R10 представляет собой OH.
[00139] В другом варианте осуществления R4 представляет собой незамещенный C1-4 алкил, например, незамещенный метил.
[00140] В другом варианте осуществления R4 представляет собой водород.
[00141] В конкретных вариантах осуществления в описании предложено соединение формулы (I), где R4 представляет собой -(CH2)nQ или -(CH2)nCHQR, где Q представляет собой -N(R)2 и n выбирают из 3, 4 и 5.
[00142] В конкретных вариантах осуществления в описании предложено соединение формулы (I), где R4 выбирают из группы, состоящей из -(CH2)nQ, -(CH2)nCHQR, -CHQR и -CQ(R)2, где Q представляет собой -N(R)2 и n выбирают из 1, 2, 3, 4 и 5.
[00143] В конкретных вариантах осуществления в описании предложено соединение формулы (I), где R2 и R3 независимо выбирают из группы, состоящей из C2-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл и R4 представляет собой -(CH2)nQ или -(CH2)nCHQR, где Q представляет собой -N(R)2 и n выбирают из 3, 4 и 5.
[00144] В конкретных вариантах осуществления R2 и R3 независимо выбирают из группы, состоящей из C2-14 алкила, C2-14 алкенила, -R*YR'', -YR'' и -R*OR'' или R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл.
[00145] В некоторых вариантах осуществления R1 выбирают из группы, состоящей из C5-20 алкила и C5-20 алкенила.
[00146] В других вариантах осуществления R1 выбирают из группы, состоящей из -R*YR'', -YR'' и -R''M'R'.
[00147] В конкретных вариантах осуществления R1 выбирают из -R*YR'' и -YR''. В некоторых вариантах осуществления Y представляет собой циклопропильную группу. В некоторых вариантах осуществления, R* представляет собой C8 алкил или C8 алкенил. В конкретных вариантах осуществления R'' представляет собой C3-12 алкил. Например, R'' может представлять собой C3 алкил. Например, R'' может представлять собой C4-8 алкил (например, C4, C5, C6, C7, или C8 алкил).
[00148] В некоторых вариантах осуществления R представляет собой (CH2)qOR*, причем q выбирают из 1, 2 и 3 и R* представляет собой C1-12 алкил, замещенный одним или более заместителями, выбранными из группы, состоящей из амино, C1-C6 алкиламино и C1-C6 диалкиламино. Например, R представляет собой (CH2)qOR*, причем q выбирают из 1, 2 и 3 и R* представляет собой C1-12 алкил, замещенный C1-C6 диалкиламино. Например, R представляет собой (CH2)qOR*, причем q выбирают из 1, 2 и 3 и R* представляет собой C1-3 алкил, замещенный C1-C6 диалкиламино. Например, R представляет собой (CH2)qOR*, q выбирают из 1, 2 и 3 и R* представляет собой C1-3 алкил, замещенный диметиламино (например, диметиламиноэтанил).
[00149] В некоторых вариантах осуществления R1 представляет собой C5-20 алкил. В некоторых вариантах осуществления изобретения R1 представляет собой C6 алкил. В некоторых вариантах осуществления изобретения R1 представляет собой C8 алкил. В других вариантах осуществления R1 представляет собой C9 алкил. В определенных вариантах осуществления R1 представляет собой C14 алкил. В других вариантах осуществления R1 представляет собой C18 алкил.
[00150] В некоторых вариантах осуществления R1 представляет собой C21-30 алкил. В некоторых вариантах осуществления изобретения R1 представляет собой C26 алкил. В некоторых вариантах осуществления изобретения R1 представляет собой C28 алкил. В конкретных вариантах осуществления R1 представляет собой  .
.
[00151] В некоторых вариантах осуществления R1 представляет собой C5-20 алкенил. В конкретных вариантах осуществления R1 представляет собой C18 алкенил. В некоторых вариантах осуществления R1 представляет собой линолеоил.
[00152] В конкретных вариантах осуществления R1 является разветвленным (например, декан-2-ил, ундекан-3-ил, додекан-4-ил, тридекан-5-ил, тетрадекан-6-ил, 2-метилундекан-3-ил, 2-метилдекан-2-ил, 3-метилундекан-3-ил, 4-метилдодекан-4-ил или гептадека-9-ил). В конкретных вариантах осуществления R1 представляет собой 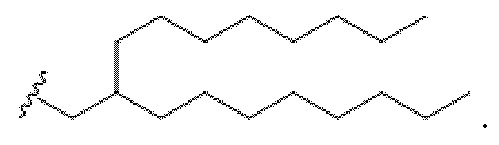
[00153] В конкретных вариантах осуществления R1 представляет собой незамещенный C5-20 алкил или C5-20 алкенил. В конкретных вариантах осуществления R' представляет собой замещенный C5-20 алкил или C5-20 алкенил (например, замещенный C3-6 карбоциклом, таким как 1-циклопропилнонил, или замещенный OH или алкокси). Например, R1 представляет собой 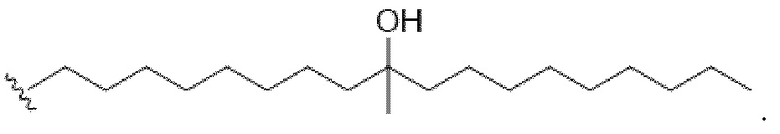
[00154] В других вариантах осуществления, R1 представляет собой -R''M'R'. В конкретных вариантах осуществления M' представляет собой -OC(O)-M''-C(O)O-. Например, R1 представляет собой 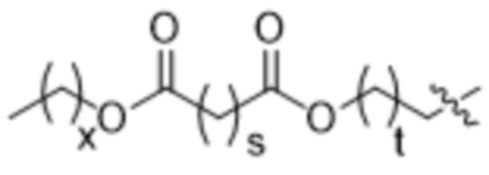 , где x равно целому числу между 1 и 13 (например, выбрано из 3, 4, 5 и 6), s равно целому числу между 1 и 13 (например, выбрано из 1, 2 и 3) и t равно целому числу между 2 и 14 (например, выбрано из 4, 5 и 6). Например, x выбирают из 3, 4, 5 и 6, s выбирают из 1, 2 и 3 и t выбирают из 4, 5 и 6.
, где x равно целому числу между 1 и 13 (например, выбрано из 3, 4, 5 и 6), s равно целому числу между 1 и 13 (например, выбрано из 1, 2 и 3) и t равно целому числу между 2 и 14 (например, выбрано из 4, 5 и 6). Например, x выбирают из 3, 4, 5 и 6, s выбирают из 1, 2 и 3 и t выбирают из 4, 5 и 6.
[00155] В других вариантах осуществления R1 отличается от -(CHR5R6)m-M-CR2R3R7.
[00156] В некоторых вариантах осуществления R' выбирают из -R*YR'' и -YR''. В некоторых вариантах осуществления Y представляет собой C3-8 циклоалкил. В некоторых вариантах осуществления, Y представляет собой C6-10 арил. В некоторых вариантах осуществления Y представляет собой циклопропильную группу. В некоторых вариантах осуществления, Y представляет собо циклогексильную группу. В конкретных вариантах осуществления R* представляет собой C1 алкил.
[00157] В некоторых вариантах осуществления, R'' выбирают из группы, состоящей из C3-12 алкила и C3-12 алкенила. В некоторых вариантах осуществления, R'', прилежащий к Y, представляет собой C1 алкил. В некоторых вариантах осуществления, R'', прилежащий к Y, представляет собой C4-9 алкил (например, C4, C5, C6, C7 или C8, или C9 алкил).
[00158] В некоторых вариантах осуществления, R'' представляет собой замещенный C3-12 (например, C3-12 алкил, замещенный, например, гидроксилом). Например, R'' представляет собой 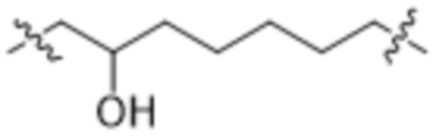 .
.
[00159] В некоторых вариантах осуществления, R' выбирают из C4 алкила и C4 алкенила. В конкретных вариантах осуществления R' выбирают из C5 алкила и C5 алкенила. В некоторых вариантах осуществления, R' выбирают из C6 алкила и C6 алкенила. В некоторых вариантах осуществления, R' выбирают из C7 алкила и C7 алкенила. В некоторых вариантах осуществления, R' выбирают из C9 алкила и C9 алкенила.
[00160] В некоторых вариантах осуществления, R' представляет собой 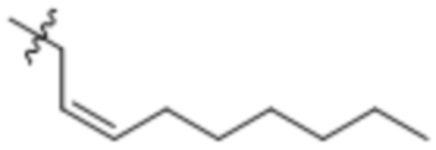 или
или 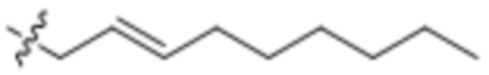 . В некоторых вариантах осуществления, R' представляет собой
. В некоторых вариантах осуществления, R' представляет собой  или
или  и M' представляет собой-OC(O)-. В других вариантах осуществления, R' представляет собой
и M' представляет собой-OC(O)-. В других вариантах осуществления, R' представляет собой  или
или  и M' представляет собой -C(O)O-.
и M' представляет собой -C(O)O-.
[00161] В других вариантах осуществления R' выбирают из C11 алкила и C11 алкенила. В других вариантах осуществления R' выбирают из C12 алкила, C12 алкенила, C13 алкила, C13 алкенила, C14 алкила, C14 алкенила, C15 алкила, C15 алкенила, C16 алкила, C16 алкенила, C17 алкила, C17 алкенила, C18 алкила и C18 алкенила. В конкретных вариантах осуществления R' представляет собой линейный C4-18 алкил или C4-18 алкенил. В конкретных вариантах осуществления R' является разветвленным (например, декан-2-ил, ундекан-3-ил, додекан-4-ил, тридекан-5-ил, тетрадекан-6-ил, 2-метилундекан-3-ил, 2-метилдекан-2-ил, 3-метилундекан-3-ил, 4-метилдодекан-4-ил или гептадека-9-ил). В конкретных вариантах осуществления R' представляет собой 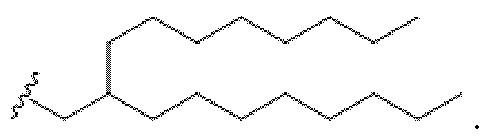
[00162] В конкретных вариантах осуществления R' представляет собой незамещенный C1-18 алкил. В конкретных вариантах осуществления R' представляет собой замещенный C1-18 алкил (например, C1-15 алкил, замещенный, например, алкокси, такой как метокси, или C3-6 карбоцикл, такой как 1-циклопропилнонил, или C(O)O-алкил или OC(O)-алкил, такой как C(O)OCH3 или OC(O)CH3). Например, R' представляет собой 
 или
или 
[00163] В конкретных вариантах осуществления R' представляет собой разветвленный C1-18 алкил. Например, R' представляет собой  .
.
[00164] В некоторых вариантах осуществления, R'' выбирают из группы, состоящей из C3-15 алкила и C3-15 алкенила. В некоторых вариантах осуществления R'' представляет собой C3 алкил, C4 алкил, C5 алкил, C6 алкил, C7 алкил или C8 алкил. В некоторых вариантах осуществления R'' представляет собой C9 алкил, C10 алкил, C11 алкил, C12 алкил, C13 алкил, C14 алкил или C15 алкил.
[00165] В некоторых вариантах осуществления M' представляет собой C(O)O-. В некоторых вариантах осуществления, M' представляет собой -OC(O)-. В некоторых вариантах осуществления M' представляет собой -OC(O)-M''-C(O)O-.
[00166] В других вариантах осуществления M' представляет собой арильную группу или гетероарильную группу. Например, M' может быть выбран из группы, состоящей из фенила, оксазола и тиазола.
[00167] В некоторых вариантах осуществления M представляет собой C(O)O-. В некоторых вариантах осуществления M представляет собой -OC(O)-. В некоторых вариантах осуществления M представляет собой C(O)N(R')-. В некоторых вариантах осуществления M представляет собой -P(O)(OR')O-. В некоторых вариантах осуществления M представляет собой -OC(O)-M''-C(O)O-.
[00168] В других вариантах осуществления M представляет собой арильную группу или гетероарильную группу. Например, M может быть выбран из группы, состоящей из фенила, оксазола и тиазола.
[00169] В некоторых вариантах осуществления M является аналогичным M'. В других вариантах осуществления M является отличным от M'.
[00170] В некоторых вариантах осуществления L представляет собой связь. В некоторых вариантах осуществления M'' представляет собой C1-13 алкил или C2-13 алкенил. В некоторых вариантах осуществления M'' представляет собой C1-6 алкил или C2-6 алкенил. В конкретных вариантах осуществления M'' представляет собой линейный алкил или алкенил. В конкретных вариантах осуществления M'' является разветвленным, например, -CH(CH3)CH2-.
[00171] В некоторых вариантах осуществления каждый R5 представляет собой H. В определенных вариантах осуществления каждый R6 также представляет собой H.
[00172] В некоторых вариантах осуществления R7 представляет собой H. В других вариантах осуществления R7 представляет собой C1-3 алкил (например, метил, этил, пропил или изопропил).
[00173] В некоторых вариантах осуществления R2 и R3 независимо представляют собой C5-14 алкил или C5-14 алкенил.
[00174] В некоторых вариантах осуществления каждый из R2 и R3 представляет собой H. В некоторых вариантах осуществления R2 и R3 представляют собой C8 алкил. В конкретных вариантах осуществления R2 и R3 представляют собой C2 алкил. В других вариантах осуществления R2 и R3 представляют собой C3 алкил. В некоторых вариантах осуществления R2 и R3 представляют собой C4 алкил. В конкретных вариантах осуществления R2 и R3 представляют собой C5 алкил. В других вариантах осуществления R2 и R3 представляют собой C6 алкил. В некоторых вариантах осуществления R2 и R3 представляют собой C7 алкил.
[00175] В некоторых вариантах осуществления R2 и R3 являются разными. В определенных вариантах осуществления R2 представляет собой C8 алкил. В некоторых вариантах осуществления R3 представляет собой C1-7 (например, C1, C2, C3, C4, C5, C6 или C7 алкил) или C9 алкил.
[00176] В некоторых вариантах осуществления каждый из R7 и R3 представляет собой H.
[00177] В конкретных вариантах осуществления R2 представляет собой H.
[00178] В некоторых вариантах осуществления m равно 7 или 9.
[00179] В некоторых вариантах осуществления R4 выбирают из -(CH2)nQ и -(CH2)nCHQR.
[00180] В некоторых вариантах осуществления Q выбирают из группы, состоящей из -OR, -OH, -O(CH2)nN(R)2, -OC(O)R, -CX3, -CN, -N(R)C(O)R, -N(H)C(O)R, -N(R)S(O)2R,
-N(H)S(O)2R, -N(R)C(O)N(R)2, -N(H)C(O)N(R)2, -N(H)C(O)N(H)(R), -N(R)C(S)N(R)2,
-N(H)C(S)N(R)2, -N(H)C(S)N(H)(R), -C(R)N(R)2C(O)OR, -N(R)S(O)2R8, карбоцикла и гетероцикла.
[00181] В конкретных вариантах осуществления Q представляет собой -N(R)R8, -N(R)S(O)2R8, -O(CH2)nOR, -N(R)C(=NR9)N(R)2, -N(R)C(=CHR9)N(R)2, -OC(O)N(R)2 или -N(R)C(O)OR.
[00182] В конкретных вариантах осуществления Q представляет собой -N(OR)C(O)R, -N(OR)S(O)2R, -N(OR)C(O)OR, -N(OR)C(O)N(R)2, -N(OR)C(S)N(R)2, -N(OR)C(=NR9)N(R)2 или -N(OR)C(=CHR9)N(R)2.
[00183] В конкретных вариантах осуществления Q представляет собой тиомочевину или ее изостер, например, 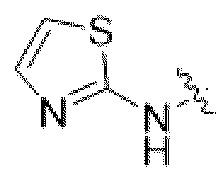 или -NHC(=NR9)N(R)2.
или -NHC(=NR9)N(R)2.
[00184] В конкретных вариантах осуществления Q представляет собой C(=NR9)N(R)2. Например, когда Q представляет собой C(=NR9)N(R)2, n равно 4 или 5. Например, R9 представляет собой -S(O)2N(R)2.
[00185] В конкретных вариантах осуществления Q представляет собой C(=NR9)R или C(O)N(R)OR, например, -CH(=N-OCH3), -C(O)NH-OH, -C(O)NH-OCH3, -C(O)N(CH3)-OH или C(O)N(CH3)-OCH3.
[00186] В конкретных вариантах осуществления Q представляет собой -OH.
[00187] В конкретных вариантах осуществления Q представляет собой замещенный или незамещенный 5-10 членный гетероарил, например, Q представляет собой триазол, имидазол, пиримидин, пурин, 2-амино-1,9-дигидро-6H-пурин-6-он-9-ил-(или гуанин-9-ил), аденин-9-ил, цитозин-1-ил или урацил-1-ил, каждый из которых необязательно замещен одним или более заместителями, выбранными из алкила, OH, алкокси, -алкил-OH, -алкил-O-алкила, и заместитель может быть дополнительно замещенным. В конкретных вариантах осуществления Q представляет собой замещенный 5-14-членный гетероциклоалкил, например, замещенный одним или более заместителями, выбранными из оксо (=O), OH, амино, моно- или ди-алкиламино и C1-3 алкила. Например, Q представляет собой 4-метилпиперазинил, 4-(4-метоксибензил)пиперазинил, изоиндолин-2-ил-1,3-дион, пирролидин-1-ил-2,5-дион или имидазолидин-3-ил-2,4-дион.
[00188] В конкретных вариантах осуществления Q представляет собой -NHR8, в которой R8 представляет собой C3-6 циклоалкил, необязательно замещенный одним или более заместителями, выбранными из оксо (=O), амино (NH2), моно- или ди-алкиламино, C1-3 алкила и галогена. Например, R8 представляет собой циклобутенил, например, 3-(диметиламино)-циклобут-3-ен-4-ил-1,2-дион. В дополнительных вариантах осуществления R8 представляет собой C3-6 циклоалкил, необязательно замещенный одним или более заместителями, выбранными из оксо (=O), тио (=S), амино (NH2), моно- или ди-алкиламино, C1-3 алкила, гетероциклоалкила и галогена, причем моно- или ди-алкиламино, C1-3 алкил и гетероциклоалкил дополнительно замещены Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо, амино и алкиламино, причем алкиламино дополнительно замещен, например, одним или более из C1-3 алкокси, амино, моно- или ди-алкиламино и галогена. Например, R8 представляет собой 3-(((диметиламино)этил)амино)циклобут-3-енил-1,2-дион. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо и алкиламино. Например, R8 представляет собой 3-(этиламино)циклобут-3-ен-1,2-дион. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо, тио и алкиламино. Например, R8 представляет собой 3-(этиламино)-4-тиоксоциклобут-2-ен-1-он или 2-(этиламино)-4-тиоксоциклобут-2-ен-1-он. Например, R8 представляет собой циклобутенил, замещенный одним или более из тио и алкиламино. Например, R8 представляет собой 3-(этиламино)циклобут-3-ен-1,2-дитион. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо и диалкиламино. Например, R8 представляет собой 3-(диэтиламино)циклобут-3-ен-1,2-дион. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо, тио и диалкиламино. Например, R8 представляет собой 2-(диэтиламино)-4-тиоксоциклобут-2-ен-1-он или 3-(диэтиламино)-4-тиоксоциклобут-2-ен-1-он. Например, R8 представляет собой циклобутенил, замещенный одним или более из тио и диалкиламино. Например, R8 представляет собой 3-(диэтиламино)циклобут-3-ен-1,2-дитион. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо и алкиламино или диалкиламино, причем алкиламино или диалкиламино дополнительно замещен, например, одним или более алкокси. Например, R8 представляет собой 3-(бис(2-метоксиэтил)амино)циклобут-3-ен-1,2-дион. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо и гетероциклоалкила. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо и пиперидинила, пиперазинила или морфолинила. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо и гетероциклоалкила, причем гетероциклоалкил дополнительно замещен, например, одним или более C1-3 алкилами. Например, R8 представляет собой циклобутенил, замещенный одним или более из оксо и гетероциклоалкила, причем гетероциклоалкил (например, пиперидинил, пиперазинил или морфолинил) дополнительно замещен метилом.
[00189] В конкретных вариантах осуществления Q представляет собой -NHR8, в которой R8 представляет собой гетероарил, необязательно замещенный одним или более заместителями, выбранными из амино (NH2), моно- или ди-алкиламино, C1-3 алкила и галогена. Например, R8 представляет собой тиазол или имидазол.
[00190] В конкретных вариантах осуществления Q представляет собой -NHC(=NR9)N(R)2, в которой R9 представляет собой CN, C1-6 алкил, NO2, -S(O)2N(R)2, -OR, -S(O)2R или H. Например, Q представляет собой -NHC(=NR9)N(CH3)2, -NHC(=NR9)NHCH3, -NHC(=NR9)NH2. В некоторых вариантах осуществления Q представляет собой -NHC(=NR9)N(R)2, в которой R9 представляет собой CN и R представляет собой C1-3 алкил, замещенный моно- или ди-алкиламино, например, R представляет собой ((диметиламино)этил)амино. В некоторых вариантах осуществления Q представляет собой -NHC(=NR9)N(R)2, в которой R9 представляет собой C1-6 алкил, NO2, -S(O)2N(R)2, -OR, -S(O)2R или H и R представляет собой C1-3 алкил, замещенный моно- или ди-алкиламино, например, R представляет собой ((диметиламино)этил)амино.
[00191] В конкретных вариантах осуществления Q представляет собой -NHC(=CHR9)N(R)2, в которой R9 представляет собой NO2, CN, C1-6 алкил, -S(O)2N(R)2, -OR, -S(O)2R или H. Например, Q представляет собой -NHC(=CHR9)N(CH3)2, -NHC(=CHR9)NHCH3 или -NHC(=CHR9)NH2.
[00192] В конкретных вариантах осуществления Q представляет собой -OC(O)N(R)2, -N(R)C(O)OR, -N(OR)C(O)OR, такой как -OC(O)NHCH3, -N(OH)C(O)OCH3, -N(OH)C(O)CH3, -N(OCH3)C(O)OCH3, -N(OCH3)C(O)CH3, -N(OH)S(O)2CH3 или -NHC(O)OCH3.
[00193] В конкретных вариантах осуществления Q представляет собой -N(R)C(O)R, в которой R представляет собой алкил, необязательно замещенный C1-3 алкоксилом или S(O)tC1-3 алкилом, в которой t равно 0, 1 или 2.
[00194] В конкретных вариантах осуществления Q представляет собой незамещенный или замещенный C6-10 арил (такой как фенил) или C3-6 циклоалкил.
[00195] В некоторых вариантах осуществления n равно 1. В других вариантах осуществления n равно 2. В дополнительных вариантах осуществления n равно 3. В определенных других вариантах осуществления n равно 4. Например, R4 может представлять собой -(CH2)2OH. Например, R4 может представлять собой -(CH2)3OH. Например, R4 может представлять собой -(CH2)4OH. Например, R4 может представлять собой бензил. Например, R4 может представлять собой 4-метоксибензил.
[00196] В некоторых вариантах осуществления R4 представляет собой C3-6 карбоцикл. В некоторых вариантах осуществления R4 представляет собой C3-6 циклоалкил. Например, R4 может представлять собой циклогексил необязательно замещенный, например, OH, галогеном, C1-6 алкилом, и.т.д. Например, R4 может представлять собой 2-гидроксициклогексил.
[00197] В некоторых вариантах осуществления R представляет собой H.
[00198] В некоторых вариантах осуществления R представляет собой C1-3 алкил, замещенный моно- или ди-алкиламино, например, R представляет собой ((диметиламино)этил)амино.
[00199] В некоторых вариантах осуществления R представляет собой C1-6 алкил, замещенный одним или более заместителями, выбранными из группы, состоящей из C1-3 алкоксила, амино и C1-C3 диалкиламино.
[00200] В некоторых вариантах осуществления R представляет собой незамещенный C1-3 алкил или незамещенный C2-3 алкенил. Например, R4 может представлять собой -CH2CH(OH)CH3, -CH(CH3)CH2OH или -CH2CH(OH)CH2CH3.
[00201] В некоторых вариантах осуществления R представляет собой замещенный C1-3 алкил, например, CH2OH. Например, R4 может представлять собой -CH2CH(OH)CH2OH, -(CH2)3NHC(O)CH2OH, -(CH2)3NHC(O)CH2OBn, -(CH2)2O(CH2)2OH, -(CH2)3NHCH2OCH3, -(CH2)3NHCH2OCH2CH3, CH2SCH3, CH2S(O)CH3, CH2S(O)2CH3 или -CH(CH2OH)2.
[00202] В некоторых вариантах осуществления R4 выбирают из любой из следующих групп:
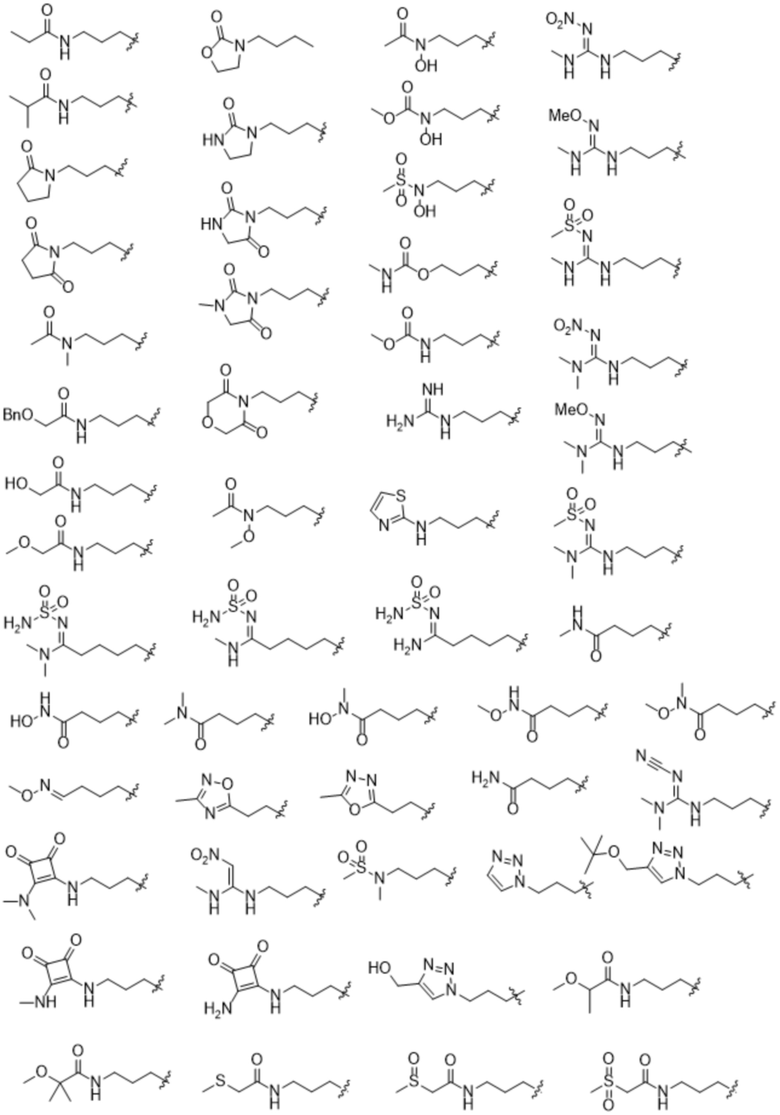


[00203] В некоторых вариантах осуществления R4 выбирают из любой из следующих групп:
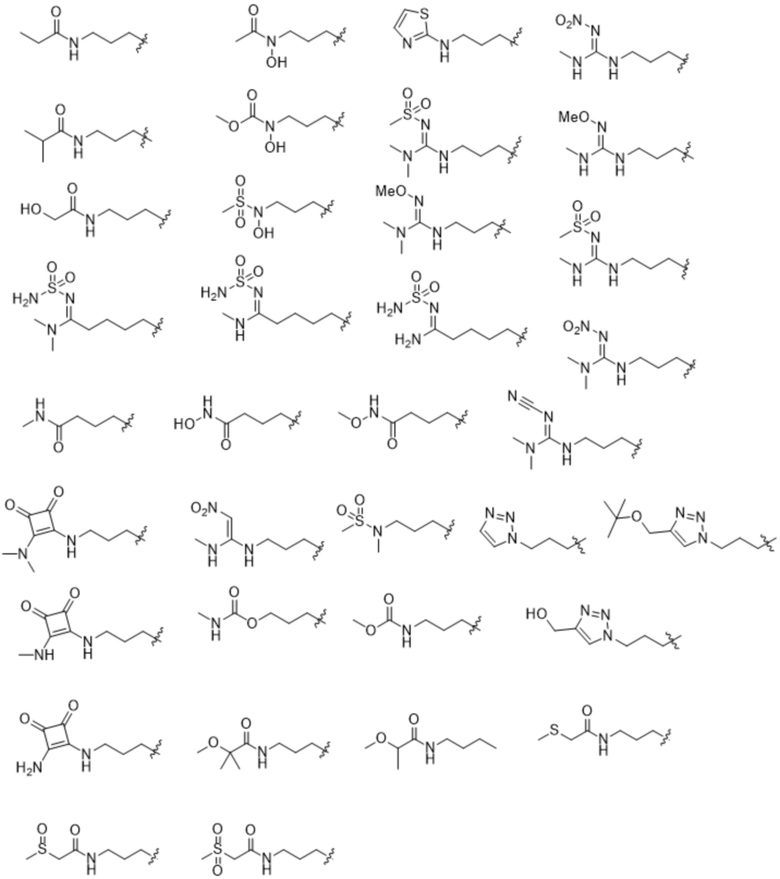
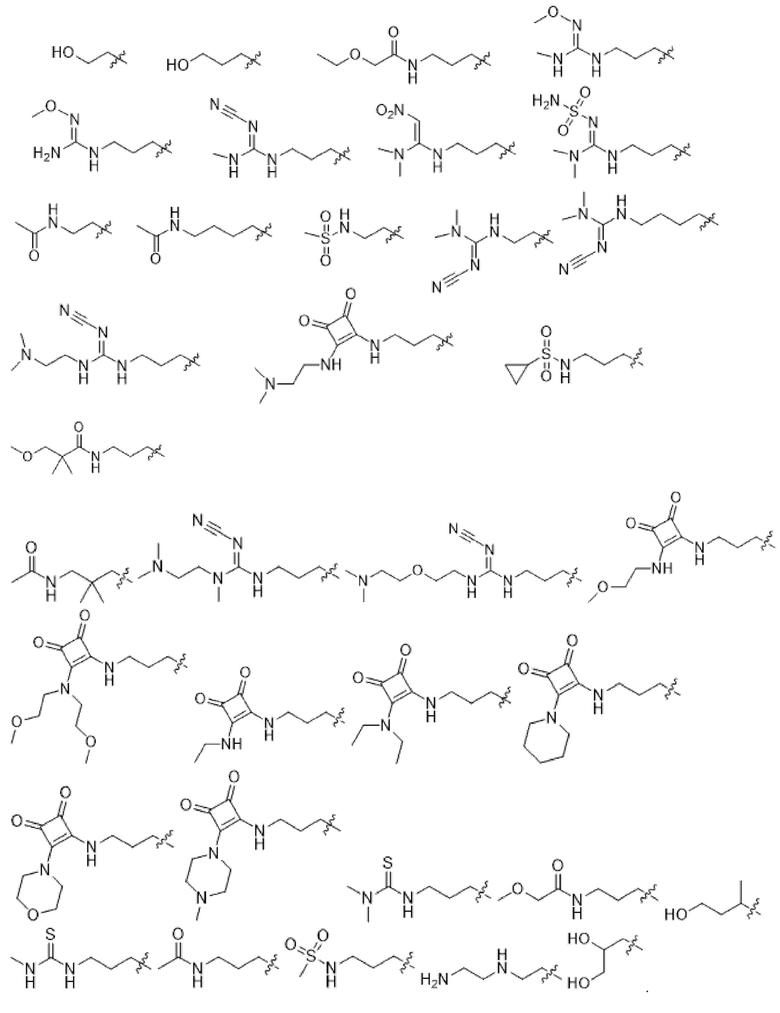
.
[00204] В некоторых вариантах осуществления, соединение формулы (III) дополнительно содержит анион. Как описано в данном документе, анионом может быть любой анион, способный вступать в реакцию с амином с образованием соли аммония. Примеры включают, но не ограничиваются ими, хлорид, бромид, иодид, фторид, ацетат, формиат, трифторацетат, дифторацетат, трихлорацетат и фосфат.
[00205] В некоторых вариантах осуществления соединение любой из формул, описанных в данном документе, пригодно для приготовления композиции наночастиц для внутримышечного введения.
[00206] В некоторых вариантах осуществления, R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл. В некоторых вариантах осуществления, R2 и R3, вместе с атомом, к которому они присоединены, образуют 5-14- членный ароматический или неароматический гетероцикл, имеющий один или более гетероатомов, выбранных из N, O, S и P. В некоторых вариантах осуществления R2 и R3, вместе с атомом, к которому они присоединены, образуют необязательно замещенный C3-20 карбоцикл (например, C3-18 карбоцикл, C3-15 карбоцикл, C3-12 карбоцикл, или C3-10 карбоцикл), как ароматический, так и неароматический. В некоторых вариантах осуществления R2 и R3, вместе с атомом, к которому они присоединены, образуют C3-6 карбоцикл. В других вариантах осуществления R2 и R3, вместе с атомом, к которому они присоединены, образуют C6 карбоцикл, такой как циклогексильная или фенильная группа. В конкретных вариантах осуществления гетероцикл или C3-6 карбоцикл замещен одной или более алкильными группами (например, по одному и тому же кольцевому атому или по смежному или по не смежным атомам). Например, R2 и R3, вместе с атомом, к которому они присоединены, могут образовать циклогексильную или фенильную группу, несущую один или более C5 алкильных заместителей. В конкретных вариантах осуществления гетероцикл или C3-6 карбоцикл, образованный R2 и R3, замещен карбоциклическими группами. Например, R2 и R3, вместе с атомом, к которому они присоединены, могут образовать циклогексильную или фенильную группу, которая замещена циклогексилом. В некоторых вариантах осуществления R2 и R3, вместе с атомом, к которому они присоединены, образуют C7-15 карбоцикл, такой как циклогептильная, циклопентадеканильная или нафтильная группа.
[00207] В некоторых вариантах осуществления R4 выбирают из -(CH2)nQ и -(CH2)nCHQR. В некоторых вариантах осуществления Q выбирают из группы, состоящей из -OR, -OH, -O(CH2)nN(R)2, -OC(O)R,
-CX3, -CN, -N(R)C(O)R, -N(H)C(O)R, -N(R)S(O)2R, -N(H)S(O)2R, -N(R)C(O)N(R)2, -N(H)C(O)N(R)2, -N(R)S(O)2R8, -N(H)C(O)N(H)(R), -N(R)C(S)N(R)2, -N(H)C(S)N(R)2, -N(H)C(S)N(H)(R) и гетероцикла. В других вариантах осуществления Q выбирают из группы, состоящей из имидазола, пиримидина и пурина.
[00208] В некоторых вариантах осуществления, R2 и R3, вместе с атомом, к которому они присоединены, образуют гетероцикл или карбоцикл. В некоторых вариантах осуществления R2 и R3, вместе с атомом, к которому они присоединены, образуют C3-6 карбоцикл, такой как фенильная группа. В конкретных вариантах осуществления гетероцикл или C3-6 карбоцикл замещен одной или более алкильными группами (например, по одному и тому же кольцевому атому или по смежному или по не смежным атомам). Например, R2 и R3, вместе с атомом, к которому они присоединены, могут образовать фенильную группу, несущую один или более C5 алкильных заместителей.
[00209] В некоторых вариантах осуществления, по меньшей мере один из случаев R5 и R6 представляет собой C1-3 алкил, например, метил. В некоторых вариантах осуществления один из R5 и R6, прилежащий к М, представляет собой C1-3 алкил, например, метил, а другой представляет собой H. В некоторых вариантах осуществления один из R5 и R6, прилежащий к М, представляет собой C1-3 алкил, например, метил, а другой представляет собой H и M представляет собой -OC(O)- или -C(O)O-.
[00210] В некоторых вариантах осуществления не более чем в одном случае R5 и R6 представляет собой C1-3 алкил, например, метил. В некоторых вариантах осуществления один из R5 и R6, прилежащий к М, представляет собой C1-3 алкил, например, метил, а другой представляет собой H. В некоторых вариантах осуществления один из R5 и R6, прилежащий к М, представляет собой C1-3 алкил, например, метил, а другой представляет собой H и M представляет собой -OC(O)- или -C(O)O-.
[00211] В некоторых вариантах осуществления каждый случай R5 и R6 представляет собой H.
[00212] В некоторых вариантах осуществления соединение формулы (I) выбирают из группы, состоящей из:

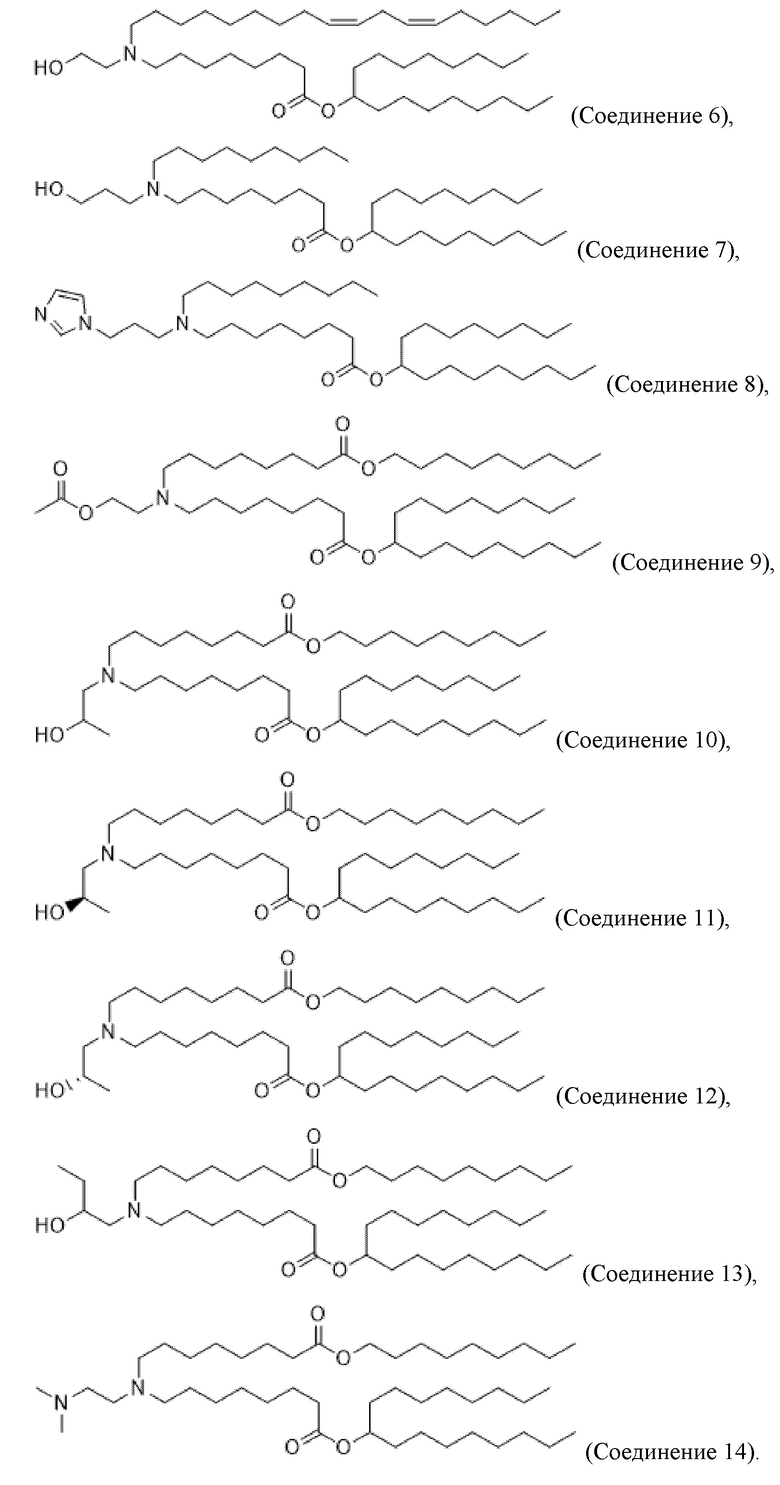

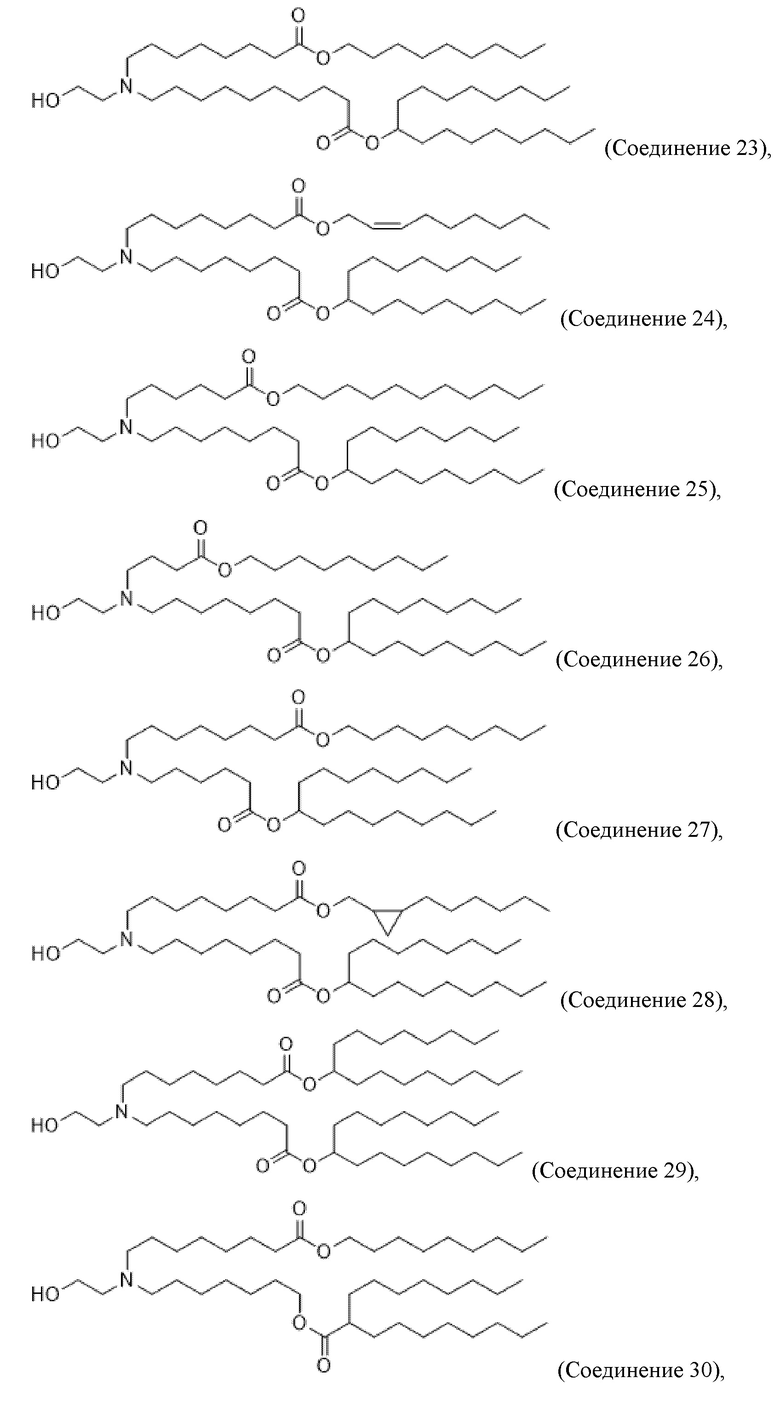
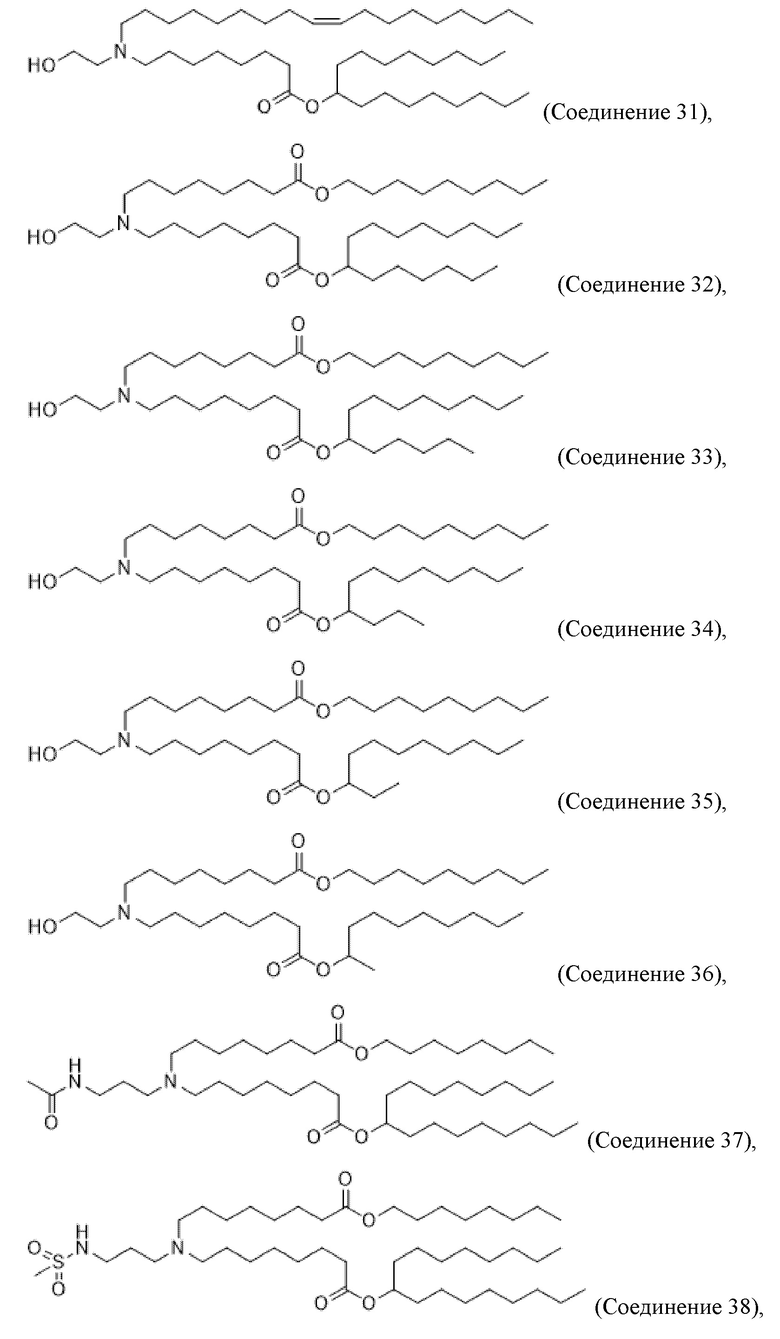
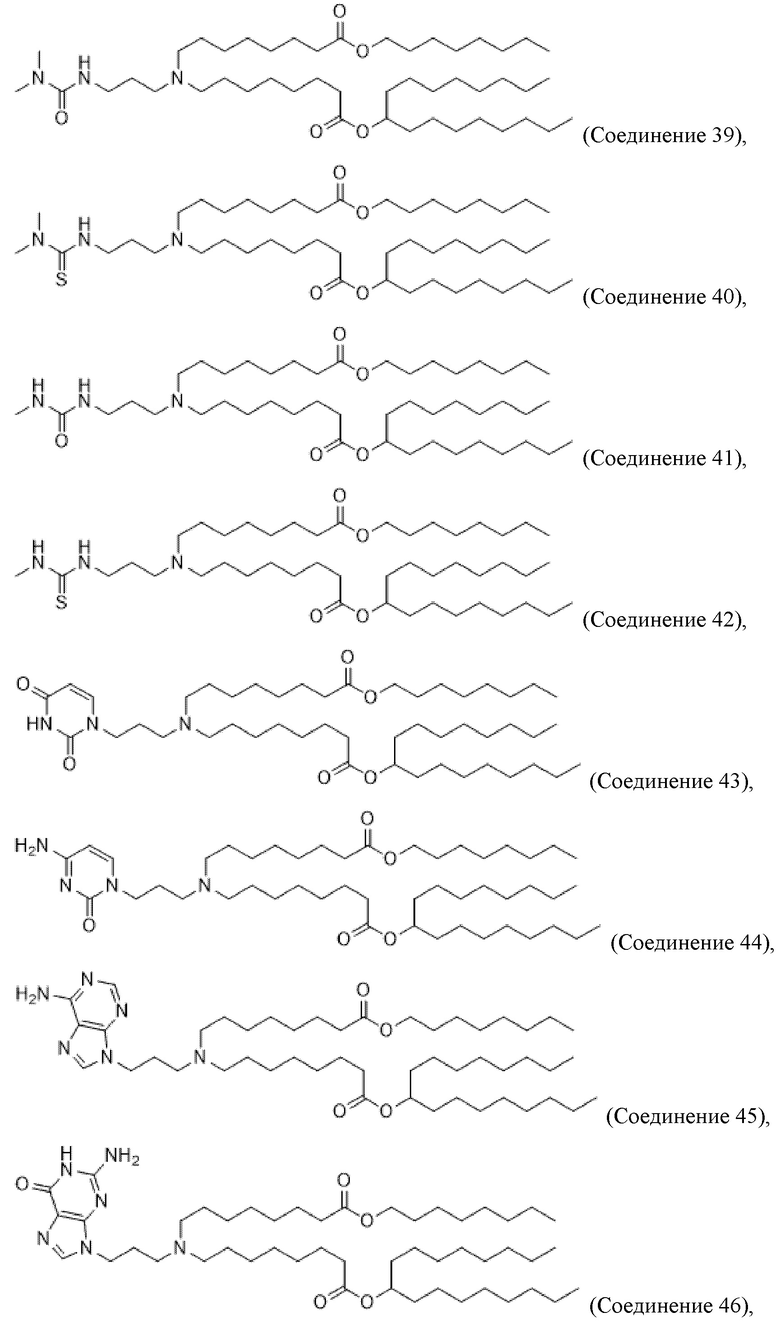
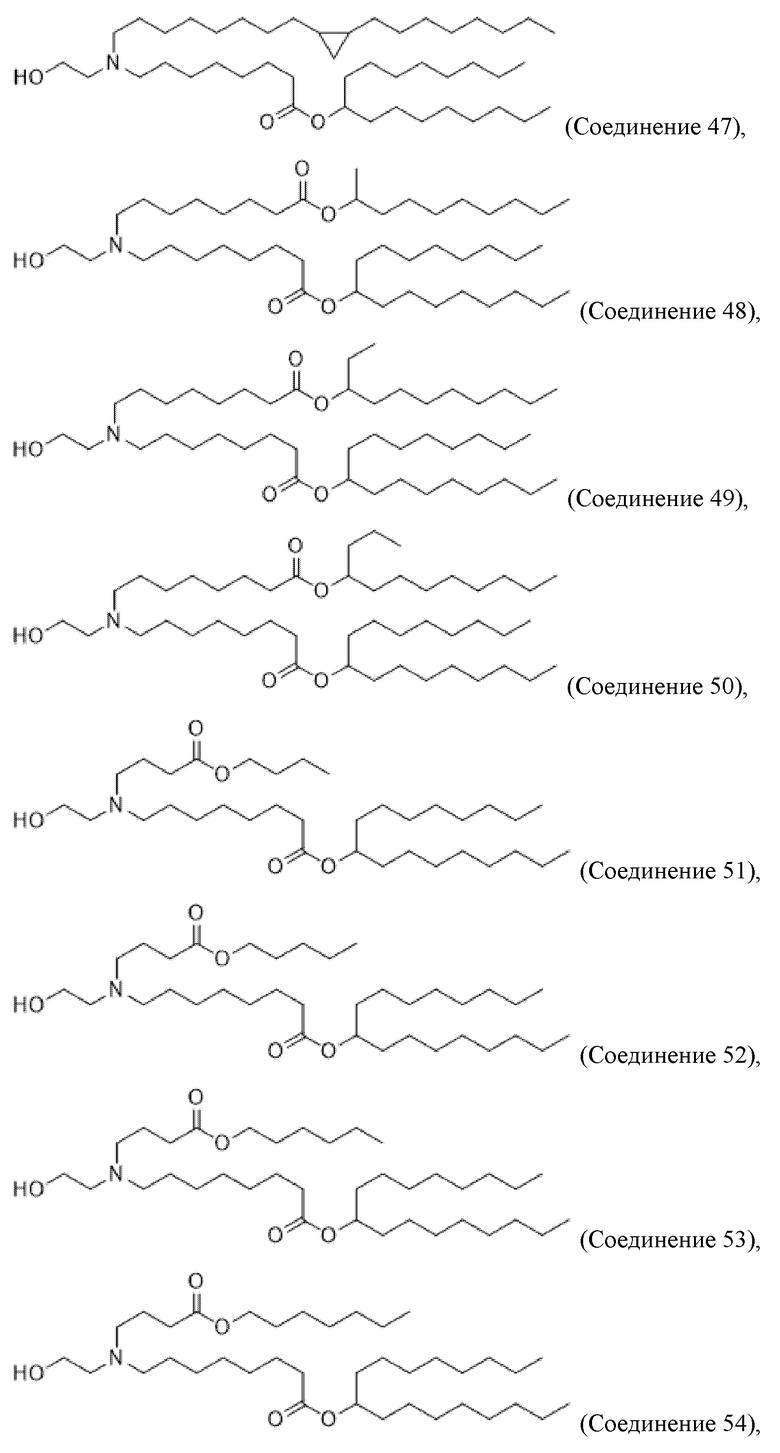

[00213] В дополнительных вариантах осуществления соединение формулы (I) выбирают из группы, состоящей из:
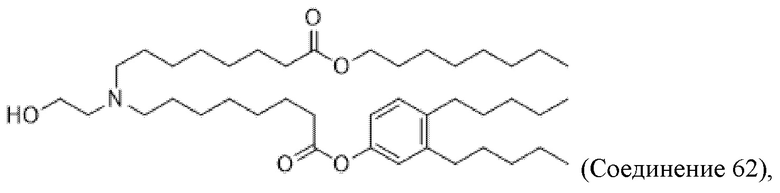
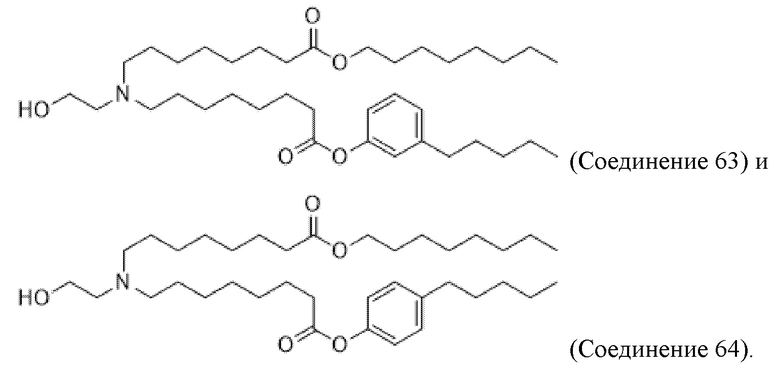
[00214] В некоторых вариантах осуществления соединение формулы (I) выбирают из группы, состоящей из:
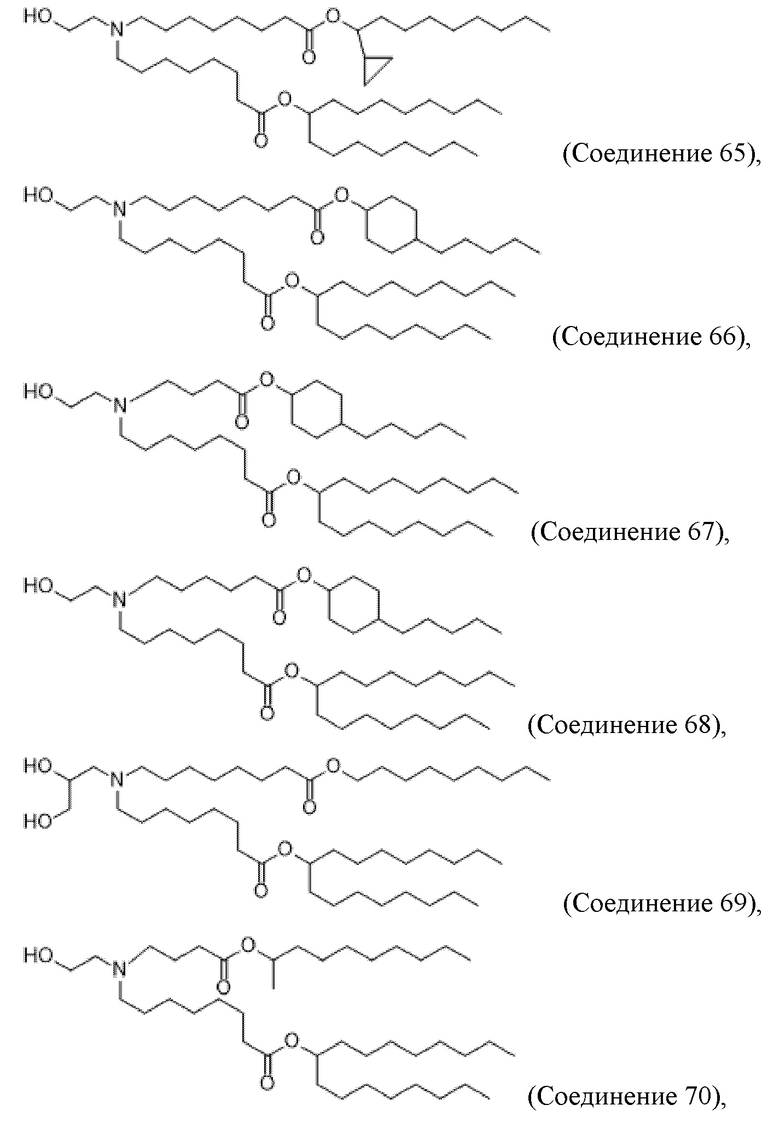

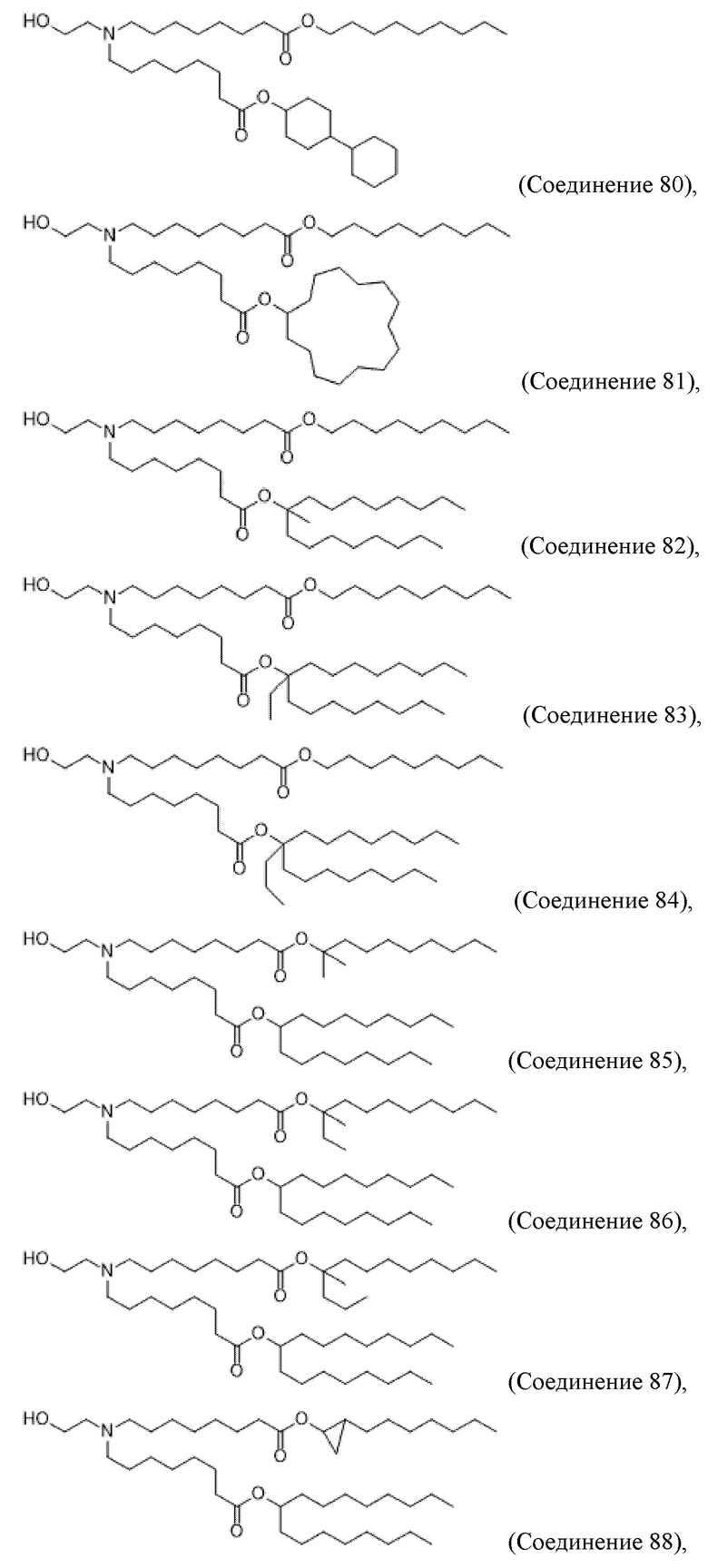
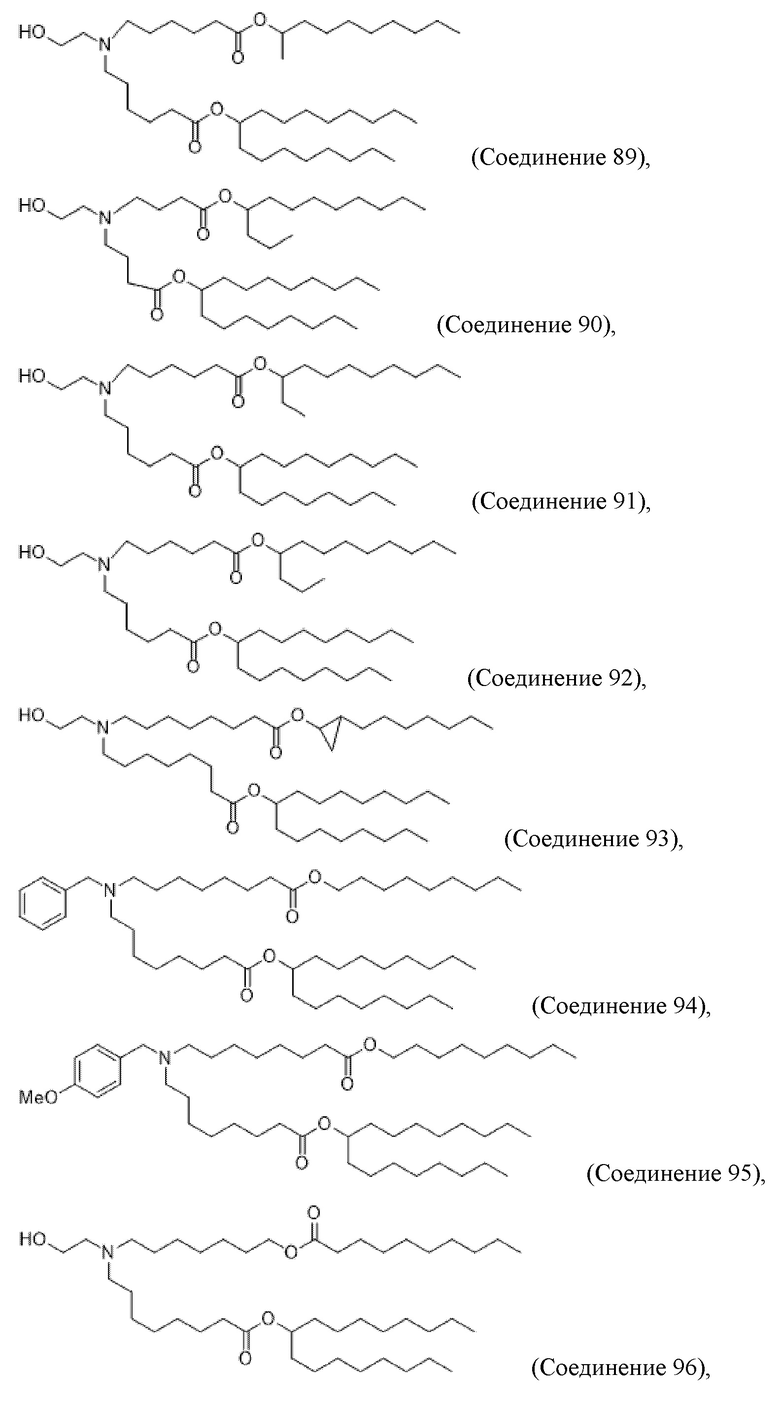
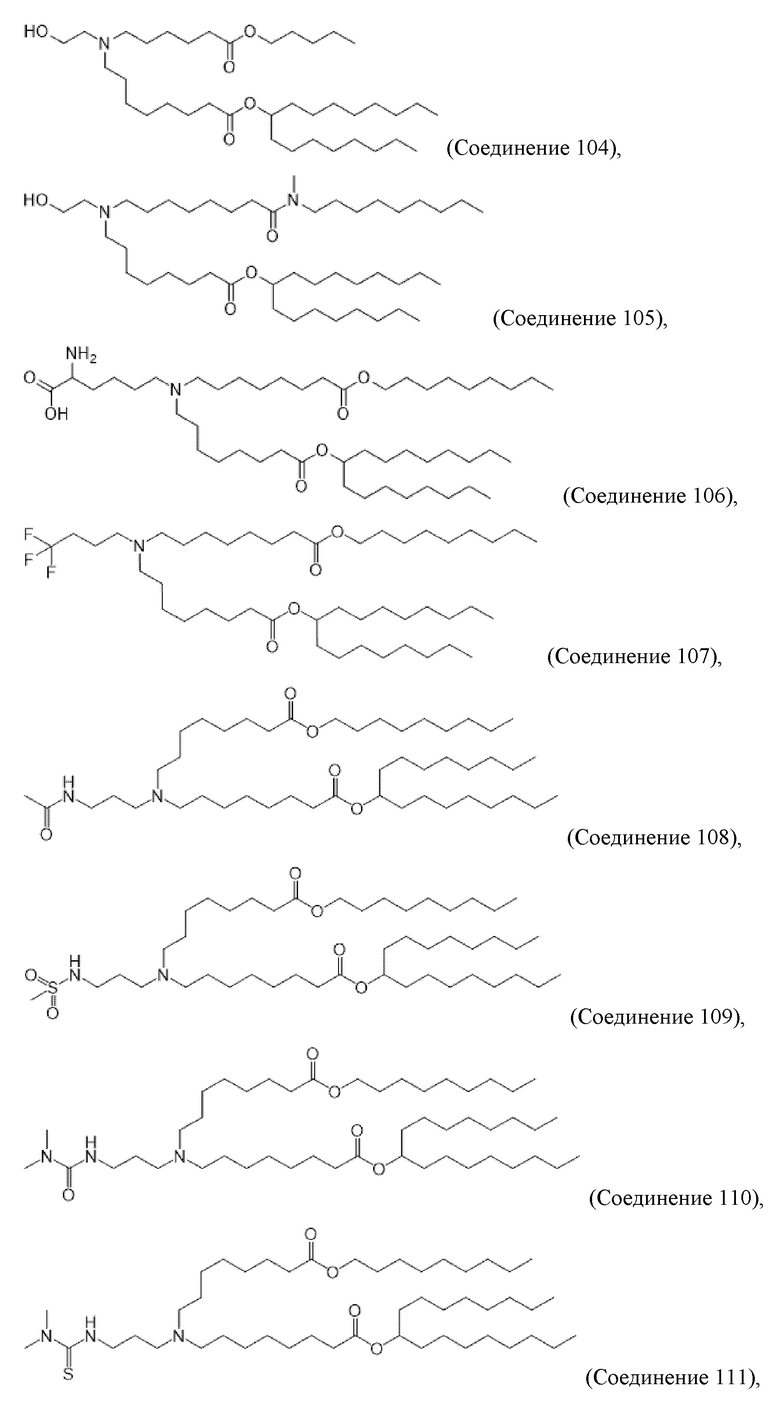
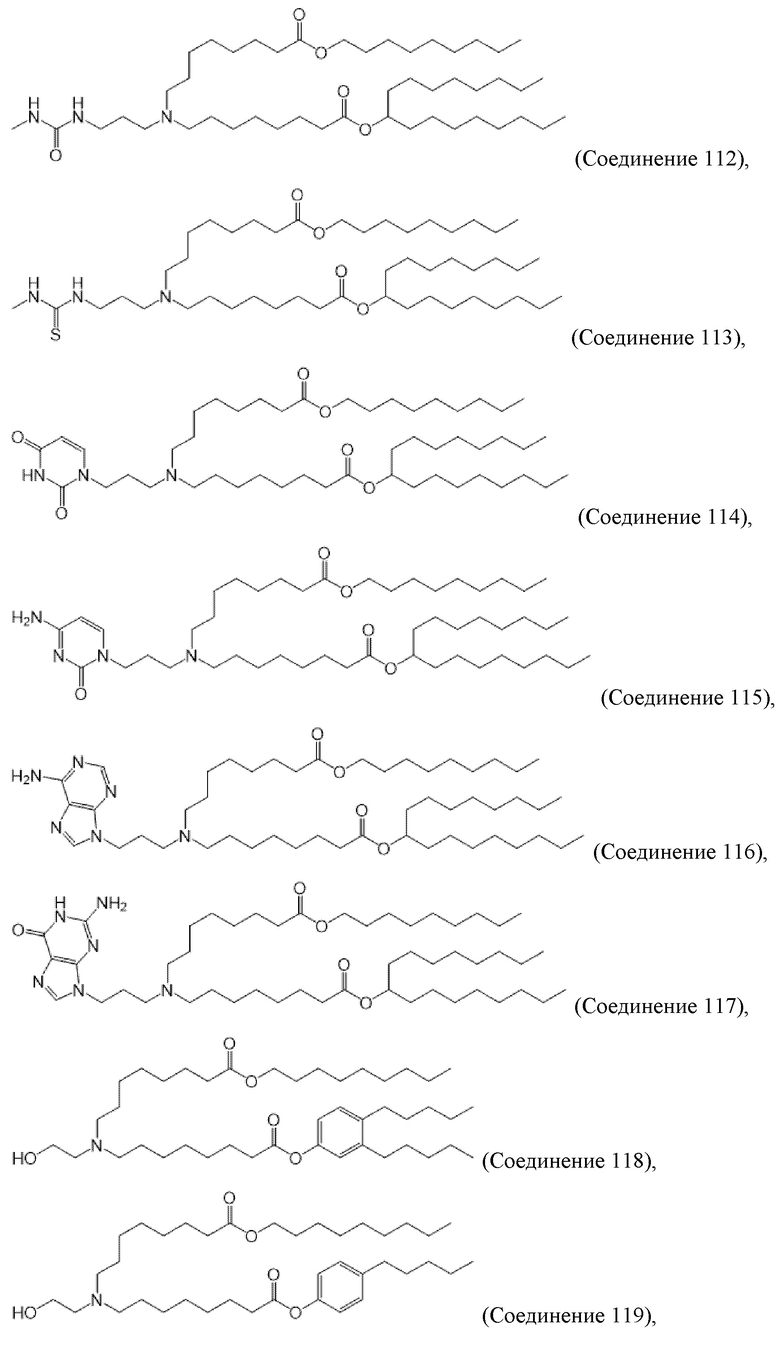
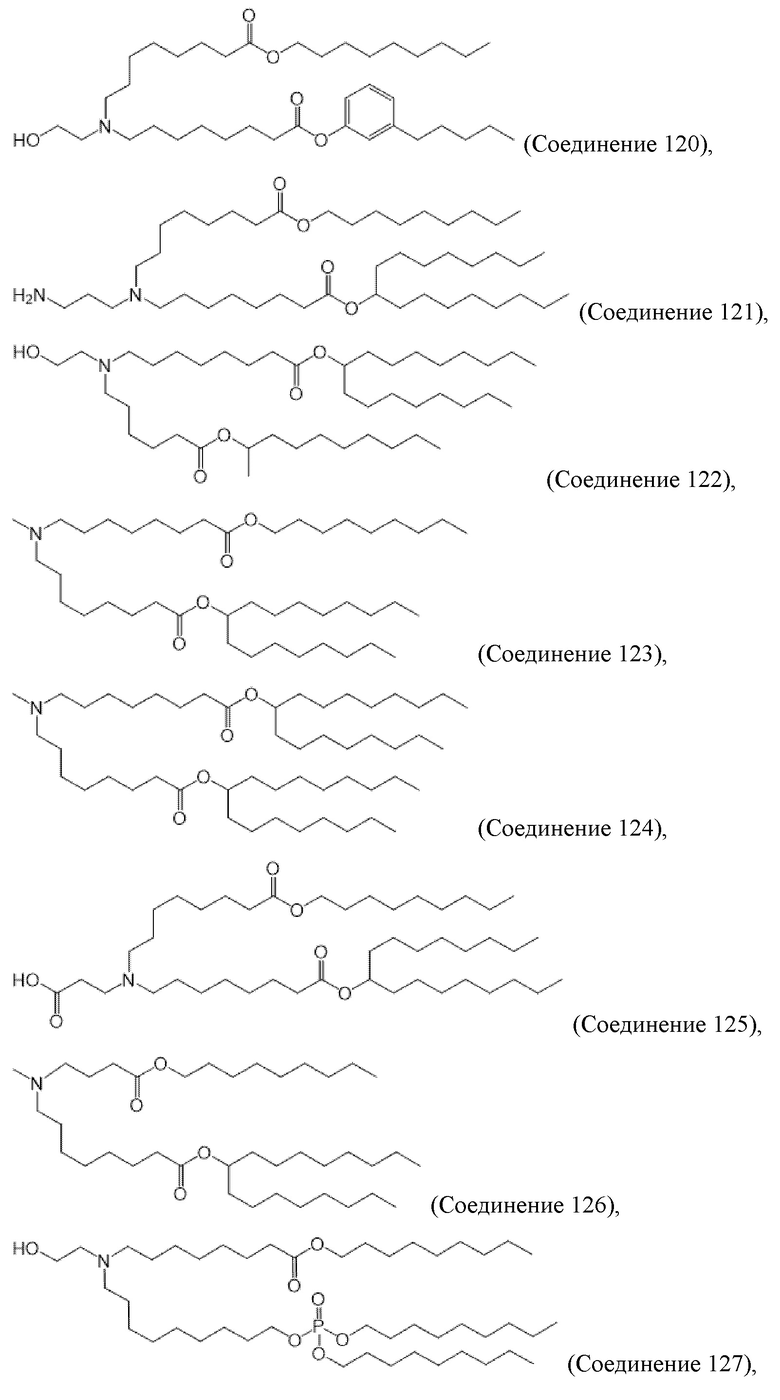
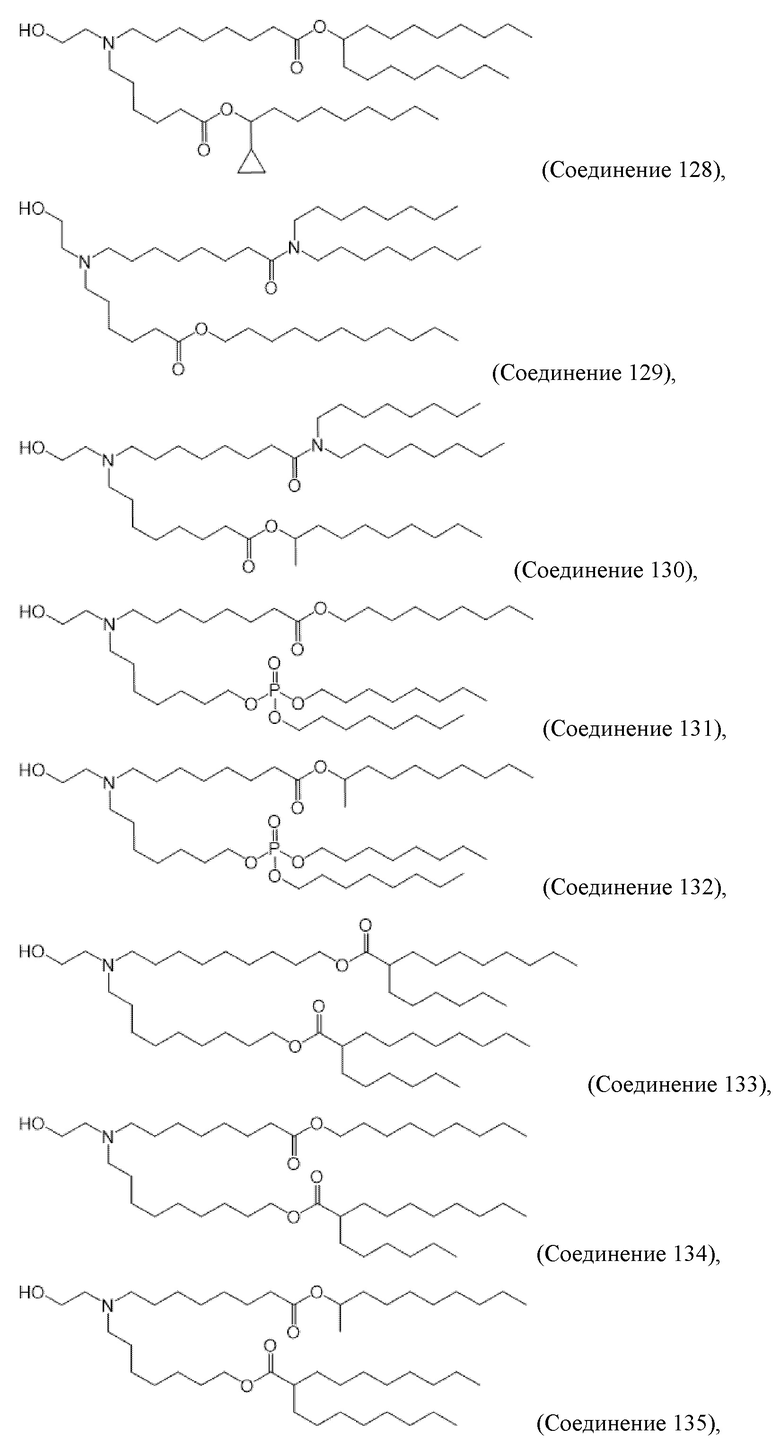
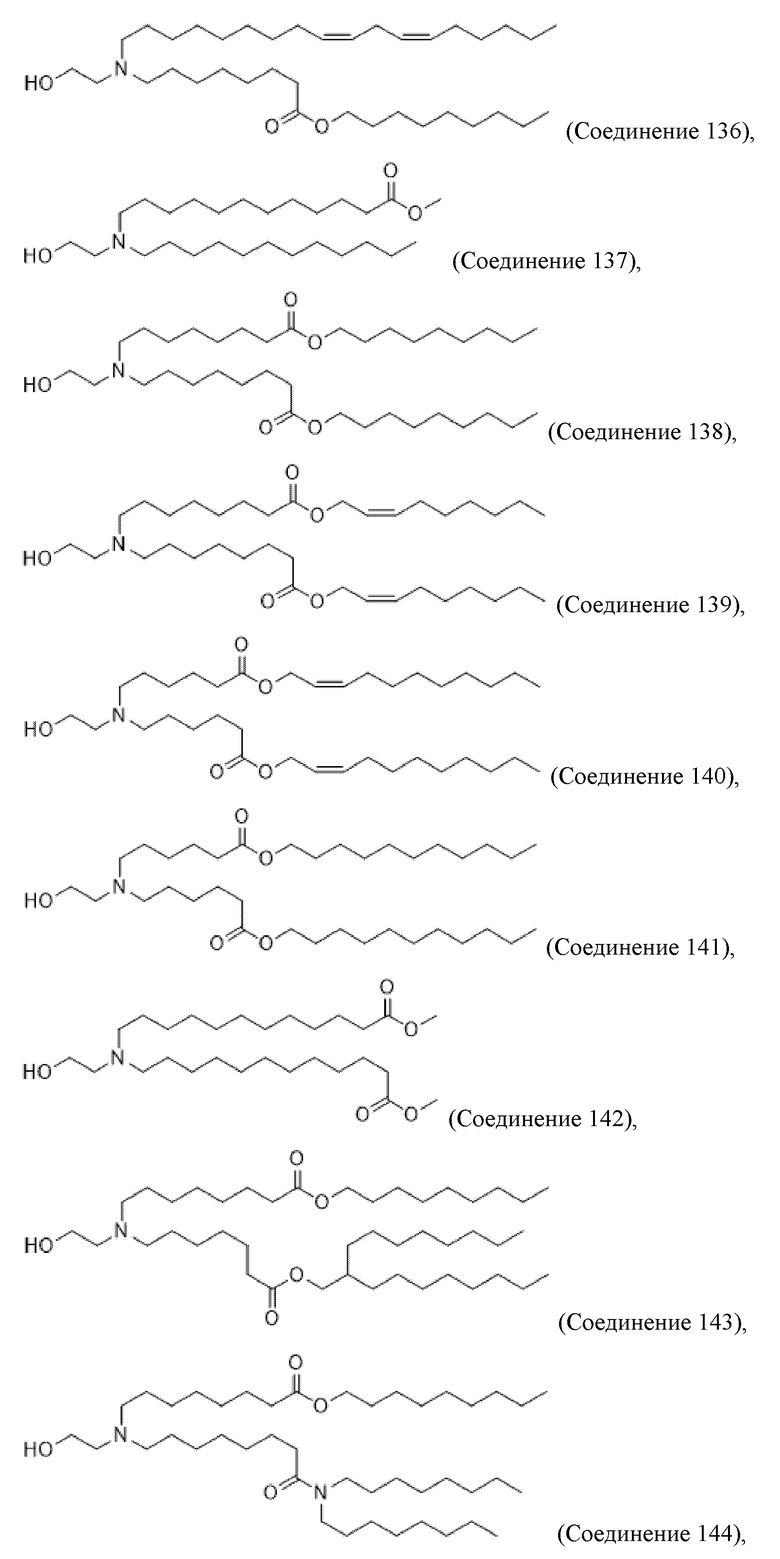

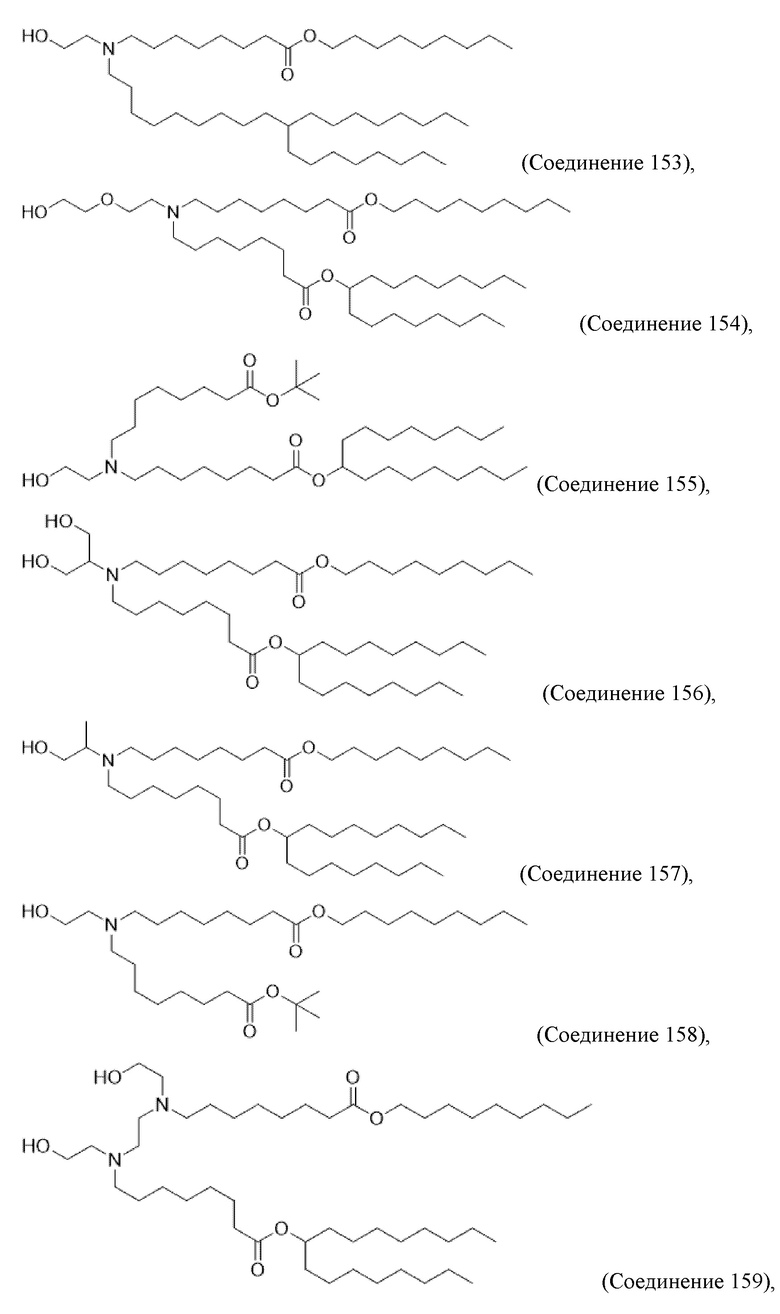
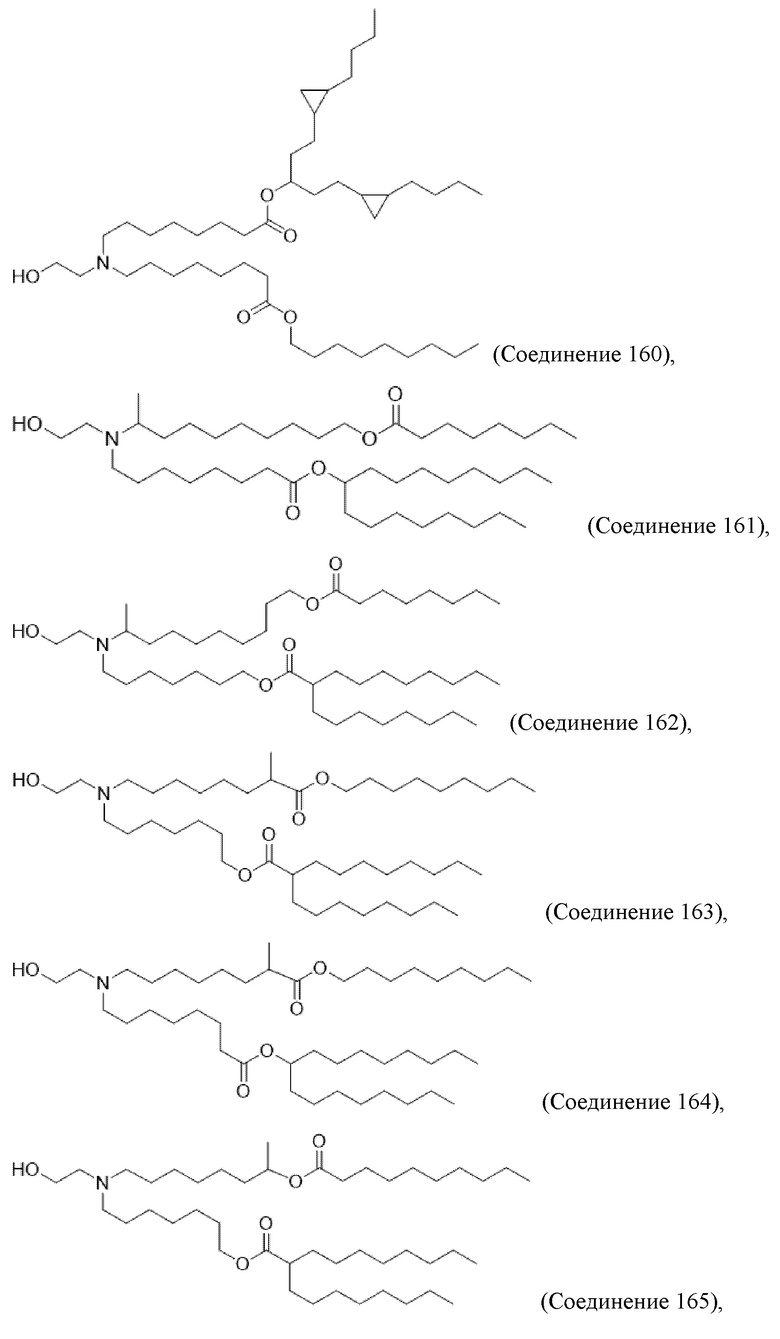
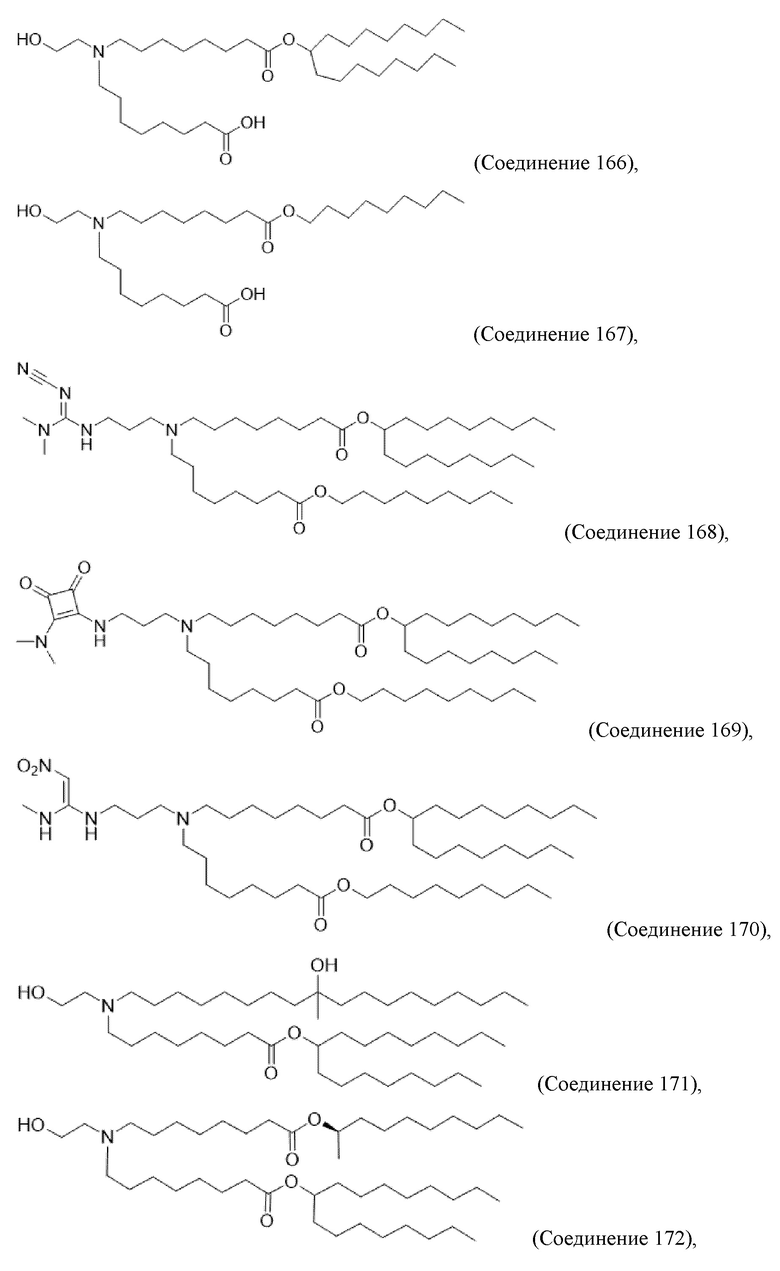

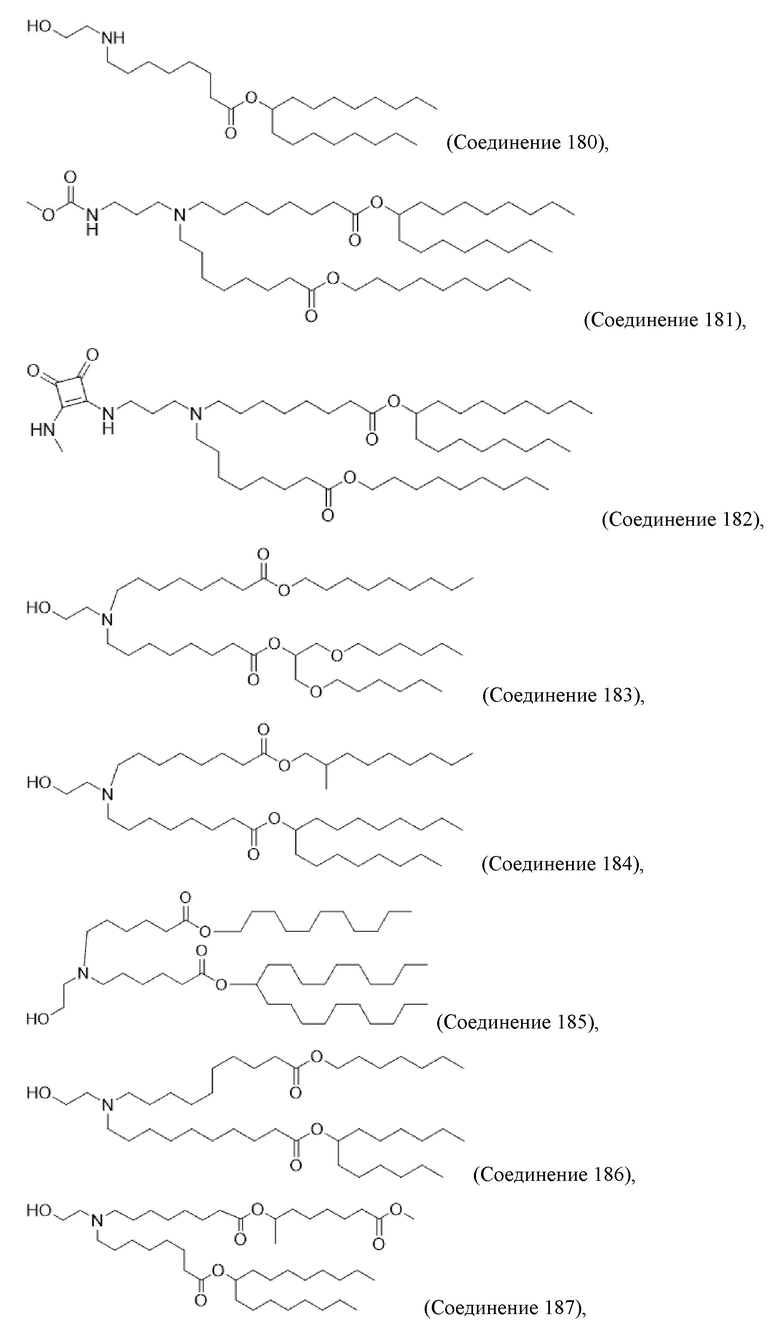
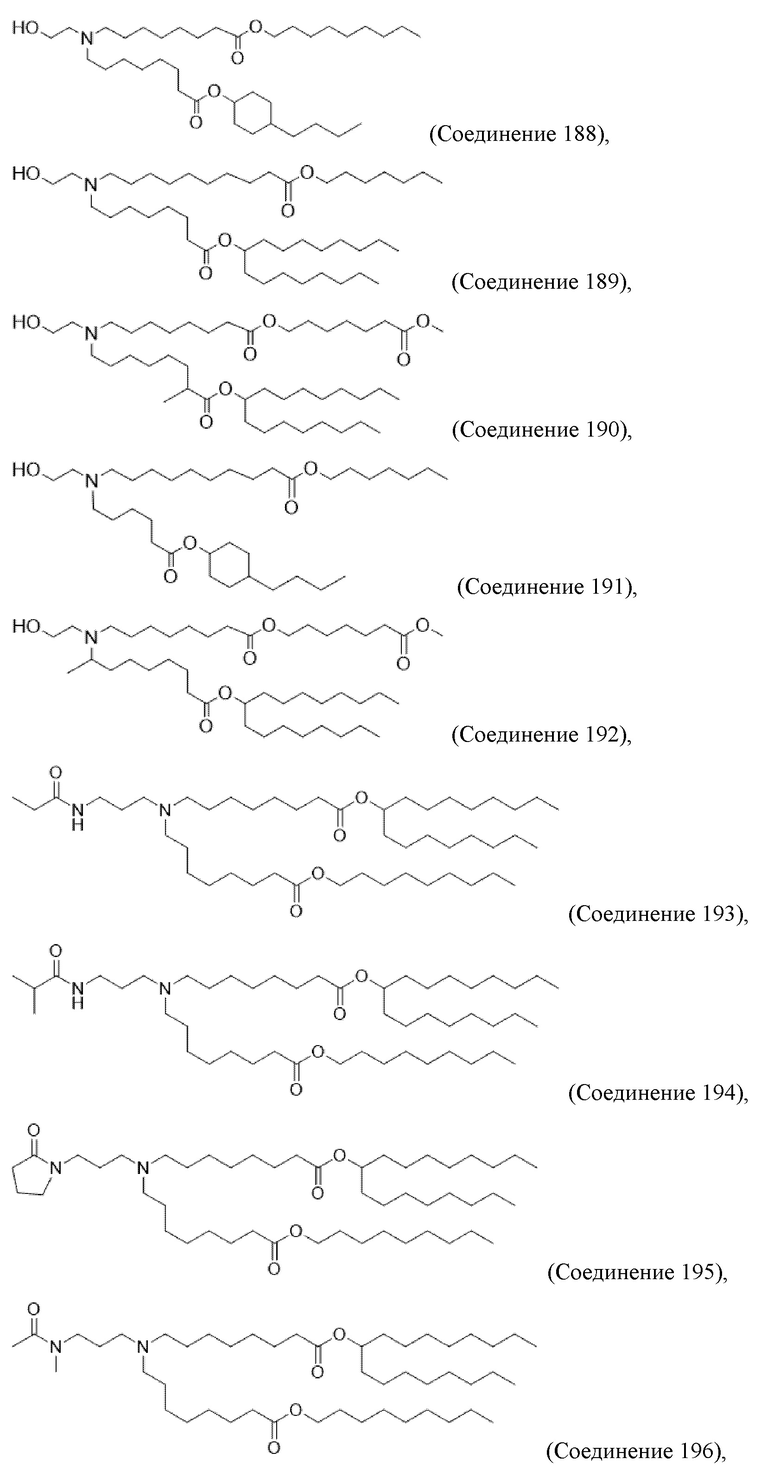
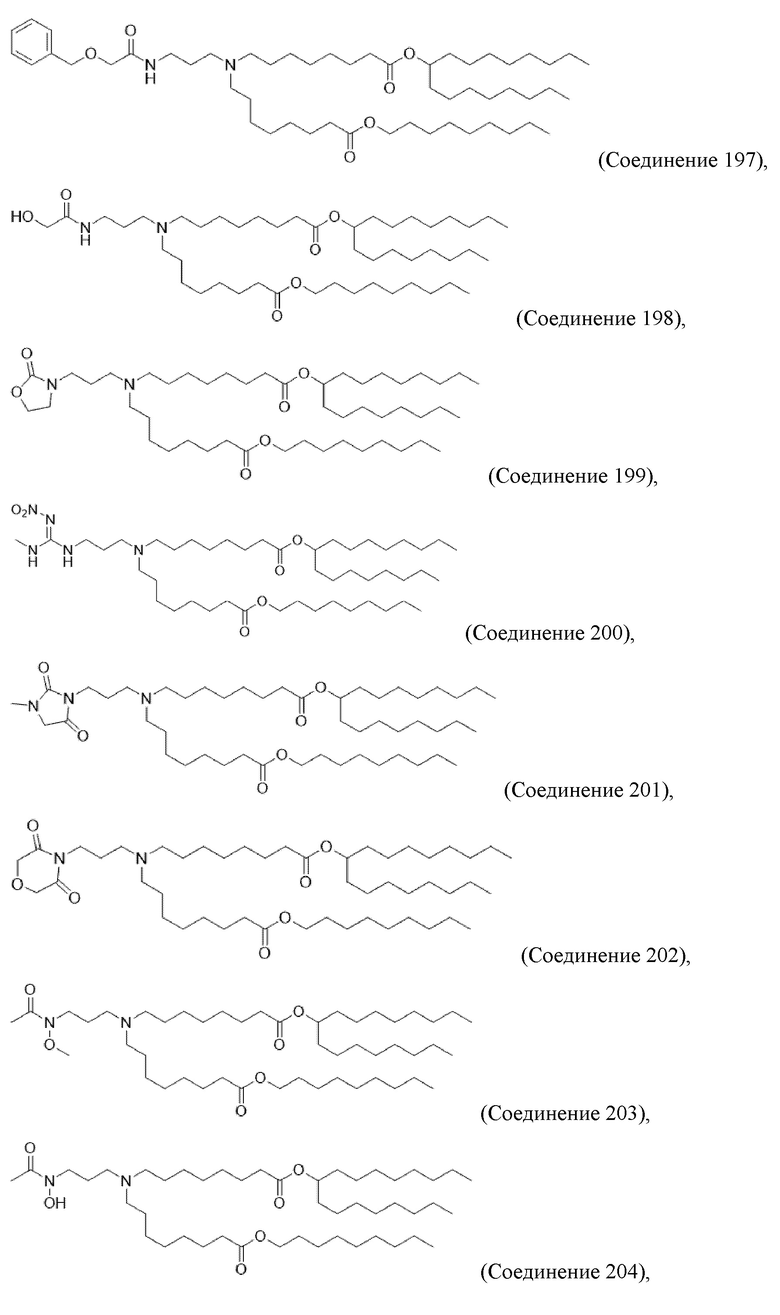
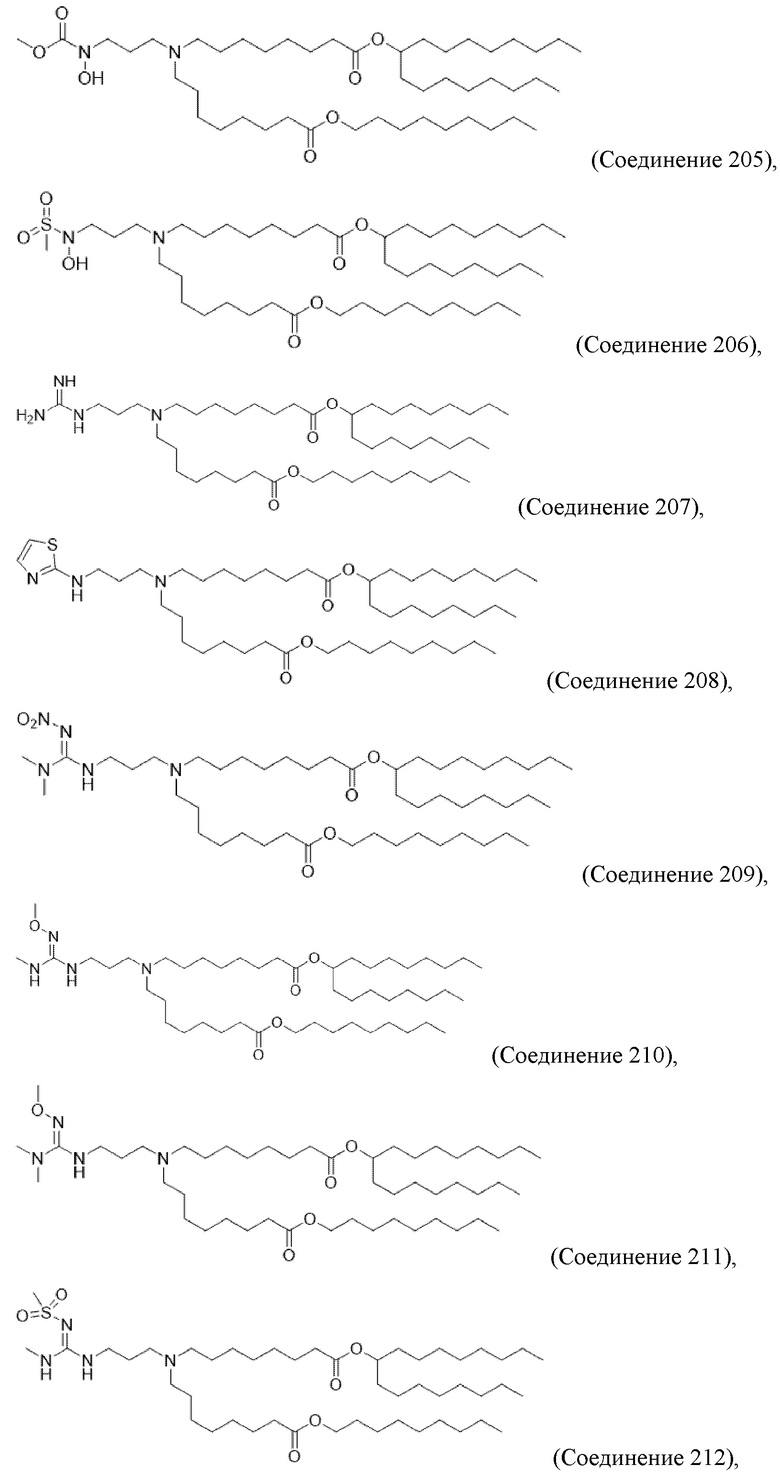

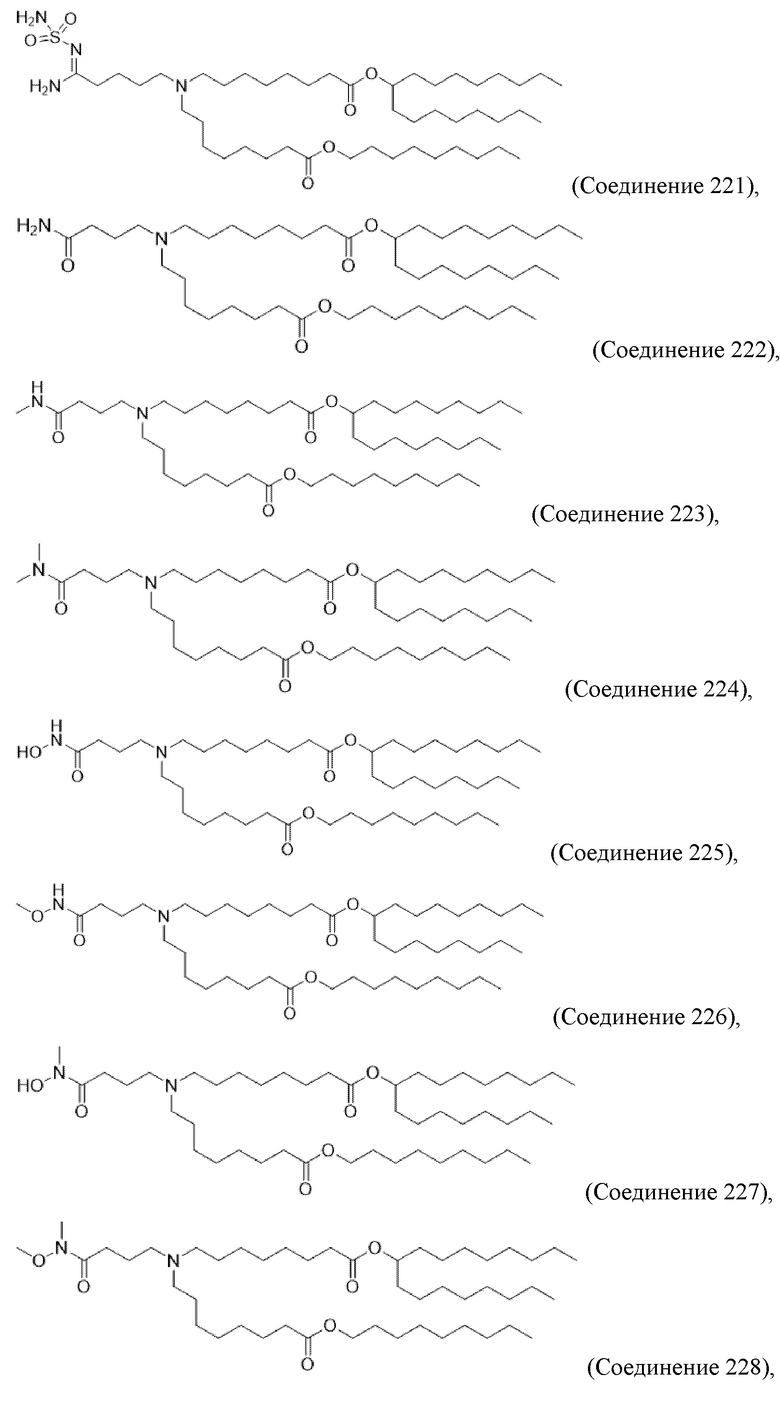
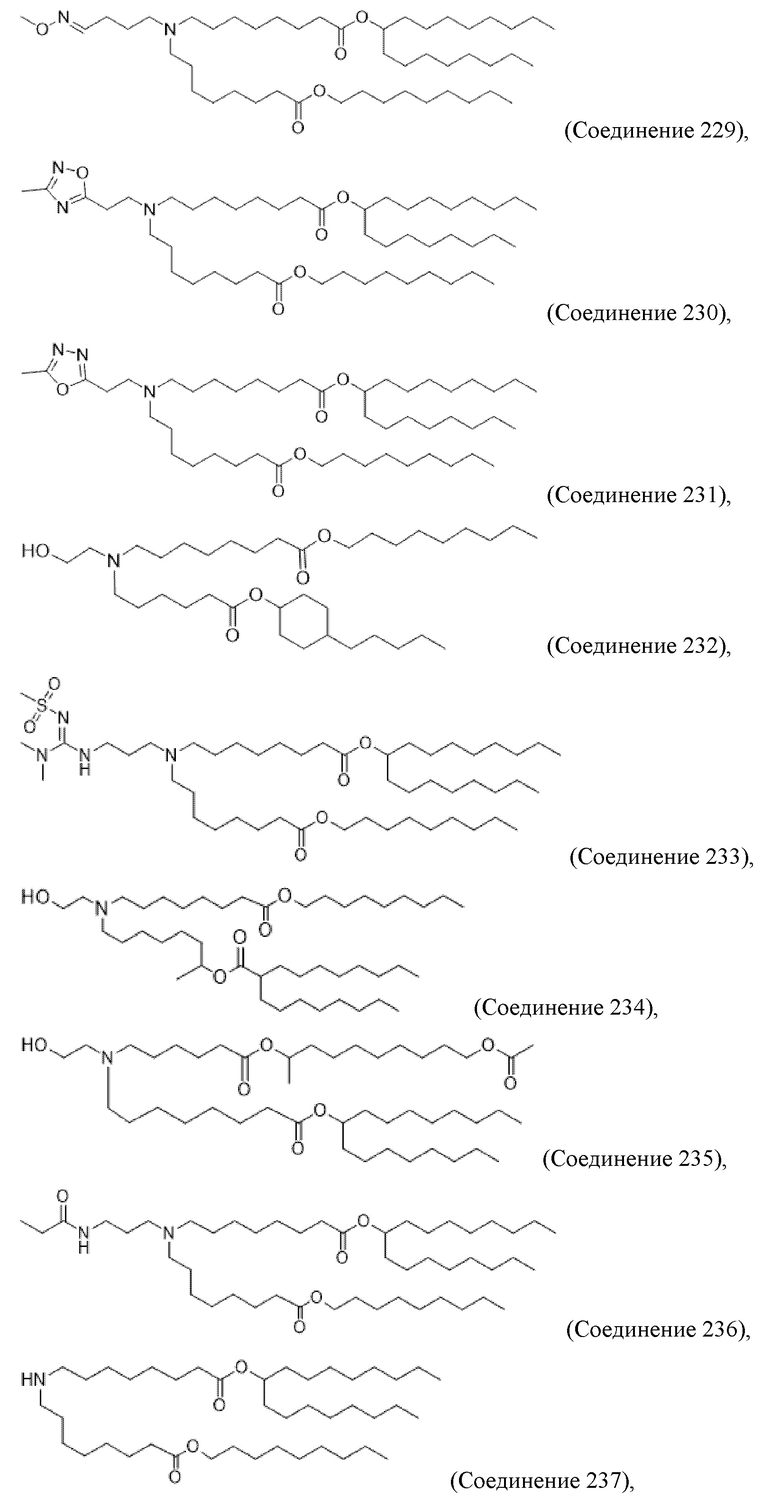
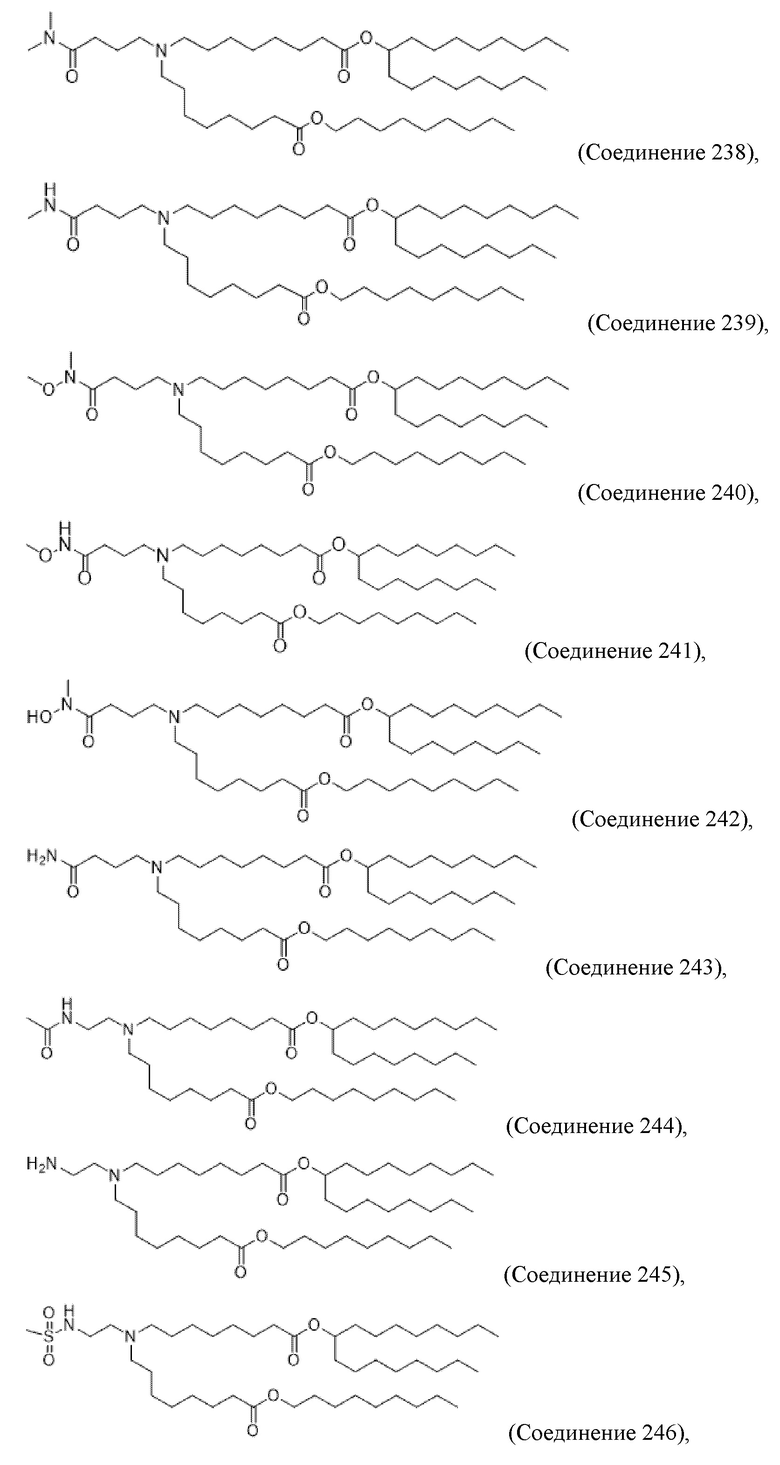
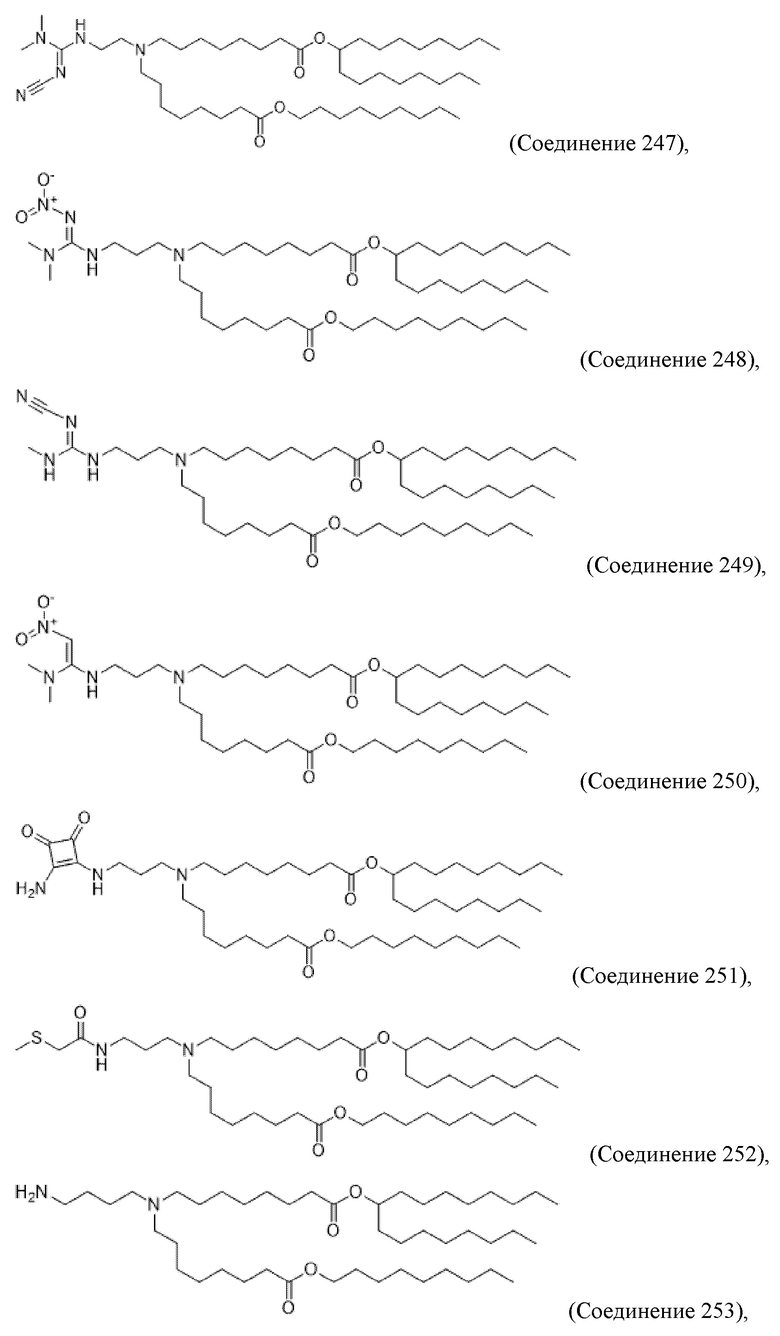
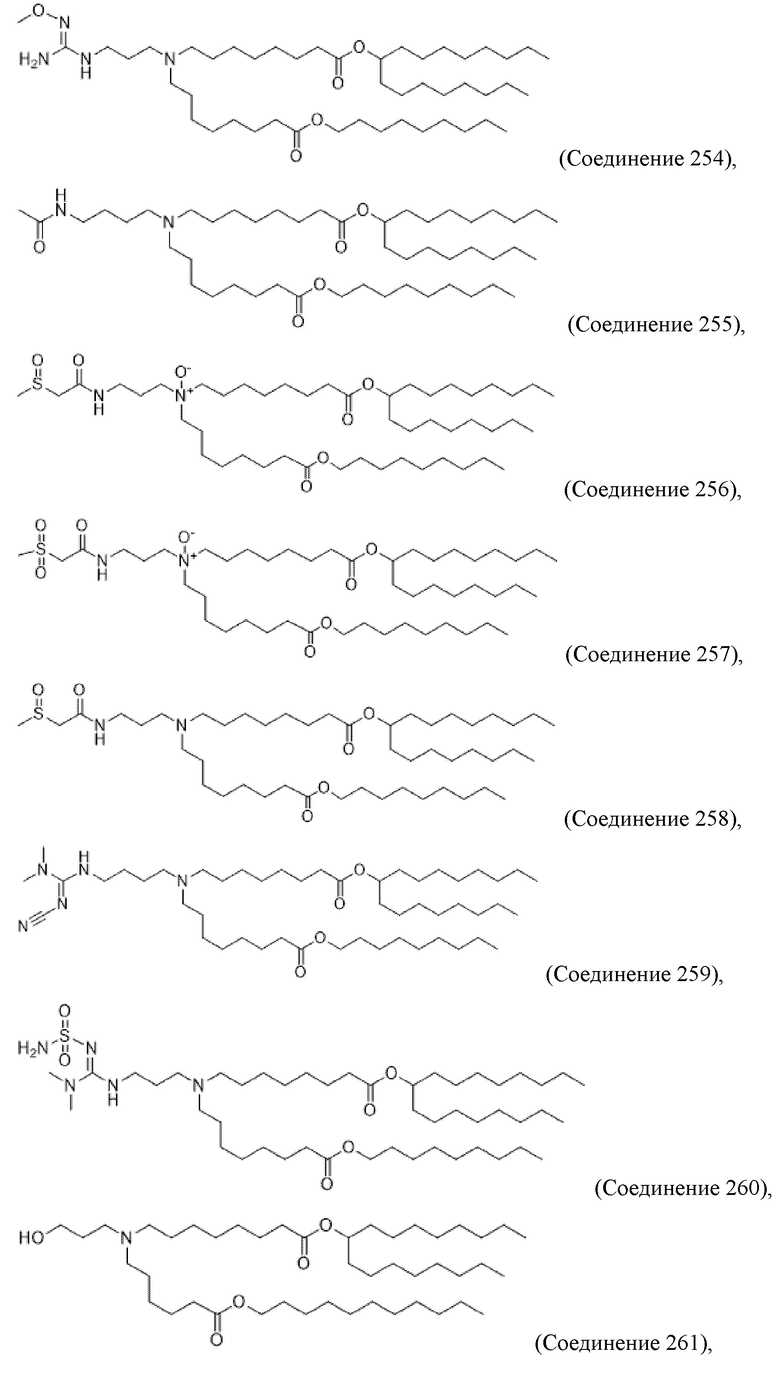
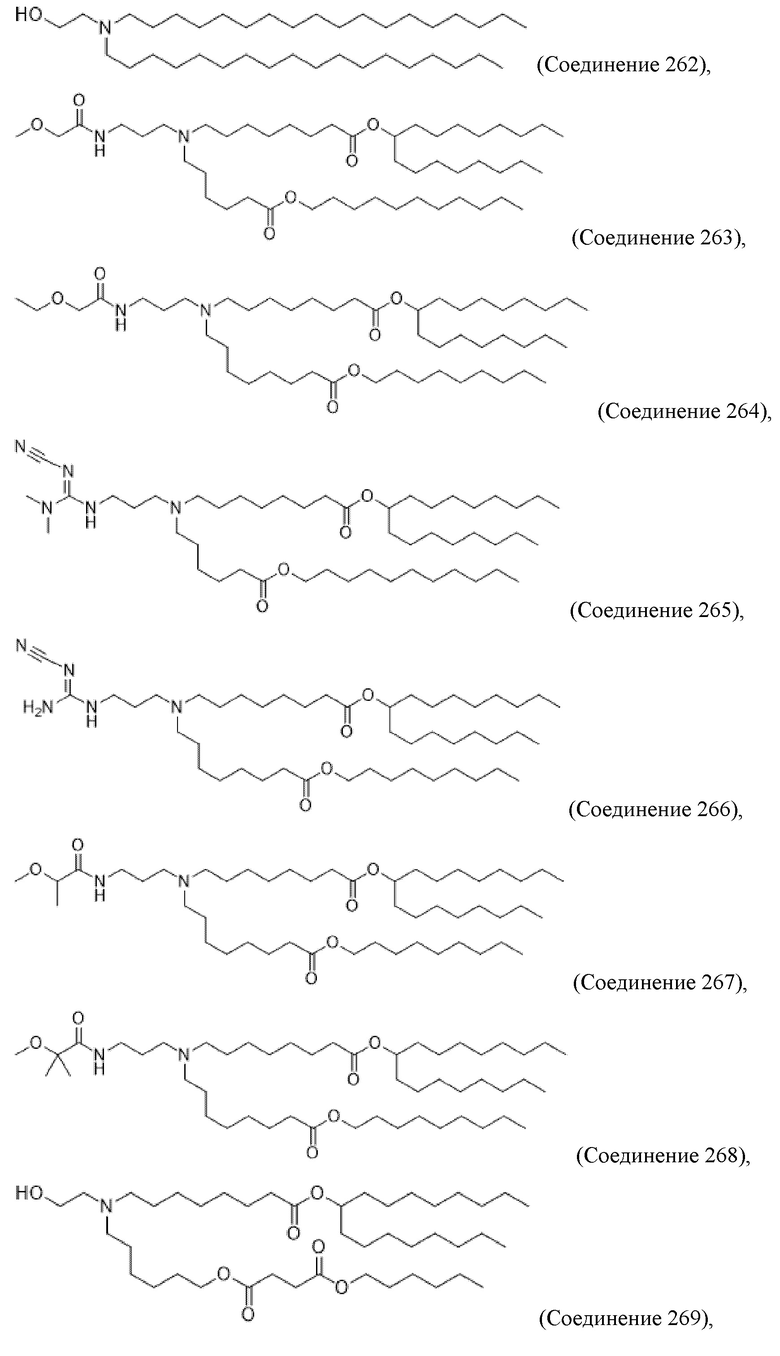
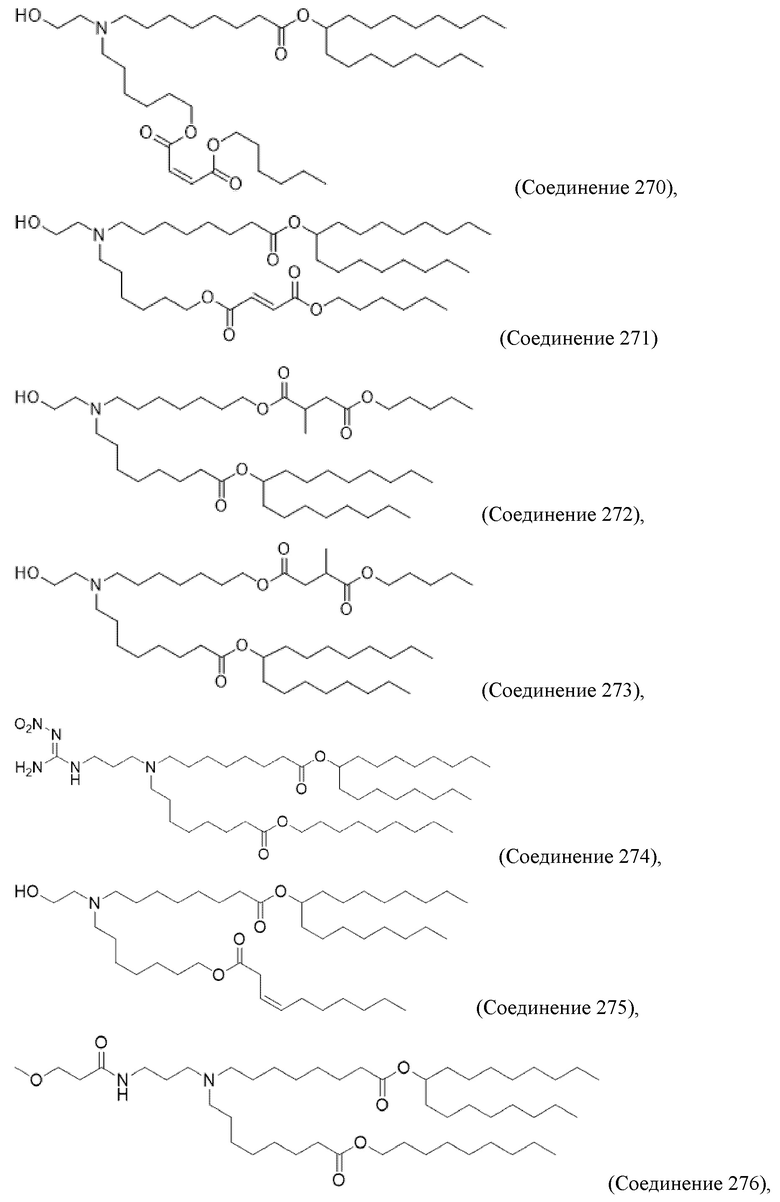

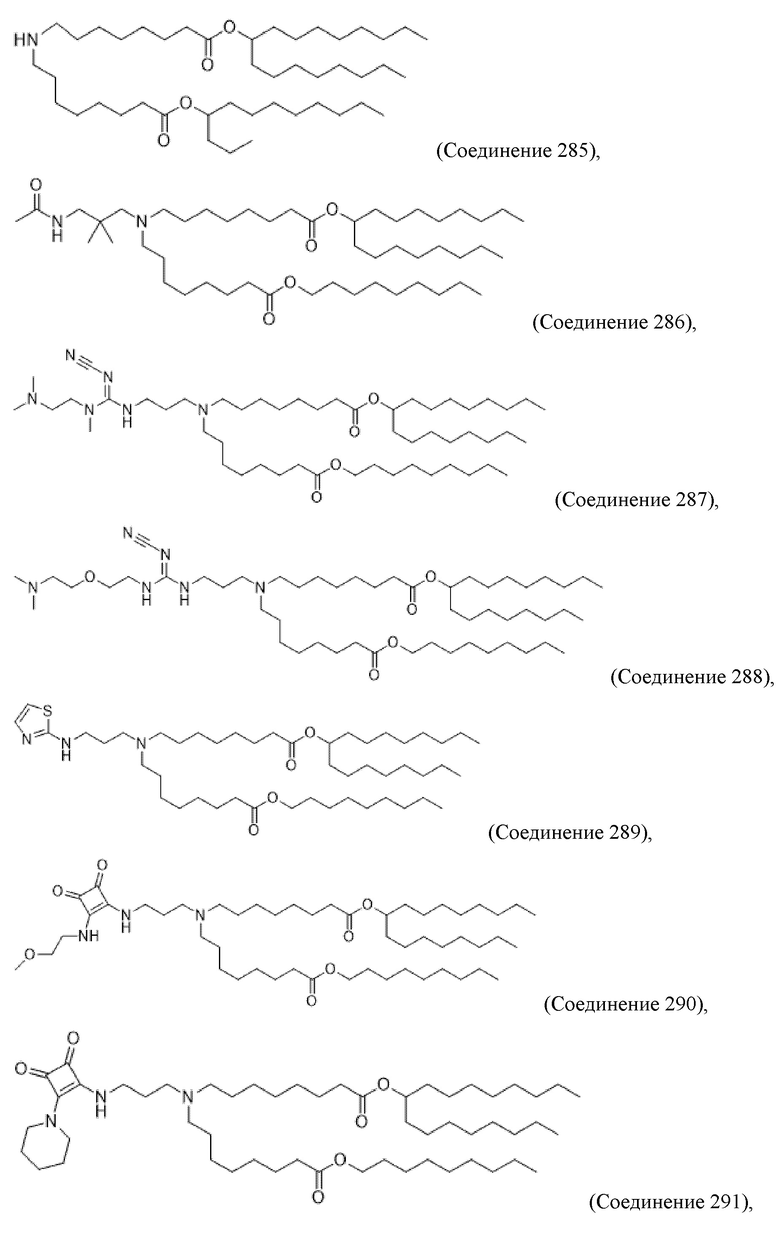


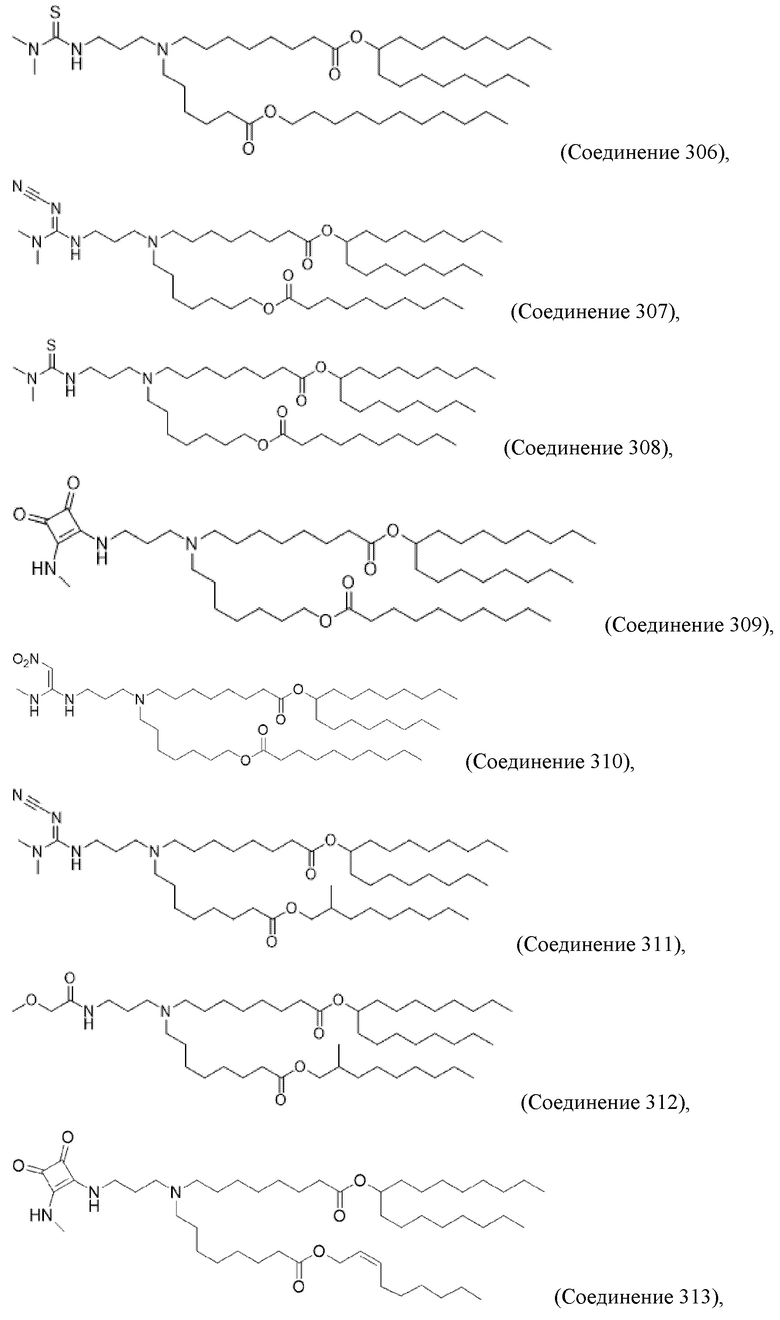
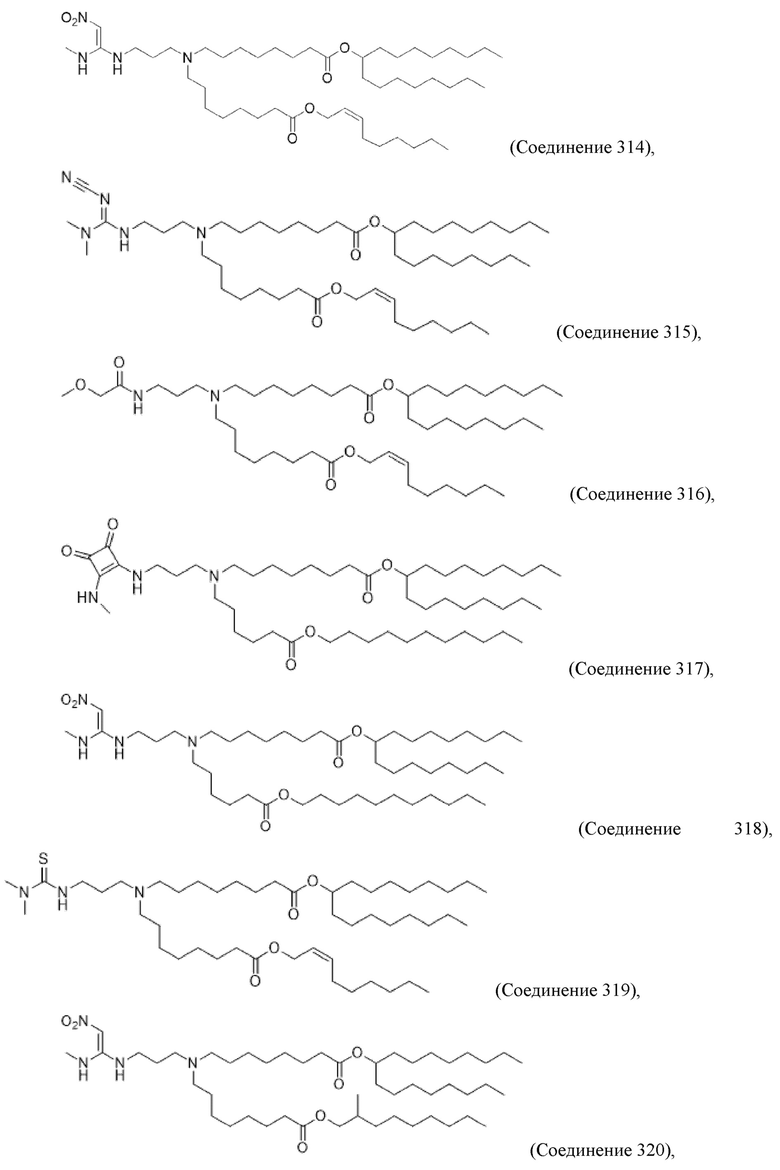
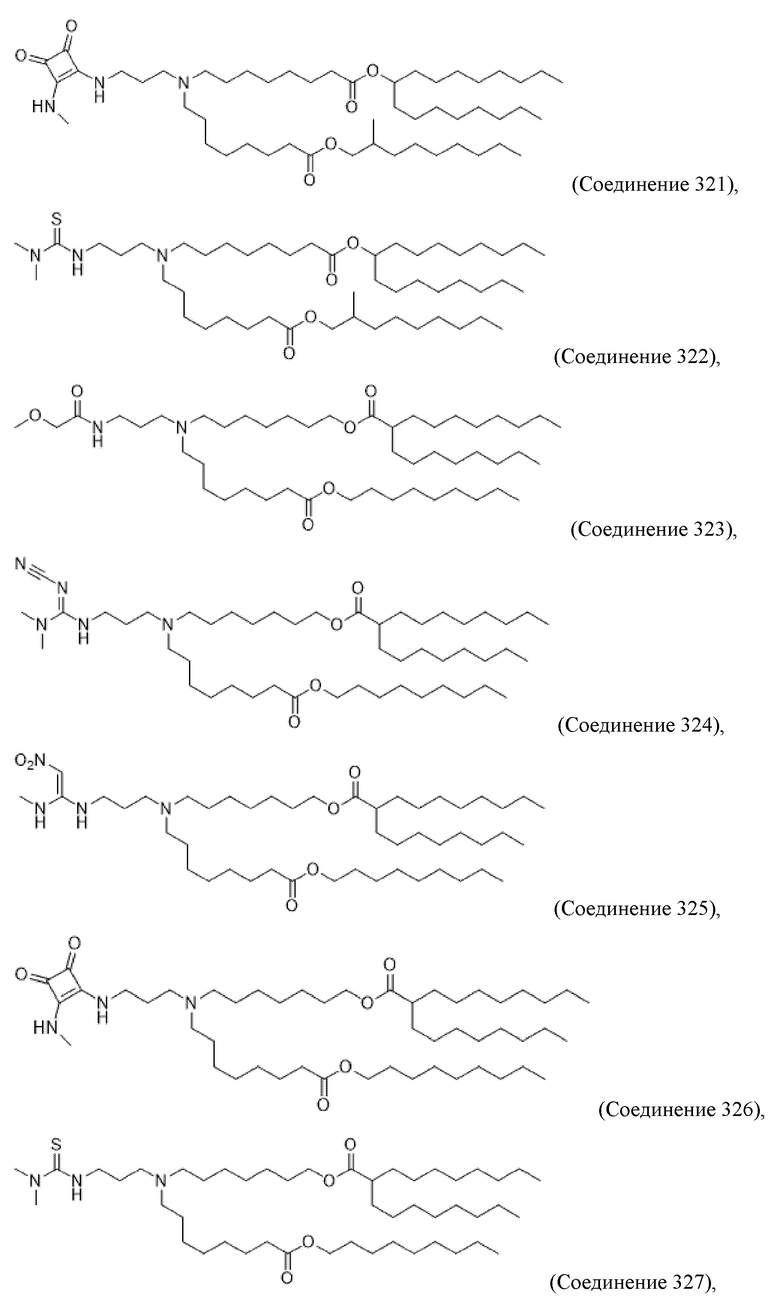
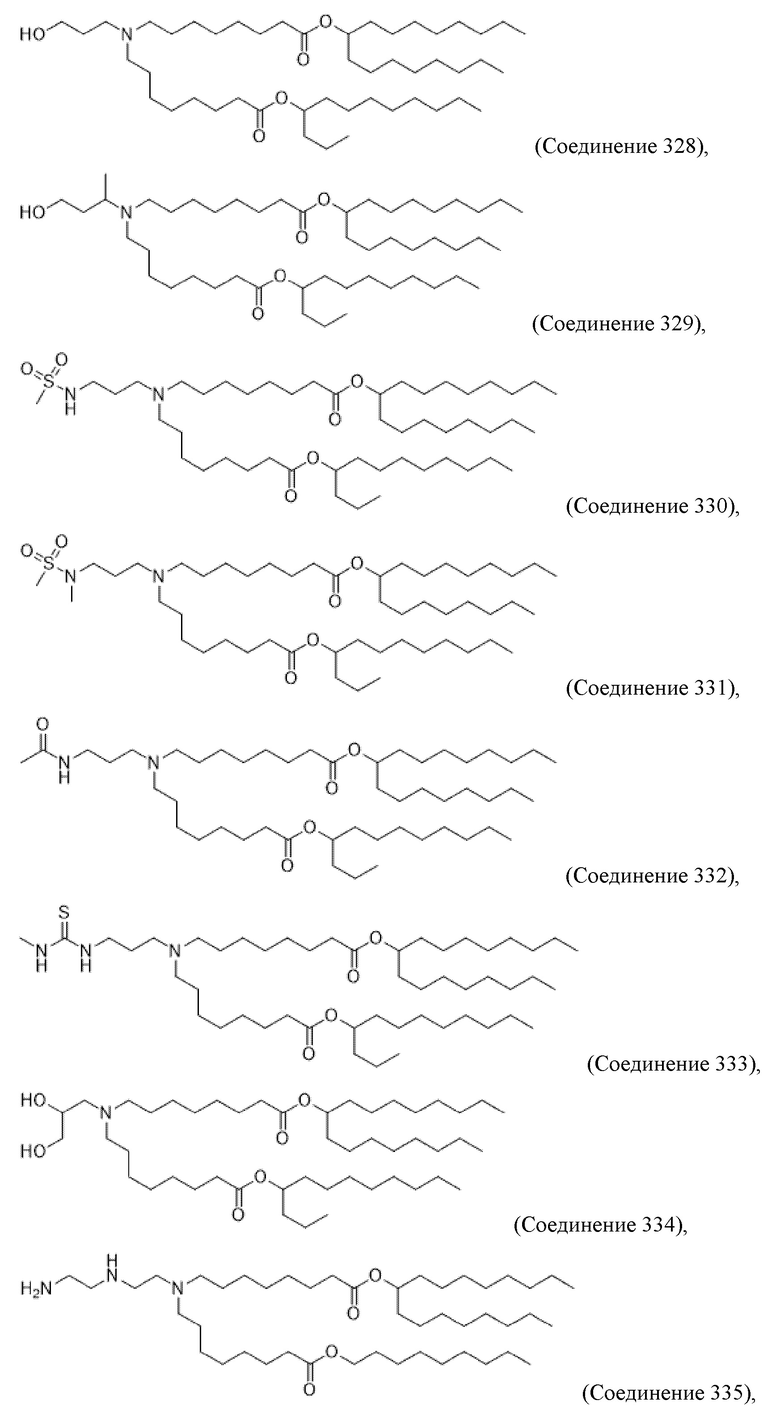
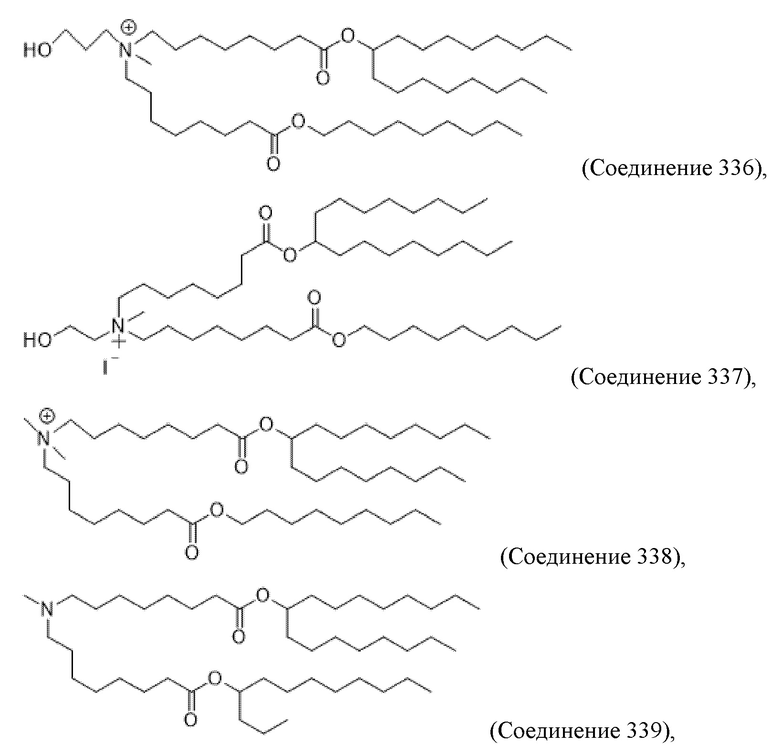
и их N-оксидов, их солей и их изомеров.
[00215] В некоторых вариантах осуществления, липид по данному изобретению содержит соединение 340:
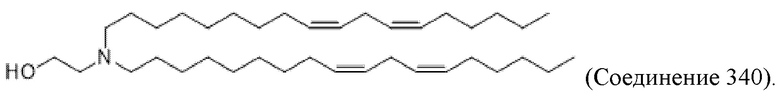
[00216] Центральный аминный фрагмент липида формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) может быть протонирован при физиологическом pH. Таким образом, липид может иметь положительный или частичный положительный заряд при физиологическом рН. Такие липиды могут относится как к катионным, так и ионизируемым (амино) липидам. Липиды также могут быть цвиттерионными, то есть нейтральными молекулами, имеющими как положительный, так и отрицательный заряд.
[00217] В контексте данного документа термин «алкил» или «алкильная группа» означает линейный или разветвленный, насыщенный углеводород, включающий один или более атомов углерода (например, один, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать или более атомов углерода), который является необязательно замещенным. Обозначение “C1-14 алкил” означает необязательно замещенный линейный или разветвленный, насыщенный углеводород, включающий 1-14 атомов углерода. Если не указано иное, алкильная группа, описанная в данном документе, относится как к незамещенным, так и к замещенным алкильным группам.
[00218] В контексте данного документа, термин «алкенил» или «алкенильная группа» означает линейный или разветвленный углеводород, включающий два или более атомов углерода (например, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать или более атомов углерода) и по меньшей мере одну двойную связь, который является необязательно замещенным. Обозначение “C2-14 алкенил” означает необязательно замещенный линейный или разветвленный углеводород, содержащий 2-14 атомов углерода и по меньшей мере одну двойную углерод-углеродную связь. Алкенильная группа может включать одну, две, три, четыре или более двойные углерод-углеродные связи. Например, C18 алкенил может включать одну или более двойных связей. Алкенильная группа C18, содержащая две двойные связи, может представлять собой линолеильную группу. Если не указано иное, алкенильная группа, описанная в данном документе, относится как к незамещенной, так и к замещенной алкенильным группам.
[00219] В контексте данного документа термин «алкинил» или «алкинильная группа» означает линейный или разветвленный углеводород, включающий два или более атомов углерода (например, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать или более атомов углерода) и по меньшей мере одну тройную углерод-углеродную связь, который является необязательно замещенным. Обозначение “C2-14 алкинил” означает необязательно замещенный линейный или разветвленный углеводород, содержащий 2-14 атомов углерода и по меньшей мере одну тройную углерод-углеродную связь. Алкинильная группа может включать одну, две, три, четыре или более тройные углерод-углеродные связи. Например, C18 алкинил может содержать одну или более тройных углерод-углеродных связей. Если не указано иное, алкинильная группа, описанная в данном документе, относится как к незамещенной, так и к замещенной алкинильным группам.
[00220] В контексте данного документа, термин “карбоцикл” или «карбоциклическая группа» означает необязательно замещенную моно- или мультициклическую систему, включающую одно или более колец атомов углерода. Кольца могут представлять собой трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати, тринадцати, четырнадцати, пятнадцати, шестнадцати, семнадцати, восемнадцати, девятнадцати или двадцати членные кольца. Обозначение “C3-6 карбоцикл” означает карбоцикл, включающий одно кольцо с 3-6 атомами углерода. Карбоциклы могут включать одну или более двойных или тройных углерод-углеродных связей и могут представлять собой неароматические или ароматические группы (например, циклоалкил или арил). Примеры карбоцикла включают циклопропильные, циклопентильные, циклогексильные, фенильные, нафтильные и 1,2-дигидронафтильные группы. В контексте данного документа, термин «циклоалкил» означает неароматический карбоцикл и может включать или не включать какую-либо двойную или тройную связь. Если не указано иное, карбоцикл, описанный в данном документе, относится как к незамещенной, так и к замещенной карбоциклической группам, т.е. необязательно замещенным карбоциклам.
[00221] В контексте данного документа термин «гетероцикл» или «гетероциклическая группа» означает необязательно замещенную моно- или мультициклическую систему, включающую одно или более колец, где по меньшей мере одно кольцо включает в себя по меньшей мере один гетероатом. Гетероатомы могут представлять собой, например, атомы азота, кислорода или серы. Кольца могут представлять собой трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати, тринадцати или четырнадцати членные кольца. Гетероциклы могут включать одну или более двойных или тройных связей и могут представлять собой неароматические или ароматические (например, гетероциклоалкильные или гетероарильные группы). Примеры гетероциклов включают имидазолильные, имидазолидинильные, оксазолильные, оксазолидинильные, тиазолильные, тиазолидинильные, пиразолидинильные, пиразолильные, изоксазолидинильные, изоксазолильные, изотиазолидинильные, изотиазолильные, морфолинильные, пирролильные, пирролидинильные, фурильные, тетрагидрофурильные, тиофенильные, пиридинильные, пиперидинильные, хинолильные и изохинолильные группы. В контексте данного документа, термин «гетероциклоалкил» означает неароматический гетероцикл и может включать или не включать какую-либо двойную или тройную связь. Если не указано иное, гетероциклы, описанные в данном документе, относятся как к незамещенным, так и к замещенным гетероциклическим группам, т.е. необязательно замещенным гетероциклам.
[00222] В данном документе «биоразлагаемая группа» представляет собой группу, которая может способствовать более быстрому метаболизму липида у млекопитающего. Биоразлагаемая группа может быть выбрана из группы, состоящей из, но не ограничивающейся ими, -C(O)O-, -OC(O)-, -C(O)N(R')-, -N(R')C(O)-, -C(O)-,
-C(S)-, -C(S)S-, -SC(S)-, -CH(OH)-, -P(O)(OR')O-, -S(O)2-, арильной группы и гетероарильной группы. В контексте данного документа «арил» представляет собой необязательно замещенный карбоциклический радикал, включающий одно или более ароматических колец. Примеры арильных групп включают фенильные и нафтильные группы. В контексте данного документа «гетероарильная группа» представляет собой необязательно замещенную гетероциклическую группу, включающую одно или более ароматических колец. Примеры гетероарильных групп включают пирролил, фурил, тиофенил, имидазолил, оксазолил и тиазолил. Как арильные, так и гетероарильные группы могут быть необязательно замененными. Например, M и M' могут быть выбраны из неограничивающей группы, состоящей из необязательно замещенного фенила, оксазола и тиазола. В приведенных в данном документе формулах М и М' могут быть независимо выбраны из списка биоразлагаемых групп, приведенного выше. Если не указано иное, арильные или гетероарильные группы, описанные в данном документе, относятся как к незамещенным, так и к замещенным группам, то есть к необязательно замещенным арильным или гетероарильным группам.
[00223] Алкильные, алкенильные и циклические (например, карбоциклильные и гетероциклильные) группы могут быть обязательно необязательно замещены, если не указано иное. Необязательные заместители могут быть выбраны из группы, состоящей из, но не ограничиваясь этим, атома галогена (например, хлоридная, бромидная, фторидная или иодидная группа), карбоновой кислоты (например, -C(O)OH), спирта (например, гидроксил, -OH), сложного эфира (например, -C(O)OR или -OC(O)R), альдегида (например,-C(O)H), карбонила (например, -C(O)R, альтернативно представленного как C=O), ацилгалогенида (например,-C(O)X, в котором X представляет собой галогенид, выбранный из бромида, фторида, хлорида и иодида), карбоната (например, -OC(O)OR), алкокси (например, -OR), ацеталя (например,-C(OR)2R'''', в которой каждый OR представляет собой алкоксигруппы, которые могут быть одинаковыми или разными, и R'''' представляет собой алкильную или алкенильную группу), фосфата (например, P(O)43-), тиола (например, -SH), сульфоксида (например, -S(O)R), сульфиновой кислоты (например, -S(O)OH),сульфоновой кислоты (например, -S(O)2OH), тиаля (например, -C(S)H), сульфата (например, S(O)42-), сульфонила (например, -S(O)2-), амида (например, -C(O)NR2 или -N(R)C(O)R), азидо (например, -N3), нитро (например, -NO2), циано (например, -CN), изoциано (например, -NC), ацилокси (например,-OC(O)R), амино (например, -NR2, -NRH или -NH2), карбамоила (например, -OC(O)NR2, -OC(O)NRH или -OC(O)NH2), сульфонамида (например, -S(O)2NR2, -S(O)2NRH, -S(O)2NH2, -N(R)S(O)2R, -N(H)S(O)2R, -N(R)S(O)2H или -N(H)S(O)2H), алкильной группы, алкенильной группы и циклильной (например, карбоциклильной или гетероциклильной) группы. В любом из предшествующих описаний, R представляет собой алкильную или алкенильную группу, определенную в данном документе. В некоторых вариантах осуществления, сами группы заместителей могут быть дополнительно замещенными, например, одним, двумя, тремя, четырьмя, пятью или шестью заместителями, как определено в данном документе. Например, C1-6 алкильная группа может быть дополнительно замещена одним, двумя, тремя, четырьмя, пятью или шестью заместителями, как описано в данном документе.
[00224] Соединения по данному изобретению, которые содержат атомы азота, могут быть преобразованы в N-оксиды путем обработки окислителем (например, 3-хлорпероксибензойной кислотой (мХПБК) и/или перекисью водорода), чтобы получить другие соединения по данному изобретению. Таким образом, считается, что все проиллюстрированные и заявленные азотсодержащие соединения, если это допускается валентностью и структурой, включают как проиллюстрированное соединение, так и его N-оксидное производное (которое можно обозначить как N→O или N+-O-). Кроме того, в других случаях азот в соединениях по данному изобретению может быть превращен в N-гидрокси или N-алкоксисоединения. Например, N-гидроксисоединения могут быть получены окислением исходного амина окислителем, таким как м-ХПБК. Все проиллюстрированные и заявленные азотсодержащие соединения также рассматриваются, когда это допускается валентностью и структурой, чтобы охватывать как проиллюстрирванное соединение, так и его N-гидрокси (т.е. N-OH) и N-алкокси (т.е. N-OR, где R представляет собой замещенный или незамещенный C1-C6 алкил, C1-C6 алкенил, C1-C 6 алкинил, 3-14-членный карбоцикл или 3-14-членный гетероцикл) производные.
[00225] Около, приблизительно: В контексте данного документа термины «приблизительно» и «около» применительно к одному или более интересующим значениям относятся к значению, аналогичному заявленному эталонному значению. В конкретных вариантах осуществления термин «приблизительно» или «около» относится к диапазону значений, которые попадают в пределы 25%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1% или менее в любом направлении (больше или меньше) указанного контрольного значения, если не указано иное или иначе видно из контекста (кроме случаев, когда такое число будет превышать 100% возможного значения). Например, при использовании в контексте количества данного соединения в липидном компоненте композиции наночастиц «около» может означать +/- 10% от приведенного значения. Например, композиция наночастиц, содержащая липидный компонент, содержащий около 40% данного соединения, может содержать 30-50% соединения.
[00226] В контексте данного документа термин «соединение» подразумевает включение всех изомеров и изотопов изображенной структуры. «Изотопы» относятся к атомам, имеющим одинаковый атомный номер, но разные массовые числа, возникающие в результате различного количества нейтронов в ядрах. Например, изотопы водорода включают в себя тритий и дейтерий. Кроме того, соединение, соль или комплекс по данному изобретению может быть получен в комбинации с молекулами растворителя или воды с образованием сольватов и гидратов обычными способами.
[00227] В контексте данного документа термин «приведение в контакт» означает установление физического соединения между двумя или более объектами. Например, приведение в контакт клетки млекопитающего с композицией наночастиц означает, что клетка млекопитающего и наночастица созданы для того, чтобы иметь общую физическую связь. Способы приведения в контакт клеток с внешними субъектами как in vivo, так и ex vivo хорошо известны в биологии. Например, приведение в контакт композиции наночастиц и клетки млекопитающего, находящейся в организме млекопитающего, могут выполнять различными способами введения (например, внутривенным, внутримышечным, внутрикожным и подкожным) и может включать различные количества композиций наночастиц. Более того, более чем одна клетка млекопитающего может быть приведена в контакт с композицией наночастиц.
[00228] В контексте данного документа, термин «доставка» означает предоставление объекта в место назначения. Например, доставка терапевтического и/или профилактического средства субъекту может включать введение композиции наночастиц, содержащей терапевтическое и/или профилактическое средство субъекту (например, внутривенным, внутримышечным, внутрикожным или подкожным путем). Введение композиции наночастиц млекопитающему или в клетку млекопитающего может включать приведение контакт одной или более клеток с композицией наночастиц.
[00229] В контексте данного документа, термин «расширенная доставка» означает доставку большего количества (например, по меньшей мере в 1,5 раза больше, по меньшей мере в 2 раза больше, по меньшей мере в 3 раза больше, по меньшей мере в 4 раза больше, по меньшей мере в 5 раз больше, по меньшей мере в 6 раз больше, по меньшей мере в 7 раз больше, по меньшей мере в 8 раз, по меньшей мере в 9 раз, по меньшей мере в 10 раз) терапевтического и/или профилактического средства с помощью наночастиц для представляющей интерес ткани (например, печени млекопитающих) по сравнению с уровнем доставки терапевтического и/или профилактического средства контрольной наночастицей в интересующую ткань-мишень (например, MC3, KC2 или DLinDMA). Уровень доставки наночастиц в конкретную ткань может быть измерен путем сравнения количества белка, продуцируемого в ткани, с весом указанной ткани, сравнения количества терапевтического и/или профилактического средства в ткани с весом указанной ткани, сравнивая количество белка, продуцируемого в ткани, с количеством общего белка в указанной ткани или сравнивая количество терапевтического и/или профилактического средства в ткани с количеством общего терапевтического и/или профилактического средства в указанной ткани. Понятно, что усиленную доставку наночастиц в ткань-мишень не нужно определять у субъекта, которого лечат, она может быть определена в суррогате, таком как животная модель (например, крысиная модель). В конкретных вариантах осуществления композиция наночастиц, содержащая соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), ( IIg) или (III) имеет практически одинаковый уровень улучшения доставки независимо от путей введения. Например, некоторые соединения, описанные в данном документе, проявляют аналогичное усиление доставки, когда их применяют для доставки терапевтического и/или профилактического средства внутривенно или внутримышечно. В других вариантах осуществления, некоторые соединения, описанные в данном документе (например, соединение формулы (IA) или (II), такое как соединение 18, 25, 30, 60, 108-112 или 122), проявляют более высокий уровень усиления доставки, когда их применяют для доставки терапевтических и/или профилактических средств внутримышечно, а не внутривенно.
[00230] В контексте данного документа, термин «специфическая доставка», «специфично доставлять» или «специфично доставляющий» означает доставку большего количества (например, по меньшей мере в 1,5 раза больше, по меньшей мере в 2 раза больше, по меньшей мере в 3 раза больше, по меньшей мере в 4 раза больше, по меньшей мере в 5 раз больше, по меньшей мере в 6 раз больше, по меньшей мере в 7 раз больше, по меньшей мере в 8 раз, по меньшей мере в 9 раз, по меньшей мере в 10 раз) терапевтического и/или профилактического средства наночастицей в целевую ткань, представляющую интерес (например, печень млекопитающего), по сравнению с тканью, не являющейся объектом воздействия (например, селезенка млекопитающего). Уровень доставки наночастиц в конкретную ткань может быть измерен путем сравнения количества белка, продуцируемого в ткани, с весом указанной ткани, сравнения количества терапевтического и/или профилактического средства в ткани с весом указанной ткани, сравнивая количество белка, продуцируемого в ткани, с количеством общего белка в указанной ткани или сравнивая количество терапевтического и/или профилактического средства в ткани с количеством общего терапевтического и/или профилактического средства в указанной ткани. Например, для реноваскулярного нацеливания терапевтическое и/или профилактическое средство специально предоставляется в почку млекопитающего по сравнению с печенью и селезенкой, если в 1,5, 2, 3, 5, 10, 15, 15 или 20 раз больше терапевтического и/или профилактического средства на 1 г ткани доставляется в почку по сравнению с доставкой в печень или селезенку после системного введения терапевтического и/или профилактического средства. Понятно, что способность наночастиц осуществлять специфичную доставку в ткань-мишень не нужно определять у субъекта, которого лечат, она может быть определена в суррогате, таком как животная модель (например, крысиная модель).
[00231] В контексте данного документа, «эффективность инкапсуляции» относится к количеству терапевтического и/или профилактического средства, которое становится частью композиции наночастиц, относительно первоначального общего количества терапевтического и/или профилактического средства, применяемого при приготовлении композиции наночастиц. Например, если 97 мг терапевтического и/или профилактического средства инкапсулированы в композиции наночастиц из общего количества 100 мг терапевтического и/или профилактического средства, первоначально обеспеченного в композиции, эффективность инкапсуляции может быть признана равной 97%. В контексте данного документа «инкапсуляция» может относиться к полной, существенной или частичной оболочке, ограничению, окружению или оболочке.
[00232] В контексте данного документа «экспрессия» последовательности нуклеиновой кислоты относится к трансляции мРНК в полипептид или белок и/или посттрансляционной модификации полипептида или белка.
[00233] В контексте данного документа, термин «in vitro» относится к событиям, которые происходят в искусственной среде, например, в пробирке или реакционном сосуде, в культуре клеток, в чашке Петри и т. д., а не внутри организма (например, животное, растение или микроб).
[00234] В контексте данного документа, термин «in vivo» относится к событиям, которые происходят в организме (например, животное, растение или микроб, клетка или ткань).
[00235] В контексте данного документа термин «ex vivo» относится к событиям, которые происходят вне организма (например, животное, растение или микроб, клетка или ткань). События ex vivo могут происходить в среде, минимально отличной от естественной (например, in vivo).
[00236] В контексте данного документа термин «изомер» означает любой геометрический изомер, таутомер, цвиттер-ион, стереоизомер, энантиомер или диастереомер соединения. Соединения могут содержать один или более хиральных центров и/или двойных связей и, таким образом, могут существовать в виде стереоизомеров, таких как изомеры с двойной связью (т.е. E/Z геометрические изомеры) или диастереомеры (например, энантиомеры (то есть (+) или (-)) или цис/транс-изомеры). Данное описание охватывает любые и все изомеры соединений, описанных в данном документе, включая стереомерно чистые формы (например, геометрически чистые, энантиомерно чистые или диастереомерно чистые) и энантиомерные и стереоизомерные смеси, например рацематы. Энантиомерные и стереомерные смеси соединений и способы их разделения на составляющие их энантиомеры или стереоизомеры хорошо известны.
[00237] «Таутомер» является одним из двух или более структурных изомеров, которые существуют в равновесии и легко превращаются из одной изомерной формы в другую. Это преобразование приводит к формальной миграции атома водорода, сопровождаемой перераспределением соседних сопряженных двойных связей. Таутомеры существуют в виде смеси таутомерного набора в растворе. В растворах, где таутомеризация равно возможна, будет достигнуто химическое равновесие таутомеров. Точное соотношение таутомеров зависит от нескольких факторов, включая температуру, растворитель и pH. Концепция таутомеров, которые могут быть преобразованы путем таутомеризации, называется таутомеризмом.
[00238] Из разнообразных возможных типов таутомерии обычно наблюдаются два. При кето-енольной таутомерии происходит одновременное смещение электронов и атома водорода. Таутомерия с кольцевой цепью возникает в результате реакции альдегидной группы (-CHO) в молекуле сахарной цепи с одной из гидроксигрупп (-OH) в той же молекуле с получением ее циклической (кольцеобразной) формы, которую демонстрирует глюкоза.
[00239] Обычными таутомерными парами являются: кетон-енол, амид-нитрил, лактам-лактим, таутомерия амид-имидовой кислоты в гетероциклических кольцах (например, в нуклеиновых основаниях, таких как гуанин, тимин и цитозин), имин-енамин и енамин-енамин. Пример таутомерии в ди-замещенном гуанидине изображен ниже.
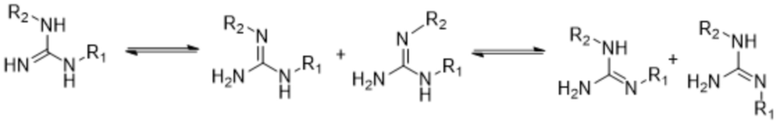
[00240] Следует понимать, что соединения по данному изобретению могут могут быть изображены в виде разных таутомеров. Следует также понимать, что когда соединения имеют таутомерные формы, все таутомерные формы предназначены для включения в объем описания, и наименование соединений не исключает какую-либо таутомерную форму.
[00241] В контексте данного документа «липидный компонент» является тем компонентом композиции наночастиц, который содержит один или более липидов. Например, липидный компонент может включать один или более катионных/ионизируемых, ПЭГилированных, структурных или других липидов, таких как фосфолипиды.
[00242] В контексте данного документа «линкер» представляет собой фрагмент, соединяющий два фрагмента, например, соединение между двумя нуклеозидами, кепированных частиц. Линкер может включать одну или более групп, включая, но не ограничиваясь этим, фосфатные группы (например, фосфаты, боранофосфаты, тиофосфаты, селенофосфаты и фосфонаты), алкильные группы, амидаты или глицерины. Например, два нуклеозида керированного аналога могут быть связаны по своим 5'-положениях трифосфатной группой или цепью, включающей два фосфатных фрагмента и боранофосфатный фрагмент.
[00243] В контексте данного документа «способы введения» могут включать внутривенные, внутримышечные, внутрикожные, подкожные или другие способы доставки композиции субъекту. Способ введения может быть выбран для целевой доставки (например, для конкретной доставки) в конкретный регион или систему организма.
[00244] В контексте данного документа «модифицированный» означает не встречающийся в природе. Например, РНК может представлять собой модифицированную РНК. То есть РНК может включать одно или более нуклеиновых оснований, нуклеозидов, нуклеотидов или линкеров, которые не встречаются в природе. «Модифицированные» частицы могут также упоминаться в данном документе как «измененные» частицы. Частицы могут быть измененными или измененными химически, структурно или функционально. Например, частицы модифицированного нуклеинового основания могут включать одну или более замещений, которые не встречаются в природе.
[00245] В контексте данного документа, «соотношение N:P» представляет собой молярное соотношение ионизируемых (в физиологическом диапазоне pH) атомов азота в липидной и фосфатной группах в РНК, например, в композиции наночастиц, содержащей липидный компонент и РНК.
[00246] В контексте данного документа «композиция наночастиц» представляет собой композицию, содержащую один или более липидов. Композиции наночастиц обычно имеют размер порядка микрометров или меньше и могут содержать липидный двойной слой. Композиции наночастиц включают липидные наночастицы (LNP), липосомы (например, липидные везикулы) и липоплексы. Например, композиция наночастиц может представлять собой липосому, имеющую липидный двойной слой диаметром 500 нм или менее.
[00247] В контексте данного документа «встречающийся в природе» означает существование в природе без искусственной помощи.
[00248] В контексте данного документа «пациент» относится к субъекту, который может искать или нуждается в лечении, нуждается в лечении, получает лечение, получит лечение, или субъект, которого лечит квалифицированный специалист по конкретному заболеванию или патологическому состоянию.
[00249] В контексте данного документа «ПЭГ-липид» или «ПЭГилированный липид» относится к липиду, содержащему компонент полиэтиленгликоля.
[00250] Выражение «фармацевтически приемлемый» в данном контексте используют для обозначения тех соединений, материалов, композиций и/или лекарственных форм, которые с медицинской точки зрения подходят для применения в контакте с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции или других проблем или осложнений, соразмерно с разумным соотношением пользы/риска.
[00251] Фраза «фармацевтически приемлемый эксципиент», как используется в данном документе, относится к любому компоненту, отличному от соединений, описанных в данном документе (например, несущая среда, способная суспендировать, образовывать комплекс или растворять активное соединение) и обладающему свойствами, по существу, нетоксичными и невоспалительными у пациента. Эксципиенты могут включать, например: антиадгезивы, антиоксиданты, связующие вещества, покрытия, вспомогательные средства для сжатия, дезинтегранты, красители (красители), смягчающие вещества, эмульгаторы, наполнители (дилюенты), пленкообразователи или покрытия, ароматизаторы, ароматизаторы, глиданты (усилители потока) смазочные материалы, консерванты, печатные краски, сорбенты, суспендирующие или диспергирующие агенты, подсластители и гидратационную воду. Примеры эксципиентов включают, но не ограничиваются ими: бутилированный гидрокситолуол (BHT), карбонат кальция, фосфат кальция (двухосновный), стеарат кальция, кроскармелозу, сшитый поливинилпирролидон, лимонную кислоту, кросповидон, цистеин, этилцеллюлозу, желатин, гидроксипропилцеллюлозу гидроксипропилметилцеллюлозу, лактозу, стеарат магния, мальтит, маннит, метилон, метилцеллюлозу, метилпарабен, микрокристаллическую целлюлозу, полиэтиленгликоль, поливинилпирролидон, повидон, прежелатинизированный крахмал, пропилпарабен, ретинилпальмитат, шеллак, диоксид кремния, карбоксиметилцеллюлозу натрия, цитрат натрия, крахмалгликолят натрия, сорбит, крахмал (кукурузный), стеариновую кислоту, сахарозу, тальк, диоксид титана, витамин А, витамин Е (альфа-токоферол), витамин С, ксилит и другие виды, описанные в данном документе.
[00252] В данном описании структурная формула соединения для удобства представляет собой определенный изомер в некоторых случаях, но данное описание включает все изомеры, такие как геометрические изомеры, оптические изомеры на основе асимметричного углерода, стереоизомеры, таутомеры и тому подобное, это следует понимать, что не все изомеры могут иметь одинаковый уровень активности. Кроме того, у соединений, представленных формулой, может присутствовать кристаллический полиморфизм. Следует отметить, что любая кристаллическая форма, смесь кристаллических форм или их ангидрид или гидрат включены в объем данного изобретения.
[00253] Термины «кристаллические полиморфы», «полиморфы» или «кристаллические формы» означают кристаллические структуры, в которых соединение (или его соль или сольват) могут кристаллизоваться в различных кристаллических упаковках, причем все они имеют одинаковый элементный состав. Различные кристаллические формы обычно имеют разные дифракционные рентгенограммы, инфракрасные спектры, температуры плавления, плотность, твердость, кристаллическую форму, оптические и электрические свойства, стабильность и растворимость. Растворитель для перекристаллизации, скорость кристаллизации, температура хранения и другие факторы могут привести к доминированию одной кристаллической формы. Кристаллические полиморфы соединений могут быть получены кристаллизацией в различных условиях.
[00254] Композиции могут также включать соли одного или более соединений. Соли могут представлять собой фармацевтически приемлемые соли. В контексте данного документа, «фармацевтически приемлемые соли» относится к производным описанных соединений, в которых исходное соединение изменяется путем преобразования существующего кислотного или основного фрагмента в его солевую форму (например, путем введения в реакцию группы свободного основания с подходящей органической кислотой). Примеры фармацевтически приемлемых солей включают в себя, но не ограничиваясь ими, соли минеральных или органических кислот с основными группами, такими как амины; соли щелочей или органических оснований с кислотными группами, такими как карбоновые кислоты; и тому подобное. Иллюстративные примеры солей присоединения кислот включают ацетатную, адипатную, альгинатную, аскорбатную, аспартатную, бензолсульфонатную, бензоатную, бисульфатную, боратную, бутиратную, камфоратную, камфорсульфонатную, цитратную, циклопентанпропионатную, диглюконатную, додецилсульфатную, этансульфонатную, фумаратную, глюкогептонатную, глицерофосфатную, гемисульфатную, гептонатную, гексаноатную, гидробромидную гидрохлоридную, гидроиодидную, 2-гидрокси-этансульфонатную, лактобионатную, лактатную, лауратную, лаурилсульфатную, малатную, малеатную, малонатную, метансульфонатную, 2-нафталинсульфонатную, никотинатную, нитратную, олеатную, оксалатную, пальмитатную, памоатную, пектинатную, персульфатную, 3-фенилпропионатную, фосфатную, пикратную, пивалатную, пропионатную, стеаратную, сукцинатную, сульфатную, тартратную, тиоцианатную, толуолсульфонатную, ундеканоатную, валератную соли и тому подобное. Типичные соли щелочных или щелочноземельных металлов включают соли натрия, лития, калия, кальция, магния и тому подобное, а также нетоксичные катионы аммония, четвертичного аммония и амина, включая, но не ограничиваясь этим, аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, этиламини и тому подобное. Фармацевтически приемлемые соли по данному изобретению включают в себя принятые нетоксичные соли исходного соединения, полученные, например, из нетоксичных неорганических или органических кислот. Фармацевтически приемлемые соли по данному изобретению могут быть синтезированы из исходного соединения, которое содержит основный или кислотный фрагмент, с помощью традиционных химических способов. Как правило, такие соли могут быть получены путем приведения в контакт данных соединений в свободной кислотной или основной формах со стехиометрическим количеством подходящего основания или кислоты в воде, или в органическом растворителе или в их смеси; в целом предпочтительными являются неводные среды, такие как простой эфир, этилацетат, этанол, изопропанол или ацетонитрил. Списки подходящих солей находятся в Remington Pharmaceutical Sciences, 17-е изд., Mack Publishing Company, Истон, Пенсильвания, 1985, стр. 1418, Pharmaceutical Salts: Properties, Selection и Use, P.H. Stahl и C.G. Wermuth (eds.), Wiley-VCH, 2008 и Berge et al., Journal of Pharmaceutical Science, 66, 1-19 (1977), каждый из которых включен в данный документ посредством ссылки в полном объеме.
[00255] Используемый в данном документе термин «фосфолипид» представляет собой липид, который содержит фосфатный фрагмент и одну или более углеродных цепей, таких как цепи ненасыщенных жирных кислот. Фосфолипид может включать одну или более кратных (например, двойных или тройных) связей (например, одну или более ненасыщенных связей). Конкретные фосфолипиды могут способствовать слиянию с мембраной. Например, катионный фосфолипид может взаимодействовать одним или более отрицательно заряженными фосфолипидами мембраны (например, клеточной или внутриклеточной мембраны). Слияние фосфолипида с мембраной может позволить одному или более элементам липидсодержащей композиции проходить через мембрану, позволяя, например, доставить один или более элементов в клетку.
[00256] Используемый в данном документе термин «коэффициент полидисперсности» представляет собой отношение, которое описывает однородность распределения частиц по размерам системы. Небольшое значение, например, менее 0,3, указывает на узкое распределение частиц по размерам.
[00257] Используемый в данном документе термин «полипептид» или «представляющий интерес полипептид» относится к полимеру из аминокислотных остатков, обычно соединенных пептидными связями, которые могут быть получены естественным путем (например, выделены или очищены) или синтетически.
[00258] Используемый в данном документе термин «РНК» относится к рибонуклеиновой кислоте, которая может встречаться в природе или не встречаться в природе. Например, РНК может содержать модифицированные и/или не встречающиеся в природе компоненты, такие как одно или более нуклеиновых оснований, нуклеозидов, нуклеотидов или линкеров. РНК может включать структуру кэпа, концевой нуклеозид цепи петлю на стебле, последовательность полиА и/или сигнал полиаденилирования. РНК может иметь нуклеотидную последовательность, кодирующую интересующий полипептид. Например, РНК может представлять собой матричную РНК (мРНК). Трансляция мРНК, кодирующей определенный полипептид, например, трансляция мРНК in vivo внутри клетки млекопитающего, может продуцировать кодированный полипептид. РНК могут быть выбраны из неограничивающей группы, состоящей из малой интерферирующей РНК (миРНК), асимметричной интерферирующей РНК (аиРНК), микроРНК (микроРНК), дайсер-субстрат мРНК (дсРНК), малая шпильковая РНК (мшРНК), мРНК, одиночная направляющая РНК (онРНК), мРНК cas9, и их смесей.
[00259] Используемый в данном документе термин «единичная стандартная доза» представляет собой дозу любого терапевтического средства, вводимого в одной дозе/в одно время/однократным путем/в одной точке контакта, то есть в случае единичного введения.
[00260] Используемый в данном документе термин «дробная доза» представляет собой разделение единичной стандартной дозы или общей суточной дозы на две или более доз.
[00261] Используемый в данном документе термин «общая суточная доза» представляет собой количество, назначаемое или назначаемое в течение 24 часов. Ее можно вводить как единичную стандартную дозу.
[00262] Используемый в данном документе термин «размер» или «средний размер» в контексте композиций наночастиц относится к среднему диаметру композиции наночастиц.
[00263] Используемый в данном документе термин «субъект» или «пациент» относится к любому организму, которому можно вводить композицию в соответствии с данным изобретением, например, для экспериментальных, диагностических, профилактических и/или терапевтических целей. Типичные субъекты включают животных (например, млекопитающих, таких как мыши, крысы, кролики, приматы, отличные от человека, и люди) и/или растения.
[00264] Используемый в данном документе термин «клетки-мишени» относится к любой одной или более интересующим клеткам. Клетки могут быть обнаружены in vitro, in vivo, in situ или в ткани или органе организма. Организм может представлять собой животное, предпочтительно млекопитающее, более предпочтительно человек и наиболее предпочтительно пациент.
[00265] Используемый в данном документе термин «ткань-мишень» относится к любому одному или нескольким интересующим типам тканей, в которых доставка терапевтического и/или профилактического средства приведет к желаемому биологическому и/или фармакологическому эффекту. Примеры тканей-мишеней, представляющих интерес, включают конкретные ткани, органы и системы или их группы. В конкретных применениях ткань-мишень может представлять собой почку, легкое, селезенку, сосудистый эндотелий в сосудах (например, внутрикоронарный или внутрибедренный) или ткань опухоли (например, посредством внутриопухолевой инъекции). «Ткань вне мишени» относится к любому одному или более типам тканей, в которых экспрессия кодируемого белка не приводит к желаемому биологическому и/или фармакологическому эффекту. В конкретных применениях ткани, не являющиеся мишенями, могут включать печень и селезенку.
[00266] Термин «терапевтический агент» или «профилактический агент» относится к любому агенту, который при введении субъекту оказывает терапевтический, диагностический и/или профилактический эффект и/или вызывает желаемый биологический и/или фармакологический эффект. Терапевтические агенты также называют «активами» или «активными агентами». Такие агенты включают, но не ограничиваются ими, цитотоксины, радиоактивные ионы, химиотерапевтические агенты, низкомолекулярные лекарственные средства, белки и нуклеиновые кислоты.
[00267] Используемый в данном документе термин «терапевтически эффективное количество» означает количество агента, подлежащего доставке (например, нуклеиновой кислоты, лекарственного средства, композиции, терапевтического агента, диагностического агента, профилактического агента и т.д.), которое является достаточным при введении субъекту, страдающему или подверженному инфекции, заболеванию, расстройству и/или состоянию, для лечения, облегчения симптомов, диагностики, предотвращения и/или задержки начала инфекции, заболевания, расстройства и/или состояния.
[00268] Используемый в данном документе термин «трансфекция» относится к введению вида (например, РНК) в клетку. Трансфекция может происходить, например, in vitro, ex vivo или in vivo.
[00269] Используемый в данном документе термин «лечение» относится к частичному или полному облегчению, улучшению, позитивному изменению, задержке наступления, ингибированию прогрессирования, уменьшению тяжести и/или уменьшению заболеваемости одним или более симптомами или признаками конкретной инфекции, заболевания, расстройства и/или состояния. Например, «лечение» рака может относиться к ингибированию выживания, роста и/или распространения опухоли. Лечение может быть назначено субъекту, у которого нет признаков заболевания, расстройства и/или состояния, и/или субъекту, у которого проявляются только ранние признаки заболевания, расстройства и/или состояния, с целью снижения риска развития патологии, связанной с заболеванием, расстройством и/или состоянием.
[00270] В данном документе «дзета-потенциал» представляет собой электрокинетический потенциал липида, например, в композиции частиц.
Композиции наночастиц
[00271] Данное изобретение также относится к композициям наночастиц, содержащим липидный компонент, содержащий соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), как описано в данном документе.
[00272] В некоторых вариантах осуществления, самый большой размер наночастиц композиции равен 1 мкм или менее (например, 1 мкм, 900 нм, 800 нм, 700 нм, 600 нм, 500 нм, 400 нм, 300 нм, 200 нм, 175 нм, 150 нм, 125 нм, 100 нм, 75 нм, 50 нм или менее), например, при измерении методом динамического рассеяния света (DLS), просвечивающей электронной микроскопии, сканирующей электронной микроскопии или другим методом. Композиции наночастиц включают, например, липидные наночастицы (LNP), липосомы, липидные везикулы и липоплексы. В некоторых вариантах осуществления, композиции наночастиц представляют собой везикулы, содержащие один или более липидных двойных слоев. В конкретных вариантах осуществления композиция наночастиц содержит два или более концентрических двойных слоя, разделенных водными компартментами. Липидные двойные слои могут быть функционализированными и/или сшитыми друг с другом. Липидный двойной слой может содержать один или более лигандов, белков или каналов.
[00273] Композиции наночастиц содержат липидный компонент, содержащий по меньшей мере одно соединение в формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III). Например, липидный компонент композиции наночастиц может содержать одно или более соединений 1-280. Композиции наночастиц могут также содержать множество других компонентов. Например, липидный компонент композиции наночастиц может содержать один или более других липидов в дополнение к липиду формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III).
Катионные/ионизируемые липиды
[00274] Композиция наночастиц может включать один или более катионных и/или ионизируемых липидов (например, липидов, которые могут иметь положительный или частичный положительный заряд при физиологическом pH) в дополнение к липиду формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III). Катионные и/или ионизируемые липиды могут быть выбраны из неограничивающей группы, состоящей из 3-(дидодециламино)-N1,N1,4-тридодецил-1-пиперазинэтанамина (KL10), N1-[2-(диоддециламино)этил]-N1,N4, N4-тридодецил-1,4-пиперазиндиэтанамина (KL22), 14,25- дитридецил-15,18,21,24-тетраазаоктатриаконтана (KL25), 1,2-дилинолeилокси-N, N-диметиламинопропана (DLin-DMA), 2,2-дилинолeил-4-диметиламинометил-[1,3]-диоксолана (DLin-K-DMA), гептатриаконта-6,9,28,31-тетраен-19-ил-4- (диметиламино)бутаноата (DLin-MC3-DMA), 2,2-дилинолейл-4-(2-диметиламиноэтил)-[1,3]-диоксолана (DLin-KC2-DMA), 1,2-диолеилокси-N, N-диметиламинопропана (DODMA), 2-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметил-3-[ (9Z, 12Z)-октадека-9,12-диен-1-илокси]пропан-1-амина (Октил-CLinDMA), (2R)-2-({8-[(3β)-холест-5-ен-3-илокси] октил}окси)-N, N-диметил-3-[(9Z,12Z)-октадека-9,12 диен-1-илокси]пропан-1-амина (Октил-CLinDMA (2R)) и (2S)-2-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметил-3-[(9Z,12Z)-октадека-9,12-диен-1-илокси]пропан-1-амина (Октил-CLinDMA (2S)). В дополнение к этому катионный липид также может быть липидом, содержащим циклическую аминную группу.
ПЭГ-липиды
[00275] Липидный компонент композиции наночастиц может включать один или более ПЭГ или ПЭГ-модифицированных липидов. Такие частицы могут быть иначе именуемыми ПЭГилированными липидами. ПЭГ-липид представляет собой липид, модифицированный полиэтиленгликолем. ПЭГ-липид может быть выбран из неограничивающей группы, состоящей из ПЭГ-модифицированных фосфатидилэтаноламинов, ПЭГ-модифицированных фосфатидных кислот, ПЭГ-модифицированных церамидов (ПЭГ-CER), ПЭГ-модифицированные диалкиламинов, ПЭГ-модифицированных диацилглицеринов (ПЭГ-DEG), ПЭГ-модифицированных диалкилглицеринов и их смесей. Например, ПЭГ-липид может представлять собой ПЭГ-c-DOMG, ПЭГ-DMG, ПЭГ-DLPE, ПЭГ-DMPE, ПЭГ-DPPC или ПЭГ-DSPE-липид.
Структурные липиды
[00276] Липидный компонент композиции наночастиц может включать один или более структурных липидов. Структурные липиды могут быть выделены из групп, состоящих из, но не ограничивающихся ими, холестерина, фекостерина, ситостерина, эргостерина, кампестерина, стигмастерина, брассикастерина, томатидина, томатина, урсоловой кислоты, альфа-токоферола и их смесей. В некоторых вариантах осуществления, структурный липид представляет собой холестерин. В некоторых вариантах осуществления, структурный липид включает холестерин и кортикостероид (такой как преднизолон, дексаметазон, преднизон и гидрокортизон) или их комбинацию.
Фосфолипиды
[00277] Липидный компонент композиции наночастиц может включать один или более фосфолипидов, таких как один или более (поли)ненасыщенных липидов. Фосфолипиды могут собираться в один или более липидных двойных слоев. Как правило, фосфолипиды могут включать фосфолипидную часть и одну или более жирных кислот. Например, фосфолипид может представлять собой липид формулы (IV):

в которой Rp представляет собой фосфолипидный фрагмент, а R1 и R2 представляют собой жирно-кислотные фрагменты с или без ненасыщенности, которые могут являться одинаковыми или разными. Фосфолипидная часть может быть выбрана из неограничивающей группы, состоящей из фосфатидилхолина, фосфатидилэтаноламина, фосфатидилглицерина, фосфатидилсерина, фосфатидной кислоты, 2-лизофосфатидилхолина и сфингомиелина. Фрагмент жирной кислоты может быть выбран из неограничивающей группы, состоящей из лауриновой кислоты, миристиновой кислоты, миристоленовой кислоты, пальмитиновой кислоты, пальмитолеиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, эруковой кислоты, фитановой кислоты, арахидиновой кислота, арахидоновой кислоты, эйкозапентаеновой кислоты, бегеновой кислота, докозапентаеновой кислоты и докозагексаеновой кислоты. Также данным изобретением охватываются природные виды, включая природные виды с модификациями и заменами, включая разветвление, окисление, циклизацию и алкины. Например, фосфолипид может быть функционализированным или сшитым с одним или более алкинами (например, алкенильная группа, в которой одна или несколько двойных связей заменены тройной связью). При соответствующих условиях реакции алкиновая группа может подвергаться катализируемому медью циклоприсоединению при воздействии азида. Такие реакции могут быть пригодны для функционализации липидного двойного слоя композиции наночастиц для облегчения проникновения через мембрану или клеточного распознавания или для конъюгирования композиции наночастиц с подходящим компонентом, таким как нацеливающий или визуализирующий фрагмент (например, краситель).
[00278] Фосфолипиды, пригодные в композициях и способах, могут быть выбраны из неограничивающей группы, состоящей из 1,2-дистеароил-sn-глицеро-3-фосфохолина (DSPC), 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламина (DOPE), 1,2-дилинолеоил-sn-глицеро-3-фосфохолина (DLPC), 1,2-димиристоил-sn-глицеро-фосфохолина (DMPC), 1,2-диолеоил-sn-глицеро-3-фосфохолина (DOPC), 1,2-дипальмитоил-sn-глицеро-3-фосфохолина (DPPC), 1,2-диундеканoил-sn-глицеро-фосфохолина (DUPC), 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолина (POPC), 1,2-ди-O-октадеценоил-sn-глицеро-3-фосфохолина (18:0 Diether PC), 1-олеоил-2-холестерилгемисукциноил-sn-глицеро-3-фосфохолина (OChemsPC), 1-гексадецил-sn-глицеро-3-фосфохолина (C16 Lyso PC), 1,2-дилиноленоил-sn-глицеро-3-фосфохолина, 1,2-диарахидоноил-sn-глицеро-3-фосфохолина, 1,2-дидокозагексаеноил-sn-глицеро-3-фосфохолина, 1,2-дифитаноил-sn-глицеро-3-фосфоэтаноламина (ME 16,0 PE), 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина, 1,2-дилинолеоил-sn-глицеро-3-фосфоэтаноламина, 1,2-дилиноленоил-sn-глицеро-3-фосфоэтаноламина, 1,2-диарахидоноил-sn-глицеро-3-фосфоэтаноламина, 1,2-дидокозагексаеноил-sn-глицеро-3-фосфоэтаноламина, натриевой соли 1,2-диолеоил-sn-глицеро-3-фосфо-rac-(1-глицерина) (DOPG), дипальмитоилфосфатидилглицерина (DPPG), пальмитоилолеоилфосфатидилэтаноламина (POPE), дистеароил-фосфатидил-этаноламина (DSPE), дипальмитоилфосфатидилэтаноламина (DPPE), димиристоилфосфоэтаноламина (DMPE), 1-стеароил-2-олеоил-фосфатидилэтаноламина (SOPE), 1-стеароил-2-олеоил-фосфатидилхолина (SOPC), сфингомиелина, фосфатидилхолина, фосфатидилэтаноламина, фосфатидилсерина, фосфатидилинозитола, фосфатидной кислоты, пальмитоилолеоилфосфатидилхолина, лизофосфатидилхолина, лизофосфатидилэтаноламина (LPE) и их смесей. В некоторых вариантах осуществления композиция наночастиц содержит DSPC. В конкретных вариантах осуществления композиция наночастиц содержит DOPE. В некоторых вариантах осуществления, композиция наночастиц содержит как DSPC, так и DOPE.
Адъюванты
[00279] В некоторых вариантах осуществления композиция наночастиц, которая включает один или более липидов, описанных в данном документе, может дополнительно включать один или более адъювантов, например, глюкопиранозил-липидный адъювант (GLA), CpG-олигодезоксинуклеотиды (например, класс A или B), поли(I:C), гидроксида алюминия и Pam3CSK4.
Терапевтические агенты
[00280] Композиции наночастиц могут включать одно или более терапевтических и/или профилактических средств. В изобретении описаны способы доставки терапевтического и/или профилактического средства в клетку или орган млекопитающего, получения интересующего полипептида в клетке млекопитающего и лечения заболевания или расстройства у млекопитающего, нуждающегося в этом, включающие введение млекопитающему и/или приведение в контакт клетки млекопитающего с композицией наночастиц, содержащих терапевтическое и/или профилактическое средство.
[00281] Терапевтические и/или профилактические средства включают биологически активные вещества и альтернативно называются «активными агентами». Терапевтическое и/или профилактическое средство может представлять собой вещество, которое после доставки в клетку или орган вызывает желательные изменения в клетке, органе или другой ткани или системе организма. Такие частицы могут быть признаны пригодными при лечении одного или более заболеваний, расстройств или патологических состояний. В некоторых вариантах осуществления терапевтическое и/или профилактическое средство представляет собой низкомолекулярное лекарственное средство, пригодное для лечения определенного заболевания, расстройства или патологического состояния. Примеры лекарственных средств, пригодных в композициях наночастиц, включают, но не ограничиваются ими, антинеопластическое средство (например, винкристин, доксорубицин, митоксантрон, камптотецин, цисплатин, блеомицин, циклофосфамид, метотрексат и стрептозотоцин), противоопухолевые средства (например, актиномин D), винбластин, цитозинарабинозид, антрациклины, алкилирующие агенты, соединения платины, антиметаболиты и аналоги нуклеозидов, такие как метотрексат и аналоги пурина и пиримидина), противоинфекционные средства, местные анестетики (например, дибукаин и хлорпромазин), бета-адренергические блокаторы (например, пропранолол, тимолол и лабеталол), антигипертензивные средства (например, клонидин и гидралазин), антидепрессанты (например, имипрамин, амитриптилин и доксепин), противосудорожные средства (например, фенитоин), антигистаминные препараты (например, дифенгидрамин, хлорфенирамин и прометазин), антибиотики/антибактериальные средства (например, гентамицин, ципрофлоксацин и цефокситин), противогрибковые средства (например, миконазол, терконазол, эконазол, изоконазол, бутоконазол, клотримазол, итраконазол, нистатин, нафтифин и амфотерицин В), противопаразитарные агенты, гормоны, антагонисты гормонов, иммуномодуляторы, антагонисты нейротрансмиттеров, агенты против глаукомы, витамины, наркотические средства и средства визуализации.
[00282] В некоторых вариантах осуществления терапевтическое и/или профилактическое средство представляет собой цитотоксин, радиоактивный ион, химиотерапевтическое средство, вакцину, соединение, вызывающее иммунный ответ, и/или другое терапевтическое и/или профилактическое средство. Цитотоксин или цитотоксический агент включает любой агент, который может быть вредоносным для клеток. Примеры включают, но не ограничиваются ими, таксол, цитохалазин В, грамицидин D, этидий бромид, эметин, митомицин, этопозид, тенипозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол, пуромицин, майтансиноиды, например, майтанзинол, рахельмицин (CC-1065) и их аналоги или гомологи. Радиоактивные ионы включают, но не ограничиваются ими, иод (например, иод 125 или иод 131), стронций 89, фосфор, палладий, цезий, иридий, фосфат, кобальт, иттрий 90, самарий 153 и празеодим. Вакцины включают соединения и препараты, которые способны обеспечить иммунитет против одного или более патологических состояний, связанных с инфекционными заболеваниями, такими как грипп, корь, вирус папилломы человека (HPV), бешенство, менингит, коклюш, столбняк, чума, гепатит и туберкулез, и могут включать мРНК кодирующие инфекционные заболевания, полученные из антигенов и/или эпитопов. Вакцины также включают соединения и препараты, которые направляют иммунный ответ против раковых клеток и могут включать мРНК, кодирующие антигены, полученные из опухолевых клеток, эпитопы и/или неоэпитопы. Соединения, вызывающие иммунные ответы, могут включать вакцины, кортикостероиды (например, дексаметазон) и другие частицы. В некоторых вариантах осуществления вакцина и/или соединение, способное вызывать иммунный ответ, вводят внутримышечно в композиции, содержащей соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) (например, соединение 3, 18, 20, 25, 26, 29, 30, 60, 108-112 или 122). Другие терапевтические и/или профилактические средства включают, но не ограничиваются ими, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацил-дакарбазин), алкилирующие агенты (например, мехлоретамин, тиотепа, хлорамбуцил рахельмицин (CC-1065), мелфалан, кармустин (BSNU), ломустин (CCNU), циклофосфамид, бусульфан, дибромманнит, стрептозотоцин, митомицин C и цис-дихлордиамин платина (II), цисплатин), антрациклины (например, даунорубицин (ранее дауномицин) и доксорубицин), антибиотики (например, дактиномицин (ранее актиномицин), блеомицин, митрамицин и антрамицин (АМС)) и антимитотические агенты (например, винкристин, винбластин, таксол и майтанзиноиды).
[00283] В других вариантах осуществления терапевтическое и/или профилактическое средство представляет собой белок. Терапевтические белки, пригодные для наночастиц по данному изобретению, включают, но не ограничиваются ими, гентамицин, амикацин, инсулин, эритропоэтин (EPO), гранулоцит-колониестимулирующий фактор (G-CSF), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) фактор VIR, аналоги, высвобождающие лютеинизирующий гормон (LHRH), интерфероны, гепарин, поверхностный антиген гепатита В, вакцина против брюшного тифа и вакцина против холеры.
Полинуклеотиды и нуклеиновые кислоты
[00284] В некоторых вариантах осуществления терапевтическое средство представляет собой полинуклеотид или нуклеиновую кислоту (например, рибонуклеиновую кислоту или дезоксирибонуклеиновую кислоту). Термин «полинуклеотид» в самом широком смысле включает любое соединение и/или вещество, которое может быть включено в олигонуклеотидную цепь. Иллюстративные примеры полинуклеотидов для применения по данному изобретению включают, но не ограничиваются ими, одно или более из дезоксирибонуклеиновой кислоты (ДНК), рибонуклеиновой кислоты (РНК), включая мРНК мессенджера (мРНК), ее гибриды, агенты, индуцирующие РНКи, агенты РНКи, миРНК, кшРНК, антисмысловые РНК, рибозимы, каталитическая ДНК, РНК, которые индуцируют образование тройной спирали, аптамеры, векторы и т. д. В некоторых аспектах терапевтическим и/или профилактическим средством является РНК. РНК, подходящие для описанных в данном документе композиций и способов, могут быть выбраны из групп, состоящих из, но не ограничивающихся ими, шортмеров, антагомиров, антисмысловых, рибозимов, малых интерферирующих РНК (миРНК), асимметричных интерферирующих РНК (aiRNA), микроРНК (miRNA), дайсер-субстратной РНК (дцРНК), короткой шпилечной РНК (мшРНК), трансферной РНК (тРНК), мессенджера РНК (мРНК) и их смесей. В конкретных вариантах осуществления РНК представляет собой мРНК.
[00285] В конкретных вариантах осуществления терапевтическое и/или профилактическое средство представляет собой мРНК. мРНК может кодировать любой интересующий полипептид, включая любой полипептид, встречающийся в природе или не встречающийся в природе, или иным образом модифицированный. Полипептид, кодируемый мРНК, может быть любого размера и может иметь любую вторичную структуру или активность. В некоторых вариантах осуществления полипептид, кодируемый мРНК, может оказывать терапевтическое действие при экспрессии в клетке.
[00286] В других вариантах осуществления терапевтическое и/или профилактическое средство представляет собой миРНК. миРНК может быть способной избирательно нокаутировать или регулировать экспрессию гена, представляющего интерес. Например, миРНК может быть выбрана для того, чтобы заставить замолчать ген, связанный с конкретным заболеванием, расстройством или патологическим состоянием, при введении субъекту, нуждающемуся в этом, композиции наночастиц, включающей миРНК. миРНК может содержать последовательность, которая комплементарна последовательности мРНК, которая кодирует представляющий интерес ген или белок. В некоторых вариантах осуществления миРНК может представлять собой иммуномодулирующую миРНК.
[00287] В конкретных вариантах осуществления терапевтическое и/или профилактическое средство представляет собой sgRNA и/или cas9 мРНК. sgRNA и/или cas9 mRNA могут быть использованы в качестве инструментов редактирования. Например, комплекс sgRNA-cas9 может влиять на трансляцию мРНК клеточных генов.
[00288] В некоторых вариантах осуществления терапевтическое и/или профилактическое средство представляет собой кшРНК или вектор или плазмиду, кодирующие их. кшРНК может продуцироваться внутри клетки-мишени при доставке соответствующей конструкции в ядро. Конструкции и механизмы, относящиеся к кшРНК, хорошо известны в соответствующих областях техники.
[00289] Нуклеиновые кислоты и полинуклеотиды, пригодные для данного изобретения, обычно включают первую область связанных нуклеозидов, кодирующую представляющий интерес полипептид (например, кодирующую область), первую фланкирующую область, расположенную на 5'-конце первой области (например, 5'-НТО), вторую фланкирующую область, расположенную на 3'-конце первой области (например, 3'-НТО) по меньшей мере одну 5'-кэп область и 3'-стабилизирующую область. В некоторых вариантах осуществления нуклеиновая кислота или полинуклеотид дополнительно включает в себя поли-A-область или последовательность Козака (например, в 5'-НТО). В некоторых случаях полинуклеотиды могут содержать одну или более интронных нуклеотидных последовательностей, которые можно вырезать из полинуклеотида. В некоторых вариантах осуществления полинуклеотид или нуклеиновая кислота (например, мРНК) может включать 5'-кэп структуру, терминирующий нуклеотид, 'петля-на-стебле', полиА последовательность и/или сигнал полиадениляции. Любая из областей нуклеиновой кислоты может включать один или более альтернативных компонентов (например, альтернативный нуклеозид). Например, 3'-стабилизирующая область может содержать альтернативный нуклеозид, такой как L-нуклеозид, инвертированный тимидин или 2'-O-метилнуклеозид и/или кодирующую область, 5'-НТО, 3'-НТО или кэп-область может включать альтернативный нуклеозид, такой как 5-замещенный уридин (например, 5-метоксиуридин), 1-замещенный псевдоуридин (например, 1-метилпсевдоуридин или 1-этилпсевдоуридин) и/или 5-замещенный цитидин (например, 5-метилцитидин).
[00290] Обычно самой короткой длиной полинуклеотида может быть длина полинуклеотидной последовательности, достаточная для кодирования дипептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования трипептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования тетрапептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования пентапептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования гексапептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования гептапептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования октапептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования нонапептида. В другом варианте осуществления длина полинуклеотидной последовательности достаточна для кодирования декапептида.
[00291] Примеры дипептидов, которые могут кодировать альтернативные полинуклеотидные последовательности, включают, но не ограничиваются ими, карнозин и ансерин.
[00292] В некоторых случаях длина молекулы полинуклеотида превышает 30 нуклеотидов. В другом варианте осуществления длина молекулы полинуклеотида превышает 35 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 40 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 45 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 55 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 50 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 60 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 80 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 90 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 100 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 120 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 140 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 160 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 180 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 200 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 250 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 300 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 350 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 400 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 450 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 500 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 600 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 700 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 800 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 900 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1000 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1100 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1200 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1300 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1400 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1500 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1600 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1800 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 2000 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 2500 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 3000 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 4000 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 5000 нуклеотидов или более 5000 нуклеотидов.
[00293] Нуклеиновые кислоты и полинуклеотиды могут включать один или более встречающихся в природе компонентов, включая любой из канонических нуклеотидов A (аденозин), G (гуанозин), C (цитозин), U (уридин) или T (тимидин). В одном варианте осуществления все или практически все нуклеотиды, включающие (а) 5'-НТО, (b) открытую рамку считывания (ORF), (c) 3'-НТО, (d) хвост поли-А и любую комбинацию (a, b, c или d выше) включают встречающиеся в природе канонические нуклеотиды A (аденозин), G (гуанозин), C (цитозин), U (уридин) или T (тимидин).
[00294] Нуклеиновые кислоты и полинуклеотиды могут включать один или более альтернативных компонентов, описанных в данном документе, которые придают пригодные свойства, включая повышенную стабильность и/или отсутствие существенной индукции врожденного иммунного ответа клетки, в которую вводится полинуклеотид. Например, альтернативный полинуклеотид или нуклеиновая кислота проявляет пониженную деградацию в клетке, в которую введен полинуклеотид или нуклеиновая кислота, по сравнению с соответствующим неизмененным полинуклеотидом или нуклеиновой кислотой. Эти альтернативные виды могут повышать эффективность продукции белка, внутриклеточную задержку полинуклеотидов и/или жизнеспособность приведенных в контакт клеток, а также обладать пониженной иммуногенностью.
[00295] Полинуклеотиды и нуклеиновые кислоты могут быть природными или не встречающимися в природе. Полинуклеотиды и нуклеиновые кислоты могут включать один или более модифицированных (например, измененных или альтернативных) нуклеиновых оснований, нуклеозидов, нуклеотидов или их комбинаций. Нуклеиновые кислоты и полинуклеотиды, используемые в композиции наночастиц, могут включать любую подходящую модификацию или изменение, такое как нуклеиновая основа, сахар или межнуклеозидная связь (например, с фосфатной/фосфодиэфирной связью/с фосфодиэфирным скелетом). В конкретных вариантах осуществления изменения (например, одно или более изменений) присутствуют в каждом из нуклеиновых оснований, сахаре и межнуклеозидной связи. Изменения по данному изобретению могут представлять собой изменения рибонуклеиновых кислот (РНК) в дезоксирибонуклеиновые кислоты (ДНК), например, замена 2'-ОН рибофуранозильного кольца на 2'-H, треозонуклеиновые кислоты (TNA), гликолевые нуклеиновые кислоты (GNA), пептидные нуклеиновые кислоты (PNA), закрытые нуклеиновые кислоты (LNA) или их гибриды. Здесь описаны дополнительные изменения.
[00296] Полинуклеотиды и нуклеиновые кислоты могут или не могут быть равномерно изменены по всей длине молекулы. Например, один или более или все типы нуклеотидов (например, пурин или пиримидин или любой один или более или все из A, G, U, C) могут или не могут быть однородно изменены в полинуклеотиде или нуклеиновой кислоте или в заданной области его последовательности. В некоторых случаях все нуклеотиды X в полинуклеотиде (или в данной области последовательности) изменены, причем X может представлять собой любой из нуклеотидов A, G, U, C или любую одну из комбинаций A+G, A+U, A+C, G+U, G+C, U+C, A+G+U, A+G+C, G+U+C или A+G+C.
[00297] Различные изменения сахара и/или межнуклеозидных связях (например, структуре скелета) могут существовать в различных положениях в полинуклеотиде. Специалист в данной области поймет, что аналоги нуклеотидов или другие изменения могут обнаруживаться в любом положении (ях) полинуклеотида, так что функция полинуклеотида существенно не снижается. Изменением также может быть изменение на 5'- или 3'-конце. В некоторых вариантах осуществления полинуклеотид включает изменение на 3'-конце. Полинуклеотид может содержать от около 1% до около 100% альтернативных нуклеотидов (либо по отношению к общему содержанию нуклеотидов, либо по отношению к одному или более типам нуклеотидов, т.е. любому одному или более из A, G, U или C) или любой промежуточный процент (например, от 1% до 20%, от 1% до 25%, от 1% до 50%, от 1% до 60%, от 1% до 70%, от 1% до 80%, от 1% до 90%, от 1% до 95%, от 10% до 20%, от 10% до 25%, от 10% до 50%, от 10% до 60%, от 10% до 70%, от 10% до 80%, от 10% до 90%, от 10% до 95%, от 10% до 100%, от 20% до 25%, от 20% до 50%, от 20% до 60%, от 20% до 70%, от 20% до 80%, от 20% до 90%, от 20% до 95%, от 20% до 100%, от 50% до 60%, от 50% до 70%, от 50% до 80%, от 50% до 90%, от 50% до 95%, от 50% до 100%, от 70% до 80%, от 70% до 90%, от 70% до 95%, от 70% до 100%, от 80% до 90%, от 80% до 95%, от 80% до 100%, от 90% до 95%, от 90% до 100% и от 95% до 100%). Понятно, что любой оставшийся процент объясняется присутствием канонического нуклеотида (например, A, G, U или C).
[00298] Полинуклеотиды могут содержать как минимум ноль и как максимум 100% альтернативных нуклеотидов или любой промежуточный процент, такой как по меньшей мере 5% альтернативных нуклеотидов, по меньшей мере 10% альтернативных нуклеотидов, по меньшей мере 25% альтернативных нуклеотидов, по меньшей мере 50% альтернативных нуклеотидов, по меньшей мере 80% альтернативных нуклеотидов или по меньшей мере 90% альтернативных нуклеотидов. Например, полинуклеотиды могут содержать альтернативный пиримидин, такой как альтернативный урацил или цитозин. В некоторых вариантах осуществления по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 50%, по меньшей мере 80%, по меньшей мере 90% или 100% урацила в полинуклеотиде заменено альтернативным урацилом (например, 5-замещенным урацилом). Альтернативный урацил может быть заменен соединением, имеющим единственную уникальную структуру, или может быть заменен множеством соединений, имеющих разные структуры (например, 2, 3, 4 или более уникальных структур). В некоторых случаях по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 50%, по меньшей мере 80%, по меньшей мере 90% или 100% цитозина в полинуклеотиде заменено альтернативным цитозином (например, 5-замещенным цитозином). Альтернативный цитозин может быть заменен соединением, имеющим единственную уникальную структуру, или может быть заменен множеством соединений, имеющих разные структуры (например, 2, 3, 4 или более уникальных структур).
[00299] В некоторых случаях нуклеиновые кислоты по существу не индуцируют врожденный иммунный ответ клетки, в которую введен полинуклеотид (например, мРНК). Особенности индуцированного врожденного иммунного ответа включают 1) повышенную экспрессию провоспалительных цитокинов, 2) активацию внутриклеточных PRR (RIG-I, MDA5 и т. д. и/или 3) прекращение или уменьшение трансляции белка.
[00300] Нуклеиновые кислоты могут необязательно включать другие агенты (например, агенты, индуцирующие РНКи, агенты РНКи, миРНК, кшРНК, миРНК, антисмысловые РНК, рибозимы, каталитическая ДНК, тРНК, РНК, которые вызывают образование тройной спирали, аптамеры и векторы). В некоторых случаях заявленные нуклеиновые кислоты могут включать одну или более РНК-мессенджеров (мРНК), имеющих один или более альтернативных нуклеозидов или нуклеотидов (т.е. альтернативных молекул мРНК).
[00301] В некоторых вариантах осуществления, молекула нуклеиновой кислоты (например, мРНК), формула, состав или способ, связанные с ней, содержат один или более полинуклеотидов, имеющих признаки, как описано в WO 2002/098443, WO 2003/051401, WO 2008/052770, WO 2009127230, WO 2006122828, WO 2008/083949, WO 2010088927, WO 2010/037539, WO 2004/004743, WO 2005/016376, WO 2006/024518, WO 2007/095976, WO 2008/014979, WO 2008/077592, WO 2009/030481, WO 2009/095226, WO 2011069586, WO 2011026641, WO 2011/144358, WO 2012019780, WO 2012013326, WO 2012089338, WO 2012113513, WO 2012116811, WO 2012116810, WO 2013113502, WO 2013113501, WO 2013113736, WO 2013143698, WO 2013143699, WO 2013143700, WO 2013/120626, WO 2013120627, WO 2013120628, WO 2013120629, WO 2013174409, WO 2014127917, WO 2015/024669, WO 2015/024668, WO 2015/024667, WO 2015/024665, WO 2015/024666, WO 2015/024664, WO 2015101415, WO 2015101414, WO 2015024667, WO 2015062738, WO 2015101416, каждый из которых включен посредством ссылки в данный документ.
Альтернативные нуклеиновые основания
[00302] Альтернативные нуклеозиды и нуклеотиды могут включать альтернативное нуклеиновое основание. Нуклеиновое основание нуклеиновой кислоты представляет собой органическое основание, такое как пурин или пиримидин или их производное. Нуклеиновое основание может представлять собой каноническое основание (например, аденин, гуанин, урацил, тимин и цитозин). Данные нуклеиновые основания могут быть изменены или полностью заменены для получения полинуклеотидных молекул, обладающих улучшенными свойствами, например, повышенной стабильностью, такой как устойчивость к нуклеазам. Неканонические или модифицированные основания могут включать, например, одно или более замещений или модификаций, включая, но не ограничиваясь ими, замещения алкилом, арилом, галогеном, оксо, гидроксилом, алкилокси и/или тио; одно или более конденсированных или открытых колец; окисление; и/или востановление.
[00303] Альтернативное спаривание нуклеотидных оснований включает не только стандартные пары оснований аденин-тимин, аденин-урацил или гуанин-цитозин, но также пары оснований, образованные между нуклеотидами и/или альтернативными нуклеотидами, включая нестандартные или альтернативные основания, причем расположение доноров водородных связей и акцепторов водородных связей обеспечивают водородную связь между нестандартным основанием и стандартным основанием или между двумя комплементарными нестандартными основными структурами. Одним примером такого нестандартного спаривания оснований является спаривание оснований между альтернативным нуклеотидом инозином и аденином, цитозином или урацилом.
[00304] В некоторых вариантах осуществления нуклеиновое основа является альтернативой урацилу. Типичные нуклеиновые основания и нуклеозиды, имеющие альтернативный урацил, включают псевдоуридин (ψ), пиридин-4-онрибонуклеозид, 5-аза-урацил, 6-аза-урацил, 2-тио-5-азаурацил, 2-тиоурацил (s2U), 4-тиоурацил (s4U), 4-тиопсевдоуридин, 2-тиопсевдоуридин, 5-гидроксиурацил (ho5U), 5-аминоаллилурацил, 5-галогенурацил (например, 5-иодурацил или 5-бромурацил), 3-метилурацил (m3U), 5-метоксиурацил (mo5U), урацил-5-оксиуксусную кислоту (cmo5U), метиловый эфир урацил-5-оксиуксусной кислоты (mcmo5U), 5-карбоксиметилурацил (cm5U), 1-карбоксиметилпсевдоуридин, 5-карбоксигидроксиметилурацил (chm5U), метиловый эфир 5-карбоксигидроксиметилурацила (mchm5U), 5-метоксикарбонилметилурацил (mcm5U), 5-метоксикарбонилметил-2-тиоурацил (mcm5s2U), 5-аминометил-2-тиоурацил (nm5s2U), 5-метиламинометилурацил (mnm5U), 5-метиламинометил-2-тио-урацил (mnm5s2U), 5-метиламинометил-2-селеноурацил (mnm5se2U), 5-карбамоилметилурацил (ncm5U), 5-карбоксиметиламинометилурацил (cmnm5U), 5-карбоксиметиламинометил-2-тиоурацил (cmnm5s2U), 5-пропинилурацил, 1-пропинилпсевдоурацил, 5-тауринометилурацил (τm5U), 1-тауринометилпсевдоуридин, 5-тауринометил-2-тиоурацил (τm5s2U), 1-тауринометил-4-тиопсевдоуридин, 5-метилурацил (m5U, т.е. имеющий нуклеиновое основание дезокситимин), 1-метилпсевдоуридин (m1ψ), 1-этилпсевдоуридин (Et1ψ), 5-метил-2-тиоурацил (m5s2U), 1-метил-4-тиопсевдоуридин (m1s4ψ), 4-тио-1-метилпсевдоуридин, 3-метилпсевдоуридин (m3ψ), 2-тио-1-метилпсевдоуридин, 1-метил-1-деазапсевдоуридин, 2-тио-1-метил-1-деазапсевдоуридин, дигидроурацил (D), дигидропсевдоуридин, 5,6-дигидроурацил, 5-метилдигидроурацил (m5D), 2-тиодигидроурацил, 2-тио-дигидропсевдоуридин, 2-метоксиурацил, 2-метокси-4-тиоурацил, 4-метоксипсевдоуридин, 4-метокси-2-тиопсевдоуридин, N1-метилпсевдоуридин, 3-(3-амино-3-карбоксипропил)урацил (acp3U), 1-метил-3-(3-амино-3-карбоксипропил)псевдоуридин (acp3ψ), 5-(изопентениламинометил)урацил (inm5U), 5-(изопентениламинометил)-2-тиоурацил (inm5s2U), 5,2'-O-диметилуридин (m5Um), 2-тио-2'-O_метил-уридин (s2Um), 5-метоксикарбонилметил-2'-O-метилуридин (mcm5Um), 5-карбамоилметил-2'-O-метилуридин (ncm5Um), 5-карбоксиметиламинометил-2'-O-метилуридин (cmnm5Um), 3,2'-O-диметилуридин (m3Um) и 5-(изопентениламинометил)-2'-O-метилуридин (inm5Um), 1-тиоурацил, дезокситимидин, 5-(2-карбометоксивинил)-урацил, 5-(карбамоилгидроксиметил)-урацил, 5-карбамоилметил-2-тиоурацил, 5-карбоксиметил-2-тиоурацил, 5-цианометилурацил, 5-метокси-2-тио-урацил и 5-[3-(1-E-пропениламино)]урацил.
[00305] В некоторых вариантах осуществления нуклеиновое основание является альтернативой цитозину. Иллюстративные примеры нуклеиновых оснований и нуклеозиды, имеющие альтернативный цитозин, включают 5-азацитозин, 6-азацитозин, псевдоизоцитидин, 3-метилцитозин (m3C), N4-ацетилцитозин (ac4C), 5-формилцитозин (f5C), N4-метилцитозин (m4C), 5-метилцитозин (m5C), 5-галогенцитозин (например, 5-иодцитозин), 5-гидроксиметилцитозин (hm5C), 1-метилпсевдоизоцитидин, пирролоцитозин, пирролопсевдоизоцитидин, 2-тиоцитозин (s2C), 2-тио-5-метилцитозин, 4-тиопсевдоизоцитидин, 4-тио-1-метилпсевдоизоцитидин, 4-тио-1-метил-1-деазапсевдоизоцитидин, 1-метил-1-деазапсевдоизоцит зебуларин, 5-азазебуларин, 5-метилзебуларин, 5-аза-2-тиозебуларин, 2-тиозебуларин, 2-метоксицитозин, 2-метокси-5-метилцитозин, 4-метоксипсевдоизоцитидин, 4-метокси-1-метилпсевдоизоцитидин, лизидин (k2C), 5,2'-O-диметилцитидин (m5Cm), N4-ацетил-2'-O-метилцитидин (ac4Cm), N4,2'-O-диметилцитидин (m4Cm), 5-формил-2'-O-метилцитидин (f5Cm), N4, N4,2'-O-триметилцитидин (m42Cm), 1-тиоцитозин, 5-гидроксицитозин, 5-(3-азидопропил)-цитозин и 5- (2-азидоэтил)-цитозин.
[00306] В некоторых вариантах осуществления нуклеиновое основание является альтернативой аденину. Иллюстративные примеры нуклеиновых оснований и нуклеозиды, имеющие альтернативный аденин, включают 2-аминопурин, 2,6-диаминопурин, 2-амино-6-галогенпурин (например, 2-амино-6-хлорпурин), 6-галогенпурин (например, 6-хлорпурин), 2-амино-6-метилпурин, 8-азидоаденин, 7-деазааденин, 7-деаза-8-азааденин, 7-деаза-2-аминопурин, 7-деаза-8-аза-2-амино-пурин, 7-деаза-2,6-диаминопурин, 7-деаза-8-аза-2,6-диаминопурин, 1-метиладенин (m1A), 2-метиладенин (m2A), N6-метиладенин (m6A), 2-метилтио-N6-метиладенин (ms2m6A), N6-изопентиниладенин (i6A), 2-метилтио-N6-изопентиниладенин (ms2i6A), N6- (цис-гидроксиизопентил)аденин (io6A), 2-метилтио-N6-(цис-гидроксиизопентенил)аденин (ms6) N6-глицинилкарбамоиладенин (g6A), N6-треонилкарбамоиладенин (t6A), N6-метил-N6-треонилкарбамоиладенин (m6t6A), 2-метилтио-N6-треонилкарбамоиладенин (ms2g6A), N6,N6-диметиладенин (m62A), N6-гидроксинорвалилкарбамоиладенин (hn6A), 2-метилтио-N6-гидроксинорвалилкарбамоиладенин (ms2hn6A), N6-ацетиладенин (ac6A), 7-метиладенин, 2-метилтиоаденин, 2-метоксиаденин, N6,2'-O-диметиладенозин (m6Am), N6,N6,2'-O-триметиладенозин (m62Am), 1,2'-O-диметиладенозин (m1Am), 2-амино-N6-метилпурин, 1-тиоаденин, 8-азидоаденин, N6-(19-аминопентаоксанонадецил)-аденин, 2,8-диметиладенин, N6-формиладенин и N6-гидроксиметиладенин.
[00307] В некоторых вариантах осуществления, нуклеиновое основание является альтернативой гуанину. Иллюстративные примеры нуклеиновых оснований и нуклеозидов, имеющие альтернативный гуанин, включают инозин (I), 1-метилинозин (m1I), виозин (imG), метилвиозин (mimG), 4-дeметилвиозин (imG-14), изовиозин (imG2), вибутозин (yW), пероксивибутозин (o2yW), гидроксивибутозин (OHyW), немодифицированный гидроксивибутозин (OHyW*), 7-деазагуанин, квеуозин (Q), epоксиквеуозин (oQ), галактозилквеуозин (galQ), маннозилквеуозин (manQ), 7-циано-7-деазагуанин (preQ0), 7-аминометил-7-деазагуанин (preQ1), археозин (G+), 7-деаза-8-аза-гуанин, 6-тио-гуанин, 6-тио-7-деазагуанин, 6-тио-7-деаза-8-азагуанин, 7-метилгуанин (m7G), 6-тио-7-метилгуанин, 7-метилинозин, 6-метоксигуанин, 1-метилгуанин (m1G), N2-метилгуанин (m2G), N2,N2-диметилгуанин (m22G), N2,7-диметилгуанин (m2,7G), N2, N2,7-диметилгуанин (m2,2,7G), 8-оксогуанин, 7-метил-8-оксогуанин, 1-метил-6-тиогуанин, N2-метил-6-тиогуанин, N2,N2-диметил-6-тиогуанин, N2-метил-2'-O-метилгуанозин (m2Gm), N2,N2-диметил-2'-O-метилгуанозин (m22Gm), 1-метил-2'-O-метилгуанозин (m1Gm), N2,7-диметил-2'-O-метилгуанозин (m2,7Gm), 2'-O-метилинозин (Im), 1,2'-O-диметилинозин (m1Im), 1-тиогуанин и O-6-метилгуанин.
[00308] Альтернативным нуклеиновым основанием нуклеотида может быть независимо пурин, пиримидин и аналог пурина или пиримидина. Например, нуклеиновое основание может быть альтернативой аденину, цитозину, гуанин, урацил или гипоксантин. В другом варианте осуществления, нуклеиновое основание может также включать, например, встречающиеся в природе и синтетические производные основания, включая пиразоло[3,4-d]пиримидины, 5-метилцитозин (5-me-C), 5-гидроксиметилцитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил- и другие алкилпроизводные аденина и гуанина, 2-пропил- и другие алкилпроизводные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-пропинилурацил и цитозин, 6-азоурацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацил, 8-галоген (например, 8-бром), 8-амино, 8-тиол, 8-тиоалкил, 8-гидрокси и др. 8-замещенные аденины и гуанины, 5-галоген, в частности 5-бром, 5-трифторметил и другие 5-замещенные урацилы и цитозины, 7-метилгуанин и 7-метиладенин, 8-азагуанин и 8-азааденин, деазагуанин, 7-деазагуанин, 3-деазагуанин, деазааденин, 7-деазааденин, 3-деазааденин, пиразоло[3,4-d]пиримидин, имидазо[1,5-a]-1,3,5-триазиноны, 9-деазапурин, имидазо[4,5-d ]пиразины, тиазоло[4,5-d]пиримидины, пиразин-2-он, 1,2,4-триазин, пиридазин; или 1,3,5 триазин. Когда нуклеотиды изображены с использованием сокращения A, G, C, T или U, каждая буква относится к типичному основанию и/или его производным, например, A включает аденин или аналоги аденина, например, 7-деазааденин).
Изменения на сахаре
[00309] Нуклеозиды включают молекулу сахара (например, сахар из 5-ти или 6-ти атомов углерода, такой как пентоза, рибоза, арабиноза, ксилоза, глюкоза, галактоза или ее дезоксипроизводное) в комбинации с нуклеотидом, в то время как нуклеотиды являются нуклеозидами, содержащими нуклеозид, и фосфатную группу или альтернативную группу (например, боранофосфат, тиофосфат, селенофосфат, фосфонат, алкильная группа, амидат и глицерин). Нуклеозид или нуклеотид может представлять собой канонический вид, например, нуклеозид или нуклеотид, включающий каноническую нуклеиновую основу, сахар и, в случае нуклеотидов, фосфатную группу, или может представлять собой альтернативный нуклеозид или нуклеотид, включающий один или более альтернативных компонентов. Например, в сахаре альтернативных нуклеозидов и нуклеотидов могут быть внесены изменения в нуклеозиде или нуклеотиде. В некоторых вариантах осуществления альтернативные нуклеозиды или нуклеотиды включают структуру:
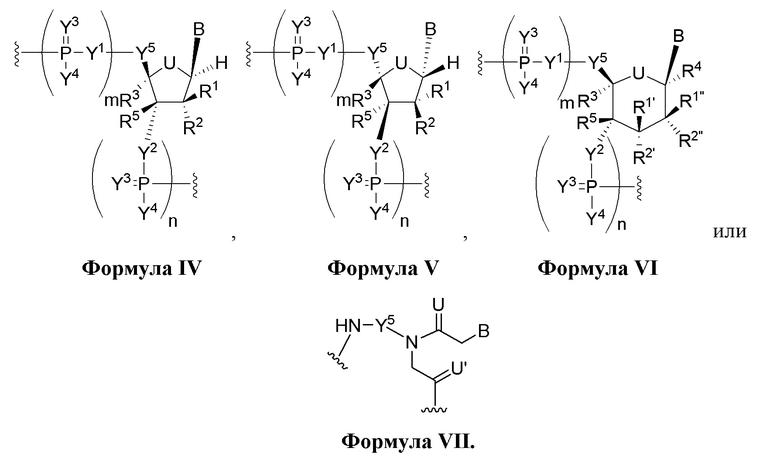
В каждой из формул IV, V, VI и VII,
каждый из m и n независимо равно целому числу от 0 до 5,
каждый из U и U' независимо представляет собой O, S, N(RU)nu или C(RU)nu, где nu равно целому числу от 0 до 2, и каждый RU независимо представляет собой, H, галоген или необязательно замещенный алкил;
каждый из R1', R2', R1'', R2'', R1, R2, R3, R4 и R5 независимо представляет собой, если присутствует, H, галоген, гидрокси, тиол, необязательно замещенный алкил, необязательно замещенный алкокси, необязательно замещенный алкенилокси, необязательно замещенный алкинилокси, необязательно замещенный аминоалкокси, необязательно замещенный алкоксиалкокси, необязательно замещенный гидроксиалкокси, необязательно замещенный амино, азидо, необязательно замещенный арил, необязательно замещенный аминоалкил, необязательно замещенный аминоалкенил, необязательно замещенный аминоалкинил или отсутствует; где комбинация R3 с одним или более из R1', R1'', R2', R2''или R5 (например, комбинация R1' и R3, комбинация R1″ и R3, комбинация R2' и R3, комбинация R2″ и R3 или комбинация R5 и R3) могут объединяться в необязательно замещенный алкилен или необязательно замещенный гетероалкилен и, взятые вместе с атомами углерода, к которым они присоединены, обеспечивать необязательно замещенный гетероциклил (например, бициклический, трициклический или тетрациклический гетероциклил); где комбинация R5 с одним или более из R1', R1'', R2' или R2'' (например, комбинация R1' и R5, комбинация R1'' и R5, комбинация R2' и R5 или комбинация R2'' и R5) могут объединяться в необязательно замещенный алкилен или необязательно замещенный гетероалкилен и, взятые вместе с атомами углерода, к которым они присоединены, обеспечивать необязательно замещенный гетероциклил (например, бициклический, трициклический или тетрациклический гетероциклил); и где комбинация R4 и одного или более из R1', R1'', R2', R2'', R3 или R5 могут объединяться в необязательно замещенный алкилен или необязательно замещенный гетероалкилен и, взятые вместе с атомами углерода, к которым они присоединены, образуют необязательно замещенный гетероциклил (например, бициклический, трициклический или тетрациклический гетероциклил)); каждый из m' и m″ независимо равен целому числу от 0 до 3 (например, от 0 до 2, от 0 до 1, от 1 до 3 или от 1 до 2);
каждый из Y1, Y2 и Y3, независимо представляет собой, O, S, Se, -NRN1-, необязательно замещенный алкилен, или необязательно замещенный гетероалкилен, где RN1 представляет собой H, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный арил или отсутствует;
каждый Y4 независимо представляет собой, H, гидрокси, тиол, боранил, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный алкокси, необязательно замещенный алкенилокси, необязательно замещенный алкинилокси, необязательно замещенный тиоалкокси, необязательно замещенный алкоксиалкокси или необязательно замещенный амино;
каждый Y5 независимо представляет собой, O, S, Se, необязательно замещенный алкилен (например, метилен), или необязательно замещенный гетероалкилен; и
B представляет собой нуклеиновую основу, либо модифицированную, либо немодифицированную.
[00310] В некоторых вариантах осуществления, 2'-гидроксигруппа (ОН) может быть модифицирована или заменена рядом различных заместителей. Иллюстративные примеры заместителей в 2'-положении включают, но не ограничиваются ими, H, азидо, галоген (например, фтор), необязательно замещенный C1-6 алкил (например, метил); необязательно замещенный C1-6 алкокси (например, метокси или этокси); необязательно замещенный C6-10 арилокси; необязательно замещенный C3-8 циклоалкил; необязательно замещенный C6-10 арил-C1-6 алкокси, необязательно замещенный C1-12 (гетероциклил) окси; сахар (например, рибоза, пентоза или любой из описанных в данном документе); полиэтиленгликоль (ПЭГ), -O(CH2CH2O)nCH2CH2OR, где R представляет собой H или необязательно замещенный алкил и n равно целому числу от 0 до 20 (например, от 0 до 4, от 0 до 8, от 0 до 10, от 0 до 16, от 1 до 4, от 1 до 8, от 1 до 10, от 1 до 16, от 1 до 20, от 2 до 4, от 2 до 8, от 2 до 10, от 2 до 16, от 2 до 20, от 4 до 8, от 4 до 10, от 4 до 16 и от 4 до 20); «закрытые» нуклеиновые кислоты (LNA), в которых 2'-гидрокси соединен С1-6 алкиленовым или C1-6 гетероалкиленовым мостиком с 4'-углеродом того же рибозного сахара, где иллюстративные примеры мостиков включают метиленовые, пропиленовые, эфирные или амино-мостики; аминоалкил, определенные в данном документе; аминоалкокси, определенные в данном документе; амино, определенные в данном документе; и аминокислоты, определенные в данном документе.
[00311] Как правило, РНК включает рибозу сахарной группы, которая представляет собой 5-членное кольцо с кислородом. Иллюстративные примеры неограничивающих альтернативных нуклеотидов включают замену кислорода в рибозе (например, S, Se или алкиленом, таким как метилен или этилен); добавление двойной связи (например, для замены рибозы на циклопентенил или циклогексенил); сокращение кольца рибозы (например, для образования 4-членного кольца циклобутана или оксетана); расширение кольца рибозы (например, с образованием 6- или 7-членного кольца, имеющего дополнительный углерод или гетероатом, например, для ангидрогексита, альтрита, маннита, циклогексанила, циклогексенил и морфолино (который также имеет фосфоамидатный скелет)); мультициклические формы (например, трицикло и «разблокированные» формы, такие как гликолевая нуклеиновая кислота (GNA) (например, R-GNA или S-GNA, где рибоза заменена гликолевыми звеньями, присоединенными к фосфодиэфирным связям), треозиновая нуклеиновая кислота (TNA, где рибоза заменена α-L-треофуранозил- (3'→2')) и пептидная нуклеиновая кислота (PNA, где 2-амино-этил-глициновые связи заменяют рибозу и фосфодиэфирный скелет).
[00312] В некоторых вариантах осуществления сахарная группа содержит один или более атомов углерода, которые обладают противоположной стереохимической конфигурацией соответствующего углерода в рибозе. Таким образом, полинуклеотидная молекула может включать нуклеотиды, содержащие, например, арабинозу или L-рибозу, в качестве сахара.
[00313] В некоторых вариантах осуществления полинуклеотид включает по меньшей мере один нуклеозид, в котором сахар представляет собой L-рибозу, 2'-O-метилрибозу, 2'-фторрибозу, арабинозу, гекситол, LNA или PNA.
Изменения межнуклеозидной связи
[00314] Альтернативные нуклеотиды могут быть изменены в межнуклеозидной связи (например, фосфатный скелет). В данном документе в контексте полинуклеотидного скелета фразы «фосфат» и «фосфодиэфир» используются взаимозаменяемо. Основные фосфатные группы могут быть изменены путем замены одного или более атомов кислорода другим заместителем.
[00315] Альтернативные нуклеотиды могут включать всецельную замену неизмененного фосфатного фрагмента другой межнуклеозидной связью, как описано в данном документе. Примеры альтернативных фосфатных групп включают, но не ограничиваются ими, фосфоротиоаты, фосфороселенаты, боранофосфаты, сложные эфиры боранофосфатов, гидрофосфоринаты, фосфорамидаты, фосфодиамидаты, алкил- или арилфосфататы и фосфотриэфиры. Фосфородитиоаты имеют оба несвязывающих кислорода, замененных серой. Фосфатный линкер также может быть изменен путем замены связующего кислорода азотом (мостиковые фосфорамидаты), серой (мостиковые фосфоротиоаты) и углеродом (мостиковые метилен-фосфонаты).
[00316] Альтернативные нуклеозиды и нуклеотиды могут включать замену одного или более немостиковых атомов кислорода борановым фрагментом (BH3), серой (тио), метилом, этилом и/или метокси. В качестве неограничивающего примера два не мостиковых атома кислорода в одном и том же положении (например, альфа (α), бета (β) или гамма (γ) положении) могут быть заменены серой (тио) и метокси.
[00317] Замена одного или более атомов кислорода в α-положении фосфатного фрагмента (например, α-тиофосфата) обеспечивается для придания стабильности (например, в отношении экзонуклеаз и эндонуклеаз) РНК и ДНК через не встречающиеся в природе фосфоротиоатные связи в скелете. Фосфортиоат ДНК и РНК имеют повышенную устойчивость к нуклеазам и, как следствие, более длительное время полужизни в клеточной среде.
[00318] Другие межнуклеозидные связи, которые могут применяться в соответствии с данным изобретением, включая межнуклеозидные связи, которые не содержат атом фосфора, описанные в данном документе.
Участки внутренней посадки рибосомы
[00319] Полинуклеотиды могут содержать участок внутренней посадки рибосомы (IRES). IRES может действовать как единственный сайт связывания рибосомы или может служить одним из нескольких сайтов связывания рибосомы мРНК. Полинуклеотид, содержащий более одного функционального сайта связывания рибосомы, может кодировать несколько пептидов или полипептидов, которые независимо транслируются рибосомами (например, мультицистронный мРНК). Когда полинуклеотиды снабжены IRES, дополнительно необязательно обеспечивается вторая трансляционная область. Примеры последовательностей IRES, которые можно применять по данному изобретению, включают, не ограничиваясь ими, последовательности пикорнавирусов (например, FMDV), вирусов-вредителей (CFFV), вирусов полиомиелита (PV), вирусов энцефаломиокардита (ECMV), вирусы ящура (ящур), вирусы гепатита C (HCV), вирусы классической чумы свиней (CSFV), вирус лейкоза мышей (MLV), вирусы иммунодефицита обезьян (SIV) или вирусы паралича сверчков (CrPV).
5'-кэп структура
[00320] Полинуклеотид (например, мРНК) может включать 5'-кэп структуру. 5'-кэп структура полинуклеотида участвует в экспорте ядер и повышении стабильности полинуклеотида и связывает мРНК с кэп-связывающим белком (CBP), который отвечает за стабильность полинуклеотида в клетке и способность к трансляции посредством ассоциации CBP с поли-А связывающим белком с образованием зрелых циклических видов мРНК. Кроме того, кэп способствует удалению 5'-проксимальных интронов во время сплайсинга мРНК.
[00321] Эндогенные полинуклеотидные молекулы могут быть представлены 5'-концом, кэппированным образующим 5'-ppp-5' трифосфатную связь между концевым остатком гуанозиновым кэп-остатком и 5'-концом транскрибированным смысловым нуклеотидом полинуклеотида. Этот 5'-гуанилатный кэп затем может быть метилирован с образованием остатка N7-метилгуанилата. Рибозные сахара терминальных и/или антеротерминальных транскрибируемых нуклеотидов 5'-конца полинуклеотида необязательно также могут быть 2'-O-метилированными. 5'-декэпированные посредством гидролиза и расщепления гуанилатной кэп-структуры может быть направлено на полинуклеотидную молекулу, такую как молекула мРНК, для деградации.
[00322] Изменения в полинуклеотидах могут генерировать негидролизуемую кэп-структуру, предотвращая декэпирование и, таким образом, увеличивая время полужизни полинуклеотида. Поскольку гидролиз кэп-структуры требует расщепления 5'-ppp-5'-фосфоэфирных связей, альтернативные нуклеотиды могут присутствовать во время реакции кэпирования. Например, фермент Vaccinia Capping от New England Biolabs (Ипсвич, Массачусетс) может быть использован с нуклеотидами α-тиогуанозина в соответствии с инструкциями производителя для создания фосфоротиоатной связи в 5'-ppp-5'-кэпе. Могут использоваться дополнительные альтернативные гуанозиновые нуклеотиды, такие как α-метилфосфонатные и селенофосфатные нуклеотиды.
[00323] Дополнительные изменения включают, но не ограничиваются этим, 2'-O-метилирование рибозных сахаров 5'-терминальных и/или 5'-антетерминальных нуклеотидов полинуклеотида (как упомянуто выше) в 2'-гидроксигруппе сахара. Множество различных 5'-кэп структур могут быть использованы для создания 5'-кэпа полинуклеотида, такого как молекула мРНК.
[00324] 5'-кэп структуры включают в себя структуры, описанные в международных патентных публикациях №№ WO 2008127688, WO 2008016473 и WO 2011015347, кэп-структуры каждого из которых включены в данный документ посредством ссылки.
[00325] Кэп-аналоги, которые в данном документе также называются синтетическими кэп-аналогами, химические кэп-производными, химическими кэп-аналогами или структурными или функциональными кэп-аналогами, отличаются от природных (то есть эндогенных, дикого типа или физиологических) 5'-кэпов своей химической структурой, сохраняя при этом функцию кэпа. Кэп-аналоги могут быть химически (т.е. неферментативно) или ферментативно синтезированы и/связаны с полинуклеотидом.
[00326] Например, анти-реверсивный кэп-аналог (ARCA) содержит два гуанозина, связанных 5'-5'-трифосфатной группой, где один гуанозин содержит N7-метильную группу, а также 3'-O-метильную группу (т.е. N7,3'-O-диметил-гуанозин-5'-трифосфат-5'-гуанозин, m7G-3'mppp-G, которые могут быть эквивалентно обозначены как 3' O-Me-m7G(5')ppp(5')G). Атом 3'-O другого неизмененного гуанозина становится связанным с 5'-терминальным нуклеотидом кэпированного полинуклеотида (например, мРНК). N7- и 3'-O-метилированный гуанозин обеспечивает концевой фрагмент кэпированного полинуклеотида (например, мРНК).
[00327] Другой иллюстративный пример кэпа представляет собой mCAP, который аналогичен ARCA, но имеет 2'-O-метильную группу на гуанозине (то есть N7,2'-O-диметил-гуанозин-5'-трифосфат-5'-гуанозин, m7Gm-ppp-G).
[00328] Кэп может представлять собой динуклеотидный кэп-аналог. В качестве неограничивающего примера, динуклеотидный кэп-аналог может быть модифицированным в различных фосфатных положениях боранофосфатной группой или фосфороселеноатной группой, такие как динуклеотидные кэп-аналоги, описанные в патенте США № 8519110, кэп-структуры которых включены в данный документ посредством ссылки.
[00329] Альтернативно, кэп-аналог может представлять собой N7-(4-хлорфеноксиэтил)-замещенный динуклеотидный кэп-аналог, известный в данной области техники и/или описанный в данном документе. Неограничивающие примеры N7-(4-хлорфеноксиэтил)-замещенных динуклеотидных кэп-аналогов включают N7-(4-хлорфеноксиэтил)-G (5') ppp(5')G и N7-(4-хлорфеноксиэтил)-m3'-OG(5')ppp(5')G кэп-аналог (см., например, различные кэп-аналоги крышки и способы синтеза кэп-аналогов, описанные в Kore et al. Bioorganic & Medicinal Chemistry 2013 21:4570-4574; кэп-структуры в которых включены в данный документ посредством ссылки). В других случаях кэп-аналог, используемый в полинуклеотидах по данному изобретению, представляет собой 4-хлор/бромфеноксиэтильный аналог.
[00330] В то время как кэп-аналоги допускают сопутствующее кэпирование полинуклеотида в реакции транскрипции in vitro, до 20% транскриптов остаются некэпированными. Это, а также структурные отличия кэп-аналога от эндогенных 5'-кэп структур полинуклеотидов, продуцируемых эндогенным клеточным механизмом транскрипции, могут привести к снижению трансляционной способности и снижению стабильности клеток.
[00331] Альтернативные полинуклеотиды также могут быть кэпированы после транскрипции с использованием ферментов, чтобы генерировать более аутентичные 5'-кэп структуры. В контексте данного документа фраза «более аутентичный» относится к признаку, который близко отражает или имитирует, структурно или функционально, признак эндогенного или дикого типа. Таким образом, «более аутентичный» признак лучше отражает эндогенную, естественную или физиологическую клеточную функцию и/или структуру дикого типа по сравнению с синтетическими признаками или аналогами известного уровня техники, или который превосходит соответствующие эндогенный, дикий тип, природный или физиологический признак в одном или нескольких отношениях. Неограничивающими примерами более аутентичных 5'-кэп структур, пригодных для полинуклеотидов по данному изобретению, являются те, которые, среди прочего, имеют улучшенное связывание с кэп-связывающими белками, увеличенное время полужизни, пониженную восприимчивость к 5'-эндонуклеазам и/или уменьшенное 5'-декэпирование по сравнению с синтетическими 5'-кэп структурами, известными в данной области техники (или с природной или физиологической 5'-кэп структурой дикого типа). Например, рекомбинантный фермент, ограничивающий проникновение вируса вакцины, и рекомбинантный фермент 2'-O-метилтрансферазы могут создавать каноническую 5'-5'-трифосфатную связь между 5'-терминальным нуклеотидом полинуклеотида и кэп-гуанозином нуклеотида, причем кэп-гуанозин содержит N7 -метилирование и 5'-терминальный нуклеотид полинуклеотида содержит 2'-O-метил. Такая структура называется структурой Cap1. Данный кэп приводит к более высокой трансляционной способности, клеточной стабильности и уменьшенной активации клеточных провоспалительных цитокинов по сравнению, например, с другими аналогичными структурами с 5'-кэп аналогами, известными в данной области. Другие иллюстративные примеры кэп-структур включают 7mG(5')ppp(5')N, pN2p (Cap 0), 7mG(5')ppp(5')NlmpNp (Cap 1), 7mG(5')-ppp(5')NlmpN2mp (Cap 2) и m(7)Gpм.д.(3)(6,6,2')Apm(2')Apm(2')Cpm(2)(3,2')Up (Cap 4).
[00332] Поскольку альтернативные полинуклеотиды могут быть кэпированы пост-транскрипционно, а поскольку этот процесс более эффективен, почти 100% альтернативных полинуклеотидов могут присутствовать самостоятельно. Это в отличие от ~ 80%, когда кэп-аналог связан с полинуклеотидом в ходе реакции транскрипции in vitro.
[00333] 5'-терминальные кэпы могут включать эндогенные кэпы или кэп-аналоги. 5'-Терминальный кэп может включать аналог гуанозина. Подходящие гуанозиновые аналоги включают инозин, N1-метил-гуанозин, 2'-фтор-гуанозин, 7-деазагуанозин, 8-оксо-гуанозин, 2-амино-гуанозин, LNA-гуанозин и 2-азидогуанозин.
[00334] В некоторых случаях полинуклеотид содержит модифицированный 5'-кэп. Модификация на 5'-кэп может увеличить стабильность полинуклеотида, увеличить время полужизни полинуклеотида и может повысить эффективность трансляции полинуклеотида. Модифицированный 5'-кэп может включать, но не ограничивается ими, одну или более из следующих модификаций: модификация в положении 2'- и/или 3'- кэпированного гуанозин-трифосфата (GTP), замена кольцевого атома кислорода сахара (который продуцировал карбоциклическое кольцо) метиленовым фрагментом (CH2), модификация в трифосфатном мостиковом фрагменте кэп-структуры или модификация в (G) фрагменте нуклеинового основания.
5'-НТО
[00335] 5'-НТО может быть предложен в качестве фланкирующей области к полинуклеотидам (например, мРНК). 5'-НТО может быть гомологичным или гетерологичным кодирующей области, обнаруженной в полинуклеотиде. Множественные 5'-НТО могут представлять собой включены во фланкирующую область и могут представлять собой одинаковые или разные последовательности. Любая часть фланкирующих областей, в том числе ни одна, может представлять собой оптимизированный кодон и любая может независимо содержать одно или более различных структурных или химических изменений до и/или после оптимизации кодона.
[00336] В Таблице 21 предварительной заявки США № 61/775509 и в Таблице 21 и в Таблице 22 предварительной заявки США № 61/829372, которые включены в данный документ посредством ссылки, приведен список сайтов инициирования и остановки альтернативных полинуклеотидов (например, мРНК). В Таблице 21 каждый 5'-НТО (от 5'-НТО-005 до 5'-НТО 68511) идентифицируется по своему инициирующему и останавливающему участкам относительно его транскрипта нативного или дикого типа (гомологичного) (ENST; идентификатор, используемый в ENSEMBL базе данных).
[00337] Чтобы изменить одно или более свойств полинуклеотида (например, мРНК), могут быть сконструированы 5'-НТО, которые гетерологичны кодирующей области альтернативного полинуклеотида (например, мРНК). Затем полинуклеотиды (например, мРНК) можно вводить в клетки, ткани или организмы, и такие результаты, как уровень белка, локализация и/или время полужизни, могут быть измерены самостоятельно, чтобы оценить благоприятные эффекты, которые гетерологичный 5'-НТО может оказывать на альтернативные полинуклеотиды (мРНК). Варианты 5'-НТО могут быть использованы в тех случаях, когда один или более нуклеотидов добавляются или удаляются на концах, включая A, T, C или G. 5'-НТО также могут быть оптимизированы по кодонам или изменены любым описанным способом в данном документе.
5'-НТО, 3'-НТО и энхансерные элементы трансляции (TEE)
[00338] 5'-НТО полинуклеотидов (например, мРНК) может включать по меньшей мере один элемент, усиливающий трансляцию. Термин «энхансерный элемент трансляции» относится к последовательностям, которые увеличивают количество полипептида или белка, продуцируемого из полинуклеотида. В качестве неограничивающего примера, TEE может быть расположенным между промотором транскрипции и инициирующим кодоном. Полинуклеотиды (например, мРНК) по меньшей мере с одним TEE в 5'-НТО могут включать в себя кэп в 5'-НТО. Кроме того, по меньшей мере один TEE может быть расположен в 5'-НТО полинуклеотидов (например, мРНК), подвергаясь кэп-зависимой или кэп-независимой трансляции.
[00339] В одном аспекте TEE являются консервативными элементами в НТО, которые могут стимулировать трансляционную активность полинуклеотида, такую как, но не ограничиваясь этим, кэп-зависимая или кэп-независимая трансляция. Консервация данных последовательностей была ранее продемонстрирована Panek et al. (Nucleic Acids Research, 2013, 1-10) на 14 видах, включая людей.
[00340] В одном неограничивающем примере известные TEE могут находиться в 5'-лидерной последовательности гомеодоменового белка Gtx (Chappell et al., Proc. Natl. Acad. Sci. USA 101:9590-9594, 2004, TEE в которых включены в данный документ посредством ссылки).
[00341] В другом неограничивающем примере TEE описаны в патентных публикациях США № 2009/0226470 и 2013/0177581, международных патентных публикациях № WO 2009/075886, WO 2012/009644 и WO 1999/024595 и патентах США № 6310197 и 6849405, TEE последовательности в каждой из которых включены в данный документ посредством ссылки.
[00342] В еще одном неограничивающем примере TEE может представлять собой участок внутренний посадки рибосомы (IRES), HCV-IRES или элемент IRES, такой как, но не ограничиваясь ими, как те, которые описаны в патенте США № 7468275, патентных публикациях США № 2007/0048776 и 2011/0124100 и международных патентных публикациях № WO 2007/025008 и WO 2001/055369, последовательности IRES каждого из которых включены в данный документ посредством ссылки. Элементы IRES могут включать в себя, но не ограничиваются ими, последовательности Gtx (например, Gtx9-nt, Gtx8-nt, Gtx7-nt), описанные Chappell et al. (Proc. Natl. Acad. Sci. USA 101:9590-9594, 2004) и Zhou et al. (PNAS 102:6273-6278, 2005) и в патентных публикациях США № 2007/0048776 и 2011/0124100 и международной патентной публикации № WO 2007/025008, последовательности IRES каждой из которых включены в данный документ посредством ссылки.
[00343] “Трансляционные энхансерные полинуклеотиды” представляют собой полинуклеотиды, которые включают в себя один или более из конкретного TEE, приведенного в качестве примера в данном документе и/или описанного в данной области техники (см., например, патенты США №№ 6310197, 6849405, 7456273, 7183395, патентной публикации США № 20090/226470, 2007/0048776, 2011/0124100, 2009/0093049, 2013/0177581, международной патентной публикации № WO 2009/075886, WO 2007/025008, WO 2012/009644, WO 2001/055371 WO 1999/024595 и европейских патентах № 2610341 и 2610340; последовательности TEE каждой из которых включены в данный документ посредством ссылки) или их варианты, гомологи или функциональные производные. Одна или более копий конкретного TEE могут присутствовать в полинуклеотиде (например, мРНК). TEE в трансляционных энхансерных полинуклеотидах могут быть организованы в один или более сегментов последовательности. Сегмент последовательности может содержать один или более конкретных TEE, приведенных в качестве примера в данном документе, причем каждый TEE присутствует в одной или более копиях. Когда в трансляционном энхансерном полинуклеотиде присутствует множество сегментов последовательности, они могут быть гомогенными или гетерогенными. Таким образом, множественные сегменты последовательности в полинуклеотиде энхансера трансляции могут содержать идентичные или различные типы конкретных TEE, приведенных в качестве примера в данном документе, идентичное или различное количество копий каждого из конкретных TEE и/или идентичную или различную организацию TEE в каждом сегменте последовательности.
[00344] Полинуклеотид (например, мРНК) может включать по меньшей мере один TEE, который описан в международных патентных публикациях № WO 1999/024595, WO 2012/009644, WO 2009/075886, WO 2007/025008, WO 1999/024595, публикации европейского патента № 2610341 и 2610340, патентах США № 6310197, 6849405, 7456273, 7183395 и публикациях патентах США № 2009/0226470, 2011/0124100, 2007/0048776, 2009/0093049 и 2013/0177581 и последовательности TEE, каждый из которых включен в данный документ посредством ссылки. TEE может быть расположен в 5'-НТО полинуклеотидов (например, мРНК).
[00345] Полинуклеотид (например, мРНК) может включать, по меньшей мере один TEE, который имеет по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 99% идентичности с TEE, описанными в патентных публикациях США № 2009/0226470, 2007/0048776, 2013/0177581 и 2011/0124100, публикациях международных патентов № WO 1999/024595, WO 2012/009644, WO 2009/075886 и WO 2007/025008, публикациях европейских патентов № 2610341 и 2610340, патентах США № 6310197, 6849405, 7456273, 7183395, TEE последовательностями, каждая из которых включена в данный документ посредством ссылки.
[00346] 5'-НТО полинуклеотида (например, мРНК) может содержать по меньшей мере 1, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18 по меньшей мере 19, по меньшей мере 20, по меньшей мере 21, по меньшей мере 22, по меньшей мере 23, по меньшей мере 24, по меньшей мере 25, по меньшей мере 30, по меньшей мере 35, по меньшей мере 40, по меньшей мере 45, по меньшей мере 50, по меньшей мере 55 или более, чем 60 последовательностей TEE. Последовательности TEE в 5'-НТО полинуклеотида (например, мРНК) могут представлять собой одинаковые или разные последовательности TEE. Последовательности TEE могут быть в виде шаблона, такого как ABABAB, AABBAABBAABB или ABCABCABC, или их варианты, повторенные один раз, два или более трех раз. В этих схемах каждая буква A, B или C представляет различную последовательность TEE на уровне нуклеотидов.
[00347] В некоторых случаях 5'-НТО может содержать спейсер для разделения двух последовательностей TEE. В качестве неограничивающего примера, спейсер может представлять собой спейсер из 15 нуклеотидов и/или другие спейсеры, известные в данной области техники. В качестве другого неограничивающего примера, 5'-НТО может включать модуль-разделитель последовательности TEE, повторяемый, по меньшей мере один раз, по меньшей мере дважды, по меньшей мере 3 раза, по меньшей мере 4 раза, по меньшей мере 5 раз, по меньшей мере 6 раз, по меньшей мере 7 раз, по меньшей мере 8 раз, по меньшей мере 9 раз или более 9 раз в 5'-НТО.
[00348] В других случаях спейсер, разделяющий две последовательности TEE, может включать другие последовательности, известные в данной области техники, которые могут регулировать трансляцию полинуклеотидов (например, мРНК) по данному изобретению, такие как, но не ограничиваясь ими, последовательности miR (микроРНК) (например, сайты связывания miR и затравочные miR). В качестве неограничивающего примера каждый спейсер, используемый для разделения двух последовательностей TEE, может содержать отличную последовательность miR или компонент последовательности miR (например, затравочную последовательность miR).
[00349] В некоторых случаях TEE в 5'-НТО полинуклеотида (например, мРНК) может содержать по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 99% или более, чему 99% последовательностей TEE, раскрытых в патентных публикациях США № 2009/0226470, 2007/0048776, 2013/0177581 и 2011/0124100, международных патентных публикациях № WO 1999/024595, WO 2012/009644, WO 2009/075886 и WO 2007/025008, европейских патентных публикациях № 2610341 и 2610340, и патентах США № 6310197, 6849405, 7456273 и 7183395 последовательности TEE каждого из которых включены в данный документ посредством ссылки. В другом варианте осуществления TEE в 5'-НТО полинуклеотидов (например, мРНК) по данному изобретению может включать 5-30 нуклеотидный фрагмент, 5-25 нуклеотидный фрагмент, 5-20 нуклеотидный фрагмент, 5-15 нуклеотидный фрагмент, 5-10 нуклеотидный фрагмент последовательностей TEE, раскрытых в патентных публикациях США № 2009/0226470, 2007/0048776, 2013/0177581 и 2011/0124100, международных патентных публикациях № WO 1999/024595, WO 2012/009644, WO 2009/075886 и WO 2007/025008, европейских патентных публикациях № 2610341 и 2610340, и патентах США № 6310197, 6849405, 7456273 и 7183395; последовательности TEE каждого из которых включены в данный документ посредством ссылки.
[00350] В определенных случаях TEE в 5'-НТО полинуклеотидов (например, мРНК) данного изобретения может содержать по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 99% или более чем 99% из последовательностей TEE, раскрытых в Chappell et al. (Proc. Natl. Acad. Sci. USA 101:9590-9594, 2004) и Zhou et al. (PNAS 102:6273-6278, 2005), в дополнительной таблице 1 и в дополнительной таблице 2, раскрытых в Wellensiek et al (Genome-wide profiling of human cap-independent translation-enhancing elements, Nature Methods, 2013; DOI:10.1038/NMETH.2522); последовательности TEE каждого из которых включены в данный документ посредством ссылки. В другом варианте осуществления TEE в 5'-НТО полинуклеотидов (например, мРНК) по данному изобретению может включать 5-30 нуклеотидный фрагмент, 5-25 нуклеотидный фрагмент, 5-20 нуклеотидный фрагмент, 5-15 нуклеотидный фрагмент, 5-10 нуклеотидный фрагмент последовательностей TEE, раскрытых в Chappell et al. (Proc. Natl. Acad. Sci. USA 101:9590-9594, 2004) и Zhou et al. (PNAS 102:6273-6278, 2005), в дополнительной таблице 1 и в дополнительной таблице 2, раскрытых в Wellensiek et al (Genome-wide profiling of human cap-independent translation-enhancing elements, Nature Methods, 2013; DOI:10.1038/NMETH.2522); последовательности TEE которой включены в данный документ посредством ссылки.
[00351] В некоторых случаях TEE, используемые в 5'-НТО полинуклеотида (например, мРНК), представляет собой последовательность IRES, такую как, но не ограничиваясь этим, последовательности, описанные в патенте США № 7468275 и международной патентой публикации № WO 2001/055369, последовательности TEE каждого из которых включены в данное описание посредством ссылки.
[00352] В некоторых случаях TEE, используемые в 5'-НТО полинуклеотида (например, мРНК), могут быть идентифицированы способами, описанными в патентных публикациях США № 2007/0048776 и 2011/0124100 и международных патентных публикациях № WO 2007/025008 и WO 2012/009644, способы каждого из которых включены в данный документ посредством ссылки.
[00353] В некоторых случаях TEE, используемые в 5'-НТО полинуклеотида (например, мРНК) по данному изобретению, могут представлять собой регуляторный элемент транскрипции, описанный в патентах США № 7456273 и 7183395, публикации патента США № 2009/0093049 и международной публикация № WO 2001/055371, последовательности TEE каждой из которых включены в данный документ посредством ссылки. Регуляторные элементы транскрипции могут быть идентифицированы способами, известными в данной области техники, такими как, но не ограничиваясь ими, способы, описанные в патентах США № 7456273 и 7183395, патентной публикации США № 2009/0093049 и международной публикации № WO 2001/055371, способы каждой из которых включены в данный документ посредством ссылки.
[00354] В других случаях TEE, используемые в 5'-НТО полинуклеотида (например, мРНК), представляет собой полинуклеотид или его часть, как описано в патентах США № 7456273 и 7183395, патентной публикации США № 2009/0093049 и международной публикации № WO 2001/055371, последовательности TEE каждой из которых включены в данный документ посредством ссылки.
[00355] 5'-НТО, содержащая по меньшей мере, одну TEE, описанный в данном документе, может быть включена в моноцистронную последовательность, такую как, но не ограничиваясь этим, векторную систему или полинуклеотидный вектор. В качестве неограничивающего примера, векторные системы и полинуклеотидные векторы могут включать системы, описанные в патентах США № 7456273 и 7183395, патентных публикациях США № 2007/0048776, 2009/0093049 и 2011/0124100, а также в международных патентных публикациях № WO 2007/025008 и WO 2001/055371, последовательности TEE каждой из которых включены в данный документ посредством ссылки.
[00356] Описанные в данном документе TEE могут быть расположены в 5'-НТО и/или 3'-НТО полинуклеотидов (например, мРНК). TEE, расположенные в 3'-НТО, могут быть такими же и/или отличаться от TEE, расположенных и/или описанных для включения в 5'-НТО.
[00357] В некоторых случаях 3'-НТО полинуклеотида (например, мРНК) может включать по меньшей мере 1, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18 по меньшей мере 19, по меньшей мере 20, по меньшей мере 21, по меньшей мере 22, по меньшей мере 23, по меньшей мере 24, по меньшей мере 25, по меньшей мере 30, по меньшей мере 35, по меньшей мере 40, по меньшей мере 45, по меньшей мере 50, по меньшей мере 55 или более, чем 60 последовательностей TEE. Последовательности TEE в 3'-НТО полинуклеотидов (например, мРНК) по данному изобретению могут представлять собой одинаковые или разные последовательности TEE. Последовательности TEE могут быть в виде шаблона, такого как ABABAB, AABBAABBAABB или ABCABCABC, или их варианты, повторенные один раз, два или более трех раз. В этих схемах каждая буква A, B или C представляет различную последовательность TEE на уровне нуклеотидов.
[00358] В одном случае 3'-НТО может содержать спейсер для разделения двух последовательностей TEE. В качестве неограничивающего примера, спейсер может представлять собой спейсер из 15 нуклеотидов и/или другие спейсеры, известные в данной области техники. В качестве другого неограничивающего примера, 3'-НТО может включать модуль-разделитель последовательности TEE, повторяемый, по меньшей мере один раз, по меньшей мере дважды, по меньшей мере 3 раза, по меньшей мере 4 раза, по меньшей мере 5 раз, по меньшей мере 6 раз, по меньшей мере 7 раз, по меньшей мере 8 раз, по меньшей мере 9 раз или более 9 раз в 3'-НТО.
[00359] В других случаях спейсер, разделяющий две последовательности TEE, может включать другие последовательности, известные в данной области техники, которые могут регулировать трансляцию полинуклеотидов (например, мРНК) по данному изобретению, такие как, но не ограничиваясь ими, последовательности miR (микроРНК), раскрытые в данном документе (например, сайты связывания miR и затравочные miR). В качестве неограничивающего примера каждый спейсер, используемый для разделения двух последовательностей TEE, может содержать отличную последовательность miR или компонент последовательности miR (например, затравочную последовательность miR).
[00360] В других случаях включение последовательности miR и/или последовательности TEE изменяет форму области петли на стебле, что может увеличивать и/или уменьшать трансляцию (см., например, Kedde et al. Pumilio-induced RNA structure switch in p27-3'UTR controls miR-221 and miR-22 accessibility. Nature Cell Biology. 2010).
Петли на стебле
[00361] Полинуклеотиды (например, мРНК) могут содержать петлю на стебле, такую как, но не ограничиваясь этим, гистоновая петля на стебле. Петля на стебле может представлять собой нуклеотидную последовательность длиной около 25 или около 26 нуклеотидов, такую как, но не ограничиваясь этим, описанная в международной патентной публикации № WO 2013/103659, которая включена в данное описание посредством ссылки. Гистоновая петля на стебле может быть расположена 3' относительно кодирующей области (например, на 3'-конце кодирующей области). В качестве неограничивающего примера петля на стебле может быть расположена на 3'-конце полинуклеотида, описанного в данном документе. В некоторых случаях полинуклеотид (например, мРНК) содержит более одной петли на стебле (например, две петли на стебле). Примеры последовательностей петель на стебле описаны в международных патентных публикациях № WO 2012/019780 и WO 2015/02667, последовательности петель на стебле которых включены в данный документ посредством ссылки. В некоторых случаях полинуклеотид содержит последовательность петли на стебле CAAAGGCTCTTTTCAGAGCCACCA (SEQ ID NO: 1). В других, полинуклеотид содержит последовательность петли на стебле CAAAGGCUCUUUUCAGAGCCACCA (SEQ ID NO: 2).
[00362] Петля на стебле может быть расположена на второй концевой области полинуклеотида. В качестве неограничивающего примера петля на стебле может быть расположена в нетранслируемой области (например, 3'-НТО) на второй концевой области.
[00363] В некоторых случаях полинуклеотид, такой как, но не ограничиваясь этим, мРНК, которая содержит гистоновую петлю на стебле, может быть стабилизирован путем добавления 3'-стабилизирующей области (например, 3'-стабилизирующей области, содержащей по меньшей мере один концевой нуклеозид цепи). Не желая быть связанными какой-либо теорией, добавление по меньшей мере одного концевого нуклеозида цепи может замедлить деградацию полинуклеотида и, таким образом, может увеличить время полужизни полинуклеотида.
[00364] В других случаях полинуклеотид, такой как, но не ограничиваясь этим, мРНК, которая содержит гистоновую петлю на стебле, может быть стабилизирован путем изменения 3'-области полинуклеотида, который может предотвращать и/или ингибировать добавление олиго (U) (см., например, международную патентную публикацию № WO 2013/103659).
[00365] В других случаях полинуклеотид, такой как, но не ограничиваясь этим, мРНК, которая содержит гистоновую петлю на стебле, может быть стабилизирован путем добавления олигонуклеотида, который заканчивается 3'-дезоксинуклеозидом, 2', 3'-дидезоксинуклеозидом, 3'-O-метилнуклеозидом, 3'-O-этилнуклеозидом, 3'-арабинозидом и другими альтернативными нуклеозидами, известными в данной области техники и/или описанными в данном документе.
[00366] В некоторых случаях полинуклеотиды по данному изобретению могут содержать гистоновую петлю на стебле, поли-A-область и/или структуру 5'-кэпа. Гистоновая петля на стебле может находиться до и/или после области поли-А. Полинуклеотиды, содержащие гистоновую петлю на стебле и последовательность поли-А-области, могут содержать нуклеозид с концевой цепью, описанный в данном документе.
[00367] В других случаях полинуклеотиды по данному изобретению могут содержать гистоновую петлю на стебле и структуру 5'-кэпа. Структура с 5'-кэпа может включать, но не ограничиваясь ими, описанные в данном документе и/или известные в данной области техники.
[00368] В некоторых случаях консервативная область петли на стебле может содержать последовательность miR, описанную в данном документе. В качестве неограничивающего примера область петли на стебле может содержать затравочную последовательность последовательности miR, описанную в данном документе. В другом неограничивающем примере область петли на стебле может содержать затравочную последовательность miR-122.
[00369] В некоторых случаях консервативная область петли на стебле может содержать последовательность miR, описанную в данном документе, и может также содержать последовательность TEE.
[00370] В некоторых случаях включение последовательности miR и/или последовательности TEE изменяет форму области петли на стебле, что может увеличивать и/или уменьшать трансляцию (см., например, Kedde et al. A Pumilio-induced RNA structure switch in p27-3'UTR controls miR-221 and miR-22 accessibility. Nature Cell Biology. 2010, включенную в данный документ посредством ссылки в полном объеме).
[00371] Полинуклеотиды могут содержать по меньшей мере одну гистоновую петлю на стебле и поли-А-область или сигнал полиаденилирования. Неограничивающие примеры полинуклеотидных последовательностей, кодирующих по меньшей мере одну гистоновую петлю на стебле и поли-А-область или сигнал полиаденилирования, описаны в международных патентных публикациях № WO 2013/120497, WO 2013/120629, WO 2013/120500, WO 2013/120627, WO 2013/120498, WO 2013/120626, WO 2013/120499 и WO 2013/120628, последовательности каждой из которой включены в данный документ посредством ссылки. В определенных случаях полинуклеотид, кодирующий гистоновую петлю на стебле и область поли-A или сигнал полиаденилирования, может кодировать патогенный антиген или его фрагмент, такой как полинуклеотидные последовательности, описанные в международных патентных публикациях № WO 2013/120499 и WO 2013/120628, последовательности обоих из которых включены в данный документ посредством ссылки. В других случаях полинуклеотид, кодирующий гистоновую петлю на стебле и область поли-A или сигнал полиаденилирования, может кодировать терапевтический белок, такой как полинуклеотидные последовательности, описанные в международных патентных публикациях № WO 2013/120497 и WO 2013/120629, последовательности обоих из которых включены в данный документ посредством ссылки. В некоторых случаях полинуклеотид, кодирующий гистоновую петлю на стебле и область поли-A или сигнал полиаденилирования, может кодировать опухолевый антиген или его фрагмент, такой как полинуклеотидные последовательности, описанные в международных патентных публикациях № WO 2013/120500 и WO 2013/120627, последовательности обоих из которых включены в данный документ посредством ссылки. В других случаях полинуклеотид, кодирующий гистоновую петлю на стебле и область поли-A или сигнал полиаденилирования, может кодировать аллергический антиген или аутоиммунный аутоантиген, такой как полинуклеотидные последовательности, описанные в международных патентных публикациях № WO 2013/120498 и WO 2013/120626, последовательности обоих из которых включены в данный документ посредством ссылки.
Поли-А области
[00372] Полинуклеотид или нуклеиновая кислота (например, мРНК) может содержать последовательность полиА и/или сигнал полиаденилирования. Последовательность полиА может состоять полностью или в основном из адениновых нуклеотидов или их аналогов или производных. Последовательность полиА может быть хвостом, расположенным рядом с 3“-нетранслируемой областью нуклеиновой кислоты.
[00373] Во время процессинга РНК длинная цепь аденозиновых нуклеотидов (поли-А-область) обычно добавляется к молекулам матричной РНК (мРНК) для увеличения стабильности молекулы. Сразу после транскрипции 3'-конец транскрипта отщепляется, чтобы освободить 3'-гидрокси. Затем поли-А-полимераза добавляет цепочку аденозиновых нуклеотидов к РНК. Процесс, называемый полиаденилированием, добавляет область поли-А длиной от 100 до 250 остатков.
[00374] Уникальные длины поли-А-области могут обеспечивать определенные преимущества альтернативным полинуклеотидам по данному изобретению.
[00375] Обычно длина поли-А области по данному изобретению составляет по меньшей мере 30 нуклеотидов в длину. В другом варианте осуществления область поли-А имеет длину по меньшей мере 35 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 40 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 45 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 55 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 60 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 70 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 80 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 90 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 100 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 120 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 140 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 160 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 180 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 200 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 250 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 300 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 350 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 400 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 450 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 500 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 600 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 700 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 800 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 900 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1000 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1100 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1200 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1300 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1400 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1500 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1600 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1700 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1800 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 1900 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 2000 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 2500 нуклеотидов. В другом варианте осуществления длина составляет по меньшей мере 3000 нуклеотидов.
[00376] В некоторых случаях поли-А область может иметь длину 80 нуклеотидов, 120 нуклеотидов, 160 нуклеотидов в альтернативной полинуклеотидной молекуле, описанной в данном документе.
[00377] В других случаях поли-А область может иметь длину 20, 40, 80, 100, 120, 140 или 160 нуклеотидов в альтернативной полинуклеотидной молекуле, описанной в данном документе.
[00378] В некоторых случаях поли-А область конструируют относительно длины общего альтернативного полинуклеотида. Эта конструкция может основываться на длине кодирующей области альтернативного полинуклеотида, длине конкретного признака или области альтернативного полинуклеотида (такого как мРНК) или на основе длины конечного продукта, экспрессируемого из альтернативного полинуклеотида. Когда относительно какого-либо признака альтернативного полинуклеотида (например, отличного от участка мРНК, который содержит область поли-А), область поли-А может быть на 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100% больше по длине, чем дополнительный признак. Поли-А область также может быть сконструирована как часть альтернативного полинуклеотида, к которому она при надлежит. В этом контексте поли-А область может составлять 10, 20, 30, 40, 50, 60, 70, 80 или 90% или более от общей длины конструкции или общей длины конструкции минус поли-А область.
[00379] В некоторых случаях сконструированные сайты связывания и/или конъюгация полинуклеотидов (например, мРНК) для поли-А связывающего белка могут быть использованы для усиления экспрессии. Сконструированные сайты связывания могут представлять собой сенсорные последовательности, которые могут действовать как сайты связывания для лигандов локального микроокружения полинуклеотидов (например, мРНК). В качестве неограничивающего примера, полинуклеотиды (например, мРНК) могут содержать по меньшей мере один сконструированный сайт связывания для изменения аффинности связывания поли-А связывающего белка (PABP) и его аналоги. Включение по меньшей мере одного сконструированного сайта связывания может увеличить аффинность связывания PABP и его аналогов.
[00380] Кроме того, множество различных полинуклеотидов (например, мРНК) могут быть связаны вместе с PABP (поли-А связывающим белком) через 3'-конец с использованием альтернативных нуклеотидов на 3'-конце поли-А области. Эксперименты по трансфекции могут проводиться в соответствующих линиях клеток, а продуцирование белка можно анализировать с помощью ИФА через 12 часов, 24 часа, 48 часов, 72 часа и 7 суток после трансфекции. В качестве неограничивающего примера эксперименты по трансфекции могут быть использованы для оценки влияния на аффинность связывания PABP или его аналогов в результате добавления по меньшей мере одного сконструированного сайта связывания.
[00381] В некоторых случаях поли-А область может использоваться для модуляции инициации трансляции. Не желая быть связанными какой-либо теорией, поли-A область рекрутирует PABP, который, в свою очередь, может взаимодействовать с комплексом инициации трансляции и, таким образом, может быть необходим для синтеза белка.
[00382] В некоторых случаях поли-А область также может быть использована в данном изобретении для защиты от расщепления 3'-5'-экзонуклеазой.
[00383] В некоторых случаях полинуклеотид (например, мРНК) может содержать поли-А-G квартет. G-квартет представляет собой циклически связанный водородный массив из четырех гуанозиновых нуклеотидов, которые могут образовываться с помощью G-богатых последовательностей как в ДНК, так и в РНК. В данном варианте осуществления G-квартет расположен в конец поли-A-области. Полученные полинуклеотиды (например, мРНК) могут быть проанализированы на стабильность, продукцию белка и другие параметры, включая период полужизни в различные временные точки. Было обнаружено, что поли-А-G квартет приводит к продуцированию белка, эквивалентному по меньшей мере 75% от того, что наблюдается при использовании поли-А только области, состоящей из 120 нуклеотидов.
[00384] В некоторых случаях полинуклеотид (например, мРНК) может содержать поли-А область и может быть стабилизирован путем добавления 3'-стабилизирующей области. Полинуклеотиды (например, мРНК) с поли-А областью могут дополнительно содержать структуру 5'-кэпа.
[00385] В других случаях полинуклеотид (например, мРНК) может содержать поли-A-G-квартет. Полинуклеотиды (например, мРНК) с поли-А-G квартетом могут дополнительно содержать структуру 5'-кэпа.
[00386] В некоторых случаях 3'-стабилизирующая область, которая может быть использована для стабилизации полинуклеотида (например, мРНК), содержащего поли-А-область или поли-AG-квартет, может представлять собой, без ограничения, описанній в международной патентной публикации № WO 2013/103659, поли-А-области и поли-АГ-квартеты, которые включены в данный документ посредством ссылки. В других случаях 3'-стабилизирующая область, которая может быть использована в данном изобретении, содержит нуклеозид обрыва цепи, такой как 3'- дезоксиаденозин (кордицепин), 3'-дезоксиуридин, 3'-дехоксицитозин, 3'-дезоксигуанозин, 3'-дезокситимин, 2',3'-дидезоксинуклеозиды, такие как 2',3'- дидезоксиаденозин, 2',3'- дидезоксиуридин, 2',3'- дидезоксицитозин, 2',3'- дидезоксигуанозин, 2',3'- дидезокситимин, 2'-дезоксинуклеозид или O-метилнуклеозид.
[00387] В других случаях полинуклеотид, такой как, без ограничения, мРНК, которая содержит область поли-A или квартет поли-AG, может быть стабилизирован путем изменения 3'-области полинуклеотида, которое может предотвращать и/или ингибировать добавление олиго(U) (см., например, международную патентную публикацию № WO 2013/103659).
[00388] В еще одних других случаях полинуклеотид, такой как, без ограничения, мРНК, которая содержит область поли-А или квартет поли-AG, может быть стабилизирован путем добавления олигонуклеотида, который заканчивается 3'-дезоксинуклеозидом, 2', 3'-дидезоксинуклеозидом, 3'-O-метилнуклеозидом, 3'-O-этилнуклеозидом, 3'-арабинозидом и другими альтернативными нуклеозидами, известными в данной области техники и/или описанными в данном документе.
Нуклеозиды обрыва цепи
[00389] Нуклеиновая кислота может содержать нуклеозид обрыва цепи. Например, нуклеозид обрыва цепи может включать те нуклеозиды, которые дезоксигенированы в положениях 2' и/или 3' их сахарной группы. Такие виды могут включать 3'- дезоксиаденозин (кордицепин), 3'-дезоксиуридин, 3'-дехоксицитозин, 3'-дезоксигуанозин, 3'-дезокситимин, 2',3'-дидезоксинуклеозиды, такие как 2',3'- дидезоксиаденозин, 2',3'- дидезоксиуридин, 2',3'- дидезоксицитозин, 2',3'- дидезоксигуанозин и 2',3'- дидезокситимин.
Другие компоненты
[00390] Композиция наночастиц может содержать один или более компонентов в дополнение к тем, которые описаны в предыдущих разделах. Например, композиция наночастиц может содержать одно или более низкомолекулярное гидрофобное вещество, такое как витамин (например, витамин А или витамин Е) или стерол.
[00391] Композиции наночастиц могут также включать одну или более молекул, улучшающих проницаемость, углеводы, полимеры, поверхностно-модифицирующие агенты или другие компоненты. Молекула усилителя проницаемости может представлять собой молекулу, описанную, например, в публикации заявки на патент США № 2005/0222064. Углеводы могут включать простые сахара (например, глюкозу) и полисахариды (например, гликоген и его производные и аналоги).
[00392] Полимер может быть включен в и/или использован для инкапсулирования или частичного инкапсулирования композиции наночастиц. Полимер может быть биоразлагаемым и/или биосовместимым. Полимер может быть выбран из, без ограничения, полиаминов, полиэфиров, полиамидов, сложных полиэфиров, поликарбаматов, полимочевин, поликарбонатов, полистеринов, полиамидов, полисульфонов, полиуретанов, полиацетиленов, полиэтиленов, полиэтиленеминов, полиизоцианатов, полиакрилатов, полиметакрилатов, полиакрилнитрилов и полиарилатов. Например, полимер может включать поли(капролактон) (PCL), этиленвинилацетатный полимер (EVA), поли(молочную кислоту) (PLA), поли(L-молочную кислоту) (PLLA), поли(гликолевую кислоту) (PGA), поли(молочная кислота-гликолевая кислота) (PLGA), поли(L- молочная кислота-гликолевая кислота) (PLLGA), поли(д,L-лактид) (PDLA), поли(L-лактид) (PLLA), поли(д,L- лактид-со-капролактон), поли(д,L-лактид- со-капролактон-co-гликолид), поли(д,L-лактид-со-PEO-со-D, L-лактид), поли(д,L-лактид-со-PPO-со-D, L-лактид), полиалкилцианоакрилат, полиуретан, поли-L-лизин (PLL), гидроксипропилметакрилат (HPMA), полиэтиленгликоль, поли-L-глутаминовая кислота, поли(гидрокси кислоты), полиангидриды, полиортоэфиры, поли(эфирамиды), полиамиды, поли(сложные эфиры), поликарбонаты, полиалкилены, такие как полиэтилен и полипропилен, полиалкиленгликоли, такие как поли(этиленгликоль) (PEG), полиалкиленоксиды (PEO), полиалкилентерефталаты такие как поли(этилентерефталаты), поливиниловые спирты (PVA), поливиниловые эфиры, сложные поливиниловые эфиры, такие как поли(винилацетат), поливинилгалогениды, такие как поли(винилхлорид) (PVC), поливинилпирролидон (PVP), полисилоксаны, полистирол (PS), полиуретаны, дериватизированные целлюлозы, такие как алкилцеллюлозы, гидроксиалкилцеллюлозы, эфиры целлюлозы, сложные эфиры целлюлозы, нитроцеллюлозы, гидроксипропилцеллюлоза, карбоксиметилцеллюлоза, полимеры акриловых кислот, такие как поли(метил(мет)акрилат) (PMMA), поли(этил(мет)акрилат), поли(бутил(мет)акрилат), поли(изобутил(мет)акрилат), поли(гексил(мет)акрилат), поли(изодецил(мет)акрилат), поли(лаурил(мет)акрилат), поли(фенил(мет)акрилат), поли(метилакрилат), поли(изопропилакрилат), поли(изобутилакрилат), поли(октадецилакрилат) и их сополимеры и смеси, полидиоксанон и его сополимеры, полигидроксиалканоаты, полипропиленфумарат, полиоксиметилен, полоксамеры, полиоксамины, поли(орто)эфиры, поли(масляная кислота), поли(валериановая кислота), поли(лактида-со-капролактон), триметиленкарбонат, поли(N- акрилоилморфолин) (PAcM), поли(2-метил-2-оксазолин) (PMOX), поли(2-этил-2-оксазолин) (PEOZ) и полиглицерол.
[00393] Поверхностно-модифицирующие агенты могут включать, без ограничения, анионные белки (например, бычий сывороточный альбумин), поверхностно-активные вещества (например, катионные поверхностно-активные вещества, такие как диметилдиоктадециламмонийбромид), сахара или производные сахаров (например, циклодекстрин), нуклеиновые кислоты, полимеры (например, гепарин, полиэтиленгликоль и полоксамер), муколитические агенты (например, ацетилцистеин, экстракт полыни, бромелайн, папаин, клеродендрум, бромгексин, карбоцистеин, эпразинон, месну, амброксол, собреролин, сестеропин, тиодеол, тиодол, тиомол), гельзолин, тимозин β4, дорназу альфа, нельтенексин и эрдостеин) и ДНКазы (например, рчДНКазу). Поверхностно-модифицирующий агент может быть расположен внутри наночастиц и/или на поверхности композиции наночастиц (например, путем нанесения покрытия, адсорбции, ковалентной связи или другого процесса).
[00394] Композиция наночастиц также может содержать один или более функционализированных липидов. Например, липид может быть функционализирован с помощью алкиновой группы, которая при воздействии азида в соответствующих условиях реакции может подвергаться реакции циклоприсоединения. В частности, липидный бислой может быть функционализирован таким образом с одной или более группами, полезными для облегчения проникновения через мембрану, распознавания клеток или визуализации. Поверхность композиции наночастиц также может быть конъюгирована с одним или более полезными антителами. Функциональные группы и конъюгаты, используемые для направленной доставки клеток, визуализации и проникновения через мембраны, хорошо известны в данной области техники.
[00395] В дополнение к этим компонентам композиции наночастиц могут содержать любое вещество, полезное в фармацевтических композициях. Например, композиция наночастиц может содержать один или более фармацевтически приемлемых наполнителей или вспомогательных ингредиентов, таких как, без ограничения, один или более растворителей, дисперсионные среды, разбавители, дисперсионные добавки, суспензионные добавки, гранулирующие добавки, дезинтегранты, наполнители, глиданты, жидкие носители, связующие вещества, поверхностно-активные вещества, изотонические агенты, загустители или эмульгаторы, буферные агенты, смазывающие агенты, масла, консерванты и другие виды. Эксципиенты, такие как воски, масла, красители, покрывающие агенты, ароматизаторы и отдушки, также могут быть включены в состав композиции. Фармацевтически приемлемые эксципиенты хорошо известны в данной области техники (см., например Remington's The Science and Practice of Pharmacy, 21st Edition, A. R. Gennaro; Lippincott, Williams & Wilkins, Baltimore, MD, 2006).
[00396] Примеры разбавителей могут включать, но не ограничиваются ими, карбонат кальция, карбонат натрия, фосфат кальция, дикальцийфосфат, сульфат кальция, гидрофосфат кальция, фосфат натрия, лактозу, сахарозу, целлюлозу, микрокристаллическую целлюлозу, каолин, маннит, сорбит, инозит, хлорид натрия, сухой крахмал, кукурузный крахмал, сахарную пудру и/или их комбинации. Гранулирующие и диспергирующие агенты могут быть выбраны из неограничивающего списка, состоящего из картофельного крахмала, кукурузного крахмала, крахмала тапиоки, гликолята крахмала натрия, глин, альгиновой кислоты, гуаровой камеди, цитрусовой пульпы, агара, бентонита, целлюлозы и древесных продуктов, натуральной губки, катионообменных смол, карбоната кальция, силикатов, карбоната натрия, сшитого поли(винил-пирролидона) (кросповидона), карбоксиметилкрахмала натрия (крахмалгликолята натрия), карбоксиметилцеллюлозы, сшитой карбоксиметилцеллюлозы натрия (кроскармеллозы), метилцеллюлозы, прежелатинизированного крахмала (крахмала 1500), микрокристаллического крахмала, микрокристаллического крахмала, нерастворимого в воде крахмала, карбоксиметилцеллюлозы кальция, силиката магния и алюминия (VEEGUM®), лаурилсульфата натрия, соединений четвертичного аммония и/или их комбинаций.
[00397] Поверхностно-активные вещества и/или эмульгаторы могут включать, но не ограничиваются ими, природные эмульгаторы (например, акацию, агар, альгиновую кислоту, альгинат натрия, трагакант, хондрус, холестерин, ксантан, пектин, желатин, яичный желток, казеин, шерстяной жир, холестерин, воск и лецитин), коллоидные глины (например, бентонит [силикат алюминия] и VEEGUM® [алюмосиликат магния]), производные аминокислот с длинной цепью, высокомолекулярные спирты (например, стеариловый спирт, цетиловый спирт, олеиловый спирт, моностеарат триацетина, дистеарат этиленгликоля, моностеарат глицерина и пропиленмоностеаратгликоль, поливиниловый спирт), карбомеры (например, карбоксиполиметилен, полиакриловая кислота, полимер акриловой кислоты и карбоксивинилполимер), каррагенан, производные целлюлозы (например, карбоксиметилцеллюлозу натрия, порошкообразная целлюлоза, гидроксиметилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, метилцеллюлоза), сложные эфиры сорбитана и жирных кислот (например, полиоксиэтилен-сорбитанмонолаурат [TWEEN®20] сорбитан-полиэтан) [TWEEN® 60], полиоксиэтиленсорбитанмоноолеат [TWEEN®80], сорбитанмонопальмитат [SPAN®40], сорбитанмоностеарат [SPAN®60], сорбитантристеарат[SPAN®65], глицерилмоноолеат, сорбитанмоноолеат [SPAN®80]), сложные эфиры полиоксиэтилена (например, полиоксиэтиленмоностеарат [MYRJ® 45], полиоксиэтиленгидрогенизированное касторовое масло, полиуретоксил, полиэтоксил) стеарат и SOLUTOL®), эфиры сахарозы и жирных кислот, сложные эфиры полиэтиленгликоля и жирных кислот (например, CREMOPHOR®), простые эфиры полиоксиэтилена (например, полиоксиэтиленлауриловый эфир [BRIJ® 30]), поли(винил-пирролидон), монолауратдиэтиленгликоль, триэтаноламинолеат, олеат натрия, олеат калия, этилолеат, олеиновую кислоту, этиллаурат, лаурилсульфат натрия, PLURONIC®F 68, POLOXAMER® 188, бромид цетримония, хлорид цетилпиридиния, хлорид бензалкония, докузат натрия и/или их комбинации.
[00398] Связующий агент может представлять собой крахмал (например, кукурузный крахмал и крахмальную пасту); желатин; сахара (например, сахароза, глюкоза, декстроза, декстрин, меласса, лактоза, лактит, маннит); натуральные и синтетические смолы (например, акация, альгинат натрия, экстракт ирландского мха, панварскую камедь, камедь гхатти, слизь шелухи семян подорожника, карбоксиметилцеллюлозу, метилцеллюлозу, этилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, микрокристаллическую целлюлозу, ацетат целлюлозы, поли(винилпирролидон), силикат магния и алюминия (VEEGUM®) и арабиногалактан лиственницы); альгинаты; полиэтиленоксид; полиэтиленгликоль; неорганические соли кальция; кремниевую кислоту; полиметакрилаты; воски; воды; спирт; и их комбинации, или любой другой подходящий связующий агент.
[00399] Примеры консервантов могут включать, но не ограничиваются ими, антиоксиданты, хелатирующие агенты, антимикробные консерванты, противогрибковые консерванты, спиртовые консерванты, кислотные консерванты и/или другие консерванты. Примеры антиоксидантов включают, но не ограничиваются ими, альфа-токоферол, аскорбиновую кислоту, аскорбилпальмитат, бутилированный гидроксианизол, бутилированный гидрокситолуол, монотиоглицерин, метабисульфит калия, пропионовую кислоту, пропилгаллат, аскорбат натрия, бисульфит натрия, метабисульфит натрия и/или сульфит натрия. Примеры хелатообразующих агентов включают этилендиаминтетрауксусную кислоту (ЭДТК), моногидрат лимонной кислоты, эдетат динатрия, эдетат дикалия, эдетиновую кислоту, фумаровую кислоту, яблочную кислоту, фосфористую кислоту, эдетат натрия, винную кислоту и/или эдетат тринатрия. Примеры антимикробных консервантов включают, но не ограничиваются ими, хлорид бензалкония, хлорид бензетония, бензиловый спирт, бронополь, цетримид, хлорид цетилпиридиния, хлоргексидин, хлорбутанол, хлоркрезол, хлороксиленол, крезол, этиловый спирт, глицерин, гексетидин, имидомочевина, фенол, фенилэтиловый спирт, нитрат фенилртути, пропиленгликоль и/или тимеросал. Примеры противогрибковых консервантов включают, но не ограничиваются ими, бутилпарабен, метилпарабен, этилпарабен, пропилпарабен, бензойную кислоту, гидроксибензойную кислоту, бензоат калия, сорбат калия, бензоат натрия, пропионат натрия и/или сорбиновую кислоту. Примеры спиртовых консервантов включают, но не ограничиваются ими, этанол, полиэтиленгликоль, бензиловый спирт, фенол, фенольные соединения, бисфенол, хлорбутанол, гидроксибензоат и/или фенилэтиловый спирт. Примеры кислотных консервантов включают, но не ограничиваются ими, витамин А, витамин С, витамин Е, бета-каротин, лимонную кислоту, уксусную кислоту, дегидроаскорбиновую кислоту, аскорбиновую кислоту, сорбиновую кислоту и/или фитиновую кислоту. Другие консерванты включают, но не ограничиваются ими, токоферол, токоферол ацетат, детероксим мезилат, цетримид, бутилированный гидроксианизол (BHA), бутилированный гидрокситолуол (BHT), этилендиамин, лаурилсульфат натрия (SLS), лауретсульфат натрия (SLES), бисульфит натрия, метабисульфит натрия, сульфит калия, метабисульфит калия, GLYDANT PLUS®, PHENONIP®, метилпарабен, GERMALL® 115, GERMABEN®II, NEOLONE™, KATHON™ и/или EUXYL®.
[00400] Примеры буферных агентов включают, но не ограничиваются ими, цитратные буферные растворы, ацетатные буферные растворы, фосфатные буферные растворы, хлорид аммония, карбонат кальция, хлорид кальция, цитрат кальция, глубионат кальция, глюцептат кальция, глюконат кальция, d-глюконовую кислоту, глицерофосфат кальция, лактат кальция, лактобионат кальция, пропановую кислоту, левулинат кальция, пентановую кислоту, двухосновный фосфат кальция, фосфористую кислоту, трехосновный фосфат кальция, гидроксид фосфата кальция, ацетат калия, хлорид калия, глюконат калия, смеси солей калия, двухосновный фосфат калия, одноосновный фосфат калия, смеси фосфатов калия, ацетат натрия, гидрокарбонат натрия, хлорид натрия, цитрат натрия, лактат натрия, двухосновный фосфат натрия, одноосновный фосфат натрия, смеси фосфатов натрия, трометамин, амино-сульфонатные буферы (например, HEPES), гидроксид магния, гидроксид алюминия, альгиновую кислоту, апирогенную воду, изотонический солевой раствор, раствор Рингера, этиловый спирт и/или их комбинации. Смазывающие агенты могут быть выбраны из неограничивающей группы, состоящей из стеарата магния, стеарата кальция, стеариновой кислоты, диоксида кремния, талька, солода, глицерилбегената, гидрогенизированных растительных масел, полиэтиленгликоля, бензоата натрия, ацетата натрия, хлорида натрия, лейцина, лаурилсульфата магния, лаурилсульфата натрия и их комбинаций.
[00401] Примеры масел включают, но не ограничиваются ими, миндальное масло, ядер абрикоса, авокадо, бабассу, бергамотовое, семен черной смородины, огуречника, можжевеловое, ромашки, рапсовое, тмина, карнаубу, касторовое масло, коричное, масло какао, кокос, печени трески, кофе, кукуруза, семена хлопчатника, эму, эвкалипт, примулы вечерней, рыбий жир, льняных семян, гераниол, тыквы, виноградных косточек, фундука, иссопа, изопропилмиристат, жожоба, плодов лакового дерева, лавандин, лаванды, лимона, лицея кубеба, ореха макадамия, мальвы, семен манго, семян пенника лугового, норковый жир, мускатного ореха, оливковое, апельсиновое, жир большеголова атлантического, пальмовое, пальмовоядровое, ядер персика, арахисовое, семян мака, тыквы, рапса, рисовых отрубей, розмарина, сафлора, сандалового дерева, саквана, пикантные, облепихи, кунжута, масло ши, силикон, сои, подсолнечника, чайного дерева, расторопши, камелии, ветиверии, масла грецкого ореха и пшеничных зародышей, а также бутилстеарат, каприловый триглицерид, каприновый триглицерид, циклометикон, диэтилсебацинат, диметикон 360, симетикон, изопропилмиристат, минеральное масло, октилдодеканол, олеиловый спирт, силиконовое масло и/или их комбинации.
Препараты.
[00402] Композиции наночастиц могут содержать липидный компонент и один или более дополнительных компонентов, таких как терапевтические и/или профилактические средства. Композиция наночастиц может быть предназначена для одного или более конкретных применений или целей. Элементы композиции наночастиц могут быть выбраны на основе конкретного применения или цели и/или на основе эффективности, токсичности, затрат, простоты применения, доступности или других характеристик одного или более элементов. Аналогично, конкретный препарат композиции наночастиц может быть выбран для конкретного применения или мишени в соответствии, например, с эффективностью и токсичностью конкретных комбинаций элементов.
[00403] Липидный компонент композиции наночастиц может содержать, например, липид формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) фосфолипид (такой как ненасыщенный липид, например, DOPE или DSPC), ПЭГ-липид и структурный липид. Элементы липидного компонента могут быть предложены в определенных фракциях.
[00404] В некоторых вариантах осуществления липидный компонент композиции наночастиц содержит липид формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), фосфолипид, ПЭГ-липид и структурный липид. В конкретных вариантах осуществления липидный компонент композиции наночастиц содержит от около 30 до около 60% моль соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), от около 0% моль до около 30% моль фосфолипида, от около 18,5% моль до около 48,5% моль структурного липида и от около 0% моль до около 10% моль ПЭГ-липида, при условии, что общее % моль не превышает 100%. В некоторых вариантах осуществления липидный компонент композиции наночастиц включает от около 35 до около 55% моль соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), от около 5% моль до около 25% моль фосфолипида, от около 30% моль до около 40% моль структурного липида и от около 0% моль до около 10% моль ПЭГ-липида. В конкретном варианте осуществления липидный компонент содержит около 50% моль указанного соединения, около 10% моль фосфолипида, около 38,5% моль структурного липида и около 1,5% моль ПЭГ-липида. В другом варианте осуществления липидный компонент содержит около 40% моль указанного соединения, около 20% моль фосфолипида, около 38,5% моль структурного липида и около 1,5% моль ПЭГ-липида. В некоторых вариантах осуществления фосфолипид может представлять собой DOPE или DSPC. В других вариантах осуществления ПЭГ-липид может представлять собой ПЭГ-DMG и/или структурный липид может представлять собой холестерин.
[00405] Композиции наночастиц могут быть предназначены для одной или более конкретных применений или целей. Например, композиция наночастиц может быть предназначена для доставки терапевтического и/или профилактического средства, такого как РНК, в конкретную клетку, ткань, орган или систему или группу в организме млекопитающего. Физико-химические свойства композиций наночастиц могут быть изменены, чтобы повысить селективность для определенных мишеней в теле. Например, размеры частиц могут регулироваться в зависимости от размеров различных органов. Терапевтическое и/или профилактическое средство, включенное в композицию наночастиц, также может быть выбрано на основании желаемой цели или целей доставки. Например, терапевтическое и/или профилактическое средство может быть выбрано для конкретного показания, патологического состояния, заболевания или расстройства и/или для доставки в конкретную клетку, ткань, орган или систему или их группу (например, локализованная или специфическая доставка). В конкретных вариантах осуществления композиция наночастиц может включать мРНК, кодирующую интересующий полипептид, способный транслироваться в клетке для получения интересующего полипептида. Такая композиция может быть предназначена для конкретной доставки в конкретный орган. В некоторых вариантах осуществления композиция может быть предназначена для конкретной доставки в печень млекопитающего.
[00406] Количество терапевтического и/или профилактического средства в композиции наночастиц может зависеть от размера, состава, желаемой цели и/или применения или других свойств композиции наночастиц, а также от свойств терапевтического и/или профилактического средства. Например, количество РНК, пригодной для композиции наночастиц, может зависеть от размера, последовательности и других характеристик РНК. Относительные количества терапевтических и/или профилактических и других элементов (например, липидов) в композиции наночастиц также могут варьироваться. В некоторых вариантах осуществления мас./мас. соотношение липидного компонента к терапевтическому и/или профилактическому в композиции наночастиц может составлять от около 5:1 до около 60:1, например, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1, 11:1, 12:1, 13:1, 14:1, 15:1, 16:1, 17:1, 18:1, 19:1, 20:1, 25:1, 30:1, 35:1, 40:1, 45:1, 50:1 и 60:1. Например, мас./мас. соотношение липидного компонента к терапевтическому и/или профилактическому средству может составлять от около 10:1 до около 40:1. В конкретных вариантах осуществления мас./мас. соотношение составляет около 20:1. Количество терапевтического и/или профилактического средства в композиции наночастиц можно, например, измерить с помощью абсорбционной спектроскопии (например, видимой в ультрафиолетовом диапазоне спектроскопии).
[00407] В некоторых вариантах осуществления, композиция наночастиц содержит одну или более РНК, и одна или несколько РНК, липиды и их количество могут быть выбраны для обеспечения конкретного соотношения N:P. Соотношение N:P в композиции относится к молярному отношению атомов азота в одном или более липидах к числу фосфатных групп в РНК. Как правило, более низкое отношение N:P является предпочтительным. Одна или более РНК, липидов и их количества могут быть выбраны для обеспечения соотношения N:P, равного от около 2:1 до около 30:1, например, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1, 12:1, 14:1, 16:1, 18:1, 20:1, 22:1, 24:1, 26:1, 28:1 или 30:1. В конкретных вариантах осуществления соотношение N:P может быть равно от около 2:1 до около 8:1. В других вариантах осуществления соотношение N:P равно от около 5:1 до около 8:1. Например, соотношение N:P может быть равно около 5,0: 1, около 5,5:1, около 5,67:1, около 6,0:1, около 6,5:1 или около 7,0:1. Например, соотношение N:P может быть равно около 5,67:1.
Физические свойства
[00408] Характеристики композиции наночастиц могут зависеть от их компонентов. Например, композиция наночастиц, включающая холестерин в качестве структурного липида, может иметь характеристики, отличные от композиции наночастиц, которая включает в себя другой структурный липид. Аналогично, характеристики композиции наночастиц могут зависеть от абсолютного или относительного количества его компонентов. Например, композиция наночастиц, включающая более высокую молярную долю фосфолипида, может иметь характеристики, отличные от композиции наночастиц, включающей более низкую молярную долю фосфолипида. Характеристики могут также варьироваться в зависимости от способа и условий приготовления композиции наночастиц.
[00409] Композиции наночастиц могут характеризоваться разнообразными способами. Например, микроскопия (например, просвечивающая электронная микроскопия или сканирующая электронная микроскопия) может быть использована для изучения морфологии и распределения по размерам композиции наночастиц. Динамическое рассеяние света или потенциометрия (например, потенциометрическое титрование) может использоваться для измерения дзета-потенциалов. Динамическое рассеяние света также может быть использовано для определения размеров частиц. Такие инструменты, как Zetasizer Nano ZS (Malvern Instruments Ltd, Малверн, Вустершир, Великобритания), также можно использовать для измерения множества характеристик композиции наночастиц, таких как размер частиц, коэффициент полидисперсности и дзета-потенциал.
[00410] Средний размер композиции наночастиц может быть равен от 10 с до 100 нм, например, измеренный методом динамического рассеяния света (DLS). Например, средний размер может быть равен от около 40 нм до около 150 нм, например, около 40 нм, 45 нм, 50 нм, 55 нм, 60 нм, 65 нм, 70 нм, 75 нм, 80 нм, 85 нм, 90 нм, 95 нм, 100 нм, 105 нм, 110 нм, 115 нм, 120 нм, 125 нм, 130 нм, 135 нм, 140 нм, 145 нм или 150 нм. В некоторых вариантах осуществления средний размер наночастиц в композиции может быть равен около 50 нм до около 100 нм, от около 50 нм до около 90 нм, от около 50 нм до около 80 нм, от около 50 нм до около 70 нм, от около 50 нм до около 60 нм, от около 60 нм до около 100 нм, от около 60 нм до около 90 нм, от около 60 нм до около 80 нм, от около 60 нм до около 70 нм, от около 70 нм до около 150 нм, от около 70 нм до около 130 нм, от около 70 нм до около 100 нм, от около 70 нм до около 90 нм, от около 70 нм до около 80 нм, от около 80 нм до около 150 нм, от около 80 нм до около 130 нм, от около 80 нм до около 100 нм, от около 80 нм до около 90 нм, от около 90 нм до около 150 нм, от около 90 нм до около 130 нм или от около 90 нм до около 100 нм. В конкретных вариантах осуществления средний размер композиции наночастиц может быть равен от около 70 нм до около 130 нм или равен от около 70 нм до около 100 нм. В конкретном варианте осуществления средний размер может быть равен около 80 нм. В других вариантах осуществления средний размер может быть равен около 100 нм. В других вариантах осуществления средний размер может быть равен около 120 нм.
[00411] Композиция наночастиц может быть относительно гомогенной. Может быть определен коэффициент полидисперсности, чтобы указывать на однородность композиции наночастиц, например, распределение частиц по размерам наночастиц композиций. Небольшой (например, менее 0,3) коэффициент полидисперсности обычно указывает на узкое распределение частиц по размерам. Композиция наночастиц может иметь коэффициент полидисперсности, равный от около от 0 до около 0,25, например, 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, 0,09, 0,10, 0,11, 0,12, 0,13, 0,14, 0,15, 0,16, 0,17, 0,18, 0,19, 0,20, 0,21, 0,22, 0,23, 0,24 или 0,25. В некоторых вариантах осуществления, коэффициент полидисперсности композиции наночастиц может быть равен от около 0,10 до около 0,20.
[00412] Дзета-потенциал композиции наночастиц может быть использован для обозначения электрокинетического потенциала композиции. Например, дзета-потенциал может описывать поверхностный заряд композиции наночастиц. Как правило, желательны композиции наночастиц с относительно низкими зарядами, положительными или отрицательными, так как более заряженные частицы могут нежелательно взаимодействовать с клетками, тканями и другими элементами в организме. В некоторых вариантах осуществления дзета-потенциал композиции наночастиц может быть равен от около -10 мВ до около +20 мВ, от около -10 мВ до около +15 мВ, от около -10 мВ до около +10 мВ, от около -10 мВ до около +5 мВ, от около -10 мВ до около 0 мВ, от около -10 мВ до около -5 мВ, от около -5 мВ до около +20 мВ, от около -5 мВ до около +15 мВ, от около -5 мВ до около +10 мВ, от около -5 мВ до около +5 мВ, от около -5 мВ до около 0 мВ, от около 0 мВ до около +20 мВ, от около 0 мВ до около +15 мВ, от около 0 мВ до около +10 мВ, от около 0 мВ до около +5 мВ, от около +5 мВ до около +20 мВ, от около +5 мВ до около +15 мВ или от около +5 мВ до около +10 мВ.
[00413] Эффективность инкапсулирования терапевтического и/или профилактического средства описывает количество терапевтического и/или профилактического средства, которое инкапсулируется или иным образом связывается с композицией наночастиц после приготовления, по отношению к первоначальному количеству. Желательно, чтобы эффективность инкапсуляции была высокой (например, близка к 100%). Эффективность инкапсуляции может быть измерена, например, путем сравнения количества терапевтического и/или профилактического средства в растворе, содержащем композицию наночастиц, до и после разрушения композиции наночастиц одним или более органическими растворителями или детергентами. Флуоресценция может использоваться для измерения количества свободного терапевтического и/или профилактического средства (например, РНК) в растворе. Для композиций наночастиц, описанных в данном документе, эффективность инкапсуляции терапевтического и/или профилактического средства может быть равна по меньшей мере 50%, например 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%. В некоторых вариантах осуществления эффективность инкапсуляции может быть равна по меньшей мере 80%. В конкретных вариантах осуществления эффективность инкапсуляции может быть равна по меньшей мере 90%.
[00414] Композиция наночастиц может необязательно содержать одно или более покрытий. Например, композиция наночастиц может быть представлена в виде капсулы, пленки или таблетки с покрытием. Капсула, пленка или таблетка, включающая композицию, описанную в данном документе, может иметь любой подходящий размер, предел прочности, твердость или плотность.
Фармацевтические композиции
[00415] Композиции наночастиц могут быть полностью или частично составлены в виде фармацевтических композиций. Фармацевтические композиции могут включать одну или более композиций наночастиц. Например, фармацевтическая композиция может включать одну или более композиций наночастиц, включая одно или более различных терапевтических и/или профилактических средств. Фармацевтические композиции могут дополнительно включать один или несколько фармацевтически приемлемых эксципиентов или вспомогательных компонентов, таких как описанные в данном документе. Общие рекомендации по составлению и производству фармацевтических композиций и агентов доступны, например, в Remington The Science and Practice of Pharmacy, 21-е издание, A. R. Gennaro; Lippincott, Williams & Wilkins, Балтимор, Мэриленд, 2006. Традиционно принятые эксципиенты и вспомогательные компоненты могут быть использованы в любой фармацевтической композиции, за исключением того, что любой принятый эксципиент или вспомогательный компонент может считаться несовместимым с одним или более компонентами композиции наночастиц. Эксципиент или вспомогательный компонент может быть несовместим с компонентом композиции наночастиц, если его сочетание с компонентом может привести к нежелательному биологическому эффекту или иным вредным эффектам.
[00416] В некоторых вариантах осуществления один или более эксципиентов или вспомогательных компонентов могут составлять более 50% от общей массы или объема фармацевтической композиции, включая композицию наночастиц Например, один или более эксципиентов или вспомогательных компонентов могут составлять 50%, 60%, 70%, 80%, 90% или более от фармацевтической композиции. В некоторых вариантах осуществления фармацевтически приемлемый эксципиент имеет чистоту по меньшей мере, 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В некоторых вариантах осуществления эксципиент одобрен для применения у людей и для применения в ветеринарии. В некоторых вариантах осуществления эксципиент одобрен Управлением по контролю за продуктами и лекарствами США. В некоторых вариантах осуществления эксципиент имеет фармацевтическую чистоту. В некоторых вариантах осуществления эксципиент соответствует стандартам Фармакопеи США (USP), Европейской Фармакопеи (EP), Британской Фармакопеи и/или Международной Фармакопеи.
[00417] Относительные количества одной или более композиций наночастиц, одного или более фармацевтически приемлемых эксципиентов и/или любых дополнительных компонентов в фармацевтической композиции по данному изобретению будут варьироваться в зависимости от индивидуальности, размера и/или состояния субъекта, которого лечат, и далее в зависимости от пути, которым композиция должна быть введена. Например, фармацевтическая композиция может содержать от 0,1 до 100% (мас./мас.) одной или более композиций наночастиц.
[00418] В конкретных вариантах осуществления композиции наночастиц и/или фармацевтические композиции по данному изобретению хранят в холодильнике или замораживают для хранения и/или отправки (например, при хранении при температуре 4°C или ниже, такой как температура между около -150°C и около 0°C или между около -80°C и около -20°C (например, около -5°C, -10°C, -15°C, -20°C, -25°C, -30°C, -40°C, -50°C, -60°C, -70°C, -80°C, -90°C, -130°C или -150°C). Например, фармацевтическая композиция, содержащая соединение любой из формул (I), (IA), (IB), (II) и (IIa) - (IIg), представляет собой раствор, который охлаждают для хранения и/или отправки при, например, около -20°C, -30°C, -40°C, -50°C, -60°C, -70°C или -80°C. В конкретных вариантах осуществления описание также относится к способу повышения стабильности композиций наночастиц и/или фармацевтических композиций, включающих соединение любой из формул (I), (IA), (IB), (II) и (IIa)-(IIg) путем хранения композиций наночастиц и/или фармацевтических композиций при температуре 4 °С или ниже, такой как температура между около -150°C и около 0°C или между около -80°C и около -20°C, например, около -5°C, -10°C, -15°C, -20°C, -25°C, -30°C, -40°C, -50°C, -60°C, -70°C, -80°C, -90°C, -130°C или -150°C). Например, композиции наночастиц и/или фармацевтические композиции, описанные в данном документе, являются стабильными в течение, по меньшей мере 1 недели, по меньшей мере 2 недель, по меньшей мере 3 недель, по меньшей мере 4 недель, по меньшей мере 5 недель, по меньшей мере 6 недель, по меньшей мере 1 месяца, по меньшей мере 2 месяцев, по меньшей мере 4 месяцев, по меньшей мере 6 месяцев, по меньшей мере 8 месяцев, по меньшей мере 10 месяцев, по меньшей мере 12 месяцев, по меньшей мере 14 месяцев, по меньшей мере 16 месяцев, по меньшей мере 18 месяцев, по меньшей мере 20 месяцев, по меньшей мере 22 месяцев или по меньшей мере 24 месяцев, например, при температуре 4°C или ниже (например, между около 4°C и -20°C). В одном варианте осуществления стабилизирован в течение по меньшей мере 4 недель при около 4°C. В конкретных вариантах осуществления фармацевтическая композиция по данному изобретению содержит композицию наночастиц, описанную в данном документе, и фармацевтически приемлемый носитель, выбранный из одного или более из Трис, ацетата (например, ацетата натрия), цитрата (например, цитрата натрия), солевого раствора, PBS и сахарозы. В конкретных вариантах осуществления фармацевтическая композиция по данному изобретению имеет значение рН между около 7 и 8 (например, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7 6, 7,7, 7,8, 7,9 или 8,0, или между 7,5 и 8 или между 7 и 7,8). Например, фармацевтическая композиция по данному изобретению содержит описанную в данном документе композицию наночастиц, Трис, физиологический раствор и сахарозу и имеет рН около 7,5-8, который подходит для хранения и/или отправки при, например, около -20°С. Например, фармацевтическая композиция по данному изобретению содержит композицию наночастиц, описанную в данном документе, и PBS и имеет рН около 7-7,8, подходящую для хранения и/или отправки при, например, около 4°С или ниже. «Стабильность», «стабилизированный» и «стабильный» в контексте данного изобретения относится к устойчивости описанных в данном изобретении композиций наночастиц и/или фармацевтических композиций к химическим или физическим изменениям (например, деградации, изменению размера частиц, агрегации, изменению в инкапсулировании и т. д.) в данных условиях производства, подготовки, транспортировки, хранения и/или применения, например, когда применяется напряжение, такое как сдвиговое усилие, напряжение замораживания/оттаивания и т. д.
[00419] Композиции наночастиц и/или фармацевтические композиции, содержащие одну или более композиций наночастиц, могут быть назначены самому пациенту или субъекту, включая тех пациентов или субъектов, которые могут независимо от терапевтического эффекта, которому обеспечивают доставку терапевтического и/или профилактического средства в одну или более конкретных клеток, тканей, органов или систем или их групп, таких как почечная система. Хотя приведенные в данном изобретении композиции наночастиц и фармацевтические композиции, включая композиции наночастиц, в основном направлены на композиции, которые подходят для введения людям, специалисту в данной области техники будет понятно, что такие композиции обычно подходят для введения любому другому млекопитающему. Модификация композиций, подходящих для введения людям для того, чтобы сделать композиции, подходящие для введения различным животным, хорошо понятна, и средний ветеринарный фармаколог может разработать и/или выполнить такую модификацию просто с помощью обычных, если таковые имеются, экспериментов. Субъекты, для которых предусмотрено введение композиций, включают, но не ограничиваются ими, людей, других приматов и других млекопитающих, включая коммерчески значимых млекопитающих, таких как крупный рогатый скот, свиньи, лошади, овцы, кошки, собаки, мыши и/или крысы.
[00420] Фармацевтическая композиция, включающая одну или более композиций наночастиц, может быть приготовлена любым способом, известным или разработанным в дальнейшем в области фармакологии. Как правило, такие подготовительные способы включают приведение активного компонента в связь с эксципиентом и/или одним или более другими вспомогательными компонентами, а затем, если желательно или необходимо, разделение, формирование и/или упаковку продукта в желаемый одно- или многократную единичную дозу.
[00421] Фармацевтическая композиция по данному изобретению может быть приготовлена, упакована и/или продана оптом, в виде единичной дозы и/или в виде множества единичных доз. В контексте данного документа «единичная доза» представляет собой дискретное количество фармацевтической композиции, содержащей заранее определенное количество активного компонента (например, композиции наночастиц). Количество активного компонента, как правило, равно дозировке активного компонента, которую вводят субъекту, и/или удобной фракции такой дозировки, такой как, например, половина или одна треть такой дозировки.
[00422] Фармацевтические композиции могут быть приготовлены в различных формах, подходящих для различных путей и способов введения. Например, фармацевтические композиции могут быть приготовлены в жидких лекарственных формах (например, эмульсии, микроэмульсии, наноэмульсии, растворы, суспензии, сиропы и эликсиры), инъекционных формах, твердых лекарственных формах (например, капсулы, таблетки, пилюли, порошки и гранулы), лекарственных формах для местного и/или трансдермального введения (например, мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, ингалянты и пластыри), суспензиях, порошках и других формах.
[00423] Жидкие лекарственные формы для перорального и парентерального введения включают, но не ограничиваются ими, фармацевтически приемлемые эмульсии, микроэмульсии, наноэмульсии, растворы, суспензии, сиропы и/или эликсиры. Кроме того, активные компоненты, жидкие лекарственные формы могут содержать инертные разбавители, обычно применяемые в данной области техники, например, такие как вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное, масло зародышей пшеницы, оливковое, касторовое и кунжутное масло), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот и сорбита, а также их смеси. Помимо инертных разбавителей композиции для перорального применения могут включать дополнительные терапевтические и/или профилактические средства, дополнительные агенты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подслащивающие, ароматизирующие агенты и/или отдушки. В конкретных вариантах осуществления для парентерального введения композиции смешивают с солюбилизирующими агентами, такими как Cremophor®, спирты, масла, модифицированные масла, гликоли, полисорбаты, циклодекстрины, полимеры и/или их комбинации.
[00424] Инъецируемые препараты, например стерильные инъецируемые водные или масляные суспензии, могут быть составлены в соответствии с известным уровнем техники с использованием подходящих диспергирующих агентов, смачивающих агентов и/или суспендирующих агентов. Стерильные инъекционные препараты могут представлять собой стерильные инъекционные растворы, суспензии и/или эмульсии в нетоксичных парентерально приемлемых разбавителях и/или растворителях, например, в виде раствора в 1,3-бутандиоле. Приемлемыми несущими средами и растворителями, которые могут быть использованы, являются вода, раствор Рингера, U.S.P. и изотонический раствор натрия хлорида. Стерильные, нелетучие масла традиционно используются в качестве растворителя или суспендирующей среды. Для данной цели можно использовать любое нелетучее масло со слабовыраженным вкусом, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота, могут быть использованы при приготовлении инъекционных препаратов.
[00425] Инъецируемые препараты могут быть стерилизованы, например, фильтрацией через удерживающий бактерии фильтр и/или путем включения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной инъецируемой среде перед использованием.
[00426] Чтобы продлить действие активного компонента, часто желательно замедлить абсорбцию активного компонента при подкожной или внутримышечной инъекции. Это может представлять собой применение жидкой суспензии кристаллического или аморфного материала с плохой растворимостью в воде. Скорость абсорбции лекарственного средства зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристаллов и кристаллической формы. В альтернативном варианте замедление абсорбции введенной парентерально лекарственной формы может быть достигнуто посредством растворения или суспендирования лекарства в масляной несущей среде. Инъекционные формы депо получают путем формирования микроинкапсулированных матриц лекарственного средства в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от соотношения лекарственного средства и полимера, а также от природы конкретного применяемого полимера, скорость высвобождения лекарственного средства можно регулировать. Примеры других биоразлагаемых полимеров включают сложные поли(ортоэфиры) и поли(ангидриды). Инъекционные препараты депо получают, захватывая лекарственное средство в липосомы или микроэмульсии, которые совместимы с тканями организма.
[00427] Композиции для ректального или вагинального введения обычно представляют собой суппозитории, которые могут быть приготовлены путем смешивания композиций с подходящими нераздражающими наполнителями, такими как масло какао, полиэтиленгликоль или воск для суппозиториев, которые являются твердыми при температуре окружающей среды, но жидкими при температуре тела и поэтому тают в прямой кишке или влагалищной полости и высвобождают активный компонент.
[00428] Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, пленки, порошки и гранулы. В таких твердых лекарственных формах активный компонент смешивают по меньшей мере с одним инертным фармацевтически приемлемым эксципиентом, таким как цитрат натрия или дикальцийфосфат и/или наполнителями или разбавителями (например, крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота), связующими веществами (например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и акация), увлажнители (например, глицерин), разрыхлители (например, агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, некоторые силикаты и карбонат натрия), замедлители растворения (например, парафин), ускорители поглощения (например, соединения четвертичного аммония), смачивающие вещества (например, цетиловый спирт и моностеарат глицерина), абсорбенты (например, каолиновая и бентонитовая глина, силикаты) и смазочные материалы (например, тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия) и их смеси. В случае капсул, таблеток и пилюль лекарственные формы могут дополнительно содержать буферные агенты.
[00429] Твердые композиции схожего типа могут быть использованы в качестве наполнителей в мягких и твердых желатиновых капсулах с использованием таких вспомогательных веществ как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т.п. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с покрытиями и оболочками, такими как энтеросолюбильные покрытия и другие покрытия, хорошо известные в области фармацевтики. Они могут дополнительно могут необязательно содержать замутнители и могут представлять собой композиции, которые высвобождают активный(-ые) ингредиент(-ы) только или предпочтительно в определенной части кишечника, необязательно замедленным образом. Примеры инкапсулирующих композиций, которые могут быть использованы, включают полимерные вещества и воски. Твердые композиции схожего типа могут быть использованы в качестве наполнителей в мягких и твердых желатиновых капсулах с использованием таких вспомогательных веществ как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т.п.
[00430] Лекарственные формы для местного и/или трансдермального введения композиции могут включать мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, ингалянты и/или пластыри. Как правило, активный компонент смешивают в стерильных условиях с фармацевтически приемлемым экспициентом и/или любыми необходимыми консервантами и/или буферами, которые могут быть необходимыми. Кроме того, в данном изобретении предусмотрено применение трансдермальных пластырей, которые часто имеют дополнительное преимущество, заключающееся в обеспечении контролируемой доставки соединения в организм. Такие лекарственные формы могут быть приготовлены, например, путем растворения и/или распределения соединения в подходящей среде. Альтернативно или дополнительно, скорость может контролироваться либо путем обеспечения регулирующей скорость мембраны и/или путем диспергирования соединения в полимерной матрице и/или геле.
[00431] Подходящие устройства для применения при доставке внутрикожных фармацевтических композиций, описанных в данном документе, включают устройства с короткой иглой, такие как устройства, описанные в патентах США 4886499; 5190521; 5328483; 5527288; 4270537; 5015235; 5141496; и 5417662. Композиции для внутрикожного введения могут быть введены с помощью устройств, которые ограничивают эффективную длину проникновения иглы в кожу, таких как описанные в публикации РСТ WO 99/34850 и их функциональные эквиваленты. Подходящими являются безыгольные инъекционные устройства, которые доставляют жидкие композиции в дерму через эжектор жидкости и/или через иглу, которая прокалывает роговой слой и создает струю, которая достигает дермы. Устройства струйного впрыска описаны, например, в патентах США 5480,381; 5599302; 5334144; 5993412; 5649912; 5569189; 5704911; 5383851; 5893397; 5,466,220; 5339163; 5312335; 5503627; 5064413; 5520639; 4596556; 4790824; 4941880; 4940460; и публикациях PCT WO 97/37705 и WO 97/13537. Пригодны баллистические устройства для доставки порошка/частиц, которые используют сжатый газ для ускорения введения вакцины в форме порошка через внешние слои кожи в дерму. Альтернативно или дополнительно, обычные шприцы могут использоваться в классическом методе Манту внутрикожного введения.
[00432] Препараты, подходящие для местного применения, включают, но не ограничиваются ими, жидкие и/или полужидкие препараты, такие как линименты, лосьоны, масло в воде и/или эмульсии вода в масле, такие как кремы, мази и/или пасты и/или растворы, и/или суспензии. Композиции для местного введения могут, например, содержать от около 1% до около 10% (мас./мас.) активного компонента, хотя концентрация действующего вещества может проявлять себя так же высоко, как предел растворимости активного компонента в растворителе. Препараты для местного применения могут дополнительно содержать один или более дополнительных компонентов, описанных в данном документе.
[00433] Фармацевтическая композиция может быть приготовлена, упакована и/или продана в препарате, пригодном для легочного введения через ротовую полость. Такой препарат может содержать сухие частицы, которые содержат активный компонент. Такие композиции традиционно находятся в форме сухих порошков для введения с использованием устройства, содержащего резервуар для сухого порошка, в который может быть направлен поток пропеллента для диспергирования порошка, и/или с использованием дозатора с самодвижущимся растворителем/порошка, такого как устройство, содержащее активный компонент, растворенный и/или суспендированный в низкокипящем пропелленте в герметичном контейнере. Сухие порошковые композиции могут содержать твердый мелкодисперсный порошковый разбавитель, такой как сахар, и обычно предоставляются в форме единичной дозы.
[00434] Низкокипящие пропелленты обычно включают жидкие пропелленты, имеющие температуру кипения ниже 65°F при атмосферном давлении. Обычно пропеллент может составлять от 50 до 99,9% (мас./мас.) композиции, а активный компонент может составлять от 0,1 до 20% (мас./мас.) композиции. Пропеллент может дополнительно содержать дополнительные компоненты, такие как жидкое неионное и/или твердое анионное поверхностно-активное вещество, и/или твердый разбавитель (который может иметь размер частиц того же порядка, что и частицы, содержащие активный компонент).
[00435] Фармацевтические композиции, составленные для легочной доставки, могут обеспечивать активный компонент в форме капель раствора и/или суспензии. Такие препараты могут быть приготовлены, упакованы и/или проданы в виде водных и/или разбавленных спиртовых растворов и/или суспензий, необязательно стерильных, содержащих активный компонент, и их можно удобно вводить с использованием любого вида распыления и/или устройства для распыления. Такие препараты могут дополнительно содержать один или более дополнительных компонентов, включая, но не ограничиваясь ими, ароматизатор, такой как сахарин-натрий, летучее масло, буферный агент, поверхностно-активный агент и/или консервант, такой как метилгидроксибензоат. Капли, предоставляемые данным путем введения, могут иметь средний диаметр в диапазоне от около 1 нм до около 200 нм.
[00436] Препараты, описанные в данном документе как подходящие для легочной доставки, подходят и для интраназальной доставки фармацевтической композиции. Другой препарат, подходящий для интраназального введения, представляет собой крупнодисперсный порошок, содержащий активный компонент и имеющий средний размер частицуот около 0,2 до 500 мкм. Такой препарат вводят нюхательным способом, то есть путем быстрого вдыхания через носовой проход из контейнера с порошком, который держат близко к носу.
[00437] Препараты, пригодные для назального введения, могут, например, содержать от около 0,1% (мас./мас.) и до 100% (мас./мас.) активного компонента и могут содержать один или более дополнительных компонентов, описанных в данном документе. Фармацевтическая композиция может быть приготовлена, упакована и/или продана в препарате, пригодном для буккального введения. Такие препараты могут, например, находиться в форме таблеток и/или пастилок, изготовленных с использованием традиционно принятых способов, и могут, например, содержать от 0,1 до 20% (мас./мас.) активного компонента, причем остаток содержит растворимую в полости рта и/или разлагающуюся композицию и, необязательно, один или более дополнительных компонентов, описанных в данном документе. Альтернативно, препараты, подходящие для буккального введения, могут содержать порошок и/или аэрозольный, и/или распыленный раствор, и/или суспензию, содержащую активный компонент. Такие порошкообразные, аэрозольные и/или аэрозольные препараты при диспергировании могут иметь средний размер частиц и/или капель в диапазоне от около 0,1 нм до около 200 нм, и могут дополнительно содержать один или более любых дополнительных компонентов, описанных в данном документе.
[00438] Фармацевтическая композиция может быть приготовлена, упакована и/или продана в препарате, пригодном для офтальмологического введения. Такие препараты могут, например, находиться в форме глазных капель, включая, например, 0,1/1,0% (мас./мас.) раствор и/или суспензию активного компонента в водном или масляном жидком эксципиенте. Такие капли могут дополнительно содержать буферные агенты, соли и/или один или более других любых дополнительных компонентов, описанных в данном документе. Другие офтальмологически вводимые препараты, которые являются пригодными, включают те, которые содержат активный компоненты в микрокристаллической форме и/или в липосомном препарате. Предполагается, что ушные капли и/или глазные капли входят в объем данного изобретения.
мРНК терапии
[00439] мРНК как лекарственное средство обладает способностью доставлять трансмембранные и внутриклеточные белки, т.е. мишени, к которым стандартные биопрепараты не могут получить доступ из-за своей неспособности пересечь клеточную мембрану. (См. Sahin, U., Karikó K., Türeci Ö. Nat. Rev. Drug. Discov. 2014, 13, 759-780, полное содержание которых включено в данный документ посредством ссылки). Одной из основных проблем, связанных с реализацией основанной на мРНК терапии, является определение оптимального средства доставки. Из-за своего большого размера, химической нестабильности и потенциальной иммуногенности мРНК требует средства доставки, которое может обеспечивать защиту от эндо- и экзонуклеаз, а также защищать груз от иммунных стражей. Липидные наночастицы (LNP) были определены в качестве ведущего варианта в этом отношении. (См. Hajj, K.A., Whitehead, K.A. Nat. Rev. Mater. 2017, 2, 1-17, полное содержание которых включено в данный документ посредством ссылки). Этот подход был недавно подтвержден путем демонстрации безопасной и эффективной доставки вакцины на основе мРНК, составленной в препарат с LNP. (См. Bahl, K. et al. Mol. Ther. 2017, 25, 1316-1327, полное содержание которых включено в данный документ посредством ссылки).
[00440] Ключевыми критериями эффективности системы доставки липидных наночастиц являются максимальное поглощение клетками и обеспечение эффективного высвобождения мРНК из эндосомы. В то же время LNP должен обеспечивать стабильный лекарственный продукт и быть в состоянии безопасно дозироваться на терапевтически значимых уровнях. LNP представляют собой многокомпонентные системы, которые обычно состоят из аминолипида, фосфолипида, холестерина и ПЭГ-липида. Каждый компонент необходим для аспектов эффективной доставки груза нуклеиновой кислоты и стабильности частицы. Ключевым компонентом, который, как считается, стимулирует клеточное поглощение, эндосомальное высвобождение и переносимость, является аминолипид. Холестерин и ПЭГ-липид способствуют стабильности лекарственного продукта как in vivo, так и на полке, в то время как фосфолипид обеспечивает дополнительную фузогенность LNP, тем самым способствуя удалению эндосом и обеспечивая биодоступность нуклеиновой кислоты в цитозоле клеток.
[00441] За последние пару десятилетий было разработано несколько серий липидов для доставки олигонуклеотидов. (См. Stanton M.G., Murphy-Benenato, K.E. RNA Therapeutics. Topics in Medicinal Chemistry, 2017, том 27, A. Garner eds., (Springer, Cham) стр. 237-253, содержание которого включено в данный документ в полном объеме посредством ссылки). В литературе подчеркиваются прямые связи между структурой аминолипида и результирующей эффективностью доставки и переносимостью LNP. Аминолипид MC3 (DLin-MC3-DMA) является наиболее клинически развитой системой доставки олигонуклеотидов, поскольку миРНК, составленной в препарате с LNP на основе MC3, которая перешла в фазу III для лечения транстиретин-опосредованного амилоидоза. (См. Coelho, T. et al. N. Engl. J. Med. 2013, 369, 819-829.; Butler, J.S. et al. Amyloid 2016, 23, 109-118, полное содержание которого включено в данный документ посредством ссылки). Совсем недавно в литературных отчетах была продемонстрирована эффективность LNP на основе MC3 для доставки мРНК. (См. Nanbhan, J.F. et al. Sci. Rep. 2016, 6, 20019, полное содержание которого включено в данный документ посредством ссылки.) LNP этого класса быстро опсонизируются аполипопротеином E (ApoE) при внутривенной доставке, что обеспечивает клеточное поглощение рецептором липопротеинов низкой плотности (LDLr). (См. Akinc, A. et al. Mol. Ther. 2010, 18, 1357-1364, полное содержание которого включено в данный документ посредством ссылки.) Тем не менее, по-прежнему существуют опасения, что длительное время полужизни MC3 в ткани может способствовать неблагоприятным побочным эффектам, препятствующим его применению при хронической терапии. (См. Maier M.A. et al. Mol. Ther. 2013, 21, 1570-1578, полное содержание которого включено в данный документ посредством ссылки). Кроме того, многочисленные литературные данные свидетельствуют о том, что хроническое дозирование липидных наночастиц может вызывать несколько токсических побочных эффектов, включая обусловленную активацией комплемента, псевдоаллергию (CARPA) и повреждение печени (см. Szebeni J. Mol. Immunol. 2014, 61, 163-173, полное содержание которого включено в данный документ посредством ссылки). Следовательно, чтобы раскрыть потенциал терапии мРНК для людей, необходим класс LNP с повышенной эффективностью доставки наряду с метаболическим и токсическим профилем, который позволял бы хроническое дозирование у людей.
[00442] Способность лечить широкий спектр заболеваний требует гибкости, позволяющей безопасно хронически дозировать при различных уровнях дозы. Посредством систематической оптимизации липидной структуры аминолипида соединения по изобретению были идентифицированы как соединения, которые уравновешивают химическую стабильность, улучшенную эффективность доставки благодаря улучшенному эндосомальному высвобождению, быстрому метаболизму in vivo и чистому профилю токсичности (Пример 26). Комбинация этих функций обеспечивает лекарственное средство-кандидат, которое можно дозировать хронически без активации иммунной системы. Первые скрины грызунов привели к идентификации лидирующего липида с хорошей эффективностью доставки и фармакокинетикой. Далее профиль лидирующего LNP у примата, не являющегося человеком, был исследован для изучения эффективности доставки после однократного и повторного дозирования. Наконец, оптимизированные LNP были оценены в одномесячных исследованиях токсичности повторных доз на крысах и приматах, не являющихся человеком. Не желая быть связанными какой-либо теорией, новые ионизируемые липиды, описанные в данном изобретении, позволяют безопасно и эффективно использовать терапию на основе мРНК при острых и хронических заболеваниях.
Способы получения полипептидов в клетках
[00443] В данном раскрытии предложены способы получения интересующего полипептида в клетке млекопитающего. Способы получения полипептидов включают приведение клетки в контакт с композицией наночастиц, содержащей мРНК, кодирующую интересующий полипептид. При контакте клетки с композицией наночастиц мРНК может быть захвачена и перенесена в клетку для получения интересующего полипептида.
[00444] Как правило, стадия контакта клетки млекопитающего с композицией наночастиц, содержащей мРНК, кодирующую интересующий полипептид, может быть проведена in vivo, ex vivo, в культуре или in vitro. Количество композиции наночастиц, контактирующей с клеткой, и/или количество мРНК в ней, может зависеть от типа клетки или ткани, с которой контактируют, способа введения, физико-химических характеристик композиции наночастиц и мРНК в ней (например, размера, заряда и химического состава) и других факторов. В общем, эффективное количество композиции наночастиц позволит эффективно продуцировать полипептид в клетке. Метрики для эффективности могут включать трансляцию полипептида (указанную экспрессией полипептида), уровень деградации мРНК и показатели иммунного ответа.
[00445] Стадия приведения в контакт композиции наночастиц, содержащей мРНК, с клеткой может включать или вызывать трансфекцию. Фосфолипид, включенный в липидный компонент композиции наночастиц, может облегчать трансфекцию и/или повышать эффективность трансфекции, например, путем взаимодействия и/или слияния с клеточной или внутриклеточной мембраной. Трансфекция может обеспечить трансляцию мРНК внутри клетки.
[00446] В некоторых вариантах осуществления композиции наночастиц, описанные в данном документе, могут использоваться терапевтически. Например, мРНК, включенная в композицию наночастиц, может кодировать терапевтический полипептид (например, в транслируемой области) и продуцировать терапевтический полипептид при контакте и/или проникновении (например, трансфекции) в клетку. В других вариантах осуществления мРНК, включенная в композицию наночастиц, может кодировать полипептид, который может улучшать или повышать иммунитет субъекта. Например, мРНК может кодировать гранулоцит-колониестимулирующий фактор или трастузумаб.
[00447] В некоторых вариантах осуществления мРНК, включенная в композицию наночастиц, может кодировать рекомбинантный полипептид, который может заменять один или более полипептидов, которые могут по существу отсутствовать в клетке, контактирующей с композицией наночастиц. Один или более по существу отсутствующих полипептидов могут отсутствовать из-за генетической мутации кодирующего гена или его метаболического пути. Альтернативно, рекомбинантный полипептид, полученный путем трансляции мРНК, может противодействовать активности эндогенного белка, присутствующего на поверхности или секретируемого клеткой. Антагонистический рекомбинантный полипептид может быть желательным для борьбы с вредными эффектами, вызванными активностями эндогенного белка, такими как измененные активности или локализации, вызванные мутацией. В другой альтернативе рекомбинантный полипептид, полученный путем трансляции мРНК, может опосредованно или непосредственно противодействовать активности биологического фрагмента, присутствующего на поверхности или секретируемого клеткой. Антагонизированные биологические фрагменты могут включать, но не ограничиваются ими, липиды (например, холестерин), липопротеины (например, липопротеин низкой плотности), нуклеиновые кислоты, углеводы и токсины малых молекул. Рекомбинантные полипептиды, продуцируемые путем трансляции мРНК, могут быть сконструированы для локализации внутри клетки, таким образом, как внутри конкретного компартмента, такого как ядро, или могут быть сконструированы для секреции из клетки или для транслокации на плазматическую мембрану клетки.
[00448] В некоторых вариантах осуществления контакт клетки с композицией наночастиц, содержащей мРНК, может снижать врожденный иммунный ответ клетки на экзогенную нуклеиновую кислоту. Клетка может быть приведена в контакт с первой композицией наночастиц, содержащей первое количество первой экзогенной мРНК, содержащей трансляционную область, и может быть определен уровень врожденного иммунного ответа клетки на первую экзогенную мРНК. Впоследствии клетка может быть приведена в контакт со второй композицией, содержащей второе количество первой экзогенной мРНК, причем второе количество представляет собой меньшее количество первой экзогенной мРНК по сравнению с первым количеством. Альтернативно, вторая композиция может содержать первое количество второй экзогенной мРНК, которая отличается от первой экзогенной мРНК. Стадии приведения в контакт клетки с первой и второй композициями могут повторяться один или более раз. Кроме того, эффективность продуцирования полипептида (например, трансляции) в клетке может быть необязательно определена, и клетка может повторно быть приведена в контакт с первой и/или второй композицией многократно, пока не будет достигнута эффективность продуцирования целевого белка.
Способы доставки терапевтических агентов в клетки и органы
[00449] В данном раскрытии предложены способы доставки терапевтического и/или профилактического средства в клетку или орган млекопитающего. Доставка терапевтического и/или профилактического средства в клетку включает введение композиции наночастиц, включая терапевтическое и/или профилактическое средство, субъекту, причем введение композиции включает приведение клетки в контакт с композицией. Например, белок, цитотоксический агент, радиоактивный ион, химиотерапевтический агент или нуклеиновая кислота (такая как РНК, например, мРНК) может быть доставлена в клетку или орган. В том случае, когда терапевтическое и/или профилактическое средство представляет собой мРНК, при контакте клетки с композицией наночастиц в клетке может транслироваться способная к трансляции мРНК для получения интересующего полипептида. Однако мРНК, которые по существу не транслируемы, также могут быть доставлены в клетки. По существу нетранслируемые мРНК могут быть полезны в качестве вакцин и/или могут изолировать трансляционные компоненты клетки для снижения экспрессии других видов в клетке.
[00450] В некоторых вариантах осуществления композиция наночастиц может нацеливаться на конкретный тип или класс клеток (например, клетки конкретного органа или его системы). Например, композиция наночастиц, содержащая терапевтическое и/или профилактическое средство, представляющее интерес, может быть конкретно доставлена в печень, почку, селезенку, бедро или легкое млекопитающего. Конкретная доставка к конкретному классу клеток, органа или системы или их группы подразумевает, что более высокая доля композиций наночастиц, содержащих терапевтическое и/или профилактическое средство, доставляется к месту назначения (например, ткани), представляющему интерес, относительно других мест назначения, например, при введении композиции наночастиц млекопитающему. В некоторых вариантах осуществления специфическая доставка может приводить к увеличению в 2, 5, 10, 15 или 20 раз количества терапевтического и/или профилактического средства на 1 г ткани целевого назначения (например, ткани, представляющей интерес, например, печени) по сравнению с другим пунктом назначения (например, селезенкой). В некоторых вариантах осуществления представляющую интерес ткань выбирают из группы, состоящей из печени, почки, легкого, селезенки, бедра, ткани глаза (например, посредством внутриглазной, субретинальной или интравитреальной инъекции), эндотелия сосудов в сосудах (например, внутрикоронарное или внутрибедренное) или почки и ткани опухоли (например, посредством внутриопухолевой инъекции).
[00451] В качестве другого примера направленной или специфической доставки в состав наночастиц может быть включена мРНК, которая кодирует белок-связывающего партнера (например, антитело или его функциональный фрагмент, каркасный белок или пептид) или рецептор на поверхности клетки. мРНК может дополнительно или вместо этого использоваться для направления синтеза и внеклеточной локализации липидов, углеводов или других биологических фрагментов. Альтернативно, другие терапевтические и/или профилактические средства или элементы (например, липиды или лиганды) композиции наночастиц могут быть выбраны на основе их сродства к конкретным рецепторам (например, рецепторам липопротеинов низкой плотности), так что композиция наночастиц может более легко взаимодействовать с популяцией клеток-мишеней, содержащей рецепторы. Например, лиганды могут включать, но не ограничиваются ими, члены специфичной пары связывания, антитела, моноклональные антитела, фрагменты Fv, одноцепочечные фрагменты Fv (scFv), фрагменты Fab', фрагменты F(ab')2, однодоменные антитела, камелизированные антитела и их фрагменты, гуманизированные антитела и их фрагменты и их мультивалентные версии; мультивалентные связывающие реагенты, включая моно- или биспецифичные антитела такие, как дисульфидно-стабилизированные фрагменты Fv, тандемы scFv, диатела, триатела или тетратела, и аптамеры, рецепторы и слитые белки.
[00452] В некоторых вариантах осуществления лиганд может представлять собой поверхностно-связанное антитело, которое может обеспечить настройку специфичности нацеливания на клетки. Это особенно полезно, так как высокоспецифичные антитела могут быть получены против эпитопа, представляющего интерес для желаемого сайта нацеливания. В одном варианте осуществления множественные антитела экспрессируются на поверхности клетки, и каждое антитело может иметь различную специфичность для желаемой мишени. Такие подходы могут повысить авидность и специфичность целевых взаимодействий.
[00453] Лиганд может быть выбран, например, специалистом в области биологии в зависимости от желаемой локализации или функции клетки. Например, лиганд рецептора эстрогена, такой как тамоксифен, может нацеливать клетки на эстрогензависимые клетки рака молочной железы, которые имеют увеличенное количество рецепторов эстрогена на поверхности клетки. Другие неограничивающие примеры взаимодействий лиганд/рецептор включают CCR1 (например, для лечения воспаленных суставных тканей или головного мозга при ревматоидном артрите и/или рассеянном склерозе), CCR7, CCR8 (например, для нацеливания на ткани лимфатических узлов), CCR6, CCR9, CCR10 (например, для нацеливания на ткань кишечника), CCR4, CCR10 (например, для нацеливания на кожу), CXCR4 (например, для общего усиленного переноса), HCELL (например, для лечения воспалений и воспалительных расстройств костного мозга), Alpha4beta7 (например, для нацеливания на слизистую оболочку кишечника) и VLA-4NCAM-1 (например, для нацеливание на эндотелий). В общем, любой рецептор, участвующий в нацеливании (например, метастазирование рака), можно использовать для применения в способах и композициях, описанных в данном документе.
[00454] Клетки-мишени могут включать, но не ограничиваются ими, гепатоциты, эпителиальные клетки, кроветворные клетки, эпителиальные клетки, эндотелиальные клетки, клетки легких, клетки костей, стволовые клетки, мезенхимальные клетки, нервные клетки, сердечные клетки, адипоциты, клетки гладких мышц сосудов, кардиомиоциты, клетки скелетных мышц, бета-клетки, гипофизарные клетки, синовиальные слизистые клетки, клетки яичников, клетки яичек, фибробласты, В-клетки, Т-клетки, ретикулоциты, лейкоциты, гранулоциты, и клетки опухоли.
[00455] В некоторых вариантах осуществления композиция наночастиц может нацеливаться на гепатоциты. Было показано, что аполипопротиены, такие как аполипопротеин E (apoE), связываются с нейтральными или почти нейтральными липидсодержащими композициями наночастиц в организме и, как известно, связываются с рецепторами, такими как рецепторы липопротеинов низкой плотности (LDLR), обнаруженные на поверхности гепатоцитов. Таким образом, композиция наночастиц, содержащая липидный компонент с нейтральным или почти нейтральным зарядом, который вводят субъекту, может приобретать apoE в организме субъекта и может впоследствии доставлять терапевтическое и/или профилактическое средство (например, РНК) в гепатоциты, включая LDLR, целенаправленным образом.
Способы лечения заболеваний и расстройств
[00456] Композиции наночастиц могут быть пригодными для лечения заболевания, расстройства или патологического состояния. В частности, такие композиции могут быть пригодны при лечении заболевания, расстройства или патологического состояния, характеризующегося отсутствием или нарушением активности белка или полипептида. Например, композиция наночастиц, содержащая мРНК, кодирующую отсутствующий или аберрантный полипептид, может назначаться или доставляться в клетку. Последующая трансляция мРНК может продуцировать полипептид, тем самым уменьшая или устраняя проблему, вызванную отсутствием или аберрантной активностью, вызванные полипептидом. Поскольку трансляция может происходить быстро, способы и композиции могут быть пригодными при лечении острых заболеваний, расстройств или патологических состояний, таких как сепсис, инсульт и инфаркт миокарда. Терапевтическое и/или профилактическое средство, включенное в композицию наночастиц, также может быть способно изменять скорость транскрипции данного вида, тем самым влияя на экспрессию гена.
[00457] Заболевания, расстройства и/или патологические состояния, характеризующиеся дисфункциональным или аберрантным белком или полипептидной активностью, для которых композиция может быть назначена, включают, но не ограничиваются ими, редкие заболевания, инфекционные заболевания (как вакцины и лекарственные средства), рак и пролиферативные заболевания, генетические заболевания (например, муковисцидоз), аутоиммунные заболевания, диабет, нейродегенеративные заболевания, сердечно-сосудистые и реноваскулярные заболевания и нарушения обмена веществ. Множественные заболевания, расстройства и/или патологические состояния могут проявляться в том, что они характеризуются отсутствием (или существенным снижением, так что надлежащая функция белка не возникает) активности белка. Такие белки могут не присутствовать, или они могут быть по существу нефункциональными. Конкретный пример дисфункционального белка представляет собой варианты миссенс-мутации гена трансмембранного регулятора проводимости муковисцидоза (CFTR), который продуцирует дисфункциональный вариант белка белка CFTR, который вызывает муковисцидоз. В данном изобретении предложен способ лечения таких заболеваний, расстройств и/или патологических состояний у субъекта путем введения композиции наночастиц, включающей РНК и липидный компонент, включающий липид формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), фосфолипид (необязательно ненасыщенный), ПЭГ-липид и структурный липид, где РНК может представлять собой мРНК, кодирующую полипептид, которая противодействует или иным образом преодолевает аберрантную активность белка, присутствующую в клетке субъекта.
[00458] В данном изобретении предложены способы, включающие введение композиций наночастиц, включающих один или более терапевтических и/или профилактических агентов, и фармацевтических композиций, включающих их. Термины терапевтический и профилактический могут использоваться в данном документе взаимозаменяемо по отношению к признакам и вариантам осуществления данного изобретения. Терапевтические композиции или их визуализирующие, диагностические или профилактические композиции могут быть назначены субъекту с использованием любого разумного количества и любого пути введения, эффективного для профилактики, лечения, диагностики или визуализации заболевания, расстройства и/или патологического состояния и/или любой другой цели. Конкретное количество, вводимое данному субъекту, может варьироваться в зависимости от вида, возраста и общего состояния субъекта; цели введения; конкретной композиции; режима введения; и тому подобного. Композиции по данному изобретению могут быть составлены в единичной лекарственной форме для простоты введения и единообразия дозировки. Понятно, однако, что общее ежедневное применение композиции по данному изобретению будет решено лечащим врачом в рамках здравого медицинского суждения. Конкретный терапевтически эффективный, профилактически эффективный или иным образом подходящий уровень дозы (например, для визуализации) для любого конкретного пациента будет зависеть от множества факторов, включая степень тяжести и идентификацию расстройства, которое лечат, если есть; одно или более применяемых терапевтических и/или профилактических средств; конкретный применяемый препарат; возраст, массу тела, общее состояние здоровья, пол и диета пациента; время введения, способ введения и скорость выведения конкретной применяемой фармацевтической композиции; продолжительность лечения; лекарственные средства, применяемые в комбинации или одновременно с конкретной применяемой фармацевтической композицией; и подобные факторы, хорошо известные в медицине.
[00459] Композиция наночастиц, включающая одно или более терапевтических и/или профилактических средств, может быть введена любым путем. В некоторых вариантах осуществления, композиции, включая профилактические, диагностические или визуализирующие композиции, включающие одну или более композиций наночастиц, описанных в данном документе, вводят одним или более различными путями, включая пероральный, внутривенный, внутримышечный, внутриартериальный, интрамедуллярный, интратекальный, внутрипаренхиматозный, подкожный, интравентрикулярный, транс- или интрадермальный, интердермальный, ректальный, интравагинальный, внутрибрюшинный, интраокулярный, субретинальный, интравитреальный, местный (например, порошки, мази, кремы, гели, лосьоны и/или капли), мукозальный, назальный, буккальный, энтеральный, витреальный, внутриопухолевый, сублингвальный, интраназальный; путем интратрахеальной инстилляции, бронхиальной инстилляции и/или ингаляции; в виде перорального спрея и/или порошка, назального спрея, и/или аэрозоля, и/или через катетер воротной вены. В некоторых вариантах осуществления композиция может быть введена внутривенно, внутримышечно, внутрикожно, внутриартериально, внутриопухолево, подкожно, внутриглазно, субретинально, интравитреально, интрапаренхимально или любым другим парентеральным путем введения или путем ингаляции. Однако данное описание охватывает доставку или введение композиций, описанных в данном документе, любым подходящим способом, принимая во внимание вероятные достижения в области доставки лекарств. Как правило, наиболее подходящий путь введения будет зависеть от множества факторов, включая природу композиции наночастиц, включая один или более терапевтических и/или профилактических средств (например, их стабильность в различных средах организма, таких как кровоток и желудочно-кишечный тракт), состояние пациента (например, способен ли пациент переносить определенные пути введения) и т. д.
[00460] В конкретных вариантах осуществления композиции по данному изобретению могут быть введены в дозах, достаточных для доставки от около 0,0001 мг/кг до около 10 мг/кг, от около 0,001 мг/кг до около 10 мг/кг, от около 0,005 мг/кг до около 10 мг/кг, от около 0,01 мг/кг до около 10 мг/кг, от около 0,05 мг/кг до около 10 мг/кг, от около 0,1 мг/кг до около 10 мг/кг, от около 1 мг/кг до около 10 мг/кг, от около 2 мг/кг до около 10 мг/кг, от около 5 мг/кг до около 10 мг/кг, от около 0,0001 мг/кг до около 5 мг/кг, от около 0,001 мг/кг до около 5 мг/кг, от около 0,005 мг/кг до около 5 мг/кг, от около 0,01 мг/кг до около 5 мг/кг, от около 0,05 мг/кг до около 5 мг/кг, от около 0,1 мг/кг до около 5 мг/кг, от около 1 мг/кг до около 5 мг/кг, от около 2 мг/кг до около 5 мг/кг, от около 0,0001 мг/кг до около 2,5 мг/кг, от около 0,001 мг/кг до около 2,5 мг/кг, от около 0,005 мг/кг до около 2,5 мг/кг, от около 0,01 мг/кг до около 2,5 мг/кг, от около 0,05 мг/кг до около 2,5 мг/кг, от около 0,1 мг/кг до около 2,5 мг/кг, от около 1 мг/кг до около 2,5 мг/кг, от около 2 мг/кг до около 2,5 мг/кг, от около 0,0001 мг/кг до около 1 мг/кг, от около 0,001 мг/кг до около 1 мг/кг, от около 0,005 мг/кг до около 1 мг/кг, от около 0,01 мг/кг до около 1 мг/кг, от около 0,05 мг/кг до около 1 мг/кг, от около 0,1 мг/кг до около 1 мг/кг, от около 0,0001 мг/кг до около 0,25 мг/кг, от около 0,001 мг/кг до около 0,25 мг/кг, от около 0,005 мг/кг до около 0,25 мг/кг, от около 0,01 мг/кг до около 0,25 мг/кг, от около 0,05 мг/кг до около 0,25 мг/кг, or от около 0,1 мг/кг до около 0,25 мг/кг терапевтического и/или профилактического средства (например, мРНК) в данной дозе, где доза 1 мг/кг обеспечивает 1 мг терапевтического и/или профилактического средства на 1 кг массы тела субъекта. В некоторых вариантах осуществления может быть введена доза от около 0,001 мг/кг до около 10 мг/кг терапевтического и/или профилактического средства (например, мРНК) композиции наночастиц. В других вариантах осуществления может быть введена доза от около 0,005 мг/кг до около 2,5 мг/кг терапевтического и/или профилактического средства В конкретных вариантах осуществления может быть введена доза около 0,1 мг/кг до около 1 мг/кг. В других вариантах осуществления может быть введена доза 0,05 мг/кг до около 0,25 мг/кг. Доза может быть назначена один или более раз в день, в том же или другом количестве, с достижением желаемого уровня экспрессии мРНК и/или терапевтического, диагностического, профилактического или визуального эффекта. Желаемая дозировка может быть доставлена, например, три раза в день, два раза в день, один раз в день, через день, каждый третий день, каждую неделю, каждые две недели, каждые три недели или каждые четыре недели. В конкретных вариантах осуществления желаемая дозировка может быть доставлена с помощью многократного введения (например, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать или более введений). В некоторых вариантах осуществления разовая доза может быть введена, например, до или после хирургической процедуры или в случае острого заболевания, расстройства или патологического состояния.
[00461] Композиции наночастиц, включающие один или более терапевтических и/или профилактических средств, могут быть использованы в комбинации с одним или более другими терапевтическими, профилактическими, диагностическими или визуализирующими агентами. Под «в комбинации с» не подразумевается, что агенты должны вводиться одновременно и/или составляться для совместной доставки, хотя эти способы доставки находятся в объеме данного изобретения. Например, одна или более композиций наночастиц, включающих одно или более различных терапевтических и/или профилактических средств, могут быть введены в комбинации. Композиции можно вводить одновременно, до или после одной или более других желательных терапевтических или медицинских процедур. Как правило, каждый агент будет вводиться в дозе и/или в соответствии с графиком, установленным для данного агента. В некоторых вариантах осуществления, данное описание охватывает доставку композиций или их визуализирующих, диагностических или профилактических композиций в сочетании с агентами, которые улучшают их биодоступность, уменьшают и/или модифицируют их метаболизм, ингибируют их экскрецию и/или модифицируют их распределение в организме
[00462] Кроме того, следует иметь в виду, что терапевтически, профилактически, диагностически или визуализирующие активные агенты, применяемые в комбинации, могут самостоятельно вводиться вместе в одной композиции или вводиться отдельно в разных композициях. В целом ожидается, что агенты, применяемые в комбинации, будут применяться на уровнях, которые не превышают уровни, в которых они используются индивидуально. В некоторых вариантах осуществления уровни, применяемые в комбинации, могут быть ниже, чем уровни, применяемые индивидуально.
[00463] Конкретная комбинация методов лечения (терапевтических средств или процедур) для применения в комбинированном режиме будет учитывать совместимость желаемых терапевтических средств и/или процедур и желаемого терапевтического эффекта, который должен быть достигнут. Также следует иметь в виду, что применяемая терапия может достигать желаемого эффекта при том же расстройстве (например, композиция, пригодная для лечения рака, может быть введена одновременно с химиотерапевтическим агентом), или они могут достигать различных эффектов (например, контроль любых побочные эффекты, таких как инфузионные реакции).
[00464] Композиция наночастиц может применяться в комбинации с агентом для повышения эффективности и/или терапевтического окна композиции. Такой агент может представлять собой, например, противовоспалительное соединение, стероид (например, кортикостероид), статин, эстрадиол, ингибитор BTK, агонист S1P1, модулятор глюкокортикоидного рецептора (GRM) или анти-гистамин. В некоторых вариантах осуществления композиция наночастиц может применяться в комбинации с дексаметазоном, метотрексатом, ацетаминофеном, блокатором рецепторов H1 или блокатором рецепторов H2. В некоторых вариантах осуществления способ лечения субъекта, нуждающегося в этом, или доставки терапевтического и/или профилактического средства субъекту (например, млекопитающему) может включать предварительную обработку субъекта одним или более агентами перед введением композиции наночастиц. Например, субъект может быть предварительно обработанным подходящим количеством (например, 10 мг, 20 мг, 30 мг, 40 мг, 50 мг, 60 мг, 70 мг, 80 мг, 90 мг, 90 мг, 100 мг или любым другим подходящим количеством) дексаметазона, метотрексата, ацетаминофена, блокатора рецепторов H1 или блокатора рецепторов H2. Предварительная обработка может иметь место за 24 часа или менее (например, 24 часа, 20 часов, 16 часов, 12 часов, 8 часов, 4 часа, 2 часа, 1 час, 50 минут, 40 минут, 30 минут, 20 минут или 10 минут) перед введением композиции наночастиц и может произойти один, два или более раз, например, в увеличивающихся дозировках.
[00465] Специалистам в данной области техники будет понятно или они смогут установить, используя не более чем рутинные методы эксперимента, множество эквивалентов конкретных вариантов реализации изобретения по данному описанию, описанных в данном документе. Объем данного изобретения не предназначен для ограничения вышеприведенным описанием, а скорее изложен так, как в прилагаемой формуле изобретения.
[0001] В тексте формулы изобретения формы единственного числа могут означать один или более чем один, если не указано иное или это иным образом не очевидно из контекста. Пункты формулы изобретения или описания, которые включают «или» между одним или более членами группы, считаются удовлетворенными, если один, более одного или все члены группы присутствуют, применяются или имеют отношение к определенному продукту или способу, если не указано иное или это иным образом не очевидно из контекста. Описание изобретения включает в себя варианты реализации изобретения, в которых ровно один член группы присутствует в, применяется в или иным образом относится к данному продукту или способу. Описание изобретения включает в себя варианты реализации изобретения, в которых более чем один из группы членов присутствует в, применяется в или иным образом относится к данному продукту или способу. В контексте данного документа, выражения «один или более из A, B или C», «один или более A, B или C», «один или более из A, B и C», «один или более A, B и C», «выбран из A, B и C,” “выбранные из группы, состоящей из A, B и C” и тому подобное используются взаимозаменяемо и все относятся к выбору из группы, состоящей из A, B и/или C, то есть одного или более A, одного или более B, одного или более C или любой их комбинации, если не указано иное.
[0002] Также отмечается, что термин «содержащий» предназначен для того, чтобы быть открытым и позволяет, но не требует включения дополнительных элементов или этапов. Когда термин «содержащий» используется в данном документе, термины «состоящий по существу из» и «состоящий из», таким образом, также охватываются и раскрываются. Во всем описании, где композиции описаны как имеющие, включающие или содержащие конкретные компоненты, предполагается, что композиции также состоят по существу или состоят из перечисленных компонентов. Аналогичным образом, когда способы или процессы описаны как имеющие или включающие в себя конкретные этапы способа, способы также состоят по существу или состоят из перечисленных этапов обработки. Кроме того, следует понимать, что порядок этапов или порядок выполнения определенных действий не имеет значения, если изобретение остается работоспособным. Кроме того, два или более этапов или действий могут быть выполнены одновременно.
[0003] Когда указаны диапазоны, конечные точки включены. Кроме того, должно быть понятно, что если не указано иное или это иным образом не очевидно из контекста и понимания специалиста в данной области техники, значения, которые выражаются как диапазоны, могут принимать любое конкретное значение или поддиапазон в указанных диапазонах в разных вариантах реализации изобретения, до десятой части единицы нижнего предела диапазона, если из контекста явно следует иное.
[0004] Способы синтеза по данному изобретению могут допускать большое разнообразие функциональных групп, поэтому могут использоваться различные замещенные исходные материалы. Способы обычно дают желаемое конечное соединение в конце или почти в конце всего способа, хотя в некоторых случаях может быть желательным дальнейшее превращение соединения в его фармацевтически приемлемую соль.
[0005] Соединения по данному изобретению могут быть получены различными способами с использованием коммерчески доступных исходных материалов, соединений, известных в литературе, или из легко приготовленных промежуточных соединений, с использованием стандартных синтетических методов и методик, известных специалистам в данной области техники или которые быть очевидным для квалифицированного специалиста в свете приведенных здесь учений. Стандартные синтетические методы и методики для получения органических молекул и превращений и манипуляций с функциональными группами могут быть получены из соответствующей научной литературы или из стандартных учебников в данной области. Хотя и не ограничиваясь одним или более источниками, классические тексты, такие как Smith, M. B., March, J., March Advanced Organic Chemistry: Reactions, Mechanisms и Structure, 5-е издание, John Wiley & Sons: Нью-Йорк, 2001; Greene, T.W., Wuts, P.G. M., Protective Groups in Organic Synthesis, 3-е издание, John Wiley & Sons: Нью-Йорк, 1999; R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989); L. Fieser и M. Fieser, Fieser and Fieser Reagents for Organic Synthesis, John Wiley and Sons (1994); и L. Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995), включенные в данный документ посредством ссылки, являются пригодными и признанными справочными учебниками по органическому синтезу, известными специалистам в данной области техники. Следующие описания синтетических способов предназначены для иллюстрации, но не для ограничения общих методик получения соединений по данному изобретению.
[0006] Соединения по данному изобретению, имеющие любую из формул, описанных в данном документе, могут быть получены в соответствии с методиками, проиллюстрированными на Схемах 1, 2 и 3 ниже, из коммерчески доступных исходных материалов или исходных материалов, которые могут быть получены с использованием литературных методик. Переменные в схемах (например, R1, R2 и R3 и т.д.) являются таковыми, как определено в данном документе. Специалист в данной области заметит, что в ходе последовательностей реакций и схем синтеза, описанных в данном документе, порядок определенных стадий может быть изменен, например, введение и удаление защитных групп.
[0007] Специалист в данной области поймет, что определенным группам может потребоваться защита от условий реакции путем использования защитных групп. Защитные группы также можно использовать для дифференциации сходных функциональных групп в молекулах. Список защитных групп и как ввести и удалить эти группы можно найти в Greene, T.W., Wuts, P.G. M., Protective Groups in Organic Synthesis, 3-е издание, John Wiley & Sons: Нью-Йорк, 1999.
[0008] Предпочтительные защитные группы включают, но не ограничиваются ими:
[0009] Для гидроксильного фрагмента: TBS, бензил, THP, Ac;
[0010] Для карбоновых кислот: бензиловый эфир, метиловый эфир, этиловый эфир, аллиловый эфир;
[0011] Для аминов: Fmoc, Cbz, BOC, DMB, Ac, Bn, Tr, Ts, трифторацетил, фталимид, бензилиденамин;
[0012] Для диолов: Ac (x2) TBS (x2) или когда вместе взяты ацетониды;
[0013] Для тиолов: Ac;
[0014] Для бензимидазолов: SEM, бензил, PMB, DMB;
[0015] Для альдегидов: ди-алкилацетали, такие как диметоксиацеталь или диэтилацеталь.
[0016] В схемах реакций, описанных в данном документе может быть получено множество стереоизомеров. Когда конкретный стереоизомер не указан, подразумевается, что он означает все возможные стереоизомеры, которые могут быть получены в результате реакции. Специалист в данной области поймет, что реакции могут быть оптимизированы с предпочтительным использованием одного изомера, или могут быть разработаны новые схемы для получения одного изомера. Если получаются смеси, для разделения изомеров могут использоваться такие методы, как препаративная тонкослойная хроматография, препаративная ВЭЖХ, препаративная хиральная ВЭЖХ или препаративная SFC.
Схема 1
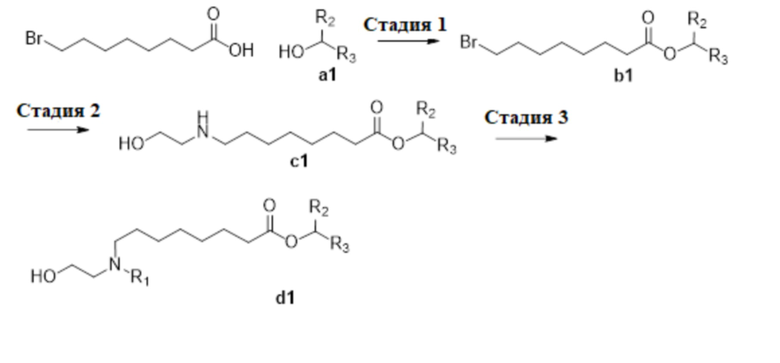
[0017] Как проиллюстрировано на Схеме 1 выше, 8-бромоктановая кислота реагирует со спиртом a1 (например, гептадекан-9-ол) с образованием эфира b1 (например, гептадекан-9-ил-8-бромоктаноат). Стадия 1 может проходить в органическом растворителе (например, дихлорметан) в присутствии, например, N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорида, N, N-диизопропилэтиламина и DMAP. Стадия 1 может проходить при комнатной температуре в течение 18 часов. Затем сложный эфир b1 вступает в реакцию с 2-аминоэтан-1-олом с образованием амина c1 (например, гептадекан-9-ил-8-((2-гидроксиэтил)амино) октаноат). Стадия 2 может проходить в этаноле, например, при температуре около 60°C. Затем амин c1 вступает в реакцию с бромалкилом R1-Br (например, 1-бромтетрадекан) с образованием соединения d1 (например, гептадекан-9-ил-8-((2-гидроксиэтил)(тетрадецил)амино)октаноат). Стадия 3 может проходить в этаноле1 в присутствии N, N-диизопропилэтиламина.
Схема 2
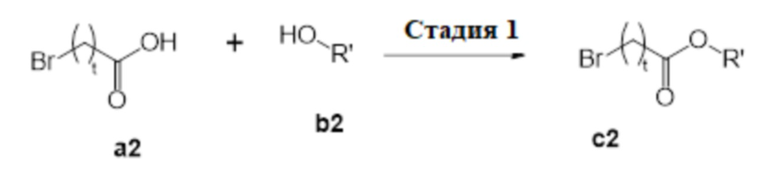
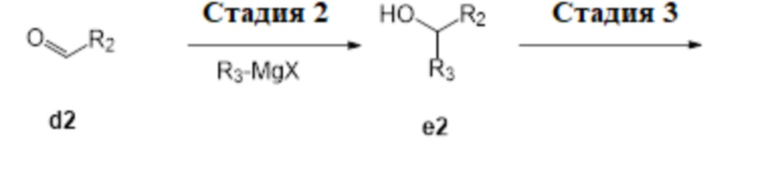


[0018] Как проиллюстрировано на Схеме 2 выше, кислота а2 (t равно целому числу от 1 до 7; например, 8-бромоктановая кислота) вступает в реакцию со спиртом b2 (например, нонан-1-ол) с образованием эфира с2 (например, нонил -8-бромоктаноат). Стадия 1 может проходить в органическом растворителе (например, дихлорметан) в присутствии, например, N- (3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорида, N, N-диизопропилэтиламина и DMAP. Спирт e2 (например, гептадекан-9-ол) может быть получен путем взаимодействия альдегида d2 (например, нонаналь1) с реактивом Гриньяра R3-MgX (например, Н-C8H17MgBr) на Стадии 2. Затем 8-бромоктановая кислота вступает в реакцию со спиртом e2 (например, гептадекан-9-ол) с образованием эфира f2 (например, гептадекан-9-ил-8-бромоктаноат). Стадия 3 может проходить в органическом растворителе (например, дихлорметан) в присутствии, например, N- (3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорида, N, N-диизопропилэтиламина и DMAP. Затем сложный эфир f2 реагирует с 2-аминоэтан-1-олом с образованием амина g2 (например, гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноат). Стадия 4 может проходить в этаноле при присутствии i-Pr2EtN. Затем амин g2 вступает в реакцию с эфиром с2 (например, нонил-8-бромоктаноат) с образованием соединения h2 (например, гептадекан-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат). Стадия 5 может проходить в органическом растворителе (например, смеси CPME и MeCN), в присутствии основания (такого как неорганическое основание (например, K2CO3) или ненуклеофильного органического основания (например, i-Pr2EtN)) и катализатора (например, иодид, такой как KI или NaI) при, например, повышенной температуре (такой как примерно при 70-90°С, например, около 80°С).
Схема 3
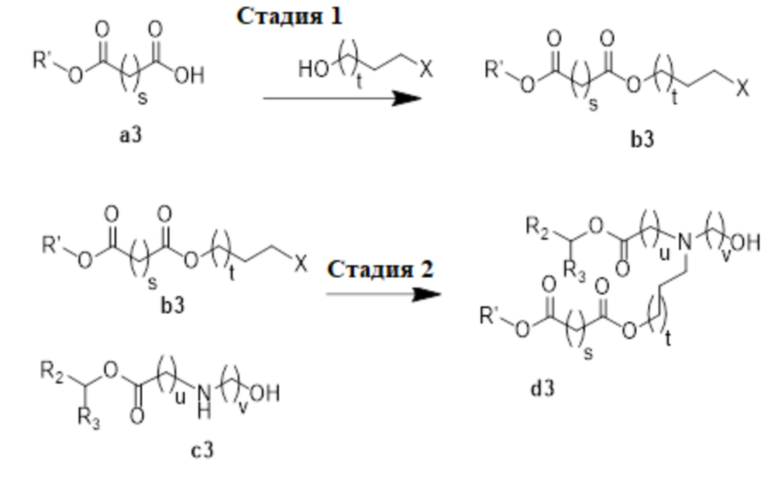
[0019] Как проиллюстрировано на Схеме 3 выше, галогеналканол (t равно целому числу между 1 и 12, например, 6- бромгексан-1-ол) вступает в реакцию с исходным материалом a3 (s равно целому числу между 1 и 6, например, 4-(гексилокси)-4-оксобутановая кислота) с получением галогенированного диэфира b3 (например, 6-бромгексилгексилсукцинат). Соединение а3 может быть получено по реакции спирта (например, гексан-1-ол) с ангидридом кислоты (например, янтарного ангидрида, дигидро-2Н-пиран-2,6 (3Н)-дион, 3-(трет-бутокси)-3-оксопропановая кислота, 4-(трет-бутокси)-3-метил-4-оксобутановая кислота или 4- (трет-бутокси)-2-метил-4-оксобутановая кислота). Стадия 1 может проходить в органическом растворителе (например, дихлорметан) в присутствии, например, N- (3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорида, N, N-диизопропилэтиламина и DMAP. Затем галогенированный диэфир b3 вступает в реакцию с амином c3 (u равно целому числу от 5 до 13, v равно целому числу от 1 до 5, например, гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноат) с образованием продукта d3. Стадия 2 может проходить в органическом растворителе (например, смеси CPME и MeCN) в присутствии основания (такого как неорганическое основание (например, K2CO3) и катализатора (например, иодида, такого как KI) и эфирного растворителя (например, циклопентилметиловый эфир) при повышенной температуре (например, около 90°C).
[0020] Специалист в данной области техники поймет, что в вышеприведенных схемах порядок определенных стадий могут быть взаимозаменяемыми.
[0021] В определенных аспектах описание также включает способы синтеза соединения любой из формул (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), ( IIe), (IIf), (IIg) или (III) и промежуточное соединение (я) для синтеза соединения.
[0022] В некоторых вариантах осуществления, метод синтеза соединения формулы (I) включает введение в реакцию соединения формулы (X2): 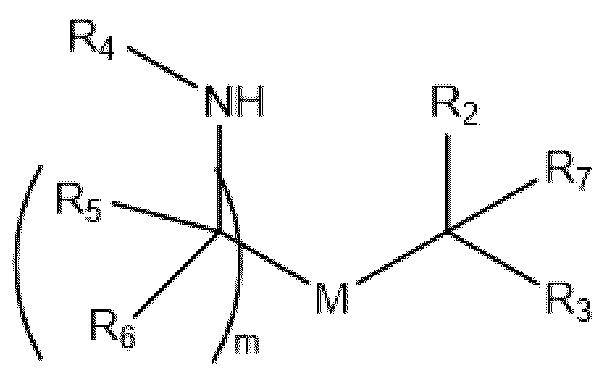 с R1-Br с образованием соединения формулы (I), где все переменные имеют значения, определенные в данном документе. Например, m равно 5, 6, 7, 8 или 9, предпочтительно 5, 7, или 9. Например, каждый из R5, R6 и R7 представляет собой H. Например, M представляет собой C(O)O- или -OC(O)-. Например, R4 представляет собой незамещенный C1-3 алкил или -(CH2)nQ, в котором n равно 2, 3 или 4 и Q представляет собой OH, -NHC(S)N(R)2, -NHC(O)N(R)2, -N(R)C(O)R или -N(R)S(O)2R. Например, реакция соединения формулы (X2) с R1-Br происходит в присутствии основания (такого как неорганическое основание) (например, K2CO3) или ненуклеофильное органическое основание (например, i-Pr2EtN)). Например, реакция протекает в присутствии неорганического основания (например, K2CO3) и катализатора (например, иодида, такого как KI или NaI). Например, реакция протекает при повышенной температуре, например, около 50-100°С, 70-90°С или около 80°C).
с R1-Br с образованием соединения формулы (I), где все переменные имеют значения, определенные в данном документе. Например, m равно 5, 6, 7, 8 или 9, предпочтительно 5, 7, или 9. Например, каждый из R5, R6 и R7 представляет собой H. Например, M представляет собой C(O)O- или -OC(O)-. Например, R4 представляет собой незамещенный C1-3 алкил или -(CH2)nQ, в котором n равно 2, 3 или 4 и Q представляет собой OH, -NHC(S)N(R)2, -NHC(O)N(R)2, -N(R)C(O)R или -N(R)S(O)2R. Например, реакция соединения формулы (X2) с R1-Br происходит в присутствии основания (такого как неорганическое основание) (например, K2CO3) или ненуклеофильное органическое основание (например, i-Pr2EtN)). Например, реакция протекает в присутствии неорганического основания (например, K2CO3) и катализатора (например, иодида, такого как KI или NaI). Например, реакция протекает при повышенной температуре, например, около 50-100°С, 70-90°С или около 80°C).
[0023] Способ также может включать введение реакция соединения формула (X1): 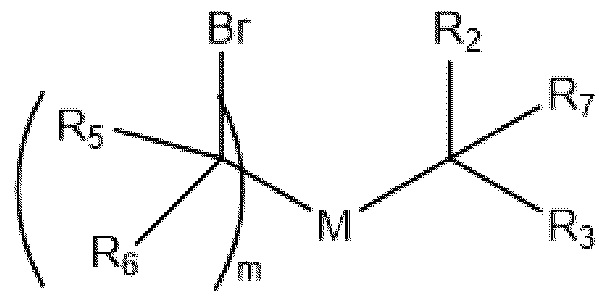 с R4NH2 для получения соединения формула (X2), где все переменные имеют значения, определенные в данном документе.
с R4NH2 для получения соединения формула (X2), где все переменные имеют значения, определенные в данном документе.
[0024] В некоторых вариантах осуществления промежуточные продукты включают те, которые имеют любую из формул (X1) и (X2): 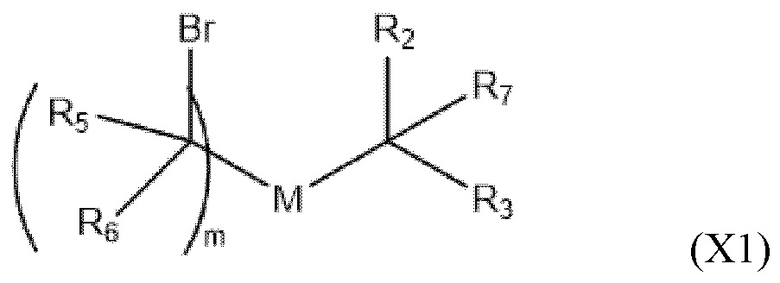 или
или 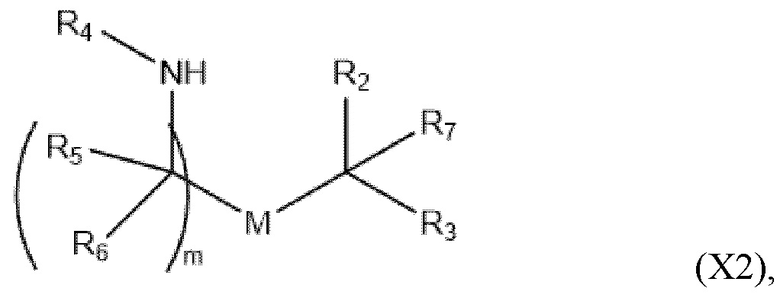 где все переменные имеют значения, определенные в данном документе. Например, промежуточное соединение включает гептадекан-9-ил-8-бромоктаноат и гептадекан-9-ил-8 - ((2-гидроксиэтил)амино)октаноат и его морфические формы (например, кристаллическая форма).
где все переменные имеют значения, определенные в данном документе. Например, промежуточное соединение включает гептадекан-9-ил-8-бромоктаноат и гептадекан-9-ил-8 - ((2-гидроксиэтил)амино)октаноат и его морфические формы (например, кристаллическая форма).
[0025] Кроме того, должно быть понятно, что любой конкретный вариант реализации изобретения, который относится к предшествующему уровню техники, может быть явно исключен из любого одного или более пунктов формулы изобретения. Поскольку такие варианты реализации изобретения считаются известными для специалиста в данной области техники, они могут быть исключены, даже если это исключение явно не изложено в данном документе.
[0026] Все цитируемые источники, например ссылки, публикации, базы данных, записи в базах данных и статьи, цитируемые в данном документе, включены в данную заявку посредством ссылки, даже если это прямо не указано в цитировании. В случае противоречивых утверждений цитируемого источника и данной заявки, заявление в данной заявке имеет преимущественную силу.
Примеры
Пример 1: Синтез соединений формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe) (IIf) или (IIg)
A. Общие положения
[0027] Все используемые растворители и реагенты были приобретены коммерчески и использованы как таковые, если не указано иное. 1H ЯМР спектры были записаны в CDCl3 при 300 K с использованием инструмента Bruker Ultrashield 300 МГц. Химические сдвиги представлены в частях на миллион (м.ч.) относительно TMС (0,00) для 1H. Хроматографию на силикагеле проводили на приборах ISCO CombiFlash Rf+Lumen с использованием флэш-картриджей ISCO RediSep Rf Gold (размер частиц: 20-40 микрон). Обращенно-фазную хроматографию проводили на приборах ISCO CombiFlash Rf+Lumen с использованием колонок высокоэффективной RediSep Rf Gold C18. Все конечные соединения были определены как имеющие чистоту более 85% с помощью анализа обращенно-фазной UPLC-MС (время удерживания, RT, в минутах) с использованием прибора Waters Acquity UPLC с DAD и ДСИО и ZORBAX с быстрым разрешением высокого разрешения (RRHD) колонка SB-C18 LC, 2,1 мм, 50 мм, 1,8 мкм и градиент от 65 до 100% ацетонитрила в воде с 0,1% ТФК в течение 5 минут со скоростью 1,2 мл/мин. Объем впрыска составлял 5 мкл, а температура колонки составляла 80°С. Обнаружение основывалось на электрораспылительной ионизации (ИЭР) в положительном режиме с использованием масс-спектрометра Waters SQD (Милфорд, Массачусетс, США) и детектора испарительного рассеяния света.
[0028] Методики, описанные ниже, подходят для синтеза Соединения 1-280.
[0029] В данном документе используются следующие условные сокращения:
ТГФ: Тетрагидрофуран
MeCN: Ацетонитрил
ЛАГ: Литийалюминийгидрид
ДХМ: Дихлорметан
DMAP: 4-Диметиламинопиридин
ЛДА: Литийдиизопропиламид
комн. темп.: Комнатная температура
DME: 1,2-Диметоксиэтан
n-BuLi: н-Бутиллитий
CPME: Циклопентилметиловый эфир
i-Pr2EtN: N, N-Диизопропилэтиламин
B. Соединение 2: Гептадекан-9-ил-8-((2-гидроксиэтил)(тетрадецил)амино)октаноат
Иллюстративный пример методики 1

Гептадекан-9-ил-8-бромоктаноат (Метод A)
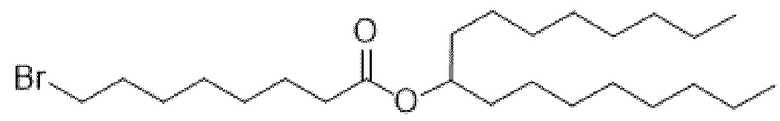
[0030] К раствору 8-бромоктановой кислоты (1,04 г, 4,6 ммоль) и гептадекан-9-ола (1,5 г, 5,8 ммоль) в дихлорметане (20 мл) прибавили N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид (1,1 г, 5,8 ммоль), N, N-диизопропилэтиламин (3,3 мл, 18,7 ммоль) и DMAP (114 мг, 0,9 ммоль). Реакционную смесь оставили перемешиваться при комн. темп. в течение 18 ч. Реакционную смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия и сушили над MgSO4. Органический слой отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-10% этилацетат в смеси гексанов) с получением гептадекан-9-ил-8-бромоктаноата (875 мг, 1,9 ммоль, 41%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 3,42 (м, 2H); 2,31 (м, 2H); 1,89 (м, 2H); 1,73-1,18 (уш. м, 36H); 0,88 (м, 6H).
Гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноат (Метод B)
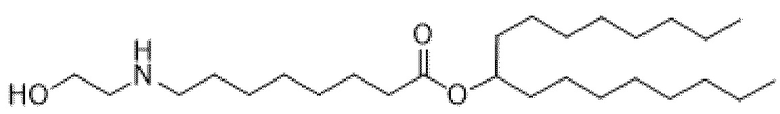
[0031] Раствор гептадекан-9-ил-8-бромоктаноата (3,8 г, 8,2 ммоль) и 2-аминоэтан-1-ола (15 мл, 248 ммоль) в этаноле (3 мл) оставили перемешиваться при 62°C в течение 18 ч. Реакционную смесь концентрировали в вакууме и остаток перенесли в этилацетат и воду. Органический слой отделили и промывали водой, насыщенным водным раствором хлорида натрия и сушили над Na2SO4. Смесь отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноата (3,1 г, 7 ммоль, 85%). СВЭЖХ/ДСИО: RT=2,67 мин. MС (ИЭР): m/z (MH+) 442,68 для C27H55NO3
1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 3,67 (т, 2H); 2,81 (т, 2H); 2,65 (т, 2H); 2,30 (т, 2H); 2,05 (уш. м, 2H); 1,72-1,41 (уш. м, 8H); 1,40-1,20 (уш. м, 30H); 0,88 (м, 6H).
Гептадекан-9-ил-8-((2-гидроксиэтил)(тетрадецил)амино)октаноат (Метод C)
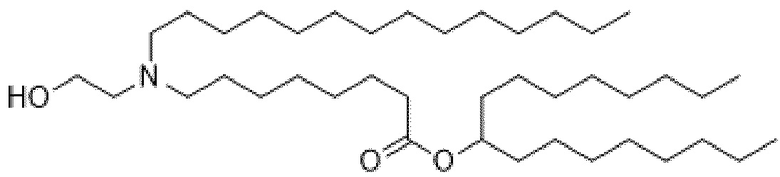
Химическая формула: C41H83NO3
Молекулярная масса: 638,12
[0032] Раствор гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноата (125 мг, 0,28 ммоль), 1-бромтетрадекан (94 мг, 0,34 ммоль) и N, N-диизопропилэтиламин (44 мг, 0,34 ммоль) в этаноле оставили перемешиваться при 65°C в течение 18 ч. Реакционную смесь охладили до комн. темп. и растворители выпарили в вакууме. Остаток перенесли в этилацетат насыщенный раствор гидрокарбоната натрия. Органический слой отделили, сушили над Na2SO4 и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((2-гидроксиэтил)(тетрадецил)амино)октаноата (89 мг, 0,14 ммоль, 50%). СВЭЖХ/ДСИО: RT=3,61 мин. MС (ИЭР): m/z (MH+) 638,91 для C41H83NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 3,72-3,47 (уш. м, 2H); 2,78-2,40 (уш. м, 5H); 2,28 (т, 2H); 1,70-1,40 (м, 10H); 1,38-1,17 (уш. м, 54H); 0,88 (м, 9H).
Синтез промежуточных соединений :
Промежуточное соединение A: 2-Октилдекановая кислота
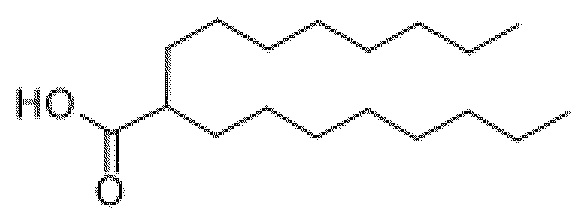
[0033] Раствор диизопропиламин (2,92 мл, 20,8 ммоль) в ТГФ (10 мл) охладили до -78°C и прибавили раствор n-BuLi (7,5 мл, 18,9 ммоль,2,5 M в смеси гексанов). Реакционную смесь оставили нагреваться до 0°C. К раствору декановой кислоты (2,96 г, 17,2 ммоль) и NaH (754 мг, 18,9 ммоль,60% мас./мас.) в ТГФ (20 мл) при 0°C прибавили раствор ЛДА и смесь оставили перемешиваться при комн. темп. в течение 30 мин. Через указанное время прибавили 1-иодоктан (5 г, 20,8 ммоль) и реакционную смесь нагревали при 45°C в течение 6 ч. Реакционную смесь погасили 1N HCl (10 мл). Органический слой сушили над MgSO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-20% этилацетат в смеси гексанов) с выходом 2-октилдекановой кислоты (1,9 г, 6,6 ммоль, 38%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 2,38 (уш. м, 1H); 1,74-1,03 (уш. м, 28H); 0,91 (м, 6H).
Промежуточное соединение B: 7-Бромгептил-2-октилдеканоат
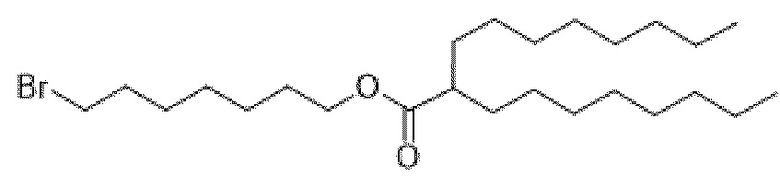
[0034] 7-бромгептил 2-октилдеканоат синтезировали, используя метод A из 2-октилдекановой кислоты и 7-бромгептан-1-ола. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,09 (уш. м, 2H); 3,43 (уш. м, 2H); 2,48-2,25 (уш. м, 1H); 1,89 (уш. м, 2H); 1,74-1,16 (уш. м, 36H); 0,90 (м, 6H).
Промежуточное соединение C: (2-Гексилциклопропил)метанол

[0035] Раствор диэтилцинка (20 мл, 20 ммоль,1 M в смеси гексанов), в дихлорметане (20 мл) оставили охлаждаться до -40°C в течение 5 мин. Затем по каплям прибавили раствор дииодметана (3,22 мл, 40 ммоль) в дихлорметане (10 мл). Затем реакционную смесь оставили перемешиваться в течение 1 ч при -40°C, прибавили раствор трихлор-уксусной кислоты (327 мг, 2 ммоль) и DME (1 мл, 9,6 ммоль) в дихлорметане (10 мл). Реакционную смесь оставили нагреваться до -15°C и перемешивали при данной температуре в течение 1 ч. Затем при -15°C к раствору прибавили раствор (Z)-нон-2-ен-1-ола (1,42 г, 10 ммоль) в дихлорметане (10 мл). Реакционную смесь затем оставили медленно нагреваться до комн. темп. и перемешивали в течение 18 ч. Через указанное время прибавили насыщенный NH4Cl (200 мл) и реакционную смесь экстрагировали дихлорметаном (3X), промывали насыщенным водным раствором хлорида натрия и сушили над Na2SO4. Органический слой отфильтровали, выпарили в вакууме и остаток очищали с помощью хроматографии на силикагеле (0-50% этилацетат в смеси гексанов) с выходом (2-гексилциклопропил)метанола (1,43 г, 9,2 ммоль, 92%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,64 (м, 2H); 1,57-1,02 (м, 12H); 0,99-0,80 (м, 4H); 0,72 (м, 1H), 0,00 (м, 1H).
C. Соединение 1: Гептадекан-9-ил-8-((2-гидроксиэтил)(октадецил)амино)октаноат
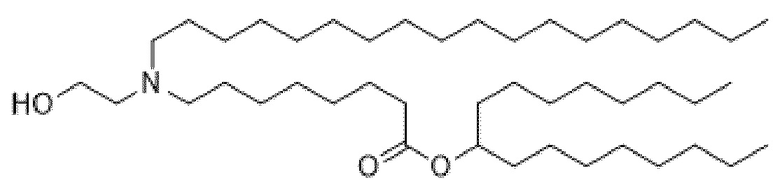
Химическая формула: C45H91NO3
Молекулярная масса: 694,23
[0036] Соединение 1 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,86 мин. MС (ИЭР): m/z (MH+) 694,93 для C45H91NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 1H); 3,77-3,47 (уш. м, 2H); 2,78-2,37 (уш. м, 5H); 2,28 (т, 2H); 1,73-1,40 (уш. м, 10H); 1,38-1,18 (уш. м, 62H); 0,88 (м, 9H).
D. Соединение 3: Гептадекан-9-ил-8-((2-гидроксиэтил)(нонил)амино)октаноат
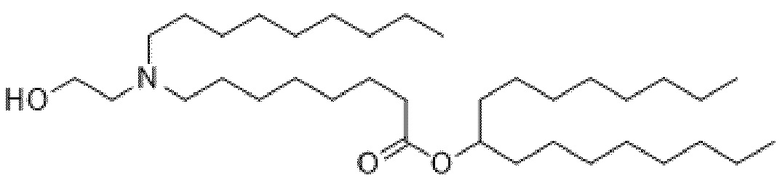
Химическая формула: C36H73NO3
Молекулярная масса: 567,98
[0037] Соединение 3 синтезировали согласно общей методике и иллюстративному примеру методики 1 и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,36 мин. MС (ИЭР): m/z (MH+) 568,80 для C36H73NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 3,72-3,45 (уш. м, 2H); 2,79-2,34 (уш. м, 5H); 2,28 (т, 2H); 1,70-1,38 (м, 10H); 1,38-1,16 (уш. м, 44H); 0,88 (м, 9H).
E. Соединение 4: Гептадекан-9-ил-8-((2-гидроксиэтил)(октил)амино)октаноат
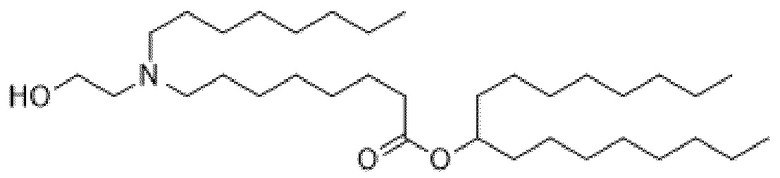
Химическая формула: C35H71NO3
Молекулярная масса: 553,96
[0038] Соединение 4 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,99 мин. MС (ИЭР): m/z (MH+) 554,777 для C35H71NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 3,71 (уш. с, 2H); 2,70 (уш. с, 5H); 2,26 (т, 2H); 1,48-1,59 (br. m., 10H); 1,24 (м, 42H); 0,86 (т, 9H).
F. Соединение 5: Гептадекан-9-ил-8-(гексил(2-гидроксиэтил)амино)октаноат
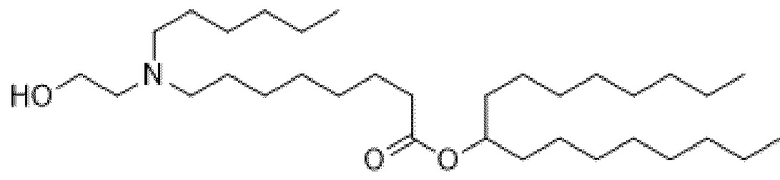
Химическая формула: C33H67NO3
Молекулярная масса: 525,90
[0039] Соединение 5 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,10 мин. MС (ИЭР): m/z (MH+) 526,73 для C33H67NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 3,67-3,48 (уш. м, 2H); 2,74-2,39 (уш. м, 5H); 2,28 (т, 2H); 1,68-1,39 (уш. м, 10H); 1,38-1,16 (уш. м, 38H); 0,88 (м, 9H).
G. Соединение 6: Гептадекан-9-ил-8-((2-гидроксиэтил)((9Z,12Z)-октадека-9,12-диен-1-ил)амино)октаноат
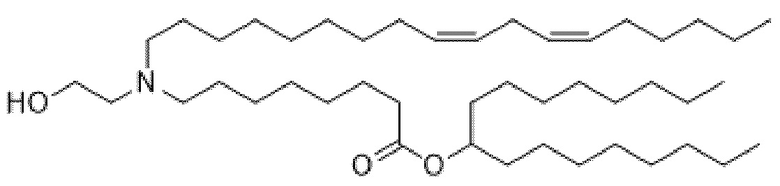
Химическая формула: C45H87NO3
Молекулярная масса: 690,20
[0040] Соединение 6 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,77 мин. MС (ИЭР): m/z (MH+) 690,84 для C45H87NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,37 (м, 4H); 4,86 (уш. м, 1H); 3,53 (br. m; 2H); 2,78 (уш. м, 2H); 2,58 (уш. м, 2H); 2,45 (уш. м, 4H); 2,28 (м, 2H); 2,05 (м, 4H); 1,68-1,15 (уш. м, 57H); 0,89 (м, 9H).
H. Соединение 7: Гептадекан-9-ил-8-((3-гидроксипропил)(нонил)амино)октаноат
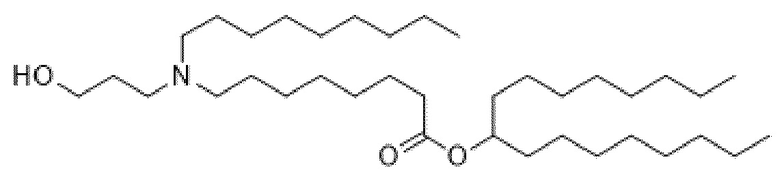
Химическая формула: C37H75NO3
Молекулярная масса: 582,01
[0041] Соединение 7 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,24 мин. MС (ИЭР): m/z (MH+) 582,987 для C37H75NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,84 (п, 1H); 3,76 (т, 2H); 2,42-2,66 (уш. с, 5H); 2,25 (т, 2H); 1,47-1,68 (уш. м, 12H); 1,24 (м, 42H); 0,86 (т, 9H).
I. Соединение 8: Гептадекан-9-ил-8-((3-(1H-имидазол-1-ил)пропил)(нонил)амино)октаноат
Стадия 1: Гептадекан-9-ил-8-((3-хлорпропил)(нонил)амино)октаноат
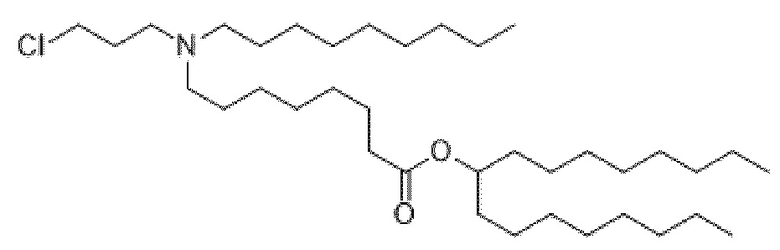
Химическая формула: C37H74ClNO2
Молекулярная масса: 600,45
[0042] К 0°C раствору гептадекан-9-ил-8-((3-гидроксипропил)(нонил)амино)октаноата (0,53 г, 0,91 ммоль) в 4 мл ДХМ прибавили мезилхлорид (0,070 мл, 0,91 ммоль) с последующим прибавлением триэтиламина (0,13 мл, 0,91 ммоль). Реакционную смесь оставили медленно нагреваться до комн. темп. и перемешивали в течение ночи. Реакционную смесь погасили прибавлением воды (~10 мл). Смесь трижды экстрагировали ДХМ и экстрагированные органические вещества промывали насыщенным водным раствором хлорида натрия, сушили над MgSO4, отфильтровали и концентрировали в вакууме. Сырое масло очищали с помощью хроматографии на силикагеле с получением гептадекан-9-ил-8-((3-хлорпропил)(нонил)амино)октаноата (0,23 г, 42%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,84 (п, 1H); 3,58 (т, 2H); 2,51 (уш. с, 2H); 2,35 (уш. с, 2H); 2,26 (2, 2H); 1,86 (уш. с, 2H); 1,40-1,60 (уш. м, 12H); 1,24 (уш. м, 42H); 0,86 (т, 9H).
Стадия 2: Гептадекан-9-ил-8-((3-(1H-имидазол-1-ил)пропил)(нонил)амино)октаноат
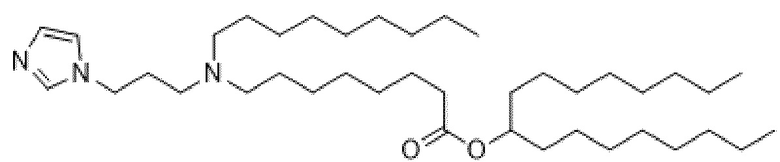
Химическая формула: C40H77N3O2
Молекулярная масса: 632,08
[0043] В круглодонной колбе гептадекан-9-ил-8-((3-хлорпропил)(нонил)амино)октаноат (50 мг, 0,083 ммоль) смешали с имидазолом (17 мг, 0,25 ммоль), K2CO3 (35 мг, 0,25 ммоль) в MeCN (0,5 мл). Колбу оснастили холодильником и поместили в нагретый до 82°C нагреватель колб и оставили перемешиваться в течение 24 ч. Через указанное время реакционную смесь оставили охлаждаться до комн. темп., отфильтровали и фильтрат концентрировали в вакууме. Сырое масло очищали с помощью хроматографии на силикагеле (0-100% [ДХМ, 20% MeOH, 1% NH4OH]/MeOH) с получением желаемого продукта в виде бесцветного масла (39 мг, 74%). СВЭЖХ/ДСИО: RT=2,92 мин. MС (ИЭР): m/z (MH+) 633,994 для C40H77N3O2. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,46 (с, 1H); 7,05 (с, 1H); 6,91 (с, 1H); 4,84 (дт, 1H); 4,02 (уш. с, 2H); 2,47 (уш. с, 4H); 2,26 (т, 2H); 2,00 (уш. с, 2H); 1,47-1,59 (уш. м, 10H); 1,24 (уш. м, 44H); 0,86 (т, 9H).
J. Соединение 9: Гептадекан-9-ил-8-((2-ацетоксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
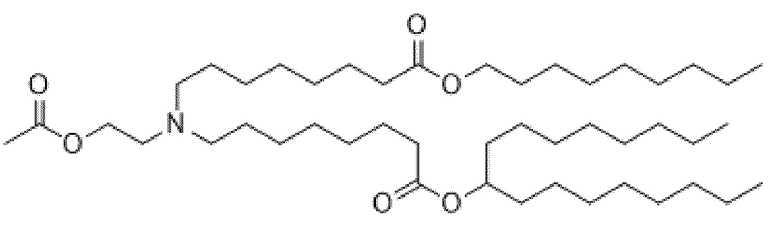
Химическая формула: C46H89NO6
Молекулярная масса: 752,22
[0044] К раствору гептадекан-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (100 мг, 0,14 ммоль) и уксусной кислоты (8 мг, 0,13 ммоль) в дихлорметане (1 мл) прибавили N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид (31 мг, 0,16 ммоль), N, N-диизопропилэтиламин (73 мг, 0,56 ммоль) и DMAP (3 мг, 0,02 ммоль). Реакционную смесь оставили перемешиваться при комн. темп. в течение 18 ч. Реакционную смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, и сушили над MgSO4. Органический слой отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с выходом гептадекан-9-ил-8-((2-ацетоксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (63 мг, 0,08 ммоль). СВЭЖХ/ДСИО: RT=3,63 мин. MС (ИЭР): m/z (MH+) 753,07 для C46H89NO6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87 (п, 1H); 4,17-3,99 (м, 4H); 2,67 (м, 2H); 2,43 (м, 3H); 2,29 (м, 4H); 2,05 (с, 3H); 1,71-1,17 (уш. м, 63H); 0,88 (м, 9H).
K. Соединение 10: Гептадекан-9-ил-8-((2-гидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
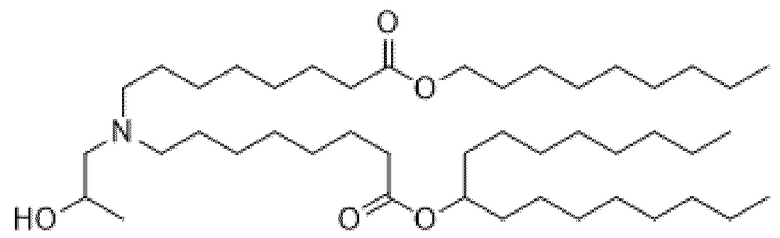
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[0045] Соединение 10 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,73 мин. MС (ИЭР): m/z (MH+) 725,10 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,80-3,54 (уш. м, 1H); 2,61-2,13 (уш. м, 9H); 1,69-1,03 (уш. м, 67H); 0,88 (м, 9H).
L. Соединение 11: Гептадекан-9-ил-(R)-8-((2-гидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
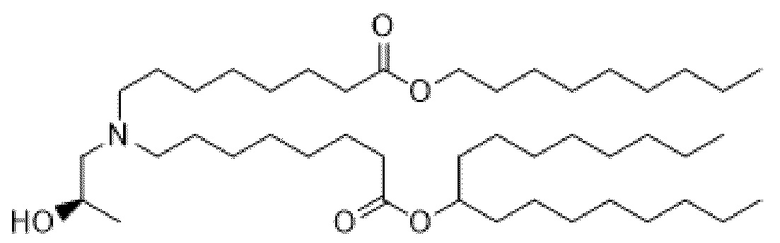
Химическая формула: C45H89NO5
Молекулярная масса: 724,21
[0046] Соединение 11 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=5,21 мин. MС (ИЭР): m/z (MH+) 725,02 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,72 (уш. м, 1H); 2,65-2,10 (уш. м, 8H); 1,71-0,99 (уш. м, 68H); 0,88 (м, 9H).
M. Соединение 12: Гептадекан-9-ил-(S)-8-((2-гидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
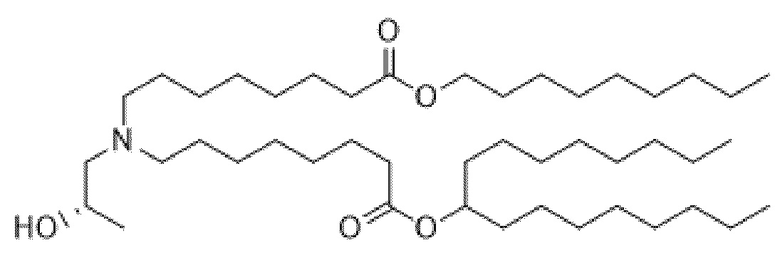
Химическая формула: C45H89NO5
Молекулярная масса: 724,21
[0047] Соединение 12 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=5,30 мин. MС (ИЭР): m/z (MH+) 725,10 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,71 (уш. м, 1H); 2,64-2,10 (уш. м, 8H); 1,71-1,03 (уш. м, 68H); 0,88 (м, 9H).
N. Соединение 13: Гептадекан-9-ил-8-((2-гидроксибутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
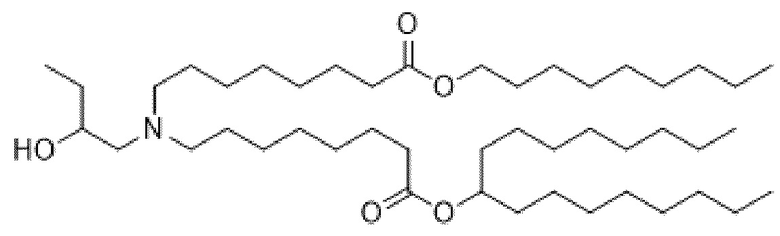
Химическая формула: C46H91NO5
Молекулярная масса: 738,24
[0048] Соединение 13 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,89 мин. MС (ИЭР): m/z (MH+) 739,21 для C46H91NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,58-3,38 (уш. м, 1H); 2,65-2,15 (уш. м, 9H); 1,72-1,12 (уш. м, 66H); 0,98 (т, 3H); 0,88 (м, 9H).
O. Соединение 14: Гептадекан-9-ил-8-((2-(диметиламино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
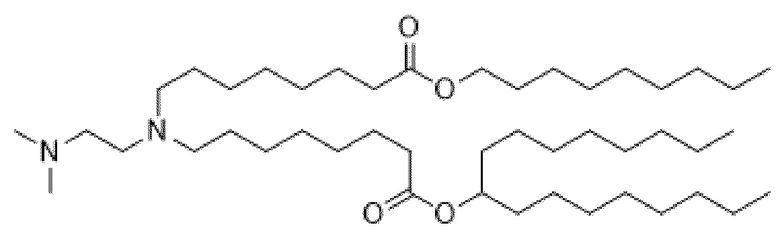
Химическая формула: C46H92N2O4
Молекулярная масса: 737,252
[0049] Соединение 14 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,51 мин. MС (ИЭР): m/z (MH+) 738,23 для C46H92N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,84 (п, 1H); 4,04 (т, 2H); 2,95 (м, 2H); 2,78 (м, 6H); 2,44 (с, 6H); 2,28 (м, 4H); 1,70-1,41 (уш. м, 14H); 1,41-1,14 (уш. м, 48H); 0,87 (м, 9H).
P. Соединение 15: Гептадекан-9-ил-8-((2-метоксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
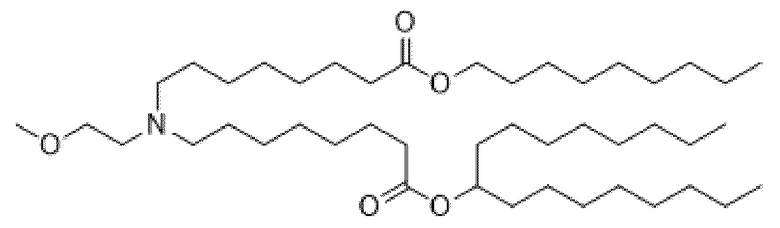
Химическая формула: C45H89NO5
Молекулярная масса: 724,21
[0050] Соединение 15 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,90 мин. MС (ИЭР): m/z (MH+) 725,19 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,43 (м, 2H); 3,34 (с, 3H); 2,61 (м, 2H); 2,43 (м, 3H); 2,29 (м, 4H); 1,70-1,15 (уш. м, 63H); 0,88 (м, 9H).
Q. Соединение 16: Гептадекан-9-ил-8-((3-метоксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
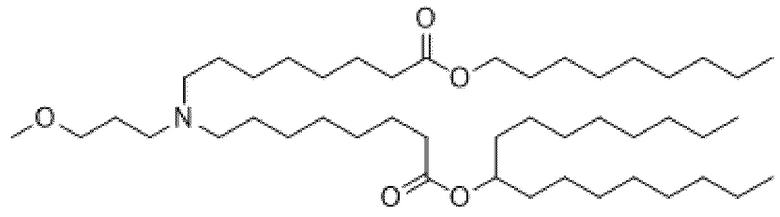
Химическая формула: C46H91NO5
Молекулярная масса: 738,236
[0051] Соединение 16 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,90 мин. MС (ИЭР): m/z (MH+) 739,13 для C46H91NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,42 (м, 2H); 3,35 (с, 3H); 2,55-2,21 (м, 9H); 1,81-1,18 (уш. м, 65H); 0,88 (м, 9H).
R. Соединение 17: Гептадекан-9-ил-8-((2-(2-(диметиламино)этокси)этил)-(8-(нонилокси)-8-оксооктил)амино)октаноат
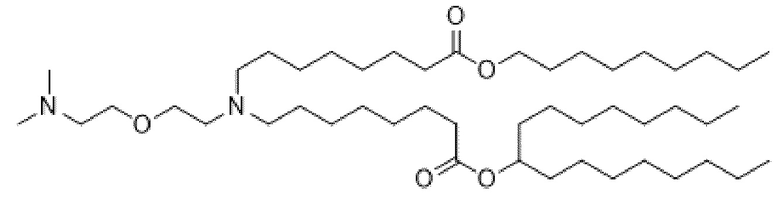
Химическая формула: C48H96N2O5
Молекулярная масса: 781,305
[0052] Соединение 17 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,72 мин. MС (ИЭР): m/z (MH+) 782,27 для C48H96N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (п, 1H); 4,08 (т, 2H); 3,57 (м, 4H); 2,72 (м, 2H); 2,52 (м, 5H); 2,38-2,13 (уш. м, 12H); 1,73-1,19 (уш. м, 61H); 0,90 (м, 9H).
S. Соединение 18: Гептадекан-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C44H87NO5
Молекулярная масса: 710,18
[0053] Соединение 18 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше, или согласно схеме ниже:
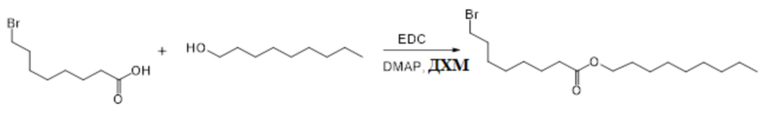

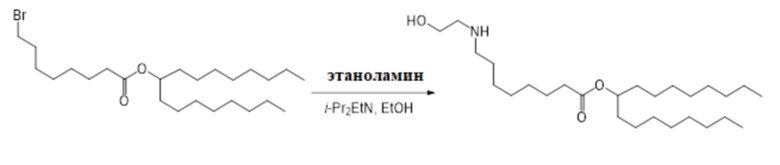
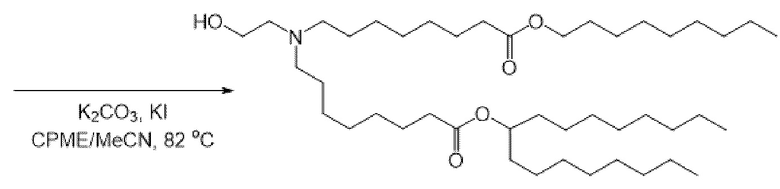
[0054] СВЭЖХ/ДСИО: RT=3,59 мин. MС (ИЭР): m/z (MH+) 710,89 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 1H); 4,05 (т, 2H); 3,53 (уш. м, 2H); 2,83-2,36 (уш. м, 5H); 2,29 (м, 4H); 0,96-1,71 (м, 64H); 0,88 (м, 9H).
T. Соединение 19: Гептадекан-9-ил-8-((3-гидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
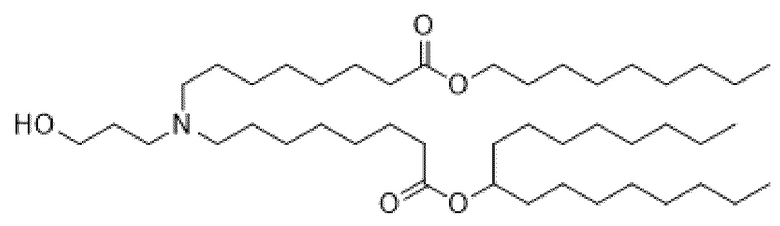
Химическая формула: C45H89NO5
Молекулярная масса: 724,21
[0055] Соединение 19 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=4,51 мин. MС (ИЭР): m/z (MH+) 725,19 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,80 (м, 2H); 2,92-2,36 (уш. м, 5H); 2,29 (м, 4H); 1,89-1,42 (уш. м, 16H); 1,42-1,02 (уш. м, 50H); 0,88 (м, 9H).
U. Соединение 20: Гептадекан-9-ил-8-((4-гидроксибутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
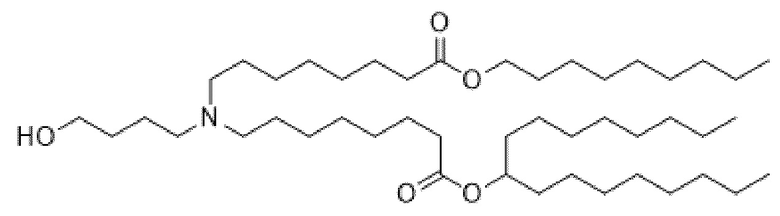
Химическая формула: C46H91NO5
Молекулярная масса: 738,24
[0056] Соединение 20 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,84 мин. MС (ИЭР): m/z (MH+) 739,21 для C46H91NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,77-3,45 (уш. м, 2H); 2,63-2,20 (уш. м, 8H); 1,82-1,40 (уш. м, 18H); 1,40-1,15 (уш. м, 51H); 0,88 (м, 9H).
V. Соединение 21: Гептадекан-9-ил-8-((2-цианоэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
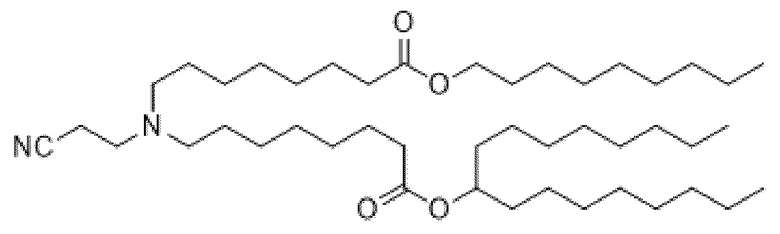
Химическая формула: C45H86N2O4
Молекулярная масса: 719,19
[0057] Соединение 21 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=4,04 мин. MС (ИЭР): m/z (MH+) 720,18 для C45H86N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (п, 1H); 4,07 (т, 2H); 2,81 (м, 2H); 2,44 (м, 5H); 2,30 (м, 4H); 1,73-1,18 (уш. м, 63H); 0,89 (м, 9H).
W. Соединение 22: Гептадекан-9-ил-8-((2-гидроксициклогексил)(8-(нонилокси)-8-оксооктил)амино)октаноат
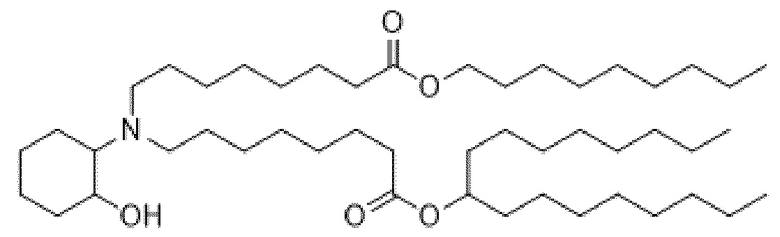
Химическая формула: C48H93NO5
Молекулярная масса: 764,27
[0058] Соединение 22 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=4,54 мин. MС (ИЭР): m/z (MH+) 765,21 для C48H93NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 2,89-2,34 (уш. м, 4H); 2,28 (м, 4H); 2,00 (м, 1H); 1,86-0,99 (уш. м, 72H); 0,88 (м, 9H).
X. Соединение 23: Гептадекан-9-ил-10-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)деканоат
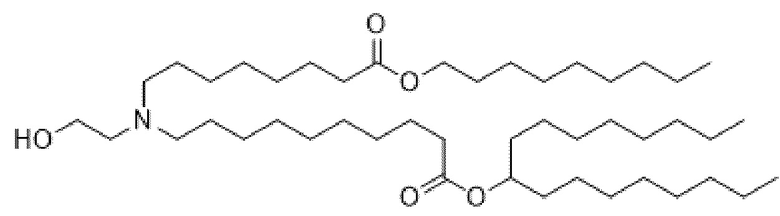
Химическая формула: C46H91NO5
Молекулярная масса: 738,24
[0059] Соединение 23 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,75 мин. MС (ИЭР): m/z (MH+) 739,13 для C46H91NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 1H); 4,05 (м, 2H); 3,72-3,46 (уш. м, 2H); 2,81-2,35 (уш. м, 5H); 2,29 (м, 4H); 1,71-1,40 (уш. м, 13H); 1,40-1,15 (уш. м, 55H); 0,88 (м, 9H).
Y. Соединение 24: Гептадекан-9-ил-(Z)-8_((2-гидроксиэтил) (8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат
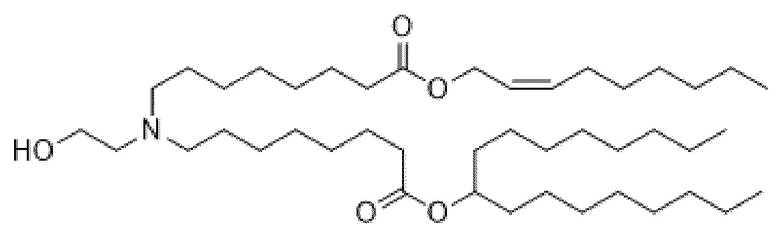
Химическая формула: C44H85NO5
Молекулярная масса: 708,17
[0060] Соединение 24 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,54 мин. MС (ИЭР): m/z (MH+) 708,95 для C44H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,74-5,44 (уш. м, 2H); 4,86 (м, 1H); 4,62 (м, 2H); 3,71-3,40 (уш. м, 2H); 2,81-2,37 (уш. м, 5H); 2,29 (м, 4H); 2,09 (м, 2H); 1,70-1,14 (уш. м, 58H); 0,88 (м, 9H).
Z. Соединение 25: Гептадекан-9-ил-8-((2-гидроксиэтил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
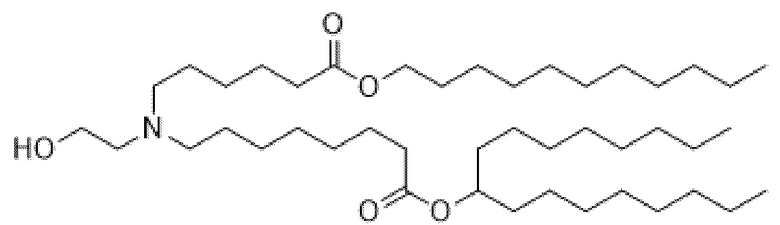
Химическая формула: C44H87NO5
Молекулярная масса: 710,182
[0061] Соединение 25 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,66 мин. MС (ИЭР): m/z (MH+) 711,00 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 1H); 4,05 (т, 2H); 3,68-3,46 (уш. м, 2H); 2,77-2,37 (уш. м, 5H); 2,29 (м, 4H); 1,74-1,41 (уш. м, 14H); 1,39-1,18 (м, 50H); 0,88 (м, 9H).
AA. Соединение 26: Гептадекан-9-ил-8-((2-гидроксиэтил)(4-(нонилокси)-4-оксобутил)амино)октаноат
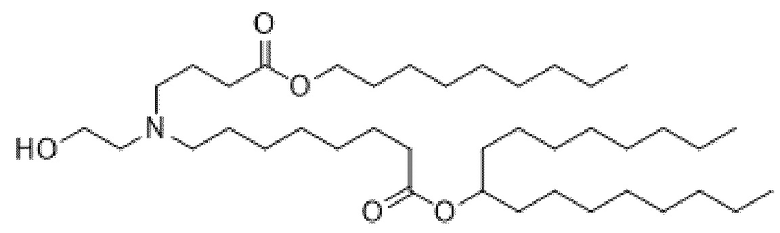
Химическая формула: C40H79NO5
Молекулярная масса: 654,07
[0062] Соединение 26 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=4,29 мин. MС (ИЭР): m/z (MH+) 655,07 для C40H79NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,06 (т, 2H); 3,79 (уш. м, 2H); 2,91-2,20 (уш. м, 10H); 1,98-1,03 (уш. м, 55H); 0,88 (м, 9H).
AB. Соединение 27: Нонил-8-((6-(гептадекан-9-илокси)-6-оксогексил)(2-гидроксиэтил)амино)октаноат
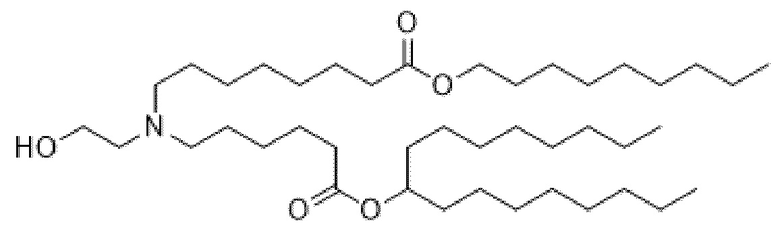
Химическая формула: C42H83NO5
Молекулярная масса: 682,13
[0063] Соединение 27 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,57 мин. MС (ИЭР): m/z (MH+) 683,12 для C42H83NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 1H); 4,05 (м, 2H); 3,70-3,45 (уш. м, 2H); 2,78-2,35 (уш. м, 5H); 2,29 (м, 4H); 1,73-1,41 (м, 13H); 1,41-1,16 (м, 47H); 0,88 (м, 9H).
AC. Соединение 28: Гептадекан-9-ил-8-((8-((2-гексилциклопропил)метокси)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
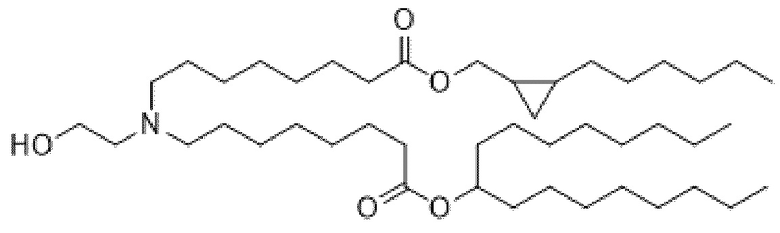
Химическая формула: C45H87NO5
Молекулярная масса: 722,19
[0064] Соединение 28 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше, используя промежуточное соединение C. СВЭЖХ/ДСИО: RT=5,17 мин. MС (ИЭР): m/z (MH+) 722,97 для C45H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,17 (м, 1H); 3,93 (м, 1H); 3,61 (уш. м, 2H); 2,97-2,37 (уш. м, 6H); 2,35-2,21 (м, 4H); 1,74-0,97 (уш. м, 60H); 0,94-0,79 (м, 10H); 0,74 (м, 1H); 0,01 (м, 1H).
AD. Соединение 29: Ди(гептадекан-9-ил) 8,8'-((2-гидроксиэтил)азандиил)диоктаноат

Химическая формула: C52H103NO5
Молекулярная масса: 822,40
[0065] Соединение 29 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,98 мин. MС (ИЭР): m/z (MH+) 823,19 для C52H103NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 2H); 3,72-3,44 (уш. м, 2H); 2,83- 2,34 (уш. м, 5H); 2,28 (м, 4H); 1,69-1,39 (уш. м, 16H); 1,39-1,16 (уш. м, 62H); 0,88 (м, 12H).
AE. Соединение 30: 7-((2-Гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат
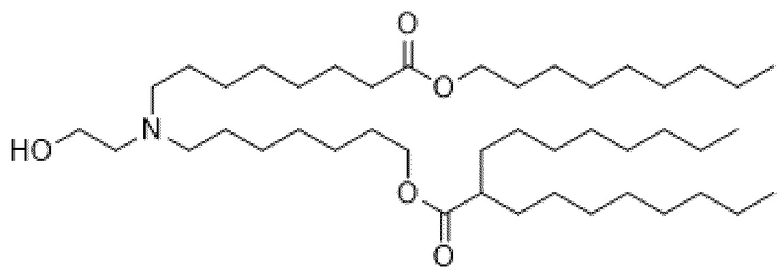
Химическая формула: C44H87NO5
Молекулярная масса: 710,18
[0066] Соединение 30 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше, используя промежуточное соединение B. СВЭЖХ/ДСИО: RT=3,55 мин. MС (ИЭР): m/z (MH+) 711,16 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,06 (м, 4H); 3,69-3,44 (уш. м, 2H); 2,71-2,39 (уш. м, 5H); 2,29 (м, 3H); 1,70-1,16 (уш. м, 64H); 0,88 (м, 9H).
AF. Соединение 31: гептадекан-9-ил-(Z)-8-((2-гидроксиэтил)(октадец-9-ен-1-ил)амино)октаноат

Химическая формула: C45H89NO3
Молекулярная масса: 692,21
[0067] Соединение 31 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,83 мин. MС (ИЭР): m/z (MH+) 693,20 для C45H89NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,37 (м, 2H); 4,89 (п, 1H); 3,58 (уш. м, 2H); 2,72-2,43 (уш. м, 5H); 2,30 (м, 2H), 2,05 (м, 4H); 1,71-1,03 (уш. м, 63H), 0,90 (м, 9H).
AG. Соединение 32: нонил-8-((2-гидроксиэтил)(8-оксо-8-(пентадекан-7-илокси)октил)амино)октаноат
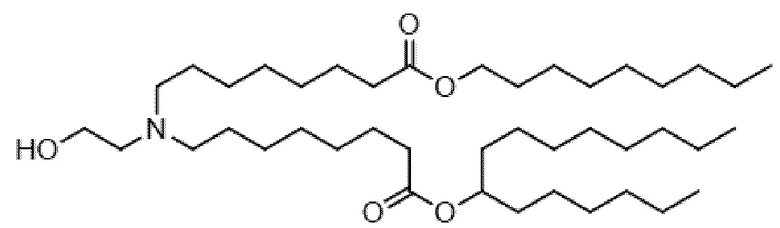
Химическая формула: C42H83NO5
Молекулярная масса: 682,13
[0068] Соединение 32 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,45 мин. MС (ИЭР): m/z (MH+) 683,20 для C42H83NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,60 (уш. м, 2H); 2,85-2,40 (уш. м, 5H); 2,31(м, 4H), 1,78-1,01 (м, 59H), 0,90 (м, 9H).
AH. Соединение 33: нонил-8-((2-гидроксиэтил)(8-оксо-8-(тетрадекан-6-илокси)октил)амино)октаноат
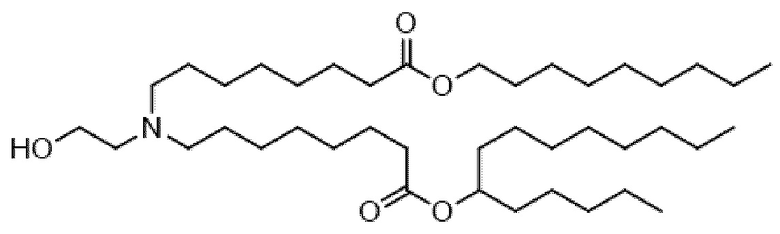
Химическая формула: C41H81NO5
Молекулярная масса: 668,10
[0069] Соединение 33 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,39 мин. MС (ИЭР): m/z (MH+) 669,09 для C41H81NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,84-3,54 (уш. м, 2H); 2,99-2,41 (уш. м, 5H); 2,31 (м, 4H), 1,76-1,02 (уш. м, 57H), 0,90 (м, 9H).
AI. Соединение 34: додекан-4-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
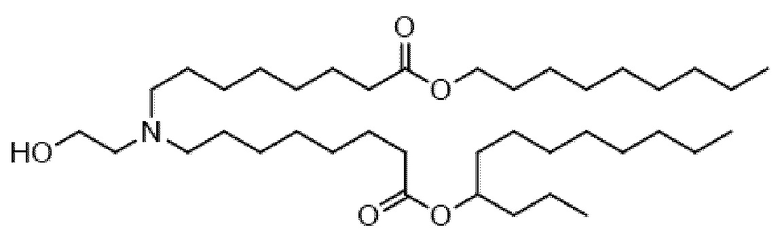
Химическая формула: C39H77NO5
Молекулярная масса: 640,05
[0070] Соединение 34 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,21 мин. MС (ИЭР): m/z (MH+) 641,05 для C39H77NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (п, 1H); 4,08 (т, 2H); 3,67 (уш. м, 2H); 3,03-2,44 (уш. м, 5H); 2,30 (м, 4H), 1,75-1,00 (уш. м, 53H), 0,90 (м, 9H).
AJ. Соединение 35: нонил-8-((2-гидроксиэтил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат
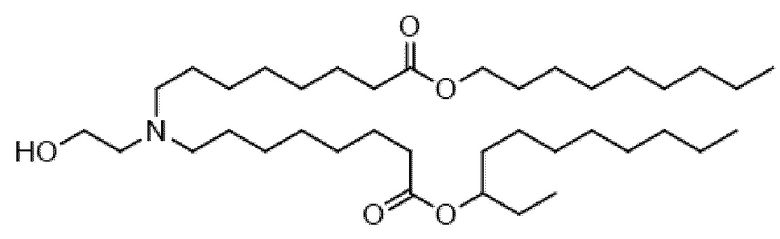
Химическая формула: C38H75NO5
Молекулярная масса: 626,02
[0071] Соединение 35 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,16 мин. MС (ИЭР): m/z (MH+) 627,11 для C38H75NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,83 (п, 1H); 4,08 (т, 2H); 3,63 (уш. м, 2H); 2,81-2,39 (уш. м, 5H); 2,31 (м, 4H), 1,74-1,01 (уш. м, 51H), 0,90 (м, 9H).
AK. Соединение 36: декан-2-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
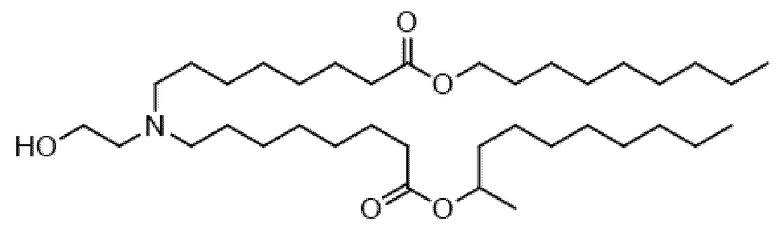
Химическая формула: C37H73NO5
Молекулярная масса: 611,99
[0072] Соединение 36 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,05 мин. MС (ИЭР): m/z (MH+) 613,00 для C37H73NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (п, 1H); 4,08 (т, 2H); 3,55 (м, 2H); 2,60 (м, 2H); 2,47 (м, 4H); 2,29 (м, 4H), 1,731-1,01 (м, 51H), 0,90 (м, 6H).
AL. Соединение 47: гептадекан-9-ил-8-((2-гидроксиэтил)(8-(2-октилциклопропил)октил)амино)октаноат
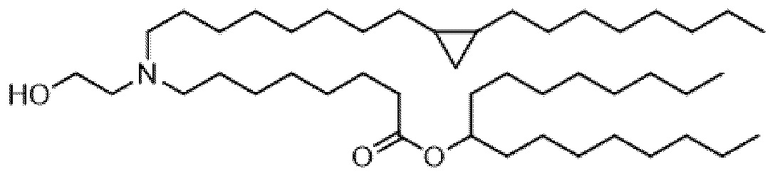
Химическая формула: C46H91NO3
Молекулярная масса: 706,24
[0073] Соединение 47 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,92 мин. MС (ИЭР): m/z (MH+) 707,39 для C46H91NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 3,56 (уш. м, 2H); 2,72-2,38 (уш. м, 5H); 2,28 (т, 2H); 1,70-1,02 (уш. м, 67H), 0,88 (м, 9H); 0,71-0,49 (м, 4H); -0,33 (м, 1H).
AM. Соединение 48: декан-2-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
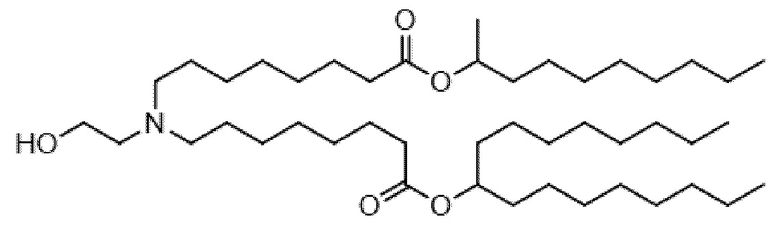
Химическая формула: C45H89NO5
Молекулярная масса: 724,21
[0074] Соединение 48 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,60 мин. MС (ИЭР): m/z (MH+) 725,10 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 2H); 3,59 (уш. м, 2H); 2,79-2,37 (уш. м, 5H); 2,29 (м, 4H); 1,74-1,13 (м, 66H); 0,90 (м, 9H).
AN. Соединение 49: гептадекан-9-ил-8-((2-гидроксиэтил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат

Химическая формула: C46H91NO5
Молекулярная масса: 738,24
[0075] Соединение 49 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,68 мин. MС (ИЭР): m/z (MH+) 739,21 для C46H91NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 2H); 3,56 (уш. м, 2H); 2,68-2,39 (уш. м, 5H); 2,30 (м, 4H); 1,71-1,19 (м, 66H); 0,90 (м, 12H).
AO. Соединение 50: додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил) амино)октаноат
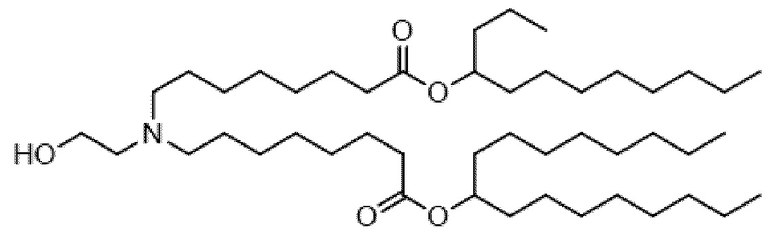
Химическая формула: C47H93NO5
Молекулярная масса: 752,26
[0076] Соединение 50 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,73 мин. MС (ИЭР): m/z (MH+) 753,23 для C47H93NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 2H); 3,60 (уш. м, 2H); 2,75-2,43 (уш. м, 5H); 2,30 (м, 4H); 1,71-1,44 (м, 16H); 1,28 (м, 51H); 0,90 (м, 12H).
AP. Соединение 51: гептадекан-9-ил-8-((4-бутокси-4-оксобутил)(2-гидроксиэтил)амино)октаноат
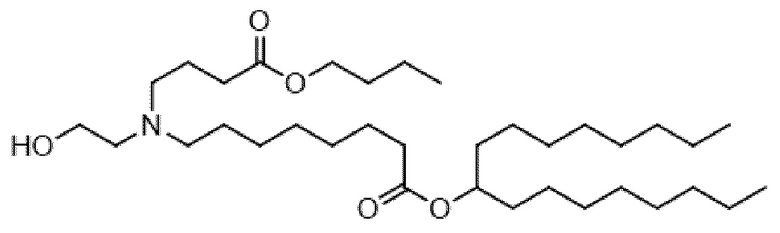
Химическая формула: C35H69NO5
Молекулярная масса: 583,94
[0077] Соединение 51 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,05 мин. MС (ИЭР): m/z (MH+) 584,87 для C35H69NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,10 (т, 2H); 3,61 (уш. м, 2H); 2,81-2,21 (уш. м, 9H); 1,87(уш. м, 2H), 1,70-1,04 (м, 43H), 0,98-0,82 (м, 9H).
AQ. Соединение 52: гептадекан-9-ил-8-((2-гидроксиэтил)(4-оксо-4-(пентилокси)бутил)амино)октаноат

Химическая формула: C36H71NO5
Молекулярная масса: 597,97
[0078] Соединение 52 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,11 мин. MС (ИЭР): m/z (MH+) 598,90 для C36H71NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,09 (т, 2H); 3,61 (уш. м, 2H); 2,89-2,22 (уш. м, 9H); 1,87(уш. м, 2H), 1,73-1,43 (м, 11H), 1,28 (м, 34H); 0,90 (м, 9H).
AR. Соединение 53: гептадекан-9-ил-8-((4-(гексилокси)-4-оксобутил)(2-гидроксиэтил)амино)октаноат
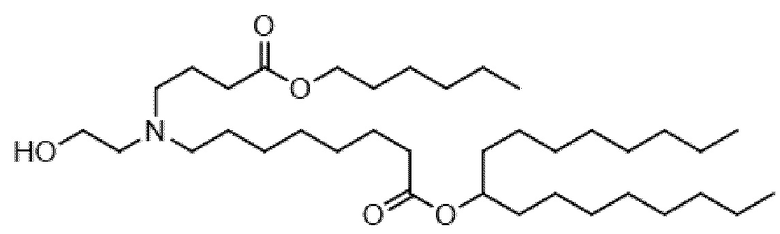
Химическая формула: C37H73NO5
Молекулярная масса: 611,99
[0079] Соединение 53 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,22 мин. MС (ИЭР): m/z (MH+) 612,92 для C37H73NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,06 (т, 2H); 3,55 (уш. м, 2H); 2,68-2,38 (уш. м, 5H); 2,28 (м, 4H); 1,79 (уш. м, 2H); 1,71-0,96 (м, 48H); 0,88 (м, 9H).
AS. Соединение 54: гептадекан-9-ил-8-((4-(гептилокси)-4-оксобутил)(2-гидроксиэтил)амино)октаноат
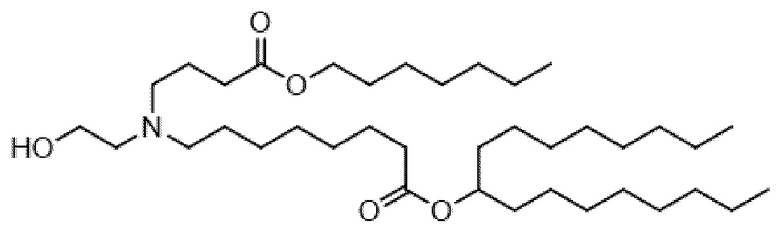
Химическая формула: C38H75NO5
Молекулярная масса: 626,02
[0080] Соединение 54 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,28 мин. MС (ИЭР): m/z (MH+) 626,94 для C38H75NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,09 (т, 2H); 3,60 (уш. м, 2H); 2,77-2,42 (уш. м, 5H); 2,32 (м, 4H); 1,84 (уш. м, 2H); 1,75-1,03 (м, 49H); 0,90 (м, 9H).
AT. Соединение 55: гептадекан-9-ил-8-((4-((2-гексилциклопропил)метокси)-4-оксобутил)(2-гидроксиэтил)амино)октаноат

Химическая формула: C41H79NO5
Молекулярная масса: 666,09
[0081] Соединение 55 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,37 мин. MС (ИЭР): m/z (MH+) 667,04 для C41H79NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,83 (п, 1H); 4,15 (м, 1H); 3,95 (м, 1H); 3,53 (уш. м, 2H); 2,66-2,39 (уш. м, 5H); 2,34-2,19 (м, 4H); 1,78 (уш. м, 2H); 1,66-0,98 (м, 50H); 0,85 (м, 10H); 0,70 (м, 1H); 0,00 (м, 1H).
AU. Соединение 56: нонил-8-((2-гидроксиэтил)(8-оксо-8-(тридекан-7-илокси)октил)амино)октаноат
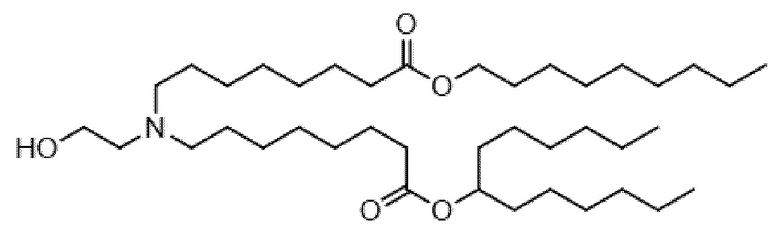
Химическая формула: C40H79NO5
Молекулярная масса: 654,07
[0082] Соединение 56 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,28 мин. MС (ИЭР): m/z (MH+) 654,99 для C40H79NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,60 (уш. м, 2H); 2,77-2,40 (уш. м, 5H); 2,30 (м, 4H); 1,78-0,99 (м, 55H); 0,90 (м, 9H).
AV. Соединение 57: нонан-5-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
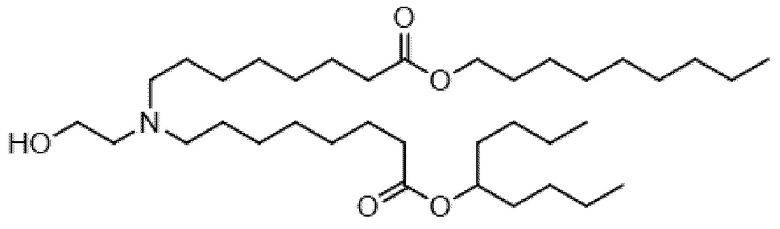
Химическая формула: C36H71NO5
Молекулярная масса: 597,97
[0083] Соединение 57 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,88 мин. MС (ИЭР): m/z (MH+) 598,98 для C36H71NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,59 (уш. м, 2H); 2,82-2,37 (уш. м, 5H); 2,31 (м, 4H); 1,73-1,03 (м, 47H); 0,91 (м, 9H).
AW. Соединение 58: гептан-4-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
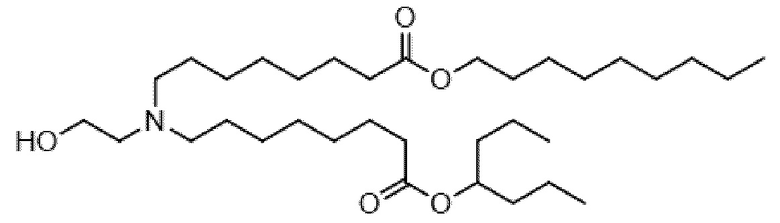
Химическая формула: C34H67NO5
Молекулярная масса: 569,91
[0084] Соединение 58 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,67 мин. MС (ИЭР): m/z (MH+) 570,93 для C34H67NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,93 (п, 1H); 4,08 (т, 2H); 3,57 (уш. м, 2H); 2,69-2,42 (уш. м, 5H); 2,30 (м, 4H); 1,72-1,04 (м, 43H); 0,93 (м, 9H).
AX. Соединение 59: нонил-8-((2-гидроксиэтил)(8-оксо-8-(пентан-3-илокси)октил)амино)октаноат
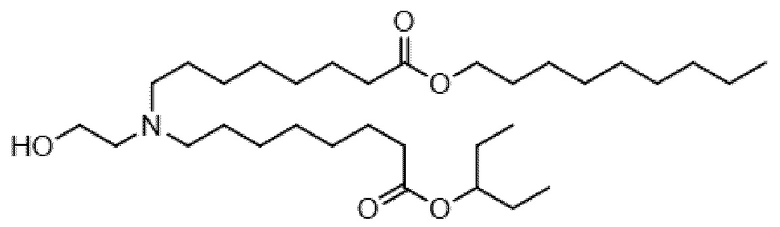
Химическая формула: C32H63NO5
Молекулярная масса: 541,86
[0085] Соединение 59 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,39 мин. MС (ИЭР): m/z (MH+) 542,80 для C32H63NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,78 (п, 1H); 4,08 (т, 2H); 3,57 (уш. м, 2H); 2,71-2,39 (уш. м, 5H); 2,31 (м, 4H); 1,77-1,05 (м, 39H); 0,90 (м, 9H).
AY. Соединение 60: (5Z,12Z)-Гептадека-5,12-диен-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
(5Z,12Z)-Гептадека-5,12-диен-9-ол
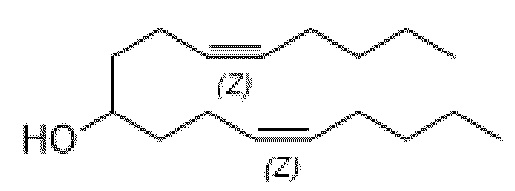
Химическая формула: C17H32O
Молекулярная масса: 252,44
[0086] К раствору (Z)-1-бромокт-3-ена (6,2 г, 32,4 ммоль) в ТГФ (45 мл) прибавили стружку Mg (0,843 г, 34,7 ммоль). Реакционную смесь нагревали до 45°C в течение 3 ч. Реакционную смесь охладили до 0°C и по каплям прибавили этилформиат (2,4 г, 32,4 ммоль) в ТГФ (5 мл). Реакционную смесь оставили нагреваться до комн. темп. и перемешивали в течение 30 мин. Реакционную смесь охладили до 0°C и погасили водой (15 мл) и 6N HCl (15 мл). Реакционную смесь перемешивали до тех пор, пока весь Mg не растворился. Прибавили воду (25 мл) и смесь экстрагировали смесью гексанов (3X25 мл). Объединенный органический слой промывали насыщенным водным раствором хлорида натрия, отделили, сушили над Na2SO4, отфильтровали и выпарили под вакуумом. Остаток растворили в EtOH (20 мл), прибавили раствор KOH в воде (1,76 г в 8 мл воды) и оставили перемешиваться в течение 15 мин. EtOH выпарили под вакуумом. Остаток разбавили водой (20 мл), подкислили 6N HCl (20 мл) и экстрагировали смесью гексанов (3x). Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, отделили, сушили над Na2SO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле с (0-5%) EtOAc в смеси гексанов с получением (5Z,12Z)-гептадека-5,12-диен-9-ола (2,3 г, 9,1 ммоль, 28%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,41 (м, 4); 3,66 (м, 1H); 2,13 (м, 8H); 1,51 (м, 5H); 1,36 (м, 8H); 0,92 (м, 6H).
(5Z,12Z)-Гептадека-5,12-диен-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C44H83NO5
Молекулярная масса: 706,15
[0087] Соединение 60 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,36 мин. MС (ИЭР): m/z (MH+) 707,10 для C44H83NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,37 (м, 4H); 4,92 (п, 1H); 4,08 (т, 2H); 3,57 (уш. м, 2H); 2,73-2,38 (уш. м, 5H); 2,31 (м, 4H); 2,04 (м, 8H); 1,73-1,01 (м, 47H); 0,92 (м, 9H).
AZ. Соединение 61: (5Z,12Z)-гептадека-5,12-диен-9-ил-8-((2-гидроксиэтил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат

Химическая формула: C44H83NO5
Молекулярная масса: 706,15
[0088] Соединение 61 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,39 мин. MС (ИЭР): m/z (MH+) 707,10 для C44H83NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,37 (м, 4H); 4,92 (п, 1H); 4,08 (т, 2H); 3,58 (уш. м, 2H); 2,70-2,41 (уш. м, 5H); 2,32 (м, 4H); 2,04 (м, 8H); 1,77-1,03 (м, 47H); 0,92 (м, 9H).
BA. Соединение 65: 1-Циклопропилнонил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
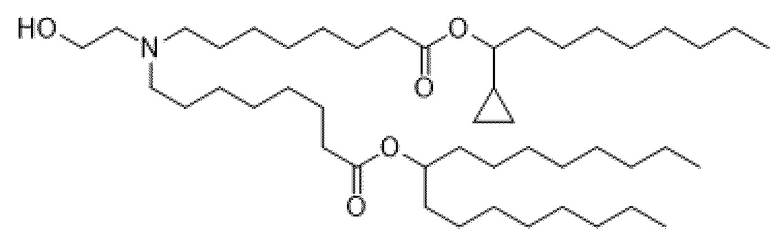
Химическая формула: C47H91NO5
Молекулярная масса: 750,247
[0089] Соединение 65 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,72 мин. MС (ИЭР): m/z (MH+) 750,9 для C47H91NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,28 (м, 1H); 3,54 (м, 2H); 2,59 (м, 2H); 2,46 (м, 4H); 2,29 (м, 4H), 1,73-1,18 (м, 61H); 0,90 (м, 10H); 0,62-0,33 (м, 3H); 0,28 (м, 1H).
BB. Соединение 66: Гептадекан-9-ил-8-((2-гидроксиэтил)(8-оксо-8-((4-пентилциклогексил)окси)октил)амино)октаноат
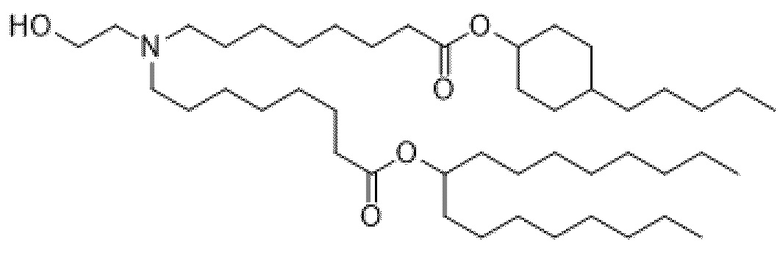
Химическая формула: C46H89NO5
Молекулярная масса: 736,220
[0090] Соединение 66 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,72 мин. MС (ИЭР): m/z (MH+) 736,9 для C46H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,00 (м, 0,5H); 4,89 (м, 1H); 4,68 (м, 0,6H); 3,56 (м, 2H), 2,61 (уш. м, 2H); 2,48 (м, 4H); 2,30 (м, 4H); 1,98 (м, 1H); 1,82 (м, 2H); 1,73-1,14 (м, 61H); 1,04 (м, 1H); 0,90 (м, 9H).
BC. Соединение 67: Гептадекан-9-ил-8-((2-гидроксиэтил)(4-оксо-4-((4-пентилциклогексил)окси)бутил)амино)октаноат
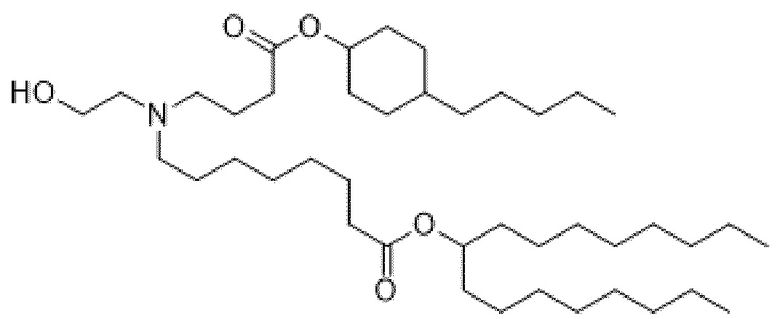
Химическая формула: C42H81NO5
Молекулярная масса: 680,112
[0091] Соединение 67 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,56 мин. MС (ИЭР): m/z (MH+) 680,8 для C42H81NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,01 (м, 0,4H); 4,89 (м, 1H); 4,68 (м, 0,6H); 3,59 (м, 2H), 2,72-2,43 (уш. м, 6H); 2,30 (м, 4H); 1,98 (м, 1H); 1,83 (м, 4H); 1,69-1,44 (м, 10H); 1,28 (м, 41H); 1,03 (м, 1H); 0,90 (м, 9H).
BD. Соединение 68: Гептадекан-9-ил-8-((2-гидроксиэтил)(6-оксо-6-((4-пентилциклогексил)окси)гексил)амино)октаноат

Химическая формула: C44H85NO5
Молекулярная масса: 708,166
[0092] Соединение 68 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,66 мин. MС (ИЭР): m/z (MH+) 708,9 для C44H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,00 (м, 0,5H); 4,89 (м, 1H); 4,68 (м, 0,6H); 3,55 (м, 2H), 2,66-2,39 (уш. м, 6H); 2,30 (м, 4H); 1,97 (м, 1H); 1,83 (м, 2H); 1,73-1,41 (м, 15H); 1,41-1,17 (м, 42H); 1,04 (м, 1H); 0,90 (м, 9H).
BE. Соединение 69: Гептадекан-9-ил-8-((2,3-дигидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
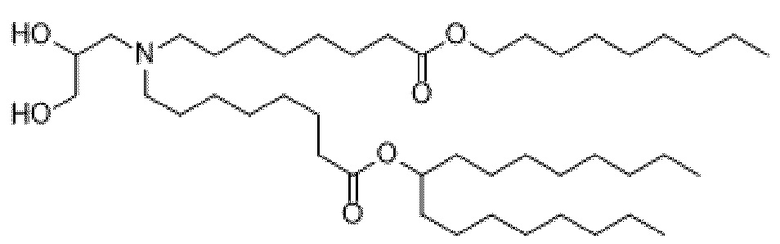
Химическая формула: C45H89NO6
Молекулярная масса: 740,21
[0093] Соединение 69 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,60 мин. MС (ИЭР): m/z (MH+) 741,0 для C45H89NO6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,76 (уш. м, 2H); 3,51 (м, 1H); 2,57 (м, 6H); 2,31 (м, 4H); 1,71-1,41 (м, 14H); 1,41- 1,12 (м, 48H); 0,90 (м, 9H).
BF. Соединение 70: Гептадекан-9-ил-8-((4-(декан-2-илокси)-4-оксобутил)(2-гидроксиэтил)амино)октаноат
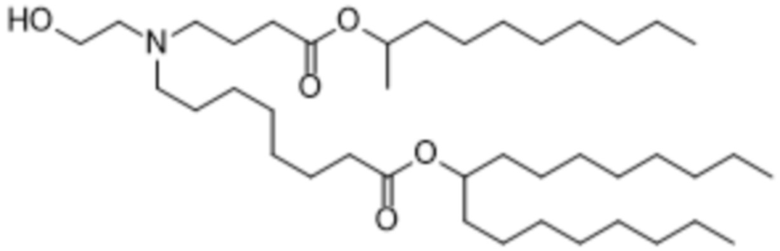
Химическая формула: C41H81NO5
Молекулярная масса: 667,61
[0094] Соединение 70 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,44 мин. MС (ИЭР): m/z (MH+) 668,9 для C41H81NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 2H); 3,57 (м, 2H); 2,71-2,40 (м, 5H); 2,30 (м, 4H), 1,80 (м, 2H); 1,71-1,40 (м, 11H); 1,39-1,05 (м, 45H); 0,90 (м, 9H).
BG. Соединение 71: Гептадекан-9-ил-8-((2-гидроксиэтил)(4-оксо-4-(тетрадекан-6-илокси)бутил)амино)октаноат
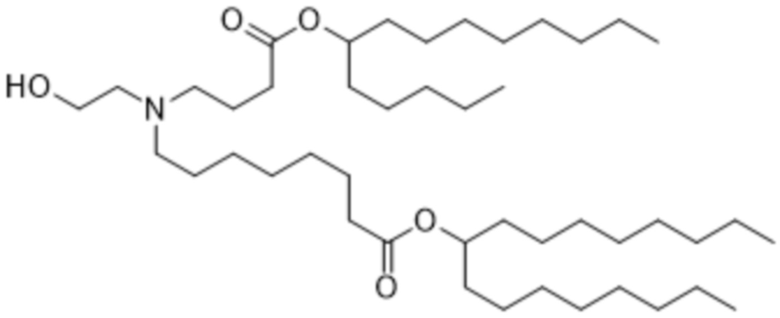
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[0095] Соединение 71 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,72 мин. MС (ИЭР): m/z (MH+) 724,9 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 2H); 3,56 (м, 2H); 2,70-2,41 (м, 6H); 2,33 (м, 4H), 1,80 (м, 2H); 1,69-1,41 (м, 13H); 1,28 (м, 48H); 0,90 (м, 12H).
BH. Соединение 72: Гептадекан-9-ил-8-((2-гидроксиэтил)(4-оксо-4-(ундекан-3-илокси)бутил)амино)октаноат
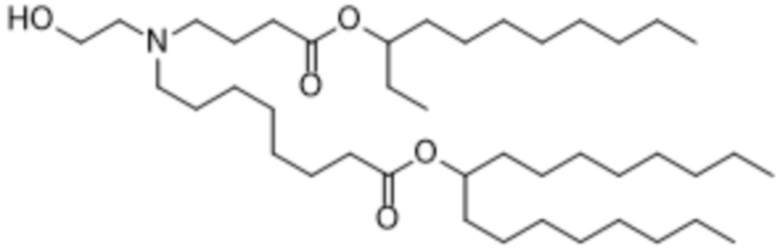
Химическая формула: C42H83NO5
Молекулярная масса: 682,13
[0096] Соединение 72 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,57 мин. MС (ИЭР): m/z (MH+) 683,0 для C42H83NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 2H); 3,58 (уш. м, 2H); 2,75-2,41 (уш. м, 5H); 2,30 (м, 4H), 1,81 (уш. м, 2H); 1,70-1,42 (м, 13H); 1,40-1,18 (м, 42H); 0,90 (м, 12H).
BI. Соединение 73: Гептадекан-9-ил-8-((2-гидроксиэтил)(4-оксо-4-(пентадекан-7-илокси)бутил)амино)октаноат
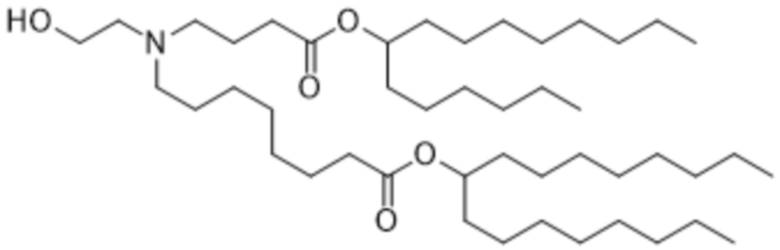
Химическая формула: C46H91NO5
Молекулярная масса: 738,236
[0097] Соединение 73 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,80 мин. MС (ИЭР): m/z (MH+) 739,09 для C46H91NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 2H); 3,59 (уш. м, 2H); 2,81-2,43 (уш. м, 6H); 2,31 (м, 4H); 1,83 (м, 2H); 1,69-1,42 (м, 12H); 1,28 (м, 50H); 0,90 (м, 12H).
BJ. Соединение 74: Гептадекан-9-ил-8-((4-(додекан-4-илокси)-4-оксобутил)(2-гидроксиэтил)амино)октаноат
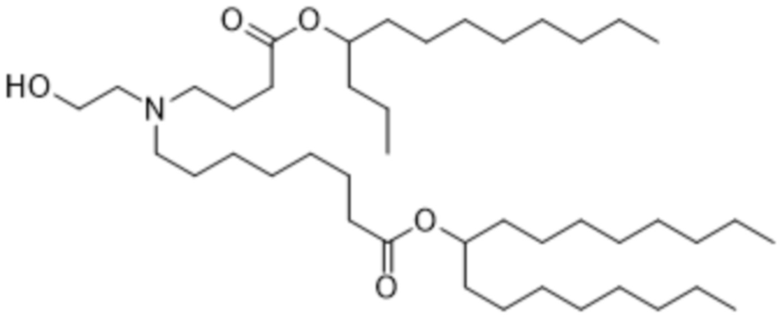
Химическая формула: C43H85NO5
Молекулярная масса: 696,155
[0098] Соединение 74 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,68 мин. MС (ИЭР): m/z (MH+) 696,9 для C43H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 2H); 3,56 (м, 2H); 2,70-2,41 (м, 6H); 2,30 (м, 4H), 1,80 (м, 2H); 1,70-1,40 (м, 12H); 1,28 (м, 44H); 0,90 (м, 12H).
BK. Соединение 75: Гептадекан-9-ил-8-((2-гидроксиэтил)(6-оксо-6-(ундекан-3-илокси)гексил)амино)октаноат
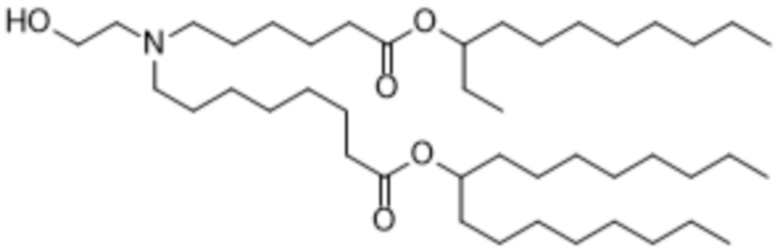
Химическая формула: C44H87NO5
Молекулярная масса: 710,18
[0099] Соединение 75 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,67 мин. MС (ИЭР): m/z (MH+) 711,1 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (м, 2H); 3,57 (м, 2H); 2,72-2,40 (уш. м, 5H); 2,30 (м, 4H); 1,70-1,42 (м, 16H); 1,28 (м, 45H); 0,90 (м, 12H).
BL. Соединение 79: Нонил-8-((2-гидроксиэтил)(8-оксо-8-((4-пентилциклогексил)окси)октил)амино)октаноат
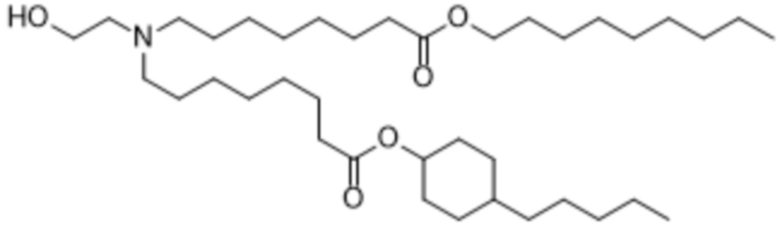
Химическая формула: C38H73NO5
Молекулярная масса: 624,00
[00100] Соединение 79 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,10 мин. MС (ИЭР): m/z (MH+) 624,8 для C38H73NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,00 (уш. м, 0,5H); 4,68 (м, 0,5H); 4,08 (т, 2H); 3,56 (м, 2H); 2,72-2,38 (м, 6H); 2,31(м, 4H), 1,97 (м, 1H); 1,82 (м, 2H); 1,73-0,95 (м, 48H), 0,90 (м, 6H).
BM. Соединение 80: [1,1'-Би(циклогексан)]-4-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
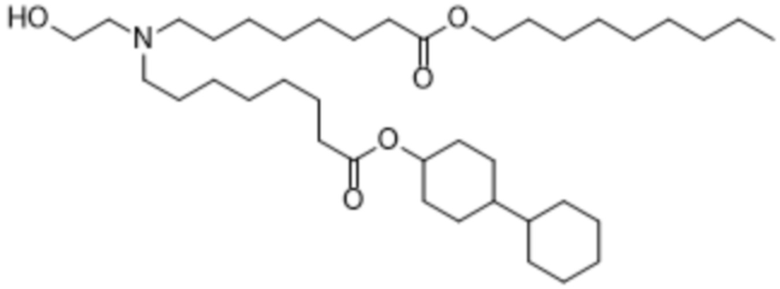
Химическая формула: C39H73NO5
Молекулярная масса: 636,02
[00101] Соединение 80 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,10 мин. MС (ИЭР): m/z (MH+) 636,9 для C39H73NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,01 (уш. м, 0,5H); 4,65 (м, 0,5H); 4,08 (т, 2H); 3,56 (м, 2H); 2,69-2,36 (м, 6H); 2,31(м, 4H); 2,07-0,84 (м, 57H).
BN. Соединение 81: Циклопентадецил 8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
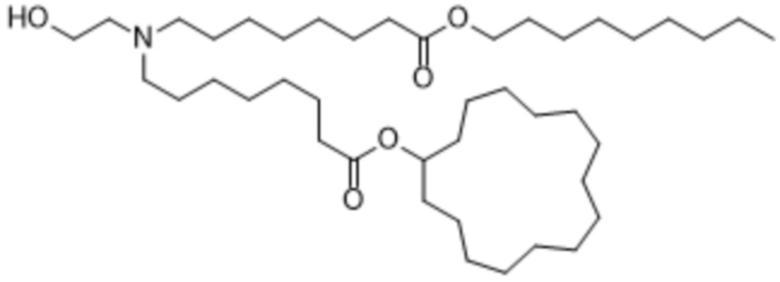
Химическая формула: C42H81NO5
Молекулярная масса: 680,11
[00102] Соединение 81 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,36 мин. MС (ИЭР): m/z (MH+) 681,0 для C42H81NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (п, 1H); 4,08 (т, 2H); 3,57 (уш. м, 2H); 2,74-2,39 (м, 6H); 2,30(м, 4H), 1,73-1,03 (м, 62H), 0,90 (м, 3H).
BO. Соединение 94: Гептадекан-9-ил)-8-(бензил(8-нонилокси)-8-оксооктил)амино)октаноат
Гептадекан-9-ил-8-(бензиламино)октаноат
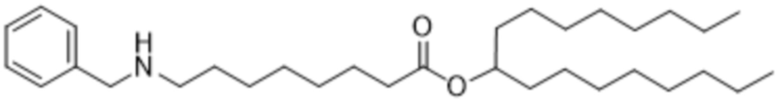
Химическая формула: C32H57NO2
Молекулярная масса: 487,81
[00103] Раствор гептадекан-9-ил-8-бромоктаноата (250 мг, 0,542 ммоль) в фенилметанамине (1,2 мл, 10,83 ммоль) оставили перемешиваться при комн. темп. в течение 6 ч. Реакционную смесь охладили до комн. темп. и растворители выпарили в вакууме. Остаток перенесли в этилацетат и промывали насыщенным водным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, сушили над Na2SO4 и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (20-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-(бензиламино)октаноата (200 мг, 0,41 ммоль,76%). СВЭЖХ/ДСИО: RT=2,87 мин. MС (ИЭР): m/z (MH+) 488,4 для C32H57NO2. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,35-7,25 (уш. м, 5H); 4,89 (п, 1H); 3,81 (с, 2H); 2,65 (т, 2H); 2,29 (т, 2H); 1,65-1,51 (уш. м, 8H); 1,28 (м, 30H); 0,90 (м, 6H).
Гептадекан-9-ил-8-(бензил(8-(нонилокси)-8-оксооктил)амино)октаноат
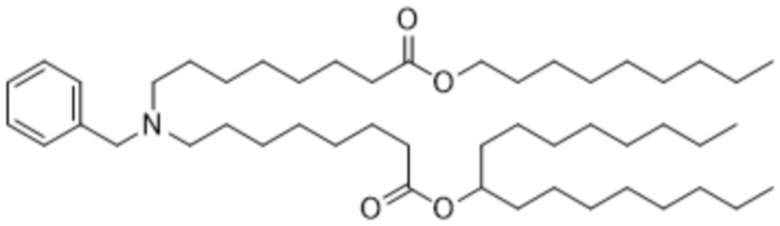
Химическая формула: C49H89NO4
Молекулярная масса: 756,25
[00104] Раствор гептадекан-9-ил-8-(бензиламино)октаноата (200 мг, 0,41 ммоль), нонил-8-бромоктаноата (172 мг, 0,49 ммоль) и N, N-диизопропилэтиламина (100 мкл, 0,57 ммоль) растворили в этаноле и оставили перемешиваться при 62°C в течение 48 ч. Реакционную смесь охладили до комн. темп. и растворители выпарили в вакууме. Остаток перенесли в этилацетат и промывали насыщенным водным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, сушили над Na2SO4 и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-(бензил(8-(нонилокси)-8-оксооктил)амино)октаноата (138 мг, 0,18 ммоль, 45%). СВЭЖХ/ДСИО: RT=3,78 мин. MС (ИЭР): m/z (MH+) 757,0 для C49H89NO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,33-7,23 (уш. м, 5H); 4,89 (п, 1H); 4,08 (т, 2H); 3,55 (с, 2H); 2,40 (м, 4H); 2,30 (м, 4H); 1,64-1,28 (уш. м, 62H); 0,90 (м, 9H).
BP. Соединение 96: 7-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гептилдеканоат

Химическая формула: C44H87NO5
Молекулярная масса: 710,182
[00105] Соединение 96 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,74 мин. MС (ИЭР): m/z (MH+) 711,0 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,61 (м, 2H); 2,88-2,37 (уш. м, 6H); 2,31 (м, 4H), 1,79-1,04 (м, 62H); 0,90 (м, 9H).
BQ. Соединение 98: 8-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октан-2-илдеканоат
Октан-1,7-диoл

Химическая формула: C8H18O2
Молекулярная масса: 146,230
[00106] Раствор 7-оксооктановой кислоты (4 г, 25,29 ммоль) в ТГФ (10 мл) прибавили к перемешиваемому раствору ЛАГ в ТГФ (70 мл) в атмосфере N2 при 0°C. Смесь оставили нагреваться до комн. темп. И перемешивали при комн. темп. в течение 4 ч, через указанное время к данному раствору медленно прибавили 10 мл насыщ. Na2SO4,10H2O (водн.). Белое твердое вещество размололи. Прибавили дополнительное количество Na2SO4,10H2O и смесь отфильтровали через слой целита. Фильтрат разбавили EtOAc и промывали насыщенным водным раствором хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-40%) EtOAc в смеси гексанов с получением октан-1,7-диoл (2,97 г, 20,31 ммоль, 80%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,81 (м, 1H); 3,66 (т, 2H); 1,66-1,31 (м, 12H); 1,22 (д, 3H).
8-((трет-Бутилдифенилсилил)окси)октан-2-ол

Химическая формула: C24H36O2Si
Молекулярная масса: 384,635
[00107] К раствору октан-1,7-диoла (1 г, 6,84 ммоль) вДХМ (75 мл) при 0°C прибавили имидазол (0,94 г, 13,81 ммоль) с последующим медленным прибавлением раствора трет-бутил(хлор)дифенилсилана (2,14 мл, 8,21 ммоль) в ДХМ (используя капельную воронку). Реакционную смесь оставили перемешиваться при 0°C в течение 1,5 ч. Реакционную смесь погасили насыщенным раствором NH4Cl(водн.). Водный слой экстрагировали 3 раза ДХМ (3 × 50 мл). Органический слой сушили над безводным MgSO4 и отфильтровали и растворитель выпарили. Сырой продукт очищали колоночной флэш-хроматографией на силикагеле 0-10% EtOAc в смеси гексанов с получением 8-((трет-бутилдифенилсилил)окси)октан-2-ола (2,29 г, 5,95 ммоль, 87%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,69 (м, 4H); 7,42 (м, 6H); 3,80 (м, 1H); 3,68 (т, 2H); 1,59 (м, 2H); 1,50-1,26 (м, 9H); 1,21 (д, 3H); 1,07 (с, 9H).
8-((трет-Бутилдифенилсилил)окси)октан-2-илдеканоат
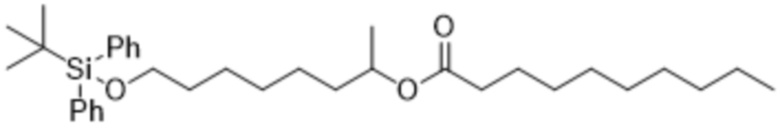
Химическая формула: C34H54O3Si
Молекулярная масса: 538,888
[00108] 8-((трет-Бутилдифенилсилил)окси)октан-2-ил деканоат синтезировали согласно методу A. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,69 (м, 4H); 7,42 (м, 6H); 4,92 (м, 1H); 3,67 (т, 2H); 2,29(т, 2H); 1,67-1,42 (м, 6H); 1,41-1,17 (м, 21H); 1,07 (с, 9H); 0,90 (м, 3H).
8-Гидроксиоктан-2-илдеканоат
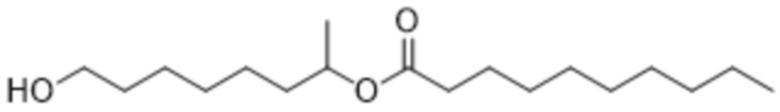
Химическая формула: C18H36O3
Молекулярная масса: 300,483
[00109] К раствору 8-[(трет-бутилдифенилсилил)окси]октан-2-ил деканоата (1,08 г, 2 ммоль) в ТГФ прибавили TBAF (8,02 мл 1 M раствор в ТГФ, 8,02 ммоль) и смесь оставили перемешиваться при комн. темп. в течение 3 ч. Органические растворители выпарили под вакуумом. Остаток разбавили EtOAc и промывали насыщ. NaHCO3, с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-40%) EtOAc в смеси гексанов с получением 8-гидроксиоктан-2-илдеканоата (0,55 г, 1,82 ммоль, 91%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 1H); 3,66 (т, 2H); 2,29 (т, 2H); 1,72-1,17 (м, 28H); 0,90 (м, 3H).
8-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октан-2-илдеканоат
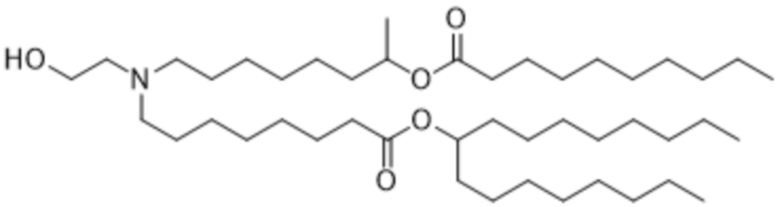
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00110] Соединение 98 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,55 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 2H); 3,58 (уш. м, 2H); 2,77-2,40 (м, 6H); 2,29 (м, 4H); 1,72-1,41(м, 14H); 1,28 (м, 51H); 0,90 (м, 9H).
BR. Соединение 101: Гептадекан-9-ил-8-((2-(4-метилпиперазин-1-ил)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Гептадекан-9-ил-8-((2-хлорэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
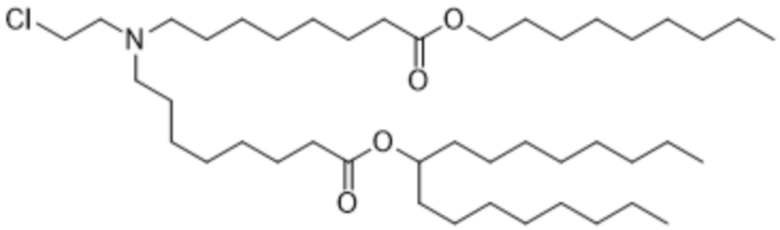
Химическая формула: C44H86ClNO4
Молекулярная масса: 728,63
[00111] К раствору гептадекан-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (1100 мг, 1,55 ммоль) в дихлорметане (25 мл) при 0°C одной порцией прибавили N-хлорсукцинимид. Реакционную смесь оставили перемешиваться при 0°C в течение 1 ч с последующим перемешиванием в течение 1 ч при комнатной температуре. Прибавили 90 мл смесь гексанов и реакционную смесь оставили перемешиваться при комнатной температуре в течение 20 мин. Белое твердое вещество отфильтровали через слой силикагеля и трижды промывали смесью гексанов. Органические слои концентрировали в вакууме. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,57 (м, 2H); 2,85 (м, 2H); 2,54 (м, 4H); 2,33-2,27 (м, 4H); 1,66-1,28 (уш. м, 62H); 0,90 (м, 9H).
Гептадекан-9-ил-8-((2-(4-метилпиперазин-1-ил)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
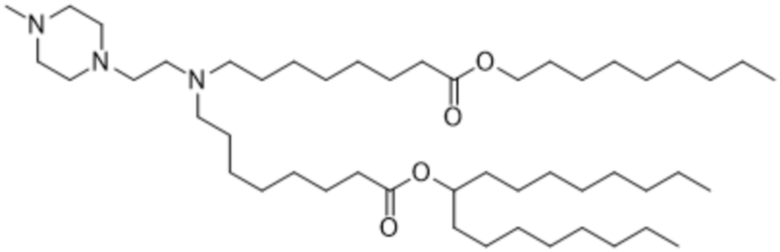
Химическая формула: C49H97N3O4
Молекулярная масса: 792,33
[00112] Раствор 1-метилпиперазина (15 мг, 0,151 ммоль), гептадекан-9-ил-8-((2-хлорэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (110 мг, 0,151 ммоль), K2CO3 (42 мг, 0,302 ммоль) и KI (3 мг, 0,0151 ммоль) растворили в 1:1 ТГФ:MeCN (1 мл:1 мл). Реакционную смесь оставили перемешиваться при 65°C в течение 18 часов. Реакционную смесь охладили до комнатной температуры, отфильтровали и промывали смесью гексанов и EtOAc. Органический фильтрат перенесли в делительную воронку и промывали водой и насыщенным водным раствором хлорида натрия. Осушенные над Na2SO4 органические слои отфильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле [0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане] с получением гептадекан-9-ил-8-((2-(4-метилпиперазин-1-ил)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (36 мг, 0,045 ммоль, 30%). СВЭЖХ/ДСИО: RT=3,25 мин. MС (ИЭР): m/z (MH+) 792,8 для C49H97N3O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (п, 1H); 4,08 (т, 2H); 2,57-2,45 (уш. м, 20H); 2,31 (м, 3H); 1,64-1,28 (уш. м, 62H); 0,90 (м, 9H).
BS. Соединение 103: Гептадекан-9-ил-8-((2-(4-метилпиперазин-1-ил)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Гептадекан-9-ил-8-((2-хлорэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C44H86ClNO4
Молекулярная масса: 728,63
[00113] К перемешиваемому раствору гептадекан-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (1100 мг, 1,55 ммоль) в дихлорметане (25 мл) при 0°C одной порцией прибавили N-хлорсукцинимид. Реакционную смесь оставили перемешиваться при 0°C в течение 1 ч с последующим перемешиванием в течение 1 ч при комнатной температуре. Прибавили 90 мл смесь гексанов и реакционную смесь оставили перемешиваться при комнатной температуре в течение 20 мин. Белое твердое вещество отфильтровали через слой силикагеля и трижды промывали смесью гексанов. Органические слои концентрировали в вакууме. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 3,57 (м, 2H); 2,85 (м, 2H); 2,54 (м, 4H); 2,33-2,27 (м, 4H); 1,66-1,28 (уш. м, 62H); 0,90 (м, 9H).
Гептадекан-9-ил-8-((2-морфолиноэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C48H94N2O5
Молекулярная масса: 779,29
[00114] Раствор морфолина (13 мг, 0,151 ммоль), гептадекан-9-ил-8-((2-хлорэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (110 мг, 0,151 ммоль), K2CO3 (42 мг, 0,302 ммоль) и KI (3 мг, 0,0151 ммоль) растворили в 1:1 ТГФ:MeCN (1 мл:1 мл). Реакционную смесь оставили перемешиваться при 65°C в течение 18 часов. Реакционную смесь охладили до комнатной температуры, отфильтровали и промывали смесью гексанов и EtOAc. Органический фильтрат перенесли в делительную воронку и промывали водой и насыщенным водным раствором хлорида натрия. Осушенные над Na2SO4 органические слои отфильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле [0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане] с получением гептадекан-9-ил-8-((2-(4-метилпиперазин-1-ил)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (58 мг, 0,074 ммоль, 49%). СВЭЖХ/ДСИО: RT=3,53 мин. MС (ИЭР): m/z (MH+) 779,8 для C48H94N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H); 4,05 (т, 2H); 3,70 (м, 4H); 2,59-2,54 (м, 2H); 2,48-2,38 (м, 10H); 2,31-2,25 (м, 4H); 1,64-1,26 (уш. м, 62H); 0,88 (м, 9H).
BT. Соединение 108: Гептадекан-9-ил-8-((3-ацетамидопропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C47H92N2O5
Молекулярная масса: 765,26
[00115] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,553 ммоль) и триэтиламина (0,15 мл, 1,10 ммоль) в 10 мл дихлорметана по каплям прибавили при 0°C ацетилхлорид (47 мкл, 0,66 ммоль) и реакционную смесь оставили нагреваться до комнатной температуры в течение 16 ч. МС показал образование продукта и смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Затем ее сушили над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде бесцветного масла (300 мг, 71%). ЖХ/УФ (202 нм): RT=9,14 мин. MС (ХИАД): m/z (MH+) 765,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,41 (уш. с, 1H); 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,40-3,25 (м, 2H); 2,53-2,23 (м, 10H); 1,91 (с, 3H); 1,65-1,16 (м, 64H); 0,86 (м, 9H).
BU. Соединение 109: Гептадекан-9-ил-8-((3-(метилсульфонамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
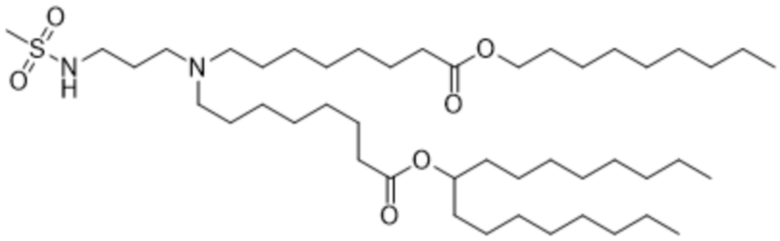
Химическая формула: C46H92N2O6S
Молекулярная масса: 801,31
[00116] Метансульфонилхлорид (51мкл, 0,66 ммоль) по каплям прибавили к 0°C раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,553 ммоль) и триэтиламина (0,15 мл, 1,10 ммоль) в 10 мл дихлорметана и реакционную смесь оставили нагреваться до комнатной температуры в течение 16 ч. МС показал образование продукта и смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. После сушки над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде бесцветного масла (296 мг, 88%). ЖХ/УФ (214 нм): RT=11,51 мин. MС (ХИАД): m/z (MH+) 801,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,22 (т, 2H, J=5,8 Гц); 2,88 (с, 3H); 2,53-2,23 (м, 10H); 1,73-1,16 (м, 64H); 0,87 (м, 9H).
BV. Соединение 110: Гептадекан-9-ил-8-((3-(3,3-диметилуреидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C48H95N3O5
Молекулярная масса: 794,30
[00117] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,553 ммоль), диметиламинопиридина (7 мг, 0,0553 ммоль) и триэтиламина (0,15 мл, 1,10 ммоль) в 10 мл дихлорметана по каплям прибавили хлорангидрид диметилкарбаминовой кислоты (56 мкл, 0,61 ммоль) при 0°C и реакционную смесь оставили перемешиваться при комнатной температуре в течение 16 ч. МС показал образование продукта. Смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Затем ее сушили над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде бесцветного масла (267 мг, 60%). ЖХ/УФ (202 нм): RT=9,81 мин. MС (ХИАД): m/z (MH+) 794,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,13 (т, 1H, J=4,5 Гц); 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,32-3,26 (м, 2H); 2,85 (с, 6H); 2,52-2,23 (м, 10H); 1,67-1,18 (м, 64H); 0,87 (м, 9H).
BW. Соединение 111: Гептадекан-9-ил-8-((3-(3,3-диметилтиоуреидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
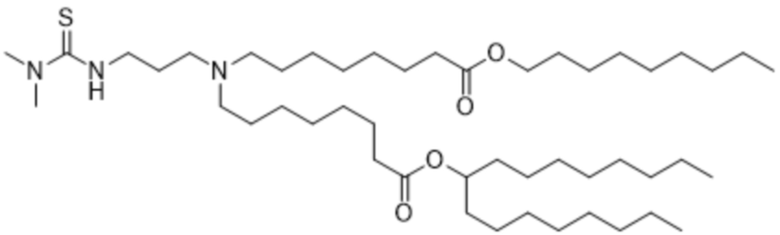
Химическая формула: C48H95N3O4S
Молекулярная масса: 810,37
[00118] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,553 ммоль) и триэтиламина (0,15 мл, 1,10 ммоль) в 10 мл дихлорметана по каплям прибавили при 0°C тиофосген (51 мкл, 0,664 ммоль) и реакционную смесь оставили перемешиваться при комнатной температуре в течение 6 ч. Через указанное время реакционную смесь охладили до 0°C и прибавили раствор диметиламина в ТГФ (2,0 M, 0,55 мл, 1,10 ммоль). Реакционную смесь затем оставили перемешиваться при комнатной температуре в течение 16 ч. МС показал образование продукта и смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. После сушки над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде коричневого масла (346 мг, 77%). ЖХ/УФ (202 нм): RT=9,89 мин. MС (ХИАД): m/z (MH+) 810,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 8,12 (уш. с, 1H); 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,74-3,64 (м, 2H); 3,20 (с, 6H); 2,62-2,23 (м, 10H); 1,77-1,17 (м, 64H); 0,87 (м, 9H).
BX. Соединение 112: Гептадекан-9-ил-8-((3-(3-метилуреидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
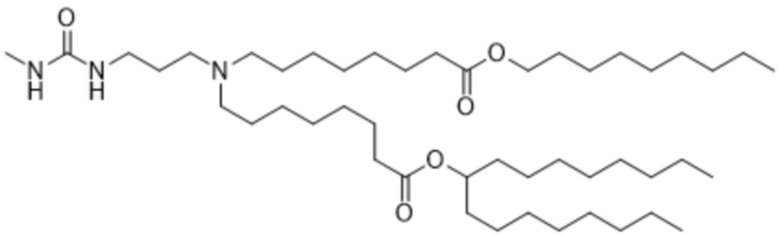
Химическая формула: C47H93N3O5
Молекулярная масса: 780,28
[00119] К 0°C раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,553 ммоль) в 10 мл дихлорметана прибавили метилизоцианат (38 мг, 0,664 ммоль) и реакционную смесь оставили перемешиваться при комнатной температуре в течение 16 ч. МС показал образование продукта. Смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Затем ее сушили над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде бесцветного масла (320 мг, 70%). ЖХ/УФ (202 нм): RT=9,63 мин. MС (ХИАД): m/z (MH+) 780,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,54 (уш. с, 1H); 4,85 (п, 1H, J=6,0 Гц); 4,76 (уш. с, 1H); 4,04 (т, 2H, J=6,6 Гц); 3,23 (т, 2H, J=5,8 Гц); 2,74 (д, 3H, J=2,0 Гц); 2,47 (т, 2H, J=6,0 Гц); 2,37 (т, 4H, J=7,4 Гц); 2,31-2,23 (м, 4H); 1,68-1,17 (м, 64H); 0,87 (м, 9H).
BY. Соединение 113: Гептадекан-9-ил-8-((3-(3-метилтиоуреидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
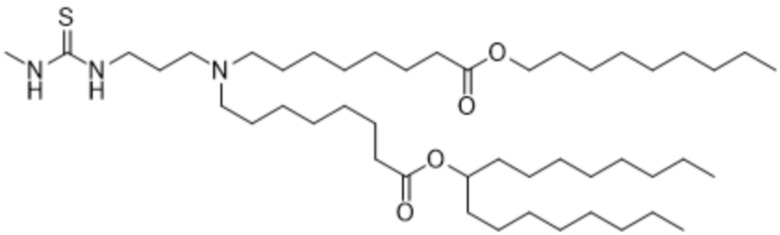
Химическая формула: C49H93N3O4S
Молекулярная масса: 795,69
[00120] К 0°C раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,553 ммоль) в 10 мл дихлорметана прибавили метилизотиоцианат (45 мкл, 0,664 ммоль) и реакционную смесь оставили перемешиваться при комнатной температуре в течение 16 ч. МС показал образование продукта. Смесь концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде бесцветного масла (312 мг, 70%). ЖХ/УФ (202 нм): RT=9,96 мин. MС (ХИАД): m/z (MH+) 796,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,51 (уш. с, 2H); 2,93 (уш. с, 3H); 2,52 (т, 2H, J=6,0 Гц); 2,41 (т, 4H, J=7,8 Гц); 2,31-2,23 (м, 4H); 1,68-1,17 (м, 66H); 0,86 (м, 9H).
BZ. Соединение 114: Гептадекан-9-ил-8-((3-(2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
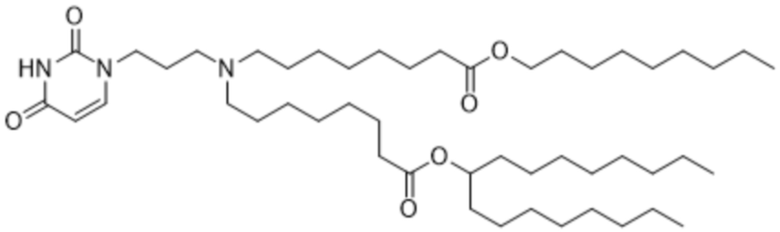
Химическая формула: C49H91N3O6
Молекулярная масса: 818,28
[00121] Смесь гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,67 ммоль), урацила (300 мг, 2,67 ммоль) и 1,8-диазабициклоундец-7-ена (150 мкл, 1,07 ммоль) в 3 мл ДМФА нагревали при 100°C в герметично закрытой пробирке в течение 16 ч. Реакционную смесь концентрировали досуха и разделили между дихлорметаном и водой. Органический слой промывали насыщенным водным раствором хлорида натрия. Затем ее сушили над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде желтого масла (268 мг, 49%). ЖХ/УФ (202 нм): RT=8,91 мин. MС (ХИАД): m/z (MH+) 818,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 8,19 (уш. с, 1H); 7,24 (д, 1H, J=7,7 Гц); 5,64 (д, 1H, J=7,7 Гц); 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,76 (т, 2H, J=7,0 Гц); 2,45-2,24 (м, 10H); 1,81 (п, 2H, J=6,6 Гц); 1,68-1,17 (м, 62H); 0,87 (м, 9H).
CA. Соединение 115: Гептадекан-9-ил-8-((3-(4-амино-2-оксопиримидин-1(2H)-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
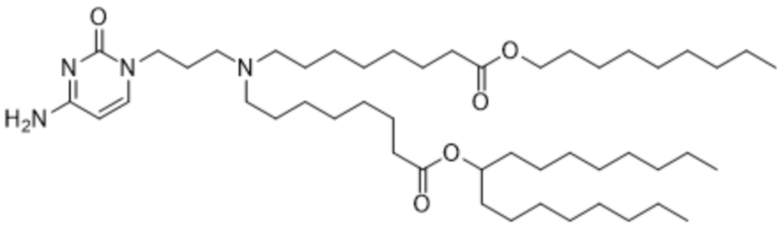
Химическая формула: C49H92N4O5
Молекулярная масса: 817,30
[00122] К суспензии цитозина (82 мг, 0,74 ммоль) в 1 мл ДМФА прибавили NaH (30 мг, 0,74 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 30 мин. Затем прибавили раствор гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,67 ммоль) в 2 мл ДМФА и смесь нагревали при 100°C в герметично закрытой пробирке в течение 16 ч. MС показал наличие продукта. Реакционную смесь погасили насыщенным раствором гидрокарбоната натрия и экстрагировали смесью гексанов (2X). Объединенный органический слой промывали водой и насыщенным водным раствором хлорида натрия. Затем ее сушили над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде желтого масла (310 мг, 56%). ЖХ/УФ (202 нм): RT=8,32 мин. MС (ХИАД): m/z (MH+) 817,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,34 (д, 1H, J=7,1 Гц); 5,61 (д, 1H, J=7,1 Гц); 5,44 (уш. с, 2H); 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,79 (т, 2H, J=7,0 Гц); 2,42-2,22 (м, 9H); 1,84 (т, 2H, J=6,6 Гц); 1,68-1,17 (м, 63H); 0,86 (м, 9H).
CB. Соединение 116: Гептадекан-9-ил-8-((3-(6-амино-9H-пурин-9-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
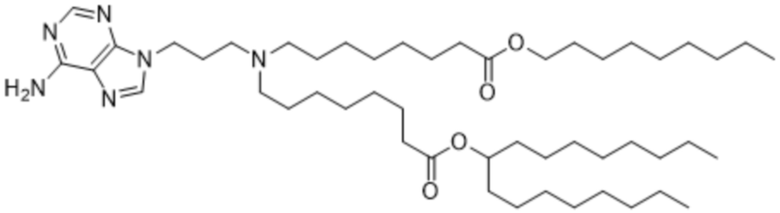
Химическая формула: C50H92N6O4
Молекулярная масса: 841,32
[00123] Смесь гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,67 ммоль), аденина (135 мг, 1,0 ммоль) и 1,8-диазабициклоундец-7-ена (137 мкл, 1,0 ммоль) в 2 мл ДМФА нагревали при 90°C в герметично закрытой пробирке в течение 16 ч. Реакционную смесь концентрировали досуха и разделили между дихлорметаном и водой. Органический слой промывали насыщенным водным раствором хлорида натрия. Затем ее сушили над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде желтого масла (325 мг, 57%). ЖХ/УФ (202 нм): RT=8,47 мин. MС (ХИАД): m/z (MH+) 841,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 8,36 (с, 1H); 7,80 (с, 1H); 5,51 (уш. с, 2H); 4,85 (п, 1H, J=6,0 Гц); 4,24 (т, 2H, J=7,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 2,45-2,24 (м, 10H); 2,01 (п, 2H, J=6,9 Гц); 1,68-1,17 (м, 62H); 0,86 (м, 9H).
CC. Соединение 118: 3,4-Дипентилфенил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
5-Mетокси-2-(пент-1-ин-1-ил)бензальдегид (см., например, Bioorg. Med. Chem. Lett. 2013, 23, 1365)
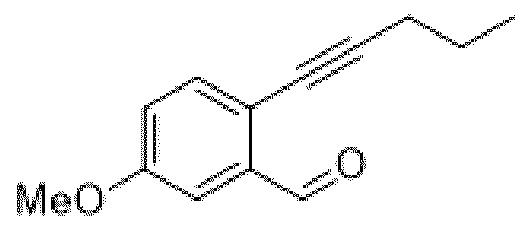
Химическая формула: C13H14O2
Молекулярная масса: 202,25
[00124] Смесь 2-бром-5-метоксибензальдегида (4,30 г, 20 ммоль), 1-пентина (3,0 мл, 30 ммоль), бис(трифенилфосфино)палладий хлорида (702 мг, 1 ммоль), CuI (380 мг, 2,0 ммоль) и триэтиламина (5,6 мл, 40 ммоль) в 60 мл ТГФ нагревали до 50°C в течение 16 ч в атмосфере азота. ТСХ показал исчезновение исходного материала. Реакционную смесь концентрировали досуха. Остаток растворили в дихлорметане и промывали водой и насыщенным водным раствором хлорида натрия. После сушки над сульфатом натрия, фильтрат концентрировали и остаток очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов от 0 до 5%) с получением продукта в виде темно-коричневого масла (3,00 г, 74%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 10,49 (с, 1H); 7,42 (д, 1H, J=8,5 Гц); 7,36 (д, 1H, J=2,8 Гц); 7,07 (дд, 1H, J=8,5 Гц, 2,8 Гц); 3,84 (с, 3H); 2,44 (т, 2H, J=7,0 Гц); 1,62 (м, 2H); 1,05 (т, 3H, J=7,2 Гц).
4-Mетокси-2-(пент-1-ен-1-ил)-1-(пент-1-ин-1-ил)бензол
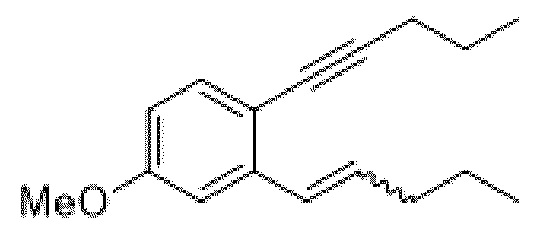
Химическая формула: C17H22O
Молекулярная масса: 242,36
[00125] К суспензии бутилтрифенилфосфонийбромида (8,88 г, 22,2 ммоль) в 75 мл ТГФ прибавили при 0°C трет-бутоксид калия (2,50 г, 22,2 ммоль). Через 30 мин раствор 5-метокси-2-(пент-1-ин-1-ил)бензальдегида (3,00 г, 14,8 ммоль) в 25 мл ТГФ затем медленно добавляли в оранжевую суспензию. Реакционную смесь оставили нагреваться до комнатной температуры и перемешивали в течение 60 ч. Прибавили насыщенный раствор хлорида аммония и смесь экстрагировали эфиром (2X) и объединенный органический слой промывали насыщенным водным раствором хлорида натрия. После сушки над сульфатом натрия, фильтрат концентрировали и остаток очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов от 0 до 5%) с получением продукта в виде коричневого масла (3,46 г, 96%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,33 (д, 0,5H, J=8,5 Гц); 7,26 (д, 0,5H, J=8,5 Гц); 6,99 (д, 0,5H, J=2,8 Гц); 6,88-6,80 (м, 1H); 6,73-6,61 (м, 1,5H); 6,25 (дт, 0,5H, J=15,9 Гц, 6,9 Гц); 5,73 (дт, 0,5H, J=11,5 Гц, 7,4 Гц); 3,80 (с, 3H); 2,45-2,37 (м, 2H); 2,31-2,18 (м, 2H); 1,71-1,41 (м, 4H); 1,09-0,90 (м, 6H).
4-Mетокси-1,2-дипентилбензол

Химическая формула: C17H28O
Молекулярная масса: 248,41
[00126] Смесь 4-метокси-2-(пент-1-ен-1-ил)-1-(пент-1-ин-1-ил)бензола (3,46 г, 14,3 ммоль) и Pd/C (10%, 300 мг) в 60 мл EtOH перемешивали в течение 60 ч в атмосфере водорода из баллона. ТСХ показал завершение реакции. Реакционную смесь отфильтровали через целит и концентрировали с получением продукта в виде желтого масла (3,70 г, колич.), которое использовали на следующей стадии без очистки. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,05 (д, 1H, J=8,2 Гц); 6,72-6,55 (м, 2H); 3,78 (с, 3H); 2,59-2,50 (м, 4H); 1,62-1,48 (м, 4H); 1,39-1,28 (м, 8H); 0,93-0,86 (м, 6H).
3,4-Дипентилфенол
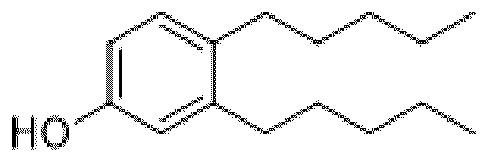
Химическая формула: C16H26O
Молекулярная масса: 234,38
[00127] К раствору 4-метокси-1,2-дипентилбензола (3,40 г, 13,7 ммоль) в 75 мл дихлорметане по каплям прибавили при -78°C BBr3 (1,65 мл, 17,1 ммоль) и затем реакционную смесь оставили нагреваться до комнатной температуры в течение 3 ч. ТСХ показал завершение реакции. Реакционную смесь погасили прибавлением насыщенного раствора гидрокарбоната натрия и затем его экстрагировали дихлорметаном (2X). Объединенный органический слой промыли насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия. После концентрирования, остаток очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов от 0 до 30%) с получением продукта в виде коричневого масла (3,35 г, 97%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,99 (д, 1H, J=8,0 Гц); 6,64-6,59 (м, 2H); 4,45 (уш. с, 1H); 2,55-2,47 (м, 4H); 1,66-1,43 (м, 4H); 1,39-1,28 (м, 8H); 0,93-0,86 (м, 6H).
3,4-Дипентилфенил-8-бромоктаноат
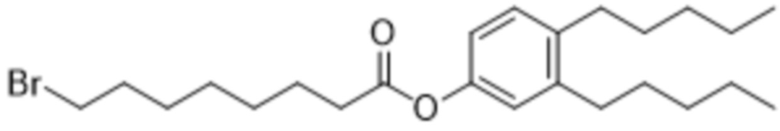
Химическая формула: C24H39BrO2
Молекулярная масса: 439,48
[00128] К раствору 8-бромоктановой кислоты (2,23g, 10 ммоль) и 3,4-дипентилфенола (2,34 г, 10 ммоль) в дихлорметане (50 мл) прибавили N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид (1,92 г, 10 ммоль) и DMAP (244 мг, 2 ммоль). Реакционную смесь оставили перемешиваться при комнатной температуре в течение 18 ч. Реакционную смесь разбавили дихлорметаном и экстрагировали насыщенным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия. Органический слой отфильтровали и выпарили под вакуумом. Остаток очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов от 0 до 10%) с получением продукта в виде коричневого масла (4,30 г, 98%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,11 (д, 1H, J=7,7 Гц); 6,84-6,77 (м, 2H); 3,41 (т, 2H, J=6,9 Гц); 2,60-2,49 (м, 6H); 1,92-1,69 (м, 4H); 1,62-1,29 (м, 18H); 0,90 (м, 6H).
Нонил-8-((2-гидроксиэтил)амино)октаноат
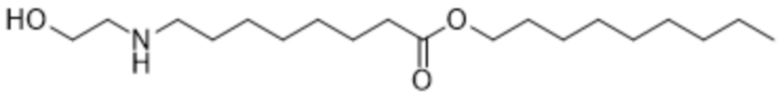
Химическая формула: C19H39NO3
Молекулярная масса: 329,53
[00129] Смесь нонил-8-бромоктаноата (2,50 г, 7,15 ммоль) и 2-аминоэтанола (4,3 мл, 71,5 ммоль) в 10 мл EtOH перемешивали при комнатной температуре в течение 60 ч. Реакционную смесь разделили между смесью гексанов и водой и органический слой промывали насыщенным водным раствором хлорида натрия. После сушки над сульфатом натрия, фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 20%) с получением продукта в виде белого твердого вещества (1,57 г, 66%). MС (ХИАД): m/z (MH+) 330,3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,04 (т, 2H, J=6,6 Гц); 3,63 (т, 2H, J=5,2 Гц); 2,77 (т, 2H, J=5,1 Гц); 2,61 (т, 2H, J=7,1 Гц); 2,28 (т, 2H, J=7,4 Гц); 1,99 (уш. с, 2H); 1,67-1,20 (м, 4H); 1,62-1,29 (м, 17H); 0,87 (м, 6H).
3,4-Дипентилфенил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
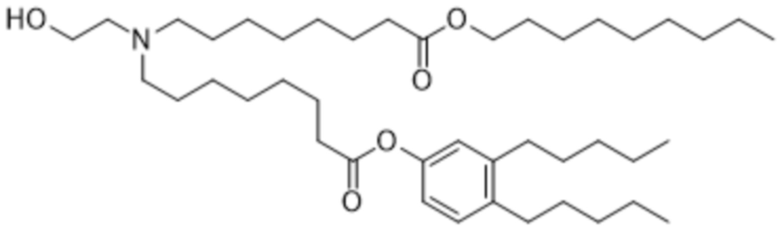
Химическая формула: C43H77NO5
Молекулярная масса: 688,09
[00130] Раствор нонил-8-((2-гидроксиэтил)амино)октаноата (500 мг, 1,52 ммоль), 3,4-дипентилфенил 8-бромоктаноата (1,00 г, 2,27 ммоль) и N, N-диизопропилэтиламина (0,40 мл, 2,27 ммоль) в трет-бутаноле (3 мл) нагревали до 60°C в герметично закрытой пробирке в течение 60 ч. Реакционную смесь охладили до комнатной температуры и растворители выпарили под вакуумом. Остаток очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением смеси (365 мг) и затем смесь очищали с помощью ISCO (EtOAc/смесь гексанов/0,5% Et3N от 0 до 50%) с получением продукта в виде бесцветного масла (80 мг). ЖХ/УФ (214 нм): RT=10,23 мин. MС (ХИАД): m/z (MH+) 688,6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,11 (д, 1H, J=8,0 Гц); 6,84-6,77 (м, 2H); 4,04 (т, 2H, J=6,6 Гц); 3,51 (т, 2H, J=5,5 Гц); 2,60-2,38 (м, 12H); 2,28 (т, 2H, J=7,4 Гц); 1,79-1,19 (м, 37H); 0,92-0,82 (м, 9H).
CD. Соединение 119: Нонил-8-((2-гидроксиэтил)(8-оксо-8-(4-пентилфенокси)октил)амино)октаноат
4-Пентилфенил-8-бромоктаноат

Химическая формула: C19H29BrO2
Молекулярная масса: 369,34
[00131] К раствору 8-бромоктановой кислоты (2,00 г, 8,96 ммоль) и 4-пентилфенола (3,07 мл г, 17,9 ммоль) в дихлорметане (50 мл) прибавили N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид (1,72 г, 8,96 ммоль) и DMAP (220 мг, 1,79 ммоль). Реакционную смесь оставили перемешиваться при комнатной температуре в течение 60 ч. Реакционную смесь разбавили дихлорметаном и экстрагировали насыщенным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, и сушили над сульфатом натрия. Органический слой отфильтровали и выпарили под вакуумом. Остаток очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов от 0 до 10%) с получением продукта в виде бесцветного масла (3,12 г, 94%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,16 (д, 2H, J=8,5 Гц); 6,96 (д, 2H, J=8,5 Гц); 3,41 (т, 2H, J=6,9 Гц); 2,61-2,49 (м, 4H); 1,92-1,69 (м, 4H); 1,65-1,25 (м, 10H); 0,88 (м, 3H).
Нонил-8-((2-гидроксиэтил)(8-оксо-8-(4-пентилфенокси)октил)амино)октаноат

Химическая формула: C38H67NO5
Молекулярная масса: 617,96
[00132] Раствор нонил-8-((2-гидроксиэтил)амино)октаноата (500 мг, 1,52 ммоль), 4-пентилфенил 8-бромоктаноата (840 мг, 2,28 ммоль) и N, N-диизопропилэтиламина (0,40 мл, 2,28 ммоль) в трет-бутаноле (3 мл) нагревали до 60°C в герметично закрытой пробирке в течение 48 ч. Реакционную смесь охладили до комнатной температуры и растворители выпарили под вакуумом. Остаток очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением смеси (360 мг) и затем смесь очищали с помощью ISCO (EtOAc/смесь гексанов/0,5% Et3N от 0 до 50%) с получением продукта в виде бесцветного масла (95 мг). ЖХ/УФ (214 нм): RT=9,63 мин. MС (ХИАД): m/z (MH+) 618,5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,11 (д, 1H, J=8,0 Гц); 6,84-6,77 (м, 2H); 4,04 (т, 2H, J=6,6 Гц); 3,51 (т, 2H, J=5,5 Гц); 2,60-2,38 (м, 12H); 2,28 (т, 2H, J=7,4 Гц); 1,79-1,19 (м, 37H); 0,92-0,82 (м, 9H).
CE. Соединение 120: Нонил-8-((2-гидроксиэтил)(8-оксо-8-(3-пентилфенокси)октил)амино)октаноат
3-Пентилфенол (Ref: Tetrahedron Lett. 2013, 54, 52)
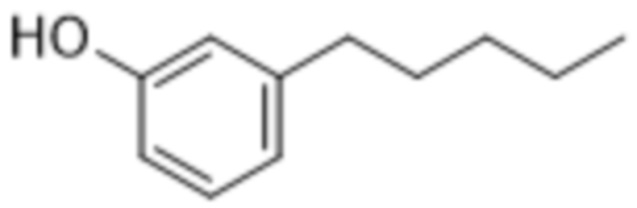
Химическая формула: C11H16O
Молекулярная масса: 164,25
[00133] При -78°C к суспензии трет-бутоксида калия (6,73 г, 60 ммоль) в 15 мл пентана последовательно прибавили тетраметилэтилдиамин (9,0 мл, 60 ммоль) и BuLi (2,5 M в гексане, 24 мл, 60 ммоль) и медленно прибавили раствор м-крезола (2,6 мл, 25 ммоль) в 10 мл пентане. Реакционную смесь нагревали до -20°C в течение 3 ч. 30 мл ТГФ прибавили и реакционную смесь охладили до -60°C. Медленно прибавили бутилбромид (4,8 мл, 45 ммоль) и смесь оставили нагреваться до комнатной температуры и перемешивали в течение 16 ч. Затем охладили до 0°C, реакционную смесь подкислили 4 M HCl до pH~3 и затем экстрагировали эфиром. Объединенный органический слой промыли насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия. После концентрирования остаток очищали с помощью ISCO (EtOAc/смесь гексанов от 0 до 5%) с получением смеси продукта с исходным материалом, которую перегнали под вакуумом с получением продукта в виде бесцветного масла (1,23 г, 65%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,14 (т, 1H, J=7,7 Гц); 6,75 (д, 1H, J=7,7 Гц); 6,67-6,61 (м, 2H); 4,62 (с, 1H); 2,55 (т, 2H, J=7,7 Гц); 1,67-1,52 (м, 2H); 1,38-1,24 (м, 4H); 0,88 (т, 3H, J=6,9 Гц).
3-Пентилфенил-8-бромоктаноат
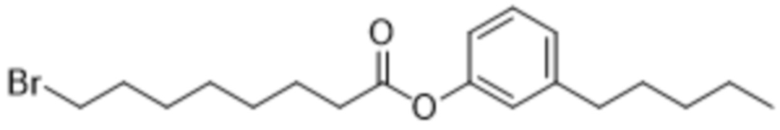
Химическая формула: C19H29BrO2
Молекулярная масса: 369,34
[00134] К раствору 8-бромоктановой кислоты (1,84 г, 8,20 ммоль) и 3-пентилфенола (1,23 г, 7,49 ммоль) в дихлорметане (40 мл) прибавили N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид (1,58 г, 8,20 ммоль) и DMAP (183 мг, 1,50 ммоль). Реакционную смесь оставили перемешиваться при комнатной температуре в течение 16 ч. Реакционную смесь разбавили дихлорметаном и экстрагировали насыщенным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия. Органический слой отфильтровали и выпарили под вакуумом. Остаток очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов от 0 до 10%) с получением продукта в виде бесцветного масла (2,23 г, 80%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,26 (т, 1H, J=8,5 Гц); 7,03 (д, 1H, J=7,6 Гц); 6,91-6,84 (м, 2H); 3,41 (т, 2H, J=6,9 Гц); 2,61-2,49 (м, 4H); 1,92-1,69 (м, 4H); 1,65-1,25 (м, 12H); 0,88 (т, 3H, J=6,9 Гц).
Нонил-8-((2-гидроксиэтил)(8-оксо-8-(3-пентилфенокси)октил)амино)октаноат
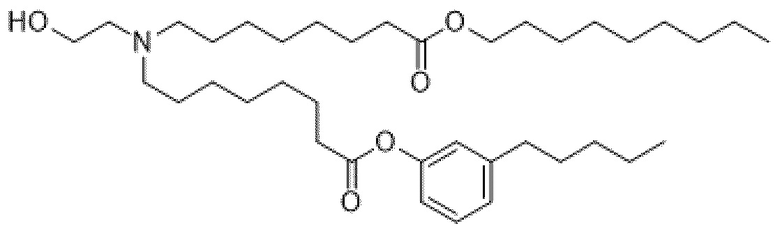
Химическая формула: C38H67NO5
Молекулярная масса: 617,96
[00135] Раствор нонил-8-((2-гидроксиэтил)амино)октаноата (500 мг, 1,52 ммоль), 3-пентилфенил 8-бромоктаноата (840 мг, 2,28 ммоль) и N, N-диизопропилэтиламина (0,40 мл, 2,28 ммоль) в трет-бутаноле (3 мл) перемешивали при 60°C в герметично закрытой пробирке в течение 16 ч. Реакционную смесь охладили до комнатной температуры и растворители выпарили под вакуумом. Остаток очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением смеси (247 мг) и затем смесь очищали с помощью ISCO (EtOAc/смесь гексанов/0,5% Et3N от 0 до 50%) с получением продукта в виде бесцветного масла (150 мг). ЖХ/УФ (202 нм): RT=7,45 мин. MС (ХИАД): m/z (MH+) 618,5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,26 (т, 1H, J=8,5 Гц); 7,03 (д, 1H, J=7,6 Гц); 6,91-6,84 (м, 2H); 4,05 (т, 2H, J=6,6 Гц); 3,51 (т, 2H, J=5,5 Гц); 2,64-2,38 (м, 10H); 2,28 (т, 2H, J=7,8 Гц); 1,79-1,19 (м, 41H); 0,91-0,82 (м, 6H).
CF. Соединение 121: Гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноат Гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C45H88ClNO4
Молекулярная масса: 742,65
[00136] К раствору гептадекан-9-ил-8-((3-гидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (8,00 г, 11,0 ммоль) и триэтиламина (2,0 мл, 14,4 ммоль) в дихлорметане (200 мл) по каплям прибавили метансульфонилхлорид (1,07 мл, 13,8 ммоль) при 0°C и реакционную смесь оставили нагреваться до комнатной температуры в течение 16 ч. ТСХ и МС показали завершение реакции. Реакционную смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. После сушки над сульфатом натрия, растворитель удалили под вакуумом с получением продукта в виде коричневого масла (7,30 г, 89%). ЯМР показал, что сырой продукт содержит небольшое количество мезилата и желаемого хлорида. Его использовали на следующей стадии без дополнительной очистки MС (ХИАД): m/z (MH+) 742,6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (п, 1H, J=6,0 Гц); 4,05 (т, 2H, J=6,9 Гц); 3,58 (т, 2H, J=6,6 Гц); 2,58-2,22 (м, 9H); 1,92-1,16 (м, 65H); 0,87 (м, 9H).
Гептадекан-9-ил-8-((3-азидопропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
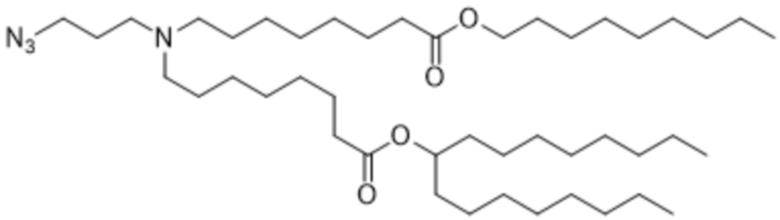
Химическая формула: C45H88N4O4
Молекулярная масса: 749,22
[00137] Смесь гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (4,20 г, 5,66 ммоль) и азида натрия (1,75 г, 28,28 ммоль) в 20 мл ДМФА в герметично закрытой пробирке нагревали до 100°C в течение 16 ч. Затем ее охладили до комнатной температуры, реакционную смесь разбавили водой и экстрагировали смесью гексанов. Объединенный органический слой промывали водой и насыщенным водным раствором хлорида натрия и затем сушили над сульфатом натрия. После фильтрования и концентрирования остаток очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 5%) с получением продукта в виде коричневого масла (3,66 г, 86%). MС (ХИАД): m/z (MH+) 749,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,7 Гц); 3,32 (т, 2H, J=6,9 Гц); 2,58-2,22 (м, 10H); 1,72-1,19 (м, 64H); 0,87 (м, 9H).
Гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
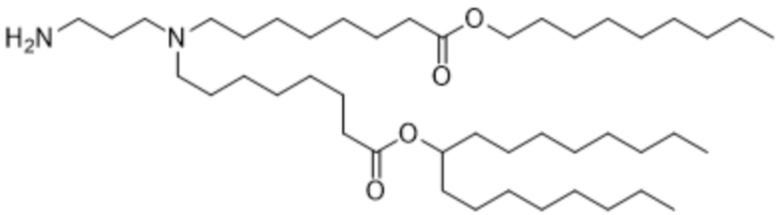
Химическая формула: C45H90N2O4
Молекулярная масса: 723,23
[00138] Смесь гептадекан-9-ил-8-((3-азидопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (3,66 г, 4,89 ммоль) и Pd/C (10%, 400 мг) в 150 мл EtOH перемешивали в атмосфере водорода из баллона в течение 16 ч. MС показал завершение реакции. Реакционную смесь отфильтровали через целит и фильтрат концентрировали и очищали с помощью ISCO (SiO2: MeOH/CH2Cl2/1% NH4OH от 0 до 20%) с получением продукта в виде коричневого масла (3,08 г, 87%). ЖХ/УФ (202 нм): RT=8,39 мин. MС (ХИАД): m/z (MH+) 723,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 2,70 (т, 2H, J=6,9 Гц); 2,46-2,24 (м, 10H); 1,65-1,16 (м, 66H); 0,87 (м, 9H).
CG. Соединение 122: Гептадекан-9-ил-8-((6-(декан-2-илокси)-6-оксогексил)(2-гидроксиэтил)амино)октаноат

Химическая формула: C43H85NO5
Молекулярная масса: 696,16
[00139] Соединение 122 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,58 мин. MС (ИЭР): m/z (MH+) 697,1 для C43H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 2H); 3,62 (м, 2H); 2,81-2,42 (уш. м, 5H); 2,30 (м, 4H); 1,73-1,43 (м, 14H); 1,28 (м, 48H); 0,90 (м, 9H).
CH. Соединение 123: Гептадекан-9-ил) 8-(метил(8-нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C26H53NO2
Молекулярная масса: 411,72
[00140] Раствор гептадекан-9-ил-8-бромоктаноата (200 мг, 0,433 ммоль) в метанамине (10 мл, 19,92 ммоль, 2M в ТГФ) оставили перемешиваться при комн. темп. в течение 18 ч. Реакционную смесь концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (10-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-(метиламино)октаноата (113 мг, 0,27 ммоль, 63%). СВЭЖХ/ДСИО: RT=2,76 мин. MС (ИЭР): m/z (MH+) 412,4 для C26H53NO2. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,92 (п, 1H); 2,62 (т, 2H); 2,48 (с, 3H); 2,32-2,27 (м, 2H); 1,66-1,52 (уш. м, 8H); 1,28 (м, 30H); 0,90 (м, 6H).
Гептадекан-9-ил-8-(метил(8-(нонилокси)-8-оксооктил)амино)октаноат
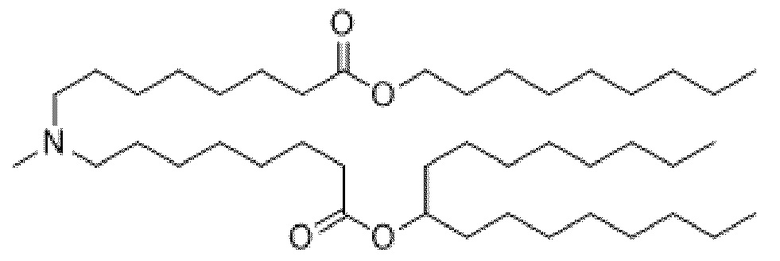
Химическая формула: C43H85NO4
Молекулярная масса: 680,16
[00141] Раствор гептадекан-9-ил-8-(метиламино)октаноата (113 мг, 0,27 ммоль), нонил-8-бромоктаноата (115 мг, 0,33 ммоль) и N, N-диизопропилэтиламина (67 мкл, 0,38 ммоль) и иодида калия (5 мг, 0,027 ммоль) растворили в этаноле и оставили перемешиваться при 62°C в течение 48 ч. Реакционную смесь охладили до комн. темп. и растворители выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-(метил(8-(нонилокси)-8-оксооктил)амино)октаноата (75 мг, 0,11 ммоль, 41%). СВЭЖХ/ДСИО: RT=3,84 мин. MС (ИЭР): m/z (MH+) 681,0 для C43H85NO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (п, 1H); 4,08 (т, 2H); 2,88-2,67 (уш. м, 7H); 2,34-2,27 (м, 4H); 1,80 (м, 4H); 1,63-1,52 (уш. м, 10H); 1,37-1,28 (уш. м, 48H); 0,90 (м, 9H).
CI. Соединение 124: Ди(гептадекан-9-ил)-8,8'-(метилазандиил)диоктаноат
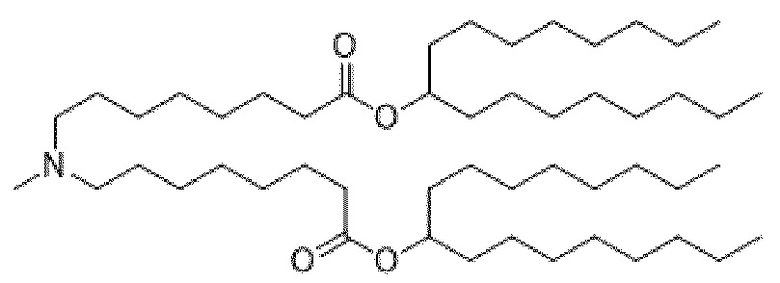
Химическая формула: C51H101NO4
Молекулярная масса: 792,37
[00142] Раствор гептадекан-9-ил-8-бромоктаноата (500 мг, 1,08 ммоль) в метанамине (11 мл, 21,67 ммоль, 2M в ТГФ) оставили перемешиваться при комн. темп. в течение 6 ч. Реакционную смесь концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (20-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением ди(гептадекан-9-ил) 8,8'-(метилазандиил)диоктаноата (26 мг, 0,03 ммоль, 3%). СВЭЖХ/ДСИО: RT=4,03 мин. MС (ИЭР): m/z (MH+) 793,3 для C51H101NO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 2H); 2,32-2,24 (м, 11H); 1,66-1,28 (уш. м, 76H); 0,90 (м, 12H).
CJ. Соединение 125: 3-((8-(Гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)пропановая кислота
Гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноат
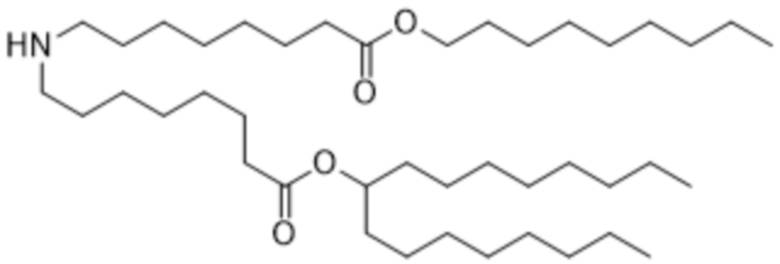
Химическая формула: C42H83NO4
Молекулярная масса: 666,13
[00143] При -78°C, к раствору оксалилхлорида (0,25 мл, 3,0 ммоль) в 3 мл дихлорметана по каплям прибавили раствор ДМСО (0,43 мл, 6,0 ммоль) в 2 мл дихлорметане и затем мгновенно прибавили раствор гептадекан-9-ил-8-((3-гидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (1,45 г, 2,0 ммоль) в дихлорметане (10 мл). Затем перемешивали в течение 30 мин при данной температуре, прибавили триэтиламин (1,45 мл, 10,4 ммоль) и реакционную смесь нагревали до комнатной температуры. ТСХ и МС показали завершение реакции (M+1: 722,7) и реакционную смесь разбавили водой и экстрагировали смесью гексанов (2X). Объединенный органический слой промывали насыщенным водным раствором хлорида натрия. После сушки над сульфатом натрия, фильтрат концентрировали и остаток очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов/0,5% Et3N от 0 до 50%) с получением продукта в виде коричневого масла (810 мг, 61%). MС (ХИАД): m/z (MH+) 666,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (п, 1H, J=6,0 Гц); 4,05 (т, 2H, J=6,9 Гц); 2,56 (т, 4H, J=7,1 Гц); 2,31-2,24 (м, 4H); 1,67-1,19 (м, 63H); 0,87 (м, 9H).
Гептадекан-9-ил-8-((3-(бензилокси)-3-оксопропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C52H93NO6
Молекулярная масса: 828,32
[00144] Раствор гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноата (798 мг, 1,2 ммоль) и бензилакрилата (293 мг, 1,8 ммоль) в дихлорметане (20 мл) перемешивали при комнатной температуре в течение 16 ч. ТСХ и MС показали отсутствие реакции, прибавили 10 мл MeOH и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. МС показал образование продукта с небольшим количеством метилового эфира (M+1: 829,8, 752,7). Реакционную смесь концентрировали досуха и очищали с помощью ISCO (SiO2: EtOAc/смесь гексанов от 0 до 35%) с получением продукта в виде бесцветного масла (280 мг, 28%). MС (ХИАД): m/z (MH+) 829,8. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,36-7,32 (м, 5H); 5,10 (с, 2H); 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,9 Гц); 2,78 (т, 2H, J=6,9 Гц); 2,46 (т, 2H, J=7,0 Гц); 2,36 (т, 4H, J=6,9 Гц); 2,30-2,24 (м, 4H); 1,67-1,19 (м, 62H); 0,87 (м, 9H).
3-((8-(Гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)пропановая кислота

Химическая формула: C45H87NO6
Молекулярная масса: 738,19
[00145] Смесь гептадекан-9-ил-8-((3-(бензилокси)-3-оксопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (280 мг, 0,34 ммоль) и Pd/C (10%, 28 мг) в 20 мл EtOAc перемешивали в атмосфере водорода из баллона в течение 1 ч. МС показал завершение реакции. Реакционную смесь отфильтровали и фильтрат концентрировали. Остаток очищали с помощью ISCO (SiO2: MeOH/CH2Cl2 от 0 до 10%) с получением продукта в виде бесцветного масла (230 мг, 91%). ЖХ/УФ (214 нм): RT=12,38 мин. MС (ХИАД): m/z (MH+) 838,7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (п, 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,6 Гц); 2,85 (т, 2H, J=6,0 Гц); 2,65 (т, 4H, J=7,7 Гц); 2,48 (т, 2H, J=6,0 Гц); 2,32-2,24 (м, 4H); 1,67-1,17 (м, 63H); 0,87 (м, 9H).
CK. Соединение 126: Гептадекан-9-ил-8-(метил(4-(нонилокси)-4-оксобутил)амино)октаноат
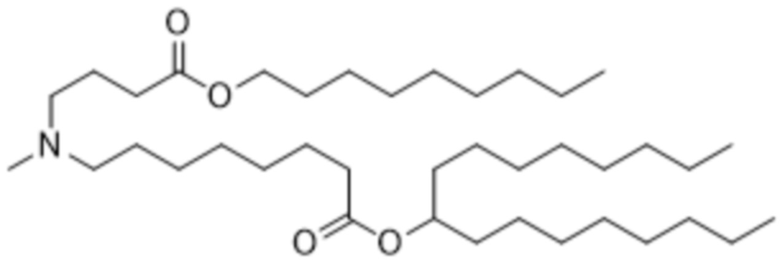
Химическая формула: C39H77NO4
Молекулярная масса: 624,05
[00146] Раствор гептадекан-9-ил-8-(метиламино)октаноата (103 мг, 0,25 ммоль), нонил-4-бромбутаноата (88 мг, 0,30 ммоль) и N, N-диизопропилэтиламина (61 мкл, 0,35 ммоль) растворили в этаноле и оставили перемешиваться при 62°C в течение 48 ч. Реакционную смесь охладили до комн. темп. и растворители выпарили в вакууме. Остаток перенесли в этилацетат и промывали насыщенным водным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, сушили над Na2SO4 и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-(метил(4-(нонилокси)-4-оксобутил)амино)октаноата (90 мг, 0,14 ммоль, 58%). СВЭЖХ/ДСИО: RT=3,58 мин. MС (ИЭР): m/z (MH+) 624,8 для C39H77NO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 4,08 (т, 2H); 2,38-2,24 (уш. м, 11H); 1,82 (м, 2H); 1,64-1,28 (уш. м, 52H); 0,90 (м, 9H).
CL. Соединение 127: Нонил-8-((9-((бис(нонилокси)фосфорил)окси)нонил)(2-гидроксиэтил)амино)октаноат
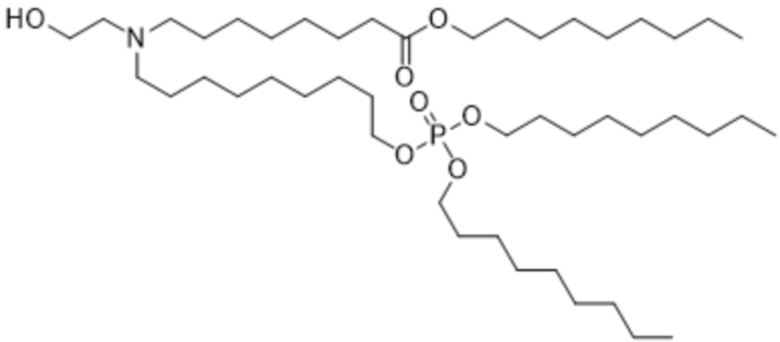
Химическая формула: C46H94NO7P
Молекулярная масса: 804,232
[00147] Соединение 127 синтезировали способом, аналогичным соединению 131 и согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,58 мин. MС (ИЭР): m/z (MH+) 805,1 для C46H94NO7P. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,05 (м, 8H); 3,55 (м, 2H); 2,59 (м, 2H); 2,46 (м, 4H); 2,31(т, 2H), 1,67 (м, 11H); 1,29 (м, 55H); 0,90 (м, 9H).
CM. Соединение 128: Гептадекан-9-ил-8-((6-((1-циклопропилнонил)окси)-6-оксогексил)(2-гидроксиэтил)амино)октаноат
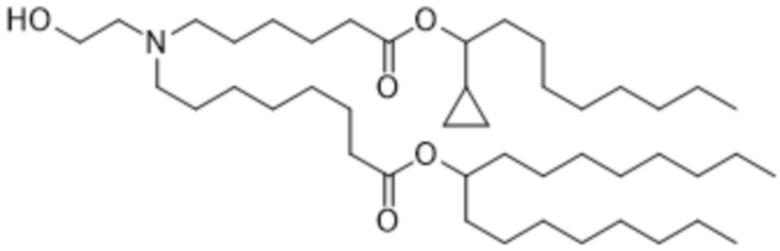
Химическая формула: C45H87NO5
Молекулярная масса: 722,193
[00148] Соединение 128 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,67 мин. MС (ИЭР): m/z (MH+) 722,9 для C45H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,30 (м, 1H); 3,56 (м, 2H); 2,72-2,39 (м, 6H); 2,30 (м, 4H), 1,76-1,17 (м, 58H); 0,90 (м, 10H); 0,61-0,35 (м, 3H); 0,28 (м, 1H).
CN. Соединение 129: Ундецил-6-((8-(диоктиламино)-8-оксооктил)(2-гидроксиэтил)амино)гексаноат

Химическая формула: C43H86N2O4
Молекулярная масса: 695,171
[00149] Соединение 129 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,45 мин. MС (ИЭР): m/z (MH+) 695,9 для C43H86N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 2H); 3,54 (м, 2H), 3,28 (м, 4H); 2,59 (м, 2H); 2,47 (м, 4H); 2,32 (q, 4H); 1,73-1,19 (м, 58H); 0,90 (м, 9H).
CO. Соединение 130: Декан-2-ил-8-((8-(диоктиламино)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
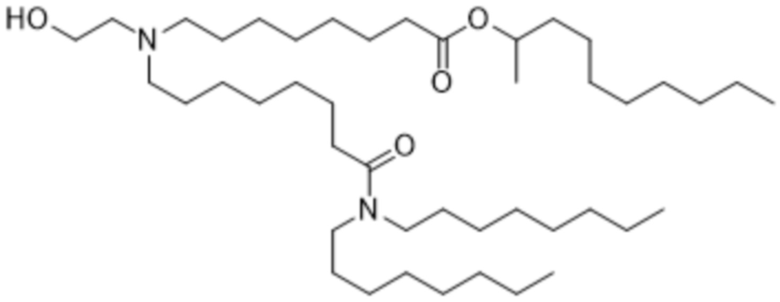
Химическая формула: C44H88N2O4
Молекулярная масса: 709,198
[00150] Соединение 130 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,46 мин. MС (ИЭР): m/z (MH+) 709,9 для C44H88N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 1H); 3,70 (уш. м, 2H), 3,35-3,15 (м, 4H); 2,96-2,41 (уш. м, 6H); 2,29 (м, 4H); 1,74-1,43 (м, 14H); 1,41-1,115 (м, 47H); 0,90 (м, 9H).
CP. Соединение 131: Нонил-8-((7-((бис(октилокси)фосфорил)окси)гептил)(2-гидроксиэтил)амино)октаноат
7-Бромгептилдиоктилфосфат
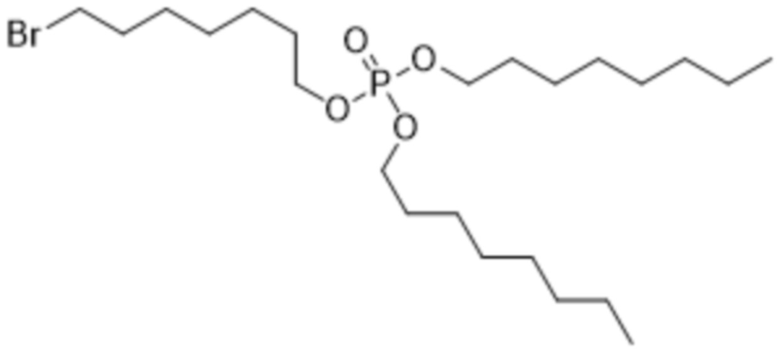
Химическая формула: C23H48BrO4P
Молекулярная масса: 499,511
[00151] К раствору POCl3 (1,91 мл, 20,5 ммоль) в ДХМ (20 мл) при 0°C, медленно прибавили Et3N (2,85 мл, 20,4 ммоль) с последующим прибавлением 7-бромгептан-1-ола (4,0 г, 20,5 ммоль). Реакционную смесь оставили перемешиваться в течение 4 ч при 0°C. Прибавили раствор октан-1-ола (7,10 мл, 45,11 ммоль) и Et3N (8,9 мл, 63,8 ммоль) в ДХМ и реакционную смесь оставили перемешиваться при комн. темп. в течение 16 ч. Реакционную смесь разбавили ДХМ и промывали насыщенным NaHCO3. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью ISCO (0-30%) EtOAc в смеси гексанов с получением 7-бромгептилдиоктилфосфата (0,58 г, 1,16 ммоль, 6%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,03 (м, 6H); 3,43 (т, 2H); 1,88 (м, 2H); 1,70 (м, 6H); 1,54-1,23 (м, 26H); 0,90 (м, 6H).
Нонил-8-((7-((бис(октилокси)фосфорил)окси)гептил)(2-гидроксиэтил)амино)октаноат
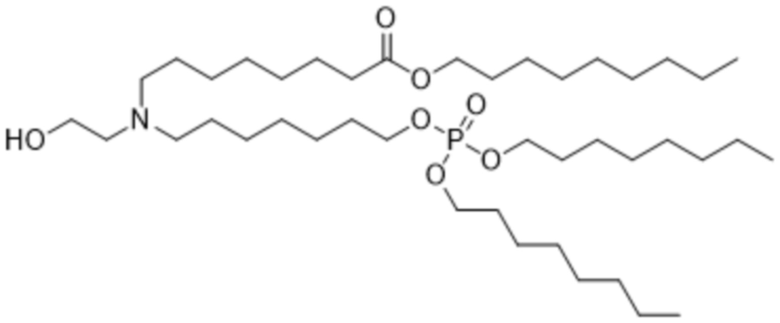
Химическая формула: C42H86NO7P
Молекулярная масса: 748,124
[00152] Соединение 131 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,22 мин. MС (ИЭР): m/z (MH+) 750,0 для C42H86NO7P. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,05 (м, 8H); 3,51 (м, 2H); 2,60 (уш. м, 2H); 2,46 (м, 4H); 2,31 (т, 2H); 1,76-1,15 (м, 58H); 0,90 (м, 9H).
CQ. Соединение 132: Декан-2-ил-8-((7-((бис(октилокси)фосфорил)окси)гептил)(2-гидроксиэтил)амино)октаноат
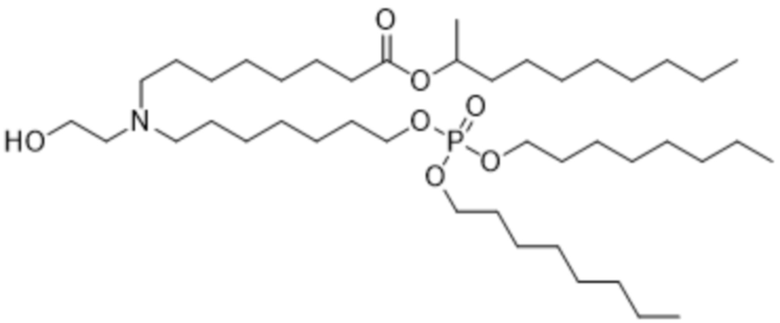
Химическая формула: C43H88NO7P
Молекулярная масса: 762,15
[00153] Соединение 132 синтезировали способом, аналогичным соединению 131 и согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,27 мин. MС (ИЭР): m/z (MH+) 764,00 для C43H88NO7P. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 1H); 4,03 (м, 6H); 3,56 (м, 2H); 2,73-2,38 (уш. м, 6H); 2,29 (т, 2H); 1,79-1,16 (м, 61H); 0,90 (м, 9H).
CR. Соединение 133: ((2-Гидроксиэтил)азандиил)бис(нонaн-9,1-диил) бис(2-гексилдеканоат)
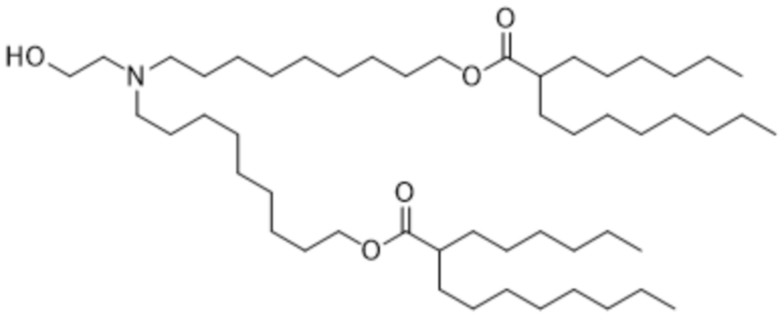
Химическая формула: C52H103NO5
Молекулярная масса: 822,398
[00154] Соединение 133 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,91 мин. MС (ИЭР): m/z (MH+) 824,0 для C52H103NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,09 (т, 4H); 3,60 (м, 2H); 2,74-2,42 (уш. м, 6H); 2,33 (м, 3H); 1,72 -1,17 (м, 76H); 0,90 (м, 12H).
CS. Соединение 134: 9-((2-Гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)нонил 2-гексилдеканоат
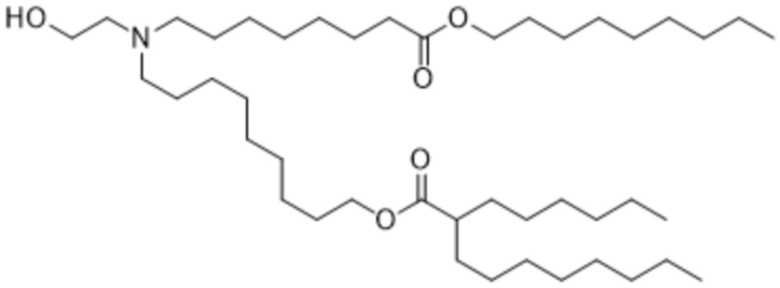
Химическая формула: C44H87NO5
Молекулярная масса: 710,182
[00155] Соединение 134 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,48 мин. MС (ИЭР): m/z (MH+) 712,0 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (м, 4H); 3,55 (м, 2H); 2,67-2,39 (уш. м, 6H); 2,31 (м, 3H); 1,71 -1,19 (м, 62H); 0,90 (м, 12H).
CT. Соединение 135: 7-((8-(Декан-2-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гептил 2-октилдеканоат
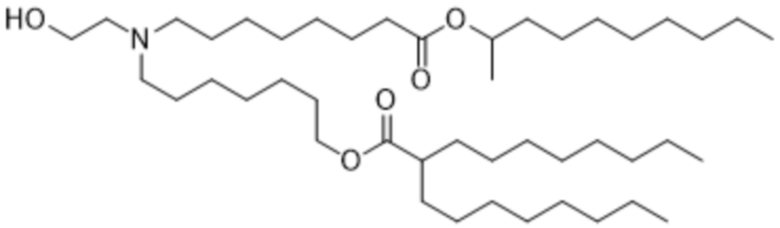
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00156] Соединение 135 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,63 мин. MС (ИЭР): m/z (MH+) 726,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 1H); 4,08 (т, 2H); 3,57 (м, 2H); 2,73-2,40 (уш. м, 6H); 2,29 (м, 3H); 1,71 -1,16 (м, 66H); 0,90 (м, 9H).
CU. Соединение 136: Нонил-8-((2-гидроксиэтил)((9Z,12Z)-октадека-9,12-диен-1-ил)амино)октаноат
Иллюстративный пример методики 2:
Нонил-8-бромоктаноат (Метод A)
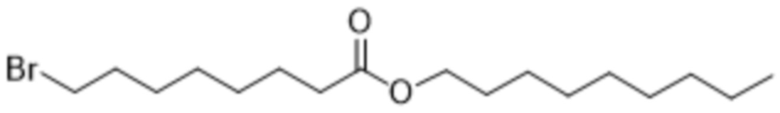
[00157] К раствору 8-бромоктановой кислоты (5 г, 22 ммоль) и нонан-1-ола (6,46 г, 45 ммоль) в дихлорметане (100 мл) прибавили N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид (4,3 г, 22 ммоль) и DMAP (547 мг, 4,5 ммоль). Реакционную смесь оставили перемешиваться при комн. темп. в течение 18 ч. Реакционную смесь разбавили дихлорметаном и промывали насыщенным раствором гидрокарбоната натрия. Органический слой отделили и промывали насыщенным водным раствором хлорида натрия, сушили над MgSO4. Органический слой отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле (0-10% этилацетат в смеси гексанов) с получением нонил-8-бромоктаноата (6,1 г, 17 ммоль, 77%).
[00158] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,06 (т, 2H); 3,40 (т, 2H); 2,29 (т, 2H); 1,85 (м, 2H); 1,72-0,97 (м, 22H); 0,88 (м, 3H).
Нонил-8-((2-гидроксиэтил)амино)октаноат
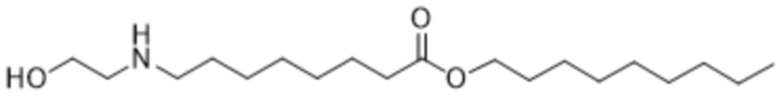
[00159] Раствор нонил-8-бромоктаноата (1,2 г, 3,4 ммоль) и 2-аминоэтан-1-ола (5 мл, 83 ммоль) в этаноле (2 мл) оставили перемешиваться при 62°C в течение 18 ч. Реакционную смесь концентрировали в вакууме и остаток экстрагировали этилацетатом и водой. Органический слой отделили и промывали водой, насыщенным водным раствором хлорида натрия и сушили над Na2SO4. Органический слой отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением нонил-8-((2-гидроксиэтил)амино)октаноата (295 мг, 0,9 ммоль, 26%).
[00160] СВЭЖХ/ДСИО: RT=1,29 мин. MС (ИЭР): m/z (MH+) 330,42 для C19H39NO3
[00161] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,07 (т, 2H); 3,65 (т, 2H); 2,78 (т, 2H); 2,63 (т, 2H); 2,32-2,19 (м, 4H); 1,73-1,20 (м, 24H); 0,89 (м, 3H)
Нонил-8-((2-гидроксиэтил)((9Z,12Z)-октадека-9,12-диен-1-ил)амино)октаноат
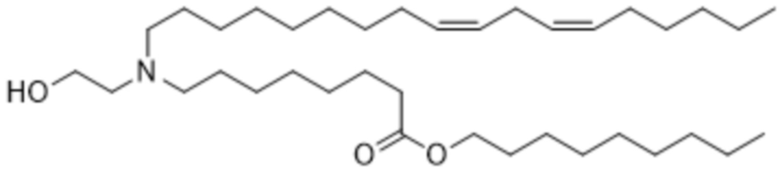
Химическая формула: C37H71NO3
Молекулярная масса: 577,98
[00162] Раствор нонил-8-((2-гидроксиэтил)амино)октаноата (150 мг, 0,46 ммоль), (6Z,9Z)-18-бромоктадека-6,9-диена (165 мг, 0,5 ммоль) и N, N-диизопропилэтиламина (65 мг, 0,5 ммоль) в этаноле (2 мл) оставили перемешиваться при кипячении с обратным холодильником в течение 48 ч. Реакционную смесь оставили охлаждаться до комн. темп. и растворители выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле (0-10% MeOH в дихлорметане) с получением нонил-8-((2-гидроксиэтил)((9Z,12Z)-октадека-9,12-диен-1-ил)амино)октаноата (81 мг, 0,14 ммоль, 30%) в виде соли HBr.
[00163] СВЭЖХ/ДСИО: RT=3,24 мин. MС (ИЭР): m/z (MH+) 578,64 для C37H71NO3
[00164] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 10,71 (br., 1H); 5,36 (уш. м, 4H); 4,04 (м, 4H); 3,22-2,96 (уш. м, 5H); 2,77 (м, 2H); 2,29 (м, 2H); 2,04 (уш. м, 4H); 1,86 (уш. м, 4H); 1,66-1,17 (уш. м, 40H); 0,89 (м, 6H)
CV. Соединение 137: Метил-12-(додецил(2-гидроксиэтил)амино)додеканоат
Метил-12-бромдодеканоат
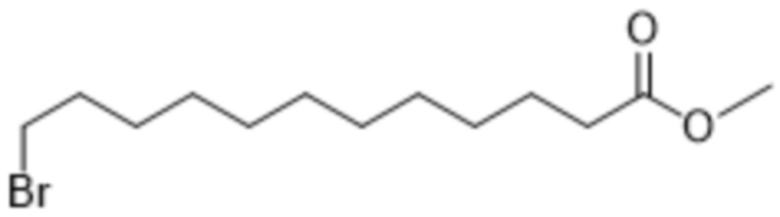
Химическая формула: C13H25BrO2
Молекулярная масса: 293,25
[00165] К раствору 12-бромдодекановой кислоты (2,5 г, 8,95 ммоль) в ТГФ (7 мл) прибавили метанол (7,2 мл, 179 ммоль). По каплям прибавили серную кислоту (0,50 мл, 8,95 ммоль) и реакционную смесь оставили перемешиваться при 65°C в течение двух часов. Реакционную смесь промывали 5% NaHCO3 и насыщенным водным раствором хлорида натрия. Органический слой сушили над безводным Na2SO4, отфильтровали и концентрировали в вакууме. Очистка с помощью хроматографии на силикагеле (0-20% EtOAc/смесь гексанов) позволила получить метил-12-бромдодеканоат (2,40 г, 92%).
[00166] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,69 (с, 3H); 3,44 (т, 2H); 2,33 (т, 2H); 1,88 (уш. м, 2H); 1,64 (уш. м, 2H); 1,45 (уш. м, 2H); 1,31 (уш. м, 12H).
Метил-12-(додецил(2-гидроксиэтил)амино)додеканоат
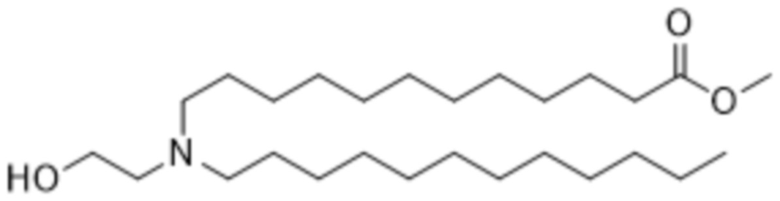
Химическая формула: C27H55NO3
Молекулярная масса: 441,74
[00167] К раствору метил-12-((2-гидроксиэтил)амино)додеканоата (413 мг, 1,51 ммоль) (выделенный из синтеза 12,12'-((2-гидроксиэтил)азандиил)дидодеканоата) в MeCN (5 мл) прибавили 1-бромдодекан (452 мг, 1,81 ммоль), K2CO3 (418 мг, 3,02 ммоль) и KI (25 мг, 0,151 ммоль). Реакционную смесь оставили перемешиваться при 82°C в течение 16 часов. Реакционную смесь охладили до комнатной температуры, разбавили H2O и экстрагировали EtOAc. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над Na2SO4, фильтровали и концентрировали в вакууме. Очистка с помощью хроматографии на силикагеле (0-100% [ДХМ, 20% MeOH, 1% NH4OH]/MeOH) позволила получить метил-12-(додецил(2-гидроксиэтил)амино)додеканоат (409 мг, 61%).
[00168] СВЭЖХ/ДСИО: RT=2,39 мин. MС (ИЭР): m/z (MH+) 442,60 для C27H55NO3
[00169] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,69 (с, 3H); 3,61 (т, 2H); 2,68 (т, 2H); 2,54 (т, 4H); 2,32 (т, 2H); 1,64 (м, 2H); 1,50 (уш. м, 4H); 1,28 (уш. м, 32H); 0,90 (т, 3H).
CW. Соединение 138: Динонил-8,8'-((2-гидроксиэтил)азандиил)диоктаноат
Иллюстративный пример методики 3:
Динонил-8,8'-((2-гидроксиэтил)азандиил)диоктаноат
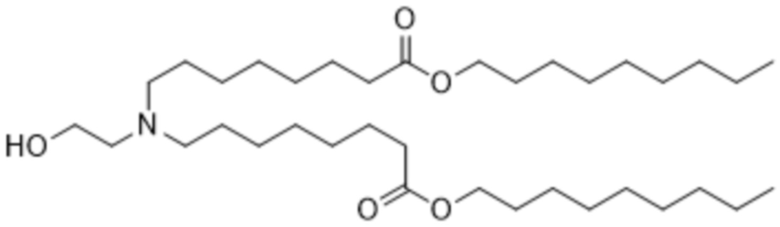
Химическая формула: C36H71NO5
Молекулярная масса: 597,97
[00170] Раствор нонил-8-бромоктаноата (200 мг, 0,6 ммоль) и 2-аминоэтан-1-ола (16 мг, 0,3 ммоль) и N, N-диизопропилэтиламина (74 мг, 0,6 ммоль) в ТГФ/CH3CN (1:1) (3 мл) оставили перемешиваться при 63°C в течение 72 ч. Реакционную смесь охладили до комн. темп. и растворители выпарили под вакуумом. Остаток экстрагировали этилацетатом и насыщенным раствором гидрокарбоната натрия. Органический слой отделили, сушили над Na2SO4 и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле (0-10% MeOH в дихлорметане) с получением динонил-8,8'-((2-гидроксиэтил)азандиил)диоктаноата (80 мг, 0,13 ммоль, 43%).
[00171] СВЭЖХ/ДСИО: RT=3,09 мин. MС (ИЭР): m/z (MH+) 598,85 для C36H71NO5
[00172] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,05 (м, 4H); 3,57 (уш. м, 2H); 2,71-2,38 (уш. м, 6H); 2,29 (м, 4H), 1,71-1,01 (уш. м, 49H), 0,88 (м, 6H).
CX. Соединение 139: Ди((Z)-нон-2-ен-1-ил)-8,8'-((2-гидроксиэтил)азандиил)диоктаноат
[00173] Соединение 139 синтезировали, следуя иллюстративному примеру методики 3.
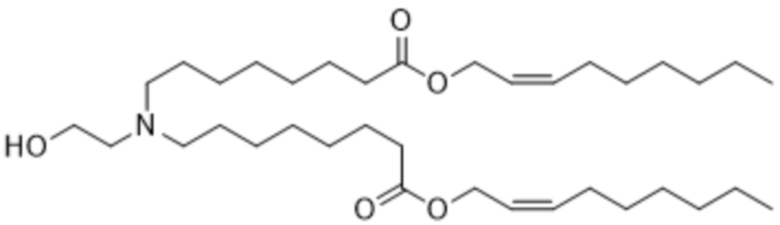
Химическая формула: C36H67NO5
Молекулярная масса: 593,93
[00174] СВЭЖХ/ДСИО: RT=2,88 мин. MС (ИЭР): m/z (MH+) 594,78 для C36H67NO5
[00175] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,60 (м, 2H); 5,50 (м, 2H); 4,59 (м, 4H); 3,96 (уш. м, 2H); 3,20-2,94 (уш. м, 5H); 2,28 (м, 4H); 2,07 (м, 4H); 1,80 (br. m 4H); 1,59 (уш. м, 6H); 1,43-1,14 (уш. м, 28H), 0,85 (м, 6H).
CY. Соединение 140: Ди((Z)-ундец-2-ен-1-ил)-6,6'-((2-гидроксиэтил)азандиил)дигексаноат
[00176] Соединение 140 синтезировали, следуя иллюстративному примеру методики 3.
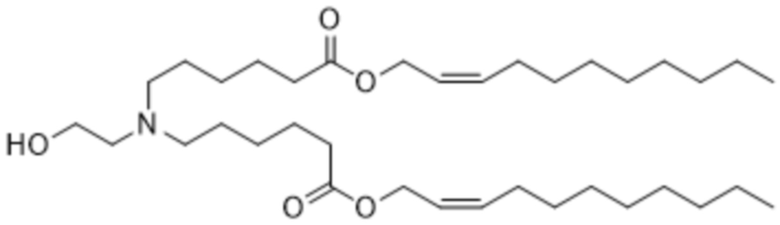
Химическая формула: C36H67NO5
Молекулярная масса: 593,93
[00177] СВЭЖХ/ДСИО: RT=2,87 мин. MС (ИЭР): m/z (MH+) 594,74 для C36H67NO5
[00178] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,73-5,44 (м, 4H); 4,62 (м, 4H); 3,55 (м, 2H); 2,73-2,39 (уш. м, 6H); 2,39 (м, 4H); 2,09 (м, 4H); 1,64 (м, 4H); 1,55-1,14 (уш. м, 33H); 0,88 (м, 6H).
CZ. Соединение 141: Диундецил-6,6'-((2-гидроксиэтил)азандиил)дигексаноат
[00179] Соединение 141 синтезировали, следуя иллюстративному примеру методики 3.
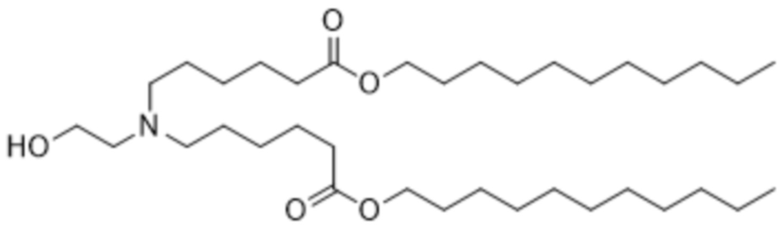
Химическая формула: C36H71NO5
Молекулярная масса: 597,97
[00180] СВЭЖХ/ДСИО: RT=3,03 мин. MС (ИЭР): m/z (MH+) 598,63 для C36H71NO5
[00181] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,05 (м, 4H); 3,53 (м, 2H); 2,95 (уш. м, 1H); 2,65-2,35 (м, 6H); 2,30 (м, 4H); 1,73-1,54 (м, 8H); 1,54-1,15 (м, 40H); 0,88 (м, 6H).
DA. Соединение 142: 12,12'-((2-Гидроксиэтил)азандиил)дидодеканоат
12,12'-((2-Гидроксиэтил)азандиил)дидодеканоат
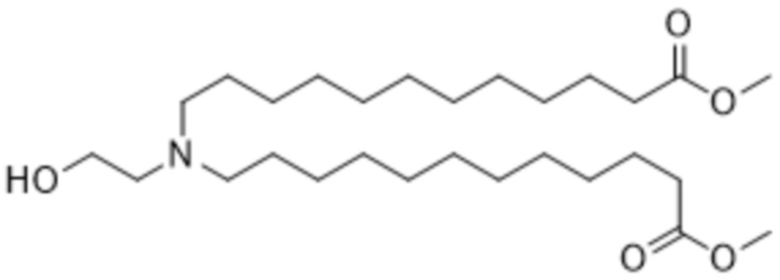
Химическая формула: C28H55NO5
Молекулярная масса: 485,75
[00182] К раствору метил 12-бромдодеканоата (1,5 г, 5,12 ммоль) в MeCN (11 мл) прибавили этаноламин (0,310 мл, 5,12 ммоль), K2CO3 (1,42 г, 10,2 ммоль) и KI (85 мг, 0,512 ммоль). Реакционную смесь оставили перемешиваться при 82°C в течение 16 часов. Реакционную смесь охладили до комнатной температуры, отфильтровали и твердые вещества промывали смесью гексанов. Фильтрат экстрагировали смесью гексанов и объединенные экстракты концентрировали в вакууме. Очистка с помощью хроматографии на силикагеле (0-100% [ДХМ, 20% MeOH, 1% NH4OH]/MeOH) позволила получить 12,12'-((2-гидроксиэтил)азандиил)дидодеканоат (563 мг, 45%).
[00183] СВЭЖХ/ДСИО: RT=1,81 мин. MС (ИЭР): m/z (MH+) 486,63 для C28H55NO5
[00184] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,69 (с, 6H); 3,59 (уш. м, 2H); 2,75-2,40 (уш. м, 6H); 2,32 (т, 4H); 1,64 (м, 4H); 1,48 (уш. м, 4H); 1,29 (уш. м, 28H).
DB. Соединение 143: Нонил-8-((2-гидроксиэтил)(7-((2-октилдецил)окси)-7-оксогептил)амино)октаноат
2-Октилдекановая кислота
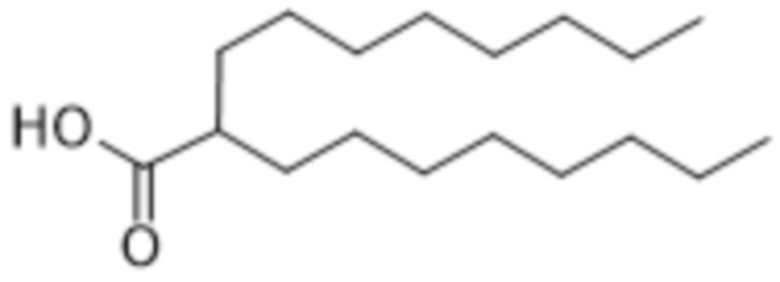
Химическая формула: C18H36O2
Молекулярная масса: 284,48
[00185] Раствор диизопропиламин (2,92 мл, 20,8 ммоль) в ТГФ (10 мл) охладили до -78°C и прибавили раствор n-BuLi (7,5 мл, 18,9 ммоль,2,5 M в смеси гексанов). Реакционную смесь оставили нагреваться до 0°C. К раствору декановой кислоты (2,96 г, 17,2 ммоль) и NaH (754 мг, 18,9 ммоль, 60% мас./мас.) в ТГФ (20 мл) при 0°C прибавили раствор ЛДА и смесь оставили перемешиваться при комн. темп. в течение 30 мин. Через указанное время прибавили 1-иодоктан (5 г, 20,8 ммоль) и реакционную смесь нагревали при 45°C в течение 6 ч. Реакционную смесь погасили 1N HCl (10 мл). Органический слой сушили над MgSO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле (0-20% этилацетат в смеси гексанов) с выходом 2-октилдекановой кислоты (1,9 г, 6,6 ммоль).
[00186] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 2,38 (уш. м, 1H); 1,74-1,03 (уш. м, 28H); 0,91 (м, 6H).
2-Октилдекан-1-ол

Химическая формула: C18H38O
Молекулярная масса: 270,50
[00187] Раствор 2-октилдекановой кислоты (746 мг, 2,6 ммоль) в сухом ТГФ (12 мл) прибавили к перемешиваемому раствору ЛАГ (5,2 мл, 5,2 ммоль, 1M раствор в ТГФ) в сухом ТГФ (6 мл) в атмосфере азота при 0°C. Реакционную смесь оставили нагреваться до комн. темп. и перемешивали при комн. темп. в течение 12 ч. Прибавили насыщенный раствор Na2SO4*10H2O (10 мл). Твердые вещества отфильтровали через слой целита. Фильтрат выпарили под вакуумом и остаток очищали с помощью хроматографии на силикагеле (0-20% этилацетат в смеси гексанов) с выходом 2-октилдекан-1-ола (635 мг, 2,3 ммоль).
[00188] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,54 (д, 2H); 1,56-1,21 (уш. м, 30H); 0,91 (т, 6H).
2-Октилдецил-7-бромгептаноат
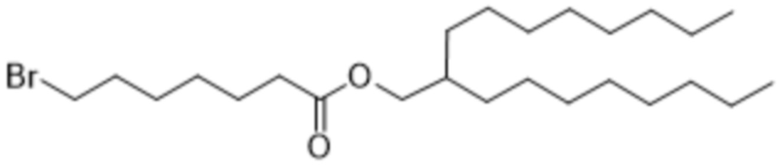
[00189] 2-Октилдецил-7-бромгептаноат синтезировали согласно методу A.
[00190] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,96 (д, 2H); 3,40 (т, 2H); 2,31 (т, 2H); 1,86 (м, 2H); 1,71-1,19 (м, 35H); 0,88 (м, 6H).
[00191] Нонил-8-((2-гидроксиэтил)(7-((2-октилдецил)окси)-7-оксогептил)амино)октаноат синтезировали, используя иллюстративный пример методики 2.
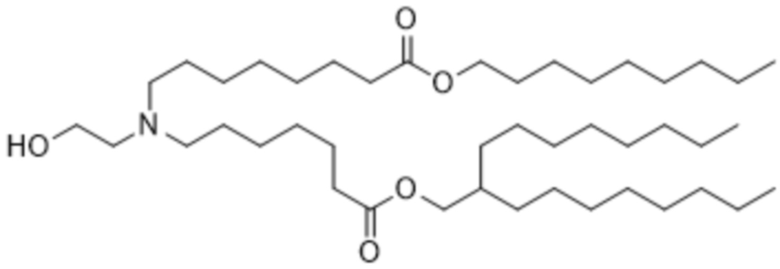
Химическая формула: C44H87NO5
Молекулярная масса: 710,182
[00192] СВЭЖХ/ДСИО: RT=5,23 мин. MС (ИЭР): m/z (MH+) 711,08 для C44H87NO5
[00193] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,05 (т, 2H); 3,96 (д, 2H); 3,58 (уш. м, 2H); 2,79-2,36 (уш. м, 5H); 2,30 (м, 4H); 1,72-1,01 (уш. м, 63H); 0,88 (м, 9H).
DC. Соединение 144: Нонил-8-((8-(диоктиламино)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
8-Бром-N, N-диоктилоктанамид

Химическая формула: C24H48BrNO
Молекулярная масса: 446,56
[00194] К раствору 8-бромоктановой кислоты (1 г, 2,2 ммоль) и ДМФА (1 капля) в дихлорметане по каплям прибавили оксалилхлорид (0,416 мл, 2,5 ммоль). Реакционную смесь оставили перемешиваться в течение 1 ч при комнатной температуре. Растворители выпарили и остаток прибавили к раствору диоктиламина (1,14 г, 4,8 ммоль) и DMAP (100 мг, 0,8 ммоль). Триэтиламин прибавили к реакционной смеси по каплям и реакционную смесь оставили перемешиваться в течение 18 ч. Растворители выпарили и остаток перенесли в этилацетат и насыщенный NaHCO3. Органический слой отделили и промывали водой и насыщенным водным раствором хлорида натрия. Органический раствор сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане с выходом смеси 8-бром-N, N-диоктилоктанамида и хлорo-N, N-диоктилоктанамида (736 мг, 1,6 ммоль).
[00195] СВЭЖХ/ДСИО: RT=4,02 мин. MС (ИЭР): m/z (MH+) 446,53 для C24H48BrNO
[00196] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,55 (т, 0,6H); 3,42 (т, 1,4H); 3,36-3,15 (м, 4H); 2,31 (т, 2H); 1,96-1,18 (м, 34H); 0,91 (м, 6H).
[00197] Нонил-8-((8-(диоктиламино)-8-оксооктил)(2-гидроксиэтил)амино)октаноат синтезировали, используя иллюстративный пример методики 2.

Химическая формула: C43H86N2O4
Молекулярная масса: 695,17
[00198] СВЭЖХ/ДСИО: RT=4,24 мин. MС (ИЭР): m/z (MH+) 696,16 для C43H86N2O4
[00199] 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,05 (т, 2H); 3,57 (уш. м, 2H); 3,35-3,14 (м, 4H); 2,80-,2,20 (м, 10H); 1,74-1,00 (уш. м, 59H); 0,88 (м, 9H).
DD. Соединение 145: Гептадекан-9-ил-8-((2-гидроксиэтил)(8-(метил(октил)амино)-8-оксооктил)амино)октаноат
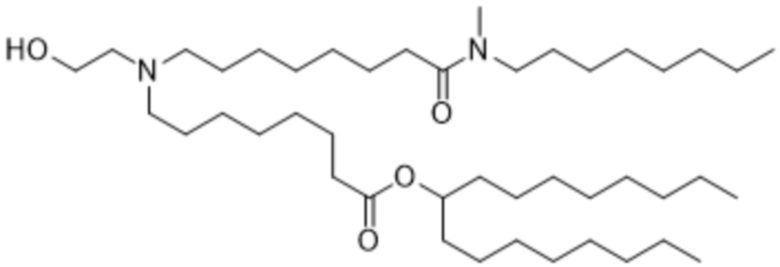
Химическая формула: C44H88N2O4
Молекулярная масса: 709,198
[00200] Соединение 145 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,17 мин. MС (ИЭР): m/z (MH+) 710,0 для C44H88N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 3,55 (м, 2H); 3,37 (т, 1H); 3,27 (т, 1H); 2,98 (с, 1,5H); 2,93 (с, 1,5H); 2,59 (м, 2H); 2,47 (м, 4H); 2,30 (м, 4H), 1,75-1,20 (м, 60H); 0,90 (м, 9H).
DE. Соединение 146: Гептадекан-9-ил-8-((2-гидроксиэтил)(6-(метил(октил)амино)-6-оксогексил)амино)октаноат
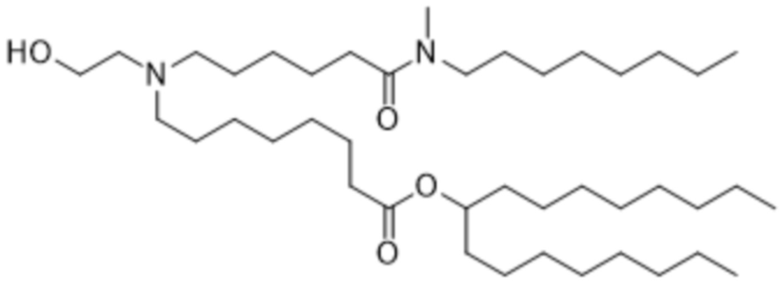
Химическая формула: C42H84N2O4
Молекулярная масса: 681,144
[00201] Соединение 146 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,01 мин. MС (ИЭР): m/z (MH+) 682,0 для C42H84N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (м, 1H); 3,55 (м, 2H); 3,37 (т, 1H); 3,26 (т, 1H); 2,98 (с, 1,5H); 2,93 (с, 1,5H); 2,59 (м, 2H); 2,48 (м, 4H); 2,31 (м, 4H), 1,76-1,18 (м, 56H); 0,90 (м, 9H).
DF. Соединение 147: Тридекан-7-ил-10-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)деканоат
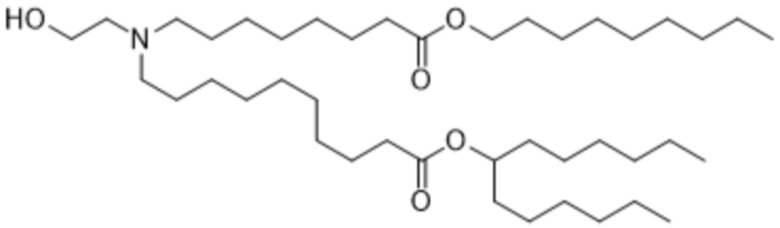
Химическая формула: C42H83NO5
Молекулярная масса: 682,128
[00202] Соединение 147 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,16 мин. MС (ИЭР): m/z (MH+) 683,0 для C42H83NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (м, 2H); 3,55 (м, 2H); 2,59 (м, 2H); 2,46 (м, 4H); 2,30 (м, 4H), 1,72-1,18 (м, 58H); 0,90 (м, 9H).
DG. Соединение 148: Гептадекан-9-ил-8-((2-гидроксиэтил)(8-((2-метоксинонил)окси)-8-оксооктил)амино)октаноат
1-((трет-Бутилдифенилсилил)окси)нонан-2-ол

Химическая формула: C25H38O2Si
Молекулярная масса: 398,662
[00203] TBDPSCl (8,58 г, 31,2 ммоль) прибавили к смеси нонан-1,2-диoла (5,0 г, 31,2 ммоль) и имидазола (4,24 г, 62,4 ммоль) в ДМФА при комн. темп. Реакционную смесь перемешивали при комн. темп. в течение ночи. Реакционную смесь разбавили водой (150 мл) и экстрагировали EtOAc/смесь гексанов (1:1) (4X). Объединенный органический слой промывали насыщенным водным раствором хлорида натрия, отделяли, сушили над Na2SO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью ISCO с (0-10%) EtOAc в смеси гексанов с получением 1-((трет-бутилдифенилсилил)окси)нонан-2-ола (7,75 г, 19,4 ммоль). 1H ЯМР (300 МГц, ДМСО) δ: м.д. 7,63 (м, 4H); 7,43 (м, 6H); 4,51 (д, 1H); 3,54 (м, 2H); 3,43 (м, 1H); 1,57 (м, 1H); 1,24 (м, 11H); 1,00 (с, 9H); 0,85 (м, 3H).
2-Mетоксинонил-8-бромоктаноат
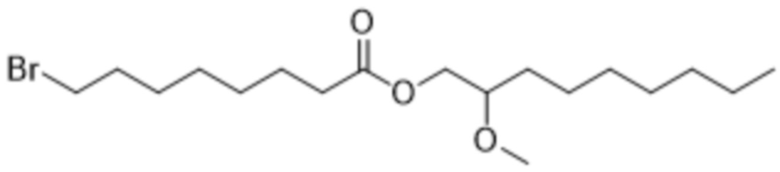
Химическая формула: C18H35BrO3
Молекулярная масса: 379,379
[00204] 2-Mетоксинонил-8-бромоктаноат синтезировали, следуя методу A в иллюстративном примере методики 1. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,19 (м, 1H); 4,04 (м, 1H); 3,42 (м, 6H); 2,36 (т, 2H); 1,87 (м, 2H); 1,73-1,22 (м, 20H); 0,93 (м, 3H).
Гептадекан-9-ил-8-((2-гидроксиэтил)(8-((2-метоксинонил)окси)-8-оксооктил)амино)октаноат
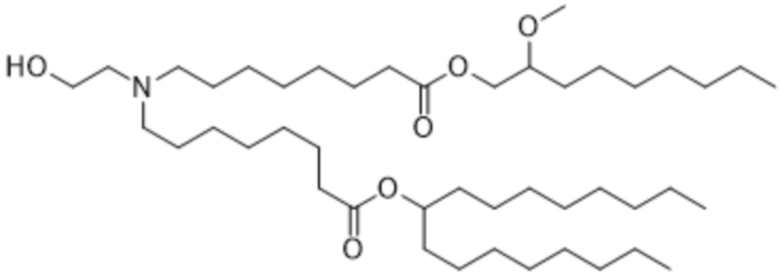
Химическая формула: C45H89NO6
Молекулярная масса: 740,208
[00205] Соединение 148 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,48 мин. MС (ИЭР): m/z (MH+) 741,0 для C45H89NO6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,19 (м, 1H); 4,04 (м, 1H); 3,57 (м, 2H); 3,42 (с, 3H); 3,37 (м, 1H); 2,73-2,41 (м, 6H); 2,33 (м, 4H), 1,73-1,19 (м, 61H); 0,90 (м, 9H).
DH. Соединение 149: Гептил-10-((8-(гептадекан-9-илокси)-8-оксооктил)(метил)амино)деканоат
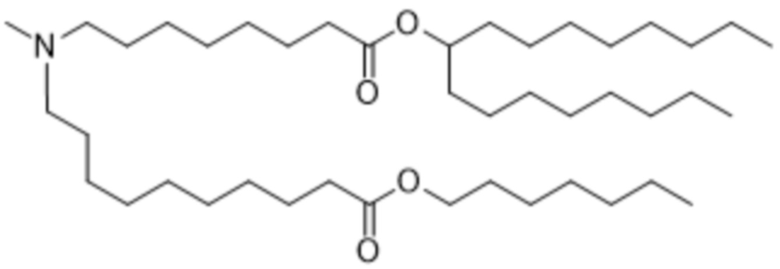
Химическая формула: C43H85NO4
Молекулярная масса: 680,156
[00206] Соединение 149 синтезировали аналогично соединению 123 и согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,55 мин. MС (ИЭР): m/z (MH+) 681,0 для C43H85NO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 2,42-2,14 (м, 11H); 1,73-1,17 (м, 62H); 0,90 (м, 9H).
DI. Соединение 150: Пентил-12-((8-(гептадекан-9-илокси)-8-оксооктил)(метил)амино)додеканоат
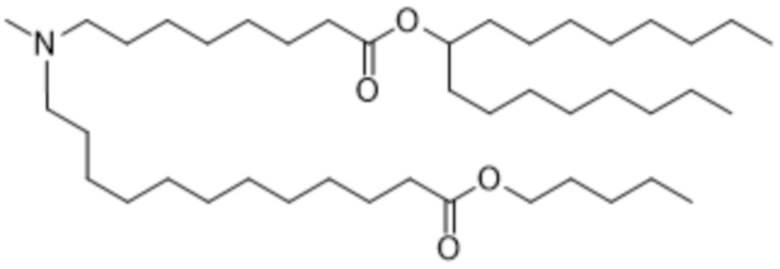
Химическая формула: C43H85NO4
Молекулярная масса: 680,156
[00207] Соединение 150 синтезировали аналогично соединению 123 и согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,47 мин. MС (ИЭР): m/z (MH+) 681,0 для C43H85NO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 2,42-2,16 (м, 10H); 1,73-1,20 (м, 63H); 0,90 (м, 9H).
DJ. Соединение 151: 7-((7-(Деканоилокси)гептил)(2-гидроксиэтил)амино)гептил-2-октилдеканоат
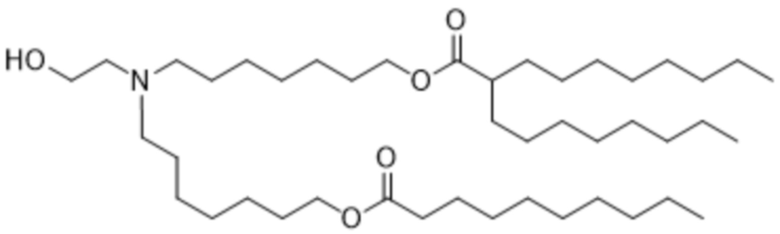
Химическая формула: C44H87NO5
Молекулярная масса: 710,182
[00208] Соединение 151 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,83 мин. MС (ИЭР): m/z (MH+) 711,0 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,07 (м, 4H); 3,57 (м, 2H); 2,63 (уш. м, 2H); 2,50 (м, 4H); 2,31 (м, 3H), 1,71-1,19 (м, 62H); 0,90 (м, 9H).
DK. Соединение 152: Нонил-(Z)-8-((2-гидроксиэтил)(10-октилоктадец-8-ен-1-ил)амино)октаноат
N-Mетокси-N-метил-2-октилдеканамид
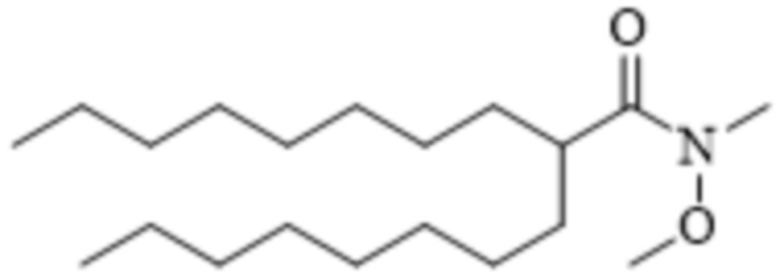
Химическая формула: C20H41NO2
Молекулярная масса: 327,553
[00209] К раствору 2-октил-декановой кислоты (11,1 г, 39,02 ммоль) и ДМФА (0,05 мл, 3,9 ммоль) вДХМ (100 мл) по каплям прибавили оксалилхлорид (3,63 мл, 42,92 ммоль). Реакционную смесь оставили перемешиваться в течение 2 ч при комн. темп. Растворители и летучие вещества выпарили под вакуумом. Полученный остаток (сырой 2-октилдеканoилхлорид) (11,82 г, 39,02 ммоль) перенесли в ДХМ (100 мл) и N, O-диметилгидроксиламин гидрохлорид (4 г, 40,97 ммоль) и прибавили 4-диметиламинопиридин (0,48 г, 3,9 ммоль). Смесь оставили охлаждаться до 0°C и медленно прибавили триэтиламин (19,04 мл, 136,57 ммоль). Реакционную смесь оставили нагреваться до комн. темп. и перемешивали в течение 1 ч. Растворители выпарили под вакуумом. Остаток разбавили EtOAc и промывали насыщ. NaHCO3, с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-40%) EtOAc в смеси гексанов с получением N-метокси-N-метил-2-октилдеканамида (7,10 г, 21,68 ммоль, 56%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,70 (с, 3H); 3,22 (с, 3H); 2,82 (уш. м, 1H); 1,62 (м, 2H); 1,51-1,19 (м, 26H); 0,90 (м, 6H).
2-Октилдеканaль
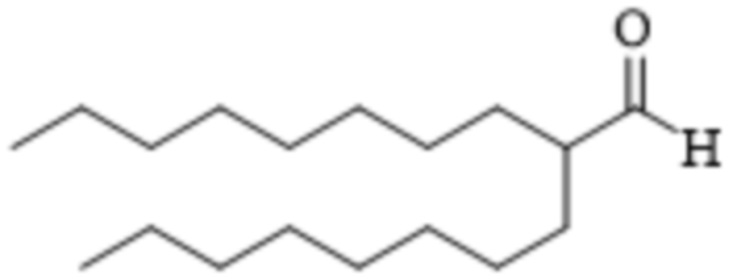
Химическая формула: C18H36O
Молекулярная масса: 268,485
[00210] Раствор N-метокси-N-метил-2-октилдеканамида (7,1 г, 21,68 ммоль) в сухом ТГФ (2 мл) прибавили к суспензии ЛАГ (27,53 мл 1 M в ТГФ, 27,53 ммоль) в сухом ТГФ (5 ил) прт -45°C. Полученную суспензию перемешивали в течение 1 ч при -45°C, через указанное время оставили нагреваться до комнатной температуры и перемешивали в течение 0,5 ч. Реакционную смесь обратно охладили до -45°C и погасили насыщ. водным раствором декагидрата сульфата натрия (2 мл). Смесь перемешивали в течение 20 мин при комнатной температуре и отфильтровали через слой целита. Фильтрат промывали насыщенным водным раствором хлорида натрия. Органический слой отделили, сушили над сульфатом натрия, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле с (0-10%) EtOAc в смеси гексанов с получением 2-октилдеканaля (4,45 г, 16,57 ммоль, 76%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 9,58 (д, 1H); 2,23 (м, 1H); 1,63 (м, 2H); 1,53-1,19 (м, 26H); 0,90 (м, 6H).
(Z)-10-Октилоктадец-8-ен-1-ол
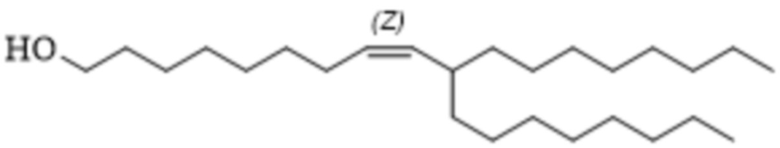
Химическая формула: C26H52O
Молекулярная масса: 380,701
[00211] Раствор (8-гидроксиоктил)трифенилфосфоний бромида (3,68 г, 7,81 ммоль) в ТГФ (16 мл) и HMPA охладили на ледяной бане и прибавили NaHMDS (19,52 мл 1 M, 19,52 ммоль). 2-Октилдеканaль (1,05 г, 3,9 ммоль) вТГФ (5 мл) медленно прибавили и реакционную смесь нагревали до 30°C. Через 16 ч реакционную смесь разбавили 20 мл воды и подкислили 2N HCl. Реакционную смесь экстрагировали EtOAc (3×50 мл). Объединенные органические экстракты сушили над сульфатом натрия, отфильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (0-50%) EtOAc в смеси гексанов с получением (Z)-10-октилоктадец-8-ен-1-ола (0,5 г, 1,30 ммоль, 33%). 1H ЯМР (300 МГц, CDCl3)δ: м.д. 5,24 (м, 1H); 4,90 (м, 1H); 3,53 (т, 2H); 2,14 (м, 1H); 1,89 (м, 2H); 1,45 (м, 3H); 1,33-0,95 (м, 36H); 0,77 (м, 6H).
(Z)-1-Бром-10-октилоктадец-8-ен
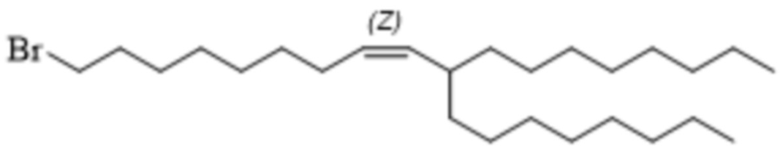
Химическая формула: C26H51Br
Молекулярная масса: 443,598
[00212] К раствору PPh3 (0,29 г, 1,11 ммоль) и (8Z)-10-октилоктадец-8-ен-1-ола (0,4 г, 1,05 ммоль) в ДХМ (10 мл) при 0°C, одной порцией прибавили NBS (0,22 г, 1,22 ммоль). Реакционную смесь оставили перемешиваться при 0°C в течение 1 ч и затем нагревали до комн. темп.и перемешивали в течение 1 ч. Прибавили 300 мл смеси гексанов и смесь отфильтровали через слой силикагеля и выпарили под вакуумом. Прибавили 200 мл смеси гексанов и смесь отфильтровали через слой силикагеля и выпарили под вакуумом с получением (Z)-1-бром-10-октилоктадец-8-ена (0,39 г, 0,88 ммоль, 83%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,24 (м, 1H); 4,90 (м, 1H); 3,53 (т, 2H); 2,14 (м, 1H); 1,89 (м, 2H); 1,45 (м, 3H); 1,33-0,95 (м, 36H); 0,77 (м, 6H).
Нонил-(Z)-8-((2-гидроксиэтил)(10-октилоктадец-8-ен-1-ил)амино)октаноат
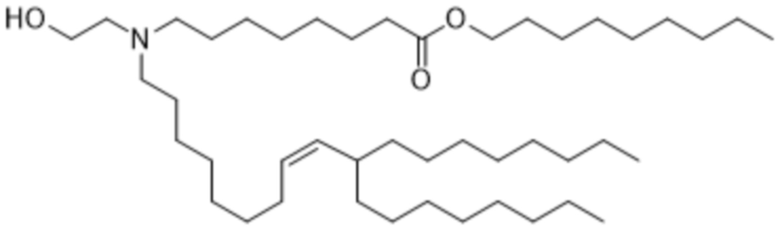
Химическая формула: C45H89NO3
Молекулярная масса: 693,211
[00213] Соединение 152 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,00 мин. MС (ИЭР): m/z (MH+) 694,0 для C45H89NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,36 (м, 1H); 5,03 (м, 1H); 4,07 (т, 2H); 3,54 (т, 2H); 2,59 (т, 2H); 2,46 (м, 4H); 2,30 (м, 3H); 2,01 (м, 2H); 1,63 (м, 4H); 1,53-1,03 (м, 58H); 0,90 (м, 9H).
DL. Соединение 153: Нонил-8-((2-гидроксиэтил)(10-октилоктадецил)амино)октаноат
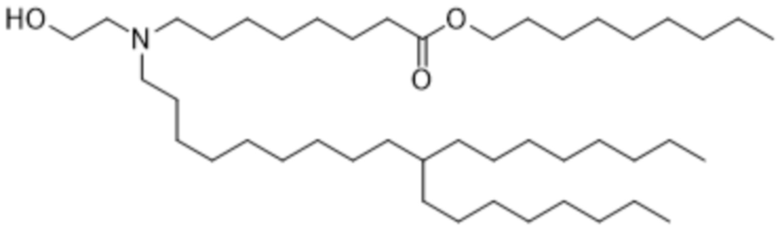
Химическая формула: C45H91NO3
Молекулярная масса: 694,227
[00214] В колбу загрузили Pd(OH)2 (20 мг) и продули N2. Прибавили раствор нонил-8-[(2-гидроксиэтил)[(8Z)-10-октилоктадец-8-ен-1-ил]амино]октаноата (100 мг, 0,14 ммоль) в EtOH (1 мл). Реакционную смесь продували H2 и поместили в атмосферу H2 (баллон) при перемешивании в течение 16 ч при комн. темп. Через указанное время реакционную смесь продували N2. Реакционную смесь отфильтровали через слой целита и промывали EtOH (50 мл). Фильтрат выпарили под вакуумом. Остаток растворили в EtOAc и промывали водой. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-50%) (1%, 20% MeOH в ДХМ) в ДХМ с получением нонил-8-((2-гидроксиэтил)(10-октилоктадецил)амино)октаноата (0,069 г, 0,099 ммоль, 69%). СВЭЖХ/ДСИО: RT=3,21 мин. MС (ИЭР): m/z (MH+) 695,08 для C45H91NO3. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 2H); 3,56 (т, 2H); 2,62 (м, 2H); 2,48 (м, 4H); 2,31 (м, 2H); 1,64 (м, 4H); 1,54-1,16 (м, 66H); 0,90 (м, 9H).
DM. Соединение 154: Гептадекан-9-ил-8-((2-(2-гидроксиэтокси)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
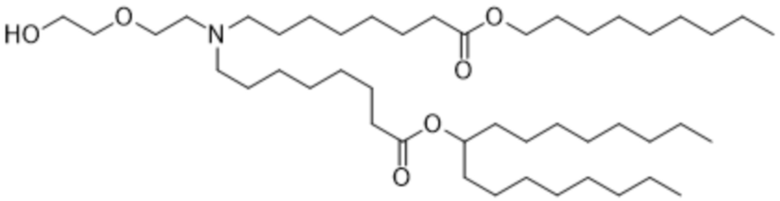
Химическая формула: C46H91NO6
Молекулярная масса: 754,235
[00215] Соединение 154 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,54 мин. MС (ИЭР): m/z (MH+) 755,0 для C46H91NO6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (м, 1H); 4,62 (м, 1H); 4,08 (т, 2H); 3,79-3,56 (м, 6H); 2,64 (м, 2H); 2,47 (м, 4H); 2,31 (м, 4H), 1,73-1,20 (м, 61H); 0,90 (м, 9H).
DN. Соединение 155: трет-Бутил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
трет-Бутил-8-бромоктаноат
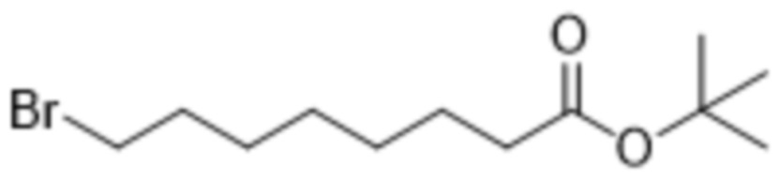
Химическая формула: C12H23BrO2
Молекулярная масса: 279,218
[00216] К раствору 8-бромоктановой кислоты (2 г, 8,96 ммоль) в ДХМ (20 мл) при 0°C по каплям прибавили трифторуксусный ангидрид (2,77 мл, 19,9 ммоль). Через 2,5 ч медленно прибавили tBuOH (3,1 мл, 32,27 ммоль). Через 1 ч реакционную нагревали до комн. темп. и оставили перемешиваться в течение 2,5 ч. Реакционную смесь погасили водой и экстрагировали диэтиловым эфиром. Органический слой отделили, сушили над MgSO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле (0-10%) с EtOAc в смеси гексанов с получением трет-бутил-8-бромоктаноата (1,5 г, 5,37 ммоль, 60%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,42 (т, 2H); 2,23 (т, 2H); 1,87 (м, 2H); 1,60 (м, 2H); 1,47 (с, 11H); 1,35(м, 4H).
трет-Бутил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
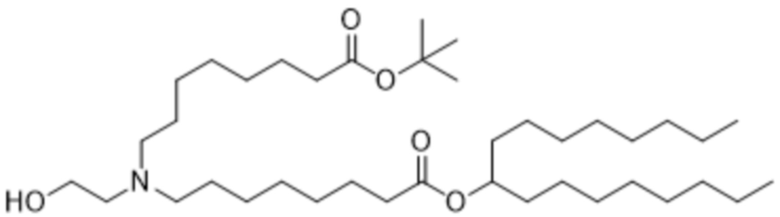
Химическая формула: C39H77NO5
Молекулярная масса: 640,047
[00217] Соединение 155 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,18 мин. MС (ИЭР): m/z (MH+) 641,0 для C39H77NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 3,58 (уш. м, 2H); 2,75-2,36 (уш. м, 6H); 2,26 (м, 4H); 1,71-1,40 (м, 22H); 1,28 (м, 35H); 0,90 (м, 6H).
DO. Соединение 156: Гептадекан-9-ил-8-((1,3-дигидроксипропан-2-ил)(8-(нонилокси)-8-оксооктил)амино)октаноат
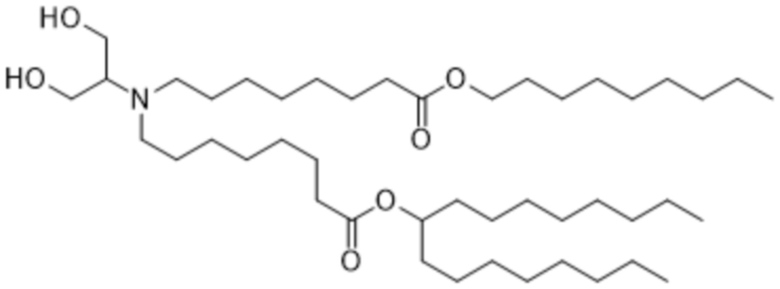
Химическая формула: C45H89NO6
Молекулярная масса: 740,208
[00218] Соединение 156 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,53 мин. MС (ИЭР): m/z (MH+) 741,0 для C45H89NO6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (м, 1H); 4,08 (т, 2H); 3,67 (уш. м, 4H); 3,04 (м, 1H); 2,65 (м, 4H); 2,32 (м, 4H), 1,72-1,44 (м, 15H); 1,28 (м, 48H); 0,90 (м, 9H).
DP. Соединение 157: Гептадекан-9-ил-8-((1-гидроксипропан-2-ил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00219] Соединение 157 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,56 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,45-3,17 (уш. м, 2H); 2,94 (уш. м, 1H); 2,55-2,22 (м, 8H); 1,70-1,17 (м, 62H); 0,90 (м, 12H).
DQ. Соединение 158: трет-Бутил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
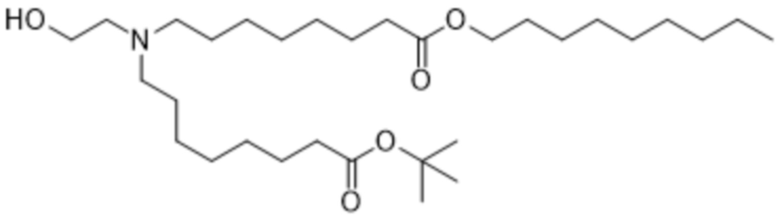
Химическая формула: C31H61NO5
Молекулярная масса: 527,831
[00220] Соединение 158 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,23 мин. MС (ИЭР): m/z (MH+) 528,0 для C31H61NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 2H); 3,55 (уш. м, 2H); 2,60 (уш. м, 2H); 2,47 (м, 4H); 2,31 (т, 2H); 2,22 (т, 2H); 1,64 (уш. м, 6H); 1,53-1,23 (м, 37H); 0,90 (м, 3H).
DR. Соединение 159: Гептадекан-9-ил-8-((2-гидроксиэтил)(2-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)этил)амино)октаноат
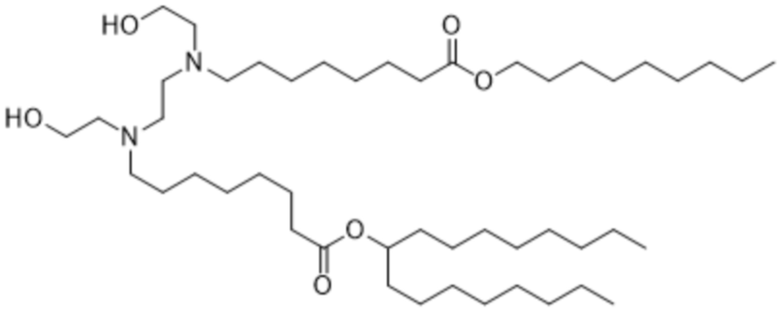
Химическая формула: C48H96N2O6
Молекулярная масса: 797,304
[00221] Соединение 159 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,15 мин. MС (ИЭР): m/z (MH+) 798,0 для C48H96N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (м, 1H); 4,07 (т, 2H); 3,62 (уш. м, 4H); 2,72-2,47 (уш. м, 12H); 2,31 (м, 4H); 1,72-1,42 (м, 14H); 1,28 (м, 47H); 0,90 (м, 12H).
DS. Соединение 160: 1,5-Бис(2-бутилциклопропил)пентан-3-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
2-(2-Бутилциклопропил)этан-1-ол

Химическая формула: C9H18O
Молекулярная масса: 142,242
[00222] 2-(2-Бутилциклопропил)этан-1-ол способом, аналогичным синтезу промежуточному соединению C. 1H ЯМР (300 МГц, CDCl3) δ: м.д.: 3,94 (т, 2H); 1,93 (м, 1H); 1,59 (м, 7H); 1,39 (м, 1H); 1,12 (м, 3H); 0,90 (м, 3H); 0,00 (м, 1H).
1-(2-Бромэтил)-2-бутилциклопропан
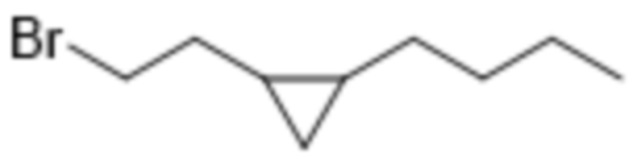
Химическая формула: C9H17Br
Молекулярная масса: 205,139
[00223] 1-(2-Бромэтил)-2-бутилциклопропан синтезировали способом, аналогичным синтезу (Z)-1-бром-10-октилоктадец-8-ена. 1H ЯМР (300 МГц, CDCl3) δ: м.д.: 3,64 (т, 2H); 2,18 (м, 1H); 1,92 (м, 1H); 1,47 (м, 6H); 0,96 (м, 6H); 0,00 (м, 1H).
1,5-Бис(2-бутилциклопропил)пентан-3-ол
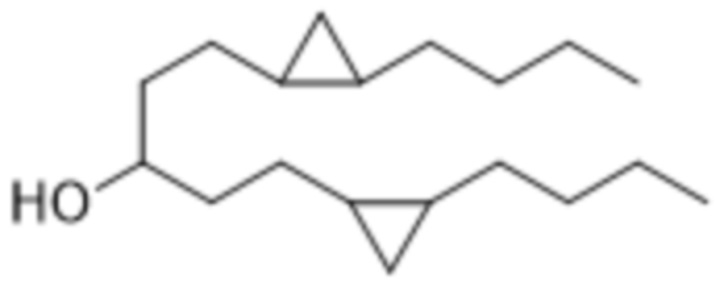
Химическая формула: C19H36O
Молекулярная масса: 280,496
[00224] 1,5-Бис(2-бутилциклопропил)пентан-3-ол синтезировали способом, аналогичным синтезу (5Z,12Z)-гептадека-5,12-диен-9-ола. 1H ЯМР (300 МГц, CDCl3) δ: м.д.: 3,96 (т, 1H); 1,64 (м, 21H); 1,16 (м, 6H); 0,91 (м, 6H); 0,03 (м, 2H).
1,5-Бис(2-бутилциклопропил)пентан-3-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
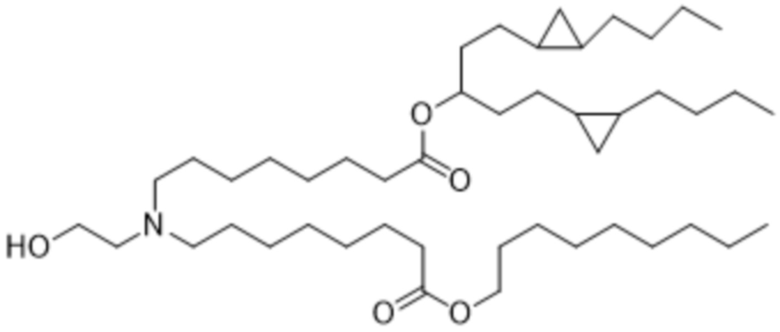
Химическая формула: C46H87NO5
Молекулярная масса: 734,204
[00225] Соединение 160 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,51 мин. MС (ИЭР): m/z (MH+) 735,0 для C46H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,97 (м, 1H); 4,08 (т, 2H); 3,56 (уш. м, 2H); 2,75-2,37 (уш. м, 6H); 2,31 (м, 4H); 1,74-1,05 (м, 54H); 0,92 (м, 9H); 0,67 (м, 6H); 0,31 (м, 2H).
DT. Соединение 161: Гептадекан-9-ил-8-((2-гидроксиэтил)(10-(октаноилокси)декан-2-ил)амино)октаноат
10-(Бензилокси)декан-2-ол

Химическая формула: C17H28O2
Молекулярная масса: 264,409
[00226] Раствор 10-(бензилокси)декан-2-она (3,5 г, 13,34 ммоль) в ТГФ (10 мл) прибавили к перемешиваемому раствору ЛАГ в ТГФ (10 мл) в атмосфере N2 при 0°C. Смесь оставили нагреваться до комн. темп. и перемешивали в течение 2 ч через указанное время медленно прибавили 10 мл насыщ. Na2SO4,10H2O (водн.) раствора. Выпал белый осадок. Прибавили дополнительный твердый Na2SO4,10H2O и смесь отфильтровали через слой целита. Фильтрат разбавили EtOAc и промывали насыщенным водным раствором хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-40%) EtOAc в смеси гексанов с получением 10-(бензилокси)декан-2-ола (3,2 г, 12,1 ммоль, 91%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,32 (м, 5H); 4,53 (с, 2H); 3,80 (м, 1H); 3,49 (т, 2H); 1,64 (м, 2H); 1,55-1,25 (м, 132H); 1,21 (д, 3H).
9-Гидроксидецилоктаноат
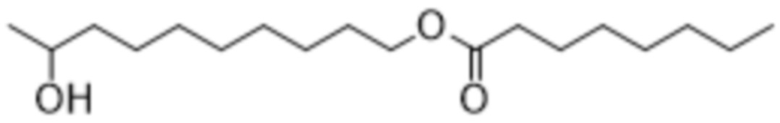
Химическая формула: C18H36O3
Молекулярная масса: 300,483
[00227] 9-Гидроксидецилоктаноат синтезировали, следуя методу A. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 2H); 3,80 (м, 1H); 2,30 (т, 2H); 1,64 (м, 4H); 1,52-1,17 (м, 23H); 0,90 (м, 3H).
Гептадекан-9-ил-8-((2-гидроксиэтил)(10-(октаноилокси)декан-2-ил)амино)октаноат
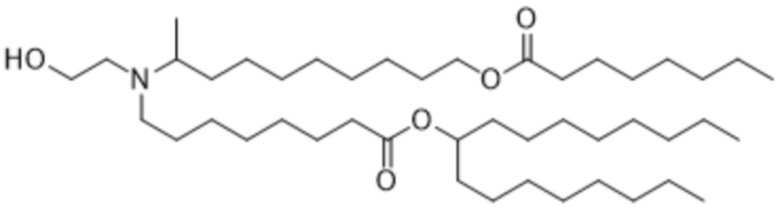
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00228] Соединение 161 синтезировали способом, аналогичным соединению 152 и согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,46 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,49 (уш. м, 2H); 2,77-2,55 (м, 2H); 2,54-2,23 (м, 7H); 1,71-1,20 (м, 63H); 0,91 (м, 12H).
DU. Соединение 162: 7-((2-Гидроксиэтил)(10-(октаноилокси)декан-2-ил)амино)гептил 2-октилдеканоат

Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00229] Соединение 162 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,49 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,99 (м, 4H); 2,72-2,48 (м, 2H); 2,48-2,17 (м, 6H); 1,55 (м, 8H); 1,44-1,10 (м, 56H); 0,92-0,75 (м, 12H).
DV. Соединение 163: 7-((2-Гидроксиэтил)(7-метил-8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат
8-Mетоксиоктановая кислота
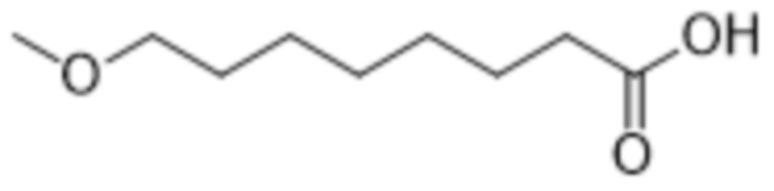
Химическая формула: C9H18O3
Молекулярная масса: 174,240
[00230] К безводному MeOH (80 мл) при 0°C KOH прибавили (7,54 г, 134,46 ммоль) и перемешивали в течение 30 мин. Прибавили раствор 8-бромоктановой кислоты (10 г, 44,82 ммоль) в безводном MeOH (70 мл) и полученный раствор кипятили в течение 18 ч. MeOH удалили под вакуумом и остаток подкислили 1N HCl и экстрагировали диэтиловым эфиром. Органический слой промывали насыщенным водным раствором хлорида натрия, отделили, сушили над Na2SO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле с (0-50%) EtOAc в смеси гексанов с получением 8-метоксиоктановой кислоты (6,3 г, 36,16 ммоль, 81%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,35 (м, 5H); 2,37 (т, 2H); 1,61 (м, 4H); 1,36 (м, 6H).
8-Mетокси-2-метилоктановая кислота
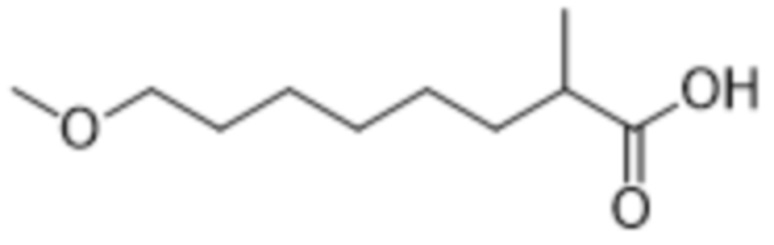
Химическая формула: C10H20O3
Молекулярная масса: 188,267
[00231] К суспензии NaH в ТГФ (100 мл) при 0°C по каплям прибавили 8-метоксиоктановую кислоту (5,6 г, 32,14 ммоль) в ТГФ (30 мл). Реакционную смесь оставили перемешиваться при комн. темп. в течение 30 мин. Реакционную смесь охладили до 0°C и по каплям прибавили ЛДА (17,86 мл, 2M в ТГФ, 35,71 ммоль). После завершения прибавления, реакционную смесь оставили перемешиваться при 45°C в течение 2 ч. Реакционную смесь охладили до комн. темп. и медленно прибавили метилиодид (2,45 мл, 39,28 ммоль) в ТГФ (15 мл). Реакционную смесь перемешивали при 45°C в течение 16 ч. Реакционную смесь погасили 1N HCl (20 мл). Погашенную реакционную смесь выпарили под вакуумом для удаления летучих веществ. Остаток растворили в смеси гексанов/EtOAc (1:1) и промывали 1N HCl (100 мл X 2) с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над сульфатом натрия, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле с (0-15%) EtOAc в смеси гексанов с получением 8-метокси-2-метилоктановой кислоты (3,25 г, 17,26 ммоль, 54%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,35 (м, 5H); 2,49 (м, 1H); 1,70 (м, 1H); 1,59(м, 2H); 1,36 (м, 7H); 1,21 (д, 3H).
8-Гидрокси-2-метилоктановая кислота
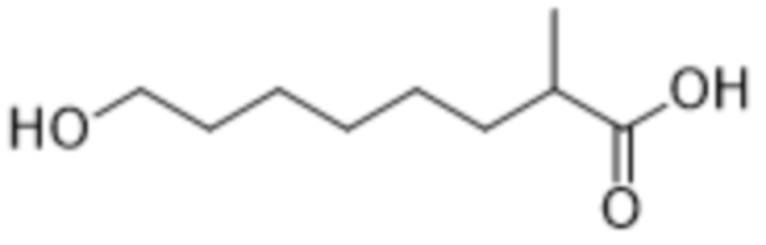
Химическая формула: C9H18O3
Молекулярная масса: 174,240
[00232] К раствору 8-метокси-2-метилоктановая кислота (1 г, 5,31 ммоль) в ДХМ (20 мл) при -78°C прибавили по каплям трибромид бора (13,28 мл 1 M в ДХМ, 13,28 ммоль). Реакционную смесь оставили нагреваться до комн. темп. и перемешивали при комн. темп. в течение 2 ч. Реакционную смесь вылили в лед и экстрагировали ДХМ. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-40%) EtOAc в смеси гексанов с получением 8-гидрокси-2-метилоктановой кислоты (0,77 г, 4,41 ммоль, 83%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,43 (т, 2H); 2,50 (м, 1H); 1,94-1,64 (м, 4H); 1,56-1,26 (м, 7H); 1,20 (д, 3H).
Нонил-8-гидрокси-2-метилоктаноат

Химическая формула: C18H36O3
Молекулярная масса: 300,483
[00233] Раствор 8-гидрокси-2-метилоктановой кислоты (0,75 г, 4,31 ммоль), нонан-1-ола (6,22 г, 43,1 ммоль), 4-диметиламинопиридина (0,11 г, 0,86 ммоль) в ДХМ (20 мл) в атмосфере N2 прибавили к (3-{[(этилимино)метилиден]амино}пропил)диметиламин гидрохлориду (0,83 г, 4,31 ммоль). Реакционную смесь оставили перемешиваться при комн. темп. в течение 16 ч. Реакционную смесь разбавили ДХМ и промывали насыщ. NaHCO3, с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-20%) EtOAc в смеси гексанов с получением нонил-8-гидрокси-2-метилоктаноата (0,68 г, 2,26 ммоль, 53%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 2H); 3,42 (т, 2H); 2,45 (м, 1H); 1,87 (м, 2H); 1,75-1,57 (м, 4H); 1,52-1,22 (м, 19H); 1,15 (д, 3H); 0,91 (м, 3H).
7-((2-Гидроксиэтил)(7-метил-8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат
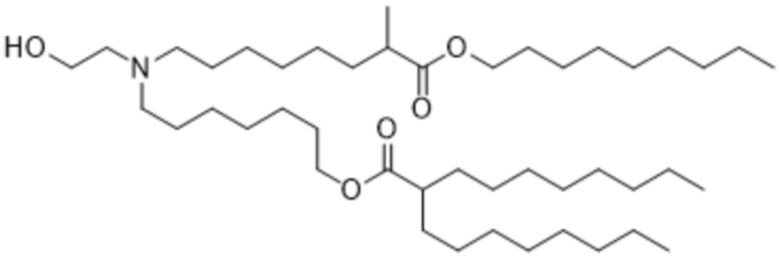
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00234] Соединение 163 синтезировали способом, аналогичным соединению 152 согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,50 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 4H); 3,55 (м, 2H); 2,67 (м, 2H); 2,53-2,24 (м, 6H); 1,72-1,10 (м, 65H); 0,90 (м, 9H).
DW. Соединение 164: Нонил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)-2-метилоктаноат

Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00235] Соединение 164 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,51 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,55 (м, 2H); 2,69-2,38 (м, 8H); 2,30 (т, 2H); 1,74-1,09 (м, 65H); 0,90 (м, 9H).
DX. Соединение 165: 7-((7-(Деканоилокси)октил)(2-гидроксиэтил)амино)гептил-2-октилдеканоат
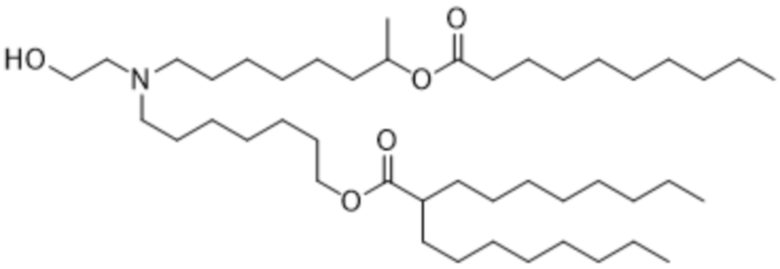
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00236] Соединение 165 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,55 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 1H); 4,08 (т, 2H); 3,55 (м, 2H); 2,68-2,39 (м, 8H); 2,29 (м, 3H); 1,72-1,15 (м, 64H); 0,90 (м, 9H).
DY. Соединение 166: 8-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октановая кислота

Химическая формула: C35H69NO5
Молекулярная масса: 583,939
[00237] К раствору гептадекан-9-ил-8-{[8-(трет-бутокси)-8-оксооктил](2-гидроксиэтил)амино}октаноата (0,11 г, 0,17 ммоль) вДХМ прибавили трифторуксусную кислоту (0,06 мл, 0,69 ммоль) и реакционную смесь оставили перемешиваться при комн. темп. в течение 40 ч. Летучие вещества выпарили под вакуумом. Остаток растворили в этилацетате и воде и экстрагировали этилацетатом. Органический слой отделили, сушили над Na2SO4, отфильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-50%) (1%, 20% MeOH в ДХМ) в ДХМ с получением 8-{[8-(гептадекан-9-илокси)-8-оксооктил](2-гидроксиэтил)амино}октановой кислоты (0,023 г, 0,04 ммоль) в виде бесцветной жидкости. СВЭЖХ/ДСИО: RT=2,72 мин. MС (ИЭР): m/z (MH+) 585,0 для C35H69NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87 (м, 1H); 3,98 (м, 2H); 3,25-3,05(м, 6H); 2,32 (м, 4H); 1,82-1,45 (м, 12H); 1,45-1,19 (м, 37H); 0,89 (м, 6H).
DZ. Соединение 167: 8-((2-Гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октановая кислота

Химическая формула: C27H53NO5
Молекулярная масса: 471,723
[00238] Соединение 167 синтезировали, следуя методике, аналогичной синтезу соединения 166. СВЭЖХ/ДСИО: RT=1,57 мин. MС (ИЭР): m/z (MH+) 472,0 для C27H53NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (м, 2H); 4,00 (м, 2H); 3,44-2,98 (м, 10H); 2,35 (т, 4H); 1,85-1,55 (м, 10H); 1,33 (м, 23H); 0,90 (м, 3H).
EA. Соединение 168: Гептадекан-9-ил-(Z)-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
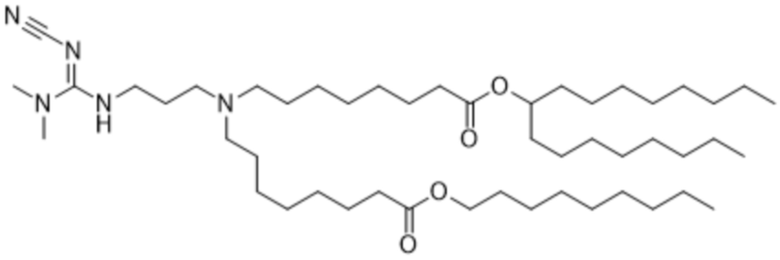
Химическая формула: C49H95N5O4
Молекулярная масса: 818,33
[00239] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (220 мг, 0,3 ммоль) в 5 мл 2-пропанола прибавили триэтиламин (0,04 мл, 0,3 ммоль) с последующим прибавлением дифенилцианокарбонимидата (72 мг, 0,3 ммоль) и смесь перемешивали при комн. темп. в течение двух часов. К реакционной смеси прибавили 2M раствор диметиламина в ТГФ (0,75 мл, 1,5 ммоль) и полученный раствор нагревали до 75°C в течение 18 часов. Прибавили дополнительный 2M раствор диметиламин/ТГФ (0,75 мл, 1,5 ммоль) температуру подняли до 85 oC. Через шесть часов реакция завершилась согласно ЖХ/MС, поэтому раствор концентрировали в вакууме, разбавили ДХМ и один раз промывали насыщенным водным раствором гидрокарбоната натрия. Органическую фазу сушили (MgSO4), отфильтровали и фильтрат выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (119,2 мг, 0,14 ммоль, 49%) в виде бесцветного сиропа. СВЭЖХ/ДСИО: RT=3,52 мин. MС (ИЭР): m/z (MH+) 819,0 для C49H95N5O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,62 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=7,5 Гц); 3,68 (д, 2H, J=3 Гц); 2,99 (с, 6H); 2,59 (уш. с, 2H); 2,43 (уш. с, 3H); 2,28 (м, 4H); 1,71 (уш. с, 2H); 1,62 (м, 8H); 1,49 (м, 5H); 1,26 (уш. м, 50H); 0,88 (т, 9H, J=7,5 Гц).
EB. Соединение 169: Гептадекан-9-ил-8-((3-((2-(диметиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
3-(Диметиламино)-4-метоксициклобут-3-ен-1,2-дион
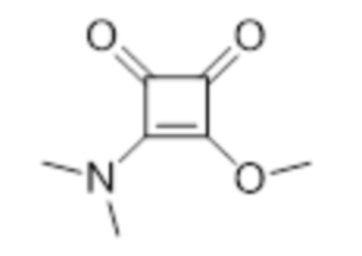
Химическая формула: C7H9NO3
Молекулярная масса: 155,15
[00240] К раствору 3,4-диметокси-3-циклобутен-1,2-диона (1 г, 7 ммоль) в 100 мл диэтиловый эфир прибавили 2M раствор диметиламина в ТГФ (3,8 мл, 7,6 ммоль) и осадок образовался практически сразу. Смесь перемешивали при комн. темп. в течение 24 часов и затем отфильтровали. Отфильтрованное твердое вещество промывали диэтиловым эфиром и сушили на воздухе. Отфильтрованное твердое вещество растворили в горячем MeOH, отфильтровали, фильтрат оставили охлаждаться до комнатной температуре, затем охладили до 0°C с получением осадка. Его отделили путем фильтрования, промывали холодным MeOH, сушили на воздухе, затем сушили в вакууме с получением 3-(диметиламино)-4-метоксициклобут-3-ен-1,2-диона (0,42 г, 2,7 ммоль, 39%) в виде бледно-желтого твердого вещества 1H ЯМР (300 МГц, ДМСО-d6) δ: м.д. 4,28 (с, 3H); 3,21 (с, 3H); 3,05 (с, 3H).
Гептадекан-9-ил-8-((3-((2-(диметиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
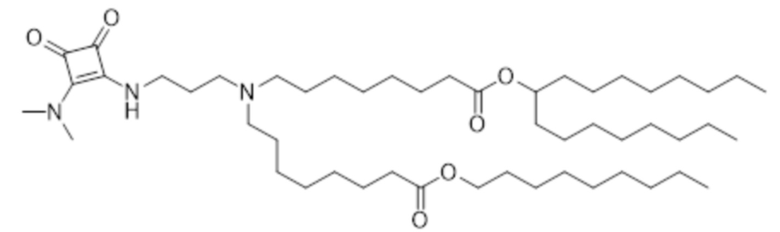
Химическая формула: C51H95N3O6
Молекулярная масса: 846,34
[00241] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (220 мг, 0,3 ммоль) в 10 мл этанола прибавили 3-(диметиламино)-4-метоксициклобут-3-ен-1,2-дион (47 мг, 0,3 ммоль) и полученный бесцветный раствор перемешивали при комн. темп. в течение 20 часов после чего согласно ЖХ/MС исходного амина не осталось. Раствор концентрировали в вакууме и остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((2-(диметиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (135 мг, 0,16 ммоль, 53%) в виде бесцветного сиропа. СВЭЖХ/ДСИО: RT=3,51 мин. MС (ИЭР): m/z (MH+) 847,3 для C51H95N3O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,86 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,92 (д, 2H, J=3 Гц); 3,20 (с, 6H); 2,63 (уш. с, 2H); 2,42 (уш. с, 3H); 2,28 (м, 4H); 1,74 (уш. с, 2H); 1,61 (м, 8H); 1,50 (м, 5H); 1,41 (м, 3H); 1,25 (уш. м, 47H); 0,88 (т, 9H, J=7,5 Гц).
EC. Соединение 170: Гептадекан-9-ил-(E)-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
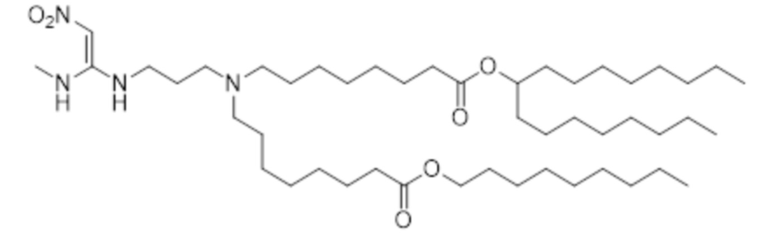
Химическая формула: C48H94N4O6
Молекулярная масса: 823,30
[00242] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (220 мг, 0,3 ммоль) в 5 мл метанол прибавили 1-метилтио-1-метиламино-2-нитроетен (45 мг, 0,3 ммоль), полученный раствор нагревали до 70°C и перемешивали в течение 24 часов, после чего согласно ЖХ/MС исходного амина не осталось. Раствор разбавили ДХМ и один раз промывали насыщенным водным раствором гидрокарбоната натрия. Органическую фазу сушили (MgSO4), отфильтровали и фильтрат выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(E)-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (90 мг, 0,11 ммоль, 36%) в виде бледно-желтого сиропа. СВЭЖХ/ДСИО: RT=3,33 мин. MС (ИЭР): m/z (MH+) 824,3 для C48H94N4O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 10,15 (д, 1H, J=9 Гц); 8,26 (д, 1H, J=27 Гц); 6,55 (д, 1H, J=9 Гц); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,32 (уш. с, 1H); 3,24 (уш. с, 1H); 2,81 (дд, 3H, J=3 Гц, 12 Гц); 2,63 (уш. с, 1H); 2,47 (уш. с, 4H); 2,28 (м, 4H); 1,77 (уш. с, 2H); 1,62 (м, 5H); 1,59 (м, 6H); 1,49 (м, 3H); 1,43 (м, 3H); 1,26 (уш. м, 46H); 0,88 (т, 9H, J=7,5 Гц).
ED. Соединение 171: Гептадекан-9-ил-8-((9-гидрокси-9-метилоктадецил)(2-гидроксиэтил)амино)октаноат
((Дец-9-ен-1-илокси)метил)бензол
Химическая формула: C17H26O
Молекулярная масса: 246,394
[00243] К суспензии гидрида натрия (3,88 г, 96,99 ммоль) вТГФ (100 мл) медленно прибавили 9-децен-1-ол (10 г, 63,99 ммоль). Через 30 мин прибавили бензилбромид (10,57 мл, 88,9 ммоль). Реакционную смесь оставили перемешиваться при комн. темп. в течение 18 ч. Реакционную смесь погасили водой. Растворители выпарили под вакуумом. Остаток разбавили EtOAc и промывали насыщ. NaHCO3, с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле с (0-20%) EtOAc в смеси гексанов с получением ((дец-9-ен-1-илокси)метил)бензола (8,5 г, 34,5 ммоль, 54%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,32 (м, 5H); 5,83 (м, 1H); 4,98 (м, 2H); 4,53 (с, 2H); 3,49 (т, 2H); 2,06 (м, 2H); 1,64 (м, 2H); 1,46-1,26 (уш. м, 10H).
10-(Бензилокси)декан-2-он
Химическая формула: C17H26O2
Молекулярная масса: 262,393
[00244] К раствору хлорида палладия (0,09 г, 0,52 ммоль) и бензохинона (3,09 г, 28,57 ммоль) вДМФА/вода (7:1, 12,8 мл) медленно прибавили [(дек-9-ен-1-илокси)метил]бензол (6,4 г, 25,98 ммоль) и темно-коричневый раствор оставили перемешиваться в течение 3 дней при комн. темп. Смесь растворили в 2N HCl (50 мл) и экстрагировали эфиром (3×50 мл). Объединенную органическую фазу промывали 2N NaOH (3×50 мл) и сушили над MgSO4. Растворители удалили в вакууме и остаток очищали с помощью хроматографии на силикагеле (0-40%) этилацетат в смеси гексанов с получением 10-(бензилокси)декан-2-она (3,44 г, 13,11 ммоль, 50%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,36 (м, 5H); 4,52 (с, 2H); 3,48 (т, 2H); 2,43 (т, 2H); 2,15 (с, 3H); 1,61 (м, 4H); 1,45-1,24 (уш. м, 8H).
1-(Бензилокси)-9-метилоктадекан-9-ол
Химическая формула: C26H46O2
Молекулярная масса: 390,652
[00245] К раствору 10-(бензилокси)декан-2-она (1 г, 3,81 ммоль) в ТГФ (30 мл) при 0°C по каплям прибавили бром(нонил)магния (4,57 мл 1 M в диэтиловом эфире, 4,57 ммоль). Реакционную смесь оставили нагреваться до комн. темп. и перемешивали в течение 4 ч. Реакционную смесь погасили водой (2мл), прибавили диэтиловый эфир (200 мл) и полученное белое твердое вещество отфильтровали через слой силикагеля. Фильтрат экстрагировали эфиром. Органический слой промывали водой, с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-40%) EtOAc в смеси гексанов с получением 1-(бензилокси)-9-метилоктадекан-9-ола (0,99 г). Продукт содержал примеси, но был использован на следующей стадии без дополнительной очистки.
9-Метилоктадекан-1,9-диoл
Химическая формула: C19H40O2
Молекулярная масса: 300,527
[00246] В атмосфере N2 в колбу загрузили 1-(бензилокси)-9-метилоктадекан-9-ол (1 г, 2,56 ммоль), Pd(OH)2 (100 мг) и EtOH. Реакционную смесь продували H2 и поместили в атмосферу H2 (баллон) при перемешивании в течение 16 ч при комн. темп. Реакционную смесь продували N2. Реакционную смесь отфильтровали через слой целита и целит промывали EtOAc (200 мл). Фильтрат выпарили под вакуумом. Остаток растворили в EtOAc и промывали водой. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с EtOAc в смеси гексанов (0-40%) с получением 9-метилоктадекан-1,9-диoла (0,65 г, 2,16 ммоль, 84%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,66 (т, 2H); 1,59 (м, 2H); 1,49-1,22 (уш. м, 29H); 1,17 (с, 3H); 0,90 (м, 3H).
1-Бром-9-метилоктадекан-9-ол
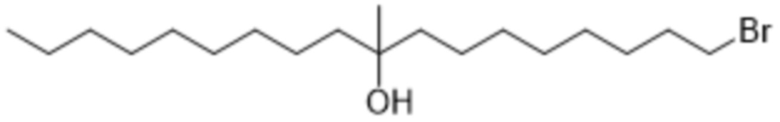
Химическая формула: C19H39BrO
Молекулярная масса: 363,42
[00247] 1-Бром-9-метилоктадекан-9-ол синтезировали способом, аналогичным синтезу (Z)-1-бром-10-октилоктадец-8-ена. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,43 (т, 2H); 1,88 (м, 2H); 1,53-1,23 (уш. м, 28H); 1,17 (с, 3H); 0,91 (м, 3H).
Гептадекан-9-ил-8-((9-гидрокси-9-метилоктадецил)(2-гидроксиэтил)амино)октаноат
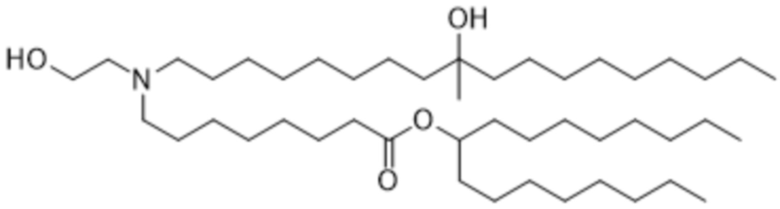
Химическая формула: C46H93NO4
Молекулярная масса: 724,253
[00248] Соединение 171 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,56 мин. MС (ИЭР): m/z (MH+) 725,0 для C46H93NO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 3,55 (м, 2H); 2,60 (м, 2H); 2,47 (м, 4H); 2,30 (т, 2H); 1,74-1,21(м, 69H); 1,17 (с, 3H); 0,90 (м, 9H).
EE. Соединение 172: (R)-Декан-2-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)октаноат
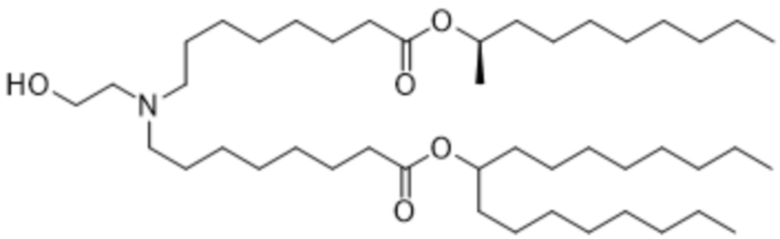
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00249] Соединение 172 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,53 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 2H); 3,54 (м, 2H); 2,59 (м, 2H); 2,46 (м, 4H); 2,30 (м, 4H); 1,70-1,19 (м, 66H); 0,90 (м, 9H).
EF. Соединение 173: Гептадекан-9-ил-8-((3-(N-метилметилсульфонамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
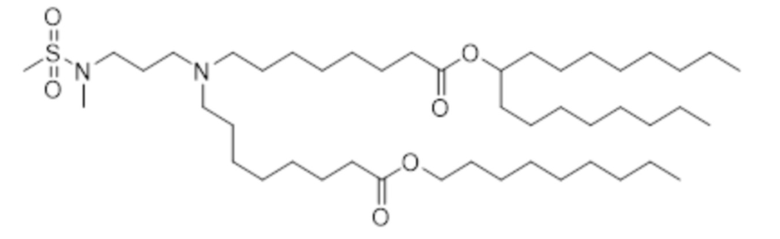
Химическая формула: C47H94N2O6S
Молекулярная масса: 815,34
[00250] К раствору гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,27 ммоль) и N-метилметансульфонамида (50 мкл, 0,54 ммоль) в 4 мл сухого ДМФА прибавили карбонат цезия (130 мг, 0,40 ммоль), полученную смесь нагревали до 60°C и перемешивали в течение 24 часов, после чего согласно ЖХ/MС исходного хлорида не осталось. Смесь оставили охлаждаться до комн. темп., разбавили 50% насыщенным водным раствором гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и концентрировали с получением желтого масла. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(N-метилметилсульфонамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (85 мг, 0,11 ммоль, 39%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=3,57 мин. MС (ИЭР): m/z (MH+) 816,1 для C47H94N2O6S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,15 (т, 2H, J=7,5 Гц); 2,85 (с, 3H); 2,79 (3, 3H); 2,40 (уш. м, 5H); 2,28 (м, 4H); 1,72 (уш. м, 2H); 1,64-1,49 (м, 13H); 1,26 (уш. м, 50H); 0,88 (т, 9H, J=7,5 Гц).
EG. Соединение 174: Гептадекан-9-ил-8-((3-(2,5-диоксоимидазолидин-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
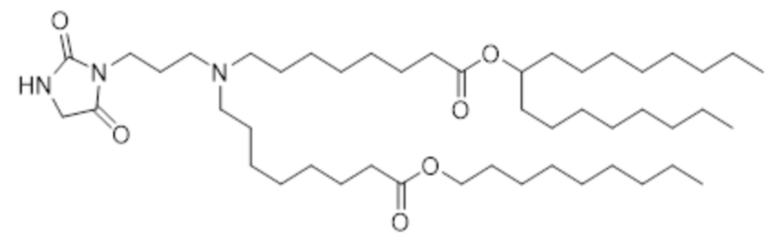
Химическая формула: C48H91N3O6
Молекулярная масса: 806,27
[00251] К раствору гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,27 ммоль) и гидантоина (50 мг, 0,54 ммоль) в 4 мл сухого ДМФА прибавили карбонат цезия (130 мг, 0,40 ммоль), полученную смесь нагревали до 60°C и перемешивали в течение 24 часов, после чего согласно ЖХ/MС исходного хлорида не осталось. Смесь оставили охлаждаться до комн. темп., разбавили 50% насыщенным водным раствором гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, один раз промыли водой, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2,5-диоксоимидазолидин-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (35 мг, 0,05 ммоль, 18%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=3,52 мин. MС (ИЭР): m/z (MH+) 807,2 для C48H91N3O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,27 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,95 (с, 2H); 3,55 (т, 2H, J=7,5 Гц); 2,50-2,34 (уш. м, 5H); 2,26 (м, 4H); 1,77 (уш. с, 2H); 1,64-1,49 (м, 15H); 1,26 (уш. м, 48H); 0,88 (т, 9H, J=7,5 Гц).
EH. Соединение 175: Гептадекан-9-ил-8-((3-((метилкарбамоил)окси)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
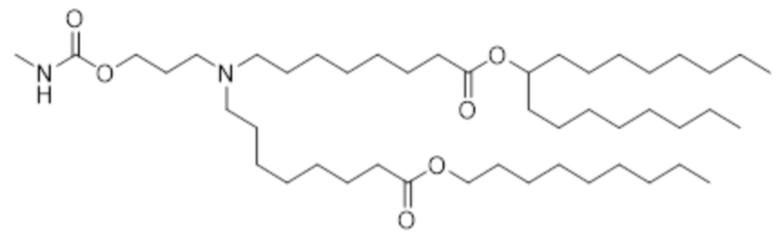
Химическая формула: C47H92N2O6
Молекулярная масса: 781,26
[00252] К раствору гептадекан-9-ил-8-((3-гидроксипропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,27 ммоль) и триэтиламина (60 мкл, 0,41 ммоль) в 5 мл сухого ДХМ при 0°C по каплям прибавили метилизоцианат (22 мкл, 0,35 ммоль). Охлаждающую баню убрали и раствор перемешивали при комн. темп. в течение 2 часов, после чего согласно ЖХ/MС исходного спирта не осталось. Реакционную смесь погасили тремя каплями метанола, смесь концентрировали в потоке азота и остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((метилкарбамоил)окси)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (115 мг, 0,15 ммоль, 53%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,54 мин. MС (ИЭР): m/z (MH+) 782,3 для C47H92N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=6 Гц); 4,62 (уш. с, 1H); 4,05 (м, 4H); 2,79 (д, 3H, J=3 Гц); 2,47 (уш. с, 2H); 2,37 (уш. м, 3H); 2,27 (м, 4H); 1,73 (уш. с, 2H); 1,61 (м, 7H); 1,50 (уш. м, 4H); 1,40 (уш. м, 4H); 1,25 (уш. м, 48H); 0,87 (т, 9H, J=7,5 Гц).
EI. Соединение 176: Гептадекан-9-ил-8-((3-(2,5-диоксопирролидин-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
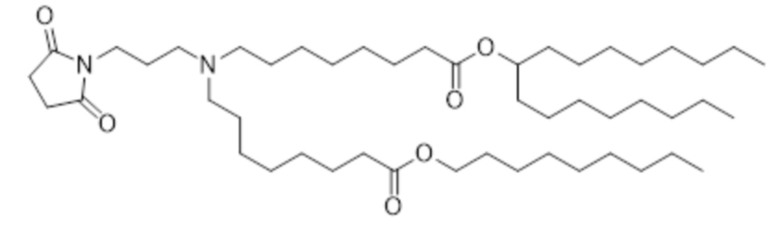
Химическая формула: C49H92N2O6
Молекулярная масса: 805,28
[00253] К раствору гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,27 ммоль) и сукцинимида (50 мг, 0,54 ммоль) в 4 мл сухого ДМСО прибавили карбонат цезия (130 мг, 0,40 ммоль), полученную смесь нагревали до 80°C и перемешивали в течение 48 часов, после чего по данным ЖХ/МС не осталось исходного хлорида. Смесь оставили охлаждаться до комн. темп., разбавили 50% насыщенным водным раствором гидрокарбоната натрия и трижды экстрагировали ДХМ. Органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и концентрировали. Остаток дважды очищали хроматографией на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2,5-диоксопирролидин-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (44 мг, 0,05 ммоль, 19%) в виде желтоватого масла. СВЭЖХ/ДСИО: RT=3,56 мин. MС (ИЭР): m/z (MH+) 806,1 для C49H92N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,52 (т, 2H, J=7,5 Гц); 2,69 (с, 4H); 2,42-2,25 (уш. м, 9H); 1,71-1,58 (м, 10H); 1,50 (уш. д, 4H, J=3 Гц); 1,26 (уш. м, 51H); 0,88 (т, 9H, J=7,5 Гц).
EJ. Соединение 177: Гептадекан-9-ил-8-((3-(4-(трет-бутоксиметил)-1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C52H100N4O5
Молекулярная масса: 861,40
[00254] К раствору гептадекан-9-ил-8-((3-азидопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,67 ммоль) и трет-бутилпропаргилового эфира (100 мкл, 0,73 ммоль) в 4 мл ТГФ прибавили суспензию безводного сульфата меди (II) (5 мг, 0,03 ммоль) и аскорбата натрия (14 мг, 0,07 ммоль) в 1 мл воды и смесь перемешивали при комн. темп. в течение 24 часов, через которые согласно ЖХ/MС исходного азида не осталось. Смесь разбавили насыщенным водным раствором гидрокарбоната натрия и трижды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(4-(трет-бутоксиметил)-1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (485 мг, 0,56 ммоль, 84%) в виде желтоватого масла. СВЭЖХ/ДСИО: RT=3,63 мин. MС (ИЭР): m/z (MH+) 862,2 для C52H100N4O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,50 (с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,59 (с, 2H); 4,36 (т, 2H, J=7,5 Гц); 4,05 (т, 2H, J=6 Гц); 2,36 (уш. м, 5H); 2,28 (м, 4H); 2,02 (уш. м, 2H); 1,62 (уш. м, 8H); 1,50 (уш. д, 4H, J=3 Гц); 1,28 (уш. м, 60H); 0,88 (т, 9H, J=7,5 Гц).
EK. Соединение 178: Гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
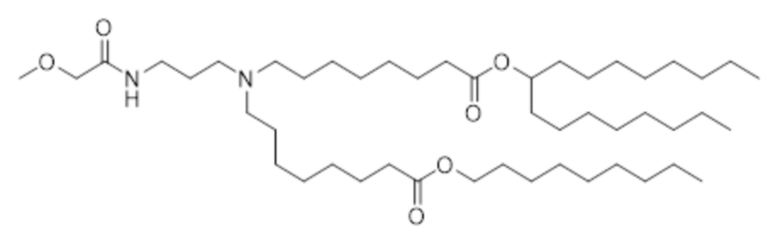
Химическая формула: C48H94N2O6
Молекулярная масса: 795,29
[00255] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,27 ммоль) и триэтиламина (60 мкл, 0,41 ммоль) в 5 мл сухого ДХМ при 0°C по каплям прибавили метоксиацетилхлорид (30 мкл, 0,33 ммоль). Охлаждающую баню убрали и раствор перемешивали при комн. темп. в течение 24 часов, после чего согласно ЖХ/MС исходного амина не осталось. Смесь разбавили a 50% насыщенным водным раствором гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (50 мг, 0,06 ммоль, 23%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,56 мин. MС (ИЭР): m/z (MH+) 796,2 для C48H94N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,53 (с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,87 (с, 2H); 3,39 (м, 5H); 2,47 (уш. с, 2H); 2,36 (уш. м, 3H); 2,27 (м, 4H); 1,61 (м, 8H); 1,46 (уш. м, 9H); 1,26 (уш. м, 48H); 0,88 (т, 9H, J=7,5 Гц).
EL. Соединение 179: Гептадекан-9-ил-8-((3-(1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)(3-(4-(триметилсилил)-1H-1,2,3-триазол-1-ил)пропил)амино)октаноат

Химическая формула: C50H98N4O4Si
Молекулярная масса: 847,44
[00256] К раствору гептадекан-9-ил-8-((3-азидопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,27 ммоль) и этинилтриметилсилана (41 мкл, 0,29 ммоль) в 2 мл ТГФ прибавили суспензию безводного сульфата меди (II) (2 мг, 0,01 ммоль) и аскорбата натрия (5 мг, 0,02 ммоль) в 0,5 мл воды и смесь перемешивали при комн. темп. в течение 20 часов, после чего согласно ЖХ/MС исходного азида не осталось. Смесь разбавили насыщенным водным раствором гидрокарбоната натрия и трижды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)(3-(4-(триметилсилил)-1H-1,2,3-триазол-1-ил)пропил)амино)октаноата (150 мг, 0,18 ммоль, 66%) в виде желтоватого масла, которое представляло собой смесь TMS/des-TMS продукта 2:1 согласно 1H-ЯМР. Использовали как есть. СВЭЖХ/ДСИО: RT=3,63 мин. MС (ИЭР): m/z (MH+) 848,3 для C50H98N4O4Si. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,55 (с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,45 (т, 2H, J=7,5 Гц); 4,05 (т, 2H, J=6 Гц); 3,42 (уш. с, 1H); 2,28 (м, 5H); 1,65-1,45 (уш. м, 14H); 1,25 (уш. м, 48H); 0,87 (т, 9H, J=7,5 Гц); 0,33 (с, 6H).
Гептадекан-9-ил-8-((3-(1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
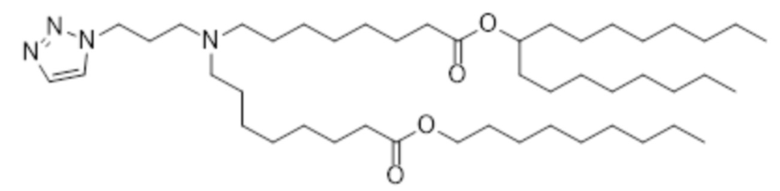
Химическая формула: C47H90N4O4
Молекулярная масса: 775,26
[00257] К раствору (150 мг, 0,18 ммоль) в 5 мл ТГФ прибавили раствор 1M тетрабутиламмоний фторида в ТГФ (0,21 мл, 0,21 ммоль) и раствор перемешивали при комн. темп. в течение 24 часов, после чего реакция прошла приблизительно на 25%. Раствор нагревали до 55°C и перемешивали в течение 24 часов, после чего согласно ЖХ/MС реакция завершилась. Раствор разбавили насыщенным водным раствором гидрокарбоната натрияи дважды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (53 мг, 0,07 ммоль, 39%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,55 мин. MС (ИЭР): m/z (MH+) 776,2 для C47H90N4O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,69 (с, 1H); 7,55 (с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,44 (т, 2H, J=7,5 Гц); 4,05 (т, 2H, J=6 Гц); 2,37 (уш. м, 5H); 2,28 (м, 4H); 2,05 (уш. м, 2H); 1,61 (уш. м, 8H); 1,49 (уш. м, 4H); 1,26 (уш. м, 51H); 0,88 (т, 9H, J=7,5 Гц).
EM. Соединение 181: Гептадекан-9-ил-8-((3-((метоксикарбонил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C47H92N2O6
Молекулярная масса: 781,26
[00258] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,27 ммоль) и триэтиламина (60 мкл, 0,41 ммоль) в 5 мл сухого ДХМ при 0°C по каплям прибавили метилхлорформиата (27 мкл, 0,33 ммоль). Охлаждающую баню убрали и раствор перемешивали при комн. темп. в течение 24 часов, после чего согласно ЖХ/MС исходного амина не осталось. Смесь разбавили a 50% насыщенным водным раствором гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((метоксикарбонил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (120 мг, 0,15 ммоль, 54%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,55 мин. MС (ИЭР): m/z (MH+) 782,1 для C47H92N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,11 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,64 (с, 3H); 3,25 (уш. д, 2H, J=6 Гц); 2,46 (уш. с, 2H); 2,38-2,24 (м, 7H); 1,61 (уш. т., 9H, J=7,5 Гц); 1,50 (м, 4H); 1,42 (уш. м, 3H); 1,26 (уш. м, 49H); 0,88 (т, 9H, J=7,5 Гц).
EN. Соединение 182: Гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
3-Mетокси-4-(метиламино)циклобут-3-ен-1,2-дион
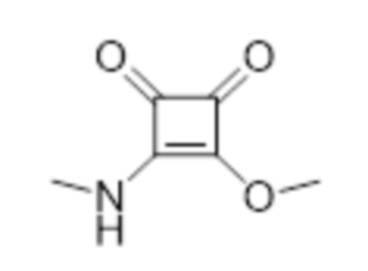
Химическая формула: C6H7NO3
Молекулярная масса: 141,13
[00259] К раствору 3,4-диметокси-3-циклобутен-1,2-диона (1 г, 7 ммоль) в 100 мл диэтилового эфира прибавили 2M раствор метиламина в ТГФ (3,8 мл, 7,6 ммоль) и осадок образовался практически немедленно. Смесь перемешивали при комн. темп. в течение 24 часов, затем фильтровали, отфильтрованные твердые вещества промывали диэтиловым эфиром и сушили на воздухе. Отфильтрованное твердое вещество растворили в горячем EtOAc, фильтровали, фильтрат оставили охлаждаться до комн. темп., затем охладили до 0°C с получением осадка. Его выделяли фильтрованием, промывали холодным EtOAc, сушили воздухом, затем сушили в вакууме с получением 3-метокси-4-(метиламино)циклобут-3-ен-1,2-диона (0,70 г, 5 ммоль, 73%) в виде белого твердого вещества. 1H ЯМР (300 МГц, ДМСО-d6) δ: м.д. 8,50 (уш. д, 1H, J=69 Гц); 4,27 (с, 3H); 3,02 (sdd, 3H, J=42 Гц, 4,5 Гц).
Гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
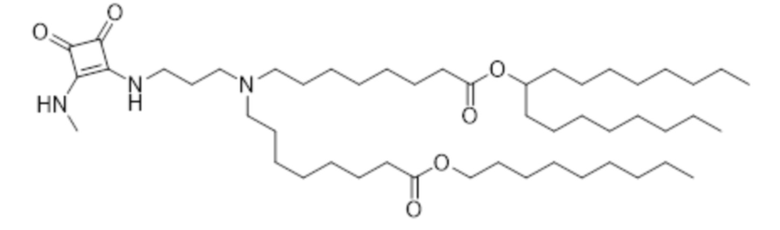
Химическая формула: C50H93N3O6
Молекулярная масса: 832,31
[00260] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,28 ммоль) в 10 мл этанола прибавили 3-метокси-4-(метиламино)циклобут-3-ен-1,2-диона (39 мг, 0,28 ммоль) и полученный бесцветный раствор перемешивали при комн. темп. в течение 20 часов после чего согласно ЖХ/MС исходного амина не осталось. Раствор концентрировали в вакууме и остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (138 мг, 0,17 ммоль, 60%) в виде смолистого белого твердого вещества. СВЭЖХ/ДСИО: RT=3. мин. MС (ИЭР): m/z (MH+) 833,4 для C51H95N3O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,86 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,92 (д, 2H, J=3 Гц); 3,20 (с, 6H); 2,63 (уш. с, 2H); 2,42 (уш. с, 3H); 2,28 (м, 4H); 1,74 (уш. с, 2H); 1,61 (м, 8H); 1,50 (м, 5H); 1,41 (м, 3H); 1,25 (уш. м, 47H); 0,88 (т, 9H, J=7,5 Гц).
EO. Соединение 183: 1,3-Бис(гексилокси)пропан-2-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
(((1,3-Бис(гексилокси)пропан-2-ил)окси)метил)бензол

Химическая формула: C22H38O3
Молекулярная масса: 350,543
[00261] К суспензии NaH (1,76 г, 43,9 ммоль) вТГФ (40 мл) в атмосфере N2 прибавили 2-(бензилокси)пропан-1,3-диoл (2 г, 10,98 ммоль) и смесь оставили перемешиваться при 40°C в течение 2 ч. Через указанное время прибавили 1-бромгексан (4,35 г, 26,34 ммоль) в ДМФА (2 мл) и каталитическое количество KI. Реакционную смесь кипятили в течение 16 ч. Растворители выпарили под вакуумом. Остаток разбавили EtOAc и промывали насыщ. NaHCO3, с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-40%) EtOAc в смеси гексанов с получением (((1,3-бис(гексилокси)пропан-2-ил)окси)метил)бензола (1,7 г, 4,75 ммоль, 43%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,34 (м, 5H); 4,73 (с, 2H); 3,75 (м, 1H); 3,61-3,40 (м, 8H); 1,59 (м, 4H); 1,32 (м, 12H); 0,91 (м, 6H).
1,3-Бис(гексилокси)пропан-2-ол
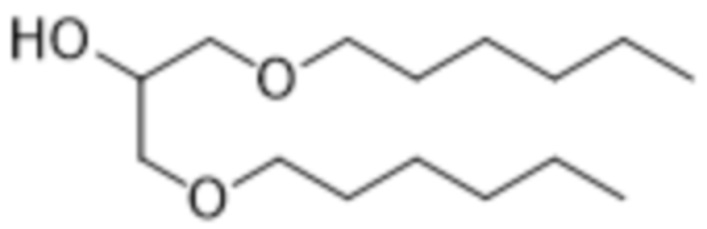
Химическая формула: C15H32O3
Молекулярная масса: 260,418
[00262] 1,3-Бис(гексилокси)пропан-2-ол синтезировали способом, аналогичным синтезу 9-метилоктадекан-1,9-диoла. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,96 (м, 1H); 3,48 (м, 8H); 2,37 (уш. с, 1H); 1,64 (м, 2H); 1,60 (м, 4H); 1,32 (м, 12H); 0,91 (м, 6H).
1,3-Бис(гексилокси)пропан-2-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
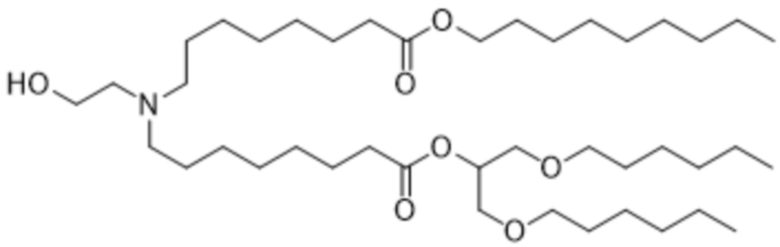
Химическая формула: C42H83NO7
Молекулярная масса: 714,126
[00263] Соединение 183 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,17 мин. MС (ИЭР): m/z (MH+) 715,0 для C42H83NO7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,15 (м, 1H); 4,08 (т, 2H); 3,66-3,34 (м, 10H); 2,71-2,41 (м, 6H); 2,34 (м, 4H); 1,74-1,20 (м, 50H); 0,91 (м, 9H).
EP. Соединение 184: Гептадекан-9-ил-8-((2-гидроксиэтил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат
2-Метилнонил-8-бромоктаноат

Химическая формула: C18H35BrO2
Молекулярная масса: 363,380
[00264] К раствору 8-бромоктановой кислоты (3,83 г, 17,18 ммоль), 2-метилнонан-1-ола (2,72 г, 17,18 ммоль), 4-диметиламинопиридина (0,42 г, 3,44 ммоль) вДХМ (25 мл) в атмосфере N2 прибавили (3-{[(этилимино)метилиден]амино}пропил)диметиламин гидрохлорид (3,29 г, 17,18 ммоль). Реакционную смесь оставили перемешиваться при комн. темп. в течение 16 ч. Реакционную смесь разбавили ДХМ и промывали насыщ. NaHCO3, с последующим прибавлением насыщенного водного раствора хлорида натрия. Органический слой отделили, сушили над Na2SO4, отфильтровали и выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле с (0-20%) EtOAc в смеси гексанов с получением 2-метилнонил-8-бромоктаноата (5,1 г, 14,04 ммоль, 82%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,98 (м, 2H); 3,43 (т, 2H); 2,33 (т, 2H); 1,93-1,74 (м, 3H); 1,72-1,09 (м, 20H); 0,93 (м, 6H).
Гептадекан-9-ил-8-((2-гидроксиэтил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат
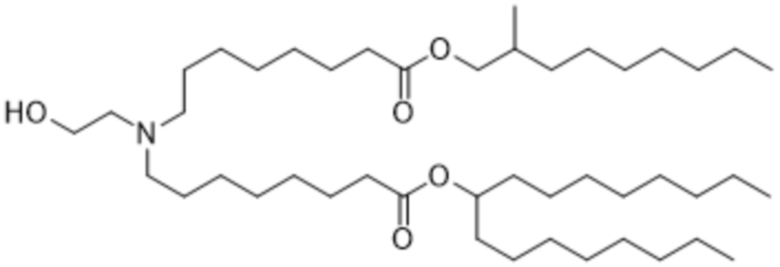
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00265] Соединение 184 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,60 мин. MС (ИЭР): m/z (MH+) 725,0 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 3,92 (м, 2H); 3,57 (м, 2H); 2,70-2,41 (м, 6H); 2,31 (м, 4H); 1,79 (м, 1H); 1,70-1,07(м, 60H); 0,93 (м, 12H).
EQ. Соединение 185: Геникозан-11-ил 6-((2-гидроксиэтил)(6-оксо-6-(ундецилокси)гексил)амино)гексаноат
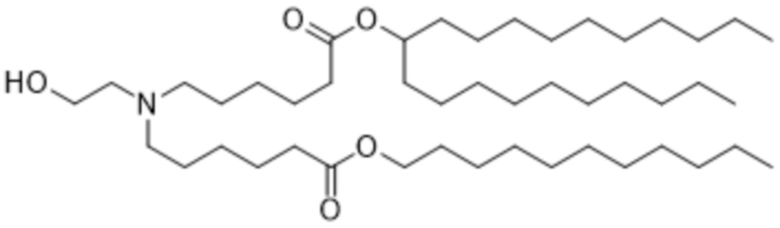
Химическая формула: C46H91NO5
Молекулярная масса: 738,236
[00266] Соединение 185 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,72 мин. MС (ИЭР): m/z (MH+) 739,0 для C46H91NO5. 1H ЯМР (300 МГц, CDCl3)δ: м.д. 4,88 (м, 1H); 4,08 (т, 2H); 3,55 (м, 2H); 2,60 (м, 2H); 2,48 (м, 4H); 2,32 (м, 4H); 1,72-1,41 (м, 15H); 1,28 (м, 52H); 0,90 (м, 9H).
ER. Соединение 186: Гептил-10-((2-гидроксиэтил)(10-оксо-10-(тридекан-7-илокси)децил)амино)деканоат
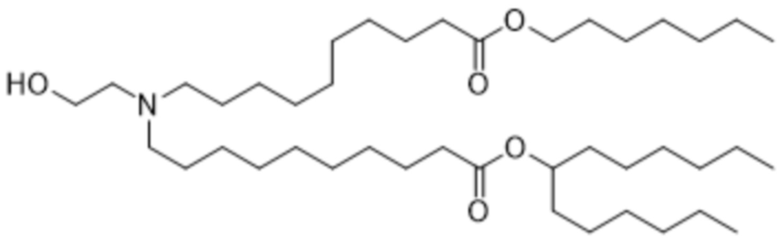
Химическая формула: C42H83NO5
Молекулярная масса: 682,128
[00267] Соединение 186 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,31 мин. MС (ИЭР): m/z (MH+) 739,0 для C42H83NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,55 (м, 2H); 2,58 (м, 2H); 2,47 (м, 4H); 2,30 (м, 4H); 1,71-1,18 (м, 58H); 0,90 (м, 9H).
ES. Соединение 189: Гептил-10-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)деканоат
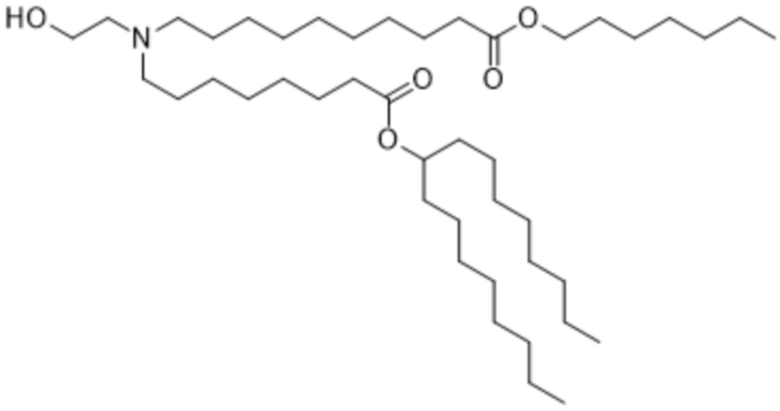
Химическая формула: C44H87NO5
Молекулярная масса: 710,182
[00268] Соединение 189 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,47 мин. MС (ИЭР): m/z (MH+) 710,98 для C44H87NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,55 (м, 2H); 2,61 (м, 2H); 2,47 (м, 4H); 2,31 (м, 4H); 1,70-1,20 (м, 62H); 0,90 (м, 9H).
ET. Соединение 194: Гептадекан-9-ил-8-((3-изобутирамидопропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
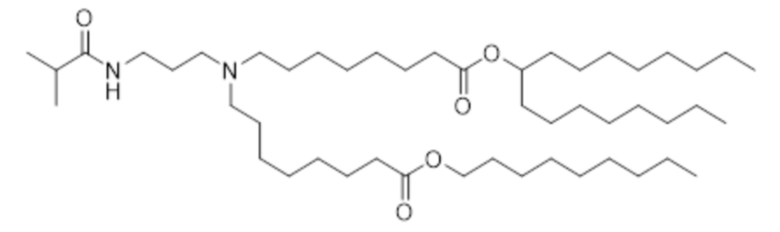
Химическая формула: C49H96N2O5
Молекулярная масса: 793,32
[00269] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (150 мг, 0,21 ммоль) и триэтиламина (90 мкл, 0,62 ммоль) в 5 мл сухого ДХМ при 0°C по каплям прибавили изобутирилхлорид (35 мкл, 0,31 ммоль). Через 30 минут охлаждающую баню убрали и раствор перемешивали при комн. темп. в течение 90 минут, после чего согласно ЖХ/MС исходного амина не осталось. Смесь разбавили a 50% насыщенным водным раствором гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-изобутирамидопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (65 мг, 0,08 ммоль, 39%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,65 мин. MС (ИЭР): m/z (MH+) 794,3 для C49H96N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,53 (с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,87 (с, 2H); 3,39 (м, 5H); 2,47 (уш. с, 2H); 2,36 (уш. м, 3H); 2,27 (м, 4H); 1,61 (м, 8H); 1,46 (уш. м, 9H); 1,26 (уш. м, 48H); 0,88 (т, 9H, J=7,5 Гц).
EU. Соединение 197: Гептадекан-9-ил-8-((3-(2-(бензилокси)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
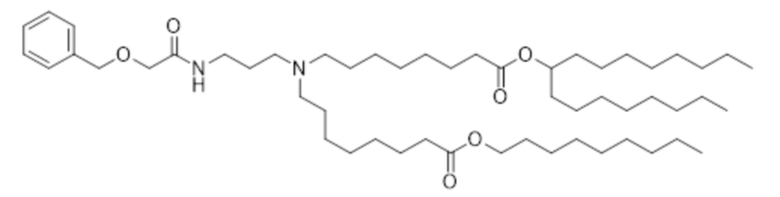
Химическая формула: C54H98N2O6
Молекулярная масса: 871,39
[00270] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (300 мг, 0,41 ммоль) и триэтиламина (145 мкл, 1 ммоль) в 10 мл сухого ДХМ при 0°C по каплям прибавили бензилоксиацетилхлорид (82 мкл, 0,52 ммоль). Охлаждающую баню убрали и раствор перемешивали при комн. темп. в течение 24 часов, после чего согласно ЖХ/MС исходного амина не осталось. Смесь разбавили a 50% насыщенным водным раствором гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-(бензилокси)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (179 мг, 0,21 ммоль, 50%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,66 мин. MС (ИЭР): m/z (MH+) 872,4 для C54H98N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,55 (с, 1H); 7,33 (м, 5H); 4,86 (квинт., 1H, J=6 Гц); 4,55 (с, 2H); 4,05 (т, 2H, J=6 Гц); 3,97 (с, 2H); 3,35 (кварт., 2H, J=6 Гц); 2,46 (уш. м, 2H); 2,28 (м, 7H); 1,65-1,48 (м, 15H); 1,26 (уш. м, 50H); 0,88 (т, 9H, J=7,5 Гц).
EV. Соединение 198: Гептадекан-9-ил-8-((3-(2-гидроксиацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
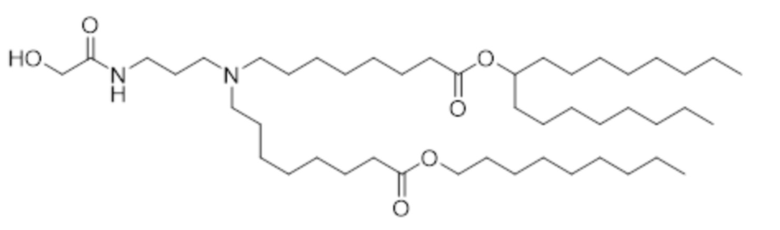
Химическая формула: C47H92N2O6
Молекулярная масса: 781,26
[00271] К раствору гептадекан-9-ил-8-((3-(2-(бензилокси)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (130 мг, 0,15 ммоль) в 5 мл этанола в атмосфере азота прибавили палладий 10% мас. на угле (приблизительно 20, кат.), стенки колбы смыли этанолом, а колбу оснастили водородным баллоном. Колбу вакуумировали и трижды заполнили водородом, затем перемешивали при комн. темп. в течение 24 часов, после чего согласно ЖХ/MC исходного эфира не осталось. Колбу продули азотом, смесь отфильтровали через диатомовую землю, отфильтрованные твердые вещества промывали этанолом и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-гидроксиацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (55 мг, 0,07 ммоль, 47%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,46 мин. MС (ИЭР): m/z (MH+) 782,2 для C47H92N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,73 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (м, 4H); 3,40 (кварт., 2H, J=6 Гц); 2,50 (м, 2H); 2,37 (т, 4H, J=6 Гц); 2,28 (м, 4H); 1,63 (м, 8H); 1,46 (уш. м, 8H); 1,26 (уш. м, 49H); 0,88 (т, 9H, J=7,5 Гц).
EW. Соединение 200: Гептадекан-9-ил-(E)-8-((3-(3-метил-2-нитрогуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Метил-(E/Z)-N-метил-N'-нитрокарбамимидотиоат
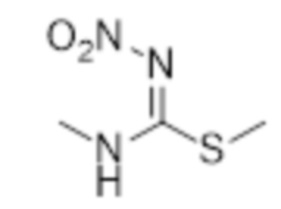
Химическая формула: C3H7N3O2S
Молекулярная масса: 149,17
[00272] К суспензии 2-метил-1-нитро-2-тиопсевдомочевины (1,0 г, 7,4 ммоль) и карбоната цезия (2,5 г, 7,8 ммоль в 8 мл сухого ДМФА прибавили иодметан (0,69 мл, 11,1 ммоль) и смесь перемешивали при комн. темп. в течение 24 часов. Желтую смесь разбавили водой и дважды экстрагировали EtOAc. Органические фазы объединили, трижды промывали 50% насыщенным водным раствором гидрокарбоната натрия, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и концентрировали с получением желтого твердого вещества. Его растворили в горячей воде, раствор отфильтровали и фильтрат охлаждали до 4°C в течение трех дней. Полученные твердые вещества выделяли фильтрованием, промывали водой, сушили воздухом, затем сушили в вакууме с получением метил-(E/Z)-N-метил-N'-нитрокарбамимидотиоата (85 мг, 0,57 ммоль, 8%) в виде бледно-желтого твердого вещества. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 10,02 (уш. с, 1H); 3,12 (д, 1H, J=6 Гц); 2,53 (с, 3H).
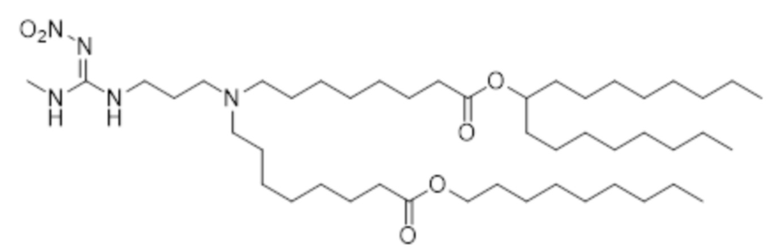
Химическая формула: C47H93N5O6
Молекулярная масса: 824,29
[00273] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,28 ммоль) в 5 мл метанола прибавили метил-(E/Z)-N-метил-N'-нитрокарбамимидотиоат (45 мг, 0,3 ммоль), полученный раствор нагревали до 70°C и перемешивали в течение 24 часов, после чего согласно ЖХ/MС исходного амина не осталось. Раствор разбавили ДХМ и один раз промывали насыщенным водным раствором гидрокарбоната натрия. Органическую фазу сушили (MgSO4), отфильтровали и фильтрат выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(E)-8-((3-(3-метил-2-нитрогуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (75 мг, 0,09 ммоль, 33%) в виде бледно-желтого сиропа. СВЭЖХ/ДСИО: RT=3,55 мин. MС (ИЭР): m/z (MH+) 825,3 для C47H93N5O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 9,26 (уш. с, 1H); 8,27 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,42 (уш. с, 2H); 2,86 (д, 3H, J=6 Гц); 2,60-2,40 (уш. м, 5H); 2,28 (м, 4H); 1,73 (уш. с, 2H); 1,65-1,40 (м, 16H); 1,26 (уш. м, 47H); 0,88 (т, 9H, J=7,5 Гц).
Пр. Соединение 207: Гептадекан-9-ил-8-((3-гуанидинопропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Гептадекан-9-ил-6-((трет-бутоксикарбонил)амино)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,7,11-триазанонадец-6-ен-19-оат
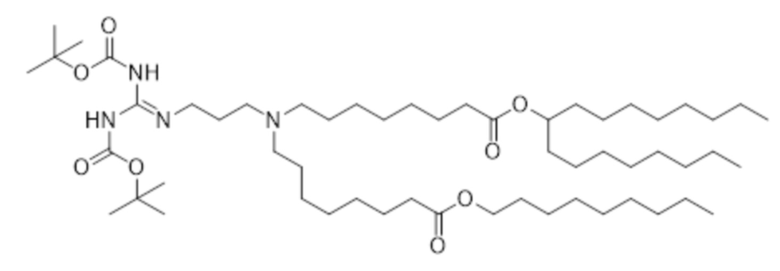
Химическая формула: C56H108N4O8
Молекулярная масса: 965,50
[00274] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (300 мг, 0,41 ммоль) и триэтиламина (230 мкл, 1,66 ммоль) в 10 мл сухом ДХМ при 0°C одной порцией прибавили 1,3-бис(трет-бутоксикарбонил)-2-(трифторметилсульфонил)гуанидин (325 мг, 0,83 ммоль) и полученный раствор и оставили постепенно нагреваться до комн. темп. при перемешивании в течение ночи. ЖХ/MC показал, что исходного материала не осталось, поэтому раствор разбавили ДХМ, промыли 50% насыщенным водным раствором гидрокарбоната натрия, органический слой сушили (MgSO4), отфильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-6-((трет-бутоксикарбонил)амино)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,7,11-триазанонадец-6-ен-19-оата (310 мг, 0,32 ммоль, 77%) в виде бесцветного масла с чистотой около 95%. Наибольшая единичная примесь имеет массу, соответствующую продукту с потерей одной группы Boc. Использовали как есть. СВЭЖХ/ДСИО: RT=3,90 мин. MС (ИЭР): m/z (MH+) 966,0 для C56H108N4O8. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 11,49 (с, 1H); 8,55 (уш. с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=7,5 Гц); 3,45 (кварт., 2H, J=6 Гц); 2,46 (м, 2H); 2,36 (м, 4H); 2,27 (м, 4H); 1,61 (м, 8H); 1,50 (м, 22H); 1,40 (м, 4H); 1,25 (уш. м, 48H); 0,88 (т, 9H, J=7,5 Гц).
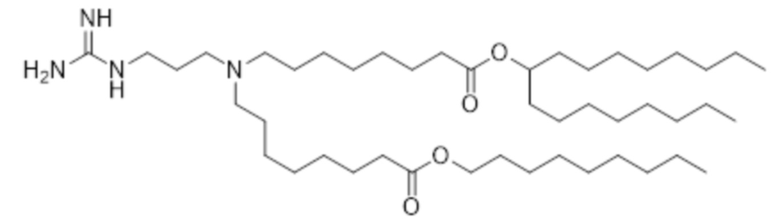
Химическая формула: C46H92N4O4
Молекулярная масса: 765,27
[00275] К раствору гептадекан-9-ил 6-((трет-бутоксикарбонил)амино)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,7,11-триазанонадец-6-ен-19-оата (310 мг, 0,32 ммоль) в 10 мл ДХМ прибавили трифторуксусную кислоту (500 мкл, избыток) и раствор перемешивали при комн. темп. в течение 48 часов, после чего согласно ЖХ/MС исходного материала не осталось. Раствор концентрировали, остаток дважды совместно перегнали с ДХМ и очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-гуанидинопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (210 мг, 0,27 ммоль, 84%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,16 мин. MС (ИЭР): m/z (MH+) 766,3 для C46H92N4O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 10,92 (уш. с, 1H); 8,82 (уш. с, 1H); 7,25 (уш. с, 2H); 4,85 (квинт., 1H, J=6 Гц); 4,05 (т, 2H, J=6 Гц); 3,38 (уш. с, 2H); 3,15 (уш. с, 2H); 3,00 (уш. с, 4H); 2,29 (м, 4H); 2,05 (уш. с, 2H); 1,91 (уш. с, 3H); 1,70-1,45 (уш. м, 12H); 1,26 (уш. м, 47H); 0,88 (т, 9H, J=7,5 Гц).
EY. Соединение 218: Гептадекан-9-ил-8-((3-(4-(гидроксиметил)-1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
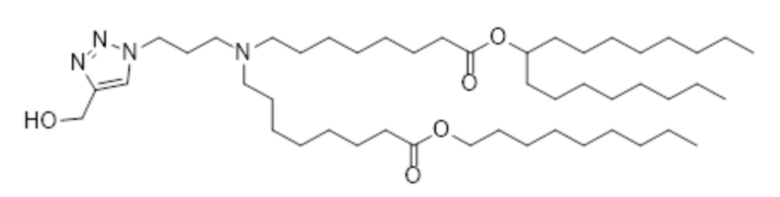
Химическая формула: C48H92N4O5
Молекулярная масса: 805,29
[00276] К раствору гептадекан-9-ил-8-((3-(4-(трет-бутоксиметил)-1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (190 мг, 0,22 ммоль) в 4 мл ДХМ прибавили трифторуксусную кислоту (675 мкл, избыток) и раствор перемешивали при комн. темп. в течение 72 часов, после чего согласно ЖХ/MС исходного материала не осталось. Раствор концентрировали, остаток дважды совместно перегоняли с ДХМ и очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(4-(гидроксиметил)-1H-1,2,3-триазол-1-ил)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (113 мг, 0,14 ммоль, 64%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,41 мин. MС (ИЭР): m/z (MH+) 806,1 для C48H92N4O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,54 (с, 1H); 4,86 (квинт., 1H, J=6 Гц); 4,80 (с, 2H); 4,40 (т, 2H, J=7,5 Гц); 4,05 (т, 2H, J=6 Гц); 2,38 (уш. м, 5H); 2,28 (м, 5H); 2,04 (уш. м, 2H); 1,61 (уш. м, 7H); 1,50 (уш. д, 4H, J=3 Гц); 1,26 (уш. м, 51H); 0,88 (т, 9H, J=7,5 Гц) (гидроксильный протон не наблюдали).
EZ. Соединение 232: Нонил-8-((2-гидроксиэтил)(6-оксо-6-((4-пентилциклогексил)окси)гексил)амино)октаноат

Химическая формула: C36H69NO5
Молекулярная масса: 595,950
[00277] Соединение 232 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=2,84 мин. MС (ИЭР): m/z (MH+) 596,84 для C36H69NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,01 (м, 0,5H); 4,68 (м, 0,5H); 4,08 (т, 2H); 3,56 (м, 2H), 2,67-2,55 (уш. м, 2H); 2,55-2,40 (уш. м, 4H); 2,31 (м, 4H); 1,97 (м, 1H); 1,82 (м, 2H); 1,73-1,15 (м, 43H); 1,02 (м, 1H); 0,90 (м, 6H).
FA. Соединение 233: Гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-(метилсульфонил)гуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Дифенил(метилсульфонил)карбонимидат
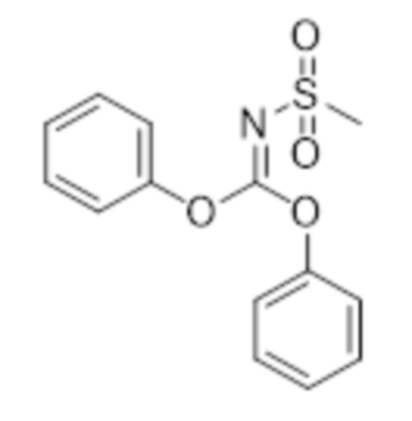
Химическая формула: C14H13NO4S
Молекулярная масса: 291,32
[00278] В 100 мл круглодонной колбе суспендировали 2,0 г (7,4 ммоль) дихлордифеноксиметана и 1,56 г (16,4 ммоль) метансульфонамида в 15 мл этилацетата при перемешивании с получением белое смеси. Ее нагревали до кипения (85 oC) и перемешивали в течение 24 часов, после чего на ЖХ/MС можно было увидеть только продукт. Смесь оставили охлаждаться до комн. темп., концентрировали, остаток суспендировали в ДХМ и отфильтровали. Отфильтрованное твердое вещество промывали ДХМ, фильтраты объединили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-40% EtOAc в смеси гексанов), содержащие продукт фракции объединили и концентрировали с получением желтоватого твердого вещества. Его растирали со смесью гексанов, отфильтровали, отфильтрованные твердые вещества промывали смесью гексанов и сушили на воздухе с получением дифенил(метилсульфонил)карбонимидата (0,84 г, 2,88 ммоль, 39%) в виде белого твердого вещества. СВЭЖХ/ДСИО: RT=0,50 мин. MС (ИЭР): m/z (MH+) 292,2 для C14H13NO4S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,45-7,37 (м, 4H); 7,30 (м, 2H); 7,21 (м, 4H); 3,01 (с, 3H).
Гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-(метилсульфонил)гуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C49H98N4O6S
Молекулярная масса: 871,41
[00279] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (200 мг, 0,28 ммоль) в 5 мл 2-пропанола прибавили триэтиламин (40 мкл, 0,28 ммоль) с последующим прибавлением дифенил(метилсульфонил)карбонимидата (81 мг, 0,28 ммоль) и белую смесь перемешивали при комн. темп. В течение трех часов, после чего согласно ЖХ/MС исходного амина не осталось. К раствору прибавили 2,0M раствор диметиламина в ТГФ (0,75 мл, 1,5 ммоль), желтоватый раствор нагревали до 80°C и перемешивали в течение 24 часов. Согласно ЖХ/MС исходного материала не осталось, поэтому раствор оставили охлаждаться до комн. темп., концентрировали в потоке азота и остаток растворили в ДХМ. Раствор один раз промывали насыщенным водным раствором гидрокарбоната натрия, затем сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Данное масло очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-(метилсульфонил)гуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (80 мг, 0,09 ммоль, 33%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,53 мин. MС (ИЭР): m/z (MH+) 872,1 для C49H98N4O6S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,22 (уш. с, 1H); 4,86 (квинт., 1H, J=12,3 Гц, 5,9 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,40 (уш. д, 2H, J=5,4 Гц); 2,97 (с, 9H); 2,52 (уш. с, 2H); 2,39 (уш. с, 3H); 2,29 (м, 4H); 1,69-1,49 (м, 15H); 1,45-1,15 (м, 50H); 0,87 (т, 9H, J=5,8 Гц)
FB. Соединение 234: 8-((2-Гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октан-2-ил 2-октилдеканоат
8-Гидроксиоктан-2-ил-2-октилдеканоат
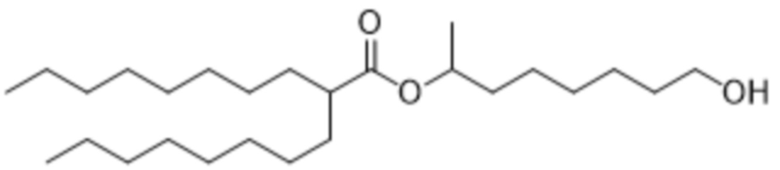
Химическая формула: C26H52O3
Молекулярная масса: 412,699
[00280] Соединение 8-гидроксиоктан-2-ил-2-октилдеканоат синтезировали согласно общей методике синтеза 8-гидроксиоктан-2-илдеканоата. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,93 (м, 1H); 3,66 (т, 2H); 2,29 (м, 1H); 1,69-1,16 (м, 42H); 0,90 (м, 6H).
8-Бромоктан-2-ил-2-октилдеканоат
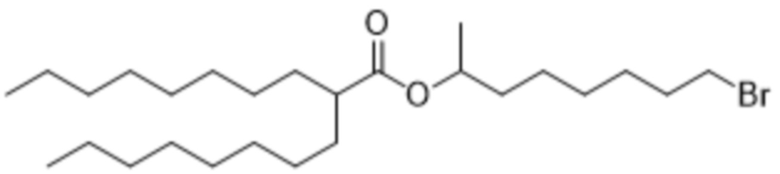
Химическая формула: C26H51BrO2
Молекулярная масса: 475,596
[00281] Соединение 8-бромоктан-2-ил-2-октилдеканоата синтезировали согласно общей методике (Z)-1-бром-10-октилоктадец-8-ена. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,94 (м, 1H); 3,42 (т, 2H); 2,30 (м, 1H); 1,87 (м, 2H); 1,69-1,16 (м, 39H); 0,90 (м, 6H).
8-((2-Гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октан-2-ил 2-октилдеканоат
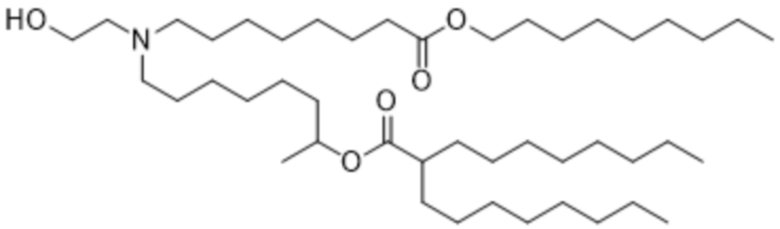
Химическая формула: C45H89NO5
Молекулярная масса: 724,209
[00282] Соединение 234 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,61 мин. MС (ИЭР): m/z (MH+) 725,08 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,93 (м, 1H); 4,08 (т, 2H); 3,71 (уш. м, 2H); 3,00-2,50 (уш. м, 6H); 2,32 (м, 3H); 1,73-1,15(м, 65H); 0,90 (м, 9H).
FC. Соединение 235: Гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)(3-пропионамидопропил)амино)октаноат
9-Гидроксидецилацетат
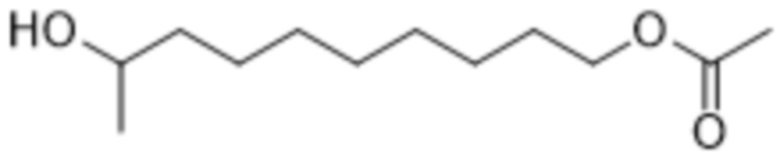
Химическая формула: C12H24O3
Молекулярная масса: 216,321
[00283] 9-Гидроксидецилацетат синтезировали согласно общей методике синтеза 8-гидроксиоктан-2-илдеканоата. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,07 (т, 2H); 3,80 (м, 1H); 2,07 (с, 3H); 1,76 (м, 2H); 1,54-1,16 (м, 16H).
10-Ацетоксидекан-2-ил-6-гидроксигексаноата
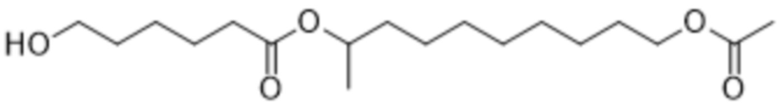
Химическая формула: C18H34O5
Молекулярная масса: 330,465
[00284] 10-Ацетоксидекан-2-ил-6-гидроксигексаноат синтезировали согласно общей методике синтеза 8-гидроксиоктан-2-илдеканоата. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,07 (т, 2H); 3,80 (м, 1H); 2,07 (с, 3H); 1,76 (м, 2H); 1,76 (м, 2H); 1,54-1,42 (м, 8H); 1,41-1,17 (м, 16H).
10-Ацетоксидекан-2-ил-6-бромгексаноат
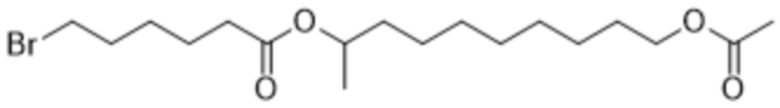
Химическая формула: C18H33BrO4
Молекулярная масса: 393,362
[00285] 10-Ацетоксидекан-2-ил-6-бромгексаноат синтезировали согласно общей методике синтеза (Z)-1-бром-10-октилоктадец-8-ена. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,93 (м, 1H); 4,07 (т, 2H); 3,43 (т, 2H); 2,32 (т, 2H); 2,07 (с, 3H); 1,90 (м, 2H); 1,76-1,42 (м, 8H); 1,41-1,17 (м, 13H).
Гептадекан-9-ил-8-((6-((10-ацетоксидекан-2-ил)окси)-6-оксогексил)(2-гидроксиэтил)амино)октаноат
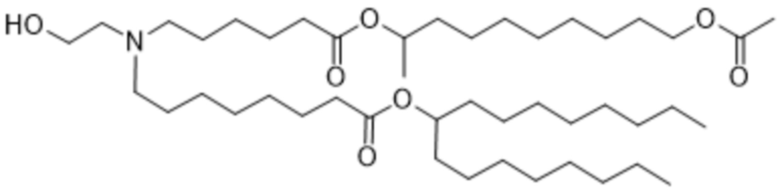
Химическая формула: C45H87NO7
Молекулярная масса: 754,191
[00286] Соединение 235 синтезировали согласно общей методике и иллюстративному примеру методики 1, описанным выше. СВЭЖХ/ДСИО: RT=3,33 мин. MС (ИЭР): m/z (MH+) 755,10 для C45H87NO7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 2H); 4,07 (т, 2H); 3,56 (м, 2H); 2,67-2,41 (м, 6H); 2,30 (т, 4H); 2,07 (с, 3H); 1,73-1,08(м, 61H); 0,90 (м, 6H).
FD. Соединение 236: Гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)(3-пропионамидопропил)амино)октаноат
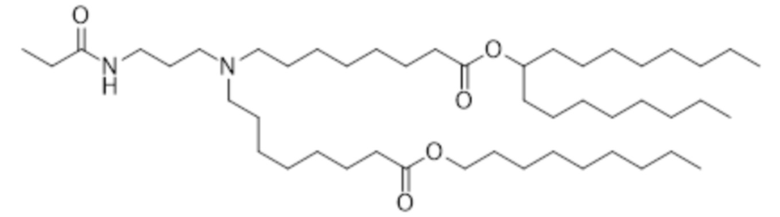
Химическая формула: C48H94N2O5
Молекулярная масса: 779,29
[00287] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (160 мг, 0,22 ммоль) и триэтиламина (95 мкл, 0,66 ммоль) в 5 мл сухого ДХМ при 0°C по каплям прибавили пропионилхлорид (30 мкл, 0,33 ммоль). Через 30 минут охлаждающую баню убрали и раствор перемешивали при комн. темп. в течение 30 минут, после чего согласно ЖХ/MС исходного амина не осталось. Смесь разбавили a 50% насыщенным водным раствором гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)(3-пропионамидопропил)амино)октаноата (90 мг, 0,12 ммоль, 52%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,59 мин. MС (ИЭР): m/z (MH+) 780,1 для C48H94N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,29 (уш. с, 1H); 4,86 (квинт., 1H, J=12,4 Гц, 5,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,34 (кварт., 2H, J=11,3 Гц, 5,9 Гц); 2,63-2,33 (м, 6H); 2,31-2,25 (м, 4H); 2,16 (кварт., 2H, J=15,1 Гц, 7,6 Гц); 1,61 (уш. т., 8H, J=6,8 Гц); 1,55-1,38 (уш. м, 9H); 1,35-1,20 (уш. м, 47H); 1,14 (т, 3H, J=7,6 Гц); 0,87 (т, 9H, J=6,4 Гц).
FE. Соединение 244: Гептадекан-9-ил-8-((2-ацетамидоэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Гептадекан-9-ил-8-((2-((трет-бутоксикарбонил)амино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
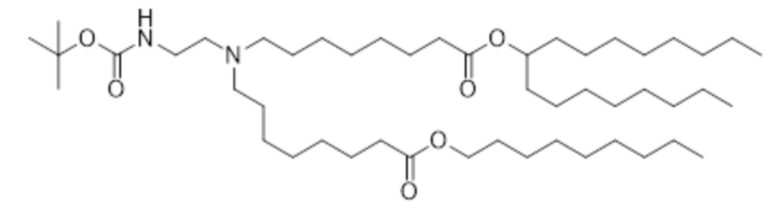
Химическая формула: C49H96N2O6
Молекулярная масса: 809,32
[00288] К раствору гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноата
(1,0 г, 1,5 ммоль) и N-Boc-глициналя (0,36 г, 2,25 ммоль) в 10 мл сухого ТГФ прибавили MgSO4 (приблизительно 0,5 г, избыток) и белую смесь перемешивали при комн. темп. в течение 30 минут. К смеси порциями прибавили триацетоксиборогидрид натрия (0,67 г, 3,0 ммоль) в в течение пяти минут и полученную смесь перемешивали при комн. темп. в течение ночи. Согласно ЖХ/MС исходного материала не осталось, поэтому реакционную смесь погасили прибавлением приблизительно 5 мл насыщенного водного раствора гидрокарбоната натрия. Полученную смесь разбавили водой, трижды экстрагировали ДХМ, органические фазы объединили, один раз промывали водой, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((2-((трет-бутоксикарбонил)амино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (930 мг, 1,15 ммоль, 77%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=3,66 мин. MС (ИЭР): m/z (MH+) 809,6 для C49H96N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (квинт., 1H, J=11,9 Гц, 6,0 Гц); 4,07 (т, 2H, J=6,7 Гц); 2,60-2,25 (м, 8H); 1,70-1,55 (м, 6H); 1,53-1,43 (м, 22H); 1,37-1,22 (м, 48H); 0,90 (т, 9H, J=6,8 Гц)
Гептадекан-9-ил-8-((2-аминоэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат
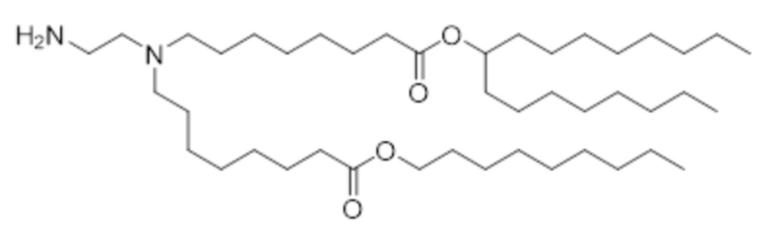
Химическая формула: C44H88N2O4
Молекулярная масса: 709,20
[00289] К раствору гептадекан-9-ил-8-((2-((трет-бутоксикарбонил)амино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (820 мг, 1,0 ммоль) в 20 мл ДХМ при 0°C прибавили 4N раствор HCl в 1,4-диоксане (2,5 мл, 10 ммоль), полученный желтый раствор оставили нагреваться до комн. темп. и перемешивали в течение трех часов, после чего согласно ЖХ/MС исходного материала не осталось. Красный/коричневый раствор разбавили ДХМ и промывали 1:1 смесью насыщенного водного раствора гидрокарбоната натрия и насыщенного водного раствора хлорида натрия. Фазы отделили и водную фазу дважды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением коричневого масла. Его очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((2-аминоэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (520 мг, 0,73 ммоль, 72%) в виде коричневого масла. СВЭЖХ/ДСИО: RT=3,15 мин. MС (ИЭР): m/z (MH+) 709,5 для C44H88N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=12,4 Гц, 5,9 Гц); 4,05 (т, 2H, J=6,7 Гц); 2,74 (т, 2H, J=6,0 Гц); 2,52-2,35 (м, 5H); 2,31-2,25 (м, 4H); 1,75-1,67 (уш. с, 5H); 1,61 (уш. т., 6H, J=6,8 Гц); 1,55-1,37 (уш. м, 8H); 1,36-1,16 (уш. м, 46H); 0,88 (т, 9H, J=6,1 Гц).
Гептадекан-9-ил-8-((2-ацетамидоэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C46H90N2O5
Молекулярная масса: 751,24
[00290] К раствору гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноат (1,0 г, 1,5 ммоль) и N-Boc-глициналя (0,36 г, 2,25 ммоль) в 10 мл сухого ТГФ прибавили MgSO4 (приблизительно 0,5 г, избыток) и белую смесь перемешивали при комн. темп. в течение 30 минут. К смеси порциями прибавили триацетоксиборогидрид натрия (0,67 г, 3,0 ммоль) в в течение пяти минут и полученную смесь перемешивали при комн. темп. в течение ночи. Согласно ЖХ/MС исходного материала не осталось, поэтому реакционную смесь погасили прибавлением приблизительно 5 мл насыщенного водного раствора гидрокарбоната натрия. Полученную смесь разбавили водой, трижды экстрагировали ДХМ, органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((2-((трет-бутоксикарбонил)амино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (930 мг, 1,15 ммоль, 77%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=3,66 мин. MС (ИЭР): m/z (MH+) 809,6 для C49H96N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,88 (квинт., 1H, J=11,9 Гц, 6,0 Гц); 4,07 (т, 2H, J=6,7 Гц); 2,60-2,25 (м, 8H); 1,70-1,55 (м, 6H); 1,53-1,43 (м, 22H); 1,37-1,22 (м, 48H); 0,90 (т, 9H, J=6,8 Гц)
FF. Соединение 246: Гептадекан-9-ил-8-((2-(метилсульфонамидо)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C45H90N2O6S
Молекулярная масса: 787,28
[00291] К раствору гептадекан-9-ил-8-((2-аминоэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (160 мг, 0,23 ммоль) в 4 мл сухом ДХМ прибавили триэтиламин (63 мкл, 0,45 ммоль) и раствор охладили до 0 oC. К нему прибавили метансульфонилхлорид (24 мкл, 0,32 ммоль), раствор оставили нагреваться до комн. темп. и перемешивали в течение четырех часов. Согласно ЖХ/MС исходного материала не осталось, поэтому раствор разбавили ДХМ, один раз промывали a 50% насыщенным водным раствором гидрокарбоната натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((2-(метилсульфонамидо)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (130 мг, 0,165 ммоль, 73%) в виде желтого масла. СВЭЖХ/ДСИО: RT=3,48 мин. MС (ИЭР): m/z (MH+) 787,6 для C45H90N2O6S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=12,4 Гц, 5,2 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,14 (уш. с, 2H); 2,95 (с, 3H); 2,61 (уш. с, 2H); 2,42 (уш. с, 3H); 2,32-2,25 (м, 4H); 1,61 (уш. т., 6H, J=7,0 Гц); 1,55-1,38 (м, 8H); 1,37-1,14 (м, 50H); 0,88 (т, 9H, J=6,1 Гц).
FG. Соединение 247: Гептадекан-9-ил-(Z)-8-((2-(2-циано-3,3-диметилгуанидино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
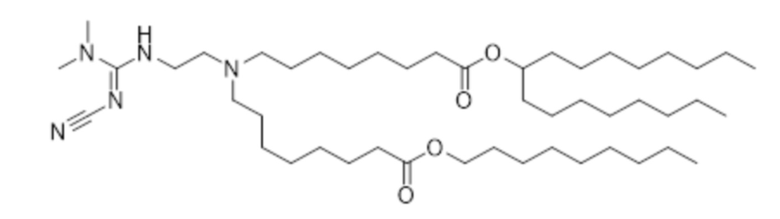
Химическая формула: C48H93N5O4
Молекулярная масса: 804,30
[00292] К раствору гептадекан-9-ил-8-((2-аминоэтил)(8-(нонилокси)-8-оксооктил)амино)октаноата (160 мг, 0,23 ммоль) в 4 мл 2-пропаноле прибавили триэтиламин (31 мкл, 0,23 ммоль) с последующим прибавлением дифенилцианокарбонимидата (54 мг, 0,23 ммоль) и белую смесь перемешивали при комн. темп. в течение двух часов после чего она превратилась в бесцветный раствор. Согласно ЖХ/MС исходного материала не осталось и наблюдали только монофенилкарбамимидат (MW=853,3). К нему прибавили 2M раствор диметиламина в метаноле (1,1 мл, 2,2 ммоль), полученный бледно-желтый раствор нагревали до 55°C и перемешивали в течение 20 часов, после чего согласно ЖХ/MС промежуточного карбамимидатного продукта не осталось. Реакционную смесь оставили охлаждаться до комн. темп., концентрировали, остаток растворили в ДХМ, дважды промывали насыщенным водным раствором гидрокарбоната натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((2-(2-циано-3,3-диметилгуанидино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (75 мг, 0,09 ммоль, 41%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,46 мин. MС (ИЭР): m/z (MH+) 804,6 для C48H93N5O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,80 (уш. с, 1H); 4,86 (квинт., 1H, J=12,5 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,60 (уш. с, 2H); 3,01 (с, 6H); 2,59 (уш. с, 2H); 2,40 (уш. с, 3H); 2,32-2,25 (м, 4H); 1,68-1,45 (м, 12H); 1,38-1,12 (м, 51H); 0,88 (т, 9H, J=6,0 Гц).
FH. Соединение 251: Гептадекан-9-ил-8-((3-((2-амино-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C49H91N3O6
Молекулярная масса: 818,28
[00293] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (220 мг, 0,28 ммоль) в 8 мл этанола прибавили 3-амино-4-метоксициклобут-3-ен-1,2-дион [JACS, 88(7), 1533-1536 (1966)](35 мг, 0,28 ммоль), полученный бесцветный раствор нагревали до 40°C и перемешивали в течение 20 часов, через которые согласно ЖХ/MС исходного амина не осталось. Раствор концентрировали в вакууме и остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((2-амино-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (175 мг, 0,21 ммоль, 77%) в виде смолистого белого твердого вещества. СВЭЖХ/ДСИО: RT=3,38 мин. MС (ИЭР): m/z (MH+) 818,6 для C49H91N3O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,43 (уш. с, 1H); 4,85 (квинт., 1H, J=12,6 Гц, 5,8 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,65 (уш. с, 2H); 2,78-2,38 (м, 5H); 2,29 (м, 4H); 1,84 (уш. с, 2H); 1,68-1,41 (м, 14H); 1,40-1,14 (м, 51H); 0,88 (т, 9H, J=6,0 Гц).
FI. Соединение 252: Гептадекан-9-ил-8-((3-(2-(метилтио)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
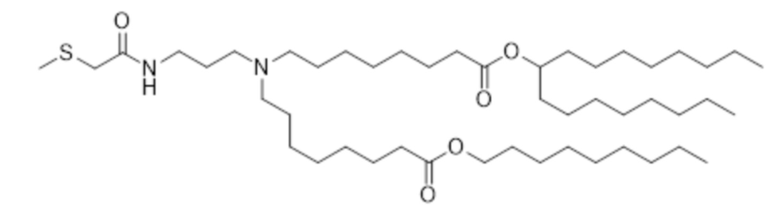
Химическая формула: C48H94N2O5S
Молекулярная масса: 811,35
[00294] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (1,0 г, 1,38 ммоль) и (метилтио)уксусной кислоты (Matrix Scientific, Колумбия, Южная Каролина) (150 мкл, 1,66 ммоль) в 20 мл сухого ДХМ прибавили 4-(диметиламино)пиридин (42 мг, 0,35 ммоль) с последующим прибавлением 1-[бис(диметиламино)метилен]-1H-1,2,3-триaзоло[4,5-b]пиридиний-3-оксид гексафторфосфата (HATU; 790 мг, 2,1 ммоль) и в конце прибавили N, N-диизопропилэтиламин (740 мкл, 4,1 ммоль) и полученную смесь перемешивали при комн. темп. в течение ночи. Согласно ЖХ/MС исходного амина не осталось, поэтому желтый раствор разбавили ДХМ, дважды промывали насыщенным водным раствором гидрокарбоната натрия, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-50% метанол в ДХМ) с получением гептадекан-9-ил-8-((3-(2-(метилтио)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (1,0 г, 1,23 ммоль, 89%) в виде желтого масла. СВЭЖХ/ДСИО: RT=3,54 мин. MС (ИЭР): m/z (MH+) 811,56 для C48H94N2O5S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,79 (уш. с, 1H); 4,86 (квинт., 1H, J=12,5 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,40 (уш. с, 2H); 3,17 (с, 2H); 2,96 (уш. с, 2H); 2,66-2,34 (уш. м, 3H); 2,28 (м, 4H); 2,15 (с, 3H); 1,88-1,41 (м, 16H); 1,39-1,18 (уш. м, 49H); 0,88 (т, 9H, J=5,8 Гц).
FJ. Соединение 255: Гептадекан-9-ил-8-((4-ацетамидобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Бензил-(4,4-диэтоксибутил)карбамат
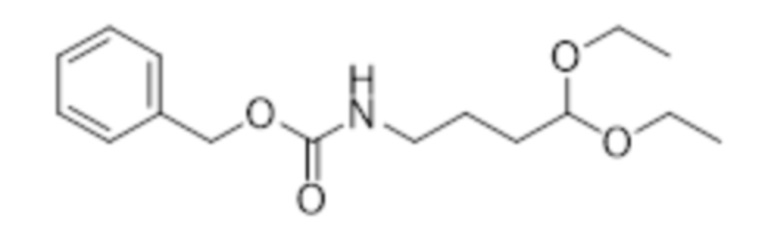
Химическая формула: C16H25NO4
Молекулярная масса: 295,38
[00295] К раствору диэтилацеталя 4-аминобутаналя (Aldrich, Сент-Луис, Миссури) (1 г, 6,2 ммоль) в 25 мл эфира прибавили 25 мл воды с последующим прибавлением карбоната калия (2,6 г, 18,6 ммоль) и полученнуый бесцветный двухфазный раствор охладили до 0°C при интенсивном перемешивании. К нему по каплям прибавляли бензилхлорформиат (0,88 мл, 6,2 ммоль) в течение десяти минут и полученную смесь оставили медленно нагреваться до комн. темп. в течение ночи. Фазы отделили и водную фазу экстрагировали эфиром. Органические фазы объединили, дважды промывали 10% водным раствором лимонной кислоты, затем насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением бесцветного масла. Его очищали с помощью хроматографии на силикагеле (0-50% EtOAc в смеси гексанов) с получением бензил-(4,4-диэтоксибутил)карбамата (1,56 г, 5,3 ммоль, 85%) в виде бесцветного масла. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,32 (м, 5H); 5,09 (с, 2H); 4,88 (с, 1H); 4,48 (т, 2H, J=5,3 Гц); 3,70-3,55 (м, 2H); 3,54-3,40 (м, 2H); 3,22 (кварт.; 2H, J=12,5 Гц, 6,2 Гц); 1,71-1,51 (м, 4H); 1,20 (т, 6H, J=7,0 Гц).
Бензил-(4-оксобутил)карбамат
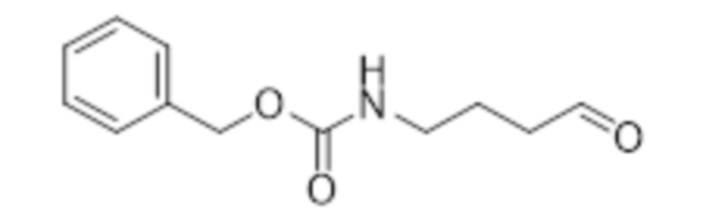
Химическая формула: C12H15NO3
Молекулярная масса: 221,26
[00296] К раствору бензил-(4,4-диэтоксибутил)карбамата (1,56 г, 5,3 ммоль) в 25 мл ацетога прибавили 1N водный раствор HCl (25 мл, 25 ммоль) с получением мутной смеси, которая быстро стала прозрачной. Ее перемешивали при комн. темп. в течение ночи, после чего согласно ТСХ исходного ацеталя не осталось. Раствор дважды экстрагировали Et2O,органические фазы смешали, один раз промывали насыщенным водным раствором гидрокарбоната натрия, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением бесцветного масла Его очищали с помощью хроматографии на силикагеле (0-50% EtOAc в смеси гексанов) с получением бензил-(4-оксобутил)карбамата (0,82 г, 5,3 ммоль, 70%) в виде бесцветной жидкости. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,36 (м, 5H); 5,52 (уш. д, 1H, J=12,0 Гц); 5,15 (с, 2H); 3,68-3,52 (м, 1H); 3,44-3,30 (м, 1H); 2,18-1,79 (м, 4H) (альдегидный протон не наблюдали).
Гептадекан-9-ил-8-((4-(((бензилокси)карбонил)амино)бутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
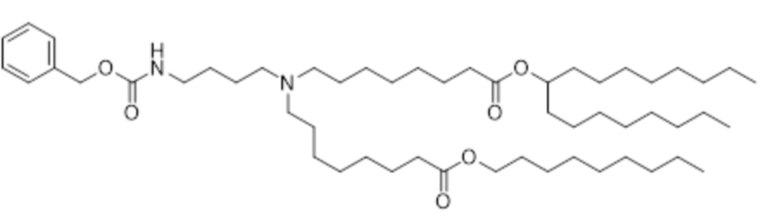
Химическая формула: C54H98N2O6
Молекулярная масса: 871,39
[00297] К раствору гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноата (1,65 г, 2,5 ммоль) и бензил-(4-оксобутил)карбамата (0,82 г, 3,71 ммоль) в 15 мл сухого ТГФ прибавили безводного MgSO4 (приблизительно 0,5 г, избыток) и белую смесь перемешивали при комн. темп. в течение 30 минут. К смеси порциями прибавляли триацетоксиборогидрид натрия (1,1 г, 4,9 ммоль) в течение пяти минут и полученную белую смесь перемешивали при комн. темп. в течение ночи. Согласно ЖХ/MС исходного материала не осталось, поэтому реакционную смесь погасили прибавлением приблизительно 5 мл насыщенного водного раствора гидрокарбоната натрия. Полученную смесь разбавили водой, трижды экстрагировали ДХМ, органические фазы объединили, один раз промывали водой водой, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((4-(((бензилокси)карбонил)амино)бутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (1,43 г, 1,64 ммоль, 66%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=3,54 мин. MС (ИЭР): m/z (MH+) 871,52 для C54H98N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,34 (м, 5H); 5,51 (м, 1H); 5,15 (м, 2H); 5,09 (с, 2H); 4,86 (квинт., 1H, J=12,3 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,60 (м, 1H); 3,38 (м, 1H); 3,20 (уш. д, 2H, J=3,8 Гц); 2,40 (уш. с, 4H); 2,27 (м, 4H); 2,15-1,75 (м, 4H); 1,61 (уш. т., 6H, J=6,3 Гц); 1,55-1,43 (м, 8H); 1,37-1,15 (м, 46H); 0,88 (т, 9H, J=5,8 Гц).
Гептадекан-9-ил-8-((4-аминобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
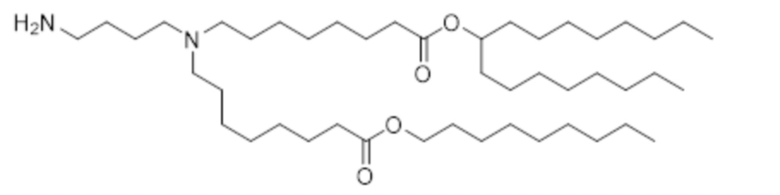
Химическая формула: C46H92N2O4
Молекулярная масса: 737,25
[00298] Гептадекан-9-ил-8-((4-(((бензилокси)карбонил)амино)бутил)(8-(нонилокси)-8-оксооктил)амино)октаноат (1,42 г, 1,63 ммоль) растворили в 20 мл этанола при перемешивании с получением бледно-желтого раствора. Реакционный сосуд продували азотом и добавляли 10% мас. палладия на угле (около 200 мг, кат.), стенки сосуда промывали 5 мл этанола, и сосуд снова продували азотом. Колбу снабдили баллоном с водородом, вакуумировали и трижды заполнили водородом. Полученную темную смесь перемешивали при комн. темп. в течение пяти часов, после чего согласно ЖХ/MС исходного материала не осталось. Колбу продували азотом, смесь отфильтровали через целит, отфильтрованные твердые вещества промывали этанолом и фильтрат концентрировали с получением мутного белого масла. Его очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((4-аминобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (706 мг, 0,96 ммоль, 59%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,09 мин. MС (ИЭР): m/z (MH+) 737,43 для C46H92N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=12,2 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 2,71 (т, 1H, J=6,4 Гц); 2,48-2,34 (м, 6H); 2,33-2,23 (м, 4H); 1,95 (уш. с, 2H); 1,61 (уш. т., 6H, J=6,6 Гц); 1,55-1,38 (м, 12H); 1,37-1,17 (м, 49H); 0,88 (т, 9H, J=5,9 Гц).
Гептадекан-9-ил-8-((4-ацетамидобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
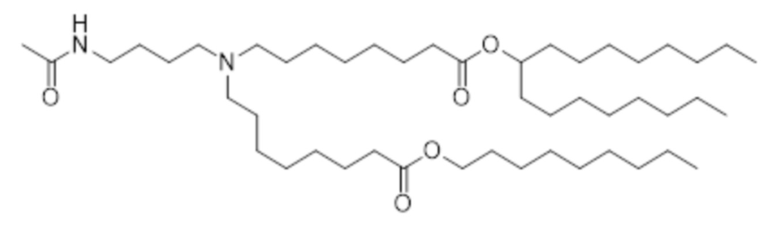
Химическая формула: C48H94N2O5
Молекулярная масса: 779,29
[00299] К раствору гептадекан-9-ил-8-((4-аминобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (220 мг, 0,3 ммоль) в 4 мл сухом ДХМ прибавили триэтиламин (125 мкл, 0,9 ммоль) и раствор охладили до 0 oC. К нему прибавили уксусный ангидрид (42 мкл, 0,45 ммоль) и раствор оставили нагреваться до комн. темп. при перемешивании в течение ночи. Согласно ЖХ/MС исходного материала не осталось, поэтому раствор разбавили ДХМ, один раз промывали a 50% насыщенным водным раствором гидрокарбоната натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((4-ацетамидобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (160 мг, 0,20 ммоль, 69%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,50 мин. MС (ИЭР): m/z (MH+) 779,66 для C48H94N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,33 (уш. с, 1H); 4,86 (квинт., 1H, J=12,3 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,23 (кварт., 2H, J=11,9 Гц, 6,1 Гц); 2,46-2,33(м, 5H); 2,32-2,22 (м, 4H); 1,95 (с, 3H); 1,68-1,56 (м, 6H); 1,54-1,36 (м, 12H); 1,35-1,15 (м, 49H); 0,87 (т, 9H, J=5,8 Гц).
FK. Соединение 256: 8-(Гептадекан-9-илокси)-N-(3-(2-(метилсульфинил)ацетамидо)пропил)-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминоксид
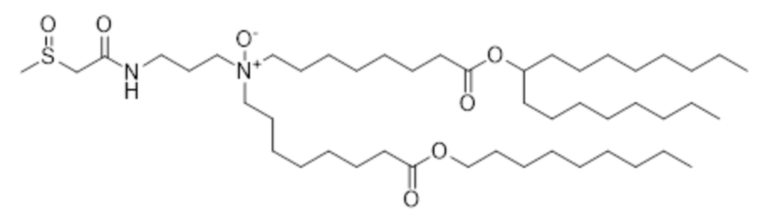
Химическая формула: C48H94N2O7S
Молекулярная масса: 843,35
FL. Соединение 257: 8-(Гептадекан-9-илокси)-N-(3-(2-(метилсульфонил)ацетамидо)пропил)-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминоксид
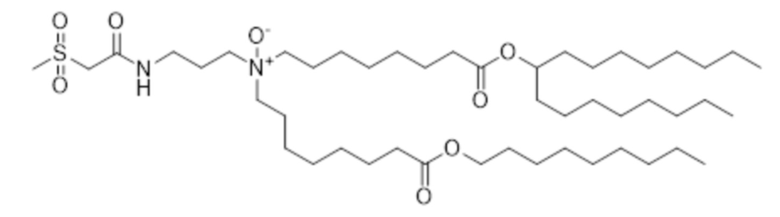
Химическая формула: C48H94N2O8S
Молекулярная масса: 859,35
[00300] К раствору гептадекан-9-ил-8-((3-(2-(метилтио)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (350 мг, 0,43 ммоль) в 5 мл ДХМ при 0°C одной порцией прибавили м-хлорпероксибензойную кислоту (50% по массе; 300 мг, 0,84 ммоль). Ледяную баню убрали и полученный желтый раствор перемешивали при комн. темп. в течение 24 часов, после чего согласно ЖХ/MС исходного материала не осталось. Раствор разбавили ДХМ, дважды промыли насыщенным водным раствором гидрокарбоната натрия, сушили (MgSO4), отфильтровали and фильтрат концентрировали с получением бледного желтого масла. Его очищали с помощью хроматографии на силикагеле (0-75% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением двух наборов фракций. Первый набор концентрировали с получением 8-(гептадекан-9-илокси)-N-(3-(2-(метилсульфонил)ацетамидо)пропил)-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминоксида (60 мг, 0,07 ммоль, 16%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,44 мин. MС (ИЭР): m/z (MH+) 859,62 для C48H94N2O8S (Соединение 257). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 10,95 (уш. с, 1H); 4,86 (квинт., 1H, J=12,3 Гц, 5,9 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,93 (с, 2H); 3,38 (уш. д, 3H, J=5,2 Гц); 3,15 (м, 6H); 2,62-2,36 (м, 1H); 2,34-2,21 (м, 4H); 2,02 (т, 2H, J=6,1 Гц); 1,86-1,55 (м, 10H); 1,54-1,43 (м, 5H); 1,41-1,14 (м, 48H); 0,88 (т, 9H, J=6,0 Гц).
[00301] Второй набор фракций концентрировали с получением 8-(гептадекан-9-илокси)-N-(3-(2-(метилсульфинил)ацетамидо)пропил)-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминоксида (75 мг, 0,09 ммоль, 20%) в виде воскообразного белого твердого вещества. СВЭЖХ/ДСИО: RT=3,42 мин. MС (ИЭР): m/z (MH+) 843,71 для C48H94N2O7S (Соединение 256). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 10,15 (уш. с, 1H); 4,86 (квинт., 1H, J=12,5 Гц, 6,3 Гц); 4,05 (т, 2H, J=6,6 Гц); 3,57 (м, 2H); 3,44-3,25 (м, 3H); 3,14 (т, 3H, J=8,2 Гц); 2,72 (с, 3H); 2,54-2,34 (м, 1H); 2,33-2,24 (м, 4H); 2,04 (т, 2H, J=5,6 Гц); 1,88-1,71 (м, 2H); 1,69-1,55 (м, 8H); 1,54-1,43 (м, 4H); 1,41-1,14 (м, 49H); 0,88 (т, 9H, J=6,0 Гц).
FM. Соединение 258: Гептадекан-9-ил-8-((3-(2-(метилсульфинил)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C48H94N2O6S
Молекулярная масса: 827,35
[00302] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,55 ммоль) и метанeсульфинилуксусной кислоты [J. Med. Chem., 38(3), 508-525 (1995)] (81 мг, 0,66 ммоль) в 10 мл сухого ДХМ прибавили 4-(диметиламино)пиридин (17 мг, 0,14 ммоль) с последующим прибавлением 1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридиний-3-оксид гексафторфосфата (HATU; 315 мг, 0,83 ммоль) и в конце прибавили N, N-диизопропилэтиламин (300 мкл, 1,66 ммоль) и полученную смесь перемешивали при комн. темп. в течение ночи. Согласно ЖХ/MС исходного амина не осталось, поэтому темно-оранжевый раствор разбавили ДХМ, дважды промывали насыщенным водным раствором гидрокарбоната натрия, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением темно-желтого масла. Его очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-(метилсульфинил)ацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (190 мг, 0,23 ммоль, 41%) в виде желтого масла. СВЭЖХ/ДСИО: RT=3,44 мин. MС (ИЭР): m/z (MH+) 827,56 для C48H94N2O6S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,74 (уш. с, 1H); 4,86 (квинт., 1H, J=12,5 Гц, 6,1 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,60 (д, 1H, J=13,7 Гц); 3,36 (м, 3H); 2,71 (с, 3H); 2,60-2,48 (уш. с, 2H); 2,47-2,34 (уш. с, 3H); 2,28 (м, 4H); 1,76-1,55 (м, 8H); 1,54-1,38 (м, 8H); 1,37-1,15 (уш. м, 49H); 0,88 (т, 9H, J=5,9 Гц).
FN. Соединение 259: Гептадекан-9-ил-(Z)-8-((4-(2-циано-3,3-диметилгуанидино)бутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
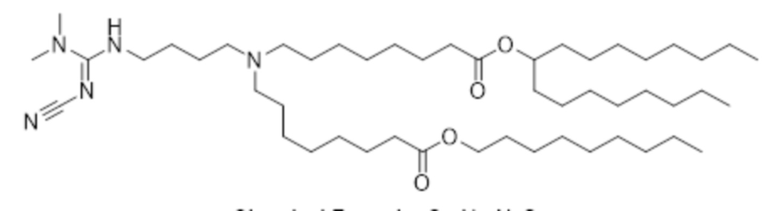
Химическая формула: C50H97N5O4
Молекулярная масса: 832,36
[00303] К раствору гептадекан-9-ил-8-((4-аминобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (235 мг, 0,32 ммоль) в 4 мл 2-пропанола прибавили триэтиламин (44 мкл, 0,32 ммоль) с последующим прибавлением дифенилцианокарбонимидата (76 мг, 0,32 ммоль) и белую смесь перемешивали при комн. темп. в течение девяноста минут после чего она стала прозрачным раствором. Согласно ЖХ/MС исходного материала не осталось и наблюдали только монофенилкарбамимидат (MW=881,4). К нему прибавили a 2M раствор диметиламина в метаноле (1,6 мл, 3,2 ммоль), полученный бледно-желтый раствор нагревали до 55°C и перемешивали в течение 20 часов, после чего согласно ЖХ/MС промежуточного карбамимидатного продукта не осталось. Реакционную смесь оставили охлаждаться до комн. темп., концентрировали, остаток растворили в ДХМ, дважды промывали насыщенным водным раствором гидрокарбоната натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-60% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((4-(2-циано-3,3-диметилгуанидино)бутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (130 мг, 0,16 ммоль, 49%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,43 мин. MС (ИЭР): m/z (MH+) 832,48 для C50H97N5O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,50 (уш. с, 1H); 4,86 (квинт., 1H, J=12,2 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,48 (кварт., 2H, J=11,4 Гц, 5,7 Гц); 3,02 (с, 6H); 2,49 (уш. с, 6H); 2,32-2,22 (м, 4H); 1,70-1,55 (м, 8H); 1,54-1,45 (м, 6H); 1,44-1,15 (м, 52H); 0,87 (т, 9H, J=5,8 Гц).
FO. Соединение 260: Гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-сульфамоилгуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Дифенилсульфамоилкарбонимидат
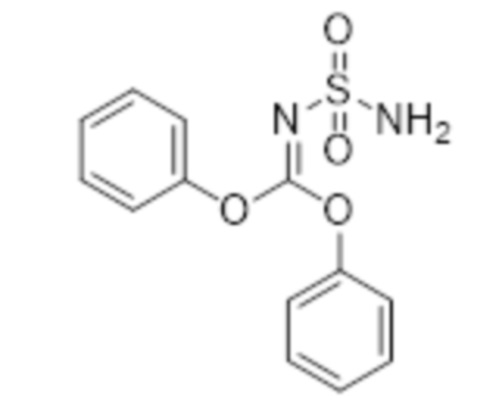
Химическая формула: C13H12N2O4S
Молекулярная масса: 292,31
[00304] К раствору дихлордифеноксиметана (1 г, 3,7 ммоль) в 10 мл сухого ацетонитрила в атмосфере азота прибавили сульфамид (0,72 г, 7,4 ммоль) и бледно-желтую смесь перемешивали при комн. темп. в течение 72 часов. Полученную смесь концентрировали, остаток растирали с ДХМ, отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-60% EtOAc в смеси гексанов) с получением дифенил сульфамоилкарбонимидата (295 мг, 1,01 ммоль, 27%) в виде бесцветного масла, которое затвердело до полупрозрачного белого твердого вещества при стоянии. СВЭЖХ/ДСИО: RT=0,31 мин. MС (ИЭР): m/z (M-SO2NH2) 213,97 для C13H12N2O4S. 1H ЯМР (300 МГц, ДМСО-d6) δ: м.д. 7,54-7,29 (дт, 10H, J=44,5 Гц, 7,5 Гц); 7,19 (с, 2H).
Гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-сульфамоилгуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C48H97N5O6S
Молекулярная масса: 872,39
[00305] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) в 5 мл 2-пропанола прибавили триэтиламин (48 мкл, 0,35 ммоль) с последующим прибавлением дифенилсульфамоилкарбонимидат (101 мг, 0,35 ммоль) и смесь перемешивали при комн. темп. в течение двух часов, после которых ЖХ/MС исходного материала не было и единственный наблюдаемый пик соответствовал монофенилкарбамимидатному промежуточному соединению (MW=921,4). К реакционной смеси прибавили 2M раствор диметиламина в метаноле (1 мл, 2 ммоль) и полученный бледно-желтый раствор нагревали до 55°C в течение 18 часов. Реакция завершилась согласно ЖХ/MС, поэтому раствор выпарили в вакууме, разбавили ДХМ и один раз промывали насыщенным водным раствором гидрокарбоната натрия. Органическую фазу сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением мутного бледно-желтого масла. Его очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-сульфамоилгуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (155 мг, 0,18 ммоль, 51%) в виде желтоватого сиропа. СВЭЖХ/ДСИО: RT=3,34 мин. MС (ИЭР): m/z (MH+) 872,58 для C48H97N5O6S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,02 (уш. с, 1H); 4,86 (квинт., 1H, J=12,4 Гц, 6,4 Гц); 4,48 (уш. с, 2H); 4,05 (т, 2H, J=6,7 Гц); 3,36 (кварт., 2H, J=11,5 Гц, 5,5 Гц); 2,97 (с, 6H); 2,54 (уш. с, 2H); 2,41 (уш. с, 3H); 2,28 (м, 4H); 1,79-1,68 (м, 2H); 1,67-1,55 (м, 6H); 1,54-1,45 (м, 4H); 1,44-1,37 (м, 2H); 1,36-1,14 (м, 51H); 0,87 (т, 9H, J=5,8 Гц).
FP. Соединение 261: Гептадекан-9-ил-8-((3-гидроксипропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
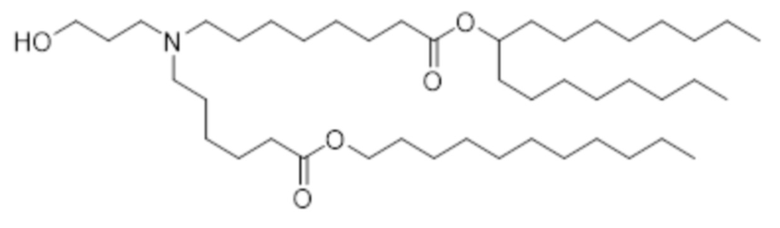
Химическая формула: C45H89NO5
Молекулярная масса: 724,21
[00306] К раствору гептадекан-9-ил-8-((3-гидроксипропил)амино)октаноата (740 мг, 1,62 ммоль) и ундецил 6-бромгексаноата (570 мг (1,62 ммоль) в 16 мл сухого ацетонитрила в атмосфере азота прибавили иодид калия (300 мг, 1,79 ммоль) с последующим прибавлением порошкообразного карбоната калия (900 мг, 6,5 ммоль) и смесь разбавили 4 мл сухого циклопентилметилового эфира. Полученную белую смесь нагревали до 90°C и перемешивали в течение 24 часов, затем оставили охлаждаться до комн. темп., отфильтровали, отфильтрованные твердые вещества промывали ДХМ и фильтрат концентрировали. Остаток суспендировали в 50% насыщенном водном растворе гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-гидроксипропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (780 мг, 1,08 ммоль, 66%) в виде желтоватого масла. СВЭЖХ/ДСИО: RT=3,55 мин. MС (ИЭР): m/z (MH+) 724,39 для C45H89NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,60 (уш. с, 1H); 4,86 (квинт., 1H, J=12,2 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,78 (т, 2H, J=4,9 Гц); 2,62 (т, 2H, J=5,2 Гц); 2,40 (квинт., 4H, J=8,3 Гц, 5,2 Гц); 2,28 (кварт., 4H, J=15,0 Гц, 7,7 Гц); 1,73-1,55 (м, 8H); 1,54-1,39 (м, 8H); 1,38-1,12 (м, 48H); 0,87 (т, 9H, J=5,9 Гц).
FQ. Соединение 263: Гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
Гептадекан-9-ил-8-((3-хлорпропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
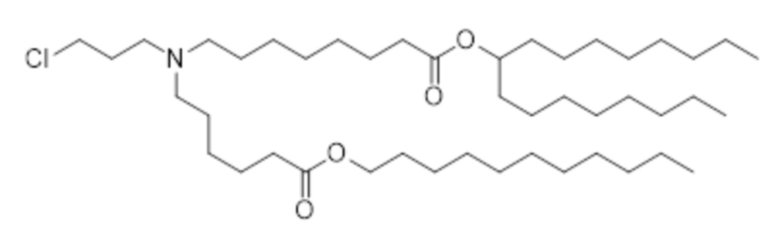
Химическая формула: C45H88ClNO4
Молекулярная масса: 742,65
[00307] К раствору гептадекан-9-ил-8-((3-гидроксипропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (700 мг, 0,97 ммоль) и триэтиламина (202 мкл, 1,45 ммоль) в сухом ДХМ при 0°C прибавили метансульфонилхлорид (90 мкл, 1,16 ммоль) и полученный раствор оставили нагреваться до комн. темп. в течение ночи, после чего согласно ЖХ/MС исходного материала не осталось. Раствор разбавили ДХМ, один раз промыли насыщенным водным раствором гидрокарбоната натрия, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением гептадекан-9-ил-8-((3-хлорпропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (720 мг ~колич.) в виде смеси бледно-желтое масло/твердое вещество, которое согласно 1H-ЯМР содержало некоторое количество мезилата. Материал использовали без дополнительной очистки. СВЭЖХ/ДСИО: RT=3,61 мин. MС (ИЭР): m/z (M-Cl) 706,68 для C45H88ClNO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=12,1 Гц, 5,9 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,59 (т, 2H, J=6,5 Гц); 2,51 (т, 2H, J=6,8 Гц); 2,40-2,23 (м, 7H); 1,86 (т, 2H, J=6,0 Гц); 1,70-1,45 (м, 12H); 1,44-1,37 (м, 4H); 1,36-1,15 (м, 47H); 0,88 (т, 9H, J=5,9 Гц).
Гептадекан-9-ил-8-((3-азидопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат

Химическая формула: C45H88N4O4
Молекулярная масса: 749,22
[00308] К раствору гептадекан-9-ил-8-((3-хлорпропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (720 мг, 0,97 ммоль) в 10 мл сухого ДМФА в сосуде Pyrex высокого давления прибавили азид натрия (250 мг, 3,9 ммоль), сосуд продували азотом и закрывали тефлоновой завинчивающейся крышкой. Реакционную смесь нагревали до 100°C и перемешивали в течение ночи, после чего согласно ТСХ исходного хлорида не оставалось. Реакционную смесь оставили охлаждаться до комн. темп., раствор разбавили водой и экстрагировали 3x смесью гексанов. Органические фазы объединили, один раз промывали водой водой, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением бледно-желтого масла. Его очищали с помощью хроматографии на силикагеле (0-20% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-азидопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (550 мг, 0,73 ммоль, 75%) в виде желтого масла. СВЭЖХ/ДСИО: RT=3,61 мин. MС (ИЭР): m/z (MH+) 749,32 для C45H88N4O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=12,5 Гц, 6,2 Гц); 4,06 (т, 2H, J=6,7 Гц); 3,33 (т, 2H, J=6,4 Гц); 2,46 (т, 2H, J=6,3 Гц); 2,42-2,34 (м, 3H); 2,28 (кварт., 4H, J=14,3 Гц, 7,1 Гц); 1,77-1,55 (м, 8H); 1,54-1,38 (м, 8H); 1,37-1,14 (м, 49H); 0,88 (т, 9H, J=5,7 Гц).
Гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат

Химическая формула: C45H90N2O4
Молекулярная масса: 723,23
[00309] Колбу, содержащую перемешиваемую дисперсию гептадекан-9-ил-8-((3-азидопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (550 мг, 0,73 ммоль) в 8 мл этанола продували азотом и прибавили 10% мас. палладий на угле (около 50 мг, кат.) с получением черной смеси. Стенки сосуда были смыты 2 мл этанола и колбу снова продували азотом. Колбу снабжали баллоном с водородом, вакуумировали и трижды заполняли водородом и перемешивали при комн. темп. в течение двух часов, после чего согласно ЖХ/МС не осталось исходного азида. Колбу продували азотом, смесь отфильтровали через целит, отфильтрованные твердые вещества промывали этанолом и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (375 мг, 0,52 ммоль, 71%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,17 мин. MС (ИЭР): m/z (MH+) 723,57 для C45H90N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,91 (уш. с, 2H); 4,86 (квинт., 1H, J=12,3 Гц, 6,1 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,06 (т, 2H, J=5,5 Гц); 2,65 (т, 2H, J=5,8 Гц); 2,48 (квинт., 4H, J=9,7 Гц, 5,3 Гц); 2,29 (кварт., 4H, J=17,1 Гц, 9,6 Гц); 1,89-1,72 (м, 2H); 1,70-1,55 (м, 6H); 1,54-1,39 (м, 8H); 1,38-1,13 (м, 48H); 0,87 (т, 9H, J=5,8 Гц).
Гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
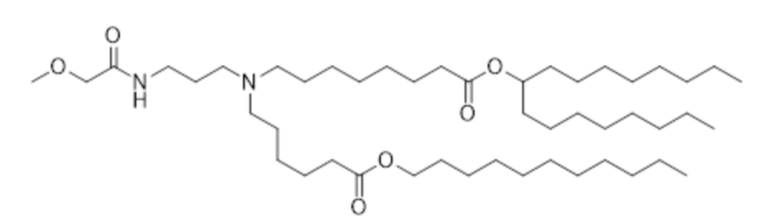
Химическая формула: C48H94N2O6
Молекулярная масса: 795,29
[00310] К раствору гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (170 мг, 0,23 ммоль) и триэтиламина (100 мкл, 0,7 ммоль) в 4 мл сухого ДХМ при 0°C и по каплям прибавили метоксиацетилхлорид (32 мкл, 0,35 ммоль), полученную смесь перемешивали и оставили нагреваться до комн. темп. в течение ночи. Согласно ЖХ/MС исходного амина не осталось, поэтому желтый раствор разбавили ДХМ, дважды промывали насыщенным водным раствором гидрокарбоната натрия, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (42 мг, 0,05 ммоль, 22%) в виде желтого масла. СВЭЖХ/ДСИО: RT=3,44 мин. MС (ИЭР): m/z (MH+) 795,25 для C48H94N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,50 (с, 1H); 4,86 (квинт., 1H, J=12,0 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,87 (с, 2H); 3,40 (м, 5H); 2,98 (уш. с, 1H); 2,54-2,34 (м, 4H); 2,28 (кварт., 4H, J=14,7 Гц, 7,4 Гц); 1,69-1,39 (м, 14H); 1,38-1,13 (м, 51H); 0,88 (т, 9H, J=5,9 Гц).
FR. Соединение 264: Гептадекан-9-ил-8-((3-(2-этоксиацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
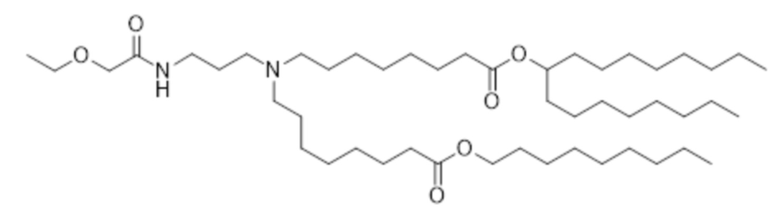
Химическая формула: C49H96N2O6
Молекулярная масса: 809,32
[00311] Соединение 264 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,55 ммоль) аналогично соединению 178 за исключением того, что этоксиацетилхлорид (Alfa Aesar, Тьюксбери, Массачусетс) (92 мкл, 0,83 ммоль) использовали вместо метоксиацетилхлорида. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-этоксиацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (140 мг, 0,55 ммоль, 31%) в виде желтого масла. СВЭЖХ/ДСИО: RT=3,51 мин. MС (ИЭР): m/z (MH+) 809,43 для C49H96N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,48 (с, 1H); 4,86 (квинт., 1H, J=12,6 Гц, 6,1 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,91 (с, 2H); 3,55 (кварт., 2H, J=13,8 Гц, 7,0 Гц); 3,36 (д, 2H, J=5,8 Гц); 2,53-2,43 (м, 2H); 2,41-2,32 (уш. м, 3H); 2,31-2,23 (м, 4H); 1,70-1,56 (м, 8H); 1,55-1,37 (м, 8H); 1,36-1,14 (м, 52H); 0,88 (т, 9H, J=7,5 Гц).
FS. Соединение 265: Гептадекан-9-ил-(Z)-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат

Химическая формула: C49H95N5O4
Молекулярная масса: 818,33
[00312] Соединение 265 получали аналогично соединению 168 за исключением того, что использовали гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат (170 мг, 0,23 ммоль). После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (40 мг, 0,05 ммоль, 21%) в виде бесцветного сиропа. СВЭЖХ/ДСИО: RT=3,52 мин. MС (ИЭР): m/z (MH+) 818,78 для C49H95N5O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,52 (уш. с, 1H); 4,86 (квинт., 1H, J=12,6 Гц, 6,3 Гц); 4,06 (т, 2H, J=6,7 Гц); 3,68 (д, 2H, J=4,3 Гц); 3,00 (с, 6H); 2,59 (уш. с, 2H); 2,44 (уш. с, 3H); 2,29 (кварт., 4H, J=13,4 Гц, 7,1 Гц); 1,80-1,58 (м, 8H); 1,56-1,38 (м, 6H); 1,37-1,13 (м, 51H); 0,88 (т, 9H, J=5,9 Гц).
FT. Соединение 267: Гептадекан-9-ил-8-((3-(2-метоксипропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
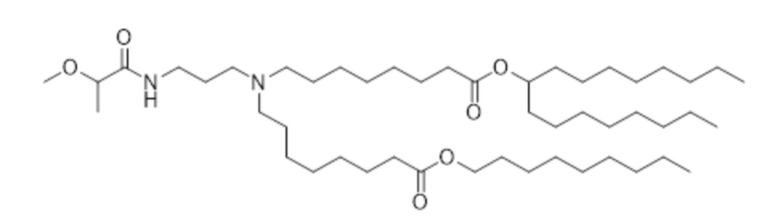
Химическая формула: C49H96N2O6
Молекулярная масса: 809,32
[00313] Соединение 267 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (300 мг, 0,42 ммоль) аналогично соединению 252 за исключением того, что 2-метоксипропановую кислоту (Ark Pharm, Арлингтон Хайтс, Иллинойс)(66 мг, 0,62 ммоль) использовали вместо (метилтио)уксусной кислоты. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-метоксипропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (45 мг, 0,06 ммоль, 54%) в виде желтоватого масла. СВЭЖХ/ДСИО: RT=3,48 мин. MС (ИЭР): m/z (MH+) 809,60 для C49H96N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,43 (с, 1H); 4,86 (квинт., 1H, J=12,2 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,71 (кварт., 1H, J=13,4 Гц, 6,7 Гц); 3,36 (м, 5H); 2,58-2,47 (м, 2H); 2,45-2,35 (м, 3H); 2,34-2,24 (м, 4H); 1,76-1,41 (м, 16H); 1,40-1,15 (м, 52H); 0,87 (т, 9H, J=5,7 Гц).
FU. Соединение 268: Гептадекан-9-ил-8-((3-(2-метокси-2-метилпропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
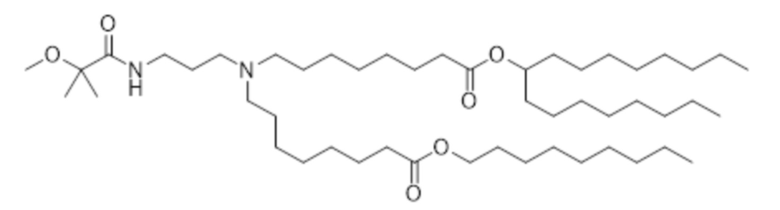
Химическая формула: C50H98N2O6
Молекулярная масса: 823,34
[00314] Соединение 268 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) аналогично соединению 252 за исключением того, что 2-метокси-2-метилпропановую кислоту (Enamine, Монмут Джанкшен, Нью-Джерси) (63 мг, 0,52 ммоль) использовали вместо (метилтио)уксусной кислоты. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-метокси-2-метилпропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (35 мг, 0,04 ммоль, 12%) в виде желтоватого масла. СВЭЖХ/ДСИО: RT=3,58 мин. MС (ИЭР): m/z (MH+) 823,62 для C50H98N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 8,96 (с, 1H); 7,49 (т, 1H, J=6,7 Гц); 4,86 (квинт., 1H, J=12,1 Гц, 6,1 Гц); 4,07 (т, 2H, J=6,6 Гц); 3,44-3,37 (м, 5H); 3,20-2,98 (м, 5H); 2,37-2,26 (м, 4H); 2,17-2,02 (м, 2H); 1,80-1,69 (м, 3H); 1,68-1,60 (м, 6H); 1,57-1,47 (м, 4H); 1,46-1,17 (м, 55H); 0,90 (т, 9H, J=5,9 Гц).
FV. Соединение 269: 6-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гексилгексилсукцинат
4-(Гексилокси)-4-оксобутановая кислота

Химическая формула: C10H18O4
Молекулярная масса: 202,25
[00315] Суспензию янтарного ангидрида (5 г, 49,4 ммоль) в 1-гексаноле (6,3 мл, 49,4 ммоль) нагревали до 80°C и перемешивали в течение 20 часов после чего она превратилась в бесцветный раствор. Его оставили охлаждаться до комн. темп., разбавили EtOAc, дважды промывали 1N раствором HCl, один раз насыщенным водным раствором хлорида натрия, сушили (Na2SO4), отфильтровали и фильтрат концентрировали с получением 4-(гексилокси)-4-оксобутановой кислоты
(9,87 г, 48,8 ммоль, 99%) в виде бесцветной жидкости, которую использовали без дополнительной очистки. 1H ЯМР (300 МГцМГц, CDCl3) δ: м.д. 10,59 (уш. с, 1H); 4,10 (кварт., 2H, J=11,9 Гц, 5,2 Гц); 2,65 (м, 4H); 1,62 (квинт., 2H, J=13,0 Гц, 6,9 Гц); 1,30 (м, 6H); 0,89 (т, 3H, J=6,7 Гц) (протон карбоксильной группы не наблюдали).
6-Бромгексилгексилсукцинат

Химическая формула: C16H29BrO4
Молекулярная масса: 365,31
[00316] К раствору 4-(гексилокси)-4-оксобутановой кислоты (1,0 г, 4,9 ммоль) и 6-бром-1-гексанола (0,75 мл, 5,2 ммоль) в 20 мл сухого ДХМ в атмосфере азота прибавили 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (1,67 г, 7,4 ммоль) с последующим прибавлением 4-(диметиламино)пиридина (0,3 г, 2,47 ммоль) и в конце прибавили N, N-диизопропилэтиламин (2,6 мл, 14,8 ммоль) с получением бледно-желтого раствора. Его перемешивали при комн. темп. в течение 24 часов, после чего ЖХ/MС показал, что исходного материала не осталось. Раствор разбавили ДХМ, один раз промывали насыщенным водным раствором гидрокарбоната натрия (густая эмульсия), сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением смеси бесцветная жидкость/белое твердое вещество. Его очищали с помощью хроматографии на силикагеле (0-25% EtOAc в смеси гексанов) с получением 6-бромгексилгексилсукцината (0,92 г, 2,5 ммоль, 51%) в виде бледно-желтого масла. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,11-4,06 (м, 4H); 3,41 (т, 2H, J=6,7 Гц); 2,62 (с, 4H); 1,87 (квинт., 2H, J=13,9 Гц, 7,2 Гц); 1,69-1,57 (м, 4H); 1,50-1,30 (м, 10H); 0,89 (т, 3H, J=6,3 Гц).
6-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гексилгексилсукцинат
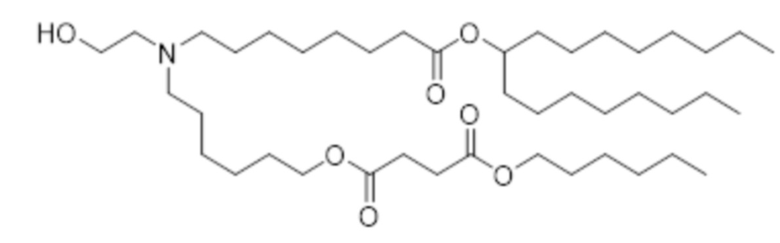
Химическая формула: C43H83NO7
Молекулярная масса: 726,14
[00317] К раствору гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноата (300 мг, 0,61 ммоль) и 6-бромгексилгексилсукцината (223 мг (0,61 ммоль) в 8 мл сухого ацетонитрила в атмосфере азота прибавили иодид калия (115 мг, 0,68 ммоль) с последующим прибавлением порошкообразного карбоната калия (340 мг, 2,4 ммоль) и смесь разбавили 2 мл сухого циклопентилметилового эфира. Полученную белую смесь нагревали до 90°C и перемешивали в течение 24 часов, затем оставили охлаждаться до комнатной температуры, отфильтровали, твердые вещества на фильтре промывали ДХМ и фильтрат концентрировали. Остаток суспендировали в 50% насыщенном водном растворе гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-30% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением 6-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гексилгексилсукцината (40 мг, 0,06 ммоль, 9%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,15 мин. MС (ИЭР): m/z (MH+) 726,36 для C43H83NO7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=12,2 Гц, 6,1 Гц); 4,08 (т, 4H, J=6,6 Гц); 3,52 (т, 2H, J=5,0 Гц); 2,96 (уш. с, 1H); 2,62 (с, 4H); 2,57 (т, 2H, J=4,9 Гц); 2,44 (т, 4H, J=6,4 Гц); 2,27 (т, 2H, J=7,4 Гц); 1,70-1,56 (м, 6H); 1,54-1,37 (м, 8H); 1,36-1,15 (м, 40H); 0,87 (т, 9H, J=5,9 Гц).
FW. Соединение 238: Гептадекан-9-ил-8-((4-(диметиламино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
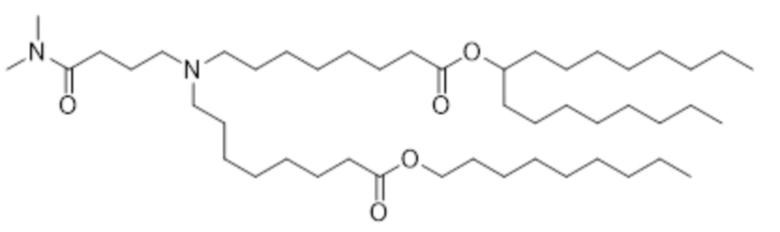
Химическая формула: C48H94N2O5
Молекулярная масса: 779,29
[00318] К раствору 4-бромбутаноилхлорид (1,6 г, 8,62 ммоль) в 15 мл сухого ТГФ охладили до -15°C прибавили 2M раствор диметиламина в ТГФ (12 мл, 24 ммоль), полученную смесь перемешивали и оставили нагреваться до комн. темп.. Выпавшие в осадок твердые вещества удаляли фильтрованием и фильтрат концентрировали с получением сырого 4-бром-N, N-диметилбутанамида. Его растворили в 20 мл смеси 1:1 ацетонитрил/метилциклопентилового эфира, прибавили гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноат (1 г, 1,5 ммоль), карбонат калия (0,8 г, 6 ммоль), иодид калия (0,3 г, 1,8 ммоль), смесь нагревали до 80°C и перемешивали в течение ночи. Реакционную смесь оставили охлаждаться до комн. темп., отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (4:1 изократическая смесь гексанов/ацетон) с получением гептадекан-9-ил-8-((4-(диметиламино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (180 мг, 0,23 ммоль,15%) в виде светло-желтого масла MС (ХИ): m/z (MH+) 779,7 для C48H94N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,83 (квинт., 1H, J=6 Гц); 4,03 (т, 2H, J=7,5 Гц); 3-2,7 (м, 10H); 2,5 (т, 2H, J=7,5 Гц); 2,26 (м, 4H); 2 (м, 2H); 1,7-1,4 (м, 14H); 1,4-1,2 (м, 50H); 0,8 (м, 9H).
FX. Соединение 239: Гептадекан-9-ил-8-((4-(метиламино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
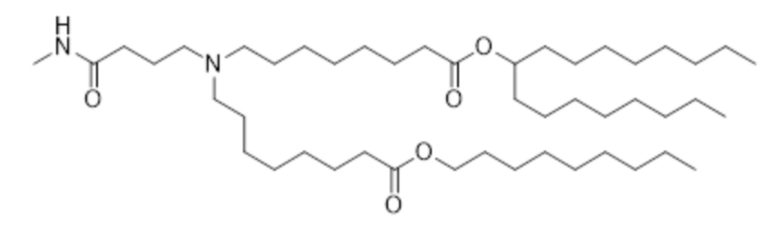
Химическая формула: C47H92N2O5
Молекулярная масса: 765,26
[00319] Соединение 239 получали из гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноата (0,8 г, 1,2 ммоль) аналогично соединению 238 за исключением того, что 2M раствор метиламина в метаноле (8 мл, 16 ммоль) использовали вместо 2M раствора диметиламина в ТГФ. Остаток реакционной смеси после фильтрования и концентрирования очищали с помощью хроматографии на силикагеле (4:1 изократическая смесь гексанов/ацетон) с получением гептадекан-9-ил-8-((4-(метиламино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,52 ммоль, 43%) в виде светло-желтого масла. MС (ХИ): m/z (MH+) 765,6 для C47H92N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,83 (квинт., 1H, J=6 Гц); 4,04 (т, 2H, J=6 Гц); 3,6 (с, 3H); 2,4-2,2 (м, 12H); 1,8-1,4 (м, 14H); 1,4-1,2 (м, 50H); 0,8 (м, 9H); (амидный протон не наблюдали).
FY. Соединение 240: Гептадекан-9-ил-8-((4-(метокси(метил)амино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
4-((8-(Гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)бутановая кислота
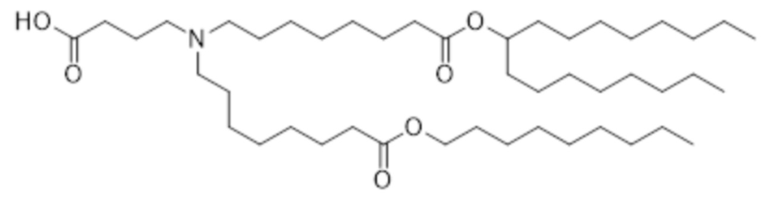
Химическая формула: C46H89NO6
Молекулярная масса: 752,22
[00320] Смесь периодной кислоты (7,3 г, 32 ммоль) в 100 мл ацетонитрила интенсивно перемешивали в течение 15 мин. при 0°C. К нему прибавили раствор гептадекан-9-ил-8-((4-гидроксибутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (10,75 г, 14,6 ммоль) в 30 мл ацетонитрила с последующим прибавлением пиридиний хлорхромата (0,16 г, 0,73 ммоль). Полученную смесь оставили нагреваться до комн. темп. В течение 4 часов, через которые ЖХ/MС показал преимущественно оставшийся исходный спирт. К смеси прибавили дополнительную порцию пиридиний хлорхромата (0,16 г, 0,73 ммоль) и переешивание продолжили в течение 1 часа. ЖХ/MС показал дополнительное образование продукта после добавления дополнительного количества пиридиний хлорхромата, однако эта стадия реакции была медленной. Реакционную смесь разбавили EtOAc, промывали смесью вода/насыщенный водный раствор хлорида натрия (1:1), насыщенным водным раствором гидрокарбоната натрия и окончательно насыщенным водным раствором хлорида натрия. После сушки (MgSO4) и концентрирования, получили 13 г сырого материала, который согласно ЯМР содержал 20% исходного спирта вместе с альдегидным промежуточным соединением. Сырой материал растворили в 120 мл 1:1 ацетонитрил/TBME, прибавили периодную кислоту (13,0 г, 57 ммоль) и пиридиний хлорхромат (0,16 г, 0,73 ммоль) и смесь перемешивали при комн. темп. в течение 3 часов. Прибавили дополнительную порцию пиридиний хлорхромата (0,16 г, 0,73 ммоль) и смесь перемешивали при комн. темп. в течение 16 часов, через которые ЖХ/MС показал, что исходного спирта почти не осталось. Реакционную смесь разбавили EtOAc, промывали смесью вода/насыщенный водный раствор хлорида натрия (1:1), насыщенным водным раствором гидрокарбоната натрия и окончательно насыщенным водным раствором хлорида натрия. Органическифазы сушили (MgSO4), отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-6% затем 10% метанол в дихлорметане) с получением 4-((8-(гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)бутановой кислоты (8,80 г, 11,7 ммоль, 80%) в виде коричневого масла. MС (ХИ): m/z (MH+) 752,6 для C46H89NO6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,84 (квинт., 1H, J=6,3 Гц); 4,03 (т, 2H, J=6,8 Гц); 3,12 (м, 2H); 3,00 (м, 4H); 2,52 (м, 2H); 2,27 (м, 4H); 2,08 (м, 2H); 1,81 (уш. м, 4H); 1,60 (м, 6H); 1,48 (м, 4H); 1,24 (уш. м, 48H); 0,86 (т, 9H, J=6,9 Гц); протон карбоксильной группы не наблюдали.
Гептадекан-9-ил-8-((4-(метокси(метил)амино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C48H94N2O6
Молекулярная масса: 795,29
[00321] К раствору 4-((8-(гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)бутановой кислоты (1,00 г, 1,33 ммоль) в 40 мл дихлорметана прибавили карбонилдиимидазол (259 мг, 1,6 ммоль) при 0°C, охлаждающую баню убрали и смесь перемешивали при комн. темп. в течение 30 мин. После охлаждения до 0°C прибавили N, O-диметилгидроксиламин гидрохлорид (156 мг, 1,6 ммоль) и триэтиламина (0,23 мл, 1,6 ммоль) и полученную смесь перемешивали при комн. темп. в течение 16 часов. Менее чем 10% исходной кислоты осталось согласно ЖХ/MС, поэтому реакционную смесь разбавили смесью гексанов, один раз промывали водой водой и насыщенным водным раствором хлорида натрия. Органический слой сушили (MgSO4), отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-6% затем 10% метанол в дихлорметане) с получением 0,77 г смеси, содержащей некоторое количество исходной кислоты. Данный материал снова очищали с помощью хроматографии на силикагеле (0-40% затем 60% ацетон в смеси гексанов) с получением гептадекан-9-ил-8-((4-(метокси(метил)амино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (210 мг, 0,26 ммоль, 20%) в виде бесцветного масла. ВЭЖХ/УФ (214 нм): RT=9,78 мин. MС (ХИ): m/z (MH+) 795,7 для C48H94N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (квинт., 1H, J=6,3 Гц); 4,04 (т, 2H, J=6,8 Гц); 3,67 (с, 3H); 3,17 (с, 3H); 2,41 (м, 6H); 2,27 (м, 6H); 1,74 (м, 2H); 1,60 (м, 8H); 1,48 (м, 4H); 1,40 (м, 2H); 1,24 (уш. м, 48H); 0,86 (т, 9H, J=6,8 Гц).
FZ. Соединение 241: Гептадекан-9-ил-8-((4-(метоксиамино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
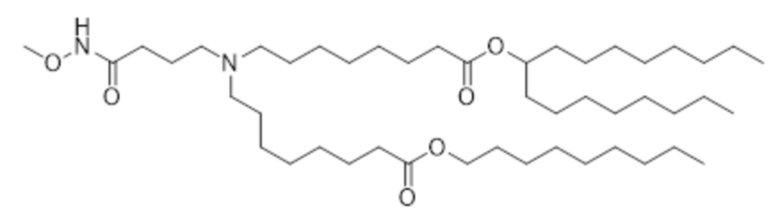
Химическая формула: C47H92N2O6
Молекулярная масса: 781,26
[00322] К смеси 4-((8-(гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)бутановой кислоты (1,00 г, 1,33 ммоль) и O-метилгидроксиламин гидрохлорида (178 мг, 2,13 ммоль) в 20 мл дихлорметана прибавили 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (460 мг, 2,39 ммоль) с последующим прибавлением триэтиламина (0,30 мл, 2,13 ммоль) и смесь перемешивали при комн. темп. в течение 16 часов. Только небольшое количество исходной кислоты осталось согласно ЖХ/MС, поэтому реакционную смесь разбавили смесью гексанов, один раз промывали водой водой и насыщенным водным раствором хлорида натрия. Органический слой сушили (MgSO4), отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-6% затем 10% метанол в дихлорметане) с получением 0,63 г смеси, содержащей некоторое количество исходной кислоты. Данный материал снова очищали с помощью хроматографии на силикагеле (0-40% затем 80% ацетон в смеси гексанов) с получением гептадекан-9-ил-8-((4-(метоксиамино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (0,56 г, 0,71 ммоль, 53%) в виде бесцветного масла. ВЭЖХ/УФ (214 нм): RT=9,49 мин. MС (ХИ): m/z (MH+) 781,6 для C47H92N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (квинт., 1H, J=6,3 Гц); 4,04 (т, 2H, J=6,8 Гц); 3,73 (с, 3H); 2,48 (м, 2H); 2,42 (м, 4H); 2,28 (м, 6H); 1,73 (м, 4H); 1,60 (м, 6H); 1,48 (м, 6H); 1,24 (уш. м, 48H); 0,87 (т, 9H, J=7,1 Гц); протон гидроксамовой группы не наблюдали.
GA. Соединение 242: Гептадекан-9-ил-8-((4-(гидрокси(метил)амино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
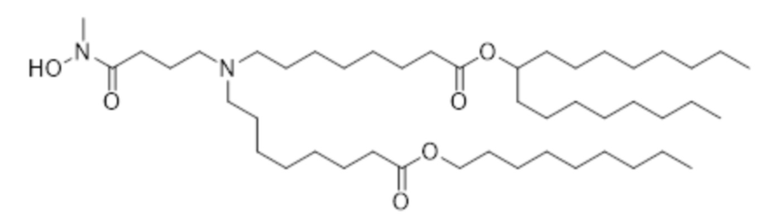
Химическая формула: C47H92N2O6
Молекулярная масса: 781,26
[00323] К раствору 4-((8-(гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)бутановой кислоты (1,08 г, 1,43 ммоль) в 25 мл дихлорметана при 0°C прибавили оксалилхлорид (121 мкл, 1,43 ммоль) с последующим прибавлением 5 капель ДМФА, охлаждающую баню убрали и реакционную смесь перемешивали при комн. темп. в течение 16 часов. К полученному раствору при 0°C прибавили N-метилгидроксиламин гидрохлорид (0,36 г, 4,3 ммоль) и DMAP (355 мг, 0,29 ммоль) с последующим прибавлением триэтиламина (1,0 мл, 7,2 ммоль), реакционную смесь оставили нагреваться до комн. темп. и перемешивали в течение 16 часов. Только небольшое количество исходной кислоты осталось согласно ЖХ/MС, поэтому реакционную смесь разбавили смесью гексанов, один раз промывали водой водой и насыщенным водным раствором хлорида натрия. Органический слой сушили (MgSO4), отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-50% затем 80% ацетон в смеси гексанов) с получением гептадекан-9-ил-8-((4-(гидрокси(метил)амино)-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (0,61 г, 0,78 ммоль, 54%) в виде желтого масла. ВЭЖХ/УФ (214 нм): RT=9,69 мин. MС (ХИ): m/z (MH+) 781,6 для C47H92N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,85 (квинт., 1H, J=6,0 Гц); 4,04 (т, 2H, J=6,9 Гц); 3,21 (с, 3H); 2,55 (м, 4H); 2,44 (м, 4H); 2,27 (м, 4H); 1,96 (м, 2H); 1,60 (м, 8H); 1,47 (м, 6H); 1,24 (уш. м, 48H); 0,87 (т, 9H, J=7,1 Гц); протон гидроксамовой группы не наблюдали.
GB. Соединение 243: Гептадекан-9-ил-8-((4-амино-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноат
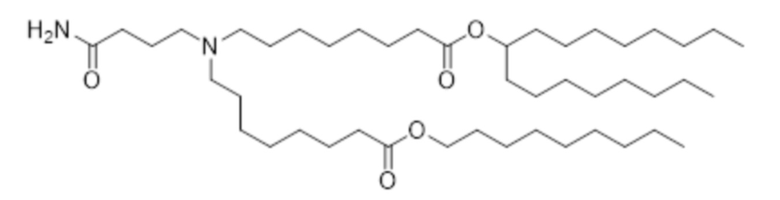
Химическая формула: C46H90N2O5
Молекулярная масса: 751,24
[00324] К раствору 4-((8-(гептадекан-9-илокси)-8-оксооктил)(8-(нонилокси)-8-оксооктил)амино)бутановой кислоты (1,0 г, 1,33 ммоль) в 25 мл дихлорметана при 0°C прибавили оксалилхлорид (120 мкл, 1,33 ммоль) с последующим прибавлением 5 капель ДМФА, охлаждающую баню убрали и реакционную смесь перемешивали при комн. темп. в течение 16 часов. Полученный раствор охладили до 0°C, продували через него газообразный аммиак в течение 5 мин и поддерживали реакцию при 0°C в течение в течение двух часов. Только небольшое количество исходной кислоты осталось согласно ЖХ/MС, поэтому реакционную смесь разбавили дихлорметаном и промывали насыщенным водным раствором хлорида натрия. Органический слой сушили (MgSO4), отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (0-40% затем 80% ацетон в смеси гексанов) с получением гептадекан-9-ил-8-((4-амино-4-оксобутил)(8-(нонилокси)-8-оксооктил)амино)октаноата (0,30 г, 0,40 ммоль, 30%) в виде коричневого масла. ВЭЖХ/УФ (214 нм): RT=9,09 мин. MС (ХИ): m/z (MH+) 751,6 для C46H90N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,73 (уш. с, 1H); 5,22 (уш. с, 1H); 4,85 (квинт., 1H, J=6,3 Гц); 4,04 (т, 2H, J=6,6 Гц); 2,45 (м, 2H); 2,37 (м, 4H); 2,27 (м, 6H); 1,75 (м, 2H); 1,60 (м, 8H); 1,50 (м, 4H); 1,40 (м, 2H); 1,24 (уш. м, 48H); 0,87 (т, 9H, J=6,5 Гц).
GC. Соединение 248: Гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-нитрогуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
S-Метил-N-нитро-Nʹ-фталоилизотиомочевина
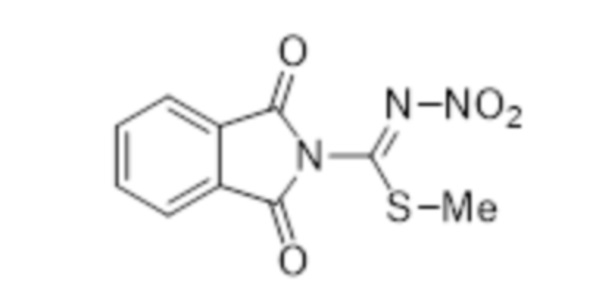
Химическая формула: C10H7N3O4S
Молекулярная масса: 265,24
[00325] К раствору S-метил-N-нитроизотиомочевины (5,0 г, 37 ммоль) в 70 мл пиридина при 0°C по каплям прибавляли фталоилхлорид (14,5 г, 10,3 мл, 72 ммоль) в течение 25 мин. Раствор перемешивали при 0°C в течение 30 мин во время чего образовался осадок. Смесь вылили в 600 мл охлажденного на льду 2N раствора соляной кислоты, полученные твердые вещества отфильтровали, промывали водой и сушили на воздухе. Твердые вещества выпали в осадок из этанола с получением S-метил-N-нитро-Nʹ-фталоилизотиомочевины (6,23 г, 23,5 ммоль, 64%) в виде белого твердого вещества. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,97-7,95 (м, 2H); 7,87-7,86 (м, 2H); 2,66 (с, 3H).
Метил N, N-диметил-Nʹ-нитрокарбамимидотиоат
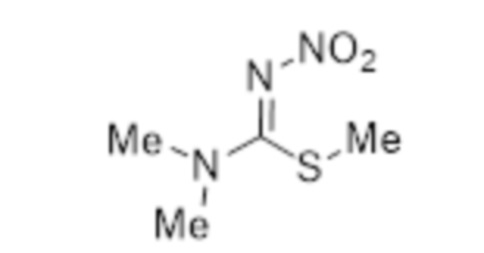
Химическая формула: C4H9N3O2S
Молекулярная масса: 163,20
[00326] К раствору S-метил-N-нитросо-Nʹ-фталоилизотиомочевины (1,5 г, 5,68 ммоль) в 10 мл дихлорметана при 0°C прибавили 2M раствор диметиламина в ТГФ (2,84 мл, 5,68 ммоль) по каплям прибавляли 5 мл метанол в течение 25 мин. Реакционную смесь перемешивали при комн. темп. в течение 3 часов, концентрировали, остаток растворили в дихлорметане и очищали с помощью хроматографии на силикагеле (4:1 изократическая смесь гексанов/ этилацетат) с получением метил-N, N-диметил-Nʹ-нитрокарбамимидотиоат (678 мг, 4,15 ммоль, 73%) в виде воскообразного белого твердого вещества. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 3,25 (с, 6H); 2,53 (с, 3H).
Гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-нитрогуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C48H95N5O6
Молекулярная масса: 838,32
[00327] К раствору гептадекан-9-ил-8-((аминопропил)(8-нонилоксил)-8-оксооктил)амино)октаноата (500 мг, 0,69 ммоль) в 20 мл метанола прибавили метил-N, N-диметил-Nʹ-нитрокарбамимидотиоат (118 мг, 0,73 ммоль), реакционную смесь нагревали до кипения и перемешивали в течение 5 часов. Согласно ЖХ/MС исходного амина не осталось, поэтому растворитель удалили и остаток очищали с помощью хроматографии на силикагеле (элюент дихлорметан, метанол, 1% гидроксид аммония) с получением 520 мг материала с примесями. Его снова очищали с помощью хроматографии на силикагеле (вначале 0-100% этилацетат в смеси гексанов, затем 0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-(3,3-диметил-2-нитрогуанидино)пропил)(8-(нонилоксил)-8-оксооктил)амино)октаноата (220 мг, 0,26 ммоль, 38%) в виде светло-желтого масла. ВЭЖХ/УФ 214 нм: RT=9,48 мин. MС (ХИ): m/z (MH+) 838,7 для C48H95N5O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,51 (т, 2H, J=5,2 Гц); 3,05 (с, 6H); 2,66 (уш. с, 1H); 2,48 (уш. с, 2H); 2,28 (дт, 4H, J=7,4 Гц, 3,8 Гц); 1,62-1,58 (м, 8H); 1,48- 1,30 (м, 8H); 1,29- 1,24 (м, 52H); 0,86 (т, 9H, J=6,6 Гц).
GD. Соединение 249: Гептадекан-9-ил-(E)-8-((3-(2-циано-3-метилгуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
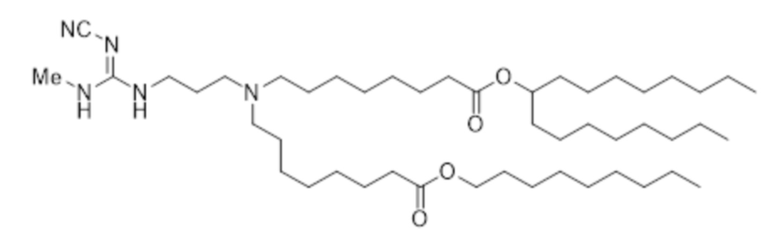
Химическая формула: C48H93N5O4
Молекулярная масса: 804,30
[00328] Соединение 249 получали из гептадекан-9-ил-8-((3-аминопропил)(8-нонилокси)-8-оксооктил)аминооктаноата (400 мг, 0,55 ммоль) аналогично соединению 168 за исключением того, что 2M раствор метиламина в метаноле (1,4 мл, 2,8 ммоль) использовали вместо 2M раствора диметиламина в ТГФ. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (дихлорметан, метанол /1% NH4OH) с получением гептадекан-9-ил-(E)-8-((3-(2-циано-3-метилгуанидино)пропил)(8-(нонилоксил)-8-оксооктил)амино)октаноата (260 мг, 0,32 ммоль, 58%) в виде светло-желтого масла. ВЭЖХ/УФ 214 нм: RT=9,83 мин. MС (ХИ): m/z (MH+) 804,7 для C48H93N5O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,29 (м, 2H); 2,77 (д, 3H, J=4,6 Гц); 2,52 (м, 1H); 2,44-2,39 (м, 3H); 2,28 (дт, 4H, J=7,4 Гц, 3,6 Гц); 1,65-1,57 (м, 16H); 1,50- 1,41 (м, 3H); 1,30- 1,24 (м, 48H); 0,86 (т, 9H, J=6,4 Гц).
GE. Соединение 250: Гептадекан-9-ил-(Z)-8-((3-((1-(диметиламино)-2-нитровинил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
(E)-N, N-Диметил-1-(метилтио)-2-нитроэтен-1-амин
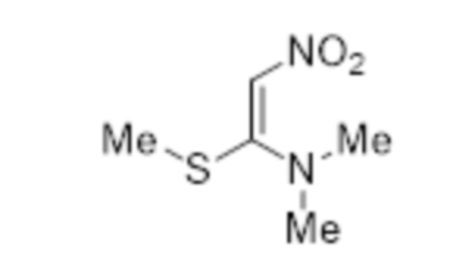
Химическая формула: C5H10N2O2S
Молекулярная масса: 162,21
[00329] К раствору (2-нитроэтен-1,1-диил)бис(метилсульфана) (EP 5984 A1)(1,0 г, 6,1 ммоль) в ацетонитриле при 0°C прибавили a 2M диметиламин в тетрагидрофуране (3 мл, 6 ммоль) и реакционную смесь перемешивали при комн. темп. в течение 3 часов. Растворитель удалили под вакуумом и сырой продукт очищали с помощью хроматографии на силикагеле (гексан, этилацетат) с получением (E)-N, N-диметил-1-(метилтио)-2-нитроэтен-1-амина (200 мг, 20%), содержащего N, N,Nʹ,Nʹ-тетраметил-2-нитроэтен-1,1-диамин, в виде красновато-желтого масла, который был использован без дальнейшей очистки. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,67 (с, 1H); 3,20 (с, 6H); 2,46 (с, 3H).
Гептадекан-9-ил-(Z)-8-((3-((1-(диметиламино)-2-нитровинил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
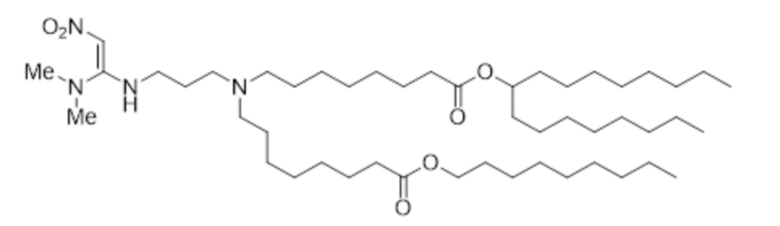
Химическая формула: C49H96N4O6
Молекулярная масса: 837,33
[00330] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,69 ммоль) в 20 мл метанола прибавили (E)-N, N-диметил-1-(метилтио)-2-нитроэтен-1-амин (112 мг, 0,69 ммоль), реакционную смесь нагревали до кипения и перемешивали в течение 5 часов. Растворитель удаляли и соединение дважды очищали хроматографией на силикагеле [колонка 1: гексан/этилацетат, затем дихлорметан, метанол/1% NH4OH), колонка 2: гексан/этилацетат, затем дихлорметан, метанол/1% NH4OH)] с получением гептадекан-9-ил-(Z)-8-((3-((1-(диметиламино)-2-нитровинил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (104 мг, 0,12 ммоль, 18%) в виде желтого масла. ВЭЖХ/УФ 214 нм: RT=8,69 мин. MС (ХИ): m/z (MH+) 837,7 для C48H96N4O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 9,56 (уш. с, 1H); 6,49 (с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,34-3,32 (м, 2H); 2,92 (с, 6H); 2,49 (м, 2H); 2,37-2,33 (м, 4H); 2,27 (дт, 4H, J=7,4 Гц, 3,8 Гц); 1,77-1,75 (м, 2H); 1,62-1,48 (м, 8H); 1,34- 1,24 (м, 54H); 0,86 (т, 9H, J=6,5 Гц).
GF. Соединение 254: Гептадекан-9-ил-4-имино-9-(8-(нонилокси)-8-оксооктил)-2-окса-3,5,9-триазагептадекан-17-оат
Гептадекан-9-ил-7-(трет-бутоксикарбонил)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-6-(1H-пиразол-1-ил)-3-окса-5,7,11-триазанонадец-5-ен-19-оат
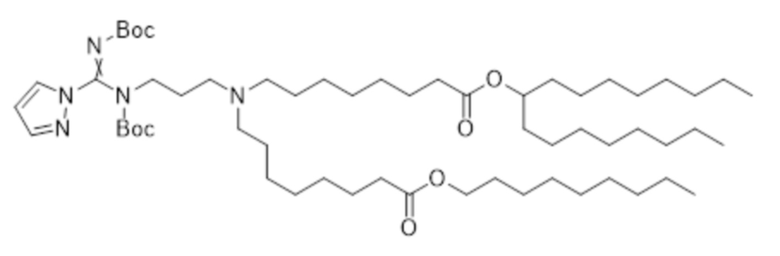
Химическая формула: C59H109N5O8
Молекулярная масса: 1016,55
[00331] К раствору гептадекан-9-ил-(8-((3-гидроксипропил)(8-(нонилокси)октил)амино)октаноата (500 мг, 0,69 ммоль) в 10 мл сухого тетрагидрофурана прибавили трифенилфосфин (271,8 мг, 1,04 ммоль) и трет-бутил-(((трет-бутоксикарбонил)амино)(1H-пиразол-1-ил)метилен)карбамата (Aldrich Chemical Co., Сент-Луис, Миссури; 214,3 мг, 0,69 ммоль) и реакционную смесь охладили до 0°C. К нему по каплям прибавили диизопропилазодикарбоксилат (0,2 мл, 1,04 ммоль), охлаждающую баню убрали и реакционную смесь перемешивали при комн. темп. в течение 24 часов. Согласно ЖХ/MС исходного спирта не осталось, поэтому растворитель удалили и остаток очищали с помощью хроматографии на силикагеле (0-40% этилацетат в смеси гексанов) с получением гептадекан-9-ил-7-(трет)-бутоксикарбонил)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-6-(1H-пиразол-1-ил)-3-окса-5,7,11-триазанонадец-5-ен-19-оата (227 мг, 0,22 ммоль, 32%) в виде бесцветного масла. MС (ХИ): m/z (MH+) 1016,8 для C59H109N5O8. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,93 (с, 1H); 7,67 (с, 1H); 6,40 (с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,69-3,67 (м, 2H); 2,45 (т, 2H, J=7,0 Гц) 2,35-2,23 (м, 8H); 1,88-1,84 (м, 2H); 1,57-1,49 (м, 10H); 1,38- 1,24 (м, 70H); 0,86 (т, 9H, J=6,5 Гц).
Гептадекан-9-ил-7-(трет-бутоксикарбонил)-6-(метоксиамино)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,7,11-триазанонадец-5-ен-19-оат

Химическая формула: C57H110N4O9
Молекулярная масса: 995,53
[00332] К раствору гептадекан-9-ил-7-(трет-бутоксикарбонил)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-6-(1H-пиразол-1-ил)-3-окса-5,7,11-триазанондец-5-ен-19-оата (227 мг, 0,22 ммоль) в 30 мл смеси 1:1 циклопентилметиловый эфир/ацетонитрил прибавили O-метилгидроксиламин гидрохлорид (93,3 мг, 1,12 ммоль) с последующим прибавлением N, N-диизопропилэтиламина (0,2 мл, 1,12 ммоль), реакционную смесь нагревали до 85°C и перемешивали в течение 24 часов. Реакции дали пройти на 80% согласно ЖХ/MС, потом прибавили дополнительную порцию O-метилгидроксиламин гидрохлорида (93,3 мг, 1,12 ммоль) с последующим прибавлением N, N-диизопропилэтиламина (144,4 мг, 0,2 мл, 1,12 ммоль) и реакционную смесь перемешивали в течение 85°C в течение дополнительных 24 часов. Согласно ЖХ/MС исходного материала не осталось, поэтому растворитель удалили и остаток очищали с помощью хроматографии на силикагеле (1:1 изократическая смесь гексан/этилацетат) с получением гептадекан-9-ил-7-(трет-бутоксикарбонил)-6-(метоксиамино)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,7,11-триазанонадец-5-ен-19-оата (189 мг, 0,19 ммоль, 85%) в виде бесцветного масла. MС (ХИ): m/z (MH+) 995,8 для C57H110N4O9. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,31 (с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,83 (с, 3H); 3,42 (т, 2H, J=7,5 Гц); 2,48-2,32 (м, 6H); 2,26 (дт, 4H, J=7,4 Гц, 3,8 Гц); 1,62-1,55 (м, 8H); 1,50-1,43 (м, 20H); 1,39-1,24 (м, 54H); 0,86 (т, 9H, J=6,4 Гц).
Гептадекан-9-ил-4-имино-9-(8-(нонилокси)-8-оксооктил)-2-окса-3,5,9-триазагептадекан-17-оат

Химическая формула: C47H94N4O5
Молекулярная масса: 795,29
[00333] К раствору гептадекан-9-ил-7-(трет-бутоксикарбонил)-6-(метоксиамино)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,7,11-триазанонадец-5-ен-19-оата (189 мг, 0,19 ммоль) в 1 мл этилацетата при 0°C по каплям прибавили раствор 4M хлороводорода в 1,4-диоксане (8 мл, 32 ммоль) и реакционную смесь перемешивали при комн. темп. в течение 3 дней. Согласно ЖХ/MС исходного материала не осталось и наблюдали только продукт без защитных групп. Реакционную смесь концентрировали, остаток растворили в этилацетат и раствор один раз промывали насыщенным водным раствором гидрокарбоната натрия, затем насыщенным водным раствором хлорида натрия, сушили (Na2SO4), отфильтровали и фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (дихлорметан, метанол/1% NH4OH) с получением гептадекан-9-ил-4-имино-9-(8-(нонилокси)-8-оксооктил)-2-окса-3,5,9-триазагептадекан-17-оата (120 мг, 0,15 ммоль, 80%). MС (ХИ): m/z (MH+) 795,7 для C47H94N4O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,64 (с, 3H); 3,15 (уш. с, 2H); 2,51-2,49 (м, 2H); 2,42-2,38 (м, 4H); 2,27 (дт, 4H, J=7,4 Гц, 3,7 Гц); 1,65-1,55 (м, 8H); 1,49-1,41 (м, 8H); 1,29- 1,24 (м, 50H); 0,86 (т, 9H, J=6,4 Гц).
GG. Соединение 266: Гептадекан-9-ил-(E)-8-((3-(2-цианогуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
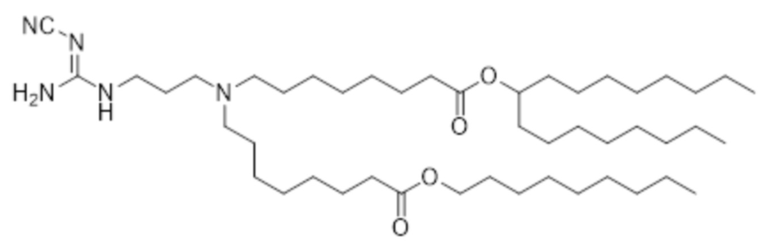
Химическая формула: C47H91N5O4
Молекулярная масса: 790,28
[00334] Соединение 266 получали из гептадекан-9-ил-8-((3-аминопропил)(8-нонилокси)-8-оксооктил)аминооктаноата (400 мг, 0,55 ммоль) аналогично соединению 168 за исключением того, что 7M раствор аммиака в метаноле (2 мл, 14 ммоль) использовали вместо раствора 2M диметиламина в ТГФ и реакцию проводили в герметично закрытой пробирке. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (дихлорметан, метанол /1% NH4OH) с получением гептадекан-9-ил-(E)-8-((3-(2-цианогуанидино)пропил)(8-(нонилоксил)-8-оксооктил)амино)октаноата (170 мг, 0,21 ммоль, 39%) в виде светло-желтого масла. ВЭЖХ/УФ 214 нм: RT=9,26 мин. MС (ХИ): m/z (MH+) 790,7 для C47H91N5O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. δ 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,29-3,27 (м, 2H); 2,51-2,48 (м, 2H); 2,43-2,38 (м, 4H); 2,31-2,25 (м, 4H); 1,68-1,55 (м, 8H); 1,50- 1,48 (м, 4H); 1,40-1,37 (м, 4H); 1,30- 1,23 (м, 50H); 0,86 (т, 9H, J=6,6 Гц); один протон гуанидиновой группы не наблюдали.
GH. Соединение 274: Гептадекан-9-ил-(E)-8-((3-(2-нитрогуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
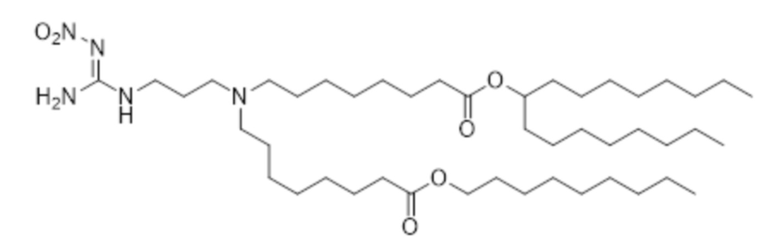
Химическая формула: C46H91N5O6
Молекулярная масса: 810,26
[00335] К раствору гептадекан-9-ил-8-((аминопропил)(8-нонилоксил)-8-оксооктил)амино)октаноата (530 мг, 0,73 ммоль) в 20 мл метанола прибавили метил-Nʹ-нитрокарбамимидотиоат (104 мг, 0,77 ммоль), реакционную смесь нагревали до кипения и перемешивали в течение 4 часов. Согласно ЖХ/MС исходного материала не осталось и наблюдались два пика продукта, которые соответствовали двум нитрогуанидиновым региоизомерам (Z и E). Количество Z-изомера уменьшается со временем реакции, поскольку он превращается в более стабильный E-изомер. Растворитель удалили и сырое соединение очищали с помощью хроматографии на силикагеле (вначале гексан, 0-100% этилацетат в смеси гексанов, затем 0-50% метанол /1% NH4OH в дихлорметане) с получением гептадекан-9-ил-(E)-8-((3-(2-нитрогуанидино)пропил)(8-(нонилоксил)-8-оксооктил)амино)октаноата (160 мг, 0,20 ммоль, 27%) в виде бесцветного масла. ВЭЖХ/УФ 214 нм: RT=9,53 мин. MС (ХИ): m/z (MH+) 810,7 для C46H91N5O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 8,41 (уш. с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,6 Гц); 3,36-3,34 (м, 2H); 2,51-2,41 (м, 6H); 2,28 (дт, 4H, J=7,6 Гц, 3,7 Гц); 1,78 (уш. с, 2H); 1,63-1,58 (м, 8H); 1,50- 1,38 (м, 6H); 1,30- 1,23 (м, 50H); 0,86 (т, 9H, J=6,8 Гц).
[00336] Также выделили гептадекан-9-ил-(Z)-8-((3-(2-нитрогуанидино)пропил)(8-(нонилоксил)-8-оксооктил)амино)октаноат (65 мг, 0,08 ммоль, 11%) в виде светло-желтого масла, который медленно превращается в E-изомер при стоянии. ВЭЖХ/УФ 214 нм: RT=10,66 мин. MС (ХИ): m/z (MH+) 810,6 для C46H91N5O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87-4,80 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,36-3,34 (м, 2H); 2,48 (уш. с, 4H); 2,30-2,24 (м, 4H); 2,16-2,15 (м, 1H); 1,79 (уш. с, 1H); 1,62-1,42 (м, 15H); 1,30- 1,24 (м, 52H); 0,86 (т, 9H, J=6,6 Гц).
GI. Соединение 275: 7-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гептил-(Z)-дец-3-еноат

Химическая формула: C12H18O3
Молекулярная масса: 210,27
[00337] К раствору 1-октин-3-ола (2,15 мл, 14,4 ммоль) и метилпропиолата (1,2 мл, 14,4 ммоль) в 100 мл сухого ДХМ прибавили триэтиламин (0,2 мл, 1,4 ммоль) и бледно-желтый раствор перемешивали при комн. темп. в течение 20 часов, через которые согласно ТСХ исходного спирта не осталось. Раствор концентрировали и остаток очищали с помощью хроматографии на силикагеле (0-20% EtOAc в смеси гексанов) с получением метил-(E)-3-(окт-1-ин-3-илокси)акрилата (2,92 г, 13,9 ммоль, 97%) в виде бесцветной жидкости. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,61 (д, 1H, J=12,5 Гц); 5,38 (д, 1H, J=12,5 Гц); 4,53 (тд, 1H, J=6,6 Гц, 2,0 Гц); 3,70 (с, 3H); 2,58 (д, 1H, J=2,0 Гц); 1,91-1,75 (м, 2H); 1,52-1,41 (м, 2H); 1,37-1,26 (м, 4H); 0,90 (т, 3H, J=6,9 Гц).

Химическая формула: C10H18O2
Молекулярная масса: 170,25
[00338] В 5 мл микроволновой пробирке смешали 840 мг (4 ммоль) метил-(E)-3-(окт-1-ин-3-илокси)акрилата и 2 мл воды с получением бесцветного двухфазного раствора. Пробирку герметично закрыли и смесь подвергали микроволновому облучению при 175°C в течение 90 минут. Полученный двухфазный дважды раствор промывали ДХМ, органические фазы промывали, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением темно-оранжевого масла. Его растворили в смеси гексанов и очищали с помощью хроматографии на силикагеле (0-20% EtOAc в смеси гексанов) с получением (Z)-дек-3-еновой кислоты (155 мг, 0,91 ммоль, 23%) в виде оранжевого масла. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 11,03 (уш. с, 1H); 5,70-5,44 (м, 2H); 3,14 (д, 2H, J=6,6 Гц); 2,04 (к, 2H, J=6,8 Гц); 1,43-1,13 (м, 8H); 0,88 (т, 3H, J=6,8 Гц). (Z)-Геометрия подтверждена экспериментами по 1D селективному градиенту NOEsy с облучением при 2,07 м.д. (протоны C-5) и 3,16 м.д. (протоны C-2).

Химическая формула: C17H31BrO2
Молекулярная масса: 347,34
[00339] К раствору (Z)-дек-3-еновой кислоты (220 мг, 1,29 ммоль) и 7-бром-1-гептанола (250 мкл, 1,42 ммоль) в 10 мл сухого ДХМ прибавили 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (440 мг, 1,94 ммоль) с последующим прибавлением DMAP (80 мг, 0,65 ммоль) и в конце прибавили N, N-диизопропилэтиламин (680 мкл, 3,88 ммоль). Полученный оранжевый раствор перемешивали при комн. темп. в течение 24 часов, через которые ЖХ/MС показал, что исходной кислоты не осталось. Раствор разбавили ДХМ, один раз промывали насыщенным водным раствором гидрокарбоната натрия (густая эмульсия), один раз 10% водным раствором лимонной кислоты, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-15% EtOAc в смеси гексанов) с получением 7-бромгептил-(Z)-дец-3-еноата (250 мг, 0,72 ммоль, 56%) в виде светло-желтой жидкости. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,65-5,49 (м, 2H); 4,07 (т, 2H, J=6,7 Гц); 3,40 (т, 2H, J=6,8 Гц); 3,08 (д, 2H, J=5,5 Гц); 2,04 (к, 2H, J=6,8 Гц); 1,92-1,79 (м, 2H); 1,70-1,56 (м, 2H); 1,51-1,20 (м, 14H); 0,88 (т, 3H, J=6,3 Гц).
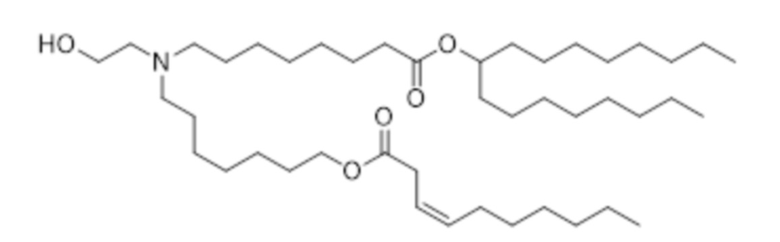
Химическая формула: C44H85NO5
Молекулярная масса: 708,17
[00340] Соединение 285 получали из гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноата (350 мг, 0,71 ммоль) аналогично соединению 284 за исключением того, что 7-бромгептил-(Z)-дец-3-еноат (250 мг, 0,72 ммоль) использовали вместо 5-бромпентилоктилмалоната. После обработки реакционной смеси водой полученное желтое масло очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением 7-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гептил (Z)-дец-3-еноата (205 мг, 0,29 ммоль, 41%) в виде бесцветного масла.
СВЭЖХ/ДСИО: RT=3,35 мин. MС (ИЭР): m/z (MH+) 708,75 для C44H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,64-5,48 (м, 2H); 4,86 (квинт., 1H, J=6,2 Гц); 4,07 (т, 2H, J=6,7 Гц); 3,55 (т, 2H, J=5,0 Гц); 3,40 (т, 2H, J=6,8 Гц); 3,08 (д, 2H, J=5,6 Гц); 2,61 (т, 2H, J=4,1 Гц); 2,47 (т, 4H, J=6,8 Гц); 2,27 (т, 2H, J=7,5 Гц); 2,04 (к, 2H, J=6,8 Гц); 1,70-1,55 (м, 4H); 1,54-1,40 (м, 6H); 1,39-1,13 (м, 45H); 0,87 (т, 9H, J=6,5 Гц).
GJ. Соединение 276: Гептадекан-9-ил-8-((3-(3-метоксипропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
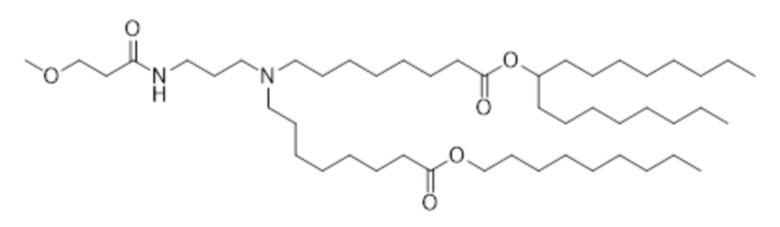
Химическая формула: C49H96N2O6
Молекулярная масса: 809,32
[00341] Соединение 276 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) аналогично соединению 178 за исключением того, что 3-метоксипропаноилхлорид (OakWO od Chemical, Эстилл, Южная Калифорния) (57 мкл, 0,52 ммоль) использовали вместо метоксиацетилхлорида. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(3-метоксипропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (140 мг, 0,55 ммоль, 31%) в виде желтого масла. СВЭЖХ/ДСИО: RT=3,48 мин. MС (ИЭР): m/z (MH+) 809,78 для C49H96N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,48 (с, 1H); 4,86 (квинт., 1H, J=12,6 Гц, 6,1 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,91 (с, 2H); 3,55 (кварт., 2H, J=13,8 Гц, 7,0 Гц); 3,36 (д, 2H, J=5,8 Гц); 2,53-2,43 (м, 2H); 2,41-2,32 (уш. м, 3H); 2,31-2,23 (м, 4H); 1,70-1,56 (м, 8H); 1,55-1,37 (м, 8H); 1,36-1,14 (м, 52H); 0,88 (т, 9H, J=7,5 Гц).
GK. Соединение 277: 4-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)бутилгептилглутарат
Стадия 1: 5-(Гептилилокси)-5-оксопентановой кислоты

Химическая формула: C12H22O4
Молекулярная масса: 230,30
[00342] Суспензию 5 г (41,6 ммоль) глутарового ангидрида в 7,2 мл (50 ммоль) 1-гептанола нагревали до 90°C и перемешивали в течение 20 часов после чего она превратилась в бесцветный раствор. Его оставили охлаждаться до комн. темп., разбавили насыщенным водным раствором гидрокарбоната натрия (~50 мл) и трижды экстрагировали диэтиловым эфиром. Водный слой привели к pH ~3 с помощью 4N водного раствора HCl и полученную мутную смесь трижды экстрагировали EtOAc. Фазы EtOAc объединили, один раз промыли насыщенным водным раствором хлорида натрия, сушили, (Na2SO4), отфильтровали и фильтрат концентрировали с получением 5-(гептилокси)-5-оксопентановой кислоты (7,36 г, 31,9 ммоль, 77%) в виде бесцветной жидкости, которую использовали на следующей стадии без дополнительной очистки. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 11,40 (уш. с, 1H); 4,06 (т, 2H, J=6,8 Гц); 2,41 (м, 4H); 1,95 (квинт., 2H, J=14,5 Гц, 7,3 Гц); 1,61 (м, 2H); 1,28 (м, 8H); 0,88 (т, 3H, J=5,8 Гц).
Стадия 2: 4-бромбутилгептилглутарат
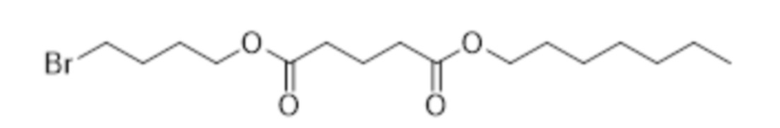
Химическая формула: C16H29BrO4
Молекулярная масса: 365,31
[00343] К раствору 5-(гептилокси)-5-оксопентановой кислоты (1,5 г, 6,5 ммоль) и 4-бром-1-бутанола (0,82 мл, 6,8 ммоль) в 20 мл сухого ДХМ в атмосфере азота прибавили 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (2,2 г, 9,8 ммоль) с последующим прибавлением 4-(диметиламино)пиридина (0,4 г, 3,26 ммоль) и в конце прибавили N, N-диизопропилэтиламин (3,4 мл, 19,5 ммоль) с получением бледно-желтого раствора. Его перемешивали при комн. темп. в течение 24 часов, после чего ЖХ/MC показал, что исходного материала не осталось. Раствор разбавили ДХМ, дважды промыли насыщенным водным раствором гидрокарбоната натрия (густая эмульсия), сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-20% EtOAc в смеси гексанов) с получением 4-бромбутилгептилглутарата (0,34 г, 0,93 ммоль, 14%) в виде бледно-желтого масла. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,11-4,06 (м, 4H); 3,41 (т, 2H, J=6,7 Гц); 2,62 (с, 4H); 1,87 (квинт., 2H, J=13,9 Гц, 7,2 Гц); 1,69-1,57 (м, 4H); 1,50-1,30 (м, 10H); 0,89 (т, 3H, J=6,3 Гц).
Стадия 3: 4-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)бутилгептилглутарат
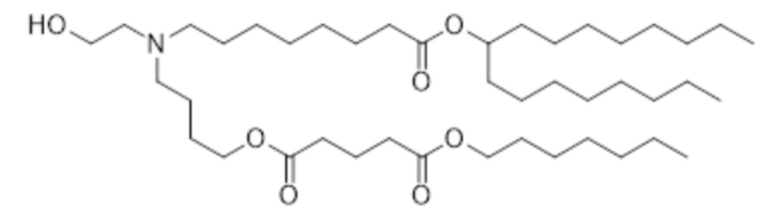
Химическая формула: C43H83NO7
Молекулярная масса: 726,14
[00344] К раствору гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноата (300 мг, 0,61 ммоль) и 6-бромгексилгексилсукцината (223 мг (0,61 ммоль) в 8 мл сухого ацетонитрила в атмосфере азота прибавили иодид калия (115 мг, 0,68 ммоль) с последующим прибавлением порошкообразного карбоната калия (340 мг, 2,4 ммоль) и смесь разбавили 2 мл сухого циклопентилметилового эфира. Полученную белую смесь нагревали до 90°C и перемешивали в течение 24 часов, затем оставили охлаждаться до комнатной температуры, отфильтровали, твердые вещества на фильтре промывали ДХМ и фильтрат концентрировали. Остаток суспендировали в 50% насыщенном водном растворе гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-30% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением 4-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)бутилгептилглутарата (140 мг, 0,19 ммоль, 32%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,22 мин. MС (ИЭР): m/z (MH+) 726,63 для C43H83NO7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=12,2 Гц, 6,1 Гц); 4,07 (кварт., 4H, J=12,1 Гц, 6,0 Гц); 3,53 (т, 2H, J=5,0 Гц); 2,88 (уш. с, 1H); 2,58 (т, 2H, J=4,7 Гц); 2,47 (кварт., 4H, J=16,8 Гц, 7,0 Гц); 2,37 (т, 4H, J=7,0 Гц); 2,27 (т, 2H, J=7,4 Гц); 1,94 (квинт., 2H, J=14,7 Гц, 7,3 Гц); 1,70-1,55 (м, 6H); 1,54-1,37 (м, 8H); 1,36-1,15 (м, 38H); 0,87 (т, 9H, J=6,1 Гц).
GL. Соединение 278: Гептадекан-9-ил-8-((3-(циклопропансульфонамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
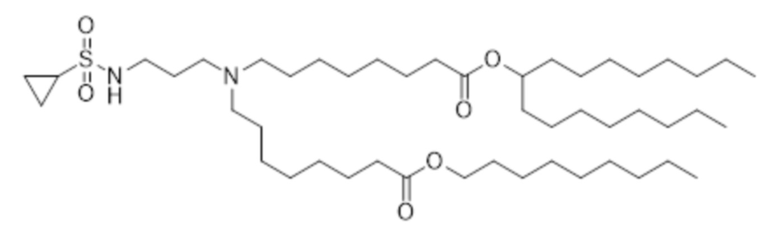
Химическая формула: C48H94N2O6S
Молекулярная масса: 827,35
[00345] Соединение 278 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) аналогично соединению 109 за исключением того, что циклопропансульфонилхлорид (OakWO od Chemical, Эстилл, Южная Калифорния) (54 мкл, 0,52 ммоль) использовали вместо метансульфонилхлорида. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(циклопропансульфонамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (125 мг, 0,15 ммоль, 44%) в виде светло-желтого масла.
СВЭЖХ/ДСИО: RT=3,45 мин. MС (ИЭР): m/z (MH+) 827,82 для C49H94N2O6S. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,95 (уш. с, 1H); 4,86 (квинт., 1H, J=12,4 Гц, 6,2 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,48 (кварт., 1H, J=14,1 Гц, 7,0 Гц); 3,26 (т, 2H, J=5,6 Гц); 2,63-2,47 (уш. м, 2H); 2,45-2,32 (уш. м, 4H); 2,31-2,21 (м, 4H); 1,77-1,68 (м, 2H); 1,61 (уш. т., 6H, J=6,8 Гц); 1,55-1,39 (м, 8H); 1,38-1,17 (м, 48H); 1,16-1,10 (м, 2H); 0,98-0,92 (м, 2H); 0,88 (т, 9H, J=6,0 Гц).
GM. Соединение 279: Гептадекан-9-ил-(Z)-6-(цианоимино)-2-метил-11-(8-(нонилокси)-8-оксооктил)-2,5,7,11-тетраазанонадекан-19-оат
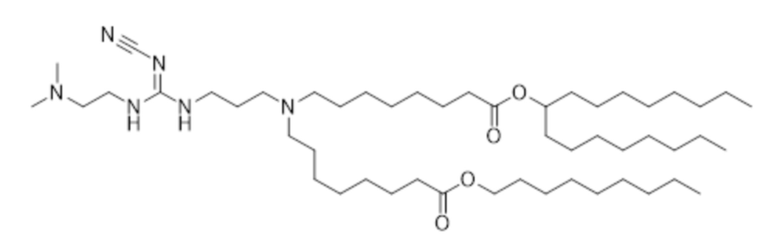
Химическая формула: C51H100N6O4
Молекулярная масса: 861,40
[00346] Соединение 279 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) аналогично соединению 168 за исключением того, что чистый N, N-диметилэтилен-1,2-диамин (160 мкл, 1,4 ммоль) использовали вместо раствора диметиламина в ТГФ. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-6-(цианоимино)-2-метил-11-(8-(нонилокси)-8-оксооктил)-2,5,7,11-тетраазанонадекан-19-оата (110 мг, 0,13 ммоль, 37%) в виде светло-желтого масла. СВЭЖХ/ДСИО: RT=3,10 мин. MС (ИЭР): m/z (MH+) 861,94 для C51H100N6O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,91 (уш. с, 1H); 4,86 (квинт., 1H, J=6,2 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,28-3,18 (м, 4H); 2,53-2,40 (м, 7H); 2,32-2,22 (м, 10H); 1,75-1,55 (м, 8H); 1,49-1,43 (м, 8H); 1,32-1,26 (уш. м, 50H); 0,88 (т, 9H, J=6,1 Гц).
GN. Соединение 280: Гептадекан-9-ил-8-((3-((2-((2-(диметиламино)этил)амино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
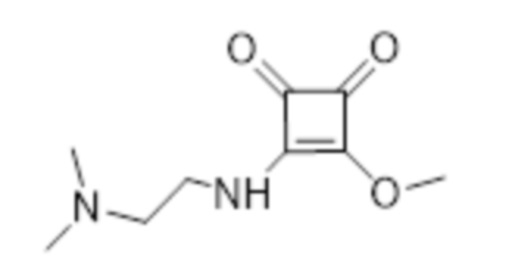
Химическая формула: C9H14N2O3
Молекулярная масса: 198,22
[00347] К раствору 3,4-диметокси-3-циклобутен-1,2-диона (500 мг, 3,45 ммоль) в 60 мл диэтиловом эфире быстро по каплям прибавили раствор 0,42 мл (3,8 ммоль) N, N-диметилэтилен-1,2-диамина в 10 мл эфира в течение пяти минут и полученную смесь перемешивали при комнатной температуре в течение 24 часов, затем отфильтровали, отфильтрованные твердые вещества промывали диэтиловым эфиром и сушили на воздухе. Отфильтрованное твердое вещество растворили в смеси гексанов, отфильтровали, фильтрат разбавили EtOAc до помутнения и смеси оставили охлаждаться до комнатной температуры., затем охладили до 0°C с получением осадка. Его отделили фильтрованием, промывали смесью гексанов, сушили на воздухе, затем сушили в вакууме с получением 3-((2-(диметиламино)этил)амино)-4-метоксициклобут-3-ен-1,2-диона (255 мг, 1,29 ммоль, 37%) в виде белого твердого вещества. Соединение существует в виде двух ротамеров при комнатной температуре в хлороформе. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,35 (уш. с, 0,65H); 6,09 (уш. с, 0,35H); 4,39 (с, 3H); 3,73 (уш. с, 0,75H); 3,46 (уш. с, 1,25H); 2,50 (м, 2H); 2,25 (с, 6H).
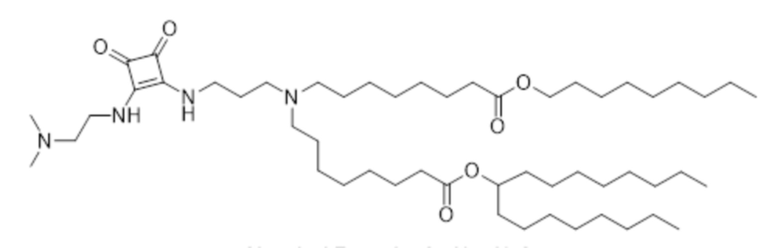
Химическая формула: C53H100N4O6
Молекулярная масса: 889,41
[00348] Соединение 280 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (300 мг, 0,42 ммоль) аналогично соединению 169 за исключением того, что 3-((2-(диметиламино)этил)амино)-4-метоксициклобут-3-ен-1,2-дион (160 мкл, 1,4 ммоль) использовали вместо 3-(диметиламино)-4-метоксициклобут-3-ен-1,2-диона и раствор нагревали до 40 oC. Раствор выпарили в потоке азота и остаток очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((2-((2-(диметиламино)этил)амино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (105 мг, 0,12 ммоль, 28%) в виде желтой пасты. СВЭЖХ/ДСИО: RT=3,16 мин. MС (ИЭР): m/z (MH+) 890,06 для C53H100N4O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,58 (уш. с, 1H); 6,20 (уш. с, 1H); 4,86 (квинт., 1H, J=5,9 Гц); 4,05 (т, 2H, J=6,7 Гц); 3,76-3,60 (м, 4H); 2,63 (уш. с, 2H); 2,54-2,44 (м, 6H); 2,28 (м, 10H); 1,74 (уш. с, 2H); 1,61 (м, 6H); 1,49 (м, 8H); 1,25 (уш. м, 48H); 0,88 (т, 9H, J=6,0 Гц).
GO. Соединение 281: Гептадекан-9-ил-8-((3-(3-метокси-2,2-диметилпропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C51H100N2O6
Молекулярная масса: 837,37
[00349] Соединение 281 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) аналогично соединению 252 за исключением того, что 3-метокси-2,2-диметилпропановую кислоту (Enamine LLC, Монмут Джанкшен, Нью-Джерси)(63 мг, 0,52 ммоль) использовали вместо (метилтио)уксусной кислоты. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(3-метокси-2,2-диметилпропанамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (125 мг, 0,15 ммоль, 43%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,63 мин. MС (ИЭР): m/z (MH+) 837,99 для C51H100N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 9,26 (с, 1H); 7,39 (т, 1H, J=6,3 Гц); 4,85 (квинт., 1H, J=6,3 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,42-3,32 (м, 7H); 3,12-2,98 (м, 5H); 2,33-2,23 (м, 4H); 2,04 (уш. с, 2H); 1,75-1,53 (уш. м, 14H); 1,51-1,10 (м, 54H); 0,88 (т, 9H, J=6,1 Гц).
GP. Соединение 282: Гептадекан-9-ил-8-((3-((1-амино-2-нитровинил)амино)пропил)(8-(нонил окси)-8-оксооктил)амино)октаноат
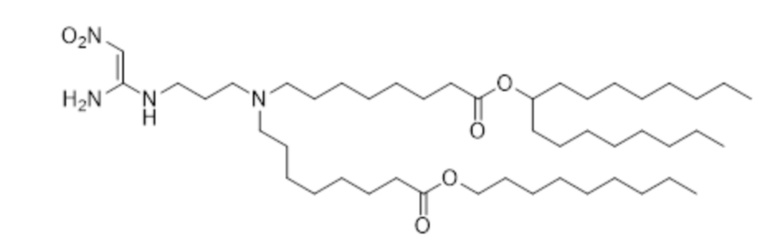
Химическая формула: C47H92N4O6
Молекулярная масса: 809,28
[00350] Раствор гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,69 ммоль) и (2-нитроэтен-1,1-диил)бис(метилсульфана) (125 мг, 0,76 ммоль) в метаноле (5 мл) перемешивали при 80°C в герметично закрытой пробирке в течение 5 часов. Затем прибавили раствор аммиака (7 N в метаноле, 5 мл, 35 ммоль) и реакционную смесь дополнительно нагревали при 80°C в течение 2 часов. Растворитель удалили и сырой материал очищали с помощью хроматографии на силикагеле (SiO2: EtOAc/гексан от 0 до 100%, затем метанол, содержащий 1% гидроксид аммония/дихлорметан от 0 до 20%) с получением гептадекан-9-ил-(E)-8-((3-((1-амино-2-нитровинил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (80 мг, 12%) в виде желтого масла. ВЭЖХ/УФ (214 нм): RT=8,78 мин. MС (ХИ): m/z (MH+) 809,6 для C47H92N4O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 6,49 (с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,36 (м, 2H); 2,49-2,39 (м, 6H); 2,27 (дт, 4H, J=4,3 Гц, 7,2 Гц); 1,77-1,75 (м, 2H); 1,62-1,48 (м, 15H); 1,34- 1,24 (м, 50H); 0,86 (т, 9H, J=6,5 Гц).
GQ. Соединение 283: Гептадекан-9-ил-8-((3-(метиламино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
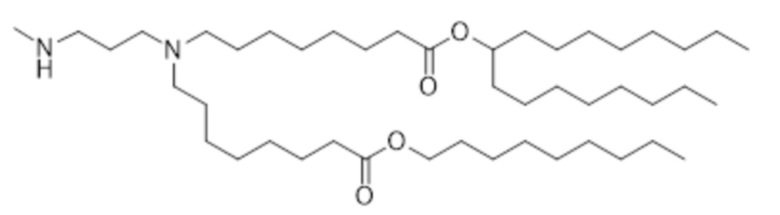
Химическая формула: C46H92N2O4
Молекулярная масса: 737,25
[00351] К раствору гептадекан-9-ил-8-((3-хлорпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (400 мг, 0,54 ммоль) в 2 мл 2-пропанола прибавили иодид натрия (10 мг, кат.) с последующим прибавлением 4 мл (8 ммоль) 2M раствора метиламина в ТГФ с получением желтого раствора. Его нагревали до 55°C и перемешивали в течение трех дней, после чего согласно ЖХ/MС исходного хлорида не осталось. Смесь концентрировали в потоке азота и остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(метиламино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (220 мг, 0,30 ммоль, 55%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=2,98 мин. MС (ИЭР): m/z (MH+) 737,70 для C46H92N2O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, J=6,1 Гц); 4,05 (т, 2H, J=6,7 Гц); 2,72 (т, 2H, J=6,5 Гц); 2,51 (т, 2H, J=6,1 Гц); 2,46 (с, 3H); 2,40 (т, 4H, J=6,3 Гц); 2,32-2,23 (м, 4H); 1,76-1,55 (м, 8H); 1,54-1,36 (м, 8H); 1,35-1,12 (уш. м, 49H); 0,87 (т, 9H, J=5,9 Гц).
GR. Соединение 284: 5-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)пентилоктилмалонат
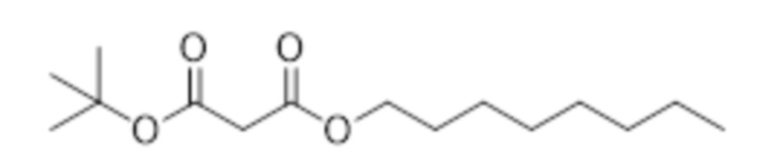
Химическая формула: C15H28O4
Молекулярная масса: 272,39
[00352] К раствору mono-трет-бутилмалоната (OakWO od Products, Inc., Эстилл, Южная Калифорния) (1,5 г, 9,2 ммоль) и 1-октанола (1,6 мл, 10,1 ммоль) в 20 мл сухого ДХМ прибавили 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (3,1 г, 13,8 ммоль) с последующим прибавлением 4-(диметиламино)пиридина (0,34 г, 2,7 ммоль) и в конце прибавили N, N-диизопропилэтиламин (4,8 мл, 27,5 ммоль) при перемешивании в атмосфере азота с получением бесцветного раствора. Его перемешивали при комн. темп. в течение 24 часов, через которые ЖХ/MС показал, что исходной кислоты не осталось. Желтый раствор разбавили ДХМ, дважды промывали насыщенным водным раствором гидрокарбоната натрия, дважды 10% водным раствором лимонной кислоты, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла, которое очищали с помощью хроматографии на силикагеле (0-15% EtOAc в смеси гексанов) с получением трет-бутилоктилмалоната (1,86 г, 6,8 ммоль, 74%) в виде бесцветной жидкости. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,11-4,06 (м, 4H); 3,41 (т, 2H, J=6,7 Гц); 2,62 (с, 4H); 1,87 (квинт., 2H, J=7,2 Гц); 1,69-1,57 (м, 4H); 1,50-1,30 (м, 10H); 0,89 (т, 3H, J=6,3 Гц).
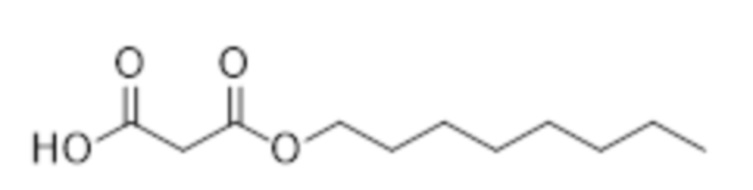
Химическая формула: C11H20O4
Молекулярная масса: 216,28
[00353] К раствору трет-бутилоктилмалоната (1,5 г, 5,5 ммоль) в 10 мл ДХМ при 0°C быстро по каплям прибавили трифторуксусную кислоту (5 мл, избыток) при перемешивании с получением бесцветного раствора. Полученный бесцветный раствор оставили нагреваться до комн. темп. и перемешивали в течение 24 часов, через которые согласно ТСХ реакция не завершилась. Раствор нагревали до 45°C и перемешивали в течение трех часов, через которые согласно ТСХ исходного материала не осталось. Бледно-желтый раствор оставили охлаждаться до комн. темп., концентрировали и остаток очищали с помощью хроматографии на силикагеле (0-30% EtOAc в смеси гексанов) с получением 3-(октилокси)-3-оксопропановой кислоты (0,9 г, 4,2 ммоль,75%) в виде бесцветной жидкости. 1H-ЯМР (500 МГц, CDCl3) δ м.д. 4,19 (т, 2H, J=6,8 Гц); 3,44 (с, 2H); 1,66 (квинт., 2H, J=7,1 Гц); 1,40-1,19 (м, 10H); 0,88 (т, 3H, J=7,0 Гц); протон карбоксильной группы не наблюдали.
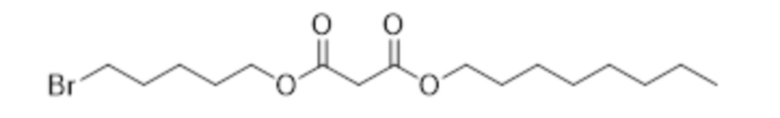
Химическая формула: C16H29BrO4
Молекулярная масса: 365,31
[00354] К раствору 3-(октилокси)-3-оксопропановой кислоты (900 мг, 4,2 ммоль) и 5-бром-1-пентанола (0,58 мл, 4,4 ммоль) в 20 мл сухого дихлорметана прибавили 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (1,4 г, 6,2 ммоль) с последующим прибавлением 4-(диметиламино)пиридина (250 мг, 2,1 ммоль) и окончательно N, N-диизопропилэтиламин (2,2 мл, 12,5 ммоль) при перемешивании в атмосфере азота. Бесцветный раствор перемешивали при комн. темп. в течение 24 часов, через которые ТСХ показал, что исходной кислоты не осталось. Раствор разбавили ДХМ, дважды промыли насыщенным водным раствором гидрокарбоната натрия (густая эмульсия), один раз 10% водным раствором лимонной кислоты, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Масло очищали с помощью хроматографии на силикагеле (0-20% EtOAc в смеси гексанов) с получением 5-бромпентилоктилмалоната (810 мг, 2,2 ммоль, 53%) в виде бесцветной жидкости. СВЭЖХ/ДСИО: RT=2,17 мин. MС (ИЭР): m/z (M+Na+) 387,24 для C16H29BrO4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,15 (дт, 4H, J=8,2 Гц, 6,6 Гц); 3,41 (т, 2H, J=6,8 Гц); 3,37 (с, 2H); 1,95-1,85 (м, 2H); 1,74-1,59 (м, 4H); 1,57-1,47 (м, 2H); 1,39-1,20 (м, 10H); 0,88 (т, 3H, J=6,6 Гц).

Химическая формула: C43H83NO7
Молекулярная масса: 726,14
[00355] К раствору гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноата (400 мг, 0,81 ммоль) и 6-бромгексилгексилсукцинат (300 мг (0,81 ммоль) в 8 мл сухого ацетонитрила в атмосфере азота прибавили иодид калия (150 мг, 0,9 ммоль) с последующим прибавлением порошкообразного карбоната калия (450 мг, 3,3 ммоль) и смесь разбавили 2 мл сухого циклопентилметилового эфира. Полученную белую смесь нагревали до 90°C и перемешивали в течение 24 часов, затем оставили охлаждаться до комн. темп., отфильтровали, отфильтрованные твердые вещества промывали ДХМ и фильтрат концентрировали. Остаток суспендировали в 50% насыщенном водном растворе гидрокарбоната натрия и дважды экстрагировали ДХМ. Органические фазы объединили, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением 5-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)пентилоктилмалоната (225 мг, 0,31 ммоль, 38%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,24 мин. MС (ИЭР): m/z (MH+) 726,87 для C43H83NO7. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,86 (квинт., 1H, 6,1 Гц); 4,14 (тд, 4H, J=6,7 Гц, 2,9 Гц); 3,57 (м, 2H); 3,37 (с, 2H); 2,63 (уш. с, 2H); 2,51 (уш. с, 4H); 2,27 (т, 2H, J=7,4 Гц); 1,73-1,56 (м, 6H); 1,55-1,42 (м, 8H); 1,41-1,16 (м, 43H); 0,88 (т, 9H, J=6,1 Гц).
GS. Соединение 285: 7-((8-(Гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гептил-(Z)-дец-3-еноат
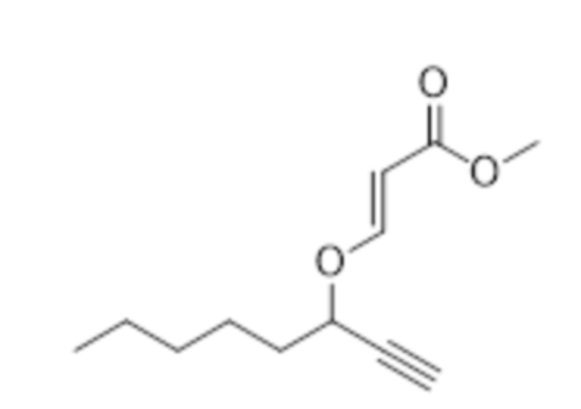
Химическая формула: C12H18O3
Молекулярная масса: 210,27
[00356] К раствору 1-октин-3-ола (2,15 мл, 14,4 ммоль) и метилпропиолата (1,2 мл, 14,4 ммоль) в 100 мл сухого ДХМ прибавили триэтиламин (0,2 мл, 1,4 ммоль) и бледно-желтый раствор перемешивали при комн. темп. в течение 20 часов, через которые согласно ТСХ исходного спирта не осталось. Раствор концентрировали и остаток очищали с помощью хроматографии на силикагеле (0-20% EtOAc в смеси гексанов) с получением метил-(E)-3-(окт-1-ин-3-илокси)акрилата (2,92 г, 13,9 ммоль, 97%) в виде бесцветной жидкости. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 7,61 (д, 1H, J=12,5 Гц); 5,38 (д, 1H, J=12,5 Гц); 4,53 (тд, 1H, J=6,6 Гц, 2,0 Гц); 3,70 (с, 3H); 2,58 (д, 1H, J=2,0 Гц); 1,91-1,75 (м, 2H); 1,52-1,41 (м, 2H); 1,37-1,26 (м, 4H); 0,90 (т, 3H, J=6,9 Гц).

Химическая формула: C10H18O2
Молекулярная масса: 170,25
[00357] В 5 мл микроволновой пробирке смешали 840 мг (4 ммоль) метил-(E)-3-(окт-1-ин-3-илокси)акрилата и 2 мл воды с получением бесцветного двухфазного раствора. Пробирку герметично закрыли и смесь подвергали микроволновому облучению при 175°C в течение 90 минут. Полученный двухфазный дважды раствор промывали ДХМ, органические фазы промывали, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением темно-оранжевого масла. Его растворили в смеси гексанов и очищали с помощью хроматографии на силикагеле (0-20% EtOAc в смеси гексанов) с получением (Z)-дек-3-еновой кислоты (155 мг, 0,91 ммоль, 23%) в виде оранжевого масла. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 11,03 (уш. с, 1H); 5,70-5,44 (м, 2H); 3,14 (д, 2H, J=6,6 Гц); 2,04 (к, 2H, J=6,8 Гц); 1,43-1,13 (м, 8H); 0,88 (т, 3H, J=6,8 Гц). (Z)-Геометрия подтверждена экспериментами по 1D селективному градиенту NOEsy с облучением при 2,07 м.д. (протоны C-5) и 3,16 м.д. (протоны C-2).
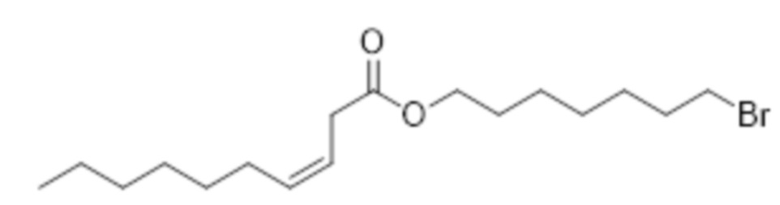
Химическая формула: C17H31BrO2
Молекулярная масса: 347,34
[00358] К раствору (Z)-дек-3-еновой кислоты (220 мг, 1,29 ммоль) и 7-бром-1-гептанола (250 мкл, 1,42 ммоль) в 10 мл сухого ДХМ прибавили 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (440 мг, 1,94 ммоль) с последующим прибавлением DMAP (80 мг, 0,65 ммоль) и в конце прибавили N, N-диизопропилэтиламин (680 мкл, 3,88 ммоль). Полученный оранжевый раствор перемешивали при комн. темп. в течение 24 часов, через которые ЖХ/MС показал, что исходной кислоты не осталось. Раствор разбавили ДХМ, один раз промывали насыщенным водным раствором гидрокарбоната натрия (густая эмульсия), один раз 10% водным раствором лимонной кислоты, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-15% EtOAc в смеси гексанов) с получением 7-бромгептил-(Z)-дец-3-еноата (250 мг, 0,72 ммоль, 56%) в виде светло-желтой жидкости. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,65-5,49 (м, 2H); 4,07 (т, 2H, J=6,7 Гц); 3,40 (т, 2H, J=6,8 Гц); 3,08 (д, 2H, J=5,5 Гц); 2,04 (к, 2H, J=6,8 Гц); 1,92-1,79 (м, 2H); 1,70-1,56 (м, 2H); 1,51-1,20 (м, 14H); 0,88 (т, 3H, J=6,3 Гц).
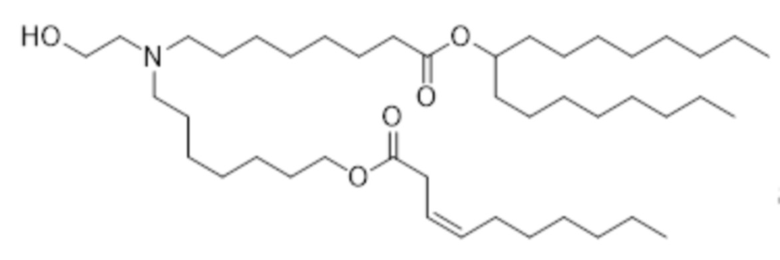
Химическая формула: C44H85NO5
Молекулярная масса: 708,17
[00359] Соединение 285 получали из гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноата (350 мг, 0,71 ммоль) аналогично соединению 284 за исключением того, что 7-бромгептил-(Z)-дец-3-еноат (250 мг, 0,72 ммоль) использовали вместо 5-бромпентилоктилмалоната. После обработки реакционной смеси водой полученное желтое масло очищали с помощью хроматографии на силикагеле (0-40% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением 7-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)гептил (Z)-дец-3-еноата (205 мг, 0,29 ммоль, 41%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,35 мин. MС (ИЭР): m/z (MH+) 708,75 для C44H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,64-5,48 (м, 2H); 4,86 (квинт., 1H, J=6,2 Гц); 4,07 (т, 2H, J=6,7 Гц); 3,55 (т, 2H, J=5,0 Гц); 3,40 (т, 2H, J=6,8 Гц); 3,08 (д, 2H, J=5,6 Гц); 2,61 (т, 2H, J=4,1 Гц); 2,47 (т, 4H, J=6,8 Гц); 2,27 (т, 2H, J=7,5 Гц); 2,04 (к, 2H, J=6,8 Гц); 1,70-1,55 (м, 4H); 1,54-1,40 (м, 6H); 1,39-1,13 (м, 45H); 0,87 (т, 9H, J=6,5 Гц).
GT. Соединение 286: Гептадекан-9-ил-8-((3-ацетамидо-2,2-диметилпропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
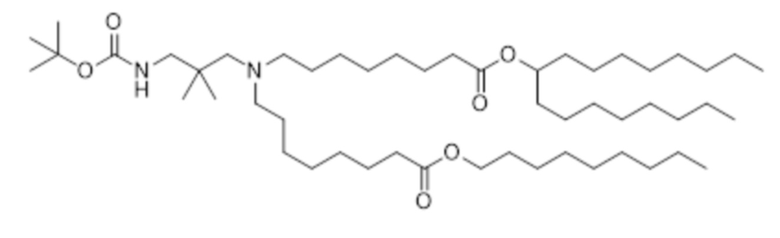
Химическая формула: C52H102N2O6
Молекулярная масса: 850,77
[00360] Гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)-2,2-диметилпропил)(8-(нонилокси)-8-оксооктил)амино)октаноат получали из гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,75 ммоль) аналогично соединению 244 за исключением того, что трет-бутил- (2,2-диметил-3-оксопропил)карбамат (Enamine LLC, Монмут Джанкшен, Нью-Джерси)(231 мг, 1,13 ммоль) использовали вместо N-Boc-глициналя, требовалось три эквивалента триацетоксиборогидрида натрия и реакцию проводили при 50°C в течение трех дней. После обработки реакционной смеси водой полученное желтое масло очищали с помощью хроматографии на силикагеле (0-50% метанол в ДХМ) и содержащие продукт фракции собирали и концентрировали с образованием смеси бесцветное масло/белое твердое вещество. Данную смесь очищали с помощью хроматографии на силикагеле (0-25% EtOAc в смеси гексанов) с получением гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)-2,2-диметилпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (85 мг, 0,1 ммоль,13%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=3,65 мин. MС (ИЭР): m/z (MH+) 852,01 для C52H102N2O6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,32 (уш. с, 1H); 4,86 (квинт., 1H, J=6,1 Гц); 4,05 (т, 2H, J=6,8 Гц); 2,99 (д, 2H, J=4,6 Гц); 2,37 (т, 4H, J=7,4 Гц); 2,32-2,19 (м, 6H); 1,69-1,55 (м, 6H); 1,54-1,37 (м, 16H); 1,36-1,15 (м, 49H); 0,91-0,84 m, 15H).

Химическая формула: C47H94N2O4
Молекулярная масса: 751,28
[00361] К раствору гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)-2,2-диметилпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (85 мг, 0,1 ммоль) в 2 мл ДХМ, охлажденному до 0 oC, при перемешивании прибавили 2M раствор хлороводорода в диэтиловом эфире (0,5 мл, избыток) с получением бесцветного раствора. Данный раствор оставили нагреваться до комн. темп., затем нагревали до 40°C и перемешивали в течение через два часа после этого по данным ЖХ/МС не осталось исходного материала. Раствор оставили охлаждаться до комнатной температуры и концентрировали в токе азота, остаток перерастворили в эфире, концентрировали и поместили в высокий вакуум в течение ночи с получением гептадекан-9-ил-8-((3-амино-2,2-диметилпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (79,3 мг, 0,096 ммоль, 96%) в виде бесцветного пенистого твердого вещества (предположительно дигидрохлорид). Использовали без дополнительной очистки. СВЭЖХ/ДСИО: RT=3,12 мин. MС (ИЭР): m/z (MH+) 751,97 для C47H94N2O4.
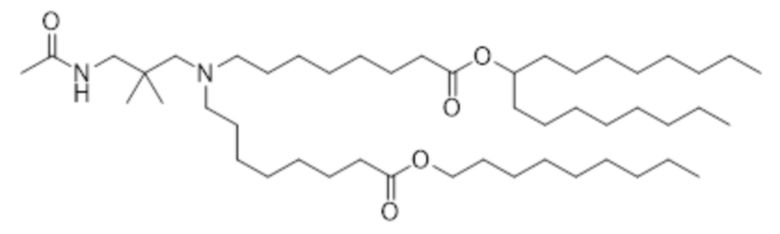
Химическая формула: C49H96N2O5
Молекулярная масса: 793,32
[00362] К раствору гептадекан-9-ил-8-((3-амино-2,2-диметилпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (предположительно дигидрохлорид)(79 мг (0,096 ммоль) и триэтиламина (41 мкл, 0,29 ммоль) в 2 мл сухом ДХМ, охлажденному до 0 oC, при перемешивании по каплям прибавили уксусный ангидрид (13 мкл, 0,15 ммоль). Через 15 минут охлаждающую баню убрали и полученную смесь перемешивали при комн. темп. в течение двух часов. Согласно ЖХ/MС исходного амина не осталось, поэтому желтый раствор разбавили ДХМ, дважды промывали насыщенным водным раствором гидрокарбоната натрия, один раз насыщенным водным раствором хлорида натрия, сушили (MgSO4), отфильтровали и фильтрат концентрировали с получением желтого масла. Его очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-ацетамидо-2,2-диметилпропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (56 мг, 0,07 ммоль, 73%) в виде бледно-желтого масла. СВЭЖХ/ДСИО: RT=3,52 мин. MС (ИЭР): m/z (MH+) 793,95 для C49H96N2O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 8,06 (т, 1H, J=4,2 Гц); 4,86 (квинт., 1H, J=6,2 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,13 (д, 2H, J=4,6 Гц); 2,41 (т, 4H, J=7,4 Гц); 2,35-2,21 (м, 6H); 1,94 (с, 3H); 1,69-1,56 (м, 6H); 1,55-1,39 (м, 8H); 1,38-1,13 (м, 48H); 0,95-0,82 m, 15H).
GU. Соединение 287: Гептадекан-9-ил-(Z)-6-(цианоимино)-2,5-диметил-11-(8-(нонилокси)-8-оксооктил)-2,5,7,11-тетраазанонадекан-19-оат

Химическая формула: C52H102N6O4
Молекулярная масса: 875,43
[00363] Соединение 287 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) аналогично соединению 168 за исключением того, что N, N,N'-триметилэтилен-1,2-диамин (90 мкл, 0,69 ммоль) использовали вместо раствора диметиламина и вторую стадию проводили при 70°C в течение двух дней. После обработки реакционной смеси водой полученное мутное бледно-желтое масло очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-6-(цианоимино)-2,5-диметил-11-(8-(нонилокси)-8-оксооктил)-2,5,7,11-тетраазанонадекан-19-оата (172 мг, 0,35 ммоль, 57%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,00 мин. MС (ИЭР): m/z (MH+) 876,20 для C52H102N6O4. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 8,68 (уш. с, 1H); 4,86 (квинт., 1H, J=6,2 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,54-3,43 (м, 2H); 3,31 (т, 2H, J=4,8 Гц); 3,03 (с, 3H); 2,55-2,44 (м, 4H); 2,44-2,33 (уш. с, 3H); 2,32-2,23 (м, 10H); 1,74-1,55 (м, 8H); 1,54-1,37 (м, 8H); 1,36-1,18 (м, 49H); 0,87 (т, 9H, J=6,8 Гц).
GV. Соединение 288: Гептадекан-9-ил-(Z)-9-(цианоимино)-2-метил-14-(8-(нонилокси)-8-оксооктил)-5-окса-2,8,10,14-тетраазадокозан-22-оат
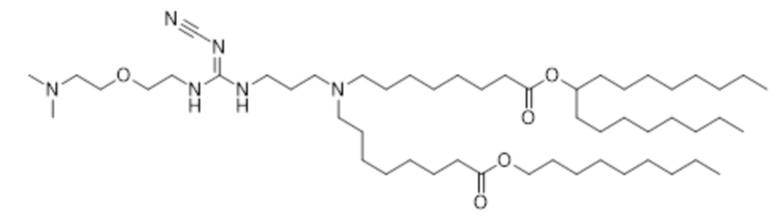
Химическая формула: C53H104N6O5
Молекулярная масса: 905,45
[00364] Соединение 288 получали из гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (250 мг, 0,35 ммоль) аналогично соединению 168 за исключением того, что 2-(2-аминоэтокси)-N, N-диметилэтан-1-амин (110 мкл, 0,76 ммоль) использовали вместо раствора диметиламина и вторую стадию проводили при 75°C в течение двух дней. После обработки реакционной смеси водой полученное бледно-желтое масло очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-9-(цианоимино)-2-метил-14-(8-(нонилокси)-8-оксооктил)-5-окса-2,8,10,14-тетраазадокозан-22-оат (147 мг, 0,16 ммоль, 47%) в виде бесцветного масла. СВЭЖХ/ДСИО: RT=3,07 мин. MС (ИЭР): m/z (MH+) 906,05 для C53H104N6O5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 6,95 (уш. с, 1H); 6,18 (уш. с, 1H); 4,86 (квинт., 1H, J=6,2 Гц); 4,05 (т, 2H, J=6,8 Гц); 3,56 (т, 4H, J=5,6 Гц); 3,37 (q, 2H, J=5,0 Гц); 3,26 (q, 2H, J=5,6 Гц); 2,52 (q, 4H, J=6,2 Гц); 2,44 (т, 4H, J=7,6 Гц); 2,35-2,20 (м, 10H); 1,75-1,55 (м, 8H); 1,54-1,38 (м, 8H); 1,37-1,15 (м, 48H); 0,87 (т, 9H, J=6,4 Гц).
GW. Соединение 289: Гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)(3-(тиазол-2-иламино)пропил)амино)октаноат
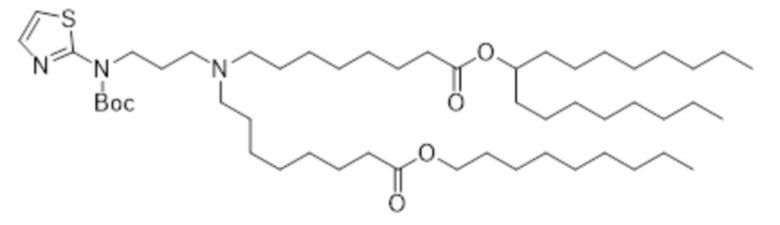
Химическая формула: C53H99N3O6S
Молекулярная масса: 906,45
[00365] К раствору гептадекан-9-ил-8-((3-гидроксипропил)(8-нонилокси)-8-оксооктил)амино)октаноата (1,0 г, 1,38 ммоль) в тетрагидрофуране (20 мл), содержащему трет-бутилтиазол-2-илкарбамат (276 мг, 1,38 моль) и трифенилфосфин (544 мг, 2,07 ммоль) при 0°C, по каплям прибавили диизопропилазодикарбоксилат (DIAD) (0,4 мл, 2,07 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель удалили под вакуумом с получением сырого продукта, который очищали с помощью хроматографии на силикагеле (0-50% EtOAc в смеси гексанов) с получением гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)(тиазол-2-ил)амино)пропил) (8-(нонилокси)-8-оксооктил)амино)октаноата (512 мг, 0,56 ммоль, 41%) в виде бесцветного масла (содержащего побочный продукт DIAD в качестве примеси). MС (ХИАД): m/z (MH+) 906,7 для C53H99N3O6S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,39 (д, 1H, J=3,6 Гц); 6,89 (д, 1H, J=3,6 Гц); 4,87-4,80 (м, 1H); 4,04 (т, 2H, J=6,6 Гц); 2,51-2,48 (м, 2H); 2,41-2,37 (м, 4H); 2,26 (дт, 4H, J=7,5 Гц, 3,7 Гц); 1,84-1,79 (м, 2H); 1,62-1,57 (м, 12H); 1,49-1,41 (м, 5H,); 1,39-1,24 (м, 56H); 0,86 (т, 9H, J=6,6 Гц).
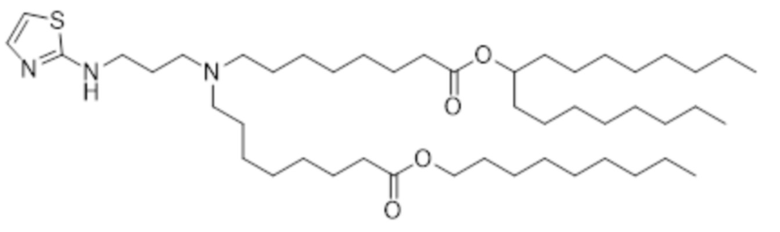
Химическая формула: C48H91N3O4S
Молекулярная масса: 806,33
[00366] К раствору гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)(тиазол-2-ил)амино)пропил) (8-(нонилокси)-8-оксооктил)амино)октаноата (512 мг, 0,56 ммоль) в дихлорметане (15 мл) при 0°C по каплям прибавили трифторуксусную кислоту (10 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Его погасили насыщенным водным раствором гидрокарбоната натрия при 0°C. Органический слой промывали насыщенным раствором гидрокарбоната натрия, 0,1 N раствором гидроксида натрия и насыщенным водным раствором хлорида натрия. После сушки над безводным сульфатом натрия органический слой отфильтровали и растворитель удалили под вакуумом с получением сырого продукта, который очищали с помощью хроматографии на силикагеле (0-100% EtOAc в смеси гексанов) с получением гептадекан-9-ил-8-((8-(нонилокси)-8-оксооктил)(3-(тиазол-2-иламино)пропил) амино)октаноата (280 мг, 0,34 ммоль, 61%) в виде светло-желтого масла. ВЭЖХ/УФ (214 нм): RT=7,01 мин. MС (ХИАД): m/z (MH+) 806,6 для C48H91N3O4S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,09 (д, 1H, J=3,6 Гц); 6,96 (уш. с, 1H); 6,42 (д, 1H, J=3,9 Гц); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,39-3,35 (м, 2H); 2,54 (т, 2H, J=5,7 Гц); 2,40-2,35 (м, 4H); 2,26 (дт, 4H, J=3,7 Гц, 7,5 Гц); 1,77-1,73 (м, 2H); 1,61-1,57 (м, 6H); 1,48-1,43 (м, 8H); 1,29-1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
GX. Соединение 290: Гептадекан-9-ил-8-((3-((2-((2-метоксиэтил)амино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C52H97N3O7
Молекулярная масса: 876,36
[00367] К раствору гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (500 мг, 0,69 ммоль) в диэтиловом эфире (50 мл) при 0°C прибавили 3,4-диметоксициклобут-3-ен-1,2-дион (148 мг, 1,04 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. ЖХМС показал отсутствие исходного материала. Затем прибавили раствор 2-метоксиэтан-1-амина (0,6 мл, 6,9 ммоль) в тетрагидрофуране (3,5 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь концентрировали и очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((2-((2-метоксиэтил)амино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноата (350 мг, 58%) в виде светло-желтого масла. ВЭЖХ/УФ (254 нм): 6,91 мин. MС (ХИ): m/z (MH+) 876,6 для C52H97N3O7. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,10 (уш. с, 1H); 6,20 (уш. с, 1H); 4,86-4,82 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,76-3,68 (м, 4H); 3,52 (т, 2H, J=4,8 Гц); 3,35 (с, 3H); 2,53 (т, 2H, J=6,0 Гц); 2,39-2,36 (м, 4H); 2,31-2,25 (м, 4H); 1,75-1,71 (м, 2H); 1,66-1,55 (м, 6H); 1,50-1,48 (м, 4H); 1,40-1,38 (м, 4H); 1,29- 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
GY. Соединение 291: Гептадекан-9-ил-8-((3-((3,4-диоксо-2-(пиперидин-1-ил)циклобут-1-ен-1-ил) амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
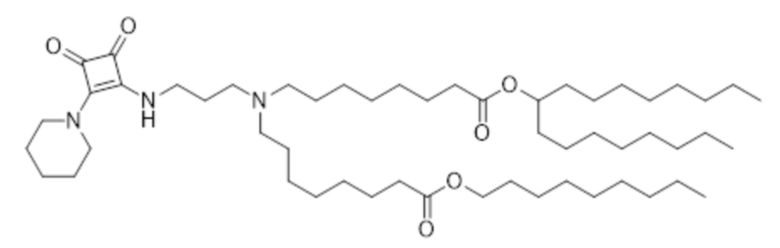
Химическая формула: C54H99N3O6
Молекулярная масса: 886,40
[00368] Соединение 291 получали аналогично соединению 290, но используя пиперидин вместо 2-метоксиэтан-1-амина. Светло-желтое масло, 290 мг, 47%. ВЭЖХ/УФ (254 нм): RT=6,70 мин. MС (ХИ): m/z (MH+) 886,7 для C54H99N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 8,01 (уш. с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,93-3,92 (м, 2H); 3,59 (уш. с, 4H); 2,63-2,60 (м, 2H); 2,39 (м, 4H); 2,31-2,24 (м, 4H); 1,72-1,54 (м, 17H); 1,49-1,48 (м, 5H); 1,38- 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
GZ. Соединение 292: Гептадекан-9-ил-8-((3-((2-(этиламино)-3,4-диоксоциклобут-1-ен-1-ил) амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
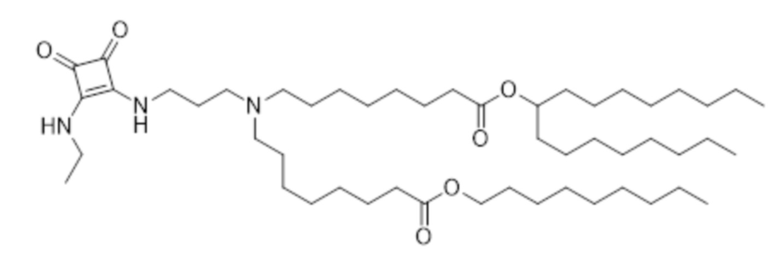
Химическая формула: C51H95N3O6
Молекулярная масса: 846,34
[00369] Соединение 292 получали аналогично соединению 290, но используя этиламин вместо 2-метоксиэтан-1-амина. Светло-желтое смолистое твердое вещество, 135 мг, 23%. ВЭЖХ/УФ (254 нм): RT=6,81 мин. MС (ХИ): m/z (MH+) 846,6 для C51H95N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 6,20 (уш. с, 1H); 4,86-4,82 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,69-3,56 (м, 4H); 2,56 (т, 2H, J=5,5 Гц); 2,44-2,39 (м, 4H); 2,31-2,25 (м, 4H); 1,76-1,72 (м, 2H); 1,70-1,52 (м, 9H); 1,51-1,44 (м, 5H); 1,42-1,38 (м, 4H); 1,28- 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
HA. Соединение 293: Гептадекан-9-ил-8-((3-((2-(диэтиламино)-3,4-диоксоциклобут-1-ен-1-ил) амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
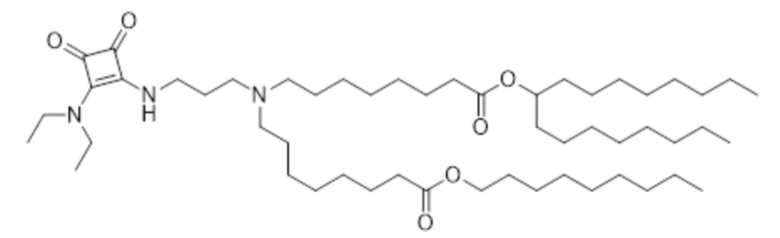
Химическая формула: C53H99N3O6
Молекулярная масса: 874,39
[00370] Соединение 293 получали аналогично соединению 290, но используя диэтиламин вместо 2-метоксиэтан-1-амина. Желтое масло, 315 мг, 52%. ВЭЖХ/УФ (254 нм): RT=6,63 мин. MС (ХИ): m/z (MH+) 874,7 для C53H99N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,52 (уш. с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,93-3,91 (м, 2H); 3,53 (м, 4H,), 2,62-2,59 (м, 2H); 2,41-2,39 (м, 4H); 2,30-2,24 (м, 4H); 1,72 (м, 2H); 1,61-1,58 (м, 11H); 1,50-1,48 (м, 5H); 1,40-1,37 (м, 4H); 1,29- 1,20 (м, 48H); 0,86 (т, 9H, J=6,7 Гц).
HB. Соединение 294: Гептадекан-9-ил-8-((3-((2-морфолино-3,4-диоксоциклобут-1-ен-1-ил) амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C53H97N3O7
Молекулярная масса: 888,37
[00371] Соединение 294 получали аналогично соединению 290, но используя морфолин вместо 2-метоксиэтан-1-амина. Светло-желтое масло, 297 мг, 48%. ВЭЖХ/УФ (254 нм): RT=6,67 мин. MС (ХИ): m/z (MH+) 888,6 для C53H97N3O7. 1H ЯМР (300 МГц, CDCl3): δ м.д. 8,12 (уш. с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,92-3,91 (м, 2H); 3,77-3,73 (м, 4H); 3,67-3,66 (м, 4H); 2,62-2,60 (м, 2H); 2,41-2,36 (м, 4H); 2,31-2,25 (м, 4H); 1,72-1,71 (м, 2H); 1,63-1,58 (м, 10H); 1,50-1,48 (м, 4H); 1,29- 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
HC. Соединение 295: Гептадекан-9-ил-8-((3-((2-(бис(2-метоксиэтил)амино)-3,4-диоксоциклобут-1 -ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
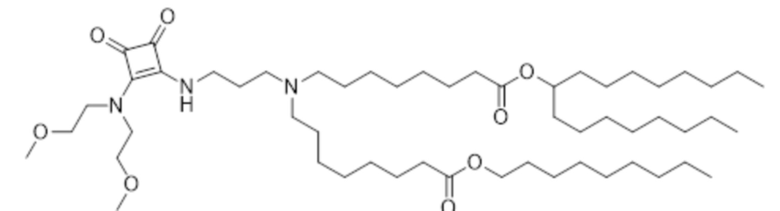
Химическая формула: C55H103N3O8
Молекулярная масса: 934,44
[00372] Соединение 295 получали аналогично соединению 290, но используя бис(2-метоксиэтил)амин вместо 2-метоксиэтан-1-амина. Желтое масло, 215 мг, 33%. ВЭЖХ/УФ (254 нм): RT=6,73 мин. MС (ХИ): m/z (MH+) 934,7 для C55H103N3O8. 1H ЯМР (300 МГц, CDCl3): δ м.д. 6,74 (т, 1H, J=5,9 Гц); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,77-3,71 (м, 4H); 3,57-3,56 (м, 4H); 3,35 (с, 6H); 2,50-2,47 (м, 2H); 2,40-2,36 (м, 4H); 2,30-2,24 (м, 4H); 1,77 (т, 2H, J=6,7 Гц); 1,62-1,52 (м, 8H); 1,50-1,42 (м, 4H); 1,40-1,36 (м, 4H); 1,29-1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
HD. Соединение 296: Гептадекан-9-ил-8-((3-((2-(4-метилпиперазин-1-ил)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)октаноат
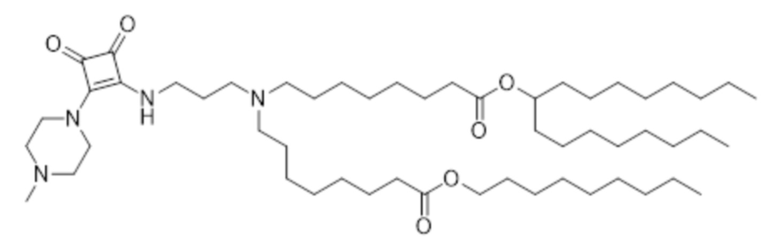
Химическая формула: C54H100N4O6
Молекулярная масса: 901,42
[00373] Соединение 296 получали аналогично соединению 290, но используя N-метилпиперазин вместо 2-метоксиэтан-1-амина. Желтое масло, 210 мг, 34%. ВЭЖХ/УФ (254 нм): RT=6,28 мин. MС (ХИАД): m/z (MH+) 901,7 для C54H100N4O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 8,05 (уш. с, 1H); 4,87-4,82 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,91-3,90 (м, 2H); 3,70 (уш. с, 4H); 2,71 (м, 2H); 2,48-2,45 (м, 8H); 2,31 (с, 3H); 2,28-2,26 (м, 4H); 1,71-1,58 (м, 10H); 1,52-1,48 (м, 6H), 1,30- 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
HE. Соединение 297: Нонил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(метил)амино)-7-гидроксиоктаноат
Стадия 1: Нонилокт-7-еноат
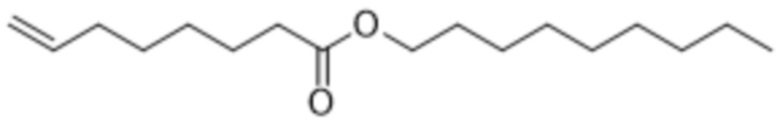
Химическая формула: C17H32O2
Молекулярная масса: 268,44
[00374] К раствору окт-7-еновой кислоты (2 г, 14,065 ммоль), 4-(диметиламино)пиридина (0,344 г, 2,813 ммоль) и 1-нонанола (2,435 г, 16,878 ммоль) в ДХМ (70 мл) прибавили EDC (2,696 г, 14,065 ммоль). Реакционную смесь оставили перемешиваться при комн. темп. в течение 16 ч. Реакционную смесь разбавили ДХМ и экстрагировали насыщ. водным раствором гидрокарбоната натрия. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над MgSO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле (0-20% этилацетат в смеси гексанов) с получением нонилокт-7-еноата (2,1 г, 7,82 ммоль, 56%). 1H ЯМР (300 МГц, CDCl3) δ м.д. 5,83 (м, 1H); 4,98 (м, 2H); 4,08 (т, 2H); 2,32 (т, 2H); 2,08 (м, 2H); 1,65 (м, 4H); 1,50-1,19 (м, 16H); 0,90 (м, 3H).
Стадия 2: Нонил-6-(оксиран-2-ил)гексаноат
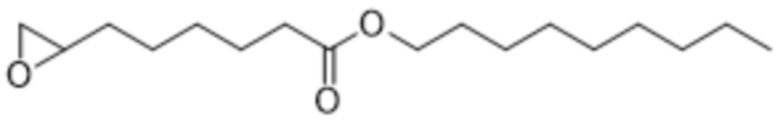
Химическая формула: C17H32O3
Молекулярная масса: 284,44
[00375] К раствору нонилокт-7-еноата (2,07 г, 7,71 ммоль) в ДХМ (38 мл) при 0°C прибавили раствор 3-хлорпербензойной кислоты (2,129 г, 8,64 ммоль) в ДХМ (38 мл). Через 2 часа реакционную смесь оставили нагреваться до комн. темп. и перемешивали в течение 16 часов Реакционную смесь разбавили ДХМ и промывали насыщ. водным раствором гидрокарбоната натрия. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия, отфильтровали выпарили в вакууме. Остаток очищали с помощью хроматографии на силикагеле (0-100% этилацетат в смеси гексанов) с получением нонил 6-(оксиран-2-ил)гексаноата (1,1 г, 3,86 ммоль, 50%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 2H); 2,92 (м, 1H); 2,77 (т, 1H); 2,48 (м, 1H); 2,33 (т, 2H); 1,71-1,26 (м, 22H); 0,91 (м, 3H).
Стадия 3: Нонил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(метил)амино)-7-гидроксиоктаноат
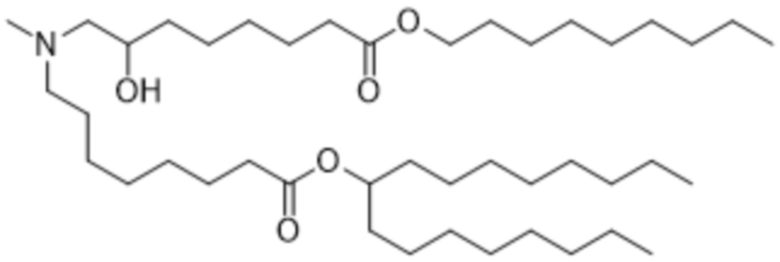
Химическая формула: C43H85NO5
Молекулярная масса: 696,15
[00376] В пробирку высокого давления прибавили нонил-6-(оксиран-2-ил)гексаноат (0,173 г, 0,61 ммоль), гептадекан-9-ил-8-(метиламино)октаноат (0,25 г, 0,61 ммоль) и каталитическое количество перхлората лития (0,003 г, 0,03 ммоль). Сосуд герметично закрыли и реакционную смесь нагревали до 100°C в течение 60 минут. Реакционную смесь оставили охлаждаться до комн. темп., растворили в смеси гексанов и очищали с помощью хроматографии на силикагеле (0-40% этилацетат в смеси гексанов) с получением нонил-8-{[8-(гептадекан-9-илокси)-8-оксооктил](метил)амино}-7-гидроксиоктаноата (0,097 г, 0,14 ммоль, 23%). ЖХ/ДСИО: RT=3,33 мин. MС (ИЭР): m/z (MH+) 697,11 для C43H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,66 (уш. м, 2H); 2,50 (уш. м,1H); 2,43-2,20 (м, 10H); 1,76-1,19 (м, 60H); 0,90 (м, 9H).
HF. Соединение 298: Нонил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(2-гидроксиэтил)амино)-7-гидроксиоктаноат
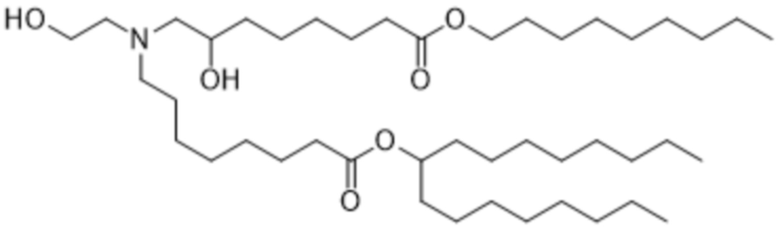
Химическая формула: C44H87NO6
Молекулярная масса: 726,18
[00377] Соединение 298 получали аналогично соединению 297, используя гептадекан-9-ил-8-((2-гидроксиэтил)амино)октаноат вместо гептадекан-9-ил-8-(метиламино)октаноата. Выход составлял 0,121 г (0,167 ммоль, 29%) ЖХ/ДСИО: RT=3,32 мин. MС (ИЭР): m/z (MH+) 727,12 для C44H87NO6. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,66 (уш. м, 3H); 2,79 (м, 1H); 2,69-2,24 (м, 10H); 1,74-1,22 (м, 60H); 0,90 (м, 9H) (протон первичной гидроксильной группы не наблюдали).
HG. Соединение 299: Гептадекан-9-ил-7-гидрокси-8-(метил(8-(нонилокси)-8-оксооктил)амино)октаноат
Стадия 1: Гептадекан-9-илокт-7-еноат

Химическая формула: C25H48O2
Молекулярная масса: 380,66
[00378] Гептадекан-9-илокт-7-еноат синтезировали способом аналогичным синтезу нонилокт-7-еноата, используя гептадекан-9-ол и окт-7-еновую кислоту. Выход составил 2,15 г (5,65 ммоль, 80%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 5,83 (м, 1H); 5,08-4,81 (м, 3H); 2,31 (т, 2H); 2,06 (м, 2H); 1,73-1,15 (м, 34H); 0,90 (м, 6H).
Стадия 2: Гептадекан-9-ил-6-(оксиран-2-ил)гексаноат
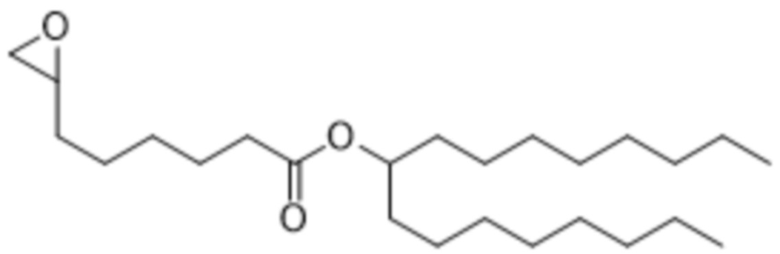
Химическая формула: C25H48O3
Молекулярная масса: 396,66
[00379] Гептадекан-9-ил 6-(оксиран-2-ил)гексаноат синтезировали способом, аналогичным синтезу нонил-6-(оксиран-2-ил)гексаноата, используя гептадекан-9-илокт-7-еноат. Выход составил 1,45 г (3,66 ммоль, 69%). 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (п, 1H); 2,92 (м, 1H); 2,77 (т, 1H); 2,48 (м, 1H); 2,32 (т, 2H); 1,74-1,21 (м, 36H); 0,90 (м, 6H).
Стадия 3: Нонил-8-(метиламино)октаноат
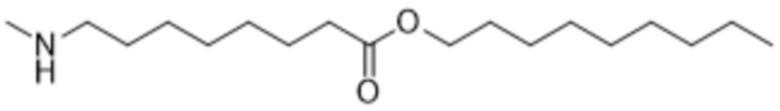
Химическая формула: C18H37NO2
Молекулярная масса: 299,49
[00380] В колбу, содержащую нонил-8-бромоктаноат (1 g, 2,86 ммоль), прибавили 2M раствор метиламина (42,9 мл, 85,87 ммоль) вТГФ. Реакционную смесь оставили перемешиваться при комн. темп. в течение 16 часов, затем концентрировали в вакууме. Остаток разбавили этилацетатом и промывали насыщенным раствором гидрокарбоната натрия. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над Na2SO4, отфильтровали и выпарили под вакуумом. Остаток очищали с помощью хроматографии на силикагеле (0-20% MeOH в ДХМ) с получением нонил-8-(метиламино)октаноата (0,625 г, 2,86 ммоль, 73%). ЖХ/ДСИО: RT=1,19 мин. MС (ИЭР): m/z (MH+) 300,17 для C18H37NO2. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,08 (т, 2H); 2,60 (т, 2H); 2,46 (с, 3H); 2,31 (т, 2H); 1,91-1,45 (м, 7H); 1,33 (м, 18H); 0,90 (м, 3H).
Стадия 4: Гептадекан-9-ил-7-гидрокси-8-(метил(8-(нонилокси)-8-оксооктил)амино)октаноат

Химическая формула: C43H85NO5
Молекулярная масса: 696,16
[00381] Соединение 299 синтезировали способом, аналогичным синтезу соединения 297, используя нонил-8-(метиламино)октаноат и гептадекан-9-ил-6-(оксиран-2-ил)гексаноат. Выход составил 0,152 мг (0,218 ммоль, 39%). ЖХ/ДСИО: RT=3,25 мин. MС (ИЭР): m/z (MH+) 697,85 для C43H85NO5. 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,89 (м, 1H); 4,08 (т, 2H); 3,66 (уш. м, 1H); 2,52 (уш. м, 1H); 2,31 (уш. м, 10H); 1,75-1,20 (м, 60H); 0,90 (м, 9H) (гидроксильный протон не наблюдали).
HH. Соединение 300: Гептадекан-9-ил-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат
Стадия 1: Ундекан-3-ил-8-бромоктаноат
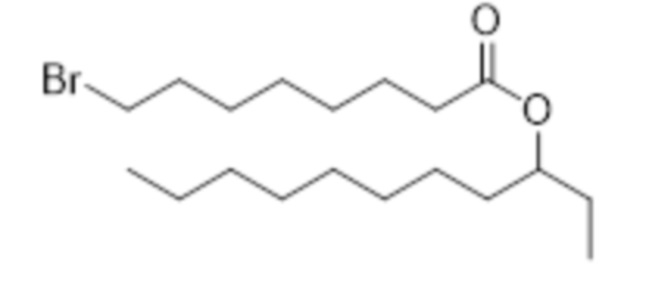
Химическая формула: C19H37BrO2
Молекулярная масса: 377,41
[00382] К раствору 3-ундеканoла (4,14 г, 24 ммоль), 8-бромоктановой кислоты (8,01 г, 36 ммоль) и DMAP (0,58 г, 4,8 ммоль) в дихлорметане (50 мл) при 0°C прибавили EDCI (6,9 г, 36 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. ТСХ показал, что реакция завершена. Реакционную смесь охладили до 0°C и раствор соляной кислоты (10 мл конц. HCl, 90 мл воды, 7,5 г хлорида натрия) очень медленно прибавляли в течение 20 минут. Затем прибавили ацетонитрил (100 мл) и гексан (100 мл) прибавили, слои разделили и органический слой сушили выпарили в вакууме с получением масла. Масло растворили в гексане (100 мл) и промывали смесью ацетонитрила (100 мл) и 5% водным раствором гидрокарбоната натрия (100 мл). Слой гексана отделили и отфильтровали через диатомовую землю, фильтр-прессную лепешку промывали гексаном и фильтрат концентрировали в вакууме с получением ундекан-3-ил-8-бромоктаноата (8,76 г, 97%) в виде бесцветного масла. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,82-4,76 (м, 1H); 3,39 (т, 2H, J=6,7 Гц); 2,44 (т, 0,3H, J=7,4 Гц, для CH2Cl); 2,28 (т, 2H, J=7,5 Гц, для CH2Br); 1,88-1,79 (м, 2H); 1,70-1,42 (м, 6H); 1,38-1,17 (м, 18H); 0,88-0,82 (м, 6H).
Стадия 2: Гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)амино)октаноат
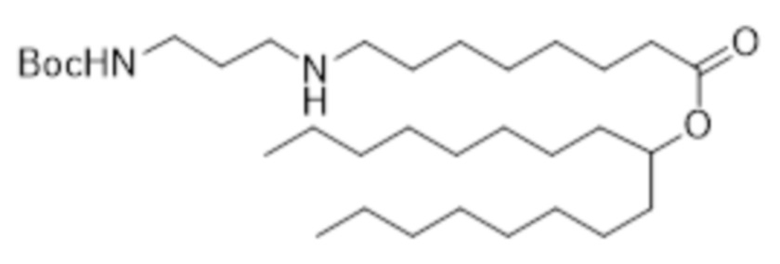
Химическая формула: C33H66N2O4
Молекулярная масса: 554,90
[00383] Раствор гептадекан-9-ил-8-бромоктаноата (69,2 г, 0,15 моль) и трет-бутил-(3-аминопропил)карбамата (130,6 г, 0,75 моль) в 500 мл этанола нагревали до 65°C в течение ночи. Реакционную смесь концентрировали и сырой продукт очищали с помощью хроматографии на силикагеле (0-20% метанол в ДХМ) с получением гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)амино)октаноата (62 г, 74%) в виде светло-желтого масла MС (ХИ): m/z (MH+) 555,5 для C33H66N2O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,15 (уш. с, 1H); 4,85 (квинт., 1H, J=6,0 Гц); 3,17 (м, 2H); 2,65 (т, 2H, J=6,6 Гц); 2,56 (т, 2H, J=6,8 Гц); 2,26 (т, 2H, J=7,6 Гц); 1,68-1,56 (м, 6H); 1,46 (м, 5H); 1,43 (с, 9H); 1,24 (м, 30H); 0,86 (т, 6H, J=6,6 Гц).
Стадия 3: Гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат

Химическая формула: C52H102N2O6
Молекулярная масса: 851,40
[00384] Раствор гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)амино)октаноата (6,0 г, 12 ммоль) и ундекан-3-ил-8-бромоктаноата (4,27 г, 11 ммоль) в циклопентилметиловом эфире (50 мл) и ацетонитриле (50 мл), содержащем карбонат калия (6,02 г, 43 ммоль) и иодид калия (1,97 г, 12 ммоль) нагревали при 86°C в течение 18 часов. После охлаждения до комнатной температуры реакционную смесь отфильтровали через диатомовую землю, фильтр-прессную лепешку промывали этилацетатом и фильтрат концентрировали в вакууме с получением сырого продукта, который очищали с помощью хроматографии на силикагеле (0-100% EtOAc в смеси гексанов) с получением гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (6,8 г, 74%) в виде масла. MС (ХИ): m/z (MH+) 851,7 для C52H102N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,66 (м, 1H); 4,87-4,80 (м, 2H); 3,17 (м, 2H); 2,42 (т, 2H, J=6,3 Гц); 2,35-2,24 (м, 8H); 1,64-1,56 (м, 12H); 1,53-1,44 (м, 9H); 1,44-1,36 (м, 3H); 1,42 (с, 9H); 1,32-1,12 (м, 42H); 0,86 (т, 12H, J=6,4Hz).
Стадия 4: Гептадекан-9-ил-8-((3-аминопропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат
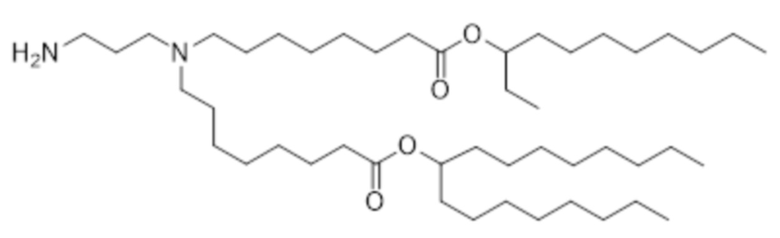
Химическая формула: C47H94N2O4
Молекулярная масса: 751,28
[00385] К раствору гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (6,8 г, 7,99 ммоль) в дихлорметане (30 мл) при 0°C, прибавили трифторуксусную кислоту (10 мл) по каплям и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь погасили насыщенным водным раствором гидрокарбоната натрия при 0°C. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия, 0,1 N раствором гидроксида натрия и насыщенным водным раствором хлорида натрия. После сушки над безводным сульфатом натрия, растворитель удалили под вакуумом с получением гептадекан-9-ил-8-((3-аминопропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (5,7 г, 97%) в виде масла. MС (ХИ): m/z (MH+) 751,7 для C47H94N2O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,87-4,79 (м, 2H); 2,70 (т, 2H, J=6,8 Гц); 2,42-2,33 (м, 6H); 2,27 (дт, 4H, J=2,8 Гц, 7,4 Гц); 1,68-1,46 (м, 22H); 1,44-1,35 (м, 4H); 1,34-1,16 (м, 42H); 0,88-0,84 (м, 12H).
Стадия 5: Гептадекан-9-ил-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат

Химическая формула: C51H99N5O4
Молекулярная масса: 846,38
[00386] Соединение 300 получали аналогично соединению 168 за исключением того, что гептадекан-9-ил-8-((3-аминопропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат (500 мг, 0,66 ммоль) использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (240 мг, 43%) в виде бесцветного масла. ВЭЖХ/УФ (254 нм): RT=8,60 мин. MС (ХИ): m/z (MH+) 846,7 для C51H99N5O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,59 (уш. с, 1H); 4,87-4,80 (м, 2H); 3,70-3,64 (м, 2H); 3,03 (с, 6H); 2,69-2,42 (м, 4H); 2,28 (дд, 4H, J=3,0 Гц, 7,4 Гц); 1,71-1,42 (м, 26H); 1,36-1,16 (м, 42H); 0,88-0,84 (м, 12H).
HI. Соединение 301: Гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат
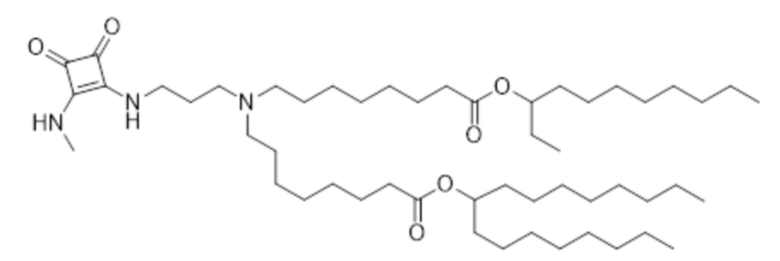
Химическая формула: C52H97N3O6
Молекулярная масса: 860,36
[00387] Соединение 301 получали аналогично соединению 182 за исключением того, что гептадекан-9-ил-8-((3-аминопропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат (500 мг, 0,66 ммоль) использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (180 мг, 32%) в виде белого воскообразного твердого вещества. ВЭЖХ/УФ (254 нм): RT=6,77 мин. MС (ХИ): m/z (MH+) 860,7 для C52H97N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,86-4,79 (м, 2H); 3,66 (уш. с, 2H); 3,25 (д, 3H, J=4,9 Гц); 2,56-2,52 (м, 2H); 2,42-2,37 (м, 4H); 2,28 (дд, 4H, J=2,7 Гц, 7,4 Гц); 1,78-1,68 (м, 3H); 1,64-1,50 (м, 16H); 1,48-1,38 (м, 6H); 1,32-1,18 (м, 43H); 0,88-0,84 (м, 12H).
HJ. Соединение 302: Гептадекан-9-ил-8-((3-(3,3-диметилтиоуреидо)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат
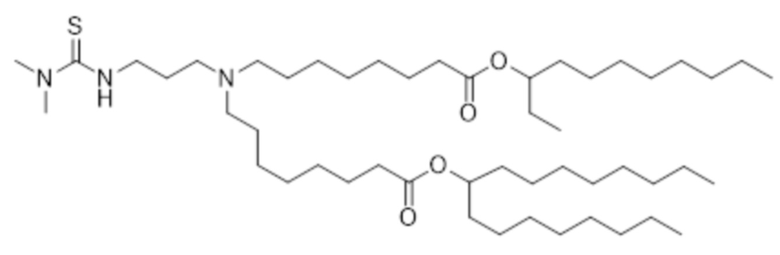
Химическая формула: C50H99N3O4S
Молекулярная масса: 838,42
[00388] Соединение 302 получали аналогично соединению 111 за исключением того, что гептадекан-9-ил-8-((3-аминопропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат (500 мг, 0,66 ммоль) использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(3,3-диметилтиоуреидо)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (140 мг, 25%) в виде желтого масла. ВЭЖХ/УФ (254 нм): RT=6,03 мин. MС (ХИ): m/z (MH+) 838,7 для C50H99N3O4S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,87-4,80 (м, 2H); 3,83 (уш. с, 2H); 3,27 (с, 6H); 2,91-2,64 (м, 4H); 2,27 (дд, 4H, J=3,1 Гц, 7,5 Гц); 1,68-1,42 (м, 27H); 1,38-1,12 (м, 42H); 0,88-0,84 (м, 12H).
HK. Соединение 303: Гептадекан-9-ил-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат
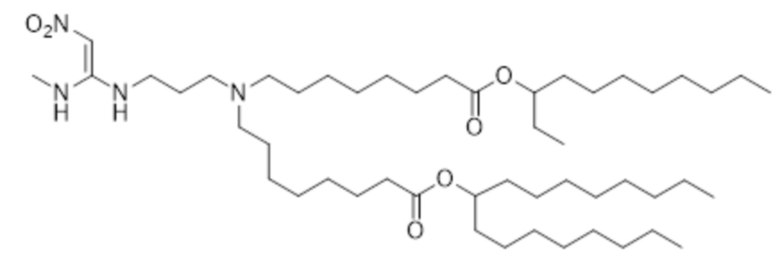
Химическая формула: C50H98N4O6
Молекулярная масса: 851,36
[00389] Соединение 303 получали аналогично соединению 170 за исключением того, что гептадекан-9-ил-8-((3-аминопропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат (500 мг, 0,66 ммоль) использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (270 мг, 40%) в виде масла. ВЭЖХ/УФ (254 нм): RT=8,19 мин. MС (ХИ): m/z (MH+) 851,6 для C50H98N4O6. 1H ЯМР (300 МГц, CDCl3 при 25°C): δ м.д. 10,15 (уш. с, 1H); 8,36, 8,22 (уш. с, 1H); 6,55 (с, 0,5H); 6,53 (с, 0,5H); 4,85-4,80 (м, 2H); 3,32-3,23 (м, 2H); 2,85 (д, 1,5H, J=4,9 Гц); 2,74-2,72 (м, 1,5H); 2,64 (м, 1H); 2,46-2,44 (м, 5H); 2,28 (дд, 4H, J=2,7 Гц, 7,4 Гц); 1,76 (м, 2H); 1,68-1,38 (м, 22H); 1,31-1,18 (м, 42H); 0,88-0,84 (м, 12H). 1H ЯМР (300 МГц, CDCl3 при 60°C): δ м.д. 10,15 (уш. с, 1H); 7,70 (уш. с, 1H); 6,51 (с, 1H); 4,86-4,80 (м, 2H); 3,27 (м, 2H); 2,82 (уш. с, 3H); 2,64-2,39 (м, 6H); 2,28 (м, 4H); 1,76 (м, 2H); 1,68-1,38 (м, 22H); 1,31-1,18 (м, 42H); 0,88-0,84 (м, 12H).
HL. Соединение 304: Гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат
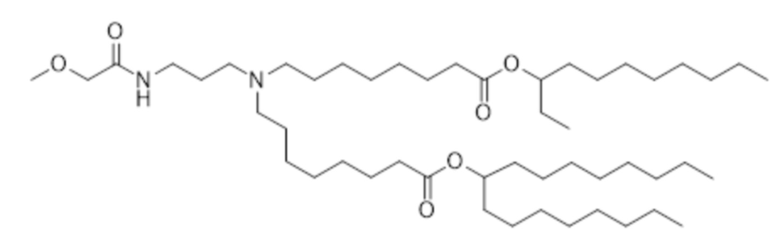
Химическая формула: C50H98N2O6
Молекулярная масса: 823,34
[00390] Соединение 303 получали аналогично соединению 170 за исключением того, что гептадекан-9-ил-8-((3-аминопропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноат (500 мг, 0,66 ммоль) использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(8-оксо-8-(ундекан-3-илокси)октил)амино)октаноата (290 мг, 53%) в виде масла. ВЭЖХ/УФ (210 нм): RT=8,52 мин. MС (ХИ): m/z (MH+) 823,7 для C50H98N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,59-7,56 (м, 1H); 4,87-4,80 (м, 2H); 3,86 (с, 2H); 3,38 (с, 3H); 3,38-3,32 (м, 2H); 2,48-2,32 (м, 6H); 2,27 (дд, 4H, J=2,7 Гц, 7,5 Гц); 1,68-1,36 (м, 24H); 1,34-1,18 (м, 42H); 0,88-0,83 (м, 12H).
HM. Соединение 305: 7-((8-(Гептадекан-9-илокси)-8-оксооктил)(3-(2-метоксиацетамидо)пропил)амино)гептилдеканоат
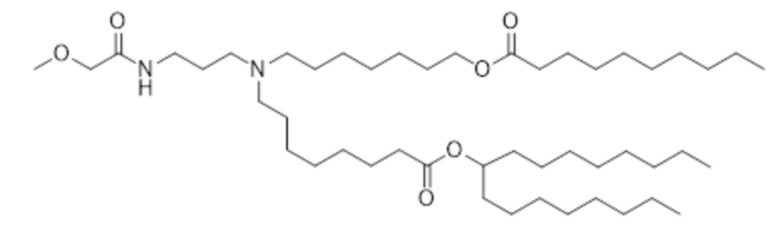
Химическая формула: C48H94N2O6
Молекулярная масса: 795,29
[00391] Соединение 305 получали аналогично соединению 178, но используя 7-((3-аминопропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)гептилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Светло-желтое масло, 230 мг, 42%. ВЭЖХ/УФ (210 нм): RT=5,76 мин. MС (ХИ): m/z (MH+) 795,6 для C48H94N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,57 (уш. с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,86 (с, 2H); 3,38 (с, 3H); 3,38-3,31 (м, 2H); 2,35-2,42 (м, 2H); 2,35-2,33 (м, 4H); 2,27 (дд, 2H, J=2,9 Гц, 7,4 Гц); 1,68-1,52 (м, 11H); 1,50-1,38 (м, 11H); 1,34-1,18 (м, 44H); 0,86 (т, 9H, J=6,5 Гц).
HN. Соединение 306: Гептадекан-9-ил-8-((3-(3,3-диметилтиоуреидо)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
Стадия 1: Гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат

Химическая формула: C50H98N2O6
Молекулярная масса: 823,34
[00392] Раствор гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)амино)октаноата (5,55 г, 10 ммоль), ундецил-6-бромгексаноата (5,24 г, 15 ммоль) в циклопентилметиловом эфире (80 мл) и ацетонитриле (80 мл), содержащем карбонат калия (5,53 г, 40 ммоль) и иодид калия (2,49 г, 15 ммоль) нагревали при 86°C в течение 18 часов. После охлаждения до комнатной температуры, реакционную смесь отфильтровали через диатомовую землю, фильтр-прессную лепешку промывали этилацетатом и фильтрат концентрировали в вакууме с получением сырого продукта, который очищали с помощью хроматографии на силикагеле (0-50% EtOAc в смеси гексанов, затем 1:1 ацетон/смесь гексанов) с получением гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (6,2 г, 73%) в виде масла. MС (ХИ): m/z (MH+) 823,7 для C50H98N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,64 (уш. с, 1H); 4,85 (квинт., 1H, J=6,3 Гц); 4,04 (т, 2H, J=6,7 Гц); 3,17 (м, 2H); 2,42 (т, 2H, J=6,8 Гц); 2,35-2,24 (м, 8H); 1,64-1,56 (м, 8H); 1,53-1,44 (м, 8H); 1,42 (с, 9H); 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
Стадия 2: Гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
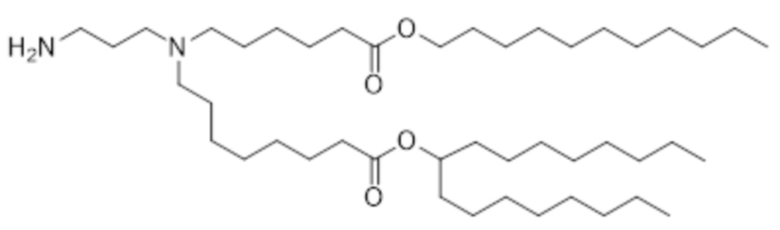
Химическая формула: C45H90N2O4
Молекулярная масса: 723,23
[00393] К раствору гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (6,2 г, 7,53 ммоль) в дихлорметане (75 мл) при 0°C по каплям прибавили трифторуксусную кислоту (5,8 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь погасили насыщенным водным раствором гидрокарбоната натрия при 0°C. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия, 0,1 N раствором гидроксида натрия и насыщенным водным раствором хлорида натрия. После сушки над безводным сульфатом натрия, растворитель удалили под вакуумом с получением гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (5,57 г, колич.) в виде желтого масла. MС (ХИ): m/z (MH+) 723,7 для C45H90N2O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,85 (квинт., 1H, J=6,3 Гц); 4,04 (т, 2H, J=6,6 Гц); 2,85 (т, 2H, J=6,3 Гц); 2,53 (т, 2H, J=6,8 Гц); 2,45-2,37 (м, 4H); 2,28 (т, 2H, J=7,4 Гц); 2,26 (т, 2H, J=7,4 Гц); 1,70-1,55 (м, 8H); 1,54-1,40 (м, 8H); 1,24 (м, 50H); 0,86 (т, 9H, J=6,6 Гц).
Стадия 3: Гептадекан-9-ил-8-((3-(3,3-диметилтиоуреидо)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат
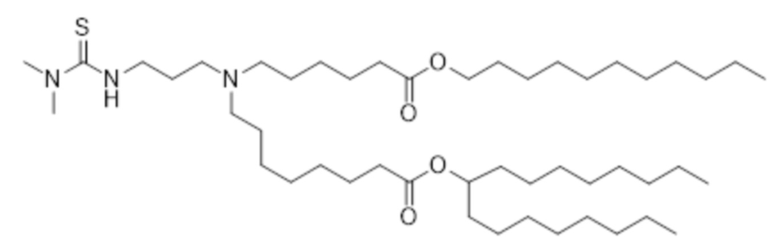
Химическая формула: C48H95N3O4S
Молекулярная масса: 810,37
[00394] Соединение 306 получали аналогично соединению 111 за исключением того, что гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат (500 мг, 0,66 ммоль) использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-(3,3-диметилтиоуреидо)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (320 мг, 57%) в виде желтого масла. ВЭЖХ/УФ (210 нм): RT=5,98 мин. MС (ХИ): m/z (MH+) 810,6 для C48H95N3O4S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 8,03 (уш. с, 1H); 4,85 (квинт., 1H, J=6,3 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,70 (м, 2H); 3,20 (с, 6H); 2,57 (м, 2H); 2,42 (м, 4H); 2,28 (м, 4H); 1,71 (м, 2H); 1,62 (м, 6H); 1,54-1,40 (м, 8H); 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
HO. Соединение 307: 7-((3-(2-Циано-3,3-диметилгуанидино)пропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)гептилдеканоат
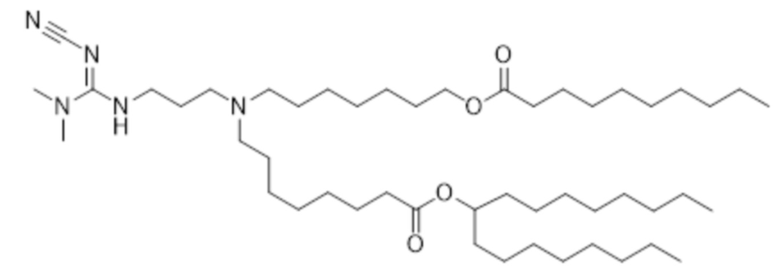
Химическая формула: C49H95N5O4
Молекулярная масса: 818,33
[00395] Соединение 307 получали аналогично соединению 168, но используя 7-((3-аминопропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)гептилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Бесцветное масло, 160 мг, 28%. ВЭЖХ/УФ (214 нм): RT=5,88 мин. MС (ХИ): m/z (MH+) 818,7 для C49H95N5O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,68-3,64 (м, 2H); 3,02 (с, 6H); 2,79-2,48 (м, 4H,); 2,27 (дд, 4H, J=1,6 Гц, 7,4 Гц); 1,89 (уш. с, 1H); 1,68-1,42 (м, 21H); 1,38-1,16 (м, 45H); 0,86 (т, 9H, J=6,7 Гц).
HP. Соединение 308: 7-((3-(3,3-Диметилтиоуреидо)пропил)(8-(гептадекан-9-илокси)-8-оксооктил) амино)гептилдеканоат
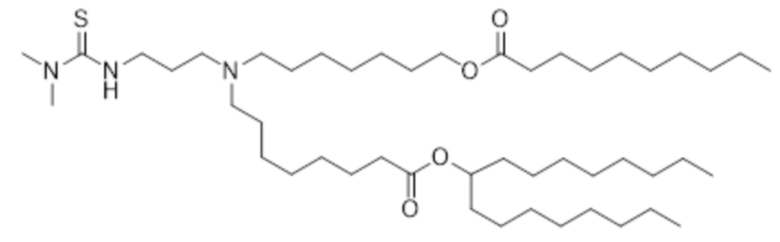
Химическая формула: C48H95N3O4S
Молекулярная масса: 810,37
[00396] Соединение 308 получали аналогично соединению 111, но используя 7-((3-аминопропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)гептилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Желтое масло, 150 мг, 27%. ВЭЖХ/УФ (254 нм): RT=6,77 мин. MС (ХИ): m/z (MH+) 810,6 для C48H95N3O4S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 8,20 (уш. с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,73 (уш. с, 2H); 3,23 (с, 6H); 2,68-2,38 (м, 4H,); 2,30-2,25 (м, 4H); 1,68-1,42 (м, 22H); 1,38-1,14 (м, 44H); 0,86 (т, 9H, J=6,5 Гц).
HQ. Соединение 309: 7-((8-(Гептадекан-9-илокси)-8-оксооктил)(3-((2-(метиламино)-3,4-диоксо циклобут-1-ен-1-ил)амино)пропил)амино)гептилдеканоат
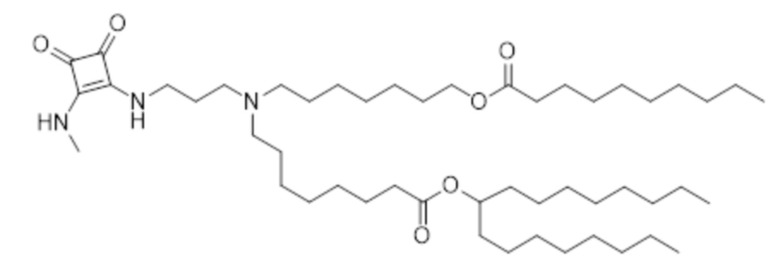
Химическая формула: C50H93N3O6
Молекулярная масса: 832,31
[00397] Соединение 309 получали аналогично соединению 182, но используя 7-((3-аминопропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)гептилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Белое воскообразное твердое вещество, 190 мг, 28%. ВЭЖХ/УФ (254 нм): RT=6,71 мин. MС (ХИ): m/z (MH+) 832,6 для C50H93N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,86-4,82 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,64 (уш. с, 2H); 3,25 (д, 3H, J=4,9 Гц); 2,53 (т, 2H, J=5,6 Гц); 2,42-2,37 (м, 4H); 2,28 (т, 4H, J=7,5 Гц); 1,76-1,71 (м, 2H); 1,64-1,58 (м, 10H); 1,52-1,38 (м, 9H); 1,30-1,18 (м, 44H); 0,86 (т, 9H, J=6,5 Гц).
HR. Соединение 310: 7-((8-(Гептадекан-9-илокси)-8-оксооктил)(3-((1-(метиламино)-2-нитровинил) амино)пропил)амино)гептилдеканоат
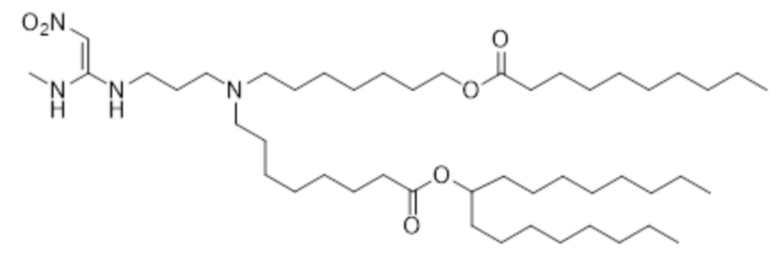
Химическая формула: C48H94N4O6
Молекулярная масса: 823,30
[00398] Соединение 310 получали аналогично соединению 170, но используя 7-((3-аминопропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)гептилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Коричневое масло, 195 мг, 28%. ВЭЖХ/УФ (214 нм): RT=6,15 мин. MС (ХИ): m/z (MH+) 823,7 для C48H94N4O6. 1H ЯМР (300 МГц, CDCl3 при 25°C): δ м.д. 10,14 (уш. с, 1H); 8,32 (с, 0,5H); 8,18 (с, 0,5H); 6,55 (с, 0,5H);, 6,53 (с, 0,5H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,33-3,23 (м, 2H); 2,86 (д, 1,5H, J=5,2 Гц); 2,73 (уш. с, 1,5H); 2,65 (м,1H); 2,48 (м, 5H); 2,27 (т, 4H, J=7,5 Гц); 1,77 (м, 2H); 1,67-1,58 (м, 10H); 1,49-1,43 (м, 8H); 1,30-1,14 (м, 44H); 0,86 (т, 9H, J=6,7 Гц). 1H ЯМР (300 МГц, CDCl3 при 60°C): δ м.д. 10,14 (уш. с, 1H); 7,70 (уш. с, 1H); 6,51 (с, 1H); 4,87-4,83 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,28 (уш. с, 2H); 2,83 (уш. с, 3H); 2,65-2,41 (м, 6H); 2,27 (т, 4H, J=7,5 Гц); 1,77 (м, 2H); 1,67-1,58 (м, 10H); 1,49-1,43 (м, 8H); 1,30-1,14 (м, 44H); 0,86 (т, 9H, J=6,7 Гц).
HS. Соединение 311: Гептадекан-9-ил-8-((3-(2-циано-3,3-диметилгуанидино)пропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат

Химическая формула: C50H97N5O4
Молекулярная масса: 832,36
[00399] Соединение 311 получали аналогично соединению 168, но используя гептадекан-9-ил-8-((3-аминопропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Бесцветное масло 350 мг, 62%. ВЭЖХ/УФ (214 нм): RT=6,04 мин. MС (ХИ): m/z (MH+) 832,7 для C50H97N5O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,62 (уш. с, 1H); 4,87-4,80 (м, 1H); 3,94 (дд, 1H, J=5,9 Гц, 10,5 Гц); 3,83 (дд, 1H, J=6,8 Гц, 10,7 Гц); 3,70-3,64 (м, 2H); 2,99 (с, 6H); 2,69-2,38 (м, 4H); 2,28 (дд, 4H, J=7,6 Гц, 15,1 Гц); 1,80-1,52 (м, 7H); 1,52-1,16 (м, 58H); 0,91-0,82 (м, 12H).
HT. Соединение 312: Гептадекан-9-ил-8-((3-(2-метоксиацетамидо)пропил)(8-((2-метил нонил)окси)-8-оксооктил)амино)октаноат
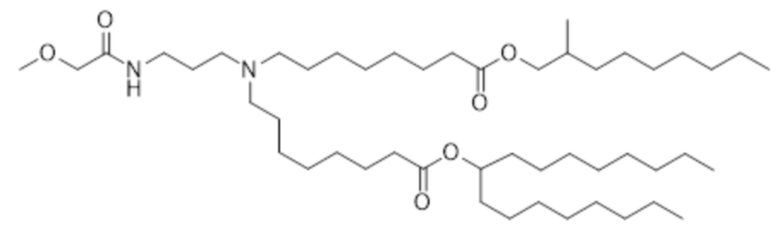
Химическая формула: C49H96N2O6
Молекулярная масса: 809,32
[00400] Соединение 312 получали аналогично соединению 178, но используя гептадекан-9-ил-8-((3-аминопропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Бесцветное масло, 300 мг, 55%. ВЭЖХ/УФ (210 нм): RT=6,02 мин. MС (ХИ): m/z (MH+) 809,7 для C49H96N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,56 (уш. с, 1H); 4,89-4,81 (м, 1H); 3,94 (дд, 1H, J=5,7 Гц, 10,4 Гц); 3,83 (дд, 1H, J=6,8 Гц, 10,7 Гц); 3,86 (с, 2H); 3,38 (с, 3H); 3,38-3,32 (м, 2H); 2,46 (м, 2H); 2,37-2,24 (м, 8H); 1,78-1,72 (м, 1H); 1,68-1,52 (м, 8H); 1,528-1,18 (м, 54H); 0,91-0,82 (м, 12H).
HU. Соединение 313: Гептадекан-9-ил-(Z)-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат
Стадия 1: (Z)-Нон-2-ен-1-ил-8-бромоктаноат
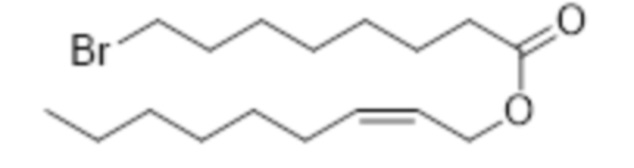
Химическая формула: C17H31BrO2
Молекулярная масса: 347,34
[00401] К раствору цис-2-нонен-1-ола (10,0 г, 70 ммоль), 8-бромоктановой кислоты (23,43 г, 105 ммоль) и DMAP (1,72 г, 14 ммоль) в дихлорметане при 0°C прибавили EDCI (20,23 г, 105 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. ТСХ показала на завершение реакции. Реакционную смесь охладили до 0°C и раствор соляной кислоты (10 мл конц. HCl, 90 мл воды, 7,5 г хлорида натрия) очень медленно прибавляли в течение 20 минут. Затем прибавили ацетонитрил (100 мл) и гексан (100 мл) прибавили, слои разделили и органический слой сушили (Na2SO4) и выпарили в вакууме с получением масла. Его растворили в гексане (100 мл) и промывали смесью ацетонитрила (100 мл) и 5% водным раствором гидрокарбоната натрия (100 мл). Слой гексана отделили и отфильтровали через диатомовую землю, фильтр-прессную лепешку промывали гексаном и фильтрат концентрировали с получением (Z)-нон-2-ен-1-ил-8-бромоктаноат (19,98 г, 82%) в виде бесцветного масла. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,65-5,59 (м, 1H); 5,53-5,49 (м, 1H); 4,61 (д, 2H, J=6,8 Гц); 3,92 (т, 2H, J=6,7 Гц); 2,44 (т, 0,5H, J =7,4 Гц, для CH2Cl); 2,29 (т, 2H, J=7,4 Гц, для CH2Br); 2,08 (дд, 2H, J=6,6 Гц, 13,7 Гц); 1,88-1,79 (м, 2H); 1,70-1,56 (м, 2H); 1,50-1,16 (м, 14H); 0,87 (т, 3H, J=6,7 Гц).
Стадия 2: Гептадекан-9-ил-(Z)-8-((3-((трет-бутоксикарбонил)амино)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат
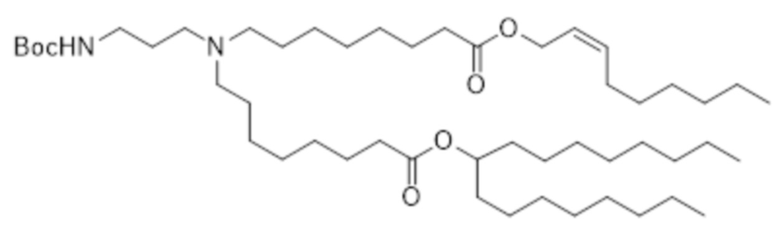
Химическая формула: C50H96N2O6
Молекулярная масса: 821,33
[00402] Раствор гептадекан-9-ил-8-((3-((трет-бутоксикарбонил)амино)пропил)амино)октаноата (6,0 г, 12 ммоль), (Z)-нон-2-ен-1-ил-8-бромоктаноата (4,49 г, 13 ммоль) и N, N-диизопропилэтиламина (2,8 мл, 16 ммоль) в этаноле (50 мл) нагревали при 70°C в течение 3 дней. Растворитель удалили под вакуумом с получением сырого продукта, который очищали с помощью хроматографии на силикагеле (0-100% EtOAc в смеси гексанов) с получением гептадекан-9-ил-(Z)-8-((3-((трет-бутоксикарбонил)амино)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноата (5,2 г, 60%) в виде светло-желтого масла. MС (ХИ): m/z (MH+) 821,7 для C50H96N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,72-5,58 (м, 2H); 5,56-5,48 (м, 1H);4,87-4,83 (м, 1H); 4,60 (д, 2H, J=6,6 Гц); 3,20-3,12 (м, 2H); 2,42 (т, 2H, J=6,3 Гц); 2,35-2,24 (м, 9H); 2,12-2,02 (м, 4H); 1,68-1,56 (м, 8H); 1,42 (с, 9H); 1,50-1,12 (м, 47H); 0,88-0,84 (м, 9H).
Стадия 3: Гептадекан-9-ил-(Z)-8-((3-аминопропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат

Химическая формула: C45H88N2O4
Молекулярная масса: 721,21
[00403] К раствору гептадекан-9-ил-(Z)-8-((3-((трет-бутоксикарбонил)амино)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноата (5,2 г, 6,33 ммоль) в дихлорметане (20 мл) при 0°C по каплям прибавили трифторуксусную кислоту (8 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь погасили прибавлением насыщенного водного раствора гидрокарбоната натрия при 0°C. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия, 0,1 N раствором гидроксида натрия, насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и растворитель удалили в вакууме с получением гептадекан-9-ил-(Z)-8-((3-аминопропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноата (4,2 г, 93%) в виде масла. MС (ХИАД): m/z (MH+) 721,6 для C45H88N2O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,68-5,58 (м, 1H); 5,54-5,46 (м, 1H); 4,89-4,82 (м, 1H); 4,60 (д, 2H, J=6,6 Гц); 2,72 (т, 2H, J=6,8 Гц); 2,44 (т, 2H, J=7,4 Гц); 2,40-2,34 (м, 4H); 2,27 (дт, 4H, J=7,5 Гц, 15,2 Гц); 2,11-2,03 (м, 2H); 1,84-1,72 (м, 4H); 1,68-1,55 (м, 6H); 1,54-1,46 (м, 6H); 1,44-1,16 (м, 44H); 0,86 (т, 9H, J=6,5 Гц).
Стадия 4: Гептадекан-9-ил-(Z)-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат
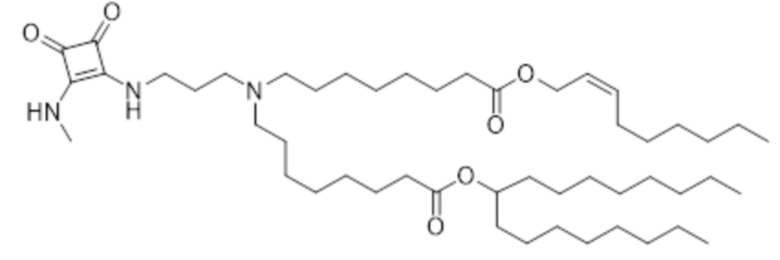
Химическая формула: C50H91N3O6
Молекулярная масса: 830,29
[00404] Соединение 313 получали аналогично соединению 182 за исключением того, что гептадекан-9-ил-(Z)-8-((3-аминопропил)(8-(нон-2-ен-1-илокси)-8-оксооктил) амино)октаноат (500 мг, 0,66 ммоль) использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат (200 мг, 29%) в виде белого воскообразного твердого вещества. ВЭЖХ/УФ (254 нм): RT=6,56 мин. MС (ХИ): m/z (MH+) 830,6 для C50H91N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,68-5,59 (м, 1H); 5,54-5,48 (м, 1H); 4,86-4,80 (м, 1H); 4,60 (д, 2H, J=6,8 Гц); 3,72-3,58 (м, 2H); 3,25 (д, 3H, J=4,9 Гц); 2,59-2,52 (м, 2H); 2,46-2,38 (м, 4H); 2,29 (дд, 4H, J=7,2 Гц, 14,6 Гц); 2,08 (дд, 2H, J=6,8 Гц, 14,0 Гц); 1,82-1,68 (м, 3H); 1,64-1,56 (м, 5H); 1,52-1,12 (м, 52H); 0,86 (т, 9H, J=6,7 Гц).
HV. Соединение 314: Гептадекан-9-ил-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(8-(((Z)-нон-2-ен-1-ил)окси)-8-оксооктил)амино)октаноат
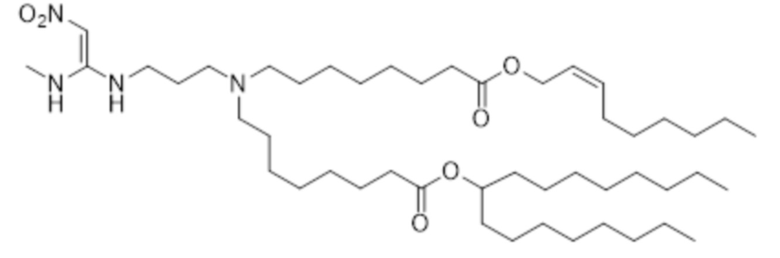
Химическая формула: C48H92N4O6
Молекулярная масса: 821,29
[00405] Соединение 314 получали аналогично соединению 170 за исключением того, что гептадекан-9-ил-(Z)-8-((3-аминопропил)(8-(нон-2-ен-1-илокси)-8-оксооктил) амино)октаноат использовали вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(8-(((Z)-нон-2-ен-1-ил)окси)-8-оксооктил)амино)октаноата (190 мг, 28%) в виде желтого масла. ВЭЖХ/УФ (254 нм): RT=6,30 мин. MС (ХИ): m/z (MH+) 821,7 для C48H92N4O6. 1H ЯМР (300 МГц, CDCl3 при 25°C): δ м.д. 10,13 (уш. с, 1H); 8,36, 8,22 (уш. с, 1H); 6,54 (с, 0,5H); 6,52 (с, 0,5H); 5,65-5,59 (м, 1H); 5,52-5,48 (м, 1H); 4,87-4,81 (м, 1H); 4,60 (д, 2H, J=6,6 Гц); 3,38-3,22 (м, 2H); 2,85 (д, 1,5H, J=5,2 Гц); 2,73-2,72 (м, 1,5H); 2,63 (м, 1H); 2,46 (м, 5H); 2,28 (дд, 4H, J=7,5 Гц, 14,9 Гц); 2,08 (дд, 2H, J=7,1 Гц, 14,0 Гц); 1,76 (м, 2H); 1,68-1,56 (м, 6H); 1,52-1,12 (м, 50H); 0,86 (т, 9H, J=6,6 Гц). 1H ЯМР (300 МГц, CDCl3 при 60°C): δ м.д. 10,15 (уш. с, 1H); 7,70 (уш. с, 1H); 6,51 (с, 1H); 5,65-5,59 (м, 1H); 5,52-5,48 (м, 1H); 4,87-4,81 (м, 1H); 4,60 (д, 2H, J=6,6 Гц); 3,27 (уш. с, 2H); 2,81 (уш. с, 3H); 2,62-2,41 (м, 6H); 2,28 (дд, 4H, J=7,5 Гц, 14,9 Гц); 2,08 (дд, 2H, J=7,1 Гц, 14,0 Гц); 1,76 (м, 2H); 1,68-1,56 (м, 6H); 1,52-1,12 (м, 50H); 0,86 (т, 9H, J=6,6 Гц).
HW. Соединение 315: Гептадекан-9-ил-8-((3-((Z)-2-циано-3,3-диметилгуанидино)пропил)(8-(((Z)-нон-2-ен-1-ил)окси)-8-оксооктил)амино)октаноат
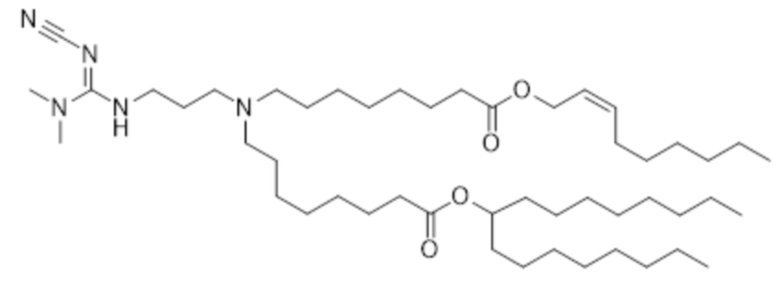
Химическая формула: C49H93N5O4
Молекулярная масса: 816,31
[00406] Соединение 315 получали аналогично соединению 168, но используя гептадекан-9-ил-(Z)-8-((3-аминопропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((Z)-2-циано-3,3-диметилгуанидино)пропил)(8-(((Z)-нон-2-ен-1-ил)окси)-8-оксооктил)амино)октаноата (150 мг, 26%) в виде бесцветного масла. ВЭЖХ/УФ (254 нм): RT=6,55 мин. MС (ХИ): m/z (MH+) 816,7 для C49H93N5O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,66 (уш. с, 1H); 5,68-5,58 (м, 1H); 5,56-5,44 (м, 1H); 4,87-4,81 (м, 1H); 4,61 (д, 2H, J=6,8 Гц); 3,72-3,64 (м, 2H); 2,98 (с, 6H); 2,59-2,54 (м, 2H); 2,44-2,38 (м, 4H); 2,28 (дд, 4H, J=7,5 Гц, 15,2 Гц); 2,08 (дд, 2H, J=7,1 Гц, 14,0 Гц); 1,68-1,58 (м, 7H); 1,52-1,42 (м, 5H); 1,38-1,12 (м, 46H); 0,88-0,84 (м, 9H).
HX. Соединение 316: Гептадекан-9-ил-(Z)-8-((3-(2-метоксиацетамидо)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат
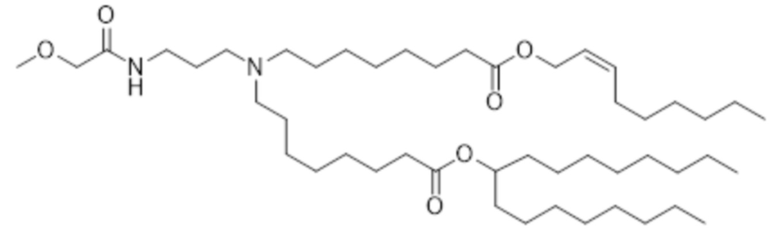
Химическая формула: C48H92N2O6
Молекулярная масса: 793,27
[00407] Соединение 316 получали аналогично соединению 178, но используя гептадекан-9-ил-(Z)-8-((3-аминопропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-(2-метоксиацетамидо)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноата (220 мг, 40%) в виде бесцветного масла. ВЭЖХ/УФ (210 нм): RT=5,73 мин. MС (ХИ): m/z (MH+) 793,7 для C48H92N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,59-7,56 (м, 1H); 5,68-5,58 (м, 1H); 5,54-5,48 (м, 1H); 4,87-4,81 (м, 1H); 4,60 (д, 2H, J=6,8 Гц); 3,86 (с, 2H); 3,37 (с, 3H); 3,37-3,31 (м, 2H); 2,46 (т, 2H, J=6,3 Гц); 2,37-2,24 (м, 8H); 2,08 (дд, 2H, J=7,1 Гц, 13,7 Гц); 1,68-1,58 (м, 5H); 1,50-1,40 (м, 8H); 1,38-1,18 (м, 45H); 0,86 (т, 9H, J=6,7 Гц).
HY. Соединение 317: Гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат

Химическая формула: C50H93N3O6
Молекулярная масса: 832,31
[00408] Соединение 317 получали аналогично соединению 182, но используя гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (180 мг, 32%) в виде белого воскообразного твердого вещества. ВЭЖХ/УФ (254 нм): RT=11,45 мин. MС (ХИ): m/z (MH+) 832,7 для C50H93N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,86-4,79 (м, 1H); 4,06 (т, 2H, J=6,8 Гц); 3,66 (уш. с, 2H); 3,26 (д, 3H, J=4,9 Гц); 2,56-2,52 (м, 2H); 2,40-2,25 (м, 8H); 1,78-1,68 (м, 2H); 1,64-1,55 (м, 8H); 1,48-1,38 (м, 8H); 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц).
HZ. Соединение 318: Гептадекан-9-ил-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат

Химическая формула: C48H94N4O6
Молекулярная масса: 823,30
[00409] Соединение 318 получали аналогично соединению 170, но используя гептадекан-9-ил-8-((3-аминопропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(6-оксо-6-(ундецилокси)гексил)амино)октаноата (270 мг, 40%) в виде желтого масла, 270 мг, 40%. ВЭЖХ/УФ (254 нм): RT=8,74 мин. MС (ХИ): m/z (MH+) 823,7 для C48H94N4O6. 1H ЯМР (300 МГц, CDCl3 при 25°C): δ м.д. 10,15 (уш. с, 1H); 8,21, 8,13 (уш. с, 1H); 6,55 (с, 0,5H); 6,53 (с, 0,5H); 4,85 (квинт., 1H, J=6,3 Гц); 4,04 (т, 2H, J=6,6 Гц); 3,32-3,23 (м, 2H); 2,85 (д, 1,5H, J=4,9 Гц); 2,74-2,72 (м, 1,5H); 2,64 (м, 1H); 2,46 (м, 5H); 2,28 (м, 4H); 1,76 (м, 2H); 1,66-1,53 (м, 6H); 1,53-1,40 (м, 8H); 1,24 (м, 48H); 0,86 (т, 9H, J=6,6 Гц). 1H ЯМР (300 МГц, CDCl3 при 50°C): δ м.д. 10,15 (уш. с, 1H); 7,79 (уш. с, 1H); 6,52 (с, 1H); 4,85 (м, 1H); 4,05 (т, 2H, J=6,6 Гц); 3,29 (м, 2H); 2,84 (уш. с, 3H); 2,64-2,44 (м, 6H); 2,28 (м, 4H); 1,76 (м, 2H); 1,61 (м, 6H); 1,53-1,40 (м, 8H); 1,24 (м, 48H); 0,86 (м, 9H).
IA. Соединение 319: Гептадекан-9-ил-(Z)-8-((3-(3,3-диметилтиоуреидо)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат
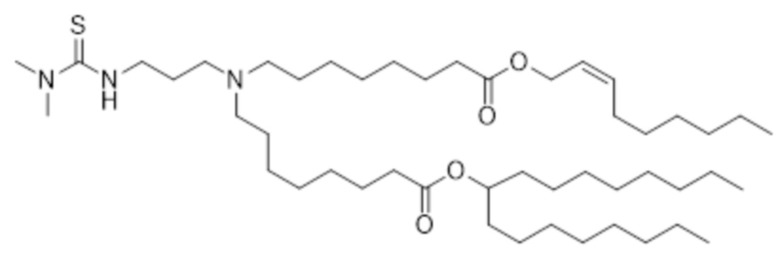
Химическая формула: C48H93N3O4S
Молекулярная масса: 808,35
[00410] Соединение 319 получали аналогично соединению 111, но используя гептадекан-9-ил-(Z)-8-((3-аминопропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. После обработки реакционной смеси водой остаток очищали с помощью хроматографии на силикагеле (0-50% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-(Z)-8-((3-(3,3-диметилтиоуреидо)пропил)(8-(нон-2-ен-1-илокси)-8-оксооктил)амино)октаноата (110 мг, 20%) в виде желтого масла. ВЭЖХ/УФ (254 нм): RT=6,67 мин. MС (ХИ): m/z (MH+) 808,6 для C48H93N3O4S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,72 (уш. с, 1H); 5,64-5,58 (м, 1H); 5,53-5,48 (м, 1H); 4,86-4,80 (м, 1H); 4,60 (д, 2H, J=6,8 Гц); 3,78-3,77 (м, 2H); 3,26 (с, 6H); 2,91-2,64 (м, 4H); 2,27 (дд, 4H, J=7,6 Гц, 15,3 Гц); 2,08 (дд, 4H, J=6,7 Гц, 13,8 Гц); 1,68-1,42 (м, 12H); 1,38-1,12 (м, 46H); 0,88-0,84 (м, 9H).
IB. Соединение 320: Гептадекан-9-ил-8-((3-((1-(метиламино)-2-нитровинил)амино)пропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат
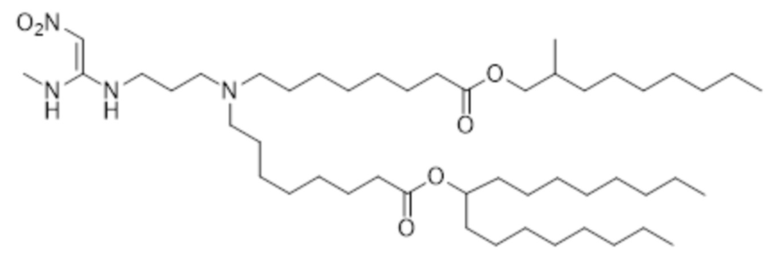
Химическая формула: C49H96N4O6
Молекулярная масса: 837,33
[00411] Соединение 320 получали аналогично соединению 170, но используя гептадекан-9-ил-8-((3-аминопропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Желтое масло, 380 мг, 56%. ВЭЖХ/УФ (254 нм): RT=6,85 мин. MС (ХИ): m/z (MH+) 837,7 для C49H96N4O6. 1H ЯМР (300 МГц, CDCl3 при 25°C): δ м.д. 10,13 (уш. с, 1H); 8,36 (с, 0,5H); 8,22 (с, 0,5H); 6,55 (с, 0,5H); 6,53 (с, 0,5H); 4,87-4,81 (м, 1H); 3,94 (дд, 1H, J=5,7 Гц, 10,4 Гц); 3,83 (дд, 1H, J=6,8 Гц, 10,7 Гц); 3,38-3,23 (м, 2H); 2,85 (д, 1,5H, J=5,1 Гц); 2,72 (д, 1,5H, J=4,1 Гц); 2,63 (м, 1H); 2,46 (м, 5H); 2,28 (дд, 4H, J=7,4 Гц, 15,1 Гц); 1,76 (м, 3H); 1,68-1,58 (м, 6H); 1,52-1,12 (м, 54H); 0,91-0,84 (м, 12H). 1H ЯМР (300 МГц, CDCl3 при 50°C): δ м.д. 10,15 (уш. с, 1H); 7,89 (уш. с, 1H); 6,51 (с, 1H); 4,87-4,81 (м, 1H); 3,94 (дд, 1H, J=5,7 Гц, 10,4 Гц); 3,83 (дд, 1H, J=6,8 Гц, 10,7 Гц); 3,25 (уш. с, 2H); 2,87-2,72 (м, 3H); 2,63 (м, 1H); 2,46 (м, 5H); 2,28 (дд, 4H, J=7,4 Гц, 15,1 Гц); 1,76 (м, 3H); 1,68-1,58 (м, 6H); 1,52-1,12 (м, 54H); 0,91-0,84 (м, 12H).
IC. Соединение 321: Гептадекан-9-ил-8-((3-((2-(метиламино)-3,4-диоксоциклобут-1-ен-1-ил) амино)пропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат
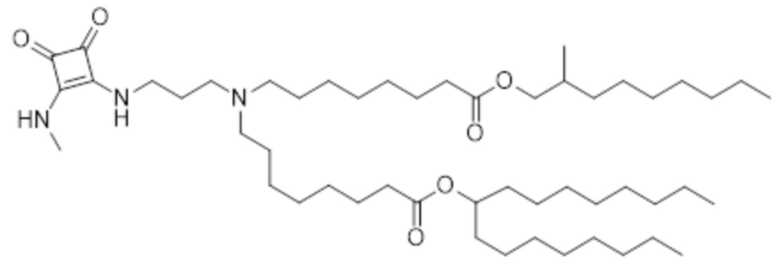
Химическая формула: C51H95N3O6
Молекулярная масса: 846,34
[00412] Соединение 321 получали аналогично соединению 182, но используя гептадекан-9-ил-8-((3-аминопропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Белое воскообразное твердое вещество, 240 мг, 41%. ВЭЖХ/УФ (ДСИО): RT=7,10 мин. MС (ХИ): m/z (MH+) 846,7 для C51H95N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,86-4,80 (м, 1H); 3,93 (дд, 1H, J=6,0 Гц, 10,7 Гц); 3,83 (дд, 1H, J=6,8 Гц, 10,7 Гц); 3,68-3,58 (м, 2H); 3,25 (д, 3H, J=4,9 Гц); 2,55-2,52 (м, 2H); 2,42-2,37 (м, 4H); 2,29 (дд, 4H, J=7,7 Гц, 15,1 Гц); 1,80-1,68 (м, 3H); 1,66-1,56 (м, 10H); 1,52-1,38 (м, 9H); 1,32-1,12 (м, 42H); 0,91-0,82 (м, 12H).
ID. Соединение 322: Гептадекан-9-ил-8-((3-(3,3-диметилтиоуреидо)пропил)(8-((2-метил нонил)окси)-8-оксооктил)амино)октаноат
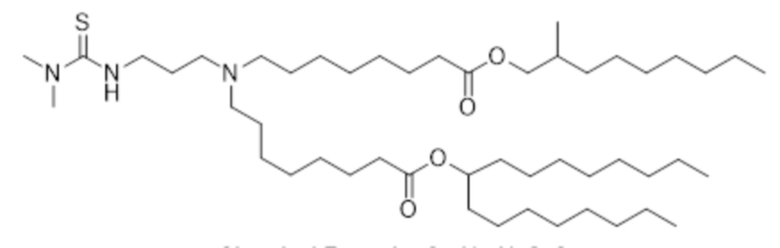
Химическая формула: C49H97N3O4S
Молекулярная масса: 824,39
[00413] Соединение 322 получали аналогично соединению 111, но используя гептадекан-9-ил-8-((3-аминопропил)(8-((2-метилнонил)окси)-8-оксооктил)амино)октаноат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Желтое масло, 150 мг, 27%. ВЭЖХ/УФ (254 нм): RT=7,27 мин. MС (ХИ): m/z (MH+) 824,7 для C49H97N3O4S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,60 (уш. с, 1H); 4,87-4,82 (м, 1H); 3,94 (дд, 1H, J=5,7 Гц, 10,7 Гц); 3,86-3,80 (м, 3H); 3,27 (с, 6H); 3,04-2,74 (м, 4H); 2,28 (дд, 4H, J=7,6 Гц, 15,1 Гц); 1,80-1,72 (м, 3H); 1,68-1,42 (м, 12H); 1,38-1,18 (м, 50H); 0,91-0,82 (м, 12H).
IE. Соединение 323: 7-((3-(2-Mетоксиацетамидо)пропил)(8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат
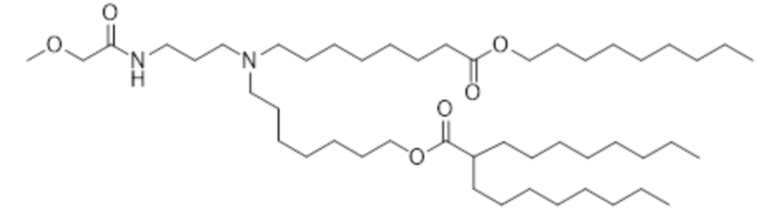
Химическая формула: C48H94N2O6
Молекулярная масса: 795,29
[00414] Соединение 323 получали аналогично соединению 178, но используя 7-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)гептил-2-октилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Желтое масло, 220 мг, 40%. ВЭЖХ/УФ (214 нм): RT=6,00 мин. MС (ХИ): m/z (MH+) 795,7 для C48H94N2O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,52 (м, 1H); 4,05-4,02 (м, 4H); 3,86 (с, 2H); 3,38 (с, 3H); 3,38-3,32 (м, 2H); 2,52-2,25 (м, 9H); 1,72-1,53 (м, 12H); 1,44-1,12 (м, 52H); 0,86 (т, 9H, J=6,7 Гц).
IF. Соединение 324: 7-((3-(2-Циано-3,3-диметилгуанидино)пропил)(8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат
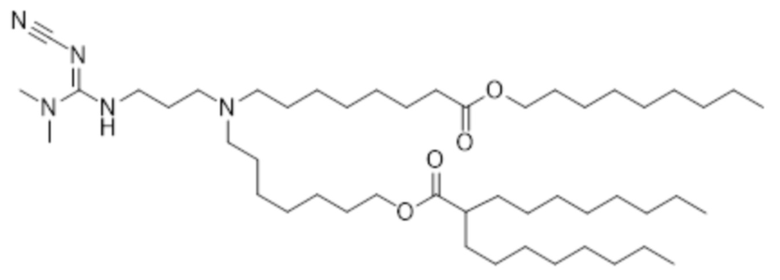
Химическая формула: C49H95N5O4
Молекулярная масса: 818,33
[00415] Соединение 324 получали аналогично соединению 168, но используя 7-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)гептил-2-октилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Бесцветное масло, 370 мг, 65%. ВЭЖХ/УФ (214 нм): RT=6,04 мин. MС (ХИ): m/z (MH+) 818,7 для C49H95N5O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,64 (м, 1H); 4,06-4,02 (м, 4H); 3,68-3,62 (м, 2H); 2,98 (с, 6H); 2,59-2,56 (м, 2H); 2,44-2,39 (м, 4H); 2,32-2,26 (м, 3H); 1,72-1,53 (м, 12H); 1,44-1,12 (м, 52H); 0,86 (т, 9H, J=6,7 Гц).
IG. Соединение 325: 7-((3-((1-(Метиламино)-2-нитровинил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат
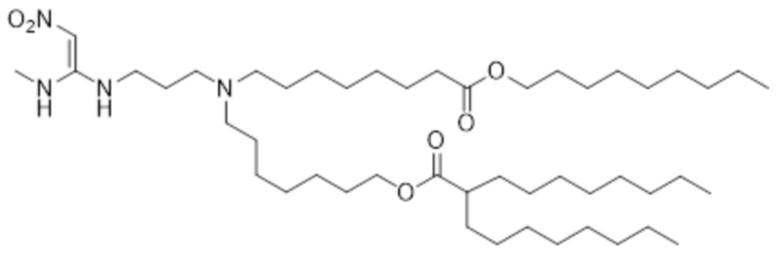
Химическая формула: C48H94N4O6
Молекулярная масса: 823,30
[00416] Соединение 325 получали аналогично соединению 170, но используя 7-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)гептил-2-октилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Желтое масло, 355 мг, 52%. ВЭЖХ/УФ (214 нм): RT=5,76 мин. MС (ХИ): m/z (MH+) 823,7 для C48H94N4O6. 1H ЯМР (300 МГц, CDCl3 при 25°C): δ м.д. 10,15 (уш. с, 1H); 8,37-8,24 (м, 1H); 6,55 (с, 0,5H); 6,53 (с, 0,5H); 4,06-4,04 (м, 4H); 3,34-3,24 (м, 2H); 2,90-2,85 (м, 1,5H); 2,74-2,73 (м, 1,5H); 2,64 (м, 1H); 2,47 (уш. с, 4H); 2,34-2,26 (м, 3H); 1,77 (м, 2H); 1,68-1,53 (м, 10H); 1,44-1,12 (м, 53H); 0,86 (т, 9H, J=6,6 Гц). 1H ЯМР (300 МГц, CDCl3 при 50°C): δ м.д. 10,15 (уш. с, 1H); 7,89 (уш. с, 1H); 6,52 (с, 1H); 4,06-4,04 (м, 4H); 3,29 (уш. с, 2H); 2,87 (м, 3H); 2,64-2,40 (м, 6H); 2,34-2,26 (м, 3H); 1,79 (м, 2H); 1,64-1,54 (м, 10H); 1,44-1,12 (м, 52H); 0,86 (т, 9H, J=6,6 Гц).
IH. Соединение 326: 7-((3-((2-(Метиламино)-3,4-диоксоциклобут-1-ен-1-ил)амино)пропил)(8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат

Химическая формула: C50H93N3O6
Молекулярная масса: 832,31
[00417] Соединение 326 получали аналогично соединению 182, но используя 7-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)гептил-2-октилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Белое воскообразное твердое вещество, 330 мг, 57%. ВЭЖХ/УФ (254 нм): RT=7,01 мин. MС (ХИ): m/z (MH+) 832,6 для C50H93N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 6,90 (уш. с, 1H); 4,05-4,01 (м, 4H); 3,63 (уш. с, 2H); 3,25 (д, 3H, J=4,9 Гц); 2,53 (т, 2H, J=5,6 Гц); 2,40 (т, 4H, J=7,4 Гц); 2,33-2,26 (м, 3H); 1,74-1,71 (м, 2H); 1,68-1,52 (м,11H); 1,48-1,12 (м, 52H); 0,86 (т, 9H, J=6,7 Гц).
II. Соединение 327: 7-((3-(3,3-Диметилтиоуреидо)пропил)(8-(нонилокси)-8-оксооктил)амино)гептил 2-октилдеканоат
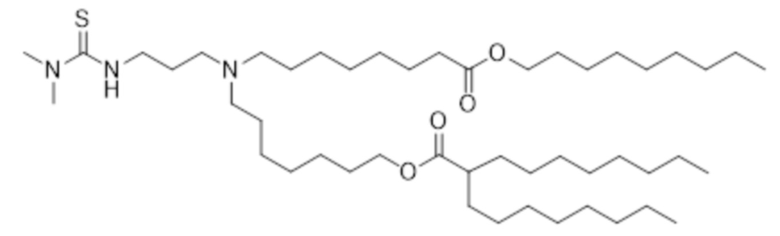
Химическая формула: C48H95N3O4S
Молекулярная масса: 810,37
[00418] Соединение 327 получали аналогично соединению 111, но используя 7-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)гептил-2-октилдеканоат вместо гептадекан-9-ил-8-((3-аминопропил)(8-(нонилокси)-8-оксооктил)амино)октаноата. Желтое масло, 200 мг, 36%. ВЭЖХ/УФ (254 нм): RT=6,95 мин. MС (ХИ): m/z (MH+) 810,6 для C48H95N3O4S. 1H ЯМР (300 МГц, CDCl3): δ м.д. 8,08 (уш. с, 1H); 4,06-4,02 (м, 4H); 3,72 (уш. с, 2H); 3,23 (с, 6H); 2,72-2,38 (м, 4H); 2,34-2,25 (м, 3H); 1,71-1,55 (м, 12H); 1,44-1,12 (м, 54H); 0,86 (т, 9H, J=6,7 Гц).
IJ. Соединение 328: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-гидроксипропил)амино)октаноат
Стадия 1: додекан-4-ил-8-((3-гидроксипропил)амино)октаноат
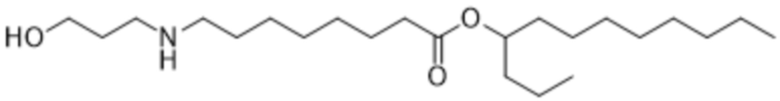
Химическая формула: C23H47NO3
Молекулярная масса: 385,63
[00419] К раствору додекан-4-ил-8-бромоктаноата (2,5 г, 6,4 ммоль) в этаноле (100 мл) прибавили пропаноламин (9,8 мл, 130 ммоль) и реакционную смесь оставили перемешиваться при 50°C в течение ночи. Раствор снова нагрели до комнатной температуры и концентрировали в вакууме. Сырой материал перенесли в ДХМ и дважды промывали 5% NaHCO3, сушили над безводным Na2SO4, отфильтровали и концентрировали в вакууме. Очистка с помощью хроматографии на силикагеле (0-100% (ДХМ 20% MeOH 1% NH4OH) в ДХМ) позволила получить додекан-4-ил-8-((3-гидроксипропил)амино)октаноат в виде прозрачного бесцветного масла (2,08 г, 84,5%). СВЭЖХ/ДСИО: RT=1,58 мин. MС (ИЭР): m/z (MH+) 386,42 для C23H47NO3. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 1H); 3,83 (т, 2H); 3,31 (br, 1H); 2,90 (т, 2H); 2,62 (т, 2H); 2,29 (т, 2H); 1,85-1,05 (уш. м, 30H); 0,91 (м, 6H) (гидроксильный протон не наблюдали).
Стадия 2: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-гидроксипропил)амино)октаноат
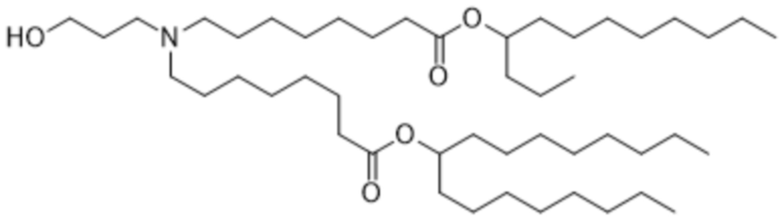
Химическая формула: C48H95NO5
Молекулярная масса: 766,29
[00420] Додекан-4-ил-8-[(3-гидроксипропил)амино]октаноат (2,08 г, 5,39 ммоль), гептадекан-9-ил-8-бромоктаноат (2,61 г, 5,66 ммоль), карбонат калия (1,49 г, 10,8 ммоль) и иодид калия ( 179 мг, 1,08 ммоль) суспендировали в MeCN (60 мл) и смесь оставили перемешиваться при 82oC в течение 12 часов. Реакционную смесь оставили охлаждаться до комнатной температуры, отфильтровали через слой целита и концентрировали в вакууме. Очистка с помощью хроматографии на силикагеле (0-50% (ДХМ 20% MeOH 1% NH4OH) в ДХМ) позволила получить додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-гидроксипропил)амино)октаноат в виде прозрачного желтоватого масла (3,26 г, 78,9%). СВЭЖХ/ДСИО: RT=3,53 мин. MС (ИЭР): m/z (MH+) 766,97 для C48H95NO5. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 3,82 (т, 2H); 2,76 (т, 2H); 2,54 (т, 4H); 2,30 (т, 4H); 1,85-1,05 (уш. м, 68H); 0,90 (м, 12H) (гидроксильный протон не наблюдали).
IK. Соединение 329: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(1-гидроксипропан-2-ил)амино)октаноат
Стадия 1: Додекан-4-ил-8-((1-гидроксипропан-2-ил)амино)октаноат
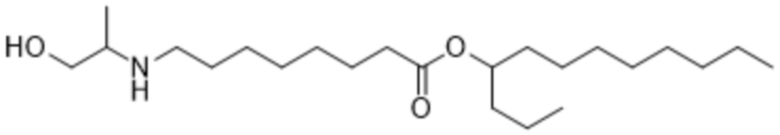
Химическая формула: C23H47NO3
Молекулярная масса: 385,63
[00421] Способом аналогичным стадии 1 для соединения 328 синтезировали додекан-4-ил-8-((1-гидроксипропан-2-ил)амино)октаноат из додекан-4-ил-8-бромоктаноата (500 мг, 1,28 ммоль) и 2-аминопропанола (2,00 мл, 25,5 ммоль) в этаноле (15 мл). Выход (343 мг, 69,6%). СВЭЖХ/ДСИО: RT=1,66 мин. MС (ИЭР): m/z (MH+) 386,50 для C23H47NO3. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,91 (м, 1H); 3,64-3,16 (уш. м, 2H); 2,76 (уш. м, 2H); 2,53 (уш. м, 1H); 2,30 (т, 2H); 2,05-1,15 (уш. м, 29H); 1,06 (д, 3H); 0,91 (м, 6H) (гидроксильный протон не наблюдали).
Стадия 2: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(1-гидроксипропан-2-ил)амино)октаноат

Химическая формула: C48H95NO5
Молекулярная масса: 766,29
[00422] Способом аналогичным стадии 2 для соединения 328 синтезировали додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(1-гидроксипропан-2-ил)амино)октаноат из додекан-4-ил-8-[(1-гидроксипропан-2-ил)амино]октаноата (343 мг, 0,889 ммоль), гептадекан-9-ил-8-бромоктаноата (431 мг, 0,934 ммоль), карбоната калия (246 мг, 1,78 ммоль) и иодида калия (30 мг, 0,18 ммоль) в MeCN (12 мл). Выход (395 мг, 58,0%). СВЭЖХ/ДСИО: RT=3,54 мин. MС (ИЭР): m/z (MH+) 766,97 для C48H95NO5. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 3,60-2,10 (уш. м, 11H); 1,81-1,05 (уш. м, 66H); 0,90 (м, 15H) (гидроксильный протон не наблюдали).
IL. Соединение 330: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-(метилсульфонамидо)пропил)амино)октаноат
Стадия 1: Додекан-4-ил-8-((3-хлорпропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)октаноат

Химическая формула: C48H94ClNO4
Молекулярная масса: 784,73
[00423] К 0°C раствору додекан-4-ил-8-{[8-(гептадекан-9-илокси)-8-оксооктил](3-гидроксипропил)амино}октаноата (3,16 г, 4,12 ммоль) и триэтиламина (750 мкл, 5,4 ммоль) в ДХМ (50 мл) прибавили раствор метансульфонилхлорида (400 мкл, 5,2 ммоль) в ДХМ (4 мл) и реакционной смеси дали вернуться к комнатной температуре и перемешивали в течение 4 часов. Реакционную смесь погасили водой и экстрагировали x3 ДХМ. Объединенные органические фазы промывали 5% NaHCO3, насыщенным водным раствором хлорида натрия, сушили над безводным Na2SO4, отфильтровали и концентрировали в вакууме с получением прозрачного оранжевого масла. Материал использовали без дополнительной очистки (3,15 г, 97,3%). СВЭЖХ/ДСИО: RT=3,50 мин. MС (ИЭР): m/z (MH+) 784,93 для C48H94ClNO4. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 4,55-4,20 (уш. м, 2H); 3,70-3,40 (уш. м, 2H); 3,15-2,15 (уш. м, 8H); 2,00-1,05 (уш. м, 68H); 0,90 (м, 12H).
Стадия 2: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-(метилсульфонамидо)пропил)амино)октаноат
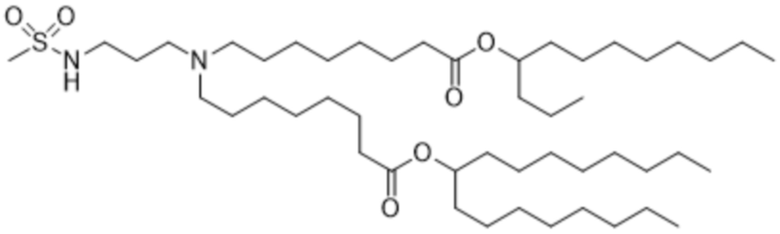
Химическая формула: C49H98N2O6S
Молекулярная масса: 843,39
[00424] К раствору додекан-4-ил-8-[(3-хлорпропил)[8-(гептадекан-9-илокси)-8-оксооктил]амино]октаноата (300 мг, 0,382 ммоль) и метансульфонамида (364 мг, 3,82 ммоль) в ДМФА (7 мл) прибавили карбонат цезия (186 мг, 0,573 ммоль) и реакционную смесь оставили перемешиваться при 60°C в течение 12 часов. Реакционную смесь оставили охлаждаться до комнатной температуры, разбавили 50% NaHCO3 и дважды экстрагировали ДХМ. Объединенные органические фазы промывали водой, сушили над безводным Na2SO4, отфильтровали и концентрировали в вакууме. Очистка с помощью хроматографии на силикагеле (0-50% (ДХМ 20% MeOH 1% NH4OH) в ДХМ) позволила получить додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-(метилсульфонамидо)пропил)амино)октаноат (79 мг, 25%). СВЭЖХ/ДСИО: RT=3,44 мин. MС (ИЭР): m/z (MH+) 844,06 для C49H98N2O6S. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 3,26 (т, 2H); 2,92 (с, 3H); 2,68-2,20 (уш. м, 10H); 1,85-1,05 (уш. м, 68H); 0,90 (м, 12H) (сульфонамидный протон не наблюдали).
IM. Соединение 331: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-(N-метилметилсульфонамидо)пропил)амино)октаноат

Химическая формула: C50H100N2O6S
Молекулярная масса: 857,42
[00425] Способом аналогичным стадии 2 для соединения 330 синтезировали додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-(N-метилметилсульфонамидо)пропил)амино)октаноат из додекан-4-ил-8-[(3-хлорпропил)[8-(гептадекан-9-илокси)-8-оксооктил]амино]октаноата (300 мг, 0,382 ммоль), N-метилметанeсульфонамида (83 мг, 0,77 ммоль) и карбоната цезия (186 мг, 0,573 ммоль) в ДМФА (7мл). Выход (213 мг, 65,0%). СВЭЖХ/ДСИО: RT=3,45 мин. MС (ИЭР): m/z (MH+) 858,00 для C50H100N2O6S. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 3,18 (т, 2H); 2,87 (с, 3H); 2,81 (с, 3H); 2,58-2,22 (уш. м, 10H); 1,80-1,05 (уш. м, 68H); 0,90 (м, 12H).
IN. Соединение 332: Додекан-4-ил-8-((3-ацетамидопропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)октаноат
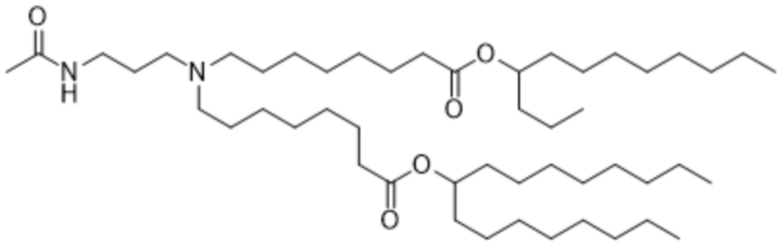
Химическая формула: C50H98N2O5
Молекулярная масса: 807,34
[00426] Способом аналогичным стадии 2 для соединения 330 синтезировали додекан-4-ил-8-((3-ацетамидопропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)октаноат из додекан-4-ил-8-[(3-хлорпропил)[8-(гептадекан-9-илокси)-8-оксооктил]амино]октаноата (300 мг, 0,382 ммоль), ацетамида (226 мг, 3,82 ммоль) и карбоната цезия (125 мг, 0,382 ммоль) в ДМФА (7 мл). Выход (74 мг, 24%). СВЭЖХ/ДСИО: RT=3,47 мин. MС (ИЭР): m/z (MH+) 807,98 для C50H98N2O5. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 3,34 (м, 2H); 2,64-2,22 (уш. м, 10H); 1,95 (с, 3H); 1,80-1,10 (уш. м, 68H); 0,90 (м, 12H) (ацетамидный протон не наблюдали).
IO. Соединение 333: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-(3-метилтиоуреидо)пропил)амино)октаноат
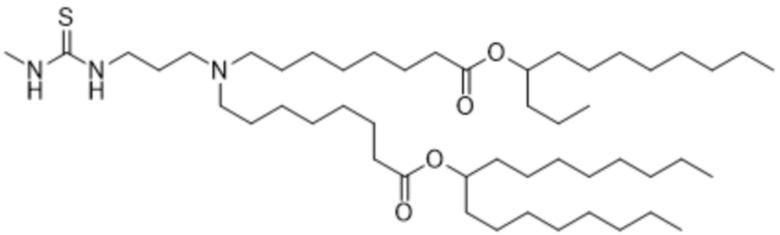
Химическая формула: C50H99N3O4S
Молекулярная масса: 838,42
[00427] Способом аналогичным стадии 2 для соединения 330 синтезировали додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(3-(3-метилтиоуреидо)пропил)амино)октаноат из додекан-4-ил-8-[(3-хлорпропил)[8-(гептадекан-9-илокси)-8-оксооктил]амино]октаноата (300 мг, 0,382 ммоль), N-метилтиомочевины (345 мг, 3,82 ммоль) и карбоната цезия (187 мг, 0,573 ммоль) в ДМФА (7 мл). Выход (29 мг, 9,0%). 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 3,04 (т, 2H); 2,88 (с, 3H); 2,60-2,20 (уш. м, 10H); 1,90-1,05 (уш. м, 70H); 0,90 (м, 12H).
IP. Соединение 334: Додекан-4-ил-8-((2,3-дигидроксипропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)октаноат
Стадия 1: Додекан-4-ил-8-((2,3-дигидроксипропил)амино)октаноат
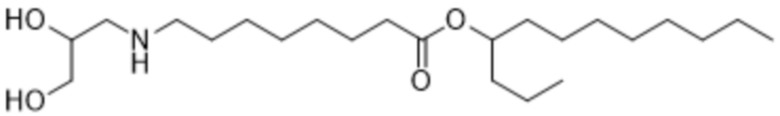
Химическая формула: C23H47NO4
Молекулярная масса: 401,63
[00428] Способом аналогичным стадии 1 для соединения 328 синтезировали додекан-4-ил-8-((2,3-дигидроксипропил)амино)октаноат из додекан-4-ил-8-бромоктаноата (500 мг, 1,28 ммоль) и 3-аминопропан-1,2-диoла (2,33 г, 1,97 ммоль) в этаноле (15 мл). Выход (359 мг, 70,0%). СВЭЖХ/ДСИО: RT=1,49 мин. MС (ИЭР): m/z (MH+) 402,49 для C23H47NO4. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 1H); 3,76 (м, 2H); 3,65 (м, 1H); 2,96-2,52 (уш. м, 7H); 2,30 (т, 2H); 1,75-1,10 (уш. м, 28H); 0,90 (м, 6H).
Стадия 2: Додекан-4-ил-8-((2,3-дигидроксипропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)октаноат
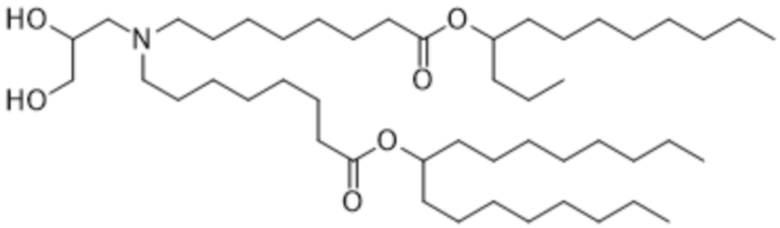
Химическая формула: C48H95NO6
Молекулярная масса: 782,29
[00429] Способом аналогичным стадии 2 для соединения 328 синтезировали додекан-4-ил-8-((2,3-дигидроксипропил)(8-(гептадекан-9-илокси)-8-оксооктил)амино)октаноат из додекан-4-ил-8-[(2,3-дигидроксипропил)амино]октаноата (359 мг, 0,894 ммоль), гептадекан-9-ил-8-бромоктаноата (454 мг, 0,983 ммоль), карбоната калия (247 мг, 1,79 ммоль) и иодида калия (30 мг, 0,18 ммоль) в MeCN (10 мл). Выход (412 мг, 58,9%). СВЭЖХ/ДСИО: RT=3,39 мин. MС (ИЭР): m/z (MH+) 782,97 для C48H95NO6. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 3,77 (м, 2H); 3,51 (м, 1H); 2,74-2,38 (уш. м, 6H); 2,30 (т, 4H); 1,75-1,10 (уш. м, 66H); 0,90 (м, 12H) (гидроксильные протоны не наблюдали).
IQ. Соединение 335: Гептадекан-9-ил-8-((2-((2-аминоэтил)амино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
Стадия 1: трет-Бутил-(2-((трет-бутоксикарбонил)амино)этил)(2-гидроксиэтил) карбамат (J. Med. Chem., 2003, 46(26), 5712-5724)
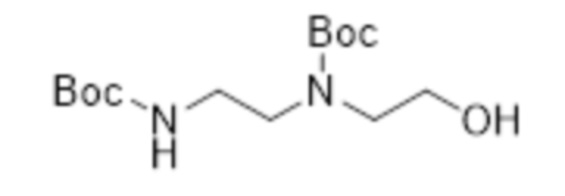
Химическая формула: C14H28N2O5
Молекулярная масса: 304,39
[00430] К раствору 2-((2-аминоэтил)амино)этанола (2,0 г, 20 ммоль) в тетрагидрофуране (40 мл) при 0°C прибавили раствор ди-трет-бутилдикарбоната (9,2 г, 40 ммоль) в тетрагидрофуране (10 мл) и реакционную смесь перемешивали в течение ночи при комнатной температуре. Растворитель удалили и остаток растворили в этилацетате. Раствор промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и растворитель удалили в вакууме для получения сырого продукта, который очищали с помощью хроматографии на силикагеле (0-40% EtOAc в смеси гексанов) с получением трет-бутил-(2-((трет-бутоксикарбонил)амино)этил)(2-гидроксиэтил)карбамата (3,8 г, 65%). 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,03-4,88 (м, 1H); 3,71 (уш. с, 2H); 3,34-3,11 (м, 7H); 1,45 (с, 9H); 1,41 (с, 9H).
Стадия 2: трет-Бутил-(2-((трет-бутоксикарбонил)амино)этил)(2-(1,3-диоксоизоиндолин-2-ил)этил)карбамат (J. Med. Chem., 2003, 46(26), 5712-5724)
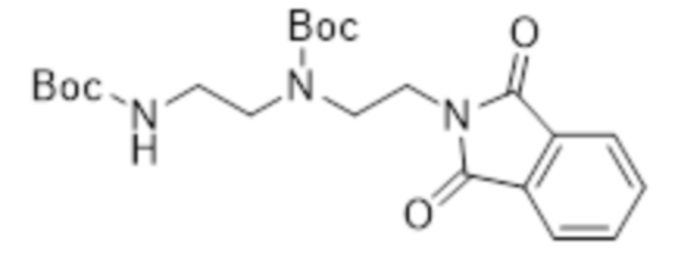
Химическая формула: C22H31N3O6
Молекулярная масса: 433,51
[00431] К раствору трет-бутил-(2-((трет-бутоксикарбонил)амино)этил)(2-гидроксиэтил)карбамат (2,3 г, 7,56 ммоль), фталимида (1,21 г, 8,24 ммоль) и трифенилфосфина (2,16 г, 8,24 ммоль) в тетрагидрофуране (50 мл) при 0°C по каплям прибавили диизопропилазодикарбоксилат (DIAD) (1,62 мл, 8,24 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение трех дней. Растворитель удалили для получения сырого продукта, который очищали с помощью хроматографии на силикагеле (0-50% EtOAc в смеси гексанов) с получением трет-бутил-(2-((трет-бутоксикарбонил)амино)этил)(2-(1,3-диоксоизоиндолин-2-ил)этил)карбамата (2,75 г, 84%) в виде пенистого белого твердого вещества. 1H ЯМР (300 МГц, CDCl3): δ м.д. 7,82 (м, 2H); 7,72-7,69 (м, 2H); 5,16 (уш. с, 1H); 3,83-3,79 (м, 2H); 3,50-3,49 (м, 2H); 3,33-3,28 (м, 4H); 1,40 (с, 9H); 1,21 (с, 9H).
Стадия 3: трет-Бутил-(2-аминоэтил)(2-((трет-бутоксикарбонил)амино)этил)карбамат (J. Med. Chem., 2003, 46(26), 5712-5724)

Химическая формула: C14H29N3O4
Молекулярная масса: 303,40
[00432] Гидразин моногидрат (0,7 мл, 12,69 ммоль) прибавили к раствору трет-бутил-(2-((трет-бутоксикарбонил)амино)этил)(2-(1,3-диоксоизоиндолин-2-ил)этил)карбамата (2,75 г, 6,35 ммоль) в метаноле (50 мл) и реакционную смесь перемешивали при кипячении в течение 18 часов. Ее оставили охлаждаться до комн. темп., смесь отфильтровали через фильтровальную воронку из спеченного стекла, фильтр-прессную лепешку промывали метанолом и фильтрат концентрировали для получения сырого продукта, который очищали с помощью хроматографии на силикагеле (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением трет-бутил-(2-аминоэтил)(2-((трет-бутоксикарбонил)амино)этил)карбамата (1,6 г, 83%). 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,50-5,20 (м, 1H); 3,29-3,24 (м, 6H); 2,84-2,82 (м, 2H); 1,44 (с, 9H); 1,41 (с, 9H) (протоны первичной аминогруппы не наблюдали).
Стадия 4: Гептадекан-9-ил-8-(трет-бутоксикарбонил)-2,2-диметил-4-оксо-3-окса-5,8,11-триазанонадекaн-19-оат
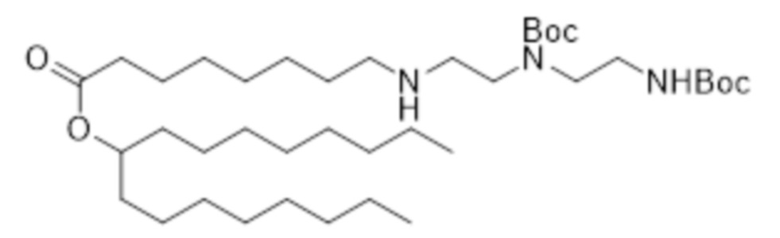
Химическая формула: C39H77N3O6
Молекулярная масса: 684,06
[00433] Раствор гептадекан-9-ил-8-бромоктаноата (0,97 г, 2,11 ммоль) и трет-бутил-(2-аминоэтил)(2-((трет-бутоксикарбонил)амино)этил)карбамата (1,6 г, 5,27 ммоль) в этаноле (20 мл) нагревали при 65°C в течение 18 часов. Растворитель удалили под вакуумом и сырой продукт очищали с помощью хроматографии на силикагеле (0-100% EtOAc в смеси гексанов, затем (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением гептадекан-9-ил-8-(трет-бутоксикарбонил)-2,2-диметил-4-оксо-3-окса-5,8,11-триазанонадекан-19-оата (670 мг, 50%) в виде масла. MС (ИЭР): m/z (MH+) 684,5 для C39H77N3O6. 1H ЯМР (300 МГц, CDCl3): δ м.д. 5,46-5,26 (уш. с, 1H); 4,88-4,82 (м, 1H); 3,59 (уш. с, 2H); 3,42-3,28 (м, 4H); 3,10-2,70 (м, 3H); 2,25 (т, 2H, J=7,5 Гц); 1,78-1,57 (м, 4H); 1,45 (с, 9H); 1,41 (с, 9H); 1,41-1,27 (м, 4H); 1,26-1,22 (м, 32H); 0,86 (т, 6H, J=6,7 Гц).
Стадия 5: Гептадекан-9-ил-8-(трет-бутоксикарбонил)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,8,11-триазанонадекан-19-оат

Химическая формула: C56H109N3O8
Молекулярная масса: 952,50
[00434] К раствору гептадекан-9-ил-8-(трет-бутоксикарбонил)-2,2-диметил-4-оксо-3-окса-5,8,11-триазанонадекан-19-оата (670 мг, 0,98 ммоль) в циклопентилметиловом эфире (10 мл) прибавили раствор нонил-8-бромоктаноата (358 мг, 1,029 ммоль) в ацетонитриле (10 мл) с последующим прибавлением карбоната калия (546 мг, 3,92 ммоль) и иодида калия (179 мг, 1,07 ммоль). Реакционную смесь нагревали до 90°C в течение 2 дней. Ее оставили охлаждаться до комн. темп., отфильтровали через диатомовую землю, фильтр-прессную лепешку интенсивно промывали этилацетатом и фильтрат концентрировали с получением сырого продукта, который очищали с помощью хроматографии на силикагеле (от 0 до 100% EtOAc в смеси гексанов) с получением гептадекан-9-ил-8-(трет-бутоксикарбонил)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,8,11-триазанонадекан-19-оата (560 мг, 60%). MС (ИЭР): m/z (MH+) 952,8 для C56H109N3O8. 1H ЯМР (300 МГц, CDCl3): δ м.д. 6,65 (уш. с, 0,5H); 5,70 (уш. с, 0,5H); 4,88-4,82 (м, 1H); 4,04 (т, 2H, J=6,7 Гц); 3,32-3,12 (м, 6H); 2,68-2,48 (м, 2H); 2,44-2,34 (м, 4H); 2,29-2,22 (м, 4H); 1,68-1,54 (м, 8H); 1,52-1,38 (м, 10H); 1,44 (с, 18H); 1,38-1,12 (м, 44H); 0,86 (т, 9H, J=6,8 Гц).
Стадия 6: Гептадекан-9-ил-8-((2-((2-аминоэтил)амино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноат
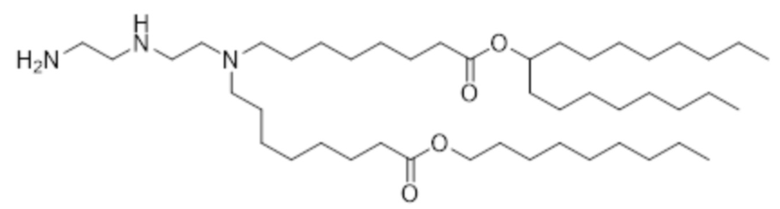
Химическая формула: C46H93N3O4
Молекулярная масса: 752,27
[00435] К раствору гептадекан-9-ил-8-(трет-бутоксикарбонил)-2,2-диметил-11-(8-(нонилокси)-8-оксооктил)-4-оксо-3-окса-5,8,11-триазанонадекан-19-оата (560 мг, 0,59 ммоль) в дихлорметане (10 мл) при 0°C прибавили трифторуксусную кислоту (3 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь погасили насыщенным водным раствором гидрокарбоната натрия. Органический слой промывали 1 N раствором гидроксида натрия, насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и растворитель удалили в вакууме для получения сырого продукта, который очищали с помощью хроматографии на силикагеле (метанол, содержащий 4% аммиака 0-100% в ДХМ) с получением гептадекан-9-ил-8-((2-((2-аминоэтил)амино)этил)(8-(нонилокси)-8-оксооктил)амино)октаноата (256 мг, 58%) в виде бесцветного масла. ВЭЖХ/УФ (ДСИО): RT=6,70 мин. MС (ИЭР): m/z (MH+) 752,7 для C46H93N3O4. 1H ЯМР (300 МГц, CDCl3): δ м.д. 4,87-4,82 (м, 1H); 4,03 (т, 2H, J=6,6 Гц); 2,78 (т, 2H, J=5,9 Гц); 2,63 (дд, 4H, J=5,9 Гц, 13,9 Гц); 2,50 (т, 2H, J=6,0 Гц); 2,36 (т, 4H, J=7,3 Гц); 2,26 (дт, 4H, J=3,8 Гц, 7,5 Гц); 1,68-1,54 (м, 7H); 1,52-1,42 (м, 8H); 1,42-1,36 (м, 7H); 1,36-1,12 (м, 43H); 0,86 (т, 9H, J=6,6 Гц).
IR. Соединение 336: 8-(Гептадекан-9-илокси)-N-(3-гидроксипропил)-N-метил-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминий иодид
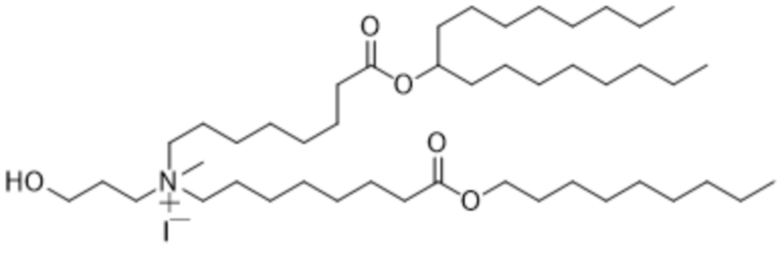
Химическая формула: C46H92INO5
Молекулярная масса: 866,15
[00436] К раствору гептадекан-9-ил-8-[(3-гидроксипропил)[8-(нонилокси)-8-оксооктил]амино]октаноата (0,21 г, 0,29 ммоль) всмеси дихлорэтана (2 мл) и ацетонитрила (3 мл) прибавили метилиодид (0,02 мл, 0,29 ммоль). Реакционную смесь перемешивали при комн. темп. в течение двух часов. Растворители выпарили. Остаток разбавили ДХМ и экстрагировали насыщ. NaHCO3. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над Na2SO4, отфильтровали и выпарили под вакуумом. Остаток очищали флэш-хроматографией (0-100% (смесь 1% NH4OH, 20% MeOH в дихлорметане) в дихлорметане) с получением 8-(гептадекан-9-илокси)-N-(3-гидроксипропил)-N-метил-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминий иодида (0,152 г, 0,29 ммоль, 70%). ЖХ/ДСИО: RT=3,29 мин. MС (ИЭР): m/z (M+) 738,85 для C46H92NO5+ 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87 (м, 1H); 4,08 (т, 2H); 3,91-3,68 (уш. м, 4H); 3,38 (уш. м, 4H); 3,26 (с, 3H); 2,33 (м, 4H); 2,07 (уш. м, 3H); 1,90-1,18 (м, 62H); 0,90 (м, 9H).
IS. Соединение 337: 8-(Гептадекан-9-илокси)-N-(2-гидроксиэтил)-N-метил-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминий иодид
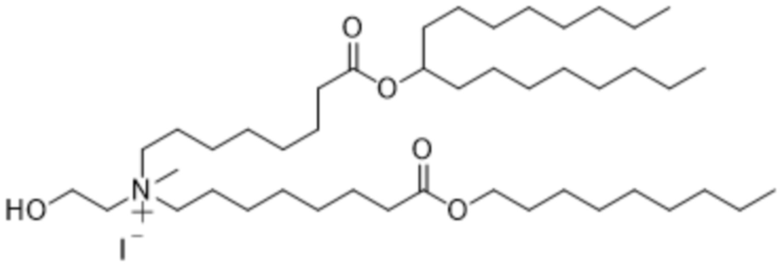
Химическая формула: C45H90INO5+
Молекулярная масса: 852,12
[00437] Соединение 337 синтезировали способом, аналогичным синтезу соединения 336, используя гептадекан-9-ил-8-((2-гидроксиэтил)(8-(нонилокси)-8-оксооктил)амино)октаноат и метилиодид. Выход составил 95 мг (0,111 ммоль, 15%). ЖХ/ДСИО: RT=3,37 мин. MС (ИЭР): m/z (M+) 724,91 для C45H90NO5+ 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87 (м, 1H); 4,20 (уш. м, 2H); 4,07 (т, 2H); 3,74 (уш. м, 2H); 3,50 (уш. м, 4H); 3,33 (с, 3H); 2,33 (м, 4H); 1,87-1,17 (уш. м, 62H); 0,90 (м, 9H).
IT. Соединение 338: 8-(Гептадекан-9-илокси)-N, N-диметил-N-(8-(нонилокси)-8-оксооктил)-8-оксооктан-1-аминий иодид
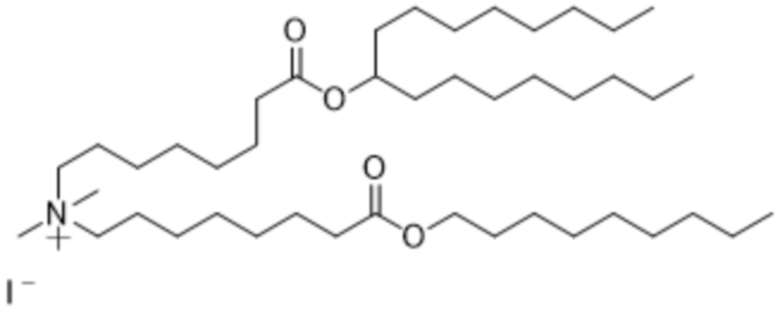
Химическая формула: C44H88INO4
Молекулярная масса: 822,09
[00438] Соединение 338 синтезировали способом, аналогичным синтезу соединения 336, используя гептадекан-9-ил-8-(метил(8-(нонилокси)-8-оксооктил)амино)октаноат и метилиодид. Выход составил 202 мг (0,29 ммоль, 39%). ЖХ/ДСИО: RT=3,33 мин. MС (ИЭР): m/z (M+) 694,89 для C44H88NO4+ 1H ЯМР (300 МГц, CDCl3) δ: м.д. 4,87 (п, 1H); 4,07 (т, 2H); 3,56 (уш. м, 4H); 3,41 (с, 6H); 2,32 (м, 4H); 1,85-1,17 (уш. м, 62H); 0,90 (м, 9H).
IU. Соединение 339: додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(метил)амино)октаноат
Стадия 1: Додекан-4-ил-8-(метиламино)октаноат
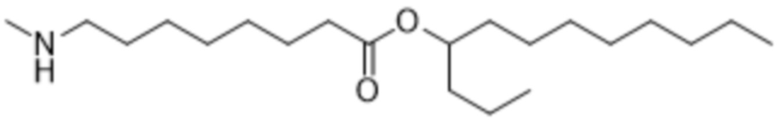
Химическая формула: C21H43NO2
Молекулярная масса: 341,58
[00439] К 2M раствору метиламина (1,19 г, 38,3 ммоль) в ТГФ (19 мл) прибавили додекан-4-ил-8-бромоктаноат (500 мг, 1,28 ммоль) и реакционную смесь оставили перемешиваться при комнатной температуре в течение 48 часов. Раствор концентрировали в вакууме, перенесли в EtOAc и промывали x3 водой, насыщенным водным раствором хлорида натрия, сушили над безводным Na2SO4, отфильтровали и концентрировали в вакууме. Очистка с помощью хроматографии на силикагеле (0-50% (ДХМ 20% MeOH 1% NH4OH) в ДХМ) позволила получить додекан-4-ил-8-(метиламино)октаноат (326 мг, 74,7%). СВЭЖХ/ДСИО: RT=1,55 мин. MС (ИЭР): m/z (MH+) 342,23 для C21H43NO2. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 1H); 2,58 (т, 2H); 2,45 (с, 3H); 2,30 (т, 2H); 1,80-1,05 (уш. м, 29H); 0,92 (м, 6H).
Стадия 2: Додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(метил)амино)октаноат
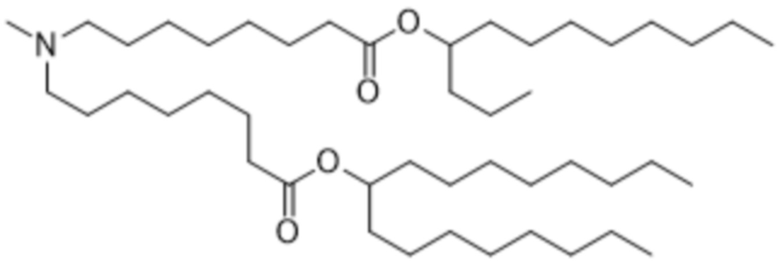
Химическая формула: C46H91NO4
Молекулярная масса: 722,24
[00440] Способом аналогичным стадии 2 для соединения 328 синтезировали додекан-4-ил-8-((8-(гептадекан-9-илокси)-8-оксооктил)(метил)амино)октаноат из додекан-4-ил-8-(метиламино)октаноата (326 мг, 0,954 ммоль), гептадекан-9-ил-8-бромоктаноата (485 мг, 1,05 ммоль), карбоната калия (264 мг, 1,91 ммоль) и иодида калия (32 мг, 0,19 ммоль) в MeCN (10 мл). Выход (392 мг, 56,9%). СВЭЖХ/ДСИО: RT=3,48 мин. MС (ИЭР): m/z (MH+) 722,94 для C46H91NO4. 1H-ЯМР (300 МГц, CDCl3) δ: м.д. 4,90 (м, 2H); 2,55-2,05 (уш. м, 11H); 1,75-1,10 (уш. м, 66H); 0,90 (м, 12H).
IV. Соединение 340: 2-(Ди((9Z,12Z)-октадека-9,12-диен-1-ил)амино)этан-1-ол
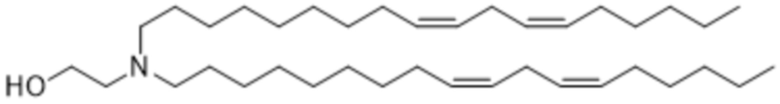
Химическая формула: C38H71NO
Молекулярная масса: 557,99
[00441] К раствору (6Z,9Z)-18-бромоктадека-6,9-диeна (4 г, 12,1 ммоль) в MeCN (26 мл) прибавили этаноламин, (0,334 мл, 5,52 ммоль), K2CO3 (3,36 г, 24,3 ммоль) и KI (92 мг, 0,552 ммоль). Реакционную смесь оставили перемешиваться при 82°C в течение 48 часов. Реакционную смесь охладили до комнатной температуры, отфильтровали и твердые вещества промывали смесью гексанов. Фильтрат экстрагировали смесью гексанов и объединенные экстракты концентрировали в вакууме. Очистка ISCO флэш-хроматографией на силикагеле (0-20% MeOH/ДХМ) позволила получить 2-(ди((9Z,12Z)-октадека-9,12-диен-1-ил)амино)этан-1-ол. Выход (1,9 г, 62%).
СВЭЖХ/ДСИО: RT=6,80 мин. MС (ИЭР): m/z (MH+) 557,94 для C38H71NO
1H-ЯМР (300 МГц, CDCl3) δ: м.д. 5,35 (м, 8H); 3,52 (т, 2H); 2,77 (т, 4H); 2,57 (т, 2H); 2,43 (т, 4H); 2,04 (q, 8H); 1,48-1,18 (уш. м, 36H); 0,89 (т, 6H).
Пример 2: Получение композиций наночастиц
A. Получение композиций наночастиц
[00442] Чтобы исследовать безопасные и эффективные композиции наночастиц для применения при доставке терапевтических и/или профилактических средств в клетки, готовят и тестируют ряд препаратов. В частности, оптимизируются конкретные элементы и их соотношения в липидном компоненте композиций наночастиц.
[00443] Наночастицы могут быть получены с помощью способов смешивания, таких как микрофлюидика и смешивание Т-образного соединения двух потоков жидкости, один из которых содержит терапевтическое и/или профилактическое средство, а другой содержит липидные компоненты.
[00444] Липидные композиции готовят путем объединения липидов формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), фосфолипида (такого как DOPE или DSPC, можно получить от Avanti Polar Lipids, Алебастр, Алабама), ПЭГ-липида (такого как 1,2-димиристоил-sn-глицерин метоксиполиэтиленгликоль, также известный как ПЭГ-DMG, полученный от Avanti Polar Lipids, Алебастр, Алабама) и структурного липида (такого как холестерин, можно получить от Sigma-Aldrich, Тауфкирхен, Германия, или кортикостероида (такого как преднизолон, дексаметазон, преднизон и гидрокортизон) или их комбинаций) в концентрациях около 50 мМ в этаноле. Растворы следует хранить в холодильнике, например, при -20°С. Липиды объединяют с выходом желаемых молярных соотношений (см., например, Таблицу 23) и разбавляют водой и этанолом до конечной концентрации липидов между около 5,5 мМ и около 25 мМ.
[00445] Композиции наночастиц, содержащие терапевтический и/или профилактический и липидный компоненты, готовят объединением раствора липидов с раствором, включающим содержащим средство в липидном компоненте, с терапевтическим и/или профилактическим средством в соотношениях мас.:мас. от около 5:1 до около 50:1. Раствор липидов быстро вводят с использованием системы на основе микрофлюидного раствора NanoAssemblr при скоростях потока от около 10 мл/мин до около 18 мл/мин в терапевтический и/или профилактический раствор для получения суспензии с соотношением воды к этанолу от около 1:1. и около 4:1.
[00446] Для композиций наночастиц, включающих РНК, растворы РНК в концентрациях 0,1 мг/мл в деионизированной воде разбавляют в 50 мМ буфере цитрата натрия при рН от 3 до 4, чтобы получить маточный раствор.
[00447] Композиции наночастиц могут быть обработаны диализом для удаления этанола и достижения буферного обмена. Препараты подвергают диализу дважды с фосфатно-солевым буфером (PBS), pH 7,4, в объемах, в 200 раз превышающих объем первичного продукта с использованием кассет Slide-A-Lyzer (Thermo Fisher Scientific Inc., Рокфорд, Иллинойс), с отсечением молекулярной массы 10 кДа. Первый диализ проводят при комнатной температуре в течение 3 часов. Затем препараты подвергают диализу в течение ночи при 4°С. Полученную суспензию наночастиц равно отфильтровывают через стерильные фильтры 0,2 мкм (Sarstedt, Нюмбрехт, Германия) в стеклянные флаконы и герметично закрывают крышками. Обычно получают растворы композиции наночастиц от 0,01 до 0,10 мг/мл.
[00448] Описанный выше способ вызывает наноосаждение и образование частиц. Альтернативные способы, включая, но не ограничиваясь этим, Т-образное соединение и прямое впрыскивание, могут быть использованы для достижения одинакового наноосаждения.
B. Характеристика композиций наночастиц
[00449] Zetasizer Nano ZS (Malvern Instruments Ltd, Малверн, Вустершир, Великобритания) можно использовать для определения размера частиц, коэффициента полидисперсности (PDI) и дзета-потенциала композиций наночастиц в 1×PBS при определении размера частиц и 15 мМ PBS в определении дзета-потенциала.
[00450] Ультрафиолетовая спектроскопия в видимом диапазоне может быть использована для определения концентрации терапевтических и/или профилактических (например, РНК) в композициях наночастиц. 100 мкл разбавленной композиции в 1×PBS добавляют к 900 мкл 4:1 (об./об.) смеси метанола и хлороформа. После перемешивания записывают спектр поглощения раствора, например, между 230 нм и 330 нм на спектрофотометре DU 800 (Beckman Coulter, Beckman Coulter, Inc., Брея, Калифорния). Концентрация терапевтического и/или профилактического средства в композиции наночастиц может быть рассчитана на основе коэффициента экстинкции терапевтического и/или профилактического средства, используемого в композиции, и разницы между оптической плотностью при длине волны, например, 260 нм, и фонового значения при длине волны, например, 330 нм.
[00451] Для композиций наночастиц, содержащих РНК, для оценки инкапсуляции РНК с помощью композиции наночастиц можно использовать анализ QUANT-IT™ RIBOGREEN® RNA (Invitrogen Corporation, Карлсбад, Калифорния). Образцы разбавляют до концентрации приблизительно 5 мкг/мл в ТЕ-буферном растворе (10 мМ Трис-HCl, 1 мМ ЭДТК, рН 7,5). 50 мкл разбавленных образцов переносят в полистирольный 96-луночный планшет и либо 50 мкл буфера TE, либо 50 мкл 2% раствора Triton X-100 добавляют в лунки. Планшет инкубируют при температуре 37°С в течение 15 минут. Реагент RIBOGREEN® разводят 1:100 в ТЕ-буфере и 100 мкл этого раствора добавляют в каждую лунку. Интенсивность флуоресценции может быть измерена с использованием флуоресцентного планшет-ридера (Wallac Victor 1420 Multilabel Counter; Perkin Elmer, Уолтем, Массачусетс) при длине волны возбуждения, например, около 480 нм и длине волны излучения, например, около 520 нм. Значения флуоресценции в холостом реагенте определяются значениями каждого образца, а процентная доля свободной флуктуации зависит от величины флуоресценции интактного образца (без добавления Triton Х-100) по значению флуоресценции разрушенного образца (вызвано добавлением Triton X-100).
C. In vivo исследования препарата
[00452] Для того чтобы отслеживать, насколько эффективно различные композиции наночастиц доставляют терапевтические и/или профилактические средства к клеткам-мишеням, готовят и вводят различные композиции наночастиц, включая конкретную терапевтическую и/или профилактическую (например, модифицированную или встречающуюся в природе РНК, такую как мРНК) популяции грызунов. Мышам внутривенно, внутримышечно, внутриартериально или внутриопухолево вводят однократную дозу, содержащую композицию наночастиц с препаратом, таким как препараты, предложенные в Примере 3. В некоторых случаях могут заставлять мышей вдыхать дозы. Размер дозы может варьироваться от 0,001 мг/кг до 10 мг/кг, причем 10 мг/кг описывает дозу, содержащую 10 мг терапевтического и/или профилактического средства в композиции наночастиц на каждый 1 кг массы тела мыши. Также может быть использована контрольная композиция, включающая PBS.
[00453] При введении композиций наночастиц мышам, профили доставки дозы, реакции на дозу и токсичность конкретных препаратов и их дозы могут быть измерены с помощью иммуноферментного анализа (ИФА), биолюминесцентной визуализации или других методов. Для композиций наночастиц, включая мРНК, также можно оценить временные ходы экспрессии белка. Образцы, взятые у грызунов для оценки, могут включать кровь, сыворотку и ткани (например, мышечную ткань из места внутримышечной инъекции и внутреннюю ткань); сбор образцов может включать умерщвление животных.
[00454] Композиции наночастиц, в том числе мРНК, подходят для оценки эффективности и пригодности различных препаратов для доставки терапевтических и/или профилактических средств. Более высокие уровни экспрессии белка, индуцированные введением композиции, содержащей мРНК, будут указывать на более высокую эффективность трансляции мРНК и/или композиции мРНК наночастиц. Поскольку не-РНК-компоненты, как полагают, не влияют на сами механизмы трансляции, более высокий уровень экспрессии белка, вероятно, свидетельствует о более высокой эффективности доставки терапевтического и/или профилактического средства данной композицией наночастиц по сравнению с другими композициями наночастиц или отсутствием его.
Пример 3: Образцы препаратов
[00455] Композиции наночастиц, содержащие терапевтические и/или профилактические средства, могут быть оптимизированы в соответствии с выбором соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), выбор дополнительных липидов, количество каждого липида в липидном компоненте и массовое соотношение липидного компонента к терапевтическому и/или профилактическому средству, описанным в данном документе.
[00456] Начальные исследования были выполнены для сравнения эффективности доставки композиций наночастиц, включая различные соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III). Катионный липид MC3 является современным стандартом в данной области. Соответственно, стандартная композиция MC3, включающая около 50% моль MC3, около 10% моль DSPC, около 38,5% моль холестерина и около 1,5% моль ПЭГ-DMG, использовалась в качестве основы для данного исследования. Композиции наночастиц, включающие DSPC в качестве фосфолипида, холестерин в качестве структурного липида, ПЭГ-DMG в качестве ПЭГ-липида, РНК и соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III), выбранные из соединений 1-159, 168-170 и 173-175, были получены в соответствии или способами, аналогичными описанным в Примерах 1 и 2. Соотношения липидов составляли 50: 10: 38,5: 1,5% моль для липидов согласно формулы (I), (IA), (IB), (II), (IIa), (IIb), ( IIc), (IId), (IIe), (IIf), (IIg) или (III): DSPC: холестерин:ПЭГ-DMG. Используемая РНК представляла собой мРНК, кодирующую люциферазу (Luc) или hEPO, причем каждый уридин был заменен N1-метилпсевдоуридином. Таблицы 1А-1Е суммируют содержание и характеристики препаратов.
[00457] Как продемонстрировано в Таблицах 1A-1E, выбор соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) существенно влияет на размер (например, диаметр), коэффициент полидисперсности и эффективность инкапсуляции (EE) композиций. Композиции имели размеры от около 53 нм до 237 нм. Композиции, содержащие соединения 5, 35, 36, 51, 59, 131, 132, 137-139, 145, 148, 155 и 158, дали самые большие частицы, тогда как композиции, содержащие соединения 9, 21, 29, 30, 65, 7175, 94 107, 114-116, 119, 124, 133, 149, 150, 152, 174 и 175, дали самые маленькие частицы. Показатели полидисперсности варьировались от 0,04 до 0,99, в то время как эффективность инкапсуляции превышала 75% для композиций, содержащих каждое тестируемое соединение, за исключением соединений 21, 94, 107, 132, 148, 155 и 158. Наибольшая эффективность инкапсуляции наблюдалась для соединений 1, 6, 18, 19, 24, 26, 28, 29, 49, 50, 55, 60, 61, 65-70, 72, 74, 75, 101, 109-116, 118, 119, 121, 122, 124, 126, 128, 130, 149, 152, 153, 156, 159, 169, 170 и 174.
Пример 4: Экспрессия Luc, индуцированная образцами препаратов
[00458] Эффективность композиций наночастиц, представленных в таблице 1А, была оценена с помощью исследования биолюминесценции. Составы вводили мышам внутривенно (n=6) в дозировке 0,5 мг/кг и измеряли биолюминесценцию через 3, 6 и 24 часа. Стандартный состав MC3 и, в некоторых случаях, контроль (например, контроль PBS) оценивали для сравнения. Как видно из таблицы 2, через 3 часа общий поток был самым высоким для композиций, содержащих соединения 4, 28, 32, 48, 66, 128 и 135, а общий поток через 3 часа был выше или сопоставим с таковым для составов МС3 у соединений 2, 3, 18, 19, 20, 24, 26, 25, 27, 31, 33, 47, 49, 50, 53-55, 60, 61, 65-68, 70, 72, 74, 75, 96, 111, 122, 130, 133, 134, 143, 147, 148, 150, 151 и 153. Эти композиции также продемонстрировали более высокий общий поток во временные точки 6 и 24 часа. Композиции, содержащие соединения 9, 17, 57, 58, 59, 121, 125, 137, 140, 141 и 158 имели значительно более низкий поток во всех измеренных временных точках. В общем, поток уменьшался с течением времени до менее чем 10% от исходного потока. Эти результаты предполагают, что соединения, описанные в данном документе, могут быть пригодны в применениях для трансфекции.
2,91E+10
[00459] Общий поток (измеренный по площади под кривой, AUC), индуцированный введением композиции, содержащей данный липид, относительно потока, индуцированного введением композиции, содержащей MC3, также измеряли для нескольких липидов. Как показано в Таблице 3А (в/в введение), поток, индуцированный составами, содержащими соединения 48 и 49, измеренный через 6 ч, был в десять раз выше, чем индуцированный составом МС3. Составы, содержащие соединения 50, 54 и 55, также демонстрировали более высокий поток, чем составы МС3. Как показано в Таблице 3В, поток, индуцированный составами, содержащими соединения 108 и 168, измеренный через 6 часов, был в четырнадцать и шестнадцать раз выше, чем поток, индуцированный составом МС3 посредством внутримышечного введения (в/м). Результаты также представлены на Фиг. 8. Как показано в таблице 3C (в/в введение), поток, индуцированный составами, содержащими соединения 66, 133-135 и 147, измеренный через 6 ч, и общий поток был заметно выше, чем индуцированный составом MC3. Как показано в таблице 3D, общий поток, индуцированный составами, содержащими соединения 96, 148 и 151, измеренный через 6 ч, был заметно выше, чем индуцированный составом МС3.
липид/MC3
0,5 мг/кг, Luc, 6 ч
липид/MC3
0,01 мг/кг, Luc, 6 ч
Сред. экспрессия Luc
оставшейся
в печени
6 ч
оставшейся
в печени
6 ч
липид/MC3
6 ч
дозы через 6 ч
24 ч
дозы через 24 ч
(AUC: 4,02)
(AUC: 5,21)
(AUC: 1,7)
(AUC: 6,38)
(AUC: 2,01)
(AUC: 3,05)
(AUC: 0,76)
(AUC: 1,19)
(AUC: 4,30)
(AUC: 3,42)
Пример 5: Экспрессия Luc в различных органах, индуцированная образцами составов
[00460] Эффективность композиций наночастиц, представленных в таблице 1А, дополнительно оценивали путем измерения экспрессии модифицированной люциферазы в печени, легких, селезенке и бедре при введении данной композиции. Композиции вводили мышам внутривенно (n=3) в дозе 0,5 мг/кг и измеряли биолюминесценцию через 6 часов. Стандартный состав MC3 и контроль PBS также были протестированы. Как видно из таблицы 4, поток почти для всех видов был выше в печени по сравнению с другими тканями. Поток в печени был самым высоким для композиций, содержащих 3, 28, 33, 48, 96 и 135, и сравним с таковым для составов МС3 для композиций, содержащих соединения 2, 4, 6, 7, 18, 20, 24-27, 30-32, 34, 47, 49, 50, 53-56, 60, 65, 67, 68, 74, 75, 111, 113, 122, 128, 130, 133, 134, 143, 147-151, 153 и 157. Поток в печени был самым низким для композиций, содержащих соединения 58, 59, 137 и 141. Поток в селезенке был самым высоким для композиций, содержащих соединения 4, 7, 33, 34, 48, 53, 108, 129, 130 и 148, и самым низким для композиций, содержащих соединения 9, 59, 124 и 141. Аналогичные результаты наблюдались в легких и бедре.
Пример 6A: Экспрессия, вызванная образцами составов при внутримышечном введении
[00461] Образцы составов, содержащих как модифицированную мРНК люциферазы (Luc), так и мРНК H10, готовили и вводили внутримышечно, а полученную экспрессию и иммуногенность оценивали одновременно. Составы, содержащие соединения по формуле (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) были приготовлены и введены в дозах 0,001 и 0,01 мг/кг (например, дозы 0,0005 мг/кг композиции, содержащей мРНК Luc, и состав, содержащий мРНК H10, или дозы 0,005 мг/кг состава, содержащего мРНК Luc, и состава, содержащего мРНК H10). Как показано в таблице 5А, соединение 20 продемонстрировало самую высокую экспрессию при обоих уровнях дозы. Низкая доза соединения 20 продемонстрировала эквивалентную экспрессию высокой дозе MC3. Составы, содержащие другие соединения, также продемонстрировали многократное усиление экспрессии относительно MC3.
Пример 6B: Экспрессия, вызванная образцами составов при внутримышечном введении
[00462] Образцы составов, содержащих модифицированную мРНК люциферазы (Luc) готовили и вводили внутримышечно, а полученную экспрессию и иммуногенность оценивали одновременно. Составы, содержащие соединения по формуле (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) были приготовлены и введены в дозе 0,01 мг/кг. Как показано в таблице 5В, соединение 108 продемонстрировало самую высокую экспрессию. Составы, содержащие другие соединения, также продемонстрировали многократное усиление экспрессии относительно MC3.
[00463] Потоки, измеренные при внутривенном и внутримышечном введении, сравниваются в таблице 6. Потоки представлены как кратное увеличение по сравнению с измеренным для составов MC3. Составы, содержащие соединение 20, продемонстрировали самое высокое кратное увеличение экспрессии Luc при внутримышечном введении, тогда как составы, содержащие соединения 18 и 26, продемонстрировали самое высокое кратное увеличение при внутривенном введении. Примечательно, что внутривенные данные, включенные в таблицу 6, были измерены при более высоких дозах, чем внутримышечные данные.
(доза 0,5 мг/кг)
(доза 0,01 мг/кг)
(доза 0,001 мг/кг)
Пример 7: Продукция цитокинов, индуцированная образцами составов
[00464] Введение инородного материала в организм млекопитающего вызывает врожденный иммунный ответ, который способствует выработке цитокинов. Такие иммунные ответы, например, на композиции наночастиц, включая терапевтические и/или профилактические, являются нежелательными. Таким образом, индукция определенных цитокинов измеряется для оценки эффективности композиций наночастиц. Концентрации различных цитокинов у мышей при внутривенном введении композиций наночастиц, представленных в таблице 1А, в дозе 0,5 мг/кг измеряли через 6 часов. Стандартный состав MC3 и контроль PBS также были протестированы. Как видно из таблицы 7, индукция IL-6 была самой высокой для композиций, содержащих соединения 1, 3, 9, 19 и 26, в то время как индукция IP-10 была самой высокой для композиций, содержащих соединения 3, 4, 7, 20 и 26. Индукция IL-6 была самой низкой для композиций, содержащих соединения 4, 11, 12 и 28. Индукция IP-10 была самой низкой для композиций, содержащих соединения 10, 11, 12, 13, 15, 17 и 18.
Пример 8: Активация комлемента, индуцированная образцами составов
[00465] Активация комплемента способствует выведению болезнетворных микроорганизмов из организма. Поскольку нежелательно, чтобы организм субъекта распознавал композицию наночастиц в качестве инородного объекта, активация системы с низким уровнем комплемента при введении такой композиции является предпочтительной. Комплекс sC5b-9 является маркером активации системы комплемента. Таким образом, клетки человека, приводили в контакт in vitro с композициями наночастиц в соответствии с таблицей 1А и оценивали уровни sC5b-9. В таблице 8 показано кратное увеличение уровней sC5b-9 по сравнению с физиологическим раствором для композиций наночастиц, содержащих соединения 1, 6, 9, 18, 24, 25, 29 и 30. Композиции, содержащие соединения 6 и 18, несколько повышают уровни sC5b-9 по сравнению с физиологическим раствором, в то время как композиции, содержащие соединения 1, 9, 24, 29 и 30, слегка снижают уровни sC5b-9 по сравнению с физиологическим раствором.
Пример 9: Клиническая химия и гематология
[00466] Образцы составов композиций наночастиц, содержащих различные липиды, вводили крысам внутривенно в дозе 2 мг/кг. Экспрессию различных клинических маркеров оценивали через 48 ч после введения дозы и сравнивали с таковой, индуцированной введением композиций MC3 или натрий-фосфатного буфера (PBS).
Пример 10: Экспрессия hEPO, индуцированная образцами составов
[00467] Образцы составов композиций наночастиц, содержащих различные липиды, обычно сначала оценивают в соответствии с экспрессией Luc in vivo. Активность нескольких таких композиций дополнительно оценивали с использованием мРНК, кодирующей hEPO. Композиции наночастиц, содержащие соединения 6, 18, 25, 30, 108-112, 60 и 122 или MC3 были приготовлены согласно Примеру 2. Как показано в таблицах 10 и 1В выше, каждая композиция имела одинаковый размер частиц и эффективность инкапсуляции.
[00468] Экспрессию hEPO и индукцию цитокинов у мышей, которым внутривенно вводили композицию наночастиц в дозе 0,5 мг/кг, измеряли через 3, 6 и 24 часа. Результирующие уровни hEPO и цитокинов приведены в таблице 11А. Композиции, содержащие соединения 6 и 18, обеспечивали более высокие концентрации hEPO, чем композиции MC3 в каждую временную точку. Экспрессию hEPO у мышей, которым внутримышечно вводили композицию наночастиц из таблицы 1B, в дозе 0,01 мг/кг, измеряли через 3, 6 и 24 часа. Результирующие уровни hEPO приведены в таблице 11B. Композиции, содержащие соединения 18, 25, 30, 108-112, 60 и 122, обеспечивали более высокие концентрации hEPO, чем композиции MC3 через 6 ч (см. также Фиг. 9).
[00469] В таблице 12 приводится сравнение композиции наночастиц, содержащих соединения по формуле (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) с композициями, содержащими MC3, на основе уровней экспрессии и потока. Как видно из таблицы 12, оба соединения 6 и 18 превосходят MC3 как по экспрессии hEPO, так и по среднему общему потоку. Таким образом, эти липиды могут быть пригодны в терапии композициями наночастиц.
Пример 11: Экспрессия hEPO, индуцированная образцами составов у крыс и уровень остаточных липидов в печени
[00470] Экспрессию hEPO и индукцию цитокинов у крыс, которым внутривенно вводили композицию наночастиц в дозе 2,0 мг/кг, измеряли через 6 часов.
[00471] Через 48 часов ткани печени собирали для количественного определения липидов. К предварительно взвешенным тканям добавляли воду Milli-Q (900 мкл воды на 100 мг ткани). Ткани гомогенизировали с использованием гомогенизатора Omni до однородного состояния. 50 мкл образцов и калибровочных стандартов матрицы были аликвотированы в 96-луночный планшет. 50 мкл пустой матрицы для матричных контролей и отрицательных контролей были аликвотированы. 400 мкл мммобилизирующего раствора IS добавляли вручную во все образцы, кроме матричных контролей. 400 мкл 50:50 ACN:IPA были добавлены вручную к матричным контролям. Планшет накрывали и образцы встряхивали и центрифугировали в течение 5 минут при> 3000 об/мин. 200 мкл образцов переносили в чистый 96-луночный планшет для анализа. Образцы анализировали на UPLC Waters Acquity с использованием колонки Higgins Analytical Clipeus C8 (5 мкМ, 30×2,1 мм) и с градиентом или 70-95%, или 60-95% (подвижная фаза A: 5 мМ формиата аммония в 50:50:1 H2O:MeOH:муравьиная кислота; подвижная фаза B: 5 мМ формиата аммония в 100:1 MeOH:муравьиная кислота) в течение 1,3 мин при 1,2 мл/мин (температура колонки 55°C). Обнаружение основывалось на электрораспылительной ионизации (ESI) в положительном режиме с использованием масс-спектрометра Sciex API5500.
[00472] Экспрессию hEPO у крыс, которым внутривенно вводили композицию наночастиц в дозе 0,2 мг/кг или 2,0 мг/кг, измеряли через 6 часов. В таблице 16 приведено соотношение уровней экспрессии hEPO с использованием различных композиций наночастиц по сравнению с уровнем экспрессии hEPO с использованием состава MC3, и уровни липидов в печени, измеренными через 48 часов после введения, как описано выше. В таблицах 17 и 18 приведены уровни липидов в печени и селезенке, измеренные через 48 часов после введения соединений 28, 33, 53 и 54. Уровни в печени и селезенки представляют собой средние значения, рассчитанные для 3 крыс в каждой группе. Как показано в таблицах 17 и 18, менее чем 10% соединений 28, 33, 53 и 54 оставались в печени через 48 часов, в то время как оставалось более 60% MC3.
в печени, 48 ч*
В таблице 19A приведена экспрессию hEPO, индукция IP-10, уровни в печени и селезенке, а также аланинаминотрансфераза (ALT) и аспартатаминотрансфераза (AST), измеренные при внутривенном введении составов, содержащим соединения 48, 49 и 50, крысам в количестве 0,2 и 2 мг/кг и мРНК hEPO. Концентрации hEPO измеряли через 6 часов после введения, тогда как индукцию цитокинов и уровни в печени и селезенке измеряли через 48 часов после введения. Концентрации hEPO и IP-10 представлены в пг/мл, а уровни в печени представлены в нг/г. Уровни ALT и AST представлены в международных единицах.
мл)
мл)
(пг/мл*ч)
Пример 12: Дозозависимость образцов составов у крыс
[00473] Экспрессию hEPO, индуцированную внутривенным введением крысам композиций наночастиц в различных дозах, измеряли во временные точки 2, 4, 6, 8, 24 и 48 часов. На Фиг. 3-6 продемонстрированы, соответственно, результаты экспрессии hEPO, измеренные при внутривенном введении крысам составов наночастиц, содержащих соединения 26, 18, 25 и MC3. Уровни липидов соединения 26 в печени через 48 часов составляли около 19%.
[00474] На Фиг. 7 продемонстрирована площадь под кривой для композиций, содержащих соединения 18, 25 и 26 и MC3, в различных дозировках: 0,005 мг/кг, 0,01 мг/кг, 0,025 мг/кг, 0,05 мг/кг, 0,1 мг/кг, 0,25 мг/кг, 0,5 мг/кг, 1 мг/кг или 2 мг/кг.
Пример 13: Фармакокинетика образцов составов у крыс
[00475] Экспрессию hEPO и уровни липидов в печени и селезенке у крыс, которым внутривенно вводили композицию наночастиц в дозе 0,2 мг/кг, измеряли в различные временные точки. Соединения 18 и 25 были отобраны для сравнения с МС3. Липиды были приготовлены в соответствии со стандартным составом МС3, описанным выше. Крысам вводили внутривенно разовую дозу, равную 0,2 мг/кг, а экспрессию контролировали через 0,25, 0,5, 1, 2, 4, 8, 24 и 48 часов после введения.
[00476]
Пример 14: Оптимизация соотношения липид:терапевтический агент
[00477] Относительные количества липидного компонента и терапевтического и/или профилактического средства в композиции наночастиц могут быть оптимизированы в соответствии с соображениями эффективности и переносимости. Для композиций, включающих РНК в качестве терапевтического и/или профилактического средства, соотношение N:P может служить подходящим показателем.
[00478] Поскольку соотношение N:P в композиции наночастиц контролирует как экспрессию, так и переносимость, желательны композиции наночастиц с низким соотношением N:P и сильной экспрессией. Соотношения N:P варьируются в зависимости от соотношения липидов к РНК в составе наночастиц. Таким образом, соотношение мас./мас. общего количества липида к РНК варьируется между 10:1, 15:1, 20:1, 32:1, 40:1, 50:1 и 60:1 для липидной композиции, содержащей около 50% моль соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) около 10% моль фосфолипидов (например, DOPE или DSPC), около 38,5% моль структурных липидов (например, холестерина) и около 1,5% моль ПЭГ- липидов (например, ПЭГ-DMG). Соотношения N:P рассчитываются для каждого препарата наночастиц с учетом одного протонированного атома азота. Также исзмеряют эффективность инкапсуляции (EE), размер и коэффициент полидисперсности каждого препарата.
[00479] Обычно композиции с более высоким общим соотношением липид:РНК дают более мелкие частицы с более высокой эффективностью инкапсуляции, обе из которых являются желательными. Однако соотношение N:P для таких препаратов обычно превышает 4. Современные стандарты в данной области техники, такие как препарат MC3, описанный выше, имеют соотношения N:P равное 5,67. Таким образом, следует соблюдать баланс между соотношением N:P, размером и эффективностью инкапсуляции.
[00480] Чтобы исследовать эффективность композиций наночастиц с различными соотношениями N:P, исследовали экспрессию люциферазы (Luc) или эритропоэтина человека (hEPO) у мышей после низкой (0,05 мг/кг) или высокой (0,5 мг/кг) дозы внутривенно вводимых композиций наночастиц. Концентрация экспрессируемого Luc или hEPO измеряется через 3, 6 и/или 24 часа после введения.
Пример 15: Оптимизация содержания соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III)
[00481] Поскольку более мелкие частицы с более высокой эффективностью инкапсуляции обычно являются желательными, относительные количества различных элементов в липидных компонентах композиций наночастиц оптимизируются в соответствии с данными параметрами.
[00482] Соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) выбирают для оптимизации. Относительное количество соединение формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) варьируется от 30 до 60% моль в композициях, включающих DOPE или DSPC в качестве фосфолипидов, для определения оптимального количества соединения формулы (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) в данных препаратах. Препараты готовят, используя стандартизированный способ с соотношением воды к этанолу в растворе липид-мРНК 3:1 и скоростью введения липидного раствора в раствор мРНК 12 мл/мин в микрофлюидной системе на основе NanoAssemblr. Этот способ вызывает нано-осаждение и образование частиц. Альтернативные процессы, включая, но не ограничиваясь этим, Т-образный переход или прямой впрыск, также могут быть использованы для достижения того же наноосаждения.
[00483] Составы для получения мельчайших частиц с наивысшей эффективностью инкапсуляции, как правило, является предпочтительным, однако большие или меньшие размеры частиц могут быть желательны на основании конкретного применения (например, на основе размера фенестрации целевого органа). Композиции также оценивают по уровням их экспрессии Luc или hEPO и профилям цитокинов.
Пример 16: Оптимизация фосфолипидов
[00484] Относительное количество фосфолипида в липидном компоненте композиции наночастиц равно варьировалось для дальнейшей оптимизации состава. Соединение по Формуле (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) выбирали для использования в составе наночастиц, а DOPE и DSPC выбирали в качестве фосфолипидов. Дополнительные фосфолипиды также могут быть оценены. Композиции наночастиц готовили с относительным содержанием фосфолипидов в диапазоне от 0 до 30 мол. %. Композиции оценивают по размеру, эффективности инкапсуляции, уровням экспрессии Luc или hEPO и профилям цитокинов.
Пример 17: Оптимизация структурного липида
[00485] Относительное количество структурного липида в липидном компоненте композиции наночастиц равно варьировалось для дальнейшей оптимизации состава. Соединение по Формуле (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) выбирали для использования в составе наночастиц, а холестерин выбрали в качестве структурного липида. Дополнительные структурные липиды также могут быть оценены. Композиции наночастиц готовили с относительным содержанием структурных липидов в диапазоне от 18,5 до 48,5 мол. %. Композиции оценивали по размеру, эффективности инкапсуляции, уровням экспрессии Luc или hEPO и профилям цитокинов.
Пример 18: Оптимизация ПЭГ липида
[00486] Относительное количество липида ПЭГ в липидном компоненте композиции наночастиц равно варьировалось для дальнейшей оптимизации состава. Соединение по Формуле (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III) выбрали для использования в составе наночастиц, а ПЭГ-DMG выбрали в качестве липида ПЭГ. Дополнительные липиды ПЭГ также могут быть оценены. Композиции наночастиц готовили с относительным содержанием липидов ПЭГ в диапазоне от 0 до 10 мол. %. Композиции оценивали по размеру, эффективности инкапсуляции, уровням экспрессии Luc или hEPO и профилям цитокинов.
[00487] Иллюстративные составы, полезные для оптимизации составов композиций наночастиц, представлены в Таблице 23.
Пример 19: Оптимизация размеров частиц
[00488] Размеры фенестрации для различных органов тела часто варьируют; например, известно, что почки имеют меньший размер фенестрации, чем печень. Таким образом, для целевой доставки терапевтического и/или профилактического средства (например, специфической доставки) в конкретный орган или группу органов может потребоваться введение композиций наночастиц с различными размерами частиц. Чтобы исследовать этот эффект, композиции наночастиц с составами, такими как составы, включенные в таблицу 23, готовят с различными размерами частиц с использованием инструмента Nanoassemblr. Композиции наночастиц содержали РНК, кодирующую Luc. Каждую композицию наночастиц различного размера равным образом ввоили мышам для оценки влияния размера частиц на селективность доставки. Экспрессия Luc в двух или более органах или группах органов может быть измерена с использованием биолюминесценции для оценки относительной экспрессии в каждом органе.
Пример 20: Введенеи после предварительного введения
[00489] Введение композиций наночастиц субъектам может привести к воспалению, реакциям, связанным с инфузией, и другим нежелательным эффектам, указывающим на низкую переносимость. Эти эффекты могут быть отнесены к нежелательной иммуноактивности.
[00490] Для борьбы с негативными эффектами композиции наночастиц вводят субъектам совместно с одним или более веществами (например, совместными лекарственными средствами или дополнительными терапевтическими и/или профилактическими средствами). Потенциально пригодные дополнительные терапевтические и/или профилактические средства включают стероиды (например, кортикостероиды), антигистамины, блокаторы рецепторов H1, блокаторы рецепторов H2, противовоспалительные соединения, статины, ингибиторы BTK (тирозинкиназы Брутона), агонисты S1P1, модуляторы глюкокортикоидных рецепторов (GRM) и эстрадиолы. Примата, не являющимся людьми, предварительно вводят одним или более дополнительных терапевтических агентов, выбранных из дексаметазона и ацетаминофена. Дополнительный терапевтический агент вводят либо за 24 часа, 1 час, либо как за 24 часа так и за 1 час до введения композиции наночастиц. Протоколы образцов приведены в таблице 24. Профили цитокинов, воспаление и другие параметры измеряли и сравнивали для оценки эффективности предварительной обработки.
[00491] Например, пригодный курс терапевтического лечения может включать введение дополнительного терапевтического и/или профилактического средства как за сутки до, так и в день (за один час до) введения композиции наночастиц при уровне дозы, равном 1,3 мг/кг. Дополнительные терапевтические и/или профилактические средства могут быть составлены для доставки различными путями. Например, дексаметазон может доставляться перорально. Как правило, дополнительные терапевтические и/или профилактические средства вводят в клинически утвержденных или типичных уровнях доз.
Пример 21: Введение приматам, отличным от человека
[00492] Переносимость и эффективность композиций наночастиц для приматов, отличных от человека оценивали на яванских макаках. Обезьянам вводили оптимизированную композицию наночастиц, содержащую мРНК, кодирующую hEPO, один раз в неделю в течение четырех недель. Уровни белка hEPO, мРНК и профили цитокинов измеряли с использованием методов на основе ИФА до и через 2, 6, 12, 24, 48, 72 и 120 часов после каждого введения.
[00493] Эффекты предварительного лечения приматов, не являющихся человеком, оценивали с использованием стандартной композиции MC3, содержащей мРНК, кодирующую hEPO. Дизайн исследования приведен в таблице 25. Самцам обезьян вводили композицию наночастиц один раз в неделю в течение четырех недель со скоростью 5 мл/кг/ч и предварительно вводили либо метотрексат, либо дексаметазон.
[00494] Результаты исследования предварительного лечения продемонстрированы на Фиг. 1. Как показано, в отсутствие какого-либо предварительного лечения максимальные уровни экспрессии снижались почти на 70% в течение исследования. Метотрексат не оказывал какого-либо особого положительного эффекта. Однако предварительное введение дексаметазона приводило к повышенной экспрессии белка по сравнению с курсами лечения, не связанными с предварительным лечением. Примечательно, что минимальное снижение экспрессии белков в плазме/сыворотке наблюдалось с течением времени у животных, которым предварительно вводили дексаметазон. Эти результаты предполагают, что предварительное введение кортикостероидов, таких как дексаметазон, улучшает переносимость и эффективность композиций наночастиц, содержащих, например, соединение по формуле (I), (IA), (IB), (II), (IIa), (IIb), (IIc), (IId), (IIe), (IIf), (IIg) или (III).
[00495] Переносимость и эффективность композиций наночастиц по отношению к приматам, отличным от человека, также исследовали с использованием состава образца, содержащего соединение 18. Состав готовили в соответствии со стандартным составом MC3, описанным выше, и содержали мРНК hEPO. Приматам вводили разовую дозу 0,05 (группа 1), 0,3 (группа 2) или 1,0 (группа 3) мг/кг путем внутривенной инфузии в течение 60 минут. Трем приматам вводили каждую дозу. Экспрессию hEPO измеряли до введения дозы и через 2, 6, 24, 48 и 96 часов после введения (таблица 26). Фармакокинетические параметры, включая Tmax, Cmax, и AUC также были определены и приведены в таблице 27. В таблице 28 приведены уровни показателей активации комплемента, а в таблице 29 приведены данные об индукции цитокинов.
(0,05 мг/кг)
(0,3 мг/кг)
(1,0 мг/кг)
(0,05 мг/кг)
(0,3 мг/кг)
(1,0 мг/кг)
(0,05 мг/кг)
(0,3 мг/кг)
(1,0 мг/кг)
(0,05 мг/кг)
(0,3 мг/кг)
(1,0 мг/кг)
[00496] В целом, состав переносился аналогично составу МС3 с эффектами доза-ответ. Аспартатаминотрансфераза (AST) увеличилась в группе с высокими дозами на 2-е сутки и вернулась к исходному уровню на 5-е сутки. Однако уровни аланинаминотрансферазы (ALT) не увеличились. В целом, более низкие дозы переносились лучше. Высокие дозы вызывали повышение температуры тела и сгорбленную позу, что аналогично поведению, наблюдаемому у приматов, которым вводили более высокие дозы композиций MC3. Количество белых кровяных телец было немного повышено у животных в группе с высокой дозой, однако во всех группах отмечалось заметное увеличение количества ретикулоцитов на 5 сутки, что указывает на сильный фармакологический ответ. Активация комплемента и высвобождение цитокинов (IL-6 и MCP-1) были зависимыми от дозы и обратимыми в течение 24 часов для групп с низкой и средней дозой и к 5-м суткам в группе с высокой дозой. Уровни hEPO были выше, чем измеренные при введении сопоставимых доз составов MC3 приматам, не являющимся человеком.
Пример 22: Введение приматам, отличным от человека
[00497] Переносимость и эффективность композиций наночастиц для приматов, не являющихся человеком, также исследовали с использованием составов образцов, содержащих соединения 18, 25, 26 и 48 и MC3, чтобы определить, дифференцируются ли эти соединения с точки зрения экспрессии белка. Составы готовили в соответствии со стандартным составом MC3, описанным выше, и содержали мРНК hEPO. В таблице 30 приведены подробности тестируемых композиций, а в таблице 31 приведена относительная экспрессия мРНК Luc и hEPO у мышей и крыс. Экспрессию измеряли через 6 часов после введения.
(доза 0,5 мг/кг мышам)
(доза 0,2 мг/кг крысам)
(доза 2 мг/кг крысам)
[00498] На Фиг. 2 продемонстрирована экспрессия мРНК hEPO, измеренная после внутривенного введения 0,01 мг/кг при 60-минутной инфузии наивным яванским макакам. Как видно на фигуре, экспрессия была самой высокой через 6 часов после введения для всех протестированных составов и была самой высокой для тех составов, содержащих соединение 18.
[00499] В таблице 32 приведены фармакокинетические параметры, измеренные при введении доз, равных 0,01 мг/кг составов приматам, не являющихся человеком.
/MC3
Пример 23: Введение приматам, отличным от человека
[00500] Результаты исследований экспрессии hEPO были подтверждены с использованием стандартной композиции MC3 и композиции наночастиц, содержащей соединение 18, содержащей мРНК, кодирующую антитело против гемагглютинина (анти-HA). Яванским макакам вводили разовую дозу, равную 0,1 мг/кг или 0,3 мг/кг композиции наночастиц, содержащей соединение 18 (см. таблицу 33; приготовленную в соответствии с примером 2), включая мРНК, кодирующую антитело против HA, путем внутривенной инфузии в течение 60 минут.
[00501] Результаты экспрессии антитела против HA (против гемагглютинина) приведены в таблице 34 и на фиг. 11.
(мг/кг)
[00502] Пятикратная более высокая экспрессия белка наблюдалась с композицией наночастиц, содержащей соединение 18, по сравнению с аналогом МС3, и была обнаружена четкая доза-реакция между 0,1 и 0,3 мг/кг для соединения 18 (например, AUC 0,3 мг/кг примерно в три раза больше, чем у дозы 0,1 мг/кг).
Пример 24: Способы лечения заболеваний и расстройств
[00503] Состав композиции наночастиц, имеющий высокую переносимость (например, провоцирующий низкий иммунный ответ) и эффективность (например, способствующий эффективной и действенной инкапсуляции терапевтического и/или профилактического средства и доставке агента к желаемой цели), выбирали для применения. Терапевтическое и/или профилактическое средство для составов с композицией наночастиц выбирают для применения в зависимости от состояния субъекта. Например, мРНК, кодирующая сосудистый эндотелиальный фактор роста A (VEGF-A), может быть выбрана для стимуляции ангиогенеза для лечения атеросклеротического реноваскулярного заболевания, тогда как миРНК, способная угнетать экспрессию аполипопротеина B (apoB), может быть выбрана для лечения метаболического заболевания или расстройства, такого как дислипидемия.
[00504] Субъекту, нуждающемуся в лечении, предварительно вводили небольшую дозу дексаметазона за один или более часов до введениея композиции наночастиц. Композицию наночастиц предпочтительно вводили субъекту внутривенно, однако также приемлемы способы внутримышечного, внутрикожного, подкожного, интраназального или ингаляционного введения. Лечение предоставляется в дозе от около 0,001 мг/кг до около 10 мг/кг терапевтического и/или профилактического средства и повторяется ежесуточно, еженедельно, раз в две недели или ежемесячно в соответствии с потребностями субъекта.
Пример 25: Подкожное введение
[00505] Было исследовано влияние липидов по изобретению на экспрессию белка при подкожном введении. Составы, содержащие липиды по данному изобретению и мРНК, экспрессирующую люциферазу или hEPO, вводили подкожно самкам мышей CD-1 в количестве, равном 0,5 мг/кг. Уровни экспрессии были получены с помощью люминесцентной визуализации всего тела (BLI) через 3, 6 и 24 часа после инъекции, а уровни экспрессии в печени, селезенке и в месте инъекции оценивались ex vivo через 24 часа. Обнаружено, что обратные эфиры превосходят MC3, например, в 6,5 раза (соединение 30). См. также таблицы 35 и 36 и Фиг. 19 и 27.
[00506] В таблице 35 приведены уровни экспрессии люциферазы с использованием различных композиций наночастиц по данному изобретению и уровни экспрессии люциферазы с использованием различных композиций наночастиц по данному изобретению по сравнению с уровнем экспрессии люциферазы с использованием состава МС3 после подкожного введения, как описано выше.
[00507] В таблице 36 приведены уровни экспрессии hEPO с использованием различных композиций наночастиц по данному изобретению по сравнению с уровнем экспрессии hEPO с использованием композиции, содержащей MC3 или соединение 18, после подкожного введения, как описано выше.
Пример 26: Разработка новых амино-липидов с улучшенным эндосомальным выходом и устойчивой эффективностью и безопасностью у приматов, не являющихся человеком
Материалы и способы
[00508] Синтез мРНК: мРНК, использованная в описанных в данном документе экспериментах, была синтезирована in vitro с помощью T7-полимеразной транскрипции с линеаризованной ДНК-матрицы, которая содержит 5'- и 3'-нетранслируемые области (НТО), включая поли-А хвост. мРНК очищали и ресуспендировали в цитратном буфере в желаемой концентрации. Донорная метильная группа S-аденозилметионин (SAM) была добавлена к метилированной кэпированной РНК (cap-0), что привело к cap-1 для повышения эффективности трансляции мРНК.
[00509] Синтез липидов: Липидные соединения, протестированные в описанных в данном документе экспериментах, были синтезированы, как описано в Примере 1.
[00510] Приготовление составов LNP: Липиды растворяли в этаноле в молярных отношениях 50:10:38,5:1,5 (ионизируемый липид: DSPC: холестерин:ПЭГ-липид). Липидную смесь объединяли с 6,25 мМ натрий-ацетатным буфером (рН 5), содержащим мРНК в соотношении 3:1 (вода:этанол), с использованием микрофлюидного смесителя. Составы диализовали против натрий-фосфатного забуфера (рН 7,4) в диализных кассетах в течение по меньшей мере 18 часов. Составы концентрировали путем центробежной фильтрации, пропускали через фильтр 0,22 мкм и хранили при 4°С до применения. Все составы были проверены на размер частиц, инкапсуляцию РНК и эндотоксин, и было обнаружено, что они имеют размер от 80 нм до 100 нм, с инкапсуляцией более 90% и <1 ЕЕ/мл эндотоксина. Предположительную pKa состава LNP определяли с помощью анализа TNS.
[00511] Анализ TNS: Стоковый раствор главного буфера (10 мМ фосфат натрия, 10 мМ борат натрия, 10 мМ цитрат натрия, 150 мМ хлорид натрия) готовили и использовали для приготовления буферов при различных значениях pH для определения предположительной pKa составов LNP. Используя гидроксид натрия (1 М) и соляную кислоту (1 М), из стокового раствора главного буфера готовили 21 уникальный буфер при значениях рН между около 3 и 12. Затем стоковый раствор 300 мкМ натриевой соли 6-(п-толуидино)-2-нафталинсульфоновой кислоты (реагент TNS) в ДМСО и LNP смешивали с буфером желаемого состава в концентрации 0,04 мг/мл мРНК. Этот анализ был подтвержден в 1x PBS и 20 мМ Трис с 8% сахарозным буфером. Буферные растворы при различных значениях pH добавляли в 96-луночный планшет в трех повторностях для каждого pH. В каждую лунку добавляли 3,26 мкл образца LNP при концентрации мРНК 0,04 мг/мл и 2,0 мкл 300 мМ раствора реагента TNS. После тщательного перемешивания полученные значения флуоресценции считывали для каждого планшета, чтобы создать сигмоидальный график зависимости значений флуоресценции от рН буфера. Лог точки перегиба этой кривой представляет собой предположительную pKa состава LNP.
Исследования in vivo
[00512] Введение LNP животным: мРНК-LNP, разведенные в натрий-фосфатном буфере (PBS), вводили внутривенно (5 мл/кг) самкам мышей CD-1 (от 18 до 22 г по массе тела) и самцам крыс Спрэг-Доули (225-250 г массы тела) через хвостовую вену с использованием 29 г, 3/10 см3 инсулиновых шприцев (мышам) или 27 г, 1 мл шприцев (крысам) после легкого нагревания животных с использованием тепловой лампы в течение 3 минут.
[00513] Биолюминесцентная визуализация всего тела и органа ex vivo у мышей: Мышам CD-1 инъецировали за 15 минут до момента визуализации внутрибрюшинно (в/б) 200 мкл соли Xenolight D-люциферин K+, разведенной в PBS, непосредственно перед использованием, до концентрации, равной 15 мг/мл. Визуализация органов ex vivo была завершена в течение 25 минут после введения люциферина. Все изображения были определены количественно по области интереса для общего потока.
[00514] Сбор крови и анализ на hEPO. Кровь отбирали у мышей или крыс через хвостовую вену, и концентрации hEPO определяли, используя анализ ИФА hEPO.
[00515] Исследования NHP: Исследования на приматах, отличных от человека проводили с использованием наивных яванских макаков (cynos), 2-4 года, массой 2-6 кг. Ни для одного из исследований на животных не использовались методы рандомизации или слепого лечения. Размеры выборки были определены методом уравнения ресурса. Для инъекции мРНК-LNP в «натрий-фосфатом буфере» (PBS) вводили путем 60-минутной внутривенной инфузии с использованием временного полостного катетера, вставленного в периферическую вену.
[00516] ИФА hEPO для образцов NHP: Уровни Epo человека измеряли с использованием иммуноанализа эритропоэтина человека. Уровни цитокинов измеряли с использованием набора цитокинов приматов, отличных от человека.
[00517] Анализ IgG человека для образцов NHP: Аликвоту матрицы 10,0 мкл переносили в 96-луночный планшет с низким связыванием белка. Добавляли аликвоту 25,0 мкл рабочего раствора внутреннего стандарта и аликвоту образца разбавляли загрузочным буфером. IgG человека и его внутренний стандарт выделяли с использованием магнитных шариков белка А. После промывания захваченные белки денатурировали с использованием Rapigest, восстанавливали с помощью DTT, алкилировали с использованием йодоуксусной кислоты и расщепляли трипсином. Конечный экстракт анализировали с помощью ВЭЖХ с МС/МС детектированием с использованием электрораспыления с положительными ионами. Для количественного определения неизвестных образцов использовали линейный регрессионный алгоритм наименьших квадратов 1/концентрация².
[00518] Уровни ALT и AST в сыворотке: Образцы анализировали с использованием анализатора Modular Analytics.
[00519] Уровни C5b9 в сыворотке: Анализ образца C5b9 проводили с использованием метода ИФА. Используемый набор представлял собой набор ИФА для C5b-9 человека и набор реагентов B от BD Bioscience. Исследуемые образцы анализировали в разведенном 1/100.
[00520] рДНК для измерения уровней мРНК: анализ образца мРНК (метод рДНК (разветвленной ДНК - bDNA - branched DNA)) проводили с использованием набора реагентной системы QuantiGene® 2.0 от Affymetrix. Образцы для исследования лизировали перед анализом с использованием набора для обработки образцов QuantiGene (образцы крови). Исследуемые образцы были проанализированы в дупликатах, разведенных между 1/100 и 1/1250000.
[00521] Количественное определение липидов с помощью LC-МС/МС: Образцы печени гомогенизировали после добавления 19 экв. (мас./об.) воды (DF=20). Белок осаждали и анализировали в отношении калибровочных стандартов, приготовленных в соответствующей заготовке. Хроматографическое разделение и количественное определение осуществляли с помощью системы ЖХ-МС/МС. Образцы инъецировали и разделяли с помощью ВЭЖХ. Для обнаружения сигнала использовали систему трехквадрупольного МС/МС, работающую в режиме положительных ионов.
[00522] Идентификация метаболита: Соединение 18 (10 мкМ) инкубировали с плазмой человека (29,0 мг белка/инкубация) в инкубационных смесях (конечный объем инкубации 200 мкл), которые состояли из 50/50 об./об. чистой плазмы (неразбавленного)/раствора субстрата в 50 мМ фосфатном буфере рН 7,4). Плазма была получена от доноров мужского и женского пола и содержала антикоагулянт K2ЭДТА. Реакции начинали добавлением раствора субстрата в плазму человека и останавливали в четыре назначенных момента времени (0, 30, 60 и 90 мин) путем добавления 600 мкл стоп-реагента (ацетонитрила). Остановленные инкубационные образцы центрифугировали (например, 10000 × g в течение 10 минут при 10°C) и фракции супернатанта анализировали с помощью ЖХ-МС/МС для характеристики метаболитов, образованных из соединения 18. Дополнительные инкубации проводили с прокаином положительного контроля (5 мкМ) для установления компетентности тест-системы. Образцы анализировали методом ЖХ-МС/МС.
[00523] Микроскопический анализ для количественной оценки эффективности эндосомального выхода: Флуоресцентно меченные LNP (0,1% Rhodamine DOPE), инкапсулирующие люциферазу светляка, химически модифицированную in vitro транскрибированную мРНК (Rhod-Luc LNP), использовали для количественного определения поглощения LNP, а одиночная молекула FISH (smFISH) позволяла количественно определять количество цитозольных молекул мРНК. Клетки HeLa высевали в 96-луночные планшеты с использованием культуральной среды DMCC АТСС, и после достижения 80% слияния клетки инкубировали с метками для цитоплазматической и ядерной детекции с последующей трансфекцией LNP Rhod-Luc при 25 нг (мРНК) на лунку в объему 100 мкл. Клетки инкубировали с LNP в течение 4 ч, затем образцы фиксировали в 4% параформальдегиде и визуализировали в системе скрининга с высоким содержанием с конфокальной визуализацией (Система скрининга с высоким содержанием Opera).
[00524] Параллельно клетки подвергали электропорации с несформированной мРНК люциферазы. Электропорированные клетки высевали в лунки рядом с лунками, обработанными LNP, и весь планшет фиксировали в одно и то же время. После визуализации планшета для поглощения LNP образцы обрабатывали для гибридизации smFISH. Планшет визуализировали, используя конфокальную визуализацию, и объектный анализ использовали для количественного определения количества одиночной молекулы цитозольной мРНК (R, высвобождаемой из эндоцитических органелл) в образцах, обработанных LNP, с использованием электропорированных образцов в качестве эталона. Совместное окрашивание эндоцитарными маркерами EEA1 (ранние эндосомы) и Lamp1 (лизосомы) использовали для подтверждения результатов анализа, основанного на интенсивности.
[00525] LNP Rhod-Luc были нанесены непосредственно на стекло и отображены с использованием тех же параметров сбора, которые использовались для клеток, обработанных LNP. Внутриклеточное поглощение LNP (количество LNP на клетку, L) рассчитывали как отношение между суммой интенсивности флуоресценции на клетку в родаминовом канале (CellInt) и средней интенсивностью флуоресценции отдельных объектов LNP на стекле (LNPInt). Коэффициент эндосомального выхода (EER), определяемый как соотношение между количеством цитозольной мРНК и интернализованными LNP (R/L), был использован для сравнения эффективности эндосомного побега между двумя составами, использованными в этом исследовании (соединение 18 и MC3).
[00526] Статистический анализ: Средние значения сравнивали с использованием обычного одностороннего ANOVA с апостериорными тестами для множественных сравнений (Dunnett для сравнения нескольких условий с одним эталоном или Šídák для сравнения пар условий). Площади под кривой (AUC) были рассчитаны с использованием правила трапеции и вычислено значение z. Для всех тестов двусторонние значения P <0,05 считались статистически значимыми и продемонстрированы на Фиг. как* < 0,05, ** < 0,005 или *** < 0,001. Использовали Prism 7.0b
Оптимизация липидного хвоста
[00527] В ходе первоначального скрининга широкого химического пространства идентифицировали этаноламин в качестве аминогруппы липидного хвоста, который мог бы эффективно стимулировать инкапсуляцию мРНК и обеспечивать LNP превосходными физико-химическими свойствами. Объединение этаноламиновой головной группы с дилинолевыми липидными хвостами (соединение 281) привело к получению LNP с высокой инкапсуляцией мРНК люциферазы, небольшим размером частиц и низким коэффициентом полидисперсности. LNP с соединением 281 имел поверхностную pKa (кажущееся значение для частицы) в диапазоне, который, как было проиллюстрировано, является оптимальным для доставки миРНК. (См. Semple, S.C. et al., Nature Biotech. 2010. 28, 172-176, Jayaraman, M., et al. Angew. Chem. Int. Ed. 2012, 51, 8529-8533, полное содержание каждой из которых в полном объеме включено в данный документ посредством ссылки). Чтобы оценить эффективность новых аминолипидов, LNP с применением новых соединений тестировали in vivo на мышах с использованием мРНК люциферазы в качестве репортера. MC3 LNP был включен в качестве контроля в каждом эксперименте, позволяя сравнивать LNP от эксперимента к эксперименту. Измеренная активность люциферазы также позволила определить биораспределение белка. Внутривенная доставка 0,5 мг/кг (доза мРНК) LNP на основе соединения 281 мышам приводила к активности люциферазы в два раза ниже, чем в контроле MC3 LNP (Фиг. 29A). Визуализация всего тела показала, что большая часть экспрессии белка была локализована в печени. Липид имел сходный клиренс с МС3 из ткани печени, при этом 66% исходной дозы оставалось в ткани печени мышей через 24 часа после введения дозы (Таблица 37).
[00528] Было проверено влияние сложноэфирных связей в липидных хвостах на тканевый клиренс (соединения 138 и 136). Ранее сообщалось, что сложноэфирные связи вызывают метаболизм эстеразами in vivo. (См. Fukami, T. et al. Drug Metab. Pharmacokinet. 2012, 27, 466-477, полное содержание которых включено в данный документ посредством ссылки). Было продемонстрировано, что данная стратегия улучшает клиренс липидов в структуре липидов на основе MC3. (См. Maier M.A., Mol. Ther. 2013, 21, 1570-1578, полное содержание которых включено в данный документ посредством ссылки). Сначала химическую стабильность липидов оценивали путем измерения стабильности этанола при комнатной температуре и температуре 37°C (Таблица 39). Изменение чистоты менее 1% наблюдали для всех исследуемых липидов. LNP, образованные с соединением 138, были больше, с поверхностной pKa> 7. Для этих LNP наблюдался быстрый тканевый клиренс, липидов не было обнаружено через 24 часа (Таблица 37). Удаление одной сложноэфирной функции (соединение 136) давало LNP с улучшенными физико-химическими характеристиками и более низкой поверхностной pKa LNP.
[00529] Улучшение экспрессии белка наблюдали при введении разветвленного сложного эфира (соединение 6). Наблюдали эквивалентную экспрессию для MC3 LNP, но скорость клиренса была ниже, чем для соединений 138 и 136 (оставалось 67% липидов, Таблица 37). Замена линолевого хвоста липидным хвостом, содержащим первичный сложный эфир (соединение 18), обеспечивала повышенную экспрессию (в 3 раза выше, чем у МС3) и оптимальный тканевый клиренс (липид не обнаружен через 24 часа, Таблица 37). Для дальнейшего увеличения экспрессии вводили дополнительный разветвленный сложный эфир (соединение 29), но это приводило к снижению поверхностной pKa до 6,00 и снижению активности люциферазы. Кроме того, соединение имело значительно более медленный клиренс в тканях: 68% оставалось на 24 часа.
[00530] Соединение 14 представляет собой один из иллюстративных примеров, в котором спиртовая функциональная группа была заменена диметиламином. Это дало LNP с физико-химическими свойствами, сопоставимыми со свойствами соединения 18, но с полной потерей эффективности доставки (Фиг. 29А).
[00531] Соотношение активности и структуры липидного хвоста было дополнительно изучено, в частности, положение первичного сложного эфира и его влияние на эффективность доставки и тканевый клиренс (сравните соединение 18, соединения 25 и 26, Таблица 37). У мышей, используя мРНК люциферазу, мы наблюдали более высокую экспрессию по сравнению с МС3 после внутривенной доставки дозы 0,5 мг/кг с соединением 25 и соединением 26, причем соединение 26 обеспечивало самую высокую активность люциферазы в ряду (Фиг. 29А). Аналогичные результаты были получены у крыс Спрег-Доули с использованием мРНК, кодирующей человеческий эритропоэтин (hEPO) (Фиг. 29C). При определении исходных уровней аминолипидов в печени по окончании исследования на крысах (48 ч после введения дозы) было установлено, что клиренс уменьшается, поскольку первичный сложный эфир приближается к азоту (<1% для соединения 18, соединения 25 и 20% для соединения 26, Таблица 37). Соединение 18 и соединение 25 обеспечили хороший баланс эффективности доставки и фармакокинетики.
[00532] Не желая быть связанными теорией, было обнаружено, что множественные структурные мотивы аминолипида важны для эффективного действия мРНК-содержащих липидных наночастиц in vivo, включая поверхностный заряд, структуру и положение сложного эфира в липидных хвостах и структуру головной группы. Липиды, которые обеспечивали высокий уровень экспрессии белка, демонстрировали быстрый клиренс в ткани и приводили к профилю токсичности, который поддерживал хронические терапевтические показания. Наблюдалась вариация на поверхности pKa частиц, которая отслеживалась по эффективности экспрессии. Среднее значение 6,6 было определено как оптимальное. Однако наличие оптимального диапазона pKa не было единственным требованием для эффективной доставки, поскольку соединение 14 демонстрировало низкие уровни экспрессии люциферазы (таблица 37). Введение первичного эфира, аналогичное тому, что наблюдалось в сериях на основе МС3, обеспечивало липиды, которые демонстрируют быстрый клиренс in vivo. Исследования по идентификации метаболитов с соединением 18 показали, что гидролиз первичного эфира является первым этапом метаболизма липидов. Чтобы этот гидролиз был эффективным, необходимо сбалансировать стерику и электронику сложного эфира. Более замещенные сложные эфиры (соединение 29) и менее электрофильные сложные эфиры (соединение 26) каждый демонстрировали более медленный клиренс в печени. Комбинация этаноламиновой головной группы, первичного эфира в положении С8 в одном липидном хвосте и вторичного эфира во втором липидном хвосте, по-видимому, обеспечивает хороший баланс клиренса липидов in vivo и экспрессии белка.
Фармакокинетическое исследование
[00533] Было проведено фармакокинетическое исследование на крысах, в котором сравнивали соединение 18 и соединение 25 с МС3 (Фиг. 29В). В отличие от MC3, который все еще присутствовал в высоких концентрациях в течение 48 часов, соединение 18 и соединение 25 были эффективно выведены из ткани печени через 24 часа. Соединение 18 было удалено из ткани печени быстрее, чем соединение 25 с периодом полужизни в ткани печени 5,8 ч против 6,9 ч соответственно (полные параметры ФК см. В таблице 40). Этот быстрый клиренс резко контрастировал с периодом полужизни> 50 ч MC3 Благоприятное расщепление липидов in vivo для соединения 18 и соединения 25 также наблюдалось в селезенке и плазме (таблица 40).
[00534] Ожидается, что повторное дозирование мРНК в LNP на основе MC3 для терапевтического показания приведет к накоплению MC3 в тканях на основе измеренного периода полужизни. Поэтому было исследовано, поддерживалась ли благоприятная однократная фармакокинетика соединения 18 при еженедельном дозировании. Клиренс МС3 и соединения 18 из множества тканей мыши измеряли после введения мРНК 0,05 мг/кг в 1, 8 и 15 сутки (Фиг. 30А). После дозирования с помощью LNP MC3 липид был обнаружен в печени, селезенке, плазме, почках, сердце и легких, при этом в печени и селезенке имелись самые высокие концентрации (Фиг. 30A, полный перечень тканей см. на Фиг. 35A). Накопление MC3 наблюдалось после каждой дозы. Печень и селезенка имели самые высокие уровни соединения 18, однако значительно более низкие уровни, чем MC3. Соединение 18 также было обнаружено в плазме, легких и почках, но не в сердце (Фиг. 35А). Последовательные уровни экспрессии наблюдались, когда мРНК hEPO 0,5 мг/кг вводили мышам внутривенно в LNP на основе соединения 18 (Фиг. 30B), демонстрируя возможность повторного введения дозы.
[00535] Также проводились исследования идентификации метаболитов in vitro с использованием соединения 18. Эти исследования показали, что начальной стадией метаболизма соединения 18 был первичный гидролиз сложного эфира до соединения 166 (таблицы 41 и 42). Исчезновение исходного соединения 18 и первичного метаболита, соединения 166, из ткани печени мыши измеряли после введения мРНК 0,25 мг/кг в дни 1, 8 и 15. Как можно видеть на Фиг. 30C, наблюдался быстрый клиренс обоих исходных соединений 18 и метаболита, соединение 166.
Экспрессия у приматов, отличных от человека
Приматы, отличные от человека более близко аппроксимирует клинические ответы для систем на основе LNP, чем грызуны (DeRosa, F., Guild, B., Karve, S., Smith, L., Love, K., Dorkin, J.R., et. al. Therapeutic efficacy in a hemophilia B model using a biosynthetic mRNA liver depot system. Gene Ther. 2016, 23, 699-707, содержание которой включено в данный документ посредством ссылки в полном объеме. Чтобы перевести данные грызунов в данные приматов, отличных от человека (NHP), липиды были протестированы на NHP. Для этой цели оценивали, может ли улучшенная экспрессия, наблюдаемая у мыши и крысы с LNP, содержащими соединение 18, также быть достигнута у NHP после однократного введения. На Фиг. 31 показаны результаты, достигнутые с двумя различными грузами мРНК. Доза 0,01 мг/кг мРНК, кодирующей hEPO, доставлялась путем 60-минутной внутривенной инфузии. Относительно контроля MC3 LNP наблюдалось в пять раз более высокое воздействие белка hEPO (Фиг. 31А). Аналогично, с использованием второго груза мРНК, кодирующего антитело против IgG-гриппа A человека, наблюдали 5-кратное увеличение экспрессии и четкую реакцию на дозу по сравнению с L3P MC3 (Фиг. 31B и Фиг.36). В отдельном исследовании оценивали накопление липида в ткани у NHP после однократного введения. В соответствии с результатами, полученными на грызунах, остаток MC3 был обнаружен во многих тканях через 12 часов после введения дозы, причем самые высокие уровни обнаружены в печени и селезенке. Напротив, соединение 18 присутствовало на значительно более низких уровнях (Фиг. 35В). Эти предварительные данные демонстрируют трансляцию улучшенной эффективности доставки и быстрого удаления соединения 18 у NHP.
[00536] Эксперименты демонстрируют межвидовую транслятивность. Многократные исследования экспрессии и фармакокинетики (ФК) у разных видов показали сходные профили у мышей, крыс и приматов, отличных от человека. Внутривенная доставка мРНК, содержащей соединения LNP на основе соединения 18, примату приводила к эффективной экспрессии множества белков (Фиг. 31А и 31В) с аналогично улучшенной экспрессией по сравнению с МС3, как это наблюдалось у грызунов. Кроме того, быстрое выведение липидов из ткани также наблюдалось у NHP. Была продемонстрирована эффективная экспрессия с LNP соединения 18 в течение 5 недель дозирования (Фиг. 31C).
Токсикологическое исследование у приматов, отличных от человека
[00537] Был оценен уровень экспрессии, обеспечиваемый LNP по изобретению в эксперименте с повторной дозой приматов. Доза мРНК hEPO, равная 0,2 мг/кг в LNP на основе соединения 18 доставляли посредством 60-минутной внутривенной инфузии яванским макакам (n=4) один раз в неделю в течение 5 недель. Наблюдалось постоянное воздействие в течение эксперимента (Фиг. 31С) в соответствии с наблюдениями на грызунах.
[00538] Затем была проведена проверка переносимости и безопасности LNP на основе соединения 18 in vivo. Полная токсикологическая оценка LNP на основе соединения 18 как у крыс Спрэг-Доули, так и у яванских макаков была выполнена с использованием стандартного одномесячного исследования с еженедельным дозированием при трех уровнях дозы для каждого вида. Крысам вводили дозу 0,05, 0,5 и 2 мг/кг, а приматам, не являющимся человеком, - дозу 0,1, 0,3 и 1 мг/кг. Связанные с LNP токсичности, связанные с системами LNP на основе MC3, обычно связаны с иммунологическими (активация цитокинов и комплемента) и поражением печени. У крысы не было никаких неблагоприятных результатов с соединением 18. На Фиг. 32 и 33 представлены 30-суточные уровни аланинтрансферазы (ALT, Фиг. 32A) и аспартатаминотрансферазы (AST, Фиг. 32B), двух показателей повреждения печени. Существует минимальное повышение уровня любого фермента при любом уровне дозы по сравнению с контролем PBS, и эта тенденция согласуется со всеми измеренными клинической химией, гематологией и иммунологическими маркерами. Это резко контрастирует с профилем токсичности мРНК на основе MC3, содержащей LNP, где при дозе мРНК 0,3 мг/кг были повышены ALT и АСТ, а патология показала признаки некроза (Фиг. 37).) (Sedic, M., Senn, J.J., Lynn, A., Laska, M., Smith, M., Platz, S.J., et al. Safety Evaluation of Lipid Nanoparticle-Formulated Modified mRNA in the Sprague-Dawley Rat and Cynomologus Monkey. Vet. Pathol. 2017, 55, 341-354., содержание которого полностью включено в данное описание посредством ссылки).
[00539] Яванские макаки также продемонстрировали минимальные результаты при всех уровнях дозы. Измерение уровней циркулирующей мРНК после каждой дозы демонстрировало постоянное воздействие в течение эксперимента (Фиг. 37). Уровни ALT (Фиг. 32C) и AST (Фиг. 32D) для дозы 1 мг/кг на 30-е сутки были на том же уровне, что и контроль. Минимальное повышение маркеров иммунной активации, включая комплемент и цитокины, не наблюдалось. Как показано на Фиг. 33A, не наблюдалось значительного изменения уровней C5b9, продукта активации терминального комплемента после дозы 1 или дозы 5. На Фиг. 33B показано небольшое изменение выше исходного уровня, наблюдаемое для «хемо-привлекательного белка моноцитов» (MCP-1).
[00540] Оптимизация нового ряда аминополипидов привела к значительному улучшению переносимости у крыс и приматов, не являющихся человеком, по сравнению с МС3, что частично связано с улучшенным метаболическим профилем. У крыс и яванских макаков в дозах до 2 мг/кг и 1 мг/кг дозы, соответственно, никаких признаков повреждения печени или активации комплемента не было обнаружено после пяти недель еженедельного приема. Эти данные показывают, что повторное дозирование мРНК, содержащейся в липидных наночастицах по данному изобретению, приводит к поддержанию уровней циркулирующего LNP без каких-либо признаков токсичности.
Оценка эффективности эндосомального выхода
[00541] Была исследована улучшенная эффективность доставки, особенно поглощение и/или эндосомального выхода, например, относительно MC3. Исследования экспрессии у мышей, нокаутированных по ApoE, и у мышей, нокаутированных по LDLr, с LNP на основе соединения 18 показали почти полную потерю экспрессии, что указывает на то, что этот ряд аминополипидов имеет механизм поглощения, сходный с MC3, и функционирует зависимым от ApoE-зависимым образом LDLr (Фиг. 38). (См. Akinc, A. et al. Mol. Ther. 2010, 18, 1357-1364, содержание которого полностью включено в данное описание посредством ссылки). Чтобы лучше понять эффективность эндосомального выхода, был разработан анализ на основе клеток in vitro с использованием меченных родамином LNP для количественного определения клеточного поглощения и флуоресцентной гибридизации in situ (FISH) для обнаружения мРНК, которая выделяет эндоцитарные компартменты. Как можно видеть на Фиг. 34, клетки, обработанные LNP на основе соединения 18, имеют значительно меньшее количество мРНК, агрегированной органеллой (красной), по сравнению с клетками, обработанными LNP на основе MC3. В то же время плотность одиночных цитозольных объектов мРНК выше в клетках, обработанных LNP на основе соединения 18. Чтобы количественно сравнить эффективность эндосомального побега для двух составов LNP, было рассчитано соотношение между количеством цитозольных мРНК и количеством интернализованных LNP на уровне отдельных клеток (таблица 38). Результаты демонстрируют 6-кратное увеличение эффективности для соединения 18 по сравнению с MC3 в LNP (соотношение 0,76 и 0,13 соответственно).
[00542] Ранее было подсчитано, что менее 2% LNP на основе миРНК, которые поглощаются клеткой, высвобождают свой груз в цитозоль. (См. Gilleron, J. et al. Nature Biotech. 2013, 31, 638-646, содержание которого полностью включено в данное описание посредством ссылки). Используя флуоресцентную микроскопию с одной молекулой, эффективность эндосомного побега (рассчитанная как соотношение между количеством цитозольных мРНК и количеством интернализованных LNP на клетку) количественно определяли в системе in vitro. Показано, что эффективность для соединения 18 увеличивается в 6 раз по сравнению с МС3 (соотношение 0,76 и 0,13 соответственно). Поскольку эти составы инкапсулируют приблизительно 5 молекул мРНК на одну частицу, представленные в данном документе коэффициенты выхода из эндосом составляют 15 и 2,5% эффективности побега эндосом для соединения 18 и МС3 соответственно.
[00543] Результаты исследования приведены в таблицах 37-42. В таблице 37 приведены физико-химические характеристики наночастиц. Эффективность эндосомального выхода представлена в таблице 38. Чистота липидов приведена в таблице 39. В таблице 40 представлены фармакокинетические параметры мыши. Результаты метаболического профилирования и характеристики соединения 18, инкубированного с гепатоцитами человека или плазмой человека, приведены в таблицах 41 и 42 соответственно.
ляции
PK-анализ отдельных данных по концентрации в плазме и ткани проводился с использованием неподтвержденной программы (Phoenix WinNonlin®, версия 7.0 (Pharsight Corp., Маунтин Вью, штат Калифорния)). Кинетические параметры оценивались с использованием некомпартментальной модели (Plasma (200-202), равномерное взвешивание, внесосудистое дозирование с разреженным отбором проб). AUC рассчитывали с использованием линейного правила трапеции.
Все производные параметры представлены в 3 значащих цифрах, за исключением времени до пиковой концентрации (Tmax) и периода полужизни (HL), которые представлены в одном десятичном знаке. Никаких дополнительных статистических анализов не проводилось для данных о концентрации в плазме или полученных фармакокинетических параметров.
Эквиваленты
Следует понимать, что хотя данное раскрытие было описано в сочетании с его подробным описанием, вышеприведенное описание предназначено для иллюстрации, а не для ограничения объема данного раскрытия, который определяется объемом прилагаемой формулы изобретения. Другие аспекты, преимущества и изменения находятся в пределах объема нижеизложенной формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2830163C2 |
| НОВЫЕ СОЕДИНЕНИЯ | 2018 |
|
RU2767652C2 |
| НОВЫЕ АЛКИЛИРУЮЩИЕ СРЕДСТВА | 2013 |
|
RU2632206C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛПИРРОЛИДИНОВ И N-АРИЛПИПЕРИДИНОВ | 2013 |
|
RU2547046C1 |
| НОВЫЕ СОЕДИНЕНИЯ | 2018 |
|
RU2783078C2 |
| Оксазолидиноны на основе производных пиридоксина, обладающие антибактериальной активностью | 2024 |
|
RU2836570C1 |
| ПРОИЗВОДНЫЕ АМИНОПИРИМИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРА АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2021 |
|
RU2826628C1 |
| ПРОИЗВОДНОЕ БЕНЗОЛА, ЗАМЕЩЕННОЕ 1,2-ДИ(ЦИКЛИЧЕСКОЙ ГРУППОЙ) | 2006 |
|
RU2407735C2 |
| 6, 6-БИЦИКЛИЧЕСКИЕ КОЛЬЦЕВЫЕ ЗАМЕЩЕННЫЕ ГЕТЕРОБИЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ ПРОТЕИНКИНАЗ | 2005 |
|
RU2379308C2 |
| ИНГИБИТОРЫ ГЛИКОЛАТОКСИДАЗЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2805308C2 |
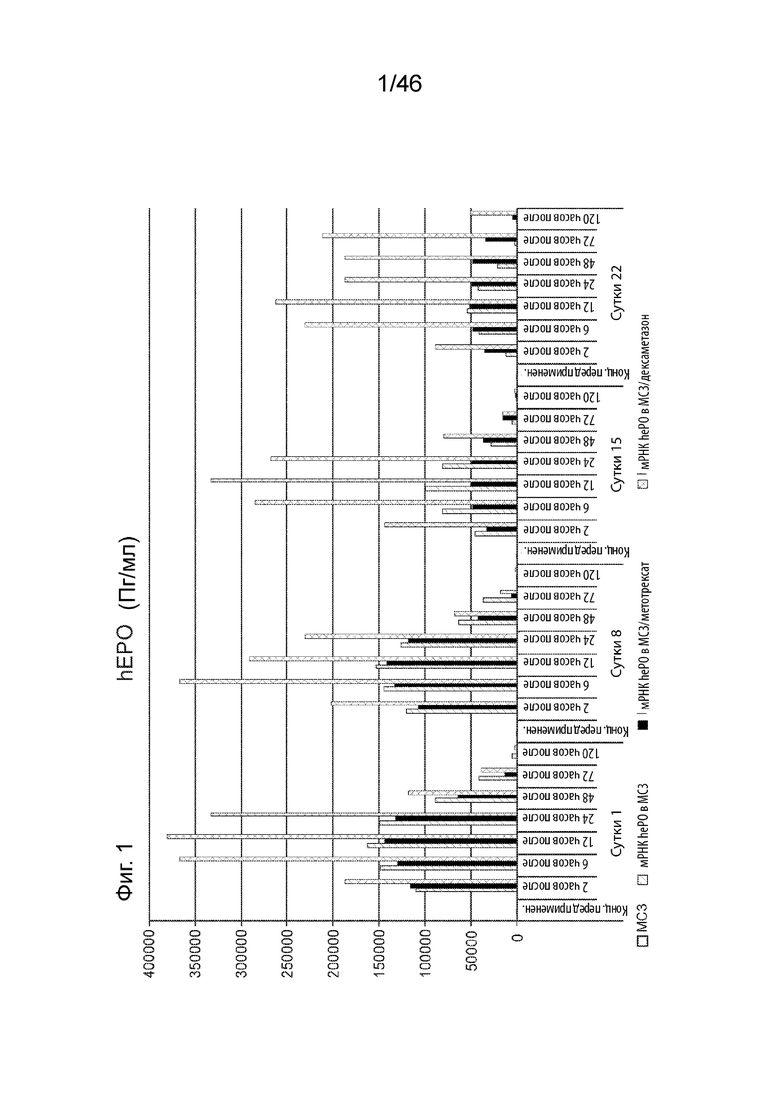
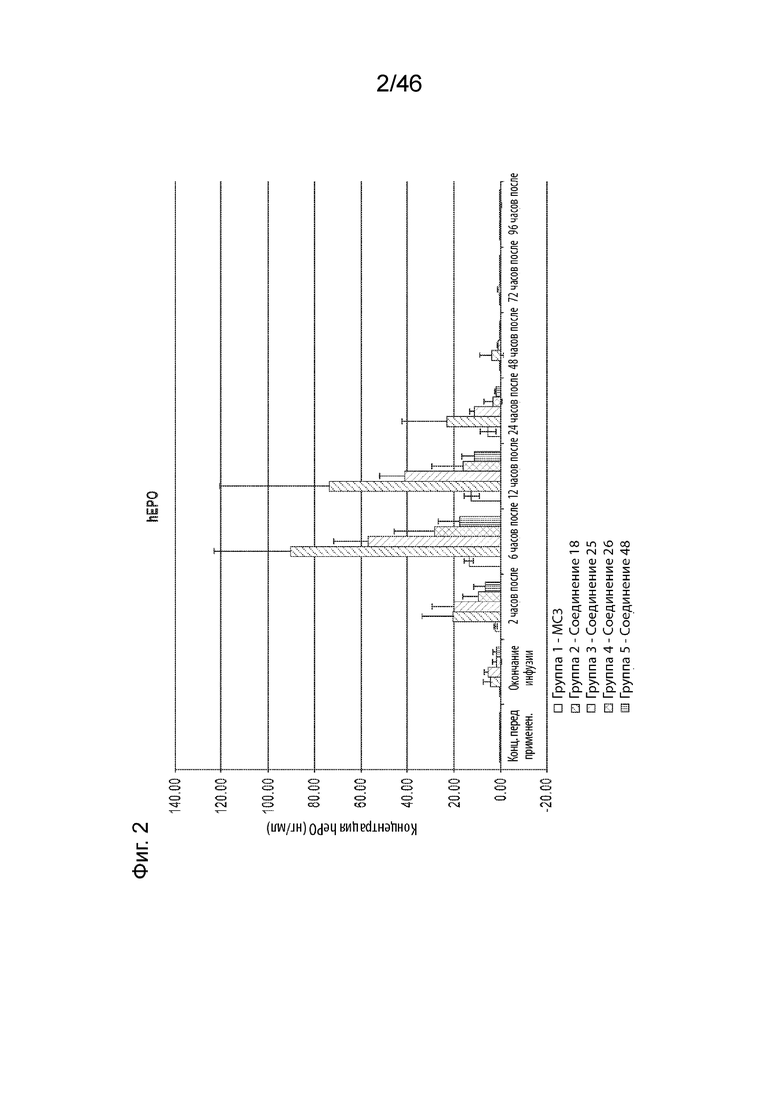
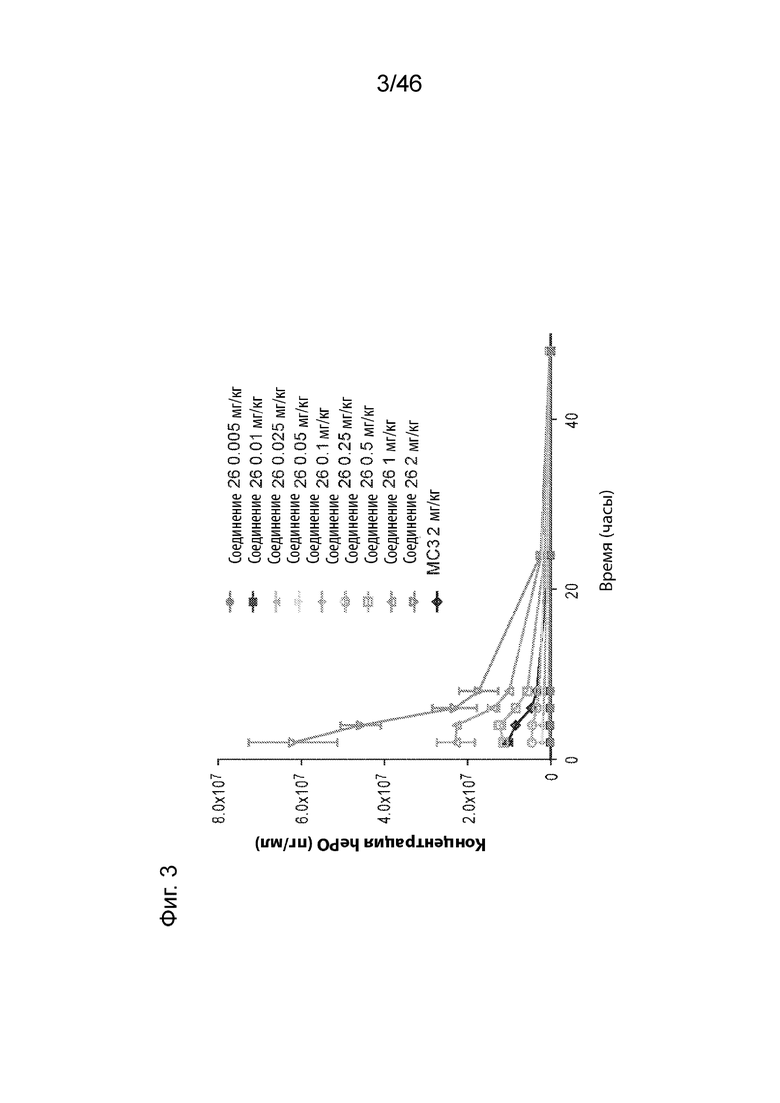
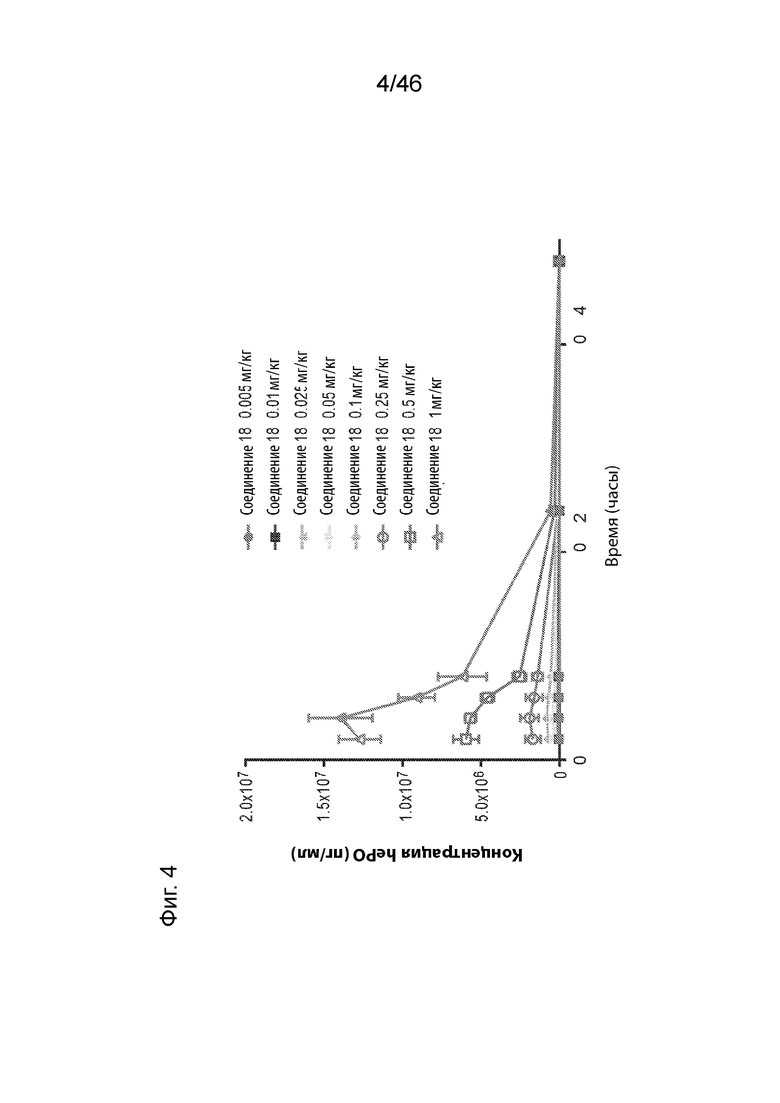

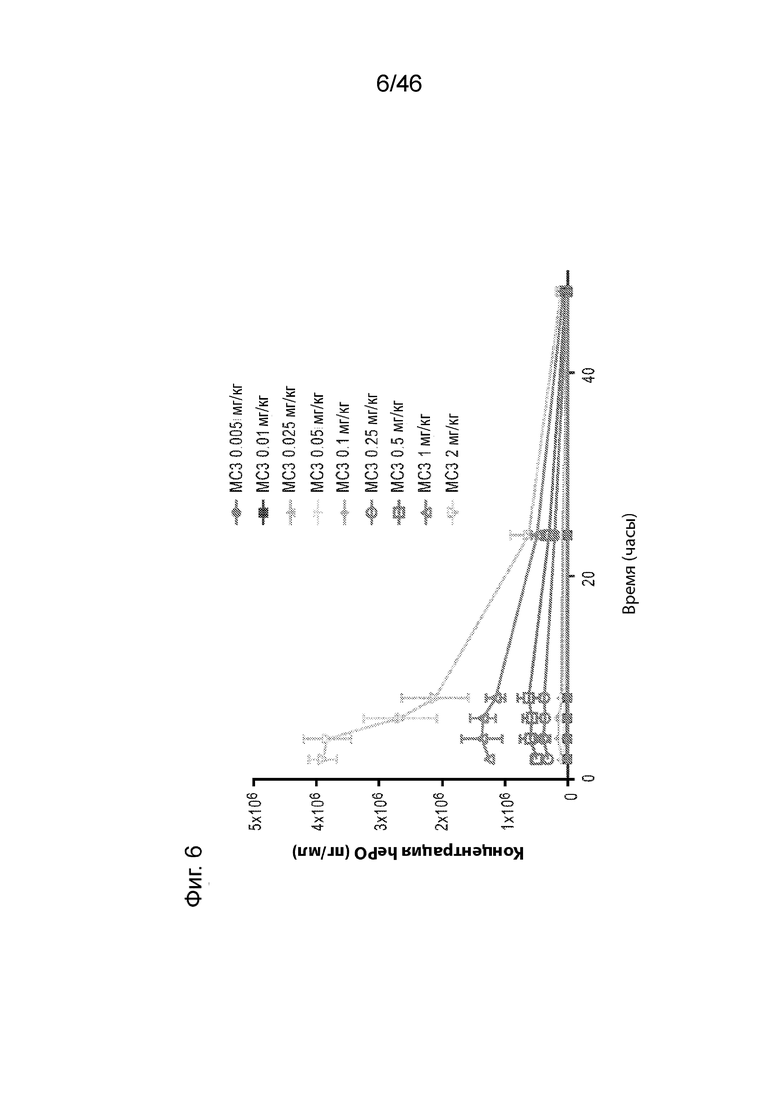
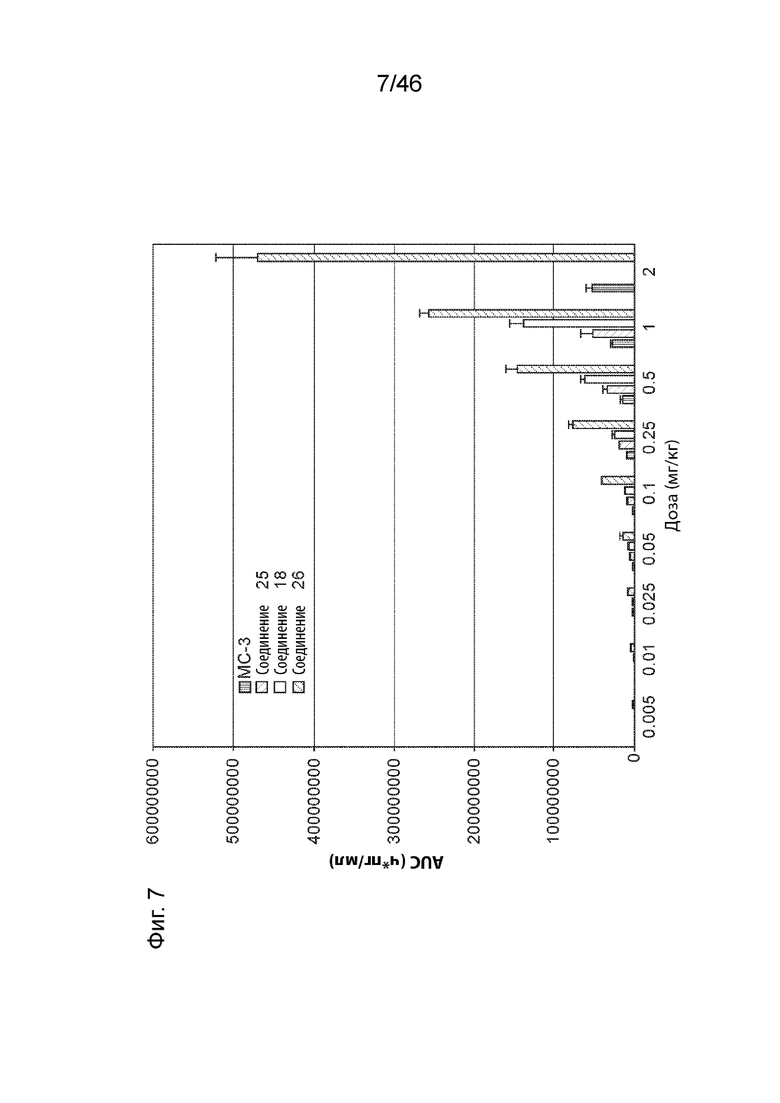
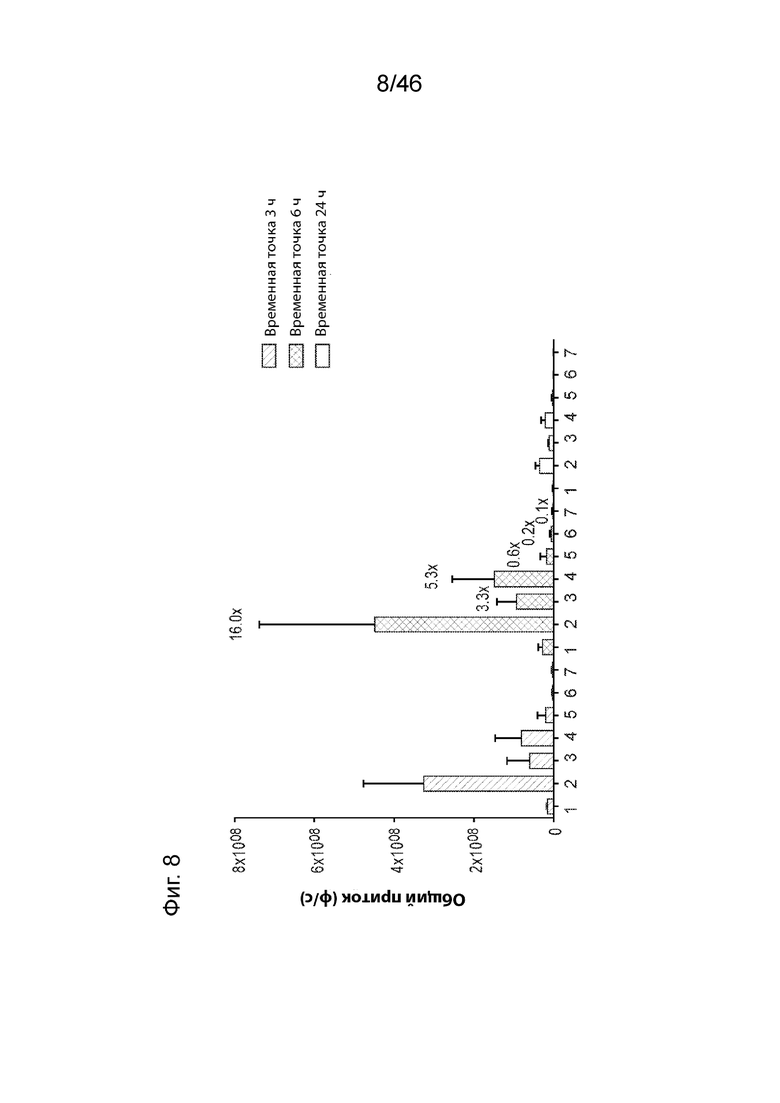
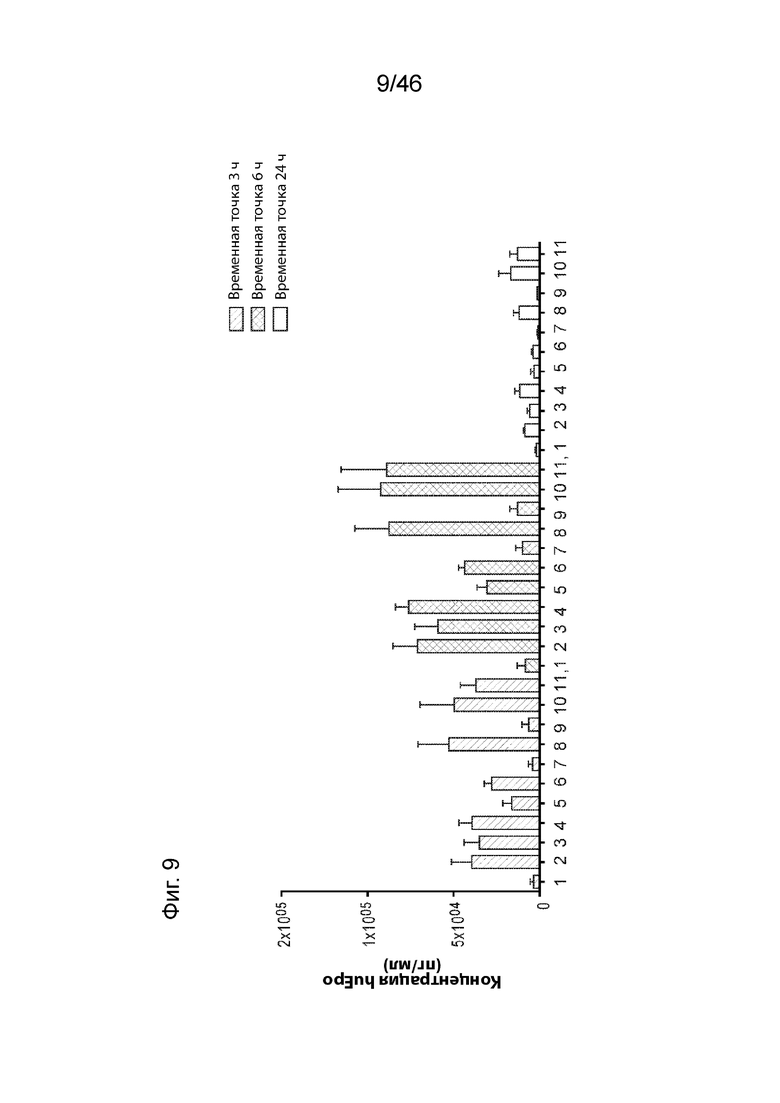
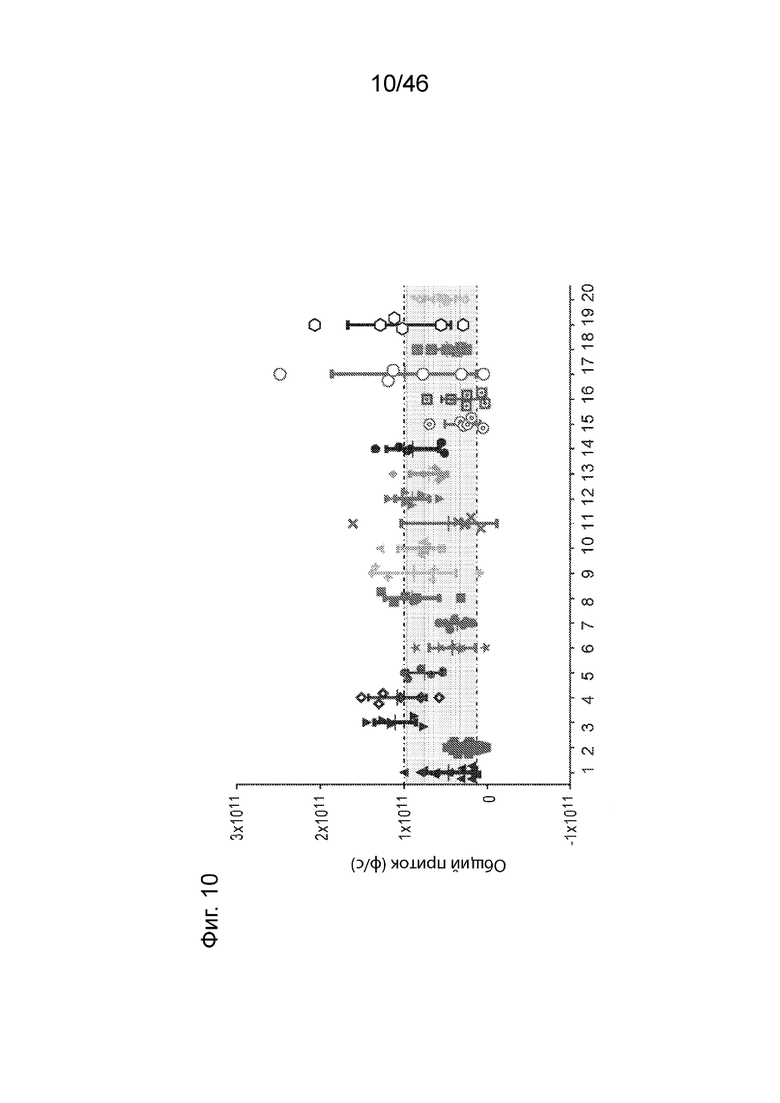
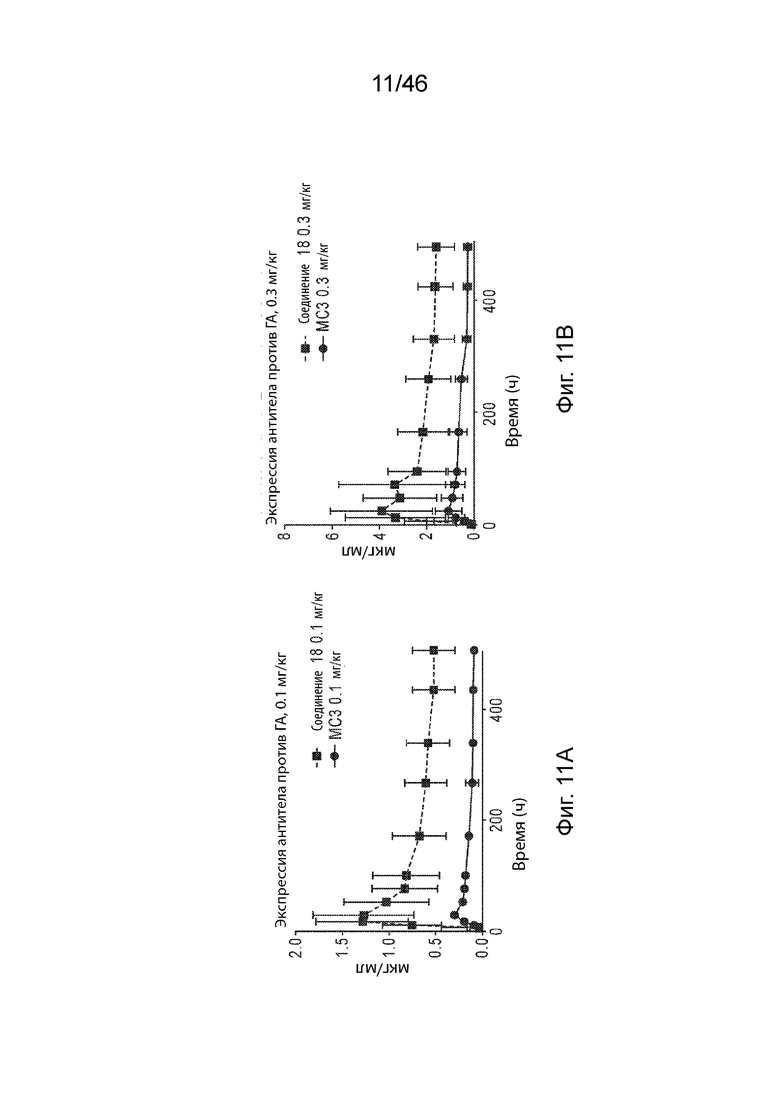
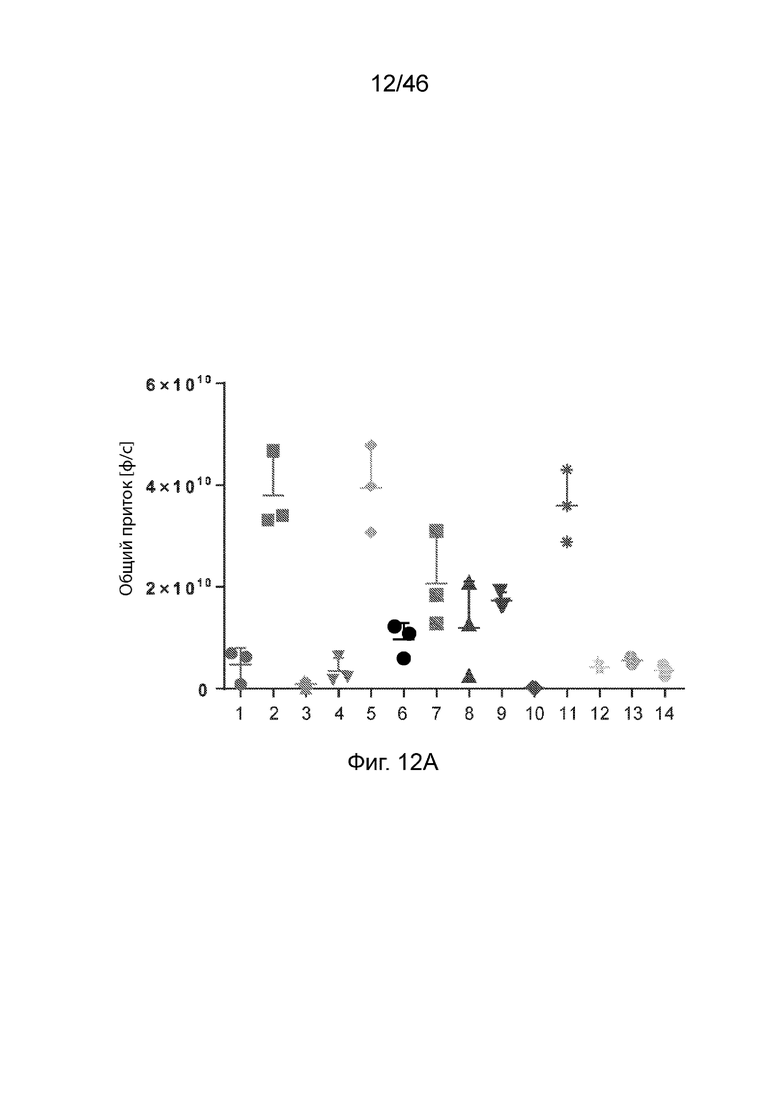
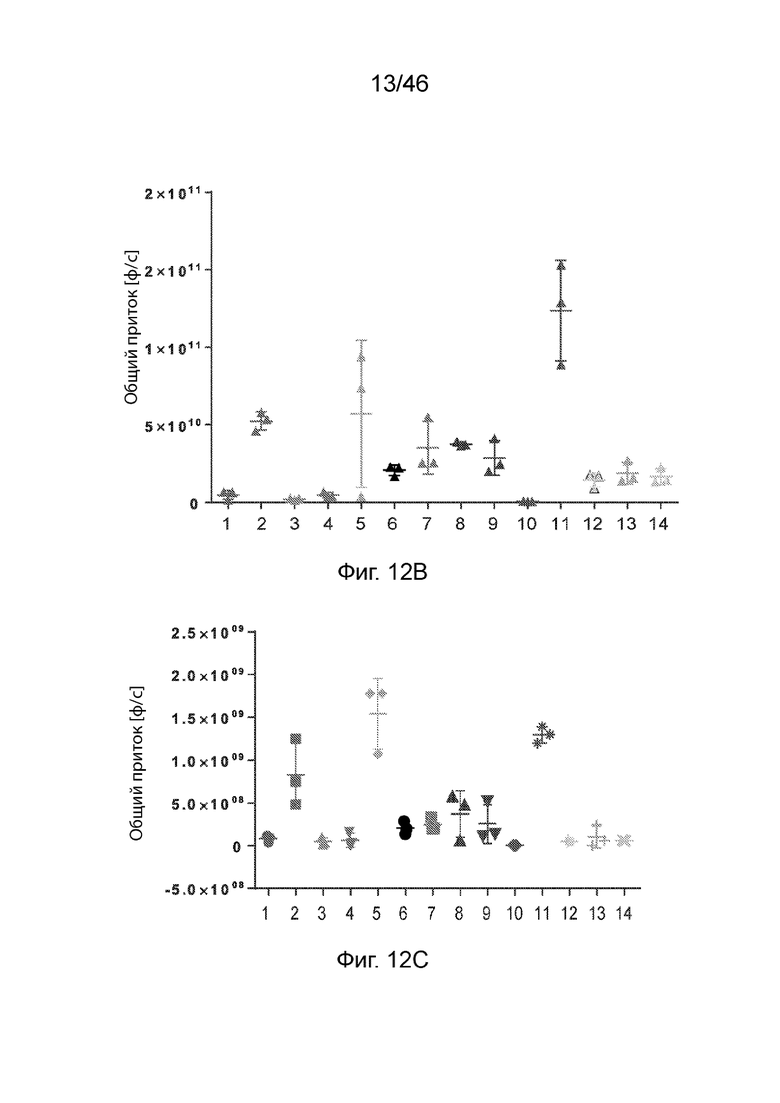
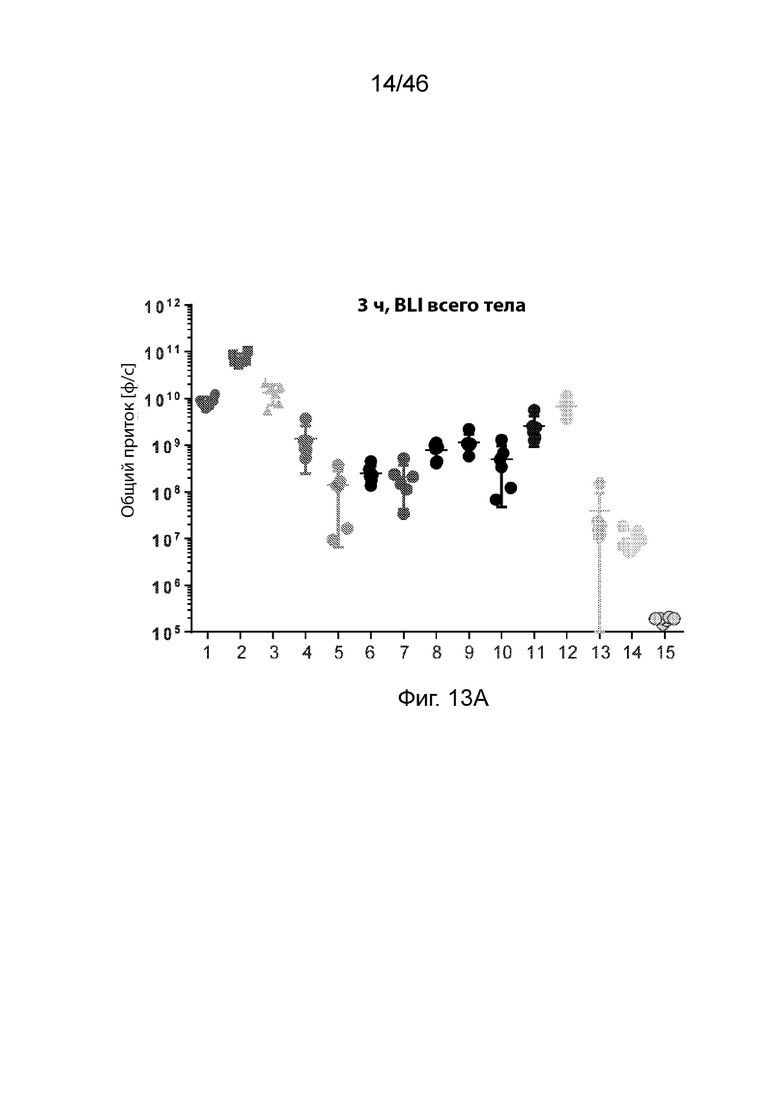
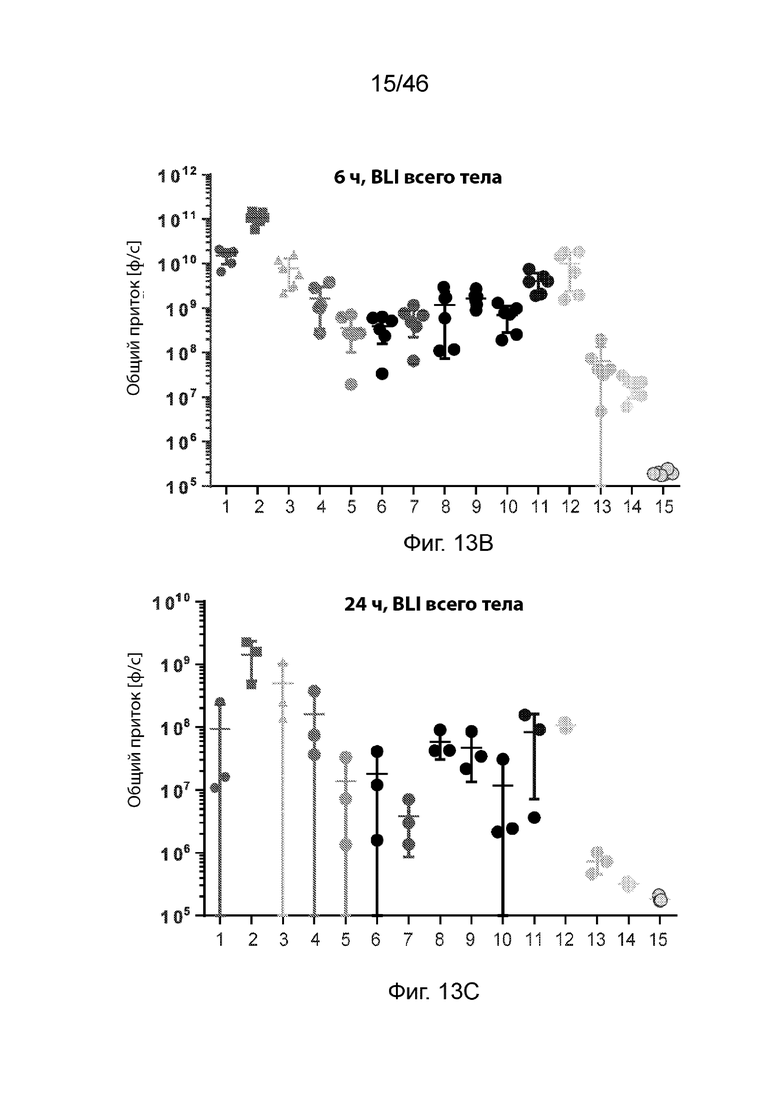
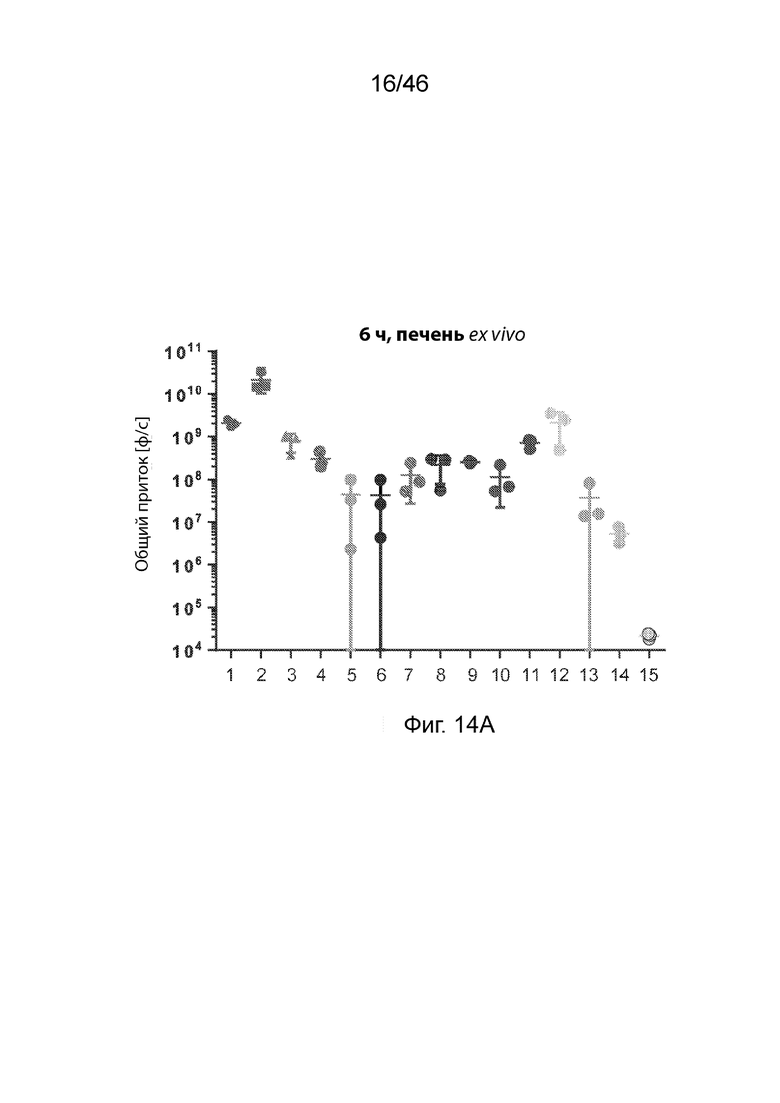
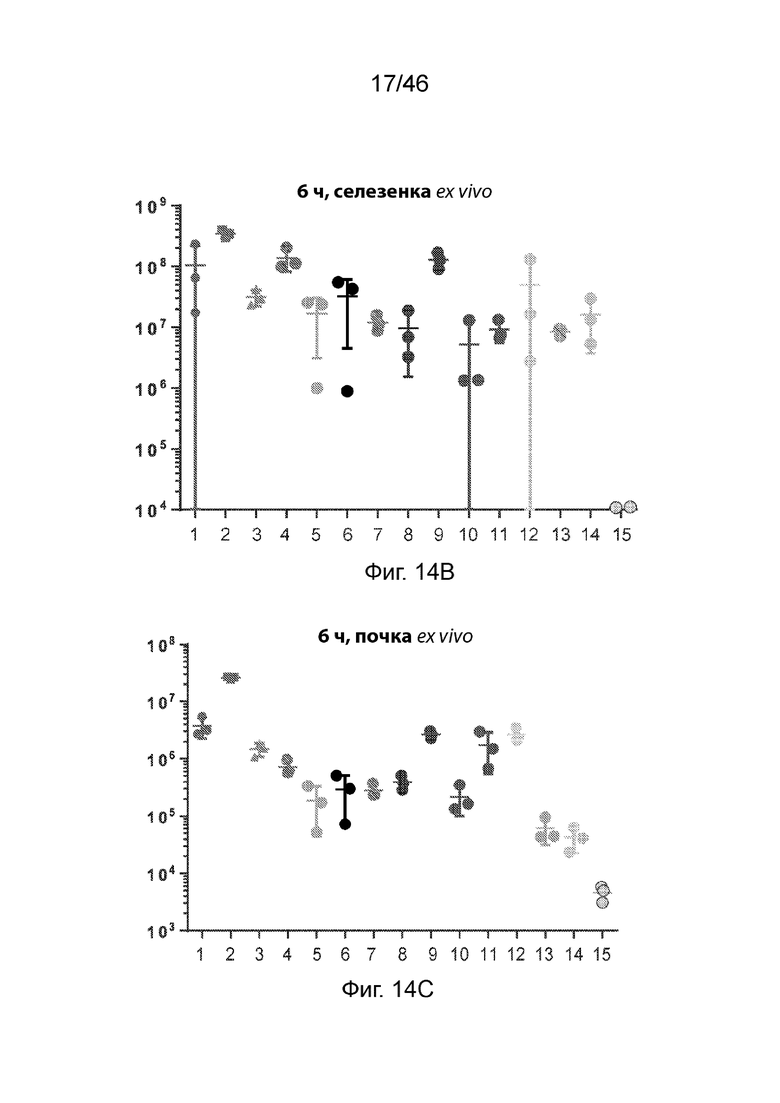
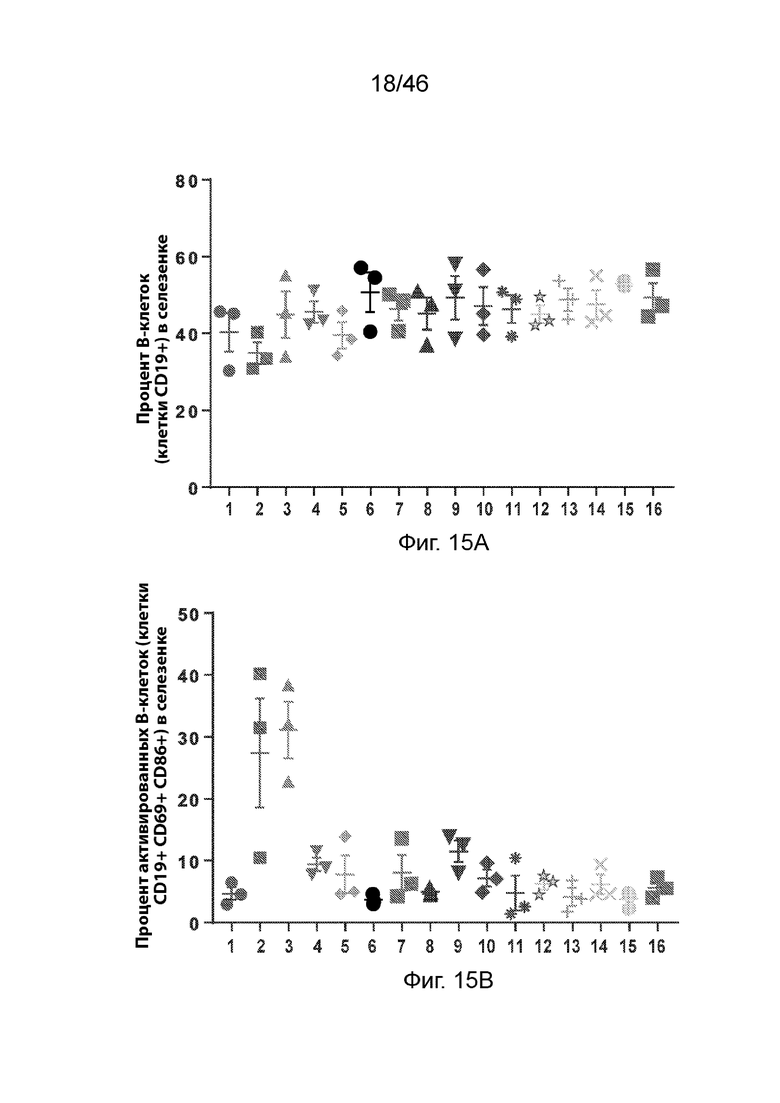
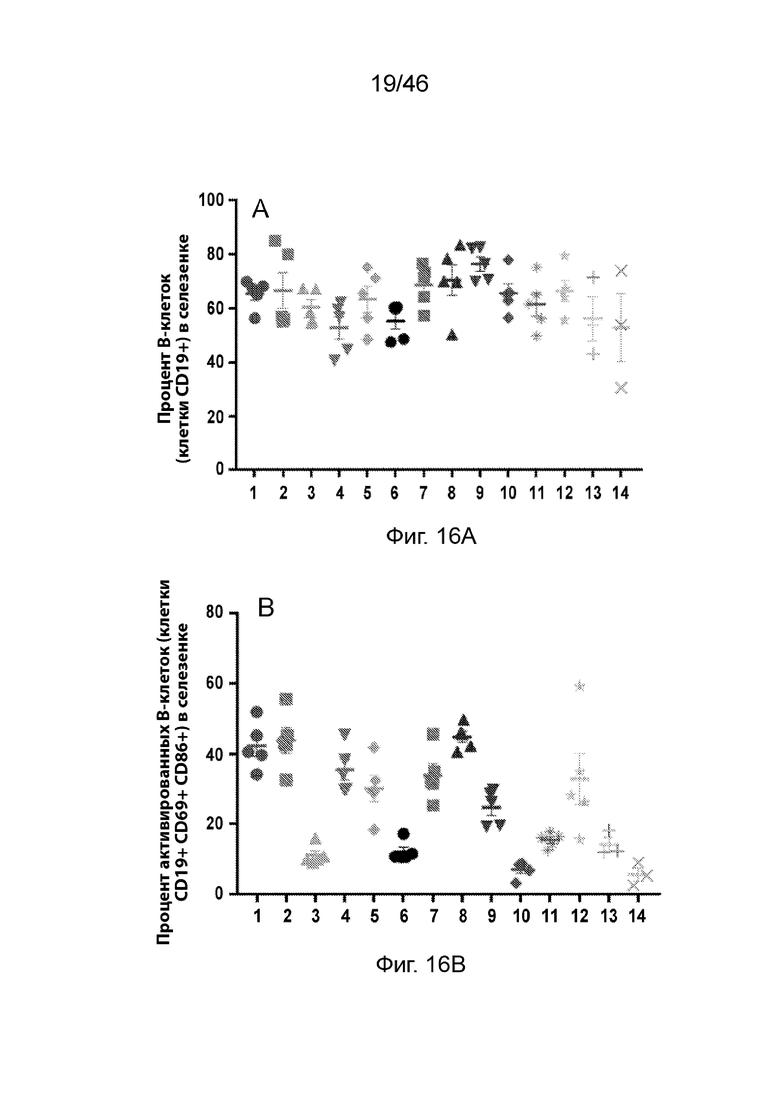

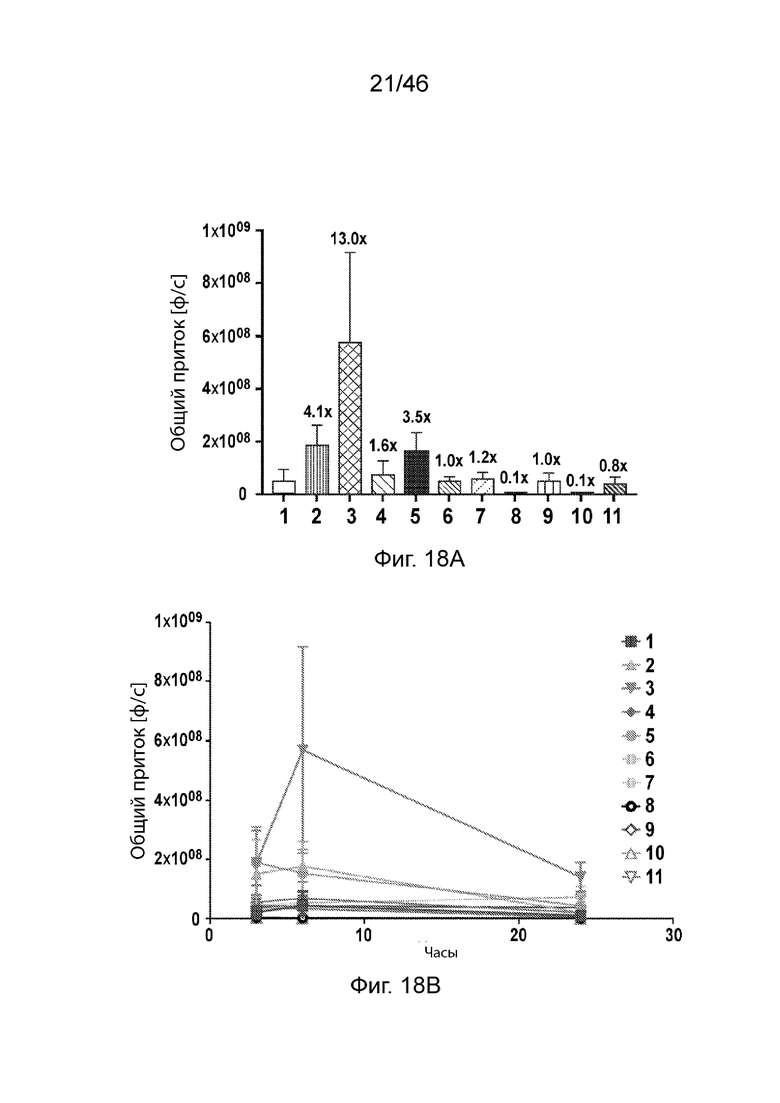


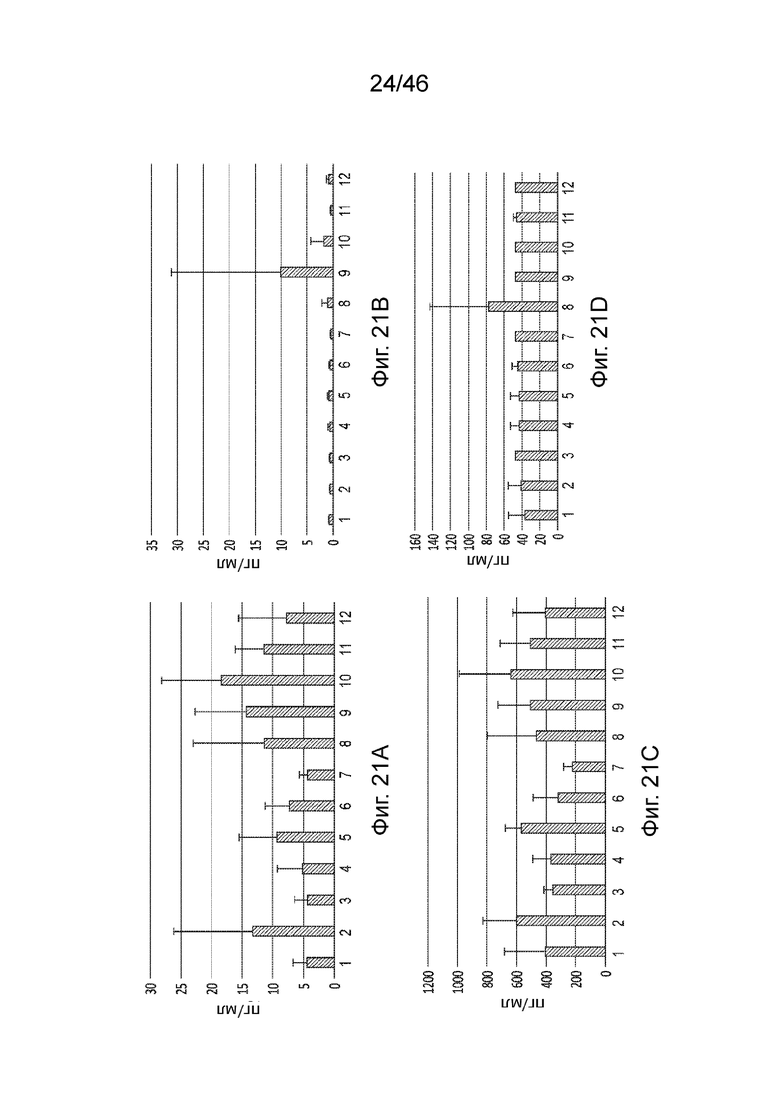
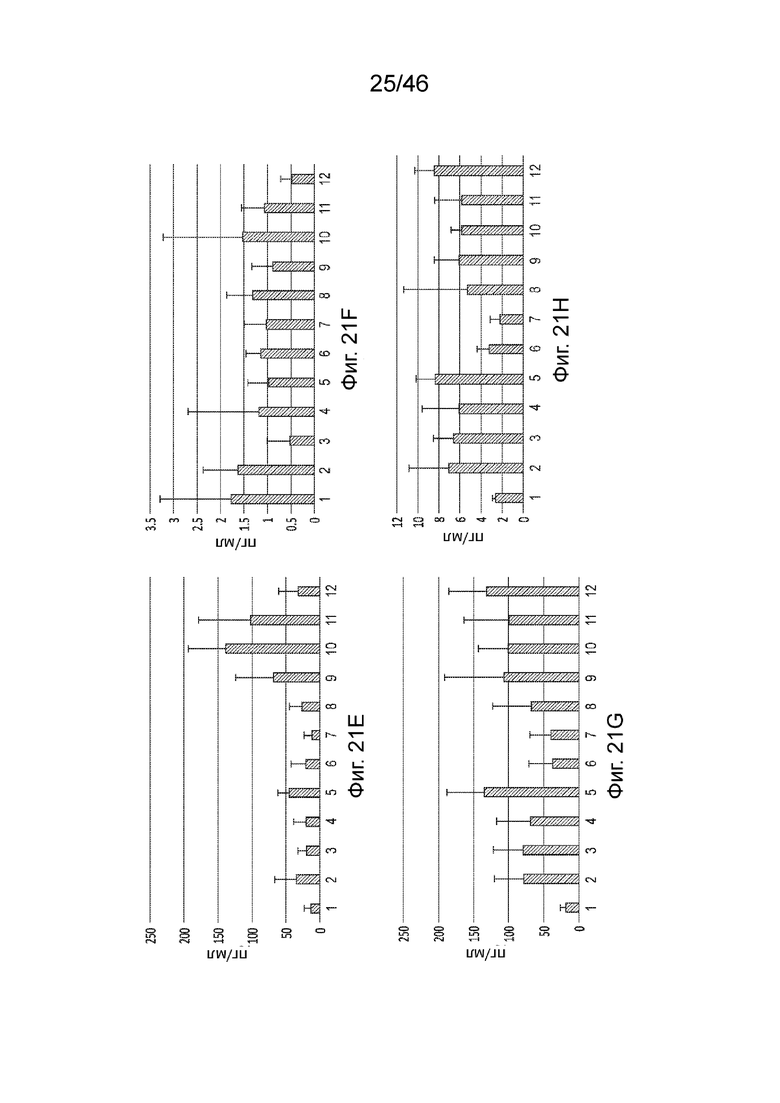
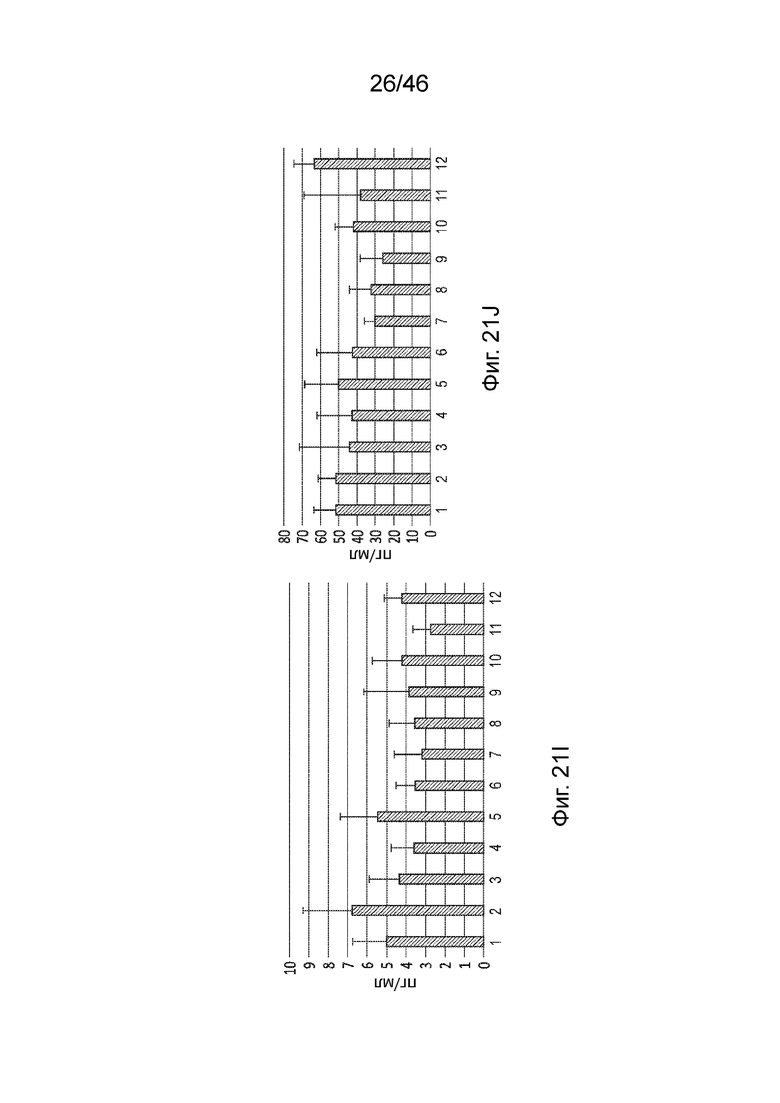
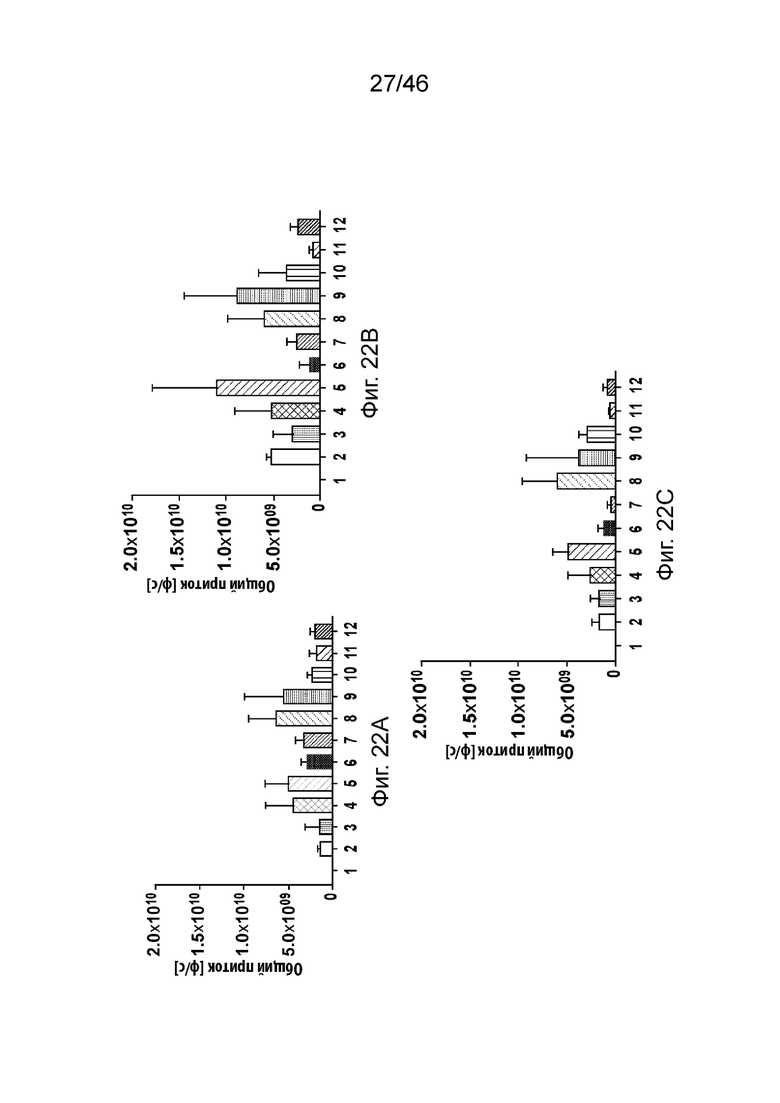

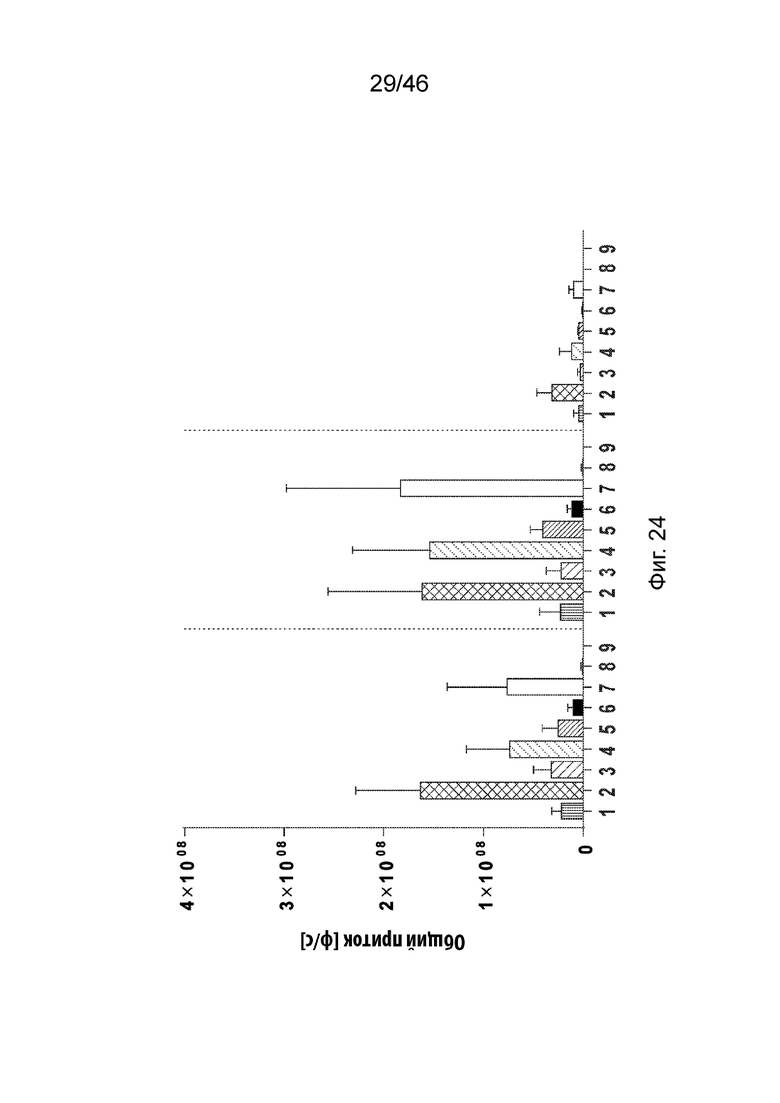
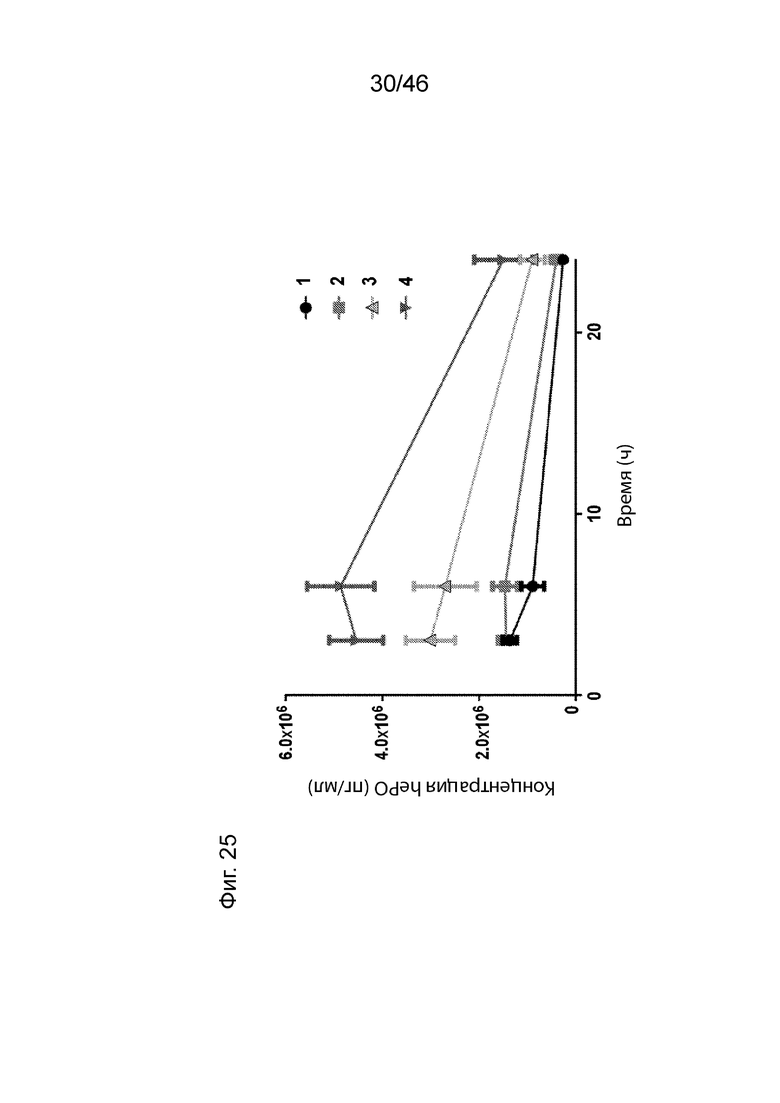


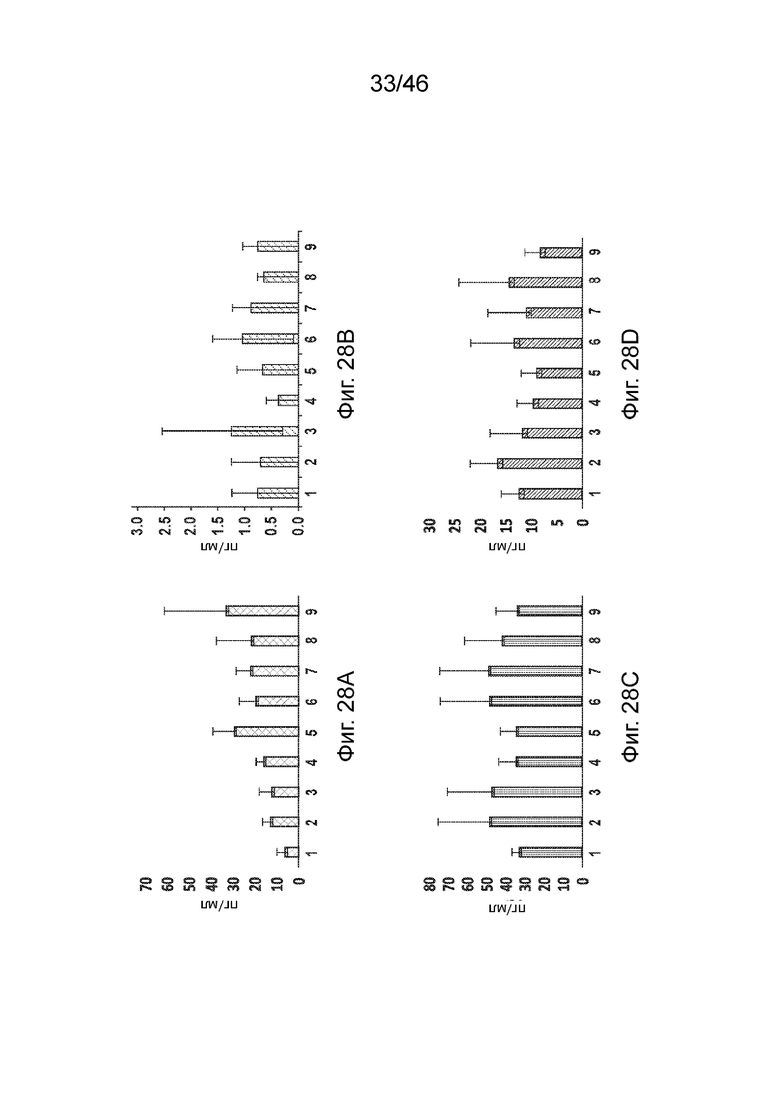
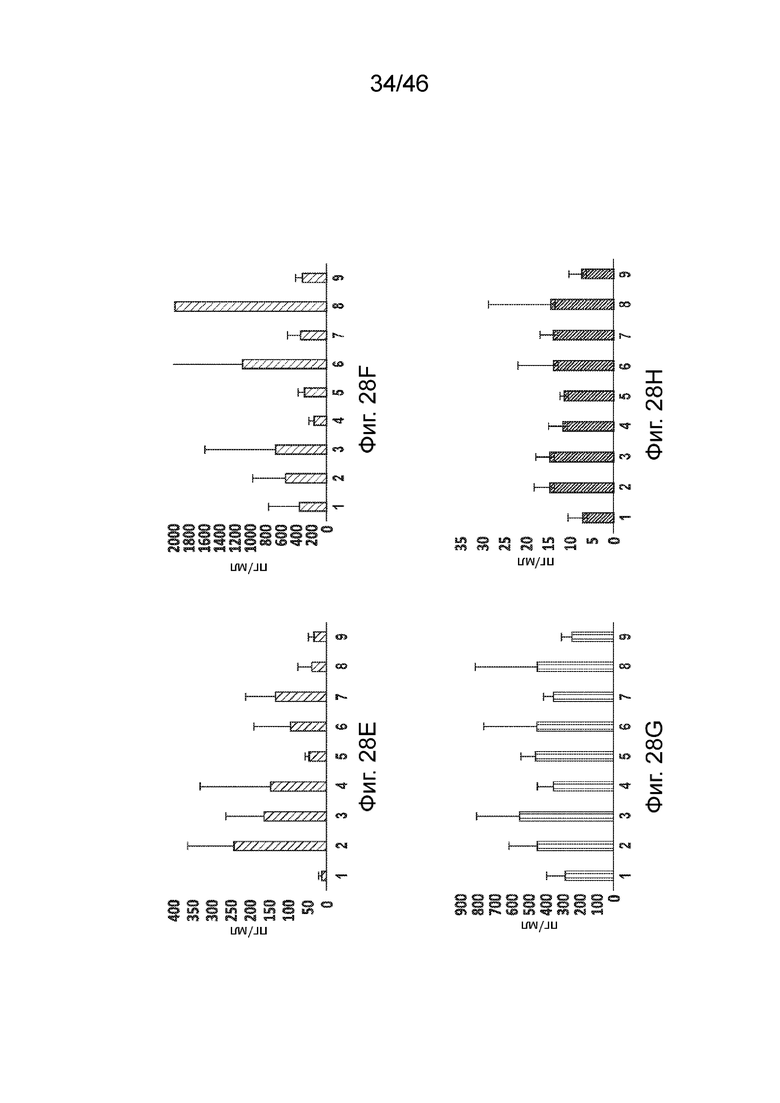
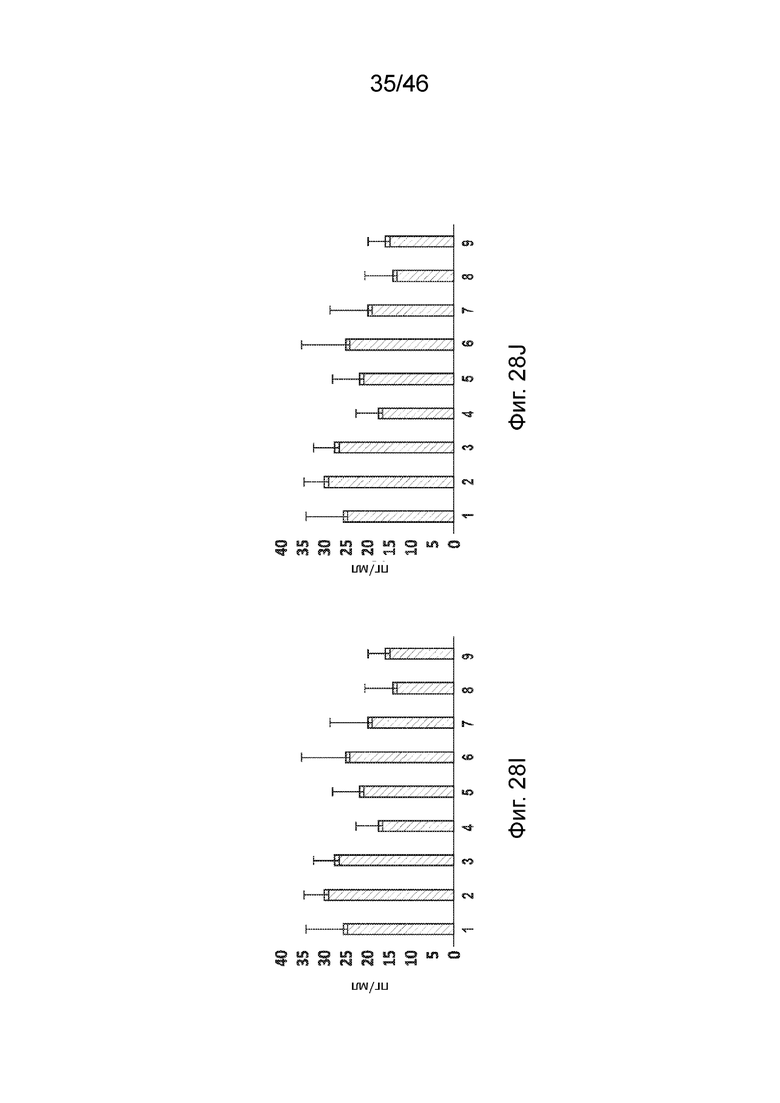
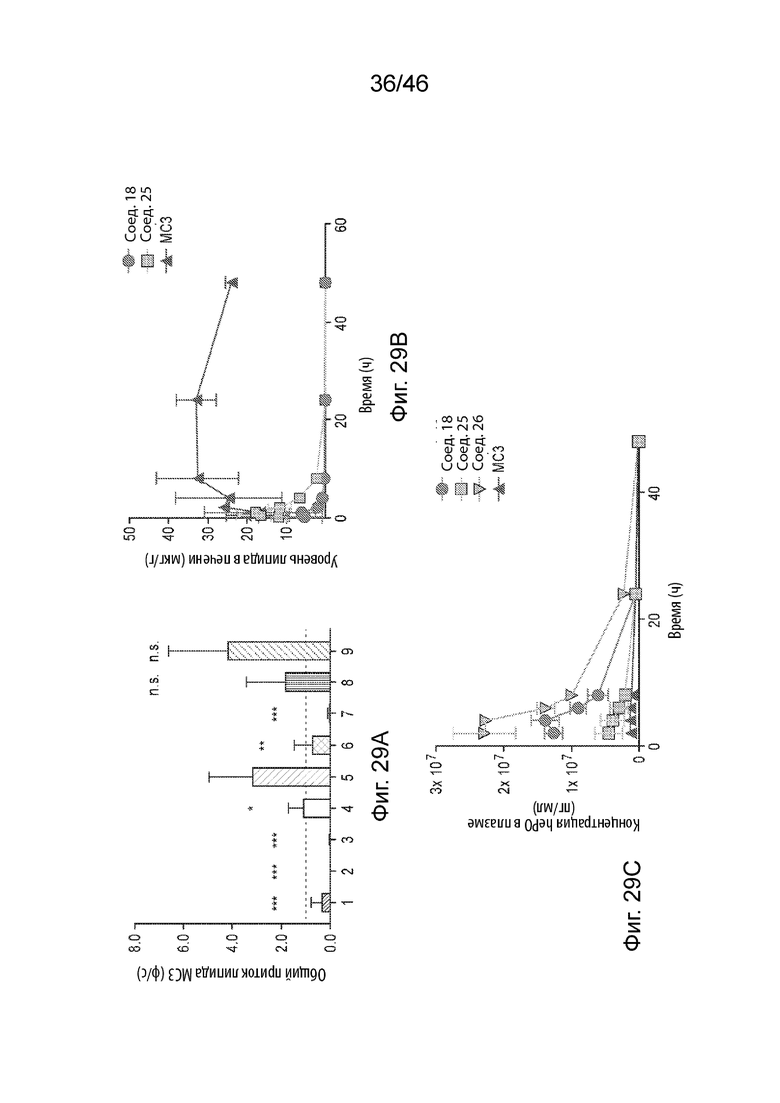

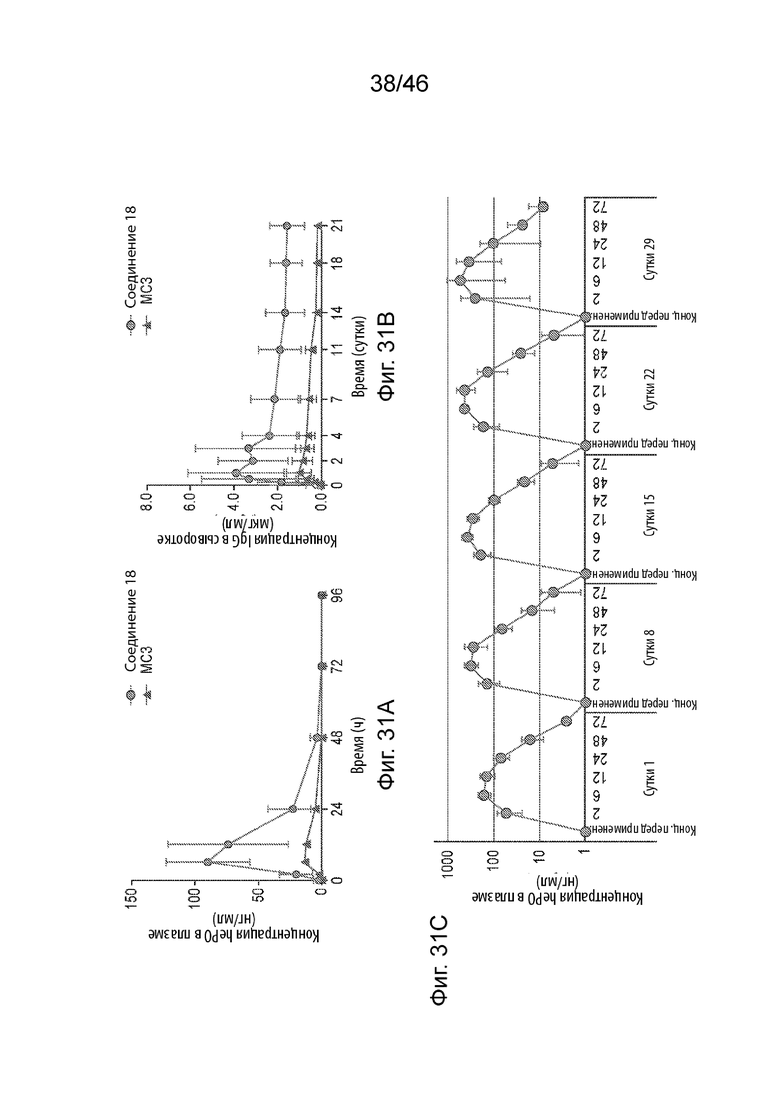

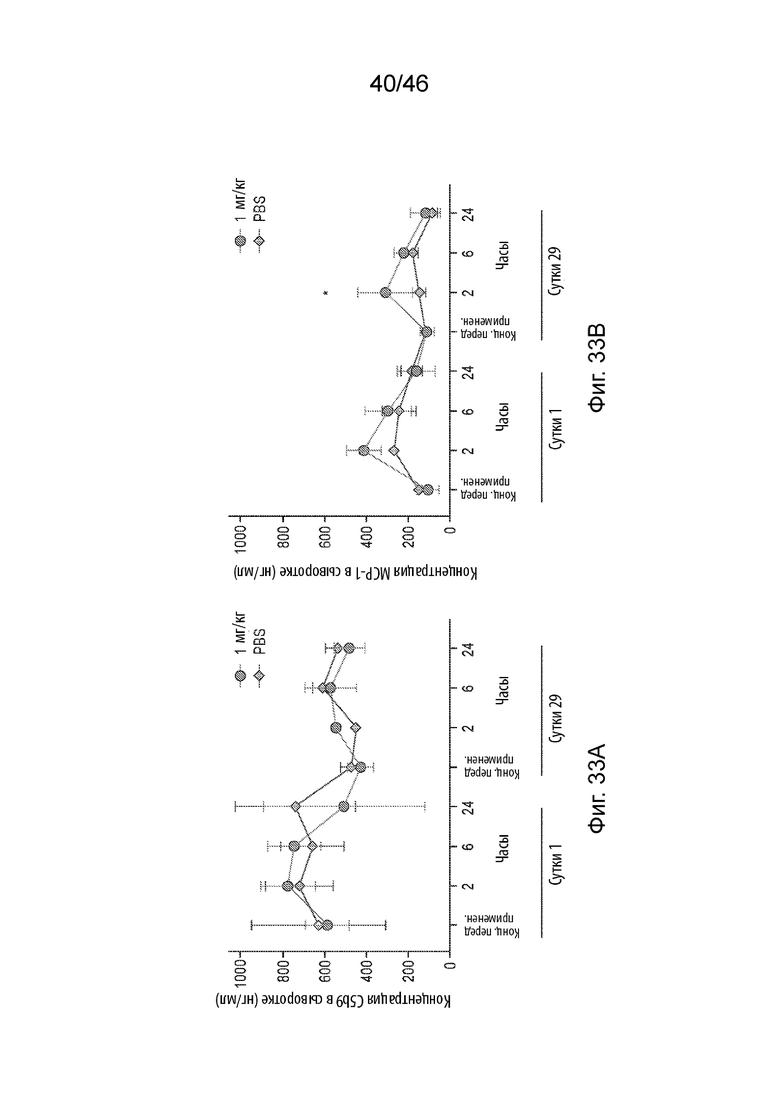
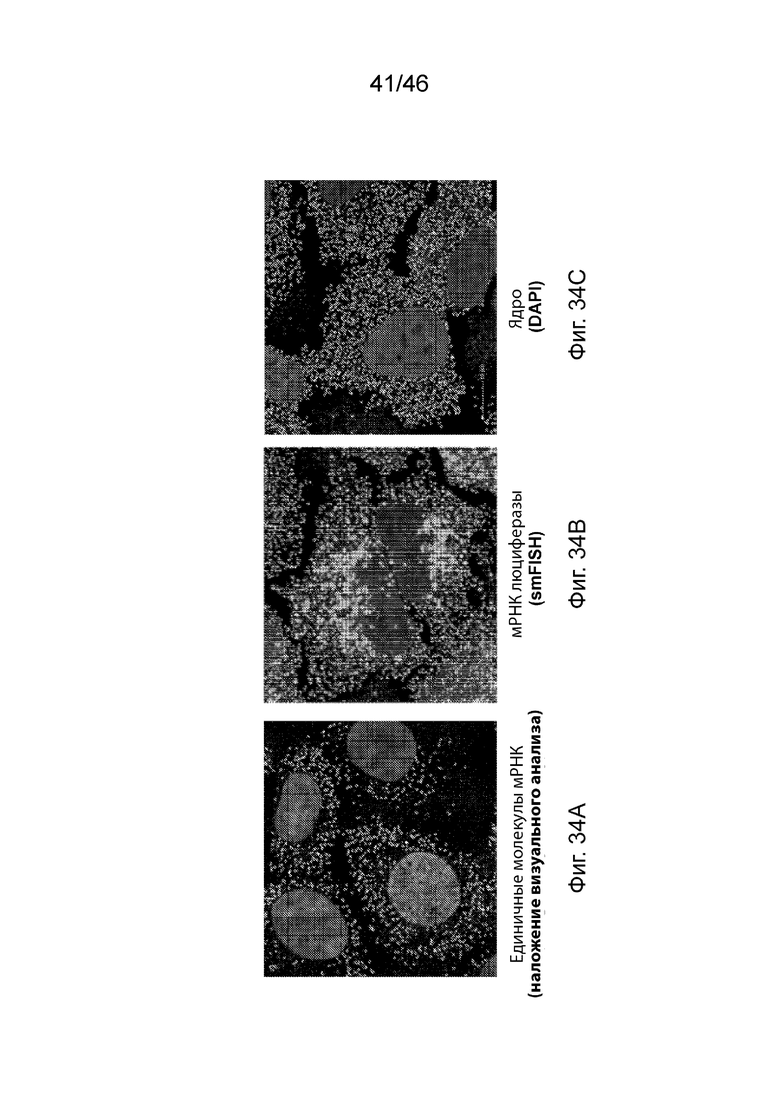
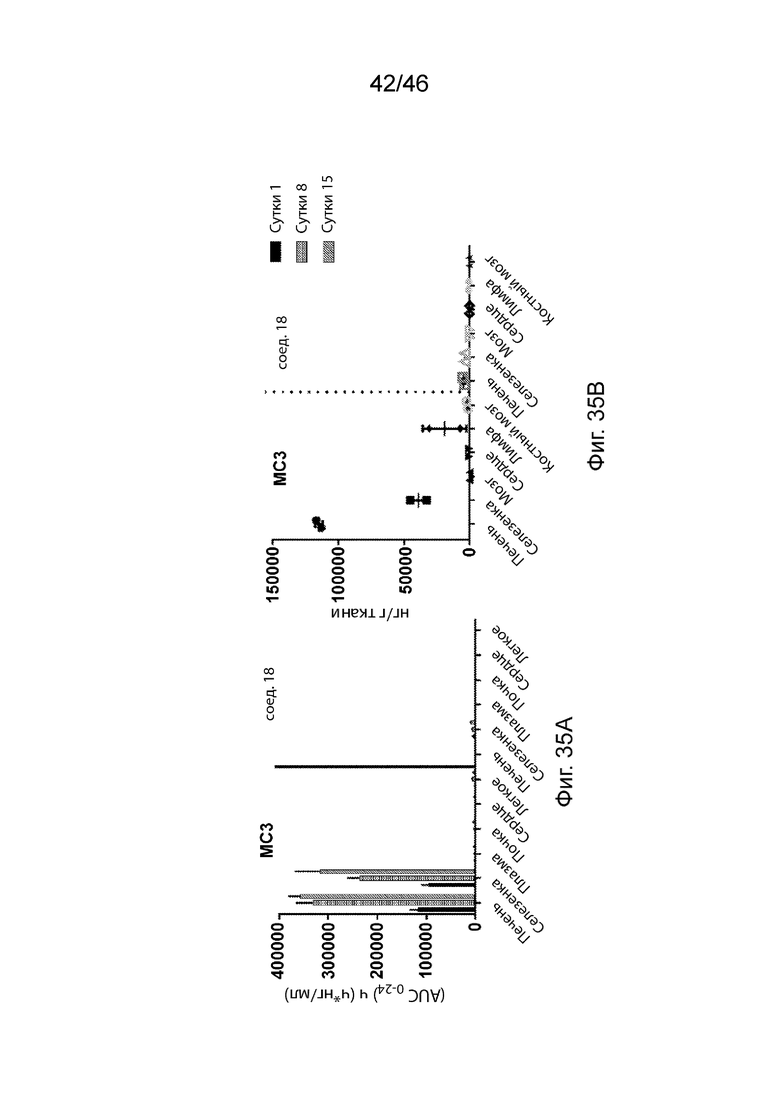

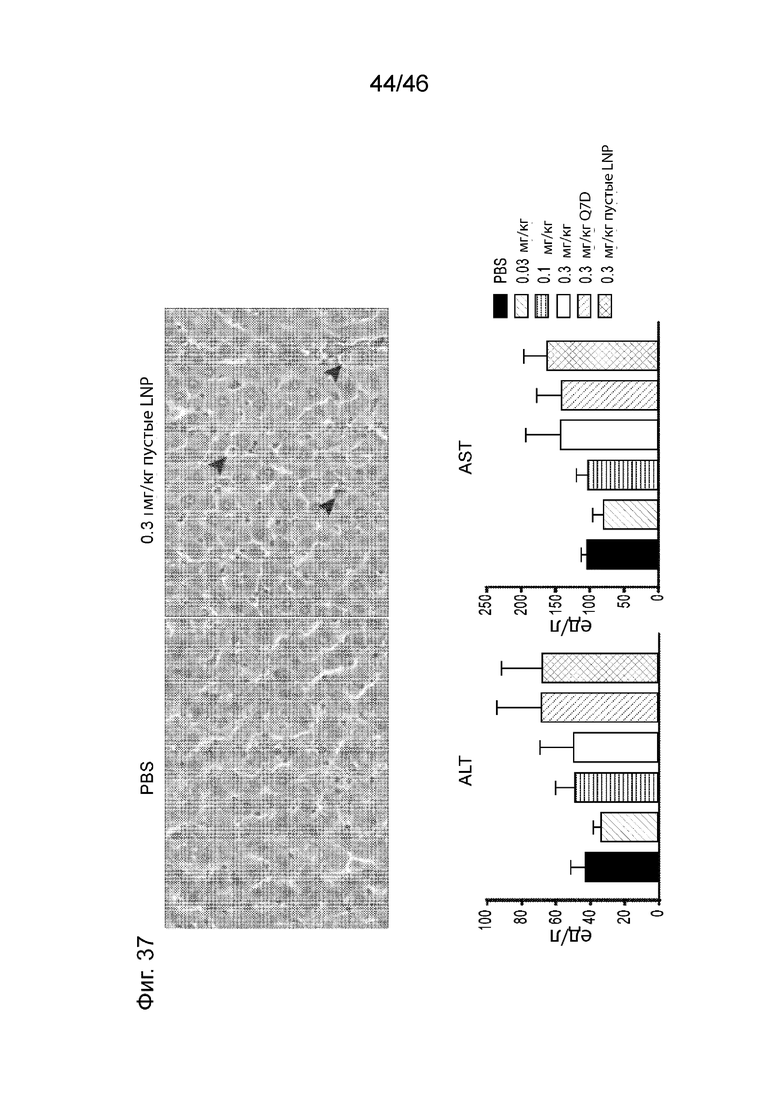

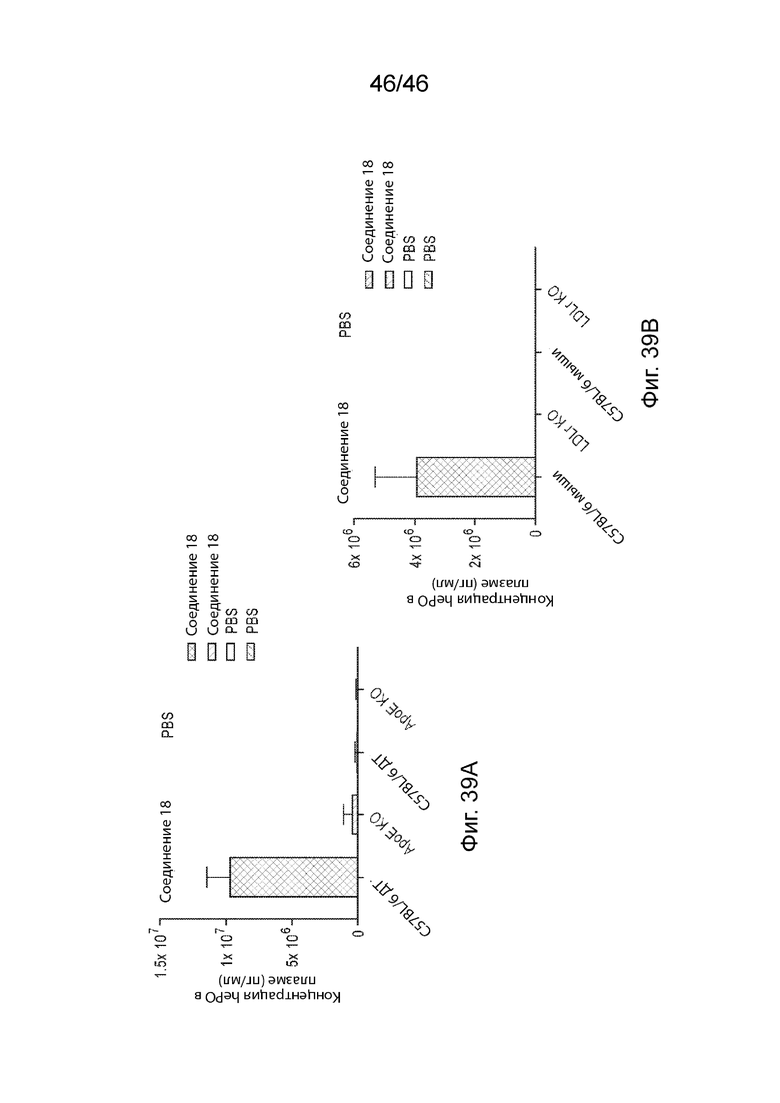
Изобретение относится к соединению формулы (IA), где l представляет собой 5; m представляет собой 7; M1 представляет собой M'; R4 представляет собой -(CH2)nQ, где Q представляет собой -N(R)R8 и n представляет собой 3; M и M' независимо выбраны из -C(O)O- и -OC(O)-; R8 представляет собой циклобутенил, замещенный одним или более оксо, амино, гетероциклоалкила, выбранного из пиперидинила, морфолинила и 4-метилпиперазин-1-ила, и моно- или диалкиламино, где моно- и диалкиламино замещены одним C1-3 алкокси или диалкиламино; R2 и R3 независимо представляет собой C8-10 алкил; R представляет собой H; и R' представляет собой C9-18 алкил. Изобретение также относится к композиции наночастиц для доставки терапевтического и/или профилактического агента на основе соединения формулы (IA). Технический результат – получены новые соединения и композиция на их основе, которые могут найти применение в медицине при доставке терапевтических и/или профилактических агентов в клетки или органы млекопитающих, например, для регуляции экспрессии полипептида, белка или гена. 6 н. и 22 з.п. ф-лы, 39 ил., 42 табл., 26 пр.
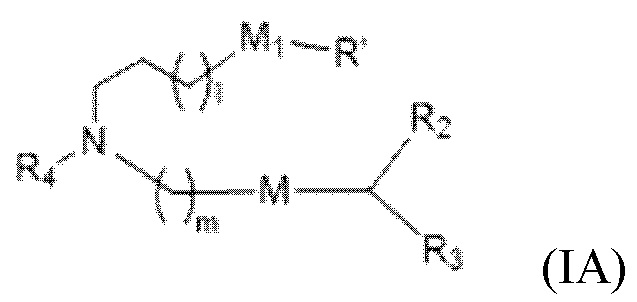
1. Соединение формулы (IA)
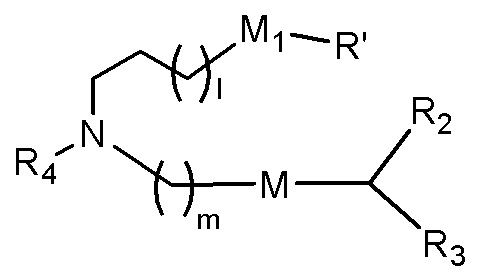
(IA),
где l представляет собой 5;
m представляет собой 7;
M1 представляет собой M';
R4 представляет собой -(CH2)nQ, где Q представляет собой -N(R)R8 и n представляет собой 3;
M и M' независимо выбраны из -C(O)O- и -OC(O)-;
R8 представляет собой циклобутенил, замещенный одним или более оксо, амино, гетероциклоалкила, выбранного из пиперидинила, морфолинила и 4-метилпиперазин-1-ила, и моно- или диалкиламино, где моно- и диалкиламино замещены одним C1-3 алкокси или диалкиламино;
R2 и R3 независимо представляет собой C8-10 алкил;
R представляет собой H; и
R' представляет собой C9-18 алкил.
2. Соединение по п. 1, где R8 представляет собой циклобутенил, замещенный одним или более оксо и моно- или диалкиламино, где моно- и диалкиламино замещены одним C1-3 алкокси или диалкиламино.
3. Соединение по п. 1, где R8 представляет собой циклобутенил, замещенный одним или более оксо и гетероциклоалкилом, выбранным из пиперидинила, морфолинила и 4-метилпиперазин-1-ила.
4. Соединение по п.1, где R4 выбран из:
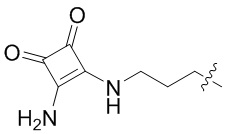 ,
, 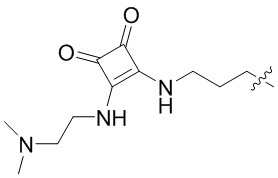 ,
, 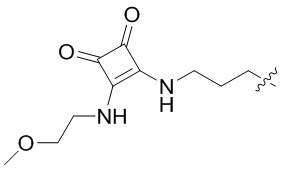 ,
, 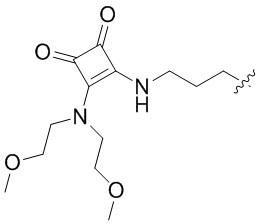 ,
, 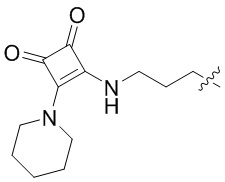 ,
, 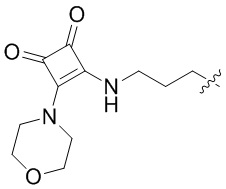 и
и 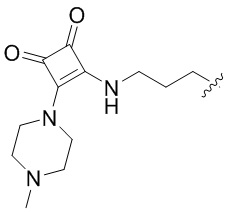 .
.
5. Соединение по п. 1, где соединение выбрано из:

6. Соединение формулы (IA)

(IA),
где l представляет собой 5;
m представляет собой 7;
M1 представляет собой M';
R4 представляет собой -(CH2)nQ, где Q представляет собой -N(R)R8 и n представляет собой 3;
R8 представляет собой циклобутенил, замещенный одним или более оксо и моноалкиламино;
M и M' независимо выбраны из -C(O)O- и -OC(O)-, где по меньшей мере один из М и М' представляет собой -ОС(О)-;
R2 и R3 независимо представляют собой C8-10 алкил;
R представляет собой H; и
R' представляет собой C9-18 алкил.
7. Соединение по п. 6, где соединение выбрано из:
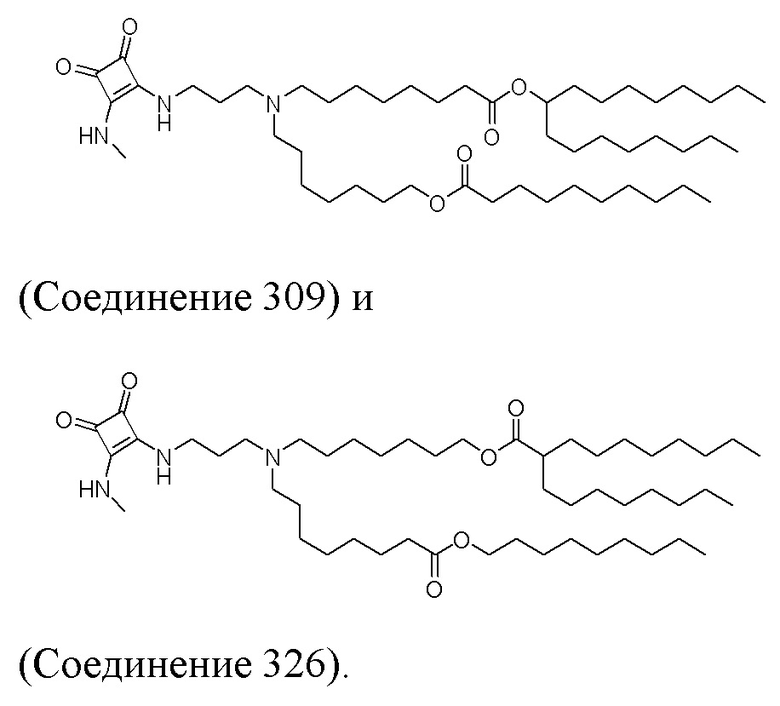
8. Соединение формулы (IA)

(IA),
где l представляет собой 5;
m представляет собой 7;
M1 представляет собой M';
R4 представляет собой -(CH2)nQ, где Q представляет собой -N(R)R8 и n представляет собой 3;
R8 представляет собой циклобутенил, замещенный одним или более оксо и моноалкиламино;
M и M' независимо выбраны из -C(O)O- и -OC(O)-;
R2 и R3 независимо представляют собой C8-10 алкил;
R представляет собой H; и
R' представляет собой разветвленный C9-18 алкил.
9. Соединение по п. 8, где R' представляет собой
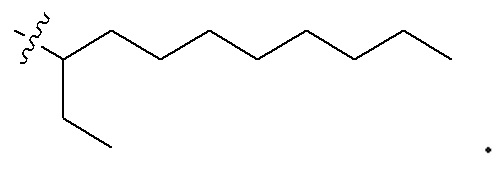
10. Соединение по п. 8, где соединение представляет собой:
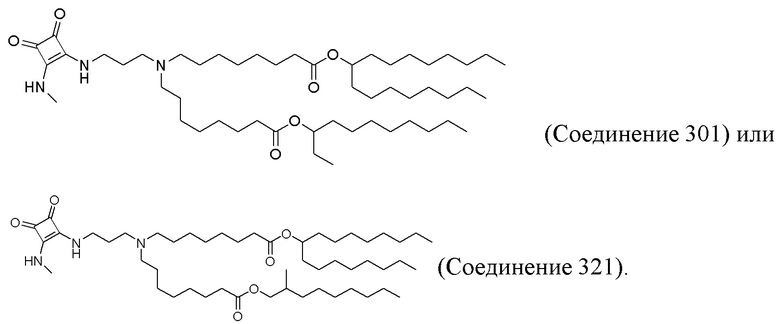
11. Композиция наночастиц для доставки терапевтического и/или профилактического агента в клетку млекопитающего, содержащая липидный компонент, который содержит от приблизительно 30% моль до приблизительно 60% моль соединения по любому из пп. 1-10; от приблизительно 0% моль до приблизительно 30% моль фосфолипида, от приблизительно 18,5% моль до приблизительно 48,5% моль структурного липида и от приблизительно 0% моль до приблизительно 10% моль ПЭГ–липида.
12. Композиция наночастиц по п.11, где фосфолипид выбирают из группы, состоящей из
1,2–дистеароил–sn–глицеро–3–фосфохолина (DSPC),
1,2–диолеоил–sn–глицеро–3–фосфоэтаноламина (DOPE)
и их смесей.
13. Композиция наночастиц по п. 11, где фосфолипид представляет собой DSPC или DOPE.
14. Композиция наночастиц по п. 11, где структурный липид представляет собой холестерин.
15. Композиция наночастиц по п. 11, где ПЭГ–липид выбирают из группы, состоящей из ПЭГ–модифицированного диалкиламина, ПЭГ–модифицированного диацилглицерина и их смесей.
16. Композиция наночастиц по п. 11, где липидный компонент содержит от приблизительно 35% моль до приблизительно 55% моль указанного соединения, от приблизительно 5% моль до приблизительно 25% моль фосфолипида, от приблизительно 30% моль до приблизительно 40% моль структурного липида и от приблизительно 0% моль до приблизительно 10% моль ПЭГ–липида.
17. Композиция наночастиц по п. 11, где липидный компонент содержит приблизительно 50% моль указанного соединения, приблизительно 10% моль фосфолипида, приблизительно 38,5% моль структурного липида и приблизительно 1,5% моль ПЭГ–липида.
18. Композиция наночастиц по п. 11, где терапевтический и/или профилактический агент представляет собой нуклеиновую кислоту.
19. Композиция наночастиц по п. 11, где терапевтический и/или профилактический агент представляет собой рибонуклеиновую кислоту (РНК).
20. Композиция наночастиц по п. 19, где РНК выбирают из группы, состоящей из малой интерферирующей РНК (миРНК), асимметричной интерферирующей РНК (aiRNA) и микроРНК (miRNA), дайсер–субстратной РНК (dsRNA), короткой шпилечной РНК (кшРНК), мессенджера РНК (мРНК) и их смесей.
21. Композиция наночастиц по п. 19, где РНК представляет собой мРНК.
22. Композиция наночастиц по п. 21, где мРНК содержит одно или более из 'петли–на–стебле', обрывающего цепь нуклеозида, последовательности полиА, сигнала полиаденилирования и/или 5'–кэп структуры.
23. Композиция наночастиц по любому из пп. 16-22, где эффективность инкапсуляции терапевтического и/или профилактического агента составляет по меньшей мере 80% или по меньшей мере 90%.
24. Композиция наночастиц по любому из пп. 16-22, где мас./мас. соотношение липидного компонента и мРНК составляет от приблизительно 10:1 до приблизительно 60:1.
25. Композиция наночастиц по п. 24, где мас./мас. соотношение липидного компонента и мРНК составляет приблизительно 20:1.
26. Композиция наночастиц по любому из пп.16-22, где соотношение N:P составляет от приблизительно 5:1 до приблизительно 8:1.
27. Способ доставки терапевтического и/или профилактического агента в клетку млекопитающего, включающий введение субъекту композиции наночастиц по любому из пп. 16-22, причем указанное введение включает приведение в контакт клетки с композицией наночастиц, посредством чего терапевтический и/или профилактический агент доставляется в клетку.
28. Способ продуцирования полипептида, представляющего интерес, в клетке млекопитающего, включающий приведение в контакт указанной клетки с композицией наночастиц по п. 21, где мРНК кодирует представляющий интерес полипептид, благодаря чему мРНК способна транслироваться в клетке с образованием представляющего интерес полипептида.
| Токарный резец | 1924 |
|
SU2016A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| RU 2014122432 A, 10.12.2015. | |||
Авторы
Даты
2023-06-21—Публикация
2018-03-15—Подача