Изобретение относится к области получения пестицидов, более конкретно - к способу получения 1-(4,6-диметоксипиримидин-2-ил)мочевины (I) (регистрационный номер CAS [151331-81-6], далее по тексту - мочевина I), являющейся предшественником важных гербицидов из класса сульфонилмочевин и их аналогов.
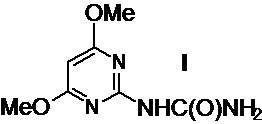
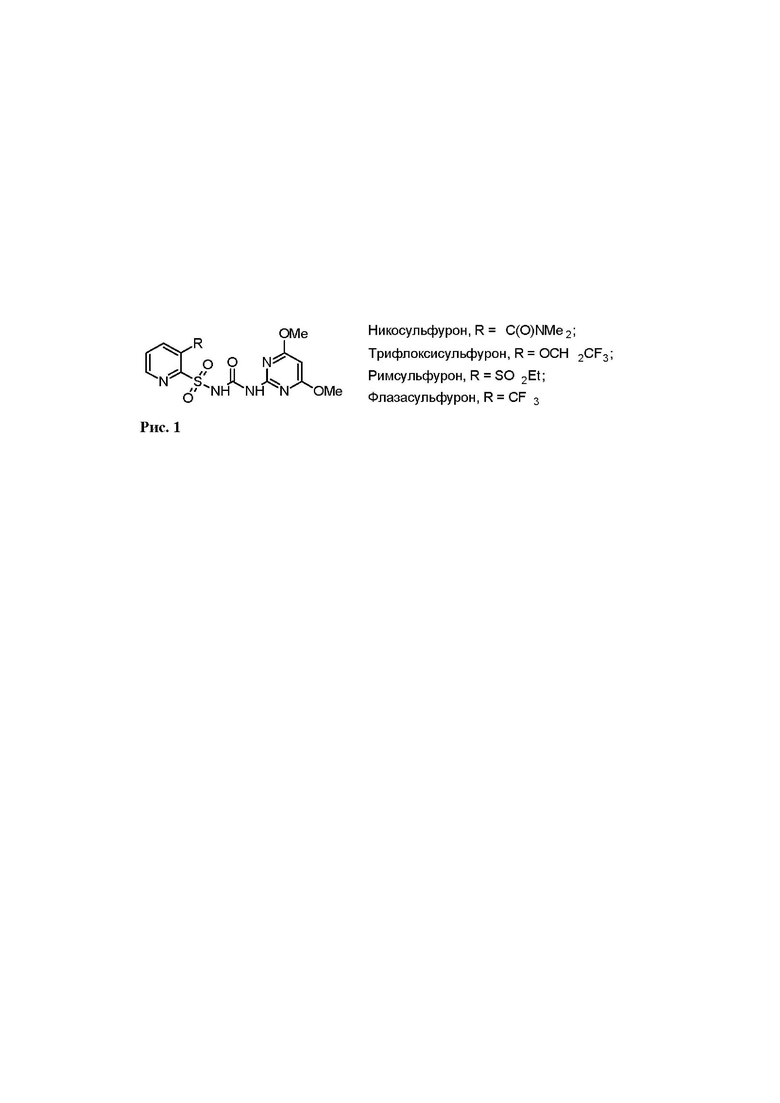
Это соединение используется в бесфосгенном синтезе многих сульфонилмочевин, обладающих разноплановой биологической активностью и содержащих в своей структуре 4,6-диметоксипиримидин-2-ильный фрагмент (Рис. 1), среди которых следует выделить такие широко используемые гербициды как никосульфурон, трифлоксисульфурон, римсульфурон, флазасульфурон, а также их производные и аналоги (патенты CN №108558830А, CN №101671327А, CN №101503403А, JPH №11140081A).
Также мочевина I образуется в ходе фотохимической деградации некоторых используемых в сельском хозяйстве гербицидов ряда сульфонилмочевин, содержащих в своей структуре указанный выше фрагмент, и может быть использована в качестве стандарта при определении остаточных количеств этих пестицидов в почве и водоемах (см., напр., M. Harir et al., J. Agric. Food Chem., 2013, 61(22), 5271-5278; Y.-B. Si et al., Pest. Manag. Sci., 2003, 60(3), 286-290).
Известно несколько способов получения мочевины I, которые кратко представлены на Схеме 1.
Так, в патенте JPH №11140081A используют реакцию 2-изоциано-4,6-диметоксипиримидина (II) с газообразным аммиаком в 1,4-диоксане при температуре 10-15°С в течение 1 ч. В результате получают мочевину I с выходом 92%.
В патенте CN №101671327А используют реакцию 2-амино-4,6-диметоксипиримидина (III) с избытком мочевины в присутствии соляной или серной кислоты в органическом растворителе, в воде или в их смесях. Процесс проводят при нагревании реакционной массы при температуре 50-150°С в течение 2-15 ч, при этом получают мочевину I с выходом 81-85%.
В патенте CN №103086983А также используют 2-амино-4,6-диметоксипиримидин (III) в качестве исходного сырья. При его взаимодействии с цианатом натрия в водно-органической среде в присутствии органической кислоты и катализатора в течение 2,5-16 ч при температуре 40-100°С получают целевую мочевину I с выходом 92-95%.
Наконец, известен 2-стадийный способ получения мочевины I из 2-хлор-4,6-диметоксипиримидина (IV) и 1-(4-метоксибензил)мочевины (V) (S. Breitler et al., Org. Lett., 2011, 13(12), 3262-3265), реакцию между которыми осуществляют в среде кипящего тетрагидрофурана в присутствии фосфиновых комплексов палладия (PdLn) в качестве катализатора и карбоната цезия в качестве основания в течение 2 ч. Промежуточный продукт этой реакции (1-(4,6-диметоксипиримидин-2-ил)-3-(4-метоксибензил)мочевина) обрабатывают трифторуксусной кислотой при нагревании в течение 20 ч и получают мочевину I с выходом 86% (Схема 1).
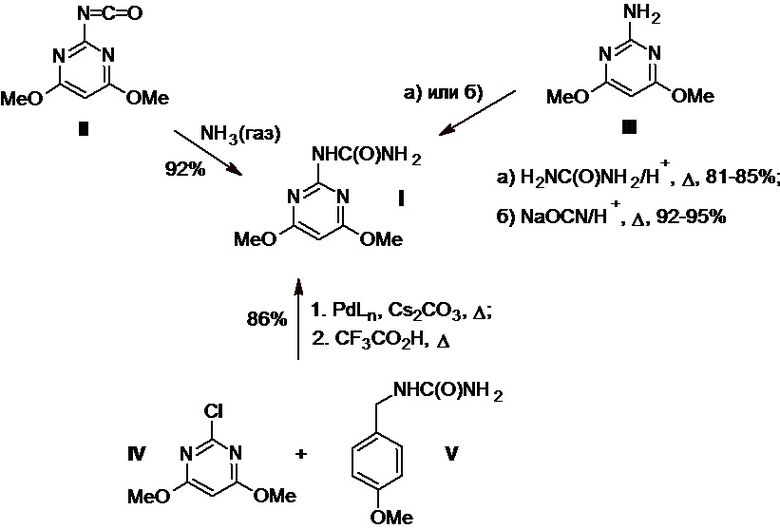
Схема 1
Суммируя вышеизложенное, известные методы получения мочевины I требуют применения в процессе органических растворителей или их смесей с водой, повышенных температур (до 100-150°С), длительного времени проведения процесса (до 22 ч), использования газообразного аммиака, чувствительных к влаге воздуха соединений (напр., изоцианат II), дорогостоящих комплексов палладия, что негативно сказывается на технико-экономических параметрах процесса и его безопасности.
Задачей предлагаемого технического решения является улучшение технико-экономических показателей процесса получения 1-(4,6-диметоксипиримидин-2-ил)мочевины (I) за счет использования новой технологии ее синтеза, исходя из 2-(R-оксикарбонил)амино-4,6-диметоксипиримидина (R = Me, Et, н-Pr, н-Bu или Ph) [далее по тексту - карбамат VIа-д] в качестве исходного сырья, позволяющей получать целевой продукт в одну стадию с высоким выходом и качеством.
Техническим результатом является: а) улучшение технико-экономических показателей технологического процесса производства мочевины I вследствие упрощения его аппаратурного оформления и сокращения продолжительности, исключения использования в нем органических растворителей (что также приводит к снижению содержания органических компонентов в отходах производства), повышенных температур и нестабильных исходных соединений или реагентов; б) повышение безопасности процесса; в) получение целевого продукта высокого качества с выходом 95-99%.
Технический результат достигается за счет использования способа получения 1-(4,6-диметоксипиримидин-2-ил)мочевины, включающего взаимодействие 2-(R-оксикарбонил)амино-4,6-диметоксипиримидина, где R = Me, Et, н-Pr, н-Bu или Ph, с водным раствором соединения аммония с получением целевого продукта, его выделением и очисткой.
В качестве соединения аммония используют гидроксид, карбонат, фосфат, формиат или ацетат аммония.
Изобретение иллюстрируется следующими примерами (Схема 2).
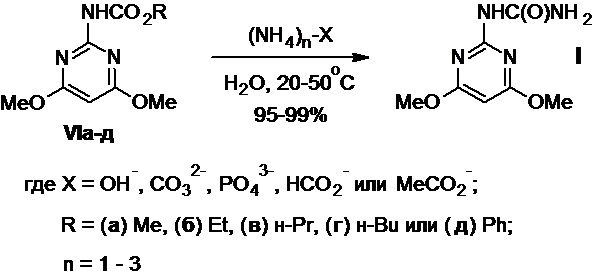
Схема 2
Пример 1
В реактор синтеза помещают 10%-ный водный раствор гидроксида аммония (123,5 г, 0,35 моль) и карбамат VIа (50,0 г, 0,23 моль). Реакционную массу перемешивают при температуре 20-25°С в течение 1-2 ч (контроль ТСХ или ВЭЖХ), после чего ее фильтруют, а полученный осадок промывают водой и высушивают на воздухе. Получают 44,5 г (96%) мочевины I в виде белого порошка с т.пл. 182-186°С и чистотой не менее 98,0% (по данным ВЭЖХ). ИК-спектр (в порошке, ν, см-1): 3589 ср, 3355 ср, 3158 ср, 2951 ср, 1672 с (С=О), 1601 с, 1565 с, 1452 ср, 1409 ср, 1345 с, 1219 с, 1171 с, 1119 с, 1080 ср, 1029 ср, 922 ср, 839 ср, 795 с; масс-спектр (APCI): 199,1 [M+H]+; масс-спектр (EI, 70 eV): m/z (%): 198 [M]+ (10), 180 (12), 155 (45), 140 (10), 125 (15), 109 (15), 95 (15), 83 (15), 68 (55), 57 (25), 43 (50), 28 (80).
Пример 2
В реактор синтеза помещают 20%-ный водный раствор ацетата аммония (105,7 г, 0,27 моль) и карбамат VIг (35,0 г, 0,14 моль). Реакционную массу перемешивают при температуре 45-50°С в течение 2-3 ч (контроль ТСХ или ВЭЖХ), после чего ее фильтруют, а полученный осадок промывают водой и высушивают на воздухе. Получают 25,9 г (95%) мочевины I в виде белого порошка.
Пример 3
В реактор синтеза помещают 25%-ный водный раствор формиата аммония (33,3 г, 0,13 моль) и карбамат VIб (10,0 г, 0,04 моль). Реакционную массу перемешивают при температуре 30-35°С в течение 1-2 ч (контроль ТСХ или ВЭЖХ), после чего ее фильтруют, а полученный осадок промывают водой и высушивают на воздухе. Получают 8,6 г (99%) мочевины I в виде белого порошка.
Пример 4
В реактор синтеза помещают 15%-ный водный раствор фосфата аммония (90,3 г, 0,09 моль) и карбамат VIд (25,0 г, 0,09 моль). Реакционную массу перемешивают при температуре 25-30°С в течение 2-3 ч (контроль ТСХ или ВЭЖХ), после чего ее фильтруют, а полученный осадок промывают водой и высушивают на воздухе. Получают 17,5 г (98%) мочевины I в виде белого порошка.
Пример 5
В реактор синтеза помещают 30%-ный водный раствор карбоната аммония (132,8 г, 0,41 моль) и карбамат VIв (40,0 г, 0,17 моль). Реакционную массу перемешивают при температуре 20-25°С в течение 1-2 ч (контроль ТСХ или ВЭЖХ), после чего ее фильтруют, а полученный осадок промывают водой и высушивают на воздухе. Получают 31,4 г (96%) мочевины I в виде белого порошка.
В результате использования предлагаемого способа получения 1-(4,6-диметоксипиримидин-2-ил)мочевины (I) удается улучшить: а) технико-экономические показатели технологического процесса ее производства вследствие упрощения его аппаратурного оформления и сокращения продолжительности, исключения использования в нем органических растворителей (что также приводит к снижению содержания органических компонентов в отходах производства), повышенных температур и нестабильных исходных соединений или реагентов; б) повысить безопасность процесса; в) получить целевой продукт высокого качества с выходом 95-99%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения никосульфурона | 2023 |
|
RU2807708C1 |
| Способ получения бенсульфурон-метила | 2024 |
|
RU2826376C1 |
| Способ получения сульфонилмочевинных гербицидов, содержащих 4,6-диметоксипиримидин-2-ильный заместитель | 2024 |
|
RU2834461C1 |
| Способ получения пиразосульфурон-этила | 2024 |
|
RU2828085C1 |
| Способ получения R-N-[[3-[(диметиламино)карбонил]пиридин-2-ил]сульфонил]карбаматов, в которых заместителем R является метил или этил | 2023 |
|
RU2816572C1 |
| Способ получения сульфонилмочевинных гербицидов, содержащих фрагмент 4-метокси-6-метил-1,3,5-триазина | 2023 |
|
RU2815938C1 |
| Способ получения моносульфурона | 2024 |
|
RU2834000C1 |
| Способ получения гербицида никосульфурона | 2024 |
|
RU2827153C1 |
| Способ получения моносульфурон-метила | 2024 |
|
RU2834839C1 |
| Способ получения этил-N-(3-гидроксифенил)карбамата | 2023 |
|
RU2805745C1 |
Изобретение относится к способу получения 1-(4,6-диметоксипиримидин-2-ил)мочевины. Способ заключается во взаимодействии 2-(R-оксикарбонил)амино-4,6-диметоксипиримидина, где R = Me, Et, н-Pr, н-Bu или Ph, с водным раствором соединения аммония и последующими выделением и очисткой целевого продукта. В качестве соединения аммония предпочтительно используют гидроксид, карбонат, фосфат, формиат или ацетат аммония. Предлагаемый способ позволяет исключить использование органических растворителей и повышенных температур, сократить время реакции и получать целевой продукт с высоким выходом 95-99%. 1 з.п. ф-лы, 1 ил., 5 пр.
1. Способ получения 1-(4,6-диметоксипиримидин-2-ил)мочевины, включающий взаимодействие 2-(R-оксикарбонил)амино-4,6-диметоксипиримидина, где R = Me, Et, н-Pr, н-Bu или Ph, с водным раствором соединения аммония с получением целевого продукта, его выделением и очисткой.
2. Способ получения 1-(4,6-диметоксипиримидин-2-ил)мочевины по п. 1, отличающийся тем, что в качестве соединения аммония используют гидроксид, карбонат, фосфат, формиат или ацетат аммония.
| CN 103086983 A, 08.05.2013 | |||
| BREITLER S | |||
| et al., Synthesis of Unsymmetrical Diarylureas via Pd-Catalyzed C-N Cross-Coupling Reactions, ORGANIC LETTERS, 2011, 13(12), pp | |||
| ПРИБОР ДЛЯ ОПРЕДЕЛЕНИЯ УРОВНЯ СТОЯНИЯ НЕФТИ И СОЛЕНОЙ ВОДЫ В БУРОВЫХ СКВАЖИНАХ | 1924 |
|
SU3262A1 |
| 1{[α-ЦИКЛОПРОПИЛ-α-(ЗАМЕЩЕННЫЕ ОКСИ)-О-ТОЛИЛ]СУЛЬФАМОИЛ}-3-(4,6-ДИМЕТОКСИ-2-ПИРИМИДИНИЛ) МОЧЕВИНЫ И СПОСОБ ПОДАВЛЕНИЯ НЕЖЕЛАТЕЛЬНЫХ ВИДОВ РАСТЕНИЙ | 1994 |
|
RU2141954C1 |
| MORRICA P | |||
| et al., Identification of photoproducts from imazosulfuron by HPLC, BIOMEDICAL CHROMATOGRAPHY, 2004, 18(7), | |||
Авторы
Даты
2023-07-07—Публикация
2023-02-14—Подача