Область техники, к которой относится настоящее изобретение
[001] Настоящее раскрытие относится к антителам, способным связываться с фактором коагуляции XI (FXI) и/или его активированной формой XIa (FXIa), а также с фрагментами FXI и/или FXIa, и их применениям, включая в себя применения в качестве антикоагулянтов для лечения тромбозов, которые не нарушают гемостаз.
Предшествующий уровень техники настоящего изобретения
[002] Тромбоз представляет собой состояние, которое предусматривает свертывание крови в кровеносном сосуде, блокируя тем самым или препятствуя кровотоку в пораженной области. Это состояние может привести к серьезным осложнениям, если сгустки крови перемещаются по кровеносной системе в важную часть тела, такую как сердце, головной мозг и легкие, вызывая сердечный приступ, инсульт, легочную эмболию и т.д. Тромбоз может лечиться или предотвращаться антикоагулянтами, такими как гепарин и варфарин. Наиболее распространенным побочным эффектом этих доступных в настоящее время способов лечения является кровотечение. Следовательно, эти способы лечения ограничены дозой и исполнительностью пациента, потому что пациенты должны подвергаться тщательному контролю после лечения.
[003] Существует необходимость в эффективной терапии или профилактике тромбоза с минимальными побочными эффектами. Настоящее раскрытие удовлетворяет потребность в настоящей области техники.
Краткое раскрытие настоящего изобретения
[004] Согласно определенным вариантам осуществления в настоящем документе представлены антитела, которые связываются с фактором XI коагуляции (FXI) и/или его активированной формой XIa (FXIa), а также с фрагментами FXI и/или FXIa. Согласно некоторым вариантам осуществления антитела представляют собой моноклональные антитела. Согласно некоторым вариантам осуществления антитела представляют собой рекомбинантные антитела. Согласно некоторым вариантам осуществления антитела представляют собой гуманизированные антитела. Согласно некоторым вариантам осуществления антитела представляют собой иммунологически активные части молекул иммуноглобулина, например, Fab, Fv или scFv. Согласно некоторым вариантам осуществления антитела связываются с доменом A3 FXI и/или FXIa. Согласно некоторым вариантам осуществления антитела включают в себя одну или несколько CDR, состоящих из аминокислотных последовательностей SEQ ID NO: 11-16, 27-32, 43-48, 59-64, 75-80, 91-96, 107-112, 123-128, 139-144, 155-160, 171-176 и 187-192 или содержащих их.
[005] В настоящем документе представлена фармацевтическая композиция для лечения и/или профилактики тромбоза и/или связанных с тромбозом осложнений или состояний. Фармацевтическая композиция содержит одно или несколько антител к FXI и/или к FXIa, как описано в настоящем документе. Согласно некоторым вариантам осуществления фармацевтическая композиция дополнительно содержит один или несколько фармацевтически приемлемых адъювантов, носителей, вспомогательных веществ, консервантов или их комбинацию.
[006] В настоящем документе представлена нуклеиновая кислота, кодирующая антитело к FXI и/или к FXIa, как описано в настоящем документе, или функциональный фрагмент любого антитела, а также вектор, содержащий нуклеиновую кислоту, и клетка-хозяин, содержащая вектор. Согласно некоторым вариантам осуществления вектор представляет собой вектор экспрессии, который способен производить антитело или его функциональный фрагмент, кодируемый нуклеиновой кислотой в клетке-хозяине.
[007] В настоящем документе представлен набор, содержащий одно или несколько описанных в настоящем документе антител к FXI и/или к FXIa для применения при лечении и/или профилактике тромбоза и/или связанных с тромбозом осложнений или состояний. Альтернативно, набор содержит фармацевтическую композицию, содержащую одно или несколько описанных в настоящем документе антител к FXI и/или к FXIa для применения при лечении и/или профилактики тромбоза и/или связанных с тромбозом осложнений или состояний. Согласно определенным вариантам осуществления набор дополнительно содержит инструкции по применению.
[008] В настоящем документе представлен способ лечения и/или профилактики тромбоза и/или связанных с тромбозом осложнений или состояний. Способ предусматривает введение нуждающемуся в этом субъекту терапевтически эффективного количества одного или нескольких описанных в настоящем документе антител к FXI и/или к FXIa. Альтернативно, способ предусматривает введение нуждающемуся в этом субъекту терапевтически эффективного количества фармацевтической композиции, содержащей антитело к FXI, антитело к FXIa или функциональный фрагмент любого антитела.
[009] В настоящем документе представлено применение описанного в настоящем документе антитела к FXI и/или к FXIa для составления лекарственного средства для лечения и/или профилактики тромбоза и/или связанных с тромбозом осложнений или состояний.
[0010] В настоящем документе представлен способ получения описанного в настоящем документе антитела к FXI и/или к FXIa. Способ предусматривает стадии трансформации клетки-хозяина вектором, содержащим нуклеиновую кислоту, кодирующую антитело, и экспрессию антитела в клетке-хозяине. Способ может дополнительно предусматривать очистку экспрессированного антитела из клетки-хозяина. Кроме того, очищенное антитело может подвергаться модификациям, так что модифицированное рекомбинантное антитело сохраняет активность соответствующего человеческого антитела. Альтернативно, раскрытое в настоящем документе антитело может быть получено путем культивирования гибридомы.
Краткое описание графических материалов
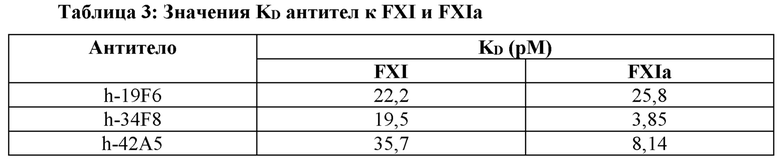
[0011] На фиг. 1 показаны эффекты пяти антител к FXI посредством анализа АРТТ в плазме человека. Человеческую плазму, дополненную пятью различными антителами в концентрации от 0 до 400 нМ, исследовали в анализе АРТТ, как описано в примере 2. Пять исследованных антител включали в себя 19F6 (A), 34F8 (В), 42А5 (С), 1А6 (D) и 14Е11 (Е). Антитела 1А6 и 14Е11 использовали в качестве положительных контролей в этом эксперименте.
[0012] На фиг. 2 показаны эффекты антител 19F6 (A), 34F8 (В) и 42А5 (С) в анализе АРТТ в плазме обезьян. Плазму обезьяны, дополненную тремя различными антителами в концентрации от 0 до 400 нМ, исследовали в анализе АРТТ, как описано в примере 3.
[0013] На фиг. 3 показаны сенсограммы SPR для связывания FXI с иммобилизованными h-19F6 (A), h-34F8 (В) и h-42A5 (С), а также сенсограммы SPR для связывания FXIa с иммобилизованными h-19F6 (D), h-34F8 (Е) и h-42A5 (F). Данные соответствовали модели связывания 1:1, и кривые, соответствующие исследованным концентрациям FXI (0,005-1 нг/мл), показаны наложенными на сенсограммах. Каждая кривая указывает на различную исследуемую концентрацию FXI или FXIa.
[0014] На фиг. 4 показаны кривые концентрация-ответ антител h-19F6 (A), h-34F8 (В) и h-42A5 (С), ингибирующих FXIa человека от гидролиза S-2366.
[0015] На фиг. 5 показано ингибирующее действие антител h-19F6 (А) и h-42A5 (В) на опосредованную FXIa активацию FIX в FIXa. Человеческий FrX (200 нМ) инкубировали с FXIa (5 нМ) в PBS с 5 мМ CaCl2 при комнатной температуре с 1 мкМ контрольного IgG или h-19F6 или h-42A5. Через указанные интервалы образцы собирали и FIX, а также FIXa определяли вестерн-блоттингом с использованием козьего IgG к человеческому FIX (Affinity Biologicals).
[0016] На фиг. 6 показаны эффекты антител h-34F8, h-19F6 и h-42A5 на АРТТ у яванских макаков. Обезьянам вводили внутривенно указанные дозы h-34F8 (A), h-19F6 (В) и h-42A5 (С). Время свертывания АРТТ ex vivo определяли до введения дозы (время 0) и через 0,5, 1, 3, 6, 12 и 24 часа после введения дозы.
[0017] На фиг. 7 показаны эффекты антител h-34F8, h-19F6 и h-42A5 на РТ у яванских макаков. Обезьянам вводили внутривенно указанные дозы h-34F8 (A), h-19F6 (В) и h-42A5 (С). Время свертывания РТ ex vivo определяли до введения дозы (время 0) и через 0,5, 1, 3, 6, 12 и 24 часа после введения дозы.
[0018] На фиг. 8 показаны эффекты антител h-34F8, h-19F6 и h-42A5 на тромбоз шунта AV у яванских макаков. Повышающиеся уровни h-34F8 (A), h-19F6 (В) или h-42A5 (С) вводили обезьянам внутривенно (n=3 для h-34F8 и h-19F6; n=4 для h-42A5), изменения массы сгустка от состояния до введения дозы определяли на модели тромбоза шунта АВ обезьяны. *Р<0,05, **Р<0,01 и ***Р<0,001 по сравнению с наполнителем.
[0019] На фиг. 9 показаны эффекты антител h-34F8, h-19F6 и h-42A5 на время кровотечения у яванских макаков. Повышающиеся уровни h-34F8 (A), h-19F6 (В) или h-42А5 (С) вводили обезьянам внутривенно (n=3 для 34F8 и h-19F6; n=4 для h-42A5), время кровотечения оценивали до введения дозы и через 30 минут после каждой дозы.
[0020] На фиг. 10 показаны антитромботические эффекты антител h-34F8, h-19F6 и h-42A5. Четырем группам обезьян (n=5) вводили внутривенно наполнитель, h-34F8, h-19F6 или h-42A5 в дозе 0,3 мг/кг, в течение 2 часов, и FeCl3 наносили на левую бедренную артерию каждого животного, чтобы индуцировать тромбоз. Время до 80% тромботической окклюзии (А) и до 100% тромботической окклюзии (В) определяли путем контроля скорости кровотока. *Р<0,05 и **Р<0,01 по сравнению с наполнителем.
[0021] На фиг. 11 показано, что воздействие антителами h-34F8, h-19F6 или h-42A5 не увеличивало время кровотечения у обезьян. Четырем группам обезьян (n=5) вводили внутривенно наполнитель, h-34F8, h-19F6 или h-42A5 в дозе 0,3 мг/кг, и точное время кровотечения измеряли до введения дозы и через 1 час после введения дозы. Индивидуальное время кровотечения в группе, получавшей h-34F8, h-19F6 и h-42A5, показано в (А), (В) и (С), соответственно. Изменение времени кровотечения при лечении наполнителем, h-34F8, h-19F6 или h-42A5 показано в (D).
[0022] На фиг. 12 показаны эффекты антител h-34F8, h-19F6 и h-42A5 на время свертывания плазмы обезьяны. Четырем группам обезьян (n=5) вводили внутривенно наполнитель, h-34F8, h-19F6 и h-42A5 в дозе 0,3 мг/кг, соответственно, и кровь собирали до введения дозы и приблизительно через 3 часа после введения дозы для получения плазмы и времени свертывания, определения АРТТ и РТ. Изменения АРТТ и РТ показаны в (А) и (В), соответственно. **Р<0,01 и ***Р<0,001 по сравнению с наполнителем.
[0023] На фиг. 13 показана аминокислотная последовательность человеческого FXI (SEQ ID NO: 203).
Подробное описание настоящего изобретения
[0024] Нижеследующее описание настоящего изобретения предназначено просто для иллюстрации различных вариантов осуществления настоящего изобретения. Как таковые, конкретные обсуждаемые модификации не должны рассматриваться как ограничения объема настоящего изобретения. Специалисту в настоящей области техники должно быть очевидно, что различные эквиваленты, изменения и модификации могут быть сделаны без отклонения от объема настоящего изобретения, и следует понимать, что такие эквивалентные варианты осуществления должны быть включены в настоящий документ.
[0025] В каскадах свертывания крови in vivo участвуют как внутренний путь, так и внешний путь. Внутренний путь, также называемый путем активации контакта, инициируется контактом с границей поверхности и приводит к активации FXII. Внутренний путь также включает в себя FXI, FIX и FVIII. Внешний путь, также называемый путем тканевого фактора (TF), инициируется повреждением сосудов и приводит к образованию активированного комплекса TF-FVIIa. Эти два пути встречаются и активируют общий путь, что приводит к превращению протромбина в тромбин и в конечном итоге к образованию сшитого фибринового сгустка. Раскрытые в настоящем документе антитела связываются с FXI и/или FXIa и нацелены на внутренний путь свертывания крови. Структура участия FXI и FXI в свертывании крови описана в различных публикациях. Смотрите, например, публикацию Emsley et al., Blood 115(13): 2569-2577 (2010), содержание которой включено посредством ссылки.
Антитела к FXI или к FXIa
[0026] В настоящем изобретении представлены антитела, которые связываются с FXI, FXIa и/или фрагментом FXI или FXIa и ингибируют образование сгустка крови. Эти антитела способны связываться с FXI, FXIa и/или фрагментом FXI или FXIa (например, фрагментом, содержащим домен A3) и проявлять ингибирующий эффект при концентрации, которая намного ниже, чем максимальная безопасная доза. Например, согласно некоторым вариантам осуществления доза антитела, составляющая от 0,1 мг/кг внутривенно до 3 мг/кг внутривенно проявляет ингибирующий эффект на превращение FXI в FXIa у яванских макаков. Кроме того, раскрытые в настоящем документе антитела могут быть использованы в качестве антикоагулянтов с повышенной безопасностью благодаря минимальному риску возникновения кровотечений по сравнению с обычными антикоагулянтами, такими как гепарин.
[0027] Используемый в настоящем документе термин «содержащий» в отношении композиции или способа означает, что композиция или способ включает в себя по меньшей мере перечисленные элементы. Термин «состоящий по существу из» означает, что композиция или способ включает в себя перечисленные элементы и может дополнительно включать в себя один или несколько дополнительных элементов, которые не оказывают существенного влияния на новые и основные характеристики композиции или способа. Например, композиция, состоящая по существу из перечисленных элементов, может включать в себя эти перечисленные элементы плюс один или несколько микроэлементов из способа выделения и очистки, фармацевтически приемлемые носители, такие как забуференный фосфатом физиологический раствор, консерванты и т.п. Термин «состоящий из» означает, что композиция или способ включают в себя только перечисленные элементы. Варианты осуществления, определенные каждым из промежуточных терминов, находятся в пределах объема настоящего изобретения.
[0028] Используемый в настоящем документе термин «антитело» относится к молекуле иммуноглобулина или ее иммунологически активной части, которая специфически связывается или проявляет иммунологическую реактивность с конкретным антигеном, например, FXI, FXIa или конкретным доменом или фрагментом FXI или FXIa, например, доменом A3. Согласно некоторым вариантам осуществления антитело для применения в настоящих способах, композициях и наборах представляет собой полноразмерную молекулу иммуноглобулина, которая содержит две тяжелые цепи и две легкие цепи, причем каждая тяжелая и легкая цепь содержат три определяющих комплементарность области (CDR). Термин «антитело» в дополнение к природным антителам также включает в себя генетически сконструированные или иным образом модифицированные формы иммуноглобулинов, такие как синтетические антитела, интратела, химерные антитела, полностью человеческие антитела, гуманизированные антитела, пептидные антитела и гетероконъюгатные антитела (например, биспецифические антитела, мультиспецифические антитела, двойные специфические антитела, антиидиотипические антитела, диатела, триатела и тетратела). Раскрытые в настоящем документе антитела могут представлять собой моноклональные антитела или поликлональные антитела. Согласно тем вариантам осуществления, в которых антитело представляет собой иммунологически активную часть молекулы иммуноглобулина, антитело может представлять собой, например, Fab, Fab', Fv, Fab' F(ab')2, дисульфид-связанное Fv, одноцепочечное антитело Fv (scFv), однодоменное антитело (dAb) или диатело. Раскрытые в настоящем документе антитела, включая в себя те, которые представляют собой иммунологически активную часть молекулы иммуноглобулина, сохраняют способность связывать специфический антиген, например, FXI или FXIa, или связывать специфический фрагмент FXI или FXIa, такой как домен A3.
[0029] Согласно некоторым вариантам осуществления раскрытые в настоящем документе антитела к FXI и/или к FXIa претерпели посттрансляционные модификации, такие как фосфорилирование, метилирование, ацетилирование, убиквитинирование, нитрозилирование, гликозилирование или липидирование, связанные с экспрессией в клеточной линии млекопитающих, включая в себя человеческую или отличную от человеческой клетку-хозяина. Способы получения рекомбинантных антител и модификации рекомбинантных антител in vitro и in vivo известны в настоящей области техники. Смотрите, например, публикацию Liu et al., mAbs 6(5): 1145-1154 (2014), содержание которой включено посредством ссылки.
[0030] Также раскрыты полинуклеотиды или нуклеиновые кислоты, кодирующие раскрытые в настоящем документе антитела к FXI и/или к FXIa. Согласно некоторым вариантам осуществления полинуклеотид или нуклеиновая кислота включает в себя ДНК, мРНК, кДНК, плазмидную ДНК. Нуклеиновая кислота, кодирующая антитело или его функциональный фрагмент, раскрытый в настоящем документе, может быть клонирована в вектор, такой как вектор экспрессии млекопитающего рТТ5, который может дополнительно включать в себя промотор и/или другие элементы контроля транскрипции или трансляции, так что нуклеиновая кислота может экспрессироваться для получения антитела или его функционального фрагмента.
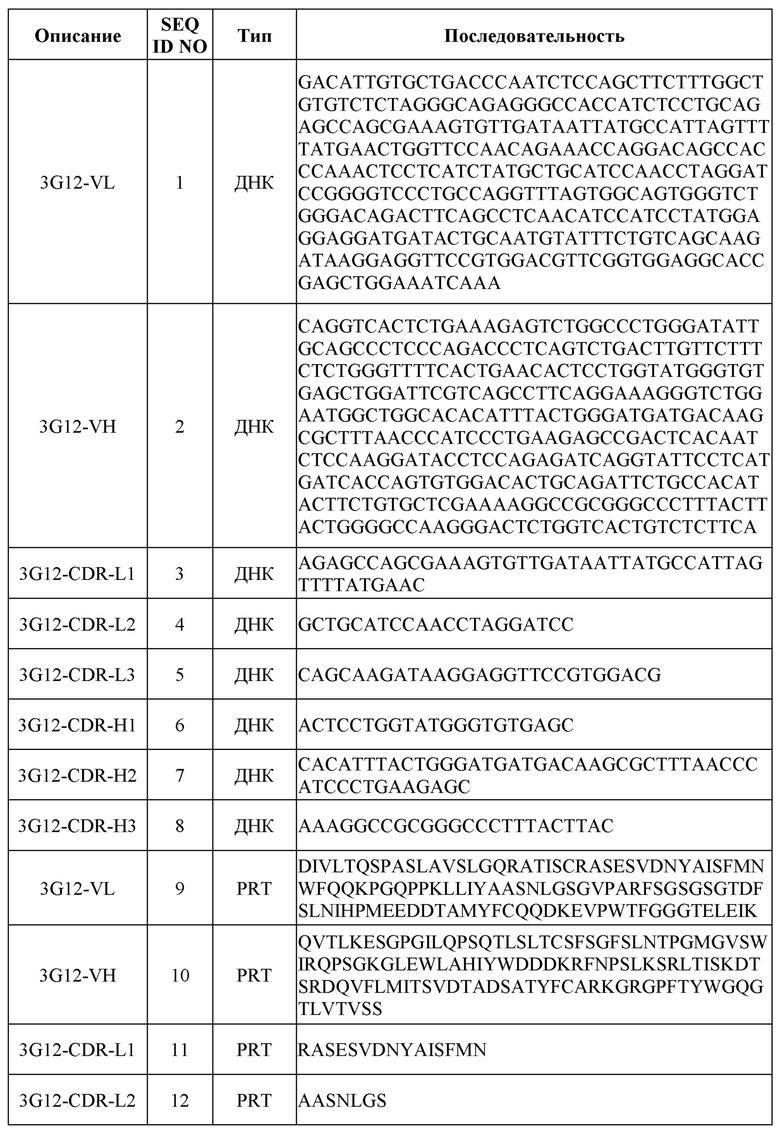
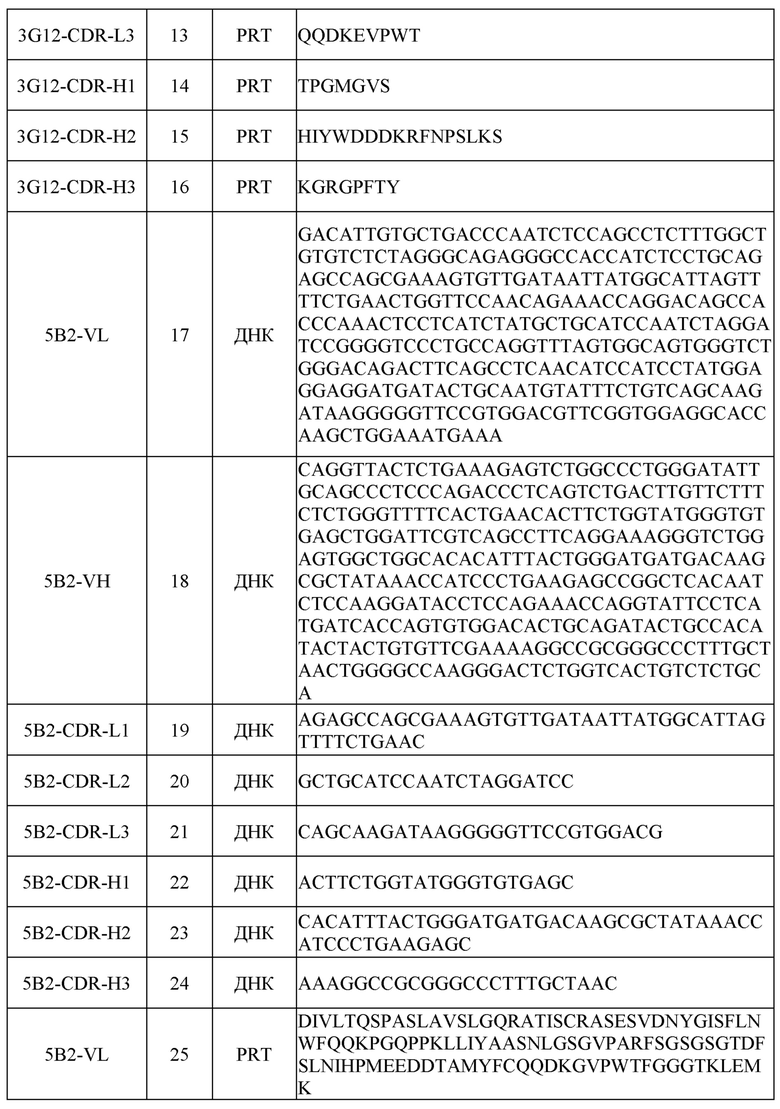
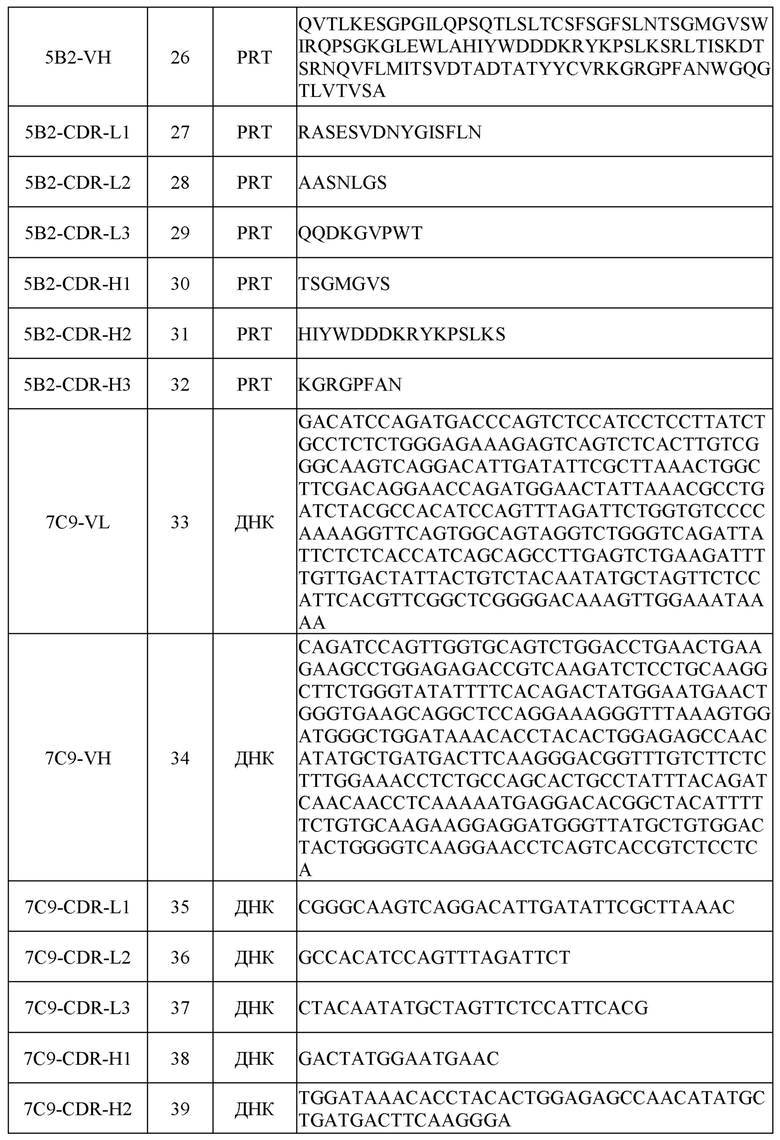
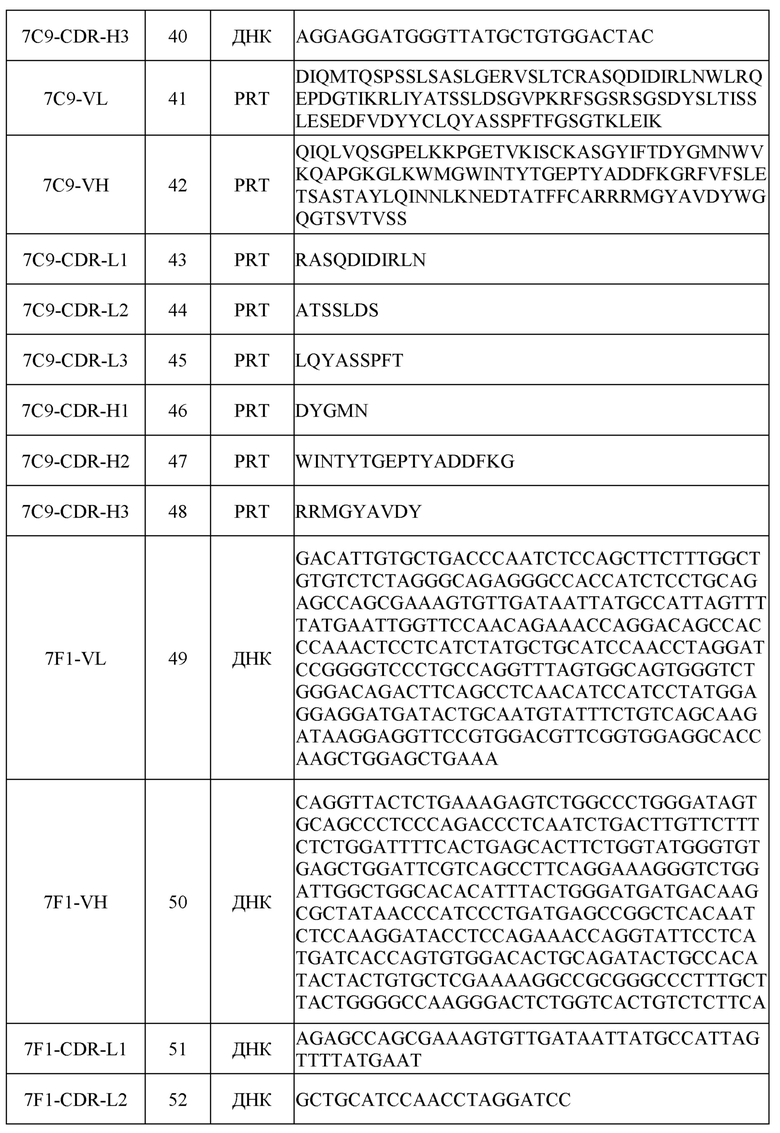
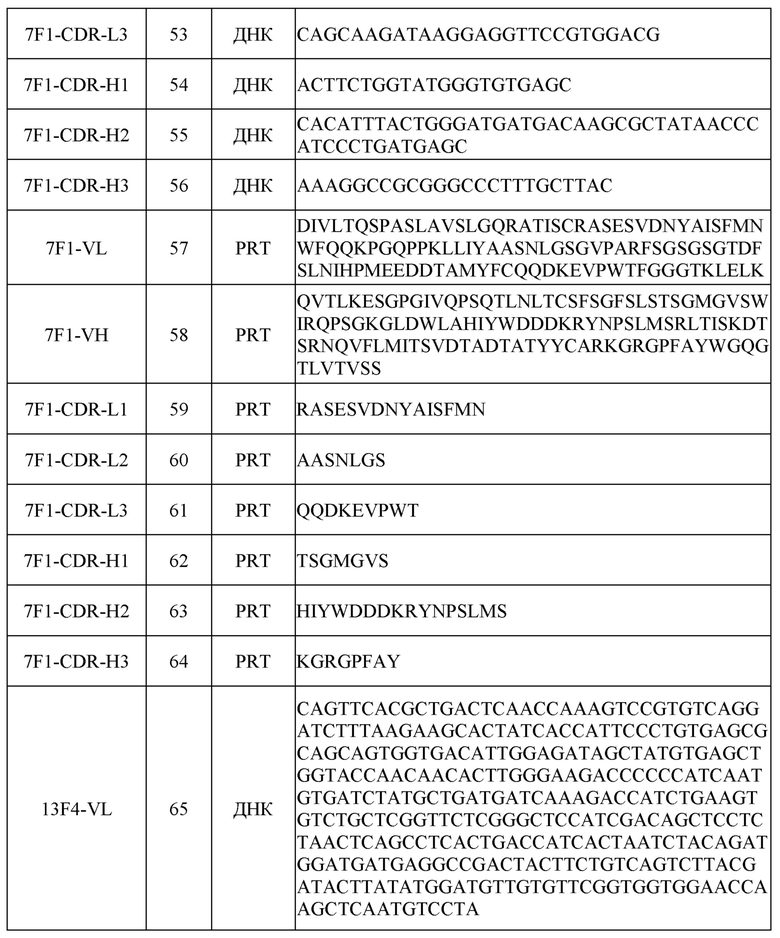
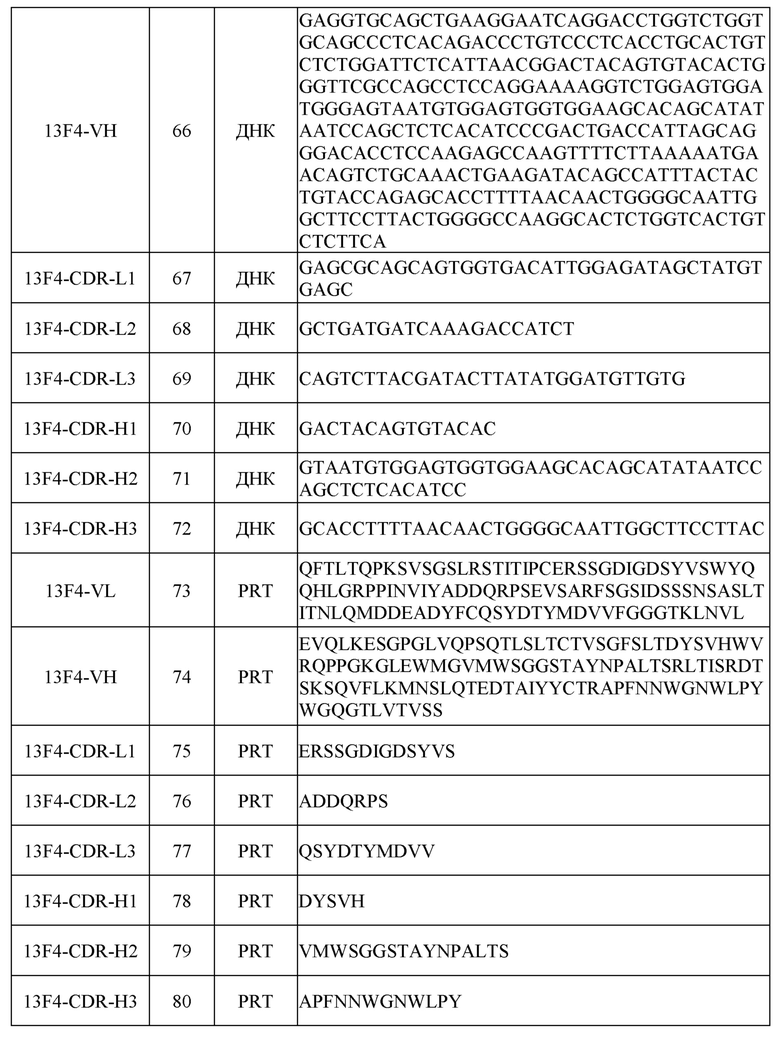
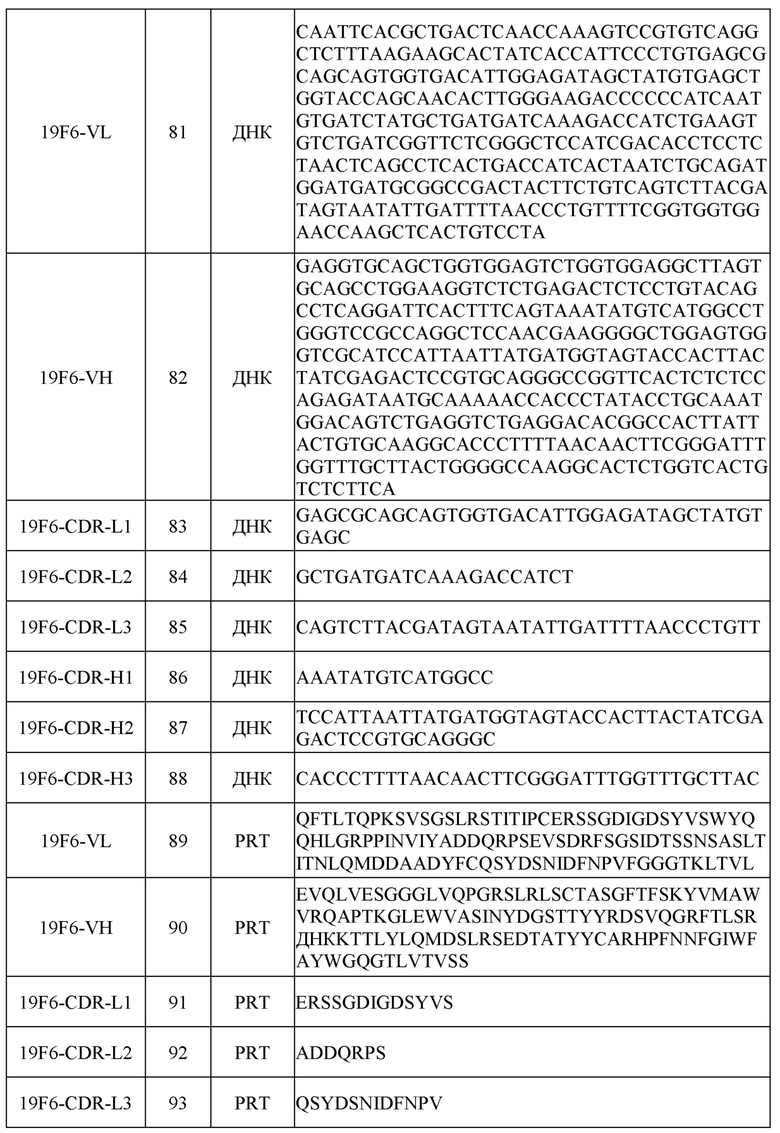
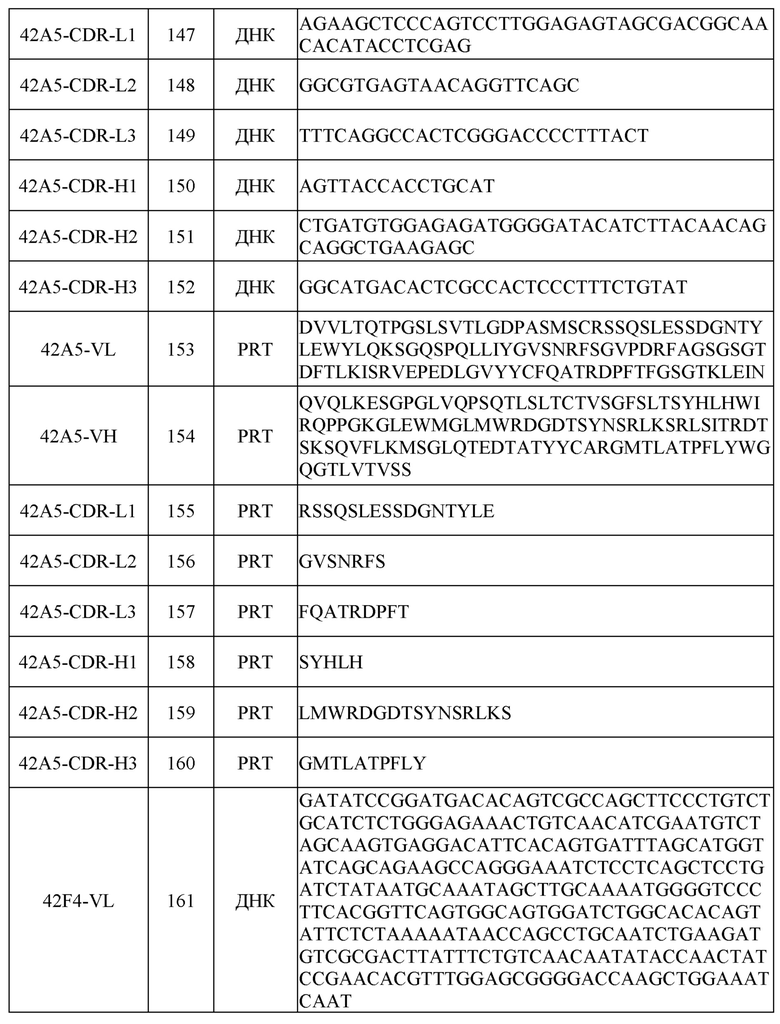
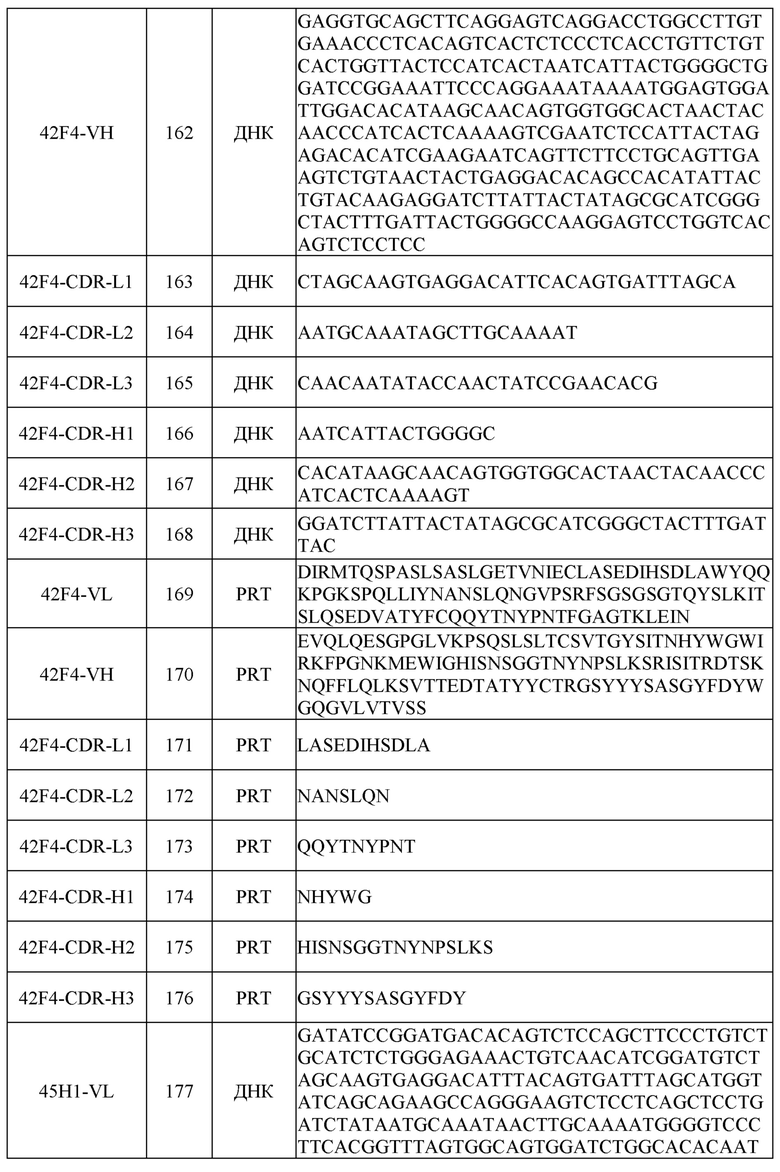
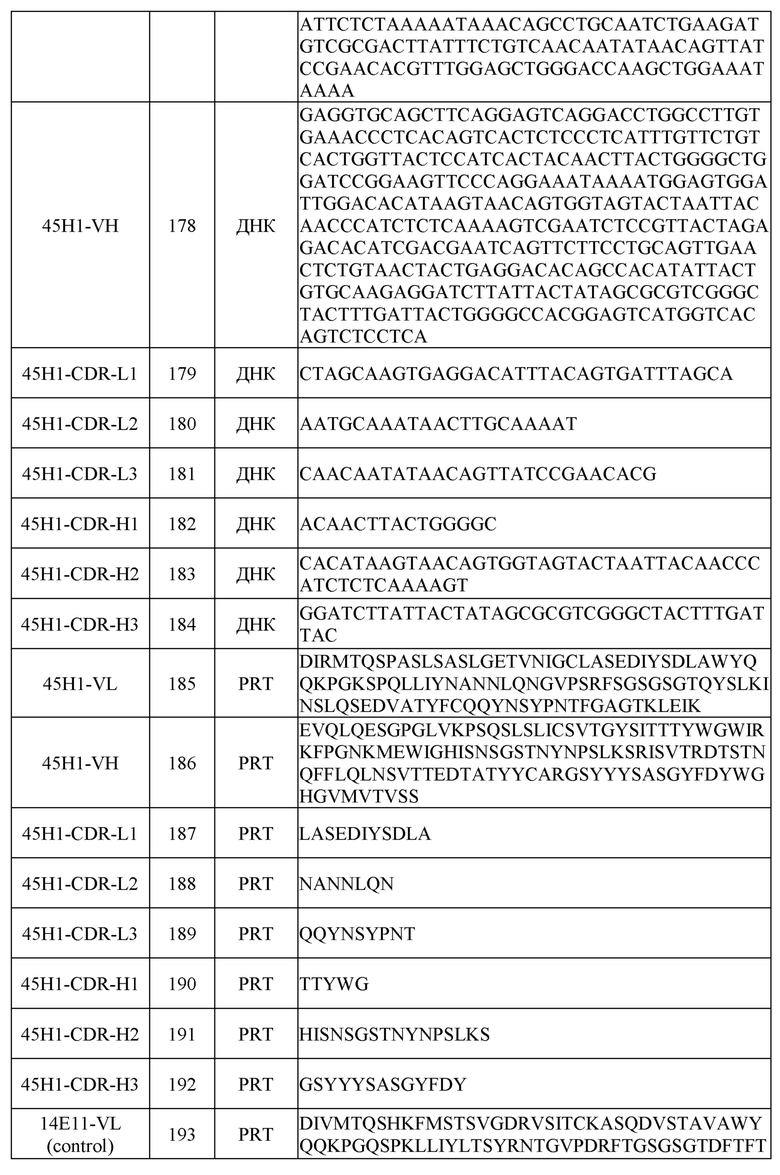
[0031] Последовательности нуклеиновых кислот (ДНК) и/или аминокислот (PRT), включая в себя последовательности VH и VL и CDR, некоторых примеров раскрытых в настоящем документе антител перечислены в таблице 1 ниже.
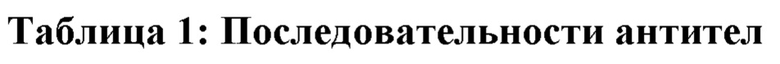
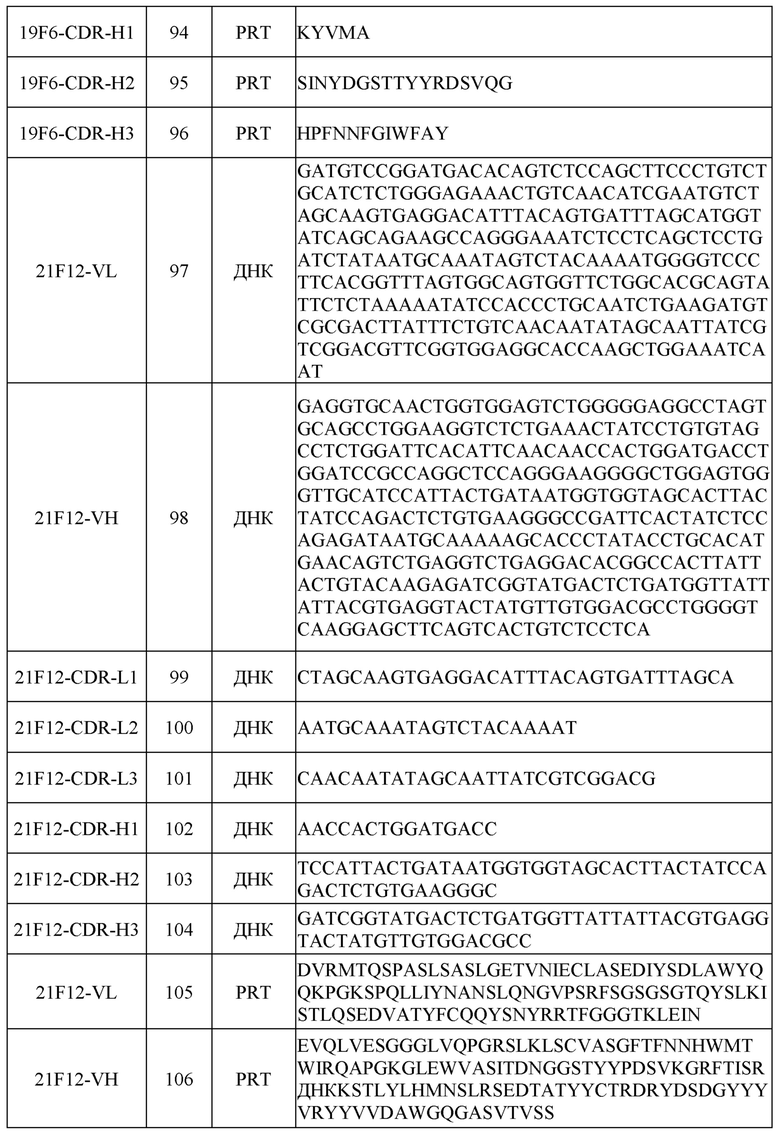
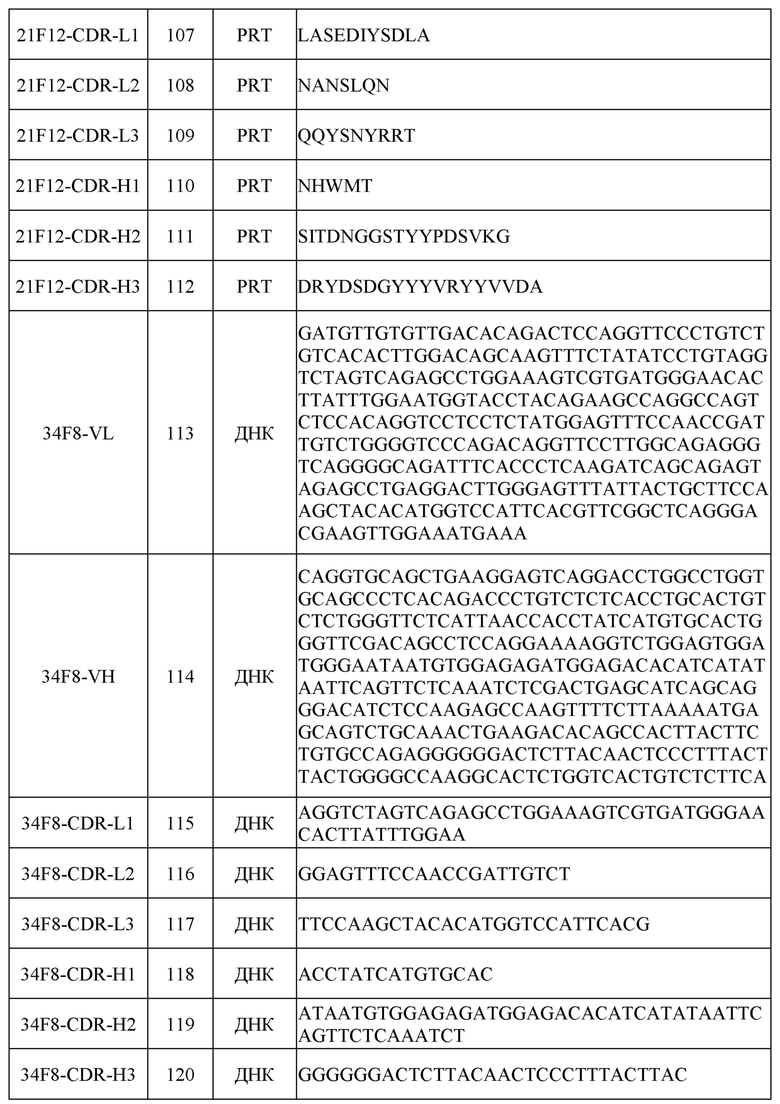
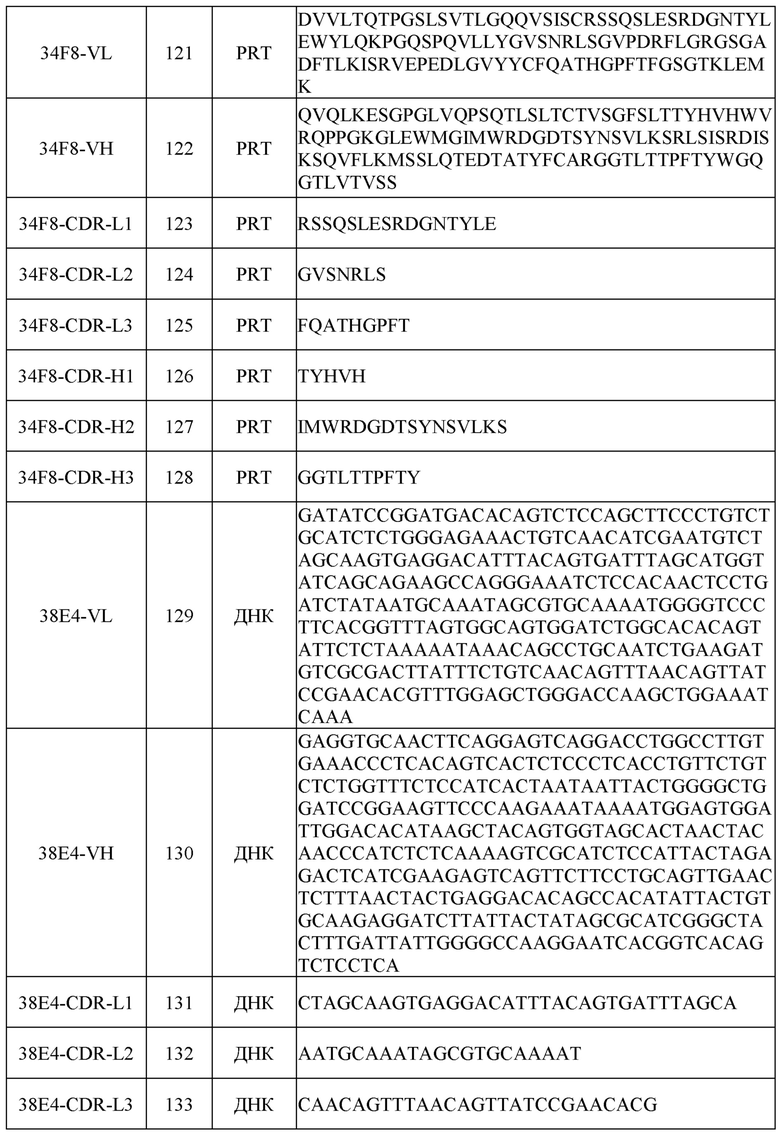
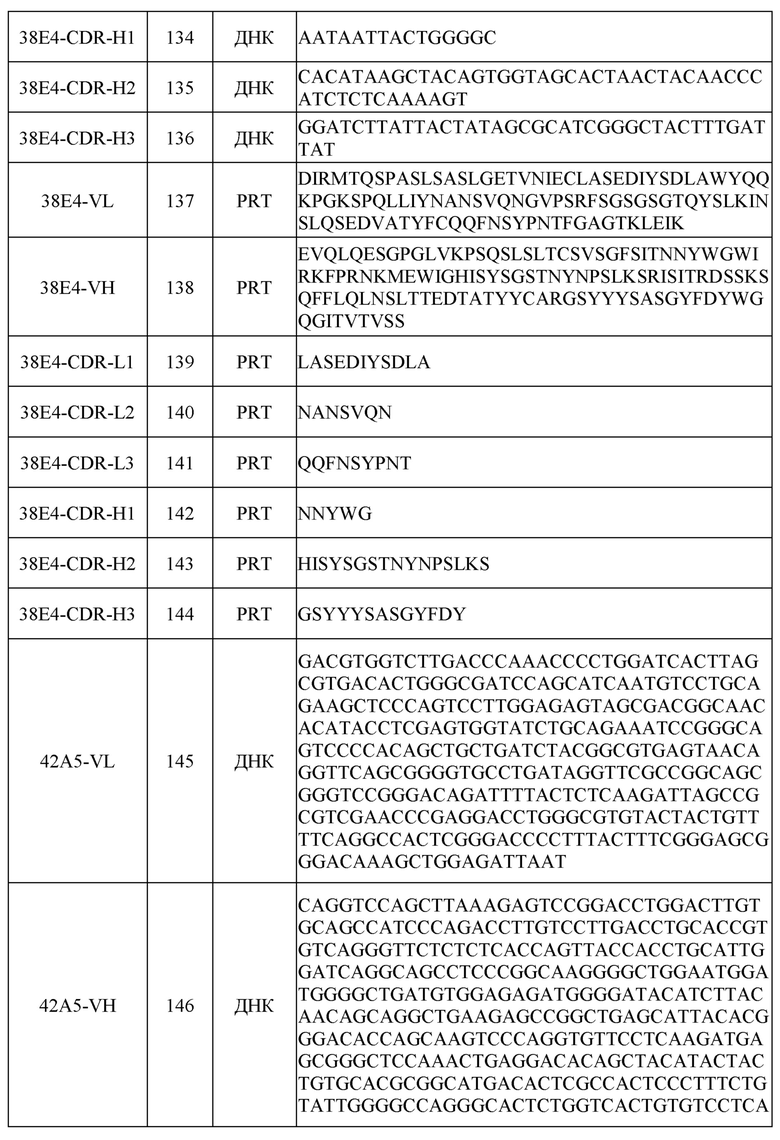

[0032] Согласно определенным вариантам осуществления в настоящем документе представлены гуманизированные антитела к FXI и/или к FXIa. В настоящей области техники известны различные способы гуманизации антител отличных от человека видов, так что антитела модифицируют для увеличения их сходства с антителами, встречающимися в природе у людей. Шесть CDR присутствуют в каждом антигенсвязывающем домене природного антитела. Эти CDR представляют собой короткие несмежные последовательности аминокислот, которые специфически расположены для образования антигенсвязывающего домена, поскольку антитело приобретает трехмерную конфигурацию. Остальные аминокислоты в антигенсвязывающих доменах, называемые «каркасными» областями, демонстрируют меньшую межмолекулярную вариабельность и образуют каркас, позволяющий правильно располагать CDR.
[0033] Например, гуманизация раскрытых в настоящем документе антител может быть осуществлена путем прививки CDR моноклональных антител, полученных иммунизацией мышей или крыс. CDR мышиного моноклонального антитела могут быть привиты в человеческий каркас, который впоследствии присоединяется к константной области человека для получения гуманизированного антитела. Вкратце, можно выполнить поиск в базе данных последовательностей антител зародышевой линии человека, в базе данных белков (PDB), в базе данных INN (международные непатентованные имена) и в других подходящих базах данных, и с помощью поиска можно определить наиболее схожие структуры антител. Кроме того, некоторые обратные мутации донорных остатков осуществляются в человеческих акцепторных каркасах. Согласно некоторым вариантам осуществления вариабельные области связаны с константной областью человеческого IgG. Например, могут быть использованы Fc домены IgG1, IgG2, IgG3 и IgG4 человека. В компетенцию специалиста в настоящей области техники входит гуманизация моноклонального антитела, производимого отличным от человека видом на основе существующей технологии.
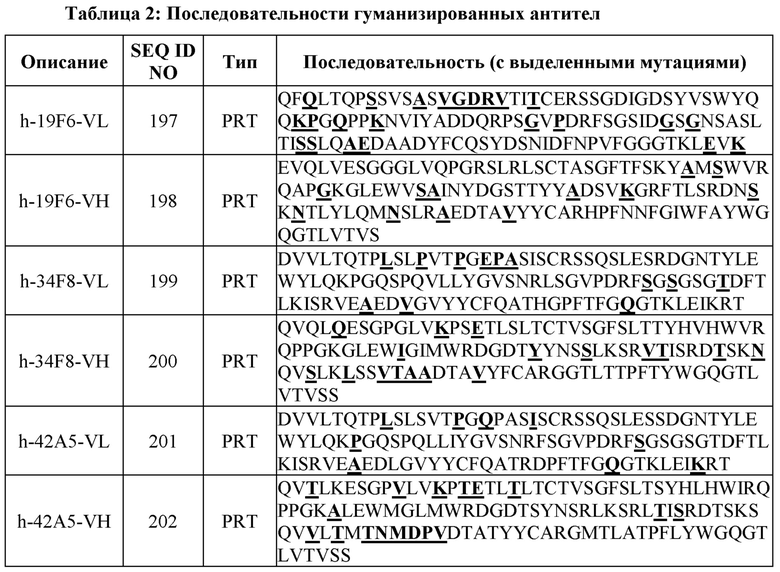
[0034] Последовательности вариабельных областей нескольких примеров гуманизированных антител показаны в таблице 2 ниже.
[0035] Представленные в настоящем документе антитела включают в себя варианты раскрытых в настоящем документе последовательностей, которые содержат одну или несколько мутаций в своих аминокислотных последовательностях, сохраняя при этом аффинность связывания с FXI, FXIa и/или их фрагментом (например, фрагментом, содержащим домен A3). Согласно некоторым вариантам осуществления антитела включают в себя вариабельную область, характеризующуюся аминокислотной последовательностью, которая по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99% идентична последовательности, выбранной из группы состоящей из SEQ IN NO: 9, 10, 25, 26, 41, 42, 57, 58, 73, 74, 89, 90, 105, 106, 121, 122, 137, 138, 153, 154, 169, 170, 185, 186 и 197-202, или их фрагмента, который сохраняет аффинность связывания с FXI, FXIa и/или их фрагментом.
[0036] В настоящее раскрытие также включены варианты нуклеиновых кислот, кодирующих антитела, которые связываются с FXI, FXIa и/или их фрагментом (например, фрагментом, содержащим домен A3). Согласно некоторым вариантам осуществления нуклеиновые кислоты, кодирующие антитела, включают в себя вариабельную область, характеризующуюся последовательностью нуклеиновой кислоты, которая по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99% идентична последовательности, выбранной из группы, состоящей из SEQ ID NO: 1, 2, 17, 18, 33, 34, 49, 50, 65, 66, 81, 82, 97, 98, 113, 114, 129, 130, 145, 146, 161, 162, 177 и 178 или их фрагмента, который кодирует полипептид с аффинностью связывания с FXI, FXIa и/или их фрагментом.
Фармацевтические композиции
[0037] Описанные в настоящем документе антитела могут быть включены в состав фармацевтических композиций. Фармацевтические композиции могут дополнительно содержать один или несколько фармацевтически приемлемых носителей, вспомогательных веществ, консервантов или их комбинацию. Фармацевтические композиции могут иметь различные составы, например, инъекционные составы, лиофилизированные составы, жидкие составы и т.д. В зависимости от состава и пути введения можно было бы выбрать подходящие добавки, такие как адъюванты, носители, вспомогательные вещества, консерванты. Смотрите, например, публикацию Wang et al., J. Pharm. Sciences 96(1): 1-26 (2007), содержание которой включено посредством ссылки. [0038] Фармацевтическая композиция может быть включена в набор с инструкцией по применению композиции.
Способы лечения
[0039] В настоящем документе представлен способ лечения и/или профилактики тромбоза у субъекта, страдающего от тромбоза и/или характеризующегося повышенным риском развития тромбоза. Также представлен способ ингибирования образования тромбов у субъекта. Эти способы предусматривают введение терапевтически эффективного количества представленного в настоящем документе антитела к FXI и/или к FXIa для вмешательства во внутренний путь. Согласно некоторым вариантам осуществления эти способы предусматривают введение субъекту фармацевтической композиции, содержащей представленное в настоящем документе антитело к FXI и/или к FXIa.
[0040] Раскрытые в настоящем документе способы могут быть использованы для профилактики и/или лечения связанных с тромбозом осложнений или состояний у нуждающегося в этом субъекта. Тромбоз вызывает ряд осложнений или состояний или связан с ними, включая в себя эмболический инсульт, венозный тромбоз, такой как венозная тромбоэмболия (VTE), тромбоз глубоких вен (DVT) и легочная эмболия (РЕ), артериальный тромбоз, такой как острый коронарный синдром (ACS), ишемическую болезнь сердца (CAD) и заболевание периферических артерий (PAD). Другие состояния, связанные с тромбозом, включают в себя, например, высокий риск VTE у подвергаемых хирургическому вмешательству пациентов, иммобилизованных пациентов, пациентов с раком, пациентов с сердечной недостаточностью, беременных пациентов или пациентов, имеющих другие медицинские состояния, которые могут вызывать тромбоз. Раскрываемые в настоящем документе способы относятся к профилактической антикоагулянтной терапии, т.е. тромбопрофилактике. Эти способы предусматривают введение субъекту, страдающему связанным с тромбозом осложнением, раскрытого выше терапевтически эффективного количества антитела к FXI и/или FXIa, как раскрыто в настоящем документе, или терапевтически эффективного количества фармацевтической композиции, содержащей антитело к FXI и/или к FXIa. Антитело или фармацевтическую композицию можно вводить отдельно или в сочетании с любой другой терапией для лечения или профилактики связанных с тромбозом осложнений или состояний.
[0041] Также представлен способ лечения и/или профилактики сепсиса у нуждающегося в этом субъекта. Была предпринята попытка введения антикоагулянтов пациентам с сепсисом для улучшения смертности или заболеваемости. Однако попытка не увенчалась успехом из-за нежелательного кровотечения, вызванного антикоагулянтами. Описанные в настоящем документе антитела могут быть использованы в качестве вторичной терапии в сочетании с другими терапевтическими средствами для лечения сепсиса, такими как антибиотики.
[0042] Используемый в настоящем документе термин «субъект» относится к субъекту-млекопитающему, предпочтительно человеку. «Нуждающийся в этом субъект» относится к субъекту, у которого был диагностирован тромбоз или связанные с тромбозом осложнения или состояния или существует повышенный риск развития тромбоза или связанных с тромбозом осложнений или состояний. Фразы «субъект» и «пациент» используются в настоящем документе взаимозаменяемо.
[0043] Термины «лечить» и «лечение», используемые в настоящем документе в отношении состояния, относятся к частичному или полному облегчению состояния, предотвращению состояния, уменьшению вероятности возникновения или повторения состояния, замедлению прогрессирования или развития состояния или устранению, уменьшению или замедлению развития одного или нескольких симптомов, связанных с состоянием. Что касается тромбоза и/или осложнений или состояний, связанных с тромбозом, «лечение» может относиться к предотвращению или замедлению роста существующего сгустка крови и/или предотвращению или замедлению образования сгустка крови. Согласно некоторым вариантам осуществления термин «лечить» или «лечение» означает, что у субъекта уменьшенное количество или размер сгустков крови по сравнению с субъектом без введения антител или его функциональных фрагментов. Согласно некоторым вариантам осуществления термин «лечить» или «лечение» означает, что один или несколько симптомов тромбоза и/или связанных с тромбозом состояний или осложнений ослаблены у субъекта, получающего описанное в настоящем документе антитело или фармацевтическую композицию, в сравнении с субъектом, который не получает такого лечения.
[0044] Используемый в настоящем документе термин «терапевтически эффективное количество» антитела или фармацевтической композиции представляет собой количество антитела или фармацевтической композиции, которое оказывает желаемое терапевтическое воздействие на субъекта, такое как лечение и/или профилактика тромбоза. Согласно определенным вариантам осуществления терапевтически эффективное количество представляет собой количество антитела или фармацевтической композиции, которое дает максимальный терапевтический эффект. Согласно другим вариантам осуществления терапевтически эффективное количество дает терапевтический эффект, который меньше максимального терапевтического эффекта. Например, терапевтически эффективное количество может представлять собой количество, которое вызывает терапевтический эффект, избегая при этом одного или нескольких побочных эффектов, связанных с дозировкой, которая дает максимальный терапевтический эффект. Терапевтически эффективное количество для конкретной композиции будет варьировать в зависимости от множества факторов, включающих в себя, помимо прочего, характеристики терапевтической композиции (например, активность, фармакокинетика, фармакодинамика и биодоступность), физиологическое состояние субъекта (например, возраст, масса тела, пол, тип и стадия заболевания, анамнез, общее физическое состояние, чувствительность к данной дозировке и другим присутствующим лекарственным средствам), природу любых фармацевтически приемлемых носителей, вспомогательных веществ и консервантов в композиции, а также пути введения. Специалист в области медицины и фармакологии сможет определить терапевтически эффективное количество путем рутинных экспериментов, а именно путем контроля реакции субъекта на введение антитела или фармацевтической композиции и соответствующей корректировки дозы. Дополнительные рекомендации смотрите, например, в Remington: The Science and Practice of Pharmacy, 22nd Edition, Pharmaceutical Press, London, 2012 и Goodman & Gilman's The Pharmacological Basis of Therapeutics, 12th Edition, McGraw-Hill, New York, NY, 2011, полное раскрытие которых включено в настоящий документ посредством ссылки.
[0045] Согласно некоторым вариантам осуществления терапевтически эффективное количество раскрытого в настоящем документе антитела находится в диапазоне от приблизительно 0,01 мг/кг до приблизительно 30 мг/кг, от приблизительно 0,1 мг/кг до приблизительно 10 мг/кг, от приблизительно 1 мг/кг до 5 мг/кг.
[0046] В компетенцию специалиста в настоящей области техники входит выбор подходящего пути введения, такого как подкожное введение, внутривенное введение, внутримышечное введение, внутрикожное введение, интратекальное введение или внутрибрюшинное введение. Для лечения нуждающегося в этом субъекта антитело или фармацевтическую композицию можно вводить непрерывно или периодически, для немедленного высвобождения, контролируемого высвобождения или замедленного высвобождения. Кроме того, антитело или фармацевтическую композицию можно вводить три раза в день, два раза в день или один раз в день в течение 3 дней, 5 дней, 7 дней, 10 дней, 2 недель, 3 недель или 4 недель. Антитело или фармацевтическую композицию можно вводить в течение заранее определенного периода времени. Альтернативно, антитело или фармацевтическую композицию можно вводить до достижения определенного терапевтического уровня. Согласно определенным вариантам осуществления представленные в настоящем документе способы предусматривают стадию оценки одного или нескольких терапевтических эталонов, чтобы определить, следует ли продолжать введение антитела или фармацевтической композиции.
Способ получения антител
[0047] В настоящем документе также представлены способы получения раскрытых в настоящем документе антител к FXI и/или к FXIa. Согласно некоторым вариантам осуществления этот способ предусматривает стадии клонирования в вектор нуклеиновой кислоты, кодирующей антитело к FXI и/или к FXIa, трансформации клетки-хозяина с вектором и культивирования клетки-хозяина для экспрессии антитела. Экспрессированное антитело может быть очищено из клетки-хозяина с использованием любого известного способа. Могут быть использованы различные векторы экспрессии, такие как вектор рТТ5 и вектор pcDNA3, а также различные линии клеток-хозяев, такие как клетки СНО (например, СНО-К1 и ExpiCHO) и клетки HEK193T.
[0048] Настоящее раскрытие также охватывает антитела, полученные раскрытым выше способом. Антитела могут быть подвергнуты одной или нескольким посттрансляционным модификациям.
[0049] Следующие примеры представлены для лучшей иллюстрации вариантов осуществления и не должны интерпретироваться как ограничение объема любого заявленного варианта осуществления. В той степени, в которой упоминаются конкретные материалы, они представлены просто для иллюстрации и не предназначены для ограничения настоящего изобретения. Специалист в настоящей области техники может разработать эквивалентные средства или реагенты без использования изобретательской способности и без отклонения от объема настоящего изобретения. Будет понятно, что в описанных в настоящем документе процедурах может быть сделано много изменений, при этом они все еще остаются в рамках настоящего изобретения. Авторы настоящего изобретения предполагают, что такие вариации включены в объем настоящего изобретения.
ПРИМЕРЫ
Пример 1: Производство и секвенирование антител к FXI
[0050] Мышей BALB/c и крыс Wistar иммунизировали человеческим FXI, и спленоциты от животных с хорошим иммунным ответом собирали для получения гибридом, которые подвергали субклонированию путем ограниченного разведения. Двенадцать моноклональных гибридомных клонов, экспрессирующих требуемые антитела к FXI, 3G12, 5В2, 7С9, 7F1, 13F4, 19F6, 21F12, 34F8, 38Е4, 42А5, 42F4 и 45Н1, получали с помощью ИФА с захватом и функционального скрининга.
[0051] Для определения аминокислотных и нуклеотидных последовательностей вариабельной области легкой (VL) и тяжелой (VH) цепей этих антител кДНК, кодирующие VL и VH, клонировали из соответствующих клеток гибридомы с помощью стандартных процедур ОТ-ПЦР. Последовательности VL и VH иллюстративных антител, включая в себя последовательности CDR, показаны в таблице 1.
Пример 2: Определение антикоагуляционной активности в плазме человека с использованием анализа активированного частичного тромбопластинового времени (АРТТ) и анализа протромбинового времени (РТ)
[0052] Анализ АРТТ измеряет активность внутренних и общих путей коагуляции, в то время как анализ РТ измеряет активность внешних и общих путей коагуляции. Антитела, исследованные в этом эксперименте, представляли собой 19F6, 34F8, 42А5, 1А6 и 14Е11. Последовательности вариабельных областей контрольных антител получали из патента США №8388959 и публикации заявки на патент США №2013/0171144 и переформатировали в IgG4. Эти антитела затем экспрессировали с использованием клеточной системы ExpiCHO. Стандартную человеческую плазму, приобретенную у Symens Inc., смешивали с равным объемом различных антител в различных концентрациях от 0 до 400 нМ в течение 5 минут перед исследованием на анализаторе СА600. В анализе АРТТ 50 мкл смеси плазма-антитело и 25 мкл реагента АРТТ (SMN 10445709, Symens Inc.) смешивали при температуре 37°С в течение 4 минут. Затем добавляли 25 мкл раствора CaCl2 (25 мМ, SMN 10446232, Symens Inc.) и определяли время образования сгустка. В анализе РТ 50 мкл смеси плазма-антитело смешивали с равным объемом реагента РТ (SMN 10446442, Symens Inc.) при температуре 37°С и определяли время образования сгустка.
[0053] Как показано на фиг. 1, все исследуемые антитела увеличивали АРТТ зависимым от концентрации образом при относительно низкой концентрации, например, до 100 нМ (или до 200 нМ для 14Е11); тогда как ни одно из этих антител не оказывало значительного влияния на РТ (данные не показаны). Эти результаты показывают, что все исследованные антитела ингибировали внутренний путь коагуляции, но не внешний путь.
Пример 3: Определение антикоагуляционной активности в плазме отличных от человека видов с использованием анализа активированного частичного тромбопластинового времени (АРТТ)
[0054] Влияние различных антител, в том числе 19F6, 34F8 и 42А5, на коагуляцию оценивали в плазме мыши, крысы и обезьяны с использованием того же способа, который описан в примере 2. Ни одно из исследованных антител не оказывало какого-либо влияния на АРТТ в плазме мыши и крысы, но все они, в относительно низкой концентрации, в зависимости от концентрации, увеличивали АРТТ в плазме обезьяны, как показано на фиг. 2, что указывает на то, что исследуемые антитела имели перекрестную активность с FXI/FXIa обезьяны, но не с FXI/FXIa мыши или крысы.
Пример 4. Гуманизация антител к FXI.
[0055] Использование мышиных моноклональных антител непосредственно в качестве терапевтических средств затруднялось из-за короткого периода полужизни и человеческих ответов на мышиные антитела. Одним из решений этой проблемы является гуманизация мышиных антител. Некоторые антитела подвергали гуманизации с помощью прививки CDR. Идентифицировали подходящие человеческие акцепторные каркасы для VL и VH каждого мышиного антитела, и в выбранные человеческие каркасы вводили различные количества обратных мутаций для поддержания структуры и/или функции полученного антитела. Если аффинность и функция этих гуманизированных антител существенно не уступали соответствующим немодифицированным антителам, модифицированные антитела считались успешно гуманизированными. Три гуманизированные последовательности VH и VL 19F6, 34F8 и 42А5, описанные как h-19F6, h-34F8 и h-42A5, соответственно, показаны в таблице 2.
Пример 5: Определение аффинности антител к FXI в отношении FXI человека
[0056] Аффинность антител к FXI/FXIa в отношении FXI/FXIa определяли с использованием технологии поверхностного плазмонного резонанса (SPR), выполненной на приборе BIAcore Т200. Гуманизированные антитела конструировали путем связывания вариабельных областей раскрытых в настоящем документе антител с Fc-доменом человеческого IgG4, и рекомбинанты экспрессировали в клетках СНО. Эти антитела захватывали на сенсорном чипе Biacore СМ5, который предварительно иммобилизовали антителом к IgG человека.
[0057] Затем различные концентрации очищенного антигена FXI или FXIa (0,005-1 мкг/мл) пропускали через чип СМ5 в течение 180 с для ассоциации с антителом к FXI/FXIa с последующим временем 1800 с для диссоциации. Данные по связыванию собирали и анализировали аффинность между FXI/FXIa и исследуемыми антителами с использованием программного обеспечения Biacore Evaluation Software, предоставляемого GE Healthcare. Сенсограммы SPR связывания FXI/FXIa с иммобилизованным h-19F6, h-34F8 и h-42A5 показаны на фиг. 3. Как показано на фиг. 3, ответ (RU) для каждого антитела становился выше с повышением концентрации FXI или FXIa. Рассчитывали константы диссоциации (KD) h-19F6, h-34F8 и h-42A5 к FXI и FXIa, и они детализированы в таблице 3. Аффинность каждого антитела к FXI и FXIa считается одинаковой, поскольку различие между ними меньше чем в 10 раз.
Пример 6: Определение сайта связывания антител к FXI на FXI
[0058] Сайты связывания 19F6 и 42А5 на FXI определяли с использованием технологии SPR. Вкратце, захватывающее IgG человека антитело предварительно иммобилизовали на сенсорном чипе Biacore СМ5, и рекомбинантный h-19F6 или h-42A5 улавливали, пропуская через чип. Равное количество (15 относительных единиц) h-19F6 и h-42A5 улавливали путем корректировки времени протекания антитела. Затем FXI дикого типа или химерный FXI, в котором отдельный домен apple заменяли соответствующим доменом из человеческого прекалликреина (химеры FXI/PK), пропускали через чип в течение 180 секунд для ассоциации с h-19F6 или h-42A5, затем в течение 1800 секунд для диссоциации. Данные по связыванию анализировали в кинетическом режиме высокой производительности, так как только одну концентрацию FXI, дикого типа или химерного, исследовали в анализе SPR. Результаты показали, что h-19F6 и h-42A5 связывали FXI, а также химеры FXI/PK, за исключением случаев, когда домен A3 FXI заменяли соответствующим доменом PK, указывая на то, что часть или полный эпитоп h-19F6 и h-42А5 на FXI находится в домене A3.
Пример 7: Функциональная нейтрализация FXIa антителами
[0059] Активность FXIa человека определяли путем измерения расщепления специфического хромогенного субстрата, S-2366 (Diapharma Inc.). Для исследования ингибирующей активности антител антитела h-19F6, h-34F8 и h-42A5 предварительно инкубировали в течение 5 минут при комнатной температуре с конечной концентрацией 5 нМ FXIa в PBS (физиологический раствор с фосфатным буфером). Затем добавляли равный объем S-2366 равного 1 мМ, чтобы инициировать реакцию расщепления FXIa, и изменения в абсорбции при 405 нм непрерывно контролировали с использованием планшет-ридера М5е (Molecular Devices Inc.). Данные анализировали с использованием программного обеспечения GraphPad Prism и они показаны на фиг. 4. Расчетные предполагаемые Ki для h-19F6, h-34F8 и h-42A5 составляют 0,67, 2,08 и 1,43 нМ, соответственно. Следовательно, все три исследованных антитела показали удовлетворительное ингибирующее действие на FXIa при относительно низкой концентрации.
Пример 8. Ингибирование опосредованной FXIa активации FIX антителами.
[0060] Человеческий FIX (200 нМ) инкубировали с FXIa (5 нМ) в PBS с 5 мМ CaCl2 при комнатной температуре с 1 мкМ контрольного IgG или h-19F6 или h-42A5. С интервалами 0, 15, 30, 45 и 60 минут образцы объемом 50 мкл собирали в буфер для образцов с додецилсульфатом. Образцы фракционировали по размеру на 10% невосстанавливающих гелях и переносили на поливинилиденфторидные мембраны. Вестерн-блоттинг проводили для определения уровней FIX, а также уровней FIXa с использованием козьего IgG к FIX человека (Affinity Biologicals). Как показано на фиг. 5, как h-19F6, так и h-42A5 ингибируют образование FIXa, индуцированное FXI, по сравнению с контролем.
Пример 9. Оценка эффектов антител к FXI на время свертывания у яванских макаков.
[0061] Яванским макакам вводили внутривенно указанные дозы различных антител. Кровь из поверхностных вен верхней конечности собирали до введения дозы и через 0,5, 1, 3, 6, 12 и 24 часа после введения дозы, и готовили цитратную плазму для определения АРТТ и РТ. В исследовании АРТТ смешивали 50 мкл разведенного образца плазмы и 25 мкл реагента АРТТ (SMN 10445709, Symens Inc.) и инкубировали при температуре 37°С в течение 4 минут. Затем добавляли 25 мкл раствора CaCl2 (25 мМ, SMN 10446232, Symens Inc.) и определяли время образования сгустка. В исследовании РТ 50 мкл разбавленной пробы плазмы смешивали с равным объемом реагента РТ (SMN 10446442, Symens Inc.) и инкубировали при температуре 37°С и определяли время до образования сгустка. Все три исследованных антитела продемонстрировали зависимое от дозы повышение АРТТ, как показано на фиг. 6, и ни одно из них не повлияло на РТ, как показано на фиг. 7.
Пример 10. Оценка эффектов антител к FXI на моделях тромбоза артериовенозного (AV) шунта и кровотечения из хвостовой вены у яванских макаков.
[0062] Как тромбоз, так и время кровотечения оценивали у одного и того же животного для множества доз каждого исследуемого антитела. Антитела, включенные в этот эксперимент, представляли собой h-34F8, h-19F6 и h42A5. Вкратце, время кровотечения и тромбоз последовательно оценивали перед введением дозы и через 30 минут после каждого введения антитела. Оценки кровотечения/тромбоза проводили четыре раза: до введения дозы и после введения дозы при трех возрастающих уровнях дозы (0,1, 0,3 и 1 мг/кг).
[0063] Для тромбоза AV-шунта шунтирующее устройство, содержащее предварительно взвешенную шелковую нить длиной 10 см, применяли для соединения бедренных артериальных и бедренных венозных канюль, и крови позволяли течь через шунт в течение 10 минут. Затем нить снимали с шунта и снова взвешивали. Массу сгустка на нити рассчитывали как разницу массы нити до и после кровотока.
[0064] Для оценки времени кровотечения в хвостовую вену животных вводили шприц объемом 2 мл. Когда объем крови в шприце прекращал увеличиваться, истекшее время записывали вручную как время кровотечения.
[0065] Все антитела в зависимости от дозы снижали массу тромба, как показано на фиг. 8, и ни одно из них не удлиняло время кровотечения в хвостовой вене, как показано на фиг. 9.
Пример 11: Оценка эффектов антител к FXI на индуцированный хлоридом железа артериальный тромбоз и время кровотечения у яванских макаков
[0066] Яванских макаков предварительно анестезировали золетилом в дозе 1,5 мг/кг, интубировали и вентилировали респиратором. Анестезию поддерживали изофлураном. Артериальное давление, частоту сердечных сокращений и температуру тела контролировали в течение всей процедуры. Исследуемые антитела, включая в себя h-34F8, h-19F6 и h-42A5, или контрольный наполнитель вводили через вену конечности путем инъекции за 2 часа до применения FeCl3. Левую бедренную артерию обнажали и выделяли тупым расслоением. На артерии устанавливали доплеровский зонд, и кровоток непрерывно регистрировали. Перед применением FeCl3 кровоток измеряли не менее 5 минут. Затем два куска фильтровальной бумаги, предварительно пропитанной FeCh, наносили на адвентициальную поверхность сосуда выше по течению от зонда в течение 10 минут. После того как удаляли фильтровальную бумагу, место нанесения промывали солевым раствором. Кровоток непрерывно измеряли до тех пор, пока он не уменьшался до 0. Записали время до 80% окклюзии (кровоток снизился до 20% от исходного кровотока) и время до 100% окклюзии (кровоток снизился до 0). У того же животного точное время кровотечения оценивали до введения дозы и через 1 час после введения дозы.
[0067] Исследовали влияние всех трех антител на индуцированный FeCl3 артериальный тромбоз. Четырем группам обезьян вводили контрольный наполнитель, h-34F8, h-19F6 или h-42A5 в течение 2 часов, соответственно, и FeCl3 наносили на левую бедренную артерию каждого животного, чтобы вызвать тромбоз. Контролировали скорость кровотока вниз по течению. Время до 80% и до 100% тромботической окклюзии в контрольной группе наполнителя составляло 14,66±1,30 мин и 18,50±1,76 мин, соответственно. Предварительное воздействие h-34F8 или h-42A5 в дозе 0,3 мг/кг значительно задержало время до 80% окклюзии до 59,53±16,95 мин и 40,80±7,94 мин, а время до 100% окклюзии до 70,40±20,76 мин и 50,61±9,48 мин, соответственно, как показано на фиг. 10. У обезьян, получавших h-19F6, также наблюдалось удлинение времени до 80% окклюзии (26,43±5,72 мин) и до 100% окклюзии (32,78±5,09 мин), хотя статистически не было значительная разница по сравнению с получавшей наполнитель контрольной группой, как показано на фиг. 10.
[0068] Влияние антител на гемостаз оценивали по точному времени кровотечения. Не было отмечено существенных различий между временем кровотечения до введения дозы и через 1 час после введения дозы для каждого исследуемого изделия (фиг. 11А, 11В и 11С). Изменение времени кровотечения после введения h-34F8, h-19F6 и h-42A5 не отличалось от изменения после контрольного воздействия наполнителя (фиг. 11D).
[0069] Также оценивали эффекты антител на время свертывания ex vivo плазмы обезьяны. Как и ожидалось, лечение с использованием h-34F8, h-19F6 и h-42A5 в дозе 0,3 мг/кг значительно продлило АРТТ в 3,29±0,20, 1,67±0,09 и 2,87±0,10 раза, соответственно, в то время как никакого увеличения АРТТ не наблюдалось после воздействия контрольным наполнителем, как показано на фиг. 12А. Кроме того, воздействие h-34F8, h-19F6 или h-42A5 не влияло на РТ, как показано на фиг. 12В.
[0070] Таким образом, было неожиданно обнаружено, что раскрытые в настоящем документе антитела не имели каких-либо побочных эффектов продолжительного кровотечения при эффективном ингибировании внутреннего пути коагуляции.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ШАНХАЙ БЕНЕМАЕ ФАРМАСЬЮТИКАЛ КОРПОРЕЙШН
<120> АНТИТЕЛА К ФАКТОРУ XI
<130> 57783-8013.WO00
<140> PCT/CN2017/119856
<141> 2017-12-29
<150> CN201710073984.X
<151> 2017-02-10
<160> 203
<170> PatentIn версия 3.5
<210> 1
<211> 333
<212> ДНК
<213> Mus musculus
<400> 1
gacattgtgc tgacccaatc tccagcttct ttggctgtgt ctctagggca gagggccacc 60
atctcctgca gagccagcga aagtgttgat aattatgcca ttagttttat gaactggttc 120
caacagaaac caggacagcc acccaaactc ctcatctatg ctgcatccaa cctaggatcc 180
ggggtccctg ccaggtttag tggcagtggg tctgggacag acttcagcct caacatccat 240
cctatggagg aggatgatac tgcaatgtat ttctgtcagc aagataagga ggttccgtgg 300
acgttcggtg gaggcaccga gctggaaatc aaa 333
<210> 2
<211> 354
<212> ДНК
<213> Mus musculus
<400> 2
caggtcactc tgaaagagtc tggccctggg atattgcagc cctcccagac cctcagtctg 60
acttgttctt tctctgggtt ttcactgaac actcctggta tgggtgtgag ctggattcgt 120
cagccttcag gaaagggtct ggaatggctg gcacacattt actgggatga tgacaagcgc 180
tttaacccat ccctgaagag ccgactcaca atctccaagg atacctccag agatcaggta 240
ttcctcatga tcaccagtgt ggacactgca gattctgcca catacttctg tgctcgaaaa 300
ggccgcgggc cctttactta ctggggccaa gggactctgg tcactgtctc ttca 354
<210> 3
<211> 45
<212> ДНК
<213> Mus musculus
<400> 3
agagccagcg aaagtgttga taattatgcc attagtttta tgaac 45
<210> 4
<211> 21
<212> ДНК
<213> Mus musculus
<400> 4
gctgcatcca acctaggatc c 21
2
<210> 5
<211> 27
<212> ДНК
<213> Mus musculus
<400> 5
cagcaagata aggaggttcc gtggacg 27
<210> 6
<211> 21
<212> ДНК
<213> Mus musculus
<400> 6
actcctggta tgggtgtgag c 21
<210> 7
<211> 48
<212> ДНК
<213> Mus musculus
<400> 7
cacatttact gggatgatga caagcgcttt aacccatccc tgaagagc 48
<210> 8
<211> 24
<212> ДНК
<213> Mus musculus
<400> 8
aaaggccgcg ggccctttac ttac 24
<210> 9
<211> 111
<212> PRT
<213> Mus musculus
<400> 9
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Asn Tyr
20 25 30
Ala Ile Ser Phe Met Asn Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Gly Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Leu Asn Ile His
65 70 75 80
Pro Met Glu Glu Asp Asp Thr Ala Met Tyr Phe Cys Gln Gln Asp Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gly Gly Thr Glu Leu Glu Ile Lys
100 105 110
3
<210> 10
<211> 118
<212> PRT
<213> Mus musculus
<400> 10
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Ile Leu Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Asn Thr Pro
20 25 30
Gly Met Gly Val Ser Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Ala His Ile Tyr Trp Asp Asp Asp Lys Arg Phe Asn Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Arg Asp Gln Val
65 70 75 80
Phe Leu Met Ile Thr Ser Val Asp Thr Ala Asp Ser Ala Thr Tyr Phe
85 90 95
Cys Ala Arg Lys Gly Arg Gly Pro Phe Thr Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 11
<211> 15
<212> PRT
<213> Mus musculus
<400> 11
Arg Ala Ser Glu Ser Val Asp Asn Tyr Ala Ile Ser Phe Met Asn
1 5 10 15
<210> 12
<211> 7
<212> PRT
<213> Mus musculus
<400> 12
Ala Ala Ser Asn Leu Gly Ser
1 5
<210> 13
<211> 9
<212> PRT
<213> Mus musculus
<400> 13
Gln Gln Asp Lys Glu Val Pro Trp Thr
1 5
4
<210> 14
<211> 7
<212> PRT
<213> Mus musculus
<400> 14
Thr Pro Gly Met Gly Val Ser
1 5
<210> 15
<211> 16
<212> PRT
<213> Mus musculus
<400> 15
His Ile Tyr Trp Asp Asp Asp Lys Arg Phe Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 16
<211> 8
<212> PRT
<213> Mus musculus
<400> 16
Lys Gly Arg Gly Pro Phe Thr Tyr
1 5
<210> 17
<211> 333
<212> ДНК
<213> Mus musculus
<400> 17
gacattgtgc tgacccaatc tccagcctct ttggctgtgt ctctagggca gagggccacc 60
atctcctgca gagccagcga aagtgttgat aattatggca ttagttttct gaactggttc 120
caacagaaac caggacagcc acccaaactc ctcatctatg ctgcatccaa tctaggatcc 180
ggggtccctg ccaggtttag tggcagtggg tctgggacag acttcagcct caacatccat 240
cctatggagg aggatgatac tgcaatgtat ttctgtcagc aagataaggg ggttccgtgg 300
acgttcggtg gaggcaccaa gctggaaatg aaa 333
<210> 18
<211> 354
<212> ДНК
<213> Mus musculus
<400> 18
caggttactc tgaaagagtc tggccctggg atattgcagc cctcccagac cctcagtctg 60
acttgttctt tctctgggtt ttcactgaac acttctggta tgggtgtgag ctggattcgt 120
cagccttcag gaaagggtct ggagtggctg gcacacattt actgggatga tgacaagcgc 180
tataaaccat ccctgaagag ccggctcaca atctccaagg atacctccag aaaccaggta 240
ttcctcatga tcaccagtgt ggacactgca gatactgcca catactactg tgttcgaaaa 300
ggccgcgggc cctttgctaa ctggggccaa gggactctgg tcactgtctc tgca 354
5
<210> 19
<211> 45
<212> ДНК
<213> Mus musculus
<400> 19
agagccagcg aaagtgttga taattatggc attagttttc tgaac 45
<210> 20
<211> 21
<212> ДНК
<213> Mus musculus
<400> 20
gctgcatcca atctaggatc c 21
<210> 21
<211> 27
<212> ДНК
<213> Mus musculus
<400> 21
cagcaagata agggggttcc gtggacg 27
<210> 22
<211> 21
<212> ДНК
<213> Mus musculus
<400> 22
acttctggta tgggtgtgag c 21
<210> 23
<211> 48
<212> ДНК
<213> Mus musculus
<400> 23
cacatttact gggatgatga caagcgctat aaaccatccc tgaagagc 48
<210> 24
<211> 24
<212> ДНК
<213> Mus musculus
<400> 24
aaaggccgcg ggccctttgc taac 24
<210> 25
<211> 111
<212> PRT
<213> Mus musculus
<400> 25
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Asn Tyr
20 25 30
Gly Ile Ser Phe Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
6
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Gly Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Leu Asn Ile His
65 70 75 80
Pro Met Glu Glu Asp Asp Thr Ala Met Tyr Phe Cys Gln Gln Asp Lys
85 90 95
Gly Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Met Lys
100 105 110
<210> 26
<211> 118
<212> PRT
<213> Mus musculus
<400> 26
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Ile Leu Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Asn Thr Ser
20 25 30
Gly Met Gly Val Ser Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Ala His Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Lys Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Arg Asn Gln Val
65 70 75 80
Phe Leu Met Ile Thr Ser Val Asp Thr Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Val Arg Lys Gly Arg Gly Pro Phe Ala Asn Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 27
<211> 15
<212> PRT
<213> Mus musculus
<400> 27
Arg Ala Ser Glu Ser Val Asp Asn Tyr Gly Ile Ser Phe Leu Asn
1 5 10 15
<210> 28
<211> 7
<212> PRT
<213> Mus musculus
7
<400> 28
Ala Ala Ser Asn Leu Gly Ser
1 5
<210> 29
<211> 9
<212> PRT
<213> Mus musculus
<400> 29
Gln Gln Asp Lys Gly Val Pro Trp Thr
1 5
<210> 30
<211> 7
<212> PRT
<213> Mus musculus
<400> 30
Thr Ser Gly Met Gly Val Ser
1 5
<210> 31
<211> 16
<212> PRT
<213> Mus musculus
<400> 31
His Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Lys Pro Ser Leu Lys Ser
1 5 10 15
<210> 32
<211> 8
<212> PRT
<213> Mus musculus
<400> 32
Lys Gly Arg Gly Pro Phe Ala Asn
1 5
<210> 33
<211> 321
<212> ДНК
<213> Mus musculus
<400> 33
gacatccaga tgacccagtc tccatcctcc ttatctgcct ctctgggaga aagagtcagt 60
ctcacttgtc gggcaagtca ggacattgat attcgcttaa actggcttcg acaggaacca 120
gatggaacta ttaaacgcct gatctacgcc acatccagtt tagattctgg tgtccccaaa 180
aggttcagtg gcagtaggtc tgggtcagat tattctctca ccatcagcag ccttgagtct 240
gaagattttg ttgactatta ctgtctacaa tatgctagtt ctccattcac gttcggctcg 300
gggacaaagt tggaaataaa a 321
<210> 34
<211> 354
<212> ДНК
8
<213> Mus musculus
<400> 34
cagatccagt tggtgcagtc tggacctgaa ctgaagaagc ctggagagac cgtcaagatc 60
tcctgcaagg cttctgggta tattttcaca gactatggaa tgaactgggt gaagcaggct 120
ccaggaaagg gtttaaagtg gatgggctgg ataaacacct acactggaga gccaacatat 180
gctgatgact tcaagggacg gtttgtcttc tctttggaaa cctctgccag cactgcctat 240
ttacagatca acaacctcaa aaatgaggac acggctacat ttttctgtgc aagaaggagg 300
atgggttatg ctgtggacta ctggggtcaa ggaacctcag tcaccgtctc ctca 354
<210> 35
<211> 33
<212> ДНК
<213> Mus musculus
<400> 35
cgggcaagtc aggacattga tattcgctta aac 33
<210> 36
<211> 21
<212> ДНК
<213> Mus musculus
<400> 36
gccacatcca gtttagattc t 21
<210> 37
<211> 27
<212> ДНК
<213> Mus musculus
<400> 37
ctacaatatg ctagttctcc attcacg 27
<210> 38
<211> 15
<212> ДНК
<213> Mus musculus
<400> 38
gactatggaa tgaac 15
<210> 39
<211> 51
<212> ДНК
<213> Mus musculus
<400> 39
tggataaaca cctacactgg agagccaaca tatgctgatg acttcaaggg a 51
<210> 40
<211> 27
<212> ДНК
<213> Mus musculus
<400> 40
aggaggatgg gttatgctgt ggactac 27
<210> 41
<211> 107
9
<212> PRT
<213> Mus musculus
<400> 41
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Ser Leu Thr Cys Arg Ala Ser Gln Asp Ile Asp Ile Arg
20 25 30
Leu Asn Trp Leu Arg Gln Glu Pro Asp Gly Thr Ile Lys Arg Leu Ile
35 40 45
Tyr Ala Thr Ser Ser Leu Asp Ser Gly Val Pro Lys Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Ser Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Ser
65 70 75 80
Glu Asp Phe Val Asp Tyr Tyr Cys Leu Gln Tyr Ala Ser Ser Pro Phe
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 42
<211> 118
<212> PRT
<213> Mus musculus
<400> 42
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Asp Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Val Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Phe Phe Cys
85 90 95
Ala Arg Arg Arg Met Gly Tyr Ala Val Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser
115
10
<210> 43
<211> 11
<212> PRT
<213> Mus musculus
<400> 43
Arg Ala Ser Gln Asp Ile Asp Ile Arg Leu Asn
1 5 10
<210> 44
<211> 7
<212> PRT
<213> Mus musculus
<400> 44
Ala Thr Ser Ser Leu Asp Ser
1 5
<210> 45
<211> 9
<212> PRT
<213> Mus musculus
<400> 45
Leu Gln Tyr Ala Ser Ser Pro Phe Thr
1 5
<210> 46
<211> 5
<212> PRT
<213> Mus musculus
<400> 46
Asp Tyr Gly Met Asn
1 5
<210> 47
<211> 17
<212> PRT
<213> Mus musculus
<400> 47
Trp Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe Lys
1 5 10 15
Gly
<210> 48
<211> 9
<212> PRT
<213> Mus musculus
<400> 48
Arg Arg Met Gly Tyr Ala Val Asp Tyr
1 5
<210> 49
<211> 333
11
<212> ДНК
<213> Mus musculus
<400> 49
gacattgtgc tgacccaatc tccagcttct ttggctgtgt ctctagggca gagggccacc 60
atctcctgca gagccagcga aagtgttgat aattatgcca ttagttttat gaattggttc 120
caacagaaac caggacagcc acccaaactc ctcatctatg ctgcatccaa cctaggatcc 180
ggggtccctg ccaggtttag tggcagtggg tctgggacag acttcagcct caacatccat 240
cctatggagg aggatgatac tgcaatgtat ttctgtcagc aagataagga ggttccgtgg 300
acgttcggtg gaggcaccaa gctggagctg aaa 333
<210> 50
<211> 354
<212> ДНК
<213> Mus musculus
<400> 50
caggttactc tgaaagagtc tggccctggg atagtgcagc cctcccagac cctcaatctg 60
acttgttctt tctctggatt ttcactgagc acttctggta tgggtgtgag ctggattcgt 120
cagccttcag gaaagggtct ggattggctg gcacacattt actgggatga tgacaagcgc 180
tataacccat ccctgatgag ccggctcaca atctccaagg atacctccag aaaccaggta 240
ttcctcatga tcaccagtgt ggacactgca gatactgcca catactactg tgctcgaaaa 300
ggccgcgggc cctttgctta ctggggccaa gggactctgg tcactgtctc ttca 354
<210> 51
<211> 45
<212> ДНК
<213> Mus musculus
<400> 51
agagccagcg aaagtgttga taattatgcc attagtttta tgaat 45
<210> 52
<211> 21
<212> ДНК
<213> Mus musculus
<400> 52
gctgcatcca acctaggatc c 21
<210> 53
<211> 27
<212> ДНК
<213> Mus musculus
<400> 53
cagcaagata aggaggttcc gtggacg 27
<210> 54
<211> 21
<212> ДНК
<213> Mus musculus
<400> 54
acttctggta tgggtgtgag c 21
12
<210> 55
<211> 48
<212> ДНК
<213> Mus musculus
<400> 55
cacatttact gggatgatga caagcgctat aacccatccc tgatgagc 48
<210> 56
<211> 24
<212> ДНК
<213> Mus musculus
<400> 56
aaaggccgcg ggccctttgc ttac 24
<210> 57
<211> 111
<212> PRT
<213> Mus musculus
<400> 57
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Asn Tyr
20 25 30
Ala Ile Ser Phe Met Asn Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Gly Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Leu Asn Ile His
65 70 75 80
Pro Met Glu Glu Asp Asp Thr Ala Met Tyr Phe Cys Gln Gln Asp Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 58
<211> 118
<212> PRT
<213> Mus musculus
<400> 58
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Ile Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Asn Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Met Gly Val Ser Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Asp
35 40 45
13
Trp Leu Ala His Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Asn Pro Ser
50 55 60
Leu Met Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Arg Asn Gln Val
65 70 75 80
Phe Leu Met Ile Thr Ser Val Asp Thr Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Lys Gly Arg Gly Pro Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 59
<211> 15
<212> PRT
<213> Mus musculus
<400> 59
Arg Ala Ser Glu Ser Val Asp Asn Tyr Ala Ile Ser Phe Met Asn
1 5 10 15
<210> 60
<211> 7
<212> PRT
<213> Mus musculus
<400> 60
Ala Ala Ser Asn Leu Gly Ser
1 5
<210> 61
<211> 9
<212> PRT
<213> Mus musculus
<400> 61
Gln Gln Asp Lys Glu Val Pro Trp Thr
1 5
<210> 62
<211> 7
<212> PRT
<213> Mus musculus
<400> 62
Thr Ser Gly Met Gly Val Ser
1 5
<210> 63
<211> 16
<212> PRT
<213> Mus musculus
<400> 63
His Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Asn Pro Ser Leu Met Ser
14
1 5 10 15
<210> 64
<211> 8
<212> PRT
<213> Mus musculus
<400> 64
Lys Gly Arg Gly Pro Phe Ala Tyr
1 5
<210> 65
<211> 333
<212> ДНК
<213> Mus musculus
<400> 65
cagttcacgc tgactcaacc aaagtccgtg tcaggatctt taagaagcac tatcaccatt 60
ccctgtgagc gcagcagtgg tgacattgga gatagctatg tgagctggta ccaacaacac 120
ttgggaagac cccccatcaa tgtgatctat gctgatgatc aaagaccatc tgaagtgtct 180
gctcggttct cgggctccat cgacagctcc tctaactcag cctcactgac catcactaat 240
ctacagatgg atgatgaggc cgactacttc tgtcagtctt acgatactta tatggatgtt 300
gtgttcggtg gtggaaccaa gctcaatgtc cta 333
<210> 66
<211> 360
<212> ДНК
<213> Mus musculus
<400> 66
gaggtgcagc tgaaggaatc aggacctggt ctggtgcagc cctcacagac cctgtccctc 60
acctgcactg tctctggatt ctcattaacg gactacagtg tacactgggt tcgccagcct 120
ccaggaaaag gtctggagtg gatgggagta atgtggagtg gtggaagcac agcatataat 180
ccagctctca catcccgact gaccattagc agggacacct ccaagagcca agttttctta 240
aaaatgaaca gtctgcaaac tgaagataca gccatttact actgtaccag agcacctttt 300
aacaactggg gcaattggct tccttactgg ggccaaggca ctctggtcac tgtctcttca 360
<210> 67
<211> 39
<212> ДНК
<213> Mus musculus
<400> 67
gagcgcagca gtggtgacat tggagatagc tatgtgagc 39
<210> 68
<211> 21
<212> ДНК
<213> Mus musculus
<400> 68
gctgatgatc aaagaccatc t 21
<210> 69
<211> 30
15
<212> ДНК
<213> Mus musculus
<400> 69
cagtcttacg atacttatat ggatgttgtg 30
<210> 70
<211> 15
<212> ДНК
<213> Mus musculus
<400> 70
gactacagtg tacac 15
<210> 71
<211> 48
<212> ДНК
<213> Mus musculus
<400> 71
gtaatgtgga gtggtggaag cacagcatat aatccagctc tcacatcc 48
<210> 72
<211> 36
<212> ДНК
<213> Mus musculus
<400> 72
gcacctttta acaactgggg caattggctt ccttac 36
<210> 73
<211> 111
<212> PRT
<213> Mus musculus
<400> 73
Gln Phe Thr Leu Thr Gln Pro Lys Ser Val Ser Gly Ser Leu Arg Ser
1 5 10 15
Thr Ile Thr Ile Pro Cys Glu Arg Ser Ser Gly Asp Ile Gly Asp Ser
20 25 30
Tyr Val Ser Trp Tyr Gln Gln His Leu Gly Arg Pro Pro Ile Asn Val
35 40 45
Ile Tyr Ala Asp Asp Gln Arg Pro Ser Glu Val Ser Ala Arg Phe Ser
50 55 60
Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Thr Ile Thr Asn
65 70 75 80
Leu Gln Met Asp Asp Glu Ala Asp Tyr Phe Cys Gln Ser Tyr Asp Thr
85 90 95
Tyr Met Asp Val Val Phe Gly Gly Gly Thr Lys Leu Asn Val Leu
100 105 110
<210> 74
<211> 120
<212> PRT
16
<213> Mus musculus
<400> 74
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Tyr
20 25 30
Ser Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Val Met Trp Ser Gly Gly Ser Thr Ala Tyr Asn Pro Ala Leu Thr
50 55 60
Ser Arg Leu Thr Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Ile Tyr Tyr Cys Thr
85 90 95
Arg Ala Pro Phe Asn Asn Trp Gly Asn Trp Leu Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 75
<211> 13
<212> PRT
<213> Mus musculus
<400> 75
Glu Arg Ser Ser Gly Asp Ile Gly Asp Ser Tyr Val Ser
1 5 10
<210> 76
<211> 7
<212> PRT
<213> Mus musculus
<400> 76
Ala Asp Asp Gln Arg Pro Ser
1 5
<210> 77
<211> 10
<212> PRT
<213> Mus musculus
<400> 77
Gln Ser Tyr Asp Thr Tyr Met Asp Val Val
1 5 10
<210> 78
<211> 5
<212> PRT
17
<213> Mus musculus
<400> 78
Asp Tyr Ser Val His
1 5
<210> 79
<211> 16
<212> PRT
<213> Mus musculus
<400> 79
Val Met Trp Ser Gly Gly Ser Thr Ala Tyr Asn Pro Ala Leu Thr Ser
1 5 10 15
<210> 80
<211> 12
<212> PRT
<213> Mus musculus
<400> 80
Ala Pro Phe Asn Asn Trp Gly Asn Trp Leu Pro Tyr
1 5 10
<210> 81
<211> 339
<212> ДНК
<213> Mus musculus
<400> 81
caattcacgc tgactcaacc aaagtccgtg tcaggctctt taagaagcac tatcaccatt 60
ccctgtgagc gcagcagtgg tgacattgga gatagctatg tgagctggta ccagcaacac 120
ttgggaagac cccccatcaa tgtgatctat gctgatgatc aaagaccatc tgaagtgtct 180
gatcggttct cgggctccat cgacacctcc tctaactcag cctcactgac catcactaat 240
ctgcagatgg atgatgcggc cgactacttc tgtcagtctt acgatagtaa tattgatttt 300
aaccctgttt tcggtggtgg aaccaagctc actgtccta 339
<210> 82
<211> 363
<212> ДНК
<213> Mus musculus
<400> 82
gaggtgcagc tggtggagtc tggtggaggc ttagtgcagc ctggaaggtc tctgagactc 60
tcctgtacag cctcaggatt cactttcagt aaatatgtca tggcctgggt ccgccaggct 120
ccaacgaagg ggctggagtg ggtcgcatcc attaattatg atggtagtac cacttactat 180
cgagactccg tgcagggccg gttcactctc tccagagata atgcaaaaac caccctatac 240
ctgcaaatgg acagtctgag gtctgaggac acggccactt attactgtgc aaggcaccct 300
tttaacaact tcgggatttg gtttgcttac tggggccaag gcactctggt cactgtctct 360
tca 363
<210> 83
<211> 39
18
<212> ДНК
<213> Mus musculus
<400> 83
gagcgcagca gtggtgacat tggagatagc tatgtgagc 39
<210> 84
<211> 21
<212> ДНК
<213> Mus musculus
<400> 84
gctgatgatc aaagaccatc t 21
<210> 85
<211> 36
<212> ДНК
<213> Mus musculus
<400> 85
cagtcttacg atagtaatat tgattttaac cctgtt 36
<210> 86
<211> 15
<212> ДНК
<213> Mus musculus
<400> 86
aaatatgtca tggcc 15
<210> 87
<211> 51
<212> ДНК
<213> Mus musculus
<400> 87
tccattaatt atgatggtag taccacttac tatcgagact ccgtgcaggg c 51
<210> 88
<211> 36
<212> ДНК
<213> Mus musculus
<400> 88
caccctttta acaacttcgg gatttggttt gcttac 36
<210> 89
<211> 113
<212> PRT
<213> Mus musculus
<400> 89
Gln Phe Thr Leu Thr Gln Pro Lys Ser Val Ser Gly Ser Leu Arg Ser
1 5 10 15
Thr Ile Thr Ile Pro Cys Glu Arg Ser Ser Gly Asp Ile Gly Asp Ser
20 25 30
Tyr Val Ser Trp Tyr Gln Gln His Leu Gly Arg Pro Pro Ile Asn Val
35 40 45
Ile Tyr Ala Asp Asp Gln Arg Pro Ser Glu Val Ser Asp Arg Phe Ser
19
50 55 60
Gly Ser Ile Asp Thr Ser Ser Asn Ser Ala Ser Leu Thr Ile Thr Asn
65 70 75 80
Leu Gln Met Asp Asp Ala Ala Asp Tyr Phe Cys Gln Ser Tyr Asp Ser
85 90 95
Asn Ile Asp Phe Asn Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val
100 105 110
Leu
<210> 90
<211> 121
<212> PRT
<213> Mus musculus
<400> 90
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Lys Tyr
20 25 30
Val Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Tyr Asp Gly Ser Thr Thr Tyr Tyr Arg Asp Ser Val
50 55 60
Gln Gly Arg Phe Thr Leu Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg His Pro Phe Asn Asn Phe Gly Ile Trp Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 91
<211> 13
<212> PRT
<213> Mus musculus
<400> 91
Glu Arg Ser Ser Gly Asp Ile Gly Asp Ser Tyr Val Ser
1 5 10
<210> 92
<211> 7
<212> PRT
20
<213> Mus musculus
<400> 92
Ala Asp Asp Gln Arg Pro Ser
1 5
<210> 93
<211> 12
<212> PRT
<213> Mus musculus
<400> 93
Gln Ser Tyr Asp Ser Asn Ile Asp Phe Asn Pro Val
1 5 10
<210> 94
<211> 5
<212> PRT
<213> Mus musculus
<400> 94
Lys Tyr Val Met Ala
1 5
<210> 95
<211> 17
<212> PRT
<213> Mus musculus
<400> 95
Ser Ile Asn Tyr Asp Gly Ser Thr Thr Tyr Tyr Arg Asp Ser Val Gln
1 5 10 15
Gly
<210> 96
<211> 12
<212> PRT
<213> Mus musculus
<400> 96
His Pro Phe Asn Asn Phe Gly Ile Trp Phe Ala Tyr
1 5 10
<210> 97
<211> 321
<212> ДНК
<213> Mus musculus
<400> 97
gatgtccgga tgacacagtc tccagcttcc ctgtctgcat ctctgggaga aactgtcaac 60
atcgaatgtc tagcaagtga ggacatttac agtgatttag catggtatca gcagaagcca 120
gggaaatctc ctcagctcct gatctataat gcaaatagtc tacaaaatgg ggtcccttca 180
cggtttagtg gcagtggttc tggcacgcag tattctctaa aaatatccac cctgcaatct 240
gaagatgtcg cgacttattt ctgtcaacaa tatagcaatt atcgtcggac gttcggtgga 300
21
ggcaccaagc tggaaatcaa t 321
<210> 98
<211> 381
<212> ДНК
<213> Mus musculus
<400> 98
gaggtgcaac tggtggagtc tgggggaggc ctagtgcagc ctggaaggtc tctgaaacta 60
tcctgtgtag cctctggatt cacattcaac aaccactgga tgacctggat ccgccaggct 120
ccagggaagg ggctggagtg ggttgcatcc attactgata atggtggtag cacttactat 180
ccagactctg tgaagggccg attcactatc tccagagata atgcaaaaag caccctatac 240
ctgcacatga acagtctgag gtctgaggac acggccactt attactgtac aagagatcgg 300
tatgactctg atggttatta ttacgtgagg tactatgttg tggacgcctg gggtcaagga 360
gcttcagtca ctgtctcctc a 381
<210> 99
<211> 33
<212> ДНК
<213> Mus musculus
<400> 99
ctagcaagtg aggacattta cagtgattta gca 33
<210> 100
<211> 21
<212> ДНК
<213> Mus musculus
<400> 100
aatgcaaata gtctacaaaa t 21
<210> 101
<211> 27
<212> ДНК
<213> Mus musculus
<400> 101
caacaatata gcaattatcg tcggacg 27
<210> 102
<211> 15
<212> ДНК
<213> Mus musculus
<400> 102
aaccactgga tgacc 15
<210> 103
<211> 51
<212> ДНК
<213> Mus musculus
<400> 103
tccattactg ataatggtgg tagcacttac tatccagact ctgtgaaggg c 51
<210> 104
<211> 54
<212> ДНК
22
<213> Mus musculus
<400> 104
gatcggtatg actctgatgg ttattattac gtgaggtact atgttgtgga cgcc 54
<210> 105
<211> 107
<212> PRT
<213> Mus musculus
<400> 105
Asp Val Arg Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Glu Thr Val Asn Ile Glu Cys Leu Ala Ser Glu Asp Ile Tyr Ser Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Asn Ala Asn Ser Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Ser Thr Leu Gln Ser
65 70 75 80
Glu Asp Val Ala Thr Tyr Phe Cys Gln Gln Tyr Ser Asn Tyr Arg Arg
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Asn
100 105
<210> 106
<211> 127
<212> PRT
<213> Mus musculus
<400> 106
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Asn Asn His
20 25 30
Trp Met Thr Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Thr Asp Asn Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu His Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
23
Thr Arg Asp Arg Tyr Asp Ser Asp Gly Tyr Tyr Tyr Val Arg Tyr Tyr
100 105 110
Val Val Asp Ala Trp Gly Gln Gly Ala Ser Val Thr Val Ser Ser
115 120 125
<210> 107
<211> 11
<212> PRT
<213> Mus musculus
<400> 107
Leu Ala Ser Glu Asp Ile Tyr Ser Asp Leu Ala
1 5 10
<210> 108
<211> 7
<212> PRT
<213> Mus musculus
<400> 108
Asn Ala Asn Ser Leu Gln Asn
1 5
<210> 109
<211> 9
<212> PRT
<213> Mus musculus
<400> 109
Gln Gln Tyr Ser Asn Tyr Arg Arg Thr
1 5
<210> 110
<211> 5
<212> PRT
<213> Mus musculus
<400> 110
Asn His Trp Met Thr
1 5
<210> 111
<211> 17
<212> PRT
<213> Mus musculus
<400> 111
Ser Ile Thr Asp Asn Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
1 5 10 15
Gly
<210> 112
<211> 18
<212> PRT
<213> Mus musculus
24
<400> 112
Asp Arg Tyr Asp Ser Asp Gly Tyr Tyr Tyr Val Arg Tyr Tyr Val Val
1 5 10 15
Asp Ala
<210> 113
<211> 336
<212> ДНК
<213> Mus musculus
<400> 113
gatgttgtgt tgacacagac tccaggttcc ctgtctgtca cacttggaca gcaagtttct 60
atatcctgta ggtctagtca gagcctggaa agtcgtgatg ggaacactta tttggaatgg 120
tacctacaga agccaggcca gtctccacag gtcctcctct atggagtttc caaccgattg 180
tctggggtcc cagacaggtt ccttggcaga gggtcagggg cagatttcac cctcaagatc 240
agcagagtag agcctgagga cttgggagtt tattactgct tccaagctac acatggtcca 300
ttcacgttcg gctcagggac gaagttggaa atgaaa 336
<210> 114
<211> 354
<212> ДНК
<213> Mus musculus
<400> 114
caggtgcagc tgaaggagtc aggacctggc ctggtgcagc cctcacagac cctgtctctc 60
acctgcactg tctctgggtt ctcattaacc acctatcatg tgcactgggt tcgacagcct 120
ccaggaaaag gtctggagtg gatgggaata atgtggagag atggagacac atcatataat 180
tcagttctca aatctcgact gagcatcagc agggacatct ccaagagcca agttttctta 240
aaaatgagca gtctgcaaac tgaagacaca gccacttact tctgtgccag aggggggact 300
cttacaactc cctttactta ctggggccaa ggcactctgg tcactgtctc ttca 354
<210> 115
<211> 48
<212> ДНК
<213> Mus musculus
<400> 115
aggtctagtc agagcctgga aagtcgtgat gggaacactt atttggaa 48
<210> 116
<211> 21
<212> ДНК
<213> Mus musculus
<400> 116
ggagtttcca accgattgtc t 21
<210> 117
<211> 27
<212> ДНК
<213> Mus musculus
<400> 117
25
ttccaagcta cacatggtcc attcacg 27
<210> 118
<211> 15
<212> ДНК
<213> Mus musculus
<400> 118
acctatcatg tgcac 15
<210> 119
<211> 48
<212> ДНК
<213> Mus musculus
<400> 119
ataatgtgga gagatggaga cacatcatat aattcagttc tcaaatct 48
<210> 120
<211> 30
<212> ДНК
<213> Mus musculus
<400> 120
ggggggactc ttacaactcc ctttacttac 30
<210> 121
<211> 112
<212> PRT
<213> Mus musculus
<400> 121
Asp Val Val Leu Thr Gln Thr Pro Gly Ser Leu Ser Val Thr Leu Gly
1 5 10 15
Gln Gln Val Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Glu Ser Arg
20 25 30
Asp Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Leu Tyr Gly Val Ser Asn Arg Leu Ser Gly Val Pro
50 55 60
Asp Arg Phe Leu Gly Arg Gly Ser Gly Ala Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Pro Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Ala
85 90 95
Thr His Gly Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Met Lys
100 105 110
<210> 122
<211> 118
<212> PRT
<213> Mus musculus
<400> 122
26
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Met Trp Arg Asp Gly Asp Thr Ser Tyr Asn Ser Val Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Ile Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala
85 90 95
Arg Gly Gly Thr Leu Thr Thr Pro Phe Thr Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 123
<211> 16
<212> PRT
<213> Mus musculus
<400> 123
Arg Ser Ser Gln Ser Leu Glu Ser Arg Asp Gly Asn Thr Tyr Leu Glu
1 5 10 15
<210> 124
<211> 7
<212> PRT
<213> Mus musculus
<400> 124
Gly Val Ser Asn Arg Leu Ser
1 5
<210> 125
<211> 9
<212> PRT
<213> Mus musculus
<400> 125
Phe Gln Ala Thr His Gly Pro Phe Thr
1 5
<210> 126
<211> 5
<212> PRT
<213> Mus musculus
<400> 126
27
Thr Tyr His Val His
1 5
<210> 127
<211> 16
<212> PRT
<213> Mus musculus
<400> 127
Ile Met Trp Arg Asp Gly Asp Thr Ser Tyr Asn Ser Val Leu Lys Ser
1 5 10 15
<210> 128
<211> 10
<212> PRT
<213> Mus musculus
<400> 128
Gly Gly Thr Leu Thr Thr Pro Phe Thr Tyr
1 5 10
<210> 129
<211> 321
<212> ДНК
<213> Mus musculus
<400> 129
gatatccgga tgacacagtc tccagcttcc ctgtctgcat ctctgggaga aactgtcaac 60
atcgaatgtc tagcaagtga ggacatttac agtgatttag catggtatca gcagaagcca 120
gggaaatctc cacaactcct gatctataat gcaaatagcg tgcaaaatgg ggtcccttca 180
cggtttagtg gcagtggatc tggcacacag tattctctaa aaataaacag cctgcaatct 240
gaagatgtcg cgacttattt ctgtcaacag tttaacagtt atccgaacac gtttggagct 300
gggaccaagc tggaaatcaa a 321
<210> 130
<211> 363
<212> ДНК
<213> Mus musculus
<400> 130
gaggtgcaac ttcaggagtc aggacctggc cttgtgaaac cctcacagtc actctccctc 60
acctgttctg tctctggttt ctccatcact aataattact ggggctggat ccggaagttc 120
ccaagaaata aaatggagtg gattggacac ataagctaca gtggtagcac taactacaac 180
ccatctctca aaagtcgcat ctccattact agagactcat cgaagagtca gttcttcctg 240
cagttgaact ctttaactac tgaggacaca gccacatatt actgtgcaag aggatcttat 300
tactatagcg catcgggcta ctttgattat tggggccaag gaatcacggt cacagtctcc 360
tca 363
<210> 131
<211> 33
<212> ДНК
<213> Mus musculus
<400> 131
28
ctagcaagtg aggacattta cagtgattta gca 33
<210> 132
<211> 21
<212> ДНК
<213> Mus musculus
<400> 132
aatgcaaata gcgtgcaaaa t 21
<210> 133
<211> 27
<212> ДНК
<213> Mus musculus
<400> 133
caacagttta acagttatcc gaacacg 27
<210> 134
<211> 15
<212> ДНК
<213> Mus musculus
<400> 134
aataattact ggggc 15
<210> 135
<211> 48
<212> ДНК
<213> Mus musculus
<400> 135
cacataagct acagtggtag cactaactac aacccatctc tcaaaagt 48
<210> 136
<211> 39
<212> ДНК
<213> Mus musculus
<400> 136
ggatcttatt actatagcgc atcgggctac tttgattat 39
<210> 137
<211> 107
<212> PRT
<213> Mus musculus
<400> 137
Asp Ile Arg Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Glu Thr Val Asn Ile Glu Cys Leu Ala Ser Glu Asp Ile Tyr Ser Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Asn Ala Asn Ser Val Gln Asn Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser
29
65 70 75 80
Glu Asp Val Ala Thr Tyr Phe Cys Gln Gln Phe Asn Ser Tyr Pro Asn
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 138
<211> 121
<212> PRT
<213> Mus musculus
<400> 138
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Ser Gly Phe Ser Ile Thr Asn Asn
20 25 30
Tyr Trp Gly Trp Ile Arg Lys Phe Pro Arg Asn Lys Met Glu Trp Ile
35 40 45
Gly His Ile Ser Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Thr Arg Asp Ser Ser Lys Ser Gln Phe Phe Leu
65 70 75 80
Gln Leu Asn Ser Leu Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Gly Ser Tyr Tyr Tyr Ser Ala Ser Gly Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Ile Thr Val Thr Val Ser Ser
115 120
<210> 139
<211> 11
<212> PRT
<213> Mus musculus
<400> 139
Leu Ala Ser Glu Asp Ile Tyr Ser Asp Leu Ala
1 5 10
<210> 140
<211> 7
<212> PRT
<213> Mus musculus
<400> 140
Asn Ala Asn Ser Val Gln Asn
1 5
30
<210> 141
<211> 9
<212> PRT
<213> Mus musculus
<400> 141
Gln Gln Phe Asn Ser Tyr Pro Asn Thr
1 5
<210> 142
<211> 5
<212> PRT
<213> Mus musculus
<400> 142
Asn Asn Tyr Trp Gly
1 5
<210> 143
<211> 16
<212> PRT
<213> Mus musculus
<400> 143
His Ile Ser Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 144
<211> 13
<212> PRT
<213> Mus musculus
<400> 144
Gly Ser Tyr Tyr Tyr Ser Ala Ser Gly Tyr Phe Asp Tyr
1 5 10
<210> 145
<211> 336
<212> ДНК
<213> Mus musculus
<400> 145
gacgtggtct tgacccaaac ccctggatca cttagcgtga cactgggcga tccagcatca 60
atgtcctgca gaagctccca gtccttggag agtagcgacg gcaacacata cctcgagtgg 120
tatctgcaga aatccgggca gtccccacag ctgctgatct acggcgtgag taacaggttc 180
agcggggtgc ctgataggtt cgccggcagc gggtccggga cagattttac tctcaagatt 240
agccgcgtcg aacccgagga cctgggcgtg tactactgtt ttcaggccac tcgggacccc 300
tttactttcg ggagcgggac aaagctggag attaat 336
<210> 146
<211> 354
<212> ДНК
<213> Mus musculus
<400> 146
caggtccagc ttaaagagtc cggacctgga cttgtgcagc catcccagac cttgtccttg 60
acctgcaccg tgtcagggtt ctctctcacc agttaccacc tgcattggat caggcagcct 120
31
cccggcaagg ggctggaatg gatggggctg atgtggagag atggggatac atcttacaac 180
agcaggctga agagccggct gagcattaca cgggacacca gcaagtccca ggtgttcctc 240
aagatgagcg ggctccaaac tgaggacaca gctacatact actgtgcacg cggcatgaca 300
ctcgccactc cctttctgta ttggggccag ggcactctgg tcactgtgtc ctca 354
<210> 147
<211> 48
<212> ДНК
<213> Mus musculus
<400> 147
agaagctccc agtccttgga gagtagcgac ggcaacacat acctcgag 48
<210> 148
<211> 21
<212> ДНК
<213> Mus musculus
<400> 148
ggcgtgagta acaggttcag c 21
<210> 149
<211> 27
<212> ДНК
<213> Mus musculus
<400> 149
tttcaggcca ctcgggaccc ctttact 27
<210> 150
<211> 15
<212> ДНК
<213> Mus musculus
<400> 150
agttaccacc tgcat 15
<210> 151
<211> 48
<212> ДНК
<213> Mus musculus
<400> 151
ctgatgtgga gagatgggga tacatcttac aacagcaggc tgaagagc 48
<210> 152
<211> 30
<212> ДНК
<213> Mus musculus
<400> 152
ggcatgacac tcgccactcc ctttctgtat 30
<210> 153
<211> 112
<212> PRT
<213> Mus musculus
<400> 153
Asp Val Val Leu Thr Gln Thr Pro Gly Ser Leu Ser Val Thr Leu Gly
32
1 5 10 15
Asp Pro Ala Ser Met Ser Cys Arg Ser Ser Gln Ser Leu Glu Ser Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Ser Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Gly Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ala Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Pro Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Ala
85 90 95
Thr Arg Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn
100 105 110
<210> 154
<211> 118
<212> PRT
<213> Mus musculus
<400> 154
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
His Leu His Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Leu Met Trp Arg Asp Gly Asp Thr Ser Tyr Asn Ser Arg Leu Lys
50 55 60
Ser Arg Leu Ser Ile Thr Arg Asp Thr Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Ser Gly Leu Gln Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Gly Met Thr Leu Ala Thr Pro Phe Leu Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 155
<211> 16
<212> PRT
<213> Mus musculus
<400> 155
33
Arg Ser Ser Gln Ser Leu Glu Ser Ser Asp Gly Asn Thr Tyr Leu Glu
1 5 10 15
<210> 156
<211> 7
<212> PRT
<213> Mus musculus
<400> 156
Gly Val Ser Asn Arg Phe Ser
1 5
<210> 157
<211> 9
<212> PRT
<213> Mus musculus
<400> 157
Phe Gln Ala Thr Arg Asp Pro Phe Thr
1 5
<210> 158
<211> 5
<212> PRT
<213> Mus musculus
<400> 158
Ser Tyr His Leu His
1 5
<210> 159
<211> 16
<212> PRT
<213> Mus musculus
<400> 159
Leu Met Trp Arg Asp Gly Asp Thr Ser Tyr Asn Ser Arg Leu Lys Ser
1 5 10 15
<210> 160
<211> 10
<212> PRT
<213> Mus musculus
<400> 160
Gly Met Thr Leu Ala Thr Pro Phe Leu Tyr
1 5 10
<210> 161
<211> 321
<212> ДНК
<213> Mus musculus
<400> 161
gatatccgga tgacacagtc gccagcttcc ctgtctgcat ctctgggaga aactgtcaac 60
atcgaatgtc tagcaagtga ggacattcac agtgatttag catggtatca gcagaagcca 120
gggaaatctc ctcagctcct gatctataat gcaaatagct tgcaaaatgg ggtcccttca 180
34
cggttcagtg gcagtggatc tggcacacag tattctctaa aaataaccag cctgcaatct 240
gaagatgtcg cgacttattt ctgtcaacaa tataccaact atccgaacac gtttggagcg 300
gggaccaagc tggaaatcaa t 321
<210> 162
<211> 363
<212> ДНК
<213> Mus musculus
<400> 162
gaggtgcagc ttcaggagtc aggacctggc cttgtgaaac cctcacagtc actctccctc 60
acctgttctg tcactggtta ctccatcact aatcattact ggggctggat ccggaaattc 120
ccaggaaata aaatggagtg gattggacac ataagcaaca gtggtggcac taactacaac 180
ccatcactca aaagtcgaat ctccattact agagacacat cgaagaatca gttcttcctg 240
cagttgaagt ctgtaactac tgaggacaca gccacatatt actgtacaag aggatcttat 300
tactatagcg catcgggcta ctttgattac tggggccaag gagtcctggt cacagtctcc 360
tcc 363
<210> 163
<211> 33
<212> ДНК
<213> Mus musculus
<400> 163
ctagcaagtg aggacattca cagtgattta gca 33
<210> 164
<211> 21
<212> ДНК
<213> Mus musculus
<400> 164
aatgcaaata gcttgcaaaa t 21
<210> 165
<211> 27
<212> ДНК
<213> Mus musculus
<400> 165
caacaatata ccaactatcc gaacacg 27
<210> 166
<211> 15
<212> ДНК
<213> Mus musculus
<400> 166
aatcattact ggggc 15
<210> 167
<211> 48
<212> ДНК
<213> Mus musculus
<400> 167
cacataagca acagtggtgg cactaactac aacccatcac tcaaaagt 48
35
<210> 168
<211> 39
<212> ДНК
<213> Mus musculus
<400> 168
ggatcttatt actatagcgc atcgggctac tttgattac 39
<210> 169
<211> 107
<212> PRT
<213> Mus musculus
<400> 169
Asp Ile Arg Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Glu Thr Val Asn Ile Glu Cys Leu Ala Ser Glu Asp Ile His Ser Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Asn Ala Asn Ser Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Thr Ser Leu Gln Ser
65 70 75 80
Glu Asp Val Ala Thr Tyr Phe Cys Gln Gln Tyr Thr Asn Tyr Pro Asn
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Asn
100 105
<210> 170
<211> 121
<212> PRT
<213> Mus musculus
<400> 170
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Asn His
20 25 30
Tyr Trp Gly Trp Ile Arg Lys Phe Pro Gly Asn Lys Met Glu Trp Ile
35 40 45
Gly His Ile Ser Asn Ser Gly Gly Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe Leu
65 70 75 80
36
Gln Leu Lys Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Thr
85 90 95
Arg Gly Ser Tyr Tyr Tyr Ser Ala Ser Gly Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Val Leu Val Thr Val Ser Ser
115 120
<210> 171
<211> 11
<212> PRT
<213> Mus musculus
<400> 171
Leu Ala Ser Glu Asp Ile His Ser Asp Leu Ala
1 5 10
<210> 172
<211> 7
<212> PRT
<213> Mus musculus
<400> 172
Asn Ala Asn Ser Leu Gln Asn
1 5
<210> 173
<211> 9
<212> PRT
<213> Mus musculus
<400> 173
Gln Gln Tyr Thr Asn Tyr Pro Asn Thr
1 5
<210> 174
<211> 5
<212> PRT
<213> Mus musculus
<400> 174
Asn His Tyr Trp Gly
1 5
<210> 175
<211> 16
<212> PRT
<213> Mus musculus
<400> 175
His Ile Ser Asn Ser Gly Gly Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 176
<211> 13
<212> PRT
<213> Mus musculus
37
<400> 176
Gly Ser Tyr Tyr Tyr Ser Ala Ser Gly Tyr Phe Asp Tyr
1 5 10
<210> 177
<211> 321
<212> ДНК
<213> Mus musculus
<400> 177
gatatccgga tgacacagtc tccagcttcc ctgtctgcat ctctgggaga aactgtcaac 60
atcggatgtc tagcaagtga ggacatttac agtgatttag catggtatca gcagaagcca 120
gggaagtctc ctcagctcct gatctataat gcaaataact tgcaaaatgg ggtcccttca 180
cggtttagtg gcagtggatc tggcacacaa tattctctaa aaataaacag cctgcaatct 240
gaagatgtcg cgacttattt ctgtcaacaa tataacagtt atccgaacac gtttggagct 300
gggaccaagc tggaaataaa a 321
<210> 178
<211> 363
<212> ДНК
<213> Mus musculus
<400> 178
gaggtgcagc ttcaggagtc aggacctggc cttgtgaaac cctcacagtc actctccctc 60
atttgttctg tcactggtta ctccatcact acaacttact ggggctggat ccggaagttc 120
ccaggaaata aaatggagtg gattggacac ataagtaaca gtggtagtac taattacaac 180
ccatctctca aaagtcgaat ctccgttact agagacacat cgacgaatca gttcttcctg 240
cagttgaact ctgtaactac tgaggacaca gccacatatt actgtgcaag aggatcttat 300
tactatagcg cgtcgggcta ctttgattac tggggccacg gagtcatggt cacagtctcc 360
tca 363
<210> 179
<211> 33
<212> ДНК
<213> Mus musculus
<400> 179
ctagcaagtg aggacattta cagtgattta gca 33
<210> 180
<211> 21
<212> ДНК
<213> Mus musculus
<400> 180
aatgcaaata acttgcaaaa t 21
<210> 181
<211> 27
<212> ДНК
<213> Mus musculus
<400> 181
caacaatata acagttatcc gaacacg 27
38
<210> 182
<211> 15
<212> ДНК
<213> Mus musculus
<400> 182
acaacttact ggggc 15
<210> 183
<211> 48
<212> ДНК
<213> Mus musculus
<400> 183
cacataagta acagtggtag tactaattac aacccatctc tcaaaagt 48
<210> 184
<211> 39
<212> ДНК
<213> Mus musculus
<400> 184
ggatcttatt actatagcgc gtcgggctac tttgattac 39
<210> 185
<211> 107
<212> PRT
<213> Mus musculus
<400> 185
Asp Ile Arg Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Glu Thr Val Asn Ile Gly Cys Leu Ala Ser Glu Asp Ile Tyr Ser Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Asn Ala Asn Asn Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser
65 70 75 80
Glu Asp Val Ala Thr Tyr Phe Cys Gln Gln Tyr Asn Ser Tyr Pro Asn
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 186
<211> 121
<212> PRT
<213> Mus musculus
<400> 186
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
39
Ser Leu Ser Leu Ile Cys Ser Val Thr Gly Tyr Ser Ile Thr Thr Thr
20 25 30
Tyr Trp Gly Trp Ile Arg Lys Phe Pro Gly Asn Lys Met Glu Trp Ile
35 40 45
Gly His Ile Ser Asn Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Val Thr Arg Asp Thr Ser Thr Asn Gln Phe Phe Leu
65 70 75 80
Gln Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Gly Ser Tyr Tyr Tyr Ser Ala Ser Gly Tyr Phe Asp Tyr Trp Gly
100 105 110
His Gly Val Met Val Thr Val Ser Ser
115 120
<210> 187
<211> 11
<212> PRT
<213> Mus musculus
<400> 187
Leu Ala Ser Glu Asp Ile Tyr Ser Asp Leu Ala
1 5 10
<210> 188
<211> 7
<212> PRT
<213> Mus musculus
<400> 188
Asn Ala Asn Asn Leu Gln Asn
1 5
<210> 189
<211> 9
<212> PRT
<213> Mus musculus
<400> 189
Gln Gln Tyr Asn Ser Tyr Pro Asn Thr
1 5
<210> 190
<211> 5
<212> PRT
<213> Mus musculus
<400> 190
Thr Thr Tyr Trp Gly
1 5
40
<210> 191
<211> 16
<212> PRT
<213> Mus musculus
<400> 191
His Ile Ser Asn Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 192
<211> 13
<212> PRT
<213> Mus musculus
<400> 192
Gly Ser Tyr Tyr Tyr Ser Ala Ser Gly Tyr Phe Asp Tyr
1 5 10
<210> 193
<211> 108
<212> PRT
<213> Mus musculus
<400> 193
Asp Ile Val Met Thr Gln Ser His Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Leu Thr Ser Tyr Arg Asn Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Lys Thr Pro Tyr
85 90 95
Ser Phe Gly Gly Gly Thr Lys Leu Glu Arg Leu Arg
100 105
<210> 194
<211> 115
<212> PRT
<213> Mus musculus
<400> 194
Gln Val Gln Leu Glu Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Gly Tyr
20 25 30
41
Gly Ile Tyr Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Arg Tyr Tyr Cys Ala
85 90 95
Arg Asp Tyr Tyr Gly Ser Lys Asp Tyr Trp Gly Gln Gly Thr Thr Leu
100 105 110
Thr Val Ser
115
<210> 195
<211> 111
<212> PRT
<213> Mus musculus
<400> 195
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Gly Asp Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 196
<211> 123
<212> PRT
<213> Mus musculus
<400> 196
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Ile Leu Lys Pro Ser Gln
1 5 10 15
42
Thr Leu Ser Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Met Gly Val Gly Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Ala His Ile Trp Trp Asp Asp Asp Lys Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Gln Leu Thr Ile Ser Lys Asp Thr Ser Arg Asn Gln Val
65 70 75 80
Phe Leu Lys Ile Thr Ser Val Asp Ala Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Lys Arg Ser Ser Val Val Ala His Tyr Tyr Ala Met Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser
115 120
<210> 197
<211> 113
<212> PRT
<213> Искусственное
<220>
<223> гуманизированное антитело
<400> 197
Gln Phe Gln Leu Thr Gln Pro Ser Ser Val Ser Ala Ser Val Gly Asp
1 5 10 15
Arg Val Thr Ile Thr Cys Glu Arg Ser Ser Gly Asp Ile Gly Asp Ser
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Asn Val
35 40 45
Ile Tyr Ala Asp Asp Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Gly Ser Gly Asn Ser Ala Ser Leu Thr Ile Ser Ser
65 70 75 80
Leu Gln Ala Glu Asp Ala Ala Asp Tyr Phe Cys Gln Ser Tyr Asp Ser
85 90 95
Asn Ile Asp Phe Asn Pro Val Phe Gly Gly Gly Thr Lys Leu Glu Val
100 105 110
Lys
<210> 198
<211> 120
43
<212> PRT
<213> Искусственное
<220>
<223> гуманизированное антитело
<400> 198
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Lys Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Asn Tyr Asp Gly Ser Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Leu Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Pro Phe Asn Asn Phe Gly Ile Trp Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser
115 120
<210> 199
<211> 114
<212> PRT
<213> Искусственное
<220>
<223> гуманизированное антитело
<400> 199
Asp Val Val Leu Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Glu Ser Arg
20 25 30
Asp Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Leu Tyr Gly Val Ser Asn Arg Leu Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Ala
85 90 95
44
Thr His Gly Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr
<210> 200
<211> 118
<212> PRT
<213> Искусственное
<220>
<223> гуманизированное антитело
<400> 200
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Ile Met Trp Arg Asp Gly Asp Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Phe Cys Ala
85 90 95
Arg Gly Gly Thr Leu Thr Thr Pro Phe Thr Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 201
<211> 114
<212> PRT
<213> Искусственное
<220>
<223> гуманизированное антитело
<400> 201
Asp Val Val Leu Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Glu Ser Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
45
Pro Gln Leu Leu Ile Tyr Gly Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Ala
85 90 95
Thr Arg Asp Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr
<210> 202
<211> 118
<212> PRT
<213> Искусственное
<220>
<223> гуманизированное антитело
<400> 202
Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu Val Lys Pro Thr Glu
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
His Leu His Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Met
35 40 45
Gly Leu Met Trp Arg Asp Gly Asp Thr Ser Tyr Asn Ser Arg Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Val Leu
65 70 75 80
Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Gly Met Thr Leu Ala Thr Pro Phe Leu Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 203
<211> 625
<212> PRT
<213> Homo sapiens
<400> 203
Met Ile Phe Leu Tyr Gln Val Val His Phe Ile Leu Phe Thr Ser Val
46
1 5 10 15
Ser Gly Glu Cys Val Thr Gln Leu Leu Lys Asp Thr Cys Phe Glu Gly
20 25 30
Gly Asp Ile Thr Thr Val Phe Thr Pro Ser Ala Lys Tyr Cys Gln Val
35 40 45
Val Cys Thr Tyr His Pro Arg Cys Leu Leu Phe Thr Phe Thr Ala Glu
50 55 60
Ser Pro Ser Glu Asp Pro Thr Arg Trp Phe Thr Cys Val Leu Lys Asp
65 70 75 80
Ser Val Thr Glu Thr Leu Pro Arg Val Asn Arg Thr Ala Ala Ile Ser
85 90 95
Gly Tyr Ser Phe Lys Gln Cys Ser His Gln Ile Ser Ala Cys Asn Lys
100 105 110
Asp Ile Tyr Val Asp Leu Asp Met Lys Gly Ile Asn Tyr Asn Ser Ser
115 120 125
Val Ala Lys Ser Ala Gln Glu Cys Gln Glu Arg Cys Thr Asp Asp Val
130 135 140
His Cys His Phe Phe Thr Tyr Ala Thr Arg Gln Phe Pro Ser Leu Glu
145 150 155 160
His Arg Asn Ile Cys Leu Leu Lys His Thr Gln Thr Gly Thr Pro Thr
165 170 175
Arg Ile Thr Lys Leu Asp Lys Val Val Ser Gly Phe Ser Leu Lys Ser
180 185 190
Cys Ala Leu Ser Asn Leu Ala Cys Ile Arg Asp Ile Phe Pro Asn Thr
195 200 205
Val Phe Ala Asp Ser Asn Ile Asp Ser Val Met Ala Pro Asp Ala Phe
210 215 220
Val Cys Gly Arg Ile Cys Thr His His Pro Gly Cys Leu Phe Phe Thr
225 230 235 240
Phe Phe Ser Gln Glu Trp Pro Lys Glu Ser Gln Arg Asn Leu Cys Leu
245 250 255
Leu Lys Thr Ser Glu Ser Gly Leu Pro Ser Thr Arg Ile Lys Lys Ser
260 265 270
Lys Ala Leu Ser Gly Phe Ser Leu Gln Ser Cys Arg His Ser Ile Pro
275 280 285
Val Phe Cys His Ser Ser Phe Tyr His Asp Thr Asp Phe Leu Gly Glu
47
290 295 300
Glu Leu Asp Ile Val Ala Ala Lys Ser His Glu Ala Cys Gln Lys Leu
305 310 315 320
Cys Thr Asn Ala Val Arg Cys Gln Phe Phe Thr Tyr Thr Pro Ala Gln
325 330 335
Ala Ser Cys Asn Glu Gly Lys Gly Lys Cys Tyr Leu Lys Leu Ser Ser
340 345 350
Asn Gly Ser Pro Thr Lys Ile Leu His Gly Arg Gly Gly Ile Ser Gly
355 360 365
Tyr Thr Leu Arg Leu Cys Lys Met Asp Asn Glu Cys Thr Thr Lys Ile
370 375 380
Lys Pro Arg Ile Val Gly Gly Thr Ala Ser Val Arg Gly Glu Trp Pro
385 390 395 400
Trp Gln Val Thr Leu His Thr Thr Ser Pro Thr Gln Arg His Leu Cys
405 410 415
Gly Gly Ser Ile Ile Gly Asn Gln Trp Ile Leu Thr Ala Ala His Cys
420 425 430
Phe Tyr Gly Val Glu Ser Pro Lys Ile Leu Arg Val Tyr Ser Gly Ile
435 440 445
Leu Asn Gln Ser Glu Ile Lys Glu Asp Thr Ser Phe Phe Gly Val Gln
450 455 460
Glu Ile Ile Ile His Asp Gln Tyr Lys Met Ala Glu Ser Gly Tyr Asp
465 470 475 480
Ile Ala Leu Leu Lys Leu Glu Thr Thr Val Asn Tyr Thr Asp Ser Gln
485 490 495
Arg Pro Ile Cys Leu Pro Ser Lys Gly Asp Arg Asn Val Ile Tyr Thr
500 505 510
Asp Cys Trp Val Thr Gly Trp Gly Tyr Arg Lys Leu Arg Asp Lys Ile
515 520 525
Gln Asn Thr Leu Gln Lys Ala Lys Ile Pro Leu Val Thr Asn Glu Glu
530 535 540
Cys Gln Lys Arg Tyr Arg Gly His Lys Ile Thr His Lys Met Ile Cys
545 550 555 560
Ala Gly Tyr Arg Glu Gly Gly Lys Asp Ala Cys Lys Gly Asp Ser Gly
565 570 575
Gly Pro Leu Ser Cys Lys His Asn Glu Val Trp His Leu Val Gly Ile
48
580 585 590
Thr Ser Trp Gly Glu Gly Cys Ala Gln Arg Glu Arg Pro Gly Val Tyr
595 600 605
Thr Asn Val Val Glu Tyr Val Asp Trp Ile Leu Glu Lys Thr Gln Ala
610 615 620
Val
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2020 |
|
RU2818588C2 |
| МОНОКЛОНАЛЬНЫЕ АГЕНТЫ, СВЯЗЫВАЮЩИЕ сМЕТ, ИХ КОНЪЮГАТЫ С ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2744914C2 |
| ЧАСТИЦЫ, КОНЪЮГИРОВАННЫЕ С ПЕПТИДОМ | 2014 |
|
RU2813163C2 |
| НАЦЕЛЕННЫЕ НА uPARAP КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2740311C2 |
| ЛЕКАРСТВЕННЫЕ КОНЪЮГАТЫ ИЗ МОНОКЛОНАЛЬНЫХ АГЕНТОВ, СВЯЗЫВАЮЩИХ cMET, И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2813828C2 |
| Антитело против PCSK9 и его применение | 2016 |
|
RU2756012C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К ИНТЕРЛЕЙКИНУ-31 ДЛЯ ВЕТЕРИНАРНОГО ПРИМЕНЕНИЯ | 2019 |
|
RU2795411C2 |
| АНТИТЕЛО К АЛЬФА-РЕЦЕПТОРУ ИНТЕРЛЕЙКИНА-4 ЧЕЛОВЕКА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2807060C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2019 |
|
RU2781542C2 |
| ТЕРАПЕВТИЧЕСКАЯ ПРОТИВОРАКОВАЯ НЕОЭПИТОПНАЯ ВАКЦИНА | 2017 |
|
RU2782422C2 |
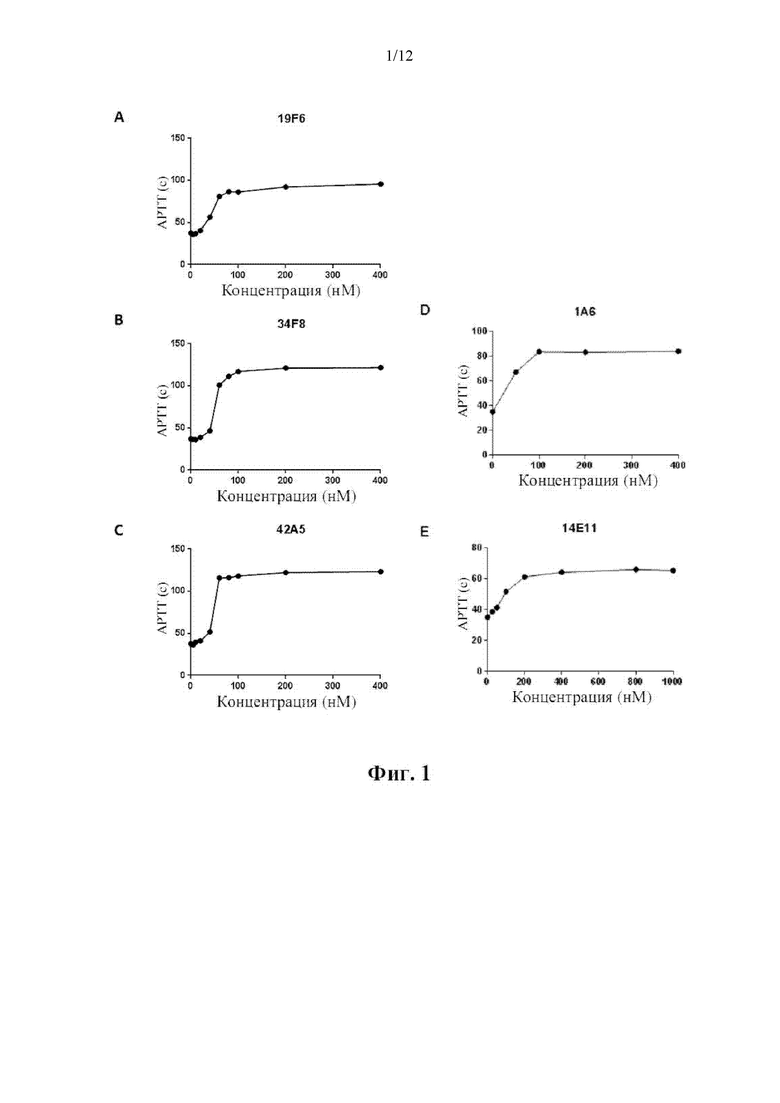
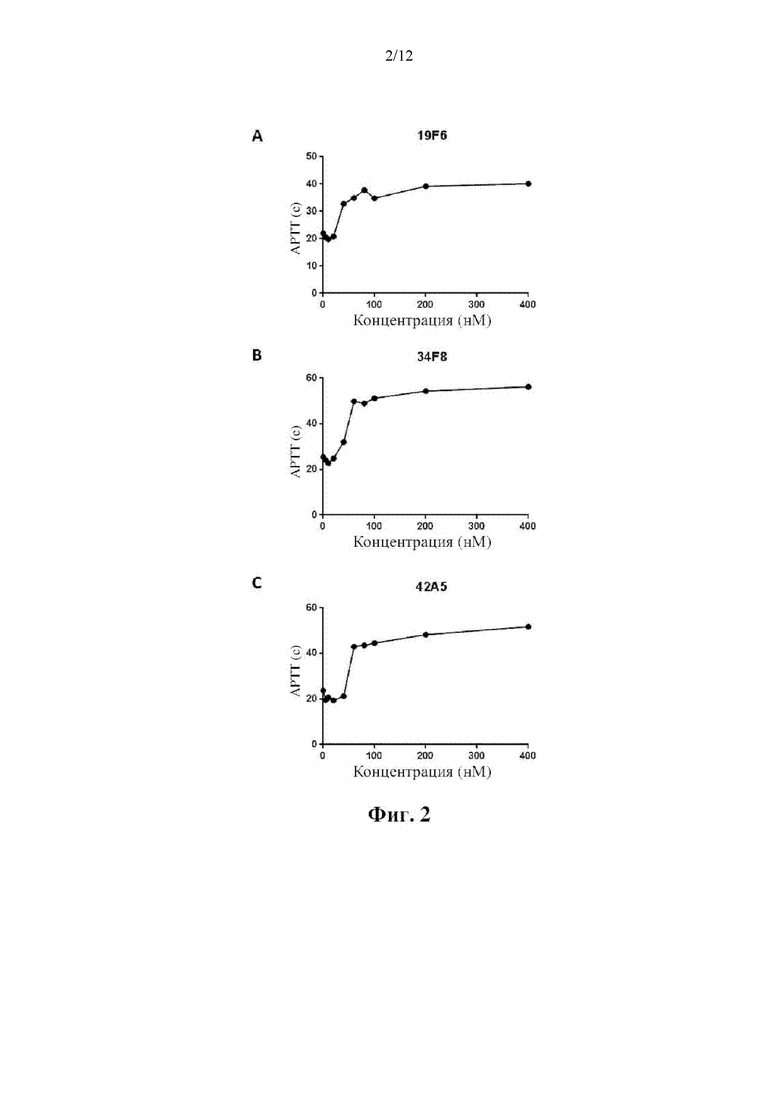
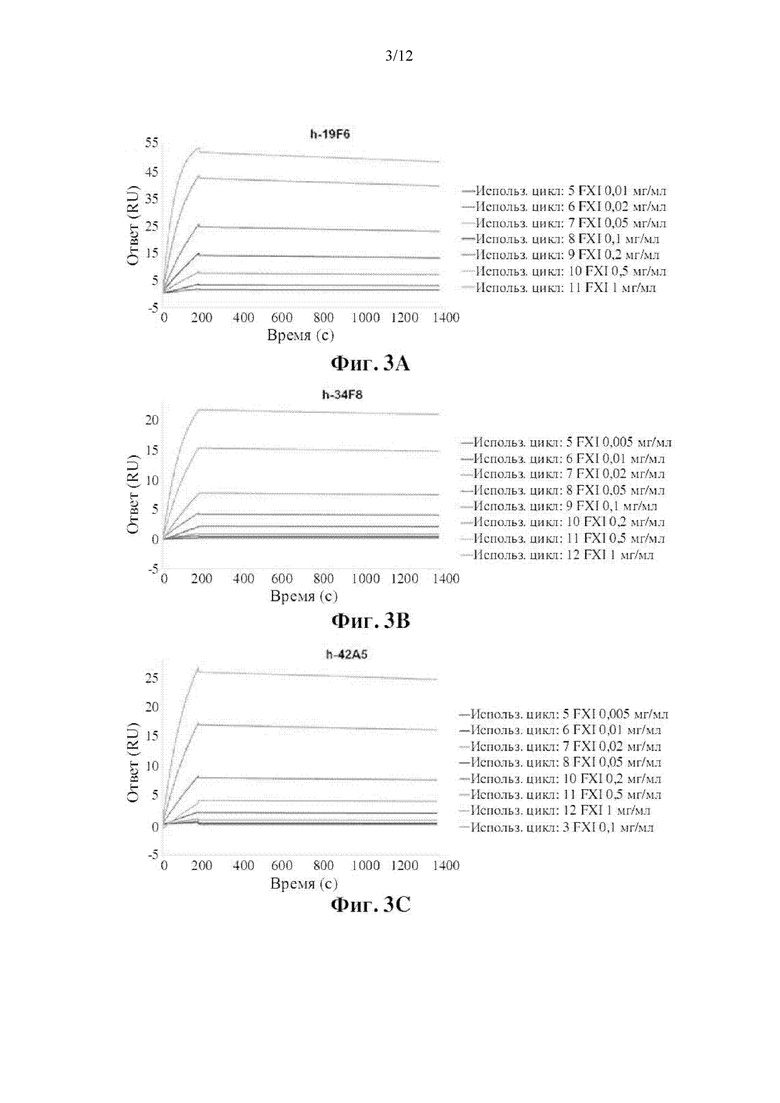
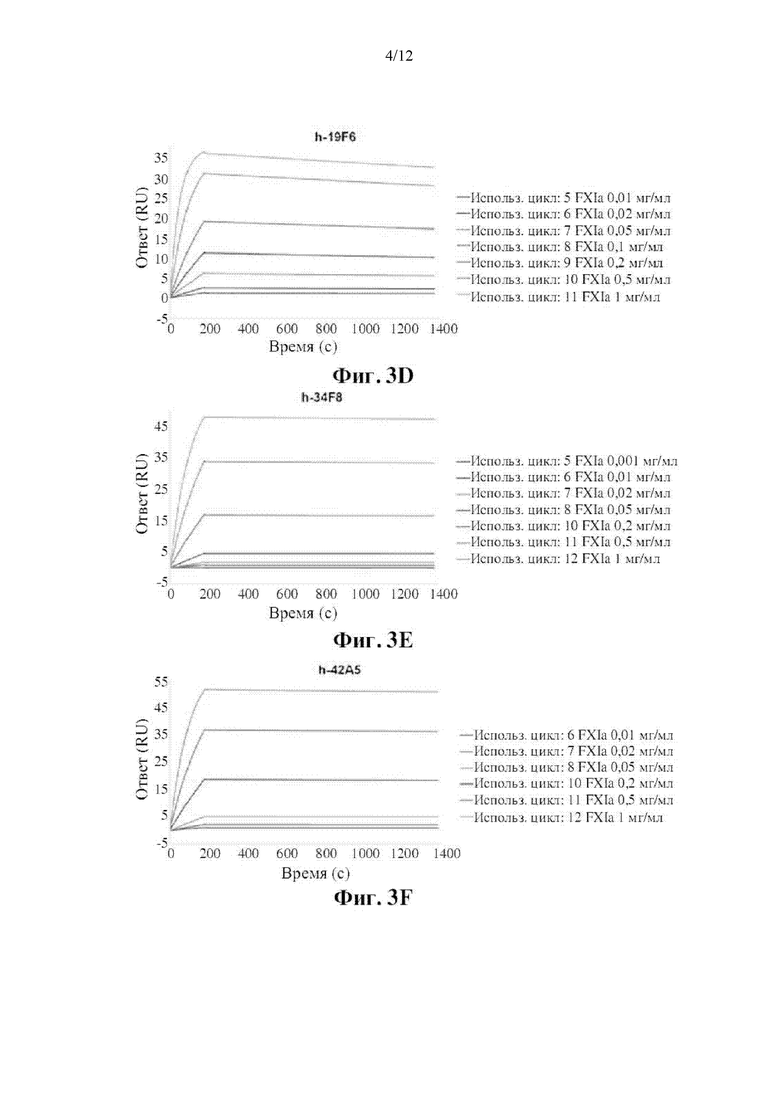
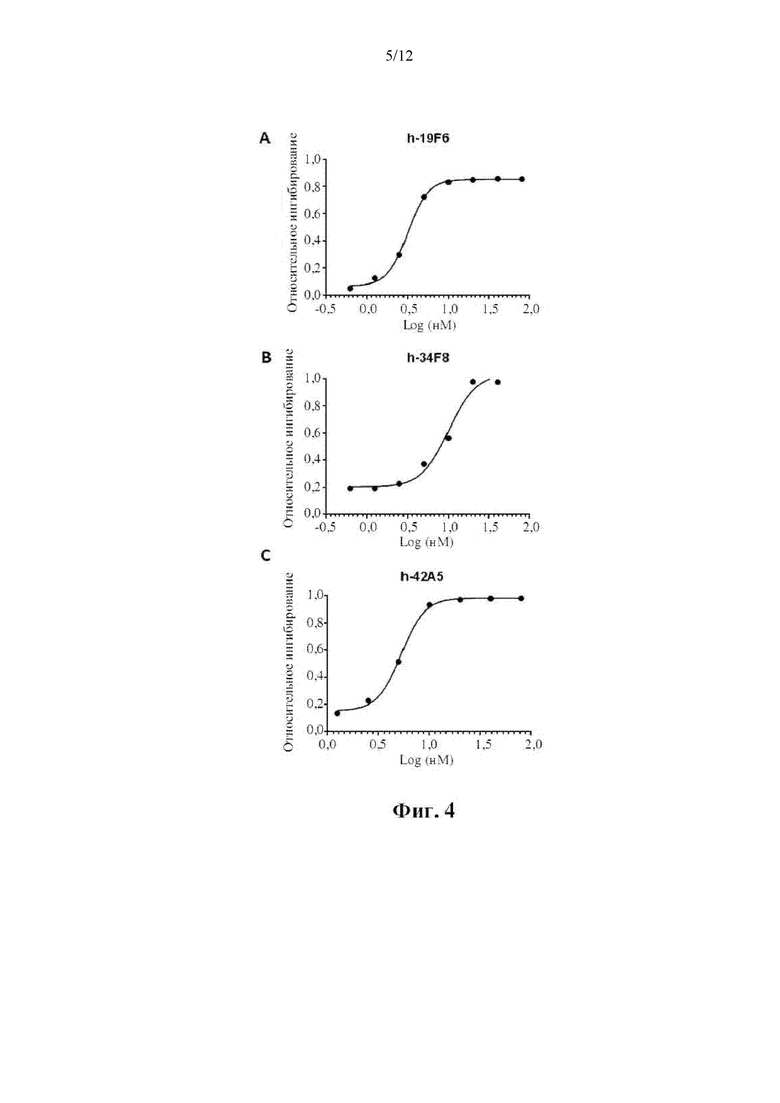
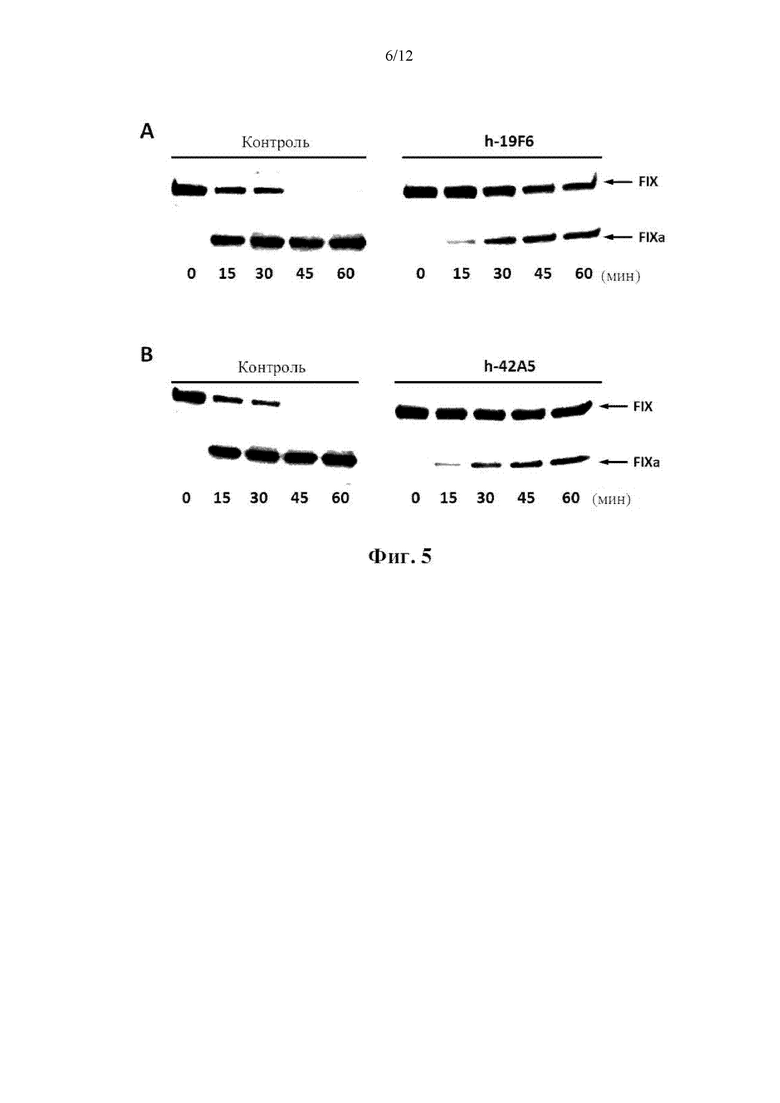
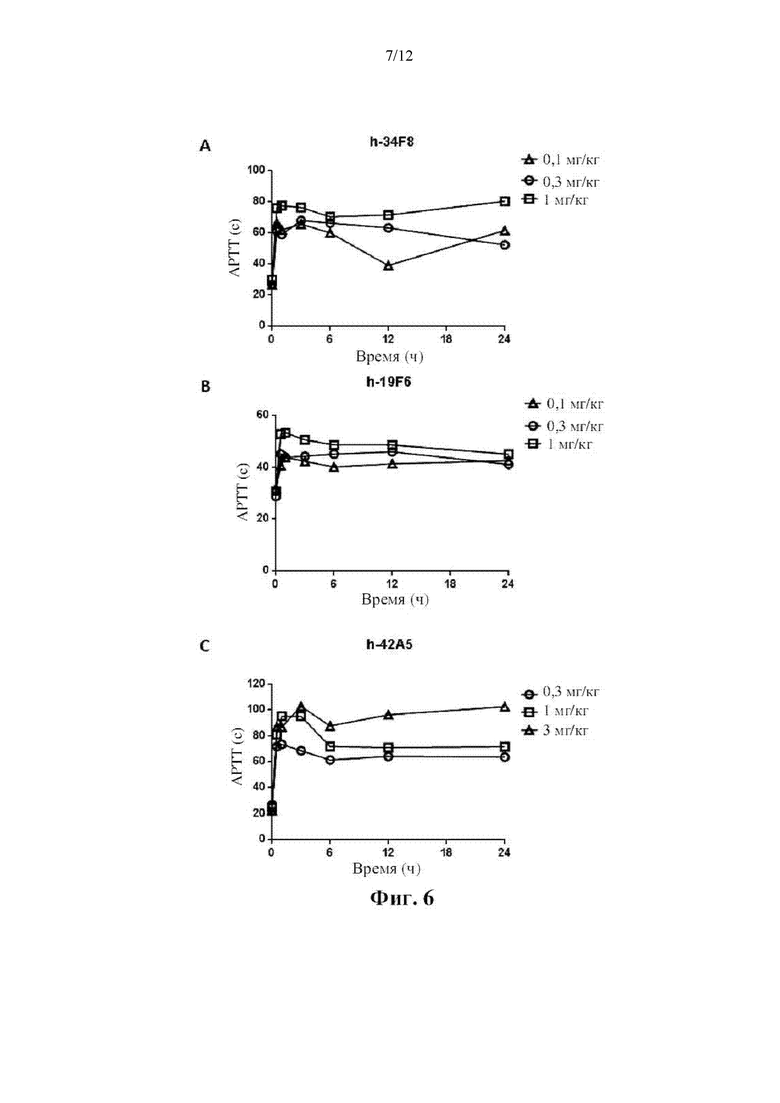
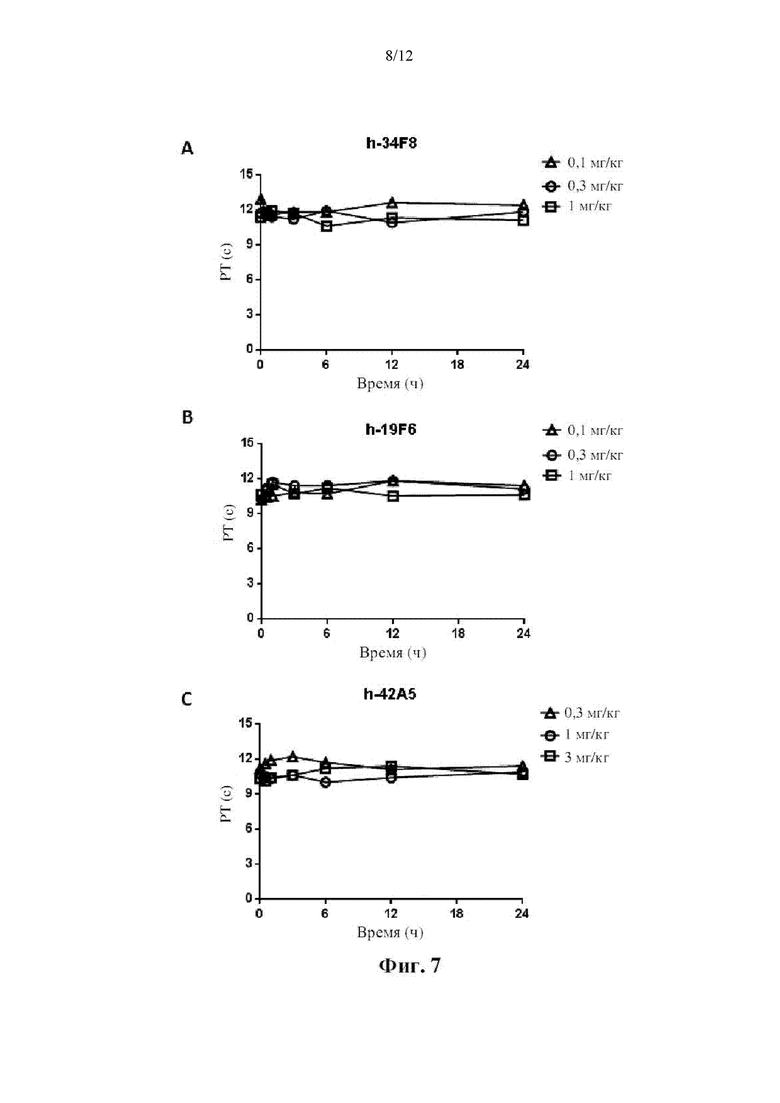
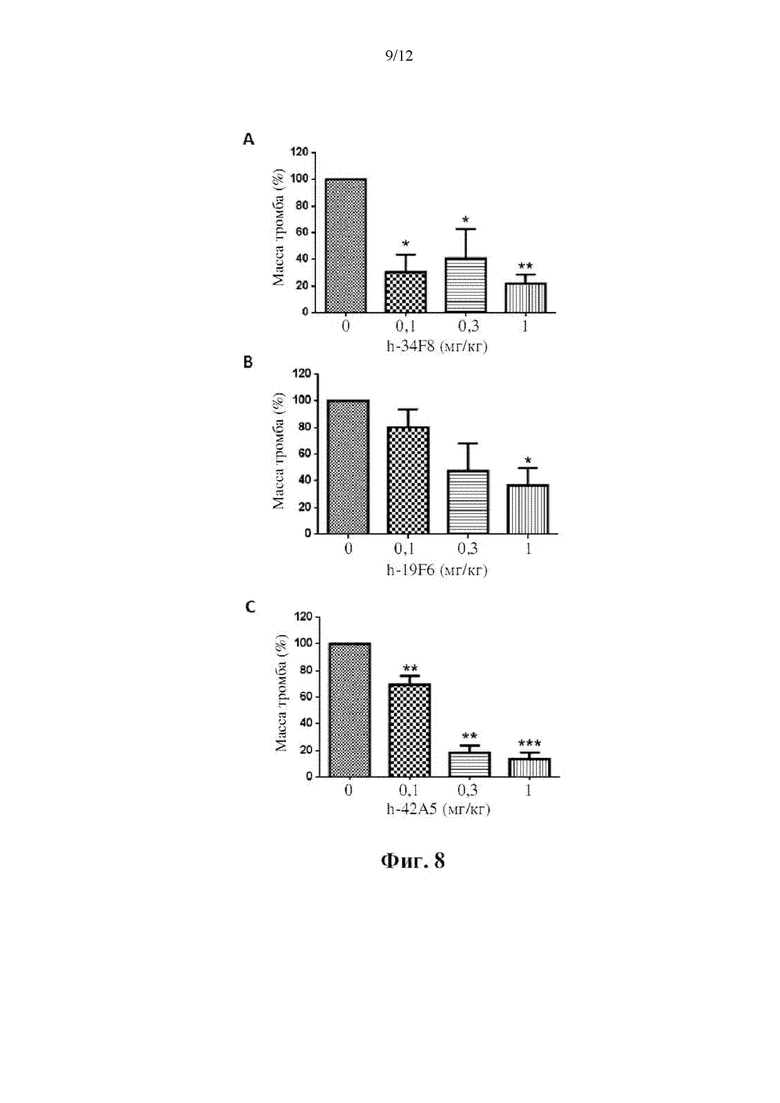
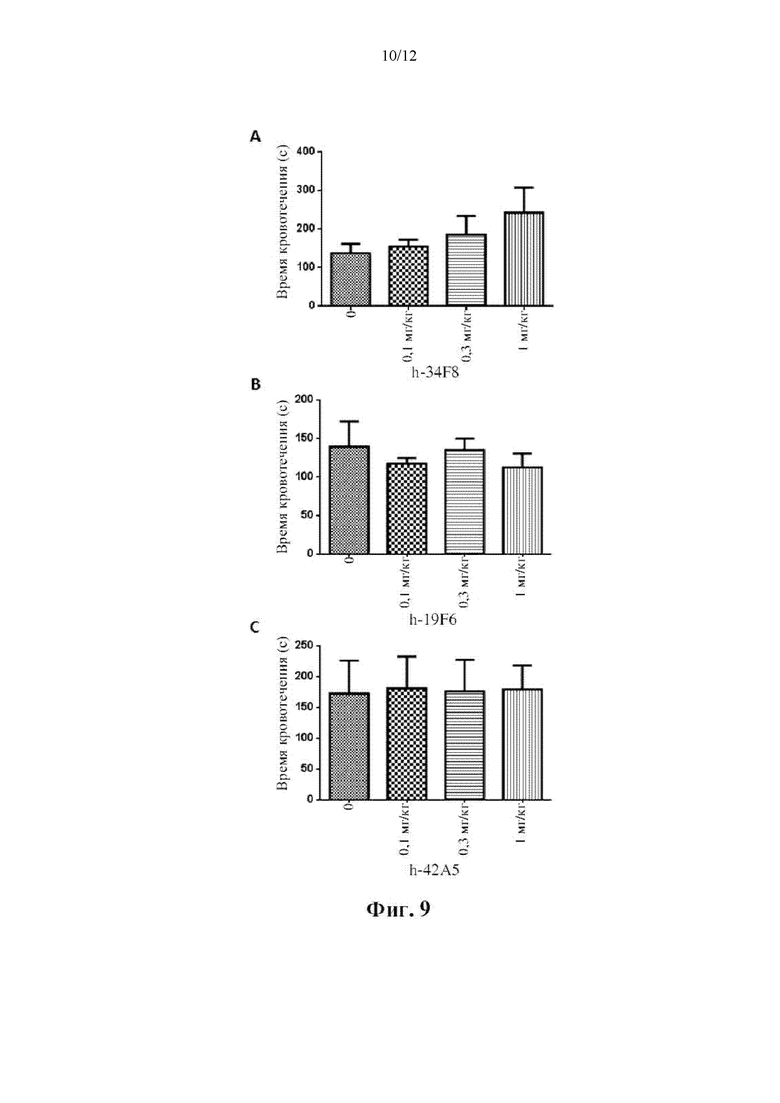
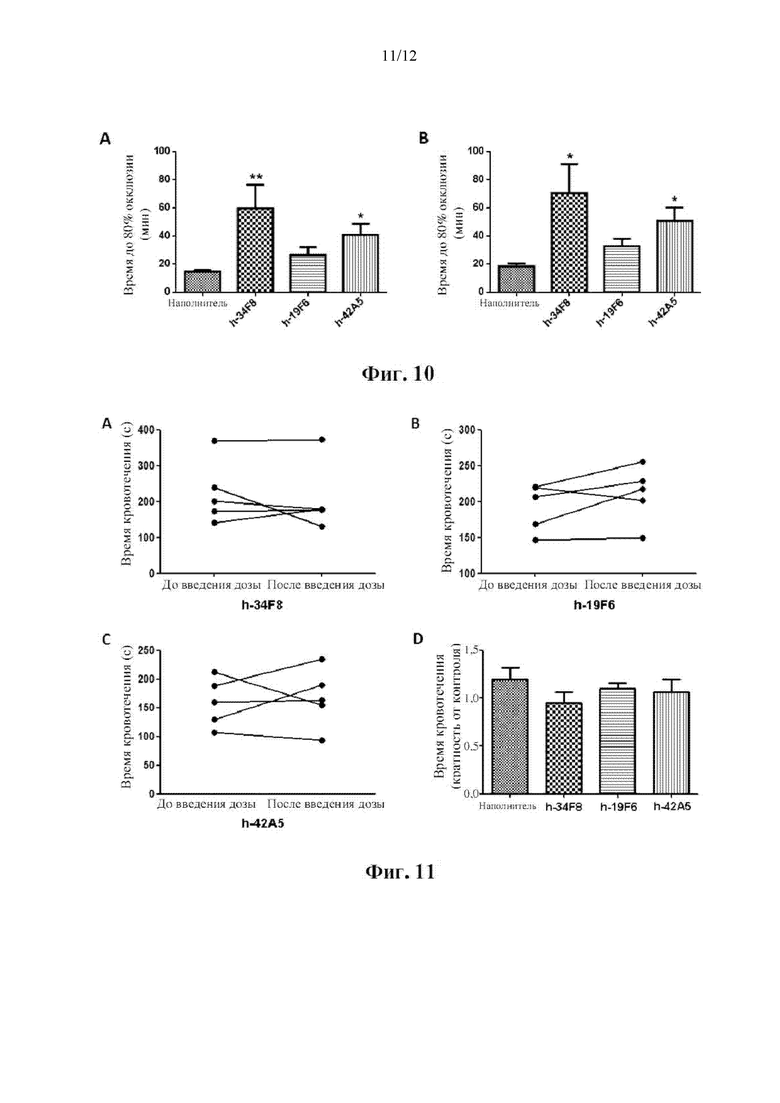
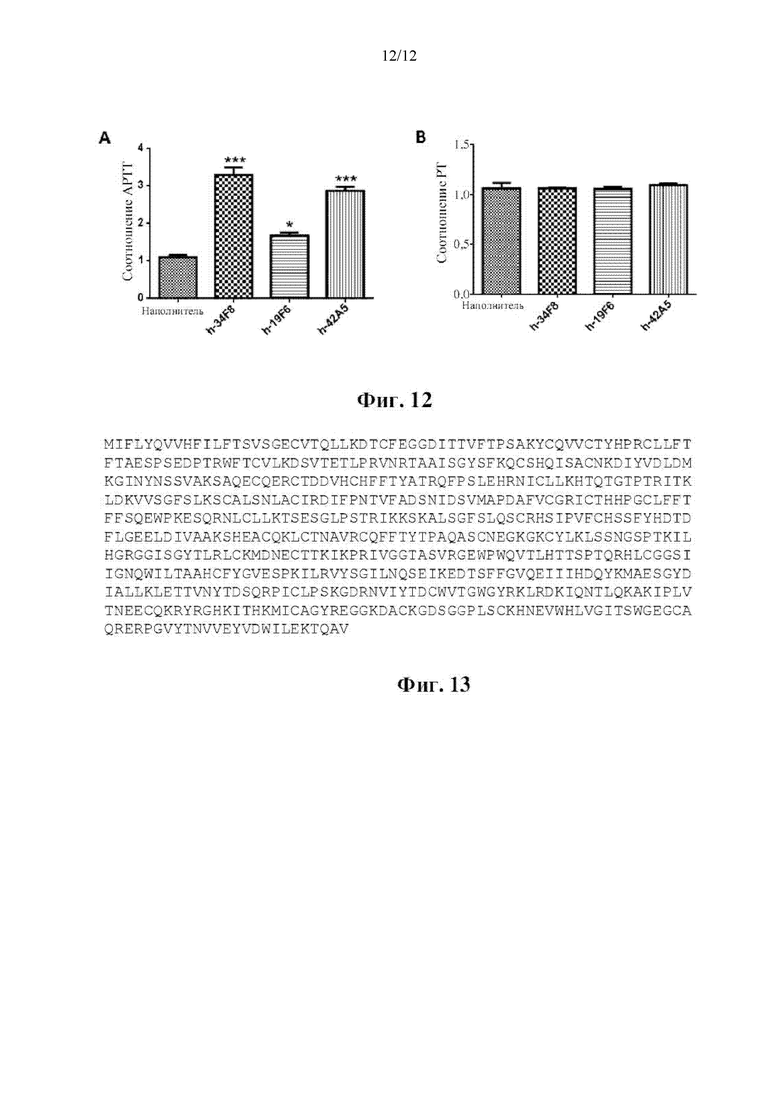
Изобретение относится к области биохимии, в частности к выделенному антителу к фактору коагуляции, которое специфически связывается с человеческим FXI. Также раскрыта фармацевтическая композиция для ингибирования образования тромбов, с помощью указанного антитела. Раскрыты применения указанного антитела для ингибирования образования тромбов у субъекта, в изготовлении лекарственного средства для лечения или ингибирования возникновения сепсиса; способ ингибирования образования тромбов у субъекта; способ лечения или ингибирования возникновения тромбоза или осложнения, или состояния, способ лечения или ингибирования возникновения сепсиса; способ получения указанного антитела. Изобретение позволяет эффективно лечить состояния, связанные с коагуляцией. 12 н. и 6 з.п. ф-лы, 13 ил., 3 табл., 11 пр.
1. Выделенное антитело к фактору коагуляции, которое специфически связывается с человеческим FXI или его активированной формой FXIa, содержащее комбинацию CDR, выбранную из группы, состоящей из комбинаций a)-l), или его антигенсвязывающий домен:
комбинацию a) CDR последовательностей SEQ ID NO: 11-16;
комбинацию b) CDR последовательностей SEQ ID NO: 27-32;
комбинацию c) CDR последовательностей SEQ ID NO: 43-48;
комбинацию d) CDR последовательностей SEQ ID NO: 59-64;
комбинацию e) CDR последовательностей SEQ ID NO: 75-80;
комбинацию f) CDR последовательностей SEQ ID NO: 91-96;
комбинацию g) CDR последовательностей SEQ ID NO: 107-112;
комбинацию h) CDR последовательностей SEQ ID NO: 123-128;
комбинацию i) CDR последовательностей SEQ ID NO: 139-144;
комбинацию j) CDR последовательностей SEQ ID NO: 155-160;
комбинацию k) CDR последовательностей SEQ ID NO: 171-176; и
комбинацию l) CDR последовательностей SEQ ID NO: 187-192.
2. Антитело по п. 1, причем антитело специфически связывается с доменом A3 FXI или FXIa человека.
3. Антитело по п. 1, причем антитело содержит пару последовательностей, выбранную из группы, состоящей из SEQ ID NO: 9-10, SEQ ID NO: 25-26, SEQ ID NO 41-42, SEQ ID NO: 57-58, SEQ ID NO: 73-74, SEQ ID NO: 89-90, SEQ ID NO: 105-106, SEQ ID NO: 121-122, SEQ ID NO: 137-138, SEQ ID NO: 153-154, SEQ ID NO: 169-170, SEQ ID NO: 185-186, SEQ ID NO; 197-198, SEQ ID NO: 199-200, SEQ ID NO: 201-202, SEQ ID NO: 204-205, SEQ ID NO: 206-207 и SEQ ID NO: 208-209, и последовательностей, имеющих по меньшей мере 90% идентичность с ними.
4. Фармацевтическая композиция для ингибирования образования тромбов, содержащая терапевтически эффективное количество антитела по любому из пп. 1-3.
5. Применение антитела по любому из пп. 1-3 в изготовлении лекарственного средства для ингибирования образования тромбов у субъекта.
6. Применение антитела по любому из пп. 1-3 в изготовлении лекарственного средства для лечения или ингибирования возникновения сепсиса.
7. Способ ингибирования образования тромбов у субъекта, включающий введение субъекту терапевтически эффективного количества антитела по любому из пп. 1-3.
8. Способ ингибирования образования тромбов у субъекта, включающий введение субъекту терапевтически эффективного количества фармацевтической композиции по п. 4.
9. Способ лечения или ингибирования возникновения тромбоза или осложнения или состояния, связанного с тромбозом, включающий введение субъекту терапевтически эффективного количества антитела по любому из пп. 1-3, причем указанное введение не нарушает гемостаз субъекта.
10. Способ лечения или ингибирования возникновения тромбоза или осложнения или состояния, связанного с тромбозом, включающий введение субъекту терапевтически эффективного количества фармацевтической композиции по п. 4, причем указанное введение не нарушает гемостаз субъекта.
11. Способ лечения или ингибирования возникновения сепсиса, включающий введение субъекту терапевтически эффективного количества антитела по любому из пп. 1-3, причем указанное введение не нарушает гемостаз субъекта.
12. Способ лечения или ингибирования возникновения сепсиса, включающий введение субъекту терапевтически эффективного количества фармацевтической композиции по п. 4, причем указанное введение не нарушает гемостаз субъекта.
13. Способ получения антитела по любому из пп. 1-3, включающий экспрессию нуклеиновой кислоты, кодирующей антитело по любому из пп. 1-3, клонированной в векторе экспрессии в клетке-хозяине.
14. Способ по п. 13, дополнительно включающий очистку экспрессированного антитела из клетки-хозяина.
15. Способ по п. 13, в котором вектор экспрессии представляет собой вектор pTT5 или вектор pcDNA3.
16. Способ по п. 13, в котором клетка-хозяин представляет собой клетку CHO или клетку HEK193T.
17. Антитело к фактору коагуляции, которое специфически связывается с человеческим FXI или его активированной формой FXIa, или его антигенсвязывающий фрагмент, полученные способом по любому из пп. 13-16, или его антигенсвязывающий домен.
18. Антитело по п. 17, причем антитело является посттрансляционно модифицированным.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПОЛИПЕПТИДЫ ФАКТОРА VII И ПОЛИПЕПТИДЫ ФАКТОРА XI | 2002 |
|
RU2298416C2 |
| ПРОИЗВОДНОЕ ТРОМБИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЕГО | 2005 |
|
RU2372402C2 |
| WO 2016207858 A1, 29.12.2016 | |||
| WO 2009067660 A2, 28.05.2009; | |||
| AU 2016203944 A1, 07.07.2016. | |||
Авторы
Даты
2023-07-26—Публикация
2017-12-29—Подача