Область техники
[0001] Область изобретения в целом относится к способам получения, очистки и составления конъюгатов антитело-лекарственное средство (ADC - англ.: antibody drug conjugate) с использованием процессов непрерывной конъюгации, однопроходной фильтрации в тангенциальном потоке, противоточной диафильтрации и/или технологий автоматизации поточных процессов.
Уровень техники
[0002] Узким местом в производственном процессе, связанным с конъюгацией конъюгата антитело-лекарственное средство (ADC), является удаление примесей и перенос ADC в стабильный буфер. В настоящее время это достигается с помощью колоночной хроматографии связывания и элюирования или объемной диафильтрации (обычной) путем фильтрации в тангенциальном потоке (TFF - англ.: tangential flow filtration). Объемная диафильтрация включает заполнение системы TFF буфером A (то есть буфером, в котором изначально находится конъюгат). Затем ADC (в буфере А) добавляют в сосуд для ретентата, где он смешивается с объемом первичного заполнения. Подающий насос для сосуда с ретентатом перекачивает конъюгат из ретентата через мембрану TFF, где он либо задерживается (и возвращается в ретентат), либо отбрасывается в отходы. Другой насос (насос для диафильтрации) будет подавать из сосуда в буфер B, содержащийся в отдельном сосуде (то есть в буфер, в который будет перенесен ADC), по линии подачи из сосуда в сосуд для ретентата. Запускают оба насоса, и конъюгат в сосуде для ретентата начинает проходить через мембрану TFF. Поскольку буфер удаляется через поток отходов, объем в ретентате поддерживают путем добавления буфера B (в равном объеме) в сосуд для ретентата. В результате конъюгат медленно переносится в буфер В. Этот способ очистки является дорогостоящим и не оптимальным для крупномасштабного производства из-за необходимости рециркулировать ADC через мембраны TFF в течение нескольких циклов. Рециркуляция приводит к большим объемам и времени обработки, а также к увеличению воздействия ADC на зоны с потенциально высоким сдвигом. Производство ADC с использованием объемной обработки занимает около 4-5 дней для производства серии очищенного составленного конъюгата, часто с низким выходом. Соответственно, необходимы улучшенные процессы конъюгации ADC.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0003] Системы однопроходной фильтрации в тангенциальном потоке (SPTFF), такие как доступные от компании Pall Life Sciences, используют на платформах биообработки, часто в качестве способа уменьшения объема или концентрации биомолекул, таких как антитела. Однако авторы настоящего изобретения неожиданно обнаружили, что SPTFF можно связать с реакциями конъюгации лекарственного средства с антителом для обеспечения не только концентрации конъюгатов антитело-лекарственное средство (ADC), но также для удаления неконъюгированных продуктов из реакции конъюгации и переноса очищенного ADC в буфер для состава, что позволяет использовать способ полностью непрерывного производства и обработки ADC. Авторы настоящего изобретения также обнаружили, что противоточная диафильтрация также может быть использована в реакциях конъюгации антитела с лекарственным средством для аналогичных целей.
[0004] В некоторых вариантах осуществления непрерывный способ получения композиции конъюгата антитело-лекарственное средство (ADC) включает (i) конъюгирование антитела или его антигенсвязывающего фрагмента с лекарственным средством для образования ADC, (ii) удаление неконъюгированного лекарственного средства и (iii) перенос ADC в стабильный буфер, причем (i)-(iii) выполняют непрерывно, и причем однопроходную фильтрацию в тангенциальном потоке (SPTFF) используют для удаления неконъюгированного лекарственного средства и/или переноса ADC в стабильный буфер.
[0005] В некоторых вариантах осуществления SPTFF используют для удаления неконъюгированного лекарственного средства для переноса ADC в стабильный буфер. В некоторых вариантах осуществления проточную колоночную хроматографию используют для удаления неконъюгированного лекарственного средства, а SPTFF используют для переноса ADC в стабильный буфер.
[0006] В некоторых вариантах осуществления непрерывный способ получения композиции конъюгата антитело-лекарственное средство (ADC) включает (i) конъюгирование антитела или его антигенсвязывающего фрагмента с лекарственным средством для образования ADC, (ii) удаление неконъюгированного лекарственного средства и (iii) перенос ADC в стабильный буфер, причем (i)-(iii) выполняют непрерывно, и причем противоточную диафильтрацию используют для удаления неконъюгированного лекарственного средства и/или переноса ADC в стабильный буфер.
[0007] В некоторых вариантах осуществления противоточную диафильтрацию используют для удаления неконъюгированного лекарственного средства для переноса ADC в стабильный буфер. В некоторых вариантах осуществления проточную колоночную хроматографию используют для удаления неконъюгированного лекарственного средства, а противоточную диафильтрацию используют для переноса ADC в стабильный буфер.
[0008] В некоторых вариантах осуществления способ дополнительно включает предварительную обработку антитела или его антигенсвязывающего фрагмента. В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят непрерывно путем (i)-(iii). В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят с использованием SPTFF. В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят с использованием противоточной диафильтрации. В некоторых вариантах осуществления только один этап SPTFF или противоточной диафильтрации используют при предварительной обработке. В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят в общем объеме перед этапами (i)-(iii).
[0009] В некоторых вариантах осуществления способ дополнительно включает предварительную обработку лекарственного средства для конъюгации.
[0010] В некоторых вариантах осуществления непрерывный способ получения композиции конъюгата антитело-лекарственное средство (ADC) включает (i) предварительную обработку антитела или его антигенсвязывающего фрагмента, (ii) конъюгирование антитела или его антигенсвязывающего фрагмента с лекарственным средством для образования ADC, (iii) удаление неконъюгированного лекарственного средства и (iv) перенос ADC в стабильный буфер, причем (i)-(iv) выполняют непрерывно, и причем однопроходную фильтрацию в тангенциальном потоке (SPTFF) используют для удаления неконъюгированного лекарственного средства и/или переноса ADC в стабильный буфер.
[0011] В некоторых вариантах осуществления непрерывный способ получения композиции конъюгата антитело-лекарственное средство (ADC) включает (i) предварительную обработку антитела или его антигенсвязывающего фрагмента, (ii) конъюгирование антитела или его антигенсвязывающего фрагмента с лекарственным средством для образования ADC, (iii) удаление неконъюгированного лекарственного средства и (iv) перенос ADC в стабильный буфер, причем (i)-(iv) выполняют непрерывно, и причем противоточную диафильтрацию используют для удаления неконъюгированного лекарственного средства и/или переноса ADC в стабильный буфер.
[0012] В некоторых вариантах осуществления предварительная обработка антитела или его антигенсвязывающего фрагмента включает перенос антитела или его антигенсвязывающего фрагмента в буфер для конъюгации. В некоторых вариантах осуществления предварительная обработка антитела или его антигенсвязывающего фрагмента включает восстановление антитела или его антигенсвязывающего фрагмента и/или окисление антитела или его антигенсвязывающего фрагмента. В некоторых вариантах осуществления восстановление и/или окисление достигают без использования SPTFF или противоточной диафильтрации. В некоторых вариантах осуществления восстановление и/или окисление достигают с использованием только одного этапа SPTFF или противоточной диафильтрации. В некоторых вариантах осуществления восстановление и/или окисление достигают с использованием более чем одного этапа SPTFF или противоточной диафильтрации.
[0013] В некоторых вариантах осуществления способ получения конъюгата антитело-лекарственное средство (ADC) путем процесса непрерывной конъюгации включает добавление одного или более реагентов реакции конъюгации к реакции конъюгации в ходе реакции конъюгации и после образования по меньшей мере одного продукта реакции конъюгации (ADC). В некоторых вариантах осуществления реагент для реакции конъюгации содержит антитело или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления реагент для реакции конъюгации содержит лекарственное средство, присоединенное к линкеру. В некоторых вариантах осуществления реагент для реакции конъюгации содержит линкер. В некоторых вариантах осуществления реагент для реакции конъюгации содержит антитело или его антигенсвязывающий фрагмент, присоединенный к линкеру. В некоторых вариантах осуществления реагент реакции конъюгации содержит лекарственное средство.
[0014] В некоторых вариантах осуществления реакция конъюгации происходит в проточном реакторе.
[0015] В некоторых вариантах осуществления способ дополнительно включает предварительную обработку антитела или его антигенсвязывающего фрагмента. В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят непрерывно при помощи реакции конъюгации. В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят с использованием SPTFF. В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят с использованием противоточной диафильтрации. В некоторых вариантах осуществления только один этап SPTFF или противоточной диафильтрации используют при предварительной обработке. В некоторых вариантах осуществления предварительную обработку антитела или его антигенсвязывающего фрагмента проводят в общем объеме перед реакцией конъюгации. В некоторых вариантах осуществления предварительная обработка антитела или его антигенсвязывающего фрагмента включает перенос антитела или его антигенсвязывающего фрагмента в буфер для конъюгации. В некоторых вариантах осуществления предварительная обработка антитела или его антигенсвязывающего фрагмента включает восстановление антитела или его антигенсвязывающего фрагмента и/или окисление антитела или его антигенсвязывающего фрагмента.
[0016] В некоторых вариантах осуществления ADC концентрируют с использованием однопроходной фильтрации в тангенциальном потоке. В некоторых вариантах осуществления ADC очищают с использованием однопроходной фильтрации в тангенциальном потоке. В некоторых вариантах осуществления ADC переносят в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке.
[0017] В некоторых вариантах осуществления ADC концентрируют с использованием противоточной диафильтрации. В некоторых вариантах осуществления ADC очищают с использованием противоточной диафильтрации. В некоторых вариантах осуществления ADC переносят в буфер для состава с использованием противоточной диафильтрации.
[0018] В некоторых вариантах осуществления ADC концентрируют, очищают и/или переносят в буфер для состава с использованием проточной хроматографии.
[0019] В некоторых вариантах осуществления способ концентрирования конъюгата антитело-лекарственное средство (ADC) включает использование однопроходной фильтрации в тангенциальном потоке. В некоторых вариантах осуществления способ очистки конъюгата антитело-лекарственное средство (ADC) включает использование однопроходной фильтрации в тангенциальном потоке. В некоторых вариантах осуществления способ переноса конъюгата антитело-лекарственное средство (ADC) в буфер для состава включает использование однопроходной фильтрации в тангенциальном потоке. В некоторых вариантах осуществления способ концентрирования конъюгата антитело-лекарственное средство (ADC) включает использование противоточной диафильтрации. В некоторых вариантах осуществления способ очистки конъюгата антитело-лекарственное средство (ADC) включает использование включает использование противоточной диафильтрации. В некоторых вариантах осуществления способ переноса конъюгата антитело-лекарственное средство (ADC) в буфер для состава включает использование противоточной диафильтрации. В некоторых вариантах осуществления ADC получали в процессе серийной конъюгации. В некоторых вариантах осуществления ADC получали в процессе непрерывной конъюгации.
[0020] В некоторых вариантах осуществления в однопроходной фильтрации в тангенциальном потоке используется ультрафильтрационная мембрана. В некоторых вариантах осуществления в однопроходной фильтрации в тангенциальном потоке используется диафильтрационная мембрана.
[0021] В некоторых вариантах осуществления способ улучшает стабильность производства ADC. В некоторых вариантах осуществления способ снижает время производства ADC.
[0022] В некоторых вариантах осуществления однопроходная фильтрация в тангенциальном потоке улучшает последовательность производства ADC. В некоторых вариантах осуществления однопроходная фильтрация в тангенциальном потоке снижает время, требуемое для концентрации, очистки или переноса ADC. В некоторых вариантах осуществления однопроходная фильтрация в тангенциальном потоке уменьшает количество используемого буфера.
[0023] В некоторых вариантах осуществления противоточная диафильтрация улучшает стабильность производства ADC. В некоторых вариантах осуществления противоточная диафильтрация снижает время, требуемое для концентрации, очистки или переноса ADC. В некоторых вариантах осуществления противоточная диафильтрация уменьшает количество используемого буфера.
[0024] В некоторых вариантах осуществления способ дополнительно включает поточный мониторинг аналита.
[0025] В некоторых вариантах осуществления способ получения конъюгата антитело-лекарственное средство (ADC) включает использование поточного мониторинга для измерения добавления компонента в реакцию конъюгации ADC.
[0026] В некоторых вариантах осуществления поточный мониторинг измеряет концентрацию компонента, добавляемого в реакцию конъюгации ADC.
[0027] В некоторых вариантах осуществления поточный мониторинг измеряет скорость потока компонента, добавляемого в реакцию конъюгации ADC. В некоторых вариантах осуществления компонент представляет собой антитело или его антигенсвязывающий фрагмент, лекарственное средство, линкер, лекарственное средство, присоединенное к линкеру, антитело или его антигенсвязывающий фрагмент, присоединенный к линкеру и/или буфер для конъюгации.
[0028] В некоторых вариантах осуществления способ дополнительно включает поточный мониторинг для измерения добавления компонента в реакцию in situ. В некоторых вариантах осуществления компонент представляет собой лекарственное средство, линкер и/или буфер для реакции in situ.
[0029] В некоторых вариантах осуществления способ получения конъюгата антитело-лекарственное средство (ADC) включает поточный мониторинг аналита для определения, когда (i) прекратить добавление буфера для конъюгации в реакцию конъюгации ADC (ii), прекратить рециркуляцию буфера для конъюгации в реакции конъюгации ADC и/или (iii) начать вымывание буфера для конъюгации из реакции конъюгации ADC. В некоторых вариантах осуществления аналит представляет собой неконъюгированное лекарственное средство или неконъюгированное лекарственное средство, присоединенное к линкеру.
[0030] В некоторых вариантах осуществления способ очистки конъюгата антитело-лекарственное средство (ADC) после процесса конъюгации ADC включает поточный мониторинг аналита. В некоторых вариантах осуществления очистка включает фильтрацию. В некоторых вариантах осуществления фильтрация представляет собой ультрафильтрацию или диафильтрацию. В некоторых вариантах осуществления фильтрация представляет собой фильтрацию в тангенциальном потоке. В некоторых вариантах осуществления фильтрация в тангенциальном потоке представляет собой однопроходную фильтрацию в тангенциальном потоке. В некоторых вариантах осуществления фильтрация представляет собой противоточную диафильтрацию.
[0031] В некоторых вариантах осуществления аналит находится в ретентате. В некоторых вариантах осуществления аналит представляет собой концентрацию неконъюгированного лекарственного средства или неконъюгированного лекарственного средства, присоединенного к линкеру. В некоторых вариантах осуществления аналит представляет собой концентрацию ADC или антитела, или его антигенсвязывающего фрагмента. В некоторых вариантах осуществления аналит представляет собой концентрацию компонента буфера для реакции конъюгации или буфера для фильтрации.
[0032] В некоторых вариантах осуществления аналит представляет собой pH.
[0033] В некоторых вариантах осуществления аналит находится в пермеате. В некоторых вариантах осуществления аналит представляет собой концентрацию ADC или антитела, или его антигенсвязывающего фрагмента. В некоторых вариантах осуществления аналит представляет собой концентрацию неконъюгированного лекарственного средства или неконъюгированного лекарственного средства, присоединенного к линкеру.
[0034] В некоторых вариантах осуществления очистка включает хроматографию, а аналит измеряют в конце хроматографической колонки. В некоторых вариантах осуществления аналит представляет собой ADC или антитело, или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления аналит представляет собой неконъюгированное лекарственное средство, неконъюгированное лекарственное средство, присоединенное к линкеру, компонент буфера для реакции конъюгации или компонент буфера для хроматографии.
[0035] В некоторых вариантах осуществления реакция конъюгации представляет собой реакцию серийной конъюгации. В некоторых вариантах осуществления реакция конъюгации представляет собой непрерывную реакцию конъюгации.
[0036] В некоторых вариантах осуществления поточный мониторинг выполняют с использованием технологии переменной длины пути, устройства с проточной ячейкой, УФ-датчика, Рамановской спектроскопии или инфракрасной спектроскопии с преобразованием Фурье (FITR - англ.: Fourier Transform Infrared spectroscopy).
[0037] В некоторых вариантах осуществления поточный мониторинг аналита выполняют с использованием FlowVPE.
[0038] В некоторых вариантах осуществления поточный мониторинг улучшает выход ADC. В некоторых вариантах осуществления поточный мониторинг улучшает выделение ADC. В некоторых вариантах осуществления поточный мониторинг снижает время производства ADC. В некоторых вариантах осуществления поточный мониторинг уменьшает количество используемого буфера.
[0039] В некоторых вариантах осуществления способ получения конъюгата антитело-лекарственное средство (ADC) включает поточный мониторинг аналита для определения момента прекращения добавление компонента реакции конъюгации в реакцию конъюгации ADC. В некоторых вариантах осуществления компонент представляет собой антитело или его антигенсвязывающий фрагмент, лекарственное средство, линкер, лекарственное средство, присоединенное к линкеру и/или буфер для реакции конъюгации.
[0040] В некоторых вариантах осуществления ADC содержит антитело. В некоторых вариантах осуществления ADC содержит антигенсвязывающий фрагмент антитела. В некоторых вариантах осуществления ADC содержит антитело или антигенсвязывающий фрагмент, который специфически связывается с CD37, CD33, FOLR1, CD123, CD19, cMET, ADAMS или HER2. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержит CDR1 VH, CDR2 VH, CDR3 VH, CDR1 VL, CDR2 VL и CDR3 VL huMovl9, Z4681A или G4732A. В некоторых вариантах осуществления CDR представляют собой CDR, определенные по Kabat, CDR, определенные по Chothia, или CDR, определенные по AbM. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержат последовательности CDR1 VH, CDR2 VH, CDR3 VH, CDR1 VL, CDR2 VL и CDR3 VL, содержащие последовательности SEQ ID NO: 1-6, соответственно, SEQ ID NO: 7-12, соответственно, SEQ ID NO: 13-18, соответственно, SEQ ID NO: 19-24, соответственно, SEQ ID NO: 25-30 или, соответственно, SEQ ID NO: 31-36, соответственно. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержит последовательности VH и VL, содержащие последовательность SEQ ID NO: 37 и 38, соответственно, SEQ ID NO: 37 и 39, соответственно, SEQ ID NO: 40 и 41, соответственно SEQ ID NO: 42 и 43, соответственно, SEQ ID NO: 44 и 45 соответственно, SEQ ID NO: 46 и 47, соответственно, или SEQ ID NO: 48 и 49, соответственно. В некоторых вариантах осуществления антитело содержит последовательности тяжелой и легкой цепей, содержащие последовательности SEQ ID NO: 50 и 51, соответственно, SEQ ID NO: 50 и 52, соответственно, SEQ ID NO: 53 и 54, соответственно, или SEQ ID NO: 55 и 56, соответственно.
[0041] В некоторых вариантах осуществления ADC содержит линкер, выбранный из группы, состоящей из SMCC, sSPDB и пептидного линкера. В некоторых вариантах осуществления ADC содержит мейтансиноид или индолинобензодиазепин. В некоторых вариантах осуществления мейтансиноид представляет собой DM1 или DM4. В некоторых вариантах осуществления индолинобензодиазепин представляет собой DGN462 или DGN549.
[0042] В некоторых вариантах осуществления ADC представляет собой IMGN529, IMGN779, IMGN853, IMGN632 или Kadcyla.
[0043] В некоторых вариантах осуществления способ получения IMGN853 включает (i) смешивание антитела huMovl9 и DM4, связанного с сульфо-SPDB, в процессе непрерывной конъюгации с образованием IMGN853, необязательно, при этом поточный мониторинг используют для измерения концентрации антитела huMovl9, добавляемого в реакцию конъюгации, (ii) необязательно, концентрирование IMGN853 с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, (iii) очистку IMGN853 с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, и (iv) перенос IMGN853 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрация примесей в ретентате.
[0044] В некоторых вариантах осуществления способ получения IMGN853 включает (i) смешивание антитела huMovl9 и DM4, связанного с сульфо-SPDB, в процессе непрерывной конъюгации с образованием IMGN853, необязательно, при этом поточный мониторинг используют для измерения концентрации антитела huMovl9, добавляемого в реакцию конъюгации, (ii) необязательно, концентрирование IMGN853 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, (iii) очистку IMGN853 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, и (iv) перенос IMGN853 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрация примесей в ретентате.
[0045] В некоторых вариантах осуществления способ получения IMGN779 включает (i) смешивание антитела Z4681A и DGN462, связанного с сульфо-SPDB, в процессе непрерывной конъюгации с образованием IMGN779, необязательно, при этом поточный мониторинг используют для измерения концентрации антитела Z4681A, добавляемого в реакцию конъюгации, (ii) необязательно, концентрирование IMGN779 с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, (iii) очистку IMGN779 с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, и (iv) перенос IMGN779 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрация примесей в ретентате.
[0046] В некоторых вариантах осуществления способ получения IMGN779 включает (i) смешивание антитела Z4681A и DGN462, связанного с сульфо-SPDB, в процессе непрерывной конъюгации с образованием IMGN779, необязательно, при этом поточный мониторинг используют для измерения концентрации антитела Z4681A, добавляемого в реакцию конъюгации, (ii) необязательно, концентрирование IMGN779 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, (iii) очистку IMGN779 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, и (iv) перенос IMGN779 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрация примесей в ретентате.
[0047] В некоторых вариантах осуществления способ получения IMGN632 включает (i) смешивание антитела G4732A и сульфированного DNG549C в процессе непрерывной конъюгации с образованием IMGN632, (ii) необязательно, концентрирование IMGN632 с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, (iii) очистку IMGN632 с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, и (iv) перенос IMGN632 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке, необязательно, при этом поточный мониторинг используют для измерения концентрация примесей в ретентате. В некоторых вариантах осуществления антитело G4732A восстанавливается и окисляется только за один этап SPTFF перед процессом конъюгации.
[0048] В некоторых вариантах осуществления способ получения IMGN632 включает (i) смешивание антитела G4732A и сульфированного DNG549C в процессе непрерывной конъюгации с образованием IMGN632, (ii) необязательно, концентрирование IMGN632 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, (iii) очистку IMGN632 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрации неконъюгированного лекарственного средства в ретентате, и (iv) перенос IMGN632 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, необязательно, при этом поточный мониторинг используют для измерения концентрация примесей в ретентате. В некоторых вариантах осуществления антитело G4732A восстанавливается и окисляется только за один этап SPTFF или противоточной диафильтрации перед процессом конъюгации.
[0049] В некоторых вариантах осуществления способ включает повышение первой температуры процесса конъюгации по меньшей мере на 5°C до повышенной температуры, причем повышенную температуру поддерживают в течение не более 20 минут.
[0050] В некоторых вариантах осуществления способ получения ADC включает повышение первой температуры процесса конъюгации по меньшей мере на 5°C до повышенной температуры, причем повышенную температуру поддерживают в течение не более 20 минут.
[0051] В некоторых вариантах осуществления повышенная температура составляет не более 55°С. В некоторых вариантах осуществления первую температуру повышают по меньшей мере на 10°С, по меньшей мере на 15°С, по меньшей мере на 20°С или по меньшей мере на 30°С.
[0052] В некоторых вариантах осуществления повышенная температура составляет от 35°С до 55°С или от 40°С до 50°С.
[0053] В некоторых вариантах осуществления повышение первой температуры до повышенной температуры занимает не более 2 минут или не более 1 минуты.
[0054] В некоторых вариантах осуществления способ дополнительно включает снижение повышенной температуры, необязательно, до первой температуры. В некоторых вариантах осуществления снижение повышенной температуры, необязательно, до первой температуры, занимает не более 2 минут или не более 1 минуты.
[0055] В некоторых вариантах осуществления этапы повышения первой температуры до повышенной температуры, а затем снижения повышенной температуры повторяют по меньшей мере дважды или по меньшей мере трижды. В некоторых вариантах осуществления этапы повышения первой температуры до повышенной температуры, а затем снижения повышенной температуры повторяют 2-20 раз или 5-10 раз.
[0056] В некоторых вариантах осуществления способ включает снижение первой температуры процесса конъюгации по меньшей мере на 5°C до пониженной температуры, при этом пониженную температуру поддерживают в течение не более 20 минут.
[0057] В некоторых вариантах осуществления способ получения ADC включает снижение первой температуры процесса конъюгации по меньшей мере на 5°C до пониженной температуры, причем пониженную температуру поддерживают в течение не более 20 минут. В некоторых вариантах осуществления первая температура снижается не более чем на 30°C. В некоторых вариантах осуществления температура снижается по меньшей мере на 10°С, по меньшей мере на 15°С или по меньшей мере на 20°С.
[0058] В некоторых вариантах осуществления снижение первой температуры до пониженной температуры занимает не больше 2 минут или не более 1 минуты.
[0059] В некоторых вариантах осуществления способ дополнительно включает повышение пониженной температуры, необязательно, до первой температуры. В некоторых вариантах осуществления повышение пониженной температуры, необязательно, до первой температуры, занимает не более 2 минут или не более 1 минуты.
[0060] В некоторых вариантах осуществления этапы понижения первой температуры до пониженной температуры, а затем повышения пониженной температуры повторяют по меньшей мере дважды или по меньшей мере трижды. В некоторых вариантах осуществления этапы понижения первой температуры до пониженной температуры, а затем повышения пониженной температуры повторяют 2-20 раз или 5-10 раз.
[0061] Некоторые варианты осуществления отличаются тем, что повышенную температуру или пониженную температуру поддерживают в течение не более 15 минут. В некоторых вариантах осуществления повышенную температуру или пониженную температуру поддерживают в течение от 30 секунд до 15 минут. В некоторых вариантах осуществления повышенную температуру или пониженную температуру поддерживают в течение 15-20 минут. В некоторых вариантах осуществления повышенную температуру или пониженную температуру поддерживают в течение 10-15 минут. В некоторых вариантах осуществления повышенную температуру или пониженную температуру поддерживают в течение 5-10 минут. В некоторых вариантах осуществления повышенную температуру или пониженную температуру поддерживают в течение 1-5 минут.
[0062] В некоторых вариантах осуществления способ включает изменение первого значения pH процесса конъюгации по меньшей мере на 0,5 до измененного значения pH, причем измененное значение pH поддерживают в течение не более чем 20 минут.
[0063] В некоторых вариантах осуществления способ получения ADC включает изменение первого значения pH процесса конъюгации по меньшей мере на 0,5 до измененного значения pH, причем измененное значение pH поддерживают в течение не более чем 20 минут.
[0064] В некоторых вариантах осуществления первое значение рН увеличивают по меньшей мере на 1, необязательно, причем измененное значение рН не превышает 9. В некоторых вариантах осуществления первое значение рН увеличивают по меньшей мере на 2 или по меньшей мере на 3.
[0065] В некоторых вариантах осуществления первое значение рН уменьшают по меньшей мере на 1, необязательно, причем измененное значение рН не опускается ниже 4. В некоторых вариантах осуществления первое значение рН уменьшают по меньшей мере на 2 или по меньшей мере на 3.
[0066] В некоторых вариантах осуществления способ дополнительно включает изменение измененного значения рН, необязательно, до первого значения рН. В некоторых вариантах осуществления этапы изменения первого значения рН до измененного значения рН, а затем изменения измененного значения рН повторяют по меньшей мере дважды или по меньшей мере трижды. В некоторых вариантах осуществления этапы изменения первого значения pH до измененного значения pH, а затем изменения измененного значения pH повторяют 2-20 раз или 5-10 раз.
[0067] В некоторых вариантах осуществления измененное значение рН поддерживают в течение не более 15 минут. В некоторых вариантах осуществления измененное значение рН поддерживают в течение от 30 секунд до 15 минут. В некоторых вариантах осуществления измененное значение рН поддерживают в течение 15-20 минут. В некоторых вариантах осуществления измененное значение рН поддерживают в течение 10-15 минут. В некоторых вариантах осуществления измененное значение рН поддерживают в течение 5-10 минут. В некоторых вариантах осуществления измененное значение рН поддерживают в течение 1-5 минут.
[0068] Также в настоящем документе предложены ADC, полученные в соответствии со способами, предложенными в данном документе.
РАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ/ФИГУР
[0069] На фиг. 1 показан полностью непрерывный процесс производства конъюгата антитело-лекарственное средство (ADC) с интегрированными механизмами контроля обратной связи (внизу) и его связь с обычной обработкой серии (вверху).
[0070] На фиг. 2 приведена блок-схема, показывающая последовательность полунепрерывных операций, включающая технологии, обеспечивающие непрерывный процесс (внизу), и ее связь с обычной обработкой серии (вверху).
[0071] На фиг. 3 приведена блок-схема, показывающая соединение последовательности полунепрерывных типовых операций (внизу) и его связь с обычной обработкой серии (вверху).
[0072] На фиг. 4 приведена блок-схема, показывающая процесс непрерывной конъюгации для конъюгации конъюгата антитело-лекарственное средство ADC «IMGN853», описанного в примере 1. «MAb» относится к моноклональному антителу (то есть huMovl9). «D» относится к лекарственному средству (то есть мейтансиноиду DM4), а «L» относится к линкеру (то есть, sSPDB).
[0073] На фиг. 5 показана установка для исследований непрерывной конъюгации, описанной в примере 1 А. Первый шприцевой насос (L/D/ДМА) подает компоненты in situ, растворенные в ДМА. Буферный (IS) шприцевой насос подает буфер для реакции in situ (такой же, как буфер реакции конъюгации, но значение pH для реакции in situ равно 7,6). Третий шприц подает антитело и буфер для реакции конъюгации со значением pH 8,7. «MAb» относится к моноклональному антителу (то есть huMovl9). «D» относится к лекарственному средству (то есть мейтансиноиду DM4), а «L» относится к линкеру (то есть, sSPDB). «IS» относится к in situ.
[0074] На фиг. 6 показаны уровни примесей свободного лекарственного средства для четырех основных видов примесей в образцах, отобранных на этапах ILC, ILDF1 и ILDF2, описанных в примере 1B.
[0075] На фиг. 7 показаны уровни примесей свободного лекарственного средства для четырех основных видов примесей в образцах, взятых на этапе ILDF1 при подаваемой концентрации 15 мг/мл, как описано в примере 1B.
[0076] На фиг. 8 показано сравнение уровней примесей свободного лекарственного средства для непрерывных и серийных процессов очистки TFF. Материал конъюгата непрерывного процесса (заштрихованные прямоугольники) обрабатывали при исходной концентрации 15 г/л, тогда как материал серии (цельные прямоугольники) обрабатывали при концентрации 30 г/л, как описано в примере 1B.
[0077] На фиг. 9 показаны уровни примесей свободного лекарственного средства для четырех основных видов примесей в образцах, взятых на этапе ILDF1 при подаваемой концентрации 30 мг/мл, как описано в примере 1B.
[0078] На фиг. 10 приведена блок-схема, показывающая процесс непрерывной конъюгации для конъюгации конъюгата антитело-лекарственное средство (ADC) «IMGN632», описанного в примере 2. «MAb» относится к моноклональному антителу (то есть G4723A).
[0079] На фиг. 11 показана химическая структура IMGN632. IMGN632 представляет собой композицию, содержащую ADC, содержащие анти-CD123 антитело G4723, связанное с цитотоксической полезной нагрузкой DGN549-C в бисульфите натрия. Большая часть ADC в составе находится в сульфированном варианте, показанном на верхней панели. На нижней панели показана несульфированная форма ADC, содержащая антитело анти-CD123 антитело G4723, связанное с цитотоксической полезной нагрузкой DGN549-C (моноиминовая структура), которая также может присутствовать в композиции IMGN632.
[0080] На фиг. 12 показано, как можно применять технологии автоматизации поточных процессов (PAT - англ.: process automation technology) для повышения контроля и выявляемости.
[0081] На фиг. 13 показана схема реакторов нагревания и охлаждения, которые можно использовать для импульсной реакции конъюгации с повышенной температурой. В импульсных реакторах (с маркировкой «PR») температура рубашки повышается, так что компоненты реакции, содержащиеся в катушке, временно нагреваются, чтобы вызвать кратковременное отклонение температуры. Затем в реакторах охлаждения (с маркировкой «CR») температуру рубашки поддерживают на более низком уровне, чтобы дать возможность компонентам реакции в катушке остыть от повышенной температуры. Это может снизить объем агрегации, происходящей во время реакции. Реактор времени пребывания (RTR) поддерживает желаемую температуру реакции после завершения импульсного воздействия, и его объем может быть основан на желаемом времени реакции.
[0082] На фиг. 14 показана скорость конъюгации IMGN853 (левая панель) и накопление высокомолекулярных (HMW; агрегат) соединений в реакциях конъюгации, подвергаемых либо постоянной температуре 20°C, либо повторяющимся импульсам при более высоких температурах.
ПОДРОБНОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Определения
[0083] В контексте данного документа термины «конъюгат антитело-лекарственное средство» (ADC) и «иммуноконъюгат» относятся к соединению или его производному, которое связано со связывающим клетки агентом (например, антителом или его антигенсвязывающим фрагментом), и определено общей формулой: D-L-A, где D = цитотоксическое лекарственное средство, L = линкер и A = антитело или фрагмент антитела. ADC также можно определить по общей формуле в обратном порядке: A-L-D. ADC может содержать несколько лекарственных средств и линкеров на антитело или его антигенсвязывающий фрагмент, например, (D-L)4-A или A-(L-D)2. Термины «антитело-лекарственное средство» и «иммуноконъюгат» используются в настоящем документе взаимозаменяемо.
[0084] «Линкер» представляет собой любой химический фрагмент, который способен связывать лекарственное средство со связывающим клетки агентом (например, антителом или его антигенсвязывающим фрагментом) стабильным ковалентным образом. Линкеры могут быть восприимчивыми или быть по существу устойчивыми к расщеплению, индуцированному кислотой, расщеплению, индуцированному светом, расщеплению, индуцированному пептидазой, расщеплению, индуцированному эстеразой, и расщеплению дисульфидной связи в условиях, при которых соединение или антитело остаются активными. Подходящие линкеры хорошо известны в данной области техники и включают, например, дисульфидные группы, тиоэфирные группы и пептидные линкеры.
[0085] Термин «антитело» означает молекулу иммуноглобулина, которая распознает и специфически связывается с мишенью, такой как белок, полипептид, пептид, углевод, полинуклеотид, липид или комбинации вышеуказанного, по меньшей мере через один сайт распознавания антигена в пределах вариабельной области молекулы иммуноглобулина. В контексте данного документа термин «антитело» охватывает интактные поликлональные антитела, интактные моноклональные антитела, химерные антитела, гуманизированные антитела, антитела человека, слитые белки, содержащие антитело, и любую другую модифицированную молекулу иммуноглобулина, при условии, что антитела проявляют желаемую биологическую активность. Антитело может относиться к любому из пяти основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM или их подклассов (изотипов) (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) на основании идентичности их константных доменов тяжелой цепи, называемых альфа, дельта, эпсилон, гамма и мю, соответственно. Различные классы иммуноглобулинов имеют разные и хорошо известные структуры субъединиц и трехмерные конфигурации. Антитела могут являться голыми или конъюгированными с другими молекулами, такими как токсины, радиоактивные изотопы и т.д.
[0086] Термин «фрагмент антитела» относится к части интактного антитела. «Антигенсвязывающий фрагмент» относится к части интактного антитела, которая связывается с антигеном. Антигенсвязывающий фрагмент может содержать определяющие антигены вариабельные области интактного антитела. Примеры фрагментов антител включают, без ограничения, фрагменты Fab, Fab', F(ab')2 и Fv, линейные антитела и одноцепочечные антитела. Фрагменты антител могут являться голыми или конъюгированными с другими молекулами, такими как токсины, радиоактивные изотопы и т.д.
[0087] В контексте данного документа термины «вариабельная область» или «вариабельный домен» используются взаимозаменяемо и являются общепринятыми в данной области техники. Вариабельная область как правило относится к части антитела, обычно к части легкой или тяжелой цепи, как правило к аминоконцу, содержащему от 110 до 120 аминокислот или от 110 до 125 аминокислот в зрелой тяжелой цепи и от около 90 до 115 аминокислот в зрелой легкой цепи, которые значительно различаются по последовательности среди антител и используются в связывании и специфичности конкретного антитела к его конкретному антигену. Вариабельность в последовательности сконцентрирована в тех областях, которые называются определяющими комплементарность областями (CDR), в то время как более высоко консервативные области в вариабельном домене называются каркасными областями (FR). Не желая быть связанными каким-либо конкретным механизмом или теорией, предполагается, что CDR легкой и тяжелой цепей главным образом отвечают за взаимодействие и специфичность антитела с антигеном. В определенных вариантах осуществления вариабельная область представляет собой вариабельную область человека. В некоторых вариантах осуществления вариабельная область включает CDR грызунов или мыши и каркасные области человека (FR). В конкретных вариантах осуществления вариабельная область представляет собой вариабельную область приматов (например, приматов, не являющихся человеком). В некоторых вариантах осуществления вариабельная область содержит CDR грызунов или мышей и каркасные области (FR) приматов (например, приматов, не являющихся человеком).
[0088] Термины «VL» и «домен VL» используются взаимозаменяемо для обозначения вариабельной области легкой цепи антитела.
[0089] Термины «VH» и «домен VH» используются взаимозаменяемо для обозначения вариабельной области тяжелой цепи антитела.
[0090] Термин «нумерация по Rabat» и подобные термины известны в данной области техники и относятся к системе нумерации аминокислотных остатков в вариабельных областях тяжелой и легкой цепи антитела или его антигенсвязывающего фрагмента. В определенных аспектах CDR могут быть определены в соответствии с системой нумерации по Rabat (см., например Rabat EA & Wu TT (1971) Ann NY Acad Sci 190: 382-391 and Rabat EA et al., (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242). При использовании системы нумерации по Rabat, CDR в молекуле тяжелой цепи антитела обычно присутствуют в аминокислотных положениях 31-35, которые необязательно могут включать одну или две дополнительные аминокислоты, следующие за 35 (в схеме нумерации по Rabat обозначены как 35А и 35В) (CDR1), аминокислотных положениях 50-65 (CDR2) и аминокислотных положениях 95-102 (CDR3). При использовании системы нумерации по Rabat, CDR в молекуле легкой цепи антитела обычно присутствуют в аминокислотных положениях 24-34 (CDR1), аминокислотных положениях 50-56 (CDR2) и аминокислотных положениях 89-97 (CDR3). В конкретном варианте осуществления CDR антител, описанных в настоящем документе, были определены в соответствии со схемой нумерации по Rabat.
[0091] Вместо этого, Chothia относится к расположению структурных петель (Chothia and Lesk, J. Mol. Biol. 196:901-917 (1987)). Конец петли CDR-H1 по Chothia, при нумерации с использованием соглашения о нумерации по Kabat, варьируется между H32 и H34 в зависимости от длины петли (это связано с тем, что схема нумерации по Kabat размещает вставки в положениях H35A и H35B; если ни 35A, ни 35B не присутствуют, петля заканчивается в положении 32; если присутствует только 35А, петля заканчивается в положении 33; если присутствуют как 35А, так и 35В, петля заканчивается в положении 34). Гипервариабельные области AbM представляют собой компромисс между CDR по Kabat и структурными петлями Chothia и используются программным обеспечением для моделирования антител AbM Oxford Molecular.
(Нумерация по Kabat)
[0092] В контексте данного документа термины «константная область» или «константный домен» используются взаимозаменяемо и являются общепринятыми в данной области техники. Константная область представляет собой часть антитела, например, карбоксильную концевую часть легкой и/или тяжелой цепи, которая не участвует непосредственно в связывании антитела с антигеном, но которая может проявлять различные эффекторные функции, такие как взаимодействие с Fc-рецептором. Константная область молекулы иммуноглобулина обычно имеет более консервативную аминокислотную последовательность относительно вариабельного домена иммуноглобулина. В определенных аспектах антитело или его антигенсвязывающий фрагмент содержит константную область или ее часть, достаточную для антителозависимой клеточно-опосредованной цитотоксичности (АЗКЦ).
[0093] В контексте данного документа термин «тяжелая цепь» при использовании в отношении антитела может относиться к любому отдельному типу, например, альфа (α), дельта (δ), эпсилон (ε), гамма (γ) и мю (μ), на основании аминокислотной последовательности константного домена, который образует антитела классов IgA, IgD, IgE, IgG и IgM, соответственно, включая подклассы IgG, например, IgG1 IgG2, IgG3 и IgG4. Аминокислотные последовательности тяжелой цепи хорошо известны в данной области техники. В конкретных вариантах осуществления тяжелая цепь представляет собой тяжелую цепь человека.
[0094] В контексте данного документа термин «легкая цепь» при использовании в отношении антитела может относиться к любому другому типу, например каппа (κ) или лямбда (λ), на основе аминокислотной последовательности константных доменов. Аминокислотные последовательности легкой цепи хорошо известны в данной области техники. В конкретных вариантах осуществления легкая цепь представляет собой легкую цепь человека.
[0095] В контексте данного документа термин «процесс конъюгации» относится к процессу, в ходе которого реагенты реакции конъюгации (например, связывающий клетки агент, лекарственное средство и линкер; связывающий клетки агент и лекарственное средство, присоединенное к линкеру, или связывающий клетки агент, присоединенный к линкеру и лекарственное средство) смешивают в условиях, которые позволяют реагентам вступать в реакцию и образовывать ADC.
[0096] В контексте данного документа термин «процесс серийной конъюгации» относится к процессу конъюгации, в котором реагенты реакции конъюгации смешивают в общем объеме, реакция конъюгации происходит с образованием продуктов реакции конъюгации (ADC), а продукты реакции конъюгации (ADC) затем удаляют в общем объеме.
[0097] В контексте данного документа термин «процесс непрерывной конъюгации» относится к процессу конъюгации, в котором один или более реагентов реакции конъюгации продолжают добавлять в реакцию конъюгации, пока протекает реакция конъюгации и после образования по меньшей мере одного продукта реакции конъюгации (ADC). Продукты реакции конъюгации (ADC) можно продолжать удалять из реакции конъюгации по мере протекания реакции конъюгации.
[0098] В контексте данного документа термин «реакция in situ» относится к процессу, в котором лекарственное средство и линкер смешивают с образованием лекарственного средства, связанного с линкером. Затем лекарственное средство, присоединенное к линкеру, можно использовать в реакции конъюгации со связывающим клетки агентом (например, антителом) для образования ADC.
[0099] В контексте данного документа термин «проточный реактор» относится к любому реакторному сосуду, как правило трубчатому, который используется для химии непрерывных реакций. Проточные реакторы могут быть изготовлены из нержавеющей стали, стекла, полимеров и т.д.
[0100] В контексте данного документа термин «поточный мониторинг» относится к мониторингу аналита в реальном времени, например, когда происходит реакция конъюгации, процесс концентрирования, процесс очистки или процесс замены буфера.
[0101] В контексте данного документа термин «фильтр» относится к селективному барьеру, который обеспечивает разделение соединений в жидкости. Разделение достигают путем селективного пропускания (проникновения) одного или более соединений жидкости через фильтр при одновременном замедлении прохождения одного или более других соединений.
[0102] В контексте данного документа термин «питающий поток» относится к жидкости, подаваемой на фильтр или мембрану для разделения компонентов в фильтре или мембране.
[0103] В контексте данного документа термин «ретентат» относится к той части питающего потока, которая не проходит через фильтр.
[0104] В контексте данного документа термин «пермеат» относится к той части питающего потока, которая проходит через фильтр.
[0105] В контексте данного документа термин «фильтрация в тангенциальном потоке» (TFF) относится к мембранному процессу фильтрации, в котором питающий поток проходит параллельно поверхности мембраны. Одна часть питающего потока проходит через мембрану (пермеат), а остальная часть (ретентат) возвращается обратно в подающий резервуар. TFF также называют фильтрацией в перекрестном потоке. Системы для проведения TFF известны и включают, например, систему типа Pellicon (Millipore, Биллерика, штат Массачусетс), кассетную систему Sartocon (Sartorius AG, Эджвуд, штат Нью-Йорк) и систему типа Centrasette (Pall Corporation, Ист Хиллз, штат Нью-Йорк).
[0106] Термин «однопроходная фильтрация в тангенциальном потоке» (SPTFF) в контексте данного документа относится к процессу фильтрации в тангенциальном потоке, в котором питающий поток проходит через фильтрующую мембрану только один раз. Системы для проведения SPTFF известны и включают, например, систему типа Cadance (Pall Corporation, Вестбороу, штат Массачусетс). Системы и способы проведения SPTFF раскрыты, например, в патенте США №7384459, патенте США №7510654, патенте США №7682511, патенте США №7967987, патенте США №8157999 и патенте США №8231787, каждый из которых включен в настоящий документ посредством ссылки во всей своей полноте.
[0107] В контексте данного документа термин «непрерывная диафильтрация» относится к процессу диафильтрации, в котором селективное разделение растворенных веществ достигается непрерывным образом путем смешивания питающего потока с разбавителем и прокачки его через мембрану с удаляемым пермеатом и ретентатом. Продукт не образуется в сосуде в процессе фильтрации; вместо этого он непрерывно выводится из системы в ходе фильтрации. «Противоточная диафильтрация» относится к непрерывному процессу диафильтрации, в котором технологический поток (например, пермеат или ретентат) рециркулирует на стадиях диафильтрации.
[0108] Термин «поточный мониторинг» относится к мониторингу аналита в режиме реального времени, например, во время процесса производства или очистки. Поточный мониторинг отличается от внутрипроцессного отбора проб или автономного анализа, которые не обеспечивают обратную связь в реальном времени.
[0109] Термин «технология автоматизации поточного процесса» относится к любому встроенному измерительному устройству, используемому для контроля аналита во время процесса.
[0110] В контексте данного документа термин «аналит» является широким термином, и он относится, без ограничения, к веществу или химическому компоненту в жидкости, которые можно проанализировать. Аналиты могут включать встречающиеся в природе вещества, искусственные вещества, метаболиты и/или продукты реакции. В некоторых вариантах осуществления аналит для измерения в раскрытых в настоящем документе способах представляет собой антитело или его антигенсвязывающий фрагмент, лекарственное средство, линкер, линкер, связанный с антителом или его антигенсвязывающим фрагментом, линкер, связанный с лекарственным средством, конъюгат антитело-лекарственное средство (ADC), соотношение лекарственное средство-антитело (DAR - англ.: drug-to-antibody ratio) и/или примесь.
[0111] В контексте данного документа термин «буфер для реакции» относится к буферу, в котором может происходить реакция. Таким образом, термины «буфер для реакции конъюгации» или «буфер для конъюгации» в контексте данного документа относятся к буферу, в котором может происходить реакция конъюгации (реакция непрерывной конъюгации или реакция серийной конъюгации). Аналогично, термины «буфер для реакции in situ» или «буфер in situ» в контексте данного документа относятся к буферу, в котором может происходить реакция in situ.
[0112] В контексте данного документа термин «буфер для состава» относится к буферу, который обеспечивает биологическую активность активного ингредиента и, который не содержит никаких дополнительных компонентов, являющихся неприемлемо токсичными для субъекта, которому будет вводиться состав.
[0113] В контексте данного документа термин «индолинобензодиазепин» (IGN) относится к соединению, имеющему структуру ядра индолинобензодиазепина. Индолинобензодиазепин может быть замещенным или незамещенным. Он также включает соединение, имеющее два индолинобензодиазепиновых ядра, связанных линкером. Функциональность имина (-C=N-) в составе индолинобензодиазепинового ядра может быть снижена. В некоторых вариантах осуществления соединение индолинобензодиазепина содержит структуру ядра, 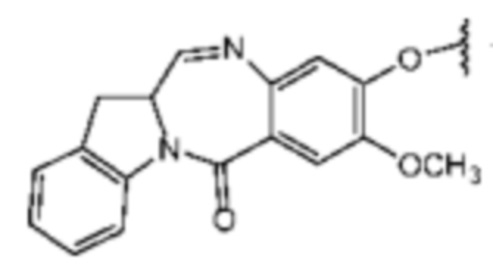 которая может быть необязательно замещена.
которая может быть необязательно замещена.
[0114] В некоторых вариантах осуществления соединение индолинобензодиазепина содержит структуру ядра, 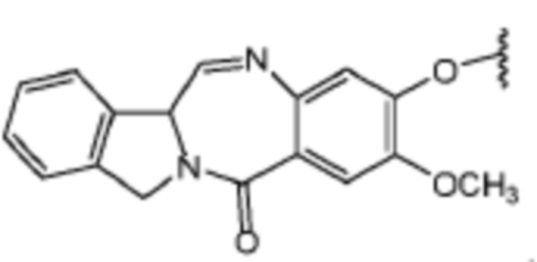 , которая может быть необязательно замещена.
, которая может быть необязательно замещена.
[0115] В контексте данного документа термин «пирролобензодиазепин» (PBD) относится к соединению, имеющему структуру ядра пирролобензодиазепина. Пирролобензодиазепин может быть замещенным или незамещенным. Он также включает соединение, имеющее два пирролобензодиазепиновых ядра, связанных линкером. Функциональность имина (-C=N-) в составе индолинобензодиазепинового ядра может быть снижена. В некоторых вариантах осуществления соединение пирролобензодиазепина содержит структуру ядра, 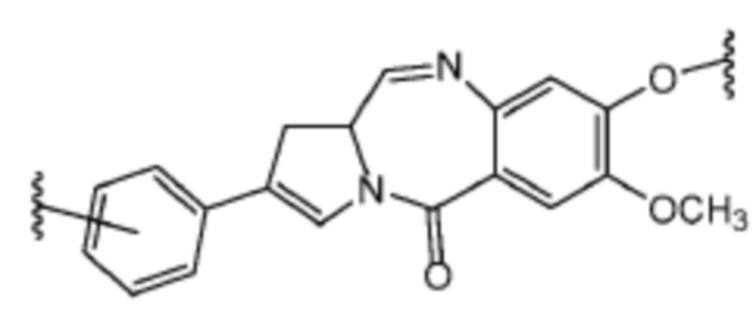 которая может быть необязательно замещена. В некоторых вариантах осуществления соединения пирролобензодиазепина содержат структуру ядра,
которая может быть необязательно замещена. В некоторых вариантах осуществления соединения пирролобензодиазепина содержат структуру ядра, 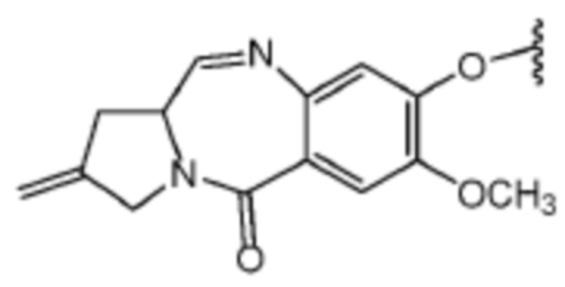 которая может быть необязательно замещена.
которая может быть необязательно замещена.
[0116] Использованные в настоящем раскрытии и формуле изобретения формы единственного числа включают формы множественного числа, если в контексте явно не указано иное.
[0117] Следует понимать, что в тех случаях, когда варианты осуществления описаны в данном документе с формулировкой «содержащий», в противном случае также предложены аналогичные варианты осуществления, описанные в терминах «состоящий из» и/или «состоящий в основном из».
[0118] Термин «и/или», используемый в фразе, такой как «A и/или B» в данном документе, предназначен для включения «A и B», «A или B», «A» и «B». Аналогично, термин «и/или», используемый во фразе, такой как «A, B и/или C», предназначен для охвата каждого из следующих вариантов осуществления: А, В и С; А, В или С; А или С; А или В; B или C; А и С; А и B; B и C; A (отдельно); B (отдельно); и С (отдельно).
Непрерывная конъюгация, однопроходная фильтрация в тангенциальном потоке и противоточная диафильтрация
[0119] В настоящем документе предложены непрерывные способы образования и/или обработки конъюгатов антитело-лекарственное средство (ADC). При формировании и обработке серии компоненты добавляют в процесс, процесс продолжается в течение некоторого времени, а затем продукты процесса удаляют в общем объеме. Напротив, в непрерывных способах, предложенных в настоящем документе, компоненты продолжают добавлять к текущему процессу, а продукты могут удалять на протяжении всего процесса, а не в общем объеме в конце процесса. Например, в непрерывном процессе конъюгации один или более реагентов реакции конъюгации продолжают добавлять в реакцию конъюгации, пока протекает реакция и после образования по меньшей мере одного продукта реакции конъюгации (ADC). Точно так же в последующих процессах непрерывной концентрации, очистки и/или замены буферов ADC, буферы и/или другие компоненты продолжают добавлять к процессам очистки концентраций и/или замены буферов по мере того, как эти процессы протекают, а концентрированные, очищенные ADC и те, в которых был заменен буфер, могут быть непрерывно удалены из этих текущих процессов. Соответственно, весь процесс ADC от конъюгации ADC до составления ADC может быть непрерывным (см., например, фиг. 1 (внизу)).
[0120] Авторы настоящего изобретения продемонстрировали, что процесс конъюгации можно выполнять непрерывно с использованием проточных реакторов. Проточные реакторы позволяют непрерывно добавлять один или более реагентов реакции конъюгации в реакцию конъюгации, когда реакция конъюгации протекает и после образования по меньшей мере одного продукта реакции конъюгации (ADC). Использование проточных реакторов в процессе конъюгации позволяет контролировать реакцию конъюгации и универсальность процесса конъюгации (например, быстрое изменение температуры/более жесткий контроль температуры, смешивание, опосредованное диффузией, следовательно, более равномерное, без ограничений по сосудам или ограничений комплекта) и улучшенная масштабируемость процесса конъюгации ADC (т.е. обычные риски масштабирования при серийной обработке не применяются, а пространственно-временной выход оптимизирован (например, выполняется псевдомасштабирование (увеличение выхода) путем выполнения текущего процесса в течение более длительного периода времени)).
[0121] Авторы настоящего изобретения дополнительно продемонстрировали, что непрерывная обработка ADC может быть выполнена с использованием однопроходной фильтрации в тангенциальном потоке (SPTFF), которая может успешно отделять неконъюгированное лекарственное средство от ADC. Объемная (обычная) диафильтрация включает в себя заполнение системы фильтрации в тангенциальном потоке (TFF) первым буфером A (буфером, в котором изначально находится продукт). Затем продукт добавляют в сосуд для ретентата, где он смешивается с основным объемом. Подающий насос для сосуда с ретентатом перекачивает продукт из ретентата через мембрану TFF, где он либо задерживается (и возвращается в ретентат), либо выбрасывается в отходы. Другой насос (насос для диафильтрации) будет подавать из сосуда в буфер B, содержащийся в отдельном сосуде (буфер, в который будет перенесен продукт), по линии подачи из сосуда в сосуд для ретентата. Запускают оба насоса, и продукт в сосуде для ретентата начинает проходить через мембрану TFF. Поскольку буфер удаляется через поток отходов, объем в ретентате поддерживают путем добавления буфера B (в равном объеме) в сосуд для ретентата. В результате продукт медленно переносится в буфер B.
[0122] В SPTFF используется родственная концепция переноса продукта, который изначально находится в буфере A, в буфер B. Однако продукт только один раз проходит через мембрану, поэтому должен быть достигнут весь необходимый объем буфера B для достижения полной замены буфера. Для этого в SPTFF можно добавить буфер B поверх в ходе проведения многоуровневых этапов. Таким образом, продукт проходит через мембраны только один раз: вход в буфер A и выход из модуля в буфер B.
[0123] Аналогично, непрерывная обработка ADC может быть выполнена с использованием противоточной диафильтрации.
[0124] Соответственно, способы непрерывной обработки ADC, предложенные в настоящем документе (например, с использованием SPTFF и/или противоточной диафильтрации), могут сократить время обработки, улучшить выход и/или улучшить консистенцию продукта по сравнению с серийной обработкой ADC. Способы непрерывной обработки ADC, предложенные в данном документе (например, с использованием SPTFF и/или противоточной диафильтрации), также могут исключать этапы выдержки, используемые в процессах серийной конъюгации. Способы непрерывной обработки ADC, предложенные в данном документе (например, с использованием SPTFF и/или противоточной диафильтрации), также могут допускать использование меньшего по размеру оборудования. SPTFF также является предпочтительной, поскольку антитела, чувствительные к окислению, потенциально вызываемому сдвигающими усилиями, могут лучше подходить для SPTFF.
[0125] Обработка ADC может включать конъюгацию (образование) ADC, концентрацию ADC, очистку ADC и/или составление ADC. Хотя особенно полезно, чтобы весь процесс от конъюгации ADC до составления был непрерывным (например, как показано на фиг. 1), также возможно комбинировать этапы непрерывной обработки с этапами серийной обработки (например, как показано на фиг. 2 и 3). Кроме того, возможно, чтобы последующие стадии обработки (например, получение антитела, линкера и/или лекарственного средства) были непрерывными и непрерывно подавались в конъюгацию ADC.
[0126] Соответственно, в некоторых способах, предложенных в настоящем документе, процесс конъюгации для образования конъюгатов антитело-лекарственное средство (ADC) является непрерывным. В непрерывном процессе конъюгации один или более реагентов реакции конъюгации продолжают добавлять в реакцию конъюгации, пока протекает реакция конъюгации и после образования по меньшей мере одного продукта реакции конъюгации (ADC). Реагенты для реакции конъюгации можно вводить в систему, в то время как собранные ADC удаляют из системы. Например, в некоторых непрерывных процессах конъюгации, предложенных в настоящем документе, связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент), лекарственное средство, связанное с линкером, и буфер для реакции конъюгации продолжают добавлять к реакции конъюгации, пока протекает реакция конъюгации и после образования по меньшей мере одного ADC. В некоторых непрерывных процессах конъюгации, предложенных в настоящем документе, связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент), присоединенный к линкеру, лекарственное средство и буфер для реакции конъюгации продолжают добавлять к реакции конъюгации, пока протекает реакция конъюгации и после образования по меньшей мере одного ADC. В некоторых непрерывных процессах конъюгации, предложенных в настоящем документе, связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент), лекарственное средство, линкер и буфер для реакции конъюгации продолжают добавлять к реакции конъюгации, пока протекает реакция конъюгации и после образования по меньшей мере одного ADC. Реагенты, которые продолжают добавлять, могут быть добавлены вместе в одном питающем потоке или могут подаваться отдельно в сосуд для сбора или непосредственно в реакционный сосуд.
[0127] В некоторых процессах непрерывной конъюгации, предложенных в настоящем документе, только один из связывающего клетки агента (например, антитела или его антигенсвязывающего фрагмента), связывающего клетки агента, присоединенного к линкеру, лекарственного средства, лекарственного средства, присоединенного к линкеру, линкера или буфера для реакции конъюгации продолжают добавлять к реакции конъюгации, пока протекает реакция конъюгации и после образования по меньшей мере одного ADC. В некоторых процессах непрерывной конъюгации, предложенных в настоящем документе, два реагента, выбранных из группы, состоящей из: связывающего клетки агента (например, антитела или его антигенсвязывающего фрагмента), связывающего клетки агента, присоединенного к линкеру, лекарственного средства, лекарственного средства, присоединенного к линкеру, линкера и буфера для реакции конъюгации продолжают добавлять к реакции конъюгации, пока протекает реакция конъюгации и после образования по меньшей мере одного ADC.
[0128] Использование SPTFF может позволить непрерывное добавление и/или удаление компонентов из реакции конъюгации. Таким образом, SPTFF можно использовать для получения реагентов для конъюгации ADC и для обработки собранных ADC. SPTFF может включать непрерывную обработку ADC, так что все (или поднабор) этапов обработки для конкретного ADC (например, производство, концентрирование, очистка и/или составление) могут выполняться одновременно. Таким образом, противоточную диафильтрацию можно использовать для получения реагентов для конъюгации ADC и для обработки собранных ADC.
[0129] В соответствии со способами, предложенными в настоящем документе, SPTFF можно использовать для концентрирования ADC, для очистки ADC и/или для получения ADC (например, путем переноса ADC в буфер для состава). SPTFF можно использоваться для переноса ADC из первого буфера во второй буфер. Противоточную диафильтрацию можно также использовать для концентрирования ADC, для очистки ADC и/или для получения ADC (например, путем переноса ADC в буфер для состава), и противоточную диафильтрацию можно также использовать для переноса ADC из первого буфера во второй буфер.
[0130] В некоторых способах, предложенных в настоящем документе, SPTFF используют в ходе производства, очистки и составления ADC, что делает непрерывным весь процесс от производства ADC до составления. В некоторых способах, предложенных в настоящем документе, противоточную диафильтрацию используют в ходе производства, очистки и составления ADC, что делает непрерывным весь процесс от производства ADC до составления. Таким образом, все процессы, показанные на иллюстративных фиг. 4 и 10 могут быть непрерывными.
[0131] В некоторых способах, предложенных в настоящем документе, SPTFF используют в сочетании с обычной TFF, так что некоторые части процессов, показанных на иллюстративных фиг. 4 и 10 являются непрерывными, тогда как другие части выполняются сериями. Например, антитело или его антигенсвязывающий фрагмент могут быть заменены буфером перед конъюгацией с использованием обычной (серийной) TFF (см., например, TFF1, показанной на фиг. 4), а затем подается в непрерывный процесс, в котором SPTFF используют для последующих процессов (см., например, TFF2 этап 1 и II, показанные на фиг. 4). Противоточную диафильтрацию можно использовать вместо или в сочетании с SPTFF в таких способах.
[0132] На фиг. 4 и 10, каждый из блоков, показанных заштрихованными пунктирными линиями, представляет отдельную часть процесса, который может проводиться как серийным, так и непрерывным образом. Например, в процессе помещения антитела в буфер для конъюгации, показанном в верхнем левом блоке на фиг. 4, можно использовать SPTFF и выполнять непрерывно или может использовать обычную TFF и выполнять серийно. Независимо от того, выполняется ли процесс помещения антитела в буфер для конъюгации серийным или непрерывным способом, в процессах концентрации и очистки ADC, показанных в блоке после реакции конъюгации, можно использовать SPTFF и выполнять непрерывно или можно использовать обычную TFF и выполнять серийно. Аналогично, независимо от того, выполняется ли процесс помещения антитела в буфер для конъюгации в ходе серийного или непрерывного процесса, и независимо от того, концентрируется ли ADC и очищается ли с использованием серийного или непрерывного процесса, ADC может быть составлен с использованием SPTFF непрерывным способом или с использованием обычной TFF серийным способом. Противоточную диафильтрацию можно использовать вместо или в сочетании с SPTFF в таких способах.
[0133] В некоторых вариантах осуществления, по меньшей мере, два этапа в процессе ADC выполняются с использованием SPTFF. Например, в некоторых вариантах осуществления SPTFF используют для переноса антитела или его антигенсвязывающего фрагмента в буфер для конъюгации и используют для концентрирования и очистки ADC после его образования, в то время как SPTFF или TFF используют для переноса ADC в буфер для состава. В некоторых вариантах осуществления SPTFF используют для переноса антитела или его антигенсвязывающего фрагмента в буфер для конъюгации и используют для переноса очищенного ADC в буфер для состава, в то время как SPTFF или TFF используют для концентрирования и очистки ADC после его образования. В некоторых вариантах осуществления SPTFF используют для концентрирования и очистки ADC и используют для переноса концентрированного и очищенного ADC в буфер для состава, где либо SPTFF, либо TFF используют для переноса антитела или его антигенсвязывающего фрагмента в буфер для конъюгации.
[0134] В SPTFF может быть использована ультрафильтрационная мембрана, например, в способах концентрирования ADC. В SPTFF может быть использована мембрана для диафильтрации, например, в способах очистки ADC и/или в способах переноса ADC в буфер (например, буфер для состава).
[0135] В некоторых вариантах осуществления, по меньшей мере, два этапа в процессе ADC выполняются с использованием SPTFF и/или противоточной диафильтрации. Например, в некоторых вариантах осуществления SPTFF и/или противоточную диафильтрацию используют для переноса антитела или его антигенсвязывающего фрагмента в буфер для конъюгации и используют для концентрирования и очистки ADC после его образования, в то время как SPTFF, противоточную диафильтрацию и/или TFF используют для переноса ADC в буфер для состава. В некоторых вариантах осуществления SPTFF и/или противоточную диафильтрацию используют для переноса антитела или его антигенсвязывающего фрагмента в буфер для конъюгации и используют для переноса очищенного ADC в буфер для состава, в то время как SPTFF, противоточную диафильтрацию и/или TFF используют для концентрирования и очистки ADC после его образования. В некоторых вариантах осуществления SPTFF и/или противоточную диафильтрацию используют для концентрирования и очистки ADC и используют для переноса концентрированного и очищенного ADC в буфер для состава, где либо SPTFF, противоточную диафильтрацию и/или TFF используют для переноса антитела или его антигенсвязывающего фрагмента в буфер для конъюгации.
[0136] Колоночную хроматографию также можно использовать в проточном режиме в способах непрерывной обработки ADC, предложенных в настоящем документе (например, в сочетании с SPTFF и/или противоточной диафильтрацией). Например, реакция конъюгации (например, реакция непрерывной конъюгации ) может подаваться в проточную колоночную хроматографию для удаления неконъюгированного лекарственного средства из реакции конъюгации (аналогично роли стадии TFF2, этапа ILDF на фиг. 4). ADC, очищенные с помощью проточной колоночной хроматографии, могут затем подавать в процесс SPTFF для замены буфера на буфер для состава (например, TFF2, стадия II, этап ILDF на фиг. 5.) ADC, очищенные с помощью проточной колоночной хроматографии, могут затем подавать в процесс противоточной диафильтрации для замены буфера на буфер для состава.
[0137] В некоторых случаях параметры реакции процессов конъюгации в непрерывном потоке, предложенные в настоящем документе, могут быть быстро изменены или «импульсными». Например, при конъюгации в непрерывном потоке температура может быть быстро изменена, например, с помощью водяной бани, герметизированного реактора, нагревателя, термоэлектрического источника и/или изоляции секции катушек и/или трубок, через которые протекает реакция. Кроме того, при конъюгации в непрерывном потоке значение pH может быстро изменяться, например, путем добавления кислоты или основания. Соответственно, в некоторых случаях реакция конъюгации выполняется с использованием импульсного параметра. Использование импульсного параметра может, например, уменьшить время реакции (т.е. увеличить скорость реакции) без ущерба для качества продукта, временно погасить или остановить реакцию путем быстрого понижения температуры, стабилизировать конъюгат в растворе перед другим возмущением (например, добавлением другого химического реагента), в то время как более длительное воздействие одного и того же параметра может значительно снизить качество продукта или его стабильность.
[0138] В некоторых случаях реакция конъюгации подвергается воздействию измененной температуры (например, повышенной или пониженной) в течение определенного приращения времени в течение определенного количества раз. Например, в одном случае температуру повышают по меньшей мере на 2°С, по меньшей мере на 3°С, по меньшей мере, на 4°С или, по меньшей мере, на 5°С. Соответственно, температура может быть повышена или понижена по меньшей мере на 5°С, 10°С, 15°С, 20°С, 25°С, 30°С или 35°С. Например, температура может быть повышена или понижена на 5°С, 10°С, 15°С, 20°С, 25°С, 30°С или 35°С. Температура также может быть повышена или понижена на около 5-10°С, на около 10-15°С, на около 15-20°С, на около 20-25°С, на около 25-30°С или на около 30-35°С. Таким образом, например, температура может быть повышена (например, на от около 20°С) до повышенной температуры 25°С, 30°С, 35°С, 40°С, 45°С, 50°С или 55°C. Температура также может быть повышена (например, на от около 25°С) до повышенной температуры 30°С, 35°С, 40°С, 45°С, 50°С или 55°С. В некоторых случаях температура не превышает 55°С. В определенном случае температуру повышают (например, на от около 20°С) до повышенной температуры в диапазоне от около 35°С до около 55°С или до повышенной температуры в диапазоне от около 40°С до около 50°С. В некоторых случаях температуру повышают (например, от около 20°С) до повышенной температуры от около 60°С до около 70°С, до около 80°С, до около 90°С или до около 100°С (например, для кратковременного приращения, например, 10 секунд). В некоторых случаях температуру повышают (например, от около 20°С) до повышенной температуры в диапазоне от 60°С до 70°С, в диапазоне от 70°С до 80°С, в диапазоне от 80°С до 90°С или в диапазоне от 90°С до 100°С (например, для кратковременного приращения, например, 10 секунд). В некоторых случаях время, необходимое для повышения или понижения температуры до повышенной или пониженной температуры, составляет не более 2 минут. В некоторых случаях время, необходимое для повышения или понижения температуры до повышенной или пониженной температуры, составляет не более 1 минуты.
[0139] В некоторых случаях реакция конъюгации подвергается воздействию измененного значения pH (например, увеличенного или уменьшенного) в течение определенного приращения времени в течение определенного количества раз. Например, в одном случае значение рН увеличивают или уменьшают на около 1, на около 2, на около 3, на около 4 или на около 5. В одном случае значение рН увеличивают на от около 1 до около 2, на от около 2 до около 3, на от около 3 до около 4 или на от около 4 до около 5. Таким образом, например, значение рН можно увеличить (например, с от около 4) до около 5, около 6, около 7, около 8 или около 9. Значение рН также может быть увеличено (например, с от около 5) до около 6, около 7, около 8 или около 9. Таким образом значение рН также может быть уменьшено (например, с от около 9) до около 8, около 7, около 6, около 5 или около 4.
[0140] В некоторых случаях импульс (например, воздействие измененной температуры и/или значения pH) происходит в течение около 30 секунд, около 1 минуты, около 2 минут, около 3 минут, около 4 минут, около 5 минут, около 6 минут около 7 минут, около 8 минут, около 9 минут, около 10 минут, около 15 минут, около 30 минут, около часа, около 1,5 часов или около 2 часов. Импульс (например, воздействие измененной температуры и/или) также может происходить, например, в течение от около 30 секунд до около 1 минуты, в течение от около 1 минуты до около 2 минут, в течение от около 2 минут до около 3 минут, в течение от около 3 минут до около 4 минут, в течение от около 4 минут до около 5 минут, в течение от около 6 минут до около 7 минут, в течение от около 7 минут до около 8 минут, в течение от около 8 минут до около 9 минут или в течение от около 9 минут до около 10 минут. Импульс (например, воздействие измененной температуры и/или) также может происходить, например, в течение от 1 до 10 минут, в течение от около 1 до 15 минут, в течение от около 1 до 30 минут, в течение от около 1 минуты до 1 часа, в течение от около 1 минуты до около 1,5 часов или в течение от около 1 минуты до около 2 часов. Импульс (например, воздействие измененной температуры и/или) также может происходить, например, в течение от около 1 до 5 минут или от около 5 до около 10 минут, от около 10 до около 15 минут, от около 15 минут до около 30 минут, от около 30 минут до около 1 часа, от около 1 часа до около 1,5 часов или от около 1,5 часов до около 2 часов. В определенных случаях импульс (например, воздействие измененной температуры и/или pH) не превышает 2 часа, 1 часа, 30 минут, 20 минут или 15 минут.
[0141] В некоторых случаях импульс (например, воздействие измененной температуры и/или значения pH) происходит один раз. В определенных случаях импульс (например, воздействие измененной температуры и/или) повторяется два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз или десять раз. В некоторых случаях импульс (например, воздействие измененной температуры и/или) происходит от одного до пяти раз. В некоторых случаях импульс (например, воздействие измененной температуры и/или) происходит от двух до двадцати раз или от пяти до десяти раз.
[0142] Способы непрерывной обработки ADC (например, с использованием SPTFF и/или противоточной диафильтрации) могут использоваться с или без процессов поточного мониторинга (обсуждается ниже).
Технология автоматизации поточного процесса (поточная PAT)
[0143] В настоящем документе предложены технологии автоматизации поточного процесса, используемые для формирования и обработки конъюгатов антитело-лекарственное средство (ADC). Такие технологии предусматривают прямые измерения, которые могут исключать автономные анализы и снижать объем обработки материалов операторами. Поточный мониторинг можно использовать для контроля концентрации ADC (белка), а также удаления свободного лекарственного средства. Это может позволить нацеливаться на конечную концентрацию ADC на основе данных, полученных из поточных показаний, вместо того, чтобы основываться на конкретном объеме или количестве диаобъемов, используемых в процессах (например, процессах очистки). Внедрение PAT позволяет улучшить контроль и выявляемость (например, изменения во время работы в установившемся режиме можно использовать для выявления проблем до того, как это повлияет на качество продукта), а использование нескольких модулей PAT (например, FlowVPE, УФ-датчики, рН-метр, измеритель проводимости, датчики давления или расходомеры) может обеспечить надежную производительность процесса при выполнении отдельных операций.
[0144] Поточный мониторинг можно использовать, например, для контроля скоростей потока в подающем потоке из любого насоса, например, в реакции in situ и/или реакции конъюгации ADC (например, в реакции непрерывной конъюгации или в реакции серийной конъюгации). Поточный мониторинг можно использовать, например, для контроля концентрации компонента, добавляемого в реакцию in situ и/или реакцию конъюгации ADC (например, в реакцию непрерывной конъюгации или в реакцию серийной конъюгации). Такой мониторинг может обеспечить адекватный контроль стехиометрии реакций. Поточный мониторинг может контролировать скорость потока или концентрацию, например, антитела или его антигенсвязывающего фрагмента, лекарственного средства, линкера, лекарственного средства, присоединенного к линкеру, антитела или его антигенсвязывающего фрагмента, присоединенного к линкеру и/или буфера для конъюгации. Поточный мониторинг может контролировать скорость потока концентрации антитела или его антигенсвязывающего фрагмента в буфере для реакции конъюгации.
[0145] Поточный мониторинг также можно использовать, например, для определения, когда остановить реакцию конъюгации, например, путем остановки для добавления буфера для конъюгации, путем остановки циркуляции буфера для конъюгации и/или начала вымывания или удаления буфера для конъюгации. В некоторых вариантах осуществления, предложенных в настоящем документе, может быть использован поточный мониторинг неконъюгированного лекарственного средства или неконъюгированного лекарственного средства, присоединенного к линкеру. Измерения неконъюгированного лекарственного средства или неконъюгированного лекарственного средства, присоединенного к линкеру, можно использовать для определения среднего количества лекарственных средств на антитело (DAR), достигаемого в реакции конъюгации. Таким образом, реакция конъюгации может быть остановлена при достижении целевого DAR.
[0146] Поточный мониторинг также можно использовать для контроля концентрации и/или очистки ADC. Например, поточный мониторинг можно использовать до или после процессов ILC и/или ILDF TFF2, показанных на иллюстративной фиг. 4, или до, или после процессов ILC или ILDF TFF3, показанных на иллюстративной фиг. 10. При концентрации и/ или очистке могут использовать фильтрацию (например, ультрафильтрацию, дифильтрацию). Фильтрация может представлять собой фильтрацию в тангенциальном потоке, включая однопроходную фильтрацию в тангенциальном потоке (SPTFF). Фильтрация может представлять собой противоточную диафильтрацию. При использовании для контроля фильтрации, поточный мониторинг можно использовать для измерения аналита в ретентате или пермеате. Таким образом, например, для оценки степени очистки ADC можно использовать поточный мониторинг неконъюгированного лекарственного средства или неконъюгированного лекарственного средства, присоединенного к линкеру в ретентате. Уровни неконъюгированного лекарственного средства или неконъюгированного лекарственного средства, присоединенного к линкеру, могут быть высокими в ретентате вскоре после реакции конъюгации, но низкими в ретентате после очистки (см., например, фиг. 12). Поточный мониторинг ADC в ретентате или пермеате можно использовать для оценки потери ADC во время процессов концентрирования и/или очистки (см., например, фиг. 12).
[0147] При очистке также можно использовать хроматографию (например, проточную колоночную хроматографию). Поточный мониторинг в конце хроматографической колонки может, например, измерять уровни ADC и его можно использовать для определения перегруза колонки или прорыва ADC.
[0148] Поточный мониторинг также можно использовать для измерения значения pH, которое можно использовать, например, для определения полноты замены буфера (см., например, фиг. 12).
[0149] Иллюстративные технологии поточного мониторинга включают использование, например, проточной ячейки с преобразованием Фурье в инфракрасной области (FTIR), высокоэффективной жидкостной хроматографии (ВЭЖХ) или ультраэффективной жидкостной хроматографии (УЭЖХ).
[0150] В технологиях поточного мониторинга может быть использован, например, датчик FlowVPE или УФ-датчик. В некоторых вариантах осуществления используется FlowVPE для выполнения поточного мониторинга. Во FlowVPE используется проточная ячейка для непрерывного мониторинга.
[0151] Эффективность фильтрации в тангенциальном потоке (например, однопроходной фильтрации в тангенциальном потоке (SPTFF) можно контролировать в потоке, используя FlowVPE, УФ-датчик, рН-метр, измеритель проводимости, датчик давления, расходомер и т.д. Эффективность противоточной диафильтрации также можно контролировать в потоке, используя FlowVPE, УФ-датчик, рН-метр, измеритель проводимости, датчик давления, расходомер и т. д.
[0152] Процессы поточного мониторинга можно использовать в сочетании с процессами непрерывной конъюгации (обсуждаемыми выше), например, с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации,или с процессами серийной конъюгации (которые известны в данной области техники).
IV Конъюгаты с антитело-лекарственное средство (ADC)
[0153] Как предусмотрено в настоящем документе, конъюгаты антитело-лекарственное средство (ADC) могут содержать связывающий клетки агент, линкер и лекарственное средство.
[0154] Связывающий клетки агент может представлять собой антитело или его антигенсвязывающий фрагмент, например, моноклональное антитело или его антигенсвязывающий фрагмент. Связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) может быть гуманизированным. Связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) может быть человеческим.
[0155] Связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) может специфически связываться с CD37, CD33, FOLR1, CD123, CD19, cMET, ADAM9 или HER2 человека.
[0156] Связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) может содержать шесть CDR антитела, приведенные в таблице 1.
Таблица 1: Последовательности определяющих комплементарность областей
[0157] Связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) может содержать вариабельную область тяжелой цепи и/или вариабельную область легкой цепи антитела, приведенную в таблице 2. В некоторых вариантах осуществления связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) содержит CDR (например, CDR согласно определению по Kabat, AbM или Chothia) вариабельной области тяжелой и вариабельной области легкой цепи антитела, приведенного в таблице 2.
Таблица 2: Последовательности вариабельных областей тяжелой цепи и вариабельных областей легкой цепи антитела
[0158] Связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) может содержать тяжелую цепь и/или легкую цепь антитела, приведенного в таблице 3.
Таблица 3: Последовательности тяжелой и легкой цепи антитела
[0159] В некоторых вариантах осуществления антитело к FOLR1 кодируется плазмидами, депонированными в Американской коллекции типовых культур (ATCC), расположенной по адресу: 10801 University Boulevard, Manassas, VA 20110, 7 апреля 2010 г. в соответствии с условиями Будапештского договора и, депонированными под номерами ATCC PTA-10772 и PTA-10773 или 10774.
[0160] Связывающий клетки агент (например, антитело или его антигенсвязывающий фрагмент) может представлять собой CD37-3, huMovl9, Z4681A, G4732A, huB4, huCMET-27, huADAM9 или Герцептин (трастузумаб).
[0161] Лекарственное средство может представлять собой цитотоксический агент. Цитотоксическим агентом может быть любое соединение, которое приводит к гибели клетки, или вызывает гибель клетки, или каким-либо образом снижает жизнеспособность клеток и включает, например, мейтансиноиды, аналоги мейтансиноидов, бензодиазепины (например, индолино-бензодиазепин (IGN) или пирролобензодиазепин (PBD)), таксоиды, CC-1065 и аналоги CC-1065, дуокармицины и аналоги дуокармицина, энедиены, такие как калихеамицины, доластатин и аналоги доластатина, включая ауристатины, производные томаймицина, производные лептомицина, метотрексат, цисплатин, карбоплатин, даунорубицина, доксорубицин, винкристин, винбластин, мелфалан, митомицин С, хлорамбуцил и морфолино-доксорубицин. В одном варианте осуществления мейтансиноид может представлять собой DM1. В другом варианте осуществления мейтансиноид может представлять собой DM4. В одном варианте осуществления индолинобензодиазепин может представлять собой DGN462. В одном варианте осуществления индолинобензодиазепин может представлять собой DGN549. В других вариантах осуществления пирролобензодиазепин может представлять собой талирин, тезирин, SJG136 или SGD1882.
[0162] Подходящие связывающие группы хорошо известны в данной области техники и включают, например, дисульфидные группы, тиоэфирные группы, кислотолабильные группы, фотолабильные группы, пептидазо-лабильные группы и эстеразо-лабильные группы. Линкерные молекулы включают, например, N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) (см., например, Carlsson et al., Biochem. J., 173: 723-737 (1978)), N-сукцинимидил-4-(2-пиридилдитио)бутаноат (SPDB) (см., например, патент США № 4563304), N-сукцинимидил-4-(2-пиридилдитио)-2-сульфобутаноат (сульфо-SPDB) (см. публикацию США № 20090274713), N-сукцинимидил-4-(2-пиридилдитио)пентаноат (SPP) (см., например, регистрационный номер CAS 341498-08-6), 2-иминотиолан или ацетилсукциновый ангидрид. Линкер может представлять собой SMCC, sSPDB или пептидный линкер.
[0163] ADC может содержать несколько лекарственных средств на антитело. Количество лекарственных средств часто называют соотношением лекарственного средства к антителу (DAR). В одном аспекте количество молекул лекарственного средства, которые могут быть присоединены к связывающему клетки агенту, может составлять в среднем от около 2 до около 8. Таким образом, в качестве примера, способы, предложенные в настоящем документе, могут нацеливаться на DAR от около 3 до около 4.
[0164] В некоторых вариантах осуществления ADC представляет собой «IMGN853». В контексте данного документа термин «IMGN853» относится к ADC, содержащему антитело huMovl9, линкер сульфо-SPDB и мейтансиноид DM4. HuMovl9 (M9346A) содержит тяжелую цепь, содержащую ту же аминокислотную последовательность, что и аминокислотная последовательность тяжелой цепи, кодируемая плазмидой, депонированной в Американской коллекции типовых культур (ATCC) как PTA-10772, и (ii) легкую цепь, содержащую ту же аминокислотную последовательность, что и аминокислотная последовательность легкой цепи, кодируемая плазмидой, депонированной в ATCC как PTA-10774. IMGN853 описан в WO2011/106528, содержание которой полностью включено в данное описание посредством ссылки.
[0165] В некоторых вариантах осуществления ADC представляет собой «IMGN779». В контексте данного документа термин «IMGN779» относится к ADC, содержащему антитело Z4681A, линкер сульфо-SPDB и индолинобензодиазепин DGN462.
[0166] В некоторых вариантах осуществления ADC представляет собой «IMGN632». В контексте данного документа термин «IMGN632» относится к составу ADC, показанному на фиг. 11. Композиция ADC содержит ADC, содержащие в среднем от 1,5 до 2,1 цитотоксических агентов DGN549-C на антитело huCD123-6Gv4.7 («G4723A») в сульфированном варианте (фиг. 11, верхняя панель). Композиция ADC также может содержать несульфированный ADC (моноиминовая структура, показанная на фиг. 11, нижняя панель).
[0167] Иллюстративные ADC, которые связываются с ADAM9, раскрыты в PCT/US2017/067823 (опубликованной как WO2018119196), которая полностью включена в настоящий документ посредством ссылки. Иллюстративные ADC, которые связываются с ADAM9, также раскрыты в заявке на патент США № 62/691,342, поданной 28 июня 2018 года, которая полностью включена в настоящий документ посредством ссылки. Иллюстративные ADC, которые связываются с cMET , раскрыты в PCT/US2018/012168 (опубликованной как WO2018129029), которая полностью включена в настоящий документ посредством ссылки. Иллюстративные ADC, которые связываются с CD19, раскрыты в WO2012156455, которая полностью включена в настоящий документ посредством ссылки.
V. Примеры
Пример 1: Процесс непрерывной конъюгации для конъюгации IMGN853
[0168] Для сокращения времени обработки и улучшения выхода для крупномасштабного производства конъюгатов антитело-лекарственное средство (ADC) был разработан процесс непрерывной конъюгации. При непрерывной конъюгации этапы обработки происходят одновременно. Рециркуляция конъюгата на этапах очистки и замены буфера, а также промежуточные этапы выдержки, которые использовали во время серийной конъюгации, были устранены с помощью непрерывной конъюгации. Таким образом, процесс протекал непрерывно в течение 4-5 дней, а конъюгат составляли непосредственно после прохождения этапов очистки TFF. Кроме того, системы поточной процессно-аналитической технологии (PAT) использовали для прямых измерений конъюгата, поэтому автономные анализы и обработка материалов операторами были исключены. Кроме того, поскольку время обработки было сокращено, была устранена потребность в большом по размеру оборудовании для производства больших объемов конъюгатов: меньшего по размеру оборудования и более коротких сроков обработки было достаточно для производства больших объемов продукта. Кроме того, для заданного количества произведенного конечного конъюгата профиль качества продукта был более постоянным при получении с использованием непрерывной обработки. Напротив, требование к нескольким сериям при конъюгации в общем объеме создает потенциал для повышения межсерийной вариабельности качества продукции.
[0169] Процесс непрерывной конъюгации для конъюгации ADC «IMGN853» подробно описан в блок-схеме последовательности операций, представленной на фиг. 4. IMGN853 содержит антитело к FOLR1 («huMovl9»), конъюгированное с мейтанзиноидными лекарственными средствами DM4 через сульфо-SPDB-линкеры. IMGN853 описан в WO 2011/106528, содержание которой полностью включено в данное описание посредством ссылки.
Пример 1A: Потоковые химические исследования
[0170] Обычная конъюгация IMGN853 включает реакцию in situ между мейтансиноидным лекарственным средством DM4 и линкером N-сукцинимидил-4-(2-пиридилдитио)-2-сульфобутаноат (sSPDB) в 70% N,N-диметилацетамиде (ДМА). Соответствующие объемы исходного раствора DM4 и sSPDB добавляют в сосуд для проведения реакции in situ. Дополнительный ДМА (растворитель) добавляют в сосуд in situ для получения 70% ДМА по объему. Конечный реагент, добавляемый в сосуд для реакции in situ, представляет собой реакционный буфер. После добавления реакционного буфера инициируют реакцию in situ с перемешиванием в течение 60-120 минут. Затем компоненты in situ добавляют в сосуд для конъюгации, содержащий антитело M9346A (huMovl9), которое подвергали диафильтрации в реакционный буфер. Все компоненты смешивают и реакция конъюгации протекает при осторожном перемешивании в течение ночи с получением желаемого конъюгата с целевым соотношением лекарственное средство-антитело (DAR), равным 3,4.
[0171] В этом исследовании была проведена непрерывная конъюгация IMGN853. В реакции непрерывной конъюгации использовали все те же стехиометрические параметры IMGN853 с одним примечательным исключением. Значение pH реакционного буфера для реакции конъюгации было увеличено с 7,6 до 8,7. Значение pH буфера для реакции in situ не изменилось и осталось на уровне 7,6. Увеличение значения рН было установлено для увеличения кинетики реакции конъюгации. Вместо целевых 18 часов для реакции конъюгации в буфере с более высоким значением pH конъюгат создали приблизительно за 4 часа, чтобы обеспечить более быстрое считывание и более гибкие экспериментальные протоколы.
[0172] В экспериментах с непрерывной конъюгацией использовали шприцевые насосы для непрерывного добавления реагентов. Установка показана на фиг. 5. Были использованы три шприцевых насоса. Первый шприцевой насос контролировал добавление компонентов in situ, растворенных в ДМА. Они включали DM4 (полезная нагрузка), sSPDB (линкер) и ДМА (дополнительный растворитель). Эти три компонента объединяли в стехиометрических соотношениях и затем вводили в шприц Hamilton Gastight объемом 2,5 мл. Второй шприцевой насос дозировал добавление буфера для реакции in situ. Использовали пластиковый шприц BD объемом 5 мл. 1/16 трубку из PEEK использовали для исследований непрерывной конъюгации. Линии подачи буфера для реакции in situ и компонентов ДМА осуществляли подачу во встроенный статический смеситель для обеспечения адекватного смешивания двух реагентов. Эти два питающих потока объединяются и выходят через одну часть трубки из статического смесителя из одного и того же материала трубки. Скорости потока для буфера in situ и компонентов ДМА составляли 952,9 нл/мин и 2,2233 мкл/мин, соответственно. Для целевой 90-минутной реакции in situ потребовалось 18,6 сантиметров трубки из PEEK на основе скорости потока для двух входных потоков и площади поперечного сечения используемой трубки. Эту длину трубки из PEEK, где происходила реакция in situ, подавали во второй встроенный статический смеситель. Другое входное отверстие для второго статического смесителя было от третьего шприцевого насоса. Третий шприц контролировал добавление антитела и буфера для реакции конъюгации (рН 8,7). Антитело и буфер для реакции конъюгации объединяли и набирали в пластиковый шприц BD объемом 30 мл. Ту же самую трубку из PEEK использовали для подачи антитела и буфера для реакции конъюгации при скорости потока 24,615 мкл/мин. Подобно статическому смесителю in situ, второй статический смеситель обеспечил хорошее перемешивание компонентов реакции конъюгации и объединение их в единый выходящий поток. Реагенты для конъюгации покидали статический смеситель в части той же трубки из PEEK, длина которой составляла 4,3 метра, с достижением целевой продолжительности реакции конъюгации, равной 4 часам.
[0173] Исследования выполняли путем заполнения всех трех шприцев до запуска любого потока. Сначала насосы буфера для реакции in situ (шприц 2) и компонентов ДМА (шприц 1) запускали одновременно. Приблизительно через 90 минут запускали насос 3 (антитело и буфер для реакции конъюгации). Приблизительно через пять часов после запуска первых двух насосов конъюгат элюировался из части трубки из PEEK длиной 4,3 метра. Анализ образцов осуществляли путем сбора образцов непосредственно с конца (т.е. объединенные образцы собирали из хорошо смешанного пула конъюгата). Для измерения расхода питающих потоков in situ и конъюгации (из любого насоса) могут быть дополнительно использованы расходомеры. Расходомеры служат механизмом процессно-аналитической технология (PAT) для обеспечения адекватного контроля над стехиометрией реакций.
[0174] Результаты первого исследования непрерывных конъюгаций IMGN853 показаны в таблице 4.
Таблица 4: Результаты первого исследования непрерывной конъюгации IMGN853.
[0175] Исследование показало, что качество продукта непрерывной конъюгации было сопоставимо с качеством контрольного (серийного) продукта, выполненного параллельно. Для достижения равновесного состояния качества продукта потребовалось некоторое время, о чем свидетельствует более низкое соотношение лекарственное средство-антитело (DAR) в «ранний» момент времени. Это согласовывалось со вторым исследованием, в котором 30-минутный образец также имел немного более низкий показатель DAR. Через 3 часа во втором исследовании качество продукта достигло равновесного состояния при целевом DAR (по сравнению с параллельным серийным контролем). В дополнение к DAR, качество продукта также было сопоставимо в отношении уровней мономеров и свободных лекарственных средств. Вместе эти результаты указывают на то, что процесс непрерывной конъюгации показал хорошие результаты и был сопоставим с параллельным серийным контролем в отношении качества продукта.
[0176] Результаты второго исследования показаны в таблице 5.
Таблица 5: Результаты второго исследования непрерывной конъюгации IMGN853.
[0177] В этом исследовании использовали те же параметры, что и в исследовании, приведенном выше, но процесс выполняли непрерывно в течение 40 часов, чтобы показать, что установку оборудования на 100 мг можно использовать для создания в 10 раз большего количества продукта при более длительном процессе. Результаты показали, что конъюгат достиг равновесного состояния в период между 30 минутами и 3 часами элюирования конъюгата и был сопоставим с параллельным серийным контролем при проведении ЭХ и анализа свободных лекарственных средств. Качество продукта через три часа было практически идентично конъюгату, элюирующемуся через 40 часов, что указывало на непрерывный процесс, выполняемый последовательно, пока реагенты подавались в реакционную трубку.
[0178] В производственных условиях насосы для каждого отдельного реагента могут использоваться для разделения исходных растворов. Вместо объединения DM4, sSPDB или ДМА в один питающий поток каждый из исходных растворов может подаваться отдельно в сосуд для сбора или непосредственно в реакцию in situ. То же самое может быть применимо для антитела и буфера для реакции конъюгации. Исходный раствор антитела можно подавать с использованием специального насоса, в то время как отдельный насос контролирует добавление буфера для реакции конъюгации в соответствующем объемном соотношении к другим компонентам реакции конъюгации.
[0179] Другие механизмы PAT могут быть использованы для мониторинга реакции in situ или конъюгации по мере ее протекания. Проточную ячейку с преобразованием Фурье в инфракрасной области (FTIR) можно использовать в потоке для контроля эффективности реакции in situ или конъюгации. Кроме того, несколько проточных ячеек FTIR или аналогичного инструмента PAT могут быть размещены в промежуточных точках вдоль трубок реакции in situ и конъюгации для контроля реакции по мере ее протекания. Образование желаемого конъюгата можно измерить от начала реакции до самого конца. Любое существенное изменение в сигнале PAT затем может быть использовано для определения того, где в реакции in situ или конъюгации (начало, середина или конец) произошла ошибка. Для конъюгата альтернативный механизм PAT может представлять собой быстрый инструмент на основе высокоэффективной жидкостной хроматографии (ВЭЖХ) (ультраэффективной жидкостной хроматографии (УЭЖХ)) с УФ-датчиком или без него. Анализ на основе ВЭЖХ может быть использован для измерения DAR, в то время как встроенные в поток УФ-датчики могут контролировать концентрацию антител в реакции конъюгации.
Пример 1B: Исследования однопроходной фильтрации в тангенциальном потоке
[0180] Обычную фильтрации в тангенциальном потоке (TFF) используют дважды во время процесса получения лекарственного вещества IMGN853. Сначала проводят TFF, чтобы буферизовать составленное антитело в буфер для реакции конъюгации до начала реакции конъюгации (TFF1). После реакции конъюгации TFF используют для удаления остаточных примесей из смесителя для неочищенной реакции и замены буфера в конъюгате с буфера для реакции конъюгации на базовый буфер для состава (TFF2). Был разработан непрерывный процесс для замены обоих этих обычных этапов TFF методом однопроходной TFF (SPTFF). В непрерывной SPTFF использовали технологии поточного концентрирования (ILC) и поточной диафильтрации (ILDF) от Pall Life Sciences.
[0181] Для TFF1 антитело подвергали диафильтрации в течение 8 диаобъемов при 30 мг/мл в ходе обычной обработки. Входящее антитело составляли в концентрации 60 мг/мл и разбавляли перед диафильтрацией в ходе обычной обработки TFF1. В ходе непрерывной обработки составленное антитело в концентрации 60 мг/мл подавали в Т-соединитель, где другой насос добавлял буфер для реакции конъюгации для разбавления антитела до целевой концентрации 30 мг/мл. После Т-соединителя в модуль ILDF подавали поток в одном питающем потоке антитела при концентрации 30 мг/мл. Буферный насос для диафильтрации ILDF контролировал добавление буфера для реакции конъюгации в модуль ILDF так, чтобы обмен буфера был достигнут за один проход. Антитело, выходящее из ILDF, находилось в концентрации 30 мг/мл в буфере для реакции конъюгации.
[0182] Управление PAT может быть реализовано в различных местах для контроля и управления этой типовой операцией. Датчик FlowVPE или УФ-датчик может быть помещен в питающий поток составленного антитела (60 мг/мл), питающий поток разбавленного антитела (30 мг/мл) и/или в антитело с замененным буфером на буфер для реакции конъюгации. Датчик FlowVPE или УФ-датчик можно использовать для измерения концентрации антител в различных питающих потоках. Кроме того, расходомеры на всех питающих потоках можно использовать для контроля и регулировки скорости потока любого компонента, чтобы обеспечить замену буфера в ILDF при концентрации 30 мг/мл. Кроме того, можно использовать датчик проводимости или pH после ILDF, чтобы обеспечить завершение замены буфера антитела на буфер для реакции конъюгации.
[0183] После конъюгирования обычный TFF2 как правило выполняют в три этапа, все из которых происходят в ходе одной типовой операции. Неочищенную реакционную смесь после конъюгации сначала концентрируют ультрафильтрацией до 30 мг/мл (м 15 мг/мл после реакции конъюгации). Затем конъюгат подвергают диафильтрации в течение 4 диаобъемов против буфера для реакции конъюгации на так называемой стадии I TFF2. На стадии I остаточные примеси удаляют из неочищенной реакционной смеси. Непосредственно после стадии I выполняют стадию II путем диафильтрации конъюгата против 8 диаобъемов буфера для базового состава. Стадия II разработана как стадия замены буфера, но не способствует дополнительному удалению остаточных примесей.
[0184] Для непрерывного процесса, использующего SPTFF, были оценены три отдельных этапа. Сначала был использован модуль ILC для концентрирования. ILC следовал за трубкой реакции конъюгации. За один проход конъюгат, поступающий в ILC при концентрации 15 мг/мл, концентрировали до 30 мг/мл, а удаляемый объем направляли в отходы. Коэффициент концентрации, использованный для IMGN853 и описанный в этом примере, был равен двум (2), но и другие коэффициенты концентрации могли бы использоваться для достижения того же результата концентрирования конъюгата перед диафильтрацией.
[0185] После ILC питающий поток исходного конъюгата в концентрации 30 мг/мл подавали в первый модуль ILDF (ILDF1), который должен был имитировать стадию I. Подаваемый буфер для диафильтрации в ILDF1 представлял собой буфер для реакции конъюгации, и его добавляли в соответствующем объеме для достижения желаемого количества диаобъемов за один проход. Для IMGN853 стадия I была достигнута через четыре обычных диаобъемов. В исследованиях для подтверждения концепции оценивали удаление остаточных примесей как функцию с числом диаобъемов путем регулирования скорости потока насоса подачи буфера для диафильтрации.
[0186] После ILDF1 конъюгат оставался в концентрации 30 мг/мл, но имел значительно более низкие концентрации присутствующих примесей. Выходной поток из ILDF1 подавали в ILDF2, где буфером для диафильтрации был буфер базового состава. Конъюгат поступал в ILDF в концентрации 30 мг/мл в буфере для реакции конъюгации (pH 7,6-8,7) и выходил из ILDF2 в концентрации 30 мг/мл в буфере с pH 5,0.
[0187] В первоначальных исследованиях для подтверждения концепции, выполненных с использованием модулей ILDF Pall Life Sciences, использовали модуль T01, который имеет площадь мембраны 0,11 м2. Модуль оценивали при скоростях потока от 1 до 4 мл/мин для подачи конъюгата. Скорости подачи буфера для диафильтрации варьировали таким образом, что количество диаобъемов отличалось. Обработку от одного до тринадцати диаобъемов оценивали с использованием ILDF. Для всех исследований материал конъюгата получали с использованием обычной серийной обработки и замораживали с разделением на аликвоты. Свободные соединения мейтансиноидов определяли количественно до замораживания и снова после размораживания (до обработки). Неочищенную реакционную смесь подавали в ILC. Скорость потока ретентата измеряли с использованием расходомера для расчета коэффициента концентрации, достигнутого в модуле. Процесс IMGN853 и все исследования были выполнены с использованием целевого коэффициента концентрации, равного двум.
[0188] Первое исследование с ILDF было проведено для оценки очистки от остаточных примесей из реакции конъюгации IMGN853. Для получения материала для исследования с использованием целевых условий реакции проводили конъюгацию в общем объеме. Неочищенную реакционную смесь после конъюгации фильтровали, аликвотировали и замораживали перед использованием. После размораживания неочищенную реакционную смесь концентрировали с использованием однопроходного модуля ILC с целевым коэффициентом концентрации, равным двум. Неочищенная реакционная смесь имела концентрацию 15 мг/мл, а целевая концентрация ретентата в конъюгате после ILC составляла 30 мг/мл. Конъюгат после ILC затем разбавляли до 10 мг/мл, используя буфер для реакции конъюгации, для тестирования модуля ILDF при низкой начальной концентрации. Разведение с 30 мг/мл до 10 мг/мл до введения в ILDF эффективно снижало нагрузку примесями свободных лекарственных средств в подаче конъюгата. Это видно на фиг. 6, иллюстрирующей уровни примесей свободных лекарственных средств для четырех основных видов примесей до и после ILC. Неочищенная реакционная смесь после конъюгации имеет высокие уровни примесей. После концентрирования при помощи ILC и последующего разбавления до 10 мг/мл концентрацию примесей снижали до приблизительно 1/3 начальной концентрации.
[0189] Конъюгат с концентрацией 10 мг/мл подавали в модуль ILDF T01 со скоростью 4 мл/мин с целевыми 7 диаобъемами обработки для стадии I. Буфер для диафильтрации на стадии I представлял собой буфер для реакции конъюгации (15 мМ фосфат калия, 2 мМ ЭДТА, pH 8,7). Образцы были взяты из линии ретентата и проанализированы на концентрацию белка, чтобы определить, когда конъюгат элюировался из системы. После того, как концентрация достигла равновесного состояния, образцы были взяты из линии ретентата и проанализированы методом ОФ-ВЭЖХ для количественного определения уровней примесей свободного лекарственного средства и расчета клиренса в ходе ILDF. На Фиг. 6 показаны результаты для трех образцов, взятых с этапа ILDF1: ранний, поздний и объединенный. Ранний образец был взят вскоре после достижения равновесного состояния при ILDF. Уровни примесей во всех трех образцах были значительно ниже пределов спецификации. Снижение уровня свободных лекарственных средств по сравнению с ILDF было значительным и приемлемым с точки зрения производительности процесса.
[0190] После первого прохождения ILDF против буфера для реакции конъюгирования для имитации стадии I TFF2 полученный объединенный конъюгат затем снова пропускали через модуль для имитации стадии II. Перед стадией II модуль промывали, а затем подвергали предварительной диафильтрации против буфера для базового состава (10 мМ ацетат, 9% сахароза, рН 5,0). Конъюгат подавали со скоростью 4 мл/мин, а скорость потока подачи буфера для диафильтрации была установлена на достижение 13 диаобъемов в ходе ILDF. Это число было выбрано так, чтобы оно соответствовало восьми диаобъемам для обычной обработки TFF
[0191] Подобно ILDF1, образцы отбирали из линии ретентата и анализировали для измерения концентрации антитела. После обнаружения концентрации белка, продукт собирали и периодически отбирали образцы из линии ретентата. После достижения системой равновесной стадии, образцы, отобранные на линии ретентата, были проанализированы методов ОФ-ВЭЖХ для количественного определения уровней остаточных примесей и расчета клиренса в ходе ILDF2. После того, как продукт был пропущен через ILDF и собран, объединенный материал был отфильтрован, а затем проанализирован методом ЭХ и ОФ-ВЭЖХ. Результаты для всех образцов из ILDF2, имитирующих замену буфера на стадии II во время обычной обработки TFF2, показаны на фиг. 6. Все уровни свободного лекарственного средства составляли <1%, что значительно ниже конечной спецификации для очищенного лекарственного вещества (ЛВ). Эти результаты демонстрируют, что непрерывная очистка конъюгата IMGN853 с помощью SPTFF возможна и способна генерировать очищенный конъюгат с приемлемым качеством продукта, измеренным методом ЭХ и ОФ-ВЭЖХ.
[0192] В следующем исследовании была исследована способность клиренса ILDF к удалению остаточных примесей при концентрации подачи 15 мг/мл. Эта концентрация была выбрана после того, как первое исследование показало адекватный клиренс при 10 мг/мл. Во время этого исследования конъюгат не был обработан методом ILC. Неочищенную реакционную смесь конъюгата из конъюгации в общем объеме размораживали и подавали непосредственно в ILDF. Был использован модуль ILDF T01, а скорость подаваемого потока составляла 4 мл/мин. Буфер для реакции конъюгации использовали для буфера для диафильтрации, а скорость подаваемого потока была установлена для первоначального достижения одного диаобъема. Когда конъюгат был обнаружен в ретентате путем измерения концентрации, образцы были взяты из линии ретентата и проанализированы методом ОФ-ВЭЖХ для количественного определения уровней свободного лекарственного средства. Результаты показаны на фиг. 7. Необработанная реакционная смесь после конъюгации имела высокие исходные уровни, которые соответствовали предыдущим конъюгациям. После одного прохода, эквивалентного одному диаобъему обработки, общие уровни свободного лекарственного средства снизились с приблизительно 26% в подающем потоке до 7% в ретентате.
[0193] Затем скорость потока для диафильтрации была увеличена до достижения семи диаобъемов, что сопоставимо с целевыми четырьмя диаобъемами для обычной обработки TFF. После достижения системой равновесного состояния, уровни свободного лекарственного средства были измерены в ретентате. Как показано на фиг. 4, уровни свободного лекарственного средства значительно снижались после одного прохода в этих условиях обработки. Конечные уровни общего количества свободных лекарственных средств были ниже 1%, что находится в пределах допустимого диапазона для качества конечного продукта. Эти результаты указывают на то, что ILDF хорошо работает при концентрации подаваемого конъюгата 15 мг/мл и удаляет примеси до уровней ниже предельных значений при обработке для семи диаобъемов.
[0194] Для сравнения, значения очистки от примесей свободного лекарственного средства в процессе серийной очистки TFF2 показаны на фиг. 8. После 4 диаобъемов обычной серийной обработки TFF2 (цельные прямоугольники) общий уровень примесей свободного лекарственного средства составлял 3,4%. После 7 диаобъемов обработки SPTFF (заштрихованные прямоугольники), что эквивалентно 4 стандартным диаобъемам, общий уровень свободного лекарственного средства составил 0,7%. Одним из важных различий между этими двумя исследованиями была концентрация конъюгата во время очистки. Для исследования непрерывной обработки подача конъюгата в модуль ILDF составляла 15 мг/мл. Обычную серийную обработку TFF проводили при 30 мг/мл.
[0195] ILDF хорошо работает при концентрации 15 мг/мл, не создавая проблемы с давлением или качеством продукта, поэтому концентрацию конъюгата в подаче увеличивали для оптимизации выхода ILDF в последующем исследовании. Целевая концентрация подаваемого конъюгата составляла 30 мг/мл. Неочищенную реакционную смесь сначала пропускали через ILC с целевым коэффициентом концентрации, равным двум. Конъюгат вводили в ILC при 15 мг/мл и концентрировали до целевого значения 30 мг/мл. Полученный конъюгат в концентрации 30 мг/мл собирали перед подачей в ILDF. Буфер для диафильтрации для ILDF представлял собой буфер для реакции конъюгации, а скорость потока подачи была установленана достижение семи диаобъемов. Скорость потока подачи для конъюгата при 30 мг/мл составляла 4 мл/мин в модуле ILDF T01. После обнаружения белка в потоке ретентата, конъюгат собирали и отбирали образцы. Системе позволяли достичь равновесного состояния до того, как образец был проанализирован методом ОФ-ВЭЖХ для количественного определения уровней свободного лекарственного средства и расчета клиренса в ходе ILDF. Результаты показаны на фиг. 9. Уровни свободного лекарственного средства после ILDF сравнивали с образцами, взятыми до ILC (15 мг/мл неочищенной реакционной смеси) и после ILC (30 мг/мл). Уровни свободного лекарственного средства после ILC немного увеличились, что было связано с незначительным чрезмерным концентрированием конъюгата. Конъюгат после ILC измеряли при 31 мг мл, что указывало на коэффициент концентрации 2,1. Полученные уровни свободного лекарственного средства были немного выше, но для точной оценки ILDF конъюгат разбавляли до 30 мг/мл, добавляя соответствующий объем буфера для реакции конъюгации к объединенному материалу перед подачей в ILDF.
[0196] Образец, отобранный и проанализированный методом ОФ-ВЭЖХ из ILDF со скоростью 4 мл/мин, показал клиренс соединений свободного лекарственного средства из образца до ILDF/после ILC. Тем не менее, концентрация конъюгата в ретентате была измерена на уровне приблизительно 20 мг/мл. Было указано, что снижение концентрации конъюгата объясняется агрегацией и накоплением продукта на мембране в кассете. Чтобы уменьшить засорение и снизить давление в системе, скорость потока подачи была снижена до 3 мл/мин. Соответственно, скорость потока насоса подачи буфера для диафильтрации также была уменьшена, так что для обработки было установлено семь диаобъемов. После снижения скорости потока на входе в ILDF, из ретентата был отобран образец и проанализирована концентрация и уровни свободного лекарственного средства. Было определено, что концентрация образца составляет 22,5 мг/мл, а уровни свободного лекарственного средства были сопоставимы с образцом, измеренным при 4 мл/мин. В совокупности это указывает на то, что для очистки конъюгата достаточно 7 диаобъемов обработки, но наблюдалась максимальная концентрация конъюгата 23 мг/мл в ретентате.
Пример 2: Процесс непрерывной конъюгации для конъюгации IMGN632
[0197] Процесс непрерывной конъюгации для конъюгации ADC «IMGN632» подробно описан в блок-схеме последовательности операций, представленной на фиг. 10. IMGN632 содержит анти-CD123 антитело («G4732A»), связанное с цитотоксической полезной нагрузкой DGN549-C. IMGN632 показан на фиг. 11.
Пример 2A: Потоковые химические исследования
[0198] Установка реакции аналогична установке, показанной на фиг. 5. Первый шприц содержит ДНК-алкилирующую полезную нагрузку IGN «DGN549C», растворенную в ДМА. Второй шприц содержит бисульфитный исходный раствор и 50 мМ сукцинат, рН 3,3 в соответствующих объемных соотношениях. Оба эти питающие потоки смешиваются в статическом встроенном смесителе для инициирования реакции сульфирования. DGN549C нацелен на конечную концентрацию 1 мМ в смешанном потоке. Полученная смесь представляет собой 50 мМ сукцинат, рН 3,3 и 50% ДМА с 1,4 молярным избытком отношения бисульфита к DGN. Два питающих потока выходят из статического встроенного смесителя в один поток. Длина трубки определяется на основе объемных скоростей потока, так что время пребывания реагентов в трубках составляет 3 часа. Температура реакции сульфирования составляет 25°С и поддерживается путем погружения трубок в водяную баню с регулируемой температурой. Третий шприц (шприц с Ab + буфером из фиг. 5), содержит повторно окисленное анти-CD123 антитело («G4723»), рН которого был доведен до 6,0 с помощью 5% янтарной кислоты. Соответствующие объемы ДМА и 50 мМ фосфата калия добавляют к повторно окисленной смеси антител. Гомогенную смесь набирают в один шприц для совмещения в потоке с реакцией сульфирования.
[0199] Поток сульфонирующего сырья поступает во второй статический смеситель, где он смешивается с повторно окисленным антителом с доведенным рН. Объемные скорости потока регулируются таким образом, чтобы конечный поток конъюгации, выходящий из второго статического смесителя, достигал желаемых условий реакции с концентрацией антитела 2,0 мг/мл, 15% ДМА и молярным отношением DGN к антителу, равным 3,5. Длину катушки трубки для конъюгации выбирают таким образом, чтобы целевое время пребывания соответствовало продолжительности реакции конъюгации в 20 часов. Аналогично трубке для сульфирования трубку для конъюгации погружают в водяную баню с регулируемой температурой, установленной на 25°C.
Пример 2B: Исследования однопроходной фильтрации в тангенциальном потоке
[0200] Неочищенную смесь конъюгата с доведенным значением рН до 4,2 подают в ILC при концентрации 2 мг/мл с целевым коэффициентом концентрации, равным четырем, таким образом ретентат составляет приблизительно 8 мг/мл. Полученный материал конъюгата в концентрации 8 мг/мл подают в модуль SPTFF ILDF. Буфер диафильтрации для первой ILDF представляет собой 10 мМ сукцината, 50 мкмМ бисульфита, рН 4,2 с 10% (об./об.) ДМА. Скорости потока ILDF регулируют таким образом, чтобы целевые 7 диаобъемов соответствовали четырем диаобъемам, используемым в ходе обычной серийной обработки.
[0201] После первой ILDF материал подают в той же концентрации во второй модуль ILDF, где диафильтрационный буфер представляет собой 10 мМ сукцината, 50 мкмМ бисульфита, pH 4,2. Скорости потока подачи буфера для диафильтрации и подачи продукта устанавливают таким образом, чтобы целевое число диаобъемов составляло 15 для достижения замены буфера, аналогичной целевым 10 диаобъемам в ходе обычной серийной обработки TFF.
Пример 3: Импульсная обработка улучшает конъюгацию IMGN853
[0202] Авторы настоящего изобретения обнаружили, что конъюгация в непрерывном потоке обеспечивает импульсное изменение параметра (например, температуры или pH). Импульсная обработка возможна в процессе конъюгации в непрерывном потоке, где реакции происходят, когда реагенты проходят через катушки и трубки с небольшими объемами. Например, короткие участки катушек или трубок могут быстро нагреваться (например, путем изоляции) или охлаждаться для создания кратковременного отклонения температуры или «импульса». (См., например, фиг. 12).
[0203] Авторы изобретения также обнаружили, что импульсные изменения параметров реакции являются более подходящими, например, когда более длительное воздействие измененного параметра может нарушить процесс или привести к отрицательному влиянию на качество продукта. Например, повышение температуры реакции конъюгации в течение продолжительного периода времени может привести к увеличению агрегации. В отличие от этого, как продемонстрировано в данном документе, повышение температуры реакции конъюгации только за короткие импульсы времени может увеличить скорость реакции без значительного увеличения образования агрегатов.
[0204] Конъюгацию IMGN853 проводили во флаконах с импульсным воздействием на температуру, что включало в себя помещение флакона, содержащего компоненты для реакции конъюгации, при температуре 20°С в течение примерно 30 минут, а затем импульсное воздействие путем помещения флакона в водяную баню при более высокой температуре в течение указанного периода времени импульсного воздействия, а затем возврат флакона до температуры 20°C. Содержимое флакона восстанавливали при температуре 20°C до появления следующего импульса, а процесс повторяли до достижения определенного количества импульсов. Были оценены четыре различных условия импульсного воздействия: 4 импульса при 40°С по 7 минут каждый; 4 импульса при 42,5°С по 7 минут каждый; 5 импульсов при 50°С в течение 1 минуты каждый и 5 импульсов при 60°С в течение 1 минуты каждый. Контрольную реакцию проводили при равновесной температуре 20°С.
[0205] Степень завершения реакции (%) использовали для определения скорости реакции. При равновесной температуре 20°C для завершения реакции конъюгации IMGN853 требуется около 8 часов. (См. фиг. 14, левая панель). Все испытанные условия импульсного воздействия уменьшали время реакции (то есть достигали 100% завершения за меньший период времени). (См. фиг. 14, левая панель). Импульсное воздействие (5 раз) при 60°C в течение 1 минуты на импульс резко увеличивало частоту появления высокомолекулярных (HMW; агрегатных) соединений. (См. фиг. 14, правая панель). Напротив, все другие испытанные условия импульсного воздействия оказали небольшое влияние на образование HWM (агрегатных) соединений.
[0206] Эти данные демонстрируют, что условия реакции, обеспечиваемые конъюгацией в непрерывном потоке, могут улучшить кинетику реакции и производительность без ущерба для качества продукта.
Пример 4: Одноэтапная подготовка антитела для конъюгации
[0207] В примере 2 процесс получения лекарственного вещества IMGN632 включает два этапа подготовки антитела G4723A для конъюгации: восстановление и повторное окисление (фиг. 10, верхний левый блок). Восстановление антитела G4723A уменьшает количество межцепочечных дисульфидов между нативными цистеинами и удаляет блокирующие группы на остатках сконструированного при помощи C442 цистеина. Этот этап включает добавление 25 молярных эквивалентов TCEP к антителу G4723A. После реакции восстановления в смеси восстановленных антител заменяют буфер для удаления любого остаточного TCEP и подготовки антитела для реакции повторного окисления. Этап повторного окисления включает добавление 8 молярных эквивалентов DHAA к восстановленному антителу G4723A для повторного формирования межцепочечных дисульфидов антитела. Реакция оставляет остатки сконструированного при помощи C442 цистеина в виде свободных тиолов, которые могут быть конъюгированы с полезной нагрузкой через функциональную группу малеимида.
[0208] Чтобы продемонстрировать возможность выполнения этих реакций в непрерывном формате, были проведены мелкомасштабные исследования с использованием микромасштабного проточного реактора.
Пример 4A: Реакция восстановления
[0209] Реакцию восстановления проводили для демонстрации того, что составленное антитело G4723A можно восстановить в проточном реакторе и получить антитело с постоянным качеством продукта в виде параллельной серийной реакции.
[0210] Шкала восстановления в 150 мг на основе антитела G4723A была выполнена для демонстрации непрерывного восстановления в проточном реакторе. Составленное антитело G4723A в концентрации 51,1 мг/мл использовали в качестве одного питающего потока. Раствор антител набирали в шприц. Исходный раствор TCEP-HCl, приготовленный при 100 мМ в 50 мМ фосфате калия, рН 7,5, объединяли с дополнительным 50 мМ фосфатом калия, рН 7,5 в качестве второго питающего потока для непрерывной реакции. Это было сделано из-за низких скоростей потока и объемных соотношений исходного раствора TCEP-HCl к питающим потокам буфера из 50 мМ фосфата калия, pH 7,5, если они содержались отдельно. Дополнительный буфер из 50 мМ фосфата калия, рН 7,5 необходим для разбавления составленного антитела G4723A до 5 мг/мл для реакции восстановления.
[0211] Реакцию проводили с использованием шприцевых насосов Harvard Apparatus и 1/16 трубки из PEEK. Объемное соотношение двух питающих потоков было выбрано таким образом, чтобы конечная стехиометрия реакции после смешивания при заданных условиях реакции составляла 25 молярных эквивалентов TCEP-HCl к антителу, 5 мг/мл антитела. Объединенная объемная скорость потока двух питающих потоков была использована для расчета длины трубки из PEEK, необходимой для того, чтобы продолжительность реакции или время пребывания в проточном реакторе составляло 16 часов. Для этого эксперимента проводили как параллельную серийную контрольную реакцию, так и непрерывные реакции при температуре окружающей среды.
[0212] Параллельную серийную контрольную реакцию восстановления устанавливали в масштабе 20 мг антитела G4723A. Все параметры реакции были сопоставлены. После 16-часовой продолжительности реакции отбирали образцы из контрольной и непрерывной реакции и маркировали для анализа. Образцы из реакции непрерывного восстановления отбирали из выходного отверстия проточного реактора. Отбирали пробы из контрольной серийной реакции в общем объеме для анализа.
[0213] Чтобы охарактеризовать реакцию восстановления, образцы метили флуорофором Alexa-MAL 488, который вступает в реакцию со свободными тиолами на антителе и может быть обнаружен с помощью УФ-спектрометрии. Образцы подвергали реакции с Alexa-MAL 488 и анализировали методом эксклюзионной ВЭЖХ для расчета соотношения Alexa-антитело. Результаты для непрерывных и параллельных контрольных реакций показаны в таблице 6.
Таблица 6: Серийная против непрерывной реакции восстановления
[0214] Данные, показанные в таблице 6, демонстрируют, что антитело G4723A было восстановлено с помощью традиционной серийной и непрерывной обработки. Для составленного антитела G4723A до восстановления метка Alexa не наблюдалась. После восстановления межцепочечных дисульфидов с образованием свободных тиолов во время реакции восстановления, Alexa-MAL 488 способен вступать в реакцию и конъюгировать свободный тиол. Полное восстановление сконструированных цистеинов и нативных цистеинов антитела привело бы к 10 меткам.
[0215] Приблизительно 7-8 меток Alexa-MAL 488 были обнаружены в обоих образцах, что указывает на восстановление антитела G4723A. Эти результаты согласуются с предыдущими исследованиями по разработке в меньшем масштабе, в которых после реакции восстановления идентифицировано 8 меток Alexa-MAL 488. Отличие от теоретической цели в 10 меток, вероятно, связано с некоторым повторным окислением, которое происходит в небольшом масштабе, вызванным воздухом в реакционном сосуде, что побуждает свободные тиолы к повторному формированию дисульфидов и приводит к уменьшению количества доступных свободных тиолов в антителе для конъюгации с Alexa-MAL 488.
[0216] Последующие исследования выполняли повторно в больших масштабах и они были нацелены на более короткие времена восстановления, равные приблизительно 3 часам. Аналогично, антитела, полученные в этих исследованиях, были помечены Alexa-MAL 488 и охарактеризованы с помощью эксклюзионной ВЭЖХ для сравнения эффективности реакции. Данные о качестве продукта из последующего исследования, в котором целевое время реакции восстановления составляло 3 часа путем увеличения объемных скоростей двух питающих потоков, приведены в таблице 7.
Таблица 7: Оценка качества продукта непрерывной реакции восстановления
[0217] В дополнение к соотношению Alexa: Ab, сравнивающему степень реакции восстановления для серийной контрольной и непрерывной реакций, измеряли значения мономера и HMW для двух продуктов реакции. Данные в Таблице 7 показывают, что в большем масштабе при более высоких объемных скоростях реакция непрерывного восстановления сопоставима с серийной контрольной реакцией. Кроме того, наблюдается небольшое увеличение мономера для антитела, полученного в результате непрерывной реакции.
[0218] Эти результаты демонстрируют, что реакция восстановления может быть успешно выполнена в непрерывном формате с использованием потоковой химии.
Пример 4B: Реакция повторного окисления
[0219] Реакция повторного окисления была проведена, чтобы продемонстрировать, что восстановленное антитело G4723A может быть повторно окислено в непрерывном формате.
[0220] Из-за масштаба реакций и оборудования проточного реактора восстановленные антитела, используемые для проведения исследований повторного окисления, были очищены методом NAP. Во время производства IMGN632 восстановленное антитело очищают TFF, чтобы удалить любой остаточный TCEP-HC1 из реакционного раствора. После удаления TCEP-HC1 в реакционный пул добавляют DHAA для повторного формирования межцепочечных дисульфидов антитела, оставляя два остатка сконструированного при помощи C442 цистеина свободными для конъюгации.
[0221] Для исследований повторного окисления антитело G4723A сначала восстанавливали с использованием серийной реакции из-за необходимости настройки оборудования проточного реактора для условий реакции повторного окисления. Реакцию восстановления проводили при 37°С в течение 1 часа, чтобы полностью восстановить антитело, используя те же 25 молярных эквивалентов TCEP-HC1 относительно антитела при концентрации антитела 5 мг/мл. После реакции восстановления образец реакции был помечен Alexa для подтверждения восстановления антитела.
[0222] Затем восстановленное антитело очищали методом NAP для удаления остаточного TCEP-HCl из раствора перед добавлением DHAA. Очищенный методом NAP материал измеряли на предмет концентрации, чтобы обеспечить, что установка реакции повторного окисления нацелена на соответствующие стехиометрические соотношения. Очищенное методом NAP восстановленное антитело расщеплялось таким образом, что параллельную серийную контрольную реакцию контроля можно было установить в качестве контроля с образцом непрерывного повторного окисления.
[0223] Для непрерывной реакции повторного окисления использовали три питающих потока. Первым было восстановленное антитело, которое было очищено методом NAP. Вторым был 100 мМ исходный раствор DHAA в ДМА в комбинации с дополнительным ДМА, как требуется для достижения целевого значения 5% (об./об.) для реакции. Третьим был буфер из 50 мМ фосфата калия с pH 7,5, который разбавляет очищенное методом NAP восстановленное антитело до целевой концентрации 2,5 мг/мл для реакции. Объемные соотношения этих трех питающих потоков были определены на основе очищенной методом NAP концентрации восстановленного антитела. Соотношения были отрегулированы таким образом, чтобы объединенные питающие потоки давали конечные целевые условия реакции повторного окисления после смешивания. Объемные скорости потока также использовали для расчета количества 1/16 трубки из PEEK, требуемого для достижения продолжительности реакции в 6 часов. Параллельную реакцию повторного окисления и реакцию непрерывного повторного окисления проводили при температуре окружающей среды.
[0224] Реакцию повторного окисления в 50 мг проводили для непрерывных и контрольных реакций. В общей сложности 19,9 футов 1/16 трубки из PEEK потребовалось для достижения 6 часов, исходя из объемных скоростей трех питающих потоков. Образцы из непрерывной реакции повторного окисления отбирали периодически из выходного отверстия проточного реактора, начиная с 6,5 часов после начала реакции. Дополнительное время было предоставлено для обеспечения того, чтобы реакция достигла равновесного состояния в зависимости от потенциального противодавления в проточном реакторе. Образцы, взятые из выходного отверстия проточного реактора или из основной части реакции повторного окисления, были помечены флуорофором Alexa-MAL 488 и охарактеризованы методом эксклюзионной ВЭЖХ. Образцы из реакции повторного окисления отбирали с течением времени, чтобы обеспечить достижение равновесного состояния. Кроме того, восстановленное антитело, которое содержалось в шприце и подавалось в качестве одного из питающих потоков для непрерывной реакции повторного окисления, также было помечено после окончания исследования. Этот образец был протестирован, чтобы убедиться, что восстановленное антитело не окислилось повторно во время нахождения в шприце в течение всего исследования. Этот образец сравнивали с образцом после восстановления, чтобы понять любые изменения в восстановленном антителе, потенциально вызванные условиями окружающей среды. Результаты этого исследования непрерывного повторного окисления приведены в таблице 8.
Таблица 8: Качество продукта непрерывной реакции повторного окисления
(T=9 ч)
[0225] Эти данные указывают на то, что реакцию повторного окисления можно успешно проводить с использованием непрерывной обработки. Реакция повторного окисления, выполненная в проточном реакторе, показала успешное повторное окисление с приблизительным показателем в 2,4 метки Alexa-MAL 488. Данные серийной контрольной реакции были сопоставимы с показателем приблизительно в 2,2 метки Alexa-MAL 488. Восстановленное антитело перед повторным окислением имело приблизительно 8 меток, что демонстрирует, что добавление DHAA вызывало повторное формирование дисульфидов. Остальные метки, которые были конъюгированы с Alexa-MAL 488, представляют собой остатки сконструированного цистеина, которые были бы доступны для конъюгации. Кроме того, данные, приведенные в таблице 8, показывают, что восстановленное антитело подвергается крайне минимальному повторному окислению в условиях окружающей среды. Восстановленное антитело имело начальный показатель в 8,15 меток и после продолжительности исследования повторного окисления показатель уменьшался всего лишь до 7,36. Эти данные указывают на то, что повторное окисление было вызвано реакцией с DHAA, а не воздухом, присутствующим в реакционном сосуде или буферах.
[0226] В совокупности эти результаты показывают, что реакция повторного окисления может быть успешно достигнута с использованием непрерывной обработки в проточном реакторе.
* * *
[0227] Следует принять во внимание, что раздел «Подробное изложение», а не разделы «Краткое изложение» и «Реферат», предназначен для интерпретации формулы изобретения. В разделах «Краткое изложение» и «Реферат» указаны один или более, но не все иллюстративные варианты осуществления данного изобретения, как это предусмотрено изобретателем(ями), и, таким образом, не предназначены для ограничения данного изобретения и прилагаемой формулы изобретения любым способом.
[0228] Данное изобретение было описано выше с помощью функциональных структурных элементов, иллюстрирующих осуществление указанных функций и их взаимосвязей. Границы этих функциональных структурных элементов были произвольно определены в данном документе для удобства описания. Альтернативные границы могут быть определены до тех пор, пока указанные функции и их отношения будут надлежащим образом выполняться.
[0229] Вышеизложенное описание конкретных вариантов осуществления полностью отражает общий характер изобретения, который другие могут, применяя знания в пределах уровня техники, легко модифицировать и/или адаптировать для различных применений подобных конкретных вариантов осуществления, без излишнего экспериментирования, не отступая от общей концепции данного изобретения. Следовательно, такие адаптации и модификации предназначены для того, чтобы быть в пределах значения и диапазона эквивалентов раскрытых вариантов осуществления на основе представленных в данном документе инструкций и указаний. Следует понимать, что формулировки или терминология в данном документе предназначены для описания, а не ограничения, так что терминология или формулировки данного описания должна интерпретироваться квалифицированным специалистом в свете инструкций и указаний.
[0230] Объем притязаний и объем данного изобретения не должны ограничиваться каким-либо из вышеописанных иллюстративных вариантов осуществления, но должны определяться только в соответствии со следующей формулой изобретения и их эквивалентами.
[0231] Формула изобретения в настоящей заявке отличается от формулы первичной заявки или других родственных заявок. В связи с этим заявитель аннулирует любой отказ от объема притязаний, сделанный в первичной заявке или любой предшествующей заявке в отношении настоящей заявки. Поэтому эксперту рекомендуется по возможности пересмотреть любой такой предыдущий отказ и цитируемые ссылки, которые были сделаны во избежание этого. Кроме того, эксперту также следует помнить, что любой отказ, сделанный в настоящей заявке, не должен быть интерпретирован в отношении первичной заявки.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ИММЮНОДЖЕН, ИНК
<120> СПОСОБЫ ПОЛУЧЕНИЯ, ОЧИСТКИ И СОСТАВЛЕНИЯ КОНЪЮГАТОВ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ
СРЕДСТВО
<130> 2921.099PC03/EKS/CLD
<150> 62/673 535
<151> 18.05.2018
<150> 62/617 021
<151> 12.01.2018
<160> 56
<170> PatentIn, версия 3.5
<210> 1
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VH huMov19
<400> 1
Gly Tyr Phe Met Asn
1 5
<210> 2
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VH huMov19
<400> 2
Arg Ile His Pro Tyr Asp Gly Asp Thr Phe Tyr Asn Gln Lys Phe Gln
1 5 10 15
Gly
<210> 3
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VH huMov19
<400> 3
Tyr Asp Gly Ser Arg Ala Met Asp Tyr
1 5
<210> 4
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VL huMov19
<400> 4
Lys Ala Ser Gln Ser Val Ser Phe Ala Gly Thr Ser Leu Met His
1 5 10 15
<210> 5
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VL huMov19
<400> 5
Arg Ala Ser Asn Leu Glu Ala
1 5
<210> 6
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VL huMov19
<400> 6
Gln Gln Ser Arg Glu Tyr Pro Tyr Thr
1 5
<210> 7
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VH Z4681A
<400> 7
Ser Tyr Tyr Ile His
1 5
<210> 8
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VH Z4681A
<400> 8
Val Ile Tyr Pro Gly Asn Asp Asp Ile Ser Tyr Asn Gln Lys Phe Gln
1 5 10 15
Gly
<210> 9
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VH Z4681A
<400> 9
Glu Val Arg Leu Arg Tyr Phe Asp Val
1 5
<210> 10
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VL Z4681A
<400> 10
Lys Ser Ser Gln Ser Val Phe Phe Ser Ser Ser Gln Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 11
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VL Z4681A
<400> 11
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 12
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VL Z4681A
<400> 12
His Gln Tyr Leu Ser Ser Arg Thr
1 5
<210> 13
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VH G4723A
<400> 13
Ser Ser Ile Met His
1 5
<210> 14
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VH G4723A
<400> 14
Tyr Ile Lys Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 15
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VH G4723A
<400> 15
Glu Gly Gly Asn Asp Tyr Tyr Asp Thr Met Asp Tyr
1 5 10
<210> 16
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VL G4723A
<400> 16
Arg Ala Ser Gln Asp Ile Asn Ser Tyr Leu Ser
1 5 10
<210> 17
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VL G4723A
<400> 17
Arg Val Asn Arg Leu Val Asp
1 5
<210> 18
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VL G4723A
<400> 18
Leu Gln Tyr Asp Ala Phe Pro Tyr Thr
1 5
<210> 19
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VH huCMET-27
<400> 19
Ser Tyr Asp Met Ser
1 5
<210> 20
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VH huCMET-27
<400> 20
Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val Lys
1 5 10 15
Gly
<210> 21
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VH huCMET-27
<400> 21
Glu Glu Ile Thr Thr Glu Met Asp Tyr
1 5
<210> 22
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VL huCMET-27
<400> 22
Arg Ala Ser Glu Ser Val Asp Ser Tyr Gly Asn Ser Phe Ile His
1 5 10 15
<210> 23
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VL huCMET-27
<400> 23
Arg Ala Ser Asn Leu Glu Ser
1 5
<210> 24
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VL huCMET-27
<400> 24
Gln Gln Ser Asn Glu Glu Pro Leu Thr
1 5
<210> 25
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VH huB4
<400> 25
Ser Asn Trp Met His
1 5
<210> 26
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VH huB4
<400> 26
Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asn
1 5 10
<210> 27
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VH huB4
<400> 27
Gly Ser Asn Pro Tyr Tyr Tyr Ala Met Asp Tyr
1 5 10
<210> 28
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VL huB4
<400> 28
Ser Ala Ser Ser Gly Val Asn Tyr Met His
1 5 10
<210> 29
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VL huB4
<400> 29
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 30
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VL huB4
<400> 30
His Gln Arg Gly Ser Tyr Thr
1 5
<210> 31
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VH huADAM9
<400> 31
Ser Tyr Trp Met His
1 5
<210> 32
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VH huADAM9
<400> 32
Glu Ile Ile Pro Ile Phe Gly His Thr Asn Tyr Asn Glu Lys Phe Lys
1 5 10 15
Ser
<210> 33
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VH huADAM9
<400> 33
Gly Gly Tyr Tyr Tyr Tyr Phe Asn Ser Gly Thr Leu Asp Tyr
1 5 10
<210> 34
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR1 VL huADAM9
<400> 34
Lys Ala Ser Gln Ser Val Asp Tyr Ser Gly Asp Ser Tyr Met Asn
1 5 10 15
<210> 35
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR2 VL huADAM9
<400> 35
Ala Ala Ser Asp Leu Glu Ser
1 5
<210> 36
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR3 VL huADAM9
<400> 36
Gln Gln Ser His Glu Asp Pro Phe Thr
1 5
<210> 37
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH huMov19
<400> 37
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Phe Met Asn Trp Val Lys Gln Ser Pro Gly Gln Ser Leu Glu Trp Ile
35 40 45
Gly Arg Ile His Pro Tyr Asp Gly Asp Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala His
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Phe Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Tyr Asp Gly Ser Arg Ala Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 38
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL huMov19, версия 1.00
<400> 38
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Asn Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<210> 39
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL huMov19, версия 1.60
<400> 39
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<210> 40
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH Z4681A
<400> 40
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Ile Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Val Ile Tyr Pro Gly Asn Asp Asp Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Val Arg Leu Arg Tyr Phe Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 41
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL Z4681A
<400> 41
Glu Ile Val Leu Thr Gln Ser Pro Gly Ser Leu Ala Val Ser Pro Gly
1 5 10 15
Glu Arg Val Thr Met Ser Cys Lys Ser Ser Gln Ser Val Phe Phe Ser
20 25 30
Ser Ser Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Ile Pro Gly Gln
35 40 45
Ser Pro Arg Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Pro Glu Asp Leu Ala Ile Tyr Tyr Cys His Gln
85 90 95
Tyr Leu Ser Ser Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg
<210> 42
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH G4723A
<400> 42
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ser Ser
20 25 30
Ile Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Arg Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly Asn Asp Tyr Tyr Asp Thr Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 43
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL G4723A
<400> 43
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Val Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Ala Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 44
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH huCMET-27
<400> 44
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 45
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL huCMET-27
<400> 45
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys Arg
100 105 110
<210> 46
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH huB4
<400> 46
Gln Val Gln Leu Val Gln Pro Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Ser Asn
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asn Tyr Asn Gln Asn Phe
50 55 60
Gln Gly Lys Ala Lys Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Val Ser Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Asn Pro Tyr Tyr Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 47
<211> 105
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL huB4
<400> 47
Glu Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Arg Val Thr Met Thr Cys Ser Ala Ser Ser Gly Val Asn Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Thr Ser Pro Arg Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Ser Met Glu Pro Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys His Gln Arg Gly Ser Tyr Thr Phe Gly
85 90 95
Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 48
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH huADAM9
<400> 48
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Glu Ile Ile Pro Ile Phe Gly His Thr Asn Tyr Asn Glu Lys Phe
50 55 60
Lys Ser Arg Phe Thr Ile Ser Leu Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Gly Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Tyr Tyr Tyr Tyr Phe Asn Ser Gly Thr Leu Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 49
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL huADAM9
<400> 49
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Ser
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asp Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser His
85 90 95
Glu Asp Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 50
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> тяжелая цепь huMov19
<400> 50
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Phe Met Asn Trp Val Lys Gln Ser Pro Gly Gln Ser Leu Glu Trp Ile
35 40 45
Gly Arg Ile His Pro Tyr Asp Gly Asp Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala His
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Phe Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Tyr Asp Gly Ser Arg Ala Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 51
<211> 218
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь huMov19, версия 1.00
<400> 51
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Asn Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 52
<211> 218
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь huMov19, версия 1.60
<400> 52
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 53
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> тяжелая цепь Z4681A
<400> 53
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Ile Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Val Ile Tyr Pro Gly Asn Asp Asp Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Val Arg Leu Arg Tyr Phe Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 54
<211> 219
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь Z4681A
<400> 54
Glu Ile Val Leu Thr Gln Ser Pro Gly Ser Leu Ala Val Ser Pro Gly
1 5 10 15
Glu Arg Val Thr Met Ser Cys Lys Ser Ser Gln Ser Val Phe Phe Ser
20 25 30
Ser Ser Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Ile Pro Gly Gln
35 40 45
Ser Pro Arg Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Pro Glu Asp Leu Ala Ile Tyr Tyr Cys His Gln
85 90 95
Tyr Leu Ser Ser Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 55
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> тяжелая цепь G4723A
<400> 55
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ser Ser
20 25 30
Ile Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Arg Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly Asn Asp Tyr Tyr Asp Thr Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Cys Leu Ser
435 440 445
Pro Gly
450
<210> 56
<211> 214
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь G4723A
<400> 56
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Val Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Ala Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ EDB И КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2758632C2 |
| НАЦЕЛЕННЫЕ НА uPARAP КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2740311C2 |
| САЙТ-СПЕЦИФИЧЕСКАЯ КОНЪЮГАЦИЯ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО ПОСРЕДСТВОМ ГЛИКОИНЖЕНЕРИИ | 2014 |
|
RU2831409C2 |
| КОНЪЮГАТЫ АНТИ-HER2 БИПАРАТОПНЫХ АНТИТЕЛ-ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2806049C2 |
| АМАТОКСИНОВЫЕ КОНЪЮГАТЫ АНТИТЕЛА С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2826004C2 |
| КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ЭРИБУЛИНА И СПОСОБЫ ПРИМЕНЕНИЯ | 2017 |
|
RU2754369C2 |
| КОНЪЮГАТ АНТИТЕЛА ПРОТИВ CEA И АНАЛОГА ЭКСАТЕКАНА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2833323C1 |
| КОНЪЮГАТЫ АНТИТЕЛА К CCR7 И ЛЕКАРСТВЕННОГО СРЕДСТВА | 2018 |
|
RU2777662C2 |
| АНТИТЕЛА И ФРАГМЕНТЫ АНТИТЕЛ ДЛЯ САЙТ-СПЕЦИФИЧЕСКОГО КОНЪЮГИРОВАНИЯ | 2016 |
|
RU2757815C2 |
| КОНЬЮГАТ АНТИТЕЛА К КЛАУДИНУ И ЛЕКАРСТВЕННОГО СРЕДСТВА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2826119C1 |
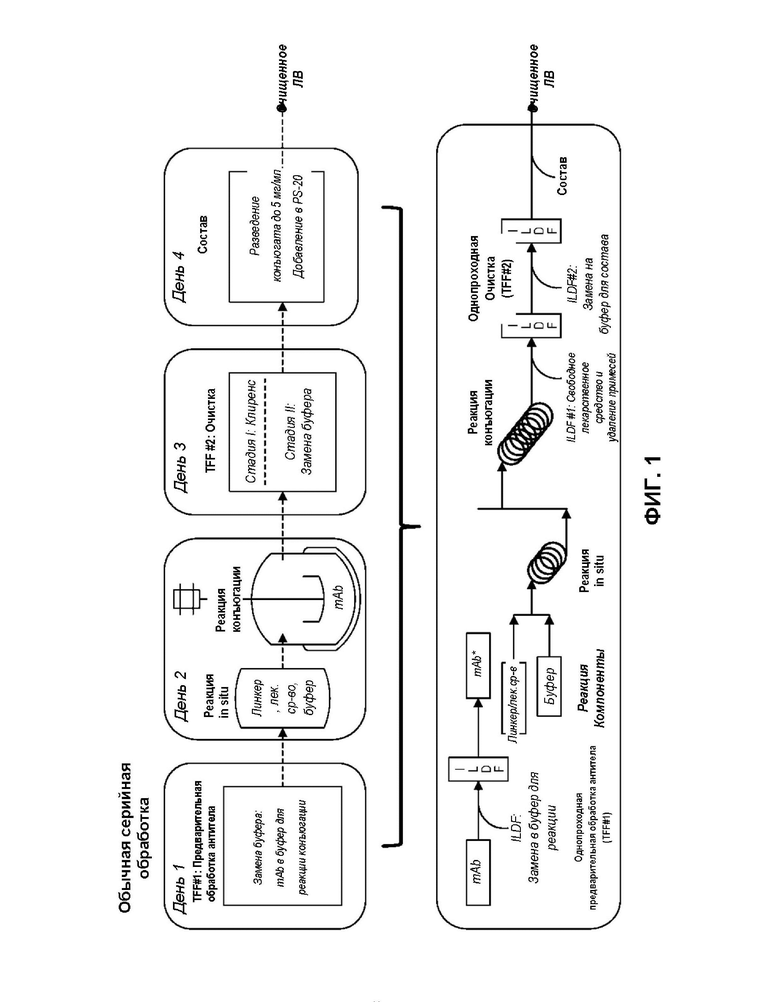
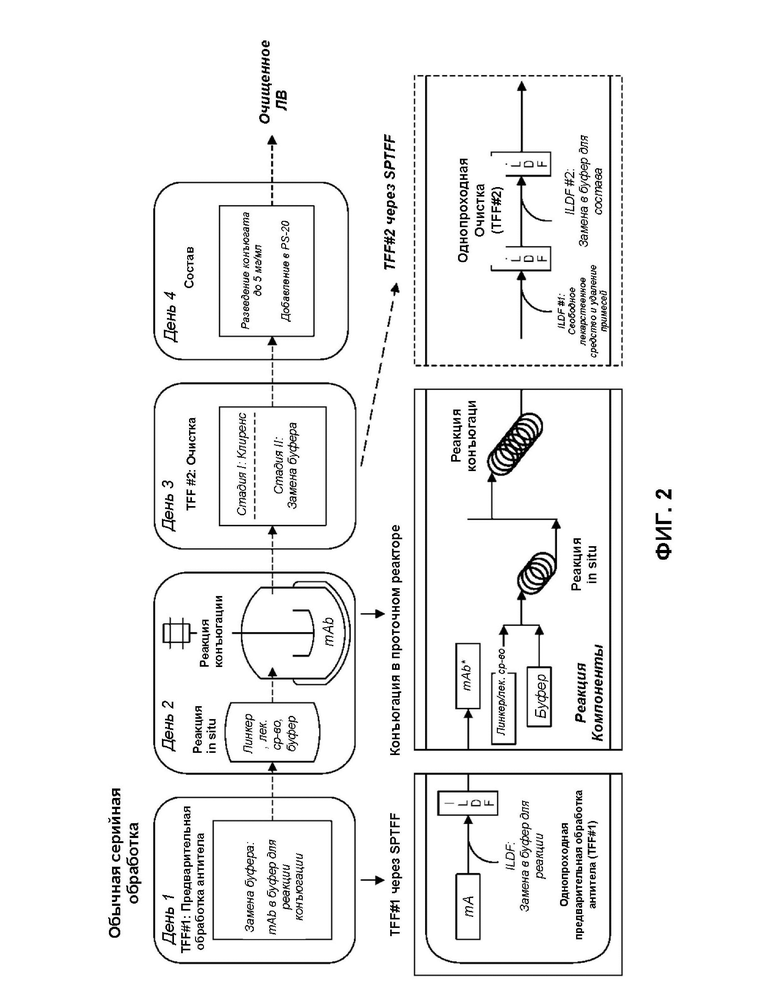
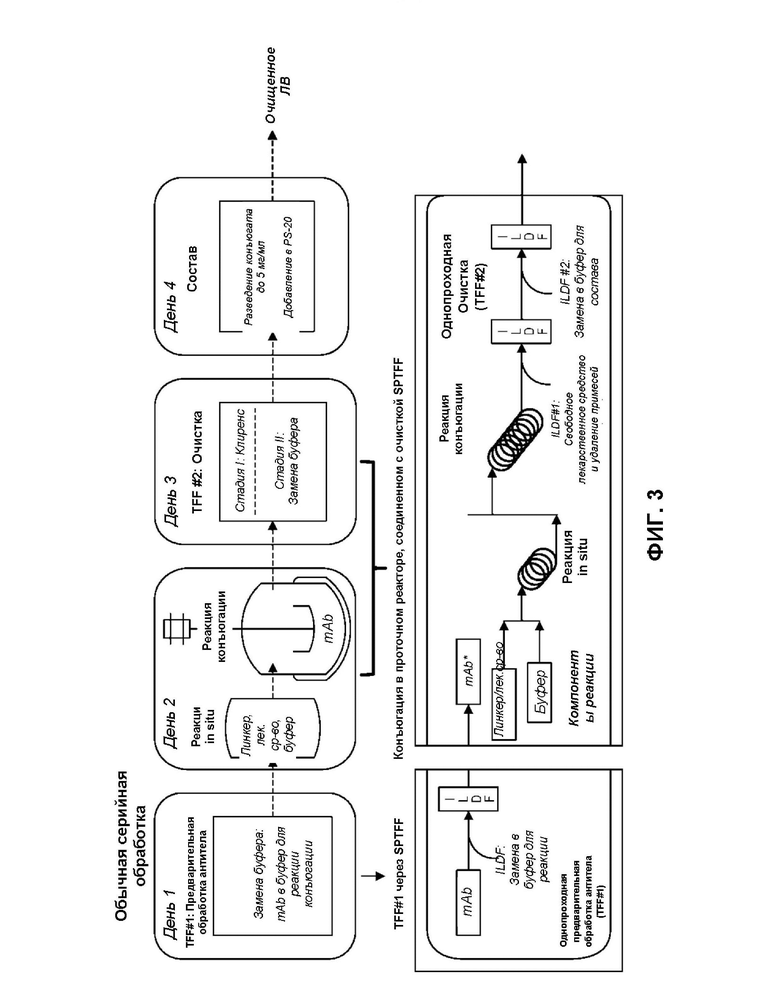
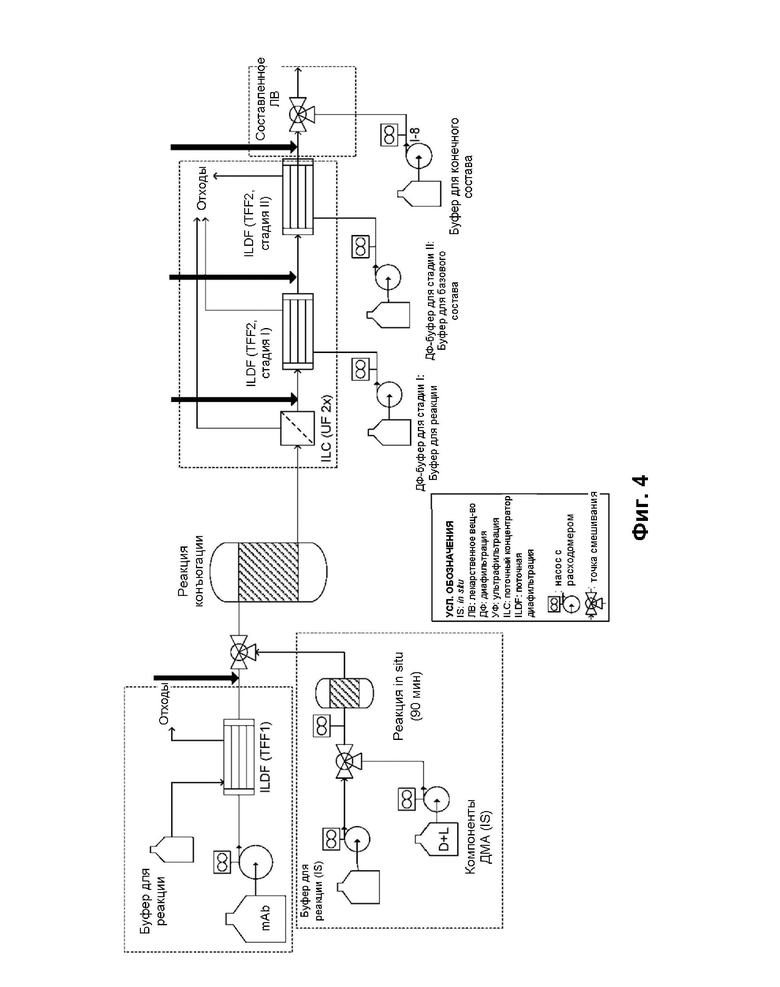
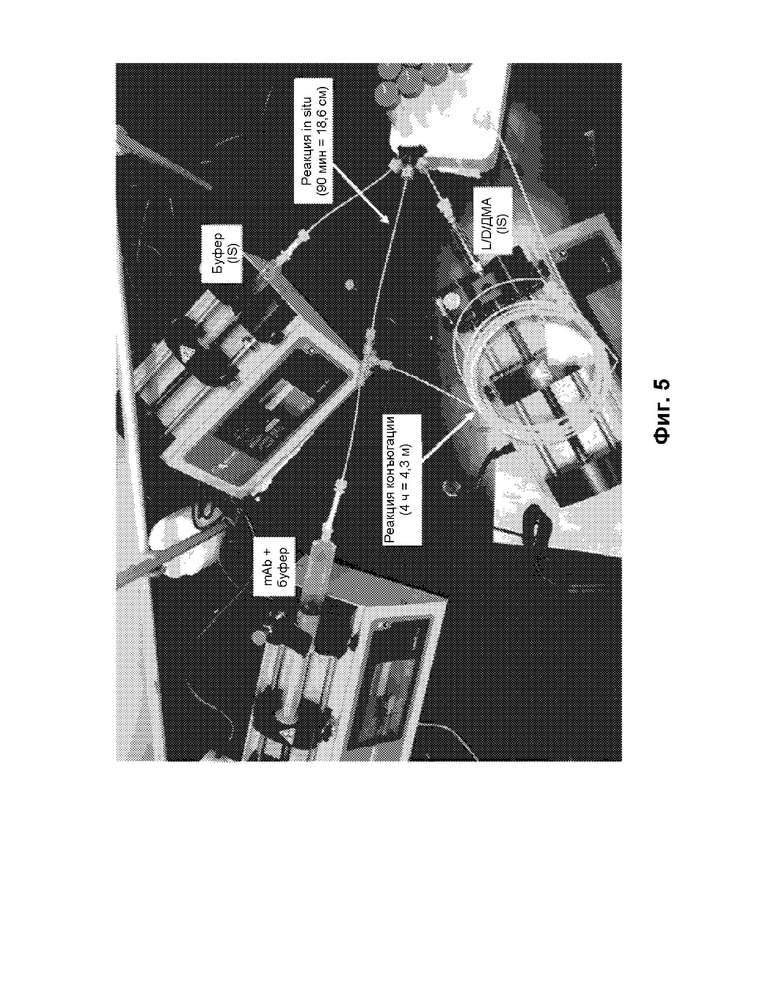
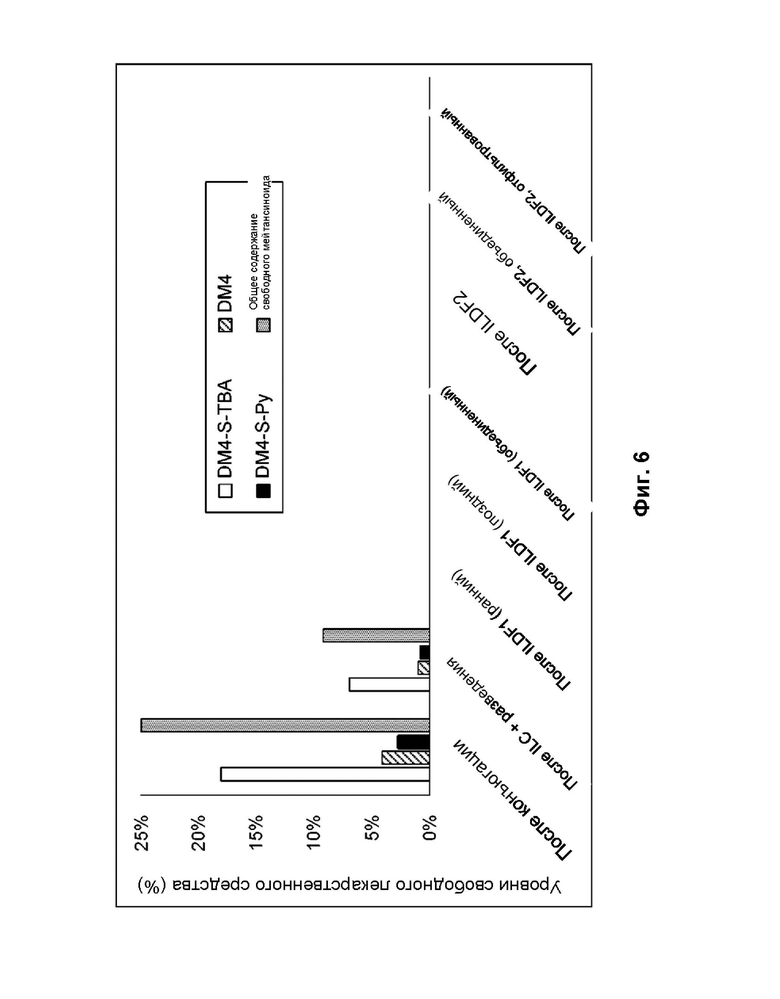
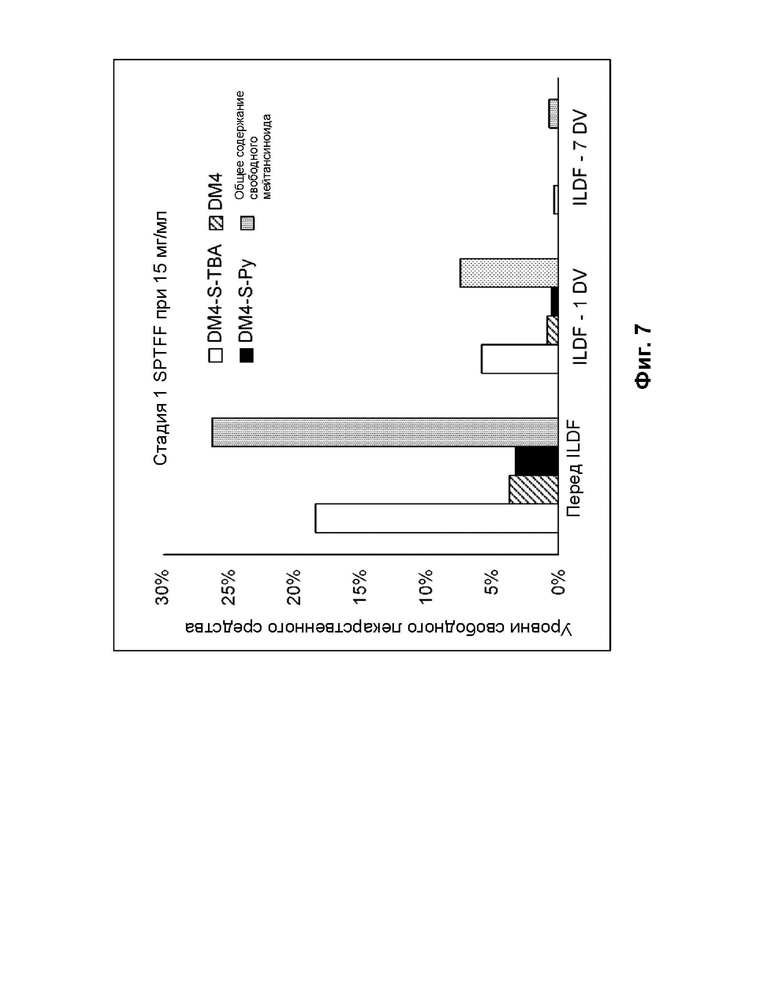
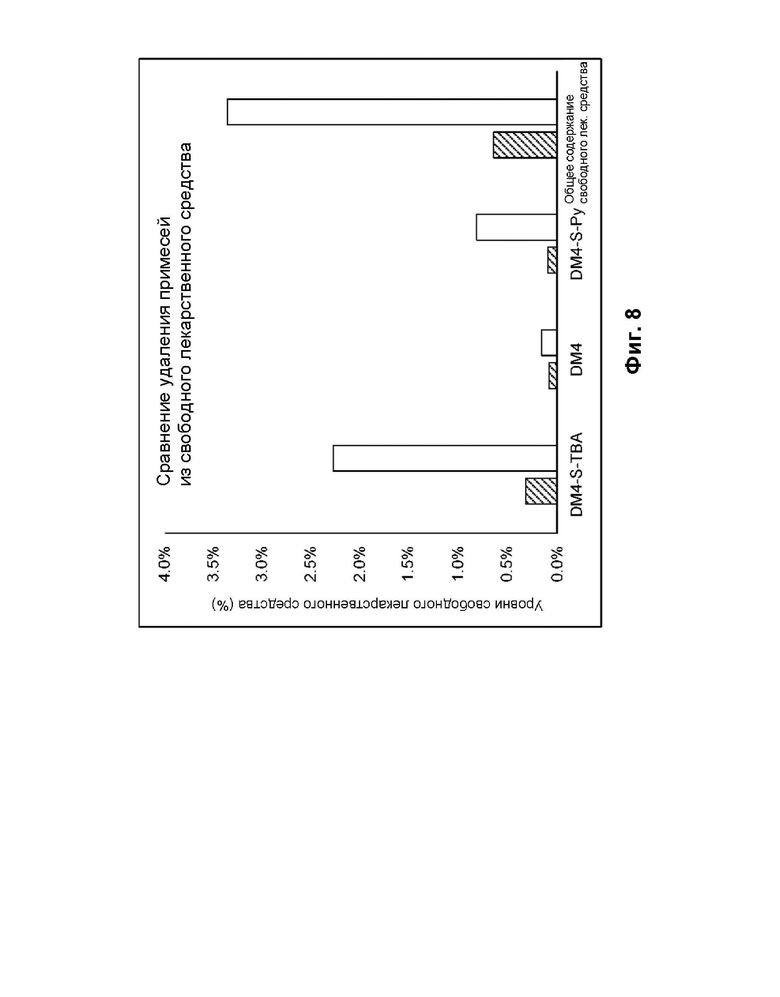
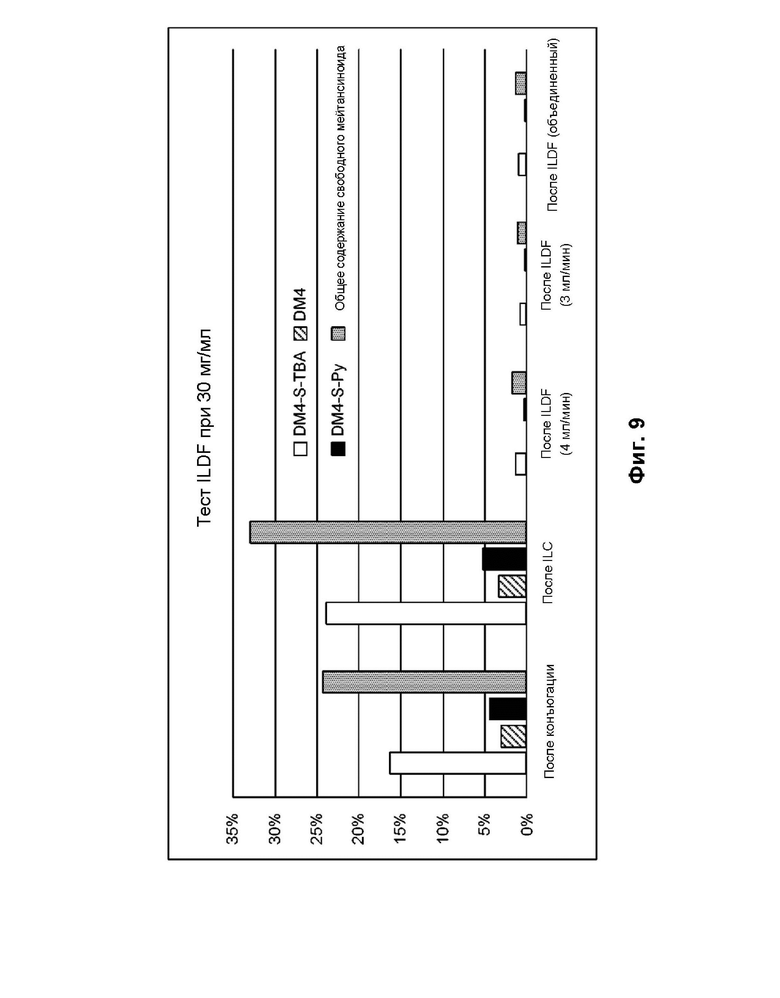
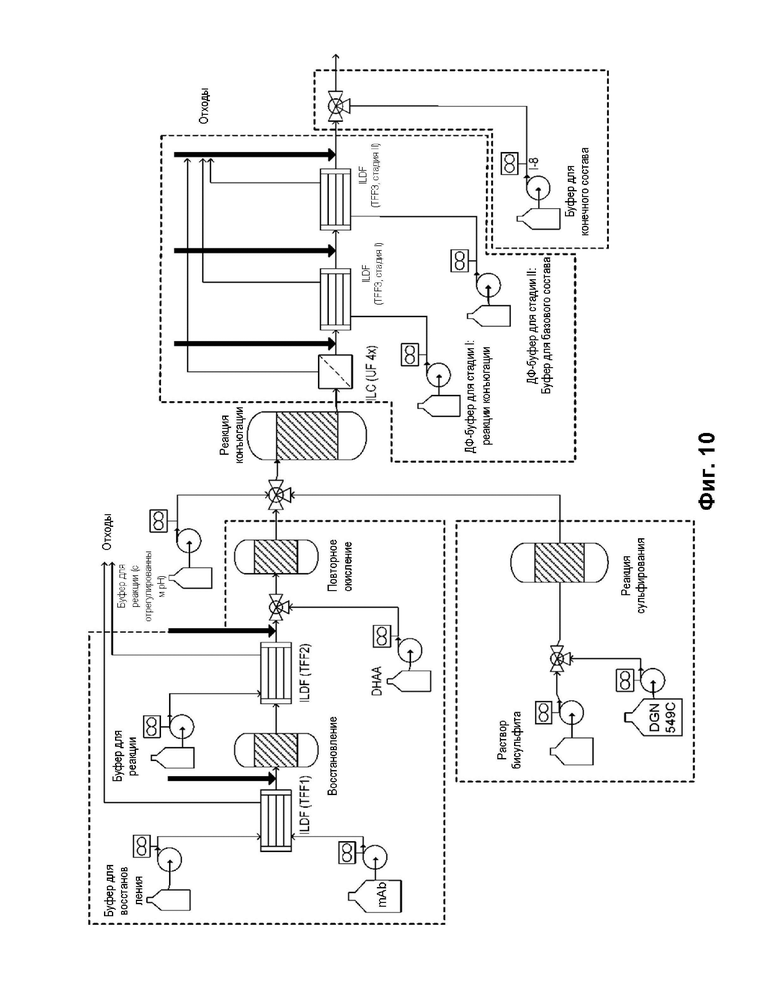
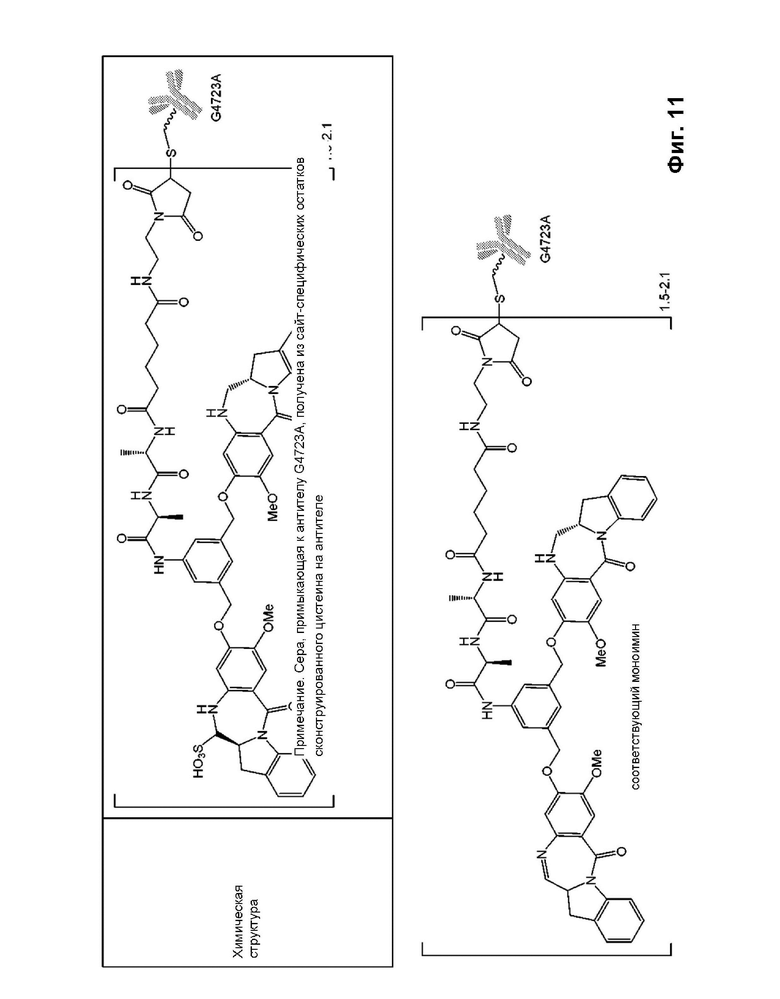
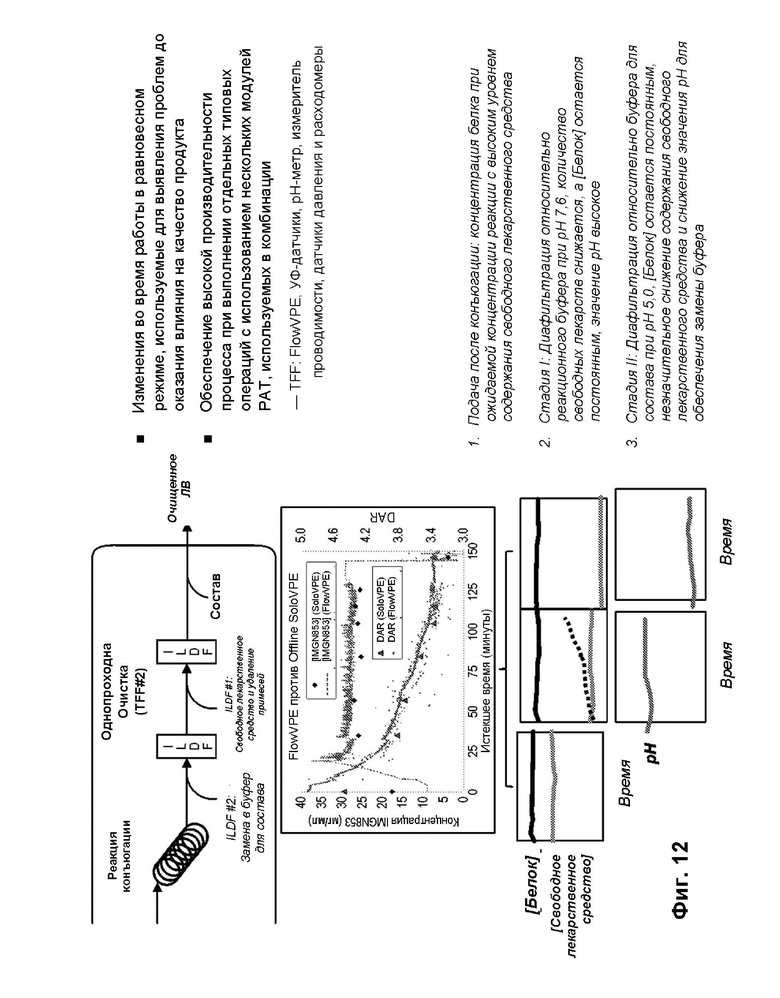
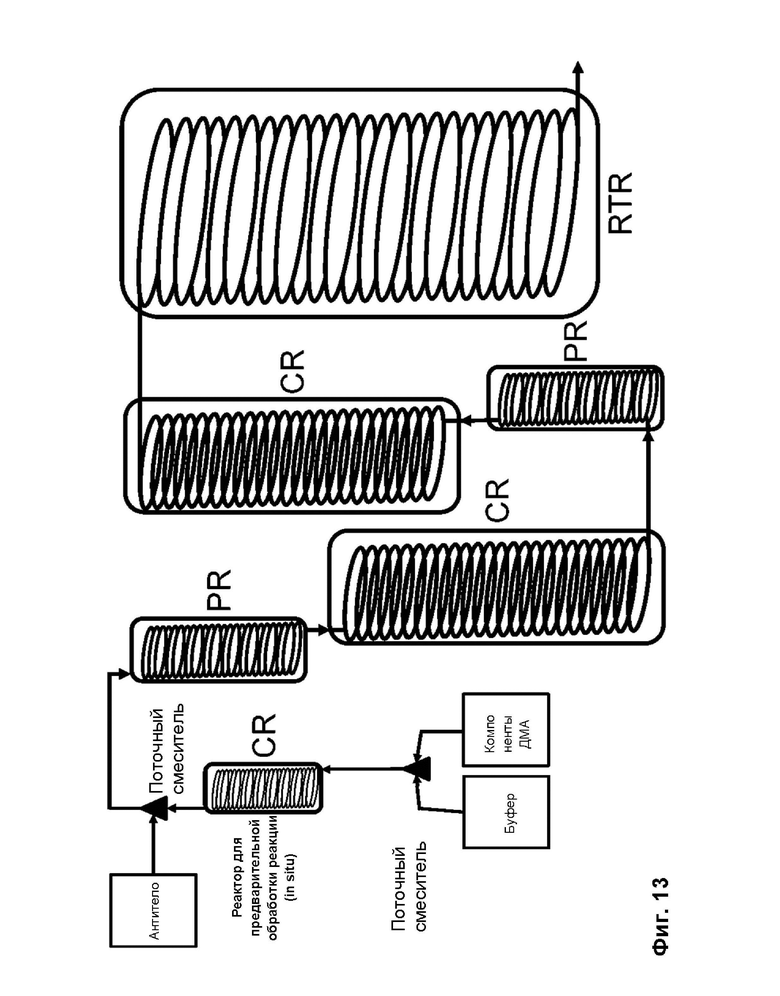
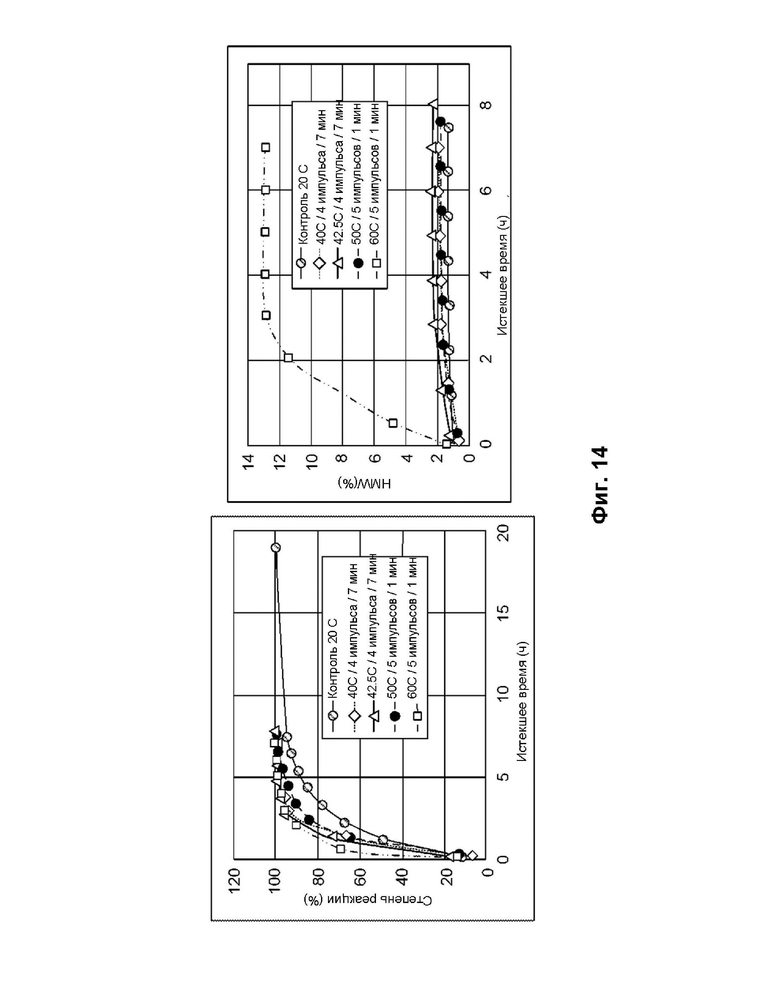
Группа изобретений относится к области биотехнологии. Представлены непрерывные способы получения композиции конъюгата антитело-лекарственное средство (ADC). В этих способах используют процессы непрерывной конъюгации, однопроходной фильтрации в тангенциальном потоке, противоточной диафильтрации и/или поточные технологии автоматизации процессов. Представленные способы сокращают время и стоимость процессов и улучшают стабильность продукта. 6 н. и 39 з.п. ф-лы, 14 ил., 8 табл., 9 пр.
1. Непрерывный способ получения композиции конъюгата антитело-лекарственное средство (ADC), включающий (i) конъюгацию антитела или его антигенсвязывающего фрагмента с лекарственным средством для образования ADC в проточном реакторе, (ii) удаление неконъюгированного лекарственного средства и (iii) перенос ADC в стабильный буфер, причем (i)–(iii) выполняют непрерывно, и при этом однопроходную фильтрацию в тангенциальном потоке (SPTFF), проточную колоночную хроматографию и/или противоточную диафильтрацию используют для удаления неконъюгированного лекарственного средства.
2. Способ по п. 1, отличающийся тем, что SPTFF и/или противоточную диафильтрацию используют для удаления неконъюгированного лекарственного средства и для переноса ADC в стабильный буфер.
3. Способ по п. 1, отличающийся тем, что проточную колоночную хроматографию используют для удаления неконъюгированного лекарственного средства, и SPTFF и/или противоточную диафильтрацию используют для переноса ADC в стабильный буфер.
4. Способ по любому из пп. 1–3, отличающийся тем, что способ дополнительно включает предварительную обработку лекарственного средства для конъюгации.
5. Непрерывный способ получения композиции конъюгата антитело-лекарственное средство (ADC), включающий (i) предварительную обработку антитела или его антигенсвязывающего фрагмента, (ii) конъюгацию антитела или его антигенсвязывающего фрагмента с лекарственным средством для образования ADC в проточном реакторе, (iii) удаление неконъюгированного лекарственного средства и (iv) перенос ADC в стабильный буфер, причем этапы (i)–(iv) выполняют непрерывно, и при этом однопроходную фильтрацию в тангенциальном потоке (SPTFF), проточную колоночную хроматографию и/или противоточную диафильтрацию используют для удаления неконъюгированного лекарственного средства.
6. Способ получения конъюгата антитело-лекарственное средство (ADC) путем процесса непрерывной конъюгации, включающий (i) добавление одного или более реагентов реакции конъюгации к реакции конъюгации в проточном реакторе в ходе реакции конъюгации и после образования по меньшей мере одного продукта реакции конъюгации (ADC) и (ii) очистку ADC с использованием однопроходной фильтрации в тангенциальном потоке (SPTFF), противоточной диафильтрации и/или проточной хроматографии.
7. Способ по любому из пп. 1-4 и 6, дополнительно включающий предварительную обработку антитела или его антигенсвязывающего фрагмента, причем предварительную обработку антитела или его антигенсвязывающего фрагмента проводят непрерывно при помощи реакции конъюгации.
8. Способ по п. 7, отличающийся тем, что предварительную обработку антитела или его антигенсвязывающего фрагмента проводят с использованием SPTFF и/или противоточной диафильтрации.
9. Способ по любому из пп. 5, 7 и 8, отличающийся тем, что предварительная обработка антитела или его антигенсвязывающего фрагмента включает перенос антитела или его антигенсвязывающего фрагмента в буфер для конъюгации.
10. Способ по любому из пп. 5 и 7-9, отличающийся тем, что предварительная обработка антитела или его антигенсвязывающего фрагмента включает восстановление антитела или его антигенсвязывающего фрагмента и/или окисление антитела или его антигенсвязывающего фрагмента.
11. Способ по любому из пп. 6-10, отличающийся тем, что ADC концентрируют, очищают и/или переносят в буфер для состава с использованием проточной хроматографии.
12. Способ по п. 11, отличающийся тем, что при однопроходной фильтрации в тангенциальном потоке используют ультрафильтрационную мембрану или диафильтрационную мембрану.
13. Способ по любому из пп. 1–12, отличающийся тем, что способ снижает время производства ADC.
14. Способ по любому из пп. 1-13, отличающийся тем, что способ дополнительно включает поточный мониторинг аналита.
15. Способ по любому из пп. 1-14, отличающийся тем, что ADC содержит антитело.
16. Способ по любому из пп. 1-15, отличающийся тем, что ADC содержит антитело или антигенсвязывающий фрагмент, который специфически связывается с CD37, CD33, FOLR1, CD123, CD19, cMET, ADAM9 или HER2.
17. Способ по п. 16, отличающийся тем, что антитело или его антигенсвязывающий фрагмент содержит последовательности CDR1 VH, CDR2 VH, CDR3 VH, CDR1 VL, CDR2 VL и CDR3 VL, содержащие последовательности SEQ ID NO: 1–6, соответственно, и лекарственное средство представляет собой мейтансиноид.
18. Способ по п. 16, отличающийся тем, что антитело или его антигенсвязывающий фрагмент содержит последовательности CDR1 VH, CDR2 VH, CDR3 VH, CDR1 VL, CDR2 VL и CDR3 VL, содержащие последовательности SEQ ID NOs:13-18, соответственно, и лекарственное средство представляет собой индолинобензодиазепин.
19. Способ по любому из пп. 1-15, отличающийся тем, что ADC содержит мейтансиноид.
20. Способ по п. 19, отличающийся тем, что мейтансиноид представляет собой DM1 или DM4.
21. Способ по любому из пп. 1-15, отличающийся тем, что ADC содержит индолинобензодиазепин.
22. Способ по п. 21, отличающийся тем, что индолинобензодиазепин представляет собой DGN462 или DGN549.
23. Способ по любому из пп. 1-16, отличающийся тем, что ADC представляет собой IMGN853.
24. Способ по любому из пп. 1-16, отличающийся тем, что ADC представляет собой IMGN632.
25. Способ по любому из пп. 1-16, отличающийся тем, что ADC представляет собой IMGN779.
26. Способ получения IMGN853, включающий (i) смешивание антитела huMovl9 и DM4, связанного с сульфо-SPDB, в процессе непрерывной конъюгации с образованием IMGN853, (ii) концентрирование IMGN853 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, (iii) удаление неконъюгированного лекарственного средства из IMGN853 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, и (iv) перенос IMGN853 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации.
27. Способ получения IMGN779, включающий (i) смешивание антитела Z4681A и DGN462, связанного с сульфо-SPDB, в процессе непрерывной конъюгации с образованием IMGN779, (ii) концентрирование IMGN779 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, (iii) удаление неконъюгированного лекарственного средства из IMGN779 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, и (iv) перенос IMGN779 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации.
28. Способ получения IMGN632, включающий (i) смешивание антитела G4732A и сульфированного DNG549C в процессе непрерывной конъюгации с образованием IMGN632, (ii) концентрирование IMGN632 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, (iii) удаление неконъюгированного лекарственного средства из IMGN632 с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации, и (iv) перенос IMGN632 в буфер для состава с использованием однопроходной фильтрации в тангенциальном потоке и/или противоточной диафильтрации.
29. Способ по любому из пп. 1–28, отличающийся тем, что способ включает повышение первой температуры процесса конъюгации по меньшей мере на 5 °C до повышенной температуры, причем повышенную температуру поддерживают в течение не более 20 минут, и при этом повышенная температура составляет не более 55 °С.
30. Способ по любому из пп. 1–29, отличающийся тем, что способ включает снижение первой температуры процесса конъюгации по меньшей мере на 5 °C до пониженной температуры, причем пониженную температуру поддерживают в течение не более 20 минут, и при этом первую температуру снижают не более чем на 30 °С.
31. Способ по п. 30, отличающийся тем, что температуру снижают по меньшей мере на 10 °С.
32. Способ по любому из пп. 30 или 31, отличающийся тем, что снижение первой температуры до пониженной температуры занимает не более 2 минут.
33. Способ по любому из пп. 30-32, дополнительно включающий повышение пониженной температуры.
34. Способ по п. 33, отличающийся тем, что пониженную температуру повышают до первой температуры.
35. Способ по п. 33 или 34, отличающийся тем, что указанное повышение занимает не более 2 минут.
36. Способ по любому из пп. 33-35, отличающийся тем, что этапы снижения первой температуры до пониженной температуры, а затем повышения пониженной температуры повторяют по меньшей мере дважды.
37. Способ по любому из пп. 29-36, отличающийся тем, что повышенную температуру или пониженную температуру поддерживают в течение не более 15 минут.
38. Способ по любому из пп. 1-37, отличающийся тем, что способ включает изменение первого значения pH процесса конъюгации по меньшей мере на 0,5 до измененного значения pH, причем измененное значение pH поддерживают в течение не более чем 20 минут, при этом первое значение рН увеличивают по меньшей мере на 1, и при этом измененное значение рН не превышает 9.
39. Способ по п. 38, отличающийся тем, что первое значение рН увеличивают по меньшей мере на 2.
40. Способ по п. 38, отличающийся тем, что первое значение рН уменьшают по меньшей мере на 1, и при этом измененное значение рН не опускается ниже 4.
41. Способ по п. 40, отличающийся тем, что первое значение рН уменьшают по меньшей мере на 2.
42. Способ по любому из пп. 38-41, дополнительно включающий изменение измененного значения рН.
43. Способ по п. 42, отличающийся тем, что рН изменяют до первого значения рН.
44. Способ по п. 42, отличающийся тем, что этапы изменения первого значения рН до измененного значения рН, а затем изменения измененного значения рН повторяют по меньшей мере дважды.
45. Способ по любому из пп. 38-44, отличающийся тем, что измененное значение рН поддерживают в течение не более 15 минут.
| EP 3134125 A1, 01.03.2017 | |||
| SEBEIKA et al | |||
| Protein and Antibody Functionalization Using Continuous Flow Microreactor Technology | |||
| J | |||
| Flow Chem | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US 20150182635 A1, 02.07.2015 | |||
| MOHANTY et al | |||
| Novel tangential-flow countercurrent cascade ultrafiltration configuration for continuous | |||
Авторы
Даты
2023-08-03—Публикация
2019-01-11—Подача