Область техники
Данное изобретение относится к новым фармацевтически активным соединениям, к фармацевтическим композициям, содержащим указанные соединения, а также к их фармацевтическому применению. В частности, данное изобретение относится к антагонистам рецептора фракталкина и к их применению для лечения заболеваний и расстройств, связанных с повышенными уровнями CX3CR1 и/или CX3CL1.
Уровень техники
В данном описании перечисление или обсуждение ранее опубликованных в явном виде документов не следует обязательно понимать как признание того, что данный документ является частью известного уровня техники или общих знаний.
7-Амино-5-тиотиазоло[4,5-d]пиримидины, такие как (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]тио}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ол (A) и 5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-он (B), являются известными антагонистами рецептора фракталкина ( et al. J. Med. Chem., 2013, 56, 3177-3190).
et al. J. Med. Chem., 2013, 56, 3177-3190).
 (A)
(A) 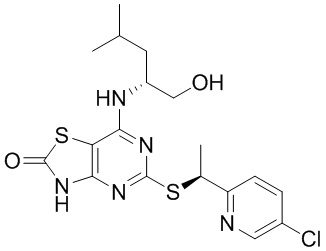 (B)
(B)
Однако указанные соединения слабо растворимы в воде, что существенно затрудняет получение пригодных фармацевтических лекарственных форм.
Подробное описание изобретения
Неожиданно было обнаружено, что некоторые фосфатные производные таких соединений, как соединения A и B, обладают определенными преимуществами по сравнению с известными антагонистами рецептора фракталкина. Помимо существенного улучшения растворимости в воде, такие соединения также значительно более стабильны при длительном хранении в водной среде и обеспечивают более высокие концентрации в плазме крови, чем при введении известных соединений.
Не ограничиваясь теорией, можно предположить, что благодаря более высоким концентрациям в плазме крови, которые достигаются при применении указанных соединений, есть основания полагать, что они, вероятно, оказывают меньший стресс на печень во время пресистемного метаболизма после перорального введения, по сравнению с введением известных антагонистов. Таким образом, указанные соединения могут лучше переноситься в более высоких дозах и/или в течение более продолжительного периода лечения, чем известные антагонисты рецептора фракталкина.
В первом аспекте данного изобретения предложено соединение формулы I,
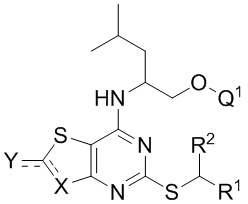 (I)
(I)
где
R1 представляет собой арил (например, фенил) или пиридил, которые оба необязательно замещены одной или более группами, выбранными из галогена, -CN, -C(O)NR3R4, -S(O)2R5, C1-6 алкила, C2-6 алкенила или C2-6 алкинила, причем последние три группы необязательно замещены одним или более F;
R2 представляет собой H или C1-6 алкил, необязательно замещенный одним или более F;
R3 и R4, каждый независимо, представляют собой H или C1-6 алкил, необязательно замещенный одним или более F;
R5 представляет собой C1-6 алкил, необязательно замещенный одним или более F;
 представляет собой
представляет собой  ,
, 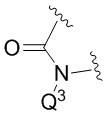 или
или 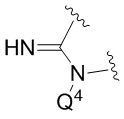 ,
,
где  означает точку присоединения к остальной части молекулы;
означает точку присоединения к остальной части молекулы;
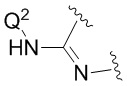
Q1 и Q2, каждый независимо, представляют собой H или -PO(OR6)(OR7);
Q3 представляет собой H или -CH2OPO(OR6)(OR7); и
Q4 представляет собой -CH2OPO(OR6)(OR7);
где R6 и R7, каждый независимо, представляют собой H, C1-4 алкил или C2-4 алкенил;
причем по меньшей мере один из Q1 и Q2, Q3 или Q4 представляет собой -PO(OR6)(OR7) или -CH2OPO(OR6)(OR7);
или его фармацевтически приемлемая соль, и указанные соединения (включая фармацевтически приемлемые соли) могут быть упомянуты в данном контексте как «соединения по данному изобретению».
Во избежание разночтений, специалистам в данной области техники следует понимать, что в данном контексте упоминание соединений из конкретных аспектов данного изобретения (например, из первого аспекта данного изобретения, т.е. упоминание соединений формулы I, определение которых приведено в первом аспекте данного изобретения) включает ссылки на все варианты реализации и их конкретные признаки, и комбинации таких вариантов реализации и конкретных признаков могут образовывать дополнительные варианты реализации и признаки данного изобретения.
Если не указано иное, все технические и научные термины, используемые в данном контексте, имеют свое обычное значение, понятное специалистам в той области техники, к которой относится данное изобретение.
Фармацевтически приемлемые соли включают соли присоединения кислот и соли присоединения оснований. Такие соли могут быть получены традиционными способами, например, посредством взаимодействия формы свободной кислоты или формы свободного основания соединения по данному изобретению с одним или более эквивалентами соответствующей кислоты или основания, необязательно в растворителе или в среде, в которой нерастворима данная соль, с последующим удалением указанного растворителя или указанной среды с применением стандартных технологий (например, in vacuo, сублимационной сушкой или фильтрованием). Соли также могут быть получены с использованием технологий, известных специалистам в данной области техники, таких как обмен противоиона соединения по данному изобретению в форме соли на другой противоион, например, с использованием подходящей ионообменной смолы.
Конкретные соли присоединения кислот, которые можно упомянуть, включают соли, образованные посредством взаимодействия с соответствующими кислотами, что приводит к протонированию соединения по данному изобретению, с образованием карбоксилатных солей (например, формиатных, ацетатных, трифторацетатных, пропионатных, изобутиратных, гептаноатных, деканоатных, капратных, каприлатных, стеаратных, акрилатных, капроатных, пропиолатных, аскорбатных, цитратных, глюкуронатных, глутаматных, гликолятных, α-гидроксибутиратных, лактатных, тартратных, фенилацетатных, манделатных, фенилпропионатных, фенилбутиратных, бензоатных, хлорбензоатных, метилбензоатных, гидроксибензоатных, метоксибензоатных, динитробензоатных, о-ацетоксибензоатных, салицилатных, никотинатных, изоникотинатных, циннаматных, оксалатных, малонатных, сукцинатных, субератных, себацинатных, фумаратных, малатных, малеатных, гидроксималеатных, гиппуратных, фталатных или терефталатных солей), галогенидных солей (например, хлоридных, бромидных или йодидных солей), сульфонатных солей (например, бензолсульфонатных, метил-, бром- или хлорбензолсульфонатных, ксилолсульфонатных, метансульфонатных, этансульфонатных, пропансульфонатных, гидроксиэтансульфонатных, 1- или 2-нафталинсульфонатных или 1,5-нафталиндисульфонатных солей) или сульфатных, пиросульфатных, бисульфатных, сульфитных, бисульфитных, фосфатных, моногидрофосфатных, дигидрофосфатных, метафосфатных, пирофосфатных или нитратных солей и т.п.
Конкретные соли присоединения оснований, которые можно упомянуть, включают соли, образованные посредством взаимодействия с соответствующими основаниями, что приводит к удалению атома протона из соединений по данному изобретению, с образованием солей с щелочными металлами (таких как соли Na и K), щелочноземельными металлами (таких как соли Mg и Ca), органическими основаниями (такими как этаноламин, диэтаноламин, триэтаноламин и трометамин) и неорганическими основаниями (такими как аммиак).
Более конкретные соли, которые можно упомянуть, включают соли Li, Na, K и аммония (включая моносоли и дисоли). В частности, для соединений по данному изобретению, в которых каждый R6 и R7 представляет собой H, конкретные соли, которые можно упомянуть, включают соли диаммония, соли динатрия, соли дилития и соли дикалия.
Во избежание разночтений, соединения по данному изобретению могут существовать в твердой форме и, следовательно, объем данного изобретения включает все их аморфные, кристаллические и частично кристаллические формы, а также они могут существовать в форме маслянистого вещества. Если соединения по данному изобретению существуют в кристаллической и частично кристаллической формах, то такие формы могут включать сольваты, которые входят в объем данного изобретения.
Во избежание разночтений, соединения по данному изобретению также могут существовать в растворе (т.е. в растворе в пригодном растворителе). Например, соединения по данному изобретению могут существовать в водном растворе, и в таком случае соединения по данному изобретению могут существовать в форме их гидратов.
Соединения по данному изобретению могут содержать двойные связи и, следовательно, если не указано иное, могут существовать как E (entgegen) и Z (zusammen) геометрические изомеры относительно каждой отдельной двойной связи. Если не указано иное, все такие изомеры и их смеси входят в объем данного изобретения.
Соединения по данному изобретению также могут демонстрировать таутомерию. Все таутомерные формы и их смеси входят в объем данного изобретения (в частности, те, которые достаточно стабильны для обеспечения возможности их выделения).
Соединения по данному изобретению также могут содержать один или более асимметричных атомов углерода и, следовательно, могут демонстрировать оптическую изомерию и/или диастереоизомерию (т.е. существовать в энантиомерных или диастереомерных формах). Диастереоизомеры можно разделять с помощью традиционных технологий, например, хроматографии или фракционной кристаллизации. Различные стереоизомеры (т.е. энантиомеры) можно выделять посредством разделения рацемической или другой смеси соединений с применением традиционных технологий, например, фракционной кристаллизации или ВЭЖХ. Альтернативно, требуемый энантиомер или диастереоизомер может быть получен из соответствующих оптически активных исходных веществ в условиях, которые не приводят к рацемизации или эпимеризации (т.е. методом «хирального пула»), посредством взаимодействия соответствующего исходного вещества с «хиральным вспомогательным агентом», который может быть затем удален на подходящей стадии, посредством дериватизации (т.е. разделения, включая динамическое разделение; например, с гомохиральной кислотой с последующим разделением диастереомерных производных традиционными способами, такими как хроматография), или посредством взаимодействия с соответствующим хиральным реагентом или хиральным катализатором, и все указанные способы и процессы можно осуществлять в условиях, известных специалистам в данной области техники. Если не указано иное, все стереоизомеры и их смеси входят в объем данного изобретения.
Если не указано иное, C1-z алкильные группы (где z представляет собой верхний предел диапазона), определенные в данном документе, могут быть неразветвленными или, если существует достаточное количество (т.е. не менее двух или трех, в зависимости от конкретного случая) атомов углерода, могут быть разветвленными и/или циклическими (образуя C3-z циклоалкильную группу). Если существует достаточное количество (т.е. не менее четырех) атомов углерода, такие группы также могут быть частично циклическими (образуя C4-z частично циклоалкильную группу). Например, циклоалкильные группы, которые можно упомянуть, включают циклопропил, циклопентил и циклогексил. Аналогично, частично циклические алкильные группы (которые также могут быть описаны как «частично циклоалкильные» группы), которые можно упомянуть, включают циклопропилметил. Если существует достаточное количество атомов углерода, такие группы также могут быть полициклическими (например, бициклическими или трициклическими) и/или спироциклическими. Во избежание разночтений, конкретные алкильные группы, которые можно упомянуть, включают алкильные группы прямого строения (т.е. неразветвленные и/или циклические).
Если не указано иное, C2-z алкенильные группы (где z представляет собой верхний предел диапазона), определенные в данном документе, могут быть неразветвленными или, если существует достаточное количество (т.е. не менее трех) атомов углерода, могут быть разветвленными и/или циклическими (образуя C4-z циклоалкенильную группу). Если существует достаточное количество (т.е. не менее пяти) атомов углерода, такие группы также могут быть частично циклическими. Например, частично циклические алкенильные группы (которые также могут быть описаны как «частично циклоалкенильные» группы), которые можно упомянуть, включают циклопентенилметил и циклогексенилметил. Если существует достаточное количество атомов углерода, такие группы также могут быть полициклическими (например, бициклическими или трициклическими) или спироциклическими. Во избежание разночтений, конкретные алкенильные группы, которые можно упомянуть, включают алкенильные группы прямого строения (т.е. неразветвленные и/или циклические).
Если не указано иное, C2-z алкинильные группы (где z представляет собой верхний предел диапазона), определенные в данном документе, могут быть неразветвленными или, если существует достаточное количество (т.е. не менее четырех) атомов углерода, могут быть разветвленными. Во избежание разночтений, конкретные алкинильные группы, которые можно упомянуть, включают алкинильные группы прямого строения (т.е. неразветвленные и/или циклические).
Во избежание разночтений, если не указано иное, группы, описанные в данном документе как «алкил», «алкенил» и/или «алкинил» следует понимать в отношении наивысшей степени ненасыщенности связи, присутствующей в таких группах. Например, такая группа, содержащая двойную углерод-углеродную связь и тройную углерод-углеродную связь в той же группе, упомянута как «алкинил». Альтернативно, может быть специально указано, что такие группы содержат только указанную степень ненасыщенности (т.е. в одной или более связях в группе, в зависимости от конкретного случая; например, в одной связи в группе).
Во избежание разночтений, алкильные, алкенильные и алкинильные группы, описанные в данном документе, также могут действовать как линкерные группы (т.е. группы, связывающие две или более частей описанного соединения), и в таком случае такие группы могут быть описаны как «алкиленовые», «алкениленовые» и/или «алкиниленовые» группы, соответственно.
Термин «арил», который может быть использован в данном контексте, может относиться к C6-14 (например, C6-10) ароматическим группам. Такие группы могут быть моноциклическими или бициклическими, и в случае бициклических групп они могут быть полностью или частично ароматическими. C6-10 арильные группы, которые можно упомянуть, включают фенил, нафтил, 1,2,3,4-тетрагидронафтил, инданил и т.п. (например, фенил, нафтил и т.п.). Во избежание разночтений, точка присоединения заместителей в арильных группах может находиться у любого пригодного атома углерода кольцевой системы.
Во избежание разночтений, специалистам в данной области техники следует понимать, что арильные группы, которые могут образовывать часть соединений по данному изобретению, представляют собой те, которые могут быть получены химическим путем, известным специалистам в данной области техники. Конкретные арильные группы, которые можно упомянуть, включают фенил и нафтил, например, фенил.
Во избежание разночтений, упоминание полициклических (например, бициклических или трициклических) групп (например, при использовании в контексте гетероциклильных или циклоалкильных групп (например, гетероциклильных групп)) относится к кольцевым системам, в которых необходимо сделать по меньшей мере два разреза для превращения таких колец в нециклическую (т.е. неразветвленную или разветвленную) цепь, при этом минимальное количество таких разрезов соответствует количеству указанных колец (например, термин «бициклические» может означать, что необходимо как минимум два разреза для превращения указанных колец в неразветвленную цепь). Во избежание разночтений, термин «бициклические» (например, при использовании в контексте алкильных групп) может относиться к группам, в которых второе кольцо двухкольцевой системы образовано между двумя соседними атомами первого кольца, к группам, в которых два несмежных атома связаны алкильной (которая, при связывании двух фрагментов, может быть упомянута как алкилен) группой (необязательно содержащей один или более гетероатомов), причем последние группы могут быть упомянуты как мостиковые, или к группам, в которых второе кольцо присоединено к одному атому, и такие группы могут быть упомянуты как спироциклические соединения.
Данное изобретение включает также меченные изотопами соединения по данному изобретению, которые идентичны описанным в данном контексте, за исключением того, что один или более атомов заменены на атом, имеющий атомную массу или массовое число, отличное от атомной массы или массового числа, обычно встречающегося в природе (или наиболее распространенного в природе). Все изотопы любого конкретного атома или элемента, указанного в данном контексте, входят в объем соединений по данному изобретению. Таким образом, соединения по данному изобретению также включают дейтерированные соединения, т.е. соединения по данному изобретению, в которых один или более атомов водорода заменены на изотоп водорода дейтерий.
Кроме того, во избежание разночтений, при указании того, что сам заместитель является необязательно замещенным одним или более заместителями (например, C1-3 алкил, необязательно замещенный одним или более F), указанные заместители, если это возможно, могут быть расположены у одного или разных атомов. Такие необязательные заместители могут присутствовать в любом пригодном количестве (например, рассматриваемая группа может быть замещена одним или более такими заместителями, например, одним таким заместителем).
Во избежание разночтений, при упоминании в данном контексте групп, которые являются необязательно замещенными, специально предусмотрено, что такие необязательные заместители могут отсутствовать (т.е. упоминание таких необязательных заместителей может быть исключено), и в таком случае необязательно замещенная группа может быть описана как незамещенная.
В случае использования, волнистая связь (т.е.  или подобное обозначение) может означать точку присоединения рассматриваемого заместителя к центральной молекуле (т.е. к соединению формулы I, к которому присоединен данный заместитель).
или подобное обозначение) может означать точку присоединения рассматриваемого заместителя к центральной молекуле (т.е. к соединению формулы I, к которому присоединен данный заместитель).
Во избежание разночтений, специалистам в данной области техники следует понимать, что соединения по данному изобретению, которые являются объектом данного изобретения, включают те, которые пригодны для получения, т.е. те, которые могут быть получены в стабильной форме. То есть соединения по данному изобретению включают соединения, которые являются достаточно прочными для того, чтобы выдерживать выделение, например, из реакционной смеси, до приемлемой степени чистоты.
В конкретных вариантах реализации соединений по данному изобретению, которые можно упомянуть, R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним или более (например, одним) атомами фтора, хлора, брома, -CN, -C(O)NR3R4, -S(O)2R5, C1-4 алкилами (например C1-3 алкилами, например C1-2 алкилами), C2-6 алкенилами (например, C2-3 алкенилами, например, этенилами) или C2-4 алкинилами (например C2-3 алкенилами, например, этинилами), причем последние три группы необязательно замещены одним или более F, при этом R3, R4 и R5 являются такими, как описано в данном документе.
В дополнительных конкретных вариантах реализации R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним или более атомами фтора, хлора, брома, группами -CN, -C(O)NR3R4 или -S(O)2Me, где R3 и R4 являются такими, как описано в данном документе.
В дополнительных конкретных вариантах реализации R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним или более (например, одним) атомами фтора, хлора, брома или метильными группами.
В дополнительных конкретных вариантах реализации R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одной или более (например, одной) группами фтора, хлора, брома.
В дополнительных конкретных вариантах реализации R1 выбран из
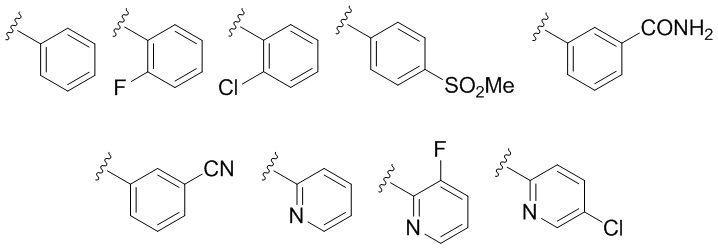
где « » означает точку присоединения к остальной части молекулы.
» означает точку присоединения к остальной части молекулы.
В дополнительных конкретных вариантах реализации R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одной или более (например, одной) группами хлора.
В более конкретных вариантах реализации R1 представляет собой фенил (т.е. является незамещенным) или 5-хлорпиридин-2-ил (например, фенил).
В конкретных вариантах реализации R2 представляет собой C1-6 алкил, необязательно замещенный одним или более F.
В конкретных вариантах реализации R2 представляет собой C1-6 алкил (т.е. является незамещенным). В более конкретных вариантах реализации R2 представляет собой C1-3 алкил, необязательно замещенный одним или более F (например, является незамещенным). В еще более конкретных вариантах реализации R2 представляет собой трифторметил, дифторметил, фторметил или, в частности, метил.
В дополнительных конкретных вариантах реализации R2 представляет собой H или, в частности, метил.
В конкретных вариантах реализации R3 и R4, каждый независимо, представляют собой H или C1-6 алкил (т.е. являются незамещенными). В более конкретных вариантах реализации R3 и R4, каждый независимо, представляют собой C1-3 алкил, необязательно замещенный одним или более F (например, являются незамещенными). В еще более конкретных вариантах реализации R3 и R4, каждый независимо, представляют собой H, трифторметил, дифторметил, фторметил или метил. В дополнительных конкретных вариантах реализации оба R3 и R4 представляют собой H.
В конкретных вариантах реализации R5 представляет собой C1-6 алкил (т.е. является незамещенным). В более конкретных вариантах реализации R5 представляет собой C1-3 алкил, необязательно замещенный одним или более F (например, является незамещенным). В еще более конкретных вариантах реализации R5 представляет собой трифторметил, дифторметил, фторметил или, в частности, метил.
В соединениях по данному изобретению по меньшей мере один из Q1 и Q2, Q3 или Q4 (т.е. по меньшей мере один из Q1 и Q2; или Q1 и Q3; или Q1 и Q4, в зависимости от конкретного случая) представляет собой -PO(OR6)(OR7) или -CH2OPO(OR6)(OR7). Таким образом, соединения по данному изобретению могут содержать одну или две фосфатные или фосфорамидные кислотные группы, или группы их сложных эфиров (-OPO(OR6)(OR7) или -NHPO(OR6)(OR7)/-NRxPO(OR6)(OR7), где Rx представляет собой углеродную группу (например, алкил)) (т.е. один или два из Q1 и Q2, Q3 или Q4 могут представлять собой -PO(OR6)(OR7) или -CH2OP(OR6)(OR7) (в зависимости от конкретного случая)). Если один из Q1 и Q2, Q3 или Q4 представляет собой -PO(OR6)(OR7) или -CH2OP(OR6)(OR7), остальная группа представляет собой H.
В более конкретных вариантах реализации один из Q1 и Q2, Q3 или Q4 представляет собой -PO(OR6)(OR7) или -CH2OPO(OR6)(OR7), а другой представляет собой Q1, и (при наличии) Q2 или Q3 представляет собой H (Q4 представляет собой -CH2OPO(OR6)(OR7) или отсутствует).
Конкретные соединения по данному изобретению, которые можно упомянуть, включают соединения, в которых
 представляет собой
представляет собой 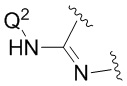 ,
,  или
или 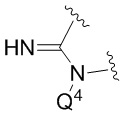 .
.
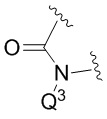
Конкретные соединения по данному изобретению, которые можно упомянуть, включают соединения, в которых если
 представляет собой
представляет собой 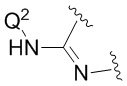 или
или 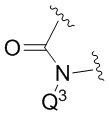 ,
,
то один из Q1 и Q2 или Q3 представляет собой -PO(OR6)(OR7) или -CH2OPO(OR6)(OR7), а другой из Q1 и Q2 или Q3 представляет собой H; и
если  представляет собой
представляет собой 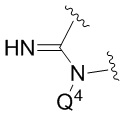 ,
,
то Q1 представляет собой H, и Q4 представляет собой -CH2OPO(OR6)(OR7).
В конкретных вариантах реализации, которые можно упомянуть,  представляет собой
представляет собой
 или
или 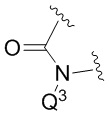 .
.
В более конкретных вариантах реализации  представляет собой
представляет собой 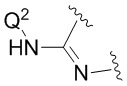 .
.
В альтернативных конкретных вариантах реализации  представляет собой
представляет собой 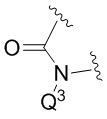 .
.
В конкретных вариантах реализации, которые можно упомянуть, Q1 представляет собой -PO(OR6)(OR7).
В конкретных вариантах реализации, которые можно упомянуть,
 представляет собой
представляет собой 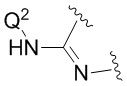 или
или 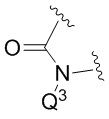 ; и
; и
Q1 представляет собой -PO(OR6)(OR7).
В дополнительных конкретных вариантах реализации, в которых  представляет собой
представляет собой 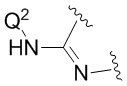 или
или 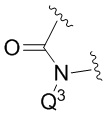 ,
,
Q1 представляет собой -PO(OR6)(OR7);
и каждый Q2 или Q3 (в зависимости от конкретного случая) представляет собой H.
В конкретных вариантах реализации Q1 представляет собой -PO(OR6)(OR7).
В конкретных вариантах реализации Q2 представляет собой -PO(OR6)(OR7).
В более конкретных вариантах реализации, в которых  представляет собой
представляет собой 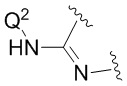 ,
,
Q2 представляет собой -PO(OR6)(OR7); и
Q1 представляет собой H.
В конкретных вариантах реализации Q3 представляет собой -CH2PO(OR6)(OR7).
В более конкретных вариантах реализации, в которых  представляет собой
представляет собой 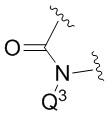 ,
,
Q3 представляет собой -CH2PO(OR6)(OR7); и
Q1 представляет собой H.
В конкретных вариантах реализации, в которых  представляет собой
представляет собой 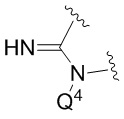 ,
,
Q1 представляет собой H.
В конкретных вариантах реализации Q2 представляет собой H.
В конкретных вариантах реализации Q3 представляет собой H.
В дополнительных конкретных вариантах реализации Q2, Q3 или Q4 (в зависимости от конкретного случая) представляет собой H.
В конкретных вариантах реализации, которые можно упомянуть,
Q1 представляет собой -PO(OR6)(OR7) (например, -PO(OH)2);
 представляет собой
представляет собой 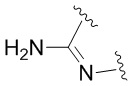 или
или 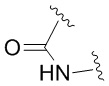 ; или
; или
Q1 представляет собой H, и
 представляет собой
представляет собой 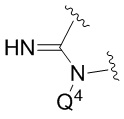 , где Q4 представляет собой -CH2OPO(OR6)(OR7) (например, -CH2OPO(OH)2);
, где Q4 представляет собой -CH2OPO(OR6)(OR7) (например, -CH2OPO(OH)2);
и R1 и R2 являются такими, как описано в данном документе.
В конкретных вариантах реализации, которые можно упомянуть, R6 и R7, каждый независимо, представляют собой C1-3 алкил (например, C1-2 алкил) или H. В более конкретных вариантах реализации каждый R6 и R7 представляет собой H.
В дополнительных вариантах реализации каждый R6 и R7 представляет собой метил, или каждый из них представляет собой этил.
В дополнительных конкретных вариантах реализации R6 представляет собой изо-пропил, и R7 представляет собой H.
В конкретных вариантах реализации, которые можно упомянуть, соединение формулы I представляет собой соединение формулы Ia,
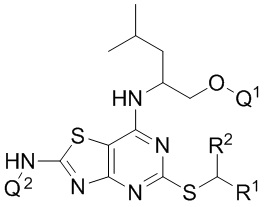 (Ia)
(Ia)
где R1, R2, Q1 и Q2 являются такими, как определено выше, или его фармацевтически приемлемую соль.
В конкретных вариантах реализации соединения формулы Ia, которые можно упомянуть,
Q1 представляет собой -PO(OR6)(OR7);
Q2 представляет собой H;
R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одной или более (например, одной) группами, выбранными из группы, состоящей из хлора, фтора, -CN, -CONH2 и -SO2Me (в частности, фенил (т.е. незамещенный));
R2 представляет собой H или C1-3 алкил (например, метил);
R6 и R7, каждый независимо, представляют собой C1-3 алкил (например, Me) или H; более конкретно, R6 представляет собой изо-пропил, и R7 представляет собой H, или каждый R6 и R7 представляет собой H (например, каждый R6 и R7 представляет собой H).
В дополнительных конкретных вариантах реализации соединения формулы Ia, которые можно упомянуть,
Q1 представляет собой -PO(OR6)(OR7);
Q2 представляет собой H;
R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним или более (например, одним) атомами хлора (в частности, фенил, т.е. незамещенный));
R2 представляет собой C1-3 алкил (например, метил);
R6 и R7, каждый независимо, представляют собой C1-2 алкил (например, Me) или, в частности, H.
В других конкретных вариантах реализации соединения формулы Ia
Q1 представляет собой H;
Q2 представляет собой -PO(OR6)(OR7);
R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одной или более (например, одной) группами, выбранными из группы, состоящей из фтора, хлора или -CN (в частности, фенил (т.е. незамещенный));
R2 представляет собой C1-3 алкил (например, метил);
R6 и R7, каждый независимо, представляют собой C1-3 алкил (например, Me) или, в частности, H.
В дополнительных конкретных вариантах реализации соединения формулы Ia
Q1 представляет собой H;
Q2 представляет собой -PO(OR6)(OR7);
R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним или более (например, одним) атомами хлора (в частности, фенил, т.е. незамещенный));
R2 представляет собой C1-3 алкил (например, метил);
R6 и R7, каждый независимо, представляют собой C1-2 алкил (например, Me) или, в частности, H.
В других конкретных вариантах реализации, которые можно упомянуть, соединение формулы I представляет собой соединение формулы Ib,
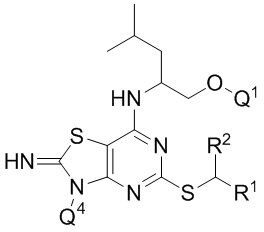 (Ib)
(Ib)
где R1, R2, Q1, Q4 являются такими, как определено выше, или его фармацевтически приемлемую соль.
В конкретных вариантах реализации соединения формулы Ib, которые можно упомянуть,
Q4 представляет собой -CH2OPO(OR6)(OR7);
Q1 представляет собой H;
R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одной или более (например, одной) группами, выбранными из фтора, хлора и -CN (в частности, фенил (т.е. незамещенный));
R2 представляет собой C1-3 алкил (например, метил); и
R6 и R7, каждый независимо, представляют собой C1-2 алкил (например, Me) или, в частности, H.
В дополнительных конкретных вариантах реализации соединения формулы Ib, которые можно упомянуть,
Q4 представляет собой -CH2OPO(OR6)(OR7);
Q1 представляет собой H;
R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним или более (например, одним) атомами хлора (в частности, фенил, т.е. незамещенный));
R2 представляет собой C1-3 алкил (например, метил); и
R6 и R7, каждый независимо, представляют собой C1-2 алкил (например, Me) или, в частности, H.
В других конкретных вариантах реализации, которые можно упомянуть, соединение формулы I представляет собой соединение формулы Ic,
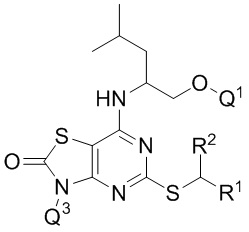 (Ic)
(Ic)
где R1, R2, Q1 и Q3 являются такими, как определено выше, или его фармацевтически приемлемую соль.
В конкретных вариантах реализации соединения формулы Ic, которые можно упомянуть,
Q1 представляет собой -PO(OR6)(OR7);
Q3 представляет собой H;
R1 представляет собой фенил, необязательно замещенный одной или более (например, одной) группами, выбранными из группы, состоящей из хлора, -SO2Me, -CN и -CONH2; или, в частности, пиридил, необязательно замещенный одним или более (например, одним) атомами хлора (например, 5-хлорпиридин-2-ил);
R2 представляет собой C1-3 алкил (например, метил); и
R6 и R7, каждый независимо, представляют собой C1-2 алкил (например, Me) или, в частности, H.
В дополнительных конкретных вариантах реализации соединения формулы Ic, которые можно упомянуть,
Q1 представляет собой -PO(OR6)(OR7);
Q3 представляет собой H;
R1 представляет собой фенил, необязательно замещенный одним или более (например, одним) атомами хлора, или, в частности, пиридил, необязательно замещенный одним или более (например, одним) атомами хлора (например, 5-хлорпиридин-2-ил);
R2 представляет собой C1-3 алкил (например, метил); и
R6 и R7, каждый независимо, представляют собой C1-2 алкил (например, Me) или, в частности, H.
В других конкретных вариантах реализации соединения формулы Ic, которые можно упомянуть,
Q1 представляет собой H;
Q3 представляет собой -CH2OPO(OR6)(OR7);
R1 представляет собой фенил, необязательно замещенный одним или более (например, одним) атомами хлора, или, в частности, пиридил, необязательно замещенный одним или более (например, одним) атомами хлора (например, 5-хлорпиридин-2-ил);
R2 представляет собой C1-3 алкил (например, метил); и
R6 и R7, каждый независимо, представляют собой C1-2 алкил (например, Me) или, в частности, H.
В дополнительных конкретных вариантах реализации соединение формулы I представляет собой соединение формулы IA
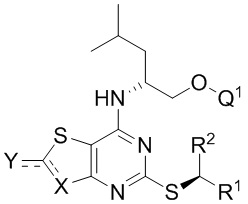 (IА)
(IА)
где R1, R2, Q1 и  являются такими, как определено выше, или его фармацевтически приемлемую соль.
являются такими, как определено выше, или его фармацевтически приемлемую соль.
Специалистам в данной области техники понятно, что соединение формулы IA представляет собой один энантиомер соединения формулы I. В соответствии с условными обозначениями, клиновидные и штриховые связи означают по существу отсутствие другой стереохимии у каждого стереоцентра.
В дополнительных конкретных вариантах реализации соединение формулы IA представляет собой соединение формулы IAa, IAb или IAc,
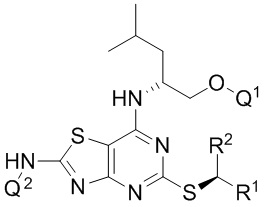 (IAa),
(IAa),
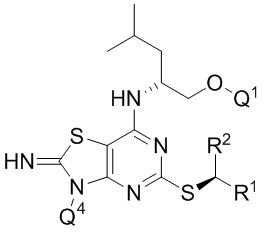 (IAb),
(IAb),
 (IAc)
(IAc)
где (для каждого из соединений IAa, IAb и IAc), R1, R2, Q1, Q2, Q3 и Q4 являются такими, как определено в данном документе, в частности, в отношении соединений формулы Ia, Ib и Ic, соответственно, или его фармацевтически приемлемую соль.
В дополнительных конкретных вариантах реализации соединение формулы I представляет собой соединение формулы IB или IC.
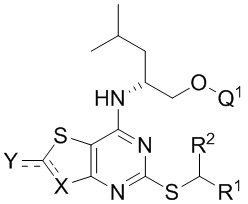 (IB)
(IB)
где R1, R2, Q1, Q2, Q3 и Q4 являются такими, как определено в данном документе, в частности, в отношении соединений формулы Ia, Ib и Ic.
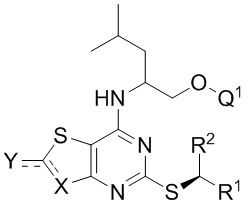 (IC)
(IC)
где R1, R2, Q1, Q2, Q3 и Q4 являются такими, как определено в данном документе, в частности, в отношении соединений формулы Ia, Ib и Ic.
Конкретные соединения по данному изобретению, которые можно упомянуть, включают соединения, описанные в примерах, приведенных в данном документе, и их фармацевтически приемлемые соли. Во избежание разночтений, если указанные соединения по данному изобретению включают соединения в конкретной солевой форме, то соединения по данному изобретению включают указанные соединения в несолевой форме и в форме любой фармацевтически приемлемой соли (которая может включать солевую форму, представленную в указанных примерах).
Более конкретные соединения по данному изобретению, которые можно упомянуть, включают:
(2R)-2-[(2-Амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат,
[7-{[(1R)-1-(Гидроксиметил)-3-метилбутил]амино}-2-имино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат и
(2R)-2-[(5-{[(1S)-1-(5-Хлорпиридин-2-ил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат,
и их фармацевтически приемлемые соли.
Фармацевтически приемлемые соли
Как упомянуто выше, соединения по данному изобретению могут быть в форме фармацевтически приемлемых солей.
В конкретных вариантах реализации фармацевтически приемлемая соль представляет собой соль присоединения основания.
В более конкретных вариантах реализации, в частности, в тех, в которых каждый R6 и R7 представляет собой H (т.е. в соединениях, содержащих фосфатные группы -OPO(OH)2), фармацевтически приемлемая соль представляет собой соль двукратного присоединения основания.
В данном контексте выражение «соль двукратного присоединения основания» можно понимать как означающее соль, образованную в результате взаимодействия кислотного соединения (такого как соединение по данному изобретению, где каждый R6 и R7 представляет собой H) с двумя моль соответствующего основания.
В конкретных вариантах реализации фармацевтически приемлемая соль представляет собой соль аммония или соль щелочного металла (Li, K или, в частности, Na) (включая моносоли и дисоли). В более конкретных вариантах реализации соль представляет собой соль диаммония или динатрия.
Медицинское применение
Как отмечено в данном документе, соединения по данному изобретению и, следовательно, содержащие их композиции и наборы пригодны в качестве фармацевтических препаратов. В частности, соединения по данному изобретению и их производные являются модуляторами активности рецептора фракталкина (CX3CR1) и, следовательно, их можно использовать для лечения и/или предупреждения заболеваний или расстройств, связанных с повышенными уровнями рецептора фракталкина (CX3CR1) и/или его ассоциированного лиганда фракталкина (CX3CL1).
Таким образом, в соответствии со вторым аспектом данного изобретения, предложено соединение по данному изобретению, определение которого приведено выше (т.е. соединение, определение которого приведено в первом аспекте данного изобретения, включая все варианты реализации и конкретные признаки), для применения в качестве фармацевтического препарата (или для применения в медицине).
Во избежание разночтений, ссылки на соединения, определение которых приведено в первом аспекте данного изобретения, включают ссылки на соединения формулы I (включая все их варианты реализации, такие как соединения формул Ia, Ib, Ic, IA, IAa, IAb, IAc, IB, IC) и их фармацевтически приемлемые соли.
Таким образом, во избежание разночтений, соединения по данному изобретению являются пригодными, поскольку они обладают фармакологической активностью и/или метаболизируются в организме после перорального или парентерального введения с образованием соединений, которые обладают фармакологической активностью.
Как описано в данном документе, соединения по данному изобретению могут быть особенно пригодны для лечения и/или предупреждения заболеваний или расстройств, связанных с повышенными уровнями CX3CR1 и/или CX3CL1.
Так, в третьем аспекте данного изобретения предложено соединение по данному изобретению, определение которого приведено ранее, для применения для лечения и/или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1.
В альтернативном третьем аспекте данного изобретения предложен способ лечения и/или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения по данному изобретению, определение которого приведено ранее.
В дополнительном альтернативном третьем аспекте данного изобретения предложено применение соединения по данному изобретению, определение которого приведено ранее, для производства лекарственного средства для лечения и/или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1.
Специалистам в данной области техники понятно, что упоминание лечения определенного патологического состояния (или также терапии указанного состояния) имеет обычное значение в области медицины. В частности, указанные термины могут относиться к достижению снижения тяжести и/или частоты возникновения одного или более клинических симптомов, связанных с патологическим состоянием, по решению врача, наблюдающего пациента, страдающего или предрасположенного к таким симптомам. Например, в случае рака указанный термин может относиться к достижению уменьшения количества присутствующих раковых клеток (например, в случае рака, образующего солидную опухоль, на это указывает уменьшение объема опухоли).
В данном контексте термин «предупреждение» (и аналогично предотвращение) включает указание профилактики заболевания или расстройства (и наоборот). Следовательно, указание предупреждения также может означать указание профилактики и наоборот. В частности, такие термины могут относиться к достижению уменьшения (например, уменьшения по меньшей мере на 10%, например, уменьшения по меньшей мере на 20%, 30% или 40%, например, уменьшения на по меньшей мере 50%) вероятности развития у пациента (или здорового субъекта) данного патологического состояния (что можно понимать как обозначение того, что состояние пациента изменяется таким образом, что врач диагностирует у пациента наличие соответствующего заболевания или расстройства, например, требующего лечения).
В данном контексте упоминание пациента (или пациентов) относится к живым субъектам, проходящим лечение, включая млекопитающих пациентов (например, людей). В частности, упоминание пациента относится к пациентам, являющимся людьми.
Во избежание разночтений, специалистам в данной области техники следует понимать, что такое лечение или предупреждение осуществляют в отношении пациента (или субъекта), нуждающегося в этом. Потребность пациента (или субъекта) в таком лечении или предупреждении может быть установлена специалистом в данной области техники стандартными способами.
В данном контексте термины «заболевание» и «расстройство» (и, аналогично, термины «патологическое состояние», «болезнь», «медицинская проблема» и т.п.) могут быть использованы взаимозаменяемо.
В данном контексте термин «эффективное количество» относится к количеству соединения, которое обеспечивает терапевтический эффект у пациента, проходящего лечение. Указанный эффект можно наблюдать объективно (например, эффект может быть измерен каким-либо тестом или маркером) или субъективно (т.е. субъект демонстрирует признаки и/или ощущает эффект). В частности, указанный эффект можно наблюдать (например, измерять) объективно, используя соответствующие тесты, известные специалистам в данной области техники.
Заболевания и расстройства, которые, как известно, связаны с повышенными уровнями CX3CR1 и/или CX3CL1, включают острое и/или хроническое воспаление, болезни глаз (такие как дегенерация желтого пятна), болезни легких (такие как легочная артериальная гипертензия, астма и легочный фиброз), болезни кожи (такие как атопический дерматит и прурит), болезни суставов и/или костей (такие как остеоартрит, остеопороз и апластическая анемия), аутоиммунные заболевания (такие как анкилозирующий спондилит, рассеянный склероз, системный склероз и ревматоидный артрит), сердечнососудистые и метаболические заболевания (такие как инсульт и артериосклероз (включая атеросклероз), нестабильная стенокардия, инфаркт миокарда, болезни сонной артерии, хроническая сердечная недостаточность, воспалительная кардиомиопатия, болезнь периферических артерий и диабет), заболевания головного мозга и нейродегенеративные заболевания (такие как болезнь Альцгеймера, болезнь Паркинсона и травматическое повреждение головного мозга), боль (такую как хроническая боль, фибромиалгия, невропатическая боль, боль, обусловленная химиотерапией, и боль при грыже межпозвоночных дисков), рак (такой как рак яичников, рак легких, рак предстательной железы, рак печени, рак поджелудочной железы, B-клеточная лимфома и рак молочной железы), болезнь печени (такую как цирроз), болезни почек (такие как IgA-нефропатия, воспаление почек, волчанка, ишемическое реперфузионное повреждение, ишемическая острая почечная недостаточность и контраст-индуцированное повреждение почек), желудочно-кишечные заболевания (такие как колит, болезнь Крона, воспалительная болезнь кишечника и панкреатит), вирус иммунодефицита человека (ВИЧ) (такой как ВИЧ-1 и ВИЧ-ассоциированная деменция) и расстройства настроения (такие как депрессия, тревога, шизофрения и расстройства аутического спектра).
Конкретные заболевания и расстройства, которые, как известно, связаны с повышенными уровнями CX3CR1 и/или CX3CL1, которые можно упомянуть, включают болезни глаз (такие как дегенерация желтого пятна), болезни легких (такие как легочная артериальная гипертензия, астма и легочный фиброз), болезни кожи (такие как атопический дерматит и прурит), болезни суставов и/или костей (такие как остеоартрит, остеопороз и апластическая анемия), аутоиммунные заболевания (такие как анкилозирующий спондилит, рассеянный склероз, системный склероз и ревматоидный артрит), сердечнососудистые и метаболические заболевания (такие как артериосклероз (включая атеросклероз), нестабильная стенокардия, инфаркт миокарда, болезни сонной артерии, хроническая сердечная недостаточность и диабет), заболевания головного мозга и нейродегенеративные заболевания (такие как болезнь Альцгеймера и травматическое повреждение головного мозга), боль (такую как хроническая боль, фибромиалгия, невропатическая боль, боль, обусловленная химиотерапией, и боль при грыже межпозвоночных дисков), рак (такой как рак яичников, рак легких, рак предстательной железы, рак печени, рак поджелудочной железы, B-клеточная лимфома и рак молочной железы), болезнь печени (такую как цирроз), болезни почек (такие как IgA-нефропатия, воспаление почек, волчанка и ишемическое реперфузионное повреждение), желудочно-кишечные заболевания (такие как колит, воспалительная болезнь кишечника и панкреатит) и вирус иммунодефицита человека (ВИЧ) (такой как ВИЧ-1 и ВИЧ-ассоциированная деменция).
В конкретных вариантах реализации (т.е. в некоторых вариантах реализации третьего аспекта данного изобретения) заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из болезней глаз, болезней легких, болезней кожи, болезней суставов и/или костей, аутоиммунных заболеваний, сердечнососудистых заболеваний, метаболических заболеваний, болезней головного мозга, нейродегенеративных заболеваний, боли, рака, болезней печени, болезней почек, желудочно-кишечных заболеваний и вируса иммунодефицита человека.
В конкретных вариантах реализации (т.е. в некоторых вариантах реализации третьего аспекта данного изобретения) заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из болезней глаз, болезней легких, болезней кожи, болезней суставов и/или костей, аутоиммунных заболеваний, сердечнососудистых заболеваний, метаболических заболеваний, болезней головного мозга, нейродегенеративных заболеваний, боли, рака, болезней печени, болезней почек, желудочно-кишечных заболеваний, вируса иммунодефицита человека и нарушений настроения.
В более конкретных вариантах реализации заболевание или расстройство, связанное с фракталкином и повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из дегенерации желтого пятна, легочной артериальной гипертензии, астмы, легочного фиброза, атопического дерматита, прурита, остеоартрита, остеопороза, апластической анемии, анкилозирующего спондилита, рассеянного склероза, системного склероза, ревматоидного артрита, артериосклероза, нестабильной стенокардии, инфаркта миокарда, болезней сонной артерии, хронической сердечной недостаточности, диабета, болезни Альцгеймера, травматического повреждения головного мозга, хронической боли, фибромиалгии, невропатической боли, боли, вызванной химиотерапией, боли при грыже межпозвоночных дисков, рака (например, рака яичников, рака легких, рака печени, рака поджелудочной железы, B-клеточной лимфомы и рака молочной железы), цирроза печени, IgA-нефропатии, воспаления почек, волчанки, ишемического реперфузионного повреждения, колита, воспалительной болезни кишечника, панкреатита, вируса-1 иммунодефицита человека и деменции на фоне вируса иммунодефицита человека, инсульта, болезни Паркинсона, депрессии, тревоги, шизофрении и расстройств аутического спектра.
В более конкретных вариантах реализации заболевание или расстройство, связанное с фракталкином и повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из дегенерации желтого пятна, легочной артериальной гипертензии, астмы, легочного фиброза, атопического дерматита, прурита, остеоартрита, остеопороза, апластической анемии, анкилозирующего спондилита, рассеянного склероза, системного склероза, ревматоидного артрита, артериосклероза, нестабильной стенокардии, инфаркта миокарда, болезней сонной артерии, хронической сердечной недостаточности, диабета, болезни Альцгеймера, травматического повреждения головного мозга, хронической боли, фибромиалгии, невропатической боли, боли, вызванной химиотерапией, боли при грыже межпозвоночных дисков, рака (например, рака яичников, рака легких, рака печени, рака поджелудочной железы, B-клеточной лимфомы и рака молочной железы), цирроза печени, IgA-нефропатии, воспаления почек, волчанки, ишемического реперфузионного повреждения, колита, воспалительной болезни кишечника, панкреатита, вируса-1 иммунодефицита человека и деменции на фоне вируса иммунодефицита человека.
В более конкретных вариантах реализации заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из атопического дерматита, рассеянного склероза, ревматоидного артрита, атеросклероза, инфаркта миокарда, хронической сердечной недостаточности, воспалительной кардиомиопатии, фибромиалгии, невропатической боли, боли, обусловленной химиотерапией, B-клеточной лимфомы, рака молочной железы, IgA-нефропатии, волчанки, ишемической острой почечной недостаточности и панкреатита.
В еще более конкретных вариантах реализации заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из инфаркта миокарда, артериосклероза, рассеянного склероза, ревматоидного артрита, болезни Крона, панкреатита, невропатической боли, боли, обусловленной химиотерапией, и рака (например, рака яичников, рака легких, рака печени, рака поджелудочной железы, B-клеточной лимфомы и рака молочной железы).
В конкретных вариантах реализации лечение заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1, проводят у пациента с существенно повышенными уровнями CX3CL1 в плазме крови. Например, у таких пациентов концентрация CX3CL1 в плазме крови может составлять более чем около 300 пикограмм на миллилитр (пг/мл). В частности, у таких пациентов концентрация CX3CL1 в плазме крови может составлять от около 350 пг/мл до около 600 пг/мл.
Фармацевтические композиции
Как описано в данном документе, соединения по данному изобретению пригодны в качестве фармацевтических средств. Такие соединения можно вводить отдельно, или их можно вводить в виде известных фармацевтических композиций/лекарственных форм.
В четвертом аспекте данного изобретения предложена фармацевтическая композиция, содержащая соединение по данному изобретению, описанное в данном документе, и необязательно одно или более фармацевтически приемлемых вспомогательных веществ.
В данном контексте термин «фармацевтически приемлемые вспомогательные вещества» включает указание жидких сред, адъювантов, носителей, разбавителей, рН-регулирующих и буферных агентов, агентов для изменения тоничности, стабилизаторов, смачивающих агентов и т.п. В частности, такие вспомогательные вещества могут включать адъюванты, разбавители или носители.
В конкретном варианте реализации четвертого аспекта данного изобретения фармацевтическая композиция содержит по меньшей одно фармацевтически приемлемое вспомогательное вещество.
Во избежание разногласий, в данном контексте указание соединений по данному изобретению, предназначенных для конкретного применения (и, точно так же, применения и способов применения, касающихся соединений по данному изобретению), также может относиться к фармацевтическим композициям, содержащим соединения по данному изобретению, описанным в данном контексте.
Таким образом, в пятом аспекте данного изобретения предложена фармацевтическая композиция, определение которой приведено в четвертом аспекте данного изобретения, для применения для лечения заболеваний, связанных в фракталкином (описанных в данном документе в отношении третьего аспекта данного изобретения и всех его вариантов реализации).
Специалистам в данной области техники понятно, что соединения по данному изобретению действуют системно и/или местно (т.е. в определенном очаге) и, следовательно, их можно вводить подходящими способами, известными специалистам в данной области техники.
Специалистам в данной области техники понятно, что соединения и композиции, описанные в данном документе, обычно вводят перорально, внутривенно, интраокулярно, подкожно, буккально, ректально, дермально, назально, трахеально, бронхиально, сублингвально, интраназально, местно, любым другим парентеральным способом или ингаляцией, в фармацевтически приемлемой лекарственной форме. В частности, предложенные соединения можно вводить перорально (т.е. посредством введения через рот) или внутривенно.
Фармацевтические композиции, описанные в данном документе, включают композиции в форме таблеток, капсул или эликсиров для перорального введения, суппозиториев для ректального введения, стерильных растворов или суспензий для парентерального (например, внутривенного) или внутримышечного введения и т.п.
Таким образом, в конкретных вариантах реализации предложена фармацевтическая композиция в фармацевтически приемлемой лекарственной форме, включая таблетки или капсулы, жидкие формы для перорального применения или инъекций, суппозитории, кремы, гели, пены или средства для ингаляции (например, для интраназального введения), или формы для местного применения (например, глазные капли). Во избежание разночтений, в таких вариантах реализации соединения по данному изобретению могут быть представлены в твердой (например, в форме дисперсии твердых частиц), жидкой (например, в растворе) или других формах, например, в форме мицелл.
Например, при получении фармацевтических лекарственных форм для перорального введения соединение можно смешивать с твердыми порошкообразными ингредиентами, такими как лактоза, сахароза, сорбит, маннит, крахмал, амилопектин, производные целлюлозы, желатин или другой пригодный ингредиент, а также с разрыхлителями и смазывающими агентами, такими как стеарат магния, стеарат кальция, стеарилфумарат натрия и полиэтиленгликолевые воски. Затем полученные смеси можно перерабатывать в гранулы или прессовать в таблетки.
Мягкие желатиновые капсулы могут быть получены с капсулами, содержащими одно или более активных соединений (например, соединений по первому и, следовательно, второму и третьему аспектам данного изобретения, и необязательно дополнительных терапевтических агентов), вместе, например, с растительным маслом, жиром или другим пригодным носителем для мягких желатиновых капсул. Аналогично, твердые желатиновые капсулы могут содержать такое соединение(я) в комбинации с твердыми порошкообразными ингредиентами, такими как лактоза, сахароза, сорбит, маннит, картофельный крахмал, кукурузный крахмал, амилопектин, производные целлюлозы или желатин.
Единичные лекарственные формы для ректального введения могут быть получены (i) в форме суппозиториев, которые содержат соединение(я), смешанное с нейтральной жировой основой; (ii) в форме желатиновой ректальной капсулы, которая содержит активное вещество в смеси с растительным маслом, парафиновым маслом или другим пригодным носителем для желатиновых ректальных капсул; (iii) в форме готовой микроклизмы; или (iv) в форме сухой композиции микроклизмы для разведения в пригодном растворителе непосредственно перед введением.
Жидкие препараты для перорального введения могут быть получены в форме сиропов или суспензий, например, растворов или суспензий, содержащих соединение(я), а остальную часть композиции составляет сахар или сахарные спирты, а также смесь этанола, воды, глицерина, пропиленгликоля и полиэтиленгликоля. При необходимости такие жидкие препараты могут содержать окрашивающие агенты, вкусоароматические агенты, сахарин и карбоксиметилцеллюлозу или другой загуститель. Жидкие препараты для перорального введения также могут быть получены в форме сухого порошка для разведения пригодным растворителем перед применением.
Растворы для парентерального введения могут быть получены в виде раствора соединения(й) в фармацевтически приемлемом растворителе (например, воде). Указанные растворы также могут содержать стабилизирующие агенты и/или буферные ингредиенты и разделены на единичные дозы в форме ампул или флаконов. Растворы для парентерального введения также могут быть получены в форме сухого препарата для разведения пригодным растворителем непосредственно перед применением.
В зависимости, например, от эффективности и физических свойств соединения по данному изобретению (т.е. активного ингредиента), фармацевтические лекарственные формы, которые можно упомянуть, включают формы, в которых активный ингредиент присутствует в количестве по меньшей мере 1% (или по меньшей мере 10%, по меньшей мере 30% или по меньшей мере 50%) по массе. То есть отношение активного ингредиента к другим компонентам (т.е. к дополнительному адъюванту, разбавителю и носителю) фармацевтической композиции составляет по меньшей мере 1:99 (или по меньшей мере 10:90, по меньшей мере 30:70 или по меньшей мере 50:50) по массе.
Специалистам в данной области техники понятно, что соединения по данному изобретению можно вводить (например, в виде лекарственных форм, описанных выше) в разных дозах, причем пригодные дозы могут быть без труда установлены специалистом в данной области техники. Пероральные, пульмональные и местные лекарственные формы (а также подкожные лекарственные формы, хотя такие дозы могут быть относительно меньше) могут варьироваться от около 0,01 мг/кг массы тела в сутки (мг/кг/сутки) до около 30 мг/кг/сутки, предпочтительно от около 0,1 до около 5,0 мг/кг/сутки, и более предпочтительно от около 0,5 до около 3,0 мг/кг/сутки. Например, при пероральном введении лечение такими соединениями может включать введение лекарственных форм, обычно содержащих от около 0,01 мг до около 5000 мг, например, от около 0,1 мг до около 500 мг или от около 1 мг до около 400 мг (например, от около 20 мг до около 200 мг) активного ингредиента(ов). При внутривенном введении наиболее предпочтительные дозы составляют от около 0,001 до около 10 мг/кг/час на протяжении инфузии с постоянной скоростью. Преимущественно, лечение может включать введение таких соединений и композиций в однократной суточной дозе, или общая суточная доза может быть введена дробными дозами два, три или четыре раза в сутки (например, дважды в сутки в отношении доз, описанных в данном документе, например, дозы 25 мг, 50 мг, 100 мг или 200 мг дважды в сутки).
При использовании в данном документе в отношении определенного значения (такого как количество), термин «около» (или подобные термины, такие как «приблизительно») следует понимать как означающий, что такие значения могут варьироваться в пределах до 10% (в частности, до 5%, например, до 1%) от указанного значения. Предусмотрено, что в каждом случае такие термины могут быть заменены указанием «“±10%» или подобными обозначениями (или указанием величины отклонения от конкретного значения, рассчитанного на основании соответствующего значения). Также предусмотрено, что в каждом случае указанные термины могут быть исключены.
Во избежание разночтений, опытный специалист (например, врач) может определить фактическую дозу, которая будет наиболее подходящей для конкретного пациента, которая вероятно варьируется в зависимости от способа введения, типа и тяжести состояния, подлежащего лечению, а также от биологического вида, возраста, массы, пола, почечной функции, печеночной функции и ответа конкретного пациента, подлежащего лечению. Несмотря на то, что вышеупомянутые дозы являются иллюстративными для среднего случая, конечно, могут иметь место отдельные случаи, в которых уместны более высокие или низкие диапазоны доз, и такие дозы входят в объем данного изобретения.
Соединения по данному изобретению демонстрируют существенно улучшенную растворимость в воде по сравнению с известными антагонистами рецептора фракталкина, а также существенно улучшенную стабильность при длительном хранении в водной среде.
Соответственно, в конкретных вариантах реализации соединения, содержащие одно или более (например, одно) соединений по данному изобретению, дополнительно содержат воду.
В более конкретных вариантах реализации предложенная фармацевтическая композиция, содержащая одно или более (например, одно) соединений по данному изобретению, представлена в форме водного раствора.
Специалистам в данной области техники понятно, что указание фармацевтических композиций, представленных в форме водного раствора, относится к композициям, в которых активный ингредиент и необязательно одно или более фармацевтически приемлемых вспомогательных веществ растворены в воде.
Существенно улучшенная растворимость в воде и стабильность при хранении в водной среде обеспечивает возможность составления соединений по данному изобретению в водные композиции (например, в форме водных растворов) без необходимости включения солюбилизирующих вспомогательных веществ.
Так, в конкретных вариантах реализации предложена фармацевтическая композиция, содержащая одно или более (например, одно) соединений по данному изобретению, воду и менее 20% (мас./мас.) солюбилизирующих вспомогательных веществ (например, менее 10%, например, менее 5%, например, менее 1%). В более конкретных вариантах реализации такая композиция представлена в форме водного раствора.
В данном контексте выражение «солюбилизирующие вспомогательные вещества» можно понимать как указание (фармацевтически приемлемых) вспомогательных веществ, которые используют для солюбилизации органических соединений в водной среде (например, в водной фармацевтической композиции), для получения стабильного раствора или суспензии активного ингредиента. Такие солюбилизирующие вспомогательные вещества включают смешиваемые с водой/растворимые в воде растворители и водорастворимые поверхностно-активные вещества. Примеры таких вспомогательных веществ включают этанол, полиэтиленгликоль (ПЭГ) (ПЭГ 400, ПЭГ 300), полисорбаты, циклодекстрины, диметилсульфоксид, полисорбат 80 (Tween 80), пропиленгликоль, этиленгликоль, глицерин, диметилацетамид, полиоксиэтилированные касторовые масла (например, Chremophor), полиоксиэтилированные глицериды, стеариловый спирт, олеиловый спирт.
В альтернативных вариантах реализации фармацевтические композиции, содержащие соединения по данному изобретению, представлены в форме (сухого) порошка (т.е. порошка, содержащего соединения по данному изобретению и необязательно одно или более фармацевтически приемлемых вспомогательных веществ). Как описано выше, предусмотрено, что такой порошок можно разбавлять пригодной жидкостью (в частности, водой, необязательно в форме водного раствора фармацевтически приемлемых вспомогательных веществ) с получением жидкой лекарственной формы (например, водного раствора) перед введением.
В конкретных вариантах реализации композиции, содержащие соединения по данному изобретению (и/или фармацевтические композиции, содержащие их), представлены в лекарственной форме, пригодной для перорального или внутривенного введения (например, перорального введения).
Комбинации и наборы компонентов
Специалистам в данной области техники понятно, что лечение с применением соединений по данному изобретению может дополнительно включать (т.е. его можно комбинировать) дополнительное средство(а) лечения или способы предупреждения того же патологического состояния. В частности, лечение с применением соединений по данному изобретению можно комбинировать со средствами лечения заболевания, связанного с фракталкином, описанного в данном документе, например, воспалительного заболевания, аутоиммунного заболевания, рака и/или сердечнососудистого заболевания, например, лечения с применением одного или более терапевтических агентов, пригодных для лечения или предупреждения заболевания, связанного с фракталкином, и/или одного или более физических способов, используемых для лечения (таких как лечение посредством хирургической операции), известных специалистам в данной области техники.
Как описано в данном документе, соединения по данному изобретению также можно комбинировать с одним или более (т.е. другими) терапевтическими агентами (т.е. агентами, которые не являются соединениями по данному изобретению), пригодными для лечения и/или предупреждения заболевания, связанного с фракталкином. Такие комбинированные продукты, которые предложены для введения соединения по данному изобретению в сочетании с одним или более другими терапевтическими агентами, либо могут быть представлены в виде отдельных лекарственных форм, причем по меньшей мере одна из таких лекарственных форм содержит соединение по данному изобретению, и по меньшей мере одна содержит другой терапевтический агент, либо могут быть представлены (т.е. составлены) в виде комбинированного препарата (т.е. представлены в виде единой лекарственной формы, содержащей соединение по данному изобретению и один или более других терапевтических агентов).
Таким образом, в соответствии с шестым аспектом настоящего изобретения, предложен комбинированный продукт, содержащий:
(I) соединение по данному изобретению, определение которого приведено выше (т.е. в первом аспекте изобретения, включая все его варианты реализации и конкретные признаки); и
(II) один или более других терапевтических агентов, пригодных для лечения и/или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1 (такого как болезни глаз, болезни легких, болезни кожи, болезни суставов и/или костей, аутоиммунные заболевания, сердечнососудистые заболевания, метаболические заболевания, болезни головного мозга, нейродегенеративные заболевания, боль, рак, болезни печени, болезни почек, желудочно-кишечные заболевания и вирус иммунодефицита человека, как описано в данном документе),
причем каждый из компонентов (I) и (II) составлен в виде смеси, необязательно с одним или более фармацевтически приемлемыми вспомогательными веществами.
В седьмом аспекте данного изобретения предложен набор компонентов, содержащий:
(a) фармацевтическую лекарственную форму, определение которой приведено выше (т.е. в четвертом аспекте изобретения); и
(b) один или более других терапевтических агентов, пригодных для лечения или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1 (такого как болезни глаз, болезни легких, болезни кожи, болезни суставов и/или костей, аутоиммунные заболевания, сердечнососудистые заболевания, метаболические заболевания, болезни головного мозга, нейродегенеративные заболевания, боль, рак, болезни печени, болезни почек, желудочно-кишечные заболевания и вирус иммунодефицита человека, как описано в данном документе), необязательно в смеси с одним или более фармацевтически приемлемыми носителями,
причем оба компонента (a) и (b) представлены в такой форме, которая пригодна для введения в сочетании (т.е. одновременно или последовательно) с другим компонентом.
В отношении наборов компонентов, описанных в данном документе, «введение в сочетании с» (и аналогично «введенный в сочетании с») включает введение соответствующих лекарственных форм последовательно, отдельно или одновременно, в рамках медицинского вмешательства, направленного на лечение релевантного состояния.
Так, в отношении данного изобретения, термин «введение в сочетании с» (и аналогично «введенный в сочетании с») включает введение (необязательно многократное) двух активных ингредиентов (т.е. соединения по данному изобретению и дополнительного агента для лечения и/или предупреждения заболеваний, связанных с фракталкином, или композиций, содержащих их) вместе или достаточно близко по времени для обеспечения благотворного действия на пациента, то есть эффекта, который в течение курса лечения и/или предупреждения релевантного состояния выше, чем при введении (необязательно многократном) любого из агентов по отдельности, без другого компонента, в течение того же курса лечения и/или предупреждения. Определение того, обеспечивает ли комбинация усиленное благотворное действие в отношении и в течение курса лечения и/или предупреждения конкретного состояния, зависит от состояния, подлежащего лечению и/или предупреждению, но может быть стандартным образом осуществлено специалистом в данной области техники.
Кроме того, в контексте данного изобретения термин «в сочетании с» включает возможность введения (необязательно многократного) одной или другой из двух лекарственных форм до, после и/или в то же время, что и введение другого компонента. При использовании в данном контексте термины «введенный одновременно» и «введенный в то же время» включают ситуации, в которых отдельные дозы соединения по данному изобретению и дополнительного соединения для лечения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1, или их фармацевтически приемлемых солей вводят в пределах 48 часов (например, в пределах 24 часов, 12 часов, 6 часов, 3 часов, 2 часов, 1 часа, 45 минут, 30 минут, 20 минут или 10 минут) относительно друг друга.
В данном контексте указание других терапевтических агентов, которые являются определенным образом «пригодными» (например, для лечения определенного заболевания или расстройства), относится к агентам, которые, как известно, пригодны для применения таким образом (например, к агентом, обычно используемым для этой цели). Таким образом, указанные ссылки могут быть заменены указанием агентов, «пригодных для» соответствующей цели.
Другие терапевтические агенты, пригодные для лечения и/или предупреждения заболеваний, связанных с фракталкином (таких как описаны в данном документе), хорошо известны специалистам в данной области техники. Например, указанные другие терапевтические агенты могут включать:
противовоспалительные препараты (такие как нестероидные противовоспалительные препараты (NSAID), кортикостероиды и противовоспалительные антитела направленного действия);
противораковые агенты (такие как алкилирующие агенты, антиметаболиты, противоопухолевые антибиотики, ингибиторы топоизомеразы, митотические ингибиторы, иммуномодуляторы, терапевтические препараты направленного действия (например, ингибиторы киназ) и препараты, препятствующие репарации ДНК);
соединения для лечения сердечнососудистых заболеваний (такие как ингибиторы ACE (ингибиторы ангиотензин-превращающего фермента), препараты против аритмии, антикоагулянты, антитромбоцитарные агенты, бета-блокаторы, блокаторы кальциевых каналов, препараты для снижения уровня холестерина (такие как статины) и ацетилсалициловую кислоту.
Получение соединений/композиций
Фармацевтические композиции/лекарственные формы, комбинированные продукты и наборы, описанные в данном документе, можно получать в соответствии со стандартной и/или принятой фармацевтической практикой.
Таким образом, в дополнительном аспекте данного изобретения предложен способ получения фармацевтической композиции/лекарственной формы, определение которой приведено выше, который включает приведение в контакт соединения по данному изобретению, определение которого приведено выше, с одним или более фармацевтически приемлемыми вспомогательными веществами.
В дополнительных аспектах данного изобретения предложен способ получения комбинированного продукта или набора компонентов, определение которого приведено выше, который включает приведение в контакт соединения по данному изобретению, определение которого приведено выше, с другим терапевтически агентом, пригодным для лечения рассматриваемого заболевания или расстройства, и по меньшей мере одним фармацевтически приемлемым вспомогательным веществом.
В данном контексте упоминание приведения в контакт означает обеспечение пригодности двух компонентов для введения в сочетании друг с другом.
Таким образом, в отношении способа получения набора компонентов, определение которого приведено выше, под приведением «в контакт» двух компонентов друг с другом понимают, что два компонента набора компонентов могут быть:
(i) представлены в виде отдельных лекарственных форм (т.е. независимо друг от друга), которые затем приводят в контакт для применения в сочетании друг с другом в комбинированной терапии; или
(ii) упакованы и представлены вместе в виде отдельных компонентов «комбинированной упаковки» для применения в сочетании друг с другом в комбинированной терапии.
Соединения по данному изобретению, описанные в данном документе, можно получать в соответствии со способами, хорошо известными специалистам в данной области техники, такими как способы, описанные в примерах, приведенных ниже.
Соединения-предшественники для соединений по данному изобретению (такие как (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола гидрохлорид и 5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-он (соединения формулы II)) могут быть получены способами, известными в данной области техники, такими как описаны в публикациях Karlström S., et al., (J. Med. Chem., 2013, 56, 3177-3190 (включая сопутствующую информацию)), WO 2006/107258 и WO 2008/039138 .
В соответствии с восьмым аспектом данного изобретения, предложен способ получения соединения по данному изобретению, определение которого приведено выше, включающий:
(a) для соединений, в которых Q1 представляет собой -PO(OR6)(OR7), где R6 и R7 являются такими, как описано в данном документе,
(i) приведение во взаимодействие соединения формулы II
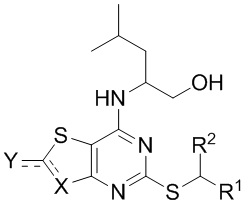 (II)
(II)
где R1 и R2 являются такими, как описано в настоящем документе; и
 представляет собой
представляет собой  или
или  ;
;
с оксихлоридом фосфора в присутствии пригодного растворителя (например, тетрагидрофурана, диэтилового эфира или метил-трет-бутилового эфира) и пригодного основания (например, пиридина или триэтиламина); затем
(ii) добавление в реакционную смесь воды или R6OH/R7OH;
(b) для соединений, в которых Q2 представляет собой -PO(OR6)(OR7);
приведение во взаимодействие соединения формулы III
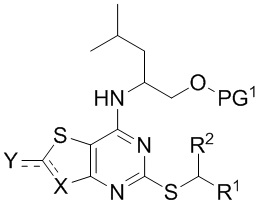 (III)
(III)
где:
R1 и R2 являются такими, как описано в данном документе;
PG1 представляет собой пригодную защитную группу для атома кислорода (например, силильную защитную группу, например, триметилсилил, трет-бутилдиметилсилил или триизопропилсилил);
в присутствии пентахлорида фосфора, пригодного растворителя (например, дихлорметана) и необязательно пригодного основания (например, пиридина),
(c) для соединений, в которых Q3 или Q4 представляет собой -CH2OPO(OR6)(OR7) и по меньшей мере один из R6 и R7 представляет собой C1-4 алкил или C2-4 алкенил,
приведение во взаимодействие соединения формулы II
 (II)
(II)
где R1 и R2 являются такими, как описано в настоящем документе; и
 представляет собой
представляет собой  или
или  ;
;
с соединением формулы IV
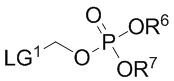 (IV)
(IV)
где R6 и R7 являются такими, как описано в данном документе, при условии, что по меньшей мере один из R6 и R7 представляет собой C1-4 алкил или C2-4 алкенил, и LG1 представляет собой пригодную уходящую группу (такую как галоген (например, Cl, Br));
в присутствии пригодного основания (например, K2CO3) и пригодного растворителя (например, ацетонитрила);
(d) для соединений, в которых Q3 или Q4 представляет собой -CH2OPO(OH)2,
(i) приведение во взаимодействие соединения формулы II
 (II)
(II)
где R1 и R2 являются такими, как описано в настоящем документе; и
 представляет собой
представляет собой  или
или  ;
;
с соединением формулы V
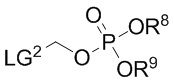 (V)
(V)
где R8 и R9 представляют собой C1-6 алкил, LG2 представляет собой пригодную уходящую группу (такую как галоген (например, Cl, Br));
в присутствии пригодного основания (например, K2CO3) и пригодного растворителя (например, ацетонитрила); и
(ii) приведение во взаимодействие полученного продукта в присутствии пригодной кислоты (например, HCl) и пригодного растворителя (например, диоксана).
Соединения формул II – V либо доступны в продаже, либо известны из литературных источников, либо могут быть получены по аналогии со способами, описанными в данном документе или традиционными способами синтеза в соответствии со стандартными методиками из доступных исходных материалов с применением соответствующих реагентов и условий реакции. В этом отношении специалисты в данной области техники могут обратиться, inter alia, к публикации “Comprehensive Organic Synthesis”, B. M. Trost and I. Fleming, Pergamon Press, 1991. Дополнительные источники, которые можно использовать, включают “Heterocyclic Chemistry”, J. A. Joule, K. Mills and G. F. Smith, 3е издание, опубликовано компанией Chapman & Hall, “Comprehensive Heterocyclic Chemistry II”, A. R. Katritzky, C. W. Rees and E. F. V. Scriven, Pergamon Press, 1996, и “Science of Synthesis”, тома 9-17 (Hetarenes and Related Ring Systems), Georg Thieme Verlag, 2006.
Специалистам в данной области техники понятно, что заместители, описанные в данном документе, и их замещения могут быть модифицированы один или более раз, после или во время осуществления способов, описанных выше, для получения соединений по данному изобретению с применением способов, хорошо известных специалистам в данной области техники. Примеры таких способов включают замещение, восстановление, окисление, дегидрирование, алкилирование, деалкилирование, ацилирование, гидролиз, эстерификацию, этерификацию, галогенирование и нитрование. Группы-предшественники могут быть заменены на другие такие группы или на группы, определенные в формуле I, в любой момент в процессе выполнения последовательности реакций. Специалисты в данной области техники также могут обратиться к публикациям “Comprehensive Organic Functional Group Transformations”, A. R. Katritzky, O. Meth-Cohn and C. W. Rees, Pergamon Press, 1995, и/или “Comprehensive Organic Transformations”, R. C. Larock, Wiley-VCH, 1999.
Соединения по данному изобретению могут быть выделены из их реакционных смесей и при необходимости очищены с помощью традиционных технологий, известных специалистам в данной области техники. Таким образом, способы получения соединений по данному изобретению, описанные в настоящем документе, могут включать в качестве последней стадии выделение и необязательно очистку соединения по данному изобретению.
Специалистам в данной области техники понятно, что в способах, описанных в данном документе, функциональные группы промежуточных соединений могут нуждаться в защите защитными группами. Защита и снятие защиты с функциональных групп можно осуществлять до или после реакции на вышеупомянутых схемах.
Соединения формул III, IV и V характеризуются наличием защитных групп. Защитные группы можно устанавливать и удалять в соответствии с технологиями, хорошо известными специалистам в данной области техники и описанными далее. Например, защищенные соединения/промежуточные соединения, описанные в данном документе, можно химически превращать в незащищенные соединения, используя стандартные технологии снятия защиты. Тип химического превращения обусловливает необходимость и тип защитных групп, а также последовательность осуществления синтеза. Использование защитных групп подробно описано в публикации “Protective Groups in Organic Synthesis”, 3е издание, T.W. Greene & P.G.M. Wutz, Wiley-Interscience (1999), содержание которой включено в данный документ посредством ссылки.
В частности, защитные группы силильных простых эфиров для атомов кислорода могут быть введены посредством приведения во взаимодействие соответствующего спирта с пригодным триалкилсилилгалогенидом (например, триметилсилилхлоридом или трет-бутилдиметилсилилхлоридом) в присутствии пригодного основания (например, N,N-диизопропилэтиламина, триэтиламина или N,N-диметиламинопиридина). Защитные группы силильных простых эфиров могут быть удалены в присутствии пригодного источника фторида (например, фторида тетрабутиламмония). Карбаматные защитные группы для атомов азота могут быть введены посредством приведения во взаимодействие соответствующей аминогруппы с пригодным хлорформиатом или карбонат-ангидридом (например, ди-трет-бутилдикарбонатом), необязательно в присутствии пригодного основания, и могут быть удалены в соответствующих кислотных или основных условиях, известных специалистам в данной области техники. Бензильные защитные группы могут быть введены посредством приведения во взаимодействие релевантного атома азота с пригодным бензилгалогенидом в присутствии пригодного основания, и могут быть удалены в соответствующих условиях, известных специалистам в данной области техники (например, 2,4-диметоксибензильная группа может быть удалена в присутствии нитрата аммония-церия и пригодного растворителя).
Можно предположить, что соединения по данному изобретению обеспечивают существенные преимущества по сравнению с известными антагонистами рецептора фракталкина с точки зрения растворимости в воде и стабильности при хранении в водной среде.
Соединения по данному изобретению могут иметь то преимущество, что они могут быть более эффективными, менее токсичными, более длительно действующими, могут вызывать меньшее количество побочных эффектов, могут легче усваиваться и/или могут иметь лучший фармакокинетический профиль (например, более высокую пероральную биодоступность и/или более низкий клиренс), и/или могут иметь другие пригодные фармакологические, физические или химические свойства по сравнению с соединениями, известными из уровня техники, при их использовании для вышеуказанных показаний или иным образом. В частности, соединения по данному изобретению могут иметь то преимущество, что они являются более эффективными и/или демонстрируют преимущественные свойства in vivo.
В частности, можно предположить, что соединения по данному изобретению могут обеспечивать возможность лечения с применением более высоких доз и/или более продолжительных терапевтических схем, чем в случае известных антагонистов рецептора фракталкина, и, следовательно, обеспечивать существенное преимущество с точки зрения возможностей лечения, доступных для пациента.
Примеры
Общие способы
В данном контексте использованы следующие сокращения:
ДХМ - дихлорметан
DMAP - 4-диметиламинопиридин
ДМФА - N,N-диметилформамид
ДМСО - диметилсульфоксид
ИЭР - электрораспылительная ионизация
EtOAc - этилацетат
EtOH - этанол
ВЭЖХ - высокоэффективная жидкостная хроматография
MeOH - метанол
МС - масс-спектрометрия
ЯМР - ядерный магнитный резонанс.
Спектры 1H ЯМР и 13C ЯМР записывали на приборе Varian Inova 600, оснащенном датчиком тройного резонанса. Все спектры записывали, используя резонанс протонов остаточного растворителя в качестве внутреннего стандарта. Аналитическую ВЭЖХ проводили на системе Agilent Series 1100, используя колонку Kinetex C18 (2,6 мкм, 3,0x50 мм) с 0,1% муравьиной кислотой в MilliQ H2O / CH3CN в качестве подвижной фазы (кислотная система) или колонку Kinetex EVO (2,6 мкм 3,0x50 мм) с 10 мМ, pH10, NH4HCO3 / CH3CN в качестве подвижной фазы (основная система). Электрораспылительную масс-спектрометрию (ЭР-МС) проводили на жидкостном хроматографе с масс-селективным детектором (MSD) Agilent серии 1100 с получением псевдомолекулярного иона [M+H]+ требуемых молекул. Препаративную ВЭЖХ проводили на ВЭЖХ системе Gilson 306, используя колонку Kinetex C18 (5 мкм, 21x100 мм) с 0,1% ТФК в MilliQ H2O / CH3CN в качестве подвижной фазы (кислотная система) или колонку Gemini NX (5 мкм, 21x100 мм) с 50 мМ, pH10, NH4HCO3 / CH3CN в качестве подвижной фазы (основная система). Фракции собирали на основании УФ сигнала при максимальной длине волны для рассматриваемого соединения. Препаративную флэш-хроматографию проводили на силикагеле Merck 60 (230-400 меш) или на геле YMC 120Å S-150 мкм. Реакции в микроволновой печи проводили на приборе Biotage Initiator, используя колбы Biotage Process объемом 0,5-2 мл или 2-5 мл, оснащенные алюминиевыми крышками и септой. Названия соединений получали с помощью программного обеспечения ACD Labs 10.0.
Пример 1
Получение (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата
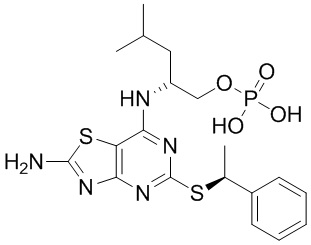
Оксихлорид фосфора (337 мг, 2,2 ммоль) растворяли в ТГФ (0,75 мл) и добавляли воду (25 мг, 1,4 ммоль). Смесь охлаждали на ледяной бане и добавляли пиридин (111 мг, 113 мкл, 1,4 ммоль), затем (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола гидрохлорид (110 мг, 0,25 ммоль) ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258). Реакционную смесь перемешивали при температуре ледяной бани в течение 1 часа. К смеси оксихлорида фосфора (337 мг, 2,2 ммоль) и воды (25 мг, 1,4 ммоль) в ТГФ при температуре ледяной бани добавляли пиридин (111 мг, 113 мкл, 1,4 ммоль). Половину полученной смеси добавляли к реакционной смеси, описанной выше. Реакционную смесь перемешивали при температуре ледяной бани еще 1 час. Добавляли воду (3 мл) и перемешивали реакционную смесь в течение 15 минут при температуре ледяной бани и в течение 20 минут при комнатной температуре. Добавляли ДХМ (3 мл) и разделяли фазы. Водную фазу экстрагировали дополнительной порцией ДХМ (3 мл) и объединяли органические фазы. В это время продукт начинал выпадать в осадок в виде бледно-желтого смолистого вещества в органической фазе. Добавляли MeOH и теперь уже однородный раствор переносили в круглодонную колбу, и выпаривали с получением 120 мг неочищенного продукта, который, по данным ВЭЖХ, имел чистоту около 93%. Неочищенный материал растворяли в смеси MeOH/вода и доводили рН до около 6-7 с помощью 1 M NaOH. Вещество очищали препаративной ВЭЖХ (основной способ). Чистые фракции объединяли, выпаривали и сушили в вакууме. После очистки продукт считали диаммониевой солью. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,43 - 7,47 (м, 2 H) 7,30 - 7,35 (м, 2 H) 7,20 - 7,24 (м, 1 H) 5,08 (к, J=7,03 Гц, 1 H) 4,59 - 4,68 (м, 1 H) 3,92 (ддд, J=10,12, 5,67, 4,30 Гц, 1 H) 3,88 (дт, J=10,12, 4,94 Гц, 1 H) 1,74 (д, J=7,03 Гц, 3 H) 1,71 - 1,79 (м, 1 H) 1,68 (ддд, J=13,87, 9,54, 5,67 Гц, 1 H) 1,57 (ддд, J=13,87, 8,54, 5,33 Гц, 1 H) 0,98 (д, J=6,71 Гц, 3 H) 0,96 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 484 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258). Реакционную смесь перемешивали при температуре ледяной бани в течение 1 часа. К смеси оксихлорида фосфора (337 мг, 2,2 ммоль) и воды (25 мг, 1,4 ммоль) в ТГФ при температуре ледяной бани добавляли пиридин (111 мг, 113 мкл, 1,4 ммоль). Половину полученной смеси добавляли к реакционной смеси, описанной выше. Реакционную смесь перемешивали при температуре ледяной бани еще 1 час. Добавляли воду (3 мл) и перемешивали реакционную смесь в течение 15 минут при температуре ледяной бани и в течение 20 минут при комнатной температуре. Добавляли ДХМ (3 мл) и разделяли фазы. Водную фазу экстрагировали дополнительной порцией ДХМ (3 мл) и объединяли органические фазы. В это время продукт начинал выпадать в осадок в виде бледно-желтого смолистого вещества в органической фазе. Добавляли MeOH и теперь уже однородный раствор переносили в круглодонную колбу, и выпаривали с получением 120 мг неочищенного продукта, который, по данным ВЭЖХ, имел чистоту около 93%. Неочищенный материал растворяли в смеси MeOH/вода и доводили рН до около 6-7 с помощью 1 M NaOH. Вещество очищали препаративной ВЭЖХ (основной способ). Чистые фракции объединяли, выпаривали и сушили в вакууме. После очистки продукт считали диаммониевой солью. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,43 - 7,47 (м, 2 H) 7,30 - 7,35 (м, 2 H) 7,20 - 7,24 (м, 1 H) 5,08 (к, J=7,03 Гц, 1 H) 4,59 - 4,68 (м, 1 H) 3,92 (ддд, J=10,12, 5,67, 4,30 Гц, 1 H) 3,88 (дт, J=10,12, 4,94 Гц, 1 H) 1,74 (д, J=7,03 Гц, 3 H) 1,71 - 1,79 (м, 1 H) 1,68 (ддд, J=13,87, 9,54, 5,67 Гц, 1 H) 1,57 (ддд, J=13,87, 8,54, 5,33 Гц, 1 H) 0,98 (д, J=6,71 Гц, 3 H) 0,96 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 484 [M+H]+.
Пример 1b
(2R)-2-[(2-Амино-5-{[1-(2-фторфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
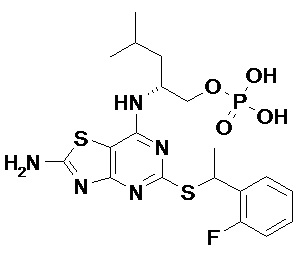
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(2-фторфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 55%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 7,98 (шс, 4 H) 8,09 (шс, 2 H) 7,50 - 7,57 (м, 2 H) 7,26 - 7,32 (м, 2 H) 7,15 - 7,20 (м, 4 H) 7,30 (шс, 4 H) 5,25 (к, J=7,0 Гц, 1 H) 5,24 (к, J=7,2 Гц, 1 H) 4,22 - 4,30 (м, 1 H) 4,14 - 4,25 (м, 1 H) 3,75 - 3,82 (м, 1 H) 3,65 - 3,76 (м, 3 H) 1,69 (д, J=7,0 Гц, 3 H) 1,66 (д, J=7,2 Гц, 3 H) 1,56 - 1,65 (м, 2 H) 1,46 - 1,57 (м, 2 H) 1,41 (ддд, J=13,4, 6,9, 6,8 Гц, 2 H) 0,88 (д, J=6,6 Гц, 3 H) 0,88 (д, J=6,6 Гц, 3 H) 0,85 (д, J=6,7 Гц, 3 H) 0,84 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 502 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 55%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 7,98 (шс, 4 H) 8,09 (шс, 2 H) 7,50 - 7,57 (м, 2 H) 7,26 - 7,32 (м, 2 H) 7,15 - 7,20 (м, 4 H) 7,30 (шс, 4 H) 5,25 (к, J=7,0 Гц, 1 H) 5,24 (к, J=7,2 Гц, 1 H) 4,22 - 4,30 (м, 1 H) 4,14 - 4,25 (м, 1 H) 3,75 - 3,82 (м, 1 H) 3,65 - 3,76 (м, 3 H) 1,69 (д, J=7,0 Гц, 3 H) 1,66 (д, J=7,2 Гц, 3 H) 1,56 - 1,65 (м, 2 H) 1,46 - 1,57 (м, 2 H) 1,41 (ддд, J=13,4, 6,9, 6,8 Гц, 2 H) 0,88 (д, J=6,6 Гц, 3 H) 0,88 (д, J=6,6 Гц, 3 H) 0,85 (д, J=6,7 Гц, 3 H) 0,84 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 502 [M+H]+.
Пример 1c
(2R)-2-[(2-Амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
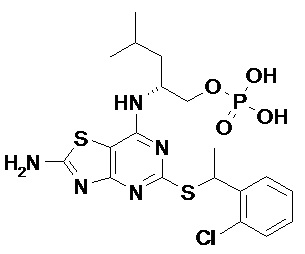
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 55%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,31 (шс, 2 H) 7,95 (шс, 4 H) 7,61 (дд, J=7,8, 1,8 Гц, 1 H) 7,60 (дд, J=7,8, 1,8 Гц, 1 H) 7,45 (дд, J=8,0, 1,4 Гц, 1 H) 7,45 (дд, J=8,0, 1,4 Гц, 1 H) 7,35 (ддд, J=7,8, 7,3, 1,4 Гц, 1 H) 7,34 (ддд, J=7,8, 7,3, 1,4 Гц, 1 H) 7,28 (ддд, J=8,0, 7,3, 1,8 Гц, 1 H) 7,28 (ддд, J=8,0, 7,3, 1,8 Гц, 1 H) 6,77 - 7,56 (м, 4 H) 5,42 (к, J=6,9 Гц, 1 H) 5,36 (к, J=6,9 Гц, 1 H) 4,16 - 4,29 (м, 2 H) 3,76 - 3,84 (м, 1 H) 3,64 - 3,76 (м, 3 H) 1,71 (д, J=6,9 Гц, 3 H) 1,67 (д, J=6,9 Гц, 3 H) 1,49 - 1,65 (м, 4 H) 1,37 - 1,45 (м, 2 H) 0,89 (д, J=6,4 Гц, 3 H) 0,88 (д, J=6,4 Гц, 3 H) 0,87 (д, J=6,6 Гц, 3 H) 0,83 (д, J=6,1 Гц, 3 H). МС (ИЭР+) m/z 518 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 55%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,31 (шс, 2 H) 7,95 (шс, 4 H) 7,61 (дд, J=7,8, 1,8 Гц, 1 H) 7,60 (дд, J=7,8, 1,8 Гц, 1 H) 7,45 (дд, J=8,0, 1,4 Гц, 1 H) 7,45 (дд, J=8,0, 1,4 Гц, 1 H) 7,35 (ддд, J=7,8, 7,3, 1,4 Гц, 1 H) 7,34 (ддд, J=7,8, 7,3, 1,4 Гц, 1 H) 7,28 (ддд, J=8,0, 7,3, 1,8 Гц, 1 H) 7,28 (ддд, J=8,0, 7,3, 1,8 Гц, 1 H) 6,77 - 7,56 (м, 4 H) 5,42 (к, J=6,9 Гц, 1 H) 5,36 (к, J=6,9 Гц, 1 H) 4,16 - 4,29 (м, 2 H) 3,76 - 3,84 (м, 1 H) 3,64 - 3,76 (м, 3 H) 1,71 (д, J=6,9 Гц, 3 H) 1,67 (д, J=6,9 Гц, 3 H) 1,49 - 1,65 (м, 4 H) 1,37 - 1,45 (м, 2 H) 0,89 (д, J=6,4 Гц, 3 H) 0,88 (д, J=6,4 Гц, 3 H) 0,87 (д, J=6,6 Гц, 3 H) 0,83 (д, J=6,1 Гц, 3 H). МС (ИЭР+) m/z 518 [M+H]+.
Пример 1d
(2R)-2-[(2-Амино-5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
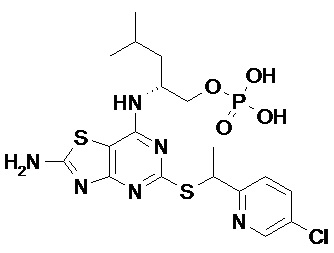
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 16%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,57 (дд, J=2,5, 0,7 Гц, 1 H) 8,55 (дд, J=2,5, 0,7 Гц, 1 H) 8,02 (шс, 4 H) 7,88 (дд, J=8,5, 2,5 Гц, 1 H) 7,84 (дд, J=8,4, 2,5 Гц, 1 H) 7,58 (дд, J=8,5, 0,7 Гц, 1 H) 7,56 (дд, J=8,5, 0,7 Гц, 1 H) 6,93 - 7,51 (м, 4 H) 5,14 (к, J=7,2 Гц, 1 H) 5,07 (к, J=7,2 Гц, 1 H) 4,40 - 4,51 (м, 1 H) 4,15 - 4,26 (м, 1 H) 3,74 - 3,82 (м, 3 H) 3,71 (дт, J=10,3, 6,0 Гц, 1 H) 1,66 (д, J=7,2 Гц, 3 H) 1,64 (д, J=7,2 Гц, 3 H) 1,54 - 1,65 (м, 2 H) 1,44 - 1,54 (м, 2 H) 1,40 (ддд, J=13,7, 8,9, 4,8 Гц, 1 H) 1,35 (ддд, J=13,7, 8,7, 4,7 Гц, 1 H) 0,87 (д, J=6,7 Гц, 3 H) 0,85 (д, J=6,4 Гц, 3 H) 0,84 (д, J=6,5 Гц, 3 H) 0,76 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 519 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 16%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,57 (дд, J=2,5, 0,7 Гц, 1 H) 8,55 (дд, J=2,5, 0,7 Гц, 1 H) 8,02 (шс, 4 H) 7,88 (дд, J=8,5, 2,5 Гц, 1 H) 7,84 (дд, J=8,4, 2,5 Гц, 1 H) 7,58 (дд, J=8,5, 0,7 Гц, 1 H) 7,56 (дд, J=8,5, 0,7 Гц, 1 H) 6,93 - 7,51 (м, 4 H) 5,14 (к, J=7,2 Гц, 1 H) 5,07 (к, J=7,2 Гц, 1 H) 4,40 - 4,51 (м, 1 H) 4,15 - 4,26 (м, 1 H) 3,74 - 3,82 (м, 3 H) 3,71 (дт, J=10,3, 6,0 Гц, 1 H) 1,66 (д, J=7,2 Гц, 3 H) 1,64 (д, J=7,2 Гц, 3 H) 1,54 - 1,65 (м, 2 H) 1,44 - 1,54 (м, 2 H) 1,40 (ддд, J=13,7, 8,9, 4,8 Гц, 1 H) 1,35 (ддд, J=13,7, 8,7, 4,7 Гц, 1 H) 0,87 (д, J=6,7 Гц, 3 H) 0,85 (д, J=6,4 Гц, 3 H) 0,84 (д, J=6,5 Гц, 3 H) 0,76 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 519 [M+H]+.
Пример 1e
(2R)-2-[(2-Амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
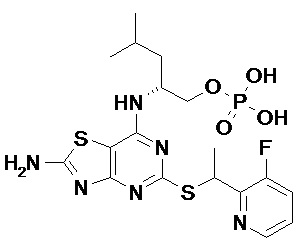
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 7%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,75 (шс, 1 H) 8,39 - 8,42 (м, 2 H) 7,95 (шс, 4 H) 7,68 - 7,74 (м, 2 H) 7,36 - 7,43 (м, 2 H) 7,15 (шс, 5 H) 5,49 (к, J=6,9 Гц, 1 H) 5,45 (к, J=6,9 Гц, 1 H) 4,13 - 4,33 (м, 2 H) 3,74 - 3,85 (м, 2 H) 3,67 - 3,75 (м, 2 H) 1,71 (д, J=6,9 Гц, 3 H) 1,68 (д, J=6,9 Гц, 3 H) 1,58 - 1,67 (м, 2 H) 1,48 - 1,59 (м, 2 H) 1,40 - 1,48 (м, 2 H) 0,90 (д, J=6,5 Гц, 3 H) 0,90 (д, J=6,5 Гц, 3 H) 0,87 (д, J=6,7 Гц, 3 H) 0,86 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 503 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 7%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,75 (шс, 1 H) 8,39 - 8,42 (м, 2 H) 7,95 (шс, 4 H) 7,68 - 7,74 (м, 2 H) 7,36 - 7,43 (м, 2 H) 7,15 (шс, 5 H) 5,49 (к, J=6,9 Гц, 1 H) 5,45 (к, J=6,9 Гц, 1 H) 4,13 - 4,33 (м, 2 H) 3,74 - 3,85 (м, 2 H) 3,67 - 3,75 (м, 2 H) 1,71 (д, J=6,9 Гц, 3 H) 1,68 (д, J=6,9 Гц, 3 H) 1,58 - 1,67 (м, 2 H) 1,48 - 1,59 (м, 2 H) 1,40 - 1,48 (м, 2 H) 0,90 (д, J=6,5 Гц, 3 H) 0,90 (д, J=6,5 Гц, 3 H) 0,87 (д, J=6,7 Гц, 3 H) 0,86 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 503 [M+H]+.
Пример 1f
(2R)-2-[(2-Амино-5-{[1-(3-цианофенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
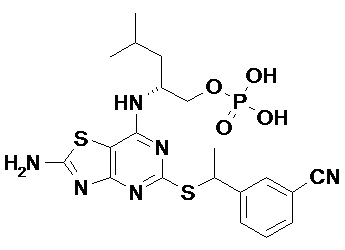
Указанное в заголовке соединение синтезировали из 3-{1-[(2-амино-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензонитрила ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 50%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,17 (шс, 1 H) 7,99 (шс, 4 H) 8,04 (шс, 1 H) 7,92 (т, J=1,6 Гц, 1 H) 7,90 (т, J=1,7 Гц, 1 H) 7,80 - 7,85 (м, 2 H) 7,67 - 7,70 (м, 2 H) 7,56 (т, J=7,8 Гц, 1 H) 7,51 (т, J=7,8 Гц, 1 H) 7,26 (шс, 4 H) 5,03 (к, J=7,2 Гц, 1 H) 5,03 (к, J=7,2 Гц, 1 H) 4,18 - 4,29 (м, 1 H) 4,06 - 4,16 (м, 1 H) 3,64 - 3,74 (м, 4 H) 1,66 (д, J=7,2 Гц, 3 H) 1,65 (д, J=7,2 Гц, 3 H) 1,53 - 1,62 (м, 2 H) 1,37 - 1,51 (м, 4 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,5 Гц, 3 H) 0,85 (д, J=6,5 Гц, 3 H) 0,78 (д, J=6,5 Гц, 3 H). МС (ИЭР+) m/z 509 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 50%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,17 (шс, 1 H) 7,99 (шс, 4 H) 8,04 (шс, 1 H) 7,92 (т, J=1,6 Гц, 1 H) 7,90 (т, J=1,7 Гц, 1 H) 7,80 - 7,85 (м, 2 H) 7,67 - 7,70 (м, 2 H) 7,56 (т, J=7,8 Гц, 1 H) 7,51 (т, J=7,8 Гц, 1 H) 7,26 (шс, 4 H) 5,03 (к, J=7,2 Гц, 1 H) 5,03 (к, J=7,2 Гц, 1 H) 4,18 - 4,29 (м, 1 H) 4,06 - 4,16 (м, 1 H) 3,64 - 3,74 (м, 4 H) 1,66 (д, J=7,2 Гц, 3 H) 1,65 (д, J=7,2 Гц, 3 H) 1,53 - 1,62 (м, 2 H) 1,37 - 1,51 (м, 4 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,5 Гц, 3 H) 0,85 (д, J=6,5 Гц, 3 H) 0,78 (д, J=6,5 Гц, 3 H). МС (ИЭР+) m/z 509 [M+H]+.
Пример 1g
(2R)-2-[(2-Амино-5-{[1-(3-карбамоилфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
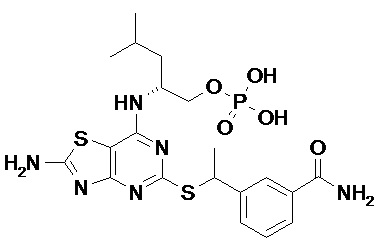
Указанное в заголовке соединение синтезировали из 3-{1-[(2-амино-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензамида ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в виде одного диастереомера, с выходом 17%, используя способ, описанный для примера 1. Продукт представлял собой один диастереомер. 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,03 (т, J=1,85 Гц, 1 H) 7,75 (ддд, J=7,70, 1,85, 1,10 Гц, 1 H) 7,71 (дддд, J=7,70, 1,85, 1,10, 0,42 Гц, 1 H) 7,42 (т, J=7,70 Гц, 1 H) 5,14 (к, J=7,19 Гц, 1 H) 4,35 - 4,43 (м, 1 H) 3,98 (ддд, J=9,85, 5,11, 4,37 Гц, 1 H) 3,91 (ддд, J=9,85, 5,20, 5,02 Гц, 1 H) 1,73 (д, J=7,19 Гц, 3 H) 1,58 - 1,67 (м, 2 H) 1,48 - 1,55 (м, 1 H) 0,91 (д, J=6,39 Гц, 3 H) 0,76 (д, J=6,39 Гц, 3 H). МС (ИЭР+) m/z 527 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в виде одного диастереомера, с выходом 17%, используя способ, описанный для примера 1. Продукт представлял собой один диастереомер. 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,03 (т, J=1,85 Гц, 1 H) 7,75 (ддд, J=7,70, 1,85, 1,10 Гц, 1 H) 7,71 (дддд, J=7,70, 1,85, 1,10, 0,42 Гц, 1 H) 7,42 (т, J=7,70 Гц, 1 H) 5,14 (к, J=7,19 Гц, 1 H) 4,35 - 4,43 (м, 1 H) 3,98 (ддд, J=9,85, 5,11, 4,37 Гц, 1 H) 3,91 (ддд, J=9,85, 5,20, 5,02 Гц, 1 H) 1,73 (д, J=7,19 Гц, 3 H) 1,58 - 1,67 (м, 2 H) 1,48 - 1,55 (м, 1 H) 0,91 (д, J=6,39 Гц, 3 H) 0,76 (д, J=6,39 Гц, 3 H). МС (ИЭР+) m/z 527 [M+H]+.
Пример 1h
(2R)-2-{[2-Амино-5-({1-[4-(метилсульфонил)фенил]этил}сульфанил)[1,3]тиазоло[4,5-d]пиримидин-7-ил]амино}-4-метилпентил-дигидрофосфат
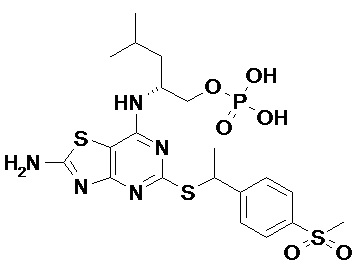
Указанное в заголовке соединение синтезировали из (2R)-2-{[2-амино-5-({1-[4-(метилсульфонил)фенил]этил}сульфанил)[1,3]тиазоло[4,5-d]пиримидин-7-ил]амино}-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в виде одного диастереомера, с выходом 39%, используя способ, описанный для примера 1. Продукт представлял собой один диастереомер. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,22 (шс, 2 H) 7,83 - 7,88 (м, 2 H) 7,73 - 7,78 (м, 2 H) 7,34 (шс, 1 H) 5,08 (к, J=7,3 Гц, 1 H) 4,22 - 4,33 (м, 1 H) 3,88 (дт, J=9,9, 5,4 Гц, 1 H) 3,76 (тд, J=9,9, 6,1 Гц, 1 H) 3,18 (с, 3 H) 1,64 (д, J=7,3 Гц, 3 H) 1,53 - 1,61 (м, 1 H) 1,51 (ддд, J=13,6, 10,3, 4,9 Гц, 1 H) 1,37 (ддд, J=13,6, 9,2, 4,3 Гц, 1 H) 0,85 (д, J=6,6 Гц, 3 H) 0,72 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 562 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в виде одного диастереомера, с выходом 39%, используя способ, описанный для примера 1. Продукт представлял собой один диастереомер. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,22 (шс, 2 H) 7,83 - 7,88 (м, 2 H) 7,73 - 7,78 (м, 2 H) 7,34 (шс, 1 H) 5,08 (к, J=7,3 Гц, 1 H) 4,22 - 4,33 (м, 1 H) 3,88 (дт, J=9,9, 5,4 Гц, 1 H) 3,76 (тд, J=9,9, 6,1 Гц, 1 H) 3,18 (с, 3 H) 1,64 (д, J=7,3 Гц, 3 H) 1,53 - 1,61 (м, 1 H) 1,51 (ддд, J=13,6, 10,3, 4,9 Гц, 1 H) 1,37 (ддд, J=13,6, 9,2, 4,3 Гц, 1 H) 0,85 (д, J=6,6 Гц, 3 H) 0,72 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 562 [M+H]+.
Пример 1i
(2R)-2-[(2-Амино-5-{[4-(метилсульфонил)бензил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
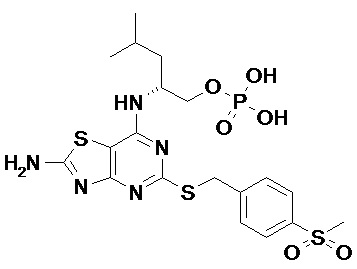
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[4-(метилсульфонил)бензил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 22%, используя способ, описанный для примера 1. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,02 (шс, 2 H) 7,81 - 7,86 (м, 2 H) 7,66 - 7,71 (м, 2 H) 7,17 (шс, 2 H) 4,45 (д, J=14,3 Гц, 1 H) 4,39 (д, J=14,3 Гц, 1 H) 4,20 - 4,34 (м, 1 H) 3,67 - 3,76 (м, 2 H) 3,17 (с, 3 H) 1,52 - 1,61 (м, 1 H) 1,46 (ддд, J=13,7, 9,0, 6,0 Гц, 1 H) 1,38 (ддд, J=13,7, 8,1, 5,5 Гц, 1 H) 0,83 (д, J=6,6 Гц, 3 H) 0,78 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 548 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 22%, используя способ, описанный для примера 1. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,02 (шс, 2 H) 7,81 - 7,86 (м, 2 H) 7,66 - 7,71 (м, 2 H) 7,17 (шс, 2 H) 4,45 (д, J=14,3 Гц, 1 H) 4,39 (д, J=14,3 Гц, 1 H) 4,20 - 4,34 (м, 1 H) 3,67 - 3,76 (м, 2 H) 3,17 (с, 3 H) 1,52 - 1,61 (м, 1 H) 1,46 (ддд, J=13,7, 9,0, 6,0 Гц, 1 H) 1,38 (ддд, J=13,7, 8,1, 5,5 Гц, 1 H) 0,83 (д, J=6,6 Гц, 3 H) 0,78 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 548 [M+H]+.
Пример 1j
(2R)-2-({2-Амино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)-4-метилпентил-дигидрофосфат
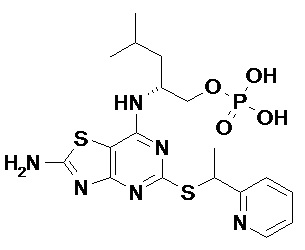
Указанное в заголовке соединение синтезировали из (2R)-2-({2-амино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 43%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,51 (ддд, J=4,8, 1,9, 1,0 Гц, 1 H) 8,51 (ддд, J=4,8, 1,9, 1,0 Гц, 1 H) 8,00 (шс, 4 H) 7,74 (ддд, J=7,9, 7,4, 1,9 Гц, 1 H) 7,73 (ддд, J=7,9, 7,4, 1,9 Гц, 1 H) 7,51 (дт, J=7,9, 1,0 Гц, 1 H) 7,49 (дт, J=7,9, 1,0 Гц, 1 H) 7,47 (шс, 1 H) 7,25 (ддд, J=7,4, 4,8, 1,0 Гц, 1 H) 7,23 (ддд, J=7,4, 4,8, 1,0 Гц, 1 H) 7,17 (шс, 4 H) 5,13 (к, J=7,0 Гц, 1 H) 5,09 (к, J=7,0 Гц, 1 H) 4,34 - 4,48 (м, 1 H) 4,15 - 4,29 (м, 1 H) 3,66 - 3,83 (м, 4 H) 1,67 (д, J=7,0 Гц, 3 H) 1,66 (д, J=7,0 Гц, 3 H) 1,54 - 1,66 (м, 2 H) 1,45 - 1,54 (м, 2 H) 1,41 (ддд, J=13,8, 8,5, 5,3 Гц, 1 H) 1,39 (ддд, J=13,8, 8,5, 5,3 Гц, 1 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,7 Гц, 3 H) 0,85 (д, J=6,6 Гц, 3 H) 0,78 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 485 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 43%, используя способ, описанный для примера 1. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,51 (ддд, J=4,8, 1,9, 1,0 Гц, 1 H) 8,51 (ддд, J=4,8, 1,9, 1,0 Гц, 1 H) 8,00 (шс, 4 H) 7,74 (ддд, J=7,9, 7,4, 1,9 Гц, 1 H) 7,73 (ддд, J=7,9, 7,4, 1,9 Гц, 1 H) 7,51 (дт, J=7,9, 1,0 Гц, 1 H) 7,49 (дт, J=7,9, 1,0 Гц, 1 H) 7,47 (шс, 1 H) 7,25 (ддд, J=7,4, 4,8, 1,0 Гц, 1 H) 7,23 (ддд, J=7,4, 4,8, 1,0 Гц, 1 H) 7,17 (шс, 4 H) 5,13 (к, J=7,0 Гц, 1 H) 5,09 (к, J=7,0 Гц, 1 H) 4,34 - 4,48 (м, 1 H) 4,15 - 4,29 (м, 1 H) 3,66 - 3,83 (м, 4 H) 1,67 (д, J=7,0 Гц, 3 H) 1,66 (д, J=7,0 Гц, 3 H) 1,54 - 1,66 (м, 2 H) 1,45 - 1,54 (м, 2 H) 1,41 (ддд, J=13,8, 8,5, 5,3 Гц, 1 H) 1,39 (ддд, J=13,8, 8,5, 5,3 Гц, 1 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,7 Гц, 3 H) 0,85 (д, J=6,6 Гц, 3 H) 0,78 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 485 [M+H]+.
Пример 1k
(2R)-2-[(2-Амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диметилфосфат
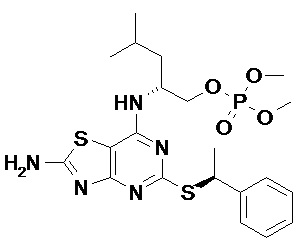
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 27%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли MeOH после 1 часа при температуре ледяной бани. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,45 - 7,48 (м, 2 H) 7,30 - 7,34 (м, 2 H) 7,20 - 7,24 (м, 1 H) 5,06 (к, J=7,1 Гц, 1 H) 4,67 - 4,74 (м, 1 H) 3,97 (ддд, J=10,2, 6,6, 5,7 Гц, 1 H) 3,94 (ддд, J=10,2, 6,5, 4,9 Гц, 1 H) 3,68 (д, J=11,1 Гц, 3 H) 3,63 (д, J=11,1 Гц, 3 H) 1,72 - 1,79 (м, 1 H) 1,72 (д, J=7,1 Гц, 3 H) 1,62 (ддд, J=13,9, 10,5, 5,0 Гц, 1 H) 1,42 (ддд, J=13,9, 9,3, 4,4 Гц, 1 H) 0,99 (д, J=6,7 Гц, 3 H) 0,97 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 512 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 27%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли MeOH после 1 часа при температуре ледяной бани. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,45 - 7,48 (м, 2 H) 7,30 - 7,34 (м, 2 H) 7,20 - 7,24 (м, 1 H) 5,06 (к, J=7,1 Гц, 1 H) 4,67 - 4,74 (м, 1 H) 3,97 (ддд, J=10,2, 6,6, 5,7 Гц, 1 H) 3,94 (ддд, J=10,2, 6,5, 4,9 Гц, 1 H) 3,68 (д, J=11,1 Гц, 3 H) 3,63 (д, J=11,1 Гц, 3 H) 1,72 - 1,79 (м, 1 H) 1,72 (д, J=7,1 Гц, 3 H) 1,62 (ддд, J=13,9, 10,5, 5,0 Гц, 1 H) 1,42 (ддд, J=13,9, 9,3, 4,4 Гц, 1 H) 0,99 (д, J=6,7 Гц, 3 H) 0,97 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 512 [M+H]+.
Пример 1l
(2R)-2-[(2-Амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфат

Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 68%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,45 - 7,48 (м, 2 H) 7,29 - 7,34 (м, 2 H) 7,20 - 7,24 (м, 1 H) 5,05 (к, J=7,1 Гц, 1 H) 4,66 - 4,74 (м, 1 H) 4,01 (дк, J=8,2, 7,1 Гц, 2 H) 3,93 - 3,98 (м, J=8,0, 7,0, 7,0, 7,0, 3,4 Гц, 2 H) 3,92 - 3,95 (м, 2 H) 1,72 - 1,79 (м, 1 H) 1,72 (д, J=7,1 Гц, 3 H) 1,62 (ддд, J=13,8, 10,4, 5,0 Гц, 1 H) 1,41 (ддд, J=13,8, 9,2, 4,5 Гц, 1 H) 1,23 (тд, J=7,1, 1,0 Гц, 3 H) 1,16 (тд, J=7,0, 1,0 Гц, 3 H) 0,99 (д, J=6,7 Гц, 3 H) 0,97 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 540 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 68%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,45 - 7,48 (м, 2 H) 7,29 - 7,34 (м, 2 H) 7,20 - 7,24 (м, 1 H) 5,05 (к, J=7,1 Гц, 1 H) 4,66 - 4,74 (м, 1 H) 4,01 (дк, J=8,2, 7,1 Гц, 2 H) 3,93 - 3,98 (м, J=8,0, 7,0, 7,0, 7,0, 3,4 Гц, 2 H) 3,92 - 3,95 (м, 2 H) 1,72 - 1,79 (м, 1 H) 1,72 (д, J=7,1 Гц, 3 H) 1,62 (ддд, J=13,8, 10,4, 5,0 Гц, 1 H) 1,41 (ддд, J=13,8, 9,2, 4,5 Гц, 1 H) 1,23 (тд, J=7,1, 1,0 Гц, 3 H) 1,16 (тд, J=7,0, 1,0 Гц, 3 H) 0,99 (д, J=6,7 Гц, 3 H) 0,97 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 540 [M+H]+.
Пример 1m
(2R)-2-[(2-Амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-бис(1-метилэтил)фосфат
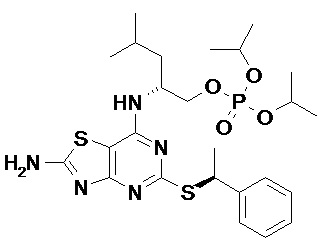
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 29%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли i-PrOH после 1 часа при температуре ледяной бани. Продукт представлял собой смесь моно- и диизопропилфосфатных эфиров, которые разделяли препаративной ВЭЖХ. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,47 (дд, J=8,1, 1,1 Гц, 2 H) 7,30 - 7,35 (м, 2 H) 7,23 (тт, J=7,2, 1,4 Гц, 1 H) 5,06 (к, J=7,2 Гц, 1 H) 4,71 (шс, 1 H) 4,51 (секстет, J=6,3 Гц, 1 H) 4,44 (секстет, J=6,3 Гц, 1 H) 3,85 - 3,95 (м, 2 H) 1,73 - 1,79 (м, 1 H) 1,72 (д, J=7,0 Гц, 3 H) 1,62 (ддд, J=13,7, 10,4, 5,2 Гц, 1 H) 1,41 (ддд, J=13,8, 9,2, 4,4 Гц, 1 H) 1,24 (д, J=6,1 Гц, 3 H) 1,21 (д, J=6,1 Гц, 3 H) 1,19 (д, J=6,1 Гц, 3 H) 1,13 (д, J=6,1 Гц, 3 H) 0,99 (д, J=6,7 Гц, 3 H) 0,98 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 540 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 29%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли i-PrOH после 1 часа при температуре ледяной бани. Продукт представлял собой смесь моно- и диизопропилфосфатных эфиров, которые разделяли препаративной ВЭЖХ. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,47 (дд, J=8,1, 1,1 Гц, 2 H) 7,30 - 7,35 (м, 2 H) 7,23 (тт, J=7,2, 1,4 Гц, 1 H) 5,06 (к, J=7,2 Гц, 1 H) 4,71 (шс, 1 H) 4,51 (секстет, J=6,3 Гц, 1 H) 4,44 (секстет, J=6,3 Гц, 1 H) 3,85 - 3,95 (м, 2 H) 1,73 - 1,79 (м, 1 H) 1,72 (д, J=7,0 Гц, 3 H) 1,62 (ддд, J=13,7, 10,4, 5,2 Гц, 1 H) 1,41 (ддд, J=13,8, 9,2, 4,4 Гц, 1 H) 1,24 (д, J=6,1 Гц, 3 H) 1,21 (д, J=6,1 Гц, 3 H) 1,19 (д, J=6,1 Гц, 3 H) 1,13 (д, J=6,1 Гц, 3 H) 0,99 (д, J=6,7 Гц, 3 H) 0,98 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 540 [M+H]+.
Пример 1n
(2R)-2-[(2-Амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-1-метилэтил-гидрофосфат

Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 37%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли i-PrOH после 1 часа при температуре ледяной бани. Продукт представлял собой смесь моно- и диизопропилфосфатных эфиров, которые разделяли препаративной ВЭЖХ. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,47 (дд, J=8,2, 1,2 Гц, 2 H) 7,32 - 7,38 (м, 2 H) 7,26 (тт, J=7,4, 1,5 Гц, 1 H) 5,13 (к, J=7,0 Гц, 1 H) 4,68 (шс, 1 H) 4,31 - 4,38 (м, 1 H) 3,81 - 3,89 (м, 2 H) 1,78 (д, J=7,0 Гц, 3 H) 1,67 - 1,77 (м, 2 H) 1,50 - 1,56 (м, 1 H) 1,18 (д, J=6,1 Гц, 3 H) 1,11 (д, J=6,4 Гц, 3 H) 0,99 (д, J=6,4 Гц, 3 H) 0,97 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 526 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 37%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли i-PrOH после 1 часа при температуре ледяной бани. Продукт представлял собой смесь моно- и диизопропилфосфатных эфиров, которые разделяли препаративной ВЭЖХ. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,47 (дд, J=8,2, 1,2 Гц, 2 H) 7,32 - 7,38 (м, 2 H) 7,26 (тт, J=7,4, 1,5 Гц, 1 H) 5,13 (к, J=7,0 Гц, 1 H) 4,68 (шс, 1 H) 4,31 - 4,38 (м, 1 H) 3,81 - 3,89 (м, 2 H) 1,78 (д, J=7,0 Гц, 3 H) 1,67 - 1,77 (м, 2 H) 1,50 - 1,56 (м, 1 H) 1,18 (д, J=6,1 Гц, 3 H) 1,11 (д, J=6,4 Гц, 3 H) 0,99 (д, J=6,4 Гц, 3 H) 0,97 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 526 [M+H]+.
Пример 1o
(2R)-2-[(2-Амино-5-{[1-(2-фторфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфат
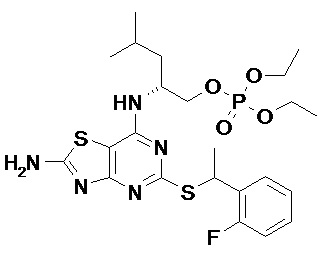
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(2-фторфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 46%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,06 (с, 4 H) 7,53 - 7,58 (м, 2 H) 7,27 - 7,33 (м, 2 H) 7,12 - 7,20 (м, 6 H) 5,22 (к, J=7,0 Гц, 2 H) 4,38 - 4,55 (м, 2 H) 3,81 - 4,00 (м, 12 H) 1,67 (д, J=7,0 Гц, 3 H) 1,65 (д, J=7,0 Гц, 3 H) 1,58 - 1,66 (м, 2 H) 1,54 (ддд, J=18,7, 5,3, 5,0 Гц, 2 H) 1,28 - 1,36 (м, 2 H) 1,16 (тд, J=7,0, 0,7 Гц, 3 H) 1,15 (тд, J=7,0, 0,7 Гц, 3 H) 1,11 (тд, J=7,0, 0,8 Гц, 6 H) 0,89 (д, J=6,6 Гц, 3 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,6 Гц, 3 H) 0,81 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 558 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 46%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,06 (с, 4 H) 7,53 - 7,58 (м, 2 H) 7,27 - 7,33 (м, 2 H) 7,12 - 7,20 (м, 6 H) 5,22 (к, J=7,0 Гц, 2 H) 4,38 - 4,55 (м, 2 H) 3,81 - 4,00 (м, 12 H) 1,67 (д, J=7,0 Гц, 3 H) 1,65 (д, J=7,0 Гц, 3 H) 1,58 - 1,66 (м, 2 H) 1,54 (ддд, J=18,7, 5,3, 5,0 Гц, 2 H) 1,28 - 1,36 (м, 2 H) 1,16 (тд, J=7,0, 0,7 Гц, 3 H) 1,15 (тд, J=7,0, 0,7 Гц, 3 H) 1,11 (тд, J=7,0, 0,8 Гц, 6 H) 0,89 (д, J=6,6 Гц, 3 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,6 Гц, 3 H) 0,81 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 558 [M+H]+.
Пример 1p
(2R)-2-[(2-Амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфат
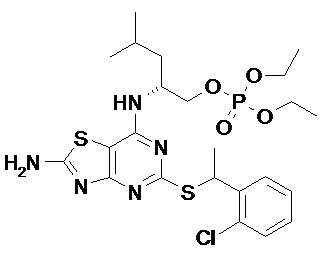
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 36%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 36%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,06 (с, 2 H) 7,63 (дд, J=7,8, 1,7 Гц, 1 H) 7,45 (дд, J=8,0, 1,3 Гц, 1 H) 7,34 (ддд, J=7,8, 7,4, 1,3 Гц, 1 H) 7,28 (ддд, J=8,0, 7,4, 1,7 Гц, 1 H) 7,15 (д, J=8,2 Гц, 1 H) 5,35 (к, J=7,0 Гц, 1 H) 4,41 - 4,52 (м, 1 H) 3,95 - 4,01 (м, 1 H) 3,86 - 3,96 (м, 5 H) 1,67 (д, J=7,0 Гц, 3 H) 1,58 - 1,65 (м, 1 H) 1,55 (ддд, J=13,5, 10,4, 5,0 Гц, 1 H) 1,30 (ддд, J=13,5, 9,2, 4,5 Гц, 1 H) 1,15 (тд, J=7,1, 0,7 Гц, 3 H) 1,11 (тд, J=7,1, 0,7 Гц, 3 H) 0,87 (д, J=6,6 Гц, 3 H) 0,78 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 574 [M+H]+. Диастереомер B: 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,06 (с, 2 H) 7,63 (дд, J=7,8, 1,7 Гц, 1 H) 7,45 (дд, J=7,9, 1,3 Гц, 1 H) 7,35 (ддд, J=7,8, 7,4, 1,3 Гц, 1 H) 7,28 (ддд, J=7,9, 7,4, 1,7 Гц, 1 H) 7,17 (д, J=8,2 Гц, 1 H) 5,36 (к, J=7,1 Гц, 1 H) 4,42 - 4,54 (м, 1 H) 3,93 (дк, J=8,2, 7,1 Гц, 2 H) 3,84 - 3,92 (м, 2 H) 3,78 - 3,86 (м, 2 H) 1,65 (д, J=7,0 Гц, 3 H) 1,60 - 1,70 (м, 1 H) 1,57 (ддд, J=13,7, 10,2, 4,8 Гц, 1 H) 1,32 (ддд, J=13,7, 9,1, 4,4 Гц, 1 H) 1,15 (тд, J=7,1, 0,8 Гц, 3 H) 1,09 (тд, J=7,1, 0,8 Гц, 3 H) 0,90 (д, J=6,6 Гц, 3 H) 0,87 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 574 [M+H]+.
Пример 1q
(2R)-2-[(2-Амино-5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфат
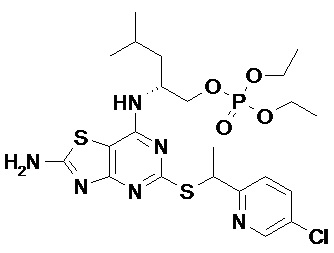
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 27%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. После препаративной ВЭЖХ очистки (кислотный способ) выделяли продукт в форме соли ТФК. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,58 (дд, J=2,6, 0,7 Гц, 1 H) 8,57 (дд, J=2,6, 0,7 Гц, 1 H) 8,36 (шс, 2 H) 8,34 (шс, 2 H) 7,89 (дд, J=8,5, 2,6 Гц, 1 H) 7,88 (дд, J=8,5, 2,6 Гц, 1 H) 7,60 (дд, J=8,5, 0,7 Гц, 1 H) 7,57 (дд, J=8,5, 0,7 Гц, 1 H) 7,58 (шс, 2 H) 5,16 (к, J=7,1 Гц, 1 H) 5,09 (к, J=7,2 Гц, 1 H) 4,51 - 4,62 (м, 1 H) 4,30 - 4,40 (м, 1 H) 3,83 - 4,02 (м, 12 H) 1,67 (д, J=7,1 Гц, 3 H) 1,66 (д, J=7,1 Гц, 3 H) 1,57 - 1,67 (м, 2 H) 1,49 - 1,57 (м, 2 H) 1,35 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,31 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,15 (дт, J=7,1, 0,8 Гц, 3 H) 1,15 (тд, J=7,1, 0,8 Гц, 3 H) 1,12 (тд, J=7,1, 0,8 Гц, 3 H) 1,11 (тд, J=7,1, 0,8 Гц, 3 H) 0,90 (д, J=6,7 Гц, 3 H) 0,87 (д, J=6,6 Гц, 6 H) 0,76 (д, J=6,5 Гц, 3 H). МС (ИЭР+) m/z 575 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 27%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. После препаративной ВЭЖХ очистки (кислотный способ) выделяли продукт в форме соли ТФК. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,58 (дд, J=2,6, 0,7 Гц, 1 H) 8,57 (дд, J=2,6, 0,7 Гц, 1 H) 8,36 (шс, 2 H) 8,34 (шс, 2 H) 7,89 (дд, J=8,5, 2,6 Гц, 1 H) 7,88 (дд, J=8,5, 2,6 Гц, 1 H) 7,60 (дд, J=8,5, 0,7 Гц, 1 H) 7,57 (дд, J=8,5, 0,7 Гц, 1 H) 7,58 (шс, 2 H) 5,16 (к, J=7,1 Гц, 1 H) 5,09 (к, J=7,2 Гц, 1 H) 4,51 - 4,62 (м, 1 H) 4,30 - 4,40 (м, 1 H) 3,83 - 4,02 (м, 12 H) 1,67 (д, J=7,1 Гц, 3 H) 1,66 (д, J=7,1 Гц, 3 H) 1,57 - 1,67 (м, 2 H) 1,49 - 1,57 (м, 2 H) 1,35 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,31 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,15 (дт, J=7,1, 0,8 Гц, 3 H) 1,15 (тд, J=7,1, 0,8 Гц, 3 H) 1,12 (тд, J=7,1, 0,8 Гц, 3 H) 1,11 (тд, J=7,1, 0,8 Гц, 3 H) 0,90 (д, J=6,7 Гц, 3 H) 0,87 (д, J=6,6 Гц, 6 H) 0,76 (д, J=6,5 Гц, 3 H). МС (ИЭР+) m/z 575 [M+H]+.
Пример 1r
(2R)-2-[(2-Амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфат
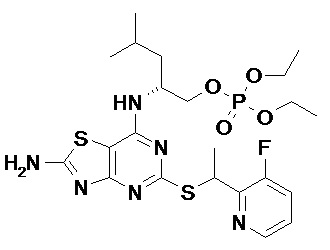
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 47%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. После препаративной ВЭЖХ очистки (кислотный способ) выделяли продукт в форме соли ТФК. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,48 (шс, 2 H) 8,46 (шс, 2 H) 8,41 - 8,43 (м, 2 H) 7,74 (ддд, J=10,1, 8,4, 1,4 Гц, 1 H) 7,79 (шс, 2 H) 7,74 (ддд, J=10,1, 8,4, 1,4 Гц, 1 H) 7,44 (ддд, J=8,4, 4,4, 3,2 Гц, 1 H) 7,43 (ддд, J=8,4, 4,4, 3,2 Гц, 1 H) 5,47 (к, J=6,9 Гц, 1 H) 5,46 (к, J=6,9 Гц, 1 H) 4,51 - 4,64 (м, 2 H) 3,99 - 4,05 (м, 1 H) 3,85 - 4,00 (м, 11 H) 1,72 (д, J=7,0 Гц, 3 H) 1,70 (д, J=7,0 Гц, 3 H) 1,60 - 1,69 (м, 2 H) 1,57 (ддд, J=13,6, 10,0, 5,0 Гц, 2 H) 1,37 (ддд, J=13,6, 9,2, 4,5 Гц, 1 H) 1,37 (ддд, J=13,6, 9,2, 4,5 Гц, 1 H) 1,16 (тд, J=7,0, 0,7 Гц, 3 H) 1,15 (тд, J=7,0, 0,7 Гц, 3 H) 1,12 (тд, J=7,0, 0,7 Гц, 3 H) 1,10 (тд, J=7,0, 0,7 Гц, 3 H) 0,91 (д, J=6,6 Гц, 3 H) 0,91 (д, J=6,6 Гц, 3 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 558 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 47%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. После препаративной ВЭЖХ очистки (кислотный способ) выделяли продукт в форме соли ТФК. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,48 (шс, 2 H) 8,46 (шс, 2 H) 8,41 - 8,43 (м, 2 H) 7,74 (ддд, J=10,1, 8,4, 1,4 Гц, 1 H) 7,79 (шс, 2 H) 7,74 (ддд, J=10,1, 8,4, 1,4 Гц, 1 H) 7,44 (ддд, J=8,4, 4,4, 3,2 Гц, 1 H) 7,43 (ддд, J=8,4, 4,4, 3,2 Гц, 1 H) 5,47 (к, J=6,9 Гц, 1 H) 5,46 (к, J=6,9 Гц, 1 H) 4,51 - 4,64 (м, 2 H) 3,99 - 4,05 (м, 1 H) 3,85 - 4,00 (м, 11 H) 1,72 (д, J=7,0 Гц, 3 H) 1,70 (д, J=7,0 Гц, 3 H) 1,60 - 1,69 (м, 2 H) 1,57 (ддд, J=13,6, 10,0, 5,0 Гц, 2 H) 1,37 (ддд, J=13,6, 9,2, 4,5 Гц, 1 H) 1,37 (ддд, J=13,6, 9,2, 4,5 Гц, 1 H) 1,16 (тд, J=7,0, 0,7 Гц, 3 H) 1,15 (тд, J=7,0, 0,7 Гц, 3 H) 1,12 (тд, J=7,0, 0,7 Гц, 3 H) 1,10 (тд, J=7,0, 0,7 Гц, 3 H) 0,91 (д, J=6,6 Гц, 3 H) 0,91 (д, J=6,6 Гц, 3 H) 0,88 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 558 [M+H]+.
Пример 1s
(2R)-2-[(2-Амино-5-{[1-(3-цианофенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфат
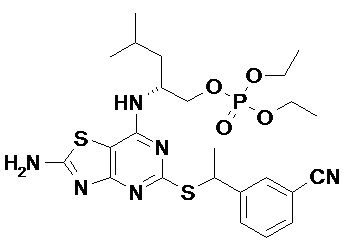
Указанное в заголовке соединение синтезировали из 3-{1-[(2-амино-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензонитрила ( S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 50%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. После препаративной ВЭЖХ очистки (кислотный способ) выделяли продукт в форме соли ТФК. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,36 (шс, 4 H) 7,95 (дд, J=1,8, 1,2 Гц, 1 H) 7,93 (дд, J=1,9, 1,2 Гц, 1 H) 7,84 (ддд, J=7,8, 1,8, 1,5 Гц, 1 H) 7,83 (ддд, J=7,8, 1,8, 1,5 Гц, 1 H) 7,72 (ддд, J=7,7, 1,5, 1,2 Гц, 1 H) 7,71 (ддд, J=7,7, 1,5, 1,2 Гц, 1 H) 7,55 (дд, J=7,8, 7,7 Гц, 1 H) 7,53 (дд, J=7,8, 7,7 Гц, 1 H) 5,08 (к, J=7,2 Гц, 1 H) 5,06 (к, J=7,2 Гц, 1 H) 4,45 - 4,56 (м, 1 H) 4,30 - 4,40 (м, 1 H) 3,84 - 3,99 (м, 12 H) 1,68 (д, J=7,2 Гц, 3 H) 1,65 (д, J=7,2 Гц, 3 H) 1,49 - 1,65 (м, 4 H) 1,34 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,31 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,16 (тд, J=7,1, 0,6 Гц, 6 H) 1,13 (тд, J=7,1, 0,8 Гц, 3 H) 1,10 (тд, J=7,1, 0,7 Гц, 3 H) 0,90 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,5 Гц, 3 H) 0,86 (д, J=6,5 Гц, 3 H) 0,73 (д, J=6,5 Гц, 3 H). МС (ИЭР+) m/z 565 [M+H]+.
S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 50%, используя способ, описанный для примера 1, за исключением того, что вместо ТГФ и воды добавляли EtOH после 1 часа при температуре ледяной бани. После препаративной ВЭЖХ очистки (кислотный способ) выделяли продукт в форме соли ТФК. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,36 (шс, 4 H) 7,95 (дд, J=1,8, 1,2 Гц, 1 H) 7,93 (дд, J=1,9, 1,2 Гц, 1 H) 7,84 (ддд, J=7,8, 1,8, 1,5 Гц, 1 H) 7,83 (ддд, J=7,8, 1,8, 1,5 Гц, 1 H) 7,72 (ддд, J=7,7, 1,5, 1,2 Гц, 1 H) 7,71 (ддд, J=7,7, 1,5, 1,2 Гц, 1 H) 7,55 (дд, J=7,8, 7,7 Гц, 1 H) 7,53 (дд, J=7,8, 7,7 Гц, 1 H) 5,08 (к, J=7,2 Гц, 1 H) 5,06 (к, J=7,2 Гц, 1 H) 4,45 - 4,56 (м, 1 H) 4,30 - 4,40 (м, 1 H) 3,84 - 3,99 (м, 12 H) 1,68 (д, J=7,2 Гц, 3 H) 1,65 (д, J=7,2 Гц, 3 H) 1,49 - 1,65 (м, 4 H) 1,34 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,31 (ддд, J=13,6, 9,1, 4,3 Гц, 1 H) 1,16 (тд, J=7,1, 0,6 Гц, 6 H) 1,13 (тд, J=7,1, 0,8 Гц, 3 H) 1,10 (тд, J=7,1, 0,7 Гц, 3 H) 0,90 (д, J=6,6 Гц, 3 H) 0,86 (д, J=6,5 Гц, 3 H) 0,86 (д, J=6,5 Гц, 3 H) 0,73 (д, J=6,5 Гц, 3 H). МС (ИЭР+) m/z 565 [M+H]+.
Пример 2
Получение [7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата
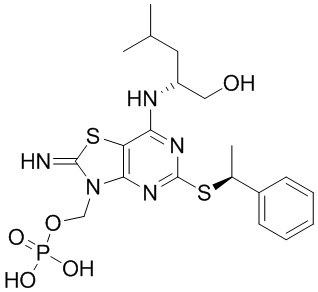
К смеси (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) (40 мг, 0,10 ммоль), K2CO3 (28 мг, 0,20 ммоль) и йодида натрия (22 мг, 0,15 ммоль) в CH3CN добавляли ди-трет-бутилхлорметилфосфат (39 мг, 0,15 ммоль). Реакционную смесь перемешивали при 50°С в течение 21 часа. Реакционную смесь выпаривали и добавляли ДХМ (5 мл) и воду (2 мл). Разделяли фазы и промывали органическую фазу водой (2×2 мл) и насыщенным солевым раствором (2 мл), сушили над MgSO4, фильтровали и выпаривали с получением 60 мг неочищенного продукта в виде оранжевого твердого вещества. К неочищенному веществу в диоксане (1,5 мл) добавляли конц. HCl (30 мкл, 0,38 ммоль) и перемешивали смесь при комнатной температуре в течение 2 часов. К полученной смеси добавляли 2 M NaOH (300 мкл), в результате чего рН составил около 7. Смесь разбавляли MeOH, ДМСО и водой, фильтровали и очищали препаративной ВЭЖХ (основной способ). Чистые фракции объединяли, выпаривали и сушили в вакууме с получением 7,2 мг (14%) чистого продукта в виде белого твердого вещества. После очистки продукт считали диаммониевой солью. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,46 - 7,50 (м, 2 H) 7,30 - 7,35 (м, 2 H) 7,20 - 7,24 (м, 1 H) 5,86 - 5,93 (м, 2 H) 5,02 (к, J=7,12 Гц, 1 H) 4,42 - 4,57 (м, 1 H) 3,53 (дд, J=11,11, 5,42 Гц, 1 H) 3,50 (дд, J=11,11, 5,32 Гц, 1 H) 1,72 (д, J=7,12 Гц, 3 H) 1,62 - 1,71 (м, 1 H) 1,53 (ддд, J=13,95, 10,10, 4,87 Гц, 1 H) 1,45 (ддд, J=13,95, 9,18, 4,58 Гц, 1 H) 0,96 (д, J=6,71 Гц, 3 H) 0,94 (д, J=6,60 Гц, 3 H). МС (ИЭР+) m/z 514 [M+H]+.
Пример 2b
[5-{[1-(2-Фторфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат
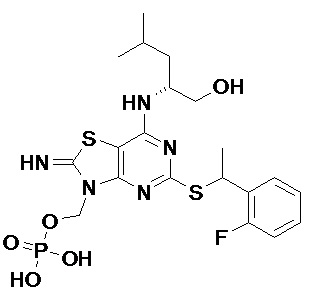
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(2-фторфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 12%, используя способ, описанный для примера 2. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,54 - 7,60 (м, 2 H) 7,23 - 7,29 (м, 2 H) 7,12 - 7,17 (м, 2 H) 7,06 - 7,13 (м, 2 H) 5,87 - 5,96 (м, 4 H) 5,32 (к, J=7,17 Гц, 1 H) 5,31 (к, J=7,17 Гц, 1 H) 4,46 - 4,53 (м, 1 H) 4,41 - 4,48 (м, 1 H) 3,62 (дд, J=11,20, 5,08 Гц, 1 H) 3,55 (дд, J=11,20, 5,56 Гц, 1 H) 3,51 (дд, J=11,20, 5,12 Гц, 1 H) 3,47 (дд, J=11,20, 4,97 Гц, 1 H) 1,72 (д, J=7,17 Гц, 3 H) 1,71 (д, J=7,17 Гц, 3 H) 1,60 - 1,69 (м, 2 H) 1,51 - 1,59 (м, 2 H) 1,43 (ддд, J=13,97, 9,06, 4,46 Гц, 1 H) 1,42 (ддд, J=13,79, 9,06, 4,46 Гц, 1 H) 0,96 (д, J=6,71 Гц, 3 H) 0,94 (д, J=6,70 Гц, 3 H) 0,94 (д, J=6,50 Гц, 3 H) 0,89 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 532 [M+H]+.
Пример 2c
[5-{[1-(2-Хлорфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат
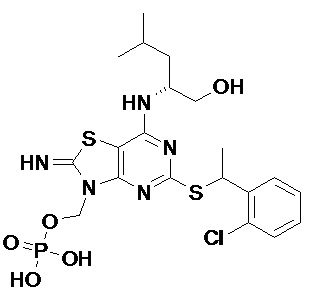
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 12%, используя способ, описанный для примера 2. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,67 (дд, J=7,78, 1,70 Гц, 1 H) 7,66 (дд, J=7,78, 1,70 Гц, 1 H) 7,43 (дд, J=7,94, 1,35 Гц, 1 H) 7,42 (дд, J=7,94, 1,35 Гц, 1 H) 7,29 (ддд, J=7,78, 7,42, 1,35 Гц, 2 H) 7,24 (ддд, J=7,94, 7,42, 1,70 Гц, 1 H) 7,23 (ддд, J=7,94, 7,42, 1,70 Гц, 1 H) 5,86 - 5,94 (м, 4 H) 5,48 (к, J=7,14 Гц, 1 H) 5,48 (к, J=7,14 Гц, 1 H) 4,43 - 4,54 (м, 2 H) 3,64 (дд, J=11,20, 4,93 Гц, 1 H) 3,56 (дд, J=11,22, 5,51 Гц, 1 H) 3,48 (дд, J=11,29, 4,80 Гц, 1 H) 3,42 (дд, J=11,20, 4,93 Гц, 1 H) 1,71 (д, J=7,14 Гц, 3 H) 1,69 (д, J=7,14 Гц, 3 H) 1,53 - 1,70 (м, 4 H) 1,41 (ддд, J=13,69, 9,15, 4,48 Гц, 1 H) 1,40 (ддд, J=13,69, 9,15, 4,48 Гц, 1 H) 0,96 (д, J=6,56 Гц, 3 H) 0,95 (д, J=6,56 Гц, 3 H) 0,93 (д, J=6,71 Гц, 3 H) 0,85 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 548 [M+H]+.
Пример 2d
[5-{[1-(5-Хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат
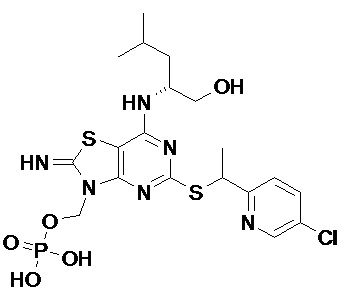
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 6%, используя способ, описанный для примера 2. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,49 (дд, J=2,46, 0,70 Гц, 1 H) 8,48 (дд, J=2,46, 0,70 Гц, 1 H) 7,83 (дд, J=8,41, 2,46 Гц, 1 H) 7,83 (дд, J=8,41, 2,46 Гц, 1 H) 7,68 (дд, J=8,41, 0,70 Гц, 1 H) 7,67 (дд, J=8,41, 0,70 Гц, 1 H) 5,87 - 5,94 (м, 2 H) 5,81 - 5,87 (м, 2 H) 5,15 (к, J=7,23 Гц, 1 H) 5,12 (к, J=7,23 Гц, 1 H) 4,41 - 4,50 (м, 1 H) 4,25 - 4,35 (м, 1 H) 3,54 (д, J=5,49 Гц, 2 H) 3,45 - 3,52 (м, 2 H) 1,71 (д, J=7,23 Гц, 3 H) 1,70 (д, J=7,23 Гц, 3 H) 1,56 - 1,69 (м, 2 H) 1,47 - 1,54 (м, 2 H) 1,42 (ддд, J=13,81, 9,23, 4,43 Гц, 1 H) 1,41 (ддд, J=13,81, 9,23, 4,43 Гц, 1 H) 0,95 (д, J=6,71 Гц, 3 H) 0,92 (д, J=6,71 Гц, 3 H) 0,92 (д, J=6,41 Гц, 3 H) 0,83 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 549 [M+H]+.
Пример 2e
[7-{[(1R)-1-(Гидроксиметил)-3-метилбутил]амино}-2-имино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат
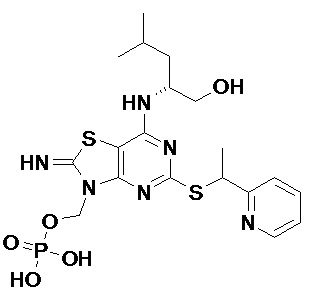
Указанное в заголовке соединение синтезировали из (2R)-2-({2-амино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 4%, используя способ, описанный для примера 2. Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,49 (ддд, J=4,95, 1,85, 1,00 Гц, 1 H) 7,83 (ддд, J=7,89, 7,54, 1,85 Гц, 1 H) 7,67 (ддд, J=7,89, 1,10, 1,00 Гц, 1 H) 7,29 (ддд, J=7,54, 4,95, 1,10 Гц, 1 H) 5,86 (дд, J=10,74, 9,88 Гц, 1 H) 5,81 (дд, J=10,74, 9,65 Гц, 1 H) 5,15 (к, J=7,28 Гц, 1 H) 4,42 - 4,51 (м, 1 H) 3,50 (дд, J=11,15, 5,52 Гц, 1 H) 3,46 (дд, J=11,15, 5,46 Гц, 1 H) 1,72 (д, J=7,28 Гц, 3 H) 1,58 - 1,68 (м, 1 H) 1,51 (ддд, J=13,94, 10,22, 4,87 Гц, 1 H) 1,43 (ддд, J=13,94, 9,20, 4,45 Гц, 1 H) 0,94 (д, J=6,56 Гц, 3 H) 0,92 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 515 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,49 (ддд, J=4,95, 1,85, 1,00 Гц, 1 H) 7,82 (ддд, J=7,89, 7,54, 1,85 Гц, 1 H) 7,68 (ддд, J=7,89, 1,10, 1,00 Гц, 1 H) 7,29 (ддд, J=7,54, 4,95, 1,10 Гц, 1 H) 5,87 (дд, J=10,74, 9,88 Гц, 1 H) 5,81 (дд, J=10,74, 9,65 Гц, 1 H) 5,13 (к, J=7,28 Гц, 1 H) 4,28 - 4,37 (м, 1 H) 3,56 (дд, J=11,15, 5,46 Гц, 1 H) 3,52 (дд, J=11,15, 5,57 Гц, 1 H) 1,71 (д, J=7,28 Гц, 3 H) 1,57 - 1,68 (м, 1 H) 1,50 (ддд, J=13,94, 10,22, 4,87 Гц, 1 H) 1,42 (ддд, J=13,94, 9,20, 4,45 Гц, 1 H) 0,92 (д, J=6,71 Гц, 3 H) 0,84 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 515 [M+H]+.
Пример 2f
[5-{[1-(3-Фторпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат
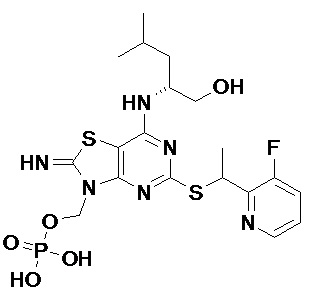
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 19%, используя способ, описанный для примера 2. Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,33 (дт, J=4,74, 1,32 Гц, 1 H) 7,65 (ддд, J=9,96, 8,39, 1,32 Гц, 1 H) 7,36 (ддд, J=8,39, 4,74, 4,12 Гц, 1 H) 5,89 (т, J=10,40 Гц, 1 H) 5,83 (т, J=10,40 Гц, 1 H) 5,48 (к, J=7,15 Гц, 1 H) 4,45 - 4,53 (м, 1 H) 3,54 (дд, J=11,22, 5,44 Гц, 1 H) 3,52 (дд, J=11,22, 5,29 Гц, 1 H) 1,73 (д, J=7,15 Гц, 3 H) 1,62 - 1,70 (м, 1 H) 1,54 (ддд, J=13,85, 10,11, 5,01 Гц, 1 H) 1,43 (ддд, J=13,85, 9,19, 4,52 Гц, 1 H) 0,95 (д, J=6,71 Гц, 3 H) 0,93 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 533 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,34 (дт, J=4,7, 1,3 Гц, 1 H) 7,64 (ддд, J=10,0, 8,4, 1,3 Гц, 1 H) 7,36 (ддд, J=8,4, 4,7, 4,1 Гц, 1 H) 5,89 (дд, J=10,7, 10,1 Гц, 1 H) 5,83 (дд, J=10,7, 10,1 Гц, 1 H) 5,48 (к, J=7,2 Гц, 1 H) 4,41 - 4,53 (м, 1 H) 3,59 (дд, J=11,2, 5,3 Гц, 1 H) 3,56 (дд, J=11,2, 5,6 Гц, 1 H) 1,75 (д, J=7,2 Гц, 3 H) 1,62 - 1,70 (м, 1 H) 1,54 (ддд, J=13,9, 10,1, 5,0 Гц, 1 H) 1,43 (ддд, J=13,9, 9,2, 4,5 Гц, 1 H) 0,95 (д, J=6,7 Гц, 3 H) 0,92 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 533 [M+H]+.
Пример 2g
[5-{[1-(3-Цианофенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат
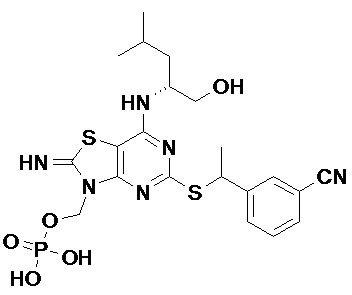
Указанное в заголовке соединение синтезировали из 3-{1-[(2-амино-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензонитрила (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) с выходом 22%, используя способ, описанные для примера 2. Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,85 - 7,88 (м, 2 H) 7,59 (дт, J=7,76, 1,38 Гц, 1 H) 7,54 (дд, J=8,44, 7,76 Гц, 1 H) 5,83 (д, J=9,82 Гц, 2 H) 5,09 (к, J=7,21 Гц, 1 H) 4,40 - 4,49 (м, 1 H) 3,51 (дд, J=11,13, 5,49 Гц, 1 H) 3,46 (дд, J=11,13, 5,35 Гц, 1 H) 1,71 (д, J=7,21 Гц, 3 H) 1,60 - 1,68 (м, 1 H) 1,52 (ддд, J=13,85, 10,25, 4,91 Гц, 1 H) 1,43 (ддд, J=13,85, 9,19, 4,35 Гц, 1 H) 0,95 (д, J=6,71 Гц, 3 H) 0,93 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 539 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,86 - 7,89 (м, 2 H) 7,58 (дт, J=7,8, 1,4 Гц, 1 H) 7,53 (дд, J=8,4, 7,8 Гц, 1 H) 5,83 (дд, J=10,6, 9,7 Гц, 1 H) 5,81 (дд, J=10,6, 9,6 Гц, 1 H) 5,08 (к, J=7,3 Гц, 1 H) 4,28 - 4,38 (м, 1 H) 3,57 (дд, J=11,4, 5,6 Гц, 1 H) 3,55 (дд, J=11,4, 5,7 Гц, 1 H) 1,70 (д, J=7,3 Гц, 3 H) 1,57 - 1,66 (м, 1 H) 1,50 (ддд, J=13,9, 10,4, 5,0 Гц, 1 H) 1,41 (ддд, J=13,9, 9,3, 4,3 Гц, 1 H) 0,92 (д, J=6,7 Гц, 3 H) 0,82 (д, J=6,6 Гц, 3 H). МС (ИЭР+) m/z 539 [M+H]+.
Пример 2h
[5-{[(1S)-1-(5-Хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-oxo[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфат
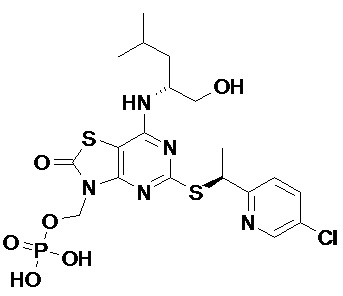
Указанное в заголовке соединение синтезировали из 5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-она (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) с выходом 39%, используя способ, описанный для примера 2. 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,49 (дд, J=2,53, 0,66 Гц, 1 H) 7,86 (дд, J=8,47, 2,53 Гц, 1 H) 7,77 (дд, J=8,47, 0,66 Гц, 1 H) 5,67 (дд, J=9,30, 5,92 Гц, 1 H) 5,63 (дд, J=9,30, 5,83 Гц, 1 H) 5,23 (к, J=7,32 Гц, 1 H) 4,35 - 4,48 (м, 1 H) 3,51 (дд, J=11,06, 5,53 Гц, 1 H) 3,45 (дд, J=11,06, 5,65 Гц, 1 H) 1,68 (д, J=7,32 Гц, 3 H) 1,58 - 1,66 (м, 1 H) 1,49 (ддд, J=13,87, 10,27, 4,85 Гц, 1 H) 1,41 (ддд, J=13,87, 9,27, 4,36 Гц, 1 H) 0,93 (д, J=6,68 Гц, 3 H) 0,90 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 550 [M+H]+.
Пример 3
Получение (2R)-2-[(5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-2-оксо-2,3-dihydro[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата
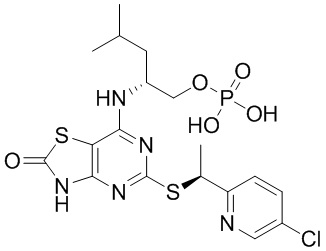
Оксихлорид фосфора (383 мг, 2,5 ммоль) растворяли в ТГФ (0,75 мл) и добавляли воду (28 мг, 1,58 ммоль). Смесь охлаждали на ледяной бане и добавляли пиридин (125 мг, 127 мкл, 1,58 ммоль), затем 5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-он (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) (110 мг, 0,25 ммоль). Реакционную смесь перемешивали при температуре ледяной бани в течение 2 часов. Добавляли воду (4 мл) и перемешивали смесь при комнатной температуре в течение 1 часа. pH доводили до 11-12 с помощью 5 M NaOH (около 2,8 мл) и промывали смесь ДХМ (3x4 мл). pH водной фазы доводили до 1, добавляя конц. HCl (около 300 мкл), в результате чего неочищенный продукт выпадал в осадок. Смесь центрифугировали и отбрасывали надосадочный раствор. Оставшееся твердое вещество промывали водой (2 мл), центрифугировали и отбрасывали надосадочный раствор. Оставшееся твердое вещество растворяли в MeOH и выпаривали с получением 47 мг продукта с чистотой 90%. Неочищенное вещество растворяли в смеси ДМСО/вода и доводили pH до около 7, и очищали препаративной ВЭЖХ (основной способ). Чистые фракции объединяли, выпаривали и сушили в вакууме с получением 34 мг (24%) чистого продукта в виде грязновато-белого твердого вещества. После очистки продукт считали диаммониевой солью. 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,47 (дд, J=2,54, 0,48 Гц, 1 H) 7,84 (дд, J=8,42, 2,54 Гц, 1 H) 7,62 (дд, J=8,42, 0,48 Гц, 1 H) 5,17 (к, J=7,20 Гц, 1 H) 4,53 - 4,68 (м, 1 H) 3,88 (дт, J=10,13, 5,09 Гц, 1 H) 3,83 (дт, J=10,13, 5,25 Гц, 1 H) 1,72 (д, J=7,20 Гц, 3 H) 1,65 - 1,73 (м, 1 H) 1,60 (ддд, J=13,86, 9,91, 5,20 Гц, 1 H) 1,54 (ддд, J=13,86, 9,04, 4,93 Гц, 1 H) 0,96 (д, J=6,63 Гц, 3 H) 0,94 (д, J=6,53 Гц, 3 H). МС (ИЭР+) m/z 520 [M+H]+.
Пример 3b
(2R)-4-Метил-2-({2-оксо-5-[(1-пиридин-2-илэтил)сульфанил]-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)пентил-дигидрофосфат
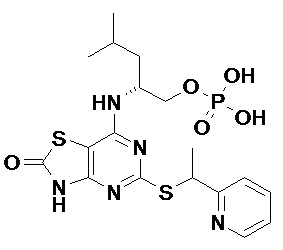
Указанное в заголовке соединение синтезировали из 7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-{[1-пиридин-2-илэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-она (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) с выходом 2%, используя способ, описанный для примера 3. Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 12,36 (шс, 2 H) 8,52 (ддд, J=1,97, 0,97 Гц, 1 H) 8,52 (ддд, J=1,87, 0,97 Гц, 1 H) 7,76 (ддд, J=7,80, 7,59, 1,87 Гц, 1 H) 7,75 (ддд, J=7,80, 7,59, 1,87 Гц, 1 H) 7,53 (дт, J=7,80, 0,97 Гц, 1 H) 7,50 (дт, J=7,80, 0,97 Гц, 1 H) 7,27 (ддд, J=7,59, 4,87, 0,97 Гц, 1 H) 7,25 (ддд, J=7,59, 4,87, 0,97 Гц, 1 H) 7,11 (шс, 1 H) 5,11 (к, J=7,07 Гц, 1 H) 5,06 (к, J=7,07 Гц, 1 H) 4,37 - 4,51 (м, 1 H) 4,16 - 4,30 (м, 1 H) 3,73 - 3,85 (м, 3 H) 3,67 - 3,73 (м, 1 H) 1,67 (д, J=7,07 Гц, 3 H) 1,66 (д, J=7,07 Гц, 3 H) 1,54 - 1,64 (м, 2 H) 1,45 - 1,54 (м, 2 H) 1,34 - 1,45 (м, 2 H) 0,89 (д, J=6,56 Гц, 3 H) 0,87 (д, J=6,71 Гц, 3 H) 0,86 (д, J=6,56 Гц, 3 H) 0,78 (д, J=6,26 Гц, 3 H). МС (ИЭР+) m/z 486 [M+H]+.
Пример 3c
(2R)-4-Метил-2-{[5-({1-[4-(метилсульфонил)фенил]этил}сульфанил)-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил]амино}пентил-дигидрофосфат
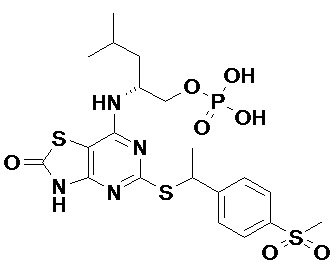
Указанное в заголовке соединение синтезировали из 7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-({1-[4-(метилсульфонил)фенил]этил}сульфанил)[1,3]тиазоло[4,5-d]пиримидин-2(3H)-она (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) в виде одного диастереомера, с выходом 43%, используя способ, описанный для примера 3. Продукт представлял собой один диастереомер. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,41 (шс, 1 H) 7,83 - 7,87 (м, 2 H) 7,73 - 7,77 (м, 2 H) 7,30 (шс, 2 H) 5,04 (к, J=7,18 Гц, 1 H) 4,07 - 4,16 (м, 1 H) 3,67 - 3,77 (м, 2 H) 3,19 (с, 3 H) 1,67 (д, J=7,18 Гц, 3 H) 1,51 - 1,60 (м, 1 H) 1,47 (ддд, J=13,50, 8,30, 6,70 Гц, 1 H) 1,37 - 1,44 (м, 1 H) 0,85 (д, J=6,56 Гц, 3 H) 0,77 (д, J=6,26 Гц, 3 H). МС (ИЭР+) m/z 563 [M+H]+.
Пример 3d
(2R)-2-[(5-{[1-(3-Карбамоилфенил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
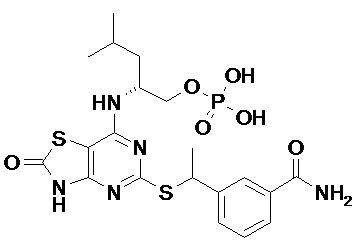
Указанное в заголовке соединение синтезировали из 3-{1-[(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензамида (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) в виде одного диастереомера, с выходом 20%, используя способ, описанный для примера 3. Продукт представлял собой один диастереомер. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,33 (шс, 1 H) 8,46 (шс, 1 H) 8,06 (шс, 1 H) 7,76 (ддд, J=7,70, 1,68, 1,22 Гц, 1 H) 7,58 (ддд, J=7,70, 1,51, 1,22 Гц, 1 H) 7,41 (т, J=7,70 Гц, 1 H) 7,30 (шс, 1 H) 7,23 (шс, 3 H) 5,07 (к, J=7,04 Гц, 1 H) 4,25 - 4,42 (м, 1 H) 3,74 (тд, J=10,15, 4,82 Гц, 1 H) 3,65 - 3,71 (м, 1 H) 1,70 (д, J=7,04 Гц, 3 H) 1,57 - 1,66 (м, 1 H) 1,40 - 1,51 (м, 2 H) 0,89 (д, J=6,56 Гц, 3 H) 0,85 (д, J=6,56 Гц, 1 H). МС (ИЭР+) m/z 528 [M+H]+.
Пример 3e
(2R)-2-[(5-{[1-(2-Хлорфенил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
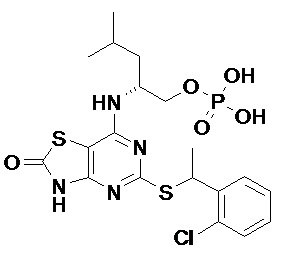
Указанное в заголовке соединение синтезировали из 5-{[1-(2-хлорфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-она (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) с выходом 49%, используя способ, описанный для примера 3. Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,43 (шс, 2 H) 7,61 (дд, J=7,75, 1,65 Гц, 1 H) 7,47 (дд, J=7,88, 1,30 Гц, 1 H) 7,36 (ддд, J=7,75, 7,40, 1,60 Гц, 1 H) 7,29 (ддд, J=7,88, 7,40, 1,65 Гц, 1 H) 6,57 - 8,60 (м, 3 H) 5,34 (к, J=6,93 Гц, 1 H) 4,17 - 4,27 (м, 1 H) 3,77 - 3,83 (м, 1 H) 3,70 (тд, J=10,07, 3,66 Гц, 1 H) 1,74 (д, J=6,93 Гц, 3 H) 1,57 - 1,65 (м, 1 H) 1,49 - 1,61 (м, 1 H) 1,38 - 1,46 (м, 1 H) 0,86 (д, J=7,00 Гц, 3 H) 0,82 (д, J=6,16 Гц, 3 H). МС (ИЭР+) m/z 519 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,90 (шс, 1 H) 7,60 (дд, J=7,82, 1,72 Гц, 1 H) 7,46 (дд, J=7,96, 1,30 Гц, 1 H) 7,36 (ддд, J=7,82, 7,50, 1,30 Гц, 1 H) 7,30 (ддд, J=7,96, 7,50, 1,72 Гц, 1 H) 6,46 - 8,26 (м, 3 H) 5,42 (к, J=6,99 Гц, 1 H) 4,15 - 4,25 (м, 1 H) 3,70 - 3,76 (м, 1 H) 3,66 (тд, J=11,41, 4,35 Гц, 1 H) 1,69 (д, J=6,99 Гц, 3 H) 1,56 - 1,65 (м, 1 H) 1,52 (дт, J=13,28, 7,48 Гц, 1 H) 1,43 (дт, J=13,28, 7,02 Гц, 1 H) 0,89 (д, J=6,71 Гц, 3 H) 0,87 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 519 [M+H]+.
Пример 3f
(2R)-2-[(5-{[1-(3-Цианофенил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат
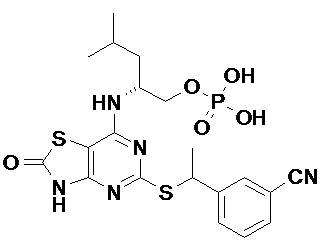
Указанное в заголовке соединение синтезировали из 3-{1-[(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензонитрила (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) с выходом 49%, используя способ, описанный для примера 3. Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 7,93 (дд, J=1,80, 1,36 Гц, 1 H) 7,83 (ддд, J=7,95, 1,80, 1,36 Гц, 1 H) 7,68 (дт, J=7,68, 1,36 Гц, 1 H) 7,51 (дд, J=7,95, 7,68 Гц, 1 H) 7,44 (шс, 4 H) 5,00 (к, J=7,15 Гц, 1 H) 4,05 - 4,13 (м, 1 H) 3,61 - 3,71 (м, 2 H) 1,65 (д, J=7,15 Гц, 3 H) 1,52 - 1,62 (м, 1 H) 1,36 - 1,48 (м, 2 H) 0,85 (д, J=6,58 Гц, 3 H) 0,78 (д, J=6,58 Гц, 3 H). МС (ИЭР+) m/z 510 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,55 (шс, 1 H) 7,94 (дд, J=1,80, 1,36 Гц, 1 H) 7,83 (ддд, J=7,95, 1,80, 1,36 Гц, 1 H) 7,69 (дт, J=7,68, 1,36 Гц, 1 H) 7,56 (дд, J=7,95, 7,68 Гц, 1 H) 7,37 (шс, 3 H) 5,00 (к, J=7,19 Гц, 1 H) 4,15 - 4,24 (м, 1 H) 3,63 - 3,73 (м, 2 H) 1,67 (д, J=7,19 Гц, 3 H) 1,54 - 1,63 (м, 1 H) 1,39 - 1,48 (м, 2 H) 0,89 (д, J=6,56 Гц, 3 H) 0,86 (д, J=6,56 Гц, 3 H). МС (ИЭР+) m/z 510 [M+H]+.
Пример 3g
(2R)-2-[(5-{[(1S)-1-(5-Хлорпиридин-2-ил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диметилфосфат
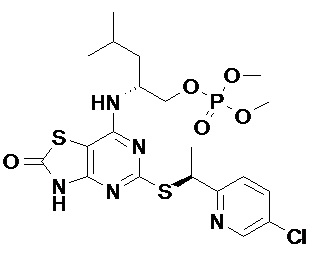
Указанное в заголовке соединение синтезировали из 5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-она (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) с выходом 27%, используя способ, описанный для примера 3, за исключением того, что вместо воды добавляли MeOH через 2 часа при температуре ледяной бани. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,48 (д, J=2,4 Гц, 1 H) 7,79 (д, J=7,9 Гц, 1 H) 7,61 (д, J=8,2 Гц, 1 H) 5,09 (к, J=7,3 Гц, 1 H) 4,63 (шс, 1 H) 3,89 - 3,97 (м, 2 H) 3,70 (д, J=11,3 Гц, 3 H) 3,67 (д, J=11,3 Гц, 3 H) 1,69 (д, 3 H) 1,64 - 1,73 (м, 1 H) 1,58 (ддд, J=14,0, 10,5, 4,9 Гц, 1 H) 1,38 (ддд, J=13,8, 9,4, 4,3 Гц, 1 H) 0,96 (д, J=6,7 Гц, 3 H) 0,94 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 548 [M+H]+.
Пример 3h
(2R)-2-[(5-{[(1S)-1-(5-Хлорпиридин-2-ил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфат
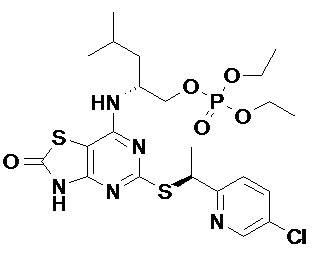
Указанное в заголовке соединение синтезировали из 5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2(3H)-она (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO2008/039138) с выходом 20%, используя способ, описанный для примера 3, за исключением того, что в качестве растворителя использовали 2-метил-ТГФ, и вместо воды добавляли EtOH через 2 часа при температуре ледяной бани. 1H ЯМР (600 МГц, ДМСО-d6) δH м.д. 8,47 (д, J=1,2 Гц, 1 H) 7,78 (д, J=7,0 Гц, 1 H) 7,61 (д, J=7,0 Гц, 1 H) 5,09 (к, J=7,0 Гц, 1 H) 4,63 (шс, 1 H) 3,96 - 4,14 (м, 4 H) 3,89 - 3,95 (м, 2 H) 1,68 (д, J=7,0 Гц, 3 H) 1,63 - 1,67 (м, 1 H) 1,58 (ддд, J=13,8, 10,6, 4,9 Гц, 1 H) 1,35 - 1,40 (м, 1 H) 1,26 (тд, J=7,2, 0,9 Гц, 3 H) 1,20 (тд, J=7,0, 0,9 Гц, 3 H) 0,96 (д, J=6,4 Гц, 3 H) 0,94 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 576 [M+H]+.
Пример 4
(7-{[(1R)-1-(Гидроксиметил)-3-метилбутил]амино}-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидная кислота
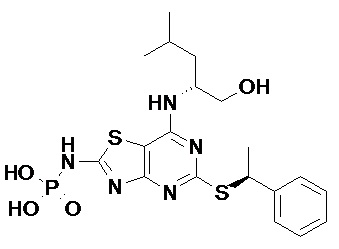
Указанный в заголовке продукт синтезировали из гидрохлорида (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии.
Стадия 1: N 7-[(1R)-1-({[трет-Бутил(диметил)силил]окси}метил)-3-метилбутил]-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2,7-диамин
К раствору гидрохлорида (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола1,2 (605 мг, 1,50 ммоль), трет-бутилдиметилсилилхлорида (520 мг, 3,46 ммоль) и DMAP (92 мг, 0,75 ммоль) в ДХМ (5 мл) добавляли Et3N (630 мкл, 5,50 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 1,5 часа. Добавляли ДХМ (25 мл) и промывали полученную органическую фазу 2 М раствором лимонной кислоты (2x5 мл) и водой (5 мл), сушили над Na2SO4, фильтровали и выпаривали с получением 969 мг неочищенного вещества. Неочищенный продукт очищали флэш-хроматографией (диоксид кремния, 3-4% MeOH в ДХМ), и чистые фракции объединяли и выпаривали с получением 741 мг (95%) продукта с чистотой >99% в виде белого твердого вещества.
1H ЯМР (600 МГц, CD3OD) δH м.д. 7,44 (дд, J=8,2, 0,9 Гц, 2 H) 7,28 - 7,32 (м, 2 H) 7,19 - 7,24 (м, 1 H) 5,07 (к, J=7,2 Гц, 1 H) 4,51 (шс, 1 H) 3,59 (дд, J=10,1, 5,5 Гц, 1 H) 3,50 (дд, J=9,9, 6,0 Гц, 1 H) 1,74 (д, J=7,0 Гц, 3 H) 1,70 - 1,79 (м, 1 H) 1,49 - 1,55 (м, 1 H) 1,43 - 1,49 (м, 1 H) 0,97 (д, J=6,7 Гц, 3 H) 0,95 (д, J=6,4 Гц, 3 H) 0,84 (с, 9 H) 0,03 (с, 3 H) 0,01 (с, 3 H). МС (ИЭР+) m/z 518 [M+H]+.
Стадия 2:
N 7-[(1R)-1-({[трет-Бутил(диметил)силил]окси}метил)-3-метилбутил]-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2,7-диамин (115 мг, 0,22 ммоль) в ДХМ (1,5 мл) добавляли к смеси пентахлорида фосфора (92 мг, 0,44 ммоль) и пиридина (53 мг, 0,67 ммоль) в ДХМ (0,5 мл) при температуре ледяной бани. Реакционную смесь перемешивали при температуре ледяной бани в течение 60 минут. Добавляли воду (1 мл) и ДМСО (1 мл) и перемешивали реакционную смесь при 50 °C в течение 1,5 часа. Реакционную смесь фильтровали через нейлонный дисковый фильтр Agilent 0,45 мкм, и очищали неочищенную смесь препаративной ВЭЖХ (основной способ) с получением 49 мг (43%) чистого указанного в заголовке продукта в виде белого твердого вещества. После очистки продукт считали диаммониевой солью. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,44 - 7,48 (м, 2 H) 7,27 - 7,33 (м, 2 H) 7,21 (тт, J=7,3, 1,2 Гц, 1 H) 5,09 (к, J=7,0 Гц, 1 H) 4,51 (шс, 1 H) 3,57 (дд, J=11,0, 5,2 Гц, 1 H) 3,49 (дд, J=11,1, 5,6 Гц, 1 H) 1,73 (д, J=7,0 Гц, 3 H) 1,70 - 1,78 (м, 1 H) 1,54 - 1,61 (м, 1 H) 1,46 - 1,53 (м, 1 H) 0,97 (д, J=6,7 Гц, 3 H) 0,95 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 484 [M+H]+.
Пример 4b
(5-{[1-(2-Хлорфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидная кислота
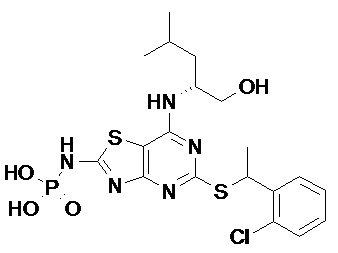
Указанный в заголовке продукт синтезировали из (2R)-2-[(2-амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4. Общий выход за две стадии: 62%.
Стадия 1: N7-[(1R)-1-({[трет-Бутил(диметил)силил]окси}метил)-3-метилбутил]-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2,7-диамин
Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,67 (дд, J=7,8, 1,7 Гц, 1 H) 7,64 (дд, J=7,8, 1,7 Гц, 1 H) 7,39 (дд, J=7,8, 1,2 Гц, 1 H) 7,39 (дд, J=7,8, 1,2 Гц, 1 H) 7,29 (тд, J=7,6, 1,2 Гц, 2 H) 7,22 (тт, J=7,7, 1,5 Гц, 2 H) 5,52 (к, J=7,0 Гц, 1 H) 5,50 (к, J=7,0 Гц, 1 H) 4,51 (шс, 2 H) 3,67 (дд, J=10,1, 5,5 Гц, 1 H) 3,63 (дд, J=9,8, 5,8 Гц, 1 H) 3,49 (дд, J=10,1, 4,3 Гц, 1 H) 3,37 (дд, J=10,1, 4,9 Гц, 1 H) 1,73 (д, J=7,0 Гц, 3 H) 1,68 (д, J=7,0 Гц, 3 H) 1,64 - 1,76 (м, 2 H) 1,56 - 1,62 (м, 1 H) 1,49 - 1,55 (м, 1 H) 1,41 (дддд, J=13,7, 9,3, 4,2, 2,4 Гц, 2 H) 0,97 (д, J=6,7 Гц, 3 H) 0,96 (д, J=6,7 Гц, 3 H) 0,92 (д, J=6,7 Гц, 3 H) 0,84 (с, 9 H) 0,81 (с, 9 H) 0,03 (с, 3 H) 0,00 (с, 3 H) -0,06 (с, 3 H) -0,07 (с, 3 H). МС (ИЭР+) m/z 552 [M+H]+.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,66 (дд, J=7,8, 1,7 Гц, 1 H) 7,42 (дд, J=7,9, 1,2 Гц, 1 H) 7,31 (тд, J=7,6, 1,4 Гц, 1 H) 7,25 (тд, J=7,7, 1,7 Гц, 1 H) 5,57 (к, J=7,0 Гц, 1 H) 4,54 (шс, 1 H) 3,49 (дд, J=11,3, 4,3 Гц, 1 H) 3,40 (дд, J=11,1, 4,7 Гц, 1 H) 1,72 (д, J=7,0 Гц, 3 H) 1,60 - 1,78 (м, 2 H) 1,44 (ддд, J=13,7, 9,2, 4,6 Гц, 1 H) 0,98 (д, J=6,7 Гц, 3 H) 0,96 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 518 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) 7,65 (дд, J=7,8, 1,7 Гц, 1 H) 7,39 (дд, J=7,9, 1,5 Гц, 1 H) 7,29 (тд, J=7,3, 1,2 Гц, 1 H) 7,22 (тд, J=7,7, 1,5 Гц, 1 H) 5,53 (к, J=7,0 Гц, 1 H) 4,46 (шс, 1 H) 3,67 (дд, J=11,0, 5,2 Гц, 1 H) 3,60 (дд, J=11,3, 4,9 Гц, 1 H) 1,74 (д, J=7,0 Гц, 3 H) 1,56 - 1,73 (м, 2 H) 1,37 - 1,42 (м, 1 H) 0,92 (д, J=6,7 Гц, 3 H) 0,82 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 518 [M+H]+.
Пример 4c
(7-{[(1R)-1-(Гидроксиметил)-3-метилбутил]амино}-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидная кислота
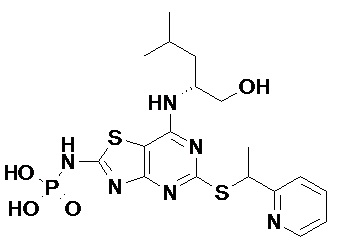
Указанный в заголовке продукт синтезировали из (2R)-2-({2-амино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4. Общий выход за две стадии: 29%.
Стадия 1: N7-[(1R)-1-({[трет-Бутил(диметил)силил]окси}метил)-3-метилбутил]-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-2,7-диамин
Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,45 - 8,50 (м, 2 H) 7,77 (тд, J=7,9, 1,8 Гц, 1 H) 7,76 (тд, J=7,7, 1,8 Гц, 1 H) 7,60 (д, J=7,9 Гц, 2 H) 7,28 (дт, J=4,9, 1,2 Гц, 1 H) 7,27 (дт, J=4,9, 1,2 Гц, 1 H) 5,19 (к, J=7,2 Гц, 1 H) 5,18 (к, J=7,2 Гц, 1 H) 4,42 (шс, 2 H) 3,60 - 3,67 (м, 2 H) 3,54 (дд, J=10,1, 5,2 Гц, 1 H) 3,44 (дд, J=9,9, 5,6 Гц, 1 H) 1,76 (д, J=7,0 Гц, 3 H) 1,74 (д, J=7,0 Гц, 3 H) 1,66 - 1,73 (м, 2 H) 1,47 - 1,55 (м, 2 H) 1,39 - 1,46 (м, 2 H) 0,96 (д, J=6,7 Гц, 3 H) 0,95 (д, J=6,7 Гц, 3 H) 0,94 (д, J=6,7 Гц, 3 H) 0,86 (д, J=6,4 Гц, 3 H) 0,83 (с, 18 H) 0,02 (с, 3 H) 0,01 (с, 3 H) 0,00 (с, 3 H) -0,01 (с, 3 H). МС (ИЭР+) m/z 519 [M+H]+.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,47 (дт, J=5,0, 0,9 Гц, 1 H) 7,78 (тд, J=7,7, 1,7 Гц, 1 H) 7,64 (дт, J=7,9, 1,0 Гц, 1 H) 7,28 (ддд, J=7,3, 4,9, 0,9 Гц, 1 H) 5,24 (к, J=7,3 Гц, 1 H) 4,50 (шс, 1 H) 3,52 (дд, J=11,0, 5,5 Гц, 1 H) 3,42 (дд, J=11,1, 5,6 Гц, 1 H) 1,75 (д, J=7,0 Гц, 3 H) 1,68 - 1,73 (м, 1 H) 1,51 - 1,60 (м, 1 H) 1,43 - 1,51 (м, 1 H) 0,97 (д, J=6,7 Гц, 3 H) 0,95 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 485 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,47 (дт, J=5,0, 0,9 Гц, 1 H) 7,78 (тд, J=7,8, 1,8 Гц, 1 H) 7,66 (д, J=7,9 Гц, 1 H) 7,26 - 7,29 (м, 1 H) 5,17 (к, J=7,2 Гц, 1 H) 4,24 (шс, 1 H) 3,65 (дд, J=11,0, 4,9 Гц, 1 H) 3,52 (дд, J=11,0, 6,1 Гц, 1 H) 1,73 (д, J=7,3 Гц, 3 H) 1,60 - 1,67 (м, 1 H) 1,51 - 1,59 (м, 1 H) 1,43 - 1,51 (м, 1 H) 0,91 (д, J=6,4 Гц, 3 H) 0,77 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 485 [M+H]+.
Пример 4d
(5-{[1-(3-Цианофенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидная кислота
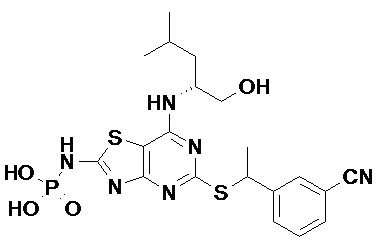
Указанное в заголовке соединение синтезировали из 3-{1-[(2-амино-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензонитрила (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4. Общий выход за две стадии: 47%.
Стадия 1: 3-{1-[(2-Амино-7-{[(1R)-1-({[трет-бутил(диметил)силил]окси}метил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензонитрил
Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,80 - 7,88 (м, 4 H) 7,59 (дт, J=6,1, 1,2 Гц, 1 H) 7,58 (дт, J=6,1, 1,2 Гц, 1 H) 7,49 (к, J=7,5 Гц, 2 H) 5,10 (к, J=7,3 Гц, 2 H) 4,44 (шс, 1 H) 4,35 (шс, 1 H) 3,68 (дд, J=9,8, 5,8 Гц, 1 H) 3,58 (дд, J=9,8, 6,1 Гц, 1 H) 3,54 (дд, J=9,9, 5,3 Гц, 1 H) 3,43 - 3,48 (м, 1 H) 1,71 (д, J=7,3 Гц, 3 H) 1,70 (д, J=7,3 Гц, 3 H) 1,63 - 1,75 (м, 2 H) 1,39 - 1,55 (м, 4 H) 0,97 (д, J=6,7 Гц, 3 H) 0,96 (д, J=6,7 Гц, 3 H) 0,93 (д, J=6,7 Гц, 3 H) 0,85 (с, 9 H) 0,81 (с, 9 H) 0,81 (д, J=6,4 Гц, 3 H) 0,05 (с, 3 H) 0,03 (с, 3 H) 0,00 (с, 3 H) -0,02 (с, 3 H). МС (ИЭР+) m/z 543 [M+H]+.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,87 (с, 1 H) 7,85 (дд, J=7,8, 1,1 Гц, 1 H) 7,57 (дд, J=7,6, 1,5 Гц, 1 H) 7,49 (т, J=7,8 Гц, 1 H) 5,13 (к, J=7,2 Гц, 1 H) 4,29 (шс, 1 H) 3,63 (дд, J=11,0, 5,2 Гц, 1 H) 3,55 (дд, J=10,7, 5,8 Гц, 1 H) 1,70 (д, J=7,3 Гц, 3 H) 1,61 - 1,68 (м, 1 H) 1,49 - 1,57 (м, 1 H) 1,41 - 1,48 (м, 1 H) 0,92 (д, J=6,7 Гц, 3 H) 0,80 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 509 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,86 (с, 1 H) 7,84 (дд, J=7,9, 1,5 Гц, 1 H) 7,58 (д, J=7,9 Гц, 1 H) 7,49 (т, J=7,8 Гц, 1 H) 5,12 (к, J=7,0 Гц, 1 H) 4,44 (шс, 1 H) 3,53 (дд, J=11,0, 5,2 Гц, 1 H) 3,43 (дд, J=11,0, 5,5 Гц, 1 H) 1,71 (д, J=7,3 Гц, 3 H) 1,67 - 1,74 (м, 1 H) 1,51 - 1,60 (м, 1 H) 1,43 - 1,51 (м, 1 H) 0,97 (д, J=6,7 Гц, 3 H) 0,95 (д, 3 H). МС (ИЭР+) m/z 509 [M+H]+.
Пример 4e
(5-{[1-(3-Фторпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидная кислота
Указанное в заголовке соединение синтезировали из (2R)-2-[(2-амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4. Общий выход за две стадии: 55%.
Стадия 1: N7-[(1R)-1-({[трет-Бутил(диметил)силил]окси}метил)-3-метилбутил]-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2,7-диамин
Продукт представлял собой смесь двух диастереомеров. 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,35 (д, J=1,2 Гц, 1 H) 8,34 (д, J=0,9 Гц, 1 H) 7,59 (дт, J=8,5, 1,2 Гц, 1 H) 7,57 (дт, J=8,2, 1,2 Гц, 1 H) 7,34 - 7,39 (м, 2 H) 5,59 (к, J=7,0 Гц, 2 H) 4,54 (шс, 2 H) 3,65 (д, J=5,8 Гц, 2 H) 3,62 (дд, J=10,1, 5,5 Гц, 1 H) 3,57 (дд, J=10,1, 5,8 Гц, 1 H) 1,79 (д, J=7,0 Гц, 3 H) 1,77 (д, J=7,0 Гц, 3 H) 1,70 - 1,76 (м, 2 H) 1,50 - 1,57 (м, 2 H) 1,42 - 1,50 (м, 2 H) 0,98 (д, J=6,7 Гц, 3 H) 0,96 (д, J=6,7 Гц, 3 H) 0,96 (д, J=6,4 Гц, 3 H) 0,93 (д, J=6,4 Гц, 3 H) 0,83 (с, 9 H) 0,82 (с, 9 H) 0,03 (с, 3 H) 0,02 (с, 3 H) 0,00 (с, 3 H) -0,01 (с, 3 H). МС (ИЭР+) m/z 537 [M+H]+.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,33 (дд, J=4,9, 1,5 Гц, 1 H) 7,59 (т, J=9,4 Гц, 1 H) 7,34 - 7,38 (м, 1 H) 5,62 (к, J=7,1 Гц, 1 H) 4,53 (шс, 1 H) 3,59 (дд, J=11,0, 4,9 Гц, 1 H) 3,54 (д, J=11,0, 4,9 Гц, 1 H) 1,77 (д, J=7,3 Гц, 3 H) 1,70 - 1,75 (м, 1 H) 1,55 - 1,64 (м, 1 H) 1,45 - 1,52 (м, 1 H) 0,98 (д, J=6,4 Гц, 3 H) 0,96 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 503 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,34 (дт, J=4,9, 1,2 Гц, 1 H) 7,58 (ддд, J=9,8, 8,4, 1,2 Гц, 1 H) 7,34 - 7,38 (м, 1 H) 5,60 (к, J=7,0 Гц, 1 H) 4,49 (шс, 1 H) 3,63 (дд, J=5,2, 1,5 Гц, 2 H) 1,79 (д, J=7,0 Гц, 3 H) 1,70 - 1,75 (м, 1 H) 1,55 - 1,64 (м, 1 H) 1,44 - 1,52 (м, 1 H) 0,97 (д, J=7,0 Гц, 3 H) 0,91 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 503 [M+H]+.
Пример 4f
Диэтил-(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфат

Указанный в заголовке продукт синтезировали из гидрохлорида (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4, за исключением того, что вместо воды и ДМСО добавляли EtOH через 1 час при температуре ледяной бани на стадии 2.
Исходное вещество для стадии 2 было таким же, как в примере 4. Общий выход за две стадии: 71%.
Стадия 2: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,44 - 7,47 (м, 2 H) 7,29 - 7,34 (м, 2 H) 7,22 (тт, J=7,3, 1,5 Гц, 1 H) 5,05 (к, J=7,0 Гц, 1 H) 4,51 (шс, 1 H) 4,08 - 4,17 (м, 4 H) 3,55 (дд, J=11,0, 5,2 Гц, 1 H) 3,49 (дд, J=11,0, 5,5 Гц, 1 H) 1,73 (д, J=7,0 Гц, 3 H) 1,67 - 1,72 (м, 1 H) 1,53 - 1,59 (м, 1 H) 1,44 - 1,50 (м, 1 H) 1,34 (тдд, J=7,0, 2,1, 0,61 Гц, 6 H) 0,97 (д, J=6,7 Гц, 3 H) 0,95 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 540 [M+H]+.
Пример 4g
Диметил-(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфат
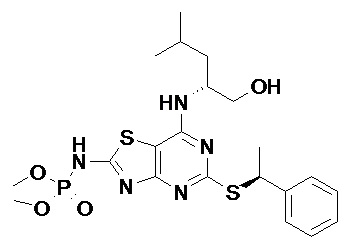
Указанный в заголовке продукт синтезировали из гидрохлорида (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4, за исключением того, что вместо воды и ДМСО добавляли MeOH через 1 час при температуре ледяной бани на стадии 2.
Исходное вещество для стадии 2 было таким же, как в примере 4. Общий выход за две стадии: 75%.
Стадия 2: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,43 - 7,47 (м, 2 H) 7,29 - 7,33 (м, 2 H) 7,22 (тт, J=7,4, 1,5 Гц, 1 H) 5,04 (к, J=7,1 Гц, 1 H) 4,50 (шс, 1 H) 3,76 (д, J=10,7 Гц, 6 H) 3,55 (дд, J=11,0, 5,5 Гц, 1 H) 3,49 (дд, J=11,0, 5,5 Гц, 1 H) 1,73 (д, J=7,0 Гц, 3 H) 1,66 - 1,75 (м, 1 H) 1,52 - 1,58 (м, 1 H) 1,44 - 1,50 (м, 1 H) 0,97 (д, J=6,7 Гц, 3 H) 0,94 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 512 [M+H]+.
Пример 4h
Диэтил-(5-{[1-(2-хлорфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфат
Указанный в заголовке продукт синтезировали из (2R)-2-[(2-амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4, за исключением того, что вместо воды и ДМСО добавляли через 1 час при температуре ледяной бани на стадии 2.
Исходное вещество для стадии 2 было таким же, как в примере 4b. Продукт представлял собой смесь двух диастереомеров. Общий выход за две стадии: 73%.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,64 (дд, J=7,6, 1,5 Гц, 1 H) 7,41 (дд, J=7,9, 1,2 Гц, 1 H) 7,30 (тд, J=7,6, 1,4 Гц, 1 H) 7,23 (тд, J=7,8, 1,7 Гц, 1 H) 5,50 (к, J=7,0 Гц, 1 H) 4,50 (шс, 1 H) 4,08 - 4,16 (м, 4 H) 3,48 (дд, J=11,0, 4,6 Гц, 1 H) 3,39 (дд, J=11,3, 4,9 Гц, 1 H) 1,70 (д, J=7,0 Гц, 3 H) 1,67 - 1,75 (м, 1 H) 1,59 - 1,66 (м, 1 H) 1,41 (ддд, J=13,7, 9,2, 4,6 Гц, 1 H) 1,34 (тд, J=7,1, 1,7 Гц, 6 H) 0,97 (д, J=6,7 Гц, 3 H) 0,95 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 574 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,63 (дд, J=7,8, 1,7 Гц, 1 H) 7,39 (дд, J=7,9, 1,2 Гц, 1 H) 7,30 (тд, J=7,6, 1,2 Гц, 1 H) 7,23 (тд, J=7,8, 1,4 Гц, 1 H) 5,50 (к, J=7,0 Гц, 1 H) 4,45 (шс, 1 H) 4,08 - 4,16 (м, 4 H) 3,64 (дд, J=11,3, 5,2 Гц, 1 H) 3,58 (дд, J=11,0, 5,2 Гц, 1 H) 1,74 (д, J=7,0 Гц, 3 H) 1,63 - 1,69 (м, 1 H) 1,56 - 1,63 (м, 1 H) 1,38 - 1,44 (м, 1 H) 1,34 (т, J=7,2 Гц, 6 H) 0,93 (д, J=6,4 Гц, 3 H) 0,83 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 574 [M+H]+.
Пример 4i
Диэтил-(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфат
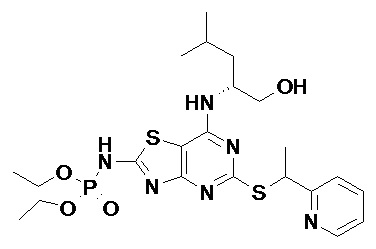
Указанный в заголовке продукт синтезировали из (2R)-2-({2-амино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4, за исключением того, что вместо воды и ДМСО добавляли EtOH через 1 час при температуре ледяной бани на стадии 2.
Исходное вещество для стадии 2 было таким же, как в примере 4c. Продукт представлял собой смесь двух диастереомеров. Общий выход за две стадии: 31%.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,47 (дт, J=4,9, 0,8 Гц, 1 H) 7,79 (тд, J=7,7, 1,4 Гц, 1 H) 7,62 (д, J=7,3 Гц, 1 H) 7,28 (дд, J=7,6, 4,9 Гц, 1 H) 5,19 (к, J=7,3 Гц, 1 H) 4,48 (шс, 1 H) 4,06 - 4,16 (м, 4 H) 3,51 (дд, J=11,1, 5,3 Гц, 1 H) 3,43 (дд, J=11,0, 5,5 Гц, 1 H) 1,74 (д, J=7,3 Гц, 3 H) 1,65 - 1,72 (м, 1 H) 1,51 - 1,57 (м, 1 H) 1,42 - 1,48 (м, 1 H) 1,33 (т, J=7,0 Гц, 6 H) 0,96 (д, J=6,4 Гц, 3 H) 0,94 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 541 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,47 (дд, J=5,1, 0,9 Гц, 1 H) 7,78 (тд, J=7,9, 1,8 Гц, 1 H) 7,65 (д, J=7,9 Гц, 1 H) 7,27 - 7,29 (м, 1 H) 5,14 (к, J=7,3 Гц, 1 H) 4,25 (шс, 1 H) 4,07 - 4,14 (м, 4 H) 3,61 (дд, J=11,0, 5,2 Гц, 1 H) 3,51 (дд, J=11,0, 5,8 Гц, 1 H) 1,72 (д, J=7,3 Гц, 3 H) 1,59 - 1,66 (м, 1 H) 1,49 - 1,54 (м, 1 H) 1,41 - 1,46 (м, 1 H) 1,33 (т, J=7,0 Гц, 6 H) 0,92 (д, J=6,4 Гц, 3 H) 0,79 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 541 [M+H]+.
Пример 4j
Диэтил-(5-{[1-(3-цианофенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфат
Указанный в заголовке продукт синтезировали из 3-{1-[(2-амино-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-5-ил)сульфанил]этил}бензонитрила (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4, за исключением того, что вместо воды и ДМСО добавляли EtOH через 1 час при температуре ледяной бани на стадии 2.
Исходное вещество для стадии 2 было таким же, как в примере 4d. Продукт представлял собой смесь двух диастереомеров. Общий выход за две стадии: 60%.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,86 (т, J=1,7 Гц, 1 H) 7,84 (дт, J=7,9, 1,4 Гц, 1 H) 7,58 (дт, J=7,6, 1,4 Гц, 1 H) 7,49 (т, J=7,8 Гц, 1 H) 5,08 (к, J=7,2 Гц, 1 H) 4,30 (шс, 1 H) 4,07 - 4,16 (м, 4 H) 3,59 (дд, J=11,0, 5,5 Гц, 1 H) 3,55 (дд, J=11,0, 5,8 Гц, 1 H) 1,70 (д, J=7,3 Гц, 3 H) 1,59 - 1,67 (м, 1 H) 1,49 - 1,55 (м, 1 H) 1,40 - 1,46 (м, 1 H) 1,33 (тд, J=7,1, 0,8 Гц, 6 H) 0,92 (д, J=6,7 Гц, 3 H) 0,80 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 565 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 7,86 (т, J=1,7 Гц, 1 H) 7,83 (дт, J=7,9, 1,4 Гц, 1 H) 7,59 (дт, J=7,6, 1,4 Гц, 1 H) 7,50 (т, J=7,8 Гц, 1 H) 5,09 (к, J=7,2 Гц, 1 H) 4,45 (шс, 1 H) 4,07 - 4,16 (м, 4 H) 3,52 (дд, J=11,0, 5,2 Гц, 1 H) 3,44 (дд, J=11,0, 5,5 Гц, 1 H) 1,71 (д, J=7,3 Гц, 3 H) 1,65 - 1,70 (м, 1 H) 1,51 - 1,57 (м, 1 H) 1,42 - 1,49 (м, 1 H) 1,33 (т, J=7,0 Гц, 6 H) 0,96 (д, J=6,7 Гц, 3 H) 0,94 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 565 [M+H]+.
Пример 4k
Диэтил-(5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфат
Указанный в заголовке продукт синтезировали из (2R)-2-[(2-амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ола (Karlström S., et al., J. Med. Chem., 2013, 56, 3177-3190; WO 2006/107258) в две стадии, используя способ, описанный для примера 4, за исключением того, что вместо воды и ДМСО добавляли EtOH через 1 час при температуре ледяной бани на стадии 2.
Исходное вещество для стадии 2 было таким же, как в примере 4e. Продукт представлял собой смесь двух диастереомеров. Общий выход за две стадии: 56%.
Стадия 2: Два диастереомера разделяли препаративной ВЭЖХ (основной способ).
Диастереомер A: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,34 (дт, J=4,9, 1,2 Гц, 1 H) 7,60 (ддд, J=9,8, 8,5, 1,2 Гц, 1 H) 7,37 (дт, J=8,5, 4,3 Гц, 1 H) 5,56 (к, J=7,1 Гц, 1 H) 4,52 (шс, 1 H) 4,07 - 4,17 (м, 4 H) 3,57 (дд, J=11,0, 5,2 Гц, 1 H) 3,53 (дд, J=11,0, 5,5 Гц, 1 H) 1,76 (д, J=7,0 Гц, 3 H) 1,67 - 1,74 (м, 1 H) 1,55 - 1,61 (м, 1 H) 1,46 (ддд, J=13,7, 9,2, 4,6 Гц, 1 H) 1,34 (тд, J=7,2, 1,8 Гц, 6 H) 0,97 (д, J=6,7 Гц, 3 H) 0,95 (д, J=6,7 Гц, 3 H). МС (ИЭР+) m/z 559 [M+H]+.
Диастереомер B: 1H ЯМР (600 МГц, CD3OD) δH м.д. 8,35 (дт, J=4,9, 1,2 Гц, 1 H) 7,59 (ддд, J=9,8, 8,4, 1,4 Гц, 1 H) 7,37 (ддд, J=8,4, 4,4, 4,3 Гц, 1 H) 5,55 (к, J=7,0 Гц, 1 H) 4,48 (шс, 1 H) 4,08 - 4,16 (м, 4 H) 3,61 (д, J=5,5 Гц, 2 H) 1,78 (д, J=7,0 Гц, 3 H) 1,67 - 1,74 (м, 1 H) 1,54 - 1,61 (м, 1 H) 1,43 - 1,50 (м, 1 H) 1,34 (т, J=7,0 Гц, 6 H) 0,97 (д, J=6,4 Гц, 3 H) 0,92 (д, J=6,4 Гц, 3 H). МС (ИЭР+) m/z 559 [M+H]+.
Пример 5. Сравнительная кинетическая растворимость примера 1 и соединения A
Образцы соединения из примера 1 и (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентан-1-ол.HCl (соединения A) разбавляли до номинальной концентрации 250 мкМ в 50 мМ фосфатном буфере с рН 7,4, затем перемешивали в течение 1 часа и фильтровали.
Получали стандартные растворы двух указанных соединений в концентрациях 25 и 250 мкМ в 50:50 смеси ацетонитрил:вода.
Затем анализировали растворы обращенно-фазовой ВЭЖХ с УФ обнаружением, и определяли растворимость по отношению пиков образца к стандартной кривой. Результаты представлены в следующей таблице.
Пример 6. Сравнительная стабильность растворов примера 1 и соединения A
Получали водный раствор соединения из примера 1 (диаммониевой соли) в воде MilliQ в концентрации 1,7 мг/мл и определяли стабильность соединения при длительном хранении в водном растворе посредством анализа раствора с помощью ВЭЖХ-МС в течение продолжительного периода времени.
Результаты данного исследования представлены в таблице 1.
Таблица 1. Стабильность примера 1 в водном растворе (1,7 мг/мл) при комнатной температуре (комн. т-ре).
% площади
Было невозможно растворить соединение A в чистой воде, поэтому получали несколько растворов с различными сорастворителями и определяли стабильность соединения при длительном хранении в водном растворе посредством анализа раствора с помощью ВЭЖХ-МС в течение продолжительного периода времени. Результаты экспериментов представлены в таблицах 2-4.
Таблица 2. Стабильность соединения A в воде + 20% MeOH (1,75 мг/мл) при комнатной температуре
% площади
В таблице 3 показана стабильность соединения A в водном растворе, содержащем различные количества данного соединения и добавленного полиэтиленгликоля.
Таблица 3. Стабильность соединения A в воде, содержащей различные количества полиэтиленгликоля, при комнатной температуре
(1,22 мг/мл)
(2,25 мг/мл)
(1,18 мг/мл)
В таблице 3 показана стабильность соединения A в водном растворе, содержащем различные количества данного соединения и добавленного полиэтиленгликоля и этанола.
Таблица 4. Стабильность соединения A в воде, содержащей полиэтиленгликоль и этанол, при комнатной температуре
(3,2 мг/мл)
(4,0 мг/мл)
Водные композиции соединения A требуют дополнительных сорастворителей, таких как полиэтиленгликоль и/или этанол, для солюбилизации соединения. Доказано, что такие композиции нестабильны при хранении при комнатной температуре, и наблюдали относительно быстрое разложение соединения. Напротив, пример 1 демонстрировал не только улучшенную растворимость в воде (при отсутствии необходимости в сорастворителях), но и неожиданно выраженную стабильность по сравнению с соединением A в водных растворах.
Продукты разложения, наблюдаемые для соединения A, по большей части представляли собой дебензилированный тиол и соответствующий дисульфид вместе с фенилэтанолом и небольшим количеством стирола.
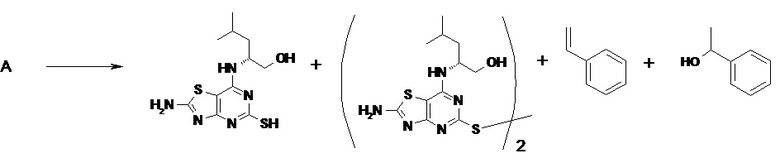
Неожиданно, указанные продукты разложения не наблюдали при хранении примера 1 в водном растворе.
Пример 6. Дополнительные исследования стабильности
Получали водные растворы нескольких иллюстративных соединений в концентрациях 1,2 мг/мл (10 мг/мл для примера 1 (не соль)) в соответствии со следующими способами.
i) Примеры 1b, 2h и 3 (диаммониевые соли) растворяли в чистой воде.
ii) Примеры 1d (диаммониевая соль) и 1n (моноаммониевая соль) суспендировали в воде и добавляли Na2HPO3 до полного перехода соединения в раствор.
iii) Примеры 1q, 4f и 4g (не соли) растворяли в воде с добавлением ДМСО (100 мкл) и добавляли (2-гидроксипропил)-β-циклодекстрин до полного перехода соединения в раствор.
Затем определяли стабильность соединений при длительном хранении в водном растворе при комнатной температуре и/или при 40 °С посредством анализа раствора с помощью ВЭЖХ-МС через 60 дней.
Таблица 5. Стабильность водных растворов после хранения при комнатной температуре в течение 60 дней
Таблица 6. Стабильность водных растворов после хранения при 40 °С в течение 60 дней.
Полученные данные демонстрируют, что соединения по данному изобретению, в целом, стабильны при хранении в водном растворе, в том числе в условиях ускоренного старения при 40 °С.
Пример 7. Сравнение концентрации в плазме примера 1 и соединения A у мышей после внутривенного и перорального введения.
Соединение А
Получали раствор для перорального введения дозы соединения A (12 мг/мл) в 30% HP-β-CD в 10 мМ Na2PO4 и раствор для внутривенного введения дозы соединения A (2,5 мг/мл) в 30% HP-β-CD в 10 мМ Na2PO4 в DPBS. Раствор для внутривенного введения дозы вводили самцам мышей CD1 (массой 28-30 г) посредством внутривенной инъекции (25 мг/кг), а раствор для перорального введения дозы вводили самцам мышей CD1 (массой 28-30 г) через желудочный зонд (120 мг/кг).
Кровь животных собирали в моменты времени 0,083, 0,25, 0,5, 1, 2, 4, 6, 12 и 24 часа и анализировали концентрацию в плазме крови, и использовали полученные данные для расчета значений площади под кривой (AUC), представленных в таблице 5.
Гидрохлоридная соль соединения A
Получали раствор для перорального введения дозы HCl соли соединения A (12 мг/мл) в 30% HP-β-CD в 10 мМ Na2PO4 и раствор для внутривенного введения дозы HCl соли соединения A (2,5 мг/мл) в 30% HP-β-CD в 10 мМ Na2PO4 в DPBS. Раствор для внутривенного введения дозы вводили самцам мышей CD1 (массой 28-30 г) посредством внутривенной инъекции (25 мг/кг), а раствор для перорального введения дозы вводили самцам мышей CD1 (массой 28-30 г) через желудочный зонд (125 мг/кг).
Кровь животных собирали в моменты времени 0,083, 0,25, 0,5, 1, 2, 4, 6, 12 и 24 часа и анализировали концентрацию в плазме крови, и использовали полученные данные для расчета значений площади под кривой (AUC), представленных в таблице 7.
Динатриевая соль примера 1
Получали раствор для перорального введения дозы динатриевой соли примера 1 в воде (15,4 мг/мл) при рН 7,18 и раствор для внутривенного введения дозы динатриевой соли примера 1 в воде (6,4 мг/мл) при рН 7,11, растворяя диаммониевую соль примера 1 в воде и регулируя рН с помощью 0,1 М раствора NaOH. Раствор для внутривенного введения дозы вводили самцам мышей CD1 (массой 24-25 г) посредством инъекции в хвост (32 мг/кг), а раствор для перорального введения дозы вводили самцам мышей CD1 (массой 24-25 г) через желудочный зонд (154 мг/кг).
Кровь животных собирали в моменты времени 0,083, 0,25, 0,5, 1, 2, 4, 6, 12 и 24 часа и анализировали концентрацию в плазме крови, и использовали полученные данные для расчета значений площади под кривой (AUC), представленных в таблице 7.
Таблица 7. Сравнение площади под кривой концентрации в плазме крови для соединения A и примера 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ 5,7-ДИЗАМЕЩЕННОГО [1,3] ТИАЗОЛО[4,5-D]ПИРИМИДИН-2(3H)-ОНА | 2006 |
|
RU2411245C9 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ КАРБОНУКЛЕОЗИДА, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ПРОТИВОРАКОВЫХ АГЕНТОВ | 2017 |
|
RU2712944C1 |
| ИНГИБИТОРЫ МУТАЦИИ HER2 | 2022 |
|
RU2834124C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ 5-ЗАМЕЩЕННОГО 7-АМИНО-[1,3]ТИАЗОЛО[4,5-d] ПИРИМИДИНА | 2006 |
|
RU2419623C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2012 |
|
RU2648997C2 |
| ИНГИБИТОРЫ RAD51 | 2018 |
|
RU2795882C2 |
| ЛЕЧЕНИЕ ИНФЕКЦИЙ H. PYLORI С ПРИМЕНЕНИЕМ ИНГИБИТОРОВ MTAN | 2015 |
|
RU2663803C2 |
| НОВОЕ ПРОИЗВОДНОЕ ЦИКЛИЧЕСКОГО ДИНУКЛЕОТИДА И ЕГО КОНЪЮГАТ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2019 |
|
RU2809547C2 |
| СПОСОБ СТЕРЕОСЕЛЕКТИВНОГО ПОЛУЧЕНИЯ ХИРАЛЬНЫХ 2-[(ГЕТЕРО)АРИЛАЛКИЛСУЛЬФАНИЛ]ПИРИМИДИНОВ И ПРОДУКТОВ, ПОЛУЧЕННЫХ ИЗ НИХ | 2019 |
|
RU2813355C2 |
| ЗАМЕЩЕННЫЕ ХРОМАНЫ | 2015 |
|
RU2718060C2 |
Группа изобретений относится к области органической химии и фармацевтики и направлена на лечение заболеваний и расстройств, связанных с повышенными уровнями CX3CR1 и/или CX3CL1. Раскрывается соединение формулы I, где значения радикалов R1, R2, Q1 являются такими, как определено в п.1 формулы изобретения. Кроме того, раскрывается фармацевтическая композиция на основе соединения формулы (I), обладающая активностью антагонистов рецептора фракталкина, способ лечения или предупреждения заболевания или расстройства, связанного с повышенными уровнями CXCR1 и/или CX3CL1 и применение указанных выше соединений для производства лекарственного средства. Также раскрыт способ получения соединений, представленных общей формулой (I). Группа изобретений обеспечивает эффективное антагонистическое действие рецептора фракталкина при высокой стабильности и биодоступности. 5 н. и 31 з.п. ф-лы, 8 табл., 7 пр.

1. Соединение формулы I
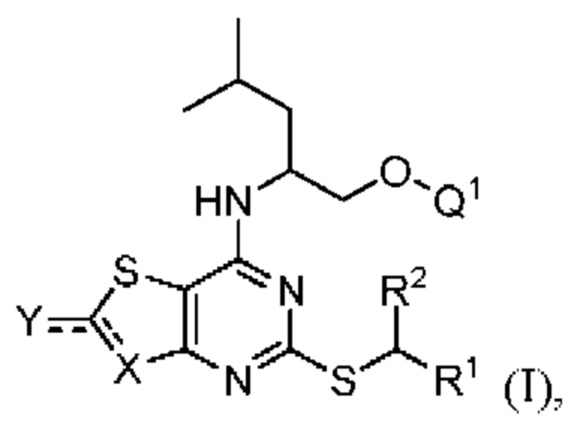
где
R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним(ой) фтором, хлором, бромом, -CN, -C(O)NR3R4 или -S(O)2Me группой;
R2 представляет собой Н или C1-6 алкил;
R3 и R4, каждый, представляют собой Н;
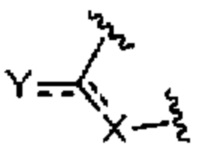 представляет собой
представляет собой 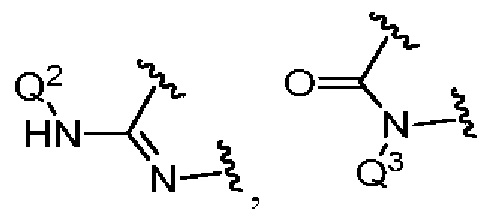 или
или 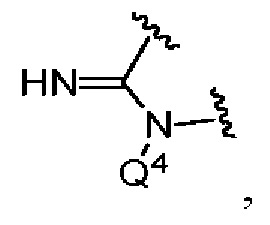
где  означает точку присоединения к остальной части молекулы;
означает точку присоединения к остальной части молекулы;
Q1 и Q2, каждый независимо, представляют собой Н или -PO(OR6)(OR7);
Q3 представляет собой Н или -CH2OPO(OR6)(OR7); и
Q4 представляет собой -CH2OPO(OR6)(OR7);
где R6 и R7, каждый независимо, представляют собой Н или С1-4 алкил;
причем по меньшей мере один из Q1 и Q2, Q3 или Q4 представляет собой -PO(OR6)(OR7) или -CH2OPO(OR6)(OR7);
или его фармацевтически приемлемая соль.
2. Соединение по п. 1, отличающееся тем, что R1 представляет собой фенил или пиридил, оба из которых необязательно замещены одним атомом фтора, хлора или брома.
3. Соединение по п. 2, отличающееся тем, что R1 представляет собой фенил или 5-хлорпиридил-2-ил.
4. Соединение по любому из пп. 1-3, отличающееся тем, что R2 представляет собой C1-6 алкил.
5. Соединение по любому из пп. 1-4, отличающееся тем, что R2 представляет собой С1-3 алкил.
6. Соединение по п. 5, отличающееся тем, что R2 представляет собой метил.
7. Соединение по любому из пп. 1-6, отличающееся тем, что один из Q1 и Q2, Q3 или Q4 представляет собой -PO(OR6)(OR7) или -CH2OPO(OR6)(OR7), а другие из Q1 и (при наличии) Q2 или Q3 представляют собой Н.
8. Соединение по любому из пп. 1-7, отличающееся тем, что 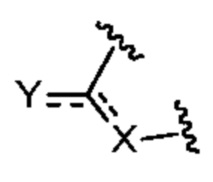 представляет собой
представляет собой
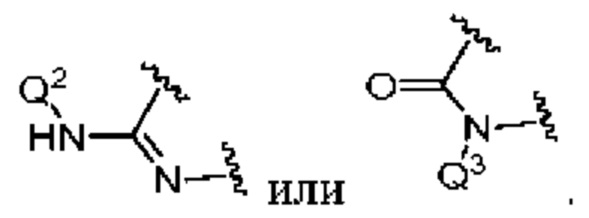
9. Соединение по п. 8, отличающееся тем, что 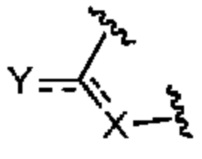 представляет собой
представляет собой
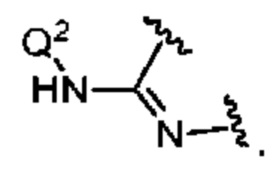
10. Соединение по п. 8, отличающееся тем, что 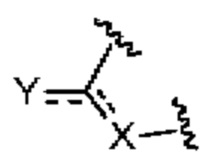 представляет собой
представляет собой
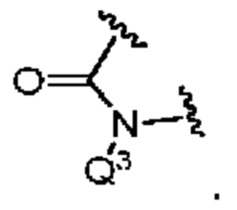
11. Соединение по любому из пп. 8-10, отличающееся тем, что Q1 представляет собой -PO(OR6)(OR7).
12. Соединение по п. 8 или 9, отличающееся тем, что Q2 представляет собой -PO(OR6)(OR7).
13. Соединение по п. 8 или 10, отличающееся тем, что Q3 представляет собой -CH2OPO(OR6)(OR7).
14. Соединение по любому из пп. 1-7, отличающееся тем, что 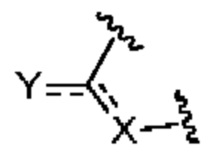 представляет собой
представляет собой
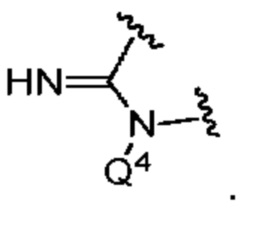
15. Соединение по любому из пп. 1-14, отличающееся тем, что указанное соединение представляет собой соединение формулы IA
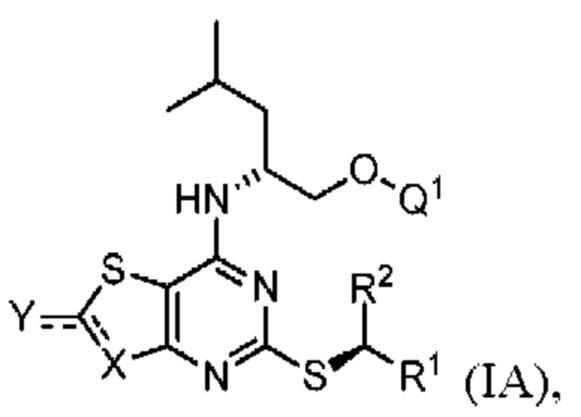
где R1, R2, Q1, Q2 и  являются такими, как определено в любом из предшествующих пунктов, или его фармацевтически приемлемую соль.
являются такими, как определено в любом из предшествующих пунктов, или его фармацевтически приемлемую соль.
16. Соединение по любому из пп. 1-15, отличающееся тем, что каждый R6 и R7 независимо представляет собой С1-3 алкил или Н.
17. Соединение по п. 16, отличающееся тем, что каждый R6 и R7 представляет собой Н.
18. Соединение по п. 16, отличающееся тем, что каждый R6 и R7 представляет собой метил, или каждый из них представляет собой этил.
19. Соединение по п. 16, отличающееся тем, что R6 представляет собой изопропил, и R7 представляет собой Н.
20. Соединение по п. 1 или 15, выбранное из группы, состоящей из:
(2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[1-(2-фторфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[1-(3-цианофенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[1-(3-карбамоилфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-{[2-амино-5-({1-[4-(метилсульфонил)фенил]этил}сульфанил)-[1,3]тиазоло[4,5-d]пиримидин-7-ил]амино}-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[4-(метилсульфонил)бензил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил]амино}-4-метилпентил-дигидрофосфата;
(2R)-2-({2-амино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)-4-метилпентил-дигидрофосфата;
(2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диметилфосфата;
(2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфата;
(2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-бис(1-метилэтил)фосфата;
(2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-1-метилэтил-гидрофосфата;
(2R)-2-[(2-амино-5-{[1-(2-фторфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфата;
(2R)-2-[(2-амино-5-{[1-(2-хлорфенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфата;
(2R)-2-[(2-амино-5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфата;
(2R)-2-[(2-амино-5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфата;
(2R)-2-[(2-амино-5-{[1-(3-цианофенил)этил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфата;
[7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата;
[5-{[1-(2-фторфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил дигидрофосфата;
[5-{[1-(2-хлорфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата;
[5-{[1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата;
[7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата;
[5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата;
[5-{[1-(3-цианофенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-имино[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата;
[5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-2-оксо[1,3]тиазоло[4,5-d]пиримидин-3(2H)-ил]метил-дигидрофосфата;
(2R)-2-[(5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-4-метил-2-({2-оксо-5-[(1-пиридин-2-илэтил)сульфанил]-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил}амино)пентил-дигидрофосфата;
(2R)-4-метил-2-{[5-({1-[4-(метилсульфонил)фенил]этил}сульфанил)-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил]амино}пентил-дигидрофосфата;
(2R)-2-[(5-{[1-(3-карбамоилфенил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(5-{[1-(2-хлорфенил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(5-{[1-(3-цианофенил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфата;
(2R)-2-[(5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диметилфосфата;
(2R)-2-[(5-{[(1S)-1-(5-хлорпиридин-2-ил)этил]сульфанил}-2-оксо-2,3-дигидро[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-диэтилфосфата;
(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидной кислоты;
(5-{[1-(2-хлорфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидной кислоты;
(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидной кислоты;
(5-{[1-(3-цианофенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидной кислоты;
(5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)фосфорамидной кислоты;
диэтил-(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфата;
диметил-(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфата;
диэтил-(5-{[1-(2-хлорфенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфата;
диэтил-(7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}-5-[(1-пиридин-2-илэтил)сульфанил][1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфата;
диэтил-(5-{[1-(3-цианофенил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфата; и
диэтил-(5-{[1-(3-фторпиридин-2-ил)этил]сульфанил}-7-{[(1R)-1-(гидроксиметил)-3-метилбутил]амино}[1,3]тиазоло[4,5-d]пиримидин-2-ил)амидофосфата,
или его фармацевтически приемлемая соль.
21. Соединение по п. 1 или 15, представляющее собой (2R)-2-[(2-амино-5-{[(1S)-1-фенилэтил]сульфанил}[1,3]тиазоло[4,5-d]пиримидин-7-ил)амино]-4-метилпентил-дигидрофосфат или его фармацевтически приемлемую соль.
22. Соединение по любому из пп. 1-21, отличающееся тем, что фармацевтически приемлемая соль представляет собой соль присоединения основания.
23. Соединение по п. 22, отличающееся тем, что фармацевтически приемлемая соль представляет собой соль аммония или соль щелочного металла.
24. Фармацевтическая композиция, обладающая активностью антагонистов рецептора фракталкина, которая содержит эффективное количество соединения по любому из пп. 1-23, включая его фармацевтически приемлемые соли, в смеси с одним или более фармацевтически приемлемыми вспомогательными веществами.
25. Фармацевтическая композиция по п. 24, отличающаяся тем, что указанная фармацевтическая композиция дополнительно содержит воду и менее 20% (мас./мас.) солюбилизирующих вспомогательных веществ.
26. Фармацевтическая композиция по п. 24, отличающаяся тем, что указанная фармацевтическая композиция представлена в форме водного раствора.
27. Фармацевтическая композиция по п. 24, отличающаяся тем, что указанная композиция представлена в форме порошка.
28. Соединение по любому из пп. 1-23, включая его фармацевтически приемлемые соли, или фармацевтическая композиция по любому из пп. 24-27 для применения в медицине.
29. Соединение по любому из пп. 1-23, включая его фармацевтически приемлемые соли, или фармацевтическая композиция по любому из пп. 24-27 для применения для лечения и/или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1.
30. Способ лечения и/или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения по любому из пп. 1-23, включая его фармацевтически приемлемые соли, или фармацевтической композиции по любому из пп. 24-27.
31. Применение соединения по любому из пп. 1-23, включая его фармацевтически приемлемые соли, или фармацевтической композиции по любому из пп. 24-27 для производства лекарственного средства для лечения и/или предупреждения заболевания или расстройства, связанного с повышенными уровнями CX3CR1 и/или CX3CL1.
32. Соединение для применения, способ или применение по любому из пп. 29-31, отличающиеся тем, что указанное заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из острого и/или хронического воспаления, болезней глаз, болезней легких, болезней кожи, болезней суставов и/или костей, аутоиммунных заболеваний, сердечно-сосудистых заболеваний, метаболических заболеваний, болезней головного мозга, нейродегенеративных заболеваний, боли, рака, болезней печени, болезней почек, желудочно-кишечных заболеваний, вируса иммунодефицита человека и нарушений настроения.
33. Соединение для применения, способ или применение по любому из пп. 29-32, отличающиеся тем, что указанное заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из дегенерации желтого пятна, легочной артериальной гипертензии, астмы, фиброза легких, атопического дерматита, прурита, остеоартрита, остеопороза, апластической анемии, анкилозирующего спондилита, рассеянного склероза, системного склероза, ревматоидного артрита, атеросклероза, нестабильной стенокардии, инфаркта миокарда, болезней сонной артерии, хронической сердечной недостаточности, воспалительной кардиомиопатии, болезни периферических артерий, диабета, болезни Альцгеймера, травматического повреждения головного мозга, хронической боли, фибромиалгии, невропатической боли, боли, вызванной химиотерапией, боли при грыже межпозвоночных дисков, рака, цирроза печени, IgA-нефропатии, воспаления почек, волчанки, ишемического реперфузионного повреждения, ишемической острой почечной недостаточности, контраст-индуцированного повреждения почек, колита, болезни Крона, воспалительной болезни кишечника, панкреатита, вируса-1 иммунодефицита человека, деменции на фоне вируса иммунодефицита человека, инсульта, болезни Паркинсона, депрессии, тревоги, шизофрении и расстройств аутического спектра.
34. Соединение для применения, способ или применение по любому из пп. 29-33, отличающиеся тем, что указанное заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из инфаркта миокарда, артериосклероза, рассеянного склероза, ревматоидного артрита, болезни Крона, панкреатита, невропатической боли, боли, вызванной химиотерапией, и рака.
35. Соединение для применения, способ или применение по любому из пп. 29-33, отличающиеся тем, что указанное заболевание или расстройство, связанное с повышенными уровнями CX3CR1 и/или CX3CL1, выбрано из атопического дерматита, рассеянного склероза, ревматоидного артрита, атеросклероза, инфаркта миокарда, хронической сердечной недостаточности, воспалительной кардиомиопатии, фибромиалгии, невропатической боли, боли, обусловленной химиотерапией, В-клеточной лимфомы, рака молочной железы, IgA-нефропатии, волчанки, ишемической острой почечной недостаточности и панкреатита.
36. Способ получения соединения по любому из пп. 1-23, включающий:
(a) для соединений, в которых Q1 представляет собой -PO(OR6)(OR7), где R6 и R7 являются такими, как определено в любом из предшествующих пунктов,
(i) приведение во взаимодействие соединения формулы II
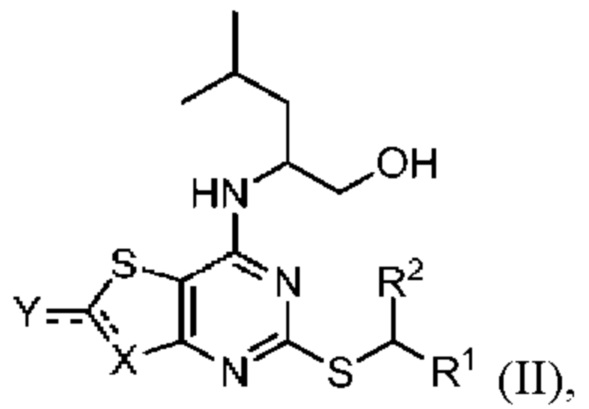
где R1 и R2 являются такими, как определено в любом из предшествующих пунктов; и
 представляет собой
представляет собой 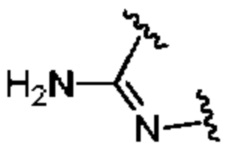 или
или 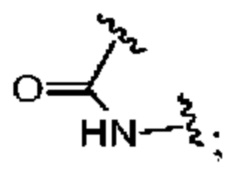
с оксихлоридом фосфора в присутствии пригодного растворителя и пригодного основания; затем
(ii) добавление в реакционную смесь воды или R6OH/R7OH;
(b) для соединений, в которых Q2 представляет собой -PO(OR6)(OR7),
приведение во взаимодействие соединения формулы III
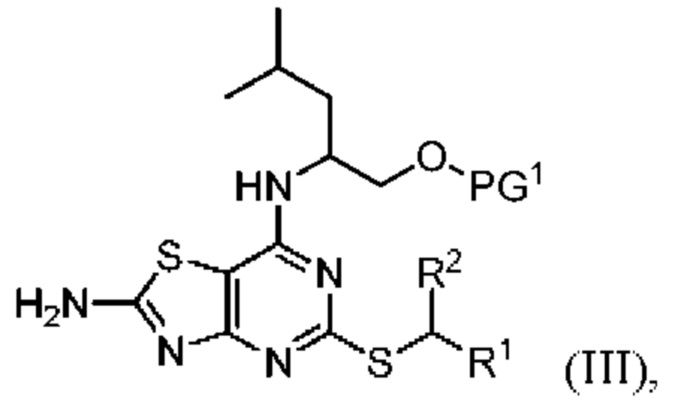
где:
R1 и R2 являются такими, как определено в любом из предшествующих пунктов; и
PG1 представляет собой пригодную защитную группу для атома кислорода;
в присутствии пентахлорида фосфора, пригодного растворителя и, необязательно, пригодного основания;
(c) для соединений, в которых Q3 или Q4 представляет собой -CH2OPO(OR6)(OR7) и по меньшей мере один из R6 и R7 представляет собой С1-4 алкил,
приведение во взаимодействие соединения формулы II
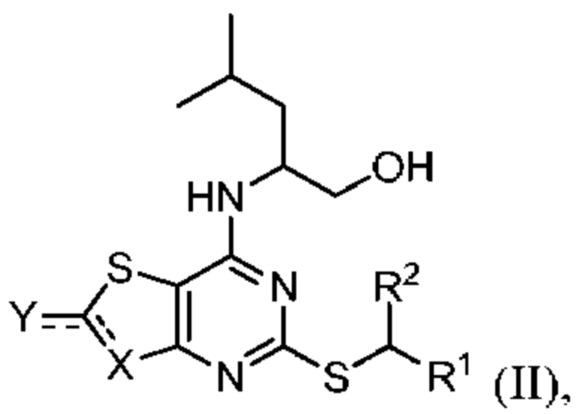
где R1 и R2 являются такими, как описано в настоящем документе; и
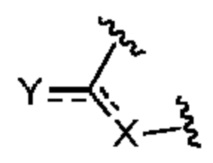 представляет собой
представляет собой 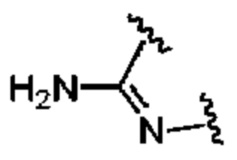 или
или 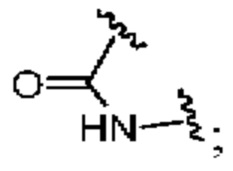
с соединением формулы IV
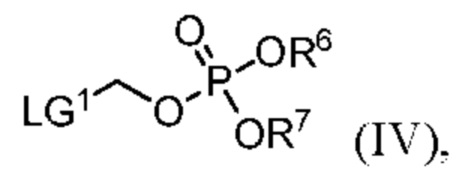
где R6 и R7 являются такими, как определено в любом из предшествующих пунктов, при условии, что по меньшей мере один из R6 и R7 представляет собой С1-4 алкил, и LG1 представляет собой пригодную уходящую группу;
в присутствии пригодного основания и пригодного растворителя;
(d) для соединений, в которых Q3 или Q4 представляет собой -CH2OPO(ОН)2,
(i) приведение во взаимодействие соединения формулы II
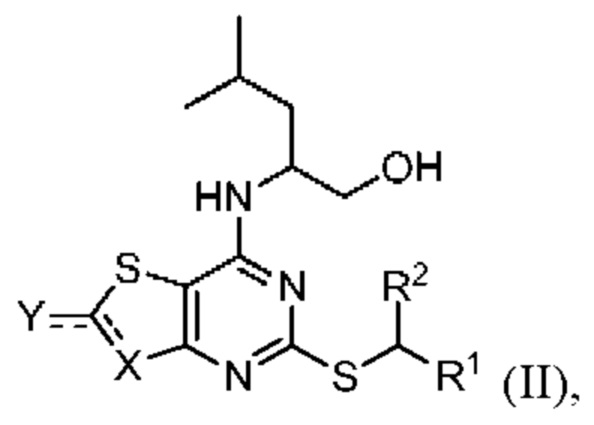
где R1 и R2 являются такими, как описано в настоящем документе; и
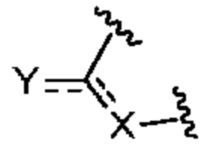 представляет собой
представляет собой  или
или 
с соединением формулы V
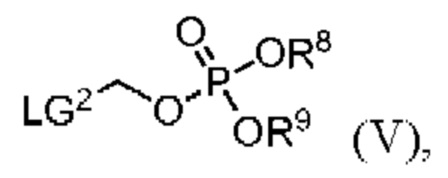
где R8 и R9 представляют собой C1-6 алкил, и LG2 представляет собой пригодную уходящую группу;
в присутствии пригодного основания и пригодного растворителя; и
(ii) приведение во взаимодействие полученного продукта в присутствии пригодной кислоты и пригодного растворителя.
| WO 2008039139 1, 03.04.2008 | |||
| WO 2006107257 A1, 12.10.2006 | |||
| WO 2006107258 A1, 12.10.2006 | |||
| WO 2009120140 A1, 01.10.2009 | |||
| Способ нанесения на предмет разметочных линий и шаблонов с целью последующей его обработки | 1926 |
|
SU4759A1 |
Авторы
Даты
2023-08-14—Публикация
2019-07-05—Подача