Изобретение относится к новым биологически активным веществам из класса арилгетероалканкарбоновых кислот и может быть использовано в фармакологии и медицине в качестве основы для создания нового лекарственного препарата для лечения рассеянного склероза.
Рассеянный склероз (PC) - хроническое нейроиммунное демиелинизирующее заболевание ЦНС, в основе которого лежит комплекс воспалительных и нейродегенеративных процессов, приводящих к множественному очаговому и диффузному поражению ЦНС и, как следствие, - к инвалидизации и значительному снижению качества жизни больных.
Новая концепция патогенеза PC рассматривает эндогенные ретровирусы человека (HERV) как одни из наиболее значимых факторов формирования аутоиммунного воспаления в нервной ткани. Установление факта токсичности РНК и протеинов HERV для нервных клеток потребовало разработки новых стратегий лечения, основанных на ингибировании активности HERV (Gröger V., Emmer A., Staege M.S., Cynis H. Endogenous Retroviruses in Nervous System Disorders. Pharmaceuticals (Basel). 2021; 14(1):70. doi: 10.3390/ph14010070; Charvet В., Pierquin J., Brunei J., et al., Human Endogenous Retrovirus Type W Envelope from Multiple Sclerosis Demyelinating Lesions Shows Unique Solubility and Antigenic Characteristics. Virol. Sin. 2021; 36(5):1006-1026. doi: 10.1007/s12250-021-00372-0). Несколько семейств HERV связаны с PC, а именно MRSV/HERV-W и HERV-H, хотя ассоциация HERV-E, HERV-Fc1 и HERV-K-18 с течением PC также доказана (Laska M.J., Brudek Т., Nissen K.K., Christensen Т., Møller-Larsen A., Petersen Т., Nexø B.A. Expression of HERV-Fc1, a human endogenous retrovirus, is increased in patients with active multiple sclerosis. J. Virol. 2012; 86(7):3713-3722. doi: 10.1128/JVI.06723-11; Li F., Karlsson H. Expression and regulation of human endogenous retrovirus W elements. APMIS. 2016; 124(1-2):52-66. doi: 10.1111/apm. 12478; Brudek T., Christensen Т., Aagaard L., Petersen Т., Hansen H.J., Moller-Larsen А. В cells and monocytes from patients with active multiple sclerosis exhibit increased surface expression of both HERV-H Env and HERV-W Env, accompanied by increased seroreactivity. Retrovirology. 2009; 6:104. doi: 10.1186/1742-4690-6-104; Гольдина И.А., Гайдуль К.B., Смагин A.A., Сафронова И.В., Гольдин Б.Г., Павлов В.В., Любарский М.С., Козлов В.А. Экспрессия гена ENVELOPE эндогенного ретровируса человека I класса в мононуклеарных клетках крови больных рассеянным склерозом. Молекулярная медицина. 2011; 1:31-35).
Одним из механизмов реализации провоспалительных свойств HERV является активация толл-подобного рецептора 3, CD283 (TLR3) на эндосомальной мембране, а также белка, ассоциированного с дифференцировкой меланомы (MDA5), РНК-активируемой протеинкиназы (PKR) и индуцируемого гена I ретиноевой кислоты (RIG-I) в цитоплазме, что в свою очередь приводит к активации ядерного фактора NF-κВ и продукции провоспалительных цитокинов, регуляторного фактора интерферона 3 (IRF3), а также интерферонов 1 типа (Melbourne J.K., Chase K.А., Feiner В., Rosen С., Sharma R.P. Long non-coding and endogenous retroviral RNA levels are associated with proinflammatory cytokine mRNA expression in peripheral blood cells: Implications for schizophrenia. Psychiatry Res. 2018; 262:465-468. doi: 10.1016/j.psych.res.2017.09.025).
Установлено также, что протеины оболочки HERV способны непосредственно индуцировать поликлональную активацию и пролиферацию Т-клеток, что приводит к системной иммунной активации, вызывая аномальный врожденный иммунный ответ и воспаление с массовым высвобождением множества цитокинов (Rolland A., Jouvin-Marche Е., Viret С., Faure М., Perron Н., Marche P.N. The envelope protein of a human endogenous retrovirus-W family activates innate immunity through CD14/TLR4 and promotes Th1-like responses. J. Immunol. 2006; 176:7636-7644. doi:10.4049/jimmunol. 176.12.7636; Emmer A., Staege M.S., Kornhuber M.E. The retrovirus/superantigen hypothesis of multiple sclerosis. CellMol. Neurobiol. 2014; 34(8):1087-96. doi: 10.1007/s10571-014-0100-7; Гольдина И.А., Маркова E.B. Влияние эндогенного ретровируса HERV -Е λ 4-1 на функциональную активность клеток иммунной системы у больных рассеянным склерозом. Якутский медицинский журнал. 2019; 4(68):32-34. doi: 10.25789/YMJ.2019.68.07). В этом контексте следует отметить, что активация и пролиферация периферических Т-клеток, а также макрофагов играют важнейшую роль в патогенезе PC (Johnson W.E. Origins and evolutionary consequences of ancient endogenous retroviruses. Nat. Rev. Microbiol. 2019; 17:355-370. doi: 10.1038/s41579-019-0189-2; Wu L., Xia J., Li D., Kang Y., Fang W., Huang P. Mechanisms of M2 Macrophage-Derived Exosomal Long Non-coding RNA PVT1 in Regulating Th17 Cell Response in Experimental Autoimmune Encephalomyelitis. Front. Immunol. 2021; 12:773900. doi: 10.3389/fimmu.2021.773900).
В зависимости от типа течения PC выделяются различные схемы его лечения, направленные на снижение нейровоспаления и нейродегенерации.
В настоящее время разработано множество средств специфической терапии PC - препаратов, изменяющих течение PC (ПИТРС), воздействующих на различные известные патогенетические механизмы заболевания (Клинические рекомендации «Рассеянный склероз». Всероссийское общество неврологов, Российское общество нейрорадиологов, Медицинская Ассоциация врачей и центров рассеянного склероза, Российский комитет исследователей PC. 2020 г. 162 с. [Электронный ресурс]. URL:https://centrems.com/downloads/Clinical recommenations of the RS-Project submitted to the MHRF.pdf (дата обращения 07.09.2020); Хайбуллин Т.И., Бабичева Н.Н., Ахмедова, Г.М. и др. Ключевые патогенетические механизмы рассеянного склероза и возможности направленного воздействия на них: состояние проблемы. Практическая медицина. 2018; 16(10):43-46; Olek M.J. Multiple Sclerosis. Ann. Intern. Med. 2021; 174(6): ITC81-ITC96. doi: 10.7326/AITC202106150).
В терапии PC выделяют следующие группы ПИТРС:
- ПИТРС первой линии, назначаемые в качестве препаратов первого выбора при PC (интерферон бета-1а, интерферон бета-1b, глатирамера ацетат, диметилфумарат, терифлуномид).
- ПИТРС второй линии назначается в качестве препаратов последующего выбора в случае неэффективности или непереносимости препаратов первой линии, либо при быстропрогрессирующем течении PC в качестве препаратов первого выбора (Hauser S.L., Cree В.А.С. Treatment of Multiple Sclerosis: A Review. Am.J.Med. 2020; 133(12):1380-1390.e2. doi: 10.1016/j.amjmed.2020.05.049).
Следует отметить, что в случае высокоактивного или агрессивного течения PC препараты второй линии (финголимод, натализумаб, алемтузумаб, окрелизумаб) рекомендовано назначать сразу после установления диагноза.
Для терапии вторично-прогрессирующего PC с обострениями с целью профилактики обострений и радиологической активности, но не с целью предотвращения прогрессирования PC рекомендованы интерферон бета-1b и окрелизумаб (Клинические рекомендации «Рассеянный склероз». Всероссийское общество неврологов, Российское общество нейрорадиологов, Медицинская Ассоциация врачей и центров рассеянного склероза, Российский комитет исследователей PC. 2020 г. 162 с. [Электронный ресурс]. URL https://centrems.com/downloads/Clinical recommendations of the RS-Project submitted to the MHRF.pdf (дата обращения 07.09.2020).
Таким образом, в настоящее время на территории РФ зарегистрировано значительное количество лекарственных препаратов, показанных для лечения PC и изменяющих его течение. В то же время, указанные препараты, наряду со значительным количеством побочных эффектов, обладают недостаточной эффективностью, о чем свидетельствует то, что в настоящее время PC по-прежнему является неизлечимым (Koch-Henriksen N., Magyari М. Apparent changes in the epidemiology and severity of multiple sclerosis. Nat. Rev. Neurol. 2021; 17(11):676-688. doi: 10.1038/s41582-021-00556-y; Vollmer B.L., Wolf A.B., Sillau S., Corboy J.R., Alvarez E. Evolution of Disease Modifying Therapy Benefits and Risks: An Argument for De-escalation as a Treatment Paradigm for Patients With Multiple Sclerosis. Front. Neurol. 2022; 12:799138. doi: 10.3389/fneur.2021.799138). Кроме того, данные препараты не обладают установленной эффективностью в отношении эндогенных ретровирусов, ассоциированных с PC.
В связи с этим, поиск новых химико-фармацевтических препаратов с целью существенного повышения эффективности лечения PC является актуальной задачей экспериментальной фармакологии и практической медицины.
Известны способы лечения рассеянного склероза, основанные на применении различных веществ, ингибирующих активность эндогенных ретровирусов человека, ассоциированных с PC.
Известен способ лечения неврологических расстройств, характеризующихся обширной демиелинизацией и/или потерей аксонов. Примеры таких расстройств включают вторично-прогрессирующий рассеянный склероз и болезнь Девика. Раскрытые способы включают введение субъекту, страдающему таким расстройством, терапевтически эффективного количества, например, диметилфумарата или монометилфумарата (WO 2008096271, А61Р 25/00, 2008).
Недостатком способа является лимфотоксичность диметилфумарата и его метаболита монометилфумарата, проявляющаяся в значительном снижении общего количества лимфоцитов в крови, в среднем на 30% от исходного значения, а также кардио-, гастро-, нефро- и эмбриотоксичность (Справочник Видаль. Видаль-Рус, 2022 - 1120 с). Кроме того, недостатком данного способа является недостаточно изученный механизм действия данных препаратов при PC, а также узкий спектр терапевтической эффективности - доказаны в доклинических исследованиях лишь антиоксидантные свойства (диметилфумарат и его активный метаболит монометилфумарат активирует Nrf2 (ядерный фактор, связанный с эритроидным фактором 2, англ. nuclear factor erythroid 2-related factor 2, Nrf2) - зависимые антиоксидантные гены.
Известен способ лечения неврологических расстройств, например, тех, которые характеризуются демиелинизацией и/или потерей аксонов (например, рассеянный склероз). Способ включает введение терапевтически эффективного количества по меньшей мере одного соединения формулы (1):
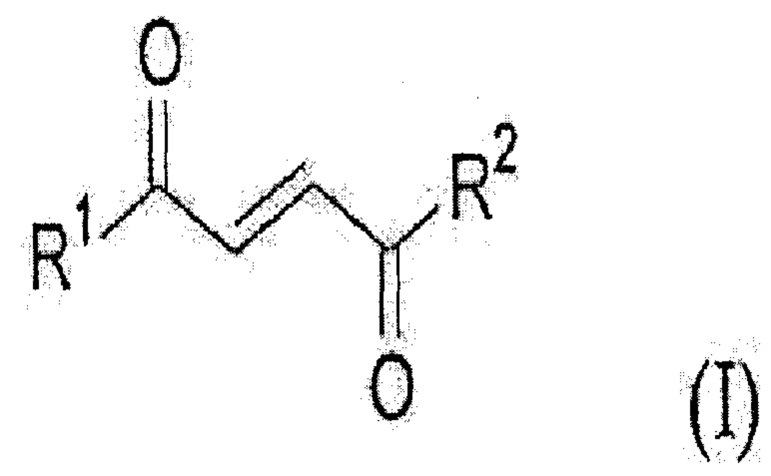 ,
,
где R1 и R2 независимо выбраны из ОН, О'' и (С1-6)алкокси, или его фармацевтически приемлемой соли и либо глатирамера ацетат, либо бета-интерферон (WO 2011100589, A61K 31/225, 2011).
Недостатком способа является наличие множества побочных эффектов у лекарственных препаратов, применяемым в данном способе (Справочник Видаль. Видаль-Рус, 2022 - 1120 с) а также отсутствие данных об воздействии на РС-ассоциированных эндогенных ретровирусов.
Известен анти-HERV-W env лиганд к протеину оболочки эндогенного ретровируса человека HERV-W (англ. human endogenous retrovirus, эндогенный ретровирус типа W человека) для его применения для профилактики и/или лечения блокады ремиелинизации при заболеваниях, связанных с экспрессией оболочечного белка HERV-W (HERV-W env, envelope protein) при рассеянном склерозе, а более конкретно, при ремиттирующе-рецидивирующем рассеянном склерозе, первично-прогрессирующем и вторично-прогрессирующем рассеянном склерозе, хронической воспалительной демиелинизирующей полинейропатии (CIDP), психических заболеваниях, таких как шизофрения и биполярное расстройство, а также других демиелинизируюицих заболеваниях, связанных с экспрессией гена белка оболочки HERV-W, в частности его подтипа MSRV (англ. multiple sclerosis-associated retrovirus), ретровирус, ассоциированный с рассеянным склерозом) (WO 2014053489, A61K 31/198, 2014).
Известен также лиганд анти-HERV-W env, применяемый для профилактики и/или лечения блокады ремиелинизации при заболеваниях, связанных с экспрессией белка оболочки (env, envelope protein) HERV-W (human endogenous retrovirus, эндогенный ретровирус типа W человека), в частности его подтипа MSRV (multiple sclerosis-associated retrovirus, ретровирус, ассоциированный с рассеянным склерозом) (2015 116 149, A61K 31/198, 2016).
Недостатком данных способов является избирательный характер воздействия полученных авторами лигандов только на экспрессию HERV-W env, в то время как влияние на активность других PC-ассоциированных эндогенных ретровирусов не исследуется.
Известно антиретровирусное лекарственное средство, нацеленное на эндогенный ретровирус человека (RU 2689326, A61K 31/7072, А61Р 31/14, 2019). В патенте предложена группа изобретений, которая относится к медицине и касается комбинированной композиции для лечения рассеянного склероза (MS) и хронической воспалительной демиелинизирующей полинейропатии (CIDP), включающей (i) антитело, фрагмент или производное, направленное против белка оболочки HERV-W (HERV-W env), и (ii) лекарственное средство, ингибирующее ретровирусную обратную транскриптазу. Группа изобретений также касается применения антитела, фрагмента или производного, направленного против белка оболочки HERV-W (HERV-W env), в комбинации с лекарственным средством, ингибирующим ретровирусную обратную транскриптазу, для лечения рассеянного склероза (MS) и хронической воспалительной демиелинизирующей полинейропатии (CIDP). Группа изобретений обеспечивает создание эффективного антиретровирусного лекарственного средства, нацеленного на HERV-W.
Недостатком данного средства является также его избирательность только в отношении ингибирования активности HERV-W env. Поэтому поиск эффективных соединений, способных подавлять активность ассоциированных с рассеянным склерозом эндогенных ретровирусов является актуальным.
Известно, что производные алканкарбоновых кислот обладают разнообразными биологическими эффектами. Среди производных арилгетероалканкарбоновых кислот были выявлены вещества, обладающие высоким уровнем воздействия на функциональные системы организма и широким интервалом фармакологического действия. В зависимости от особенностей химической структуры, среди них идентифицированы соединения, способные оказывать цитостатическое, канцеростатическое и антиагрегантное действие, повышать сопротивляемость организма. Наибольший уровень биологической активности показало соединение трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты, оказывающее влияние на гуморальное звено иммунного ответа и способное подавлять рост малигнизированных клеток (Колесникова О.П., Кудаева О.Т., Сухенко Т.Г., Лыков А.П., Гайдуль К.В., Лимонов В.Л., Мирскова А.Н., Левковская Г.Г., Воронков М.Г., Козлов В.А. Изучение иммунотропной активности у новых производных арилгетероалканкарбоновых кислот. Экспериментальная и клиническая фармакология. 2006; 69(3):47-49; Колесникова О.П., Кудаева О.Т., Ненашева Е.В., Гольдина И.А., Гойман Е.В., Лыков А.П., Сафронова И.В., Лимонов В.Л., Широкова А.Н., Рудякова Е.В., Гайдуль К.В. Селективные иммунодепрессивные свойства нового производного индолилтиоалканкарбоновой кислоты. Бюллетень Сибирского отделения Российской академии медицинских наук. 2007; 27(2):14-18). Трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты не является мутагеном, не обладает цитогенетическим и эмбриотоксическим эффектом (Горохова Л.Г., Жукова А.Г., Кизиченко Н.В. Казицкая А.С.Токсикологическая оценка воздействия на организм некоторых арилгетероалканкарбоновых соединений. Гигиена и санитария. 2019; 98(7), 734-737).
Трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты влияет на функциональную активность клеток иммунной системы - проявляет антипролиферативные свойства в отношении интактных, а также обогащенных в результате митогенной стимуляции Т - и В - лимфоцитами клеток селезенки мышей и мононуклеарных клеток крови доноров, а также подавляет продукцию гамма - интерферона и интерлейкина 2 (Гольдина И.А., Сафронова И.В., Гайдуль К.В., Козлов В.А. Цитокинсинтезирующая функция мононуклеарных клеток крови доноров при воздействии производного индолил-тио-алканкарбоновой кислоты с селективными иммунодепрессивными свойствами. Экспериментальная и клиническая фармакология. 2010. Т. 73. №3. С. 25-27). Трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты обладает свойствами стабилизации клеточных мембран (RU 1401850, A61K 31/40, 2009; "Клиническая эффективность и безопасность цефалоспориновых антибиотиков производства ООО "АБОЛмед". Сб. трудов НИИКИ, АГМУ и МКБ. Новосибирск, 2002. - Стр. 179; www. abolmed.ru/pages/article33.htm). Известно использование ряда лекарственных препаратов, содержащих соли алканкарбоновых кислот, в качестве местных противовоспалительных и/или анальгетических средств (GB 2093693, A61K 31/405, 1985; US4551475, A61K 31/405, 1985).
Известно применение трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты, ранее известной как стабилизатор клеточных мембран, в качестве иммунодепрессанта (RU 2228178, A61K 31/405, 2004).
Также известно применение трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты, ранее известной как стабилизатор клеточных мембран, в качестве противоопухолевого средства, а также средства, тормозящего метастазирование (RU 2240793, A61K 31/404, 2004).
Известно применение трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты в качестве средства для лечения аутоиммунных заболеваний. Свойство трис-(2-гидроксиэтил)аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты ингибировать Т-зависимую активацию В-лимфоцитов, в том числе в условиях угнетения функции костного мозга и лейкопении позволит создать на ее основе новые фармакологические препараты для лечения аутоиммунных заболеваний, таких, например, как системная красная волчанка, ревматоидный полиартрит, отторжение трансплантата при пересадке органов или костного мозга (RU 2252760, A61K 31/405, А61Р 37/00, 2005).
С целью расширения арсенала средств для ингибирования активности эндогенного ретровируса человека HERV-Eλ 4-1 env при рассеянном склерозе предлагается использовать трис-(2-гидроксиэтил) аммониевую соль 1-бензилиндолил-3-тиоуксусной кислоты.
Поставленная цель достигается применением трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты в качестве ингибитора активности эндогенного ретровируса человека HERV-E λ 4-1 env в мононуклеарных клетках периферической крови и мононуклеарных клетках спинномозговой жидкости при рассеянном склерозе.
Предложенное изобретение, на наш взгляд, является новым.
Сущность изобретения заключается в том, что при оценке влияния трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты на экспрессию эндогенного ретровируса HERV-E λ 4-1 env в мононуклеарных клетках крови и спинномозговой жидкости больных показан позитивный, ингибирующий активность эндогенного ретровируса, эффект.
Для подтверждения ингибирующих активность эндогенного ретровируса HERV-E λ 4-1 env свойств трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты использовались мононуклеарные клетки крови и спинномозговой жидкости больных непрерывно-прогредиентным и ремиттирующим рассеянным склерозом, поскольку у этих больных выявлялась активация эндогенного ретровируса HERV-E λ 4-1, ассоциированная с активностью заболевания (Гольдина И.А., Гайдуль К.В., Смагин А.А., Сафронова И.В., Гольдин Б.Г., Павлов В.В., Любарский М.С., Козлов В.А. Экспрессия гена ENVELOPE эндогенного ретровируса человека I класса в мононуклеарных клетках крови больных рассеянным склерозом. Молекулярная медицина. 2011. №1. С. 31-35; Смагин А.А., Гольдина И.А., Гайдуль К.В., Любарский М.С.Исследование пролиферативной активности мононуклеарных клеток крови больных рассеянным склерозом при воздействии пептида региона ENVELOPE эндогенного ретровируса человека HERV-E λ 4-1. Медицинская иммунология. 2014. Т. 16. №3. С.247-256; Гольдина И.А., Маркова Е.В. Влияние эндогенного ретровируса HERV-E λ 4-1 на функциональную активность клеток иммунной системы у больных рассеянным склерозом. Якутский медицинский журнал. 2019. №4 (68). С. 32-34).
Поскольку больные PC характеризуются различным профилем экспрессии эндогенных ретровирусов, в исследование были включены 20 больных (9 мужчин и 11 женщин в возрасте 35-50 лет) с установленным диагнозом PC, непрерывно-прогредиентным типом течения заболевания и 20 больных (8 мужчин и 12 женщин в возрасте 32-50 лет) с ремиттирующим типом течения PC в стадии обострения, находившихся на лечении в неврологическом отделении ФГБНУ НИИКэЛ СО РАМН, подписавшие добровольное информированное согласие, с выявленной в серии предварительных экспериментов экспрессией эндогенного ретровируса HERV-E λ 4-1 env. Протокол исследования был разработан в соответствии с Хельсинской Декларацией Всемирной Медицинской Ассоциации «Этические принципы проведения научных медицинских исследований с участием человека» с поправками 2013 г. и «Правилами надлежащей клинической практики», утвержденными Приказом МЗ РФ №200н от 01.04.2016 г., и был регламентирован этическим комитетом ФГБНУ НИИКэЛ СО РАМН.
Оценка эффективности способа осуществлялась путем сравнения частоты экспрессии HERV-E λ 4-1 env в мононуклеарных клетках (МНК) периферической крови и спинномозговой жидкости больных PC, которые культивировали в присутствии различных концентраций трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты, растворенной в физиологическом растворе, или физиологического раствора, а также продукции ряда цитокинов, вовлеченных в нейровоспалительные и нейродегенеративные процессы в патогенезе PC и коррелирующих со степенью тяжести заболевания.
Пример 1. Влияние трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты на экспрессию эндогенного ретровируса HERV-E λ 4-1 env в МНК периферической крови и спинномозговой жидкости больных PC.
Образцы МНК периферической крови и спинномозговой жидкости, которые культивировали в присутствии различных концентраций трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты, растворенной в физиологическом растворе, составили опытную группу. Контрольную группу составили образцы МНК, культивированные в присутствии аналогичного количества физиологического раствора.
С целью определения влияния трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты на экспрессию эндогенного ретровируса HERV-E λ 4-1 env у больных PC, МНК периферической крови и спинномозговой жидкости выделяли при помощи центрифугирования на градиенте плотности фиколла 1,078 г/см3 (Lymphocyte separation medium, MP Biomedicals, LLC, Eschwege, Germany) при 1500 оборотов/мин. в течение 40 мин. Клетки, собранные из интерфазы, трехкратно отмывали средой RPMI-1640 (ГНЦ вирусологии и биотехнологии «Вектор», Новосибирская область, п. Кольцово) и осаждали центрифугированием. Осадок МНК ресуспендировали в полной культуральной среде RPMI-1640 (ГНЦ вирусологии и биотехнологии «Вектор», Новосибирская область, п. Кольцово) содержащей 10% сыворотки крови человека АВ (IV) (Новосибирский центр крови), 10 мМ Hepes (ICN Biomedicals Inc, Aurora,Ohio), 4×10-5 M 2-меркаптоэтанола (L. Oba Feinchemie, Fischamene), 2Мм L-глутамина (ГНЦ вирусологии и биотехнологии «Вектор», Новосибирская область, п. Кольцово), 40 мкг/мл гентамицина (ФГУП НПО «Вирион») и доводили до концентрации 2×106 /мл. В серии предварительных экспериментов оценивали влияние различных концентраций (30 мкг/мл, 100 мкг/мл и 300 мкг/мл) трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты на жизнеспособность МНК в культуре в течение 72 часов. С этой целью по окончании периода культивирования клетки окрашивали 0,5% раствором трипанового синего и подсчитывали процентное содержание жизнеспособных клеток. Было установлено, что трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты в исследованных концентрациях не оказывает влияния на жизнеспособность МНК периферической крови и спинномозговой жидкости больных PC.
Экспрессию HERV-E λ 4-1 env определяли методом обратно-транскриптазной ПЦР. Геномную РНК получали методом фенольной экстракции с использованием тест - системы ВектоРНК- экстракция (Вектор - Бест, Новосибирск). Амплификацию проводили в программируемом амплификаторе «Терцик», ДНК - технологии, Москва), с использованием пар олигонуклеотидных праймеров к HERV-E А 4-1 env (sense: AGAGCCTACATTCGTTTAC, antisense: ACCGTATGATCCGATTGAG), гомологичных консервативным участкам антипараллельных цепей ДНК. Для контроля реакции проводили амплификацию всех исследуемых образцов с праймерами β - актина. Продукты амплификации анализировали методом электрофореза в 2% геле агарозы с добавлением 0,00001% бромистого этидия (ВектоДНК - ЭФ, Вектор - Бест, Новосибирск). Электрофорез проводили в трис - ацетатном буфере при напряжении 15 В/см геля. Полученный фрагмент кДНК соответствующего размера (274п.н.) выявляли в виде дискретной полосы после электрофоретического разделения молекул кДНК. Положительными считали образцы с наличием в геле видимой полосы кДНК, соответствующей ожидаемому размеру ампликона. Продукты амплификации визуализировали на денситометре Pharmacia - LKB.


Представленные в таблице 1 данные свидетельствуют о том, что трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты дозозависимо (в концентрациях 100 мкг/мл и 300 мкг/мл) подавляет экспрессию HERV-E λ 4-1 env в МНК периферической крови и спинномозговой жидкости больных PC.
Пример 2. Продукция иммунорегуляторных цитокинов, обеспечивающих нейровоспаление при рассеянном склерозе, под действием трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты в культуре МНК периферической крови.
Количественное определение спонтанной и стимулированной митогенами продукции цитокинов МНК периферической крови in vitro проводилось «сэндвич» - вариантом метода твердофазного иммуноферментного анализа в кондиционных средах клеточных культур Стандарты концентрации цитокинов, содержащие известные количества цитокина (от 0 до 2000пг/мл) представляли собой разведения соответствующих рекомбинантных белков. МНК периферической крови больных PC культивировали в концентрации 2×106/мл, по 2 мл на лунку, в 24 - луночных планшетах в полной культуральной среде при 37°С в атмосфере, содержащей 5% CO2 в течение 24 часов для исследования продукции IL - 1β, TNF-α; 48 часов для IL - 6; 72 часа - для IFN -γ. По окончании периода культивирования клеточную суспензию собирали, клетки осаждали центрифугированием, а культуральный супернатант замораживали при - 18°С и использовали для исследования. Определение IL - 1β, TNF - α и IL - 6 проводили с использованием тест - системы фирмы «Протеиновый контур» (ГНЦ НИИ ОЧБ, Санкт - Петербург), изучение уровня продукции IFN - γ проводили с использованием тест - системы фирмы «Цитокин» (Санкт - Петербург), согласно прилагаемой инструкции, на иммуноферментном анализаторе «Мультискан» (TITERTEK, Финляндия). Коэффициент вариации результатов 10 определений данными наборами в одном образце не превышал 10%. Фермент-субстратную реакцию останавливали, добавляя в каждую лунку 50 мкл 10% раствора серной кислоты. Уровень неспецифического связывания с пластиком меченных антител и субстратной смеси оценивали как фоновый. Расчет количества цитокинов в исследуемых образцах производили путем построения калибровочной кривой по соотношениям разности среднего значения оптической плотности в лунках, содержащих калибровочные или исследуемые пробы и среднего значения оптической плотности в лунках, содержащих калибровочную пробу 0пг/мл, к концентрации цитокина после измерения оптической плотности раствора в лунках планшета (при длине волны 450 нм), соответствующий интенсивности окрашивания раствора, прямо пропорциональное количеству связавшихся меченных антител, с помощью соответствующей программы. Количество цитокинов выражали в пг/мл.
Для изучения влияния трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты на продукцию цитокинов МНК периферической крови и спинномозговой жидкости больных PC, его вносили в культуральную среду в конечных концентрациях 30мкг/мл, 100 мкг/мл и 300мкг/мл в физиологическом растворе. В контрольной группе клетки культивировали в присутствии аналогичного количества физиологического раствора.
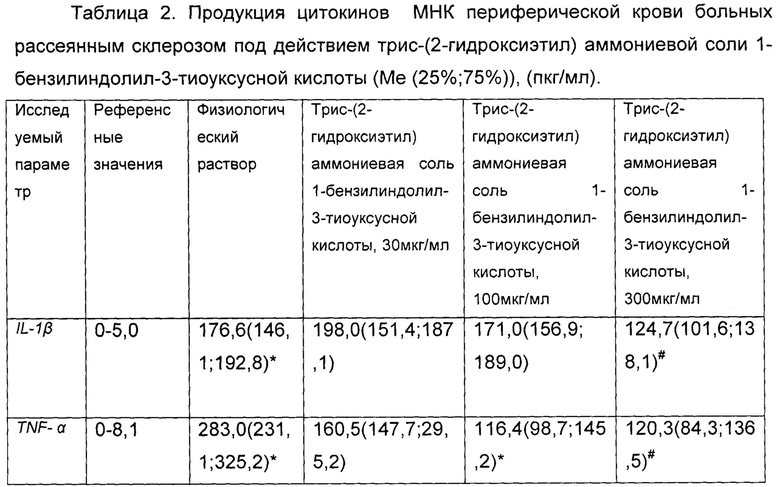
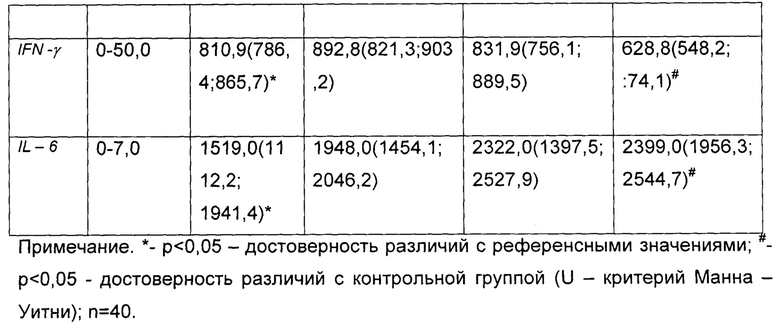
Представленные в таблице 2 данные свидетельствуют о том, что трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты снижает уровни продукции IL-1β, TNF- α, IFN- γ, IL-6 МНК периферической крови больных рассеянным склерозом, что свидетельствует о снижении системного воспаления.
При оценке корреляционной связи между экспрессией HERV-E λ 4-1 env и продукцией цитокинов МНК периферической крови под действием трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты была обнаружена положительная корреляционная связь (коэффициент ранговой корреляции Спирмена r=0,75), что свидетельствует об ассоциации подавления экспрессии HERV-E λ 4-1 env со снижением продукции вышеуказанных цитокинов под действием трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты.
В данном примере демонстрируется модулирующее действие трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты на уровень ряда иммунорегуляторных цитокинов, вовлеченных в нейровоспаление при рассеянном склерозе. Повышенная продукция МНК периферической крови и спинномозговой жидкости больных PC IL-1β, TNF- α, IFN - γ, IL-6 связана с манифестацией клинической симптоматики и формированием патологического процесса при данном заболевании.
Таким образом, трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты, наряду с подавлением экспрессии HERV-E λ 4-1 env в МНК периферической крови больных PC, снижает уровень продукции этими клетками провоспалительных цитокинов IL-1β, TNF- α, IFN - γ, IL-6 у больных PC, что свидетельствует о противовоспалительном эффекте трис-(2-гидроксиэтил) аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты.
Трис-(2-гидроксиэтил) аммониевая соль 1-бензилиндолил-3-тиоуксусной кислоты, обладает эффектами, проявляющимися в подавлении экспрессии HERV-Е λ 4-1 env в МНК периферической крови и спинномозговой жидкости и ассоциированным с ним снижения уровня продукции провоспалительных цитокинов IL-1β, TNF- α, IFN - γ, IL-6, указывающим на уменьшение интенсивности нейровоспаления у больных PC.
Выявленные эффекты свидетельствуют о позитивном влиянии указанного соединения на патогенетические механизмы рассеянного склероза, направленном на подавления активности эндогенного ретровируса человека HERV-E λ 4-1 env и снижение интенсивности нейровоспаления.
Предложенное изобретение позволяет использовать трис-(2-гидроксиэтил) аммониевую соль 1-бензилиндолил-3-тиоуксусной кислоты на подавление активности эндогенного ретровируса человека HERV-E λ 4-1 env и снижение ассоциированного с ней нейровоспаления при рассеянном склерозе.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИРЕТРОВИРУСНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО, НАЦЕЛЕННОЕ НА ЭНДОГЕННЫЙ РЕТРОВИРУС ЧЕЛОВЕКА | 2015 |
|
RU2689326C1 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ БЛОКАДЫ РЕМИЕЛИНИЗАЦИИ ПРИ ЗАБОЛЕВАНИЯХ, СВЯЗАННЫХ С ЭКСПРЕССИЕЙ БЕЛКА ОБОЛОЧКИ HERV-W | 2013 |
|
RU2636355C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2003 |
|
RU2252760C1 |
| Способ получения 1-R-индол-3-илсульфанилацетатов (2-гидроксиэтил)аммония | 2016 |
|
RU2642778C2 |
| ВЫДЕЛЕНИЕ И ИДЕНТИФИКАЦИЯ Т-КЛЕТОК | 2003 |
|
RU2327487C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИКЛОНАЛЬНОЙ Т-КЛЕТОЧНОЙ ВАКЦИНЫ ДЛЯ ЛЕЧЕНИЯ ИММУНОЛОГИЧЕСКИХ РАССТРОЙСТВ | 2004 |
|
RU2277422C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ОПТИЧЕСКОГО НЕВРИТА ПРИ РАССЕЯННОМ СКЛЕРОЗЕ | 2001 |
|
RU2200326C2 |
| СПОСОБ ТЕРАПИИ РЕМИТТИРУЮЩЕГО РАССЕЯННОГО СКЛЕРОЗА | 2012 |
|
RU2523058C2 |
| ИММУНОДЕПРЕССАНТ | 2003 |
|
RU2253448C1 |
| АНАЛОГИ ЖИРНЫХ КИСЛОТ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ И АУТОИММУННЫХ РАССТРОЙСТВ | 2001 |
|
RU2259823C2 |
Заявленное изобретение относится к области фармакологии и медицины и раскрывает применение соединения трис-(2-гидроксиэтил)аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты в качестве ингибитора активности эндогенного ретровируса человека HERV-E λ 4-1env в мононуклеарных клетках периферической крови и мононуклеарных клетках спинномозговой жидкости при рассеянном склерозе. Техническим результатом изобретения является позитивный, ингибирующий активность эндогенного ретровируса эффект при применении трис-(2-гидроксиэтил)аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты при рассеянном склерозе. 2 табл., 2 пр.
Применение соединения трис-(2-гидроксиэтил)аммониевой соли 1-бензилиндолил-3-тиоуксусной кислоты в качестве ингибитора активности эндогенного ретровируса человека HERV-E λ 4-1env в мононуклеарных клетках периферической крови и мононуклеарных клетках спинномозговой жидкости при рассеянном склерозе.
| ГОЛЬДИНА И.А | |||
| и др | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| WO 2021044009 A1, 11.03.2021 | |||
| ИММУНОДЕПРЕССАНТ | 2002 |
|
RU2228178C1 |
| US 20190040106 A1, 07.02.2019. | |||
Авторы
Даты
2023-08-15—Публикация
2022-06-07—Подача