ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По этой заявке испрашивается приоритет временной заявки на патент США № 62/718,106, поданной 13 августа 2018 г., которая полностью включена в настоящее описание посредством ссылки для любых целей.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к OX40-связывающим полипептидам и способам применения OX40-связывающих полипептидов для модуляции биологической активности OX40. Такие способы включают, без ограничения, способы лечения рака. В некоторых вариантах осуществления OX40-связывающие полипептиды представляют собой поливалентные OX40-связывающие полипептиды.
УРОВЕНЬ ТЕХНИКИ
[0003] Суперсемейство рецепторов фактора некроза опухоли (TNFRSF) включает несколько структурно родственных рецепторов клеточной поверхности. Активация мультимерными лигандами характерна для многих из этих рецепторов, и такая активация имеет терапевтическую ценность при многочисленных патологиях при правильной активации. Для эффективного агонизма этого семейства рецепторов может потребоваться кластеризация более высокого порядка, чем та, которая достигается при использовании традиционных бивалентных антител.
[0004] OX40 (TNFRSF4, CD134) является членом суперсемейства рецепторов TNF и экспрессируется на поверхности Т-клеток через 24-72 часа после активации Т-клеток. Антигенпрезентирующие клетки, находящиеся в непосредственной близости от активированных Т-клеток, презентируют лиганд OX40 (OX40L) на своей поверхности, который связывается с OX40 на Т-клетках с образованием кластеров, посылая костимулирующий сигнал, который вызывает усиление экспансии Т-клеток и усиление дифференцировки эффекторных Т-клеток. Таким образом, активация OX40 служит для поддержания иммунного ответа, например, путем улучшения выживаемости и функционирования Т-клеток.
[0005] Следовательно, существует терапевтическая потребность в более сильных агонистах OX40.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0006] Настоящее изобретение относится к полипептидам, содержащим по мньшей мере один домен VHH, который связывается с OX40, причем домен VHH содержит CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12. В некоторых вариантах осуществления домен VHH является гуманизированным. В некоторых вариантах осуществления домен VHH включает каркасную область 2 (FR2), содержащую аминокислотную последовательность SEQ ID NO: 22. В некоторых вариантах осуществления домен VHH содержит FR2, содержащую аминокислотную последовательность SEQ ID NO: 22, и FR3, содержащую аминокислотную последовательность SEQ ID NO: 23. В некоторых вариантах осуществления домен VHH содержит аминокислотную последовательность SEQ ID NO: 9.
[0007] В некоторых вариантах осуществления полипептид содержит два домена VHH. В некоторых вариантах осуществления полипептид содержит три домена VHH. В некоторых вариантах осуществления полипептид содержит четыре домена VHH. В некоторых вариантах осуществления полипептид содержит по меньшей мере один связывающий домен, который связывается со вторым антигеном, отличным от OX40. В некоторых таких вариантах осуществления второй антиген выбирают из PD-1, PD-L1 и 41BB. В некоторых вариантах осуществления по меньшей мере один связывающий домен, который связывается со вторым антигеном, является антагонистом или агонистом. В некоторых вариантах осуществления по меньшей мере один связывающий домен, который связывается со вторым антигеном, представляет собой домен VHH.
[0008] В некоторых вариантах осуществления каждый домен VHH связывается с OX40. В некоторых вариантах осуществления каждый домен VHH содержит CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12. В некоторых вариантах осуществления каждый домен VHH содержит каркасную область 2 (FR2), содержащую аминокислотную последовательность SEQ ID NO: 22. В некоторых вариантах осуществления каждый домен VHH содержит FR2, содержащую аминокислотную последовательность SEQ ID NO: 22, и FR3, содержащую аминокислотную последовательность SEQ ID NO: 23. В некоторых вариантах осуществления каждый домен VHH содержит аминокислотную последовательность SEQ ID NO: 9.
[0009] В некоторых вариантах осуществления полипептид содержит Fc-домен. В некоторых вариантах осуществления Fc-домен содержит аминокислотную последовательность, выбранную из SEQ ID NO: 25 и 26. В некоторых вариантах осуществления полипептид содержит аминокислотную последовательность SEQ ID NO: 14. В некоторых вариантах осуществления полипептид содержит аминокислоту последовательность SEQ ID NO: 15. В некоторых вариантах осуществления настоящего изобретения предоставляется полипептид, связывающий OX40, содержащий аминокислотную последовательность SEQ ID NO: 15. В некоторых вариантах осуществления настоящего изобретения предоставляется полипептид, связывающий OX40, состоящий из аминокислотной последовательности SEQ ID NO: 15.
[0010] В различных вариантах осуществления полипептид, представленный в настоящем описании, образует димер в физиологических условиях. В некоторых таких вариантах осуществления полипептид содержит Fc-домен.
[0011] В некоторых вариантах осуществления полипептид, представленный в настоящем описании, усиливает пролиферацию CD4+ и/или CD8+ Т-клеток in vitro и/или in vivo. В некоторых вариантах осуществления полипептид усиливает пролиферацию CD4+ и/или CD8+ Т-клеток в присутствии Treg-клеток. В некоторых вариантах осуществления полипептид усиливает пролиферацию CD4+ и/или CD8+ Т-клеток in vitro по меньшей мере в 1,5 раза или по меньшей мере в 2 раза. В некоторых вариантах осуществления полипептид усиливает пролиферацию CD4+ и/или CD8+ Т-клеток in vivo по меньшей мере в 1,5 раза или по меньшей мере в 2 раза.
[0012] В некоторых вариантах осуществления полипептид усиливает экспрессию CD25 на CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo. В некоторых вариантах осуществления полипептид усиливает экспрессию CD25 на CD4+ и/или CD8+ Т-клетках in vitro по меньшей мере в 1,5 раза или по меньшей мере в 2 раза. В некоторых вариантах осуществления полипептид усиливает экспрессию CD25 на CD4+ и/или CD8+ Т-клетках in vivo по меньшей мере в 1,5 раза или по меньшей мере в 2 раза.
[0013] В некоторых вариантах осуществления полипептид усиливает экспрессию CD71 на CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo. В некоторых вариантах осуществления полипептид усиливает экспрессию CD71 на CD4+ и/или CD8+ Т-клетках in vitro по меньшей мере в 1,5 раза или по меньшей мере в 2 раза. В некоторых вариантах осуществления полипептид усиливает экспрессию CD71 на CD4+ и/или CD8+ Т-клетках in vivo по меньшей мере в 1,5 раза или по меньшей мере в 2 раза.
[0014] В некоторых вариантах осуществления полипептид усиливает сигнализацию NFκB в CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo. В некоторых вариантах осуществления полипептид усиливает сигнализацию NFκB в CD4+ и/или CD8+ Т-клетках in vitro по меньшей мере в 1,5 раза, по меньшей мере в 2 раза, по меньшей мере в 3 раза или по меньшей мере в 5 раз. В некоторых вариантах осуществления полипептид усиливает сигнализацию NFκB в CD4+ и/или CD8+ Т-клетках in vivo по меньшей мере в 1,5 раза, по меньшей мере в 2 раза, по меньшей мере в 3 раза или по меньшей мере в 5 раз.
[0015] В некоторых вариантах осуществления полипептид усиливает экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo. В некоторых вариантах осуществления полипептид усиливает экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках in vitro по меньшей мере в 1,5 раза, по меньшей мере в 2 раза, по меньшей мере в 3 раза или по меньшей мере в 5 раз. В некоторых вариантах осуществления полипептид увеличивает экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках in vivo по меньшей мере в 1,5 раза, по меньшей мере в 2 раза, по меньшей мере в 3 раза или по меньшей мере в 5 раз.
[0016] В различных вариантах осуществления полипептид усиливает экспрессию CD25, CD71 и/или IFNγ и/или усиливает сигнализацию NFκB в присутствии Treg-клеток. В различных вариантах осуществления величину усиления определяют в виде среднего значения результатов измерений, полученных для Т-клеток от по меньшей мере пяти или по меньшей мере десяти разных здоровых доноров-людей.
[0017] В различных вариантах осуществления полипептид по настоящему изобретению, содержащий по меньшей мере один домен VHH, который связывается с OX40, является агонистом биологической активности OX40. В некоторых вариантах осуществления OX40 представляет собой OX40 человека. В некоторых вариантах осуществления полипептид связывается с человеческим OX40 с аффинностью (KD) менее 10 нМ, менее 5 нМ, менее 2 нМ или менее 1 нМ. В некоторых вариантах осуществления полипептид связывается с OX40 яванского макака с аффинностью (KD) менее 10 нМ, менее 5 нМ, менее 2 нМ или менее 1 нМ.
[0018] В некоторых вариантах осуществления изобретение относится кизобретение относится к фармацевтическим композициям, содержащим полипептид по настоящему изобретению, содержащий по меньшей мере один домен VHH, который связывается с OX40, и фармацевтически приемлемый носитель.
[0019] В некоторых вариантах осуществления изобретение относится к выделенной нуклеиновой кислоте, которая кодирует полипептид по настоящему изобретению, содержащий по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления изобретение относится к вектору, который содержит нуклеиновую кислоту. В некоторых вариантах осуществления изобретение относится к клетке-хозяину, содержащей нуклеиновую кислоту или вектор. В некоторых вариантах осуществления изобретение относится к клетке-хозяину, которая экспрессирует полипептид по настоящему изобретению, содержащий по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления клетка-хозяин секретирует OX40-связывающий полипептид. В некоторых вариантах осуществления клетка-хозяин представляет собой первичную клетку человека. В некоторых вариантах осуществления клетка-хозяин представляет собой Т-клетку. В некоторых вариантах осуществления клетка-хозяин представляет собой Т-клетку с химерным антигенным рецептором (CAR).
[0020] В некоторых вариантах осуществления изобретение относится к способу получения полипептида, содержащего по меньшей мере один домен VHH, который связывается с OX40, включающий инкубацию клетки-хозяина в условиях, подходящих для экспрессии полипептида. В некоторых вариантах осуществления способ дополнительно включает выделение полипептида.
[0021] В некоторых вариантах осуществления изобретение относится к способу усиления пролиферации CD4+ и/или CD8+ Т-клеток, включающему контактирование Т-клеток с полипептидом, содержащим по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления изобретение относится к способу усиления экспрессии CD25 на CD4+ и/или CD8+ Т-клетках, включающему контактирование Т-клеток с полипептидом, содержащим по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления изобретение относится к способу усиления экспрессии CD71 на CD4+ и/или CD8+ Т-клетках, включающему контактирование Т-клеток с полипептидом, содержащим по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления изобретение относится к способу усиления экспрессии IFNγ в CD4+ и/или CD8+ Т-клетках, включающему контактирование Т-клеток с полипептидом, содержащим по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления изобретение относится к способу усиления сигнализации NFκB в CD4+ и/или CD8+ Т-клетках, включающему контактирование Т-клеток с полипептидом, содержащим по меньшей мере один домен VHH, который связывается с OX40. В различных вариантах осуществления CD4+ и/или CD8+ Т-клетки находятся in vitro. В различных вариантах осуществления CD4+ и/или CD8+ Т-клетки находятся in vivo. В различных вариантах осуществления CD4+ и/или CD8+ Т-клетки находятся в присутствии Treg-клеток. В различных вариантах осуществления усиление составляет по меньшей мере 1,5 раза, по меньшей мере 2 раза, по меньшей мере 3 раза или по меньшей мере 5 раз.
[0022] В некоторых вариантах осуществления изобретение относится к способам лечения рака, включающим введение страдающему раком субъекту фармацевтически эффективного количества полипептида по настоящему изобретению, содержащего по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления изобретение относится к способам лечения рака, включающим введение страдающему раком субъекту фармацевтически эффективного количества клетки-хозяина, которая экспрессирует полипептид по настоящему изобретению, содержащий по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления клетка-хозяин секретирует OX40-связывающий полипептид. В некоторых вариантах осуществления клетка-хозяин экспрессирует OX40-связывающий полипептид на поверхности. В некоторых вариантах осуществления рак выбирают из базальноклеточной карциномы, рака желчных путей; рака мочевого пузыря; рака кости; рака головного мозга и центральной нервной системы; рака молочной железы; рака брюшины; рака шейки матки; хориокарциномы; рака толстой и прямой кишки; рака соединительной ткани; рака пищеварительной системы; рака эндометрия; рака пищевода; рака глаза; рака головы и шеи; рака желудка; рака желудочно-кишечного тракта; глиобластомы; карциномы печени; гепатомы; внутриэпителиального новообразования; рака почек или почечного рака; рака гортани; рака печени; рака легкого; мелкоклеточного рака легкого; немелкоклеточного рака легкого; аденокарциномы легкого; плоскоклеточного рака легкого; меланомы; миеломы; нейробластомы; рака полости рта; рака яичников; панкреатического рака; рака простаты; ретинобластомы; рабдомиосаркомы; рака прямой кишки; рака дыхательной системы; карциномы слюных желез; саркомы; рака кожи; плоскоклеточного рака; рака желудка; рака яичек; рака щитовидной железы; рака матки или эндометрия; рака мочевыводящей системы; рака вульвы; лимфомы; лимфомы Ходжкина; неходжкинской лимфомы; В-клеточной лимфомы; низкой степени злокачественности/фолликулярной неходжкинской лимфомы (НХЛ); НХЛ из малых лимфоцитов (МЛ); НХЛ средней степени злокачественности/фолликулярной НХЛ; диффузной НХЛ средней степени злокачественности; иммунобластной НХЛ высокой степени злокачественности; лимфобластной НХЛ высокой степени злокачественности; НХЛ из мелких нерасщепленных клеток высокой степени злокачественности; массивного поражения НХЛ; лимфомы из клеток мантийной зоны; лимфомы, связанной со СПИДом; макроглобулинемии Вальденстрема; хронического лимфолейкоза (ХЛЛ); острого лимфобластного лейкоза (ОЛЛ); волосатоклеточного лейкоза; и хронического миелобластного лейкоза.
[0023] В некоторых вариантах осуществления способ лечения рака дополнительно включает введение дополнительного терапевтического агента. В некоторых вариантах осуществления дополнительный терапевтический агент представляет собой противораковый агент. В некоторых вариантах осуществления противораковый агент выбирают из химиотерапевтического агента, противоракового биологического агента, лучевой терапии, CAR-T-терапии и онколитического вируса. В некоторых вариантах осуществления дополнительный терапевтический агент представляет собой противораковый биологический агент. В некоторых вариантах осуществления противораковый биологический агент представляет собой агент, который ингибирует PD-1 и/или PD-L1. В некоторых вариантах осуществления изобретения противораковый биологический агент выбирают из ниволумаба, пидилизумаба, пембролизумаба, дурвалумаба, атезолизумаба, авелумаба, AMP-224, BMS-936559, AMP-514, MDX-1105, TSR-042, STI-A1010 и STI-A1110. В некоторых вариантах осуществления противораковый биологический агент представляет собой агент, который ингибирует VISTA, gpNMB, B7H3, B7H4, HHLA2, CD73, CTLA4 или TIGIT. В некоторых вариантах осуществления противораковый биологический агент представляет собой антитело. В некоторых вариантах осуществления противораковый биологический агент представляет собой цитокин. В некоторых вариантах осуществления противораковый агент представляет собой CAR-T терапию. В некоторых вариантах осуществления противораковый агент представляет собой онколитический вирус. В некоторых вариантах осуществления способ лечения рака, представленный в настоящем описании, дополнительно включает резекцию опухоли и/или лучевую терапию.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0024] На фиг. 1 показано неспецифическое связывание 1D10v1-Fc и 1D10v6-Fc с нетрансфицированными клетками HEK293.
[0025] На фиг. 2A-2B показано связывание 1D10v1-Fc и 1D10v6-Fc с клетками СНО, которые экспрессируют OX40 человека (A) и OX40 яванского макака (B).
[0026] На фиг. 3A-3B показано связывание шестивалентного 3x1D10v1-Fc и шестивалентного 3x1D10v6-Fc (также упоминаемые как Hex-1D10v1 и Hex-1D10v6, соответственно) с клетками HEK293, которые экспрессируют OX40 человека (A), и с нетрансфицированными клетками HEK293 (B).
[0027] На фиг. 4 показана активация экспрессии люциферазы шестивалентным 3x1D10v1-Fc и шестивалентным 3x1D10v6-Fc в клетках Jurkat, которые экспрессируют OX40 и в которых содержание гена люциферазы ниже ответного элемента OX40.
[0028] На фиг. 5 показана экспрессия люциферазы в клетках Jurkat, которые экспрессируют OX40 и в которых содержание гена люциферазы ниже ответного элемента OX40, контактирующего с шестивалентным 3x1D10v6-Fc, четырехвалентным 2x1D10v6-Fc и двухвалентным 1D10v6-Fc.
[0029] На фиг. 6 показана дозозависимая пролиферация CD4+ Т-клеток от четырех разных доноров (L556, Leuko 20, Leuko 22 и Leuko 9), костимулированных шестивалентным 3x1D10v6-Fc и двухвалентным 1D10v6-Fc.
[0030] На фиг. 7 показано дозозависимое усиление CD25+ экспрессии на CD4+ Т-клетках от четырех разных доноров (L556, Leuko 20, Leuko 22 и Leuko 9), костимулированных шестивалентным 3x1D10v6-Fc и двухвалентным 1D10v6-Fc.
[0031] На фиг. 8 показано дозозависимое усиление CD71+ экспрессии на CD4+ Т-клетках от четырех разных доноров (L556, Leuko 20, Leuko 22 и Leuko 9), костимулированных шестивалентным 3x1D10v6-Fc и двухвалентным 1D10v6-Fc.
[0032] На фиг. 9 показано дозозависимое усиление секретируемого IFNγ из CD4+ Т-клеток от четырех разных доноров (L556, Leuko 20, Leuko 22 и Leuko 9), костимулированных шестивалентным 3x1D10v6-Fc и двухвалентным 1D10v6-Fc.
[0033] На фиг. 10 показано увеличение количества CD4+ Т-клеток и CD8+ Т-клеток после костимуляции человеческих Т-клеток анти-CD3-антителом и шестивалентным 3x1D10v6-Fc («без антитела» означает стимуляцию анти-CD3-антителом без шестивалентного 3x1D10v1-Fc).
[0034] На фиг. 11 показано усиление пролиферации CD4+ и CD8+ Т-клеток (две верхние панели), увеличение процентного содержания CD25+ CD4+ и CD25+ CD8+ Т-клеток (две средние панели) и увеличение процентного содержания CD71+ CD4+ и CD71+ CD8+ Т-клеток (две нижние панели) после костимуляции Т-клеток, полученных от 10 здоровых доноров, шестивалентным 3x1D10v6-Fc.
[0035] На фиг. 12 показано увеличение процентного содержания IFNγ+ CD4+ и IFNγ+ CD8+ Т-клеток после костимуляции Т-клеток, полученных от 4 здоровых доноров, шестивалентным 3x1D10v6-Fc.
[0036] На фиг. 13 показано, что обработка шестивалентным 3x1D10v6-Fc устраняет Treg-опосредованное подавление пролиферации CD4+ Т-клеток-респондеров и увеличивает процентное содержание CD4+ Т-клеток, экспрессирующих маркеры активации CD25 и CD71.
[0037] На фиг. 14A-14B показано, что комбинация пембролизумаба, антитела, нацеленного на PD-1, и шестивалентного 3x1D10v6-Fc (Hex-1D10v6) усиливает продуцирование IL-2 в реакции смешанной культуры лимфоцитов (MLR). На фиг. 14А показана комбинация 10 нМ пембролизумаба с различными концентрациями шестивалентного 3x1D10v6-Fc. На фиг. 14B показана комбинация 1 нМ шестивалентного 3x1D10v6-Fc с различными концентрациями пембролизумаба.
[0038] На фиг. 15 показан фармакокинетический (PK) профиль 5 мг/кг, 20 мг/кг или 60 мг/кг шестивалентного 3x1D10v6-Fc (Hex-1D10v6), вводимого яванским макакам. Достигнуто системное воздействие, которое усиливается пропорционально дозе.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0039] Варианты осуществления, представленные в настоящем описании, относятся к поливалентным OX40-связывающим полипептидам, которые модулируют активность OX40, и к их применению в различных способах лечения рака.
Определения и различные варианты осуществления
[0040] Заголовки разделов, используемые в настоящем описании, служат исключительно для организационных целей и не должны быть истолкованы как ограничивающие сущность излагаемого.
[0041] Все ссылки, цитируемые в настоящем описании, включая заявки на патенты, патентные публикации и номера доступа Genbank, включены в настоящее описание в качестве ссылки, как если бы каждая отдельная ссылка была специально и отдельно указана как включенная в качестве ссылки во всей своей полноте.
[0042] Способы и процедуры, описанные или упомянутые в настоящем описании, в целом хорошо понятны специалистами в данной области техники и обычно применяются ими при применении традиционных методов, таких как, например, широко используемые методы, описанные в Sambrook et al., Molecular Cloning: A Laboratory Manual 3rd. edition (2001) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. CURRENT PROTOCOLS IN MOLECULAR BIOLOGY (F.M. Ausubel, et al. eds., (2003)); серии METHODS IN ENZYMOLOGY (Academic Press, Inc.): PCR 2: A PRACTICAL APPROACH (M.J. MacPherson, B.D. Hames and G.R. Taylor eds. (1995)), Harlow and Lane, eds. (1988) ANTIBODIES, A LABORATORY MANUAL, and ANIMAL CELL CULTURE (R.I. Freshney, ed. (1987)); Oligonucleotide Synthesis (M.J. Gait, ed., 1984); Methods in Molecular Biology, Humana Press; Cell Biology: A Laboratory Notebook (J.E. Cellis, ed., 1998) Academic Press; Animal Cell Culture (R.I. Freshney), ed., 1987); Introduction to Cell and Tissue Culture (J.P. Mather and P. E. Roberts, 1998) Plenum Press; Cell and Tissue Culture Laboratory Procedures (A. Doyle, J.B. Griffiths, and D.G. Newell, eds., 1993-8) J. Wiley and Sons; Handbook of Experimental Immunology (D.M. Weir and C. C. Blackwell, eds.); Gene Transfer Vectors for Mammalian Cells (J.M. Miller and M.P. Calos, eds., 1987); PCR: The Polymerase Chain Reaction, (Mullis et al., eds., 1994); Current Protocols in Immunology (J.E. Coligan et al., eds., 1991); Short Protocols in Molecular Biology (Wiley and Sons, 1999); Immunobiology (C.A. Janeway and P. Travers, 1997); Antibodies (P. Finch, 1997); Antibodies: A Practical Approach (D. Catty., ed., IRL Press, 1988-1989); Monoclonal Antibodies: A Practical Approach (P. Shepherd and C. Dean, eds., Oxford University Press, 2000); Using Antibodies: A Laboratory Manual (E. Harlow and D. Lane (Cold Spring Harbor Laboratory Press, 1999); The Antibodies (M. Zanetti and J.D. Capra, eds., Harwood Academic Publishers, 1995); and Cancer: Principles and Practice of Oncology (V.T. DeVita et al., eds., J.B. Lippincott Company, 1993); и их обновленные версии.
[0043] Если не указано иное, научные и технические термины, используемые в связи с раскрытием настоящего изобретения, имеют значения, которые обычно понятны специалистам в данной области техники. Кроме того, если иное не следует из контекста или не указано в явном виде, термины в единственном числе включают множественное число, а термины во множественном числе включают единственное число. При любом противоречии в определениях между различными источниками или ссылками преимущественную силу имеет определение, приведенное в настоящем описании.
[0044] В общем случае, нумерация остатков в тяжелой цепи иммуноглобулина соответствует индексу EU, как у Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1991). «Индекс EU по Кабат» относится к нумерации остатков в EU антителе IgG1 человека.
[0045] Следует учитывать, что варианты осуществления изобретения, раскрытые в настоящем описании, включают варианты «состоящие из» и/или «по существу состоящие из». В контексте настоящего описания формы единственного числа включают ссылки на множественное число, если не указано иное. Использование в настоящем описании термина «или» не означает, что альтернативы являются взаимоисключающими.
[0046] В настоящей заявке использование «или» означает «и/или», если в явном виде не указано иное или иное является очевидным для специалиста в данной области. В контексте пункта формулы изобретения с множественной зависимостью использование «или» относится к более чем одному предшествующему независимому или зависимому пункту формулы изобретения.
[0047] Фраза «эталонный образец», «эталонная клетка» или «эталонная ткань» обозначает образец по меньшей мере с одной известной характеристикой, которую можно использовать в качестве сравнения с образцом по меньшей мере с одной неизвестной характеристикой. В некоторых вариантах осуществления эталонный образец можно использовать в качестве положительного или отрицательного индикатора. Эталонный образец можно использовать для определения уровня белка и/или мРНК, присутствующей, например, в здоровой ткани, по сравнению с уровнем белка и/или мРНК, присутствующей в образце с неизвестными характеристиками. В некоторых вариантах осуществления эталонный образец получают от одного и того же субъекта, но из другой части субъекта, отличной от тестируемой. В некоторых вариантах осуществления эталонный образец получают из области ткани, окружающей или прилегающей к раку. В некоторых вариантах осуществления эталонный образец получают не от тестируемого субъекта, а он представляет собой образец, полученный от субъекта, о котором известно, что у него имеется или не имеется рассматриваемое расстройство (например, конкретный рак или расстройство, связанное с OX40). В некоторых вариантах осуществления эталонный образец получают от одного итого же субъекта, но в момент времени до того, как у этого субъекта развилось раковое заболевание. В некоторых вариантах осуществления эталонный образец берут из образца доброкачественной опухоли от того же самого или другого субъекта. Когда для сравнения используется отрицательный эталонный образец, уровень экспрессии или количество исследуемой молекулы в отрицательном эталонном образце будет указывать на уровень, по которому специалист в данной области техники поймет, учитывая настоящее изобретение, что эта молекула отсутствует и/или присутствует на низком уровне. Когда для сравнения используется положительный эталонный образец, уровень экспрессии или количество исследуемой молекулы в положительном эталонном образце будет указывать на уровень, по которому специалист в данной области поймет, учитывая настоящее изобретение, что исследуемая молекула присутствует на некотором уровне.
[0048] Термины «польза», «клиническая польза», «восприимчивости» и «терапевтическая восприимчивость», используемые в настоящем описании в контексте положительного воздействия или реакции на введение терапевтического агента, могут быть измерены путем оценки различных конечных точек, например, ингибирования, до некоторой степени, прогрессирования заболевания, включая замедление и полную остановку; уменьшения количества приступов и/или симптомов заболевания; уменьшения размера поражения; ингибирования (т.е. уменьшения, замедления или полного прекращения) инфильтрации болезнетворных клеток в соседние периферические органы и/или ткани; ингибирования (т.е. уменьшения, замедления или полного прекращения) распространения заболевания; облегчения, до некоторой степени, одного или более симптомов, связанных с расстройством; увеличения продолжительности безрецидивного периода после лечения, например выживаемости без прогрессирования заболевания; повышенной общей выживаемости; более высокой скорости ответа; и/или снижения смертности в определенный момент времени после лечения. Субъект или рак, которые являются «невосприимчивыми» или «не реагируют», представляет собой субъекта или рак, которые не соответствуют указанным выше оценкам «восприимчивости».
[0049] Термины «молекула нуклеиновой кислоты», «нуклеиновая кислота» и «полинуклеотид» могут использоваться взаимозаменяемо и относиться к полимеру нуклеотидов. Такие полимеры нуклеотидов могут содержать природные и/или неприродные нуклеотиды и включают, без ограничения, ДНК, РНК и ПНК. «Последовательность нуклеиновой кислоты» относится к линейной последовательности нуклеотидов, содержащихся в молекуле нуклеиновой кислоты или полинуклеотиде.
[0050] Термины «полипептид» и «белок» используются взаимозаменяемо для обозначения полимера, состоящего из аминокислотных остатков, и не ограничиваются минимальной длиной. Такие полимеры аминокислотных остатков могут содержать природные или неприродные аминокислотные остатки и включают, без ограничения, пептиды, олигопептиды, димеры, тримеры и мультимеры аминокислотных остатков. Это определение охватывает как полноразмерные белки, так и их фрагменты. Термины также включают постэкспрессионные модификации полипептида, например гликозилирование, сиалирование, ацетилирование, фосфорилирование и т.п. Кроме того, для целей настоящего изобретения «полипептид» относится к белку, который включает модификации в нативной последовательности, такие как делеции, добавления и замены (обычно консервативные по природе), при условии, что белок сохраняет требуемую активность. Эти модификации могут быть преднамеренными, например, как результат сайт-направленного мутагенеза, или могут быть случайными, например, в результате мутаций хозяев, которые продуцируют белки, или ошибок амплификации ПЦР.
[0051] «OX40» в контексте настоящего описания относится к любому природному зрелому OX40, который является результатом процессинга предшественника OX40 в клетке. Термин включает OX40, полученного из любого позвоночного в качестве источника, включая млекопитающих, таких как приматы (например, люди, яванские макаки или макаки-резус) и грызуны (например, мыши и крысы), если не указано иное. Термин также включает встречающиеся в природе варианты OX40, такие как варианты сплайсинга или аллельные варианты. Неограничивающая иллюстративная аминокислотная последовательность OX40 человека показана, например, под номером доступа GenBank CAE11757.1. См. SEQ ID NO. 1. Неограничивающая иллюстративная аминокислотная последовательность OX40 яванского макака показана, например, под номером доступа NCBI XP_005545179. См. SEQ ID NO. 2.
[0052] Термин «специфически связывается» с антигеном или эпитопом является хорошо известным в данной области, и способы определения такого специфического связывания также хорошо известны в данной области. Говорят, что молекула проявляет «специфическое связывание» или «предпочтительное связывание», если она реагирует или связывается более часто, быстрее, с большей продолжительностью и/или с более высокой аффинностью к конкретной клетке или веществу по сравнению с альтернативными клетками или веществами. Однодоменное антитело (sdAb) или полипептид, содержащий VHH, «специфически связывается» или «предпочтительно связывается» с мишенью, если оно связывается с более высокими аффинностью, авидностью, легче и/или находится связанным дольше, чем с другими веществами. Например, sdAb или VHH-содержащий полипептид, который специфически или предпочтительно связывается с некоторым эпитопом OX40, представляет собой sdAb или VHH-содержащий полипептид, который связывается с этим эпитопом с большей аффинностью, авидностью, легче и/или находится связанным дольше, чем с другими эпитопами OX40 или эпитопами, отличными от OX40. Из этого определения также понятно, что, например, sdAb или VHH-содержащий полипептид, который специфически или предпочтительно связывается с первой мишенью, может специфически или предпочтительно связываться или не связываться со второй мишенью. По существу, «специфическое связывание» или «предпочтительное связывание» не обязательно означает (хотя может включать) исключительное связывание. Обычно, но не обязательно, указание на связывание означает предпочтительное связывание. «Специфичность» относится к способности связывающего белка избирательно связываться с антигеном.
[0053] Используемый в настоящем описании термин «модулировать» в отношении активности OX40 относится к изменению активности OX40. В некоторых вариантах осуществления «модулировать» относится к увеличению активности OX40 по сравнению с OX40 в отсутствие модулятора.
[0054] Используемый в настоящем описании термин «эпитоп» относится к участку на молекуле-мишени (например, антигене, таком как белок, нуклеиновая кислота, углевод или липид), с которым связывается антигенсвязывающая молекула (например, sdAb или VHH-содержащий полипептид). Эпитопы часто включают химически активную поверхностную группу молекул, такую как аминокислоты, полипептиды или боковые цепи сахаров, и имеют специфические трехмерные структурные характеристики, а также специфические характеристики заряда. Эпитопы могут быть образованы как из смежных, так и/или расположенных рядом несмежных остатков (например, аминокислот, нуклеотидов, сахаров, липидной части) молекулы-мишени. Эпитопы, образованные из смежных остатков (например, аминокислот, нуклеотидов, сахаров, липидной части), обычно сохраняются при воздействии денатурирующих растворителей, тогда как эпитопы, образованные в результате сборки третичной структуры, обычно теряются при обработке денатурирующими растворителями. Эпитоп может включать, без ограничения, по меньшей мере 3, по меньшей мере 5 или 8-10 остатков (например, аминокислот или нуклеотидов). В некоторых вариантах осуществления эпитоп имеет длину менее 20 остатков (например, аминокислот или нуклеотидов), менее 15 остатков или менее 12 остатков. Два антитела могут связываться с одним и тем же эпитопом внутри антигена, если они демонстрируют конкурентное связывание с антигеном. В некоторых вариантах осуществления эпитоп можно идентифицировать по определенному минимальному расстоянию до остатка CDR на антигенсвязывающей молекуле. В некоторых вариантах осуществления эпитоп можно идентифицировать по указанному выше расстоянию и дополнительно ограничивать теми остатками, которые участвуют в образовании связи (например, водородной связи) между остатком антигенсвязывающей молекулы и остатком антигена. Эпитоп также можно идентифицировать с помощью различных типов сканирования, например аланиновое или аргининовое сканирование может указывать на один или более остатков, с которыми может взаимодействовать антигенсвязывающая молекула. Если в явном виде не указано иное, набор остатков в качестве эпитопа не исключает другие остатки, входящие в состав эпитопа для конкретной антигенсвязывающей молекулы. Скорее, наличие такого набора означает минимальную последовательность (или набор последовательностей) эпитопов. Таким образом, в некоторых вариантах осуществления набор остатков, идентифицированных как эпитоп, обозначает минимальный эпитоп, релевантный для антигена, а не исчерпывающий список остатков для эпитопа на антигене.
[0055] «Нелинейный эпитоп» или «конформационный эпитоп» содержит несмежные полипептиды, аминокислоты и/или сахара в антигенном белке, с которым связывается антигенсвязывающая молекула, специфичная для эпитопа. В некоторых вариантах осуществления по меньшей мере один из остатков не является смежным по отношению к другим указанным остаткам эпитопа; однако один или более остатков также могут быть смежными с другими остатками.
[0056] «Линейный эпитоп» включает смежные полипептиды, аминокислоты и/или сахара в антигенном белке, с которым связывается антигенсвязывающая молекула, специфичная для эпитопа. Следует отметить, что в некоторых вариантах осуществления не обязательно, чтобы каждый из остатков в линейном эпитопе был напрямую связан (или вовлечен в связь) с антигенсвязывающей молекулой. В некоторых вариантах осуществления линейные эпитопы могут быть получены в результате иммунизации пептидом, который фактически состоит из последовательности линейного эпитопа или из структурных участков белка, относительно изолированных от остальной части белка (таким образом, чтобы антигенсвязывающая молекула могла взаимодействовать по меньшей мере в первую очередь только с этим отрезком последовательности).
[0057] Термины «антитело» и «антигенсвязывающая молекула» используются взаимозаменяемо в самом широком смысле и охватывают различные полипептиды, которые содержат антителоподобные антигенсвязывающие домены, включая, без ограничения, обычные антитела (обычно содержащие по меньшей мере одну тяжелую цепь и по меньшей мере одну легкую цепь), однодоменные антитела (sdAb, содержащие только одну цепь, которая обычно похожа на тяжелую цепь), VHH-содержащие полипептиды (полипептиды, содержащие по меньшей мере один вариабельный домен антитела только тяжелой цепи, или VHH) и фрагменты любого из вышеперечисленного, если они проявляют требуемую антигенсвязывающую активность. В некоторых вариантах осуществления антитело содержит домен димеризации. Такие домены димеризации включают, без ограничения, константные домены тяжелой цепи (включая CH1, шарнир, CH2 и CH3, где CH1 обычно спарен с константным доменом легкой цепи, CL, в то время как шарнир опосредует димеризацию) и Fc-домены (содержащие шарнир, CH2 и CH3, где шарнир опосредует димеризацию).
[0058] Термин антитело также включает, без ограничения, химерные антитела, гуманизированные антитела и антитела различных видов, такие как антитела верблюда (включая ламу), акулы, мыши, человека, яванского макака и т.д.
[0059] Термины «однодоменное антитело» и «sdAb» используются в настоящем описании взаимозаменяемо для обозначения антитела, имеющего один мономерный домен, например пару вариабельных доменов тяжелых цепей (или VHH) без легкой цепи.
[0060] Термин «VHH» или «домен VHH», или «антигенсвязывающий домен VHH», используемый в настоящем описании, относится к антигенсвязывающей части однодоменного антитела, такого как антитело верблюда или антитело акулы. В некоторых вариантах осуществления VHH содержит три CDR и четыре каркасные области, обозначенные FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. В некоторых вариантах осуществления VHH может быть укороченным на N-конце или C-конце и содержать только часть FR1 и/или FR4 или может не иметь одну или обе из этих каркасных областей при условии, что VHH, по существу, сохраняет связывание с антигеном и специфичность.
[0061] Термин «VHH-содержащий полипептид» относится к полипептиду, который содержит по меньшей мере один домен VHH. В некоторых вариантах осуществления полипептид VHH содержит два, три или четыре или более доменов VHH, где все домены VHH могут быть одинаковыми или разными. В некоторых вариантах осуществления VHH-содержащий полипептид содержит Fc-домен. В некоторых таких вариантах осуществления полипептид VHH может образовывать димер. Неограничивающие структуры VHH-содержащих полипептидов включают VHH1-Fc, VHH1-VHH2-Fc и VHH1-VHH2-VHH3-Fc, где VHH1, VHH2 и VHH3 могут быть одинаковыми или разными. В некоторых вариантах осуществления таких структур один VHH может быть соединен через линкер с другим VHH, или один VHH может быть соединен через линкер с Fc. В некоторых таких вариантах осуществления линкер содержит 1-20 аминокислот, предпочтительно 1-20 аминокислот, преимущественно состоящих из глицина и, необязательно, серина. В некоторых вариантах осуществления, когда VHH-содержащий полипептид включает Fc, он образует димер. Таким образом, структура VHH1-VHH2-Fc, если она образует димер, считается четырехвалентной (т.е. димер имеет четыре домена VHH). Аналогично, структура VHH1-VHH2-VHH3-Fc, если она образует димер, считается шестивалентной (т.е. димер имеет шесть доменов VHH).
[0062] Термин «моноклональное антитело» относится к антителу (включая sdAb или VHH-содержащий полипептид) по существу гомогенной популяции антител, т.е. отдельные антитела, составляющие популяцию, идентичны за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в незначительных количествах. Моноклональные антитела высокоспецифичны и направлены против одного антигенного участка. Кроме того, в отличие от препаратов поликлональных антител, которые обычно включают разные антитела, направленные против разных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты антигена. Таким образом, образец моноклональных антител может связываться с одним и тем же эпитопом на антигене. Модификатор «моноклональное» указывает на характер антитела как полученного из, по существу, гомогенной популяции антител, и его не следует толковать как требующий получения антитела каким-либо конкретным методом. Например, моноклональные антитела могут быть получены методом гибридомы, впервые описанным Kohler and Milstein, 1975, Nature 256:495, или могут быть получены методами рекомбинантной ДНК, описанными в патенте США № 4816567. Моноклональные антитела также могут быть выделены из фаговых библиотек, созданных методами, описанными, например, в McCafferty et al., 1990, Nature 348:552-554.
[0063] Термин «CDR» обозначает определяющую комплементарность область, определенную по меньшей мере одним из способов идентификации специалистом в данной области. В некоторых вариантах осуществления CDR могут быть определены в соответствии с любой из схем нумерации: схемой нумерации Чотиа, схемой нумерации Кабат, комбинацией Кабат и Чотиа, определения AbM и/или определения контакта. VHH содержит три CDR, обозначенные CDR1, CDR2 и CDR3.
[0064] В контексте настоящего описания термин «константная область тяжелой цепи» относится к области, содержащей по меньшей мере три константных домена тяжелой цепи, CH1, шарнир, CH2 и CH3. Конечно, не изменяющие функцию делеции и изменения внутри доменов входят в объем термина «константная область тяжелой цепи», если не указано иное. Неограничивающие иллюстративные константные области тяжелой цепи включают γ, δ и α. Неограничивающие иллюстративные константные области тяжелой цепи также включают ε и μ. Каждая тяжелая константная область соответствует изотипу антитела. Например, антитело, содержащее константную область γ, представляет собой антитело IgG, антитело, содержащее константную область δ, представляет собой антитело IgD, и антитело, содержащее константную область α, представляет собой антитело IgA. Кроме того, антитело, содержащее константную область μ, представляет собой антитело IgM, и антитело, содержащее константную область ε, представляет собой антитело IgE. Некоторые изотипы можно разделить на подклассы. Например, антитела IgG включают, без ограничения, антитела IgG1 (содержащие константную область γ1), IgG2 (содержащие константную область γ2), IgG3 (содержащие константную область γ3) и IgG4 (содержащие константную область γ4); антитела IgA включают, без ограничения, антитела IgA1 (содержащие константную область α1) и IgA2 (содержащие константную область α2); и антитела IgM включают, без ограничения, IgM1 и IgM2.
[0065] Термин «Fc-область» в контексте настоящего описания относится к части константной области тяжелой цепи, содержащей СН2 и СН3. В некоторых вариантах осуществления Fc-область содержит шарнир, CH2 и CH3. В различных вариантах осуществления, когда Fc-область содержит шарнир, шарнир опосредует димеризацию между двумя Fc-содержащими полипептидами. Fc-область может иметь любой изотип константной области тяжелой цепи антитела, обсуждаемый в настоящем описании. В некоторых вариантах осуществления Fc-область представляет собой IgG1, IgG2, IgG3 или IgG4.
[0066] «Акцепторная каркасная область человека» в контексте настоящего описания представляет собой каркасную область, содержащую аминокислотную последовательность каркасной области вариабельного домена тяжелой цепи (VH), полученную из каркасной области человеческого иммуноглобулина или консенсусной каркасной области человека, как обсуждается в настоящем описании. Акцепторная каркасная область человека, полученная из каркасной области иммуноглобулина человека или консенсусной каркасной области человека, может содержать такую же аминокислотную последовательность или может содержать изменения в аминокислотной последовательности. В некоторых вариантах осуществления количество аминокислотных замен составляет менее 10 или менее 9, или менее 8, или менее 7, или менее 6, или менее 5, или менее 4, или менее 3 по всем каркасным областям человека в одном антигенсвязывающем домене, таком как VHH.
[0067] «Аффинность» относится к силе общих суммарных нековалентных взаимодействий между одним связывающим участком молекулы (например, антитела или VHH-содержащего полипептида) и ее партнером по связыванию (например, антигеном). Аффинность или кажущаяся аффинность молекулы X к ее партнеру Y обычно может быть представлена константой диссоциации (KD) или кажущейся KD, соответственно. Аффинность можно измерить обычными методами, известными в данной области (такими как, например, KD ELISA, KinExA, устройствами для проточной цитометрии и/или поверхностного плазмонного резонанса), включая раскрытые в настоящем описании. Такие методы включают, без ограничения, методы с использованием BIAcore®, Octet® или проточную цитометрию.
[0068] Термин «KD» в контексте настоящего описания относится к константе равновесной диссоциации взаимодействия антигенсвязывающей молекулы/антигена. В контексте настоящего описания термин «KD» включает KD и KD-apparent.
[0069] В некоторых вариантах осуществления KD антигенсвязывающей молекулы измеряют методом проточной цитометрии с использованием линии антиген-экспрессирующих клеток и путем подгонки средней флуоресценции, измеренной для каждой концентрации антитела, к нелинейному уравнению связывания с одним участком (Prism Software graphpad). В некоторых таких вариантах осуществления KD представляет собой KD-apparent.
[0070] Термин «биологическая активность» относится к любому одному или более биологическим свойствам молекулы (присутствующей либо в том виде, в котором она встречается в природе in vivo, либо в виде, модифицированном с помощью рекомбинантных средств). Биологические свойства включают, без ограничения, связывание лиганда, индукцию или усиление пролиферации клеток (например, пролиферации Т-клеток) и индукцию или усиление экспрессии цитокинов.
[0071] Термин «активность OX40» или «биологическая активность» OX40, используемый в настоящем описании, включает любой биологический эффект или по меньшей мере одну из биологически значимых функций белка OX40. В некоторых вариантах осуществления активность OX40 включает способность OX40 взаимодействовать или связываться с лигандом OX40 (OX40L). Неограничивающие примеры активности OX40 включают усиление сигнализации NFκB, усиление пролиферации CD4+ и/или CD8+ Т-клеток, усиление экспрессии IFNγ в Т-клетках, усиление экспрессии CD25 и/или CD71 на Т-клетках и снижение супрессивной активности Treg-клеток в отношении активации и пролиферации эффекторных Т-клеток.
[0072] «Агонист» или «активирующее» антитело (такое как sdAb или VHH-содержащий полипептид) представляет собой антитело, которое увеличивает и/или активирует биологическую активность антигена-мишени. В некоторых вариантах осуществления агонистическое антитело связывается с антигеном и увеличивает его биологическую активность по меньшей мере на примерно 20%, 40%, 60%, 80%, 85% или более.
[0073] «Антагонист», «блокирующее» или «нейтрализующее» антитело представляет собой антитело, которое снижает и/или инактивирует биологическую активность антигена-мишени. В некоторых вариантах осуществления нейтрализующее антитело связывается с антигеном и снижает его биологическую активность по на меньшей мере примерно 20%, 40%, 60%, 80%, 85%, 90%, 95%, 99% или более.
[0074] VHH-содержащий полипептид с «созревшей аффинностью» относится к VHH-содержащему полипептиду с одним или более изменениями в одной или более CDR по сравнению с родительским VHH-содержащим полипептидом, который не имеет таких изменений, причем такие изменения приводят к улучшению аффинности VHH-содержащего полипептида к антигену.
[0075] В контексте настоящего описания термин «гуманизированный VHH» относится к VHH, в котором одна или несколько каркасных областей, по существу, заменены человеческими каркасными областями. В некоторых случаях определенные остатки каркасной области (FR) иммуноглобулина человека заменены соответствующими остатками нечеловеческого происхождения. Кроме того, гуманизированный VHH может содержать остатки, которые не встречаются ни в исходном VHH, ни в последовательностях человеческих каркасных областей, но включены для дальнейшего улучшения и оптимизации характеристик VHH или VHH-содержащих полипептидов. В некоторых вариантах осуществления гуманизированный VHH-содержащий полипептид содержит Fc-область человека. Понятно, что гуманизированную последовательность можно идентифицировать по первичной последовательности, и это не обязательно означает процесс, посредством которого было создано антитело.
[0076] «Функциональная Fc-область» обладает «эффекторной функцией» Fc-области с нативной последовательностью. Примеры «эффекторных функций» включают связывание с рецептором Fc; связывание Clq и комплемент-зависимую цитотоксичность (CDC); связывание с рецептором Fc; антителозависимую клеточно-опосредованную цитотоксичность (ADCC); фагоцитоз; подавление рецепторов клеточной поверхности (например, рецептора B-клеток); и активацию B-клеток и т.д. Такие эффекторные функции обычно требуют, чтобы Fc-область была объединена со связывающим доменом (например, вариабельным доменом антитела), и их можно оценить с помощью различных анализов.
[0077] «Fc-область с нативной последовательностью» включает аминокислотную последовательность, идентичную аминокислотной последовательности Fc-области, встречающейся в природе. Fc-области человека с нативной последовательностью включают Fc-область человеческого IgG1 с нативной последовательностью (не-A- и A-аллотипы); Fc-область человеческого IgG2 с нативной последовательностью; Fc-область человеческого IgG3 с нативной последовательностью; и Fc-область человеческого IgG4 с нативной последовательностью, а также их природные варианты.
[0078] «Вариант Fc-области» включает аминокислотную последовательность, которая отличается от последовательности Fc-области с нативной последовательностью из-за по меньшей мере одной модификации аминокислоты. В некоторых вариантах осуществления «вариант Fc-области» содержит аминокислотную последовательность, которая отличается от последовательности Fc-области с нативной последовательностью из-за по меньшей мере одной модификации аминокислоты, но сохраняет по меньшей мере одну эффекторную функцию Fc-области с нативной последовательностью. В некоторых вариантах осуществления вариант Fc-области имеет по меньшей мере одну аминокислотную замену по сравнению с Fc-областью с нативной последовательностью или с Fc-областью родительского полипептида, например, от примерно одной до примерно десяти аминокислотных замен, и предпочтительно от примерно одной до примерно пяти аминокислотных замен в Fc-области с нативной последовательностью или в Fc-области родительского полипептида. В некоторых вариантах осуществления вариант Fc-области по настоящему изобретению имеет по меньшей мере примерно 80% идентичности последовательности с нативной последовательностью Fc-области и/или с Fc-областью родительского полипептида, по меньшей мере примерно 90% идентичности последовательности, по меньшей мере примерно 95%, по меньшей мере примерно 96%, по меньшей мере примерно 97%, по меньшей мере примерно 98% или по меньшей мере примерно 99% идентичности последовательности.
[0079] «Fc-рецептор» или «FcR» описывает рецептор, который связывается с Fc-областью антитела. В некоторых вариантах осуществления FcγR представляет собой нативный человеческий FcR. В некоторых вариантах осуществления FcR представляет собой FcR, который связывается с антителом IgG (гамма-рецептором) и включает рецепторы подклассов FcγRI, FcγRII и FcγRIII, включая аллельные варианты и альтернативно сплайсированные формы этих рецепторов. Рецепторы FcγRII включают FcγRIIA («активирующий рецептор») и FcγRIIB («ингибирующий рецептор»), которые имеют сходные аминокислотные последовательности, которые различаются, прежде всего, цитоплазматическими доменами. Активирующий рецептор FcγRIIA содержит в цитоплазматическом домене иммунорецепторный активирующий мотив на основе тирозина (ITAM). Ингибирующий рецептор FcγRIIB содержит в цитоплазматическом домене иммунорецепторный ингибирующий мотив на основе тирозина (ITIM). (См., например, Daeron, Annu. Rev. Immunol. 15:203-234 (1997)). Обзор FcR представлен, например, в Ravetch and Kinet, Annu. Rev. Immunol 9:457-92 (1991); Capel et al., Immunomethods 4:25-34 (1994); и de Haas et al., J. Lab. Clin. Med. 126:330-41 (1995). Другие FcR, включая те, которые будут идентифицированы в будущем, входят в объем, используемого в настоящем описании термина «FcR». Например, термин «рецептор Fc» или «FcR» также включает неонатальный рецептор, FcRn, который отвечает за передачу материнских IgG плоду (Guyer et al., J. Immunol. 117:587(1976) и Kim et al., J. Immunol. 24:249(1994)) и регуляцию гомеостаза иммуноглобулинов. Способы измерения связывания с FcRn известны (см., например, Ghetie and Ward, Immunol. Today 18(12):592-598 (1997); Ghetie et al., Nature Biotechnology, 15 (7):637-640(1997); Hinton et al., J. Biol. Chem.279 (8):6213-6216 (2004); WO 2004/92219 (Hinton et al.).
[0080] Термин «по существу аналогичный» или «по существу такой же», используемый в настоящем описании, обозначает достаточно высокую степень сходства между двумя или более числовыми значениями, настолько, что позволило бы специалисту в данной области техники определить разницу между двумя или более значениями как являющуюся небольшой или не имеющей биологической и/или статистической значимости в контексте биологической характеристики, измеренной с помощью указанного значения. В некоторых вариантах осуществления два или более практически одинаковых значения различаются не более чем примерно на любое из: 5%, 10%, 15%, 20%, 25% или 50%.
[0081] «Вариант» полипептида означает биологически активный полипептид, имеющий по меньшей мере примерно 80% идентичности аминокислотной последовательности с полипептидом с нативной последовательностью после выравнивания последовательностей и введения пробелов (зазоров), если необходимо, для достижения максимального процента идентичности последовательностей без учета любых консервативных замен как части идентичности последовательности. Такие варианты включают, например, полипептиды, в которых один или более аминокислотных остатков добавлены или удалены на N- или C-конце полипептида. В некоторых вариантах осуществления вариант будет иметь по меньшей мере примерно 80% идентичности аминокислотной последовательности. В некоторых вариантах осуществления вариант будет иметь по меньшей мере примерно 90% идентичности аминокислотной последовательности. В некоторых вариантах осуществления вариант будет иметь по меньшей мере примерно 95% идентичности аминокислотной последовательности с полипептидом с нативной последовательностью.
[0082] В контексте настоящего описания «процент (%) идентичности аминокислотной последовательности» и «гомология» по отношению к последовательности пептида, полипептида или антитела определяют как процент аминокислотных остатков в последовательности-кандидате, которые идентичны аминокислотным остаткам в конкретной пептидной или полипептидной последовательности после выравнивания последовательностей и введения пробелов (зазоров), если необходимо, для достижения максимального процента идентичности последовательностей без учета каких-либо консервативных замен как части идентичности последовательностей. Выравнивание для целей определения процента идентичности аминокислотной последовательности может быть достигнуто различными способами, которые известны специалистам в данной области, например, с помощью общедоступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN или MEGALIGNTM (DNASTAR). Специалисты в данной области могут определить подходящие параметры для измерения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей.
[0083] Аминокислотная замена может включать, без ограничения, замену одной аминокислоты в полипептиде другой аминокислотой. Типичные замены показаны в таблице 1. Аминокислотные замены могут быть введены в представляющее интерес антитело, и продукты могут быть подвергнуты скринингу на наличие требуемой активности, например сохранение/улучшение связывания антигена, снижение иммуногенности или улучшение ADCC или CDC.
Таблица 1
[0084] Аминокислоты можно сгруппировать в соответствии с общими свойствами боковой цепи:
(1) гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, влияющие на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
[0085] Неконсервативные замены повлекут за собой замену члена одного из этих классов на другой класс.
[0086] Термин «вектор» используется для описания полинуклеотида, который может быть сконструирован таким образом, чтобы он содержал клонированный полинуклеотид или полинуклеотиды, которые могут размножаться в клетке-хозяине. Вектор может включать один или более из следующих элементов: точку начала репликации, одну или более регуляторных последовательностей (таких как, например, промоторы и/или энхансеры), которые регулируют экспрессию представляющего интерес полипептида, и/или один или более селективных маркерных генов (таких как, например, гены устойчивости к антибиотикам, и гены, которые можно использовать в колориметрических анализах, например, β-галактозидаза). Термин «вектор экспрессии» относится к вектору, который используется для экспрессии представляющего интерес полипептида в клетке-хозяине.
[0087] «Клетка-хозяин» относится к клетке, которая может быть или была реципиентом вектора или выделенного полинуклеотида. Клетки-хозяева могут быть прокариотическими клетками или эукариотическими клетками. Примеры эукариотических клеток включают клетки млекопитающих, такие как клетки приматов или животных, не относящихся к приматам; клетки грибов, такие как дрожжи; клетки растений; и клетки насекомых. Неограничивающие иллюстративные клетки млекопитающих включают, без ограничения, клетки NSO, клетки PER.C6® (Crucell) и клетки 293 и CHO, и их производные, такие как клетки 293-6E, CHO-DG44, CHO-K1, CHO-S и CHO-DS. Клетки-хозяева включают потомство одной клетки-хозяина, и это потомство не обязательно может быть полностью идентичным (по морфологии или комплементу геномной ДНК) исходной родительской клетке из-за естественной, случайной или преднамеренной мутации. Клетки-хозяева также включают первичные клетки, такие как первичные иммунные клетки человека.
[0088] Термин «выделенный» в контексте настоящего описания относится к молекуле, которая была отделена по меньшей мере от некоторых компонентов, с которыми она обычно встречается в природе или продуцируется. Например, полипептид называют «выделенным», когда он отделен по меньшей мере от некоторых компонентов клетки, в которой он был продуцирован. Когда полипептид секретируется клеткой после экспрессии, физическое отделение супернатанта, содержащего полипептид, от клетки, которая его продуцирует, считается «выделением» полипептида. Точно так же полинуклеотид называют «выделенным», когда он не является частью более крупного полинуклеотида (такого как, например, геномная ДНК или митохондриальная ДНК, в случае ДНК-полинуклеотида), в котором он обычно встречается в природе, или отделен по меньшей мере от некоторых компонентов клетки, в которой он был продуцирован, например, в случае РНК-полинуклеотида. Таким образом, ДНК-полинуклеотид, который содержится в векторе внутри клетки-хозяина, можно назвать «выделенным».
[0089] Термины «индивидуум» и «субъект» используются в настоящем описании взаимозаменяемо для обозначения животного; например, млекопитающего. В некоторых вариантах осуществления предоставляются способы лечения млекопитающих, включая, без ограничения, людей, грызунов, обезьян, кошек, собак, лошадей, крупного рогатого скота, свиней, овец, коз, лабораторных животных-млекопитающих, сельскохозяйственных животных-млекопитающих, спортивных животных-млекопитающих и домашних животных-млекопитающих. В некоторых примерах «индивидуум» или «субъект» относится к индивиду или субъекту, нуждающимся в лечении заболевания или расстройства. В некоторых вариантах осуществления субъект, получающий лечение, может быть пациентом, что указывает на тот факт, что субъект был идентифицирован как страдающий расстройством, поддающимся лечению, или имеющий соответствующий риск развития заболевания.
[0090] Термин «заболевание» или «нарушение» в контексте настоящего описания относится к состоянию, при котором необходимо и/или желательно лечение.
[0091] Термин «опухолевая клетка», «раковая клетка», «рак», «опухоль» и/или «новообразование», если не указано иное, используются в настоящем описании взаимозаменяемо и относятся к клетке (или клеткам), проявляющей неконтролируемый рост и/или с аномальным увеличением выживаемости и/или ингибированием апоптоза, что мешает нормальному функционированию органов и систем организма. Это определение включает доброкачественные и злокачественные опухоли, полипы, гиперплазию, а также латентные опухоли или микрометастазы.
[0092] Термины «рак» и «опухоль» охватывают солидный и гематологический/лимфатический рак, а также включают злокачественные, предзлокачественные и доброкачественные образования, такие как дисплазия. Также это определение включает клетки, имеющие аномальную пролиферацию, которой не препятствует (например, уклонение от иммунного надзора и механизмы избегания иммунного надзора) иммунная система (например, клетки, инфицированные вирусом). Примеры рака включают, без ограничения: базальноклеточную карциному, рак желчных путей; рак мочевого пузыря; рак кости; рак головного мозга и центральной нервной системы; рак молочной железы; рак брюшины; рак шейки матки; хориокарциному; рак толстой и прямой кишки; рак соединительной ткани; рак пищеварительной системы; рак эндометрия; рак пищевода; рак глаза; рак головы и шеи; рак желудка (включая рак желудочно-кишечного тракта); глиобластому; карциному печени; гепатому; внутриэпителиальное новообразование; рак почек или почечный рак; рак гортани; лейкемию; рак печени; рак легкого (например, мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого и плоскоклеточный рак легкого); меланому; миелому; нейробластому; рак полости рта (губы, языка, ротовой полости и глотки); рак яичников; панкреатический рак; рак простаты; ретинобластому; рабдомиосаркому; рак прямой кишки; рак дыхательной системы; карциному слюнных желез; саркому; рак кожи; плоскоклеточный рак; рак желудка; рак яичек; рак щитовидной железы; рак матки или эндометрия; рак мочевыводящей системы; рак вульвы; лимфому, включая лимфому Ходжкина и неходжкинскую лимфому и В-клеточную лимфому (включая низкой степени злокачественности/фолликулярную неходжкинскую лимфому (НХЛ); НХЛ из малых лимфоцитов (МЛ); средней степени злокачественности/фолликулярную НХЛ; диффузную НХЛ средней степени злокачественности; иммунобластную НХЛ высокой степени злокачественности; лимфобластную НХЛ высокой степени злокачественности; НХЛ из мелких нерасщепленных клеток высокой степени злокачественности; массивное поражение НХЛ; лимфому из клеток мантийной зоны; лимфому, связанную со СПИДом; и макроглобулинемию Вальденстрема; хронический лимфолейкоз (ХЛЛ); острый лимфобластный лейкоз (ОЛЛ); волосатоклеточный лейкоз; хронический миелобластный лейкоз; и другие карциномы и саркомы; и посттрансплантационное лимфопролиферативное расстройство (PTLD), а также аномальную пролиферацию сосудов, связанную с факоматозами, отеками (например, связанными с опухолями головного мозга) и синдром Мейгса.
[0093] Термин «неопухолевые клетки» в контексте настоящего описания относится к нормальным клеткам или ткани. Примеры неопухолевых клеток включают, без ограничения: Т-клетки, В-клетки, естественные киллерные клетки (NK), естественные киллерные Т-клетки (NKT), дендритные клетки, моноциты, макрофаги, эпителиальные клетки, фибробласты, гепатоциты, интерстициальные клетки почек, фибробластоподобные синовиоциты, остеобласты и клетки, расположенные в груди, скелетных мышцах, поджелудочной железе, желудке, яичнике, тонком кишечнике, плаценте, матке, яичках, почках, легкого, сердце, мозге, печени, простате, толстой кишке, лимфоидных органах, кости, и мезенхимальные стволовые клетки костного происхождения. Используемый в настоящем описании термин «клетка или ткань, расположенная на периферии» относится к неопухолевым клеткам, которые не располагаются рядом с опухолевыми клетками и/или внутри микроокружения опухоли.
[0094] Термин «клетки или ткань в микроокружении опухоли» в контексте настоящего описания относится к клеткам, молекулам, внеклеточному матриксу и/или кровеносным сосудам, которые окружают и/или питают опухолевую клетку. Примеры клеток или ткани в микроокружении опухоли включают, без ограничения: сосудистую сеть опухоли; лимфоциты, инфильтрирующие опухоль; ретикулярные клетки фибробластов; эндотелиальные клетки-предшественники (EPC); ассоциированные с раком фибробласты; перициты; другие стромальные клетки; компоненты внеклеточного матрикса (ЕСМ); дендритные клетки; антигенпрезентирующие клетки; Т-клетки; регуляторные Т-клетки (Treg-клетки); макрофаги; нейтрофилы; супрессорные клетки миелоидного происхождения (MDSC) и другие иммунные клетки, расположенные проксимальнее опухоли. Способы идентификации опухолевых клеток и/или клеток/тканей, расположенных в микроокружении опухоли, хорошо известны в данной области, как описано в настоящем описании ниже.
[0095] В некоторых вариантах осуществления «увеличение» или «уменьшение» относится к статистически значимому увеличению или уменьшению, соответственно. Как будет ясно специалисту в данной области, «модуляция» также может включать изменение (которое может быть либо увеличением, либо уменьшением) аффинности, авидности, специфичности и/или селективности мишени или антигена по отношению к одному или более из его лигандов, партнеров по связыванию, партнеров для ассоциации в гомомультимерную или гетеромультимерную форму или субстраты; изменение (которое может быть повышением или понижением) чувствительности мишени или антигена к одному или более условиям в среде или окружении, в котором присутствует мишень или антиген (например, pH, сила ионов, присутствие кофакторов и др.); и/или пролиферацию клеток или продуцирование цитокинов по сравнению с теми же условиями, но без присутствия тестируемого агента. Это может быть определено любым подходящим способом и/или с использованием любого подходящего анализа, известного как такового или раскрытого в настоящем описании, в зависимости от задействованной мишени.
[0096] Используемый в настоящем описании термин «иммунный ответ» означает клеточные и/или гуморальные иммунные ответы, которые являются достаточными для подавления или предотвращения появления или для уменьшения симптомов заболевания (например, рака или метастазов рака). «Иммунный ответ» может охватывать аспекты как врожденной, так и адаптивной иммунной системы.
[0097] Используемый в настоящем описании термин «лечение» представляет собой подход для получения полезных или желаемых клинических результатов. «Лечение» в контексте настоящего описания охватывает любое введение или применение терапевтического агента для лечения заболевания у млекопитающего, включая человека. Для целей настоящего раскрытия полезные или желаемые клинические результаты включают, без ограничения, любое одно или более из следующего: облегчение одного или более симптомов, уменьшение степени заболевания, профилактику или задержку распространения (например, метастазов, например, метастазов в легкое или лимфатический узел) заболевания, профилактику или отсрочку рецидива заболевания, задержку или замедление прогрессирования заболевания, облегчение болезненного состояния, подавление заболевания или прогрессирования заболевания, подавление или замедление заболевания или его прогрессирования, задержку его развития и ремиссию (частичную или полную). «Лечение» также включает уменьшение патологических последствий пролиферативного заболевания. Способы, представленные в настоящем описании, предусматривают любой один или более из этих аспектов лечения. В соответствии с вышеизложенным, термин «лечение» не требует полного устранения всех аспектов расстройства.
[0098] «Облегчение» означает уменьшение или улучшение одного или более симптомов по сравнению с состоянием без введения терапевтического агента. «Облегчение» также включает сокращение или уменьшение продолжительности симптома.
[0099] Термин «противораковый агент» используется в настоящем описании в самом широком смысле для обозначения агентов, которые используются для лечения одного или более видов рака. Примеры классов таких агентов включают, без ограничения, химиотерапевтические агенты, противораковые биологические агенты (такие как цитокины, слитые белки, состоящие из Fc-фрагмента и внеклеточного домена рецептора, и антитела), лучевую терапию, CAR-T терапию, терапевтические олигонуклеотиды (такие как антисмысловые олигонуклеотиды и миРНК) и онколитические вирусы.
[00100] Термин «биологический образец» означает количество вещества, полученного от живого существа или ранее живого существа. Такие вещества включают, без ограничения, кровь (например, цельную кровь), плазму, сыворотку, мочу, амниотическую жидкость, синовиальную жидкость, эндотелиальные клетки, лейкоциты, моноциты, другие клетки, органы, ткани, костный мозг, лимфотические узлы и селезенку.
[00101] Термин «контроль» или «эталон» относится к композиции, о которой известно, что она не содержит аналита («отрицательный контроль») или содержит аналит («положительный контроль»). Положительный контроль может включать известную концентрацию аналита.
[00102] Термины «ингибирование» или «ингибировать» относятся к уменьшению или прекращению проявления какой-либо фенотипической характеристики или к снижению или прекращению распространения, степени или вероятности появления этой характеристики. «Снижать» или «ингибировать» означает уменьшать, снижать или блокировать активность, функцию и/или количество по сравнению с эталоном. В некоторых вариантах осуществления «снижение» или «ингибирование» означает способность обеспечивать общее снижение на 10% или более. В некоторых вариантах осуществления «снижение» или «ингибирование» означает способность обеспечивать общее снижение на 50% или более. В некоторых вариантах осуществления «снижение» или «ингибирование» означает способность обеспечивать общее снижение на 75%, 85%, 90%, 95% или более. В некоторых вариантах осуществления указанное выше количество подавляется или снижается в течение некоторого периода времени по сравнению с контролем за тот же период времени.
[00103] В контексте настоящего описания, «задержка развития заболевания» означает задержку, затруднение, замедление, отсрочку, стабилизацию, подавление и/или отсрочку развития заболевания (такого как рак). Эта задержка может быть различной по продолжительности в зависимости от истории болезни и/или человека, получающего лечение. Как очевидно для специалиста в данной области, достаточная или значительная отсрочка может фактически включать профилактику в том смысле, что у индивидуума не разовьется заболевание. Например, возможна отсрочка развития поздней стадии рака, такой как метастазирование.
[00104] «Профилактика» в контексте настоящего описания включает обеспечение профилактики в отношении возникновения или рецидива заболевания у субъекта, который может быть предрасположен к еще не диагностированному заболеванию. Если не указано иное, термины «уменьшать», «ингибировать» или «предотвращать» не означают и не требуют полного предотвращения в течение всего времени, а только в течение измеряемого периода времени.
[00105] «Терапевтически эффективное количество» вещества/молекулы, агониста или антагониста может меняться в зависимости от таких факторов, как стадия заболевания, возраст, пол и вес человека, а также способность вещества/молекулы, агониста или антагониста вызывать желаемый ответ у человека. Терапевтически эффективным количеством также является такое количество, при котором терапевтически полезные эффекты перевешивают любые токсические или вредные эффекты вещества/молекулы, агониста или антагониста. Терапевтически эффективное количество может быть доставлено за одно или несколько введений. Терапевтически эффективное количество относится к количеству, эффективному в дозах и в течение необходимого периода времени для достижения желаемого терапевтического и/или профилактического результата.
[00106] Термины «фармацевтический состав» и «фармацевтическая композиция» относятся к препарату, находящемуся в такой форме, которая обеспечивает эффективную биологическую активность активного ингредиента(ов) и которая не содержит дополнительных компонентов, которые являются неприемлемо токсичными для субъекта, которому будет введен этот состав. Такие составы могут быть стерильными.
[00107] «Фармацевтически приемлемый носитель» относится к нетоксичному твердому, полутвердому или жидкому наполнителю, разбавителю, инкапсулирующему материалу, вспомогательному веществу состава или носителю, обычному в данной области, предназначенному для применения с терапевтическим агентом, которые вместе составляют «фармацевтическую композицию», вводимую субъекту. Фармацевтически приемлемый носитель нетоксичен для реципиентов в используемых дозировках и концентрациях и совместим с другими ингредиентами препарата. Фармацевтически приемлемый носитель подходит для используемого состава.
[00108] Введение «в комбинации с» одним или более дополнительными терапевтическими агентами включает одновременное (параллельное) и последовательное введение в любом порядке.
[00109] Термин «параллельно» используется в настоящем описании для обозначения введения двух или более терапевтических агентов, когда по меньшей мере часть введения перекрывается по времени, или когда введение одного терапевтического агента находится в пределах короткого промежутка времени относительно введения другого терапевтического агента, или когда терапевтические эффекты обоих агентов перекрываются по меньшей мере в течение некоторого периода времени.
[00110] Термин «последовательно» используется в настоящем описании для обозначения введения двух или более терапевтических агентов, которые не перекрываются по времени, или при котором терапевтические эффекты агентов не перекрываются.
[00111] В контексте настоящего описания «в сочетании с» относится к предоставлению одного лечебного воздействия в дополнение к другому лечебному воздействию. Таким образом, «в сочетании с» относится к предоставлению одного лечебного воздействия до, во время или после предоставления другого лечебного воздействия индивиду.
[00112] Термин «вкладыш в упаковку» используется для обозначения инструкций, обычно включаемых в коммерческие упаковки терапевтических продуктов, которые содержат информацию о показаниях, применении, дозировке, способах введения, комбинированной терапии, противопоказаниях и/или предупреждениях относительно применения таких терапевтических продуктов.
[00113] «Изделие» представляет собой любой продукт (например, упаковку или контейнер) или набор, включающий по меньшей мере один реагент, например, лекарственное средство для лечения заболевания или расстройства (например, рака) или зонд для специфического обнаружения биомаркера, раскрытого в настоящем описании. В некоторых вариантах осуществления продукт или набор рекламируют, распространяют или продают как единое целое для осуществления раскрытых в настоящем описании способов.
[00114] Термины «метка» и «детектируемая метка» означают фрагмент, присоединенный, например, к антителу или антигену, который позволяет обнаружить реакцию специфического связывания (например, связывание) между членами пары. Меченый член пары специфического связывания называется «детектируемо меченным». Таким образом, термин «меченый связывающий белок» относится к белку с включенной меткой, которая обеспечивает идентификацию связывающего белка. В некоторых вариантах осуществления метка представляет собой детектируемый маркер, способный продуцировать сигнал, который может быть обнаружен визуальными или инструментальными средствами, например, путем включения радиоактивно меченой аминокислоты или присоединения к полипептиду биотинилированных фрагментов, которые могут быть обнаружены меченым авидином (например, стрептавидин, содержащий флуоресцентный маркер, или ферментативная активность, которая может быть обнаружена оптическими или колориметрическими методами). Примеры меток для полипептидов включают, без ограничения, следующие: радиоизотопы или радионуклиды (например, 3H, 14C, 35S, 90Y, 99Tc, 111In, 125I, 131I, 177Lu, 166Ho или 153Sm); хромогены, флуоресцентные метки (например, FITC, родамин, люминофоры на основе лантаноидов), ферментативные метки (например, пероксидаза хрена, люцифераза, щелочная фосфатаза); хемилюминесцентные маркеры; биотинилированные группы; заранее определенные полипептидные эпитопы, распознаваемые вторичным репортером (например, последовательности пары лейциновой молнии, участки связывания для вторичных антител, домены, связывающие металлы, эпитопные метки); и магнитные агенты, такие как хелаты гадолиния. Репрезентативные примеры меток, обычно используемых для иммуноанализов, включают фрагменты, которые продуцируют свет, например соединения акридиния, и фрагменты, которые продуцируют флуоресценцию, например флуоресцеин. При этом сам фрагмент не может быть детектируемо меченным, но может стать детектируемым после реакции с еще одним фрагментом.
Примеры OX40-связывающих полипептидов
[00115] В настоящем описании представлены агонистические OX40-связывающие полипептиды. В различных вариантах осуществления агонистические OX40-связывающие полипептиды содержат по меньшей мере один домен VHH, который связывается с OX40. В некоторых вариантах осуществления предлагаемый в настоящем описании агонистический OX40-связывающий полипептид содержит один, два, три, четыре, пять, шесть, семь или восемь доменов VHH, которые связываются с OX40. В некоторых вариантах осуществления предлагаемый в настоящем описании агонистический OX40-связывающий полипептид содержит один, два, три или четыре домена VHH, которые связываются с OX40. Такие OX40-связывающие полипептиды могут содержать один или более дополнительных доменов VHH, которые связываются с одним или более белками-мишенями, отличными от OX40.
[00116] В некоторых вариантах осуществления агонистический OX40-связывающий полипептид содержит по меньшей мере один домен VHH, который связывается с OX40, и Fc-домен. В некоторых вариантах осуществления предлагаемый в настоящем описании агонистический OX40-связывающий полипептид содержит один, два, три или четыре домена VHH, которые связываются с OX40, и Fc-домен. В некоторых вариантах осуществления Fc-домен опосредует димеризацию OX40-связывающего полипептида в физиологических условиях, с образованием димера, который удваивает количество OX40-связывающих участков. Например, OX40-связывающий полипептид, содержащий три домена VHH, которые связываются с OX40, и Fc-область, является трехвалентным в виде мономера, но в физиологических условиях Fc-область может опосредовать димеризацию, при которой в таких условиях OX40-связывающий полипептид существует в виде шестивалентного димера. Неограничивающие иллюстративные шестивалентные OX40-связывающий полипептиды включают 3x1D10v1-Fc и 3x1D10v6-Fc, которые также упоминаются как Hex-1D10v1 и Hex-1D10v6, соответственно. Не ограничиваясь какой-либо конкретной теорией, есть основания полагать, что костимуляция через OX40 улучшается за счет кластеризации OX40, что означает, что поливалентные OX40-связывающие полипептиды (такие как четырехвалентные или шестивалентные) являются более эффективными, чем одновалентные или двухвалентные OX40-связывающие полипептиды.
[00117] В различных вариантах осуществления домен VHH, который связывается с OX40, содержит CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12. В некоторых вариантах осуществления домен VHH является гуманизированным.
[00118] В некоторых вариантах осуществления домен VHH, который связывается с OX40, может быть гуманизированным. Гуманизированные антитела (такие как VHH-содержащие полипептиды) полезны в качестве терапевтических молекул, поскольку гуманизированные антитела снижают или устраняют иммунный ответ у человека на нечеловеческие антитела, что может вызвать иммунный ответ на терапевтическое антитело и снизить эффективность терапевтического агента. Обычно гуманизированное антитело включает один или более вариабельных доменов, в которых CDR (или их части) происходят из нечеловеческого антитела, и FR (или их части) происходят из последовательностей человеческого антитела. Гуманизированное антитело необязательно также может содержать по меньшей мере часть константной области человека. В некоторых вариантах осуществления некоторые остатки FR в гуманизированном антителе заменены соответствующими остатками нечеловеческого антитела (например, антитела, из которого происходят остатки CDR), например, для восстановления или улучшения специфичности или аффинности антитела.
[00119] Гуманизированные антитела и способы их получения рассмотрены, например, в Almagro and Fransson, (2008) Front. Biosci. 13:1619-1633 и дополнительно описаны, например, в Riechmann et al., (1988) Nature 332:323-329; Queen et al., (1989) Proc. Natl Acad. Sci. USA 86:10029-10033; патентах США №№ 5821337, 7527791, 6982321 и 7087409; Kashmiri et al., (2005) Methods 36:25-34; Padlan, (1991) Mol. Immunol. 28:489-498 (описывающий «изменение поверхности»); Dall'Acqua et al., (2005) Methods 36:43-60 (описывающий «перестановку FR»); и Osbourn et al., (2005) Methods 36:61-68 и Klimka et al., (2000) Br. J. Cancer, 83: 252-260 (описывающий подход «управляемого выбора» для перестановки FR).
[00120] Человеческие каркасные области, которые можно использовать для гуманизации, включают, без ограничения: каркасные области, выбранные с помощью метода «наилучшего соответствия» (см., например, Sims et al. (1993) J. Immunol. 151:2296); каркасные области, полученные из консенсусной последовательности человеческих антител конкретной подгруппы вариабельных областей тяжелой цепи (см., например, Carter et al. (1992) Proc. Natl. Acad. Sci. USA, 89:4285; и Presta et al. (1993) J. Immunol, 151:2623); зрелые (соматически мутировавшие) каркасные области человека или каркасные области зародышевой линии человека (см., например, Almagro and Fransson, (2008) Front. Biosci. 13:1619-1633); и каркасные области, полученные в результате скрининга библиотек FR (см., например, Baca et al., (1997) J. Biol. Chem. 272:10678-10684 и Rosok et al., (1996) J. Biol. Chem. 271:22611-22618). Обычно области VHH FR заменяют областями FR человека, с получением гуманизированного VHH. В некоторых вариантах осуществления некоторые остатки FR человеческого FR заменены для улучшения одного или более свойств гуманизированного VHH. Домены VHH с такими замененными остатками все еще называют в настоящем описании «гуманизированными».
[00121] В некоторых вариантах осуществления, домен VHH, который связывается с OX40, содержит CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12; и каркасную область 2 (FR2), содержащую аминокислотную последовательность SEQ ID NO: 22. В некоторых вариантах осуществления домен VHH дополнительно содержит FR3, содержащую аминокислотную последовательность SEQ ID NO: 23.
[00122] В некоторых вариантах осуществления OX40-связывающий полипептид содержит по меньшей мере один домен VHH, содержащий аминокислотную последовательность SEQ ID NO: 9. В некоторых вариантах осуществления OX40-связывающий полипептид содержит один, два, три или четыре домена VHH, содержащих аминокислотную последовательность SEQ ID NO: 9.
[00123] В некоторых вариантах осуществления OX40-связывающий полипептид содержит три домена VHH, которые связываются с OX40, и Fc-домен. В некоторых таких вариантах осуществления каждый домен VHH содержит CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12. В некоторых вариантах осуществления каждый домен VHH содержит CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12; и каркасную область 2 (FR2), содержащую аминокислотную последовательность SEQ ID NO: 22. В некоторых вариантах осуществления каждый домен VHH дополнительно содержит FR3, содержащую аминокислотную последовательность SEQ ID NO: 23. В некоторых вариантах осуществления каждый домен VHH содержит аминокислотную последовательность SEQ ID NO: 9.
[00124] В различных вариантах осуществления Fc-домен, включенный в OX40-связывающий полипептид представляет собой Fc-домен человека или происходит из Fc-домена человека.
[00125] В некоторых вариантах осуществления Fc-домен, включенный в OX40-связывающий полипептид происходит из Fc-домена человека и содержит делецию трех аминокислот в нижнем шарнире, соответствующих E233, L234 и L235 в IgG1, и упоминается в настоящем описании как «xELL Fc». Полипептиды xELL Fc не взаимодействуют с FcγR и, таким образом, называются «молчащими эффекторами» или «нулевыми эффекторами», однако в некоторых вариантах осуществления xELL Fc-домены связываются с FcRn и, следовательно, имеют увеличенный период полувыведения и трансцитоз, связанный с FcRn-опосредованной рециркуляцией.
[00126] В некоторых вариантах осуществления Fc-домен, включенный в OX40-связывающий полипептид происходит из Fc-домена человека и содержит мутации M252Y и M428V, упоминаемый в настоящем описании как «Fc-YV». В некоторых вариантах осуществления такие мутации усиливают связывание с FcRn при кислом pH эндосомы (примерно 6,5), при этом теряя детектируемое связывание при нейтральном pH (примерно 7,2), что обеспечивает усиленный FcRn-опосредованную рециркуляцию и увеличенный период полувыведения.
[00127] В некоторых вариантах осуществления Fc-домен, включенный в OX40-связывающий полипептид, происходит из человеческого Fc-домена и содержит мутации, предназначенные для гетеродимеризации, называемые в настоящем описании «выступом» и «впадиной». В некоторых вариантах осуществления Fc-домен с «выступом» содержит мутацию T366W. В некоторых вариантах осуществления Fc-домен со «впадиной» содержит мутации T366S, L368A и Y407V. В некоторых вариантах осуществления Fc-домены, используемые для гетеродимеризации, содержат дополнительные мутации, такие как мутация S354C в первом члене гетеродимерной пары Fc, которая образует асимметричный дисульфид с соответствующей мутацией Y349C во втором члене гетеродимерной пары Fc. В некоторых вариантах осуществления один член гетеродимерной пары Fc содержит модификацию H435R или H435K для предотвращения связывания с белком A, сохраняя при этом связывание с FcRn. В некоторых вариантах осуществления один член гетеродимерной пары Fc содержит модификацию H435R или H435K, в то время как второй член гетеродимерной пары Fc не модифицирован по H435. В различных вариантах осуществления удерживающий Fc-домен содержит модификацию H435R или H435K (в некоторых случаях называемую «впадина-R», когда модификация представляет собой H435R), в то время как Fc-домен с выступом не содержит. В некоторых случаях мутация впадина-R улучшает очистку гетеродимера по сравнению с гомодимерными Fc-доменами со впадиной, присутствие которых возможно.
[00128] Неограничивающие иллюстративные Fc-домены, которые могут использоваться в OX40-связывающем полипептиде, включают Fc-домены, содержащие аминокислотные последовательности SEQ ID NO: 25 и 26.
[00129] В некоторых вариантах осуществления OX40-связывающий полипептид, который содержит три домена VHH и Fc-домен, содержит аминокислотную последовательность SEQ ID NO: 14 и Fc-домен, слитый с С-концом этой аминокислотной последовательности. В некоторых вариантах осуществления OX40-связывающий полипептид, содержащий три домена VHH и Fc-домен, содержит аминокислотную последовательность SEQ ID NO: 15. В некоторых вариантах осуществления OX40-связывающий полипептид состоит из аминокислотной последовательности SEQ ID NO: 15.
Примеры видов активности OX40-связывающих полипептидов
[00130] В различных вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды являются агонистами активности OX40. В некоторых вариантах осуществления агонистическая активность может быть определена с помощью способов, представленных в настоящем описании в примерах, таких как использование репортерных клеток Jurkat/OX40 или подобных клеток.
[00131] В некоторых вариантах осуществления OX40-связывающие полипептиды, представленные в настоящем описании, усиливают пролиферацию CD4+ и/или CD8+ Т-клеток in vitro и/или in vivo. В некоторых вариантах осуществления предлагаемый в настоящем описании OX40-связывающий полипептид усиливает пролиферацию CD4+ и/или CD8+ Т-клеток in vitro. В некоторых вариантах осуществления OX40-связывающий полипептид усиливает пролиферацию CD4+ и/или CD8+ Т-клеток по меньшей мере в 1,5 или по меньшей мере в 2 раза. Усиление пролиферации CD4+ и/или CD8+ Т-клеток может быть определено любым способом в данной области, таким как, например, способы, представленные в настоящем описании в примерах. Неограничивающий иллюстративный анализ заключается в следующем. CD4+ и/или CD8+ Т-клетки могут быть получены от одного или более здоровых доноров-людей и окрашены CellTrace Violet (CTV). Затем Т-клетки костимулируют анти-CD3 антителом и OX40-связывающим полипептидом, после чего анализируют с помощью FACS. Отсутствие окрашивания CTV указывает на пролиферацию. В некоторых вариантах осуществления усиление пролиферации CD4+ и/или CD8+ Т-клеток определяют как среднее значение для серии экспериментов или объединенных Т-клеток, например, путем измерения пролиферации CD4+ и/или CD8+ Т-клеток, полученных от разных здоровых доноров-людей. В некоторых вариантах осуществления усиление пролиферации CD4+ и/или CD8+ Т-клеток определяют как среднее значение экспериментов, проведенных с использованием Т-клеток, полученных от меньшей мере пяти или по меньшей мере десяти разных здоровых доноров, или из пула Т-клеток, полученных от по меньшей мере пяти или по меньшей мере десяти разных здоровых доноров. В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды усиливают пролиферацию CD4+ и/или CD8+ Т-клеток даже в присутствии Treg-клеток.
[00132] В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды усиливают экспрессию CD25 на CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo. Экспрессия CD25 указывает на активацию Т-клеток. В некоторых вариантах осуществления предлагаемый в настоящем описании OX40-связывающий полипептид усиливает экспрессию CD25 на CD4+ и/или CD8+ Т-клетках in vitro. В некоторых вариантах осуществления OX40-связывающий полипептид усиливает экспрессию CD25 на CD4+ и/или CD8+ Т-клетках по меньшей мере в 1,5 или по меньшей мере в 2 раза. Усиление экспрессии CD25 на CD4+ и/или CD8+ Т-клетках может быть определено любым способом в данной области, таким как, например, способы, представленные в настоящем описании в примерах. Неограничивающий иллюстративный анализ заключается в следующем. CD4+ и/или CD8+ Т-клетки могут быть получены от одного или более здоровых доноров-людей и костимулированы анти-CD3 антителом и OX40-связывающим полипептидом, и затем проанализированы с помощью FACS на экспрессию CD25. В некоторых вариантах осуществления усиление экспрессии CD25 при пролиферации CD4+ и/или CD8+ Т-клеток определяют как среднее значение серии экспериментов или объединенных Т-клеток, например, путем измерения экспрессии CD25 на CD4+ и/или CD8+ Т-клетках, полученных от разных здоровых доноров. В некоторых вариантах осуществления усиление экспрессии CD25 на CD4+ и/или CD8+ Т-клетках определяют как среднее значение экспериментов, проведенных с использованием Т-клеток, полученных от по меньшей мере пяти или по меньшей мере десяти разных здоровых доноров, или из пула Т-клеток, полученных от по меньшей мере пяти или десяти разных здоровых доноров. В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды увеличивают экспрессию CD25 на CD4+ и/или CD8+ Т-клетках даже в присутствии Treg-клеток.
[00133] В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды усиливают экспрессию CD71 на CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo. Экспрессия CD71 указывает на активацию Т-клеток. В некоторых вариантах осуществления предлагаемый в настоящем описании OX40-связывающий полипептид усиливает экспрессию CD71 на CD4+ и/или CD8+ Т-клетках in vitro. В некоторых вариантах осуществления OX40-связывающий полипептид усиливает экспрессию CD71 на CD4+ и/или CD8+ Т-клетках по меньшей мере в 1,5 или по меньшей мере в 2 раза. Усиление экспрессии CD71 на CD4+ и/или CD8+ Т-клетках может быть определено любым способом, известным в данной области, таким как, например способы, представленные в настоящем описании в примерах. Неограничивающий иллюстративный анализ заключается в следующем. CD4+ и/или CD8+ Т-клетки могут быть получены от одного или более здоровых доноров-людей и костимулированы анти-CD3-антителом и OX40-связывающим полипептидом, и затем проанализированы с помощью FACS на экспрессию CD71. В некоторых вариантах осуществления усиление экспрессии CD71 при пролиферации CD4+ и/или CD8+ Т-клеток определяют как среднее значение серии экспериментов или объединенных Т-клеток, например, путем измерения экспрессии CD71 на CD4+ и/или CD8+ Т-клетках, полученных от разных здоровых доноров. В некоторых вариантах осуществления усиление экспрессии CD71 на CD4+ и/или CD8+ Т-клетках определяют как среднее значение экспериментов, проведенных с использованием Т-клеток, полученных от по меньшей мере пяти или по меньшей мере десяти разных здоровых доноров, или пула Т-клеток, полученных от по меньшей мере пяти или десяти разных здоровых доноров. В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды усиливают экспрессию CD71 на CD4+ и/или CD8+ Т-клетках даже в присутствии Treg-клеток.
[00134] В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды усиливают экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo. Экспрессия IFNγ указывает на активацию Т-клеток. В некоторых вариантах осуществления предлагаемый в настоящем описании OX40-связывающий полипептид усиливает экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках in vitro. В некоторых вариантах осуществления OX40-связывающий полипептид усиливает экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках по меньшей мере в 1,5 раза, по меньшей мере в 2 раза, по меньшей мере в 3 раза или по меньшей мере в 5 раз. Усиление экспрессии IFNγ в CD4+ и/или CD8+ Т-клетках может быть определено любым способом в данной области, таким как, например, способы, представленные в примерах в настоящем описании. Неограничивающий иллюстративный анализ заключается в следующем. CD4+ и/или CD8+ Т-клетки могут быть получены от одного или более здоровых доноров-людей и костимулированы анти-CD3 антителом и OX40-связывающим полипептидом. Для определения внутриклеточной экспрессии IFNγ клетки осаждают и маркируют поверхность детектируемыми анти-CD4 и анти-CD8 антителами. Затем клетки фиксируют и пермеаблизируют, после чего окрашивают детектируемым анти-IFNγ антителом. Затем IFNγ+ CD4+ или IFNγ+ CD8+ клетки детектируют с помощью FACS. В некоторых вариантах осуществления увеличение экспрессии IFNγ при пролиферации CD4+ и/или CD8+ Т-клеток определяют как среднее значение серии экспериментов или объединенных Т-клеток, например, путем измерения экспрессии IFNγ в CD4+ и/или CD8+ Т-клетках, полученных от разных здоровых доноров. В некоторых вариантах осуществления усиление экспрессии IFNγ в CD4+ и/или CD8+ Т-клетках определяют как среднее значение экспериментов, проведенных с использованием Т-клеток, полученных от по меньшей мере пяти или по меньшей мере десяти разных здоровых доноров, или пула Т-клеток, полученных от по меньшей мере пяти или десяти разных здоровых доноров. В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды усиливают экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках даже в присутствии Treg-клеток.
[00135] В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды снижают или ослабляют супрессивную активность регуляторных Т-клеток (Treg). В некоторых вариантах осуществления OX40-связывающий полипептид снижает супрессивную активность Treg в отношении CD4+ и/или CD8+ Т-клеток на по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 30% или по меньшей мере 50%. Снижение супрессивной активности Treg в отношении обычных CD4+ и/или CD8+ Т-клеток может быть определено любым методом в данной области, таким как, например способы, представленные в настоящем описании в примерах. Неограничивающий иллюстративный анализ заключается в следующем. Treg и CD4+ T-клетки метят разными флуоресцентными красителями клеточной пролиферации после их выделения из PBMC здорового человека. CD4+ T-клетки стимулируют анти-CD3-антителами, и Treg-клетки инкубируют в присутствии OX40-связывающих полипептидов, представленных в настоящем описании. Две популяции Т-клеток культивируют совместно в течение 3 дней, и пролиферацию и активацию CD4+ Т-клеток отслеживают с помощью проточной цитометрии. В некоторых вариантах осуществления предлагаемые в настоящем описании OX40-связывающие полипептиды усиливают активацию и пролиферацию CD4+ и/или CD8+ Т-клеток в присутствии Treg-клеток, например, по сравнению с активацией и пролиферацией CD4+ и/или CD8+ Т-клеток в присутствии Treg-клеток, но в отсутствие OX40-связывающего полипептида, представленного в настоящем описании.
[0134] В некоторых вариантах осуществления OX40-связывающий полипептид является поливалентным, содержащим более одного OX40-связывающего домена. В различных вариантах осуществления OX40-связывающий полипептид содержит два, три, четыре, пять, шесть, семь или восемь OX40-связывающих доменов. В некоторых таких вариантах осуществления по меньшей мере один или все OX40-связывающие домены являются одинаковыми. В некоторых таких вариантах осуществления все OX40-связывающие домены содержат CDR1, CDR2 и CDR3 из 1D10v6 (SEQ ID NO: 10, 11 и 12, соответственно). В некоторых вариантах осуществления по меньшей мере один или все OX40-связывающие домены содержат VHH из 1D10v6 (SEQ ID NO: 9). В некоторых вариантах осуществления по меньшей мере один OX40-связывающий домен содержит CDR или VHH из 1D10v6, и по меньшей мере один OX40-связывающий домен не содержит CDR или VHH из 1D10v6. В некоторых вариантах осуществления OX40-связывающий полипептид является полиспецифическим, содержащим по меньшей мере один домен, который связывается с OX40, и по меньшей мере один домен, который связывается с другим антигеном. В некоторых вариантах осуществления второй антиген выбирают из PD1, PDL1, CTLA4, TIGIT, LAG3, VISTA, gpNMB, B7H3, B7H4, HHLA2, CD73, CD39, 41BB, GITR, CD28, ICOS, HVEM, 5T4, интегрина альфа-4, интегрина альфа-V, интегрина альфа4бета1, интегрина альфа4бета7, AGR2, анти-Lewis-Y, рецептора апелина J, APRIL, B7-H3, B7-H4, B7-H6, BAFF, BTLA, комплемента C5, C-242, CA9, CA19-9, (Lewis а), карбоангидразы 9, CD2, CD3, CD6, CD9, CD11a, CD19, CD20, CD22, CD24, CD25, CD27, CD28, CD30, CD33, CD38, CD40, CD40L, CD41, CD44, CD44v6, CD47, CD51, CD52, CD56, CD64, CD70, CD71, CD74, CD80, CD81, CD86, CD95, CD117, CD123, CD125, CD132, (IL-2RG), CD133, CD138, CD166, CD172A, CD248, CDH6, CEACAM5 (CEA), CEACAM6 (NCA-90), CLAUDIN-3, CLAUDIN-4, cMet, коллагена, Cripto, CSFR, CSFR-1, CTLA-4, CTGF, CXCL10, CXCL13, CXCR1, CXCR2, CXCR4, CYR61, DL44, DLK1, DLL3, DLL4, DPP-4, DSG1, EDA, EDB, EGFR, EGFRviii, рецептора эндотелина B (ETBR), ENPP3, EpCAM, EPHA2, EPHB2, ERBB3, F-белка RSV, FAP, FGF-2, FGF8, FGFR1, FGFR2, FGF R3, FGFR4, экстрадомена B фибронектина (EDB), FLT-3, рецептора фолиевой кислоты альфа (FRα), GAL3ST1, G-CSF, G-CSFR, GD2, GITR, GLUT1, GLUT4, GM-CSF, GM-CSFR, рецепторов GP IIb/IIIa, Gp130, GPIIB/IIIA, GPNMB, GRP78, HER2/neu, HER3, HER4, HGF, hGH, HVEM, гиалуронидазы, IFN-альфа, IFN-бета, IFN-гамма, IgE, рецептора IgE (FceRI), IGF, IL1B, IL1R, IL2, IL11, IL12, IL12p40, IL-12R, IL-12R-бета1, IL13, IL13R, IL15, IL17, IL18, IL21, IL23, IL23R, IL27/IL27R (wsx1), IL29, IL-31R, IL31/IL31R, IL2R, IL4, IL4R, IL6, IL6R, рецептора инсулина, лигандов Jagged, Jagged 1, Jagged 2, KISS1-R, LAG-3, LIF-R, Lewis X, LIGHT, LRP4, LRRC26, Ly6G6D, LyPD1, MCSP, мезотелина, MRP4, MUC1, Муцина-16 (MUC16, CA-125), Na/K-АТФазы, NGF, Нектина 4, никастрина, рецепторов Notch, Notch 1, Notch 2, Notch 3, Notch 4, NOV, OSM-R, OX-40, PAR2, PDGF-AA, PDGF-BB, PDGFR-альфа, PDGFR-бета, PD-1, PD-L1, PD-L2, фосфатидилсерина, P1GF, PSCA, PSMA, PSGR, RAAG12, RAGE, SLC44A4, сфингозин-1 Фосфата, STEAP1, STEAP2, TAG-72, TAPA1, TEM-8, TGF-бета, TIGIT, TIM-3, TLR2, TLR4, TLR6, TLR7, TLR8, TLR9, TMEM31, TNF-альфа, TNFR, TNFRS12A, TRAIL-R1, TRAIL-R2, трансферрина, рецептора трансферрина, TRK-A, TRK-B, uPAR, VAP1, VCAM-1, VEGF, VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGFR1, VEGFR2, VEGFR3, VISTA, WISP-1, WISP-2 и WISP-3. В некоторых вариантах осуществления по меньшей мере один связывающий домен, который связывается со вторым антигеном, является антагонистом или агонистом. В некоторых вариантах осуществления по меньшей мере один связывающий домен, который связывается со вторым антигеном, представляет собой домен VHH.
[0135] В настоящем описании представлены сконструированные клетки, которые экспрессируют OX40-связывающий полипептид, представленный в настоящем описании. В некоторых вариантах осуществления OX40-связывающий полипептид секретируется из клетки. В некоторых вариантах осуществления OX40-связывающий полипептид включает сигнальный пептид, например, сигнальный пептид антитела или другую сигнальную последовательность, которая вызывает секрецию полипептида клеткой. Сигнальный пептид или часть сигнального пептида может быть отщеплена от полипептида, когда он секретируется. В некоторых вариантах осуществления OX40-связывающий полипептид может кодироваться нуклеиновой кислотой в клетке, и затем экспрессироваться и секретироваться клеткой. Нуклеиновая кислота обычно содержит подходящие регуляторные последовательности (такие как, например, промоторы и/или энхансеры) для экспрессии в требуемых условиях. Нуклеиновая кислота может быть включена в геном клетки или может присутствовать в виде внегеномной нуклеиновой кислоты. В некоторых вариантах осуществления клетка представляет собой иммунную клетку, такую как, например, первичная иммунная клетка.
[0136] В некоторых вариантах осуществления OX40-связывающий полипептид представляет собой химерный антигенный рецептор (CAR). CAR представляют собой синтетические рецепторы, обычно содержащие внеклеточный нацеливающий или связывающий фрагмент, такой как антигенсвязывающий домен, трансмембранный домен и один или более сигнальных доменов в слитой молекуле, которая экспрессируется на поверхности клетки, такой как Т-клетка. Таким образом, CAR объединяют в одной молекуле антиген-специфичность и свойства активации Т-клеток. CAR первого поколения обычно включают цитоплазматическую область γ-цепи рецептора CD3-дзета или Fc1 в качестве своего сигнального домена. CAR первого поколения были протестированы в фазе I клинических исследований у пациентов с раком яичников, раком почек, лимфомой и нейробластомой, где они вызвали умеренный ответ (обзор Sadelain et al., Curr Opin Immunol, 21(2):215-223, 2009). CAR второго поколения, которые содержат сигнальные домены костимулирующей молекулы, такой как CD28 и CD3-дзета, обеспечивают двойную сигнализацию для направления комбинированных активирующего и костимулирующего сигналов. CAR третьего поколения являются более сложными и содержат три или более сигнальных домена (см. обзор в Sadelain et al., Cancer Discovery (3), 388-398, 2013 и Dotti et al, Immuno. Rev, 257(1), 1-36, 2014).
[0137] В некоторых вариантах осуществления внеклеточный связывающий фрагмент CAR включает один или более связывающих доменов, таких как домены VHH, которые связываются с OX40. В некоторых вариантах осуществления внеклеточный связывающий фрагмент является поливалентным и содержит более одного связывающего домена, который связывается с OX40. В различных вариантах осуществления внеклеточный связывающий фрагмент содержит два, три, четыре, пять, шесть, семь или восемь OX40-связывающих доменов. В некоторых таких вариантах осуществления по меньшей мере один или все OX40-связывающие домены одинаковы. В некоторых таких вариантах осуществления все OX40-связывающие домены содержат CDR1, CDR2 и CDR3 из 1D10v6 (SEQ ID NO: 10, 11 и 12, соответственно). В некоторых вариантах осуществления по меньшей мере один или все OX40-связывающие домены содержат VHH из 1D10v6 (SEQ ID NO: 9). В некоторых вариантах осуществления по меньшей мере один OX40-связывающий домен содержит CDR или VHH из 1D10v6, и по меньшей мере один OX40-связывающий домен не содержит CDR или VHH из 1D10v6. В некоторых вариантах осуществления внеклеточный связывающий фрагмент является полиспецифическим, содержащим по меньшей мере один домен, который связывается с OX40, и по меньшей мере один домен, который связывается с другим антигеном. В некоторых вариантах осуществления второй антиген выбирают из PD1, PDL1, CTLA4, TIGIT, LAG3, VISTA, gpNMB, B7H3, B7H4, HHLA2, CD73, CD39, 41BB, GITR, CD28, ICOS, HVEM, 5T4, интегрина альфа-4, интегрина альфа-V, интегрина альфа4бета1, интегрина альфа4бета7, AGR2, анти-Lewis-Y, рецептора апелина J, APRIL, B7-H3, B7-H4, B7-H6, BAFF, BTLA, комплемента C5, C-242, CA9, CA19-9, (Lewis а), карбоангидразы 9, CD2, CD3, CD6, CD9, CD11a, CD19, CD20, CD22, CD24, CD25, CD27, CD28, CD30, CD33, CD38, CD40, CD40L, CD41, CD44, CD44v6, CD47, CD51, CD52, CD56, CD64, CD70, CD71, CD74, CD80, CD81, CD86, CD95, CD117, CD123, CD125, CD132, (IL-2RG), CD133, CD138, CD166, CD172A, CD248, CDH6, CEACAM5 (CEA), CEACAM6 (NCA-90), CLAUDIN-3, CLAUDIN-4, cMet, коллагена, Cripto, CSFR, CSFR-1, CTLA-4, CTGF, CXCL10, CXCL13, CXCR1, CXCR2, CXCR4, CYR61, DL44, DLK1, DLL3, DLL4, DPP-4, DSG1, EDA, EDB, EGFR, EGFRviii, рецептора эндотелина B (ETBR), ENPP3, EpCAM, EPHA2, EPHB2, ERBB3, белок F RSV, FAP, FGF-2, FGF8, FGFR1, FGFR2, FGF R3, FGFR4, экстрадомена B фибронектина (EDB), FLT-3, рецептора фолиевой кислоты альфа (FRα), GAL3ST1, G-CSF, G-CSFR, GD2, GITR, GLUT1, GLUT4, GM-CSF, GM-CSFR, рецепторов GP IIb/IIIa, Gp130, GPIIB/IIIA, GPNMB, GRP78, HER2/neu, HER3, HER4, HGF, hGH, HVEM, гиалуронидазы, IFN-альфа, IFN-бета, IFN-гамма, IgE, рецептора IgE (FceRI), IGF, IL1B, IL1R, IL2, IL11, IL12, IL12p40, IL-12R, IL-12R-бета1, IL13, IL13R, IL15, IL17, IL18, IL21, IL23, IL23R, IL27/IL27R (wsx1), IL29, IL-31R, IL31/IL31R, IL2R, IL4, IL4R, IL6, IL6R, рецептора инсулина, лигандов Jagged, Jagged 1, Jagged 2, KISS1-R, LAG-3, LIF-R, Lewis X, LIGHT, LRP4, LRRC26, Ly6G6D, LyPD1, MCSP, мезотелина, MRP4, MUC1, муцина-16 (MUC16, CA-125), Na/K-АТФазы, NGF, Нектина 4, никастрина, рецепторов Notch, Notch 1, Notch 2, Notch 3, Notch 4, NOV, OSM-R, OX-40, PAR2, PDGF-AA, PDGF-BB, PDGFR-альфа, PDGFR-бета, PD-1, PD-L1, PD-L2, фосфатидилсерина, P1GF, PSCA, PSMA, PSGR, RAAG12, RAGE, SLC44A4, сфингозин-1 фосфата, STEAP1, STEAP2, TAG-72, TAPA1, TEM-8, TGF-бета, TIGIT, TIM-3, TLR2, TLR4, TLR6, TLR7, TLR8, TLR9, TMEM31, TNF-альфа, TNFR, TNFRS12A, TRAIL-R1, TRAIL-R2, трансферрина, рецептора трансферрина, TRK-A, TRK-B, uPAR, VAP1, VCAM-1, VEGF, VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGFR1, VEGFR2, VEGFR3, VISTA, WISP-1, WISP-2 и WISP-3. В некоторых вариантах осуществления один или более антигенсвязывающих доменов внеклеточного связывающего фрагмента представляют собой scFv или VHH. В некоторых вариантах осуществления внеклеточный связывающий фрагмент связывается или способен связываться с антигеном-мишенью с достаточной аффинностью, такой, что CAR может быть полезным в терапии, например, для нацеливания на клетку или ткань, экспрессирующую антиген-мишень.
[0138] Трансмембранный домен CAR представляет собой домен, который обычно пересекает или способен пересекать или простираться сквозь плазматическую мембрану и связан, прямо или косвенно (например, через спейсер, такой как шарнирная последовательность иммуноглобулина) с внеклеточным антигенсвязывающим доменом и эндоплазматическим участком, содержащим внутриклеточный сигнальный домен. В некоторых вариантах осуществления трансмембранный домен CAR представляет собой трансмембранную область трансмембранного белка (например, трансмембранных белков типа I), искусственную гидрофобную последовательность или их комбинации. В некоторых вариантах осуществления трансмембранный домен включает домен CD3-дзета или трансмембранный домен CD28. Другие трансмембранные домены будут очевидны специалистам в данной области и могут быть использованы в связи с вариантами осуществления CAR, представленными в настоящем описании.
[0139] Внутриклеточная сигнальная область CAR, представленная в настоящем описании, содержит один или более внутриклеточных сигнальных доменов, которые передают сигнал Т-клетке при задействовании антигенсвязывающего домена CAR, например при связывании с антигеном. В некоторых вариантах осуществления внутриклеточная область содержит внутриклеточный сигнальный домен, который является или содержит сигнальный домен ITAM. Типичные внутриклеточные сигнальные домены включают, например, сигнальный домен, полученный из ζ-цепи комплекса Т-клеточного рецептора или любого из его гомологов (например, η-цепи, FcsRIy и β-цепей, MB 1 (Iga) цепи, B29 (Ig) цепи и т.д.), CD3-цепи человека, полипептидов CD3 (Δ, δ и ε), тирозинкиназы семейства syk (Syk, ZAP 70 и т.д.), тирозинкиназы семейства src (Lck, Fyn, Lyn и т.д.) и других молекул, участвующих в трансдукции Т-клеток, таких как CD2, CD5, OX40 и CD28. В конкретных вариантах осуществления внутриклеточная сигнальная область содержит внутриклеточный сигнальный домен, полученный из дзета-цепи CD3 человека.
[0140] В некоторых вариантах осуществления эндодомен содержит сигнальный домен CD3-дзета. В некоторых вариантах осуществления сигнальный домен CD3-дзета содержит последовательность аминокислот, приведенную в SEQ ID NO: 27, или последовательность аминокислот, которая имеет по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более идентичности последовательности с SEQ ID NO: 27 и сохраняет активность передачи сигналов Т-клеткам.
[0141] В некоторых вариантах осуществления внутриклеточная сигнальная область CAR может дополнительно содержать внутриклеточный сигнальный домен, полученный из костимулирующей молекулы. В таких примерах такой сигнальный домен может усиливать активность CAR-T-клеток, например, за счет увеличения пролиферации, выживания и/или развития клеток памяти, после антиген-специфического взаимодействия, например, по сравнению с CAR, который содержит только ITAM содержащий сигнальный домен, например CD3-дзета. В некоторых вариантах осуществления костимулирующий домен представляет собой функциональный сигнальный домен, полученный из белка, выбранного из: CD28, CD137 (4-IBB), CD134 (OX40), DapIO, CD27, CD2, CD5, ICAM-1, LFA-1 (CD1a/CD18), Lck, TNFR-I, TNFR-II, Fas, CD30, CD40 или их комбинации. В конкретных вариантах осуществления костимулирующий сигнальный домен происходит или получен из человеческого белка. В некоторых аспектах костимулирующий сигнальный домен происходит или получен из CD28 человека или CD137 человека (4-IBB).
[0142] В некоторых вариантах осуществления костимулирующий сигнальный домен происходит от CD28 или 4-1BB и включает аминокислотную последовательность, приведенную в любой из SEQ ID NO: 28-31, или аминокислотную последовательность, которая имеет по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более идентичности последовательности с SEQ ID NO: 28-31 и сохраняет активность передачи костимулирующих сигналов Т-клеткам.
[0143] В некоторых вариантах осуществления CAR дополнительно содержит шарнирную или спейсерную область, которая соединяет внеклеточный антигенсвязывающий домен и трансмембранный домен. Эта шарнирная или спейсерная область может использоваться для получения различной длины и гибкости получаемого CAR. Примеры шарнирной или спейсерной области, которые можно использовать, включают, без ограничения, Fc-фрагменты антител или их фрагменты или производные, шарнирные области антител или их фрагменты или производные, области CH2 антител, области CH3 антител, искусственные спейсерные последовательности, например пептидные последовательности или их комбинации. Другие шарнирные или спейсерные области будут очевидны специалистам в данной области техники и могут быть использованы. В одном из вариантов осуществления шарнир представляет собой шарнир lgG4 или шарнир CD8A.
[0144] В некоторых вариантах осуществления спейсер и трансмембранный домен представляют собой шарнир и трансмембранный домен, полученный из CD8, например, имеющий иллюстративную последовательность, приведенную в SEQ ID NO: 32-34, или аминокислотную последовательность, которая имеет по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 32-34.
[0145] В настоящем описании также представлены выделенные нуклеиновые кислоты, содержащие полинуклеотид, кодирующий CAR, содержащий OX40-связывающий полипептид, представленный в настоящем описании. В некоторых вариантах осуществления первая нуклеиновая кислота, кодирующая CAR, отделена от второй нуклеиновой кислоты, кодирующей OX40-связывающий полипептид, бицистронным элементом, таким как IRES или последовательностью пропуска рибосомы (например, T2A или P2A). В некоторых аспектах конструкция представляет собой вектор экспрессии для экспрессии OX40-связывающего полипептида и/или CAR в клетке. Вектор экспрессии может быть вирусным вектором. Технология вирусных векторов хорошо известна в данной области и описана, например, в Sambrook et al. (Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 2013). Для переноса генов в клетки млекопитающих разработан ряд вирусных систем. Например, используются ретровирусы, такие как аденовирусные векторы. В одном из вариантов осуществления используется лентивирусный вектор.
[0146] В дополнительном аспекте также предоставлена выделенная клетка или популяция клеток, содержащая одну или более конструкций нуклеиновых кислот, описанных выше. Также предоставлена выделенная клетка или популяция клеток, которые являются генетически модифицированными для экспрессии OX40-связывающего полипептида и/или CAR, представленных в настоящем описании. Таким образом, в настоящем описании представлены сконструированные клетки, которые содержат и могут стабильно экспрессировать CAR, представленный в настоящем описании. В одном из вариантов осуществления клетку выбирают из Т-клетки, естественной киллерной (NK) клетки, цитотоксического Т-лимфоцита (CTL), регуляторной Т-клетки, гемопоэтической стволовой клетки и/или плюрипотентной эмбриональной/индуцированной стволовой клетки. В некоторых случаях клетка является Т-клеткой, например CD4+ и/или CD8+ Т-клеткой. В некоторых вариантах осуществления клетки являются аутологичными по отношению к субъекту. Например, в некоторых вариантах осуществления Т-клетки могут быть получены от пациента (также называемые первичными Т-клетками) для инженерии, например трансфекции или трансдукции конструкцией нуклеиновой кислоты CAR.
[0147] В типичном способе первичные Т-клетки могут быть очищены ex vivo (клетки CD4+ или клетки CD8+, или и те, и другие) и стимулированы агонистами TCR/CD28, такими как гранулы, покрытые анти-CD3/анти-CD28 антителами. После 2-х или 3-х дневного процесса активации рекомбинантный вектор экспрессии, кодирующий CAR, может быть стабильно введен в первичные Т-клетки с помощью стандартных протоколов трансдукции лентивирусным или ретровирусным вектором или стратегий плазмидной электропорации. Секрецию OX40-связывающего полипептида и/или экспрессию CAR в клетках можно отслеживать, например, с помощью проточной цитометрии с использованием антиэпитопной метки или антител, которые перекрестно реагируют с нативной родительской молекулой. Т-клетки, которые экспрессируют CAR, могут быть обогащены путем сортинга с помощью антител к эпитопным меткам или для получения высокого или низкого уровня экспрессии в зависимости от применения.
[0148] OX40-связывающие полипептиды и/или сконструированные CAR Т-клетки могут быть проанализированы на наличие соответствующей функции различными способами. В некоторых случаях для оценки функции сконструированных Т-клеток могут быть использованы in vitro анализы цитотоксичности, пролиферации, анализы OX40 с использованием репортера или цитокиновые анализы (например, экспрессия IFN-гамма, IL-2, TNFα). Типичные стандартные конечные точки представляют собой процент лизиса опухолевой линии, пролиферация сконструированных Т-клеток или экспрессия белка IFN-гамма в супернатанте культуры. В некоторых случаях способность стимулировать активацию Т-клеток при стимуляции CAR, например через антиген, можно оценивать, например, путем мониторинга экспрессии маркеров активации, таких как CD69, CD44 или CD62L, пролиферации и/или продуцирования цитокинов.
[0149] В настоящем описании также представлены способы профилактики и/или лечения заболевания или состояния у субъекта, такого как рак, которые включают введение субъекту сконструированных клеток, представленных в настоящем описании. Как правило, субъект нуждается в лечении заболевания или состояния фармацевтически активным количеством клеток и/или фармацевтической композиции по изобретению. В некоторых вариантах осуществления в процессе лечения используются клетки, которые экспрессируют и секретируют OX40-связывающий полипептид, представленный в настоящем описании. В некоторых вариантах осуществления для лечения используются сконструированные CAR Т-клетки, которые экспрессируют OX40-связывающий полипептид, представленный в настоящем описании.
Экспрессия и продуцирование полипептидов
[00149] Представлены молекулы нуклеиновых кислот, содержащие полинуклеотиды, которые кодируют OX40-связывающий полипептид. Таким образом, в различных вариантах осуществления представлены молекулы нуклеиновых кислот, которые кодируют домен VHH, который связывается с OX40, содержащий CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12. В некоторых вариантах осуществления представлены молекулы нуклеиновых кислот, которые кодируют домен VHH, который связывается с OX40, содержащий CDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, CDR2, содержащую аминокислотную последовательность кислотная последовательность SEQ ID NO: 11, и CDR3, содержащую аминокислотную последовательность SEQ ID NO: 12; и каркасную область 2 (FR2), содержащую аминокислотную последовательность SEQ ID NO: 22. В некоторых вариантах осуществления молекула нуклеиновой кислоты дополнительно кодирует FR3, содержащую аминокислотную последовательность SEQ ID NO: 23. В некоторых вариантах осуществления представлены молекулы нуклеиновых кислот, которые кодируют OX40-связывающий полипептид, содержащий по меньшей мере один, например один, два, три или четыре домена VHH, содержащий аминокислотную последовательность SEQ ID NO: 9. В различных вариантах осуществления молекула нуклеиновой кислоты дополнительно кодирует Fc-домен, такой как Fc-домен SEQ ID NO: 25 или 26. В некоторых вариантах осуществления представлена молекула нуклеиновой кислоты, которая кодирует OX40-связывающий полипептид, который содержит три домена VHH, и Fc-домен содержит аминокислотную последовательность SEQ ID NO: 14, при этом Fc-домен слит с С-концом этой аминокислотной последовательности. В некоторых вариантах осуществления представлена молекула нуклеиновой кислоты, которая кодирует OX40-связывающий полипептид, содержащий аминокислотную последовательность SEQ ID NO: 15 или состоящий из нее. В любом из вышеупомянутых вариантов осуществления молекула нуклеиновой кислоты также может кодировать лидерную последовательность, которая управляет секрецией OX40-связывающего полипептида, причем лидерная последовательность обычно отщепляется и не присутствует в секретируемом полипептиде. Лидерная последовательность может быть лидерной последовательностью нативной тяжелой цепи (или VHH) или может быть другой гетерологичной лидерной последовательностью.
[00150] Молекулы нуклеиновой кислоты могут быть сконструированы методами рекомбинантной ДНК, хорошо известными в данной области техники. В некоторых вариантах осуществления молекула нуклеиновой кислоты представляет собой вектор экспрессии, который подходит для экспрессии в выбранной клетке-хозяине.
[00151] Представлены векторы, содержащие нуклеиновые кислоты, кодирующие OX40-связывающие полипептиды, раскрытые в настоящем описании. Такие векторы включают, без ограничения, ДНК-векторы, фаговые векторы, вирусные векторы, ретровирусные векторы и т.д. В некоторых вариантах осуществления выбирают вектор, который оптимизирован для экспрессии полипептидов в предпочтительном типе клеток, например СНО или СНО-производных клетках, или NSO клетках. Примеры таких векторов описаны, например, в Running Deer et al., Biotechnol. Prog. 20:880-889(2004).
[00152] В некоторых вариантах осуществления OX40-связывающий полипептид может экспрессироваться в прокариотических клетках, таких как бактериальные клетки; или в эукариотических клетках, таких как клетки грибов (таких как дрожжи), клетках растений, клетках насекомых и клетках млекопитающих. Такую экспрессию можно осуществлять, например, согласно процедурам, известным в данной области. Примеры эукариотических клеток, которые можно использовать для экспрессии полипептидов, включают, без ограничения, клетки COS, включая клетки COS 7; клетки 293, включая клетки 293-6E; клетки СНО, включая СНО-S, DG44.CHO Lec13 клетки и клетки CHO FUT8; клетки PER.C6® (Crucell); и клетки НСО. В некоторых вариантах осуществления OX40-связывающие полипептиды могут экспрессироваться в дрожжах. См., например, публикацию США US 2006/0270045 A1. В некоторых вариантах осуществления конкретную эукариотическую клетку-хозяина выбирают, исходя из ее способности осуществлять требуемые посттрансляционные модификации полипептида. Например, в некоторых вариантах осуществления клетки СНО продуцируют полипептиды, которые имеют более высокий уровень сиалирования, чем тот же полипептид, продуцируемый в клетках 293.
[00153] Введение одной или более нуклеиновых кислот (таких как векторы) в нужную клетку-хозяина может быть выполнено любым способом, включая, помимо прочего, трансфекцию фосфатом кальция, трансфекцию, опосредованную DEAE-декстраном, трансфекцию, опосредованную катионными липидами, электропорацию, трансдукцию, инфекцию и т.д. Неограничивающие примеры способов описаны, например, в Sambrook et al., Molecular Cloning, A Laboratory Manual, 3rd ed. Cold Spring Harbor Laboratory Press (2001). Нуклеиновые кислоты можно временно или стабильно трансфицировать в нужные клетки-хозяева любым подходящим способом.
[00154] Также предоставлены клетки-хозяева, содержащие любую из нуклеиновых кислот или векторов, раскрытых в настоящем описании. В некоторых вариантах осуществления представлена клетка-хозяин, которая экспрессирует OX40-связывающий полипептид, раскрытый в настоящем описании. OX40-связывающие полипептиды, экспрессируемые в клетках-хозяевах, могут быть очищены любым подходящим способом. Такие способы включают, без ограничения, использование аффинных матриц или хроматографию гидрофобного взаимодействия. Подходящие аффинные лиганды включают ROR1 ECD и агенты, которые связываются с Fc-областями. Например, для связывания с Fc-областью и для очистки OX40-связывающего полипептида, который содержит Fc-область, можно использовать аффинную колонку с белком A, белком G, белком A/G или антителом. Гидрофобная интерактивная хроматография, например, на бутильной или фенильной колонке, также является подходящей для очистки некоторых полипептидов, таких как антитела. Для очистки некоторых полипептидов, таких как антитела, также может быть подходящей ионообменная хроматография (например, анионообменная хроматография и/или катионообменная хроматография). Для очистки некоторых полипептидов, таких как антитела, также может быть подходящей смешанная хроматография (например, обращенно-фазовая/анионообменная, обращенно-фазовый/катионобменная, гидрофильного взаимодействия/анионообменная, гидрофильного взаимодействия/катионобменная и т.д.). В данной области известны многие методы очистки полипептидов.
[00155] В некоторых вариантах осуществления OX40-связывающий полипептид продуцируют в бесклеточной системе. Неограничивающие примеры бесклеточных систем описаны, например, в Sitaraman et al., Methods Mol. Biol. 498:229-44 (2009); Spirin, Trends Biotechnol. 22:538-45 (2004); Endo et al., Biotechnol. Adv. 21:695-713 (2003).
[00156] В некоторых вариантах осуществления представлены OX40-связывающие полипептиды, полученные описанными выше способами. В некоторых вариантах осуществления OX40-связывающий полипептид получают в клетке-хозяине. В некоторых вариантах осуществления OX40-связывающий полипептид получают в бесклеточной системе. В некоторых вариантах осуществления OX40-связывающий полипептид очищают. В некоторых вариантах осуществления представлена среда для культивирования клеток, содержащая OX40-связывающий полипептид.
[00157] В некоторых вариантах осуществления представлены композиции, содержащие антитела, полученные описанными выше способами. В некоторых вариантах осуществления композиция содержит OX40-связывающий полипептид, полученный в клетке-хозяине. В некоторых вариантах осуществления композиция содержит OX40-связывающий полипептид, полученный в бесклеточной системе. В некоторых вариантах осуществления композиция содержит очищенный OX40-связывающий полипептид.
Примеры способов лечения заболеваний с использованием OX40-связывающих полипептидов
[00158] В некоторых вариантах осуществления изобретение относится к способам лечения заболевания у индивидуума, включающим введение OX40-связывающего полипептида. Такие заболевания включают любое заболевание, в случае которого усиление пролиферации и активации CD4+ и/или CD8+ Т-клеток может обеспечить положительный результат. В некоторых вариантах осуществления изобретение относится к способам лечения рака у человека. Способ включает введение индивидууму эффективного количества OX40-связывающего полипептида, представленного в настоящем описании. Такие способы лечения могут применяться на людях или животных. В некоторых вариантах осуществления изобретение относится к способам лечения людей. Неограничивающие примеры рака, которые можно лечить с помощью OX40-связывающих полипептидов, представленных в настоящем описании, включают базальноклеточную карциному, рак желчных путей; рак мочевого пузыря; рак кости; рак головного мозга и центральной нервной системы; рак молочной железы; рак брюшины; рак шейки матки; хориокарциному; рак толстой и прямой кишки; рак соединительной ткани; рак пищеварительной системы; рак эндометрия; рак пищевода; рак глаза; рак головы и шеи; рак желудка; рак желудочно-кишечного тракта; глиобластому; карциному печени; гепатому; внутриэпителиальное новообразование; рак почек или почечный рак; рак гортани; рак печени; рак легкого; мелкоклеточный рак легкого; немелкоклеточный рак легкого; аденокарциному легкого; плоскоклеточный рак легкого; меланому; миелому; нейробластому; рак полости рта; рак яичников; панкреатический рак; рак простаты; ретинобластому; рабдомиосаркому; рак прямой кишки; рак дыхательной системы; карциному слюнных желез; саркому; рак кожи; плоскоклеточный рак; рак желудка; рак яичек; рак щитовидной железы; рак матки или эндометрия; рак мочевыводящей системы; и рак вульвы; лимфому; лимфому Ходжкина; неходжкинскую лимфому; В-клеточную лимфому; низкой степени злокачественности/фолликулярную неходжкинскую лимфому (НХЛ); НХЛ из малых лимфоцитов (МЛ); средней степени злокачественности/фолликулярную НХЛ; диффузную НХЛ средней степени злокачественности; иммунобластную НХЛ высокой степени злокачественности; НХЛ из мелких нерасщепленных клеток высокой степени злокачественности; массивное поражение НХЛ; лимфому из клеток мантийной зоны; лимфому, связанную со СПИДом; макроглобулинемию Вальденстрема; хронический лимфолейкоз (ХЛЛ); острый лимфобластный лейкоз (ОЛЛ); волосатоклеточный лейкоз; и хронический миелобластный лейкоз.
[00159] OX40-связывающие полипептиды можно вводить субъектам при необходимости. Определение частоты введения может быть выполнено специалистами в данной области, такими как лечащий врач, с учетом состояния, подлежащего лечению, возраста пациента, подлежащего лечению, тяжести состояния, подлежащего лечению, общего состояния здоровья пациента, подлежащего лечению, и т.п. В некоторых вариантах осуществления эффективную дозу OX40-связывающих полипептидов вводят субъекту один или более раз. В некоторых вариантах осуществления эффективную дозу OX40-связывающих полипептидов вводят субъекту ежедневно, каждые две недели, еженедельно, каждые две недели, один раз в месяц и т.д. Эффективную дозу OX40-связывающих полипептидов вводят субъекту по меньшей мере один раз. В некоторых вариантах осуществления эффективную дозу OX40-связывающих полипептидов можно вводить несколько раз, в том числе несколько раз в течение по меньшей мере месяца, по меньшей мере шести месяцев или по меньшей мере года.
[00160] В некоторых вариантах осуществления фармацевтические композиции вводят в количестве, эффективном для лечения (включая профилактику) рака и/или усиления пролиферации Т-клеток. Терапевтически эффективное количество обычно зависит от веса субъекта, подвергаемого лечению, его или ее физического состояния или состояния здоровья, степени распространенности состояния, подлежащего лечению, или возраста субъекта, подвергаемого лечению. Обычно антитела можно вводить в количестве от примерно 0,05 мг/кг массы тела до примерно 100 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 10 мкг/кг массы тела до примерно 100 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 50 мкг/кг массы тела до примерно 5 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 100 мкг/кг массы тела до примерно 10 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 100 мкг/кг массы тела до примерно 20 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 0,5 мг/кг массы тела до примерно 20 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 0,5 мг/кг массы тела до примерно 10 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 0,05 мг/кг массы тела до примерно 20 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве от примерно 0,05 мг/кг массы тела до примерно 10 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела можно вводить в количестве в диапазоне примерно 5 мг/кг массы тела или менее, например, менее 4, менее 3, менее 2 или менее 1 мг/кг антитела.
[00161] В некоторых вариантах осуществления OX40-связывающие полипептиды можно вводить in vivo различными путями, включая, без ограничения, внутривенный, внутриартериальный, парентеральный, внутрибрюшинный или подкожный. Подходящий состав и способ введения могут быть выбраны в соответствии с предполагаемым применением.
[00162] В некоторых вариантах осуществления терапевтическое лечение с использованием OX40-связывающего полипептида достигается за счет усиления пролиферации и/или активации Т-клеток. В некоторых вариантах осуществления усиление пролиферации и/или активации Т-клеток подавляет рост рака.
Фармацевтические композиции
[00163] В некоторых вариантах осуществления композиции, содержащие OX40-связывающие полипептиды, представлены в составах с широким спектром фармацевтически приемлемых носителей (см., например, Gennaro, Remington: The Science and Practice of Pharmacy with Facts and Comparsions: Drugfacts Plus, 20th ed. (2003); Ansel et al., Pharmaceutical Dosage Forms and Drug Delivery Systems, 7-е ed., Lippencott Williams and Wilkins (2004); Kibbe et al., Handbook of Pharmaceutical Excipients, 3 ed., Pharmaceutical Press (2000)). Доступны различные фармацевтически приемлемые носители, которые включают несущие среды, адъюванты и разбавители. Кроме того, также доступны различные фармацевтически приемлемые вспомогательные вещества, такие как регуляторы pH и буферные агенты, агенты, регулирующие тоничность, стабилизаторы, смачивающие агенты и т.п. Неограничивающие примеры носителей включают физиологический раствор, забуференный физиологический раствор, декстрозу, воду, глицерин, этанол и их комбинации.
[00164] В некоторых вариантах осуществления фармацевтическая композиция содержит OX40-связывающий полипептид в концентрации по меньшей мере 10 мг/мл, 20 мг/мл, 30 мг/мл, 40 мг/мл, 50 мг/мл, 60 мг/мл, 70 мг/мл, 80 мг/мл, 90 мг/мл, 100 мг/мл, 125 мг/мл, 150 мг/мл, 175 мг/мл, 200 мг/мл, 225 мг/мл или 250 мг/мл.
Комбинированная терапия
[00165] OX40-связывающие полипептиды можно вводить отдельно или в комбинации с другими режимами лечения, такими как другие противораковые агенты. Их можно вводить до, практически одновременно или после других режимов лечения (т.е. одновременно или последовательно). В некоторых вариантах осуществления способ лечения, раскрытый в настоящем описании, может дополнительно включать предоставление: лучевой терапии, химиотерапии, вакцинации, таргетной противоопухолевой терапии, CAR-T-терапии, онколитической вирусной терапии, иммунотерапии рака, цитокинотерапии, хирургической резекции, модификации хроматина, абляции, криотерапии, антисмыслового агента против опухолевой мишени, миРНК (siRNA) против опухолевой мишени, агента микроРНК против опухолевой мишени или противоракового/противоопухолевого агента, или биологического агента, такого как антитело, цитокина или слитого белка, состоящего из внеклеточного домена рецептора и Fc-фрагмента.
[00166] В некоторых вариантах осуществления OX40-связывающий полипептид, представленный в настоящем описании, вводят одновременно со вторым терапевтическим агентом, например, PD-1 терапевтическим средством. Примеры PD-1/PD-L1 терапевтических средств включают ниволумаб (BMS); пидилизумаб (CureTech, CT-011), пембролизумаб (Merck); дурвалумаб (Medimmune/AstraZeneca); атезолизумаб (Genentech/Roche); авелумаб (Pfizer); AMP-224 (Amplimmune); BMS-936559; AMP-514 (Amplimmune); MDX-1105 (Merck); ТСР-042 (Tesaro/AnaptysBio, ANB-011); STI-A1010 (Sorrento Therapeutics); STI-A1110 (Sorrento Therapeutics); и другие средства, направленные против белка запрограммированной клеточной смерти-1 (PD-1) или лиганда запрограммированной клеточной смерти 1 (PD-L1).
[00167] В некоторых вариантах осуществления OX40-связывающий полипептид, представленный в настоящем описании, вводят одновременно с CAR-T (Т-клеточный химерный антигенный рецептор) терапией, онколитической вирусной терапией, цитокинотерапией и/или агентами, нацеленными на другие молекулы контрольных точек, такие как VISTA, gpNMB, B7H3, B7H4, HHLA2, CD73, CTLA4, TIGIT и др.
Неограничивающие примеры способов диагностики и лечения
[00168] В некоторых вариантах осуществления способы, раскрытые в настоящем описании, полезны для оценки субъекта и/или образца, полученного от субъекта (например, больного раком). В некоторых вариантах осуществления оценка представляет собой одно или более из следующего: диагностику, прогноз и/или ответ на лечение.
[00169] В некоторых вариантах осуществления способы, раскрытые в настоящем описании, включают оценку наличия, отсутствия или уровня белка. В некоторых вариантах осуществления способы, раскрытые в настоящем описании, включают оценку наличия, отсутствия или уровня экспрессии нуклеиновой кислоты. Раскрытые в настоящем описании композиции можно использовать для этих измерений. Например, в некоторых вариантах осуществления способы, раскрытые в настоящем описании, включают контактирование образца опухоли или клеток, культивируемых из опухоли, с терапевтическим агентом, раскрытым в настоящем описании.
[00170] В некоторых вариантах осуществления оценка позволяет осуществить направленное лечение (включая лечение антителами, раскрытыми в настоящем описании). В некоторых вариантах осуществления оценка позволяет определять, следует ли применять или следует отказаться от применения адъювантной терапии после резекции. Адъювантная терапия, также называемая адъювантным лечением, представляет собой лечение, которое проводят в дополнение к первичному, основному или начальному лечению. В качестве неограничивающего примера адъювантная терапия может представлять собой дополнительное лечение, обычно предоставляемое после хирургического вмешательства, в результате которого устранены все выявленные очаги заболевания, но при этом остается статистический риск рецидива из-за скрытых очагов заболевания. В некоторых вариантах осуществления антитела используются в качестве адъювантной терапии при лечении рака. В некоторых вариантах осуществления антитела используются в качестве единственной адъювантной терапии при лечении рака. В некоторых вариантах осуществления раскрытые в настоящем описании прекращают введение антител в качестве адъювантной терапии при лечении рака. Например, когда получение ответа у пациента на раскрытое в настоящем описании антитело является маловероятным или когда у пациента наблюдается минимальный ответ, лечение нельзя назначать в интересах качества жизни и во избежание ненужной токсичности вследствие неэффективной химиотерапии. В таких случаях может предоставляться паллиативная медицинская помощь.
[00171] В некоторых вариантах осуществления молекулы вводят в качестве неоадъювантной терапии перед резекцией. В некоторых вариантах осуществления неоадъювантная терапия относится к терапии, применяемой с целью уменьшения и/или снижения степени злокачественности опухоли перед любой операцией. В некоторых вариантах осуществления неоадъювантная терапия означает химиотерапию, проводимую онкологическим больным перед операцией. В некоторых вариантах осуществления неоадъювантная терапия означает, что антитело вводят больным раком до операции. Типы рака, при которых обычно предусмотрена неоадъювантная химиотерапия, включают, например, рак груди, колоректальный рак, рак яичников, шейки матки, мочевого пузыря и легких. В некоторых вариантах осуществления при лечении рака в качестве неоадъювантной терапии применяют антитела. В некоторых вариантах осуществления указанное применение осуществляется перед резекцией.
[00172] В некоторых вариантах осуществления микросреда опухоли, подразумеваемая в способах, раскрытых в настоящем описании, представляет собой одно или более из следующего: сосудистую сеть опухоли; лимфоциты, инфильтрирующие опухоль; ретикулярные клетки фибробластов; эндотелиальные клетки-предшественники (EPC); ассоциированные с раком фибробласты; перициты; другие стромальные клетки; компоненты внеклеточного матрикса (ЕСМ); дендритные клетки; антигенпрезентирующие клетки; Т-клетки; регуляторные Т-клетки; макрофаги; нейтрофилы; и другие иммунные клетки, расположенные проксимальнее опухоли.
Наборы
[00173] Также предоставляются промышленные изделия и наборы, которые включают любой из OX40-связывающих полипептидов, раскрытых в настоящем описании, и подходящую упаковку. В некоторых вариантах осуществления изобретение включает набор с (i) OX40-связывающим полипептидом и (ii) инструкциями по применению указанного набора для введения OX40-связывающего полипептида индивидууму.
[00174] Подходящие упаковки для раскрытых в настоящем описании композиций известны в данной области и включают, например, флаконы (например, герметичные флаконы), сосуды, ампулы, бутыли, банки, гибкую упаковку (например, герметичные майларовые или пластиковые пакеты) и т.п. Эти промышленные изделия могут быть дополнительно стерилизованы и/или герметично запечатаны. Также предусмотрены единичные дозированные формы, содержащие раскрытые в настоящем описании композиции. Эти единичные дозированные формы могут храниться в подходящей упаковке в виде одной или более единичных дозированных форм, и также могут быть дополнительно стерилизованы и герметично запечатаны. Инструкции, поставляемые в наборах по изобретению, обычно представляют собой письменные инструкции на этикетке или вкладыше в упаковку (например, на листе бумаги, входящем в комплект), но также приемлемы машиночитаемые инструкции (например, инструкции на магнитном или оптическом запоминающем диске). Инструкции, относящиеся к применению антител, обычно включают информацию о дозировке, графике дозирования и способе введения для предполагаемого лечения или промышленного использования. Набор может дополнительно содержать описание выбора подходящего для индивидуума лечения.
[00175] Контейнеры могут представлять собой единичные дозированные формы, упаковки с нефасованным лекарственным веществом (например, многодозовые упаковки) или субъединичные дозы. Например, также могут быть предоставлены наборы, которые содержат дозы раскрытых в настоящем описании молекул, достаточные для обеспечения эффективного лечения индивидуума в течение длительного периода времени, например, примерно в течение недели, 2 недель, 3 недель, 4 недель, 6 недель, 8 недель, 3 месяцев, 4 месяцев, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев или более. Наборы также могут включать несколько единичных дозированных форм молекул и инструкции по применению и могут быть упакованы в количествах, достаточных для хранения и использования в аптеках, например, в больничных аптеках и рецептурных аптеках. В некоторых вариантах осуществления набор включает сухую (например, лиофилизированную) композицию, которую можно восстановить, ресуспендировать или регидратировать с образованием, как правило, стабильной водной суспензии антитела.
ПРИМЕРЫ
[00176] Примеры, обсуждаемые ниже, предназначены исключительно для иллюстрации изобретения и не должны рассматриваться как ограничивающие изобретение каким-либо образом. Примеры не предназначены для демонстрации того, что приведенные ниже эксперименты представляют собой все выполненные эксперименты или только те эксперименты, которые были выполнены. Хотя были предприняты все усилия для обеспечения точности используемых чисел (например, количеств, температуры и т.д.), следует учитывать наличие некоторых экспериментальных ошибок и отклонений. Если не указано иное, части являются массовыми частями, молекулярная масса представляет собой среднюю молекулярную массу, температура приведена в градусах Цельсия, и давление равно или близко к атмосферному.
Пример 1: 1D10v6-Fc имеет пониженное неспецифическое связывание по сравнению с 1D10v1-Fc
[00177] Однодоменные антитела (sdAb), содержащие домены VHH, которые связываются с OX40, были разработаны ранее. См. публикацию PCT № WO 2017/123673 A2. Для гуманизации было выбрано SdAb 1D10, в результате которой было получено 1D10v1. См. Id. и SEQ ID NO: 3.
[00178] 1D10v1 было оптимизировано для уменьшения неспецифического связывания. Эта оптимизация привела к замене одной аминокислоты в CDR3 домена VHH sdAb и двух аминокислот в каркасной области 2 (FR2), что дало 1D10v6 (SEQ ID NO: 9). CDR3 1D10v6 (SEQ ID NO: 12) имеет замену G на A относительно CDR3 1D10v1 (SEQ ID NO: 6), и FR2 1D10v6 имеет замену GL на ER (SEQ ID NO: 22). Неожиданно было обнаружено, что эти замены снижают неспецифическое связывание sdAb с сохранением аффинности к OX40 человека и яванского макака, как описано ниже.
[00179] Неспецифическое связывание двухвалентных sdAb определяли методом проточной цитометрии после высокотемпературного стресса. В очищенных 1D10v1-Fc и 1D10v6-Fc заменяли буфер на 20 мМ Tris с pH 8,0, содержащий 150 мМ NaCl, 2% трегалозу, 0,2% ТВИН-20, и подвергали стрессу путем инкубации при 50°C в течение 7 дней. Затем антитела фильтровали с использованием шприцевого фильтра Acrodisc 0,2 мкм, и определяли количество путем измерения A280. Клетки HEK293 не экспрессировали OX40 на клеточной поверхности на детектируемом уровне, и поэтому их использовали в качестве контрольной клеточной линии для неспецифического связывания. 30000 клеток на лунку инкубировали, используя серийные разведения подвергнутых температурному стрессу 1D10v1-Fc или 1D10v6-Fc. После инкубации с первичными антителами использовали вторичное антитело к человеческому Fc, конъюгированное с Alexa Fluor 647, при разведении 1/2000, затем связанное антитело измеряли методом проточной цитометрии с помощью Intellicyte iQue Plus, и результаты измерения флуоресценции наносили на график в виде медианной интенсивности флуоресценции. Как показано на фиг. 1, 1D10v1-Fc демонстрировало неспецифическое связывание с нетрансфицированными клетками HEK293, начиная примерно с 33 нМ sdAb, причем связывание резко возрастало по мере увеличения концентрации sdAb. Напротив, 1D10v6-Fc не имело детектируемого связывания с нетрансфицированными клетками HEK293 вплоть до 1000 нМ sdAb.
[00180] Связывание sdAb с OX40 человека и яванского макака определяли следующим образом. Стабильно трансфицированные клетки СНО, экспрессирующие OX40 полной длины человека или OX40 яванского макака, высевали с плотностью 50000 клеток на лунку. Антитела титровали, используя серийное разведение 1:3, начиная с 400 нМ, и детектировали вторичным антителом к человеческому Fc 488. Анализ методом проточной цитометрии выполняли на анализаторе Intellicyte iQue, и результаты измерений флуоресценции наносили на график в виде средней интенсивности флуоресценции. Как показано на фиг. 2, 1D10v6-Fc показал связывание с OX40 человека (фиг. 2A) и OX40 яванского макака (фиг. 2B), сопоставимое с 1D10v1-Fc. Аффинность (KD) 1D10v6-Fc к OX40 человека и яванского макака составила 0,81 нМ и 0,66 нМ, соответственно. Аффинность (KD) 1D10v1-Fc к OX40 человека и яванского макака составила 0,86 нМ и 0,79 нМ, соответственно.
Пример 2: Шестивалентное 3x1D10v6-Fc имеет пониженное неспецифическое связывание по сравнению с шестивалентным 3x1D10v1-Fc
[00181] Шестивалентные sdAb к OX40 получали путем присоединения трех доменов VHH к Fc, полипептид которого образует шестивалентный димер. Неспецифическое связывание шестивалентного 3x1D10v1-Fc (SEQ ID NO: 8; также упоминаемого как Hex-1D10v1) и шестивалентного 3x1D10v6-Fc (SEQ ID NO: 14; также упоминаемого как Hex-1D10v6) определяли следующим образом. 3x1D10v1-Fc и 3x1D10v6-Fc инкубировали в течение 48 часов при комнатной температуре в буфере, состоящем из 20 мМ His, 150 мМ NaCl, 0,02% Твин-20, pH 9, с нетрансфицированными клетками HEK293 Freestyle или с временно трансфицированными клетками HEK293 Freestyle, экспрессирующими полноразмерный OX40. Для обнаружения связанных 3x1D10v1-Fc и 3x1D10v6-Fc использовали флуоресцентное анти-Fc-специфическое вторичное антитело, которое измеряли методом проточной цитометрии с помощью анализатора Intellicyte iQue. Для каждой концентрации антитела строили график средней интенсивности флуоресценции.
[00182] Как показано на фиг. 3, 3x1D10v1-Fc и 3x1D10v6-Fc в этих условиях показали сравнимое специфическое связывание с кажущейся KD 0,82 нМ и 0,90 нМ, соответственно (фиг. 3A). Однако 3x1D10v1-Fc имело неспецифическое связывание с нетрансфицированными клетками HEK293, в то время как 3x1D10v6-Fc не показало неспецифического связывания (фиг. 3B).
Пример 3: Шестивалентный 3x1D10v6-Fc сохраняет активность агониста OX40
[00183] Как описано выше, 3x1D10v6-Fc обладало пониженным неспецифическим связыванием с клетками HEK293 при сохранении аффинности связывания OX40. Агонистическую активность 3x1D10v6-Fc подтверждали следующим образом.
[00184] Пассаж 5 репортерных клеток Jurkat/OX40 (Promega) в формате Thaw-and-Use извлекали из жидкого азота и размораживали на водяной бане при 37°C. Клетки стабильно экспрессировали OX40 и содержали ген-репортер люциферазы, расположенный ниже ответного элемента NFκB. Клетки осторожно перемешивали и переносили в 9 мл предварительно нагретой культуральной среды (RPMI+10% FBS). Клетки центрифугировали при 400xg в течение 5 минут и ресуспендировали в 5 мл аналитической среды (RPMI+10% FBS). Плотность и жизнеспособность клеток определяли, используя трипановый синий и автоматический счетчик клеток TC20. Внутренние лунки 60-луночных планшетов для анализа засевали клетками с плотностью 6×104 клеток/лунку в 50 мкл/лунку аналитической среды. Во внешние лунки добавляли 100 мкл/лунку аналитической среды. В каждый угловой резервуар планшета для анализа добавляли 2,5 мл среды для анализа.
[00185] 3x1D10v1-Fc и 3x1D10v6-Fc разводили в аналитической среде так, чтобы концентрация была в два раза выше желаемой максимальной конечной концентрации. Выполняли 9-точечное серийное разведение (5-кратное, 5-кратное, 2-кратное, 2-кратное, 2-кратное, 2-кратное, 5-кратное, 5-кратное) с максимальной концентрацией 50 нМ и минимальной концентрацией 0,005 нМ. Таким образом, самая высокая конечная концентрация в анализе составляла 25 нМ, и самая низкая - 0,0025 нМ. Разведения антител осуществляли в 96-луночном планшете для разведения. В аналитические планшеты добавляли 50 мкл/лунку 2-кратных разведений антител. Конечный анализируемый объем на лунку составлял 100 мкл. Планшеты для анализа закрывали крышками и помещали в инкубатор с CO2 при 37°C на 6 часов.
[00186] После 6-часовой инкубации планшеты для анализа вынимали из инкубатора и оставляли при комнатной температуре на 10 минут. В каждую лунку аналитических планшетов, содержащую клетки, добавляли 100 мкл восстановленного реагента люциферазы Bio-Glo (Promega). Планшеты для анализа инкубировали в течение 10 минут при комнатной температуре. 100 мкл/лунку из аналитического планшета переносили в белый 96-луночный планшет для измерения относительных единиц люминесценции (RLU). Планшеты считывали на планшетном ридере Molecular Devices SpectraMax L, используя программное обеспечение SoftMax Pro v5.4 в соответствии с настройками, указанными в таблице реагентов (PMT-MaxRange, Target Wave-470 нм).
[00187] Результаты этого эксперимента показаны на фиг. 4. Максимальное связывание (Bmax) и концентрация фермента при 50% ответе (KD) показывают, что 3x1D10v6-Fc имеет активность в анализе OX40 с использованием гена-репортера люциферазы, сравнимую с 3x1D10v1-Fc.
Пример 4: Шестивалентное 3x1D10v6-Fc имеет высокую OX40-агонистическую активность
[00188] Для демонстрации того, что шестивалентное 3x1D10v6-Fc является более эффективным агонистом OX40 по сравнению с двухвалентным и четырехвалентным вариантами (SEQ ID NO: 13 и 16, соответственно), применяли анализ OX40 с использованием гена-репортера люциферазы, по существу, как описано в Примере 3.
[00189] Результаты этого эксперимента показаны на фиг. 5. В этом анализе шестивалентное 3x1D10v6-Fc было более эффективным по сравнению с четырехвалентным 2x1D10v6-Fc, что указывает на то, что 3x1D10v6-Fc является сильным агонистом. Двухвалентное 1D10v6-Fc в этом анализе имело минимальную активность.
Пример 5: Шестивалентное 3x1D10v6-Fc усиливает пролиферацию Т-клеток
[00190] Выделение PBMC: PBMC выделяли из образцов лейкафереза, полученных от нормальных доноров или из цельной крови с помощью центрифугирования в градиенте плотности следующим образом. Образцы крови разбавляли PBS/2% FBS (1:2), и 30 мл разбавленной крови наслаивали на 15 мл среды с градиентом плотности Lymphoprep (Stemcell Technologies). После центрифугирования при 800×g в течение 30 минут слой PBMC на границе раздела плазмы и лимфопрепарата удаляли, и оставшиеся эритроциты лизировали с использованием буфера для лизиса эритроцитов (BioLegend) в течение 5 минут при комнатной температуре. Клетки промывали PBS, и затем замораживали свежими в Cryostor CS10 (Stemcell Technologies) из расчета 100×106 клеток на мл.
[00191] Обогащение Т-клеток: не относящиеся к Т-клеткам (не-Т-клеточные) популяции метили anti-Lineage коктейлем биотинилированных антител-маркеров к CD14, CD16, CD19, CD20, CD36, CD56, CD123, TCRγ/δ (BioLegend) в течение 20 минут при комнатной температуре. Затем не-Т-клеточные популяции истощали путем инкубации в течение 20 минут при комнатной температуре с магнитными стрептавидиновыми гранулами (500 мкл суспензии гранул плюс 500 мкл клеточной суспензии на 100×106, инкубация 2×8 минут на магните). Супернатант несвязанных клеток содержал Т-клетки. В качестве альтернативы, Т-клетки обогащали из образцов PBMC с помощью набора EasySep Human T-Cell Enrichment Kit (Stemcell Technologies) в соответствии с рекомендациями производителя. Для получения обогащенных CD4+ Т-клеток, обогащенные Т-клетки инкубировали с биотинилированным анти-CD8-антителом и подвергали истощению, используя магнитные стрептавидиновые гранулы, по существу, как описано выше.
[00192] Покрытие тозилактивированными гранулами M-450: Стимулирующие гранулы, используемые для анализа активации Т-клеток, покрывали 200 мкг мышиного антитела к человеческому CD3 (клон OKT3; eBioscience) с плотностью 4x108 гранул в соответствии с процедурой нанесения покрытия, рекомендованной производителем. Вкратце, гранулы промывали один раз буфером 1 (0,1 М натрий-фосфатный буфер, pH 7,4–8,0), и затем инкубировали в ротаторе для пробирок в течение 18 часов при комнатной температуре в буфере 1, содержащем 200 мкг антитела к человеческому CD3. Затем гранулы промывали 4 раза буфером 2 (PBS, 0,1% BSA, 2 мМ EDTA, pH 7,4). Свободные тозильные группы дезактивировали путем инкубации гранул в течение 4 часов при 37°C в буфере 3 (0,2 М Трис, 0,1% BSA, pH 8,5). Затем гранулы один раз промывали буфером 2 и ресуспендировали до концентрации 400×106 гранул/мл.
[00193] Анализ костимуляции: обогащенные CD4+ Т-клетки (от четырех разных доноров) метили с помощью CellTrace Violet (CTV; Invitrogen) при разведении 1:1000. Затем клетки высевали в трех экземплярах по 200000 клеток на лунку в 96-луночные планшеты с круглым дном и объединяли со 100000 гранул, покрытыми антителами к человеческому CD3. Культуры инкубировали, используя титрование 3x1D10v6-Fc или двухвалентного 1D10v6-Fc, начиная с конечной концентрации 50 нМ и титруя с разведением 1:5 по всему планшету. Конечный объем культуры составлял 200 мкл на лунку, и клетки инкубировали при 37°C/5% CO2 в течение 4 дней.
[00194] Окрашивание FACS: в день 4 культивирования Т-клеток клетки промывали один раз в 150 мкл буфера для FACS, и осадок клеток ресуспендировали в 50 мкл раствора для окрашивания поверхностных маркеров (содержащего антитела к CD4, CD25 и CD71 и иодид пропидия). Клетки инкубировали в течение 20 минут при комнатной температуре перед окончательной промывкой и анализом на проточном цитометре SONY Analyzer. Для анализа популяций Т-клеток использовали программное обеспечение FlowJo. Затем экспортировали необработанные средние значения интенсивности флуоресценции для различных маркеров активации, которые анализировали с помощью Excel и GraphPad PRISM. Значения наносили на график, и аппроксимировали кривые титрования для оценки зависимости доза-ответ путем подбора нелинейной кривой зависимости [Агонист]-ответ с переменным наклоном (четыре параметра). Эту аппроксимацию также использовали для определения эффективной концентрации (ЕС50) для каждого донора.
[00195] Стратегия стробирования FACS: для оценки уровня пролиферации Т-клеток и уровня экспрессии маркера активации в субпопуляциях Т-клеток использовали следующую стратегию стробирования: клеточный дебрис исключали путем исключения размера FSC/SSC, и мертвые клетки исключали на основании положительного сигнала йодида пропидия. Одиночные клетки отбирали с помощью дублета FSC-A/FSC-H и исключения агрегированных клеток. Подтверждали тот факт, что оставшаяся популяция клеток является CD4+. Потеря окрашивания CellTrace Violet (CTV+) по сравнению с контролем, состоящим только из Т-клеток, была признаком пролиферации клеток. Повышение уровней MFI маркеров активации CD25 и CD71 было признаком активации Т-клеток.
[00196] ELISA IFNγ и анализ данных: В день 4 отбирали образцы супернатанта клеточной культуры и помещали на хранение при -80ºC. Уровни IFNγ в супернатантах клеточных культур измеряли с помощью набора ELISA для IFNγ в соответствии с протоколом производителя. Вкратце, планшеты для ELISA покрывали иммобилизованным анти-IFNγ антителом в течение ночи при 4ºC. На следующий день планшеты блокировали в течение 1 часа буфером для анализа перед инкубацией клеточных супернатантов, который выполняли в течение 2 часов. Образцы разбавляли 1:25 в буфере для анализа. Связывание антигена детектировали путем инкубации планшетов в течение 1 часа с биотинилированным идентифицирующим антителом и последующей инкубации с реагентом стрептавидина, конъюгированным с пероксидазой хрена. Активность HRP измеряли после добавления раствора субстрата и инкубации в течение 15 минут. После добавления стоп-раствора планшеты анализировали на прецизионном микропланшетном ридере Emax при длине волны 450 нм.
[00197] Необработанные значения, полученные с помощью прецизионного микропланшетного ридера Emax, анализировали с помощью программного обеспечения для анализа Softmax Pro, используемого для микропланшетного ридера. Уровни IFNγ в образцах в пг/мл рассчитывали, используя значения оптической плотности стандартной кривой и четырехпараметрическую логистическую регрессию. Проанализированные значения экспортировали в Excel (Microsoft, версия 15.27) для дальнейшего анализа данных. На основе полученных значений строили график с помощью PRISM (GraphPad Software Inc., версия 7.0c), и кривые титрования аппроксимировали для оценки зависимости доза-ответ путем подбора нелинейной кривой зависимости [Агонист]-ответ с переменным наклоном (четыре параметра).
[00198] Как показано на фиг.6, обработка шестивалентным 3x1D10v6-Fc, но не двухвалентным 1D10v6-Fc, приводила к усиленной пролиферации CD4+ Т-клеток от всех четырех доноров. Обработка шестивалентным 3x1D10v6-Fc также приводила к более высоким уровням маркеров активации CD25 и CD71 у всех четырех доноров (фиг.7 и фиг.8). Уровни секретируемого IFNγ также были выше при обработке 3x1D10v6-Fc (фиг. 9). Значения интенсивности костимуляции различались в зависимости от донора, но в целом зависели от дозы. Рассчитанные значения ЕС50 приведены в таблице 2 ниже.
Таблица 2: Значения EC50 для 3x1D10v6-Fc:
[00199] Таким образом, 3x1D10v6-Fc улучшало опосредованную анти-CD3-антителами стимуляцию Т-клеток in vitro. Не ограничиваясь какой-либо конкретной теорией, выяснилось, что для эффективной костимуляции в этом анализе требуется кластеризация OX40, например, с шестивалентным 3x1D10v6-Fc.
Пример 6: Шестивалентный 3x1D10v6-Fc усиливает костимуляцию Т-клеток и продуцирование IFNγ
[00200] Обогащенные Т-клетки от 10 здоровых доноров-людей стимулировали субоптимальным количеством анти-CD3 антитела в присутствии или в отсутствие 3x1D10v6-Fc.
[00201] PBMC получали от 10 здоровых доноров-людей, и популяции Т-клеток в значительной степени обогащали, как описано в примере 5.
[00202] Стимуляция Т-клеток: Обогащенные Т-клетки от 10 здоровых доноров оттаивали и дважды промывали антиагрегатной средой CTL. Т-клетки метили красителем CellTrace Violet (CTV) (ThermoFisher) для оценки пролиферации в течение 10 минут при 37°C. После промывки Т-клетки ресуспендировали до 1,5х106 клеток/мл в RPMI с добавлением 10% FBS и 1X антибиотика/антимикотика, и в каждую лунку добавляли 150000 Т-клеток в 100 мкл в 96-луночном планшете с плоским дном. Тозилактивированные Dynabeads M-450 (ThermoFisher) покрывали 200 мкг анти-CD3 антитела (клон OKT3, eBioscience) и оставляли на ночь в соответствии с инструкциями производителя. Гранулы, покрытые анти-CD3-антителом, добавляли по 50 мкл на лунку к меченым Т-клеткам в соотношении 1:2 для обеспечения первичного стимула Т-клеток. 3x1D10v6-Fc добавляли в 50 мкл до конечной концентрации 10 нМ. Планшеты инкубировали при 37°C/5% CO2 в течение 3 дней и анализировали методом проточной цитометрии.
[00203] Проточная цитометрия: через 3 дня Т-клетки центрифугировали и метили в буфере FACS (PBS/2% FBS/0,05% азид натрия) пропидий йодидом (PI), маркером для определения жизнеспособности, вместе со следующими флуоресцентно меченными антителами: CD4-PE, CD8-APC, CD25-FITC и CD71-PE/Cy7 (Biolegend), в течение 20 минут при комнатной температуре. Т-клетки промывали и ресуспендировали в 70 мкл буфера FACS и анализировали с помощью спектрального анализатора Sony SA3800. Программное обеспечение Flowjo использовали для стробирования живых (PI-)CD4 и CD8 популяций, и процент клеток, подвергшихся пролиферации, определяли путем стробирования Т-клеток, которые подверглись минимум одному делению, которое определяли разведением CTV. Процент CD4 и CD8 Т-клеток, экспрессирующих маркеры активации CD25 и CD71, определяли путем сравнения с популяциями нестимулированных Т-клеток. Данные экспортировали в Microsoft Excel и строили графики с помощью Prism.
[00204] Окрашивание внутриклеточных цитокинов: клетки центрифугировали и метили поверхность с помощью PE-конъюгированного анти-CD4-антитела и APC-конъюгированного анти-CD8-антитела вместе с красителем для оценки жизнеспособности Zombie Red (BioLegend) в течение 20 минут при комнатной температуре в буфере FACS (2% FBS/0,1% азид натрия в PBS). После промывки клетки фиксировали в течение 30 минут буфером BD Fix/Perm. Клетки промывали 1X буфером BD Perm/Wash и метили анти-IFNγ антителом PE/Cy7 в буфере Perm/Wash в течение 45 минут при комнатной температуре. После промывки клетки ресуспендировали в буфере FACS и считывали на спектральном анализаторе Sony SA3800. Анализ данных для популяций CD4+ и CD8+ Т-клеток выполняли с помощью программного обеспечения Flowjo и отображали в виде графика с помощью Prism.
[00205] В Т-клетках от всех 10 протестированных доноров обработка 3x1D10v6-Fc привела к значительному увеличению процента CD4+ и CD8+ Т-клеток, которые подверглись пролиферации в ответ на стимуляцию анти-CD3-антителами (фиг. 10, фиг. 11). Более того, процент CD4 и CD8 Т-клеток, которые экспрессировали маркеры активации CD25 и CD71, увеличился при обработке 3x1D10v6-Fc (фиг. 11). В отдельном эксперименте немногочисленная подгруппа от 4 доноров показала увеличение внутриклеточных уровней IFNγ в обеих подгруппах Т-клеток после обработки 3x1D10v6-Fc (фиг.12). Таким образом, 3x1D10v6-Fc обеспечивает мощный костимулирующий сигнал в Т-клетки, что приводит к усилению активации, пролиферации и эффекторной функции.
Пример 7: Шестивалентный 3x1D10v6-Fc отменяет опосредованное Treg-опосредованное подавление пролиферации CD4+ Т-клеток
[00206] Обогащение Т-клеток: Treg и обычные CD4+ Т-клетки обогащали из свежих РВМС, полученных от здоровых доноров, с использованием набора EasySep Human для выделения регуляторных CD4+ CD127lowCD25+ Т-клеток (стволовых клеток) в соответствии с инструкциями производителя.
[00207] Анализ подавления Т-клеток: Для возможности различения двух популяций клеток, обогащенные Treg и CD4+ Т-клетки-респондеры метили пролиферативными красителями CellTrace Violet (CTV) и CFSE, соответственно, в течение 10 минут при 37°C. После промывки Treg и CD4+ Т-клетки ресуспендировали до 1,5×106 клеток/мл в RPMI с добавлением 10% FBS и 1X антибиотика/антимикотика. Treg засевали в 96-луночный круглодонный планшет в объеме 50 мкл, получая 75000 Treg/лунку. Treg инкубировали в течение ночи при 37°C в присутствии 10 нМ шестивалентного 3x1D10v6-Fc к OX40, 10 нМ обычного (HC/LC) двухвалентного антитела к OX40 или в отсутствие антитела. Параллельно, меченые CD4+ Т-клетки-респондеры активировали в течение ночи при 37°C с помощью покрытых анти-CD3 антителами гранул Dynabeads при соотношении гранул к Т-клеткам 1:2. На следующий день планшет с Treg промывали 2 раза средой для удаления антител. Стимулированные CD4+ Т-клетки-респондеры добавляли в 100 мкл среды с плотностью 150000 CD4+ Т-клеток/лунку в планшет, содержащий Treg, в соотношении 1 Treg на каждые 2 CD4+ Т-клетки-респондеры. Шестивалентные 3x1D10v6-Fc или обычные двухвалентные антитела к OX40 снова добавляли в 100 мкл среды в конечной концентрации 10 нМ в двух экземплярах к субпопуляции клеток. Кроме того, включали группу CD4+ Т-клеток-респондеров, которые не инкубировали совместно с Treg. Планшет инкубировали при 37°C/5% CO2 в течение 3 дней и анализировали методом проточной цитометрии.
[00208] Проточная цитометрия: через 3 дня Т-клетки центрифугировали и метили в буфере FACS (PBS/2% FBS/0,05% азид натрия) пропидий йодидом (PI), маркером для определения жизнеспособности, вместе со следующими флуоресцентно меченными антителами: CD4-PE, CD25-APC и CD71-PE/Cy7 (Biolegend), в течение 20 минут при комнатной температуре. Т-клетки промывали и ресуспендировали в 70 мкл буфера FACS и анализировали с помощью спектрального анализатора Sony SA3800. Для стробирования живых (PI-)CFSE+-респондеров CD4+ или CTV+ Treg популяций использовали программное обеспечение Flowjo, и определяли процент клеток, подвергшихся пролиферации, путем стробирования по Т-клеткам-респондерам, которые подверглись минимум одному делению, определенному с помощью разведения CFSE. Процент CD4+ Т-клеток-респондеров, экспрессирующих маркеры активации CD25 и CD71, определяли путем сравнения с популяциями нестимулированных Т-клеток. Данные экспортировали в Microsoft Excel, и строили графики с помощью программного обеспечения Prism.
[00209] Стимуляция анти-CD3 гранулами в течение всего 4 дней привела к пролиферации 66% CD4+ Т-клеток-респондеров (фиг. 13). Добавление в культуру обогащенных Treg привело к резкому снижению пролиферации CD4+ Т-клеток-респондеров (пролиферировало 34%). Обработка 10 нМ шестивалентным 3x1D10v6-Fc приводила к почти полному восстановлению пролиферации CD4+ Т-клеток-респондеров (пролиферировало 62%). Более того, экспрессия Т-клеточных маркеров активации CD25 и CD71 восстанавливалась до уровней, аналогичных уровням у CD4+ Т-клеток-респондеров без экспериментальной группы Treg. Напротив, обработка обычным бивалентным антителом к OX40 не могла восстановить пролиферацию CD4+ Т-клеток или увеличить экспрессию CD25 или CD71 по сравнению с группой без антител.
Пример 8: Шестивалентное 3x1D10v6-Fc в комбинации с пембролизумабом усиливает активацию Т-клеток
[00210] После связывания TCR костимулирующие молекулы, такие как OX40, активируются вместе с негативными регуляторными молекулами, которые противодействуют активации T-клеток, подавляя сигнализацию TCR. Клинически было показано, что блокада одного из таких путей, оси PD-1/PD-L1, успешно восстанавливает функцию невосприимчивых опухолеспецифических Т-клеток, ослабляя этот ингибирующий сигнал. OX40 достигает аналогичного результата, усиления Т-клеточных ответов, с помощью другого механизма: обеспечения экзогенных костимулирующих сигналов, которые синергируют с сигналами TCR. Эти неперекрывающиеся, но взаимодополняющие механизмы предполагают, что комбинирование агонизма OX40 с блокадой контрольных точек даст более сильный клинический эффект.
[00211] Реакция смешанной культуры аллогенных лимфоцитов (MLR) представляет собой анализ in vitro, используемый для демонстрации функциональной модуляции Т-клеток; в этой реакции используется смесь незрелых дендритных клеток, полученных in vitro (iDC), и несовместимых по HLA Т-клеток для индукции TCR-зависимой активации Т-клеток. Шестивалентное 3x1D10v6-Fc показало умеренную активность в этом анализе. (Данные не показаны.) Активность шестивалентного 3x1D10v6-Fc тестировали в комбинации с пембролизумабом, анти-PD-1 антителом, чтобы определить, демонстрирует ли комбинация повышенную активацию Т-клеток.
[00212] Выделение CD4+ Т-клеток: PBMC выделяли из лейкопака человеческой донорской крови путем центрифугирования в градиенте плотности, по существу, следующим образом. Образцы крови разбавляли PBS/2% FBS (1:2), и 30 мл разбавленного образца наслаивали на 15 мл среды LymphoprepТМ с градиента плотности. После центрифугирования при 800×g в течение 30 минут слой PBMC на границе раздела плазмы и LymphoprepТМ собирали, и оставшиеся эритроциты лизировали с использованием буфера для лизиса красных кровяных телец в течение 7 минут при комнатной температуре. Затем PBMC обогащали моноцитами, как описано ниже, или замораживали при концентрации 100×1060x106 клеток/мл в среде для криоконсервации CryoStor® и хранили в жидком азоте. CD4+ T-клетки обогащали, используя свежие PBMC от здоровых доноров с помощью набора для выделения EasySepTM Human CD4+ T-клеток (Stemcell Technologies) в соответствии с инструкциями производителя. PBMC ресуспендировали при концентрации 50×106 клеток/мл в PBS, содержащем 2% FBS и 1 мМ EDTA. CD4+ Т-клетки отрицательно обогащали, используя коктейль для выделения CD4+ Т-клеток с последующей инкубацией с Dextran RapidSpheresТМ на магните EasySepТМ. После двух раундов обогащения на магните подсчитывали CD4+ Т-клетки и промывали PBS/0,1% BSA (буфер CTV). Клетки метили фиолетовым красителем CellTraceТМ (1:1000) из расчета 10×106 клеток/мл в буфере CTV в течение 10 минут при 37°C. Меченые клетки промывали один раз PBS/2% FBS и ресуспендировали с плотностью 3,5×106 клеток/мл в аналитической среде (RPMI+10% FBS плюс пенициллин, стрептомицин и амфотерицин).
[00213] Обогащение моноцитов и генерация незрелых дендритных клеток (iDC): моноциты обогащали из PBMC, выделенных из лейкопака доноров, с помощью набора для отрицательного обогащения без истощения CD16 в соответствии с протоколом производителя (набор для обогащения человеческих моноцитов EasySepТМ без истощения CD16; Stemcell Technologies). Вкратце, популяции не-моноцитов метили комплексами тетрамерных антител, распознающих маркеры, специфические для этой популяции, и истощали с использованием магнитных частиц. Супернатант несвязанных клеток содержал моноциты. Моноциты культивировали при концентрации 1×106 клеток/мл в RPMI с добавлением 10% FBS плюс пенициллин, стрептомицин и амфотерицин, 500 ед/мл GM-CSF и 250 ед/мл IL-4. Половинный объем среды пополняли каждые 2 дня до момента сбора незрелых дендритных клеток (iDC) на 7-й день путем сбора непрочно прикрепившихся и суспендированных клеток. Клетки промывали PBS, и затем замораживали свежими в CryoStor® из расчета 3×106 клеток на мл. Индукцию фенотипа iDC после этого режима подтверждали методом проточной цитометрии путем исключения размера FSC/SSC и детектирования CD14- CD11c+ HLA-DR+ окрашивания у по меньшей мере 60% популяции.
[00214] Реакция смешанной культуры лимфоцитов (MLR): Полученные из моноцитов незрелые дендритные клетки (iDC) ресуспендировали в среде для анализа с плотностью 0,8×106 клеток/мл. 1,75×105 CD4+ Т-клеток от другого донора суспендировали в 50 мкл и смешивали с 4×104 iDC в 50 мкл в 96-луночных планшетах с U-образным дном.
[00215] Шестивалентное 3×1D10v6-Fc добавляли в исходной аналитической концентрации 10 нМ и титровали в планшете используя серийное разведение 1:4 в трех повторах либо в присутствии, либо в отсутствие постоянной аналитической концентрации 10 нМ пембролизумаба. В отдельном эксперименте пембролизумаб добавляли в исходной аналитической концентрации 50 нМ и титровали в планшете, используя серийное разведение 1:4 в трех повторах либо в присутствии, либо в отсутствие постоянной аналитической концентрации 1 нМ шестивалентного 3×1D10v6-Fc. Фиксированную концентрацию шестивалентного 3×1D10v6Fc (1 нМ) выбирали, исходя из насыщающих концентраций антитела, которые показали максимальную активность в анализе костимуляции Т-клеток, и для пембролизумаба (10 нМ) использовали насыщающую концентрацию антитела, которая дала максимальную репортерную активность в анализе блокады PD1/PD-L1. Все аналитические планшеты инкубировали при 37°C в течение 7 дней.
[00216] ELISA для человеческого IL-2: аликвоты супернатанта для анализа собирали на 3 день для определения концентрации человеческого IL-2 с помощью ELISA с использованием набора Human IL-2 ELISA MAXТМ Deluxe (Biolegend), следуя инструкциям производителя. Планшеты ELISA MaxiSorp покрывали в течение ночи антителами, захватывающими человеческий IL-2, промывали, затем блокировали буфером для разбавления в течение часа. Стандартные кривые получали в двух экземплярах из исходной концентрации IL-2 1000 пг/мл, и образцы супернатанта для анализа разбавляли 1:5 или 1:10 буфером для разбавления. Образцы и стандарты инкубировали на планшетах для ELISA в течение двух часов с последующими промывками и инкубацией с детектирующими антителами в течение часа. Планшеты для анализа промывали и инкубировали со стрептавидином, конъюгированным с пероксидазой хрена (HRP), в течение 30 минут. После последнего этапа промывки захваченный человеческий IL-2 детектировали на планшетах для ELISA с предоставленным раствором субстрата. Реакцию обнаружения останавливали через 10-30 минут равным объемом 1М HCl. Значения поглощения при 450 нм считывали на планшетном ридере EMax® (Molecular Devices), и концентрации человеческого IL-2 в супернатантах для анализа MLR рассчитывали по стандартным кривым.
[00217] Как показано на фиг. 14A-14B, комбинация пембролизумаба и шестивалентного 3×1D10v6-Fc усиливала продуцирование IL-2 CD4+ Т-клетками в реакции смешанной культуры лимфоцитов (MLR). Эти результаты демонстрируют преимущество, обеспечиваемое комбинацией блокады оси PD-1/PD-L1 с агонизмом OX40.
Пример 9: Оценка фармакокинетических свойств шестивалентного 3×1D10v6-Fc
[00218] Фармакокинетические (PK) свойства и токсикокинетический профиль терапевтического агента важны для понимания отношений доза/воздействие, скорости клиренса и профиля безопасности. Ослабленное воздействие и/или профиль ускоренного клиренса могут выявить недостатки в самом агенте, вызванные неспецифическими взаимодействиями, плохой стабильностью или иммуногенностью; или в мишени, что подтверждается токсичностью или изменениями в распределении лекарственного средства. Обычно фармакокинетические свойства терапевтических антител оценивают на грызунах и/или приматах, не относящихся к человеку. Плохие PK параметры в этих моделях могут указывать на неспецифическое связывание и быстрый клиренс антитела.
[00219] Шестивалентное 3×1D10v6Fc вводили путем внутривенной инъекции яванским макакам (5 самцов и 5 самок в группе) в дозах 5 мг/кг, 20 мг/кг и 60 мг/кг. Количественный метод ELISA использовали для определения концентраций шестивалентного 3×1D10v6-Fc в сыворотке, по существу, следующим образом. Лунки микропланшетов предварительно покрывали рекомбинантной формой внеклеточного домена OX40 человека, слитого с Fc-доменом мыши (OX40-mFc). После блокирования и промывки титры шестивалентного 3×1D10v6-Fc (для стандартной кривой), контрольные образцы, содержащие заранее определенные концентрации шестивалентного 3×1D10v6-Fc, и тестируемые образцы добавляли в лунки и инкубировали для обеспечения связывания шестивалентного 3×1D10v6Fc, содержащегося в образцах, с иммобилизованным OX40-mFc. Планшеты промывали, и добавляли конъюгированное с пероксидазой хрена (HRP) вторичное человеческое IgG антитело, специфическое к Fcγ-фрагменту, для детектирования связанного с планшетом шестивалентного 3×1D10v6Fc. В лунки добавляли раствор, содержащий тетраметилбензидин (TMB), субстрат HRP, что обеспечивало колориметрический сигнал, который пропорционален концентрации конъюгированного с HRP человеческого IgG антитела, связанного с шестивалентным 3×1D10v6-Fc. Реакцию останавливали добавлением кислого раствора и определяли оптическую плотность при 450 нм. Для контрольных и тестируемых образцов преобразование значений спектрофотометрической абсорбции (количественно определяемой по оптической плотности [OD450]) в концентрацию выполняли путем сравнения с параллельно анализируемой калибровочной кривой, построенной с помощью четырехпараметрической логистической регрессионной модели (4-PL). Нижний предел количественного определения (LLOQ) шестивалентного 3×1D10v6Fc в сыворотке этим методом составил 100 нг/мл.
[00220] Системное воздействие (Cmax и AUC0-168h) достигалось во всем диапазоне доз, которое увеличивалось пропорционально дозе, без гендерных различий. В диапазоне доз от 5 до 60 мг/кг, в случае использования некомпартментного анализа, среднее значение T1/2 по группам составляло 55-89,7 часа, скорость клиренса (CL) находилась в пределах 0,683-0,832 мл/ч/кг, и объем распределения в равновесном состоянии (Vdss) составлял 55,9-86,2 мл/кг. PK-профиль шестивалентного 3×1D10v6-Fc показан на фиг. 15.
[00221] Эти результаты демонстрируют, что шестивалентное 3×1D10v6-Fc имеет хороший PK-профиль, подходящий для терапевтического применения, и позволяет предположить уменьшение неспецифического связывания, наблюдаемого для 1D10v1.
[00222] Осуществление изобретения возможно в других конкретных формах без отступления от его сущности или существенных характеристик. Следовательно, вышеизложенные варианты осуществления следует рассматривать во всех отношениях как иллюстративные, а не ограничивающие изобретение. Следовательно, объем изобретения определен прилагаемой формулой изобретения, а не предшествующим описанием, и все изменения, которые попадают в смысловое содержание и диапазон эквивалентности формулы изобретения входят в объем изобретения.
Таблица определенных последовательностей
--->
СПИСКИ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> INHIBRX, INC.
<120> OX40-СВЯЗЫВАЮЩИЕ ПОЛИПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ
<130> 01202-0014-00PCT
<150> US 62/718,106
<151> 2018-08-13
<160> 34
<170> PatentIn version 3.5
<210> 1
<211> 277
<212> Белок
<213> Homo sapiens
<400> 1
Met Cys Val Gly Ala Arg Arg Leu Gly Arg Gly Pro Cys Ala Ala Leu
1 5 10 15
Leu Leu Leu Gly Leu Gly Leu Ser Thr Val Thr Gly Leu His Cys Val
20 25 30
Gly Asp Thr Tyr Pro Ser Asn Asp Arg Cys Cys His Glu Cys Arg Pro
35 40 45
Gly Asn Gly Met Val Ser Arg Cys Ser Arg Ser Gln Asn Thr Val Cys
50 55 60
Arg Pro Cys Gly Pro Gly Phe Tyr Asn Asp Val Val Ser Ser Lys Pro
65 70 75 80
Cys Lys Pro Cys Thr Trp Cys Asn Leu Arg Ser Gly Ser Glu Arg Lys
85 90 95
Gln Leu Cys Thr Ala Thr Gln Asp Thr Val Cys Arg Cys Arg Ala Gly
100 105 110
Thr Gln Pro Leu Asp Ser Tyr Lys Pro Gly Val Asp Cys Ala Pro Cys
115 120 125
Pro Pro Gly His Phe Ser Pro Gly Asp Asn Gln Ala Cys Lys Pro Trp
130 135 140
Thr Asn Cys Thr Leu Ala Gly Lys His Thr Leu Gln Pro Ala Ser Asn
145 150 155 160
Ser Ser Asp Ala Ile Cys Glu Asp Arg Asp Pro Pro Ala Thr Gln Pro
165 170 175
Gln Glu Thr Gln Gly Pro Pro Ala Arg Pro Ile Thr Val Gln Pro Thr
180 185 190
Glu Ala Trp Pro Arg Thr Ser Gln Gly Pro Ser Thr Arg Pro Val Glu
195 200 205
Val Pro Gly Gly Arg Ala Val Ala Ala Ile Leu Gly Leu Gly Leu Val
210 215 220
Leu Gly Leu Leu Gly Pro Leu Ala Ile Leu Leu Ala Leu Tyr Leu Leu
225 230 235 240
Arg Arg Asp Gln Arg Leu Pro Pro Asp Ala His Lys Pro Pro Gly Gly
245 250 255
Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala Asp Ala His Ser
260 265 270
Thr Leu Ala Lys Ile
275
<210> 2
<211> 277
<212> Белок
<213> Macaca fascicularis
<400> 2
Met Cys Val Gly Ala Arg Arg Leu Gly Arg Gly Pro Cys Ala Ala Leu
1 5 10 15
Leu Leu Leu Gly Leu Gly Leu Ser Thr Thr Ala Lys Leu His Cys Val
20 25 30
Gly Asp Thr Tyr Pro Ser Asn Asp Arg Cys Cys Gln Glu Cys Arg Pro
35 40 45
Gly Asn Gly Met Val Ser Arg Cys Asn Arg Ser Gln Asn Thr Val Cys
50 55 60
Arg Pro Cys Gly Pro Gly Phe Tyr Asn Asp Val Val Ser Ala Lys Pro
65 70 75 80
Cys Lys Ala Cys Thr Trp Cys Asn Leu Arg Ser Gly Ser Glu Arg Lys
85 90 95
Gln Pro Cys Thr Ala Thr Gln Asp Thr Val Cys Arg Cys Arg Ala Gly
100 105 110
Thr Gln Pro Leu Asp Ser Tyr Lys Pro Gly Val Asp Cys Ala Pro Cys
115 120 125
Pro Pro Gly His Phe Ser Pro Gly Asp Asn Gln Ala Cys Lys Pro Trp
130 135 140
Thr Asn Cys Thr Leu Ala Gly Lys His Thr Leu Gln Pro Ala Ser Asn
145 150 155 160
Ser Ser Asp Ala Ile Cys Glu Asp Arg Asp Pro Pro Pro Thr Gln Pro
165 170 175
Gln Glu Thr Gln Gly Pro Pro Ala Arg Pro Thr Thr Val Gln Pro Thr
180 185 190
Glu Ala Trp Pro Arg Thr Ser Gln Arg Pro Ser Thr Arg Pro Val Glu
195 200 205
Val Pro Arg Gly Pro Ala Val Ala Ala Ile Leu Gly Leu Gly Leu Ala
210 215 220
Leu Gly Leu Leu Gly Pro Leu Ala Met Leu Leu Ala Leu Leu Leu Leu
225 230 235 240
Arg Arg Asp Gln Arg Leu Pro Pro Asp Ala Pro Lys Ala Pro Gly Gly
245 250 255
Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala Asp Ala His Ser
260 265 270
Ala Leu Ala Lys Ile
275
<210> 3
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1
<400> 3
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Gly Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro
115
<210> 4
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1 CDR1
<400> 4
Gly Phe Thr Phe Ser Asp Ala Phe
1 5
<210> 5
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1 CDR2
<400> 5
Ile Ser Asn Arg Gly Leu Lys Thr
1 5
<210> 6
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1 CDR3
<400> 6
Ser Arg Asp Val Asp Gly Asp Phe
1 5
<210> 7
<211> 346
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1-Fc (бивалентное)
<400> 7
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Gly Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro Gly Gly Gly Gly Asp Lys Thr His Thr Cys Pro Pro Cys
115 120 125
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
130 135 140
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
145 150 155 160
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
165 170 175
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
180 185 190
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
195 200 205
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
210 215 220
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
225 230 235 240
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
245 250 255
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
260 265 270
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
275 280 285
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
290 295 300
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
305 310 315 320
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
325 330 335
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
340 345
<210> 8
<211> 588
<212> Белок
<213> Искусственная последовательность
<220>
<223> 3x1D10v1-Fc (шестивалентеное; также упоминаемое как Hex-1D10v1)
<400> 8
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Gly Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro Gly Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser
115 120 125
Gly Gly Gly Glu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Ser Asp Ala Phe Met Tyr Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Asn Arg Gly
165 170 175
Leu Lys Thr Ala Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser
180 185 190
Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg
195 200 205
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Asp Val Asp Gly Asp
210 215 220
Phe Arg Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Ser Gly
225 230 235 240
Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro
245 250 255
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
260 265 270
Asp Ala Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
275 280 285
Trp Val Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu
290 295 300
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
305 310 315 320
Leu Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
325 330 335
Tyr Cys Ser Arg Asp Val Asp Gly Asp Phe Arg Gly Gln Gly Thr Leu
340 345 350
Val Thr Val Lys Pro Gly Gly Gly Gly Asp Lys Thr His Thr Cys Pro
355 360 365
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
370 375 380
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
385 390 395 400
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
405 410 415
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
420 425 430
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
435 440 445
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
450 455 460
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
465 470 475 480
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
485 490 495
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
500 505 510
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
515 520 525
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
530 535 540
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
545 550 555 560
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
565 570 575
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
580 585
<210> 9
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6
<400> 9
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Ala Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro
115
<210> 10
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6 CDR1
<400> 10
Gly Phe Thr Phe Ser Asp Ala Phe
1 5
<210> 11
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6 CDR2
<400> 11
Ile Ser Asn Arg Gly Leu Lys Thr
1 5
<210> 12
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6 CDR3
<400> 12
Ser Arg Asp Val Asp Ala Asp Phe
1 5
<210> 13
<211> 346
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6-Fc (bivalent)
<400> 13
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Ala Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro Gly Gly Gly Gly Asp Lys Thr His Thr Cys Pro Pro Cys
115 120 125
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
130 135 140
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
145 150 155 160
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
165 170 175
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
180 185 190
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
195 200 205
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
210 215 220
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
225 230 235 240
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
245 250 255
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
260 265 270
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
275 280 285
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
290 295 300
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
305 310 315 320
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
325 330 335
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
340 345
<210> 14
<211> 357
<212> Белок
<213> Искусственная последовательность
<220>
<223> 3x1D10v6
<400> 14
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Ala Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro Gly Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser
115 120 125
Gly Gly Gly Glu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Ser Asp Ala Phe Met Tyr Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Glu Arg Glu Trp Val Ser Ser Ile Ser Asn Arg Gly
165 170 175
Leu Lys Thr Ala Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser
180 185 190
Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg
195 200 205
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Asp Val Asp Ala Asp
210 215 220
Phe Arg Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Ser Ser
225 230 235 240
Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro
245 250 255
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
260 265 270
Asp Ala Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu
275 280 285
Trp Val Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu
290 295 300
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
305 310 315 320
Leu Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
325 330 335
Tyr Cys Ser Arg Asp Val Asp Ala Asp Phe Arg Gly Gln Gly Thr Leu
340 345 350
Val Thr Val Lys Pro
355
<210> 15
<211> 588
<212> Белок
<213> Искусственная последовательность
<220>
<223> 3x1D10v6-Fc (шестивалентное; также упоминаемое как Hex-1D10v6)
<400> 15
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Ala Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro Gly Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser
115 120 125
Gly Gly Gly Glu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Ser Asp Ala Phe Met Tyr Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Glu Arg Glu Trp Val Ser Ser Ile Ser Asn Arg Gly
165 170 175
Leu Lys Thr Ala Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser
180 185 190
Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg
195 200 205
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Asp Val Asp Ala Asp
210 215 220
Phe Arg Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Ser Ser
225 230 235 240
Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro
245 250 255
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
260 265 270
Asp Ala Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu
275 280 285
Trp Val Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu
290 295 300
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
305 310 315 320
Leu Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
325 330 335
Tyr Cys Ser Arg Asp Val Asp Ala Asp Phe Arg Gly Gln Gly Thr Leu
340 345 350
Val Thr Val Lys Pro Gly Gly Gly Gly Asp Lys Thr His Thr Cys Pro
355 360 365
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
370 375 380
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
385 390 395 400
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
405 410 415
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
420 425 430
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
435 440 445
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
450 455 460
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
465 470 475 480
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
485 490 495
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
500 505 510
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
515 520 525
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
530 535 540
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
545 550 555 560
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
565 570 575
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
580 585
<210> 16
<211> 467
<212> Белок
<213> Искусственная последовательность
<220>
<223> 2x1D10v6-Fc (четырехвалентное)
<400> 16
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Phe Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu Trp Val
35 40 45
Ser Ser Ile Ser Asn Arg Gly Leu Lys Thr Ala Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Val Asp Ala Asp Phe Arg Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Lys Pro Gly Gly Ser Ser Gly Ser Glu Val Gln Leu Leu Glu Ser
115 120 125
Gly Gly Gly Glu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Ser Asp Ala Phe Met Tyr Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Glu Arg Glu Trp Val Ser Ser Ile Ser Asn Arg Gly
165 170 175
Leu Lys Thr Ala Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser
180 185 190
Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg
195 200 205
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Asp Val Asp Ala Asp
210 215 220
Phe Arg Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Gly Gly
225 230 235 240
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
245 250 255
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
260 265 270
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
275 280 285
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
290 295 300
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
305 310 315 320
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
325 330 335
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
340 345 350
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
355 360 365
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
370 375 380
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
385 390 395 400
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
405 410 415
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
420 425 430
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
435 440 445
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
450 455 460
Pro Gly Lys
465
<210> 17
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1 FR1
<400> 17
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 18
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1 FR2
<400> 18
Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
1 5 10 15
Ser
<210> 19
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1 FR3
<400> 19
Ala Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ala Lys Asn Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 20
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v1 FR4
<400> 20
Arg Gly Gln Gly Thr Leu Val Thr Val Lys Pro
1 5 10
<210> 21
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6 FR1
<400> 21
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 22
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6 FR2
<400> 22
Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Glu Arg Glu Trp Val Ser
1 5 10 15
Ser
<210> 23
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6 FR3
<400> 23
Ala Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ala Lys Asn Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 24
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> 1D10v6 FR4
<400> 24
Arg Gly Gln Gly Thr Leu Val Thr Val Lys Pro
1 5 10
<210> 25
<211> 227
<212> Белок
<213> Homo sapiens
<400> 25
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
130 135 140
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly Lys
225
<210> 26
<211> 224
<212> Белок
<213> Homo sapiens
<400> 26
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly Pro Ser
1 5 10 15
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
20 25 30
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
35 40 45
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
50 55 60
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
65 70 75 80
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
85 90 95
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
100 105 110
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
115 120 125
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
130 135 140
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
145 150 155 160
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
165 170 175
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
180 185 190
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
195 200 205
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215 220
<210> 27
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: сигнальный домен CD3-дзета
<400> 27
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 28
<211> 42
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: сигнальный домен, полученный из CD28 или 4-1BB
<400> 28
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 29
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: сигнальный домен, полученный из CD28 или 4-1BB
<400> 29
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
1 5 10 15
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
20 25 30
Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 30
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: сигнальный домен, полученный из CD28 или 4-1BB
<400> 30
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 31
<211> 44
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: сигнальный домен, полученный из CD28 или 4-1BB
<400> 31
Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met
1 5 10 15
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
20 25 30
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 32
<211> 71
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: шарнир или трансмембранный домен, полученный из CD8
<400> 32
Lys Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
1 5 10 15
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala
20 25 30
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Ser Asp Ile
35 40 45
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
50 55 60
Leu Val Ile Thr Leu Tyr Cys
65 70
<210> 33
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: шарнир или трансмембранный домен, полученный из CD8
<400> 33
Ala Lys Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
1 5 10 15
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
20 25 30
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
50 55 60
<210> 34
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический: шарнир или трансмембранный домен, полученный из CD8
<400> 34
Val Leu Leu Leu Ser Leu Val Ile Thr
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИ-ОХ40 АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2753493C2 |
| БИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2766199C2 |
| БИСПЕЦИФИЧЕСКИЕ 2+1 КОНТОРСТЕЛА | 2018 |
|
RU2797305C2 |
| МОЛЕКУЛЫ АНТИТЕЛ, КОТОРЫЕ СВЯЗЫВАЮТ CD137 И OX40 | 2019 |
|
RU2817602C2 |
| АНТИТЕЛА ПРОТИВ OX40 И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2783314C2 |
| АНТИ-TIGIT АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2732591C2 |
| ИММУНОЦИТОКИНЫ И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2818371C1 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, СПЕЦИФИЧЕСКИЕ В ОТНОШЕНИИ КОСТИМУЛЯТОРНОГО TNF-РЕЦЕПТОРА | 2016 |
|
RU2761115C1 |
| АНТИ-TIGIT АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2817838C2 |
| ПОЛИВАЛЕНТНЫЕ И ПОЛИСПЕЦИФИЧЕСКИЕ ОХ40-СВЯЗЫВАЮЩИЕ СЛИТЫЕ БЕЛКИ | 2017 |
|
RU2773052C2 |
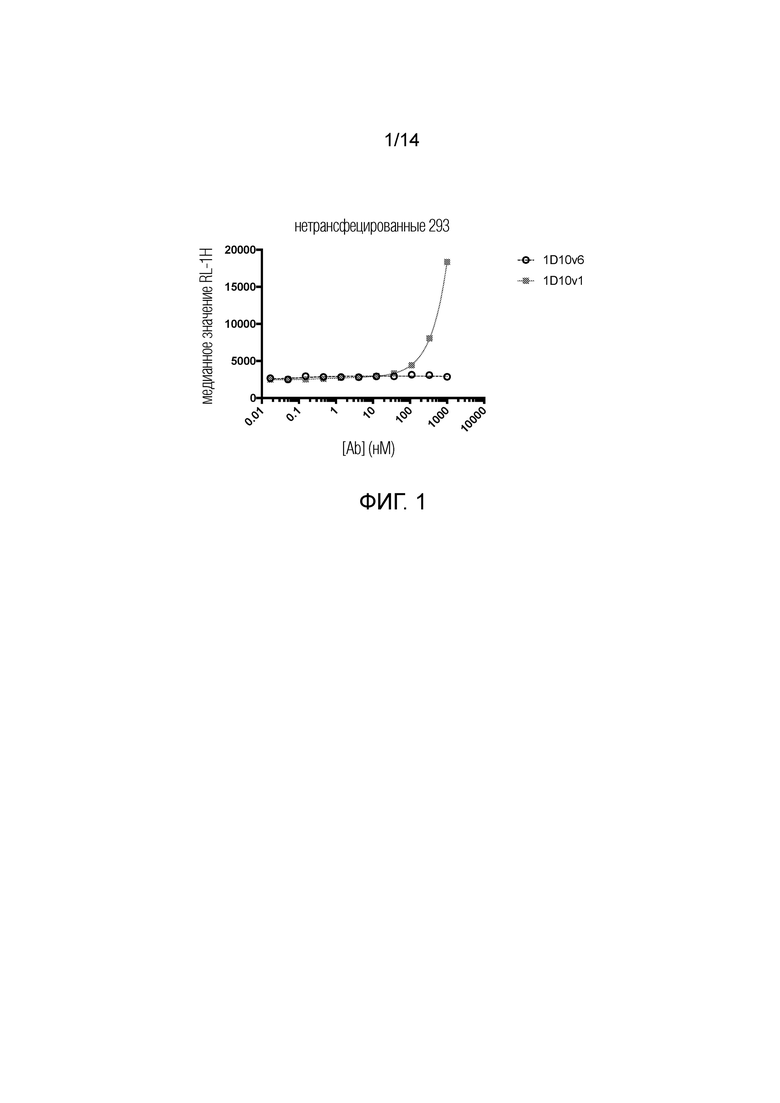
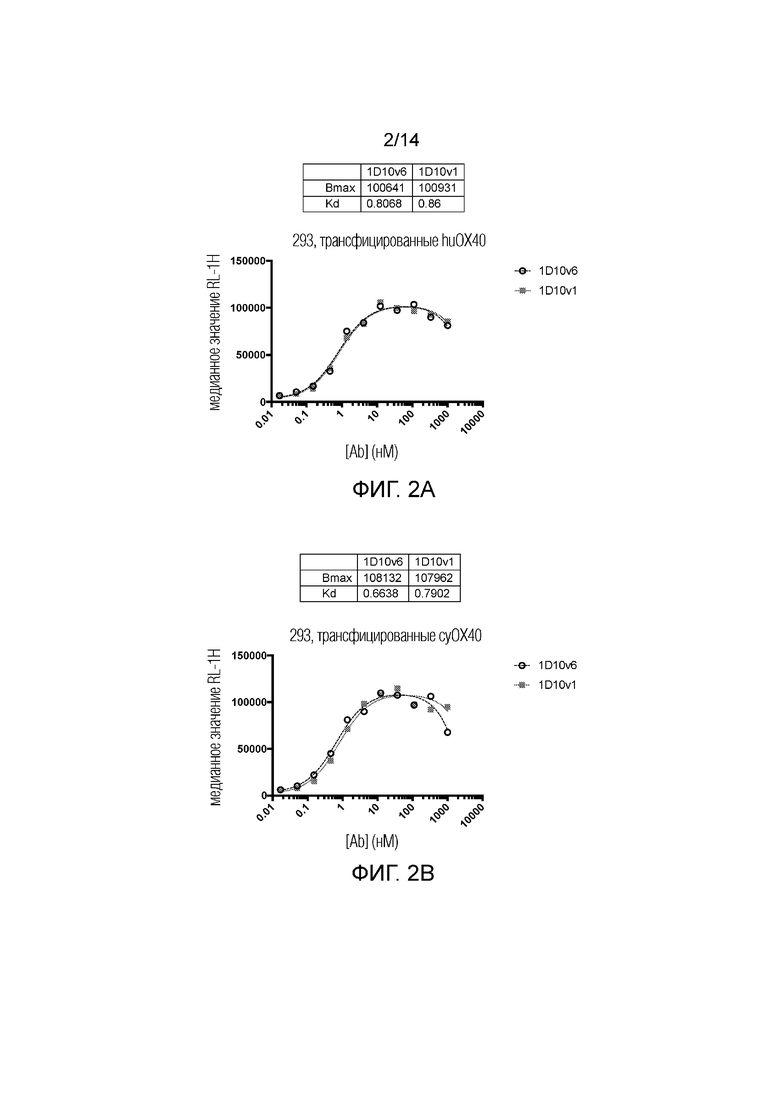
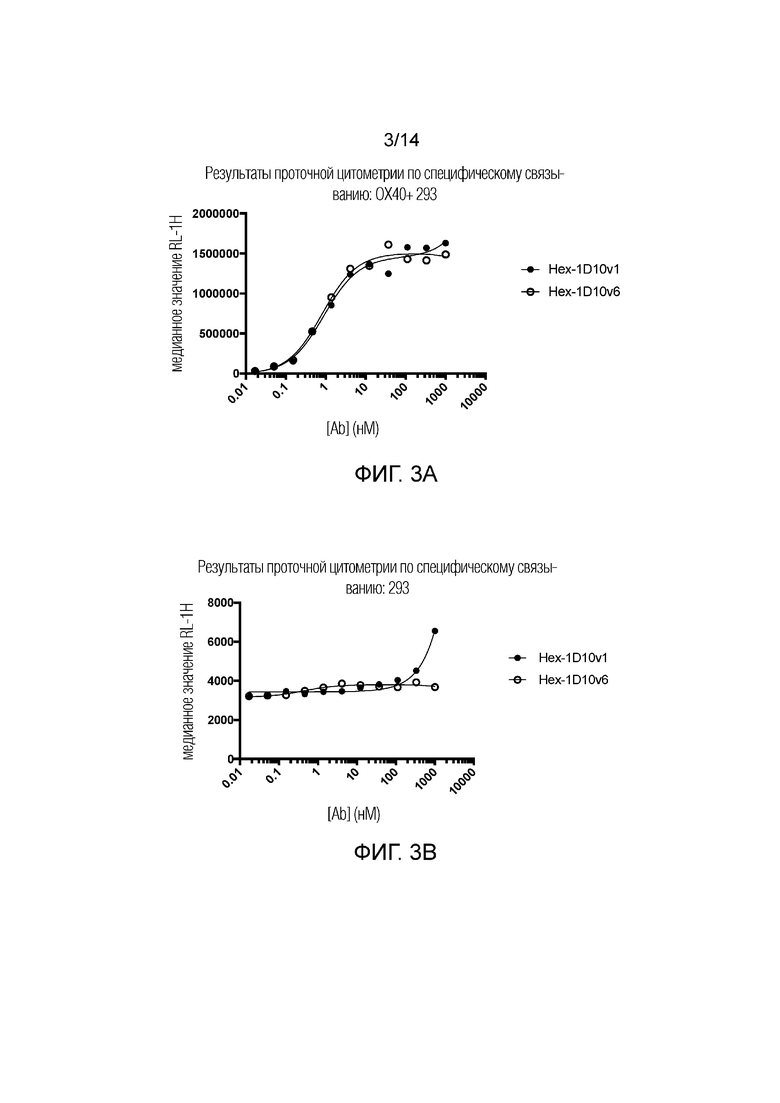
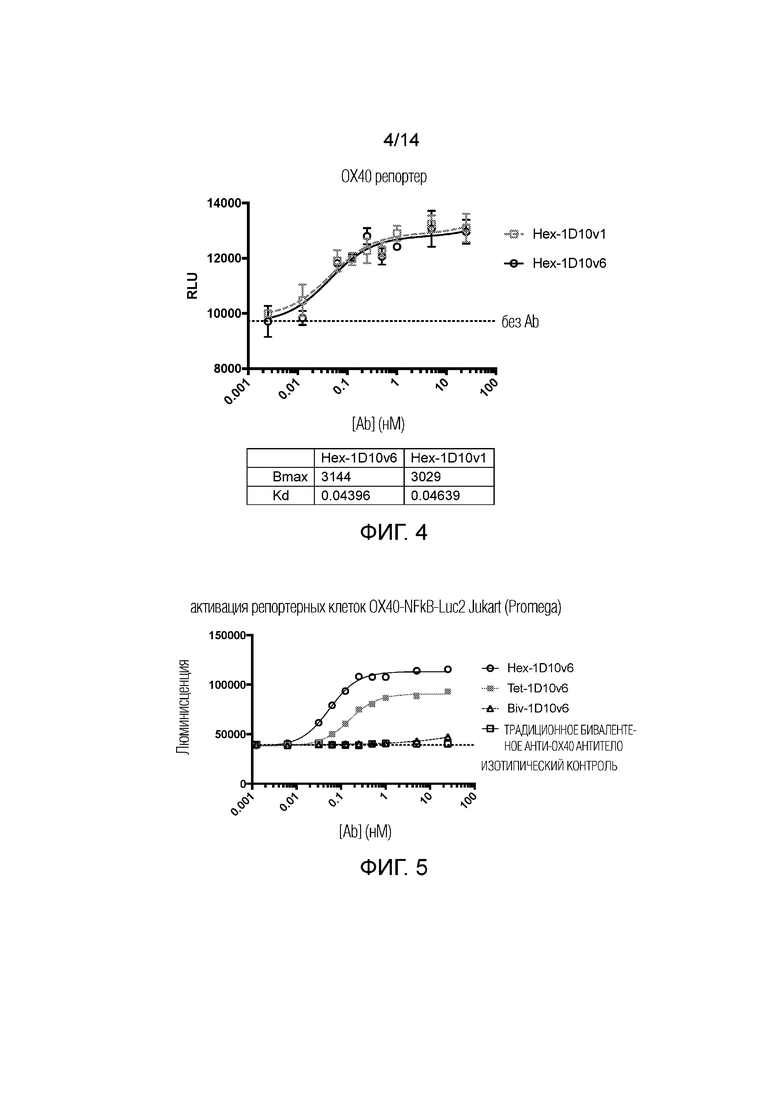
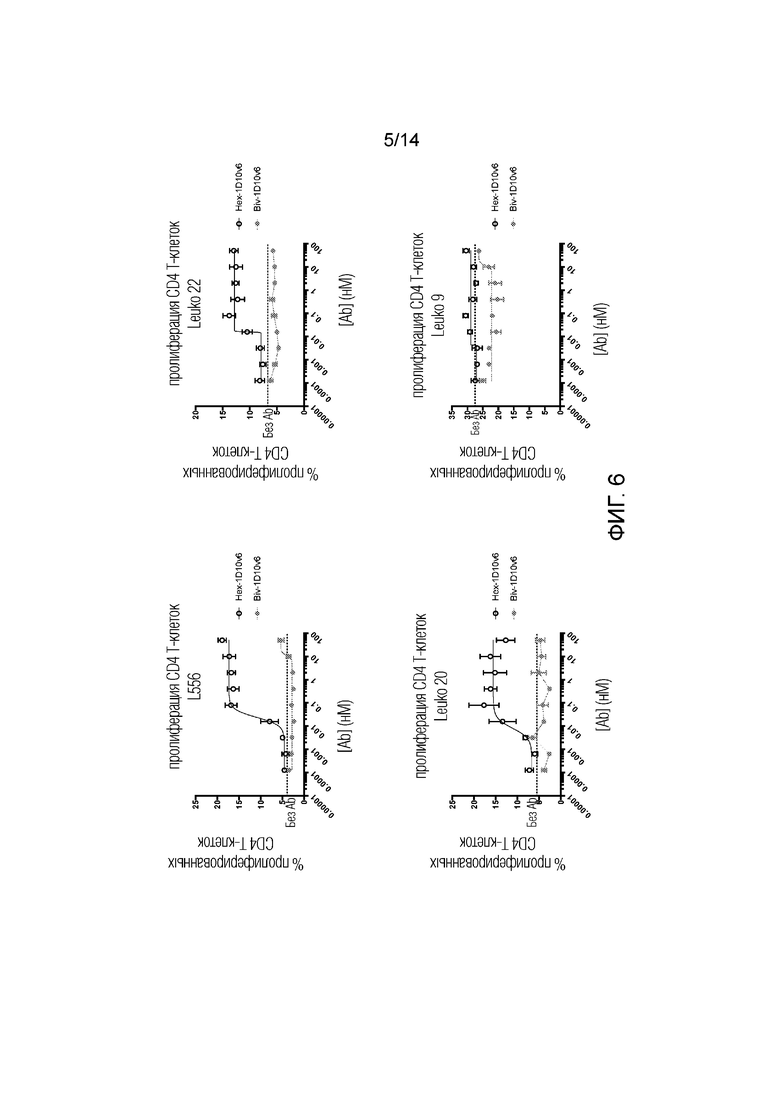
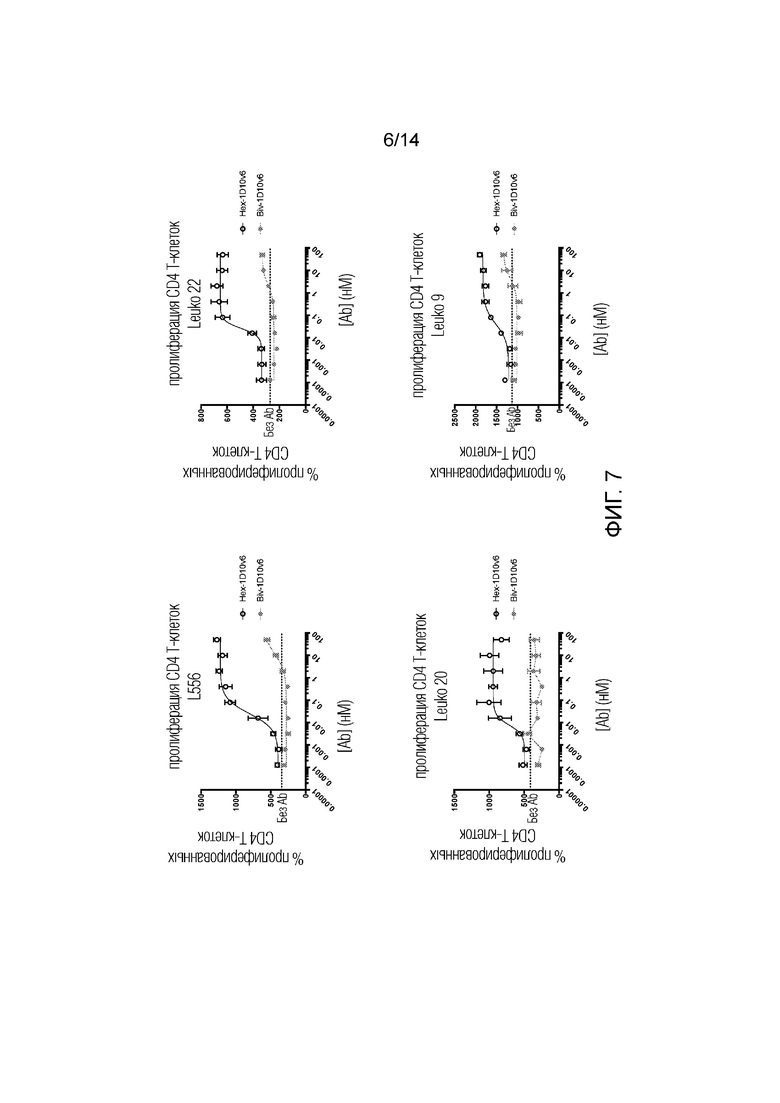
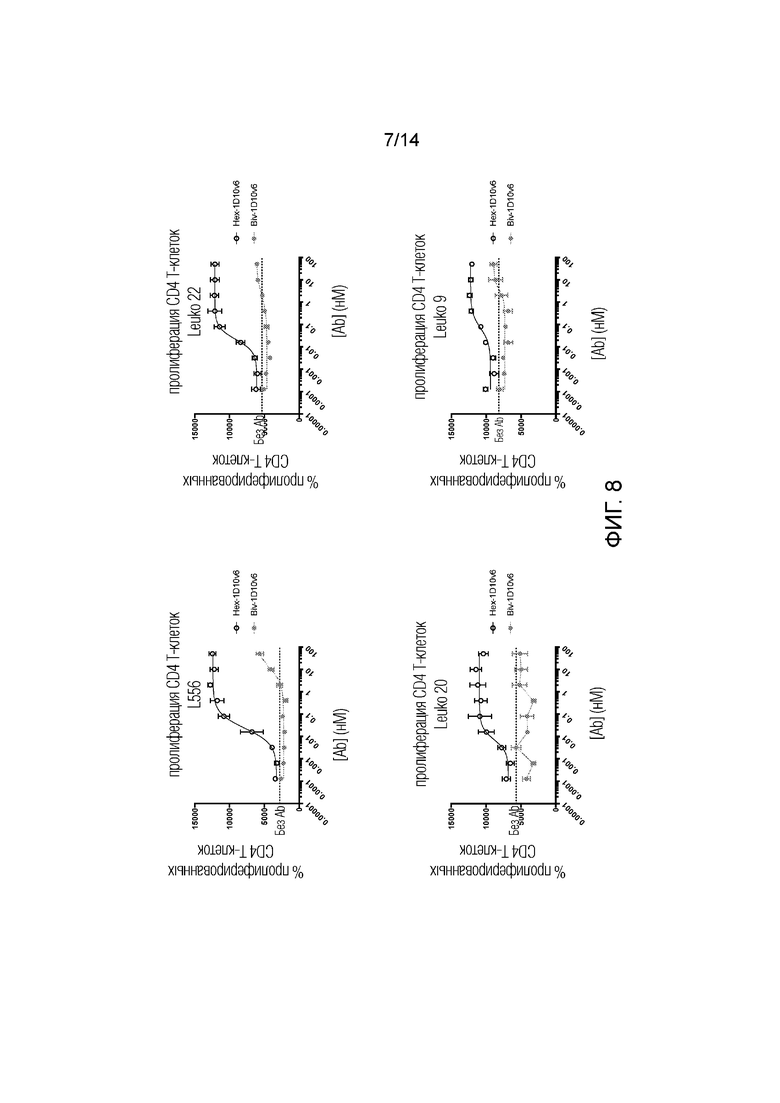
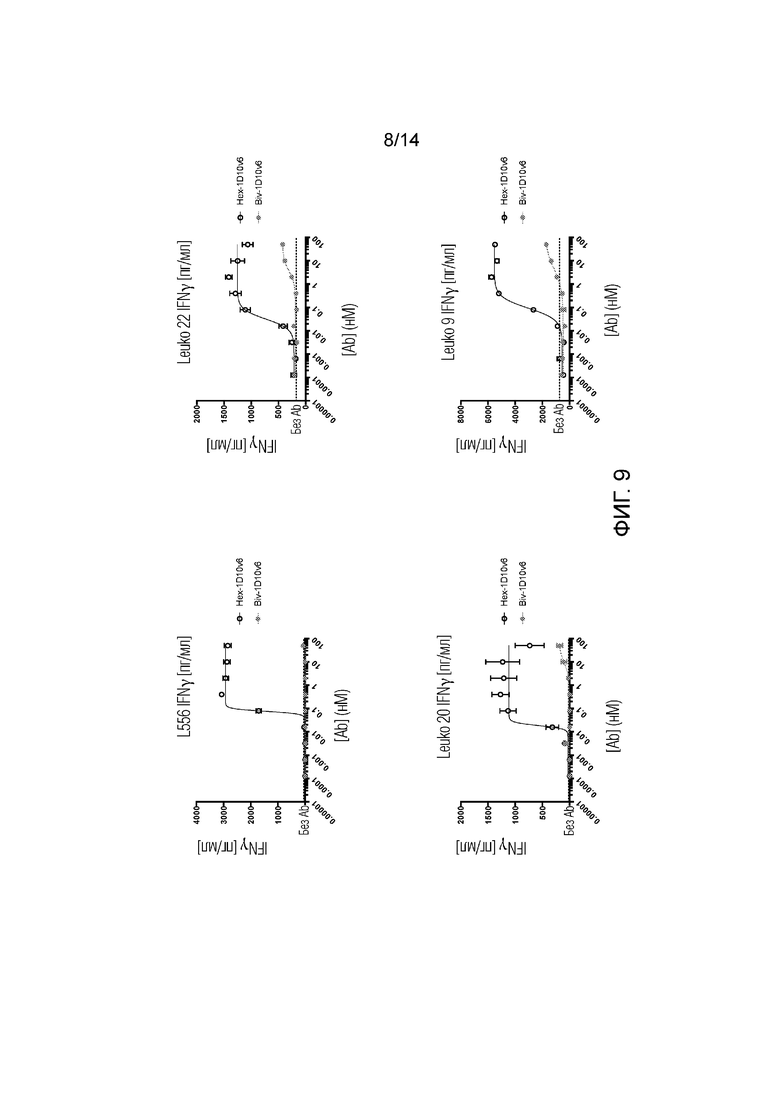
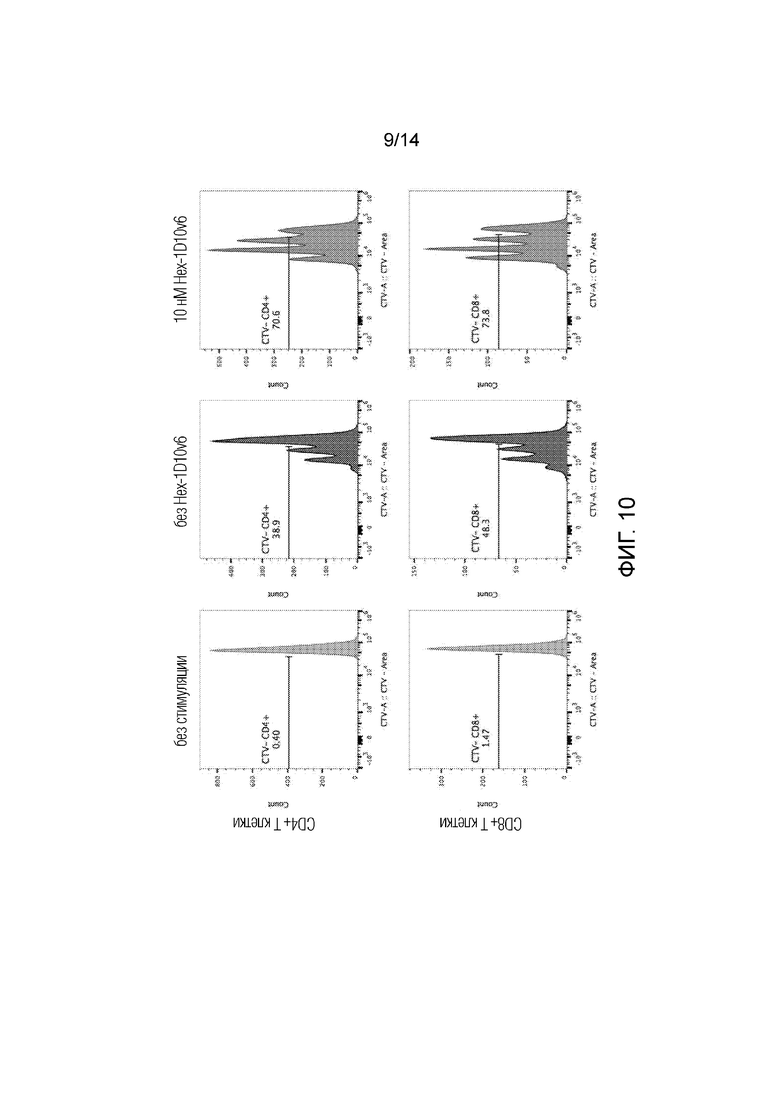
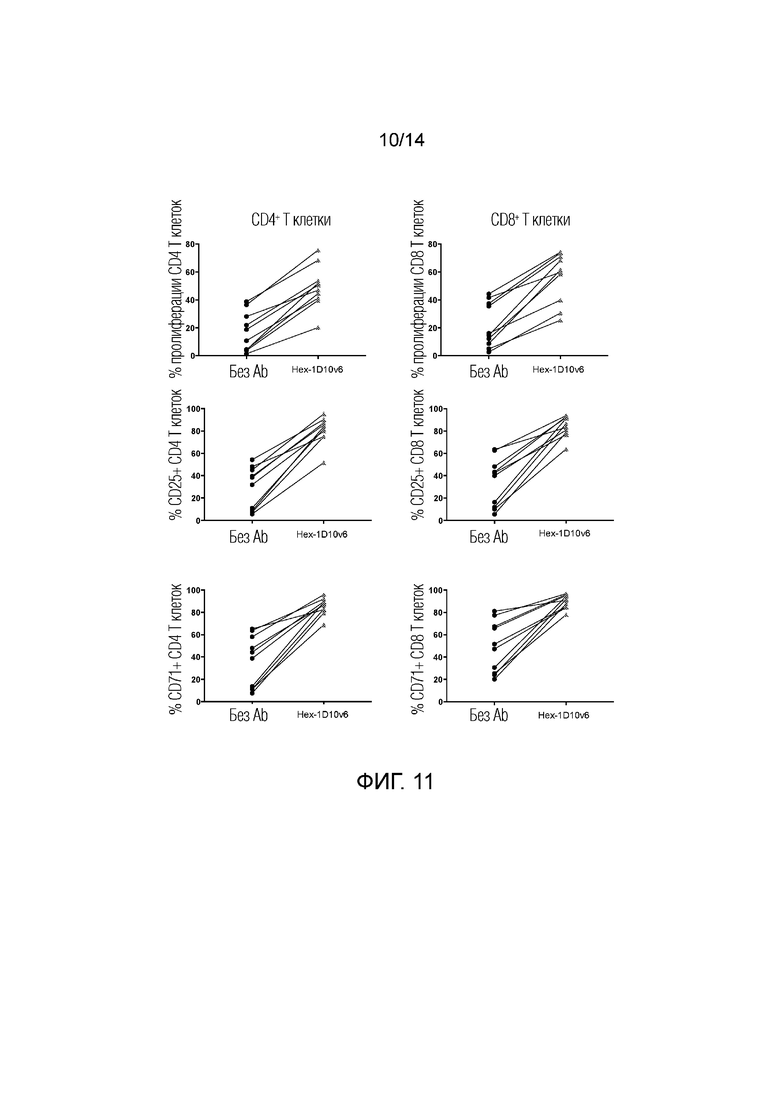

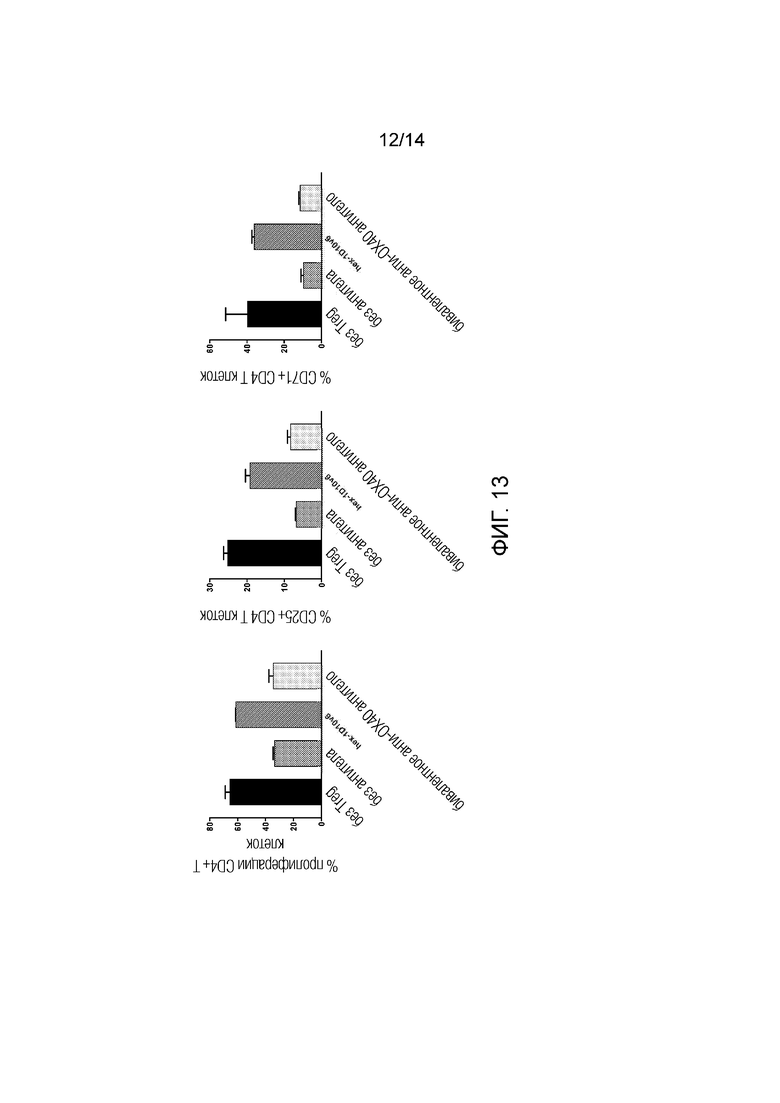
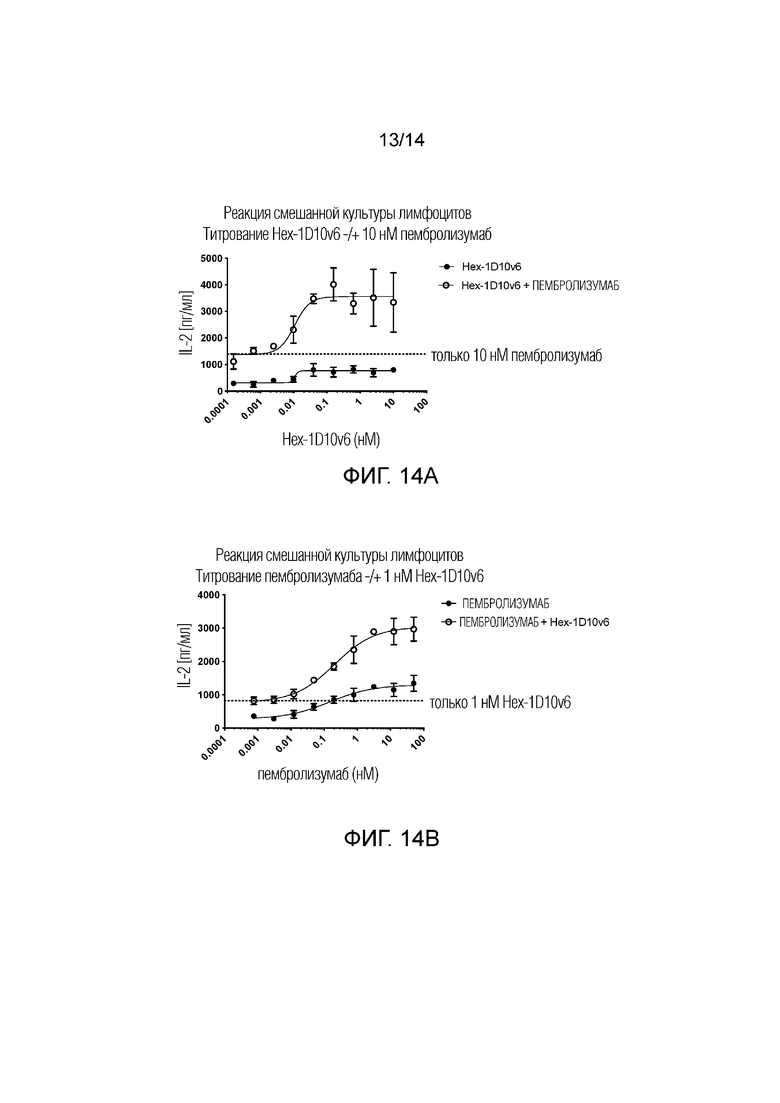
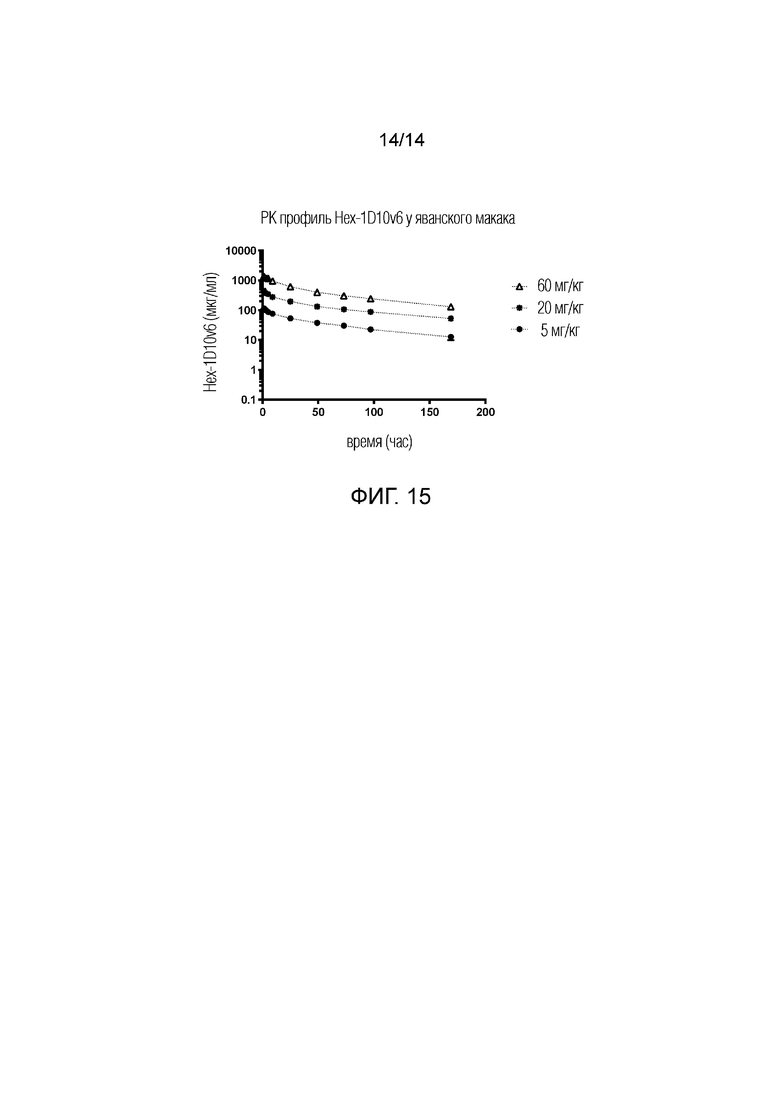
Изобретение относится к области биотехнологии, конкретно к полипептидам, которые связываются с OX40, и может быть использовано в медицине для лечения рака. Предложен полипептид, связывающийся с OX40, содержащий по меньшей мере один домен VHH, который связывается с OX40 и содержит аминокислотную последовательность SEQ ID NO: 9, и домен Fc. Изобретение обеспечивает получение однодоменного антитела (sdAb), которое в бивалентном формате имеет пониженное неспецифическое связывание с нетрансфицированными клетками HEK293 по сравнению с 1D10v1-Fc, а в шестивалентном формате, помимо пониженного неспецифического связывания по сравнению с шестивалентным 3x1D10v1-Fc, является также более эффективным агонистом OX40 по сравнению с двухвалентным и четырехвалентным вариантами. 13 н. и 47 з.п. ф-лы, 15 ил., 3 табл., 9 пр.
1. Полипептид, связывающийся с OX40, содержащий по меньшей мере один домен VHH, который связывается с OX40, и домен Fc, причем домен VHH содержит аминокислотную последовательность SEQ ID NO: 9.
2. Полипептид по п. 1, содержащий два домена VHH, причем каждый домен VHH связывается с OX40.
3. Полипептид по п. 1, содержащий три домена VHH, причем каждый домен VHH связывается с OX40.
4. Полипептид по п. 1, содержащий четыре домена VHH, причем каждый домен VHH связывается с OX40.
5. Полипептид по любому из пп. 1-4, в котором каждый домен VHH содержит аминокислотную последовательность SEQ ID NO: 9.
6. Полипептид по любому из пп. 1-5, в котором Fc-домен содержит аминокислотную последовательность, выбранную из SEQ ID NO: 25 и 26.
7. Полипептид по любому из пп. 1-6, содержащий аминокислотную последовательность SEQ ID NO: 14.
8. Полипептид по любому из пп. 1-7, содержащий аминокислотную последовательность SEQ ID NO: 15.
9. Полипептид, связывающийся с OX40, состоящий из аминокислотной последовательности SEQ ID NO: 15.
10. Полипептид по любому из пп. 1-9, который образует димер в физиологических условиях.
11. Полипептид по любому из пп. 1-10, усиливающий пролиферацию CD4+ и/или CD8+ Т-клеток in vitro и/или in vivo.
12. Полипептид по п. 11, усиливающий пролиферацию CD4+ и/или CD8+ Т-клеток в присутствии Treg-клеток.
13. Полипептид по п. 11 или 12, усиливающий пролиферацию CD4+ и/или CD8+ Т-клеток in vitro по меньшей мере в 1,5 раза или по меньшей мере в 2 раза.
14. Полипептид по любому из пп. 1-13, усиливающий экспрессию CD25 на CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo.
15. Полипептид по п. 14, усиливающий экспрессию CD25 на CD4+ и/или CD8+ Т-клетках in vitro по меньшей мере в 1,5 раза или по меньшей мере в 2 раза.
16. Полипептид по любому из пп. 1-15, усиливающий экспрессию CD71 на CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo.
17. Полипептид по п. 16, усиливающий экспрессию CD71 на CD4+ и/или CD8+ Т-клетках in vitro по меньшей мере в 1,5 раза или по меньшей мере в 2 раза.
18. Полипептид по любому из пп. 1-17, усиливающий сигнализацию NFκB в CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo.
19. Полипептид по п. 18, усиливающий сигнализацию NFκB в CD4+ и/или CD8+ T-клетках in vitro по меньшей мере в 1,5 раза, по меньшей мере в 2 раза, по меньшей мере в 3 раза или по меньшей мере в 5 раз.
20. Полипептид по любому из пп. 1-19, усиливающий экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках in vitro и/или in vivo.
21. Полипептид по п. 20, усиливающий экспрессию IFNγ в CD4+ и/или CD8+ Т-клетках in vitro по меньшей мере в 1,5 раза, по меньшей мере в 2 раза, по меньшей мере в 3 раза или по меньшей мере в 5 раз.
22. Полипептид по любому из пп. 13-21, усиливающий экспрессию в присутствии Treg-клеток.
23. Полипептид по любому из пп. 11-21, где усиление определяют как среднее значение результатов, полученных для Т-клеток от по меньшей мере пяти или по меньшей мере десяти разных здоровых доноров-людей.
24. Полипептид по любому из пп. 1-23, который является агонистом биологической активности OX40.
25. Полипептид по любому из пп. 1-24, где OX40 представляет собой OX40 человека.
26. Полипептид по любому из пп. 1-25, который связывается с человеческим OX40 с аффинностью (KD) менее 10 нМ, менее 5 нМ, менее 2 нМ или менее 1 нМ.
27. Полипептид по любому из пп. 1-26, который связывается с OX40 яванского макака с аффинностью (KD) менее 10 нМ, менее 5 нМ, менее 2 нМ или менее 1 нМ.
28. Фармацевтическая композиция для лечения рака, содержащая эффективное количество полипептида по любому из пп. 1-27 и фармацевтически приемлемый носитель.
29. Выделенная нуклеиновая кислота, кодирующая полипептид по любому из пп. 1-27.
30. Вектор экспрессии для экспрессии OX40-связывающего полипептида по любому из пп. 1-27, содержащий нуклеиновую кислоту по п. 29.
31. Клетка-хозяин для экспрессии OX40-связывающего полипептида по любому из пп. 1-27, содержащая вектор экспрессии по п. 30, причем клетка-хозяин не является эмбриональной стволовой клеткой человека.
32. Клетка-хозяин по п. 31, которая секретирует полипептид по любому из пп. 1-27.
33. Клетка-хозяин по п. 31 или 32, которая является первичной клеткой человека.
34. Клетка-хозяин по п. 33, которая является первичной Т-клеткой человека.
35. Клетка-хозяин по любому из пп. 31-34, которая представляет собой Т-клетку с химерным антигенным рецептором (CAR).
36. Способ получения полипептида по любому из пп. 1-27, включающий инкубацию клетки-хозяина по п. 31 или 32 в условиях, подходящих для экспрессии полипептида.
37. Способ по п. 36, дополнительно включающий выделение полипептида.
38. Способ усиления пролиферации CD4+ Т-клеток, включающий контактирование Т-клеток с полипептидом по любому из пп. 1-27.
39. Способ усиления экспрессии CD25 на CD4+ Т-клетках, включающий контактирование Т-клеток с полипептидом по любому из пп. 1-27.
40. Способ усиления экспрессии CD71 на CD4+ Т-клетках, включающий контактирование Т-клеток с полипептидом по любому из пп. 1-27.
41. Способ усиления сигнализации NFκB в CD4+ Т-клетках, включающий контактирование Т-клеток с полипептидом по любому из пп. 1-27.
42. Способ усиления экспрессии IFNγ в CD4+ Т-клетках, включающий контактирование Т-клеток с полипептидом по любому из пп. 1-27.
43. Способ по любому из пп. 38-42, в котором CD4+ Т-клетки находятся in vitro.
44. Способ по любому из пп. 38-42, в котором CD4+ Т-клетки находятся in vivo.
45. Способ по п. 43 или 44, в котором CD4+ Т-клетки находятся в присутствии Treg-клеток.
46. Способ по любому из пп. 38-45, в котором усиление составляет по меньшей мере 1,5 раза, по меньшей мере 2 раза, по меньшей мере 3 раза или по меньшей мере 5 раз.
47. Способ лечения рака, включающий введение страдающему раком субъекту фармацевтически эффективного количества полипептида по любому из пп. 1-27 или фармацевтической композиции по п. 28.
48. Способ по п. 47, где рак выбирают из базальноклеточной карциномы, рака желчных путей; рака мочевого пузыря; рака кости; рака головного мозга и центральной нервной системы; рака молочной железы; рака брюшины; рака шейки матки; хориокарциномы; рака толстой и прямой кишки; рака соединительной ткани; рака пищеварительной системы; рака эндометрия; рака пищевода; рака глаза; рака головы и шеи; рака желудка; рака желудочно-кишечного тракта; глиобластомы; карциномы печени; гепатомы; внутриэпителиального новообразования; рака почек или почечного рака; рака гортани; рака печени; рака легкого; мелкоклеточного рака легкого; немелкоклеточного рака легкого; аденокарциномы легкого; плоскоклеточного рака легкого; меланомы; миеломы; нейробластомы; рака полости рта; рака яичников; панкреатического рака; рака простаты; ретинобластомы; рабдомиосаркомы; рака прямой кишки; рака дыхательной системы; карциномы слюнных желез; саркомы; рака кожи; плоскоклеточного рака; рака желудка; рака яичек; рака щитовидной железы; рака матки или эндометрия; рака мочевыводящей системы; рака вульвы; лимфомы; лимфомы Ходжкина; неходжкинской лимфомы; В-клеточной лимфомы; низкой степени злокачественности/фолликулярной неходжкинской лимфомы (НХЛ); НХЛ из малых лимфоцитов (МЛ); средней степени злокачественности/фолликулярной НХЛ; диффузной НХЛ средней степени злокачественности; иммунобластной НХЛ высокой степени злокачественности; лимфобластной НХЛ высокой степени злокачественности; НХЛ из мелких нерасщепленных клеток высокой степени злокачественности; массивного поражения НХЛ; лимфомы из клеток мантийной зоны; лимфомы, связанной со СПИДом; макроглобулинемии Вальденстрема; хронического лимфолейкоза (ХЛЛ); острого лимфобластного лейкоза (ОЛЛ); волосатоклеточного лейкоза; и хронического миелобластного лейкоза.
49. Способ по п. 47 или 48, дополнительно включающий введение дополнительного терапевтического агента.
50. Способ по п. 49, в котором дополнительный терапевтический агент представляет собой противораковый агент.
51. Способ по п. 50, в котором противораковый агент выбирают из химиотерапевтического агента, противоракового биологического агента, лучевой терапии, CAR-T терапии и онколитического вируса.
52. Способ по любому из пп. 49-51, в котором дополнительный терапевтический агент представляет собой противораковый биологический агент.
53. Способ по п. 52, в котором противораковый биологический агент представляет собой агент, который ингибирует PD-1 и/или PD-L1.
54. Способ по п. 53, в котором противораковый биологический агент выбирают из ниволумаба, пидилизумаба, пембролизумаба, дурвалумаба, атезолизумаба, авелумаба, AMP-224, BMS-936559, AMP-514, MDX-1105, TSR-042, STI-A1010 и STI-A1110.
55. Способ по п. 52, в котором противораковый биологический агент представляет собой агент, который ингибирует VISTA, gpNMB, B7H3, B7H4, HHLA2, CD73, CTLA4 или TIGIT.
56. Способ по любому из пп. 52-55, в котором противораковый агент представляет собой антитело.
57. Способ по п. 52, в котором противораковый биологический агент представляет собой цитокин.
58. Способ по п. 52, в котором противораковый агент представляет собой CAR-T терапию.
59. Способ по п. 52, в котором противораковый агент представляет собой онколитический вирус.
60. Способ по любому из пп. 47-59, дополнительно включающий резекцию опухоли и/или лучевую терапию.
| WO 2017123673 A2, 20.07.2017, WO 2018115003 A2, 28.06.2018, KANEKO E | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Е | |||
| и др., Опухолевое микроокружение как мишень терапии злокачественных глиом, Злокачественные опухоли, 2015, н | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2023-08-22—Публикация
2019-08-12—Подача