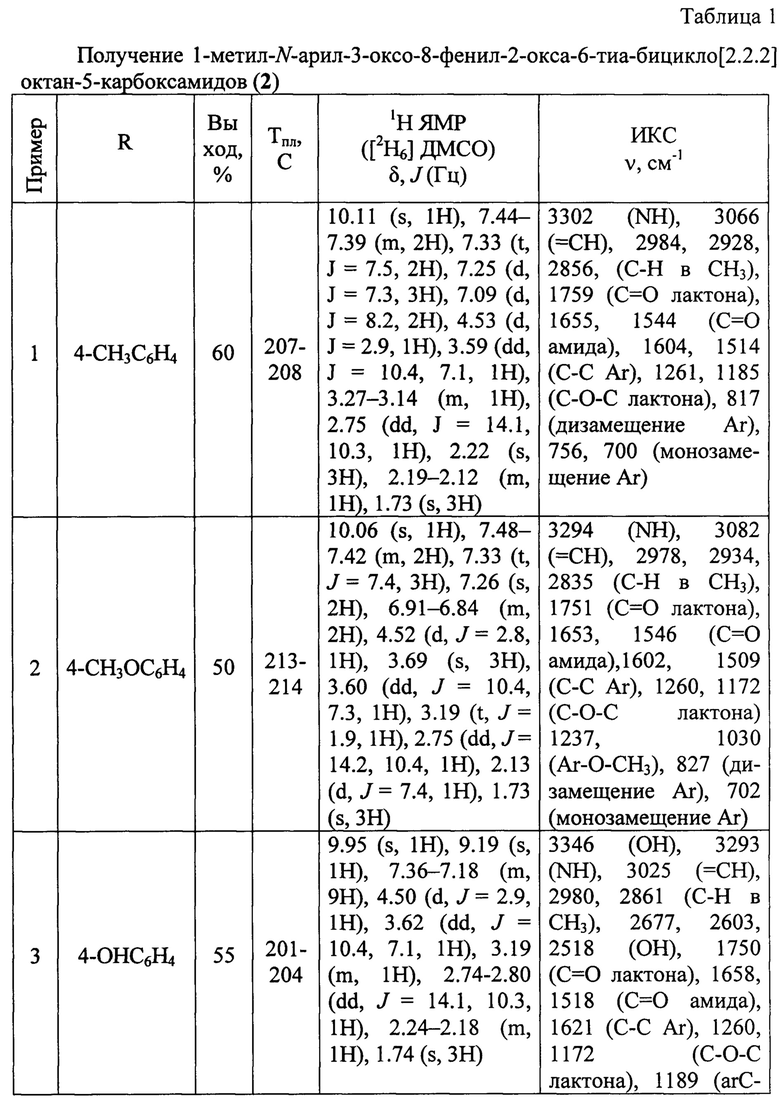
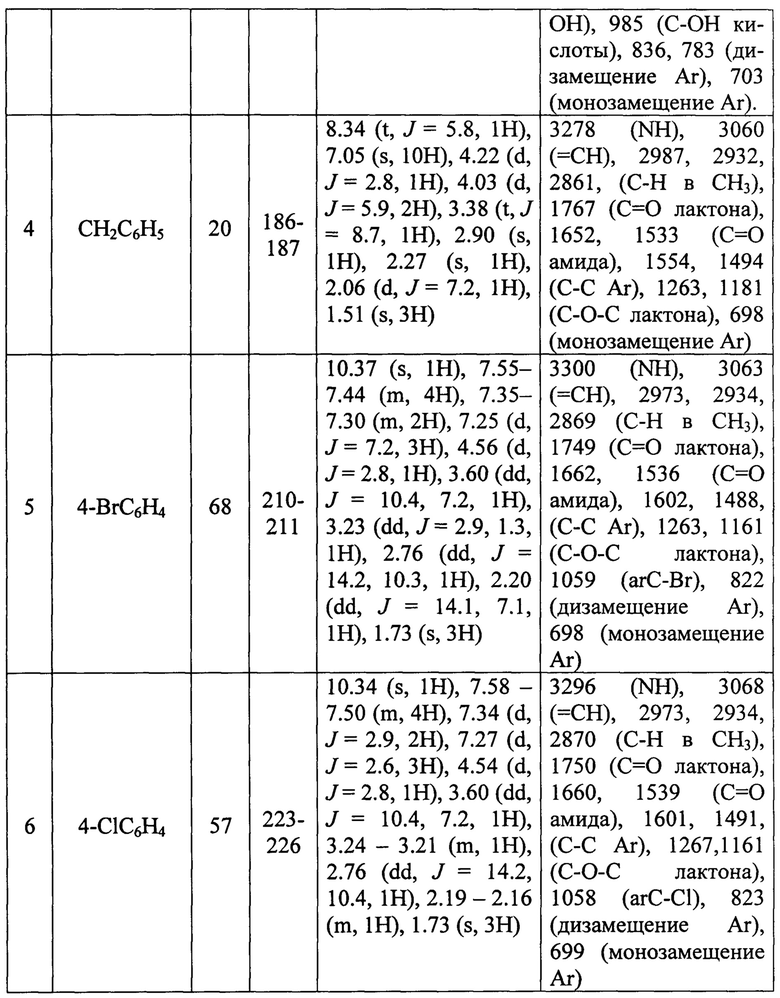
Изобретение относится к способу получения ряда веществ 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбокса мидов, имеющих бициклическую каркасную структуру, содержащую тиопирановый и лактоновый фрагменты, общей формулы:
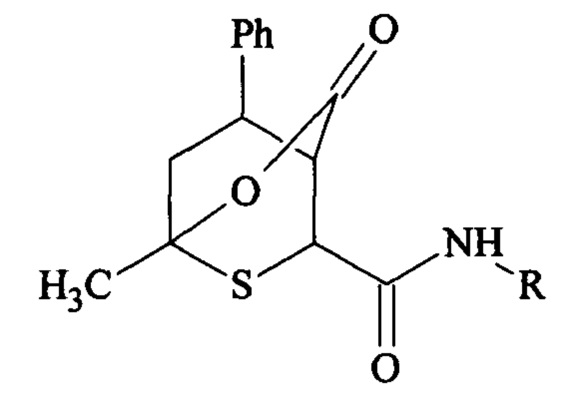
где R - 4-СН3С6Н4, 4-СН3ОС6Н4, 4-НОС6Н4, 4-ClC6H4, 4-BrC6H4, СН2С6Н5.
Данные соединения представляют интерес в качестве полупродуктов в синтезе практически значимых соединений. Они могут являться исходными соединениями для синтеза биологически активных веществ: противораковых, антибактериальных, антиатеросклеротических препаратов.
Известен метод синтеза 5-метилдигидрофуран-2(3H)-онов и 6-метилтетрагидро-2H-пиран-2-она. Метод включает в себя каталитическую циклизацию пент-5-еновых кислот и гекс-5-еновой кислоты соответственно (Adrio Luis A., Copper-catalysed intramolecular О-Н addition to unactivated alkenes / Luis A. Adrio, Louisa Shuyi Quek, Jason G. Taylor, et al. // Tetrahedron. - 2009. - №65. - P. 10334 - 10338).
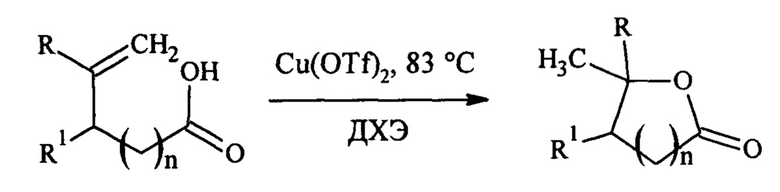
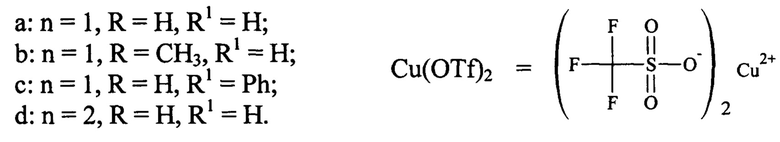
Исходную алкеновую кислоту (1 ммоль), трифторметансульфонат меди (II) (0,02 ммоль, 2 мол.% или 0,05 ммоль, 5 мол.%) и 1,2-дихлорэтан (2 мл) нагревали 18-48 часов с обратным холодильником. После охлаждения до комнатной температуры растворитель удаляли при пониженном давлении с получением остатка, который очищали колоночной хроматографией с получением соответствующих лактонов. Выход лактонов составляет 72-92%.
Главными недостатками данного способа являются его высокая длительность и относительная дороговизна катализатора трифторметансульфоната меди (II). Длительность обусловлена продолжительностью химических превращений.
Также существует способ получения лактонов из γ-непредельных кар-боновых кислот, принятый нами за протип (Winska К. Antimicrobial activity of new bicyclic lactones with three or four methyl groups obtained both synthetically and biosynthetically / K. Winska, M. Grabarczyk, W. Mazczka, et al. // Journal of Saudi Chemical Society. - 2018. - Vol.22, №3. - P. 363-371.).
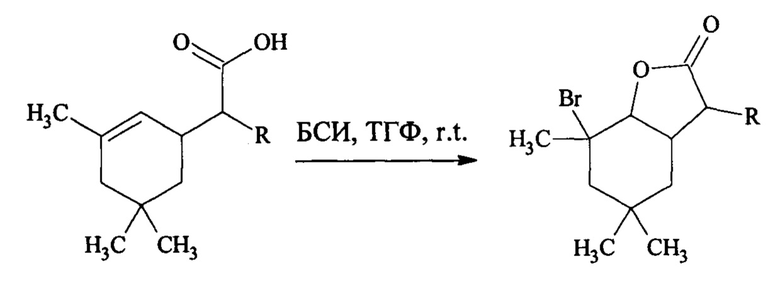
R=H, CH3.
На первой стадии 0,011 моль исходной кислоты и 0,092 моль N-бромсукцинимида (БСИ) растворяют в 30 мл тетрагидрофурана (ТГФ). Реакционную смесь перемешивают в течение 24 часов при комнатной температуре (r.t). После этого к реакционной смеси добавляют воду, продукт экстрагируют диэтиловым эфиром. Объединенные эфирные фракции промывают водным раствором гидрокарбоната натрия, отделяют водный слой, сушат безводным сульфатом магния. Загрязненный продукт очищают с помощью флэш-хроматографии (гексан: ацетон=3:1). Получают целевой продукт с выходами 23-59%.
Главными недостатками данного способа являются его высокая длительность и относительная дороговизна N-бромсукцинимида.
Задачей настоящего изобретения является разработка простого и эффективного способа получения 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбокса мидов, который позволил бы получить данное соединение с использованием доступных реагентов и высоким выходом.
Заявляется способ получения 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2] октан-5-карбоксамидов общей формулы (2).
Способ включает в себя одну стадию (непрерывно в одном реакторе), выделение целевых продуктов путем фильтрования выпадающих осадков и их дальнейшей очистки перекристаллизацией из ледяной уксусной кислоты.

где R - 4-СН3С6Н4, 4-СН3ОС6Н4, 4-НОС6Н4, 4-ClC6H4, 4-BrC6H4, СН2С6Н5.
При проведении синтеза готовят раствор амидокислоты (1) в растворителе. В качестве растворителя могут быть использованы четыреххлористый углерод, хлороформ, дихлорметан. Далее к полученному раствору приливают кислоту в мольном соотношении от 5% до 110% по отношению к амидод-кислоте 1. В качестве кислоты могут быть использованы серная, соляная, фосфорная, уксусная, трифторуксусная кислоты. Реакционную смесь перемешивают при температуре от 40 С° до 77 С° в течение от 1 до 3 часов. Далее выпавший осадок - 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамид (2) фильтруют и промывают тем же растворителем. Продукт перекристаллизовывают из ледяной уксусной кислоты.
Изобретение иллюстрируется следующими примерами:
Пример 1.
Готовят раствор 2,725 моль 2-[(4-метил)карбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновой кислоты в 5 мл хлороформа. Далее к полученному раствору приливают 0,1363 моль серной кислоты. Реакционную смесь перемешивают при температуре 50 С° в течение 1 часа. Далее выпавший осадок - 1-ме-тил-N-(4-метилфенил)-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамид фильтруют и промывают хлороформом. Продукт перекристаллизовывают из ледяной уксусной кислоты.
Пример 2.
Готовят раствор 2,725 моль 2-[(4-метокси)карбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновой кислоты в 5 мл дихлорметана. Далее к полученному раствору приливают 0,2725 моль концентрированной соляной кислоты. Реакционную смесь перемешивают при температуре 40 С° с обратным холодильником в течение 1,5 часа. Далее выпавший осадок - 1-метил-N-(4-метоксифенил)-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2] октан-5-карбоксамид фильтруют и промывают дихлорметаном. Продукт перекристаллизовывают из ледяной уксусной кислоты.
Пример 3.
Готовят раствор 2,725 моль 2-[(4-гидрокси)карбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновой кислоты в 5 мл четыреххлористого углерода. Далее к полученному раствору приливают 1,3625 моль фосфорной кислоты. Реакционную смесь перемешивают при температуре 60 С° в течение 2 часов. Далее выпавший осадок - 1-метил-N-(4-гидроксифенил)-3-оксо-8-фенил-2-окса-6-тиа-бицикло [2.2.2] октан-5-карбоксамид фильтруют и промывают четыреххлористым углеродом. Продукт перекристаллизовывают из ледяной уксусной кислоты.
Пример 4.
Готовят раствор 2,725 моль 2-[бензилкарбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновой кислоты в 5 мл хлороформа. Далее к полученному раствору приливают 2,998 моль трифторуксусной кислоты. Реакционную смесь перемешивают при температуре 50 С° в течение 3 часов. Далее выпавший осадок - 1-метил-N-бензил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамид фильтруют и промывают хлороформом. Продукт перекристаллизовывают из ледяной уксусной кислоты.
Пример 5.
Готовят раствор 2,725 моль 2-[(4-бром)карбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновой кислоты в 5 мл хлороформа. Далее к полученному раствору приливают 2,725 моль трифторуксусной кислоты. Реакционную смесь перемешивают при температуре 50 С° в течение 1 часа. Далее выпавший осадок - 1-метил-N-(4-бромфенил)-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамид фильтруют и промывают хлороформом. Продукт перекристаллизовывают из ледяной уксусной кислоты.
Пример 6.
Получение 1-
метил-N-(4-хлорфенил)-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамида проводят аналогично примеру 5.
Выходы целевых продуктов реакций, результаты анализов приведены в таблице 1.
Результатом изобретения является простой способ синтеза новых 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамидов (2), использующий доступные реагенты.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 3,4-дигидро-2H-тиопирана | 2018 |
|
RU2670977C1 |
| ПРОИЗВОДНЫЕ ХИНОЛОН- И НАФТИРИДОНКАРБОНОВОЙ КИСЛОТЫ, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ В ВИДЕ ГИДРАТА ИЛИ СОЛИ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ, ПРОИЗВОДНЫЕ ИЗОИНДОЛА В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ ДЛЯ ПОЛУЧЕНИЯ УКАЗАННЫХ ПРОИЗВОДНЫХ ХИНОЛОН- И НАФТИРИДОНКАРБОНОВОЙ КИСЛОТЫ | 1995 |
|
RU2145604C1 |
| ПРОИЗВОДНЫЕ ХИНОЛОН- И НАФТИРИДОНКАРБОНОВОЙ КИСЛОТЫ В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫХ ИЗОМЕРОВ, ИХ ГИДРАТЫ И СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2105770C1 |
| ПРОИЗВОДНЫЕ ХИНОЛОНКАРБОНОВОЙ КИСЛОТЫ, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ ГИДРАТЫ И СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2077533C1 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА КАК ИНГИБИТОРЫ 11-БЕТА-ГИДРОКСИСТЕРОИДДЕГИДРОГЕНАЗЫ-1 | 2003 |
|
RU2360910C2 |
| ФЕНИЛОКСАЗОЛИДИНОНЫ, ИМЕЮЩИЕ С-С-СВЯЗЬ С 4-8-ЧЛЕННЫМИ ГЕТЕРОЦИКЛИЧЕСКИМИ КОЛЬЦАМИ | 1996 |
|
RU2175324C2 |
| ПРОИЗВОДНЫЕ 7-ИЗОИНДОЛИНИЛХИНОЛОНА И 7-ИЗОИНДОЛИНИЛНАФТИРИДОНА | 1993 |
|
RU2111964C1 |
| ЗАМЕЩЕННЫЕ 2Н-ПИРАНО[2,3-С]ПИРИДИНЫ, КОМБИНАТОРНАЯ И ФОКУСИРОВАННАЯ БИБЛИОТЕКИ | 2003 |
|
RU2261251C2 |
| Способ получения 4-окси-2н-нафто (2,1-е) -1,2-тиазин-3-карбоксамид-1,1-диоксидов или их солей | 1975 |
|
SU575027A3 |
| ЗАМЕЩЕННЫЕ 3-АМИНОХИНУКЛИДИНЫ | 1992 |
|
RU2092486C1 |
Изобретение относится к области органической химии и включает способ получения 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамидов формулы (2)
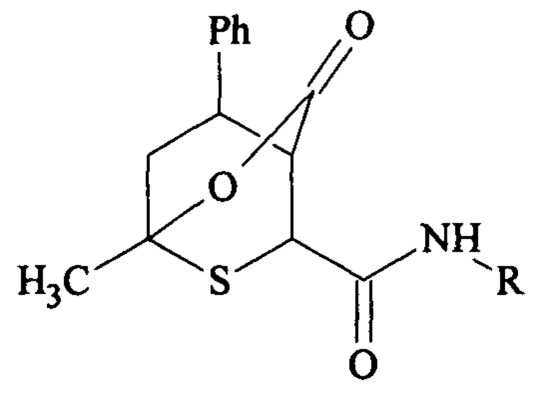
где R=4-СН3С6Н4, 4-СН3ОС6Н4, 4-НОС6Н4, 4-ClC6H4, 4-BrC6H4, СН2С6Н5. Способ включает в себя одну стадию реакции, выделение целевых продуктов путем фильтрования выпавшего осадка и его дальнейшую очистку перекристаллизацией из ледяной уксусной кислоты. При проведении синтеза готовят раствор 2-[арилкарбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновой кислоты в растворителе. В качестве растворителя используют четыреххлористый углерод, хлороформ или дихлорметан. Далее к полученному раствору приливают кислоту, выбранную из серной, соляной, фосфорной, уксусной или трифторуксусной, в мольном соотношении от 5 до 110%. Реакционную смесь перемешивают при температуре от 40 до 77°С в течение от 1 до 3 ч. Выпавший осадок - 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамид (2) фильтруют и промывают тем же растворителем. Продукт перекристаллизовывают из ледяной уксусной кислоты. Технический результат - способ синтеза новых 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамидов (2), использующий доступные реагенты. 1 табл., 6 пр.
Способ получения 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло [2.2.2]октан-5-карбоксамидов
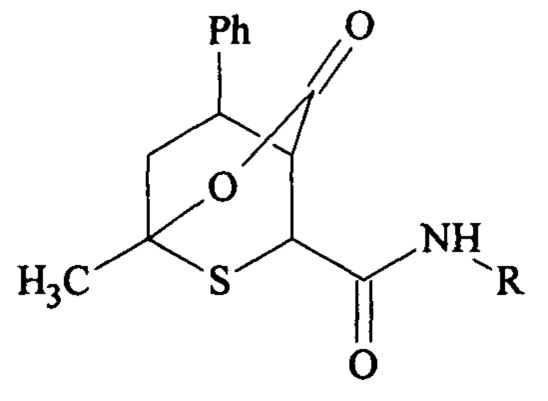
где R=4-СН3С6Н4, 4-СН3ОС6Н4, 4-НОС6Н4, 4-ClC6H4, 4-BrC6H4, СН2С6Н5,
взаимодействием 2-[арилкарбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновых кислот с реагентом в растворителе при повышенной температуре с замыканием лактонового цикла, отличающийся тем, что реакцию проводят непрерывно в одном реакторе в растворе 2-[арилкарбамоил]-6-метил-4-фенил-3,4-дигидро-2H-тиопиран-3-карбоновых кислот в четыреххлористом углероде, или хлороформе, или дихлорметане, затем добавляют кислоту, выбранную из серной, соляной, фосфорной, уксусной или трифторуксусной, в мольном соотношении от 5 до 110%, смесь перемешивают при температуре от 40 до 77°С в течение от 1 до 3 ч, далее фильтруют и промывают тем же растворителем выпавший осадок - 1-метил-N-арил-3-оксо-8-фенил-2-окса-6-тиа-бицикло[2.2.2]октан-5-карбоксамид, который перекристаллизовывают из ледяной уксусной кислоты.
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-НУКЛЕОЗИДНЫХ АНАЛОГОВ, ИХ СОЛЕЙ И СЛОЖНЫХ ЭФИРОВ | 1994 |
|
RU2139870C1 |
| WO 2014206349 A1, 31.12.2014 | |||
| Баева Л.А | |||
| Серосодержащие реагенты в реакции тиометилирования кетонов | |||
| Автореферат диссертации на соискание ученой степени кандидата химических наук, Уфа, 1997, 24 с | |||
| Меркулова А | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Химия гетероциклических соединений, 2021, 57 (7/8), | |||
Авторы
Даты
2023-10-25—Публикация
2022-10-07—Подача