где RI - алкил, содержащий 1-6 атомов угле-; рода или аралкил, содержащий 7-10 атомов углерода;
R имеет указанные значения, подвергают взаимодействию с ароматическим амином общей формулы
IMHj-Ar(III),
где Ar имеет указанные значения, в среде инертного органического растворителя или в изб-тке амина общей формулы ((II) при 60-200° С.
В качестве органического растворителя можно использовать, например, ароматические углеводороды, такие как бензол, толуол, ксилол, хлорбензол, о-дихлорбензол или тетрагидронафталин; диме1илформамид, диметилацетамид или диметилсульфоксид или триамид гексаметилфосфорной кислоты, простые эфиры, такие как диметоксиэтан, дизтиленгликоль, диметиловый эфир или дифениловый эфир.
Реакцию проводят предпочтительно в толуоле или ксилоле при температуре кипения реакдионной смеси, образовавщийся спирт удаляют азеотропной дистиллящ1ей или нагреванием с обратным холодильником в аппарате Соксклета, снабженного молекулярным ситом.
Продзтст выкристаллизовьшают из реакционной смеси или выделяют путем упаривания растворителя, или путем добавления воды.
Соединения общей формулы (t) известными методами могут быть переведены в их соли с неорганическими или органическими основаниями. В качестве оснований пригодны, например, алкоголяты щелочного металла, гидроокиси щелочного или щелочноземельного металла, гидроокиси триалкиламмония, адкиламины.
Исходные соединения общей формулы (II) по-, лучают путем взаимодействия 3 - оксо - нафт 2,1-d изотиазолин - 1,1 - диоксида со спиртовым раствором алкоголята щелочного металла, спирт затем удалят. Реакцией образовавщейся соли щелочного металла 3 - оксо - нафт 2,1-d изотиазолин - 1,. 1 - диоксида в диметилсульфоксиде со сложным эфиром галоидоуксусной кислоты при 120-150° С получают 1,1- оксид алкилового эфира 3 - оксо - нафт 2,1-d изотиазолин - 2- уксусной кислоты, который обрабатывают 2-3 зкв алкоголята щелочного металла, нагревают,: подвергая каталитической перегруппировке в присутствии с/снования. После подкислё шя получают 1, 1 диоксид алкилового эфира 4 - окси- 2Н- нафто 2,1-е - 1, 2 - тиазин - 3 - карбоновой кислоты общей формулы (II), где RI -водород.
Соединения общей формулы (II), где RI - метил или этил, ползя1ают алкилированием галоидметилом или -этилом, например метшгаодидом или этилйодидом, в спиртовом или водно-спиртовом растворе при применении 1 экв гидроокиси щелочного металла.
Примерам- (3- хлорфенил) - 4 - окси - 2 -метил - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 карбоксамид - 1, 1 - диоксид.
9,58 г (0,03 моль) 1, 1 - диоксида метилового эфира 4- окси - 2 - метил - 2Н- нафто 2,1-е - 1, 2- тиазин - 3 - карбоновой кислоты и 5,1 г (0,04 моль) 3 - хлоранилина в 400 мл безводного ксилрла 24 ч нагревают с обратным холодильником в аппарате Сокслета с молекулярным ситом 4 А. После охлаждения и отстаивания в течение ночи отфильтровьтают от кристаллов. OjaeM последующей перекристаллизации из этиленхлорида получают 9,1 г (73%) целевого вещества с Т.ПЛ.248-249° С jJ)aзл.).
Исходные соединения получают путем следующих промежуточных стадий.
А. 1, 1 - Диоксид метилового эфира 3 - оксо -нафт 2,1 -d изотиазолин - 2 - уксусной кислоты.
К раствору из 7,82 г (0,34 г. атома) натрия в 300 мл абсолютного метанола добавляют 70,0 г (0,30моль) 3-оксо - нафт 2,1-dl изотиазолин- 1, 1 - диоксида. Затем отгоняют почти весь спирт и оставщуюся натриевзто соль 3 - оксо - нафт 2,1-d изотиазолин - 1, 1 - диоксида растворяют в 100мл абсолютного диметилсульфоксида. К этому раствору при 50° С по каплям добавляют 43,41 г (0,40 моль) метилового эфира хлоруксусной кислоты. 1 змещивают 30 мин при комнатной температуре, медленно, нагревают до 130 С и реакционную смесь выдерживают 2,5 ч при этой температуре. Затем в вакууме отгоняют диметилсульфоксид. Из остатка после перенесения в раствор из 40 г ацетата натрия в 400 мл воды, фильтрования и промывания водой и ледяным метанолом получают 90,0 г (98%) вещества с Т.ПЛ. 188°С (метанол-этиленхлорид).
Б. 1, 1 - Диоксид метилового эфира 4 - окси -2Н - нафто 2,1-е - 1, 2 - тиазин - 3 - карбоновой
кислоты.
0,90, моль метилата натрия получают растворением 20,7 г (0,90 г. атома) натрия в 350мл абсолютного метанола и последующей отгонкой спирта и повторной азеотропной дистилляцией ксилолом.
После добавления 91,5 г (0,30 моль) 1,1 - диоксида метилового эфира 3 - оксо- нафт 2,1-d изотиазолин - 2 -, уксусной кислоты добавляют еще 250 мл безводного трег-бутанола. Реакционнзто смесь медленно нагревают до 60° С, выдерживают 1 ч 30 мин
при 60-65° С и затем кипятят с обратным холодильником. Охлаждают, разлагают льдом и концентрированной соляной кислотой доводят рН смеси до 3-4. Образовавщееся твердое вещество отфильтровьтают, промывают водой и сущат. Получают 72,0 г (78%) продукта с т.пл. 218-220° С (после 2-кратной перекристаллизации их этиленхлорида).
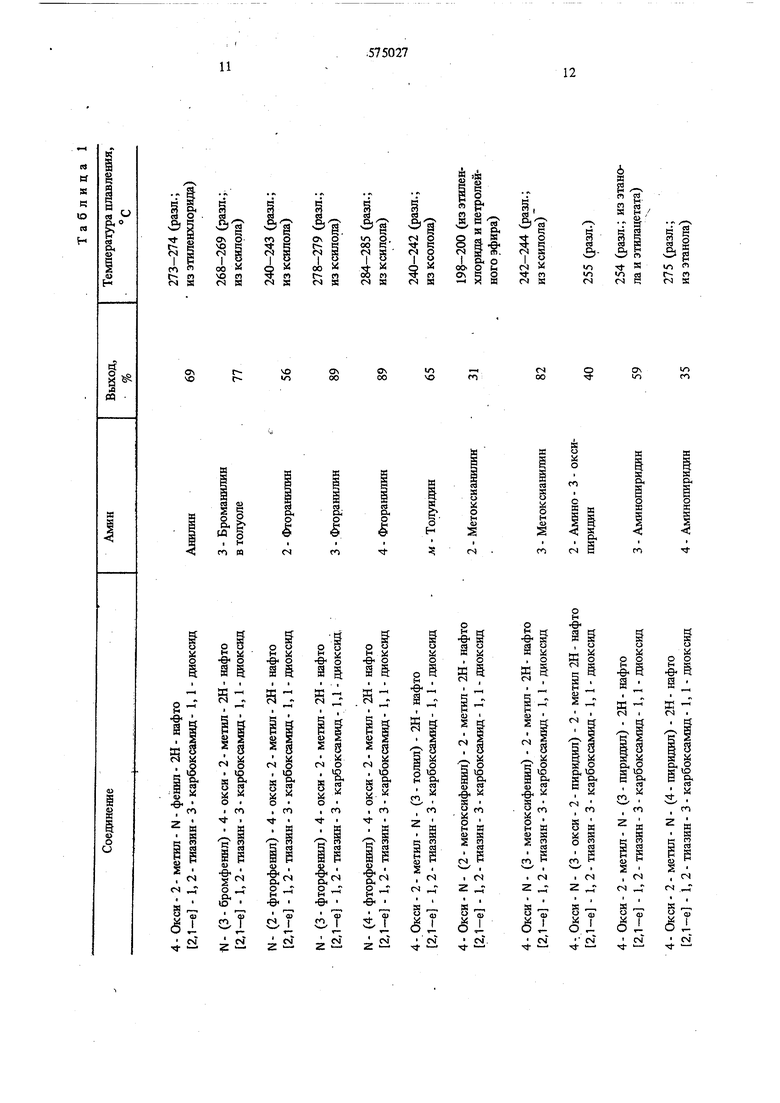
В..1, 1 - Диоксид метилового эфира 4- окси- 2 - метил - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 -карбоновой кислоты. К суспензии из 61,0 г (0,2 моль) 1, 1 - диоксида метилового эфира 4 - окон- 2Н- нафто 2,1-е - 1, 2 тиазин - 3 - карбоновой кислоты и 85,1 г (0,6 моль) метилйодида в 500 мл метанола 40 мин при 20-25° С добавляют по каплям раствор 8,2 г (0,205 моль) гидроокиси натрия в 200 мл водьт. Перемешивая 4ч, охлаждают до 5°С, осадок(50г сырого продукта) отфильтровьшают и промьшают ледяным метанолом. Соединенные фильтраты нагревают 15 мин до 40° С и сгущают в вакууме до начала кристаллизации. Фильтрованием и промьшкой ледяным метанолом получают еще 9 г сырого продукта. Путем нерекристаллизации соединенных сырых , продуктов из эталенхлорида получают 53,3 г (85%) вещества. В табл. 1 приведены соединения, полученные аналогично примеру 1 из 1, 1 - диоксида метилового зфира 4 - окси - 2 - метил- 2Н- нафто 2,1-е -I, 2 тиазин - 3 - карбоновой кислоты и амина общей формулы (111). Пример 2. 4- Окси - 2 метил - N - (2 -пиридил) - 2Н - }1афто 2,1-е -1,2- тиазин- 3 -карбоксамид -1,1- диоксид. 9,58 г (0,03 моль) 1, 1 - диоксида метилового эфира 4- окси - 2 - метил - 2Н нафто 2,1-е - 1, 2-тиазин - 3 - карбоновой кислоты и 3,8 г (0,04 моль) 2 - аминопиридина в 250 мл безводного ксилола нагревают 14 ч с обратным холодильником в аппарате Сокслета с молекулярным ситом 4 А. После охлаждения и отстаивания в течение ночи отфильтровьшают от кристаллов. Путем перекристаллизации , из этиленхлорида получают 5,4 г (42%) соединения с т.пл. 237-238°С (разл.). ПримерЗ. 4- Окси - 2 - метил - N - (4 -метил - 2 - пиридил) - 2Н - нафто 2,1-8 -1,2-тиазин - 3 - карбокса шд - Ь 1 - диоксид. Аналогично примеру 2 5,0 г (0,016 моль) 1,1-диоксида метилового 4 - окси - 2 - метил -2Н - нафто 2,1-е - 1, 2 - тиазин - 3 - карбоновой кислоты взаимодействует с 2,2 г (0,02 моль) 2 амино - 4 - метилниридина в 220 мл ксилола, после перекристаллизации из этилового эфира уксусной кислоты 3,5 г (58%) продукта с Т.ПЛ. 221°С (разл.). Пример 4. 4- Окси - 2 - метил - N - (6 -метил - 2 - пиридил) 2Н- нафто 2,1-е - 1, 2 -тиазин - 3 - карбоксамид - 1, 1 - диоксид получают аналогично примеру 2 из 1,1 - диоксида метилового эфира 4- окси- 2- метил- 2Н- нафто 2,1-е - 1, 2-тиазин - 3 - карбоновой кислоты и 2 - амино - 6 -метилпиридина, выход 51%, т.пл. 221-223° С (разл.; из этилацетата). Пример 5. N- (6- хлор - 3 - пиридазинил) -4 - окси - 2 - метил - 2Н - нафто 2,1-е - 1, 2 -тиазин - 3 - карбоксамид- 1,1- диоксид. 3, 2т (0,01 моль) 1, 1 - диоксида метилового эфира 4- окси- 2- метил- 2Н- нафто 2,1-е - 1, 2 -тиазин - 3 - карбоновой кислоты с 1,7 г (0,013 МО ль) 3 - амино - 6 - хлорпиридазина в 200 мл безводного ксилола нагревают 60 ч с обратным холодильникол в аппарате Сокслета с молекулярным ситом 4 А. После охлаждения и сгущения до сиропа очищают на колонне с силикагелем (фирмы Мерк, хроматография на колонне 0,2-0,5 мм) с применением смеси хлороформ-метанол (95:5) в качестве растворителя. Получают 1,4 г (34%) вещества с т.пл. 235-237°С (разл.). Пример 6. 14 - Окси - 2 - метил - N пиразинил - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 карбоксамид -1,1- диоксид. 4,8 г (0,015 моль) 1, 1 - диоксида метилового эфира 4- окси- 2- метил- 2Н- нафто 2,1-е - 1, 2-тиазин- 3 - карбоновой кислоты с 2,1 г (0,022 моль) аминопиразина в 200 мл сухогоксилола нагревают 8 ч с обратным холодильником в аппарате Сокслета с молекулярным ситом 4 А. Добавляют еще 0,5 г аминопиразина, нагревают 8 ч с обратным холодильником, охлаждают и оставляют стоять в течение ночи, осажденный осадок отфильтровывают и фильтрат упаривают в вакууме. Объединенные твердые частицы перекристаялизовьшают из уксусного эфира и получают 3,0 г (52%) вещества с т.пл. 245° С (разл,). Пример 7. 4- Окси - 2 - метил - N - (2 тиазолил) - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 карбоксамид- 1, 1 - диоксид. Аналогично примеру 1 из 19,8 г (0,062 моль) 1, 1 - диоксида метилового эфира 4 - окси - 2 - метил 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 - карбоновой кислоты и 9,3 г (0,093 моль) 2 - аминотиазола в 500 мл ксилола после перекристаллизации из этиленхлорида получают 13,5 г (56%) вещества с т.пл. 248-249°С (разл.). П р и м е р 8. 4 - Окси - 2 - метил - N - (4 метил 2- тиазолил) - 2Н - нафто 2,1-е - 1, 2тиазин- 3 - карбоксамид- 1,1- диоксид. Аналогшшо примеру 1 из 5,0 г (0,016 моль) 1, 1 - диоксида метилового эфира 4 - окси - 2 - метил 2Н - нафто 2,1-е -1,2- тиазин - 3 - карбоновой кислоты и 2,75 г (0,025 моль) 2 - амино - 4 метилтиазола в 200 мл ксилола получают 2,52 г (40%) вещества с т.пл. 177°С (разл.; из этилацетаПример 9. N- (4- этил - 2 - тиазолил) - 4 окси - 2 - метил - 2Н - нафто 2,1-е - тиазин - 3 карбоксамид- 1, 1 - диоксид. 8 г (0,025 моль) 1, 1 - диоксида метилового зфира 4 - окси - 2 - метил - 2Н - нафто 2,1-е 1, 2-тиазин - 3 - карбоновой кислоты и 3,8 г (0,03 моль) 2 - амино - 4 - этилтиазола в 500 мл сухого ксилола 24 ч нагревают с обратньп холодилышко в аппарате Сокслета с молекулярным ситом 4 А. Реакционную смесь фильтрзтот в горячем состоянии и после охлаждения и отстаивания в течеьше нош отфильтровьшают от кристаллов. Из маточного раствора путем сгущения по.пучают дополнительное количество кристаллов. Перекристаллизацией из смеси ксилола и простого эфира получают 6,6 г (64%) вещества с т.пл. 194-195° С.
2 - Амино - 4 - этилтиазол получают обычным способом.
0,5 моль алкилкетона, 0,5 моль йода и 1 моль тиомочевины смешивают и 15 мин нагревают до 100 С. Реакционную смесь выливают в воду и g отфильтровывают от нерастворимых частиц. При охлаждении водного раствора выкристаллизовывается гадрохлорид замещенного 2 - аминотиазола. Концентрированным водным аммиаком отделяют
амин от соли.JQ
Аналогично из диэтилкетона получают 2 амино-4-этил-5-метилтиазол, Т.1Ш. 72°С, выход 0%; изтетрагидротиопиран- 4 - она - 2 - ямина- -6 дигидро - 7Н тиопирано 4,3-d тиазол, 15 т.пл. 170-172° С, выход 64%; из этилметилкетона смесь 2 - амино - 4, 5 - диметилтиазола и 2 - амино 4 - этилтиазола, из которой выделяют 2 - амино - 4 этилтиазол, т.пл. 36° С, выход 20%, хроматографией на колонне (растворитель хлороформ-этанол; 20 95:5; изомер с болыяим коэффициентом Rf); из метилпропилкетона полушют смесь 2 - амино - 5 этил - 4 - метилтиазола и 2 - амино - 4 - пропилтиазола, из которой выделяют 2 - амино- 5 - этил-4 - метилтиазол (сироп; т. пл. гидрохлорида 25 179-180° С, выход 58%) хроматографией на колонне (растворитель хлороформ-этанол, 95:5; изомер с меньшим коэффициентом Rf). Отделешю изомеров осуществляют путем фракционированного осаждения гидрохлорида или путем фракцио- 30 нированной кристаллизации гидройодидов.
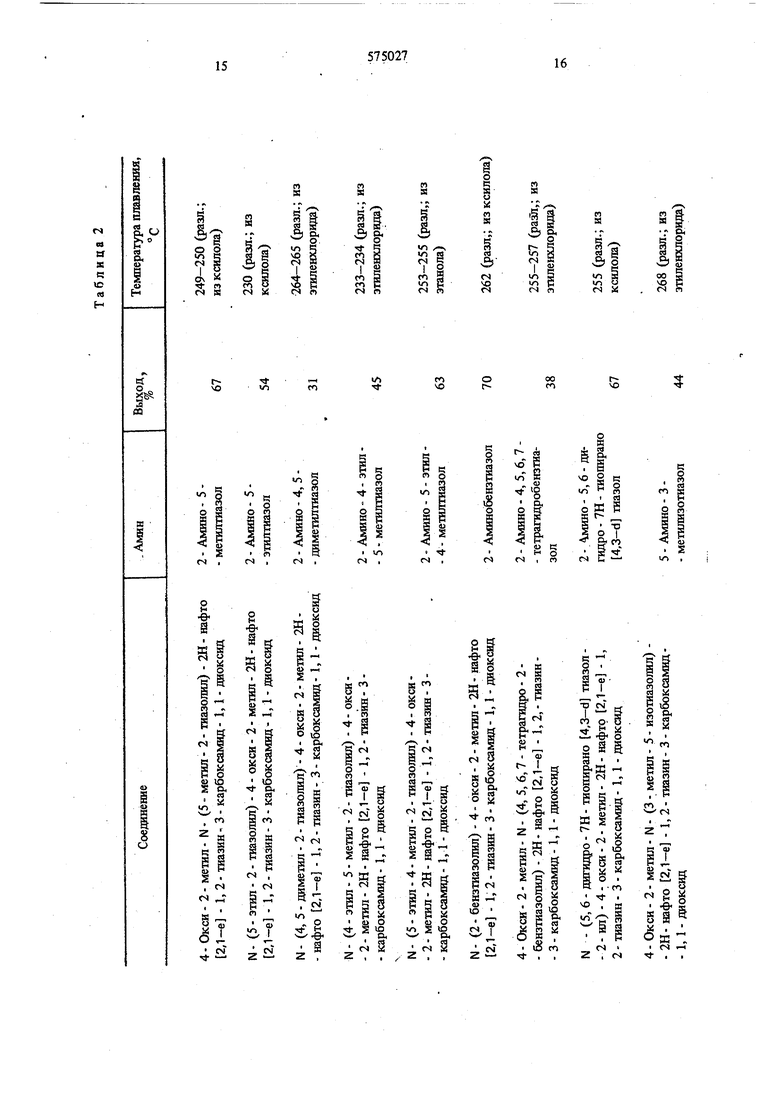
В табл. 2 приведены соединения, гюлученшю аналогично примеру 9 из 1, 1 диоксида меиетового эфира 4 - окси- 2- метил- 2Н - нафто . 1, 2 - тиазин - 3 - карбоновой кислоты и амина йй общей формулы (III).
Пример 10. 4 - Окси - 2 - метил N - (5 -метил - 3 - изоксазолил) - 2Н- нафто 2,1-е I, 2- тиазин- 3- карбоксамид- 1, 1 - диоксид.. 10
Аналогично примеру из 4,8 г (0,015 моль) 1, 1 - диоксида метилового эфира 4 - окси - 2 - метил 2Н- нафто 2,1-е - 1, 2 - тиазин - 3- карбоновой кислоты и 2,11 г (0,021 моль) 3 амино - 5 метилизоксазола в 250мл сухого ксилола после 45 перекристаллизации из ксилола получают 3,3 г (57%) вещества с т.пл. 253° С.
П р и м е р 11. 4 - Окси - N - фенил - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 - карбоксамид, - 1, 1 -даоксид.50
9,58 г (0,03 моль) 1, 1 - диоксида метилового эфира 4 - окси - 2Н - нафто 2,1-е - 1,2- тиазин -3 - карбоновой кислоты и 3,72 г (0,04 моль) аншшira в 150мл безводного ксилола нагревают 10ч с обратным холодильник( в аппарате Сокслета с 55 молекулярным ситом 4 А. После охлаждения оставляют стоять в тече1ше ночи, отфильтровывают осажденные кристаллы и, перекриста;шизовывая из этипенхлорида, получают 6,10 г (55%) вещества с т.пл. 260-262° С.60
Пример 12. N - (3 - хлорфенил) - 4 - окси -2Н нафто 2, - 1,2- тиазин - 3 - карбоксамид-1, 1 - диоксид.
1 г (3,3 моль) 1, 1 - диоксида метилового эфира 4 - окси - 2Н - нафто 2,1-е - Г азин 3 - карбоновой кислоты и 0,5 г (4 ) 3 -хлорани)шш в 200 мл безводного ксин.уга 25 ч нагревают с обратным холодильником в аппарате Сокслета с молекулярным ситом 4 А. После охлаждения выкристаллизовывают 0,9 г (68%) продукта с х.пл. 262° С (разл.).
Пример 13. 4 - Окси - N - (2 - тиазолил) - 2Н-шфто 2,1-е - 1, 2 - тиазин - 3 - карбоксамид - 1,
1- диоксид.
I 3,2 г (0,01 моль) 1, 1 - диоксида метилового эфира 4 - окси - 2Н - нафто 2,1-е - I, 2- тиазин-3 - карбоновой кислоты и 1,5 г (0,015 моль) 2 аминотиазола в 200 мл сухого ксилола аналогично примеру И нагревают 16ч. После охлаждения отфильтровывают осадок, маточный раствор сгущают в вакууме, сырой 4 - окси - N - (2 -тиазолил) - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 карбоксамид - 1, 1 - диоксид. Обе фракции объединяют и три раза перекристаллизовывают из ацетонитрила. Выход 0,85 г (23%); т.пл. 238°С (разл.). 0 р и м е р 14. N - (4, 5 - диметил - 2 -тиазолял) 4 - окси - 2Н - нафто - 2,1-е 1,2-таазин - 3 - карбоксамид - 1, 1 - щюксид.
Аналогично примеру 13 из 1, 1 - диоксида метилового эфира 4 - окси- 2Н- нафто 2,1-е - 1,
2- тиазин - 3 - карбо1говой кислоты и 2 - амино - 4, 5 - диметилтиазола получают вещество с выходом 35%, т.пл. 253°С (разл.; из ксилола), а из 1, 1 диоксида метилового эфира 4 - окси - 2Н - нафто 2, 1,2 - тиазин - 3 - карбоновой кислоты и 2 -амино - 4 - эшл - 5 - метилтиазола получают N- (4 -э:гал - 5 - метил 2 - тиазолил) - 4 - окси - 2Ы - нафто 2, - 1,2-тиазш1 - 3 - карбоксамвд - 1,1 - диоксид выход 55%, т.пл. 268-270°С (разл.; из ксилола).
Пример 15. 2 - Этил - 4 - окси - N - фенил -2Н - нафто 2,1-е - 1, 2 - тиазин- 3 - карбоксамид - 1, 1 диоксид.
1,65 г (5 ммоль) 1, 1 - диоксида метилового Эфира 2- этил- 4- окси- 2Н- нафто 2,1-е - 1, 2-,
-тиазин - 3 - карбоновой кислоты и 0,56 г (6 ммоль) анилина .в 150 мл безводного ксилола нагревают 24ч в аппарате Сокслета с молекулярным ситом 4 А с обратным холодильником. Из охлажденной реакщюнной смеси кристаллизуют 1,8 г (90%) вещества с т.пл. 245-247° С (из ксилола).
Исходный 1, 1 - диоксид метилового эфира 2 -этил - 4 - окси - 2Н - нафто 2,1-е - 1, 2 - тиазин-3 - карбоновой кислоты получают следующей реакцией.
К суспензии из 10,1 г (0,033 моль) I, 1 -диоксида метилового эфира 4 - окск - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 - карбоновой кислоты и 20 г (0,12 моль) этилйодида в 400мл 75%-ного водного этанола 25 мин и по каплям добавляют
33 мл раствора едкого натра, причем исходтга материал полностью растворяется. Реакционную смесь размешивают 30ч при комнатной температуре. Выкристаллизованный продукт фильтруют, промьшают небольшим количеством этанола, выход 8,7 г (79%), т.пл. 179° С (из этанола).
Пример 16. 2 - Этил - 4 - окси - N - (2
-пиридил) - 2Н нафто 2,1-е - 1, 2 - тиазин - 3 карбоксамид - 1, 1 - диоксид получают аналогично примеру 15 из 1, 1 - дик сила метилового эфира 2 -этил - 4 - окси 2Н - нафто 2,1-е - 1, 2 - тиазин-3 - карбоновой кислоты и , 2 - аминопиридина, выход 86%, т.пл. 230-231°С (из ксилола).
Пример 17.. 2 - Этил - 4 - окси - N - (2 -тиазояил) - 2Ы - нафто 2,1-е 1, 2 - тиазин - 3 -карбоксамид- 1, 1 - диоксид.
Из 3,3 г (0,01 моль) 1,1- диоксида метилового эфира 2 - этил - 4 - окси - 2Н - нафто 12,т-е -1,2-ат1азин-- 3 - карбонсвой кислоты и 1,5 г (0,015 моль) 2 - аглинотиазола в 150мл кс1шола аналогично примеру 15 и после перекристаллизации из уксусного эфира получают 1,0 г (25%) вещества СТ.ПЛ. 261-262° С (разл.).
Пример 18. М- (3- хлорфешш) 4 - окси -2 - метил - 2Н- нафто 2,1-е - 1, 2 - тиазин-З-карбоксамид - 1,1- диоксид получают аналогично примеру 1 из 1, 1 - диоксида этилового эфира 4 - 2 - метил - 2Н- гафто 2,1-е - 1, 2- тиазин3 - карбоновой кислоты и 3 - хлоранилина, выход |71%, т.пл. 248-249°С (разд.; из этиленхлорида).
Исходные соединения получают путем следующих реакций.
A.1, 1 - Диоксид этилового эфира 3 - оксо -нафт 2,1-d иэотиазолин - 2 - уксусной кислоты
получают аналогично примеру 1 А из натриевой соли 3 - оксо - нафт 2,1-d - изотиаэолин - 1, 1 -диоксида и этилового эфира хлоруксусной кислоты, выход 72%, т.пл. 149-150,5° С (иэ этанола). Б. 1,1- Диоксид этилового эфира 4 - окси - 2Н -нафто 2,1-е) 1, 2 тиаэин 3 - карбоновой кислоты.
4,2 г (0,18 г-атома) натрия растворяют в 100 мл этанола. После добавления 23,1 г (0,072 ммоль) 1,1- диоксида этилового эфира 3 toKco - нафт 2,1-d - изотиазолил - 2 - уксусной кислоты 2ч нагревают до 60-6 5° С и исходную смесь разделяют аналогично примеру 1 Б. Получают 9,7 г (42%) вещества с т.пл. 202-204° С (из этанола).
B.1, 1 - Диоксид этилового эфира 4 - окси - 2 -метил - 2Н - нафто - 2,1-е - 1, 2 - тиазин - 3 -карбоновой кислоты получают аналогично примеру 1 В иэ 1, 1 - диоксида этилового эфира 4 - окси -2Н - нафто 2,1-е - 1, 2 - тиазин - 3 - карбоновой кислоты и метилйодидд, выход 82% т.пл. 163-165° С.
Пример 19. Натриевая соль 4 - окси - 2 , -метил - N - (2 - тиазолил) - 2Н- нафто 2,1-е - 1, 2 - тиазин - 3 - карбоксамид - 1, 1 - диоксида.
К суспензии из 1,94 г (5 ммоль) 4 - окси - 2 -метил - N - (2 - тиаэолил) - 2Н - нафто 2,1 -е - 1, 2 - тиазин - 3 - карбоксамид - 1, 1 - диоксида в 30 мл метанола добавляют раствор 0,2 г (5 ммоль) гидроокиси натрия в 20 мл метанола, оставляют стоять 24 ч при комштной температуре. Реакционную смесь упаривают, смешивают с эфиром, фильтруют и сушат.в вакууме. Получают 1,9г (93%) соли с т.пл. 230° С (разл.).
Пример 20. Натриевая соль 4 - окси - 2 -метил - N - (4 - метил - 2 - пиридил) - 2Н - нафто I 2,1-е - 1, 2 - тиазин - 3 - карбоксамид -1,1-диоксида.
1,9 г (4,8 ммоль) 4 - окси - 2 - метил - N - (4 -метил - 2 - пиридил) - 2Н - нафто ,1-е -1,2-тиазин - 3 - карбоксамид - 1, 1 - диоксида смешивают с раствором 0,192 г (4,8 ммоль) гидроокиси натрия в 75 мл метанола. Реакционную смесь 3ч размешивают при 30° С, сгущают, добавляют эфир, фильтруют и сушат в вакууме. Получают 2,0 г (99,7%) соли с т.пл. 218-220° С (разл.).
Пример 21. Циклогексиламин 4 - окси - 2 -метил - N - (2 - тиазолил) - 2Н- нафто 2,1-е - 1, 2 - тиаэин - 3 - карбоксамид - 1, 1 - диоксида.
0,5 г (1,5 ммоль) 4 - окси 2 - метил - N - (2 -тиазолил) - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3-карбоксамид - 1, 1 - диоксида суспендируют в 10мл метанола и добавляют 0,15 г (1,5 ммоль) циклогексиламина. Образовавишйся раствор в вакууме сгущают и остаток растирают ацетоном. Полученные кристаллы отсасывают и промывают небольшим количеством ацетона и эфиром. Получают 0,55 г (76%) кристаллов с т.пл. 205-207° С.
П р и м е р 22. N - (4 - фторфенил) - 4 - окси - 2-мстил - 2Н 1ЙФТО 2,1-е - 1, 2 - тиазин - 3 -карбоксамид - 1, 1 - диоксид получают аналогично
примеру 1 из бутилового эфира 4 - окси - 2 метил-2Н нафто 2,1-е -1,2- тиазин- 3 - карбоновой кислоты, т.пл. 115° С (иэ четыреххлористого углерода - этилового спирта), и 4 - фтора1шлина в ксилоле (время реакции 48ч), выход 61%, т.пл. 284-285°С (раэл.; из ксилола).
П р и м е р 23. N - (4 - фторфенил) - 4 - окси -2 - метил - 2Н - нафто 2,1-е - 1, 2 - тиазин - 3 -карбоксамид - 1, 1 - диоксид получают аналогично примеру 1 из бенэилового эфира 4 - окси - 2 - метил-2Н - шфто 2,1-е - 1, 2 - тиазин - 3 - карбоновой кислоты, т.пл. 159-161° С (из четыреххлористого углерода - этилового спирта), и 4 - фторанилина в ксилоле (время реакции 48 ч), выход 72%, т.пл. 284-285°С (разл.; из ксилола).
ё
а
5
i2
(N К







VO v
ОЧ
ON
t t-00Ю
го
гч
о
l/
о ю
оо го
о
S «
s
Н.
cs
«N 17 Формула изобретения Способ получения 4 окси 2Н - нафто 2,1-е 1, 2 тиазин - 3 - карбоксамид - 1, 1 - диоксидов общей формулы СО-ИН-Аг ,-R где R - водород, метил или этил; Аг -фенил, 3 хлор -, 3 - бром -, 2 - фтор -, 3 фтор -, 4 - фторфенил, 3 - толил, 2 - метокси -, 3 метоксифенил, 2 - пиридил, 4 - метил -, 6 - метил -, 3- окси - 2 - пиридил, 3 - пиридил, 4 - пиридил, 6 -хлор - 3 - пиридазинил, 3 - пиразинил, 6 - хлор - 2 -пиразинил, 6 - хлор - 4 - пиримидинил, 2 - тиазолил, 4- метил -, 4 - этил 5 - метил -, 5 - этил -, 4, 5 -диметил -, 4 - этил - 5 - метил -, 5 - этил - 4 - метил 2 - тиазолил, 2 - бензтиазолил, 4, 5, 6,7 - тетрагидро -. 2 - бензтиазолил, 5, 6 - дигидро - 7Н - тиопирано 4,3-d тиазол - 2 - ил, 3 - метил - 5 - изотиазолил, 1, 3, 4 - тнадиазолил, 5 - метил - 1, 3, 4 - тиадиазол -2 - ил или 5 - метил - 3 - изоксазолил, или их солей, заключающийся в том, что эфир 1, 1 - диоксидов 4 - окси - 2.Н - нафто 2,1-е -1,2тиазин - 3 - карбонов ой кислоты общей формулы -RJ (I) где RI - алкил, содержащий 1-6 атомов углерода или аралкил, содержащий 7-10 атомов углерода, R имеет указанные значения, подвергают взаимодействию с аромагичес ким амином общей) формулы NHj-ArСи О, где Аг имеет указанные значения, в среде инерт ногр оргашческого растворителя или в избытке амина общей формулы (lil) при 60-200° С с последующим выделением целевого продукта в свободном виде или в виде соли. Приоритет по признакам 08.11.74 при R- водород или метил; Аг- фенил, 2 - пиридил, 2 - пиразишш, 2 - тиазолил, 4 метил - 2 - тиазолил, 4, 5 - диметил - 2 - тиазолил, 2- бензогиазолил или 5 - метил - 3 - изоксазолил; RI - алк1Ш с 1-6 атомами углерода 03.09.95 - все значения радикалов R, RI Аг, за исключением значений, указанных выше. Источники информации, принятые во внимание при зкспертизе; 1. Патент США N 3591584, кл. 260-243, опублик. 1971.
Авторы
Даты
1977-09-30—Публикация
1975-10-29—Подача