Способ диагностики острых лейкозов и наборы для его выполнения являются группой изобретений, относящейся к медицине, а именно онкогематологии, и может быть использован для диагностики острых лейкозов.
Предложен способ диагностики острых лейкозов, основанный на последовательном определении уровня экспрессии отдельных РНК в пробах крови методом ПЦР с использованием на первом скрининговом этапе мультиплексного набора для определения уровня мРНК генов WT1, EVI1 и HMGA2 с последующим уточнением молекулярно-генетического варианта лейкоза путем постановки реакции с набором мультиплексной ПЦР для выявления РНК транскриптов слитых при хромосомных транслокациях генов PICALM-MLLT10, PML-RARa, MLL-AF4, MLL-AF6, MLL-AF9, MLL-AF10, MLL-ENL, MLL-ELL, CBFB-MYH11, AML1-ETO, TEL-AML, Е2А-РВХ1, BCR-ABL1, SIL-TAL, а при выявлении патологической экспрессии данных РНК, выполнение заключительного этапа молекулярно-генетической диагностики, заключающегося в количественном определении их исходного уровня, используя лейкозо-специфический набор, приемлемый в дальнейшем, для индивидуального молекулярного мониторинга развития заболевания и эффективности терапии.
Предложенная группа изобретений на основе последовательного использования разработанных вариантов комплектаций наборов для ОТ-ПЦР позволяет выявлять пациентов с острым лейкозом на этапе скрининга проб венозной крови, в том числе при отсутствии или низком уровне циркулирующих бластных клеток, уточнить молекулярно-генетический вариант их заболевания, а также сформировать лейкозо-специфический набор для количественной оценки уровня экспрессии РНК-маркеров, и дальнейшего контроля за развитием заболевания и эффективностью терапии. Указанное изобретение является новым подходом к диагностике острых лейкозов с включением молекулярно-генетического тестирования уже на первом этапе обследования пациентов с подозрением на острый лейкоз параллельно с классическим морфологическим исследованием клеток крови.
Лейкозы - гетерогенная группа онкологических заболеваний крови, обусловленных генетическими дефектами и дисбалансом экспрессии генов, отвечающих за пролиферацию и дифференцировку клеток. Острый лейкоз (ОЛ) - самое распространенное злокачественное заболевание у детей и наиболее неблагоприятное заболевание крови у взрослых трудоспособного возраста. В соответствии с международной статистикой ежегодно регистрируют около 50 новых случаев ОЛ на 1 млн населения. В 2019 году число смертей от ОЛ составило 2% от всех пациентов, умерших от онкологического заболевания (6 и 8 место по смертности среди всех видов рака среди мужчин и женщин соответственно). Однако, выявляемость ОЛ у взрослых в Российской Федерации существенно ниже ожидаемого уровня [Ахмерзаева З.Х., Паровичникова Е.Н., Русинов М.А., Зотина Е.Н., Гаврилова Л.В., Приступа А.С., Борисенкова Е.А., Вопилина Н.А., Куликов С.М. Эпидемиологическое исследование острых лейкозов в пяти регионах Российской Федерации. Гематология и трансфузиология. 2017; 62(1): 46-51].
Постановка диагноза ОЛ и начало лечения пациентов от момента появления первых симптомов в реальной клинической практике занимает от нескольких недель до нескольких месяцев. Особые сложности вызывают случаи ОЛ, при которых в периферической крови не выявляются незрелые (бластные) клетки или их уровень ниже достаточного для постановки диагноза. На данный момент существует общепринятый алгоритм лабораторной диагностики острых лейкозов, который предполагает первичное исследование соотношения форменных элементов крови с описанием их морфологических характеристик. Выявление более 20% бластных клеток в пробах венозной крови или костного мозга является основанием для их дальнейшего исследования цитохимическими, иммуноцитометрическими и цитогенетическими методами анализа для уточнения диагноза в соответствии с международной классификацией, включающей конкретные молекулярно-генетические варианты заболевания. При этом отдельные молекулярно-генетические маркеры, в том числе соматические мутации и РНК-транскрипты слитых (химерных) генов хромосомных транслокаций, рассматриваются как важные прогностические маркеры и перспективные инструменты мониторинга эффективности терапии и оценки минимальной остаточной болезни (Клинические рекомендации «Острые миелоидные лейкозы взрослых», 2020; Клинические рекомендации «Острые лимфобластные лейкозы взрослых», 2020 https://npngo.ru/biblioteka/klinicheskie_rekomendatsii__2019_god_).
Хромосомные транслокации и их РНК-транскрипты выявляют примерно в 50-60% всех ОЛ наиболее частые среди них: PML-RARa, BCR-ABL, PICALM-MLLT10, MLL-AF4, MLL-AF6, MLL-AF9, MLL-AF10, MLL-ENL, CBFB-MYH11, AML1-ETO, TEL-AML, Е2А-РВХ1, SIL-TAL [Ольховский И.А., Комина А.В., Столяр М.А., Горбенко А.С. Молекулярно-генетические нарушения при острых лейкозах как основа разработки диагностических тестов (обзор литературы). Лабораторная служба. 2020;9(4):26-45]. Вместе с тем, за редким исключением (PML-RARa и BCR (210)-ABL1), РНК маркеры ОЛ редко используют в практической диагностике ОЛ в связи отсутствием доступных коммерческих диагностических наборов для выполнения ПЦР.
Цитогенетический метод выявления хромосомных транслокаций предусматривает визуальное исследование строения хромосом в бластотрансформированных мононуклеарных клетках с использованием техники световой микроскопии [Young-Uk Cho, Hyun-Sook Chi, Chan-Jeoung Park, Seongsoo Jang, and Eul-Ju Seo. Rapid Detection of Prognostically Significant Fusion Transcripts in Acute Leukemia Using Simplified Multiplex Reverse Transcription Polymerase Chain Reaction. Oncology & Hematology. Korean Med Sci 2012; 27: 1155-1161]. Для его выполнения необходимо предварительное выделение мононуклеарных клеток с последующей 24-часовой инкубацией со стимуляторами пролиферации для получения метафазных ядерных клеток. При этом в ряде случаев несмотря на влияние индукторов, пролиферация клеток не наступает. Кроме длительности выполнения, цитогенетический метод требует участия специально обученного квалифицированного специалиста.
Выявление отдельных хромосомных транслокаций также может выполняться методом флуоресцентной гибридизации "in situ" (FISH), в том числе и на интерфазных ядрах клеток без необходимости предварительной индукции пролиферации [Kerney L. The impact of the new FISH technologies on the cytogenetics of haematological malignancies. Br. J. Haematol. 1999, 104(4): 648-658]. Метод является высокоспецифичным и достаточно чувствительным, однако трудоемким и требующим специального люминесцентного микроскопического оборудования и визуальной верификации результата с участием специально подготовленного персонала. При этом количество одновременно анализируемых транслокаций ограничено возможностями дифференциальной флюоресценции используемых зондов. Недостатком данного метода также является необходимость в дорогостоящих реактивах.
Известны также молекулярно-генетические методы определения экспрессии матричных РНК, синтезированных клеткой на матрице участка ДНК генов, соединенных в процессе хромосомной транслокации - так называемых, слитых (химерных) транскриптов [Р Scurto, МН suRocha, J R Kane, WK Williams, DM Haney, WP Conn, SA Shurtleffand JR Downing. A multiplex RT-PCR assay for thedetection of chimeric transcript sencoded by therisk-stratifying translocation sofpediatric acute lymphoblastic leukemia. Leukemia (1998) 12, 1994-2005; JGabert, EBeillard, VH JvanderVelden, WBi, D Grimwade, N Pallisgaard, G Barbany, G Cazzaniga, JM Cayuela, H Cave, F Pane, JLE Aerts, D De Micheli, X Thirion, VPradel, M Gonzalez, SV iehmann, M Malec, GSaglioand JJMvanDongen. Standardization and quality control studies of 'real-time' quantitative reverse transcriptase polymerase chain reaction of fusion gene transcripts for residual disease detection in leukemia - A Europe Against Cancer Program. Leukemia (2003) 17, 2318-2357].
Использование ПЦР с обратной транскрипцией (ОТ-ПЦР) с целью обнаружения основных хромосомных транслокаций при лейкемии имеет многочисленные преимущества перед традиционной цитогенетикой, в том числе за счет более короткого времени выполнения теста, отсутствия необходимости в индукции пролиферации клеток. Кроме того, ОТ-ПЦР позволяет обнаружить транслокации, которые могут быть пропущены традиционной цитогенетикой, поскольку обеспечивают гораздо более чувствительное тестирование, достаточное для последующего контроля минимальной остаточной болезни. Выполнение методики ОТ-ПЦР для выявления РНК маркеров не зависит от субъективности визуальной детекции результатов анализа и не требует специального обучения персонала, доступно в любых клинико-диагностических лабораториях с минимальным комплектом оборудования для выполнения ПЦР-тестов.
Кроме выявления химерных транскриптов слитых при хромосомных транслокациях генов, при ОЛ описано диагностическое значение определения уровня экспрессии мРНК генов, высокая активность которых характерна для клеток в период эмбрионального развития организма [Marjanovic I., Karan-Djurasevic Т., Ugrin М., Virijevic М., Vidovic A., Tomin D., Vukovic N., Pavlovic S., Tosic N. Use of Wilms Tumor 1 Gene Expressionas a Reliable Marker for Prognosis and Minimal Residual Disease Monitoring in Acute Myeloid Leukemia with Normal Karyotype Patients. OriginalStudy.2017. Vol. 17, No. 5, 312-9]. Так описано увеличение экспрессии мРНК генов WT1, HGMA2 и EVI1 при ОЛ у детей и взрослых, их прогностическое значение и возможность использования для молекулярного мониторинга развития заболевания [Н.Н. Мамаев, А.В. Горбунова, И.М. Бархатов, Я.В. Гудожникова, Т.Л. Гиндина, В.А. Катерина, Е.В. Волчков, А.Л. Алянский, Е.В. Бабенко, О.А. Слесарчук, Н.В. Станчева, С.Н. Бондаренко, Б.В. Афанасьев. Молекулярный мониторинг течения острых миелоидных лейкозов по уровню экспрессии гена WT1 после аллогенной трансплантации гемопоэтических стволовых клеток. Клин. онкогематол. 2015; 8(3): 309-320; Мамаев Н.Н., Шакирова А.И., Морозова Е.В., Гиндина Т.Л. EVI1-позитивные лейкозы и миелодиспластические синдромы: теоретические и клинические аспекты (обзор литературы). Клиническая онкогематология. 2021; 14(1): 103-17]. При этом частота выявления фактов повышенной экспрессии данных генов эмбрионального периода развития при ОЛ составляет 70-90% и не зависит от присутствия химерных транскриптов [Ольховский И.А., Комина А.В., Столяр М.А., Горбенко А.С. Молекулярно-генетические нарушения при острых лейкозах как основа разработки диагностических тестов (обзор литературы). Лабораторная служба. 2020;9(4):26-45].
Наиболее часто для определения уровня экспрессии генов WT1, HGMA2 и EVI1, используют реакцию ПЦР [Cilloni D., Gottardi Е., Micheli D., Serra A., Volpe G., Messa F., Rege-Cambrin G., Guerrasio A., Divona M., LoCocoand, Saglio G. Quantitative assessment of WT1 expression by real time quantitative PCR maybe a use ful tool formonitoring minimal residual disease in acute leukemia patients. Leukemia. - 2002. №16. P. 2115-2121]. Ранее были предложены наборы на основе ПЦР для определения уровня экспрессии мРНК гена WT1 и EVI1 "QIAGEN" (https://www.qiagen.com/us/) и ООО "Иноген" (https://inogene.ru/). Описаны также молекулярно-генетические методы оценки уровня экспрессии мРНК гена HGMA2 [Li Tan, Xiaoping Wei, Lixia Zheng, JincaiZeng, HaiboLiu, ShaojiangYang, HuoTan, Amplified HMGA2 promotes cell growth by regulating Aktpathwayin AML, J Cancer Res ClinOncol, 2016, 389-399].
Известны коммерческие наборы, основанные на выполнении ПЦР, для выявления отдельных химерных РНК-транскриптов PML-RARa, CBFB-MYH11, AML1-ETO, TEL-AML, E2A-PBX1, BCR-ABL1(p190, p210 и p230) ("ipsogen" Qiagen, Германия https://www.qiagen.com/). Однако, выявление конкретных транскриптов при использовании этих наборов предполагает проведение тестирования образцов биоматериала последовательно разными наборами для каждого из транскриптов, что требует больших затрат рабочего времени, реактивов и объема биологических образцов необходимых для выполнения анализа.
Известно также одновременное, в одной аналитической постановке (мультиплексное) исследование ряда химерных транскриптов с использованием набора «ЛК-БИОЧИП» [Патенты РФ №2286798 опубл. 10.11.2006, №2643333 опубл. 31.01.2018]. Использование данной технологии предполагает наличие специального оборудования биочип-ридера для считывания результатов теста с чипа, дополнительного программного обеспечения и участия квалифицированного персонала, при этом тесты выполняются более двух рабочих дней. Кроме того методика, на которой основан набор «ЛК-БИОЧИП» менее чувствительная чем классический ПЦР-ОТ и не позволяет выполнять количественный мониторинг минимальной остаточной болезни.
Известны наборы для одновременного выявления нескольких химерных транскриптов, производимые фирмой «DNA Diagnostic A/S» (Дания, www.clna-diagnostic.com) методом ПЦР, однако их использование не приемлемо для тестов первичного скрининга, или мониторинга эффективности терапии.
Известные методы и наборы позволяют выявлять указанные выше химерные транскрипты и мРНК генов WT1, EVI1 и HMGA2 только раздельно в разных постановках ПЦР с разными режимами амплификации, что существенно увеличивает время проведения анализа, требует больших затрат клинического материала, объем которого органичен возможностью его взятия, особенно у ребенка.
Известен набор и метод скрининга и выявления химерных транскриптов при лейкозах (патент CN №107385031 опубл. 24.11.2017) включающий предварительное выделение мононуклеарных клеток из образца, выделение РНК, обратную транскрипцию и выполнение двух последовательных реакций вложенной и гнездовой ПЦР с детекцией продуктов амлификации методом электрофореза геле. Учитывая, что химерные транскрипты при ОМЛ выявляются не более чем в 70%, а при ОЛЛ - не более чем при 40% случаев, их диагностическая эффективность при скрининге существенно уступает определению мРНК эмбриональных генов. Выполнение предварительного выделения мононуклеарных клеток из образца крови вносит дополнительных этап аналитических процедур требующих дополнительных расходных материалов, времени и большего уровня минимального объема пробы. Электрофоретическая детекция результатов требует предварительно приготовления геля и более трудоемкая в сравнении с ПЦР «в реальном времени».
Наиболее близким к заявляемому способу (прототип) является способ определения химерных транскриптов до или вместо выполнения цитогенетического анализа с использованием единого набора реактивов для выполнения мультиплексной реакции одновременного выявления нескольких химерных транскриптов методом ПЦР в режиме реального времени с использованием флуоресцентно-меченных олигонуклеотидов [Xiaodong Lyu, Xianwei Wang, Lina Zhang, Zhenzhu Chen, Yu Zhao, Jieying Hu, Ruihua Fan, Yongping Song. Detection of 22 common leukemic fusion genes using a single-step multiplex qRT-PCR- based assay. Lyu et al. Diagnostic Pathology (2017) 12:55]. Данный способ диагностики ОЛ позволяет в течение одного рабочего дня выявлять транскрипты слияния генов и верифицировать молекулярно-генетический диагноз у 53,7% больных лейкемией - в 69,4% пациентов с острым миелоидным лейкозом (ОМЛ) и 33,3% с острым лимфобластным лейкозом (ОЛЛ). Недостатком данного способа является отсутствие возможности определения описанным набором уровня экспрессии мРНК генов WT1, HMGA2 и EVI1, которые часто повышены при ОЛ, влияют на прогноз заболевания и могут быть использованы для мониторинга терапии. Кроме того, часто выявляемый высокий уровень экспрессии этих мРНК при ОЛ мог бы быть использован для скрининга при первичном обследовании у пациентов с подозрением на ОЛ на амбулаторном этапе.
Описанные способы молекулярно-генетической диагностики и наборы для их осуществления не предполагают использование единой технологической платформы, включающей общие реагенты: ферменты, олигонуклеотидные праймеры и зонды, единый режим амплификации, а также использование образца кДНК, полученного на первом этапе диагностики (при выделении РНК и выполнении реакции обратной транскрипции) на последующих этапах диагностики.
Способ диагностики острых лейкозов и наборы для его выполнения решают задачу молекулярно-генетической диагностики ОЛ с использованием единой технологической платформы для всех трех этапов лабораторного диагностического процесса, включающего первичный скрининг, уточнение молекулярно-генетического варианта заболевания и количественное определение уровня лейкозо-специфических РНК-маркеров для дальнейшего использования при мониторинге эффективности терапии. Позволяют быстро и с высокой точностью выявить у пациента молекулярно-генетический вариант лейкоза и определить количественный уровень экспрессии молекулярно-генетических маркеров, требуют минимальных затрат труда, времени, материалов и реагентов.
Техническим результатом, достигаемым предлагаемым способом диагностики с использованием разработанных диагностических наборов, содержащих оригинальные комбинации олигонуклеотидных праймеров и зондов, является:
- их целевое использование на разных этапах диагностики ОЛ, а именно при скрининге пациентов с подозрением на заболевание, для уточнения диагноза и для молекулярного контроля эффективности терапии;
- выполнение рутинных скрининговых исследований в любой лаборатории, оснащенной оборудованием для выполнения ПЦР тестов за счет применения широкодоступной технологии ПЦР диагностики;
- сокращение времени верификации молекулярно-генетического варианта ОЛ до 1 дня, снижение затрат рабочего времени, экономия расходных материалов и объема используемого для анализа биологического материала при использовании заявляемого способа;
- использование единой технологической платформы формирования и применения наборов для ПЦР, включающей единые ферменты, стандарты, контрольные образцы и режимы амплификации, что позволяет подобрать наиболее эффективную комбинацию молекулярно-генетических маркеров для дальнейшего мониторинга развития заболевания и оценки эффективности терапии, сохраняя преемственность и сопоставимость результатов, полученных на разных этапах диагностики.
Заявляемый способ соответствует критерию новизны, так как впервые предполагает использование в качестве скринингового теста при подозрении на острый лейкоз выполнение анализа для одновременной оценки экспрессии мРНК генов WT1, HMGA2, EVI1 и оптимального подбора выявляемых химерных траснкриптов в наборе для верификации молекулярно-генетического диагноза в мультиплексном формате ОТ-ПЦР, а также впервые предлагает использование оригинальных комбинаций олигонуклеотидных праймеров и зондов для формирования наборов в зависимости от цели каждого этапа диагностики с момента подозрения диагноза до контролируемого сопровождения эффективности терапевтических воздействий.
Оптимальные сочетания специфичных смесей праймеров и олигонуклеотидных зондов к перечисленным генетическим локусам искомых генов были определены на основании исключения вероятности взаимного отжига и образования димеров и с учетом лучшей визуализации отдельных ПЦР-продуктов, разделенных по длине и каналу флуоресценции, а также условиям проведения ПЦР и соотношения концентраций реагентов, что является оригинальной особенностью заявляемого изобретения.
Дополнительный технический результат группы изобретений заключается в возможности диагностики ОЛ в пробах крови с минимальным уровнем циркулирующих бластных клеток, за счет более высокой чувствительности ПЦР для обнаружения содержащихся в этих клетках мРНК WT1, HMGA2 и EVI1.
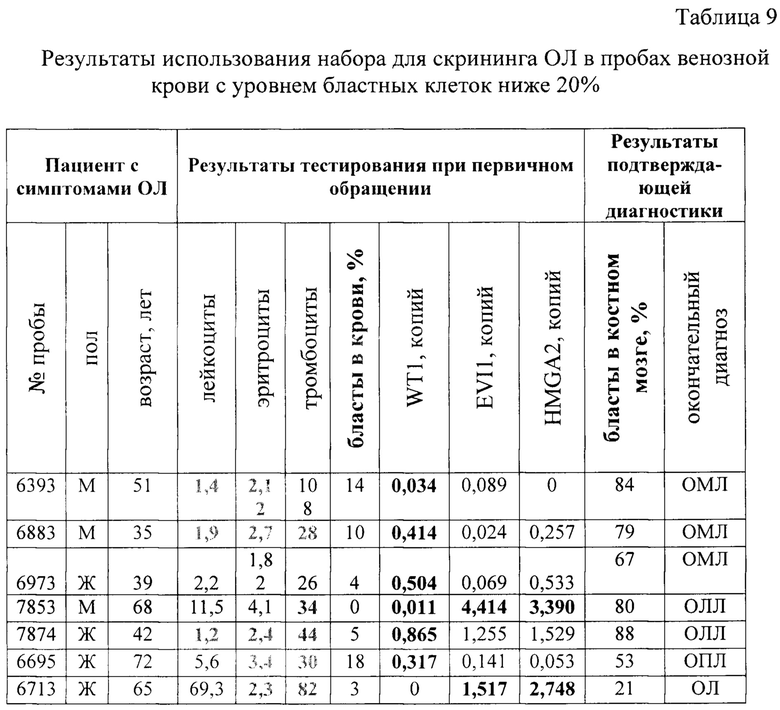
Указанный единый технический результат предлагаемого изобретения по способу диагностики достигается за счет использования оригинальных комбинаций праймеров и зондов в смесях для одновременного определения мРНК генов эмбриональной активности WT1, HMGA2, EVI1 и патогенетических химерных транскриптов TEL-AML, PML-RARα, AML-ETO, MLL-AF4, MLL-AF6, MLL-AF9, MLL-AF10, MLL-ENL, CBFB-MYH11, BCR-ABL (р190, р210, р230), S1L-TAL, PICALM-MLLT10, тем, что при выявлении в анализе крови пациентов изменений количества и состава форменных элементов, которые позволяют подозревать возможное онкогематологическое заболевание, с данными образцами крови пациента проводят скрининговый тест с использованием набора для мультиплексной ПЦР с целью оценки уровня экспрессии мРНК генов WT1, HMGA2 и EVI1. Разработанный способ позволяет определить риск наличия ОЛ у пациента с чувствительностью 96% и специфичностью 71%. ROC-кривая при использовании набора для скрининга ОЛ представлена на Фиг. 1. Эта модель включает в себя оценку экспрессии мРНК генов WT1, EVI1 и HMGA2, которые в сочетании обеспечивают лучший прогноз (95% ДИ: 0,782-0,895, AUC=0,844). Расчеты проведены по результатам тестирования проб крови 61 пациента с верифицированным ОЛ и 56 пациентов из группы сравнения, имеющих изменения формулы клеток крови, но не имеющих подтвержденного диагноза ОЛ. Образец крови, показавший значения экспрессии РНК генов WT1, HMGA2 или EVI1 на этапе скрининга, свидетельствующие о высоком риске наличия ОЛ у пациента в дальнейшем тестируют с использованием второго набора оригинальных комбинаций олигонуклеотидных праймеров и зондов в мультиплексной ПЦР с целью выявления химерных транскриптов PICALM-MLLT10, PML-RARa, MLL-AF4, MLL-AF6, MLL-AF9, MLL-AF10, MLL-ENL, MLL-ELL, CBFB-MYH11, AML1-ETO, TEL-AML, Е2А-РВХ1, BCR-ABL1 (р190, р210, р230), SIL-TAL. Выявление хотя бы одного из указанных химерных транскриптов подтверждает соответствующий молекулярно-генетический вариант ОЛ. Затем в зависимости от выявленных в первом скрининговом и втором уточняющем этапе диагностики РНК-маркеров формируют соответствующую комбинацию олигонуклеотидных праймеров, зондов и калибраторов лейкозо-специфического набора количественной ПЦР с целью проведения в дальнейшем оценки развития заболевания и молекулярной оценки эффективности терапии.
Указанный технический результат предлагаемого изобретения по наборам для диагностики острых лейкозов достигается тем, что кроме стандартных компонентов (ферментов, дезоксирибонуклеотидов и буфера) для выполнения ПЦР в «реальном времени» с обратной транскрипцией:
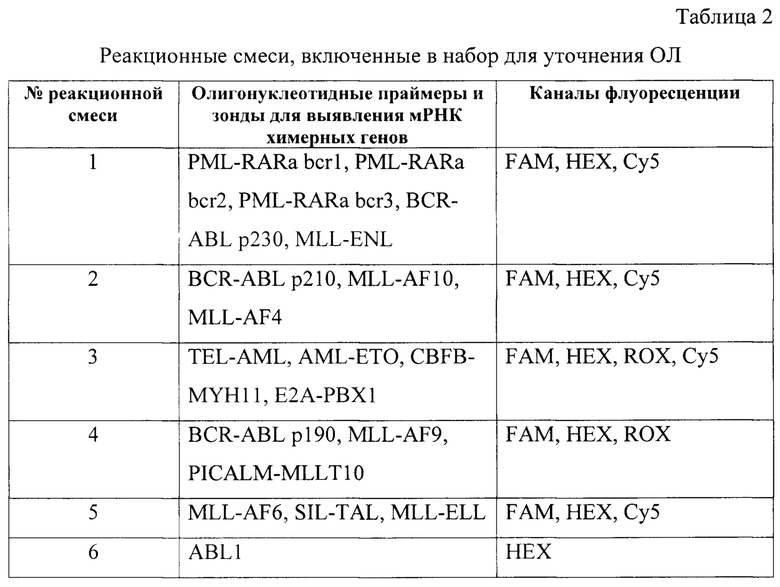
- в состав набора для скрининга острого лейкоза входят 12 специфичных олигонуклеотидных праймеров и флуоресцентно-меченых ДНК-зондов, имеющих нуклеотидные последовательности SEQ ID NO:1-SEQ ID NO:12, объединенные в оригинальные мультиплексные реакционные смеси с учетом оптимального режима проведения амплификации, представленные в таблице 1;
- в состав набора для уточнения молекулярно-генетического варианта острого лейкоза входят 62 специфичных олигонуклеотидных праймера и флуоресцентно-меченых ДНК-зонда, имеющих нуклеотидные последовательности SEQ ID NO:10 - SEQ ID NO:71, объединенные в оригинальные мультиплексные реакционные смеси с учетом оптимального режима проведения амплификации, представленные в таблице 2;
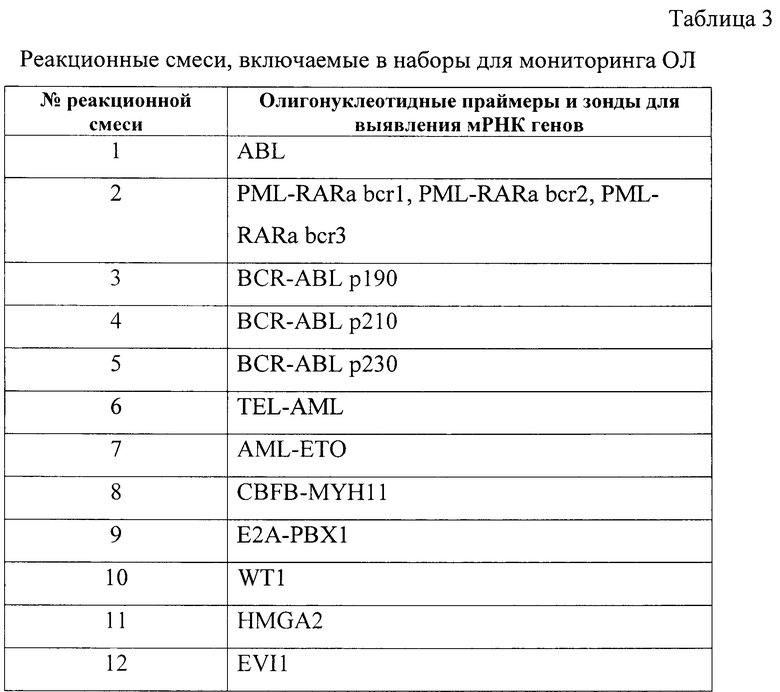
- состав лейкозо-специфического набора для количественной оценки исходного уровня и последующей динамики выявленных у пациента РНК-маркеров ОЛ в процессе терапии формируется индивидуально для каждого пациента, включая мРНК одного из генов WT1, HMGA2 или EVI1, имеющих максимальную экспрессию в скрининговом тесте и/или выявленного на втором этапе диагностики химерного транскрипта, представленные в таблице 3. При этом набор комплектуется пробирками с калибровочными растворами, содержащими специфические плазмидные стандарты с известным определенным количеством молекул для построения калибровочной кривой и получения результатов тестирования в количественном формате;
- в качестве источника флуоресценции в TaqMan-зондах на 5' конце применяют красители: флуоресцеин (FAM), карбокси-Х-родамин (ROX) и хлорированный флуоресцеин (HEX), а для тушения флуоресценции используют BlackHoleQuencher-1 (BHQ1) на 3' конце.
Из результатов информационно-патентного поиска и практики ПЦР-исследований неизвестно о способе выполнения мультиплексного ПЦР-анализа для первичного скрининга ОЛ, а также для уточнения молекулярно-генетического варианта заболевания и определения лейкозо-специфического РНК-маркера для дальнейшего мониторинга эффективности терапии с использованием на каждом из этих этапов диагностики единых технологических режимов амплификации, применяемых ферментов, субстратных смесей, буферных растворов и реакционных смесей с оригинальными комбинациями специфических праймеров и зондов.
Преимуществом заявляемой группы изобретений является то, что наборы для выполнения мультиплексной ПЦР позволяют проводить исследование экспрессии мРНК трех генов активных в эмбриональных клетках и всех 16 онкогенных химерных транскриптов в течение одного рабочего дня с использованием стандартного оборудования клинико-диагностических ПЦР лабораторий, при этом лейкозо-специфический набор количественного определения уровня РНК-маркеров в дальнейшем используют при мониторинге эффективности проводимой терапии.
Сущность предлагаемого изобретения пояснена на следующих графических материалах:
Фиг. 1 - Оценка диагностической эффективности определения экспрессии мРНК генов WT1, EVI1 и HMGA2.
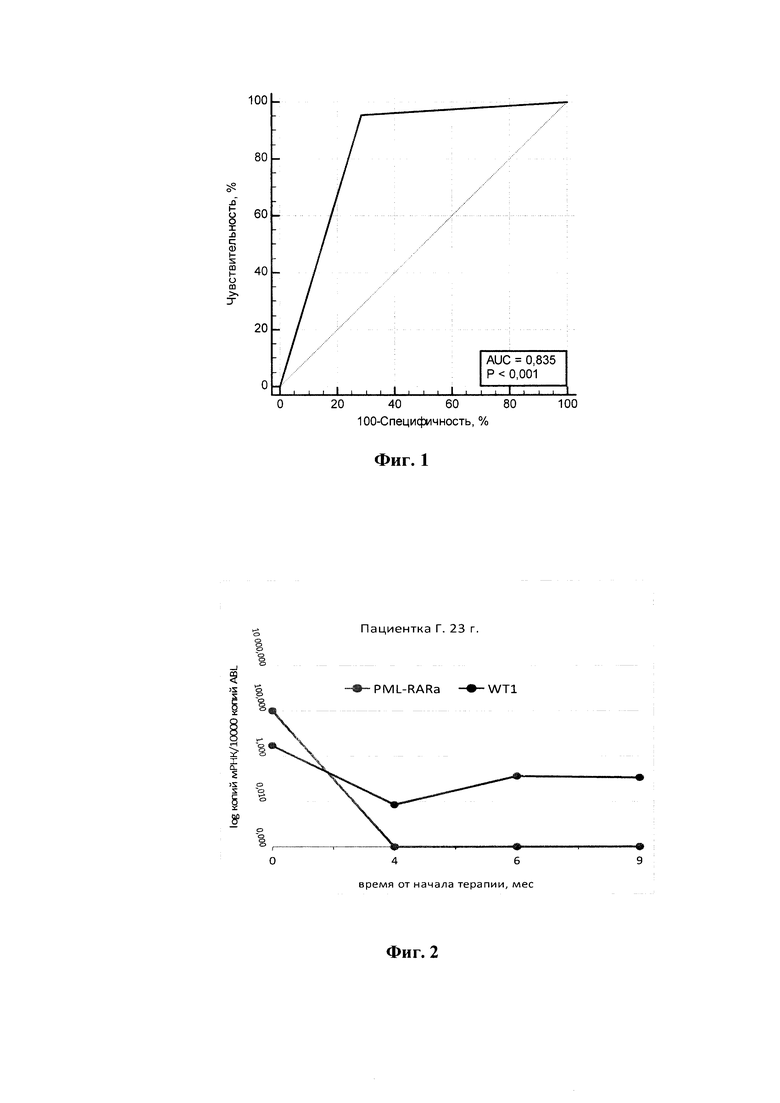
Фиг. 2 - Экспрессия мРНК гена WT1 и химерного транскрипта PML-RARa в динамике лечения пациента.
Сущность предлагаемой группы изобретений пояснена следующими перечнями последовательностей дезоксинуклеотидов, комплементарных участкам специфических локусов РНК (cDNA) Homo sapiens (5-3'-):
SEQ ID NO:1 последовательность нуклеотидов прямого праймера WT1;
SEQ ID NO:2 последовательность нуклеотидов обратного праймера WT1;
SEQ ID NO:3 последовательность нуклеотидов флуоресцентного зонда WT1;
SEQ ID NO:4 последовательность нуклеотидов прямого праймера EVI1;
SEQ ID NO:5 последовательность нуклеотидов обратного праймера EVI1;
SEQ ID NO:6 последовательность нуклеотидов флуоресцентного зонда EVI1;
SEQ ID NO:7 последовательность нуклеотидов прямого праймера HMGA2;
SEQ ID NO:8 последовательность нуклеотидов обратного праймера HMGA2;
SEQ ID NO:9 последовательность нуклеотидов флуоресцентного зонда HMGA2;
SEQ ID NO:10 последовательность нуклеотидов прямого праймера ABL1;
SEQ ID NO:11 последовательность нуклеотидов обратного праймера ABL1;
SEQ ID NO:12 последовательность нуклеотидов флуоресцентного зонда ABL1;
SEQ ID NO:13 последовательность нуклеотидов прямого праймера TEL-AML1;
SEQ ID NO:14 последовательность нуклеотидов обратного праймера TEL-AML1;
SEQ ID NO:15 последовательность нуклеотидов флуоресцентного зонда TEL-AML1;
SEQ ID NO:17 последовательность нуклеотидов прямого праймера PML-RARa bcr3;
SEQ ID NO:18 последовательность нуклеотидов обратных праймеров PML-RARa bcr1, bcr2, bcr3;
SEQ ID NO:19 последовательность нуклеотидов флуоресцентного зонда PML-RARa bcr1;
SEQ ID NO:20 последовательность нуклеотидов флуоресцентного зонда PML-RARa bcr2;
SEQ ID NO:21 последовательность нуклеотидов флуоресцентного зонда PML-RARa bcr3;
SEQ ID NO:22 последовательность нуклеотидов прямого праймера AML1-ETO;
SEQ ID NO:23 последовательность нуклеотидов обратного праймера AML1-ETO;
SEQ ID NO:24 последовательность нуклеотидов флуоресцентного зонда AML1-ETO;
SEQ ID NO:25 последовательность нуклеотидов прямых праймеров MLL-AF4, MLL-AF9, MLL-ENL, MLL-ELL;
SEQ ID NO:26 последовательность нуклеотидов прямых праймеров MLL-AF4, MLL-AF9, MLL-ENL, MLL-ELL;
SEQ ID NO:27 последовательность нуклеотидов обратного праймера MLL-AF4;
SEQ ID NO:28 последовательность нуклеотидов обратного праймера MLL-AF4;
SEQ ID NO:29 последовательность нуклеотидов флуоресцентных зондов MLL-AF4, MLL-AF9, MLL-ENL, MLL-ELL;
SEQ ID NO:30 последовательность нуклеотидов флуоресцентных зондов MLL-AF4, MLL-AF9, MLL-ENL, MLL-ELL;
SEQ ID NO:31 последовательность нуклеотидов обратного праймера MLL-AF6;
SEQ ID NO:32 последовательность нуклеотидов обратного праймера MLL-AF9;
SEQ ID NO:33 последовательность нуклеотидов обратного праймера MLL-AF9;
SEQ ID NO:34 последовательность нуклеотидов обратного праймера MLL-AF9;
SEQ ID NO:35 последовательность нуклеотидов прямого праймера MLL-AF10;
SEQ ID NO:36 последовательность нуклеотидов прямого праймера MLL-AF10;
SEQ ID NO:37 последовательность нуклеотидов обратных праймеров MLL-AF10, PICALM-MLLT10;
SEQ ID NO:38 последовательность нуклеотидов обратных праймеров MLL-AF10, PICALM-MLLT10;
SEQ ID NO:39 последовательность нуклеотидов обратных праймеров MLL-AF10, PICALM-MLLT10;
SEQ ID NO:40 последовательность нуклеотидов обратного праймера MLL-AF6;
SEQ ID NO:41 последовательность нуклеотидов флуоресцентных зондов MLL-AF10, PICALM-MLLT10;
SEQ ID NO:42 последовательность нуклеотидов флуоресцентных зондов MLL-AF10, PICALM-MLLT10;
SEQ ID NO:43 последовательность нуклеотидов флуоресцентных зондов MLL-AF10, PICALM-MLLT 10;
SEQ ID NO:44 последовательность нуклеотидов прямого праймера MLL-AF6;
SEQ ID NO:45 последовательность нуклеотидов флуоресцентного зонда MLL-AF6;
SEQ ID NO:46 последовательность нуклеотидов прямого праймера MLL-AF6;
SEQ ID NO:47 последовательность нуклеотидов флуоресцентного зонда MLL-AF6;
SEQ ID NO:48 последовательность нуклеотидов прямого праймера MLL-AF6;
SEQ ID NO:49 последовательность нуклеотидов флуоресцентного зонда MLL-AF6;
SEQ ID NO:50 последовательность нуклеотидов обратного праймера MLL-ENL;
SEQ ID NO:51 последовательность нуклеотидов обратного праймера MLL-ENL;
SEQ ID NO:52 последовательность нуклеотидов прямого праймера CBFB-MYH11;
SEQ ID NO:53 последовательность нуклеотидов обратного праймера CBFB-MYH11;
SEQ ID NO:54 последовательность нуклеотидов обратного праймера CBFB-MYH11;
SEQ ID NO:55 последовательность нуклеотидов обратного праймера CBFB-MYH11;
SEQ ID NO:56 последовательность нуклеотидов флуоресцентного зонда CBFB-MYH11;
SEQ ID NO:57 последовательность нуклеотидов прямого праймера Е2А-РВХ1;
SEQ ID NO:58 последовательность нуклеотидов обратного праймера Е2А-РВХ1;
SEQ ID NO:59 последовательность нуклеотидов флуоресцентного зонда Е2А-РВХ1;
SEQ ID NO:60 последовательность нуклеотидов обратного праймера MLL-ELL;
SEQ ID NO:61 последовательность нуклеотидов прямого праймера BCR-ABL1 р190;
SEQ ID NO:62 последовательность нуклеотидов прямого праймера BCR-ABL1 р230;
SEQ ID NO:63 последовательность нуклеотидов прямого праймера PICALM-MLLT10;
SEQ ID NO:64 последовательность нуклеотидов прямого праймера PICALM-MLLT10;
SEQ ID NO:65 последовательность нуклеотидов прямого праймера BCR-ABL1 р210;
SEQ ID NO:66 последовательность нуклеотидов прямого праймера BCR-ABL1 р210;
SEQ ID NO:67 последовательность нуклеотидов обратных праймеров BCR-ABL1 р210, р190, р230;
SEQ ID NO:68 последовательность нуклеотидов флуоресцентных зондов BCR-ABL1 р210, р190, р230;
SEQ ID NO:69 последовательность нуклеотидов прямого праймера SIL-TAL1;
SEQ ID NO:70 последовательность нуклеотидов обратного праймера SIL-TAL1;
SEQ ID NO:71 последовательность нуклеотидов флуоресцентного зонда SIL-TAL1.
Предлагаемый способ осуществляется следующим образом.
1. Отбор проб крови и подготовка для тестирования методом ОТ-ПЦР
Образцы крови у пациентов с подозрением на ОЛ получают из локтевой вены в стандартные вакутейнеры или пробирки с ЭДТА К2 или с цитратом натрия в качестве антикоагулянтов.
Пробы крови берут для тестирования также в случае, когда в результате проведения стандартного гематологического исследования с подсчетом формулы клеток крови пациентов выявлены изменения в количестве и (или) соотношении форменных элементов, не противоречащих диагнозу ОЛ, в том числе при отсутствии или низком содержании циркулирующих в крови бластных клеток.
В процессе исследования кровь сохраняют в закрытых пластиковых пробирках при комнатной температуре, с соблюдением общепринятых мер предосторожности при работе с клетками крови. При отсутствии гарантий доставки проб в лабораторию ПЦР для исследования в течение 48 часов после взятия крови, следует использовать любой раствор, стабилизирующий РНК в соответствии с инструкциями использования выбранных стабилизирующих растворов.
Выделение тотальной РНК из лейкоцитов крови проводят любым доступным методом, позволяющим получить РНК в количестве и качестве, достаточном для выполнения ПЦР в реальном времени, затем проводят реакцию обратной транскрипции для получения комплементарной ДНК (кДНК). Объем образца кДНК, используемой для анализа заявляемым способом, должен составлять не менее 140 мкл.
Для достижения оптимального для выполнения анализа количества молекул РНК (кДНК) в исследуемом образце достаточным является наличие 107 лейкоцитов (что соответствует приблизительно 1,5 мл венозной крови).
2. Проведение ОТ-ПЦР в реальном времени для скринингового тестирования
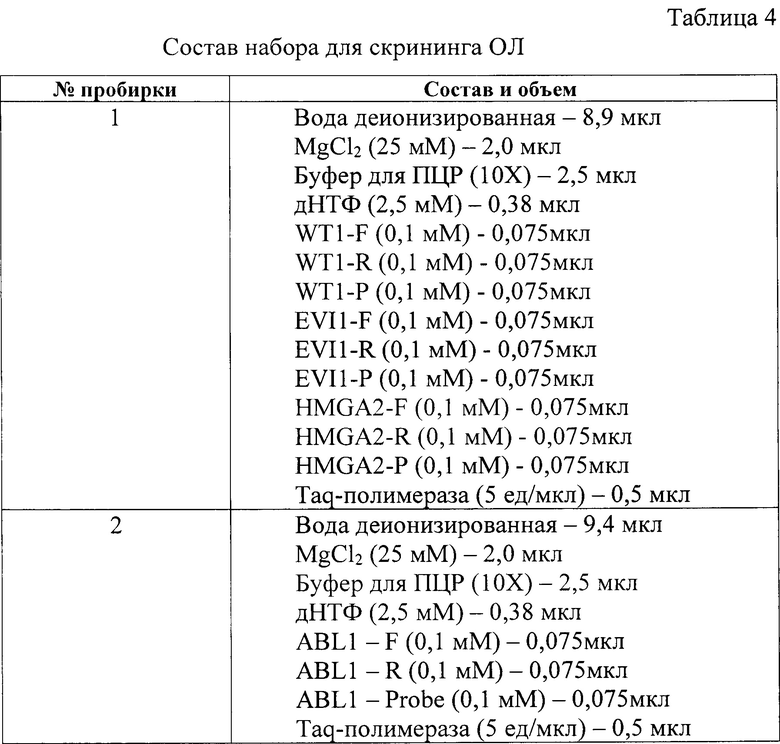
На этапе скрининга полученную кДНК в объеме 10 мкл добавляют к каждой из 2 пробирок, содержащих оригинальные смеси праймеров, зондов и прочих реактивов в соответствии с таблицей 4.
В качестве положительного контрольного образца используют смесь плазмидных ДНК, включающую последовательности генов WT1, HMGA2, EVI1, ABL1. В качестве отрицательного контроля используется буферная смесь.
Температурно-временной режим проведения реакции для амплификатора «CFX96» («Bio-Rad», США) следующий: предварительная активация при 95°С - 5 минут и последующие циклы, включающие денатурацию при 95°С - 15 секунд, отжиг и элонгацию при 60°С - 60 секунд, цикл повторяют 50 раз.
Полученные данные - кривые накопления флуоресцентного сигнала анализируют с помощью стандартного программного обеспечения используемых приборов для проведения ПЦР в режиме реального времени. Устанавливают пороговый уровень флуоресценции, выше которого сигнал считается положительным (если он не устанавливается или не рассчитывается прибором автоматически). Номер цикла, в котором график интенсивности флуоресценции для данной пробы пересек пороговый уровень и стал положительным, называют пороговым циклом Ct. В случае, если в пробирке №1 наблюдается флуоресцентный сигнал, следует выполнить расчеты количества копий онкогенных мРНК в соответствии с формулами 1-3:
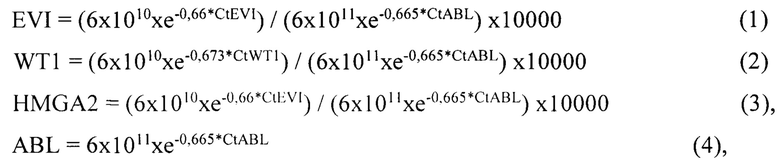
где е=2,71828.
В результате получают расчетное количество копий мРНК искомых генов на 10000 копий мРНК гена ABL. По формуле (4) необходимо рассчитать количество копий гена ABL, оно должно быть не менее 10000 в реакционной пробирке, иначе реакцию необходимо переставить, начиная со стадии выделения РНК.
Высокая вероятность (более 95%, р<0,05) первичного ОЛ, независимо от количества бластных клеток в венозной крови, определяется в случаях:
- экспрессия мРНК гена WT1 более чем 0,0001 копий на 10000 копий мРНК гена ABL;
- или уровень экспрессии мРНК гена HMGA2 определяется ниже, чем 0,27 копий или выше, чем 2,13 копий на 10000 копий мРНК гена ABL;
- или экспрессия мРНК гена EVI1 определяется ниже, чем 0,16 копий или выше, чем 1,35 копий. 1. если в пробе крови определяется экспрессия мРНК WT1 (предел чувствительности 0,0001 копий).
Высокие значения уровня экспрессии мРНК генов WT1, HMGA2, EVI1 свидетельствуют о более вероятном негативном прогнозе течения заболевания.
3. Проведение ОТ-ПЦР в реальном времени для уточнения молекулярно-генетического варианта заболевания
При получении результата тестирования на этапе скрининга, свидетельствующем о наличии высокого риска ОЛ, проводят уточнение варианта ОЛ с помощью набора для выявления химерных транскриптов (таблица 5). При выполнении данного теста допускается возможность использования пробы кДНК, полученной ранее для тестирования в скрининговом наборе.
В качестве положительного контрольного образца используют смесь плазмидных ДНК, включающую последовательности генов PML-RARa, MLL-AF10, MLL-AF4, MLL-AF6, AML-ETO, TEL-AML, CBFB-MYH11, Е2А-РВХ1, BCR-ABL, MLL-AF9, MLL-ELL, MLL-ENL, SIL-TAL, PICALM-MLLT10, ABL1.
В качестве отрицательного контроля используется буферная смесь.
Условия проведения ПЦР для всех смесей: предварительная денатурация 95°С - 5 минут; 50 циклов реакции в режиме 95°С - 15 секунд, 60°С - 40 секунд (детекция флуоресценции).
По окончании реакции анализируют графики уровня флуоресцентного сигнала в пробах. Устанавливают пороговый уровень флуоресценции, выше которого сигнал считают положительным (если он не рассчитывается прибором автоматически). Номер цикла, в котором график интенсивности флуоресценции для данной пробы пересек пороговый уровень и стал положительным, называют пороговым циклом Ct. По формуле (4) необходимо рассчитать количество копий гена ABL, оно должно быть не менее 10000 в реакционной пробирке, иначе реакцию необходимо переставить, начиная со стадии выделения РНК.
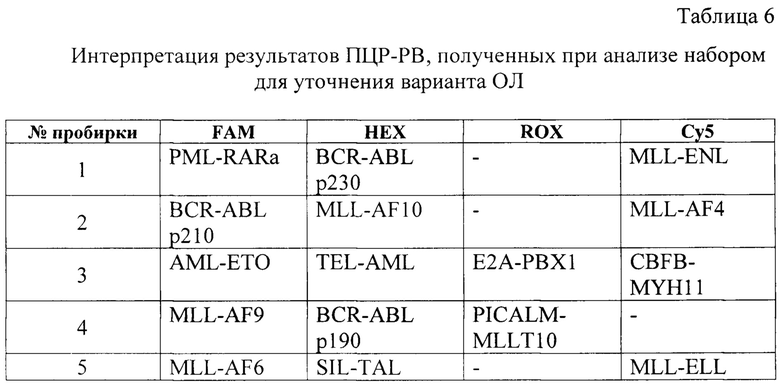
Если пороговый цикл Ct флюоресценции хотя бы в одной из реакционных смесей в пробирках №№1-5 менее 40, то образец считают положительным по одной из соответствующих транслокаций (таблица 6). Получение положительного результата присутствия в пробе хотя бы одного из химерных транскриптов, слитых в результате хромосомной транслокации определяет молекулярно-генетический вариант острого лейкоза,
Например, если проба имеет Ct менее 40 в смеси №3 по каналу детекции ROX, то образец пациента считают положительным по транслокации Е2А-РВХ1. Если значение Ct в пробе менее 40 в смеси №4 по каналу FAM, то в образец пациента считают положительным по транслокации MLL-AF9 и так далее.
4. Проведение ОТ-ПЦР в реальном времени для определения количественного уровня лейкозо-специфических РНК-маркеров
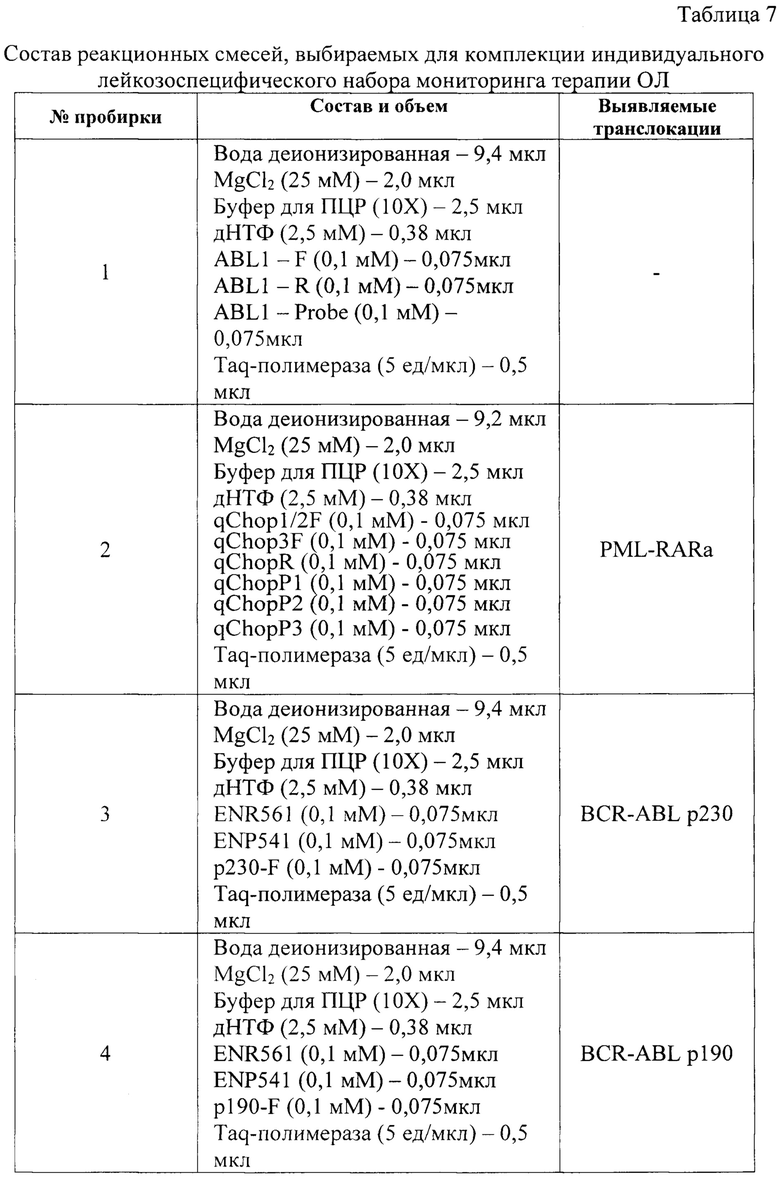
На следующем этапе осуществляют количественный анализ обнаруженных в пробе конкретного пациента двух РНК: максимально экспрессированной мРНК одного из генов WT1, HMGA2 или EVI1 и выявленного химерного транскрипта. Для этого формируют лейкозо-специфический набор для выполнения количественного анализа, включающего постановку ПЦР с использованием соответствующих реакционных смесей из представленных в таблице 7. Так, для количественного определения химерного транскрипта выбирают пробирки из №2-9, для количественного определения мРНК генов эмбриональной активности выбирают пробирки из №10-12 и пробирку №1 для определения уровня мРНК гена сравнения - «гена домашнего хозяйства» ABL1. После проведения теста выполняют построение трех калибровочных графиков с использованием соответствующих выбранным РНК стандартов, полученных путем трансформации бактериального клона E.coli, с известным количеством молекул (таблица 8) для эмбрионального онкогена, химерного транскрипта и ABL1. При этом пробы и стандарты анализируют в 2-х повторах. По калибровочному графику, зная пороговый цикл в пробе пациента, определяют количество копий химерного транскрипта и/или мРНК онкогена, которое присутствует в пробе пациента и будет использовано в дальнейшем как исходное значение для молекулярного контроля развития заболевания и эффективности терапии. В качестве отрицательного контроля используется буферная смесь.
Таким образом, сформированный индивидуальный лейкозо-специфический набор для одновременного количественного измерения уровня экспрессии мРНК, выявленной в скрининговом тесте, и обнаруженного химерного транскрипта в уточняющем тесте исследуемой пробы, в последующем будет использоваться для контроля течения заболевания и эффективности терапии.
Условия проведения ПЦР для всех смесей: предварительная денатурация 95°С - 5 минут; 50 циклов реакции в режиме 95°С - 15 секунд, 60°С - 40 секунд (детекция флуоресценции). Детекция флуоресценции осуществляется по каналу FAM для всех смесей.
Сущность группы изобретений пояснена примерами конкретной реализации, которые не ограничивают объем прав.
Пример 1. Использование набора для скрининга ОЛ в пробах венозной крови пациентов с подозрением на ОЛ
Пробы венозной крови пациентов с клиническими симптомами, позволяющими подозревать наличие ОЛ, и недостаточным для однозначной верификации диагноза уровнем бластных клеток (менее 20%) были исследованы на скрининговом наборе реактивов для определения экспрессии мРНК генов WT1, HGMA2 и EVIL Для этого с образцом тотальной РНК, выделенной из лейкоцитов крови, проводили реакцию обратной транскрипции с использованием набора реагентов Реверта-L (Amplisens, Россия). Полученную кДНК использовали для постановки ПЦР с использованием разработанного набора реагентов для скрининга ОЛ.
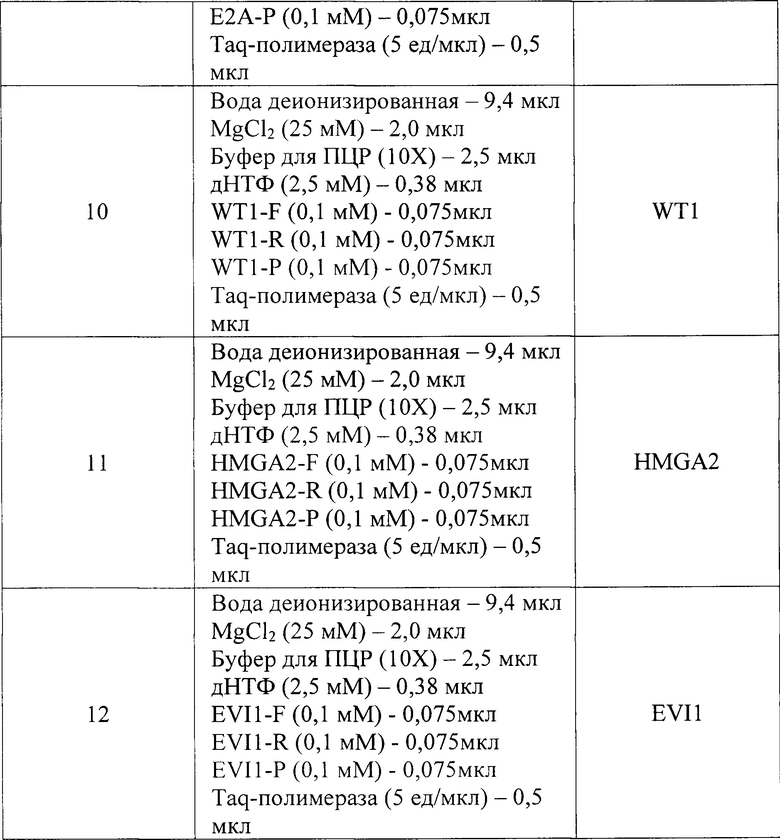
В таблице 9 представлены примеры результатов тестирования пациентов с низким уровнем бластных клеток в венозной крови, жирным шрифтом выделены значения экспрессии мРНК, свидетельствующие о высокой вероятности ОЛ. Проведенная в последующем уточняющая диагностика и результаты морфологического анализа костного мозга подтвердили диагноз ОЛ (ОМЛ - острый миелобластный лейкоз, ОЛЛ - острый лимфобластный лейкоз, ОПЛ - острый промиелоцитарный лейкоз).
Таким образом, использование набора для скрининга проб крови пациентов с подозрением на ОЛ позволяет получить дополнительные свидетельства в пользу данного диагноза в течение не более 3 часов после выполнения общего анализа крови при первичном обследовании пациента.
Пример 2. Использование наборов для уточнения молекулярно-генетического варианта заболевания и количественного мониторинга лейкозо-специфических маркеров
Пациентка Г., 23 года, с подозрением на ОЛ. В результате предварительно выполненного анализа крови с помощью набора для скрининга ОЛ обнаружили экспрессию мРНК гена WT1 (2,98 копий), что позволяло сделать вывод о высокой вероятности лейкоза. Затем выполнили исследование полученного на скрининговом этапе диагностики образца кДНК набором для уточнения варианта ОЛ. В результате выявили транслокацию PML-RARa. Далее был сформирован индивидуальных лейкозо-специфический набор, включающий смеси №1, №2, №10 из таблицы 7 и с оставшейся после выполнения предыдущих тестов пробе кДНК провели количественный анализ, полученные значения (PML-RARa 102,2 копии и WT1 3 копии на 10000 копий ABL1) послужили исходными значениями для дальнейшего их контроля в динамике терапии пациента.
Время выполнения всех трех последовательных тестов, включая выделение РНК, проведение обратной транскрипции и последовательных амплификаций в скрининговом, уточняющем тесте и количественном формате мультиплексной ОТ-ПЦР, не превысило 8 часов, исследования были выполнены в течение одного рабочего дня.
Возможность использования сформированного лейкозоспецифического набора для данной пациентки продемонстрирована на Фиг. 2, где представлены результаты молекулярного мониторинга в течение первых 9 месяцев после начала терапии.
Достигнута клиническая ремиссия, полный гематологический и молекулярный ответ по химерному транскрипту PML-RARa. Снизился и стабилизировался уровень экспрессии мРНК гена WT1.
Таким образом, проведенные авторами исследования позволили разработать способ молекулярно-генетической диагностики острых лейкозов включающий все этапы лабораторной диагностики: скрининг проб венозной крови, уточнение молекулярно-генетического варианта лейкоза и формирование лейкозоспецифического набора для последующего мониторинга эффективности терапии заболевания путем последовательного использованием оригинальных комбинаций специфических олигонуклнотидных праймеров и зондов объединенных в наборы для выявления экспрессии мРНК трех эмбриональных генов и отдельных химерных транскриптов 13 хромосомных транслокаций.




Настоящее изобретение относится к области биотехнологии и может быть использовано в медицине. Изобретение раскрывает новый способ диагностики острых лейкозов, основанный на выявлении у пациента мРНК генов WT1, HMGA2 и EVI1 при скрининговом тестировании и выявления РНК транскриптов слитых при хромосомных транслокациях генов PICALM-MLLT10, TEL-AML, PML-RARα, AML-ETO, MLL-AF4, MLL-AF6, MLL-AF9, MLL-AF10, MLL-ENL, CBFB-MYH11, BCR-ABL (р190, р210, р230) с использованием мультиплексной реакции ОТ-ПЦР в реальном времени для уточняющего теста. Предложенный способ требует минимальных затрат труда, времени, материалов и реагентов. Изобретение может быть применимо в онкогематологии: позволяет в течение одного рабочего дня с высокой точностью выявить у пациента молекулярно-генетический вариант лейкоза и сформировать тест индивидуального мониторинга заболевания. 4 н. и 1 з.п. ф-лы, 2 пр., 9 табл., 2 ил.
1. Способ молекулярно-генетической диагностики острых лейкозов (ОЛ), основанный на использовании полимеразной цепной реакции в реальном времени с обратной транскрипцией, заключающийся в последовательном исследовании ряда молекул РНК, экспрессия которых характерна для эмбриональных клеток, а также ряда молекул РНК химерных генов, образованных при хромосомных транслокациях, с последующим выбором из них молекул РНК наиболее специфичных для лейкоза конкретного пациента с целью молекулярного мониторинга эффективности терапии, отличающийся тем, что
для анализа используют однократно взятую пробу венозной крови, из которой проводят выделение РНК с реакцией обратной транскрипции, и
в полученном образце нуклеиновых кислот последовательно:
- проводят одновременное тестирование методом мультиплексного анализа экспрессии мРНК генов WT1, EVI1 и HMGA2, экспрессия которых характерна для эмбриональных клеток, на основании их соотношения делают заключение о степени риска ОЛ;
- затем, в случае высокого риска ОЛ, в том же образце нуклеиновых кислот методом мультиплексного анализа выполняют тестирование экспрессии ряда РНК химерных генов, проводят определение РНК транскриптов, слитых при хромосомных транслокациях генов PICALM-MLLT10, PML-RARa, MLL-AF4, MLL-AF6, MLL-AF9, MLL-AF10, MLL-ENL, MLL-ELL, CBFB-MYH11, AML1-ETO, TEL-AML, Е2А-РВХ1, BCR-ABL1(p190, р210, р230), SIL-TAL, при этом, выявление в пробе хотя бы одного из указанных химерных транскриптов определяет молекулярно-генетический вариант ОЛ;
- в заключении в том же образце нуклеиновых кислот методом количественного анализа проводят измерение уровня выбранных молекул РНК, наиболее специфичных для лейкоза у конкретного пациента, полученные количественные значения содержания лейкозоспецифических молекул РНК в пробе крови конкретного пациента используют для сравнения в качестве их исходного уровня.
2. Способ по п. 1, отличающийся тем, что при выполнении тестирования в качестве положительного контроля используют стандартные растворы нуклеиновых кислот, предварительно полученных путем трансформации бактериального клона E.coli, с известным количеством молекул, имеющих нуклеотидные последовательности, идентичные выбранным РНК генов, экспрессия которых характерна для эмбриональных клеток и РНК химерных генов, при этом, для количественного определения уровня молекул РНК-маркеров используют средние значения результатов анализа образцов и стандартов в двух повторах, по последовательно разведенным стандартам выполняют построение калибровочных графиков и по калибровочному графику, зная пороговый цикл в образце пробы крови пациента, определяют количество копий искомых молекул РНК.
3. Набор для выполнения мультиплексной полимеразной цепной реакции в реальном времени с обратной транскрипцией для определения уровня экспрессии отдельных РНК, экспрессия которых характерна для эмбриональных клеток, и предназначенный для использования в способе молекулярно-генетической диагностики ОЛ по п. 1, содержащий буфер, полимеразу, специфичные олигонуклеотидные праймеры и флуоресцентно-меченые ДНК-зонды, имеющие нуклеотидные последовательности SEQ ID NO: 1-SEQ ID NO: 12, объединенные в 2 смеси следующего состава:
пробирка № 1: вода деионизированная - 8,9 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, WT1-F 0,1 мМ - 0,075 мкл, WT1-R 0,1 мМ - 0,075 мкл, WT1-P 0,1 мМ - 0,075 мкл, EVI1-F 0,1 мМ -0,075 мкл, EVI1-R 0,1 мМ - 0,075 мкл, EVI1-P 0,1 мМ - 0,075 мкл, HMGA2-F 0,1 мМ - 0,075 мкл, HMGA2-R 0,1 мМ - 0,075 мкл, HMGA2-P 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл;
пробирка № 2: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, ABL1 - F 0,1 мМ - 0,075 мкл, ABL1 - R 0,1 мМ - 0,075 мкл, ABL1 - Probe 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл;
и в качестве положительного контрольного образца содержащий смесь плазмидных ДНК, включающую последовательности генов WT1, HMGA2, EVI1, ABL1.
4. Набор для выполнения мультиплексной полимеразной цепной реакции в реальном времени с обратной транскрипцией для уточнения молекулярно-генетического варианта ОЛ путем определения РНК химерных генов слитых при хромосомных транслокациях, предназначенный для использования в способе молекулярно-генетической диагностики ОЛ по п 1, после тестирования пробы крови набором по п. 3, содержащий буфер, полимеразу, специфичные олигонуклеотидные праймеры и флуоресцентно-меченые ДНК-зонды, имеющие нуклеотидные последовательности SEQ ID NO: 10-SEQ ID NO: 71, объединенные в 6 смесей следующего состава:
пробирка № 1: вода деионизированная - 8,5 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, qChopl/2F 0,1 мМ -0,075 мкл, qChop3F 0,1 мМ - 0,075 мкл, qChopR 0,1 мМ - 0,075 мкл, qChopP1 0,1 мМ - 0,075 мкл, qChopP2 0,1 мМ - 0,075 мкл, qChopP3 0,1 мМ - 0,075 мкл, ENR561 0,1 мМ - 0,075 мкл, ENP541 0,1 мМ - 0,075 мкл, p230-F 0,1 мМ -0,075 мкл, ENL-R1 0,1 мМ - 0,075 мкл, ENL-R2 0,1 мМ - 0,075 мкл, MLL-F1 0,1 мМ - 0,075 мкл, MLL-F2 0,1 мМ - 0,075 мкл, MLL-P1 0,1 мМ - 0,075 мкл, MLL-Р2 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 2: вода деионизированная - 8,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, ENR561 0,1 мМ - 0,075 мкл, ENP541 0,1 мМ - 0,075 мкл, ENF501C 0,1 мМ - 0,075 мкл, ENF501T 0,1 мМ - 0,075 мкл, AF10-R4 0,1 мМ - 0,075 мкл, AF10-R5 0,1 мМ - 0,075 мкл, AF10-R6 0,1 мМ - 0,075 мкл, AF10-P1 0,1 мМ - 0,075 мкл, AF10-P2 0,1 мМ -0,075 мкл, AF10-P3 0,1 мМ - 0,075 мкл, MLL-F3 0,1 мМ - 0,075 мкл, MLL-F4 0,1 мМ - 0,075 мкл, AF4-R1 0,1 мМ - 0,075 мкл, AF4-R2 0,1 мМ - 0,075 мкл, MLL-F1 0,1 мМ - 0,075 мкл, MLL-F2 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
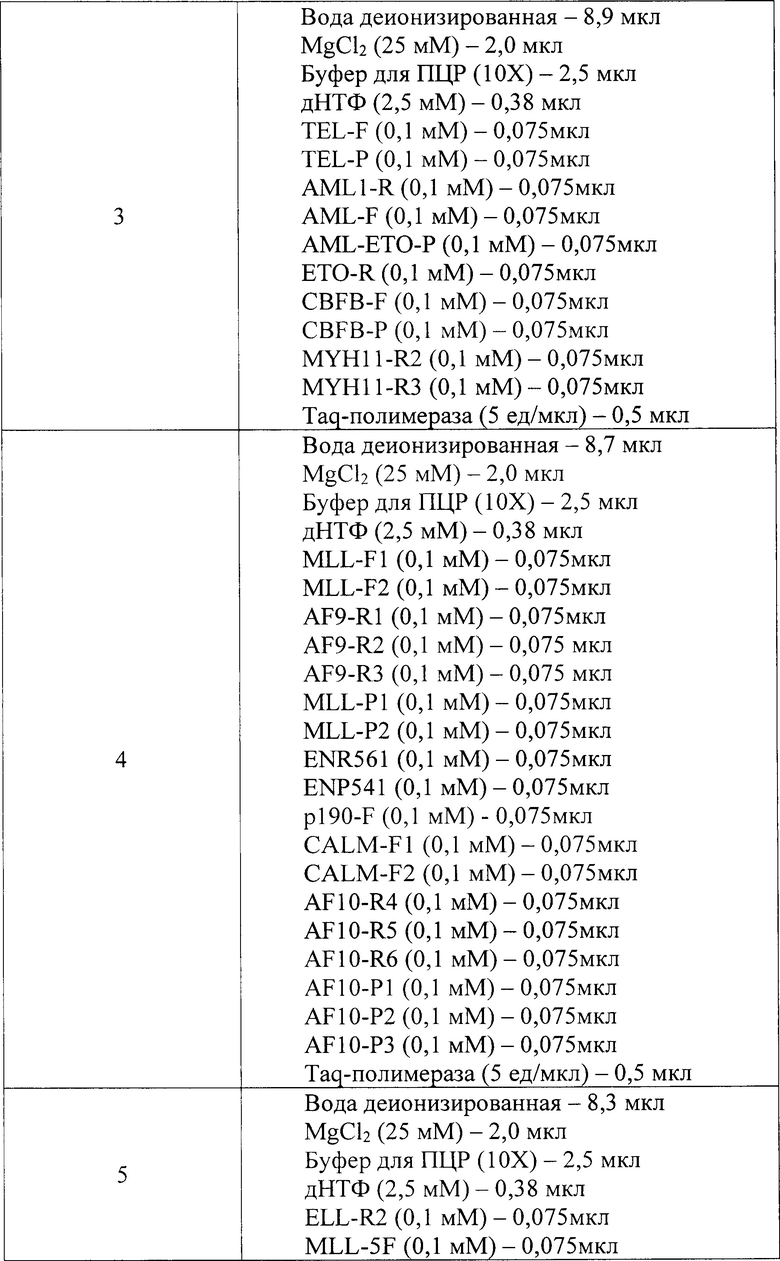
пробирка № 3: вода деионизированная - 8,9 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, TEL-F 0,1 мМ -0,075 мкл, TEL-P 0,1 мМ - 0,075 мкл, AML1-R 0,1 мМ - 0,075 мкл, AML-F 0,1 мМ - 0,075 мкл, AML-ETO-P 0,1 мМ - 0,075 мкл, ETO-R 0,1 мМ - 0,075 мкл, CBFB-F 0,1 мМ - 0,075 мкл, CBFB-P 0,1 мМ - 0,075 мкл, MYH11-R2 0,1 мМ -0,075 мкл, MYH11-R3 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 4: вода деионизированная - 8,7 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х-2,5 мкл, дНТФ2,5 мМ-0,38 мкл, MLL-F1 0,1 мМ-0,075 мкл, MLL-F2 0,1 мМ - 0,075 мкл, AF9-R 0,1 мМ - 0,075 мкл, AF9-R1 0,1 мМ -0,075 мкл, AF9-R2 0,1 мМ - 0,075 мкл, MLL-P1 0,1 мМ - 0,075 мкл, MLL-P2 0,1 мМ - 0,075 мкл, ENR561 0,1 мМ - 0,075 мкл, ENP541 0,1 мМ - 0,075 мкл, p190-F 0,1 мМ - 0,075 мкл, CALM-F1 0,1 мМ - 0,075 мкл, CALM-F2 0,1 мМ -0,075 мкл, AF10-R4 0,1 мМ - 0,075 мкл, AF10-R5 0,1 мМ - 0,075 мкл, AF10-R6 0,1 мМ - 0,075 мкл, AF10-P1 0,1 мМ - 0,075 мкл, AF10-P2 0,1 мМ - 0,075 мкл, AF10-P3 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
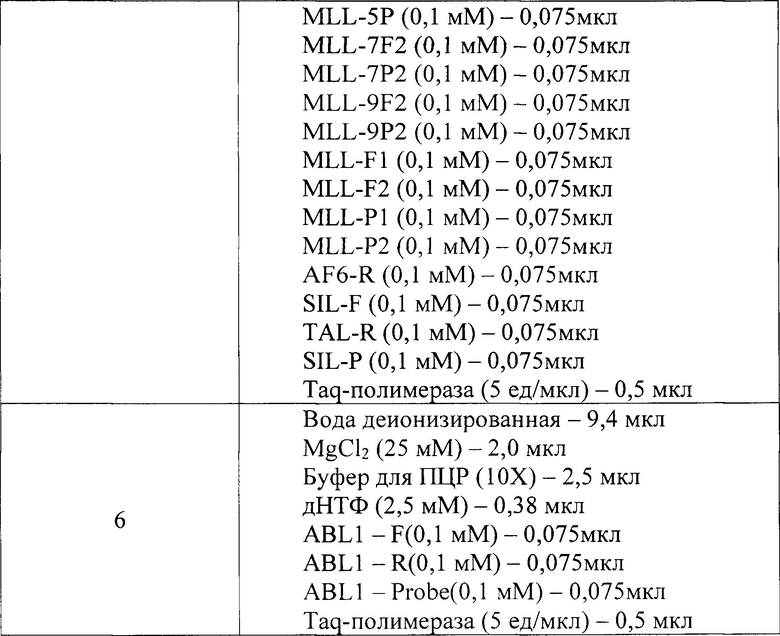
пробирка № 5: вода деионизированная - 8,3 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, ELL-R2 0,1 мМ - 0,075 мкл, MLL-5F 0,1 мМ - 0,075 мкл, MLL-5P 0,1 мМ - 0,075 мкл, MLL-7F2 0,1 мМ - 0,075 мкл, MLL-7P2 0,1 мМ - 0,075 мкл, MLL-9F2 0,1 мМ - 0,075 мкл, MLL-9P2 0,1 мМ - 0,075 мкл, MLL-F1 0,1 мМ - 0,075 мкл, MLL-F2 0,1 мМ -0,075 мкл, MLL-P1 0,1 мМ - 0,075 мкл, MLL-P2 0,1 мМ - 0,075 мкл, AF6-R 0,1 мМ - 0,075 мкл, SIL-F 0,1 мМ - 0,075 мкл, TAL-R 0,1 мМ - 0,075 мкл, SIL-P 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 6: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, ABL1 - F 0,1 мМ -0,075 мкл, ABL1 - R 0,1 мМ - 0,075 мкл, ABL1 - Probe 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл;
и в качестве контрольного образца содержащий смесь плазмидных ДНК, включающую последовательности генов PML-RARa, MLL-AF10, MLL-AF4, MLL-AF6, AML-ETO, TEL-AML, CBFB-MYH11, Е2А-РВХ1, BCR-ABL, MLL-AF9, MLL-ELL, MLL-ENL, SIL-TAL, PICALM-MLLT10, ABL1.
5. Набор для выполнения полимеразной цепной реакции в реальном времени с обратной транскрипцией для количественного определения лейкозо-специфических маркеров, предназначенный для использования в способе молекулярно-генетической диагностики ОЛ по п. 1 после тестирования пробы крови пациента наборами по п. 3 и п. 4, содержащий буфер, полимеразу, специфичные олигонуклеотидные праймеры и флуоресцентно-меченые ДНК-зонды, включающий 12 олигонуклеотидных смесей, следующего состава:
пробирка № 1: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, ABL1 - F 0,1 мМ -0,075 мкл, ABL1 - R 0,1 мМ - 0,075 мкл, ABL1 - Probe 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 2: 9,2 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х -2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, qChopl/2F 0,1 мМ - 0,075 мкл, qChop3F 0,1 мМ - 0,075 мкл, qChopR 0,1 мМ - 0,075 мкл, qChopPl 0,1 мМ - 0,075 мкл, qChopP2 0,1 мМ - 0,075 мкл, qChopP3 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 3: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПНР 10Х-2,5 мкл, дНТФ 2,5 мМ-0,38 мкл, ENR561 0,1 мМ-0,075 мкл, ENP541 0,1 мМ - 0,075 мкл, p230-F 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 4: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х-2,5 мкл, дНТФ 2,5 мМ-0,38 мкл, ENR561 0,1 мМ-0,075 мкл, ENP541 0,1 мМ - 0,075 мкл, p190-F 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 5: вода деионизированная - 9,3 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х-2,5 мкл,дНТФ2,5 мМ-0,38 мкл, ENR561 0,1 мМ-0,075 мкл, ENP541 0,1 мМ - 0,075 мкл, ENF501C 0,1 мМ - 0,075 мкл, ENF501T 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 6: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, TEL-F 0,1 мМ - 0,075 мкл, TEL-P 0,1 мМ - 0,075 мкл, AML1-R 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 7: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, AML1-R 0,1 мМ-0,075 мкл, AML-F 0,1 мМ - 0,075 мкл, AML-ETO-P 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 8: вода деионизированная - 9,3 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, CBFB-F 0,1 мМ - 0,075 мкл, CBFB-P 0,1 мМ - 0,075 мкл, MYH11-R2 0,1 мМ - 0,075 мкл, MYH11-R3 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 9: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, E2A-F 0,1 мМ - 0,075 мкл, PBX1-R 0,1 мМ - 0,075 мкл, Е2А-Р 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 10: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, WT1-F 0,1 мМ -0,075 мкл, WT1-R 0,1 мМ - 0,075 мкл, WT1-P 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 11: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, HMGA2-F 0,1 мМ - 0,075 мкл, HMGA2-R 0,1 мМ - 0,075 мкл, HMGA2-P 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл,
пробирка № 12: вода деионизированная - 9,4 мкл, MgCl2 25 мМ - 2,0 мкл, буфер для ПЦР 10Х - 2,5 мкл, дНТФ 2,5 мМ - 0,38 мкл, EVI1-F 0,1 мМ -0,075 мкл, EVI1-R 0,1 мМ - 0,075 мкл, EVI1-P 0,1 мМ - 0,075 мкл, Taq-полимераза 5 ед/мкл - 0,5 мкл;
а также калибраторы стандартных растворов нуклеиновых кислот с известным количественным уровнем копий искомых РНК: 1-10000 копий/мкл, 2-1000 копий/мкл, 3-100 копий/мкл, 4-10 копий/мкл.
| LYU X | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| CN 107385031 A, 24.11.2017 | |||
| WO 2019215394 A1, 14.11.2019 | |||
| US 20200354434 A1, 12.11.2020 | |||
| СПОСОБ ДИАГНОСТИКИ ОСТРОГО ЛЕЙКОЗА | 1991 |
|
RU2007720C1 |
Авторы
Даты
2023-11-01—Публикация
2021-12-30—Подача