Изобретение относится к области медицины и молекулярной биологии, а именно к молекулярно-генетической диагностике мутаций гена NPM1 высокочувствительным количественным методом на основе аллель-специфичной ПЦР в реальном времени. Аналитическая чувствительность данного метода составляет 10-4-10-5 и позволяет выявлять минимальную остаточную болезнь (МОБ) в биологическом материале (пунктате костного мозга и крови) пациентов с диагнозом острый миелоидный лейкоз.
Острый миелоидный лейкоз (ОМЛ) является довольно редким заболеванием и составляет всего 1.1% от всех случаев злокачественных новообразований [1], однако это наиболее распространенный острый лейкоз среди взрослого населения. Заболеваемость в России составляет 1,3 случая на 100 тыс. человек [2]. Несмотря на все последние достижения в терапии, новые таргетные препараты, широкое применение аллогенной трансплантации стволовых клеток, ОМЛ остается прогностически крайне неблагоприятным заболеванием: пятилетняя выживаемость при ОМЛ не превышает 25-30% [1-2]. Острый миелоидный лейкоз развивается вследствие накопления хромосомных аберраций и генных мутаций. Мутации в гене нуклеофозмина 1 (NPM1) относятся к наиболее распространенным генетическим поломкам при ОМЛ у взрослых, на них приходится 25-30% всех случаев и 50-60% случаев ОМЛ с нормальным кариотипом [3-4]. Мутация гена NPM1 представляет собой 4-х нуклеотидную вставку в положении с.956-959. До 75-80% мутаций имеют вставку “типа А” - TCtG, и еще 10-14% приходится на вставку “типа D и В” - CCtG и CATG [4].
К основным методам диагностики мутаций NPM1 относится секвенирование, фрагментный анализ и аллель-специфичная ПЦР. Однако только последний метод способен обеспечить чувствительность определения, необходимую для мониторинга минимальной остаточной болезни. Современные молекулярные методы обнаружения минимальной остаточной болезни должны выявлять опухолевые клетки в количестве 10-4-10-5, т.е. одну опухолевую клетку на 10000-100000 нормальных клеток. Касательно методов определения МОБ необходимо отметить следующее. Методы определения МОБ представляют значимый интерес для клиницистов, так как позволяют оценить “излеченность” пациента, глубину полученной ремиссии, принять более взвешенное терапевтическое решение и вовремя перейти к терапии другой линии или провести аллогенную трансплантацию стволовых клеток [5-8]. Многочисленными группами ученых показана клиническая значимость количественного мониторинга мутации NPM1 при ОМЛ [9-16]. Эти и другие исследования вошли в основу рекомендаций Европейской рабочей группы по МОБ мониторингу 2018 и 2021 года, согласно которым МОБ-мониторинг NPM1 мутации при ОМЛ необходимо осуществлять с помощью количественной ПЦР, аналитическая чувствительность которой должна составлять 10-4-10-5 [17-18]. Для определения пациентов с высоким риском развития рецидива оценку МОБ следует проводить в костном мозге после 2 курсов полихимиотерапии [18]. По окончании терапии выявление NPM1-мутации в костном мозге неизбежно сопровождается рецидивом в среднем в течение нескольких месяцев [16-18].
В настоящее время, существует несколько описанных в научных статьях способов определения мутаций NPM1, а также коммерческие наборы, самым известным из которых является набор реагентов для определения мутации в гене NPM1 A «ipsogen NPM1 mut A MutaQuant» и набор реагентов для определения мутации в гене NPM1 «ipsogen NPM1 mut B&D MutaQuant» компании QIAGEN Group, США. Большинство исследований, посвященных определению МОБ по мутации гена NPM1 методом ПЦР в реальном времени [13-17] используют методику Gorello Р. c соавт, 2005 и Chou WC c соавт., 2007 [20-21]. Данные методики основаны на аллель-специфичной ПЦР со специфичными праймерами к области мутации, а их высокая аналитическая чувствительность достигается за счет использования TaqMan MGB-зонда. Данный вид зондов обеспечивает более прочное связывание с мишенью за счет фрагмента на 3’ конце зонда (пробы), который связывается с малой бороздкой ДНК (MGB - minor groove binder), что повышает Tm (температуру плавления) и стабильность зонда. Такие зонды обеспечивают лучшую дискриминацию мишеней. Они обладают интегрированным гасителем NFQ, который позволяет им лучше абсорбировать (гасить) сигнал от флуоресцирующих красителей на другом конце пробы. Все эти свойства по сравнению с другими пробами приводят к повышению чувствительности методики и точности полученных результатов. При этом в методике Gorello P. С соавт., 2005, прямой общий праймер располагается в 11 экзоне, а обратные праймеры, специфичные к области мутаций, и праймер дикого типа располагаются в 12 экзоне, что предполагает возможным анализ только на материале РНК (кДНК), так как 11-12 интрон гена NPM1 содержит более 1000 нуклеотидов. С другой стороны, Chou WC c соавт., 2007, расположили прямой общий праймер в 11-12 интроне, что делает возможным анализ только с использованием геномной ДНК, но не РНК (кДНК). В наборах реагентов для определения мутации в гене NPM1 “ipsogen NPM1 mut A, B&D MutaQuant Kits” компании QIAGEN Group, США технический подход не разглашается, но расположение праймеров аналогично Gorello P. С соавт., 2005, таким образом, в данном наборе реагентов в качестве материала для анализа используется РНК (кДНК). Указанные способы определения МОБ по мутации гена NPM1 методом ПЦР являются ближайшими аналогами предлагаемого изобретения. Данные аналоги не позволяют использовать для выявления мутации сразу два биологических материала: РНК и ДНК. При этом очевидно, что ДНК является более устойчивой молекулой, чем РНК, и ее использование в качестве материала дает неоспоримые преимущества, например, возможность исследования архивного материала из замороженных клеток. С другой стороны, некоторые лаборатории также применяют РНК (кДНК) для первичного исследования при ОМЛ, в частности для обнаружения химерных транскриптов.
Основной задачей, на решение которой направлено настоящее изобретение является разработка специфических синтетических олигонуклеотидов (специфичных наборов праймеров) и флуоресцентных зондов (проб), амплифицирующих в реакции ПЦР-РВ определенный участок гена NPM1 и мутаций гена NPM1 A, B, D типа, и разработка способа для количественного определения относительной доли клеток с мутацией как в ДНК, так и РНК, способа аллель-специфичной полимеразной цепной реакции в режиме реального времени для выявления мутаций гена NPM1 A, B, D типа, определения МОБ, обладающего аналитической чувствительностью 10-4-10-5. В рамках поставленной задачи были сконструированы специфичные праймеры и пробы, которые расположили внутри 12 экзона, что сделало возможным использование в качестве материала ДНК и РНК (кДНК). Кроме того, интегрировали LNA (locked nucleotide acid) модифицированные нуклеотиды в последовательность аллель-специфичных праймеров, что привело к увеличению их специфичности и увеличению чувствительности определения мутантного аллеля. LNA-модифицированный нуклеотид обладает большей связывающей способностью при комплементарном взаимодействии нуклеотидов по сравнению с обычным нуклеотидом. Это при определенных условиях приводит к более прочному связыванию праймера с мишенью, что в свою очередь увеличивает специфичность и чувствительность определения [22-26].
Поставленная задача решается представленной группой изобретений. В рамках представленного изобретения сконструированы специфичные наборы праймеров) и флуоресцентных зондов (проб), амплифицирующих в реакции ПЦР-РВ нуклеотидные последовательности гена NPM1 и мутаций гена NPM1 A, B, D типа и разработан надежный способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления мутаций гена NPM1 A, B, D типа, определения МОБ.
Данная группа изобретений является более дешевым альтернативным способом определения мутаций гена NPM1 A, B, D типа и определения МОБ которая гарантирует надежный результат анализа с чувствительностью 10-4-10-5 и возможность использовать в качестве материала как ДНК, так и РНК, выделенные из клеток костного мозга или крови пациента, в том числе возможность исследования архивного материала из замороженных клеток костного мозга или крови пациентов.
При описании реализации заявленного изобретения используются следующие сокращения и определения, которые имеют указанные значения в данном описании, если не оговорено другое значение:
NPM1 - ген нуклеофозмина;
ОМЛ - острый миелоидный лейкоз;
ПЦР-РВ - полимеразная цепная реакция в реальном времени;
МОБ - это устоявшийся термин в гематологии и онкологии, означающий минимальные количества опухолевых клеток после терапии, которые определяются в количестве 10-4-10-5
КМ - костный мозг;
ДНК - дезоксирибонуклеиновая кислота;
кДНК - комплементарная ДНК;
РНК - рибонуклеиновая кислота;
АС - аллель специфичный;
МОБ-ИФ - определение МОБ методом проточной цитофлуориметрии;
ПХТ - полихимиотерапия;
Специфичные (амплификационные) праймеры - это нуклеиновые кислоты, которые связываются с одной или более целевой последовательностью, позволяя протекание ее амплификации.
Пробирка - это индивидуальный сосуд, который имеет форму и размер типичной лабораторной пробирки (например, вакуумные пластиковые пробирки типа Vacuette объёмом 4,0 мл для взятия крови, костного мозга или пробирки типа Eppendorf объемом 2, 1,5, 0,5 мл для работы с ДНК/РНК, подготовки ПЦР-смесей, или пробирки 0,2, 0,1 мл для проведения ПЦР).
Олигонуклеотид - короткий фрагмент ДНК, получаемый путём химического синтеза, используемый в качестве праймера в рамках настоящего изобретения.
Праймер - олигонуклеотид, комплементарный ДНК-мишени служит затравкой для синтеза комплементарной цепи с помощью ДНК-полимеразы.
Отрицательный контрольный образец - образец ДНК здорового донора который используется в качестве отрицательного контроля.
Положительный контрольный образец - образец ДНК с мутацией NPM1 типа А который используется в качестве положительного контроля для мутаций A, B и D.
Диагностическая специфичность - процент корректных отрицательных результатов обследования к общему числу контрольной группы.
Экзон - это участок ДНК, который кодирует белки.
Проба - это флуоресцентный зонд, используемый в последовательности нуклеотидов.
Флуоресцентный зонд - представляет собой олинуклеотид с флуоресцентной меткой и гасителем, который может связываться с цепью ДНК в процессе амплификации и обеспечивает флуоресценцию в процессе амплификации.
Чувствительность обнаружения - это минимальное количество копий, которое удается обнаружить. «Более высокая или улучшенная чувствительность» в данном контексте означает, что минимальное детектируемое количество копий мутантного аллеля уменьшено.
LNA (locked nucleotide acid) - модифицированный нуклеотид РНК, в котором фрагмент рибозы модифицирован дополнительным мостиком, соединяющим 2'-кислородную группу и 4' углерод, что обеспечивает оптимальное расположение гетероциклических оснований в дуплексе и приводит к более эффективному (сильному) Уотсон-Криковскому взаимодействию между комлементарными основаниями. При соблюдении условий, описанных при реализации способа, как одного из аспектов настоящего изобретения приводит к более прочному связыванию праймера с мишенью, что в свою очередь увеличивает специфичность и чувствительность определения.
FAM (карбоксифлуоресцеин) - это флуоресцентный краситель, который добавляют к 5'-концу олигонуклеотида для синтеза меченых зондов для ПЦР в реальном времени.
BHQ1 - это гаситель, который добавляют к 3'-концу олигонуклеотида для синтеза меченых зондов для ПЦР в реальном времени.
Целевые последовательности (мишени) - это последовательности, которые требуется обнаружить.
Биологический материал - это ДНК и РНК, выделенные из клеток костного мозга, крови пациента включая архивный материал из замороженных клеток.
Аллельная нагрузка - это % соотношение мутантного аллеля к общему количеству аллелей (мутантные плюс дикие).
Раскрытие изобретения
Решение проблемы, соответствующее первому аспекту настоящего изобретения, основано на перечне последовательностей нуклеотидов SEQ ID №1-6, образующие из них группы последовательностей комплементарные NPM1 и мутациям NPM1 A, B, D типа и их применение в качестве праймеров для амплификации NPM1 и мутаций NPM1 A, B, D типа, а именно:
SEQ ID NO: 1 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер дикого типа, состоящая из 22 нуклеотидов, содержащая в 19 и 21 положении LNA-модифицированный нуклеотид;
SEQ ID NO: 2 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер мутантного типа A, состоящая из 23 нуклеотидов, содержащая в 16 и 20 положении LNA-модифицированный нуклеотид;
SEQ ID NO: 3 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер мутантного типа B, состоящая из 23 нуклеотидов, содержащая в 17 и 20 положении LNA-модифицированный нуклеотид;
SEQ ID NO: 4 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер мутантного типа D, состоящая из 23 нуклеотидов, содержащая в 20 положении LNA-модифицированный нуклеотид;
SEQ ID NO: 5 последовательность нуклеотидов ДНК Homo sapiens, TaqMan зонд, состоящая из 28 нуклеотидов, содержащая на 3’ конце BHQ1, а на 5’ конце FAM;
SEQ ID NO: 6 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер, состоящая из 22 нуклеотидов.
Детальное описание последовательностей нуклеотидов, входящих в состав перечне последовательностей нуклеотидов SEQ ID №1-6 указан в таблице 1:
праймеров
(нуклеотидов)
Описание последовательностей нуклеотидов, флуоресцентных зондов представлены отдельно в XML формате, являющимся приложением к настоящему описанию.
Схематическое изображение расположения праймеров представлено на фигуре 3.
Предпочтительно в рамках реализации данного аспекта изобретения нуклеотидные последовательности образуют следующие группы:
- нуклеотидные последовательности, включающие последовательности SEQ ID № 1, 5 и 6, составляют группу последовательностей, предназначенных для определения клеток без мутаций;
- нуклеотидные последовательности, включающие последовательности SEQ ID № 2, 5 и 6, составляют группу последовательностей, предназначенные для определения клеток с мутацией А;
- нуклеотидные последовательности, включающие последовательности SEQ ID № 3, 5 и 6, составляют группу последовательностей, предназначенные для определения клеток с мутацией В;
- нуклеотидные последовательности, включающие последовательности SEQ ID № 4, 5 и 6, составляют группу последовательностей, предназначенные для определения клеток с мутацией D.
Применительно к данному аспекту изобретения, сконструированные специфичные наборы праймеров и проб расположили внутри 12 экзона гена NPM1, что сделало возможным использование в качестве материала ДНК и РНК (кДНК).
Данные заявителя о встречаемости вставок типа A, B, D и нестандартных вставок у российских пациентов с ОМЛ представлены на фигуре 2.
Схематическое изображение расположения внутри 12 экзона праймеров изображено на фигуре 3.
Решение проблемы, соответствующее второму аспекту настоящего изобретения основано на создании набора реакционных смесей, который включает 4 смеси олигонуклеотидов для амплификации, а именно:
1. NPM1 W, для определения клеток без мутации (прямой праймер SEQ ID NO: 1; обратный праймер SEQ ID NO: 6, TaqMan зонд, SEQ ID NO: 5, меченная FAM и BHQ1);
2. NPM1 A, для определения клеток c мутацией А (прямой праймер SEQ ID NO: 2; обратный праймер SEQ ID NO: 6, TaqMan зонд, SEQ ID NO: 5, меченная FAM и BHQ1);
3. NPM1 B, для определения клеток c мутацией B (прямой праймер SEQ ID NO: 3; обратный праймер SEQ ID NO: 6, TaqMan зонд, SEQ ID NO: 5, меченная FAM и BHQ1);
4. NPM1 D, для определения клеток c мутацией D (прямой праймер SEQ ID NO: 4; обратный праймер SEQ ID NO: 6, TaqMan зонд, SEQ ID NO: 5, меченная FAM и BHQ1);
Каждой смеси олигонуклеотидов соответствует одна пробирка, которая подготавливается путем разведения олигонуклеотидов в деионизированой воде до конечной концентрации 5 пкмоль/мкл праймера и 3,5 пкмоль/мкл пробы.
Каждая смесь олигонуклеотидов для амплификации предусматривает следующее:
Таблица №2. Состав смеси последовательностей нуклеотидов NPM1 W, для определения клеток без мутации. Конечный объем смеси 200 мкл (100 реакций).
(концентрация стокового раствора 100 пкмоль/мкл)
(концентрация стокового раствора 100 пкмоль/мкл)
Таблица №3. Состав смеси последовательностей нуклеотидов NPM1 А, для определения клеток с мутацией А. Конечный объем смеси 200 мкл (100 реакций).
(концентрация стокового раствора 100 пкмоль/мкл)
(концентрация стокового раствора 100 пкмоль/мкл)
Таблица №4. Состав смеси последовательностей нуклеотидов NPM1 В, для определения клеток с мутацией В. Конечный объем смеси 200 мкл (100 реакций).
(концентрация стокового раствора 100 пкмоль/мкл)
(концентрация стокового раствора 100 пкмоль/мкл)
Таблица №5. Состав смеси последовательностей нуклеотидов NPM1 D, для определения клеток с мутацией D. Конечный объем смеси 200 мкл (100 реакций).
(концентрация стокового раствора 100 пкмоль/мкл)
(концентрация стокового раствора 100 пкмоль/мкл)
Сведения об упаковке - пробирка с маркировкой. Пробирка с приготовленным составом может храниться при t-20°С в течении 30 дней.
Решение проблемы, соответствующее третьему аспекту настоящего изобретения основано на создании способа обнаружения мутаций гена NPM1 A, B, D типа в тестируемом образце и способа определения МОБ, включающий следующие этапы:
1. Подготовка материалов и компонентов.
2. Проведение ПЦР-РВ для первичного исследования (проводится при наличии мутации (вставки +4bp) гена NPM1, доказанной другими методами, например, методом фрагментного анализа).
3. Проведение ПЦР для тестирования МОБ.
1. Подготовка материалов и компонентов:
Для осуществления способа в рамках настоящего изобретения по меньшей мере осуществляется взятие пунктата костного мозга в вакуумные пластиковые пробирки с добавленной в качестве антикоагулянта солью этилендиаминтетраацетата (ЭДТА) в конечной концентрации 2,0 мг/мл. В качестве антикоагулянта допускается также использование цитрата натрия. Для перемешивания пунктата костного мозга с антикоагулянтом после взятия материала необходимо перевернуть пробирку 2-3 раза. Для выделения ДНК и РНК из лейкоцитов костного мозга или периферической крови используется любой способ, который обеспечивает достаточный по количеству и качеству выход ДНК или РНК. Предобработку и хранение материала проводят в соответствии с инструкциями к комплектам/наборам реагентов для выделения ДНК/РНК из соответствующего биологического материала. При реализации заявленного изобретения мы проводили выделение геномной ДНК из клеток костного мозга методом солевой экстракции [29]. Измерение концентрации ДНК проводили спектрофотометрически. Хранение ДНК возможно при температуре ниже -16 градусов в течение неопределенного срока. РНК (кДНК) выделяли по стандартной методике гуанидин/фенол/хлороформной экстракции по Chomczynski [30]. Измерение концентрации РНК проводили спектрофотометрически. Хранение РНК возможно при температуре ниже -40 градусов в течение года. В реакцию обратной транскрипции брали 1-2 мкг тотальной РНК, кДНК получали при помощи набора Реверта-L (Amplisens, Россия) в соответствии с инструкцией производителя.
При осуществлении заявленного способа не допускается:
1) наличие ингибиторов ПЦР-реакции, например, гепарина;
2) количество копий ДНК в одной реакции менее 500 нг., а количество кДНК менее 10000 копий ABL1.
2. Подготовка и проведение ПЦР-РВ для первичного исследования.
Для каждого исследуемого образца, для отрицательного контрольного образца и для положительного контрольного образца подготавливаются по 8 пробирок, совместимых с прибором для ПЦР в реальном времени.
В пробирках 0,5 или 1,5 мл приготовить смесь для ПЦР из расчета:
• 2,5 х (8N+1) мкл ПЦР-буфера
• 2,0 х (8N+1) мкл MgCL2
• 2,0 х (8N+1) мкл dNTP
• 0,5 х (8N+1) мкл Taq Pol
• 13 х (8N+1) мкл деионизированной воды,
где N - количество исследуемых образцов с учётом образцов отрицательного и положительного контроля.
Пробирки с ПЦР смесью встряхиваются в течение 3-5 с и центрифугируются в течение 1-3 с на микроцентрифуге/вортексе (8000-14000g).
В каждую из 8 пробирок для ПЦР в реальном времени вносится по 2 мкл смеси соответствующей смеси олигонуклеотидов, а именно:
- отдельно 2 пробирки для праймера к NPM1W;
- отдельно 2 пробирки для праймера к NPM1A;
- отдельно 2 пробирки для праймера к NPM1B;
- отдельно 2 пробирки для праймера к NPM1D;
В каждую пробирку из 8-ми пробирок добавляется смесь для ПЦР по 20 мкл и по 3 мкл ДНК исследуемого контрольного образца в концентрации 20-80 нг/мкл (предварительно развести ДНК в концентрации 100-400 нг/мкл в 5 раз: 5 мкл ДНК +20 мкл деионизированной H2O) или 3 мкл кДНК предварительно разведенной в 5 раз (5 мкл кДНК +20 мкл деионизированной H2O). Осуществляется центрифугирование пробирок в течение 1-3 секунд (8000-14000g) на микроцентрифуге.
Далее все пробирки устанавливаются в блок прибора для проведения ПЦР в реальном времени. Под прибором для проведения ПЦР в реальном времени понимается многофункциональные устройства, сочетающие в себе функции стандартного амплификатора и флуоресцентного детектора- амплификаторы Real-Time (в реальном времени). В рамках заявленного изобретения количественную TaqMan ПЦР-РВ проводили на амплификаторах Step One Real-Time PCR (Applied Biosystems, USA) или Real-time CFX96 Touch (Bio-Rad Laboratories, США).
ПЦР реакция (амплификация) проводится с соблюдением следующих температурных режимов:
- денатурация 95° 5 мин;
- затем 50 циклов амплификации, включающих: денатурацию при 95°- 30 сек; отжиг при 65° - 30 сек; синтез 72° - 20 сек.
При первичном тестировании биологического материала выявляется тип мутации NPM1: A, B, D или нестандартная вставка. Результат оценивается по общим принципам ПЦР в реальном времени. Чем выше концентрация мишени в образце, тем раньше начинается подъем кривой амплификации (флуоресценции) и тем ниже пороговый цикл Ct, т.е. цикл амплификации, на котором начинается подъем. Тип мутации в биологическом материале определяется по тому, какой подъем кривой флуоресценции ПЦР-РВ начался раньше: для реакции амплификации мутаций гена NPM1 A или мутаций гена NPM1 B или мутаций гена NPM1 D типа. Результаты отражаются в виде численных значений порогового цикла Ct на приборе. Подсчет аллельной нагрузки мутантного аллеля (для ДНК) или относительной экспрессии мутантного аллеля (для РНК) проводится по формуле представленной в разделе Учет результатов ПЦР в РВ.
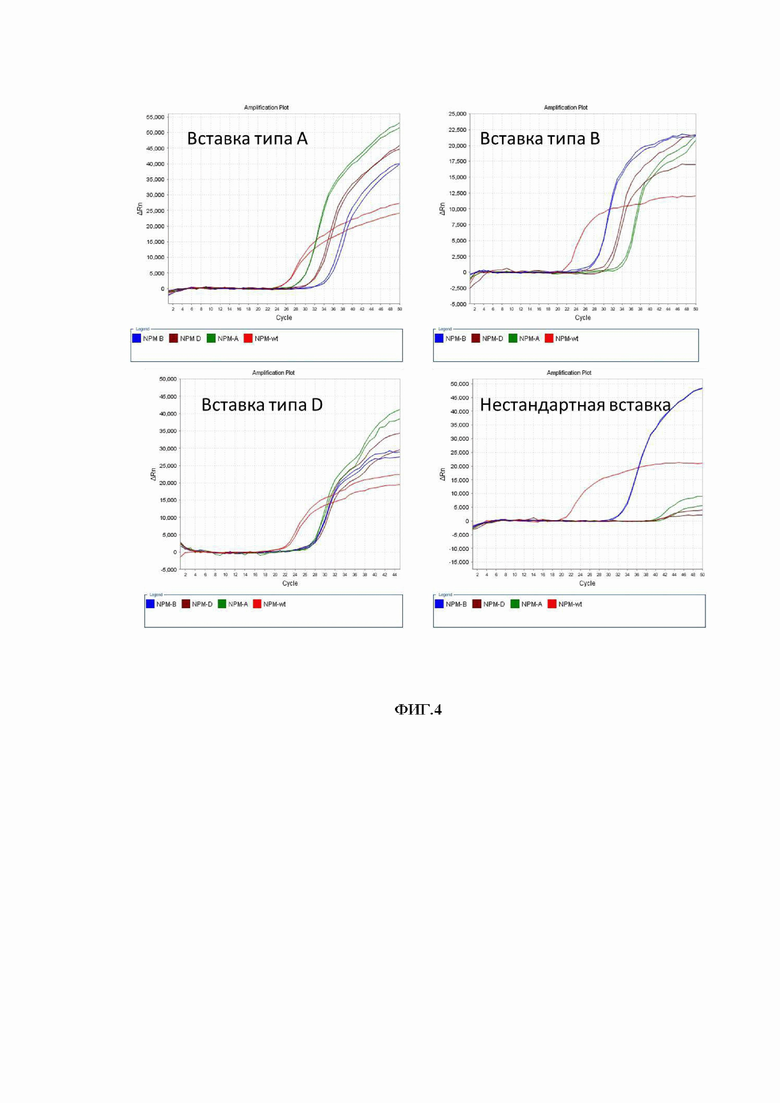
Далее проводится интерпретация полученных результатов. При отсутствии амплификации при первичном исследовании или при относительном количестве мутантного аллеля менее 10% образец признается непригодным для тестирования МОБ данным методом в связи с наличием нестандартной вставки. Нестандартная вставка отличается по нуклеотидному составу или местоположению от вставок А, В, D типа (представлена на Фигуре 4 - «нестандартная вставка»). При интерпретации результатов учитывается количество бластов в материале костного мозга по данным морфологического исследования или аллельную нагрузку мутации NPM1, полученную при проведении исследования другим методом, обычно для первичной верификации вставки NPM1 используется фрагментный анализ. Аллельная нагрузка мутантного аллеля, как правило составляет 30-50% от количества бластов в образце. При количестве бластов менее 20-30% в образце, можно получить аллельную нагрузку менее 10% при стандартной вставке. В сложных случаях можно использовать дополнительные методы подтверждения наличия у пациента нестандартной вставки NPM1, например, секвенирование, в том числе NGS секвенирование.
Таким образом, при первичном исследовании выдавалось два типа ответов:
- Тестирование МОБ возможно с указанием типа обнаруженной мутации, например - обнаружена мутация гена NPM1 типа А (В или D).
- Тестирование МОБ данным методом невозможно - нестандартный (не A, B, D) тип мутации гена NPM1. Рекомендован мониторинг МОБ методом проточной цитофлуоримерии.
Иллюстрация первичного исследования методом ПЦР-РВ мутаций генов NPM1. Кривые амплификации и варианты интерпретации результатов анализа для стандартных вставок типа A, B, D и нестандартной вставки приведены на фигуре 4.
2. Подготовка и проведение ПЦР-РВ для тестирования МОБ.
У пациентов с мутациями гена NPM1 типа А (В или D), обнаруженными на этапе первичного исследования, в дальнейшим определяется МОБ в ходе терапии. В соответствии с рекомендациями оценку МОБ проводят после 2 курса индукции, перед поддерживающей терапией, по окончанию терапии или перед алло-ТГСК, каждые 3 месяца после окончания терапии и также в любые другие точки терапии и сроки по показаниям [19].
Для каждого исследуемого образца, для отрицательного контрольного образца и для положительного контрольного образца подготавливается 6 пробирок, совместимых с прибором для ПЦР в реальном времени.
ПЦР-РВ для определения МОБ проводится в трипликатах с праймером дикого типа и уже известного мутантного типа (3W+3M).
В пробирках 0,5 или 1,5 мл приготавливается смесь для ПЦР из расчета:
2,5 х (6N+1) мкл ПЦР-буфера;
2,0 х (6N+1) мкл MgCL2;
2,0 х (6N+1) мкл dNTP;
2,0 х (6N+1) мкл смесь олигонуклеотидов
0,5 х (6N+1) мкл Taq Pol
13 х (6N+1) мкл деионизированной воды
где N - количество исследуемых образцов с учётом образцов отрицательного и положительного контроля. В качестве отрицательных контролей используется ДНК здоровых доноров. В качестве положительного контроля - положительный образец с мутацией NPM1 типа А, или типа В или типа D.
Далее пробирку с ПЦР смесью встряхивают в течение 3-5 с на вортексе и центрифугировать в течение 1-3 с на микроцентрифуге (8000-14000g).
В каждую из 6 пробирок для ПЦР в реальном времени вносится по 2 мкл смеси соответствующих олигонуклеотидов, как указано ниже:
Для исследуемого образца, в котором на 1 этапе была выявлена мутация гена NPM1 типа А, для отрицательного контрольного образца и для положительного контрольного образца:
- отдельно 3 пробирки для праймера к NPM1W;
- отдельно 3 пробирки для праймера к NPM1A;
Для исследуемого образца, в котором на 1 этапе была выявлена мутация гена NPM1 типа В, для отрицательного контрольного образца и для положительного контрольного образца:
- отдельно 3 пробирки для праймера к NPM1W;
- отдельно 3 пробирки для праймера к NPM1B;
Для исследуемого образца, в котором на 1 этапе была выявлена мутация гена NPM1 типа D, для отрицательного контрольного образца и для положительного контрольного образца:
- отдельно 3 пробирки для праймера к NPM1W;
- отдельно 3 пробирки для праймера к NPM1D;
Далее в эти пробирки вносится по 20 мкл ПЦР смеси. В каждую пробирку из 6-ти пробирок добавляется по 3 мкл ДНК исследуемого или контрольного образца в концентрации 200-300нг в мкл или 3 мкл кДНК.
Осуществляют процесс амплификации, при этом количество ДНК в одной реакции должно составлять более 500 нг., а количество кДНК должно превышать 10000 копий ABL1 (отдельно тестируется со стандартами ABL1), что позволяет достичь высокой чувствительности заявленного способа. При более низком количестве ДНК (кДНК) или плохом качестве ДНК (кДНК) возможно получение ложноотрицательного результата.
Далее осуществляют центрифугирование пробирки в течение 1-3 с на микроцентрифуге (8000-14000g).
Далее все пробирки устанавливаются в блок прибора для проведения ПЦР в реальном времени для амплификации.
ПЦР реакция (амплификация) проводится с соблюдением следующих температурных режимов:
- денатурация 95° 5 мин;
- затем 50 циклов амплификации, включающих: денатурацию при 95°- 30 сек; отжиг при 65°-30 сек; синтез 72°- 20 сек.
Учет результатов ПЦР в РВ.
По разнице в циклах амплификации Ct между мутантным и диким праймером для мутаций гена NPM1 A или мутаций гена NPM1 B или мутаций гена NPM1 D типа определяют количественное значение мутантного аллеля.
Для ДНК подсчет аллельной нагрузки (АН) мутантного аллеля в процентах осуществлялся по формуле 100*AO/(1+AO), где АО- результат подсчета аллельного отношения. Расчет аллельного отношения (АО) w/m производится по формуле 5/2ΔCt; где ΔCt разница в циклах амплификации между мутантным и диким праймером.
Для РНК (кДНК) подсчет относительной экспрессии (%) мутантного аллеля, производится по формуле 100/2ΔCt; где ΔCt разница в циклах амплификации между мутантным и диким праймером.
В случае NPM1 позитивного ОМЛ, каждая опухолевая клетка содержит данную мутацию, следовательно, определяя аллельную нагрузку или относительную экспрессию мутантного аллеля, в процессе диагностики, фактически определяется % остаточных опухолевых клеток (МОБ).
Интерпретация результатов:
В соответствии с общими принципами оценки ПЦР-РВ van der Velden (2003) [31] выделяют несколько типов ответов: отрицательный, положительный (с количественной оценкой и без количественной оценки). Положительный неколичественный ответ означает наличие мутации в таком малом количестве, что делает невозможным ее количественный подсчет.
Производится следующая интерпретация результатов определения МОБ методом ПЦР-РВ:
Критерии отрицательного ответа об отсутствии мутации A, B, D типа:
1) начало амплификации дикого праймера не позднее 21 цикла, это соответствует количеству ДНК более 500 нг и говорит о ее хорошем качестве, для кДНК необходимо ориентироваться на копийность ABL1, которая должна соответствовать более 10000 копий;
2) амплификация с праймером мутантного типа не происходит; и/или при подсчете МОБ количество % опухолевых клеток выходит за пределы чувствительности метода, т.е. составляет менее 0,001%. В случае ДНК это соответствует разнице в циклах амплификации (ΔCt) дикого и мутантного праймера более 19 циклов, а в случае РНК (кДНК) соответствует ΔCt > 16,5 и/или амплификация с мутантным праймером происходит позже 39 цикла, что также соответствует максимальной чувствительности определения, см. график определения аналитической чувствительности (фигура 6).
В таблице №6, представлены результаты исследования, иллюстрирующие примеры, удовлетворяющие критериям отрицательного ответа. Из данной таблицы следует, что все случаи удовлетворяют критериям отрицательного ответа: Δ Ct≥19 или Ct NPM1 M > 39; при этом Ct NPM1 W <21 цикла. Подсчет аллельной нагрузки в данном случае не проводится. В данном примере цифра АН (%) приводится только для того, чтобы показать, что она ниже заявленной границы определения чувствительности <0,001%. *на - нет амплификации.
Таблица 6. Примеры отрицательных результатов при определении МОБ в образцах ДНК костного мозга.
Критерии положительного количественного ответа (наличие мутации с возможностью ее количественного определения):
1) имеется специфическая амплификация с мутантными праймерами в 2-х или 3-х повторах и началом подъема не позднее 39 цикла;
2) При подсчете МОБ определяется количество более 0,001%, что соответствует ΔCt дикого и мутантного праймера менее 19 циклов и менее 16,5 циклов для РНК (кДНК);
3) 3 из 3-х повторов имеют разницу Ct менее 1,5 циклов или 2 из 3-х повторов имеют разницу Ct менее 1цикла;
4) цикл амплификации (Ct), должен быть как минимум на 3 единицы меньше, чем наименьший Ct поликлонального контроля. Обычно амплификация поликлонального контроля либо не происходит, либо происходит позже 40 цикла.
В таблице № 7 и 8 показаны результаты исследования, подтверждающие факт специфической амплификации с мутантными праймерами и удовлетворяющие критериям положительного количественного ответа при первичном тестировании ДНК (таблица 6) и при определении МОБ (указаны в таблице 8). Все случаи удовлетворяют критериям положительного количественного ответа и имеют аллельную нагрузку (АН) более 10% за исключением пациентов, помеченных *. При АН < 10% необходимо оценить уровень бластных клеток в материале или АН другим методом, при очевидном несовпадении, вставка - нестандартная (Н). В данной таблице пациенты, помеченные * имели низкий процент аллельной нагрузки, но только у пациентов 146-167 и 146-544 имелось явное несоответствие АН и количества бластных клеток, в дальнейшем методом NGS у этих двух пациентов подтвердили нестандартную вставку NPM1.
Таблица 7. Примеры первичного тестирования ДНК для определения типа мутации у пациентов, для которых мутация NPM1 +4bp подтверждена методом фрагментного анализа.
Нестандартная вставка подтверждена NGS - “ GCtG ”
Нестандартная вставка подтверждена NGS - “CtGG”
Примеры положительных количественных ответов при определении МОБ в образцах ДНК костного мозга у пациентов с ОМЛ и уже известным типов вставки в гене NPM1, выявленным при первичном исследовании приведены в таблице 8. Все случаи удовлетворяют критериям положительного количественного ответа: Δ Ct<19; Ct NPM1 M < 39; три повтора Ct NPM1 M имеют разницу менее 1,5 циклов или два повтора Ct NPM1 M имеют разницу менее 1 циклов и амплифицируются раньше поликлонального контроля на три цикла.
Таблица 8. Примеры положительных количественных ответов при определении МОБ в образцах ДНК костного мозга у пациентов с ОМЛ и уже известным типов вставки в гене NPM1, выявленным при первичном исследовании.
Критерии положительного неколичественного ответа (наличие мутации в количестве ниже подсчётной чувствительности): соблюдены все критерии положительного количественного ответа за исключением разброса между повторами: разброс между двумя или тремя повторами составляет более 1 или 1,5 циклов, соответственно.
В таблице №9 показаны результаты исследования, подтверждающие факт специфической амплификации с мутантными праймерами и удовлетворяющие критериям положительного неколичественного ответа.
Примеры положительного ответа при определении МОБ в образцах ДНК костного мозга без определения количества (неколичественного) приведены в таблице 9. Данные случаи лишь частично удовлетворяют критериям положительного количественного ответа, кроме пункта о совпадении по циклам 2-х - 3-х повторов, что делает подсчет АН невозможным. В примере №1 - три повтора Ct NPM1 M удовлетворяют критериям положительного ответа, но имеют большой разброс. В примере №2 - два повтора Ct NPM1 M удовлетворяют критериям положительного ответа, но имеют разницу более 1 цикла.
Таблица 9. Примеры положительного ответа при определении МОБ в образцах ДНК костного мозга без определения количества (неколичественного).
среднее
среднее
(в скобках повторы)
17,95
При соблюдении критериев отрицательного ответа, но недостаточном для достижения чувствительности 10-5 количестве ДНК в исследовании, т.е. когда Ct W (среднее)> 21 цикла, или копийности в случае РНК (кДНК) менее 10000 копий, необходимо выдать соответствующий ответ: “Недостаточная чувствительность, требуется повторное исследование”.
Существует небольшая группа результатов, так называемая “серая зона” или результаты подозрительные на наличие МОБ. Такие результаты по критериям относятся отрицательными, однако критерии положительного образца соблюдены частично. Например, амплификация удовлетворяет положительным критериям только в одном повторе или амплификация в 2-х, 3-х повторах удовлетворяет положительным критериям частично, например, прошла немного позже 39 цикла, но на три цикла раньше, чем поликлональный контроль. Такая ситуация возможна, если у пациента с МОБ+ не хватило клеток (ДНК) для полноценного исследования или процент опухолевых клеток в исследуемом образце крайне низок. В любом случае, такие случаи подозрительные на наличие МОБ, необходимо отмечать в виде комментариев к анализу, или в виде ответа со специальной формулировкой, что “анализ подозрителен на наличие МОБ, рекомендуется активное наблюдение пациента, в том числе повтор исследования через месяц”. Примеры результатов “серой зоны”, т.е. подозрительных на наличие МОБ. Есть частичное соблюдение положительных критериев, примеры приведены в таблице 10. Из приведенных примеров видно, что есть частичное соблюдение положительных критериев (см. комментарии). Амплификация прошла ранее 3-х циклов от поликлонального контроля, т.е. находится в положительной области. В таких случаях, когда у исследователя возникает подозрение, что данный случай не отрицательный, мы предлагаем ввести ответ “подозрительно на наличие МОБ”. Подсчет аллельной нагрузки в данном случае не проводится. В данном примере цифра АН (%) приводится только для демонстрации. *на - нет амплификации.
Таблица 10. Примеры результатов “серой зоны”, т.е. подозрительных на наличие МОБ. Есть частичное соблюдение положительных критериев
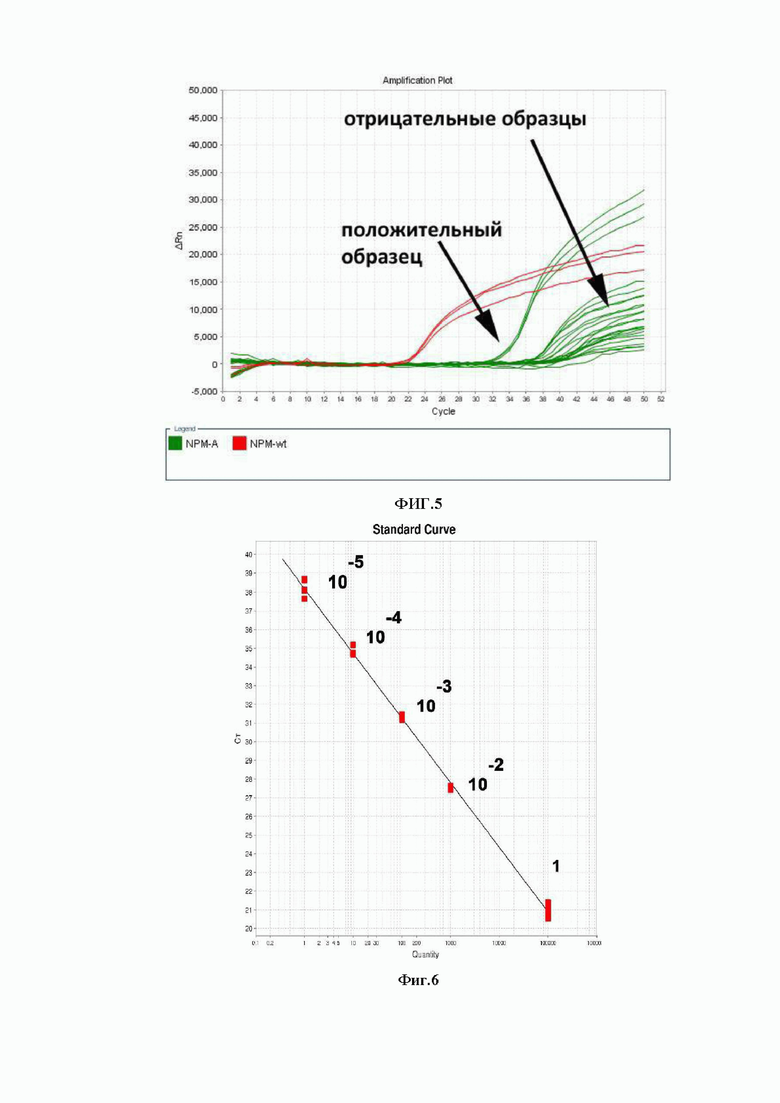
Кривые амплификации, иллюстрирующие результат определения МОБ приведены на фигуре 5.
Заявленный способ показал следующие результаты
Аналитическая чувствительность метода составила 10-5. Чувствительность определения мутации NPM1 (тип А) методом АС-ПЦР в виде калибровочной (стандартной) кривой приведена на фигуре 6.
Диагностическая специфичность составила 98,7%. Оценка клинической чувствительности и точности не проводилась в связи отсутствием референсного метода, обладающего схожей аналитической чувствительностью для оценки МОБ. У всех первичных пациентов (n - 55) с доказанной мутацией гена NPM1 A, B, D типа выявлен положительный результат при первичном исследовании.
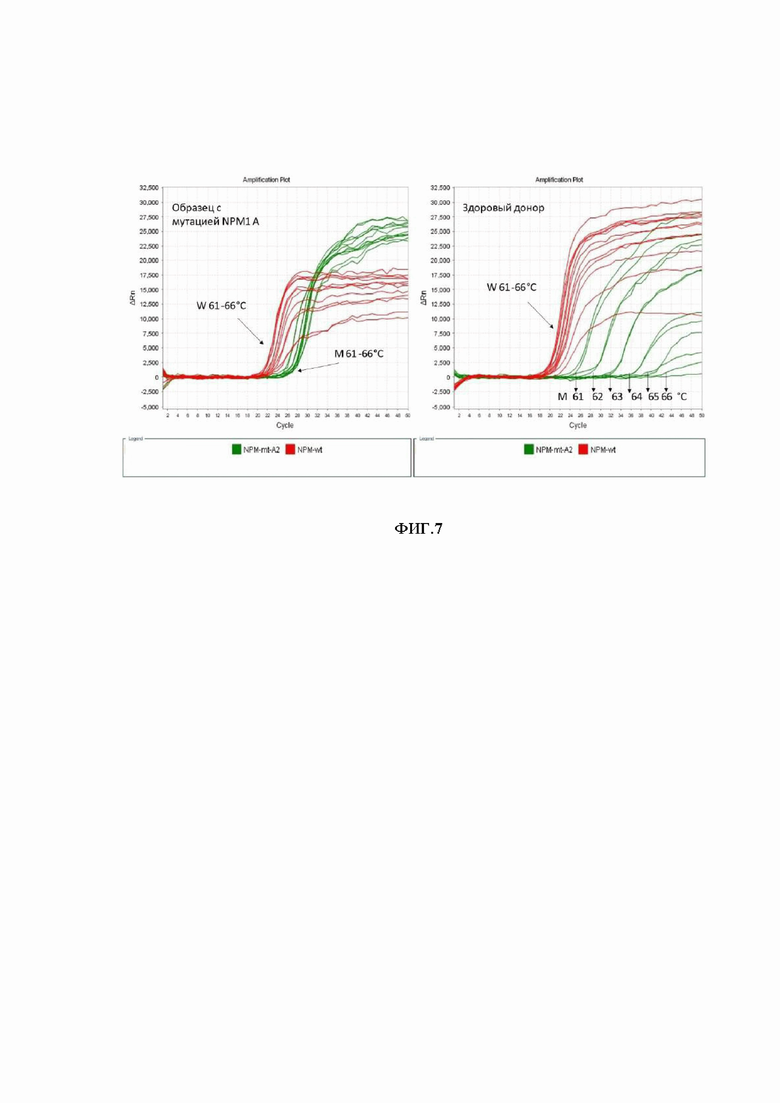
Подбор температурных условий для максимальной специфичности ПЦР представлен на фигуре 7.
Графики кривых ПЦР-РВ и значение пороговых циклов в зависимости от температуры отжига праймеров. Максимальная специфичность определения достигнута при температуре 65°С. (фигура 7).
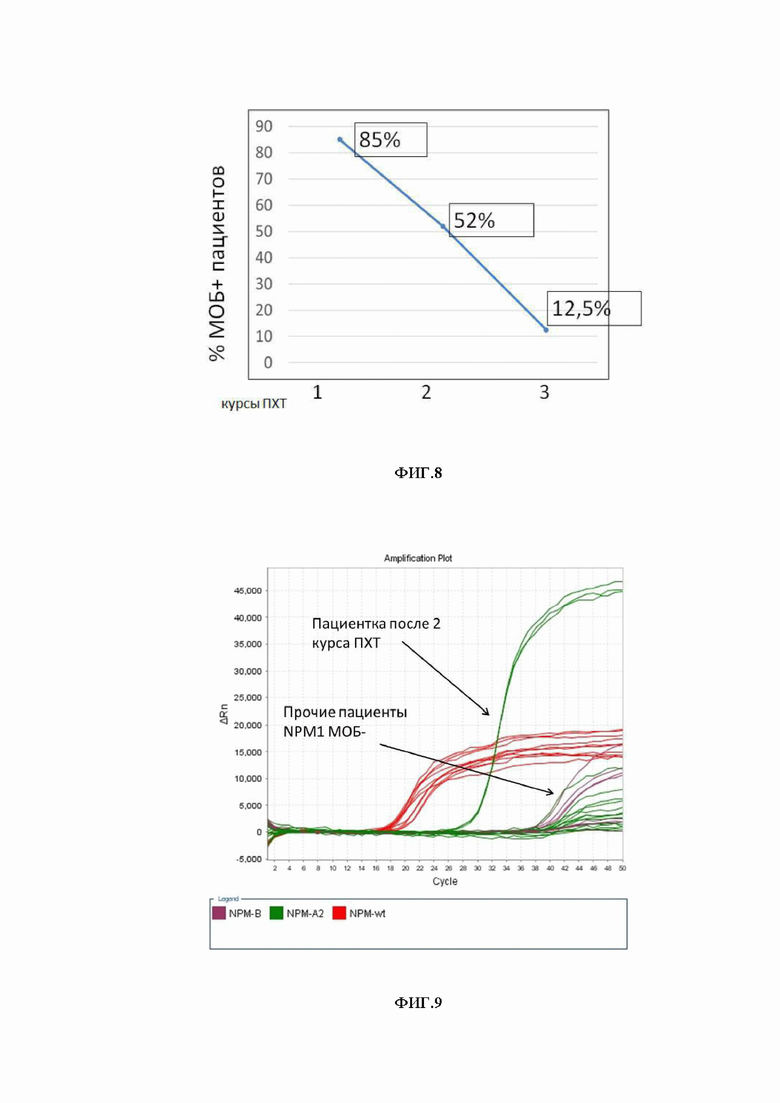
Для подтверждения возможностей данной методики мы приводим наш 2-х летний опыт применения ее в клинической практике. К настоящему времени проанализировано 152 первичных пациента, которые имели доказанную фрагментным анализом мутацию (вставку +4 bp) в 12 экзоне гена NPM1. Возможность мониторирования МОБ показана у 87,5% (133 из 152). То есть, 19 пациентов в нашей когорте имели вставку NPM1 нестандартного типа, что было подтверждено методом NGS. Сорока пациентам проводился мониторинг МОБ данным методом. Суммарные результаты клиренса опухолевых клеток представлены на фигуре 8. Показано, что только к третьему курсу ПХТ количество МОБ-позитивных пациентов сокращается до 12,5%. Представлены суммарные результаты клиренса опухолевых клеток (% МОБ позитивных пациентов) после 1, 2 и 3 -го курса ПХТ (фигура 8).
Сущность группы изобретений пояснена примерами конкретной реализации, которые не ограничивают объем изобретения.
Клинический случай 1. Пациентка Ш, 37 лет. Поставлен диагноз острого миелоидного лейкоза. При первичном обследовании обнаружена мутация гена NPM1 методом фрагментного анализа (вставка + 4 нуклеотида в 12 экзоне). Проведено первичное исследование методом ПЦР-РВ на наличие вставок А, В, D типа и возможности определения в дальнейшем МОБ. Ответ - обнаружена мутация NPM1 тип А, аллельная нагрузка составила 47%, определение МОБ возможно. При проведении исследования после второго курса ПХТ обнаружена МОБ, аллельная нагрузка составила 1,9%, что говорило о первичной резистентности к проводимой терапии. Врачи пересмотрели тактику лечения и перешли на терапию второй линии.
Фигура 9. Результаты ПЦР-РВ демонстрируют положительный результат определения МОБ после 2 курса ПХТ (клинический случай №1).
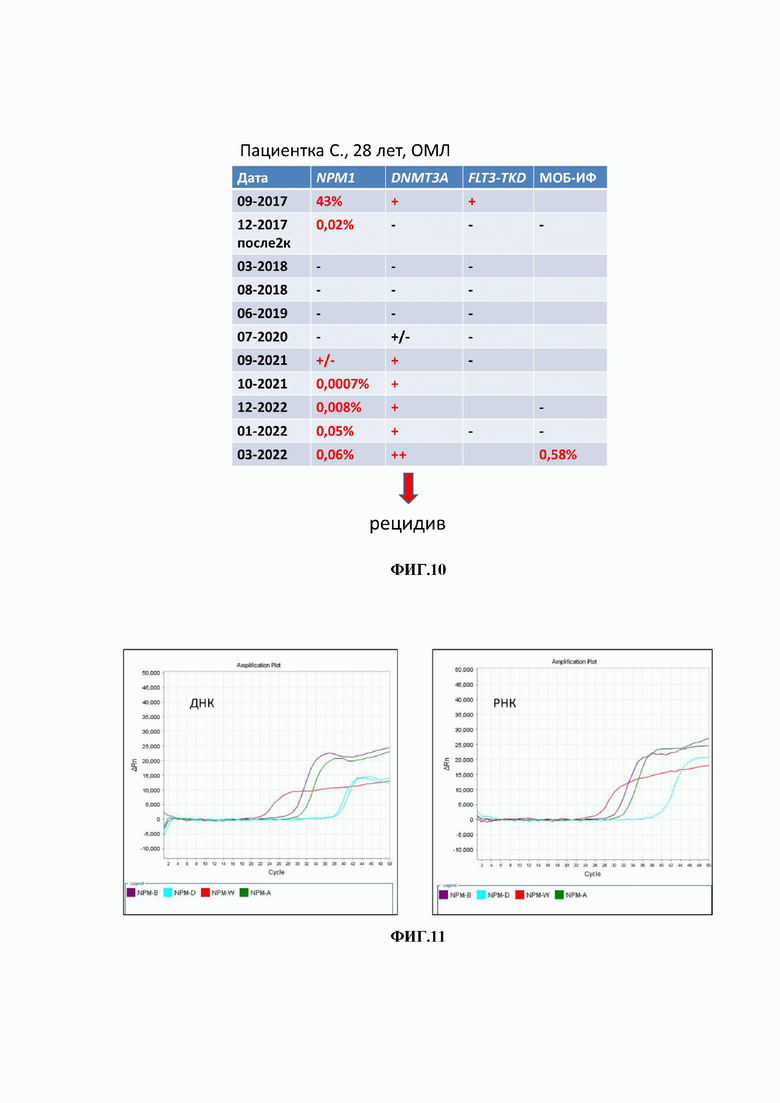
Клинический случай 2. Пациентка С, 28 лет. Наблюдалась в длительной ремиссии острого миелоидного лейкоза. При очередном обследовании обнаружен сомнительный результат (положительный без определения количества) определения мутации гена NPM1 патентуемым методом. Пациентка взята под наблюдение и уже через месяц получен положительный ответ, с дальнейшим ростом аллельной нагрузки. Согласно международным рекомендациям при 10-кратном росте алллельной нагрузки мутации NPM1 в крови или костном мозге рекомендовано переходить к терапии-спасения, так как такой рост неизбежно сопровождается рецидивом в среднем в течение 3-х месяцев. Пациентке был начат подбор неродственного донора. Рецидив ОМЛ был констатирован в марте 2022, через полгода после первичного обнаружения мутации NPM1. Таким образом, врачи имели время, чтобы начать подбор донора и продумать терапию. Данный клинический случай очень хорошо иллюстрирует высокую аналитическую чувствительность методики, поскольку МОБ - иммунофенотипирование (МОБ-ИФ) стало позитивным только перед развитием рецидива (Фигуре 10).
Результаты ПЦР-РВ по определению мутации NPM1, DNMT3A, FLT3-TKD и данных проточной цитофлуориметрии как иллюстрация клинического случая №2 (фигура 10).
Далее приводим примеры реализации заявленного изобретения в виде сравнительного анализа на примере ДНК и РНК.
Пациент 3. Приводятся циклы амплификации дикого праймера и праймеров на мутации А, B, D типа для ДНК и РНК, выделенной из одного образца костного мозга. Определяется вставка типа В. Расчетные значения аллельной нагрузки (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК приводятся в соответствии с формулами подсчета для ДНК и РНК, приведенных в разделе учет результатов ПЦР в РВ настоящего описания.
Таблица 11 иллюстрирует циклы амплификации (Ct) для ДНК и РНК, значение аллельной нагрузки мутантного аллеля (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК у пациента 3.
для ДНК и РНК
Кривые амплификации, иллюстрирующее настоящий пример приведены на Фигуре 11.
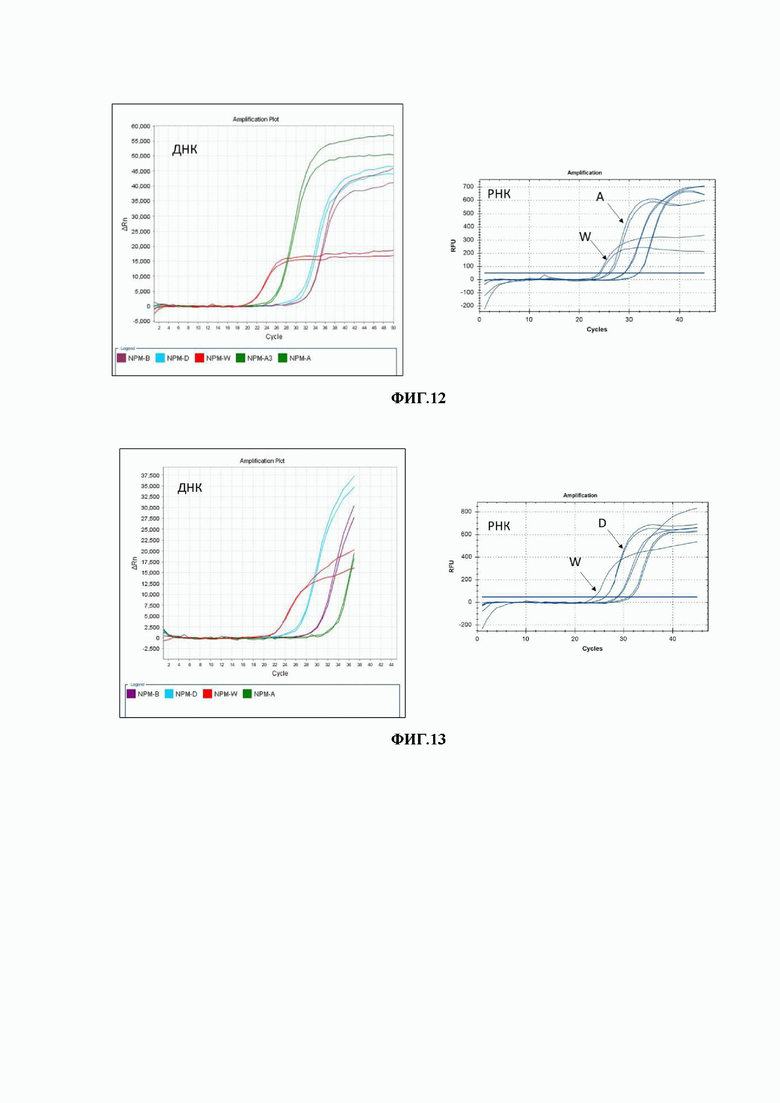
Пациент 4. Приводятся циклы амплификации дикого праймера и праймеров на мутации А, B, D типа для ДНК и РНК, выделенной из одного образца костного мозга. Определяется вставка типа А. Расчетные значения аллельной нагрузки (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК приводятся в соответствии с формулами подсчета для ДНК и РНК, приведенных в разделе учет результатов ПЦР в РВ настоящего описания.
Таблица 12 иллюстрирует циклы амплификации (Ct) для ДНК и РНК, значение аллельной нагрузки мутантного аллеля (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК у пациента 4.
для ДНК и РНК
Кривые амплификации, иллюстрирующее настоящий пример приведены на Фигуре 12.
Пациент 5. Приводятся циклы амплификации дикого праймера и праймеров на мутации А, B, D типа для ДНК и РНК, выделенной из одного образца костного мозга. Определяется вставка типа D. Расчетные значения аллельной нагрузки (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК приводятся в соответствии с формулами подсчета для ДНК и РНК, приведенных в разделе учет результатов ПЦР в РВ настоящего описания.
Таблица 13 иллюстрирует циклы амплификации (Ct) для ДНК и РНК, значение аллельной нагрузки мутантного аллеля (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК у пациента 5.
для ДНК и РНК
Кривые амплификации, иллюстрирующее настоящий пример приведены на Фигуре 13.
Пациент 6. Приводятся циклы амплификации дикого праймера и праймеров на мутацию А типа для ДНК и РНК, выделенной из одного образца костного мозга. Расчетные значения МОБ (%), т.е. аллельной нагрузки (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК приводятся в соответствии с формулами подсчета для ДНК и РНК, приведенных в разделе учет результатов ПЦР в РВ настоящего описания.
Таблица 14 иллюстрирует циклы амплификации (Ct) для ДНК и РНК, значение МОБ (%) для ДНК и РНК у пациента 6.
ДНК и РНК
Кривые амплификации, иллюстрирующие настоящий пример приведены на Фигуре 14.
Пациент 7. Приводятся циклы амплификации дикого праймера и праймеров на мутацию B типа для ДНК и РНК, выделенной из одного образца костного мозга. Расчетные значения МОБ (%), т.е. аллельной нагрузки (%) для ДНК и относительной экспрессии мутантного аллеля (%) для РНК приводятся в соответствии с формулами подсчета для ДНК и РНК, приведенных в разделе учет результатов ПЦР в РВ настоящего описания.
Таблица 15 иллюстрирует циклы амплификации (Ct) для ДНК и РНК, значение МОБ (%) для ДНК и РНК у пациента 7.
ДНК и РНК
Кривые амплификации, иллюстрирующие настоящий пример приведены на Фигуре 15.
Сущность изобретения пояснена на графических материалах:
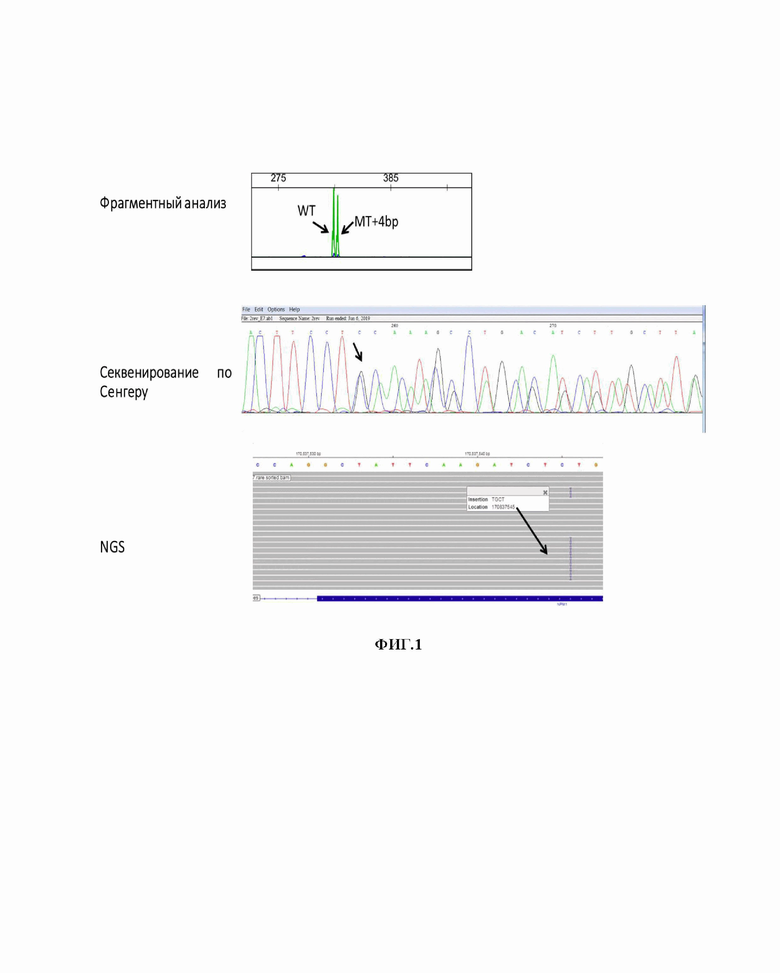
Фигура 1. Представление методов первичного подтверждения наличия мутации гена NPM1 (секвенирование по Сенгеру, фрагментный анализ, NGS - секвенирование нового поколения). Чувствительность определения данными методами не превышает 10-2;
Фигура 2. Данные заявителя о встречаемости вставок типа A, B, D и нестандартных вставок у российских пациентов с ОМЛ;
Фигура 3. Схематическое изображение расположения праймеров/ проб;
Фигура 4. Иллюстрация первичного исследования методом ПЦР-РВ мутаций гена NPM1. Кривые амплификации и варианты интерпретации результатов анализа для стандартных вставок типа A, B, D и нестандартной вставки;
Фигура 5. Кривые амплификации, иллюстрирующие результат определения МОБ;
Фигура 6. Чувствительность определения мутации NPM1 методом АС-ПЦР (тип А). Калибровочная (стандартная) кривая;
Фигура 7. Графики кривых ПЦР-РВ и значение пороговых циклов в зависимости от температуры отжига праймеров. Максимальная чувствительность и специфичность определения достигнута при температуре 65°С;
Фигура 8. Представлены суммарные результаты клиренса опухолевых клеток (% МОБ позитивных пациентов) после 1, 2 и 3 -го курса ПХТ;
Фигура 9. Результаты ПЦР-РВ демонстрируют положительный результат определения МОБ после 2 курса ПХТ (клинический случай №1);
Фигура 10. Результаты ПЦР-РВ по определению мутации NPM1, DNMT3A, FLT3-TKD и данных проточной цитофлуориметрии как иллюстрация клинического случая №2.
Фигура 11. Кривые амплификации, иллюстрирующие первичное исследование методом ПЦР-РВ мутаций гена NPM1 (вставок A, B, D типа) на материале ДНК и РНК у пациента 3.
Фигура 12 Кривые амплификации, иллюстрирующие первичное исследование методом ПЦР-РВ мутаций гена NPM1 (вставок A, B, D типа) на материале ДНК и РНК у пациента 4.
Фигура 13 Кривые амплификации, иллюстрирующие первичное исследование методом ПЦР-РВ мутаций гена NPM1 (вставок A, B, D типа) на материале ДНК и РНК у пациента 5.
Фигура 14 Кривые амплификации, иллюстрирующие определение МОБ методом ПЦР-РВ (вставка NPM1 A типа) на материале ДНК и РНК у пациента 6.
Фигура 15 Кривые амплификации, иллюстрирующие определение МОБ методом ПЦР-РВ (вставка NPM1 B типа) на материале ДНК и РНК у пациента 7.
Источники информации, принятые во внимание при подготовке описания изобретения:
1) Каприн А.Д. Клинические рекомендации. Острые миелоидные лейкозы. Взрослые. 2020. https://oncology-association.ru/wp-content/uploads/2020/09/ostrye_mieloidnye_lejkozy.pdf.
2) Злокачественные новообразования в России в 2021 году (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2018.
3) Falini B., Nicoletti I., Martelli M.F., Mecucci C. Acute myeloid leukemia carrying cytoplasmic/mutated nucleophosmin (NPMc+ AML): Biologic and clinical features. Blood. 2007; 109: 874-885. doi: 10.1182/blood-2006-07-012252.
4) Heath E.M., Chan S.M., Minden M.D., Murphy T., Shlush L.I., Schimmer A.D. Biological and clinical consequences of NPM1 mutations in AML. Leukemia. 2017; 31: 798-807. doi: 10.1038/leu.2017.30.
5) Ossenkoppele G., Schuurhuis G.J. MRD in AML: Does it already guide therapy decision-making? Hematol. Am. Soc. Hematol. Educ. Program. 2016; 2016: 356-365. doi: 10.1182/asheducation-2016.1.356.
6) Tomlinson B., Lazarus H.M. Enhancing acute myeloid leukemia therapy-Monitoring response using residual disease testing as a guide to therapeutic decision-making. Expert Rev. Hematol. 2017; 10: 563-574. doi: 10.1080/17474086.2017.1326811.
7) Hourigan C.S., Gale R.P., Gormley N.J., Ossenkoppele G.J., Walter R.B. Measurable residual disease testing in acute myeloid leukemia. Leukemia. 2017; 31: 1482-1490. doi: 10.1038/leu.2017.113.
8) Mosna F., Capelli D., Gottardi M. Minimal residual disease in acute myeloid leukemia: Still a work in progress? J. Clin. Med. 2017; 6: 57. doi: 10.3390/jcm6060057.
9) Buccisano F., Maurillo L., Del Principe M.I., Di Veroli A., De Bellis E., Biagi A., Zizzari A., Rossi V., Rapisarda V., Amadori S., et al. Minimal residual disease as a biomarker for outcome prediCtion and therapy optimization in acute myeloid leukemia. Expert Rev. Hematol. 2018; 11: 307-313. doi: 10.1080/17474086.2018.1447378.
10) Coltoff A., Houldsworth J., Keyzner A., Renteria A.S., Mascarenhas J. Role of minimal residual disease in the management of acute myeloid leukemia-A case-based discussion. Ann. Hematol. 2018;97:1155-1167. doi: 10.1007/s00277-018-3330-9.
11) Shayegi N, Kramer M, Bornha¨user M, et al; Study Alliance Leukemia (SAL). The level of residual disease based on mutant NPM1 is an independent prognostic faCtor for relapse and survival in AML. Blood. 2013; 122(1):83-92.
12) Hubmann M, Köhnke T, Hoster E, Schneider S, Dufour A, Zellmeier E, Fiegl M, Braess J, Bohlander SK, Subklewe M, Sauerland MC, Berdel WE, Büchner T, Wörmann B, Hiddemann W, Spiekermann K. Molecular response assessment by quantitative real-time polymerase chain reaCtion after induCtion therapy in NPM1-mutated patients identifies those at high risk of relapse. Haematologica. 2014; 99 (8):1317-1325. doi: 10.3324/haematol.2014.104133.
13) Balsat M, Renneville A, Thomas X, et al. PostinduCtion minimal residual disease prediCts outcome and benefit from allogeneic stem cell transplantation in acute myeloid leukemia with NPM1 mutation: a study by the Acute Leukemia French Association Group. J Clin Oncol. 2017; 35(2):185-193.
14) Krönke J, Schlenk RF, Jensen K-O, et al. Monitoring of minimal residual disease in NPM1-mutated acute myeloid leukemia: a study from the German-Austrian acute myeloid leukemia study group. J Clin Oncol. 2011; 29: 2709-2716.
15) Ivey A., Hills R.K., Simpson M.A., Jovanovic J.V., Gilkes A., Grech A., Patel Y., Bhudia N., Farah H., Mason J., et al. Assessment of minimal residual disease in standard-risk AML. N. Engl. J. Med. 2016; 374: 422-433. doi: 10.1056/NEJMoa1507471
16) Lambert J, Lambert J, Nibourel O, Pautas C, Hayette S, Cayuela JM, Terré C, Rousselot P, Dombret H, Chevret S, Preudhomme C, Castaigne S, Renneville A. MRD assessed by WT1 and NPM1 transcript levels identifies distinCt outcomes in AML patients and is influenced by gemtuzumab ozogamicin. Oncotarget. 2014 Aug 15;5(15):6280-8. doi: 10.18632/oncotarget.2196.
17) Dvorakova D., Racil Z., Jeziskova I., Palasek I., Protivankova M., Lengerova M., Razga F., Mayer J. Monitoring of minimal residual disease in acute myeloid leukemia with frequent and rare patient-specific NPM1 mutations. Am. J. Hematol. 2010;85:926-929. doi: 10.1002/ajh.21879.
18) Schuurhuis G.J., Heuser M., Freeman S., Béné M.C., Buccisano F., Cloos J., Grimwade D., Haferlach T., Hills R.K., Hourigan C.S., et al. Minimal/measurable residual disease in AML: A consensus document from the European LeukemiaNet MRD Working Party. Blood. 2018; 131: 1275-1291. doi: 10.1182/blood-2017-09-801498.
19) Heuser M, et al. 2021 Update on MRD in acute myeloid leukemia: a consensus document from the European LeukemiaNet MRD Working Party. Blood. 2021;138(26):2753-2767. doi: 10.1182/blood.2021013626.
20) Gorello P, Cazzaniga G, Alberti F, Dell’oro MG, Gottardi E, Specchia G et al. Quantitative assessment of minimal residual disease in acute myeloid leukemia carrying nucleophosmin (NPM1) gene mutations. Leukemia 2006; 20: 1103-1108.
21) Chou WC, Tang JL, Wu SJ, et al. Clinical implications of minimal residual disease monitoring by quantitative polymerase chain reaCtion in acute myeloid leukemia patients bearing nucleophosmin (NPM1) mutations. Leukemia. 2007 May;21(5):998-1004. doi: 10.1038/sj.leu.2404637. Epub 2007 Mar 15.
22) Vester B, Wengel J. LNA (locked nucleic acid): high-affinity targeting of complementary RNA and DNA. Biochemistry 2004; 43: 13233-13241.
23) Latorra D, Campbell K, Wolter A, Hurley JM. Enhanced allele-specific PCR discrimination in SNP genotyping using 3' locked nucleic acid (LNA) primers. Hum Mutat 2003; 22(1):79-85. DOI: 10.1002/humu.10228. PMID: 12815597.
24) Morandi L, de Biase D, Visani M, et al. Allele specific locked nucleic acid quantitative PCR (ASLNAqPCR): an accurate and cost-effeCtive assay to diagnose and quantify KRAS and BRAF mutation. PLoS One 2012; 7 (4): e36084. DOI: 10.1371/journal.pone.0036084. PMID: 22558339.
25) Abdelhamid E, Besbes S, Renneville A, et al. Minimal Residual Disease assessment of IDH1/2 mutations in Acute Myeloid Leukemia by LNA-RQ-PCR. Tunis Med 2016; 94(3):190-7. PMID: 27575502.
26) Albitar A. Ma W, DeDios I, et al. Positive seleCtion and high sensitivity test for MYD88 mutations using locked nucleic acid. Int J Lab Hematol 2016; 38(2):1 33-40. DOI: 10.1111/ijlh.12456. PMID: 26797804.
27) Thiede С, Creutzig Е, Illmer T, Schaich M, V Heise, G Ehninger, O Landt. Rapid and sensitive typing of NPM1 mutations using LNA-mediated PCR clamping. Leukemia. 2006 OCt;20(10):1897-9. doi: 10.1038/sj.leu.2404367.
28) Thiede C, Koch S, Creutzig E, Steudel C, Illmer T, Schaich M et al. Prevalence and prognostic impaCt of NPM1 mutations in 1485 adult patients with acute myeloid leukemia (AML). Blood 2006; 107: 4011-4020.
29) Сидорова Ю.В., Сорокина Т.В., Бидерман Б.В., Никулина Е.Е., Кисиличина Д.Г., Наумова Е.В., Почтарь М.Е., Луговская С.А., Иванова В.Л., Ковалева Л.Г., Птушкин В.В., Никитин Е.А., Судариков А.Б. Определение минимальной остаточной болезни у больных В-клеточным хроническим лимфолейкозом методом пациент-специфичной ПЦР. Клиническая лабораторная дигностика. 2011; №12: 22-35.
30) Chomczynski P, Sacchi N. The single-step method of RNA isolation by acid guanidinium thiocyanate-phenol-chloroform extraCtion: twenty-something years on. Nat Protoc 2006;1(2):581-5. doi: 10.1038/nprot.2006.83.
31) van der Velden VH, Hochhaus A, Cazzaniga G, Szczepanski T, Gabert J, van Dongen JJ. DeteCtion of minimal residual disease in hematologic malignancies by real-time quantitative PCR: principles, approaches, and laboratory aspeCts. Leukemia. 2003;17(6): 1013-34. doi: 10.1038/sj.leu.2402922.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCtYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing originalFreeTextLanguageCode="ru"
dtdVersion="V1_3" fileName="Перечень последовательностей.xml"
softwareName="WIPO Sequence" softwareVersion="2.3.0"
produCtionDate="2023-05-24">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>1</ApplicationNumberText>
<FilingDate>2023-05-23</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>1</ApplicantFileReference>
<ApplicantName languageCode="ru">Федеральное государственное
бюджетное учреждение "НМИЦ гематологии" Минздрава
России</ApplicantName>
<ApplicantNameLatin>Federal State Budgetary Institution
"National Medical Rasearch Center of Hematology" of the
Ministry of Healthcare of the Russion Federation</ApplicantNameLatin>
<InventionTitle languageCode="ru">Набор олигонуклеотидов и способ
высокочувствительной полимеразной цепной реакции в режиме реального
времени для выявления A, B, D мутаций гена NPM1</InventionTitle>
<SequenceTotalQuantity>6</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>22</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..22</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q7">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>19</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q8">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>locked nucleic acid
(LNA)</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>21</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q9">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>locked nucleic acid
(LNA)</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>ttccaggCtattcaagatCtCt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>23</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..23</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q12">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>16</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q13">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>locked nucleic acid
(LNA)</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>20</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q14">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>locked nucleic acid
(LNA)</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>CtattcaagatCtCtgtCtggca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>23</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..23</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q16">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>17</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q17">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>locked nucleic acid
(LNA)</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>20</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q18">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>locked nucleic acid
(LNA)</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>CtattcaagatCtCtgcatggca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="4">
<INSDSeq>
<INSDSeq_length>23</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..23</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q20">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>20</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q21">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>locked nucleic acid
(LNA)</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>CtattcaagatCtCtgcCtggca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="5">
<INSDSeq>
<INSDSeq_length>28</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..28</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q23">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sp.</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>1</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q24">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>FAM-labeled</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>modified_base</INSDFeature_key>
<INSDFeature_location>28</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mod_base</INSDQualifier_name>
<INSDQualifier_value>OTHER</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q25">
<INSDQualifier_name>note</INSDQualifier_name>
<INSDQualifier_value>BHQ1-labeled</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>tgcagagtgagaaCtttccCtaccgtgt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="6">
<INSDSeq>
<INSDSeq_length>22</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..22</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q27">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>accatttccatgtCtgagcacc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА, ОПРЕДЕЛЯЮЩЕГО ПРЕДРАСПОЛОЖЕННОСТЬ К ОНКОЛОГИЧЕСКИМ ЗАБОЛЕВАНИЯМ И ИНДИВИДУАЛЬНУЮ ЧУВСТВИТЕЛЬНОСТЬ К ФАРМАЦЕВТИЧЕСКИМ ПРЕПАРАТАМ С ИСПОЛЬЗОВАНИЕМ ОЛИГОНУКЛЕОТИДНОГО БИОЛОГИЧЕСКОГО МИКРОЧИПА (БИОЧИПА) | 2005 |
|
RU2303634C2 |
| ПРИМЕНЕНИЕ СПЕЦИФИЧЕСКИХ МАРКЕРОВ ГЕНА КОРИЧНЕВОЙ СРЕДНЕЙ ЖИЛКИ 3 (BROWN MIDRIB-3) У КУКУРУЗЫ ДЛЯ ИНТРОГРЕССИИ ПРИЗНАКОВ | 2011 |
|
RU2593958C2 |
| Способ поиска мутаций гена ATP7B для постановки диагноза болезни Вильсона (Вильсона-Коновалова) | 2023 |
|
RU2821573C1 |
| Способ генотипирования полиморфного локуса rs139794067 (G>T) гена MYL3 | 2025 |
|
RU2837876C1 |
| НОВЫЕ ПРАЙМЕРЫ ДЛЯ СКРИНИРОВАНИЯ ШИЗОФРЕНИИ И СПОСОБ ЕЕ СКРИНИРОВАНИЯ | 2002 |
|
RU2338788C2 |
| Панель последовательностей олигонуклеотидов для определения мутации Q61R гена NRAS в опухолевых образованиях щитовидной железы | 2019 |
|
RU2688189C1 |
| Количественный метод определения экспрессии аллелей GNAO1 здоровой формы и с мутацией c.607 G>A | 2021 |
|
RU2777663C1 |
| НАБОР ОЛИГОНУКЛЕОТИДНЫХ ПРАЙМЕРОВ И ЗОНДОВ ДЛЯ ГЕНОТИПИРОВАНИЯ ПОЛИМОРФНЫХ ЛОКУСОВ ДНК, АССОЦИИРОВАННЫХ С РИСКОМ РАЗВИТИЯ СПОРАДИЧЕСКОЙ ФОРМЫ БОЛЕЗНИ АЛЬЦГЕЙМЕРА В РОССИЙСКИХ ПОПУЛЯЦИЯХ | 2014 |
|
RU2600874C2 |
| Способ диагностики варианта SOPH c.5741G>A в гене NBAS | 2024 |
|
RU2819985C1 |
| СПОСОБ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА ДЛЯ ОПРЕДЕЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К ШИЗОФРЕНИИ И АЛКОГОЛИЗМУ | 2012 |
|
RU2565036C2 |


Изобретение относится к области медицины и молекулярной биологии. Описан способ выявления мутаций гена NPM1 А, В, D типа в тестируемом образце и определения МОБ, включающий: проведение ПЦР-РВ для первичного исследования на определение мутаций гена NPM1 А, В, D типа; постановку ПЦР-РВ для тестирования МОБ; определение МОБ в процентах, в случае образца, содержащего ДНК, по формуле подсчета аллельной нагрузки (АН) мутантного аллеля 100*АО/(1+АО), где АО - результат подсчета аллельного отношения, при этом расчет аллельного отношения (АО) производится по формуле 5/2ΔCt, где ΔCt - разница в циклах амплификации по мутантному и дикому аллелю, в случае образца, содержащего РНК, по формуле подсчета относительной экспрессии мутантного аллеля 100/2∆Ct, где ∆Ct - разница в циклах амплификации по мутантному и дикому аллелю, при этом для ПЦР-РВ используют набор реакционных смесей, включающий четыре смеси: смесь олигонуклеотидов NPM1 W с последовательностями SEQ ID NO: 1, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 А с последовательностями SEQ ID NO: 2, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 В с последовательностями SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 D с последовательностями SEQ ID NO: 4, SEQ ID NO: 6, SEQ ID NO: 5, предназначенные для амплификации исследуемой ДНК или РНК, являющиеся специфичными для гена NPM1 дикого типа и для каждого вида мутаций гена NPM1 А, В, D, после выявления мутации NPM1 типа А, В, D. Раскрыты соответствующие наборы. Изобретение позволяет проводить молекулярно-генетическую диагностику мутаций гена NPM1 высокочувствительным количественным методом на основе аллель-специфичной ПЦР в реальном времени. Аналитическая чувствительность данного метода составляет 10-4-10-5 и позволяет выявлять минимальную остаточную болезнь (МОБ) в биологическом материале (пунктате костного мозга и крови) пациентов с диагнозом острый миелоидный лейкоз. 3 н. и 29 з.п. ф-лы, 15 ил., 15 табл.
1. Способ выявления мутаций гена NPM1 А, В, D типа в тестируемом образце и определения МОБ, включающий:
- проведение ПЦР-РВ для первичного исследования на определение мутаций гена NPM1 А, В, D типа;
- постановку ПЦР-РВ для тестирования МОБ;
- определение МОБ в процентах, в случае образца, содержащего ДНК, по формуле подсчета аллельной нагрузки (АН) мутантного аллеля 100*АО/(1+АО), где АО - результат подсчета аллельного отношения, при этом расчет аллельного отношения (АО) производится по формуле 5/2ΔCt, где ΔCt - разница в циклах амплификации по мутантному и дикому аллелю, в случае образца, содержащего РНК, по формуле подсчета относительной экспрессии мутантного аллеля 100/2ΔCt, где ΔCt - разница в циклах амплификации по мутантному и дикому аллелю,
при этом для ПЦР-РВ используют набор реакционных смесей, включающий четыре смеси: смесь олигонуклеотидов NPM1 W с последовательностями SEQ ID NO: 1, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 А с последовательностями SEQ ID NO: 2, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 В с последовательностями SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 D с последовательностями SEQ ID NO: 4, SEQ ID NO: 6, SEQ ID NO: 5, предназначенные для амплификации исследуемой ДНК или РНК, являющиеся специфичными для гена NPM1 дикого типа и для каждого вида мутаций гена NPM1 А, В, D, после выявления мутации NPM1 типа А, В, D.
2. Способ по п. 1, где в качестве исследуемого образца используется ДНК или РНК, выделенная из клеток костного мозга или крови пациента.
3. Способ по п. 2, где использование в качестве образца ДНК позволяет исследовать архивный материал из замороженных клеток костного мозга или крови пациентов.
4. Способ по п. 1, где для выявления типа мутации NPM1 А, В, D для первичного исследования при подготовке и проведении ПЦР-РВ для каждого исследуемого образца, для отрицательного контрольного образца и для положительного контрольного образца подготавливаются по 8 пробирок, совместимых с прибором для ПЦР в реальном времени.
5. Способ по п. 4, где в качестве отрицательного контрольного образца используется образец ДНК здорового донора.
6. Способ по п. 4, где в качестве положительного контрольного образца используется образец ДНК с мутацией NPM1 типа А, типа В или типа D.
7. Способ по п. 4, где смесь для ПЦР приготавливается в пробирках 0,5 или 1,5 мл из расчета:
2,5 х (8N+1) мкл ПЦР-буфера
2,0 x (8N+1) мкл MgCL2
2,0 х (8N+1) мкл dNTP
0,5 x (8N+1) мкл TaqPol
13 х (8N+1) мкл деионизированной воды,
где N - количество исследуемых образцов с учетом образцов отрицательного и положительного контроля.
8. Способ по п. 7, где пробирки с ПЦР смесью встряхиваются в течение 3-5 с и центрифугируются в течение 1-3 с на микроцентрифуге/вортексе с центробежным ускорением 8000-14000g.
9. Способ по п. 4, отличающийся тем, что в каждую из 8-ми пробирок для ПЦР в реальном времени вносится по 2 мкл соответствующей смеси олигонуклеотидов: отдельно 2 пробирки к NPM1 W со смесью олигонуклеотидов с последовательностями SEQ ID NO: 1, SEQ ID NO: 5, SEQ ID NO: 6, отдельно 2 пробирки к NPM1 A со смесью олигонуклеотидов с последовательностями SEQ ID NO: 2, SEQ ID NO: 5, SEQ ID NO: 6, отдельно 2 пробирки к NPM1 B со смесью олигонуклеотидов с последовательностями SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, отдельно 2 пробирки к NPM1 D со смесью олигонуклеотидов с последовательностями SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6.
10. Способ по п. 4, где в каждую пробирку из 8-ми пробирок добавляется смесь для ПЦР по 20 мкл и по 3 мкл ДНК или 3 мкл кДНК исследуемого контрольного образца в концентрации 20-80 нг/мкл.
11. Способ по п. 10, где ДНК предварительно разводят в концентрации 100-400 нг/мкл до объема 5 мкл ДНК и 20 мкл деионизированной Н2О, а кДНК предварительно разводят до объема 5 мкл кДНК и 20 мкл деионизированной Н2О.
12. Способ по п. 10, где осуществляется центрифугирование пробирок в течение 1-3 секунд с центробежным ускорением 8000-14000g на микроцентрифуге.
13. Способ по п. 1, в котором для выявления типа мутации NPM1 А, В, D для первичного исследования при проведении ПЦР-РВ определяют тип мутации в биологическом материале на основании реакции амплификации с праймерами NPM1 A, NPM1 В и NPM1 D по численным значениям порогового цикла Ct на приборе и определяют по тому, какой подъем кривой флуоресценции ПЦР-РВ начался раньше.
14. Способ по п. 1, где при выявлении типа мутации NPM1 А, В, D осуществляют подсчет аллельной нагрузки мутантного аллеля для ДНК или относительной экспрессии мутантного аллеля для РНК.
15. Способ по п. 13, где по разнице в циклах амплификации Ct между праймером NPM1 W и праймером NPM1 A, NPM1 В или NPM1 D определяют аллельную нагрузку мутантного аллеля для ДНК или относительную экспрессию мутантного аллеля для РНК.
16. Способ по п. 1, где ПЦР РВ проводят с соблюдением режимов: денатурация 95° 5 мин, затем 50 циклов амплификации, включающих: денатурацию при 95° - 30 с; отжиг при 65° -30 с; синтез 72° - 20 с.
17. Способ по п. 1, где оценку МОБ проводят после 2 курса индукции, перед поддерживающей терапией, по окончании терапии или перед алло-ТГСК, каждые 3 месяца после окончания терапии и также в любые другие точки терапии и сроки по показаниям.
18. Способ по п. 1, где для определения МОБ для каждого исследуемого образца, для отрицательного контрольного образца и для положительного контрольного образца подготавливается 6 пробирок, совместимых с прибором для ПЦР в реальном времени.
19. Способ по п. 18, где в качестве отрицательных контролей используется ДНК или кДНК здоровых доноров, а в качестве положительного контроля положительный образец с мутацией NPM1 типа А, или типа В, или типа D.
20. Способ по п. 1, где смесь для ПЦР-РВ приготавливается в пробирках 0,5 или 1,5 мл из расчета: 2,5 х (6N+1) мкл ПЦР-буфера; 2,0 х (6N+1) мкл MgCL2; 2,0 х (6N+1) мкл dNTP; 2,0 х (6N+1) мкл смесь олигонуклеотидов 0,5 х (6N+1), мкл TaqPol, 13 х (6N+1) мкл деионизированной воды, где N - количество исследуемых образцов с учетом образцов отрицательного и положительного контроля.
21. Способ по п. 20, где пробирки со смесью встряхивают в течение 3-5 с на вортексе и центрифугируют в течение 1-3 с на микроцентрифуге с центробежным ускорением 8000-14000g.
22. Способ по пп. 18 и 20, отличающийся тем, что в каждую из 6-ти пробирок для ПЦР в реальном времени вносится по 2 мкл соответствующей смеси олигонуклеотидов: отдельно 3 пробирки для NPM1 W со смесью олигонуклеотидов с последовательностями SEQ ID NO: 1, SEQ ID NO: 5, SEQ ID NO: 6, отдельно 3 пробирки со смесью олигонуклеотидов к NPM1 А с последовательностями SEQ ID NO: 2, SEQ ID NO: 5, SEQ ID NO: 6, или со смесью олигонуклеотидов к NPM1 В с последовательностями SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, или со смесью олигонуклеотидов к NPM1 D с последовательностями SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6.
23. Способ пo п. 18, где в пробирки вносится по 20 мкл смеси и в каждую пробирку из 6-ти пробирок добавляется по 3 мкл ДНК в концентрации 200-300 нг в мкл или по 3 мкл кДНК исследуемого или контрольного образца.
24. Способ по п. 1, где при амплификации количество ДНК в одной реакции должно составлять более 500 нг, а количество кДНК должно превышать 10000 копий ABL1.
25. Способ по п. 23, где центрифугирование пробирки осуществляют в течение 1-3 с на микроцентрифуге с центробежным ускорением 8000-14000g.
26. Способ по п. 23, где ПЦР реакция проводится с соблюдением следующих температурных режимов: денатурация 95° - 5 мин; затем 50 циклов амплификации, включающих: денатурацию при 95° - 30 с; отжиг при 65° -30 с; синтез 72° - 20 с.
27. Набор реакционных смесей, предназначенных для амплификации исследуемой ДНК или РНК, являющихся специфичными для каждого вида мутаций гена NPM1 А, В, D, включающий: смесь олигонуклеотидов NPM1 W, предназначенную для определения клеток без мутации, с последовательностями SEQ ID NO: 1, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 А, предназначенную для определения клеток с мутацией типа А, с последовательностями SEQ ID NO: 2, SEQ ID NO: 6, SEQ ID NO: 5; смесь олигонуклеотидов NPM1 В, предназначенную для определения клеток с мутацией типа В, с последовательностями SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 5 и смесь олигонуклеотидов NPM1 D, предназначенную для определения клеток с мутацией типа D, с последовательностями SEQ ID NO: 4, SEQ ID NO: 6, SEQ ID NO: 5.
28. Набор no п. 27, где смесь NPM1 W, предназначенная для определения клеток без мутации, состоит из прямого праймера SEQ ID NO: 1 с конечной концентрацией 5 пкмоль в мкл, обратного праймера SEQ ID NO: 6 с конечной концентрацией 5 пкмоль в мкл, TaqMan зонда, SEQ ID NO: 5, меченной FAM и BHQ1, с конечной концентрацией 3,5 пкмоль в мкл.
29. Набор по п. 27, где смесь NPM1 А, предназначенная для определения клеток с мутацией А, состоит из прямого праймера SEQ ID NO: 2 с конечной концентрацией 5 пкмоль в мкл, обратного праймера SEQ ID NO: 6 с конечной концентрацией 5 пкмоль в мкл, TaqMan зонда, SEQ ID NO: 5, меченной FAM и BHQ1, с конечной концентрацией 3,5 пкмоль в мкл.
30. Набор по п. 27, где смесь NPM1 В, предназначенная для определения клеток с мутацией В, состоит из прямого праймера SEQ ID NO: 3 с конечной концентрацией 5 пкмоль в мкл, обратного праймера SEQ ID NO: 6 с конечной концентрацией 5 пкмоль в мкл, TaqMan зонда, SEQ ID NO: 5, меченной FAM и BHQ1, с конечной концентрацией 3,5 пкмоль в мкл.
31. Набор по п. 27, где смесь NPM1 D, предназначенная для определения клеток с мутацией D, состоит из прямого праймера SEQ ID NO: 4 с конечной концентрацией 5 пкмоль в мкл, обратного праймера SEQ ID NO: 6 с конечной концентрацией 5 пкмоль в мкл, TaqMan зонда, SEQ ID NO: 5, меченной FAM и BHQ1, с конечной концентрацией 3,5 пкмоль в мкл.
32. Набор олигонуклеотидов для амплификации гена NPM1 дикого типа и с мутациями типа А, В, D, включающий следующие олигонуклеотиды:
- прямой праймер к последовательности ДНК Homo sapiens дикого типа, SEQ ID NO: 1, состоящий из 22 нуклеотидов и содержащий в 19 и 21 положении LNA-модифицированный нуклеотид;
- прямой праймер к последовательности ДНК Homo sapiens мутантного типа A, SEQ ID NО: 2, состоящий из 23 нуклеотидов и содержащий в 16 и 20 положении LNA- модифицированный нуклеотид;
- прямой праймер к последовательности ДНК Homo sapiens мутантного типа В, SEQ ID NO: 3, состоящий из 23 нуклеотидов и содержащий в 17 и 20 положении LNA-модифицированный нуклеотид;
- прямой праймер к последовательности ДНК Homo sapiens мутантного типа D, SEQ ID NO: 4, состоящий из 23 нуклеотидов и содержащий в 20 положении LNA-модифицированный нуклеотид;
- TaqMan зонд к последовательности ДНК Homo sapiens, SEQ ID NO: 5, состоящий из 28 нуклеотидов и содержащий на 3' конце BHQ1, а на 5' конце FAM;
- обратный праймер к последовательности ДНК Homo sapiens, SEQ ID NO: 6, состоящий из 22 нуклеотидов.
| Машина для нанизывания табачных листьев | 1930 |
|
SU35033A1 |
| WO 2018096351 A1, 31.05.2018 | |||
| CN 110885879 A, 17.03.2020. | |||
Авторы
Даты
2024-11-21—Публикация
2023-09-25—Подача