Изобретение относится к области ветеринарии, в частности к средствам для профилактики колибактериоза и других желудочно-кишечных заболеваний сельскохозяйственных животных и птицы.
Бактериальные инфекции в животноводческих и птицеводческих хозяйствах России ежегодно регистрируются у 20-50% поголовья. Согласно многочисленным исследованиям, распространенность колибактериоза колеблется в широких пределах, а связанная с ним смертность животных, по приблизительным оценкам, составляет от 20 до 70% (Мотузко С.Н. Возрастные особенности амилолитической активности желудочно-кишечного тракта у коров. Ученые записки УО ВГАВМ. 2015, 51(1): 84-87;  М. et al. Diversity of multi-drug resistant avian pathogenic Escherichia coli (APEC) causing outbreaks of colibacillosis in broilers during 2012 in Spain. PLoS One. 2015, 10(11): e0143191; Bashahun G.M., Amina A. Colibacillosis in calves: A review of literature. Journal of Animal Science and Veterinary Medicine Volume. 2017, 2(3): 62-71. doi.org/10.31248/JASVM2017.041; Barros M.M. et al. Swine Colibacillosis: Global Epidemiologic and Antimicrobial Scenario. Antibiotics. 2023, 12(4):682. doi.org/10.3390/antibiotics12040682). Наиболее значимые в эпизоотическом плане представители энтерогеморрагических и энтеротоксигенных штаммов Е. coli различных серогрупп, в том числе O8, O15, О20, О101, О115, O149, O157 (Ishimaru K. et al. Escherichia coli O8:H8 Carrying a Novel Variant of the Heat-Labile Enterotoxin LT2 Gene Caused Outbreaks of Diarrhea. Open Forum Infect Dis. 2020, 7(1): ofaa021. doi: 10.1093/ofid/ofaa021; Frydendahl K. Prevalence of serogroups and virulence genes in Escherichia coli associated with postweaning diarrhoea and edema disease in pigs and a comparison of diagnostic approaches. Vet Microbiol. 2002, 85(2): 169-182. doi: 10.1016/s0378-1135(01)00504-1; Veilleux S., Dubreuil D.J. Presence of Escherichia coli carrying the EAST1 toxin gene in farm animals. Veterinary Research. 2006, 37(1), pp. 3-13.10.1051/vetres:2005045.hal-00903013).
М. et al. Diversity of multi-drug resistant avian pathogenic Escherichia coli (APEC) causing outbreaks of colibacillosis in broilers during 2012 in Spain. PLoS One. 2015, 10(11): e0143191; Bashahun G.M., Amina A. Colibacillosis in calves: A review of literature. Journal of Animal Science and Veterinary Medicine Volume. 2017, 2(3): 62-71. doi.org/10.31248/JASVM2017.041; Barros M.M. et al. Swine Colibacillosis: Global Epidemiologic and Antimicrobial Scenario. Antibiotics. 2023, 12(4):682. doi.org/10.3390/antibiotics12040682). Наиболее значимые в эпизоотическом плане представители энтерогеморрагических и энтеротоксигенных штаммов Е. coli различных серогрупп, в том числе O8, O15, О20, О101, О115, O149, O157 (Ishimaru K. et al. Escherichia coli O8:H8 Carrying a Novel Variant of the Heat-Labile Enterotoxin LT2 Gene Caused Outbreaks of Diarrhea. Open Forum Infect Dis. 2020, 7(1): ofaa021. doi: 10.1093/ofid/ofaa021; Frydendahl K. Prevalence of serogroups and virulence genes in Escherichia coli associated with postweaning diarrhoea and edema disease in pigs and a comparison of diagnostic approaches. Vet Microbiol. 2002, 85(2): 169-182. doi: 10.1016/s0378-1135(01)00504-1; Veilleux S., Dubreuil D.J. Presence of Escherichia coli carrying the EAST1 toxin gene in farm animals. Veterinary Research. 2006, 37(1), pp. 3-13.10.1051/vetres:2005045.hal-00903013).
Распространение заболеваний желудочно-кишечного тракта (ЖКТ), и, в частности, колибактериоза на животноводческих и птицеводческих комплексах зависит от многих факторов: наличия источника возбудителя инфекции, восприимчивости животных, а также от эффективности проводимых профилактических мероприятий (Овод А.С., Ирский А.Г., Сидоренко Н.М. Система профилактических мероприятий и контроль за их выполнением при бактериальных и вирусных заболеваниях телят, 2001: 19). Специфическая профилактика животных осуществляется путем вакцинации поголовья препаратами, имеющими в своем составе эшерихиозные антигены факторов адгезии и энтеротоксинов ограниченного ряда. При этом, показано, что О-серотипы применяемых вакцинных штаммов Е. coli встречаются у полевых изолятов с частотой от 30,3 до 55,2%, а у заболевших и павших телят отмечался рост числа изолятов, несущих антигены, отсутствующие в коммерческих вакцинах (Ломако Ю.В., Андросик Н.Н. Антигенная структура изолятов кишечной палочки, выделяемых в Республике Беларусь при колибактериозе новорожденных телят.Известия Академии аграрных наук Республики Беларусь. 2002, 2: 70-72). Еще одним крайне важным аспектом профилактики, а также лечения заболеваний ЖКТ и колибактериоза на предприятиях животноводства и птицеводства считается применение пробиотических препаратов, имеющих различную природу и состав, и обеспечивающих позитивное воздействие на микробиоту животных (Markowia P., Slizewska К. The role of probiotics, prebiotics and synbiotics in animal nutrition. Gut Pathog. 2018, 10:21). Можно полагать, что для профилактики колибактериоза в качестве дополнительного этапа/шага в регионах целесообразно использовать пероральный краткосрочный прием штаммов микроорганизмов, относящихся к серогруппам, представители которых постоянно циркулируют и вызывают заболевания животных в регионе.
Наиболее известен штамм Escherichia coli М-17, на основе которого создан пробиотический препарат «Колибактерин», содержащий лиофилизированные живые бактерии (Авторское свидетельство №189128 опубл. 17.11.1966), который секционирован на основе штаммаЕ. coli O6:К5:Н1 Nissle 1917 (Schultz М., Burton J.P. Chapter 5 - Escherichia coli Nissle 1917, Editor(s): Floch M.H., Ringel Y., Walker W.A. The Microbiota in Gastrointestinal Pathophysiology. Academic Press. 2017, pp.59-69). Штамм содержит введенную неконъюгативную, немо бил изуемую плазмиду pColap с генами продукции колицина Е1 и устойчивости к ампициллину. Лечебное действие обусловлено антагонистической активностью Е. coli в отношении патогенных и условно-патогенных микроорганизмов. Недостатком штамма является то, что он создан на основе штамма М-17, выделенным от человека, то есть имеет невысокий уровень колонизационной активности в отношении животных. Штамм имеет антигены комменсальной группы. Кроме того, штамм не в достаточной степени адаптирован к изменившимся современным условиям окружающей среды (рост антибиотикорезистентности и толерантности к бактериоцинам у бактерий возбудителей кишечных инфекций сельскохозяйственной птицы), а именно, данный штамм теряет свои антагонистические свойства и обладает выраженной чувствительностью к колицинам.
Известен также штамм природный штамм ЛЭГМ N18 (ВКПМ В-6240), предложенный для производства колибактерина - средства, способствующего восстановлению нормального биоценоза кишечника (Пшеничное Р.А., Вотяков В.Н., Колотов В.М. Патент РФ №2065875 С1. 1996.). Штамм ЛЭГМ N18 отличается высокими репродуктивными свойствами, высокой антагонистической активностью в отношении болезнетворных шигелл Флекснера и Зонне, повышенной резистентностью к большинству колицинов и антибиотиков, апатогенен, нетоксичен, обладает повышенной устойчивостью к действию активного хлора и УФ облучения. Недостатком штамма является то, что он выделен от человека, то есть имеет невысокий уровень колонизационной активности в отношении животных. Штамм имеет антигены комменсальной группы.
Наиболее близким к данному изобретению может быть препарат, созданный на основе штаммов Е. coli, выделенных от животных (Е. coli 271 АТСС 202020, Е. coli 786 АТСС 202018, Е. coli 797 АТСС 202019) (US 5965128 A, Doyle et al., 12.10.1999; WO 99/08532 A1, 25.02.1999). Штаммы способны снижать или уничтожать инокулированную предварительно в кишечник телят Е. coli 0157:Н7. Недостатком штаммов, входящих в препарат, является также их серогрупповая принадлежность штаммы отнесены к комменсальным серогруппам.
В связи с этим изучение лечебной эффективности пробиотиков в ветеринарной практике является актуальным и своевременным. Арсенал штаммов, используемых для создания препаратов при лечении и профилактике бактериальных кишечных инфекций, может быть значительно расширен за счет новых культур, адаптированных к имеющимся условиям, выделенных от здоровых животных, с высокой колонизационной и антагонистической активностью.
Задачей изобретения является получение штамма с более высокими качественными и количественными действующими характеристиками по сравнению со штаммом М-17, а именно, обладающего более высокой колонизационной способностью и антагонистической активностью против возбудителей колибактериоза животных, и более широким спектром протективной активности в отношении энтеропатогенных эшерихий.
Данная задача решается путем выделения и характеристики нового штамма-продуцента бактериоцинов, выделенного от здорового перепела Е. coli Q5, что повышает шанс «прижиться» бактериям в кишечнике животных и птицы. Кроме того, штамм является представителем энтеропатогенной серогруппы эшерихий, но не имеет энтеротоксинов, что может приводить к антигенной стимуляции и формированию адаптивного иммунитета в отношении представителей энтеропатогенных Е. coli.
Технический результат, обеспечивающий решение задачи, заключается в получении штамма с более выраженным и расширенным спектром антагонистической активности, более высоким уровнем колонизационной способности, принадлежащего к группе энтеротоксигенных эшерихий (ЕТЕС), но не продуцирующего токсины, что создает предпосылки для создания препарата, эффективного для профилактики и лечения колибактериоза и других заболеваний сельскохозяйственных животных и птицы.
Заявляемый штамм бактерий Е. coli Q5 депонирован во «Всероссийской коллекции микроорганизмов» (ВКМ), и имеет регистрационный символ ВКМ В-3706Д как штамм с антагонистической активностью в отношении патогенных и условно-патогенных микроорганизмов iv vitro и защитным действием in vivo. Штамм выделен из фекалий здорового перепела Манчьжурской породы (Coturnix coturnix) частного фермерского хозяйства Пермского края, Россия.
Заявляемое изобретение полезно для предотвращения инфицирования, либо снижения или элиминации энтеропатогенных эшерихий у животных и/или птицы путем введения эффективного количества штаммов или комбинации потенциально пробиотических штаммов бактерий.
Изобретение поясняется иллюстрирующими материалами:
На Фиг. 1. Представлена гистоархитектоника кишечника крыс, инфицированных Е. coli С55: А - интактные животные, Б - инфицированные животные, В - животные, предварительно получившие Е. coli Q5 в течение 5 дней в дозе 5×108 КОЕ/голову. Примечание. Черной стрелкой указаны участки десквамации эпителия.
Изобретение поясняется следующими примерами.
Пример 1. Характеристика комменсального генотипа штамма Е. coli Q5.
Полный геном штамма Е. coli Q5 был получен методом секвенирования длинными прочтениями с использованием технологии Oxford Nanopore (MinION, проточная ячейка R10.4.1). Функциональная аннотация генома Е. coli Q5 подтвердила отсутствие генов энтеротоксинов (stx1/2, est, elt, ehxa и пр.), гемолизинов, капсул, вирулент-ассоциированных фимбрий (pap, sfa, afa/dra), мобильных генов устойчивости к антибиотикам. Штамм Е. coli Q5 содержал хромосомные геномные локусы, кодирующие фимбрий типа 1 (гены fimB, fimE, fimAICDFGH), общие пили Е. coli (гены ecpRABCDE), керли (гены csgDEFG и csgBAC) и адгезии FdeC (ген fdeC). Геном Е. coli Q5 содержал три полных набора функциональных генов, необходимых для синтеза колицинов Ia и Ib (расположены на плазмиде pQ501) и колицина Y (расположены на плазмиде pQ504). Биосинтетические кластеры синтеза энтеробактина и иерсиниабактина были обнаружены в хромосоме штамма Е. coli Q5. Согласно результатам мультилокусного сиквенс-типирования штамм Е. coli Q5 принадлежал к серогруппе O8.
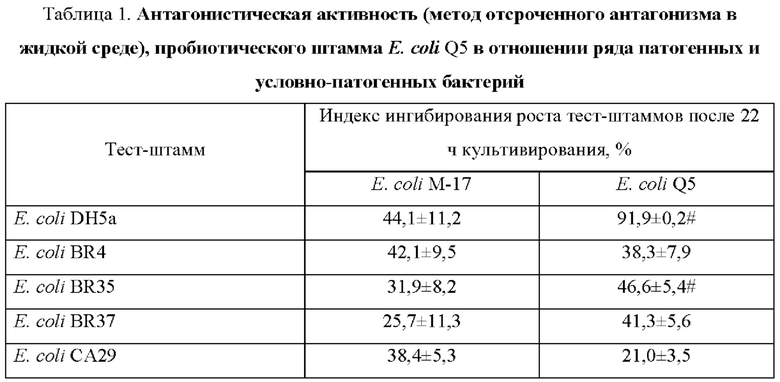
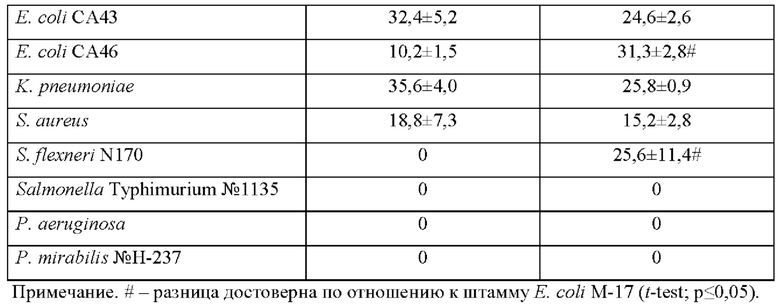
Пример 2. Антагонистическая активность in vtro штамма Е. coli Q5. При изучении антагонистической активности использовали методику отсроченного антагонизма в жидкой питательной среде. В качестве патогенных использовали полевые и референтные культуры: Е. coli - возбудители колибактериоза птиц (Е. coli BR4, Е. coli BR35, Е. coli BR37J, диареегенные Е. coli (Е. coli СА29, Е. coli СА43, Е. coli СА46), Klebsiella pneumoniae АТСС®700603, Staphylococcus aureus ATCC®25923, Shigella flexneri, Salmonella enterica serotype Typhimurium (далее Salmonella Typhimurium), P. aeruginosa ATCC®27853, Proteus mirabilis. О наличии и степени антагонистического действия судили по снижению оптической плотности в присутствии супернатантов бактерий в сравнении с контролем - ростом культуры без добавления супернатантов. Рассчитывали индекс ингибирования (ИИ) для 22 ч культивирования. Антагонистическая активность штамма в отношении ряда представителей условно-патогенных и патогенных микроорганизмов представлена в таблице 1.
Супернатанты оказывали антагонистическое действие на патогенные для птиц E. coli (BR4, BR35, BR37), диареегенные Е. coli (СА29, СА43, СА46, O157), K. pneumoniae, и, в меньшей степени, на S. flexneri и S. aureus. После 22 ч культивирования супернатанты Е. coli Q5 ингибировали рост птичьей патогенной Е. coli BR35 более эффективно, чем Е. coli М-17 (р=0,03), а также энтеротоксигенного штамма Е. coli СА46 (p=0,02) (таблица 1). Следует отметить, что супернатанты Е. coli Q5 ингибировали рост S. flexneri на 25,6%.
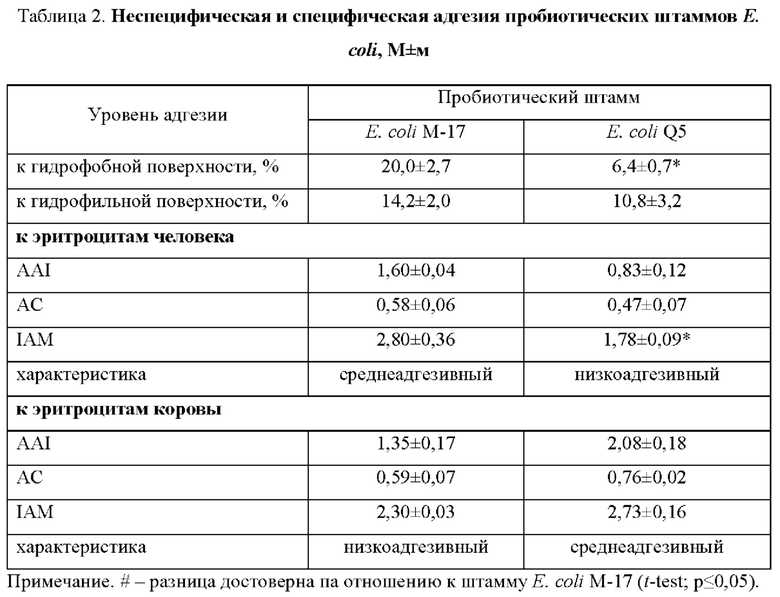
Пример 3. Изучение специфической и неспецифической адгезии штамма Е. coli Q5. Изучение бактериальной адгезии к эритроцитам проводили по методу В.И. Бриллиса и соавт. в эппендорфах (Брилис В.И., Брилене Т.А., Ленцнер Х.П. Лабораторное дело. 1986. №4. С. 210-212). Для учета адгезивных свойств бактерий использовали эритроциты человека О (I) группы крови Rh (+) и животных (коровы). Эритроциты отмывали фосфатным буфером, затем разводили до концентрации 108 эритроцитов в мл. Суспензию бактерий готовили в концентрации 108 клеток/мл, смешивали с эритроцитарной массой в соотношении 1:1 и инкубировали при 37°C с перемешиванием 120 об/мин в течение 30 мин. Мазки крови готовили и окрашивали 0,5% раствором генцианвиолета (Lenchenko Е. et al. Morphological and adhesive properties of Klebsiella pneumoniae biofilms. Veterinary World. 2020, 13:197-200. doi: 10.14202/vetworld.2020.197-200). При оптической микроскопии препаратов учитывали три следующих показателя: 1 - средний индекс адгезии (AAI), представляющий собой среднее количество микроорганизмов, прикрепленных к поверхности одного эритроцита; 2 - коэффициент адгезии (АС), процент эритроцитов, имеющих на поверхности бактерии; 3 - индекс адгезии микроорганизмов (IAM), известный как соотношение AAI и АС. Подсчет проводили на 100 клетках, просматривая все предметное стекло. В зависимости от значений IAM микроорганизмы считались: неадгезивными (IAM<1,75), низкоадгезивными (IAM - 1,76-2,49), среднеадгезивными (IAM - 2,50-3,99), высокоадгезивными (IAM>4,0).
Оценка адгезивных свойств исследуемых бактерий показала, что уровень не специфической адгезии Е. coli Q5 к гидрофильной поверхности был сопоставим с Е. coli М-17. При этом штамм Е. coli Q5 был низкоадгезивным к эритроцитам человека и среднеадгезивным к эритроцитам животных, тогда как Е. coli М-17, напротив, имел средний уровень адгезии к эритроцитам человека и низкий к эритроцитам животных.
Пример 4. Безвредность штамма Е. coli Q5. Оценку безвредности (токсичности) препарата для животных проводили в соответствии с ГОСТ Р 54063-2010 «Средства лекарственные для животных. Методы определения безвредности» (https://docs.cntd.ru/document/1200084458). Эксперименты выполняли в условиях вивария на крысах линии Wistar в период 10 дней. Животные были разделенных на три группы (контрольная и две опытные) по 6 особей в каждой. Опытным животным препарат вводили перорально в дозе 5×108 и 5×1010 клеток//голову. Условия содержания (плотность посадки, фронт кормления и поения, температура, влажность, освещенность) были в пределах норм, рекомендуемых ВНИТИП. Общий уход за животными осуществлялся в соответствии с ГОСТ №33215-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур» (https://docs.cntd.ru/document/1200127789). В период проведения испытания вели ежедневное наблюдение.
Выживаемость крыс при 5-дневном пероральном введении в дозах 5×108 и 5×1010 клеток//голову для штамма Е. coli Q5 составила 100%. Симптомов заболеваний, отклонений в поведении не было, животные были активны, хорошо потребляли корм и воду. При скармливании Е. coli Q5 в дозе 5×108 КОЕ//голову средняя живая масса животных превышала контрольную на 2,7%. Введение бактерий в дозе 5×1010 не оказывало токсических эффектов (была безвредна). При изучении гематологических и биохимических показателей отклонений от норы не выявлено. При вскрытии животных патологических изменений в органах не обнаружено.
Пример 5. Защитная активность пробиотика Е. coli Q5 in vivo. Протективная активность потенциально пробиотического штамма оценивалась по изменениям в составе микробиома кишечника крыс, а также по влиянию на клетки кишечного эпителия в экспериментальной инфекции. Предварительное введение штамма Е. coli Q5 на протяжении 5 дней в дозе 5×108 КОЕ//голову оказывало профилактическое действие, защищая крыс от колонизации и патогенного действия Е. coli С55, введенного животным однократно в дозе 5×108 КОЕ//голову. В группе без предварительного введения потенциально пробиотического штамма (инфекционный контроль) после инфицирования токсигенным штаммом Е. coli С55 в кишечной микробиоте крыс появилась гемолитическая кишечная палочка (Е. coli hem+). У крыс, которые предварительно получали Е. coli Q5, количество Е. coli hem+было существенно ниже по сравнению с группой крыс инфекционного контроля (р=0,04). Важно подчеркнуть, что при применении Е. coli Q5 не происходило значимых сдвигов в составе нативной микробиоты: сохранялся уровень полезных представителей, таких как Bifidobacterium, Lactobacillus и Enterococcus. 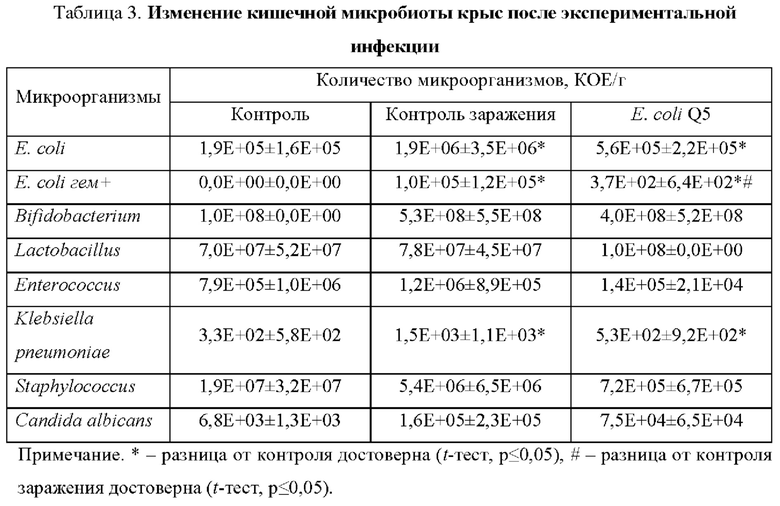
В крысиной модели показано, что предварительное пероральное введение Е. coli Q5 эффективно предотвращало разрушение кишечного барьера, блокирующего доступ патогенных микроорганизмов и их метаболитов к субэпителиальным клеткам (Фиг. 1).
| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм бактерий Escherichia coli С41для получения пробиотического препарата для профилактики колибактериоза сельскохозяйственных животных | 2023 |
|
RU2807738C1 |
| ПРОБИОТИК ДЛЯ ПРОФИЛАКТИКИ И КОРРЕКЦИИ ЖЕЛУДОЧНО-КИШЕЧНЫХ ЗАБОЛЕВАНИЙ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПТИЦЫ | 2022 |
|
RU2785174C1 |
| Пробиотический штамм Lactobacillus gasseri и его композиция с лактоферрином для профилактики диареи, некротизирующего энтероколита и сепсиса, вызываемых штаммами Escherichia coli у преждевременно рожденных детей | 2016 |
|
RU2641258C1 |
| ШТАММ БАКТЕРИЙ Escherichia coli M 17 fimH::kan/p Colap, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПРОБИОТИЧЕСКОГО ПРЕПАРАТА | 1998 |
|
RU2144953C1 |
| ШТАММ БАКТЕРИЙ ESCHERICHIA COLI, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРОИЗВОДСТВА ПРОБИОТИКА МИКРОЦИКОЛА В5/98 | 2003 |
|
RU2268297C2 |
| ШТАММ БАКТЕРИЙ Escherichia coli M 17/p Colap, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПРОБИОТИЧЕСКОГО ПРЕПАРАТА | 1998 |
|
RU2144954C1 |
| Способ оценки патотипа и эпидемической/эпизоотической значимости штаммов Escherichia coli, выделенных в условиях сельскохозяйственного предприятия | 2021 |
|
RU2779827C1 |
| Способ получения кормовой композиции с функциональными свойствами для птицеводства | 2023 |
|
RU2819889C1 |
| Штамм Lactobacillus salivarius ВКШМ-Г-08ПД | 2024 |
|
RU2822455C1 |
| Штамм бактерий Lactobacillus plantarum ВКШМ-Г-06ПД | 2024 |
|
RU2827608C1 |
Изобретение относится к области ветеринарии, в частности к средствам для профилактики и коррекции колибактериоза и других желудочно-кишечных заболеваний сельскохозяйственных животных и птицы. Штамм бактерий Е. coli Q5 депонирован во «Всероссийской коллекции микроорганизмов» (ВКМ) и имеет регистрационный символ ВКМ В-3706Д, как штамм с антагонистической активностью в отношении патогенных и условно-патогенных микроорганизмов in vitro и защитным действием in vivo. Штамм выделен из фекалий здоровой птицы, может быть использован для изготовления бактериальных препаратов для профилактики колибактериозов и других бактериальных инфекций сельскохозяйственных животных. Достигаемый изобретением технический результат заключается в получении штамма с более выраженным и расширенным спектром антагонистической активности, более высоким уровнем колонизационной способности, принадлежащего к группе энтеротоксигенных эшерихий (ЕТЕС), но не продуцирующего энтеротоксины, что создает предпосылки для создания препарата, эффективного для профилактики и лечения колибактериоза и других заболеваний сельскохозяйственных животных и птицы. 5 пр., 3 табл., 1 ил.
Штамм бактерий Escherichia coli Q5 под регистрационным номером ВКМ В-3706Д, обладающий антагонистической активностью в отношении патогенных и условно-патогенных микроорганизмов in vitro и защитным действием in vivo.
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| ШТАММ БАКТЕРИЙ ESCHERICHIA COLI, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ КОЛИБАКТЕРИНА | 1993 |
|
RU2065875C1 |
| МОТУЗКО С.Н | |||
| Возрастные особенности амилолитической активности желудочно-кишечного тракта у коров | |||
| Учёные записки УО ВГАВМ, 2015, 51(1): 84-87. | |||
Авторы
Даты
2023-11-08—Публикация
2023-07-07—Подача