Изобретение относится к медицине, а именно к кардиологии и может быть использовано в лечении хронической сердечной недостаточности (СН) у пациентов с желудочковыми тахиаритмиями (ЖТА) и имплантированным кардиовертером-дефибриллятором (ИКД).
Основной проблемой в лечении хронической СН является отсутствие и недостаточная информативность имеющихся прогностических показателей, которые позволили бы пациентам и врачам сформировать реалистичные ожидания относительно прогноза, выбора соответствующей терапии и метода наблюдения. Не хватает универсальных параметров или шкал, на основе которых можно было бы легко фиксировать момент ухудшения состояния больных с хронической СН. Следовательно, крайне важно определить факторы, которые были бы широко доступными, дешевыми и простыми в использовании. В качестве предикторов тяжести хронической СН предложено использовать снижение теста 6-минутной ходьбой, кардиопульмонального нагрузочного теста, увеличение концентрации биомаркеров (натрийуретический N-концевой мозговой пропептид, тропонин Т, галектин-3, С-реактивный белок). Некоторые из них очень перспективны, но необходимы дополнительные исследования для создания специальной панели, на основе которой оценивается тяжесть хронической СН. В настоящее время, несмотря на идентификацию многих маркеров неблагоприятных исходов, принятие клинических решений при хронической СН по-прежнему преимущественно основывается на нескольких основных параметрах, таких как функциональный класс (ФК) СН по классификации Нью-Йоркской ассоциации сердца (NYHA), фракция выброса левого желудочка, продолжительность и морфология комплекса QRS.
Оценка прогноза играет особую роль у пациентов с ЖТА и ИКД. Во-первых, предиктор тяжести хронической СН не только позволяет заранее выявить пациента группы высокого риска, но и позволяет контролировать и проводить индивидуальную профилактическую терапию. Во-вторых, выявление факторов, влияющих на неблагоприятный прогноз хронической СН, может помочь разработать новые целенаправленные (таргетные) методы лечения [1].
Предикторы тяжести хронической СН должны быть легко доступны, связаны с некоторыми терапевтическими и клиническими результатами [1]. В рекомендациях Европейского общества кардиологов по СН от 2016 г. названо более 70 предикторов у пациентов с хронической СН [2]. Также были предложены различные модели риска развития хронической СН такие как, GWTC-HF [3], ADHERE [4], OPTIMIZE-HF [5], калькулятор риска хронической СН MAGGIC [6], I-PRESERVE [7], Seattle Heart Failure [8], AHFI [9] и др. [1]. Однако ни один из вышеперечисленных факторов риска не является достаточным для прогнозирования тяжести хронической СН у пациентов с ЖТА и ИКД.
По данным исследования Zhao T-J. и соавт. был разработан способ комплексной оценки тяжести хронической СН, основанный на определении Д-димера, общего холестерина, высокочувствительного сердечного тропонина Т и сывороточного альбумина [10]. Недостатком данного способа является то, что комплексная оценка проводилась лишь по результатам лабораторных показателей, без использования инструментальных методов диагностики (эхокардиография). Ограничением данного исследования является то, что это ретроспективное когортное исследование, проведенное в одном центре. Также все данные были отобраны из одной относительно небольшой выборки пациентов.
Широко продемонстрирована роль натрийуретического мозгового пептида (BNP) и натрийуретического N-концевого мозгового пропептида (NT-proBNP) в диагностике и стратификации риска при хронической СН, и эти биомаркеры становятся новыми инструментами для скрининга населения и в качестве руководства для начало лечения пациентов с хронической СН. Однако даже в сочетании с тестом на натрийуретические пептиды частота ошибочной классификации СН остается на уровне 14-29% [11]. Более того, существует «серая зона» в BNP и NT-proBNP [12]. Мета-анализ [11], включающий 41 исследование, показал, что при диагностике хронической СН чувствительность BNP составила 93,5%, а специфичность - 52,9% при пороговом значении 100 пг/мл. Когда пороговое значение было увеличено до 500 пг/мл, чувствительность снизилась до 67,7%, а специфичность увеличилась до 89,8%. Для NT-proBNP чувствительность составила 90,4%, а специфичность - 38,2% при пороговом значении 300 пг/мл, в то время как чувствительность снизилась до 75,5%, а специфичность увеличилась до 72,9% при пороговом значении 1550 пг/мл. Соответственно при использовании данного способа диагностика хронической СН остается неопределенным, когда значения BNP или NT-proBNP находятся в серой зоне 100-500 пг/мл. Также недостатком данного способа является использование исключительно лабораторных показателей, без использования других методов диагностики хронической СН (например: эхокардиография).
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не обнаружено.
Задачей изобретения является разработка способа, повышающего точность прогноза риска развития III ФК хронической СН у пациентов с ЖТА и ИКД.
Поставленная задача решается проведением трансторакальной допплеровской эхокардиографии с оценкой систолического давления в правом желудочке (СДПЖ) и проведением забора венозной крови для определения скорости дыхания митохондрий в среде после израсходования аденозиндифосфата. Затем рассчитывают вероятность развития III ФК хронической СН по формуле. Формула рассчитывается с использованием показателей СДПЖ и скорости дыхания митохондрий в среде. Если прогностический коэффициент составляет более 0,43, то у пациента прогнозируют III ФК хронической СН.
Новым в предлагаемом изобретении является то, что определяют СДПЖ, отражающее систолическое давление легочной артерии, и скорость дыхания митохондрий в среде после израсходования аденозиндифосфата, отражающую функциональное состояние митохондрий, и определяют прогностическую вероятность развития III ФК хронической СН по формуле:
 (1)
(1)
где P – прогностическая вероятность,
е – основание натурального логарифма (е=2,7182818284),
-0,07197 – коэффициент постоянной,
-0,004575 – коэффициент переменной скорости дыхания митохондрий в среде после израсходования аденозиндифосфата,
х1 – числовое значение скорости дыхания митохондрий в среде после израсходования аденозиндифосфата,
0,01784 – коэффициент переменной систолического давления в правом желудочке,
х2 – числовое значение систолического давления в правом желудочке,
и при значении Р более 0,43 прогнозируют III ФК хронической СН у пациентов с ЖТА и ИКД.
Существенные признаки, характеризующие изобретение, проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не являющиеся очевидными для специалиста.
Идентичной совокупности признаков не обнаружено при изучении патентной и научно-медицинской литературы.
Данное изобретение может быть использовано в практическом здравоохранении для своевременной диагностики риска развития тяжести хронической СН, улучшения качества жизни пациентов, для снижения частоты госпитализации по поводу декомпенсации хронической СН.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость».
Изобретение будет понятно из следующего описания и предложенной к нему фигуры.
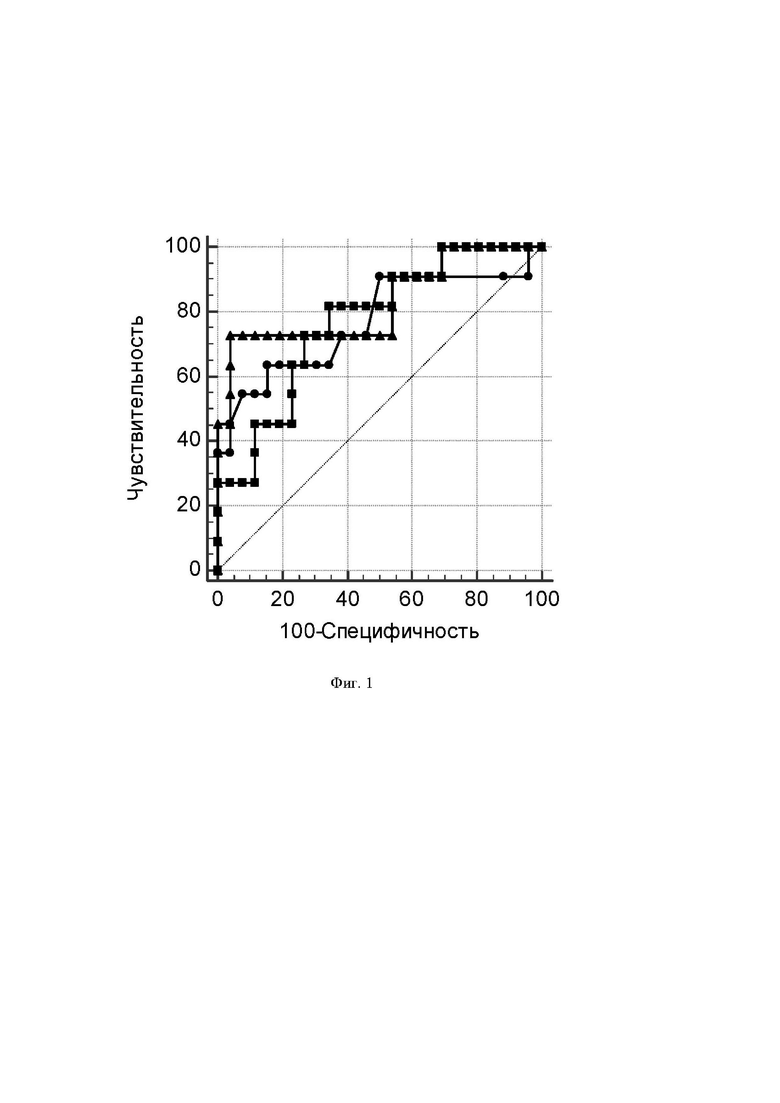
На Фиг. 1 изображены ROC-кривые скорости дыхания митохондрий в среде после израсходования аденозиндифосфата (линия с квадратами), СДПЖ (линия с кружками) и выявленной прогностической модели (линия с треугольниками) в определении III ФК хронической СН.
Способ осуществляется следующим образом.
Трансторакальную эхокардиографию проводят на ультразвуковом аппарате. Исследование проводят из стандартных эхокардиографических позиций с определением СДПЖ. Величину СДЖП выражали в мм рт. ст.
Скорость дыхания митохондрий в среде после израсходования аденозиндифосфата определяли следующим образом. У пациентов производили забор венозной крови (объем 9 мл) в вакутейнеры с этилендиаминтетрауксусной кислотой (ЭДТА). Осуществляли выделение фракции мононулеарных клеток периферической крови на градиенте плотности Histopaque-1077 (Sigma). Полученное «кольцо» мононуклеаров отмывали в фосфатно-солевом буфере (Sigma). Осадок клеток подвергали осмотическому лизису посредством внесения в сахарозную среду (0,25 М сахароза с ЭДТА) и последующего мягкого пипетирования для выхода митохондрий в раствор. Митохондрии изолировали дифференциальным центрифугированием в сахарозной среде [13]. Полученный осадок ресуспендировали в минимальном объеме 0,25 М сахарозы для дальнейшей работы.
Скорость дыхания митохондрий определяли в предварительно оксигенированных инкубационных средах (в мМ): сахароза – 250,0; KCI – 10,0; KH2PO4 – 5,0; MgCI2 – 1,25; HEPES – 5,0; пируват – 6,0; малат – 8,0, или сукцинат – 5,0; pH = 7,35-7,40. Исследования проводили в термостатируемой ячейке (объем 1 мл) при постоянном перемешивании магнитной мешалкой и температуре 25-27 оС. Концентрацию кислорода в инкубационной среде измеряли амперометрически с применением кларковского электрода, подключенного к анализатору жидкости. Скорость дыхания митохондрий рассчитывали в нМоль О2/мин/мг белка митохондрий. Сопряженность процессов окисления и фосфорилирования оценивали по коэффициенту дыхательного контроля, формула расчета которого V3/V4, где V3 – скорость потребления кислорода митохондриями в среде при наличии субстрата окисления – пируват-малатная смесь или сукцинат, и субстрата фосфорилирования – АДФ (200 мкМ); V4 – скорость потребления кислорода после исчерпания АДФ в среде инкубации [14].
Предлагаемый способ апробирован у 37 (100,0%) пациентов с ЖТА, ИКД и хронической СН I-III ФК согласно NYHA.
Трансторакальную эхокардиографию проводили с использованием ультразвукового аппарата Philips HD15 PureWave, Netherlands.
Статистический анализ результатов проводили с помощью пакета программ Statistica 10.0 и MedCalc 12.1.14.0. Для оценки нормальности распределения признака использовали критерий Шапиро-Уилка. Для оценки достоверности межгрупповых различий использовали непараметрический критерий Манна-Уитни для независимых выборок. Для сравнительной оценки информативности методов диагностики проводился однофакторный (с расчетом индекса Юдена) и многофакторный ROC-анализ. Информативность диагностического теста определяли путем оценки площади под кривой – Area Under Curve (AUC), а также сравнения показателей чувствительности и специфичности. Для построения модели прогнозирования использовали регрессионный анализ в виде бинарной логистической регрессии с расчетом отношения шансов (ОШ) и доверительного интервала (ДИ). При уровне значимости p меньше 0,05 считалось, что исследуемый показатель в сравниваемых группах имел статистически значимые различия.
За период наблюдения (6,0 [4,0; 17,0] месяцев) у 11 (29,7%) пациентов документирован III ФК хронической СН, они составили первую группу. У остальных 26 (70,3%) пациентов выявлен I и II ФК хронической СН, они составили вторую группу. Клиническая характеристика пациентов по группам представлена в таблице 1.
Таблица 1. Клиническая характеристика пациентов по группам.
(n=11)
(n=26)
Примечание: Me [Q1; Q3] – медиана [нижний квартиль; верхний квартиль], n – количество, V3.1 – скорость дыхания митохондрий в среде, где есть субстрат окисления (пируват + малат) и субстрат фосфорилирования (аденозиндифосфат (АДФ)), V3.2 – скорость дыхания митохондрий в среде, где есть субстрат окисления (сукцинат) и субстрат фосфорилирования (АДФ), V4.1 – скорость дыхания митохондрий в среде, где есть субстрат окисления (пируват + малат) и нет субстрата фосфорилирования (АДФ), V4.2 – скорость дыхания митохондрий в среде, где есть субстрат окисления (сукцинат) и нет субстрата фосфорилирования (АДФ), АРА II – антагонисты рецепторов ангиотензина II, БМ – белок митохондрий, ВСС – внезапная сердечная смерть, ГГП – гипогликемические препараты, ГМЛЖ – гипертрофия миокарда левого желудочка, ДК1 – коэффициент дыхательного контроля (отношение между V3.1 и V4.1), ДК2 – коэффициент дыхательного контроля (отношение между V3.2 и V4.2), иАПФ – ингибиторы ангиотензинпревращающего фермента, КА – коронарные артерии, нМоль – наномоль, СДПЖ – систолическое давление в правом желудочке, СКФ – скорость клубочковой фильтрации, ТШХ – тест шестиминутной ходьбы, ФВЛЖ – фракция выброса левого желудочка, ФК – функциональный класс, ФП – фибрилляция предсердий, ХСН – хроническая сердечная недостаточность.
По данным однофакторного ROC-анализа СДПЖ, V3.1, V3.2, V4.1 и V4.2 были статистическими значимыми прогностическими критериями III ФК хронической СН у пациентов с ЖТА и ИКД. Подробный ROC-анализ вышеперечисленных показателей представлен в таблице 2.
Таблица 2. Результаты ROC-анализа.
Примечание: 95% CI – 95% доверительный интервал, AUC – площадь под кривой, cut-off – точка отсечения, Sen – чувствительность, Spe – специфичность, V3.1 – скорость дыхания митохондрий в среде, где есть субстрат окисления (пируват + малат) и субстрат фосфорилирования (аденозиндифосфат (АДФ)), V3.2 – скорость дыхания митохондрий в среде, где есть субстрат окисления (сукцинат) и субстрат фосфорилирования (АДФ), V4.1 – скорость дыхания митохондрий в среде, где есть субстрат окисления (пируват + малат) и нет субстрата фосфорилирования (АДФ), V4.2 – скорость дыхания митохондрий в среде, где есть субстрат окисления (сукцинат) и нет субстрата фосфорилирования (АДФ), БМ – белок митохондрий, нМоль – наномоль, СДПЖ – систолическое давление в правом желудочке.
Многофакторная логистическая регрессия с включением таких факторов как возраст, индекс массы тела, скорость клубочковой фильтрации, наличие ишемической кардиомиопатии, длительность QRS комплекса, V3.1, V3.2, V4.1, V4.2, фракция выброса левого желудочка, конечно-диастолический и конечно-систолический объем левого желудочка показала, что только V4.1 (p=0,04) и СДПЖ (p=0,004) были независимыми предикторами III ФК хронической СН у пациентов с ЖТА и ИКД.
Используя коэффициенты регрессии выявленных показателей V4.1 и СДПЖ, было выведено уравнение для расчета прогностической вероятности III ФК хронической СН у пациентов с ЖТА и ИКД:
 (1)
(1)
где P – прогностическая вероятность,
е – основание натурального логарифма (е=2,7182818284),
-0,07197 – коэффициент постоянной,
-0,004575 – коэффициент переменной скорости дыхания митохондрий в среде после израсходования аденозиндифосфата,
х1 – числовое значение скорости дыхания митохондрий в среде после израсходования аденозиндифосфата,
0,01784 – коэффициент переменной систолического давления в правом желудочке,
х2 – числовое значение систолического давления в правом желудочке.
При значении прогностической вероятности более 0,43 прогнозируют III ФК хронической СН у пациентов с ЖТА и ИКД (р=0,0002). При использовании полученной при многофакторном регрессионном анализе модели определения прогноза III ФК хронической СН у пациентов с ЖТА и ИКД, площадь под ROC-кривой составила 0,829, чувствительность – 72,73, специфичность – 96,15 (оранжевая линия с зелеными квадратами на Фиг. 1).
Таким образом, способ прогнозирования III ФК хронической СН у пациентов с ЖТА и ИКД заключается в следующем: пациенту выполняют трансторакальную эхокардиографию и лабораторный анализ для оценки систолического давления легочной артерии и скорости дыхания митохондрий. Используя показатели СДПЖ и V4.1 в выведенной формуле, при значении Р более 0,43 прогнозируют III ФК хронической СН у пациентов с ЖТА и ИКД.
Клинические примеры
Пример 1 (пациентка с ЖТА, ИКД и III ФК хронической СН). Пациентка А., 64 г. Диагноз – Ишемическая болезнь сердца. Постинфарктный кардиосклероз. Ишемическая кардиомиопатия. Пароксизмальная неустойчивая желудочковая тахикардия. ХСН III ФК по классификации NYHA. По данным электрокардиографии: ритм синусовый, длительность комплекса QRS 140 мс. По данным теста шестиминутной ходьбы пациентка прошла 160 м без одышки, что соответствует III ФК по классификации NYHA. Пациентке имплантирован ИКД с целью первичной профилактики внезапной сердечной смерти. По данным эхокардиографии отмечалось значительное увеличение СДПЖ, который составил 73 мм рт. ст., а также снижение фракции выброса левого желудочка (36%). По лабораторным данным отмечалось выраженное снижение скорости дыхания митохондрий и показатель V4.1 составил 33,44 нМоль О2/мин/мг БМ. Используя полученные данные, было рассчитано значение вероятности III ФК хронической СН:
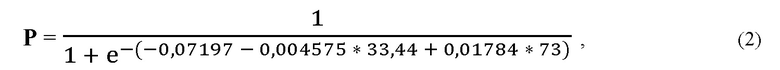
Р = 0,71.
Полученное значение Р = 0,71 оказалось больше диагностического порога 0,43, что позволяет точно прогнозировать тяжесть хронической СН, а именно III ФК, и своевременно начать терапию у пациентки с ЖТА и ИКД.
Пример 2 (пациент с ЖТА, ИКД и III ФК хронической СН). Пациент М., 50 л. Диагноз – Неишемическая кардиомиопатия. Пароксизмальная устойчивая желудочковая тахикардия. ХСН III ФК по классификации NYHA. По данным электрокардиографии: ритм синусовый, длительность комплекса QRS 150 мс. По данным теста шестиминутной ходьбы пациент прошел 270 м без одышки, что соответствует III ФК по классификации NYHA. Пациенту имплантирован ИКД с целью вторичной профилактики внезапной сердечной смерти. По данным эхокардиографии отмечалось значительное увеличение СДПЖ, который составил 64 мм рт. ст., а также снижение фракции выброса левого желудочка (25%). По лабораторным данным отмечалось выраженное снижение скорости дыхания митохондрий и показатель V4.1 составил 38,39 нМоль О2/мин/мг БМ. Используя полученные данные, было рассчитано значение вероятности III ФК хронической СН:
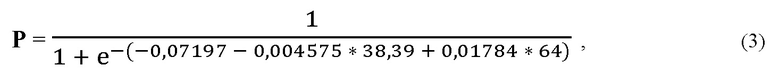
Р = 0,7.
Полученное значение Р=0,7 оказалось больше диагностического порога 0,43, что позволяет точно прогнозировать тяжесть хронической СН, а именно III ФК, и своевременно начать терапию у пациентки с ЖТА и ИКД.
Предлагаемый в качестве изобретения способ апробирован на 37 больных и позволяет повысить точность прогнозирования III ФК хронической СН у пациентов с ЖТА и ИКД.
Источники информации:
1. Kaplon-Cieslicka A., Drozdz J., Filipiak KJ. Prognostic factors in heart failure - are they all equally important? Kardiol Pol. 2017;75(6):519-526. doi: 10.5603/KP.a2017.0088.
2. Ponikowski P., Voors A.A., Anker S.D., Bueno H., Cleland JGF., Coats AJS., Falk V., Gonzalez-Juanatey J.R., Harjola V.P., Jankowska E.A., Jessup M., Linde C., Nihoyannopoulos P., Parissis J.T., Pieske B., Riley J.P., Rosano GMC., Ruilope L.M., Ruschitzka F., Rutten F.H., van der Meer P; ESC Scientific Document Group. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Eur Heart J. 2016;37(27):2129-2200. doi: 10.1093/eurheartj/ehw128.
3. Peterson P.N., Rumsfeld J.S., Liang L., Albert N.M., Hernandez A.F., Peterson E.D., Fonarow G.C., Masoudi F.A.; American Heart Association Get With the Guidelines-Heart Failure Program. A validated risk score for in-hospital mortality in patients with heart failure from the American Heart Association get with the guidelines program. Circ Cardiovasc Qual Outcomes;3(1):25-32. doi: 10.1161/CIRCOUTCOMES.109.854877.
4. Fonarow G.C., Adams KF Jr, Abraham W.T., Yancy C.W., Boscardin W.J.; ADHERE Scientific Advisory Committee, Study Group, and Investigators. Risk stratification for in-hospital mortality in acutely decompensated heart failure: classification and regression tree analysis (ADHERE). JAMA. 2005;293(5):572-80. doi: 10.1001/jama.293.5.572.
5. Abraham W.T., Fonarow G.C., Albert N.M., Stough W.G., Gheorghiade M., Greenberg B.H., O'Connor C.M., Sun J.L., Yancy C.W., Young J.B.; OPTIMIZE-HF Investigators and Coordinators. Predictors of in-hospital mortality in patients hospitalized for heart failure: insights from the Organized Program to Initiate Lifesaving Treatment in Hospitalized Patients with Heart Failure (OPTIMIZE-HF). J Am Coll Cardiol. 2008;52(5):347-56. doi: 10.1016/j.jacc.2008.04.028.
6. Pocock S.J., Ariti C.A., McMurray J.J., Maggioni A., Kober L., Squire I.B., Swedberg K., Dobson J., Poppe K.K., Whalley G.A., Doughty R.N.; Meta-Analysis Global Group in Chronic Heart Failure. Predicting survival in heart failure: a risk score based on 39 372 patients from 30 studies. Eur Heart J.;34(19):1404-13. doi: 10.1093/eurheartj/ehs337.
7. Komajda M., Carson P.E., Hetzel S., McKelvie R., McMurray J., Ptaszynska A., Zile M.R., Demets D., Massie B.M. Factors associated with outcome in heart failure with preserved ejection fraction: findings from the Irbesartan in Heart Failure with Preserved Ejection Fraction Study (I-PRESERVE). Circ Heart Fail. 2011;4(1):27-35. doi: 10.1161/CIRCHEARTFAILURE.109.932996.
8. Levy W.C., Mozaffarian D., Linker D.T., Sutradhar S.C., Anker S.D., Cropp A.B., Anand I., Maggioni A., Burton P., Sullivan M.D., Pitt B., Poole-Wilson P.A., Mann D.L., Packer M. The Seattle Heart Failure Model: prediction of survival in heart failure. Circulation. 2006;113(11):1424-33. doi: 10.1161/CIRCULATIONAHA.105.584102.
9. Auble T.E., Hsieh M., Gardner W., Cooper G.F., Stone R.A., McCausland J.B., Yealy D.M. A prediction rule to identify low-risk patients with heart failure. Acad Emerg Med. 2005;12(6):514-21. doi: 10.1197/j.aem.2004.11.026.
10. Zhao T-J., Yang Q-K., Bi L-D., Li J., Tan C-Y., Miao Z-L. Prognostic value of DCTA scoring system in heart failure. Herz. 2021;46(Suppl 2):243-252. doi: 10.1007/s00059-020-04993-1.
11. Martindale J.L., Wakai A., Collins S.P., Levy P.D., Diercks D., Hiestand B.C., Fermann G.J., deSouza I., Sinert R.. Diagnosing acute heart failure in the emergency department: a systematic review and meta-analysis. Acad Emerg Med. 2016;23(3):223-42. doi: 10.1111/acem.12878.
12. Maisel A.S., Peacock W.F., Shah K.S., Clopton P., Diercks D., Hiestand B., Kontos M.C., Mueller C., Nowak R., Chen W.J., Collins S.P. Acoustic cardiography S3 detection use in problematic subgroups and B-type natriuretic peptide “gray zone”: secondary results from the heart failure and Audicor technology for rapid diagnosis and initial treatment multinational investigation. Am J Emerg Med. 2011; 29(8):924-31. doi: 10.1016/j.ajem.2010.03.032.
13. Егорова М.В., Афанасьев С.А. Выделение митохондрий из клеток и тканей животных и человека: современные методические приемы. СМЖ. 2011;26(1):22-28.
14. Rebrova T.Y., Korepanov V.A., Afanasiev S.A. Age peculiarities of respiratory activity and membrane microviscosity of mitochondria from rat cardiomyocytes. Bull Exp Biol Med. 2021;170(3):368-370. doi: 10.1007/s10517-021-05069-8.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития желудочковых тахикардий у пациентов с постинфарктным кардиосклерозом и фракцией выброса левого желудочка менее 35% | 2021 |
|
RU2770267C1 |
| Способ прогнозирования риска развития желудочковых тахикардий у пациентов с ишемической болезнью сердца | 2021 |
|
RU2752362C1 |
| Способ прогнозирования положительного ответа на кардиоресинхронизирующую терапию у пациентов с хронической сердечной недостаточностью II и III функционального класса | 2022 |
|
RU2786467C1 |
| СПОСОБ ПРОВЕДЕНИЯ ФЕНОТИПИРОВАНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ НА ОСНОВЕ МЕТАБОЛОМНОГО ПРОФИЛИРОВАНИЯ | 2024 |
|
RU2841230C1 |
| Способ прогнозирования «супер-ответа» на сердечную ресинхронизирующую терапию у пациентов с полной блокадой левой ножки пучка Гиса и хронической сердечной недостаточностью различной этиологии | 2023 |
|
RU2813796C1 |
| Способ прогнозирования риска развития неаритмической смерти в четырехлетний период наблюдения у пациентов с сердечной недостаточностью со сниженной фракцией левого желудочка и имплантированным кардиовертером-дефибриллятором | 2023 |
|
RU2820923C1 |
| Способ прогнозирования отдаленных неблагоприятных исходов у пациентов с сердечной недостаточностью и имплантированным кардиовертером-дефибриллятором | 2023 |
|
RU2819279C1 |
| Способ прогнозирования положительного ответа на сердечную ресинхронизирующую терапию у пациентов с электрокардиографическими критериями блокады левой ножки пучка Гиса по Штраусу | 2024 |
|
RU2830640C1 |
| Способ прогнозирования прогрессирования сердечной недостаточности у больных с синдромом обструктивного апноэ | 2022 |
|
RU2796311C1 |
| Способ прогнозирования риска развития острой декомпенсации сердечной недостаточности у пациентов с низкой фракцией выброса левого желудочка и имплантированным кардиовертером-дефибриллятором | 2023 |
|
RU2809775C1 |
Изобретение относится к медицине, а именно к кардиологии, и может быть использовано в профилактике и лечении III функционального класса хронической сердечной недостаточности (ХСН) у пациентов с желудочковыми тахиаритмиями и имплантированным кардиовертером-дефибриллятором. Пациентам проводят трансторакальную допплеровскую эхокардиографию с оценкой систолического давления в правом желудочке, отражающего систолическое давление легочной артерии, и производят забор венозной крови для определения скорости дыхания митохондрий в среде после израсходования аденозиндифосфата. Затем рассчитывают вероятность развития III функционального класса ХСН по оригинальной формуле. Если прогностический коэффициент составляет более 0,43, то у пациента прогнозируют III функциональный класс ХСН. Способ позволяет повысить эффективность терапии ХСН у больных с желудочковыми тахиаритмиями и имплантированным кардиовертером-дефибриллятором, тем самым улучшить качество жизни пациентов. 1 ил., 2 табл., 2 пр.
Способ прогнозирования риска развития III функционального класса хронической сердечной недостаточности у пациентов с желудочковыми тахиаритмиями и имплантированным кардиовертером-дефибриллятором, характеризующийся тем, что проводят трансторакальную допплеровскую эхокардиографию, по данным которой оценивают систолическое давление в правом желудочке, а также оценивают скорость дыхания митохондрий мононуклеаров периферической венозной крови в среде после израсходования аденозиндифосфата и определяют прогностическую вероятность развития III функционального класса хронической сердечной недостаточности по формуле:

где P – прогностическая вероятность,
е – основание натурального логарифма (е=2,7182818284),
-0,07197 – коэффициент постоянной,
-0,004575 – коэффициент переменной скорости дыхания митохондрий в среде после израсходования аденозиндифосфата,
х1 – числовое значение скорости дыхания митохондрий в среде после израсходования аденозиндифосфата,
0,01784 – коэффициент переменной систолического давления в правом желудочке,
х2 – числовое значение систолического давления в правом желудочке,
и при значении Р более 0,43 прогнозируют III функциональный класс хронической сердечной недостаточности у пациентов с желудочковыми тахиаритмиями и имплантированным кардиовертером-дефибриллятором.
| СПОСОБ ПРОГНОЗА ВОЗНИКНОВЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ КОРОНАРНОЙ БОЛЕЗНЬЮ СЕРДЦА | 2010 |
|
RU2444982C1 |
| Приспособление для перемещения матричных стержней в наборно-словолитных машинах системы "Типограф" | 1926 |
|
SU5433A1 |
| Супергетеродинный радиоприемник | 1930 |
|
SU20157A1 |
| JP 2014210034 A, 13.11.2014 | |||
| КУРЛЯНСКАЯ Е.К | |||
| и др | |||
| Прогрессирование хронической сердечной недостаточности: прогностические критерии и немедикаментозная профилактика | |||
| Кардиология | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| VERDU-ROTELLAR J.M | |||
| et al | |||
| Risk stratification in heart failure | |||
Авторы
Даты
2023-11-13—Публикация
2023-06-27—Подача