Область техники
Группа изобретений относится к области биотехнологии и микробиологии и конкретно касается способа обнаружения Listeria monocytogenes методом, основанным на реакциях антиген-антитело, представляющим собой готовую ИФА-тест систему. Также изобретение позволяет дифференцировать L.monocytogenes от других представителей рода Listeria и позволяет дифференцировать вирулентные штаммы от авирулентных штаммов, и может быть использована для эпидемиологического надзора за листериозом.
Уровень техники
Listeria monocytogenes - грамположительная бактерия, которая может вызвать опасную пищевую инфекцию с высокой (около 30 %) летальностью для людей и животных, находящихся в группе риска. Listeria spp включает 26 вид (Carlin et al., 2021), 19 из которых являются сапрофитическими, а вид L. ivanovii вызывает заболевания животных и крайне редко вызывать проявление гастроэнтерита у человека (Snapir et al., 2006). Поскольку вид L.monocytogenes является единственным патогенным для человека представителем Listeria spp, необходимо четко дифференцировать этот вид от близкородственных видов. Более того генетическая структура вида L. monocytogenes подразделяется на 4 филогенетические линии, отличающиеся по эпидемическому потенциалу (Maury et al., 2016a). Листериоз у человека и с/х животных чаще всего вызывается штаммами, которые относятся к I и II филогенетическим линиям (Rasmussen et al., 1995; Nightingale et al., 2005; Cantinelli et al., 2013), а штаммы филогенетических линий III и IV обнаруживаются редко, но в большинстве случаев выделяются из животных (Haase et al., 2014). Анализ случаев листериоза у человека, основанный на методах молекулярного типирования, показал, что эволюционные линии, характеризуются различными патогенными потенциалами: первая линия - штаммы, связанные с эпидемическими вспышками листериоза (серотипы 1/2b, 3b, 4b, 4d и 4е); вторая линия - штаммы, выделенные во время спорадических случаев листериоза (серотипы 1/2a, 1/2c, 3a и 3c); третья линия - штаммы, редко связанные со случаями листериоза (серотипы 4a и 4c) (Orsi et al., 2011). Анализ заболеваемости листериозом продемонстрировал, что около 50 % всех случаев листериоза в мире вызывают штаммы серовара 4b, хотя среди штаммов, выделяемых из заражённых продуктов, доминируют сероварианты L. monocytogenes 1/2а, 1/2b, 1/2с. В пределах I и II филогенетических линиях встречаются клональные комплексы (СС), отличающиеся по вирулентному потенциалу. Так, например, высоковирулентные CC принадлежать к I первой филогенетической линии к ним относятся СС1, СС4, СС6; CC7 - средневирулентный клональный комплекс из II филогенетической линии и СС9 - низковирулентный из II филогенетической линии, при этом практически все штаммы L. monocytogenes несут основные островки патогенности (Maury et al., 2016b).
Несмотря на то, что «золотым стандартом» в диагностике листериоза признаны микробиологические методы, основанные на выделении чистой культуры возбудителя и посевах на дифференциальные питательные среды (Lovett et al., 1987; McClain and Lee, 1988), они все же дополняются разнообразными вспомогательными серологическими и иммунологическими методами для определения антигенной природы возбудителя. К достоинствам серологических и иммунологических методов можно отнести: экспресс-результат, относительную простоту постановки реакций, а также возможность исследования разнообразного биологического материала, с выявлением определенных ключевых антигенных детерминант.
Основываясь на эпидемиологических данных в качестве дополнительного метода диагностики, был предложен подход серологического типирования L. monocytogenes на основе выявления поверхностных антигенов листерий, с помощью моноклональных антител или специфических сывороток. Первая панель моноклональных антител для выявления листерий была предложена J.M. Farber (1987). Метод выявлял общий флагеллярный Н-антиген листерий у L. monocytogenes, L. ivanovi, L. innocua, L. weishimeri и L.seeligeri. Однако выделение поверхностного антигена не отвечало на вопрос о принадлежности L. monocytogenes к серогруппе. В России выпускаются сыворотки, такие как «Сыворотка диагностическая поливалентная листериозная сухая для реакции агглютинации на стекле» (Иркутск, НИПЧИ) и «Поливалентная и моновалентная сыворотки» (ВНИИВВиМ, г.Покров), которые позволяют оценить антигенную принадлежность листерий к одной и к двум серогруппам, соответственно, в то время как за рубежом идентифицируют до 16 серовариантов. Важно подчеркнуть, что недостатком отечественной серологической диагностики является то, что сероварианты с 1/2а по 3с, используемые в международной классификации, объединены в 1-ю, а остальные - во 2-ю серогруппу. Анализ антигенной структуры L. monocytogenes с использованием отечественных сывороток двух типов показал относительно низкую специфичность данной системы дифференциации. В мировой литературе также известна панель антител из 15 специфичных к роду Listeria моноклональных антител, выявляюшая термостабильный родоспецифичный белок молекулярной массой от 30 000 до 38 000 Да. Два моноклона из этой панели были в дальнейшем использованы для создания коммерческой иммуноферментной тест-системы (Listeria - ЕеK) для выявления Listeria spp (Curiale MS, 1994). Данная тест-система широко применялась в качестве дополнительного, но не альтернативного метода для выявления листерий в продуктах питания. Однако она также не отвечает на вопрос о вирулентном потенциале выявляемых L. monocytogenes.
Для определения серологической принадлежности культур, согласно мировой классификации, рекомендуется использовать в практической и научной работе метод мультиплексной ПЦР, основанный на корреляции между серогрупповой принадлежностью изолята и наличием специфических открытых рамок считывания в его геноме (Зайцева Е. А. и Ермолаева С.А., 2014). Использование этого метода позволяет выявить разнообразие культур L. monocytogenes, циркулирующих на разных географических территориях России с дифференциацией эпидемически значимых и опасных для человека штаммов. Однако общеизвестно, что серовары и серотипы листерий не являются видоспецифичными. Они могут быть общими для разных видов листерий независимо от патогенности для человека. Анализ серологической структуры листерий показал, что она крайне неудобна для диагностики. L. monocytogenes, имеет одну или несколько общих антигенных детерминант с другими видами листерий, кроме L. welshimeri. Поэтому само по себе определение серовара без применения иных методов не позволяет установить диагноз инфекции, вызванной L. monocytogenes.
Более того, отмечено, что шесть видов Listeria spp имеют специфические антигены, которые характерны для 16 серотипов: 1/2a, 1/2b, 1/2c, 3a, 3b, 3c, 4a, 4ab, 4b, 4c, 4d, 4e, 7, 5,6a, 6b. А применительно к L.monocytogenes широкий спектр организмов-хозяев, в которых может размножаться патоген, обусловил антигенную гетерогенность внешней оболочки L. monocytogenes. Кроме того, установлено, что не только гены, кодирующие поверхностные детерминанты, но и некоторые другие фрагменты генома этого микроорганизма могут быть специфическими для различных серогрупп L. monocytogenes. В то же время не обнаружено закономерностей между сероварами выделяемых штаммов и биологическим типом хозяина, а также тяжестью заболевания.
Специфичность к хозяину и течение патологического процесса обусловлены факторами патогенности листерий, такими как листериолизин О(LLO), белок полимеризующий актин (ActA), InlА и InlB, фосфолипаза С (plcA, plcB) и др.
Поэтому еще одним подходом для идентификации L. monocytogenes от близкородственных видов является использование иммунологических методов, основанных на обнаружении специфических факторов патогенности. Иммунологические методы обнаружения, описанные для L. monocytogenes, основаны, главным образом, на тех мишенях, которые играют роль в патогенности L. monocytogenes. Известно, что некоторые из этих генов расположены на хромосоме рядом друг с другом в островках патогенности. Поскольку листериолизин О (ген hlyA) был впервые описан как необходимый для патогенности, то большинство методов генотипической детекции основаны на этом гене. Разработаны тест-системы для выявления белка АctA, который участвует в полимеризации актина хозяйской клетки и таким образом помогает листерии избегать иммунологической защиты макроорганизма (CN114574448). Также использованы антитела против p60 в разных форматах ИФА-тест систем (Yu et al., 2004) (CN105527441A, CN104099299A), дот-блоттинга (Wióckowska-Szakiel et al., 2002; Yu et al., 2004) и ПЦР (Патент США 5,932,415). Некоторые тест-наборы для выявления с помощью антител уже имеются в продаже. Однако большинство из этих тестов демонстрируют низкую чувствительность и специфичность. В обзоре (Banada and Bhunia, 2008) описаны некоторые из них. Известно использование антител против белка InlB и ActA в комбинации с иммуномагнитными шариками (CN114574448A) или в иммуноблотинге (Lathrop et al., 2008). Однако данные методы трудоемки и требуют специфических навыков. Другие иммунологические методы, часто ограничены разделением антигенов клеточной поверхности с другими видами Listeria spp., что не позволяет дифференцировать L. monocytogenes от непатогенных видов, часто встречающихся в образцах пищевых продуктов.
Таким образом в уровне техники существует потребность в разработке нового метода идентификации листерий, который будет лишен указанных недостатков. В предлагаемом методе дифференциации сочетаются традиционные микробиологические методы, характеризующиеся надежностью, с иммунологическим анализом, предоставляющем специфичность. При этом мишенями для иммунологического анализа являются поверхностные белки, отсутствующие у других видов Listeria spp. Специфические поверхностные белки L. monocytogenes, отсутствующие у других видов Listeria, в основном представлены факторами вирулентности. Поверхностный белок интерналин В (InlB), является фактором вирулентности, опосредующим бактериальную инвазию в непрофессиональные фагоциты, и отсутствует у других видов Listeria. InlB представляет собой секретируемый белок, который может быть закреплен на поверхности клетки посредством нековалентных взаимодействий его С-концевые GW-доменов с тейхоевыми кислотами клеточной стенки (Braun et al., 1997). Интерналин А-второй поверхностный белок L. monocytogenes, который также является фактором вирулентности и представляет собой инвазин, взаимодействующий с E-кадгерином эпителиальных клеток. Пересечение эпителиальных барьеров является ключевым аспектом для развития системного листериоза.
Ряд исследователей установили, что штаммы, полученные от случаев листериоза человека и животных, и штаммы, выделенные из пищевых продуктов, отличаются уровнем продукции интерналина А и интерналина В (Werbrouck et al., 2006; Tamburro et al., 2015). Более того в международной литературе известно, что штаммы, несущие преждевременный стоп-кодон в гене InlA считаются авирулентными (Nightingale et al., 2008). Учитывая эти данные, мы решили разработать ИФА-тест систему, позволяющую дать качественную и количественную оценку для обоих белков (InlA и InlB).
Ранее была разработана тест-система на основе нуклеиновых кислот-лигандов, предназначенных для обнаружения присутствия или отсутствия интерналина В, интерналина А или Listeria в пищевых продуктах, клинических образцах или образцах из окружающей среды. Однако данная система отвечает только на вопрос есть ли оба белка на поверхности бактерии и не отвечает на вопрос об их количестве (US2009264512A1). С использованием моноклональных антител против InlA и методом иммуномагнитной сепарации удалось обнаружить L. monocytogenes и L. ivanovii в образцах пищи (Mendonça et al., 2012). Однако исходя из результатов очевидно, что отличить один вид от другого данная система не позволяет, хотя и проявляет чувствительность на уровне 103 КОЕ/мл (Mendonça et al., 2012). Также были получены моноклональные антитела против InlA L.monocytogenes 1/2a, которые позволяли обнаруживать бактерий в концентрациях 107 КОЕ/ мл (Hearty et al., 2006). Также в 2022 году в международной литературе была опубликована статья о разработке ИХА-тест система для определения обоих антигенов (Lopes-Luz et al., 2023). Время анализа занимает 20 минут, но тест-система также отвечает только на вопрос о наличии белка без указания его количества (Lopes-Luz et al., 2023). Таким образом ни в мировой, ни в отечественной литературе подобных ИФА тест-систем, основанных на выявлении и количественном определении инвазинов InlA и InlB одномоментно не сообщалось.
Раскрытие изобретения
Технической задачей заявленного изобретения является разработка недорогого и быстрого способа идентификации и дифференциации вирулентных штаммов L. monocytogenes от авирулентных штаммов и других видов Listeria spp.
Технический результат представляет собой получение быстрой и эффективной тест системы для идентификации Listeria spp и получения характеристики бактерий, позволяющей определить вирулентный потенциал Listeria spp через 4 часа от момента получения чистых культур.
Также технический результат заключается в том, что создан способ идентификации и дифференциации вирулентных штаммов L. monocytogenes от авирулентных штаммов и других видов Listeria spp, который основан на создании ИФА-тест системы, позволяющей обнаружить и определить количественно поверхностные белки InlB и InlA в условиях роста бактерий на жидкой питательной среде BHI.
Технический результат также представляет собой высокую и стабильную экспрессию рекомбинантного белка InlA бактерии L.monocytogenes. Кроме того, технический результат заключается в получении высокочувствительных поликлональных моноспецифичных антител против InlA и InlB.
Технический результат достигается за счет разработки тест-система для иммуноферментного анализа штаммов L. monocytogenes, представляющая собой набор реагентов, включающая планшет для иммуноферментного анализа, калибровочные стандарты рекомбинантных белков InlA, имеющих последовательность SEQ ID NO:2, и InlB в концентрации 1 мг/мл, положительный контроль, представляющий собой культуру L. monocytogenes EGDe, отрицательный контроль, представляющий собой культуру L. innocua SLCC 3379, поликлональные моноспецифические антитела к InlA, поликлональные моноспецифические антитела к InlB, буфер трис-HCl (TBS) с твином-20, pH 7.4 для приготовления раствора объемом 1 л для промывания планшетов, буфер для разведения антител, буфер для разведения бактерий, раствор хромогена, содержащий раствор тетраметилбензидина и стоп-реагент.
Также разработан способ идентификации и дифференциации вирулентных штаммов Listeria monocytogenes от авирулентных штаммов и других видов Listeria spp, включающий в себя использование тест-системы, представляющий собой непрямой ИФА-анализ, где выращивают бактерии в жидкой питательной среде, отделяют клетки от супернатанта методом центрифугирования, инкубируют для калибровки бактериальные клетки и рекомбинантные белки InlA и InlB от +36°С до +38°С на планшете в течение 1 часа, промывают лунки 3 раза раствором промывочного буфера, блокируют незанятые участки блокировочным буфером на 1 час при комнатной температуре, инкубируют бактериальные клетки с поликлональными моноспецифическими антителами против интерналина А и интерналина В, промывают лунки 3 раза раствором промывочного буфера, инкубируют со вторичными поликлональными антителами конъюгированными с HRP, промывают лунки 3 раза раствором промывочного буфера, визуализируют с добавлением TMB субстрата, останавливают реакцию, измеряют оптическую плотность на спектрофотометре в каждой лунке при длине волны 450 нм и интерпретируют результаты.
Краткое описание чертежей
На фиг. 1 представлена схема плазмидного вектора InlA-pET28a, где
Ori - последовательность начала репликации
BamHI - сайты узнавания для рестриктазы BamHI
Histag - метка из 6гистидинов
Kmr - ген устойчивости к канамицину
LacI - ген репрессора лактозного оперона
На фиг. 2 представлена электрофореграмма аффинной очистки рекомбинантного InlA, где
М - маркер молекулярных весов
L - бактериальный лизат E. coli BL21 InlA-pET28a
FT - «проскок»
W - фракция отмывки
100 1 - элюция 100 мМ имидазолом
300 1 - 1-ая элюция 300 мМ
300 2 - 2-ая элюция 300 мМ
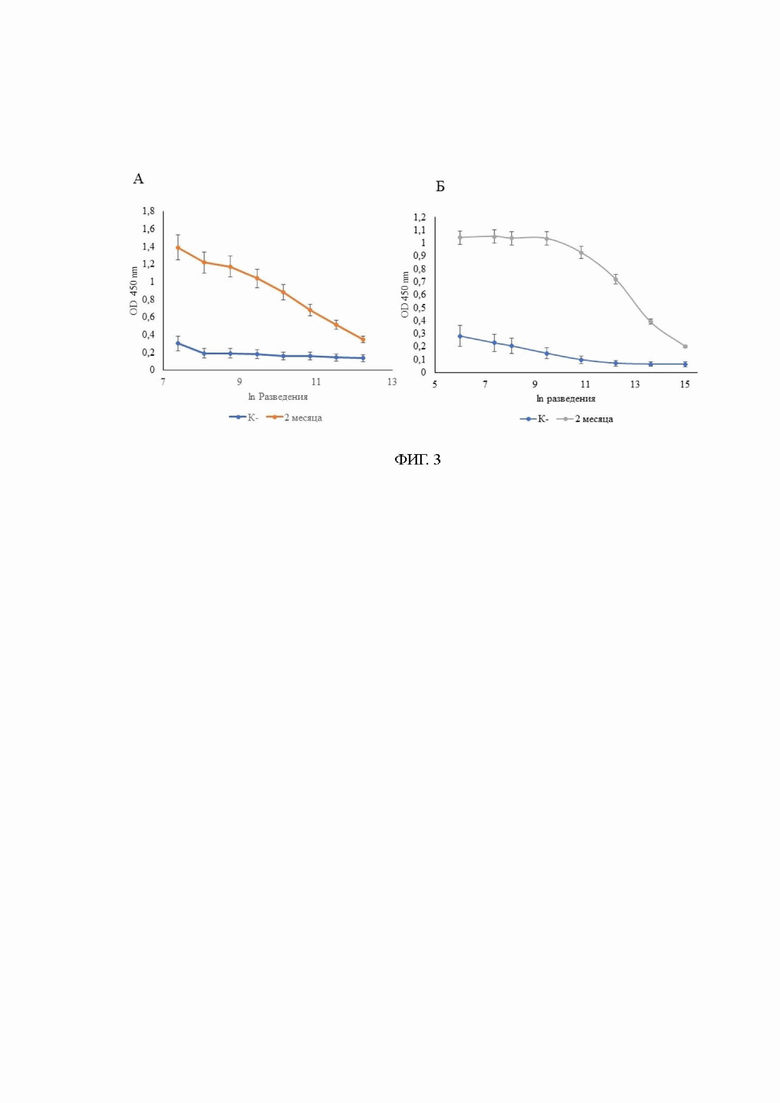
На фиг. 3 представлено определение титра сывороток у животных.
А - определение титра сыворотки против InlА;
Б - определение сыворотки титра против InlВ.
На фиг .4 представлена схема получения моноспецифичных антител на примере антител к InlA.
На фиг. 5 представлен результат выделения антител после хроматографии на ДЭАЭ-сефадексе А-50.
А - для антител против InlA;
Б - для антител против InlB.
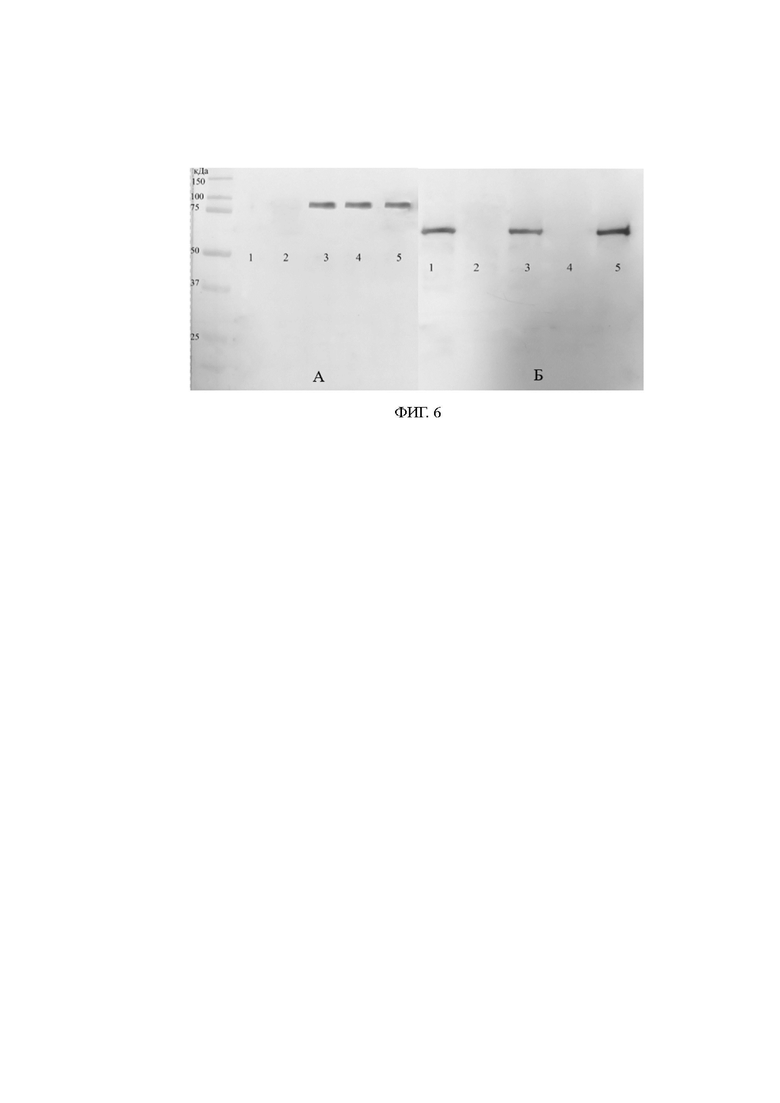
На фиг. 6 представлен иммуноблот клеточных лизатов бактерий Listeria spp.
А - моноспецифичные антитела против InlA;
Б - моноспецифичные антитела против InlB
1 - L. monocytogenes EGDe ΔinlA;
2 - L. ivanovii ATCC 19119;
3 - L. monocytogenes EGDe (CC9);
4 - L. monocytogenes EGDe ΔinlB;
5 - L. monocytogenes L.mo49 (CC9).
На фиг. 7 представлен непрямой ИФА-анализ бактерий Listeria spp.
На фиг. 8 представлен иммуноблот клеточных лизатов бактерий Listeria spp.
А - моноспецифичные антитела против InlA;
1 - L. monocytogenes EGDe;
2-5 - рекомбинантные штаммы L. monocytogenes EGDe ΔinlA::pInlA ;
Б - моноспецифичные антитела против InlB
1 - L. monocytogenes EGDe;
2-5 - рекомбинантные штаммы L. monocytogenes EGDe ΔinlB::pInlB;
B - Электрофорез белковых лизатов клеточной поверхности Listeria
1 - L. monocytogenes EGDe;
2-5 - рекомбинантные штаммы L. monocytogenes EGDe ΔinlA::pInlA.
На фиг. 9 представлено определение чувствительности рекомбинантных антигенов InlA и InlB.
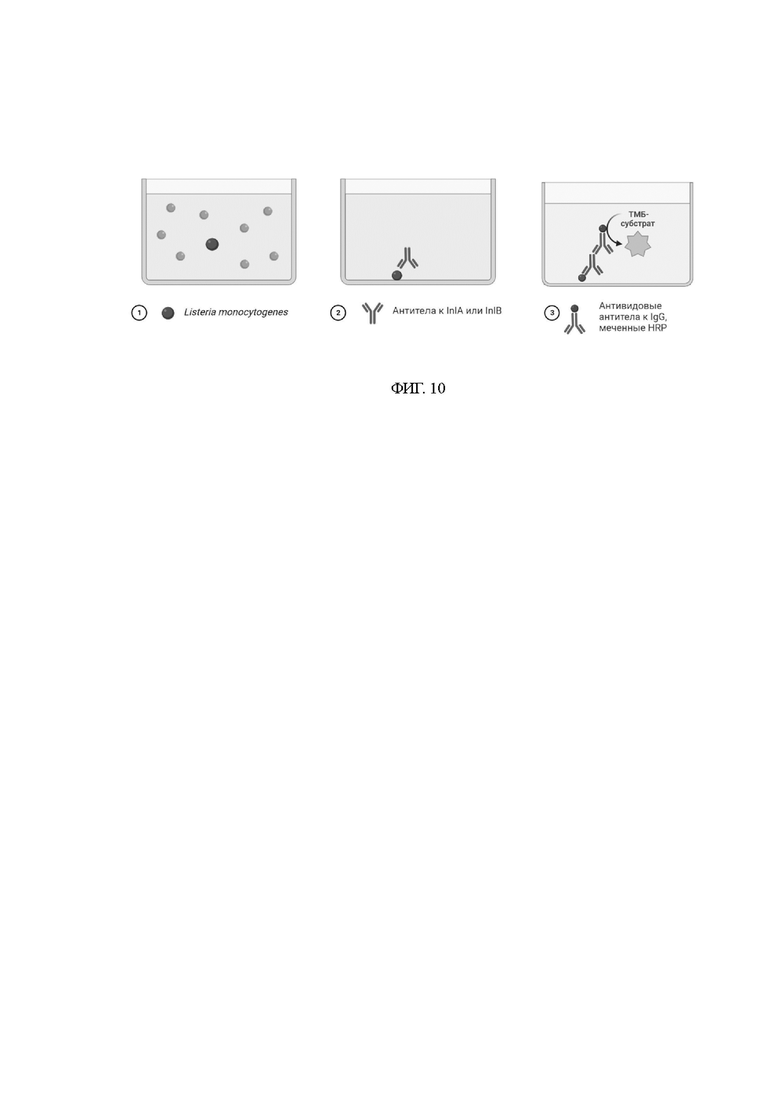
На фиг. 10 представлена схема ИФА, применяемая для оценки активности антител по отношению к клеткам.
На фиг. 11 представлен непрямой ИФА-анализ рекомбинантных штаммов L. monocytogenes.
Реализация изобретения
Предлагаемый авторами способ анализа чистой культуры бактерий, включающий применение тест-системы, заключается в следующем:
1. Для анализа используется чистая культура микроорганизмов, выращенная на жидкой питательной среде BHI (Brain Heart Infusion). Анализ проводится в двух планшетах №1 (предназначенный для определения InlA) и №2 (предназначенный для определения InlB).
2. Методом центрифугирования осуществляют отделение клеточной биомассы от культуральной среды и полученный осадок трижды промывают фосфатно-солевым буфером, каждый раз отделяя супернатант.
3. Полученную биомассу доводят до одинаковой оптической плотности, после чего иммобилизуют 100 мкл бактериальной суспензии в лунки 96-луночного плоскодонного планшета и оставляют при 37oC на 1 час.
4. Для построения калибровочной кривой делают серийные разведения стандартных белков с начальной концентрацией 1мг/мл (InlA для планшета №1 и InlB для планшета №2). Полученные титры последовательно вносят по 100 мкл в лунки 96-луночного плоскодонного планшета и оставляют при 37oC на 1 час.
5. После инкубации каждую лунку трижды промывают трис-буферным раствором (TTBS).
6. Далее в каждую лунку добавляют по 100 мкл 2% BSA в фосфатно-соленом буфере и инкубируют в течение 30 минут.
7. Затем каждую лунку трижды промывают TTBS и добавляют 100 мкл моноспецифичных антител в разведении 1:4000 для InlA и 1:20000 для InlB. Для планшета №1 используются моноспецифичные антитела против InlA, для планшета №2 используются моноспецифичные антитела против InlВ. Инкубацию осуществляют при 25oC в течение 1 часа.
8. Затем каждую лунку трижды промывают TTBS и добавляют 100 мкл вторичных анти-кроличьих козьих антител, меченных HRP, в разведении 1:50000. Инкубация проводится при 25oC в течение 1 часа.
9. Далее каждую лунку трижды промывали TTBS и добавляли 100 мкл субстрата для пероксидаpы хрена (TMB). Планшет помещают в темное место до появления желаемой окраски (10-20 минут). Далее реакцию останавливают добавлением 100 мкл 2М серной кислоты.
10. Анализ результатов проводят с использованием фотометра при длине волны 450 нм. Уровень белков в образцах определяют по калибровочной кривой.
Интерпретация результатов: Значимыми для подтверждения степени вирулентного потенциала считаются следующие показатели1:
1-отсутствие обоих белков свидетельствует о том, что анализируемые штаммы не принадлежать к L.monocytogenes.
2-практически авирулентным признается штамм, лишенный InlA при наличии InlA
Осуществление изобретения подтверждается примерами
Пример 1. Получение очищенного рекомбинантного белка InlA
Продукт амплификации гена inlA по праймерам InlAF 5’ gctacaattacacaaGGATCCcctatt и InlAR 5’ cttcttttgaattataGGATCCataagc клонировали в промежуточный вектор pGemTEasy и переклонировали по сайту рестрикции BamHI в экспрессирующий вектор pET28a (фигура 1). Штамм клеток E. coli BL21 InlA-pET28a был получен на основе клеток E. coli BL21, в которую путем электропорации была трансформирована плазмида InlA-pET28a. Для экспрессии белка ночную культуру E. coli BL21 InlA-pET28a, выращенной на среде LB с канамицином 100 мкг/мл, пересевали в 500 мл флаконы с объёмом среды 50 мл. Культивировали до достижения оптической плотности 0,4 - 0,6 при λ=600 нм. Добавляли индуктор экспрессии ИПТГ до концентрации 1 мМ на 3 часа. Клетки центрифугировали 10 мин 4200 об/мин и подвергали воздействию ультразвука трижды по 20 секунд с перерывами на 1 минуту. Супернатант, содержащий рекомбинантный белок, отделяли от клеточного дебриса центрифугированием и использовали для аффинной хроматографии. Для этого на колонку HisTrap, содержащий иммобилзованный Ni2+ наносили приготовленный лизат, промывали буферным раствором, содержащий 20 мМ имидазола, и элюировали буферными растворами, содержащими 100 мМ и 300 мМ имидазола. Искомый белок содержался во фракциях, элюировавших при 300 мМ имидазола (фигура 2). Фракции, содержащие белок InlA, диализовали против фосфатно-солевого буфера и использовали для получения гипериммунных сывороток.
Пример 2. Получение гипериммунных сывороток.
Для получения гипериммунных сывороток использовали самцов кроликов породы «Советская шиншила» массой 3-4 кг. Для каждого антигена использовали по три кролика. Иммунизации животных проводилась по схеме, представленной в табл. 1.
Таблица 1. Схема иммунизации кроликов для получения гипериммунной сыворотки к InlB. ПАФ - полный адъювант Фрейнда; НАФ - неполный адъювант Фрейнда; в/в - внутривенно; в/м - внутримышечно в лапку, п/к - подкожно по боковым поверхностям тела в 5 точек с одной стороны.
Через две недели после третей иммунизации оценивали титр сывороток у животных (фигура 3). В 96-луночные планшеты добавляли белки InlA или InlB в концентрации 4 мкг/мл инкубировали при 4°C в течение 12 часов, отмывали трижды по 250 мкл трис-буферным раствором, содержащий 0,05% неионогенного детергента Твин-20 (TTBS), а затем блокировали добавлением в лунки 200 мкл 2% бычьего сывороточного альбумина (БСА), разведённом в фосфатно-солевом буфере (PBS) в течение 30 минут. Удаляли буфер для блокировки и добавляли 100 мкл анти-InlA или анти-InlB антител в разведении от 1:1600 до 1:512000 в блокировочном буфере с добавлением 0,05% Твин-20 и инкубировали 1 час при комнатной температуре на качалке при 140 об/мин. Лунки трижды промывали TTBS и добавляли 100 мкл вторичных антител (козьи антител против IgG кролика, меченные пероксидазой хрена), разбавленные в фосфатно-солевом буфере с добавлением 0,05% Tween-20 (PBST), содержащий 2% BSA. После отмывали 6 раз TTBS по 250 мкл. Проявляли ТМВ-субстратом 100 мкл. Для остановки реакции использовали 100 мкл 2 М серной кислоты. Измерение оптической плотности проводили при длине волны 450 нм на планшетном фотометре iMark (Bio Rad). Титр сыворотки считали удовлетворительным, если он был больше 100000 в ИФА. Как в случае сыворотки против InlA, так и сыворотки против InlB титр был выше 100000 (204800 и 512000, соответственно).
У иммунизированных животных титр антител поддерживали внутривенными подколами каждого антигена с интервалом в 6 месяцев.
Пример 3. Получение поликлональных моноспецифичных антител против InlА.
Получение моноспецифичных антител против InlA из гипериммунных осуществляли по схеме, представленной на фигуре 4. Глобулиновую фракцию высаливали, добавляя насыщенный раствор (NH4)2SO4. Выпавший осадок, содержащий IgG растворяли в PBS и диализовали против 0,01 М натрий-фосфатного буфера, pH 6.5. Полученный раствор пропускали через колонку с ДЭАЭ-сефадексом А-50. Фракция IgG выходила с колонки в свободном объеме буфера. Согласно электрофорезу в ПААГ эта фракция содержала единственный белок с молекулярной массой примерно 155 кДа (при разрыве S-S связей 55 и 22 кДа) (фигура 5А).
Для выделения аффинных антител на колонку с иммобилизованным на активированной BrCN-сефарозе InlА, наносили фракцию, полученную после ДЭАЭ-хроматографии, промывали тремя объемами колонки 0,3 М NaCl и элюировали в объеме 4 мл 4,5 М MgCl2. Полученные фракции иммуноглобулинов диализовали против 0,01 М натрий-фосфатного буфера для удаления MgCl2. Полученный раствор концентрировали методом ультрацентрифугирования. Полученный концентрат смешивали с глицерином 1:1 по объему. Хранили при -20оС.
Пример 4. Получение поликлональных моноспецифичных антител против InlB.
Для получения поликлональных моноспецифичных антител против InlB глобулины из гипериммунной сыворотки осаждали насыщенным раствором (NH4)2SO4, растворяли в фосфатно-солевом буфере и диализовали против 0,01 М натрий-фосфатный буфер, pH 6.5, для удаления сульфата аммония. Для получения IgG проводили ионообменную хроматографию с ДЭАЭ-сефадексом А-50 и собирали фракцию IgG (фигура 5Б). Для получения специфического иммуносорбента очищенный белок, соответствующий области интерналинового домена интерналина В (idInlB), иммобилизовали на BrCN-сефарозе ® 4B. Фракцию иммуноглобулинов наносили на колонку с иммуносорбентом. Колонку промывали фосфатно-солевым буфером с 0,3 М NaCl для удаления несвязанных примесей. InlB-специфические антитела элюировали в объеме 4 мл 4,5 М MgCl2 и подвергали диализу в фосфатно-солевом буфере, рН 7,4 (PBS). Полученный раствор концентрировали методом ультрацентрифугирования. Полученный концентрат смешивали с глицерином 1:1 по объему. Хранили при -20оС. Схема получения отражена на фигуре 6.
Пример 5. Проверка специфичности антител.
Специфичность полученных антител оценивали методом иммуноблота. В качестве образцов использовались бактериальные лизаты следующих штаммов: 1 - L. monocytogenes EGDeΔinlA; 2 - L. ivanovii ATCC 19119 3 - L. monocytogenes EGDe (CC9); 4 - L. monocytogenes EGDeΔinlB; 5 - L. monocytogenes L.mo49 (CC9).
Бактериальные лизаты получали из 50 мл ночной культуры, выращенной в BHI-бульоне с добавлением 1% Амберлита XAD 4. Клетки отмывали дважды в PBS, ресуспендировали в 150-200 мкл 2% SDS и инкубировали 1 час при 37оС на качалке. Центрифугировали при 11000 об/мин. Супернатант смешивали в соотношении 3:1 с 4хЛеммли буфером. Лизаты разделяли на 10% SDS-PAGE и переносили на нитроцеллюлозную мембрану с диаметром пор 0,45 мкм (Bio-Rad). Белки визуализировали с помощью полученных нами моноспецифичных антител (в разведении 1:10000), против которых были добавлены анти-кроличьи козьи антитела меченные пероксидазой хрена (в разведении 1:20000). Визуализация образцов осуществлялась с использование ECL-субстрата.
Антитела против InlA связывались с белком молекулярной массой примерно 80 кДа у штаммов L. monocytogenes EGDe, L. monocytogenes VIMPA064 (CC7), L. monocytogenes EGDeΔinlB (Фигура 6А), что совпадает с теоретической массой InlA. Отрицательный результат наблюдался для L. monocytogenes EGDeΔinlA, L. monocytogenes GIMC2035:Lmc7218(CC9) - имеющий стоп-кодон в последовательности гена inlA и L. ivanovii ATCC 19119.
Антитела против InlB связывались с белком молекулярной массой около 66 кДа (Фигура 6Б) у штаммов L. monocytogenes EGDeΔinlA, L. monocytogenes EGDe (CC9), L. monocytogenes GIMC2035:Lmc7218 (CC9) и L. monocytogenes VIMPA064 (CC7) что совпадает с теоретической массой InlB. Отрицательный результат наблюдался для L. monocytogenes EGDeΔinlB и L. ivanovii ATCC 19119.
Таким образом, полученные антитела к InlA и InlB специфически реагирует с L. monocytogenes, несущими на своей поверхности белки InlA и InlB соответственно, и не дают перекрестных и неспецифических реакций при иммуноблоте.
Полученные моноспецифичные антитела против InlA и InlB были проверены на штаммах Listeria spp. Результат ИФА для контрольной сыворотки, антител к InlA и InlB (Фигура 7)
Полученные моноспецифичные антитела против InlA и InlB были проверены на рекомбинантных штаммах, характеризующихся повышенной продукцией интерналина А и интерналина В (Фигура 8). При выровненной белковой нагрузке антитела достоверно уловили разницу в образцах по целевым антигенам.
Пример 6. Построение калибровочной кривой (InlA и InlB)
Лунки 96-луночного планшета покрывали очищенными рекомбинантными белками InlA и InlB в концентрациях от 1 до 100 нг/мл. Планшеты инкубировали при 4°C в течение 18 часов, отмывали трижды по 250 мкл трис-буферным физиологическим раствором, содержащий 0,05% неионогенного детергента Твин-20 (TTBS), а затем блокировали добавлением в лунки 200 мкл 2% бычьего сывороточного альбумина (БСА), разведённом в фосфатно-солевом буфере (PBS) в течение 30 минут. Удаляли буфер для блокировки и добавляли 100 мкл анти-InlB (в разведение 1:20000) или анти-InlA антител (в разведении 1:4000) в блокировочном буфере с добавлением 0,05% Твин-20 и инкубировали 1 час при комнатной температуре на качалке при 140 об/мин. Лунки трижды промывали TTBS и добавляли 100 мкл вторичных антител (козьи антитела против IgG кролика, меченные пероксидазой хрена), разбавленный в фосфатно-солевом буфере с добавлением 0,05% Tween-20 (PBST), содержащий 2% БСА. После отмывали 6 раз TTBS по 250 мкл. Проявляли ТМВ-субстратом 100 мкл. Для остановки реакции использовали 100 мкл 2 М серной кислоты. Измерение оптической плотности проводили при длине волны 450 нм на планшетном фотометре iMark (Bio Rad) (Фигура 9).
Пример 7. Анализ рекомбинантных L.monocytogenes в ИФА-тест системе.
Рекомбинантные штаммы L.monocytogenes выращивали в жидкой питательно среде BHI в течение 12 часов. Бактериальную культуру центрифугировали, удаляли среду и промывали клеточную биомассу фосфатно-солевым буфером. Процедуру повторяли 3 раза. Полученный осадок бактериальной биомассы доводили до оптической плотности 0,2. В лунки 96-луночного планшета вносили по 100 мкл соответствующих тестируемых клеток L. monocytogenes. Планшеты инкубировали при 37°C в течение 1 часа, затем 3 раза отмывали трис-буферным раствором, содержащим 0,05% неионогенного детергента Твин-20 (TTBS). Далее в течение 30 минут осуществляли блокировку системы добавлением в лунки 200 мкл 2% БСА, разведённого в фосфатно-соленом буфере. После удаления блокировочного буфер добавляли 100 мкл анти-InlB (1:20000) или анти-InlA антител (1:4000) и инкубировали 1 час при комнатной температуре при постоянном перемешивании 140 об/мин. После инкубации лунки трижды промывали TTBS и добавляли 100 мкл вторичных антител (козьи антитела против IgG кролика, меченные пероксидазой хрена). Инкубацию осуществляли в течение 1 часа при 25°С. Далее каждую лунку отмывали по 3 раз TTBS в объеме 250 мкл. Для визуализации результатов добавляли 100 мкл ТМВ-субстрата и инкубировали в течение 10-20 минут до появление желаемого окрашивания. Для остановки реакции использовали 100 мкл 2 М серной кислоты. Измерение оптической плотности проводили при длине волны 450 нм на планшетном фотометре iMark (Bio Rad). Схема ИФА представлена на Фигуре 10. Результаты ИФА-анализа рекомбинантных штаммов L. monocytogenes представлены на Фигуре 11.
Пример 8. Анализ изолятов L.monocytogenes, полученных из клинических образцов и объектов окружающей среды.
Было проанализировано 39 изолятов. Все бактериальные клетки выращивали до экспоненциальной фазы на основе BHI, а затем центрифугировали и промывали три раза фосфатно-солевым буфером (PBS). Доводили оптическую плотность до 0,2. Лунки 96-луночного планшета покрывали аликвотами по 100 мкл соответствующих тестируемых клеток L. monocytogenes. Планшеты инкубировали при 37°C в течение 1 часа, отмывали трижды по 250 мкл трис-буферным физиологическим раствором, содержащий 0,05% неиогенного детергента Твин-20 (TTBS), а затем блокировали добавлением в лунки 200 мкл 2% БСА, разведённом в фосфатно-солевом буфере (PBS) в течение 30 минут. Удаляли буфер для блокировки и добавляли 100 мкл анти-InlB (1:20000) или анти-InlA антител (1:4000) в блокировочном буфере с добавлением 0,05% Твин-20 и инкубировали 1 час при комнатной температуре на качалке при 140 об/мин. Лунки трижды промывали TTBS и добавляли 100 мкл вторичных антител (козьи антител против IgG кролика, меченные пероксидазой хрена), разбавленный в фосфатно-солевом буфере с добавлением 0,05% Tween-20 (PBST), содержащий 2% БСА. После отмывали 6 раз TTBS по 250 мкл. Проявляли ТМВ-субстратом 100 мкл. Для остановки реакции использовали 100 мкл 2 М серной кислоты. Измерение оптической плотности проводили при длине волны 450 нм на планшетном фотометре iMark (Bio Rad). Полученные данные для некоторых изолятов представлены в Таблице 2.
Таблица 2. Уровень InlA и InlB в различных изолятах L. monocytogenes, относящиеся к разным клональным комплексам (СС1, СС2 - высоковирулентные, СС7, СС37 - средней вирулентности, СС9 - низковирулентные). «++» - высоковирулентный изолят, «+» средневирулентный изолят, «-» - низковирулентный изолят.
Промышленная применимость
Все приведенные примеры подтверждают эффективность предложенного способа идентификации и дифференциации вирулентных штаммов L. monocytogenes от авирулентных штаммов и других видов Listeria spp и его промышленную применимость.
Литература:
1. Banada, P. P., and Bhunia, A. K. (2008). Antibodies and Immunoassays for Detection of Bacterial Pathogens. Princ. Bact. Detect. Biosensors, Recognit. Recept. Microsystems, 567-602. doi:10.1007/978-0-387-75113-9_21.
2. Braun, L., Dramsi, S., Dehoux, P., Bierne, H., Lindahl, G., and Cossart, P. (1997). InlB: an invasion protein of Listeria monocytogenes with a novel type of surface association. Mol. Microbiol. 25, 285-294. doi:10.1046/J.1365-2958.1997.4621825.X.
3. Cantinelli, T., Chenal-Francisque, V., Diancourt, L., Frezal, L., Leclercq, A., Wirth, T., et al. (2013). Epidemic clones" of listeria monocytogenes are widespread and ancient clonal groups. J. Clin. Microbiol. doi:10.1128/JCM.01874-13.
4. Carlin, C. R., Liao, J., Weller, D., Guo, X., Orsi, R., and Wiedmann, M. (2021). Listeria cossartiae sp. nov., Listeria immobilis sp. nov., Listeria portnoyi sp. nov. and Listeria rustica sp. nov., isolated from agricultural water and natural environments. Int. J. Syst. Evol. Microbiol. 71, 4795. doi:10.1099/IJSEM.0.004795.
5. Haase, J. K., Didelot, X., Lecuit, M., Korkeala, H., Achtman, M., Leclercq, A., et al. (2014). The ubiquitous nature of Listeria monocytogenes clones: a large-scale Multilocus Sequence Typing study. Environ. Microbiol. 16, 405-416. doi:10.1111/1462-2920.12342.
6. Hearty, S., Leonard, P., Quinn, J., and O’Kennedy, R. (2006). Production, characterisation and potential application of a novel monoclonal antibody for rapid identification of virulent Listeria monocytogenes. J. Microbiol. Methods 66, 294-312. doi:10.1016/J.MIMET.2005.12.009.
7. Lathrop, A. A., Banada, P. P., and Bhunia, A. K. (2008). Differential expression of InlB and ActA in Listeria monocytogenes in selective and nonselective enrichment broths. J. Appl. Microbiol. 104, 627-639. doi:10.1111/J.1365-2672.2007.03574.X.
8. Lopes-Luz, L., Silva-Filho, E.,  Venceslau, A., de Sousa, D. R., et al. (2023). Combined antibodies against internalins A and B proteins have potential application in immunoassay for detection of Listeria monocytogenes. J. Food Sci. Technol. 60, 123-131. doi:10.1007/S13197-022-05597-9.
Venceslau, A., de Sousa, D. R., et al. (2023). Combined antibodies against internalins A and B proteins have potential application in immunoassay for detection of Listeria monocytogenes. J. Food Sci. Technol. 60, 123-131. doi:10.1007/S13197-022-05597-9.
9. Lovett, J., Francis, D. W., and Hunt, J. M. (1987). Listeria monocytogenes in Raw Milk: Detection, Incidence, and Pathogenicity. J. Food Prot. 50, 188-192. Available at: http://meridian.allenpress.com/jfp/article-pdf/50/3/188/1654024/0362-028x-50_3_188.pdf [Accessed January 17, 2023].
10. Maury, M. M., Tsai, Y. H., Charlier, C., Touchon, M., Chenal-Francisque, V., Leclercq, A., et al. (2016a). Uncovering Listeria monocytogenes hypervirulence by harnessing its biodiversity. Nat. Genet. 48, 308-313. doi:10.1038/ng.3501.
11. Maury, M. M., Tsai, Y. H., Charlier, C., Touchon, M., Chenal-Francisque, V., Leclercq, A., et al. (2016b). Uncovering Listeria monocytogenes hypervirulence by harnessing its biodiversity. Nat. Genet. doi:10.1038/ng.3501.
12. McClain, D., and Lee, W. (1988). Development of USDA-FSIS method for isolation of Listeria monocytogenes from raw meat and poultry - PubMed. Available at: https://pubmed.ncbi.nlm.nih.gov/3134339/ [Accessed January 17, 2023].
13.  Da Silva, W. P., Aleixo, J. A. G., et al. (2012). Highly specific fiber optic immunosensor coupled with immunomagnetic separation for detection of low levels of Listeria monocytogenes and L. ivanovii. BMC Microbiol. 12, 1-15. doi:10.1186/1471-2180-12-275/TABLES/2.
Da Silva, W. P., Aleixo, J. A. G., et al. (2012). Highly specific fiber optic immunosensor coupled with immunomagnetic separation for detection of low levels of Listeria monocytogenes and L. ivanovii. BMC Microbiol. 12, 1-15. doi:10.1186/1471-2180-12-275/TABLES/2.
14. Nightingale, K. K., Fortes, E. D., Ho, A. J., Schukken, Y. H., Grohn, Y. T., and Wiedmann, M. (2005). Evaluation of farm management practices as risk factors for clinical listeriosis and fecal shedding of Listeria monocytogenes in ruminants. J. Am. Vet. Med. Assoc. 227, 1808-1814. doi:10.2460/javma.2005.227.1808.
15. Nightingale, K. K., Ivy, R. A., Ho, A. J., Fortes, E. D., Njaa, B. L., Peters, R. M., et al. (2008). inlA Premature Stop Codons Are Common among Listeria monocytogenes Isolates from Foods and Yield Virulence-Attenuated Strains That Confer Protection against Fully Virulent Strains. Appl. Environ. Microbiol. 74, 6570. doi:10.1128/AEM.00997-08.
16. Orsi, R. H., Bakker, H. C. de., and Wiedmann, M. (2011). Listeria monocytogenes lineages: Genomics, evolution, ecology, and phenotypic characteristics. Int. J. Med. Microbiol. 301, 79-96. doi:10.1016/J.IJMM.2010.05.002.
17. Rasmussen, O. F., Skouboe, P., Dons, L., Rosen, L., and Olsen, J. E. (1995). Listeria monocytogenes exists in at least three evolutionary lines: evidence from flagellin, invasive associated protein and listeriolysin O genes. Microbiology 141 ( Pt 9), 2053-2061. doi:10.1099/13500872-141-9-2053.
18. Snapir, Y. M., Vaisbein, E., and Nassar, F. (2006). Low virulence but potentially fatal outcome-Listeria ivanovii. Eur. J. Intern. Med. 17, 286-287. doi:10.1016/J.EJIM.2005.12.006.
19. Tamburro, M., Sammarco, M. L., Ammendolia, M. G., Fanelli, I., Minelli, F., and Ripabelli, G. (2015). Evaluation of transcription levels of inlA, inlB, hly, bsh and prfA genes in Listeria monocytogenes strains using quantitative reverse-transcription PCR and ability of invasion into human CaCo-2 cells. FEMS Microbiol. Lett. 362. doi:10.1093/FEMSLE/FNV018.
20. Werbrouck, H., Grijspeerdt, K., Botteldoorn, N., Van Pamel, E., Rijpens, N., Van Damme, J., et al. (2006). Differential inlA and inlB expression and interaction with human intestinal and liver cells by Listeria monocytogenes strains of different origins. Appl. Environ. Microbiol. 72, 3862-3871. doi:10.1128/AEM.02164-05.
21.  M., Bubert, A.,
M., Bubert, A.,  Krajewska, U., Rudnicka, W., and
Krajewska, U., Rudnicka, W., and  (2002). Colony-blot assay with anti-p60 antibodies as a method for quick identification of Listeria in food. Int. J. Food Microbiol. 72, 6371. doi:10.1016/S0168-1605(01)00606-7.
(2002). Colony-blot assay with anti-p60 antibodies as a method for quick identification of Listeria in food. Int. J. Food Microbiol. 72, 6371. doi:10.1016/S0168-1605(01)00606-7.
22. Yu, K. Y., Noh, Y., Chung, M., Park, H. J., Lee, N., Youn, M., et al. (2004). Use of monoclonal antibodies that recognize p60 for identification of Listeria monocytogenes. Clin. Diagn. Lab. Immunol. 11, 446-451. doi:10.1128/CDLI.11.3.446-451.2004.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ дифференциации Listeria monocytogenes от других видов Listeria spp. методом дот-блоттинга с использованием конъюгированных антител против фактора патогенности InlB | 2023 |
|
RU2812147C1 |
| Штаммы-продуценты вариантов рекомбинантного белка Интерналин 321, агониста рецептора фактора роста | 2017 |
|
RU2634416C1 |
| Рекомбинантный интерналин В 321, полученный с помощью штамма Escherichia coli | 2018 |
|
RU2688422C1 |
| ВАКЦИНА ПРОТИВ КРАСНУХИ НА ОСНОВЕ СТРУКТУРНО-МОДИФИЦИРОВАННОГО ВИРУСА РАСТЕНИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2016 |
|
RU2660563C2 |
| РЕЦЕПТОР-НАПРАВЛЕННЫЕ КОНСТРУКЦИИ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2682335C2 |
| ШТАММ ENTERОCOCCUS MUNDTII, ПРОДУЦИРУЮЩИЙ СУБСТАНЦИЮ ПЕПТИДНОЙ ПРИРОДЫ С АНТИЛИСТЕРИОЗНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532227C1 |
| Способ очистки мундтицина Р436 (КС) | 2021 |
|
RU2794803C1 |
| Штамм бактерий Escherichia coli - продуцент рекомбинантного белка NS1 | 2021 |
|
RU2789735C1 |
| Рекомбинантный штамм VV-GMCSF/lact-dGF вируса осповакцины, обладающий онколитической активностью и продуцирующий секретируемый химерный белок, состоящий из гранулоцитарно-макрофагального колониестимулирующего фактора человека и онкотоксического белка лактаптина | 2016 |
|
RU2630672C1 |
| Штамм гибридных культивируемых клеток Homo sapiens/Mus musculus 1B9C7 - продуцент человеческих моноклональных антител, специфичных к протеолитическому домену ботулинического токсина типа A | 2021 |
|
RU2783897C1 |








Группа изобретений относится к области биотехнологии и микробиологии. Представлен способ идентификации штаммов Listeria monocytogenes, а также дифференциации вирулентных штаммов Listeria monocytogenes от авирулентных штаммов и других видов Listeria spp. с помощью выявления ключевых факторов инвазии InlA и InlB в результате комбинации двух последовательных действий: выращивание микроорганизмов в жидкой питательной среде, постановка ИФА-анализа с использованием поликлональных моноспецифических антител против InlA и InlB. Также представлена соответствующая тест-система для осуществления способа. Группа изобретений позволяет дифференцировать вирулентные штаммы L. monocytogenes от авирулентных штаммов и может быть использована для подтверждения наличия вирулентного потенциала штаммов L. monocytogenes, выделенных из загрязненных продуктов питания и клинических образцов. 2 н.п. ф-лы, 11 ил., 2 табл., 8 пр.
1. Тест-система для иммуноферментного анализа штаммов L. monocytogenes, представляющая собой набор реагентов, включающая планшет для иммуноферментного анализа; калибровочные стандарты рекомбинантного белка InlA, имеющего последовательность SEQ ID NO: 2, и рекомбинантного белка InlB в концентрации 1 мг/мл; положительный контроль, представляющий собой культуру L. monocytogenes EGDe; отрицательный контроль, представляющий собой культуру L. innocua SLCC 3379; поликлональные моноспецифические антитела к InlA; поликлональные моноспецифические антитела к InlB; буфер трис-HCl (TBS) с твином-20, pH 7.4 для приготовления раствора объемом 1 л для промывания планшетов; буфер для разведения антител; буфер для разведения бактерий; раствор хромогена, содержащий раствор тетраметилбензидина и стоп-реагент.
2. Способ идентификации и дифференциации вирулентных штаммов Listeria monocytogenes от авирулентных штаммов и других видов Listeria spp, включающий в себя использование тест-системы по п. 1 и представляющий собой непрямой ИФА-анализ, где выращивают бактерии в жидкой питательной среде, отделяют клетки от супернатанта методом центрифугирования, инкубируют для калибровки бактериальные клетки и рекомбинантный белок InlA, имеющий последовательность SEQ ID NO: 2, и рекомбинантный белок InlB от +36°С до +38°С на планшете в течение 1 часа, промывают лунки 3 раза раствором промывочного буфера, блокируют незанятые участки блокировочным буфером на 1 час при комнатной температуре, инкубируют бактериальные клетки с поликлональными моноспецифическими антителами к InlA и к InlB, промывают лунки 3 раза раствором промывочного буфера, инкубируют со вторичными поликлональными антителами, конъюгированными с HRP, промывают лунки 3 раза раствором промывочного буфера, визуализируют с добавлением TMB субстрата, останавливают реакцию, измеряют оптическую плотность на спектрофотометре в каждой лунке при длине волны 450 нм и интерпретируют результаты.
| Центробежная фрикционная муфта для сцепления ведущего вала электродвигателя с ведомым валом машины-орудия | 1926 |
|
SU20412A1 |
| WO 2015126921 A1, 27.08.2015 | |||
| ОДНОВРЕМЕННОЕ ОПРЕДЕЛЕНИЕ, ИДЕНТИФИКАЦИЯ И ДИФФЕРЕНЦИАЦИЯ ЭУБАКТЕРИАЛЬНЫХ ТАКСОНОВ С ПОМОЩЬЮ ГИБРИДИЗАЦИОННОГО АНАЛИЗА | 1995 |
|
RU2154106C2 |
Авторы
Даты
2023-11-29—Публикация
2023-05-04—Подача