В данном документе предусмотрены конъюгаты, содержащие сульфонамид формулы (I) и активный фармацевтический ингредиент, такой как аналог инсулина, содержащий по меньшей мере одну мутацию по сравнению с исходным инсулином, где аналог инсулина содержит мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой. Дополнительно в данном документе представлены сульфонамиды формулы (A) и аналоги инсулина, содержащие по меньшей мере одну мутацию по сравнению с исходным инсулином, где аналоги инсулина содержат мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Более чем 400 миллионов человек по всему миру страдают от сахарного диабета 1 или 2 типа. Диабет 1 типа лечат с помощью замещения инсулина. В отличие от сахарного диабета 1 типа при сахарном диабете 2 типа по сути не наблюдается дефицит инсулина, но в целом ряде случаев, особенно на поздних стадиях, пациентов с диабетом 2 типа лечат инсулином.
У здорового человека высвобождение инсулина поджелудочной железой тесно связано с концентрацией глюкозы в крови. Повышенные уровни глюкозы в крови, как те, которые возникают после приема пищи, быстро компенсируются соответствующим повышением секреции инсулина. В состоянии натощак уровень инсулина в плазме крови падает до базального значения, которое является достаточным для обеспечения непрерывного поступления глюкозы к чувствительным к инсулину органам и тканям, и для поддержания продуцирования глюкозы в печени на низком уровне ночью. Зачастую замещение эндогенной секреции инсулина экзогенной, в основном подкожным введением инсулина, не обеспечивает достижение качества физиологической регуляции глюкозы в крови, описанной выше. Могут возникать отклонения уровней глюкозы в крови в сторону повышения или сторону понижения, которые в их наиболее тяжелых формах могут представлять собой угрозу жизни. Из этого следует, что улучшенная терапия сахарного диабета в первую очередь должна быть направлена на поддержание уровня глюкозы в крови в физиологическом диапазоне, насколько это возможно.
Человеческий инсулин представляет собой полипептид из 51 аминокислоты, который разделен на 2 аминокислотных цепи: А-цепь, имеющую 21 аминокислоту, и цепь В, имеющую 30 аминокислот. Цепи соединяются между собой с помощью 2 дисульфидных мостиков. Третья дисульфидная связь существует между остатками цистеина в положениях 6 и 11 A-цепи. Некоторые продукты, используемые в настоящее время для лечения сахарного диабета, содержат аналоги инсулина, т. е. варианты инсулина, последовательность которых отличается от последовательности человеческого инсулина одной или несколькими аминокислотными заменами в А-цепи и/или в B-цепи.
Как и многие другие пептидные гормоны человеческий инсулин имеет короткий период полужизни in vivo. Таким образом его вводят часто, что ассоциировано с дискомфортом для пациента. Следовательно, необходимы аналоги инсулина с увеличенным периодом полужизни in vivo и, таким образом, с увеличенной продолжительностью действия.
В настоящее время существуют разные подходы к увеличению периода полужизни вариантов инсулина.
Один подход основан на разработке растворимого состава при низком pH, но с пониженной растворимостью по сравнению с нативным инсулином при физиологическом pH. Изоэлектрическая точка аналога инсулина увеличена за счет добавления двух остатков аргинина к С-концу В-цепи. Добавление двух остатков аргинина в комбинации с заменой глицина в положении A21 (инсулин гларгин) обеспечивает инсулин с увеличенной продолжительностью действия. Аналог инсулина осаждается в присутствии цинка при инъекции в подкожные участки и медленно растворяется, что приводит к постоянному присутствию инсулина гларгина.
В WO 2016/006963 раскрыты аналоги инсулина, имеющие пониженную скорость выведения, опосредованного рецепторами инсулина, по сравнению с человеческим инсулином.
В WO 2018/056764 раскрыты аналоги инсулина, имеющие пониженную скорость выведения, опосредованного рецепторами инсулина, по сравнению с человеческим инсулином.
В WO 2008/034881 раскрыты аналоги инсулина, стабилизированные протеазой.
В другом подходе группа длинноцепочных жирных кислот конъюгирована с эпсилон-аминогруппой LysB29 инсулина. Присутствие этой группы позволяет присоединять инсулин к сывороточному альбумину посредством нековалентного обратимого связывания. Как следствие, этот аналог инсулина имеет значительно более длительный профиль действия по сравнению с человеческим инсулином (см., например Mayer et al., Inc. Biopolymers (Pept Sci) 88: 687-713, 2007; или WO 2009/115469).
КРАТКОЕ ОПИСАНИЕ
В данном документе предусмотрены аналоги инсулина длительного действия. Предусмотренные аналоги инсулина длительного действия имеют очень низкую аффинность связывания (следовательно, более низкую скорость выведения), при этом сохраняя высокую степень передачи сигнала. Аналоги инсулина описаны в разделе А ниже.
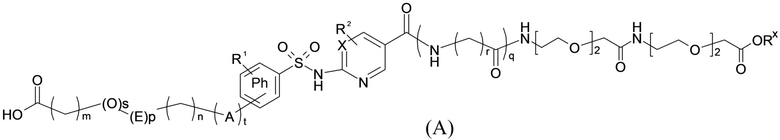
В данном документе предусмотрены связывающие сывороточный альбумин фрагменты (в данном документе также называемые "связывающие альбумин вещества" или "связывающие вещества"), которые при связывании с пептидом, таким как аналог инсулина, предусмотренный выше, приводят, например, к улучшению фармакодинамических и/или фармакокинетических свойств пептида, например, увеличению фармакокинетического периода полужизни в крови и/или плазме крови, и/или длительному профилю действия, т. е. длительному снижению уровня глюкозы в крови. Предусмотренные связывающие альбумин вещества представляют собой сульфонамиды формулы (A).
 .
.
Фрагменты, связывающие сывороточный альбумин, описаны в разделе B ниже.
В данном документе также предусмотрены конъюгаты, содержащие активный фармацевтический ингредиент, такой как аналог инсулина, определенный в разделе A, и связывающее инсулин вещество, такое как сульфонамид формулы (A), определенный в разделе B. Конъюгаты описаны в разделе C ниже.
ПОДРОБНОЕ ОПИСАНИЕ
Раздел А. Аналоги инсулина
Для увеличения продолжительности действия лекарственного средства период полужизни играет большую роль. Период полужизни (t1/2) пропорционален объему распределения, деленному на клиренс. В случае человеческого инсулина клиренс в основном обусловлен связыванием с рецептором инсулина, интернализацией и последующим разрушением.
Соответственно, существует потребность в аналогах инсулина, которые имеют пониженную связывающую активность инсулина с рецептором и, следовательно, пониженную скорость выделения, опосредованную рецептором, но которые имеют активность передачи сигнала, которая позволяет в достаточной степени снизить уровень глюкозы в крови in vivo.
Неожиданно в контексте исследований, лежащих в основе настоящего изобретения, было показано, что замена в положении B16 и/или B25 человеческого инсулина гидрофобной аминокислотой (такой как лейцин, изолейцин, валин, аланин и триптофан) приводила к снижению активности связывания с рецептором инсулина (по сравнению с активностью связывания с рецептором инсулина исходного инсулина, см. "Примеры"). Наиболее сильные эффекты на активность связывания рецептора инсулина наблюдались при заменах аминокислот с разветвленной цепью (лейцин, изолейцин и валин). Интересно, что аналоги инсулина с такими заменами в этих положениях (например, в положении B25) показали в 6 раз большее усиление передачи сигнала, чем ожидалось, исходя из их аффинности связывания изоформы B (IR-B) рецептора инсулина (см. "Примеры"). Дополнительно некоторые тестированные аналоги инсулина показали улучшенную протеолитическую стабильность к α-химотрипсину, катепсину D и ферменту, разрушающему инсулин (см. "Примеры").
Соответственно, в данном документе предусмотрены аналоги инсулина, содержащие по меньшей мере одну мутацию по сравнению с исходным инсулином, при этом аналоги инсулина содержат мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой.
Выражение "аналог инсулина", используемое в данном документе, относится к пептиду, который характеризуется молекулярной структурой, которая формально может быть получена исходя из структуры встречающегося в природе инсулина (в данном документе также называемого "исходный инсулин", например, человеческий инсулин) посредством делеции и/или замены по меньшей мере одного аминокислотного остатка, который присутствует во встречающемся в природе инсулине, и/или добавления по меньшей мере одного аминокислотного остатка. Добавленный и/или замененный аминокислотный остаток могут представлять собой либо кодируемые аминокислотные остатки, либо другие встречающиеся в природе остатки, либо аминокислотные остатки, полученные исключительно синтетическим путем. Аналог, который указывается в данном документе, способен снижать уровень глюкозы в крови in vivo, например у субъекта-человека.
В некоторых вариантах осуществления аналог инсулина, предусмотренный в данном документе, содержит две пептидные цепи, A-цепь и B-цепь. Как правило, две цепи связаны дисульфидными мостиками между остатками цистеина. Например, в некоторых вариантах осуществления аналоги инсулина, предусмотренные в данном документе, содержат три дисульфидных мостика: один дисульфидный мостик между остатками цистеина в положении A6 и A11, один дисульфидный мостик между цистеином в положении A7 A-цепи и цистеином в положении B7 B-цепи и один между цистеином в положении A20 A-цепи и цистеином в положении B19 B-цепи. Соответственно, аналоги инсулина, предусмотренные в данном документе, могут содержать остатки цистеина в положениях A6, A7, A11, A20, B7 и B19.
В некоторых вариантах осуществления, предусмотренных в данном документе, аналог инсулина представляет собой одноцепочечный инсулин. Одноцепочечный инсулин представляет собой одиночные полипептидные цепи, в которых B-цепь инсулина смежно связана с A-цепью инсулина через не расщепляемый соединяющий пептид.
Мутации инсулина, т. е. мутации исходного инсулина, обозначены в данном документе со ссылкой на цепь, то есть либо на A-цепь, либо на B-цепь аналога, положение мутированного аминокислотного остатка в A- или B-цепи (такое как A14, B16 и B25) и трехбуквенный код аминокислоты, заменяющей нативную аминокислоту в исходном инсулине. Термин "desB30" относится к аналогу, в котором отсутствует аминокислота B30 из исходного инсулина (т. е. аминокислота в положении B30 отсутствует). Например, человеческий инсулин Glu(A14)Ile (B16)desB30 представляет собой аналог человеческого инсулина, в котором аминокислотный остаток в положении 14 А-цепи (A14) человеческого инсулина заменен глутаминовой кислотой, аминокислотный остаток в положении 16 B-цепи (B16) заменен изолейцином и аминокислота в положении 30 B-цепи удалена (т. е. отсутствует).
Предусмотренные в данном документе аналоги инсулина содержат по меньшей мере одну мутацию (замену, делецию или добавление аминокислоты) по сравнению с исходным инсулином. Используемый в данном документе термин "по меньшей мере один" означает один или более чем один, например "по меньшей мере два", "по меньшей мере три", "по меньшей мере четыре", "по меньшей мере пять" и т. д. В некоторых вариантах осуществления аналоги инсулина, предусмотренные в данном документе, содержат по меньшей мере одну мутацию в B-цепи и по меньшей мере одну мутацию в A-цепи. В дополнительном варианте осуществления аналоги инсулина, предусмотренные в данном документе, содержат по меньшей мере две мутации в B-цепи и по меньшей мере одну мутацию в A-цепи. Например, аналог инсулина может содержать замену в положении B16, делецию в положении B30 и замену в положении A14. В качестве альтернативы, аналог инсулина может содержать замену в положении B25, делецию в положении B30 и замену в положении A14. Дополнительно аналог инсулина может содержать замену в положении B16, замену в положении В25, делецию в положении B30 и замену в положении A14.
Предусмотренные в данном документе аналоги инсулина могут содержать мутации в дополнение к мутациям, указанным выше. В некоторых вариантах осуществления количество мутаций не превышает определенного количества. В некоторых вариантах осуществления аналоги инсулина содержат менее двенадцати мутаций (т. е. делеций, замен, добавлений) по сравнению с исходным инсулином. В другом варианте осуществления аналог содержит менее десяти мутаций по сравнению с исходным инсулином. В другом варианте осуществления аналог содержит менее восьми мутаций по сравнению с исходным инсулином. В другом варианте осуществления аналог содержит менее семи мутаций по сравнению с исходным инсулином. В другом варианте осуществления аналог содержит менее шести мутаций по сравнению с исходным инсулином. В другом варианте осуществления аналог содержит менее пяти мутаций по сравнению с исходным инсулином. В другом варианте осуществления аналог содержит менее четырех мутаций по сравнению с исходным инсулином. В другом варианте осуществления аналог содержит менее трех мутаций по сравнению с исходным инсулином.
Выражение "исходный инсулин", используемое в данном документе, относится к встречающемуся в природе инсулину, т. е. к немутантному инсулину дикого типа. В некоторых вариантах осуществления исходный инсулин представляет собой инсулин животного происхождения, такой как инсулин млекопитающих. Например, исходный инсулин может представлять собой инсулин человека, свиной инсулин или бычий инсулин.
В некоторых вариантах осуществления исходный инсулин представляет собой человеческий инсулин. Последовательность человеческого инсулина хорошо известна в данной области техники и показана в таблице 4 в разделе "примеры". Человеческий инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 1 (GIVEQCCTSICSLYQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 2 (FVNQHLCGSHLVEALYLVCGERGFFYTPKT).
В другом варианте осуществления исходный инсулин представляет собой бычий инсулин. Последовательность бычьего инсулина хорошо известна в данной области техники. Бычий инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 81 (GIVEQCCASVCSLYQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 82 (FVNQHLCGSHLVEALYLVC-GERGFFYTPKA).
В другом варианте осуществления исходный инсулин представляет собой свиной инсулин. Последовательность свиного инсулина хорошо известна в данной области техники. Свиной инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 83 (GIVEQCCTSICSLYQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 84 (FVNQHLCGSHLVEALYLVC GERGFFYTPKA).
Человеческий, бычий и свиной инсулин содержат три дисульфидных мостика: один дисульфидный мостик между остатками цистеина в положении A6 и A11, один дисульфидный мостик между цистеином в положении A7 A-цепи и цистеином в положении B7 B-цепи и один между цистеином в положении A20 A-цепи и цистеином в положении B19 B-цепи.
Предусмотренные в данном документе аналоги инсулина имеют аффинность связывания с рецепторами инсулина, которая снижена по сравнению с аффинностью связывания с рецепторами инсулина соответствующего исходного инсулина, например человеческого инсулина.
Рецептор инсулина может представлять собой любой рецептор инсулина млекопитающего, такой как рецептор бычьего, свиного или человеческого инсулина. В некоторых вариантах осуществления рецептор инсулина представляет собой рецептор человеческого инсулина, например изоформу A рецептора человеческого инсулина или изоформу B рецептора человеческого инсулина (которая использовалась в разделе "Примеры").
Преимущественно аналоги человеческого инсулина, предусмотренные в данном документе, имеют значительно сниженную аффинность связывания с рецептором человеческого инсулина по сравнению с аффинностью связывания человеческого инсулина с рецептором человеческого инсулина (см. примеры). Таким образом, аналоги инсулина имеют очень низкую скорость выведения, то есть очень низкую скорость выведения, опосредованную рецепторами инсулина.
В некоторых вариантах осуществления аналоги инсулина, т. е. проявляют, менее 20% аффинности связывания с соответствующим рецептором инсулина по сравнению с его исходным инсулином. В другом варианте осуществления аналоги инсулина, предусмотренные в данном документе, имеют менее 10% аффинности связывания с соответствующим рецептором инсулина по сравнению с его исходным инсулином. В другом варианте осуществления аналоги инсулина, предусмотренные в данном документе, имеют менее 5% аффинности связывания с соответствующим рецептором инсулина по сравнению с его исходным инсулином, например менее 3% аффинности связывания по сравнению с его исходным инсулином. Например, аналоги инсулина, предусмотренные в данном документе, могут иметь от 0,1% до 10%, например от 0,3% до 5% аффинности связывания с соответствующим рецептором инсулина по сравнению с его исходным инсулином. Также аналоги инсулина, предусмотренные в данном документе, могут иметь от 0,5% до 3%, например от 0,5% до 2% аффинности связывания с соответствующим рецептором инсулина по сравнению с его исходным инсулином.
Способы определения аффинности связывания аналога инсулина с рецептором инсулина хорошо известны в данной области техники. Например, аффинность связывания с рецепторами инсулина может быть определена с помощью сцинтилляционного анализа сближения, который основан на оценке конкурентного связывания между [125I]-меченным исходным инсулином, таким как [125I]-меченый человеческий инсулин, и (немеченым) аналогом инсулина с рецептором инсулина. Рецептор инсулина может присутствовать в мембране клетки, например клетки СНО (яичника китайского хомячка), которая сверхэкспрессирует рецептор рекомбинантного инсулина. В варианте осуществления аффинность связывания с рецепторами инсулина определяют, как описано в разделе "Примеры".
Связывание встречающегося в природе инсулина или аналога инсулина с рецептором инсулина активирует сигнальный путь инсулина. Рецептор инсулина имеет тирозинкиназную активность. Связывание инсулина с его рецептором индуцирует конформационное изменение, которое стимулирует аутофосфорилирование рецептора на остатках тирозина. Аутофосфорилирование рецептора инсулина стимулирует тирозинкиназную активность рецептора в отношении внутриклеточных субстратов, участвующих в передаче сигнала. Аутофосфорилирование рецептора инсулина аналогом инсулина, таким образом, рассматривается как мера передачи сигнала, вызванной указанным аналогом.
Аналоги инсулина в таблице 4 раздела "Примеры" подвергали анализам аутофосфорилирования. Интересно, что аналоги инсулина с алифатическими заменами в положениях B16 и B25 обуславливали более высокую, чем ожидалось, степень аутофосфорилирования рецептора инсулина на основании их значений аффинности связывания с рецепторами инсулина. Таким образом, аналоги инсулина, предусмотренные в данном документе, имеют низкую связывающую активность и, следовательно, более низкую скорость выведения, опосредованную рецептором, но, тем не менее, способны обуславливать относительно высокую степень передачи сигнала. Следовательно, аналоги инсулина, предусмотренные в данном документе, могут быть использованы в качестве вариантов инсулина длительного действия. В некоторых вариантах осуществления аналог инсулина, предусмотренный в данном документе, способен индуцировать аутофосфорилирование от 1 до 10%, например от 2 до 8%, рецепторов инсулина по сравнению с исходным инсулином (таким как человеческий инсулин). Дополнительно в некоторых вариантах осуществления аналоги инсулина, предусмотренные в данном документе, способны индуцировать аутофосфорилирование от 3 до 7%, например от 5 до 7% рецепторов инсулина по сравнению с исходным инсулином (таким как человеческий инсулин). Аутофосфорилирование рецептора инсулина по сравнению с исходным инсулином может быть определено, как описано в разделе "Примеры".
Предусмотренные в данном документе аналоги инсулина подвергали анализам устойчивости к протеазам. Как показано в таблице 6, аналоги инсулина, предусмотренные в данном документе, имели более высокой устойчивостью по отношению к по меньшей мере некоторым из протестированных протеаз по сравнению с человеческим инсулином. Повышенная протеолитическая стабильность наблюдалась в отношении α-химотрипсина, катепсина D и фермента, разрушающего инсулин (IDE). Соответственно, аналоги инсулина, предусмотренные в данном документе, как правило, являются протеолитически стабильными аналогами инсулина. Таким образом, они медленнее разрушаются протеазами по сравнению с исходным инсулином. В некоторых вариантах осуществления аналог инсулина, предусмотренный в данном документе, стабилен в отношении разрушения α-химотрипсином, катепсином D и ферментом, разрушающим инсулин (IDE), по сравнению с исходным инсулином.
Как изложено выше, аналог инсулина содержит по меньшей мере одну мутацию по сравнению с исходным инсулином.
В некоторых вариантах осуществления аналоги инсулина, предусмотренные в данном документе, содержат мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой. Таким образом, аминокислота в положении B16 (тирозин в человеческом, бычьем и свином инсулине) замещается гидрофобной аминокислотой.
В другом варианте осуществления аналоги инсулина, предусмотренные в данном документе, содержат мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой. Таким образом, аминокислота в положении B25 (фенилаланин в человеческом, бычьем и свином инсулине) заменяется гидрофобной аминокислотой.
В другом варианте осуществления аналоги инсулина, предусмотренные в данном документе, содержат мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой.
Гидрофобная аминокислота может представлять собой любую гидрофобную аминокислоту. Например, гидрофобная аминокислота может представлять собой алифатическую аминокислоту, такую как аминокислота с разветвленной цепью.
В некоторых вариантах осуществления аналогов инсулина, предусмотренных в данном документе, гидрофобная аминокислота, используемая для замены в положении B16 и/или B25, представляет собой изолейцин, валин, лейцин, аланин, триптофан, метионин, пролин, глицин, фенилаланин или тирозин (или производные вышеперечисленных аминокислот).
Некоторые исходные варианты инсулина, такие как человеческий, бычий и свиной инсулин, содержат тирозин в положении B16 и фенилаланин в положении B25. Таким образом, аминокислота в положении B16 исходного инсулина может быть замещена изолейцином, валином, лейцином, аланином, триптофаном, метионином, пролином, глицином или фенилаланином (или производным вышеперечисленных аминокислот). Дополнительно аминокислота в положении B25 исходного инсулина может быть заменена изолейцином, валином, лейцином, аланином, триптофаном, метионином, пролином, глицином или тирозином (или производным вышеперечисленных аминокислот).
Производные вышеперечисленных аминокислот известны в данной области техники.
Производные лейцина включают без ограничения гомолейцин и трет-лейцин. Таким образом, аминокислота в положении B16 и/или B25 может быть замещена гомолейцином или трет-лейцином.
Производным валина является, например, 3-этилнорвалин. Таким образом, аминокислота в положении B16 и/или B25 может быть замещена 3-этилнорвалином.
Производные глицина включают без ограничения циклогексил-глицин, циклопропилглицин и трифторэтилглицин.
Производные аланина включают без ограничения бета-трет-бутилаланин, циклобутилаланин, циклопропилаланин и гомоциклогексилаланин.
В некоторых вариантах осуществления гидрофобная аминокислота, используемая для замены в положении B16 и/или B25, представляет собой изолейцин, валин, лейцин, аланин или триптофан.
В некоторых вариантах осуществления алифатическая аминокислота не является аланином. Соответственно гидрофобная аминокислота, используемая для замены в положении B16 и/или B25 может представлять собой изолейцин, валин, лейцин или триптофан.
В некоторых вариантах осуществления гидрофобная аминокислота, используемая для замены в положении B16 и/или B25, представляет собой изолейцин, валин или лейцин.
В некоторых вариантах осуществления указанные в данном документе аминокислоты представляют собой L-аминокислоты (такие как L-изолейцин, L-валин или L-лейцин). Соответственно, аминокислоты (или их производные), используемые, например, для замены в положении B16, B25 и/или A14, как правило являются L-аминокислотами.
В некоторых вариантах осуществления гидрофобная аминокислота представляет собой алифатическую аминокислоту. Соответственно, аналоги инсулина, предусмотренные в данном документе, содержат мутацию в положении B16, которая представляет собой замену алифатической аминокислотой, и мутацию в положении B25, которая представляет собой замену алифатической аминокислотой (и, необязательно, дополнительные мутации, включая без ограничения Des(B30) и Glu(A14)).
Алифатические аминокислоты представляют собой неполярные и гидрофобные аминокислоты, содержащие функциональную группу алифатической боковой цепи. Гидрофобность увеличивается с увеличением числа атомов углерода в углеводородной цепи. Мерой гидрофобности алифатического соединения является индекс гидрофобности согласно шкале Кайта-Дулиттла, которая, например, может быть определена, как описано Kyte J. et al. Journal of Molecular Biology. 1982 157 (1): 105-32. В некоторых вариантах осуществления алифатическая аминокислота представляет собой алифатическую аминокислоту, имеющую индекс гидрофобности (согласно шкале Кайта-Дулиттла) больше 2,0, например больше 3,0 или больше 3,5.
Алифатические аминокислоты включают без ограничения изолейцин, валин, лейцин, аланин и глицин. Например, алифатическая аминокислота может представлять собой аминокислоту, выбранную из изолейцина, валина, лейцина и глицина, такую как аминокислота, выбранная из изолейцина, валина и лейцина.
Изолейцин, валин и лейцин представляют собой аминокислоты с разветвленной цепью (сокращенно BCAA). Таким образом, алифатическая аминокислота может представлять собой аминокислоту с разветвленной цепью. В некоторых вариантах осуществления аналоги инсулина, предусмотренные в данном документе, содержат мутацию в положении B16, которая представляет собой замену аминокислотой с разветвленной цепью, и мутацию в положении B25, которая представляет собой замену аминокислотой с разветвленной цепью (и, необязательно, дополнительные мутации, включая без ограничения Des(B30) и Glu(A14)).
BCAA представляют собой аминокислоты, такие как изолейцин, валин и лейцин, которые являются аминокислотами с алифатическими боковыми цепями, которые являются нелинейными, т. е. аминокислотами с разветвленной цепью, которые представляют собой аминокислоты, имеющие алифатическую боковую цепь с разветвлением (центральный атом углерода связан с тремя или более атомами углерода).
Аминокислота с разветвленной цепью может представлять собой протеиногенную BCAA, т. е. аминокислоту, которая биосинтетически встраивается в структуру белков во время трансляции, или непротеиногенную BCAA, т. е. аминокислоту, которая не кодируется в естественных условиях или не встречается в генетическом коде ни одного из организмов. Например, протеиногенными BCAA являются лейцин, изолейцин и валин. Таким образом, гидрофобная/алифатическая аминокислота с разветвленной цепью может представлять собой лейцин, изолейцин или валин (или производное лейцина, изолейцина или валина, такое как производное лейцина или валина, как изложено выше).
В некоторых вариантах осуществления аминокислота с разветвленной цепью представляет собой изолейцин. В некоторых вариантах осуществления аминокислота с разветвленной цепью представляет собой валин. В некоторых вариантах осуществления аминокислота с разветвленной цепью представляет собой лейцин.
В дополнение к мутации в положении B16 и/или мутации в положении B25, описанным выше, аналоги инсулина, предусмотренные в данном документе, могут содержать дополнительные мутации по сравнению с исходным инсулином.
Например, аналог инсулина может дополнительно содержать мутацию в положении A14. Известно, что такие мутации повышают устойчивость к протеазам (см., например, WO 2008/034881). В некоторых вариантах осуществления аминокислота в положении A14 заменена глутаминовой кислотой (Glu). В некоторых вариантах осуществления аминокислота в положении A14 заменена аспарагиновой кислотой (Asp). В некоторых вариантах осуществления аминокислота в положении A14 заменена гистидином (His).
Дополнительно аналоги инсулина, предусмотренные в данном документе, могут содержать мутацию в положении B30. В некоторых вариантах осуществления мутация в положении B30 представляет собой делецию треонина в положении B30 исходного инсулина (также называемую Des(B30)-мутацией).
Дополнительно аналог инсулина по настоящему изобретению может дополнительно содержать мутацию в положении B3, которая представляет собой замену глутаминовой кислотой (Glu), и/или мутацию в положении A21, которая представляет собой замену глицином (Gly).
В варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 22 (FVNQHLCGSHLVEALYLVCGERGFLYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 24 (FVNQHLCGSHLVEALYLVCGERGFVYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 44 (FVNQHLCGSHLVEALYLVCGERGFIYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 48 (FVNQHLCGSHLVEALYLVCGERGFVYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 50 (FVEQHLCGSHLVEALYLVCGERGFVYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 58 (FVNQHLCGSHLVEALILVCGERGFIYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 60 (FVEQHLCGSHLVEALILVCGERGFIYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 64 (FVNQHLCGSHLVEALILVCGERGFVYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 66 (FVEQHLCGSHLVEALILVCGERGFVYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 70 (FVNQHLCGSHLVEALVLVCGERGFIYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 78 (FVEQHLCGSHLVEALVLVCGERGFVYTPK).
В другом варианте осуществления B-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность или состоит из аминокислотной последовательности, показанной под SEQ ID NO: 80 (FVEQHLCGSHLVEALVLVCGERGFVYTPK).
Обобщенные выше B-цепи содержат мутацию Des(B30). Соответственно, аминокислота, которая присутствует в положении B30 исходного инсулина (треонин в человеческом инсулине и аланин в свином и бычьем инсулине) удалена, т. е. отсутствует. Однако предусматривается также, что B-цепи аналогов по настоящему изобретению не содержат эту мутацию, т. е. содержат треонин в положении 30. Соответственно, B-цепь аналога инсулина по настоящему изобретению может содержать аминокислотную последовательность, выбранную из группы, состоящей из:
• FVNQHLCGSHLVEALYLVCGERGFLYTPKT (SEQ ID NO: 85);
• FVNQHLCGSHLVEALYLVCGERGFVYTPKT (SEQ ID NO: 86);
• FVNQHLCGSHLVEALYLVCGERGFIYTPKT (SEQ ID NO: 87);
• FVNQHLCGSHLVEALYLVCGERGFVYTPKT (SEQ ID NO: 88);
• FVEQHLCGSHLVEALYLVCGERGFVYTPKT (SEQ ID NO: 89);
• FVNQHLCGSHLVEALILVCGERGFIYTPKT (SEQ ID NO: 90);
• FVEQHLCGSHLVEALILVCGERGFIYTPKT (SEQ ID NO: 91);
• FVNQHLCGSHLVEALILVCGERGFVYTPKT (SEQ ID NO: 92);
• FVEQHLCGSHLVEALILVCGERGFVYTPKT (SEQ ID NO: 93);
• FVNQHLCGSHLVEALVLVCGERGFIYTPKT (SEQ ID NO: 94);
• FVNQHLCGSHLVEALVLVCGERGFVYTPKT (SEQ ID NO: 95);
• FVEQHLCGSHLVEALVLVCGERGFVYTPKT (SEQ ID NO: 96);
• FVEQHLCGSHLVEALVLVCGERGFVYTPKT (SEQ ID NO: 97), или состоять из нее.
В варианте осуществления А-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность, показанную под SEQ ID NO: 1 (GIVEQCCTSICSLYQLENYCN), или состоит из нее.
В другом варианте осуществления А-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность, показанную под SEQ ID NO: 43 (GIVEQCCTSICSLEQLENYCN), или состоит из нее.
В другом варианте осуществления А-цепь аналога инсулина по настоящему изобретению содержит аминокислотную последовательность, показанную под SEQ ID NO: 45 (GIVEQCCTSICSLEQLENYCG), или состоит из нее.
Как правило, аналог инсулина по настоящему изобретению содержит А-цепь и В-цепь, как изложено выше.
Например, аналог инсулина по настоящему изобретению выбран из группы, состоящей из
Leu(B16)-инсулина (например, человеческого инсулина, т. е. Leu(B16)-человеческого инсулина),
Val(B16)-инсулина (например, человеческого инсулина, т. е. Val(B16)-человеческого инсулина),
Ile(В16)-инсулина (например, человеческого инсулина),
Leu(B16)Des(B30)-инсулина (например, человеческого инсулина),
Val(B16)Des(B30)-инсулина (например, человеческого инсулина),
Ile(B16)Des(B30)-инсулина (например, человеческого инсулина),
Leu(B25)-инсулина (например, человеческого инсулина),
Val(B25)-инсулина (например, человеческого инсулина),
Ile(B25)-инсулина (например, человеческого инсулина),
Leu(B25)Des(B30)-инсулина (например, человеческого инсулина),
Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Leu(B16)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B16)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B16)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Leu(B16)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B16)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B16)-инсулина (например, человеческого инсулина),
Glu(A14)Leu(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Leu(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Glu(A14)Gly(A21)Glu(B3)Val(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B16)Ile(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Glu(B3)Ile(B16)Ile(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Ile(B16)Val(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B16)Ile(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Val(B16)Val(B25)-инсулина (например, человеческого инсулина),
Glu(A14)Glu(B3)Val(B16)Val(B25)-инсулина (например, человеческого инсулина) и
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)-инсулина (например, человеческого инсулина).
В другом варианте осуществления аналоги инсулина, предусмотренные в данном документе, выбраны из группы, состоящей из
Asp(A14)Leu(B16)Des(B30)-инсулина (например, человеческого инсулина, т. е. Asp(A14)Leu(B16)Des(B30)-человеческого инсулина),
Asp(A14)Ile(B16)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B16)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Leu(B16)-инсулина (например, человеческого инсулина),
Asp(A14)Ile(B16)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B16)-инсулина (например, человеческого инсулина),
Asp(A14)Leu(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Leu(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Ile(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Ile(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Ile(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
Asp(A14)Gly(A21)Glu(B3)Val(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Ile(B16)Ile(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Glu(B3)Ile(B16)Ile(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Ile(B16)Val(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B16)Ile(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Val(B16)Val(B25)-инсулина (например, человеческого инсулина),
Asp(A14)Glu(B3)Val(B16)Val(B25)-инсулина (например, человеческого инсулина), и
Asp(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)-инсулина (например, человеческого инсулина).
В другом варианте осуществления аналоги инсулина, предусмотренные в данном документе, выбраны из группы, состоящей из
His(A14)Leu(B16)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Ile(B16)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Val(B16)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Leu(B16)-инсулина (например, человеческого инсулина),
His(A14)Ile(B16)-инсулина (например, человеческого инсулина),
His(A14)Val(B16)-инсулина (например, человеческого инсулина),
His(A14)Leu(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Leu(B25)-инсулина (например, человеческого инсулина),
His(A14)Ile(B25)-инсулина (например, человеческого инсулина),
His(A14)Val(B25)-инсулина (например, человеческого инсулина),
His(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Ile(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Ile(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Val(B16)Ile(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулина (например, человеческого инсулина),
His(A14)Gly(A21)Glu(B3)Val(B25)-инсулина (например, человеческого инсулина),
His(A14)Ile(B16)Ile(B25)-инсулина (например, человеческого инсулина),
His(A14)Glu(B3)Ile(B16)Ile(B25)-инсулина (например, человеческого инсулина),
His(A14)Ile(B16)Val(B25)-инсулина (например, человеческого инсулина),
His(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)-инсулина (например, человеческого инсулина),
His(A14)Val(B16)Ile(B25)-инсулина (например, человеческого инсулина),
His(A14)Val(B16)Val(B25)-инсулина (например, человеческого инсулина),
His(A14)Glu(B3)Val(B16)Val(B25)-инсулина (например, человеческого инсулина),
His(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)-инсулина (например, человеческого инсулина).
В другом варианте осуществления аналог инсулина представляет собой Leu(B25)Des(B30)-инсулин (такой как Leu(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 11). Например, Leu(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 21 (GIVEQCCTSICSLYQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 22 (FVNQHLCGSHLVEALYLVCGERGFLYTPK).
В другом варианте осуществления аналог инсулина представляет собой Val(B25)Des(B30)-инсулин (такой как Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 12). Например, Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 23 (GIVEQCCTSICSLYQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 24 (FVNQHLCGSHLVEALYLVCGERGFVYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Ile(B25)Des(B30)-инсулин (такой как Glu(A14)Ile(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 22). Например, Glu(A14)Ile(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 43 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 44 (FVNQHLCGSHLVEALYLVCGERGFIYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 24). Например, Glu(A14)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 47 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 48 (FVNQHLCGSHLVEALYLVCGERGFVYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 25). Например, Glu(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 49 (GIVEQCCTSICSLEQLENYCG), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 50 (FVEQHLCGSHLVEALYLVCGERGFVYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Ile(B16)Ile(B25)Des(B30)-инсулин (такой как Glu(A14)Ile(B16)Ile(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 29). Например, Glu(A14)Ile(B16)Ile(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 57 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 58 (FVNQHLCGSHLVEALILVCGERGFIYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-инсулин (такой как Glu(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 30). Например, Glu(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 56 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 60 (FVEQHLCGSHLVEALILVCGERGFIYTPK).
В другом варианте осуществления аналогом инсулина является Glu(A14)Ile(B16)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Ile(B16)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 32). Например, Glu(A14)Ile(B16)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 63 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 64 (FVNQHLCGSHLVEALILVCGERGFVYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 33). Например, Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 65 (GIVEQCCTSICSLEQLENYCG), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 66 (FVEQHLCGSHLVEALILVCGERGFVYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Val(B16)Ile(B25)Des(B30)-инсулин (такой как Glu(A14)Val(B16)Ile(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 35). Например, Glu(A14)Val(B16)Ile(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 69 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 70 (FVNQHLCGSHLVEALVLVCGERGFIYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Val(B16)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Val(B16)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 38). Например, Glu(A14)Val(B16)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 75 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 76 (FVNQHLCGSHLVEALVLVCGERGFVYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 39). Например, Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 77 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 78 (FVEQHLCGSHLVEALVLVCGERGFVYTPK).
В другом варианте осуществления аналог инсулина представляет собой Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 40). Например, Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 79 (GIVEQCCTSICSLEQLENYCG), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 80 (FVEQHLCGSHLVEALVLVCGERGFVYTPK).
Аналог инсулина можно получить любым способом, считающимся подходящим. Например, аналог инсулина можно получить рекомбинантными способами или посредством твердофазного синтеза.
Определения и пояснения, приведенные в данном документе выше, применяются mutatis mutandis к нижеследующему.
В данном документе предусмотрены B-цепи инсулина, т. е. пептиды B-цепи инсулина, определенные в данном документе выше, применительно к B-цепи аналога инсулина, предусмотренного в данном документе. Соответственно, в данном документе предусмотрены B-цепи инсулина, которые содержат по меньшей мере одну мутацию относительно инсулиновой B-цепи исходного инсулина, где B-цепи содержат мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой. B-цепь инсулина может содержать дополнительные мутации, описанные в данном документе выше, такие как делеция des(B30).
Также в данном документе предусмотрены проинсулины, содержащие А-цепь инсулина и/или инсулиновую В-цепь аналогов инсулина, предусмотренных в данном документе. B-цепь может представлять собой любую B-цепь, определенную в данном документе выше для аналогов инсулина, предусмотренных в данном документе. Например, в данном документе предусмотрены проинсулины, содержащие А-цепь инсулина и B-цепь инсулина, где указанная B-цепь содержит по меньшей мере одну мутацию относительно B-цепи исходного инсулина, где мутация находится в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутация находится в положении B25, которая представляет собой замену гидрофобной аминокислотой. B-цепь инсулина может содержать дополнительные мутации, описанные в данном документе выше для B-цепи.
А-цепь, содержащаяся в проинсулине, предусмотренном в данном документе, может представлять собой любую А-цепь, определенную в данном документе выше для аналогов инсулина, предусмотренных в данном документе. В некоторых вариантах осуществления A-цепь указанного проинсулина содержит мутацию в положении A14, которая представляет собой замену аминокислотой, выбранной из глутаминовой кислоты (Glu), аспарагиновой кислоты (Asp) и гистидина (His).
В дополнение к А-цепи инсулина и/или В-цепи инсулина, проинсулины, предусмотренные в данном документе, могут содержать дополнительные элементы, такие как лидерные последовательности или С-пептид. В некоторых вариантах осуществления проинсулин может дополнительно содержать C-пептид, который расположен между B-цепью инсулина и A-цепью инсулина. С-пептид может иметь длину от 4 до 10 аминокислот, например от 4 до 9 аминокислот. Ориентация может быть следующей (от N-конца к C-концу): В-цепь, С-пептид, А-цепь.
В данном документе предусмотрены полинуклеотиды, кодирующие аналоги инсулина, В-цепи инсулина и проинсулины, предусмотренные в данном документе. Указанный полинуклеотид может быть функционально связан с промотором, который обеспечивает экспрессию указанного полинуклеотида. В некоторых вариантах осуществления промотор является гетерологичным по отношению к указанному полинуклеотиду. В некоторых вариантах осуществления промотор представляет собой конститутивный промотор. В другом варианте осуществления промотор представляет собой индуцируемый промотор.
Дополнительно в данном документе предусмотрены векторы, содержащие полинуклеотид, кодирующий аналоги инсулина, предусмотренные в данном документе. В некоторых вариантах осуществления указанный вектор представляет собой вектор экспрессии.
В данном документе предусмотрены клетки-хозяева, содержащие нуклеиновые кислоты, кодирующие аналоги инсулина, В-цепи инсулина и проинсулины, полинуклеотиды и/или векторы, предусмотренные в данном документе. В некоторых вариантах осуществления клетка-хозяин представляет собой бактериальную клетку, такую как клетка, принадлежащая к роду Escherichia, например клетка E. coli. В другом варианте осуществления клетка-хозяин представляет собой дрожжевую клетку, такую как клетка Pichia pastoris или клетка Klyveromyces lactis.
В данном документе предусмотрены фармацевтические композиции, содержащие фармацевтически эффективное количество аналога инсулина, предусмотренного в данном документе, и фармацевтически приемлемое вспомогательное вещество.
В данном документе предусмотрены способы лечения заболевания, включающие введение субъекту фармацевтически эффективного количества одного или нескольких аналогов инсулина, предусмотренных в данном документе, или их фармацевтической композиции.
В некоторых вариантах осуществления заболевание представляет собой сахарный диабет, такой как сахарный диабет II типа.
В данном документе предусмотрены аналоги инсулина или их фармацевтические композиции для применения в медицине.
В данном документе предусмотрены аналоги инсулина или их фармацевтическая композиция для применения в лечении сахарного диабета, такого как сахарный диабет II типа.
Наконец, в данном документе предусмотрены варианты применения аналогов инсулина, предусмотренных в данном документе, или их фармацевтических композиций для приготовления лекарственного препарата или лекарственного средства для лечения сахарного диабета, такого как сахарный диабет II типа.
Аналоги инсулина, B-цепи инсулина, проинсулины и варианты их применения, описанные в разделе A, дополнительно проиллюстрированы следующими вариантами осуществления и комбинациями вариантов осуществления, как указано с помощью соответствующих зависимостей и обратных ссылок. Определения и пояснения, приведенные в данном документе выше, применяются mutatis mutandis к следующим вариантам осуществления.
1. Аналог инсулина, содержащий по меньшей мере одну мутацию по сравнению с исходным инсулином, где аналог инсулина содержит мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой.
2. Аналог инсулина по варианту осуществления 1, где исходный инсулин представляет собой человеческий инсулин, свиной инсулин или бычий инсулин.
3. Аналог инсулина по вариантам осуществления 1 и 2, где гидрофобная аминокислота в положении B16 и/или положении B25 представляет собой алифатическую аминокислоту.
4. Аналог инсулина по любому из вариантов осуществления 1-3, где указанная алифатическая аминокислота в положении B16 и/или положении B25 представляет собой аминокислоту с разветвленной цепью, такую как аминокислота с разветвленной цепью, выбранная из группы, состоящей из валина (Val), изолейцина (Ile) и лейцина (Leu).
5. Аналог инсулина по любому из вариантов осуществления 1-3, где указанный аналог инсулина дополнительно содержит мутацию в положении A14, которая представляет собой замену аминокислотой, выбранной из группы, состоящей из глутаминовой кислоты (Glu), аспарагиновой кислоты (Asp) и гистидина (His).
6. Аналог инсулина по любому из вариантов осуществления 1-5, где указанный аналог инсулина дополнительно содержит мутацию в положении B30, например, где мутация в положении B30 представляет собой делецию аминокислоты в положении B30 исходного инсулина (Des(B30)-мутация).
7. Аналог инсулина по любому из вариантов осуществления 1-6, где указанный аналог инсулина дополнительно содержит мутацию в положении B3, которая представляет собой замену глутаминовой кислотой (Glu).
8. Аналог инсулина по любому из вариантов осуществления 1-7, где указанный инсулин дополнительно содержит мутацию в положении A21, которая представляет собой замену глицином (Gly).
9. Аналог инсулина по любому из вариантов осуществления 1-8, где B-цепь аналога инсулина содержит аминокислотную последовательность, выбранную из группы, состоящей из
FVNQHLCGSHLVEALYLVCGERGFLYTPK (SEQ ID NO: 22),
FVNQHLCGSHLVEALYLVCGERGFIYTPK (SEQ ID NO: 44),
FVNQHLCGSHLVEALYLVCGERGFVYTPK (SEQ ID NO: 48),
FVEQHLCGSHLVEALYLVCGERGFVYTPK (SEQ ID NO: 50),
FVNQHLCGSHLVEALILVCGERGFIYTPK (SEQ ID NO: 58),
FVEQHLCGSHLVEALILVCGERGFIYTPK (SEQ ID NO: 60),
FVNQHLCGSHLVEALILVCGERGFVYTPK (SEQ ID NO: 64),
FVEQHLCGSHLVEALILVCGERGFVYTPK (SEQ ID NO: 66),
FVNQHLCGSHLVEALVLVCGERGFIYTPK (SEQ ID NO: 70),
FVNQHLCGSHLVEALVLVCGERGFVYTPK (SEQ ID NO: 76),
FVEQHLCGSHLVEALVLVCGERGFVYTPK (SEQ ID NO: 78),
FVEQHLCGSHLVEALVLVCGERGFVYTPK (SEQ ID NO: 80),
FVNQHLCGSHLVEALYLVCGERGFLYTPKT (SEQ ID NO: 85),
FVNQHLCGSHLVEALYLVCGERGFVYTPKT (SEQ ID NO: 86),
FVNQHLCGSHLVEALYLVCGERGFIYTPKT (SEQ ID NO: 87),
FVNQHLCGSHLVEALYLVCGERGFVYTPKT (SEQ ID NO: 88),
FVEQHLCGSHLVEALYLVCGERGFVYTPKT (SEQ ID NO: 89),
FVNQHLCGSHLVEALILVCGERGFIYTPKT (SEQ ID NO: 90),
FVEQHLCGSHLVEALILVCGERGFIYTPKT (SEQ ID NO: 91),
FVNQHLCGSHLVEALILVCGERGFVYTPKT (SEQ ID NO: 92),
FVEQHLCGSHLVEALILVCGERGFVYTPKT (SEQ ID NO: 93),
FVNQHLCGSHLVEALVLVCGERGFIYTPKT (SEQ ID NO: 94),
FVNQHLCGSHLVEALVLVCGERGFVYTPKT (SEQ ID NO: 95),
FVEQHLCGSHLVEALVLVCGERGFVYTPKT (SEQ ID NO: 96) и
FVEQHLCGSHLVEALVLVCGERGFVYTPKT (SEQ ID NO: 97) или состоит из нее.
10. Аналог инсулина по любому из вариантов осуществления 1-9, содержащий
(a) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 43 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 44 (FVNQHLCGSHLVEALYLVCGERGFIYTPK),
(b) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 47 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 48 (FVNQHLCGSHLVEALYLVCGERGFVYTPK), или
(c) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 77 (GIVEQCCTSICSLEQLENYCN) и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 78 (FVEQHLCGSHLVEALVLVCGERGFVYTPK).
11. Аналог инсулина, выбранный из группы, состоящей из
Leu(B16)-человеческого инсулина,
Val(B16)-человеческого инсулина,
Ile(B16)-человеческого инсулина,
Leu(B16)Des(B30)-человеческого инсулина,
Val(B16)Des(B30)-человеческого инсулина,
Ile(B16)Des(B30)-человеческого инсулина,
Leu(B25)-человеческого инсулина,
Val(B25)-человеческого инсулина,
Ile(B25)-человеческого инсулина,
Leu(B25)Des(B30)-человеческого инсулина,
Val(B25)Des(B30)-человеческого инсулина,
Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B16)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B16)-человеческого инсулина,
Glu(A14)Ile(B16)-человеческого инсулина,
Glu(A14)Val(B16)-человеческого инсулина,
Glu(A14)Leu(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B25)-человеческого инсулина,
Glu(A14)Ile(B25)-человеческого инсулина,
Glu(A14)Val(B25)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B25)-человеческого инсулина,
Glu(A14)Ile(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Glu(B3)Ile(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Ile(B16)Val(B25)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)-человеческого инсулина,
Glu(A14)Val(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Val(B16)Val(B25)-человеческого инсулина,
Glu(A14)Glu(B3)Val(B16)Val(B25)-человеческого инсулина и
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)-человеческого инсулина.
12. B-цепь инсулина, содержащая по меньшей мере одну мутацию относительно B-цепи исходного инсулина, где B-цепь содержит мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой.
13. B-цепь инсулина по варианту осуществления 12, где исходный инсулин представляет собой человеческий инсулин, свиной инсулин или бычий инсулин.
14. B-цепь инсулина по вариантам осуществления 12 и 13, где гидрофобная аминокислота в положении B16 и/или положении B25 представляет собой алифатическую аминокислоту.
15. B-цепь инсулина по любому из вариантов осуществления 12-14, где указанная алифатическая аминокислота представляет собой аминокислоту с разветвленной цепью, такую как аминокислота с разветвленной цепью, выбранная из группы, состоящей из валина (Val), изолейцина (Ile) и лейцина (Leu).
16. B-цепь инсулина по любому из вариантов осуществления от 12-15, где указанная В-цепь инсулина дополнительно содержит мутацию в положении B3, которая представляет собой замену глутаминовой кислотой (Glu).
17. B-цепь инсулина по любому из вариантов осуществления от 12-16, где указанная В-цепь инсулина дополнительно содержит мутацию в положении B30, где мутация в положении B30 представляет собой делецию аминокислоты в положении B30 исходного инсулина (Des(B30)-мутация).
18. Проинсулин, содержащий А-цепь инсулина и В-цепь инсулина, где В-цепь инсулина содержит по меньшей мере одну мутацию относительно B-цепи исходного инсулина, где B-цепь содержит мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой.
19. Проинсулин по варианту осуществления 18, где A-цепь инсулина указанного проинсулина содержит мутацию в положении A14, которая представляет собой замену аминокислотой, выбранной из глутаминовой кислоты (Glu), аспарагиновой кислоты (Asp) и гистидина (His).
20. Проинсулин по вариантам осуществления 18 и 19, где исходный инсулин представляет собой человеческий инсулин, свиной инсулин или бычий инсулин.
21. Проинсулин по любому из вариантов осуществления 18-20, где гидрофобная аминокислота в положении B16 и/или положении B25 представляет собой алифатическую аминокислоту.
22. Проинсулин по любому из вариантов осуществления 18-21, где указанная алифатическая аминокислота представляет собой аминокислоту с разветвленной цепью, такую как аминокислота с разветвленной цепью, выбранная из группы, состоящей из валина (Val), изолейцина (Ile) и лейцина (Leu).
23. Проинсулин по любому из вариантов осуществления 18-22, где указанный проинсулин дополнительно содержит мутацию в положении B3, которая представляет собой замену глутаминовой кислотой (Glu).
24. Проинсулин по любому из вариантов осуществления 18-23, где указанный проинсулин дополнительно содержит мутацию в положении B30, где мутация в положении B30 представляет собой делецию аминокислоты в положении B30 исходного инсулина (Des(B30)-мутация).
25. Полинуклеотид, кодирующий аналог инсулина по любому из вариантов осуществления 1-11, В-цепь инсулина по любому из вариантов осуществления 12-17 и/или проинсулин по любому из вариантов осуществления 18-24.
26. Вектор экспрессии, содержащий полинуклеотид по варианту осуществления 25.
27. Клетка-хозяин, содержащая аналог инсулина по любому из вариантов осуществления 1-11, В-цепь инсулина по любому из вариантов осуществления 12-17, проинсулин по любому из вариантов осуществления 18-24, полинуклеотид по варианту осуществления 25 и/или вектор экспрессии по варианту осуществления 26.
28. Способ лечения пациента, страдающего сахарным диабетом, включающий введение пациенту одного или нескольких аналогов инсулина, как определено в любом из вариантов осуществления 1-11.
29. Аналог инсулина, определенный в любом из вариантов осуществления 1-11 для применения в лечении сахарного диабета.
Раздел В. Фрагменты, связывающие сывороточный альбумин
В данном документе предусмотрены связывающие сывороточный альбумин фрагменты (в данном документе также называемые "связывающие альбумин вещества" или "связывающие вещества"), которые при связывании с пептидом, таким как аналог инсулина, предусмотренный выше, приводят, например, к улучшению фармакодинамических и/или фармакокинетических свойств пептида, например, увеличению фармакокинетического периода полужизни в крови и/или плазме крови, и/или длительному профилю действия, т. е. длительному снижению уровня глюкозы в крови. Предусмотренные связывающие сывороточный альбумин фрагменты представляют собой сульфонамиды, описанные в данном документе ниже.
Неожиданно было обнаружено, что такие пептидные конъюгаты могут быть получены с использованием специфических сульфонамидов, которые могут быть использованы для пептидных конъюгатов. Полученные пептидные конъюгаты обладают благоприятным периодом полужизни в крови и/или плазме крови и длительным профилем действия. Можно показать, что полученные пептидные конъюгаты имеют увеличенный фармакокинетический период полужизни (t1/2) и также увеличенное среднее время удержания (MRT) по сравнению с неконъюгированными пептидами. Более того, пептидные конъюгаты имеют значительное продление продолжительности действия in vivo по сравнению с неконъюгированными пептидами.
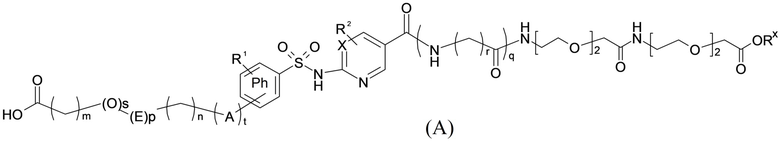
Таким образом, в данном документе предусмотрены сульфонамиды формулы (A)
 ,
,
где:
A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU [1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридин 3-оксид-гексафторфосфата] или HBTU [3-[бис(диметиламино)метилиумил]-3H-бензотриазол-1-оксид-гексафторфосфата]), 4-нитробензол и N-сукцинимидильную группу, где Rx необязательно представляет собой N-сукцинимидильную группу.
В некоторых вариантах осуществления комбинация s, представляющего собой 1, p, представляющего собой ноль, n, представляющего собой ноль, A, представляющего собой атом кислорода, и t, представляющего собой 1, исключается. В некоторых вариантах осуществления s представляет собой ноль, при этом оставшиеся остатки и индексы имеют значение, указанное выше для формулы (A).
Например, галогенированная C1-C3алкильная группа R1 и/или галогенированная C1-C3алкильная группа R2 частично галогенирована(-ы) или пергалогенирована(-ы). В некоторых вариантах осуществления галогенированная C1-C3алкильная группа R1 и/или галогенированная C1-C3алкильная группа R2 пергалогенирована(-ы).
Используемый в данном документе термин "сульфонамиды формулы (A)" включает сульфонамиды формулы (A), их фармацевтически приемлемые соли и все фармацевтически приемлемые изотопно меченные сульфонамиды формулы (A), где один или несколько атомов замещены атомами, которые имеют то же атомное число, но атомную массу или массовое число, отличные от атомной массы или массового числа, которые преобладают в природе. То же самое относится ко всем подтипам сульфонамидов формулы (A), т. е. к сульфонамидам формул (A-1)-(A-5), как подробно описано ниже, и также к их субструктурам соответственно, например, сульфонамидам формулы (А-1-1). Таким образом, термин "сульфонамиды формулы (A-…)", где (A-…) представляет количество сульфонамидов формулы (A-1)-(A-5), как подробно описано ниже, и также их субструктуры, включает сами соединения, их фармацевтически приемлемые соли и все их фармацевтически приемлемые изотопно меченые соединения.
Фармацевтически приемлемые соли сульфонамидов формулы (A) включают основные соли. Подходящие основные соли образуются из оснований, которые образуют нетоксичные соли. Примеры включают соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, бис(2-гидроксиэтил)амин(диоламина), глицина, лизина, магния, меглумина, 2-аминоэтанол(оламина), калия, натрия, 2-амино-2-(гидроксиметил)пропан-1,3-диола (трис или трометамина) и цинка. Обзор подходящих солей см. в Handbook of Pharmaceutical Salts: Properties, Selection, and Use by Stahl and Wermuth (Wiley-VCH, 2002).
Сульфонамиды формулы (A) и их фармацевтически приемлемые соли могут существовать в несольватированной и сольватированной формах. Термин "сольват" используется в данном документе, чтобы описать молекулярный комплекс, содержащий сульфонамиды формулы (A) или их фармацевтически приемлемые соли и одну или несколько молекул фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" применяется, когда указанным растворителем является вода.
Примеры изотопов, подходящих для включения в сульфонамиды формулы (A), включают изотопы водорода, такие как 2H и 3H, углерода, такие как 11C, 13C и 14C, хлора, такие как 36Cl, фтора, такие как 18F, йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15O, 17O и 18O, и серы, такие как 35S.
Определенные изотопно меченые сульфонамиды формулы (A), например те, которые включают радиоактивный изотоп, являются полезными в исследованиях распределения лекарственного средства и/или субстрата в тканях. Радиоактивные изотопы трития, т. е. 3H, и углерода-14, т. е. 14C, особенно полезны для этой цели ввиду простоты их включения и готовых средств обнаружения.
Замена более тяжелыми изотопами, такими как дейтерий, например, 2H, может обеспечивать определенные терапевтические преимущества, которые являются результатом большей метаболической стабильности, например, увеличенного периода полураспада in vivo или уменьшения необходимой дозировки.
Замена изотопами, излучающими позитроны, такими как 11C, 18F, 15O и 13N, может быть полезной в исследованиях позитронно-эмиссионной томографии (PET) для изучения степени занятости рецептора субстратом.
Изотопно меченые сульфонамиды формулы (A) обычно могут быть получены с помощью традиционных методик, известных специалистам в данной области техники.
Фармацевтически приемлемые сольваты в соответствии с настоящим изобретением включают те, где растворитель для кристаллизации может быть изотопно замещен, например D2O, d6-ацетон, d6-DMSO.
Чтобы идентифицировать подходящие связывающие молекулы, которые при связывании с пептидом, таким как инсулин, способны улучшать период полужизни в плазме крови и продлевать профиль действия, была создана система, основанная на аффинной хроматографии с колонками с сывороточным альбумином, т. е. колонками с иммобилизованным сывороточным альбумином.
Эффективное время удерживания связующих веществ (образцов) рассчитывали в соответствии со следующей формулой:
эффективное время удерживания=время удерживания образца - время удерживания t0 маркера.
Сульфонамиды формулы (A) имеют эффективное удерживание в диапазоне 9-19, например в диапазоне 9,5-18, и, следовательно, считались полезными связывающими веществами для пептидных конъюгатов, таких как конъюгаты инсулина.
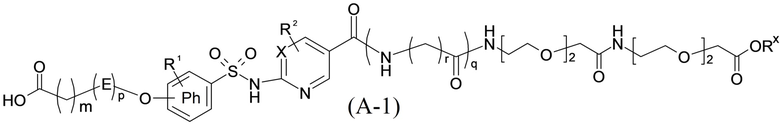
Согласно одному варианту осуществления сульфонамид характеризуется формулой (A-1)
 ,
,
где:
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода, и представляет собой, например, атом фтора;
X представляет собой атом азота или группу -CH-;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода и атома галогена, где атом галогена представляет собой, например, атом фтора или хлора;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, C1-C3алкильной группы и галогенированной C1-C3алкильной группы, где C1-C3алкильная группа представляет собой, например, метильную группу, и галогенированная C1-C3алкильная группа представляет собой, например, пергалогенированную группу, такую как трифторметильная группа;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; где m представляет собой целое число в диапазоне 5-15, если p представляет собой ноль, или m представляет собой целое число в диапазоне 7-15, если p представляет собой 1.
В одном варианте осуществления R1 и R2 представляют собой атомы водорода.
В одном варианте осуществления сульфонамида X представляет собой атом азота.
Согласно другому варианту осуществления сульфонамида группа HOOC-(CH2)m-(O)s-(E)p-(CH2)n-(A)t- формулы (A) или группа HOOC-(CH2)m-(E)p-O- формулы (A-1) находятся в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления сульфонамида если p представляет собой 1, группа HOOC-(CH2)m-(O)s- и группа -(CH2)n-(A)t- находятся в мета- или пара-положении на (E)p формулы (A) или группа HOOC-(CH2)m- и -O- находятся в мета- или пара-положении на (E)p формулы (A-1).
Согласно другому варианту осуществления сульфонамида q представляет собой ноль.
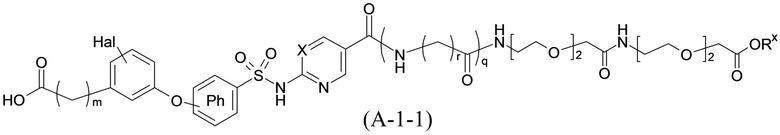
Согласно другому варианту осуществления сульфонамид характеризуется формулой (A-1-1)
 ,
,
где X представляет собой атом азота или группу -CH-, например атом азота; m представляет собой целое число в диапазоне 7-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1, например ноль; Hal представляет собой атом галогена, выбранный из группы, состоящей из атома фтора, хлора, брома и йода, например атома фтора; Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; и группа HOOC-(CH2)m-C6H3Hal-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно одному варианту осуществления сульфонамид характеризуется формулой (A-1-1a)
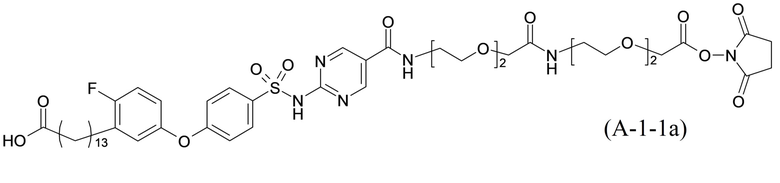 .
.
Согласно другому варианту осуществления сульфонамид характеризуется формулой (A-1-2)
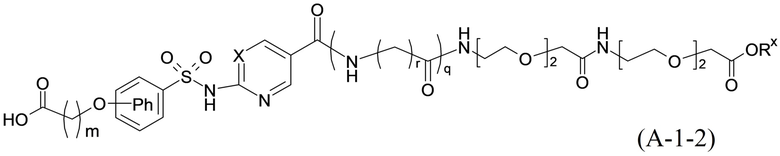 ,
,
где X представляет собой атом азота или группу -CH-, например атом азота; m представляет собой целое число в диапазоне 5-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1, например ноль; Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; и группа HOOC-(CH2)m-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно одному варианту осуществления сульфонамид характеризуется формулой (A-1-2a)
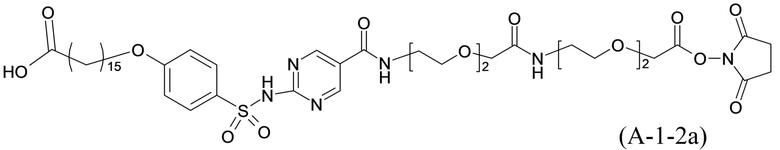 ,
,
или формулой (A-1-2b):
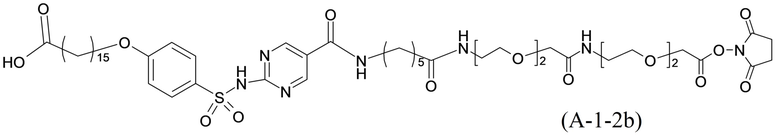 ,
,
или формулой (A-1-2c):
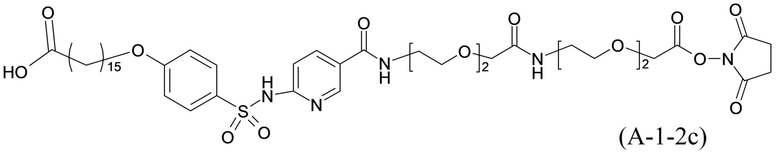 .
.
Согласно другому варианту осуществления сульфонамид характеризуется формулой (A-2)
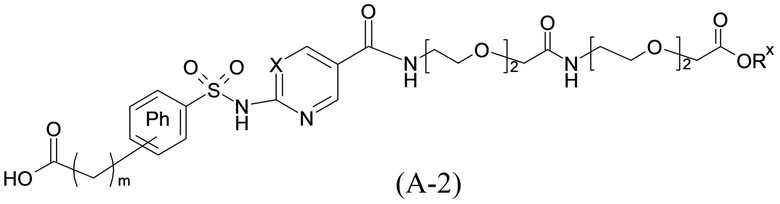 ,
,
где
X представляет собой атом азота или группу -CH-;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; и
m представляет собой целое число в диапазоне 5-17, например в диапазоне 11-17.
Согласно одному варианту осуществления сульфонамида формулы (A-2) группа HOOC-(CH2)m- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления сульфонамид характеризуется формулой (A-3)
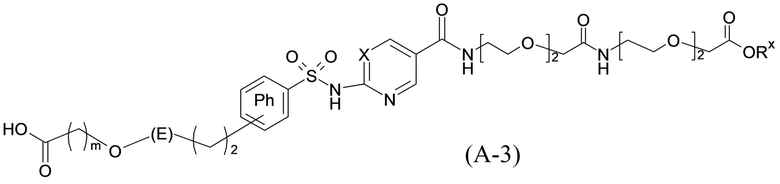 ,
,
где
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; и
m представляет собой целое число в диапазоне 5-17, например 11.
Согласно одному варианту осуществления сульфонамида формулы (A-3), группа HOOC-(CH2)m-O- и группа -(CH2)2- находятся в пара-положении на (E) формулы (A-3) и группа HOOC-(CH2)m-O-(E)-(CH2)2- находится в пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления сульфонамид характеризуется формулой (A-4)
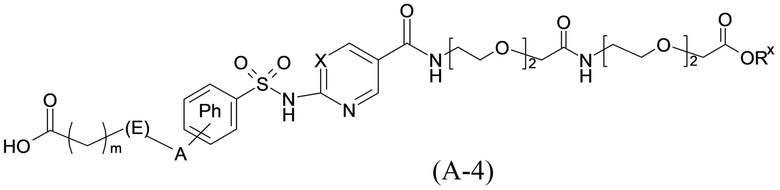 ,
,
где
A представляет собой группу -OCH2- или группу -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; и
m представляет собой целое число в диапазоне 5-17, например в диапазоне 9-13.
Согласно одному варианту осуществления сульфонамида формулы (A-4), группа HOOC-(CH2)m- и группа -А- находятся в пара-положении на (E) формулы (A-4) и группа -А- находится в пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления сульфонамид характеризуется формулой (A-5)
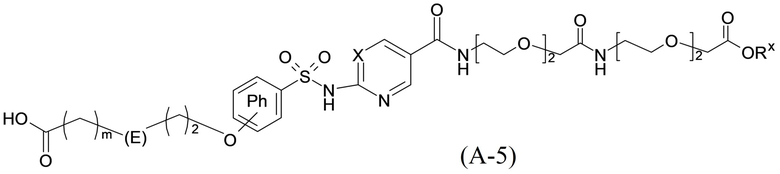 ,
,
где
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; и
m представляет собой целое число в диапазоне 5-17, например в диапазоне 7-9.
Согласно одному варианту осуществления сульфонамида формулы (A-5), группа HOOC-(CH2)m- и группа -(CH2)2- находятся в пара-положении на (E) формулы (A-5) и группа HOOC-(CH2)mE)-(CH2)2-О- находится в пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Связывающие альбумин вещества, описанные в разделе B, дополнительно проиллюстрированы следующими вариантами осуществления и комбинациями вариантов осуществления, как указано с помощью соответствующих зависимостей и обратных ссылок. В частности, следует отметить, что в каждом случае, когда упоминается диапазон вариантов осуществления, например, в контексте такого термина, как "…по любому из вариантов осуществления 1-4", каждый вариант осуществления в этом диапазоне предназначен для того, чтобы быть подробно раскрытым для специалиста, т. е. формулировка этого термина должна пониматься специалистом как синоним "…по любому из вариантов осуществления 1, 2, 3 и 4".
1. Сульфонамид формулы (А)
 ,
,
где:
A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу.
2. Сульфонамид по варианту осуществления 1, имеющий формулу (A-1)
 ,
,
где:
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода и атома галогена;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу, и
где m представляет собой целое число в диапазоне 5-15, если p представляет собой ноль, или m представляет собой целое число в диапазоне 7-15, если p представляет собой 1.
3. Сульфонамид по варианту осуществления 1 или 2, где R1 и R2 представляют собой атомы водорода.
4. Сульфонамид по любому из вариантов осуществления 1-3, где X представляет собой атом азота.
5. Сульфонамид по любому из вариантов осуществления 1-4, где группа HOOC-(CH2)m-(O)s-(E)p-(CH2)n-(A)t- формулы (A) или группа HOOC-(CH2)m-(E)p-O- формулы (A-1) находятся в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
6. Сульфонамид по любому из вариантов осуществления 1-5, где, если p представляет собой 1, группа HOOC-(CH2)m-(O)s- и группа -(CH2)n-(A)t- находятся в мета- или пара-положении на (E)p формулы (A) или группа HOOC-(CH2)m- и -O- находятся в мета- или пара-положении на (E)p формулы (A-1).
7. Сульфонамид по любому из вариантов осуществления 1-6, где q представляет собой ноль.
8. Сульфонамид по любому из вариантов осуществления 1-7, где сульфонамид характеризуется формулой (A-1-1):
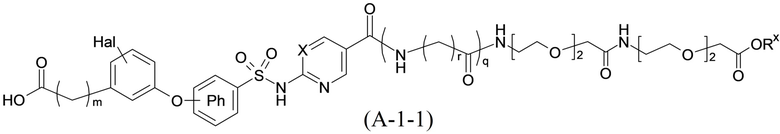 ,
,
где X представляет собой атом азота или группу -CH-; m представляет собой целое число в диапазоне 7-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1; Hal представляет собой атом галогена, выбранный из группы, состоящей из атома фтора, хлора, брома и йода; Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу;
и группа HOOC-(CH2)m-C6H3Hal-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
9. Сульфонамид по любому из вариантов осуществления 1-8, где сульфонамид характеризуется формулой (A-1-1a):
 .
.
10. Сульфонамид по любому из вариантов осуществления 1-7, где сульфонамид характеризуется формулой (A-1-2):
 ,
,
где X представляет собой атом азота или группу -CH-; m представляет собой целое число в диапазоне 5-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1; и группа HOOC-(CH2)m-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
11. Сульфонамид по любому из вариантов осуществления 1-7 или 10, где сульфонамид характеризуется формулой (A-1-2a):
 ,
,
или формулой (A-1-2b):
 , или формулой (A-1-2c):
, или формулой (A-1-2c):
 .
.
Раздел С. Конъюгат
В даном документе предусмотрены конъюгаты, содержащие связывающее альбумин вещество и активный фармацевтический ингредиент или диагностическое соединение. В варианте осуществления связывающее альбумин вещество представляет собой связывающее альбумин вещество, определенное в разделе B выше, и активный фармацевтический ингредиент представляет собой аналог инсулина, определенный в разделе A выше.
В данном документе предусмотрены конъюгаты, содержащие сульфонамид формулы (I) и активный фармацевтический ингредиент или диагностическое соединение.
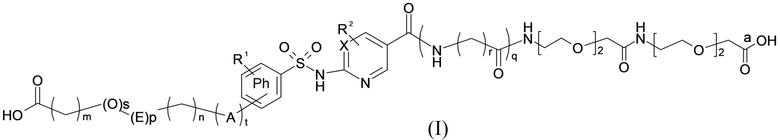 ,
,
где в сульфонамиде формулы (I):
A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
где сульфонамид формулы (I) ковалентно связан с активным фармацевтическим ингредиентом или диагностическим соединением.
В некоторых вариантах осуществления комбинация s, представляющего собой 1, p, представляющего собой ноль, n, представляющего собой ноль, A, представляющего собой атом кислорода, и t, представляющего собой 1, исключается для сульфонамида формулы (I). В некоторых вариантах осуществления s представляет собой ноль, при этом оставшиеся остатки и индексы имеют значение, указанное выше для формулы (I).
В некоторых вариантах осуществления сульфонамид формулы (I) ковалентно связан с активным фармацевтическим ингредиентом или диагностическим соединением, при этом концевая карбоксильная группа "а" сульфонамида формулы (I) ковалентно связана с подходящей функциональной группой активного фармацевтического ингредиента или диагностического соединения, например, с аминогруппой или гидроксильной группой активного фармацевтического ингредиента или диагностического соединения. Например, активный фармацевтический ингредиент представляет собой пептид, где пептид и сульфонамид формулы (I), например, связаны амидной связью, например, образованной между концевой карбоксильной группой "а" сульфонамида формулы (I) и аминогруппой пептида. Само собой разумеется, что в случае амидной связи карбоксильная группа "a" присутствует в конъюгате как карбонильная группа -C(=O)-, как показано ниже, где все остатки E, A, R1, R2, X, а также индексы m, s, p, n, t, r и q имеют значение, указанное выше для формулы (I), и группа NH---- уже является частью, оставшейся от пептидной аминогруппы:
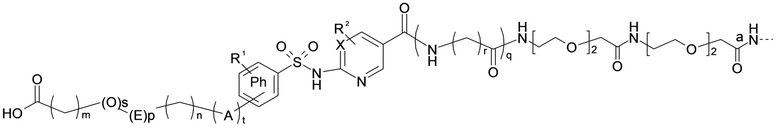 .
.
В некоторых вариантах осуществления галогенированная C1-C3алкильная группа R1 и/или галогенированная C1-C3алкильная группа R2 сульфонамида формулы (I) частично галогенирована(-ы) или пергалогенирована(-ы). В некоторых вариантах осуществления галогенированная C1-C3алкильная группа R1 и/или галогенированная C1-C3алкильная группа R2 сульфонамида формулы (I) частично пергалогенирована(-ы).
Как уже обсуждалось выше, неожиданно было обнаружено, что указанные конъюгаты обладают благоприятным периодом полужизни в крови и/или плазме крови и длительным профилем действия, что, например, было доказано на доклинических моделях на животных.
Используемое в данном документе выражение "активный фармацевтический ингредиент" (API) включает любое фармацевтически активное химическое или биологическое соединение, и любую его фармацевтически приемлемую соль, и любую его смесь, которая обеспечивает некоторый фармакологический эффект и используется для лечения или предупреждения состояния. Подразумевается, что используемые в данном документе выражения "активный фармацевтический ингредиент", "активное средство", "активный ингредиент", "действующее вещество" и "лекарственное средство" являются синонимами, т. е. имеют одинаковое значение.
Используемый в данном документе термин "конъюгаты, содержащие сульфонамид формулы (I) и активный фармацевтический ингредиент или диагностическое соединение" включает сами конъюгаты, их фармацевтически приемлемые соли и фармацевтически приемлемые изотопно меченые конъюгаты, где один или несколько атомов замещены атомами, которые имеют то же атомное число, но атомную массу или массовое число, отличные от атомной массы или массового числа, которые преобладают в природе. То же самое относится ко всем подтипам конъюгатов, т. е. к конъюгатам, содержащим сульфонамиды формул (I-1)-(I-5), как подробно описано ниже, и также к их субструктурам, например, конъюгатам, содержащим сульфонамиды формулы (I-1-1). То же самое относится ко всем подтипам сульфонамидов формулы (I), т. е. к сульфонамидам формул (I-1)-(I-5), как подробно описано ниже, и также к их субструктурам соответственно, например, сульфонамидам формулы (I-1-1). Таким образом, термин "конъюгат, содержащий сульфонамид формулы (I-…)", где (I-…) представляет количество сульфонамидов формулы (I-1)-(I-5), как подробно описано ниже, и также их субструктуры, включает сами конъюгаты, их фармацевтически приемлемые соли и все их фармацевтически приемлемые изотопно меченые соединения.
Фармацевтически приемлемые соли конъюгатов включают соли присоединения кислоты и основные соли. Подходящие соли присоединения кислоты образуются из кислот, которые образуют нетоксичные соли. Примеры включают ацетат, адипат, аспартат, бензоат, безилат, бикарбонат/карбонат, бисульфат/сульфат, борат, камсилат, цитрат, цикламат, эдисилат, эзилат, формиат, фумарат, глюцепат, глюконат, глюкуронат, гексафторфосфат, гибензат, гидрохлорид/хлорид, гидробромид/бромид, гидроиодид/йодид, изетионат, лактат, малат, малеат, малонат, мезилат, метилсульфат, нафтилат, 2-напсилат, никотинат, нитрат, оротат, оксалат, пальмитат, памоат, фосфат/гидрофосфат/дигидрогенфосфат, пироглутамат, сахарат, стеарат, сукцинат, таннат, тартрат, тозилат, трифторацетат, 1,5-нафаталендисульфоновая кислота и соли ксинафоата. Подходящие основные соли образуются из оснований, которые образуют нетоксичные соли. Примеры включают соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, бис(2-гидроксиэтил)амин(диоламина), глицина, лизина, магния, меглумина, 2-аминоэтанол(оламина), калия, натрия, 2-амино-2-(гидроксиметил)пропан-1,3-диола (трис или трометамина) и цинка. Также могут быть образованы полусоли кислот и оснований, например, гемисульфатные и гемикальциевые соли. Обзор подходящих солей см. в Handbook of Pharmaceutical Salts: Properties, Selection, and Use by Stahl and Wermuth (Wiley-VCH, 2002).
Конъюгаты и их фармацевтически приемлемые соли могут существовать в несольватированной и сольватированной формах. Термин "сольват" используется в данном документе, чтобы описать молекулярный комплекс, содержащий соединение формулы I или его фармацевтически приемлемую соль и одну или несколько молекул фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" применяется, когда указанным растворителем является вода.
Примеры изотопов, подходящих для включения в конъюгаты, включают изотопы водорода, такие как 2H и 3H, углерода, такие как 11C, 13C и 14C, хлора, такие как 36Cl, фтора, такие как 18F, йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15O, 17O и 18O, и серы, такие как 35S.
Определенные изотопно меченые конъюгаты, например те, которые включают радиоактивный изотоп, полезны в исследованиях распределения лекарственного средства и/или субстрата в тканях. Радиоактивные изотопы трития, т. е. 3H, и углерода-14, т. е. 14C, особенно полезны для этой цели ввиду простоты их включения и готовых средств обнаружения.
Замена более тяжелыми изотопами, такими как дейтерий, например, 2H, может обеспечивать определенные терапевтические преимущества, которые являются результатом большей метаболической стабильности, например, увеличенного периода полураспада in vivo или уменьшения необходимой дозировки.
Замена изотопами, излучающими позитроны, такими как 11C, 18F, 15O и 13N, может быть полезной в исследованиях позитронно-эмиссионной томографии (PET) для изучения степени занятости рецептора субстратом.
Изотопно меченые конъюгаты обычно могут быть получены с помощью традиционных методик, известных специалистам в данной области техники.
Фармацевтически приемлемые сольваты в соответствии с настоящим изобретением включают те, где растворитель для кристаллизации может быть изотопно замещен, например D2O, d6-ацетон, d6-DMSO.
В одном варианте осуществления активный фармацевтический ингредиент выбран из группы, включающей противодиабетическое средство, средство против ожирения, средство, регулирующее аппетит, антигипертензивное средство, средство для лечения и/или предупреждения осложнений, возникающих вследствие диабета или ассоциированных с ним, и средства для лечения и/или предупреждения осложнений и нарушений, возникающих вследствие ожирения или ассоциированных с ним. Примерами этих активных фармацевтических ингредиентов являются: инсулин, сульфонилмочевины, бигуаниды, меглитиниды, ингибиторы глюкозидазы, антагонисты глюкагона, ингибиторы DPP-IV (дипептидилпептидазы-IV), ингибиторы печеночных ферментов, участвующих в стимуляции глюконеогенеза и/или гликогенолиза, модуляторы поглощения глюкозы, соединения, модифицирующие метаболизм липидов, такие как антигиперлипидемические средства, например ингибиторы HMG CoA (статины), желудочные ингибиторные полипептиды (аналоги GIP), соединения, снижающие потребление пищи, агонисты RXR и средства, действующие на ATP-зависимый калиевый канал клеток; холестирамин, колестипол, клофибрат, гемфиброзил, ловастатин, правастатин, симвастатин, пробукол, декстротироксин, нетеглинид, репаглинид; блокаторы, такие как альпренолол, атенолол, тимолол, пиндолол, пропранолол и метопролол, ингибиторы ACE (ангиотензинпревращающего фермента), такие как беназеприл, каптоприл, эналаприл, фозиноприл, лизиноприл, алатриоприл, хинаприл и рамиприл, блокаторы кальциевых каналов, такие как нифедипин, фелодипин, никардипин, исрадипин, нимодипин, дилтиазем и верапамил, и альфа-блокаторы, такие как доксазозин, урапидил, празозин и теразозин; агонисты CART (кокаин- и амфетамин-регулируемый транскрипт), антагонисты NPY (нейропептида Y), агонисты PYY, агонисты PYY2, агонисты PYY4, смешанные агонисты PPY2/PYY4, агонисты MC4 (меланокортин 4), антагонисты орексина, агонисты TNF (фактора некроза опухоли), агонисты CRF (коритикотропин-рилизинг-фактор), антагонисты CRF BP (белок, связывающий рилизинг-фактор кортикотропина), агонисты урокортина, 3 агониста, агонисты MSH (меланоцит-стимулирующий гормон), антагонисты MCH (меланоцит-концентрирующий гормон), агонисты CCK (холецистокинин), ингибиторы обратного захвата серотонина, ингибиторы обратного захвата серотонина и норадреналина, смешанные серотониновые и норадренергические соединения, агонисты 5HT (серотонина), агонисты бомбезина, антагонисты галанина, гормон роста, соединения, высвобождающие гормон роста, агонисты TRH (тиреотропин-рилизинг гормон), модуляторы UCP 2 или 3 (разобщающий белок 2 или 3), агонисты лептина, агонисты DA (бромокриптин, допрексин), ингибиторы липазы/амилазы, модуляторы RXR (ретиноидного X рецептора), агонисты TR; антагонисты гистамина H3, агонисты или антагонисты желудочного ингибиторного полипептида (аналоги GIP), гастрин и аналоги гастрина. В одном варианте осуществления активный фармацевтический ингредиент выбран из группы, состоящей из противодиабетического средства, средства против ожирения, средства, регулирующего аппетит, антигипертензивного средства, средства для лечения и/или предупреждения осложнений, возникающих вследствие диабета или ассоциированных с ним, и средства для лечения и/или предупреждения осложнений и нарушений, возникающих вследствие ожирения или ассоциированных с ним. Примерами этих активных фармацевтических ингредиентов являются: инсулин, сульфонилмочевины, бигуаниды, меглитиниды, ингибиторы глюкозидазы, антагонисты глюкагона, ингибиторы DPP-IV (дипептидилпептидазы-IV), ингибиторы печеночных ферментов, участвующих в стимуляции глюконеогенеза и/или гликогенолиза, модуляторы поглощения глюкозы, соединения, модифицирующие метаболизм липидов, такие как антигиперлипидемические средства, например ингибиторы HMG CoA (статины), желудочные ингибиторные полипептиды (аналоги GIP), соединения, снижающие потребление пищи, агонисты RXR и средства, действующие на ATP-зависимый калиевый канал клеток; холестирамин, колестипол, клофибрат, гемфиброзил, ловастатин, правастатин, симвастатин, пробукол, декстротироксин, нетеглинид, репаглинид; блокаторы, такие как альпренолол, атенолол, тимолол, пиндолол, пропранолол и метопролол, ингибиторы ACE (ангиотензинпревращающего фермента), такие как беназеприл, каптоприл, эналаприл, фозиноприл, лизиноприл, алатриоприл, хинаприл и рамиприл, блокаторы кальциевых каналов, такие как фелодипин, никардипин, исрадипин, нимодипин, дилтиазем и верапамил, и альфа-блокаторы, такие как доксазозин, урапидил, празозин и теразозин; агонисты CART (кокаин- и амфетамин-регулируемый транскрипт), антагонисты NPY (нейропептида Y), агонисты PYY, агонисты PYY2, агонисты PYY4, смешанные агонисты PPY2/PYY4, агонисты MC4 (меланокортин 4), антагонисты орексина, агонисты TNF (фактора некроза опухоли), агонисты CRF (кортикотропин-рилизинг-фактор), антагонисты CRF BP (белок, связывающий рилизинг-фактор кортикотропина), агонисты урокортина, 3 агониста, агонисты MSH (меланоцит-стимулирующий гормон), антагонисты MCH (меланоцит-концентрирующий гормон), агонисты CCK (холецистокинин), ингибиторы обратного захвата серотонина, ингибиторы обратного захвата серотонина и норадреналина, смешанные серотониновые и норадренергические соединения, агонисты 5HT (серотонина), агонисты бомбезина, антагонисты галанина, гормон роста, соединения, высвобождающие гормон роста, агонисты TRH (тиреотропин-рилизинг гормон), модуляторы UCP 2 или 3 (разобщающий белок 2 или 3), агонисты лептина, агонисты DA (бромокриптин, допрексин), ингибиторы липазы/амилазы, модуляторы RXR (ретиноидного X рецептора), агонисты TR; антагонисты гистамина H3, агонисты или антагонисты желудочного ингибиторного полипептида (аналоги GIP), гастрин и аналоги гастрина.
В одном варианте осуществления активный фармацевтический ингредиент представляет собой терапевтически активный пептид, где пептид содержит по меньшей мере 2 аминокислоты. В некоторых вариантах осуществления пептид содержит по меньшей мере 10 аминокислот или по меньшей мере 20 аминокислот. В некоторых вариантах осуществления пептид содержит не более 1000 аминокислот, например не более 500 аминокислот, например не более 100 аминокислот.
В одном варианте осуществления конъюгата активным фармацевтическим ингредиентом является антидиабетическое средство, такое как пептид. В некоторых вариантах осуществления пептид представляет собой GLP-1, аналог GLP-1, агонист GLP-1; двойной агонист рецептора GLP-1/рецептора глюкагона; человеческий FGF21, аналог FGF21, производное FGF21; инсулин (например, человеческий инсулин), аналог инсулина или производное инсулина.
Согласно одному варианту осуществления конъюгата активный фармацевтический ингредиент выбран из группы, включающей инсулин, аналог инсулина, GLP-1 и аналог GLP-1 (например, агонист GLP(-1)). В одном варианте осуществления конъюгата активный фармацевтический ингредиент выбран из группы, состоящей из инсулина, аналога инсулина, GLP-1 и аналога GLP-1 (например, агониста GLP(-1)).
Используемый в данном документе термин "аналог GLP-1" относится к полипептиду, который характеризуется молекулярной структурой, которая формально может быть получена исходя из структуры встречающегося в природе глюкагоноподобного пептида-1 (GLP-1), например, человеческого GLP-1, посредством делеции и/или замены по меньшей мере одного аминокислотного остатка, который присутствует во встречающемся в природе GLP-1, и/или добавления по меньшей мере одного аминокислотного остатка. Добавленный и/или замененный аминокислотный остаток могут представлять собой либо кодируемые аминокислотные остатки, либо другие встречающиеся в природе остатки, либо аминокислотные остатки, полученные исключительно синтетическим путем.
Используемый в данном документе термин "агонист GLP(-1)" относится к аналогам GLP(-1), которые активируют рецептор глюкагоноподобного пептида-1 (рецептор GLP-1). Примеры агонистов GLP(-1) включают без ограничения следующие: ликсисенатид, экзенатид/эксендин-4, семаглутид, таспоглутид, альбиглутид, дулаглутид.
Ликсисенатид имеет следующую аминокислотную последовательность (SEQ ID NO: 98): His-Gly-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Met-Glu-Glu-Glu-Ala-Val-Arg-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser-Lys-Lys-Lys-Lys-Lys-Lys-NH2
Эксенатид имеет следующую аминокислотную последовательность (SEQ ID NO: 99):
His-Gly-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Met-Glu-Glu-Glu-Ala-Val-Arg-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser- NH2
Семаглутид - связывающее альбумин вещество, связанное с Lys(20), имеет следующую аминокислотную последовательность (SEQ ID NO: 100):
His-Aib-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Val-Ser-Ser-Tyr-Leu-Glu-Gly-Gln-Ala-Ala-Lys(AEEAc-AEEAc-γ-Glu-17-карбоксигептадеканоил)-Glu-Phe-Ile-Ala-Trp-Leu-Val-Arg-Gly-Arg-Gly.
Дулаглутид (GLP1 (7-37), связанный через пептидный линкер с fc-фрагментом) имеет следующую аминокислотную последовательность (SEQ ID NO: 101):
His-Ala-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Val-Ser-Ser-Tyr-Leu-Glu-Gly-Gln-Ala-Ala-Lys-Glu-Phe-Ile-Ala-Trp-Leu-Val-Lys-Gly-Arg-Gly
Используемое в данном документе выражение "FGF-21" означает "фактор роста фибробластов 21". Соединения FGF-21 могут представлять собой человеческий FGF-21, аналог FGF-21 (называемый "аналог FGF-21") или производное FGF-21 (называемое "производное FGF-21").
В некоторых вариантах осуществления активным фармацевтическим ингредиентом является аналог инсулина. Примеры аналогов инсулина включают без ограничения следующие.
(i) 'Инсулин аспарт' представляет собой человеческий инсулин, в котором аминокислота B28 (т. е. аминокислота под номером 28 в B-цепи человеческого инсулина), которая представляет собой пролин, замещена аспарагиновой кислотой.
(ii) "Инсулин лизпро" представляет собой человеческий инсулин, в котором предпоследние остатки лизина и пролина в C-концевой области B-цепи поменяны местами (человеческий инсулин: ProB28LysB29; инсулин лизпро: LysB28ProB29).
(iii) "Инсулин глулизин" отличается от человеческого инсулина тем, что аминокислота аспарагин в положении B3 замещена лизином, а лизин в положении B29 замещен глутаминовой кислотой.
(iv) "Инсулин гларгин" отличается от человеческого инсулина тем, что аспарагин в положении A21 замещен глицином, а B-цепь удлинена на карбоксиконце на два остатка аргинина.
Дополнительный аналог инсулина может представлять собой"инсулин детемир", который отличается от человеческого инсулина тем, что аминокислота треонин в положении B30 удалена и остаток жирной кислоты (миристиновой кислоты) присоединен к эпсилон-аминофункциональной группе лизина в положении B29. Альтернативно, аналог инсулина может представлять собой"инсулин деглудек", который отличается от человеческого инсулина тем, что аминокислота треонин в положении B30 удалена и что гексадекандикарбоновая кислота конъюгирована с аминокислотой лизином B29 через гамма-L-глутамиллинкер. Инсулин деглудек представляет собой инсулин длительного действия.
В некоторых вариантах осуществления аналог инсулина представляет собой аналог инсулина, описанный в разделе A выше. Предусмотренные выше определения и пояснения применяются соответственно. В некоторых вариантах осуществления аналог инсулина, содержащийся в конъюгате, представляет собой аналог инсулина, содержащий по меньшей мере одну мутацию по сравнению с исходным инсулином, где аналог инсулина содержит мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой. Описанный в данном документе выше в разделе А аналог инсулина может необязательно содержать дополнительные мутации. Например, аминокислотный остаток в положении 14 A-цепи (A14) исходного инсулина (такого как человеческий инсулин) может быть заменен глутаминовой кислотой и аминокислота в положении 30 B-цепи может быть удалена, т. е. отсутствовать (мутация desB30).
В некоторых вариантах осуществления аналог инсулина, содержащийся в конъюгате, представляет собой Glu(A14)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 24). Например, Glu(A14)Val(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 47 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 48 (FVNQHLCGSHLVEALYLVCGERGFVYTPK).
В некоторых вариантах осуществления аналог инсулина, содержащийся в конъюгате, представляет собой Glu(A14)Ile(B25)Des(B30)-инсулин (такой как Glu(A14)Ile(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 4 раздела "Примеры" (см. аналог 22). Например, Glu(A14)Ile(B25)Des(B30)-инсулин содержит А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 43 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 44 (FVNQHLCGSHLVEALYLVCGERGFIYTPK).
В некоторых вариантах осуществления аналог инсулина, содержащийся в конъюгате, представляет собой Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-инсулин (такой как Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческий инсулин). Последовательность этого аналога, например, показана в таблице 1 раздела "Примеры" (см. аналог 39).
Согласно одному варианту осуществления конъюгата активный фармацевтический ингредиент представляет собой инсулин или аналог инсулина, например аналог инсулина, указанный выше (такой как Glu(A14)Val(B25)Des(B30)-человеческий инсулин, Glu(A14)Ile(B25)Des(B30)-человеческий инсулин) или Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческий инсулин), где аминогруппа пептида, с которомым сульфонамид формулы (I) ковалентно связан, представляет собой эпсилон-аминогруппу лизина, присутствующего в инсулине или аналоге инсулина, или представляет собой N-концевую аминогруппу В-цепи инсулина или аналога инсулина. Например, инсулин или аналог инсулина имеют один лизин в А-цепи и/или B-цепи. В некоторых вариантах осуществления инсулин или аналог инсулина содержат один лизин в А-цепи и B-цепи.
Согласно одному варианту осуществления конъюгата аминогруппа пептида, с которым ковалентно связан сульфонамид формулы (I), представляет собой эпсилон-аминогруппу лизина, присутствующего в положениях B26-B29, например, B29, B-цепи человеческого инсулина или аналога человеческого инсулина, например аналога человеческого инсулина.
В некоторых вариантах осуществления в аналогах инсулина, предусмотренных в разделе А выше, присутствует один остаток лизина. Например, Glu(A14)Val(B25)Des(B30)-человеческий инсулин, Glu(A14)Ile(B25)Des(B30)-человеческий инсулин) и Glu(A14)Glu(B3)Val(B16)Val(B25) Des(B30)-человеческий инсулин имеют остаток лизина в положении B29. Указанный остаток лизина представляет собой концевую аминокислоту на С-конце B-цепи, поскольку аминокислота в положении B30 отсутствует. В некоторых вариантах осуществления конъюгатов, предусмотренных в данном документе, сульфонамид формулы (I) ковалентно связан с эпсилон-аминогруппой указанного остатка лизина, как правило, через амидную связь.
Типичные конъюгаты показаны на фиг. 5-8 и описаны в разделе "Примеры", например, в примере 10.
В некоторых вариантах осуществления конъюгата, предусмотренного в данном документе, конъюгат содержит Glu(A14)Val(B25)Des(B30)-человеческий инсулин (в качестве аналога инсулина) и сульфонамид следующей формулы (в качестве связывающего альбумин вещества):
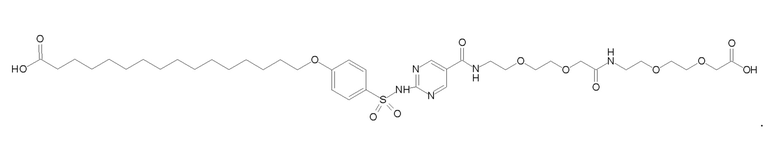
Указанный выше конъюгат может иметь следующую структуру (см. также фиг. 5, конъюгат 1):
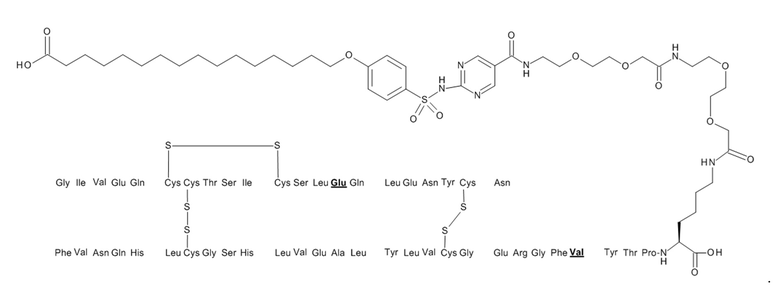 .
.
Последовательности А-цепи (SEQ ID NO: 47) и В-цепи (SEQ ID NO: 48) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминокислоту остатка лизина).
В некоторых вариантах осуществления конъюгата, предусмотренного в данном документе, конъюгат содержит Glu(A14)Val(B25)Des(B30)-человеческий инсулин (в качестве аналога инсулина) и сульфонамид следующей формулы (в качестве связывающего альбумин вещества):
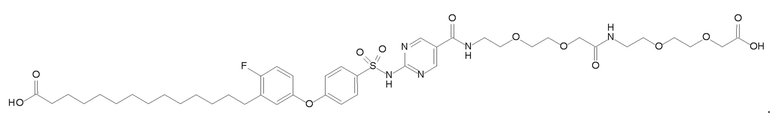
Указанный выше конъюгат может иметь следующую структуру (см. также фиг. 6, конъюгат 2):
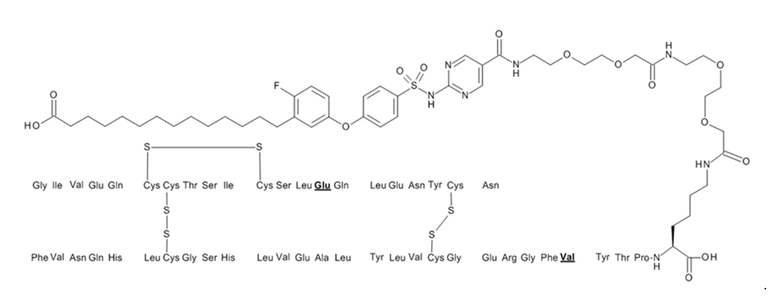
Последовательности А-цепи (SEQ ID NO: 47) и В-цепи (SEQ ID NO: 48) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминокислоту остатка лизина).
В некоторых вариантах осуществления конъюгата, предусмотренного в данном документе, конъюгат содержит Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческий инсулин (в качестве аналога инсулина) и сульфонамид следующей формулы (в качестве связывающего альбумин вещества):
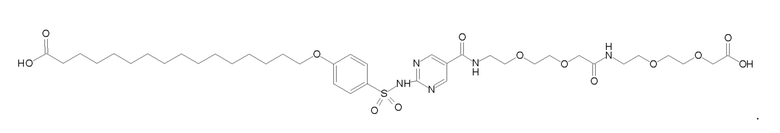
Указанный выше конъюгат может иметь следующую структуру (см. также фиг. 7, конъюгат 3):
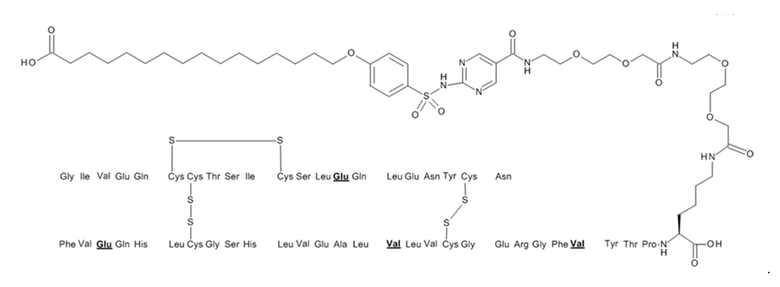
Последовательности А-цепи (SEQ ID NO: 77) и В-цепи (SEQ ID NO: 78) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминокислоту остатка лизина).
В некоторых вариантах осуществления конъюгатов, предусмотренных в данном документе, конъюгат содержит Glu(A14)Ile(B25)Des(B30)-человеческий инсулин (в качестве аналога инсулина) и сульфонамид следующей формулы (в качестве связывающего альбумин вещества):
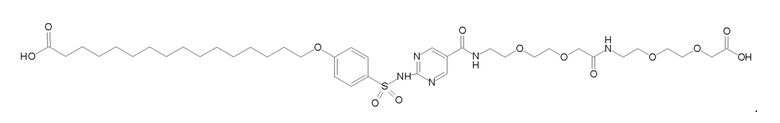
Указанный выше конъюгат может иметь следующую структуру (см. также фиг. 8, конъюгат 4):
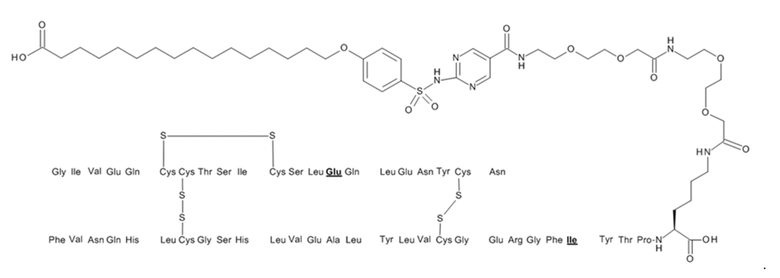
Последовательности А-цепи (SEQ ID NO: 43) и В-цепи (SEQ ID NO: 44) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминогруппу остатка лизина).
Также в данном документе предусмотрены конъюгаты, содержащие диагностическое соединение. В некоторых вариантах осуществления конъюгата диагностическое соединение представляет собой контрастное средство, такое как радиоконтрастное средство. В некоторых вариантах осуществления контрастное средство представляет собой контрастное средство для магнитно-резонансной томографии (MRI) с использованием гадолиния или йода. В некоторых вариантах осуществления контрастное средство представляет собой гадопентетат димеглумина, гадотерат меглумина, гадобенат димеглумина, гадотеридол, гадодиамид, гадоверсетамид, динатрий гадоксетат, амидотризоат или соль амидотризоата, например, соль меглумина, натрия и/или соль лизина амидотризоата, йогексол (5-[ацетил(2,3-дигидроксипропил)амино]-1-N,3-N-бис(2,3-дигидроксипропил)-2,4,6-трийодбензол-1,3-дикарбоксамид), йопамидол (1-N,3-N-бис(1,3-дигидроксипропан-2-ил)-5-[[(2S)-2-гидроксипропаноил]амино]-2,4,6-трийодбензол-1,3-дикарбоксамид), йопромид (1-N,3-N-бис(2,3-дигидроксипропил)-2,4,6-трийод-5-[(2-метоксиацетил)амино]-3-N-метилбензол-1,3-дикарбоксамид) или йоксиданол (5-[ацетил-[3-[ацетил-[3,5-бис(2,3-дигидроксипропилкарбамоил)-2,4,6-трийодфенил]амино]-2-гидроксипропил]амино]-N, N'-бис(2,3-дигидроксипропил)-2,4,6-трийодобензол-1,3-дикарбоксамид). В некоторых вариантах осуществления контрастное средство, выбранное из группы состоящей из гадопентетата димеглумина, гадотерата меглумина, гадобената димеглумина, гадотеридола, гадодиамида, гадоверсетамида, динатрия гадоксетата, амидотризоата или соли амидотризоата, например, соли меглумина, натрия и/или соли лизина амидотризоата, йогексола (5-[ацетил(2,3-дигидроксипропил)амино]-1-N,3-N-бис(2,3-дигидроксипропил)-2,4,6-трийодбензол-1,3-дикарбоксамида), йопамидола (1-N,3-N-бис(1,3-дигидроксипропан-2-ил)-5-[[(2S)-2-гидроксипропаноил]амино]-2,4,6-трийодбензол-1,3-дикарбоксамида), йопромида (1-N,3-N-бис(2,3-дигидроксипропил)-2,4,6-трийод-5-[(2-метоксиацетил)амино]-3-N-метилбензол-1,3-дикарбоксамида) или йоксиданола (5-[ацетил-[3-[ацетил-[3,5-бис(2,3-дигидроксипропилкарбамоил)-2,4,6-трийодфенил]амино]-2-гидроксипропил]амино]-N, N'-бис(2,3-дигидроксипропил)-2,4,6-трийодобензол-1,3-дикарбоксамида).
Как обсуждалось выше, сульфонамид формулы (I) ковалентно связан с диагностическим соединением, при этом концевая карбоксильная группа "а" сульфонамида формулы (I) ковалентно связана с подходящей функциональной группой диагностического соединения. Подходящей функциональной группой может быть, например, аминогруппа (первичная или вторичная) или гидроксильная группа диагностического соединения.
Согласно одному варианту осуществления конъюгата сульфонамид характеризуется формулой (I-1)
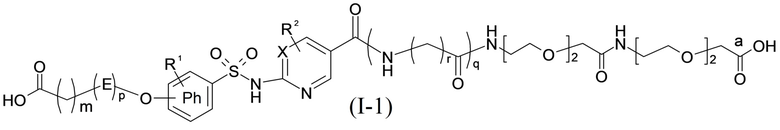 ,
,
где:
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода, и представляет собой, например, атом фтора;
X представляет собой атом азота или группу -CH-;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода и атома галогена, где атом галогена представляет собой, например, атом фтора или хлора;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, C1-C3алкильной группы и галогенированной C1-C3алкильной группы, где C1-C3алкильная группа представляет собой, например, метильную группу и галогенированная C1-C3алкильная группа представляет собой, например, пергалогенированную группу, такую как трифторметильная группа;
где m представляет собой целое число в диапазоне 5-15, если p представляет собой ноль, или m представляет собой целое число в диапазоне 7-15, если p представляет собой 1.
В одном варианте осуществления конъюгата остатки R1 и R2 сульфонамида представляют собой атомы водорода.
В одном варианте осуществления конъюгата остаток X сульфонамида представляет собой атом азота.
Согласно другому варианту осуществления конъюгата группа HOOC-(CH2)m-(O)s-(E)p-(CH2)n-(A)t- формулы (I) или группа HOOC-(CH2)m-(E)p-O- формулы (I-1) сульфонамида находятся в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления конъюгата если p представляет собой 1, группа HOOC-(CH2)m-(O)s- и группа -(CH2)n-(A)t- находятся в мета- или пара-положении на (E)p формулы (I) сульфонамида или группа HOOC-(CH2)m- и -O- находятся в мета- или пара-положении на (E)p формулы (I-1).
Согласно другому варианту осуществления конъюгата индекс q сульфонамида представляет собой ноль.
Согласно другому варианту осуществления конъюгата сульфонамид характеризуется формулой (I-1-1)
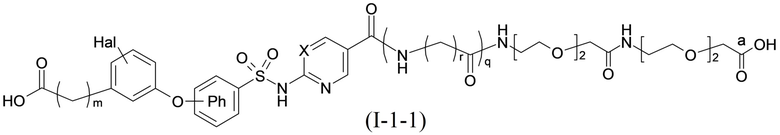 ,
,
где X представляет собой атом азота или группу -CH-, например атом азота; m представляет собой целое число в диапазоне 7-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1, например ноль; Hal представляет собой атом галогена, выбранный из группы, состоящей из атома фтора, хлора, брома и йода, например атома фтора; и группа HOOC-(CH2)m-C6H3Hal-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно одному варианту осуществления конъюгата сульфонамид характеризуется формулой (I-1-1a)
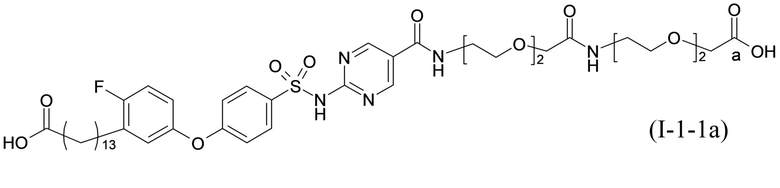 .
.
Согласно другому варианту осуществления конъюгата сульфонамид характеризуется формулой (I-1-2)
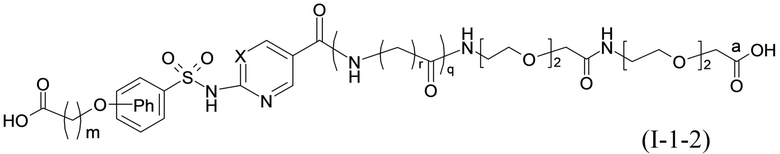 ,
,
где X представляет собой атом азота или группу -CH-, например, атом азота; m представляет собой целое число в диапазоне 5-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1, например, ноль; и группа HOOC-(CH2)m-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно одному варианту осуществления конъюгата сульфонамид характеризуется формулой (I-1-2a)
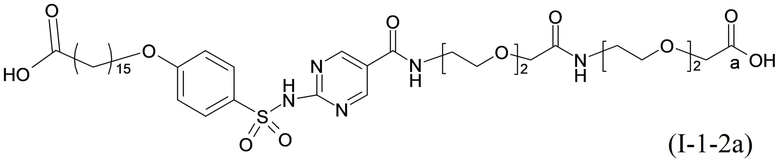 ,
,
или формулой (I-1-2b):
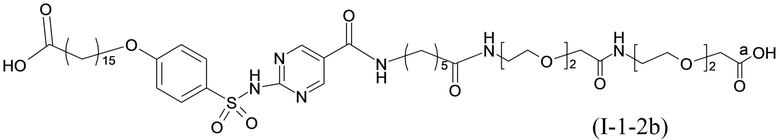 ,
,
или формулой (I-1-2c):
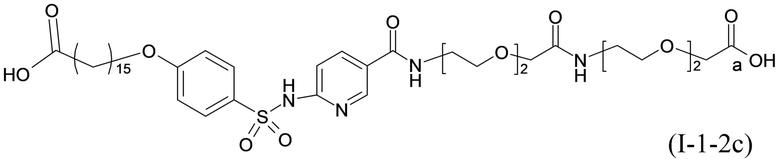 .
.
Согласно одному варианту осуществления конъюгата сульфонамид характеризуется формулой (I-2)
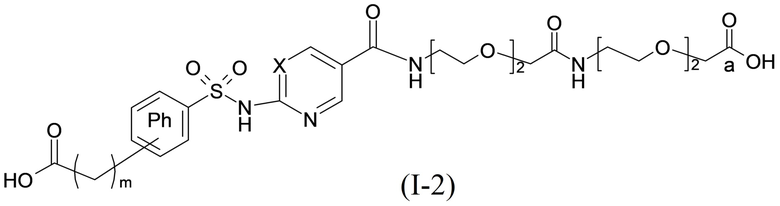 ,
,
где
X представляет собой атом азота или группу -CH-; и
m представляет собой целое число в диапазоне 5-17, например в диапазоне 11-17.
Согласно одному варианту осуществления конъюгата группа HOOC-(CH2)m- сульфонамида формулы (I-2) находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления конъюгата сульфонамид характеризуется формулой (I-3)
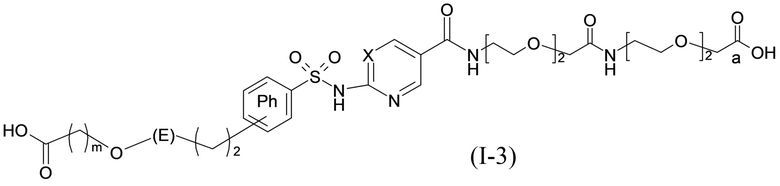 ,
,
где
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17, например 11.
Согласно одному варианту осуществления конъюгата группа HOOC-(CH2)m-O- и
-(CH2)2- группа сульфонамида формулы (I-3) находится в пара-положении на (E) формулы (I-3) и группа HOOC-(CH2)m-O-(E)-(CH2)2- находится в пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления конъюгата сульфонамид характеризуется формулой (I-4)
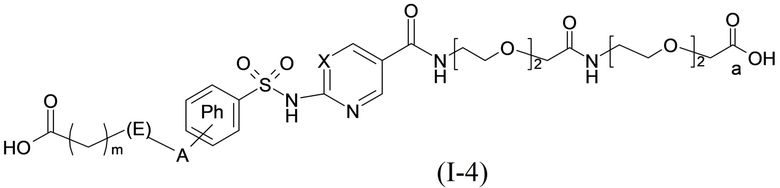 ,
,
где
A представляет собой группу -OCH2- или группу -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17, например в диапазоне 9-13.
Согласно одному варианту осуществления конъюгата, группа HOOC-(CH2)m- и группа -А- сульфонамида формулы (I-4) находятся в пара-положении на (E) формулы (I-4) и группа -А- находится в пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Согласно другому варианту осуществления конъюгата сульфонамид характеризуется формулой (I-5)
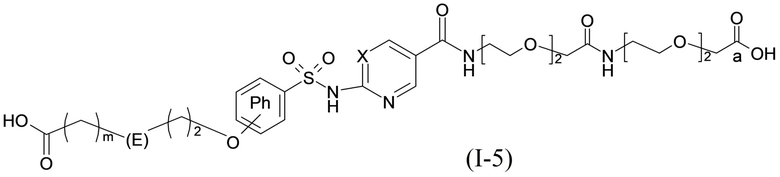 ,
,
где
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17, например в диапазоне 7-9.
Согласно одному варианту осуществления конъюгата группа HOOC-(CH2)m- и группа -(CH2)2- сульфонамида формулы (I-5) находятся в пара-положении на (E) формулы (I-5) и группа HOOC-(CH2)m(E)-(CH2)2-О- находится в пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
Способ получения конъюгата
В данном документе предусмотрены способы получения конъюгата, описанного в разделе C выше. Соответственно, в данном документе предусмотрены способы получения конъюгата, содержащего сульфонамид формулы (I) и активный фармацевтический ингредиент
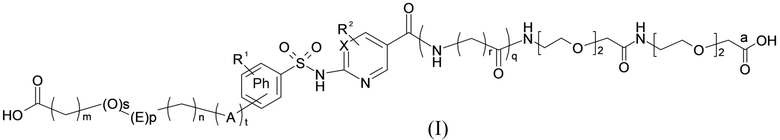 ,
,
где в сульфонамиде формулы (I):
A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
где сульфонамид формулы (I) ковалентно связан с активным фармацевтическим ингредиентом, при этом концевая карбоксильная группа "а" сульфонамида формулы (I) ковалентно связана с аминогруппой активного фармацевтического ингредиента;
(а) получение сульфонамида формулы (Aa)
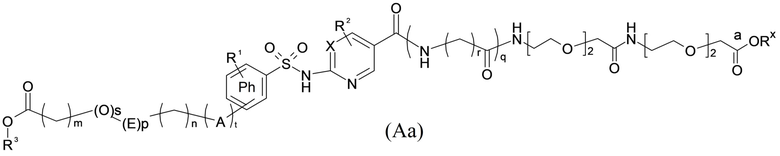 ,
,
где X, Y, A, E, R1, R2 и индексы m, n, p, q, r, s, t имеют значения, указанные выше в отношении формулы (I), Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу,
и R3 представляет собой защитную группу или атом водорода, необязательно атом водорода; и активный фармацевтический ингредиент, имеющий С-конец, содержащий или не содержащий защитную группу;
(b) осуществление реакции сульфонамида формулы (Aa) и активного фармацевтического ингредиента, имеющего С-конец, содержащий или не содержащий защитную группу, в условиях, подходящих для образования амидной связи между свободной или активированной, необязательно активированной, карбоксильной группой "a" сульфонамида формулы (Aa) и аминогруппой активного фармацевтического ингредиента, имеющей С-конец, содержащий или не содержащий защитную группу;
(c) необязательно удаление одной или обеих защитных групп, например удаление обеих защитных групп.
В некоторых вариантах осуществления способа комбинация s, представляющего собой 1, p, представляющего собой ноль, n, представляющего собой ноль, A, представляющего собой атом кислорода, и t, представляющего собой 1, исключается для сульфонамида формулы (I), а также для сульфонамида формулы (Аа). В некоторых вариантах осуществления s представляет собой ноль для сульфонамида формулы (I), а также для сульфонамида формулы (Aa), при этом оставшиеся остатки и индексы имеют значения, указанные выше для формулы (I) и (Aa) соответственно.
Также возможно получить конъюгат, описанный в данном документе в разделе C выше, с помощью способа, включающего:
а) получение сульфонамида формулы (Aa), где Rx представляет собой активирующую группу (Rx=активирующая группа);
b) получение водного раствора активного фармацевтического ингредиента, где водный раствор необязательно содержит спирт;
c) приведение в контакт водного раствора b) с сульфонамидом формулы (Аа) (Rx=активирующая группа) из а); и
d) осуществление реакции сульфонамида формулы (Aa) с активным фармацевтическим ингредиентом с получением раствора, содержащего конъюгат сульфонамида и активного фармацевтического ингредиента, где сульфонамид ковалентно связан с активным фармацевтическим ингредиентом.
В этом процессе активный фармацевтический ингредиент необязательно представляет собой полипептид инсулин, имеющий свободную аминогруппу, необязательно аналог инсулина, как в разделе А выше, или его предшественник, каждый из которых имеет свободную аминогруппу, при этом предшественник аналога инсулина содержит дополнительный линкерный пептид, который имеет длину по меньшей мере две аминокислоты, или длину в диапазоне 2-30 аминокислот, или длину в диапазоне 4-9 аминокислот. В этом способе водный раствор, предусмотренный в а), имеет значение pH в диапазоне 9-12, или в диапазоне 9,5-11,5, или в диапазоне 10-11, где значение pH определяется pH-чувствительным стеклянным электродом согласно ASTM E 70:2007; где значение pH необязательно регулируется в соответствующем диапазоне путем добавления основания или основания, выбранного из группы, состоящей из гидроксидов щелочных металлов (гидроксида лития, гидроксида натрия, гидроксида калия), алкиламинов и смесей двух или более из них; или выбранного из группы третичных алкиламинов N(C1-C5 алкил)3, первичных алкиламинов H2N-C(C1-C5 алкил)3 и смесей двух или более из них, где каждая из C1C5алкильных группы третичных аминов и первичных аминов независимо выбрана из разветвленных или прямых C1-C5алкильных групп, и где каждая C1-C5алкильная группа имеет по меньшей мере один заместитель, выбранный из группы, состоящей из атома водорода, гидроксильной группы и карбоксильной группы; или выбранного из группы третичных алкиламинов N(C1-C3 алкил)3, первичных алкиламинов H2N-C(C1-C3 алкил)3 и смесей двух или более из них, где каждая из C1-C3алкильных группы третичных аминов и первичных аминов независимо выбрана из разветвленных или линейных C1-C3алкильных групп, и где каждая от C1-C3алкильная группа имеет по меньшей мере один заместитель, выбранный из группы, состоящей из атома водорода, гидроксильной группы и карбоксильной группы; или выбранный из группы, состоящей из бицина, триметиламина, трис(гидроксиметил)аминометана и смесей двух или более из них; где основание необязательно включает по меньшей мере триэтиламин.
В одном варианте этого процесса приведение в контакт водного раствора b) с сульфонамидом формулы (Aa) (Rx=активирующая группа) из a) в соответствии со стадией c) осуществляется таким образом, чтобы сульфонамид формулы (Aa) (Rx=активирующая группа) из a) был добавлен в виде раствора сульфонамида формулы (Aa) (Rx=активирующая группа) к водному раствору b), где раствор сульфонамида формулы (Aa) (Rx=активирующая группа) представляет собой необязательно органический раствор, необязательно раствор, содержащий сульфонамид формулы (Aa) (Rx=активирующая группа) и полярный апротонный органический растворитель, необязательно полярный апротонный органический растворитель, имеющий коэффициент распределения октанол/вода (KOW) в диапазоне 1-5 или в диапазоне 2-4 при стандартных условиях (T: 20-25°C, p: 1013 мбар); или выбран из группы, состоящей из тетрагидрофурана, ацетонитрила, диметилформамида и смесей двух или более из них; или выбран из группы, состоящей из тетрагидрофурана, ацетонитрила и смесей тетрагидрофурана и ацетонитрила.
В одном варианте этого процесса приведение в контакт водного раствора b) с сульфонамидом формулы (Aa) (Rx=активирующая группа) из a) в соответствии со стадией c) осуществляется таким образом, что сульфонамид формулы (Aa) (Rx=активирующая группа) из а) добавляют в твердой форме к водному раствору b) или по меньшей мере частично в кристаллической форме, или по меньшей мере 90 вес % в кристаллической форме.
В этом способе стадия d) необязательно включает: d.1) осуществление реакции сульфонамида формулы (Aa) (Rx=активирующая группа) с предшественником аналога инсулина при pH в диапазоне 9-12 или в диапазоне 9,5-11,5, или в диапазоне 10-11 с получением предварительного конъюгата, содержащего сульфонамид формулы (I) и предшественник аналога инсулина, где сульфонамид формулы (I) ковалентно связан с предшественником аналога инсулина амидной связью C(=O)-NH-, образованной между -C(=O)-O(R) сульфонамида формулы (I) и аминогруппой предшественника аналога инсулина; d.2) ферментативное расщепление, необязательно при pH в диапазоне ниже 9 или при pH в диапазоне 7-9, предшественника аналога инсулина предварительного конъюгата, полученного в соответствии с d.1), с получением раствора, содержащего конъюгат сульфонамида формулы (I) и аналог инсулина. Способ дополнительно необязательно включает: e) выделение конъюгата сульфонамида формулы (I) и аналога инсулина из раствора, полученного в d) или d.2).
В этом процессе активирующая группа Rx сульфонамида формулы (Aa) необязательно выбрана из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx более необязательно представляет собой N-сукцинимидильную группу.
В одном варианте этого способа водный раствор предшественника аналога инсулина в соответствии с b) содержит спирт, который выбран из группы, состоящей из C1-C4моноспиртов и смесей двух или более из них, или из группы, состоящей из метанола, этанола, пропан-2-ола, пропан-1-ола, бутан-1-ола и смесей двух или более из них, или из группы, состоящей из этанола, пропан-2-ола, пропан-1-ола и смесей двух или более из них. Необязательно, спирт присутствует в водном растворе в количестве от 0,0001 до 35 об. %, или от 0,001 до 30 об. %, или от 0,01 до 25 об. %, или в диапазоне от 0,1 до 20 об. %, каждый в расчете на общий объем воды и спирта. В этом процессе ферментативное расщепление согласно d.2) включает использование по меньшей мере одного фермента, выбранного из группы, состоящей из трипсина, протеазы TEV (протеазы вируса гравировки табака) и смесей двух или более из них. В этом процессе аналог инсулина представляет собой аналог инсулина, описанный в разделе A выше и/или в данном документе в разделе C выше. В этом способе сульфонамид формулы (I) ковалентно связан с аналогом инсулина и его предшественником соответственно амидной связью C(=O)-NH-, образованной между -C(=O)-O(R3) сульфонамида формулы (I) и свободной аминогруппой аналога инсулина и его предшественника соответственно, где свободная аминогруппа аналога инсулина и его предшественника соответственно необязательно представляет собой аминогруппу лизина, содержащегося в аналоге инсулина и его предшественнике соответственно, необязательно концевой лизин, необязательно лизин, присутствующий на С-конце аналога инсулина и его предшественника соответственно, необязательно лизин, присутствующий на С-конце В-цепи.
В данном документе предусмотрены процессы получения конъюгата, содержащего сульфонамид формулы (I) и диагностическое соединение, где диагностическое соединение ковалентно связано с подходящей функциональной группой со свободной или активированной, необязательно активированной карбоксильной группой "а" сульфонамида формулы (Aa) в соответствии с описанным выше способом связывания с активным фармацевтическим ингредиентом.
В данном документе предусмотрены конъюгаты, содержащие сульфонамид формулы (I) и активный фармацевтический ингредиент или диагностическое соединение, полученные или получаемые с помощью способов, описанных выше.
В данном документе предусмотрены фармацевтические композиции, содержащие в фармацевтически или диагностически эффективном количестве конъюгат, содержащий сульфонамид формулы (I) и активный фармацевтический ингредиент или диагностическое соединение, описанные выше.
В данном документе предусмотрены конъюгаты, содержащие сульфонамид формулы (I) и активный фармацевтический ингредиент, описанный выше, для использования в качестве лекарственного препарата.
Один вариант осуществления относится к конъюгату, содержащему сульфонамид формулы (I) и активный фармацевтический ингредиент, описанные выше, для применения в качестве лекарственного препарата для лечения заболевания, выбранного из группы, состоящей из гестационного диабета, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии и/или для снижения уровней глюкозы в крови. В некоторых вариантах осуществления заболевание представляет собой сахарный диабет 2 типа.
В данном документе предусмотрены способы лечения пациента, страдающего заболеванием, выбранным из группы, состоящей из гестационного диабета, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии, и/или нуждающегося в снижении уровней глюкозы в крови; включающие введение терапевтически эффективного количества конъюгата, содержащего сульфонамид формулы (I) и активный фармацевтический ингредиент, описанные выше.
В данном документе предусмотрены варианты применения конъюгата, содержащего сульфонамид формулы (I) и активный фармацевтический ингредиент, описанные выше, для изготовления лекарственного препарата для лечения заболевания, выбранного из группы, состоящей из гестационного диабета, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии и/или для снижения уровней глюкозы в крови.
В данном документе предусмотрены конъюгаты, содержащие сульфонамид формулы (I) и диагностическое соединение, описанные выше, для использования в качестве диагностического средства.
В данном документе предусмотрены способы диагностики заболевания, например заболевания, выбранного из группы сердечно-сосудистых заболеваний и видов рака, у пациента или для определения риска развития у пациента заболевания, например заболевания, выбранного из группы сердечно-сосудистых заболеваний и видов рака, включающие введение диагностически эффективного количества конъюгата, содержащего сульфонамид формулы (I) и диагностическое соединение, описанные выше.
В данном документе предусмотрены варианты применения конъюгата, содержащего сульфонамид формулы (I) и диагностическое соединение, описанные выше, для изготовления диагностического средства для диагностики заболевания, например заболевания, выбранного из группы сердечно-сосудистых заболеваний и видов рака.
Композиции, фармацевтические композиции и варианты применения, описанные в разделе С, дополнительно проиллюстрированы следующими вариантами осуществления и комбинациями вариантов осуществления, как указано с помощью соответствующих зависимостей и обратных ссылок. Определения и пояснения, приведенные в данном документе выше в разделах A, B и C, применяются mutatis mutandis к следующим вариантам осуществления.
1. Конъюгат, содержащий аналог инсулина и сульфонамид формулы (I):
 ,
,
где:
A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы
где сульфонамид формулы (I) ковалентно связан с аналогом инсулина таким образом, что концевая карбоксильная группа "а" сульфонамида формулы (I) ковалентно связана с аминогруппой аналога инсулина.
2. Конъюгат по варианту осуществления 1, где сульфонамид характеризуется формулой (I-1):
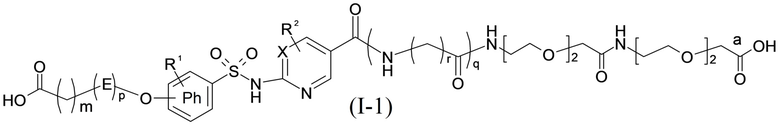 ,
,
где:
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода и атома галогена;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
где m представляет собой целое число в диапазоне 5-15, если p представляет собой ноль, или m представляет собой целое число в диапазоне 7-15, если p представляет собой 1.
3. Конъюгат по вариантам осуществления 1 или 2, где сульфонамид характеризуется формулой (I-1-1):
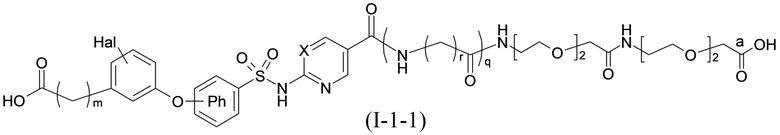 ,
,
где X представляет собой атом азота или группу -CH-; m представляет собой целое число в диапазоне 7-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1; Hal представляет собой атом галогена, выбранный из группы, состоящей из атома фтора, хлора, брома и йода; и группа HOOC-(CH2)m-C6H3Hal-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
4. Конъюгат по любому из вариантов осуществления 1-3, где сульфонамид характеризуется формулой (I-1-1a):
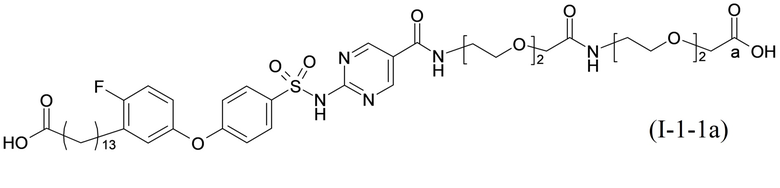 .
.
5. Конъюгат по вариантам осуществления 1 или 2, где сульфонамид характеризуется формулой (I-1-2):
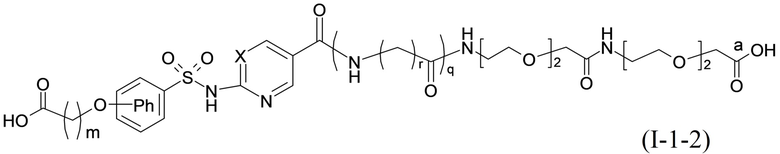 ,
,
где X представляет собой атом азота или группу -CH-; m представляет собой целое число в диапазоне 5-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1; и группа HOOC-(CH2)m-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
6. Конъюгат по любому из вариантов осуществления 1-2 или 5, где сульфонамид характеризуется формулой (I-1-2a):
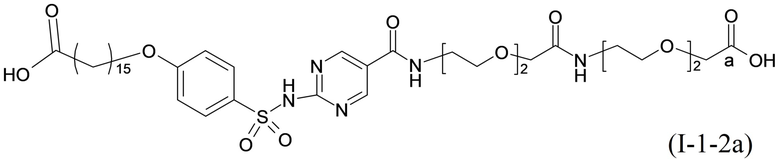 ,
,
или формулой (I-1-2b):
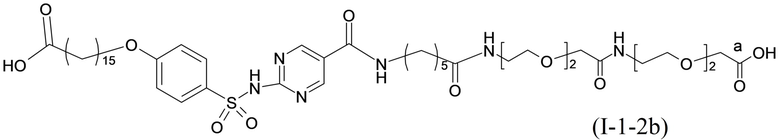 ,
,
или формулой (I-1-2c):
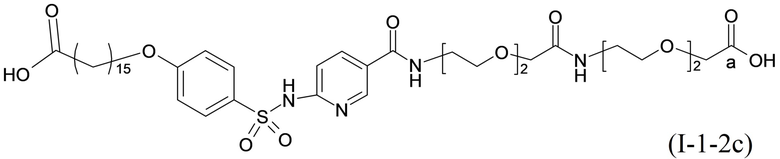 .
.
7. Конъюгат по любому из вариантов осуществления 1-6, где аналог инсулина содержит по меньшей мере одну мутацию по сравнению с исходным инсулином, где аналог инсулина содержит мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой, и где указанный аналог инсулина необязательно дополнительно содержит мутацию в положении A14, которая представляет собой замену аминокислотой, выбранной из группы, состоящей из глутаминовой кислоты (Glu), аспарагиновой кислоты (Asp) и гистидина (His), и/или мутацию в положении B30.
8. Конъюгат по варианту осуществления 7, где исходный инсулин представляет собой человеческий инсулин, свиной инсулин или бычий инсулин.
9. Конъюгат по вариантам осуществления 7-8, где гидрофобная аминокислота представляет собой аминокислоту с разветвленной цепью, такую как аминокислота с разветвленной цепью, выбранная из группы, состоящей из валина (Val), изолейцина (Ile) и лейцина (Leu).
10. Конъюгат по любому из вариантов осуществления 1-9, где аналог инсулина выбран из
Leu(B16)-человеческого инсулина,
Val(B16)-человеческого инсулина,
Ile(B16)-человеческого инсулина,
Leu(B16)Des(B30)-человеческого инсулина,
Val(B16)Des(B30)-человеческого инсулина,
Ile(B16)Des(B30)-человеческого инсулина,
Leu(B25)-человеческого инсулина,
Val(B25)-человеческого инсулина,
Ile(B25)-человеческого инсулина,
Leu(B25)Des(B30)-человеческого инсулина,
Val(B25)Des(B30)-человеческого инсулина,
Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B16)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B16)-человеческого инсулина,
Glu(A14)Ile(B16)-человеческого инсулина,
Glu(A14)Val(B16)-человеческого инсулина,
Glu(A14)Leu(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B25)-человеческого инсулина,
Glu(A14)Ile(B25)-человеческого инсулина,
Glu(A14)Val(B25)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B25)-человеческого инсулина,
Glu(A14)Ile(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Glu(B3)Ile(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Ile(B16)Val(B25)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)-человеческого инсулина,
Glu(A14)Val(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Val(B16)Val(B25)-человеческого инсулина,
Glu(A14)Glu(B3)Val(B16)Val(B25)-человеческого инсулина и
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)-человеческого инсулина.
11. Конъюгат по любому из вариантов осуществления 1-10, где аналог инсулина содержит
(a) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 43 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 44 (FVNQHLCGSHLVEALYLVCGERGFIYTPK),
(b) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 47 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 48 (FVNQHLCGSHLVEALYLVCGERGFVYTPK), или
(c) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 77 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 78 (FVEQHLCGSHLVEALVLVCGERGFVYTPK).
12. Конъюгат по любому из вариантов осуществления 1-11, где аминогруппа аналога инсулина, с которой ковалентно связан сульфонамид формулы (I), представляет собой эпсилон-аминогруппу лизина, присутствующего в аналоге инсулина, или представляет собой N-концевую аминогруппу В-цепи инсулина или аналога инсулина.
13. Конъюгат по варианту осуществления 12, где аминогруппа представляет собой эпсилон-аминогруппу лизина, присутствующего в положении B29 B-цепи.
14. Конъюгат по любому из вариантов осуществления 1-13, где конъюгат представляет собой конъюгат 1 (последовательность А-цепи: SEQ ID NO: 47; последовательность B-цепи: SEQ ID NO: 48):
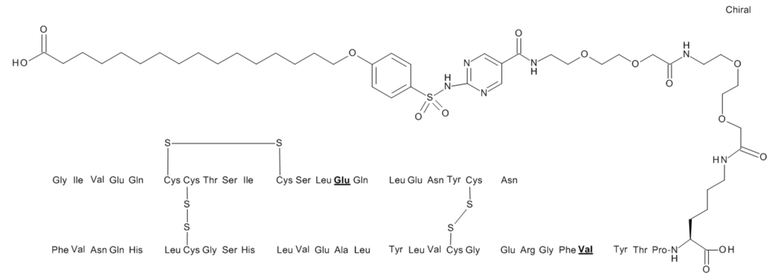 ,
,
или конъюгат 3 (последовательность А-цепи: SEQ ID NO: 77; последовательность B-цепи: SEQ ID NO: 78):
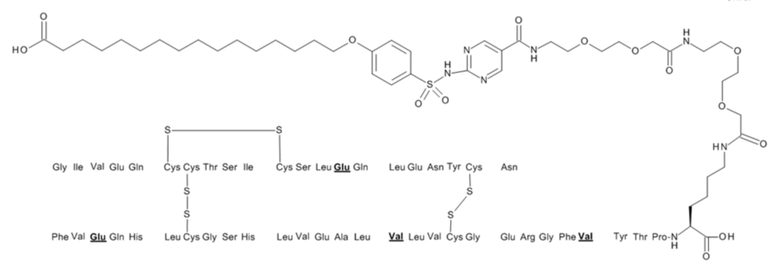 ,
,
или
конъюгат 4 (последовательность А-цепи: SEQ ID NO: 43; последовательность B-цепи: SEQ ID NO: 44):
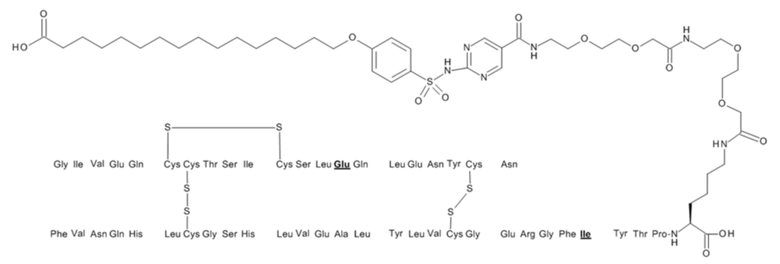 .
.
15. Процесс получения конъюгата, содержащего сульфонамид формулы (I) и аналог инсулина
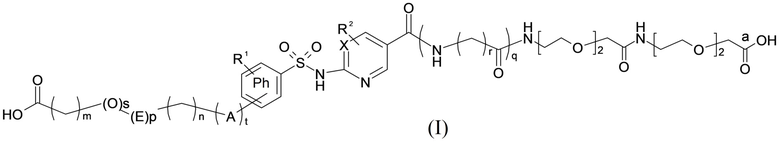 ,
,
где в сульфонамиде формулы (I):
A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода, необязательно атома фтора;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
где сульфонамид формулы (I) ковалентно связан с активным фармацевтическим ингредиентом, при этом концевая карбоксильная группа "а" сульфонамида формулы (I) ковалентно связана с аминогруппой активного фармацевтического ингредиента;
включающий:
(а) получение сульфонамида формулы (Aa)
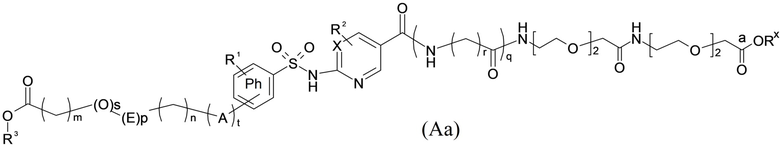 ,
,
где X, Y, A, E, R1, R2 и индексы m, n, p, q, r, s, t имеют значения, указанные в варианте осуществления 1, Rx представляет собой атом водорода или активирующую группу, необязательно активирующую группу, выбранную из группы, состоящей из 7-азабензотриазола (необязательно полученного из HATU или HBTU), 4-нитробензола и N-сукцинимидильной группы, где Rx необязательно представляет собой N-сукцинимидильную группу; и R3 представляет собой защитную группу или атом водорода, необязательно атом водорода; и аналог инсулина, имеющий С-конец, содержащий или не содержащий защитную группу;
(b) осуществление реакции сульфонамида формулы (Aa) и аналога инсулина, имеющего С-конец, содержащий или не содержащий защитную группу, в условиях, подходящих для образования амидной связи между свободной или активированной, необязательно активированной, карбоксильной группой "a" сульфонамида формулы (Aa) и аминогруппой аналога инсулина, имеющей С-конец, содержащий или не содержащий защитную группу;
(c) необязательно удаление одной или обеих защитных групп.
16. Конъюгат, содержащий сульфонамид формулы (I) и аналог инсулина, полученный или получаемый с помощью способа по варианту осуществления 15.
17. Фармацевтическая композиция, содержащая фармацевтически эффективное количество конъюгата, содержащего сульфонамид формулы (I) и аналог инсулина по любому из вариантов осуществления 1-15 или по варианту осуществления 16.
18. Конъюгат, содержащий сульфонамид формулы (I) и аналог инсулина по любому из вариантов осуществления 1-15 или по варианту осуществления 16 для применения в качестве лекарственного препарата.
19. Конъюгат, содержащий сульфонамид формулы (I) и аналог инсулина по любому из вариантов осуществления 1-15 или по варианту осуществления 16 для применения в качестве лекарственного препарата для лечения заболевания, выбранного из группы, состоящей из гестационного диабета, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии, и/или для снижения уровней глюкозы в крови.
20. Способ лечения заболевания, выбранного из группы, состоящей из гестационного диабета, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии, и/или снижения уровней глюкозы в крови, включающий введение пациенту, нуждающемуся в этом, конъюгата, содержащего аналог инсулина и сульфонамид формулы (I)
 ,
,
где:
A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом
галогена, где атом галогена выбран из группы, состоящей из атома фтора, хлора, брома и йода;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы,
где сульфонамид формулы (I) ковалентно связан с аналогом инсулина таким образом, что концевая карбоксильная группа "а" сульфонамида формулы (I) ковалентно связана с аминогруппой аналога инсулина,
тем самым осуществляя лечение болезни.
Настоящее изобретение дополнительно проиллюстрировано следующими примерами.
Примеры
1. Список использованных сокращений
Общие способы, подходящие для получения соединений формулы (I), описаны ниже. Соединения формулы I были получены с помощью различных химических способов. Группы и индексы, упомянутые в следующих способах, особенно на схемах, имеют вышеуказанное значение, указанное для формулы (I), если они явно не определены иначе.
2. Общий синтез соединений формулы (I)
Соединения формулы (I) были синтезированы, начиная из соответствующего промежуточного соединения I (схема 1). После активации с помощью TSTU промежуточное соединение I было связано либо с аминокислотой (4) (стадия 3), либо с соединением (2) (стадия 2), для получения частиц (3) и (6) соответственно. В случае использования на стадии 3 сложного алкилового эфира (R=алкил) достигалось омыление с помощью LiOH. Обе карбоновые кислоты (6) и (7) активировали с помощью TSTU и они связывались с (2) с образованием частиц (3). Для завершения синтеза соединений формулы (I) трет-бутиловый эфир (3) отщепляли на последней стадии 7 посредством обработки CF3CO2H. Синтез промежуточного соединения I показан на схеме 2.
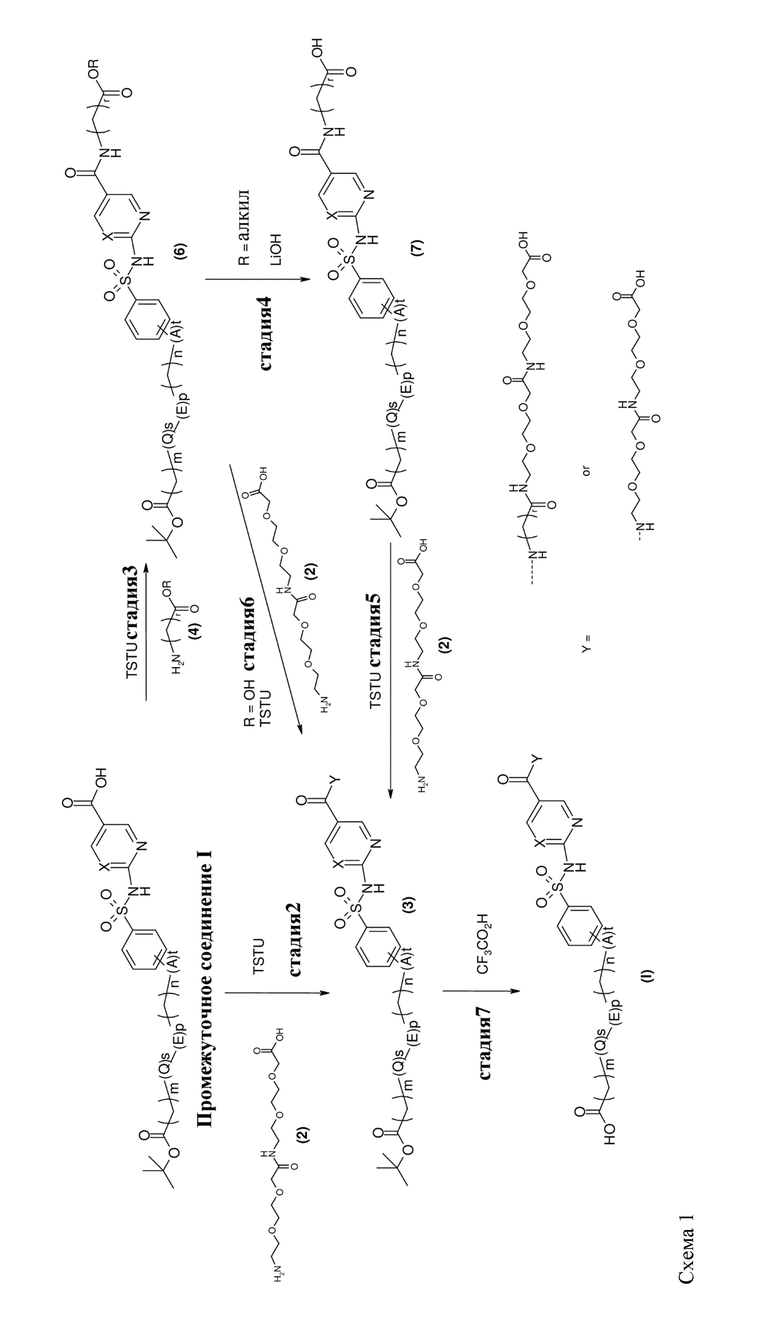
2.1 Общий синтез промежуточного соединения I
Промежуточное соединение I синтезировали как показано на схеме 2. Начиная с бромида I или тозилата I алкилирование промежуточного соединения III достигалось в присутствии K2CO3 (стадия 8). Альтернативно, вещества (8) выделяли после последовательности реакций, начиная с реакции Соногаширы алкина I и промежуточного соединения II (стадия 11) с последующей гидрогенизацией полученного соединения (11) в водородной атмосфере, катализируемой палладием и платиной соответственно (стадия 12). Затем вещества (8) конденсировали либо 2-хлорпиридином (9) (стадия 9) в реакции, катализируемой палладием, либо конденсировали 2-хлорпиримидином (10) (стадия 10) посредством нагревания. В обоих случаях сложный алкиловый эфир впоследствии гидролизовали LiOH с получением требуемого промежуточного соединения I.
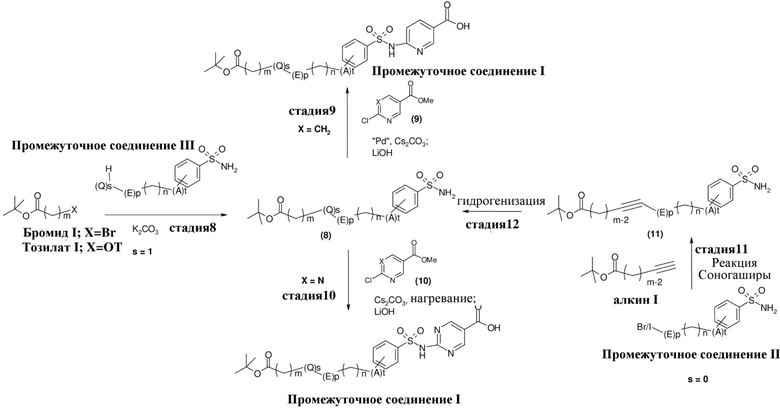
Схема 2
2.2 Общий синтез промежуточного соединения II
Как показано на схеме 3, промежуточное соединение II выделяли после реакции Мицунобу с участием фенола (13) и спирта (12) (стадия 13). Альтернативно, промежуточное соединение II синтезировали путем алкилирования либо фенола (13) (стадия 14), либо фенола (15) (стадия 15), в присутствии K2CO3. Подходящими алкилирующими средствами были (14) и (16) соответственно. Нуклеофильное замещение в ароматическом ядре фторида (18) фенолом (17) также приводила к получению промежуточного соединения II (стадия 16).
Промежуточное соединение II
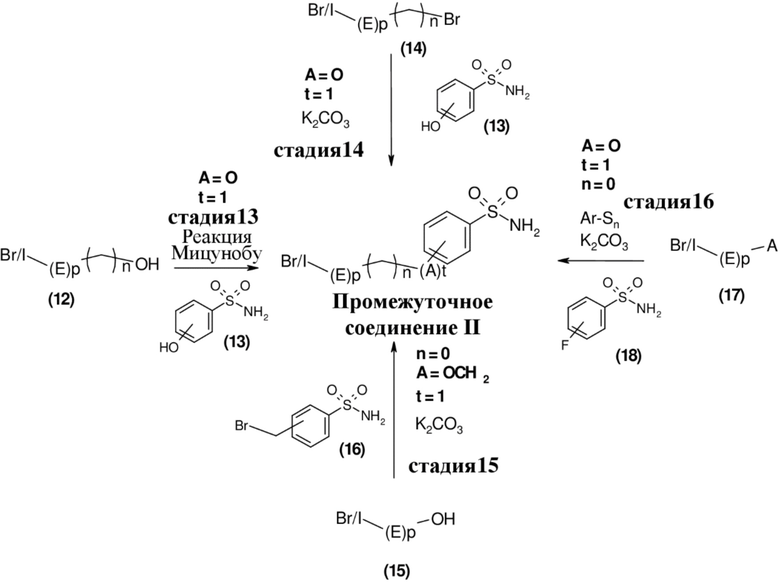
Схема 3
2.3 Общий синтез промежуточного соединения III
Промежуточное соединение III получали после линейной последовательности реакций, описанной на схеме 4. Начиная с алкилирования алкина (20) бромидом (19), выделяли алкин, защищенный ТМС (21). Защитную группу алкина (21) удаляли в основных условиях с использованием NaOH. Последующая реакция Соногаширы выделенного алкина (22) с соответствующим ароматическим галогенидом (23) (стадия 19) приводила к получению вещества (24). Подходящей защитной группой для веществ (24) был, например, ацетил (PG=Ac), который отщеплялся при обработке NaOH (стадия 20). Последняя стадия 21 гидрогенизации катализировалась палладием или платиной в атмосфере H2 с получением требуемого промежуточного соединения III.
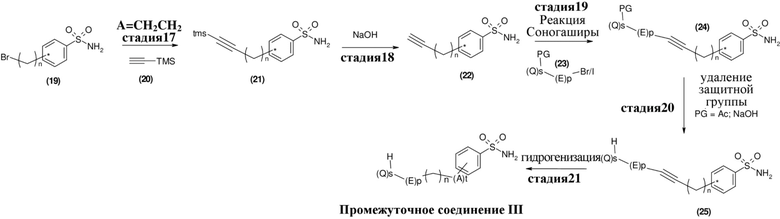
Схема 4
2.4 Общий синтез алкина I и бромида I
Исходные вещества бромид I и алкин I синтезировали, как показано на схеме 5. Для алкина I использовали два разных пути синтеза. Карбоновую кислоту (28) выделяли либо после окисления спирта (29) - указанного окисления достигали с помощью смеси NaOCl и NaClO2 в присутствии каталитического количества TEMPO (стадия 24), либо посредством алкилирования/удаления защитной группы последовательности бромида (26). Для алкилирования использовали реагент (20). Затем выделенный продукт (27) обрабатывали NaOH для отщепления защитной группы ТМС. Добавление защитной группы карбоновой кислоты (28), представляющей собой трет-бутиловый эфир с получением требуемого алкина I, было достигнута после активации (CF3CO)2O и реакции с трет-бутанолом.
Для синтеза бромида I использовалась аналогичная последовательность, описанная для превращения (29) в алкин I (стадия 24 и 25). Окисление спирта (30) и последующее добавление защитной группы к полученной карбоновой кислоте (31) приводили к получению требуемого бромида I.
Тозилат I можно синтезировать посредством тозилирования спирта (33) (стадия 29). Соединение (33) выделяли после восстановления карбоновой кислоты (32), которую in situ переносили в смешанный ангидрид и затем восстанавливали с помощью NaBH4 (стадия 28).
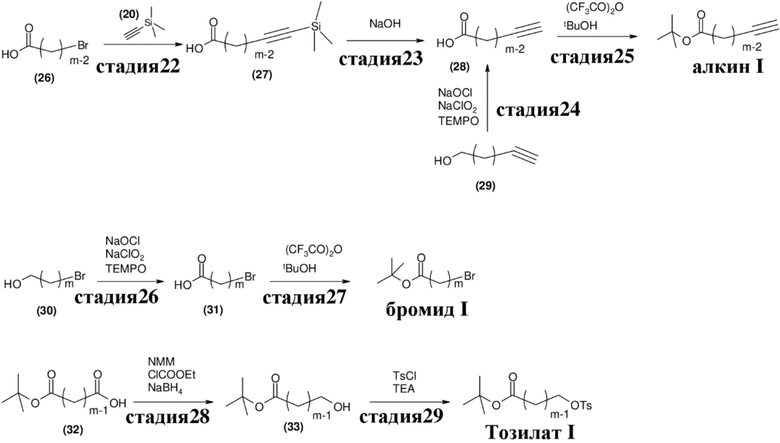
Схема 5
2.5 Примеры для синтеза алкинов I и бромидов I по схеме 5
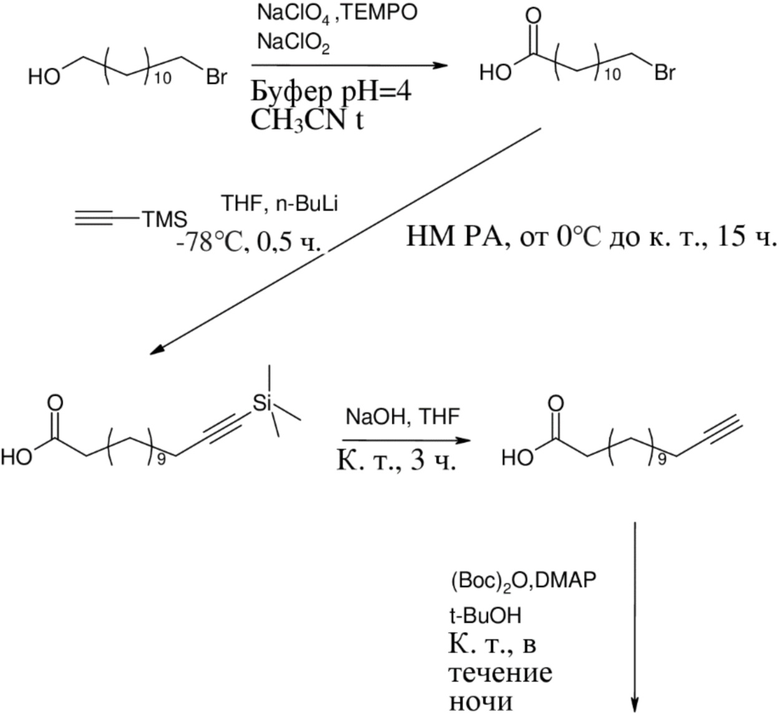
2.5.1 Синтез 12-бромододекановой кислоты
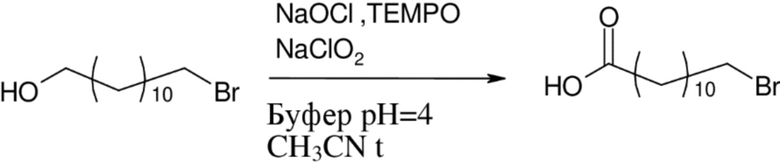
Раствор NaClO2 (37,5 г, 414,8 ммоль) в H2O (60 мл) и 10% раствор NaOCl (28 г, 37,7 ммоль) одновременно добавляли в раствор 12-бром-додекан-1-ола (20 г, 75,4 ммоль) и TEMPO (5,9 г, 37,7 ммоль) в CH3CN (400 мл) и в буферный раствор с pH 4 (60 мл). Реакционную смесь перемешивали при к. т. в течение ночи. Смесь разбавляли EA (1200 мл), промывали водой (1000 мл) и солевым раствором, высушивали над Na2SO4 и концентрировали под вакуумом с получением требуемого продукта 12-бромододекановой кислоты (20 г, 71,6 ммоль, выход 95%) в виде желтого твердого вещества.
1H ЯМР (400 МГц, DMSO) δ 11,96 (s, 1H), 3,52 (t, J=6,6 Гц, 2H), 2,18 (t, J=7,2 Гц, 2H), 1,85-1,72 (m, 2H), 1,55-1,43 (m, 2H), 1,37 (s, 2H), 1,21 (d, J=32,6 Гц, 12H).
Следующие соединения синтезировали соответственно.
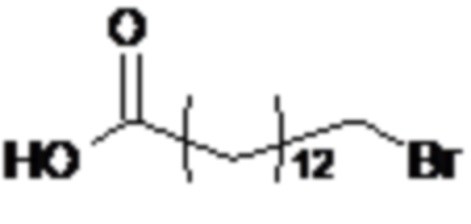
2.5.2 Синтез 14-(триметилсилил)тетрадец-13-иновой кислоты
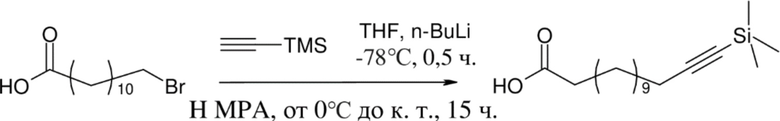
К смеси этинил-триметил-силана (63,3 г, 644,7 ммоль) в THF (300 мл) добавляли n-бутиллитий (2,5 М в гексане) (258 мл, 644,7 ммоль) при -78°C в атмосфере N2. Через 10 минут добавляли HMPA (115,5 г, 644,7 ммоль) и смесь нагревали до 0°C в течение 30 минут. Затем добавляли 12-бромододекановую кислоту (30 г, 107,45 ммоль) в THF (300 мл). Затем смесь перемешивали при к. т. в течение ночи. В смесь медленно добавляли воду (1200 мл) при 0°C, затем значение pH доводили до 3 водным раствором HCl, экстрагировали EA (800 мл). Органическую фазу промывали солевым раствором, высушивали над Na2SO4, концентрировали под вакуумом с получением неочищенного продукта 14-(триметилсилил)тетрадец-13-иновой кислоты (35 г) в виде коричневого масла и использовали на следующей стадии.
Следующие соединения синтезировали соответственно.
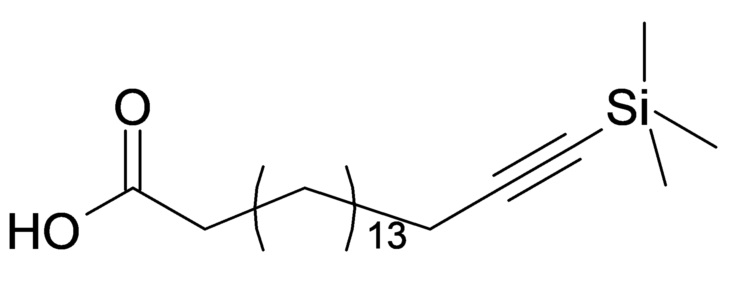
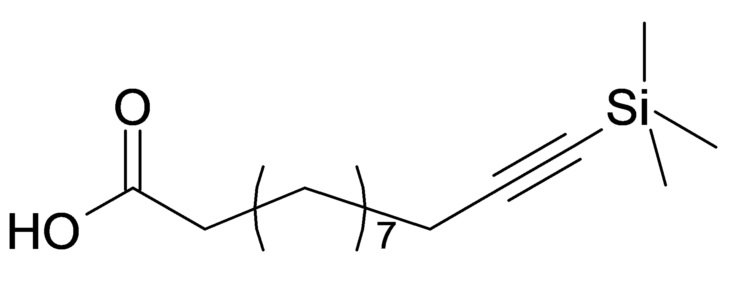

2.5.3 Синтез тетрадец-13-иновой кислоты
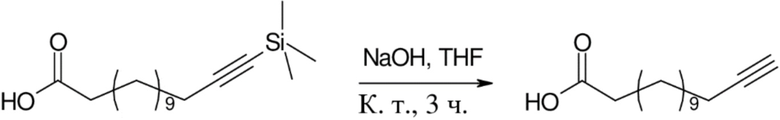
NaOH (8,6 г, 214,9 ммоль) добавляли к смеси 14-(триметилсилил)тетрадец-13-иновой кислоты (35 г, 107,45 ммоль) в H2O (150 мл) и THF (150 мл). Затем смесь перемешивали при к. т. в течение 3 часов. Затем значение pH доводили до 4 водным раствором HCl, экстрагировали ЕА (2 х 300 мл). Органические фазы промывали солевым раствором, высушивали над Na2SO4, концентрировали под вакуумом. Неочищенный продукт очищали посредством хроматографии на силикагеле (PE:EA=4:1) с получением требуемого продукта тетрадец-13-иновой кислоты (23 г, 102,5 ммоль, 2 стадия выход: 95%) в виде желтого твердого вещества.
1H ЯМР (400 МГц, DMSO) δ 11,96 (s, 1H), 2,73 (s, 1H), 2,17 (dd, J=16,3, 8,9 Гц, 4H), 1,51-1,21 (m, 18H).
Следующие соединения синтезировали соответственно.
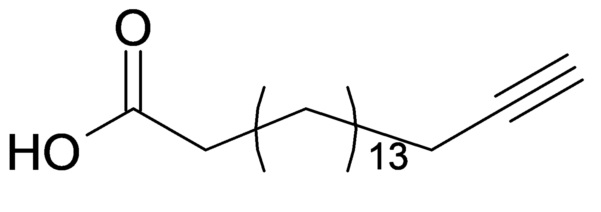
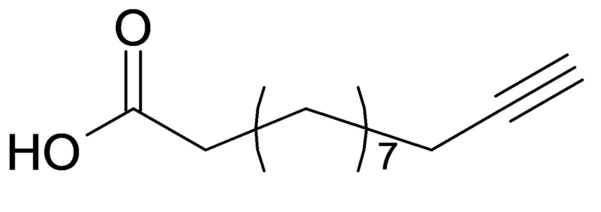

2.5.4 Синтез дец-9-иновой кислоты
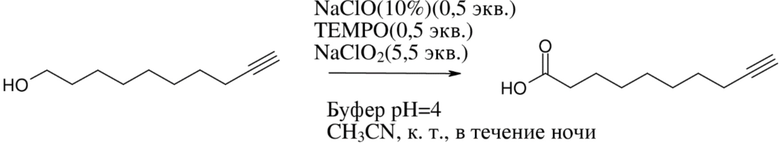
Раствор NaClO2 (48,2 г, 536 ммоль) и NaOCl (36,0 г, 48,7 ммоль) одновременно добавляли в раствор дек-9-ин-1-ола (15 г, 97,4 ммоль) и TEMPO (7,6 г, 48,7 ммоль) в CH3CN (300 мл) и в буферный раствор с pH 4 (75 мл). Реакционную смесь перемешивали при к. т. в течение ночи, разбавляли ЕА (900 мл), промывали водой (900 мл) и солевым раствором, высушивали над Na2SO4, концентрировали под вакуумом. Неочищенный продукт очищали посредством хроматографии на силикагеле (PE:EA=1:1) с получением требуемой дец-9-иновой кислоты (20 г, неочищенный продукт) в виде бесцветного масла.
1H ЯМР (400 МГц, CDCl3) δ 2,36 (t, J=7,3 Гц, 2H), 2,18 (td, J=6,9, 2,3 Гц, 2H), 1,93 (t, J=2,3 Гц, 1H), 1,72-1,59 (m, 2H), 1,54 (td, J=14,1, 7,2 Гц, 2H), 1,48-1,30 (m, 6H) ppm.
Следующие соединения синтезировали соответственно.
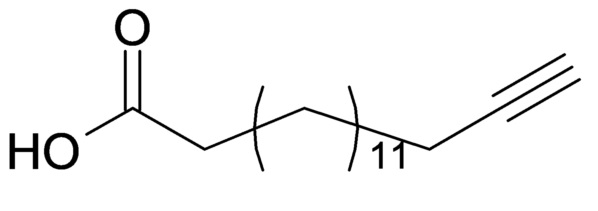
2.5.5 Синтез трет-бутил-тетрадец-13-иноата
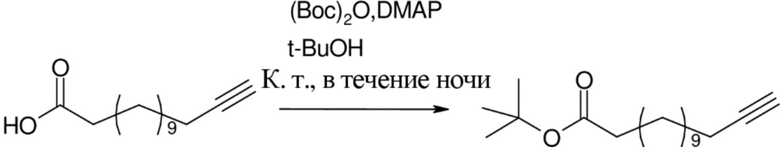
(Boc)2O (33,6 г, 153,8 ммоль) и DMAP (3,7 г, 30,7 ммоль) добавляли к смеси тетрадец-13-иновой кислоты (23 г, 102,5 ммоль) в t-BuOH (200 мл). Затем смесь перемешивали при к. т. в течение ночи. Растворитель удаляли под вакуумом. К смеси добавляли воду (400 мл) и экстрагировали ЕА (400 мл). Органическую фазу промывали солевым раствором, высушивали над Na2SO4, фильтровали и концентрировали. Остаток очищали посредством хроматографии на силикагеле (PE:EA=30:1) с получением требуемого продукта трет-бутилтетрадец-13-иноата (23,5 г, 83,8 ммоль, выход 82%) в виде желтой жидкости.
1H ЯМР (400 МГц, DMSO) δ 2,72 (s, 1H), 2,15 (d, J=8,4 Гц, 4H), 1,49-1,21 (m, 27H).
Следующие соединения синтезировали соответственно.
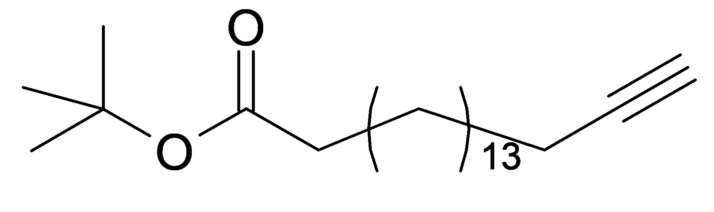
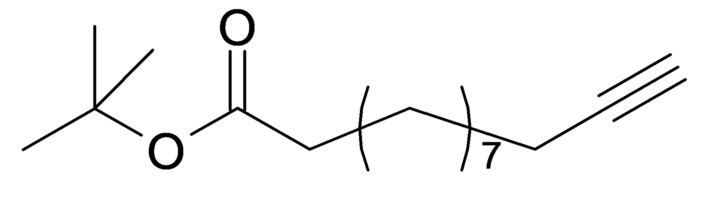
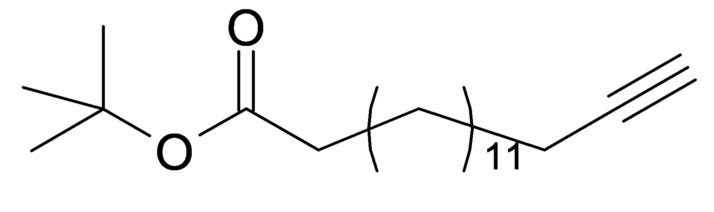
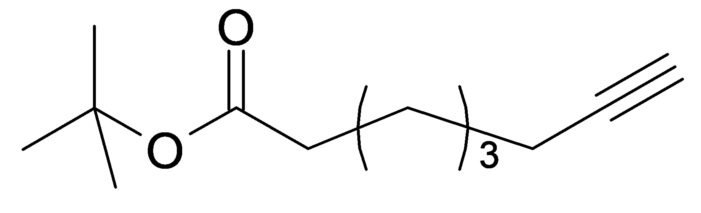
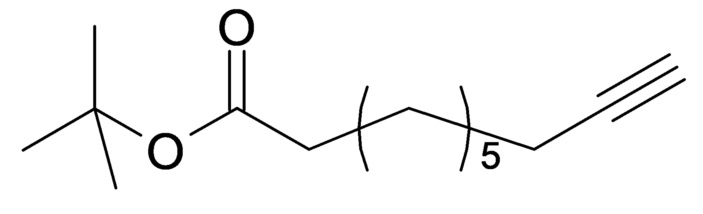
2.5.6 Синтез трет-бутил-6-бромгексаноата
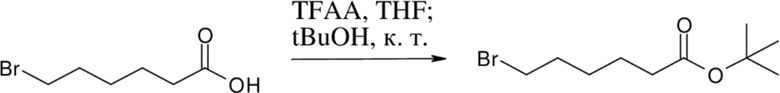
6-Бромгексановую кислоту (6,0 г, 31 ммоль), TFAA (26,0 г, 124 ммоль) добавляли к THF (60 мл), смесь подвергали реакции при к. т. в течение 1 часа. Затем к смеси добавляли трет-бутанол (30 мл) и перемешивали в течение 16 часов при к. т. Затем pH реакционной смеси доводили до pH=8 с помощью раствора NaHCO3, смесь экстрагировали EA (3×150 мл), высушивали над Na2SO4, концентрировали с получением целевого соединения трет-бутил-6-бромгексаноата (7,6 г, 30,4 ммоль, выход 98%).
1H ЯМР (400 МГц, DMSO) δ 3,52 (t, J=6,6 Гц, 2H), 2,20 (dd, J=15,0, 7,8 Гц, 2H), 1,85-1,74 (m, 2H), 1,52 (ddd, J=19,3, 10,9, 5,7 Гц, 2H), 1,44-1,32 (m, 9H).
2.5.6 Синтез тозилатов I
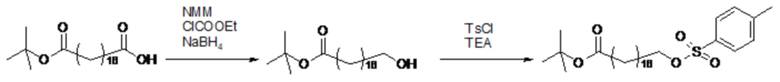
2.5.7 Синтез трет-бутил-18-гидроксиоктадеканоата

N-Метилморфолин (1638 мг, 16,5 ммоль) добавляли к раствору 18-трет-бутокси-18-оксооктадекановой кислоты (5 г, 13,5 ммоль) в THF (150 мл). Смесь охлаждали до -25°C перед добавлением по каплям этилхлорформиата (1277 мг, 13,5 ммоль). Смесь перемешивали при -25°C в течение 20 минут и твердое вещество удаляли посредством фильтрации. Раствор осторожно добавляли к раствору NaBH4 (770 мг, 20,25 ммоль) в воде (15 мл) при 0°C. Смесь перемешивали в течение 1 часа при комнатной температуре. THF удаляли под вакуумом и водную фазу экстрагировали ЕА (3 × 50 мл). Объединенные органические фазы высушивали над MgSO4 и концентрировали под вакуумом, с получением трет-бутил-18-гидроксиоктадеканоата в виде белого твердого вещества (4,7 г, выход 99,8%).
1H ЯМР (400 МГц, CDCl3) δ 3,63 (t, J=6,6 Гц, 2H), 2,19 (t, J=7,5 Гц, 2H), 1,57 (dd, J=13,0, 6,5 Гц, 4H), 1,43 (d, J=3,9 Гц, 9H), 1,38-1,20 (m, 27H).
Следующие соединения синтезировали соответственно.
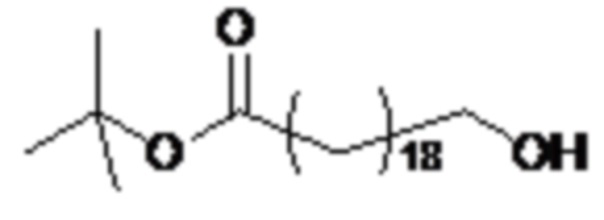
2.5.8 Синтез трет-бутил-18-(п-толилсульфонилокси)октадеканоата
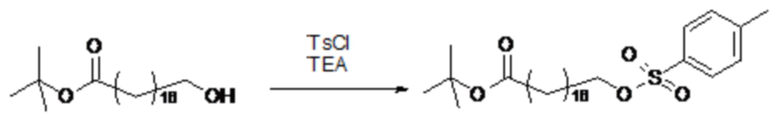
TEA (400 мг, 39,6 ммоль) добавляли к раствору трет-бутил-18-гидроксиоктадеканоата (4700 мг, 13,2 ммоль) и TsCl (2508 мг, 13,2 ммоль) в DCM (100 мл). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Добавляли воду (50 мл) и экстрагировали с помощью DCM (2 × 50 мл). Объединенную органическую фазу промывали солевым раствором (100 мл), высушивали над Na2SO4, фильтровали и концентрировали. Неочищенный продукт очищали на колонке с силикагелем (EA/n-гексан=1:20) с получением трет-бутил-18-(п-толилсульфонилокси)октадеканоата (4,5 г, выход 67%).
1H ЯМР (400 МГц, CDCl3) δ 7,79 (d, J=8,2 Гц, 2H), 7,34 (d, J=8,1 Гц, 2H), 4,02 (t, J=6,5 Гц, 2H), 2,45 (s, 3H), 2,20 (t, J=7,5 Гц, 2H), 1,69-1,57 (m, 4H), 1,44 (s, 9H), 1,25 (t, J=12,1 Гц, 24H).
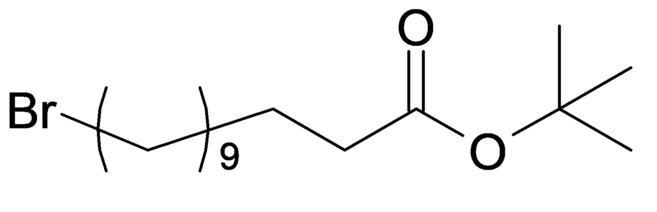
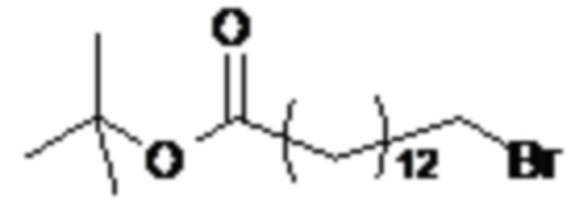
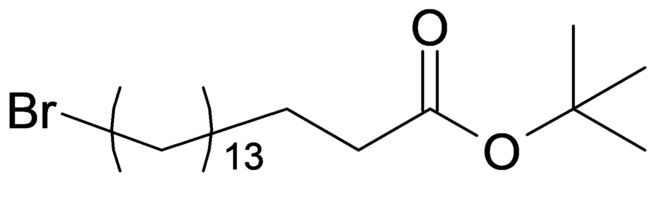
Следующие соединения синтезировали соответственно.
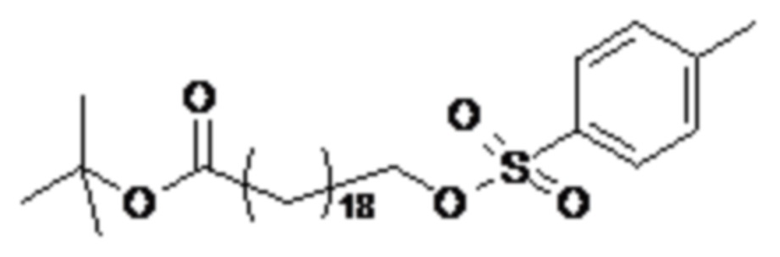
2.6 Примеры для синтеза промежуточных соединений III по схеме 4
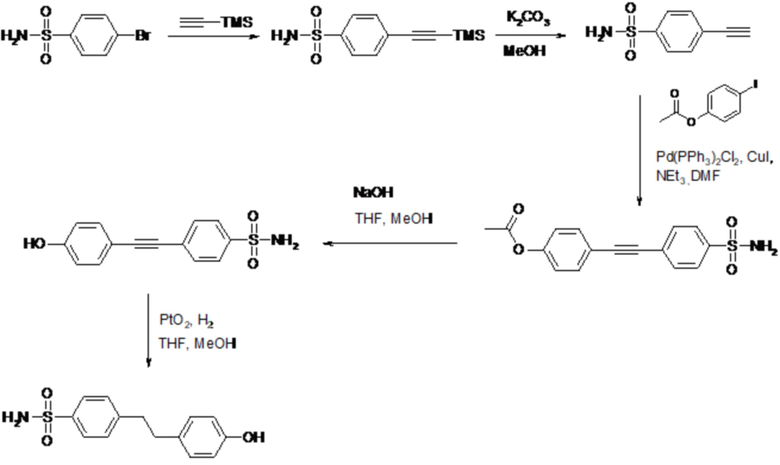
2.6.1 Синтез 4-((триметилсилил)этинил)бензолсульфонамида
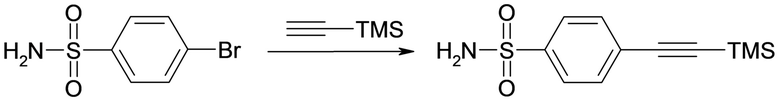
Смесь 4-бромбензолсульфонамида (61 г, 260 ммоль), триметилсилилацетилена (38,2 г, 0,09 моль), тетракис(трифенилфосфин)палладия (7,5 г, 6,5 ммоль) и йодида меди (2,5 г, 13 ммоль) в триэтиламине (500 мл) нагревали до 80°C в атмосфере азота в течение 8 часов. Смесь концентрировали in vacuo и экстрагировали ЕА (300 мл). Объединенные органические слои высушивали над (Na2SO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали посредством хроматографии на силикагеле (элюирование 70% DCM в PE), с получением 4-((триметилсилил)этинил)бензолсульфонамид (50 г, 75%).
Способ LC-масс-спектрометрии: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 2,0 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 90% (214 нм); масс-спектрометрия: обнаружен пик 254,0 (M+H)+ на 1,98 мин.
2.6.2 Синтез 4-этинилбензолсульфонамида
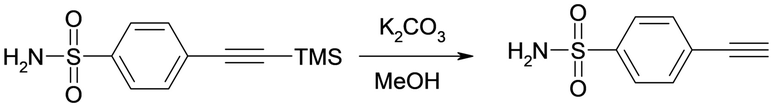
4-((Триметилсилил)этинил)бензолсульфонамид (40 г, 158 ммоль), K2CO3 (2,2 г, 15,8 ммоль) и метанол (400 мл) перемешивали при к. т. в течение 12 часов. После завершения реакции (контролируемой посредством LCMS) реакционную смесь разбавляли водой (200 мл) и экстрагировали ЕА (2 × 200 мл). Объединенные органические слои высушивали над (Na2SO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали посредством хроматографии на силикагеле (элюирование 100% DCM в PE) с получением 4-этинилбензолсульфонамида (22 г, 77%).
Способ LC-масс-спектрометрии: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 2,0 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 90% (214 нм); масс-спектрометрия: обнаружен пик 182,1 (M+H) + на 1,65 мин.
2.6.3 Синтез 4-((4-сульфамоилфенил)этинил)фенилацетата
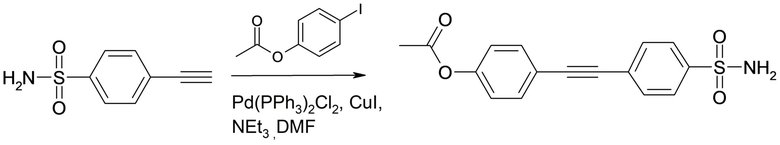
Pd(PPh3)2Cl2 (5,8 г, 8,3 ммоль), CuI (1,6 г, 8,3 ммоль), Et3N (25 г, 249 ммоль) и (4-йодфенил)ацетат (27 г, 103 ммоль) добавляли к смеси 4-этинилбензолсульфонамида (15 г, 83 ммоль) в DMF (150 мл). Колбу освобождали от содержимого и заполняли N2. Затем смесь перемешивали при к. т. в течение ночи. К смеси добавляли воду (200 мл), посредством фильтрования с отсасыванием и высушивания на воздухе получают 4-((4-сульфамоилфенил)этинил)фенилацетат в виде коричневого твердого вещества (18 г, 70%).
Способ LC-масс-спектрометрии: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 2,0 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 90% (214 нм); масс-спектрометрия: обнаружен пик 338 (M+Na)+ на 1,88 мин.
2.6.4 Синтез 4-((4-гидроксифенил)этинил)бензолсульфонамида
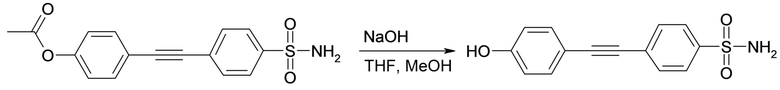
При 0°C NaOH (4,5 г, 114 ммоль) добавляли к раствору 4-((4-сульфамоилфенил)этинил)фенилацетата (18 г, 57 ммоль) в THF (60 мл), MeOH (60 мл) и H2O (30 мл). Смесь перемешивали при к. т. в течение 2 часов. После завершения реакции (контролируемой посредством LCMS) раствор разбавляли EA (50 мл) и промывали водой (20 мл) и насыщенным водным NaCl, высушивали над MgSO4. Фильтрат концентрировали in vacuo с получением неочищенного продукта. Неочищенный продукт суспендировали с помощью DCM. Посредством фильтрации с отсасыванием и высушивания на воздухе получают 4-((4-гидроксифенил)этинил)бензолсульфонамид в виде коричневого твердого вещества (10,9 г, 70%).
Способ LC-масс-спектрометрии: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 2,0 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 95% (214 нм); масс-спектрометрия: обнаружен пик 296,1 (M+Na)+ на 1,75 мин.
2.6.5 Синтез 4-(4-гидроксифенэтил)бензолсульфонамида
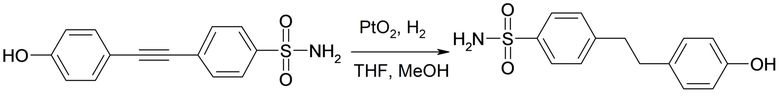
PtO2 (1 г) добавляли к раствору 4-((4-гидроксифенил)этинил)бензолсульфонамида (10,9 г, 40 ммоль) в 40 мл THF и 40 мл MeOH. Реакционную смесь перемешивали при к. т. в атмосфере H2 в течение 24 часов. После завершения реакции (контролируемой посредством LCMS) смесь фильтровали. Фильтрат концентрировали in vacuo с получением 4-(4-гидроксифенэтил)бензолсульфонамида (9,5 г, 86%).
Способ LC-масс-спектрометрии: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 2,0 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 100% (214 нм); масс-спектрометрия: обнаружен пик 278,1 (M+H) + на 1,67 мин.
1H ЯМР (400 МГц, DMSO) δ 9,14 (s, 1H), 7,71 (d, J=8,3 Гц, 2H), 7,38 (d, J=8,3 Гц, 2H), 7,26 (s, 2H), 7,00 (d, J=8,4 Гц, 2H), 6,72-6,60 (m, 2H), 2,96-2,84 (dd, J=9,2, 6,2 Гц, 2H), 2,77 (dd, J=9,2, 6,3 Гц, 2H).
2.7 Примеры для синтеза промежуточных продуктов II по схеме 3
2.7.1 Синтез 4-(3-бромо-4-фторфенокси)бензолсульфонамида
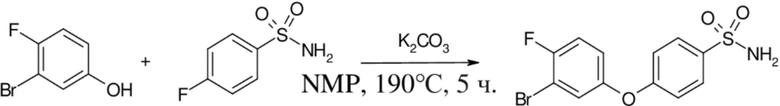
Смесь 3-бромо-4-фторфенола (12,8 г, 66,8 ммоль), 4-фторбензолсульфонамида (9,00 г, 51,4 ммоль) и K2CO3 (14,2 г, 103 ммоль) в NMP (50 мл) перемешивали при 190°C в течение 5 часов. Реакционную смесь разбавляли ЕА (500 мл), промывали водой (50 мл), солевым раствором (3 × 50 мл), высушивали над Na2SO4, фильтровали и концентрировали. Остаток очищали посредством флэш-хроматографии на силикагеле (элюирование PE/EA=3/1) с получением 4-(3-бромо-4-фторфенокси)бензолсульфонамида в виде белого твердого вещества (10,8 г, 31,3 ммоль, выход 61%).
Способ LC-масс-спектрометрии: подвижная фаза: A=2,5 мМ TFA/H2O, B=2,5 мМ TFA/MeCN; градиент: B=10%-95% за 1,0 мин.; скорость потока: 1,5 мл/мин.; колонка: Xbridge-C18, 30 × 4,6 мм, 2,5 мкм. Чистота по LC (требуемый продукт): 88% (214 нм); масс-спектрометрия: обнаружен пик 368,0 (M+Na)+ на 1,74 мин.
Следующие соединения синтезировали соответственно.
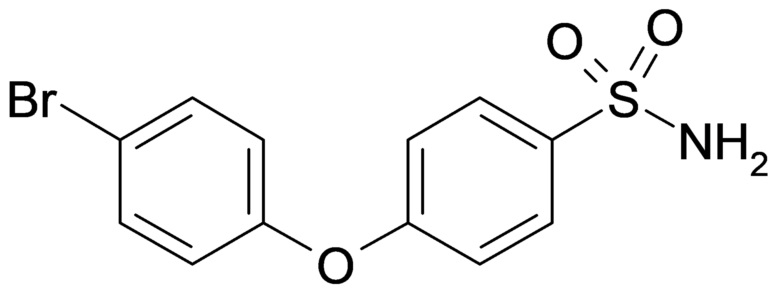
2.7.2 Синтез 4-(4-бромфенэтокси)бензолсульфонамида
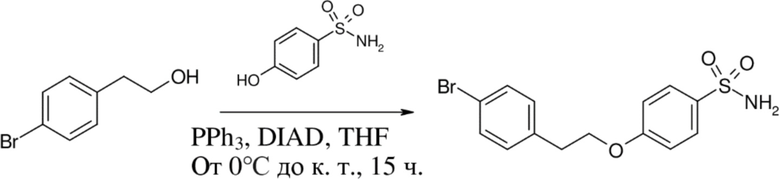
DIAD (11,1 г, 54,7 ммоль) добавляли при 0°C по каплям к раствору 2-(4-бромфенил)этанола (10 г, 49,8 ммоль), 4-гидроксибензолсульфонамида (8,6 г, 49,8 ммоль) и PPh3 (14,3 г, 54,795 ммоль) в сухом THF (200 мл). Обеспечивали нагревание реакционной смеси до к. т. с перемешиванием в течение 20 часов. Растворитель удаляли при пониженном давлении и остаток растворяли в EA (200 мл) и затем промывали водой (50 мл) и солевым раствором (50 мл). Органическую фазу высушивали над Na2SO4. После фильтрации растворитель удаляли при пониженном давлении и остаток очищали посредством колоночной хроматографии (силикагель, элюирование EA в РЕ от 0 до 40%) с получением 4-(4-бромфенэтокси)бензолсульфонамида (6,8 г в виде белого твердого вещества) с выходом 39%.
Способ LC-масс-спектрометрии: подвижная фаза: H2O (0,01%TFA (A)/MeCN (0,01%TFA ), (B); градиент: 5% B в течение 0,2 мин., увеличение до 95% B в течение 1,3 мин.; скорость потока: 1,8 мл/мин.; колонка: SunFire, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 95% (214 нм); масс-спектрометрия: обнаружен пик 356 (M+H) + на 2,08 мин.
2.7.3 Схема синтеза 4-((4-йодфенокси)метил)бензолсульфонамида
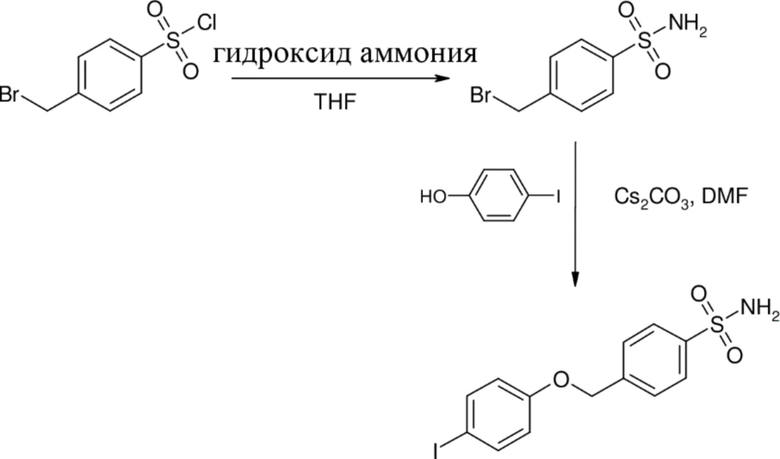
2.7.4 Синтез 4-(бромметил)бензолсульфонамида

Раствор 4-(бромметил)бензолсульфонилхлорида (7 г, 26 ммоль) в THF (80 мл) охлаждали до 0°C, к нему добавляли 28% водный раствор аммиака (6,5 мл) и смесь перемешивали при к. т. в течение 2 часов. Реакционный раствор концентрировали и добавляли этилацетат (200 мл). Органический слой отделяли, высушивали и концентрировали. Неочищенный продукт 4-(бромметил)бензолсульфонамид использовали непосредственно без дополнительной очистки. (5,5 г, 86%)
Способ LC-масс-спектрометрии: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 2,0 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 90% (214 нм); масс-спектрометрия: обнаружен пик 250,1 (M+H) + на 1,64 мин.
2.7.5 Синтез 4-((4-йодфенокси)метил)бензолсульфонамида
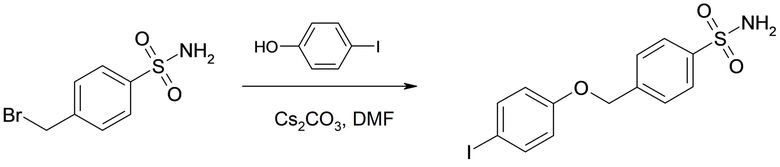
Cs2CO3 (10,7 г, 33 ммоль) и 4-йодфенол (6 г, 27,5 ммоль) добавляли к смеси 4-(бромметил)бензолсульфонамида (5,5 г, 22 ммоль) в DMF (50 мл). Затем смесь перемешивали при к. т. в течение 12 часов. К смеси добавляли воду (200 мл), полученное твердое вещество фильтровали и затем суспендировали с помощью Et2O (50 мл); посрдством фильтрации с отсасыванием и высушивания на воздухе получают требуемый продукт в виде белого твердого вещества (5,5 г, 65%).
Способ LC-масс-спектрометрии: способ: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 1,8 мл/мин.; колонка: Xbridge-C18, 50×4,6 мм, 3,5 мкм. Чистота по LC: 80% (214 нм); масс-спектрометрия: обнаружен пик 389,7 (M+H)+ на 1,98 мин.
2.7.6 Синтез 4-(4-бромбензилокси)бензолсульфонамида
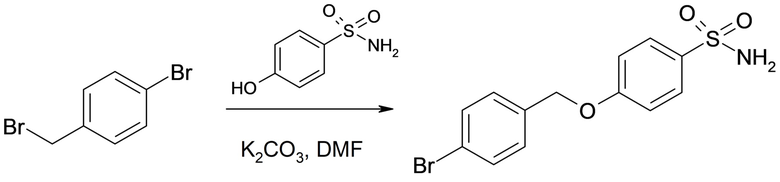
К смеси 1-бром-4-(бромметил)бензола (6,5 г, 26 ммоль) в DMF (50 мл) добавляли K2CO3 (5,5 г, 40 ммоль) и 4-гидроксибензолсульфонамид (4,5 г, 26 ммоль). Затем смесь перемешивали при 50oC в течение 2 часов. К смеси добавляли воду (200 мл), твердое вещество фильтровали. Затем твердое вещество суспендировали с PE:EA=1:2 (50 мл), посредством фильтрации с отсасыванием и высушивания на воздухе получали требуемый продукт в виде белого твердого вещества. (5,3 г, 60%).
Способ LC-масс-спектрометрии: способ: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 1,8 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 80% (214 нм); масс-спектрометрия: обнаружен пик 364 (M+Na)+ на 1,81 мин.
2.8 Примеры для синтеза промежуточных продуктов I по схеме 2
2.8.1 Синтез трет-бутил-12-(4-сульфамоилфенокси)додеканоата
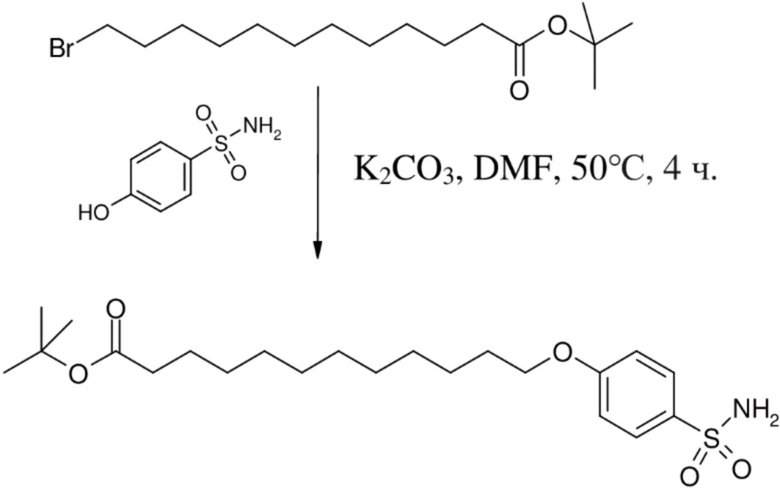
Смесь трет-бутил-12-бромододеканоата (6 г, 18 ммоль), 4-гидроксибензолсульфонамида (3 г, 18 ммоль) и K2CO3 (5 г, 36 ммоль) в DMF (50 мл) нагревали до 50°C и перемешивали в течение 4 часов. Затем добавляли воду (300 мл). Полученный осадок собирали и высушивали с получением неочищенного продукта трет-бутил-12-(4-сульфамоилфенокси)додеканоата, который суспендировали EA/PE (1/5, 100 мл) с получением 7 г (93%) 12-(4-сульфамоилфенокси)додеканоата:
Способ LC-масс-спектрометрии: подвижная фаза: A: вода (0,01%TFA) B: MeCN (0,01%TFA). градиент: 5% B в течение 0,2 мин., увеличение до 95% B в течение 1,3 мин., 95% B в течение 1,5 мин., возврат к 5% B в течение 0,01 мин.; скорость потока: 1,8 мл/мин.; колонка: Sunfire, 50*4,6 мм, 3,5 мкм, температура колонки: 50°C. Чистота по LC-MS: 100% (214 нм); масс-спектрометрия: обнаружен пик 450,2 (M+Na)+ на 2,23 мин.
1H ЯМР (400 МГц, CDCl3) δ 7,83 (t, J=14,8 Гц, 2H), 6,96 (d, J=8,8 Гц, 2H), 4,89 (s, 2H), 4,03 (dt, J=13,0, 6,6 Гц, 2H), 2,20 (t, J=7,5 Гц, 2H), 1,73-1,80 (m, 2H), 1,50-1,57 (m, 2H), 1,40-1,48 (m, 11H), 1,37-1,19 (m, 12H).
Следующие соединения синтезировали соответственно.
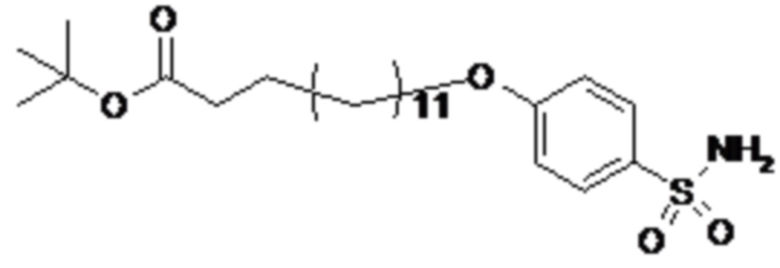
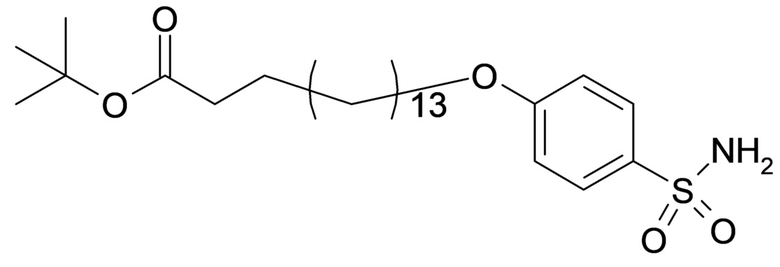
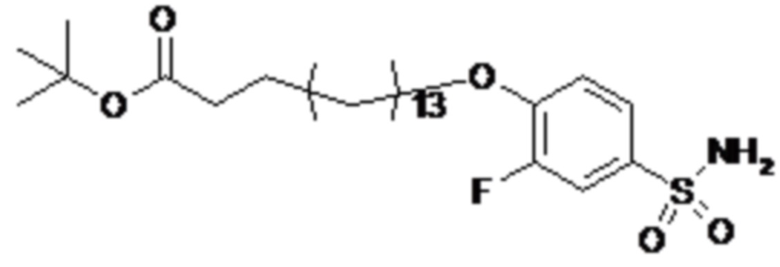
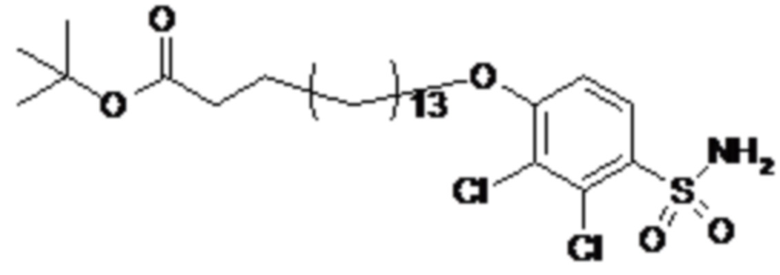
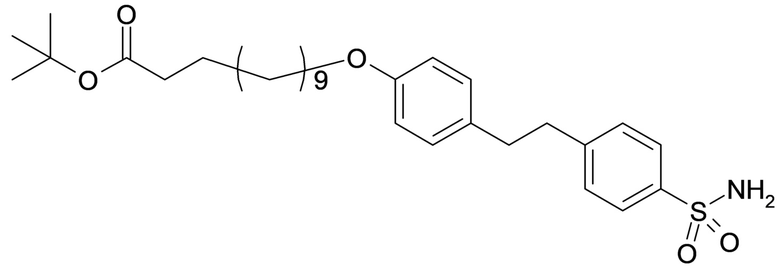
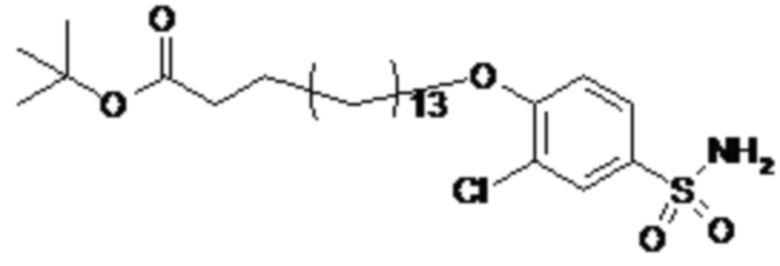
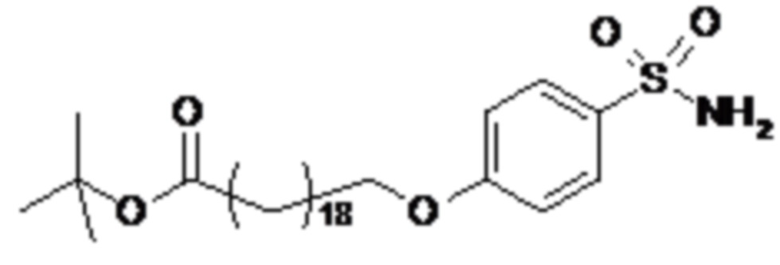
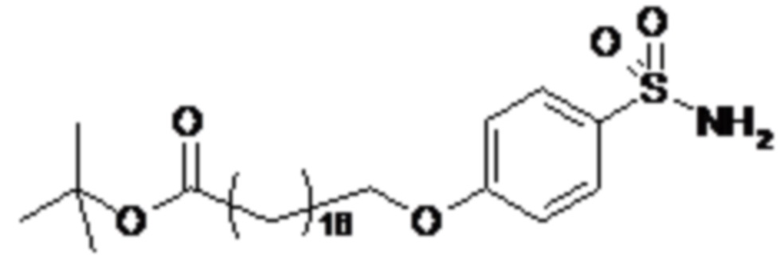
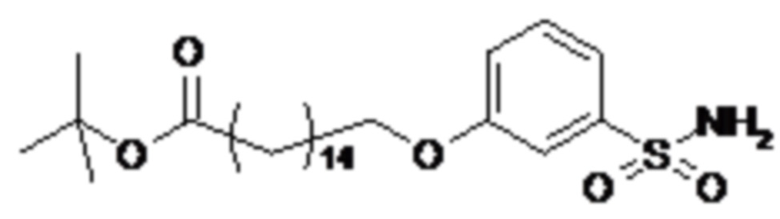
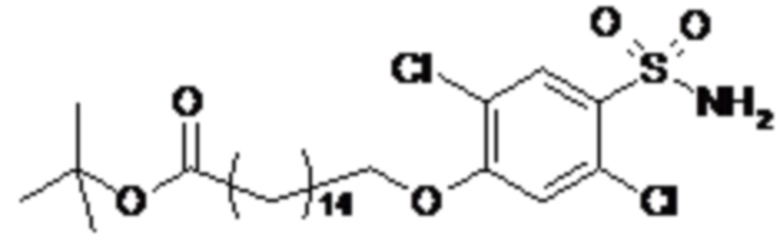
Схема синтеза. Синтез 14-(4-сульфамоилфенил)тетрадеканоата
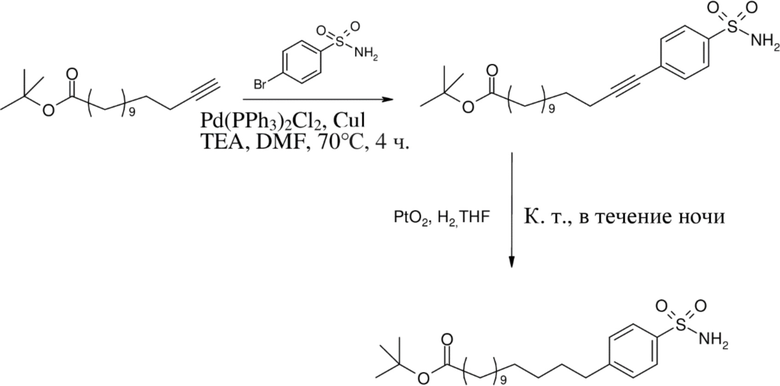
2.8.2 Синтез трет-бутил-14-(4-сульфамоилфенил)тетрадец-13-иноата
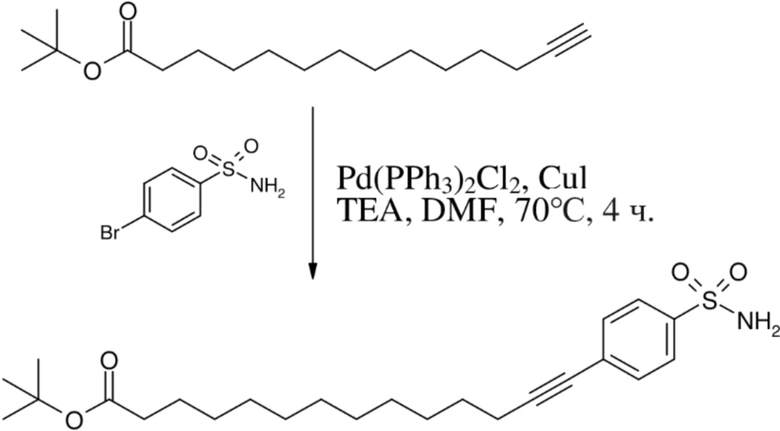
Pd(PPh3)2Cl2 (0,47 г, 0,68 ммоль), CuI (0,13 г, 0,68 ммоль), Et3N (2 г, 20,33 ммоль) и трет-бутилтетрадец-13-иноат (2,2 г, 7,8 ммоль) добавляли к смеси 4-бромбензолсульфонамида (1,6 г, 6,8 ммоль) в DMF (20 мл). Колбу освобождали от содержимого и заполняли N2. Затем смесь перемешивали при 70°C в течение 4 часов. К смеси добавляли воду (80 мл), экстрагировали ЕА (2 × 80 мл). Объединенную органическую фазу промывали солевым раствором, высушивали над Na2SO4, концентрировали под вакуумом. Неочищенный продукт очищали посредством хроматографии на силикагеле (PE:EA=4:1) с получением трет-бутил-14-(4-сульфамоилфенил)тетрадец-13-иноата (2,2 г, 5,05 ммоль, выход: 76%) в виде желтого твердого вещества.
Способ LC-масс-спектрометрии: способ: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 1,8 мл/мин.; колонка: Xbridge-C18, 50×4,6 мм, 3,5 мкм. Чистота по LC: 98% (214 нм); масс-спектрометрия: обнаружен пик 458 (M+H)+ на 2,37 мин.
Следующие соединения синтезировали соответственно.
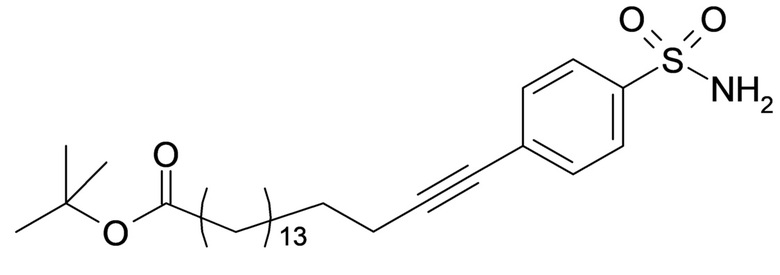
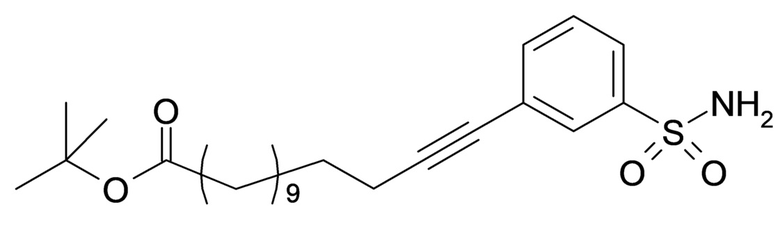
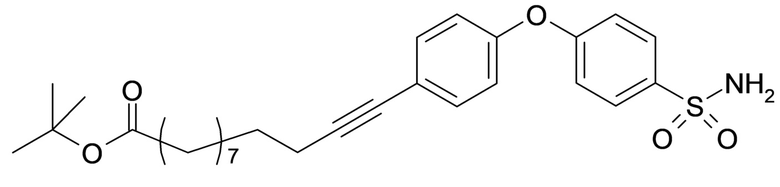
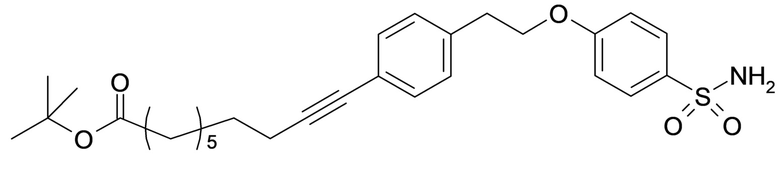
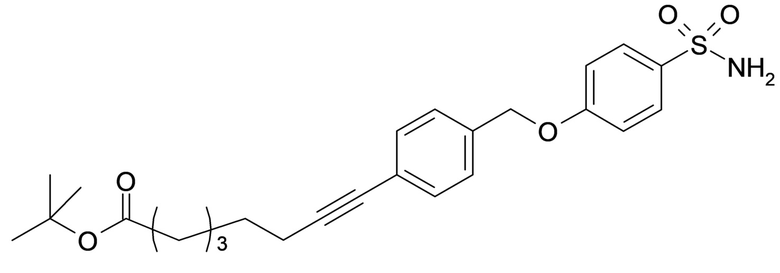
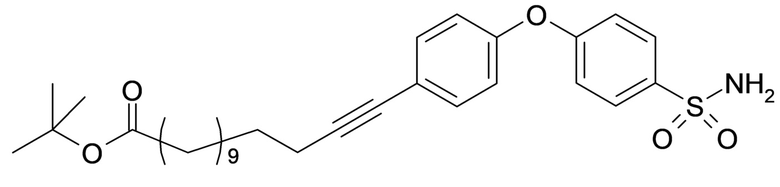
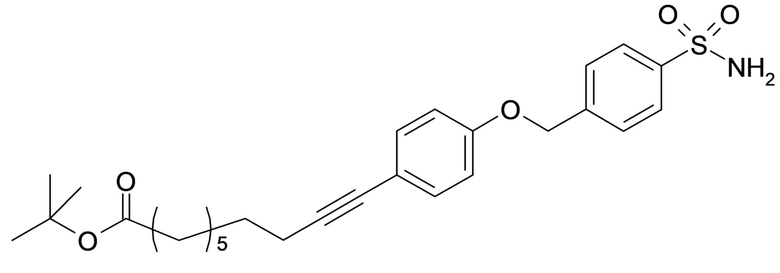
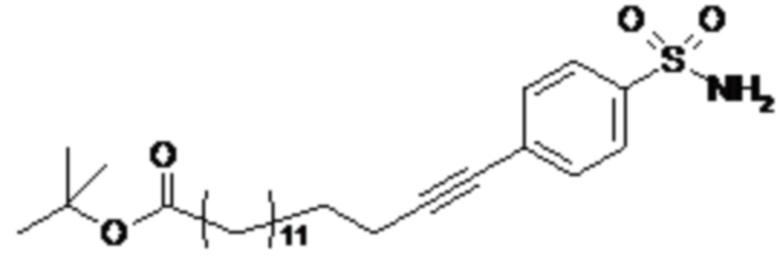

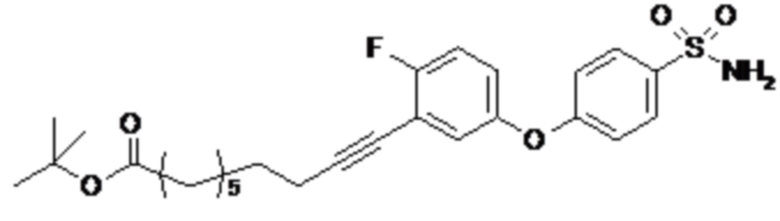
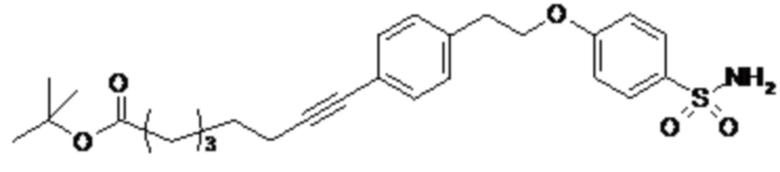
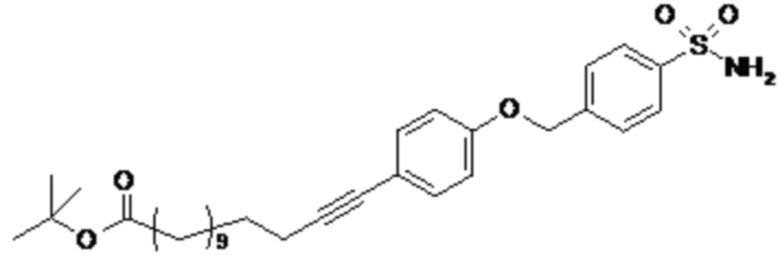
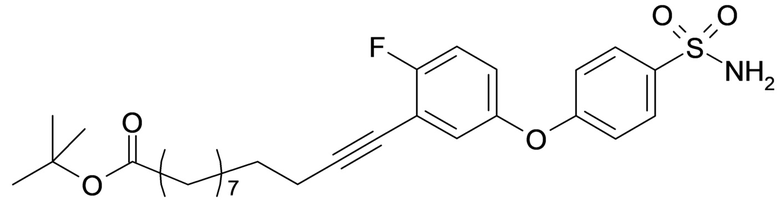
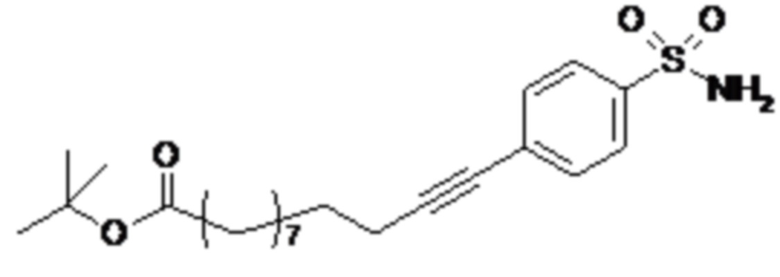
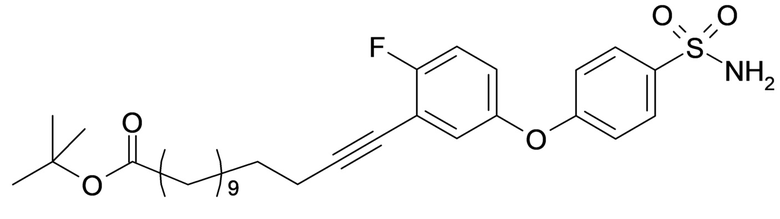
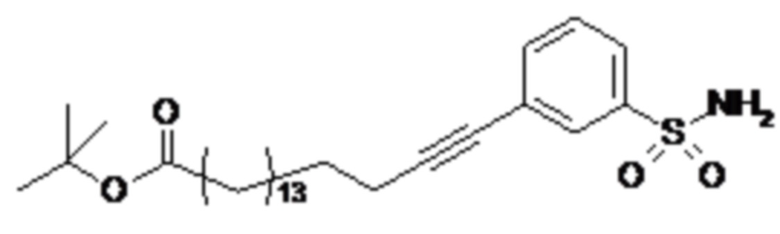
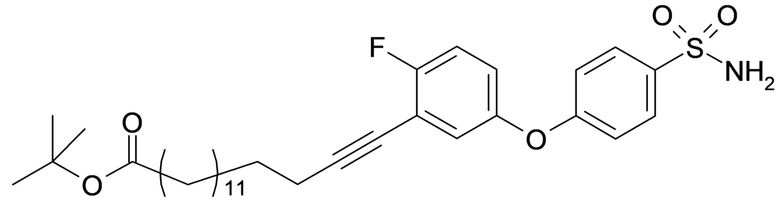
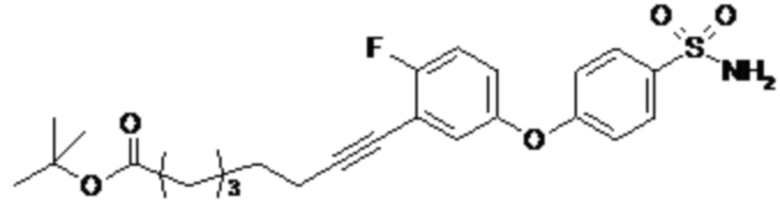
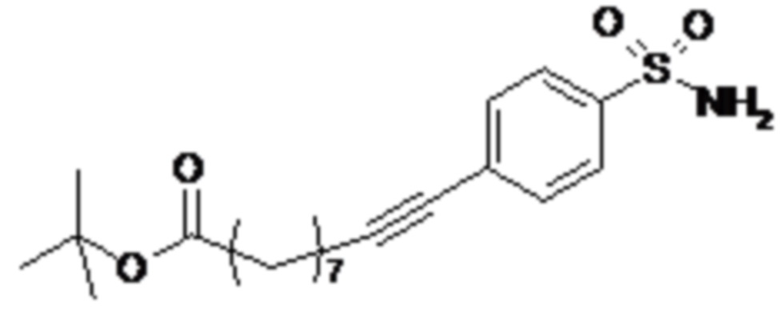
2.8.3 Синтез трет-бутил-14-(4-сульфамоилфенил)тетрадеканоата
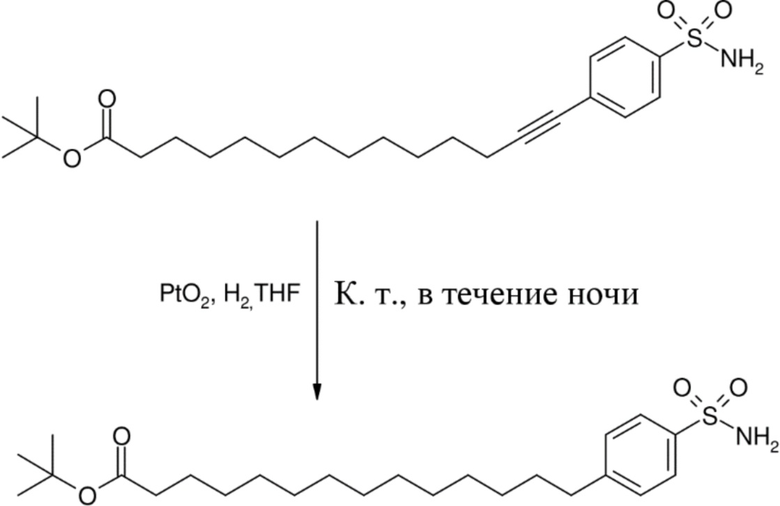
PtO2 (0,23 г, 1,01 ммоль) добавляли к смеси трет-бутил-14-(4-сульфамоилфенил)тетрадец-13-иноата (2,2 г, 5,05 ммоль) в THF (30 мл). Колбу освобождали от содержимого и заполняли H2. Затем смесь перемешивали при к. т. в течение ночи. Фильтровали, концентрировали под вакуумом, с получением 14-(4-сульфамоилфенил)тетрадеканоата (2 г, 4,55 ммоль, выход: 90%) в виде серого твердого вещества.
Способ LC-масс-спектрометрии: подвижная фаза: A=10 мМ TFA/H2O, B=MeCN; градиент: B=5% - 95% за 1,5 мин.; скорость потока: 1,8 мл/мин.; колонка: Xbridge-C18, 50 × 4,6 мм, 3,5 мкм. Чистота по LC: 93% (214 нм); масс-спектрометрия: обнаружен пик 462 (M+H)+ на 2,44 мин.
1HNMR (400 МГц, DMSO) δ 7,72 (d, J=8,1 Гц, 2H), 7,37 (d, J=8,1 Гц, 2H), 7,26 (s, 2H), 2,63 (t, J=7,6 Гц, 2H), 2,16 (t, J=7,3 Гц, 2H), 1,57 (s, 2H), 1,51-1,43 (m, 2H), 1,38 (s, 9H), 1,25 (d, J=14,5 Гц, 18H).
Следующие соединения синтезировали соответственно.
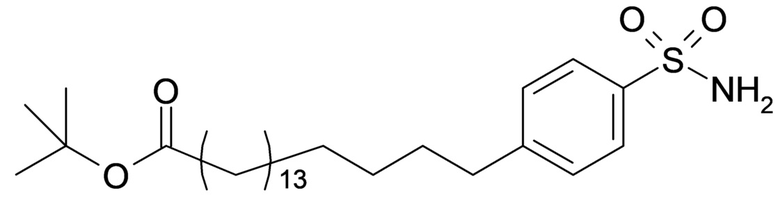
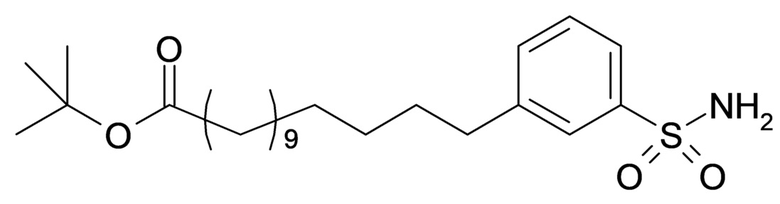
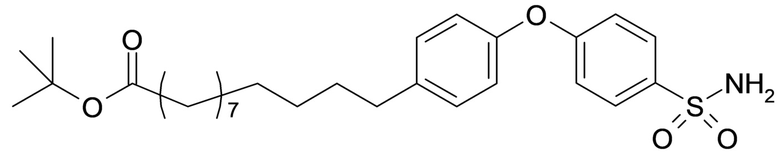
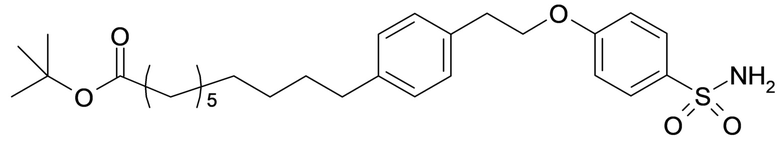
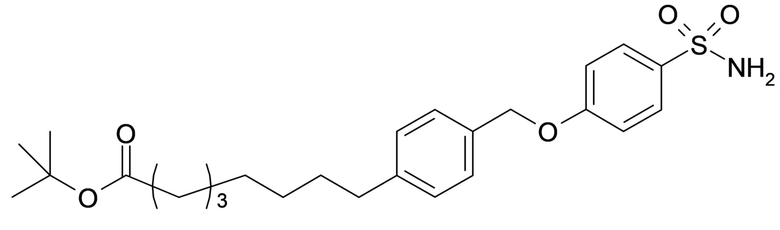
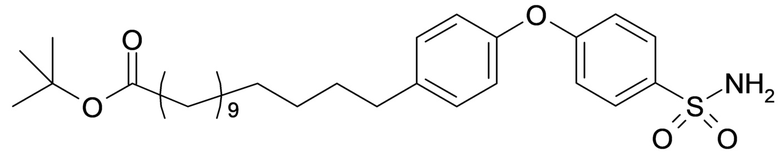
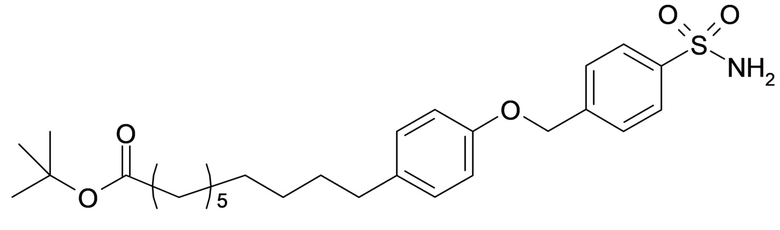
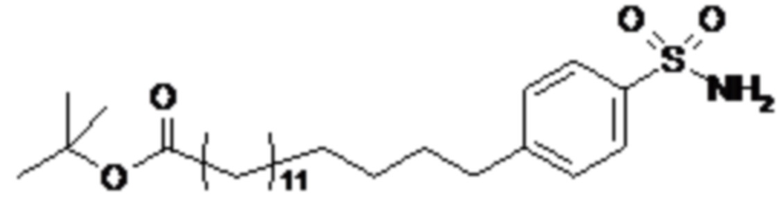
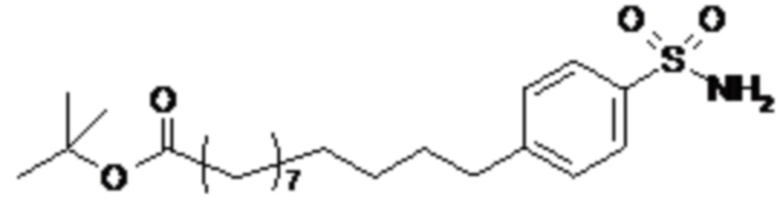
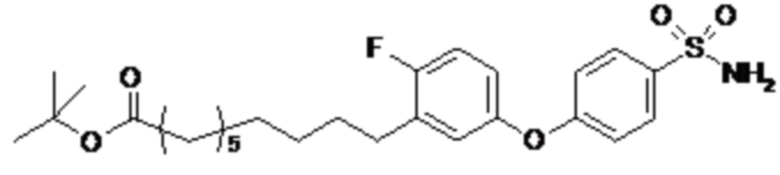
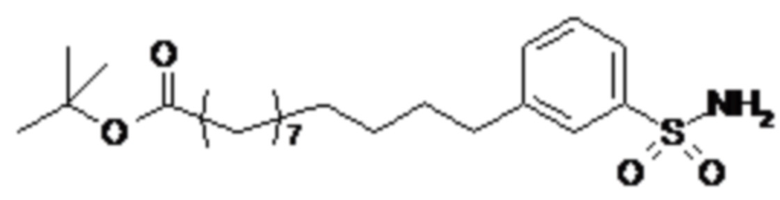
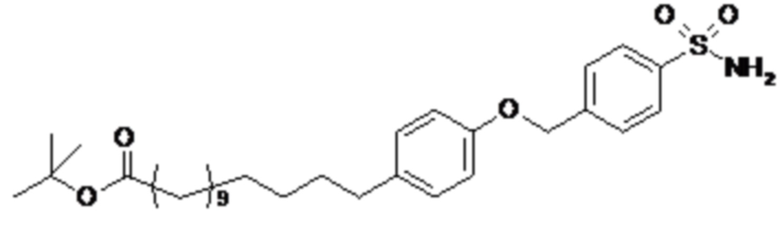
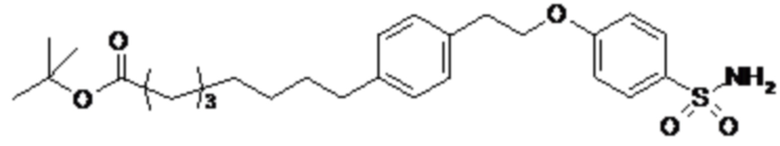
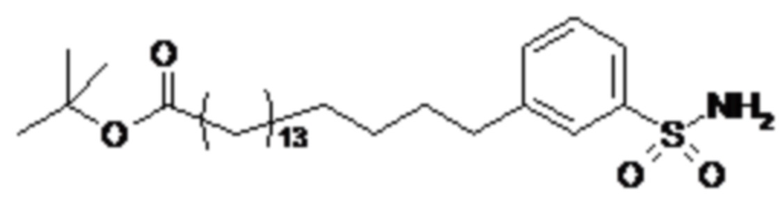
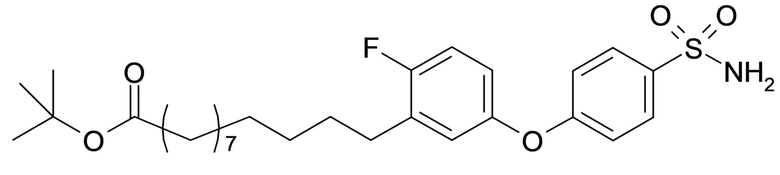
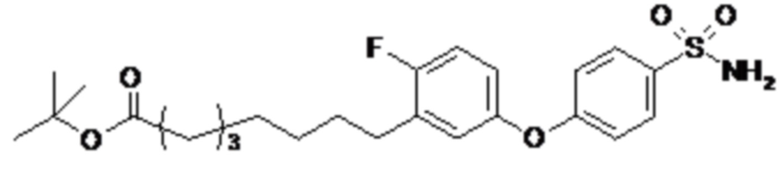
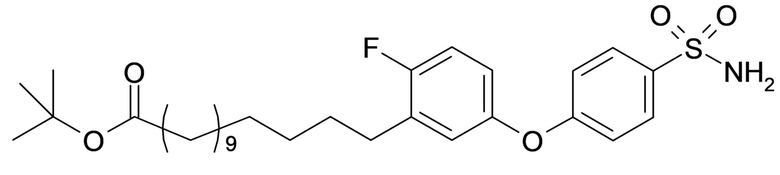
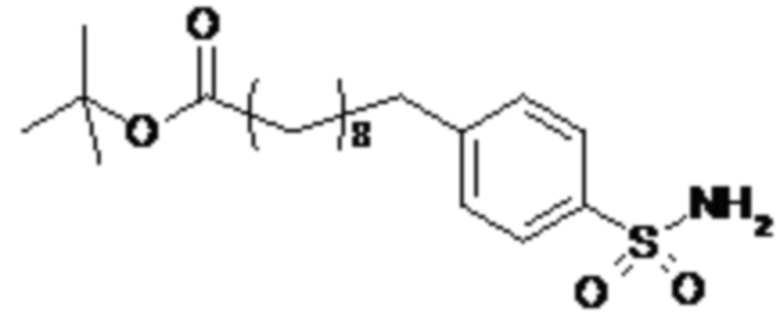
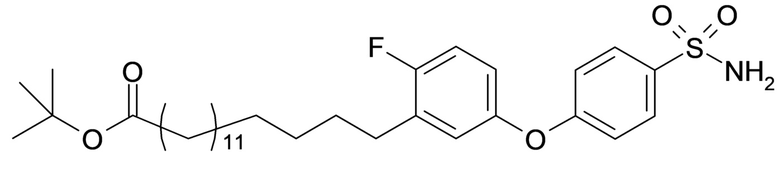
2.8.4 Синтез 2-[[4-[3-(12-трет-бутокси-12-оксододецил)-4-фторфенокси]фенил]сульфониламино]пиримидин-5-карбоновой кислоты
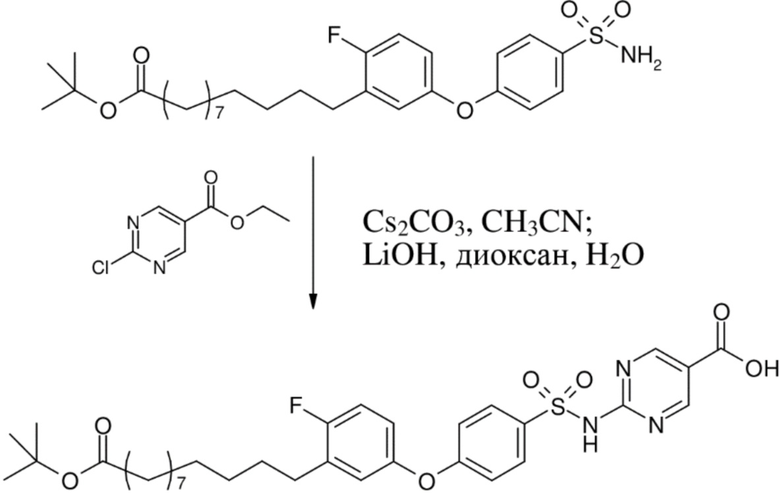
Смесь трет-бутил-12-[2-фтор-5-(4-сульфамоилфенокси)фенил]додеканоата (300 мг, 575 мкмоль), этил-2-хлорпиримидин-5-карбоксилата (112 мг, 603 мкмоль) и Cs2CO3 (656 мг, 2,01 ммоль) в MeCN (6 мл) нагревали до 60°C и перемешивали в течение 3 часов (контроль TLC). Реакционную смесь применяли на следующей стадии омыления без дополнительной очистки.
Суспензию разбавляли диоксаном (6 мл) и добавляли раствор LiOH (37 мг, 1,56 ммоль) в воде (6 мл). Смесь перемешивали при к. т. в течение 16 часов и добавляли дополнительное количество LiOH (37 мг, 1,56 ммоль). В целом смесь перемешивали при к. т. в течение 36 часов. Суспензию выливали в водный раствор лимонной кислоты (10 процентов, 50 мл). Суспензию фильтровали, осадок на фильтре промывали водой и высушивали под вакуумом. Указанное в заголовке соединение 2-[[4-[3-(12-трет-бутокси-12-оксододецил)-4-фторфенокси]фенил]сульфониламино]пиримидин-5-карбоновую кислоту получали в виде белого твердого вещества (350 мг, кол.).
1H ЯМР (400,23 МГц, DMSO-d6) δ ppm 12,2 (bs, 2 H), 8,89 (s, 2 H), 7,99 (d, J=8,93 Гц, 2 H), 7,21 (t, J=9,17 Гц, 1 H), 7,05 (m, 4 H), 2,58 (br t, J= 7,46 Гц, 2 H), 2,15 (t, J= 7,27 Гц, 2 H), 1,53 (m, 2 H), 1,47 (m, 2 H), 1,38 (s, 9 H), 1,26-1,22 (m, 14 H).
Если требуемый продукт не выпадал в осадок при вливании водной лимонной кислоты, водный слой экстрагировали этилацетатом, объединенные органические слои высушивали над Na2SO4, фильтровали и концентрировали in vacuo. Неочищенные продукты подвергали колоночной хроматографии, используя MeOH/CH2Cl2 в качестве элюента.
Следующие соединения синтезировали соответственно.
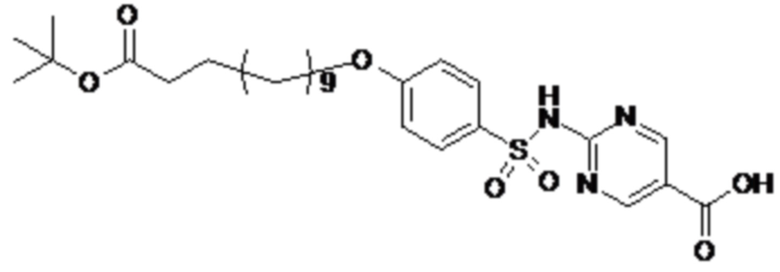
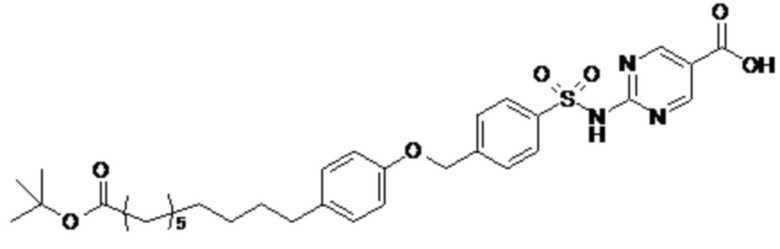
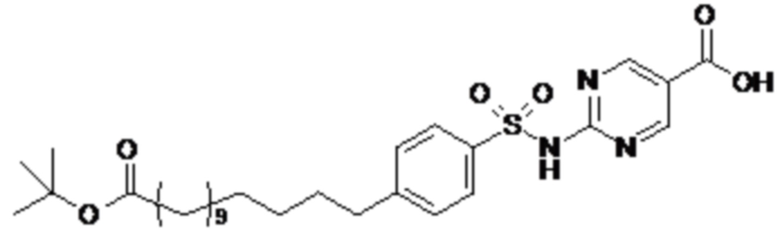
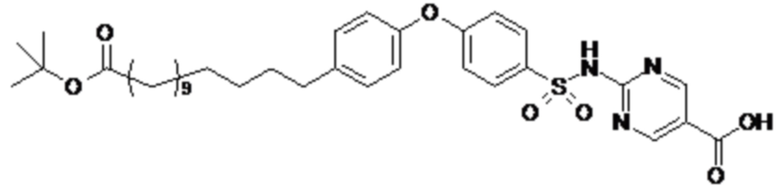
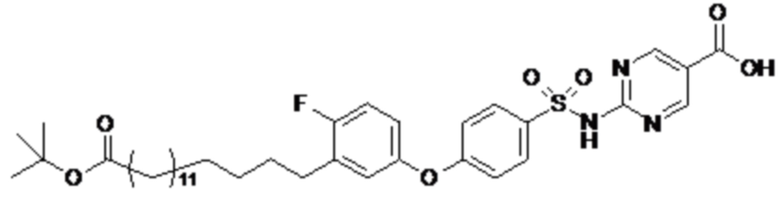
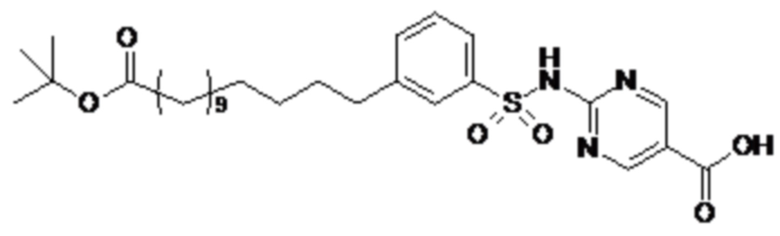
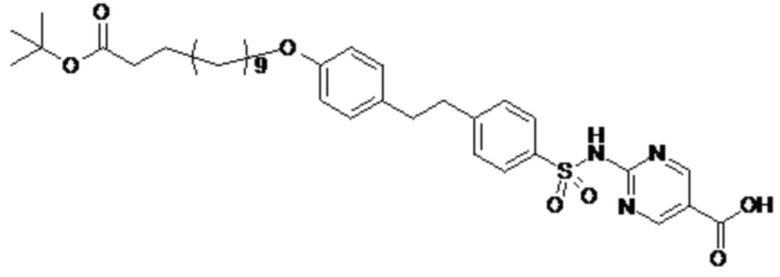
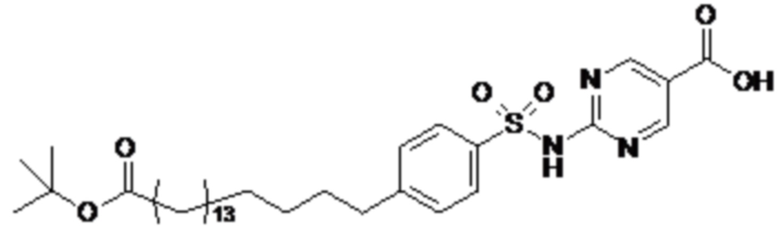
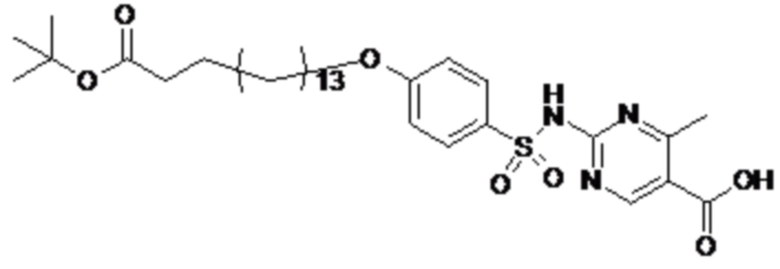
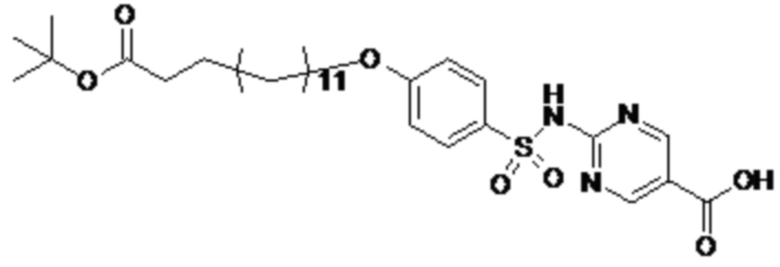
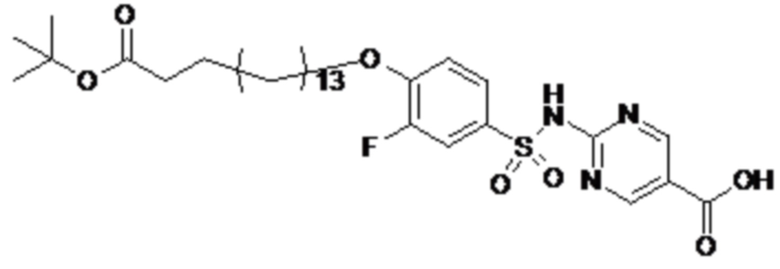
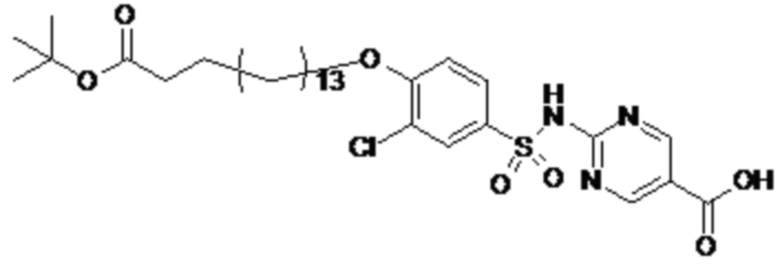
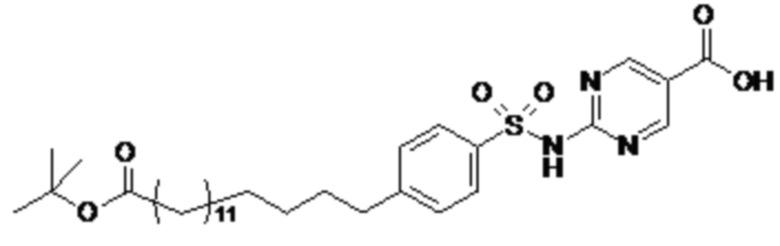
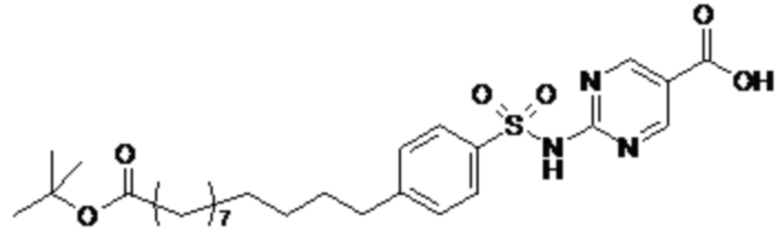
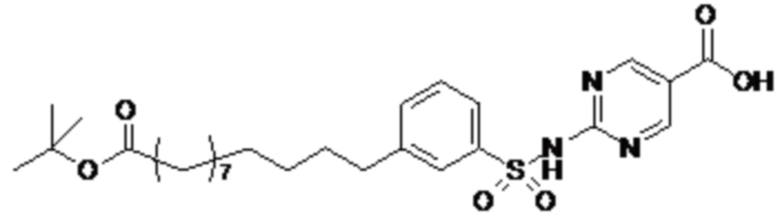
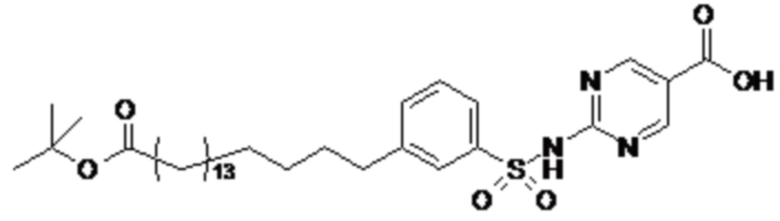
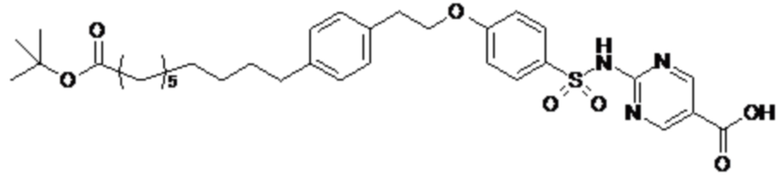
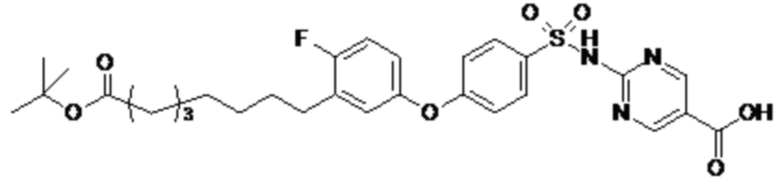
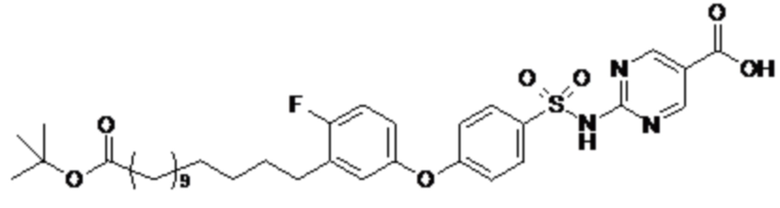
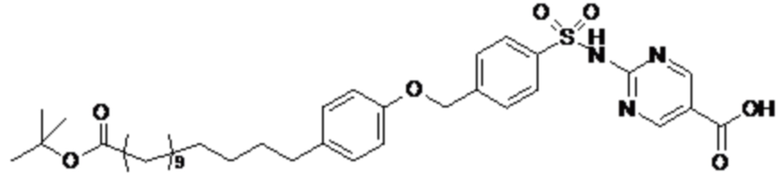
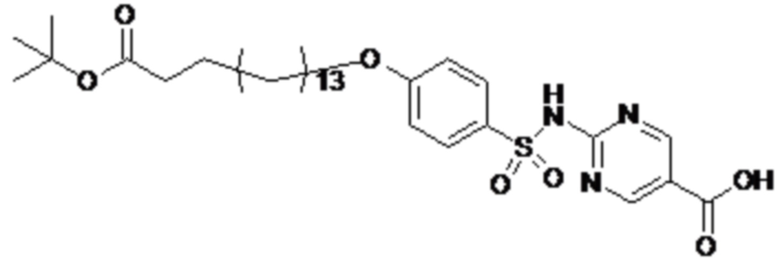
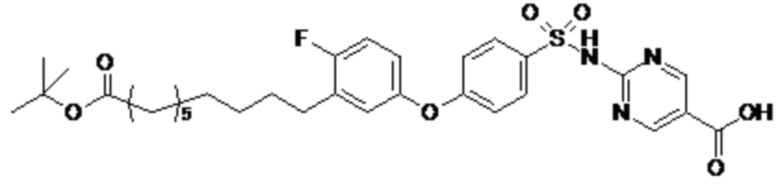
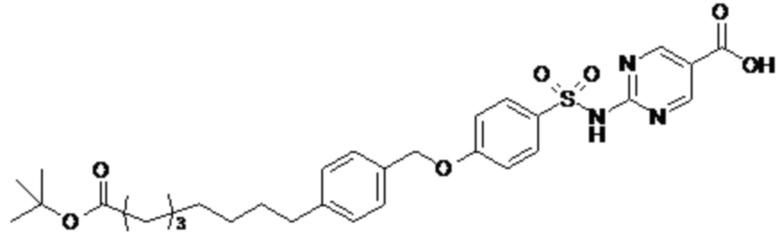
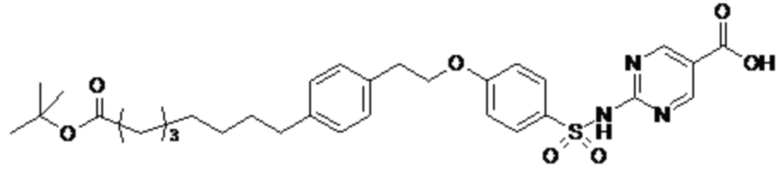
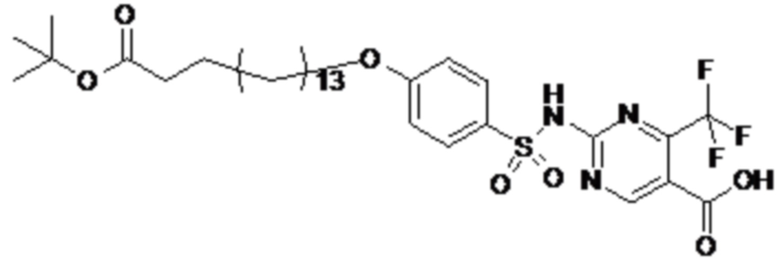
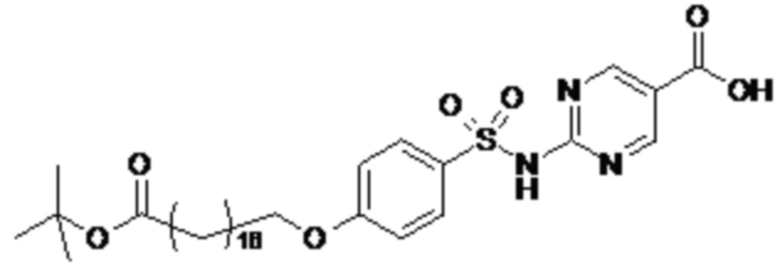
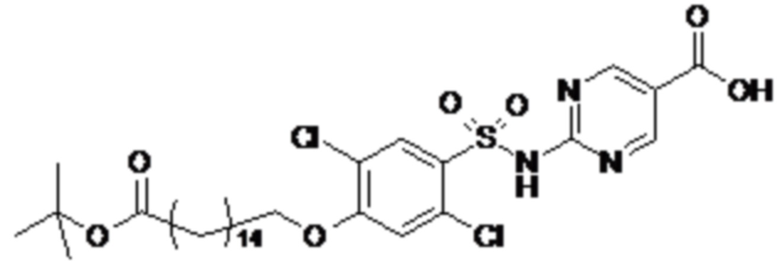
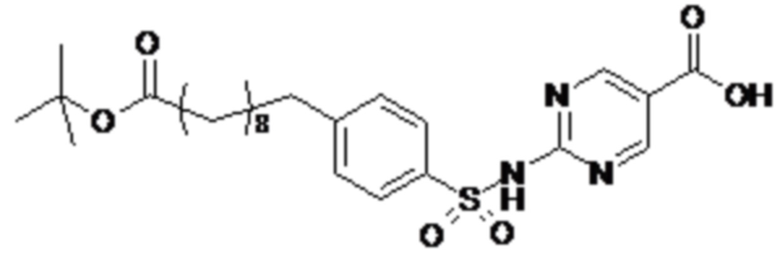
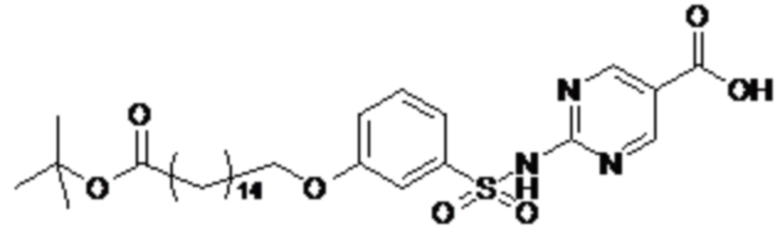
2.8.5 Синтез 6-[[4-[3-(12-трет-бутокси-12-оксододецил)-4-фторфенокси]фенил]сульфониламино]пиридин-3-карбоновой кислоты
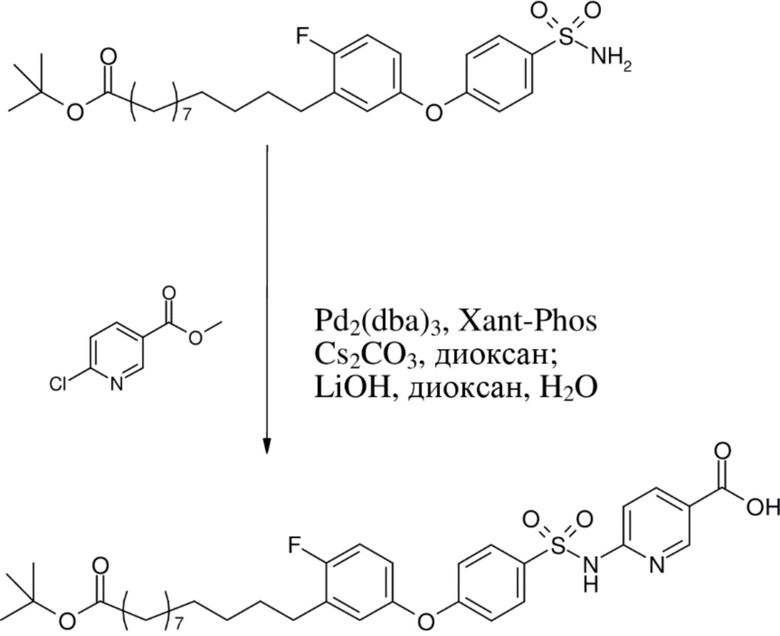
Смесь трет-бутил 12-[2-фтор-5-(4-сульфамоилфенокси)фенил]додеканоат (300 мг, 575 мкмоль), метил-6-хлорникотиноат (102 мг, 603 мкмоль), Cs2CO3 (468 мг, 1,44 ммоль), трис(дибензилиденацетон)дипалладий (26 мг, 29 мкмоль) и 4,5-бис(дифенилфосфино)-9,9-диметилксантен ("xantphos", 17 мг, 29 мкмоль) в диоксане (6 мл) нагревали до 80°C в атмосфере аргона в течение 3 часов (контроль TLC). Реакционную смесь применяли на следующей стадии омыления без дополнительной очистки.
Суспензию разбавляли диоксаном (6 мл) и добавляли раствор LiOH (37 мг, 1,56 ммоль) в воде (6 мл). Смесь перемешивали при к. т. в течение 16 часов и добавляли дополнительное количество LiOH (37 мг, 1,56 ммоль). В целом смесь перемешивали при к. т. в течение 36 часов. Суспензию выливали в водный раствор лимонной кислоты (10 процентов, 50 мл). Суспензию фильтровали, осадок на фильтре промывали водой и высушивали под вакуумом. Указанное в заголовке соединение 6-[[4-[3-(12-трет-бутокси-12-оксододецил)-4-фторфенокси]фенил]сульфониламино]пиридин-3-карбоновую кислоту получали в виде белого твердого вещества (350 мг, кол.).
1H ЯМР (400,23 МГц, DMSO-d6) δ ppm 12,5 (br s, 1H), 8,54 (br s, 1 H), 8,11 (dd, J=8,93, 2,20 Гц, 1 H), 7,91 (br d, J=8,68 Гц, 2 H), 7,80 (m, 1 H), 7,19 (m, 2 H), 7,04 (m, 4 H), 2,58 (br t, J= 7,46 Гц, 2 H), 2,15 (t, J=7,27 Гц, 2 H), 1,48 (m, 4 H), 1,38 (s, 9 H), 1,26-1,22 (m, 14 H).
Если требуемый продукт не выпадал в осадок при вливании водной лимонной кислоты, водный слой экстрагировали этилацетатом, объединенные органические слои высушивали над Na2SO4, фильтровали и концентрировали in vacuo. Неочищенные продукты подвергали колоночной хроматографии, используя MeOH/CH2Cl2 в качестве элюента.
Следующие соединения синтезировали соответственно.
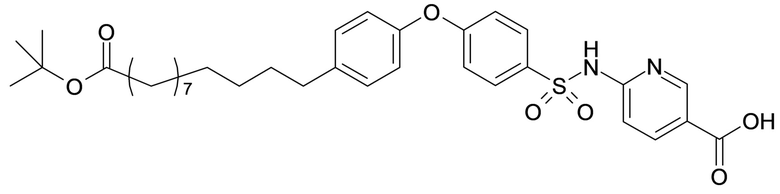
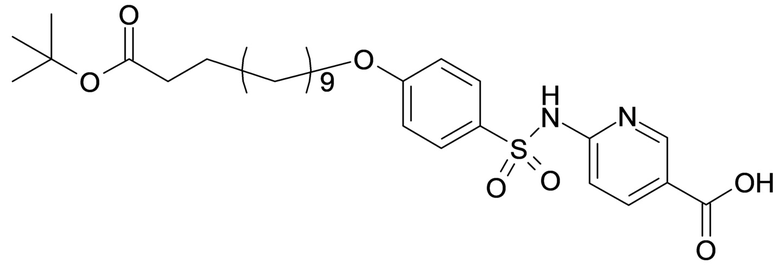
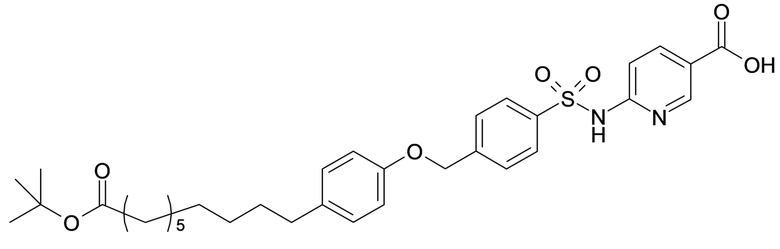
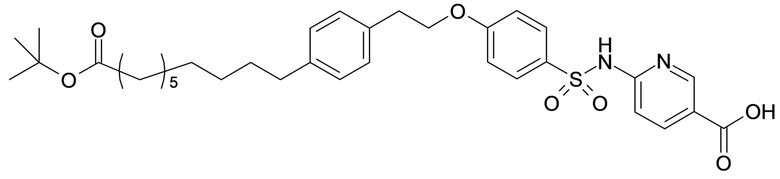
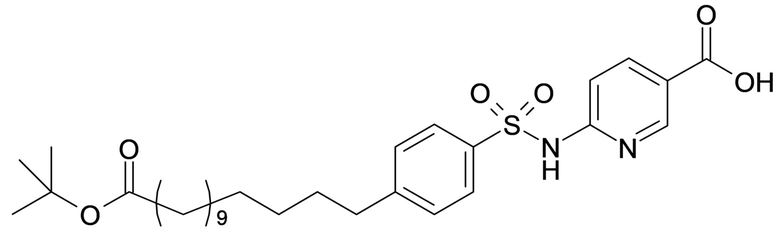
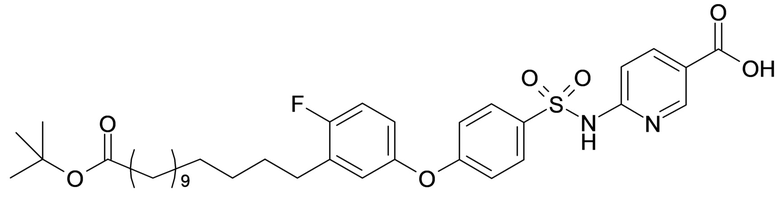
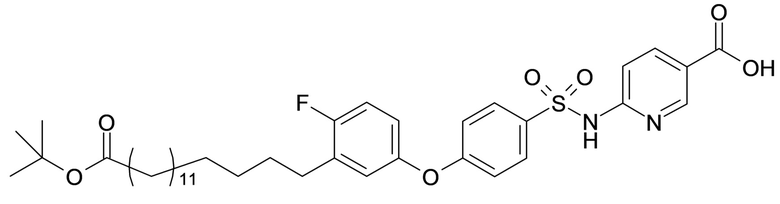
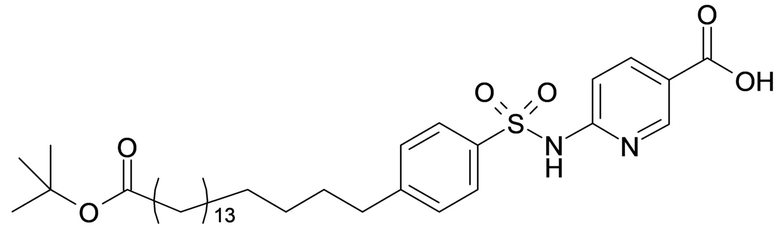
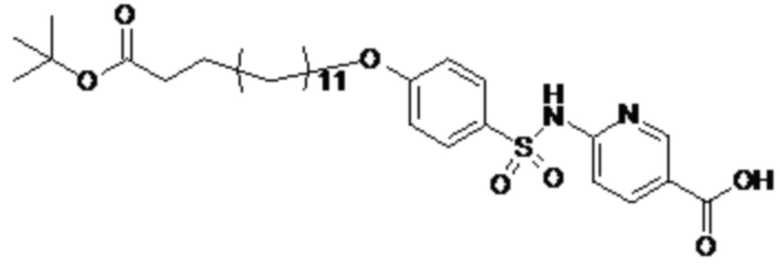
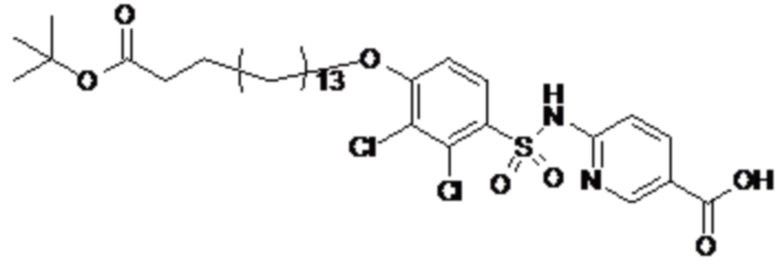
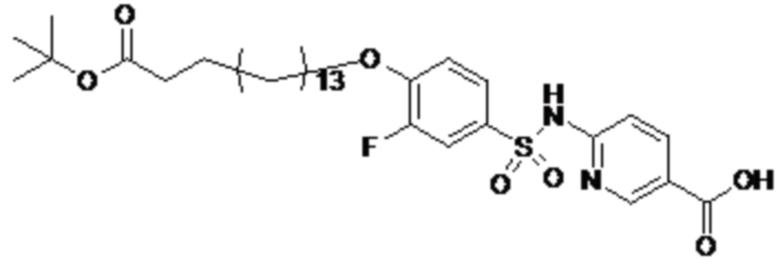
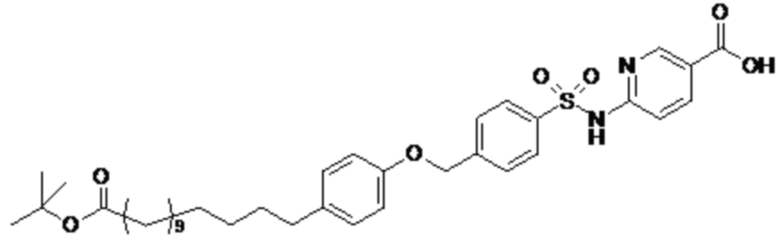
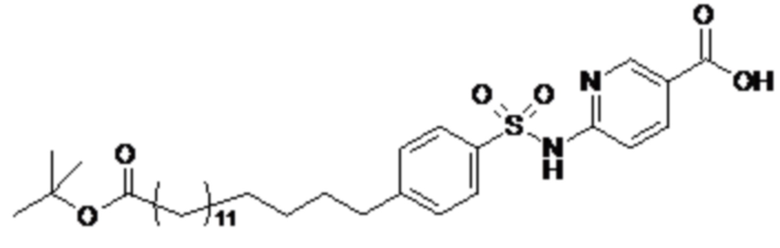
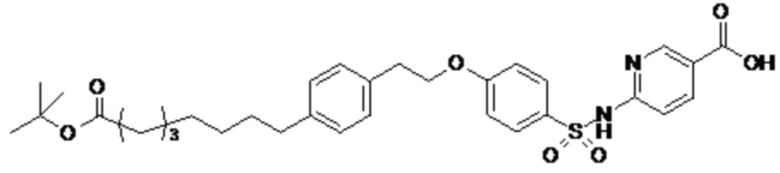
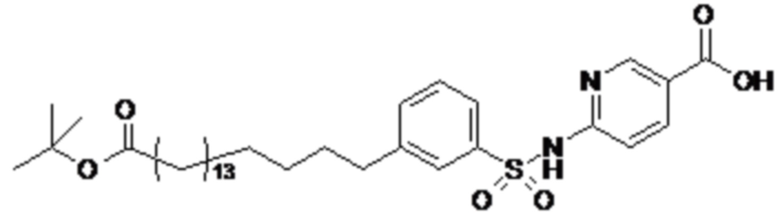
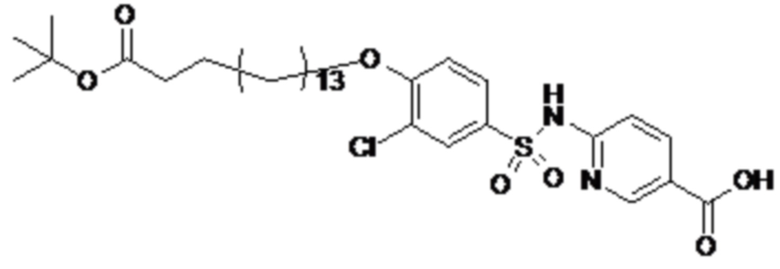
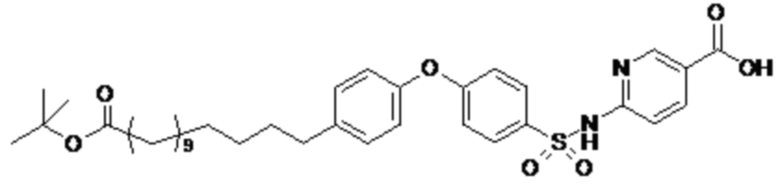
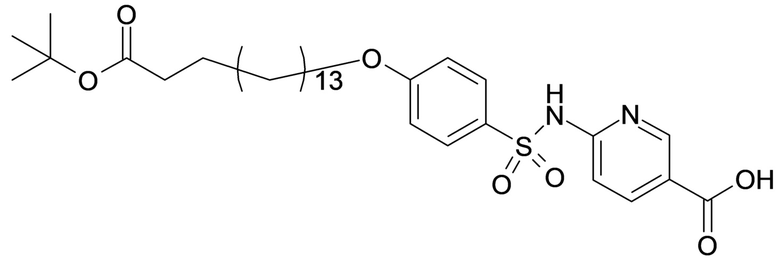
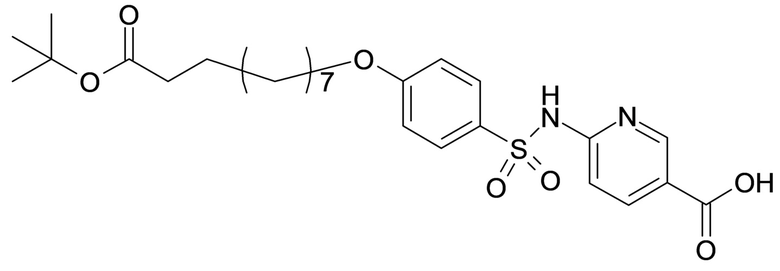
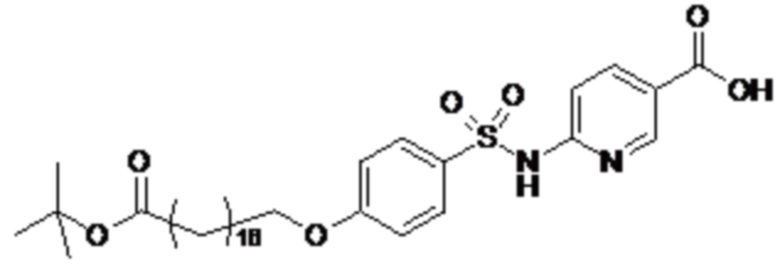
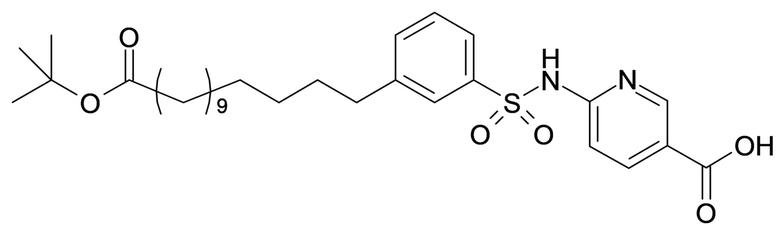
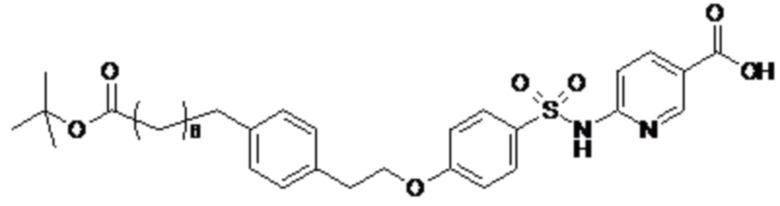

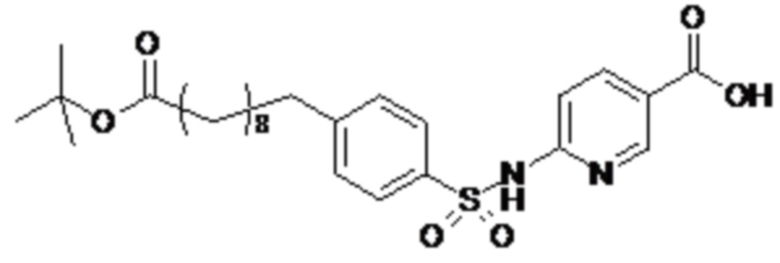

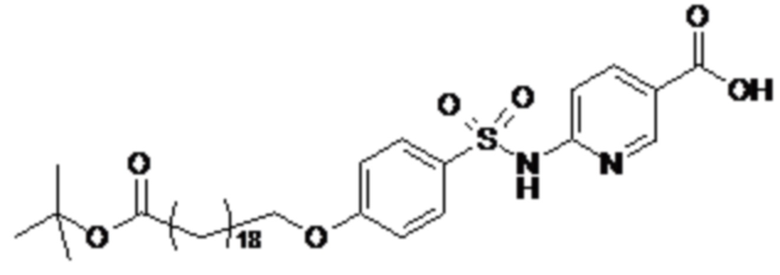

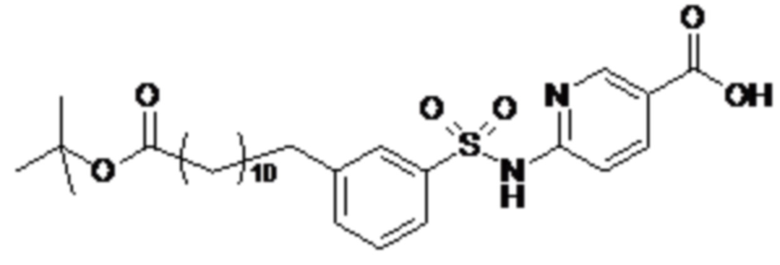
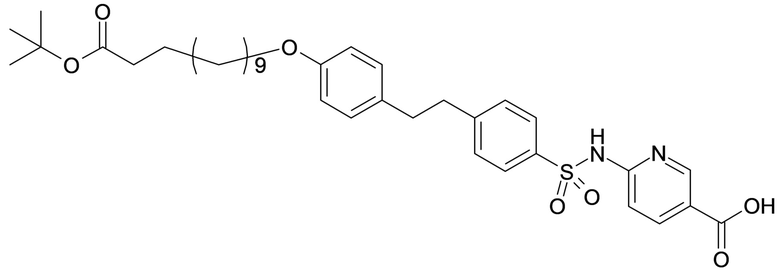
2.9 Примеры синтеза соединений формулы I по схеме 1
2.9.1 Синтез 2-[2-[2-[[2-[2-[2-[[6-[[4-[3-(14-трет-бутокси-14-оксо-тетрадецил)-4-фторфенокси]фенил]сульфониламино]пиридин-3-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты
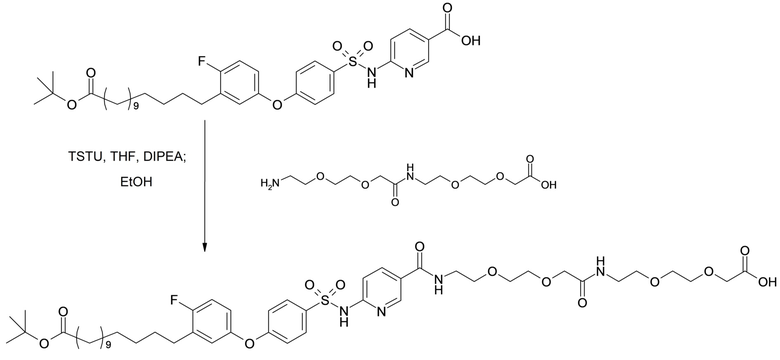
Смесь 6-[[4-[3-(14-трет-бутокси-14-оксо-тетрадецил)-4-фторфенокси]фенил]сульфониламино]пиридин-3-карбоновой кислоты (169 мг, 251 мкмоль), TSTU (80 мг, 264 мкмоль) и DIPEA (132 мкл, 97 мг, 1,25 ммоль) в 6 мл THF перемешивали при к. т. в течение 16 часов. Через 16 часов растворитель удаляли при пониженном давлении и добавляли раствор [2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]уксусной кислоты (85% мг, 277 мкмоль) в 6 мл абс. EtOH и смесь перемешивали при к. т. в течение 16 часов. Летучие компоненты удаляли при пониженном давлении, полученный остаток растворяли в CH2Cl2 и промывали водным 10% раствором KHSO4. Органический слой промывали с помощью воды и солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали с помощью RP HPLC с получением 2-[2-[2-[[2-[2-[2-[[6-[[4-[3-(14-трет-бутокси-14-оксо-тетрадецил)-4-фторфенокси]фенил]сульфониламино]пиридин-3-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты (106 мг, 44%).
1H ЯМР (400,23 МГц, DMSO-d6) δ ppm 12,29 (br s, 1 H), 8,52 (m, 2 H), 8,09 (dd, J=8,93, 2,32 Гц, 1 H), 7,89 (d, J=8,80 Гц, 2 H), 7,61 (br t, J=5,69 Гц, 1 H), 7,18 (m, 2 H), 7,03 (m, 4 H), 4,01 (s, 2 H), 3,86 (s, 2 H), 3,20-3,68 (m, 16 H), 2,58 (br t, J=7,52 Гц, 2 H), 2,15 (t, J=7,27 Гц, 2 H), 1,49 (m, 4 H), 1,38 (s, 9 H), 1,25 (m, 18 H).
Следующие соединения синтезировали соответственно.
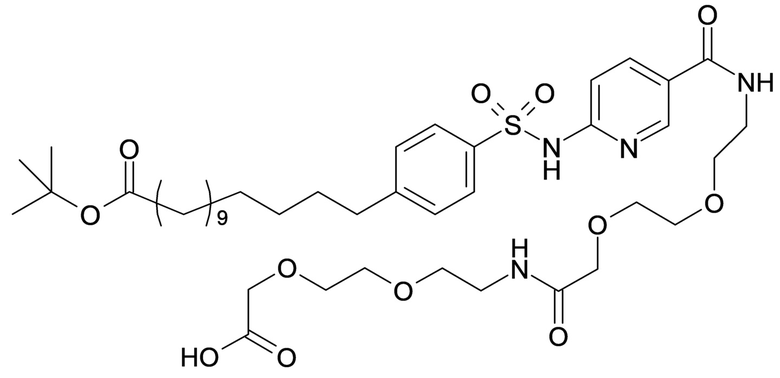
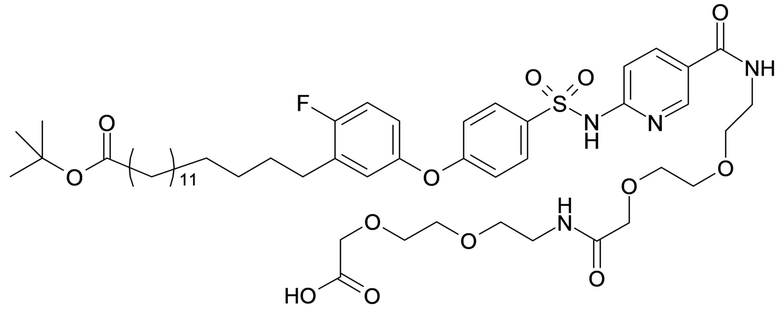
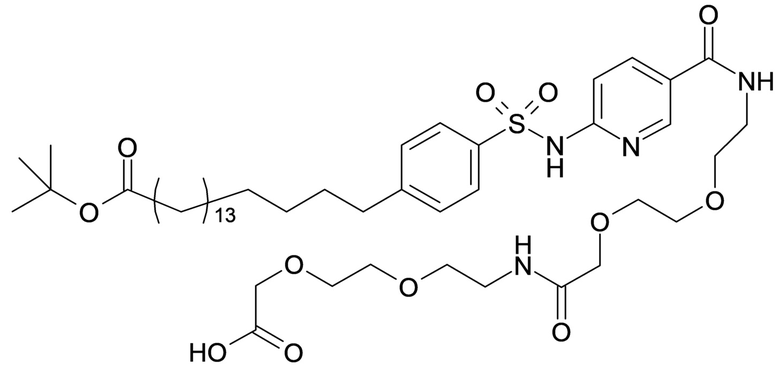
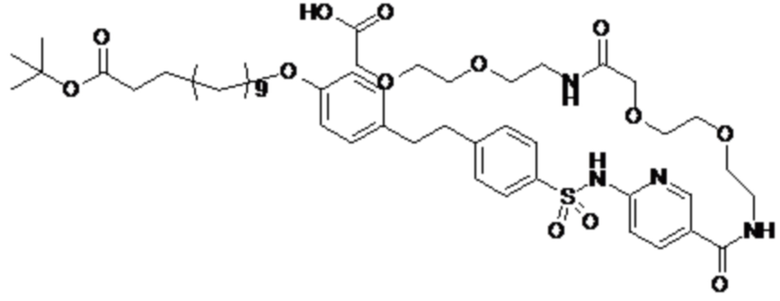
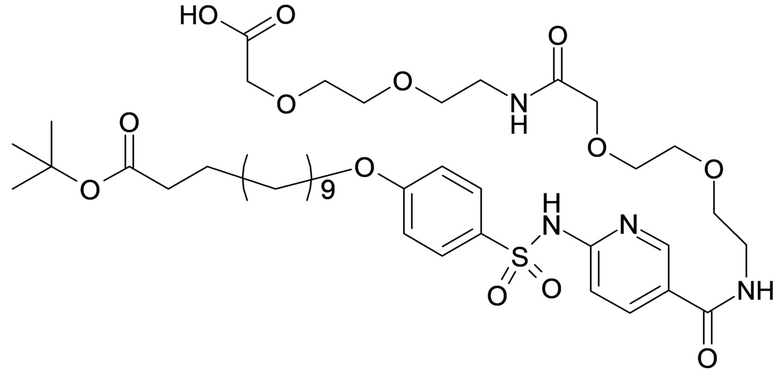
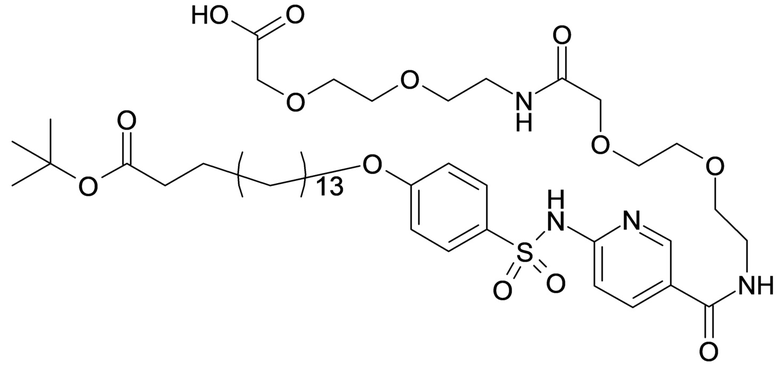
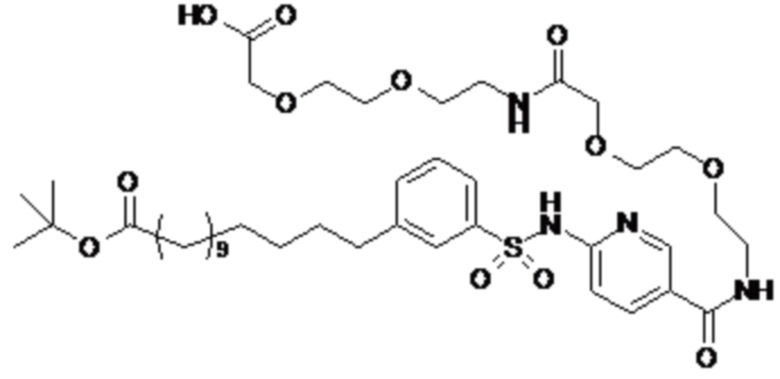
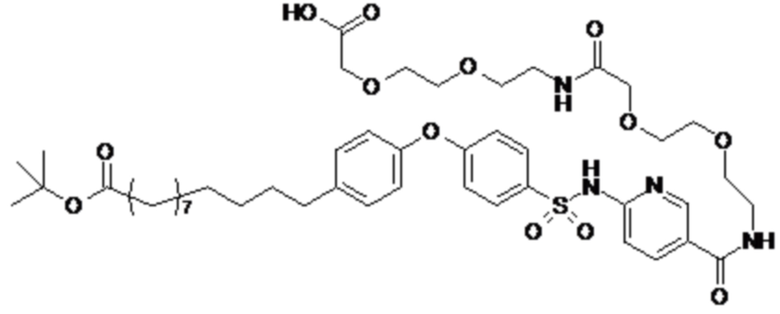
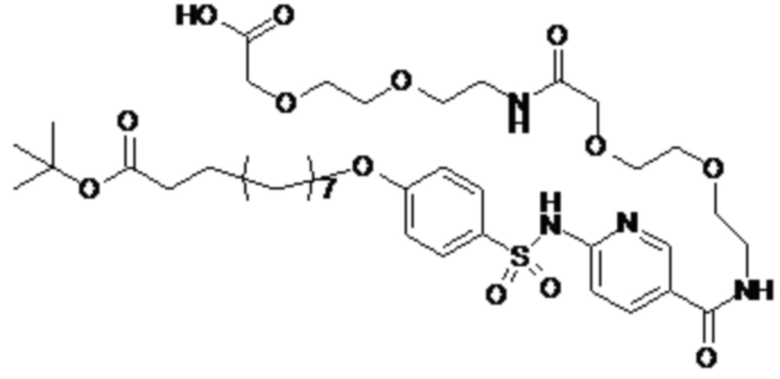
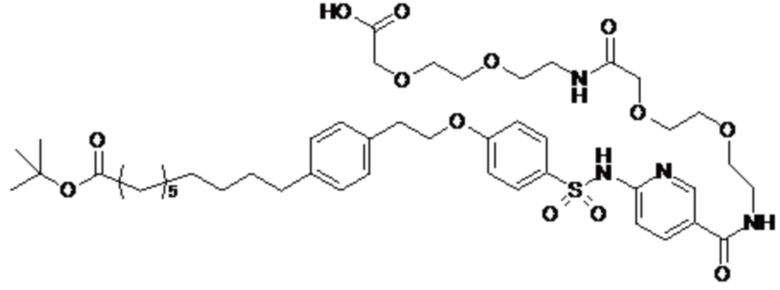
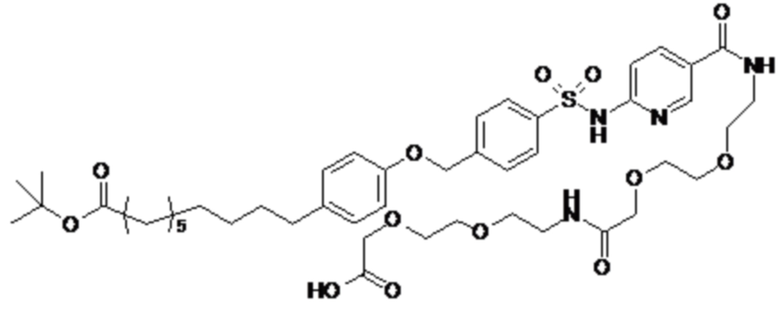
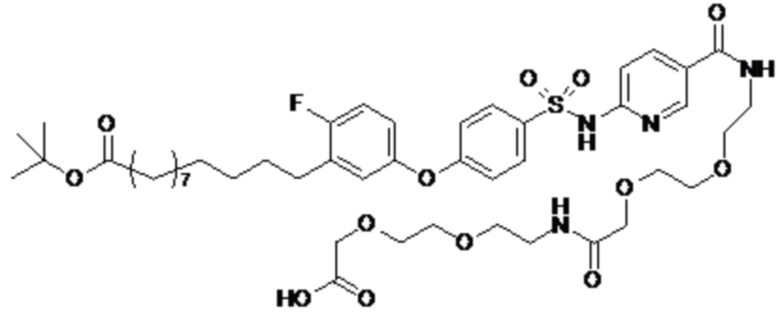
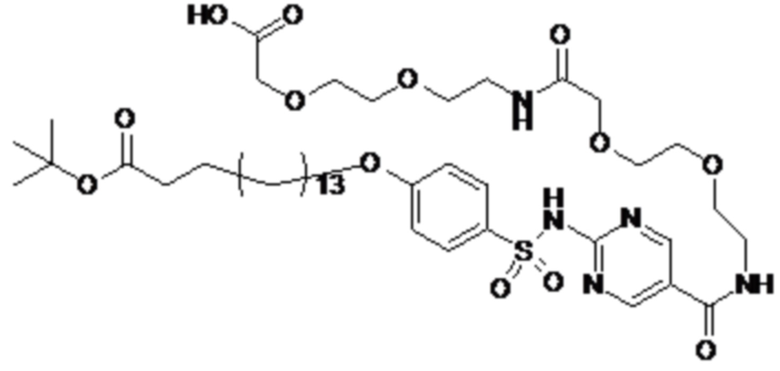
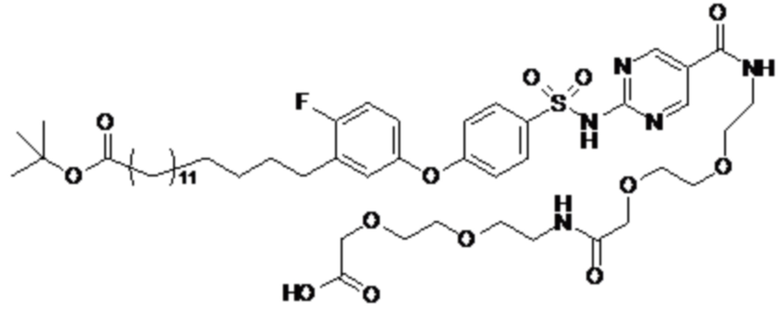
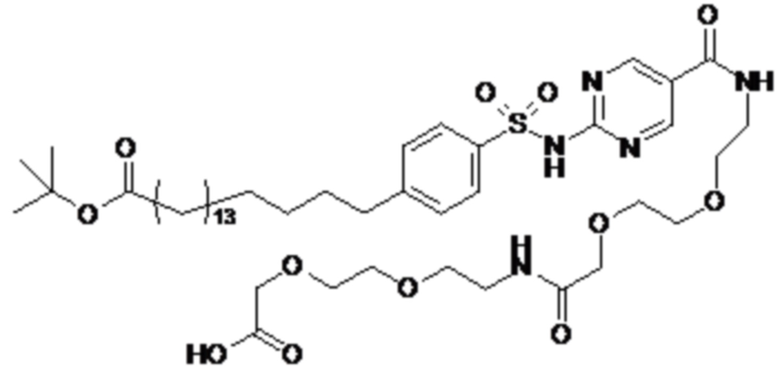
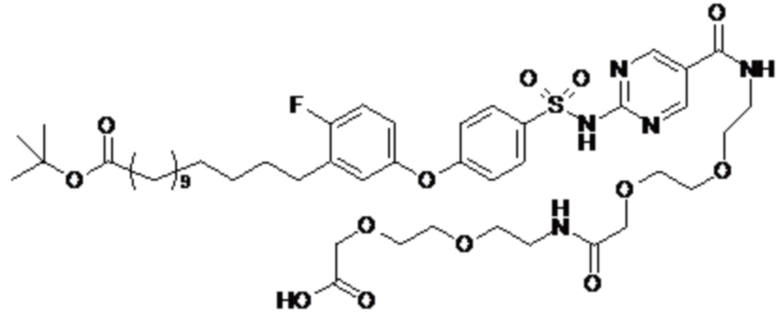
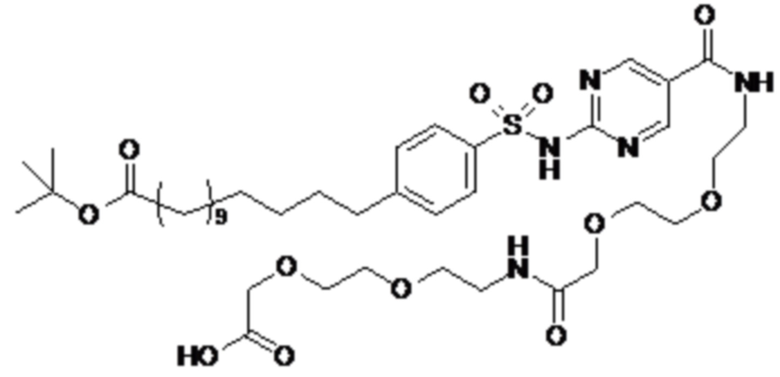
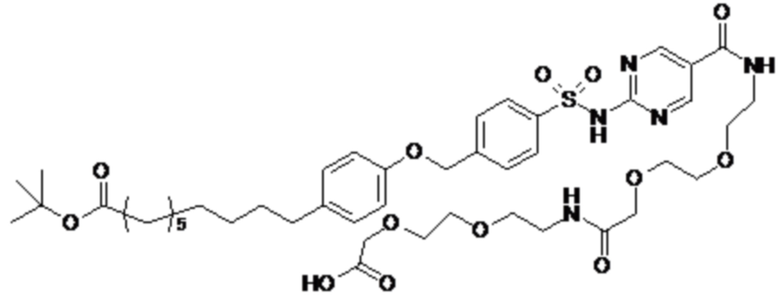
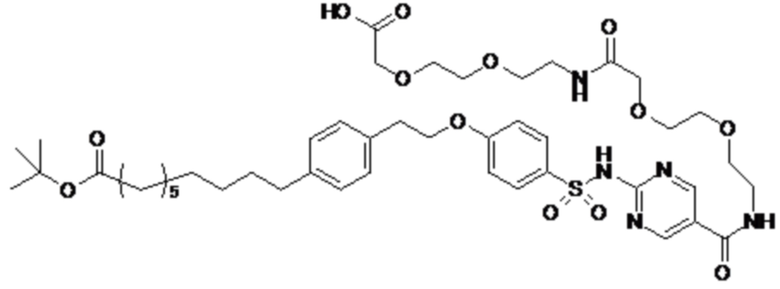
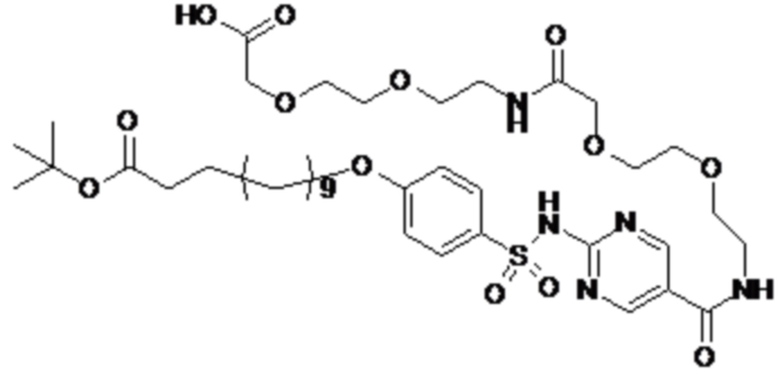
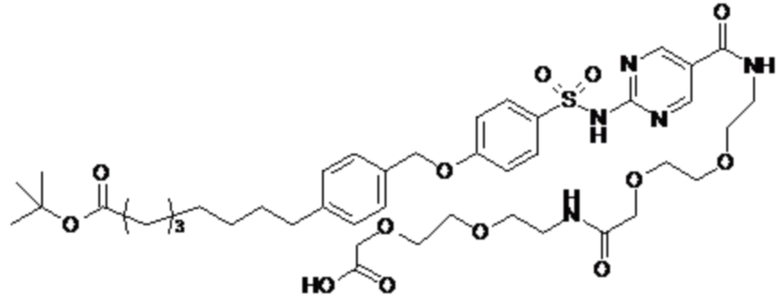
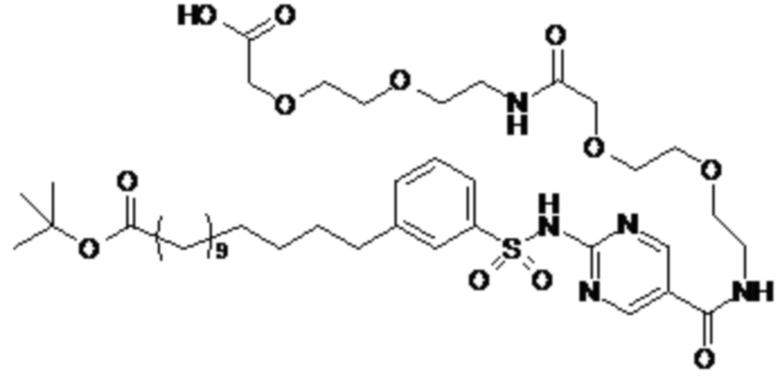
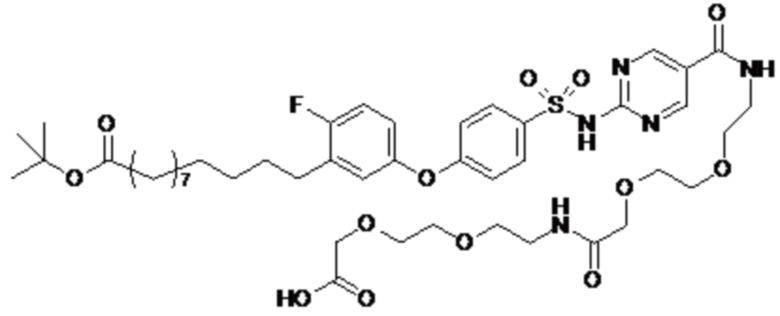
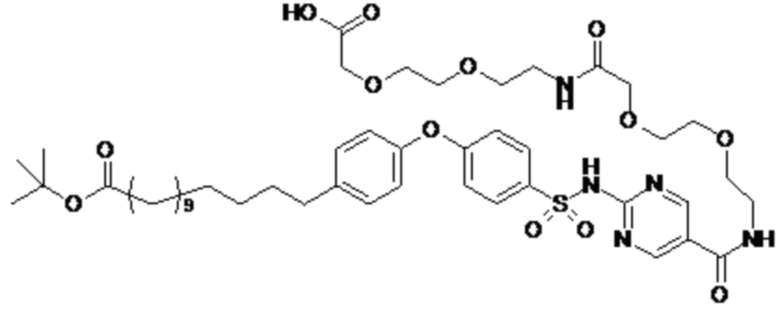
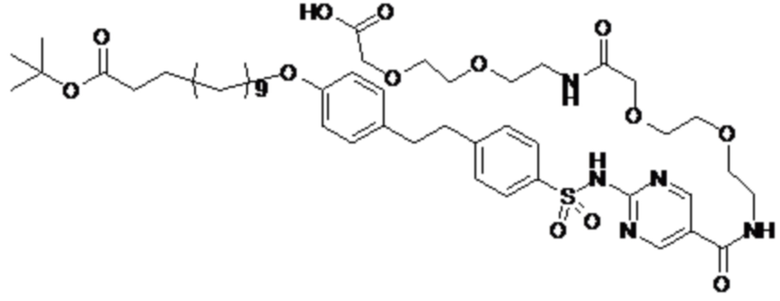
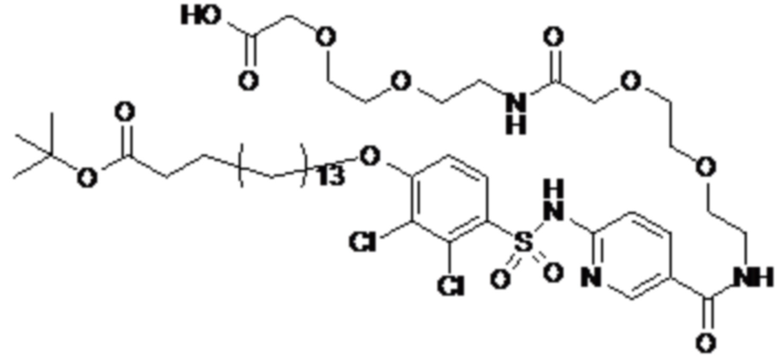
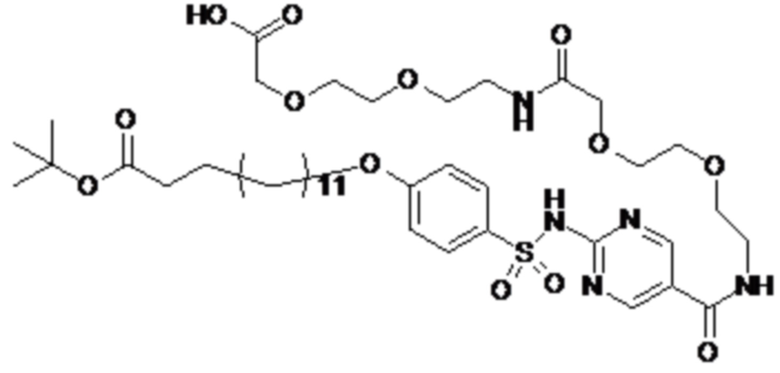
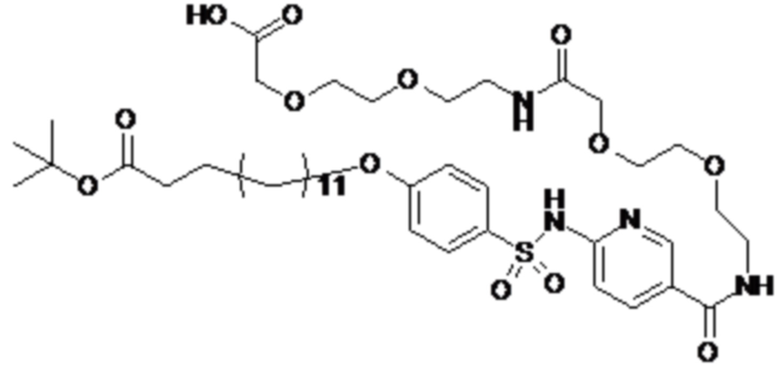
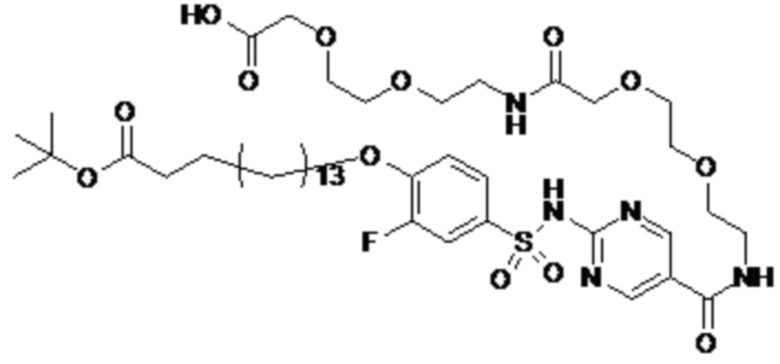
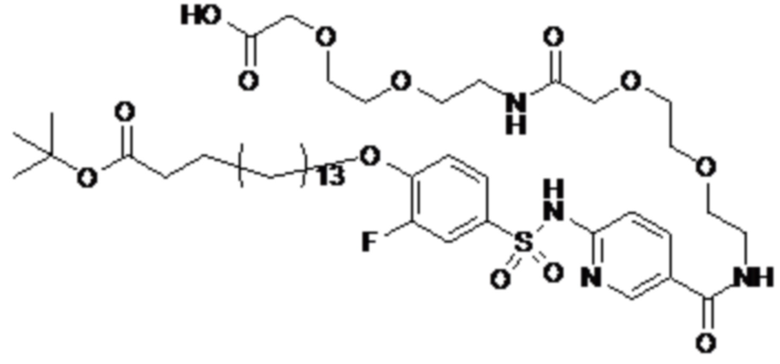
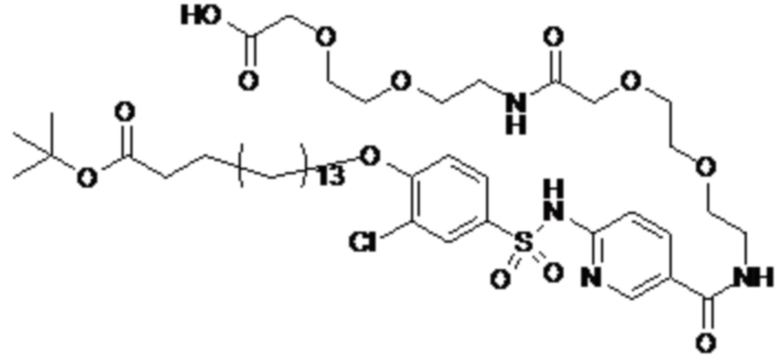
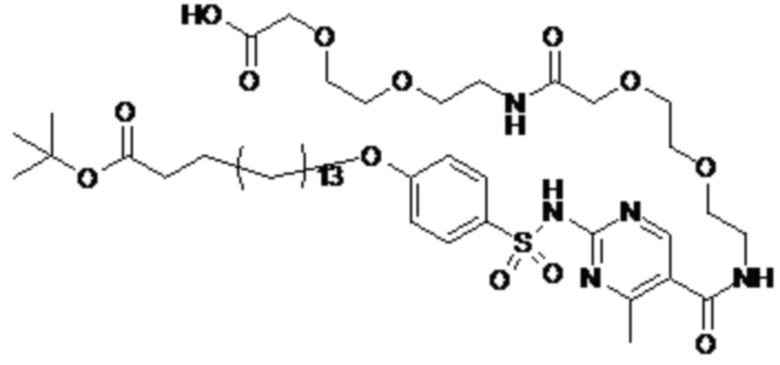
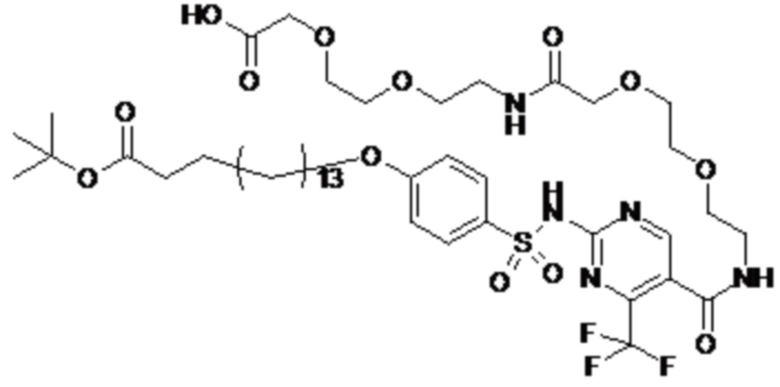
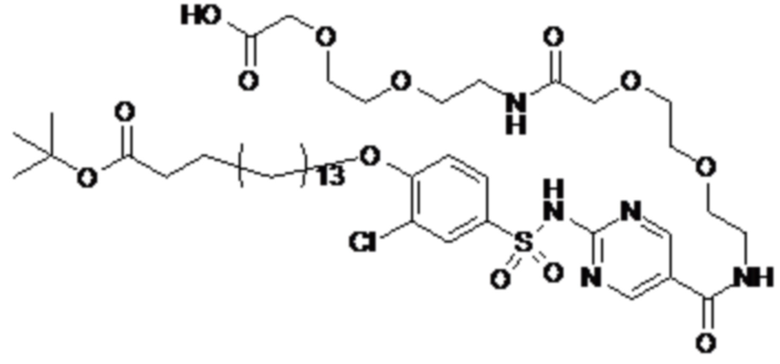
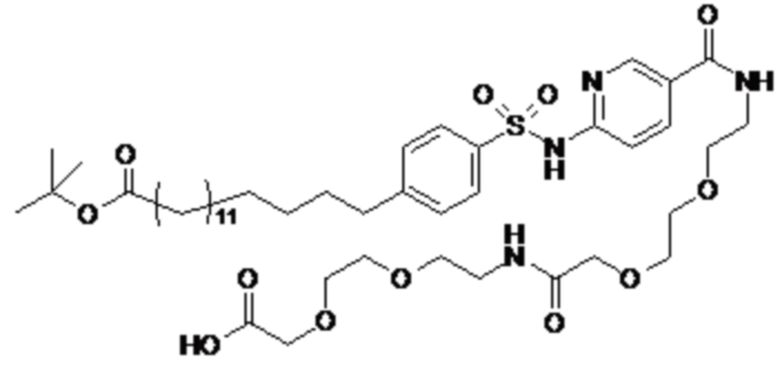
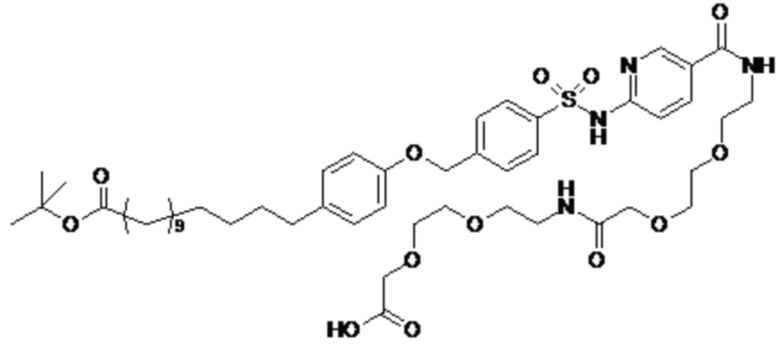
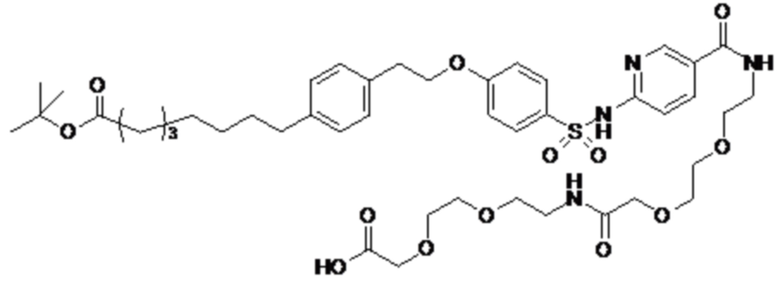
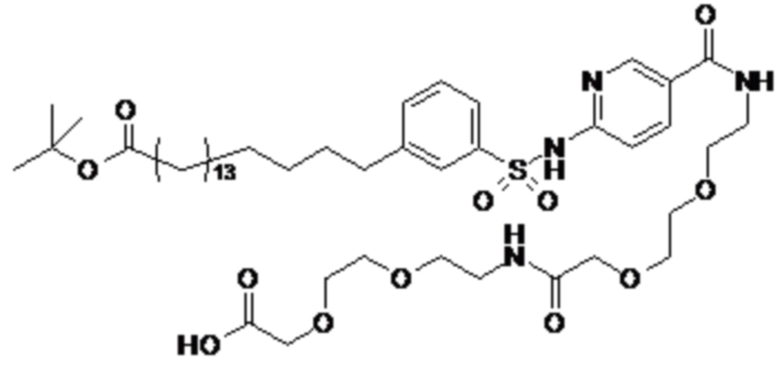
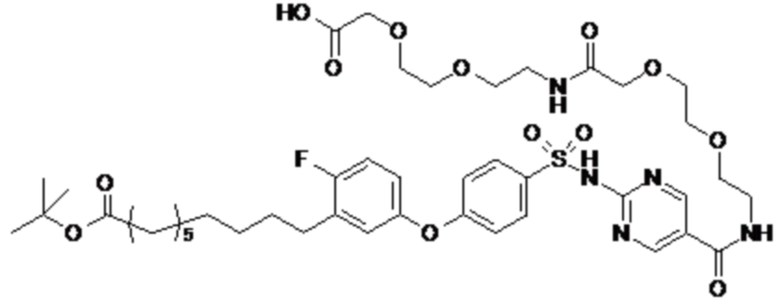
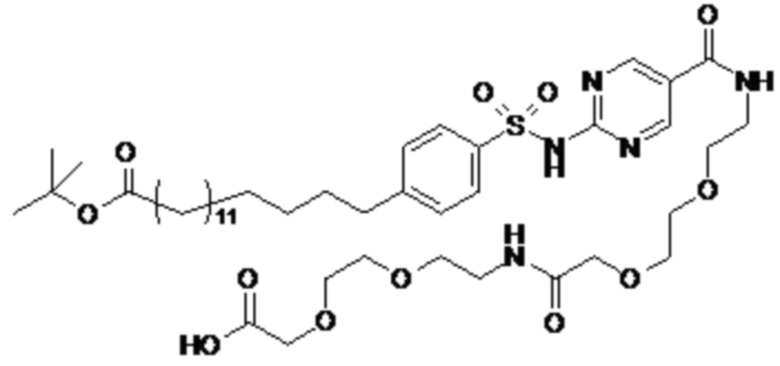
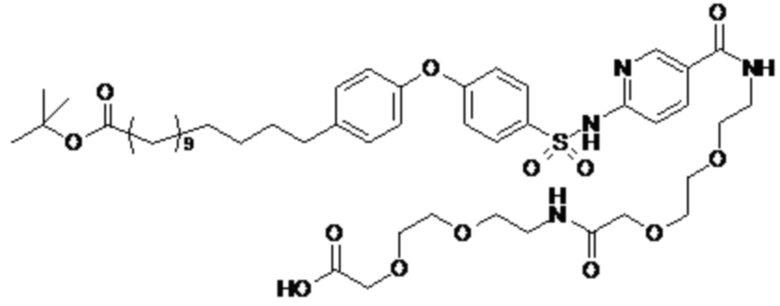
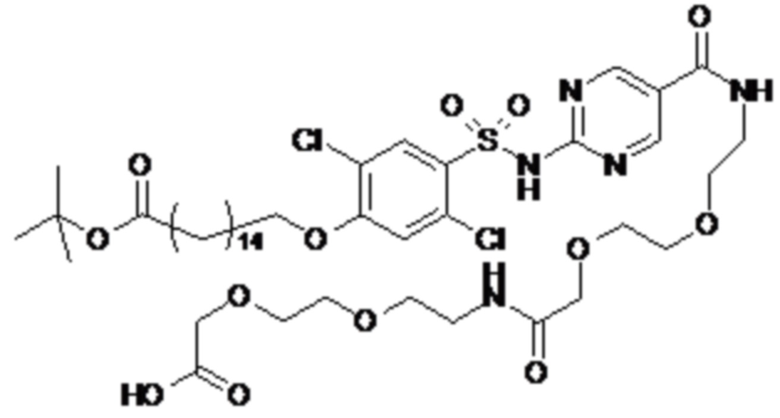
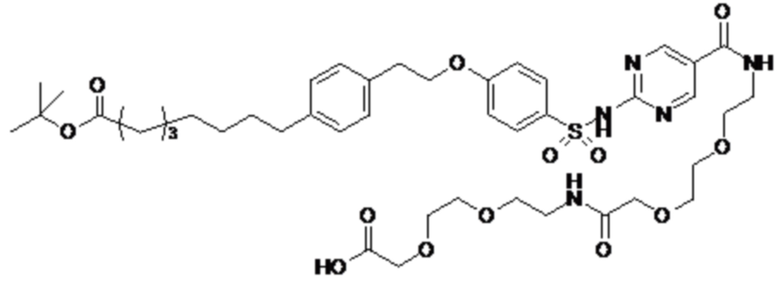
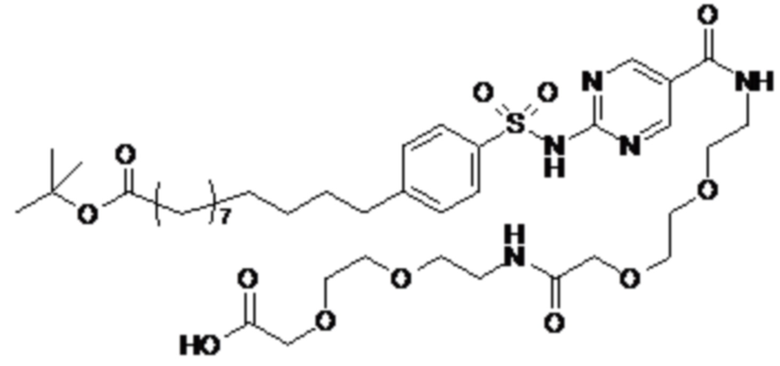
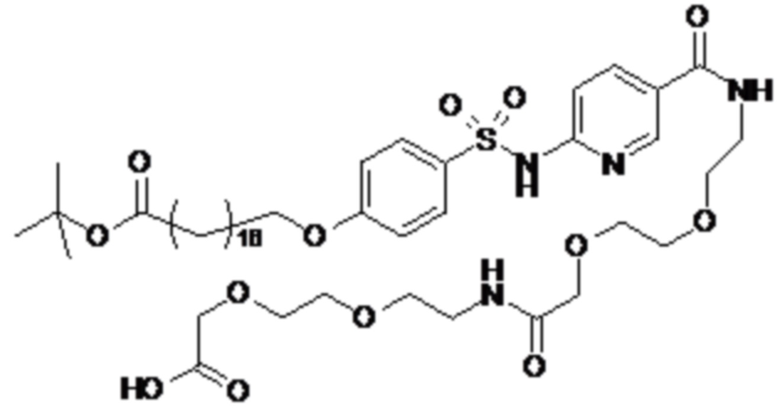
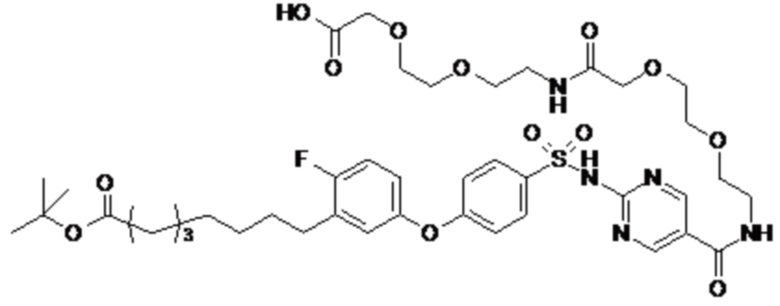
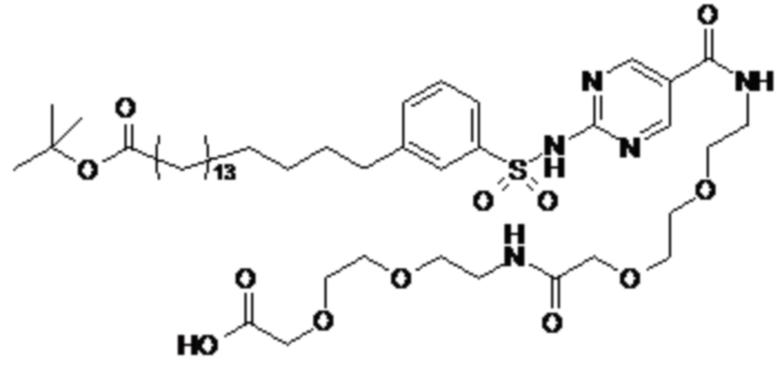
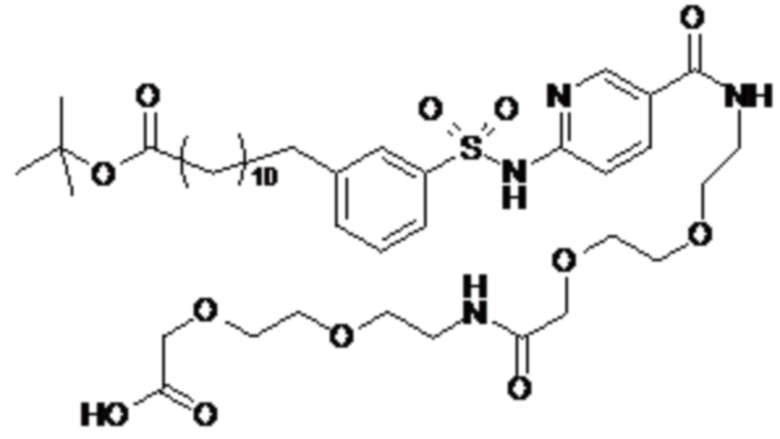
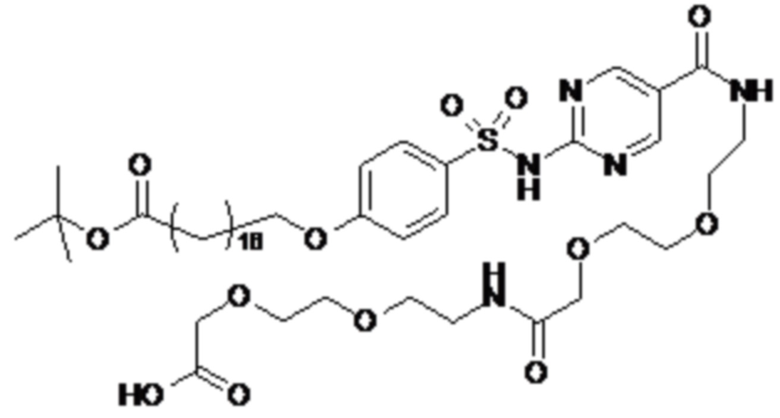
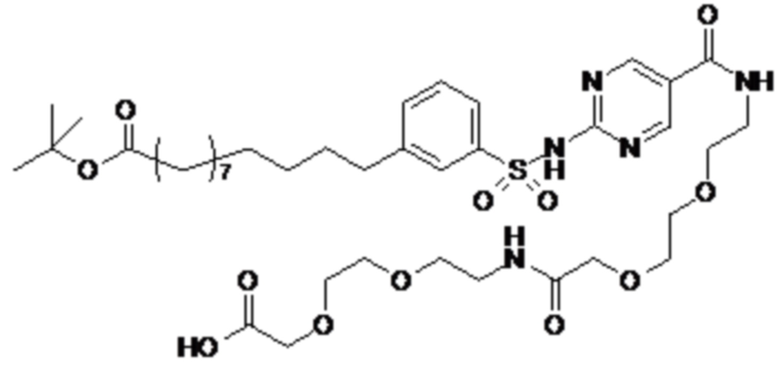
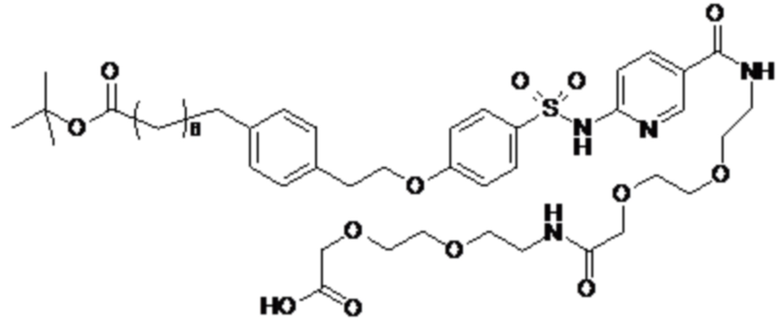
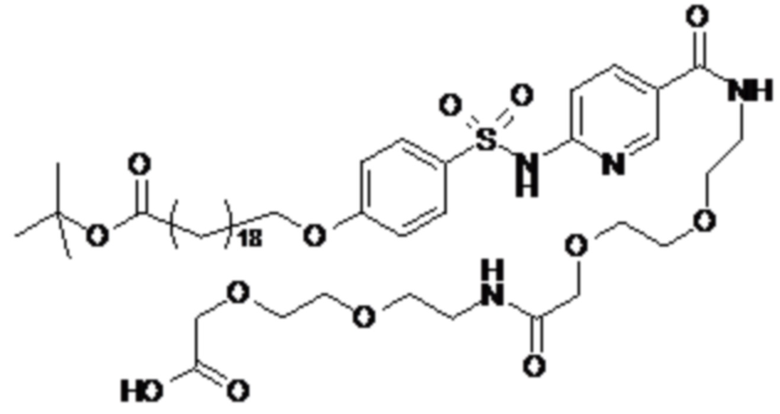
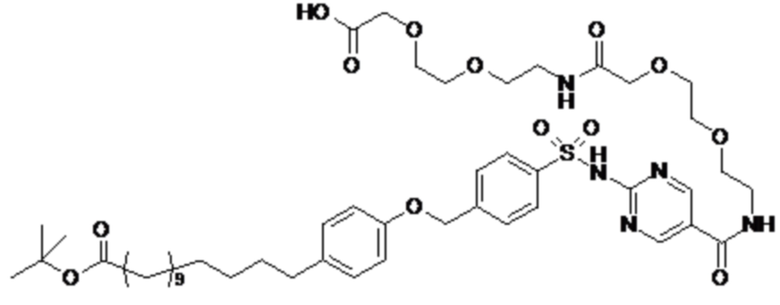
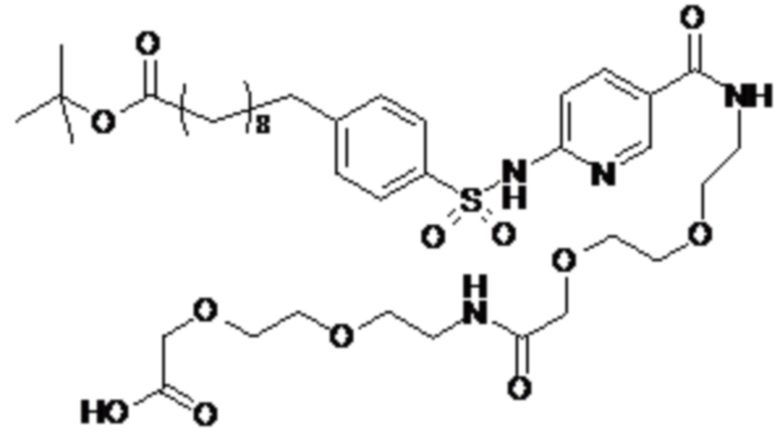
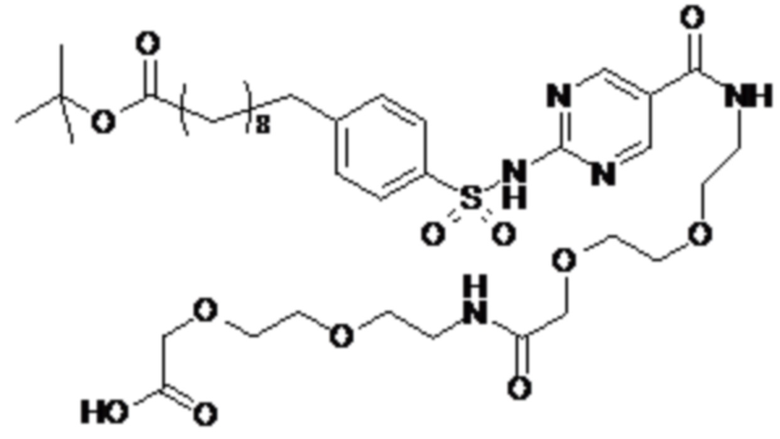
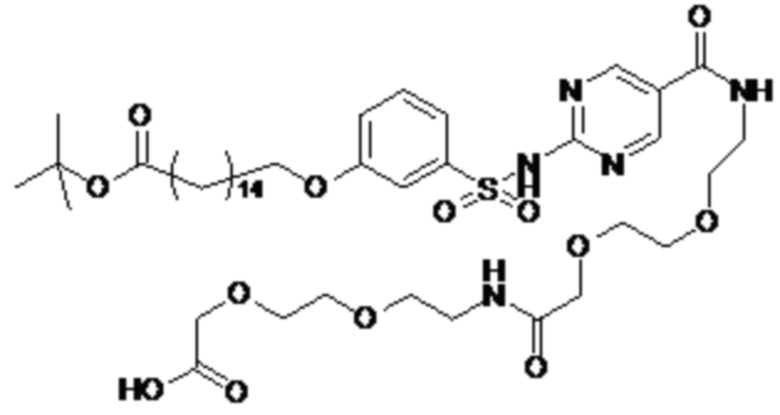
2.9.2 Синтез 2-[2-[2-[[2-[2-[2-[6-[[5-[[4-(16-трет-бутокси-16-оксогексадекокси)фенил]сульфониламино]пиримидин-2-карбонил]амино]гексаноиламино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты
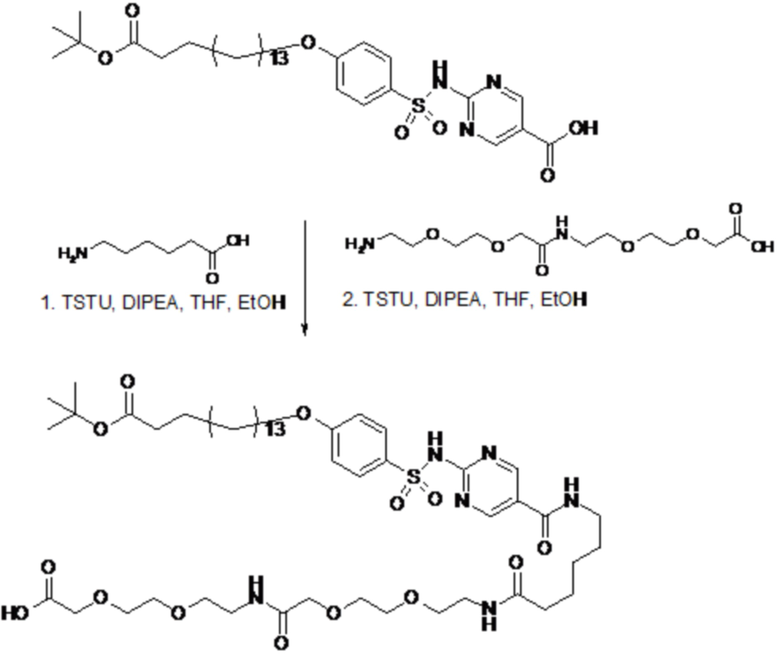
Смесь 5-[[4-(16-трет-Бутокси-16-оксогексадекокси)фенил]сульфониламино]пиримидин-2-карбоновой кислоты (500 мг, 825 мкмоль), TSTU (310 мг, 1,0 ммоль) и DIPEA (360 мкл, 266 мг, 2,06 ммоль) в 6 мл THF перемешивали при к. т. в течение 16 часов. Через 16 часов растворитель удаляли при пониженном давлении и добавляли раствор 6-аминогексановой кислоты (130 мг, 990 мкмоль) и DIPEA (360 мкл, 266 мг, 2,06 ммоль) в 6 мл абс. EtOH и смесь перемешивали при к. т. в течение 16 часов. Летучие компоненты удаляли при пониженном давлении, полученный остаток растворяли в CH2Cl2 и промывали водным 10% раствором KHSO4. Органический слой промывали с помощью воды и солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. 900 мг полученного неочищенного продукта 6-[[5-[[4-(16-трет-бутокси-16-оксогексадекокси)фенил]сульфониламино]пиримидин-2-карбонил]амино]гексановой кислоты использовали на следующем этапе без дополнительной очистки.
Смесь 6-[[5-[[4-(16-трет-бутокси-16-оксогексадекокси)фенил]сульфониламино]пиримидин-2-карбонил]амино]гексановой кислоты (900 мг неочищенного продукта, чистота 65%, 814 мкмоль), TSTU (306 мг, 1,02 ммоль) и DIPEA (355 мкл, 262 мг, 2,03 ммоль) в 6 мл THF перемешивали при к. т. в течение 16 часов. Через 16 часов растворитель удаляли при пониженном давлении и добавляли раствор 2-[2-[2-[[2-[2-(2-аминоэтокси)этокси]ацетил]амино]этокси]этокси]уксусной кислоты (301 мг, 976 мкмоль) и DIPEA (355 мкмоль, 262 мг, 2,03 ммоль) в 6 мл абс. EtOH и смесь перемешивали при к. т. в течение 16 часов. Летучие компоненты удаляли при пониженном давлении, полученный остаток растворяли в CH2Cl2 и промывали водным 10% раствором KHSO4. Органический слой промывали с помощью воды и солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали с помощью RP HPLC с получением 2-[2-[2-[[2-[2-[2-[6-[[5-[[4-(16-трет-бутокси-16-оксо-гексадекокси)фенил]сульфониламино]пиримидин-2-карбонил]амино]гексаноиламино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты (78 мг, 10%).
1H ЯМР (400,23 МГц, DMSO-d6) δ ppm 12,29 (br s, 1 H), 8,82 (s, 2 H), 8,47 (br s, 1 H), 7,90 (d, J=8,93 Гц, 2 H), 7,79 (t, J=5,50 Гц, 1 H), 7,63 (t, J=5,75 Гц, 1 H), 7,07 (d, J=8,93 Гц, 2 H), 4,01 (m, 4 H), 3,87 (s, 2 H), 3,20-3,68 (m, 18 H), 2,15 (t, J=7,27 Гц, 2 H), 2,05 (t, J=7,34 Гц, 2 H), 1,70 (m, 2 H), 1,48 (m, 6 H), 1,38 (s, 9 H), 1,25 (m, 24 H).
Следующее соединение синтезировали соответственно.
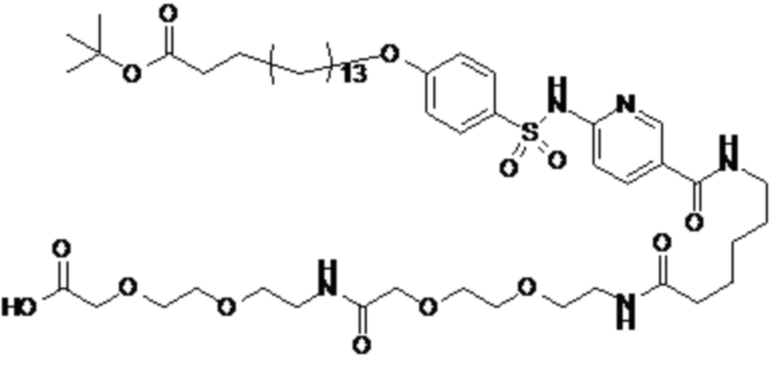
2.10 Включение веществ (2)
2.10.1 Синтез 2-[2-[2-[[2-[2-[2-[3-[[5-[[4-[4-(14-трет-бутокси-14-оксо-тетрадецил)фенокси]фенил]сульфониламино]пиримидин-2-карбонил]амино]пропаноиламино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты
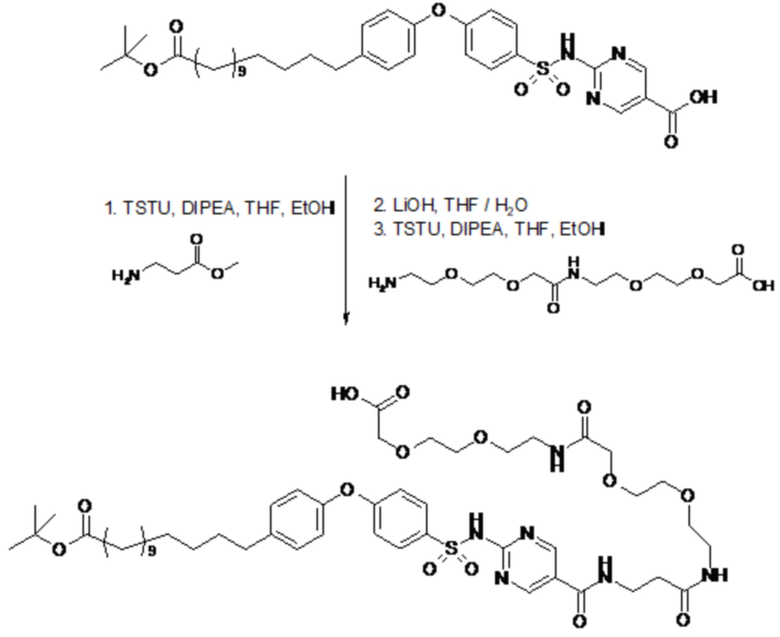
2.10.2 Синтез трет-бутил-14-[4-[4-[[5-[(3-метокси-3-оксопропил)карбамоил]пиримидин-2-ил]сульфамоил]фенокси]фенил]тетрадеканоата
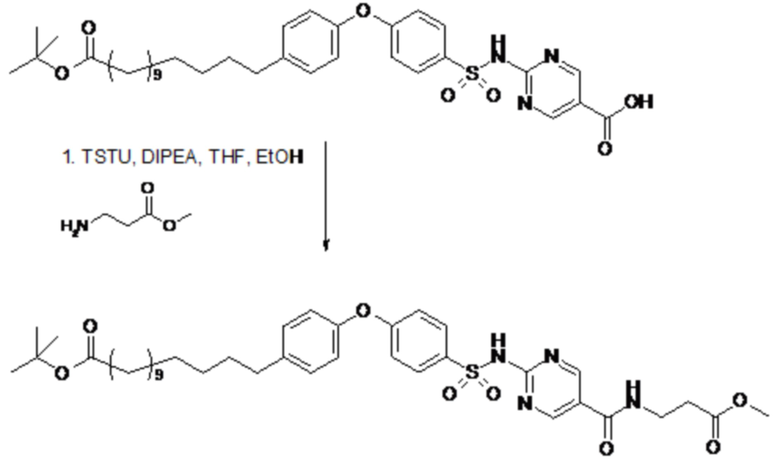
Смесь 5-[[4-[4-(14-трет-бутокси-14-оксо-тетрадецил)фенокси]фенил]сульфониламино]пиримидин-2-карбоновой кислоты (1,0 г, 764 мкмоль), TSTU (241 мг , 803 мкмоль) и DIPEA (494 мг, 3,82 ммоль) в 10 мл THF перемешивали при к. т. в течение 16 часов. Добавляли дополнительное количество TSTU (80 мг, 267 мкмоль) и перемешивание при к. т. продолжали в течение 2 часов. Добавляли гидрохлорид метил-3-аминопропаноата (117 мг, 841 мкмоль) и перемешивание при к. т. продолжали в течение 16 часов. Летучие компоненты удаляли при пониженном давлении, полученный остаток растворяли в CH2Cl2 и промывали водным 10% раствором KHSO4. Органический слой промывали с помощью воды и солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали посредством препаративной HPLC с обращенной фазой с получением 14-[4-[4-[[5-[(3-метокси-3-оксопропил)карбамоил]пиримидин-2-ил]сульфамоил]фенокси]фенил]тетрадеканоата (235 мг, 42%).
1H ЯМР (400,23 МГц, DMSO-d6) δ ppm 12,11 (br s, 1 H), 8,84 (s, 2 H), 8,66 (t, J=5,44 Гц, 1 H), 7,98 (d, J=8,93 Гц, 2 H), 7,26 (d, J=8,44 Гц, 2 H), 7,04 (m, 4 H), 3,60 (s, 3 H), 3,46 (m, 2H), 2,57 (m, 4 H), 2,15 (t, J=7,27 Гц, 2 H), 1,56 (m, 2 H), 1,46 (m, 2 H), 1,38 (s, 9 H), 1,29 (m, 18 H).
2.10.3 Синтез 2-[2-[2-[[2-[2-[2-[3-[[5-[[4-[4-(14-трет-бутокси-14-оксо-тетрадецил)фенокси]фенил]сульфониламино]пиримидин-2-карбонил]амино]пропаноиламино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты
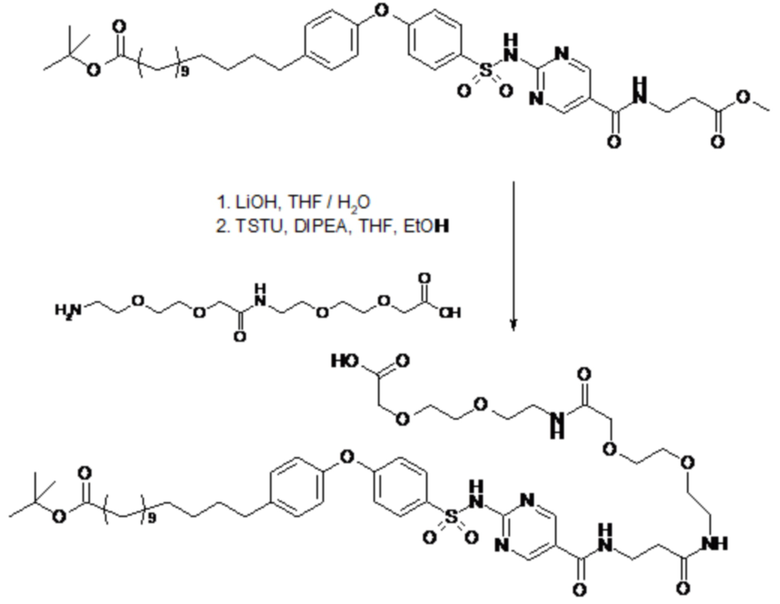
Смесь 14-[4-[4-[[5-[(3-метокси-3-оксопропил)карбамоил]пиримидин-2-ил]сульфамоил]фенокси]фенил]тетрадеканоата (235 мг, 318 мкмоль), LiOH (38 мг, 1,59 ммоль), THF (5 мл) и H2O (5 мл) перемешивали при к. т. в течение 2 часов. Реакционную смесь подкисляли до прибл. pH=1,0 с помощью HCl (2,0 M) и экстрагировали CH2Cl2. Органический слой промывали солевым раствором, высушивали над Na2SO4, фильтровали и концентрировали с получением 3-[[5-[[4-[4-(14-трет-бутокси-14-оксо-тетрадецил)фенокси]фенил]сульфониламино]пиримидин-2-карбонил]амино]пропановой кислоты (207 мг, выход 89%) в виде белого твердого вещества, которое использовали в следующей реакции без дополнительной очистки.
Смесь 3-[[5-[[4-[4-(14-трет-бутокси-14-оксотетрадецил)фенокси]фенил]сульфониламино]пиримидин-2-карбонил]амино]пропановой кислоты (207 мг, 285 мкмоль), TSTU (90 мг, 300 мкмоль) и DIPEA (150 мкл, 110 мг, 850 мкмоль) в 6 мл THF перемешивали при к. т. в течение 1 часа. Через 1 час растворитель удаляли при пониженном давлении и добавляли раствор 2-[2-[2-[[2-[2-(2-аминоэтокси)этокси]ацетил]амино]этокси]этокси]уксусной кислоты (97 мг, 314 мкмоль) и DIPEA (150 мкл, 110 мг, 850 мкмоль) в 6 мл абс. EtOH и смесь перемешивали при к. т. в течение 16 часов. Летучие компоненты удаляли при пониженном давлении, полученный остаток растворяли в CH2Cl2 и промывали водным 10% раствором KHSO4. Органический слой промывали с помощью воды и солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали с помощью RP HPLC с получением 2-[2-[2-[[2-[2-[2-[3-[[5-[[4-[4-(14-трет-бутокси-14-оксо-тетрадецил)фенокси]фенил]сульфониламино]пиримидин-2-карбонил]амино]пропаноиламино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты (163 мг, 56%).
1H ЯМР (400,23 МГц, DMSO-d6) δ ppm 12,11 (br s, 2 H), 8,84 (s, 2 H), 8,61 (t, J= 5,62 Гц, 1 H), 7,97 (m, 3 H), 7,62 (t, J=5,56 Гц, 1 H), 7,26 (d, J=8,44 Гц, 2 H), 7,04 (m, 4 H), 4,01 (s, 2 H), 3,86 (s, 2 H), 3,20-3,60 (m, 18 H), 2,58 (m, 2 H), 2,34 (t, J=7,03 Гц, 2 H), 2,15 (t, J=7,27 Гц, 2 H), 1,56 (m, 2 H), 1,46 (m, 2 H), 1,38 (s, 9 H), 1,29 (m, 18 H).
2.11 Удаление защитных групп
Синтез 14-[5-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]-2-пиридил]сульфамоил]фенокси]-2-фторфенил]тетрадекановой кислоты
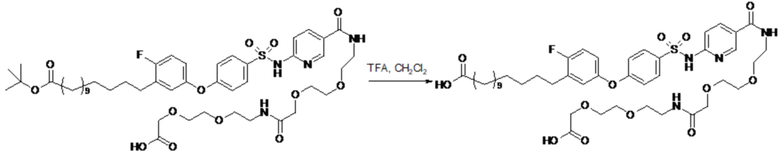
2-[2-[2-[[2-[2-[2-[[6-[[4-[3-(14-трет-Бутокси-14-оксо-тетрадецил)-4-фторфенокси]фенил]сульфониламино]пиридин-3-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусную кислоту (20 мг, 21 мкмоль) растворяли в DCM (3, 0 мл) и TFA (0,5 мл) добавляли при к. т. Перемешивание продолжали при к. т. в течение 16 часов. Летучие компоненты удаляли при пониженном давлении, полученный остаток растворяли в DCM и повторно выпаривали дважды. Неочищенный продукт очищали с помощью препаративной HPLC с обращенной фазой. Указанное в заголовке соединение 14-[5-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]-2-пиридил]сульфамоил]фенокси]-2-фторфенил]тетрадекановую кислоту получали в виде бесцветного твердого вещества (19 мг, 21 мкмоль, кол.).
1H ЯМР (400,23 МГц, DMSO-d6) δ ppm 12,19 (br s, 1 H), 8,51 (m, 2 H), 8,09 (dd, J=8,93, 2,32 Гц, 1 H), 7,89 (d, J=8,93 Гц, 2 H), 7,61 (br t, J=5,56 Гц, 1 H), 7,20 (t, J=8,93 Гц, 1 H), 7,15 (d, J=8,19 Гц, 1 H), 7,03 (m, 4 H), 4,01 (s, 2 H), 3,86 (s, 2 H), 3,20-3,68 (m, 16 H), 2,58 (br t, J=7,52 Гц, 2 H), 2,17 (t, J=7,34 Гц, 2 H), 1,49 (m, 4 H), 1,25 (m, 18 H).
Следующие соединения синтезировали соответственно.
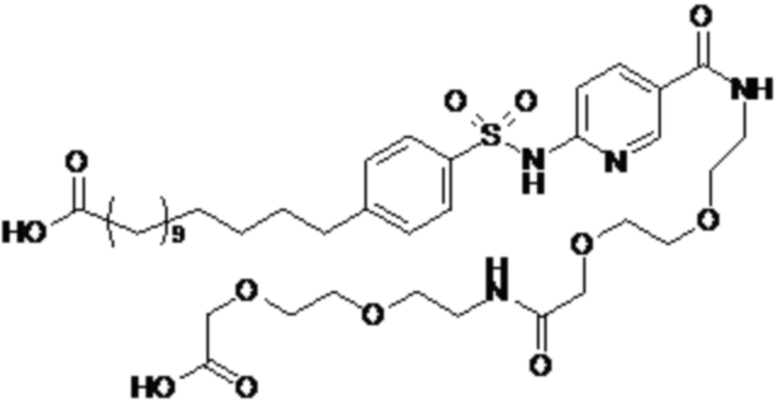
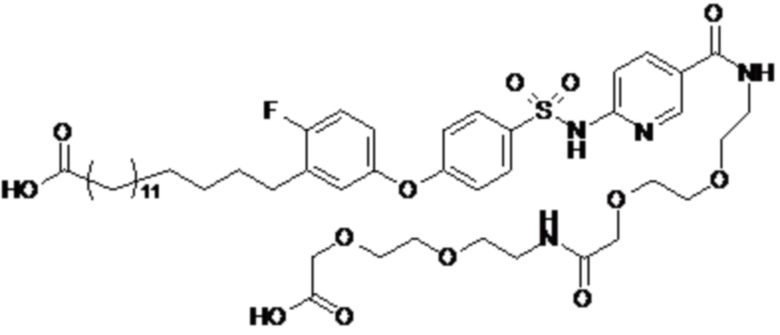
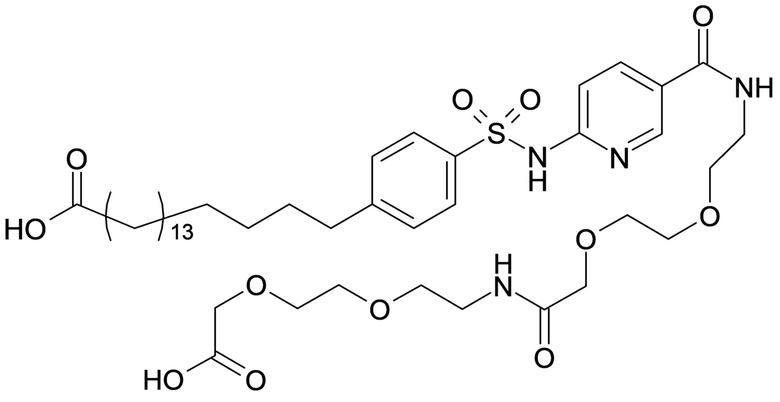
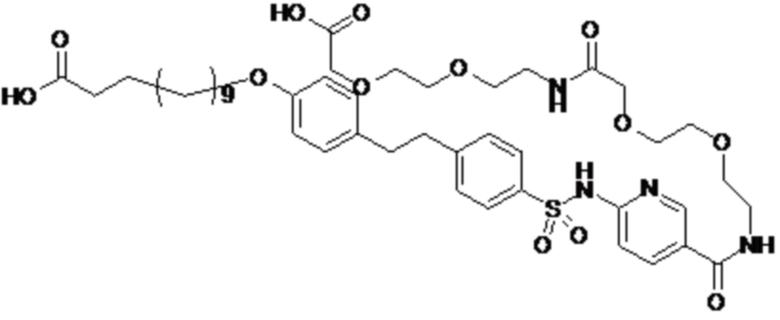
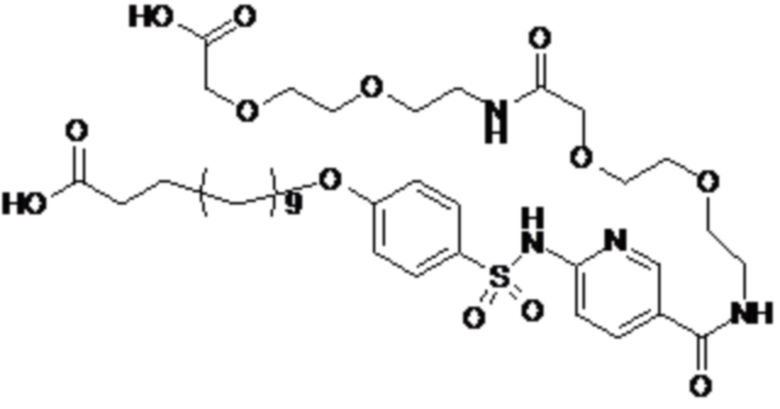
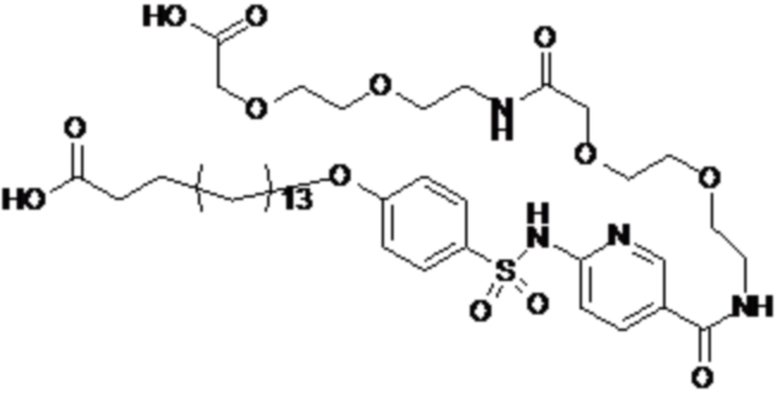
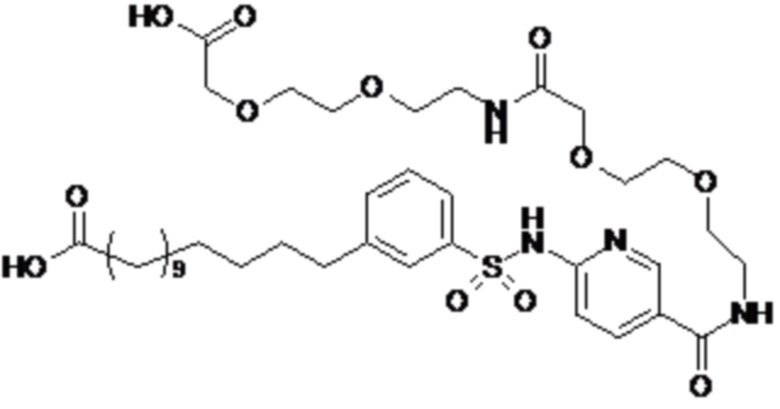
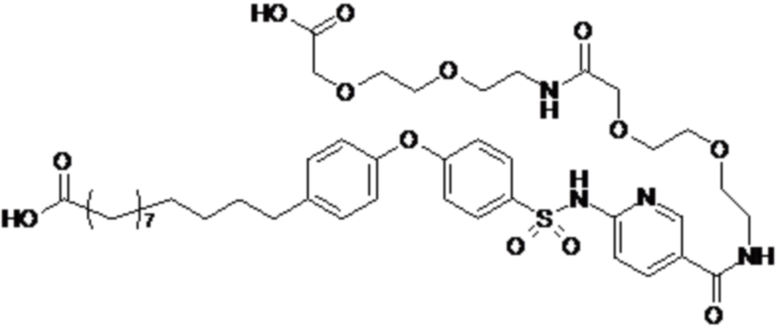
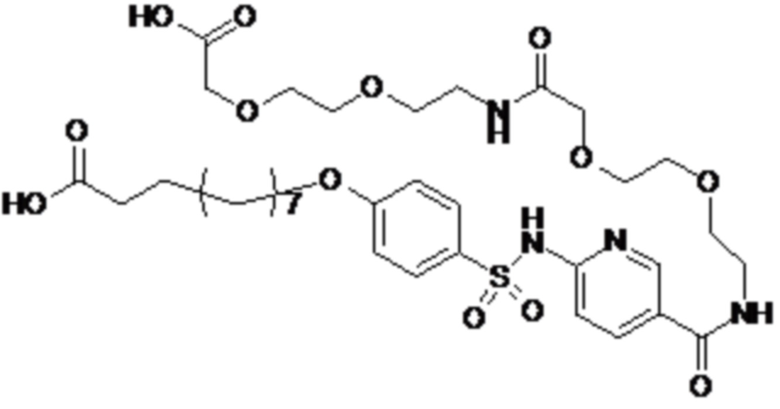
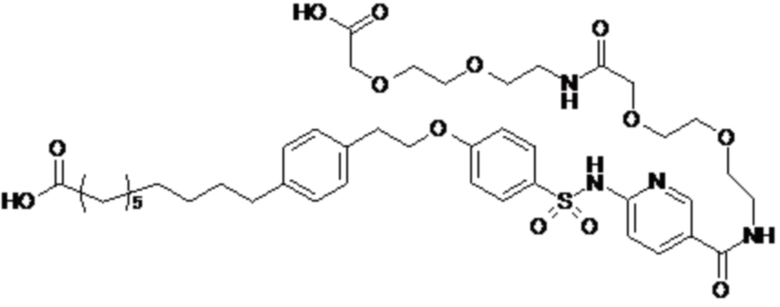
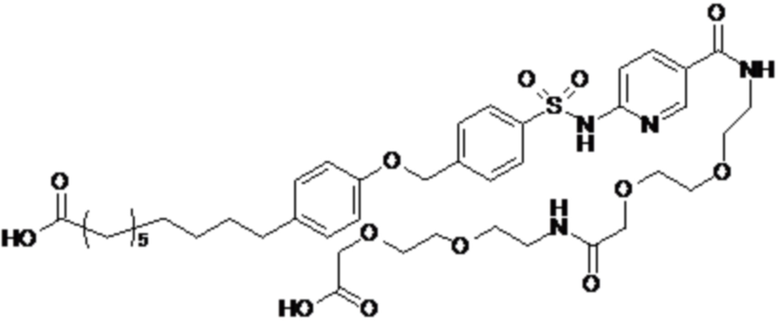
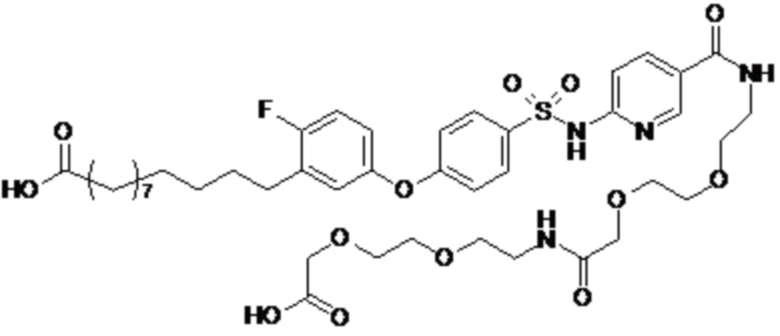
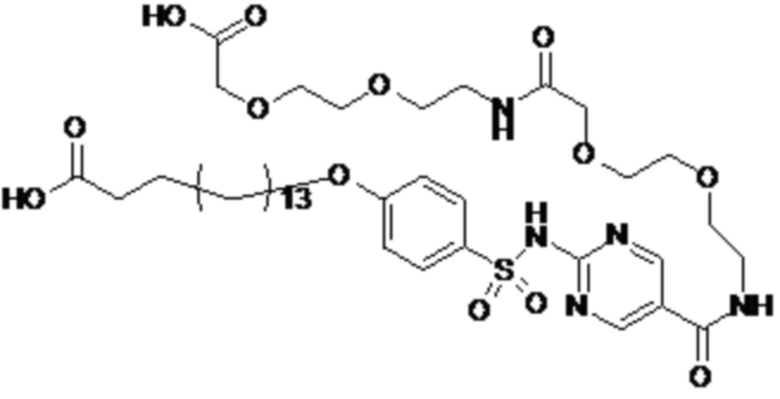
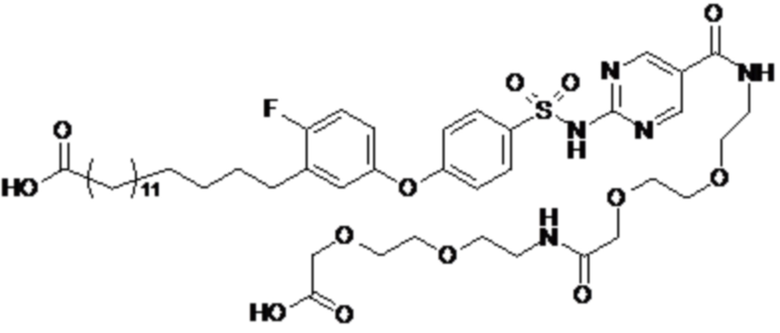
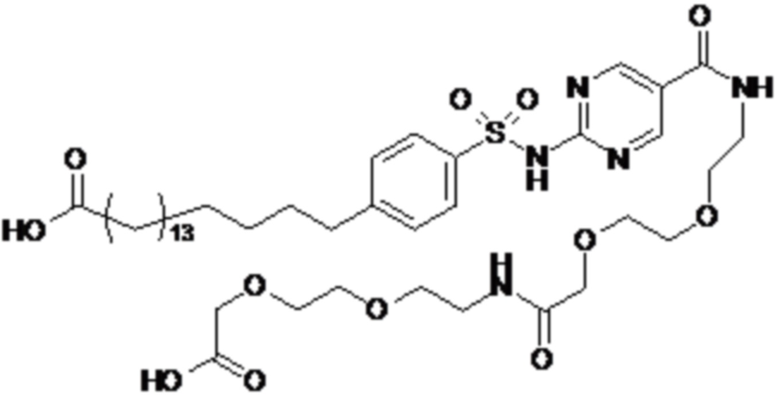
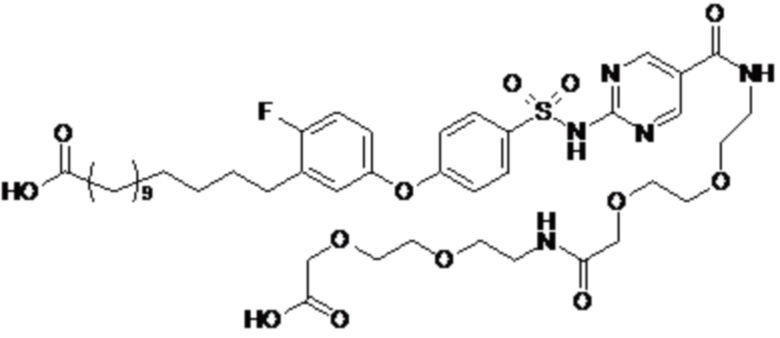
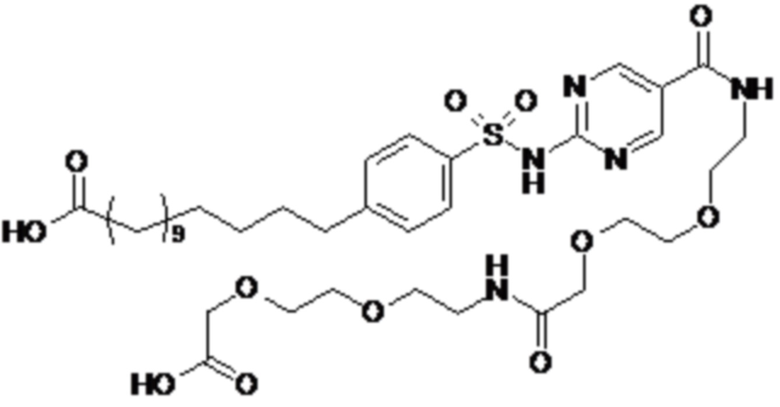
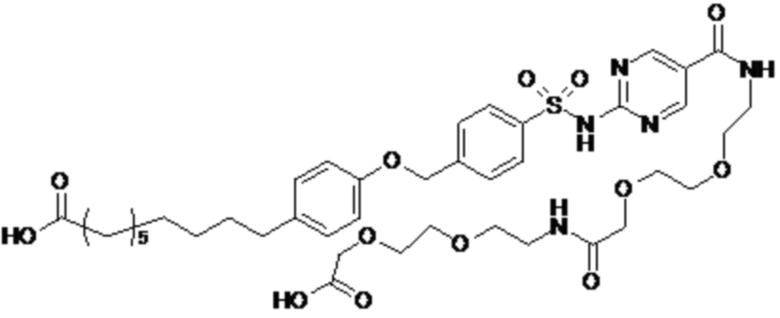
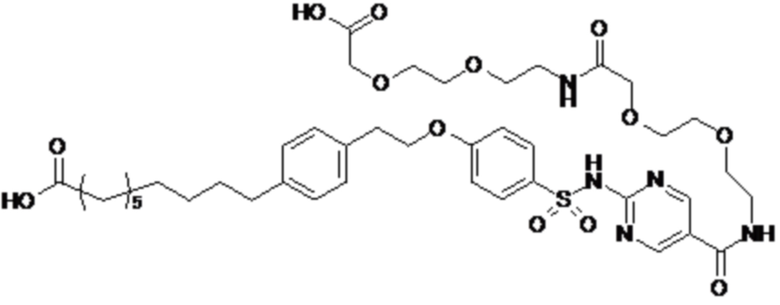
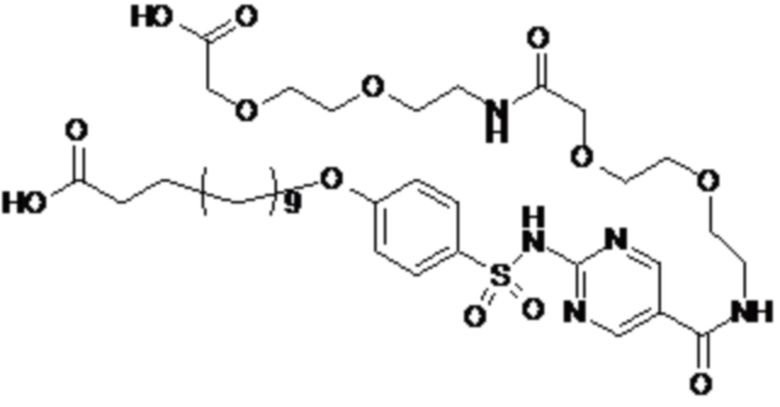
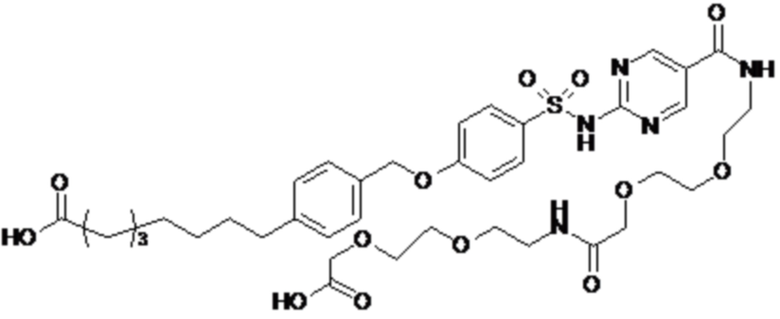
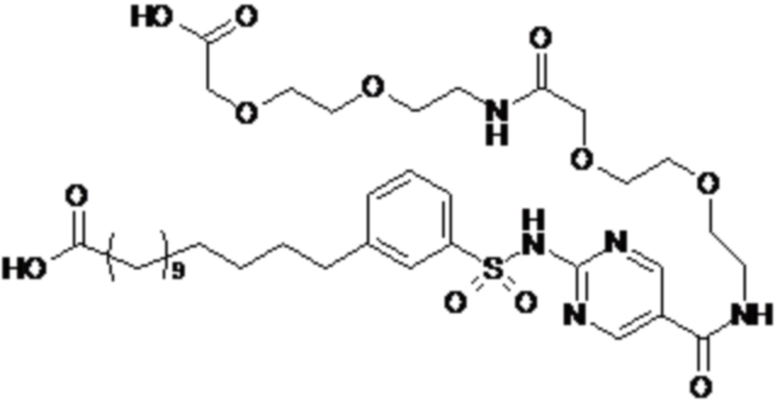
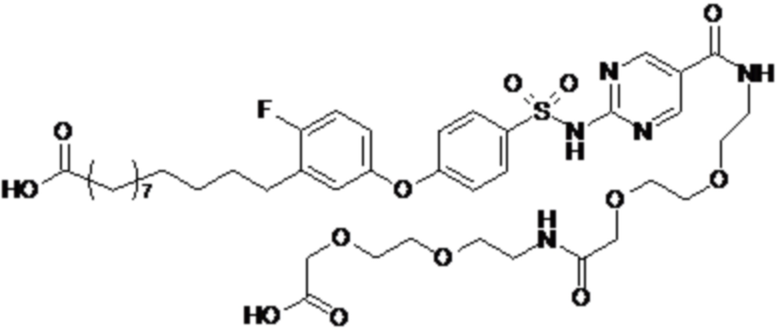
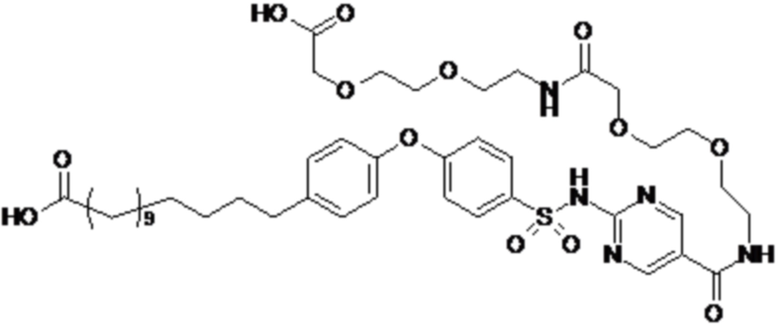
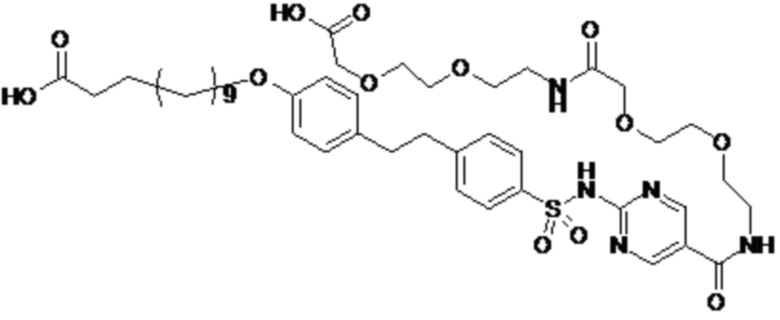
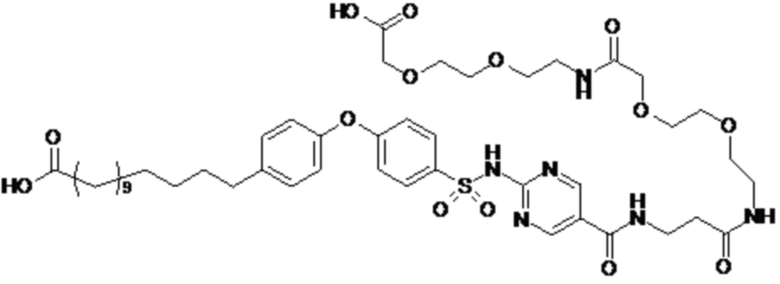
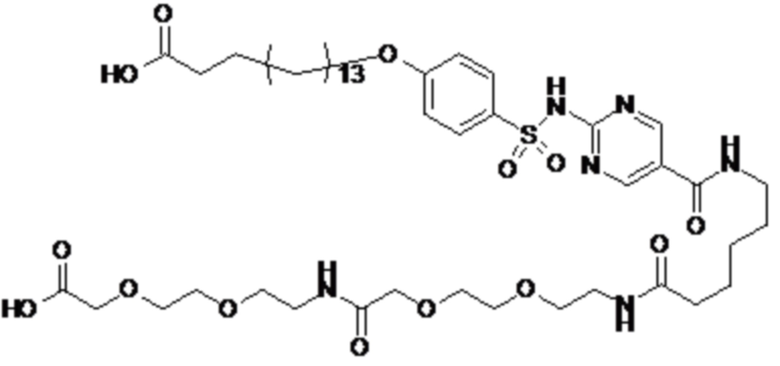
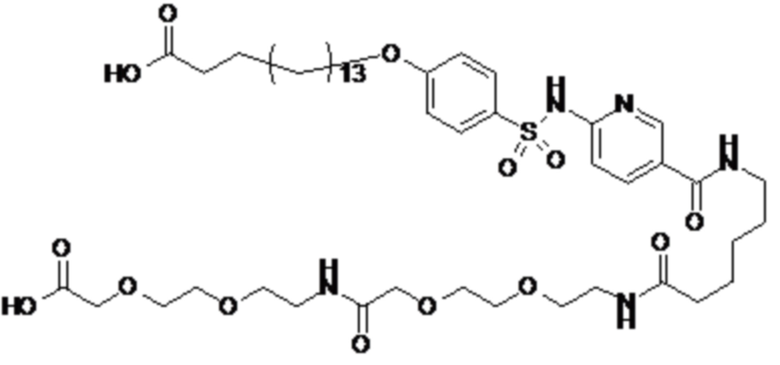
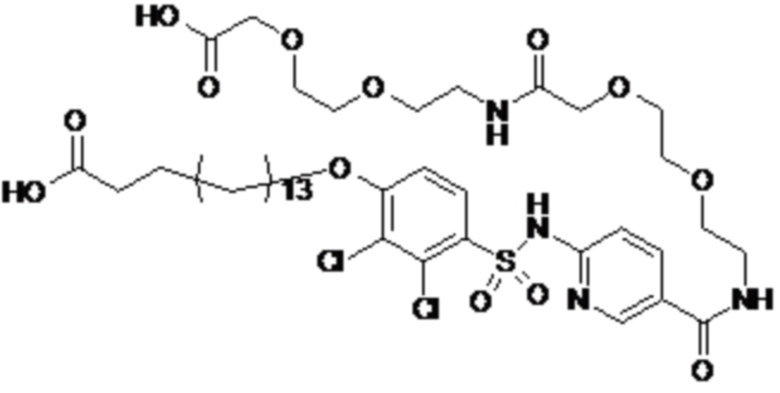
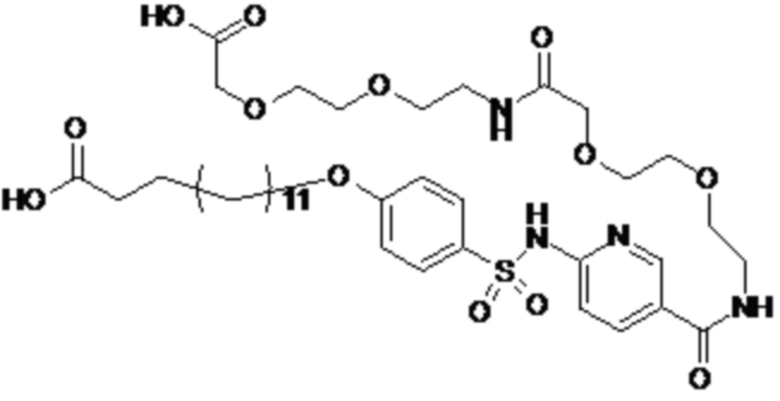
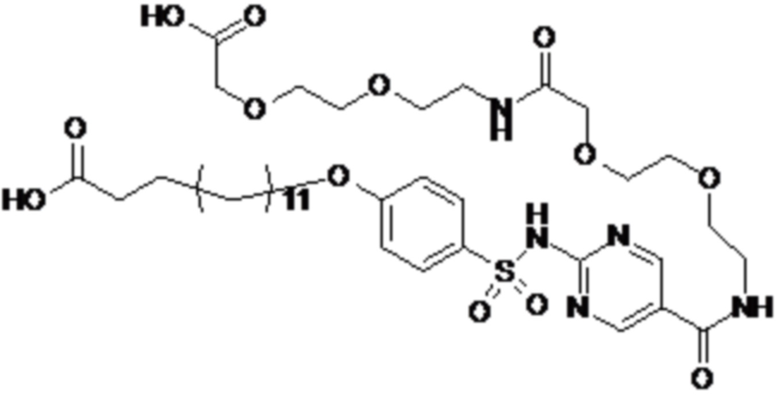
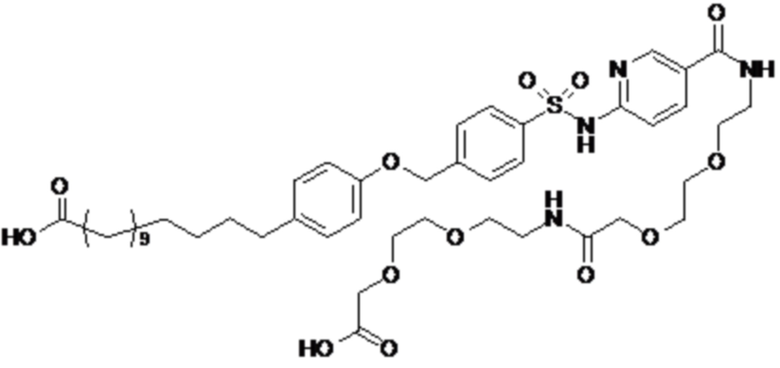
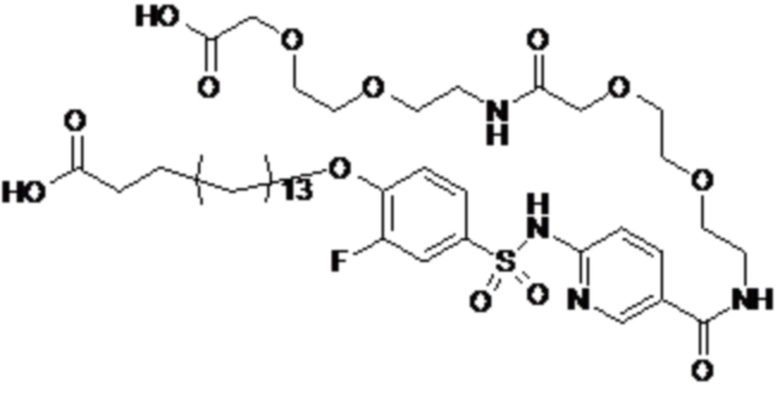
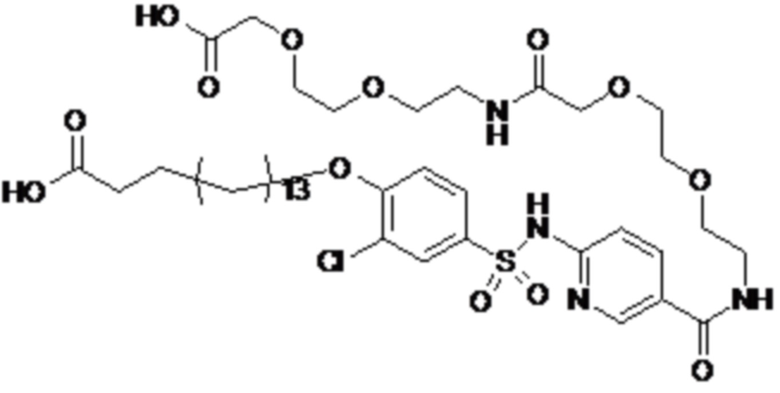
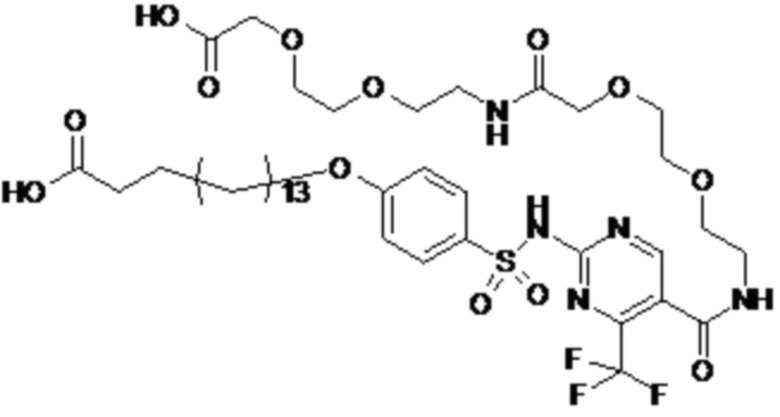
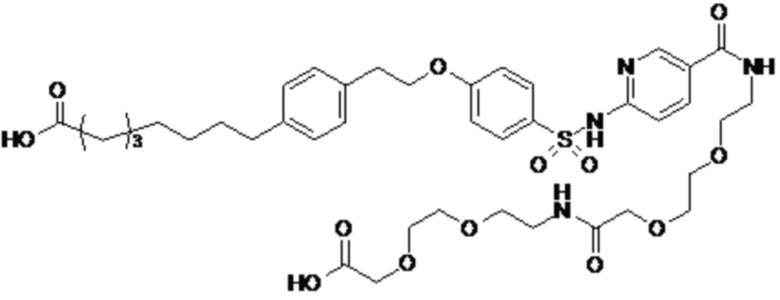
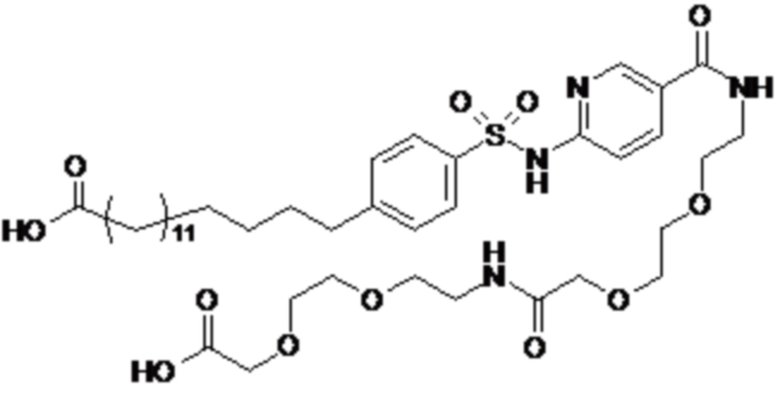
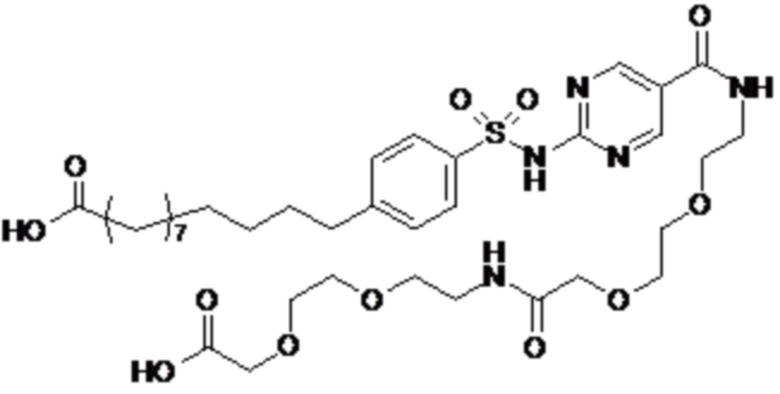
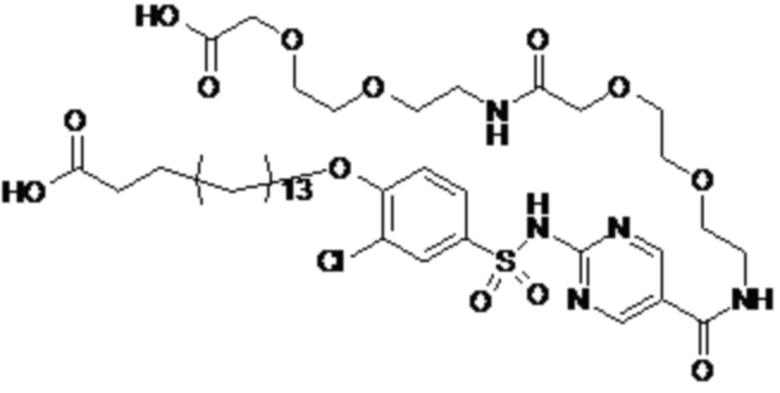
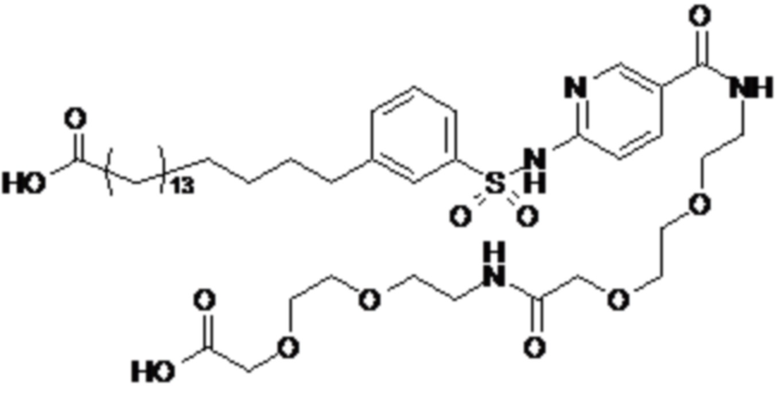
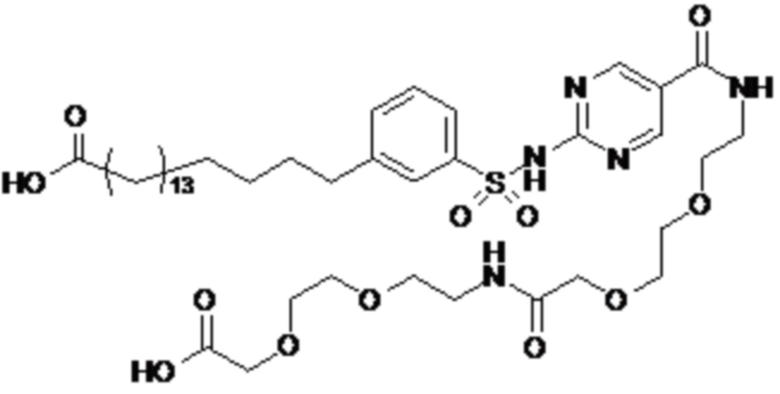
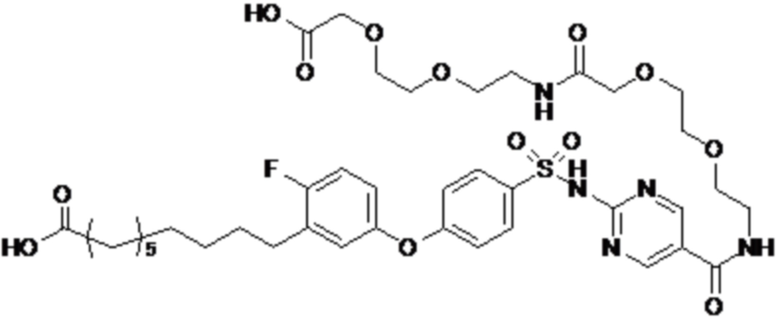
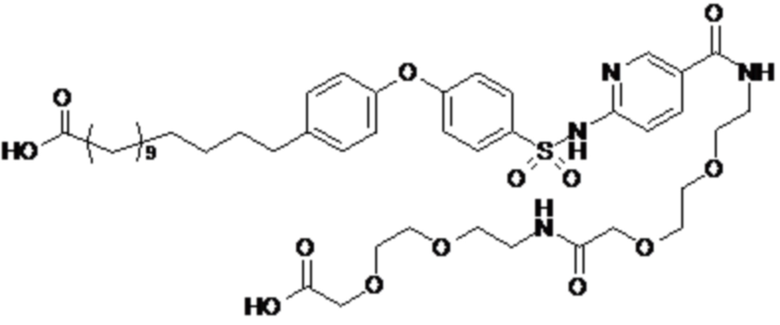
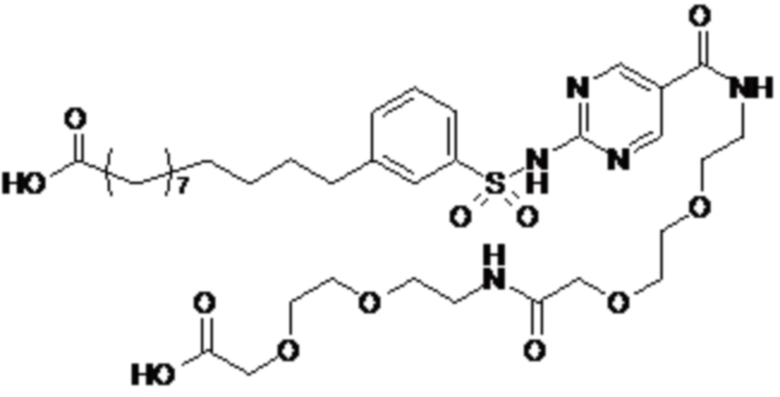
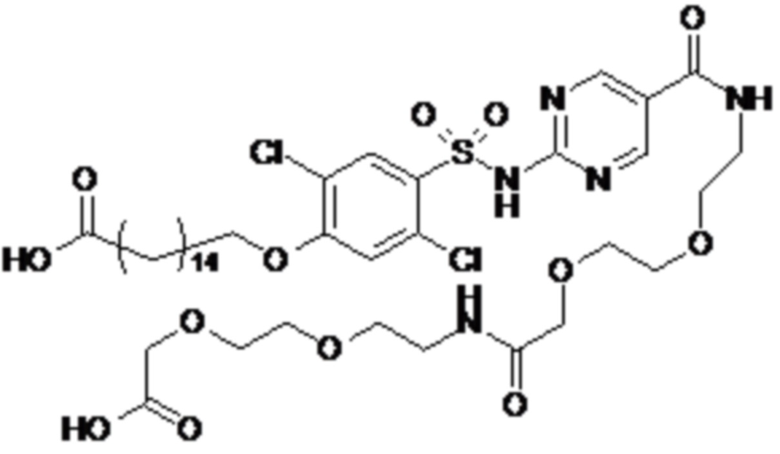
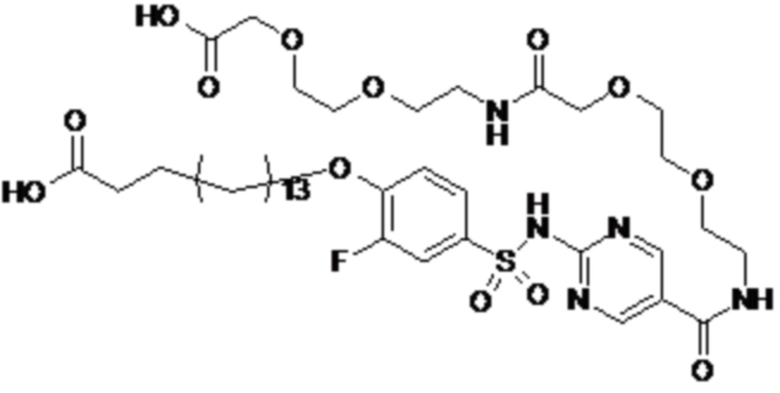
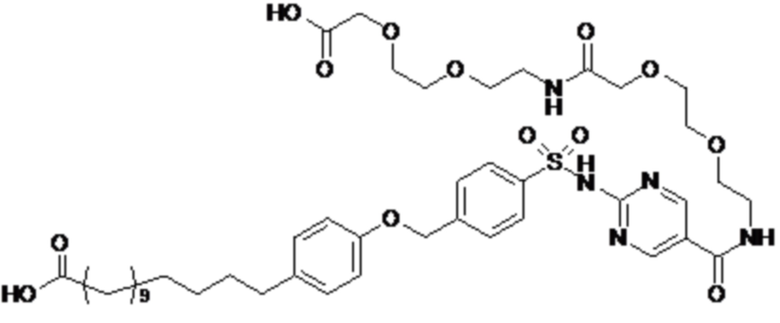
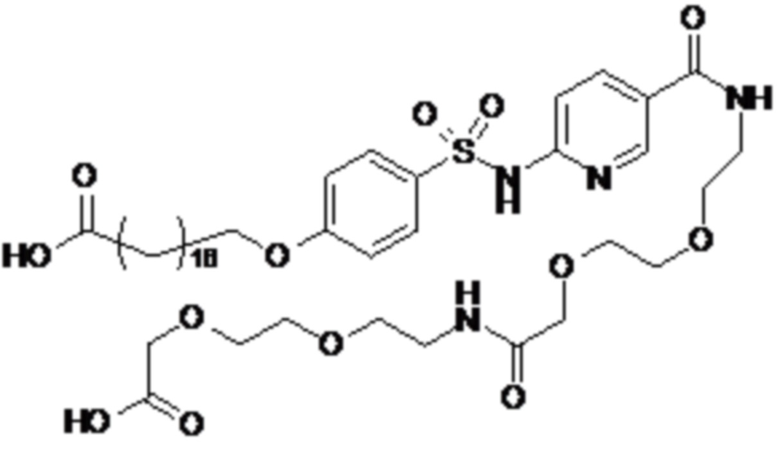
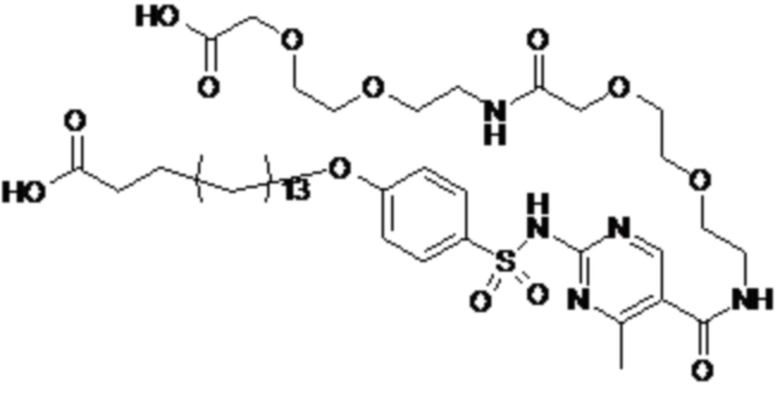
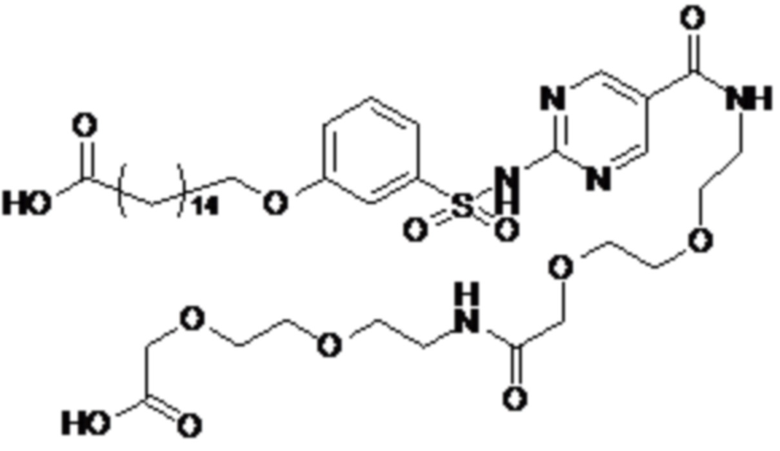
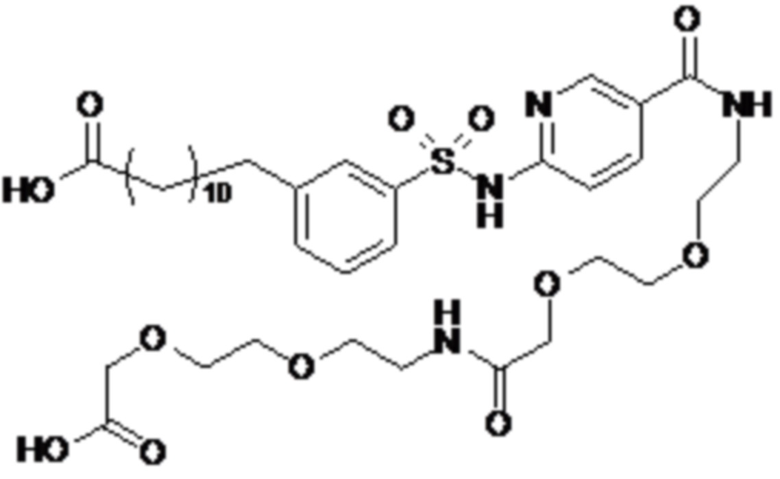
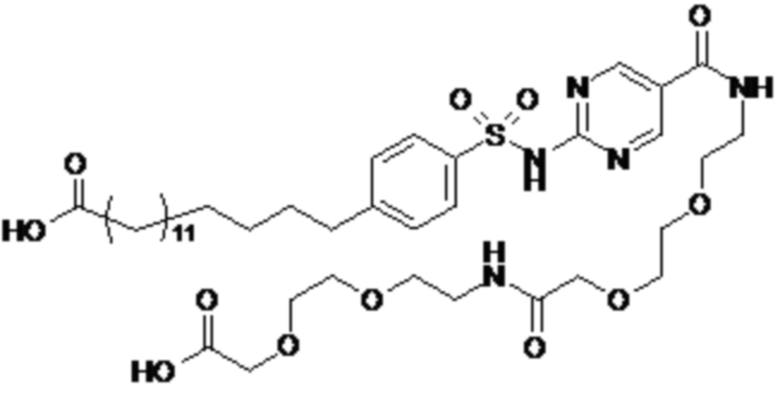
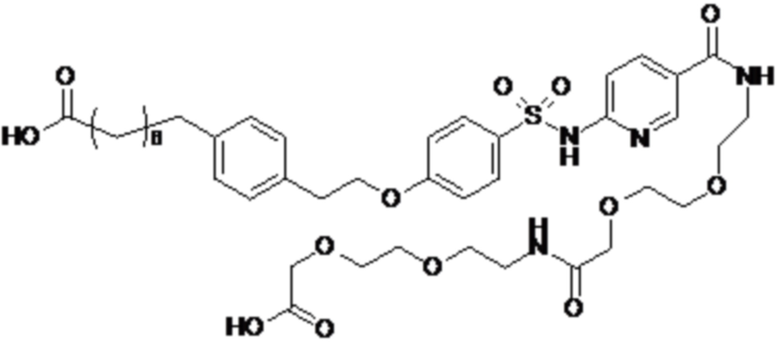
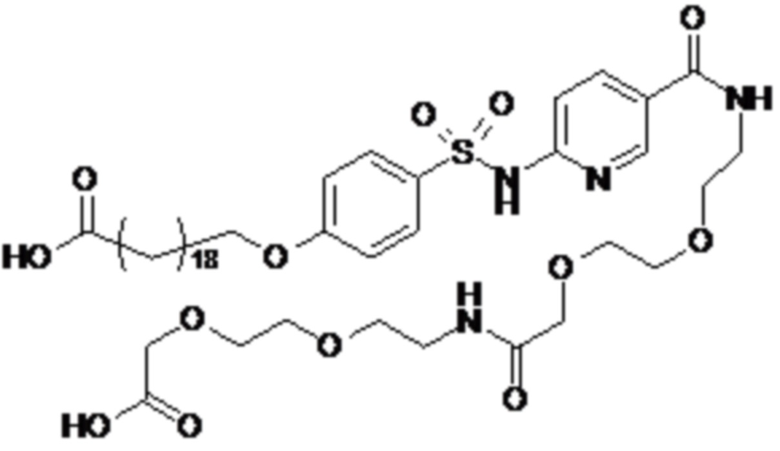
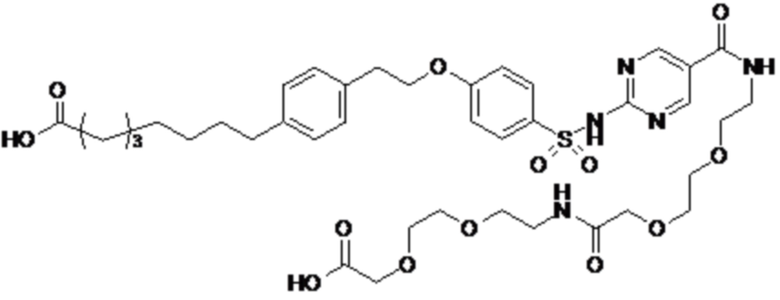
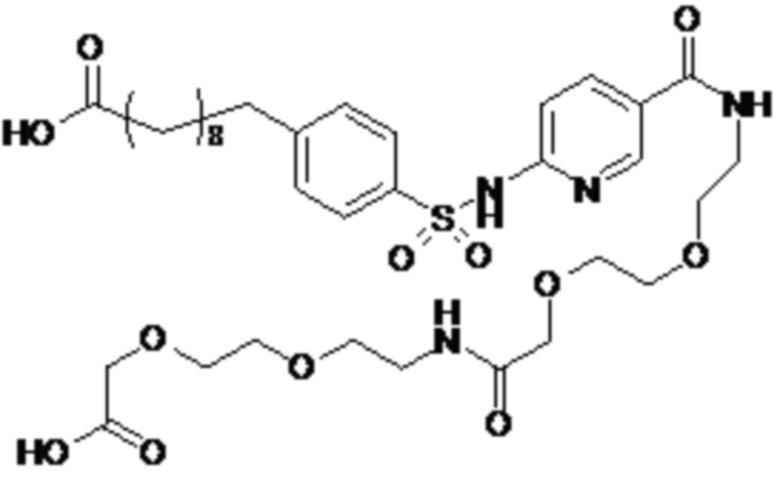
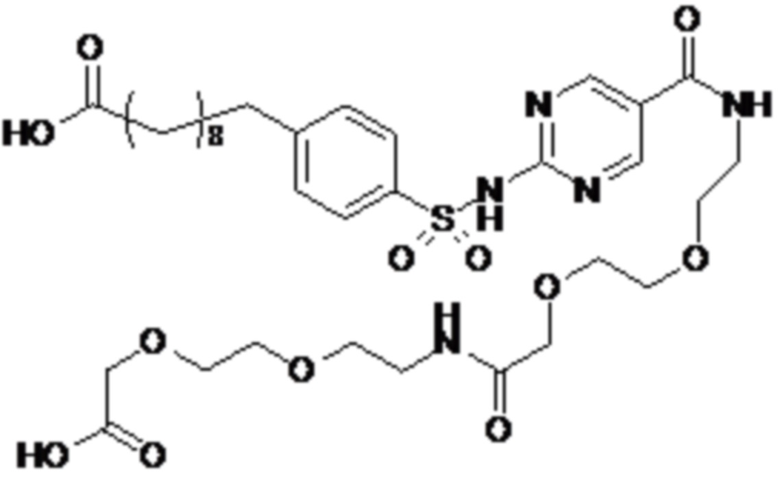
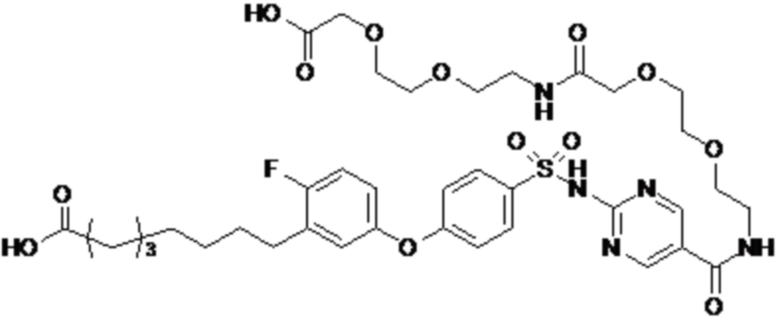
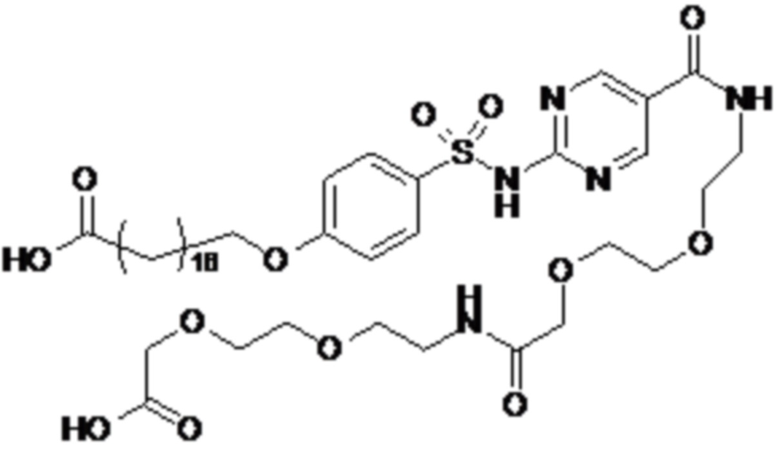
3. Синтез вариантов инсулина и конъюгатов
3.1 Человеческий инсулин
Аминокислотные последовательности A и B цепей человеческого инсулина:
A-цепь: GIVEQCCTSICSLYQLENYCN (SEQ ID NO: 102),
B-цепь: FVNQHLCGSHLVEALYLVCGERGFFYTPKT (SEQ ID NO:103)
Внутрицепочечный дисульфидный мостик присутствует между Cys(A6) и Cys(A11), два межцепочечных дисульфидных мостика присутствуют между Cys(A7) и Cys(B7) и между Cys(A20) и (Cys(B19).
3.2 Аналог инсулина 41
Аналог инсулина 41 основан на человеческом инсулине с мутациями в положениях A14, B16, B25 и удалением аминокислоты в положении B30:
Glu(A14): аминокислота в положении 14 А-цепи человеческого инсулина (Y, тирозин, Tyr) замещена глутаминовой кислотой (E, Glu),
His(B16): аминокислота в положении 16 B-цепи человеческого инсулина (Y, тирозин, Tyr) замещена гистидином (H, His),
His(B25): аминокислота в положении 25 B-цепи человеческого инсулина (F, фенилаланин, Phe) замещена гистидином (H, His),
Des(B30): аминокислота в положении 30 B-цепи человеческого инсулина удалена.
Полная аминокислотная последовательность аналога инсулина 41 с учетом цепей A и B:
A-цепь: GIVEQCCTSICSLEQLENYCN (SEQ ID NO: 104),
B-цепь: FVNQHLCGSHLVEALHLVCGERGFHYTPK- (SEQ ID NO: 105).
Одни внутрицепочечный и два межцепочечных мостика соответствуют человеческому инсулину.
3.3 Конъюгат с человеческим инсулином/Синтез [16-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]фенокси]гексадекановая кислота]Lys(B29)-инсулина
Конъюгат получали из человеческого инсулина в соответствии с 3.1 и 2-[2-[2-[[2-[2-[2-[[2-[[4-(16-трет-бутокси-16-оксо-гексадекокси)фенил]сульфониламино]пиримидин-5-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты из примера 2.9.
Синтез 16-[4-[[5-[2-[2-[2-[2-[2-[2-(2,5-диоксопирролидин-1-ил)окси-2-оксоэтокси]этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]фенокси]гексадеканоата.
К раствору 296 мг 2-[2-[2-[[2-[2-[2-[[2-[[4-(16-трет-бутокси-16-оксогексадекокси)фенил]сульфониламино]пиримидин-5-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты в 9 мл DMF добавляли 92,7 мкл триэтиламина, 106 мг TSTU и следовое количество DMAP. Раствор перемешивали в течение одного часа. Добавляли 100 мл хлористого метилена и полученный раствор трижды промывали 50 мл солевого раствора. Органический слой отделяли, высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт растворяли в 11 мл метиленхлорида и 5,5 мл трифторуксусной кислоты и хранили в течение ночи при 5°C.
Раствор концентрировали. Затем неочищенный продукт трижды растворяли в 30 мл хлористого метилена и выпаривали. Твердый материал суспендировали в 5 мл метил-трет-бутилового эфира, эфир декантировали. Остаток высушивали in vacuo и использовали без дополнительной очистки.
Раствор 480 мг инсулина суспендировали в 25 мл воды и затем добавляли 0,45 мл триэтиламина. К прозрачному раствору добавляли 25 мл MeCN и затем 0,9 мл (45,89 мМ в DMF) 16-[4-[[5-[2-[2-[2-[2-[2-[2-(2,5-диоксопирролидин-1-ил)окси-2-оксоэтокси]этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]фенокси]гексадеканоата. Раствор перемешивали в течение 3 часов при комнатной температуре. Реакцию анализировали с помощью Waters UPLC H-класса при 214 нм в натрий-фосфатном буфере. Waters BEH300 10 см. Время удерживания инсулина: 3,85 мин. Время удерживания инсулинового конъюгата 6,46 мин. Продукт очищали с помощью HPLC с ÄKTA avant 25. Kinetex 5 мкм C18 100 A 250×21,2 мм. Объем колонки (CV) 88 мл.
Объем колонки (CV) 88 мл.
Растворитель A: 0,5% уксусной кислоты в воде
Растворитель B: 0,5 уксусной кислоты в воде/MeCN 2: 8
Градиент: от 95% A 5% B до 40% A 60% B в 14 CV
Реакцию анализировали с помощью Waters UPLC H-класса при 214 нм в натрий-фосфатном буфере. Waters BEH300 10 см. Время удерживания конъюгата инсулина: 6,419 мин. Раствор лиофилизировали и получали требуемый продукт. 93 мг выход 34%. Масс-спек.: 6629,6 г/моль.
3.4 Конъюгаты с аналогом инсулина 41
Конъюгаты аналога инсулина 41 согласно 3.2 получали с молекулами связующего вещества из примера 2.9 (для структуры, см. также таблицу 1).
Связующее вещество 5: 16-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]фенокси]гексадекановая кислота;
трет-бутиловый эфир:
2-[2-[2-[[2-[2-[2-[[2-[[4-(16-трет-бутокси-16-оксогексадекокси)фенил]сульфониламино]пиримидин-5-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусная кислота.
Связующее вещество 8: 14-[5-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]фенокси]-2-фторфенил]тетрадекановая кислота; трет-бутиловый эфир:
2-[2-[2-[[2-[2-[2-[[5-[[4-[3-(14-трет-бутокси-14-оксотетрадецил)-4-фторфенокси]фенил]сульфониламино]пиримидин-2-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусная кислота.
Связующее вещество 50: 16-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]-2-хлорфенокси]гексадекановая кислота; трет-бутиловый эфир:
2-[2-[2-[[2-[2-[2-[[2-[[4-(16-трет-бутокси-16-оксогексадекокси)-3-хлорфенил]сульфониламино]пиримидин-5-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусная кислота.
Связующее вещество 54: 16-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]-фенил]гексадекановая кислота; и трет-бутиловый эфир:
2-[2-[2-[[2-[2-[2-[[2-[[4-(16-трет-бутокси-16-оксогексадецил)фенил]сульфониламино]пиримидин-5-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусная кислота.
3.4.1 Синтез Glu(A14)His(B16)His(B25)[16-[4-[[5-[2-[2-[2-[2-[2-(карбоксиметилокси)этокси]этиламино]2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]фенокси]гексадекановая кислота]Lys(B29)Des(B30)-инсулина
Амидная связь образовалась между ε-аминогруппой лизина B29 и активированным остатком уксусной кислоты связующего вещества в форме его трет-бутилового эфира 2-[2-[2-[[2-[2-[2-[[2-[[4-(16-трет-бутокси-16-оксогексадекокси)фенил]сульфониламино]пиримидин-5-карбонил]амино]этокси]этокси]ацетил]амино]этокси]этокси]уксусной кислоты, как указано ниже.
Раствор 400 мг аналога инсулина 41 (Glu(A14)His(B16)His(B25)Des(B30)-инсулина согласно примеру 3.2) суспендировали в 20 мл воды и затем добавляли 0,4 мл триэтиламина. К прозрачному раствору добавляли 20 мл DMF и затем 5 мл (17,04 мМ в DMF) трет-бутил-16-[4-[[5-[2-[2-[2-[2-[2-[2-(2,5-диоксопирролидин-1-ил)окси-2-оксоэтокси]этокси]этиламино]-2-оксоэтокси]этокси]этилкарбамоил]пиримидин-2-ил]сульфамоил]фенокси]гексадеканоата. Раствор перемешивали в течение 2 часов при комнатной температуре. Реакцию анализировали с помощью Waters UPLC H-класса при 214 нм в натрий-фосфатном буфере.
Waters BEH300 10 см.
Время удерживания инсулина: 2,643 мин.
Время удерживания инсулинового конъюгата 6,224 мин.
Продукт очищали с помощью HPLC с ÄKTA avant 25.
Kinetex 5 мкм C18 100 A 250×21,2 мм. Объем колонки (CV) 88 мл.
Растворитель A: 0,5% уксусной кислоты в воде
Растворитель B: 0,5% уксусной кислоты в воде/MeCN 4 : 6
Градиент: от 80% A 20% B до 20% A 80% B в 10 CV
После лиофилизации продукта порошок растворяли в 2 мл трифторуксусной кислоты. Через час раствор нейтрализовали разбавленным бикарбонатом натрия. Продукт очищали с помощью HPLC с ÄKTA avant 25. Kinetex 5 мкм C18 100 A 250×21,2 мм. Объем колонки (CV) 88 мл.
Растворитель A: 0,5% уксусной кислоты в воде
Растворитель B: 0,5% уксусной кислоты в воде/MeCN 4 : 6
Градиент: от 70% A 30% B до 30% A 70% B в 8 CV
Реакцию анализировали с помощью waters UPLC H-класса при 214 нм в натрий-фосфатном буфере.
Waters BEH300 10 см.
Время удерживания конъюгата инсулина: 5,121 мин.
Раствор лиофилизировали и получали требуемый продукт.
63 мг выход 14%.
Масс-спек.: 6453,9 г/моль.
Получали конъюгаты связующих веществ 8, 50 и 54 и аналога инсулина 41 соответственно.
4. Аналитические данные
4.1 Анализ жидкостной хроматографии/масс-спектрометрии (LCMS)
В таблице 1 в разделе 4.2 показаны результаты анализа LCMS выделенных связывающих веществ.
4.2 Анализ связывания альбумина
Колонка:
CHIRALPAK® HSA 50×4 мм; размер частиц 5 мкм
Gibco PBS pH7,4 (10x) фосфатно-солевой буферный раствор, 500 мл; порядковый номер: 70011-036 (500 мл)
Порядковый номер Fisher: A461-1 (1 л)
Градиент:
5 мкл 10 мМ исходного раствора DMSO (DMSO выпаривали и повторно растворяли в 200 мкл изопропанол/вода 1:1 об./об.) для изолированных образцов связующего вещества (250 мкМ, 0,2 мг/мл при молекулярной массе 800 Да)
Разбавлен из исходного водного раствора 1 мг/мл (порядковый номер Fluka: 74246-100ML)
Аффинную хроматографию проводили i) для конъюгатов инсулина согласно примерам 3.3 и 3.4 в сепарационном модуле Waters Alliance 2695, оснащенном детектором 2996 с фотодиодной матрицей Waters или Waters UPLC H-класса, оснащенном детектором с фотодиодной матрицей Waters Acquity и ii) для выделенных связывающих веществ согласно примеру 2.11 в сепарационном модуле 2795 Waters Alliance, оснащенном детектором 2996 с фотодиодной матрицей Waters, или Waters UPLC H-класса, оснащенном детектором с фотодиодной матрицей Waters Acquity.
Waters Empower 3 использовали для всех измерений в качестве программного обеспечения для обработки данных.
Колонки с иммобилизованным человеческим сывороточным альбумином (50 х 4 мм; размер частиц 5 мкм) приобретали у Chiralpak и использовали для разделений.
Фосфатно-солевой буферный раствор (PBS) приобретали у Gibco и использовали в качестве элюента А, изопропанол приобретали у Fisher и использовали в качестве элюента B.
Применяемый градиент со скоростью потока 1,0 мл/мин. показан ниже:
Колонки с иммобилизованным сывороточным альбумином поддерживали при 25°C во время цикла LC, UV-детектирование проводили при 220 нм и объем вводимой пробы составлял 20 мкл.
Эффективное время удерживания образцов сообщалось в соответствии с формулой:
эффективное время удерживания=время удерживания образца - время удерживания t0 маркера
В таблице 1 показаны результаты связывания с альбумином изолированных связывающих веществ вместе с данными LCMS из раздела 4.1.
Сокращения, используемые в таблице 1, определены следующим образом:
NRT: эффективное время удерживания на колонках с иммобилизованным сывороточным альбумином человека
LCMS: жидкостная хроматография/масс-спектрометрия
MSM: Способ масс-спектрометрии
OIM: Наблюдаемая масса иона
OIT: Наблюдаемый тип иона
IM: Способ ионизации
LCRT: Эффективное время удерживания при жидкостной хроматографии
LCM: Способ жидкостной хроматографии
Результаты из колонок с иммобилизованным сывороточным альбумином и данные LCMS
[мин.]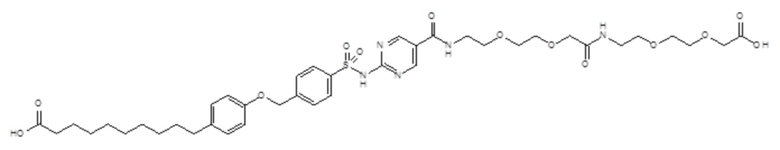
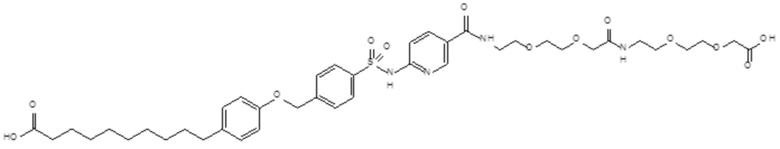
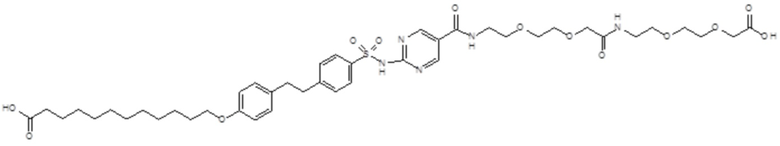
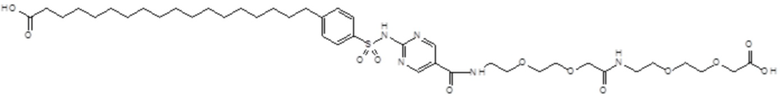
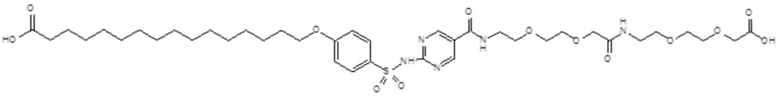
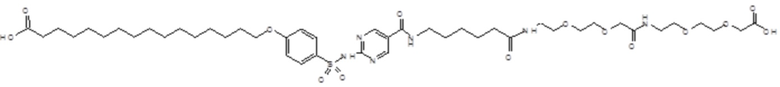
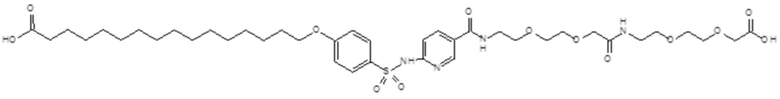
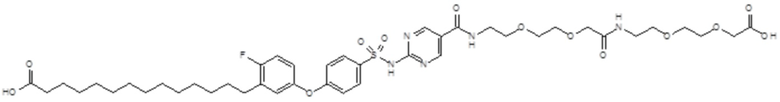
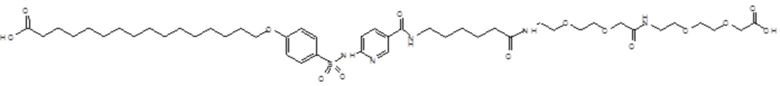
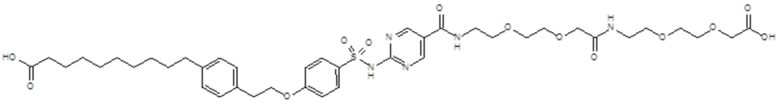
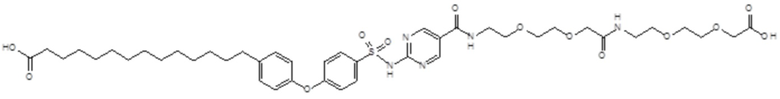
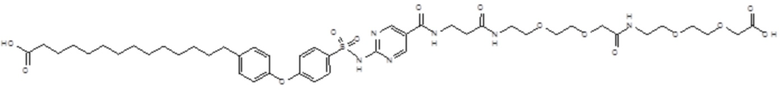
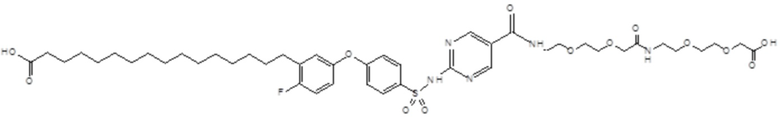
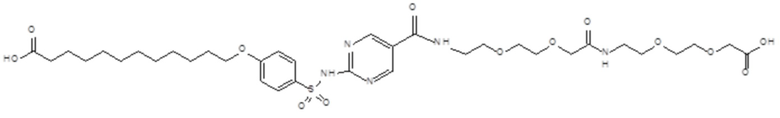
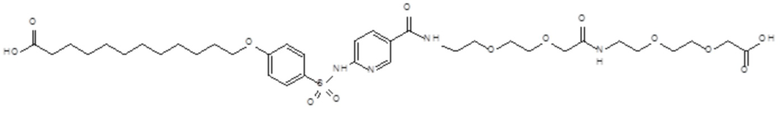
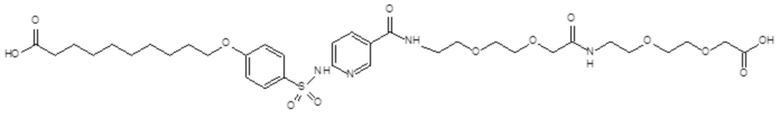
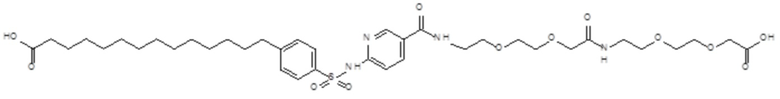
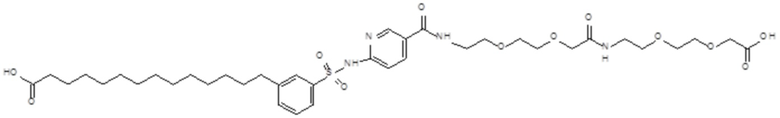
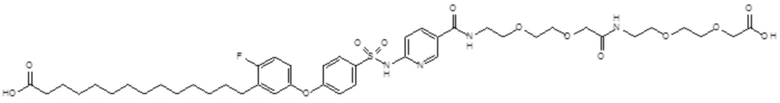
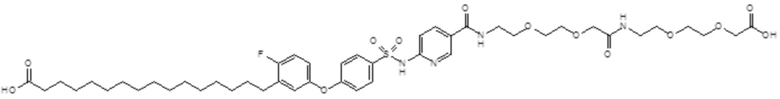
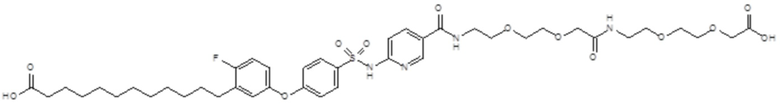
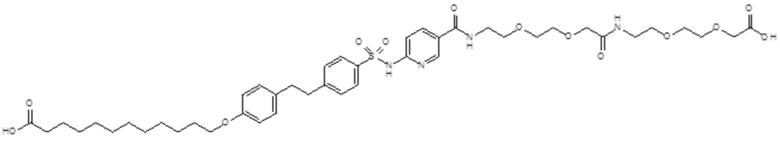
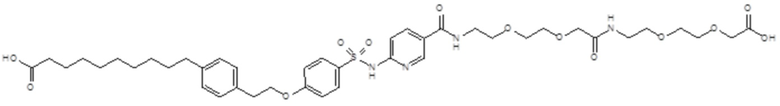
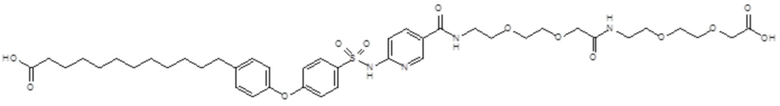
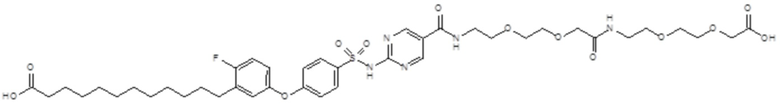
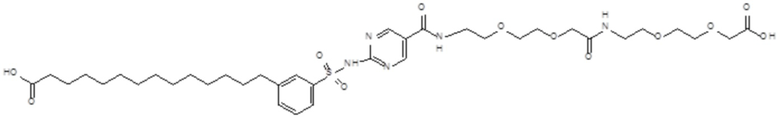
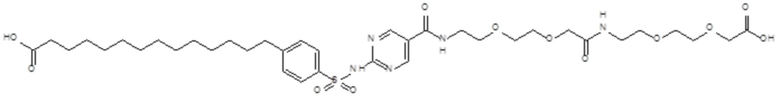
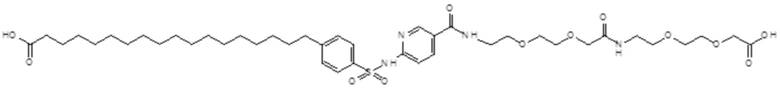
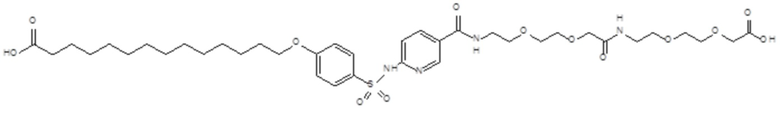
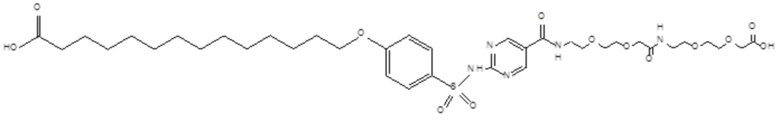
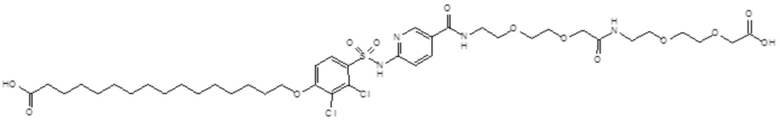
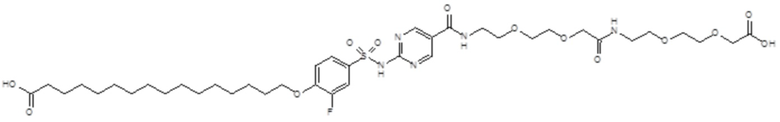
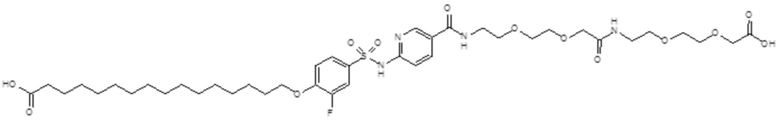
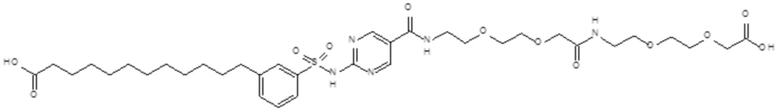
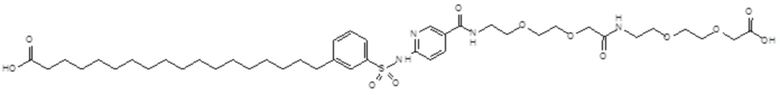
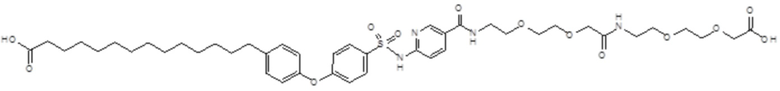
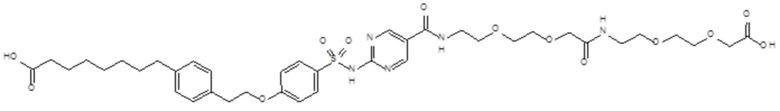
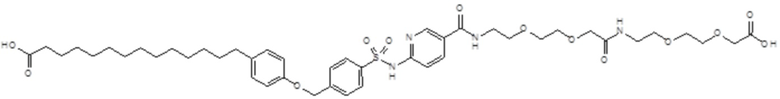
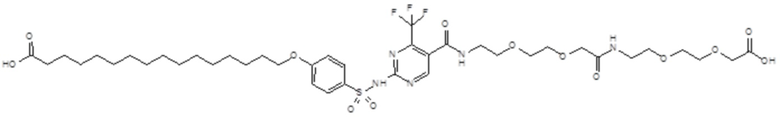
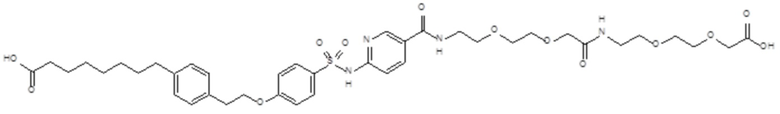
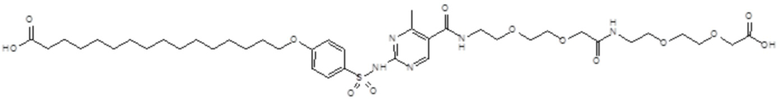
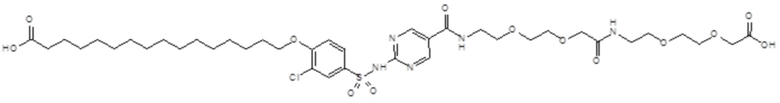
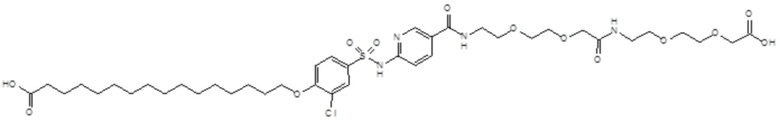
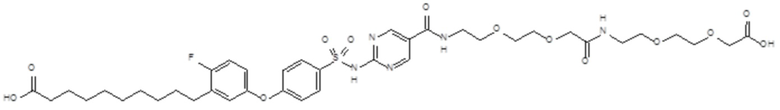
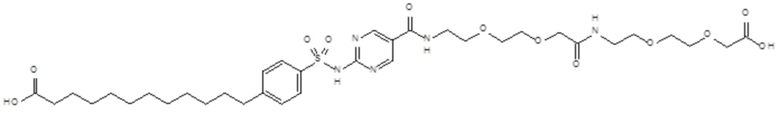
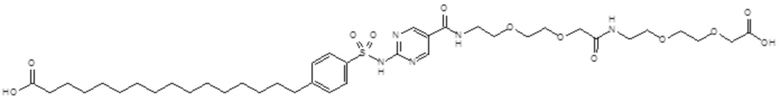
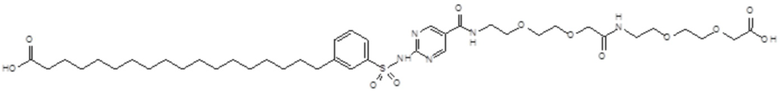
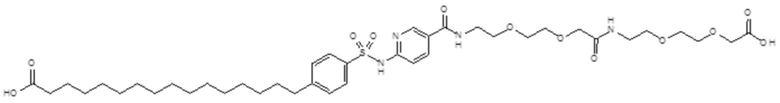
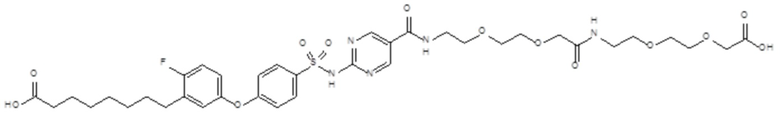
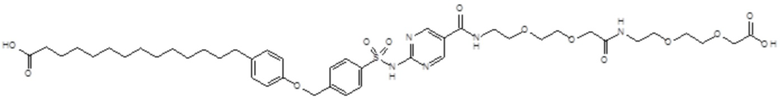
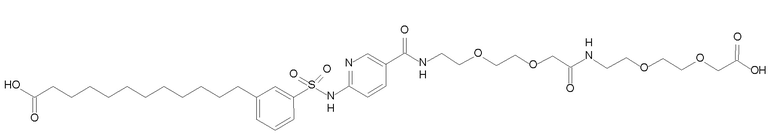
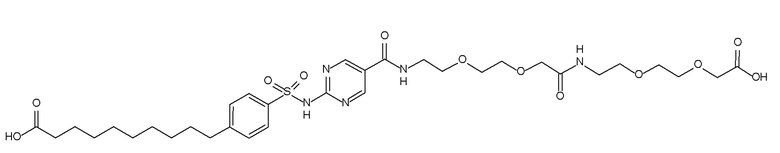
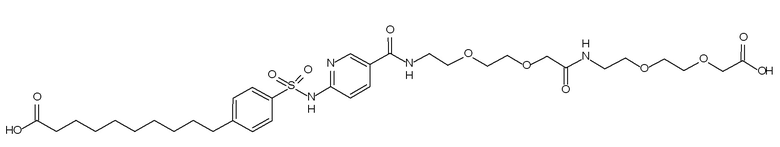
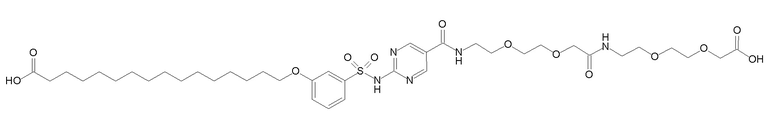
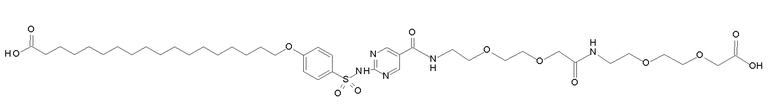
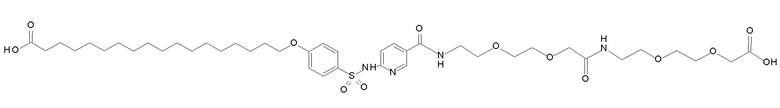
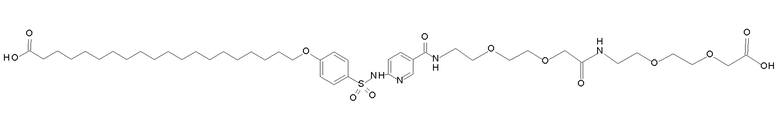
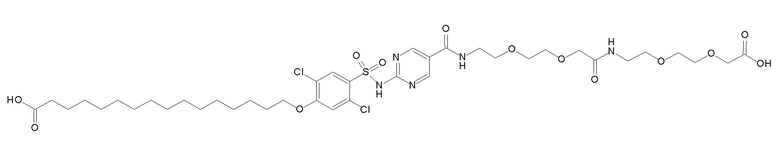
5 Аффинность связывания с рецепторами инсулина
Аффинность связывания с рецепторами инсулина для инсулина, аналога инсулина 41 и соответствующих конъюгатов, перечисленных в таблице 2, определяли, как описано в Hartmann et al. (Effect of the long-acting insulin analogues glargine and degludec on cardiomyocyte cell signaling and function. Cardiovasc Diabetol. 2016;15:96). Выделение рецепторов инсулина, встроенных в плазматические мембраны (M-IR), и эксперименты по конкурентному связыванию проводили, как описано ранее (Sommerfeld et al., PLoS One. 2010; 5(3): e9540). Вкратце, клетки СНО, сверхэкспрессирующие IR, собирали и ресуспендировали в охлажденном на льду буфере 2,25 STM (2,25 М сахароза, 5 мМ Tris-HCl pH 7,4, 5 мМ MgCl2, полный ингибитор протеазы) и разрушали с использованием гомогенизатора Даунса с последующей обработкой ультразвуком. На гомогенат наносили буфер 0,8 STM (0,8 М сахароза, 5 мМ Tris-HCl pH 7,4, 5 мМ MgCl2, полный ингибитор протеазы) и подвергали ультрацентрифугированию в течение 90 мин. при 100000g. Плазматические мембраны на границе раздела собирали и дважды промывали фосфатно-солевым буферным раствором (PBS). Конечный осадок ресуспендировали в буфере для разведения (50 мМ Tris-HCl pH 7,4, 5 мМ MgCl2, полный ингибитор протеазы) и снова гомогенизировали с помощью гомогенизатора Даунса. Эксперименты по конкурентному связыванию проводили в буфере для связывания (50 мМ Tris-HCl, 150 мМ NaCl, 0,1% BSA, полный ингибитор протеазы, доведенный до pH 7,8) в 96-луночных микропланшетах. В каждой лунке 2 мкг изолированной мембраны инкубировали с 0,25 мг поливинилтолуоловых и полиэтилениминовых гранул для сцинтилляционного анализа сближения (SPA), покрытых агглютинином из паростков пшеницы Постоянные концентрации [125I]-меченного человеческого Ins (100 пМ) и различные концентрации соответствующих немеченных Ins (0,001-1000 нМ) добавляли в течение 12 часов при комнатной температуре (23°C). Радиоактивность измеряли в равновесном состоянии на сцинтилляционном счетчике микропланшета (Wallac Microbeta, Фрайбург, Германия).
Аффинность связывания с рецепторами инсулина относительно человеческого инсулина для аналога, представленного в таблице 2, включает следующие диапазоны: A ( ≥ 40%); B ( < 20%). Конъюгат человеческого инсулина+связывающее вещество № 5 относятся к категории A, тогда как все другие конъюгаты и аналог инсулина 41 были классифицированы в категории B.
Аффинность связывания рецептора инсулина B относительно человеческого инсулина
6. Тестирование in vivo - оценка фармакокинетических эффектов
Здоровых, карликовых свиней Göttingen с нормогликемией (в возрасте от 8 до 11 месяцев, массой тела ~ от 12 до 18 кг) использовали для оценки фармакодинамических и фармакокинетических эффектов аналогов инсулина очень длительного действия у животных. Свиней содержали в стандартных условиях помещения для животных и кормили один раз в день с доступом к водопроводной воде ad libitum. После голодания в течение ночи свиньям вводили однократную подкожную инъекцию раствора, который содержал либо состав плацебо, либо инсулин, либо аналог инсулина, либо соответствующий конъюгат. Тестировали чистый человеческий инсулин и чистый аналог инсулина 41, а также конъюгат связывающего вещества №. 5 с человеческим инсулином и конъюгаты связывающих веществ 5, 50 и 54 с аналогом инсулина 41.
Сбор крови выполняли через предварительно имплантированные центральные венозные катетеры для определения уровня глюкозы в крови, фармакокинетических параметров и дополнительных биомаркеров из K-EDTA плазмы. Забор крови начинали перед введением исследуемого объекта (исходный уровень) и повторяли 1-4 раза в день до конца исследования. Во время исследования животных кормили после последнего за сутки забора крови. За всеми животными регулярно ухаживали и клинические признаки регистрировались по меньшей мере дважды в день обработки и один раз в день в течение оставшейся продолжительности исследования. За животными тщательно наблюдали на предмет любых клинических признаков гипогликемии, включая поведение, шерстный покров, мочу и фекальные выделения, состояние отверстий в теле и любые признаки болезни. В случае тяжелой гипогликемии исследователю разрешалось обеспечивать наличие пищи или вводить раствор глюкозы внутривенно (i.v.), если прием пищи был невозможен. После последнего забора крови животных транспортировали обратно в не соответствующее требованиям GLP помещение для содержания животных.
Для определения фармакокинетических параметров использовались следующие экспериментальные условия.
6.1 Материалы и химические вещества
MeCN (hyperSolv chromanorm), диметилсульфоксид (uvasol), 2-пропанол, метанол (hyperSolv chromanorm), воду (hyperSolv chromanorm), муравьиную кислоту (98-100%) приобретали у Merck (Дармштадт, Германия). Аналит и подходящий внутренний стандарт получали от Sanofi. Контрольную плазму (K2-EDTA в качестве антикоагулянта) получали от Seralab (Западный Суссекс, Великобритания).
6.2 Исходный и рабочий растворы исследуемого соединения и внутреннего стандарта
Исходные растворы тестируемого соединения и внутренний стандарт получали в смеси MeCN/вода/муравьиная кислота (50:50:1, об./об./об.) в концентрации 1 мг/мл. Рабочие растворы тестируемого соединения и соответствующего внутреннего стандарта получали в одном и том же растворителе в концентрации соответственно 100 мкг/мл и 1250 нг/мл.
6.3 Получение образцов плазмы
К 25 мкл части плазмы добавляли 10 мкл внутреннего стандарта рабочего раствора (1250 нг/мл) в пробирку Eppendorf на 1,5 мл. После закупоривания и перемешивания добавляли 75 мкл MeCN/метанола (80:20, об./об.) и образцы перемешивали вихревым способом в течение 5 с и перемешивали вихревым способом в течение 10 мин. при приблизительно 5°C и 3000g. Затем 75 мкл супернатанта переносили во флакон автоматического пробоотборника, содержащего 75 мкл воды. Флаконы закупоривали, перемешивали и анализировали.
6.4 Анализ LC-MS/MS
Анализ LC-MS/MS интактного инсулина выполняли на Agilent 1290 Series HPLC (Вальдбронн, Германия) с подключением к масс-спектрометру ABSciex QqQ API 4000 (Дармштадт, Германия). LC выполняли с оборудованной аналитической колонкой Aeris PEPTIDE XB-C18 (100×2,1 мм, размер частиц 3,6 мкм, Phenomenex), функционирующей при 40°C. Подвижная фаза А состояла из воды/муравьиной кислоты/DMSO (100:0,1:1, об./об./об.) и подвижная фаза В из MeCN/муравьиной кислоты/DMSO (100:0,1:1, об./об./об.). Программа HPLC начинали с выдерживания начальных условий 2% B в течение 0,5 мин., затем применяли градиент от 2% B до 90% B в течение 7,5 минут и колонку повторно уравновешивали в течение 2 минут. Скорость потока составляла 600 мкл/мин. и объем 40 мкл вводили в систему. Масс-спектрометр функционировал в положительном режиме при напряжении ионораспыления 5500 В, и потенциал декластеризации был оптимизирован для эффективного выделения молекул, протонированных в 5 раз. Масс-спектрометр функционировал в положительном режиме, и параметры, специфичные для соединения МС, оптимизировали для достижения наилучшей чувствительности. В качестве газа для соударений использовали азот.
Фармакокинетические (PK) параметры, время полужизни (t1/2) и среднее время удерживания (MRT) показаны в таблице 3.
Для человеческого инсулина приведено литературное значение MRT, полученное у юкатанских карликовых свиней с хроническим диабетом (Senshang Lin, Li-Lan H. Chen and Yie W. Chien, The journal of pharmacology and experimental therapeutics, 1998, 286, 959-966). Указанное t1/2 было рассчитано в качестве приблизительного значения с использованием формулы t1/2 * 1,44 в соответствии с учебником Clinical Pharmacokinetics Concepts and applications by Tozer and Rowland, 3rd edition (издатель Lippincott Williams & Wilkins), 1995- Section II-6).
Как можно видеть, конъюгирование производных инсулина, в данном случае человеческого инсулина или аналога инсулина 41, со связующими веществами настоящего изобретения оказала значительное влияние на PK (фармакокинетические) свойства полученных конъюгатов, что во всех случаях привело к увеличению t1/2 и MRT.
Фармакокинетические результаты чистых вариантов инсулина по сравнению с конъюгатами

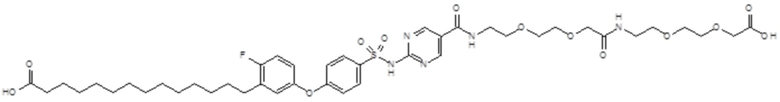
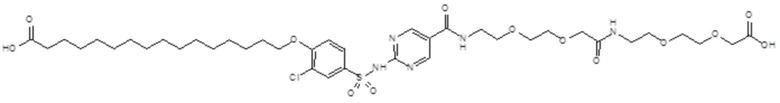
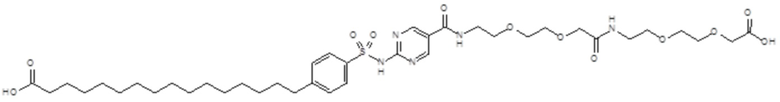
** Рассчитано из t1/2=MRT/1,44 в соответствии с Clinical Pharmacokinetics Concepts and applications by Tozer and Rowland, 3rd edition (издатель Lippincott Williams & Wilkins), 1995- Section II-6).
Фармакодинамические эффекты некоторых вариантов инсулина и конъюгатов показаны на фигурах 1 и 2, т. е. показано влияние на глюкозу в крови после s.c. введения. Данные продемонстрировали значительное увеличение продолжительности действия для всех протестированных конъюгатов инсулин-связывающее вещество (> 48 ч.) относительно аналога инсулина 41 и человеческого инсулина соответственно, для которых наблюдалась продолжительность действия при испытанных дозах, составляющая менее 24 часов. Для тестируемых конъюгатов инсулина со сниженной аффинностью связывания с рецепторами инсулина выбранная доза in vivo была выше, чем для соответствующих исходных вариантов инсулина, которые не тестировались в более высоких дозах, чтобы избежать гипогликемичесих эффектов.
Пример 7. Получение человеческого инсулина и аналогов инсулина
Человеческий инсулин, а также аналоги инсулина получали рекомбинантным путем. Полинуклеотиды, кодирующие препроинсулин, заказывали у Geneart®. Сконструированные полинуклеотиды были оптимизированы для экспрессии в дрожжах. Их вставляли в вектор экспрессии с помощью классического рестрикционного клонирования, обеспечивая функциональную экспрессию и секрецию в Klyveromyces lactis K. В качестве лидера секреции ген был слит на С-конце с последовательностью ДНК, кодирующей сигнал альфа-фактора спаривания Saccharomyces cerevisiae. Экспрессию рекомбинантного гена контролировали с помощью индуцируемого лактозой промотора K. lactis.
Человеческий инсулин, а также аналоги инсулина изготавливали в качестве препроинсулина. Генетически слитую N-концевую препоследовательность использовали для улучшения значений выхода экспрессии и секреции и для стабилизации пептида в бульонной культуре. Для этой цели можно использовать широкий спектр последовательностей, эффективность которых была проверена. Сам проинсулин состоит из B-цепи, слитой с C-пептидом, за которой следует C-концевая A-цепь. В качестве С-пептида описаны различные комбинации аминокислот. Было показано, что короткие пептиды от 1 до 10 аминокислот хорошо работают в качестве С-последовательностей. Для дальнейшей обработки инсулина важны сайты узнавания для специфических протеаз, которые фланкируют С-пептид, чтобы сделать возможным его вырезание.
Клетки K. lactis были сделаны компетентными с помощью химических средств. Впоследствии клетки трансформировали плазмидой экспрессии, кодирующей соответствующий препроинсулин. После вставки плазмиды, клетки высевали на чашки с селективным агаром, содержащим генетицин. Выращенные колонии выделяли и тестировали на предмет экспрессии рекомбинантных генов. Клетки выращивали до достаточно высокой плотности клеток в дрожжевой среде пептон-декстроза, дополненной генетицином. После начальной фазы роста к культурам добавляли забуференную солью среду дрожжевого экстракта с генетицином, дополненным лактозой, чтобы индуцировать экспрессию рекомбинантного гена. Культуры выращивали несколько дней и супернатанты собирали посредством центрифугирования.
Очистку функционального инсулина или аналогов инсулина начинали с помощью процедуры фильтрации. Первоначальная процедура хроматографического захвата проводилась с использованием ионообменной смолы. Гидролиз препроинсулина до инсулина проводили с помощью высокоспецифичной протеазы. Истощение белка клетки-хозяина, препоследовательности и продуктов, связанных с продуктами, осуществляли с помощью каскада из двух дополнительных хроматографических стадий. Наряду с хроматографией гидрофобного взаимодействия для достижения этой цели применяли другую процедура ионного обмена. Заключительную очистку осуществляли посредством хроматографии с обращенной фазой. Фильтрацию, осаждение и сублимационную сушку использовали для завершения процесса получения молекулы инсулина.
После реакций сочетания с активированным производным карбоновой кислоты раствор с конъюгированными молекулами инсулина фильтровали. Заключительное очистку осуществляли посредством хроматографии с обращенной фазой. Фильтрацию, осаждение и сублимационную сушку использовали для завершения синтеза целевой молекулы.
Были получены различные аналоги вариантов инсулина с мутациями, например, в положениях B16, B25 и/или A14. В таблице 4 представлен обзор полученных вариантов инсулина.
Пример 8. Анализы аффинности связывания с рецепторами инсулина/ нализы аутофосфорилирования рецептора инсулина
Связывание инсулина и передачу сигнала различных полученных аналогов инсулина определяли с помощью анализа связывания и анализа аутофосфорилирования рецептора.
А) Анализ аффинности связывания с рецепторами инсулина
Аффинность связывания с рецепторами инсулина аналогов, перечисленных в таблице 4, определяли, как описано в Hartmann et al. (Effect of the long-acting insulin analogues glargine and degludec on cardiomyocyte cell signaling and function. Cardiovasc Diabetol. 2016; 15:96). Выделение рецепторов инсулина, встроенных в плазматические мембраны (M-IR), и эксперименты по конкурентному связыванию проводили, как описано ранее (Sommerfeld et al., PLoS One. 2010; 5(3): e9540). Вкратце, клетки СНО, сверхэкспрессирующие IR, собирали и ресуспендировали в охлажденном на льду буфере 2,25 STM (2,25 М сахароза, 5 мМ Tris-HCl pH 7,4, 5 мМ MgCl2, полный ингибитор протеазы) и разрушали с использованием гомогенизатора Даунса с последующей обработкой ультразвуком. На гомогенат наносили буфер 0,8 STM (0,8 М сахароза, 5 мМ Tris-HCl pH 7,4, 5 мМ MgCl2, полный ингибитор протеазы) и подвергали ультрацентрифугированию в течение 90 мин. при 100000g. Плазматические мембраны на границе раздела собирали и дважды промывали фосфатно-солевым буферным раствором (PBS). Конечный осадок ресуспендировали в буфере для разведения (50 мМ Tris-HCl pH 7,4, 5 мМ MgCl2, полный ингибитор протеазы) и снова гомогенизировали с помощью гомогенизатора Даунса. Эксперименты по конкурентному связыванию проводили в буфере для связывания (50 мМ Tris-HCl, 150 мМ NaCl, 0,1% BSA, полный ингибитор протеазы, доведенный до pH 7,8) в 96-луночных микропланшетах. В каждой лунке 2 мкг изолированной мембраны инкубировали с 0,25 мг поливинилтолуоловых и полиэтилениминовых гранул для сцинтилляционного анализа сближения (SPA), покрытых агглютинином из паростков пшеницы. Постоянные концентрации [125I]-меченного человеческого инсулина (100 пМ) и различные концентрации соответствующего немеченного инсулина (0,001-1000 нМ) добавляли в течение 12 часов при комнатной температуре (23°C). Радиоактивность измеряли в равновесном состоянии на сцинтилляционном счетчике микропланшета (Wallac Microbeta, Фрайбург, Германия).
Результаты анализа аффинности связывания с рецепторами инсулина для тестируемых аналогов относительно человеческого инсулина показаны в таблице 5.
Б) Анализы аутофосфорилирования рецепторов инсулина (в качестве показателя передачи сигнала)
Чтобы определить передачу сигнала связывания аналога инсулина с рецептором инсулина B, уровень аутофосфорилирования измеряли in vitro.
Клетки СНО, экспрессирующие изоформу В рецептора человеческого инсулина (IR-B), использовали для анализа аутофосфорилирования IR с использованием технологии In-Cell Western, описанной ранее (Sommerfeld et al., PLoS One. 2010; 5(3): e9540). Для анализа аутофосфорилирования IGF1R рецептор сверхэкспрессировали в клеточной линии фибробластов 3T3 Tet-off эмбриона мыши (BD Bioscience, Гейдельберг, Германия), которая была стабильно трансфицирована плазмидой экспрессии, регулируемой тетрациклином IGF1R. Для определения уровня фосфорилирования тирозина рецептора клетки высевали на 96-луночные планшеты и выращивали в течение 44 часов. Клетки подвергали сывороточному голоданию в бессывороточной среде Ham's F12 (Life Technologies, Дармштадт, Германия) в течение 2 часов. Затем клетки обрабатывали возрастающими концентрациями либо человеческого инсулина, либо аналога инсулина в течение 20 минут при 37°C. После инкубации среду удаляли и клетки фиксировали в 3,75% свежеприготовленном параформальдегиде в течение 20 мин. Клетки пермеабилизировали 0,1% Triton X-100 в PBS в течение 20 мин. Блокирование проводили блокирующим буфером Odyssey (LICOR, Бад-Хомбург, Германия) в течение 1 часа при комнатной температуре. Anti-pTyr 4G10 (Millipore, Швальбах, Германия) инкубировали в течение 2 часов при комнатной температуре. После инкубации первичного антитела клетки промывали PBS+0,1% Tween 20 (Sigma-Aldrich, Сент-Луис, Миссури, США). Вторичное антитело к мышиному IgG-800-CW (LICOR, Бад-Хомбург, Германия) инкубировали в течение 1 часа. Результаты нормализировали посредством количественного определения ДНК с красителем TO-PRO3 (Invitrogen, Карлсруэ, Германия). Данные получены в относительных единицах (RU).
Результаты анализов аутофосфорилирования рецептора инсулина для тестируемых аналогов относительно человеческого инсулина показаны в таблице 5.
** значение 0 означает, что аффинность связывания была ниже предела обнаружения
C) Выводы
Как видно из таблицы 5, были протестированы различные гидрофобные замены в положениях B16 и/или B25 (триптофан, аланин, валин, лейцин и изолейцин). Хотя и в различной степени, все тестированные аналоги инсулина с гидрофобными заменами в этих положениях показали снижение активности связывания рецептора инсулина. По сравнению с заменами триптофана (см., например, аналоги 4, 15 и 23) замены алифатическими аминокислотами, такими как аланин, валин, лейцин и изолейцин, оказали более сильное влияние на активность связывания рецептора инсулина. Наиболее сильные эффекты наблюдались для валина, лейцина и изолейцина, которые являются аминокислотами с разветвленной цепью. Замены изолейцином, валином и лейцином приводили к значительному снижению связывающей активности рецептора инсулина. Интересно, что аналоги инсулина с такими заменами в положении B25 (например, замена валина, лейцина или изолейцина в B25, аналоги 11, 12, 22, 24, 25, 29, 30, 32, 33, 35, 38, 39, 40) показали в 6 раз большее увеличение передачи сигнала, чем ожидалось, исходя из их аффинности связывания с IR-B. В частности, Leu(B25)Des(B30)-инсулин и Val(B25)Des(B30)-инсулин (аналоги 11 и 12, соответственно) показали только 1% связывание с рецептором B инсулина и 6% аутофосфорилирование по сравнению с человеческим инсулином. Аналогичным образом, единичная замена лейцином в положении B16 (аналог 3) также показала аналогичное усиление передачи сигнала, хотя и в несколько меньшей степени. Для сравнения, за исключением аналога 26, аналоги с заменой гистидина B25 (аналоги 10, 13, 14, 21, 28) также показали пониженный уровень связывания рецептора, однако сопутствующее снижение аутофосфорилирования.
В некоторых случаях (аналоги 30, 32, 35, 38, 39) связывание с рецептором инсулина составляло 0%, при этом все еще проявлялась активность в анализе аутофосфорилирования. Все эти аналоги имеют комбинации замен валина и/или изолейцина в положениях B16 и B25 совместно, что позволяет предположить, что комбинация ответственна за дополнительное снижение уровня связывания с рецептором инсулина. Варианты инсулина без замены в положении B25, но с заменами в положении B16 проявляли немного более высокую аффинность связывания по сравнению с их значениями аутофосфорилирования (аналоги 3, 4, 16, 17, 18, 19, 20).
Аланин в положении B25 проявляет эффекты, аналогичные действию замены валина, лейцина или изолейцина (аналоги 11, 12, 22), хотя и в меньшей степени. Аффинность связывания рецептора и активность аутофосфорилирования аналогов с заменой валином, лейцином или изолейцином ниже, чем у аналогов с заменой аланином.
Пример 9. Определение устойчивости in vitro в различных рекомбинантных протеазах и искусственном желудочном соке
Полученные аналоги инсулина тестировали на протеолитическую устойчивость (α-химотрипсином, катепсином D, ферментом, расщепляющим инсулин (IDE), и искусственным желудочным соком).
А) Условия анализа
Б) Получение искусственного желудочного сока
Два грамма хлорида натрия и 3,2 г очищенного пепсина (из слизистой оболочки желудка свиньи с активностью от 800 до 2500 единиц на мг белка) растворяли в 7,0 мл соляной кислоты. Объем доводили водой до 1000 мл. Полученный раствор смешивали и доводили либо 0,2 н. гидроксидом натрия, либо 0,2 н. соляной кислотой до pH 1,2 ± 0,1.
C) Общая процедура анализа
Определение устойчивости проводили с использованием соответствующих моментов времени (для SIF и SGF 15, 30, 60, 120 и 240 минут; для протеаз 15, 30, 60 и 120 минут). Инкубацию проводили при 37°C и % оставшегося исходного соединения рассчитывали относительно точки времени T0.
Для определения исходного соединения использовали соответствующий биоаналитический способ LC-MS/MS или LC-HRMS, используя супернатант, после осаждения белка этанолом (1 экв. об./об.) и стадии центрифугирования.
D) Получение образцов
Соединения растворяли в разбавленной соляной кислоте до конечной концентрации 40 мкМ. Концентрация соединения в анализе составляла 2 мкМ. Разведение рабочего раствора 1:20 осуществляли в протеазном буфере и затем образцы инкубировали при 37°C при перемешивании. В соответствующий момент времени и когда аликвота была взята, реакционную смесь гасили этанолом (1 экв. об./об.), затем центрифугировали. Супернатант анализировали.
E) Выводы
В частности, были исследованы липофильные аминокислотные замены, такие как замены в отношении валина и изолейцина в положениях 16 и 25 в B-цепи. Из протестированных аналогов (2, 7, 11, 12, 14, 16, 19, 22, 23, 24 и 38) наблюдались лишь незначительные различия в устойчивости в отношении протеаз трипсина, карбоксипептидазы A и карбоксипептидазы B по сравнению с человеческим инсулином (данные не показаны). В целом, все аналоги, с заменой в положениях A14 и B25 (аналоги 22, 24, 38), показали улучшенную протеолитическую устойчивость к α-химотрипсину, катепсину D и ферменту, разрушающему инсулин (IDE). Например, в случае α-химотрипсина человеческий инсулин полностью разрушился в течение 2 часов, тогда как аналог 22 оказался почти полностью устойчивым. Аналогичным образом все протестированные B25-замещенные аналоги показали улучшенную устойчивость по отношению к катепсину D, хотя аналог 38 (вариант B16/B25) показал более высокую устойчивость по сравнению с другими вариантами B25.
Одно заметное исключение наблюдалось в случае IDE, в котором аналог 19 с заменами A14/B16 показал улучшенную производительность по сравнению с вариантами B25. Однако данные позволяют предположить, что замена в A14, протестированная в данном документе с глутаминовой кислотой, важна для повышения устойчивости. Также было показано, что другие замены полезны для повышения устойчивости: такие как замены в положении B16 и в положении B25. Например, аналог 7 с заменой аминокислот в положении B25 приводит к повышенной неустойчивости.
(30 минут) [%]
(120 минут) [%]
(30 минут) [%]
(30 минут) [%]
Пример 10. Получение дополнительных конъюгатов - тестирование in vivo - оценка фармакокинетических эффектов
Конъюгаты инсулина 1-4 получали (как описано в примере 3.4.1) и тестировали. В качестве контроля получали конъюгат инсулина 5, который был описан в WO2018109162A1.
Полученные конъюгаты инсулина обобщены в следующей таблице (таблица 7). Дополнительно конъюгаты инсулина 1-4 показаны на фиг. 5-8.
(см. фиг. 5)
(Аналог 24 в таблице 4)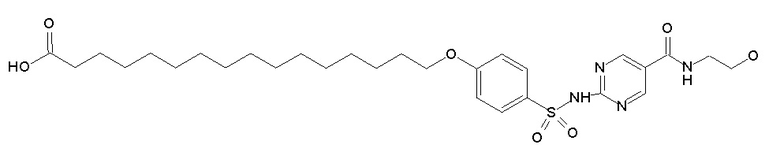
(см. фиг. 6)
(Аналог 24 в таблице 4)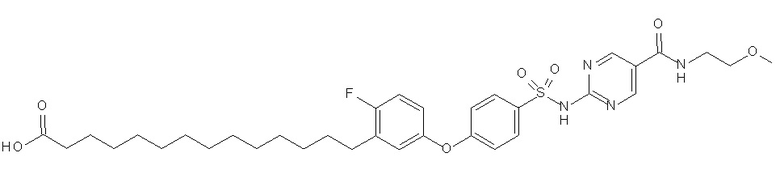
(см. фиг. 7)
(Аналог 39 в таблице 4)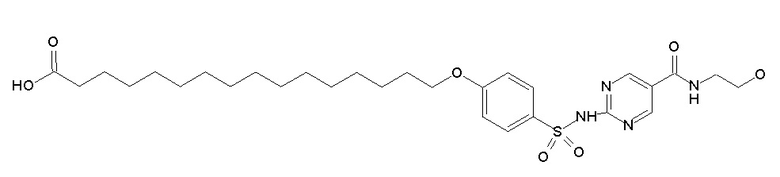
(см. фиг. 8)
(Аналог 22 в таблице 4)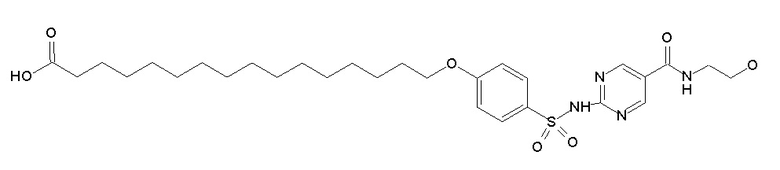
Аналог 28 в таблице 4
Здоровых, карликовых свиней Göttingen с нормогликемией использовали для оценки фармакодинамических и фармакокинетических эффектов конъюгатов инсулина очень длительного действия in vivo (использовали свиней в возрасте от 0,5 до 6 лет с диапазоном массы тела, в зависимости от возраста, ~ от 12 до 40 кг). Свиней содержали в стандартных условиях содержания лабораторных животных и кормили один раз в день с доступом к водопроводной воде ad libitum. После голодания в течение ночи свиньям вводили однократную подкожную инъекцию раствора, который содержит либо состав плацебо, либо соответствующий конъюгат инсулина. Тестировали конъюгаты инсулина 1-4, а также конъюгат инсулина 5 (описанный в WO2018109162A1).
Сбор крови выполняли через предварительно имплантированные центральные венозные катетеры для определения уровня глюкозы в крови, фармакокинетических параметров и дополнительных биомаркеров из K-EDTA плазмы. Забор крови начинали перед введением исследуемого объекта (исходный уровень) и повторяли 1-4 раза в день до конца исследования. Во время исследования животных кормили после последнего за сутки забора крови. За всеми животными регулярно ухаживали и клинические признаки регистрировались по меньшей мере дважды в день обработки и один раз в день в течение оставшейся продолжительности исследования. За животными тщательно наблюдали на предмет любых клинических признаков гипогликемии, включая поведение, шерстный покров, мочу и фекальные выделения, состояние отверстий в теле и любые признаки болезни. В случае тяжелой гипогликемии исследователю разрешалось обеспечивать наличие пищи или вводить раствор глюкозы внутривенно (i.v.), если прием пищи был невозможен. После последнего забора крови животных транспортировали обратно в помещения для содержания животных.
А) Влияние на уровень глюкозы в крови натощак
Результаты также показаны на фигуре 3.
кг]
В) Измерения фармакокинетических параметров
Результаты также показаны на фигуре 4.
(B16)Val(B25)Des
(B30)-инсулин
C) Выводы
Однократное введение конъюгата инсулина 4 (Ile(B25)) в дозе 30 нМ/кг показало эффект снижения глюкозы от низкого до умеренного с плоским профилем до 152 часов. Конъюгат инсулина 3, который содержит мутации Val(B16) и Val(B25), показал плоский профиль до 152 часов с эффектом снижения уровня глюкозы от умеренного до среднего. Кроме того, оба конъюгата инсулина 1 и 2, содержащие мутацию Val(B25), приводят к стабильному эффекту снижения уровня глюкозы без индуцирования гипогликемии в дозе 30 нМ/кг. Напротив, конъюгат инсулина 5 (описанный в WO2018109162A1), как было обнаружено, проявлял более сильный эффект снижения глюкозы с менее плоским профилем время-действие по сравнению с конъюгатами инсулина 1-4 в дозе, составляющей лишь 18 нМ/кг. Соединение может иметь более высокий риск возникновения гипогликемии.
Фармакокинетические параметры показывают, что конъюгаты инсулина 1-4 демонстрируют более раннее Tmax в диапазоне от 8 до 20 часов в комбинации с плато при Cmax до 50 часов. Поскольку они показывают конечное длинное t½ в диапазоне от 39 до 45 часов, достигается плоский PK (фармакокинетический) профиль, который необходим для дозировки один раз в неделю из-за потенциально сниженного риска гипогликемических явлений.
Краткое описание графических материалов
На фиг. 1 показан эффект снижения уровня глюкозы в крови после s.c. введения конъюгатов аналога инсулина 41 со связывающим веществом № 50 и связывающим веществом № 54 соответственно у карликовых свиней (Göttingen) (от 12 до 18 кг, n=3). Оба соединения тестировали в дозе (18 нмоль/кг).
На фиг. 2 показан эффект снижения уровня глюкозы в крови после s.c. введения инсулина и конъюгатов инсулина соответственно у карликовых свиней (Göttingen) (от 19 до 20 кг, n=3): Человеческий инсулин+связывающее вещество № 5 (18 нмоль/кг), человеческий инсулин (3 нмоль/кг), аналог инсулина 41+связывающее вещество № 5 (18 нмоль/кг), аналог инсулина 41 (3 нмоль/кг).
На фиг. 3 показаны уровни глюкозы в крови [% относительно плацебо] после подкожного введения конъюгатов инсулина 1-5 (см. таблицу 7 в примере 10).
На фиг.4 показаны нормализованные кривые концентрации в плазме крови [нг/мл] - время [ч.] для конъюгатов инсулина 1-5 (см. таблицу 7 в примере 10).
На фиг. 5 показан конъюгат инсулина № 1 (см. более подробную информацию в примере 10). Последовательности А-цепи (SEQ ID NO: 47) и В-цепи (SEQ ID NO: 48) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминокислоту остатка лизина).
На фиг. 6 показан конъюгат инсулина № 2 (см. более подробную информацию в примере 10). Последовательности А-цепи (SEQ ID NO: 47) и В-цепи (SEQ ID NO: 48) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминокислоту остатка лизина).
На фиг. 7 показан конъюгат инсулина № 3 (см. более подробную информацию в примере 10). Последовательности А-цепи (SEQ ID NO: 77) и В-цепи (SEQ ID NO: 78) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминокислоту остатка лизина).
На фиг. 8 показан конъюгат инсулина № 4 (см. более подробную информацию в примере 10). Последовательности А-цепи (SEQ ID NO: 43) и В-цепи (SEQ ID NO: 44) обозначены трехбуквенным кодом, кроме последней аминокислоты в B-цепи (лизин в положении B29). Показана структура остатка лизина. Остаток лизина ковалентно связан со связывающим веществом (через эпсилон-аминокислоту остатка лизина).
Список литературы
- Senshang Lin, Li-Lan H. Chen and Yie W. Chien, The journal of pharmacology and experimental therapeutics, 1998, 286, 959-966.
- Clinical Pharmacokinetics Concepts and applications by Tozer and Rowland, 3rd edition (издатель Lippincott Williams & Wilkins), 1995- Section II-6).
- Hartmann et al., Effect of the long-acting insulin analogues glargine and degludec on cardiomyocyte cell signaling and function, Cardiovasc Diabetol. 2016;15:96.
- Sommerfeld et al., PLoS One. 2010; 5(3): e9540.
- Handbook of Pharmaceutical Salts: Properties, Selection, and Use by Stahl and Wermuth (Wiley-VCH, 2002).
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Sanofi
<120> Конъюгат инсулина
<130> DE2018/057
<150> EP 18 306 657.0
<151> 2018-12-11
<150> EP 18 306 658.8
<151> 2018-12-11
<150> EP 18 306 659.6
<151> 2018-12-11
<160> 105
<170> BiSSAP 1.3.6
<210> 1
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<220>
<223> Цепь A
<400> 1
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 2
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<220>
<223> Цепь B
<400> 2
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys Thr
20 25 30
<210> 3
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 3
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 4
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 4
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 5
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 5
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 6
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 6
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Leu
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 7
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 7
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 8
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 8
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Trp
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 9
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 9
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 10
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 10
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu His
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 11
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 11
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 12
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 12
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 13
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 13
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 14
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 14
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ala Tyr Thr Pro Lys Thr
20 25 30
<210> 15
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 15
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 16
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 16
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ala Tyr Thr Pro Lys
20 25
<210> 17
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 17
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 18
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 18
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Glu Tyr Thr Pro Lys
20 25
<210> 19
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 19
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 20
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 20
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe His Tyr Thr Pro Lys
20 25
<210> 21
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 21
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 22
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 22
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Leu Tyr Thr Pro Lys
20 25
<210> 23
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 23
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 24
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 24
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 25
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 25
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 26
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 26
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu His
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe His Tyr Thr Pro Lys
20 25
<210> 27
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 27
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 28
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 28
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Trp
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe His Tyr Thr Pro Lys
20 25
<210> 29
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 29
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 30
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 30
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Trp
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Trp Tyr Thr Pro Lys
20 25
<210> 31
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 31
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 32
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 32
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu His
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 33
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 33
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 34
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 34
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Trp
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 35
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 35
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 36
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 36
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 37
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 37
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 38
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 38
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 39
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 39
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 40
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 40
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys
20 25
<210> 41
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 41
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 42
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 42
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe His Tyr Thr Pro Lys
20 25
<210> 43
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 43
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 44
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 44
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 45
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 45
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 46
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 46
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Trp Tyr Thr Pro Lys
20 25
<210> 47
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 47
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 48
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 48
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 49
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 49
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 50
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 50
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 51
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 51
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 52
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 52
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Glu
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe His Tyr Thr Pro Lys
20 25
<210> 53
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 53
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 54
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 54
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu His
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ala Tyr Thr Pro Lys
20 25
<210> 55
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 55
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 56
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 56
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu His
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe His Tyr Thr Pro Lys
20 25
<210> 57
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 57
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 58
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 58
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 59
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 59
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 60
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 60
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 61
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 61
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 62
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 62
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Trp Tyr Thr Pro Lys
20 25
<210> 63
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 63
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 64
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 64
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 65
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 65
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 66
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 66
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 67
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 67
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 68
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 68
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Leu
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ala Tyr Thr Pro Lys
20 25
<210> 69
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 69
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 70
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 70
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 71
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 71
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 72
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 72
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Trp Tyr Thr Pro Lys
20 25
<210> 73
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 73
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 74
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 74
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Trp Tyr Thr Pro Lys
20 25
<210> 75
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 75
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 76
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 76
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 77
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 77
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 78
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 78
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 79
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь A
<400> 79
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Gly
20
<210> 80
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 80
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 81
<211> 21
<212> БЕЛОК
<213> Bos
<220>
<223> Цепь A
<400> 81
Gly Ile Val Glu Gln Cys Cys Ala Ser Val Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 82
<211> 30
<212> БЕЛОК
<213> Bos
<220>
<223> Цепь B
<400> 82
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys Ala
20 25 30
<210> 83
<211> 21
<212> БЕЛОК
<213> Sus
<220>
<223> Цепь A
<400> 83
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 84
<211> 30
<212> БЕЛОК
<213> Sus
<220>
<223> Цепь B
<400> 84
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys Ala
20 25 30
<210> 85
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 85
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Leu Tyr Thr Pro Lys
20 25
<210> 86
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 86
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 87
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 87
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 88
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 88
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 89
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 89
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 90
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 90
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 91
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 91
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 92
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 92
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 93
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 93
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Ile
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 94
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 94
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Ile Tyr Thr Pro Lys
20 25
<210> 95
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 95
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 96
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 96
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 97
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Цепь B
<400> 97
Phe Val Glu Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Val
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Val Tyr Thr Pro Lys
20 25
<210> 98
<211> 44
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Ликсисенатид
<400> 98
His Gly Glu Gly Thr Phe Thr Ser Asp Leu Ser Lys Gln Met Glu Glu
1 5 10 15
Glu Ala Val Arg Leu Phe Ile Glu Trp Leu Lys Asn Gly Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Ser Lys Lys Lys Lys Lys Lys
35 40
<210> 99
<211> 39
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Эксенатид
<400> 99
His Gly Glu Gly Thr Phe Thr Ser Asp Leu Ser Lys Gln Met Glu Glu
1 5 10 15
Glu Ala Val Arg Leu Phe Ile Glu Trp Leu Lys Asn Gly Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 100
<211> 31
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Семаглутид
<220>
<221> MOD_RES
<222> 2
<223> Aib
<400> 100
His Ala Glu Gly Thr Phe Thr Ser Asp Val Ser Ser Tyr Leu Glu Gly
1 5 10 15
Gln Ala Ala Lys Glu Phe Ile Ala Trp Leu Val Arg Gly Arg Gly
20 25 30
<210> 101
<211> 31
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Дулаглутид
<400> 101
His Ala Glu Gly Thr Phe Thr Ser Asp Val Ser Ser Tyr Leu Glu Gly
1 5 10 15
Gln Ala Ala Lys Glu Phe Ile Ala Trp Leu Val Lys Gly Arg Gly
20 25 30
<210> 102
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<220>
<223> Человеческий инсулин, A-цепь
<400> 102
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Tyr Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 103
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<220>
<223> Человеческий инсулин, B-цепь
<400> 103
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu Tyr
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe Phe Tyr Thr Pro Lys Thr
20 25 30
<210> 104
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аналог инсулина 1, A-цепь
<400> 104
Gly Ile Val Glu Gln Cys Cys Thr Ser Ile Cys Ser Leu Glu Gln Leu
1 5 10 15
Glu Asn Tyr Cys Asn
20
<210> 105
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аналог инсулина 1, B-цепь
<400> 105
Phe Val Asn Gln His Leu Cys Gly Ser His Leu Val Glu Ala Leu His
1 5 10 15
Leu Val Cys Gly Glu Arg Gly Phe His Tyr Thr Pro Lys
20 25
| название | год | авторы | номер документа |
|---|---|---|---|
| АНАЛОГИ ИНСУЛИНА, ХАРАКТЕРИЗУЮЩИЕСЯ СНИЖЕННОЙ АФФИННОСТЬЮ СВЯЗЫВАНИЯ С РЕЦЕПТОРАМИ ИНСУЛИНА | 2019 |
|
RU2816595C2 |
| СВЯЗЫВАЮЩЕЕ ВЕЩЕСТВО ДЛЯ ПЕПТИДОВ | 2019 |
|
RU2808687C2 |
| ИНСУЛИН И ЕГО ПРОИЗВОДНЫЕ С ПОВЫШЕННОЙ СПОСОБНОСТЬЮ СВЯЗЫВАТЬ ЦИНК | 1997 |
|
RU2176646C2 |
| ЛИНКЕРЫ НА ОСНОВЕ СУЛЬФОМАЛЕИМИДА И СООТВЕТСТВУЮЩИЕ КОНЪЮГАТЫ | 2019 |
|
RU2815199C2 |
| Фармацевтическая композиция, содержащая инсулин и глюкагон | 2019 |
|
RU2823246C2 |
| НОВЫЕ АНАЛОГИ ИНСУЛИНА С ПОВЫШЕННЫМ СВЯЗЫВАНИЕМ ЦИНКА | 1999 |
|
RU2225723C2 |
| Комплекс аналога инсулина со сниженной аффинностью к инсулиновому рецептору и его применение | 2018 |
|
RU2779462C2 |
| КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ЭРИБУЛИНА И СПОСОБЫ ПРИМЕНЕНИЯ | 2017 |
|
RU2754369C2 |
| ВАРИАНТЫ СВИНОГО ТРИПСИНА | 2019 |
|
RU2783315C2 |
| АНАЛОГИ ИНСУЛИНА ЧЕЛОВЕКА, СПОСОБ ИХ ПОЛУЧЕНИЯ, РАСТВОР ДЛЯ ИНЪЕКЦИЙ | 1986 |
|
RU2104305C1 |
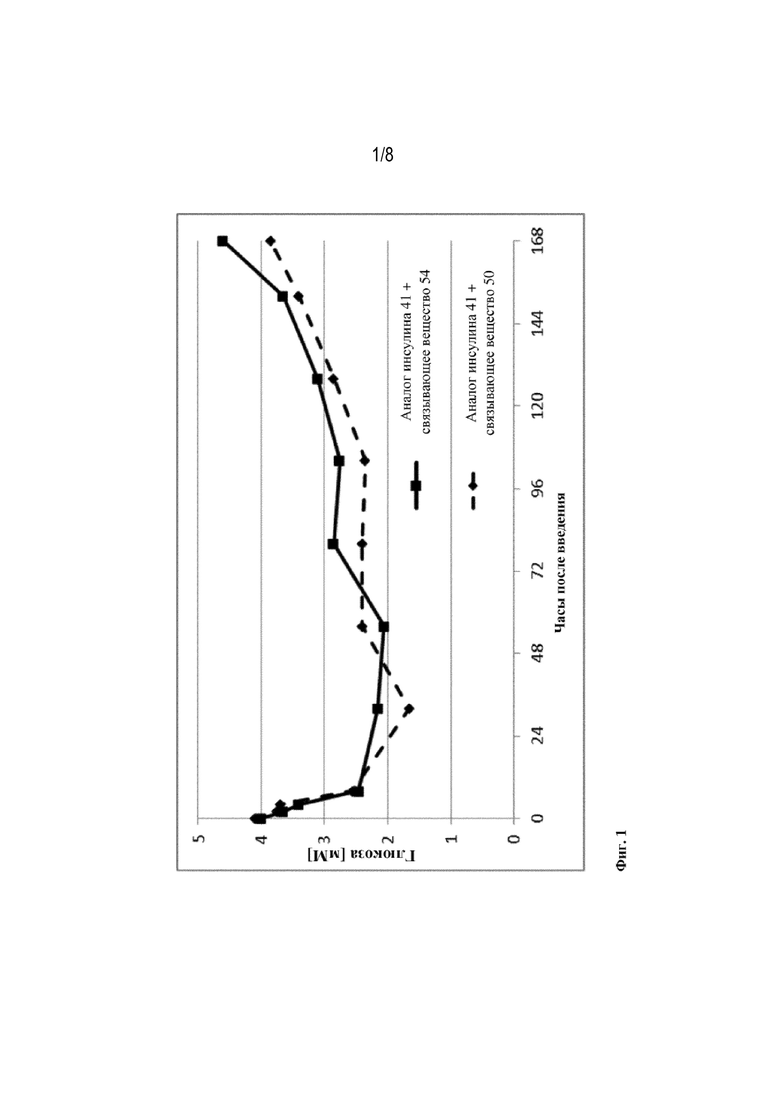

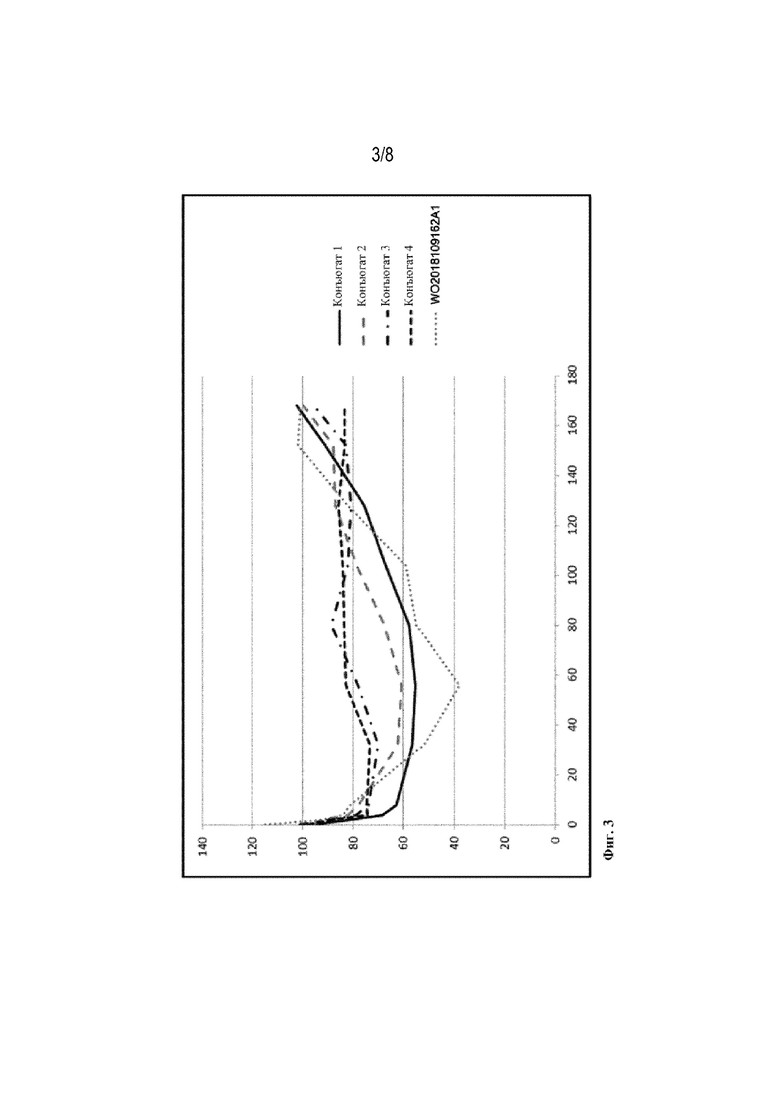
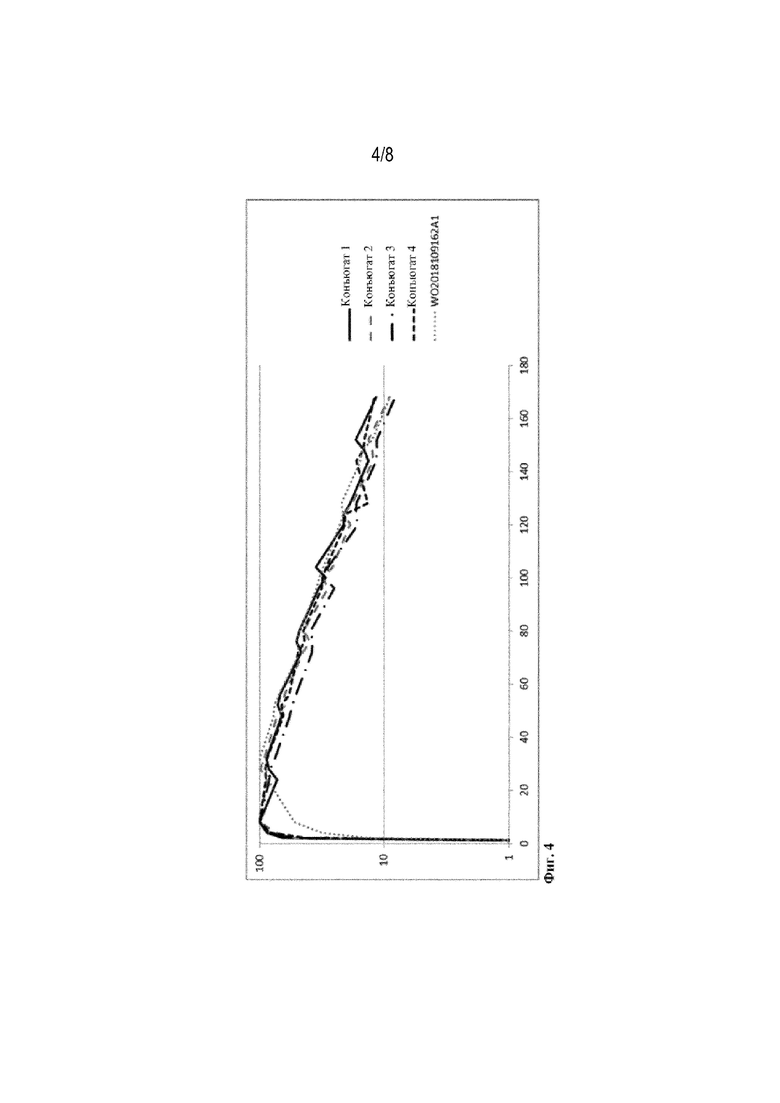
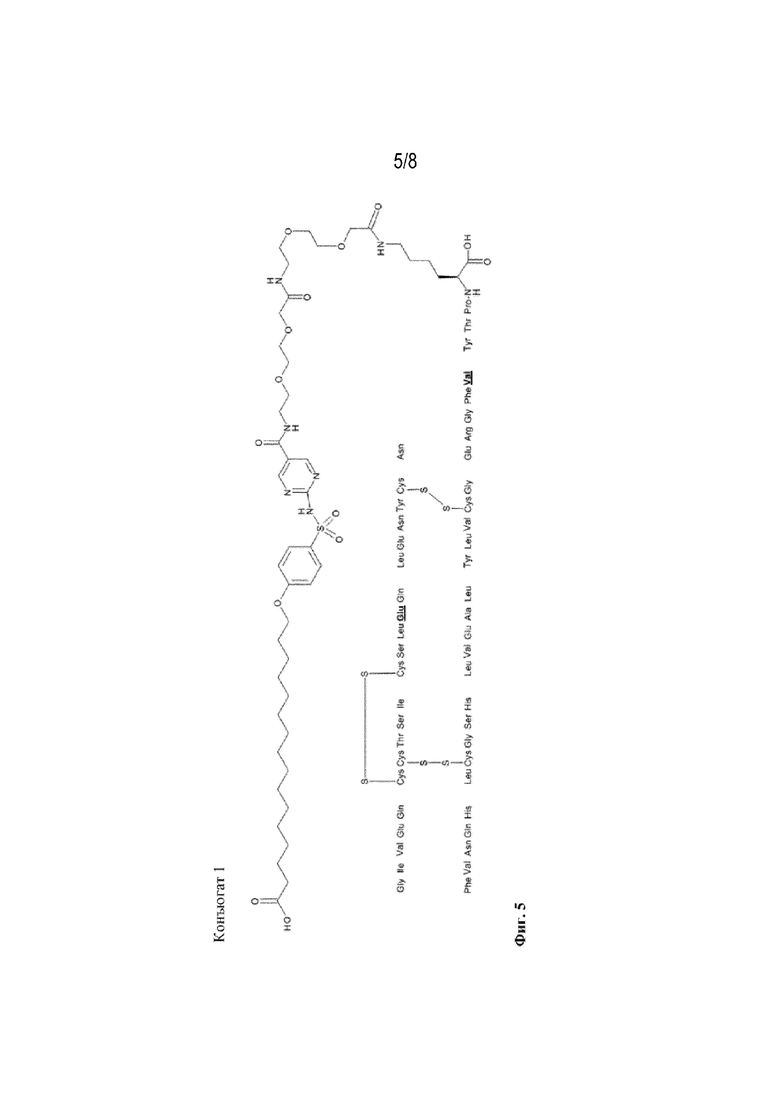
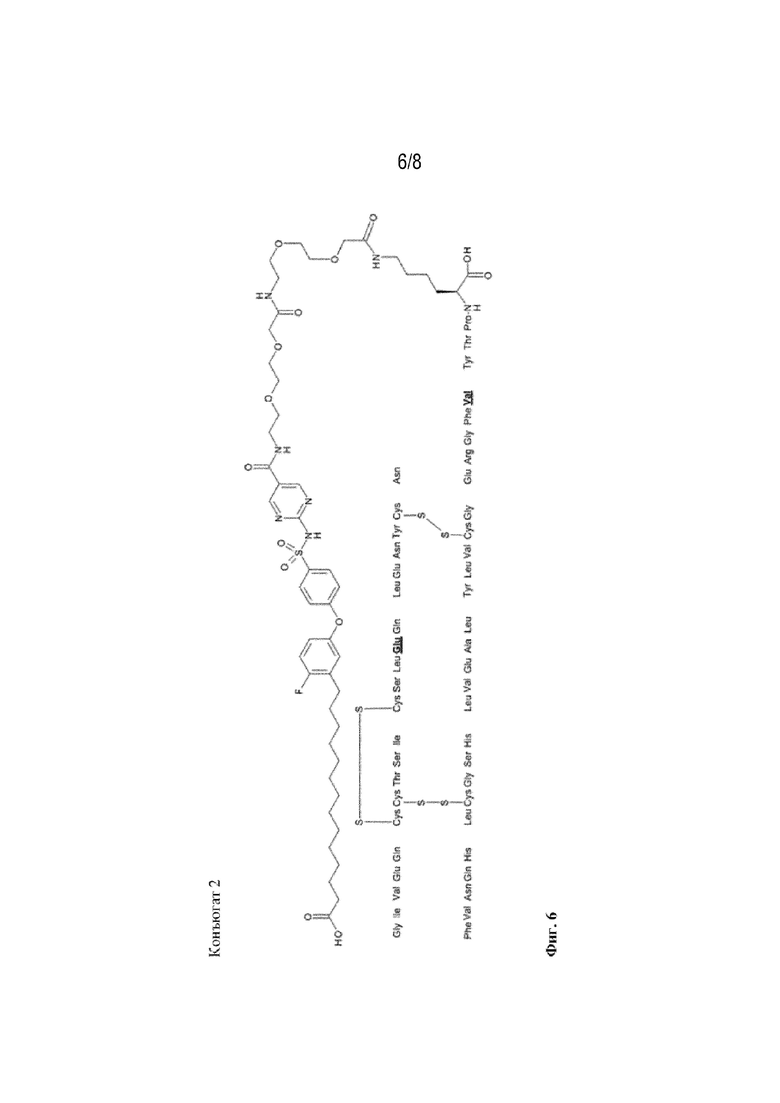
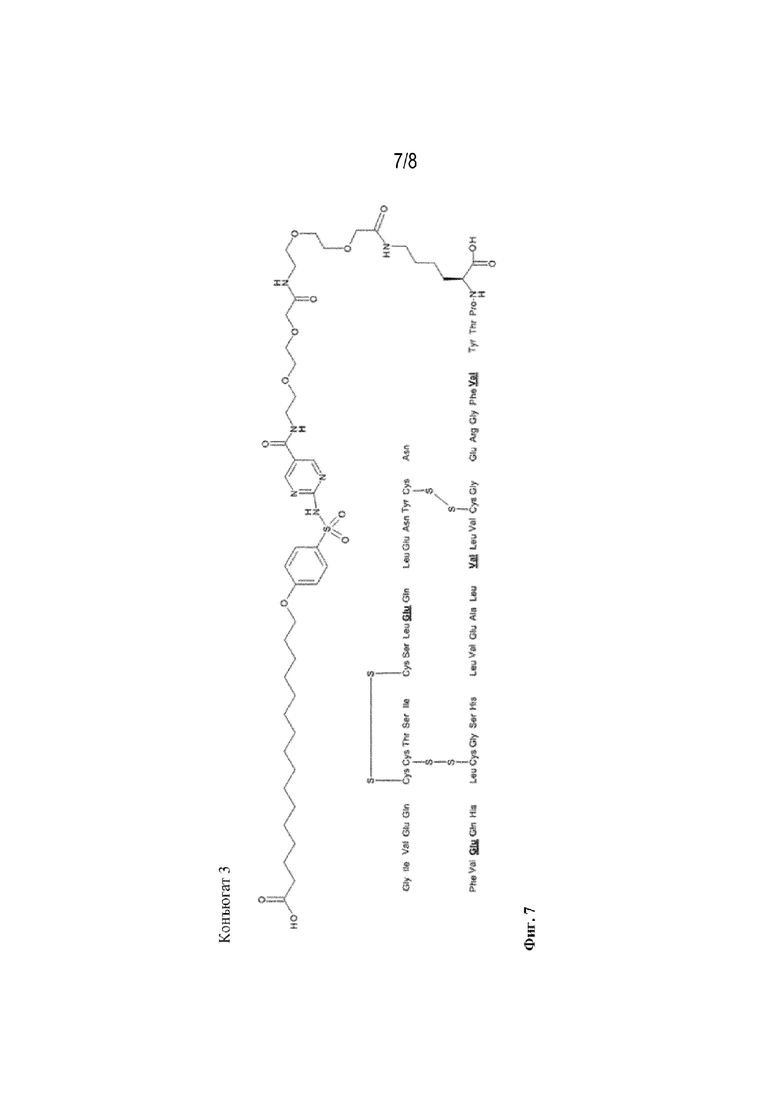
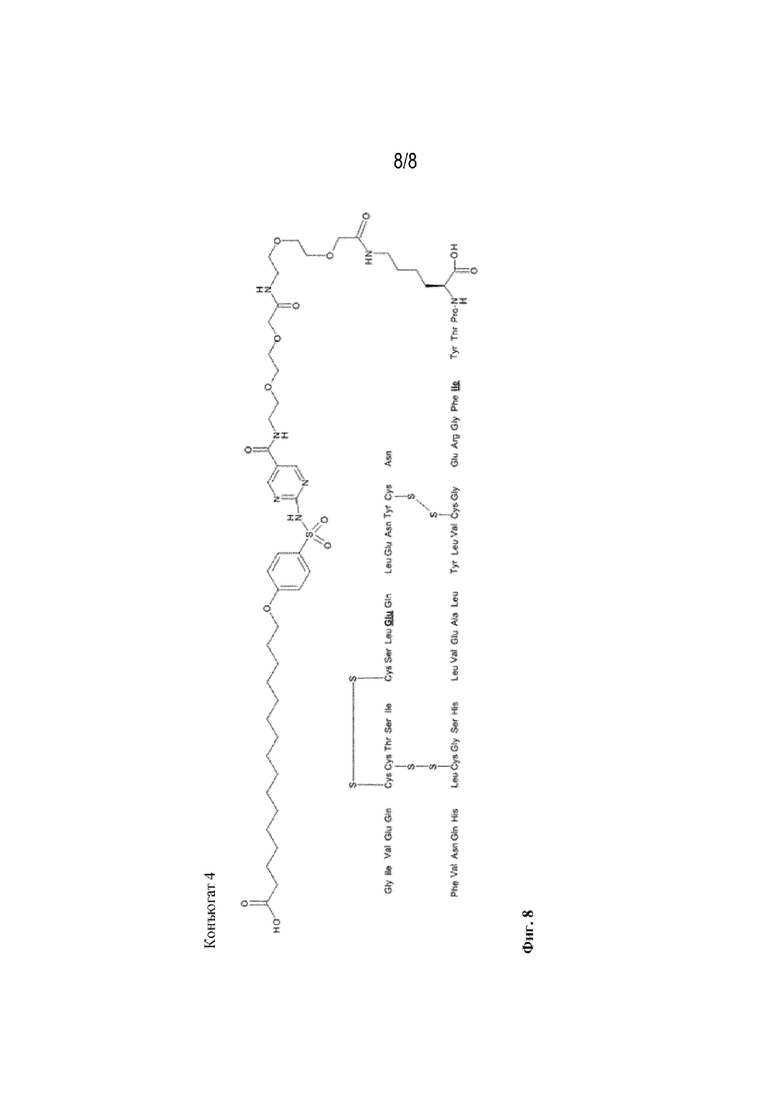
Изобретение относится к конъюгату, содержащему сульфонамид формулы (I) и аналог человеческого инсулина. Также предложена фармацевтическая композиция, содержащая конъюгат, для лечения заболевания, например, такого как из гестационный диабет, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии и/или для снижения уровней глюкозы в крови. 2 н. и 13 з.п. ф-лы, 8 ил., 9 табл., 10 пр.
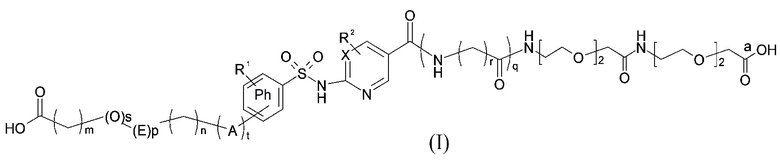
1. Конъюгат, содержащий аналог инсулина и сульфонамид формулы (I)
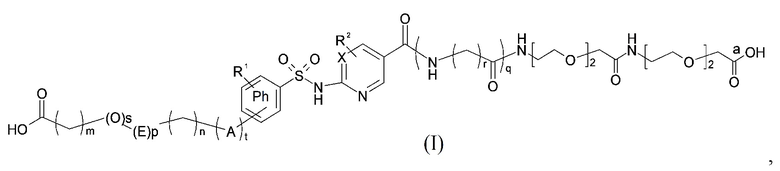
где A выбран из группы, состоящей из атома кислорода, группы -CH2CH2-, группы -OCH2- и группы -CH2O-;
E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом галогена, где атом галогена выбран из фтора и атома хлора;
X представляет собой атом азота или группу -CH-;
m представляет собой целое число в диапазоне 5-17;
n представляет собой ноль или целое число в диапазоне 1-3;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
s представляет собой ноль или 1;
t представляет собой ноль или 1;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода и атома галогена;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, атома галогена, C1-C3алкильной группы и галогенированной C1-C3алкильной группы,
где аналог инсулина представляет собой аналог человеческого инсулина, и
где сульфонамид формулы (I) ковалентно связан с аналогом инсулина таким образом, что концевая карбоксильная группа "а" сульфонамида формулы (I) ковалентно связана с эпсилон-аминогруппой лизина, присутствующего в аналоге инсулина, или с N-концевой аминогруппой В-цепи аналога инсулина.
2. Конъюгат по п. 1, где сульфонамид характеризуется формулой (I-1)
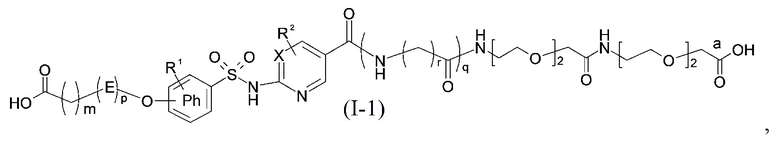
где E представляет собой группу -C6H3R-, где R представляет собой атом водорода или атом галогена, где атом галогена выбран из фтора или хлора;
X представляет собой атом азота или группу -CH-;
p представляет собой ноль или 1;
q представляет собой ноль или 1;
r представляет собой целое число в диапазоне 1-6;
R1 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода и атома галогена;
R2 представляет собой по меньшей мере один остаток, выбранный из группы, состоящей из атома водорода, C1-C3алкильной группы и галогенированной C1-C3алкильной группы;
где m представляет собой целое число в диапазоне 5-15, если p представляет собой ноль, или m представляет собой целое число в диапазоне 7-15, если p представляет собой 1.
3. Конъюгат по п. 1 или 2, где сульфонамид характеризуется формулой (I-1-1)
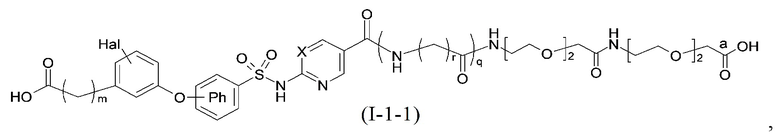
где X представляет собой атом азота или группу -CH-; m представляет собой целое число в диапазоне 7-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1; Hal представляет собой атом галогена, выбранный из группы, состоящей из атома фтора и атома хлора; и группа HOOC-(CH2)m-C6H3Hal-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
4. Конъюгат по любому из пп. 1-3, где сульфонамид характеризуется формулой (I-1-1a)
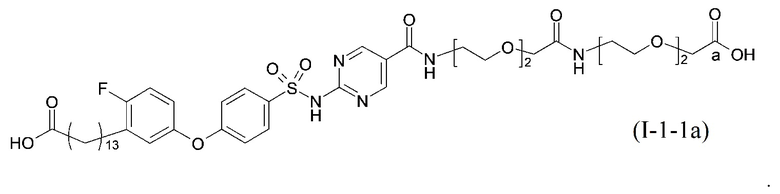
5. Конъюгат по п. 1 или 2, где сульфонамид характеризуется формулой (I-1-2)
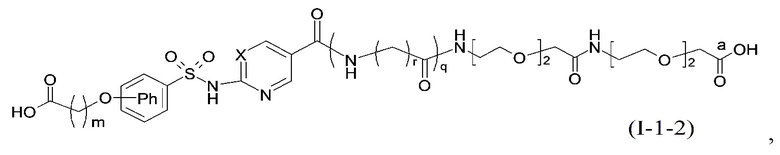
где X представляет собой атом азота или группу -CH-; m представляет собой целое число в диапазоне 5-15; r представляет собой целое число в диапазоне 1-6; q представляет собой ноль или 1; и группа HOOC-(CH2)m-O- находится в мета- или пара-положении на фенильном кольце Ph по отношению к группе -S(O)2-.
6. Конъюгат по любому из пп. 1-2 или 5, где сульфонамид характеризуется формулой (I-1-2a)
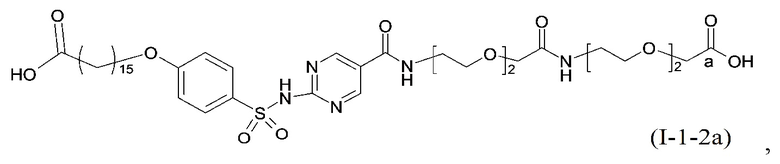
или формулой (I-1-2b)
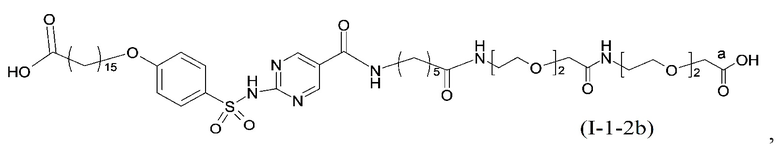
или формулой (I-1-2c)
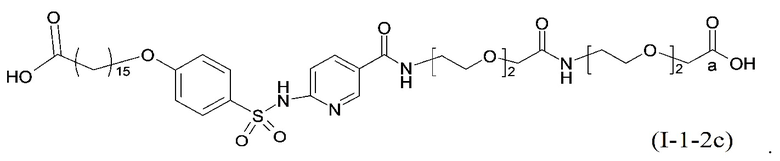
7. Конъюгат по любому из пп. 1-6, где аналог инсулина содержит по меньшей мере одну мутацию по сравнению с человеческим инсулином, при этом аналог инсулина содержит мутацию в положении B16, которая представляет собой замену гидрофобной аминокислотой, и/или мутацию в положении B25, которая представляет собой замену гидрофобной аминокислотой, и где указанный аналог инсулина необязательно дополнительно содержит мутацию в положении A14, которая представляет собой замену аминокислотой, выбранной из группы, состоящей из глутаминовой кислоты (Glu), аспарагиновой кислоты (Asp) и гистидина (His), и/или мутацию в положении B30.
8. Конъюгат по п. 7, где гидрофобная аминокислота представляет собой аминокислоту с разветвленной цепью, такую как аминокислота с разветвленной цепью, выбранная из группы, состоящей из валина (Val), изолейцина (Ile) и лейцина (Leu).
9. Конъюгат по любому из пп. 1-8, где аналог инсулина выбран из
Leu(B16)-человеческого инсулина,
Val(B16)-человеческого инсулина,
Ile(B16)-человеческого инсулина,
Leu(B16)Des(B30)-человеческого инсулина,
Val(B16)Des(B30)-человеческого инсулина,
Ile(B16)Des(B30)-человеческого инсулина,
Leu(B25)-человеческого инсулина,
Val(B25)-человеческого инсулина,
Ile(B25)-человеческого инсулина,
Leu(B25)Des(B30)-человеческого инсулина,
Val(B25)Des(B30)-человеческого инсулина,
Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B16)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B16)-человеческого инсулина,
Glu(A14)Ile(B16)-человеческого инсулина,
Glu(A14)Val(B16)-человеческого инсулина,
Glu(A14)Leu(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Leu(B25)-человеческого инсулина,
Glu(A14)Ile(B25)-человеческого инсулина,
Glu(A14)Val(B25)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Glu(B3)Ile(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Ile(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Ile(B25)Des(B30)-человеческого инсулина,
Glu(A14)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)Des(B30)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Val(B25)-человеческого инсулина,
Glu(A14)Ile(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Glu(B3)Ile(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Ile(B16)Val(B25)-человеческого инсулина,
Glu(A14)Gly(A21)Glu(B3)Ile(B16)Val(B25)-человеческого инсулина,
Glu(A14)Val(B16)Ile(B25)-человеческого инсулина,
Glu(A14)Val(B16)Val(B25)-человеческого инсулина,
Glu(A14)Glu(B3)Val(B16)Val(B25)-человеческого инсулина и
Glu(A14)Gly(A21)Glu(B3)Val(B16)Val(B25)-человеческого инсулина.
10. Конъюгат по любому из пп. 1-9, где аналог инсулина содержит:
(a) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 43 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 44 (FVNQHLCGSHLVEALYLVCGERGFIYTPK),
(b) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 47 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 48 (FVNQHLCGSHLVEALYLVCGERGFVYTPK), или
(c) А-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 77 (GIVEQCCTSICSLEQLENYCN), и B-цепь, имеющую аминокислотную последовательность, показанную под SEQ ID NO: 78 (FVEQHLCGSHLVEALVLVCGERGFVYTPK).
11. Конъюгат по любому из пп. 1-10, где аминогруппа аналога инсулина, с которой ковалентно связан сульфонамид формулы (I), представляет собой эпсилон-аминогруппу лизина, присутствующего в положении B29 B-цепи.
12. Конъюгат по любому из пп. 1-11, где конъюгат представляет собой конъюгат 1 (последовательность А-цепи: SEQ ID NO: 47; последовательность B-цепи: SEQ ID NO: 48):
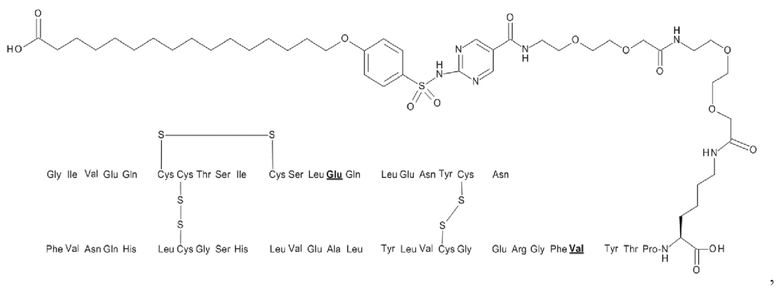 или
или
конъюгат 3 (последовательность А-цепи: SEQ ID NO: 77; последовательность B-цепи: SEQ ID NO: 78):
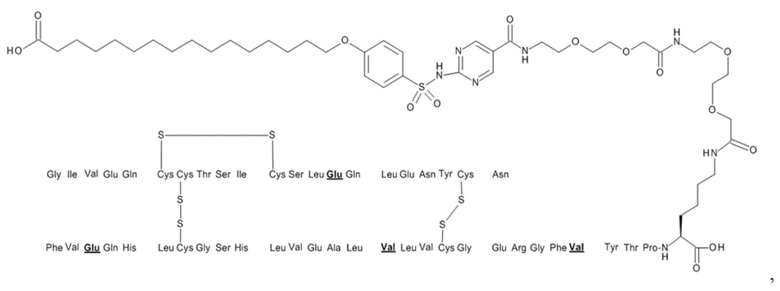
или
конъюгат 4 (последовательность А-цепи: SEQ ID NO: 43; последовательность B-цепи: SEQ ID NO: 44):
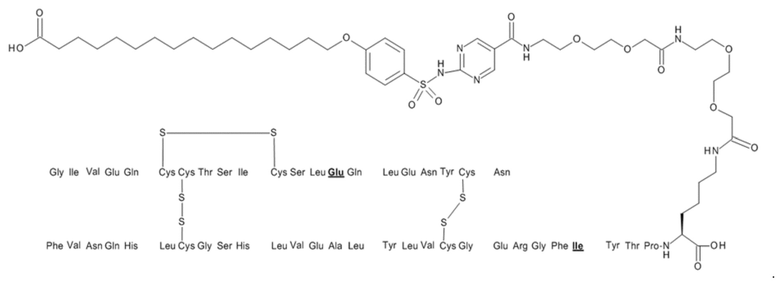
13. Фармацевтическая композиция, содержащая фармацевтически эффективное количество конъюгата, содержащего сульфонамид формулы (I) и аналог инсулина по любому из пп. 1-12 для лечения заболевания, выбранного из группы, состоящей из гестационного диабета, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии и/или для снижения уровней глюкозы в крови.
14. Конъюгат, содержащий сульфонамид формулы (I) и аналог инсулина по любому из пп. 1-12 для применения в качестве лекарственного препарата.
15. Конъюгат, содержащий сульфонамид формулы (I) и аналог инсулина по любому из пп. 1-12 для применения в качестве лекарственного препарата для лечения заболевания, выбранного из группы, состоящей из гестационного диабета, сахарного диабета 1 типа, сахарного диабета 2 типа и гипергликемии, и/или для снижения уровней глюкозы в крови.
| СТАБИЛИЗИРОВАННЫЕ ПО ОТНОШЕНИЮ К ПРОТЕАЗАМ АЦИЛИРОВАННЫЕ АНАЛОГИ ИНСУЛИНА | 2009 |
|
RU2571857C2 |
| WO 2008053360 A2,05.08.2008 | |||
| EP 3156066 A1, 19.04.2017 | |||
| RU 2016130933 A, 01.02.2018. | |||
Авторы
Даты
2023-12-07—Публикация
2019-12-10—Подача