Включение перечня последовательностей посредством ссылки
Настоящая заявка подается с перечнем последовательностей в электронной форме. Полное содержание перечня последовательностей настоящим включено в данный документ посредством ссылки.
Уровень техники
У пациентов с коагулопатией, таких как люди с гемофилией A и B, функция различных этапов коагуляционного каскада становится нарушенной, например, из-за отсутствия или недостаточного наличия функционального фактора свертывания крови. Такое нарушение функции одной части коагуляционного каскада приводит к недостаточному свертыванию крови и потенциально опасному для жизни кровотечению или повреждению внутренних органов, таких как суставы.
Дефицит фактора свертывания крови VIII (FVIII), обычно называемый гемофилией А, представляет собой врожденное нарушение свертываемости крови, поражающее примерно 420000 человек во всем мире, из которых около 105000 в настоящее время имеют поставленный диагноз.
Пациенты с гемофилией А могут получать заместительную терапию фактором свертывания крови, таким как экзогенный FVIII. Традиционное лечение состоит из заместительной терапии, предоставляемой в качестве профилактики или при необходимости для лечения эпизодов кровотечения. До недавнего времени профилактическим лечением пациента с тяжелой гемофилией А было введение не более трех внутривенных инъекций в неделю или полученного из плазмы крови FVIII, или рекомбинантного FVIII, или его вариантов длительного действия.
Однако у таких пациентов существует риск развития нейтрализующих антител, так называемых ингибиторов, к таким экзогенным факторам, что делает ранее эффективную терапию неэффективной. Гемофилия А у пациентов с наличием ингибиторов представляет собой неограничивающий пример коагулопатии, которая является частично врожденной и частично приобретенной. Пациентов, у которых развились ингибиторы FVIII, нельзя лечить с помощью традиционной заместительной терапии. Экзогенные факторы свертывания крови можно вводить только внутривенно, что создает значительные неудобства и дискомфорт для пациентов. Например, младенцам и детям младшего возраста может потребоваться введение внутривенных катетеров в грудную вену хирургическим путем, чтобы гарантировать доступ в вену. Это приводит к большому риску развития у них бактериальных инфекций.
У индивидуума с кровотечением коагуляция инициируется образованием комплекса тканевой фактор/фактор VIIa (TF/FVIIa), когда внесосудистый TF подвергается воздействию активированного FVII (FVIIa) в крови. Образование комплекса TF/FVIIa приводит к активации фактора свертывания крови X (FX) до активированного фактора свертывания крови Xa (FXa), который вместе с активированным фактором свертывания крови V (FVa) приводит к образованию ограниченного количества тромбина, который, в свою очередь, активирует тромбоциты в крови. Активированные тромбоциты поддерживают сборку теназного комплекса, состоящего из активированного фактора VIII (FVIIIa) и активированного фактора свертывания крови IX (FIXa). Теназный комплекс является очень эффективным катализатором активации FX, и FXa, образуемый на этой второй стадии, служит в качестве активной протеазы в протромбиназном комплексе FVa/FXa, который отвечает за окончательный тромбиновый «взрыв». Тромбин расщепляет фибриноген с образованием фибриновых мономеров, которые полимеризуются с образованием фибриновой сети, герметизирующей протекающий сосуд и останавливающей кровотечение. Быстрый и обширный тромбиновый «взрыв» является необходимым условием для образования твердого и стабильного фибринового сгустка.
Недостаточное образование FXa и снижение выработки тромбина, вызванное снижением или отсутствием активности FVIII, является причиной, лежащей в основе геморрагического диатеза у пациентов с гемофилией А.
Как уже упоминалось, протеолитическое превращение FX в его ферментативно активную форму FXa может быть достигнуто с помощью собственного FX-активирующего комплекса, содержащего FIXa и его кофактор FVIIIa. Связывание кофактора увеличивает ферментативную активность FIXa на приблизительно пять порядков, и, как полагают, это происходит благодаря нескольким механизмам, описанным в Scheiflinger et al. (2008) J Thromb Haemost, 6:315–322. Следует отметить, было обнаружено, что FVIIIa стабилизирует конформацию FIXa, которая обладает повышенной протеолитической активностью в отношении FX (Kolkman JA, Mertens K (2000) Biochemistry, 39:7398–7405, Zögg T, Brandstetter H (2009) Biol Chem, 390:391–400). Основываясь на этом наблюдении и осознавая, что антитела являются универсальными связывающими белками, способными имитировать различные белок-белковые взаимодействия, Scheiflinger et al. выполнили скрининг на агонистические антитела к FIXa, характеризующиеся способностью усиливать активацию FX с помощью FIXa в присутствии фосфолипидной поверхности и кальция, но в отсутствие природного кофактора FVIIIa. В результате скрининга супернатантов от 5280 гибридом обнаружили 88, которые вырабатывают антитела, проявляющие различные степени агонистической активности в отношении FIXa, см. EP1220923 B1 и EP1660536 B1. С точки зрения кинетики активации FX и способности стимулировать образование тромбина в плазме крови человека с дефицитом FVIII в EP1660536 B1 постоянно указывается на антитело 224F3 к FIXa как наиболее эффективное антитело.
В последнее время новое лекарственное средство эмицизумаб (HEMLIBRA®), также известное как ACE910, было одобрено для подкожного профилактического лечения гемофилии А с наличием ингибиторов против факторов традиционной заместительной терапии или без них. Эмицизумаб представляет собой гуманизированное биспецифическое моноклональное антитело к FIX(a)/FX(a), разработанное Chugai Pharmaceuticals/Roche Pharmaceuticals для лечения гемофилии A. Эмицизумаб имитирует функцию кофактора FVIII (см. Sampei et al.: (2013) PLoS One, 8, e57479 и WO2012067176), однако у некоторых пациентов развились ингибиторы против эмицизумаба, делающие лечение с помощью этого соединения неэффективным.
Все еще остается множество неудовлетворенных медицинских потребностей у группы лиц с гемофилией, в частности, и у субъектов с типами коагулопатии, в целом, и настоящее изобретение относится к усовершенствованным соединениям, способным заменить FVIII и, таким образом, пригодным для лечения коагулопатии, такой как гемофилия A.
Краткое описание изобретения
Настоящее изобретение относится к соединениям, которые служат заменой фактора свертывания крови VIII (FVIII) у пациентов, страдающих коагулопатией, и, в частности, у пациентов, у которых отсутствует функциональный FVIII, таких как пациенты с гемофилией A, включая пациентов с гемофилией A с наличием ингибиторов.
Следовательно, один аспект настоящего изобретения относится к соединениям, способным усиливать выработку FXa и, таким образом, частично или полностью восстанавливать коагуляцию у пациентов, у которых отсутствует функциональный FVIII.
В одном аспекте соединение представляет собой антитело или его антигенсвязывающий фрагмент. В одном таком аспекте соединение представляет собой полиспецифическое антитело или его антигенсвязывающий фрагмент, такое как биспецифическое антитело или его антигенсвязывающий фрагмент.
В одном конкретном аспекте настоящее изобретение относится к прокоагулянтным антителам или их антигенсвязывающим фрагментам, которые служат заменой FVIII у пациентов,у которых отсутствует функциональный FVIII, таких как пациенты с гемофилией A.
В одном таком аспекте антитело или его антигенсвязывающий фрагмент способны связывать FIX(a) и увеличивать ферментативную активность FIXa в отношении FX, необязательно также будучи способными связывать FX.
В одном аспекте настоящее изобретение относится к прокоагулянтному антителу или его антигенсвязывающему фрагменту, которые способны связывать FIX(a) и FX(a), включая биспецифические прокоагулянтные антитела или их антигенсвязывающие фрагменты, которые повышают ферментативную активность FIXa в отношении FX.
В одном аспекте настоящее изобретение относится к прокоагулянтному биспецифическому антителу или его антигенсвязывающему фрагменту, которые способны связываться с FIX(a) и FX(a).
Дополнительный аспект настоящего изобретения относится к отдельным компонентным антителам (промежуточным соединениям) или их антигенсвязывающим фрагментам, которые являются частью прокоагулянтного антитела, таким как конкретное антитело к FIX(a) или его антигенсвязывающий фрагмент или конкретное антитело к FX(a) или его антигенсвязывающий фрагмент.
Дополнительный аспект настоящего изобретения относится к изготовлению антител или их антигенсвязывающих фрагментов и их компонентов (промежуточных соединений), раскрытых в данном документе.
Дополнительный аспект настоящего изобретения относится к антителу, которое конкурирует с прокоагулянтным антителом или его антигенсвязывающим фрагментом, раскрытыми в данном документе, за связывание с FIX(a) и/или FX(a).
Дополнительный аспект настоящего изобретения относится к антителу или его антигенсвязывающему фрагменту, которые имеют общие остатки эпитопа или остатки-«горячие точки» эпитопа на FIX(a) и/или FX(a) с прокоагулянтным антителом или его антигенсвязывающим фрагментом, раскрытыми в данном документе.
Дополнительный аспект настоящего изобретения направлен на прокоагулянтные антитела или их антигенсвязывающие фрагменты, раскрытые в данном документе, для предупреждения и/или лечения коагулопатии, заболевания, сопровождающего коагулопатию, или заболевания, вызванного коагулопатией. В одном аспекте коагулопатия представляет собой гемофилию А с наличием ингибиторов или без них.
Еще один дополнительный аспект настоящего изобретения относится к фармацевтической композиции, содержащей прокоагулянтное антитело или его антигенсвязывающий фрагмент, раскрытые в данном документе, составленной для доставки указанного антитела для предупреждения и/или лечения коагулопатии, такой как гемофилия A с наличием ингибиторов или без них, а также к инъекционному устройству с его содержимым.
Дополнительный аспект настоящего изобретения направлен на набор, содержащий (i) антитело или его антигенсвязывающий фрагмент, раскрытые в данном документе, такое как биспецифическое антитело, и (ii) инструкции по применению.
Настоящее изобретение также может обеспечить решение дополнительных задач, которые будут очевидны из раскрытия иллюстративных вариантов осуществления.
Краткое описание графических материалов
На фигуре 1A-D показано выравнивание последовательностей, представляющих вариабельные домены тяжелой и легкой цепей антител IgG к FIX(a) (фиг. 1A и 1B) и к FX(a) (фиг. 1C и 1D), раскрытых в данном документе. Последовательности CDR1, 2 и 3 выделены жирным шрифтом и подчеркнуты в самой верхней последовательности и характерны для остальных последовательностей.
На фигуре 2 показаны результаты теста тромбинообразования (TGT) для биспецифических антител bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113, bimAb05-2114 и ACE910 в активированной тканевым фактором обедненной тромбоцитами плазме крови человека при гемофилии А (PPP). Эксперимент выполняли, как описано в примере 16. Точечные и штриховые линии показывают пиковый уровень (нМ) тромбина, наблюдаемый в отсутствие антитела в HA-PPP и нормальной PPP соответственно, и их стандартное отклонение, обозначенное точечными линиями. Профили bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113 и bimAb05-2114 обозначены направленными вниз треугольниками, тогда как профиль ACE910 обозначен направленными вверх треугольниками. Результаты представлены в виде среднего значения ± стандартное отклонение на основе по меньшей мере трех независимых экспериментов.
На фигуре 3 показаны результаты теста тромбинообразования (TGT) для биспецифических антител bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113, bimAb05-2114 и ACE910 в активированной тканевым фактором обогащенной тромбоцитами плазме крови человека при гемофилии А (PRP). Эксперимент выполняли, как описано в примере 16. Точечные и штриховые линии показывают пиковый уровень (нМ) тромбина, наблюдаемый в отсутствие антитела в HA-PRP и нормальной PRP соответственно, и их стандартное отклонение, обозначенное точечными линиями. Профили bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113 и bimAb05-2114 обозначены направленными вниз треугольниками, тогда как профиль ACE910 обозначен направленными вверх треугольниками. Результаты представлены в виде среднего значения ± стандартное отклонение на основе по меньшей мере трех независимых экспериментов.
На фигуре 4A и 4B показаны результаты экспериментов по сортировке антител по группам в системе Octet Fortebio с использованием модифицированного тандемного режима. Вкратце, биотинилированный человеческий FIXa захватывали на наконечниках со стрептавидином. Затем захваченный FIXa насыщали за счет первоначального воздействия первого (1-го) бивалентного антитела к FIXa, за которым следовало второе воздействие эквимолярной смесью первого (1-го) антитела и второго (2-го) бивалентного антитела к FIXa. Показаны ответы связывания для каждой из трех фаз, а также обозначение используемых антител.
На фигуре 5 показаны результаты экспериментов по сортировке антител по группам в системе Octet Fortebio с использованием модифицированного тандемного режима. Вкратце, биотинилированный человеческий FXa захватывали на наконечниках со стрептавидином. Затем захваченный FXa насыщали за счет первоначального воздействия первого (1-го) бивалентного антитела к FXa, за которым следовало второе воздействие эквимолярной смесью первого (1-го) антитела и второго (2-го) бивалентного антитела к FXa. Показаны ответы связывания для каждой из трех фаз, а также обозначение используемых антител.
Краткое описание последовательностей
SEQ ID NO:1 представляет аминокислотную последовательность фактора свертывания крови IX человека.
SEQ ID NO:2 представляет аминокислотную последовательность фактора свертывания крови X человека.
SEQ ID NO:3–1194 и 1202–1249 представляют последовательности вариабельных доменов тяжелой цепи (VH), вариабельных доменов легкой цепи (VL) и определяющих комплементарность областей (CDR) моноклональных антител (mAb) к FIX(a) и к FX(a), описанных в данном документе.
SEQ ID NO:1195 представляет константную область тяжелой цепи IgG4 человека с S228P и усечением C-концевого лизина.
SEQ ID NO:1196 представляет константную область тяжелой цепи IgG4 человека с S228P, F405L, R409K и усечением C-концевого лизина.
SEQ ID NO:1197 представляет константную область легкой каппа-цепи человека.
SEQ ID NO:1198 представляет константную область тяжелой цепи IgG1 человека с F405L и усечением C-концевого лизина.
SEQ ID NO:1199 представляет константную область тяжелой цепи IgG1 человека с K405R и усечением C-концевого лизина.
SEQ ID NO:1200 представляет N-концевую His-метку.
SEQ ID NO:1201 представляет GS-линкер.
Таблицы в примере 6 связывают SEQ ID NO с отдельными (компонентными) антителами к FIX(а) и к FX(а) и биспецифическими антителами по настоящему изобретению.
ОПИСАНИЕ
У субъектов с коагулопатией, таких как люди с гемофилией A, функция коагуляционого каскада становится нарушенной из-за отсутствия или недостаточного наличия функционального FVIII. Такое нарушение функции одной части коагуляционного каскада приводит к недостаточному свертыванию крови и потенциально опасному для жизни кровотечению или повреждению внутренних органов, таких как суставы. Настоящее изобретение относится к соединениям, которые служат заменой фактора свертывания крови VIII (FVIII) у пациентов, страдающих коагулопатией, и, в частности, у пациентов, у которых отсутствует функциональный FVIII, таких как пациенты с гемофилией A, включая пациентов с гемофилией A с наличием ингибиторов. В одном аспекте такое соединение представляет собой антитело.
В частности, авторы настоящего изобретения неожиданно идентифицировали антитела, которые имитируют активность кофактора FVIII с высокой активностью и эффективностью. В одном конкретном аспекте настоящее изобретение относится к прокоагулянтным антителам, которые служат заменой FVIII у пациентов, у которых отсутствует функциональный FVIII, таких как пациенты с гемофилией A. В одном таком аспекте прокоагулянтные антитела связываются с фактором свертывания крови IXa (FIXa) и увеличивают его ферментативную активность в отношении фактора свертывания крови X (FX), необязательно также связывая FX. В одном таком аспекте антитела по настоящему изобретению представляют собой биспецифические антитела, способные связываться с FIX/FIXa и FX.
Дополнительный аспект настоящего изобретения относится к отдельным компонентным антителам (промежуточным соединениям) или их антигенсвязывающим фрагментам, которые являются частью полиспецифического прокоагулянтного антитела, таким как конкретное антитело к FIX(a) или его антигенсвязывающий фрагмент или конкретное антитело к FX(a) или его антигенсвязывающий фрагмент.
Дополнительный аспект настоящего изобретения относится к изготовлению антител или их антигенсвязывающих фрагментов и их компонентов (промежуточных соединений), раскрытых в данном документе.
Дополнительный аспект настоящего изобретения относится к антителу, которое конкурирует с прокоагулянтным антителом или его антигенсвязывающим фрагментом, раскрытыми в данном документе, за связывание с FIX(a) и/или FX(a).
Дополнительный аспект настоящего изобретения относится к антителу или его антигенсвязывающему фрагменту, которые имеют общие остатки эпитопа или остатки-«горячие точки» эпитопа на FIX(a) и/или FX(a) с прокоагулянтным антителом или его антигенсвязывающим фрагментом, раскрытыми в данном документе.
В одном аспекте антитело представляет собой человеческое или гуманизированное антитело, такое как человеческое или гуманизированное биспецифическое антитело.
Дополнительный аспект настоящего изобретения направлен на прокоагулянтные антитела или их антигенсвязывающие фрагменты, раскрытые в данном документе, для предупреждения и/или лечения коагулопатии, заболевания, сопровождающего коагулопатию, или заболевания, вызванного коагулопатией. В одном аспекте коагулопатия представляет собой гемофилию А с наличием ингибиторов или без них.
Еще один дополнительный аспект настоящего изобретения относится к фармацевтической композиции, содержащей прокоагулянтное антитело или его антигенсвязывающий фрагмент, раскрытые в данном документе, составленной для доставки указанного антитела для предупреждения и/или лечения коагулопатии, такой как гемофилия A с наличием ингибиторов или без них, а также к инъекционному устройству с его содержимым.
Дополнительный аспект настоящего изобретения направлен на набор, содержащий (i) антитело или его антигенсвязывающий фрагмент, раскрытые в данном документе, такое как биспецифическое антитело, и (ii) инструкции по применению.
Фактор свертывания крови IX
Фактор свертывания крови IX (FIX) представляет собой витамин К-зависимый фактор свертывания крови со структурным сходством с фактором VII, протромбином, фактором X и С-белком. FIX циркулирует в плазме крови в виде одноцепочечного зимогена (SEQ ID NO:1). Циркулирующая зимогенная форма состоит из 415 аминокислот, разделенных на четыре отдельных домена, включая N-концевой домен, обогащенный γ-карбоксиглутаминовой кислотой (Gla), два EGF-домена и C-концевой домен, представляющий собой трипсиноподобную сериновую протеазу. Активация FIX происходит путем ограниченного протеолиза по Arg145 и Arg180 с высвобождением активационного пептида (остатки 146–180 из SEQ ID NO:1). Таким образом, активированный FIX (FIXa) состоит из остатков 1–145 из SEQ ID NO:1 (легкая цепь) и остатков 181–415 из SEQ ID NO:1 (тяжелая цепь).
Таким образом, циркулирующие молекулы FIX включают зимоген FIX и активированную форму FIX, которые в данном документе в целом обозначаются как FIX и FIXa со ссылкой на SEQ ID NO:1.
Активированный фактор IX обозначается как фактор IXa или FIXa. Термин «FIX (SEQ ID NO:1) и/или его активированная форма (FIXa)» также может обозначаться как «FIX/FIXa» или просто «FIX(a)».
FIXa представляет собой трипсиноподобную сериновую протеазу, которая играет ключевую роль в гемостазе, находясь в составе теназного комплекса, он образует большую часть фактора Xa, необходимого для поддержания надлежащего образования тромбина во время коагуляции.
FIX представлен в данном документе под SEQ ID NO:1, что соответствует аллельной форме Ala148 FIX человека (Anson et al. EMBO J. 1984 3:1053–1060; McGraw et al., Proc Natl Acad Sci USA. 1985 82:2847–2851; Graham et al. Am. J. Hum. Genet. 1988 42:573–580). В настоящем изобретении подразумевается, что FIX охватывает все природные варианты FIX, такие как вариант T148 (ID P00740 в Uniprot).
Фактор свертывания крови X
FX представляет собой витамин К-зависимый фактор свертывания крови со структурным сходством с фактором VII, протромбином, FIX и С-белком. FX циркулирует в плазме крови в виде двухцепочечного зимогена, включающего остатки 1–139 из SEQ ID NO:2 (легкая цепь) и остатки 143–448 из SEQ ID NO:2 (тяжелая цепь). Зимоген FX человека содержит четыре отдельных домена, содержащие N-концевой домен, обогащенный гамма-карбоксиглутаминовой кислотой (Gla) (остатки 1–45), два домена EGF, EGF1 (остатки 46–82) и EGF2 (остатки 85–125) соответственно, и C-концевой домен, представляющий собой трипсиноподобную сериновую протеазу (остатки 195–448). Активация FX происходит путем ограниченного протеолиза по Arg194, что приводит к высвобождению активационного пептида (остатки 143–194). Таким образом, активированный FX (FXa) состоит из остатков 1–139 из SEQ ID NO:2 (легкая цепь) и остатков 195–448 из SEQ ID NO:2 (активированная тяжелая цепь). Таким образом, циркулирующие молекулы фактора X включают зимоген FX и активированную форму FX, которые в данном документе обозначаются как FX и FXa соответственно, со ссылкой на SEQ ID NO:2. В настоящем изобретении подразумевается, что FX охватывает все природные варианты FX. Термин «FX (SEQ ID NO:2) и/или его активированная форма (FXa)» также может обозначаться как «FX/FXa» или «FX(a)».
Антитела
Термин «антитело» в данном документе относится к белку, полученному из последовательности иммуноглобулина, который способен связываться с антигеном или его частью. Термин антитело включает без ограничения полноразмерные антитела любого класса (или изотипа), то есть IgA, IgD, IgE, IgG, IgM и/или IgY. Термин антитело включает без ограничения антитела, которые являются бивалентными, такие как биспецифические антитела.
Природные полноразмерные антитела содержат по меньшей мере четыре полипептидные цепи: две тяжелые цепи (HC) и две легкие цепи (LC), которые соединены дисульфидными связями. В некоторых случаях природные антитела содержат менее четырех цепей, как в случае IgNAR, обнаруженных у Chondrichthyes. Особый интерес для получения фармацевтических препаратов представляет один класс иммуноглобулинов, IgG. У людей класс IgG можно разделить на четыре подкласса IgG1, IgG2, IgG3 и IgG4 на основании последовательности их константных областей тяжелой цепи. Легкие цепи можно разделить на два типа: каппа- и лямбда-цепи, на основании различий в составе их последовательностей. Молекулы IgG состоят из двух тяжелых цепей, связанных между собой двумя или более дисульфидными связями, и двух легких цепей, каждая из которых прикреплена к тяжелой цепи за счет дисульфидной связи. Тяжелая цепь IgG может содержать вариабельный домен тяжелой цепи (VH) и не более трех константных доменов тяжелой цепи (CH): CH1, CH2 и CH3. Легкая цепь может содержать вариабельный домен легкой цепи (VL) и константный домен легкой цепи (CL). Области VH и VL можно дополнительно подразделить на области гипервариабельности, называемые определяющими комплементарность областями (CDR) или гипервариабельными областями (HvR), чередующиеся с более консервативными областями, называемыми каркасными областями (FR). Домены VH и VL обычно состоят из трех CDR и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные домены тяжелой и легкой цепей, содержащие гипервариабельные области (CDR), образуют структуру, которая способна взаимодействовать с антигеном, в то время как константная область антитела может опосредовать связывание иммуноглобулина с тканями или факторами хозяина, в том числе, без ограничения, с различными клетками иммунной системы (эффекторными клетками), Fc-рецепторами и первым компонентом, C1q, из комплекса C1 классической системы комплемента.
Антитела по настоящему изобретению могут быть моноклональными антителами (mAb) в том смысле, что они представляют собой набор уникальных последовательностей вариабельных доменов тяжелой и легкой цепей, экспрессируемый одной B-клеткой или клональной популяцией B-клеток. Антитела по настоящему изобретению можно получать и очищать с использованием различных способов, которые известны специалисту в данной области. Например, антитела можно получать из клеток гибридомы. Антитела можно получать путем размножения B-клеток. Антитела или их фрагменты можно рекомбинантным образом экспрессировать в системах экспрессии на основе клеток млекопитающих или микроорганизмов или за счет трансляции in vitro. Антитела или их фрагменты также можно рекомбинантным образом экспрессировать в виде молекул, связанных с поверхностью клетки, например, с помощью фагового дисплея, бактериального дисплея, дрожжевого дисплея, дисплея на клетках млекопитающих или рибосомального или mRNA-дисплея.
Антитела по настоящему изобретению могут быть выделенными. Термин «выделенное антитело» относится к антителу, которое было отделено от и/или извлечено из другого(-их) компонента(-ов) в среде, в которой оно было произведено, и/или которое было очищено от смеси компонентов, присутствующих в среде, в которой оно было произведено.
В контексте настоящего изобретения могут быть подходящими определенные антигенсвязывающие фрагменты антител, поскольку было показано, что антигенсвязывающую функцию антитела могут выполнять фрагменты полноразмерного антитела. Термин «антигенсвязывающий фрагмент» антитела относится к одному или нескольким фрагментам антитела, которые сохраняют способность специфически связываться с антигеном, таким как FIX/FIXa, FX/FXa или другая целевая молекула, описанные в данном документе, или распознавать его. Примеры антигенсвязывающих фрагментов включают (без ограничения) Fab, Fab', Fab2, Fab'2, Fv (как правило, комбинация доменов VL и VH из одного плеча антитела), одноцепочечный Fv (scFv); см., например, Bird et al. Science 1988; 242:423–426 и Huston et al. PNAS 1988; 85:5879–5883), dsFv, Fd (как правило, домен VH и CH1), одновалентные молекулы, содержащие как один домен VH, так и один домен VL; минитела, диатела, триотела, тетратела и каппа-тела (см., например, Ill et al (1997) Protein Eng 10: 949–57); а также один или более выделенных CDR или функциональный паратоп, где выделенные CDR или антигенсвязывающие остатки или полипептиды могут быть ассоциированы или связаны вместе с образованием функционального фрагмента антитела. Эти фрагменты антител можно получать с использованием традиционных методик, известных специалистам в данной области, и фрагменты можно подвергать скринингу в отношении их применимости таким же образом, как и интактные антитела.
«Fab-фрагменты» антитела, включая «Fab»- и «Fab’2»-фрагменты, можно получать из антитела путем расщепления тяжелой цепи в шарнирной области на N-концевой или C-концевой стороне соответственно шарнирных остатков цистеина, соединяющих тяжелые цепи антитела. «Fab»-фрагмент включает вариабельный и константный домены легкой цепи и вариабельный домен и домен CH1 тяжелой цепи. «Fab'2»-фрагменты содержат пару «Fab'»-фрагментов, которые обычно ковалентно связаны своими шарнирными остатками цистеинов. Fab' обычно получают из Fab'2-фрагмента путем расщепления шарнирных дисульфидных связей, соединяющих тяжелые цепи в Fab'2. Из уровня техники также известны другие химические связи, фрагментов антител, отличные от дисульфидных связей. Fab-фрагмент сохраняет способность родительского антитела связываться со своим антигеном, потенциально с более низкой аффинностью. Fab'2-фрагменты способны к бивалентному связыванию, тогда как фрагменты Fab и Fab’ могут связываться только моновалентно. Обычно у Fab-фрагментов отсутствуют константные домены CH2 и CH3, т. e. Fc-часть, где могло бы происходить взаимодействие с Fc-рецепторами и C1q. Таким образом, Fab-фрагменты в целом лишены эффекторных функций. Fab-фрагменты можно получить с помощью способов, известных из уровня техники, или за счет ферментативного расщепления антитела, например, с использованием папаина для получения Fab или пепсина для получения Fab'2, или Fab-фрагменты, в том числе Fab, Fab', Fab'2 можно получить рекомбинантным образом с использованием методик, которые хорошо известны специалисту в данной области.
«Fv»-фрагмент (вариабельный фрагмент) представляет собой фрагмент антитела, который содержит полный участок распознавания и связывания антигена и обычно содержит один вариабельный домен тяжелой и один вариабельный домен легкой цепи в ассоциации, которая может быть ковалентной по природе, например, в виде одноцепочечного фрагмента из вариабельных доменов (scFv). Именно в этой конфигурации три гипервариабельных области каждого вариабельного домена взаимодействуют с образованием антигенсвязывающего участка на поверхности димера VH-VL. В совокупности шесть гипервариабельных областей или их подмножество придают антителу специфичность связывания антигена.
«Одноцепочечный Fv» или «scFv»-антитело содержат домены VH и VL антитела, где эти домены присутствуют в одной полипептидной цепи. Обычно полипептид Fv дополнительно содержит полипептидный линкер между доменами VH и VL, который позволяет scFv формировать структуру, необходимую для связывания антигена. Обзор scFv см. в Pluckthun, 1994, в: The Pharmacology of Monoclonal Antibodies, Vol. 113, Rosenburg and Moore eds. Springer-Verlag, New York, pp. 269–315.
«Одноцепочечный Fab» или «scFab»-антитело содержит домены VH, CH1, VL и CL антитела, где эти домены присутствуют в одной полипептидной цепи. Обычно полипептид Fab дополнительно содержит полипептидный линкер между доменами VH и CL или VL и CH1, который позволяет scFab формировать структуру, необходимую для связывания антигена (Koerber et al. (2015) J Mol Biol. 427:576–86).
Термин «диатела» относится к небольшим фрагментам антител с двумя антигенсвязывающими участками, причем фрагменты содержат вариабельный домен тяжелой цепи (VH), соединенный с вариабельным доменом легкой цепи (VL) в одной и той же полипептидной цепи (VH и VL). При использовании линкера, который является слишком коротким, чтобы обеспечить спаривание между двумя вариабельными доменами на одной и той же цепи, вариабельные домены вынуждены образовывать пару с комплементарными доменами другой цепи, создавая два антигенсвязывающих участка.
Выражение «линейные антитела» относится к антителам, описываемым в Zapata et al. (1995) Protein Eng. 8: 1057–1062. Вкратце, эти антитела содержат пару тандемных сегментов Fd (VH-CH1-VH-CH1), которые вместе с комплементарными полипептидами легкой цепи образуют пару антигенсвязывающих областей. Линейные антитела могут быть биспецифическими или моноспецифичными.
Фрагменты антител можно получать с использованием традиционных методик рекомбинантной или белковой инженерии, и фрагменты можно подвергать скринингу в отношении связывания с FIX и его активированной формой, FX или другим функциональным элементом таким же образом, как и интактные антитела.
Фрагменты антител по настоящему изобретению можно получать путем усечения, например, за счет удаления одной или нескольких аминокислот с N- и/или С-концов полипептида. Фрагменты также можно получать за счет одной или нескольких внутренних делеций.
Антитело по настоящему изобретению может представлять собой или может содержать фрагмент антитела или вариант любого из антител, раскрытых в данном документе. Антитело по настоящему изобретению может представлять собой или может содержать антигенсвязывающую часть одного из этих антител или их вариантов. Например, антитело по настоящему изобретению может представлять собой Fab-фрагмент одного из этих антител или его вариантов или это может быть одноцепочечное антитело, полученное из одного из этих антител или его варианта. Также антитело по настоящему изобретению может представлять собой комбинацию полноразмерного антитела и его фрагмента.
Используемый в данном документе термин «одноплечее» относится к моновалентному антителу конкретного типа, состоящему из тяжелой цепи антитела, усеченной тяжелой цепи, у которой отсутствует область Fab, и одной легкой цепи.
Используемый в данном документе термин «моноспецифическое» антитело относится к антителу, которое способно связываться с одним конкретным эпитопом (включая без ограничения бивалентные антитела).
Используемый в данном документе термин «биспецифическое» антитело относится к антителу, которое способно связываться с двумя разными антигенами или двумя разными эпитопами на одном и том же антигене.
Используемый в данном документе термин «триспецифическое» антитело относится к антителу, которое способно связываться с тремя разными антигенами, или тремя разными эпитопами на одном и том же антигене, или тремя разными эпитопами, присутствующими на двух разных антигенах.
Используемый в данном документе термин «полиспецифическое» антитело относится к антителу, которое способно связываться с двумя или более разными антигенами или двумя или более разными эпитопами на одном и том же антигене. Таким образом, полиспецифические антитела включают би- и триспецифические антитела.
Биспецифические антитела в формате полноразмерного IgG можно получать за счет слияния двух отдельных гибридом с образованием гибридной квадромы, которая продуцирует смесь антител, включающую фракцию биспецифических гетеродимеризующихся антител (Chelius D. et al.; MAbs. 2010 May-Jun; 2(3): 309–319). Биспецифические гетеродимеризующиеся антитела можно альтернативно получать с использованием рекомбинантных методик. Гетеродимеризацию также можно обеспечивать за счет конструирования поверхности контакта для димеризации в Fc-области, чтобы содействовать гетеродимеризации. Одним из примеров этого являются так называемые мутации «выступ-во-впадину», когда стерически объемные боковые цепи (выступы) вводят в один Fc, совпадающий со стерически небольшими боковыми цепями (впадины) на противоположном Fc, за счет чего создается стерическая комплементарность, способствующая гетеродимеризации. Другими способами конструирования поверхностей контакта на Fc для гетеродимеризации являются электростатическая комплементарность, слияние с доменами гетеродимеризации, отличными от IgG, или использование природного явления обмена Fab-плечами в IgG4 человека для управления гетеродимеризацией. Примеры гетеродимеризованных биспецифических антител хорошо описаны в литературе, например (Klein C, et al.; MAbs. 2012 Nov-Dec; 4(6): 653–663). Особое внимание следует уделить легким цепям в гетеродимерных антителах. Правильного спаривания LC и HC можно достичь за счет применения общей легкой цепи. Опять же, конструирование поверхности контакта LC/HC можно использовать для содействия гетеродимеризации или конструирования перекреста легких цепей, как в CrossMabs. Повторную сборку антител in vitro в слегка восстанавливающих условиях из двух отдельных IgG, содержащих соответствующие мутации, также можно использовать для получения биспецифических антител (например, Labrijn et al., PNAS, 110, 5145–5150 (2013)). Также сообщается, что природный способ обмена Fab-плечами обеспечивает правильное спаривание легких цепей.
Молекулы на основе полиспецифических антител также можно экспрессировать рекомбинантным образом в виде слитых белков, объединяющих природные модули IgG с образованием полиспецифических и поливалентных производных антител, описанных в литературе. Примерами слитых антител являются DVD-Ig, IgG-scFV, диатела, DART и т. д. В слитые белки можно вводить специфические метки для обнаружения или очистки, фрагменты для удлинения времени полужизни или другие компоненты. Дополнительные, отличные от IgG элементы также можно вводить в слитые белки. Биспецифические полноразмерные антитела, основанные на гетеродимеризации Fc, обычно называют асимметричными IgG, независимо от методологии спаривания LC.
Обычно биспецифические антитела можно получать в различных молекулярных форматах, как описано Brinkmann et al. (Brinkmann et al. The making of bispecific antibodies. Mabs 9, 182–212 (2017)).
Молекулы на основе полиспецифических антител также можно получать путем химической конъюгации или сопряжения отдельных полноразмерных IgG или сопряжения фрагментов IgG с образованием полиспецифических и поливалентных производных антител, описанных в литературе. Примерами являются химически сопряженные Fab-фрагменты, димер IgG и т. д. В конъюгированные белки можно вводить специфические метки для обнаружения или очистки, молекулы для удлинения времени полужизни или другие компоненты. Дополнительные, отличные от IgG полипептиды также можно вводить в слитые белки. Полиспецифические молекулы также можно получать за счет объединения рекомбинантных и химических способов, в том числе описанных выше.
В одном аспекте антитело по настоящему изобретению представляет собой химерное антитело, человеческое антитело или гуманизированное антитело. Такое антитело можно получать с использованием, например, подходящих платформ для дисплея антител или иммунизации или других подходящих платформ или способов, известных из уровня техники. Подразумевается, что используемый в данном документе термин «человеческое антитело» обозначает антитела, имеющие вариабельные домены, в которых по меньшей мере часть каркасной области и/или по меньшей мере часть области CDR получены из последовательностей иммуноглобулина зародышевой линии человека. Например, человеческое антитело может иметь вариабельные домены, в которых как каркасные, так и области CDR получены из последовательностей иммуноглобулина зародышевой линии человека. Кроме того, если антитело содержит константную область, то константная область или ее часть также получены из последовательностей иммуноглобулина зародышевой линии человека. Человеческие антитела по настоящему изобретению могут включать аминокислотные остатки, не кодируемые последовательностями иммуноглобулинов зародышевой линии человека (например, мутации, введенные за счет случайного или сайт-специфического мутагенеза in vitro или за счет соматической мутации in vivo).
Такое человеческое антитело может представлять собой человеческое моноклональное антитело. Такое человеческое моноклональное антитело может продуцироваться гибридомой, которая включает В-клетку, полученную от трансгенного животного, отличного от человека, например, трансгенной мыши, имеющей геном, включающий репертуары генных сегментов тяжелой и легкой цепей иммуноглобулина человека, слитую с иммортализованной клеткой.
Человеческие антитела можно выделять из библиотек последовательностей, построенных на наборах последовательностей зародышевой линии человека, дополнительно диверсифицированных с помощью введения природного и синтетического разнообразия последовательностей.
Человеческие антитела можно получать за счет иммунизации человеческих лимфоцитов in vitro с последующей трансформацией лимфоцитов с помощью вируса Эпштейна-Барр.
Человеческие антитела можно получать за счет рекомбинантных способов, известных из уровня техники.
Термин «производное человеческого антитела» относится к любой модифицированной форме человеческого антитела, такой как конъюгат антитела и другого средства или антитела.
Используемый в данном документе термин «гуманизированное антитело» относится к человеческому/отличному от человеческого антителу, которое содержит последовательность (области CDR или их части), полученную из иммуноглобулина, отличного от человеческого. Таким образом, гуманизированное антитело представляет собой человеческий иммуноглобулин (реципиентное антитело), в котором остатки из по меньшей мере гипервариабельной области реципиентного антитела заменены остатками из гипервариабельной области антитела вида, отличного от человека (донорское антитело), такого как мышь, крыса, кролик или отличный от человека примат, которое обладает необходимой специфичностью, аффинностью, составом и функциональностью последовательности. В некоторых случаях каркасные (FR) остатки человеческого иммуноглобулина заменяют соответствующими остатками, отличными от человеческих. Примером такой модификации является введение одной или нескольких так называемых обратных мутаций, которые, как правило, представляют собой аминокислотные остатки, полученные из донорского антитела. Гуманизацию антитела можно осуществлять с использованием рекомбинантных методик, известных специалисту в данной области (см., например, Antibody Engineering, Methods in Molecular Biology, vol. 248, edited by Benny K. Lo). Подходящий человеческий реципиентный каркас для вариабельного домена как легкой, так и тяжелой цепи, можно идентифицировать, например, по гомологии последовательности или структуры. В качестве альтернативы можно использовать фиксированные реципиентные каркасы, например, на основании знания структуры, биофизических и биохимических свойств. Реципиентные каркасы можно получать из зародышевой линии или получать из последовательности зрелого антитела. Области CDR от донорского антитела можно переносить за счет прививания CDR. CDR-привитое гуманизированное антитело можно дополнительно оптимизировать, например, в отношении аффинности, функциональности и биофизических свойств, за счет идентификации критически важных положений в каркасе, где повторное введение (обратная мутация) аминокислотного остатка из донорского антитела оказывает благотворное влияние на свойства гуманизированного антитела. В дополнение к обратным мутациям на основе донорских антител гуманизированное антитело можно конструировать за счет введения остатков зародышевой линии в CDR или каркасные области, удаления иммуногенных эпитопов, сайт-направленного мутагенеза, созревания аффинности и т.д.
Более того, гуманизированные антитела могут содержать остатки, которые не обнаружены ни в реципиентном антителе, ни в донорском антителе. Эти модификации производят для дополнительного улучшения эксплуатационных характеристик антитела. В целом, гуманизированное антитело будет содержать по меньшей мере один, как правило, два вариабельных домена, в которых все или практически все области CDR соответствуют областям иммуноглобулина, отличного от человеческого, и в которых все или практически все остатки FR представляют собой остатки из последовательности иммуноглобулина человека. Гуманизированное антитело необязательно также может содержать по меньшей мере часть константной области (Fc) иммуноглобулина, как правило, иммуноглобулина человека.
Термин «производное гуманизированного антитела» относится к любой модифицированной форме гуманизированного антитела, такой как конъюгат антитела и химического средства или конъюгат антитела с другим антителом.
Используемый в данном документе термин «химерное антитело» относится к антителу, содержащему части антител, полученные от двух или более видов. Например, гены, кодирующие такое антитело, содержат гены, кодирующие вариабельные домены, и гены, кодирующие константные домены, происходящие от двух разных видов. Например, гены, кодирующие вариабельные домены мышиного моноклонального антитела, можно присоединять к генам, кодирующим константные домены антитела человеческого происхождения.
Область кристаллизующегося фрагмента («Fc-область»/«домен Fc») антитела представляет собой C-концевую область антитела, которая содержит шарнир и константные домены CH2 и CH3. Домен Fc может взаимодействовать с рецепторами клеточной поверхности, называемыми Fc-рецепторами, а также с некоторыми белками системы комплемента. Fc-область позволяет антителам взаимодействовать с иммунной системой. В одном аспекте настоящего изобретения можно конструировать антитела с включением модификаций в пределах Fc-области, как правило, для изменения одного или нескольких его функциональных свойств, таких как время полужизни в сыворотке крови, связывание комплемента, связывание с Fc-рецептором, стабильность белка и/или антиген-зависимая клеточная цитотоксичность или ее отсутствие, среди прочего. Кроме того, антитело по настоящему изобретению можно химически модифицировать (например, к антителу можно присоединять одну или более химических групп) или модифицировать для изменения его гликозилирования, опять же, для изменения одного или нескольких функциональных свойств антитела. Антитело IgG1 может нести модифицированный домен Fc, содержащий одну или более и, возможно, все из следующих мутаций, которые будут приводить к снижению аффинности к определенным Fc-гамма-рецепторам (L234A, L235E и G237A) и к уменьшению опосредованного C1q связывания комплемента (A330S и P331S) соответственно (нумерация остатков в соответствии с индексом EU). В качестве альтернативы можно использовать другие аминокислотные замены и их комбинации и комбинации с вышеупомянутым, известные из уровня техники, чтобы получить измененное (уменьшенное или увеличенное) связывание с Fc-гамма-рецептором.
Изотип антитела по настоящему изобретению может представлять собой IgG, такой как IgG1, такой как IgG2, такой как IgG4. При необходимости класс антитела можно «переключать» с помощью известных методик. Например, у антитела, которое первоначально было получено в виде молекулы IgM, можно переключить класс на антитело IgG. Методики переключения классов также можно использовать для преобразования одного подкласса IgG в другой, например, из IgG1 в IgG2 или IgG4; из IgG2 в IgG1 или IgG4; или из IgG4 в IgG1 или IgG2. Можно также выполнять конструирование антител с получением химерных по константной области молекул путем объединения областей из разных подклассов IgG.
В одном варианте осуществления шарнирную область антитела модифицируют таким образом, что количество остатков цистеина в шарнирной области изменяется, например увеличивается или уменьшается. Этот подход дополнительно описан, например, в патенте США № 5677425 от Bodmer et al.
Константную область можно модифицировать для стабилизации антитела, например для снижения риска разделения бивалентного антитела на полуантитела. Например, в константной области lgG4 остаток S228 (согласно индексу нумерации EU и S241 в соответствии с Kabat) можно мутировать в остаток пролина (P) для стабилизации образования дисульфидного мостика между тяжелыми цепями в шарнире (см., например, Angal et al. Mol Immunol. 1993; 30:105–8).
Антитела или их фрагменты можно определить с точки зрения их определяющих комплементарность областей (CDR). Используемый в данном документе термин «определяющая комплементарность область» или «гипервариабельная область» относится к областям антитела, в которых расположены аминокислотные остатки, участвующие в связывании антигена. Область гипервариабельности или CDR можно идентифицировать как области с самой высокой вариабельностью при аминокислотном выравнивании вариабельных доменов антител. Для идентификации CDR можно использовать базы данных, такие как база данных Kabat, при этом CDR, например, определяются как содержащие аминокислотные остатки 24–34 (L1), 50–56 (L2) и 89–97 (L3) вариабельного домена легкой цепи и 31–35 (H1), 50–65 (H2) и 95–102 (H3) в вариабельном домене тяжелой цепи (Kabat et al. 1991; Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91–3242). В качестве альтернативы CDR можно определять как остатки из «гипервариабельной петли» (остатки 26–33 (L1), 50–52 (L2) и 91–96 (L3) в вариабельном домене легкой цепи и 26–32 (H1), 53–55 (H2) и 96–101 (H3) в вариабельном домене тяжелой цепи; Chothia and Lesk, J. Mol. Biol. 1987; 196:901–917). Как правило, нумерацию аминокислотных остатков в этой области выполняют с помощью способа, описанного в Kabat et al. выше. В данном документе такие фразы, как «положение по Kabat», «остаток по Kabat» и «в соответствии с Kabat», относятся к этой системе нумерации для вариабельных доменов тяжелой цепи или вариабельных доменов легкой цепи. При применении системы нумерации по Kabat, фактическая линейная аминокислотная последовательность пептида может содержать меньшее количество или дополнительные аминокислоты, соответствующие укорочению или вставке в каркас (FR) или CDR вариабельного домена. Например, вариабельный домен тяжелой цепи может включать аминокислотные вставки (остатки 52a, 52b и 52c в соответствии с Kabat) после остатка 52 из CDR H2 и вставленные остатки (например, остатки 82a, 82b и 82c и т. д. в соответствии с Kabat) после остатка 82 в FR тяжелой цепи. Нумерацию остатков по Kabat можно определить для данного антитела путем выравнивания по областям гомологии последовательности антитела со «стандартной» последовательностью, пронумерованной по Kabat.
Термин остатки «каркасной области» или «FR» относятся к тем аминокислотным остаткам в VH или VL, которые не находятся в пределах CDR, определенных в данном документе.
Антитело по настоящему изобретению может содержать область CDR из одного или более специфических антител, раскрытых в данном документе.
Термин «прокоагулянтное антитело» относится к антителу, которое усиливает свертывание крови, например, за счет ускорения процесса свертывания крови и/или увеличения ферментативной активности одного или нескольких факторов свертывания крови.
Термин «прокоагулянтная активность» относится к способности соединения, такого как антитело, усиливать свертывание крови, например, за счет ускорения процесса свертывания крови и/или увеличения ферментативной активности одного или нескольких факторов свертывания крови.
Термин «антиген» (Ag) относится к молекулярному объекту, используемому для иммунизации иммунокомпетентного позвоночного животного, чтобы образовалось антитело (Ab), которое распознает Ag. В данном документе Ag определяется более широко и обычно подразумевается, что он включает целевые молекулы, которые специфически распознаются Ab, таким образом, включая фрагменты или имитаторы молекулы, используемой в процессе иммунизации или в другом процессе, например фаговом дисплее, используемом для выработки Ab.
Настоящее изобретение охватывает варианты антител или их антигенсвязывающих фрагментов по настоящему изобретению, которые могут содержать 1, 2, 3, 4 или 5 аминокислотных замен, и/или делеций, и/или вставок в отдельных последовательностях, раскрытых в данном документе.
Варианты с «заменой» предпочтительно включают замену одной или нескольких аминокислот тем же количеством аминокислот. Замены без ограничения могут представлять собой консервативные замены. Например, аминокислота может быть заменена аминокислотой с аналогичными биохимическими свойствами, например, основная аминокислота может быть заменена другой основной аминокислотой (например, лизин аргинином), кислая аминокислота может быть заменена другой кислой аминокислотой (например, глутамат аспартатом), нейтральная аминокислота может быть заменена другой нейтральной аминокислотой (например, треонин серином), заряженная аминокислота может быть заменена другой заряженной аминокислотой (например, глутамат аспартатом), гидрофильная аминокислота кислота может быть заменена другой гидрофильной аминокислотой (например, аспарагин глутамином), гидрофобная аминокислота может быть заменена другой гидрофобной аминокислотой (например, аланин валином), полярная аминокислота может быть заменена другой полярной аминокислотой (например, серин треонином), ароматическая аминокислота может быть заменена другой ароматической аминокислотой (например, фенилаланин триптофаном), а алифатическая аминокислота может быть заменена другой алифатической аминокислотой (например, лейцин изолейцином).
Предпочтительные варианты включают те, в которых вместо аминокислоты, которая появляется в последовательности, содержится структурный аналог аминокислоты.
Эпитоп и паратоп
Используемый в данном документе термин «эпитоп» определяется в контексте молекулярного взаимодействия между «антигенсвязывающим полипептидом», таким как антитело (Ab), и его соответствующим антигеном (Ag). Обычно «эпитоп» относится к области или участку на Ag, с которыми связывается Ab, т. е. к зоне или области физического контакта с Ab. Физический контакт можно определить с использованием различных критериев (например, предела расстояния 2–6 Å, такого как 3 Å, такого как 3,5 Å, такого как 4 Å, такого как 4,5 Å, такого как 5 Å, или доступности для растворителя) для атомов в молекулах Ab и Ag.
FIX/FIXa и FX/FXa могут содержать целый ряд различных эпитопов, которые могут включать без ограничения: (1) линейные пептидные эпитопы, (2) конформационные эпитопы, которые состоят из одной или нескольких несмежных аминокислот, расположенных рядом друг с другом в зрелой конформации FIX/FIXa или FX/FXa; и (3) эпитопы, которые полностью или частично состоят из молекулярных структур, ковалентно присоединенных к FIX/FIXa или FX/FXa, таких как углеводные группы.
Эпитоп для данной пары антитело (Ab)/антиген (Ag) можно описать и охарактеризовать на разных уровнях детализации с использованием различных экспериментальных и вычислительных способов картирования эпитопов. Экспериментальные способы включают мутагенез, рентгеновскую кристаллографию, ядерную магнитно-резонансную (ЯМР) спектроскопию, масс-спектрометрию водородно-дейтериевого обмена (HDX-MS) и различные способы конкурентного связывания; способы, которые известны из уровня техники. Поскольку каждый способ основан на уникальном принципе, описание эпитопа тесно связано со способом, с помощью которого он был определен. Таким образом, в зависимости от используемого способа картирования эпитопа, эпитоп для данной пары Ab/Ag может описываться по-разному.
В контексте полученной с помощью рентгеновских лучей кристаллической структуры, определяемой пространственными координатами комплекса между Ab, например Fab-фрагментом, и его Ag, термин «эпитоп» в данном документе, если иное не указано или не противоречит контексту, конкретно определен как остатки FIX/FIXa или FX/FXa, характеризующиеся наличием тяжелого атома (т. е. отличного от водорода атома) на расстоянии 3,5 Å от тяжелого атома в Ab.
Считается, что эпитопы, описанные на уровне аминокислот, например определенные на основании рентгеновской структуры, являются идентичными, если они содержат одинаковый набор аминокислотных остатков. Считается, что эпитопы перекрываются, если по меньшей мере один аминокислотный остаток является общим для эпитопов. Считается, что эпитопы являются отдельными (уникальными), если отсутствуют аминокислотные остатки, которые являются общими для эпитопов.
Определение термина «паратоп» получено из приведенного выше определения «эпитоп» путем обращения угла зрения. Таким образом, термин «паратоп» относится к зоне или области на антителе или его фрагменте, с которым связывается антиген, т. е. с помощью которых оно вступает в физический контакт с антигеном.
В контексте полученной с помощью рентгеновских лучей кристаллической структуры, определяемой пространственными координатами комплекса между Ab, таким как Fab-фрагмент, и его Ag, термин «паратоп» в данном документе, если иное не указано или не противоречит контексту, конкретно определен как остатки Ab, характеризующиеся наличием тяжелого атома (т. е. отличного от водорода атома) на расстоянии 3,5 Å от тяжелого атома в FIX/FIXa или FX/FXa.
Эпитоп и паратоп для данной пары антитело (Ab)/антиген (Ag) можно идентифицировать обычными способами. Например, общее местоположение эпитопа можно определить путем оценки способности антитела связываться с различными фрагментами или вариантами FIX/FIXa или FX/FXa. Специфические аминокислоты в пределах FIX/FIXa или FX/FXa, которые вступают в контакт с антителом (эпитоп), и специфические аминокислоты в антителе, которые вступают в контакт с FIX/FIXa или FX/FXa (паратоп), также можно определять обычными способами. Например, антитело и целевую молекулу можно объединять и комплекс Ab:Ag можно кристаллизовать. Кристаллическую структуру комплекса можно определять и использовать для идентификации специфических участков взаимодействия между антителом и его мишенью.
Эпитопы на антигене могут содержать один или более остатков-«горячих точек», т. е. остатков, которые особенно важны для взаимодействия с когнатным антителом, и где взаимодействия, опосредованные боковой цепью указанного остатка-«горячей точки», вносят значительный вклад в энергию связывания для взаимодействия антитело/антиген (Peng et al. (2014) PNAS 111, E2656–E2665). Остатки-«горячие точки» можно идентифицировать путем тестирования вариантов антигена (в данном документе FIX/FIXa и FX), в которых отдельные остатки эпитопа были заменены, например аланином, в отношении связывания с когнатным антителом. Если замена эпитопного остатка аланином оказывает сильное влияние на связывание с антителом, то указанный остаток эпитопа считается остатком-«горячей точкой» и, следовательно, имеет особое значение для связывания антитела с антигеном.
Антитела, которые связываются с одним и тем же антигеном, можно характеризовать с точки зрения их способности связываться с их общим антигеном одновременно и можно подвергать «конкурентному связыванию»/«сортировке по группам». В контексте настоящего изобретения термин «сортировка по группам» относится к способу группировки антител, которые связываются с одним и тем же антигеном. «Сортировка по группам» антител может быть основана на конкурентном связывании двух антител с их общим антигеном в анализах на основании стандартных методик.
«Группу» антитела определяют с использованием эталонного антитела. Если второе антитело не способно связываться с антигеном одновременно с эталонным антителом, считается, что второе антитело относится к той же «группе», что и эталонное антитело. В этом случае эталонное и второе антитело конкурентно связывают одну и ту же часть антигена и представляют собой «конкурирующие антитела». Если второе антитело способно связываться с антигеном одновременно с эталонным антителом, считается, что второе антитело относится к отдельной «группе». В этом случае эталонное и второе антитело не связывают конкурентно одну и ту же часть антигена и обозначаются как «неконкурирующие антитела».
«Сортировка по группам» антител не дает прямой информации об эпитопе.
Конкурирующие антитела, т. е. антитела, принадлежащие к одной и той же «группе», могут быть характерны идентичные эпитопы, перекрывающиеся эпитопы или даже отдельные эпитопы. Последнее имеет место, если эталонное антитело, связанное со своим эпитопом на антигене, занимает пространство, необходимое для того, чтобы второе антитело вошло в контакт со своим эпитопом на антигене («стерическое затруднение»). Неконкурирующие антитела обычно характеризуются отдельными эпитопами. Таким образом, в некоторых вариантах осуществления антитела по настоящему изобретению будут связываться с тем же эпитопом, что и по меньшей мере одно из антител, конкретно раскрытых в данном документе.
Конкурентные анализы для определения того, конкурирует ли антитело за связывание с антителом к FIX/FIXa или антителом к FX/FXa, раскрытыми в данном документе, известны из уровня техники. Иллюстративные конкурентные анализы включают иммунологические анализы (например, анализы ELISA, анализы RIA), анализ с использованием поверхностного плазмонного резонанса (например, с использованием прибора BIAcore™), интерферометрию биослоев (ForteBio®) и проточную цитометрию.
Как правило, конкурентный анализ предусматривает применение антигена, связанного с твердой поверхностью или экспрессированного на клеточной поверхности, тестируемого антитела, связывающего FIX- или FIXa, и эталонного антитела. Эталонное антитело является меченым, а тестируемое антитело немеченым. Конкурентное ингибирование измеряют путем определения количества меченого эталонного антитела, связанного с твердой поверхностью или клетками в присутствии тестируемого антитела. Обычно тестируемое антитело присутствует в избытке (например, при 1-, 5-, 10-, 20-, 100-, 1000-, 10000- или 100000-кратном). Антитела, идентифицированные как конкурировавшие в конкурентном анализе (т.е. конкурирующие антитела), включают антитела, связывающиеся с тем же эпитопом или с перекрывающимися эпитопами, что и эталонное антитело, и антитела, связывающиеся с прилежащим эпитопом, достаточно близким к эпитопу, связанному эталонным антителом, для возникновения стерического затруднения.
В иллюстративном конкурентном анализе эталонное антитело к FIX или к FIXa биотинилируют с использованием коммерчески доступных реагентов. Биотинилированное эталонное антитело смешивают с серийными разведениями тестируемого антитела или немеченого эталонного антитела (контроль самоконкуренции), что приводит к смеси при различных молярных соотношениях (например, 1-, 5-, 10-, 20-, 100-, 1000-, 10000- или 100000-кратном) тестируемого антитела (или немеченого эталонного антитела) и меченого эталонного антитела. Смесь антител добавляют в планшет для ELISA, покрытый полипептидом FIX или FIXa. Затем планшет промывают и в качестве реагента для обнаружения в планшет добавляют пероксидазу хрена (HRP)-стрептавидин. Количество меченого эталонного антитела, связанного с целевым антигеном, обнаруживают после добавления хромогенного субстрата (например, TMB (3,3',5,5'-тетраметилбензидин) или ABTS (2,2"-азино-ди-(3-этилбензтиазолин-6-сульфонат)), которые известны из уровня техники. Данные оптической плотности (единицы OD) получают с использованием спектрометра (например, спектрометра SpectraMax® M2 (Molecular Devices)). Ответ (единицы OD), соответствующий нулевому проценту ингибирования, определяют на основании лунок без какого-либо конкурирующего антитела. Ответ (единицы OD), соответствующий 100% ингибированию, т. е. фоновое значение анализа, определяют на основании лунок без какого-либо меченого эталонного антитела или тестируемого антитела. Процент ингибирования меченого эталонного антитела к FIX или FIXa тестируемым антителом (или немеченым эталонным антителом) при каждой концентрации рассчитывают следующим образом: % ингибирования = (1- (единицы OD - 100% ингибирования)/(0% ингибирования - 100% ингибирования))* 100.
Специалисту в данной области будет понятно, что аналогичные анализы можно выполнить для определения того, характеризуются ли два или более антител к FX/FXa общей областью связывания, группой и/или конкурентным связыванием антигена. Специалисты в данной области также будут понимать, что конкурентный анализ можно выполнять с использованием различных систем обнаружения, известных из уровня техники.
Тестируемое антитело конкурирует с эталонным антителом за связывание с антигеном, если избыток одного антитела (например, 1-, 5-, 10-, 20-, 100-, 1000-, 10000- или 100000-кратный) ингибирует связывание другого антитела, например на по меньшей мере 50%, 75%, 90%, 95% или 99%, как измерено в анализе конкурентного связывания.
Если не указано иное, конкуренцию определяют с использованием конкурентного анализа ELISA, описанного выше.
Термин «аффинность связывания» используется в данном документе как показатель силы нековалентного взаимодействия между двумя молекулами, например, антителом или его фрагментом и антигеном. Термин «аффинность связывания» используется для описания моновалентных взаимодействий.
Аффинность связывания между двумя молекулами, например антителом или его фрагментом и антигеном, посредством моновалентного взаимодействия можно оценить количественно путем определения равновесной константы диссоциации (KD). KD можно определить путем измерения кинетики образования и диссоциации комплекса, например, с помощью способа поверхностного плазмонного резонанса (SPR) или способа изотермической титрационной калориметрии (ITC). Константы скорости, соответствующие ассоциации и диссоциации моновалентного комплекса, обозначаются как константа скорости ассоциации, ka (или kon), и константа скорости диссоциации, kd (или koff), соответственно. KD соотносится с ka и kd через уравнение KD = kd / ka.
Следуя приведенному выше определению, аффинности связывания, ассоциированные с различными молекулярными взаимодействиями, такие как сравнение аффинности связывания различных антител для данного антигена, можно сравнивать путем сравнения значений KD для отдельных комплексов антитело/антиген.
Значение константы диссоциации можно определить напрямую хорошо известными способами. Стандартные анализы для оценки способности связывания лигандов, таких как антитела, с мишенями известны из уровня техники и включают, например, анализы ELISA, вестерн-блоттинг, RIA и проточную цитометрию. Кинетику связывания и аффинность связывания антитела также можно оценить с помощью стандартных анализов, известных из уровня техники, таких как SPR. Однако предпочтительно для измерения аффинностей взаимодействия антитело/мишень, а также для получения термодинамических параметров взаимодействия можно использовать изотермическую титрационную калориметрию (ITC).
Можно проводить анализ конкурентного связывания, в котором связывание антитела с мишенью сравнивают со связыванием мишени другим лигандом этой мишени, таким как другое антитело.
KD антитела по настоящему изобретению для его мишени может составлять меньше 100 мкМ, как, например, меньше 10 мкМ, как, например, меньше 9 мкМ, как, например, меньше 8 мкМ, как, например, меньше 7 мкМ, как, например, меньше 6 мкМ, как, например, меньше 5 мкМ, как, например, меньше 4 мкМ, как, например, меньше 3 мкМ, как, например, меньше 2 мкМ, как, например, меньше 1 мкМ, как, например, меньше 0,9 мкМ, как, например, меньше 0,8 мкМ, как, например, меньше 0,7 мкМ, как, например меньше 0,6 мкМ, как, например, меньше 0,5 мкМ, как, например, меньше 0,4 мкМ, как, например, меньше 0,3 мкМ, как, например, меньше 0,2 мкМ, как, например, меньше 0,1 мкМ.
В одном таком варианте осуществления антитело представляет собой биспецифическое антитело, содержащее плечо к FX с KD в отношении FX, составляющей меньше 100 мкM, как, например, меньше 10 мкM как, например, меньше 9 мкM, как, например, меньше 8 мкM, как, например, меньше 7 мкM, как, например, меньше 6 мкM, как, например, меньше 5 мкM, как, например, меньше 4 мкM, как, например, меньше 3 мкМ, как, например, меньше 2 мкМ, как, например, меньше 1 мкМ, как, например, меньше 0,9 мкМ, как, например, меньше 0,8 мкМ, как, например, меньше 0,7 мкМ, как, например, меньше 0,6 мкМ, как, например, меньше 0,5 мкМ, как, например, меньше 0,4 мкМ, как, например, меньше 0,3 мкМ, как, например, меньше 0,2 мкМ, как, например, меньше 0,1 мкМ, как, например, меньше 0,09 мкМ, как, например, меньше 0,08 мкМ, как, например, меньше 0,07 мкМ, как, например, меньше 0,06 мкМ, как, например, меньше 0,05 мкМ, как, например, меньше 0,04 мкМ, как, например, меньше 0,03 мкМ, как, например, меньше 0,02 мкМ, как, например, меньше 0,01 мкМ, как, например, меньше 9 нM, как, например, меньше 8 нM, как, например, меньше 7 нM, как, например, меньше 6 нM, как, например, меньше 5 нM, как, например, меньше 4 нM, как, например, меньше 3 нM, как, например, меньше 2 нM, как, например, меньше 1 нM, как, например, меньше 0,5 нM.
Антитела и фрагменты таких антител, описанные в данном документе, можно объединять с другими антителами и фрагментами антител, известными из уровня техники, с образованием молекул биспецифических, триспецифических или полиспецифических антител. Соединения, имитирующие функцию кофактора FVIII, ранее были созданы с использованием других связывающих FIX(a) и FX(a) доменов, каждый из которых потенциально может заменять описанные в данном документе связывающие FIX(a) и/или FX(a) домены. Таким образом, ясно, что связывающие FIX(a) и FX(a) домены по настоящему изобретению представляют самостоятельный интерес как отдельные компонентные молекулы (промежуточные соединения) в качестве частей би-, три- или полиспецифического антитела, содержащего по меньшей мере один связывающий FIX(a) и/или FX(a) домен.
Активность прокоагулянтных антител, включая би-, три- и полиспецифические антитела, можно определять с помощью способов, известных из уровня техники. Стандартные анализы включают тест тромбинообразования (TGT) в цельной крови, измерение времени свертывания с помощью тромбоэластографии (TEG) и анализы образования FXa.
Идентичность
Как известно в данной области термин «идентичность» относится к взаимосвязи между последовательностями двух или более полипептидов, определяемой путем сравнения последовательностей. В данной области «идентичность» также означает степень родства последовательностей у разных полипептидов, определяемую по количеству совпадений между отрезками из двух или более аминокислотных остатков. «Идентичность» измеряет процент идентичных совпадений у меньшей из двух или более последовательностей при выравниваниях с гэпами (если они есть), рассматриваемых с помощью конкретной математической модели или компьютерной программы (т. е. «алгоритмов»). Идентичность родственных полипептидов можно легко рассчитать известными способами.
В настоящем изобретении сходство и идентичность определяли с использованием алгоритма Needleman (Needleman et al. J. Mol. Biol. 1970; 48:443–453) в EMBOSS-6.6.0 с использованием параметров 10 и 0,5 для внесения и продления гэпов соответственно (gapopen=10, gapextend=0,5).
Фармацевтические составы
В другом аспекте настоящего изобретения предусмотрены композиции и составы, содержащие соединения по настоящему изобретению, такие как антитела, описанные в данном документе. Например, в настоящем изобретении предусмотрена фармацевтическая композиция, которая содержит одно или более антител по настоящему изобретению, составленных вместе с фармацевтически приемлемым носителем.
Соответственно, одна цель настоящего изобретения заключается в том, чтобы обеспечить фармацевтический состав, содержащий такое антитело, которое присутствует в концентрации от 0,25 мг/мл до 250 мг/мл, и где указанный состав характеризуется рН от 2,0 до 10,0. Состав может дополнительно содержать одно или более из буферной системы, консерванта, средства регуляции тоничности, хелатообразующего средства, стабилизатора или поверхностно-активного вещества, а также их различных комбинаций. Применение консервантов, изотонических средств, хелатообразующих средств, стабилизаторов и поверхностно-активных веществ в фармацевтических композициях хорошо известно специалисту. Можно сделать ссылку на Remington: The Science and Practice of Pharmacy, 19th edition, 1995.
В одном варианте осуществления фармацевтический состав представляет собой водный состав. Такой состав, как правило, представляет собой раствор или суспензию, но также может включать коллоиды, дисперсии, эмульсии и многофазные материалы. Термин «водный состав» определяется как состав, содержащий по меньшей мере 50% вес/вес воды. Аналогично, термин «водный раствор» определяется как раствор, содержащий по меньшей мере 50% вес/вес воды, а термин «водная суспензия» определяется как суспензия, содержащая по меньшей мере 50% вес/вес воды.
В другом варианте осуществления фармацевтический состав представляет собой лиофилизированный состав, в который растворитель и/или разбавитель добавляют перед применением.
В дополнительном аспекте фармацевтический состав содержит водный раствор такого антитела и буфер, где антитело присутствует в концентрации от 1 мг/мл или более, и где указанный состав характеризуется рН от приблизительно 2,0 до приблизительно 10,0.
В одном варианте осуществления настоящее изобретение относится к инъекционному устройству, содержащему указанную композицию. В некоторых вариантах осуществления фармацевтическая композиция по настоящему изобретению предназначена для применения и/или содержится в инъекционном устройстве. В некоторых вариантах осуществления инъекционное устройство представляет собой одноразовую предварительно заполненную многодозовую шприц-ручку типа FlexTouch® (поставщик Novo Nordisk A/S, Дания). В некоторых вариантах осуществления инъекционное устройство представляет собой устройство однократного действия.
В некоторых вариантах осуществления инъекционное устройство представляет собой устройство с фиксированной дозой, такое как устройство, выполненное с возможностью доставки нескольких заранее определенных доз лекарственного средства, иногда называемое устройством с несколькими фиксированными дозами или устройством с фиксированной дозой многократного действия.
В одном варианте осуществления фармацевтическую композицию по настоящему изобретению вводят с использованием инъекционного устройства, содержащего трубку с диаметром иглы 20 или более.
В одном варианте осуществления биспецифическое антитело в соответствии с таблицей 1 в данном документе вводят с использованием инъекционного устройства, содержащего трубку с диаметром иглы 20 или более.
В одном варианте осуществления биспецифическое антитело в соответствии с таблицей 1 в данном документе вводят с использованием инъекционного устройства, содержащего трубку с диаметром иглы от 20 до 36. В одном таком варианте осуществления биспецифическое антитело выбрано из перечня, состоящего из bimAb05-0745, bimAb05-3761, bimAb05-3761, bimAb05-2112, bimAb05-2113, bimAb05-2114, bimAb05-3769, bimAb05-4271, bimAb05-4756, bimAb05-0396, bimAb05-0417 и bimAb05-0438.
Введение и дозировки
Соединение по настоящему изобретению, такое как антитело, можно вводить парентерально, например внутривенно, например внутримышечно, например подкожно. В качестве альтернативы антитело по настоящему изобретению можно вводить непарентеральным путем, например перорально или местно. Антитело по настоящему изобретению можно вводить профилактически. Антитело по настоящему изобретению можно вводить терапевтически (при необходимости).
Доза соединений, которые требуется доставить, может составлять от приблизительно 0,01 мг до 500 мг соединения в сутки, предпочтительно от приблизительно 0,1 мг до 250 мг в сутки и более предпочтительно от приблизительно 0,5 мг до приблизительно 250 мг в сутки, в неделю, в две недели или в месяц в качестве нагрузочных и поддерживающих доз в зависимости от тяжести состояния. Подходящую дозу также можно отрегулировать для конкретного соединения на основе свойств этого соединения, включая его время полужизни in vivo или среднее время удержания и его биологическую активность. Например, соединения, которые требуется доставить, в одном варианте осуществления можно вводить один раз в неделю, или в другом варианте осуществления один раз в две недели, или в другом варианте осуществления один раз в месяц, и в каждом из указанных вариантов осуществления в дозе, например, 0,025, 0,05, 0,075, 0,1, 0,125, 0,15, 0,175, 0,2, 0,25, 0,3, 0,35, 0,4, 0,45, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5, 7, 7,5, 8, 8,5, 9, 9,5 или 10 мг на кг массы тела.
Композиции, содержащие соединения, раскрытые в данном документе, можно вводить для профилактического и/или, в некоторых вариантах осуществления, для терапевтического лечения. При терапевтических путях применениях композиции вводят субъекту, уже страдающему заболеванием, таким как любое нарушение свертываемости крови, описанное выше, в количестве, достаточном для излечения, облегчения или частичной задержки развития заболевания и его осложнений. Количество, достаточное для достижения этого, определяется как «терапевтически эффективное количество». Как будет понятно специалисту в данной области, количества, эффективные для этой цели, будут зависеть от тяжести заболевания или поражения, а также от массы и общего состояния субъекта.
Варианты осуществления
Настоящее изобретение дополнительно описывается следующими вариантами осуществления.
1. Антитело или его антигенсвязывающий фрагмент, способные связываться с фактором IX (FIX) под SEQ ID NO:1 и/или его активированной формой (FIXa).
2. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 1, где антитело или его антигенсвязывающий фрагмент являются частью «группы B», описанной в данном документе.
3. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 1, где антитело или его антигенсвязывающий фрагмент конкурируют с эталонным антителом, где эталонное антитело содержит:
a. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:35, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:39,
b. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:43, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:47, или
c. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:51, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:55, или
d. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:67, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:71, или
e. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1202, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1206, или
f. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1210, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1214, или
g. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1218, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1222, или
h. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1226, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1230, или
i. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1234, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1238, или
j. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1242, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1246.
4. Антитело или его антигенсвязывающий фрагмент по предыдущему варианту осуществления, где эталонное антитело представляет собой Fab.
5. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент содержат:
a. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:35, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:39; или
b. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:43, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:47; или
c. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:51, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:55; или
d. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:67, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:71, или
e. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1202, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1206, или
f. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1210, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1214, или
g. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1218, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1222, или
h. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1226, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1230, или
i. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1234, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1238, или
j. вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1242, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:1246.
6. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 5, где вариабельный домен тяжелой цепи на по меньшей мере 92, 94, 96, 97, 98, 99, 99,1 или 99,2% идентичен последовательности, идентифицированной под SEQ ID NO:35, 43, 51, 67, 1202, 1210, 1218, 1226, 1234 или 1242 соответственно.
7. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 5, где вариабельный домен легкой цепи на по меньшей мере 92, 94, 96, 97, 98, 99, 99,1 или 99,2% идентичен последовательности, идентифицированной под SEQ ID NO: 39, 47, 55, 71, 1206, 1214, 1222, 1230, 1238 или 1246 соответственно.
8. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 6 и 7, где как вариабельный домен тяжелой цепи, так и вариабельный домен легкой цепи на по меньшей мере 92, 94, 96, 97, 98, 99, 99,1 или 99,2% идентичны идентифицированным SEQ ID.
9. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий один или более аминокислотных остатков L337, R338, S339, T340, K341 и T343 из SEQ ID NO:1.
10. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий аминокислотный остаток R338 из SEQ ID NO:1.
11. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий аминокислотные остатки R338 и K341 из SEQ ID NO:1.
12. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий два или три аминокислотных остатка L337, R338, S339, T340, K341 и T343 из SEQ ID NO:1.
13. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий четыре или пять аминокислотных остатков L337, R338, S339, T340, K341 и T343 из SEQ ID NO:1.
14. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий:
a. R338, S339, T340, K341 и T343,
b. L337, S339, T340, K341 и T343,
c. L337, R338, T340, K341 и T343,
d. L337, R338, S339, K341 и T343,
e. L337, R338, S339, T340 и T343,
f. L337, R338, S339, T340 и K341,
g. L337, R338, S339 и T340 или
h. R338, T340 и K341
из SEQ ID NO:1.
15. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1–11, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий аминокислотные остатки:
a. R338, T340 и K341 из SEQ ID NO:1 или
b. L337, R338, S339, T340 и K341 из SEQ ID NO:1.
16. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, содержащие паратоп, содержащий следующие аминокислотные остатки:
a. H30, D31, W53, D56, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:67) и Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:71), необязательно содержащие одну, две или три аминокислотные замены в десяти перечисленных аминокислотных остатках паратопа, или
b. H30, D31, W53, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:51) и остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO: 55), необязательно содержащие одну, две или три аминокислотные замены в девяти перечисленных аминокислотных остатках паратопа.
17. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1–16, содержащие паратоп, содержащий следующие аминокислотные остатки D30, D31, W53, S102, S104 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO: 35) и Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO: 39), необязательно содержащие одну, две или три аминокислотные замены в восьми перечисленных аминокислотных остатках паратопа.
18. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 16 или 17, где указанная(-ые) замена(-ы) представляет(-ют) собой консервативную(-ые) замену(-ы).
19. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент содержат:
a.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:35, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:39, или
b.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:43, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:47, или
c.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:51, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:55, или
d.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:67, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:71, или
e.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1202, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1206, или
f.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1210, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1214, или
g.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1218, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1222, или
h.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1226, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1230, или
i.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1234, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1238, или
j.
i. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1242, и
ii. три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замени по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1246.
20. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 19, где три последовательности CDR тяжелой цепи содержат максимум 9, как, например, 8, как, например, 7 или, как, например, 6 аминокислотных замен по сравнению с CDR из идентифицированных SEQ ID.
21. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 19, где три последовательности CDR тяжелой цепи содержат максимум 5, как, например, 4, как, например, 3, как, например, 2 или максимум 1 аминокислотную замену по сравнению с CDR из идентифицированных SEQ ID.
22. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 19, где три последовательности CDR легкой цепи содержат максимум 9, как, например, 8, как, например, 7 или, как, например, 6 аминокислотных замен по сравнению с CDR из идентифицированных SEQ ID.
23. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 19, где три последовательности CDR легкой цепи содержат максимум 5, как, например, 4, как, например, 3, как, например, 2 или максимум 1 аминокислотную замену по сравнению с CDR из идентифицированных SEQ ID.
24. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент содержат:
a. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:35, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:39, или
b. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:43, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:47, или
c. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:51, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:55, или
d. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:67, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:71, или
e. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1202, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1206, или
f. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1210, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1214, или
g. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1218, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1222, или
h. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1226, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1230, или
i. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1234, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1238, или
j. последовательности CDR из вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1242, и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1246.
25. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент содержат:
a. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:35, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:39, или
b. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:43, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:47, или
c. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:51, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:55, или
d. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:67, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:71, или
e. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1202, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1206, или
f. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1210, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1214, или
g. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1218, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1222, или
h. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1226, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1230, или
i. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1234, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1238, или
j. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1242, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1246.
26. Антитело или его антигенсвязывающий фрагмент, способные связываться с FX (SEQ ID NO:2) и/или его активированной формой (FXa).
27. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 26, где антитело или его антигенсвязывающий фрагмент является частью «группы 2».
28. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 26, где антитело или его антигенсвязывающий фрагмент конкурируют с эталонным антителом, где эталонное антитело содержит:
a. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:467, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:471, или
b. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:483, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:487, или
c. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:707, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:711, или
d. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:731, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:735, или
e. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:907, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:911, или
f. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1075, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1079.
29. Антитело по любому из предыдущих вариантов осуществления, где эталонное антитело представляет собой Fab.
30. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент содержат вариабельный домен тяжелой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:467, 483, 707, 731, 907 или 1075, и вариабельный домен легкой цепи, который на по меньшей мере 90% идентичен последовательности, идентифицированной под SEQ ID NO:471, 487, 711, 735, 911 или 1079.
31. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 30, где вариабельный домен тяжелой цепи на по меньшей мере 92, 94, 96, 97, 98, 99, 99,1 или 99,2% идентичен последовательности, идентифицированной под SEQ ID NO: 467, 483, 707, 731, 907 или 1075.
32. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 30, где вариабельный домен легкой цепи на по меньшей мере 92, 94, 96, 97, 98, 99, 99,1 или 99,2% идентичен последовательности, идентифицированной под SEQ ID NO:471, 487, 711, 735, 911 или 1079.
33. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 31 и 32, где как вариабельный домен тяжелой цепи, так и вариабельный домен легкой цепи на по меньшей мере 92, 94, 96, 97, 98, 99 или 99,1% идентичны идентифицированным SEQ ID.
34. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий один или более аминокислотных остатков E103, Q104, V108, R113, T116, L117, D119, I125, T127, E228, F229, Y230, E266, R287, P291, I292, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a).
35. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 аминокислотных остатка E103, Q104, V108, R113, T116, L117, D119, I125, T127, E228, F229, Y230, E266, R287, P291, I292, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a)
36. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий аминокислотные остатки Y230, D423, R424 и K427 из FX(a).
37. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий аминокислотные остатки E103, Q104, V108, R113, T116, L117, D119, I125, T127, E228, F229, Y230, E266, R287, P291, I292, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a).
38. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, содержащие паратоп, содержащий следующие аминокислотные остатки: K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103, S104 в вариабельном домене тяжелой цепи (SEQ ID NO:467) и остатки V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO:471), необязательно содержащие одну, две, три, четыре или пять аминокислотных замен, делеций или вставок в 26 перечисленных аминокислотных остатках паратопа.
39. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий один или более аминокислотных остатков E103, Q104, V108, R113, T116, L117, A118, D119, I125, T127, S227, E228, Y230, R287, I292, L303, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a).
40. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 аминокислотных остатка E103, Q104, V108, R113, T116, L117, A118, D119, I125, T127, S227, E228, Y230, R287, I292, L303, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a).
41. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент способны связывать эпитоп, содержащий аминокислотные остатки E103, Q104, V108, R113, T116, L117, D119, I125, T127, E228, F229, Y230, E266, R287, P291, I292, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a).
42. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, содержащие паратоп, содержащий следующие аминокислотные остатки: K23, G24, S25, G26, Y27, W33, D52, S54, D55, Y57, S77, L99, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:483) и остатки S30, S31, Y33, Y50, Q52, S54, R55, R57, Y92 и D94 в вариабельном домене легкой цепи (SEQ ID NO:487), необязательно содержащие одну, две, три, четыре или пять аминокислотных замен, делеций или вставок в 27 перечисленных аминокислотных остатках паратопа.
43. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 38 или 42, где указанная(-ые) замена(-ы) представляет(-ют) собой консервативную(-ые) замену(-ы).
44. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 26-43, где антитело или его антигенсвязывающий фрагмент содержит:
a. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:467, и
три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:471; или
b. три последовательности CDR тяжелой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:483, и
три последовательности CDR легкой цепи, содержащие максимум 10 аминокислотных замен по сравнению с последовательностями CDR вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:487.
45. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 44, где три последовательности CDR тяжелой цепи содержат максимум 9, как, например, 8, как, например, 7 или, как, например, 6 аминокислотных замен по сравнению с CDR из идентифицированных SEQ ID.
46. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 44, где три последовательности CDR тяжелой цепи содержат максимум 5, как, например, 4, как, например, 3, как, например, 2 или максимум 1 аминокислотную замену по сравнению с CDR из идентифицированных SEQ ID.
47. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 44, где три последовательности CDR легкой цепи содержат максимум 9, как, например, 8, как, например, 7 или, как, например, 6 аминокислотных замен по сравнению с CDR из идентифицированных SEQ ID.
48. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 44, где три последовательности CDR легкой цепи содержат максимум 5, как, например, 4, как, например, 3, как, например, 2 или максимум 1 аминокислотную замену по сравнению с CDR из идентифицированных SEQ ID.
49. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент содержат последовательности CDR из:
a. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:467 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:471; или
b. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:483 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:487; или
c. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:555 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:559; или
d. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:587 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:591; или
e. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:707 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:711; или
f. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:731 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:735; или
g. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:907 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:911; или
h. вариабельного домена тяжелой цепи, идентифицированного под SEQ ID NO:1075 , и последовательности CDR из вариабельного домена легкой цепи, идентифицированного под SEQ ID NO:1079.
50. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент содержат:
a. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:467, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:471; или
b. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:483, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:487; или
c. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:555, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:559; или
d. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:587, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:591; или
e. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:707, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:711; или
f. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:731, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:735; или
g. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:907, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:911; или
h. вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO:1075, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO:1079.
51. Полиспецифическое антитело или его антигенсвязывающий фрагмент, способные связываться с FIX под SEQ ID NO:1 или его активированной формой (FIXa) и FX (SEQ ID NO:2) или его активированной формой (FXa).
52. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 51, где антитело предусматривает антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 0–50.
53. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 51, где антитело предусматривает антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 2–25.
54. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 51, где антитело предусматривает антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 26–50.
55. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 51, где антитело предусматривает антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 27–50.
56. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 51, где антитело предусматривает антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 0–25 и антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 26–50.
57. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 51, где антитело предусматривает антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 2–25 и антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления 27–50.
58. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–57, содержащее:
a. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:38, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:42, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
b. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:38, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:42, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:486, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:490, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
c. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:46, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:50, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
d. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
e. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:486, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:490, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
f. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:558, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:562, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
g. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:590, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:594, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
h. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:710, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:714, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
i. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:734, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:738, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
j. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:910, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:914, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
k. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:54, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:58, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:1078, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:1082, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
l. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:70, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:74, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
m. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:70, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:74, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:486, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:490, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
n. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1205, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1209, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:1213, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:1217, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
o. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1221, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1225, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
p. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1229, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1233, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
q. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1237, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1241, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
r. последовательность CDR3 тяжелой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1245, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FIX(a), идентифицированную под SEQ ID NO:1249, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 тяжелой цепи антитела к FX(a), идентифицированную под SEQ ID NO:470, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательность CDR3 легкой цепи антитела к FX(a), идентифицированную под SEQ ID NO:474, необязательно содержащей 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
59. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–57, содержащее:
a. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:36, 37 и 38 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:40, 41 и 42 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
b. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:36, 37 и 38 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:40, 41 и 42 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:484, 485 и 486 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:488, 489 и 490 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
c. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:44, 45 и 46 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:48, 49 и 50 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
d. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:52, 53 и 54 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:56, 57 и 58 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
e. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:52, 53 и 54 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:56, 57 и 58 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:708, 709 и 710 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:712, 713 и 714 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
f. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:52, 53 и 54 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:56, 57 и 58 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:732, 733 и 734 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:736, 737 и 738 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
g. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:52, 53 и 54 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:56, 57 и 58 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:908, 909 и 910 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:912, 913 и 914 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
h. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:52, 53 и 54 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:56, 57 и 58 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:1076, 1077 и 1078 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:1080, 1081 и 1082 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
i. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:52, 53 и 54 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:56, 57 и 58 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:484, 485 и 486 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:488, 489 и 490 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
j. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:68, 69 и 70 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:72, 73 и 74 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
k. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:68, 69 и 70 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:72, 73 и 74 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:484, 485 и 486 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:488, 489 и 490 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
l. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1203, 1204 и 1205 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1207, 1208 и 1209 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
m. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1211, 1212 и 1213 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1215, 1216 и 1217 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
n. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1219, 1220 и 1221 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1223, 1224 и 1225 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
o. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1227, 1228 и 1229 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1231, 1232 и 1233 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
p. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1235, 1236 и 1237 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1239, 1240 и 1241 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащие 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; или
q. последовательности CDR1-3 тяжелой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1243, 1244 и 1245 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FIX(a), идентифицированные под SEQ ID NO:1247, 1248 и 1249 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 тяжелой цепи антитела к FX(a), идентифицированные под SEQ ID NO:468, 469 и 470 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки; и
последовательности CDR1-3 легкой цепи антитела к FX(a), идентифицированные под SEQ ID NO:472, 473 и 474 соответственно, необязательно содержащими 1, 2 или 3 аминокислотные замены, и/или делеции, и/или вставки.
60. Полиспецифическое антитело или его антигенсвязывающий фрагмент согласно варианту осуществления 51, где антитело представляет собой биспецифическое антитело, способное специфически связывать FIX(a) и FX(a), где доменами связывания являются домены связывания пар mAb, состоящих из: mAb01-9933/mAb01-8174, mAb01-9933/mAb01-9772, mAb01-9978/mAb01-8174, mAb01-9978/mAb01-9772, mAb01-9985/mAb01-8174, mAb01-9985/mAb01-9772, mAb01-9994/mAb01-8174, mAb01-9994/mAb01-9772, mAb01-9985/mAb11-1431, mAb01-9985/mAb11-1434, mAb01-9985/mAb11-1457, mAb01-9985/mAb11-1480, mAb01-9985/mAb11-1121, mAb01-9985/mAb11-1125, mAb11-0173/mAb01-8174, mAb11-1204/mAb01-8174, mAb11-1495/mAb01-8174, mAb11-1501/mAb01-8174 или mAb11-1502/mAb01-8174.
61. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–60, где антитело или его антигенсвязывающий фрагмент представляют собой прокоагулянтное антитело.
62. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–60, где антитело или его антигенсвязывающий фрагмент способны увеличивать прокоагулянтную активность FIXa.
63. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–60, где антитело или его антигенсвязывающий фрагмент способны увеличивать ферментативную активность FIXa в отношении FX.
64. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–60, где антитело или его антигенсвязывающий фрагмент способны функционально замещать FVIII и/или FVIIIa.
65. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–64, где антитело или его антигенсвязывающий фрагмент представляют собой биспецифическое антитело.
66. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 63–65, где увеличение ферментативной активности FIXa в отношении FX определяется в анализе образования FXa, описанном в данном документе, с использованием моновалентного одноплечего антитела к FIX/FIXa, где индекс стимуляции является по меньшей мере 1300-, 1400-, 1500-, 1600-, 1700-, 1800-, 1900-, 2000-, 2100-, 2200-, 2300-, 2400-, 2500-, 3000-, 3500-, 4000-, 4500-, 5000-, 5500-, 6000-, 6500-, 7000-, 7500-, 8000-, 8500-, 9000-, 9500-, 10000-, 10500-, 11000-, 11500-, 12000-, 12500-, 13000-, 13500-, 13730, 14000-, 14500-, 15000-, 15500-, 16000-, 16500-, 17000-, 17500-, 18000-, 18500-, 19000- или 19500-кратным при измерении с использованием концентрации одноплечего антитела, приводящей к по меньшей мере 80% насыщению FIXa.
67. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 51–65, где указанное антитело или его антигенсвязывающий фрагмент способны обеспечивать средний пиковый уровень тромбина (в нM), составляющий по меньшей мере 47, 48, 49, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 105 или 107, при концентрации соединения 900 нM в анализе TGT (в HA-PRP) в соответствии с примером 16 в данном документе.
68. Антитело по любому из предыдущих вариантов осуществления, где изотип антитела представляет собой IgG1, IgG2, IgG3 или IgG4 или их комбинацию.
69. Фармацевтическая композиция, содержащая антитело или его антигенсвязывающий фрагмент по любому из предыдущих вариантов осуществления и необязательно один или более фармацевтически приемлемых носителей.
70. Фармацевтическая композиция, содержащая антитело или его антигенсвязывающий фрагмент по варианту осуществления 69, для лечения коагулопатии или нарушения свертываемости крови, такого как гемофилия А с наличием ингибиторов или без них.
71. Антитело или его антигенсвязывающий фрагмент или композиция по любому из предыдущих вариантов осуществления для применения в способе лечения коагулопатии или нарушения свертываемости крови.
72. Антитело или его антигенсвязывающий фрагмент или композиция по любому из предыдущих вариантов осуществления для применения в лечении гемофилии А с наличием ингибиторов или без них.
73. Способ лечения субъекта, страдающего коагулопатией или нарушением свертываемости крови, включающий введение указанному субъекту антитела или его антигенсвязывающего фрагмента или композиции по любому из предыдущих вариантов осуществления.
74. Способ по варианту осуществления 73, где коагулопатия или нарушение свертываемости крови представляют собой гемофилию А или гемофилию А с наличием ингибиторов.
75. Применение антитела или его антигенсвязывающего фрагмента или композиции по любому из вариантов осуществления 1–69 для изготовления лекарственного препарата для лечения субъекта, нуждающегося в этом.
76. Применение антитела или его антигенсвязывающего фрагмента или композиции по любому из вариантов осуществления 1–69 для изготовления лекарственного препарата для лечения гемофилии А с наличием ингибиторов или без них.
77. Эукариотическая клетка, которая экспрессирует антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1–68.
78. Набор, содержащий антитело или его антигенсвязывающий фрагмент или композицию по любому из вариантов осуществления 1–69 и инструкции по применению.
79. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1–25, где антитело или его антигенсвязывающий фрагмент являются компонентом (промежуточным соединением) для применения в прокоагулянтном полиспецифическом антителе.
80. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 26–50, где антитело или его антигенсвязывающий фрагмент являются компонентом (промежуточным соединением) для применения в прокоагулянтном полиспецифическом антителе.
81. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1–25, где антитело или его антигенсвязывающий фрагмент являются компонентом (промежуточным соединением) для применения в изготовлении прокоагулянтного полиспецифического антитела.
82. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 26–50, где антитело или его антигенсвязывающий фрагмент являются компонентом (промежуточным соединением) для применения в изготовлении прокоагулянтного полиспецифического антитела.
83. Полиспецифическое антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 61–68, где прокоагулянтная активность указанного антитела увеличена по сравнению с полиспецифическими антителами, раскрытыми в WO2018/141863.
84. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 83, где указанное увеличение определяют с использованием анализа, раскрытого в данном документе, такого как анализ образования FXa с использованием моновалентных одноплечих (OA) антител к FIXa (описанный в примере 12 в данном документе), анализ TGT в плазме крови пациентов с гемофилией A (HA) (описанный в примере 15 в данном документе), в анализе TGT в HA-PPP или в анализе TGT в HA-PRP (описанных в примере 16 в данном документе) или на мышиной модели рассечения хвостовой вены (TVT) (описанной в примере 17 в данном документе).
85. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 51, где антитело или его антигенсвязывающий фрагмент представляют собой биспецифическое антитело, содержащее антитело или его антигенсвязывающий фрагмент по варианту осуществления 14 и антитело или его антигенсвязывающий фрагмент по варианту осуществления 36 или 37.
86. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 85, где стимуляцию ферментативной активности FIXa в отношении FX определяют в анализе образования FXa, описанном в примере 12 в данном документе, с использованием моновалентного одноплечего антитела к FIX/FIXa, где индекс стимуляции является по меньшей мере 1300-, 1400-, 1500-, 1600-, 1700-, 1800-, 1900-, 2000-, 2100-, 2200-, 2300-, 2400-, 2500-, 3000-, 3500-, 4000-, 4500-, 5000-, 5500-, 6000-, 6500-, 7000-, 7500-, 8000-, 8500-, 9000-, 9500-, 10000-, 10500-, 11000-, 11500-, 12000-, 12500-, 13000-, 13500-, 13730-, 14000-, 14500-, 15000-, 15500-, 16000-, 16500-, 17000-, 17500-, 18000-, 18500-, 19000- или 19500-кратным при измерении с использованием концентрации одноплечего антитела, приводящей к по меньшей мере 80% насыщению FIXa.
87. Полиспецифическое антитело или его антигенсвязывающий фрагмент по варианту осуществления 85, где указанное антитело или его антигенсвязывающий фрагмент способны обеспечивать средний пиковый уровень тромбина (в нM), составляющий по меньшей мере 47, 48, 49, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 105 или 107, при концентрации соединения 900 нM в анализе TGT (в HA-PRP) в соответствии с примером 16 в данном документе.
88. Антитело по любому из вариантов осуществления 85–87, где изотип антитела представляет собой IgG1 или IgG4.
89. Фармацевтическая композиция, содержащая антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 85–88 и необязательно один или более фармацевтически приемлемых носителей.
90. Фармацевтическая композиция, содержащая антитело или его антигенсвязывающий фрагмент по варианту осуществления 89, для лечения коагулопатии или нарушения свертываемости крови, такого как гемофилия А с наличием ингибиторов или без них.
91. Антитело или его антигенсвязывающий фрагмент или композиция по любому из вариантов осуществления 83–90 для применения в способе лечения коагулопатии или нарушения свертываемости крови.
92. Антитело или его антигенсвязывающий фрагмент или композиция по варианту осуществления 91 для применения в лечении гемофилии А с наличием ингибиторов или без них.
93. Способ лечения субъекта, страдающего коагулопатией или нарушением свертываемости крови, включающий введение указанному субъекту антитела или его антигенсвязывающего фрагмента или композиции по любому из вариантов осуществления 83–90.
94. Способ по варианту осуществления 93, где коагулопатия или нарушение свертываемости крови представляют собой гемофилию А или гемофилию А с наличием ингибиторов.
95. Применение антитела или его антигенсвязывающего фрагмента или композиции по любому из вариантов осуществления 83–89 для изготовления лекарственного препарата для лечения субъекта, нуждающегося в этом.
96. Применение антитела или его антигенсвязывающего фрагмента или композиции по любому из вариантов осуществления 83-89 для изготовления лекарственного препарата для лечения гемофилии А с наличием ингибиторов или без них.
97. Эукариотическая клетка, которая экспрессирует антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 83–88.
98. Набор, содержащий антитело или его антигенсвязывающий фрагмент или композицию по любому из вариантов осуществления 83–89 и инструкции по применению.
99. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 83–88, где антитело или его антигенсвязывающий фрагмент, способные связываться с FIX(a), представляют собой компонент (промежуточное соединение) для применения в прокоагулянтном полиспецифическом антителе.
100. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 83–88, где антитело или его антигенсвязывающий фрагмент, способные связываться с FIX(a), представляют собой компонент (промежуточное соединение) для применения в изготовлении прокоагулянтного полиспецифического антитела.
101. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 83–88, где антитело или его антигенсвязывающий фрагмент являются компонентом (промежуточным соединением) для применения в изготовлении прокоагулянтного полиспецифического антитела.
102. Инъекционное устройство, содержащее антитело или его антигенсвязывающий фрагмент или композицию по любому из вариантов осуществления 51–69.
103. Инъекционное устройство, содержащее антитело или его антигенсвязывающий фрагмент или композицию по любому из вариантов осуществления 83–90.
104. Инъекционное устройство по варианту осуществления 102, где указанное устройство представляет собой одноразовое и/или предварительно заполненное и/или многодозовое устройство, такое как ручка.
105. Инъекционное устройство по варианту осуществления 104, где указанное устройство представляет собой предварительно заполненную ручку.
106. Инъекционное устройство по варианту осуществления 104, где указанное устройство представляет собой многодозовую ручку.
107. Инъекционное устройство по любому из вариантов осуществления 102, 104, 105 или 106, где указанное инъекционное устройство содержит трубку с диаметром иглы 20–36.
108. Инъекционное устройство по варианту осуществления 103, где указанное устройство представляет собой одноразовое и/или предварительно заполненное и/или многодозовое устройство, такое как ручка.
109. Инъекционное устройство по варианту осуществления 103, где указанное устройство представляет собой предварительно заполненную ручку.
110. Инъекционное устройство по варианту осуществления 108, где указанное устройство представляет собой многодозовую ручку.
111. Инъекционное устройство по любому из вариантов осуществления 103, 108, 109 или 110, где указанное инъекционное устройство содержит трубку с диаметром иглы 20–36.
В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты по настоящему изобретению представляют собой прокоагулянтные биспецифические антитела, способные связываться с FIX (SEQ ID NO:1) и/или его активированной формой (FIXa) и с FX (SEQ ID NO:2) и/или его активированной формой (FXa).
В одном варианте осуществления биспецифическое антитело (bimAb) представляет собой bimAb05-0745, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:68): DYAMH;
CDR2 VH (SEQ ID NO:69): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:70): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:72): RASQSISSWLA;
CDR2 VL (SEQ ID NO:73): KASRLDR;
CDR3 VL (SEQ ID NO:74): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-0746, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:44): DYAMH;
CDR2 VH (SEQ ID NO:45): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:46): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:48): RASQSISSWLA;
CDR2 VL (SEQ ID NO:49): KASRLER;
CDR3 VL (SEQ ID NO:50): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-1229, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:4): DYAMH;
CDR2 VH (SEQ ID NO:5): GISWRGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:6): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:8): RASQSISSWLA;
CDR2 VL (SEQ ID NO:9): KASRLER;
CDR3 VL (SEQ ID NO:10): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:460): TSWIV;
CDR2 VH (SEQ ID NO:461): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:462): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:464): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:465): GASSRAR;
CDR3 VL (SEQ ID NO:466): QQFGSSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-2112, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:68): DYAMH;
CDR2 VH (SEQ ID NO:69): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:70): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:72): RASQSISSWLA;
CDR2 VL (SEQ ID NO:73): KASRLDR;
CDR3 VL (SEQ ID NO:74): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:484): TSWIS;
CDR2 VH (SEQ ID NO:485): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:486): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:488): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:489): GQSSRTR;
CDR3 VL (SEQ ID NO:490): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-2113, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:36): DYAMH;
CDR2 VH (SEQ ID NO:37): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:38): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:40): RASQSISSWLA;
CDR2 VL (SEQ ID NO:41): KASKLDR;
CDR3 VL (SEQ ID NO:42): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:484): TSWIS;
CDR2 VH (SEQ ID NO:485): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:486): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:488): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:489): GQSSRTR;
CDR3 VL (SEQ ID NO:490): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-2114, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:484): TSWIS;
CDR2 VH (SEQ ID NO:485): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:486): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:488): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:489): GQSSRTR;
CDR3 VL (SEQ ID NO:490): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-2115, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:44): DYAMH;
CDR2 VH (SEQ ID NO:45): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:46): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:48): RASQSISSWLA;
CDR2 VL (SEQ ID NO:49): KASRLER;
CDR3 VL (SEQ ID NO:50): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:484): TSWIS;
CDR2 VH (SEQ ID NO:485): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:486): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:488): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:489): GQSSRTR;
CDR3 VL (SEQ ID NO:490): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-2375, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:4): DYAMH;
CDR2 VH (SEQ ID NO:5): GISWRGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:6): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:8): RASQSISSWLA;
CDR2 VL (SEQ ID NO:9): KASRLER;
CDR3 VL (SEQ ID NO:10): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-2379, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:4): DYAMH;
CDR2 VH (SEQ ID NO:5): GISWRGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:6): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:8): RASQSISSWLA;
CDR2 VL (SEQ ID NO:9): KASRLER;
CDR3 VL (SEQ ID NO:10): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:476): TSWIV;
CDR2 VH (SEQ ID NO:477): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:478): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:480): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:481): GASSRAR;
CDR3 VL (SEQ ID NO:482): QQFGSSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-2532, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:12): DYAMH;
CDR2 VH (SEQ ID NO:13): GISWRGDIIGYVDSVKG;
CDR3 VH (SEQ ID NO:14): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:16): RASKSISSWLA;
CDR2 VL (SEQ ID NO:17): KASRLDR;
CDR3 VL (SEQ ID NO:18): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:460): TSWIV;
CDR2 VH (SEQ ID NO:461): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:462): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:464): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:465): GASSRAR;
CDR3 VL (SEQ ID NO:466): QQFGSSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3279, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:36): DYAMH;
CDR2 VH (SEQ ID NO:37): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:38): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:40): RASQSISSWLA;
CDR2 VL (SEQ ID NO:41): KASKLDR;
CDR3 VL (SEQ ID NO:42): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:460): TSWIV;
CDR2 VH (SEQ ID NO:461): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:462): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:464): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:465): GASSRAR;
CDR3 VL (SEQ ID NO:466): QQFGSSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3409, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:44): DYAMH;
CDR2 VH (SEQ ID NO:45): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:46): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:48): RASQSISSWLA;
CDR2 VL (SEQ ID NO:49): KASRLER;
CDR3 VL (SEQ ID NO:50): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:460): TSWIV;
CDR2 VH (SEQ ID NO:461): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:462): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:464): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:465): GASSRAR;
CDR3 VL (SEQ ID NO:466): QQFGSSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3416, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:460): TSWIV;
CDR2 VH (SEQ ID NO:461): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:462): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:464): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:465): GASSRAR;
CDR3 VL (SEQ ID NO:466): QQFGSSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3755, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:68): DYAMH;
CDR2 VH (SEQ ID NO:69): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:70): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:72): RASQSISSWLA;
CDR2 VL (SEQ ID NO:73): KASRLDR;
CDR3 VL (SEQ ID NO:74): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:460): TSWIV;
CDR2 VH (SEQ ID NO:461): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:462): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:464): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:465): GASSRAR;
CDR3 VL (SEQ ID NO:466): QQFGSSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3761, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:36): DYAMH;
CDR2 VH (SEQ ID NO:37): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:38): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:40): RASQSISSWLA;
CDR2 VL (SEQ ID NO:41): KASKLDR;
CDR3 VL (SEQ ID NO:42): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3769, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3770, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:60): DYAMH;
CDR2 VH (SEQ ID NO:61): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:62): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:64): RASQSISSWLA;
CDR2 VL (SEQ ID NO:65): KASRLER;
CDR3 VL (SEQ ID NO:66): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3862, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:20): DYAMH;
CDR2 VH (SEQ ID NO:21): GISWRGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:22): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:24): RASQSISSWLA;
CDR2 VL (SEQ ID NO:25): KASRLDR;
CDR3 VL (SEQ ID NO:26): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3863, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:28): DYAMH;
CDR2 VH (SEQ ID NO:29): GISWRGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:30): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:32): RASQSISSWLA;
CDR2 VL (SEQ ID NO:33): KASRLER;
CDR3 VL (SEQ ID NO:34): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3880, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:76): DYAMH;
CDR2 VH (SEQ ID NO:77): GISWRGDIKGYVDSVKG;
CDR3 VH (SEQ ID NO:78): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:80): RASKSISSWLA;
CDR2 VL (SEQ ID NO:81): KASRLDR;
CDR3 VL (SEQ ID NO:82): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3886, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:84): DYAMH;
CDR2 VH (SEQ ID NO:85): GISWRGDIKGYVDSVKG;
CDR3 VH (SEQ ID NO:86): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:88): RASQSISSWLA;
CDR2 VL (SEQ ID NO:89): KASRLDR;
CDR3 VL (SEQ ID NO:90): LEYNSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-3955, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:92): DYAMH;
CDR2 VH (SEQ ID NO:93): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:94): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:96): RASQSISSWLA;
CDR2 VL (SEQ ID NO:97): KAQRLDR;
CDR3 VL (SEQ ID NO:98): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4100, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:100): DYAMH;
CDR2 VH (SEQ ID NO:101): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:102): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:104): RASQSIKSWLA;
CDR2 VL (SEQ ID NO:105): KASRLDR;
CDR3 VL (SEQ ID NO:106): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4114, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:108): DYAMH;
CDR2 VH (SEQ ID NO:109): GISWKGDIGGYADSVKG;
CDR3 VH (SEQ ID NO:110): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:112): RASKSISSWLA;
CDR2 VL (SEQ ID NO:113): KASRLER;
CDR3 VL (SEQ ID NO:114): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4121, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:116): DYAMH;
CDR2 VH (SEQ ID NO:117): GISWKGDIGGYADSVKG;
CDR3 VH (SEQ ID NO:118): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:120): RASQSISSWLA;
CDR2 VL (SEQ ID NO:121): KASRLER;
CDR3 VL (SEQ ID NO:122): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4220, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:212): DYAMH;
CDR2 VH (SEQ ID NO:213): GISWKGDIGGYADSVKG;
CDR3 VH (SEQ ID NO:214): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:216): RASQSISSWLA;
CDR2 VL (SEQ ID NO:217): KASKLDR;
CDR3 VL (SEQ ID NO:218): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4226, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:220): DYAMH;
CDR2 VH (SEQ ID NO:221): GISWKGDIGGYADSVKG;
CDR3 VH (SEQ ID NO:222): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:224): RASQSISSWLA;
CDR2 VL (SEQ ID NO:225): KASKLER;
CDR3 VL (SEQ ID NO:226): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4283, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:228): DYAMH;
CDR2 VH (SEQ ID NO:229): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:230): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:232): RASQSISSWLA;
CDR2 VL (SEQ ID NO:233): KASKLDR;
CDR3 VL (SEQ ID NO:234): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4289, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:236): DYAMH;
CDR2 VH (SEQ ID NO:237): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:238): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:240): RASQSISSWLA;
CDR2 VL (SEQ ID NO:241): KASKLER;
CDR3 VL (SEQ ID NO:242): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4292, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:252): DYAMH;
CDR2 VH (SEQ ID NO:253): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:254): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:256): RASQSISSWLA;
CDR2 VL (SEQ ID NO:257): KASKLER;
CDR3 VL (SEQ ID NO:258): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4293, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:244): DYAMH;
CDR2 VH (SEQ ID NO:245): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:246): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:248): RASQSISSWLA;
CDR2 VL (SEQ ID NO:249): KASKLDR;
CDR3 VL (SEQ ID NO:250): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4387, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:260): DYAMH;
CDR2 VH (SEQ ID NO:261): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:262): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:264): RASQSISSWLA;
CDR2 VL (SEQ ID NO:265): KASKLDR;
CDR3 VL (SEQ ID NO:266): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4392, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:268): DYAMH;
CDR2 VH (SEQ ID NO:269): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:270): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:272): RASQSISSWLA;
CDR2 VL (SEQ ID NO:273): KASKLER;
CDR3 VL (SEQ ID NO:274): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4419, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:124): DYAMH;
CDR2 VH (SEQ ID NO:125): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:126): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:128): RASQSISSWLA;
CDR2 VL (SEQ ID NO:129): KASKLDR;
CDR3 VL (SEQ ID NO:130): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4422, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:276): DYAMH;
CDR2 VH (SEQ ID NO:277): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:278): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:280): RASQSISSWLA;
CDR2 VL (SEQ ID NO:281): KASKLDR;
CDR3 VL (SEQ ID NO:282): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4428, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:284): DYAMH;
CDR2 VH (SEQ ID NO:285): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:286): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:288): RASQSISSWLA;
CDR2 VL (SEQ ID NO:289): KASKLER;
CDR3 VL (SEQ ID NO:290): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4443, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:300): DYAMH;
CDR2 VH (SEQ ID NO:301): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:302): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:304): RASQSISSWLA;
CDR2 VL (SEQ ID NO:305): KASKLER;
CDR3 VL (SEQ ID NO:306): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4444, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:292): DYAMH;
CDR2 VH (SEQ ID NO:293): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:294): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:296): RASQSISSWLA;
CDR2 VL (SEQ ID NO:297): KASKLDR;
CDR3 VL (SEQ ID NO:298): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4601, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:188): DYAMH;
CDR2 VH (SEQ ID NO:189): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:190): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:192): RASQSISSWLA;
CDR2 VL (SEQ ID NO:193): KASRLDR;
CDR3 VL (SEQ ID NO:194): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4604, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:140): DYAMH;
CDR2 VH (SEQ ID NO:141): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:142): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:144): RASQSISSWLA;
CDR2 VL (SEQ ID NO:145): KASRLDR;
CDR3 VL (SEQ ID NO:146): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4608, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:204): DYAMH;
CDR2 VH (SEQ ID NO:205): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:206): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:208): RASQSISSWLA;
CDR2 VL (SEQ ID NO:209): KASRLDR;
CDR3 VL (SEQ ID NO:210): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4611, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:180): DYAMH;
CDR2 VH (SEQ ID NO:181): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:182): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:184): RASQSISSWLA;
CDR2 VL (SEQ ID NO:185): KASRLDR;
CDR3 VL (SEQ ID NO:186): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4612, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:196): DYAMH;
CDR2 VH (SEQ ID NO:197): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:198): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:200): RASQSISSWLA;
CDR2 VL (SEQ ID NO:201): KASRLDR;
CDR3 VL (SEQ ID NO:202): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4613, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:172): DYAMH;
CDR2 VH (SEQ ID NO:173): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:174): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:176): RASQSISSWLA;
CDR2 VL (SEQ ID NO:177): KASRLDR;
CDR3 VL (SEQ ID NO:178): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4615, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:164): DYAMH;
CDR2 VH (SEQ ID NO:165): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:166): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:168): RASQSISSWLA;
CDR2 VL (SEQ ID NO:169): KASRLDR;
CDR3 VL (SEQ ID NO:170): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4617, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:148): DYAMH;
CDR2 VH (SEQ ID NO:149): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:150): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:152): RASQSISSWLA;
CDR2 VL (SEQ ID NO:153): KASRLDR;
CDR3 VL (SEQ ID NO:154): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4618, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:156): DYAMH;
CDR2 VH (SEQ ID NO:157): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:158): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:160): RASQSISSWLA;
CDR2 VL (SEQ ID NO:161): KASRLDR;
CDR3 VL (SEQ ID NO:162): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4684, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:500): TSWIS;
CDR2 VH (SEQ ID NO:501): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:502): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:504): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:505): GQSSRTR;
CDR3 VL (SEQ ID NO:506): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4685, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:508): TSWIS;
CDR2 VH (SEQ ID NO:509): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:510): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:512): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:513): GQSSRTR;
CDR3 VL (SEQ ID NO:514): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4686, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:516): TSWIS;
CDR2 VH (SEQ ID NO:517): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:518): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:520): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:521): GQSSRTR;
CDR3 VL (SEQ ID NO:522): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4687, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:524): TSWIS;
CDR2 VH (SEQ ID NO:525): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:526): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:528): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:529): GQSSRTR;
CDR3 VL (SEQ ID NO:530): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4688, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:532): TSWIS;
CDR2 VH (SEQ ID NO:533): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:534): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:536): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:537): GQSSRTR;
CDR3 VL (SEQ ID NO:538): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4689, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:540): TSWIV;
CDR2 VH (SEQ ID NO:541): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:542): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:544): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:545): GQSSRTR;
CDR3 VL (SEQ ID NO:546): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4690, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:556): TSWIV;
CDR2 VH (SEQ ID NO:557): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:558): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:560): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:561): GQSSRTR;
CDR3 VL (SEQ ID NO:562): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4692, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:564): TSWIS;
CDR2 VH (SEQ ID NO:565): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:566): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:568): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:569): GQSSRTR;
CDR3 VL (SEQ ID NO:570): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4693, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:572): TSWIS;
CDR2 VH (SEQ ID NO:573): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:574): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:576): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:577): GQSSRTR;
CDR3 VL (SEQ ID NO:578): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4694, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:580): TSWIS;
CDR2 VH (SEQ ID NO:581): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:582): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:584): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:585): GQSSRTR;
CDR3 VL (SEQ ID NO:586): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4695, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:492): TSWIS;
CDR2 VH (SEQ ID NO:493): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:494): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:496): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:497): GQSSRTR;
CDR3 VL (SEQ ID NO:498): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4696, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:588): TSWIV;
CDR2 VH (SEQ ID NO:589): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:590): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:592): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:593): GQSSRTR;
CDR3 VL (SEQ ID NO:594): QQYGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4697, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:596): TSWIV;
CDR2 VH (SEQ ID NO:597): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:598): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:600): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:601): GASSRAR;
CDR3 VL (SEQ ID NO:602): QQYGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4698, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:604): TSWIS;
CDR2 VH (SEQ ID NO:605): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:606): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:608): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:609): GASSRAR;
CDR3 VL (SEQ ID NO:610): QQYGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4699, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:612): TSWIS;
CDR2 VH (SEQ ID NO:613): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:614): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:616): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:617): GASSRAR;
CDR3 VL (SEQ ID NO:618): QQYGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4700, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:620): TSWIS;
CDR2 VH (SEQ ID NO:621): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:622): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:624): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:625): GASSRAR;
CDR3 VL (SEQ ID NO:626): QQYGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4701, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:628): TSWIS;
CDR2 VH (SEQ ID NO:629): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:630): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:632): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:633): GASSRAR;
CDR3 VL (SEQ ID NO:634): QQYGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4702, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:636): TSWIS;
CDR2 VH (SEQ ID NO:637): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:638): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:640): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:641): GASSRAR;
CDR3 VL (SEQ ID NO:642): QQYGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4703, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:644): TSWIV;
CDR2 VH (SEQ ID NO:645): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:646): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:648): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:649): GASSRAR;
CDR3 VL (SEQ ID NO:650): QQYGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4704, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:652): TSWIV;
CDR2 VH (SEQ ID NO:653): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:654): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:656): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:657): GQSSRTR;
CDR3 VL (SEQ ID NO:658): QQFGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4705, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:660): TSWIS;
CDR2 VH (SEQ ID NO:661): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:662): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:664): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:665): GQSSRTR;
CDR3 VL (SEQ ID NO:666): QQFGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4706, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:668): TSWIS;
CDR2 VH (SEQ ID NO:669): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:670): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:672): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:673): GQSSRTR;
CDR3 VL (SEQ ID NO:674): QQFGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4707, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:676): TSWIS;
CDR2 VH (SEQ ID NO:677): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:678): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:680): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:681): GQSSRTR;
CDR3 VL (SEQ ID NO:682): QQFGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4708, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:684): TSWIS;
CDR2 VH (SEQ ID NO:685): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:686): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:688): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:689): GQSSRTR;
CDR3 VL (SEQ ID NO:690): QQFGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4709, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:692): TSWIS;
CDR2 VH (SEQ ID NO:693): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:694): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:696): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:697): GQSSRTR;
CDR3 VL (SEQ ID NO:698): QQFGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4710, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:700): TSWIV;
CDR2 VH (SEQ ID NO:701): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:702): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:704): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:705): GQSSRTR;
CDR3 VL (SEQ ID NO:706): QQFGDSRLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4788, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:308): DYAMH;
CDR2 VH (SEQ ID NO:309): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:310): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:312): RASQSISSWLA;
CDR2 VL (SEQ ID NO:313): KASRLDR;
CDR3 VL (SEQ ID NO:314): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4884, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:316): DYAMH;
CDR2 VH (SEQ ID NO:317): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:318): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:320): RASQSISSWLA;
CDR2 VL (SEQ ID NO:321): KASRLDR;
CDR3 VL (SEQ ID NO:322): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4895, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:340): DYAMH;
CDR2 VH (SEQ ID NO:341): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:342): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:344): RASQSIQSWLA;
CDR2 VL (SEQ ID NO:345): KASRLDR;
CDR3 VL (SEQ ID NO:346): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4896, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:324): DYAMH;
CDR2 VH (SEQ ID NO:325): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:326): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:328): RASQKISSWLA;
CDR2 VL (SEQ ID NO:329): KASRLDR;
CDR3 VL (SEQ ID NO:330): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4898, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:332): DYAMH;
CDR2 VH (SEQ ID NO:333): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:334): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:336): RASQQISSWLA;
CDR2 VL (SEQ ID NO:337): KASRLDR;
CDR3 VL (SEQ ID NO:338): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4903, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:356): DYAMH;
CDR2 VH (SEQ ID NO:357): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:358): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:360): RASQSISSWLA;
CDR2 VL (SEQ ID NO:361): KASRLDR;
CDR3 VL (SEQ ID NO:362): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4906, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:348): DYAMH;
CDR2 VH (SEQ ID NO:349): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:350): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:352): RASQSISSWLA;
CDR2 VL (SEQ ID NO:353): KASRLDK;
CDR3 VL (SEQ ID NO:354): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4910, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:364): DYAMH;
CDR2 VH (SEQ ID NO:365): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:366): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:368): RASQSISSWLA;
CDR2 VL (SEQ ID NO:369): KASRLDR;
CDR3 VL (SEQ ID NO:370): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4914, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:372): DYAMH;
CDR2 VH (SEQ ID NO:373): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:374): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:376): RASQSISSWLA;
CDR2 VL (SEQ ID NO:377): KASRLDR;
CDR3 VL (SEQ ID NO:378): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4915, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:380): DYAMH;
CDR2 VH (SEQ ID NO:381): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:382): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:384): RASQSISSWLA;
CDR2 VL (SEQ ID NO:385): KASRLDR;
CDR3 VL (SEQ ID NO:386): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4919, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:388): DYAMH;
CDR2 VH (SEQ ID NO:389): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:390): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:392): RASQSISSWLA;
CDR2 VL (SEQ ID NO:393): KASRLDR;
CDR3 VL (SEQ ID NO:394): LEYQSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4920, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:404): DYAMH;
CDR2 VH (SEQ ID NO:405): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:406): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:408): RASQSISSWLA;
CDR2 VL (SEQ ID NO:409): KASRLDR;
CDR3 VL (SEQ ID NO:410): LEYSSWIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4921, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:396): DYAMH;
CDR2 VH (SEQ ID NO:397): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:398): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:400): RASQSISSWLA;
CDR2 VL (SEQ ID NO:401): KASRLDR;
CDR3 VL (SEQ ID NO:402): LEYKSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4924, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:420): DYAMH;
CDR2 VH (SEQ ID NO:421): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:422): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:424): RASQSISSWLA;
CDR2 VL (SEQ ID NO:425): KASRLDR;
CDR3 VL (SEQ ID NO:426): LEYNSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4927, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:412): DYAMH;
CDR2 VH (SEQ ID NO:413): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:414): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:416): RASQSISSWLA;
CDR2 VL (SEQ ID NO:417): KASRLDR;
CDR3 VL (SEQ ID NO:418): LEYRSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5092, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:428): DYAMH;
CDR2 VH (SEQ ID NO:429): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:430): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:432): RASQSISSWLA;
CDR2 VL (SEQ ID NO:433): KASKLDR;
CDR3 VL (SEQ ID NO:434): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5095, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:132): DYAMH;
CDR2 VH (SEQ ID NO:133): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:134): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:136): RASQSISSWLA;
CDR2 VL (SEQ ID NO:137): KASRLDR;
CDR3 VL (SEQ ID NO:138): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5204, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:436): DYAMH;
CDR2 VH (SEQ ID NO:437): GISWRGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:438): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:440): RASQSISSWLA;
CDR2 VL (SEQ ID NO:441): KASKLDR;
CDR3 VL (SEQ ID NO:442): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5205, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:444): DYAMH;
CDR2 VH (SEQ ID NO:445): GISWRGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:446): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:448): RASQSISSWLA;
CDR2 VL (SEQ ID NO:449): KASRLER;
CDR3 VL (SEQ ID NO:450): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5240, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:452): DYAMH;
CDR2 VH (SEQ ID NO:453): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:454): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:456): RASQSISSWLA;
CDR2 VL (SEQ ID NO:457): KASRLDR;
CDR3 VL (SEQ ID NO:458): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5339, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:772): TSWIS;
CDR2 VH (SEQ ID NO:773): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:774): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:776): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:777): GQSSRTR;
CDR3 VL (SEQ ID NO:778): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5340, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:708): TSWIV;
CDR2 VH (SEQ ID NO:709): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:710): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:712): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:713): GQSSRTR;
CDR3 VL (SEQ ID NO:714): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5341, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:780): TSWIS;
CDR2 VH (SEQ ID NO:781): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:782): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:784): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:785): GQSSRTR;
CDR3 VL (SEQ ID NO:786): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5342, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:764): TSWIS;
CDR2 VH (SEQ ID NO:765): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:766): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:768): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:769): GQSSRTR;
CDR3 VL (SEQ ID NO:770): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5343, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:788): TSWIS;
CDR2 VH (SEQ ID NO:789): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:790): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:792): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:793): GQSSRTR;
CDR3 VL (SEQ ID NO:794): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5344, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:796): TSWIS;
CDR2 VH (SEQ ID NO:797): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:798): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:800): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:801): GQSSRTR;
CDR3 VL (SEQ ID NO:802): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5345, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:820): TSWIS;
CDR2 VH (SEQ ID NO:821): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:822): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:824): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:825): GQSSRTR;
CDR3 VL (SEQ ID NO:826): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5346, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:804): TSWIV;
CDR2 VH (SEQ ID NO:805): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:806): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:808): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:809): GQSSRTR;
CDR3 VL (SEQ ID NO:810): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5347, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:828): TSWIS;
CDR2 VH (SEQ ID NO:829): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:830): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:832): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:833): GQSSRTR;
CDR3 VL (SEQ ID NO:834): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5348, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:812): TSWIV;
CDR2 VH (SEQ ID NO:813): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:814): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:816): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:817): GQSSRTR;
CDR3 VL (SEQ ID NO:818): QQFGSSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5349, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:836): TSWIS;
CDR2 VH (SEQ ID NO:837): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:838): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:840): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:841): GQSSRTR;
CDR3 VL (SEQ ID NO:842): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5350, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:716): TSWIV;
CDR2 VH (SEQ ID NO:717): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:718): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:720): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:721): GQSSRTR;
CDR3 VL (SEQ ID NO:722): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5351, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:844): TSWIS;
CDR2 VH (SEQ ID NO:845): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:846): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:848): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:849): GQSSRTR;
CDR3 VL (SEQ ID NO:850): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5352, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:852): TSWIS;
CDR2 VH (SEQ ID NO:853): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:854): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:856): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:857): GQSSRTR;
CDR3 VL (SEQ ID NO:858): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5353, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:876): TSWIS;
CDR2 VH (SEQ ID NO:877): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:878): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:880): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:881): GQSSRTR;
CDR3 VL (SEQ ID NO:882): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5354, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:860): TSWIV;
CDR2 VH (SEQ ID NO:861): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:862): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:864): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:865): GQSSRTR;
CDR3 VL (SEQ ID NO:866): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5355, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:884): TSWIS;
CDR2 VH (SEQ ID NO:885): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:886): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:888): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:889): GQSSRTR;
CDR3 VL (SEQ ID NO:890): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5356, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:868): TSWIV;
CDR2 VH (SEQ ID NO:869): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:870): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:872): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:873): GQSSRTR;
CDR3 VL (SEQ ID NO:874): QQFGESQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5357, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:892): TSWIS;
CDR2 VH (SEQ ID NO:893): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:894): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:896): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:897): GQSSRTR;
CDR3 VL (SEQ ID NO:898): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5358, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:724): TSWIV;
CDR2 VH (SEQ ID NO:725): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:726): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:728): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:729): GQSSRTR;
CDR3 VL (SEQ ID NO:730): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5359, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:900): TSWIS;
CDR2 VH (SEQ ID NO:901): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:902): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:904): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:905): GQSSRTR;
CDR3 VL (SEQ ID NO:906): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5361, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:924): TSWIV;
CDR2 VH (SEQ ID NO:925): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:926): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:928): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:929): GQSSRTR;
CDR3 VL (SEQ ID NO:930): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5362, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:908): TSWIS;
CDR2 VH (SEQ ID NO:909): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:910): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:912): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:913): GQSSRTR;
CDR3 VL (SEQ ID NO:914): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5363, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:732): TSWIV;
CDR2 VH (SEQ ID NO:733): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:734): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:736): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:737): GQSSRTR;
CDR3 VL (SEQ ID NO:738): QQFGQSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5364, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:916): TSWIV;
CDR2 VH (SEQ ID NO:917): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:918): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:920): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:921): GQSSRTR;
CDR3 VL (SEQ ID NO:922): QQFGNSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5365, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:932): TSWIS;
CDR2 VH (SEQ ID NO:933): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:934): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:936): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:937): GQSSRTR;
CDR3 VL (SEQ ID NO:938): QQFGQSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5366, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:940): TSWIS;
CDR2 VH (SEQ ID NO:941): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:942): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:944): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:945): GQSSRTR;
CDR3 VL (SEQ ID NO:946): QQFGQSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5367, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:964): TSWIV;
CDR2 VH (SEQ ID NO:965): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:966): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:968): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:969): GQSSRTR;
CDR3 VL (SEQ ID NO:970): QQFGQSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5369, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:972): TSWIV;
CDR2 VH (SEQ ID NO:973): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:974): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:976): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:977): GQSSRTR;
CDR3 VL (SEQ ID NO:978): QQFGQSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5370, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:948): TSWIS;
CDR2 VH (SEQ ID NO:949): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:950): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:952): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:953): GQSSRTR;
CDR3 VL (SEQ ID NO:954): QQFGQSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5371, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:740): TSWIV;
CDR2 VH (SEQ ID NO:741): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:742): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:744): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:745): GQSSRTR;
CDR3 VL (SEQ ID NO:746): QQFGDAQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5372, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:956): TSWIS;
CDR2 VH (SEQ ID NO:957): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:958): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:960): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:961): GQSSRTR;
CDR3 VL (SEQ ID NO:962): QQFGQSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5373, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:980): TSWIS;
CDR2 VH (SEQ ID NO:981): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:982): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:984): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:985): GQSSRTR;
CDR3 VL (SEQ ID NO:986): QQFGDAQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5374, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:988): TSWIS;
CDR2 VH (SEQ ID NO:989): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:990): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:992): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:993): GQSSRTR;
CDR3 VL (SEQ ID NO:994): QQFGDAQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5375, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1012): TSWIV;
CDR2 VH (SEQ ID NO:1013): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1014): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1016): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1017): GQSSRTR;
CDR3 VL (SEQ ID NO:1018): QQFGDAQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5377, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1020): TSWIV;
CDR2 VH (SEQ ID NO:1021): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1022): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1024): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1025): GQSSRTR;
CDR3 VL (SEQ ID NO:1026): QQFGDAQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5378, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:996): TSWIS;
CDR2 VH (SEQ ID NO:997): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:998): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1000): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1001): GQSSRTR;
CDR3 VL (SEQ ID NO:1002): QQFGDAQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5379, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:748): TSWIV;
CDR2 VH (SEQ ID NO:749): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:750): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:752): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:753): GQSSRTR;
CDR3 VL (SEQ ID NO:754): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5380, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1004): TSWIS;
CDR2 VH (SEQ ID NO:1005): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:1006): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1008): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1009): GQSSRTR;
CDR3 VL (SEQ ID NO:1010): QQFGDAQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5381, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1028): TSWIS;
CDR2 VH (SEQ ID NO:1029): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1030): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1032): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1033): GQSSRTR;
CDR3 VL (SEQ ID NO:1034): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5383, где плечо к FIX(a) содержит следующие последовательности CDR:
VH CDR1(SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1052): TSWIS;
CDR2 VH (SEQ ID NO:1053): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1054): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1056): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1057): GQSSRTR;
CDR3 VL (SEQ ID NO:1058): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5384, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1036): TSWIS;
CDR2 VH (SEQ ID NO:1037): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:1038): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1040): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1041): GQSSRTR;
CDR3 VL (SEQ ID NO:1042): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5385, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1060): TSWIS;
CDR2 VH (SEQ ID NO:1061): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:1062): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1064): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1065): GQSSRTR;
CDR3 VL (SEQ ID NO:1066): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5386, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1044): TSWIS;
CDR2 VH (SEQ ID NO:1045): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1046): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1048): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1049): GQSSRTR;
CDR3 VL (SEQ ID NO:1050): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5387, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1068): TSWIV;
CDR2 VH (SEQ ID NO:1069): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1070): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1072): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1073): GQSSRTR;
CDR3 VL (SEQ ID NO:1074): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5388, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1076): TSWIV;
CDR2 VH (SEQ ID NO:1077): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1078): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1080): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1081): GQSSRTR;
CDR3 VL (SEQ ID NO:1082): QQFGDTQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5389, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1100): TSWIS;
CDR2 VH (SEQ ID NO:1101): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1102): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1104): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1105): GQSSRTR;
CDR3 VL (SEQ ID NO:1106): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5390, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:756): TSWIV;
CDR2 VH (SEQ ID NO:757): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:758): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:760): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:761): GQSSRTR;
CDR3 VL (SEQ ID NO:762): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5391, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1108): TSWIS;
CDR2 VH (SEQ ID NO:1109): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1110): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1112): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1113): GQSSRTR;
CDR3 VL (SEQ ID NO:1114): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5392, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1084): TSWIS;
CDR2 VH (SEQ ID NO:1085): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1086): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1088): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1089): GQSSRTR;
CDR3 VL (SEQ ID NO:1090): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5393, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1116): TSWIS;
CDR2 VH (SEQ ID NO:1117): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:1118): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1120): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1121): GQSSRTR;
CDR3 VL (SEQ ID NO:1122): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5394, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1092): TSWIS;
CDR2 VH (SEQ ID NO:1093): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:1094): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1096): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1097): GQSSRTR;
CDR3 VL (SEQ ID NO:1098): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5395, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1124): TSWIV;
CDR2 VH (SEQ ID NO:1125): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1126): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1128): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1129): GQSSRTR;
CDR3 VL (SEQ ID NO:1130): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5396, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1132): TSWIV;
CDR2 VH (SEQ ID NO:1133): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1134): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1136): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1137): GQSSRTR;
CDR3 VL (SEQ ID NO:1138): QQFGDNQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5397, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1156): TSWIS;
CDR2 VH (SEQ ID NO:1157): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1158): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1160): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1161): GQSSRTR;
CDR3 VL (SEQ ID NO:1162): QQFGDDQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5399, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1164): TSWIS;
CDR2 VH (SEQ ID NO:1165): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1166): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1168): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1169): GQSSRTR;
CDR3 VL (SEQ ID NO:1170): QQFGDDQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5400, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1140): TSWIS;
CDR2 VH (SEQ ID NO:1141): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1142): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1144): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1145): GQSSRTR;
CDR3 VL (SEQ ID NO:1146): QQFGDDQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5401, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1172): TSWIS;
CDR2 VH (SEQ ID NO:1173): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:1174): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1176): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1177): GQSSRTR;
CDR3 VL (SEQ ID NO:1178): QQFGDDQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5402, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1148): TSWIS;
CDR2 VH (SEQ ID NO:1149): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:1150): LHYYHSEEFDV;
CDR1 VL (SEQ ID NO:1152): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1153): GQSSRTR;
CDR3 VL (SEQ ID NO:1154): QQFGDDQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5403, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1180): TSWIV;
CDR2 VH (SEQ ID NO:1181): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1182): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1184): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1185): GQSSRTR;
CDR3 VL (SEQ ID NO:1186): QQFGDDQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5406, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1188): TSWIV;
CDR2 VH (SEQ ID NO:1189): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:1190): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:1192): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:1193): GQSSRTR;
CDR3 VL (SEQ ID NO:1194): QQFGDDQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-5413, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:52): DYAMH;
CDR2 VH (SEQ ID NO:53): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:54): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:56): RASQSISSWLA;
CDR2 VL (SEQ ID NO:57): KASKLER;
CDR3 VL (SEQ ID NO:58): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:548): TSWIV;
CDR2 VH (SEQ ID NO:549): MIDPSDSYTSYSPSFQG;
CDR3 VH (SEQ ID NO:550): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:552): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:553): GQSSRTR;
CDR3 VL (SEQ ID NO:554): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4271, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1203): DYAMH;
CDR2 VH (SEQ ID NO:1204): GISWKGDIGGYVDSVKG;
CDR3 VH (SEQ ID NO:1205): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:1207): RASQSISSWLA;
CDR2 VL (SEQ ID NO:1208): KASKLDR;
CDR3 VL (SEQ ID NO:1209): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-4756, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1211): DYAMH;
CDR2 VH (SEQ ID NO:1212): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:1213): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:1215): RASQSISSWLA;
CDR2 VL (SEQ ID NO:1216): KASKLER;
CDR3 VL (SEQ ID NO:1217): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-0396, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1219): DYAMH;
CDR2 VH (SEQ ID NO:1220): GISWRGDIGGYAKSVKG;
CDR3 VH (SEQ ID NO:1221): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:1223): RASQSISSWLA;
CDR2 VL (SEQ ID NO:1224): KASKLDR;
CDR3 VL (SEQ ID NO:1225): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-0417, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1227): DYAMH;
CDR2 VH (SEQ ID NO:1228): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:1229): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:1231): RASQSISSWLA;
CDR2 VL (SEQ ID NO:1232): KASKLDR;
CDR3 VL (SEQ ID NO:1233): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело представляет собой bimAb05-0438, где плечо к FIX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:1235): DYAMH;
CDR2 VH (SEQ ID NO:1236): GISWRGDIGGYVKSVKG;
CDR3 VH (SEQ ID NO:1237): SYGSGSFYNAFDS;
CDR1 VL (SEQ ID NO:1239): RASQSISSWLA;
CDR2 VL (SEQ ID NO:1240): KASKLDR;
CDR3 VL (SEQ ID NO:1241): LEYSSYIRT;
и где плечо к FX(a) содержит следующие последовательности CDR:
CDR1 VH (SEQ ID NO:468): TSWIV;
CDR2 VH (SEQ ID NO:469): MIDPSDSFTSYSPSFQG;
CDR3 VH (SEQ ID NO:470): LHYYNSEEFDV;
CDR1 VL (SEQ ID NO:472): RASQSVSSSYLA;
CDR2 VL (SEQ ID NO:473): GQSSRTR;
CDR3 VL (SEQ ID NO:474): QQFGDSQLFT.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:67 и SEQ ID NO:71 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:43 и SEQ ID NO:47 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:3 и SEQ ID NO:7 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:459 и SEQ ID NO:463 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:67 и SEQ ID NO:71 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:483 и SEQ ID NO:487 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:35 и SEQ ID NO:39 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:483 и SEQ ID NO:487 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:483 и SEQ ID NO:487 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:43 и SEQ ID NO:47 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:483 и SEQ ID NO:487 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:3 и SEQ ID NO:7 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:3 и SEQ ID NO:7 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:475 и SEQ ID NO:479 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:11 и SEQ ID NO:15 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:459 и SEQ ID NO:463 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:35 и SEQ ID NO:39 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:459 и SEQ ID NO:463 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:43 и SEQ ID NO:47 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:459 и SEQ ID NO:463 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:459 и SEQ ID NO:463 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:67 и SEQ ID NO:71 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:459 и SEQ ID NO:463 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:35 и SEQ ID NO:39 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:59 и SEQ ID NO:63 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:19 и SEQ ID NO:23 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:27 и SEQ ID NO:31 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:75 и SEQ ID NO:79 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:83 и SEQ ID NO:87 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:91 и SEQ ID NO:95 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:99 и SEQ ID NO:103 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:107 и SEQ ID NO:111 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:115 и SEQ ID NO:119 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:211 и SEQ ID NO:215 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:219 и SEQ ID NO:223 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:227 и SEQ ID NO:231 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:235 и SEQ ID NO:239 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:251 и SEQ ID NO:255 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:243 и SEQ ID NO:247 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:259 и SEQ ID NO:263 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:267 и SEQ ID NO:271 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:123 и SEQ ID NO:127 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:275 и SEQ ID NO:279 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:283 и SEQ ID NO:287 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:299 и SEQ ID NO:303 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:291 и SEQ ID NO:295 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:187 и SEQ ID NO:191 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:139 и SEQ ID NO:143 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:203 и SEQ ID NO:207 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:179 и SEQ ID NO:183 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:195 и SEQ ID NO:199 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:171 и SEQ ID NO:175 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:163 и SEQ ID NO:167 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:147 и SEQ ID NO:151 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:155 и SEQ ID NO:159 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:499 и SEQ ID NO:503 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:507 и SEQ ID NO:511 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:515 и SEQ ID NO:519 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:523 и SEQ ID NO:527 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:531 и SEQ ID NO:535 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:539 и SEQ ID NO:543 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:555 и SEQ ID NO:559 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:563 и SEQ ID NO:567 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:571 и SEQ ID NO:575 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:579 и SEQ ID NO:583 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:491 и SEQ ID NO:495 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:587 и SEQ ID NO:591 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:595 и SEQ ID NO:599 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:603 и SEQ ID NO:607 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:611 и SEQ ID NO:615 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:619 и SEQ ID NO:623 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:627 и SEQ ID NO:631 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:635 и SEQ ID NO:639 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:643 и SEQ ID NO:647 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:651 и SEQ ID NO:655 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:659 и SEQ ID NO:663 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:667 и SEQ ID NO:671 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:675 и SEQ ID NO:679 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:683 и SEQ ID NO:687 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:691 и SEQ ID NO:695 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:699 и SEQ ID NO:703 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:307 и SEQ ID NO:311 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:315 и SEQ ID NO:319 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:339 и SEQ ID NO:343 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:323 и SEQ ID NO:327 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:331 и SEQ ID NO:335 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:355 и SEQ ID NO:359 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:347 и SEQ ID NO:351 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:363 и SEQ ID NO:367 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:371 и SEQ ID NO:375 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:379 и SEQ ID NO:383 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:387 и SEQ ID NO:391 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:403 и SEQ ID NO:407 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:395 и SEQ ID NO:399 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:419 и SEQ ID NO:423 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:411 и SEQ ID NO:415 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:427 и SEQ ID NO:431 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:131 и SEQ ID NO:135 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:435 и SEQ ID NO:439 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:443 и SEQ ID NO:447 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:451 и SEQ ID NO:455 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:771 и SEQ ID NO:775 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:707 и SEQ ID NO:711 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:779 и SEQ ID NO:783 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:763 и SEQ ID NO:767 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:787 и SEQ ID NO:791 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:795 и SEQ ID NO:799 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:819 и SEQ ID NO:823 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:803 и SEQ ID NO:807 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:827 и SEQ ID NO:831 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:811 и SEQ ID NO:815 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:835 и SEQ ID NO:839 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:715 и SEQ ID NO:719 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:843 и SEQ ID NO:847 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:851 и SEQ ID NO:855 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:875 и SEQ ID NO:879 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:859 и SEQ ID NO:863 соответственно. В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:883 и SEQ ID NO:887 соответственно. В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:867 и SEQ ID NO:871 соответственно. В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:891 и SEQ ID NO:895 соответственно. В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:723 и SEQ ID NO:727 соответственно. В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:899 и SEQ ID NO:903 соответственно. В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:923 и SEQ ID NO:927 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:907 и SEQ ID NO:911 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:731 и SEQ ID NO:735 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:915 и SEQ ID NO:919 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:931 и SEQ ID NO:935 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:939 и SEQ ID NO:943 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:963 и SEQ ID NO:967 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:971 и SEQ ID NO:975 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:947 и SEQ ID NO:951 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:739 и SEQ ID NO:743 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:955 и SEQ ID NO:959 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:979 и SEQ ID NO:983 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:987 и SEQ ID NO:991 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1011 и SEQ ID NO:1015 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1019 и SEQ ID NO:1023 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:995 и SEQ ID NO:999 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:747 и SEQ ID NO:751 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1003 и SEQ ID NO:1007 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1027 и SEQ ID NO:1031 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1051 и SEQ ID NO:1055 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1035 и SEQ ID NO:1039 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1059 и SEQ ID NO:1063 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1043 и SEQ ID NO:1047 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1067 и SEQ ID NO:1071 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1075 и SEQ ID NO:1079 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1099 и SEQ ID NO:1103 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:755 и SEQ ID NO:759 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1107 и SEQ ID NO:1111 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1083 и SEQ ID NO:1087 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1115 и SEQ ID NO:1119 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1091 и SEQ ID NO:1095 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1123 и SEQ ID NO:1127 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1131 и SEQ ID NO:1135 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1155 и SEQ ID NO:1159 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1163 и SEQ ID NO:1167 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1139 и SEQ ID NO:1143 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1171 и SEQ ID NO:1175 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1147 и SEQ ID NO:1151 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1179 и SEQ ID NO:1183 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:1187 и SEQ ID NO:1191 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:51 и SEQ ID NO:55 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:547 и SEQ ID NO:551 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:1202 и SEQ ID NO:1206 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:1210 и SEQ ID NO:1214 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:1218 и SEQ ID NO:1222 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:1226 и SEQ ID NO:1230 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:1234 и SEQ ID NO:1238 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления биспецифическое антитело содержит домены VH и VL плеча к FIX(a), соответствующие SEQ ID NO:1242 и SEQ ID NO:1246 соответственно, и
домены VH и VL плеча к FX(a), соответствующие SEQ ID NO:467 и SEQ ID NO:471 соответственно.
В одном варианте осуществления паратоп антитела к FIX(a) или его антигенсвязывающего фрагмента по настоящему изобретению содержит аминокислотные остатки H30, D31, W53, D56, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:67) и остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:71).
В одном варианте осуществления антитело к FIX(a) или его антигенсвязывающий фрагмент по настоящему изобретению содержат одну, две или три аминокислотные замены или делеции в пределах группы аминокислотных остатков паратопа H30, D31, W53, D56, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:67) и остатков Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:71).
В другом варианте осуществления паратоп антитела к FIX(a) или его антигенсвязывающего фрагмента по настоящему изобретению содержит аминокислотные остатки D30, D31, W53, S102, S104 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:35) и остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:39).
В другом варианте осуществления антитело к FIX(a) по настоящему изобретению содержит одну, две или три аминокислотные замены или делеции в пределах группы аминокислотных остатков паратопа: D30, D31, W53, S102, S104 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:35) и остатков Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:39).
В одном варианте осуществления последовательности CDR антитела или его антигенсвязывающего фрагмента по настоящему изобретению можно описать с помощью аминокислотных остатков паратопа антитела к FIX(a), являющихся частью этих CDR.
В одном таком варианте осуществления CDR паратопа антитела к FIX(a) представляют собой:

где аминокислотные остатки паратопа выделены жирным шрифтом, а X представляет встречающийся в природе аминокислотный остаток.
В другом таком варианте осуществления CDR паратопа антитела к FIX(a) представляют собой:

где аминокислотные остатки паратопа выделены жирным шрифтом, а X представляет встречающийся в природе аминокислотный остаток.
В другом таком варианте осуществления CDR паратопа антитела к FIX(a) представляют собой:

CDR1 VH (на основе SEQ ID NO:52): DXXXX;
CDR2 VH (на основе SEQ ID NO:53): XXXWXXXXXXXXXXXXX;
CDR3 VH (на основе SEQ ID NO:54): XXXSXSXYNXXXX;
CDR1 VL (на основе SEQ ID NO:56): XXXXXXXXXXX;
CDR2 VL (на основе SEQ ID NO:57): XXXXXXX;
CDR3 VL (на основе SEQ ID NO:58): XXYSXXXXX;
где аминокислотные остатки паратопа выделены жирным шрифтом, а X представляет встречающийся в природе аминокислотный остаток.
В одном варианте осуществления паратоп антитела к FX(a) по настоящему изобретению содержит остатки K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:467) и остатки V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO:471).
В другом варианте осуществления антитело к FX(a) по настоящему изобретению содержит одну, две или три аминокислотные замены или делеции в пределах группы остатков паратопа K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:467) и остатков V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO:471).
В другом варианте осуществления паратоп антитела к FX(a) по настоящему изобретению содержит остатки K23, G24, S25, G26, Y27, W33, D52, S54, D55, Y57, S77, L99, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:483) и остатки S30, S31, Y33, Y50, Q52, S54, R55, R57, Y92 и D94 в вариабельном домене легкой цепи (SEQ ID NO:487).
В другом варианте осуществления антитело к FX(a) по настоящему изобретению содержит одну, две или три аминокислотные замены или делеции в пределах группы остатков паратопа K23, G24, S25, G26, Y27, W33, D52, S54, D55, Y57, S77, L99, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:483) и остатков S30, S31, Y33, Y50, Q52, S54, R55, R57, Y92 и D94 в вариабельном домене легкой цепи (SEQ ID NO:487).
В одном варианте осуществления последовательности CDR такого антитела можно описать с помощью аминокислотных остатков паратопа антитела к FX(a), являющихся частью этих CDR.
В одном таком варианте осуществления CDR паратопа антитела к FX(a) представляют собой

где аминокислотные остатки паратопа выделены жирным шрифтом, а X представляет встречающийся в природе аминокислотный остаток.
В другом таком варианте осуществления CDR паратопа антитела к FX(a) представляют собой:
 где аминокислотные остатки паратопа выделены жирным шрифтом, а X представляет встречающийся в природе аминокислотный остаток.
где аминокислотные остатки паратопа выделены жирным шрифтом, а X представляет встречающийся в природе аминокислотный остаток.
В одном варианте осуществления антитело по настоящему изобретению представляет собой полиспецифическое антитело или его антигенсвязывающий фрагмент, способные стимулировать ферментативную активность FIXa в отношении FX, содержащие первый антигенсвязывающий участок, способный связываться с FIX (SEQ ID NO:1) и/или его активированной формой FIXa, и второй антигенсвязывающий участок, способный связываться с FX (SEQ ID NO:2) или его активированной формой (FXa).
В одном таком варианте осуществления первый антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки D30, D31, W53, S102, S104 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:35) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:39), и второй антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки K23, G24, S25, G26, Y27, W33, D52, S54, D55, Y57, S77, L99, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:483) и аминокислотные остатки S30, S31, Y33, Y50, Q52, S54, R55, R57, Y92 и D94 в вариабельном домене легкой цепи (SEQ ID NO:487).
В одном таком варианте осуществления первый антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки H30, D31, W53, D56, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:67) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:71), и второй антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки K23, G24, S25, G26, Y27, W33, D52, S54, D55, Y57, S77, L99, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:483) и аминокислотные остатки S30, S31, Y33, Y50, Q52, S54, R55, R57, Y92 и D94 в вариабельном домене легкой цепи (SEQ ID NO:487).
В одном таком варианте осуществления первый антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки H30, D31, W53, D56, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:67) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:71), и второй антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:467) и аминокислотные остатки V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO:471).
В одном таком варианте осуществления первый антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки D30, D31, W53, S102, S104 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:35) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:39), и второй антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:467) и аминокислотные остатки V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO:471).
В одном таком варианте осуществления первый антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки H30, D31, W53, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:51) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:55), и второй антигенсвязывающий участок содержит паратоп, содержащий аминокислотные остатки K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:467) и аминокислотные остатки V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO:471).
В одном варианте осуществления антитело представляет собой биспецифическое антитело, способное связываться с FIX(a) и FX(a).
В одном варианте осуществления антитело по настоящему изобретению способно связывать FIXa с более высокой аффинностью, чем аффинность, с которой оно связывает FIX.
В одном варианте осуществления антитело по настоящему изобретению способно увеличивать ферментативную активность FIXa в отношении FX.
В одном таком варианте осуществления антитело по настоящему изобретению способно увеличивать ферментативную активность FIXa в отношении FX, измеряемую в анализе образования FXa с использованием моновалентных одноплечих антител, описанных в данном документе.
В одном варианте осуществления антитело по настоящему изобретению способно увеличивать ферментативную активность FIXa в отношении FX, измеряемую в анализе образования FXa с использованием бивалентных антител, описанных в данном документе.
В одном варианте осуществления полиспецифические антитела, такие как биспецифические антитела, по настоящему изобретению не препятствуют воздействию FVIII, такого как рекомбинантный FVIII, вводимый пациенту, страдающему гемофилией A, когда указанные антитела используют в клинически значимых дозах для лечения гемофилии A.
В одном варианте осуществления антитело по настоящему изобретению не является антителом к FIX CLB-FIX 13, которое описано в Rohlena et al. (2003) J. Biol. Chem. 278(11):9394–9401. В одном варианте осуществления антитело по настоящему изобретению не является антителом к FIX HIX-1 (мышиный IgG1) (Merck KGaA, SigmaAldrich). В одном варианте осуществления антитело или его антигенсвязывающий фрагмент по настоящему изобретению не являются антителом к FIX AHIX-5041 (IgG1) (Haematologic Technologies, Inc.).
В одном варианте осуществления антитело или его антигенсвязывающий фрагмент по настоящему изобретению обладают пониженной иммуногенностью по сравнению с прокоагулянтными антителами из уровня техники.
В предпочтительном варианте осуществления антитела по настоящему изобретению, если не указано иное или не противоречит контексту, экспрессированы в формате IgG4/каппа.
Для плеча к FIX(a) области константного домена тяжелой цепи (CH1-CH2-CH3) были получены из IgG4 человека с заменой S228P (нумерация по EU) и с усечением C-концевого лизина:

В одном варианте осуществления для плеча к FX(a) области константного домена тяжелой цепи (CH1-CH2-CH3) были получены из IgG4 человека с заменой S228P и с двумя дополнительными заменами, F405L и R409K (нумерация по EU), в домене CH3 для облегчения гетеродимеризации тяжелых цепей (описанной в примере 4) и с усечением C-концевого лизина:

При этом константная область легкой цепи (CL) представляла собой каппа-цепь человека:
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO:1197).
В другом варианте осуществления антитела также можно экспрессировать в формате IgG4, при этом области константных доменов тяжелой цепи (CH1-CH2-CH3) для плеча к FIX(a) несут замены S228P, F405L и R409K и при этом области константных доменов тяжелой цепи для плеча к FX(a) несут замену S228P, с делецией С-концевого лизина или без нее.
В одном варианте осуществления антитела также можно экспрессировать в формате IgG1/каппа. В этом случае области константного домена тяжелой цепи плеча к FIX(a) представляют собой IgG1 человека с F405L, с усечением С-концевого лизина:

При этом области константного домена тяжелой цепи плеча к FX(a) представляют собой IgG1 человека с K409R, с усечением С-концевого лизина:

Антитела также можно экспрессировать в формате IgG1, при этом области константных доменов тяжелой цепи (CH1-CH2-CH3) для плеча к FIX(a) несут замену K409R и при этом области константных доменов тяжелой цепи для плеча к FX(a) несут замену F405L, с делецией С-концевого лизина или без нее.
Области константных доменов могут дополнительно содержать дополнительные замены или другие модификации, например, для модулирования эффекторных функций, времени полужизни или других свойств.
В настоящем изобретении также предусмотрены наборы, которые содержат антитела или их антигенсвязывающие фрагменты, раскрытые в данном документе, подходящие для лечения, описанного в данном документе. В некоторых вариантах осуществления набор включает: (i) антитело, такое как биспецифическое антитело или его антигенсвязывающий фрагмент, фармацевтическую композицию, нуклеиновую кислоту, вектор или клетку (например, клетку-хозяина), раскрытые в данном документе, или их комбинацию и (ii) инструкции по применению. Специалист легко поймет, что антитела, биспецифические молекулы (например, биспецифические антитела), фармацевтические композиции, нуклеиновые кислоты, векторы или клетки (например, клетка-хозяин), раскрытые в данном документе, или их комбинации могут быть легко включены в один из установленных форматов наборов, которые хорошо известны в данной области техники.
Примеры
Перечень сокращений
Ссылки на ACE910 следует понимать как относящиеся к антителу, имеющему аминокислотную последовательность, которая идентична последовательности ACE910.
Пример 1. Разработка антител к FIX(a) и к FX(a)
Раскрытые в данном документе антитела, связывающие FIX(a) и FX(a),-идентифицировали с использованием различных способов разработки антител. Чтобы создать разнообразный набор антител, выполняли процедуры иммунизации мышей и кроликов, а также использовали платформы экспрессии антител на основе фагового дисплея и дрожжей Adimab.
Платформа для антител на основе дрожжей Adimab
Платформа Adimab представляет собой дрожжевую систему экспрессии антител, вмещающую библиотеку полностью человеческих антител IgG1/каппа, не подвергавшихся воздействию антигена, с разнообразием, составляющим 1010. Процесс отбора антител проводили с использованием способов на основе MACS и FACS, которые позволяют отслеживать применяемые критерии отбора в режиме реального времени. Поскольку процедуры отбора основаны на MACS и FACS, были необходимы меченые антигены (например, биотином). Операции по отбору проводили с использованием меченного биотином hFIXa с ингибированным активным сайтом (FIXa-EGR-биотин) или опосредованной антителами иммобилизации hFIXa. «Хиты» оценивали в отношении связывания с использованием биослойной интерферометрии (системы Octet ForteBio).
Фаговый дисплей
Используемая платформа фагового дисплея антител представляет собой проприетарную библиотеку дисплея с полностью человеческими Fab. Размер библиотеки составляет 1010, и она была создана с помощью комбинаторного подхода с использованием химического синтеза легкой цепи, а также CDR1 и CDR2 тяжелой цепи, дополненных ПЦР-амплификацией CDR3 тяжелой цепи из мононуклеарных клеток периферической крови человека. Чтобы максимально увеличить разнообразие эпитопов, исследовали различные стратегии пэннинга, включая пэннинг с использованием биотинилированного FIXa-EGR, FX, FXa с ингибированным активным сайтом, или захват антигена с использованием антител к FIXa. Первоначальные «хиты» идентифицировали с помощью фагового ELISA. После анализа последовательностей уникальные «хиты» клонировали и экспрессировали рекомбинантным образом в виде антител IgG1 и ранжировали с использованием SPR (Biacore) или биослойной интерферометрии (системы Octet ForteBio).
Платформы in vivo
Мышей и кроликов использовали для получения антител с применением платформ in vivo. Для получения антител к FIX/FIXa мышей или кроликов иммунизировали с помощью FIXa, FIXa-EGR или FIX человека с использованием стандартных протоколов. Клетки селезенки, полученной от мышей, сливали с клетками миеломы с использованием стандартных методик, и для полученных супернатантов гибридом, содержащих антитела, проводили скрининг в отношении связывания с FIXa с использованием ELISA. Для В-клеток кролика, связывающих FIXa, осуществляли сортировку отдельных клеток с использованием FACS путем гейтирования по клеткам, связывающим случайным образом биотинилированный FIXa-EGR (обнаруживали с помощью флуорофора, конъюгированного со стрептавидином). Отсортированные В-клетки кролика культивировали в течение семи дней в 384-луночных планшетах с использованием питающих клеток и кондиционированной среды от спленоцитов перед проведением скрининга против FIXa в ELISA. В-клетки кролика и клоны гибридомы мыши, экспрессирующие «хиты» антител, связывающих FIXa, либо использовали для секвенирования VH/VL с последующей рекомбинантной экспрессией (в случае mAb кролика или полученных с помощью гибридомы), либо дополнительно размножали для получения mAb (гибридомы мыши).
Для получения антител к FX мышей и кроликов иммунизировали с помощью FX с использованием стандартных протоколов. В-клетки кролика выделяли с помощью сортировки отдельных клеток на основе FACS и с использованием случайным образом биотинилированного FX (обнаруживали с помощью флуофора, конъюгированного со стрептавидином), при этом клетки селезенки, полученные от иммунизированных мышей, использовали для стандартного образования гибридомы. Полученные клоны B-клеток или гибридомы мыши, вырабатывающие антитела, подвергали скринингу на связывание FX с использованием ELISA и систем Octet ForteBio. Клоны B-клеток кролика или гибридомы мыши, экспрессирующие «хиты» антител, либо использовали для секвенирования VH/VL с последующей рекомбинантной экспрессией (в случае mAb кролика или полученных с помощью гибридомы), либо дополнительно размножали для получения mAb (гибридомы мыши).
Секвенирование антител, полученных из гибридомы
Антитела к FIXa и к FX, вырабатываемые гибридомами, секвенировали и экспрессировали в клетках HEK293 с использованием стандартных методик. Экспрессированные антитела оценивали на связывание антигена с использованием систем Octet ForteBio.
Общую РНК экстрагировали из клонов, вырабатывающих антитела, и последовательности ДНК, кодирующие вариабельные домены (VH и VL), амплифицировали с использованием RT-PCR. Последовательности VH и VL определяли и вводили в вектор экспрессии в клетках млекопитающих на основе pTT (Durocher et al (2002) Nucleic Acid Res. 30: E9) или в вектор экспрессии в клетках млекопитающих pcDNA3.4 (Invitrogen), содержащий последовательности ДНК, кодирующей константную область антитела. В случае векторов экспрессии pTT/pcDNA3.4 для mAb последовательности ДНК VH и VL вводили в рамку считывания с последовательностями ДНК, кодирующими константные области IgG1 или IgG4 человека с S228P (CH1CH2CH3, необязательно с дополнительными аминокислотными заменами и делециями, например, заменами в домене CH3 и делецией C-концевого лизина) или CL каппа-цепи человека соответственно. В случае соответствующих векторов экспрессии pTT/pcDNA3.4 для Fab последовательности ДНК VH вводили в рамку считывания с последовательностями ДНК, кодирующими CH1 IgG4 человека.
Пример 2. Рекомбинантная экспрессия антител и Fab-фрагментов антител
Антитела и Fab-фрагменты антител экспрессировали с использованием временной трансфекции суспензии клеток HEK293 (293Expi, Invitrogen), в основном следуя инструкциям производителя. Как правило, клетки 293Expi пересевали каждые 3–4 дня в среду для экспрессии Expi293F (Invitrogen, номер по каталогу A1435104), дополненную 1% P/S (GIBCO, номер по каталогу 15140-122). Клетки Expi293F трансфицировали при плотности клеток 2,5–3 млн./мл с использованием Expifectamine. Для каждого литра клеток Expi293F трансфекцию проводили путем разведения суммарно 1 мг плазмидной ДНК (плазмиды с VH-CH1 (в случае Fab) или VH-CH1-CH2-CH3 (в случае mAb) и LC в соотношении 1:1) в 50 мл Optimem (GIBCO, номер по каталогу 51985-026, разведение A) и путем разведения 2,7 мл Expifectamine в 50 мл Optimem (разведение B). Для совместных трансфекций с выработкой Fab и mAb использовали плазмиды с VH-CH1 и LC (Fab) и плазмиды с VH-CH1-CH2-CH3 и LC (mAb) соответственно в соотношении 1:1. Разведения A и B смешивали и инкубировали при комнатной температуре в течение 10–20 минут. После этого смесь для трансфекции добавляли к клеткам Expi293F и клетки инкубировали при 37°C в увлажненном инкубаторе с ротационным вращением (85–125 об/мин). Через день после трансфекции к трансфицированным клеткам добавляли 5 мл усилителя 1 трансфекции ExpiFectamine 293 и 50 мл усилителя 2 трансфекции ExpiFectamine 293. Супернатанты клеточных культур, как правило, собирали через 4–5 дней после трансфекции путем центрифугирования с последующей фильтрацией.
Пример 3. Очистка и определение характеристик Fab и антител
Все стадии очистки проводили при 4°C. В лабораторных масштабах для приготовления буфера использовали воду Milli-Q. Для анализа SE-HPLC использовали систему HPLC Aglient 1100. В качестве контроля качества оценивали агрегацию и результаты LC/MS.
Захват Fab выполняли с помощью аффинной HP-хроматографии с белком G HiTrap со связывающим буфером в 1× PBS (10 мМ Na2HPO4, 1,8 мМ KH2PO4, 137 мМ NaCl, 2,7 мМ KCl), pH 7,4. Одностадийное элюирование выполняли с помощью 0,1 М глицина, pH 2,8. Обессоливание конечного продукта осуществляли, пропуская его через колонку для обессоливания GE Hiprep 16 объемом 52 мл в буфере для составления (25 мМ HEPES, 150 мМ NaCl) с pH 7,4, и концентрировали с помощью центрифужного ультрафильтра (отсечение 30 кДа) для хранения при -80°C.
Для оценки качества очищенного Fab выполняли SDS-PAGE и анализ на основе высокоэффективной эксклюзионной хроматографии (SE-HPLC). Партии, которые не соответствовали стандартам качества (например, <95% мономеров по данным SE-HPLC), дополнительно очищали с помощью эксклюзионной хроматографии. Для проверки идентичности белка Fab проводили LC/MS. Было показано, что значения молекулярной массы (MW) всех Fab согласуются с теоретической MW тяжелой цепи и легкой цепи соответственно.
Очистка и определение характеристик антител
Очистку антител проводили с помощью аффинной хроматографии с использованием смол с белком A MabSelect SuRe (GE Healthcare, номер по каталогу 17-5438-01). Для мелкомасштабного производства антител очистку на основе белка A выполняли в 96-луночных планшетах, тогда как для более крупномасштабного производства использовали хроматографическую систему ÄktaExplorer (GE Healthcare, номер по каталогу 18-1112-41). Буферные системы, используемые для стадии аффинной очистки, представляли собой: 1) уравновешивающий буфер, состоящий из 20 мМ фосфата Na, pH 7,2, 150 мМ NaCl, 2) элюирующий буфер, состоящий из 10 мМ муравьиной кислоты, pH 3,5, и 3) буфер для регулирования pH, состоящий из 0,4 M фосфата Na, pH 9,0. Супернатанты клеток без каких-либо корректировок наносили непосредственно на предварительно уравновешенную колонку MabSelect SuRe. Колонку промывали приблизительно 10 объемами колонки уравновешивающего буфера и антитела элюировали изократически в приблизительно 2–5 объемах колонки элюирующего буфера. рН объединенных фракций доводили до нейтрального с использованием описанного буфера для регулирования рН сразу после элюирования.
Характеристики очищенных антител определяли с использованием различных способов, таких как анализы на основе SDS-PAGE/кумасси, эксклюзионной жидкостной хроматографии высокого давления (SE-HPLC) и жидкостной хроматографии/масс-спектрометрии (LC-MS). Анализ SDS-PAGE/кумасси проводили с использованием 4–12% гелей Bis-Tris NuPage (Invitrogen, номер по каталогу NP0321BOX). В данном случае для всех антител показаны ожидаемые компоненты легкой цепи и тяжелой цепи. Определение интактной молекулярной массы выполняли с использованием установки для способа жидкостной хроматографии/времяпролетной масс-спектрометрии с ионизацией электрораспылением на приборе Agilent 6210 и колонки для обессоливания MassPREP (Waters, номер по каталогу USRM10008656). Используемая буферная система представляла собой уравновешивающий буфер, состоящий из 0,1% муравьиной кислоты в H2O со степенью чистоты для LC-MS, и элюирующий буфер, состоящий из 0,1% муравьиной кислоты в ACN со степенью чистоты для LC-MS. Анализы выполняли с N-гликозидазой F (Roche Diagnostics, номер по каталогу 11365177001) и восстановителем (т. е. меркаптоэтанолом или DTT) и без них. Для всех антител показаны ожидаемые значения интактной молекулярной массы в соответствии с последовательностью и одним N-гликаном тяжелой цепи. Чистоту определяли на основании SE-HPLC. Конечную чистоту белка анализировали на основании установки для способа SE-HPLC в системе Agilent LC 1100/1200 и с использованием колонки BIOSep-SEC-S3000 300×7,8 мм (Phenomenex, номер по каталогу 00H-2146-K0) и рабочего буфера, состоящего из 200 мМ фосфата Na, рН 6,9, 300 мМ NaCl и 10% изопропанола. Для обнаружения использовали UV280 и детекторы флуоресценции (возбуждение 280 нм/излучение 354 нм). Антитела элюировались как единичные симметричные пики с временем удержания, отражающим размер антител. Все оценки чистоты составляли между 95–99% для разных антител. Для измерения конечных концентраций белка использовали спектрофотометр NanoDrop (Thermo Scientific) вместе с конкретными коэффициентами экстинкции для каждого из антител.
Пример 4. Биспецифические антитела, полученные при сборке in vitro
Биспецифические антитела получали путем сборки in vitro первого и второго антитела с помощью способа Duobody® (Genmab), описанного (Labrijn et al. PNAS 2013, vol. 110, pp. 5145–5150) в случае биспецифических антител на основе IgG1 человека и с использованием слегка модифицированного варианта в случае биспецифических антител на основе IgG4 человека, как подробно описано ниже.
В случае IgG1 константная область тяжелой цепи первого антитела представляет собой IgG1 человека K409R (антитело к FIX/FIXa), а константная область тяжелой цепи второго антитела представляет собой IgG1 человека F405L (антитело к FX/FXa). IgG1 может представлять собой вариант IgG1 со сниженными эффекторными функциями, как упоминалось ранее.
В случае IgG4 человека константная область тяжелой цепи первого антитела представляет собой IgG4 к S228P (антитело к FIX/FIXa), а константная область тяжелой цепи второго антитела представляет собой IgG4 с S228P, F405L+R409K (антитело к FX). Два исходных антитела получают, как описано в примерах 1–3. Реакцию обмена Fab-плеча проводят в буфере HEPES (pH 7,4) в восстанавливающих условиях с использованием 75 мМ 2-меркаптоэтиламина (2-MEA) и инкубации при 30°C в течение 4 часов.
Пример 5. Получение моновалентных (одноплечих) антител
Чтобы избежать любых потенциальных эффектов авидности, ассоциированных с традиционными моноспецифическими и бивалентными антителами, например, в анализах образования FXa (пример 12) и в определенных экспериментах на основе SPR (примеры 10 и 11), использовали формат моновалентного одноплечего (ОА) антитела, описанный в Martens et al.: A Novel One-Armed Anti-c-Met Antibody Inhibits Glioblastoma Growth In vivo. Clin. Cancer Res. 12, 6144–6152 (2006), где совместно экспрессируют полную тяжелую цепь, усеченную тяжелую цепь (без области Fab) и легкую цепь. Вместо совместной экспрессии трех цепей, описанной в Martens et al., в настоящем изобретении моновалентные антитела получали с использованием принципа Duobody®, описанного для биспецифических антител (пример 4). При этом моновалентные антитела получали путем смешивания полного моноспецифического и бивалентного антитела и димера усеченных тяжелых цепей (формально полученного из полного антитела путем удаления области Fab) и обеспечивали возможность прохождения обмена цепями при тех же экспериментальных условиях, что описаны в примере 4. Для образования моновалентного антитела требуется, чтобы антитело и димер усеченных тяжелых цепей несли соответствующие комплементарные мутации для стимуляции гетеродимеризации, т. е. F405L/K409R для IgG1 человека и F405L+R409K/WT для IgG4 человека, как описано в примере 4.
В случае моновалентных антител подтипа IgG1 усечение тяжелой цепи может простираться от N-конца до положения между Cys 220 и верхним шарнирным Cys 226 (нумерация по EU). Конкретным примером усеченной тяжелой цепи IgG1 человека является цепь, в которой усечены остатки 1-220.
В случае моновалентных антител подтипа IgG4 человека усечение тяжелой цепи может простираться от N-конца до положения между Cys 200 и верхним шарнирным Cys 226 (нумерация по EU). Конкретным примером усеченной тяжелой цепи IgG4 человека является цепь, в которой усечены остатки 1-214.
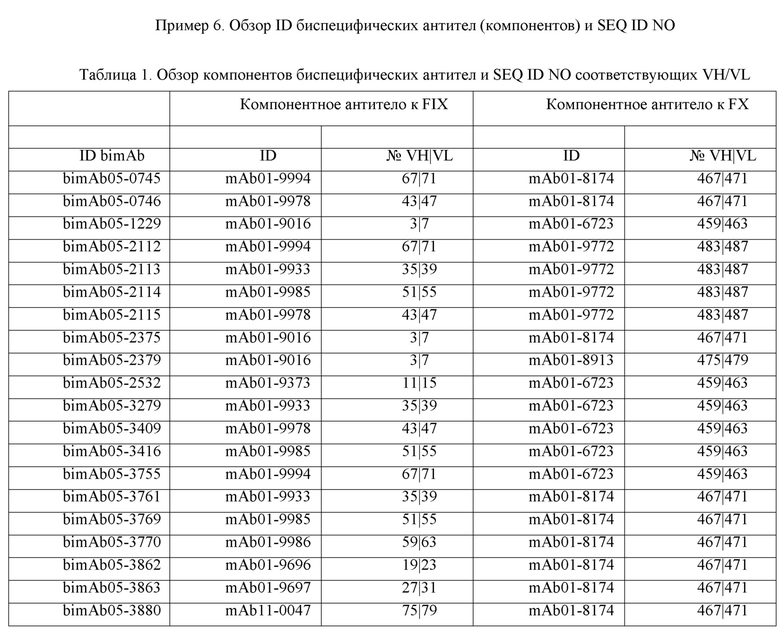
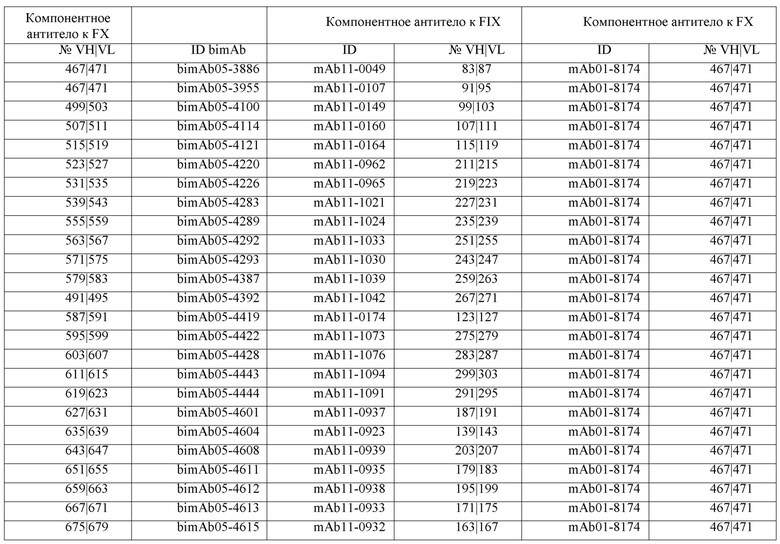
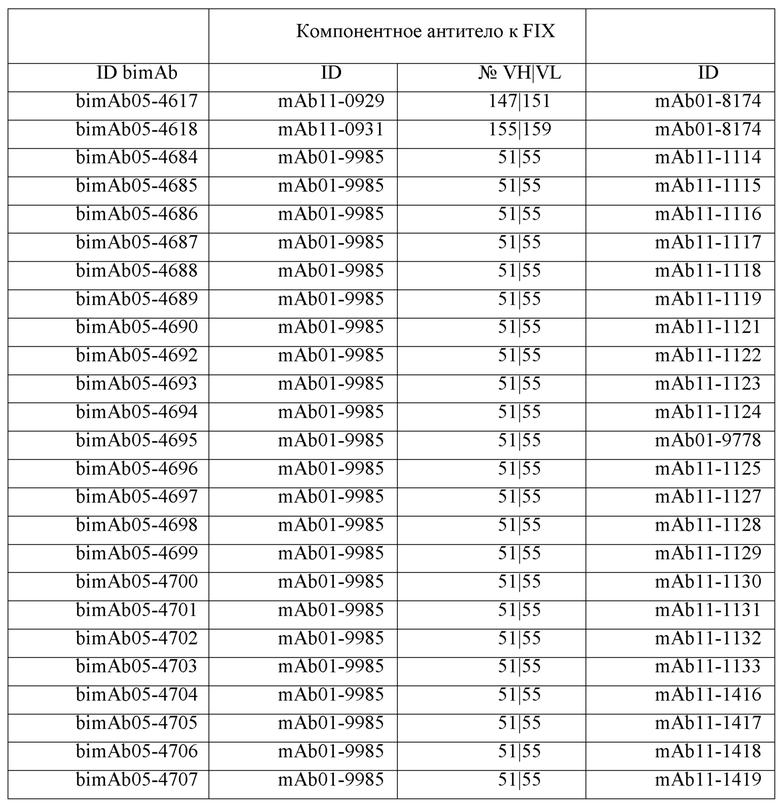
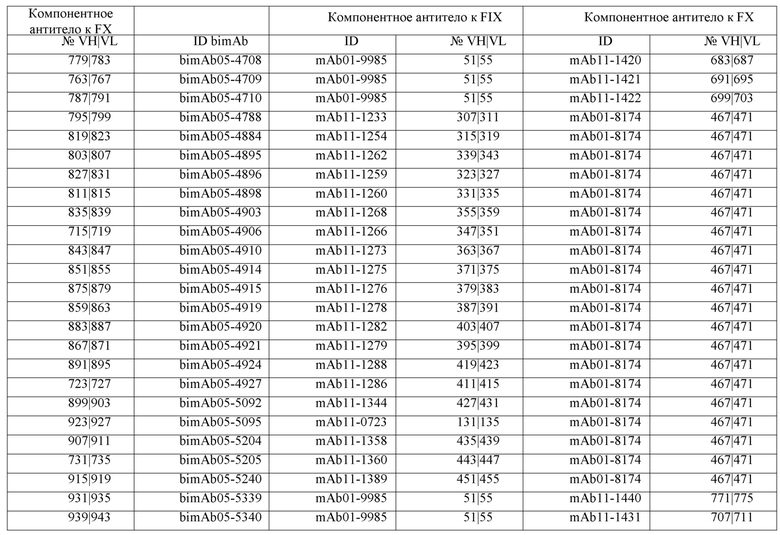
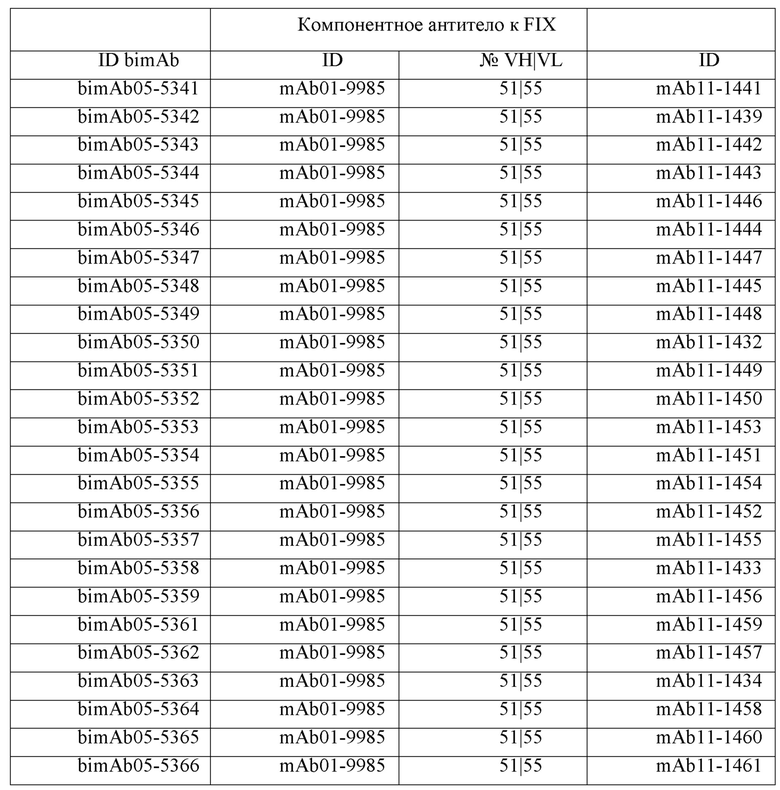
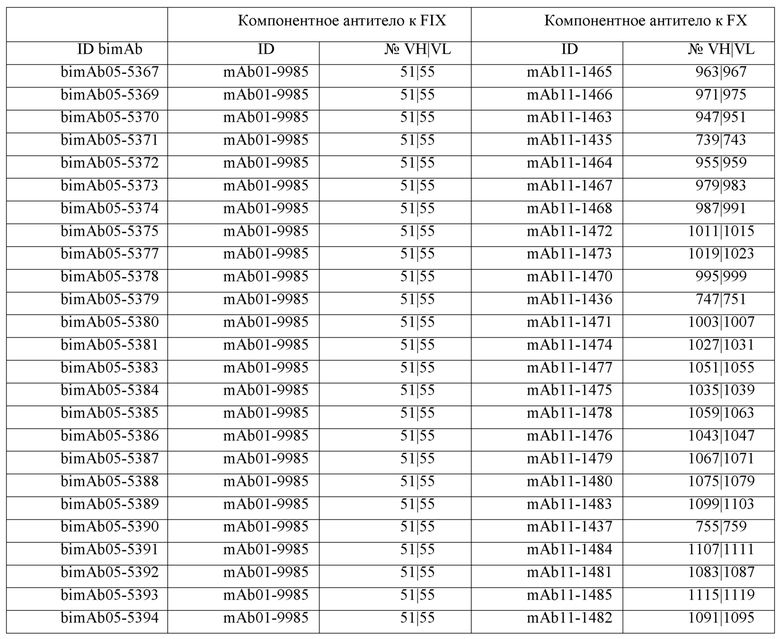
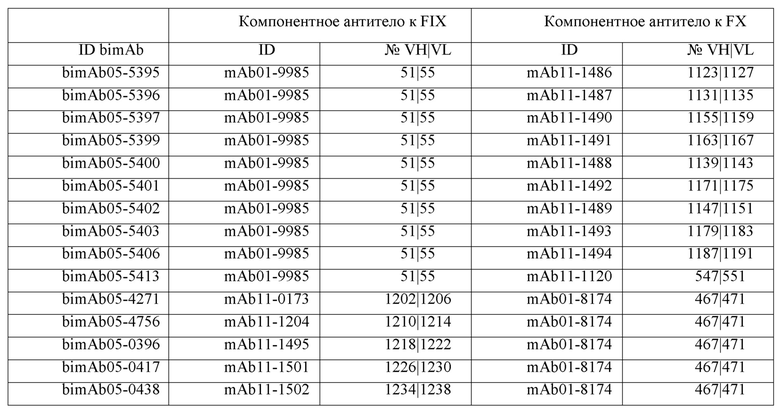
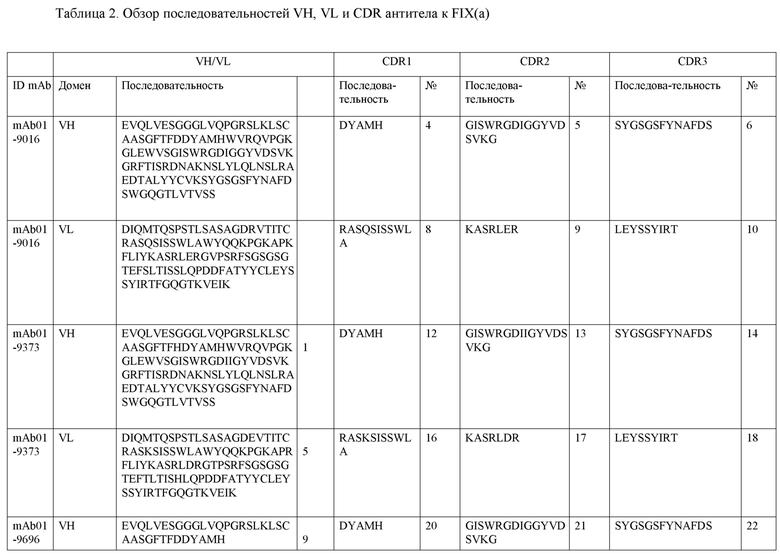
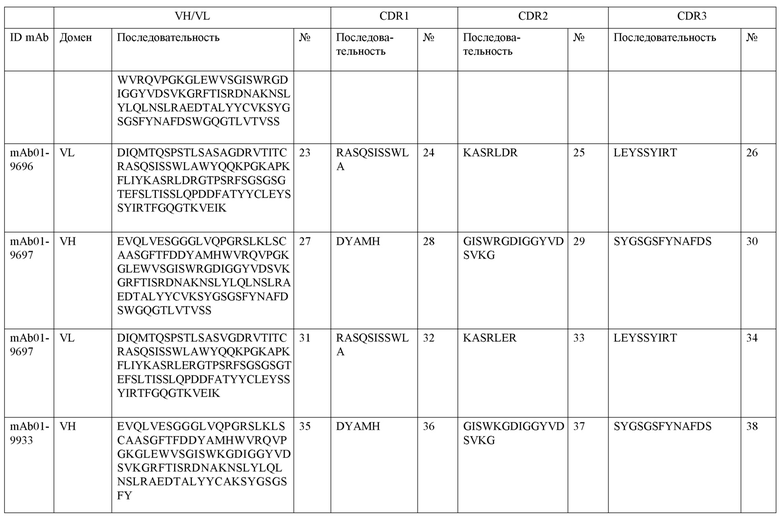
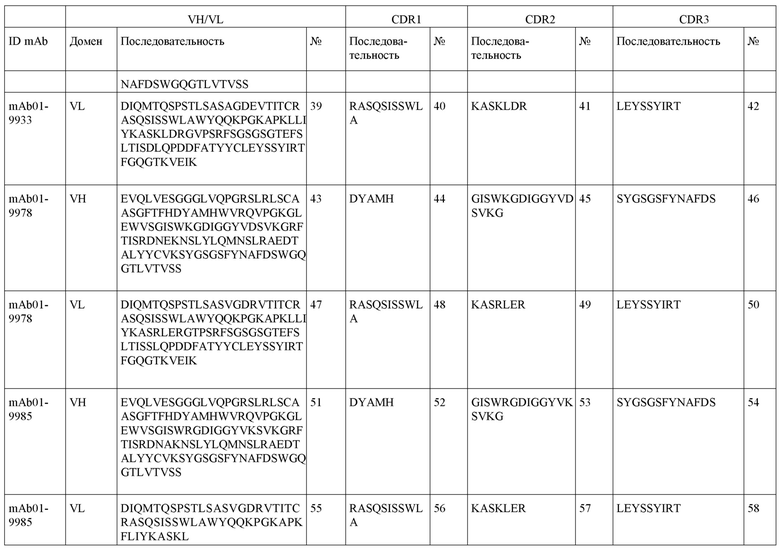
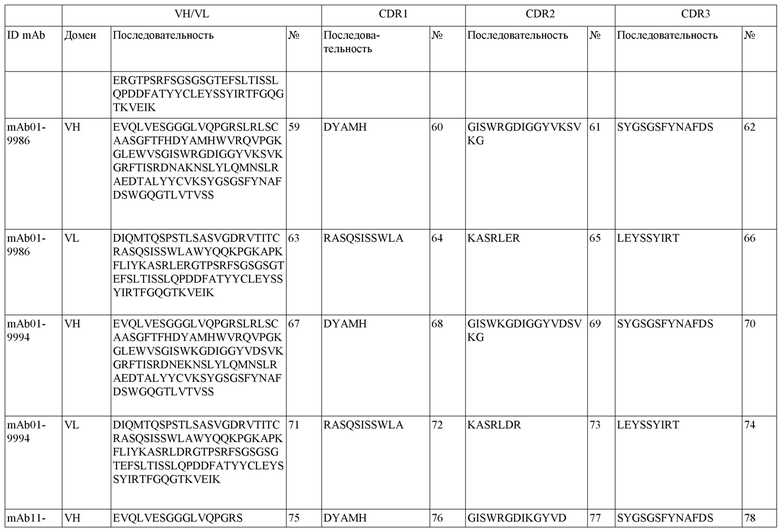
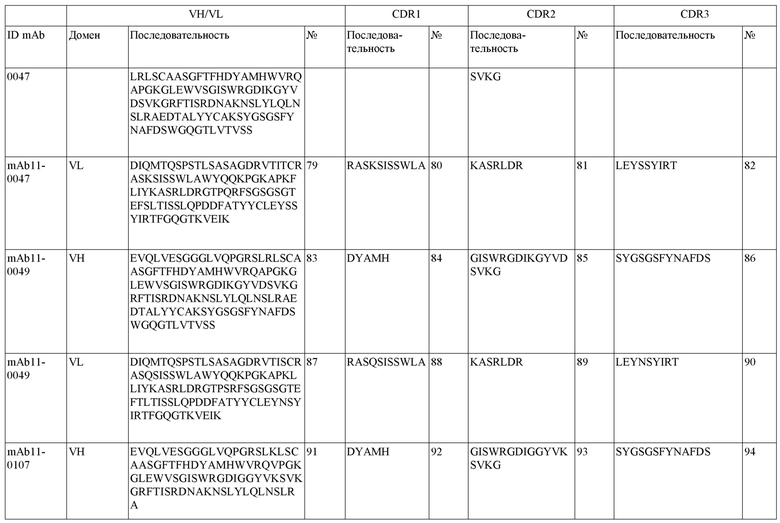
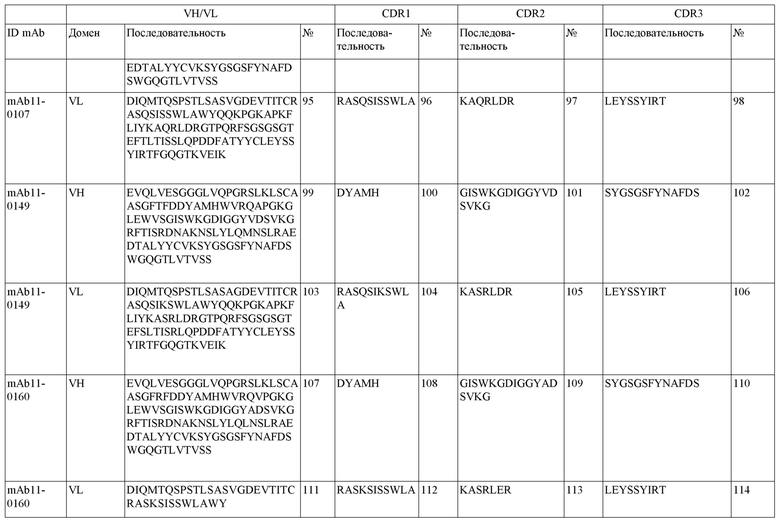
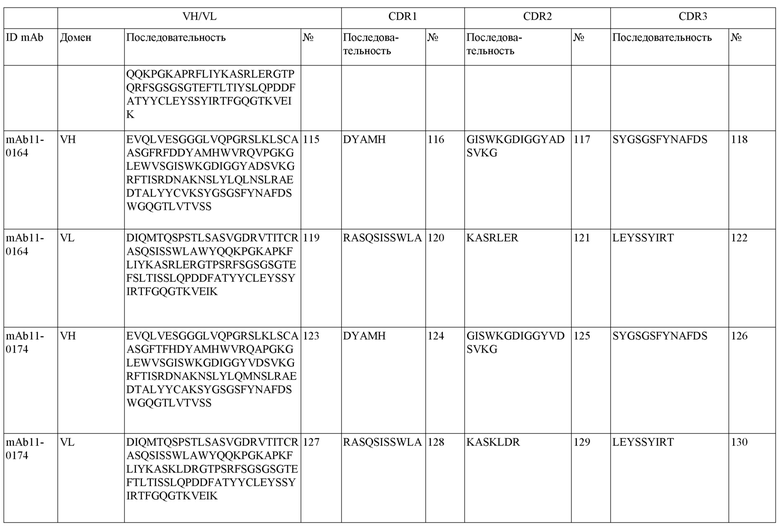
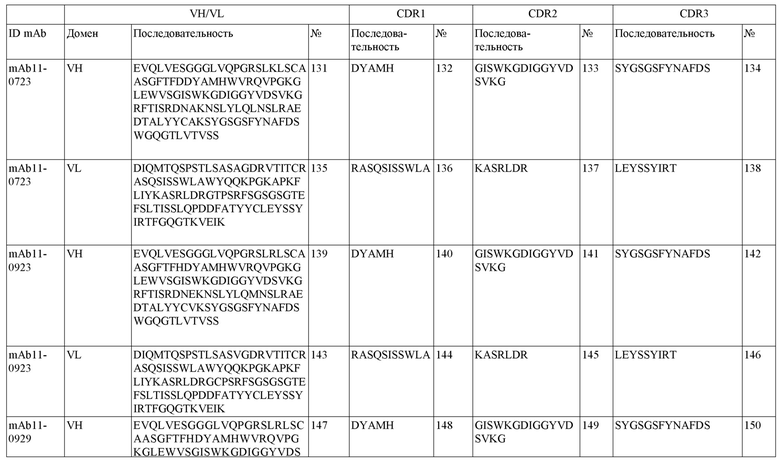
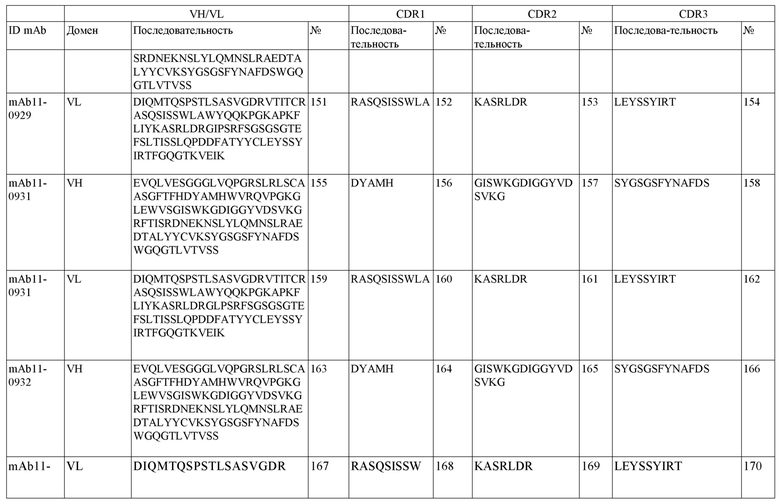
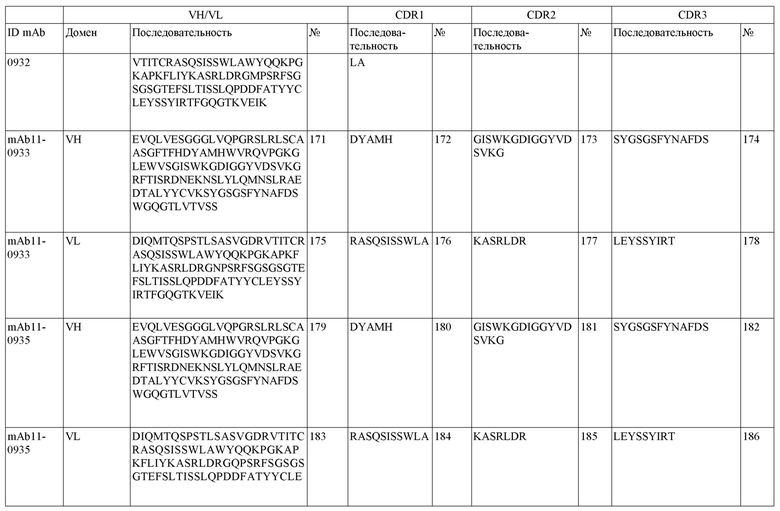
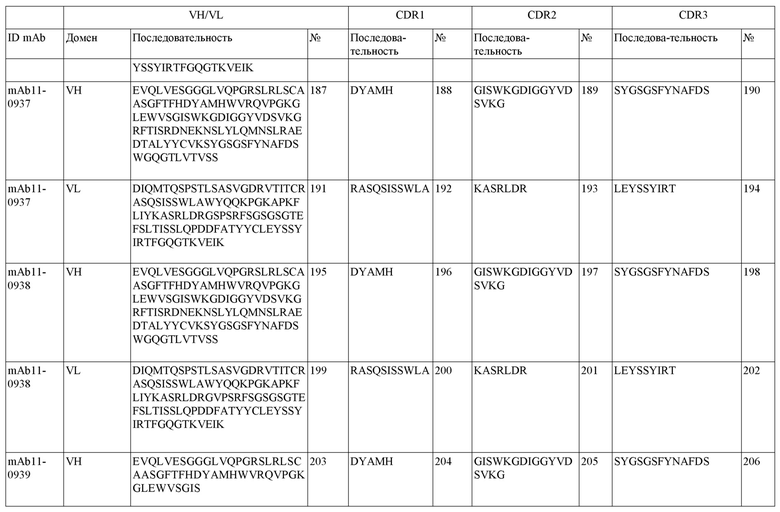
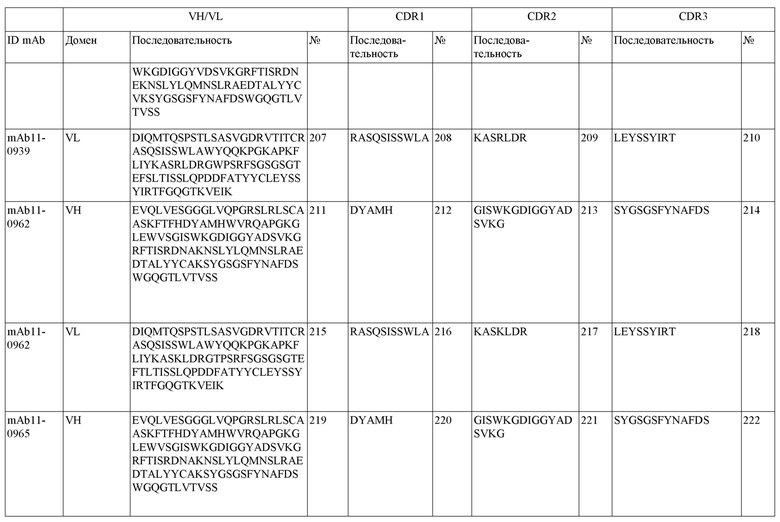
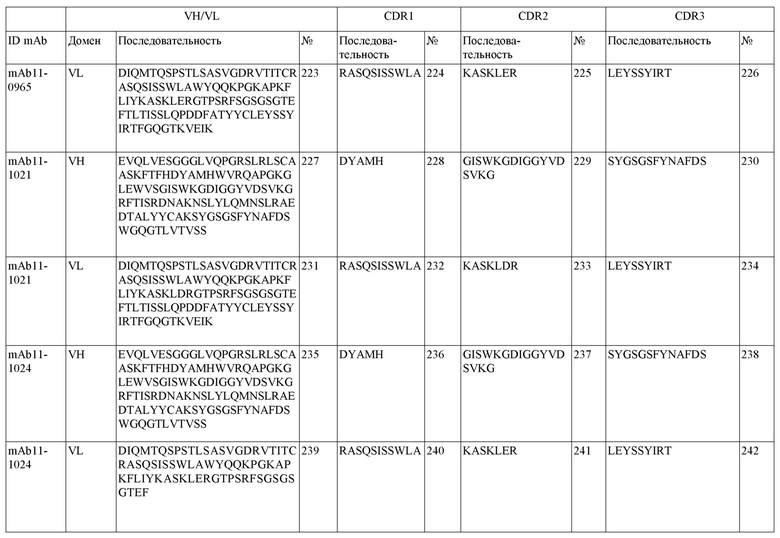
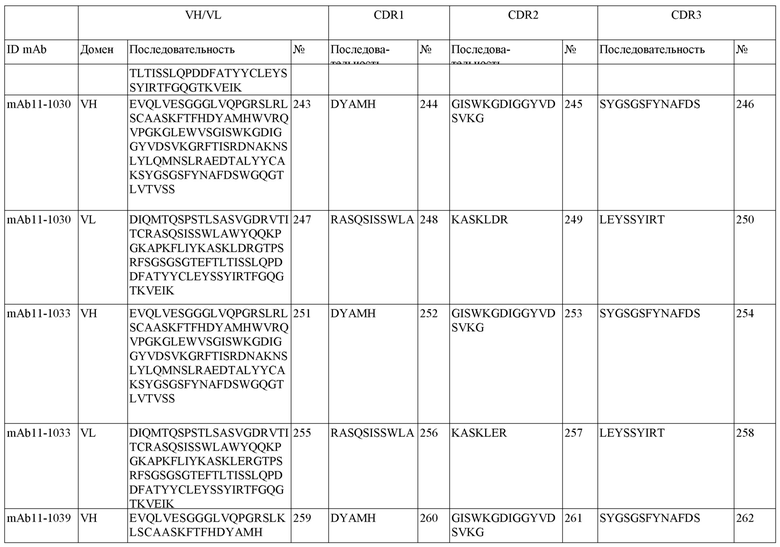
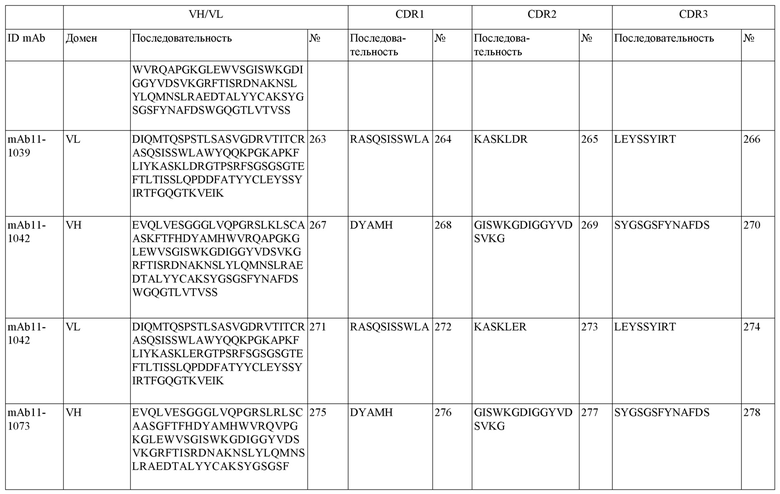
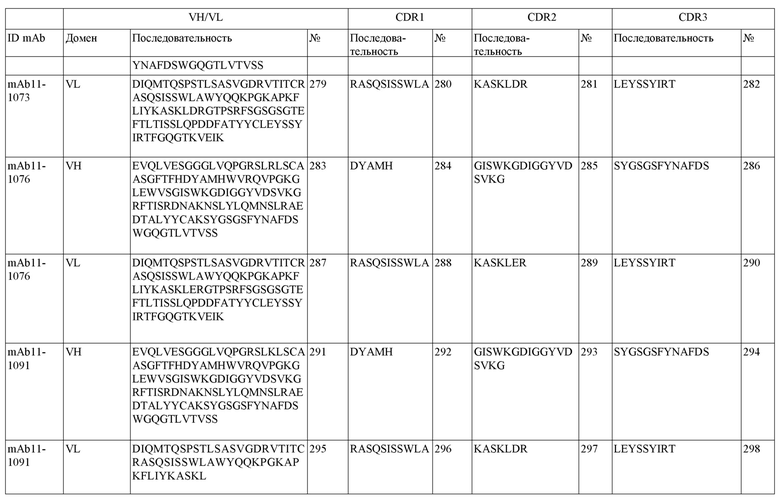
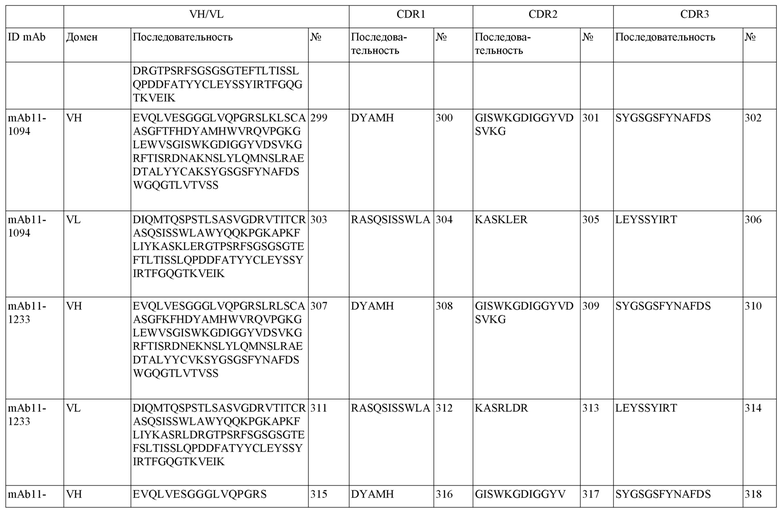
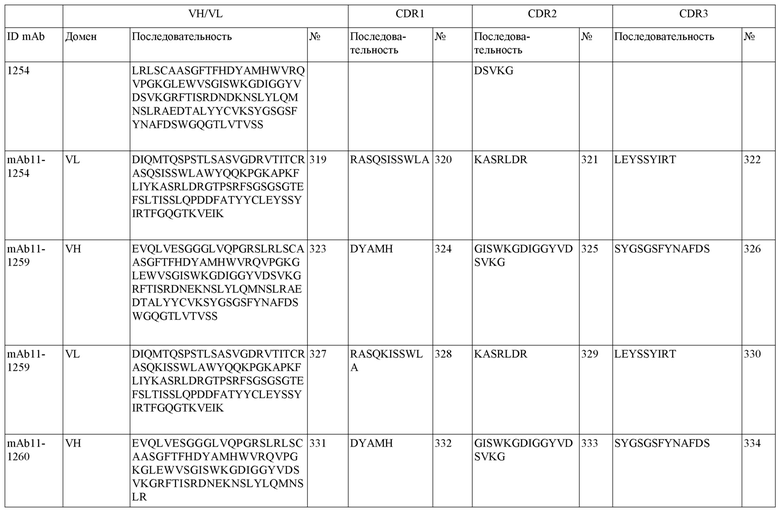
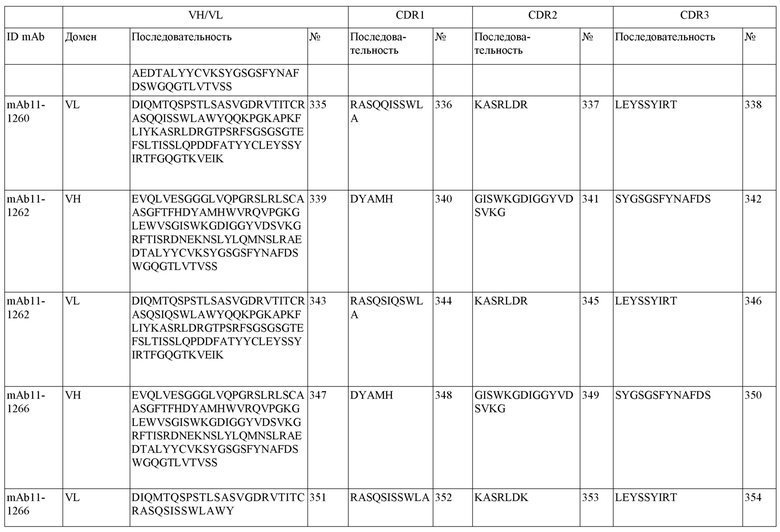
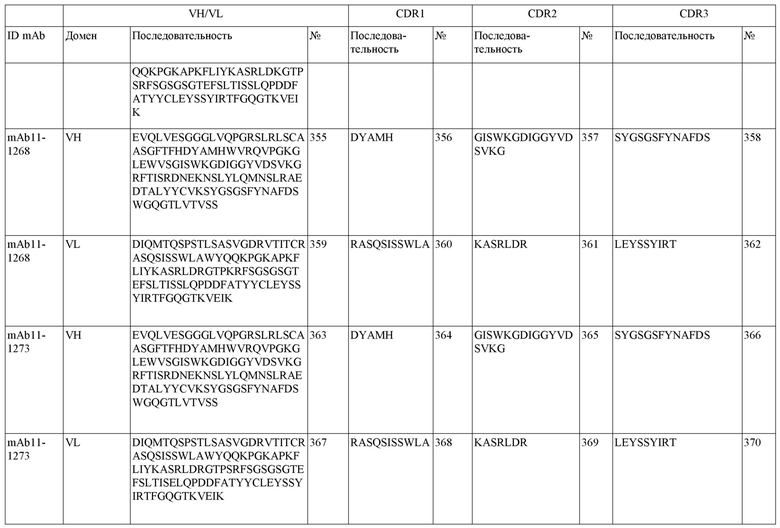
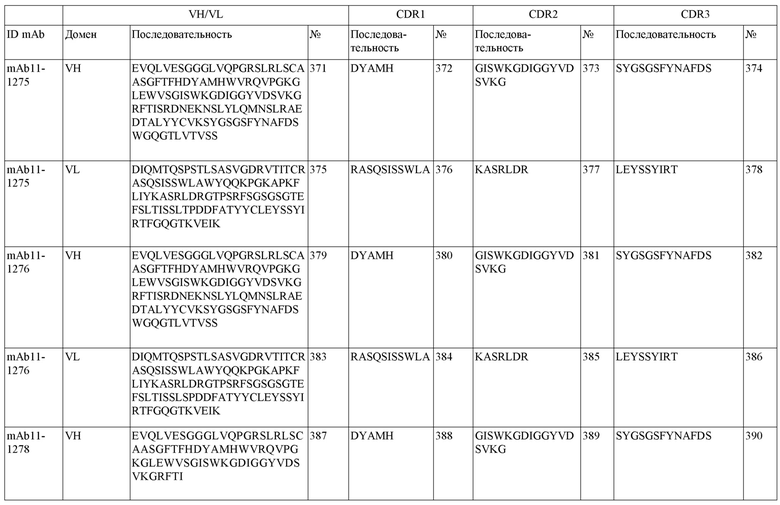
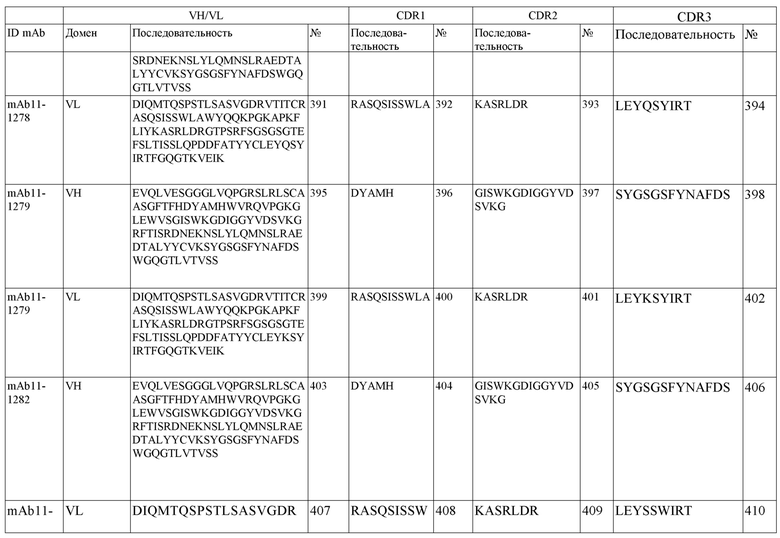
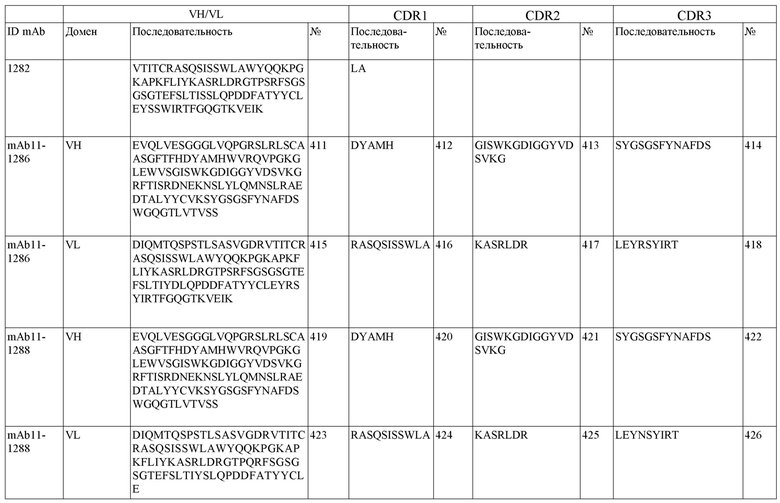
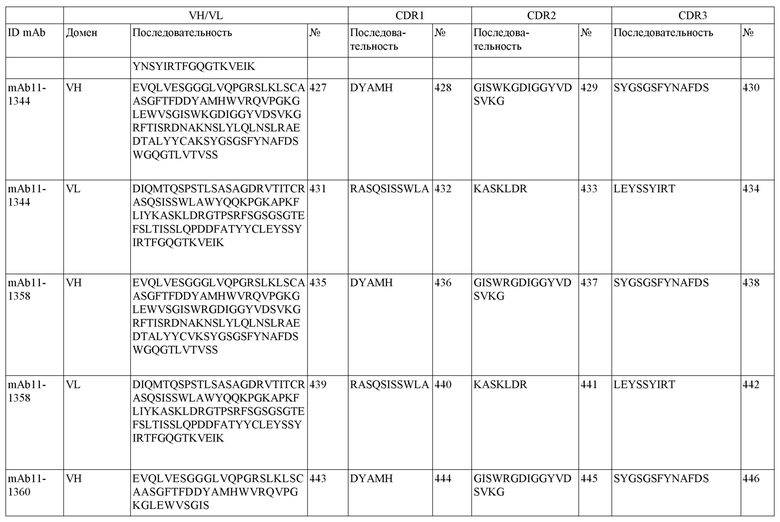
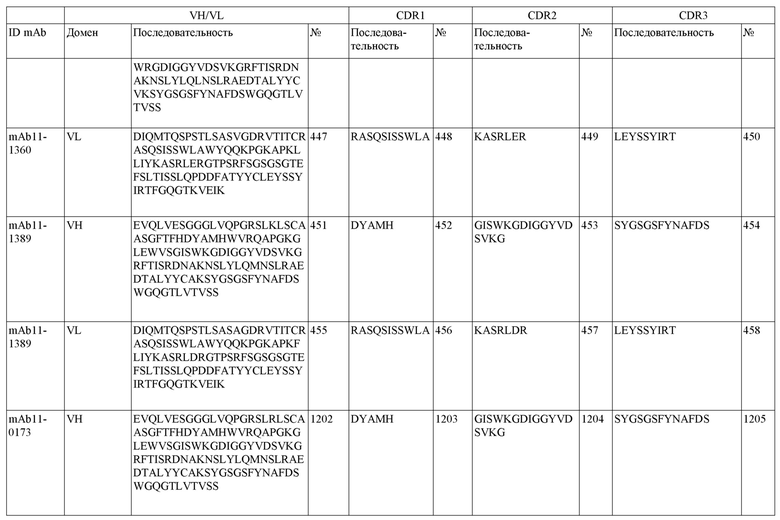
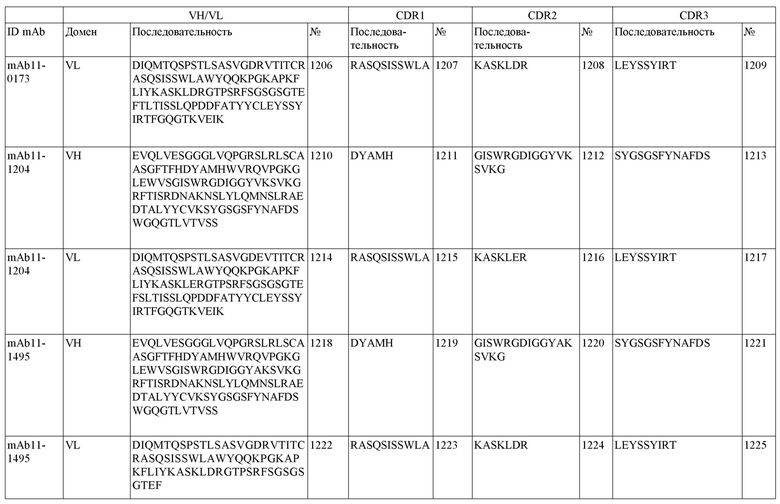
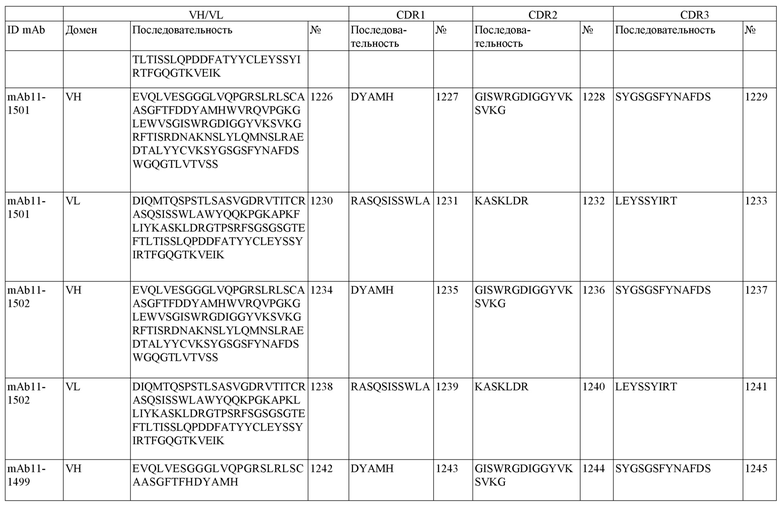
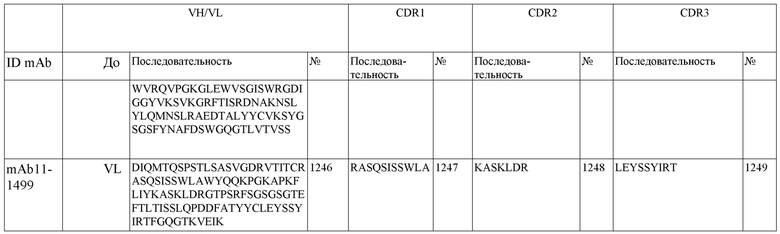
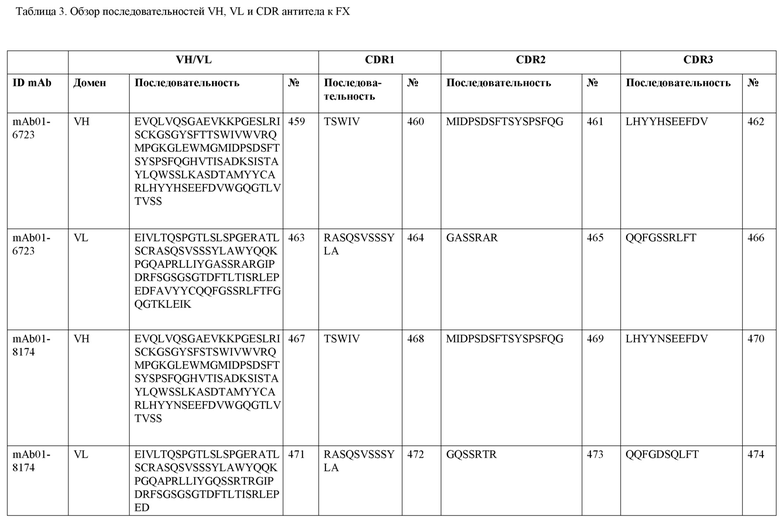
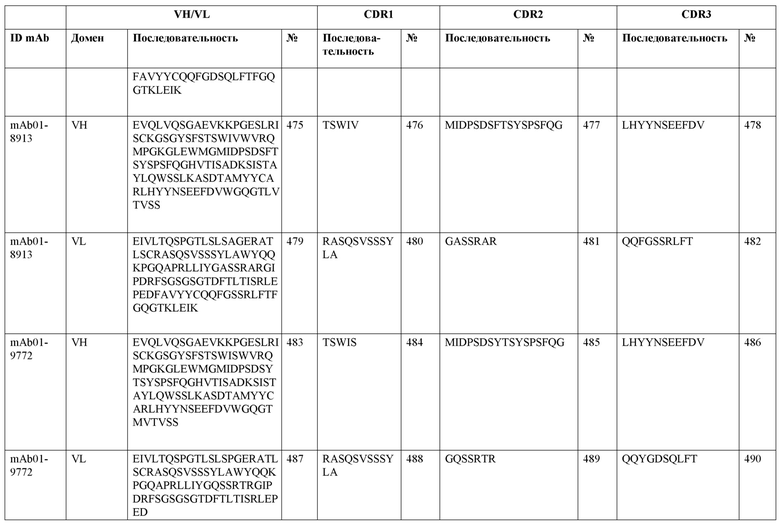
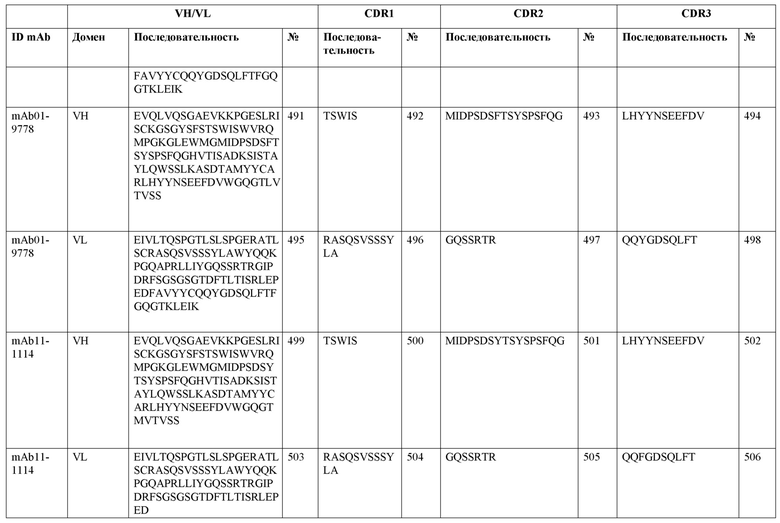
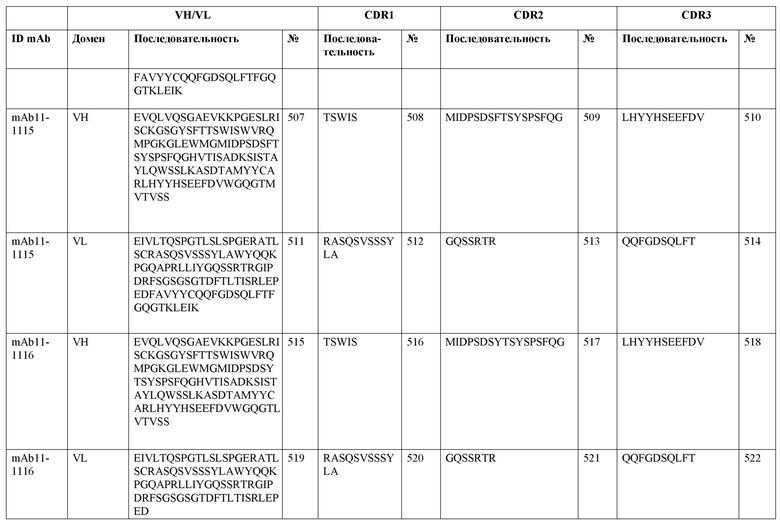
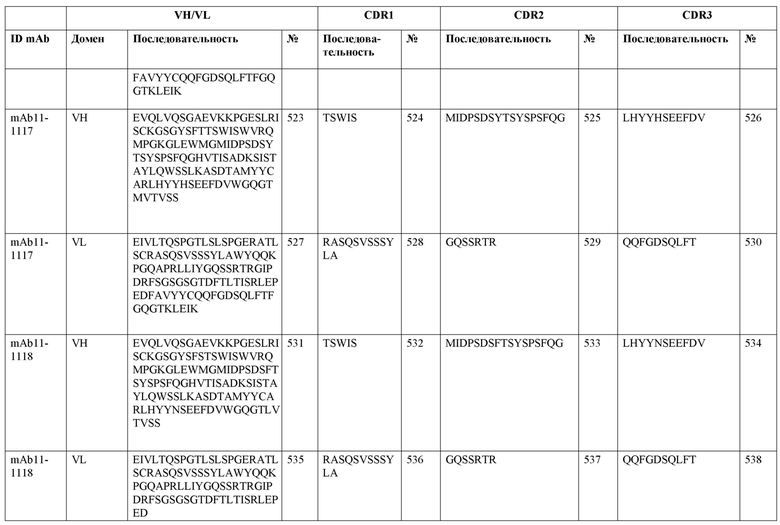
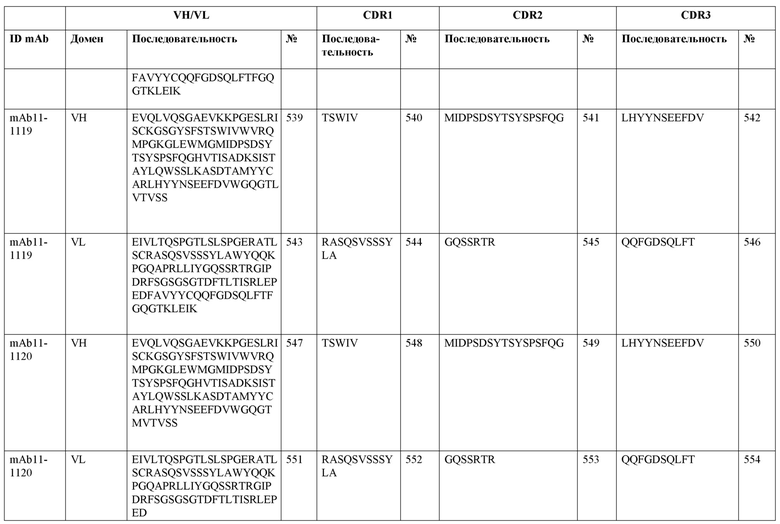
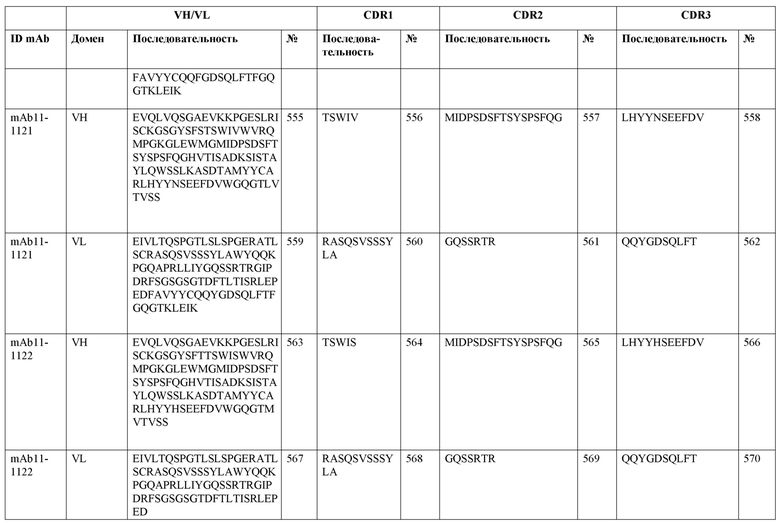
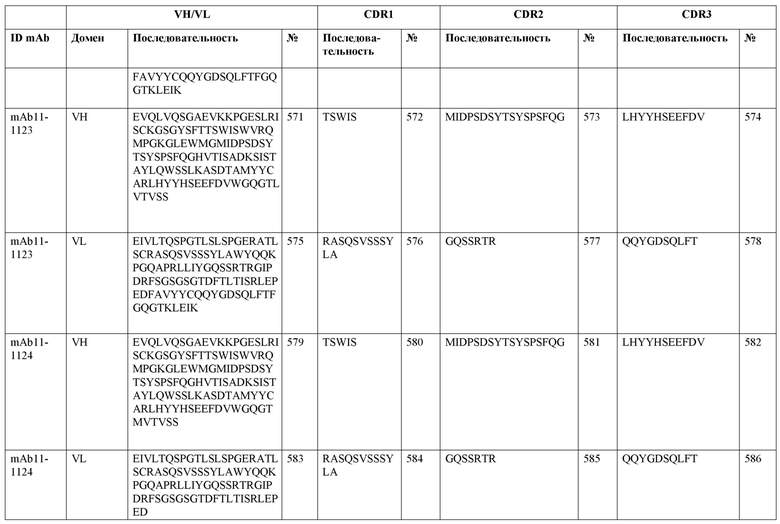
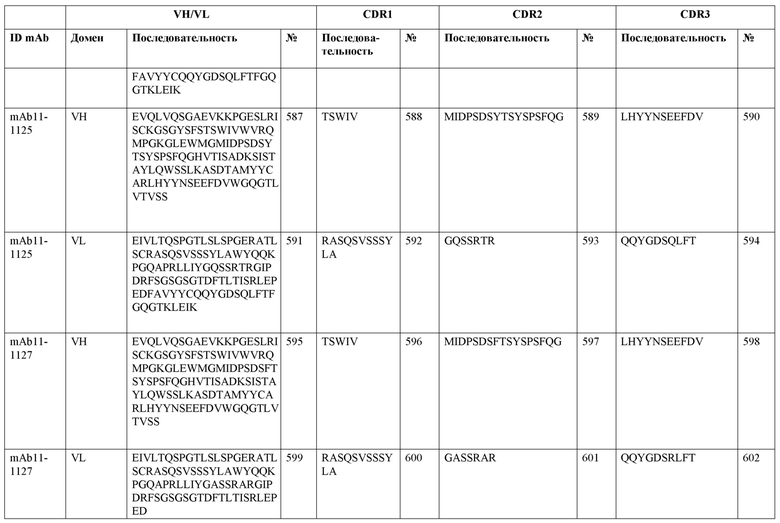
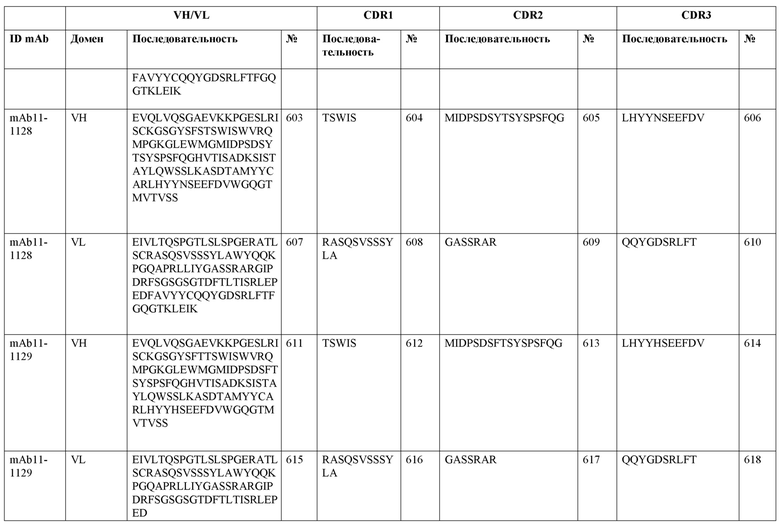
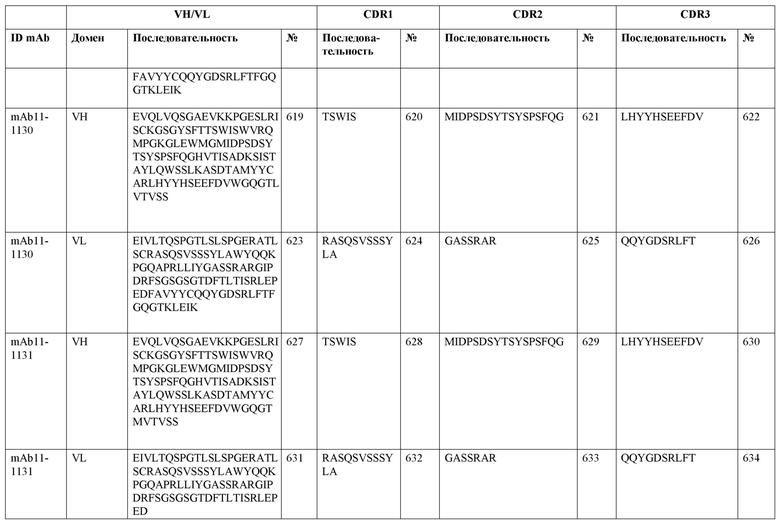
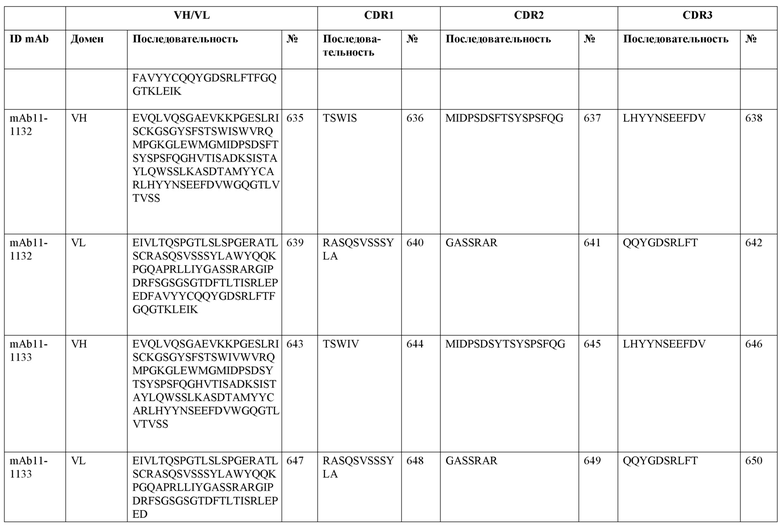
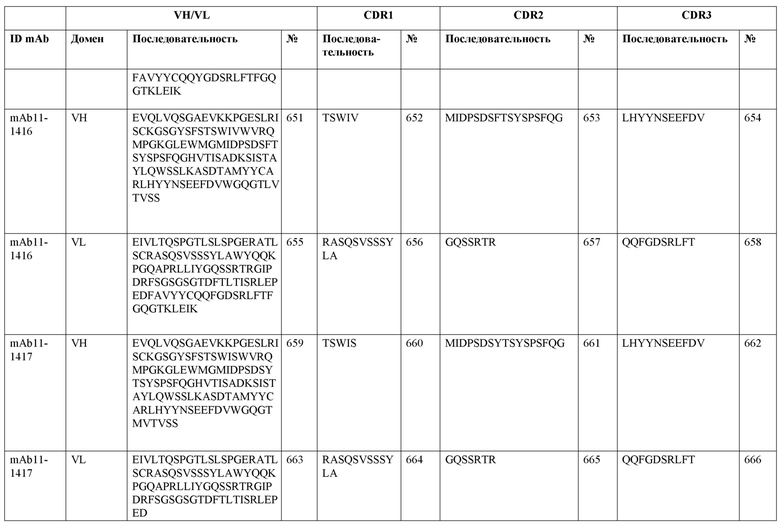
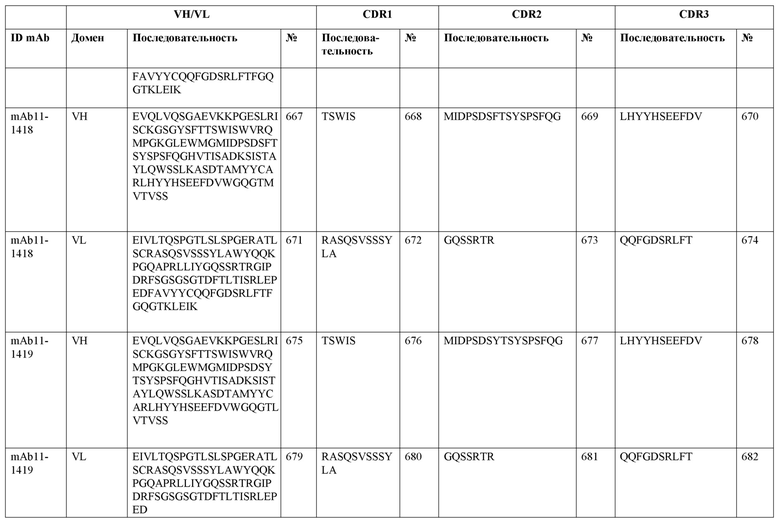
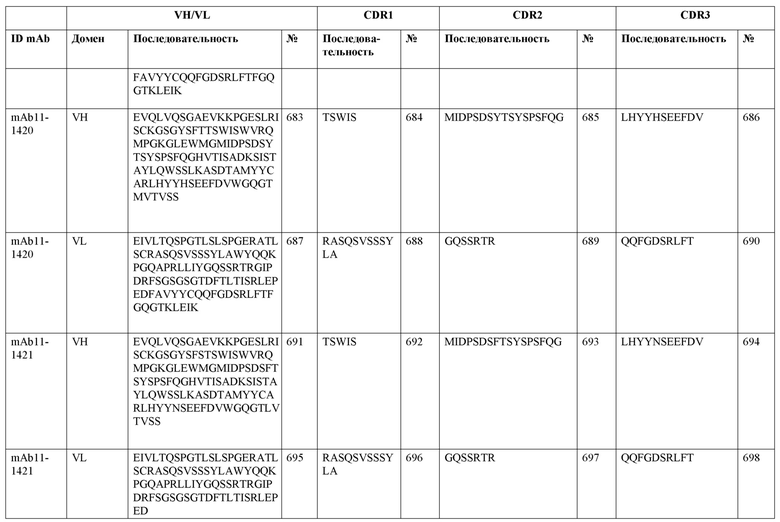
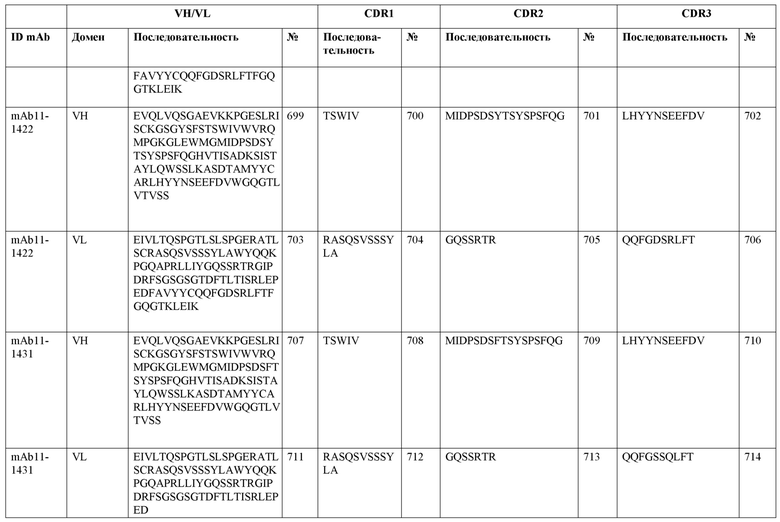
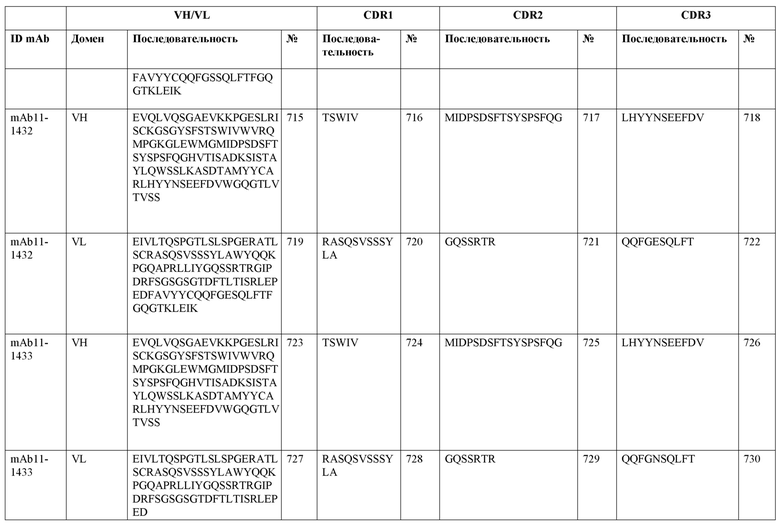
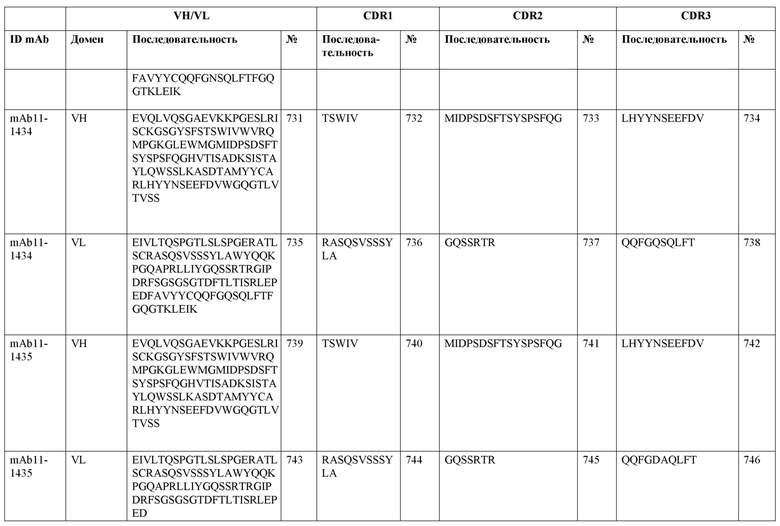
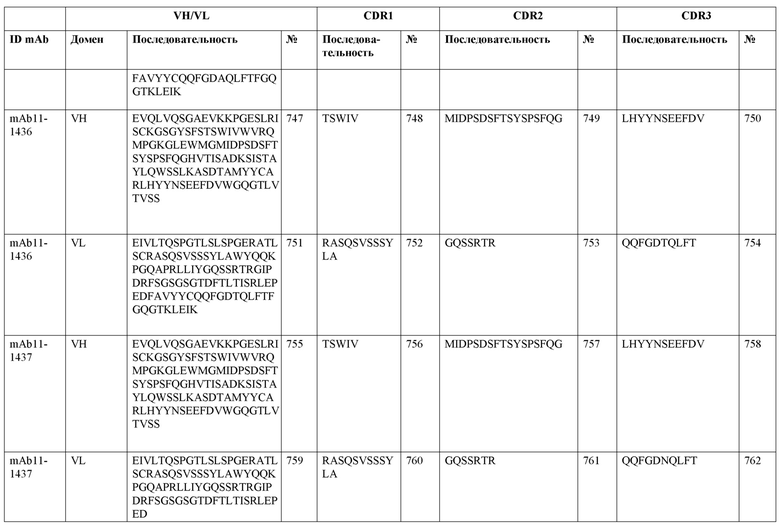
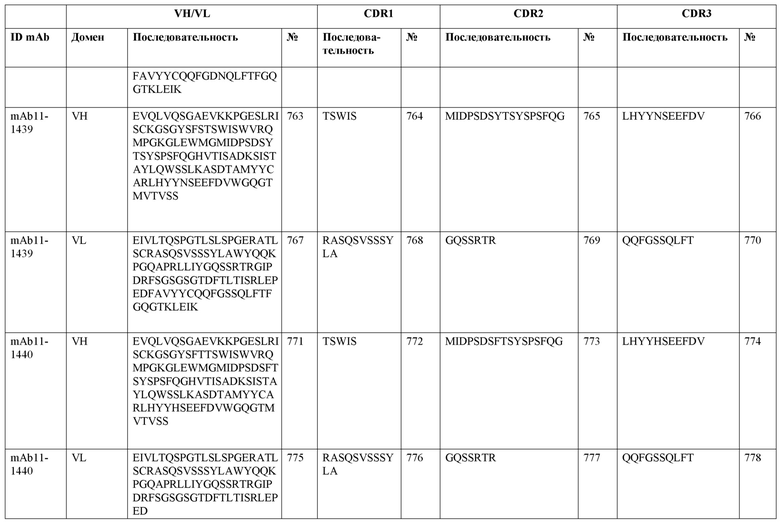
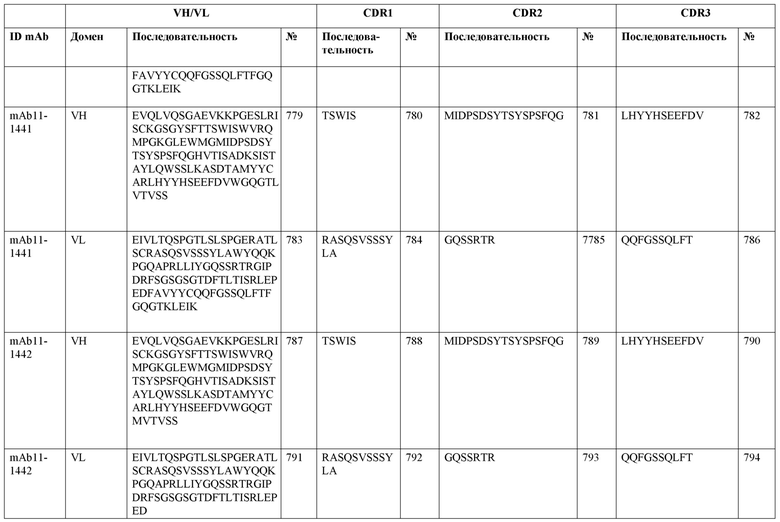
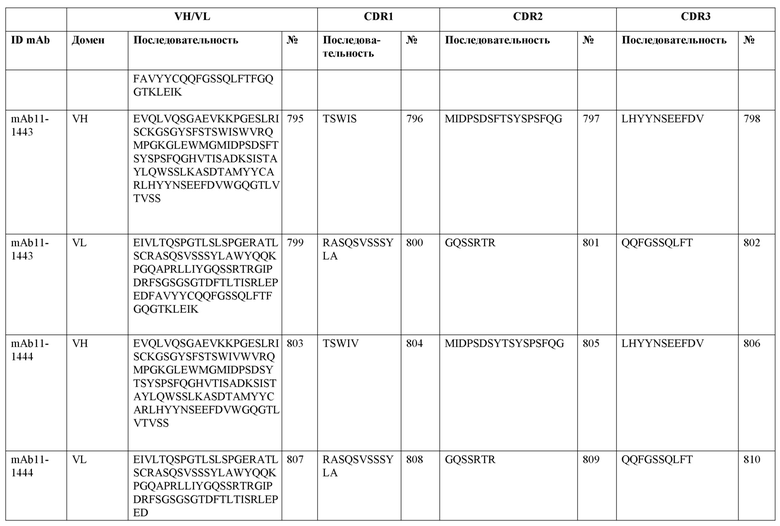
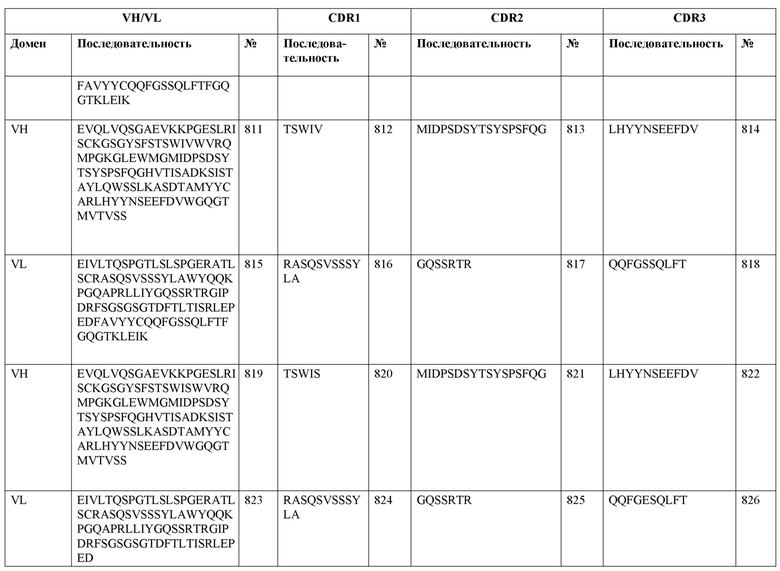
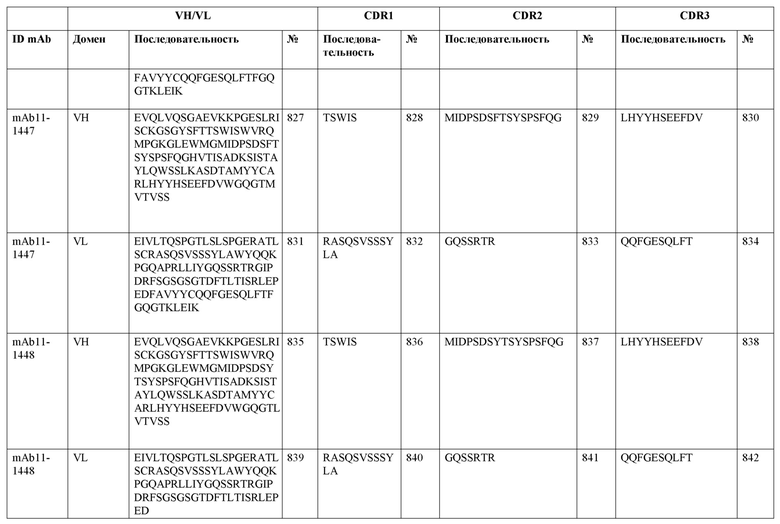
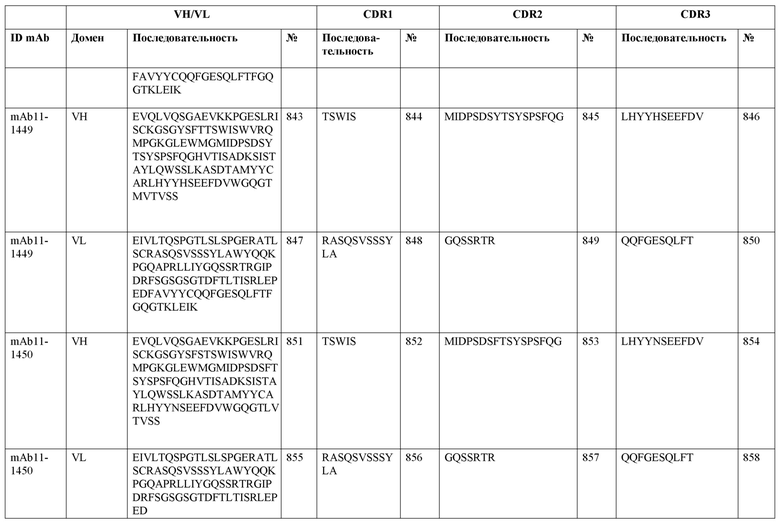
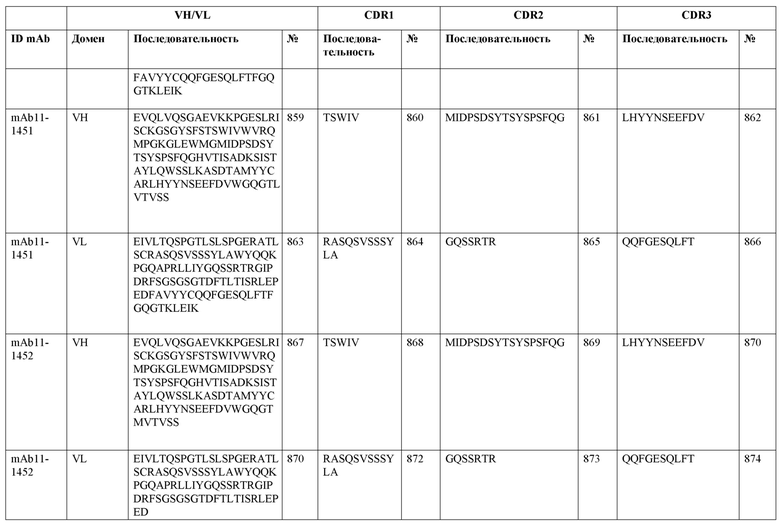
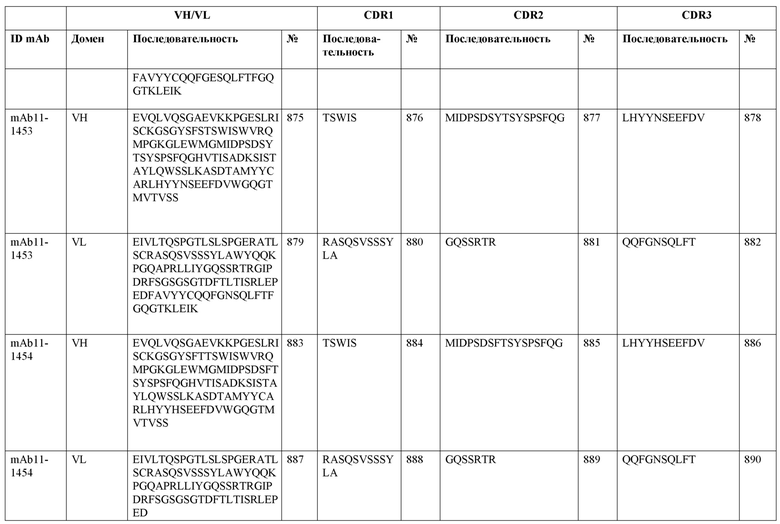
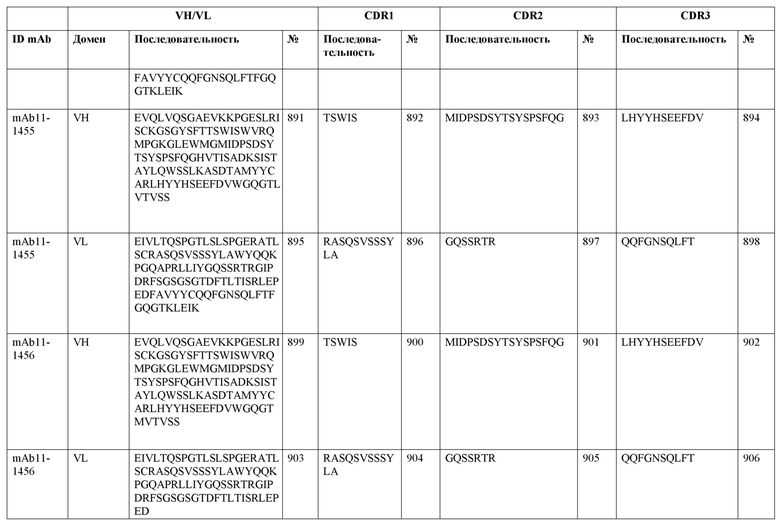
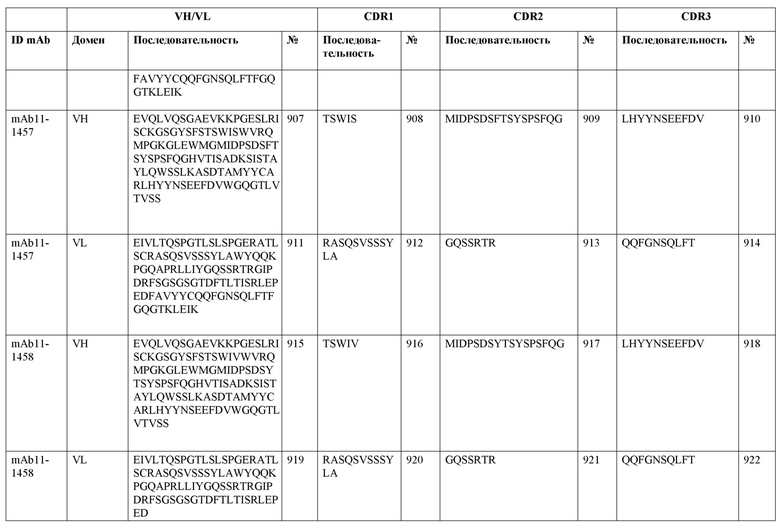
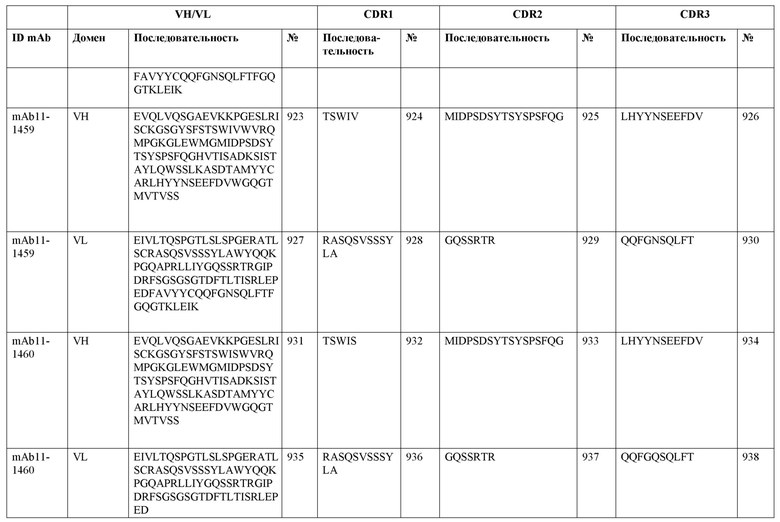
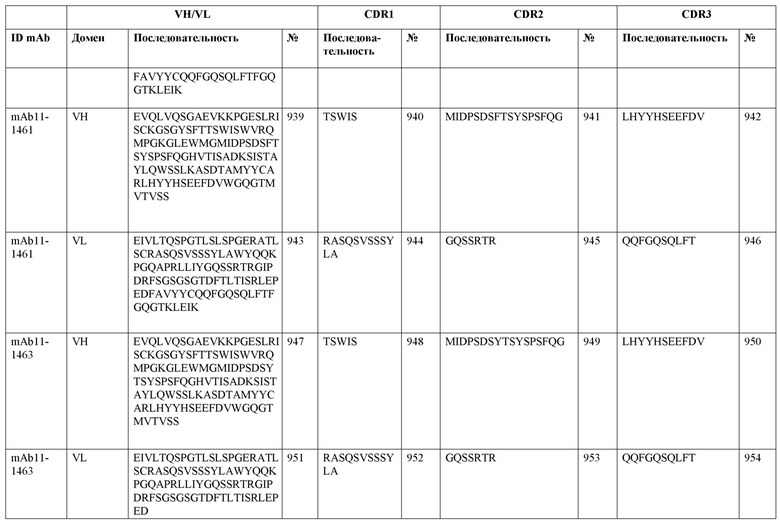
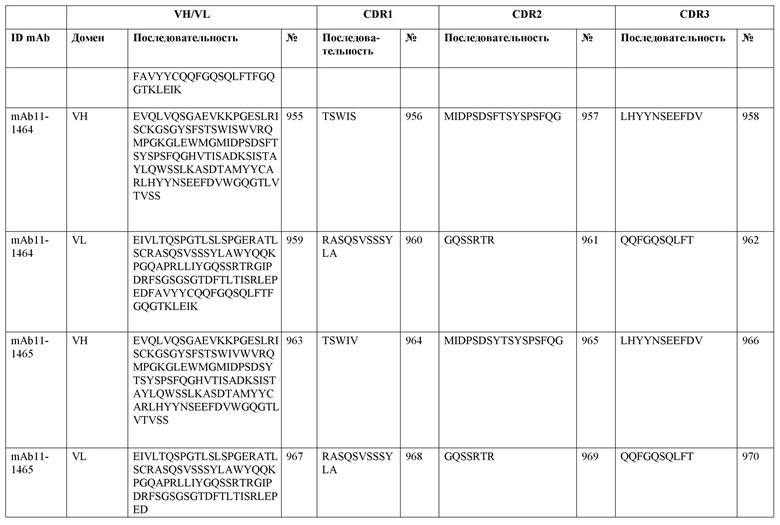
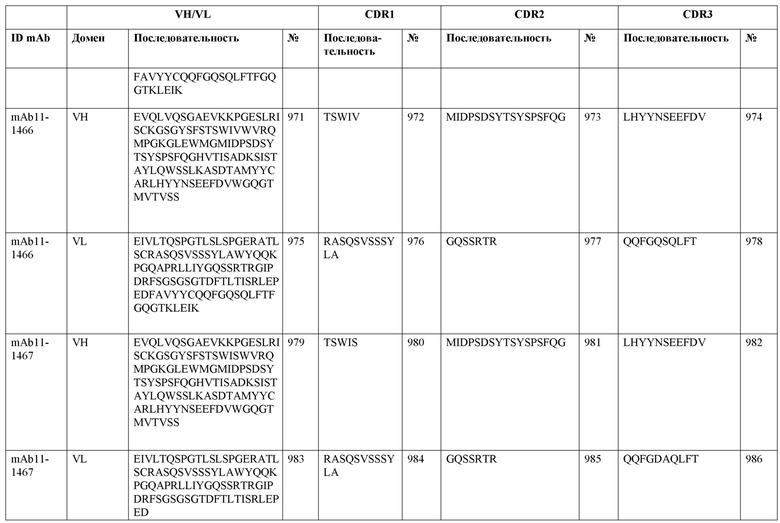
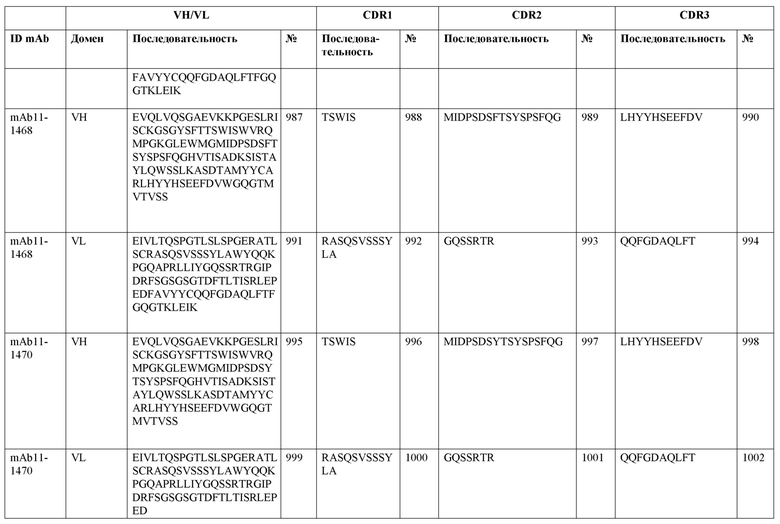
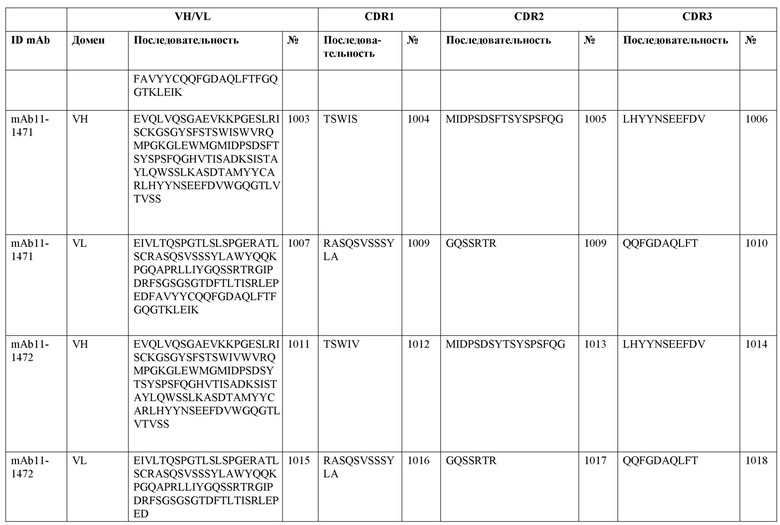
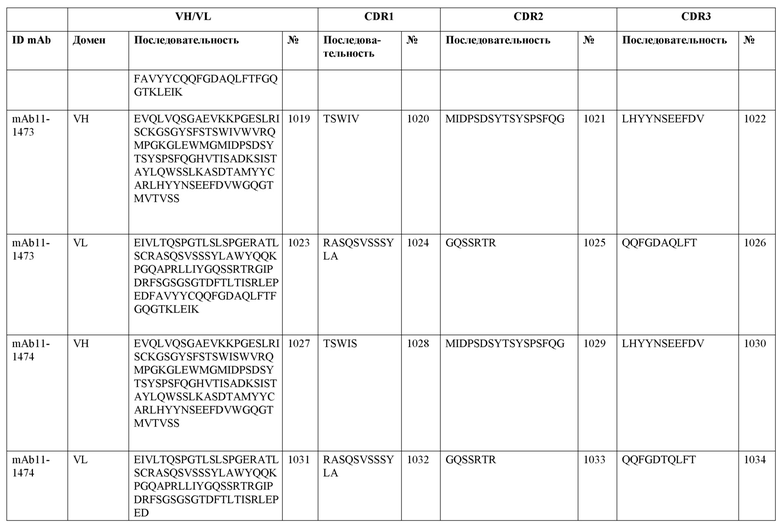
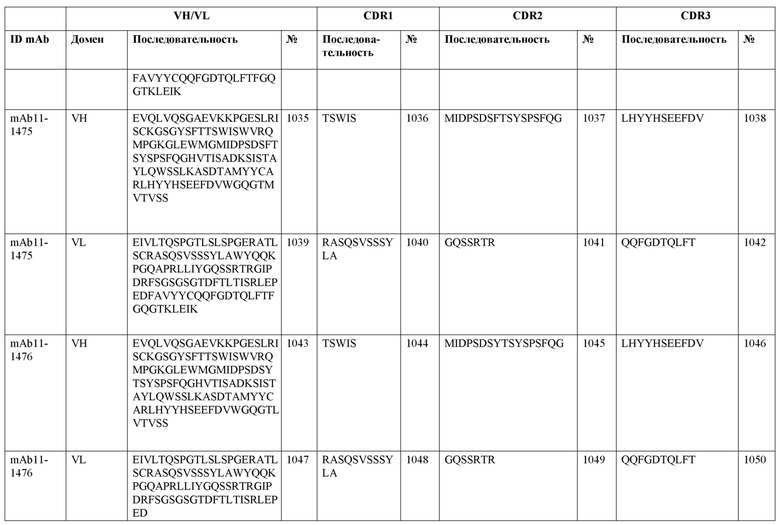
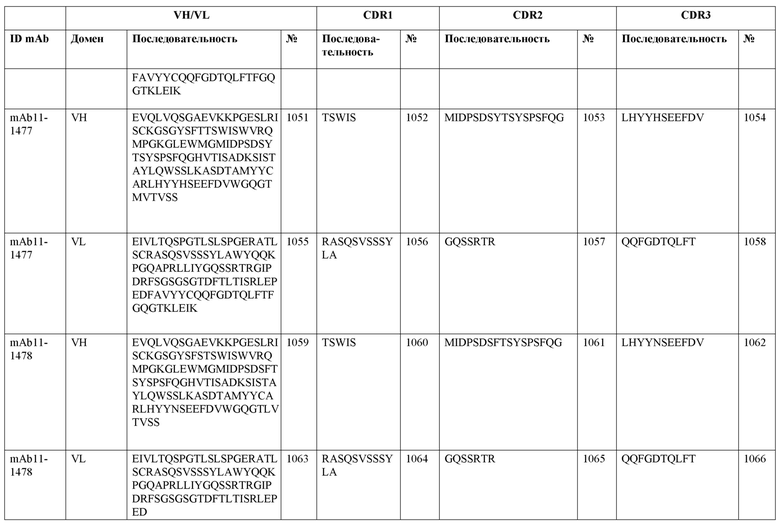
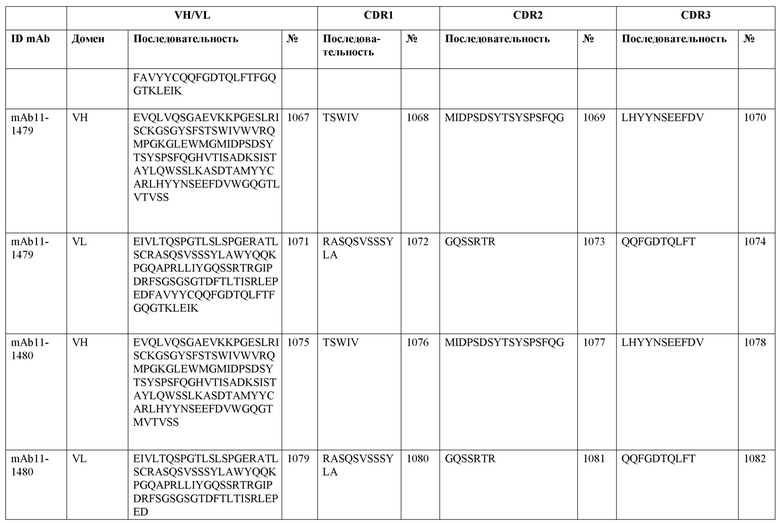
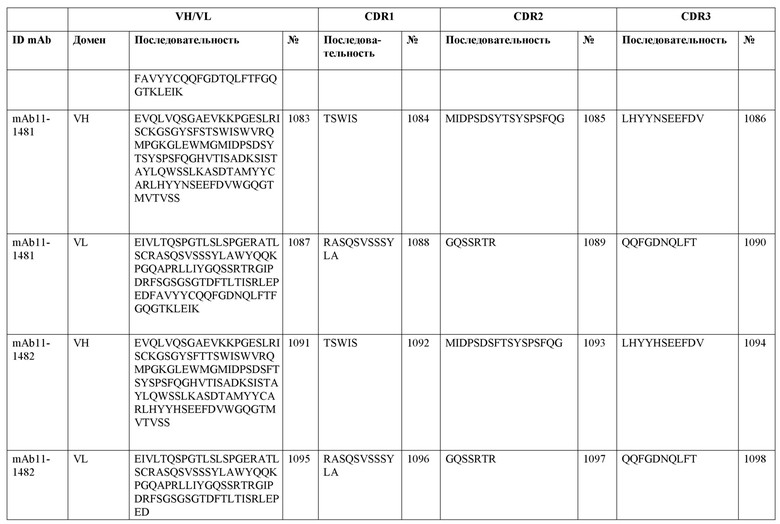
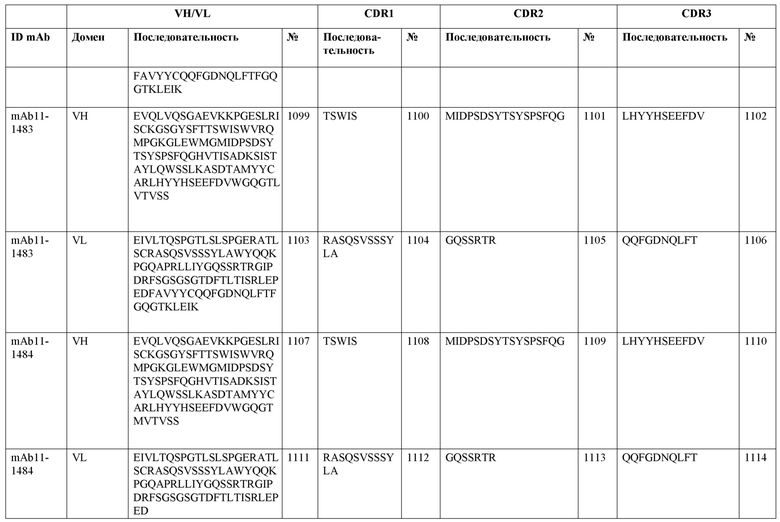
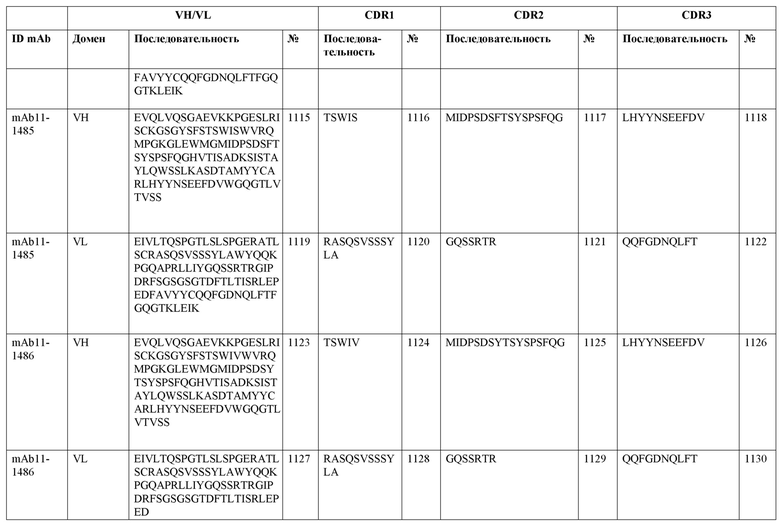
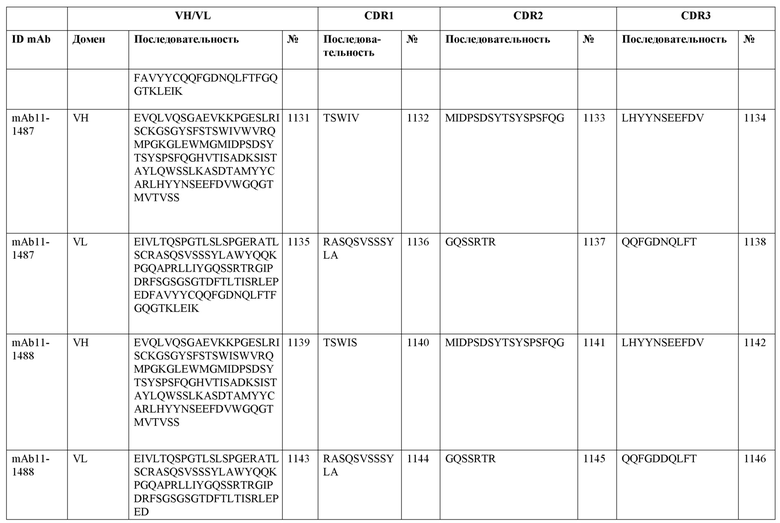
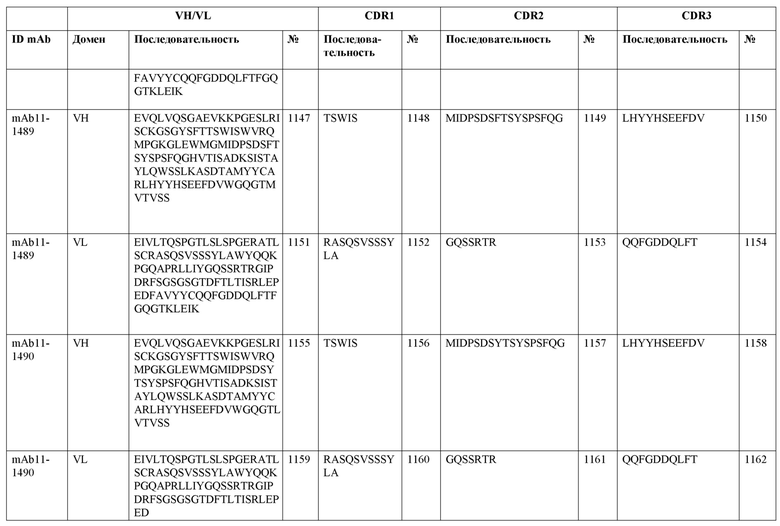
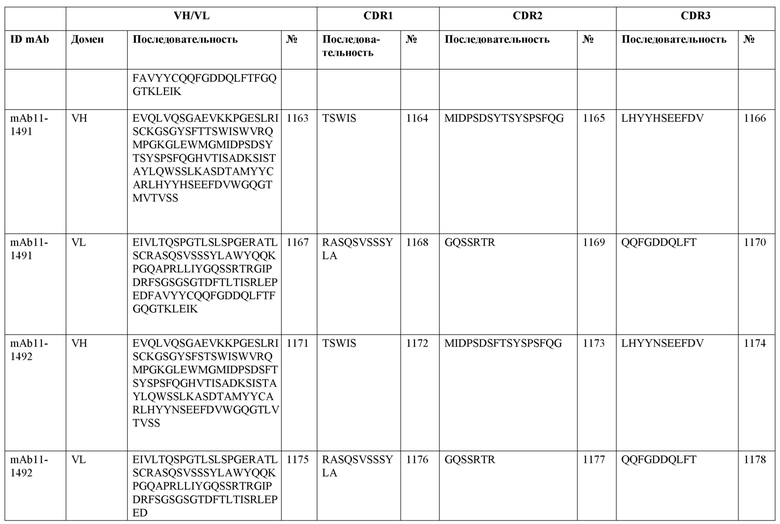
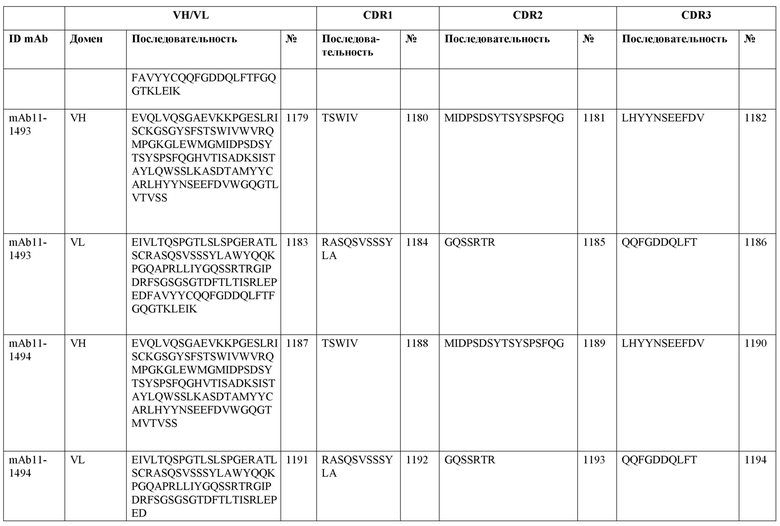
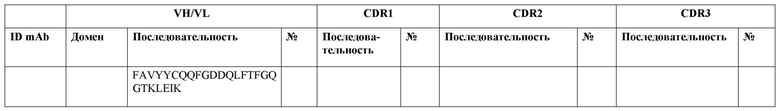
Пример 7a. Сортировка по группам стимулирующих антител к FIX/FIXa
Антитела, способные стимулировать ферментативную активность FIXa в отношении FX, анализировали в экспериментах с сортировкой по группам для определения характеристик связывания у идентифицированных антител с использованием способа, описанного ниже. Анализировали как родительские антитела, так и сконструированные варианты и сравнивали их с другими известными антителами.
Способ сортировки антител по группам
Эксперименты с сортировкой по группам проводили с использованием систем Octet ForteBio (HTX, Red384), основанных на принципе биослойной интерферометрии и оснащенных датчиками со стрептавидином (Pall Life Sciences, Менло Парк, Калифорния), а также с использованием 8-канального режима. Анализы для сортировки по группам проводили с использованием модифицированного тандемного режима. Вкратце, (1) 370 нМ случайным образом биотинилированного FIXa человека (биотинилированного с использованием NHS-d-биотина от Sigma H1759 и FIXa человека, полученного от Haematologic Technologies, Эссекс Джанкшен, Вермонт) захватывали наконечниками со стрептавидином (погружные и считываемые биосенсоры, № позиции:18-5019, Pall Life Sciences, Менло Парк, Калифорния) в течение 5 минут, (2) затем под наконечники со стрептавидином подносили 330 нМ первого бивалентного антитела к FIXa и инкубировали в течение 10 минут до тех пор, пока биотинилированный FIXa не становился полностью насыщенным, и (3) затем под наконечники подносили эквимолярный раствор из 330 нМ первого антитела и 330 нМ второго бивалентного антитела к FIXa в течение 5 минут. Этот модифицированный тандемный режим с включением эквимолярной концентрации первого антитела на стадии инкубации второго антитела был предпочтительным из-за очень низкой аффинности (и высоких скоростей koff) некоторых используемых антител. Неспецифическое связывание оценивали путем включения неродственного бивалентного антитела IgG4 человека в качестве первого и второго контрольных антител. Как видно из таблицы 4, в которой представлены значения ответа на стадии (3), в анализе идентифицировали три разные группы, представленные бивалентными антителами к FIXa, 224F3 (mAb01-1582), mAb01-1767 и mAb01-2434 (плечи ACE910 к FIX(a)). Из таблицы 4 также ясно, что сконструированные антитела mAb01-9933, mAb01-9978, mAb01-9985 и mAb01-9994 демонстрируют тот же тип сортировки по группам, что и их родительское антитело mAb01-1767, и, следовательно, принадлежат к группе B (как показано в таблице 4).
Таблица 4. Значения ответа согласно интерферометрии
(группа A)
(группа B)
(группа С)
(контроль)
Как видно из таблицы 4, IgG4 человека, служащее контрольным антителом, не могло связываться с FIXa при использовании в качестве второго антитела (последняя строка таблицы 4) и не препятствовало связыванию второго антитела с FIXa при использовании в качестве первого антитела (последний столбец таблицы 4). Для 224F3 и mAb01-2434 характерны значения самоконкурентного ответа выше нуля, а именно 0,11 и 0,14 соответственно, что все еще значительно ниже самых низких значений ответа для вторых антител, принадлежащих к другой группе, например, 0,24 для mAb01-9978 (2е антитело)/224F3 (1е антитело) и 0,34 для mAb01-9978 (2е антитело)/mAb01-2434(1е антитело). Некоторые примеры кривых полного связывания показаны на фигурах 4A и 4B (C, D, E и F).
Пример 7b. Сортировка по группам стимулирующих антител к FX/FXa
Антитела к FX(а) анализировали в экспериментах с сортировкой по группам для определения характеристик связывания у идентифицированных антител с использованием способа, описанного ниже. Анализировали как родительские антитела, так и сконструированные варианты и сравнивали их с другими известными антителами.
Способ сортировки антител по группам
Эксперименты с сортировкой по группам проводили с использованием систем Octet ForteBio (HTX, Red384), оснащенных датчиками со стрептавидином (Pall Life Sciences, Менло Парк, Калифорния), а также с использованием 8-канального режима (Red384 и HTX). Анализы для сортировки по группам проводили с использованием модифицированного тандемного режима. Вкратце, (1) 363 нМ случайным образом биотинилированного FXa человека (полученного от Haematologic technologies и биотинилированного с использованием NHS-d-биотина) захватывали наконечниками со стрептавидином в течение 5 минут (погружные и считываемые биосенсоры, № позиции:18-5019, Pall Life Sciences, Менло Парк, Калифорния), (2) затем под наконечники со стрептавидином подносили 330 нМ первого бивалентного антитела к FX(a) и инкубировали в течение 10 минут до тех пор, пока биотинилированный FXa не становился полностью насыщенным, и (3) затем под наконечники подносили эквимолярный раствор из 330 нМ первого антитела и 330 нМ второго бивалентного антитела к FX(a) в течение 5 минут. Режим с включением эквимолярной концентрации первого антитела на стадии инкубации второго антитела был предпочтительным из-за очень низкой аффинности (и высоких скоростей koff) некоторых используемых антител. Неспецифическое связывание оценивали путем включения неродственного бивалентного антитела IgG4 человека в качестве первого и второго контрольных антител. Как видно из таблицы 5, в которой представлены значения ответа на стадии (3), в анализе идентифицировали две разные группы, представленные бивалентными антителами к FX(a), mAb01-2435 (плечи ACE910 к FX(a)) и mAb01-6723. Из таблицы 5 также ясно, что сконструированные антитела mAb01-8174 и mAb01-9772 демонстрируют тот же тип сортировки по группам, что и их родительское антитело mAb01-6723, и, следовательно, принадлежат к группе 2 (как показано в таблице 5).
Некоторые примеры кривых полного связывания показаны на фигуре 5 (A и B).
Таблица 5. Значения ответа согласно интерферометрии
(группа 1)
(группа 2)
(контроль)
Пример 8. Кристаллизация и картирование эпитопов/паратопов антител к FIX(a) с использованием рентгеновской кристаллографии
Кристаллизация и картирование эпитопа/паратопа антитела к FIX(a) mAb01-9994
Кристаллизация
Fab-фрагмент, соответствующий mAb01-9994, смешивали при молярном соотношении 1:1 с фактором IXa человека без домена Gla (дикого типа), c ингибированным EGR-CK, экспрессированным в бактериальных клетках, партия № hGDFIXAWTEGR_05 (приобретен у Cambridge ProteinWorks), и кристаллы комплекса Fab/FIXa выращивали с использованием методики диффузии пара в сидячей капле при 18°C. 100 нл белкового раствора, содержащего 5,5 мг/мл комплекса в 20 мМ Tris-HC, рН 7,4, 50 мM NaCl и 2,5 мM CaCl2, смешивали с 100 нл 0,1 M бицина, pH 9,0, 2% (объем/объем) 1,4-диоксана, 10 % ПЭГ 20000 в качестве осадителя и инкубировали над 60 мкл осадителя.
Сбор данных дифракции
Кристалл подвергали криозащите путем добавления 1 мкл осадителя с добавлением 20% этиленгликоля к кристаллизационной капле перед мгновенным охлаждением в жидком азоте. Данные дифракции собирали при 100K в пучке синхротронного излучения i03 от Diamond Light Source (длина волны 0,9763 Å) с использованием пиксельного детектора Pilatus3 6M от Dectris. Автоиндексирование, интеграцию и масштабирование данных выполняли с помощью программ из пакета XDS (статистические значения данных дифракции обобщены в таблице 6).
Определение и уточнение структуры
Асимметричная единица содержит один комплекс Fab:FIXa, исходя из анализа коэффициента Мэтьюса. Структуру определяли путем молекулярной замены с использованием Phaser, реализованной в программном пакете Phenix, с применением структуры заранее определенного комплекса Fab:FIXa в качестве модели поиска. Правильную аминокислотную последовательность моделировали с помощью COOT, а затем структуру уточняли с использованием стадий уточнения в Phenix и ручной реконструкции в COOT. Статистические значения уточнений приведены в таблице 6.
Таблица 6. Статистические значения собранных и уточненных данных
Статистические значения для оболочки с самым высоким разрешением показаны в скобках.
Определение эпитопа для mAb01-9994
Эпитоп для mAb01-9994, определяемый как остатки FIX(a), характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в Fab, включает следующие остатки: L337, R338, Т340, К341 и Т343 согласно SEQ ID NO:1.
Определение паратопа в mAb01-9994
Паратоп в mAb01-9994, определяемый как остатки Fab, характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в FIXa, содержит остатки (последовательная нумерация): H30, D31, W53, D56, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:67) и остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:71).
Остатки, выделенные жирным шрифтом, расположены в последовательностях CDR, как определено с использованием определения по Kabat, в то время как оставшийся остаток паратопа H30 (в вариабельном домене тяжелой цепи) представляет собой каркасный остаток.
Кристаллизация и картирование эпитопа/паратопа антитела к FIX/FIXa mAb01-9933
Кристаллизация
Fab-фрагмент, соответствующий mAb01-9933, смешивали при молярном соотношении 1:1 с фактором IXa человека без домена Gla (дикого типа), c ингибированным EGR-CK, экспрессированным в бактериальных клетках, партия № hGDFIXAWTEGR_05 (приобретен у Cambridge ProteinWorks), и кристаллы комплекса Fab/FIXa выращивали с использованием методики диффузии пара в сидячей капле при 18°C. 150 нл белкового раствора, содержащего 8,1 мг/мл комплекса в 20 мМ Tris-HCl, рН 7,4, 50 мM NaCl и 2,5 мM CaCl2, смешивали с 50 нл 0,1 M Bis-Tris, pH 6,5, 20 % (вес/объем) PEG 5000 MME в качестве осадителя, и инкубировали над 60 мкл осадителя.
Сбор данных дифракции
Кристалл подвергали криозащите путем добавления 1 мкл осадителя с добавлением 20% этиленгликоля к кристаллизационной капле перед мгновенным охлаждением в жидком азоте. Данные дифракции собирали при 100K в пучке синхротронного излучения i03 от Diamond Light Source (длина волны 0,9763 Å) с использованием пиксельного детектора Pilatus3 6M от Dectris. Автоиндексирование, интеграцию и масштабирование данных выполняли с помощью программ из пакета XDS (статистические значения данных дифракции обобщены в таблице 7).
Определение и уточнение структуры
Асимметричная единица содержит один комплекс Fab:FIXa, исходя из анализа коэффициента Мэтьюса. Структуру определяли путем молекулярной замены с использованием Phaser, реализованной в программном пакете Phenix, с применением структуры заранее определенного комплекса Fab:FIXa в качестве модели поиска. Правильную аминокислотную последовательность моделировали с помощью COOT, а затем структуру уточняли с использованием стадий уточнения в Phenix и ручной реконструкции в COOT. Статистические значения уточнений приведены в таблице 7.
Таблица 7. Статистические значения собранных и уточненных данных
Статистические значения для оболочки с самым высоким разрешением показаны в скобках.
Определение эпитопа для mAb01-9933
Эпитоп для mAb01-9933, определяемый как остатки FIX(a), характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в Fab, включает следующие остатки: L337, R338, Т340 и К341 согласно SEQ ID NO:1.
Определение паратопа в mAb01-9933
Дополнительно, паратоп в mAb01-9933, определяемый как остатки Fab, характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в FIXa, включает остатки (последовательная нумерация): D30, D31, W53, S102, S104, N107 в вариабельном домене тяжелой цепи (SEQ ID NO:35) и остатки: Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:39).
Остатки, выделенные жирным шрифтом, расположены в последовательностях CDR, как определено с использованием определения по Kabat, в то время как оставшийся остаток паратопа D30 (в вариабельном домене тяжелой цепи) представляет собой каркасный остаток.
Пример 8a Кристаллизация и картирование эпитопа/паратопа антитела к FIX(a) mAb01-9985
Кристаллизация
Fab-фрагмент, соответствующий mAb01-9985, смешивали при молярном соотношении 1:1 с фактором IXa человека без домена Gla (дикого типа), c ингибированным EGR-CK, экспрессированным в бактериальных клетках, партия № hGDFIXAWTEGR_11 (приобретен у Cambridge ProteinWorks). Комплекс подвергали эксклюзионной хроматографии на колонке HiLoad 16/60 Superdex 200 пг (GE Healthcare), выполняемой с буфером, содержащим 20 мМ Hepes, pH 7,5, 140 мМ NaCl, 1 мМ CaCl2. Фракции, содержащие комплекс Fab/FIXa, объединяли и концентрировали до 10,1 мг/мл. Кристаллы комплекса Fab/FIXa выращивали с использованием методики скрининга с микропереносом кристаллов, описанной в D’Arcy et al. (2014) Acta Crystallographica Section F 70, 1117–1126, с использованием диффузии пара в сидячей капле при 18°C. Используемый кристалл выращивали с применением 200 нл белкового раствора, содержащего 10,1 мг/мл комплекса в 20 мM Hepes, pH 7,4, 140 мM NaCl, 1 мM CaCl2, смешанных с 100 нл затравочного материала и 300 нл 2 M сульфата аммония, 0,1 М Hepes, pH 7,5, в качестве осадителя, и инкубировали над 80 мкл осадителя. Затравочный материал получали из кристаллов Fab-фрагмента, соответствующего mAb01-9933, в комплексе с фактором IXa человека без домена Gla (дикого типа), c ингибированным EGR-CK.
Сбор данных дифракции
Кристалл подвергали криозащите путем добавления 1,5 мкл осадителя с добавлением 20% этиленгликоля к кристаллизационной капле перед мгновенным охлаждением в жидком азоте. Данные дифракции собирали при 100K в пучке синхротронного излучения X10SA от Swiss Light Source (длина волны 1,00 Å) с использованием пиксельного детектора Pilatus3 6M от Dectris. Автоиндексирование, интеграцию и масштабирование данных выполняли с помощью программ из пакета XDS (статистические значения данных дифракции обобщены в таблице 7a).
Определение и уточнение структуры
Асимметричная единица содержит один комплекс Fab:FIXa, исходя из анализа коэффициента Мэтьюса. Структуру определяли путем молекулярной замены с использованием Phaser, реализованной в программном пакете Phenix, с применением структуры заранее определенного комплекса Fab:FIXa в качестве модели поиска. Правильную аминокислотную последовательность моделировали с помощью COOT, а затем структуру уточняли с использованием стадий уточнения в Phenix и ручной реконструкции в COOT. Статистические значения уточнений приведены в таблице 7a.
Таблица 7a. Статистические значения собранных и уточненных данных
Статистические значения для оболочки с самым высоким разрешением показаны в скобках.
Определение эпитопа для mAb01-9985
Эпитоп для mAb01-9985, определяемый как остатки FIX(a), характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в Fab, включает следующие остатки: L337, R338, S339, Т340 и К341 согласно SEQ ID NO:1.
Определение паратопа в mAb01-9985
Паратоп в mAb01-9985, определяемый как остатки Fab, характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в FIXa, содержит остатки (последовательная нумерация): H30, D31, W53, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO:51) и остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO:55). Остатки, выделенные жирным шрифтом, расположены в последовательностях CDR, как определено с использованием определения по Kabat, в то время как оставшийся остаток паратопа H30 (в вариабельном домене тяжелой цепи) представляет собой каркасный остаток.
Пример 9. Кристаллизация и картирование эпитопов/паратопов антител к FX с использованием рентгеновской кристаллографии
Кристаллизация и картирование эпитопа/паратопа антитела к FXa mAb01-8174
Кристаллизация
Fab-фрагмент, соответствующий mAb01-8174, смешивали при молярном соотношении 1:1 с фактором Xa человека без домена Gla (дикого типа), c ингибированным EGR-CK, экспрессированным в бактериальных клетках, партия № hGDFXAEGR_026 (приобретен у Cambridge ProteinWorks), и кристаллы комплекса Fab/FXa выращивали с использованием методики диффузии паров в сидячей капле при 18°C. 150 нл белкового раствора, содержащего 4,7 мг/мл комплекса в 20 мМ Tris-HCl, рН 7,4, 50 мM NaCl и 2,5 мM CaCl2, смешивали с 50 нл 0,2 M ацетата натрия, 0,1 M какодилата натрия, pH 6,5, 18% (вес/объем) PEG 8000 в качестве осадителя, и инкубировали над 60 мкл осадителя.
Сбор данных дифракции
Кристалл подвергали криозащите путем добавления 1 мкл осадителя с добавлением 20% этиленгликоля к кристаллизационной капле перед мгновенным охлаждением в жидком азоте. Данные дифракции собирали при 100K в пучке синхротронного излучения X06DA от Swiss Light Source (длина волны 1,00 Å) с использованием пиксельного детектора Pilatus2M от Dectris. Автоиндексирование, интеграцию и масштабирование данных выполняли с помощью программ из пакета XDS (статистические значения данных дифракции обобщены в таблице 8).
Определение и уточнение структуры
Асимметричная единица содержит два комплекса Fab:FXa, исходя из анализа коэффициента Мэтьюса. Структуру определяли путем молекулярной замены с помощью Molrep, реализованной в программном пакете CCP4, с применением структур заранее определенных комплексов Fab:FXa в качестве моделей поиска. Правильную аминокислотную последовательность для Fab моделировали с помощью COOT, а затем структуру уточняли с использованием стадий уточнения в Phenix и ручной реконструкции в COOT. Статистические значения уточнений приведены в таблице 8.
Таблица 8. Статистические значения собранных и уточненных данных
Статистические значения для оболочки с самым высоким разрешением показаны в скобках.
Определение эпитопа для mAb01-8174
Эпитоп для mAb01-8174, определяемый как остатки FXa, характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в Fab в одном или обоих комплексах в асимметричной единице, включает следующие остатки: E103, Q104, V108, R113, T116, L117, D119, I125, T127, E228, F229, Y230, E266, R287, P291, I292, P304, L419, K420, D423, R424, M426, K427 и T428 согласно SEQ ID NO:2.
Определение паратопа в mAb01-8174
Паратоп в mAb01-8174, определяемый как остатки Fab, характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в FXa в одном или обоих комплексах в асимметричной единице, включает остатки (последовательная нумерация): K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103, S104 в вариабельном домене тяжелой цепи (SEQ ID NO:467) и остатки V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO:471).
Остатки, выделенные жирным шрифтом, расположены в последовательностях CDR, как определено с использованием определения по Kabat, в то время как оставшиеся остатки паратопа K23, S25, G26, Y27, F29 и S77 (в вариабельном домене тяжелой цепи) и Y50 (в вариабельном домене легкой цепи) представляют собой каркасные остатки.
Кристаллизация и картирование эпитопа/паратопа антитела к FXa mAb01-9772
Fab-фрагмент, соответствующий mAb01-9772, смешивали при молярном соотношении 1:1 с фактором Xa человека без домена Gla (дикого типа), c ингибированным EGR-CK, экспрессированным в бактериальных клетках, партия № hGDFXAEGR_026 (приобретен у Cambridge ProteinWorks), и кристаллы комплекса Fab/FXa выращивали с использованием методики диффузии паров в сидячей капле при 18°C. 150 нл белкового раствора, содержащего 3,7 мг/мл комплекса в 20 мМ Tris-HCl, рН 7,4, 50 мM NaCl и 2,5 мM CaCl2, смешивали с 50 нл 0,2 M формиата натрия, 20% (вес/объем) PEG 3350 в качестве осадителя, и инкубировали над 60 мкл осадителя.
Сбор данных дифракции
Кристалл подвергали криозащите путем добавления 1 мкл осадителя с добавлением 20% этиленгликоля к кристаллизационной капле перед мгновенным охлаждением в жидком азоте. Данные дифракции собирали при 100K в пучке синхротронного излучения X06DA от Swiss Light Source (длина волны 1,00 Å) с использованием пиксельного детектора Pilatus2M от Dectris. Автоиндексирование, интеграцию и масштабирование данных выполняли с помощью программ из пакета XDS (статистические значения данных дифракции обобщены в таблице 9).
Определение и уточнение структуры
Асимметричная единица содержит два комплекса Fab:FXa, исходя из анализа коэффициента Мэтьюса. Структуру определяли путем молекулярной замены с помощью Molrep, реализованной в программном пакете CCP4, с применением структур заранее определенных комплексов Fab:FXa в качестве моделей поиска. Правильную аминокислотную последовательность для Fab моделировали с помощью COOT, а затем структуру уточняли с использованием стадий уточнения в Phenix и ручной реконструкции в COOT. Статистические значения уточнений приведены в таблице 9.
Таблица 9: Статистические значения собранных и уточненных данных
Статистические значения для оболочки с самым высоким разрешением показаны в скобках.
Определение эпитопа для mAb01-9772
Эпитоп для mAb01-9772, определяемый как остатки FXa, характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в Fab в одном или обоих комплексах в асимметричной единице, включает следующие остатки: E103, Q104, V108, R113, T116, L117, A118, D119, I125, T127, S227, E228, Y230, R287, I292, L303, P304, L419, K420, D423, R424, M426, K427 и T428 согласно SEQ ID NO:2.
Определение паратопа в mAb01-9772
Паратоп в mAb01-9772, определяемый как остатки Fab, характеризующиеся наличием тяжелого атома (т. е. атома, отличного от атома водорода) на расстоянии 3,5 Å от тяжелого атома в FXa в одном или обоих комплексах в асимметричной единице, включает остатки (последовательная нумерация):K23, G24, S25, G26, Y27, W33, D52, S54, D55, Y57, S77, L99, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO:483) и остатки S30, S31, Y33, Y50, Q52, S54, R55, R57, Y92 и D94 в вариабельном домене легкой цепи (SEQ ID NO:487).
Остатки, выделенные жирным шрифтом, расположены в последовательностях CDR, как определено с использованием определения по Kabat, в то время как оставшиеся остатки паратопа K23, G24, S25, G26,Y27 и S77 (в вариабельном домене тяжелой цепи) и Y50 (в вариабельном домене легкой цепи) представляют собой каркасные остатки.
Пример 10. Идентификация остатков-«горячих точек» на FIX
Чтобы определить остатки, критически важные для взаимодействия (называемые «горячей точкой») между антителами к FIX/FIXa mAb01-9994 и mAb01-9985 и FIX, выбрали набор вариантов FIX, исходя из структуры Fab/FIXa для Fab-фрагмента mAb01-9994 и FIXa. Как подробно описано ниже, выбранные варианты FIX временно экспрессировали в клетках млекопитающих, очищали и определяли характеристики, касающиеся их связывания с моновалентными вариантами mAb01-9994 и mAb01-9985 с использованием поверхностного плазмонного резонанса (SPR).
Получение мутантов FIX
ДНК-плазмиду, подходящую для временной экспрессии в клетках млекопитающих, конструировали с использованием кассеты экспрессии, кодирующей аминокислотные остатки 1–461 FIX человека (UNIPROT P00740, за исключением мутации T194A согласно нумерации UNIPROT, соответствующей T148A из SEQ ID NO:1), за которыми непосредственно следуют шесть остатков гистидина (6×His-метка, предназначенная для аффинной очистки). Секретируемая зрелая белковая цепь FIX, полученная с использованием этой конструкции, идентична аллельной форме A148 FIX человека (Anson et al. EMBO J. 1984 3:1053–1060, McGraw et al., Proc Natl Acad Sci USA. 1985 82:2847–2851), за исключением добавления С-концевой His-метки.
Используя конструкцию в качестве матрицы, выбранные мутации вводили с помощью ПЦР. Для каждой точковой мутации, перечисленной в таблице 10, разрабатывали прямой праймер, содержащий необходимую аминокислотную замену, и обратный праймер без аминокислотных мутаций. Эти праймеры использовали в стандартной реакции ПЦР с описанным выше вектором в качестве матрицы для амплификации полной последовательности вектора. Клонирование без лигирования использовали для соединения концов полученного фрагмента амплифицированной ДНК в кольцевую плазмиду экспрессии с использованием перекрывающихся последовательностей, введенных прямым и обратным праймерами.
Кольцевые плазмиды трансформировали в клетки E. coli, которые выращивали на чашках с селективным агаром для образования колоний, и эти колонии использовали как посевной материал для культивирования E. сoli в жидкой питательной среде. После роста культур E. coli на протяжении ночи получали препараты плазмид и мутантов идентифицировали с помощью секвенирования ДНК.
Получение рекомбинантного белка осуществляли путем трансфекции клеток expi293F, выращиваемых в суспензионной культуре в среде Expi293 Expression™ (ThermoFisher Scientific, номер по каталогу A1435101), с использованием набора для трансфекции ExpiFectamine™ 293 (ThermoFisher Scientific, номер по каталогу A14525) и плазмидной ДНК, кодирующей каждый из необходимых вариантов FIX, а также FIX дикого типа (соответствует SEQ ID NO:1 с С-концевой His-меткой). Во время трансфекции добавляли витамин К до конечной концентрации 5 мг/мл. Усилители 1 и 2 трансфекции из набора для трансфекции ExpiFectamine™ 293 добавляли на следующий день после трансфекции. Культуры клеток собирали через 5 дней после трансфекции с помощью центрифугирования.
С-концевую His-метку в каждом варианте FIX использовали для очистки партии белка в многолуночной роботизированной установке. Кратко, собранные супернатанты клеточных культур корректировали для условий связывания, смешивали со смолой для аффинной очистки Ni Sepharose 6 Fast Flow (GE Healthcare, номер по каталогу 17-5318-02, 50 мкл осажденной смолы/мл среды для культивирования клеток) и инкубировали при встряхивании в течение 20 минут. Затем смеси смола/супернатант переносили на фильтровальный планшет и жидкость прокачивали через фильтровальный планшет с применением вакуума. Смолу, оставшуюся на фильтровальном планшете, трижды промывали перед элюированием в буфере с высоким содержанием имидазола.
Определение концентрации очищенных белковых растворов выполняли с помощью ELISA с использованием антитела к FIX для обнаружения и рекомбинантного FIX дикого типа с высокой степенью чистоты для построения стандартных кривых.
Определяли характеристики вариантов FIX по их связыванию с mAb01-9994 и mAb01-9985 с использованием поверхностного плазмонного резонанса (SPR) при захвате варианта FIX посредством C-концевой His-метки. Чтобы избежать эффектов авидности, т. e. обеспечить взаимодействие 1:1, в качестве анализируемых веществ использовали одноплечие (OA) варианты mAb01-9994 и mAb01-9985 (полученные, как описано в примере 5).
Анализы SPR выполняли на приборах Biacore T200 (Biacore AB, Уппсала, Швеция). Для экспериментов на приборе T200 применяли следующие условия: измерения проводили при температуре 25°C. Антитело к His из расчета 25 мкг/мл (R&D Systems, номер по каталогу MAB050) иммобилизовали на сенсорном чипе CM5 с использованием стандартных химических соединений для иммобилизации по аминогруппе. Варианты антител к FIX из расчета 25 нМ вводили при скорости потока 10 мкл/мин в течение 1 мин, и они захватывались посредством их His-метки иммобилизованным антителом к His. Впоследствии вводили 20 мкМ (2,5-кратное разведение) OA mAb01-9994 и OA mAb01-9985 при скорости потока 50 мкл/мин в течение 3 минут, чтобы обеспечить связывание с захваченным вариантом FIX, а затем проводили 3-минутное введение буфера для обеспечения возможности диссоциации моновалентных антител к FIX. В качестве рабочего буфера использовали 20 мМ Tris, 150 мМ NaCl, 5 мМ CaCl2, 0,05% Tween-20, 10 мг/мл BSA, pH 7,4. Его также использовали для разведения образцов антитела к FIX и образцов FIX. Регенерацию чипа проводили с использованием 10 мМ глицина, рН 2,0. Данные по связыванию анализировали в соответствии с моделью 1:1 с использованием BiaEvaluation 4.1, предоставляемого производителем (Biacore AB, Уппсала, Швеция).
Данные по связыванию представлены как % связывания антитела с вариантом FIX относительно связывания антитела с FIX дикого типа, рассчитанный по формуле:
Связывание (%) = 100% × [(Rmax_Ab,FIX_вар)/(Rmax_FIXвар)]/[(Rmax_Ab,FIX_wt)/(Rmax_FIXwt)]
где Rmax_FIXвар и Rmax_FIXwt представляют уровень захвата (RU) варианта FIX и FIX дикого типа соответственно, и где Rmax_Ab,FIX_вар и Rmax_Ab,FIX_wt представляют Rmax (RU) 20 мкМ антитела с захваченным вариантом FIX и FIX дикого типа соответственно. Результаты показаны в таблицах 10 и 11.
Таблица 10. Результаты анализа SPR (mAb01-9994)
Результаты анализа «горячих точек» для OA-варианта mAb01-9994
Таблица 11. Результаты анализа SPR (mAb01-9985)
Результаты анализа «горячих точек» для OA-варианта mAb01-9985
Остатки-«горячие точки» для mAb01-9994 и mAb01-9985
Остатки-«горячие точки» для mAb01-9994 и mAb01-9985 определяются как положения, в которых замена остатка дикого типа аланином снижает связывание антитела до 30% или менее относительно связывания антитела с FIX дикого типа.
Остатки-«горячие точки» для mAb01-9994:
R338, T340 и K341.
Остатки-«горячие точки» для mAb01-9985:
R338, T340 и K341.
Для обоих mAb01-9994 и mAb01-9985 остатком, вносящим наибольший вклад в связыванию, является R338; для замены R338 аланином (R338A) в FIX показано наибольшее влияние на связывание антитела, которое было значительно снижено вплоть до отсутствия наблюдаемого связывания и 8% в случае mAb01-9994 и mAb01-9985 соответственно относительно связывания антител с FIX дикого типа.
Пример 11. Идентификация остатков-«горячих точек» на FX
Данные, представленные в настоящем примере, определяют остатки-«горячие точки» эпитопа на FX для mAb01-8174. Используемые варианты FX представляли собой варианты desGla-desEGF1-FX с аланином в одном сайте (за исключением положения 118, которое представляет собой аланин у белка дикого типа, где вводили замену аланина на серин), соответствующие остаткам 86-448 из SEQ ID NO:2 с N-концевой His-меткой (HHHHHH) (SEQ ID NO:1200), для аффинной очистки), присоединенной посредством короткого GS-линкера (GGGGSGGGGS) (SEQ ID NO:1201). Протестированные варианты FX перечислены в таблице 12.
Таблица 12. Перечень полученных мутантов desGla-desEGF1-FX
1. Согласно SEQ ID NO:2
2. EGF2 и PD относятся ко второму подобному эпидермальному фактору роста домену и протеазному домену соответственно.
DesGla-desEGF1-FX дикого типа и варианты, перечисленные в таблице 12, экспрессировали в системе HEK293 и очищали с помощью аффинной хроматографии. Идентификацию остатков-«горячих точек» эпитопа проводили с использованием прибора Biacore 4000 при 25°C. DesGla-desEGF1-FX дикого типа и его варианты иммобилизовали на сенсорном чипе CM5 Series-S (GE Healthcare, номер по каталогу BR100530) с использованием стандартных химических соединений для иммобилизации по аминогруппе. 10 мкМ (2-кратные серийные разведения) одноплечего варианта mAb01-8174 вводили при скорости потока 10 мкл/мин в течение 300 с, чтобы обеспечить связывание с иммобилизованным desGla-desEGF1-FX дикого типа и его вариантами, а затем проводили 600-секундное введение буфера для обеспечения возможности диссоциации моновалентного антитела. Рабочий буфер (также используемый для разбавления моновалентного антитела и вариантов desGLA-desEGF1-hFX) содержал 10 мМ HEPES, 150 мМ NaCl, 1 мг/мл BSA и 5 мМ CaCl2 (pH 7,4). Буфер для регенерации не использовали, поскольку наблюдали почти полную диссоциация антитела от сенсорного чипа во время 600-секундной стадии диссоциации. Данные связывания анализировали в соответствии с моделью 1:1 и аффинность (т. е. равновесную константу диссоциации) для каждого связывания получали путем аппроксимации равновесного состояния кривых связывания с использованием программного обеспечения Biacore 4000 Evaluation 1.0, предоставляемого GE Healthcare. Данные связывания представлены как кратное значение аффинности всех вариантов FX к антителу относительно аффинности FX дикого типа. Относительные значения аффинности, измеренные для вариантов FX, показаны в таблице 13.
Таблица 13. Относительные значения аффинности (KD(вариант)/KD(дикий тип)) при связывании одноплечего mAb01-8174 с вариантами FX
«Отсутствие связывания» означает, что связывание было слишком слабым, чтобы его можно было обнаружить.
Остатки-«горячие точки» для mAb01-8174
Как показано в таблице 13, замены аланином в положениях 230, 423, 424 и 427 в FX полностью устраняли связывание с одноплечим mAb01-8174. Таким образом, остатки-«горячие точки» на FX для связывания с mAb01-8174 представляют собой:
Y230, D423, R424 и K427.
Пример 12. Активность моновалентных антител к FIX/FIXa в анализе образования FXa
Чтобы избежать любых потенциальных эффектов авидности, возникающих вследствие бивалентности традиционного формата антитела IgG, стимулирующую активность антител к FIX(a) на ферментативную активность FIXa в отношении FX определяли после преобразования в формат моновалентного одноплечего (ОА) антитела (см. пример 5). Протестированные антитела перечислены в таблице 14 ниже. Моновалентные OA-версии антител к FIXa, 224F3 и ACE910, включили для сравнения.
Стимулирующую активность ОА-антител измеряли в буфере для анализа (50 мМ HEPES, 100 мМ NaCl, 5 мМ CaCl2, 0,1% (вес/объем) PEG8000, pH 7,3, +1 мг/мл BSA) при фиксированных концентрациях фосфолипидных везикул из фосфатидилсерина (PS): фосфатидилхолина (PC) (конечная концентрация 500 мкМ; Haematologic Technologies Inc, США) и полученного из плазмы крови FIXa (конечные концентрации 0,04, 0,1, 0,17, 0,2, 0,3, 0,5 или 1 нM; Haematologic Technologies Inc, США). Концентрацию FIXa подбирали для обеспечения того, чтобы менее 15% субстрата FX превращалось в FXa. После предварительной инкубации в присутствии моновалентного ОА-антитела (конечные концентрации перечислены в таблице 14) добавляли 100 нМ полученного из плазмы крови FX (Haematologic Technologies Inc, США) с получением конечного объема реакционной смеси 50 мкл и обеспечивали прохождение активации в течение 20 мин при комнатной температуре. Затем реакцию останавливали с помощью добавления 25 мкл буфера для остановки реакции (50 мМ HEPES, 100 мМ NaCl, 60 мМ EDTA, 0,1% PEG8000, pH 7,3, +1 мг/мл BSA) и количество образованного FXa определяли с помощью дальнейшего добавления 25 мкл 2 мМ хромогенного субстрата S-2765 (Chromogenix, Швеция) и измерения преобразования хромогенного субстрата путем измерения поглощения при 405 нм (ΔOD/мин) в считывающем устройстве для микропланшетов. Измеренную активность корректировали на фоновую активность путем вычитания сигнала, измеренного в том же анализе, но с заменой FIXa и антитела на буфер для анализа, а затем нормализовали в соответствии с концентрацией FIXa, присутствующего в анализе ([FIXa]общий). Разделив это число на аналогичным образом нормализованную скорость образования FXa в отсутствие антитела (AFIXa,норм), рассчитывали индекс стимуляции антитела, показывающий кратную стимуляцию активности FIXa под действием антитела в использованной концентрации. Из-за низкой скорости образования FXa под действием свободного FIXa реакции активации в отсутствие антитела проводили, как описано выше, но в присутствии 5, 10 или 20 нМ FIXa. Затем из измеренных значений активности вычитали фон и нормализовали в соответствии с концентрацией FIXa в анализе. Для расчета индекса стимуляции использовали среднее значение трех нормализованных значений активности свободного FIXa.
Определение индекса стимуляции
Таким образом, расчет индекса стимуляции можно описать следующим образом.
Индекс стимуляции = ((AFIXa+OA – Aфон)/[FIXa]общий)/AFIXa,норм,
где AFIXa+OA представляет собой активность, измеренную в присутствии OA-антитела, Aфон представляет собой фоновую активность, измеренную в отсутствие FIXa и OA-антитела, [FIXa]общий представляет собой концентрацию FIXa в анализе, и AFIXa,норм представляет собой среднее значение нормализованной активности свободного FIXa.
Определение насыщения FIXa
Долю FIXa, насыщенного OA-антителом в анализе, определяют по концентрациям FIXa и OA-антитела и равновесной константе диссоциации (Kd), обуславливающей их взаимодействие. Последнее можно измерить с помощью методик, известных из уровня техники, таких как изотермическая титрационная калориметрия (ITC).
Поскольку индекс стимуляции будет увеличиваться по мере увеличения концентрации ОА-антитела до тех пор, пока не будет достигнуто насыщение FIXa, концентрацию ОА-антитела в анализе следует выбирать так, чтобы гарантировать по меньшей мере 80% насыщение FIXa в анализе для обеспечения надлежащего определения индекса стимуляции при полном насыщении FIXa.
Долю FIXa, связанного с ОА-антителом в равновесном состоянии (fFIXa+OA), можно рассчитать из общих концентраций FIXa ([FIXa]общий) и OA-антитела ([OA]общий) в анализе и равновесной константы диссоциации (Kd) для их взаимодействия с использованием квадратного уравнения связывания, описанного в Krishnaswamy et al. (1992) J. Biol. Chem., 267:23696–23706 и подробно описанного в уравнениях 1 и 2 ниже, где
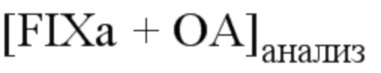 представляет рассчитанную концентрацию комплекса FIXa-OA-антитело в равновесном состоянии в анализе;
представляет рассчитанную концентрацию комплекса FIXa-OA-антитело в равновесном состоянии в анализе;
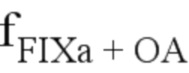 представляет рассчитанную долю (в процентах) FIXa, который связан с ОА-антителом в равновесном состоянии в анализе.
представляет рассчитанную долю (в процентах) FIXa, который связан с ОА-антителом в равновесном состоянии в анализе.
Уравнение 1:

Уравнение 2:
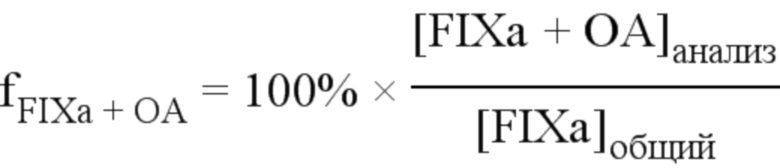
Индекс стимуляции для каждого ОА-антитела приведен в таблице 14. При концентрации OA-антитела 224F3, составляющей 3260 нМ в анализе, и Kd для взаимодействия с FIXa, составляющей 0,477 нМ, как сообщалось в Kerschbaumer et al. (US7297336B2), больше 95% FIXa связывалось с OA-антителом 224F3 в анализе. В случае OA-антитела ACE910 стимуляцию FIXa определяли при восьми различных концентрациях антитела, что позволяло оценить индекс стимуляции при полном насыщении FIXa, используя квадратное уравнение связывания, описанное выше. Это также давало расчетную равновесную константу диссоциации (Kd) для взаимодействия ACE910 с FIXa, составляющую 1,1 мкМ, что хорошо согласуется с величиной 1,52 мкМ, сообщаемой в Kitazawa et al. (2017) Thromb Haemost, 117:1348–1357, и значением 1,97 мкМ, определенным с помощью ITC в примере 13. Для остальных антител степень насыщения FIXa не была известна, и, следовательно, перечисленные индексы стимуляции представляют собой предварительные оценки стимуляции, которые могут быть получены при степени насыщения FIXa 80% или более. Было обнаружено, что для протестированных антител измеренный индекс стимуляции выше, чем индекс стимуляции, измеренный для OA-антител 224F3 и ACE910.
Таблица 14. Стимуляция активности FIXa под действием моновалентных одноплечих (ОА) антител к FIXa
ID mAb к FIX относится к ID антитела, используемого для преобразования в формат ОА. В столбцах, помеченных как «Концентрация ОА-антитела (нМ)» и «Индекс стимуляции», перечислены концентрация ОА-антитела (нМ), использованная в анализе, и соответствующая стимуляция активности FIXa, измеренная относительно свободного FIXa. В случае ACE910 приведен расчетный индекс стимуляции при полном насыщении FIXa.
Пример 13 Аффинности связывания, определенные с помощью изотермической титрационной калориметрии (ITC)
Аффинности связывания для антител к FIX(a) и к FX(a) измеряли с помощью изотермической титрационной калориметрии (ITC) с использованием калориметра PEAQ-ITC (Малверн, Великобритания). Эксперименты проводили при 37°С и рН 7,4 с использованием 25 мМ Tris, 150 мМ NaCl, 5 мМ CaCl2 (Tris-буфер). Ячейка для образца (200 мкл) содержала одно из FIX, FIXa или FX (макромолекулу), и антитела к FIX(a) и к FX(a) (лиганд) вводили через шприц (40 мкл). Все белки подвергали интенсивному диализу в Tris-буфере перед проведениями измерений для сохранения подходящих буферных условий. За стадией термического уравновешивания следовала 60-секундная задержка и затем начальная инъекция 0,2 мкл антитела с последующими 12-16 инъекциями по 1,5-3 мкл антитела с интервалом в 120 с. Скорость перемешивания поддерживали на уровне 750 об/мин, а исходный уровень мощности поддерживали на постоянном уровне 5-10 мккал/с. Тепло, ассоциированное с каждой инъекцией антитела, интегрируют и наносят на график в зависимости от молярного отношения лиганда к макромолекуле. Полученную изотерму аппроксимируют к модели связывания в одном участке для получения аффинности (KD), стехиометрии (n) и энтальпии взаимодействия (ΔH) с использованием программного обеспечения, предоставленного производителем. Эксперименты проводили по меньшей мере в двух повторностях. Значения KD в единицах мкМ представлены в таблице 15.
Таблица 15. Значения константы диссоциации (KD) с использованием ITC
NA: Не применимо, поскольку антитело является специфическим для другой макромолекулы.
Пример 14. Активность биспецифических антител к FIX(а)/FX(a) в анализе образования FXa
Прокоагулянтную активность биспецифических антител к FIXa/FX определяли на основании их способности стимулировать активацию FX с помощью FIXa в присутствии прокоагулянтной фосфолипидной мембраны. Протестированные биспецифические антитела (BiAb) перечислены в таблице 16, а ACE910 включили для сравнения.
Прокоагулянтную активность каждого биспецифического антитела описывают как кратность стимуляции по сравнению с активацией FX под действием свободного FIXa при данной концентрации антитела. Биспецифические антитела тестировали в 8 концентрациях (полученных путем последовательных трехкратных разведений в буфере для анализа) путем предварительной инкубации с 35 или 125 пМ FIXa, полученного из плазмы крови человека (Haematologic Technologies Inc., США), и 500 мкМ фосфолипидных везикул из 25:75 фосфатидилсерина:фосфатидилхолина (Haematologic Technologies Inc, США) в буфере для анализа (50 мМ HEPES, 100 мМ NaCl, 5 мМ CaCl2, 0,1% (вес/объем) PEG8000, pH 7,3, +1 мг/мл BSA) в течение 10 мин. Затем инициировали активацию путем добавления FX, полученного из плазмы крови человека (Haematologic Technologies Inc, США), до концентрации 25 нМ. После 15-минутной активации при комнатной температуре реакцию (50 мкл) останавливали путем добавления 25 мкл буфера для остановки реакции (50 мМ HEPES, 100 мМ NaCl, 60 мМ EDTA, 0,1% PEG8000, pH 7,3, +1 мг/мл BSA). Количество образованного FXa определяли путем добавления 25 мкл 2 мМ хромогенного субстрата S-2765 (Chromogenix, Швеция) и измерения преобразования хромогенного субстрата путем измерения поглощения при 405 нм (ΔOD/мин) в считывающем устройстве для микропланшетов. Аналогичным образом, активацию FX под действием свободного FIXa определяли при концентрации FIXa, составляющей 25 нМ, и времени реакции 60 мин.
Измеренную активность нормализовали в соответствии с концентрацией FIXa, присутствующей в анализе, и временем реакции. Путем деления этого числа на аналогичным образом нормализованную скорость образования FXa в отсутствие антитела рассчитывали кратность стимуляции антителом при данной концентрации.
Таким образом, расчет стимуляции biAb можно описать следующим образом:
Стимуляция biAb = (AFIXa+biAb/([FIXa]анализ× tреакции))/AFIXa,норм,
где AFIXa+biAb представляет активность, измеренную в присутствии биспецифического антитела, [FIXa]анализ представляет концентрацию FIXa в анализе, tреакции представляет время реакции, и AFIXa,норм представляет нормализованную активность свободного FIXa.
В таблице 16 перечислены максимальная стимуляция, определенная для каждого биспецифического антитела среди 8 протестированных концентраций антитела, а также концентрация, при которой наблюдалась максимальная стимуляция. Было обнаружено, что для всех протестированных биспецифических антител максимальная стимуляция была выше, чем измеренная для ACE910, которое было протестировано в интервале концентраций от 0 до 15300 нМ.
Таблица 16: Максимальная стимуляция биспецифическими антителами к FIXa/FX
Пример 15. TGT для биспецифических антител к FIX(a)/FX(a) в плазме крови при гемофилии A (HA)
Тесты тромбинообразования (TGT) проводили в автоматизированной 384-луночной установке HTP со стимуляцией тканевым фактором. Вкратце, 10 мкл антител добавляли к 30 мкл плазмы крови при гемофилии A (HA) (George King). Затем добавляли 10 мкл стимулятора TissueFactor (Thrombinoscope, № TS31.00) в смеси с фосфолипидами с последующим добавлением 10 мкл субстрата тромбина (FluCa, Thrombinoscope, № TS50.00) до конечного объема анализа 60 мкл. Динамические ряды флуоресценции измеряли при комнатной температуре на считывающем устройстве для планшетов с несколькими метками EnVision Perkin Elmer с 1-минутными интервалами в течение 2 часов. Тромбограммы рассчитывали как сглаженную первую производную динамических рядов флуоресценции. Высоту пика рассчитывали как максимальное значение, наблюдаемое на тромбограмме, и нормализовали (отношение пиков) к высоте пика, наблюдаемой для эталонного антитела ACE910 при самой высокой концентрации (333 нM). Результаты теста для биспецифических антител (bimAb) показаны в таблице 17. Отношение пиков (кратность) представляет собой максимальное значение, наблюдаемое для bimAb на тромбограмме, по сравнению со значением для ACE910 при 333 нМ. Также указана концентрация (нM), при которой наблюдается пик.
Таблица 17. Активность TGT для bimAb к FIX/FX относительно ACE910
Пример 16. Активность биспецифических антител к FIX(a)/FX(a) в тесте тромбинообразования (TGT) в обедненной тромбоцитами или обогащенной тромбоцитами плазме крови человека с имитацией гемофилии А
Прокоагулянтную активность биспецифических антител bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113 и bimAb005-2114 определяли, исходя из их способности стимулировать тромбинообразование в присутствии либо прокоагулянтной синтетической фосфолипидной мембраны, либо тромбоцитов в соответствии с принципами, описанными в Hemker et al. (Pathophysiol Haemost Thromb, 2002;32:249–253). ACE910 включили для сравнения. Каждое антитело (тестируемое соединение) испытывали в тесте тромбинообразования (TGT) с использованием коммерчески доступной объединенной обедненной тромбоцитами плазмы крови пациентов с гемофилией A (HA) (HA-PPP) и обогащенной тромбоцитами плазмы крови человека с индуцированной HA (HA-PRP), свежеприготовленной из крови здоровых давших свое согласие доноров.
Материалы и способы
Получение обогащенной тромбоцитами плазмы крови человека с индуцированной гемофилией A (HA-PRP)
Кровь получали от здоровых, давших свое согласие доноров путем венепункции. Собирали шесть объемов крови в 1 объем кислой цитратной декстрозы (ACD; 85 мМ цитрата натрия, 110 мМ декстрозы и 62,3 мМ лимонной кислоты, рН 4,9), конечное значение рН 6,5, и центрифугировали в течение 20 мин при 220 g при комнатной температуре (RT). Обогащенную тромбоцитами плазму крови (PRP) собирали и определяли концентрации тромбоцитов с помощью гематологического анализатора Medonic CA 620 (Boule Diagnostics AB, Спонга, Швеция).
Часть плазмы крови, содержащую эритроциты, центрифугировали еще 10 мин при 600 g при RT. Обедненную тромбоцитами плазму крови (PPP) собирали и использовали для разбавления PRP до ~300000 тромбоцитов/мкл. Условия HA индуцировали добавлением FVIII-нейтрализующего антитела к FVIII человека (овечье антитело к фактору VIII человека - 5 мг, Haematologic Technologies, Вермонт, США) до конечной концентрации 0,1 мг/мл и осторожно перемешивали при 2 об/мин в течение 30 минут при RT.
Тест тромбинообразования
Тесты тромбинообразования (TGT) в HA-PPP (George King Bio-Medical Inc, Канзас, США) (эксперимент A) и HA-PRP (эксперимент B) выполняли с помощью откалиброванной стандартом автоматической тромбографии с использованием флуориметра для 96-луночных планшетов (Fluoroscan Ascent FL, Thermolabsystems, Хельсинки, Финляндия). Реакционные смеси содержали 70 мкл HA-PRP (~300000 тромбоцитов/мкл) или HA-PPP, 10 мкл разведения тестируемого соединения (разведенного в 20 мМ HEPES, 140 мМ NaCl, pH 7,4, 2% BSA), 20 мкл реагентов CAT, содержащих тканевый фактор (TF) (реагент PRP; TF без синтетических фосфолипидов, реагент PPP LOW; TF с синтетическими фосфолипидами, конечная концентрация TF 1 пМ, Thrombinoscope BV, Маастрихт, Нидерланды) или калибратор тромбина (Thrombinoscope BV) и 20 мкл смеси, содержащей флуоресцентно меченный субстрат тромбина z-Gly-Gly-Arg-AMC (3 мМ) и CaCl2 (90 мM) (Thrombinoscope BV). TGT проводили при восьми концентрациях тестируемого соединения (0,3, 1,0, 3, 10, 30, 100, 300 и 900 нМ, конечная концентрация в плазме крови) или при добавлении буфера (20 мМ HEPES, 140 мМ NaCl, рН 7,4, 2% BSA) (представляет контроль HA). Диапазоны концентраций тестировали по меньшей мере в трех независимых экспериментах в HA-PPP из того же исходного препарата или в крови от четырех других доноров. Нормальные контрольные уровни TGT измеряли с использованием необработанную PRP человека или объединенной нормальной PPP плазмы крови человека CRYOcheck™ (Precision Biologic Inc., Дартмут, Канада) с добавлением буфера (20 мМ HEPES, 140 мМ NaCl, pH 7,4, 2% BSA). TGT проводили суммарно в течение 90 минут и параметр TGT пиковой высоты тромбина (нМ) анализировали с помощью программного обеспечения Thrombinoscope (Thrombinoscope BV).
Результаты и обсуждение
Эксперимент A. На фигуре 2 и в таблице 18 показаны измеренные пиковые скорости тромбинообразования для каждого биспецифического антитела при протестированных концентрациях в HA-PPP. Данные показывают, что все тестируемые соединения увеличивают пик образования тромбина выше уровня, наблюдаемого в отсутствие антитела, т. е. проявляют прокоагулянтную активность. Кроме того, уровни тромбинообразования для bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113 и bimAb05-2114 при концентрациях от 10 до 300 нM были выше, чем уровни, наблюдаемые для ACE910, что демонстрирует их превосходящую активность. Кроме того, уровни тромбинообразования для bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-2112 и bimAb05-2114 при концентрации при 300–900 нM были выше, чем уровни, наблюдаемые при концентрации 900 нM ACE910, что демонстрирует более высокие значения активности и эффективности этих соединений по сравнению с ACE910.
Эксперимент B На фигуре 3 и в таблице 19 показаны измеренные пиковые уровни тромбинообразования для каждого биспецифического антитела при протестированных концентрациях в HA-PRP. В этих условиях bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113 и bimAb05-2114 также демонстрируют лучшие значения активности и эффективности по сравнению с ACE910.
Таблица 18. Тест тромбинообразования (TGT) в HA-PPP (эксперимент A)
Тест тромбинообразования (TGT) для биспецифических антител bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113, bimAb05-2114 и ACE910 в активированной тканевым фактором обедненной тромбоцитами плазме крови человека при гемофилии А (PPP). Средние пиковые уровни тромбинообразования ± стандартное отклонение, измеренные при каждой из концентраций тестируемого соединения в HA-PPP в по меньшей мере трех независимых экспериментах (эксперимент A).
Концентрация соединения (нM)
(среднее значение ± SD в нM)
для ACE910
(среднее значение ± SD в нM)
для bimAb05-0745
(среднее значение ± SD в нM)
для bimAb05-3761
Концентрация соединения (нM)
(среднее значение ± SD в нM)
дляbimAb05-3769
(среднее значение ± SD в нM)
для bimAb05-0746
(среднее значение ± SD в нM)/
для bimAb05-2112
Концентрация соединения (нM)
(среднее значение ± SD в нM)
для bimAb05-2113
(среднее значение ± SD в нM)
для bimAb05-2114
Таблица 19. Тест тромбинообразования (TGT) в HA-PRP (эксперимент B)
Тест тромбинообразования (TGT) для биспецифических антител bimAb05-0745, bimAb05-3761, bimAb05-3769, bimAb05-0746, bimAb05-2112, bimAb05-2113, bimAb05-2114 и ACE910 в активированной тканевым фактором обогащенной тромбоцитами плазме крови человека при гемофилии А (PRP). Средний пиковый уровень тромбинообразования ± стандартное отклонение при каждой из концентраций тестируемого соединения в четырех независимых экспериментах в HA-PRP (эксперимент B).
Концентрация соединения (нM)
(среднее значение ± SD в нM)
для ACE910
(среднее значение ± SD в нM)
для bimAb05-0745
(среднее значение ± SD в нM)
для bimAb05-3761
Концентрация соединения (нM)
(среднее значение ± SD в нM)
для bimAb05-3769
(среднее значение ± SD в нM)
для bimAb05-0746
(среднее значение ± SD в нM)
для bimAb05-2112
Концентрация соединения (нM)
(среднее значение ± SD в нM)
для bimAb05-2113
(среднее значение ± SD в нM)
для bimAb05-2114
Пример 17. Эффективность in vivo биспецифических антител к FIX(a)/FX(a) на модели рассечения хвостовой вены (TVT)
Эффективность in vivo определяли с использованием модели рассечения хвостовой вены (TVT) у нокаутных по FVIII мышей. Эффективность высокой дозы (8 мг/кг) тестируемых соединений антител и ACE910 изучали в исследовании с рассечением хвостовой вены (TVT) у нокаутных по FVIII мышей (B6;129S-F8tm1Kaz/J, The Jackson Laboratory, БарХарбор, Мэн, США) обработанных совместно FIX человека (2 мг/кг) (Benefix, Pfizer, Нью-Йорк, Нью-Йорк, США) и FX человека (1,5 мг/кг) (Haematologic Technologies, INC, Эссекс Джанкшен, Вермонт, США). Вкратце, мышей анестезировали изофлураном и помещали на грелку-подушку, настроенную на поддержание температуры тела животного на уровне 37°C, при этом их хвосты погружали в физиологический раствор (37°C). Введение дозы выполняли в правую боковую хвостовую вену за 5 минут до повреждения. В настоящей модели TVT (Johansen et al., Haemophilia, 2016, 625–31) рассекали боковую вену. Если кровотечение прекращалось через 10, 20 или 30 минут, хвост вынимали из физиологического раствора и осторожно протирали рану марлевым тампоном, смоченным физиологическим раствором. Общую кровопотерю определяли через 40 мин путем определения количества гемоглобина в физиологическом растворе (см. таблицу 20). Эффективность тестируемого соединения антитела сравнивали с помощью однофакторного ANOVA с последующим применением критерия Тьюки для множественных сравнений. Значимым считали значение p<0,05.
Таблица 20. Сравнение эффективности на моделях кровотечения у нокаутных по F8 мышей
(нмоль гемоглобина)
*Значимо отличается от нокаутных по FVIII мышей, обработанных средой-носителем
Хотя определенные признаки настоящего изобретения были проиллюстрированы и описаны в данном документе, средним специалистам в данной области будут очевидны многие модификации, замены, изменения и эквиваленты. Следовательно, следует понимать, что прилагаемая формула изобретения предназначена для охвата всех таких модификаций и изменений, которые находятся в пределах истинной сущности настоящего изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> НОВО НОРДИСК А/С
<120> Усовершенствованные прокоагулянтные антитела
<130> 180021WO03
<160> 1249
<170> PatentIn версия 3.5
<210> 1
<211> 415
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Tyr Asn Ser Gly Lys Leu Glu Glu Phe Val Gln Gly Asn Leu Glu Arg
1 5 10 15
Glu Cys Met Glu Glu Lys Cys Ser Phe Glu Glu Ala Arg Glu Val Phe
20 25 30
Glu Asn Thr Glu Arg Thr Thr Glu Phe Trp Lys Gln Tyr Val Asp Gly
35 40 45
Asp Gln Cys Glu Ser Asn Pro Cys Leu Asn Gly Gly Ser Cys Lys Asp
50 55 60
Asp Ile Asn Ser Tyr Glu Cys Trp Cys Pro Phe Gly Phe Glu Gly Lys
65 70 75 80
Asn Cys Glu Leu Asp Val Thr Cys Asn Ile Lys Asn Gly Arg Cys Glu
85 90 95
Gln Phe Cys Lys Asn Ser Ala Asp Asn Lys Val Val Cys Ser Cys Thr
100 105 110
Glu Gly Tyr Arg Leu Ala Glu Asn Gln Lys Ser Cys Glu Pro Ala Val
115 120 125
Pro Phe Pro Cys Gly Arg Val Ser Val Ser Gln Thr Ser Lys Leu Thr
130 135 140
Arg Ala Glu Ala Val Phe Pro Asp Val Asp Tyr Val Asn Ser Thr Glu
145 150 155 160
Ala Glu Thr Ile Leu Asp Asn Ile Thr Gln Ser Thr Gln Ser Phe Asn
165 170 175
Asp Phe Thr Arg Val Val Gly Gly Glu Asp Ala Lys Pro Gly Gln Phe
180 185 190
Pro Trp Gln Val Val Leu Asn Gly Lys Val Asp Ala Phe Cys Gly Gly
195 200 205
Ser Ile Val Asn Glu Lys Trp Ile Val Thr Ala Ala His Cys Val Glu
210 215 220
Thr Gly Val Lys Ile Thr Val Val Ala Gly Glu His Asn Ile Glu Glu
225 230 235 240
Thr Glu His Thr Glu Gln Lys Arg Asn Val Ile Arg Ile Ile Pro His
245 250 255
His Asn Tyr Asn Ala Ala Ile Asn Lys Tyr Asn His Asp Ile Ala Leu
260 265 270
Leu Glu Leu Asp Glu Pro Leu Val Leu Asn Ser Tyr Val Thr Pro Ile
275 280 285
Cys Ile Ala Asp Lys Glu Tyr Thr Asn Ile Phe Leu Lys Phe Gly Ser
290 295 300
Gly Tyr Val Ser Gly Trp Gly Arg Val Phe His Lys Gly Arg Ser Ala
305 310 315 320
Leu Val Leu Gln Tyr Leu Arg Val Pro Leu Val Asp Arg Ala Thr Cys
325 330 335
Leu Arg Ser Thr Lys Phe Thr Ile Tyr Asn Asn Met Phe Cys Ala Gly
340 345 350
Phe His Glu Gly Gly Arg Asp Ser Cys Gln Gly Asp Ser Gly Gly Pro
355 360 365
His Val Thr Glu Val Glu Gly Thr Ser Phe Leu Thr Gly Ile Ile Ser
370 375 380
Trp Gly Glu Glu Cys Ala Met Lys Gly Lys Tyr Gly Ile Tyr Thr Lys
385 390 395 400
Val Ser Arg Tyr Val Asn Trp Ile Lys Glu Lys Thr Lys Leu Thr
405 410 415
<210> 2
<211> 448
<212> БЕЛОК
<213> Homo sapiens
<400> 2
Ala Asn Ser Phe Leu Glu Glu Met Lys Lys Gly His Leu Glu Arg Glu
1 5 10 15
Cys Met Glu Glu Thr Cys Ser Tyr Glu Glu Ala Arg Glu Val Phe Glu
20 25 30
Asp Ser Asp Lys Thr Asn Glu Phe Trp Asn Lys Tyr Lys Asp Gly Asp
35 40 45
Gln Cys Glu Thr Ser Pro Cys Gln Asn Gln Gly Lys Cys Lys Asp Gly
50 55 60
Leu Gly Glu Tyr Thr Cys Thr Cys Leu Glu Gly Phe Glu Gly Lys Asn
65 70 75 80
Cys Glu Leu Phe Thr Arg Lys Leu Cys Ser Leu Asp Asn Gly Asp Cys
85 90 95
Asp Gln Phe Cys His Glu Glu Gln Asn Ser Val Val Cys Ser Cys Ala
100 105 110
Arg Gly Tyr Thr Leu Ala Asp Asn Gly Lys Ala Cys Ile Pro Thr Gly
115 120 125
Pro Tyr Pro Cys Gly Lys Gln Thr Leu Glu Arg Arg Lys Arg Ser Val
130 135 140
Ala Gln Ala Thr Ser Ser Ser Gly Glu Ala Pro Asp Ser Ile Thr Trp
145 150 155 160
Lys Pro Tyr Asp Ala Ala Asp Leu Asp Pro Thr Glu Asn Pro Phe Asp
165 170 175
Leu Leu Asp Phe Asn Gln Thr Gln Pro Glu Arg Gly Asp Asn Asn Leu
180 185 190
Thr Arg Ile Val Gly Gly Gln Glu Cys Lys Asp Gly Glu Cys Pro Trp
195 200 205
Gln Ala Leu Leu Ile Asn Glu Glu Asn Glu Gly Phe Cys Gly Gly Thr
210 215 220
Ile Leu Ser Glu Phe Tyr Ile Leu Thr Ala Ala His Cys Leu Tyr Gln
225 230 235 240
Ala Lys Arg Phe Lys Val Arg Val Gly Asp Arg Asn Thr Glu Gln Glu
245 250 255
Glu Gly Gly Glu Ala Val His Glu Val Glu Val Val Ile Lys His Asn
260 265 270
Arg Phe Thr Lys Glu Thr Tyr Asp Phe Asp Ile Ala Val Leu Arg Leu
275 280 285
Lys Thr Pro Ile Thr Phe Arg Met Asn Val Ala Pro Ala Cys Leu Pro
290 295 300
Glu Arg Asp Trp Ala Glu Ser Thr Leu Met Thr Gln Lys Thr Gly Ile
305 310 315 320
Val Ser Gly Phe Gly Arg Thr His Glu Lys Gly Arg Gln Ser Thr Arg
325 330 335
Leu Lys Met Leu Glu Val Pro Tyr Val Asp Arg Asn Ser Cys Lys Leu
340 345 350
Ser Ser Ser Phe Ile Ile Thr Gln Asn Met Phe Cys Ala Gly Tyr Asp
355 360 365
Thr Lys Gln Glu Asp Ala Cys Gln Gly Asp Ser Gly Gly Pro His Val
370 375 380
Thr Arg Phe Lys Asp Thr Tyr Phe Val Thr Gly Ile Val Ser Trp Gly
385 390 395 400
Glu Gly Cys Ala Arg Lys Gly Lys Tyr Gly Ile Tyr Thr Lys Val Thr
405 410 415
Ala Phe Leu Lys Trp Ile Asp Arg Ser Met Lys Thr Arg Gly Leu Pro
420 425 430
Lys Ala Lys Ser His Ala Pro Glu Val Ile Thr Ser Ser Pro Leu Lys
435 440 445
<210> 3
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 3
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 4
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 4
Asp Tyr Ala Met His
1 5
<210> 5
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 5
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 6
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 6
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 7
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 7
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Glu Arg Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 8
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 8
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 9
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 9
Lys Ala Ser Arg Leu Glu Arg
1 5
<210> 10
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 10
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 11
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 11
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Ile Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 12
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 12
Asp Tyr Ala Met His
1 5
<210> 13
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 13
Gly Ile Ser Trp Arg Gly Asp Ile Ile Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 14
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 14
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 15
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 15
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Glu Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Arg Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser His Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 16
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 16
Arg Ala Ser Lys Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 17
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 17
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 18
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 18
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 19
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 19
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 20
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 20
Asp Tyr Ala Met His
1 5
<210> 21
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 21
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 22
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 22
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 23
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 23
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 24
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 24
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 25
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 25
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 26
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 26
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 27
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 28
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 28
Asp Tyr Ala Met His
1 5
<210> 29
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 29
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 30
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 30
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 31
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 31
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 32
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 32
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 33
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 33
Lys Ala Ser Arg Leu Glu Arg
1 5
<210> 34
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 34
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 35
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 35
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 36
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 36
Asp Tyr Ala Met His
1 5
<210> 37
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 37
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 38
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 38
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 39
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 39
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Glu Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Asp Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 40
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 40
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 41
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 41
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 42
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 42
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 43
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 43
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 44
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 44
Asp Tyr Ala Met His
1 5
<210> 45
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 45
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 46
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 46
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 47
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 47
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 48
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 48
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 49
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 49
Lys Ala Ser Arg Leu Glu Arg
1 5
<210> 50
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 50
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 51
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 51
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 52
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 52
Asp Tyr Ala Met His
1 5
<210> 53
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 53
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val Lys
1 5 10 15
Gly
<210> 54
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 54
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 55
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 55
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 56
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 56
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 57
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 57
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 58
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 58
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 59
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 59
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 60
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 60
Asp Tyr Ala Met His
1 5
<210> 61
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 61
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val Lys
1 5 10 15
Gly
<210> 62
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 62
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 63
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 63
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 64
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 64
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 65
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 65
Lys Ala Ser Arg Leu Glu Arg
1 5
<210> 66
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 66
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 67
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 67
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 68
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 68
Asp Tyr Ala Met His
1 5
<210> 69
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 69
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 70
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 70
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 71
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 71
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 72
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 72
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 73
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 73
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 74
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 74
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 75
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 75
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Lys Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 76
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 76
Asp Tyr Ala Met His
1 5
<210> 77
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 77
Gly Ile Ser Trp Arg Gly Asp Ile Lys Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 78
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 78
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 79
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 79
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Gln Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 80
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 80
Arg Ala Ser Lys Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 81
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 81
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 82
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 82
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 83
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 83
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Lys Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 84
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 84
Asp Tyr Ala Met His
1 5
<210> 85
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 85
Gly Ile Ser Trp Arg Gly Asp Ile Lys Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 86
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 86
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 87
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 87
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Asn Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 88
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 88
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 89
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 89
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 90
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 90
Leu Glu Tyr Asn Ser Tyr Ile Arg Thr
1 5
<210> 91
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 91
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 92
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 92
Asp Tyr Ala Met His
1 5
<210> 93
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 93
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val Lys
1 5 10 15
Gly
<210> 94
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 94
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 95
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 95
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Glu Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Gln Arg Leu Asp Arg Gly Thr Pro Gln Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 96
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 96
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 97
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 97
Lys Ala Gln Arg Leu Asp Arg
1 5
<210> 98
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 98
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 99
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 99
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 100
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 100
Asp Tyr Ala Met His
1 5
<210> 101
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 101
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 102
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 102
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 103
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 103
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Glu Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Lys Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Gln Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Arg Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 104
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 104
Arg Ala Ser Gln Ser Ile Lys Ser Trp Leu Ala
1 5 10
<210> 105
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 105
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 106
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 106
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 107
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 107
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Arg Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 108
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 108
Asp Tyr Ala Met His
1 5
<210> 109
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 109
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 110
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 110
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 111
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 111
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Glu Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Arg Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Glu Arg Gly Thr Pro Gln Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Tyr Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 112
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 112
Arg Ala Ser Lys Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 113
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 113
Lys Ala Ser Arg Leu Glu Arg
1 5
<210> 114
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 114
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 115
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 115
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Arg Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 116
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 116
Asp Tyr Ala Met His
1 5
<210> 117
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 117
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 118
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 118
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 119
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 119
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 120
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 120
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 121
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 121
Lys Ala Ser Arg Leu Glu Arg
1 5
<210> 122
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 122
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 123
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 123
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 124
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 124
Asp Tyr Ala Met His
1 5
<210> 125
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 125
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 126
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 126
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 127
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 127
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 128
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 128
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 129
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 129
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 130
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 130
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 131
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 131
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 132
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 132
Asp Tyr Ala Met His
1 5
<210> 133
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 133
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 134
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 134
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 135
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 135
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 136
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 136
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 137
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 137
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 138
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 138
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 139
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 139
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 140
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 140
Asp Tyr Ala Met His
1 5
<210> 141
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 141
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 142
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 142
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 143
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 143
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Cys Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 144
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 144
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 145
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 145
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 146
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 146
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 147
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 147
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 148
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 148
Asp Tyr Ala Met His
1 5
<210> 149
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 149
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 150
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 150
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 151
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 151
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 152
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 152
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 153
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 153
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 154
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 154
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 155
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 155
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 156
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 156
Asp Tyr Ala Met His
1 5
<210> 157
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 157
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 158
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 158
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 159
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 159
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Leu Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 160
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 160
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 161
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 161
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 162
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 162
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 163
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 163
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 164
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 164
Asp Tyr Ala Met His
1 5
<210> 165
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 165
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 166
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 166
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 167
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 167
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Met Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 168
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 168
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 169
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 169
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 170
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 170
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 171
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 171
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 172
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 172
Asp Tyr Ala Met His
1 5
<210> 173
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 173
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 174
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 174
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 175
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 175
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Asn Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 176
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 176
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 177
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 177
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 178
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 178
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 179
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 179
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 180
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 180
Asp Tyr Ala Met His
1 5
<210> 181
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 181
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 182
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 182
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 183
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 183
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Gln Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 184
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 184
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 185
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 185
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 186
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 186
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 187
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 187
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 188
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 188
Asp Tyr Ala Met His
1 5
<210> 189
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 189
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 190
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 190
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 191
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 191
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Ser Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 192
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 192
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 193
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 193
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 194
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 194
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 195
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 195
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 196
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 196
Asp Tyr Ala Met His
1 5
<210> 197
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 197
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 198
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 198
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 199
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 199
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 200
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 200
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 201
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 201
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 202
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 202
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 203
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 203
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 204
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 204
Asp Tyr Ala Met His
1 5
<210> 205
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 205
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 206
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 206
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 207
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 207
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Trp Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 208
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 208
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 209
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 209
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 210
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 210
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 211
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 211
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 212
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 212
Asp Tyr Ala Met His
1 5
<210> 213
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 213
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 214
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 214
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 215
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 215
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 216
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 216
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 217
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 217
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 218
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 218
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 219
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 219
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 220
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 220
Asp Tyr Ala Met His
1 5
<210> 221
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 221
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 222
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 222
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 223
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 223
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 224
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 224
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 225
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 225
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 226
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 226
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 227
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 227
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 228
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 228
Asp Tyr Ala Met His
1 5
<210> 229
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 229
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 230
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 230
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 231
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 231
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 232
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 232
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 233
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 233
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 234
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 234
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 235
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 235
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 236
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 236
Asp Tyr Ala Met His
1 5
<210> 237
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 237
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 238
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 238
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 239
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 239
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 240
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 240
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 241
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 241
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 242
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 242
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 243
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 243
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 244
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 244
Asp Tyr Ala Met His
1 5
<210> 245
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 245
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 246
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 246
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 247
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 247
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 248
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 248
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 249
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 249
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 250
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 250
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 251
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 251
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 252
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 252
Asp Tyr Ala Met His
1 5
<210> 253
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 253
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 254
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 254
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 255
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 255
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 256
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 256
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 257
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 257
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 258
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 258
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 259
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 259
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 260
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 260
Asp Tyr Ala Met His
1 5
<210> 261
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 261
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 262
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 262
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 263
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 263
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 264
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 264
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 265
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 265
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 266
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 266
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 267
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 267
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Lys Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 268
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 268
Asp Tyr Ala Met His
1 5
<210> 269
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 269
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 270
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 270
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 271
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 271
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 272
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 272
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 273
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 273
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 274
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 274
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 275
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 275
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 276
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 276
Asp Tyr Ala Met His
1 5
<210> 277
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 277
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 278
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 278
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 279
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 279
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 280
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 280
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 281
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 281
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 282
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 282
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 283
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 283
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 284
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 284
Asp Tyr Ala Met His
1 5
<210> 285
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 285
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 286
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 286
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 287
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 287
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 288
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 288
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 289
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 289
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 290
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 290
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 291
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 291
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 292
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 292
Asp Tyr Ala Met His
1 5
<210> 293
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 293
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 294
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 294
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 295
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 295
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 296
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 296
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 297
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 297
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 298
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 298
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 299
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 299
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 300
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 300
Asp Tyr Ala Met His
1 5
<210> 301
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 301
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 302
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 302
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 303
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 303
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 304
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 304
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 305
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 305
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 306
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 306
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 307
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 307
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Lys Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 308
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 308
Asp Tyr Ala Met His
1 5
<210> 309
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 309
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 310
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 310
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 311
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 311
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 312
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 312
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 313
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 313
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 314
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 314
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 315
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 315
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asp Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 316
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 316
Asp Tyr Ala Met His
1 5
<210> 317
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 317
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 318
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 318
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 319
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 319
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 320
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 320
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 321
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 321
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 322
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 322
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 323
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 323
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 324
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 324
Asp Tyr Ala Met His
1 5
<210> 325
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 325
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 326
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 326
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 327
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 327
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Lys Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 328
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 328
Arg Ala Ser Gln Lys Ile Ser Ser Trp Leu Ala
1 5 10
<210> 329
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 329
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 330
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 330
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 331
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 331
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 332
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 332
Asp Tyr Ala Met His
1 5
<210> 333
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 333
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 334
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 334
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 335
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 335
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gln Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 336
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 336
Arg Ala Ser Gln Gln Ile Ser Ser Trp Leu Ala
1 5 10
<210> 337
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 337
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 338
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 338
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 339
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 339
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 340
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 340
Asp Tyr Ala Met His
1 5
<210> 341
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 341
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 342
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 342
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 343
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 343
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gln Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 344
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 344
Arg Ala Ser Gln Ser Ile Gln Ser Trp Leu Ala
1 5 10
<210> 345
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 345
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 346
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 346
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 347
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 347
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 348
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 348
Asp Tyr Ala Met His
1 5
<210> 349
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 349
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 350
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 350
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 351
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 351
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Lys Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 352
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 352
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 353
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 353
Lys Ala Ser Arg Leu Asp Lys
1 5
<210> 354
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 354
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 355
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 355
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 356
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 356
Asp Tyr Ala Met His
1 5
<210> 357
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 357
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 358
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 358
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 359
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 359
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Lys Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 360
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 360
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 361
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 361
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 362
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 362
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 363
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 363
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 364
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 364
Asp Tyr Ala Met His
1 5
<210> 365
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 365
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 366
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 366
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 367
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 367
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Glu Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 368
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 368
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 369
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 369
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 370
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 370
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 371
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 371
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 372
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 372
Asp Tyr Ala Met His
1 5
<210> 373
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 373
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 374
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 374
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 375
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 375
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Thr Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 376
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 376
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 377
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 377
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 378
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 378
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 379
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 379
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 380
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 380
Asp Tyr Ala Met His
1 5
<210> 381
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 381
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 382
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 382
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 383
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 383
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Ser Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 384
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 384
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 385
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 385
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 386
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 386
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 387
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 387
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 388
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 388
Asp Tyr Ala Met His
1 5
<210> 389
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 389
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 390
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 390
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 391
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 391
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Gln Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 392
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 392
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 393
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 393
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 394
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 394
Leu Glu Tyr Gln Ser Tyr Ile Arg Thr
1 5
<210> 395
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 395
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 396
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 396
Asp Tyr Ala Met His
1 5
<210> 397
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 397
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 398
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 398
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 399
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 399
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Lys Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 400
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 400
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 401
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 401
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 402
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 402
Leu Glu Tyr Lys Ser Tyr Ile Arg Thr
1 5
<210> 403
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 403
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 404
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 404
Asp Tyr Ala Met His
1 5
<210> 405
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 405
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 406
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 406
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 407
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 407
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Trp Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 408
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 408
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 409
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 409
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 410
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 410
Leu Glu Tyr Ser Ser Trp Ile Arg Thr
1 5
<210> 411
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 411
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 412
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 412
Asp Tyr Ala Met His
1 5
<210> 413
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 413
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 414
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 414
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 415
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 415
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Tyr Asp Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Arg Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 416
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 416
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 417
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 417
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 418
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 418
Leu Glu Tyr Arg Ser Tyr Ile Arg Thr
1 5
<210> 419
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 419
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Glu Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 420
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 420
Asp Tyr Ala Met His
1 5
<210> 421
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 421
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 422
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 422
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 423
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 423
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Gln Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Tyr Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Asn Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 424
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 424
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 425
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 425
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 426
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 426
Leu Glu Tyr Asn Ser Tyr Ile Arg Thr
1 5
<210> 427
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 427
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 428
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 428
Asp Tyr Ala Met His
1 5
<210> 429
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 429
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 430
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 430
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 431
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 431
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 432
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 432
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 433
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 433
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 434
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 434
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 435
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 435
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 436
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 436
Asp Tyr Ala Met His
1 5
<210> 437
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 437
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 438
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 438
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 439
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 439
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 440
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 440
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 441
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 441
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 442
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 442
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 443
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 443
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Leu Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 444
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 444
Asp Tyr Ala Met His
1 5
<210> 445
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 445
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 446
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 446
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 447
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 447
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 448
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 448
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 449
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 449
Lys Ala Ser Arg Leu Glu Arg
1 5
<210> 450
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 450
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 451
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 451
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 452
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 452
Asp Tyr Ala Met His
1 5
<210> 453
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 453
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 454
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 454
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 455
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 455
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Arg Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 456
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 456
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 457
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 457
Lys Ala Ser Arg Leu Asp Arg
1 5
<210> 458
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 458
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 459
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 459
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 460
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 460
Thr Ser Trp Ile Val
1 5
<210> 461
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 461
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 462
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 462
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 463
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 463
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 464
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 464
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 465
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 465
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 466
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 466
Gln Gln Phe Gly Ser Ser Arg Leu Phe Thr
1 5 10
<210> 467
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 467
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 468
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 468
Thr Ser Trp Ile Val
1 5
<210> 469
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 469
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 470
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 470
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 471
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 471
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 472
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 472
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 473
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 473
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 474
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 474
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 475
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 475
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 476
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 476
Thr Ser Trp Ile Val
1 5
<210> 477
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 477
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 478
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 478
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 479
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 479
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Ala Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 480
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 480
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 481
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 481
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 482
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 482
Gln Gln Phe Gly Ser Ser Arg Leu Phe Thr
1 5 10
<210> 483
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 483
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 484
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 484
Thr Ser Trp Ile Ser
1 5
<210> 485
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 485
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 486
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 486
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 487
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 487
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 488
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 488
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 489
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 489
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 490
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 490
Gln Gln Tyr Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 491
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 491
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 492
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 492
Thr Ser Trp Ile Ser
1 5
<210> 493
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 493
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 494
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 494
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 495
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 495
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 496
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 496
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 497
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 497
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 498
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 498
Gln Gln Tyr Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 499
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 499
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 500
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 500
Thr Ser Trp Ile Ser
1 5
<210> 501
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 501
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 502
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 502
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 503
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 503
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 504
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 504
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 505
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 505
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 506
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 506
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 507
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 507
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 508
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 508
Thr Ser Trp Ile Ser
1 5
<210> 509
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 509
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 510
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 510
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 511
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 511
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 512
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 512
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 513
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 513
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 514
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 514
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 515
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 515
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 516
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 516
Thr Ser Trp Ile Ser
1 5
<210> 517
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 517
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 518
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 518
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 519
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 519
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 520
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 520
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 521
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 521
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 522
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 522
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 523
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 523
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 524
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 524
Thr Ser Trp Ile Ser
1 5
<210> 525
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 525
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 526
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 526
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 527
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 527
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 528
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 528
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 529
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 529
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 530
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 530
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 531
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 531
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 532
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 532
Thr Ser Trp Ile Ser
1 5
<210> 533
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 533
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 534
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 534
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 535
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 535
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 536
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 536
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 537
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 537
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 538
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 538
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 539
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 539
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 540
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 540
Thr Ser Trp Ile Val
1 5
<210> 541
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 541
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 542
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 542
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 543
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 543
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 544
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 544
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 545
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 545
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 546
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 546
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 547
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 547
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 548
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 548
Thr Ser Trp Ile Val
1 5
<210> 549
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 549
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 550
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 550
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 551
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 551
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 552
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 552
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 553
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 553
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 554
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 554
Gln Gln Phe Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 555
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 555
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 556
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 556
Thr Ser Trp Ile Val
1 5
<210> 557
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 557
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 558
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 558
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 559
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 559
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 560
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 560
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 561
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 561
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 562
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 562
Gln Gln Tyr Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 563
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 563
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 564
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 564
Thr Ser Trp Ile Ser
1 5
<210> 565
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 565
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 566
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 566
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 567
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 567
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 568
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 568
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 569
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 569
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 570
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 570
Gln Gln Tyr Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 571
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 571
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 572
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 572
Thr Ser Trp Ile Ser
1 5
<210> 573
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 573
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 574
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 574
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 575
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 575
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 576
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 576
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 577
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 577
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 578
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 578
Gln Gln Tyr Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 579
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 579
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 580
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 580
Thr Ser Trp Ile Ser
1 5
<210> 581
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 581
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 582
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 582
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 583
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 583
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 584
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 584
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 585
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 585
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 586
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 586
Gln Gln Tyr Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 587
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 587
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 588
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 588
Thr Ser Trp Ile Val
1 5
<210> 589
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 589
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 590
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 590
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 591
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 591
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 592
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 592
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 593
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 593
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 594
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 594
Gln Gln Tyr Gly Asp Ser Gln Leu Phe Thr
1 5 10
<210> 595
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 595
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 596
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 596
Thr Ser Trp Ile Val
1 5
<210> 597
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 597
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 598
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 598
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 599
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 599
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 600
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 600
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 601
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 601
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 602
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 602
Gln Gln Tyr Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 603
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 603
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 604
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 604
Thr Ser Trp Ile Ser
1 5
<210> 605
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 605
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 606
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 606
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 607
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 607
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 608
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 608
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 609
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 609
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 610
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 610
Gln Gln Tyr Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 611
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 611
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 612
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 612
Thr Ser Trp Ile Ser
1 5
<210> 613
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 613
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 614
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 614
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 615
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 615
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 616
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 616
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 617
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 617
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 618
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 618
Gln Gln Tyr Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 619
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 619
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 620
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 620
Thr Ser Trp Ile Ser
1 5
<210> 621
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 621
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 622
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 622
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 623
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 623
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 624
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 624
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 625
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 625
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 626
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 626
Gln Gln Tyr Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 627
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 627
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 628
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 628
Thr Ser Trp Ile Ser
1 5
<210> 629
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 629
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 630
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 630
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 631
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 631
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 632
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 632
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 633
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 633
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 634
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 634
Gln Gln Tyr Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 635
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 635
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 636
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 636
Thr Ser Trp Ile Ser
1 5
<210> 637
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 637
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 638
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 638
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 639
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 639
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 640
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 640
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 641
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 641
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 642
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 642
Gln Gln Tyr Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 643
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 643
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 644
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 644
Thr Ser Trp Ile Val
1 5
<210> 645
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 645
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 646
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 646
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 647
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 647
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 648
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 648
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 649
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 649
Gly Ala Ser Ser Arg Ala Arg
1 5
<210> 650
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 650
Gln Gln Tyr Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 651
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 651
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 652
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 652
Thr Ser Trp Ile Val
1 5
<210> 653
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 653
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 654
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 654
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 655
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 655
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 656
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 656
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 657
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 657
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 658
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 658
Gln Gln Phe Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 659
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 659
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 660
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 660
Thr Ser Trp Ile Ser
1 5
<210> 661
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 661
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 662
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 662
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 663
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 663
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 664
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 664
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 665
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 665
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 666
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 666
Gln Gln Phe Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 667
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 667
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 668
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 668
Thr Ser Trp Ile Ser
1 5
<210> 669
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 669
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 670
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 670
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 671
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 671
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 672
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 672
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 673
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 673
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 674
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 674
Gln Gln Phe Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 675
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 675
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 676
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 676
Thr Ser Trp Ile Ser
1 5
<210> 677
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 677
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 678
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 678
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 679
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 679
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 680
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 680
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 681
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 681
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 682
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 682
Gln Gln Phe Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 683
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 683
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 684
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 684
Thr Ser Trp Ile Ser
1 5
<210> 685
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 685
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 686
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 686
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 687
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 687
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 688
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 688
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 689
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 689
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 690
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 690
Gln Gln Phe Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 691
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 691
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 692
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 692
Thr Ser Trp Ile Ser
1 5
<210> 693
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 693
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 694
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 694
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 695
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 695
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 696
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 696
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 697
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 697
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 698
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
400> 698
Gln Gln Phe Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 699
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 699
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 700
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 700
Thr Ser Trp Ile Val
1 5
<210> 701
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 701
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 702
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 702
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 703
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 703
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ser Arg
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 704
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 704
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 705
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 705
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 706
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 706
Gln Gln Phe Gly Asp Ser Arg Leu Phe Thr
1 5 10
<210> 707
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 707
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 708
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 708
Thr Ser Trp Ile Val
1 5
<210> 709
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 709
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 710
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 710
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 711
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 711
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 712
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 712
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 713
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 713
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 714
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 714
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 715
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 715
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 716
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 716
Thr Ser Trp Ile Val
1 5
<210> 717
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 717
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 718
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 718
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 719
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 719
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 720
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 720
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 721
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 721
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 722
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 722
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 723
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 723
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 724
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 724
Thr Ser Trp Ile Val
1 5
<210> 725
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 725
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 726
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 726
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 727
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 727
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 728
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 728
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 729
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 729
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 730
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 730
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 731
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 731
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 732
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 732
Thr Ser Trp Ile Val
1 5
<210> 733
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 733
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 734
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 734
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 735
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 735
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Gln Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 736
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 736
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 737
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 737
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 738
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 738
Gln Gln Phe Gly Gln Ser Gln Leu Phe Thr
1 5 10
<210> 739
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 739
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 740
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 740
Thr Ser Trp Ile Val
1 5
<210> 741
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 741
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 742
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 742
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 743
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 743
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ala Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 744
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 744
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 745
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 745
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 746
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 746
Gln Gln Phe Gly Asp Ala Gln Leu Phe Thr
1 5 10
<210> 747
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 747
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 748
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 748
Thr Ser Trp Ile Val
1 5
<210> 749
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 749
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 750
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 750
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 751
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 751
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 752
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 752
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 753
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 753
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 754
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 754
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 755
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 755
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 756
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 756
Thr Ser Trp Ile Val
1 5
<210> 757
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 757
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 758
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 758
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 759
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 759
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 760
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 760
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 761
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 761
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 762
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 762
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 763
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 763
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 764
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 764
Thr Ser Trp Ile Ser
1 5
<210> 765
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 765
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 766
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 766
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 767
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 767
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 768
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 768
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 769
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 769
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 770
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 770
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 771
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 771
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 772
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 772
Thr Ser Trp Ile Ser
1 5
<210> 773
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 773
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 774
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 774
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 775
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 775
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 776
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 776
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 777
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 777
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 778
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 778
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 779
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 779
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 780
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 780
Thr Ser Trp Ile Ser
1 5
<210> 781
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 781
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 782
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 782
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 783
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 783
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 784
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 784
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 785
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 785
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 786
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 786
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 787
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 787
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 788
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 788
Thr Ser Trp Ile Ser
1 5
<210> 789
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 789
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 790
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 790
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 791
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 791
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 792
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 792
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 793
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 793
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 794
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 794
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 795
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 795
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 796
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 796
Thr Ser Trp Ile Ser
1 5
<210> 797
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 797
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 798
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 798
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 799
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 799
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 800
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 800
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 801
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 801
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 802
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 802
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 803
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 803
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 804
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 804
Thr Ser Trp Ile Val
1 5
<210> 805
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 805
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 806
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 806
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 807
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 807
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 808
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 808
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 809
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 809
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 810
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 810
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 811
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 811
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 812
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 812
Thr Ser Trp Ile Val
1 5
<210> 813
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 813
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 814
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 814
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 815
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 815
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Ser Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 816
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 816
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 817
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 817
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 818
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 818
Gln Gln Phe Gly Ser Ser Gln Leu Phe Thr
1 5 10
<210> 819
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 819
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 820
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 820
Thr Ser Trp Ile Ser
1 5
<210> 821
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 821
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 822
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 822
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 823
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 823
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 824
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 824
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 825
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 825
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 826
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 826
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 827
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 827
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 828
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 828
Thr Ser Trp Ile Ser
1 5
<210> 829
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 829
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 830
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 830
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 831
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 831
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 832
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 832
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 833
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 833
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 834
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 834
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 835
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 835
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 836
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 836
Thr Ser Trp Ile Ser
1 5
<210> 837
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 837
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 838
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 838
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 839
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 839
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 840
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 840
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 841
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 841
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 842
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 842
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 843
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 843
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 844
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 844
Thr Ser Trp Ile Ser
1 5
<210> 845
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 845
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 846
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 846
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 847
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 847
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 848
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 848
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 849
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 849
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 850
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 850
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 851
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 851
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 852
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 852
Thr Ser Trp Ile Ser
1 5
<210> 853
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 853
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 854
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 854
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 855
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 855
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 856
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 856
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 857
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 857
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 858
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 858
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 859
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 859
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 860
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 860
Thr Ser Trp Ile Val
1 5
<210> 861
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 861
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 862
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 862
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 863
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 863
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 864
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 864
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 865
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 865
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 866
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 866
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 867
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 867
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 868
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 868
Thr Ser Trp Ile Val
1 5
<210> 869
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 869
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 870
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 870
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 871
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 871
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Glu Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 872
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 872
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 873
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 873
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 874
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 874
Gln Gln Phe Gly Glu Ser Gln Leu Phe Thr
1 5 10
<210> 875
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 875
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 876
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 876
Thr Ser Trp Ile Ser
1 5
<210> 877
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 877
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 878
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 878
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 879
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 879
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 880
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 880
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 881
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 881
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 882
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 882
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 883
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 883
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 884
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 884
Thr Ser Trp Ile Ser
1 5
<210> 885
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 885
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 886
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 886
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 887
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 887
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 888
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 888
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 889
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 889
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 890
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 890
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 891
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 891
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 892
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 892
Thr Ser Trp Ile Ser
1 5
<210> 893
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 893
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 894
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 894
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 895
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 895
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 896
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 896
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 897
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 897
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 898
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 898
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 899
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 899
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 900
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 900
Thr Ser Trp Ile Ser
1 5
<210> 901
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 901
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 902
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 902
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 903
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 903
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 904
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 904
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 905
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 905
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 906
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 906
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 907
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 907
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 908
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 908
Thr Ser Trp Ile Ser
1 5
<210> 909
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 909
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 910
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 910
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 911
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 911
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 912
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 912
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 913
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 913
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 914
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 914
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 915
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 915
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 916
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 916
Thr Ser Trp Ile Val
1 5
<210> 917
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 917
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 918
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 918
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 919
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 919
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 920
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 920
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 921
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 921
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 922
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 922
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 923
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 923
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 924
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 924
Thr Ser Trp Ile Val
1 5
<210> 925
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 925
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 926
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 926
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 927
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 927
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asn Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 928
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 928
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 929
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 929
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 930
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 930
Gln Gln Phe Gly Asn Ser Gln Leu Phe Thr
1 5 10
<210> 931
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 931
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 932
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 932
Thr Ser Trp Ile Ser
1 5
<210> 933
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 933
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 934
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 934
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 935
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 935
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Gln Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 936
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 936
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 937
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 937
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 938
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 938
Gln Gln Phe Gly Gln Ser Gln Leu Phe Thr
1 5 10
<210> 939
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 939
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 940
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 940
Thr Ser Trp Ile Ser
1 5
<210> 941
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 941
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 942
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 942
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 943
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 943
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Gln Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 944
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 944
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 945
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 945
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 946
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 946
Gln Gln Phe Gly Gln Ser Gln Leu Phe Thr
1 5 10
<210> 947
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 947
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 948
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 948
Thr Ser Trp Ile Ser
1 5
<210> 949
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 949
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 950
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 950
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 951
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 951
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Gln Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 952
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 952
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 953
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 953
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 954
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 954
Gln Gln Phe Gly Gln Ser Gln Leu Phe Thr
1 5 10
<210> 955
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 955
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 956
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 956
Thr Ser Trp Ile Ser
1 5
<210> 957
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 957
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 958
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 958
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 959
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 959
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Gln Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 960
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 960
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 961
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 961
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 962
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 962
Gln Gln Phe Gly Gln Ser Gln Leu Phe Thr
1 5 10
<210> 963
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 963
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 964
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 964
Thr Ser Trp Ile Val
1 5
<210> 965
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 965
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 966
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 966
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 967
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 967
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Gln Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 968
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 968
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 969
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 969
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 970
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 970
Gln Gln Phe Gly Gln Ser Gln Leu Phe Thr
1 5 10
<210> 971
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 971
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 972
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 972
Thr Ser Trp Ile Val
1 5
<210> 973
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 973
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 974
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 974
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 975
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 975
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Gln Ser Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 976
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 976
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 977
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 977
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 978
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 978
Gln Gln Phe Gly Gln Ser Gln Leu Phe Thr
1 5 10
<210> 979
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 979
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 980
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 980
Thr Ser Trp Ile Ser
1 5
<210> 981
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 981
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 982
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 982
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 983
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 983
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ala Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 984
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 984
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 985
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 985
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 986
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 986
Gln Gln Phe Gly Asp Ala Gln Leu Phe Thr
1 5 10
<210> 987
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 987
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 988
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 988
Thr Ser Trp Ile Ser
1 5
<210> 989
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 989
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 990
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 990
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 991
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 991
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ala Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 992
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 992
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 993
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 993
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 994
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 994
Gln Gln Phe Gly Asp Ala Gln Leu Phe Thr
1 5 10
<210> 995
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 995
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 996
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 996
Thr Ser Trp Ile Ser
1 5
<210> 997
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 997
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 998
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 998
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 999
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 999
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ala Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1000
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1000
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1001
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1001
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1002
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1002
Gln Gln Phe Gly Asp Ala Gln Leu Phe Thr
1 5 10
<210> 1003
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1003
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1004
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1004
Thr Ser Trp Ile Ser
1 5
<210> 1005
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1005
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1006
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1006
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1007
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1007
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ala Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1008
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1008
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1009
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1009
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1010
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1010
Gln Gln Phe Gly Asp Ala Gln Leu Phe Thr
1 5 10
<210> 1011
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1011
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1012
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1012
Thr Ser Trp Ile Val
1 5
<210> 1013
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1013
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1014
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1014
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1015
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1015
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ala Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1016
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1016
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1017
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1017
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1018
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1018
Gln Gln Phe Gly Asp Ala Gln Leu Phe Thr
1 5 10
<210> 1019
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1019
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1020
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1020
Thr Ser Trp Ile Val
1 5
<210> 1021
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1021
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1022
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1022
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1023
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1023
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Ala Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1024
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1024
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1025
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1025
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1026
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1026
Gln Gln Phe Gly Asp Ala Gln Leu Phe Thr
1 5 10
<210> 1027
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1027
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1028
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1028
Thr Ser Trp Ile Ser
1 5
<210> 1029
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1029
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1030
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1030
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1031
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1031
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1032
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1032
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1033
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1033
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1034
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1034
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 1035
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1035
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1036
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1036
Thr Ser Trp Ile Ser
1 5
<210> 1037
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1037
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1038
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1038
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1039
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1039
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1040
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1040
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1041
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1041
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1042
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1042
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 1043
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1043
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1044
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1044
Thr Ser Trp Ile Ser
1 5
<210> 1045
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1045
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1046
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1046
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1047
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1047
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1048
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1048
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1049
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1049
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1050
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1050
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 1051
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1051
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1052
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1052
Thr Ser Trp Ile Ser
1 5
<210> 1053
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1053
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1054
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1054
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1055
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1055
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1056
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1056
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1057
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1057
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1058
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1058
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 1059
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1059
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1060
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1060
Thr Ser Trp Ile Ser
1 5
<210> 1061
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1061
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1062
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1062
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1063
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1063
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1064
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1064
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1065
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1065
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1066
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1066
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 1067
<211> 120
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1067
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1068
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1068
Thr Ser Trp Ile Val
1 5
<210> 1069
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1069
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1070
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1070
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1071
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1071
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1072
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1072
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1073
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1073
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1074
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1074
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 1075
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1075
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1076
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1076
Thr Ser Trp Ile Val
1 5
<210> 1077
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1077
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1078
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1078
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1079
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1079
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Thr Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1080
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1080
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1081
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1081
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1082
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1082
Gln Gln Phe Gly Asp Thr Gln Leu Phe Thr
1 5 10
<210> 1083
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1083
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1084
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1084
Thr Ser Trp Ile Ser
1 5
<210> 1085
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1085
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1086
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1086
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1087
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1087
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1088
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1088
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1089
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1089
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1090
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1090
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 1091
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1091
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1092
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1092
Thr Ser Trp Ile Ser
1 5
<210> 1093
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1093
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1094
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1094
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1095
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1095
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1096
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1096
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1097
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1097
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1098
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1098
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 1099
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1099
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1100
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1100
Thr Ser Trp Ile Ser
1 5
<210> 1101
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1101
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1102
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1102
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1103
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1103
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1104
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1104
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1105
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1105
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1106
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1106
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 1107
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1107
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1108
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1108
Thr Ser Trp Ile Ser
1 5
<210> 1109
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1109
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1110
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1110
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1111
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1111
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1112
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1112
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1113
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1113
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1114
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1114
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 1115
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1115
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1116
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1116
Thr Ser Trp Ile Ser
1 5
<210> 1117
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1117
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1118
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1118
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1119
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1119
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1120
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1120
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1121
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1121
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1122
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1122
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 1123
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1123
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1124
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1124
Thr Ser Trp Ile Val
1 5
<210> 1125
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1125
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1126
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1126
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1127
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1127
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1128
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1128
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1129
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1129
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1130
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1130
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 1131
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1131
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1132
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1132
Thr Ser Trp Ile Val
1 5
<210> 1133
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1133
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1134
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1134
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1135
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1135
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asn Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1136
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1136
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1137
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1137
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1138
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1138
Gln Gln Phe Gly Asp Asn Gln Leu Phe Thr
1 5 10
<210> 1139
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1139
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1140
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1140
Thr Ser Trp Ile Ser
1 5
<210> 1141
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1141
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1142
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1142
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1143
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1143
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asp Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1144
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1144
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1145
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1145
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1146
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1146
Gln Gln Phe Gly Asp Asp Gln Leu Phe Thr
1 5 10
<210> 1147
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1147
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1148
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1148
Thr Ser Trp Ile Ser
1 5
<210> 1149
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1149
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1150
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1150
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1151
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1151
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asp Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1152
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1152
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1153
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1153
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1154
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1154
Gln Gln Phe Gly Asp Asp Gln Leu Phe Thr
1 5 10
<210> 1155
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1155
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1156
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1156
Thr Ser Trp Ile Ser
1 5
<210> 1157
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1157
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1158
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1158
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1159
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1159
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asp Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1160
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1160
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1161
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1161
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1162
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1162
Gln Gln Phe Gly Asp Asp Gln Leu Phe Thr
1 5 10
<210> 1163
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1163
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1164
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1164
Thr Ser Trp Ile Ser
1 5
<210> 1165
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1165
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1166
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1166
Leu His Tyr Tyr His Ser Glu Glu Phe Asp Val
1 5 10
<210> 1167
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1167
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asp Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1168
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1168
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1169
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1169
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1170
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1170
Gln Gln Phe Gly Asp Asp Gln Leu Phe Thr
1 5 10
<210> 1171
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1171
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1172
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1172
Thr Ser Trp Ile Ser
1 5
<210> 1173
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1173
Met Ile Asp Pro Ser Asp Ser Phe Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1174
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1174
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1175
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1175
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asp Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1176
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1176
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1177
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1177
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1178
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1178
Gln Gln Phe Gly Asp Asp Gln Leu Phe Thr
1 5 10
<210> 1179
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1179
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1180
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1180
Thr Ser Trp Ile Val
1 5
<210> 1181
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1181
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1182
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1182
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1183
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1183
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asp Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1184
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1184
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1185
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1185
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1186
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1186
Gln Gln Phe Gly Asp Asp Gln Leu Phe Thr
1 5 10
<210> 1187
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1187
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Ser
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 1188
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1188
Thr Ser Trp Ile Val
1 5
<210> 1189
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1189
Met Ile Asp Pro Ser Asp Ser Tyr Thr Ser Tyr Ser Pro Ser Phe Gln
1 5 10 15
Gly
<210> 1190
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1190
Leu His Tyr Tyr Asn Ser Glu Glu Phe Asp Val
1 5 10
<210> 1191
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1191
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Gln Ser Ser Arg Thr Arg Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Asp Asp Gln
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1192
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1192
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 1193
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1193
Gly Gln Ser Ser Arg Thr Arg
1 5
<210> 1194
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1194
Gln Gln Phe Gly Asp Asp Gln Leu Phe Thr
1 5 10
<210> 1195
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1195
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly
325
<210> 1196
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1196
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Leu Leu Tyr Ser
275 280 285
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly
325
<210> 1197
<211> 107
<212> БЕЛОК
<213> Homo sapiens
<400> 1197
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 1198
<211> 329
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1198
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Leu
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly
325
<210> 1199
<211> 329
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1199
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly
325
<210> 1200
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1200
His His His His His His
1 5
<210> 1201
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1201
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 1202
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1202
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1203
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1203
Asp Tyr Ala Met His
1 5
<210> 1204
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1204
Gly Ile Ser Trp Lys Gly Asp Ile Gly Gly Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 1205
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1205
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 1206
<211> 107
<212> БЕЛОК
<213> Homo sapiens
<400> 1206
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1207
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1207
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 1208
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1208
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 1209
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1209
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 1210
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1210
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1211
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1211
Asp Tyr Ala Met His
1 5
<210> 1212
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1212
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val Lys
1 5 10 15
Gly
<210> 1213
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1213
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 1214
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1214
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Glu Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Glu Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1215
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1215
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 1216
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1216
Lys Ala Ser Lys Leu Glu Arg
1 5
<210> 1217
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1217
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 1218
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1218
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Ala Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1219
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1219
Asp Tyr Ala Met His
1 5
<210> 1220
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1220
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Ala Lys Ser Val Lys
1 5 10 15
Gly
<210> 1221
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1221
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 1222
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1222
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1223
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1223
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 1224
<211> 7
<212> БЕЛОК
<213> Homo sapiens
<400> 1224
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 1225
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1225
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 1226
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1226
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1227
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1227
Asp Tyr Ala Met His
1 5
<210> 1228
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1228
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val Lys
1 5 10 15
Gly
<210> 1229
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1229
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 1230
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1230
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1231
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1231
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 1232
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1232
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 1233
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1233
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 1234
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1234
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1235
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1235
Asp Tyr Ala Met His
1 5
<210> 1236
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1236
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val Lys
1 5 10 15
Gly
<210> 1237
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1237
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 1238
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1238
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1239
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1239
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 1240
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1240
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 1241
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1241
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<210> 1242
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1242
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 1243
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1243
Asp Tyr Ala Met His
1 5
<210> 1244
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1244
Gly Ile Ser Trp Arg Gly Asp Ile Gly Gly Tyr Val Lys Ser Val Lys
1 5 10 15
Gly
<210> 1245
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1245
Ser Tyr Gly Ser Gly Ser Phe Tyr Asn Ala Phe Asp Ser
1 5 10
<210> 1246
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1246
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Lys Ala Ser Lys Leu Asp Arg Gly Thr Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Glu Tyr Ser Ser Tyr Ile Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1247
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1247
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 1248
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1248
Lys Ala Ser Lys Leu Asp Arg
1 5
<210> 1249
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Рекомбинантный белок
<400> 1249
Leu Glu Tyr Ser Ser Tyr Ile Arg Thr
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СТАБИЛЬНЫЕ И РАСТВОРИМЫЕ АНТИТЕЛА, ИНГИБИРУЮЩИЕ VEGF | 2019 |
|
RU2747735C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К FLT3, И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2758513C2 |
| CD131-СВЯЗЫВАЮЩИЕ БЕЛКИ И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2773927C2 |
| ВЫСОКОАФФИННЫЕ АНТИ-PD-1 И АНТИ-LAG-3 АНТИТЕЛА И ПОЛУЧЕННЫЕ ИЗ НИХ БИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ | 2019 |
|
RU2782381C2 |
| АНТИТЕЛА, СПЕЦИФИЧЕСКИЕ В ОТНОШЕНИИ CD70, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2801093C2 |
| АНТИТЕЛО, СПЕЦИФИЧНО СВЯЗЫВАЮЩЕЕСЯ С ICAM-1, И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2789757C2 |
| НЕВИРУСНЫЙ ИММУНОТАРГЕТИНГ | 2020 |
|
RU2833379C2 |
| АНТИТЕЛА ПРОТИВ СИГНАЛ-РЕГУЛЯТОРНОГО БЕЛКА АЛЬФА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2771964C2 |
| АНТИТЕЛА, СОДЕРЖАЩИЕ ПОЛИПЕПТИД, ВСТРОЕННЫЙ В УЧАСТОК КАРКАСНОЙ ОБЛАСТИ 3 | 2019 |
|
RU2796254C2 |
| АНТИ-CEACAM1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2754876C2 |








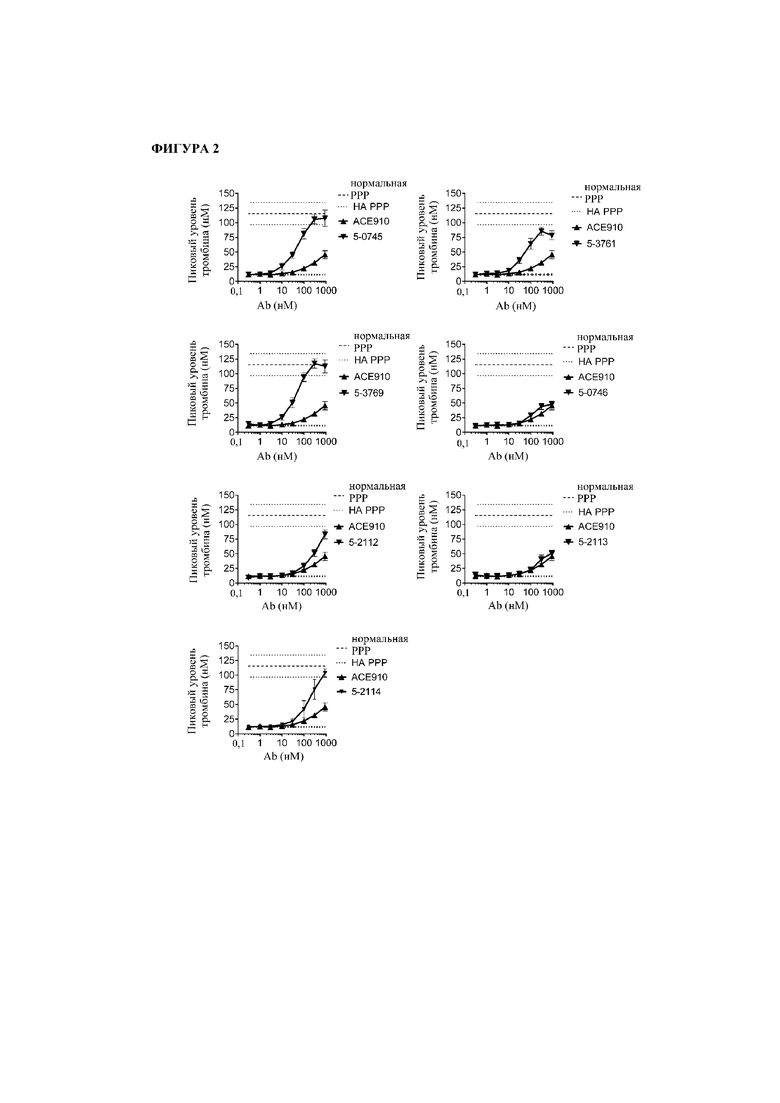
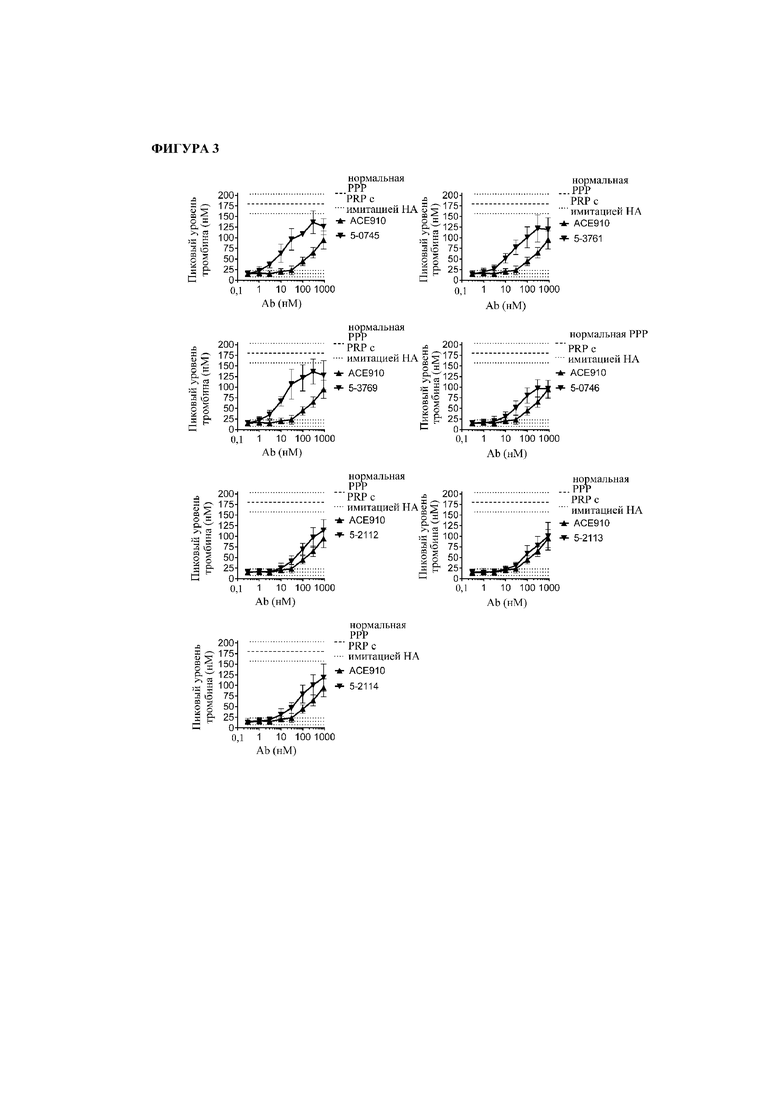
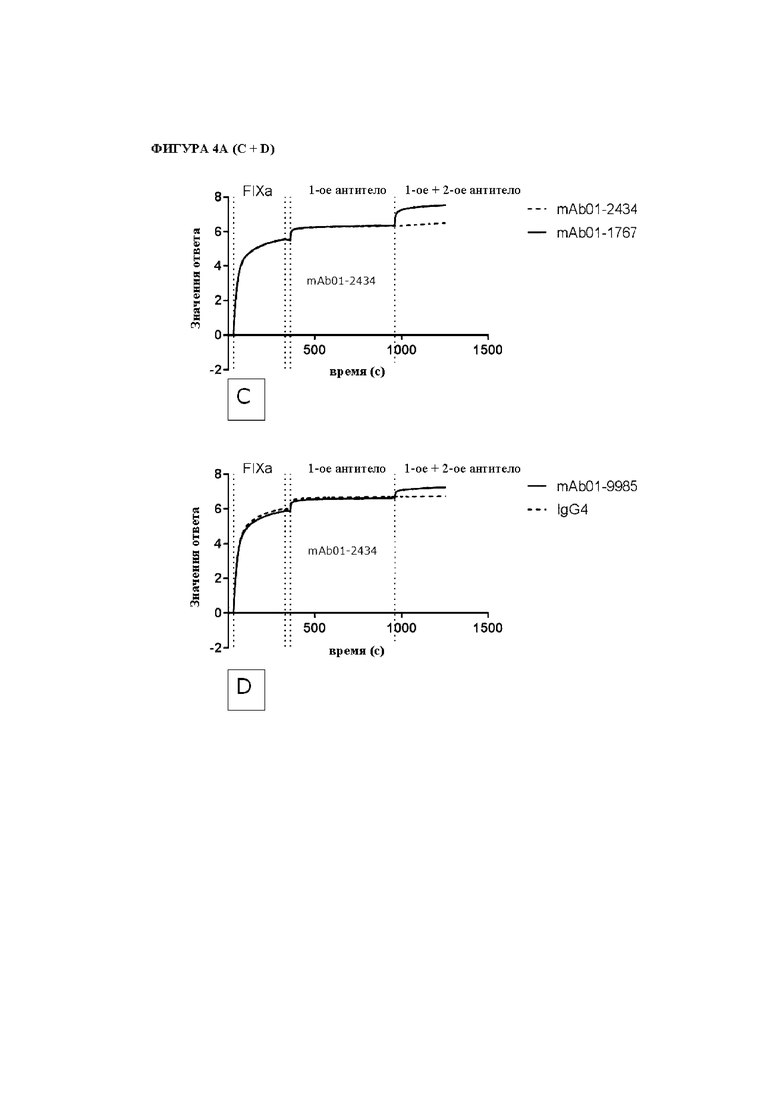
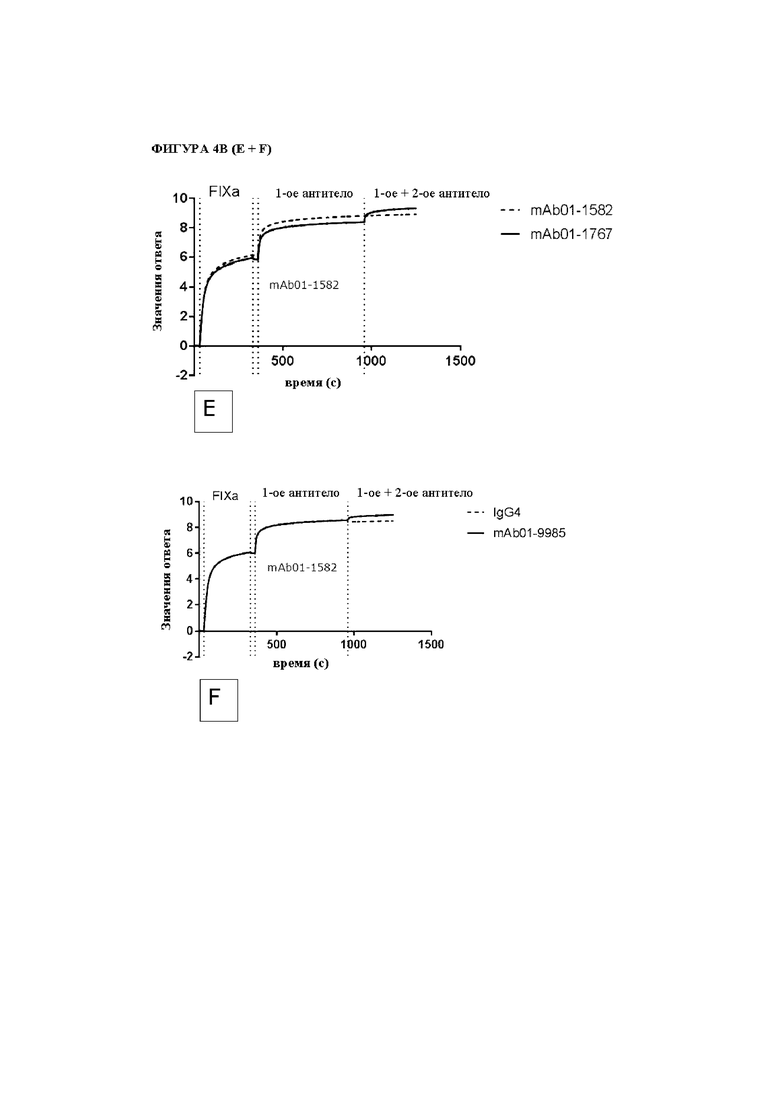
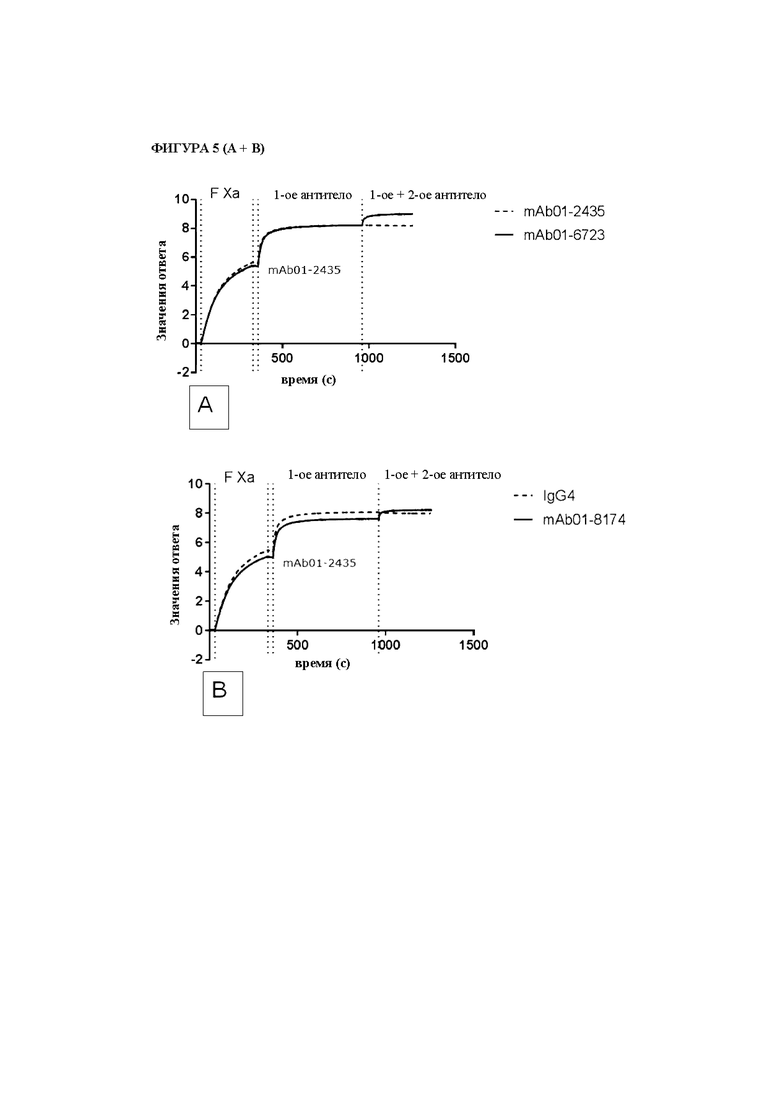
Изобретение относится к области биотехнологии. Предложены биспецифические антитела, способные связываться с фактором свертывания крови IX (FIX) и/или его активированной формой (FIXa) и с фактором X (FX) и/или его активированной формой (FXa) и стимулировать активацию FX под действием FIXa. Также предложены антитело или его антигенсвязывающий фрагмент, которые связываются с FIX и/или его активированной формой (FIXa) и являются промежуточными соединениями в изготовлении указанных биспецифических антител. Также изобретение относится к фармацевтической композиции и набору для лечения коагулопатии или нарушения свертываемости крови, содержащим указанные биспецифические антитела. Изобретение обеспечивает улучшенную стимуляцию ферментативной активности FIXa в отношении FX. 5 н. и 14 з.п. ф-лы, 9 ил., 21 табл., 17 пр.
1. Биспецифическое антитело или его антигенсвязывающий фрагмент, стимулирующие ферментативную активность FIXa в отношении FX, содержащие первый антигенсвязывающий участок и второй антигенсвязывающий участок, где
указанный первый антигенсвязывающий участок связывается с эпитопом, содержащим аминокислотные остатки R338, T340, K341 согласно SEQ ID NO: 1, и где второй антигенсвязывающий участок связывается с эпитопом, содержащим аминокислотные остатки:
i) E103, Q104, V108, R113, T116, L117, D119, I125, T127, E228, F229, Y230, E266, R287, P291, I292, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a) согласно SEQ ID NO: 2
или
ii) E103, Q104, V108, R113, T116, L117, A118, D119, I125, T127, S227, E228, Y230, R287, I292, L303, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a) согласно SEQ ID NO: 2.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, где первый антигенсвязывающий участок связывается с эпитопом, содержащим L337, R338, S339, T340 и K341 из FIX(a) согласно SEQ ID NO: 1, и где второй антигенсвязывающий участок связывается с эпитопом, содержащим аминокислотные остатки:
i) E103, Q104, V108, R113, T116, L117, D119, I125, T127, E228, F229, Y230, E266, R287, P291, I292, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a) согласно SEQ ID NO: 2
или
ii) E103, Q104, V108, R113, T116, L117, A118, D119, I125, T127, S227, E228, Y230, R287, I292, L303, P304, L419, K420, D423, R424, M426, K427 и T428 из FX(a) согласно SEQ ID NO: 2.
3. Антитело или его антигенсвязывающий фрагмент по п. 1, где первый антигенсвязывающий участок содержит:
i) паратоп, содержащий аминокислотные остатки D30, D31, W53, S102, S104 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO: 35) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO: 39), или
ii) паратоп, содержащий аминокислотные остатки H30, D31, W53, D56, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO: 67) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO: 71), или
iii) паратоп, содержащий аминокислотные остатки H30, D31, W53, S102, S104, Y106 и N107 в вариабельном домене тяжелой цепи (SEQ ID NO: 51) и аминокислотные остатки Y91 и S92 в вариабельном домене легкой цепи (SEQ ID NO: 55),
и второй антигенсвязывающий участок содержит:
a) паратоп, содержащий аминокислотные остатки K23, G24, S25, G26, Y27, W33, D52, S54, D55, Y57, S77, L99, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO: 483) и аминокислотные остатки S30, S31, Y33, Y50, Q52, S54, R55, R57, Y92 и D94 в вариабельном домене легкой цепи (SEQ ID NO: 487), или
b) паратоп, содержащий аминокислотные остатки K23, S25, G26, Y27, F29, W33, D52, S54, D55, F57, S77, H100, Y101, Y102, N103 и S104 в вариабельном домене тяжелой цепи (SEQ ID NO: 467) и остатки V29, S30, S31, Y33, Y50, Q52, S54, R55, R57 и D94 в вариабельном домене легкой цепи (SEQ ID NO: 471).
4. Биспецифическое антитело или его антигенсвязывающий фрагмент, связывающиеся с FIX (SEQ ID NO: 1) и/или его активированной формой (FIXa) и связывающиеся с FX (SEQ ID NO: 2) и/или его активированной формой (FXa), где указанное биспецифическое антитело содержит
антитело к FIX(a) или его антигенсвязывающий фрагмент, содержащие тяжелую цепь и легкую цепь, и
антитело к FX(a) или его антигенсвязывающий фрагмент, содержащие тяжелую цепь и легкую цепь,
где:
a) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 36, 37 и 38 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 40, 41 и 42 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
b) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 36, 37 и 38 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 40, 41 и 42 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 484, 485 и 486 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 488, 489 и 490 соответственно, или
c) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 44, 45 и 46 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 48, 49 и 50 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
d) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 52, 53 и 54 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 56, 57 и 58 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
e) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 52, 53 и 54 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 56, 57 и 58 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 484, 485 и 486 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 488, 489 и 490 соответственно, или
f) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 68, 69 и 70 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 72, 73 и 74 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
g) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 68, 69 и 70 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 72, 73 и 74 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 484, 485 и 486 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 488, 489 и 490 соответственно, или
h) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1203, 1204 и 1205 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1207, 1208 и 1209 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
i) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1211, 1212 и 1213 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1215, 1216 и 1217 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
j) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1219, 1220 и 1221 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1223, 1224 и 1225 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
k) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1227, 1228 и 1229 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1231, 1232 и 1233 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
l) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1235, 1236 и 1237 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1239, 1240 и 1241 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно, или
m) последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1243, 1244 и 1245 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 1247, 1248 и 1249 соответственно, и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, и
последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно.
5. Антитело или его антигенсвязывающий фрагмент по п. 4, где
последовательности CDR1-3 тяжелой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 52, 53 и 54 соответственно, а последовательности CDR1-3 легкой цепи антитела к FIX(a) идентифицированы под SEQ ID NO: 56, 57 и 58 соответственно и
последовательности CDR1-3 тяжелой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 468, 469 и 470 соответственно, а последовательности CDR1-3 легкой цепи антитела к FX(a) идентифицированы под SEQ ID NO: 472, 473 и 474 соответственно.
6. Антитело или его антигенсвязывающий фрагмент по п. 4, где антитело к FIX(a) или его антигенсвязывающий фрагмент содержат
a) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 35, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 39, или
b) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 43, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 47, или
c) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 51, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 55, или
d) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 67, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 71, или
e) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1202, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1206, или
f) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1210, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1214, или
g) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1218, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1222, или
h) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1226, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1230, или
i) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1234, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1238, или
j) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1242, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1246,
и где антитело к FX(a) или его антигенсвязывающий фрагмент содержат
k) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 467, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 471, или
l) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 483, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 487.
7. Антитело или его антигенсвязывающий фрагмент по п. 6, где антитело к FIX(a) или его антигенсвязывающий фрагмент содержат вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 51, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 55, и где антитело к FX(a) или его антигенсвязывающий фрагмент содержат вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 467, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 471.
8. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих пунктов, где изотип указанного антитела или его антигенсвязывающего фрагмента представляют собой IgG1 или IgG4.
9. Антитело или его антигенсвязывающий фрагмент по любому из предыдущих пунктов, где указанное антитело или его антигенсвязывающий фрагмент представляют собой прокоагулянтное антитело или его антигенсвязывающий фрагмент.
10. Антитело или его антигенсвязывающий фрагмент по любому из пп. 4-9, где указанное антитело или его антигенсвязывающий фрагмент стимулируют ферментативную активность FIXa.
11. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-10 для применения в лечении коагулопатии или нарушения свертываемости крови.
12. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-10 для применения в лечении гемофилии А с наличием ингибиторов или без них.
13. Фармацевтическая композиция, обладающая прокоагулянтной активностью, содержащая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-10 и один или более фармацевтически приемлемых носителей.
14. Композиция по п. 13 для применения в лечении коагулопатии или нарушения свертываемости крови.
15. Композиция по п. 13 для применения в лечении гемофилии А с наличием ингибиторов или без них.
16. Набор для лечения коагулопатии или нарушения свертываемости крови, содержащий (i) антитело или его антигенсвязывающий фрагмент по любому из пп. 1-10 или композицию по п. 13 и (ii) инструкции по применению.
17. Антитело или его антигенсвязывающий фрагмент, которые связываются с FIX (SEQ ID NO: 1) и/или его активированной формой (FIXa), содержащие тяжелую цепь и легкую цепь, где:
a) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 36, 37 и 38 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 40, 41 и 42 соответственно, или
b) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 44, 45 и 46 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 48, 49 и 50 соответственно, или
c) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 52, 53 и 54 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 56, 57 и 58 соответственно, или
d) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 68, 69 и 70 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 72, 73 и 74 соответственно, или
e) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 1203, 1204 и 1205 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 1207, 1208 и 1209 соответственно, или
f) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 1211, 1212 и 1213 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 1215, 1216 и 1217 соответственно, или
g) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 1219, 1220 и 1221 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 1223, 1224 и 1225 соответственно, или
h) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 1227, 1228 и 1229 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 1231, 1232 и 1233 соответственно, или
i) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 1235, 1236 и 1237 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 1239, 1240 и 1241 соответственно, или
j) последовательности CDR1-3 тяжелой цепи идентифицированы под SEQ ID NO: 1243, 1244 и 1245 соответственно и
последовательности CDR1-3 легкой цепи идентифицированы под SEQ ID NO: 1247, 1248 и 1249 соответственно,
где указанное антитело или его антигенсвязывающий фрагмент являются промежуточным соединением в изготовлении биспецифического антитела, связывающегося с FIX и/или его активированной формой (FIXa) и связывающегося с FX (SEQ ID NO: 2) и/или его активированной формой (FXa).
18. Антитело или его антигенсвязывающий фрагмент по п. 17, где антитело или его антигенсвязывающий фрагмент содержат
a) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 35, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 39, или
b) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 43, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 47, или
c) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 51, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 55, или
d) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 67, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 71, или
e) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1202, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1206, или
f) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1210, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1214, или
g) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1218, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1222, или
h) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1226, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1230, или
i) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1234, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1238, или
j) вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 1242, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 1246.
19. Антитело или его антигенсвязывающий фрагмент по п. 18, где антитело или его антигенсвязывающий фрагмент содержат вариабельный домен тяжелой цепи, идентифицированный под SEQ ID NO: 51, и вариабельный домен легкой цепи, идентифицированный под SEQ ID NO: 55.
| ТАТУИРОВОЧНАЯ МАШИНА И САМОУСТАНАВЛИВАЮЩАЯСЯ ОПОРА ВАЛА ЭЛЕКТРОДВИГАТЕЛЯ ТАТУИРОВОЧНОЙ МАШИНЫ | 2017 |
|
RU2644698C1 |
| ZENJIRO SAMPEI et al., Identification and Multidimensional Optimization of an Asymmetric Bispecific IgG Antibody Mimicking the Function of Factor VIII Cofactor Activity, PLOS ONE, 2013, vol | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| SCHEIFLINGER F | |||
| et al., Enhancement of the enzymatic activity of activated coagulation factor IX by | |||
Авторы
Даты
2023-12-28—Публикация
2019-07-31—Подача