ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка испрашивает приоритет заявки США №62/731,101, поданной 14 сентября 2018 года, полное раскрытие которой включено в настоящем описании в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
В настоящем документе раскрыты фармацевтические композиции, содержащие по меньшей мере одну липосому, инкапсулирующую слабо кислотное лекарственное средство, где уменьшенное количество стерола во внешнем липидном бислое липосомы замедляет или предотвращает «взрывное» (burst) высвобождение и/или обеспечивает устойчивое высвобождение слабокислотного лекарственного средства.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Липосомы представляют собой микроструктуры, состоящие из двойного слоя (бислоя) природных или синтетических липидов, образующего внутренний компартмент, который служит резервуаром для терапевтического средства. В качестве носителей для доставки лекарств были разработаны различающиеся размером, проницаемостью и стабильностью разнообразные липосомальные композиции, каждая из которых предназначена для обеспечения замедленного высвобождения лекарственного средства. Однако, данные липосомальные композиции замедленного высвобождения обычно демонстрируют высокий начальный всплеск в высвобождении лекарственного средства, что приводит к усилению побочных эффектов во время взрывного высвобождения и/или уровням лекарственного средства в плазме крови за пределами терапевтического окна.
Профиль высвобождения липосомальной композиции зависит от структуры липосомальной мембраны и влияет на эффективность липосом. Следовательно, контроль над профилем высвобождения становится важной предпосылкой для эффективного применения липосом в качестве средства доставки лекарств. Например, холестерол добавляется к внешнему липидному бислою для увеличения жесткости мембраны, ее стабильности и уменьшения проницаемости липидного бислоя (S. Kaddah et al., Food Chem Toxicol. 2018 Mar; 113: 40-48). S. Kaddah et al. показывает, что высвобождение инкапсулированного лекарственного средства уменьшается с увеличением содержания холестерола (до 30%) в липосомальном бислое. Е. Corvera et al. (Biochim Biophys Acta. 1992 Jun 30; 1107(2):261-70) сообщает, что добавление низких концентраций холестерола (от 5 до 8%) в липосомы из димиристоилфосфатидилхолина (dimyristoylphosphatidylcholine, DMPC) и дипальмитоилфосфатидилхолина (dipalmitoylphosphatidylcholine, DPPC) понижает стабильность липосом и увеличивает проницаемость мембран.
Остается потребность в липосомальной композиции, не дающей начального взрывного высвобождения, с тем чтобы уменьшить потенциальный побочный эффект и увеличить терапевтическую эффективность слабокислотного лекарственного средства. Настоящее изобретение удовлетворяет данные и другие потребности.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает фармацевтическую композицию, содержащую одну или несколько липосом, суспендированных во внешней среде, причем указанная липосома включает: (а) внешний липидный бислой, содержащий по меньшей мере один везикулообразующий фосфолипид и менее 15 мол. % стерола и (b) внутреннюю водную среду, содержащую слабокислотное лекарственное средство и соль слабой кислоты, где менее 65 масс. % слабокислотного лекарственного средства высвобождается во внешнюю среду в течение 1 часа после введения фармацевтической композиции.
Настоящее изобретение также раскрывает способы лечения респираторного заболевания, включающие стадию введения фармацевтической композиции, описанной в настоящем документе.
Настоящее изобретение также обеспечивает способ уменьшения побочного эффекта слабокислотного лекарственного средства, включающий стадию введения субъекту, нуждающемуся в приеме слабокислотного лекарственного средства, эффективного количества фармацевтической композиции, описанной в данном документе.
Термины «изобретение», «такое изобретение», «данное изобретение» и «настоящее изобретение», используемые в данном патенте, предназначены для широкого обозначения всего предмета данного патента и приведенной ниже формулы изобретения. Следует понимать, что утверждения, содержащие данные термины, не ограничивают предмет изобретения, описанный в данном документе, и не ограничивают значение или объем приведенной ниже формулы изобретения. Варианты осуществления изобретения, на которые распространяется данный патент, определяются приведенной ниже формулой изобретения, а не данным кратким изложением. Данное краткое изложение представляет собой общий обзор различных аспектов изобретения и знакомит с некоторыми концепциями, которые дополнительно описаны в разделе «Подробное описание» ниже. Данное краткое изложение не предназначено для идентификации ключевых или существенных характеристик заявленного предмета изобретения и не предназначено для использования отдельно для определения объема заявленного предмета изобретения. Для понимания предмета изобретения необходимо обращаться к соответствующим частям полного описания, любым или всем чертежам и каждому пункту формулы изобретения.
Изобретение станет более очевидным при прочтении с сопровождающими фигурами и подробным описанием, которое следует ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Иллюстративные варианты осуществления настоящего изобретения подробно описаны ниже со ссылкой на следующие фигуры.
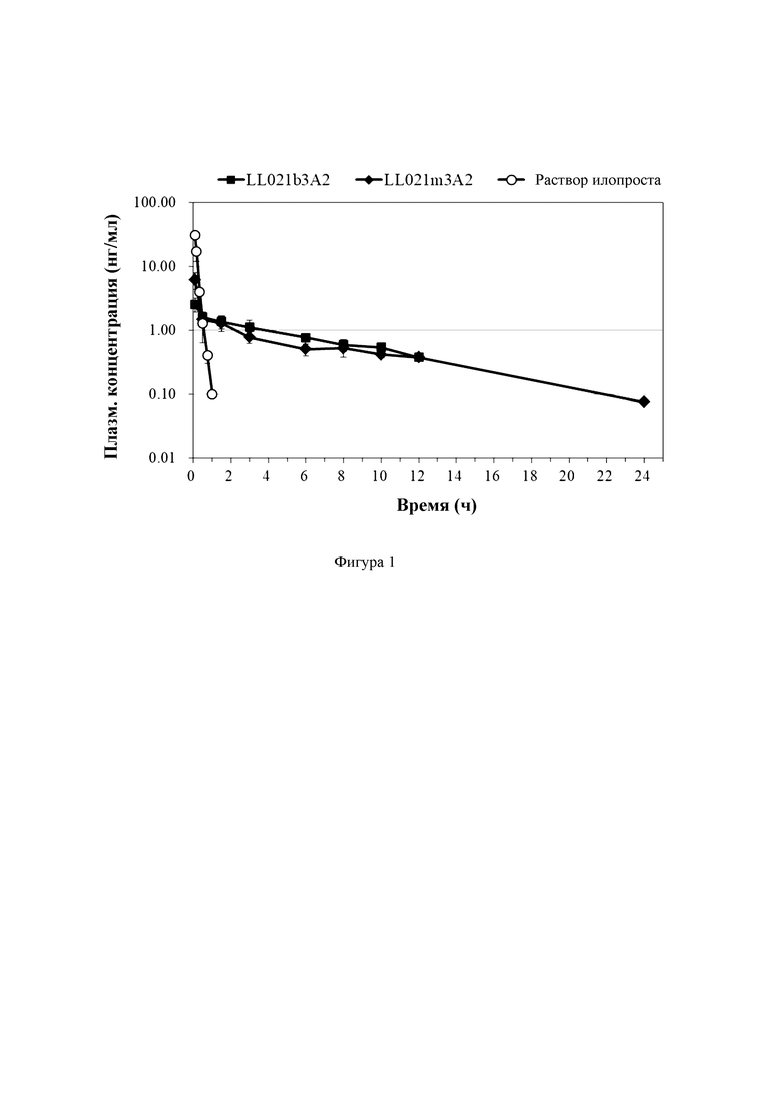
ФИГ. 1 представляет собой график, показывающий логарифм средней концентрации илопроста в плазме у крыс, которым вводили липосомальную композицию, содержащую ило прост, бикарбонат и HP-β-CD (LL021b3A2), липосомальную композицию, содержащую илопрост, бикарбонат и RM-β-CD (LL021m3A2), или раствор илопроста
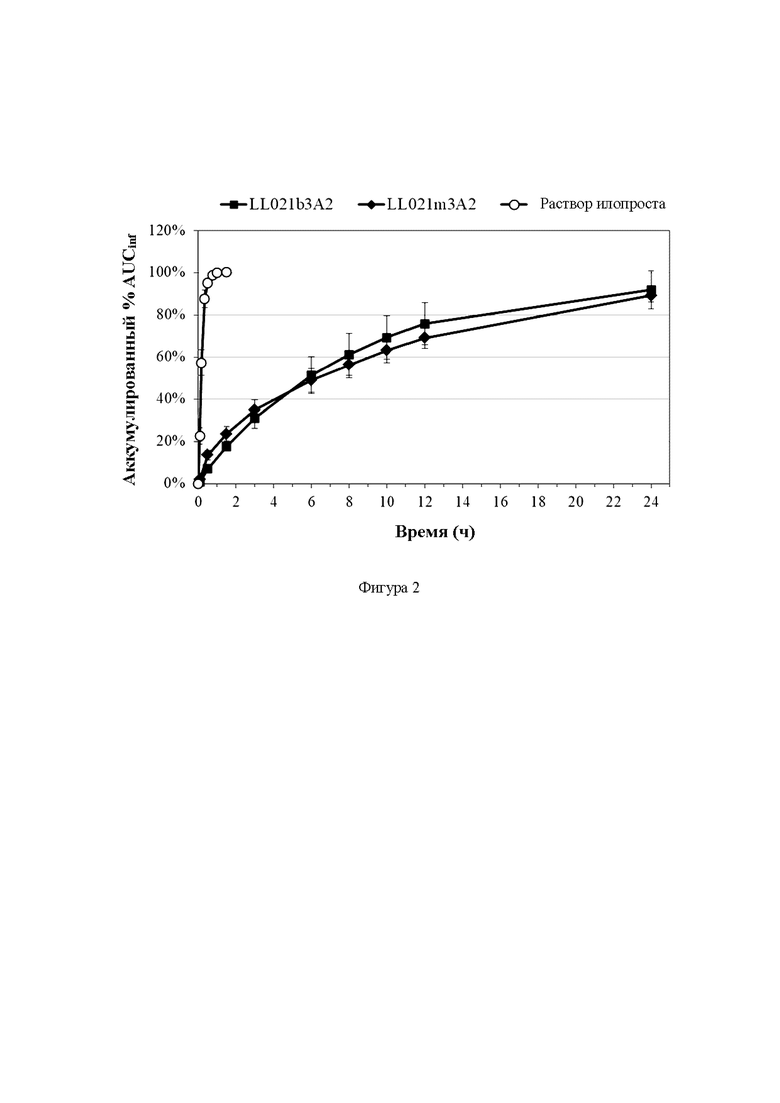
ФИГ. 2 представляет собой график, иллюстрирующий соотношение площади под кривой зависимости концентрации в плазме от времени от нуля до определенного времени (AUCt) и площади под кривой зависимости концентрации в плазме от времени от нуля до бесконечности (AUCinf) для липосомальной композиции, содержащей илопрост, бикарбонат и HP-β-CD (LL021b3A2), липосомальной композиции, содержащей илопрост, бикарбонат и RM-β-CD (LL021m3A2), или раствора илопроста.
ПОДРОБНОЕ ОПИСАНИЕ
В данном контексте артикли «а» и «an» относятся к одному или более чем одному (то есть, по меньшей мере одному) грамматическому объекту статьи. В качестве примера, «элемент» означает один или более чем один элемент.
Все числа модифицированы термином «около». Используемый в настоящем описании термин «около» относится к диапазону ±10% от указанного значения.
Термин «содержать» или «содержащий» обычно используется в смысле «включать/включающий», что означает допущение наличия одного или нескольких признаков, ингредиентов или компонентов.
Термин «субъект» может относиться к позвоночному животному, страдающему респираторным заболеванием, или к позвоночному животному, которое, как считается, нуждается в лечении респираторного заболевания. Субъекты включают теплокровных животных, таких как млекопитающие, таких как приматы, и, более предпочтительно, человека. Приматы также являются субъектами. Термин «субъект» включает домашних животных, таких как кошки, собаки и т.д., домашний скот (например, крупный рогатый скот, лошади, свиньи, овцы, козы и т.д.) и лабораторных животных (например, мышь, кролик, крыса, песчанка, морская свинка и др.). Таким образом, в настоящем описании рассматриваются ветеринарные применения и медицинские составы.
Термин «лечение» относится как к терапевтическому лечению, так и к профилактическим или превентивным мерам. Лица, нуждающиеся в лечении, включают тех, кто уже страдает респираторным заболеванием или родственным расстройством, а также тех, кто склонен к респираторному заболеванию или родственному расстройству, или тех, у которых респираторное заболевание необходимо предотвратить.
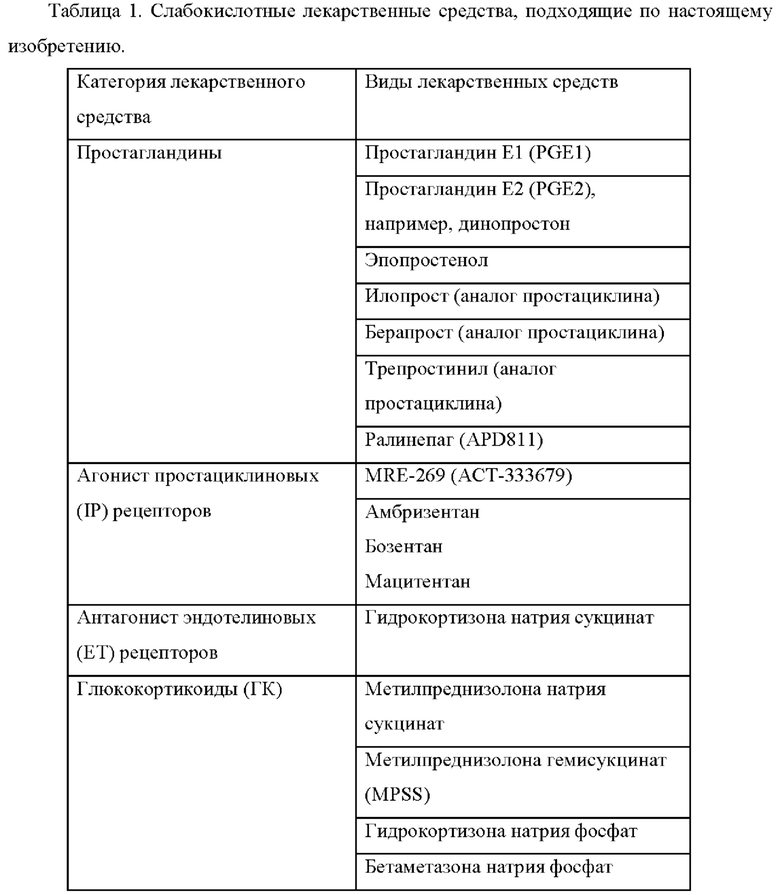
Слабокислотное лекарственное средство, как используется в настоящем описании, если не указано иное или иное не очевидно из контекста, также включает его фармацевтически приемлемую соль и его протонированную форму. В одном варианте осуществления слабо кислотное лекарственное средство содержит по меньшей мере одну функциональную группу, выбранную из группы, состоящей из карбоксильной группы (-СООН), гидроксильной группы (-ОН), фосфатной группы (-РО4) и любой их комбинации. В другом варианте осуществления слабо кислотное лекарственное средство имеет pKa от 1 до менее чем около 7, от 2 до менее чем около 6, от 2 до 6,9 или от 2,5 до 6. Слабокислотное лекарственное средство также может содержать одну или несколько функциональных групп в дополнение к вышеуказанной карбоксильной группе (-СООН), гидроксильной группе (-ОН) и фосфатной группе (-РО4); такая дополнительная функциональная группа (группы) не должна существенно изменять кислотность лекарственного средства по сравнению с кислотностью его нефункционализированных аналогов. В одном из вариантов осуществления слабокислотное лекарственное средство применяется для лечения легочной гипертензии. В другом варианте осуществления слабокислотное лекарственное средство представляет собой простагландин, агонист рецептора простациклина, глюкокортикоид или нестероидное противовоспалительное средство. В таблице 1 показаны неограничивающие примеры слабокислотного лекарственного средства по настоящему изобретению.

Используемые в настоящем описании термины «инкапсуляция», «нагруженный» и «захваченный» могут использоваться взаимозаменяемо и относятся к включению или связыванию биологически активного средства (например, илопроста) во внутренней водной среде липосомы.
Настоящее изобретение обеспечивает фармацевтическую композицию, содержащую одну или несколько липосом, суспендированных во внешней среде, причем указанная липосома включает: (а) внешний липидный бислой, содержащий по меньшей мере один везикулообразующий фосфолипид и менее 15 мол. % стерола и (b) внутреннюю водную среду, содержащую слабокислотное лекарственное средство и соль слабой кислоты, где менее 65 масс. % слабокислотного лекарственного средства высвобождается во внешнюю среду в течение 1 часа после введения фармацевтической композиции.
В служащем примером варианте осуществления стерол во внешнем липидном бислое составляет менее 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 мол. %. В другом служащем примером варианте осуществления внешний липидный бислой по существу не содержит стерола.
Эффективность инкапсуляции слабокислотного лекарственного средства в фармацевтической композиции выше чем около 70, 75 или 80%.
Фармацевтическая композиция уменьшает взрывное высвобождение инкапсулированного слабокислотного лекарственного средства. В одном из вариантов осуществления менее чем около 70%, 69%, 68%, 67%, 66% или 65% слабокислотного лекарственного средства высвобождается в течение 1 часа после введения фармацевтической композиции. В результате, побочные эффекты слабокислотного лекарственного средства на месте целевого действия (например, кашель, раздражение горла, боль в глотке, носовое кровотечение, кровохарканье и свистящее дыхание в верхних дыхательных путях) уменьшаются по сравнению с побочными эффектами фармацевтической композиции, в которой стерол во внешнем липидном бислое составляет 15 мол. % или более. Кроме того, фармацевтическая композиция продлевает высвобождение слабокислого лекарственного средства и снижает частоту дозирования.
В одном варианте осуществления взрывное высвобождение слабокислотного лекарственного средства из описанной фармацевтической композиции дополнительно уменьшается при добавлении или инкапсулировании циклодекстрина во внутренней водной среде. Неограничивающие примеры циклодекстрина включают α-CD, β-CD, γ-CD, 2-гидроксипропил β-CD (HP-β-CD), сульфобутиловый эфир β-CD (SBE-β-CD), случайно метилированный β-CD (RM-β-CD) или их комбинацию. Предпочтительно циклодекстрин представляет собой HP-β-CD, RM-β-CD или их комбинацию. В одном примерном варианте осуществления мольное соотношение слабокислотного лекарственного средства и циклодекстрина (соотношение лекарственное средство/CD) меньше или равно около 0,06, 0,055, 0,05, 0,045, 0,04, 0,035 или 0,03.
Также раскрыт способ лечения респираторного заболевания, включающий стадию введения субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, раскрытой в данном документе, в которой количество стерола во внешнем липидном бислое составляет менее 15 мол. %. Взрывное высвобождение слабокислотного лекарственного средства описанной в данном документе фармацевтической композиции уменьшено по сравнению с таковым фармацевтической композиции с содержанием стерола во внешнем липидном бислое, составляющим 15 мол. % или превышающим 15 мол. %. Неограничивающие примеры респираторного заболевания включают легочную гипертензию и интерстициальное заболевание легких.
Дополнительно раскрыто применение фармацевтической композиции, раскрытой в данном документе, для лечения респираторного заболевания или применение фармацевтической композиции, раскрытой в данном документе, для производства лекарственного средства для лечения респираторного заболевания.
Настоящее изобретение также относится к способам уменьшения побочного эффекта слабокислотного лекарственного средства, включающим введение субъекту, нуждающемуся в приеме слабокислотного лекарственного средства, эффективного количества фармацевтической композиции, описанной в данном документе, в которой количество стерола во внешнем липидном бислое составляет менее 15 мол. %.
В некоторых вариантах осуществления фармацевтическую композицию, раскрытую в настоящем документе, вводят путем ингаляции для уменьшения побочного действия слабокислотного лекарственного средства в верхних дыхательных путях.
А. Липосомальные компоненты
Используемый в настоящем описании термин «липосома» относится к микроскопическим везикулам или частицам, состоящим из одного или нескольких липидных бислоев, окружающих внутреннюю водную среду. Для образования липосом необходимо присутствие по меньшей мере одного «везикулообразующего липида», который представляет собой амфипатический липид, способный либо образовывать липидный бислой, либо встраиваться в него. Любой подходящий везикулообразующий липид может быть использован для образования липидного бислоя, составляющего липосомы. Везикулообразующий липид включает, но без ограничения, фосфолипиды, такие как фосфатидилхолин (PC), фосфатидилглицерин (PG), фосфатидилинозитол (PI), фосфатидную кислоту (РА), фосфатидилэтаноламин (РЕ) или фосфатидилсерин (PS), и заряженные липиды, такие как положительно заряженный липид или отрицательно заряженный липид.
Липидный бислой липосомы включает в себя по меньшей мере один везикулообразующий липид и от 0 (нуля) до менее чем 15 мол. % стерола (например, от 0 до 14,99 мол. %), причем указанный стерол выбран из группы, состоящей из холестерола, холестерола гексасукцината, эргостерола, ланостерола и любой их комбинации, но без ограничения ими. В служащем примером варианте осуществления стерол представляет собой холестерол.
В некоторых вариантах осуществления везикулообразующий липид представляет собой смесь первого фосфолипида и второго фосфолипида. В некоторых вариантах осуществления первый фосфолипид представляет собой фосфатидилхолин (PC), который выбран из группы, состоящей из гидрогенизированного яичного фосфатидилхолина (НЕРС), гидрогенизированного соевого фосфатидилхолина (HSPC), дипальмитоилфосфатидилхолина (DPPC), дистеарилохолинфосфатидил-фосфатидилфосфолина (DSPC) димиристоилфосфатидилхолина (DMPC), яичного фосфатидилхолина (ЕРС), соевого фосфатидилхолина (SPC), олеоилпальмитоилфосфатидилхолинаа, диолеоилфосфатидилхолинаа (DOPC), дипетрозелиноилфосфатидилхолина, пальмитоилелаидоилфосфатидилхолина, пальмитоилолеилфосфатидилхолина, дилауроилфосфатидилхолина (DLPC), диундеканоилфосфатидилхолина, дидеканоилфосфатидилхолина, динонилфосфатидилхолина и любой их комбинации. В других вариантах осуществления второй фосфолипид представляет собой модифицированный полиэтиленгликолем фосфолипид, содержащий полиэтиленгликоль с молекулярной массой от около 500 до около 10000 дальтон, такой как 1,2-дистеаролили-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000] (DSPE-PEG2000), отрицательно заряженный фосфолипид, например, дистеарилоилфосфатидилглицерин (DSPG), дипальмитоилфосфатидилглицерин (DPPG) или димиристоилфосфатидилглицерин (DMPG) или диолеоилфосфатидилглицерин (DOPG). В служащем примером варианте осуществления соотношение первый фосфолипид : холестерол : второй фосфолипид в мольных процентах составляет 75-99:0-14,9:0,1-25.
В других вариантах осуществления липиды, образующие везикулы, представляют собой смесь первого фосфолипида и заряженного липида. В служащем примером варианте осуществления липиды, образующие везикулы, представляют собой смесь первого фосфолипида, второго фосфолипида и заряженного липида. Заряженный липид включает стеариламин, 1,2-диолеоил-3-триметиламмоний-пропан (DOTAP), 3β-[N-(N',N'-диметиламиноэтан)-карбамоил]холестерол (DC-холестерол), N4-холестерил-спермин (GL67), диметилдиоктадециламмоний (DDAB), 1,2-ди-О-октадеценил-3-триметиламмоний пропан (DOTMA), этилфосфохолин (этил PC) или их комбинацию. В другом служащем примером варианте осуществления соотношение первый фосфолипид : холестерол : второй фосфолипид в мольных процентах составляет 75-99:0-14,9:0,1-25.
В одном из вариантов осуществления соотношение в липидном бислое HSPC, холестерола и DSPG в мольных процентах составляет 75-99:0-14,9:0,1-25. В другом варианте осуществления соотношение HSPC, холестерола и DSPE-PEG2000 в мольных процентах в липидном бислое составляет 75-99:0-14,9:0,1-25.
В одном варианте осуществления внешний липидный бислой липосом дополнительно содержит поверхностно-активное вещество, которое может быть неионным поверхностно-активным веществом, катионным поверхностно-активным веществом или цвиттерионным поверхностно-активным веществом. Неионное поверхностно-активное вещество не имеет на своей головной части формально заряженных групп. Катионное поверхностно-активное вещество несет на своей головной части только положительный заряд. Цвиттерионное поверхностно-активное вещество электрически нейтрально, но несет формальные положительные и отрицательные заряды на различных атомах.
Неограничивающие примеры неионного поверхностно-активного вещества включают в себя неионные водорастворимые моно-, ди- и три-глицериды; неионные водорастворимые сложные эфиры моно- и дижирных кислот и полиэтиленгликоля; неионные водорастворимые сложные эфиры сорбитана и жирных кислот (например, моноолеаты сорбитана, такие как TWEEN 20 (полиоксиэтилен 20 сорбитанмоноолеат), SPAN 80); неионные водорастворимые триблок-сополимеры (например, триблок-сополимеры поли(этиленоксида)/полипропиленоксида)/поли(этиленоксида), такие как POLOXAMER 406 (PLURONIC F-127), или их производные.
Неограничивающие примеры катионного поверхностно-активного вещества включают бромид диметилдиалкиламмония или бромид додецилтриметиламмония.
Неограничивающие примеры цвиттерионного поверхностно-активного вещества включают 3-(N,N-диметилпальмитилламмонио)пропансульфонат.
Согласно настоящему изобретению, липосомы получают в среде, содержащей соль слабой кислоты, чтобы обеспечить градиент рН между внутренней водной средой и внешней средой липосомы. Когда везикулообразующий фосфолипид и менее чем 15% стерола находятся в контакте со средой, содержащей соль слабой кислоты, образуется суспензия липосом.
Липосома в суспензии подвергается уменьшению размера. Размер липосомы обычно определяется ее диаметром. Уменьшение размера липосом может быть достигнуто с помощью ряда способов, таких как экструзия, обработка ультразвуком, способы гомогенизации или способы измельчения, которые хорошо известны и могут быть выполнены специалистами в данной области техники. Экструзия включает пропускание липосом под давлением один или несколько раз через фильтры с определенными размерами пор. Фильтры обычно изготавливаются из поликарбоната, но также могут быть изготовлены из любого прочного материала, который не взаимодействует с липосомами и который достаточно прочен, чтобы обеспечить экструзию при достаточном давлении. Размер липосом можно уменьшить с помощью обработки ультразвуком, которая использует звуковую энергию для разрушения или сдвига липосом, которые спонтанно превращаются в липосомы меньшего размера. Например, обработка ультразвуком может быть проведена путем погружения стеклянной пробирки, содержащей суспензию липосом, в звуковой эпицентр, созданный в ультразвуковом устройстве типа ванны, или может быть использован ультразвуковой излучатель зондового типа, в котором звуковая энергия генерируется вибрацией титанового зонда в прямом контакте с суспензией липосом. В настоящем изобретении липосомы обычно имеют диаметр от около 50 нм до 500 нм, например около 500 нм или менее, около 400 нм или менее, около 300 нм или менее, около 200 нм или менее, или около 100 нм или менее.
После получения нужного размера концентрацию кислоты слабой соли во внешней среде регулируют таким образом, чтобы обеспечить градиент рН между внутренней водной средой и внешней средой, что может быть осуществлено несколькими способами, например, путем замены внешней среды подходящим буфером, в котором отсутствуют соли слабой кислоты, таким как буфер лимонной кислоты (Н3С6Н5О) и буфер фосфорной кислоты (H3PO4), такими способами, как диафильтрация, диализ, ультрафильтрация или фильтрация с тангенциальным потоком.
Соль слабой кислоты обеспечивает градиент рН, более низкий снаружи и более высокий внутри, между внешней средой и внутренней водной средой липосом. В одном варианте осуществления рН внутренней водной среды по меньшей мере на 0,1 единицы выше рН внешней среды. В другом варианте осуществления рН внутренней водной среды по меньшей мере на 1 единицу выше рН внешней среды. В еще одном варианте осуществления рН внутренней водной среды составляет около 7, 8, 9 или 10, и рН внешней среды составляет менее 7, менее 6, менее 5, менее 4, менее 3, около 3-7, около 3,5-6,5 или около 4-6. В еще одном служащем примером варианте осуществления рН внешней среды превышает pKa слабокислотного лекарственного средства.
Неограничивающие примеры соли слабой кислоты включают соли карбоновой кислоты и бикарбонатную соль.
Термин «бикарбонатная соль», как он используется в настоящем описании, относится к фармацевтически приемлемой соли соединения, включающей бикарбонатный анион и катионный компонент. В одном варианте осуществления катионный компонент солевого соединения представляет собой металл. Неограничивающие примеры металла включают металл группы IA или IIA, такой как калий (K), натрий (Na), кальций (Са), магний (Mg), цезий (Cs) и литий (Li), или металл, отличный от металлов группы IA или IIA, такой как двухвалентное железо (Fe) и никель (Ni). Примеры бикарбонатной соли включают, но не ограничиваются ими, бикарбонат калия, бикарбонат натрия, бикарбонат кальция, бикарбонат магния, бикарбонат цезия, бикарбонат лития, бикарбонат никеля, бикарбонат двухвалентного железа или любую их комбинацию.
Используемый в настоящем описании термин «соль карбоновой кислоты» включает, но не ограничивается ими, формиат, ацетат, пропионат, бутират, изобутират, валерат, изовалерат или их комбинацию. В одном служащем примером варианте осуществления ацетат представляет собой ацетат натрия, ацетат кальция или их комбинацию.
Концентрация соли бикарбоната или кислоты карбоновой соли составляет 50 мМ или выше, 100 мМ или выше, 150 мМ или выше, 200 мМ или выше, 250 мМ или выше, 300 мМ или выше, 350 мМ или выше, 400 мМ или выше, 450 мМ или выше, 500 мМ или выше, 600 мМ или выше, 700 М или выше, 800 мМ или выше 900 мМ, менее 1000 мМ, от 50 мМ до менее 1000 мМ, от 50 мМ до 800 мМ, от 200 до менее 1000 мМ, от 200 до 800 мМ или от 200 до 600 мМ, от 250 до менее 1000 мМ, от 250 до 800 мМ или от 250 до 600 мМ, от 300 от мМ до 600 мМ.
Приготовленные липосомы можно хранить в течение значительных периодов времени перед загрузкой слабокислотного лекарственного средства и введением субъекту. Например, липосомы можно хранить в условиях охлаждения в течение значительных периодов времени перед загрузкой слабокислотного лекарственного средства. Альтернативно, липосомы можно дегидратировать, хранить и затем регидратировать и нагружать слабокислотным лекарственным средством перед введением. Липосомы также могут быть дегидратированы после загрузки слабокислотным лекарственным средством. Дегидратация может быть проведена рядом способов, доступных и известных в данной области техники. В некоторых вариантах осуществления липосомы дегидратируют с использованием стандартного устройства для сублимационной сушки, то есть дегидратации в условиях низкого давления. Также липосомы можно замораживать, например, с использованием жидкого азота. Сахариды можно добавлять в липосомальную среду, например, в буфер, содержащий липосомы, до дегидратации, чтобы гарантировать стабильность и целостность липосом во время дегидратации. Примеры сахаридов включают, но не ограничиваются ими, мальтозу, лактозу, сахарозу, трегалозу, декстрозу, сорбит, маннит, ксилит или их комбинации.
Суспензия липосом, содержащая менее 15 мол. % стерола или практически не содержащая стерола, как описано выше, готова для нагрузки слабо кислотным лекарственным средством. Обычно, слабо кислотное лекарственное средство добавляют во внешнюю среду липосомы, и полученную суспензию инкубируют, обеспечивая диффузию слабокислотного лекарственного средства во внутреннюю водную среду липосомы и до достижения желаемой концентрации нагрузки и эффективности инкапсуляции (процентное содержание внутреннего/инкапсулированного количества слабокислотного лекарственного средства по отношению к общему количеству слабокислотного лекарственного средства в фармацевтической композиции).
В. Связь между содержанием стерола во внешнем липидном бислое и профилем контролируемого высвобождения
Фармацевтическая композиция по настоящему изобретению, имеющая менее 15 мольных процентов (например, от 0 до 14,99 мол. %) стерола в липосомальном внешнем липидном бислое уменьшает взрывное высвобождение инкапсулированной кислоты слабокислотного лекарственного средства и, следовательно, уменьшает побочный эффект слабокислотного лекарственного средства. Дополнительно, количество слабокислотного лекарственного средства, достаточное для достижения желаемого терапевтического эффекта, высвобождается из фармацевтической композиции и профиль высвобождения неожиданно расширяется по сравнению с таковым фармацевтической композиции с более чем 15 мол. % стерола в липосомальном внешнем липидном бислое.
Как использован в данном описании, термин «взрывное высвобождение» относится к быстрому и/или в некоторой степени неконтролируемому высвобождению более чем 70, 69, 68, 67, 66 или 65% инкапсулированного слабокислотного лекарственного средства из фармацевтической композиции в течение 1 часа (60 минут) после введения фармацевтической композиции.
Используемый в настоящем описании термин «продленное высвобождение» может использоваться взаимозаменяемо с «контролируемым высвобождением», «отсроченным высвобождением», «модифицированным высвобождением», «пролонгированным высвобождением», «запрограммированным высвобождением», «высвобождением по времени», «с контролируемой скоростью» или «замедленным высвобождением» и относится к высвобождению менее чем 50, 45 или 40% слабокислотного лекарственного средства в течение 1 часа после введения фармацевтической композиции.
В одном варианте осуществления профиль быстрого высвобождения или замедленного высвобождения фармацевтической композиции основан на анализе высвобождения in vitro (in vitro release (IVR)) и/или исследовании in vivo фармакокинетики захваченного слабокислотного лекарственного средства.
В некоторых вариантах осуществления, основанных на анализе высвобождения in vitro (IVR) и/или исследовании in vivo фармакокинетики, фармацевтическая композиция имеет профиль высвобождения, где менее чем около 70, 69, 68, 67, 66 или 65% по массе захваченного слабокислотного лекарственного средства высвобождается в течение 1 часа с момента введения фармацевтической композиции.
С. Введение
Фармацевтическая композиция по настоящему изобретению может быть введена в полость субъекта, которая не имеет непосредственного контакта с кровотоком. Примеры способов введения включают, но не ограничиваются ими, ингаляцию, интратрахеальную инъекцию, подкожную инъекцию, внутрисуставную инъекцию, внутримышечную инъекцию, интравитреальную инъекцию и интратекальную инъекцию.
Фармацевтическая композиция по настоящему изобретению также может вводиться непосредственно в кровоток субъекта.
Согласно данному раскрытию, фармацевтическая композиция может вводиться от одного до трех раз в день, один раз каждые 2 дня или один раз каждые 3 дня.
Настоящее раскрытие будет дополнительно описано в следующих примерах. Однако следует понимать, что следующие примеры предназначены исключительно для целей иллюстрации и не должны толковаться как ограничение настоящего раскрытия на практике.
Примеры
Общие экспериментальные процедуры:
1. Приготовление липосомальной композиции с илопростом
Липосомальную коллоидную суспензию получали с использованием техники этанольной инъекции. Все липидные ингредиенты, включая первый фосфолипид (HSPC) и второй фосфолипид (DSPE-PEG2000 или DSPG) в мольном соотношении 98:2 или 98,5:1,5, растворяли в 2,86 мл раствора этанола при приблизительно 60°С. Полученный раствор липидов вводили в 17,4 мл раствора натрия бикарбоната (от 100 до 400 мМ; рН 8,5) и, необязательно, с (2-гидроксипропил)-β-циклодекстрином (т.е. от 45 до 120 мМ), и смешивали при интенсивном перемешивании при 60°С для гидратации липосом. Смесь экструдировали от 6 до 10 раз через поликарбонатные мембраны с размером пор 0,2 или 0,1 мкм для получения суспензии липосом, имеющих средний размер частиц в диапазоне от около 100 нм до 200 нм и индекс полидисперсности (PdI) <0,2. Суспензию липосом диализовали с помощью системы фильтрации с тангенциальным потоком против 10 мМ натрий-цитратного буфера (рН 5,5) для образования трансмембранного градиента рН между внутренней водной средой липосомы и внешней средой (т.е. градиента с более высоким внутренним и более низким внешним рН). Суспензию липосом, имеющих такой градиент рН, затем хранили при 4°С перед процессом нагрузки лекарственным средством.
Илопрост (приобретенный у Cayman Chemical, США) растворяли в 50 мМ растворе цитрата натрия и добавляли в суспензию липосом для достижения концентрации лекарственного средства от 1000 до 250 мкг/мл и инкубировали при 37°С в течение 30 мин. К полученному продукту добавляли натрий-цитратный буфер (рН 5,5) для получения липосомальной композиции, содержащей илопрост, имеющей рН 5,5 во внешней среде и фосфолипидную концентрацию 10 мМ в суспензии липосом.
2. Приготовление липосомальной композиции с амбризентаном
Суспензию липосом готовили в соответствии с описанной выше стадией 1 с использованием или без использования (2-гидроксипропил)-β-циклодекстрина. Амбризентан (приобретенный у Cayman Chemical, США) растворяли в диметилсульфоксиде (ДМСО), затем добавляли в суспензию липосом для достижения заданной концентрации лекарственного средства около 500 мкг/мл и инкубировали при 37°С в течение 30 мин. К полученному продукту добавляли натрий-цитратный буфер (рН 5,5), чтобы получить нагруженную амбризентаном липосомальную композицию, имеющую рН 5,5 во внешней среде и концентрацию афосфолипидов 10 мМ в суспензии липосом.
3. Количественная характеристика липосомальных композиций
а. Концентрации инкапсулированного и свободного илопроста/амбрисентана:
Липосомальную композицию, содержащую илопрост или амбризентан, заливали в колонку PD MiniTrapTM G-25 (GE Healthcare) для отделения инкапсулированного лекарственного средства от свободного лекарственного средства. Липосомальную композицию, содержащую илопрост или амбризентан, смешивали с метанолом (90% по объему метанола и 10% по объему суспензии липосом) с образованием липосомально-метанольной смеси.
Концентрации инкапсулированного илопроста и свободного илопроста анализировали путем инъекции 30 мкл липосомально-метанольной смеси в систему Waters Acquity HPLC, оборудованную детектором на фотодиодной матрице (PDA). Подвижная фаза представляла собой смесь ацетонитрила, метанола и фосфатного буфера (рН 2,5) при объемном соотношении 36:17:47, скорость потока подвижной фазы составляла 1,0 мл/мин. Разделение выполняли с использованием колонки С8, имеющей размер 3,9 мм×15,0 см, 5,0 мкм, при 25°С, и пик поглощения обнаруживали при 205 нм.
Концентрации инкапсулированного амбризентана и концентрацию свободного амбризентана анализировали путем инъекции 1 мкл смеси липосом и метанола в систему Waters Acquity UPLC, снабженную масс-детектором (QDa). Подвижная фаза А включала 0,1% муравьиной кислоты в ацетонитриле, и подвижная фаза В содержала 0,1% муравьиной кислоты в ddH2O. Градиентные условия были следующими: 50% подвижной фазы А в течение 0,2 минуты, 10% подвижной фазы А до 2 минут и 50% подвижной фазы А до 5,5 минут. Разделение выполняли с использованием колонки С18, имеющей размер 4,6 мм×10,0 см, 3,0 мкм, при 35°С со скоростью потока 1,0 мл/мин. Регистрация МС была выполнена в режиме SIR с использованием ионов [М+Н]+, m/z 347,2 для амбризентана.
b. Эффективность инкапсулирования (ЕЕ) и соотношение лекарственного средства и циклодекстрина:
Концентрация общего количества лекарственного средства (илопроста или амбризентана) в липосомальной композиции включает инкапсулированное лекарственное средство во внутренней водной среде (L) и свободное лекарственное средство во внешней среде (F).
Эффективность инкапсулирования (Encapsulation efficiency (ЕЕ)) лекарственного средства рассчитывали как процент от инкапсулированного лекарственного средства во внутренней водной среде липосом (L) по отношению к общему количеству препарата (L+F), см. формулу А ниже:
ЕЕ(%)=[L/(L+F)]X100
Соотношение ILO/CD липосомальной композиции илопроста и соотношение AMB/CD липосомальной композиции амбризентана рассчитывали по следующим формулам:
Соотношение ILO/CD={[ILO]×EE}/[CD]
Соотношение AMB/CD={[АМВ]×EE}/[CD]
[ILO] (мМ) = концентрация общего количества илопроста (L+F)
[АМВ] (мМ) = концентрация общего количества амбристентана (L+F)
ЕЕ (%) = эффективность инкапсуляции
[CD] (мМ) = концентрация циклодекстрина
c. Средний размер частиц и индекс полидисперсности (PdI):
Средний размер частиц липосомы оценивали динамическим светорассеянием. Индекс полидисперсности (PdI), значение, показывающее распределение липосом по размерам, определяли с использованием той же методики оценки, что и для среднего размера частиц, с использованием анализатора частиц Beckman Coulter Delsa ТМ Nano С.
Пример 1: Профиль высвобождения in vitro (IVR) липосомальных композиций с илопростом с различным количеством стерола
А. Анализ высвобождения in vitro (IVR)
Были приготовлены липосомальные композиции с илопростом, и концентрация илопроста была проанализирована в соответствии с процедурами, описанными в предыдущих разделах «Общие экспериментальные процедуры». Средний размер частиц липосом составлял от 100 до 200 нм, и PdI был менее чем 0,20.
Для оценки профиля IVR можно использовать различные анализы IVR. Фактический анализ IVR известен или будет очевиден специалистам в данной области техники в зависимости от илопроста в заявленной липосомальной композиции. Профили высвобождения илопроста из липосом были получены путем десятикратного разбавления раствора липосом, нагруженного илопорстом, с исходной концентрацией фосфолипидов 10 мМ в имитации легочной жидкости (simulated lung fluid (SLF)) [Dissolution Technologies 2011, 18, 15-28] при 37°C при скорости встряхивания 100 об/мин. Процент высвобожденного илопроста (% высвобождения) в каждый момент времени рассчитывали путем сравнения эффективности инкапсуляции (ЕЕ) после инкубации в определенный момент времени (Т) с исходной эффективностью инкапсуляции (Т0) по следующей формуле:
Высвобождениепри T(%)=(ЕЕпри T0-ЕЕпри T)/ЕЕ при Т0
Результаты:
Физико-химические характеристики и IVR профиль липосомальных композиций с илопростом с различным количеством стерола показаны в таблице 1.
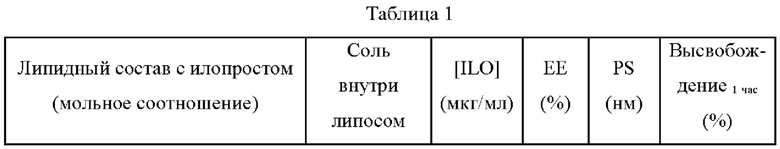
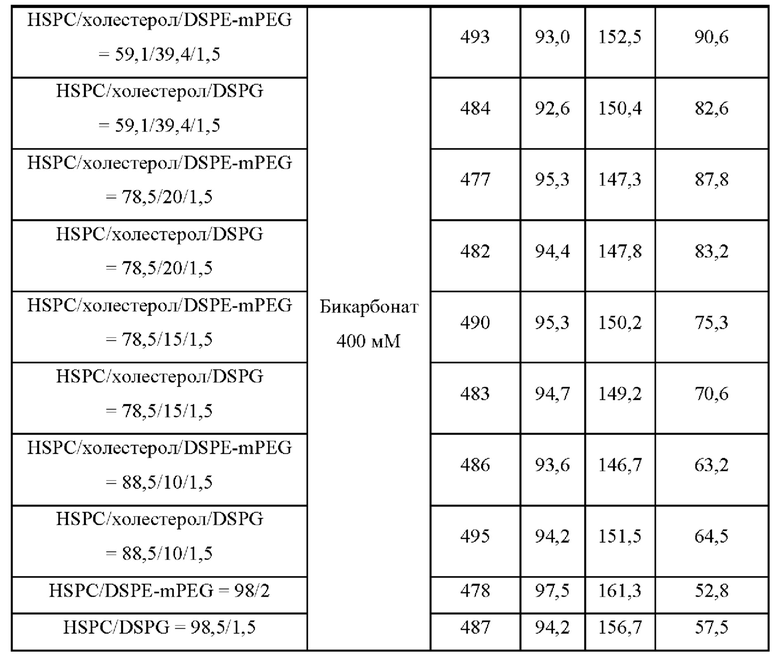
Таблица 1 показывает, что >90% ЕЕ было достигнуто с солью бикарбоната натрия и содержащими илопрост липосомальными композициями с менее чем 15 мол % холестерола, высвобождающими менее 65% илопроста в течение 1 часа с момента SLF инкубации, в то время как содержащие илопрост липосомальные композиции с 15 мол % или более чем 15 мол % холестерола высвобождали более 70% илопроста в течение 1 часа с момента SLF инкубации при 37°С.
Пример 2: Профиль высвобождения in vitro (IVR) липосомальных композиций с амбризентаном, различающихся количеством стерола
Были приготовлены липосомальные композиции, содержащие амбризентан, и концентрация амбризентана была проанализирована в соответствии с процедурами, описанными в предыдущих разделах «Общие экспериментальные процедуры». Средний размер частиц липосомы составлял от 100 до 200 нм, и PdI был менее чем 0,20.
Результаты:
Физико-химические характеристики и IVR профиль содержащих амбризентан липосомальных композиций с различным количеством стерола показаны в таблице 2.
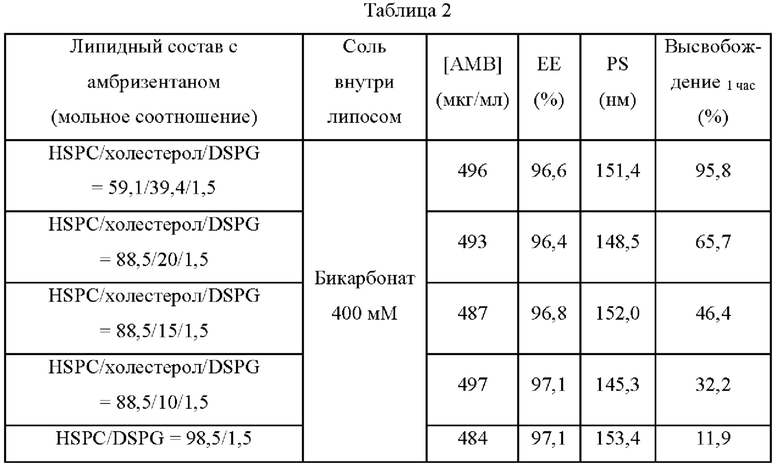
Таблица 2 показывает, что >95% ЕЕ было достигнуто с солью бикарбоната натрия и содержащими амбризентан липосомальными композициями с менее чем 15 мол % холестерола, высвобождающими менее 50% амбризентана в течение 1 часа с момента SLF инкубации при 37°С.
Пример 3: Профиль высвобождения in vitro (IVR) липосомальных композиций с илопростом с циклодекстрином (CD) или без него
Исследование in vitro было выполнено для оценки влияния циклодекстрина ((2-гидроксипропил)-β-циклодекстрина (HP-β-CD)) во внутренней водной среде липосомы на профиль высвобождения в случае липосомальных композиций с илопростом из Примера 1.
Результаты:
Физико-химические характеристики и профиль IVR липосомальных композиций с илопростом с циклодекстрином (HP-β-CD) или без него показаны в таблице 3.
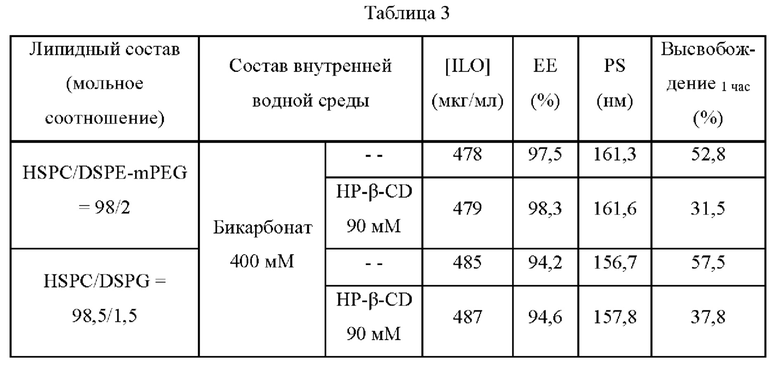
В таблице 3 показано, что добавление циклодекстрина дополнительно уменьшает взрывное высвобождение (менее 60% илопроста высвобождалось в течение 1 часа с момента SLF инкубации при 37°С) и обеспечивает устойчивое высвобождение из липосомальных композиций с илопростом (менее 40% илопроста высвобождалось в течение 1 часа с момента SLF инкубации при 37°С).
Пример 4: Эффективность инкапсуляции для липосомальных композиций с илопростом при использовании различных солей слабой кислоты
Было проведено исследование in vitro для оценки влияния различных солей слабой кислоты на эффективность инкапсуляции в случае липосомальных композиций с илопростом из Примера 1. Для загрузки илопроста в данном примере использовали раствор бикарбоната натрия (400 мМ) и раствор ацетата натрия.
Результаты:
Эффективность инкапсуляции липосомальных композиций с илопростом при использовании различных солей слабых кислот показана в таблице 4.
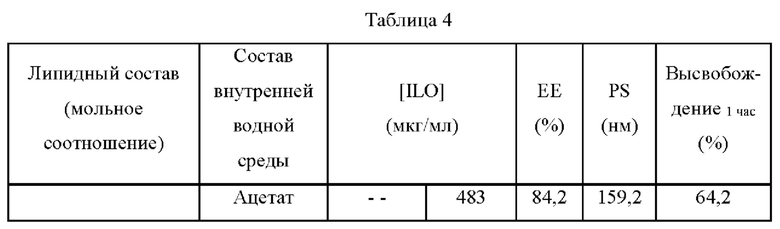
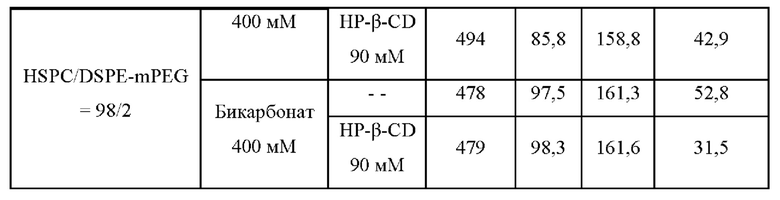
Таблица 4 показывает, что >80% ЕЕ было достигнуто с бикарбонатными и ацетатными солями, и присутствие циклодекстрина во внутренней водной среде дополнительно уменьшает взрывное высвобождение и поддерживает высвобождение илопроста из липосомальных композиций.
Пример 5: Профиль высвобождения in vitro (IVR) и in vivo фармакокинетический (PK) параметр липосомальных композиций с илопростом, различающихся соотношением илопроста и циклодекстрина (ILO/CD)
Было проведено in vitro исследование с целью оценки влияния различных соотношений ILO/CD на IVR профиль липосомальных композиций с илопростом. Были приготовлены липосомальные композиции данного исследования, и IVR профили были проанализированы в соответствии с процедурами, описанными в примере 1. Раствор илопроста (20 мкг/мл) был приготовлен путем растворения илопроста в 2 мМ растворе трометамина с доведением рН до приблизительно 8,4.
В. Исследование in vivo фармакокинетики (РК) липосомальных композиций с илопростом
В данном in vivo PK исследовании три крысы-самца Sprague-Dawley (приобретенные у BioLASCO Taiwan Co., Ltd.) в каждой группе были анестезированы изофлураном и надежно размещены на спине на изогнутой платформе в дорсальном положении на плоскости под углом от 45° до 50° с помощью ленты, закрепленной на верхних резцах. Наконечник для аэрозоля с микроспреем (Microsprayer, PennCentury, Филадельфия, США) вставляли в бифуркацию трахеи каждой крысы, и тестируемый образец (т.е. композиции в таблице 5 или раствор илопроста) вводили интратрахеально каждой крысе в заданной дозе 60 мкг/г с помощью шприца высокого давления, который был прикреплен к устройству для распыления аэрозоля.
В заранее определенный момент времени (т.е. через 5, 30 мин, 1,5, 3, 6, 7 и 8 часов после введения) у каждой крысы собирали образец крови в пробирку, покрытую гепарином, и помещали на влажный лед. Затем образец крови центрифугировали при приблизительно 2500×g в течение 15 минут и при 4±2°С в течение 1 часа после сбора для отделения плазмы от клеток крови. Около 0,1 мл образца плазмы от каждой крысы добавляли в новую пробирку для хранения и хранили при -70±2°С.
Для определения концентрации илопроста в плазме 50 мкл образца плазмы переносили в лунку 96-луночного планшета с последующим добавлением 150 мкл ацетонитрила в каждую лунку. Полученную смесь встряхивали в течение 1 минуты, чтобы нарушить связывание белков плазмы с илопростом, с последующим центрифугированием при 3000 об/мин в течение 5 минут. Надосадочную жидкость (150 мкл) смешивали с равным объемом Н2О и анализировали методом жидкостной хроматографии-тандемной масс-спектрометрии (ЖХ-МС/МС) для определения концентрации илопроста в плазме крысы.
Результаты:
IVR профиль и PK-параметр (Cmax) липосомальных композиций с илопростом с различным соотношением ILO/CD показаны в таблице 5, на ФИГ. 1 и ФИГ. 2.
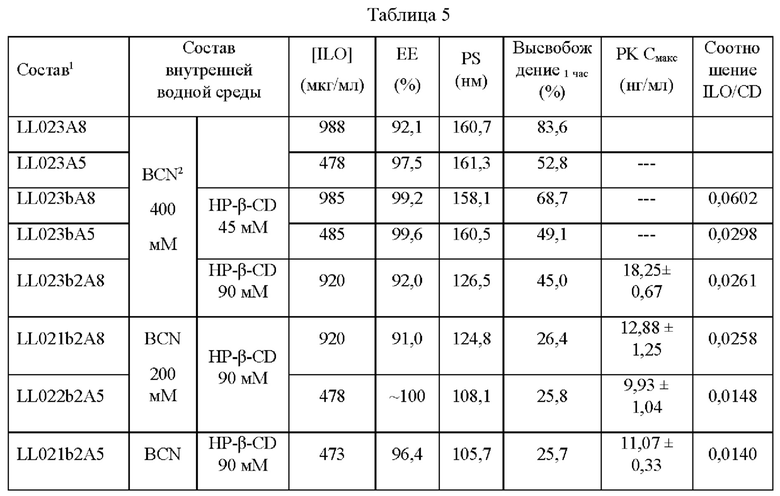
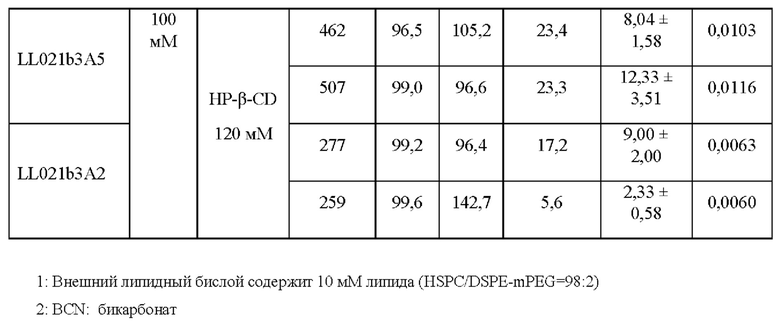
В таблице 5 показаны илопрост-липосомальные композиции с соотношением ILO/CD менее 0,06, демонстрирующие уменьшенный профиль взрывного высвобождения (менее 68,7% илопроста высвобождается в течение 1 часа с момента введения). Свойство более устойчивого высвобождения (менее 45% илопроста высвобождается в течение 1 часа с момента инкубации SLF при 37°С) было отмечено в илопрост-липосомальных композициях с соотношением ILO/CD менее 0,026. Аналогичная тенденция была отмечена при добавлении циклодекстрина во внутреннюю водную среду.
На ФИГ. 1 показан логарифм средней концентрации илопроста в плазме у крыс, которым вводили илопрост-липосомальные композиции из таблицы 6 (LL021b3A2/LL021m3A2) или раствор илопроста в заданной дозе в зависимости от времени введения на временном интервале до 24 часов. После введения липосомальных композиций с илопростом нет значимого пика по сравнению с пиком в течение 1 часа после введения раствора илопроста. Уменьшение пикового высвобождения предотвращает побочный эффект лекарственного средства, например меньшее местное раздражение в верхних дыхательных путях при прямом контакте с заявленной липосомальной композицией.
На ФИГ. 2 показано соотношение площади под кривой зависимости концентрации в плазме от времени от нуля до определенного времени (AUCt) и площади под кривой зависимости концентрации в плазме от времени от нуля до бесконечности (AUCinf) для определения общего воздействия илопроста в течение определенного периода времени и для нормализации различных доз илопроста в каждой композиции (илопрост-липосомальные композиции из таблицы 6 или раствор илопроста). Более 80% илопроста высвобождалось в течение 24 часов с момента введения илопрост-липосомальных композиций по сравнению с 100% высвобождения илопроста в течение 1 часа после введения раствора илопроста. Результаты показывают снижение накопления лекарственного средства в целевом участке и, следовательно, меньший побочный эффект.
Пример 6: Профиль высвобождения in vitro (IVR) и in vivo фармакокинетический (PK) параметр липосомальных композиций с илопростом, различающихся содержанием циклодекстрина (CD).
Были приготовлены липосомальные композиции с илопростом, содержащие (2-гидроксипропил)-β-циклодекстрин (HP-β-CD) или случайно метилированный-β-циклодекстрин (RM-β-CD), и профили IVR были оценены в соответствии с процедурами, изложенными в Примере 1.
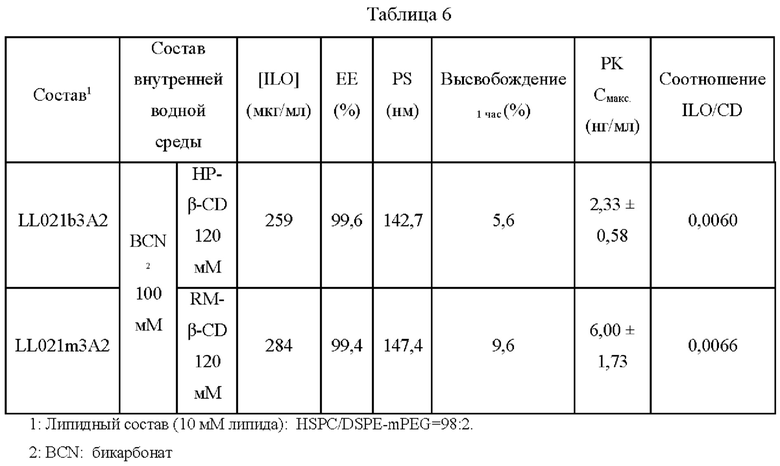
Результаты:
В таблице 6 представлены физико-химические характеристики липосомальных композиций с илопростом, различающихся по CD. Как HP-β-CD, так и RM-β-CD уменьшали быстрое высвобождение из илопрост-липосомальных композиций (менее 20% илопроста высвобождается в течение 1 часа с момента инкубации SLF при 37°С).
В приведенном выше описании с целью пояснения были изложены многочисленные конкретные детали с тем, чтобы обеспечить полное понимание вариантов осуществления. Однако для специалиста в данной области техники будет очевидно, что один или несколько других вариантов осуществления могут быть реализованы на практике без некоторых из данных конкретных деталей. Также следует принимать во внимание, что ссылки в данном описании на «один вариант осуществления», «вариант осуществления», вариант осуществления с указанием порядкового номера и так далее означают, что конкретная особенность, структура или характеристика могут быть включены в практику раскрытия. Также следует понимать, что в описании различные признаки иногда сгруппированы вместе в одном варианте осуществления, чертеже или их описании с целью упрощения раскрытия и помощи в понимании различных аспектов изобретения, и что один или несколько признаков или конкретные детали из одного варианта осуществления могут быть применены на практике вместе с одной или несколькими особенностями или конкретными деталями из другого варианта осуществления, где это уместно, на практике раскрытия.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ СЛАБОКИСЛОТНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА И СПОСОБЫ ПРИМЕНЕНИЯ | 2020 |
|
RU2832678C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ КОНТРОЛИРОВАННОГО ВЫСВОБОЖДЕНИЯ ТРЕПРОСТИНИЛА | 2019 |
|
RU2796305C2 |
| ЛИПОСОМАЛЬНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СЛАБОКИСЛОТНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2778886C2 |
| ЛИПОСОМА, ИМЕЮЩАЯ ВНУТРЕННЮЮ ВОДНУЮ ФАЗУ, СОДЕРЖАЩУЮ СОЛЬ СУЛЬФОБУТИЛОВОГО ЭФИРА ЦИКЛОДЕКСТРИНА | 2010 |
|
RU2575793C2 |
| ЛИПОСОМНЫЕ КОМПОЗИЦИИ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2015 |
|
RU2757110C2 |
| СТАБИЛИЗИРУЮЩИЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ КАМПТОТЕЦИНА | 2016 |
|
RU2833053C2 |
| СТАБИЛИЗИРОВАННЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ КАМПТОТЕЦИНА | 2016 |
|
RU2732567C2 |
| ЗАМЕДЛЕННОЕ ВЫСВОБОЖДЕНИЕ ПРОТИВОИНФЕКЦИОННЫХ АГЕНТОВ | 2006 |
|
RU2438655C2 |
| УСОВЕРШЕНСТВОВАННЫЕ ЛИПОСОМЫ И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2482837C2 |
| ЛИПОСОМАЛЬНОЕ СРЕДСТВО НА ОСНОВЕ УБИХИНОЛА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2605616C1 |
Группа изобретений относится к области медицины и раскрывает фармацевтическую композицию для лечения легочной гипертензии или интерстициального заболевания легких, содержащую: одну или несколько липосом, суспендированных во внешней среде, причем указанная липосома содержит: (а) внешний липидный бислой, содержащий смесь первого фосфолипида, второго фосфолипида и стерола, и (b) внутреннюю водную среду, содержащую слабокислотное лекарственное средство, представляющее собой простагландин, агонист простациклиновых (IP) рецепторов, антагонист эндотелиновых (ЕТ) рецепторов, глюкокортикоид или нестероидный противовоспалительный препарат (НПВП), или любую их комбинацию, и соль слабой кислоты, которая представляет собой соль карбоновой кислоты или бикарбонатную соль, где соотношение первый фосфолипид : стерол : второй фосфолипид в мольных процентах составляет 75-99:0-14,9:0,1-25. Также группа изобретения раскрывает способ лечения легочной гипертензии или интерстициального заболевания легких и способ уменьшения побочного действия слабокислотного лекарственного средства. Заявленная группа изобретений обеспечивает высокую терапевтическую активность, с уменьшением потенциального побочного эффекта за счет липосомальной композиции, не дающей начального взрывного высвобождения. 3 н. и 21 з.п. ф-лы, 2 ил., 6 табл., 6 пр.
1. Фармацевтическая композиция для лечения легочной гипертензии или интерстициального заболевания легких, содержащая:
одну или несколько липосом, суспендированных во внешней среде, причем указанная липосома содержит:
(а) внешний липидный бислой, содержащий смесь первого фосфолипида, второго фосфолипида и стерола, и
(b) внутреннюю водную среду, содержащую слабокислотное лекарственное средство, представляющее собой простагландин, агонист простациклиновых (IP) рецепторов, антагонист эндотелиновых (ЕТ) рецепторов, глюкокортикоид или нестероидный противовоспалительный препарат (НПВП), или любую их комбинацию, и соль слабой кислоты, которая представляет собой соль карбоновой кислоты или бикарбонатную соль,
где соотношение первый фосфолипид : стерол : второй фосфолипид в мольных процентах составляет 75-99:0-14,9:0,1-25.
2. Фармацевтическая композиция по п. 1, в которой внешний липидный бислой содержит менее 10 мол.% стерола.
3. Фармацевтическая композиция по п. 1, в которой внешний липидный бислой по существу не содержит стерола.
4. Фармацевтическая композиция по п. 1, в которой стерол выбран из группы, состоящей из холестерола, холестерола гексасукцината, эргостерола, ланостерола и их комбинации.
5. Фармацевтическая композиция по п. 1, в которой внешний липидный бислой содержит менее 13 мол.% стерола.
6. Фармацевтическая композиция по п. 1, в которой первый фосфолипид представляет собой фосфатидилхолин (PC), второй фосфолипид представляет собой модифицированный полиэтиленгликолем фосфолипид или отрицательно заряженный фосфолипид.
7. Фармацевтическая композиция по п. 6, в которой указанный PC представляет собой гидрогенизированный яичный фосфатидилхолин (HEPC), гидрогенизированный соевый фосфатидилхолин (HSPC), дипальмитоилфосфатидилхолин (DPPC), дистеарилохолинфосфатидил-фосфатидилфосфолин (DSPC) димиристоилфосфатидилхолин (DMPC), яичный фосфатидилхолин (EPC), соевый фосфатидилхолин (SPC), олеоилпальмитоилфосфатидилхолин, диолеоилфосфатидилхолин (DOPC), дипетрозелиноилфосфатидилхолин, пальмитоилелаидоилфосфатидилхолин, пальмитоилолеилфосфатидилхолин, дилауроилфосфатидилхолин (DLPC), диундеканоилфосфатидилхолин, дидеканоилфосфатидилхолин, динонилфосфатидилхолин или любую их комбинацию, причем указанный модифицированный полиэтиленгликолем фосфолипид представляет собой 1,2-дистеаролили-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000] (DSPE-PEG2000) и указанный отрицательно заряженный фосфолипид представляет собой дистеарилоилфосфатидилглицерин (DSPG), дипальмитоилфосфатидилглицерин (DPPG) или димиристоилфосфатидилглицерин (DMPG) или диолеоилфосфатидилглицерин (DOPG).
8. Фармацевтическая композиция по п. 6, в которой первый фосфолипид представляет собой HSPC и второй фосфолипид представляет собой DSPE-PEG2000 или DSPG.
9. Фармацевтическая композиция по п. 1, в которой соль карбоновой кислоты представляет собой формиат, ацетат, пропионат, бутират, изобутират, валерат, изовалерат, бензоат или любую их комбинацию.
10. Фармацевтическая композиция по п. 1, в которой бикарбонатная соль представляет собой бикарбонат калия, бикарбонат натрия, бикарбонат кальция, бикарбонат магния, бикарбонат цезия, бикарбонат лития, бикарбонат никеля, бикарбонат двухвалентного железа или любую их комбинацию.
11. Фармацевтическая композиция по п. 1, в которой внутренняя водная среда дополнительно содержит циклодекстрин.
12. Фармацевтическая композиция по п. 11, в которой мольное соотношение слабокислотного лекарственного средства и циклодекстрина меньше или равно 0,06.
13. Фармацевтическая композиция по п. 11, в которой мольное соотношение слабокислотного лекарственного средства и циклодекстрина меньше или равно 0,03.
14. Фармацевтическая композиция по п. 1, в которой простагландин представляет собой илопрост или трепростинил.
15. Фармацевтическая композиция по п. 1, в которой антагонист ЕТ рецепторов представляет собой амбризентан или бозентан.
16. Фармацевтическая композиция по п. 1, в которой указанный агонист IP рецепторов представляет собой MRE-269.
17. Фармацевтическая композиция по п. 1, в которой указанный НПВП представляет собой кеторолак или мелоксикам.
18. Фармацевтическая композиция по п. 1, в которой глюкокортикоид представляет собой метилпреднизолон или дексаметазон.
19. Способ лечения легочной гипертензии или интерстициального заболевания легких, включающий стадии введения эффективного количества фармацевтической композиции по пп. 1-18 путем интратрахеальной инъекции, ингаляции или введения непосредственно в кровоток.
20. Способ по п. 19, в котором слабокислотное лекарственное средство представляет собой трепростинил, илопрост, амбризентан, бозентан, MRE-269, метилпреднизолона гемисукцинат (MPSS), дексаметазон, мелоксикам или кеторолак.
21. Способ по п. 20, в котором слабокислотное лекарственное средство представляет собой простагландин или антагонист эндотелиновых (ЕТ) рецепторов.
22. Способ уменьшения побочного действия слабокислотного лекарственного средства, включающий стадию введения субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции по пп. 1-18.
23. Способ по п. 22, в котором слабокислотное лекарственное средство вдыхают для уменьшения побочного действия слабокислотного лекарственного средства на верхние дыхательные пути.
24. Способ по п. 23, в котором слабокислотное лекарственное средство представляет собой трепростинил, илопрост, амбризентан, бозентан, MRE-269, метилпреднизолона гемисукцинат (MPSS), дексаметазон, мелоксикам или кеторолак.
| US 5939096 A1, 17.08.1999 | |||
| US 20120128757 A1, 24.05.2012 | |||
| US 20160058705 A1, 03.03.2016 | |||
| US 20080058294 A1, 06.03.2008 | |||
| JAIN, PRITESH P et al | |||
| Liposomal nanoparticles encapsulating iloprost exhibit enhanced vasodilation in pulmonary arteries | |||
| International journal of nanomedicine, vol | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Устройство для указания требуемого направления | 1923 |
|
SU3249A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| НАБОР ДЛЯ ПРИГОТОВЛЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ | 2002 |
|
RU2279292C2 |
Авторы
Даты
2023-12-28—Публикация
2019-09-12—Подача