Изобретение относится к области медицины, в частности к средствам для лечения заболеваний сердечно-сосудистой системы, а именно к средству для лечения и предотвращения кальцификации кровеносных сосудов.
Сердечно-сосудистая кальцификация - широко распространенная патология. У современного населения данное заболевание наблюдается все более часто в связи с увеличением продолжительности жизни, малоподвижным образом жизни, избыточным потреблением калорий и многими другими факторами. Кальцификация коронарных артерий наблюдалась у 50,5% британской когорты из 16222 бессимптомных пациентов без документально подтвержденной ишемической болезни сердца или хронического заболевания почек. Некоторые формы сердечно-сосудистой кальцификации представляют непосредственную опасность для жизни. Кальцифицирующая болезнь аортального клапана, или кальцинированный аортальный стеноз (КАС) - одна из наиболее опасных форм кальцификации сосудов, которая в 2017 году привела к 102700 летальных исходов и 12,6 миллионам случаев по всему миру. Несмотря на такую высокую частоту в развитых странах и высокий уровень смертности, медикаментозного лечения КАС пока нет.
Известно, что нтерстициальные клетки клапанов (ИКК) играют центральную роль в прогрессировании КАС. В норме эти клетки поддерживают гомеостаз створок клапана, но во время прогрессирования КАС они могут подвергаться остеогенной дифференцировке, что приводит к кальцификационному ремоделированию клапанных тканей (Rutkovskiy Arkady, Anna Malashicheva, Gareth Sullivan, Maria Bogdanova, Anna Kostareva, Kåre-Olav Stenslоkken, Arnt Fiane, and Jarle Vaage. (2017). Valve Interstitial Cells: The Key to Understanding the Pathophysiology of Heart Valve Calcification. Journal of the American Heart Association 6 (9). https://doi.org/10.1161/JAHA.117.006339). Таким образом, ингибирование остеогенной дифференцировки ИКК является эффективной целью терапии против КАС, а оценка влияния возможных лекарств на остеогенную дифференцировку ИКК могла бы быть плодотворной модельной системой для разработки терапии против КАС.
Предполагается, что нарушение регуляции передачи сигналов пути Notch является важным фактором прогрессирования КАС. Было показано дозозависимое действие передачи сигналов Notch на стимуляцию остеогенной дифференцировки (Semenova, D.; Bogdanova, M.; Kostina, A.; Golovkin, A.; Kostareva, A.; Malashicheva, A. Dose-dependent mechanism of Notch action in promoting osteogenic differentiation of mesenchymal stem cells. Cell Tissue Res 2020, 379, 169-179, doi:10.1007/s00441-019-03130-7).
Также было показано, что ИКК от пациентов с КАС чувствительны к проостеогенным стимулам и демонстрируют высокий остеогенный потенциал, когда передача сигналов Notch активируется или не регулируется (Kostina, A.; Shishkova, A.; Ignatieva, E.; Irtyuga, O.; Bogdanova, M.; Levchuk, K.; Golovkin, A.; Zhiduleva, E.; Uspenskiy, V.; Moiseeva, O. Different Notch signaling in cells from calcified bicuspid and tricuspid aortic valves. Journal of Molecular and Cellular Cardiology 2018, 114, 211-219) Таким образом, было сделано предположение, что ингибирование передачи сигналов Notch в ИКК может рассматриваться как перспективное направление лечения КАС.
Известно соединение-ингибитор сигнального пути Notch (US2013029972 A1 2013-01-31) кренигацестат (Crenigacestat), применимое для лечения рака. Кренигацестат (LY3039478) представляет собой низкомолекулярный селективный ингибитор расщепления рецептора Notch, блокирующий высвобождение его внутриклеточного домена и, как следствие, подавляющий передачу сигнала Notch. Препарат успешно прошел первую фазу клинических испытаний и представляется многообещающим кандидатом для лечения онкозаболеваний.
Техническим результатом заявленного изобретения является создание средства, подавляющего остеогенную дифференцировку интерстициальных клеток клапана сердца человека.
Заявленный технический результат достигается при использовании средства для подавления остеогенной дифференцировки интерстициальных клеток клапана сердца человека, содержащего в качестве действующего вещества кренигацестат в эффективном количестве.
Целесообразно использовать кренигацестат в концентрации 50-100 нМ.
При создании изобретения были проведены исследования способности ингибировать остеогенную дифференцировку ИКК сердца человека, выделенных от пациентов с КАС, селективным ингибитором сигнального пути Notch кренигацестат и CB-103, представляющим собой низкомолекулярный селективный ингибитор комплекса CSL-NICD. CB-103 активирует гены-мишени Notch, поэтому его ингибирование приводит к прерыванию передачи сигнала Notch.
В результате исследования было обнаружено, что кренигацестат (crenigacestat) в концентрации 50-100 нМ способен полностью подавлять остеогенную дифференцировку ИКК in vitro, а CB-103 не обладает подобным действием.
Изобретение иллюстрируется следующими графическими материалами.
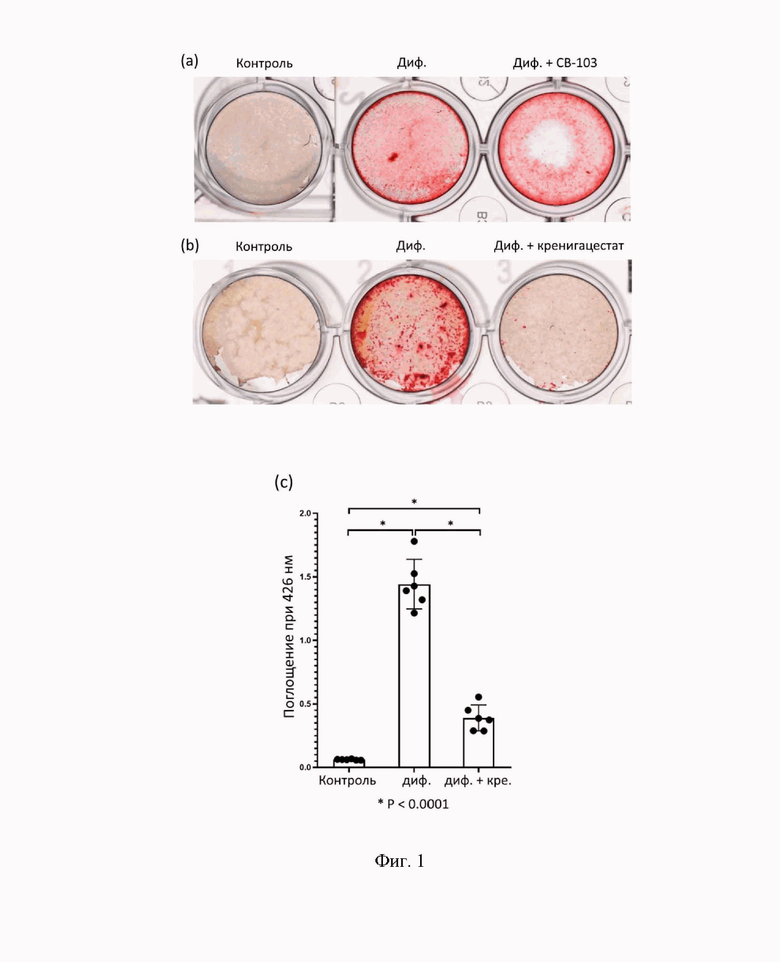
На фиг.1 представлено влияние CB-103 и кренигацестата (LY3039478) на остеогенную дифференцировку ИКК человека
- (а) окрашивание ИКК ализариновым красным в контроле, в остеогенной среде (диф.) и в остеогенной среде с добавлением CB-103 (диф.+CB-103).
- (b) окрашивание ИКК ализариновым красным в контроле, остеогенной среде (диф.) и остеогенной среде с добавлением кренигацестата (диф.+кренигацестат).
- (c) количественное измерение окрашивания ализариновым красным с помощью спектрофотометрии ИКК в контроле, в остеогенной среде (диф.) и в остеогенной среде с добавлением кренигацестата (диф.+кре.). Группы сравнивались с помощью Т-теста.
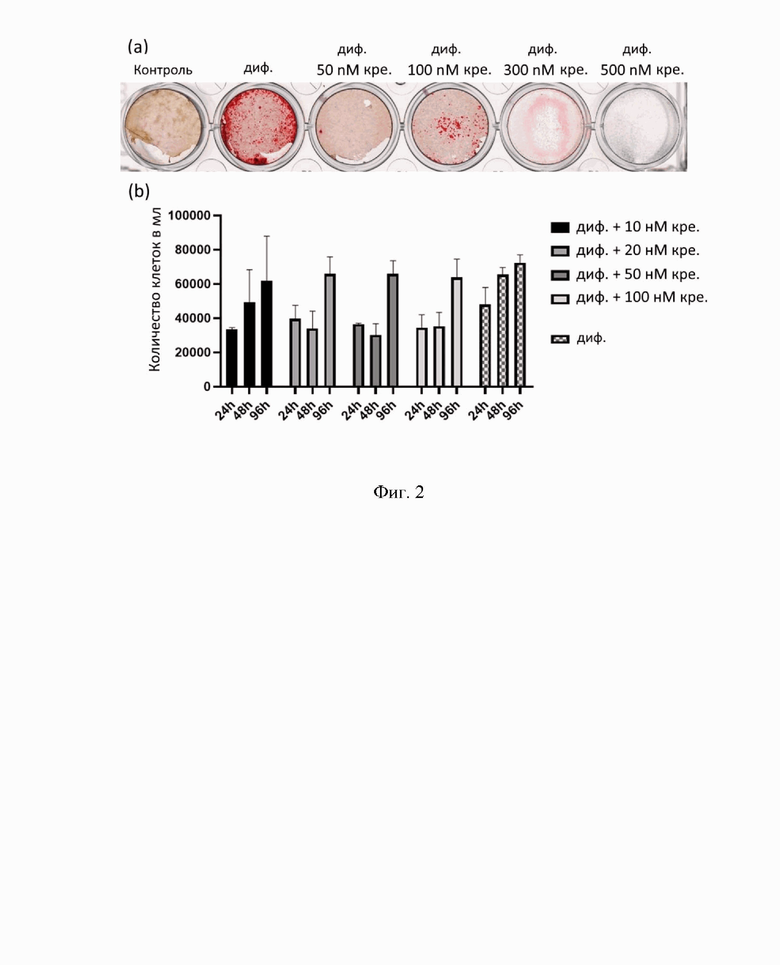
На Фиг. 2 представлено влияние различных доз кренигацестата на выживание и остеогенную дифференцировку ИКК человека
- (а) окрашивание ИКК ализариновым красным на 21 день культивирования в контроле, в остеогенной среде (диф.) и в остеогенной среде с добавлением различных доз кренигацестата (кре) от 50 до 500 нМ;
- (b) столбчатая диаграмма демонстирует количество ИКК, культивированных в остеогенных средах в контрольных условиях или при обработке различными дозами кренигацестата.
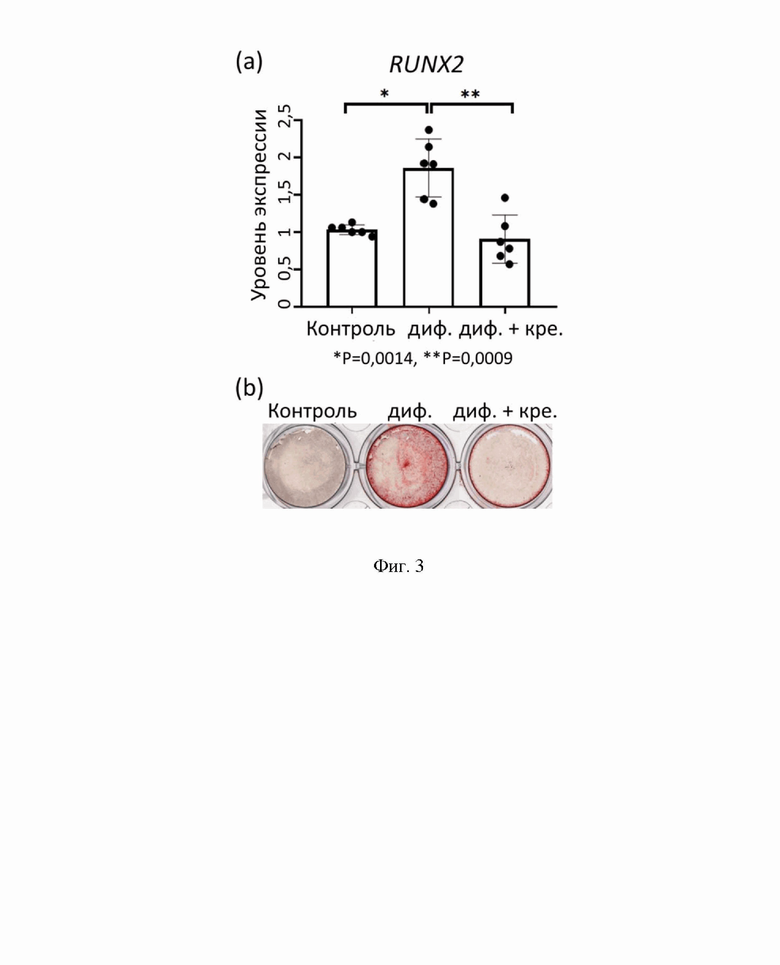
На Фиг. 3 показано ингибирование экспрессии гена RUNX2 кренигацестатом во время остеогенной дифференцировки ИКК человека
- (а) - уровень экспрессии мастер-гена остеогенной дифференцировки RUNX2 в контрольных клетках (Контроль), клетках, обработанных остеогенной средой (диф.), и клетках, обработанных остеогенной средой и 100 нМ кренигацестата (диф.+кре.). Группы сравнивали с помощью Т-теста, *p<0,05.
- (b) - окрашивание ализариновым красным, показывающее уровень минерализации внеклеточного матрикса в контрольных клетках (Контроль), в клетках, обработанных остеогенной средой (диф.), и в клетках, обработанных остеогенной средой и 100 нМ кренигацестата (диф.+кре.).
Сущность заявленного изобретения подтверждается следующим примером.
Все эксперименты проводили в трех биологических повторностях на ИКК сердца человека, выделенных от трех доноров с кальцифицирующей болезнь аортального клапана.
1. Получение клеточных культур
ИКК человека были выделены из тканей клапанов аорты человека. Выделение первичных культур ИКК проводили путем диссоциации тканей коллагеназой II в концентрации 2 мг/мл. Для дальнейшего культивирования ИКК использовали Dulbecco's modified Eagle's medium (DMEM; Gibco, США) с добавлением 15% фетальной телячьей сыворотки (FBS; Gibco, США), 1% пенициллина/стрептомицина (Invitrogene, США), 1% L-глютамин (Invitrogen, США). Питательные среды меняли два раза в неделю. Все клеточные линии поддерживали в инкубаторе с 5% CO2 при 37°C. Использовали клетки 3-5 пассажа. Отсутствие контаминации микоплазмой проверяли с помощью рвПЦР.
2. Остеогенная дифференцировка
Остеогенную дифференцировку ИКК индуцировали остеогенной средой ОМ: DMEM с добавлением 10% FBS, 1% пенициллина/стрептомицина и 50 мкМ аскорбиновой кислоты, 100 нМ дексаметазона и 10 мМ β-глицерофосфата (Sigma, СШA). Для индукции остеогенной дифференцировки клетки высевали с плотностью 26×103/см2.
Отложение кальция выявляли окрашиванием ализариновым красным (Sigma, США) на 21 день дифференцировки. Клетки промывали фосфатно-солевым буфером (PBS), фиксировали в 70% этаноле в течение 60 минут, дважды промывали дистиллированной водой и окрашивали раствором ализаринового красного. После окрашивания ализариновый красный экстрагировали 10% уксусной кислотой и измеряли спектрофотометрически при 426 нм на планшетном спектрофотометре Varioskan Lux (ThermoFisher S Scientific, США). Обработку данных проводили с использованием Microsoft Excel и GraphPad Prism.
3. Ингибирование остеогенной дифференцировки
CB-103 растворяли в диметилсульфоксиде (DMSO) до 100 мМ, кренигацестат (LY3039478; Medchemexpress, США) растворяли в DMSO до 10 мМ.
Чтобы выявить потенциальный антикальцифицирующий эффект кренигацестата и CB-103 на ИКК, клетки культивировали в контрольной среде и в остеогенной среде с добавлением кренигацестата или CB-103. На 21 день от начала дифференцировки клетки окрашивали ализариновым красным для измерения уровня кальцификации внеклеточного матрикса (ЕСМ). Препараты были протестированы в разной концентрации вплоть до цитотоксического действия.
Было обнаружено, что CB-103 не оказывает значительного влияния на остеогенную дифференцировку ИКК (Фиг. 1 а). Напротив, кренигацестат сильно ингибировал остеогенную дифференцировку (Фиг. 1 b, c). Количественное измерение окрашивания ализариновым красным с помощью спектрофотометрии показало, что уровень кальцификации был значительно ниже в клетках, обработанных кренигацестатом, по сравнению с контрольными клетками после остеогенной дифференцировки (Фиг.1 c). Было показано, что кренигацестат, но не CB-103, ингибирует остеогенную дифференцировку ИКК (Фиг. 1).
Чтобы проанализировать влияние различных доз кренигацестата на пролиферацию ИКК, клетки культивировали в остеогенных условиях с добавлением кренигацестата в различной концентрации (10 нМ, 20 нМ, 50 нМ, 100 нМ, 300 нМ, 500 нМ). При добавлении кренигацестата в концентрации 10 и 20 нМ подавления остеогенной дифференцировки не наблюдалось. Кренигацестат в концентрации 50 и 100 нМ эффективно подавлял остеогенную дифференцировку. Добавление кренигацестата в концентрации выше 300 нМ вызывало гибель большинства клеток на 21-й день культивирования (Фиг. 2а). Таким образом оптимальная концентрация кренигацестата для подавления остеогенной дифференцировки ИКК в условиях in vitro находится в диапазоне 50-100 нМ.
Чтобы подтвердить подавление остеогенной дифференцировки при действии кренигацестата, был проанализирован уровень экспрессии мастер-гена остеогенной дифференцировки RUNX2 (Фиг. 3). Действие кренигацестата приводило к снижению экспрессии RUNX2 на уровне мРНК (Фиг.3а) и одновременному снижению количества кальцификатов в клетках, что подтверждено спектрофотометрическим анализом окраски кальцификатов раствором ализаринового красного (Фиг. 3б).
Экспериментально показано, что ингибитор гамма-секретазы кренигацестат (LY3039478) в концентрации 50-100 нМ полностью ингибирует остеогенную дифференцировку интерстициальных клеток клапана человека, выделенных от пациентов с кальцифицируемой болезнью аортального клапана.
Таким образом, высокая селективность кренигацестата и сильный антикальцифицирующий эффект в нетоксичной дозировке делают его перспективным для дальнейших доклинических исследований.
Из клинических испытаний кренигацестата для лечения онкологических заболеваний известна возможность его применения в клинике и интервал дозирования, который безопасен для людей при пероральном или внутривенном введении. Это позволяет предположить, что кренигацестат может быть использован для дальнейших клинических испытаний и при КАС.
Заявленное средство обладает высокой селективностью и сильным антикальцифицирующим эффектом в нетоксичной дозировке, что делает его перспективным для дальнейших доклинических исследований.
| название | год | авторы | номер документа |
|---|---|---|---|
| Модель аортального клапана человека ex vivo при его патологической кальцификации и ее применение | 2024 |
|
RU2839805C1 |
| КОМПОЗИЦИИ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ЛЕЧЕНИЯ КАЛЬЦИНОЗА КЛАПАНА, СОДЕРЖАЩИЕ DPP-4 ИНГИБИТОР | 2015 |
|
RU2680527C1 |
| СПОСОБ ОЦЕНКИ ОСТЕОГЕННОГО ПОТЕНЦИАЛА МЕЗЕНХИМАЛЬНЫХ СТРОМАЛЬНЫХ КЛЕТОК | 2016 |
|
RU2674336C2 |
| СРЕДА КУЛЬТИВИРОВАНИЯ МУЛЬТИПОТЕНТНЫХ СТРОМАЛЬНЫХ КЛЕТОК ИЗ ЖИРОВОЙ ТКАНИ ЧЕЛОВЕКА И СПОСОБ КУЛЬТИВИРОВАНИЯ ЭТИХ КЛЕТОК С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2010 |
|
RU2418855C1 |
| МНОГОМЕРНЫЙ БИОМАТЕРИАЛ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2010 |
|
RU2542430C2 |
| Способ оценки дифференцировки мезенхимальных стволовых клеток в трёхмерных скаффолдах | 2023 |
|
RU2818354C1 |
| АНАЛОГ ОКСИСТЕРОЛА OXY133 ИНДУЦИРУЕТ ОСТЕОГЕНЕЗ И СИГНАЛЬНЫЙ ПУТЬ HEDGEHOG И ИНГИБИРУЕТ ЛИПОГЕНЕЗ | 2013 |
|
RU2632191C2 |
| Способ in vitro пролиферации стволовых клеток и применение устройства для усиления пролиферации стволовых клеток in vitro | 2015 |
|
RU2688444C1 |
| Способы получения индуцированных клеток гладких мышц | 2020 |
|
RU2815906C2 |
| СПОСОБ ВЫДЕЛЕНИЯ ПРОИСХОДЯЩИХ ИЗ ПУПОВИННОЙ КРОВИ ПЛЮРИПОТЕНТНЫХ СТВОЛОВЫХ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ ZNF281 | 2010 |
|
RU2511417C2 |
Изобретение относится к области медицины, в частности к средствам для лечения заболеваний сердечно-сосудистой системы. Раскрыто применение средства, содержащего в качестве действующего вещества кренигацестат в концентрации 50-100 нМ, для подавления остеогенной дифференцировки интерстициальных клеток клапана сердца человека. Изобретение обеспечивает высокую селективность и антикальцифицирующий эффект в нетоксичной дозировке. 3 ил., 3 пр.
Применение средства, содержащего в качестве действующего вещества кренигацестат в концентрации 50-100 нМ, для подавления остеогенной дифференцировки интерстициальных клеток клапана сердца человека.
| КОМПОЗИЦИИ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ЛЕЧЕНИЯ КАЛЬЦИНОЗА КЛАПАНА, СОДЕРЖАЩИЕ DPP-4 ИНГИБИТОР | 2015 |
|
RU2680527C1 |
| US 20130029972 A1, 31.01.2013 | |||
| Краткий курс молекулярной фармакологии под ред | |||
| П.В | |||
| Сергеева, М., 1975, с | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| ХОЛОДОВ Л.Е | |||
| и др | |||
| Клиническая фармакокинетика: М., Медицина, 1985, с | |||
| Пуговица | 0 |
|
SU83A1 |
Авторы
Даты
2023-12-28—Публикация
2022-10-28—Подача