РОДСТВЕННАЯ ЗАЯВКА
[0001] В заявке испрашивается приоритет по предварительной заявке на патент Австралии № 2016902643, поданной 5 июля 2016 г., полное содержание которой включено в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] В этом изобретении описаны способы получения гексаплоидных растений пшеницы, содержащих высокоамилозный крахмал, и использование таких растений и, в частности, зерен или полученного из них крахмала, в широком диапазоне пищевых и непищевых продуктов.
УРОВЕНЬ ТЕХНИКИ
[0003] Ссылки на любой известный уровень техники, приведенные в этом описании, не являются и не должны восприниматься, как признание или любая форма предположения, что этот существующий уровень техники формирует часть общеизвестных сведений в какой-либо стране. В тексте этой заявки приведены ссылки на различные публикации, включая ссылки, приведенные в скобках. Полный список цитируемых публикаций, ссылки на которые приведены в скобках, можно найти в алфавитном порядке в конце описания непосредственно перед формулой изобретения. Описание всех цитируемых публикаций в полном объеме включено в эту заявку посредством ссылки для более полного описания уровня техники, к которой относится это изобретение.
[0004] Пищевые продукты, производимые из зерен пшеницы, поставляют по меньшей мере 20% пищевых килоджоулей для населения планеты и обеспечивают существенную часть белка и некрахмальных полисахаридов, а также энергетический вклад в рацион человека. Крахмал является основным компонентом зерен пшеницы и используется в широком диапазоне пищевых и непищевых продуктов. Характеристики крахмала варьируются и играют ключевую роль при определении пригодности пшеничного крахмала для конкретного конечного применения. Несмотря на огромное глобальное потребление и несмотря на растущее понимание важности функциональных характеристик крахмала на качество конечного продукта, исследования генетических вариаций в пшенице и их точного влияния на характеристики крахмала отстают от исследований в отношении других промышленно важных зерновых растений.
[0005] Углеводы составляют около 65-75% зрелых пшеничных зерен (Stone and Morell, 2009). Основным углеводом в пшеничных зернах является крахмал, который состоит из двух полимеров глюкозы, амилозы и амилопектина. Амилоза представляет собой преимущественно линейный полимер α-1,4-связанных единиц глюкозы с несколькими ответвлениями, тогда как амилопектин является относительно сильно разветвленным с α-1,6-глюкозидными связями, связывающими α-1,4-связанные единицы глюкозы. Соотношение между амилозой и амилопектином является основной детерминантой для (i) пользы пшеничных зерен и пшеничного крахмала для здоровья и (ii) конечного качества продуктов, содержащих пшеничный крахмал.
[0006] Второй важной для здоровья детерминантой в пшеничных зернах является количество некрахмальных полисахаридов в зернах, которые образуют часть пищевых волокон. Зерна дикой пшеницы содержат около 1% по массе олигосахаридов, таких как раффиноза, около 1% фруктанов и около 10% полисахаридов клеточной стенки, в основном целлюлозу, арабиноксилан и β-глюкан (Stone and Morell, 2009). Они составляют основные компоненты пищевых волокон, которые не перевариваются и не всасываются в тонком кишечнике, но попадают в толстый кишечник, где они подвергаются бактериальной деградации. Пищевые волокна важны для регуляции уровней глюкозы и инсулина в крови, а также для здоровья кишечника.
[0007] Зерна злаковых, содержащие крахмал с повышенным относительным количеством амилозы, представляют особенный интерес в связи с их пользой для здоровья. Было обнаружено, что пища, содержащая повышенное количество амилозы, имеет более высокие уровни резистентного крахмала (РК), являющегося формой пищевых волокон. РК представляет собой крахмальные или частично расщепленные крахмальные продукты, которые не перевариваются и не всасываются в тонком кишечнике. Становится все более очевидным, что резистентный крахмал играет важную роль в обеспечении здоровья кишечника и в защите против заболеваний, таких как колоректальный рак, диабет II типа, ожирение, заболевание сердца и остеопороз. Были выведены некоторые злаки с высокоамилозным крахмалом, такие как кукуруза и ячмень, для использования в пищевых продуктах и в качестве средства обеспечения здоровья кишечника. Полезное действие резистентного крахмала связано с поставкой питательных веществ в толстый кишечник, где кишечная микрофлора получает источник энергии, который ферментируется с образованием короткоцепочечных жирных кислот. Эти короткоцепочечные жирные кислоты обеспечивают питательные вещества для колоноцитов, увеличивают поглощение некоторых питательных веществ толстым кишечником и стимулируют физиологическую активность толстой кишки. В целом, если в толстую кишку не будут поступать резистентные крахмалы или другие пищевые волокна, она становится относительно метаболически неактивной. Таким образом, высокоамилозные продукты имеют потенциал в отношении обеспечения повышенного потребления волокон. Дополнительная потенциальная польза для здоровья при потреблении высокоамилозных пшеничных зерен или их продуктов, таких как крахмал, включает в себя улучшение регуляции уровней сахара, инсулина и липидов в крови. Кроме того, такая пища может обеспечивать чувство сытости, улучшать перистальтику кишечника, стимулировать рост пробиотических бактерий и усиливать выделение с фекалиями желчных кислот.
[0008] Большинство пищи на основе обработанного крахмала содержит очень мало РК. Хлеб, изготовленный из муки пшеницы дикого типа посредством традиционных процессов замешивания и выпекания, содержит < 1% РК. Для сравнения, хлеб, испеченный с применением таких же процесса и условий хранения, но содержащий высокоамилозную пшеничную муку вследствие снижения активности крахмал-ветвящих ферментов в зернах, имеет уровни РК в 10 раз выше (WO2006/069422). Бобовые, являющиеся одним из нескольких богатых источников РК в рационе человека, имеют уровни РК, обычно составляющие < 5%. Следовательно, потребление высокоамилозного пшеничного хлеба в количествах, которые обычно потребляет взрослый человек (например, 200 г/сутки), легко могло бы обеспечить по меньшей мере 5-12 г РК. Таким образом, включение высокоамилозных пшеничных зерен в пищевые продукты потенциально может сделать существенный вклад в потребление пищевых РК людьми.
[0009] Крахмал изначально синтезируется растениями в хлоропластах фотосинтезирующих тканей, таких как листья, в виде переходной формы крахмала. Она мобилизуется во время последующих темных периодов для поставки углерода для экспорта в акцептирующие органы и энергетического метаболизма или для хранения в органах, таких как семена или корнеплоды. Синтез и долгосрочное хранение крахмала происходит в амилопластах запасающих органов, таких как эндосперм у злаковых, где крахмал откладывается в виде полукристаллических гранул диаметром до 100 мкм. Гранулы содержат как амилозу, так и амилопектин, первую, как правило, в виде аморфного материала в нативных крахмальных гранулах, тогда как последний является полукристаллическим вследствие упаковки линейных глюкозидных цепей. Гранулы также содержат некоторые белки, вовлеченные в биосинтез крахмала.
[0010] В синтез крахмала в эндосперме вовлечено по меньшей мере четыре типа ферментов (Фиг. 1). Во-первых, АДФ-глюкозопирофосфорилаза (АДФГ) катализирует синтез АДФ-глюкозы из глюкозо-1-фосфата и АТФ. Во-вторых, ряд разнообразных крахмальных синтаз (SS, от англ. «starch synthase»; EC 2.4.1.21) катализирует перенос остатков глюкозы от АДФ-глюкозы к невосстанавливающему концу посредством α-1,4-связей для удлинения α-глюкановой цепи. В-третьих, крахмал-ветвящие ферменты (КВФ) образуют новые α-1,6-связи в α-полиглюканах. И наконец, крахмал-деветвящие ферменты (ДВФ) удаляют некоторые из связей разветвлений с помощью механизма, который еще до конца не выяснен.
[0011] Хотя понятно, что для нормального синтеза крахмальных гранул у высших растений необходимы по меньшей мере эти четыре вида активности, в эндосперме высших растений находится множество изоформ каждого из ферментов. Конкретные роли некоторых из ферментов были предположены на основании мутационного анализа или посредством модификации уровней генной экспрессии с применением трансгенных подходов (Abel et al., 1996; Jobling et al., 1999; Schwall et al., 2000). Однако вклад каждого из изоферментов значительно характеризуется среди разных видов и точный вклад каждой изоформы в биосинтез крахмала до сих пор неизвестен. В особенности это касается гексаплоидной обыкновенной пшеницы (Triticum aestivum), которая имеет три набора гомологичных хромосом, определяющих геномы A, B и D. Гексаплоидность считалась существенной помехой при изучении и выведении полезных сортов пшеницы. Действительно, информация относительно того, как взаимодействуют гомологичные гены пшеницы, каким образом регулируется их экспрессия и каким образом разные белки, являющиеся продуктами гомологичных генов, работают по отдельности или в комбинации, является ограниченной.
[0012] У кукурузы, риса и пшеницы ферменты крахмальная синтаза I (SSI), крахмальная синтаза IIa (SSIIa) и крахмальная синтаза IIIa (SSIIIa) участвуют в синтезе амилопектина, возможно, наряду с другими SS. У риса, например, существует 10 разных крахмальных синтаз, включая две связанные с гранулами формы (GBSS). Были выделены мутантные варианты пшеницы, ячменя и риса, дефектные в отношении SSIIa, но эти три вида демонстрируют разное действие на фенотип, получаемый вследствие недостатка SSIIa, в особенности в отношении степени проявления этого действия. Было получено мутантное растение пшеницы ssIIa, в котором полностью отсутствует белок SGP-1 (SSIIa), путем скрещивания линий, в которых отсутствовали специфические для геномов A, B и D формы белка SGP-1 (Yamamori et al., 2000). Тройные нулевые в отношении ssIIa зерна демонстрировали наличие деформированных гранул крахмала, а сам крахмал имел измененную структуру амилопектина. Этот крахмал имел содержание амилозы 30-37% масс./масс., что являлось увеличением приблизительно на 8% относительно уровня дикого типа, и существенно сниженное содержание крахмала (Yamamori et al., 2000). Крахмал из тройных нулевых мутантов ssIIa демонстрировал снижение температуры желатинизации по сравнению с крахмалом из соответствующего зерна дикого типа. Содержание крахмала тройных нулевых в отношении ssIIa зерен было снижено до менее чем 50% относительно по меньшей мере 60% масс./масс. в зерне дикого типа. В работе Yamamori et al., (2000) отсутствуют предположения, что пшеницу, имеющую более чем 45% содержание амилозы в крахмале, можно получать, комбинируя генные мутации ssIIa, в действительности, в Yamamori et al. говорится обратное. Это было подтверждено в работе Konik-Rose et al., (2007), в которой получали максимум 43,98% амилозы в крахмале тройного нулевого мутанта ssIIa, скрещиваемого с вариететом пшеницы Sunco.
[0013] В случае ячменя химически индуцированная нулевая мутация в гене SSIIa сильно снижала синтез амилопектина и тем самым повышала относительное содержание амилозы в крахмале зерна до 65-70% масс./масс. (WO02/37955-A1; Morell et al., 2003). Рис Japonica содержит мутацию SSIIa, которая снижает количество фермента SSIIa в эндосперме по сравнению с рисом Indica, но уровень амилозы в крахмале зерна Japonica не был существенно выше по сравнению с крахмалом зерна Indica. В случае риса комбинация мутаций в генах SBEIIb и SSIIIa оказывала более существенное действие на относительное содержание амилозы (Asai et al., 2014).
[0014] Разное действие нулевых мутаций ssIIa в пшенице, ячмене и рисе было связано с разной степенью плейотропного действия вследствие отсутствия белка SSIIa на разделение ферментов крахмальной синтазы I (SSI) и крахмал-ветвящего фермента IIb (SBEIIb) внутри и за пределами крахмальных гранул в развивающемся эндосперме этих ssIIa-мутантов (Luo et al., 2015). Кроме того, разное действие белков SSI и SBEIIb на посттрансляционном уровне могло влиять на структуру оставшегося амилопектина. Это был один из примеров, когда наблюдения для одного вида злаковых невозможно просто экстраполировать на другие виды злаковых в области синтеза крахмала.
[0015] В случае кукурузы и риса высокоамилозные фенотипы создавали с помощью мутаций в гене SBEIIb, кодирующем крахмал-ветвящий фермент IIb, больше известном как ген удлинения амилозы (ae) (Boyer and Preiss, 1981, Mizuno et al., 1993; Nishi et al., 2001), а не как ген SSIIa. В этих sbeIIb-мутантах содержание амилозы было существенно повышено в пропорции к содержанию крахмала, частота ветвления остаточного амилопектина была снижена и доля коротких цепей (< СП 17, в особенности СП 8-12) была снижена. Кроме того, была повышена температура желатинизации крахмала. Чтобы получить дополнительное повышение уровней амилозы в кукурузе, получали вариететы, имеющие сниженную активность крахмал-ветвящего фермента I (SBEI) наряду с практически полной инактивацией активности SBEII (Sidebottom et al., 1998).
[0016] Пшеницу, имеющую по меньшей мере 50% амилозы в пропорции к содержанию крахмала, получали путем снижения активности одного SBEIIa (Regina et al., 2006), но не снижения активности SBEIIb или SSIIa. В отличие от кукурузы и риса, само по себе снижение SBEIIb в пшенице не приводит к повышению содержания амилозы. В Международной публикации № WO2005/001098 и Международной публикации № WO2006/069422 описана трансгенная гексаплоидная пшеница, содержащая экзогенную дуплексную РНК, которая снижает экспрессию одного из генов SBEIIa и SBEIIb или их обоих в эндосперме. Зерно из трансгенных линий экспрессировало сниженные уровни белков SBEIIa и/или SBEIIb. Снижение количества белка SBEIIa было связано с повышением относительных уровней амилозы более чем на 50%, тогда как отсутствие самого белка SBEIIb, как оказалось, существенно не меняло пропорцию амилозы в крахмале зерна. В Международных публикациях № WO2012/058730 и WO2013/063653 сообщается о получении нетрансгенных тройных нулевых мутантов sbeIIa и/или sbeIIb, в которых практически отсутствует экспрессия белков SBEIIa и SBEIIb, которые демонстрировали повышенные уровни амилозы. Зерно с тройным нулевым генотипом sbeIIa было жизнеспособным при условии, что по меньшей мере одна из генных мутаций sbeIIa была точечной мутацией, а не делецией, выходящей за пределы гена в смежные области. Следовательно, если бы была необходимость в получении высокоамилозной пшеницы, имеющей по меньшей мере 50% амилозы, ген SBEIIa являлся бы геном обыкновенной пшеницы, на который бы происходило нацеливание. Уровни некрахмальных полисахаридов, таких как фруктаны, не были повышены в пшенице, имеющей сниженную активность SBEII и повышенное содержание (> 50%) амилозы в крахмале (например, WO2010/006373).
[0017] В данной области техники существует потребность в улучшенных растениях высокоамилозной пшеницы и в способах их получения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0018] Авторы изобретения неожиданно обнаружили, что гексаплоидное зерно пшеницы с содержанием амилозы по меньшей мере 45%, выраженном в виде массовой процентной доли от общего содержания крахмала в зерне, можно получать, комбинируя мутации в трех генах SSIIa в геномах A, B и D пшеницы путем скрещивания и отбора. Согласно известному уровню техники содержание амилозы в 45% было недостижимым, и в действительности, уровень амилозы в ssIIa-мутантной пшенице в целом составлял 30-38% (Yamamori et al., 2000). По меньшей мере две из этих трех мутаций были нулевыми мутациями, а предпочтительно - все три. Так как связанные с потерей функциональности мутации в SSIIa являются рецессивными, фенотип проявлялся, когда мутации были в гомозиготном состоянии. Авторы изобретения также обнаружили, что ssIIa-мутантное пшеничное зерно имело существенно повышенные уровни некрахмальных полисахаридов, в частности β-глюкана, фруктана, арабиноксилана и целлюлозы, каждый из которых выражен в виде процентной доли от массы зерна. Это приводило к существенному повышению общего содержания волокон, а также к связанному с этим повышению содержания белка и другим выгодным фенотипам.
[0019] Следовательно, в первом аспекте в настоящем изобретении предложено зерно пшеницы вида Triticum aestivum, включающее в себе:
i) мутации в каждом из генов SSIIa, при этом зерно является гомозиготным в отношении мутации в гене SSIIa-A, гомозиготным в отношении мутации в гене SSIIa-B и гомозиготным в отношении мутации в гене SSIIa-D, причем по меньшей мере две из данных мутаций в указанных генах SSIIa являются нулевыми мутациями, предпочтительно все три являются нулевыми мутациями,
ii) общее содержание крахмала, включающее содержание амилозы и содержание амилопектина,
iii) содержание фруктана которое повышено по сравнению с зерном пшеницы дикого типа в массовом отношении, предпочтительно от 3% до 12% массы зерна,
iv) содержание β-глюкана,
v) содержание арабиноксилана и
vi) содержание целлюлозы,
при этом зерно имеет массу зерновок от 25 мг до 60 мг, причем содержание амилозы составляет от 45% и 70% в массовом отношении от общего содержания крахмала зерна при определении анализом связывания йода, содержание амилопектина в массовом отношении снижено по сравнению с зерном пшеницы дикого типа, каждое из содержания β-глюкана, содержания арабиноксилана и содержания целлюлозы повышено по сравнению с зерном пшеницы дикого типа в массовом отношении так, что суммарное содержание фруктана, содержание β-глюкана, содержание арабиноксилана и содержание целлюлозы составляет от 15% до 30% массы зерна.
[0020] В настоящем изобретении дополнительно предложены растения пшеницы, которые способны давать зерно или которые получены из этого зерна, или продукты, такие как мука, отруби, гранулы пшеничного крахмала или пшеничный крахмал, полученные из этого зерна.
[0021] В настоящем изобретении также предложены пищевые ингредиенты, содержащие зерно согласно настоящему изобретению или материал, полученный из этого зерна. Также предложены пищевые продукты, включающие эти пищевые ингредиенты, и композиции, содержащие зерно согласно настоящему изобретению или материал, полученный из этого зерна. Пищевой ингредиент может представлять собой крупноразмолотое, дробленное, пропаренное, плющеное, рушеное, измельченное или молотое зерно или любую комбинацию этих вариантов. Предпочтительным ингредиентом является мука, предпочтительно цельнозерновая, или смесь цельнозерновой муки и муки высшего сорта. Эти ингредиенты имеют повышенный уровень общего содержания волокон по сравнению с соответствующим ингредиентом из пшеницы дикого типа вследствие включения материала из пшеничного зерна согласно изобретению.
[0022] В другом аспекте предложен процесс получения растения пшеницы, способного давать зерно согласно изобретению, включающий этап (i) скрещивания двух родительских растений пшеницы, каждое из которых содержит нулевую мутацию в каждом из одного, двух или трех генов SSIIa, выбранных из группы, состоящей из SSIIa-A, SSIIa-B и SSIIa-D, или воздействие мутагенеза на родительское растение, предпочтительно содержащее одну или две указанные нулевые мутации; и этап (ii) скрининга растений или зерен, полученных при скрещивании или мутагенезе, или полученных от них дочерних растений или зерен, путем анализа ДНК, РНК, белка, гранул крахмала или крахмала, взятых из растений или зерен, и этап (iii) отбора фертильного растения пшеницы, имеющего сниженную активность SSIIa по сравнению по меньшей мере с одним из родительских растений с этапа (i).
[0023] В другом аспекте в настоящем изобретении предложен процесс улучшения одного или более параметров метаболического здоровья, здоровья кишечника или здоровья сердечно-сосудистой системы у нуждающегося в этом субъекта, или предотвращения или снижения тяжести или частоты случаев метаболических заболеваний, таких как диабет, заболевания кишечника или сердечно-сосудистого заболевания, включающий предоставление субъекту зерна или пищевого продукта согласно настоящему изобретению.
[0024] В дополнительном аспекте в настоящем изобретении предложен процесс получения бункеров с пшеничным зерном, включающий:
a) срезание стеблей пшеницы, содержащих пшеничное зерно согласно настоящему изобретению;
b) обмолачивание и/или провеивание стеблей для отделения зерна от мякины; и
c) просеивание и/или сортировку зерна, отделенного на этапе b), и загрузку просеянного и/или отсортированного зерна в бункеры с получением, таким образом, бункеров с пшеничным зерном.
[0025] В вариантах реализации каждого из вышеприведенных аспектов пшеничное зерно дополнительно характеризуется одним или всеми следующими признаками. Содержание амилозы повышено по сравнению с пшеничным зерном дикого типа, например составляет от 48% до 70%, предпочтительно от 50% до 65% от общего содержания крахмала зерна при определении анализом связывания йода. В вариантах реализации содержание амилозы составляет от 50% до 70% или около 48%, около 50%, около 53%, около 55%, около 60% или около 65%. Содержание крахмала зерна снижено по сравнению с пшеничным зерном дикого типа, например составляет по меньшей мере 25%. В вариантах реализации содержание крахмала в зерне согласно изобретению составляет от 30% до 70% массы зерна, от 25% до 65%, от 25% до 60%, от 25% до 55%, от 25% до 50%, от 30% до 70%, от 30% до 65%, от 30% до 60%, от 30% до 55% или от 30% до 50%. В дополнительных вариантах реализации содержание крахмала составляет около 35%, около 40%, около 45%, около 50%, около 55%, около 60% или около 65% в виде процентной доли от массы зерна (масс./масс.). В одном варианте реализации по меньшей мере 50%, предпочтительно по меньшей мере 60% или по меньшей мере 70%, более предпочтительно по меньшей мере 80% крахмальных гранул, полученных из зерна согласно изобретению, имеют искривленную форму и/или морфологию поверхности. Крахмал зерна содержит по меньшей мере 2% резистентного крахмала, предпочтительно по меньшей мере 3% резистентного крахмала, более предпочтительно от 3% до 15% РК или от 3% до 10% РК. Крахмал характеризуется сниженной температурой желатинизации, которую легко измерить методом дифференциальной сканирующей калориметрии (ДСК), например первый пик на ДСК-скане появляется при температуре, на 2-8°C меньшей, чем в случае крахмала дикого типа. В вариантах реализации содержание БГ в зерне представляет содержание β-глюкана и повышено на 1% или 2% по абсолютной величине по сравнению с зерном дикого типа и/или повышено в 2-7 раз по сравнению с пшеничным зерном дикого типа в массовом отношении. В вариантах реализации уровень БГ составляет по меньшей мере 1% или по меньшей мере 2%, предпочтительно от 1% до 4% или от 1% до 5% по массе зерна, предпочтительно около 2%, около 3%, около 4%, более предпочтительно от 2% до 5%. В вариантах реализации содержание арабиноксилана повышено на от 1% до 5% по абсолютной величине и/или содержание целлюлозы повышено на от 1% до 5% по абсолютной величине. В предпочтительном варианте реализации зерно (перед какой-либо обработкой, которая препятствует его прорастанию) имеет степень прорастания, составляющий от около 70% до около 100%, по сравнению с пшеничным зерном дикого типа, при этом зерно при посеве дает растения пшеницы с мужской и женской фертильностью. Каждый из этих фенотипов связан со снижением активности SSIIa во время развития зерна в растении пшеницы в результате мутаций в генах SSIIa.
[0026] Вышеприведенное изложение сущности изобретения не следует никоим образом воспринимать как исчерпывающее перечисление всех вариантов реализации настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[0027] Фигура 1. Схематическое представление ферментов, вовлеченных в синтез крахмала в зернах злаковых, для амилозы и амилопектина.
[0028] Фигура 2. Схематическая генная карта мутации гена SSIIa-A пшеницы в геноме A линии пшеницы C57. Вверху приведена карта экзонов гена SSIIa-A. Ниже представлены нуклеотидные последовательности области гена SSIIa-A из Chinese Spring дикого типа и мутантного вида C57, демонстрирующие делецию 289 нуклеотидов в экзоне 1, включая кодон начала трансляции ATG, и вставку 8 нуклеотидов, при этом суммарный размер делеции составляет 281 нуклеотид. Показаны позиции праймеров JKSS2AP1F и JKSS2AP2R.
[0029] Фигура 3. Схематическая генная карта мутации гена SSIIa-B пшеницы в геноме B линии пшеницы K79. Вверху приведена карта экзонов гена SSIIa-B. Ниже представлены нуклеотидные последовательности области гена SSIIa-B из Chinese Spring (CS) дикого типа и мутантного вида K79, демонстрирующие вставку 179 нуклеотидов в экзон 8 SSIIa-B. Показаны позиции праймеров JKSS2BP7F и JLTSS2BPR1.
[0030] Фигура 4. Схематическая генная карта мутации гена SSIIa-D пшеницы в геноме D линии пшеницы Turkey 116. Вверху приведена карта экзонов гена SSIIa-D. Ниже представлены нуклеотидные последовательности области гена SSIIa-D из Chinese Spring (CS) дикого типа и мутантного вида T116, демонстрирующие делецию 63 нуклеотидов, находящихся в месте соединения экзона 5 и интрона 5 (сайт сплайсинга интрона 5) SSIIa-B. Показаны позиции праймеров JTSS2D3F и JTSS2D4R.
[0100] Фигура 5. Схема программы скрещивания и обратного скрещивания для получения тройных нулевых ssIIa-мутантов в генетическом окружении Sunco.
[0101] Фигура 6. Схема программы скрещивания и обратного скрещивания для получения тройных нулевых ssIIa-мутантов в генетическом окружении EGA Hume.
[0102] Фигура 7. Схема программы скрещивания и обратного скрещивания для получения тройных нулевых ssIIa-мутантов в генетическом окружении Westonia.
[0103] Фигура 8. На верхней панели приведена средняя масса зерна (мг на зерно), а на нижней панели приведено общее содержание липидов (% массы зерна) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0104] Фигура 9. Средние значения по данным Фиг. 8 для генотипов с тройной нулевой мутацией (abd) и генотипа ДТ в генетическом окружении EGA Hume, Sunco и Westonia с указанием стандартного отклонения. Столбики, обозначенные одинаковыми буквами (a, b, c), не характеризуются статистической разницей, тогда как столбики с разными буквами статистически различны.
[0105] Фигура 10. На самой верхней панели приведено содержание амилопектина (% содержания крахмала в массовом отношении), на средней панели приведено содержание амилозы (% содержания крахмала в массовом отношении по методу связывания йода), а на нижней панели приведено общее содержание крахмала (% массы зерна) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0106] Фигура 11. Средние значения по данным Фиг. 10 для генотипов с тройной нулевой мутацией (abd) и генотипа ДТ в генетическом окружении EGA Hume, Sunco и Westonia с указанием стандартного отклонения. Столбики, обозначенные одинаковыми буквами (a, b, c), не характеризуются статистической разницей, тогда как столбики с разными буквами статистически различны.
[0107] Фигура 12. На верхней панели приведено общее содержание волокон (% зерна в массовом отношении), а на нижней панели приведено общее содержание БГ (% зерна в массовом отношении) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0108] Фигура 13. Средние значения по данным Фиг. 12 для генотипов с тройной нулевой мутацией (abd) и генотипа ДТ в генетическом окружении EGA Hume, Sunco и Westonia с указанием стандартного отклонения. Столбики, обозначенные одинаковыми буквами (a, b, c), не характеризуются статистической разницей, тогда как столбики с разными буквами статистически различны.
[0109] Фигура 14. На самой верхней панели приведено содержание фруктана (% зерна в массовом отношении), на средней панели приведено содержание арабиноксилана (% зерна в массовом отношении), а на нижней панели приведено содержание целлюлозы (% зерна в массовом отношении) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0110] Фигура 15. На верхней панели приведена средняя масса зерна (мг на зерно), а на нижней панели приведено общее содержание липидов (мг на зерно) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0111] Фигура 16. Средние значения по данным Фиг. 15 для генотипов с тройной нулевой мутацией (abd) и генотипа ДТ в генетическом окружении EGA Hume, Sunco и Westonia с указанием стандартного отклонения. Столбики, обозначенные одинаковыми буквами (a, b, c), не характеризуются статистической разницей, тогда как столбики с разными буквами статистически различны.
[0112] Фигура 17. На самой верхней панели приведено содержание амилопектина (мг на зерно), на средней панели приведено содержание амилозы (мг на зерно), а на нижней панели приведено общее содержание крахмала (мг на зерно) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0113] Фигура 18. Средние значения по данным Фиг. 17 для генотипов с тройной нулевой мутацией (abd) и генотипа ДТ в генетическом окружении EGA Hume, Sunco и Westonia с указанием стандартного отклонения. Столбики, обозначенные одинаковыми буквами (a, b, c), не характеризуются статистической разницей, тогда как столбики с разными буквами статистически различны.
[0114] Фигура 19. На верхней панели приведено общее содержание волокон (мг на зерно), а на нижней панели приведено общее содержание БГ (мг на зерно) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0115] Фигура 20. Средние значения по данным Фиг. 19 для генотипов с тройной нулевой мутацией (abd) и генотипа ДТ в генетическом окружении EGA Hume, Sunco и Westonia с указанием стандартного отклонения. Столбики, обозначенные одинаковыми буквами (a, b, c), не характеризуются статистической разницей, тогда как столбики с разными буквами статистически различны.
[0116] Фигура 21. На самой верхней панели приведено содержание фруктана (мг на зерно), на средней панели приведено содержание арабиноксилана (мг на зерно), а на нижней панели приведено содержание целлюлозы (мг на зерно) в тройном нулевом зерне ssIIa (abd) и зерне SSIIa дикого типа (ДТ) для отдельных линий пшеницы в генетическом окружении EGA Hume, Sunco и Westonia.
[0117] Фигура 22. Средние значения по данным Фиг. 21 для генотипов с тройной нулевой мутацией (abd) и генотипа ДТ в генетическом окружении EGA Hume, Sunco и Westonia с указанием стандартного отклонения. Столбики, обозначенные одинаковыми буквами (a, b, c), не характеризуются статистической разницей, тогда как столбики с разными буквами статистически различны.
[0001] Фигура 23. Содержание резистентного крахмала в виде процента крахмала в трех выбранных тройных нулевых ssIIa-мутантах (Sunco-abd) и зерне дикого типа (ДТ) в генетическом окружении Sunco. Три мутанта статистически не отличались друг от друга, но были статистически отличными от ДТ.
[0002] Фигура 24. Профили средней мол.% разницы распределения по длинам цепей (РДЦ) для деветвленного крахмала из 5 тройных ssIIa-мутантных линий в сравнении с соответствующим крахмалом дикого типа. Частота появления коротких цепей (СП 6-10) была повышена, тогда как частота появления цепей средней длины (СП 11-24) была снижена для ssIIa-мутантного крахмала по сравнению с соответствующим диким типом.
[0118] Фигура 25. Профили эксклюзионной хроматографии (ЭХ) для крахмала из зерна с тройной нулевой мутацией ssIIa и крахмала из соответствующей пшеницы дикого типа после деветвления крахмалов изоамилазой. Кривые иллюстрируют распределение нормализованных сигналов рефрактометрического индекса (РИ) элюированных фракций в соответствии со степенью их полимеризации (ось X). Первый пик элюирования (I) относится к амилозе, второй (II) относится к длинноцепочечному амилопектину, а пик III относится к амилопектину (деветвленному). Черная кривая относится к ssIIa-мутантному крахмалу, серая кривая относится к крахмалу дикого типа.
[0119] Фигура 26. Иммунологические характеристики белков, связанных с крахмальными гранулами, из зрелых пшеничных зерен мутантной пшеницы ssIIa (B22) и пшеницы дикого типа SSIIa (B70). Верхняя полоса результатов Вестерн-блоттинга была идентифицирована как SSIIa, вторая сверху полоса была идентифицирована как смесь SBEIIa и SBEIIb, а полосы по 70 и 60 кДа представляли SSI и GBSSI по данным их связывания со специфическими антисыворотками. Идентификация каждой полосы помечена и указана стрелками. Идентификация антител, применяемых для разных блотов, приведена слева или под каждой панелью. M: белковый маркер молекулярной массы (кДа).
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0120] SEQ ID NO:1 Аминокислотная последовательность полипептида SSIIa-A, кодируемая геномом A пшеницы; Номер доступа: AAD53263, 799 ак.
[0121] SEQ ID NO:2 Аминокислотная последовательность полипептида SSIIa-B, кодируемая геномом B пшеницы; Номер доступа: CAB96627, 798 ак.
[0122] SEQ ID NO:3 Аминокислотная последовательность полипептида SSIIa-D, кодируемая геномом D пшеницы; Номер доступа: BAE48800, 799 ак; Shimbata et al., (2005).
[0123] SEQ ID NO:4 Нуклеотидная последовательность полноразмерной кДНК гена SSIIa-A пшеницы; 2821 нуклеотидов; Номер доступа: AF155217; Li et al., (1999); нуклеотиды 89-91 стартового кодона трансляции, стоп-кодон 2486-2488.
[0124] SEQ ID NO:5 Нуклеотидная последовательность полноразмерной кДНК гена SSIIa-B пшеницы; 2793 нуклеотида; Номер доступа: AJ269504; Gao and Chibbar, (2000); нуклеотиды 135-137 стартового кодона трансляции, стоп-кодон 2529-2531.
[0125] SEQ ID NO:6 Нуклеотидная последовательность полноразмерной кДНК гена SSIIa-D пшеницы; 2846 нуклеотидов; Номер доступа: AJ269502; Gao and Chibbar, (2000); нуклеотиды 210-212 стартового кодона трансляции, стоп-кодон 2607-2609. Транзитный пептид, кодируемый нуклеотидами 201-384, зрелый пептид 385-2606.
[0126] SEQ ID NO:7 Нуклеотидная последовательность гена SSIIa-A пшеницы; Номер доступа: AB201445; 6898 нт (IWGSC: хромосома 7AS, Traes_7AS_53CAFB43A, от 52346437 п. о. до 52346905 п. о., от 52351676 до 52351931 п. о. обратная цепь).
[0127] SEQ ID NO:8 Нуклеотидная последовательность гена SSIIa-B пшеницы; Номер доступа: AB201446) (IWGSC: хромосома 7DS, Traes_7DS_E6C8AF743, 3877787: 1 до 396 п. о., от 5137 до 5419 п. о. прямая цепь), 6811 нт.
[0128] SEQ ID NO:9 Нуклеотидная последовательность гена SSIIa-D пшеницы; Номер доступа: AB201447) (IWGSC: хромосома 7DS, Traes_7DS_E6C8AF743, 3877787: 1 до 396 п. о., от 5137 до 5419 п. о. прямая цепь), 6950 нт.
[0129] SEQ ID NO:10 Аминокислотная последовательность SSIIb-A пшеницы, кодируемая геномом A, 676 ак, получена по нуклеотидной последовательности с Номером доступа AK332724.
[0130] SEQ ID NO:11 Аминокислотная последовательность SSIIb-D пшеницы, кодируемая геномом D, 674 ак, Номер доступа ABY56824 (которая имеет 100% идентичность с EU333947).
[0131] SEQ ID NO:12 Нуклеотидная последовательность полноразмерной кДНК гена SSIIb-A в геноме А пшеницы; Номер доступа: AK332724. 2727 нт (IWGSC: хромосома 6AL, Traes_6AL_AE01DC0EA, от 187500495 п. о. до 187505249 п. о. прямая цепь).
[0132] SEQ ID NO:13 Нуклеотидная последовательность частичной кДНК SSIIb-B в геноме B пшеницы; 1282 нт, IWGSC: хромосома 6DL, ген: Traes_6BL_61D83E262, от 162113784 п. о. до 162116959 п. о. обратная цепь).
[0133] SEQ ID NO:14 Нуклеотидная последовательность полноразмерной кДНК SSIIb-D в геноме D пшеницы; 2025 нт (Номер доступа: EU333947) (IWGSC: хромосома 6DL, ген: Traes_6DL_19F1042C7, от 147°049°693 п. о. до 147°051°708 п. о. обратная цепь).
[0134] SEQ ID NO:15-49 Олигонуклеотидные праймеры.
[0135] SEQ ID NO:50-51 Аминокислотные последовательности пептидов.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0136] В тексте этого описания, если контекст не требует иного, слово «содержать» или его вариации, такие как «содержит» или «содержащий», следует понимать как подразумевающее включение указанного элемента или целого числа, или группы элементов или целых чисел, но не исключение любого другого элемента или целого числа, или группы элементов или целых чисел. Под выражением «состоящий из» подразумевается включение и ограничение теми элементами, которые следуют за выражением «состоящий из». Таким образом, выражение «состоящий из» указывает на то, что перечисленные элементы являются необходимыми или обязательными и не могут присутствовать никакие другие элементы. Под выражением «состоящий преимущественно из» подразумевается включение любых элементов, перечисленных после этого выражения, и ограничение в отношении других элементов теми, которые не препятствуют или не способствуют активности или действию, указанным в описании для перечисленных элементов. Таким образом, выражение «состоящий по существу из» указывает на то, что перечисленные элементы являются необходимыми или обязательными, но любые другие элементы являются необязательными и могут присутствовать или нет в зависимости от того, влияют ли они на активность или действие перечисленных элементов.
[0137] В контексте данного документа формы единственного числа включают множественные аспекты и наоборот, если иное четко не следует из контекста. Таким образом, например, ссылка на «мутацию» включает одну мутацию, а также две или более мутаций; ссылка на «растение» включает одно растение, а также два или более растений; и так далее.
[0138] В контексте данного документа подразумевается, что термин «около» в отношении числового значения или диапазона охватывает числа, попадающие в пределы ± 10% от указанного числового значения или диапазона.
[0139] Каждый вариант реализации в этом описании следует применять mutatis mutandis (с соответствующими изменениями) к каждому другому варианту реализации, если четко не указано иное.
[0140] Гены и другой генетический материал (например, мРНК, конструкции и т. д.) выделены курсивом, а белковые продукты их экспрессии представлены без выделения курсивом. Таким образом, например, SSIIa является продуктом экспрессии SSIIa.
[0141] Ссылки на нуклеотидные и аминокислотные последовательности приведены с помощью идентификационного номера последовательности (SEQ ID NO:). SEQ ID NO: численно соответствуют идентификаторам последовательностей <400>1 (SEQ ID NO:1), <400>2 (SEQ ID NO:2), и т. д. Перечень последовательностей приведен после формулы изобретения. Перечень с описанием SEQ ID NO в перечне последовательностей приведен после подписей к фигурам.
[0142] Если не указано иное, все употребляемые в данном документе технические и научные термины имеют значение, обычно подразумеваемое специалистами в области техники, к которой относится это изобретение. Хотя при практической реализации или испытании настоящего изобретения можно использовать любые способы и материалы, аналогичные или эквивалентные описанным в данном документе, ниже описаны предпочтительные способы и материалы.
[0143] Настоящее изобретение частично основано на неожиданном открытии, сделанном в описанных в данном документе экспериментах, что возможно получение гексаплоидного зерна пшеницы, содержащего нулевые мутации в каждом из трех генов SSIIa, которое имеет содержание амилозы, составляющее по меньшей мере 45% (масс./масс.). Это было неожиданным, учитывая результаты, полученные другими исследователями, что уровень амилозы в тройном нулевом ssIIa гексаплоидном зерне пшеницы был меньше 45% (Yamamori et al., 2000; Konik-Rose et al., 2007). В этом случае содержание амилозы определяется в виде процентной доли от общего содержания крахмала в зерне на основании соотношения масса/масса. Кроме того, пшеничное зерно имеет другие необходимые свойства, включая повышенное общее содержание волокон, обусловленное повышением содержания фруктана, β-глюкана, арабиноксилана и целлюлозы, что обеспечивает пользу для здоровья при употреблении зерна или полученных из зерна продуктов в виде пищи или корма.
[0144] Соответственно, в первом аспекте в настоящем изобретении предложено зерно пшеницы вида Triticum aestivum, содержащее:
i) мутации в каждом из генов SSIIa, при этом зерно является гомозиготным в отношении мутации в гене SSIIa-A, гомозиготным в отношении мутации в гене SSIIa-B и гомозиготным в отношении мутации в гене SSIIa-D, причем по меньшей мере две из данных мутаций в указанных генах SSIIa являются нулевыми мутациями,
ii) общее содержание крахмала, включающее содержание амилозы и содержание амилопектина,
iii) содержание фруктана, которое повышен по сравнению с зерном пшеницы дикого типа в массовом отношении, предпочтительно от 3% до 12% массы зерна,
iv) содержание β-глюкана,
v) содержание арабиноксилана и
vi) содержание целлюлозы,
при этом зерно имеет массу зерновок от 25 мг до 60 мг, причем содержание амилозы составляет от 45% и 70% в массовом отношении от общего содержания крахмала зерна при определении анализом связывания йода, содержание амилопектина в массовом отношении снижено по сравнению с зерном пшеницы дикого типа, каждое из содержания β-глюкана, содержания арабиноксилана и содержания целлюлозы повышено по сравнению с зерном пшеницы дикого типа в массовом отношении так, что суммарное содержание фруктана, содержание β-глюкана, содержание арабиноксилана и содержание целлюлозы составляет от 15% до 30% массы зерна.
[0145] В настоящем изобретении дополнительно предложены растения пшеницы, которые получены из этого зерна, и мука и/или гранулы пшеничного крахмала, полученные из этого зерна.
[0146] В настоящем изобретении также предложены пищевые ингредиенты, содержащие зерно согласно настоящему изобретению или материал, полученный из этого зерна. Также предложены пищевые продукты, включающие эти пищевые ингредиенты, и композиции, содержащие зерно согласно настоящему изобретению или материал, полученный из этого зерна. Пищевой ингредиент может представлять собой крупноразмолотое, дробленное, пропаренное, плющеное, рушеное, измельченное или молотое зерно или любую комбинацию этих вариантов.
[0147] В другом аспекте в настоящем изобретении предложен процесс получения растения пшеницы, которое дает зерно согласно настоящему изобретению, включающий этап (i) скрещивания двух родительских растений пшеницы, каждое из которых содержит нулевую мутацию в каждом из одного, двух или трех генов SSIIa, выбранных из группы, состоящей из SSIIa-A, SSIIa-B и SSIIa-D, или воздействие мутагенеза на родительское растение, содержащее указанные нулевые мутации; и этап (ii) скрининга растений или зерен, полученных при скрещивании или мутагенезе, или полученных от них дочерних растений или зерен, путем анализа ДНК, РНК, белка, гранул крахмала или крахмала, взятых из растений или зерен, и этап (iii) отбора фертильного растения пшеницы, имеющего сниженную активность SSIIa по сравнению по меньшей мере с одним из родительских растений пшеницы с этапа (i).
[0148] В другом аспекте в настоящем изобретении предложен процесс улучшения одного или более параметров метаболического здоровья, здоровья кишечника или сердечно-сосудистого здоровья у нуждающегося в этом субъекта, или предотвращения или снижения тяжести или частоты случаев метаболических заболеваний, таких как диабет, заболевания кишечника или сердечно-сосудистые заболевания, включающий предоставление субъекту зерна или пищевого продукта согласно настоящему изобретению.
[0149] В контексте данного документа «улучшение одного или более параметров метаболического здоровья» является относительным термином и означает улучшение по сравнению с потреблением эквивалентного количества пищи или напитков, полученных из пшеницы дикого типа.
[0150] В дополнительном аспекте в настоящем изобретении предложен процесс получения бункеров с пшеничным зерном, включающий:
a) срезание стеблей пшеницы, содержащих пшеничное зерно согласно настоящему изобретению;
b) обмолачивание и/или провеивание стеблей для отделения зерна от мякины; и
c) просеивание и/или сортировку зерна, отделенного на этапе b), и загрузку просеянного и/или отсортированного зерна в бункеры с получением, таким образом, бункеров с пшеничным зерном.
[0151] В определенных вариантах реализации пшеничное зерно согласно настоящему изобретению дополнительно характеризуется одним или более или всеми из следующих признаков:
i) содержание крахмала от 30% до 70% массы зерна,
ii) содержание амилозы составляет от 45% до 65% от общего содержания крахмала в зерне при определении анализом связывания йода,
iii) содержание крахмала имеет распределение по длинам цепей при определении методом капиллярного электрофореза с активацией флуоресценцией (FACE) после деветвления образцов крахмала, в котором увеличена доля длин цепей с СП 7-10 и снижена доля длин цепей с СП 11-24 по сравнению с крахмалом пшеницы дикого типа,
iv) содержание фруктана включает фруктан с СП 3-12 так, что по меньшей мере 50% содержания фруктана представлено СП 3-12,
v) содержание фруктана повышено в 2-10 раз по сравнению с пшеничным зерном дикого типа в массовом отношении,
vi) содержание β-глюкана повышено на 1% или 2% по абсолютной величине и/или повышено в 2-7 раз по сравнению с пшеничным зерном дикого типа в массовом отношении,
vii) содержание β-глюкана составляет от 1% до 4% массы зерна,
viii) содержание арабиноксилана повышено на 1% - 5% по абсолютной величине,
ix) содержание целлюлозы повышено на 1% - 5% по абсолютной величине,
x) зерно имеет степень прорастания от около 70% до около 100% по сравнению с пшеничным зерном дикого типа и
xi) зерно при посеве дает растения пшеницы с мужской и женской фертильностью.
[0152] Зерно также может характеризоваться уровнем и/или активностью белка SSIIa, которые составляют менее 5% от уровня или активности белка SSIIa в зерне пшеницы дикого типа, или в которых отсутствует один или более, или все из белка SSIIa-A, белка SSIIa-B и белка SSIIa-D. Зерно также может быть гомозиготным в отношении нулевой мутации в гене SSIIa-A, гомозиготным в отношении нулевой мутации в гене SSIIa-B и гомозиготным в отношении нулевой мутации в гене SSIIa-D. Каждая нулевая мутация может быть независимо выбрана из группы, состоящей из мутации с делецией, мутации со вставкой, стоп-кодона преждевременной терминации трансляции, мутации сайта сплайсинга и мутации с неконсервативной аминокислотной заменой, предпочтительно зерно при этом содержит мутации с делециями в каждом из двух или трех генов SSIIa, или полные делеции этих генов.
[0153] В определенных вариантах реализации зерно дополнительно содержит мутацию с потерей функции в эндогенном гене, который кодирует полипептид синтеза крахмала, или химерный полинуклеотид, который кодирует РНК, снижающую экспрессию эндогенного гена, который кодирует полипептид синтеза крахмала, при этом указанный полипептид синтеза крахмала выбран из группы, состоящей из SSI, SSIIIa и SSIV, причем указанная мутация выбрана из группы, состоящей из мутации с делецией, мутации со вставкой, стоп-кодона преждевременной терминации трансляции, мутации сайта сплайсинга и мутации с неконсервативной аминокислотной заменой. Предпочтительно, чтобы по меньшей мере одна, более чем одна или все мутации представляли собой i) внесенные мутации, ii) были индуцированы в родительских растениях пшеницы или семенах посредством мутагенеза с помощью мутагенного агента, такого так химический агент, биологический агент или облучение, или iii) были внесены, чтобы модифицировать геном растения.
[0154] Предпочтительно, чтобы зерно имело содержание амилозы около 60% по массе от общего содержания крахмала в зерне и/или чтобы зерно не было трансгенным или не содержало никакую экзогенную нуклеиновую кислоту, кодирующую РНК, которая снижает экспрессию гена SSIIa и/или гена SBEIIa.
[0155] Уровень и/или активность SSIIa определяют, анализируя уровень и/или активность SSIIa в развивающемся эндосперме или анализируя количество белка SSIIa в собранном зерне иммунологическими или другими способами. Эндосперм может принадлежать растению, из которого было получено зерно, или дочернему растению.
[0156] Крахмальные гранулы зерна и/или крахмал из зерна согласно настоящему изобретению также могут характеризоваться одним или более свойствами, выбранными из группы, состоящей из:
i) содержание по меньшей мере 2% резистентного крахмала;
ii) крахмал характеризуется сниженным гликемическим индексом (ГИ);
iii) крахмальные гранулы имеют деформированную форму;
iv) крахмальные гранулы имеют сниженное двулучепреломление при наблюдении в поляризованном свете;
v) крахмал характеризуется сниженным объемным разбуханием;
vi) модифицированные распределение по длинам цепей и/или частота ветвления в крахмале;
vii) крахмал характеризуется сниженной пиковой температурой желатинизации;
viii) крахмал характеризуется сниженной пиковой вязкостью;
ix) снижена температура клейстеризации крахмала;
x) снижена пиковая молекулярная масса амилозы при определении методом эксклюзионной хроматографии;
xi) снижена степень кристаллизации крахмала; и
xii) снижена доля крахмала A-типа и/или B-типа, и/или повышена доля кристаллического крахмала V-типа;
при этом каждое свойство определяется в сравнении с крахмальными гранулами пшеницы дикого типа или крахмалом пшеницы дикого типа.
[0157] В определенных вариантах реализации настоящего изобретения зерно обрабатывают так, чтобы оно не могло прорастать. Примеры такого обработанного зерна включают термически обработанное зерно и крупноразмолотое, дробленное, пропаренное, плющеное, рушеное, измельченное или молотое зерно. В альтернативном варианте способность зерна к прорастанию составляет от 70% до 100% по сравнению с диким типом.
[0158] Настоящее изобретение явным образом распространяется на описанное выше зерно, содержащееся в растении пшеницы. Настоящее изобретение также распространяется на растения пшеницы, которые дают зерно или получены из зерна согласно настоящему изобретению. Такие растения пшеницы могут характеризоваться уровнем и/или активностью белка SSIIa в своем эндосперме, которые составляют менее 5% от уровня или активности белка SSIIa в зерне пшеницы дикого типа, или в которых отсутствует один или более, или все из белка SSIIa-A, белка SSIIa-B и белка SSIIa-D. Предпочтительно растение пшеницы характеризуется мужской и женской фертильностью.
[0159] Также включена мука, полученная из зерна согласно настоящему изобретению. В одном варианте реализации мука является мукой высшего сорта. Мука предпочтительно является цельнозерновой или представляет собой смесь муки высшего сорта и цельнозерновой, например, в соотношении от 1:2 до 2:1. В изобретении также предложены пшеничные отруби из зерна согласно изобретению. Каждый из этих продуктов содержит клетки пшеницы, имеющие набор генов пшеничного зерна (т. е. ДНК пшеничного зерна).
[0160] Гранулы пшеничного крахмала или пшеничный крахмал, полученные из зерна, также являются частью настоящего изобретения. Гранулы пшеничного крахмала или пшеничный крахмал, как правило, содержат 45%, предпочтительно около 50%, около 55% или около 60% амилозы, или от 45% до 70% амилозы, каждое значение в массовом отношении в виде доли от общего содержания крахмала гранул крахмала или крахмала, причем гранулы крахмала предпочтительно содержат полипептид GBSSI пшеницы. Гранулы крахмала и/или крахмал также могут характеризоваться одним или более из следующего:
a) отсутствие выявляемого полипептида SSIIa при определении иммунологическими способами;
b) содержание по меньшей мере 2% резистентного крахмала в массовом отношении;
c) крахмал характеризуется сниженным гликемическим индексом (ГИ);
d) крахмальные гранулы имеют деформированную форму;
e) крахмальные гранулы имеют сниженное двулучепреломление при наблюдении в поляризованном свете;
f) крахмал характеризуется сниженным объемным разбуханием;
g) модифицированные распределение по длинам цепей и/или частота ветвления в крахмале;
h) крахмал характеризуется сниженной пиковой температурой желатинизации;
i) крахмал характеризуется сниженной пиковой вязкостью;
j) снижена температура клейстеризации крахмала;
k) снижена пиковая молекулярная масса амилозы при определении методом эксклюзионной хроматографии;
l) снижена степень кристаллизации крахмала; и
m) снижена доля крахмала A-типа и/или B-типа и/или повышена доля кристаллического крахмала V-типа;
при этом каждое свойство определяется в сравнении с крахмальными гранулами или крахмалом пшеницы дикого типа.
[0161] В настоящем изобретении также предложен пищевой ингредиент, который содержит зерно, муку, предпочтительно цельнозерновую, или пшеничные отруби, или гранулы пшеничного крахмала или пшеничный крахмал согласно настоящему изобретению, предпочтительно на уровне, составляющем по меньшей мере 10%, предпочтительно от около 20% до около 80% на основании сухой массы. Пищевой ингредиент может представлять собой крупноразмолотое, дробленное, пропаренное, плющеное, рушеное, измельченное или молотое зерно или любую комбинацию этих вариантов. Пищевой ингредиент также может быть включен в пищевой продукт, предпочтительно на уровне по меньшей мере 10% на основании сухой массы.
[0162] В настоящем изобретении также предложена композиция, содержащая зерно пшеницы, муку, предпочтительно цельнозерновую, или пшеничные отруби, или гранулы пшеничного крахмала или пшеничный крахмал согласно настоящему изобретению на уровне, составляющем по меньшей мере 10% по массе, или зерно пшеницы, имеющее уровень амилозы менее 45% (масс./масс.), или полученные из него муку, цельнозерновую муку, гранулы крахмала или крахмал. Композиция может содержать смесь разных видов муки.
[0163] В настоящем изобретении также предложен процесс получения пищевого продукта, включающий этапы (i) добавления пищевого ингредиента согласно настоящему изобретению к другому пищевому ингредиенту и (ii) смешивания пищевых ингредиентов с получением, таким образом, пищевого продукта. Процесс также может включать этап обработки зерна для получения пищевого ингредиента перед этапом (i), или этап нагревания смешанных пищевых ингредиентов с этапа (ii) при температуре, составляющей по меньшей мере 100°C, в течение по меньшей мере 10 минут.
[0164] В контексте данного документа термин «по массе» или «в массовом отношении» относится к массе вещества в виде процентной доли от массы материала или компонента, содержащего указанное вещество. В данном документе это сокращенно обозначается «масс./масс.». Например, содержание амилозы определяется как масса амилозы в виде процентной доли от общего содержания крахмала.
[0165] Синтез крахмала в эндосперме высших растений, включая пшеницу, происходит посредством набора ферментов, которые катализируют четыре ключевых этапа, схематически показанных на Фиг. 1. Во-первых, АДФ-глюкозо-пирофосфорилаза (EC 2.7.7.27) активирует мономерный предшественник крахмала посредством синтеза АДФ-глюкозы из G-1-P и АТФ. Во-вторых, активированный глюкозильный донор, АДФ-глюкоза, переносится к невосстанавливающему концу уже существующей α-1,4-связи крахмальными синтазами (EC 2.4.1.24). В-третьих, крахмал-ветвящие ферменты вносят точки ветвления посредством расщепления области α-1,4-связанного глюкана с последующим переносом отщепленной цепи к акцепторной цепи с образованием новой α-1,6-связи. Крахмал-ветвящие ферменты являются единственными ферментами, которые могут вносить α-1,6-связи в α-полиглюканы, и, следовательно, играют важную роль в образовании амилопектина. В-четвертых, крахмал-деветвящие ферменты (EC 2.4.4.18) удаляют некоторые связи ветвления.
[0166] В эндосперме злаковых присутствуют две формы АДФ-глюкозо-пирофосфорилазы (АДФП), одна форма в амилопластах, а одна форма в цитоплазме. Каждая форма состоит из двух типов субъединиц. Морщинистые (sh2) и хрупкие (bt2) мутанты кукурузы представляют поражения в большой и малой субъединицах соответственно.
[0167] В контексте данного документа термин «крахмальная синтаза» относится к ферменту, который переносит глюкозильный остаток от активированного глюкозильного донора, АДФ-глюкозы, к невосстанавливающему концу предсуществующей глюкановой цепи посредством α-1,4-связи (EC 2.4.1.24). Активность фермента КС можно анализировать, как описано у Guan and Keeling (1998). В эндосперме злаковых, включая гексаплоидную пшеницу T. aestivum, обнаружено по меньшей мере пять классов крахмальных синтаз, а именно изоформу, локализованную исключительно в гранулах крахмала или связанную с ними, связанную с гранулами крахмальную синтазу (GBSS), две формы, которые разделены между гранулой и растворимой фракцией (SSI и SSII), форму, которая целиком локализована в растворимой фракции (SSIII), и недавно обнаруженную пятую форму, SSIV (Фиг. 1). Каждая из них включена в термин «крахмальная синтаза». Они активны во время развития эндосперма во время роста растения пшеницы, когда происходит синтез и отложение запасов крахмала, но могут присутствовать в неактивном состоянии в зрелом (находящемся в состоянии покоя) зерне пшеницы. Было показано, что GBSS важна для синтеза амилозы. Каждая из SSI-IV участвует, в первую очередь, в синтезе амилопектина согласно биохимическим и генетическим данным. Например, было показано, что мутации в генах SSII и SSIII меняют структуру амилопектина (Schondelmaier et al., 1992; Yamamori et al., 2000). Крахмальные синтазы классифицируют в соответствии с их аминокислотной последовательностью как принадлежащие к одной из этих пяти групп на основании степени гомологии с известными представителями этих классов.
[0168] Среди злаковых было идентифицировано по меньшей мере два подкласса SSII, SSIIa и SSIIb, хотя в рисе был идентифицирован третий подкласс SSIIc (Ohdan et al., 2005), а гены, которые, вероятно, кодируют соответствующий фермент SSIIc в пшенице, идентифицированы, как описано в примере 2. Крахмальная синтаза IIa (SSIIa), главным образом, катализирует полимеризацию глюкановых цепей средней длины (СП 12-24) амилопектина в эндосперме злаковых посредством переноса глюкозильного фрагмента от АДФ-глюкозы к невосстанавливающему концу уже существующих α-1,4-связанных глюкановых цепей (Fontaine et al., 1993). SSIIa, таким образом, удлиняет короткие цепи (СП < 10) амилопектина. В ssIIa-мутанте пшеницы была повышена частота появления глюкановых цепей с СП 6-11 и снижена частота появления цепей с СП 11-25 (Yamamori et al, 2000). Разные классы SSII различаются по своей гомологии с аминокислотными последовательностями типичных представителей каждого класса, т. е. по филогенетическому анализу. Разные ферменты SSII и, в некоторых случаях, разные изоферменты SSIIa пшеницы могут отличаться числом аминокислот в полипептидах, как описано ниже.
[0169] Уровень экспрессии генов, кодирующих SSII или, в частности, SSIIa, можно оценить, анализируя уровни транскриптов, например, с помощью анализа гибризидации методом Нозерн-блоттинга или анализа методом ОТ-ПЦР. В предпочтительном способе количество белка SSIIa в зерне или развивающемся эндосперме определяют, разделяя белки в экстрактах зерна/эндосперма в геле посредством электрофореза, затем перенося белки на мембрану с помощью Вестерн-блоттинга с последующим количественным выявлением белка на мембране с применением специфических антител («Вестерн-блот-анализ»). Типовые способы гель-электрофореза и иммуноблоттинга описаны в примере 1.
[0170] Крахмальная синтаза I (SSI), вероятно, существует в злаковых в одной изоформе. В рисе на SSI приходится около 70% активности всех растворимых SS в эндосперме (Fujita et al, 2006). SSI преимущественно синтезирует короткие глюкановые цепи с СП 6-15, предпочитая в качестве субстрата самые короткие цепи амилопектина. Несмотря на важную роль полное отсутствие фермента SSI в эндосперме риса не влияет на размер и форму семян или гранул крахмала, что позволяет предположить, что другие ферменты SS способны компенсировать отсутствие функции SSI.
[0171] В противоположность этому, SSIII вырабатывает относительно длинные цепи амилопектина, в частности с СП > 30, и удлиняет глюкановые цепи средней длины. Мутанты ssIII демонстрируют увеличение цепей средней длины в амилопектине. Существует две формы, из которых SSIIIa является основной формой, экспрессируемой в эндосперме, а SSIIIb является второстепенной формой. О вкладе изоформ SSIV в длину глюкановых цепей в зерне злаковых известно мало, но, вероятно, ее функция проявляется преимущественно в листьях (Leterrier et al., 2008). Два гена SSIV, SSIVa и SSIVb, экспрессируются в рисе во всем растении целиком и на относительно постоянных уровнях во время наливания зерна, поэтому вероятно, что их функция проявляется во всем растении целиком. Мутанты ssIV в Arabidopsis имели сниженные уровни крахмала в листьях.
[0172] Каждая из крахмальных синтаз экспрессируется в виде полипептидов с N-концевыми сигнальными пептидами, которые отщепляются во время перемещения в амилопласты.
[0173] В контексте данного документа «крахмал-ветвящий фермент» (SBE - от англ. «starch branching enzyme») означает фермент, который вносит α-1,6 гликозидные связи между цепями из остатков глюкозы (EC 2.4.1.18), внося, таким образом, α-1,6 точки ветвления в амилопектин. Известно два основных класса SBE у растений, SBEI и SBEII. У злаковых SBEII можно дополнительно отнести к двум типам, SBEIIa и SBEIIb (Hedman and Boyer, 1982; Boyer and Preiss, 1978; Mizuno et al., 1992, Sun et al., 1997). Также сообщалось о дополнительных формах SBE у некоторых злаковых, предполагаемом SBEI размером 149 кДа из пшеницы и SBE размером 50/51 кДа из ячменя. Выравнивание последовательностей позволило выявить высокую степень сходства как на нуклеотидном, так и на аминокислотном уровнях, и позволило провести группирование по классам SBEI, SBEIIa и SBEIIb. Аминокислотные последовательности SBEIIa и SBEIIb в общем случае демонстрируют около 80% идентичности друг с другом, сконцентрированной в основном в центральных областях полипептидов.
[0174] SBEI, SBEIIa и SBEIIb также можно различать по профилю их экспрессии, но этот аспект характеризуется для разных видов. В эндосперме пшеницы SBEI (Morell et al, 1997) обнаружен исключительно в растворимой фракции, тогда как SBEIIa и SBEIIb обнаружены как в растворимой, так и в связанной с крахмальными гранулами фракциях (Rahman et al., 1995). В кукурузе SBEIIb является преобладающей формой в эндосперме, тогда как SBEIIa экспрессируется относительно сильнее в листьях и, вероятно, экспрессируется во всем растении (Gao et al., 1997). В рисе SBEIIa и SBEIIb можно обнаружить в эндосперме в приблизительно одинаковых количествах. Однако существует также разница во времени генной экспрессии. SBEIIa экспрессируется на более ранней стадии развития семени, регистрируется через 3 дня после цветения и экспрессируется в листьях, тогда как SBEIIb не регистрировался через 3 дня после цветения и не был распространен в развивающихся семенах через 7-10 суток после цветения, и не экспрессировался в листьях. В эндосперме пшеницы SBEIIa экспрессируется приблизительно в 3-4 раза сильнее, чем SBEIIb. Разные виды злаковых демонстрируют существенную разницу в экспрессии SBEIIa и SBEIIb, а выводы, сделанные по одному виду, нельзя применять к другим видам. Для того, чтобы различать ферменты, также можно использовать специфические антитела.
[0175] Были получены характеристики последовательностей геномной ДНК и кДНК для каждого из генов SBE за исключением пшеницы. Выравнивание последовательностей позволило выявить высокую степень сходства последовательностей как на нуклеотидном, так и на аминокислотном уровнях, но также и различия в последовательностях, и позволило провести группирование по классам SBEI, SBEIIa и SBEIIb. В пшенице наблюдаемые явления дупликации генов повышают число генов SBEI в каждом геноме (Rahman et al., 1999). Элиминация более чем 97% активности SBEI в эндосперме пшеницы посредством комбинации мутаций в наиболее экспрессирующих формах генов SBEI из геномов A, B и D не оказывала определимого влияния на структуру или функциональность крахмала (Regina et al., 2004). В противоположность этому, снижение экспрессии SBEIIa с помощью конструкции для сайленсинга генов в гексаплоидной пшенице приводило к высоким уровням амилозы (> 70%), тогда как соответствующая конструкция, которая снижала экспрессию SBEIIb, но не SBEIIa, оказывала минимальное действие (Regina et al., 2006). В ячмене конструкцию для сайленсинга генов, которая снижала экспрессию SBEIIa и SBEIIb в эндосперме, использовали для создания высокоамилозного зерна ячменя (Regina et al., 2010). В кукурузе мутанты SBEIIb, известные как удлинители амилозы (ae), обуславливали высокоамилозные фенотипы.
[0176] Анализ ферментативной активности ветвящих ферментов для выявления активности всех трех изоформ, SBEI, SBEIIa и SBEIIb, основан на способе Nishi et al., 2001 с небольшими следующими модификациями. После электрофореза гель дважды промывают в 50 мМ ГЭПЕС, pH 7,0, содержащем 10% глицерина, и инкубируют при комнатной температуре в реакционной смеси, состоящей из 50 мМ ГЭПЕС, pH 7,4, 50 мМ глюкозо-1-фосфата, 2,5 мМ АМФ, 10% глицерина, 50 Ед. фосфорилазы a, 1 мМ ДТТ и 0,08% мальтотриозы в течение 16 ч. Полосы визуализируют с помощью раствора 0,2% (масс./об.) I2 и 2% KI. Специфические для изоформ SBEI, SBEIIa и SBEIIb виды активности разделяют в этих условиях электрофореза. Это подтверждается иммуноблоттингом с применением анти-SBEI, анти-SBEIIa и анти-SBEIIb антител. Денситометрический анализ иммуноблотов, в котором измеряется интенсивность каждой полосы, проводят для определения уровня ферментативной активности каждой изоформы.
[0177] Активность крахмал-ветвящих ферментов (SBE) можно определять с помощью ферментативного анализа, например, с помощью анализа стимуляции фосфорилазы (Boyer and Preiss, 1978). В этом анализе измеряют стимуляцию SBE включения глюкозо-1-фосфата в метанол-нерастворимый полимер (α-D-глюкан) фосфорилазой A. Изоформы SBE демонстрируют разную специфичность в отношении субстрата, например SBEI демонстрирует более высокую активность в ветвлении амилозы, тогда как SBEIIa и SBEIIb демонстрируют более высокие уровни ветвления с субстратом из амилопектина. SBEI преимущественно вырабатывает более длинные цепи с СП > 16 посредством ветвления менее разветвленных полиглюканов, тогда как изоферменты SBEII генерируют более короткие цепи с СП < 12. Эти изоформы также можно различать на основании длины переносимой глюкановой цепи.
[0178] У злаковых известно два класса деветвящих ферментов (DBE - от англ. «debranching enzyme»), а именно - изоамилаза (ISA) и пуллуланаза (PUL). ISA, главным образом, обеспечивает деветвление фитогликогена и амилопектина, тогда как PUL действует на пуллулан и амилопектин, но не на фитогликоген (Nakamura et al., 1996). Мутанты в отношении ISA были названы сахарными и вырабатывают более короткие цепи амилопектина, и, следовательно, действие ISA, вероятно, состоит в редактировании излишне разветвленных цепей или неправильных цепей в амилопектине. В противоположность этому, считается, что PUL функционирует при разрушении крахмала в прорастающих зернах, а также при синтезе крахмала.
[0179] Развивающийся эндосперм гексаплоидной пшеницы экспрессирует SSIIa из генов SSIIa в каждом из геномов A, B и D. В контексте данного документа «SSIIa, экспрессируемый из генома A» или «SSIIa-A» означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO:1 или который по меньшей мере на 99% идентичен аминокислотной последовательности, приведенной в SEQ ID NO: 1, или содержит такую последовательность. Аминокислотная последовательность, приведенная как SEQ ID NO:1 (Li et al., 1999; № доступа в Genbank AAD53263), используется в данном документе в качестве эталонной последовательности для полипептида SSIIa-A дикого типа. Длина полипептида с SEQ ID NO:1 составляет 799 аминокислотных остатков, как и в случае мутантов с аминокислотными заменами в SEQ ID NO:1. Ферментативно активные варианты этого фермента существуют в пшенице, например в сорте Fielder, смотрите № доступа CAB96626.1 (Gao and Chibbar, 2000), чья аминокислотная последовательность на 99,5% (795/799) идентична SEQ ID NO.1, и в диплоидных родственных формах Triticum aestivum, таких как из Triticum urartu, приведенных под № доступа CUS28065.1 и CDI68213.1. Такие варианты включены в «SSIIa-A». SSIIa-A не включает гомологичные полипептиды, SSIIa-B и SSIIa-D, так как эти полипептиды являются на около 96% идентичными с SEQ ID NO:1.
[0180] В контексте данного документа «SSIIa, экспрессируемый из генома B» или «SSIIa-B» означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO:2 или который по меньшей мере на 99% идентичен аминокислотной последовательности, приведенной в SEQ ID NO:2, или содержит такую последовательность. Аминокислотная последовательность, приведенная как SEQ ID NO:2 (№ доступа в Genbank CAB99627.1) соответствует крахмальной синтазе IIa, экспрессируемой из генома B пшеницы вариетета Fielder, которая используется в данном документе в качестве эталонной последовательности для полипептида SSIIa-B дикого типа. Длина полипептида с SEQ ID NO:2 составляет 798 аминокислот, как и в случае мутантов с аминокислотными заменами в SEQ ID NO:2. Ферментативно активные варианты этого фермента существуют в пшенице и такие варианты включены в «SSIIa-B». SSIIa-B не включает гомологичные полипептиды, SSIIa-А и SSIIa-D, так как эти полипептиды являются на около 96% идентичными с SEQ ID NO:2 (Li et al., 1999).
[0181] В контексте данного документа «SSIIa, экспрессируемый из генома D» или «SSIIa-D» означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO:3 или который по меньшей мере на 99% идентичен аминокислотной последовательности, приведенной в SEQ ID NO:3, или содержит такую последовательность. Аминокислотная последовательность SEQ ID NO:3 (№ доступа в Genbank BAE48800; Shimbata et al., 2005) соответствует SSIIa, экспрессируемой из генома D пшеницы сорта Chinese Spring, которая используется в данном документе в качестве эталонной последовательности для SSIIa-D дикого типа. Длина белка SEQ ID NO:3 составляет 799 аминокислот. Ферментативно активные варианты этого фермента существуют в пшенице, например в сорте Fielder, смотрите № доступа CAB86618 (Gao and Chibbar, 2000), чья аминокислотная последовательность на 99,9% (798/799) идентична SEQ ID NO.3, и в диплоидных родственных формах Triticum aestivum, таких как из Aegilops tauschii, вероятных предшественниках генома D гексаплоидной пшеницы, приведенных под № доступа CAB86618. Такие варианты включены в «SSIIa-D». SSIIa-D не включает гомологичные полипептиды, SSIIa-А и SSIIa-B, так как эти полипептиды являются на около 96% идентичными с SEQ ID NO:3. Аминокислотная последовательность, приведенная как SEQ ID NO: 3 является на 95,9% идентичной с каждой из SEQ ID NO:1 и SEQ ID NO:2. Выравнивание этих трех аминокислотных последовательностей демонстрирует аминокислотные отличия, которые можно использовать, чтобы различать белки или чтобы классифицировать варианты как SSIIa-A, SSIIa-B или SSIIa-D.
[0182] При сравнении аминокислотных последовательностей для определения процента идентичности в этом контексте, например с помощью Blastp, следует сравнивать полноразмерные последовательности, а гэпы в последовательностях учитывать как аминокислотные отличия.
[0183] В контексте данного документа «полипептид SSIIa» означает полипептид SSIIa-A, полипептид SSIIa-B или полипептид SSIIa-D.
[0184] В контексте данного документа каждый из полипептидов SSIIa-A, SSIIa-B и SSIIa-D включает полипептидные варианты, обладающие сниженной активностью фермента крахмальной синтазы или не обладающие ей, а также полипептиды, обладающие ферментативной активностью дикого типа или практически дикого типа. Сравнение аминокислотной последовательности мутантной формы полипептида SSIIa с SEQ ID NO:1, 2 и 3 используется для определения, из какого из полипептидов SSIIa-A, -B или -D она получена и, таким образом, для классификации мутантной формы. Например, мутантный полипептид SSIIa считается мутантным полипептидом SSIIa-A, если его аминокислотная последовательность более близкородственна, т. е. имеет большую степень идентичности последовательности с SEQ ID NO:1, чем с SEQ ID NO:2 и 3. Аналогично, мутантный полипептид SSIIa является мутантным полипептидом SSIIa-B, если он является более близкородственным с SEQ ID NO:2, чем с SEQ ID NO:1 или 3, а мутантный полипептид SSIIa является мутантным полипептидом SSIIa-D, если он является более близкородственным с SEQ ID NO:3, чем с SEQ ID NO:1 и 2. Таким образом, специалисты в данной области техники могут классифицировать мутантный полипептид SSIIa.
[0185] Мутантный полипептид SSIIa может обладать сниженной активностью фермента крахмальной синтазы (частичный мутант) или не обладать активностью крахмальной синтазы (полипептид нулевого мутанта). Мутантный ген SSIIa может экспрессироваться с выработкой полипептида SSIIa в эндосперме пшеницы, например усеченного полипептида, или он может не экспрессироваться и не вырабатывать никакой полипептид вовсе. Также он может экспрессироваться с выработкой транскрипта, но не продукта трансляции.
[0186] Также следует понимать, что белки SSIIa могут присутствовать в зерне, в частности в зрелом зерне, которое обычно собирается в коммерческих целях, но в неактивном состоянии или состоянии покоя вследствие физиологических условий в зерне. В контексте данного документа такие полипептиды включены в «полипептиды SSIIa». Полипептиды SSIIa могут быть ферментативно активными во время только части развития зерна, в частности в развивающемся эндосперме, когда происходит отложение запасов крахмала, но в ином случае они являются неактивными. Такие полипептиды SSIIa легко можно выявить и количественно оценить, используя иммунологические способы, такие как Вестерн-блот-анализ.
[0187] Таким образом, в контексте данного документа выражение «дикого типа», используемое в отношении полипептида SSIIa-A, означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO: 1, или ферментативно активные варианты, по меньшей мере на 99% идентичные по аминокислотной последовательности, которые встречаются в природе и которые обладают практически такой же активностью, что и SEQ ID NO:1; в контексте данного документа выражение «дикого типа», используемое в отношении полипептида SSIIa-B, означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO: 2, или ферментативно активные варианты, по меньшей мере на 99% идентичные по аминокислотной последовательности, которые встречаются в природе и которые обладают практически такой же активностью, что и полипептид, чья последовательность приведена в SEQ ID NO:2; в контексте данного документа выражение «дикого типа», используемое в отношении полипептида SSIIa-D, означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO: 3, или ферментативно активные варианты, по меньшей мере на 99% идентичные по аминокислотной последовательности, которые встречаются в природе и которые обладают практически такой же активностью, что и SEQ ID NO:3. В каждом случае полипептид дикого типа обладает активностью крахмальной синтазы II и не был модифицирован согласно настоящему изобретению.
[0188] В пшенице дикого типа вырабатывается два других класса полипептидов SSII, а именно - полипептиды SSIIb и SSIIc. В контексте данного документа «SSIIb, экспрессируемый из генома А» или «SSIIa-А» означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO:10 или который по меньшей мере на 99% идентичен аминокислотной последовательности, приведенной в SEQ ID NO:10, или содержит такую последовательность. Аминокислотная последовательность, приведенная как SEQ ID NO:10 (выведенная из нуклеотидной последовательности с № доступа в Genbank AK332724), используется в данном документе в качестве эталонной последовательности для полипептида SSIIb-A дикого типа. Длина полипептида с SEQ ID NO:10 составляет 676 аминокислотных остатков. Ферментативно активные варианты этого фермента включены в «SSIIb-A». SSIIb-A не включает гомологичный полипептид SSIIb-D, который является на около 90% идентичным с SEQ ID NO:8.
[0189] В контексте данного документа «SSIIb, экспрессируемый из генома D» или «SSIIb-D» означает полипептид, чья аминокислотная последовательность приведена в SEQ ID NO:11 или который по меньшей мере на 99% идентичен аминокислотной последовательности, приведенной в SEQ ID NO:11 или содержит такую последовательность. Аминокислотная последовательность, приведенная как SEQ ID NO:11 (№ доступа в Genbank ABY56824) соответствует крахмальной синтазе IIb, экспрессируемой из генома D обыкновенной пшеницы, которая используется в данном документе в качестве эталонной последовательности для полипептида SSIIb-D дикого типа. Длина полипептида с SEQ ID NO:11 составляет 674 аминокислоты. Ферментативно активные варианты этого фермента включены в «SSIIb-D». SSIIb-D не включает гомологичный полипептид SSIIb-А, который является на около 90% идентичным с SEQ ID NO:11.
[0190] Аминокислотные последовательности гомологов SSIIa и гомологов SSIIb являются на 71-79% идентичными и, следовательно, полипептиды можно легко отличить, даже если они имеют аналогичную ферментативную активность.
[0191] Как описано в примере 2 данного документа, также были идентифицированы последовательности SSIIc пшеницы, которые легко можно отличить от последовательностей SSIIa.
[0192] В контексте данного документа «ген SSIIa» и «ген SSIIa пшеницы» и подобные термины относятся к генам, кодирующим полипептид SSIIa, включая полипептид SSIIa дикого типа, такой как гомологичные полипептиды, присутствующие в других сортах пшеницы, а также к мутантным формам генов, которые либо кодируют полипептиды SSIIa со сниженной активностью или невыявляемой активностью, либо к генам, которые получены из них с помощью мутации. Гены SSIIa включают, но не ограничиваются этим, гены SSIIa пшеницы, которые были клонированы, включая последовательности геномной ДНК и кДНК, перечисленные в таблице 1, которые подписаны как гены SSIIa. Термин ген SSIIa включает, в целом, каждый из более определенных терминов «ген SSIIa-A», «ген SSIIa-B» и «ген SSIIa-D», кодирующих полипептиды SSIIa-A, SSIIa-B и SSIIa-D соответственно, или мутантные формы, полученные из таких генов. В контексте данного документа гены SSIIa включают мутантные формы, которые вообще не кодируют никакой полипептид, или полипептиды, не обладающие активностью крахмальной синтазы, в случае чего мутантные формы представляют нулевые аллели генов. Аллели генов включают мутантные аллели, в которых удалена по меньшей мере часть гена, включая те, в которых удален целый ген, которые также представляют нулевые аллели генов.
[0193] «Эндогенный ген SSIIa» относится к гену SSIIa, который находится в своей нативной локации в геноме пшеницы, включая формы дикого типа и мутантные формы. Как известно в данной области техники, гексаплоидная пшеница, такая как обыкновенная пшеница, имеет три генома, которые обычно обозначаются как геномы A, B и D, тогда как тетраплоидная пшеница, такая как пшеница дурум, имеет два генома, обычно обозначаемые как геномы A и B. Каждый геном содержит 7 пар хромосом, которые можно наблюдать цитологическими методами во время мейоза и таким образом идентифицировать, как хорошо известно в данной области техники. В гексаплоидной пшенице эндогенные гены SSIIa-A, гены SSIIa-B и гены SSIIa-D расположены в коротком плече хромосом 7A, 7B и 7D, соответственно. В противоположность этому, термины «выделенный ген SSIIa» и «экзогенный ген SSIIa» относятся к гену SSIIa, который не находится в своей нативной локации, например удаленному из растения пшеницы, клонированному, синтезированному, содержащемуся в векторе или в форме трансгена в клетке, например трансгена в трансгенном растении пшеницы. В этом контексте ген SSIIa может находиться в любой из определенных нижеописанных форм.
Таблица 1. Гены фермента крахмальной синтазы, типичные для злаковых
Li et al., 1999
Shimbata et al., 2005
Shimbata et al., 2005
Shimbata et al., 2005
Базы данных IWGSC
Базы данных IWGSC
Базы данных IWGSC
Li et al., 2000
Leterrier et al., 2008
[0195] В контексте данного документа «ген SSIIa в геноме A пшеницы» или «ген SSIIa-A» означает любой полинуклеотид, который кодирует полипептид SSIIa-A по определению данного документа или который получен из полинуклеотида, который кодирует SBEIIa-A в растении пшеницы, включая полинуклеотиды природного происхождения, вариантные последовательности или синтетические полинуклеотиды, включая «ген (-ы) SSIIa-A дикого типа», который (-ые) кодирует (-ют) полипептид SSIIa-A с активностью преимущественно SSIIa дикого типа, и «мутантный (-ые) ген (-ы) SSIIa-A», который (-ые) не кодирует (-ют) полипептид SSIIa-A с активностью преимущественно дикого типа, но который (-ые) явно получен (-ы) из гена SSIIa-A дикого типа. Сравнение нуклеотидной последовательности мутантной формы гена SSIIa с набором генов SSIIa дикого типа используется для определения, из какого из генов SSIIa он получен и, таким образом, для его классификации. Например, мутантный ген SSIIa считается мутантным геном SSIIa-A, если его нуклеотидная последовательность более близкородственна, т. е. имеет большую степень идентичности последовательности с геном SSIIa-A дикого типа, чем с любым другим геном SSIIa. Мутантный ген SSIIa-A кодирует полипептид SSIIa со сниженной активностью фермента крахмальной синтазы (частичный мутант) или полипептид с отсутствием активности крахмальной синтазы или вообще не кодирует белок (нулевой мутантный ген). Типовая нуклеотидная последовательность кДНК, соответствующая гену SSIIa-A, приведена в SEQ ID NO:4 (№ доступа в Genbank AF155217; Li et al., 1999). Другие типовые нуклеотидные последовательности приведены под № доступа AK330838 (кДНК из гена SSIIa-A сорта Chinese Spring, Kawaura et al., 2009) и № доступа AJ269503, который представляет кДНК из гена SSIIa-A сорта Fielder (Gao and Chibbar, 2000).
[0196] В контексте данного документа термины «ген SSIIa в геноме B» или «ген SSIIa-B», и «ген SSIIa в геноме D» или «ген SSIIa-D» имеют значения, соответствующие значению для SSIIa-A в предыдущем параграфе. Типовая нуклеотидная последовательность кДНК, соответствующая гену SSIIa-B, приведена в SEQ ID NO:5 (№ доступа в Genbank AJ269504; Gao and Chibbar 2000), а соответствующая гену SSIIa-D приведена в SEQ ID NO:6 (№ доступа в Genbank AJ269502; из сорта Fielder, Gao and Chibbar, 2000). Последовательности частей генов SSIIa также приведены в данном документе, как показано на Фиг. 2-4.
[0197] В контексте данного документа «ген SSIIb в геноме A пшеницы» или «ген SSIIb-A» означает любой полинуклеотид, который кодирует полипептид SSIIb-A по определению данного документа или который получен из полинуклеотида, который кодирует SSIIb-A в растении пшеницы, включая полинуклеотиды природного происхождения, вариантные последовательности или синтетические полинуклеотиды, включая «ген (-ы) SSIIb-A дикого типа», который (-ые) кодирует (-ют) полипептид SSIIb-A с активностью преимущественно SSIIb дикого типа, и «мутантный (-ые) ген (-ы) SSIIb-A», который (-ые) не кодирует (-ют) полипептид SSIIb-A с активностью преимущественно дикого типа, но который (-ые) явно получен (-ы) из гена SSIIb-A дикого типа. Сравнение нуклеотидной последовательности мутантной формы гена SSIIb с набором генов SSIIb дикого типа используется для определения, из какого из генов SSIIb он получен и, таким образом, для его классификации. Например, мутантный ген SSIIb считается мутантным геном SSIIb-A, если его нуклеотидная последовательность более близкородственна, т. е. имеет большую степень идентичности последовательности с геном SSIIb-A дикого типа, чем с любым другим геном SSIIb. Мутантный ген SSIIb-A кодирует полипептид SSIIb со сниженной активностью фермента крахмальной синтазы (частичный мутант) или полипептид с отсутствием активности крахмальной синтазы или вообще не кодирует белок (нулевой мутантный ген). Типовая нуклеотидная последовательность кДНК, соответствующая гену SSIIb-A, приведена в SEQ ID NO:12 (№ доступа в Genbank AK332724).
[0198] В контексте данного документа термины «ген SSIIa в геноме B» или «ген SSIIa-B», и «ген SSIIa в геноме D» или «ген SSIIa-D» имеют значения, соответствующие значению для SSIIa-A в предыдущем параграфе. Типовая нуклеотидная последовательность кДНК, соответствующая гену SSIIa-B, приведена в SEQ ID NO:5 (№ доступа в Genbank AJ269504; Gao and Chibbar 2000), а соответствующая гену SSIIa-D приведена в SEQ ID NO:6 (№ доступа в Genbank AJ269502; из сорта Fielder, Gao and Chibbar, 2000).
[0199] Гены SSIIa по определению выше включают любые регуляторные последовательности, расположенные на 5' или 3' цепях транскрибируемой области, включая область промотора, которые регулируют экспрессию связанной транскрибируемой области, и интроны в транскрибируемых областях. Типовая нуклеотидная последовательность гена SSIIa приведена в виде SEQ ID NO:7, которая представляет нуклеотидную последовательность гена SSIIa-A из генома A пшеницы; № доступа AB201445. Аналогично, нуклеотидная последовательность гена SSIIa-B пшеницы дикого типа приведена под номером доступа AB201446 (IWGSC: хромосома 7DS, Traes_7DS_E6C8AF743, 3877787: от 1 до 396 п. о., от 5137 до 5419 п. о. прямая цепь), а последовательность гена SSIIa-D пшеницы приведена под номером доступа AB201447 (IWGSC: хромосома 7DS, Traes_7DS_E6C8AF743, 3877787: от 1 до 396 п. о., от 5137 до 5419 п. о. прямая цепь). Каждый из этих генов дикого типа был получен из пшеницы сорта Chinese Spring (Shimbata et al., 2005).
[0200] Следует понимать, что существуют природные вариации в последовательностях генов SSIIa разных сортов пшеницы. Специалист в данной области техники может легко распознать гомологичные гены на основании идентичности последовательности. Степень идентичности последовательностей между нуклеотидными последовательностями гомологичных генов SSIIa дикого типа и аминокислотными последовательностями полипептидов дикого типа составляет 95-96%.
[0201] Аллель представляет собой вариант гена в одном генетическом локусе. Диплоидный организм имеет два набора хромосом. Гексаплоидная пшеница имеет шесть наборов хромосом, по 7 хромосом в каждом наборе, и считается выведенной с помощью гибридизации трех диплоидных растений-предшественников, внесших свой вклад в A-, B- и D-геномы. Каждая хромосома в паре хромосом имеет по одной копии (т. е. одному аллелю) каждого гена. Если оба аллеля гена одинаковые, организм является гомозиготным в отношении этого аллеля или гена. Если два аллеля гена разные, организм является гетерозиготным в отношении этого гена. Взаимосвязь между аллелями в локусе в общем случае описывается как доминантная или рецессивная. Два аллеля гена в растении или зерне пшеницы могут иметь одинаковую мутацию и, таким образом, считаются гомозиготными в отношении этой мутации, или два аллеля могут содержать разные мутации по отношению друг к другу и считаются гетерозиготными в отношении этих мутаций. Разные аллели гена или множество генов можно комбинировать, используя известные в данной области техники способы. Например, можно скрестить два родительских растения пшеницы, которые имеют разные аллели одного гена, чтобы получить потомство (F1), содержащее оба аллеля в гетерозиготном состоянии, а затем провести самооплодотворение дочерних растений, чтобы получить следующее поколение растений (F2), которые содержат один или другой из этих аллелей в гомозиготном состоянии или оба аллеля в гетерозиготном состоянии в соответствии с менделевской генетикой.
[0202] Аллели, которые не кодируют или не способны приводить к выработке какого-либо активного фермента, представляют собой нулевые аллели. Такие нулевые аллели могу кодировать или не кодировать полипептид, например кодируют усеченный полипептид или полипептид, имеющий инактивирующее изменение в аминокислотной последовательности по сравнению с полипептидом SSIIa дикого типа.
[0203] Ссылка на нулевую (-ые) мутацию (-ии) включает нулевую мутацию, независимо выбранную из группы, состоящей из мутации с делецией, мутации со вставкой, мутации сайта сплайсинга, мутации с преждевременной терминацией трансляции и мутации со сдвигом рамки, или любую их комбинацию. В одном варианте реализации одна или более нулевых мутаций являются мутациями с неконсервативной аминокислотной заменой или же нулевая мутация включает комбинацию двух или более неконсервативных аминокислотных замен. В этом контексте неконсервативные аминокислотные замены соответствуют определению данного документа.
[0204] Мутация с потерей функции, которая включает мутацию с частичной потерей функции в аллеле гена, а также мутацию с полной потерей функции (нулевую мутацию), означает мутацию в аллеле, приводящую к снижению уровня или активности фермента, такого как фермент SSIIa, в зерне. Мутация в аллеле может означать, например, что транслируется меньше белка, имеющего активность дикого типа или сниженную активность, или что за уровнями транскрипции дикого типа или сниженными уровнями транскрипции следует трансляция фермента со сниженной ферментативной активностью, или предпочтительно мутантный аллель транскрибируется на сниженном уровне по сравнению с диким типом и любой продукт трансляции имеет активность меньшую, чем у соответствующего полипептида дикого типа. Мутация может приводить, например, к тому, что из гена, содержащего мутацию, не транскрибируется или транскрибируется меньше РНК, или что вырабатываемый полипептид не имеет или имеет сниженную активность по сравнению с диким типом, предпочтительно к обоим вариантам. Если невозможно зарегистрировать транскрипт из аллеля, например методом ОТ-ПЦР, этот результат указывает на то, что аллель является нулевым аллелем.
[0205] «Точечная мутация» относится к изменению одного нуклеотидного основания, которое включает делецию, замену или вставку одного нуклеотида. Точечная мутация может дополнительно представлять собой мутацию сайта сплайсинга, мутацию с преждевременной терминацией трансляции, мутацию со сдвигом рамки или другую мутацию с потерей функции, которая приводит к отсутствию выработки белка, или к выработке белка в меньших количествах, или к выработке белка, обладающего меньшей активностью SSII. Мутация со сдвигом рамки в кодирующей белок области гена считается нулевой мутацией, так как она влияет на структуру кодируемого полипептида. Аналогично, мутация с преждевременной терминацией трансляции считается нулевой мутацией, если она не находится очень близко к С-концу кодирующей белок области гена, в случае чего можно использовать ферментный анализ для определения того, обладает ли белок ферментативной активностью. В некоторых вариантах реализации точечная мутация приводит к консервативной или предпочтительно неконсервативной аминокислотной замене.
[0206] «Сниженные» или «меньшие» количество или уровень полипептида или ферментной активности означают сниженные или меньшие количество или уровень по сравнению с количеством или уровнем, обеспечиваемыми соответствующим аллелем или геном дикого типа. Как правило, снижение составляет по меньшей мере 40%, предпочтительно по меньшей мере 50% или по меньшей мере 60%, более предпочтительно по меньшей мере 80% или 90% относительно дикого типа. В наиболее предпочтительном варианте реализации белок не выявляется, например, в описанном в данном документе Вестерн-блот-анализе, предпочтительно в случае каждого из SSIIa-A, SSIIa-B и SSIIa-D.
[0207] «Сниженная» активность означает снижение относительно соответствующего фермента дикого типа, такого как SSIIa, SSSIIa, или другого фермента.
[0208] Белковая «активность» относится к активности SS, которую можно измерять прямым или непрямым образом различными способами, известными в данной области техники и описанными в данном документе.
[0209] В некоторых вариантах реализации количество по массе SSIIa или другого полипептида снижено, даже если большое число полипептидных молекул в зерне являются такими же как и в диком типе, но каждая молекула имеет активность, меньшую, чем в диком типе. Например, вырабатываемые полипептиды короче белка SSIIa дикого типа или другого белка, как происходит в случае усечения мутантного белка SSIIa или другого белка по причине сигнала преждевременной терминации трансляции.
[0210] В контексте данного документа выражение «два идентичных аллеля гена SSIIa-A» означает, что два аллеля гена SSIIa-A являются идентичными друг с другом, т. е. растение или зерно являются гомозиготными в отношении этих аллелей или этого гена; «два идентичных аллеля гена SSIIa-B» означает, что два аллеля гена SSIIa-B являются идентичными друг с другом; «два идентичных аллеля гена SSIIa-D» означает, что два аллеля гена SSIIa-D являются идентичными друг с другом.
[0211] Можно получать растения пшеницы согласно изобретению и проводить их идентификацию после мутагенеза. В некоторых вариантах реализации растение пшеницы является нетрансгенным, что является желательным на некоторых рынках сбыта, или не содержит никакой экзогенной нуклеиновой кислоты, которая снижает экспрессию гена SSIIa. В другом варианте реализации растение пшеницы является трансгенным, например содержит молекулу экзогенной нуклеиновой кислоты, отличную от той, которая снижает экспрессию гена SSIIa и/или гена SBEIIa, такую как, например, молекула экзогенной нуклеиновой кислоты, которая кодирует полипептид, придающий растению стойкость к гербицидам.
[0212] Мутантные растения пшеницы, содержащие мутацию в одном гене SSIIa, которую можно комбинировать посредством скрещивания растений и отбора потомства, содержащего другие мутации гена SSIIa, для создания растений пшеницы согласно изобретению, могут быть синтетическими, например, вследствие проведения сайт-направленного мутагенеза в нуклеиновой кислоте, или индуцированными мутагенной обработкой, или могут иметь природное происхождение, т. е. быть выделенными из природного источника. В некоторых вариантах реализации клетку, ткань, семя растения-предшественника или само растение можно подвергать мутагенезу для создания одиночных или множественных мутаций, таких как нуклеотидные замены, делеции, вставки и/или модификации кодонов. Предпочтительные растения и зерно пшеницы согласно изобретению содержат по меньшей мере одну внесенную мутацию гена SSIIa, более предпочтительно две или более внесенных мутаций гена SSIIa, и могут не содержать мутаций природного происхождения, т. е. все мутантные аллели SSIIa в растении получены синтетическим образом или посредством мутагенной обработки. В контексте данного документе «внесенная мутация» или «введенная мутация» представляет собой искусственно индуцированную генетическую вариацию, которая может являться результатом химического, радиоактивного или биологического мутагенеза, например вставкой транспозона или Т-ДНК, или индуцированной эндонуклеазой мутацией.
[0213] Мутагенез можно осуществлять химическими или радиационными способами, например с помощью обработки семян EMS или азидом натрия (Zwar and Chandler, 1995), или гамма-облучения, как хорошо известно в данной области техники. В химическом мутагенезе наблюдается тенденция к нуклеотидным заменам, а не делециям. Облучение пучком тяжелых ионов (ПТИ) известно как эффективная технология мутационной селекции для получения новых сортов растений, смотрите, например, Hayashi et al., 2007 и Kazama et al, 2008. Облучение пучком ионов характеризуется двумя физическими факторами, дозой (Гр) и ЛПЭ (линейный перенос энергии, кэВ/мкм), в отношении биологического действия, определяющего степень повреждения ДНК и размер делеции ДНК, которые можно корректировать в соответствии с желаемой степенью мутагенеза. Метод с ПТИ позволяет создавать ряд мутантов, многие из которых содержат делеции, для которых можно проводить скрининг в отношении мутаций в конкретных генах SSIIa. Можно проводить обратное скрещивание идентифицированных мутантов с немутированными растениями пшеницы в качестве рекуррентных родителей, чтобы устранить и, следовательно, снизить влияние нежелательных мутаций в подвергнутом мутагенезу геноме.
[0214] Выделение мутантов можно осуществлять посредством скрининга подвергнутых мутагенезу растений или семян. Например, можно проводить скрининг подвергнутой мутагенезу популяции пшеницы прямым образом в отношении генотипа SSIIa или непрямым образом посредством скрининга в отношении фенотипа, полученного в результате мутаций в генах SSIIa. Прямой скрининг в отношении генотипа предпочтительно включает анализ наличия мутаций в генах SSIIa, которые можно наблюдать в анализе ПЦР по отсутствию специфических маркеров SSIIa, как ожидается при удалении некоторых генов, или в гетеродуплексном анализе, таком как TILLING. Скрининг предпочтительно основан на нуклеотидном секвенировании, которое часто проводят на пулах кандидатных мутантов. Скрининг в отношении фенотипа может включать скрининг в отношении отсутствия или снижения количества одного или более полипептидов SSIIa методом ELISA или аффинной хроматографии, или изменения фенотипа крахмала в крахмале зерна. В гексаплоидной пшенице скрининг предпочтительно проводят для генотипа, в котором уже отсутствуют один или более видов активности SSIIa, например для растения пшеницы, уже содержащего мутации в генах SSIIa двух или трех геномов, так, чтобы проводить поиск мутанта с дополнительным отсутствием функциональной активности. Можно использовать аффинную хроматографию для того, чтобы различить полипептиды SSIIa-A, SSIIa-B и SSIIa-D. Можно проводить скрининг больших популяций подвергнутых мутагенезу семян (тысяч или десятков тысяч семян) в отношении высокоамилозных фенотипов, используя ближнюю инфракрасную спектроскопию (NIR). Этими способами можно легко осуществлять высокопроизводительный скрининг, что позволяет проводить выделение мутантов с частотой приблизительно один мутант на несколько сотен семян.
[0215] Растения и семена согласно изобретению можно получать, используя процесс, известный как TILLING (Targeting Induced Local Lesions IN Genomes (нацеленное индуцированное локальное повреждение в геномах)), с помощью которого можно создавать одну или более мутацию в растениях или зернах пшеницы. На первом этапе в популяции растений индуцируют внесенные мутации, такие как новые изменения в одной паре оснований, путем обработки семян или пыльцы химическим или радиоактивным мутагеном, а затем выращивая растения до поколения, в котором мутации будут стабильно наследоваться, как правило, до поколения M2, в котором можно идентифицировать гомозиготных мутантов. Выделяют ДНК и хранят семена всех представителей популяции для создания ресурса, который можно повторно оценивать со временем. Для анализа TILLING конструируют ПЦР-праймеры для специфической амплификации одного представляющего интерес гена-мишени. После этого меченые красителем праймеры можно использовать для амплификации ПЦР-продуктов из объединенной ДНК множества отдельных растений. Эти ПЦР-продукты денатурируют и повторно гибридизируют, чтобы обеспечить образование несовпадающих пар оснований. Несовпадения или гетеродуплексы представляют как однонуклеотидные полиморфизмы (ОНП) природного происхождения (т. е. несколько растений из популяции с некоторой вероятностью несут один и тот же полиморфизм), так и индуцированные ОНП (т. е. только редкие отдельные растения с некоторой вероятностью демонстрируют мутацию). После образования гетеродуплексов используют эндонуклеазу, такую как Cel I, которая распознает и расщепляет ДНК с несовпадениями, или используют плавление с высоким разрешением для обнаружения новых ОНП в популяции TILLING. Например, смотрите Botticella et al., 2011.
[0216] Используя этот подход, можно проводить скрининг многих тысяч растений для идентификации любого отдельного растения с изменением в одной паре оснований или небольшими вставками или делециями (1-30 п. о.) в любом гене или конкретной области генома. Диапазон размеров анализируемых геномных фрагментов может составлять от 0,3 до 1,6 т. п. о. При 8-кратном объединении и амплификации 1,4 т. п. о. фрагментов с 96 дорожками в анализе эта комбинация позволяет проводить скрининг до миллиона пар оснований геномной ДНК в одном анализе, что делает TILLING высокопроизводительной методикой. TILLING дополнительно описан в Slade and Knauf, 2005, и Henikoff et al., 2004.
[0217] Кроме обеспечения эффективного выявления мутаций, высокопроизводительная технология TILLING идеально подходит для выявления природного полиморфизма. Следовательно, детальное исследование неизвестной гомологичной ДНК посредством гетеродуплексирования по известной последовательности позволяет выявить число и расположение сайтов полиморфизма. Можно идентифицировать как нуклеотидные изменения, так и небольшие вставки и делеции, включая по меньшей мере некоторое количество повторений полиморфизма. Это называется Ecotilling (Comai et al., 2004). Можно проводить скрининг планшетов, содержащих упорядоченную экотипическую ДНК, вместо пулов ДНК из подвергнутых мутагенезу растений. Так как выявление проводится в гелях с разрешением практически одна пара оснований, а фоновые структуры являются одинаковыми для всех дорожек, можно получать соответствие полос одинакового размера, проводя таким образом обнаружение и генотипирование мутаций за один этап. При таком подходе сайленсинг мутантного гена является простым и эффективным.
[0218] В контексте данного документа термин «биологический агент» означает агент, применяемый для создания сайт-специфических мутантов и включает ферменты, которые индуцируют двухцепочечные разрывы в ДНК, стимулирующие эндогенные механизмы репарации. Они включают эндонуклеазы, цинк-пальцевые нуклеазы, TAL-эффекторные белки, транспозазы, сайт-специфические рекомбиназы и предпочтительно представляют собой CRISPR-эндонуклеазы. Цинк-пальцевые нуклеазы (ZFN), например, облегчают сайт-специфическое расщепление в пределах выбранного гена в геноме, что позволяет эндогенным или другим соединяющим концы механизмам репарации вносить делеции или вставки для ликвидации разрыва. Обзор технологии цинк-пальцевых нуклеаз приведен в Le Provost et al., 2009, также смотрите Durai et al., 2005 и Liu et al., 2010.
[0219] Короткие палиндромные повторы, регулярно расположенные группами (CRISPR), представляют собой сегменты прокариотической ДНК, содержащие короткие повторы последовательностей оснований. За каждым повтором следует короткий сегмент «спейсерной ДНК» от предыдущего воздействия бактериофагового вируса или плазмиды. Система CRISPR/Cas является прокариотической иммунной системой, которая придает устойчивость к чужеродным генетическим элементам, таким как те, что присутствуют в плазмидах и фагах, и обеспечивает некоторую форму приобретенного иммунитета. Спейсеры CRISPR распознают и разрезают эти экзогенные генетические элементы способом, аналогичным РНК-интерференции в эукариотических организмах. CRISPR можно обнаружить приблизительно в 40% секвенированных бактериальных геномов и 90% секвенированных архей.
[0220] Путем доставки нуклеазы Cas9 и соответствующих направляющих РНК в клетку можно разрезать геном клетки в необходимом месте, что позволяет удалять существующие гены и/или добавлять новые. CRISPR использовали вместе со специфическими эндонуклеазными ферментами для редактирования генома и регуляции генов в различных видах. Дополнительную информацию в отношении CRISPR можно найти в WO 2013/188638, WO 2014/093622 и Doudna et al., (2014).
[0221] Подобные активаторам транскрипции эффекторные нуклеазы (TALEN) представляют собой рестрикционные ферменты, которые могут быть сконструированы так, чтобы разрезать конкретные последовательности ДНК. Их создают путем слияния TAL-эффекторного ДНК-связывающего домена с ДНК-расщепляющим доменом (нуклеазой, разрезающей цепи ДНК). Подобные активаторам транскрипции эффекторы (TALE) могут быть сконструированы так, чтобы связывать практически любую необходимую последовательность ДНК и, таким образом, в комбинации с нуклеазой можно разрезать ДНК в конкретных местах. Рестрикционные ферменты можно вносить в клетки для применения в редактировании генов или для редактирования генома in situ - технологии, известной как редактирование генома сконструированными нуклеазами. Наряду с цинк-пальцевыми нуклеазами и CRISPR/Cas9 TALEN является важным инструментом в области редактирования генома. Дополнительную информацию в отношении TALEN можно найти в Boch (2011); Juong et al., (2013) и Sune et al., (2013).
[0222] Затем идентифицированные мутации можно вносить в необходимое генетическое окружение путем скрещивания мутанта с растением с необходимым генетическим окружением и проведения необходимого числа обратных скрещиваний для исключения изначально нежелательного родительского окружения. Смотрите, например, пример 3 в данном документе.
[0223] В некоторых вариантах реализации мутации представляют собой нулевые мутации, такие как несмысловые мутации, мутации со сдвигом рамки, делеции, мутации со вставкой или варианты сайта сплайсинга, которые полностью инактивируют ген. Производные с нуклеотидными вставками включают 5' и 3' концевые слияния, а также вставки одного или множества нуклеотидов внутри последовательности.
[0224] Варианты последовательностей с нуклеотидными вставками представляют собой такие варианты, в которых в некоторый участок нуклеотидной последовательности внесено один или более нуклеотидов, как в предопределенный участок, что возможно с цинк-пальцевыми нуклеазами (ZFN), CRISPR-нуклеазами или другими методами гомологичной рекомбинации, так и в виде случайной вставки с соответствующим скринингом получаемого в результате продукта.
[0225] Варианты с делециями характеризуются удалением одного или более нуклеотидов из последовательности. В одном варианте реализации мутантный ген содержит только одну вставку или делецию последовательности нуклеотидов по сравнению с геном дикого типа. Делеция может быть достаточно большой, чтобы включать один или более экзонов или интронов, как экзоны, так и интроны, границу раздела интрон-экзон, часть промотора, сайт инициации трансляции или даже целый ген. Делеции могут простираться достаточно далеко, чтобы включать по меньшей мере часть гена SSIIa или целый ген и один или более соседних генов в геноме A, B или D. Вставки или делеции в экзонах кодирующей белок области гена, которые приводят к добавлению или удалению некоторого числа нуклеотидов, которое не обязательно кратно трем, тем самым приводя к изменению рамки считывания во время трансляции, почти всегда приводят к устранению активности мутантного гена, содержащего такую вставку или делецию; такие мутации являются нулевыми мутациями. Вставки или делеции в экзонах кодирующей белок области гена, которые приводят к добавлению или удалению некоторого числа нуклеотидов, которое точно кратно трем, могут приводить или не приводить к устранению активности гена, содержащего такую вставку или делецию. В случае делеции числа нуклеотидов, точно кратного трем, ожидается, что делеция будет инактивировать кодируемый полипептид, если удаленные нуклеотиды кодируют высококонсервативную аминокислоту. Можно использовать ферментный анализ или фенотипический анализ, чтобы определить, являются ли мутации со вставкой или делецией нулевыми мутациями.
[0226] Варианты с заменой нуклеотидов представляют собой такие варианты, в которых по меньшей мере один нуклеотид в последовательности был удален, а на его место вставлен другой нуклеотид. В некоторых вариантах реализации число нуклеотидов, в которых проведены замены в мутантном гене относительно гена дикого типа, максимально составляет десять нуклеотидов, более предпочтительно - максимум 9, 8, 7, 6, 5, 4, 3 или 2, или наиболее предпочтительно - только один нуклеотид. Замены могут быть «молчащими» в том смысле, что замена нуклеотида не приводит к изменению аминокислоты, определяемой данным кодоном. Нуклеотидные замены могут снижать эффективность трансляции и тем самым снижать уровень экспрессии соответствующего гена SSIIa, например, за счет снижения стабильности мРНК, или, в случае расположения вблизи границы раздела экзон-интрон, изменять эффективность сплайсинга. Ожидается, что молчащие замены, которые не меняют эффективность трансляции гена SSIIa, не будут изменять активность гена и, следовательно, считаются в данном документе не-мутантными, т. е. такие гены представляют собой активные варианты и не включены в термин «мутантный ген». В альтернативном варианте нуклеотидная (-ые) замена (ы) может (могут) изменять кодируемую аминокислотную последовательность и тем самым изменять активность кодируемого фермента, в частности, если происходит замещение консервативных аминокислот другой аминокислотой, которая достаточно сильно характеризуется, т. е. в случае неконсервативной замены. Информацию в отношении консервативных замен смотрите в таблице 3. Консервативные аминокислоты в полипептидах SSIIa пшеницы можно идентифицировать путем выравнивания аминокислотных последовательностей SSIIa от разных видов, например выравнивания SEQ ID NO:1 с SSII Arabidopsis thaliana и определения, какие аминокислоты являются общими.
[0227] В контексте данного документа термин «мутация» не включает молчащие нуклеотидные замены, которые не влияют на активность гена, и, следовательно, включает только те изменения в последовательности гена, которые влияют на активность гена. Термин «полиморфизм» относится к любому изменению в нуклеотидной последовательности гена, включая такие молчащие нуклеотидные замены. Методы скрининга могут, во-первых, включать скрининг в отношении полиморфизма и, во-вторых, в отношении мутаций в группе полиморфных вариантов. Мутации включают делеции всего или части гена, вставки, такие как вставка в экзон гена, и нуклеотидные замены, а также любую их комбинацию.
[0228] В контексте данного документа термины «растение (-ия)» и «растение (-ия) пшеницы» в общем случае относятся к целым растениям, а термины «растительный» или «пшеничный» применяются как описывающие, эти термины относятся к любому веществу, который присутствует в, получен из, выделен из или связан с растением или растением пшеницы, такому как, например, органы растения (например, листья, стебли, корни, цветы), одиночные клетки (например, пыльца), семена или зерна, при этом клетки растений включают, например, клетки тканевой культуры, продукты, полученные из растения, такие как «пшеничная мука», «пшеничное зерно», «пшеничный крахмал», «гранулы пшеничного крахмала» и т. п. Ростки и пророщенное зерно, из которого появились корни и побеги, также включены в значение термина «растение». В контексте данного документа термин «части растения» относится к одной или более тканям или органам растения, которые получены из целого растения, предпочтительно растения пшеницы. В контексте данного документа части растения содержат клетки растения. Части растения включают вегетативные структуры (например, листья, включая влагалище листа и пластинку листа, стебли, включая междоузлия), корни, отростки, цветковые органы/структуры, такие как колос (также называемый кистью или метелкой), пыльцу, семяпочки, семя (включая зародыш, эндосперм и оболочку семени), ткань растения (например, проводящую ткань, покровную ткань и т. п.), его клетки и потомство. В контексте данного документа термин «клетка растения» относится к клетке, полученной из растения или находящейся в составе растения, предпочтительно растения пшеницы, и включает протопласты или другие клетки, полученные из растений, гаметопродуцирующие клетки и клетки, которые регенерируют в полные растения. Клетки растений могут представлять собой клетки в культуре. Под «тканью растения» подразумевается дифференцированная ткань в растении или полученная из растения («эксплантат») или недифференцированная ткань, полученная из зрелых или незрелых эмбрионов, семян, корней, побегов, плодов, пыльцы и различных форм агрегации клеток растений в культуре, таких как каллус. Ткани растений в семенах или полученные из семян, таких как зерна пшеницы, представляют собой оболочку семени, эндосперм, иток, алейроновый слой и эмбрион. Все ткани или органы растения пшеницы и клетки пшеницы содержат генетический материал (нуклеиновую кислоту) растения пшеницы, из которого они получены.
[0229] В контексте данного документа злаковые означают растения или зерно представителей семейств однодольных Poaceae или Graminae, которые культивируют ради съедобных компонентов их зерен, и включают пшеницу, ячмень, кукурузу, овес, рожь, рис, сорго, тритикале, просо, гречиху. Предпочтительно злаковое растение или зерно представляет собой растение или зерно пшеницы. В дополнительном предпочтительном варианте реализации клетка, растение или зерно пшеницы или полученные из них продукты согласно изобретению принадлежат виду Triticum aestivum.
[0230] В контексте данного документа термин «пшеница» относится к любому виду рода Triticum, включая его предшественников, а также его потомство, полученное при скрещивании с другими видами. Пшеница включает «гексаплоидную пшеницу», которая имеет геномную организацию типа AABBDD, состоящую из 42 хромосом, и «тетраплоидную пшеницу», которая имеет геномную организацию типа AABB, состоящую из 28 хромосом. Растения и зерно согласно изобретению принадлежат гексаплоидному виду T. aestivum и не включают тетраплоидный вид T. durum, также называемый пшеницей дурум или Triticum turgidum ssp. durum. Считается, что диплоидными предшественниками T. aestivum являются T. uartu, T. monococcum или T. boeoticum в случае генома A, Aegilops speltoides в случае генома B и T. tauschii (также известный как Aegilops squarrosa or Aegilops tauschii) в случае генома D. Предпочтительно растение T. aestivum согласно изобретению подходит для промышленного производства зерна, имеет подходящие агрономические характеристики, известные специалистам в данной области техники. Наиболее предпочтительно пшеница представляет собой вид Triticum aestivum ssp. aestivum, называемый в данном документе «обыкновенной пшеницей».
[0231] В аспектах изобретения предложены способы выращивания и сбора зерна пшеницы согласно изобретению и способы создания бункеров с зерном пшеницы согласно изобретению. Например, после подготовки почвы посредством вспахивания и/или некоторых других способов семена, как правило, высаживают путем засевания методом бороздового посева и высаживают семена рядами. Чтобы предотвратить рассеивание зерна, получаемого после достижения растением зрелости, пшеницу нужно убирать до достижения полной зрелости, но, как правило, ее убирают, когда растения полностью утрачивают зеленый цвет. Уборка урожая состоит из нескольких этапов: срезание или жатва стеблей; обмолачивание и провеивание для отделения зерна от колосьев, шелухи и прочей мякины; просеивание и сортировка зерна; как правило осуществляемые уборочным комбайном, а затем загрузка зерна в грузовые машины. В некоторых вариантах реализации собранное зерно пшеницы можно хранить в сухих, хорошо вентилируемых помещениях, которые уберегают от насекомых-вредителей. В некоторых вариантах реализации собранное зерно пшеницы можно хранить в течение короткого времени в бункерах или амбарах. Затем зерно пшеницы можно отправлять на заготовительные элеваторы - высокие конструкции, в которых сушат и хранят зерно до его продажи или транспортировки на терминальные элеваторы. Следовательно, в вариантах реализации изобретения предложен способ получения бункеров с зерном пшеницы, включающий: a) срезание стеблей пшеницы, содержащих зерно пшеницы по определению данного документа; b) обмолачивание и/или провеивание стеблей для отделения зерна от мякины; и c) просеивание и/или сортировку зерна, отделенного на этапе b), и загрузку просеянного и/или отсортированного зерна в бункеры с получением, таким образом, бункеров с зерном пшеницы.
[0232] Растения и зерно пшеницы согласно изобретению имеют применения, отличные от применения для создания пищи или корма для животных, например применения в исследованиях или разведении. В случае растений, размножающихся семенами, таких как пшеница, растения могут самоопыляться с получением растения, являющегося гомозиготным в отношении необходимых генов, или же гаплоидные ткани, такие как развивающиеся зародышевые клетки, можно индуцировать для удвоения хромосомного набора для получения гомозиготного растения. Таким образом, самоопыленное растение пшеницы согласно изобретению дает зерно, содержащее комбинацию мутантных аллелей SSIIa, которые являются гомозиготными. Зерно можно выращивать для получения растений, которые могут иметь выбранный фенотип, такой как, например, высокое содержание амилозы в крахмале.
[0233] Растения пшеницы согласно изобретению можно скрещивать с растениями, содержащими более предпочтительное генетическое окружение, и, следовательно, изобретение включает перенос сниженного признака SSIIa в другое генетическое окружение. В контексте данного документа «скрещивание» или «скрещивать» относится к процессу переноса (искусственным или естественным образом) пыльцы цветка одного растения на рыльце цветка другого растения. После исходного скрещивания можно проводить необходимое число обратных скрещиваний для исключения менее предпочтительного генетического окружения. Специфические в отношении аллеля SSIIa ПЦР-маркеры, такие как описанные в данном документе, можно использовать для скрининга или идентификации дочерних растений или зерна с необходимой комбинацией аллелей, отслеживая, таким образом, присутствие аллелей в программе скрещивания. Желательное генетическое окружение может включать подходящую комбинацию генов, обеспечивающих урожайность при промышленном производстве и другие характеристики, такие как агрономическая эффективность или устойчивость к абиотическому стрессу. Генетическое окружение также может включать другие измененные гены биосинтеза или модификации крахмала, например нулевые аллели генов SSIIIa или предпочтительные аллели генов GBSS. Генетическое окружение может содержать один или более трансгенов, таких как, например, ген, придающий устойчивость к гербицидам, таким как глифосат.
[0234] Предпочтительное генетическое окружение растения пшеницы подбирается с учетом урожайности при промышленном производстве и других характеристик. Такие характеристики могут включать необходимость иметь зимний или весенний тип, агрономическую эффективность, устойчивость к болезням и устойчивость к абиотическому стрессу. При применении в Австралии может быть желательно скрестить измененный связанный с крахмалом признак растения пшеницы согласно изобретению с сортами пшеницы, такими как Baxter, Kennedy, Janz, Frame, Rosella, Cadoux, Diamondbird или другими обычно выращиваемыми вариантами. Для других районов произрастания подходят другие варианты. Предпочтительно, чтобы растение пшеницы согласно изобретению обеспечивало выход зерна (в тоннах/гектар), составляющий по меньшей мере 50% относительно выхода соответствующего варианта дикого типа в по меньшей мере некоторых районах произрастания, более предпочтительно по меньшей мере 60% или по меньшей мере 70%, или по меньшей мере 80%, или по меньшей мере 90% относительно выхода варианта дикого типа, имеющего приблизительно такое же генетическое окружение и выращиваемого в таких же условиях. В одном варианте реализации выход зерна составляет менее 90% относительно варианта дикого типа, имеющего приблизительно такое же генетическое окружение и выращиваемого в таких же условиях. Выход можно легко определить в контролируемых полевых исследованиях или в моделируемых полевых исследованиях в теплице, но предпочтительно в поле.
[0235] Отбор с помощью маркера является хорошо известным способом отбора гетерозиготных растений, получаемых при обратном скрещивании с рекуррентным родителем по классической программе скрещивания. Популяция растений в каждом поколении обратного скрещивания будет гетерозиготной в отношении представляющего (-их) интерес гена (-ов), обычно присутствующего (-их) в соотношении 1:1 в популяции обратного скрещивания, а молекулярный маркер, связанный с геном, можно использовать для того, чтобы различить два аллеля гена. Можно проводить анализ присутствия двух маркеров: одного в отношении мутантного аллеля, а другого в отношении аллеля дикого типа. Выделяя ДНК, например, из молодых побегов, и исследуя ее с помощью специфического маркера в отношении интрогрессированного необходимого признака, проводят ранний отбор растений для дополнительного обратного скрещивания, пока энергия и ресурсы сконцентрированы в меньшем количестве растений. Процедуры, такие как скрещивание растений пшеницы, самоопыление растений пшеницы или отбор с помощью маркера, являются стандартными процедурами и хорошо известны в данной области техники. Перенос аллелей из тетраплоидной пшеницы, такой как дурум, в гексаплоидную, или другие формы гибридизации являются более трудными, но также известны в данной области техники.
[0236] Чтобы идентифицировать необходимую фенотипическую характеристику, растения пшеницы, которые содержат комбинацию мутантных генов ssIIa или других необходимых генов, как правило, сравнивают с контрольным растением. При оценке фенотипической характеристики, связанной с мутантными генами ssIIa, такой как содержание амилозы в крахмале зерна, или общее содержание волокон, или масса или выход зерна, подлежащие исследованию растения и контрольные растения выращивают в условиях климатической камеры, теплицы или предпочтительно в полевых условиях, в одинаковых условиях (температура, почва, обеспечение влагой, обеспечение удобрениями, сезон и т. д.). Идентификация конкретного фенотипического признака и сравнение с контролем основаны на обычном статистическом анализе и подсчете. Экспрессию генов или ферментативную активность сравнивают с параметрами роста, развития и урожайности, которые включают один или более из уровня прорастания, мощности всходов, включая появление всходов, морфологии растения, его цвета, числа, размера, объемов, сухой и влажной массы, вызревания, соотношения наземной и подземной биомассы, и времени, скорости и длительности различных стадий роста вплоть до старения, включая вегетативный рост, плодоношение, цветение, выхода и состояния покоя зерна, индекса урожайности и содержания растворимых углеводов, включая уровни сахарозы, глюкозы, фруктозы и крахмала, а также эндогенные уровни крахмала. В некоторых вариантах реализации растения пшеницы согласно изобретению отличаются от растений дикого типа по одному или более из этих параметров менее чем на 50%, более предпочтительно менее чем на 40%, менее чем на 30%, менее чем на 20%, менее чем на 15%, менее чем на 10%, менее чем на 5%, менее чем на 2% или менее чем на 1% при выращивании в таких же условиях. Предпочтительно растение или зерно согласно изобретению является приблизительно таким же, что и растение или зерно дикого типа, в отношении одного или более из этих параметров.
[0237] В контексте данного документа термин «связанный» или «генетически связанный» относится к маркерному локусу и второму локусу, расположенным достаточно близко в хромосоме так, что они будут наследоваться вместе в более чем 50% случаев мейоза, например, не случайным образом. Это определение включает ситуацию, когда маркерный локус и второй локус образуют часть одного гена. Кроме того, это определение включает ситуацию, когда маркерный локус содержит полиморфизм, который отвечает за представляющий интерес признак, в случае чего полиморфизм будет на 100% связан с этим фенотипом. Таким образом, процент рекомбинации, наблюдаемый между локусами в одном поколении (рассчитываемый в сантиморганах (сМ)) будет составлять менее 50. В конкретных вариантах реализации изобретения генетически связанные локусы в хромосоме может разделять 45, 35, 25, 15, 10, 5, 4, 3, 2 или 1 или менее сМ. Предпочтительно маркеры разделяет менее чем 5 сМ или 2 сМ и наиболее предпочтительно их разделяет практически 0 сМ.
[0238] В контексте данного документа «другие генетические маркеры» могут представлять собой любые молекулы, которые связаны с необходимым признаком в растениях пшеницы согласно изобретению. Такие маркеры хорошо известны специалистам в данной области техники и включают молекулярные маркеры, связанные с генами, определяющими признаки, такие как устойчивость к болезням, урожайность, морфология растения, качество зерна, другие признаки состояния покоя, такие как цвет зерна, содержание гибберелловой кислоты в семени, высота растения, цвет муки и т. п. Примерами таких генов являются гены устойчивости к стеблевой ржавчине Sr2 или Sr38, гены устойчивости к желтой ржавчине Yr10 или Yr17, гены устойчивости к нематодам, такие как Cre1 и Cre3, аллели в локусах глютенина, которые определяют силу восковой спелости, такие как аллели Ax, Bx, Dx, Ay, By и Dy, гены Rht, которые определяют полукарликовую форму роста и, следовательно, устойчивость к полеганию (Eagles et al., 2001; Langridge et al., 2001; Sharp et al., 2001).
[0239] Растения пшеницы, части растений пшеницы и продукты из них согласно изобретению предпочтительно являются нетрансгенными в отношении генов, которые ингибируют экспрессию гена SSIIa и/или гена SBEIIa, т. е. они не содержат трансген, кодирующий молекулу РНК, которая снижает экспрессию эндогенного гена SSIIa, хотя в этом варианте реализации они могут содержать другие трансгены, например гены устойчивости к гербицидам, такой как устойчивость к глифосату. Более предпочтительно растение, зерно пшеницы и продукты из них являются нетрансгенными, т. е. они не содержат какой-либо трансген, который является предпочтительным в некоторых маркерах. Такие продукты также описаны в данном документе как «нетрансформированные» продукты. Такие нетрансгенные растения и зерно содержат множество мутантных аллелей SSIIa, как описано в данном документе, таких, какие получают после мутагенеза.
[0240] В контексте данного документа термины «трансгенное растение» и «трансгенное растение пшеницы» относятся к растению, которое содержит генетическую конструкцию («трансген»), не встречающуюся в растении дикого типа того же вида, вариетета или сорта. Это означает, что трансгенные растения (трансформированные растения) содержат генетический материал, который не содержали до трансформации. Термины «трансген» или «генетическая конструкция», употребляемые в данном документе, имеют общепринятое в области биотехнологии значение и относятся к генетической последовательности, которая была создана или изменена посредством рекомбинантной ДНК- или РНК-технологии. В случае его наличия в клетке растения, трансген был внесен в клетку растения или клетку-предшественника человеком. Трансген может включать генетические последовательности, полученные из клетки растения, или из клетки другого растения, или из нерастительного источника, или синтетическую последовательность. Как правило, трансген был внесен в растение вследствие вмешательства человека, такого как, например, трансформация, но, как понятно специалисту в данной области техники, можно использовать любой способ. Генетический материал, как правило, стабильно интегрирован в геном растения. Внесенный генетический материал может содержать последовательности, которые встречаются в природе в том же виде, но в перестроенном порядке или с отличным расположением элементов, например в виде антисмысловой последовательности или последовательности, экспрессирующей ингибиторную двухцепочечную РНК. Согласно данному документу растения, содержащие такие последовательности, включены в понятие «трансгенные растения». Трансгенные растения по определению данного документа включают все потомство изначально трансформированного и регенерированного растения (растения T0), которое было генетически модифицировано рекомбинантными методами, при этом потомство содержит трансген. Такое потомство можно получать путем самоопыления первичного трансгенного растения или путем скрещивания таких растений с другим растением того же вида. В одном варианте реализации трансгенные растения являются гомозиготными в отношении каждого гена, который был внесен (трансгена), так, что их потомство не разделяется по необходимому фенотипу. Части трансгенных растений включают все части и клетки указанных растений, которые содержат трансген, например, семена, культивируемые ткани, каллус и протопласты.
[0241] «Нетрансгенное растение», предпочтительно нетрансгенное растение пшеницы, представляет собой растение, которое не было генетически модифицировано путем введения генетического материала посредством технологий рекомбинантных ДНК. Согласно данному документу присутствие в растении или зерне делеций части гена, созданных сайт-специфическими эндонуклеазами, такими как ZFN, TAL-эффекторы или нуклеазы типа CRISPR, с последующим негомологичным соединением концов в клетке растения и его потомства включены в понятие «нетрансгенный». В контексте данного документа «потомство» включает все потомство растения пшеницы, как в непосредственно следующем, так и в последующих поколениях, и как растения, так и семена (зерно). Потомство включает семена и растения, полученные после самоопыления («самооплодотворения»), а также зерно и растения, полученные в результате скрещивания между двумя родительскими растениями, такое как потомство F1 (первое поколение), при этом F2, F3, F4 и т. д. являются потомством от второго и т. д. поколений после самооплодотворения растений F1.
[0242] В контексте данного документа термин «соответствующее нетрансгенное растение» относится к растению, которое является таким же или сходным по большинству характеристик, предпочтительно изогенным или практически изогенным с трансгенным растением, но не содержит представляющий интерес трансген. Предпочтительно соответствующее нетрансгенное растение принадлежит тому же сорту или вариетету, что и предшественник представляющего интерес трансгенного растения, или родственной линии растений, в которых отсутствует конструкция, часто называемое «сегрегантом», или является растением того же сорта или вариетета, трансформированным конструкцией в виде «пустого вектора», и может быть считающимся нетрансгенным растением.
[0243] В контексте данного документа выражение «дикий тип» относится к клетке, ткани, растению или части растения, предпочтительно растению, части растения или зерну Triticum aestivum, которые не были модифицированы в соответствии с изобретением. Такое растение или зерно дикого типа по меньшей мере имеет дикий тип по отношению к генам SSIIa. «Соответствующий дикий тип» относится к клетке, ткани, растению, части растения или растительному продукту, подходящим для сравнения с клеткой, тканью, растением, частью растения или растительным продуктом согласно изобретению, как общеизвестно в данной области техники. В общем случае соответствующий дикий тип принадлежит растению пшеницы или части растения, генетически сходным, предпочтительно изогенным с растением или частью растения согласно изобретению, но не имеющим мутаций в гене ssIIa. Клетки, ткани или растения дикого типа известны в данной области техники и могут использоваться в качестве контроля для сравнения генных или полипептидных последовательностей, в частности генных последовательностей SSIIa, уровней экспрессии гена SSIIa или степени и природы модификации признака, с клетками, тканями или растениями, модифицированными так, как описано в данном документе. В контексте данного документа выражение «зерно пшеницы дикого типа» означает соответствующее не подвергнутое мутагенезу, нетрансгенное зерно пшеницы. В контексте данного документа конкретные виды зерна пшеницы включают, но не ограничиваются этим, Sunstate, Chara и Cadoux. Сорт пшеницы Sunstate описан в Ellison et al., (1994).
[0244] Любой из нескольких существующих способов можно применять для определения присутствия трансгена в трансформированном растении. Например, можно использовать полимеразную цепную реакцию (ПЦР), чтобы амплифицировать последовательности, уникальные для трансформированного растения, с выявлением амплифицированных продуктов с помощью гель-электрофореза или других способов. ДНК можно выделять из растений, используя традиционные способы и ПЦР-реакции, проводимые с праймерами, которые будут разделять трансформированные и нетрансформированные растения. Альтернативным способом для подтверждения положительных трансформантов является хорошо известная в данной области техники Саузерн-блот-гибридизация. Трансформированные растения пшеницы также можно идентифицировать, т. е. отличить от нетрансформированных или принадлежащих дикому типу растений пшеницы, по их фенотипу, например, обусловленному присутствием гена селективного маркера, или с помощью иммуноанализа, определяющего количество экспрессии фермента, кодируемого трансгеном, или по любому другому фенотипу, обусловленному трансгеном.
[0245] Растения пшеницы, предпочтительно вид Triticum aestivum, согласно настоящему изобретению можно выращивать или собирать для получения зерна, преимущественно для применения в качестве пищи для потребления человеком или в качестве корма для животных, или для ферментации или промышленного производства сырья, такого как производство этанола, помимо прочих применений. В альтернативном варианте зеленые, надземные части растений пшеницы можно непосредственно использовать в качестве корма для животных, как напрямую посредством выпаса, так и после сбора урожая. Солому и мякину также можно использовать в качестве пищи или для непищевых применений. Растение согласно настоящему изобретению предпочтительно подходит для производства пищи и, в частности, для промышленного производства пищи для потребления человеком. Такое производство пищи может включать производство муки, теста, манной крупы или других продуктов из зерна, таких как крахмальные гранулы или выделенный крахмал, которые могут быть ингредиентами в промышленном производстве пищи.
[0246] В контексте данного документа термин «зерно» в общем случае относится к зрелому, собранному семени (также называемому ядром) растения, но также может относиться к зерну после набухания или прорастания, в зависимости от контекста. Зерна включают зрелые ядра, производимые сельхозпроизводителями в целях, отличных от выращивания дополнительных растений. Зрелое зерно злакового растения, такого как пшеница, обычно имеет содержание влаги, составляющее менее чем около 18-20%, как правило, около 8-10% влаги. В контексте данного документа термин «семя» включает собранные семена, но также включает семена, которые развиваются в растении после цветения, и зрелые семена, содержащиеся в растении перед сбором. Части зерна включают кожуру (оболочку семени), перикарпий (оболочку плода), алейроновый слой, крахмалистый эндосперм и эмбрион (зародыш), который состоит из щитка, почечки (проростка) и корешка (первичного корешка). Кожуру, перикарпий и алейроновый слой вместе обычно называются «отрубями», которые можно удалять из зерна с помощью помола, и которые также могут содержать зародыш. Щиток представляет собой область, которая секретирует некоторые ферменты, вовлеченные в прорастание, и абсорбирует растворимые сахара при разрушении крахмала в эндосперме для роста проростка после прорастания. Алейрон, который окружает крахмалистый эндосперм, также секретирует ферменты во время прорастания.
[0247] В контексте данного документа «прорастание» относится к появлению кончика корня (корешка) из оболочки семени после набухания. Сначала обычно появляется корешок, а потом почечка. «Уровень прорастания» относится к проценту семян в популяции, которые проросли в течение некоторого периода времени после набухания, например 7 или 10 суток. Уровни прорастания можно рассчитать, используя известные в данной области техники методики. Например, популяцию семян, как правило, из по меньшей мере 100 зерен, можно ежесуточно оценивать в течение нескольких суток для определения процента прорастания со временем. В отношении зерна согласно настоящему изобретению в контексте данного документа выражение «степень прорастания, являющийся практически аналогичным» означает, что степень прорастания зерна, составляет по меньшей мере 90% от степени соответствующего зерна дикого типа.
В одном варианте реализации зерно согласно изобретению имеет степень прорастания от около 70% до около 100% относительно зерна дикого типа, предпочтительно от около 90% до около 100% относительно зерна дикого типа. При определении уровня прорастания зерно пшеницы согласно изобретению и зерно дикого типа, используемое в качестве контроля, следует выращивать в одинаковых условиях и хранить в одинаковых условиях в течение приблизительно одинакового времени.
[0248] В изобретении также предложены пищевые ингредиенты, такие как мука, предпочтительно цельнозерновая, отруби и другие продукты, производимые из зерна. Они могут быть необработанными или обработанными, например, с помощью термической обработки, фракционирования или отбеливания.
[0249] Зерно согласно изобретению можно обрабатывать, чтобы получить пищевой ингредиент или пищевой или непищевой продукт, используя известные в данной области техники способы. В одном варианте реализации пищевой ингредиент представляет собой муку, такую как, например, цельнозерновая мука (мука грубого помола) или мука высшего сорта. В контексте данного документа «мука» представляет собой молотый продукт из зерна, которое было перемолото в порошок. Порошок обычно фракционируют путем просеивания, центрифугирования или других известных в данной области техники способов, и могут дополнительно рафинировать, обрабатывать термически и/или отбеливать. Употребляемое в данном документе выражение рафинированная мука или «мука высшего сорта» относится к муке, которая была обогащена полученной из эндосперма частью молотого порошка по сравнению с цельнозерновой мукой, что осуществляется посредством удаления по меньшей мере некоторого количества отрубей и зародышевых компонентов из молотого порошка. Управление по контролю пищевых продуктов и лекарственных средств США (FDA) требует, чтобы мука отвечала определенным стандартам размеров частиц для того, чтобы быть включенной в категорию рафинированной муки. В соответствии с FDA размер частиц рафинированной муки описывается как мука, для которой не менее 98% проходит через материал с отверстиями не более чем у металлотканого материала с обозначение «212 микрометров (U.S. Wire 70)».
[0250] В контексте данного документа «цельнозерновая мука», также называемая мукой грубого помола или цельномолотой мукой, представляет собой молотую муку, которая была получена практически из 100% зерна и которая содержит составляющую рафинированной муки (муки высшего сорта) и грубую фракцию (грубую фракцию ультрамелкого помола). Грубая фракция содержит по меньшей мере один компонент из отрубей и зародышей, как правило, оба. Зародыш представляет собой растение в зачаточном состоянии в ядре зерна, содержащее эмбрион и щиток. Зародыш содержит липиды, волокна, витамины, белок, минеральные и фитопитательные вещества, такие как флавоноиды, на уровнях, больших чем в зрелом эндосперме зерна. Отруби включают несколько клеточных слоев, включая перикарпий (оболочку плода) и кожуру (оболочку семени), и также содержат значительно количество липидов, волокон, витаминов, белка, минералов и фитопитательных веществ, таких как флавоноиды. Алейроновый слой, хотя технически считается частью эндосперма зрелого зерна, во многом демонстрирует такие же характеристики, что и отруби, и, следовательно, как правило, удаляется вместе с отрубями и зародышем во время процесса помола и/или просеивания. Алейроновый слой также содержит липиды, волокна, витамины, белок, минеральные и фитопитательные вещества, такие как флавоноиды, и феруловую кислоту.
[0251] Кроме того, грубую фракцию можно смешивать с составляющей рафинированной муки. Предпочтительно грубую фракцию гомогенно смешивают с составляющей рафинированной муки. Грубую фракцию можно смешивать с составляющей рафинированной муки для получения цельнозерновой муки, обеспечивая, таким образом, цельнозерновую муку с повышенными питательной ценностью, содержанием волокон и антиоксидантной способностью по сравнению с рафинированной мукой. Например, грубую фракцию или цельнозерновую муку можно использовать в различных количествах для замещения рафинированной муки в выпечке, закусочных продуктах и пищевых продуктах. Цельнозерновую муку согласно настоящему изобретению (т. е. цельнозерновую муку ультрамелкого помола) также можно непосредственно продавать потребителям для использования в домашней выпечке. В типовом варианте реализации профиль гранулирования цельнозерновой муки является таким, что 98% частиц по массе цельнозерновой муки имеют диаметр менее 212 микрометров.
[0252] В дополнительных вариантах реализации ферменты, содержащиеся в отрубях и зародышах цельнозерновой муки и/или грубой фракции, инактивированы для стабилизации цельнозерновой муки и/или грубой фракции. В настоящем изобретении подразумевается, что «инактивированный» также может означать ингибированный, денатурированный и т. п. Стабилизация представляет собой процесс, в котором используется пар, нагрев, излучение или другие виды обработки для инактивации ферментов, содержащихся в отрубях и зародышевом слое. В отсутствие стабилизации ферменты природного происхождения в отрубях и зародышах катализируют изменения в соединениях в муке, что может оказывать негативное влияние на кулинарные характеристики муки и ее срок годности. Инактивированные ферменты не катализируют изменения в соединениях, содержащихся в муке, следовательно, стабилизированная мука сохраняет свои кулинарные характеристики и имеет больший срок годности. Например, в настоящем изобретении можно применять два способа потокового помола для измельчения грубой фракции. После отделения и стабилизации грубой фракции ее измельчают на дробилке, предпочтительно вальцовой мельнице, для образования грубой фракции, имеющей распределение размера частиц, меньшее или равное приблизительно 500 микрометрам. После просеивания измельченную грубую фракцию, имеющую размер частиц более 500 микрометров, можно возвращать в процесс для дополнительного размола.
[0253] В дополнительных вариантах реализации мука, цельнозерновая мука или грубая фракция могут быть компонентами пищевого продукта, например, их можно использовать в качестве ингредиента в производстве пищи. Пищевой продукт может представлять собой, например, бублик, бисквит, хлеб, сдобную булочку, круассан, клецки, маффин, такой как английский маффин, питу, бездрожжевой хлеб, замороженные или охлажденные продукты из теста, тесто, консервированную фасоль, буррито, чили, тако, тамал, тортилью, закрытый пирог, готовый к употреблению зерновой продукт, готовое к употреблению блюдо, начинку, разогреваемое в микроволновке блюдо, брауни, пирог, чизкейк, кекс к кофе, печенье, десерт, кондитерские изделия, сладкий ролл, сладкий батончик, корку пирога, начинку пирога, детское питание, смесь для выпечки, жидкое тесто, панировку, смесь для подливы, мясной наполнитель, мясной заменитель, смесь специй, суповую смесь, подливу, заправку для соуса, заправку для салата, суп, сметану, лапшу, пасту, лапшу рамен, лапшу чоу-мейн, лапшу ло-мейн, мороженое в упаковке, брикет мороженого, рожок мороженого, мороженое в вафлях, крекер, крутон, пончик, эгг ролл, прессованные закуски, фруктово-зерновой батончик, разогреваемый в микроволновке закусочный продукт, питательный батончик, панкейк, полуфабрикат хлебобулочного продукта, крендель, пудинг, продукт на основе гранолы, закуску из чипсов, закуску, смесь закусок, вафлю, основу для пиццы, корм для животных или корм для домашних животных.
[0254] В других вариантах реализации мука, цельнозерновая мука или грубая фракция могут быть компонентами питательной добавки. Например, питательная добавка может представлять собой продукт, добавляемый в рацион, содержащий один или более ингредиентов, как правило, включающих: витамины, минеральные вещества, липиды, такие как омега-3 жирные кислоты, аминокислоты, ферменты, антиоксиданты, такие как лютеин, травы, специи, пробиотики, экстракты, пребиотики и волокна. Мука, цельнозерновая мука или грубая фракция согласно настоящему изобретению содержат витамины, минералы, аминокислоты, ферменты и волокна. Например, грубая фракция содержит концентрированное количество пищевых волокон, а также другие важные питательные вещества, такие как витамины B, селен, хром, марганец, магний и антиоксиданты, которые важны для здорового питания. Например, 15 граммов грубой фракции согласно настоящему изобретению обеспечивают 33% индивидуального рекомендуемого суточного потребления волокон. Кроме того, всего 9 граммов достаточно для обеспечения 20% индивидуального рекомендуемого суточного потребления волокон. Таким образом, грубая фракция является превосходным дополнительным источником для потребления индивидуально необходимого количества волокон.
[0255] В дополнительных вариантах реализации цельнозерновая мука или грубая фракция могут быть добавкой, содержащей волокна, или ее компонентом. Многие современные содержащие волокна добавки, такие как шелуха семян подорожника, производные целлюлозы и гидролизованная гуаровая камедь, имеют ограниченную питательную ценность, помимо содержания в них волокон. Кроме того, многие содержащие волокна добавки имеют нежелательную текстуру и плохой вкус. Следовательно, в варианте реализации в пищевых ингредиентах согласно изобретению отсутствуют содержащие волокна добавки, полученные из источников, отличных от пшеничного зерна. Добавки, полученные из цельнозерновой муки или грубой фракции зерна пшеницы, таким образом, обеспечивают волокна, а также белок и антиоксиданты. Содержащая волокна добавка может быть предоставлена, без ограничений, в следующих формах: смеси для напитков быстрого приготовления, готовые к употреблению напитки, питательные батончики, вафли, печенье, крекеры, гели, капсулы, жвачка, жевательные таблетки и пилюли. В одном варианте реализации содержащая волокна добавка предоставлена в форме ароматизированного коктейля или солодового напитка, этот вариант реализации может быть в особенности привлекательным в качестве содержащей волокна добавки для детей.
[0256] В дополнительном варианте реализации процесс помола и смешивания можно использовать для получения мультизерновой муки или мультизерновой грубой фракции. Например, отруби и зародыши из одного типа зерна, такого как зерно согласно изобретению, можно измельчать и смешивать с измельченным эндоспермом или цельнозерновой мукой другого типа пшеницы или другого злака. Подразумевается, что настоящее изобретение включает смешивание любой комбинации одного или более компонента из отрубей, зародышей, эндосперма и цельнозерновой муки из одного или более типов зерен. Такой мультизерновой подход можно использовать для производства обычной муки и извлечения пользы из качества и содержания питательных веществ из многих типов зерен, таких как пшеничные зерна, для получения муки.
[0257] Муку или цельнозерновую муку согласно настоящему изобретению можно получать с помощью любого процесса помола, известного в данной области техники. Типовой вариант реализации включает измельчение зерна в одном потоке без разделения эндосперма, отрубей и зародышей зерна по отдельным потокам. Чистое и кондиционированное зерно переносят в дробилку для первого прохода, такую как молотковая дробилка, вальцовая мельница, штифтовая мельница, ударная дробилка, дисковая мельница, воздушная жерновая мельница, вальцовая мельница и т. п. После измельчения зерно выгружают и переносят на сито. Можно использовать любое сито, известное в данной области техники, для просеивания измельченных частиц. Материал, проходящий через сетку сита, представляет собой цельнозерновую муку согласно настоящему изобретению и не требует дополнительной обработки. Материал, который остается на сите, называется второй фракцией. В случае второй фракции необходимо дополнительное измельчение частиц. Таким образом, вторую фракцию можно переносить в дробилку для второго прохода. После измельчения вторую фракцию можно переносить на второе сито.
[0258] Подразумевается, что муку, цельнозерновую муку, грубую фракцию и/или зерновые продукты согласно настоящему изобретению можно модифицировать или улучшать их качества посредством многочисленных других процессов, таких как: ферментация, инстантизация, экструзия, инкапсулирование, запекание, обжаривание и т. п. Мука и цельнозерновая мука согласно изобретению могут содержать генетический материал, включая ДНК, зерна пшеницы, из которого они были получены, как и приготовленные из них продукты. Смотрите, например, Tilley (2004) и Bryan et al., (1998).
[0259] Солодовые напитки, предложенные в настоящем изобретении, включают алкогольные напитки (включая дистиллированные напитки) и безалкогольные напитки, которые производятся с применением солода в качестве части или всего исходного материала. Примеры включают пиво, хаппосю (низкосолодовое пиво), виски, слабоалкогольные солодовые напитки (например, солодовые напитки, содержащие менее 1% алкоголя) и безалкогольные напитки.
[0260] Солодование представляет собой процесс контролируемого намачивания и проращивания с последующим высушиванием зерна. Эта последовательность действий важна для синтеза многочисленных ферментов, которые вызывают модификацию зерна - процесс, который, главным образом, приводит к деполимеризации клеточных стенок мертвого эндосперма и мобилизует питательные вещества зерна. В последующем процессе сушки вследствие реакций химического потемнения формируются вкус и цвет. Хотя основное применение солода связано с производством напитков, его также можно использовать в других промышленных процессах, например, в качестве источника ферментов в хлебопекарной промышленности или в качестве вкусового агента и красителя в пищевой промышленности, например в виде солода или солодовой муки, или непрямым образом в виде солодового сиропа и т. д.
[0261] В одном варианте реализации настоящее изобретение относится к способам получения солодовой композиции. Этот способ предпочтительно включает этапы:
(i) обеспечения зерна пшеницы согласно изобретению,
(ii) намачивания указанного зерна,
(iii) проращивания намоченных зерен в заданных условиях и
(iv) сушки указанных пророщенных зерен.
[0262] Солод можно готовить, используя только зерно согласно изобретению, или в смеси, содержащей другие зерна. Солод, главным образом, используется для пивоварения, но также для производства дистиллированных алкогольных напитков. Пивоварение включает производство сусла, основную и вторичную ферментации и последующую обработку. Сначала солод размалывают, вмешивают в воду и нагревают. Во время этого «затирания» ферменты, активируемые при солодовании, расщепляют крахмал ядра на ферментируемые сахара. Полученное сусло осветляют, добавляют дрожжи, а смесь ферментируют и проводят последующую обработку.
[0263] В общем случае первым этапом в процессе производства сусла является размалывание солода, чтобы вода могла получить доступ к частицам зерна во время фазы затирания, которая по большому счету является продолжением процесса солодования с ферментативной деполимеризацией субстрата. Во время затирания молотый солод инкубируют с жидкой фракцией, такой как вода. Температуру либо поддерживают постоянной (изотермическое затирание) или постепенно повышают. В любом случае растворимые вещества, образуемые при солодовании и затирании, экстрагируются в указанную жидкую фракцию перед ее разделением посредством фильтрации на сусло и остаточные твердые частицы, называемые пивной дробиной. Композицию сусла также можно получать путем инкубации зерна пшеницы согласно изобретению или его частей с одним или более подходящими ферментами, такими как композиции ферментов или композиции смесей ферментов, например, Ultraflo или Cereflo (Novozymes). Композицию сусла также можно получать, используя смесь солода и не прошедших солодование растений или их частей, необязательно, добавляя один или более подходящих ферментов во время получения.
[0264] При включении в пищевые продукты крахмал из муки или цельнозерновой муки обеспечивает модифицированные пищеварительные свойства, например, пищевой ингредиент содержит больше резистентного крахмала по сравнению с соответствующим пищевым ингредиентом, полученным из зерна пшеницы дикого типа, например от 1% до 20%, от 2% до 18%, от 3% до 18% или от 5% до 15% резистентного крахмала, и имеет сниженный гликемический индекс (ГИ), например, сниженный по меньшей мере на 5 единиц, предпочтительно на 5-25 единиц. Это может идти в комбинации с повышенным общим содержанием волокон, например, составляющим в пищевом ингредиенте от 15% до 30% по массе.
[0265] Углеводы, соединения, содержащие одну или более сахаридных единиц, состоящих из углерода, водорода и кислорода, можно классифицировать в соответствии с числом и составом моносахаридных единиц, составляющих углевод. Они включают полисахариды (> 10 моносахаридных единиц), олигосахариды (3-10 моносахаридных единиц), дисахариды и моносахариды, включая глюкозу, фруктозу, ксилозу и арабинозу. Углеводы составляют более чем 65% по массе зрелого зерна пшеницы дикого типа, в том числе 65-75% крахмала и около 10% полисахаридов клеточных стенок, таких как целлюлоза, арабиноксилан и БГ.
[0266] Крахмал является основным запасаемым углеводом в большинстве растений, включая злаковые, такие как пшеница. По определению данного документа «крахмал» представляет собой полисахарид, состоящий из единиц глюкопиранозы, полимеризованных посредством α-1,4-связей и с отсутствием или с несколькими α-1,6-связями. Крахмал синтезируется в амилопластах и образуется и запасается в гранулах развивающегося запасающего органа, такого как зерно; в данном документе он называется «запасенным крахмалом» или «зерновым крахмалом», или «крахмалом зерна». В зернах злаковых, включая Triticum aestivum, подавляющее большинство запасенного крахмала откладывается в эндосперме в виде крахмальных гранул. Крахмал синтезируется и запасается в амилопластах во время развития зерна, в частности во время фазы налива зерна при росте растения, и образует дискретные кристаллические структуры, называемые крахмальными гранулами. В Triticum aestivum гранулы крахмала делятся по размеру на два класса, а именно большие эллипсоидные гранулы с диаметром в диапазоне 10-40 мкм (гранулы A-типа) и меньшие сферические гранулы с диаметром в диапазоне 1-10 мкм (гранулы B-типа).
[0267] Молекулы крахмала классифицируют как принадлежащие к двум фракциям компонентов, известным как амилоза и амилопектин, которые отличаются по степени полимеризации (СП) и соотношению между α-1,6- и α-1,4-связями в полимерах. Амилоза содержит практически полностью линейные α-1,4-связанные глюкозильные цепи, которые могут не содержать или содержать несколько глюкановых цепей, соединенных α-1,6-связью с другими α-1,4-связанными цепями, и имеет молекулярную массу 104-105 дальтон. Согласно определению данного документа термин «амилоза» включает по существу линейные молекулы α-1,4-связанных глюкозидных (глюкопиранозных) единиц, иногда называемые «истинной амилозой», и амилозо-подобный длинноцепочечный крахмал, который иногда называется «промежуточным материалом» или «амилозо-подобным амилопектином», который является йод-связывающим материалом в йодометрическом анализе наряду с истинной амилозой (Takeda et al., 1993; Fergason, 1994). Линейные молекулы в истинной амилозе, как правило, имеют СП, составляющую от 500 до 5000, и содержат менее 1% α-1,6-связей. Недавние исследования показали, что в амилозе может находиться около 0,1% α-1,6-гликозидных участков ветвления, следовательно, она описывается как «по существу линейная». В этом контексте процент (%) относится к числу α-1,6-гликозидных связей по отношению к общему числу гликозидных связей, представляющему сумму α-1,4-гликозидных связей и α-1,6-гликозидных связей. Связанная с гранулами крахмальная синтаза (GBSS) является основным ферментом, вовлеченным в синтез амилозы.
[0268] Амилопектин представляет собой относительно сильно разветвленный глюкановый полимер, в котором α-1,4-связанные глюкозильные цепи с 3-60 глюкозильными единицами соединены α-1,6-связями так, что приблизительно 4-6% от общего числа глюкозильных связей являются α-1,6-связями. Следовательно, амилопектин является намного большей молекулой с СП в диапазоне от 5000 до 500000 и разветвлен сильнее, чем амилоза. Амилоза имеет спиральную конформацию с молекулярной массой от около 104 до около 106 Дальтон, тогда как амилопектин имеет молекулярную массу от около 107 до около 108 Дальтон. Эти два типа крахмала можно легко различить или разделить способами, хорошо известными в данной области техники, например, с помощью эксклюзионной хроматографии или по их разной аффинности связывания в отношении йода. Амилоза более медленно расщепляется α-амилазами в тонком кишечнике, чем амилопектин, при этом последний имеет множество участков для ферментативного гидролиза вследствие своей сильно разветвленной структуры.
[0269] Крахмал из зерна Triticum aestivum дикого типа, как правило, содержит 20%-30% амилозы и около 70%-80% амилопектина по данным измерения йодометрическим способом, тогда как крахмал из зерна согласно изобретению имеет содержание амилозы от около 45% до около 70% в массовом отношении. Содержание амилозы может составлять от 45% и 70%, в некоторых вариантах реализации - от 45% до 65%, или около 50%, около 55%, около 60% или около 65%. Чем выше уровень, тем более предпочтительным является зерно. Доля амилозы в крахмале по определению данного документа приведена на основании масса/масса (масс./масс.), т. е. как масса амилозы в виде процентной доли от массы общего крахмала, экстрагируемого из зерна, по отношению к крахмалу до фракционирования на фракции амилозы и амилопектина. Термины «доля амилозы в крахмале» и «содержание амилозы», употребляемые в данном документе в контексте зерна, муки или другого продукта согласно изобретению, являются по существу взаимозаменяемыми терминами. Содержание амилозы можно определять любыми способами, известными в данной области техники, включая эксклюзионную высокоэффективную жидкостную хроматографию (ВЭЖХ), например, в 90% (масс./об.) ДМСО, способы с применение конканавалина А (Megazyme Int, Ирландия), или, предпочтительно, йодометрическим методом, например, описанным в примере 1. Метод ВЭЖХ может включать деветвление крахмала (Batey and Curtin, 1996) или не включать деветвление. Следует понимать, что такие методы, как метод ВЭЖХ по Batey and Curtin, 1996, в которых анализируется только «истинная амилоза», могут привести к недооценке содержания амилозы по определению данного документа. Такие методы, как ВЭЖХ или гель-проникающая хроматография, зависят от фракционирования крахмала на фракции амилозы и амилопектина, тогда как йодометрические методы зависят от дифференциального связывания йода и, следовательно, не требуют фракционирования.
[0270] По массе зерна и содержанию амилозы можно рассчитать количество амилозы, которое откладывается в расчете на зерно, и сравнить между исследуемыми и контрольными линиями.
[0271] Крахмал можно легко выделять из зерна пшеницы, используя стандартные способы, например способ Schulman and Kammiovirta, 1991. В промышленном масштабе можно использовать влажный или сухой помол. Размер крахмальной гранулы важен для промышленной обработки крахмала, которая может включать отделение более крупных гранул А от меньших гранул B.
[0272] Выращиваемая промышленно пшеница дикого типа имеет содержание крахмала в зерне, которое обычно находится в диапазоне 55-75%, в некоторой мере завися от выращиваемого сорта. По сравнению с этим зерно согласно изобретению имеет содержание крахмала, составляющее от около 25% до около 70%, таким образом, в большинстве вариантов реализации содержание крахмала снижено по сравнению с соответствующим зерном дикого типа. В вариантах реализации содержание крахмала в зерне согласно изобретению составляет от 25% до 65%, от 25% до 60%, от 25% до 55%, от 25% до 50%, от 30% до 70%, от 30% до 65%, от 30% до 60%, от 30% до 55% или от 30% до 50%. В дополнительных вариантах реализации содержание крахмала составляет около 35%, около 40%, около 45%, около 50%, около 55%, около 60% или около 65% в виде процентной доли от массы зерна (масс./масс.). Содержание крахмала в зерне согласно изобретению также можно определять в относительных величинах, т. е. относительно содержания крахмала в соответствующем зерне дикого типа. В вариантах реализации содержание крахмала составляет от около 50% до около 90% или от 50% до 80%, от 50% до 75%, от 50% до 70%, от 60% до 90% или от 60% до 80% относительно содержания в зерне дикого типа. Содержание крахмала также может составлять от 90% до 100% относительно содержания крахмала в зерне дикого типа. В каждом случае сравнение следует проводить, выращивая растения в одинаковых условиях, например в полевых исследованиях.
[0273] Муку, крахмальные гранулы и отруби согласно изобретению можно получать из зерна с помощью процесса помола, за которым необязательно следует процесс просеивания. Очищенный крахмал также можно получать из зерна с помощью процесса помола, например процесса влажного помола, с последующим дополнительным отделением крахмала от белка, масла и волокон зерна. В контексте данного документа термин «молотый продукт» относится к продукту, полученному при измельчении зерна, предпочтительно зерна пшеницы согласно изобретению, и включает муку (например, цельнозерновую муку), промежуточные продукты (также известные как пшеничная мучка), отруби (включая зародыши) и крахмальные гранулы. Промежуточные продукты обычно находятся в форме гранулярных частиц и включают отруби и зародыши из зерна, и, как правило, содержат около 18% белка, 20-30% крахмала и около 5-6% липидов. Эта фракция, получаемая в процессе помола, является относительно богатой питательными веществами по сравнению с мукой высшего сорта. Форма зерна является признаком, который может влиять на промышленную пригодность растения, так как форма может иметь влияние на легкость помола зерна или какое-либо еще влияние. Намол является важным параметром для промышленной пригодности зерна. Намол зерна согласно изобретению может быть снижен по меньшей мере на 10% относительно зерна дикого типа, но в альтернативном варианте может быть таким же, как у зерна дикого типа.
[0274] В другом аспекте в изобретении предложены гранулы крахмала или крахмал, полученные из зерна или растения согласно изобретению. Крахмал гранул имеет повышенную долю амилозы и сниженную долю амилопектина по сравнению с гранулами крахмала пшеницы дикого типа. Исходный продукт процесса помола представляет собой смесь или композицию, которая содержит гранулы крахмала, такие как, например, мука высшего сорта или цельнозерновая мука, и, следовательно, изобретение включает такие гранулы. Гранулы крахмала из пшеницы дикого типа содержат связанные с крахмальными гранулами белки, включая GBSS, SSI, SBEIIa и SBEIIb, помимо прочих белков, и, следовательно, присутствие этих белков отличает крахмальные гранулы пшеницы от крахмальных гранул других злаковых. В противоположность этому, гранулы крахмала из зерна пшеницы согласно изобретению содержат GBSS пшеницы, включая полипептиды GBSS, кодируемые каждым из геномов A, B и D гексаплоидной пшеницы, но имеют сниженное содержание полипептида SSIIa, а в действительности в некоторых вариантах реализации полипептид SSIIa отсутствует. Эти гранулы крахмала также могут содержать сниженные уровни одного или более, или всех полипептидов SSI, SBEIIa и SBEIIb пшеницы, даже если зерно пшеницы принадлежит дикому типу в отношении генов, кодирующих эти ферменты. Гранулы крахмала из зерна пшеницы согласно изобретению, как правило, имеют деформированную форму и морфологию поверхности при наблюдении в световом микроскопе, смотрите пример 7, в частности, в отношении зерна пшеницы, имеющего содержание амилозы, составляющее по меньшей мере 45% или по меньшей мере 50% в виде процента от общего содержания крахмала в зерне. В одном варианте реализации по меньшей мере 50%, предпочтительно по меньшей мере 60% или по меньшей мере 70%, более предпочтительно по меньшей мере 80% крахмальных гранул, полученных из зерна согласно изобретению, имеют искривленную форму и/или морфологию поверхности. Гранулы крахмала также демонстрируют снижение двулучепреломления при наблюдении в поляризованном свете. Смотрите, например, пример 7 данного документа в отношении определения уровня двулучепреломления. Например, менее 50% или менее 25% гранул крахмала демонстрируют «мальтийский крест», наблюдаемый при наблюдении гранул крахмала дикого типа в поляризованном свете.
[0275] Крахмал из крахмальных гранул можно очищать путем удаления белков после разрушения и диспергирования крахмальных гранул путем термической и/или химической обработки. Крахмал из зерна, крахмал из крахмальных гранул и очищенный крахмал согласно изобретению можно дополнительно охарактеризовать одним или более, или всеми из следующих свойств:
i) содержание амилозы в нем составляет по меньшей мере 45% (масс./масс.), предпочтительно от 45% до 70% в массовом отношении или по меньшей мере 50% (масс./масс.), или около 60% (масс./масс.) амилозы в виде доли от общего содержания крахмала;
ii) содержание по меньшей мере 2% резистентного крахмала, предпочтительно по меньшей мере 3% резистентного крахмала;
iii) крахмал характеризуется сниженным гликемическим индексом (ГИ);
iv) гранулы крахмала имеют деформированную форму;
v) гранулы крахмала имеют сниженное двулучепреломление при наблюдении в поляризованном свете;
vi) крахмал характеризуется сниженным объемным разбуханием;
vii) модифицированные распределение по длинам цепей и/или частота ветвления в крахмале;
viii) крахмал характеризуется сниженной пиковой температурой желатинизации;
ix) крахмал характеризуется сниженной пиковой вязкостью;
x) снижена температура клейстеризации крахмала;
xi) снижена пиковая молекулярная масса амилозы при определении методом эксклюзионной хроматографии;
xii) снижена степень кристаллизации крахмала; и
xiii) снижена доля крахмала A-типа и/или B-типа и/или повышена доля кристаллического крахмала V-типа;
при этом каждое свойство определяется в сравнении с гранулами крахмала или крахмалом пшеницы дикого типа.
[0276] Муку или крахмал согласно изобретению также можно охарактеризовать по объемному разбуханию в нагретом избыточном количестве воды по сравнению с мукой или крахмалом дикого типа. Объемное разбухание, как правило, измеряют, смешивая крахмал или муку с избытком воды и нагревая до повышенных температур, как правило, более 90°C. Затем путем центрифугирования получают образцы, а объемное разбухание выражают как массу осажденного материала, деленную на сухую массу образца. Низкие характеристики разбухания целесообразны при необходимости повысить содержание крахмала в пищевом образце, в частности в увлажненном пищевом образце. Мука или крахмал согласно изобретению предпочтительно имеют сниженное объемное разбухание, например сниженное на 30-70% по сравнению с пшеничной мукой или крахмалом дикого типа.
[0277] Одним из показателей изменения в структуре амилопектина является распределение по длинам цепей или степень полимеризации крахмала. Распределение по длинам цепей можно определять, используя метод электрофореза углеводов с использованием флуорофоров (FACE) с последующим деветвлением изоамилазой. Амилопектин из крахмала согласно изобретению может иметь распределение по длинам цепей в диапазоне от 5 до 60, или в поддиапазоне, таком как СП 7-11, что больше, чем соответствующее распределение по длинам цепей для крахмала из растений дикого типа, и/или характеризоваться сниженной частотой в других поддиапазонах, например, СП 12-24. Смотрите, например, пример 7 в данном документе. Крахмал с большей длиной цепей также характеризуется соизмеримым снижением частоты ветвления. Крахмал зерна согласно изобретению отчетливо характеризуется от крахмала зерна пшеницы, имеющего сниженную активность SBEIIa (Regina et al., 2006), в котором амилопектин зерна содержит повышенную долю фракции с длинами цепей СП 4-12 по сравнению с амилопектином зерна дикого типа согласно измерениям после деветвления амилопектина изоамилазой. Эту разницу можно легко определить методом FACE.
[0278] В другом аспекте изобретения пшеничный крахмал может иметь измененную температуру желатинизации, предпочтительно сниженную температуру желатинизации, которую легко измерить методом дифференциальной сканирующей калориметрии (ДСК). Желатинизация представляет собой термически индуцированное нарушение (разрушение) молекулярного упорядочения в грануле крахмала в избыточном количестве воды с одновременными и необратимыми изменениями в свойствах, таких как объемное разбухание, плавление кристаллитов, утрата двулучепреломления, появление вязкости и солюбилизация крахмала. Температура желатинизации может быть как повышена, так и снижена по сравнению с крахмалом из растений дикого типа в зависимости от длин цепей оставшегося амилопектина. Высокоамилозный крахмал из мутантов кукурузы с удлиненной амилозой (ae) демонстрировал более высокую температуру желатинизации, чем нормальная кукуруза (Fuwa et al., 1999; Krueger et al., 1987).
[0279] Температура желатинизации, в частности температура появления первого пика или температура вершины первого пика, может быть снижена по меньшей мере на 3°C, предпочтительно по меньшей мере на 5°C или более предпочтительно по меньшей мере на 7°C согласно измерениям ДСК по сравнению с крахмалом, экстрагированным из сходного, но не содержащего изменений зерна. Крахмал может содержать повышенный уровень резистентного крахмала, при этом на изменение в структуре указывают конкретные физические характеристики, включая одну или более из группы, состоящей из физической недоступности для пищеварительных ферментов, что может быть причиной изменений в морфологии гранул крахмала, присутствия существенного количества связанных с крахмалом липидов, изменения кристалличности и изменения распределения по длинам цепей для амилопектина. Высокая доля амилозы также влияет на уровень резистентного крахмала, когда крахмал нагревают, а затем охлаждают.
[0280] Структура крахмала пшеницы согласно настоящему изобретению также может отличаться снижением степени кристалличности и/или модифицированным типом кристалличности по сравнению с крахмалом, выделенным из зерна пшеницы дикого типа. Кристалличность, как правило, исследуют методом рентгеноструктурной кристаллографии. Снижение кристалличности крахмала также считается связанным с повышением органолептических свойств и является причиной более гладкого ощущения во рту.
[0281] В изобретении также предложены зерно пшеницы, мука, цельнозерновая мука, гранулы крахмала и крахмал из зерна, содержащего повышенные количества пищевых волокон вследствие по меньшей мере повышения уровня РК, но также вследствие повышения уровней других компонентов пищевых волокон, таких как арабиноксиланы, β-глюкан и фруктаны. В контексте данного документа выражения «пищевые волокна» (ПВ) или «общее содержание пищевых волокон» (ОПВ) означают суммарное количество углеводных полимеров в пище, которые не расщепляются в тонком кишечнике здорового человека и оказывают полезное физиологическое действие в толстом кишечнике. В контексте данного документа ПВ характеризуется от «общего содержания пищевых волокон» (ниже). ПВ не расщепляются и не всасываются в тонком кишечнике, а проходят в толстую кишку, где они могут подвергаться деградации бактериями. ПВ включают РК, не-α-глюкановые олигосахариды и некрахмальные полисахариды (НКП), такие как арабиноксиланы, β-глюкан и фруктаны. ПВ обычно разделяют на формы, которые растворимы в воде (растворимые волокна) или нерастворимы (нерастворимые волокна), и РК. Наиболее полезной для здоровья фракцией пищевых волокон в зерне пшеницы дикого типа являются растворимые волокна, которые, главным образом, содержат компонент арабиноксилана (AК), так как крахмал дикого типа имеет очень низкое содержание РК. В противоположность этому, в овсе и ячмене растворимые волокна представлены главным образом БГ. Национальный фонд кардиологии Австралии рекомендует ежесуточное потребление 30-35 г ПВ для здоровья сердечно-сосудистой системы и толстого кишечника. В пшенице было идентифицировано множество кандидатных генов, которые влияют на содержание пищевых волокон (Quraishi et al., 2011), но ни один из них не обеспечивает уровень, обеспечиваемый зерном согласно изобретению. ПВ можно определять методом AOAC 991.43 (Megazyme).
[0282] В контексте данного документа термин «пребиотический» означает неперевариваемый (пищеварительными ферментами человека) пищевой ингредиент, который благоприятно влияет на субъекта, избирательно стимулируя рост и/или активность одной бактерии или ограниченного числа бактерий в толстой кишке после прохождения тонкого кишечника. Например, фруктаны и БГ не могут перевариваться иначе, чем посредством бактериальной активности, но могут менять композицию микроорганизмов в человеческом кишечнике посредством специфической ферментации, вырабатывая короткоцепочечные карбоновые кислоты, включая ацетат, пропионат и бутират.
[0283] В вариантах реализации зерно пшеницы, мука, гранулы крахмала и крахмал согласно изобретению обеспечивают модифицированные пищеварительные свойства, такие как повышенное количество резистентного крахмала. В контексте данного документа «резистентный крахмал» (РК) относится к крахмалу и продуктам расщепления крахмала, которые не всасываются в тонком кишечнике здоровых индивидов, но попадают в толстый кишечник. Его определяют в терминах процента от общего крахмала в зерне или процента от общего содержания крахмала в пище в зависимости от контекста. Следовательно, резистентный крахмал исключает продукты, расщепляемые и всасываемые в тонком кишечнике. Следовательно, РК является частью содержания пищевых волокон в пищевом ингредиенте (муке и т. д.) или пищевом продукте согласно изобретению. РК делится на пять категорий: физически недоступный крахмал (РКI), такой как, например, неполностью перемолотое зерно, гранулы резистентного крахмала (РКII), такие как, например, встречающиеся в небольших количествах в картофеле и зеленых бананах, ретроградный крахмал (РКIII), который образуется при охлаждении желатинизированного крахмала в течение длительного периода времени, химически модифицированный крахмал (РКIV), такой, как образуется при этерификации или эстерификации свободных гидроксильных групп в гликозильных остатках, и крахмал, способный образовывать комплексы между амилозой или длинными разветвленными цепями амилопектина и липидами (РКV) (Birt et al., 2013). В частности, РКIII образуется из более длинных цепей амилозы, которые имеют склонность к перекристаллизации и образованию ретроградного крахмала после желатинизации. РК в продуктах на основе крахмала с повышенным содержанием амилозы представляет собой, главным образом, ретроградную амилозу (Hung et al., 2006). Считается, что повышенное количество РК в крахмале зерна, крахмальных гранулах, крахмале и продуктах из них согласно изобретению связано с повышением содержания РКII и РКV, а также РКIII после ретроградации, если крахмал нагревают, а затем охлаждают, по сравнению с соответствующим продуктом дикого типа. Ассоциация крахмал-липид при определении кристалличности V-комплекса также, вероятно, влияет на уровень резистентного крахмала, повышая компонент РКV за счет повышения содержания липидов в зерне согласно изобретению. Некоторая часть крахмала также может находиться в форме РКI, которая в некоторой степени недоступна для расщепления.
[0284] Для определения уровней РК в пищевых ингредиентах или в пище доступно несколько методов, которые все основаны на изначальном удалении перевариваемого крахмала с помощью ферментов, гидролизующих крахмал (Dupuis et al., 2014). В оценке РК по методу Prosky (AOAC 985.29) используется гравиметрическое определение пищевых волокон после расщепления α-амилазой, глюкоамилазой и протеазой (Prosky et al., 1985). Метод McCleary (AOAC 2009.01) является официальным методом AOAC и является коммерчески доступным (Megazyme International, Ирландия). Он является предпочтительным методом определения РК, смотрите пример 1 данного документа. В этом анализе нерезистентный крахмал солюбилизируют путем обработки панкреатической α-амилазой, РК восстанавливают и растворяют в 2 M KOH, а затем гидролизуют до глюкозы амилоглюкозидазой и проводят определение.
[0285] В вариантах реализации крахмал содержит от 2% до 20%, от 2% до 18%, от 3% до 18%, от 3% до 15% или от 5% до 15% резистентного крахмала в массовом отношении в виде процента от общего содержания крахмала. В вариантах реализации содержание РК повышено в 2-10 раз по сравнению с соответствующим пищевым ингредиентом или пищевым продуктом, полученным из эквивалентного количества пшеничного крахмала дикого типа. В вариантах реализации содержание РК повышено в около 3 раз, около 4 раз, около 5 раз, около 6 раз, около 7 раз, около 8 раз или около 9 раз по сравнению с диким типом. Степень повышения количества РК можно корректировать путем смешивания продуктов согласно изобретению с соответствующим продуктом дикого типа. Изменение структуры крахмала и, в частности, высокие уровни амилозы в крахмале согласно изобретению, обеспечивают повышение количества РК при употреблении в виде пищи. РК оказывает благоприятное физиологическое действие, связанное с продуктами метаболизма, выделяемыми во время его ферментации в кишечнике (Topping and Clifton, 2001), в частности КЦЖК бутиратом, пропионатом и ацетатом, и является эффективным для снижения уровней глюкозы в крови после еды.
[0286] Зерно, пищевые ингредиенты и полученные из них пищевые продукты согласно изобретению можно преимущественно использовать для обеспечения рациона или для получения композиций, богатых β-глюканом, целлюлозой, фруктаном или арабиноксиланом, на основании повышенных уровней этих компонентов в зерне согласно изобретению. Клеточные стенки зерен злаковых представляют собой сложные и динамические структуры, состоящие из различных полисахаридов, таких как целлюлоза, ксилоглюканы, пектин (в большом количестве содержится в остатках галактуроновой кислоты), каллоза (1,3-β-D-глюкан), арабиноксиланы (арабино-1,4-β-D-ксилан, далее обозначаемый в данном документе АК) и БГ, а также полифенолов, таких как лигнин. В клеточных стенках травянистых и некоторых других однодольных растений доминируют глюкуроноарабиноксиланы и БГ, а уровни пектиновых полисахаридов, глюкоманнанов и ксилоглюканов являются относительно низкими (Carpita et al., 1993). Эти полисахариды синтезируются большим количеством разнообразных полисахаридных синтаз и гликозилтрансфераз, при этом в растениях представлены по меньшей мере 70 генных семейств и во многих случаях - множество представителей генных семейств.
[0287] В контексте данного документа термин «(1,3;1,4)-β-D-глюкан», также называемый «β-глюканом» и сокращаемый до «БГ», относится к по существу линейному полимеру из незамещенных и по существу неразветвленных мономеров β-глюкопиранозила, ковалентно связанных, главным образом, посредством 1,4-связей, с некоторым количеством 1,3-связей. Остатки глюкопиранозила, соединенные 1,4- и 1,3-связями, упорядочены неповторяющимся, но не случайным образом, т. е. 1,4- и 1,3-связи не являются случайным образом упорядоченными, но также они не упорядочены в виде регулярных, повторяющихся последовательностей (Fincher, 2009a, 2009b). Большинство (около 90%) 1,3-связанных остатков идут за 2 или 3-мя 1,4-связанными остатками в БГ пшеницы, как и в БГ овса и ячменя. Следовательно, БГ может считаться цепью, состоящей в основном из β-1,4-связанных единиц целлотриозила (каждая с 3 остатками глюкопиранозила) и целлотетрозила (каждая с 4 остатками глюкопиранозила), соединенными вместе одинарными β-1,3-связями, с приблизительно на 10% более длинными β-1,4-связанными единицами целлодекстрина из около четырех-десяти 1,4-связанных остатков глюкопиранозила, до около 28 остатков глюкопиранозила (Fincher and Stone, 2004). Как правило, полимеры БГ содержат по меньшей мере 1000 гликозильных остатков и принимают растянутую конформацию в водных средах. Соотношение три- и тетрасахаридных единиц варьируется (соотношение СП3/СП4) для разных видов и, следовательно, является характеристикой БГ, принадлежащего конкретному виду. БГ из разных злаковых отличаются по растворимости, при этом БГ из овса является более растворимым, чем БГ из пшеницы. Считается, что это связано с соотношением между СП3 иСП4 в полимере БГ.
[0288] В зерне пшеницы дикого типа уровни БГ больше в цельном зерне, чем в эндосперме (Henry, 1985). Содержание БГ в цельном пшеничном зерне дикого типа составляло 0,6% в массовом отношении по сравнению с около 4,2% для ячменя, 3,9% для овса и 2,5% для ржи (Henry 1987). В зерне пшеницы дикого типа диапазон составлял 0,4-1,4% по массе (Lazaridou et al., 2007). БГ из зерна пшеницы, как правило, имеет соотношение СП3/СП4 равное 3-4,5 (Lazaridou et al., 2007). Хотя БГ ячменя связывали со снижением холестерина в плазме, снижением гликемического индекса и снижением риска рака толстой кишки, БГ пшеницы не связывали с подобными эффектами, так как зерно пшеницы имеет намного меньшие уровни БГ, чем ячмень. Уровень БГ в зерне обычно измеряют путем размола зерна до цельнозерновой муки и анализа в отношении БГ, например, методом, описанным в примере 1.
[0289] В пшеничном зерне дикого типа уровень фруктана составляет всего 0,6%-2,6% по массе зерна. В контексте данного документа термин «фруктан» означает полимеры фруктозы, которые содержат остатки фруктозила, полимеризованные с одной терминальной единицей глюкозы. Фруктаны синтезируются из сахарозы, что объясняет присутствие терминальной глюкозы. Компоненты фруктозы связаны друг с другом β-1,2- и/или β-2,6-связями, а глюкоза может быть связана с концом цепи α-1,2-связью как в сахарозе, образуясь вследствие повторяемого переноса фруктозила от сахарозы. Ферменты, вовлеченные в синтез фруктана, включают сахароза-сахароза фруктозилтрансферазу (EC 2.4.1.99), которая образует кетозу, и 1- или 6-фруктан-фруктан фруктозилтрансферазу (EC 2.4.1.100). Степень полимеризации (СП) варьируется от 3 до нескольких сотен, но, как правило, составляет 3-60, а в зерне согласно изобретению - в основном СП 3-10. Вследствие такого состава фруктаны хорошо растворяются в воде и не осаждаются в 78% этаноле. Связи между остатками фруктозила имеют исключительно тип β-1,2, образуя линейную молекулу (инулин), в которой остатки фруктозила присоединены к остатку фруктозила начальной сахарозы, или тип β-2,6 (леван), или же в разветвленных фруктанах присутствуют оба типа (граминаны). Граминаны, которые содержат β-2,6-связанные единицы фруктозы с точками ветвления β-1,2 и, следовательно, являются более сложными структурами, также могут присутствовать в злаковых, и могут быть смешаны с леванами. Уровень фруктана в зерне согласно изобретению обычно измеряют путем размола зерна до цельнозерновой муки и анализа в отношении фруктана, например, методом, описанным в примере 1, который основан на методе Prosky and Hoebregs (1999). Этот метод зависит от гидролиза фруктанов с последующим определением высвобождаемых сахаров.
[0290] Фруктаны представляют собой некрахмальные углеводы с потенциально благоприятным действием в качестве пищевого ингредиента на здоровье человека (Tungland and Meyer, 2002; Ritsema and Smeekens, 2003). Человеческие пищеварительные ферменты α-глюкозидаза, мальтаза, изомальтаза и сахараза не способны гидролизовать фруктаны вследствие β-конфигурации связей фруктанов. Кроме того, в тонком кишечнике людей и других млекопитающих отсутствуют ферменты фруктан-экзогидролазы, которые разрушают фруктаны и, следовательно, пищевые фруктаны не расщепляются в тонком кишечнике и достигают толстого кишечника в интактном виде. Однако присутствующие там бактерии способны ферментировать фруктаны и, таким образом, использовать их, например, в качестве источника энергии или углерода для роста и выработки короткоцепочечных жирных кислот (КЦЖК). Следовательно, пищевые фруктаны способны стимулировать рост полезных бактерий, таких как бифидобактерии, в толстой кишке, что помогает предотвратить заболевания кишечника, такие как констипация и инфицирование патогенными кишечными бактериями. Пищевые фруктаны также усиливают всасывание питательных веществ из рациона, в частности, кальция и железа, возможно, вследствие выработки КЦЖК, что в свою очередь снижает люминальный pH и модифицирует формообразование и, следовательно, растворимость соединений кальция или оказывает прямое действие на пути мукозального транспорта, таким образом, улучшая минерализацию костей и снижая риск железодефицитной анемии. Кроме того, рацион с высоким содержанием фруктанов может улучшить здоровье пациентов с диабетом и снизить риск раковых заболеваний толстой кишки путем подавления очагов аберрантных крипт, которые являются предшественниками рака толстой кишки (Kaur and Gupta, 2002). Также фруктаны имеют сладкий вкус и все больше используются в качестве низкокалорийных подсластителей и в качестве функциональных пищевых ингредиентов.
[0291] Получение выделенных фруктанов из зерна согласно изобретению является затратным по сравнению с существующими способами получения фруктанов, например, включающими экстрагирование инулинов из цикория. Крупномасштабное экстрагирование фруктанов можно осуществлять путем размола зерна до цельнозерновой муки и последующего экстрагирования всех сахаров, включая фруктаны, из муки в воду. Это можно осуществлять при температуре окружающей среды, а смесь центрифугировать или фильтровать. Затем супернатант нагревают до около 80°C и центрифугируют для удаления белков, а затем высушивают. В альтернативном варианте экстрагирование муки можно осуществлять, используя 80% этанол с последующей фазой разделения с применением смеси вода/хлороформ, а водную фазу, содержащую сахара и фруктаны, сушат и повторно растворяют в воде. Сахарозу в экстракте, полученном любым способом, можно удалять ферментативно путем добавления α-глюкозидазы, а затем удаления гексоз (моносахаридов) гель-фильтрацией для получения фракций фруктанов различных размеров. Это приведет к получению обогащенной фракции фруктанов, содержащей по меньшей мере 50%, предпочтительно по меньшей мере 60% или по меньшей мере 70%, более предпочтительно по меньшей мере 80% фруктанов.
[0292] Разработка мелкомасштабного анализа фруктанов. Содержание фруктанов в зернах злаковых и полученных из них пищевых продуктах обычно определяют, используя высокоэффективную жидкостную хроматографию (ВЭЖХ ) (Huynh et al., 2008) или спектрофотометрию (McCleary et al., 2000; McCleary et al., 2013; Steegmans et al., 2004). Официальный метод AOAC 999.03 (AOAC, 2000b) на основе спектрофотометрии был выведен на рынок в виде наборов K-FRUCHK и K-FRUC компанией Megazyme International Limited (Bray, Ирландия). Эти коммерческие наборы удобно и легко использовать для определения уровней фруктана в зернах злаковых (Karppinen et al., 2003; Whelan et al., 2011). В анализе K-FRUCHK сахарозу и мальтосахариды с низкой степенью полимеризации (СП) гидролизуют до фруктозы и глюкозы. Их концентрацию измеряют с помощью системы на основе гексокиназы/фосфор-глюкозо изомеразы/глюкозо-6-фосфатдегидрогеназы (HK/PGI/G6PGH), используя спектрофотометр. После гидролиза фруктанов повторно измеряют общую концентрацию фруктозы и глюкозы, а затем определяют содержание фруктанов по разнице между двумя измерениями. В анализе K-FRUC сахарозу, мальтозу, мальтодекстрины и крахмал гидролизуют до фруктозы и глюкозы, которые дополнительно восстанавливают борогидридом натрия до соответствующих сахарных спиртов (сорбита и маннита). Фруктозу и глюкозу, полученные после гидролиза фруктанов, соединяют с гидразидом 4-гидроксибензойной кислоты (PAHBAH) для проявления цвета в кипящей водяной бане, а их поглощение считывают, используя спектрофотометр, для расчета содержания фруктанов.
[0293] Недавно был разработан упрощенный ферментативный гидролиз с последующим анализом ВЭЖХ для исследования содержания фруктанов в популяции двойной гаплоидной (ДГ) пшеницы (Huynh et al., 2008b). Существует потребность в точном и быстром определении содержания фруктанов в больших популяциях для размножения с сотнями или тысячами линий. Однако все современные методы анализа фруктанов, используемые для зерен злаковых, являются относительно низкоэффективными, позволяя анализировать около 10 образцов в сутки одним рабочим, и требуют по несколько граммов каждого образца муки. Чтобы разработать высокоэффективный метод анализа фруктанов, авторы изобретения уменьшили масштаб анализов K-FRUCHK и K-FRUC до формата планшета, обеспечивающий этот масштаб, как описано в примере 1.
[0294] Арабиноксилан представляет собой другой полисахарид, встречающийся в клеточных стенках растений, включая клеточные стенки зерна пшеницы. Уровни арабиноксилана в зерне и муке согласно изобретению повышены по сравнению с соответствующими зерном или мукой дикого типа, например, по меньшей мере в 1,5 раза или по меньшей мере в 2 раза в массовом отношении. Уровень может быть повышен в 1,5-3 раза. В контексте данного документа «арабиноксилан» (АК) относится к имеющему линейную цепь каркасу остатков β-D-ксилопиранозила, связанных посредством 1,4-гликозидных связей с остатками α-L-арабинофуранозила, присоединенными к некоторым из остатков ксилопиранозила в позициях O-2, O-3 и/или O-2,3. Остатки ксилопиранозила могут быть монозамещенными в O-2 или O-3, дизамещенными в O-2,3 и незамещенными. Боковые ветви кроме арабинозы могут содержать небольшие количества ксилопиранозы, галактопиранозы, α-D-глюкуроновой кислоты или 4-O-метил-α-D-глюкуроновые остатки. В злаковых соотношение Ara/Xyl (АК) может варьироваться от 0,3 до 1,1. АК из внешнего перикарпия, щитка и эмбриональной оси являются относительно высокозамещенными арабинозой, тогда как АК из алейронового и гиалинового слоя менее замещены. АК может дополнительно содержать гидрокоричные кислоты, феруловую кислоту и п-кумаровую кислоту, эстерифицированные O-5 остатками арабинозы, связанными с O-3 остатками ксилозы (Smith and Hartley, 1983). Биосинтез 1,4-β-D-ксиланового каркаса катализируется 1,4-β-ксилозилтрансферазой, которая использует UDP-D-ксилозу в качестве субстрата и переносит единицу ксилозы к невосстанавливающему концу ксилоолигосахаридной цепи.
[0295] В синтез АК в злаковых вовлечены ксилозилтрансферазы, которые используют UDP-Xyl в качестве субстрата, и могут быть вовлечены сложные тетрасахариды в качестве праймеров (Carpita et al., 2011). Арабиноксиланы слабо растворяются в воде, а для их эффективного экстрагирования требуются щелочные растворители. Например, гидроксид бария может избирательно экстрагировать АК (Gruppen et al., 1992). В противоположность этому, гидроксид натрия экстрагирует как БГ, так и АК. Уровень АК в зерне обычно измеряют путем размола зерна до цельнозерновой муки и анализа в отношении АК, например, методом, описанным в примере 1.
[0296] Исследования АК кукурузы, ржи и пшеницы продемонстрировали положительное действие на ферментацию в слепой кишке, выработку КЦЖК, снижение сывороточного холестерина и улучшение всасывания кальция и магния (Hopkins et al. 2003).
[0297] В контексте данного документа целлюлоза относится к кристаллическому комплексу из около 24-36 цепей (1-4)-β-D-глюкана, которые образуют микрофибриллы, встречающиеся, главным образом, в клеточных стенках растений. Она является одним из наиболее распространенных полимеров в природе. Глюкановые цепи образуются целлюлозосинтазами генного семейства CesA в плазматической мембране (Giddings et al., 1980), а затем 24-36 цепей объединяются в функциональную микрофибриллу. Arabidopsis имеет 10 генов CesA, по меньшей мере 3 из которых совместно экспрессируются во время образования первичной клеточной стенки, а три других - во время образования вторичной клеточной стенки (Carpita et al., 2011), при этом каждая из них добавляет гликозильные остатки к невосстанавливающему концу акцепторных глюкановых цепей для удлинения полимеров. Гены CesA родственны с генами Csl как однодольных, так и двудольных, которые вовлечены в синтез других полисахаридов. Например, ферменты CslF и CslH, встречающиеся только в травянистых растениях, включая злаковые, вовлечены в синтез БГ.
[0298] Пищевые продукты, приготовленные из зерна, пищевых ингредиентов, гранул крахмала и крахмала, характеризуются сниженным гликемическим индексом. ГИ является простым маркером действия богатой углеводами пищи на уровни глюкозы после приема пищи в крови человека. В контексте данного документа «гликемический индекс» или «ГИ» означает результат измерения площади под кривой концентрации глюкозы в крови после употребления порции исследуемого пищевого продукта, содержащей 50 г углеводов, деленный на дополнительную площадь, получаемую при наличии такого же количества углеводов в эквивалентном количестве глюкозы или белом хлебе. Следовательно, ГИ относится к уровню переваривания пищи, содержащей крахмал, и поглощению продуктов пищеварения, и является сравнением действия исследуемого пищевого продукта с действием белого хлеба или глюкозы на отклонения в концентрации глюкозы в крови. Следовательно, ГИ является мерой действия пищи на концентрацию глюкозы в сыворотке после приема пищи и связан с потребностью в инсулине для гомеостаза глюкозы в крови. Одной из важных характеристик, обеспечиваемых пищевыми продуктами согласно изобретению, является сниженный ГИ по сравнению с соответствующими пищевыми продуктами, приготовленными из такого же количества пшеницы дикого типа, муки, гранул крахмала или крахмала в качестве пищевого ингредиента. Кроме того, пищевые продукты согласно изобретению могут иметь сниженный уровень конечного расщепления и, следовательно, являются относительно низкокалорийными по сравнению с соответствующими пищевыми продуктами, приготовленными из такого же количества пшеницы дикого типа в качестве пищевого ингредиента. Низкокалорийный продукт может быть основан на включении муки, получаемой из молотого пшеничного зерна. Такие пищевые продукты могут давать эффект насыщения, улучшения здоровья кишечника, снижения концентрации глюкозы и липидов в сыворотке после приема пищи, а также обеспечивать низкокалорийный пищевой продукт.
[0299] ГИ крахмала согласно изобретению, или пищевого ингредиента или пищевого продукта согласно изобретению легко определить, используя in vitro анализ, как описано в примере 9 данного документа. In vitro имитирует расщепление крахмала в продуктах, которое происходит после приема пищи у здоровых людей, и является прогностическим в отношении ГИ, определяемого у людей после приема таких продуктов.
[0300] Способ лечения субъекта, в частности человека, может включать этап употребления субъектом зерна, муки, крахмала или пищевого или питьевого продукта измененной пшеницы по определению данного документа в одной или более дозах, в количестве и в течение периода времени, за которые происходит улучшение одного или более показателей здоровья кишечника или метаболизма. Этот показатель может меняться по сравнению с употреблением соответствующего неизмененного пшеничного крахмала, или пшеницы или продукта из них, в течение периода времени до 24 часов, как в случае некоторых показателей, таких как pH, повышение уровней КЦЖК, флуктуации уровня глюкозы после приема пищи, или это может занимать несколько суток, как в случае увеличения объема фекалий или улучшения перистальтики кишечника, или, возможно, даже дольше, порядка недель или месяцев, как в случае измерения усиленной бутиратом пролиферации нормальных колоноцитов. Может существовать необходимость приема измененного крахмала, или пшеницы, или пшеничного продукта в течение всей жизни. Однако есть хорошие шансы соблюдения такого режима проходящим лечение индивидом, учитывая относительную легкость приема измененного крахмала.
[0301] Дозировки могут варьироваться в зависимости от подлежащего лечению или предотвращению патологического состояния, но предусматривается, что для людей они составляют по меньшей мере 10 г пшеничного зерна или крахмала согласно изобретению в сутки, более предпочтительно по меньшей мере 15 г в сутки, предпочтительно по меньшей мере 20 или по меньшей мере 30 г в сутки. Прием более чем около 100 граммов в сутки может требовать значительных объемов потребления и снижать соблюдение режима. Наиболее предпочтительно дозировка для человека составляет от 10 до 100 г пшеничного зерна согласно изобретению, или муки, цельнозерновой муки или модифицированного крахмала согласно изобретению в сутки, или, для взрослых людей, от 20 до 100 г в сутки.
[0302] Показатели улучшения здоровья кишечника могут включать, но не обязательно ограничены этим:
i) снижение pH содержимого кишечника,
ii) повышение общей концентрации КЦЖК или общего количества КЦЖК в содержимом кишечника,
iii) повышение концентрации или количества одной или более КЦЖК в содержимом кишечника,
iv) увеличение объема фекалий;
v) увеличение общего объема воды в кишечнике или фекалиях без диареи,
vi) улучшение перистальтики кишечника,
vii) повышение числа или активности одного или более видов пробиотических бактерий,
viii) повышение выделения желчных кислот с фекалиями,
ix) снижение уровней продуктов гниения в моче,
x) снижение уровней продуктов гниения в фекалиях,
xi) повышение пролиферации нормальных колоноцитов,
xii) снижение воспаления в кишечнике индивидов с воспаленным кишечником или тенденцией к воспалению кишечника,
xiii) снижение уровней любого компонента из мочи, креатинина и фосфата в фекалиях или толстом кишечнике у пациентов с уремией и
xiv) любую комбинацию вышеперечисленного.
[0303] Показатели улучшения метаболического здоровья могут включать, но не обязательно ограничены этим:
i) стабилизацию флуктуации уровня глюкозы после приема пищи,
ii) улучшение (снижение) гликемического ответа,
iii) снижение концентрации инсулина в плазме до приема пищи,
iv) улучшение липидного профиля крови,
v)снижение плазменного ЛПНП холестерина,
vi) снижение плазменных уровней одного или более компонентов из мочи, креатинина и фосфата у пациентов с уремией,
vii) улучшение дисгликемического ответа или
viii) любую комбинацию вышеперечисленного.
[0304] Показатель pH содержимого кишечника может быть снижен по меньшей мере на 0,1 единицы, предпочтительно по меньшей мере на 0,15 или 0,2 единицы. Каждый из других показателей здоровья кишечника или метаболического здоровья может быть улучшен по меньшей мере на 10%, предпочтительно по меньшей мере на 20%.
[0305] Следует понимать, что одним из преимуществ настоящего изобретения является то, что оно обеспечивает такие продукты, как хлеб, которые имеют исключительную питательную ценность, и, кроме того, это происходит без необходимости в модификации крахмала или других компонентов зерна пшеницы после сбора урожая. Однако может существовать необходимость в проведении таких модификаций в крахмале или другом компоненте зерна, и изобретение включает такой модифицированный компонент. Способы модификации хорошо известны и включают экстракцию крахмала или другого компонента традиционными способами и модификацию крахмала для повышения количества резистентной формы. Крахмал можно модифицировать путем обработки нагреванием и/или влагой, физически (например, шаровым помолом), ферментативно (используя, например, α- или β-амилазу, пуллуланазу и т. п.), химического гидролиза (влажного или сухого, используя жидкие или газообразные реагенты), окисления, перекрестного связывания с дифункциональными реагентами (например, триметафосфатом натрия, оксихлоридом фосфора) или карбоксиметилирования.
[0306] Хотя изобретение может быть исключительно полезным при лечении или профилактике людей, следует понимать, что изобретение также применимо к отличным от человека субъектам, включающим, но не ограничивающимся этим, сельскохозяйственных животных, таких как коровы, овцы, свиньи и т. п., домашних животных, таких как собаки или кошки, лабораторных животных, таких как кролики или грызуны, такие как мыши, крысы, хомяки, или животных, которых можно использовать в спортивных целях, таких как лошади. В частности, способ может быть применим к нежвачным млекопитающим или животным, таким как моногастричные млекопитающие. Изобретение также может быть применимо к другим сельскохозяйственных животным, например, домашней птице, включая, например, кур, гусей, уток, индюшек или перепелов, или рыбе.
[0307] Термины «полипептид» и «белок» в общем случае взаимозаменяемо употребляются в данном документе. В контексте данного документа термины «белки» и «полипептиды» также включают варианты, мутантов, модификации и/или производные полипептидов согласно изобретению, описанные в данном документе. В контексте данного документа выражение «по существу очищенный полипептид» относится к полипептиду, который был отделен от липидов, нуклеиновых кислот, других пептидов и других молекул, с которыми он связан в своем нативном состоянии. Предпочтительно по существу очищенный полипептид является по меньшей мере на 60% свободным, более предпочтительно по меньшей мере на 75% свободным и более предпочтительно по меньшей мере на 90% свободным от других компонентов, с которыми он связан естественным образом. Под «рекомбинантным полипептидом» подразумевается полипептид, созданный с помощью рекомбинантных технологий, т. е. посредством экспрессии рекомбинантного полинуклеотида в клетке, предпочтительно клетке растения, и наиболее предпочтительно клетке пшеницы. В одном варианте реализации полипептид обладает активностью фермента крахмальной синтазы, в частности активностью SSIIa, и является по меньшей мере на 98% идентичным описанному в данном документе полипептиду SSIIa.
[0308] Величину % идентичности полипептида относительно эталонного полипептида можно определить с помощью любой программы, известной в данной области техники для выравнивания аминокислотных последовательностей, такой как программа GAP (Needleman and Wunsch, 1970, программа GCG), со штрафом за открытие гэпа = 5, и штрафом за продление гэпа = 0,3. Этот анализ позволяет выравнивать две последовательности по всей длине аминокислотной последовательности эталонной последовательности. Например, если эталонная последовательность представляет собой аминокислотную последовательность, приведенную как SEQ ID NO:1, выравнивание проводится вдоль полной длины SEQ ID NO:1. Гэпом в выровненной последовательности считается позиция «не идентичности» для каждой недостающей аминокислоты.
[0309] В отношении определенного полипептида следует понимать, что значение % идентичности, большее, чем приведенные выше, будет включать предпочтительные варианты реализации. Таким образом, в соответствующих случаях в свете минимального значения % идентичности предпочтительно, чтобы полипептид содержал аминокислотную последовательность, которая по меньшей мере на 75%, более предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 91%, более предпочтительно по меньшей мере на 92%, более предпочтительно по меньшей мере на 93%, более предпочтительно по меньшей мере на 94%, более предпочтительно по меньшей мере на 95%, более предпочтительно по меньшей мере на 96%, более предпочтительно по меньшей мере на 97%, более предпочтительно по меньшей мере на 98%, более предпочтительно по меньшей мере на 99%, более предпочтительно по меньшей мере на 99,1%, более предпочтительно по меньшей мере на 99,2%, более предпочтительно по меньшей мере на 99,3%, более предпочтительно по меньшей мере на 99,4%, более предпочтительно по меньшей мере на 99,5%, более предпочтительно по меньшей мере на 99,6%, более предпочтительно по меньшей мере на 99,7%, более предпочтительно по меньшей мере на 99,8% и даже более предпочтительно по меньшей мере на 99,9% идентична релевантной указанной SEQ ID NO.
[0310] Делеции или вставки в аминокислотной последовательности в общем случае имеют диапазон от около 1 до 15 остатков, более предпочтительно от около 1 до 10 остатков и, как правило, от около 1 до 5 непрерывных остатков. Однако они могут составлять больше, чем 15 аминокислот, вплоть до полной длины полипептида. Полипептидная последовательность может представлять собой усеченную последовательность относительно соответствующей последовательности дикого типа или эталонной SEQ ID NO. Например, если кодирующая белок область, кодирующая полипептид, имеет кодон преждевременной терминации трансляции (стоп-кодон), получаемый в результате полипептид будет усечен при трансляции. Степень усечения зависит от положения стоп-кодона, укорачивая полипептид по меньшей мере на 5%, предпочтительно по меньшей мере на 10% относительно последовательности дикого типа.
[0311] Кодирующую белок область гена согласно изобретению можно разрушать путем внесения мутации сайта сплайсинга, которая приводит к ошибочному сплайсингу и может приводить к изменению РНК-транскрипта с нарушением открытой рамки считывания. Тогда аминокислотная последовательность полипептида может быть идентичной с диким типом до точки ошибочного сплайсинга или ниже этой точки, а далее отличаться от дикого типа. В целом, активность таких полипептидов оказывается затронутой так же, как и в случае усеченного полипептида. Примеры стоп-кодонов и мутаций сайта сплайсинга в гене SSIIa описаны в примере 11 данного документа.
[0312] Мутанты с замещением имеют по меньшей мере один удаленный аминокислотный остаток с вставленным на его место отличным остатком. Участки, представляющие наибольший интерес для заместительного мутагенеза для снижения активности полипептида, включают участки, идентифицированные как активные участки. Другими представляющими интерес участками являются те, в которых конкретные остатки, полученные из различных штаммов или видов, являются идентичными, т. е. консервативными аминокислотами. Эти позиции, вероятно, важны для биологической активности. Эти аминокислоты, в особенности попадающие в непрерывную последовательность из по меньшей мере трех других идентично консервативных аминокислот, предпочтительно замещены относительно консервативным образом с сохранением функции, такой как ферментативная активность SSIIa, или неконсервативным образом со снижением активности. Консервативные замены приведены в таблице 3 под заголовком «типовые замены». «Неконсервативные аминокислотные замены» по определению данного документа представляют собой замены, отличные от перечисленных в таблице 3 (типовые консервативные замены). Ожидается, что неконсервативные замены в полипептиде SSIIa будут снижать активность фермента и многие будут соответствовать SSIIa, кодируемому «мутантным геном SSIIa с частичной потерей функции».
Таблица 2. Подклассификация аминокислот
на ориентацию цепей
Таблица 3. Типовые и предпочтительные консервативные аминокислотные замены
замены
[0313] В некоторых вариантах реализации настоящее изобретение включает модификацию активности гена, в частности активности гена SSIIa, комбинации мутантных генов и конструирование и применение химерных генов. В контексте данного документа термин «ген» включает любую дезоксирибонуклеотидную последовательность, которая содержит кодирующую белок область или которая транскрибируется, но не транслируется в клетке, вместе со связанными с ней некодирующими и регуляторными областями. Термин «ген» также включает мутантные формы гена дикого типа, при этом мутантные гены могут не транскрибироваться и/или не транслироваться, например, как в случае удаления промоторной области. Связанные некодирующие и регуляторные области, как правило, расположены рядом с кодирующей белок областью, как с 5', так и с 3' концов, на расстоянии около 2 т. п. о. с каждой стороны. В этом отношении ген содержит сигналы управления, такие как промоторы, энхансеры, сигналы терминации транскрипции и/или полиаденилирования, которые естественным образом связаны с данным геном, или гетерологичные сигналы управления, в случае чего ген называется «химерным геном». Последовательности, которые расположены на цепи 5' кодирующей белок области и которые присутствуют в мРНК, называются 5' нетранслируемыми последовательностями (5'-НТО). Последовательности, которые расположены на цепи 3' или ниже кодирующей белок области и которые присутствуют в мРНК, называются 3' нетранслируемыми последовательностями (3'-НТО). Термин «ген» включает как кДНК, так и геномные формы гена. «кДНК» представляет собой ДНК-копию РНК-транскрипта гена и описана в данном документе как «соответствующая гену». Например, нуклеотидная последовательность кДНК, приведенная как SEQ ID NO:4, соответствует гену SSIIa-A, чья последовательность дикого типа приведена как SEQ ID NO:7. Термин «ген» включает синтетические или слитые молекулы, кодирующие белки согласно изобретению, описанные в данном документе. Гены обычно присутствуют в геноме пшеницы в виде двухцепочечной ДНК. Химерный ген может быть внесен в соответствующий вектор для внехромосомного нахождения в клетке или для интеграции в геном хозяина. В данном документе гены или генотипы выделены курсивом (например, SSIIa), тогда как белки, ферменты или фенотипы курсивом не выделены (SSIIa).
[0314] В контексте данного документа термин «генотип» относится к генетическому строению клетки пшеницы, ткани, растения, части растения или растительного продукта. Генетическое строение может быть идентичным с растением пшеницы, из которого был получен продукт. В контексте данного документа термин «фенотип» относится к наблюдаемой характеристике или набору из множества характеристик клетки, ткани, растения, части растения или растительного продукта, которые являются результатом взаимодействия между генотипом растения и окружающей средой, в которой было выращено растение.
[0315] Геномная форма или клон гена, содержащие кодирующую область, могут прерываться некодирующими последовательностями, называемыми «интронами» или «промежуточными областями» или «промежуточными последовательностями». В контексте данного документа «интрон» представляет собой сегмент гена, который транскрибируется как часть первичного РНК-транскрипта, но не присутствует в зрелой молекуле мРНК. Интроны удаляются или «вырезаются» из ядра или первичного транскрипта; следовательно, интроны отсутствуют в матричной РНК (мРНК). Интроны могут содержать регуляторные элементы, такие как энхансеры. В контексте данного документа «экзоны» относятся к областям ДНК, соответствующим последовательностям РНК, которые присутствуют в зрелой мРНК или зрелой молекуле РНК в случаях, когда молекула РНК не транслируется. мРНК функционирует во время трансляции, определяя последовательность или порядок аминокислот в кодируемом полипептиде.
[0316] Настоящее изобретение относится к различным полинуклеотидам. В контексте данного документа «полинуклеотид», или «нуклеиновая кислота», или «молекула нуклеиновой кислоты» означает полимер из нуклеотидов, который может представлять собой ДНК или РНК и включает, например, кДНК, мРНК, тРНК, киРНК, кшРНК, шРНК и одно- или двухцепочечную ДНК. Он может представлять собой ДНК или РНК клеточного, геномного или синтетического происхождения. Предпочтительно полинуклеотид представляет собой исключительно ДНК или исключительно РНК и находится в клетке. Полимер может быть одноцепочечным, преимущественно двухцепочечным или частично двухцепочечным. Примером частично двухцепочечной молекулы РНК является шпилечная РНК (шРНК), короткая шпилечная РНК (кшРНК) или самокомплементарная РНК, которая содержит двухцепочечный «стебель», образуемый спариванием оснований между нуклеотидной последовательностью и ее комплементарной последовательностью, и петлевую последовательность, которая ковалентно соединяет нуклеотидную последовательность и ее комплементарную последовательность. В контексте данного документа спаривание оснований относится к стандартному спариванию оснований между нуклеотидами, включая спаривание оснований G:U в молекуле РНК. «Комплементарные» означает, что два полинуклеотида способны к спариванию оснований на протяжении части своей длины или на протяжении всей длины одного или обоих (полная комплементарность).
[0317] Под «выделенным» подразумевается материал, который по существу или практически свободен от компонентов, которые обычно сопутствуют ему в его нативном состоянии. В контексте данного документа «выделенный полинуклеотид» или «выделенная молекула нуклеиновой кислоты» означает полинуклеотид, который по меньшей мере частично отделен от, предпочтительно по существу или практически свободен от полинуклеотидных последовательностей такого же типа, с которыми он ассоциирован или связан в своем нативном состоянии. Например, «выделенный полинуклеотид» включает полинуклеотид, который был очищен или отделен от последовательностей, которые фланкируют его в естественном состоянии, т. е. фрагмент ДНК, который был удален из последовательностей, которые обычно прилегают к этому фрагменту. Предпочтительно выделенный полинуклеотид также является по меньшей мере на 90% свободным от других компонентов, таких как белки, углеводы, липиды и т. д. В контексте данного документа термин «рекомбинантный полинуклеотид» относится к полинуклеотиду, образованному in vitro посредством придания нуклеиновой кислоте формы, которая обычно не встречается в природе. Например, рекомбинантный полинуклеотид может находиться в форме экспрессионного вектора. В общем случае такие экспрессионные векторы содержат транскрипционную и трансляционную регуляторную нуклеиновую кислоту, функционально связанную с нуклеотидной последовательностью, подлежащей транскрибированию в клетке.
[0318] Настоящее изобретение относится к применению олигонуклеотидов, которые можно использовать как «зонды» или «праймеры». В контексте данного документа «олигонуклеотиды» представляют собой полинуклеотиды длиной до 50 нуклеотидов, предпочтительно длиной 15-50 нуклеотидов. Они могут представлять собой РНК, ДНК или их комбинации или производные. Олигонуклеотиды, как правило, представляют собой относительно короткие одноцепочечные молекулы из 10-30 нуклеотидов, обычно длиной 15-25 нуклеотидов, как правило, состоящие из 10-30 или 15-25 нуклеотидов, которые идентичны или комплементарны части гена SSIIa или кДНК, соответствующей гену SSIIa. При применении зонда или праймера в реакции амплификации минимальным размером такого олигонуклеотида является размер, необходимый для образования стабильного гибрида между олигонуклеотидом и комплементарной последовательностью в целевой молекуле нуклеиновой кислоты. Полинуклеотиды, применяемые как зонды, как правило, конъюгированы с выявляемой меткой, такой как радиоизотоп, фермент, биотин, флуоресцентная молекула или хемилюминесцентная молекула. Олигонуклеотиды и зонды согласно изобретению применимы в способах выявления аллеля SSIIa или другого гена, связанного с представляющим интерес признаком, например, модифицированным крахмалом. В таких способах используется гибридизация нуклеиновых кислот, и во многих случаях они включают удлинение олигонуклеотидного праймера подходящей полимеразой, например, как это происходит в ПЦР, для выявления или идентификации аллелей дикого типа или мутантных. Предпочтительные олигонуклеотиды и зонды гибридизируются с последовательностью гена SSIIa из пшеницы или других злаковых, включая любые описанные в данном документе последовательности, например, SEQ ID NO: 15-49. Предпочтительными парами олигонуклеотидов являются те, которые распространяются на один или более интронов, или часть интрона и, следовательно, могут быть использованы для амплификации последовательности интрона в ПЦР-реакции. В примерах данного документа приведены многочисленные примеры.
[0319] Термины «полинуклеотидный вариант», «вариант» и т. п. относятся к полинуклеотидам, демонстрирующим существенную идентичность последовательности с эталонной полинуклеотидной последовательностью и способным функционировать аналогичным образом или с такой же активностью, что и эталонная последовательность. Эти термины также включают полинуклеотиды, которые отличаются от эталонного полинуклеотида добавлением, делецией или заменой по меньшей мере одного нуклеотида или которые содержат одну или более мутаций по сравнению с молекулами природного происхождения. Соответственно, термины «полинуклеотидный вариант» и «вариант» включают полинуклеотиды, в которых один или более нуклеотидов были добавлены или удалены, или замещены другими нуклеотидами. В этой связи в данной области техники хорошо известно, что некоторые изменения, включающие мутации, добавления, делеции и замены, можно осуществлять в эталонном полинуклеотиде, при этом измененный полинуклеотид сохраняет биологическую функцию или активность эталонного полинуклеотида. Соответственно, эти термины включают полинуклеотиды, которые кодируют полипептиды, демонстрирующие ферментативную или регуляторную активность, или полинуклеотиды, способные служить в качестве селективных зондов или других гибридизирующихся агентов. Термины «полинуклеотидный вариант» и «вариант» также включают аллельные варианты природного происхождения. Мутанты могут быть как природного происхождения (то есть, выделенными из природного источника) или синтетическими (например, полученными при проведении сайт-направленного мутагенеза в нуклеиновой кислоте). Предпочтительно полинуклеотидный вариант согласно изобретению, который кодирует полипептид с ферментативной активностью, имеет длину, составляющую по меньшей мере 90%, по сравнению с диким типом, вплоть до полной длины гена.
[0320] Вариант олигонуклеотида согласно изобретению включает молекулы различного размера, которые способны гибридизироваться, например, с геномом пшеницы в позиции, близкой к конкретным олигонуклеотидным молекулам, определенным в данном документе. Например, варианты могут содержать дополнительные нуклеотиды (например, 1, 2, 3, 4 или более) или меньшее количество нуклеотидов при условии, что они гибридизируются с целевой областью. Кроме того, несколько нуклеотидов может быть замещено без влияния на способность олигонуклеотида гибридизироваться с целевой областью. Кроме того, можно легко создавать варианты, которые гибридизируются вблизи (например, без ограничений, в пределах 50 нуклеотидов) области растительного генома, с которой гибридизируются конкретные олигонуклеотиды, определенные в данном документе.
[0321] Под «соответствует» или «соответствующий» в контексте полинуклеотидов или полипептидов подразумевается полинуклеотид, (a) имеющий нуклеотидную последовательность, которая является по существу идентичной или комплементарной по меньшей мере части, предпочтительно всей (полностью комплементарной) эталонной полинуклеотидной последовательности, или (b) кодирующий аминокислотную последовательность, идентичную аминокислотной последовательности в полипептиде. В объем этого выражения также входит полипептид, имеющий аминокислотную последовательность, которая по существу идентична последовательности аминокислот в эталонном полипептиде. Термины, используемые для описания взаимосвязи между двумя или более полинуклеотидами или полипептидами, включают «эталонную последовательность», «идентичность последовательности», «процент идентичности последовательности», «существенную идентичность» и «идентичный» и определяются по отношению к определенному минимальному числу нуклеотидов или аминокислотных остатков или, предпочтительно, относительно всей длины. Термины «идентичность последовательности» и «идентичность» взаимозаменяемо употребляются в данном документе и относятся к степени, в которой последовательности идентичны на основании сравнения нуклеотид к нуклеотиду или аминокислота к аминокислоте в окне сравнения. Таким образом, «процент идентичности последовательности» рассчитывают, сравнивая две оптимально выровненные последовательности в окне сравнения, определяя число позиций, в которых находятся идентичные основания нуклеиновых кислот (например, A, T, C, G, U) или идентичные аминокислотные остатки в обеих последовательностях, для получения числа совпадающих позиций, деля число совпадающих позиций на общее число позиций в окне сравнения (т. е. по размеру окна) и умножая результат на 100 для получения процента идентичности последовательности.
[0322] Величину % идентичности полинуклеотида относительно эталонного полинуклеотида можно определить с помощью любой программы, известной в данной области техники для этой цели, такой как, например, программа GAP (Needleman and Wunsch, 1970, программа GCG), со штрафом за открытие гэпа = 5, и штрафом за продление гэпа = 0,3. Можно также сослаться на семейство программ BLAST, например, описанных Altschul et al., 1997. Подробное обсуждение вопроса анализа последовательностей можно найти в разделе 19.3 Ausubel et al., 1994-1998, глава 15. Если не указано иное, выравнивание проводится вдоль полной длины эталонной последовательности.
[0323] Нуклеотидные или аминокислотные последовательности считаются «практически аналогичными», если такие последовательности имеют идентичность последовательности, составляющую по меньшей мере 98%, в частности, по меньшей мере около 98,5%, в частности, около 99%, в особенности около 99,5%, особенно около 99,8%, включая случаи идентичности последовательностей. Понятно, что последовательности РНК описаны практически аналогично или имеют определенную степень идентичности последовательности с последовательностями ДНК, при этом тимин (T) в последовательности ДНК считается эквивалентным урацилу (U) в последовательности РНК.
[0324] В отношении определенных полинуклеотидов следует понимать, что более высокое значение % идентичности будет включать предпочтительные варианты реализации. Таким образом, в соответствующих случаях в свете минимального значения % идентичности предпочтительно, чтобы полинуклеотид содержал полинуклеотидную последовательность, которая по меньшей мере на 75%, более предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 91%, более предпочтительно по меньшей мере на 92%, более предпочтительно по меньшей мере на 93%, более предпочтительно по меньшей мере на 94%, более предпочтительно по меньшей мере на 95%, более предпочтительно по меньшей мере на 96%, более предпочтительно по меньшей мере на 97%, более предпочтительно по меньшей мере на 98%, более предпочтительно по меньшей мере на 99%, более предпочтительно по меньшей мере на 99,1%, более предпочтительно по меньшей мере на 99,2%, более предпочтительно по меньшей мере на 99,3%, более предпочтительно по меньшей мере на 99,4%, более предпочтительно по меньшей мере на 99,5%, более предпочтительно по меньшей мере на 99,6%, более предпочтительно по меньшей мере на 99,7%, более предпочтительно по меньшей мере на 99,8% и даже более предпочтительно по меньшей мере на 99,9% идентична релевантной указанной SEQ ID NO.
[0325] В некоторых вариантах реализации настоящее изобретение относится к жесткости условий гибридизации для определения степени комплементарности двух полинуклеотидов. В контексте данного документа «жесткость» относится к условиям температуры и ионной силы, а также присутствию или отсутствию определенных органических растворителей во время гибридизации. Чем выше жесткость, тем большей будет степень комплементарности между целевой нуклеотидной последовательностью и меченой полинуклеотидной последовательностью. «Жесткие условия» относятся к температурным и ионным условиям, в которых гибридизироваться будут только нуклеотидные последовательности, имеющие высокую частоту появления комплементарных оснований. В контексте данного документа термин «гибридизируется в условиях низкой жесткости, средней жесткости, высокой жесткости или очень высокой жесткости» описывает условия гибридизации и промывки. Руководство по проведению реакций гибридизации можно найти в Current Protocols in Molecular Biology, John Wiley & Sons, N.Y. (1989), 6.3.1-6.3.6, включенной в данный документ посредством ссылки. Конкретные условия гибридизации, используемые в данном документе, являются следующими: 1) условия гибридизации низкой жесткости в 6 X растворе хлорида натрия/цитрата натрия (SSC) при около 45°C, с последующими двумя промывками в 0,2 X SSC, 0,1% ДСН при 50-55°C; 2) условия гибридизации средней жесткости в 6 X SSC при около 45°C, с последующими одной или более промывками в 0,2 X SSC, 0,1% ДСН при 60°C; 3) условия гибридизации высокой жесткости в 6 X SSC при около 45°C, с последующими одной или более промывками в 0,2 X SSC, 0,1% ДСН при 65°C; и 4) условия гибридизации очень высокой жесткости включают 0,5 M фосфата натрия, 7% ДСН при 65°C, с последующими одной или более промывками в 0,2 X SSC, 1% ДСН при 65°C.
[0326] В контексте данного документа «химерный ген» или «генетическая конструкция» относятся к любому гену, который не является нативным геном в своей нативной локации, т. е. был искусственно обработан, включая химерный ген или генетическую конструкцию, интегрированные в геном пшеницы. Как правило, химерный ген или генетическая конструкция содержит регуляторные и транскрибируемые или кодирующие белок последовательности, которые не встречаются вместе в природе. Соответственно, химерный ген или генетическая конструкция может содержать регуляторные последовательности и кодирующие последовательности, полученные из разных источников, или регуляторные последовательности и кодирующие последовательности, полученные из одного источника, но расположенные таким образом, который не встречается в природе. Термин «эндогенный» употребляется в данном документе для обозначения вещества, которое обычно вырабатывается в немодифицированном растении на той же стадии развития, что и в растении, подлежащем исследованию, предпочтительно растении пшеницы, такого как крахмал или ген SSIIa полипептида SSIIa. «Эндогенный ген» относится к нативному гену в его природной локации в геноме организма, предпочтительно гену SSIIa в растении пшеницы. Термины «чужеродный полинуклеотид», или «экзогенный полинуклеотид», или «гетерологичный полинуклеотид» и т. п. относятся к любой нуклеиновой кислоте, которую вносят в геном клетки с помощью экспериментальных процедур, предпочтительно геном пшеницы, но которая не встречается в клетке в природе. Они включают модифицированные формы генных последовательностей, встречающиеся в этой клетке, при условии, что внесенный ген содержит некоторые модификации, например, внесенную мутацию или наличие гена селективного маркера, по сравнению с геном природного происхождения. Чужеродные или экзогенные гены могут представлять собой гены, встречающиеся в природе, которые внесены в ненативный организм, нативные гены, внесенные в новую локацию в нативном организме-хозяине, или химерные гены или генетические конструкции. Термин «генетически модифицированный» включает внесение генов в клетки, мутацию генов в клетках и искусственное изменение или модуляцию регуляции гена в клетке путем модификации генома, или организмы, к которым были применены эти действия, или их потомство, или части, такие как зерно.
[0327] Настоящее изобретение относится к элементам, которые функциональным образом соединены или связаны. Выражения «функционально соединенный» или «функционально связанный» и т. п. относятся к связыванию элементов полинуклеотидов в функциональную взаимосвязь. Как правило, функционально связанные последовательности нуклеиновых кислот связаны непрерывно и, в случае необходимости соединения двух кодирующих белок областей, непрерывно и в рамке считывания. Кодирующая последовательность «функционально связана» с другой кодирующей последовательностью, если РНК-полимераза транскрибирует две кодирующие последовательности в одну РНК, которая при трансляции транслируется в один полипептид, содержащий аминокислоты, полученные из обеих кодирующих последовательностей. Кодирующие последовательности не обязательно должны быть непрерывными относительно друг друга при условии, что экспрессируемые последовательности в конечном итоге проходят процессинг с получением необходимого белка.
[0328] В контексте данного документа термин «цис-действующая последовательность», «цис-действующий элемент» или «цис-регуляторная область», или «регуляторная область», или аналогичные термины следует понимать как означающие любую последовательность нуклеотидов, которая регулирует экспрессию генетической последовательности. Это может быть цис-действующая последовательность природного происхождения в своем нативном окружении, например, регулирующая ген SSIIa пшеницы, или последовательность в генетической конструкции, которая при соответствующем расположении относительно экспрессируемой генетической последовательности регулирует ее экспрессию. Такая цис-регуляторная последовательность может быть способна к активации, сайленсингу, усилению, репрессии или какому-либо иному изменению уровня экспрессии, и/или специфичности в отношении типа клетки, и/или специфичности в отношении стадии развития генной последовательности на транскрипционном и посттранскрипционном уровне. Например, было показано, что наличие интрона в 5'-лидерной последовательности (НТО) генов усиливает экспрессию генов в однодольных растениях, таких как пшеница (Tanaka et al., 1990). Другим типом цис-действующей последовательности является участок прикрепления к матриксу (MAR), который может влиять на генную экспрессию посредством прикрепления активных доменов хроматина к ядерному матриксу.
[0329] Под «вектором» подразумевается молекула нуклеиновой кислоты, предпочтительно молекула ДНК, полученная из плазмиды или растительного вируса, в которую можно вставлять последовательность нуклеиновой кислоты. Вектор также может содержать селективный маркер, такой как ген устойчивости к антибиотикам, который можно использовать для отбора подходящих бактериальных или растительных трансформантов или последовательностей, которые усиливают трансформацию прокариотических или эукариотических (в особенности пшеничных) клеток, такой как последовательности Т-ДНК или П-ДНК. Примеры таких генов и последовательностей, обеспечивающих устойчивость, хорошо известны специалистам в данной области техники.
[0330] Под «маркерным геном» подразумевается ген, который придает отличный фенотип клеткам, экспрессирующим маркерный ген, и, таким образом, позволяет отличать такие трансформированные клетки от клеток, которые не содержат маркер, как хорошо известно в данной области техники. «Ген селективного маркера» обеспечивает признак, в отношении которого можно проводить «отбор», основанный на устойчивости к селективному агенту (например, гербициду, антибиотику, излучению, температуре или другому виду обработки, повреждающему нетрансформированные клетки) или основанный на связанных с ростом преимуществах в присутствии метаболизируемого субстрата. Типовые гены селективных маркеров для отбора растительных трансформантов включают, но не ограничиваются этим, ген hyg, который придает устойчивость к гигромицину B; ген неомицинфосфотрансферазы (npt), придающий устойчивость к канамицину и т. п., например, описанный Potrykus et al., 1985; ген глутатион-S-трансферазы из печени крыс, придающий устойчивость к глутатионовым гербицидам, например, описанный в EP-A-256223; ген глутаминсинтетазы, придающий, в случае сверхэкспрессии, устойчивость к ингибиторам глутаминсинтетазы, таким как фосфинотрицин, например, описанный в WO87/05327, ген ацетилтрансферазы из Streptomyces viridochromogenes, придающий устойчивость к селективному агенту фосфинотрицину, например, описанный в EP-A-275957, ген, кодирующий 5-энолшикимат-3-фосфат-синтазу (EPSPS), придающий устойчивость к N-фосфонометилглицину, например, описанный Hinchee et al., 1988, ген bar, придающий устойчивость к биалафосу, например, описанный в WO91/02071; или ген нитрилазы, такой как bxn из Klebsiella ozaenae, который придает устойчивость к бромоксинилу (Stalker et al., 1988). Предпочтительные подлежащие скринингу маркеры включают, но не ограничиваются этим, ген uidA, кодирующий фермент β-глюкуронидазу (GUS), для которого известны различные хромогенные субстраты, ген β-галактозидазы, кодирующий фермент, для которого известны хромогенные субстраты, ген экворина (Prasher et al., 1985), который можно использовать в кальций-чувствительном биолюминесцентном выявлении; ген зеленого флуоресцентного белка (ЗФБ, Niedz et al., 1995) или один из его вариантов; ген люциферазы (luc) (Ow et al., 1986), который позволяет проводить биолюминесцентное выявление, и другие известные в данной области техники гены.
[0331] В некоторых вариантах реализации уровень ферментативной активности модулируют, снижая уровень экспрессии генов, кодирующих этот фермент в растении пшеницы, или повышая уровень экспрессии нуклеотидной последовательности, которая кодирует этот фермент в растении пшеницы. Повышение экспрессии можно осуществлять на уровне транскрипции, используя промоторы разной силы или индуцибельные промоторы, которые способны регулировать уровень транскрипта, экспрессируемого из кодирующей последовательности. Можно вносить гетерологичные последовательности, которые кодируют транскрипционные факторы, которые модулируют или усиливают экспрессию генов, чьи продукты оказывают понижающую регуляцию на синтез крахмала, такие как SSIIa. Уровень экспрессии гена можно модулировать, изменяя число копий на клетку конструкции, содержащей кодирующую последовательность и транскрипционный регуляторный элемент, функционально с ней связанный, которая является функциональной в клетке. В альтернативном варианте можно проводить отбор множества трансформантов и скрининг в отношении тех, которые имеют подходящие уровень и/или специфичность экспрессии трансгена, обусловленные влиянием эндогенных последовательностей вблизи участка интеграции трансгена. Подходящий уровень и профиль экспрессии трансгена является таким, который приводит к существенному повышению содержания амилозы в растении пшеницы. Это можно легко выявить путем исследования трансформантов.
[0332] Снижение генной экспрессии также можно осуществлять посредством внесения и транскрипции «химерного гена для генного сайленсинга», вносимого в растение пшеницы. Химерный ген для генного сайленсинга предпочтительно стабильным образом вносят в геном пшеницы, предпочтительно ядерный геном пшеницы, так, чтобы он стабильно наследовался потомством. В контексте данного документа «эффект генного сайленсинга» относится к снижению экспрессии целевой нуклеиновой кислоты в клетке пшеницы, предпочтительно клетке эндосперма, во время развития семян при росте растения, что можно осуществлять путем внесения обеспечивающей сайленсинг РНК. В предпочтительном варианте реализации вносят химерный ген для генного сайленсинга, который кодирует молекулу РНК, которая снижает экспрессию одного или более эндогенных генов, например, генов, отличных от генов SSIIa, или предпочтительно трех эндогенных генов SSIIa. Такое снижение может быть результатом снижения транскрипции, включая снижение, обусловленное метилированием промоторных областей посредством ремоделирования хроматина или посттранскрипционной модификацией молекул РНК, включая деградацию РНК, или обоими вариантами. Генный сайленсинг не обязательно следует интерпретировать как прекращение экспрессии целевой нуклеиновой кислоты или гена. Достаточно, чтобы уровень экспрессии целевой нуклеиновой кислоты в присутствии обеспечивающей сайленсинг РНК был ниже, чем в ее отсутствие. Уровень экспрессии целевого гена может быть снижен по меньшей мере на около 40%, или по меньшей мере на около 45%, или по меньшей мере на около 50%, или по меньшей мере на около 55%, или по меньшей мере на около 60%, или по меньшей мере на около 65%, или по меньшей мере на около 70%, или по меньшей мере на около 75%, или по меньшей мере на около 80%, или по меньшей мере на около 85%, или по меньшей мере на около 90%, или по меньшей мере на около 95%, или эффективно уменьшен до невыявляемого уровня.
[0333] Для снижения генной экспрессии в клетках пшеницы можно использовать антисмысловые технологии. Термин «антисмысловая РНК» следует понимать, как означающий молекулу РНК, которая является комплементарной по меньшей мере части конкретной молекулы мРНК и способна снижать экспрессию гена, кодирующего мРНК, предпочтительно гена SSIIa. Такое снижение, как правило, зависит от последовательности и считается обусловленным вмешательством в посттранскрипционные события, такие как транспорт мРНК из ядра в цитоплазму, стабильность мРНК или ингибирование трансляции. Применение антисмысловых методов хорошо известно в данной области техники (смотрите, например, Hartmann and Endres, 1999).
[0334] В контексте данного документа «искусственно внесенная молекула дцРНК» относится к внесению молекулы двухцепочечной РНК (дцРНК), которая предпочтительно синтезируется в клетке пшеницы путем транскрипции из химерного гена, кодирующего такую молекулу дцРНК. РНК-интерференция (РНКи) исключительно подходит для направленного снижения экспрессии гена или ингибирования выработки конкретного белка, также в пшенице (смотрите, например, Regina et al., 2006). Эта технология основана на присутствии молекул дцРНК, которые содержат последовательность, являющуюся практически идентичной мРНК представляющего интерес гена или его части, и ее комплементарную последовательность, с образованием, таким образом, дцРНК. дцРНК удобно получать из одного промотора в клетке-хозяине, когда смысловая и антисмысловая последовательности транскрибируются с получением шпилечной РНК, в которой смысловая и антисмысловая последовательности гибридизируются с образованием области дцРНК с родственной (гену SSIIa) или неродственной последовательностью, образуя петлевую структуру так, что шпилечная РНК содержит структуру типа стебель-петля. Конструирование и получение подходящих для настоящего изобретения молекул дцРНК входит в компетентность специалиста в данной области техники, в частности, принимая во внимание работы Waterhouse et al., 1998; Smith et al., 2000; WO 99/32619; WO 99/53050; WO 99/49029; и WO 01/34815.
[0335] ДНК, кодирующая дцРНК , как правило, содержит как смысловую, так и антисмысловую последовательности, упорядоченные в виде инвертированного повтора. В предпочтительном варианте реализации смысловая и антисмысловая последовательности разделены спейсерной областью, которая может содержать (или не содержать) интрон, который вырезается при транскрибировании в РНК. Было показано, что такое упорядочение приводит к более высокой эффективности генного сайленсинга (Smith et al., 2000). Двухцепочечная область может содержать одну или две молекулы РНК, транскрибируемые из одной или двух областей ДНК. дцРНК можно классифицировать как длинную шРНК, имеющую длинные смысловые и антисмысловые области, которые могут быть высококомплементарными, но не обязательно должны быть полностью комплементарными (как правило, более чем на около 200 п. о., например от 200 до 1000 п. о.). шРНК также может быть довольно небольшой с двухцепочечной частью размером в диапазоне от около 30 до около 42 п. о., но не намного длиннее чем 94 п. о. (смотрите WO04/073390). Считается, что присутствие двухцепочечной области РНК инициирует отклик эндогенной системы растения, которая разрушает как двухцепочечную РНК, так и гомологичный РНК-транскрипт из целевого (-ых) гена (-ов) растения, эффективно снижая или элиминируя активность целевого гена.
[0336] Длина каждой из смысловой и антисмысловой последовательностей, которые гибридизируются, должна составлять по меньшей мере 19 или по меньшей мере 21 непрерывный нуклеотид, предпочтительно по меньшей мере 30 или 50 нуклеотидов, и более предпочтительно по меньшей мере 100, 200, 500 или 1000 нуклеотидов. Можно использовать полноразмерную последовательность, соответствующую целому генному транскрипту. Длина наиболее предпочтительно составляет 100-2000 нуклеотидов. Степень идентичности смысловой и антисмысловой последовательностей с целевым транскриптом должна составлять по меньшей мере 85%, предпочтительно по меньшей мере 90% и более предпочтительно 95-100%. Чем длиннее последовательность, тем менее жесткие требования в отношении общей идентичности последовательностей. Конечно, молекула РНК может содержать неродственные последовательности, чьей функцией может быть стабилизация молекулы. Промотор, применяемый для экспрессии дцРНК-образующей конструкции, может являться промотором любого типа, который экспрессируется в клетках, экспрессирующих целевой ген, предпочтительно промотором, который преимущественно экспрессируется в эндосперме развивающегося зерна пшеницы по сравнению с отличными от зерна тканями растения пшеницы. Если целевой ген представляет собой SSIIa или другой ген, избирательно экспрессируемый в эндосперме, предпочтительным является специфический для эндосперма промотор, который не экспрессируется в тканях листьев или стеблей, чтобы не влиять на экспрессию целевого (-ых) гена (-ов) в других тканях.
[0337] В контексте данного документа «обеспечивающие сайленсинг РНК» представляют собой молекулы РНК, которые содержат 21-24 непрерывных нуклеотида, комплементарные к области мРНК, транскрибируемой из целевого гена, предпочтительно SSIIa. Последовательность из 21-24 нуклеотидов предпочтительно является полностью комплементарной последовательности из 21-24 непрерывных нуклеотидов мРНК, т. е. идентичной комплементарной последовательности из 21-24 нуклеотидов области мРНК. При этом также можно использовать последовательности миРНК, которые содержат до пяти несовпадений в области мРНК (Palatnik et al., 2003), а спаривание оснований может включать одну или две пары оснований G-U. Когда не все из 21-24 нуклеотидов обеспечивающей сайленсинг РНК способны к спариванию оснований с мРНК, предпочтительно, чтобы присутствовали всего одно или два несовпадения между 21-24 нуклеотидами обеспечивающей сайленсинг РНК и областью мРНК. В отношении миРНК предпочтительно, чтобы любые несовпадения, максимум до пяти, находились в направлении 3' конца миРНК. В предпочтительном варианте реализации присутствует не более одного или двух несовпадений между последовательностями обеспечивающей сайленсинг РНК и целевой мРНК.
[0338] Обеспечивающие сайленсинг РНК происходят из более длинных молекул РНК, которые кодируются химерными ДНК согласно изобретению. Более длинные молекулы РНК, также называемые в данном документе «РНК-предшественниками», представляют собой исходные продукты, получаемые при транскрипции из химерных ДНК в клетках пшеницы, и имеют частично двухцепочечную структуру, образуемую вследствие внутримолекулярного спаривания оснований между комплементарными областями. РНК-предшественники процессируются специальным классом РНКаз, обычно называемых «дайсерами», в обеспечивающие сайленсинг РНК, как правило, длиной 21-24 нуклеотида. В контексте данного документа обеспечивающие сайленсинг РНК включают короткие интерферирующие РНК (киРНК) и микроРНК (миРНК), которые отличаются своим биосинтезом. киРНК происходят из полностью или частично двухцепочечных РНК, содержащих по меньшей мере 21 непрерывную пару оснований, включая возможные пары оснований G-U, без несовпадений или неспаренных нуклеотидов, выступающих из двухцепочечной области. Двухцепочечные РНК образуются либо из одного самокомплементарного транскрипта, который образуется путем складывания и образования структуры типа стебель-петля, называемой в данной документе «шпилечной РНК», либо из двух отдельных РНК, которые являются по меньшей мере частично комплементарными и гибридизируются с образованием двухцепочечной области РНК. миРНК получаются при процессировании более длинных одноцепочечных транскриптов, которые содержат комплементарные области, не являющиеся полностью комплементарными и, таким образом, образующие структуру с неполным спариванием оснований, содержащую несовпадения или неспаренные нуклеотиды в пределах частично двухцепочечной структуры. Структура со спаренными основаниями также может содержать пары оснований G-U. Процессинг РНК-предшественников для образования миРНК приводит к преимущественному накоплению одной или более отличных малых РНК, каждая из которых имеет определенную последовательность, или миРНК. Они получены из одной цепи РНК-предшественника, как правило, «антисмысловой» цепи РНК-предшественника, тогда как процессинг длинных комплементарных РНК-предшественников для образования киРНК позволяет получить популяцию киРНК, которые неоднородны по последовательности, но соответствуют разным частям из обеих цепей предшественника.
[0339] РНК-предшественники миРНК согласно изобретению, также называемые в данном документе «искусственными миРНК-предшественниками», как правило, получены из миРНК-предшественников природного происхождения путем изменения нуклеотидной последовательности миРНК-части предшественника природного происхождения так, чтобы она была комплементарной, предпочтительно полностью комплементарной, области из 21-24 нуклеотидов целевой мРНК, и изменения нуклеотидной последовательности комплементарной области миРНК-предшественника, которая способна к спариванию оснований с последовательностью миРНК для сохранения спаривания оснований. Оставшаяся часть РНК-предшественника миРНК может оставаться неизменной и, таким образом, иметь такую же последовательность, что и миРНК-предшественник природного происхождения, или она также может быть изменена в последовательности посредством нуклеотидных замен, нуклеотидных вставок или, предпочтительно, нуклеотидных делеций, или любой их комбинации. Считается, что оставшаяся часть РНК-предшественника миРНК вовлечена в распознавание структуры ферментом дайсер, называемым дайсер-подобным ферментом 1 (DCL1), и следовательно, предпочтительно, чтобы в оставшуюся часть структуры было внесено как можно меньше изменений. Например, спаренные нуклеотиды могут быть замещены другими спаренными нуклеотидами без существенного изменения общей структуры. миРНК-предшественник природного происхождения, из которого получен миРНК-предшественник согласно изобретению, может происходить из пшеницы, другого растения, такого как другое злаковое растение, или из нерастительных источников. Примерами таких РНК-предшественников являются предшественник mi395 риса, предшественник mi159b Arabidopsis или предшественник mi172. Применение искусственных миРНК было продемонстрировано на растениях, например, Alvarez et al., 2006; Parizotto et al., 2004; Schwab et al., 2006.
[0340] Другим молекулярным биологическим подходом, который можно использовать для снижения регуляции экспрессии эндогенного гена, является косупрессия. Механизм косупрессии не до конца понятен, но считается, что он включает посттранскрипционный генный сайленсинг (ПТГС) и в этой связи может быть очень сходен со многими примерами антисмысловой супрессии. Он включает внесение лишней копии гена или его фрагмента в растение в «смысловой ориентации» по отношению к промотору для его экспрессии, которая в контексте данного документа называется ориентацией, совпадающей с транскрипцией и трансляцией (если они происходят) последовательности относительно последовательности в целевом гене. Размер смыслового фрагмента, его соответствие областям целевого гена и степень его гомологии с целевым геном являются такими же, что и для антисмысловых последовательностей, описанных выше. В некоторых случаях дополнительная копия генной последовательности препятствует экспрессии целевого гена растения. В отношении методов применения подходов косупрессии можно сделать ссылку на описание патента WO 97/20936 и описание Европейского патента 0465572.
[0341] Любые из этих технологий для снижения генной экспрессии можно использовать для координированного снижения активности множества генов. Например, одна молекула РНК может быть нацелена против семейства родственных генов посредством нацеливания на область генов, которая является общей. В альтернативном варианте можно проводить нацеливание на неродственные гены путем включения в одну молекулу РНК множества областей, каждая из которых нацелена на разные гены. Это легко осуществить путем слияния множества областей под управлением одного промотора.
[0342] Как хорошо известно специалистам в данной области техники, для внесения молекул нуклеиновых кислот в клетки пшеницы доступно большое число разных техник. В контексте данного документа термин «трансформация» означает изменение генотипа клетки, например бактериальной или растительной, в частности растения пшеницы, путем внесения чужеродной или экзогенной нуклеиновой кислоты. Под «трансформантом» подразумевается измененный таким образом организм. Внесение ДНК в растение пшеницы посредством скрещивания родительских растений или посредством мутагенеза per se не включено в понятие трансформации. Молекулу нуклеиновой кислоты можно реплицировать как внехромосомный элемент или же, предпочтительно, она стабильно интегрируется в геном растения. Под «геномом» подразумевается полный наследуемый генетический набор клетки, растения или части растения, включая хромосомную ДНК, пластидную ДНК, митохондриальную ДНК и внехромосомные молекулы ДНК. В одном варианте реализации трансген интегрирован в ядерный геном пшеницы, который в случае гексаплоидной пшеницы включает подгеномы A, B и D, называемые в данном документе «геномами» A, B и D.
[0343] Наиболее распространенные способы получения фертильных трансгенных растений пшеницы включают два этапа: доставка ДНК в способные к регенерации клетки пшеницы и регенерация растения путем in vitro тканевого культивирования. Для доставки ДНК обычно используют два способа: Т-ДНК-перенос с помощью Agrobacterium tumefaciens или родственных бактерий и прямое внесение ДНК посредством бомбардировки частицами, хотя использовались и другие способы для интеграции последовательностей ДНК в пшеницу или другие злаковые. Специалисту в данной области техники будет понятно, что конкретный выбор системы трансформации для внесения конструкции нуклеиновой кислоты в клетки растений не является важным или ограничивающим для изобретения при условии, что он обеспечивает приемлемый уровень переноса нуклеиновой кислоты. Такие технологии для пшеницы хорошо известны в данной области техники.
[0344] Трансформированные растения пшеницы можно получать путем внесения конструкции нуклеиновой кислоты в соответствии с изобретением в реципиентную клетку и выращивания нового растения, которое содержит и экспрессирует полинуклеотид в соответствии с изобретением. Процесс выращивания нового растения из трансформированной клетки, находящейся в клеточной культуре, называется в данном документе «регенерацией». Способные к регенерации клетки пшеницы включают клетки зрелых эмбрионов, меристематическую ткань, такую как мезофилльные клетки основания листа, или предпочтительно клетки из щитка незрелых эмбрионов, полученные через 12-20 суток после цветения, или каллус, полученный из любого из этих компонентов. Наиболее распространенным путем для восстановления регенерированных растений пшеницы является соматический эмбриогенез с применением среды, такой как МС-агар, дополненной ауксином, таким как 2,4-D, и низким уровнем цитокинина (смотрите Sparks and Jones, 2004).
[0345] Agrobacterium-опосредованную трансформацию пшеницы можно проводить методами Cheng et al., 1997; Weir et al., 2001; Kanna and Daggard, 2003 или Wu et al., 2003. Можно использовать любой штамм Agrobacterium с достаточной вирулентностью, предпочтительно штаммы, имеющие дополнительные вирулентные генные функции, такие как LBA4404, AGL0 или AGL1 (Lazo et al., 1991), или версии C58. Также можно использовать бактерии, родственные с Agrobacterium. ДНК, которая переносится (Т-ДНК) из Agrobacterium реципиентным клеткам пшеницы, находится в генетической конструкции (химерной плазмиде), которая содержит одну или две граничные области Т-ДНК Ti-плазмиды дикого типа, фланкирующие подлежащую переносу нуклеиновую кислоту. Генетическая конструкция может содержать две или более Т-ДНК, например, когда одна Т-ДНК содержит представляющий интерес ген, а вторая Т-ДНК содержит ген селективного маркера, обеспечивая независимую вставку двух Т-ДНК и возможную сегрегацию гена селективного маркера от представляющего интерес трансгена. Вектор Т-ДНК предпочтительно представляет собой «супер-бинарную» плазмиду, как известно в данной области техники.
[0346] Можно использовать любой тип пшеницы, способной к регенерации; сообщалось об успешных результатах для вариететов Bob White, Fielder, Veery-5, Cadenza и Florida. Явления трансформации в одном из этих более способных к регенерации вариететов можно переносить на любые другие сорта пшеницы, включая элитные вариететы, путем стандартного обратного скрещивания. Другие способы, включающие применение Agrobacterium, включают: совместное культивирование Agrobacterium с культивируемыми выделенными протопластами; трансформацию семян, верхушек или меристем Agrobacterium или инокуляцию in planta, такую как метод окунания цветков Arabidopsis, описанный Bechtold et al., 1993.
[0347] Другим способом, обычно применяемым для внесения конструкции нуклеиновой кислоты в клетку растения, является высокоскоростная биолистическая пенетрация мелкими частицами (также известная как бомбардировка частицами или бомбардировка микрочастицами), когда подлежащая внесению нуклеиновая кислота содержится либо в матрице мелких гранул или частиц, либо на их поверхности, например, как описано у Klein et al., 1987.
[0348] Предпочтительные гены селективных маркеров для применения в трансформации пшеницы включают ген Streptomyces hygroscopicus bar или ген pat в сочетании с отбором с применением гербицида глуфосината аммония, ген hpt в сочетании с антибиотиком гигромицином или ген nptII с канамицином или G418. В альтернативном варианте можно использовать положительные селективные маркеры, такие как ген manA, кодирующий фосфоманнозоизомеразу (PMI) с сахарным маннозо-6-фосфатом в качестве единственного источника C.
[0349] Настоящее изобретение дополнительно описано с помощью следующих неограничивающих примеров.
Пример 1. Материалы и методы
[0350] Растительные материалы. Три сорта пшеницы, каждый из которых содержал одну нулевую мутацию в гене SSIIa в геномах A, B или D, были любезно предоставлены доктором М. Ямамори из Национального института агробиологических ресурсов, Япония (Dr M Yamamori, National Institute of Agrobiological Resources, Tsukuba, Japan). Это были Chousen 57 (C57), содержащий нулевую мутацию в SSIIa-A и, следовательно, не содержащий полипептид SSIIa-A (SGP-A1), Kanto 79 (K79), содержащий нулевую мутацию в SSIIa-B и, следовательно, не содержащий полипептид SSIIa-B (SGP-B1), и Turkey 116 (T116), содержащий нулевую мутацию в SSIIa-D и, следовательно, не содержащий полипептид SGP-D1 (Yamamori et al., 2000).
[0351] Нуллисомные/тетрасомные линии Chinese Spring (CS) в отношении гомологичной группы из семи хромосом, обозначаемые N7AT7D, N7BT7D и N7DT7B (Sears and Miller, 1985), были любезно предоставлены доктором Е. Лагуда (Dr E. Lagudah) (CSIRO Agriculture, Канберра, Австралия).
[0352] Растения пшеницы, включая C57, K79, T116, три австралийских сорта пшеницы Sunco, EGA Hume и Westonia, выращивали в CSIRO Agriculture, Канберра, в теплице с естественным освещением и температурой 18°C (ночью) и 24°C (днем). Зрелое зерно каждой линии собирали и сушили на воздухе до содержания влаги приблизительно 9%. Если не указано иное, по 5 г высушенного зерна на линию мололи на мельнице Udy Cyclone (Fort Collins, CO, США) с ситом с размером ячеек 0,5 мм для получения цельнозерновой муки или на мельнице Brabender Quadrumat Junior (Brabender® GmbH & Co. KG, Дуйсбург, Германия) для получения муки высшего сорта.
[0353] Для анализа белков и крахмала в развивающемся зерне и зрелом зерне, описанного в примере 12, получали мутантные растения пшеницы и растения пшеницы дикого типа (ssIIa и SSIIa, соответственно) из двойной гаплоидной популяции, описанной Konik-Rose et al. (2007). От двадцати до сорока развивающихся эндоспермов собирали через 15 суток после цветения (СПЦ) в пробирки с сухим льдом и хранили при -80°C для анализа РНК, растворимых белков и связанных с гранулами крахмала белков, как описано в примере 12. Для анализа белков и свойств крахмала в зерне собирали созревшее зерно выращенных в теплице или в поле растений.
[0354] ДНК-анализ растений пшеницы. Для выявления присутствия или отсутствия мутантных аллелей ssIIa или аллелей дикого типа SSIIa с помощью ПЦР образцов геномной ДНК собирали молодые листья растений и выделяли геномную ДНК, используя набор Fast DNA Kit (система BIO101, Q-BIOgene). Для скрещивания с помощью маркера использовали пары праймеров JKSS2AP1F (5'-TGCGTTTACCCCACAGAGCA CA-3' (SEQ ID NO:15), расположенная между нуклеотидами 91 и 113 нуклеотидной последовательности с № доступа AB201445) и JKSS2AP2R (5'-TGCCAAAGGTCCGGAATCATGG-3' (SEQ ID NO:16), расположенная между нуклеотидами 1225 и 1246 AB201445) для гена SSIIa генома A (Фиг. 2); праймеров JKSS2BP7F (5'-GCGGACCAGGTTGTCGTC-3' (SEQ ID NO:17), расположенная между нуклеотидами 5978 и 5995 нуклеотидной последовательности с № доступа AB201446) и JLTSS2BPR1 (5' CTGGCTCACGATCCAGGGCATC-3' (SEQ ID NO:18), расположенная между нуклеотидами 6313 и 6335 AB201446) для гена SSIIa генома B (Фиг. 3); и праймеров JTSS2D3F (5'-GTACCAAGGTATGGGGACTATGAA-3' (SEQ ID NO:19), расположенная между нуклеотидами 2369 и 2392 нуклеотидной последовательности с № доступа AB201447) и JTSS2D4R (5'-GTTGGAGAGATACCTCAACAGC-3' (SEQ ID NO:20), расположенная между нуклеотидами 2774 и 2796 AB201447) для гена SSIIa генома D пшеницы (Фиг. 4).
[0355] ПЦР-реакции включали применение 50 нг геномной ДНК, 1,5 мМ MgCl2, 0,125 мМ каждого дНТФ, 10 пмоль праймеров, 0,5 М глицинбетаина, 1 мкл диметилсульфоксида (ДМСО) и 1,5-3,5 Е Taq-полимеразы Hot-star (QIAGEN) в реакционном объеме 20 мкл. Реакции амплификации проводили, используя HYBAID PCR Express (Integrated Sciences) с одним циклом при 95°C в течение 5 мин, 35 циклами плавления при 94°C в течение 45 с, температурой гибридизации 52°C (геном A) или 60°C (для генома B и D) в течение 30 с, и удлинением при 72°C в течение 2 мин 30 с, затем 1 циклом при 72°C в течение 10 мин с последующим охлаждением до 25°C. Полученные в результате ПЦР-фрагменты разделяли в 1% или 2% агарозном геле и визуализировали (UVitec) после окрашивания этидием. В других стандартных реакциях амплификации использовали 59°C в качестве температуры гибридизации, но в остальном использовали такие же условия ПЦР, если не указано иное.
[0356] Саузерн-блот-анализ гибридизации проводили для ДНК из более крупномасштабного (9 мл) экстракта из лиофилизированной измельченной ткани (Stacey and Isaac, 1994). Образцы ДНК доводили до 0,2 мг/мл и расщепляли рестрикционными ферментами, такими как BamHI и EcoRI. Расщепление рестрикционными ферментами, гель-электрофорез и вакуумный блоттинг проводили, как описано Stacey and Isaac, (1994). 32P-меченые зонды получали из кДНК и использовали в гибридизации с для анализов Саузерн-блот. Гибридизирующиеся последовательности выявляли с помощью авторадиографии в соответствии с методом Jolly et al. (1996).
[0357] Выделение РНК и количественная ПЦР в режиме реального времени (кОТ-ПЦР). Общую РНК из эндосперма через 15 СПЦ выделяли, используя набор NucleoSpin® RNA Plant Kit (Macherey-Nagel), и количественно оценивали, используя Nanodrop 1000 (Thermo Scientific). По 0,5 мкг РНК-матриц использовали для синтеза кДНК в 50 мкл реакционных смесей при 50°C, используя обратную транскриптазу SuperScript III (Invitrogen). Матрицу кДНК (100 нг) использовали в 10 мкл реакционной смеси кОТ-ПЦР с температурой гибридизации 58°C, используя праймеры для ОТ-ПЦР (таблица 4). В качестве количественного контроля использовали пару праймеров, которые амплифицировали область, расположенную в экзоне на 3’ конце гена тубулина. Реакции амплификации проводили в Rotor-Gene 6000 (Corbett), используя набор Rotor-Gene™ SYBR® Green PCR Kit (QIAGEN). Сравнительную количественную оценку анализировали, используя амплификацию фрагмента гена тубулина в качестве эталонной амплификации, с помощью программного обеспечения для роторного анализатора в режиме реального времени (Corbett). Для каждого образца реакции кОТ-ПЦР проводили в трех повторностях.
Таблица 4. Праймеры кОТ-ПЦР, применяемые для определения экспрессии РНК
[0358] Выделение растворимых и связанных с крахмальными гранулами белков из развивающегося эндосперма. Развивающиеся эндоспермы из развивающихся семян, собранные через 15 СПЦ, гомогенизировали и суспендировали в предварительно охлажденном буфере для экстракции белка в соотношении 1,5 мкл/мг (0,25 М K2HPO4, pH 7,5, 0,05 М ЭДТА, 20% глицерина, коктейль ингибиторов протеаз Sigma и 0,5 М ДТТ). Гомогенат центрифугировали при 16000 g в течение 15 мин при 4°C. Супернатант, содержащий растворимые белки, использовали для оценки концентрации белка, используя реагент для анализа содержания белка Coomassie Plus (Bio-Rad). В случае необходимости образцы хранили при -20°C до проведения анализа. Осадок, полученный из препаратов растворимого белка, непосредственно обрабатывали протеиназой K после промывки водой, а затем следующим образом очищали крахмал. Связанные с крахмальными гранулами белки получали из очищенного крахмала в соответствии с Rahman et al., (1995) с небольшими изменениями. Крахмальные гранулы кипятили в течение 5-10 мин в денатурирующем буфере для экстракции белка (50 мМ Трис-буфера, pH 6,8, 10% глицерина, 5% ДСН, 5% β-меркаптоэтанола и бромфеноловый синий) в соотношении 15 мкл/мг крахмала. После центрифугирования при 13000 g в течение 20 мин супернатант использовали для анализа ДСН-ПААГ.
[0359] Выделение крахмала и экстракция связанных с крахмальными гранулами белков из зрелых зерен. Цельные зерна (100-150 мг) из каждого растения измельчали в центробежной шаровой мельнице при скорости 30 об/мин в течение 30 с, используя миксер WIG-L-BUG Mixer MSD (США). Цельнозерновые продукты сначала обрабатывали 12,5 мМ NaOH, фильтровали через 0,5 мм нейлоновые сита, три раза промывали водой, а затем инкубировали с 0,5 мг протеиназы K в 1 мл 50 мМ фосфатного буфера при 37°C в течение 2 ч. Крахмальный осадок, полученный при центрифугировании при 5000 g, суспендировали и промывали водой 3 раза с центрифугированием после каждой промывки. После промывки ацетоном остаток крахмала сушили на воздухе при 37°C в течение ночи. Приготовление связанных с крахмальными гранулами белков из крахмала зрелого зерна было таким же, как описано ранее для крахмала из развивающегося эндосперма.
[0360] ДСН-ПААГ и окрашивание гелей. Для количественной оценки содержания белка в крахмале использовали одинаковые количества крахмала (4 мг) для экстракции связанных с крахмальными гранулами белков. Для каждого образца такой же объем супернатанта, содержащего общий белок, загружали в 4-12% Бис-Трис гели NuPAGE Novex (Life technologies). Это позволяло проводить выявление вариаций в профилях связывания белка в одинаковом количестве крахмала. Для растворимых белков использовали образцы, содержащие 20 мкг общего белка. Эксперименты и выявление с применением ДСН-ПААГ гелей проводили, как было описано ранее (Butardo et al. 2012).
[0361] Иммуноблоттинг. Варианты антисыворотки против GBSSI, SSI, SSIIa, SBEIIa и SBEIIb из предыдущих исследований перечислены и пронумерованы в таблице 5, включая их источники антигенов и виды специфичности. Вестерн-блоттинг и выявление проводили, как было описано ранее (Butardo et al. 2012), используя те же белковые стандарты, что приведены выше.
Таблица 5. Поликлональные антитела, применяемые для выявления белков крахмальных синтаз злаковых.
[0362] Количественная оценка белковых полос в ДСН-ПААГ гелях и иммуноблотах. Для количественной оценки и сравнения распространенности белков между разными генотипами в качестве эталона использовали две белковые полосы (80 кДа и 60 кДа) в 5 мкл наборах белков MagicMark™ XP (Invitrogen). После визуализации белковых полос сканировали ДСН-ПААГ гели и иммуноблоты (Epson Perfection 2450 PHOTO; Epson America Inc., CA, США), чтобы получить графические файлы для анализа интенсивности полос, используя пакет программного обеспечения Quantity One и придерживаясь рекомендованных методов (Bio-Rad). Полосу 80 кДа использовали для количественной оценки SBEIIa, SBEIIb и SSIIa, а полосу 60 кДа - для SSI и GBSSI.
[0363] Масс-спектрометрия. Протеолитическое расщепление в геле можно проводить для выбранных белковых полос из окрашенных голубым кумасси ДСН-ПААГ гелей. Тандемную МС с применением ионных ловушек можно проводить, как описано у Butardo et al. (2012). Белки можно идентифицировать путем корреляции непрерывных данных МС с данными в SwissProt/TREMBL посредством глобального сервера ProteinLynx (Version 1, Micromass) (Colgrave et al. 2013).
[0364] Масса зерновок. Зерно собирали со зрелых растений, когда растения были полностью желтыми. Колосья собирали и хранили при 37°C в течение по меньшей мере двух недель, чтобы гарантировать полное высушивание, затем хранили при комнатной температуре в случае необходимости в дальнейшем хранении, а затем обмолачивали для получения зрелого зерна. Это зерно или полученную из него цельнозерновую муку анализировали в отношении параметров, описанных в данном документе, которые зависят от массы зерна, а также массы самой зерновки. Массу зерновок для каждой линии пшеницы определяли по общей массе 100 зерен. Содержание влаги в зерне измеряли с помощью спектрометра MPA FT-NIR (BRUKER); для зрелого зерна она обычно составляла около 9% в массовом отношении. Параметры, которые зависят от массы зерна, такие как содержание крахмала, содержание БГ, содержание фруктана и т. д., описанные в данном документе, рассчитывали на основании сухой массы, принимая содержание влаги за 9% (масс./масс.), если его не измеряли с помощью NIR.
[0365] Анализ липидов в зерне пшеницы. Общее количество липидов из образцов цельнозерновой муки массой около 300 мг экстрагировали смесью хлороформа/метанола/0,1 М KCl (в соотношении 2:1:1, об./об./об.). Метиловые эфиры жирных кислот (МЭЖК) готовили, инкубируя образцы липидов в 1 Н метанольной HCl (Supelco, Bellefonte, PA) при 80°C в течение 2 ч. TAG и пулы полярных мембранных липидов фракционировали из общего количества липидов с помощью тонкослойной хроматографии (ТСХ) (силикагель 60, Merck, Germany), используя смесь растворителей гексан:диэтиловый эфир:уксусная кислота (70:30:1, об./об./об.), а отдельные классы мембранных липидов разделяли, используя смесь растворителей хлороформ/метанол/уксусная кислота/вода (90/15/10/3, об./об./об./об.). Действующие липидные стандарты загружали и исследовали в отдельных дорожках на тех же пластинах для идентификации липидных классов. Полосы из диоксида кремния, содержащие отдельный класс липидов, использовали для приготовления МЭЖК, как было указано выше, и анализировали с помощью газовой хроматографии GC-FID 7890A (Agilent Technologies, Пало-Альто, Калифорния, США) с применением колонки BPX70 на 30 м (SGE, Остин, Техас, США) для количественной оценки отдельных жирных кислот на основании площади пика известного количества гептадеканоина, который добавляли в качестве внутреннего стандарта.
[0366] Экстракция крахмала. Если не указано иное, крахмал экстрагировали из образцов зерен, сначала измельчая зерно (10 г) до цельнозерновой муки, используя мельницу Cyclone (Cyclote 1093, Tecator, Швеция). Крахмал выделяли из цельнозерновой муки методом протеазной экстракции (Morrison et al., 1984) и промывали водой, используя 10 мл воды на грамм цельнозерновой муки, при комнатной температуре с удалением остатков. Затем крахмал лиофилизировали и взвешивали для анализа. Крахмал также выделяют в небольших масштабах из развивающегося зерна пшеницы, используя метод Regina et al., (2006).
[0367] Содержание крахмала. Общее содержание крахмала в зерне оценивали методом 76.13 AACC, используя набор для анализа общего крахмала (K-TSTA), предоставленный Megazyme (Bray, Co, Уиклоу, Республика Ирландия), и рассчитывали в массовом отношении в виде процентной доли от массы зрелого неизмельченного зерна. Вычитание массы крахмала из общей массы зерна с получением некрахмального содержания зерна позволяет определить, было ли снижение общей массы связано со снижением содержания крахмала.
[0368] Содержание амилозы. Если не указано иное, содержание амилозы в образцах крахмала определяли в трех повторностях йодометрическим (связывание йода) методом по Morrison and Laignelet (1983) с небольшими следующими модификациями. Приблизительно 2 мг крахмала точно отвешивали (точность до 0,1 мг) в 2 мл пробирки с завинчивающимися крышками, имеющими резиновую прокладку в области крышки. Для удаления липидов смешивали 1 мл 85% (об./об.) метанола с крахмалом и нагревали пробирку на водяной бане при 65°C в течение 1 часа с периодическим перемешиванием. После центрифугирования при 13000 g в течение 5 мин аккуратно удаляли супернатант и повторяли этап экстракции. Затем крахмал сушили при 65°C в течение 1 часа и растворяли в растворе мочевины и диметилсульфоксида (МДМСО; 9 объемов диметилсульфоксида к 1 объему 6 М мочевины), используя 1 мл МДМСО на 2 мг крахмала. Смесь незамедлительно интенсивно перемешивали вихревым способом и инкубировали на водяной бане при 95°C в течение 1 часа с периодическим перемешиванием для полного растворения крахмала. Аликвоту раствора крахмал-МДМСО (50 мкл) обрабатывали 20 мкл реагента I2-KI, который содержал 2 мг йода и 20 мг йодида калия на мл воды. Смесь доводили до 1 мл водой. Поглощение смеси при 620 нм измеряли, перенося 200 мкл в микропланшет и считывая поглощение с помощью микропланшетного ридера Emax Precision (Molecular Devices, США). Стандартные образцы, содержащие от 0 до 100% амилозы и от 100% до 0% амилопектина, получали из картофельной амилозы (Sigma, № в каталоге A-0512) и картофельного амилопектина (Sigma, № в каталоге A-8515) и обрабатывали как и исследуемые образцы. Содержание амилозы (процент амилозы) определяли по значениям поглощения, используя регрессионное уравнение, полученное по данным поглощения для стандартных образцов.
[0369] Если указано, также определяли содержание амилозы в образцах крахмала посредством деветвления образцов крахмала и последующего измерения с помощью эксклюзионной хроматографии (ЭХ), как было описано ранее (Butardo et al. 2012; Castro et al. 2005). Этим способом отделяли короткие цепи, полученные в результате деветвления амилопектина, от более длинных амилозных цепей и определяли их относительное количество. Пуллулановые стандарты (Shodex P-82), откалиброванные с помощью уравнения Марка-Хаувинка-Сакурады, использовали для оценки молекулярной массы по времени элюирования. Образцы готовили и анализировали в трех повторностях.
[0370] Также можно проводить анализ соотношения амилоза/амилопектин в недеветвленных крахмалах в соответствии с Case et al., (1998) или методом ВЭЖХ, используя 90% ДМСО для разделения деветвленных крахмалов, как описано у Batey and Curtin, (1996).
[0371] Содержание резистентного крахмала (РК). Содержание РК в зерне определяли в трех повторностях, используя набор для анализа РК (K-RSTARCH), предоставленный Megazyme (Bray, Co, Уиклоу, Республика Ирландия), и рассчитывали в массовом отношении в виде процентной доли от содержания крахмала. Вместо 100 мг образца, предлагаемого в наборе для анализа РК, для каждого анализа в этой работе использовали сниженное количество цельнозерновой муки (40 мг) в 15 мл пробирках с крышками и коническим дном (№ в каталоге 188271, Greiner bio-one), используя pro rata количества растворов и буферов из набора. Стандартные образцы, содержащие от 0 до 20 мг/мл глюкозы, получали из глюкозы (набор K-RSTARCH) и обрабатывали как и исследуемые образцы. Содержание РК в массовом отношении и содержание нерезистентного крахмала для исследуемых образцов определяли по значениям поглощения, используя регрессионное уравнение, полученное по данным поглощения для стандартных образцов. Затем рассчитывали содержание РК как массу РК в виде процентной доли от массы общего содержания крахмала.
[0372] Уровень РК в образцах пищевых продуктов, таких как хлеб, также можно измерять in vitro, как описано, например, в WO2012/058730. В этом способе описано приготовление образца и in vitro расщепление крахмала в обычно употребляемых пищевых продуктах. Этот способ состоит из двух частей: во-первых, крахмал в пище гидролизуют в искусственно созданных физиологических условиях; во-вторых, удаляют побочные продукты путем промывки, а определение РК проводят после гомогенизации и сушки образца. Крахмал, количественно оцениваемый в конце расщепления, представляет содержание РК в пище.
[0373] β-глюкан (БГ). Уровни БГ определяли в трех повторностях, используя набор (K-BGLU), предоставленный Megazyme (Bray, Co, Уиклоу, Республика Ирландия).
[0374] Содержание фруктана. Экстракцию и анализ фруктана проводили в 2 мл пробирках или 96-луночных планшетах (2 мл на лунку), используя модифицированную процедуру с применением набора для анализа фруктана Megazyme (K-FRUC) следующим образом. Пшеничную цельнозерновую муку (40 мг) смешивали с 1 мл воды (80°C) и инкубировали со встряхиванием (1200 об/мин) при 80°C в течение 30 мин. После охлаждения до комнатной температуры пробирки центрифугировали в течение 5 мин и отбирали 20 мкл супернатанта, содержащего фруктаны и другие сахара, для анализа фруктана. Сахарозу, мальтозу, мальтодекстрины и крахмал в супернатанте гидролизовали до глюкозы и фруктозы путем добавления 20 мкл раствора ферментов, содержащего сахаразу, амилазу и мальтазу из набора K-FRUC, и инкубировали смеси при 40°C со встряхиванием (1000 об/мин) в течение 30 мин. Затем восстанавливали глюкозу и фруктозу в образцах путем добавления 20 мкл 10 мг/мл раствора щелочного борогидрида и инкубации при 40°C со встряхиванием (1000 об/мин) в течение 30 мин. Фруктаны в этом растворе гидролизовали фруктаназами (40°C в течение 30 мин со встряхиванием при 1000 об/мин) до глюкозы и фруктозы. Добавляли п-гидроксибензойной кислоты гидразид (PAHBAH) для образования цветного комплекса при 98°C в течение 6 мин. После охлаждения образцов проводили измерение цветного комплекса при 410 нм, используя спектрофотометр, а значения поглощения переводили в содержание фруктана, используя стандартную кривую, которая содержала от 0 до 0,27 мг/мл фруктозы (Megazyme, набор K-FRUC), которую обрабатывали как и исследуемые образцы после гидролиза фруктаназой. Содержание фруктана (процент фруктана) для исследуемых образцов определяли по значениям поглощения, используя регрессионное уравнение, полученное по данным поглощения для стандартных образцов.
[0375] Анализ фруктана в уменьшенном масштабе в формате планшета. Для анализа фруктана в уменьшенном масштабе в 10 раз уменьшали все количества растворов ферментов, буферов и реагентов в наборах Megazyme и проводили реакции в 96-луночном планшете. Использовали образцы цельнозерновой муки по 20 мг в случае образцов с высоким содержанием фруктана или по 40 мг в случае более низких уровней фруктана, составляющих около 0,5-2%. Предварительное замачивание муки в этаноле было необязательным для экстракции фруктана, так как цельнозерновая мука хорошо диспергировалась в горячей воде при перемешивании перед экстракцией фруктанов. Для экстракции фруктана было достаточно времени экстракции 20 мин. Реакции гидролиза проводили в 1,1 мл в 96-луночных планшетах, закрываемых крышками, при 40°C в течение 30 мин со встряхиванием при 1000 об/мин, используя BioShake iQ и 96-луночный адаптер (Q Instruments, Йена, Германия). В модифицированном анализе K-FRUC планшеты после гидролиза фруктана и добавления п-гидроксибензойной кислоты гидразида (PAHBAH) закрывали крышками и плотно зажимали в специально сделанном держателе для планшетов для проявления цвета при 100°C в течение 6 мин, используя водяную баню (WiseBath, Thermoline Scientific, Уэтерилл Парк, Нов. Юж. Уэльс, Австралия). Гидролизованные образцы (250 мкл) переносили в 96-луночный микротитровальный планшет с плоским дном (UV-Sta®Microplate или PS-Microplate, Greiner Bio-One, Германия) для считывания поглощения при 340 нм (в случае K-FRUCHK) или 410 нм (в случае K-FRUC), используя планшет-ридер Multiskan Spectrum (Thermo Scientific, Финляндия).
[0376] Общий арабиноксилан (АК). АК измеряли, используя 20 мг образцы цельнозерновой муки в 2 мл пробирках с завинчивающимися крышками. Каждый образец смешивали с 1 мл 0,5 М серной кислоты, перемешивали вихревым способом и инкубировали смеси при 99°C со встряхиванием (1000 об/мин) в течение 30 мин. Затем пробирки охлаждали в ледяной воде в течение 5 мин. Пробирки центрифугировали при 10000 g в течение 5 мин, а супернатант (800 мкл) из каждой пробирки переносили в 96-луночный планшет. В случае необходимости эти планшеты хранили при -20°C перед дополнительной обработкой. Для разведения 100 мкл аликвоты супернатанта переносили в другой 96-луночный планшет (Greiner bio-one masterblock) и добавляли по 900 мкл воды Milli Q в каждую лунку. Разведенный супернатант (100 мкл) переносили в аналитический планшет (BioRad Titre tube Microtubes Racked, № в каталоге 223-9390). Для создания стандартов ксилозы готовили 100 мкл стандартных растворов, имеющих концентрации 30, 50, 75, 100, 150 и 200 мкг/мл, используя 2 мг/мл исходный раствор (Sigma, № в каталоге X-3877). В каждую лунку добавляли 0,5 мл свежеприготовленного реагента флороглюцина (PGR, смотрите ниже). Планшеты герметизировали лентами MicroCap (National Scientific, TN3346-08C), зажимали и инкубировали при 100°C в течение 25 мин в вытяжном шкафу. Затем образцы тщательно смешивали, переворачивая планшеты. После этого 200 мкл образцы переносили в планшет UV star в вытяжном шкафу. Поглощение каждого образца измеряли при 510 и 552 нм, используя планшетный спектрофотометр, например Thermo multiscan.
[0377] Реагент флороглюцин (PGR) готовили заново для каждого анализа в вытяжном шкафу. Для этого отдельно готовили два раствора, а затем смешивали их. Раствор 1 готовили, растворяя 0,6 г флороглюцина (Sigma, № в каталоге 7933) в 2,4 мл абсолютного этанола в течение нескольких минут в 50 мл пробирке. Раствор 2 содержал 55 мл ледяной уксусной кислоты с 1,1 мл концентрированной хлористоводородной кислоты (HCl), которую медленно добавляли в уксусную кислоту. Раствор 1 переносили в 250 мл бутылку. Затем 50 мл пробирку, содержащую остатки раствора 1, промывали раствором 2, чтобы количественно перенести весь раствор 1, а затем смешивали весь раствор 2 с раствором 1 в бутылке. И наконец, в смесь растворов 1 и 2 добавляли 0,6 мл раствора глюкозы (70 мг/мл в воде Milli Q).
[0378] Содержание целлюлозы. Анализ целлюлозы проводили в 2 мл пробирках или 96-луночных планшетах (2 мл на лунку), используя 50 мг образцы цельнозерновой муки. Лигнин, гемицеллюлозу и солюбилизированный крахмал из цельнозерновой муки удаляли путем добавления 600 мкл азотнокислого реагента (10:1 (об./об.) смесь 80% уксусной кислоты: 70% азотной кислоты) и инкубации смеси при 99°C со встряхиванием (1000 об/мин) в течение 1 ч. После охлаждения образцы центрифугировали при максимальной скорости в течение 5 мин и сливали супернатанты. Каждый осадок промывали 1 мл воды, центрифугировали при максимальной скорости в течение 5 мин и сливали каждый супернатант. Для солюбилизации кристаллической целлюлозы в каждом осадке в каждую пробирку с образцом добавляли 1 мл 72% H2SO4. Образцы разводили с учетом оцененного содержания целлюлозы и стандартов целлюлозы. Для проявления цвета в каждую пробирку с образцом добавляли 100 мкл антронового реагента (0,2% антрона в 72% H2SO4) и инкубировали смеси при 98°C в течение 10 минут. Поглощение обработанных образцов считывали при 620 нм, используя спектрофотометр, а содержание целлюлозы рассчитывали, используя стандартную кривую, для которой использовали от 0 до 0,75 мг/мл целлюлозы (Sigma: № в каталоге G-6413).
[0379] Анализ распределения по длинам цепей. Определение распределения по длинам цепей амилопектина проводили методом капиллярного электрофореза с активацией флуоресценцией (FACE) после деветвления образцов крахмала, используя установку для капиллярного электрофореза в соответствии с Morell et al., (1998). Образцы готовили, как было описано ранее (O’Shea and Morell, 1996).
[0380] Желатинизация крахмала. Температурные профили желатинизации образцов крахмала определяли на дифференциальном сканирующем калориметре Pyris 1 (Perkin Elmer, Норуолк, Коннектикут, США). Вязкость образцов крахмала измеряли на экспресс-анализаторе вязкости (ЭАВ, Newport Scientific Pty Ltd, Уорривуд, Сидней), например, используя условия, описанные Batey et al., (1997). Измеряемые параметры включали пиковую вязкость (максимальную вязкость горячей пасты), силу удержания, конечную вязкость и температуру клейкости. Объемное разбухание муки или крахмала определяли в соответствии с методом Konik-Rose et al., (2001). Поглощение воды измеряли, взвешивая образец до и после смешивания образца муки или крахмала в воде при определенных температурах и собирая впоследствии желатинизированный материал.
[0381] Морфология крахмальных гранул. Морфологию крахмальных гранул исследовали под микроскопом. Суспензии очищенных крахмальных гранул в воде исследовали в обычном и поляризованном свете, используя составной микроскоп Leica-DMR для определения морфологии крахмальных гранул. Эксперименты по сканирующей электронной микроскопии проводили на инструменте Joel JSM 35C. Очищенный крахмал покрывали методом напыления золотом и сканировали при 15 кВ при комнатной температуре.
[0382] Анализ белковой экспрессии в эндосперме. Специфическую экспрессию белков SBEI, SBEIIa и SBEIIb в эндосперме, в частности, уровень экспрессии или накопления этих белков, анализировали с помощью процедур Вестерн-блоттинга. Эндосперм удаляли из всех материнских тканей, а образцы приблизительно по 0,2 мг гомогенизировали в 600 мкл 50 мМ калий-фосфатного буфера (42 мМ K2HPO4 и 8 мМ KH2PO4), pH 7,5, содержащего 5 мМ ЭДТА, 20% глицерин, 5 мМ ДТТ и 1 мМ Pefabloc. Измельченные образцы центрифугировали в течение 10 мин при 13000 g, а супернатант аликвотировали и замораживали при -80°C до использования. Для оценки общего белка строили стандартную кривую БСА, используя 0, 20, 40, 60, 80 и 100 мкл аликвоты 0,25 мг/мл стандарта БСА. Образцы (3 мкл) доводили до 100 мкл дистиллированной водой и в каждый добавляли 1 мл реагента Coomassie Plus Protein. Поглощение считывали через 5 мин при 595 нм, используя нулевой образец БСА со стандартной кривой в качестве контроля, и определяли уровни белка в образцах. Образцы, содержащие 20 мкг общего белка из каждого эндосперма, исследовали в 8% неденатурирующем полиакриламидном геле, содержащем 0,34 М Трис-HCl (pH 8,8), акриламид (8,0%), персульфат аммония (0,06%) и TEMED (0,1%). После электрофореза белки переносили на нитроцеллюлозную мембрану в соответствии с Morell et al., 1997 и проводили иммунную реакцию со специфическими антителами к SBEIIa, SBEIIb или SBEI (таблица 5). Антисыворотку против белка SBEIIa пшеницы (анти-wBEIIa) создавали, используя синтетический пептид, имеющий аминокислотную последовательность N-концевой последовательности зрелого SBEIIa пшеницы, AASPGKVLVPDGESDDL (SEQ ID NO: 49) (Rahman et al., 2001). Антисыворотку против SBEIIb пшеницы (анти-wBEIIb) создавали аналогичным способом, используя N-концевой синтетический пептид AGGPSGEVMI (SEQ ID NO: 50) (Regina et al., (2005). Считалось, что этот пептид представляет N-концевую последовательность зрелого пептида SBEIIb и, более того, он был идентичным N-концу белка SBEIIb ячменя (Sun et al., 1998). Поликлональное антитело против SBEI пшеницы синтезировали аналогичным способом, используя N-концевой синтетический пептид VSAPRDYTMATAEDGV (SEQ ID NO:51) (Morell et al., 1997). Такую антисыворотку получали от кроликов, иммунизированных синтетическими пептидами, в соответствии со стандартными способами.
[0383] Статистический анализ. Статистический анализ данных по амилозе проводили, используя 16-ое издание Genstat для Windows (VSN International Ltd, Хартфордшир, Великобритания). Другие данные подвергали статистическому анализу (t-критерий и однофакторный ANOVA с апостериорным критерием Тьюки), используя GraphPad Prism, версия 5.01. Планки погрешностей представляют стандартную погрешность среднего (СПС). Статистическую значимость определяли как P < 0,05 и P < 0,01.
Пример 2. Идентификация последовательностей кДНК и последовательностей геномной ДНК для генов SSIIb и SSIIc пшеницы и кодируемых полипептидов и сравнение с SSIIa
[0384] Чтобы идентифицировать гены, кодирующие изоферменты крахмальной синтазы II (SSIIb и SSIIc) в пшенице, соответствующие SSIIb и SSIIc в рисе (Ohdan et al., 2005), и сравнить их с SSIIa, проводили поиск по базе данных NCBI, используя последовательности кДНК из риса, а именно соответствующие № доступа AF419099 для SSIIa, AF395537 для SSIIb и AF383878 для SSIIc. Гомологи пшеницы идентифицировали следующим образом. Для генов SSIIa пшеницы было идентифицировано три гомологичные последовательности кДНК, соответствующие генам SSIIa в пшенице. Они соответствовали № доступа: AF155217 (SEQ ID NO:4) для SSIIa-A в геноме A, AJ269504 (SEQ ID NO:5) для SSIIa-B в геноме B и AJ269502 (SEQ ID NO:6) для SSIIa-D в геноме D. Были идентифицированы нуклеотидные последовательности ДНК, соответствующие этим трем гомологичным последовательностям кДНК: № доступа AB201445 для гена SSIIa-A (SEQ ID NO:7), AB201446 для гена SSIIa-B (SEQ ID NO:8) и AB201447 для гена SSIIa-D (SEQ ID NO:9). Поиск по базе данных IWGSC позволил идентифицировать положение трех соответствующих гомологичных генов в хромосоме 7AS (Traes_7AS_53CAFB43A, 7A:52346437-52346905 п. о., обратная цепь), 7BS (IWGSC: хромосома 7BS, Traes_7BS_7BEAF5EC0, 7B: 31821573-31821749 п. о., прямая цепь) и 7DS (IWGSC: хромосома 7DS, Traes_7DS_E6C8AF743, IWGSC_CSS_7DS_scaff_3877787: от 1 до 396 п. о., от 5137 до 5419 п. о., прямая цепь), соответственно. Аминокислотные последовательности были, соответственно, следующими: № доступа: AAD53263 для SSIIa-A, CAB96627 для SSIIa-B и CAB86618 для SSIIa-D полипептидов.
[0385] Когда аминокислотные и соответствующие нуклеотидные последовательности SSIIa попарно сравнивали с помощью BLAST вдоль всей длины последовательностей, гомологичные последовательности были на 95-96% идентичными для каждого сравнения. Следовательно, их было легко отличить друг от друга.
[0386] В базе данных NCBI было идентифицировано две последовательности кДНК, кодирующие гены SSIIb пшеницы, которые соответствовали № доступа AK332724 из генома A и EU333947 из генома D. В базе данных NCBI не было идентифицировано соответствующих последовательностей геномной ДНК, однако последовательности геномной ДНК были найдены в базе данных IWGSC. Было идентифицировано три гомологичные последовательности геномной ДНК, кодирующие SSIIb, а именно ген SSIIb-A в хромосоме 6AL (гомология с IWGSC: хромосома 6AL, Traes_6AL_AE01DC0EA, 6A: от 187503905 п. о. до 187505233 п. о., прямая цепь при поиске BLAST на веб-сайте EnsemblPlants) (последовательность кДНК SEQ ID NO:12), ген SSIIb-B в хромосоме 6BL (хромосома 6BL, ген: Traes_6BL_61D83E262, 6B:162116364-162116691 п. о., обратная цепь при поиске BLAST на веб-сайте EnsemblPlants) (последовательность кДНК SEQ ID NO:13) и ген SSIIb-D в хромосоме 6DL (гомология с IWGSC: хромосома 6DL, ген: Traes_6DL_19F1042C7, 6D: от 147050072-147051031 п. о., обратная цепь при поиске BLAST на веб-сайте EnsemblPlants) (последовательность кДНК SEQ ID NO:14). Была идентифицирована одна аминокислотная последовательность (№ доступа: ABY56824, SEQ ID NO:11) в базе данных NCBI, которая была на 100% идентичной аминокислотным последовательностям, полученным из EU333947; следовательно, она была полипептидной последовательностью SSIIb-D. Полноразмерная аминокислотная последовательность (SEQ ID NO:10) была получена из нуклеотидной последовательности AK332724 для полипептида SSIIb-A, которая имела 90% гомологии с ABY56824 из SSIIb генома D. Аминокислотная последовательность для полипептида SSIIb-B была получена из фрагмента ДНК из IWGSC (Traes_6BL_61D83E262, 6B:162116364 - 162116691 п. о., обратная цепь). Полноразмерные аминокислотные последовательности SSIIb-A и SSIIb-D были приблизительно на 90% идентичными. При попарном сравнении три соответствующие нуклеотидные последовательности ДНК были на 91-95% идентичными. По сравнению с аминокислотными или нуклеотидными последовательностями SSIIa последовательности SSIIb были на 71-79% идентичными соответствующему паралогу SSIIa. Следовательно, любые последовательности SSII можно легко идентифицировать как SSIIa или SSIIb либо по аминокислотным, либо нуклеотидным последовательностям.
[0387] В случае генов SSIIc пшеницы была идентифицирована одна последовательность кДНК (№ доступа: EU307274) в базе данных NCBI, которая соответствовала гену, расположенному в хромосоме пшеницы 1DL (гомология с IWGSC: хромосома 1DL, ген: Traes_1DL_F667ED844, IWGSC_CSS_1DL_scaff_2205619:1950-3041 п. о., прямая цепь при поиске BLAST на веб-сайте EnsemblPlants), следовательно, она соответствует SSIIc-D. Последовательность кДНК для другого гена SSIIc была идентифицирована с помощью поиска по базе данных IWGSC, как ген, расположенный в хромосоме 1AL (IWGSC: хромосома 1AL, ген: Traes_1AL_729BF3204, 1A: 68687585-68688377, прямая цепь при поиске BLAST на веб-сайте EnsemblPlants). Последовательность кДНК имела 98% идентичности с последовательностью нуклеотидов 1679-2469 под номером доступа: EU307274. Также была идентифицирована последовательность из хромосомы 1BL, которая представляла собой последовательность кДНК частичной длины для SSIIc-B (IWGSC: хромосома 1BL, ген: Traes_1BL_447468BDE, 1B: 31475067-314776087 п. о., прямая цепь при поиске BLAST на веб-сайте EnsemblPlants). Была идентифицирована одна аминокислотная последовательность (№ доступа: ABY639) в базе данных NCBI, которая имела 100% идентичности с аминокислотной последовательностью, полученной из последовательности кДНК с № доступа EU307274. Две аминокислотные последовательности частичной длины также были получены из нуклеотидных последовательностей других фрагментов геномной ДНК для SSIIc из геномов A и B. При попарном сравнении последовательности SSIIc были практически на 98% идентичны друг с другом. Они довольно сильно отличались от последовательностей SSIIa.
[0388] Был сделан вывод, что гены SSIIa и полипептидные последовательности SSIIa можно легко отличить от соответствующих последовательностей SSIIb и SSIIc.
Пример 3. Геном-специфические ДНК-маркеры для скрещивания с помощью маркера
[0389] Чтобы создать тройные нулевые ssIIa-мутантные растения, изогенные с растениями дикого типа по нескольким разным вариантам генетического окружения, использовали растения трех линий пшеницы C57 (нулевая в отношении SSIIa-A), K79 (нулевая в отношении SSIIa-B) и T116 (нулевая в отношении SSIIa-D) (Yamamori et al., 2000) в серии скрещиваний, обратных скрещиваний и скрещиваний между собой. Чтобы выявить и отследить мутации, каждая из которых является рецессивной, в программе скрещивания с молекулярными маркерами создавали и использовали геном-специфические ДНК-маркеры на основании последовательностей гена SSIIa. Специфические мутации в генах SSIIa из C57, K79 и T116 в геномах A, B и D, соответственно, были описаны Shimbata et al., (2005). Каждая из мутаций представляла собой делецию или вставку ДНК в соответствующих генах SSIIa (Фиг. 2-4) и, следовательно, эти мутации идеально подходили для создания молекулярных маркеров. ДНК-маркер создавали для каждого гена путем размещения прямого олигонуклеотидного праймера выше каждого из сайтов мутации и обратного праймера после каждого из сайтов мутации, а последовательности описаны в примере 1 «ДНК-анализ растений пшеницы».
[0390] Эти праймеры использовали для амплификации фрагментов ДНК, специфических для каждого генома из растений дикого типа и растений с нулевой мутацией ssIIa. В случае гена SSIIa генома A амплифицировали 1072 п. о. фрагмент из дикого типа и 778 п. о. фрагмент из нулевого мутантного гена ssIIa-A. В случае гена SSIIa генома B амплифицировали 374 п. о. фрагмент из дикого типа и 522 п. о. фрагмент из нулевого мутантного гена ssIIa-B. В случае гена SSIIa генома D амплифицировали 427 п. о. фрагмент из дикого типа и 364 п. о. фрагмент из нулевого мутантного гена ssIIa-D. Эти геном-специфические фрагменты можно было легко отличить по размеру с помощью гель-электрофореза и, следовательно, их можно было использовать как кодоминантные ДНК-маркеры для выявления мутантных аллелей и аллелей дикого типа. Для получения альтернативных вариантов молекулярных маркеров легко можно сконструировать другие специфические пары праймеров на основании последовательности гена SSIIa.
Пример 4. Создание тройных нулевых ssIIa-мутантов в разном генетическом окружении
[0391] Чтобы создать тройные нулевые ssIIa-мутантные растения, изогенные по нескольким разным вариантам генетического окружения, использовали растения трех линий пшеницы C57 (нулевая в отношении SSIIa-A), K79 (нулевая в отношении SSIIa-B) и T116 (нулевая в отношении SSIIa-D) (Yamamori et al., 2000) в серии скрещиваний, обратных скрещиваний, скрещиваний между собой и отбора потомства, что схематически показано на Фиг. 5-7. ДНК-маркеры, описанные в примере 1, использовали для скрининга дочерних растений в каждом поколении, что позволило провести различие между нулевыми мутантными аллелями ssIIa и соответствующими аллелями дикого типа в вариететах пшеницы Sunco, EGA Hume или Westonia, которые использовали в качестве рекуррентных родителей. Сначала растения из линий C57, K79 и T116 скрещивали с растениями пшеницы сорта Sunco, используя растения Sunco как женские растения, чтобы получить C57-Sunco F1, K79-Sunco F1 и T116-Sunco F1. Затем получали двойных нулевых ssIIa-мутантов для C57-K79-Sunco F1 и K79-T116-Sunco F1 путем скрещивания растений с одной нулевой мутацией в генетическом окружении Sunco с последующим самоопылением потомства с получением растений F2 при скрещивании. ДНК-маркеры использовали для отбора потомства, гетерозиготного в отношении двух нулевых мутаций ssIIa. Затем этих мутантов использовали в трех последовательных обратных скрещиваниях с Sunco в качестве рекуррентных родителей для получения гетерозигот BC3, имеющих две нулевые мутации. Затем скрещивали растения BC3, а потомство самоопыляли с отбором тройных нулевых ssIIa-мутантов (C57-K79-T116-Sunco BC3 F2) в генетическом окружении Sunco (Фиг. 5).
[0392] Получение семян BC3F8 для нулевых мутантов ssIIa и линий пшеницы дикого типа в генетическом окружении сортов EGA Hume, Sunco и Westonia. Чтобы получить растения и зерно в двух разных вариантах генетического окружения, отличных от Sunco, двойных мутантов в Sunco (C57-K79-Sunco F1 или F2, K79-T116-Sunco F1 или F2) использовали в качестве доноров пыльцы при скрещивании с растениями сортов EGA Hume и Westonia (Фиг. 6 и 7), используя ДНК-маркеры в каждом поколении для выявления и отбора мутантных аллелей в потомстве. Отобранное потомство двойных мутантов ssIIa использовали в трех последовательных обратных скрещиваниях с EGA Hume или Westonia в качестве рекуррентных родителей, что приводило к получению растений BC3. Двойных мутантов скрещивали и самоопыляли, получая 466 дочерних растений поколения F2, из которых было отобрано всего 21 растение с тройной нулевой мутацией ssIIa (обозначаемой как генотип «abd») (Фиг. 6 и 7). 466 дочерних растений имели генотипы дикого типа, включающие одну нулевую мутацию ssIIa и две нулевые мутации ssIIa, а также все комбинации гетерозигот в отношении трех генов SSIIa.
[0393] После получения и отбора 21 тройного нулевого мутанта, охватывающих все варианты генетического окружения, получали три поколения потомка одного семени (ПОС) для повышения гомозиготности в каждом из трех вариантов генетического окружения, получая поколения зерна BC3F3, BC3F4 и BC3F5. Зерновка BC3F5 дополнительно увеличивалась в объеме в трех выращиваемых поколениях с получением от 10 до 20 г зерновки поколения BC3F8 для каждой из линий.
[0394] Также путем скрещивания создавали тройных сегрегантов SSIIa дикого типа (генотип ABD) и отбирали в качестве контрольных линий. В каждом поколении использовали ДНК-маркеры для всех трех геномов для отбора ssIIa-мутантов или аллелей SSIIa дикого типа для каждого генома для каждого поколения. В конечном итоге было создано 4, 6 и 11 линий с тройной нулевой мутацией ssIIa поколения BC3F8 для генетического окружения EGA Hume, Sunco и Westonia, соответственно, и было создано 5 линий SSIIa BC3F8 дикого типа для генетического окружения EGA Hume, Sunco и Westonia. Их выращивали в одно время в одинаковых условиях роста, собирали зерно по достижению растением зрелости и сушили зерно до содержания влаги около 9% (в массовом отношении). Эти партии зерен анализировали в отношении различных параметров, включая массу семян, содержание крахмала, содержание амилозы, общее содержание пищевых волокон, содержание липидов и т. д., как описано ниже.
Пример 5. Анализ параметров зерна и крахмала
[0395] Масса зерновок. Среднюю массу зерновки (мг на зерновку) тройных нулевых ssIIa-мутантов и зерна дикого типа в трех вариантах генетического окружения рассчитывали, измеряя массу 100 зерен из каждой линии. Средняя приходящаяся на зерновку масса находилась в диапазоне от 25 мг до 36 мг для нулевых ssIIa-мутантов и от 29 мг до 48 мг для линий дикого типа (таблица 6, Фиг. 8). Растения выращивали далеко не в идеальных условиях роста, что объясняет малую массу даже для контролей дикого типа. Средние данные приведены на Фиг. 9. По сравнению с линиями дикого типа зерно тройных нулевых ssIIa-мутантов имело меньшую массу со значимой разницей (P < 0,05) для каждого варианте генетического окружения, включая Sunco (таблица 7, Фиг. 9). Мутанты в Sunco, EGA Hume и Westonia имели на 25%, 15% и 30% меньшую массу зерна соответственно. Это было не удивительно, учитывая, что SSIIa кодирует крахмальную синтазу, которая участвует в выработке крахмала, и было известно, что мутанты в SSIIa вырабатывают меньше крахмала (Yamamoto et al., 2000; Konik-Rose et al., 2007).
[0396] Между массой зерна мутантов Sunco и Westonia статистически значимой разницы не было. Зерно мутанта EGA Hume было существенно тяжелее по массе, чем у тройных нулевых ssIIa-мутантов в двух других вариантах генетического окружения.
[0397] Содержание липидов. Общее содержание жирных кислот (ОЖК, содержание липидов) определяли так, как описано в примере 1. Данные для отдельных линий приведены в таблице 5 и на Фиг. 8. Было отмечено, что наблюдалось существенное увеличение в содержании ОЖК в тройных нулевых ssIIa-линиях по сравнению с диким типом. В частности, зерно из трех мутантных линий Sunco (JTSBC3F7_190, JTSBC3F7_287 и JTSBC3F7_294) имело существенно повышенное содержание липидов, выраженное в виде процентной доли от массы зерна.
[0398] Если содержание липидов определяли в расчете на зерно, наблюдали, что мутантные линии демонстрировали повышенный уровень липидов, выраженный в мг на зерно (Фиг. 15 и 16).
[0399] Содержание амилозы. Содержание амилозы в виде доли содержания крахмала в тройных нулевых ssIIa-мутантах и зерне дикого типа в трех вариантах генетического окружения определяли в анализе связывания йода, описанном в примере 1. Данные также приведены в таблице 6 и на Фиг. 10, а средние значения приведены в таблице 7 и на Фиг. 11 (Sunco). Содержание амилозы для тройных нулевых мутантов находилось в диапазоне от 36,6% до 64%, а для зерна дикого типа - от 22,6% до 31,0%. По сравнению с зерном дикого типа нулевые ssIIa-мутанты имели большее содержание амилозы, выраженное в виде доли общего содержания крахмала, при этом разница была статистически значимой. Мутантное зерно Sunco, EGA Hume и Westonia имело уровень амилозы, составляющий 187%, 135% и 165% соответственно, по сравнению с соответствующим диким типом. При сравнении зерна тройных нулевых мутантов в трех вариантах генетического окружения, зерно Sunco содержало существенно большую долю амилозы по сравнению с образцами зерна двух других нулевых мутантов. Между мутантами EGA Hume и Westonia статистически значимой разницы не было. Аналогично, не было статистически значимой разницы между тремя образцами зерна дикого типа. Зерно из трех из 6 тройных нулевых мутантных линий Sunco содержало 61,6%, 64% и 55,1% амилозы в виде доли от содержания крахмала в зерне. Эти значения были намного выше, чем наблюдаемые ранее для ssIIa-мутантного зерна в гексаплоидной пшенице (Yamamoto et al., 2000; Konik-Rose et al., 2007) и, следовательно, это было неожиданно и удивительно для авторов изобретения.
[0400] Когда содержание амилозы определяли в расчете на зерно (мг амилозы на зерно), наблюдали, что мутантные линии в целом не демонстрировали повышенный уровень амилозы в мг на зерно (Фиг. 17 и 18), но скорее демонстрировали сниженный уровень амилопектина и, следовательно, сниженное общее содержание крахмала. Авторы изобретения сделали вывод, что это происходило вследствие мутаций в трех генах SSIIa и, следовательно, потери активности фермента SSIIa во время развития эндосперма при росте растений.
[0401] Содержание крахмала. Содержание крахмала в зерне для трех тройных нулевых ssIIa-мутантов и трех линий дикого типа определяли, как описано в примере 1. Данные представлены в таблице 6 и на Фиг. 10, а средние значения приведены в таблице 7 (Sunco) и на Фиг. 11. Содержание крахмала находилось в диапазоне от 30,4% до 70,0% для тройных нулевых ssIIa-мутантов и от 58,1% до 74,3% для зерна дикого типа. По сравнению с содержанием крахмала в линиях дикого типа мутантное зерно EGA Hume, Sunco и Westonia в среднем содержало соответственно на 15%, 28% и 18% меньше крахмала, чем соответствующие линии дикого типа. Эта разница была статистически значимой (p < 0,05). Мутантное зерно Sunco содержало существенно меньше крахмала, чем мутантное зерно ssIIa, в двух других вариантах генетического окружения. Содержание крахмала в мутантном зерне EGA Hume существенно не отличалось от зерна Westonia. Зерно из трех мутантных линий Sunco (JTSBC3F7_190, JTSBC3F7_287 и JTSBC3F7_294) имело низкое содержание крахмала, составляющее 42,5%, 34,8% и 30,4%, соответственно. Те же самые линии также имели наибольшее содержание амилозы, в виде доли от содержания в них крахмала, что указывает на то, что в этих линиях наиболее сильно был снижен синтез амилопектина. При расчете в мг крахмала на зерно было очевидным снижение содержания крахмала в мутантном зерне ssIIa (Фиг. 17 и 18), что снова было вызвано потерей активности SSIIa.
[0402] Содержание β-глюкана. Содержание β-глюкана (БГ) в зерне тройных нулевых ssIIa-мутантов и зерне дикого типа определяли, как описано в примере 1. Данные приведены в таблице 6 и на Фиг. 12 в виде процентного отношения масса/масса цельного зерна, а средние значения приведены в таблице 7 (Sunco) и на Фиг. 13. Содержание БГ находилось в диапазоне от 1,3% до 3,3% для тройных нулевых ssIIa-мутантов и от 0,3% до 0,8% для зерна дикого типа. По сравнению с зерном дикого типа мутанты EGA Hume, Sunco и Westonia имели на 144%, 245% и 177% больше БГ, соответственно. Это повышение, составляющее около 1,5-2,5 раза, было неожиданным для авторов изобретения, так как ранее не сообщалось от таком проявлении в гексаплоидной пшенице. Мутантное зерно Sunco содержало существенно больше БГ, чем мутантное зерно EGA Hume и Westonia (P < 0,05). Зерно трех мутантных линий Sunco (JTSBC3F7_190, JTSBC3F7_287 и JTSBC3F7_294), которое имело наибольшие уровни амилозы, также содержало наибольшее количество БГ, составляющее 2,5%, 3,3% и 3,2%, соответственно. Это демонстрирует корреляцию между повышением содержания амилозы и повышением содержания БГ в ssIIa-мутантах, в каждом случае в массовом отношении.
[0403] При расчете на зерно наблюдали, что мутантное зерно имело существенно повышенные уровни БГ (Фиг. 19 и 20). Авторы изобретения считают, что это связано с разницей в количестве углерода, поступающего в зерно в виде дисахаридов или моносахаридов, из амилопектина в БГ по сравнению с диким типом.
[0404] Содержание фруктана. Содержание фруктана в зерне тройных нулевых ssIIa-мутантов и зерне дикого типа определяли, как описано в примере 1. Данные приведены в таблице 6 и на Фиг. 14 в виде процентного отношения масса/масса цельного зерна, а средние значения приведены в таблице 7 для Sunco. Содержание фруктана находилось в диапазоне от 3,1% до 10,8% для тройных нулевых ssIIa-мутантов и от 0,7% до 1,5% для зерна дикого типа. По сравнению с зерном дикого типа мутантное зерно EGA Hume, Sunco и Westonia содержало соответственно на 242%, 521% и 376% больше фруктанов. Мутантное зерно Sunco содержало существенно больше фруктанов, чем мутантное зерно EGA Hume и Westonia (P < 0,05). Три высокоамилозные мутантные линии Sunco (JTSBC3F7_190, JTSBC3F7_287 и JTSBC3F7_294) также имели наибольшее содержание фруктана, составляющее 7,7%, 10,8% и 10,5%, соответственно. О таких уровнях фруктана в гексаплоидной пшенице в массовом отношении никогда раньше не сообщалось. Это демонстрирует корреляцию не только между повышением содержания амилозы и повышением содержания БГ, но также повышение содержания фруктана в ssIIa-мутантах.
[0405] При расчете на зерно наблюдали, что мутантное зерно имело существенно повышенные уровни фруктана (Фиг. 21 и 22). Авторы изобретения считают, что это связано с разницей в количестве углерода, поступающего в зерно в виде дисахаридов или моносахаридов, из амилопектина во фруктан по сравнению с диким типом во время развития эндосперма.
[0406] Содержание арабиноксилана. Содержание арабиноксилана (АК) в зерне тройных нулевых ssIIa-мутантов и зерне дикого типа определяли, как описано в примере 1. Данные приведены в таблице 6 и на Фиг. 14 в виде процентного отношения масса/масса цельного зерна, а средние значения приведены в таблице 7 для Sunco. Содержание АК находилось в диапазоне от 6,7% до 8,8% для тройных нулевых ssIIa-мутантов и от 4,3% до 5,7% для зерна дикого типа. По сравнению с зерном дикого типа мутантное зерно EGA Hume, Sunco и Westonia содержало соответственно на 35%, 65% и 43% больше АК. Мутантное зерно Sunco содержало существенно больше АК, чем мутантное зерно EGA Hume и Westonia (P < 0,05). Три высокоамилозные мутантные линии Sunco (JTSBC3F7_190, JTSBC3F7_287 и JTSBC3F7_294) также имели наибольшее содержание АК, составляющее 8,7%, 8,5% и 8,4%, соответственно. Это демонстрирует корреляцию между четырьмя параметрами, а именно повышением содержания амилозы, повышением содержания БГ, повышением содержания фруктана и повышением содержания АК в ssIIa-мутантах. Содержание арабиноксилана в расчете на зерно также было существенно повышено (Фиг. 21 и 22).
[0407] Содержание целлюлозы. Содержание целлюлозы в зерне тройных нулевых ssIIa-мутантов и зерне дикого типа определяли, как описано в примере 1. Данные приведены в таблице 6 и на Фиг. 14 в виде процентного отношения масса/масса цельного зерна, а средние значения приведены в таблице 7 для Sunco. Содержание целлюлозы находилось в диапазоне от 2,6% до 4,6% для тройных нулевых ssIIa-мутантов и от 2,0% до 3,4% для зерна дикого типа. По сравнению с линиями дикого типа мутанты EGA Hume, Sunco и Westonia содержали на 19%, 43% и 29% больше целлюлозы, соответственно. Существенной разницы в содержании целлюлозы между тремя нулевыми мутантами не было. Три высокоамилозные мутантные линии Sunco (JTSBC3F7_190, JTSBC3F7_287 и JTSBC3F7_294) также имели наибольшее содержание целлюлозы, составляющее 4,3%, 3,9% и 4,6%, соответственно. Содержание целлюлозы на зерно не было существенно повышено (Фиг. 21 и 22).
[0408] Общее содержание волокон. Общее содержание волокон в зерне тройных нулевых ssIIa-мутантов и зерне дикого типа рассчитывали как сумму содержания β-глюкана (БГ), фруктана, арабиноксилана (АК) и целлюлозы (каждое в виде процентной доли от массы зерна). Данные приведены в таблице 6 и на Фиг. 12 в виде процентного отношения масса/масса цельного зерна, а средние значения приведены в таблице 7 и на Фиг. 13. Общее содержание волокон в зерне находилось в диапазоне от 15,9% до 27,5% для нулевых ssIIa-мутантов и от 8,5% до 10,4% для зерна дикого типа. По сравнению с зерном дикого типа мутанты EGA Hume, Sunco и Westonia имели на 68%, 125% и 88% большее общее содержание волокон, соответственно. Мутантное зерно Sunco имело существенно большее общее содержание волокон, чем мутантное зерно EGA Hume и Westonia (P < 0,05). Между мутантным зерном EGA Hume и Westonia не было существенной разницы в общем содержании волокон. Три высокоамилозные мутантные линии Sunco (JTSBC3F7_190, JTSBC3F7_287 и JTSBC3F7_294) имели наибольшее общее содержание волокон, составляющее 23,2%, 26,5% и 27,5%, соответственно. Общее содержание волокон на зерно также было существенно повышено (Фиг. 19 и 20).
[0409] Содержание резистентного крахмала (РК). Содержание РК в виде процентной доли содержания крахмала в тройных нулевых ssIIa-мутантах и зерне дикого типа в генетическом окружении Sunco определяли, используя коммерческий набор для анализа резистентного крахмала, как описано в примере 1. Данные приведены в таблице 8, а средние значения приведены на Фиг. 23. Содержание РК для тройных нулевых мутантов находилось в диапазоне от 1,0% до 3,8%, а для зерна дикого типа - от 0,4% до 0,8%. По сравнению с зерном дикого типа ssIIa-мутанты имели приблизительно в 5 раз большее содержание РК, и эта разница была статистически значимой. Зерно из трех из 6 тройных нулевых ssIIa-мутантных линий в генетическом окружении Sunco содержало 3,8%, 2,8% и 3,1% РК в виде процентной доли от содержания крахмала в зерне (Фиг. 23, верхняя панель). Уровни РК, рассчитанные как мг на зерно, также были существенно повышены (Фиг. 23, нижняя панель).
[0410] Обсуждение. Ранее сообщалось о модификации некоторого числа свойств крахмала в тройной нулевой ssIIa гексаплоидной пшенице, включая морфологию крахмальных гранул, содержание амилозы, распределение по длинам цепей в амилопектине, кристалличность и температуру желатинизации крахмала, анализ ЭАВ и набухаемость (Yamamori et al. 2000; Yamamori et al. 2006; Konik-Rose et al. 2007). В настоящем изобретении обнаружили, что генетическое окружение нулевых мутаций ssIIa оказывало влияние на параметры состава зерна, включая, к удивлению авторов изобретения, содержание амилозы в крахмале, которое в некоторых линиях было повышено до более 45%. Создавали три подвергнутые обратному скрещиванию популяции в разных вариантах генетического окружения, используя промышленно выращиваемые сорта пшеницы, и генотипировали, используя ДНК-маркеры для тройных нулевых мутаций ssIIa. Было отобрано и проанализировано от четырех до одиннадцати линий тройных нулевых ssIIa-мутантов в каждом варианте генетического окружения и пять линий дикого типа из каждой из трех размножаемых популяций.
[0411] С помощью анализа массы семян и состава зерна в каждом варианте генетического окружения было идентифицировано три линии, характеризующиеся высоким содержанием амилозы, высоким содержанием волокон, высоким содержанием АК и БГ и высоким содержанием фруктана. Эти три линии были получены при скрещивании растений с одинаковым генетическим окружением, а именно Sunco. Были идентифицированы и отобраны линии пшеницы, содержащие около 60% амилозы, более 23% общих волокон и более 7% фруктана. О таких уровнях никогда ранее не сообщалось для гексаплоидной пшеницы, и это было полной неожиданностью для авторов изобретения. Повышение также наблюдали в расчете на зерновку. Эти высокоамилозные нулевые мутанты ssIIa также имели повышенное содержание БГ, АК и целлюлозы, что демонстрирует корреляцию этих параметров. Однако эти три мутантные линии также демонстрировали сниженные содержание крахмала и массу зерновки вследствие существенно сниженного синтеза амилопектина.
Таблица 6. Параметры зерен для тройных мутантов ssIIa (abd) и SSIIa пшеницы дикого типа (ABD) в трех вариантах генетического окружения.
Таблица 7. Средние значения и стандартные отклонения (стд.) для параметров зерна для трех тройных ssIIa-мутантов (abd) по сравнению с пшеницей дикого типа (ABD) в генетическом окружении Sunco
Таблица 8. Содержание резистентного крахмала в крахмале зерна ssIIa-мутантов в окружении Sunco
*За показатель массы семян брали среднюю массу 100 семян
Пример 6. Комбинация мутаций SSIIa и других мутаций в генах, связанных с синтезом крахмала, или ингибиторных конструкций.
[0412] Растения пшеницы, являющиеся тройными нулевыми мутантами в отношении трех генов SSIIa, как описано в примере 1, скрещивали с растениями, содержащими конструкцию шпилечной РНК, обозначаемую hp-SBEIIa, и имеющими сниженную активность крахмал-ветвящего фермента II (SBEII) в эндосперме (Regina et al., 2006). Родительские растения hp-SBEIIa демонстрировали высокоамилозный фенотип в отношении крахмала в зерне (Regina et al., 2006). Получали растения F1 и самоопыляли их для получения зерна от потомства F2. Скрининг 288 зерен F2 проводили с помощью ПЦР, используя три разные пары праймеров, описанные в Konik-Rose et al. (2007), при этом каждая пара праймеров была специфической в отношении мутантного гена ssIIa из конкретного генома. Это позволило идентифицировать одно гомозиготное тройное нулевое ssIIa зерно, обозначаемое YDH7, в котором отсутствовали аллели дикого типа для каждого из трех генов SSIIa. Дополнительное исследование ДНК YDH7 подтвердило наличие генетической конструкции hp-SBEIIa в этом зерне вдобавок к трем мутированным генам ssIIa. Зерно проращивали, чтобы получить дочерние растения и зерно, обозначаемые в данном документе как линия YDH7.
[0413] Аналогичным образом, растения, содержащие тройные нулевые мутации в SSIIa, скрещивали с растениями тройной нулевой sbeI линии пшеницы, описанной в Regina et al., 2004. ДНК, выделенную из семян половины F2, исследовали в отношении нулевых мутаций в каждом из генов SBEI, используя маркер расщепленных продуктов амплификации ПЦР (РПА), сконструированный из области интрона 2 гена SBEI пшеницы. Этот маркер создает 460 п. о. фрагмент ДНК из гена SBEI-D из генома D, 390 п. о. фрагмент ДНК из гена SBEI-B из генома B и 200 п. о. фрагмент ДНК из гена SBEI-A из генома A. Помимо этих геном-специфических фрагментов SBEI этот РПА-маркер также создает 250 п. о. фрагмент ДНК, неспецифический к генам SBEI и применяемый в качестве внутреннего контроля в реакциях ПЦР. Проводят идентификацию зерен, в которых отсутствуют SBEI-специфические фрагменты ДНК, амплифицированные из генов дикого типа, что указывает на то, что они являются тройными нулевыми мутантами в отношении sbeI. Затем эти тройные нулевые зерна исследуют методом ПЦР в отношении наличия нулевых мутаций ssIIa. Эти зерна высевают для получения растений, которые содержат комбинацию мутаций ssIIa и sbeI, гомозиготных в отношении каждого из мутантных аллелей.
Пример 7. Анализ гранул крахмала и свойств крахмала
[0414] Исследовали гранулы крахмала в цельнозерновой муке, полученной из тройного ssIIa-мутантного зерна. Также следующим образом анализировали свойства крахмала, выделенного из цельнозерновой муки. Для этого анализа отбирали пять ssIIa-мутантных линий пшеницы, обозначаемых A24, B22, B29, B63 и E24, из двойной гаплоидной популяции по Konik-Rose et al. (2007) и анализировали в отношении свойств крахмала и гранул. Образцы зерна (20 г) из каждой линии и из соответствующей линии дикого типа размалывали до цельнозерновой муки в мельнице Quadramat Jnr. (Brabender, Cyrulla's Instruments, Sydney, Australia) после кондиционирования зерен до содержания влаги 14%. Крахмал выделяли из образцов цельнозерновой муки методом протеазной экстракции (Morrison et al., 1984) с последующей промывкой водой и удалением остатков.
[0415] Изменение в морфологии и двулучепреломлении крахмальных гранул. Морфологию крахмальных гранул и их двулучепреломление в поляризованном свете исследовали для гранул в образцах цельнозерновой муки. Для выявления макроскопических изменений в размере и структуре крахмальных гранул использовали сканирующую электронную микроскопию. По сравнению с гранулами дикого типа крахмальные гранулы из эндосперма с отсутствием SSIIa демонстрировали существенные морфологические изменения. Они были очень разные по форме и многие из A-гранул (диаметром > 10 мкм) имели серповидную форму. В противоположность этому, как А, так и B (диаметром < 10 мкм) гранулы крахмала в цельнозерновой муке дикого типа имели гладкую поверхность и сферическую или эллипсоидную форму.
[0416] При наблюдении в микроскоп в поляризованном свете гранулы крахмала дикого типа, как правило, демонстрировали сильное двулучепреломление. Однако проявления двулучепреломления были сильно снижены для гранул из тройного нулевого ssIIa зерна. Менее 10% крахмальных гранул из мутантных зерен ssIIa характеризовались двулучепреломлением при визуализации в поляризованном свете. В противоположность этому, около 94% крахмальных гранул дикого типа демонстрировали полное двулучепреломление. Следовательно, снижение двулучепреломления коррелировало с отсутствием SSIIa и повышением содержания амилозы.
[0417] Распределение по длинам цепей в крахмале согласно FACE. Распределение по длинам цепей в деветвленном изоамилазой крахмале определяли методом электрофореза углеводов с использованием флуорофора (FACE), как описано в примере 1. Эта технология обеспечивает анализ высокого разрешения для распределения по длинам цепей в диапазоне от СП 1 до 50 и относительной частоты появления цепей разной длины в модифицированном крахмале по сравнению с диким типом. На графике молярной разницы (Фиг. 24), где нормализованное распределение по длинам цепей для крахмала дикого типа вычтено из нормализованного распределения для крахмала тройных нулевых мутантов ssIIa, видно заметное увеличение доли длин цепей с СП 7-10 и существенное снижение количества длин цепей с СП 11-24 в крахмале из тройного нулевого ssIIa зерна. Также было небольшое увеличение количества длин цепей с СП 26-36.
[0418] Молекулярная масса амилопектина и амилозы. Распределение по молекулярной массе для крахмала из мутантного зерна определяли методом эксклюзионной хроматографии (ЭХ) после деветвления изоамилазой. Обработка в виде деветвления изоамилазой расщепляет каждую из α-1,6-связей в амилопектине с высвобождением отдельных цепей, но оставляет амилозу в целом нетронутой, позволяя, таким образом, проводить отделение амилозы (сначала элюирование) и глюкановых цепей от амилопектина на основании размера. На Фиг. 25 показаны полученные ЭХ-треки для деветвленного крахмала в соответствии со степенью его полимеризации. Относительное содержание амилозы (первый пик) в крахмале зерна тройных нулевых ssIIa-мутантов было существенно повышено относительно крахмала дикого типа, а количество амилопектина (пик III) было сильно снижено по сравнению с диким типом. Средняя молекулярная масса амилозы в крахмале зерна тройных нулевых ssIIa-мутантов была снижена по сравнению с амилозой в крахмале дикого типа, при этом положения пика амилозы приходилось на 274 кДа по сравнению с 330 кДа для дикого типа (Фиг. 25).
[0419] Набухаемость крахмала (НК). Набухаемость крахмала для желатинизированного крахмала определяли, проводя мелкомасштабное исследование по Konik-Rose et al., (2001), в котором измеряется поглощение воды во время желатинизации крахмала. Оцененное значение НК было существенно ниже для крахмала из тройного нулевого ssIIa зерна и составляло 6,85 по сравнению с 11,79 для крахмала дикого типа.
[0420] Клейстеризационне свойства крахмала. Параметры вязкости крахмальной пасты определяли, используя экспресс-анализатор вязкости (ЭАВ), в целом, как описано в Regina et al., (2004). Температурный профиль для ЭАВ включал следующие стадии: выдерживание при 60°C в течение 2 мин, нагревание до 95°C в продолжение 6 мин, выдерживание при 95°C в течение 4 мин, охлаждение до 50°C в продолжение 4 мин и выдерживание при 50°C в течение 4 мин. Результаты показали, что пиковая и конечная вязкость была существенно ниже в крахмале из тройного нулевого ssIIa зерна (105,5 и 208,6 соответственно) по сравнению с крахмалом из пшеницы дикого типа (232,3 и 350,6 соответственно).
[0421] Свойства желатинизации крахмала. Свойства желатинизации крахмала исследовали, используя дифференциальную сканирующую калориметрию (ДСК), как описано в Regina et al., (2004). ДСК проводили на дифференциальном сканирующем калориметре Perkin Elmer Pyris 1. Крахмал и воду предварительно смешивали в соотношении 1:2, и приблизительно 50 г отвешивали в кювету для ДСК, которую запечатывали и оставляли на ночь для достижения равновесия. Для нагревания исследуемых и эталонных образцов от 30 до 130°C использовали нагревание при скорости 10°C в минуту. Данные анализировали, используя программное обеспечение, поставляемое вместе с прибором. Результаты четко показали снижение конечной температуры желатинизации (61,5°C) для крахмала из тройного нулевого ssIIa зерна по сравнению с контролем (67,1°C). Пиковая температура желатинизации также была ниже в тройном нулевом ssIIa крахмале (55,4°C) по сравнению с контрольным крахмалом (61,3°C). Следовательно, крахмал из тройного нулевого ssIIa зерна имел существенно меньшую температуру желатинизации и сниженную энтальпию желатинизации.
[0422] Изменения состава зерна. Приблизительный состав тройного нулевого ssIIa зерна пшеницы анализировали, чтобы определить изменения, индуцированные в компонентах зерна вследствие потери активности SSIIa. Уровень сахарозы в цельнозерновой муке ssIIa был повышен по сравнению с пшеницей дикого типа NB1. Общее содержание сахара также было выше в ssIIa-мутантном крахмале по сравнению с крахмалом дикого типа. Цельнозерновая мука из зерна ssIIa и второго типа зерна, содержащего генетическую конструкцию hp-SBEIIa (Regina et al., 2006), имела повышенный уровень белка > 19% в зерне, тогда как цельнозерновая мука дикого типа имела уровень в пределах диапазона 11-13%. Общее содержание пищевых волокон (ОПВ) было выше в крахмале ssIIa с уровнем 19,2% по сравнению со значением для дикого типа, составляющим 11,0%. Уровень других компонентов зерна, таких как нейтральные некрахмальные полисахариды (ННКП), общее содержание антиоксидантов и общее содержание липидов было сравнительно выше в муке ssIIa по сравнению с мукой из пшеницы дикого типа. В случае ННКП наибольшее значение 13,8% было зарегистрировано для ssIIa-мутанта по сравнению с 8,3% в NB1 дикого типа. Общее содержание крахмала составляло около 53% в зерне ssIIa-мутанта по сравнению с > 60% в NB1 и YDH7.
Пример 8. Приготовление хлеба и других пищевых продуктов
[0423] Пищевые продукты, такие как хлеб и зерновые завтраки представляют эффективные способы внесения модифицированного пшеничного крахмала в рацион. Чтобы показать, что высокоамилозную пшеницу легко можно включать в хлеб и зерновые завтраки, и исследовать факторы, которые позволяют сохранять качество пищевых продуктов, получали образцы муки, анализировали их и использовали в экспериментах с выпеканием или прессованием. Мелкомасштабное выпекание хлеба проводили, используя муку YDH7 с тремя уровнями добавления, 30%, 60% и 100%, в сравнении с выпечкой из муки из зерна, содержащего генетическую конструкцию hp-SBEIIa, и NB1 дикого типа. Повышение уровня YDH7 или hp-SBEIIa в муке приводило к существенному повышению в РК и снижению ГИ.
[0424] Прессованный зерновой завтрак готовили из цельнозерновой муки мутантной ssIIa пшеницы и сравнивали с соответствующим зерновым завтраком из пшеницы дикого типа. Зерновой завтрак содержал повышенный уровень РК (4,3%) при использовании тройной нулевой ssIIa пшеницы по сравнению с пшеницей дикого типа (1,3%). Повышение температуры плавления от 110°C до 140°C в процессе прессования немного снижало содержание РК при использовании тройной нулевой ssIIa пшеницы. Результаты также показывают, что цельнозерновые зерновые завтраки из тройной нулевой ssIIa пшеницы имели более низкий ИГ (индекс гидролиза для оценки значения ГИ), составляющий 72, по сравнению с индексом пшеницы дикого типа 82.
[0425] Следующие способы применяют для изготовления хлеба из ssIIa пшеницы в большем масштабе. Некоторое количество пшеничного зерна кондиционируют до содержания влаги 16,5% в течение ночи перед помолом и просеиванием для получения конечного среднего размера частиц около 150 мкм. Содержание белка и влаги в молотых образцах определяют по инфракрасному отражению (NIR) в соответствии с методом AACC 39-11 (1999) или методом Dumas, используя воздушно-тепловой метод в соответствии с AACC 44-15 A (AACC5 1999).
[0426] Смешивание на микро-Z-образном смесителе. Оптимальные значения поглощения воды пшеничной мукой определяли с помощью Z-образного смесителя, например, используя 4 г исследуемой муки на смесь (Gras et al., (2001); Bekes et al., (2002), с постоянной угловой скоростью и скоростью вращения вала для быстрой или медленной лопастей 96 и 64 об/мин соответственно. Смешивание проводили в течение около 20 минут. Перед добавлением муки в воду автоматически записывался исходный уровень в течение 30 с при смешивании только твердых компонентов. Добавление воды проводили за один этап, используя автоматический водный насос. Следующие параметры определяли в отдельных экспериментах по смешиванию, беря средние значения: ПВ% - поглощение воды определяли при консистенции теста 500 единиц Брабендера (ЕБ); время образования теста (ВОТ): время до пикового сопротивления (с).
[0427] Миксограммы. Чтобы определить оптимальные параметры смешивания теста из модифицированной пшеничной муки, образцы с разным поглощением воды, соответствующим поглощению воды, определенному на Z-образном смесителе, смешивали в миксографе, сохраняя общую массу теста постоянной. Для каждого из образцов муки записывали следующие параметры: ВС - время смешивания (с); ПС - пиковое сопротивление миксографа (условные единицы, У.Е.); ШППС - ширина полосы при пиковом сопротивлении (условные единицы, У.Е.); НС - нарушение сопротивления (%); НШП - ширина полосы нарушения (%); ВМШП - время до достижения максимальной ширины полосы (с); и МШП - максимальная ширина полосы (условные единицы, У.Е.). Параметры растяжимости теста определяли следующим образом: тесто замешивали до пикового образования теста в миксографе. Исследования по удлинению при 1 см/с проводили на анализаторе текстуры TA.XT2i с установкой Kieffer с модифицированной геометрией для определения растяжимости теста и глютена (Mann et al., 2003). Образцы теста для исследования удлинения (~1,0 г/опыт) формовали с помощью формовочной машины Kieffer и оставляли при 30°C и 90% ОВ на 45 мин до исследования удлинения. R_Max и Ext_Rmax определяют по данным с помощью программного обеспечения Exceed Expert (Smewing, руководство по использованию анализатора текстуры TX2, SMS Ltd: Суррей, Великобритания, 1995).
[0428] Иллюстративный рецепт на основе 14 г муки, принимаемых за 100%, следующий: мука 100%, соль 2%, сухие дрожжи 1,5%, растительное масло 2% и улучшитель (аскорбиновая кислота, 100 м. д., грибковая амилоза, 15 м. д., ксиланаза, 40 м. д., соевая мука 0,3%, полученная от Goodman Fielder Pty Ltd, Австралия) 1,5%. Уровень добавления воды основан на значениях поглощения воды, полученных на Z-образном миксере, которые корректировали для полной формулы. Муку (14 г) и другие ингредиенты вмешивают до пикового времени образования теста в миксографе. Формовку и укладку в форму проводят с двумя проверочными этапами при 40С при 85% ОВ. Выпекание проводят в духовке Rotel в течение 15 мин при 190°C. Измерения объема (определяемого методом с использованием вытеснения семян канолы) и массы буханок проводят после охлаждения буханок на полке в течение 2 часов. Суммарную потерю воды определяют, взвешивая буханки в течение времени.
[0429] Муку или цельнозерновую муку можно смешивать с мукой или цельнозерновой мукой из немодифицированной пшеницы или других злаковых, таких как ячмень, чтобы обеспечить необходимые тесто или выпекание хлеба или питательные качества. Например, мука из сортов Chara или Glenlea имеет высокую прочность теста, тогда как мука из сорта Janz имеет среднюю прочность теста. В частности, уровни высоко- и низкомолекулярных субъединиц глютенина в муке положительно коррелируют с прочностью теста, и дополнительно зависят от природы присутствующих аллелей.
[0430] Муку из линии YDH7 использовали при уровнях добавления 100%, 60% и 30% в соответствии с вышеописанными способами для приготовления теста и выпекания хлеба. Это означает, что либо 100% муки, полученной из YDH7, либо контрольной муки, или 60% или 30% по массе муки YDH7 смешивали с мукой контроля выпекания (B. extra). Процентные значения взяты относительно общего содержания муки в составе хлеба. Немодифицированная пшеничная мука принадлежала сорту NB1. Образцы зерна мололи на мельнице Brabender Quadramat Junior. Поглощение воды для всех смесей муки было определено на Z-образном смесителе, а оптимальное время смешивания определено на миксографе, как описано выше. Эти условия использовали для изготовления тестовых выпекаемых буханок.
[0431] Свойства смешивания. За исключением контрольного образца, в котором полностью использовалась мука дикого типа (контроль выпекания, NB1), все другие образцы муки демонстрировали повышенные значения поглощения воды. Повышенные уровни включения муки из линии YDH7 также приводили к снижению оптимального времени смешивания на миксографе. В соответствии с данными по поглощению воды, весь хлеб, содержащий муку из линии YDH7, демонстрировал снижение удельного объема буханки (объем буханки/масса буханки), что коррелировало с повышенными уровнями добавления муки YDH7.
[0432] Эти исследования показали, что хлеб с коммерческим потенциалом, включая приемлемую структуру мякиша, текстуру и внешний вид, можно получать, используя модифицированную ssIIa пшеничную муку, смешанную с образцами контрольной муки. Кроме того, высокоамилозную ssIIa пшеницу можно использовать в комбинации с предпочтительными характеристиками генетического окружения (например, предпочтительно высоко- и низкомолекулярным глютенинами) или модификациями в обработке пищевых продуктов, такими как, например, добавление улучшителей, таких как глютен, аскорбат или эмульсификаторы, или используя разные стили изготовления хлеба (например, изготовление хлеба с опарным приготовлением теста, приготовлением теста на закваске, применением смешанного зерна или цельнозерновой муки) для получения ряда продуктов с конкретной практической ценностью или питательной эффективностью для улучшения здоровья кишечника и метаболизма.
[0433] Другие пищевые продукты. Желтую яичную лапшу (ЖЯЛ) (100% муки, 32% воды, 1% Na2CO3) готовят в смесителе Hobart, используя стандартный способ производства лапши от BRI Research (AFL 029). Лист-заготовку для лапши формируют в вальцах из нержавеющей стали в машине для изготовления лапши Otake. После отлеживания (30 мин) лист-заготовку для лапши уменьшают и нарезают на полосы. Размеры лапши составляют 1,5 × 1,5 мм.
[0434] Лапшу быстрого приготовления (100% муки, 32% воды, 1% NaCl и 0,2% Na2CO3) готовят в смесителе Hobart, используя стандартный способ производства лапши от BRI Research (AFL 028). Лист-заготовку для лапши формируют в вальцах из нержавеющей стали в машине для изготовления лапши Otake. После отлеживания (5 мин) лист-заготовку для лапши уменьшают и нарезают на полосы. Размеры лапши составляют 1,0 × 1,5 × 25 мм. Полосы лапши обрабатывают паром в течение 3,5 мин, а затем жарят в масле при 150°C в течение 45 с.
[0435] Хлеб с опарным приготовлением теста (S&D). Выпекание хлеба с опарным приготовлением теста согласно BRI Research включает двухэтапный процесс. На первом этапе делают опару, смешивая часть муки с водой, дрожжами и питательной средой для дрожжей. Опару оставляют для ферментации на 4 ч. На втором этапе опару смешивают с оставшейся мукой, водой и другими ингредиентами, чтобы сделать тесто. Опарную стадию процесса проводят с 200 г муки и дают 4 часа на ферментацию. Тесто готовят путем смешивания оставшихся 100 г муки и других ингредиентов с ферментированной опарой.
[0436] Паста-спагетти. Способ, используемый для получения пасты, соответствует описанному в Sissons et al., (2007). Муку из ssIIa-модифицированной пшеницы и пшеницы дикого типа смешивают с манной крупой Manildra в различных процентных соотношениях (исследуемый образец: 0, 20, 40, 60, 80, 100%), чтобы получить смеси муки для мелкомасштабного изготовления пасты. Образцы доводят до 30% содержания влаги. В образцы добавляют необходимое количество воды и слегка смешивают перед переносом в чашу фаринографа на 50 г для дополнительного 2-минутного перемешивания. Полученное в результате тесто, которое напоминает комки размера кофейного зерна, переносят в камеру из нержавеющей стали и оставляют под давлением 7000 кПа на 9 мин при 50°C. Затем пасту прессуют при постоянной скорости и нарезают на полоски длиной приблизительно 48 см. Пасту сушат, используя камеру с температурным и влажным режимом. В цикле сушки используется температура удержания 25°C с последующим повышением до 65°C в течение 45 мин, затем период около 13 ч при 50°C с последующим охлаждением. Во время цикла контролируют влажность. Высушенную пасту нарезают на 7 см полосы для следующих испытаний.
Пример 9. In vitro определение гликемического индекса (ГИ) образцов пищи
[0437] Гликемический индекс (ГИ) образцов пищи определяли in vitro следующим образом. In vitro метод моделирует то, что происходит с образцами пищи при употреблении человеком и является прогностическим в отношении in vivo определения ГИ. Образцы пищи гомогенизировали на домашнем кухонном комбайне. Количество образца, представляющее приблизительно 50 мг углеводов, отвешивали в 120 мл пластиковый контейнер для образцов и добавляли 100 мкл карбонатного буфера без α-амилазы. Приблизительно через 15-20 секунд после добавления карбонатного буфера добавляли 5 мл раствора пепсина (65 мг пепсина (Sigma), растворенного в 65 мл HCl 0,02 М, pH 2,0, приготовленного в день использования) и инкубировали смесь при 37°C в течение 30 минут в качающейся водяной бане при 70 об/мин. После инкубации образец нейтрализовали 5 мл NaOH (0,02 М) и добавляли 25 мл ацетатного буфера 0,2 М, pH 6. Затем добавляли 5 мл смеси ферментов, содержащей 2 мг/мл панкреатина (α-амилаза, Sigma) и 28 Ед./мл амилоглюкозидазы из Aspergillus niger (AMG, Sigma), растворенных в Na-ацетатном буфере (натриевом ацетатном буфере, 0,2 М, pH 6,0, содержащем 0,20 М хлорида кальция и 0,49 мМ хлорида магния), и инкубировали смесь в течение 2-5 минут. Переносили 1 мл раствора из каждого флакона в 1,5 мл пробирку и центрифугировали при 3000 об/мин в течение 10 минут. Супернатант переносили в новую пробирку и хранили в морозильной камере. Остаток каждого образца закрывали алюминиевой фольгой и инкубировали контейнеры при 37°C в течение 5 часов на водяной бане. Затем из каждого флакона дополнительно отбирали по 1 мл раствора, центрифугировали и переносили супернатант как и ранее. Супернатанты хранили в морозильной камере до появления возможности считывания поглощения.
[0438] Все супернатанты размораживали и центрифугировали при 3000 об/мин в течение 10 минут. Образцы разводили как это необходимо (обычно достаточно разведения 1 к 10), 10 мкл супернатанта из каждого образца переносили в 96-луночные микротитровальные планшеты в двух или трех повторностях. Стандартную кривую для каждого микротитровального планшета строили, используя глюкозу (0 мг, 0,0625 мг, 0,125 мг, 0,25 мг, 0,5 мг и 1,0 мг). В каждую лунку добавляли по 20 мкл реагента Glucose Trinder (Microgenetics Diagnostics Pty Ltd, Лидкомб, Нов. Юж. Уэльс) и инкубировали планшеты при комнатной температуре приблизительно в течение 20 минут. Поглощение каждого образца измеряли при 505 нм, используя планшет-ридер, а количество глюкозы рассчитывали, используя стандартную кривую.
[0439] Буханки хлеба, выпеченные с использованием муки из линии пшеницы YDH7, исследовали в отношении ГИ, используя вышеописанный способ, наряду с хлебом, изготовленным из нетрансформированной пшеницы дикого типа, а также смесями двух видов муки, применяя уровни включения 60% и 30% муки YDH7 с остатком 40% или 70% муки из зерна дикого типа. Повышенное включение муки YDH7 приводило к существенному снижению ГИ согласно измерениям в in vitro исследовании.
Пример 10. Обработка высокоамилозной пшеницы и результирующие уровни РК
[0440] Проводили небольшое исследования для определения содержания резистентного крахмала (РК) в обработанном зерне из пшеницы YDH7, которое было расплющено или превращено в хлопья. Этот способ включал кондиционирование зерна до уровня влаги 25% в течение одного часа с последующей обработкой зерен паром. После обработки паром зерна превращали в хлопья, используя небольшие мелкомасштабные вальцы. Затем хлопья обжаривали в духовке при 120°C в течение 35 мин. Использовали два варианта ширины вальцов и три значения времени обработки паром для приблизительно 200 г образцов из высокоамилозной пшеницы, имеющей сниженное количество SSIIa, и контрольной пшеницы дикого типа (сорт Hartog). Испытуемые значения ширины вальцов составляла 0,05 мм и 0,15 мм. Время обработки паром составляло 60', 45' и 35'.
[0441] Это исследование показало четкое и существенное повышение количества РК в обработанной высокоамилозной пшенице по сравнению с контролем. Также наблюдалось некоторое влияние условий обработки на уровень РК. Например, в случае высокоамилозного зерна увеличение времени обработки паром приводило к небольшому снижению уровня РК, наиболее вероятно - вследствие повышения желатинизации крахмала во время паровой обработки. Больший зазор между вальцами обуславливал более высокий уровень РК за исключением варианта с наибольшим временем обработки паром. Это может быть связано с повышением сдвигового повреждения крахмальных гранул при прокатке зерен при меньшем зазоре, что немного снижает уровни РК. Меньший зазор между вальцами также приводил к более высоким уровням РК в контроле Hartog, несмотря на намного меньшие общие уровни РК. В отличие от результатов для высокоамилозных образцов, повышение времени обработки паром приводило к более высоким уровням РК, возможно, вследствие повышения желатинизации крахмала при большем времени обработки паром, что влияет на ретроградацию крахмала во время последующей обработки и охлаждения.
Пример 11. Генерация и идентификация дополнительных мутаций ssIIa
[0442] Мутагенез пшеницы с помощью бомбардировки тяжелыми ионами. Мутагенез с помощью облучения, например посредством бомбардировки тяжелыми ионами (БТИ), позволяет легко вносить в геном пшеницы мутации с делециями с практически приемлемой частотой. Подвергаемую мутагенезу популяцию пшеницы создавали в вариетете Chara, широко применяемом промышленном вариетете, путем БТИ семян пшеницы. Использовали два источника тяжелых ионов, а именно углерод и неон, для мутагенеза, который проводили в Центре Riken Nishina Centre, Вако, Сайтама, Япония. Подвергнутые мутагенезу семена высевали в теплице для получения растений M1. Затем их самоопыляли для получения поколения M2. Из каждого из приблизительно 15000 растений M2, каждое от отдельного растения M1, выделяли образцы ДНК.
[0443] Каждую ДНК индивидуально исследовали в отношении мутаций в каждом из генов SSIIa методом ПЦР, используя геном-специфические олигонуклеотидные праймеры, которые позволяли получать амплифицированные фрагменты для каждого из генов SSIIa в геномах A, B и D. Такие диагностические ПЦР-праймеры могут легко быть сконструированы специалистами в данной области техники путем сравнения трех геномных нуклеотидных последовательностей (SEQ ID NO:7, 8 и 9) и выбора олигонуклеотидных последовательностей, которые специфически гибридизируются с одной геномной последовательностью, но не с другими двумя, или когда полученные в результате амплифицированные фрагменты дифференциально расщепляются рестрикционным ферментом с получением фрагментов разного размера для трех геномных генов SSIIa. Таким образом, каждая из ПЦР-реакций на образцах ДНК дикого типа (не подвергнутых мутагенезу) давала 3 разных продукта амплификации, которые соответствовали амплифицированным областям генов SSIIa в геномах A, B и D, при этом отсутствие одного из фрагментов в ПЦР подвергнутых мутагенезу образцов ДНК M2 указывает на отсутствие соответствующей области в одном из геномов, т. е. на наличие мутантного аллеля, в котором была удалена по меньшей мере часть гена. Такие мутантные аллели определенно являются нулевыми аллелями. При таком скрининге с использованием специфических к генам SBEIIa и SBEIIb праймеров для 15000 растений M2 было идентифицировано всего 34 мутанта, которые представляли собой делеционных мутантов в отношении генов SBEIIa и/или SBEIIb (WO2012/058730), что указывает на то, что частота делеционных мутаций в отношении представляющего интерес гена в этих подвергнутых мутагенезу популяциях M2 составляла около 1 на 1000 линий. Следовательно, скрининг линий M2 позволил идентифицировать около 15 мутантов, каждый из которых содержит делеционную мутацию гена SSIIa или в нем. Так как гены SSIIa в геномах A, B и D можно различить с помощью диагностических ПЦР-реакций, мутантные аллели приписывают одному из геномов в соответствии с тем, какой продукт амплификации отсутствует. Таким образом было идентифицировано около 5 мутантов для каждого из генов SSIIa-A, SSIIa-B и SSIIa-D в популяции из 15000 растений M2.
[0444] Степень хромосомной делеции в каждом из мутантов определяют путем картирования микросателлитов. Микросателлитные маркеры ранее картировали на коротком плече хромосом 7A, 7B и 7D, хромосомные локации генов SSIIa исследуют на этих мутантах для определения присутствия или отсутствия каждого маркера в каждом мутанте. Мутантные растения, в которых все или большинство специфических хромосомных микросателлитных маркеров были сохранены согласно выработке соответствующего продукта амплификации в реакциях, считаются относительно небольшими делеционными мутантами. Такие мутанты были предпочтительными, учитывая, что в этом случая существовала меньшая вероятность повреждения мутациями важных генов.
[0445] Скрещивание мутантов. Мутантные растения, которые были гомозиготными в отношении более мелких делеций гена SSIIa или в нем, судя по анализу микросателлитных маркеров, отбирают для скрещивания для создания дочерний растений и зерна, которые имеют мутантные ssIIa аллели в нескольких геномах. Дочерние растения F1, полученные при скрещивании, самоопыляют и получают семена F2, которые анализируют в отношении генотипа SSIIa. Таких мутантов также можно скрещивать с мутантами, содержащими точечные мутации в генах SSIIa, для получения тройных генных мутантов, содержащих комбинации делеций и точечных мутаций ssIIa.
[0446] Точечные мутации. Точечные мутации, включая однонуклеотидный полиморфизм (ОНП), можно идентифицировать в общедоступных библиотеках подвергнутых мутагенезу растений пшеницы. Такие библиотеки включают, например, доступную от John Innes Centre, Великобритания. Нуклеотидную последовательность SSIIa пшеницы (№ доступа в Genbank: AB201445) использовали для запроса по базе данных John Innes Centre по пшенице, используя программное обеспечение BLAST, и идентифицировали линии, содержащие ОНП в каждом из трех генов SSIIa. ОНП относили к трем классам. Первая группа содержала мутантов, которые имели мутированный ген SSIIa, содержащий новый стоп-кодон в кодирующей белок области гена. По прогнозам эти мутации должны приводить к преждевременной терминации трансляции белка SSIIa, кодируемого этим геном. Мутации с преждевременной терминацией, также известные как несмысловые мутации или «мутации, обусловленные внесением стоп-кодона», почти всегда представляют собой нулевые мутации при условии, что мутация не находится близко к 3’ концу кодирующей белок области, хотя даже они могут быть нулевыми мутациями. Вторая группа мутантов содержали линии, которые имели нуклеотидный полиморфизм в сайте сплайсинга гена SSIIa, как в донорном сайте сплайсинга, так и в акцепторном сайте сплайсинга. Ожидалось, что такие мутации будут приводить к неправильному сплайсингу РНК-транскрипта из гена SSIIa и сильно влиять на мРНК; мутации сайта сплайсинга наиболее часто являются нулевыми мутациями. Третья группа состояла из мутантов, которые содержали точечную мутацию в одном из генов SSIIa, которая приводила к аминокислотной замене в кодируемом полипептиде SSIIa; они называются «миссенс-мутациями». Влияние каждой миссенс-мутации на структуру кодируемого белка прогнозируют, используя матрицы Blosum 62 и Pam 250.
[0447] Мутанты гена SSIIa, которые были идентифицированы в первой и второй группах, перечислены в таблице 9. В случае гена SSIIa-A по базе данных было идентифицировано 5 несмысловых мутаций, 2 мутации сайта сплайсинга и 49 миссенс-мутаций. Две из несмысловых мутаций, идентифицированные в разных пулах, были идентичными. В случае гена SSIIa-B было идентифицировано 2 несмысловые мутации, 7 мутаций вариантов сайта сплайсинга и 22 миссенс-мутации. В случае гена SSIIa-D было идентифицировано 2 сплайс-мутации и 49 миссенс-мутаций. Несколько мутантов имели более одного полиморфизма в гене SSIIa, включая некоторые, которые имели полиморфизм в интроне, а также полиморфизм в кодирующей белок области.
[0448] Идентификация мутаций методом TILLING. Выращивали популяция мутированных линий растений после мутагенеза с помощью обработки азидом натрия семян пшеницы сорта Sunstate, используя способ, описанный в WO2014/028980. Пять тысяч растений M1 выращивали до зрелости, позволяя им самоопыляться. Семена M2 собирали отдельно с каждого растения, получая, таким образом, подвергнутую мутагенезу популяцию из 5000 линий. ДНК выделяли из листовой части (~2 см) растений в каждой из линий. ДНК из листьев пшеницы количественно оценивали, используя планшет-ридер (FLUOstar Omega, BMG LABTECH) и нормализовали относительно 10 нг/мкл, используя роботизированную машину (Corbett Life Science). Для TILLING образцы ДНК из наборов по 8 растений объединяли вместе в каждой лунке 96-луночного планшета. Реакции ПЦР проводили для амплификации сегментов генов SSIIa, например с одним циклом при 95°C в течение 5 мин, затем 35 циклами плавления при 94°C в течение 45 с, температурой гибридизации от 60 до 62°C в течение 30 с и удлинением при 72°C в течение 2 мин 30 с, затем 1 циклом при 72°C в течение 10 мин с последующим охлаждением до 25°C. Полученные в результате ПЦР-фрагменты (5 мкл) разделяли в 1% или 2% агарозных гелях и визуализировали (UVitec) после окрашивания этидием для изучения качества ПЦР-амплификации.
[0449] Гетеродуплексирование ПЦР-фрагментов с РНК-транскриптом дикого типа проводят, используя установку для ПЦР с 1 циклом при 99°C в течение 5 мин, 70 циклами гибридизации, начиная с 70°C, и восстановлением при скорости 0,6°C на цикл в течение 20 с, с последующим охлаждением до 25°C. Гетеродуплексы расщепляют ферментом CelI, используя 5 мкл гетеродуплексированного ПЦР-продукта с 5 мкл 2х буферной смеси и 0,5 мкл фермента CelI. Буферная смесь состоит из 20 мМ ГЭПЭС, pH 7,5, 20 мМ MgSO4, 20 мМ KCl, 0,004% Тритон X-100 и 0,4 мкг/мл БСА. Укомплектованные реакции смешивают и инкубируют при 45°C в течение 15-30 мин. Затем расщепленные фрагменты ДНК загружают в анализатор ДНК-фрагментов (Advanced Analytical Technologies) для разделения ДНК-фрагментов в соответствии с набором для обнаружения мутаций (DNF-910-K1000T). В альтернативном варианте наборы из 10 продуктов амплификации объединяют после нормализации ПЦР-продуктов и секвенируют, используя один пул ДНК на проточную кювету. Данные секвенирования анализируют для отбора линий, имеющих полиморфизм гена ssIIa. Анализы ОНП разрабатывают для каждого полиморфизма на основании технологии kaspar и проводят генотипирование линий M1 в каждом пуле, положительном в отношении конкретного полиморфизма. Таким образом, идентифицируют индивидуальную мутантную линию, содержащую каждый мутантный ген, и подтверждают мутантные последовательности SSIIa.
[0450] Растения, содержащие точечную мутацию в одном гене SSIIa, скрещивают с растениями, содержащими мутации в других двух генах SSIIa, чтобы получить тройных нулевых ssIIa-мутантов.
Таблица 9. ssIIa-мутанты, идентифицированные в мутагенизированной библиотеке JIC
Пример 12. Анализ белка в ssIIa-мутантном зерне
[0451] Экспрессия генов биосинтеза крахмала в ssIIa-мутантах. Отбирали пять ssIIa-мутантных линий пшеницы, обозначаемых A24, B22, B29, B63 и E24, из двойной гаплоидной популяции по Konik-Rose et al. (2007), а содержание нескольких мРНК и белков биосинтеза крахмала анализировали следующим образом. Уровень экспрессии мРНК в развивающихся зернах ssIIa-мутантных растений пшеницы через 15 СПЦ сравнивали с диким типом с помощью количественной ПЦР с обратной транскрипцией (кОТ-ПЦР), как описано в примере 1. Количественную оценку РНК в каждом образце проводили по сравнению с конститутивно экспрессируемым геном тубулина. Данные кОТ-ПЦР показали, что уровень мРНК ssIIa в эндосперме гомозиготных тройных мутантов ssIIa был существенно ниже, чем в соответствующем зерне дикого типа (p < 0,01), составляя всего около 8% уровня по сравнению с соответствующим эндоспермом пшеницы дикого типа. В противоположность этому, уровни транскриптов SSI, SBEIIa и SBEIIb в мутантном зерне были приблизительно такими же, что и в соответствующем развивающемся зерне дикого типа. Это указывает на специфический эффект на мРНК ssIIa в мутантном эндосперме.
[0452] Анализ распространенности связанных с гранулами белков в крахмале зрелого зерна. Чтобы сравнить интенсивность полос в белковом геле и количество белка, загружаемого в гель, использовали от одного до четырех мг крахмала в виде крахмальных гранул из зрелого зерна ssIIa-мутантов и SSIIa дикого типа для экстракции связанных с гранулами крахмала белков. Белки разделяли в белковом геле, как описано в примере 1. Четыре белка с молекулярной массой по меньшей мере 60 кДа по наблюдениям были связаны с крахмальными гранулами в зрелом зерне дикого типа. В случае мутантного зерна ssIIa наблюдали один белок при приблизительно 60 кДа, идентифицированный как GBSSI. После количественной оценки белковых полос обнаружили положительную корреляцию между интенсивностью белковых полос и количеством крахмала, используемым для экстракции белка, для каждого из SSIIa, SBEII и SSI из зерна дикого типа и для GBSSI из мутантного зерна. Вследствие низких уровней белков SSIIa, SBEII и SSI внутри крахмальных гранул количество в четыре мг крахмала было выбрано для экстракции связанных с крахмальными гранулами белков для дополнительного анализа, описанного ниже.
[0453] Наблюдали четыре связанных с крахмальными гранулами белка, имеющих молекулярную массу около 60 кДа, когда белковые экстракты зерна пшеницы дикого типа подвергали гель-электрофорезу и окрашивали Sypro. Они были идентифицированы как полипептиды SSIIa (~88 кДа), SBEIIa и SBEIIb (каждый ~83 кДа), SSI (~75 кДа) и GBSSI (~60 кДа) в анализе иммуноблоттинга. SBEIIa и SBEIIb сдвинулись в гелях практически на одинаковую позицию, но распространенность SBEIIb внутри гранул крахмала дикого типа была намного больше, чем SBEIIa, судя по окрашиванию Sypro.
[0454] Когда белки из крахмальных гранул ssIIa-мутантной пшеницы анализировали методом гель-электрофореза, белки SSIIa и SBEIIa не выявлялись. Белки SSI и SBEIIb не выявлялись при окрашивании Sypro, но их можно было зарегистрировать анализами иммуноблоттинга, хотя их распространенность была слишком низкой, чтобы провести точный подсчет (Фиг. 26).
[0455] Анализ распространенности белков ферментов биосинтеза крахмала в растворимой строме и внутри крахмальных гранул развивающегося эндосперма. Чтобы определить, связана ли низкая концентрация SSI, SBEIIa и SBEIIb внутри крахмальных гранул в зрелом мутантном зерне с более низким уровнем синтеза во время развития зерна, в то время, когда белок SSIIa отсутствовал в мутантном зерне, белки SSI, SBEIIa и SBEIIb в растворимой фракции стромы и внутри крахмальных гранул развивающихся эндоспермов количественно оценивали через 15 СПЦ. Количественную оценку проводили методом иммунодетекции. Когда анализировали растворимые белки развивающихся эндоспермов, существенно повышенные количества SBEIIb и SSI присутствовали в ssIIa-мутантном зерне по сравнению с SSIIa развивающегося зерна дикого типа на той же стадии (15 СПЦ). В противоположность этому, уровень SBEIIa был аналогичным в ssIIa-мутантном зерне и зерне SSIIa дикого типа. SBEIIa был более представлен в растворимой фракции амилопластов, чем SBEIIb. Сделали заключение о том, что сниженные уровни белков SSI, SBEIIa и SBEIIb внутри крахмальных гранул не были связаны со сниженными уровнями экспрессии, но вместо этого отображали снижение связывания в гранулах крахмала, что указывает на локализацию в стороне от крахмальных гранул и в растворимой фракции стромы.
[0456] Когда анализировали связанные с крахмальными гранулами белки в развивающемся зерне, не было выявлено белка SSIIa в зерне мутантной пшеницы ssIIa анализом иммуноблоттинга. Уровень SBEIIb был снижен до около 25% по сравнению с диким типом. Уровень SSI внутри крахмальных гранул мутанта ssIIa также составлял приблизительно 25% от уровня дикого типа. Аналогичные профили снижения количества связанных с крахмальными гранулами белков наблюдали в зрелых эндоспермах. Однако в расчете на содержание крахмала концентрация ферментов биосинтеза крахмала в связанных с крахмальными гранулами белках развивающихся эндоспермов была выше, чем в зрелых зернах в результате эффекта разведения более высоких уровней крахмала в эндосперме зрелого зерна.
ЛИТЕРАТУРА
Abel et al., (1996). Plant Journal 10:981-991.
Altschul et al., (1997). Nucl. Acids Res. 25:3389-3402.
Alvarez et al., (2006). Plant Cell 18:1134-1151.
Asai et al., (2014). J. Exper. Biol. 65:5497-5507.
Batey and Curtin, (1996). Starch 48:338-344.
Batey et al., (1997). Cereal Chemistry 74:497-501.
Bechtold et al., (1993). C.R. Acad. Sci. Paris, 316:1194-1199.
Bekes et al., (2002). Crit Care Med. 30:1906-1907.
Birt et al., (2013). Adv. Nutrition 4:587-601.
Boch (2011). Nature Biotechnology, 29:135-136.
Botticella et al., (2011). BMC Plant Biology 11: 156.
Boyer and Preiss, (1978). Carbohydrate Research, 61: 321-334.
Boyer and Preiss, (1981). Plant Phys. 67: 1141-1145.
Bryan et al., (1998). J. Cereal Sci. 28:135-145.
Butardo et al., (2012). J Agr Food Chem 60:11576-11585.Ausubel et al., "Current Protocols in Molecular Biology", John Wiley & Sons Inc, Chapter 15, 1994-1998
Carpita et al., (1993). Plant J. 3:1-30.
Carpita et al., (2011) Plant Physiol. 155:171-184.
Case et al., (1998). Journal of Cereal Science 27: 301-314.
Castro et al., (2005). Biomacromolecules 6: 2260-2270.
Cheng et al., (1997). Plant Physiol 115: 971-980.
Colgrave et al., (2013). Food Res Int 54:1001-1012.
Comai et al., (2004). Plant J. 37: 778-786.
Doudna et al., (2014) Science 346 (6213).
Dupuis et al., (2014). Comprehensive Reviews in Food Science and Food Safety 13:1219-1234.
Durai et al., (2005). Nucleic Acids Research 33: 5978-5990.
Eagles et al., (2001). Aust. J. Agric. Res. 52: 1349-1356.
Ellison et al., (1994) Aust. J. Exp. Agric. 34:869-869.
Fergason, (1994). Speciality Corns eds, CRC Press Inc. pp 55-77.
Fontaine et al., (1993). J Biol Chem 268:16223-16230.
Fujita et al., (2006). Plant Physiol 140:1070-1084.
Fuwa et al., (1999). Starch-Stärke 51: 147-151.
Gao et al., (1997). Plant Physiol 114: 69-78.
Gao and Chibbar (2000). Genome 43:768-775.
Giddings et al., (1980). J Cell Biol. 84:327-339.
Gras et al., (2001). In: Proc. ICC 11th Int. Cereal and Bread Congress. RACI: Melbourne.
Gruppen et al., (1992). J. Cereal Sci. 16:41-51.
Guan and Keeling (1998). Trends Glycosci. Glycotechnol. 10:307-319.
Harn et al., (1998). Plant Mol. Biol. 37:639-649.
Hartmann and Endres, (1999). Manual of Antisense Methodology, Kluwer.
Hayashi et al., (2007). Cyclotrons and Their Applications. Eighteenth International Conference 237-239.
Hedman and Boyer, (1982). Biochemical Genetics 20: 483-492.
Henikoff et al., (2004). Plant Physiol. 135: 630-636.
Henry (1985). J. Sci. Food Agric. 36:1243-1253.
Hinchee et al., (1988). Biotech., 6: 915-922.
Hopkins et al., (2003). Appl. Environ. Microbiol. 69:6354-6360.
Hung et al., (2006). Trends Food Sci. Technol. 17:448-456.
Huynh et al (2008a). J Cereal Sci. 48:369-378.
Huynh et al (2008b). Theor. Appl. Genet. 117:701-709.
Jobling et al.,(1999). Plant Journal 18: 163-171.
Jolly et al. (1996). Proc. Natl. Acad. Sci. U.S.A. 93: 2408-2413.
Juong et al, (2013). Nat Rev Mol Cell Biol 14:49-55.
Kanna and Daggard, (2003). Plant Cell Rep 21: 429-436.
Karppinen et al., (2003). Cereal Chem. 80:168-171.
Kaur and Gupta (2002) J. Biosci. 27:703-714.
Kawaura et al., (2009). BMC Genomics 10:271.
Kazama et al., (2008). Plant Biotechnology 25: 113-117.
Klein et al., (1987). Nature 327: 70-73.
Konik-Rose et al., (2001). Starch-Stärke, 53: 14-20.
Konik-Rose et al., (2007). Theor Appl Genet 115:1053-1065.
Kosar-Hashemi et al., (2007). Funct Plant Biol. 34:431-438.
Krueger et al., (1987). Cereal Chemistry 64: 187-190.
Langridge et al., (2001). Aust. J. Agric. Res. 52: 1043-1077.
Lazaridou et al., (2007). In: Biliaderis and Izydorczyk (Eds.) Functional food carbohydrates (pp 1-72). CRC Press, Boca Raton FL.
Lazo et al., (1991). Biotechnology (N Y). 9(10): 963-967.
Le Provost et al., (2009). Trends in Biotechnology 28(3): 134-141.
Leterrier et al., (2008) BMC Plant Biol. 8:98.
Li et al., (1999a). Plant Physiol 120:1147-1155.
Li et al., (1999b). Theor. Appl. Genet. 98: 1208-1216.
Li et al., (2000). Plant Physiol 123: 613-624.
Li et al., (2003). Funct. Integr. Genomics 3:76-85.
Liu et al., (2010). Biotechnology and Bioengineering, 106: 97-105.
Luo et al., (2015). Theor. Appl. Genet. 128: 1407-1419.
Mann et al., (2003). In 'Workshop on gluten proteins' Eds. Lafiandra et al., The Royal Society of Chemistry: Cambridge, UK, pp. 215-218.
Matsumoto et al., (2011). Plant Physiol. 156:20-28.
McCleary et al., (2000). J AOAC Int. 83:997-1005.
McCleary et al., (2013). Cereal Chem. 90:396-414.
Mizuno et al., (1992). J. Biochem 112:643-651.
Mizuno et al., (1993). J. Biol. Chem. 268: 19084-19091.
Morell et al., (1998). Electrophoresis 19: 2603-2611.
Morell et al., (1997). Plant Physiol 113: 201-208.
Morell et al., (2003). Plant J 34:172-184.
Morrison and Laignelet, (1983). J Cereal Sci, 1: 9-20.
Morrison et al., (1984). J Cereal Sci. 2:257-271.
Nakamura et al., (1996). Planta 199:209-218.
Nakamura and Yamanouchi, (1992). Plant Physiol. 99:1265-1266.
Needleman and Wunsch, (1970). J. Mol. Biol. 48:443-453.
Niedz et al., (1995). Plant Cell Reports, 14:403-406.
Nishi et al., (2001). Plant Physiol 127:459-472.
Ohdan et al., (2005). J Exp Bot 56:3229-3244.
O’Shea and Morell (1996). Electrophoresis 17:681-686.
Ow et al., (1986). Science, 234:856-859.
Palatnik et al., (2003). Nature 425:257-263.
Parizotto et al., (2004). Genes Dev 18:2237-2242.
Potrykus et al., (1985). Mol. Gen. Genet., 199:183-188.
Prasher et al., (1985). Biochem. Biophys. Res. Comm. 126:1259-1268.
Prosky et al., (1985). J Assoc. Off. Anal. Chem. Int. 68:677-679.
Quraishi et al., (2011). Funct Integr Genomics 11:71-83.
Rahman et al., (1999). Theor. Appl. Genet. 98:156-163.
Rahman et al., (1995). Aust. J. Plant Physiol. 22:793-803.
Rahman et al., (2001). Plant Physiol 125:1314-1324.
Regina et al., (2006). Proc. Natl. Acad. Sci. U.S.A. 103:3546-3551.
Regina et al., (2005). Planta 222:899-909.
Regina et al., (2010). J Exp Bot. 61(5): 1469-1482.
Regina et al., (2004). Funct Plant Biol, 31: 591-601.
Ritsema and Smeekens (2003) Curr. Opin. Plant Biol. 6:223-230.
Salanoubat et al., (2000). Nature 408:820-822.
Schnable et al., (2009). Science 326:1112-1115.
Schondelmaier et al., (1992) Plant Breeding 109:274-280.
Schulman and Kammiovirta, (1991). Starch 43: 387-389.
Schwab et al., (2006). Plant Cell 18: 1121-1133.
Schwall et al., (2000). Nature Biotechnology 18: 551-554.
Sestili et al., (2010). Mol Breeding 25:145-154.
Sharp et al., (2001). Aust J Agric Res 52: 1357-1366.
Shimbata et al., (2005). Theor. Appl. Genet. 111:1072-1079.
Sidebottom et al., (1998). J. Cereal Sci 27: 279-287.
Sissons et al., (2007). J. Sci. Food and Agric. 87: 1874-1885.
Slade and Knauf, (2005). Transgenic Res. 14: 109-115.
Smewing, (1995). TX2 texture analyzer handbook, SMS Ltd: Surrey, UK.
Smith et al., (2000). Nature, 407: 319-320.
Smith and Hartley (1983). Carbohydrate Research 118: 65-80.
Sparks and Jones (2004). In Transgenic Crops of the World- Essential protocols, Ed. IP Curtis, Kluwer Academic Publishers, Dordrecht, Netherlands, pp 19-34.
Stalker et al., (1988). Science, 242: 419-423.
Steegmans et al (2004). J. AOAC Int. 87, 1200e1207.
Stone and Morell (2009). In: Khan and Shewry (Eds.) Wheat: Chemistry and Technology. American Association of Cereal Chemists, St Paul, MN, pp 299-362.
Sun et al., (1997). New Phytol. 137:215-222.
Sun et al., (1998). Plant Physiol 118: 37-49.
Sune et al., (2013). Biotechnology and Bioengineering 110:1811-1821.
Takeda et al., (1993). Carbohydrate Research 246: 273-281.
Tanaka et al., (1990). Nucl. Acids Res. 18: 6767-6770.
Tilley (2004). Cereal Chem 81:44-47.
Toyota et al., (2006). Planta 223:248-257.
Tungland and Meyer (2002) Comprehensive Reviews in Food Science and Food Safety 2:73-77.
Waterhouse et al., (1998). Proc. Natl. Acad. Sci. U.S.A.95: 13959-13964.
Weir et al., (2001). Aust J Plant Physiol 28: 807-818.
Whelan et al (2011). Int J. Food Sci. Nutr. 62:498-503.
Wu et al., (2003). Plant Cell Rep 21: 659-668.
Yamamori et al., (2000). Theor Appl Genet 101:21-29.
Yamamori et al., (2006). Aust. J. Agric. Res. 57:531-535.
Yan et al., (2008). Plant Sci. 176:51-57.
Zwar and Chandler, (1995). Planta 197: 39-48.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Государственное объединение научных и
прикладных исследований
<120> ВЫСОКОАМИЛОЗНАЯ ПШЕНИЦА – III
<130> 35269906/WJP
<160> 51
<170> PatentIn версия 3.5
<210> 1
<211> 799
<212> Белок
<213> Triticum aestivum
<400> 1
Met Ser Ser Ala Val Ala Ser Ala Ala Ser Phe Leu Ala Leu Ala Ser
1 5 10 15
Ala Ser Pro Gly Arg Ser Arg Arg Arg Ala Arg Val Ser Ala Pro Pro
20 25 30
Pro His Ala Gly Ala Gly Arg Leu His Trp Pro Pro Trp Pro Pro Gln
35 40 45
Arg Thr Ala Arg Asp Gly Gly Val Ala Ala Arg Ala Ala Gly Lys Lys
50 55 60
Asp Ala Arg Val Asp Asp Asp Ala Ala Ser Ala Arg Gln Pro Arg Ala
65 70 75 80
Arg Arg Gly Gly Ala Ala Thr Lys Val Ala Glu Arg Arg Asp Pro Val
85 90 95
Lys Thr Leu Asp Arg Asp Ala Ala Glu Gly Gly Ala Pro Ala Pro Pro
100 105 110
Ala Pro Arg Gln Asp Ala Ala Arg Pro Pro Ser Met Asn Gly Thr Pro
115 120 125
Val Asn Gly Glu Asn Lys Ser Thr Gly Gly Gly Gly Ala Thr Lys Asp
130 135 140
Ser Gly Leu Pro Ala Pro Ala Arg Ala Pro His Pro Ser Thr Gln Asn
145 150 155 160
Arg Val Pro Val Asn Gly Glu Asn Lys Ala Asn Val Ala Ser Pro Pro
165 170 175
Thr Ser Ile Ala Glu Val Val Ala Pro Asp Ser Ala Ala Thr Ile Ser
180 185 190
Ile Ser Asp Lys Ala Pro Glu Ser Val Val Pro Ala Glu Lys Pro Pro
195 200 205
Pro Ser Ser Gly Ser Asn Phe Val Val Ser Ala Ser Ala Pro Arg Leu
210 215 220
Asp Ile Asp Ser Asp Val Glu Pro Glu Leu Lys Lys Gly Ala Val Ile
225 230 235 240
Val Glu Glu Ala Pro Asn Pro Lys Ala Leu Ser Pro Pro Ala Ala Pro
245 250 255
Ala Val Gln Glu Asp Leu Trp Asp Phe Lys Lys Tyr Ile Gly Phe Glu
260 265 270
Glu Pro Val Glu Ala Lys Asp Asp Gly Trp Ala Val Ala Asp Asp Ala
275 280 285
Gly Ser Phe Glu His His Gln Asn His Asp Ser Gly Pro Leu Ala Gly
290 295 300
Glu Asn Val Met Asn Val Val Val Val Ala Ala Glu Cys Ser Pro Trp
305 310 315 320
Cys Lys Thr Gly Gly Leu Gly Asp Val Ala Gly Ala Leu Pro Lys Ala
325 330 335
Leu Ala Lys Arg Gly His Arg Val Met Val Val Val Pro Arg Tyr Gly
340 345 350
Asp Tyr Glu Glu Ala Tyr Asp Val Gly Val Arg Lys Tyr Tyr Lys Ala
355 360 365
Ala Gly Gln Asp Met Glu Val Asn Tyr Phe His Ala Tyr Ile Asp Gly
370 375 380
Val Asp Phe Val Phe Ile Asp Ala Pro Leu Phe Arg His Arg Gln Glu
385 390 395 400
Asp Ile Tyr Gly Gly Ser Arg Gln Glu Ile Met Lys Arg Met Ile Leu
405 410 415
Phe Cys Lys Ala Ala Val Glu Val Pro Trp His Val Pro Cys Gly Gly
420 425 430
Val Pro Tyr Gly Asp Gly Asn Leu Val Phe Ile Ala Asn Asp Trp His
435 440 445
Thr Ala Leu Leu Pro Val Tyr Leu Lys Ala Tyr Tyr Arg Asp His Gly
450 455 460
Leu Met Gln Tyr Thr Arg Ser Ile Met Val Ile His Asn Ile Ala His
465 470 475 480
Gln Gly Arg Gly Pro Val Asp Glu Phe Pro Phe Thr Glu Leu Pro Glu
485 490 495
His Tyr Leu Glu His Phe Arg Leu Tyr Asp Pro Val Gly Gly Glu His
500 505 510
Ala Asn Tyr Phe Ala Ala Gly Leu Lys Met Ala Asp Gln Val Val Val
515 520 525
Val Ser Pro Gly Tyr Leu Trp Glu Leu Lys Thr Val Glu Gly Gly Trp
530 535 540
Gly Leu His Asp Ile Ile Arg Gln Asn Asp Trp Lys Thr Arg Gly Ile
545 550 555 560
Val Asn Gly Ile Asp Asn Met Glu Trp Asn Pro Glu Val Asp Val His
565 570 575
Leu Lys Ser Asp Gly Tyr Thr Asn Phe Ser Leu Gly Thr Leu Asp Ser
580 585 590
Gly Lys Arg Gln Cys Lys Glu Ala Leu Gln Arg Glu Leu Gly Leu Gln
595 600 605
Val Arg Ala Asp Val Pro Leu Leu Gly Phe Ile Gly Arg Leu Asp Gly
610 615 620
Gln Lys Gly Val Glu Ile Ile Ala Asp Ala Met Pro Trp Ile Val Ser
625 630 635 640
Gln Asp Val Gln Leu Val Met Leu Gly Thr Gly Arg His Asp Leu Glu
645 650 655
Ser Met Leu Arg His Phe Glu Arg Glu His His Asp Lys Val Arg Gly
660 665 670
Trp Val Gly Phe Ser Val Arg Leu Ala His Arg Ile Thr Ala Gly Ala
675 680 685
Asp Ala Leu Leu Met Pro Ser Arg Phe Glu Pro Cys Gly Leu Asn Gln
690 695 700
Leu Tyr Ala Met Ala Tyr Gly Thr Val Pro Val Val His Ala Val Gly
705 710 715 720
Gly Val Arg Asp Thr Val Pro Pro Phe Asp Pro Phe Asn His Ser Gly
725 730 735
Leu Gly Trp Thr Phe Asp Arg Ala Glu Ala His Lys Leu Ile Glu Ala
740 745 750
Leu Gly His Cys Leu Arg Thr Tyr Arg Asp Tyr Lys Glu Ser Trp Arg
755 760 765
Gly Leu Gln Glu Arg Gly Met Ser Gln Asp Phe Ser Trp Glu His Ala
770 775 780
Ala Lys Leu Tyr Glu Asp Val Leu Leu Lys Ala Lys Tyr Gln Trp
785 790 795
<210> 2
<211> 798
<212> Белок
<213> Triticum aestivum
<400> 2
Met Ser Ser Ala Val Ala Ser Ala Ala Ser Phe Leu Ala Leu Ala Ser
1 5 10 15
Ala Ser Pro Gly Arg Ser Arg Arg Arg Thr Arg Val Ser Ala Ser Pro
20 25 30
Pro His Thr Gly Ala Gly Arg Leu His Trp Pro Pro Ser Pro Pro Gln
35 40 45
Arg Thr Ala Arg Asp Gly Ala Val Ala Ala Arg Ala Ala Gly Lys Lys
50 55 60
Asp Ala Gly Ile Asp Asp Ala Ala Pro Ala Arg Gln Pro Arg Ala Leu
65 70 75 80
Arg Gly Gly Ala Ala Thr Lys Val Ala Glu Arg Arg Asp Pro Val Lys
85 90 95
Thr Leu Asp Arg Asp Ala Ala Glu Gly Gly Ala Pro Ser Pro Pro Ala
100 105 110
Pro Arg Gln Glu Asp Ala Arg Leu Pro Ser Met Asn Gly Met Pro Val
115 120 125
Asn Gly Glu Asn Lys Ser Thr Gly Gly Gly Gly Ala Thr Lys Asp Ser
130 135 140
Gly Leu Pro Ala Pro Ala Arg Ala Pro Gln Pro Ser Ser Gln Asn Arg
145 150 155 160
Val Pro Val Asn Gly Glu Asn Lys Ala Asn Val Ala Ser Pro Pro Thr
165 170 175
Ser Ile Ala Glu Val Ala Ala Pro Asp Pro Ala Ala Thr Ile Ser Ile
180 185 190
Ser Asp Lys Ala Pro Glu Ser Val Val Pro Ala Glu Lys Ala Pro Pro
195 200 205
Ser Ser Gly Ser Asn Phe Val Pro Ser Ala Ser Ala Pro Gly Ser Asp
210 215 220
Thr Val Ser Asp Val Glu Leu Glu Leu Lys Lys Gly Ala Val Ile Val
225 230 235 240
Lys Glu Ala Pro Asn Pro Lys Ala Leu Ser Pro Pro Ala Ala Pro Ala
245 250 255
Val Gln Gln Asp Leu Trp Asp Phe Lys Lys Tyr Ile Gly Phe Glu Glu
260 265 270
Pro Val Glu Ala Lys Asp Asp Gly Arg Ala Val Ala Asp Asp Ala Gly
275 280 285
Ser Phe Glu His His Gln Asn His Asp Ser Gly Pro Leu Ala Gly Glu
290 295 300
Asn Val Met Asn Val Val Val Val Ala Ala Glu Cys Ser Pro Trp Cys
305 310 315 320
Lys Thr Gly Gly Leu Gly Asp Val Ala Gly Ala Leu Pro Lys Ala Leu
325 330 335
Ala Lys Arg Gly His Arg Val Met Val Val Val Pro Arg Tyr Gly Asp
340 345 350
Tyr Glu Glu Ala Tyr Asp Val Gly Val Arg Lys Tyr Tyr Lys Ala Ala
355 360 365
Gly Gln Asp Met Glu Val Asn Tyr Phe His Ala Tyr Ile Asp Gly Val
370 375 380
Asp Phe Val Phe Ile Asp Ala Pro Leu Phe Arg His Arg Gln Glu Asp
385 390 395 400
Ile Tyr Gly Gly Ser Arg Gln Glu Ile Met Lys Arg Met Ile Leu Phe
405 410 415
Cys Lys Ala Ala Val Glu Val Pro Trp His Val Pro Cys Gly Gly Val
420 425 430
Pro Tyr Gly Asp Gly Asn Leu Val Phe Ile Ala Asn Asp Trp His Thr
435 440 445
Ala Leu Leu Pro Val Tyr Leu Lys Ala Tyr Tyr Arg Asp His Gly Leu
450 455 460
Met Gln Tyr Thr Arg Ser Ile Met Val Ile His Asn Ile Ala His Gln
465 470 475 480
Gly Arg Gly Pro Val Asp Glu Phe Pro Phe Thr Glu Leu Pro Glu His
485 490 495
Tyr Leu Glu His Phe Arg Leu Tyr Asp Pro Val Gly Gly Glu His Ala
500 505 510
Asn Tyr Phe Ala Ala Gly Leu Lys Met Ala Asp Gln Val Val Val Val
515 520 525
Ser Pro Gly Tyr Leu Trp Glu Leu Lys Thr Val Glu Gly Gly Trp Gly
530 535 540
Leu His Asp Ile Ile Arg Gln Asn Asp Trp Lys Thr Arg Gly Ile Val
545 550 555 560
Asn Gly Ile Asp Asn Met Glu Trp Asn Pro Glu Val Asp Val His Leu
565 570 575
Lys Ser Asp Gly Tyr Thr Asn Phe Ser Leu Gly Thr Leu Asp Ser Gly
580 585 590
Lys Arg Gln Cys Lys Glu Ala Leu Gln Arg Glu Leu Gly Leu Gln Val
595 600 605
Arg Gly Asp Val Pro Leu Leu Gly Phe Ile Gly Arg Leu Asp Gly Gln
610 615 620
Lys Gly Val Glu Ile Ile Ala Asp Ala Met Pro Trp Ile Val Ser Gln
625 630 635 640
Asp Val Gln Leu Val Met Leu Gly Thr Gly Arg His Asp Leu Glu Gly
645 650 655
Met Leu Arg His Phe Glu Arg Glu His His Asp Lys Val Arg Gly Trp
660 665 670
Val Gly Phe Ser Val Arg Leu Ala His Arg Ile Thr Ala Gly Ala Asp
675 680 685
Ala Leu Leu Met Pro Ser Arg Phe Glu Pro Cys Gly Leu Asn Gln Leu
690 695 700
Tyr Ala Met Ala Tyr Gly Thr Val Pro Val Val His Ala Val Gly Gly
705 710 715 720
Leu Arg Asp Thr Val Pro Pro Phe Asp Pro Phe Asn His Ser Gly Leu
725 730 735
Gly Trp Thr Phe Asp Arg Ala Glu Ala Gln Lys Leu Ile Glu Ala Leu
740 745 750
Gly His Cys Leu Arg Thr Tyr Arg Asp Tyr Lys Glu Ser Trp Arg Gly
755 760 765
Leu Gln Glu Arg Gly Met Ser Gln Asp Phe Ser Trp Glu His Ala Ala
770 775 780
Lys Leu Tyr Glu Asp Val Leu Val Lys Ala Lys Tyr Gln Trp
785 790 795
<210> 3
<211> 799
<212> Белок
<213> Triticum aestivum
<400> 3
Met Ser Ser Ala Val Ala Ser Ala Ala Ser Phe Leu Ala Leu Ala Ser
1 5 10 15
Ala Ser Pro Gly Arg Ser Arg Arg Arg Ala Arg Val Ser Ala Gln Pro
20 25 30
Pro His Ala Gly Ala Gly Arg Leu His Trp Pro Pro Trp Pro Pro Gln
35 40 45
Arg Thr Ala Arg Asp Gly Ala Val Ala Ala Leu Ala Ala Gly Lys Lys
50 55 60
Asp Ala Gly Ile Asp Asp Ala Ala Ala Ser Val Arg Gln Pro Arg Ala
65 70 75 80
Leu Arg Gly Gly Ala Ala Thr Lys Val Ala Glu Arg Arg Asp Pro Val
85 90 95
Lys Thr Leu Asp Arg Asp Ala Ala Glu Gly Gly Gly Pro Ser Pro Pro
100 105 110
Ala Ala Arg Gln Asp Ala Ala Arg Pro Pro Ser Met Asn Gly Met Pro
115 120 125
Val Asn Gly Glu Asn Lys Ser Thr Gly Gly Gly Gly Ala Thr Lys Asp
130 135 140
Ser Gly Leu Pro Thr Pro Ala Arg Ala Pro His Pro Ser Thr Gln Asn
145 150 155 160
Arg Ala Pro Val Asn Gly Glu Asn Lys Ala Asn Val Ala Ser Pro Pro
165 170 175
Thr Ser Ile Ala Glu Ala Ala Ala Ser Asp Ser Ala Ala Thr Ile Ser
180 185 190
Ile Ser Asp Lys Ala Pro Glu Ser Val Val Pro Ala Glu Lys Thr Pro
195 200 205
Pro Ser Ser Gly Ser Asn Phe Glu Ser Ser Ala Ser Ala Pro Gly Ser
210 215 220
Asp Thr Val Ser Asp Val Glu Gln Glu Leu Lys Lys Gly Ala Val Val
225 230 235 240
Val Glu Glu Ala Pro Lys Pro Lys Ala Leu Ser Pro Pro Ala Ala Pro
245 250 255
Ala Val Gln Glu Asp Leu Trp Asp Phe Lys Lys Tyr Ile Gly Phe Glu
260 265 270
Glu Pro Val Glu Ala Lys Asp Asp Gly Arg Ala Val Ala Asp Asp Ala
275 280 285
Gly Ser Phe Glu His His Gln Asn His Asp Ser Gly Pro Leu Ala Gly
290 295 300
Glu Asn Val Met Asn Val Val Val Val Ala Ala Glu Cys Ser Pro Trp
305 310 315 320
Cys Lys Thr Gly Gly Leu Gly Asp Val Ala Gly Ala Leu Pro Lys Ala
325 330 335
Leu Ala Lys Arg Gly His Arg Val Met Val Val Val Pro Arg Tyr Gly
340 345 350
Asp Tyr Glu Glu Ala Tyr Asp Val Gly Val Arg Lys Tyr Tyr Lys Ala
355 360 365
Ala Gly Gln Asp Met Glu Val Asn Tyr Phe His Ala Tyr Ile Asp Gly
370 375 380
Val Asp Phe Val Phe Ile Asp Ala Pro Leu Phe Arg His Arg Gln Glu
385 390 395 400
Asp Ile Tyr Gly Gly Ser Arg Gln Glu Ile Met Lys Arg Met Ile Leu
405 410 415
Phe Cys Lys Ala Ala Val Glu Val Pro Trp His Val Pro Cys Gly Gly
420 425 430
Val Pro Tyr Gly Asp Gly Asn Leu Val Phe Ile Ala Asn Asp Trp His
435 440 445
Thr Ala Leu Leu Pro Val Tyr Leu Lys Ala Tyr Tyr Arg Asp His Gly
450 455 460
Leu Met Gln Tyr Thr Arg Ser Ile Met Val Ile His Asn Ile Ala His
465 470 475 480
Gln Gly Arg Gly Pro Val Asp Glu Phe Pro Phe Thr Glu Leu Pro Glu
485 490 495
His Tyr Leu Glu His Phe Arg Leu Tyr Asp Pro Val Gly Gly Glu His
500 505 510
Ala Asn Tyr Phe Ala Ala Gly Leu Lys Met Ala Asp Gln Val Val Val
515 520 525
Val Ser Pro Gly Tyr Leu Trp Glu Leu Lys Thr Val Glu Gly Gly Trp
530 535 540
Gly Leu His Asp Ile Ile Arg Gln Asn Asp Trp Lys Thr Arg Gly Ile
545 550 555 560
Val Asn Gly Ile Asp Asn Met Glu Trp Asn Pro Glu Val Asp Ala His
565 570 575
Leu Lys Ser Asp Gly Tyr Thr Asn Phe Ser Leu Arg Thr Leu Asp Ser
580 585 590
Gly Lys Arg Gln Cys Lys Glu Ala Leu Gln Arg Glu Leu Gly Leu Gln
595 600 605
Val Arg Ala Asp Val Pro Leu Leu Gly Phe Ile Gly Arg Leu Asp Gly
610 615 620
Gln Lys Gly Val Glu Ile Ile Ala Asp Ala Met Pro Trp Ile Val Ser
625 630 635 640
Gln Asp Val Gln Leu Val Met Leu Gly Thr Gly Arg His Asp Leu Glu
645 650 655
Ser Met Leu Gln His Phe Glu Arg Glu His His Asp Lys Val Arg Gly
660 665 670
Trp Val Gly Phe Ser Val Arg Leu Ala His Arg Ile Thr Ala Gly Ala
675 680 685
Asp Ala Leu Leu Met Pro Ser Arg Phe Glu Pro Cys Gly Leu Asn Gln
690 695 700
Leu Tyr Ala Met Ala Tyr Gly Thr Val Pro Val Val His Ala Val Gly
705 710 715 720
Gly Leu Arg Asp Thr Val Pro Pro Phe Asp Pro Phe Asn His Ser Gly
725 730 735
Leu Gly Trp Thr Phe Asp Arg Ala Glu Ala His Lys Leu Ile Glu Ala
740 745 750
Leu Gly His Cys Leu Arg Thr Tyr Arg Asp Phe Lys Glu Ser Trp Arg
755 760 765
Ala Leu Gln Glu Arg Gly Met Ser Gln Asp Phe Ser Trp Glu His Ala
770 775 780
Ala Lys Leu Tyr Glu Asp Val Leu Val Lys Ala Lys Tyr Gln Trp
785 790 795
<210> 4
<211> 2821
<212> ДНК
<213> Triticum aestivum
<400> 4
gctgccacca cctccgcctg cgccgcgctc tgggcggagg accaacccgc gcatcgtacc
60
atcgcccgcc ccgatcccgg ccgccgccat gtcgtcggcg gtcgcgtccg ccgcgtcctt
120
cctcgcgctc gcctccgcct cccccgggag atcacgcagg cgggcgaggg tgagcgcgcc
180
gccaccccac gccggggccg gcaggctgca ctggccgccg tggccgccgc agcgcacggc
240
tcgcgacgga ggtgtggccg cgcgcgccgc cgggaagaag gacgcgaggg tcgacgacga
300
cgccgcgtcc gcgaggcagc cccgcgcacg ccgcggtggc gccgccacca aggtcgcgga
360
gcggagggat cccgtcaaga cgctcgatcg cgacgccgcg gaaggtggcg cgccggcacc
420
gccggcaccg aggcaggacg ccgcccgtcc accgagtatg aacggcacgc cggtgaacgg
480
tgagaacaaa tctaccggcg gcggcggcgc gaccaaagac agcgggctgc ccgcacccgc
540
acgcgcgccc catccgtcga cccagaacag agtaccagtg aacggtgaaa acaaagctaa
600
cgtcgcctcg ccgccgacga gcatagccga ggtcgtggct ccggattccg cagctaccat
660
ttccatcagt gacaaggcgc cggagtccgt tgtcccagcc gagaagccgc cgccgtcgtc
720
cggctcaaat ttcgtggtct cggcttctgc tcccaggctg gacattgaca gcgatgttga
780
acctgaactg aagaagggtg cggtcatcgt cgaagaagct ccaaacccaa aggctctttc
840
gccgcctgca gcccccgctg tacaagaaga cctttgggac ttcaagaaat acattggctt
900
cgaggagccc gtggaggcca aggatgatgg ctgggctgtt gcagatgatg cgggctcctt
960
tgaacatcac cagaaccatg attccggacc tttggcaggg gagaacgtca tgaacgtggt
1020
cgtcgtggct gctgaatgtt ctccctggtg caaaacaggt ggtcttggag atgttgccgg
1080
tgctttgccc aaggctttgg cgaagagagg acatcgtgtt atggttgtgg taccaaggta
1140
tggggactat gaggaagcct acgatgtcgg agtccgaaaa tactacaagg ctgctggaca
1200
ggatatggaa gtgaattatt tccatgctta tatcgatgga gttgattttg tgttcattga
1260
cgctcctctc ttccgacacc gccaggaaga catttatggg ggcagcagac aggaaattat
1320
gaagcgcatg attttgttct gcaaggccgc tgtcgaggtt ccttggcacg ttccatgcgg
1380
cggtgtccct tatggggatg gaaatctggt gtttattgca aatgattggc acacggcact
1440
cctgcctgtc tatctgaaag catattacag ggaccatggt ttgatgcagt acactcggtc
1500
cattatggtg atacataaca tcgcgcacca gggccgtggc ccagtagatg aattcccgtt
1560
caccgagttg cctgagcact acctggaaca cttcagactg tacgaccccg tgggtggtga
1620
gcacgccaac tacttcgccg ccggcctgaa gatggcggac caggttgtcg tggtgagccc
1680
cgggtacctg tgggagctca agacggtgga gggcggctgg gggcttcacg acatcatacg
1740
gcagaacgac tggaagaccc gcggcatcgt caacggcatc gacaacatgg agtggaaccc
1800
cgaggtggac gtccacctca agtcggacgg ctacaccaac ttctccctgg ggacgctgga
1860
ctccggcaag cggcagtgca aggaggccct gcagcgcgag ctgggcctgc aggtccgcgc
1920
cgacgtgccg ctgctcggct tcatcggccg cctggacggg cagaagggcg tggagatcat
1980
cgcggacgcc atgccctgga tcgtgagcca ggacgtgcag ctggtcatgc tgggcaccgg
2040
ccgccacgac ctggagagca tgctgcggca cttcgagcgg gagcaccacg acaaggtgcg
2100
cgggtgggtg gggttctccg tgcgcctggc gcaccggatc acggcgggcg ccgacgcgct
2160
cctcatgccc tcccggttcg agccgtgcgg gttgaaccag ctttacgcca tggcctacgg
2220
caccgtcccc gtcgtgcacg ccgtcggcgg ggtgagggac accgtgccgc cgttcgaccc
2280
cttcaaccac tccggcctcg ggtggacgtt cgaccgcgcc gaggcgcaca agctgatcga
2340
ggcgctcggg cactgcctcc gcacctaccg ggactacaag gagagctgga ggggcctcca
2400
ggagcgcggc atgtcgcagg acttcagctg ggagcatgcc gccaagctct acgaggacgt
2460
cctcctcaag gccaagtacc agtggtgaac gctagctgct agccgctcca gccccgcatg
2520
cgtgcatgca tgagagggtg gaactgcgca ttgcgcccgc aggaacgtgc catccttctc
2580
gatgggagcg ccggcatccg cgaggtgcag tgacatgaga ggtgtgtgtg gttgagacgc
2640
tgattccgat ctcgatctgg tccgtagcag agtagagcgg acgtagggaa gcgctccttg
2700
ttgcaggtat atgggaatgt tgtcaacttg gtattgtagt ttgctatgtt gtatgcgtta
2760
ttacaatgtt gttacttatt cttgttaagt cggaggcaaa gggcgaaagc tagctcacat
2820
g
2821
<210> 5
<211> 2793
<212> ДНК
<213> Triticum aestivum
<400> 5
gcactccagt ccagtccagc ccactgccgc gctactcccc actcccactg ccaccacctc
60
cgcctgcgcc gcgctctggg cggaccaacc cgcgcatcgt atcacgatca cccaccccga
120
tcccggccgc cgccatgtcg tcggcggtcg cgtccgccgc gtccttcctc gcgctcgcgt
180
ccgcctcccc cgggagatca cggaggagga cgagggtgag cgcgtcgcca ccccacaccg
240
gggctggcag gttgcactgg ccgccgtcgc cgccgcagcg cacggctcgc gacggagcag
300
tggccgcgcg cgccgccggg aagaaggacg cggggatcga cgacgccgcg cccgcgaggc
360
agccccgcgc actccgcggt ggcgccgcca ccaaggttgc ggagcggagg gatcccgtca
420
agacgctcga tcgcgacgcc gcggaaggtg gcgcgccgtc cccgccggca ccgaggcagg
480
aggacgcccg tctgccgagc atgaacggca tgccggtgaa cggtgaaaac aaatctaccg
540
gcggcggcgg cgcgactaaa gacagcgggc tgcccgcacc cgcacgcgcg ccccagccgt
600
cgagccagaa cagagtaccg gtgaatggtg aaaacaaagc taacgtcgcc tcgccgccga
660
cgagcatagc cgaggtcgcg gctccggatc ccgcagctac catttccatc agtgacaagg
720
cgccagagtc cgttgtccca gccgagaagg cgccgccgtc gtccggctca aatttcgtgc
780
cctcggcttc tgctcccggg tctgacactg tcagcgacgt ggaacttgaa ctgaagaagg
840
gtgcggtcat tgtcaaagaa gctccaaacc caaaggctct ttcgccgcct gcagcacccg
900
ctgtacaaca agacctttgg gacttcaaga aatacattgg tttcgaggag cccgtggagg
960
ccaaggatga tggccgggct gttgcagatg atgcgggctc cttcgaacac caccagaatc
1020
acgattccgg gcctttggca ggggagaacg tcatgaacgt ggtcgtcgtg gctgctgaat
1080
gttctccctg gtgcaaaaca ggtggtcttg gagatgttgc cggtgctttg cccaaggctt
1140
tggcgaagag aggacatcgt gttatggttg tggtaccaag gtatggggac tatgaggaag
1200
cctacgatgt cggagtccga aaatactaca aggctgctgg acaggatatg gaagtgaatt
1260
atttccatgc ttatatcgat ggagttgatt ttgtgttcat tgacgctcct ctcttccgac
1320
accgccagga agacatttat gggggcagca gacaggaaat tatgaagcgc atgattttgt
1380
tctgcaaggc cgctgtcgag gttccatggc acgttccatg cggcggtgtc ccttatgggg
1440
atggaaatct ggtgtttatt gcaaatgatt ggcacacggc actcctgcct gtctatctga
1500
aagcatatta cagggaccat ggtttgatgc agtacactcg gtccattatg gtgatacata
1560
acatcgctca ccagggccgt ggcccagtag atgagttccc gttcaccgag ttgcctgagc
1620
actacctgga acacttcaga ctgtacgacc ccgtgggtgg tgaacacgcc aactacttcg
1680
ccgccggcct gaagatggcg gaccaggttg tcgtcgtgag cccggggtac ctgtgggagc
1740
tgaagacggt ggagggcggc tgggggcttc acgacatcat acggcagaac gactggaaga
1800
cccgcggcat cgtgaacggc atcgacaaca tggagtggaa ccccgaggtg gacgtccacc
1860
tcaagtcgga cggctacacc aacttctccc tggggacgct ggactccggc aagcggcagt
1920
gcaaggaggc cctgcagcgg gagctgggcc tgcaggtccg cggcgacgtg ccgctgctcg
1980
gcttcatcgg gcgcctggac gggcagaagg gcgtggagat catcgcggac gcgatgccct
2040
ggatcgtgag ccaggacgtg cagctggtca tgctgggcac cgggcgccac gacctggagg
2100
gcatgctgcg gcacttcgag cgggagcacc acgacaaggt gcgcgggtgg gtggggttct
2160
ccgtgcggct ggcgcaccgg atcacggccg gcgccgacgc gctcctcatg ccctcccggt
2220
tcgagccgtg cggactgaac cagctctacg ccatggccta cggcaccgtc cccgtcgtgc
2280
atgccgtcgg cggcctgagg gacaccgtgc cgccgttcga ccccttcaac cactccgggc
2340
tcgggtggac gttcgaccgc gcagaggcgc agaagctgat cgaggcgctc gggcactgcc
2400
tccgcaccta ccgggactac aaggagagct ggagggggct ccaggagcgc ggcatgtcgc
2460
aggacttcag ctgggagcat gccgccaagc tctacgagga cgtcctcgtc aaggccaagt
2520
accagtggtg aacgctagct gctagccggt ccagccccgc atgcgtgcat gacaggatgg
2580
aattgcgcat tgcgcacgca ggaatgtgcc atggagcgcc ggcatccgcg aagtacagtg
2640
acatgaggtg tgtgtggttg agacgctgat tccgatctgg tccgtagcag agtagagcgg
2700
aggtagggaa gcgctccttg ttacaggtat atgggaatgt tgttaacttg gtattgtaat
2760
ttgttatgtt gtgtgcatta ttacaaaggg caa
2793
<210> 6
<211> 2846
<212> ДНК
<213> Triticum aestivum
<400> 6
ggagaatagc cacatccctg gtttggagag accatcgcag caacaaccat taccaccaca
60
acaaacatta tcgcaccaac aaccacaaca acccatccag tccagcccac tgccaccgcg
120
ctactctcca ctcccactgc caccacctcc gcctgcgccg cgctctgggc ggaccaaccc
180
gcgaaccgta ccatctcccg ccccgatcca tgtcgtcggc ggtcgcgtcc gccgcatcct
240
tcctcgcgct cgcgtcagcc tcccccggga gatcacgcag gcgggcgagg gtgagcgcgc
300
agccacccca cgccggggcc ggcaggttgc actggccgcc gtggccgccg cagcgcacgg
360
ctcgcgacgg agctgtggcg gcgctcgccg ccgggaagaa ggacgcgggg atcgacgacg
420
ccgccgcgtc cgtgaggcag ccccgcgcac tccgcggtgg cgccgccacc aaggtcgcgg
480
agcgaaggga tcccgtcaag acgctcgacc gcgacgccgc ggaaggcggc gggccgtccc
540
cgccggcagc gaggcaggac gccgcccgtc cgccgagtat gaacggcatg ccggtgaacg
600
gcgagaacaa atctaccggc ggcggcggcg cgactaaaga cagcgggctg cccacgcccg
660
cacgcgcgcc ccatccgtcg acccagaaca gagcaccggt gaacggtgaa aacaaagcta
720
acgtcgcctc gccgccgacg agcatagccg aggccgcggc ttcggattcc gcagctacca
780
tttccatcag cgacaaggcg ccggagtccg ttgtcccagc tgaggagacg ccgccgtcgt
840
ccggctcaaa tttcgagtcc tcggcctctg ctcccgggtc tgacactgtc agcgacgtgg
900
aacaagaact gaagaagggt gcggtcgttg tcgaagaagc tccaaagcca aaggctcttt
960
cgccgcctgc agcccccgct gtacaagaag acctttggga tttcaagaaa tacattggtt
1020
tcgaggagcc cgtggaggcc aaggatgatg gccgggctgt cgcagatgat gcgggctcct
1080
ttgaacacca ccagaatcac gactccggac ctttggcagg ggagaatgtc atgaacgtgg
1140
tcgtcgtggc tgctgagtgt tctccctggt gcaaaacagg tggtctggga gatgttgcgg
1200
gtgctctgcc caaggctttg gcaaagagag gacatcgtgt tatggttgtg gtaccaaggt
1260
atggggacta tgaagaagcc tacgatgtcg gagtccgaaa atactacaag gctgctggac
1320
aggatatgga agtgaattat ttccatgctt atatcgatgg agttgatttt gtgttcattg
1380
acgctcctct cttccgacac cgtcaggaag acatttatgg gggcagcaga caggaaatta
1440
tgaagcgcat gattttgttc tgcaaggccg ctgttgaggt tccatggcac gttccatgcg
1500
gcggtgtccc ttatggggat ggaaatctgg tgtttattgc aaatgattgg cacacggcac
1560
tcctgcctgt ctatctgaaa gcatattaca gggaccatgg tttgatgcag tacactcggt
1620
ccattatggt gatacataac atcgctcacc agggccgtgg ccctgtagat gaattcccgt
1680
tcaccgagtt gcctgagcac tacctggaac acttcagact gtacgacccc gtgggtggtg
1740
aacacgccaa ctacttcgcc gccggcctga agatggcgga ccaggttgtc gtggtgagcc
1800
ccgggtacct gtgggagctg aagacggtgg agggcggctg ggggcttcac gacatcatac
1860
ggcagaacga ctggaagacc cgcggcatcg tcaacggcat cgacaacatg gagtggaacc
1920
ccgaggtgga cgcccacctc aagtcggacg gctacaccaa cttctccctg aggacgctgg
1980
actccggcaa gcggcagtgc aaggaggccc tgcagcgcga gctgggcctg caggtccgcg
2040
ccgacgtgcc gctgctcggc ttcatcggcc gcctggacgg gcagaagggc gtggagatca
2100
tcgcggacgc catgccctgg atcgtgagcc aggacgtgca gctggtgatg ctgggcaccg
2160
ggcgccacga cctggagagc atgctgcagc acttcgagcg ggagcaccac gacaaggtgc
2220
gcgggtgggt ggggttctcc gtgcgcctgg cgcaccggat cacggcgggg gcggacgcgc
2280
tcctcatgcc ctcccggttc gagccgtgcg ggctgaacca gctctacgcc atggcctacg
2340
gcaccgtccc cgtcgtgcac gccgtcggcg gcctcaggga caccgtgccg ccgttcgacc
2400
ccttcaacca ctccgggctc gggtggacgt tcgaccgcgc cgaggcgcac aagctgatcg
2460
aggcgctcgg gcactgcctc cgcacctacc gagacttcaa ggagagctgg agggccctcc
2520
aggagcgcgg catgtcgcag gacttcagct gggagcacgc cgccaagctc tacgaggacg
2580
tcctcgtcaa ggccaagtac cagtggtgaa cgctagctgc tagccgctcc agccccgcat
2640
gcgtgcatga caggatggaa ctgcattgcg cacgcaggaa agtgccatgg agcgccggca
2700
tccgcgaagt acagtgacat gaggtgtgtg tggttgagac gctgattcca atccggcccg
2760
tagcagagta gagcggaggt atatgggaat cttaacttgg tattgtaatt tgttatgttg
2820
tgtgcattat tacaatgttg ttactt
2846
<210> 7
<211> 6898
<212> ДНК
<213> Triticum aestivum
<400> 7
gggggccgtt cgtacgtacc cgcccctcgt gtaaagccgc cgccgtcgtc gccgtccccc
60
gctcgcggcc atttccccgg cctgaccccg tgcgtttacc ccacagagca cactccagtc
120
cagtccagcc cactgccgcc gcgctactcc ccactcccgc tgccaccacc tccgcctgcg
180
ccgcgctctg ggcggaggac caacccgcgc atcgtaccat cgcccgcccc gatcccggcc
240
gccgccatgt cgtcggcggt cgcgtccgcc gcgtccttcc tcgcgctcgc ctccgcctcc
300
cccgggagat cacgcaggcg ggcgagggtg agcgcgccgc caccccacgc cggggccggc
360
aggctgcact ggccgccgtg gccgccgcag cgcacggctc gcgacggagg tgtggccgcg
420
cgcgccgccg ggaagaagga cgcgagggtc gacgacgacg ccgcgtccgc gaggcagccc
480
cgcgcacgcc gcggtggcgc cgccaccaag gtagttggtt cgttatgact tgctgtatgg
540
cgcgtgcgcc tcgagatcag ctcacgaatt gtttctacaa aacgcacgcg ctcgtgtgca
600
ggtcgcggag cggagggatc ccgtcaagac gctcgatcgc gacgccgcgg aaggtggcgc
660
gccggcaccg ccggcaccga ggcaggacgc cgcccgtcca ccgagtatga acggcacgcc
720
ggtgaacggt gagaacaaat ctaccggcgg cggcggcgcg accaaagaca gcgggctgcc
780
cgcacccgca cgcgcgcccc atccgtcgac ccagaacaga gtaccagtga acggtgaaaa
840
caaagctaac gtcgcctcgc cgccgacgag catagccgag gtcgtggctc cggattccgc
900
agctaccatt tccatcagtg acaaggcgcc ggagtccgtt gtcccagccg agaagccgcc
960
gccgtcgtcc ggctcaaatt tcgtggtctc ggcttctgct cccaggctgg acattgacag
1020
cgatgttgaa cctgaactga agaagggtgc ggtcatcgtc gaagaagctc caaacccaaa
1080
ggctctttcg ccgcctgcag cccccgctgt acaagaagac ctttgggact tcaagaaata
1140
cattggcttc gaggagcccg tggaggccaa ggatgatggc tgggctgttg cagatgatgc
1200
gggctccttt gaacatcacc agaaccatga ttccggacct ttggcagggg agaacgtcat
1260
gaacgtggtc gtcgtggctg ctgaatgttc tccctggtgc aaaacaggca tggacattac
1320
ctcttcagtc tctcttcccg ttgttcataa aactttgctc gaatcactca taagaacaaa
1380
cattgtgttg cataggtggt cttggagatg ttgcgggtgc tctgcccaag gctttggcaa
1440
agagaggaca tcgtgttatg gtactgcagg ctttcactta actctgttga gtccatatgt
1500
tcgaataata tcagtgattg gcataatgtt attaagtgca agacatgaaa gtgttcttct
1560
gttagagtat ttcatagcca accctggagg ttaggttgtt ggggcctact gggtgcggga
1620
gggggtttgc aaaaagtggt ggttagcagt cggatttcac aaataaggag gctgataacc
1680
acgccatcag tgaagggaat gagtgtcggg tacccgatcg accgttttgc ccgacgtcag
1740
gtttacctgc cctgtagatc cgaataagta gttcctatcc tcagttaagt accaaatatc
1800
gccagcaccc gtgtgtgtat ttatagtact ggatgatcaa tttatcaaca tttccggtta
1860
atggttgcta tcatattcac tgtaattgtt agtaaacagt ggatgtttgt aatgtagatg
1920
atggctaaat gtatgttgtc aagctttcat tttaaagaaa attttattgg gagctagttt
1980
tcgggtttgg ttagagccac caaaacccca gaatttttgg gagttggctt gtgacagagg
2040
gttttgggga gttaactttc gggattcagt tagagacgct cttactagtt ccagtaaaga
2100
gtaaactatt ttctgcagtc atcccaattg ttctgtagaa attaaaagta gaaaatagtt
2160
gtggtatcat ataaaccata tattattcaa aatctagaat catggacttg gctagacttt
2220
gatgatctga aattttaaat ttgatgataa ttgagaaatg atcctttcta tcttaggttg
2280
tggtaccaag gtatggggac tatgaggaag cctacgatgt cggagtccga aaatactaca
2340
aggctgctgg acaggtaagc gaaaatgcaa tcaaagggga gctgaaattt caatgcttac
2400
tatcataata aatcaatttt aagtaaaaaa atttgtcctg caggatatgg aagtgaatta
2460
tttccatgct tatatcgatg gagttgattt tgtgttcatt gacgctccta tcttccgaca
2520
ccgtcaggaa gacatttatg ggggcagcag acaggttaat tttctatatg ttggtgtttg
2580
attgcactga taaactgaga ataagccaag gcctactgac tggcatatga ttacacattt
2640
tattttttca ggaaattatg aagcgcatga ttttgttctg caaggccgct gtcgaggtat
2700
cctctccaac tcaattgaca acctattacc actatacaat tatgtgtatg catgtatttc
2760
aacagatacg taatctccct tgtgaagtgt atatatacta ataacatttc aatacctcac
2820
atgcacattt ggtcaagcgt tatgatttaa cttctgataa tctattgcac tgatgaacaa
2880
taatattgat gatccttgtt acttcatcgt tatgtttatg ttctcttcac cggcgcattg
2940
attttggaaa tagcatttcc acctgccaca aacaataata tatactccta ctttcatcca
3000
atgtagatat tttcgcactt ggcatatcat cccattaaat attattggtc catcattttt
3060
attcctctat aatttgcagg ttccttggca cgttccatgc ggcggtgtcc cttatgggga
3120
tggaaatctg gtgtttattg caaatgattg gcacacggca ctcctgcctg tctatctgaa
3180
agcatattac agggaccatg gtttgatgca gtacactcgg tccattatgg tgatacataa
3240
catcgcgcac caggttcctt ttctcctaat cttgtttttt ctctagtctc tactattcac
3300
tccacattgt ttgaggaaac taaaggggtt gcaaaattat gatggcttat gaaagttatg
3360
gaggtaaatg catcagtggt gcttgaactt gtcacgcatg ttcactttgg tgcttacagt
3420
tgtagactac ggaaaactgg tgcaaaaact tggctattgt gtgcaatacg gtgtattttc
3480
cgtatgtagg gtcaaatgtt gcctatgtgg cattgtattc ccgtctatag atgttagacc
3540
gtgcctacat cgccattggg cccacacact ccctattaca tgtgggaccc acttgtcagc
3600
ctatgacata aataaaatgg aaatttataa taaaaatgat ggcctggggt cttgaaaatg
3660
ggacctcgca ggtatgccgc tagccagcac gccctaatca ttaatcccct atgcacttca
3720
gtatgtgtgt gtctgtgtgt ggagtcgggg gggggggggg tatgtattct tatatccttt
3780
gctctaaggc tatcattggc gtgctagcac cgccgggtct ccatcaacac cgacatcatc
3840
cacgacccca tccagctctt cctcaacaag cccacctcca gcctcaactc gggcagcacc
3900
ttcatggtgg cctaggtgct ctgcaccatc gctcgaagtg gcaacgtcgt tgtcatgacc
3960
atccaccaac ccaacacgca aaatcctcaa catcatttga cagtgagcat gcccctcttg
4020
tcatttcccc ctcataccca aacctgtctc gataaccctt ggagctgcac aagttgtgac
4080
catcgcctgc gtcgctgcac aacgcctgac ctagccggac cattatagaa gcctgccttg
4140
ggagcccata cctccctgca catcctcctc tttccccata gaccgtgccg ccatcgcaaa
4200
tcgacttctc ctctcctcct tctcctgctc tggccgtttt ccccgccgcg aagctgcaat
4260
ccatggcgag ttggccatgg ccctattccc caattgctcg cactaggagg tcctccttga
4320
agcctagcac ctttccccct cactaattgc aagttgggga gcccctcacg agctccctac
4380
attggccgta gtcgcctgcc gcctcaactc tggtccagac ctcgttcccg tggcctcgac
4440
gacatctcct cgacctccca ttccacacgc ggcctggaga ggatcaccgc atgttcatcc
4500
atccgacccg aatcatcata gaaccaacgc cagagaggtc atcccgacga cgtcgcactg
4560
ttcctctatt tcccccaagc tgtgtcgcgt cataatataa gacgggcttg tttgtatctc
4620
taggggtcat cgggttcaat ggctagctca tgcatggacc tgactttagg tcccaggttc
4680
gaacccccgc gtgcacataa tttatttgct atttatttct cctatctact aataagtggg
4740
acccacacat catactaagc cctttttgtc tcttgcctgc tgataagtgg gacccacacg
4800
caatacttag ccagagagag aacatgagct tgttggtgcc gcgttggcaa gccacgccag
4860
cagtcttaac ggctacaaac agaggatatg gtgtcacatc aacgtgcaga gcgtttacga
4920
atggaaagtg tactatatgc acacaagagc cagagccagg tttttgcacc agttttttgt
4980
attctacaac tgcgagcacc aaagtgtaca tgccgaacca aagtgaacac ggcgagtcca
5040
ttcttttctg gtacgatggg tggctcaaag acaccccaat agaagctatc acctcggaca
5100
ttgccaattg ggtgccgaac tacattaaag tggcaaggtc agttgattgc gctatgtgtt
5160
ggatcaggga cataaacgat tccataaata ttgcaatgtt cattcaaatt cttaacattt
5220
gcgaggcgct tcatgatttc catctccctc atatcagaga catttggtcg tgtacactaa
5280
atttctcagg tcacttctcg tctaaatccg catatgtagc tcacttcaat gacttgactt
5340
tggtccagct aacgccattt ggcgctcttg ggcccctttg cgtagcaatt ttttcatatg
5400
gctcgctccg cgcaatagga tttggatcac gggcagacgc gctagatgag gtcttccaca
5460
caatgaacat tgcgttcttt gctctgctct tccagaagac acttgtgatt ttattacgag
5520
ttgtgccata gatgccggtg ggtttcagct aggaacaggg tgtcaccttc ggacaagaag
5580
aagttgcata gtttggtcgt cttaactgct tggtcgattt ggaaggagca caacaacagt
5640
ctttgaaggc aaagctaatt ccctcgatca agttattaga cggatcaaat gtggtacagt
5700
gccatggcta gttgcttgga gtcactttta agctaggtcg cttgccatca cgctttgtgt
5760
taagcgcttg gggtcgcttt tgctcaattt gtattttgtt gttatgtgtt tttagttatg
5820
tagcctgaac tttctggact tagttttttc ctctataatg atcacatgct ttggtcagtt
5880
attcctttct tgggtactcc gttgggctaa ttctttctct tgattgatgt tgtatatgca
5940
gggccgtggc ccagtagatg aattcccgtt caccgagttg cctgagcact acctggaaca
6000
cttcagactg tacgaccccg tgggtggtga gcacgccaac tacttcgccg ccggcctgaa
6060
gatggcggac caggttgtcg tggtgagccc cgggtacctg tgggagctca agacggtgga
6120
gggcggctgg gggcttcacg acatcatacg gcagaacgac tggaagaccc gcggcatcgt
6180
caacggcatc gacaacatgg agtggaaccc cgaggtggac gtccacctcc agtcggacgg
6240
ctacaccaac ttctccctga gcacgctgga ctccggcaag cggcagtgca aggaggccct
6300
gcagcgcgag ctgggcctgc aggtccgcgc cgacgtgccg ctgctcggct tcatcggccg
6360
cctggacggg cagaagggcg tggagatcat cgcggacgcc atgccctgga tcgtgagcca
6420
ggacgtgcag ctggtcatgc tgggcaccgg ccgccacgac ctggagagca tgctgcggca
6480
cttcgagcgg gagcaccacg acaaggtgcg cgggtgggtg gggttctccg tgcgcctggc
6540
gcaccggatc acggcgggcg ccgacgcgct cctcatgccc tcccggttcg agccgtgcgg
6600
gctgaaccag ctctacgcca tggcctacgg caccgtcccc gtcgtgcacg ccgtcggcgg
6660
gctgagggac accgtgccgc cgttcgaccc cttcaaccac tccggcctcg ggtggacgtt
6720
cgaccgcgcc gaggcgcaca agctgatcga ggcgctcggg cactgcctcc gcacctaccg
6780
ggactacaag gagagctgga ggggcctcca ggagcgcggc atgtcgcagg acttcagctg
6840
ggagcatgcc gccaagctct acgaggacgt cctcctcaag gccaagtacc agtggtga
6898
<210> 8
<211> 6811
<212> ДНК
<213> Triticum aestivum
<400> 8
gggggccgtt cgtacgtacc cacccctcgt gtaaagccgc cgccgtcgtc gccgtccccc
60
gctcgcggcc atttcctcgg cctgaccccg tgcgtttacc ccacacagag cacactccag
120
tccagtccag cccactgccg cgctactccc cactcccact gccaccacct ccgcctgcgc
180
cgcgctctgg gcggaccaac ccgcgcatcg tatcacgatc acccaccccg atcccggccg
240
ccgccatgtc gtcggcggtc gcgtccgccg cgtccttcct cgcgctcgcg tccgcctccc
300
ccgggagatc acggaggagg acgagggtga gcgcgtcgcc accccacacc ggggctggca
360
ggttgcactg gccgccgtcg ccgccgcagc gcacggctcg cgacggagca gtggccgcgc
420
gcgccgccgg gaagaaggac gcggggatcg acgacgccgc gcccgcgagg cagccccgcg
480
cactccgcgg tggcgccgcc accaaggtag ttagttatga ccaagttatg acgcgtgcgc
540
gcgccttgag atcatcgtcg tctcgctgac aaattgttta tacaaaacgc acgcgcgcgc
600
gtgtgtgcag gttgcggagc ggagggatcc cgtcaagacg ctcgatcgcg acgccgcgga
660
aggtggcgcg ccgtccccgc cggcaccgag gcaggaggac gcccgtctgc cgagcatgaa
720
cggcatgccg gtgaacggtg aaaacaaatc taccggcggc ggcggcgcga ctaaagacag
780
cgggctgccc gcacccgcac gcgcgcccca gccgtcgagc cagaacagag taccggtgaa
840
tggtgaaaac aaagctaacg tcgcctcgcc gccgacgagc atagccgagg tcgcggctcc
900
ggatcccgca gctaccattt ccatcagtga caaggcgcca gagtccgttg tcccagccga
960
gaaggcgccg ccgtcgtccg gctcaaattt cgtgccctcg gcttctgctc ccgggtctga
1020
cactgtcagc gacgtggaac ttgaactgaa gaagggtgcg gtcattgtca aagaagctcc
1080
aaacccaaag gctctttcgc cgcctgcagc acccgctgta caacaagacc tttgggactt
1140
caagaaatac attggtttcg aggagcccgt ggaggccaag gatgatggcc gggctgttgc
1200
agatgatgcg ggctccttcg aacaccacca gaatcacgat tccgggcctt tggcagggga
1260
gaacgtcatg aacgtggtcg tcgtggctgc tgaatgttct ccctggtgca aaacaggcat
1320
ggacattacc tcttcagtgt cttttttctc tctgttcata aaacctggct tgaattactc
1380
ataagaacaa acgttgtgtt gcataggtgg tcttggagat gttgccggtg ctttgcccaa
1440
ggctttggcg aagagaggac atcgtgttat ggtaccacat gctttcattt aactctgttg
1500
aatccatatg ttcgaataat atcagtgagc agtataatgt tattaagtgc aagacatgaa
1560
agtgttcttc tgttatagag tatttcatag ccaaccctgg aggttaggtt gttggggcct
1620
actgggtgtg ggagggggtt tgaaaaaagt gttggttagc agtcggattt cacaaagaac
1680
gctgataacc acgccatcag tgaagggaat gaatgtcggg tacccgatcg accgttttgc
1740
ccgacgtcag gtttacccgc cctgtaggtc cgaataagta gttcctatcc tcagttaagt
1800
accaaatatc ggcagcgccc gtgtgtgtat ttatagtact ggatgatcaa tttatcaaca
1860
ttttcagtta atggttgcta tcatattcac tgtaattgtt agtaaacagt ggatgtttgt
1920
aatgtagatg atggctaaat gtatgttgtc aagctttcat ttcaatgcaa tttttattgg
1980
gagctagttt tggggttcgg ttagagccac caaaacccca gaatttctgg gagttggctt
2040
gtgagagagg gttttggcga gttgactttc gggattcagt tagagacgct cttactagtt
2100
ccagtaaaga agtaaactat tttctgcaga catcccaatt attctgtaga aattagaagt
2160
agaaaatagt tatggtatca tataaccata tattattcaa aatctagaat catggacttg
2220
gctagacttt gatgatctga aattttaaat ttgatgataa ttgagaaatg atcctttcta
2280
tcttaggttg tggtaccaag gtatggggac tatgaggaag cctacgatgt cggagtccga
2340
aaatactaca aggctgctgg acaggtaagc gaaaatgcaa tcaaagggga gctgaaattt
2400
caatgcttac tatcataata aatcaatttt aagtgttttt ttttgtcctg caggatatgg
2460
aagtgaatta tttccatgct tatatcgatg gagttgattt tgtgttcatt gacgctcctc
2520
tcttccgaca ccgccaggaa gacatttatg ggggcagcag acaggttaat cttctatatg
2580
ttggtgtttg attgcactga taaactgaga acaagccaag gcctactgac cggcatatga
2640
ttacacattt tattttttca ggaaattatg aagcgcatga ttttgttctg caaggccgct
2700
gtcgaggtat cctctccaac tcaattgaca acctattaca actatacaat tatgtgtatg
2760
catgtatttc aacagatacg taatctcttg tgaagtgcat atatactaac aacatttcaa
2820
taccttacat gcacatttgg tcaagcgtta tgatttaact tctaataatc tattgcactg
2880
atgaacaatt atcttgatga tccttggtac ttcatcgtta tgtttccatg ttctcttcac
2940
cgattgattt ggaaatagca tttccacctg ccacaaacaa taatatacac tcctactttc
3000
atccaatgta gatattttcg cacttggcat atcatcccat taaatattat tggtccatca
3060
tttttattcc tctataattt gcaggttcca tggcacgttc catgcggcgg tgtcccttat
3120
ggggatggaa atctggtgtt tattgcaaat gattggcaca cggcactcct gcctgtctat
3180
ctgaaagcat attacaggga ccatggtttg atgcagtaca ctcggtccat tatggtgata
3240
cataacatcg ctcaccaggt tccttttctc caaatcttga tttttctcta gtctctacta
3300
tttactccac attgtttgag gaaactaaac gggttgcaaa attatgatgg cttatgaaag
3360
ttatagtctt atataggtaa atgcaccagt ggtgcttgca cttgtcacgc gtgttcactt
3420
tggtgcttac agttgtagac aataaaaaac tagtgcaaaa acttggctgt tgtgtgcaat
3480
acggtgcatt ttccgtatgt aggagtcaaa tattgcctgt gtggcattgt attcccgtct
3540
atagctgtta gaccatgcct acgtcgccat tgggcccaca caccctctat tacatgtggg
3600
ccccacttgt cagcctatga cataaataaa tggaaattta taatgaaaat gatggcctgg
3660
ggtcttgaaa atgggccgtc gcaggtatgc tggtagccag catgccctaa tcattaatcc
3720
ccctatgcac ttcatgtctt gtgtatgtgt gtgtgggaaa gggggggggt atgtatgctt
3780
atgcttatat cctttgctcc aaggctgcca tcctcaacaa gcccacctcc agcttcaaca
3840
cggccagcgc cttcatgatg gcccaggtgc tccgcaccat cgatcgaagc ggcaacgtcg
3900
tcgtcacgac catccaccaa cccaacgcac aaaatcctca ggctccgttc ggtacggagg
3960
aagagaaaat gcaggaaaaa acaacttcat gggaacaagg tttggtgaac agtaaaaaca
4020
tgtggaatct gaaaatgtag gtaccagaaa aaccggcctg ttcggtttgc aggaaaaagc
4080
atacttgcag cagcactgtt tggccctttc cagtgtaagg ctaaccatag tgggagtaac
4140
ataactaata ttatgtactt ggaactcaca aacatgctta tgtggcaggc aattaaagaa
4200
gagagagaga gtcatagtaa catagttaga taccgtatca taataaatat tatgttacta
4260
tgtgtcatgc atgacaataa atgagaccat ctgtgatact acgttatgat attatgcact
4320
atagatgtag tatcatacac tagtatcata tgcatgatac tagtgtatgt tactccccac
4380
tatgaccagc ctaacgaggg gatgggcatc agtagtgatt accagttttt attatttttt
4440
attcggctgg acgccctact cttgtggtgc gtagcggaaa aaggcagtgc tagcttcggg
4500
actccgcgag cacatgaggt tctaccggat tttagatttc ctataaaaag tacaggctca
4560
cgcaactttt caatggaaca gaccatcaag attcctttga accgaacgca ctgcatgcaa
4620
gaattccaat gaaaaacgag ccgtcaaatg ttcctgcgaa tttcctctat accgaacaga
4680
ccctcaacat cctcaaatag tgagcatgcc cctcttgtcc tttccccctc gtacccaaac
4740
gccatttggc gctcttggtg ttggatcatt tgcctcgggc atttgccaat ttggcgccga
4800
accatattaa agctatgact acttggtgtt ggatcaggga cgcaaagaat cccataaata
4860
ttgcaacgtt cattcaaatt cttaacattt gcgaggcgct tcatgatttc catctccgtc
4920
aggtctgaga catttggtcg tgtacactaa atttctcagg tcacttctcg tctaaatccg
4980
catatgtagc tcacttcaat gacttgcctt tggtctagct aacgccattt ggcgctcttg
5040
ggcccccttg cttagcaaat ttttcatatg gctcgcactg cgcaagagga tttagatcac
5100
gggcagacgc gctagacgag gtcttccgca caatgaacat tgcgttcttt gctctgctct
5160
tcccggagac acttgtgatc ttattacgag ttgtgccatt tcaaacatct gtctctccat
5220
ggtcgctcca gccatagatg ccttgttctc tgaatggtgg gtttcagcta ggaacagggt
5280
gccaccttcg acaagaagtt gcatagtttg gtcgtcttga ctgcttggtc gatttggaag
5340
gaacgcaaca taagagtctt tgaaggcaaa gctaatttct ttgatcaagt tattagccag
5400
atcaaatgtg atgtattcta ctggtacaag gccggggcta tttgctttga gtcacttttt
5460
agctaaggcc gcttgggcta agcgcttggg gtcgtttttg ctcaactgta gcctgaactt
5520
tctggacttt gtaatttttt ttatcctcta taatgatcac atacagctct cctgcatggt
5580
tcgaaaagga aaaatgtgaa catgtgtggc aagtttaagc acaacccgtg catttacctc
5640
aaagttatac aacactgaca tgctgaatta catttttttt gaggatctga catgccgaat
5700
tacatgcttt ggacagttat tcatttcttc ggtacaccat tggctaatta tttctcttga
5760
cagttgctga attagtacat gctttggtcg cagttattcc tttgttcggt actctgttgg
5820
gctaattatt tctcttgatt gatgttgcat gcagggccgt ggcccagtag atgagttccc
5880
gttcaccgag ttgcctgagc actacctgga acacttcaga ctgtacgacc ccgtgggtgg
5940
tgaacacgcc aactacttcg ccgccggcct gaagatggcg gaccaggttg tcgtcgtgag
6000
cccggggtac ctgtgggagc tgaagacggt ggagggcggc tgggggcttc acgacatcat
6060
acggcagaac gactggaaga cccgcggcat cgtgaacggc atcgacaaca tggagtggaa
6120
ccccgaggtg gacgtccacc tcaagtcgga cggctacacc aacttctccc tggggacgct
6180
ggactccggc aagcggcagt gcaaggaggc cctgcagcgg gagctgggcc tgcaggtccg
6240
cggcgacgtg ccgctgctcg gcttcatcgg gcgcctggac gggcagaagg gcgtggagat
6300
catcgcggac gcgatgccct ggatcgtgag ccaggacgtg cagctggtca tgctgggcac
6360
cgggcgccac gacctggagg gcatgctgcg gcacttcgag cgggagcacc acgacaaggt
6420
gcgcgggtgg gtggggttct ccgtgcggct ggcgcaccgg atcacggccg gcgccgacgc
6480
gctcctcatg ccctcccggt tcgagccgtg cggactgaac cagctctacg ccatggccta
6540
cggcaccgtc cccgtcgtgc atgccgtcgg cggcctgagg gacaccgtgc cgccgttcga
6600
ccccttcaac cactccgggc tcgggtggac gttcgaccgc gcagaggcgc agaagctgat
6660
cgaggcgctc gggcactgcc tccgcaccta ccgggactac aaggagagct ggagggggct
6720
ccaggagcgc ggcatgtcgc aggacttcag ctgggagcat gccgccaagc tctacgagga
6780
cgtcctcgtc aaggccaagt accagtggtg a
6811
<210> 9
<211> 6950
<212> ДНК
<213> Triticum aestivum
<400> 9
gggggccgtt cgtacgtacc cgcccctcgt gtaaagccgc cgccgtcgtc gccgtccccc
60
gctcgcggcc atttcttcgg cctgaccccg ttcgtttacc cccacacaga gcacactcca
120
gtccagtcca gcccactgcc accgcgctac tctccactcc cactgccacc acctccgcct
180
gcgccgcgct ctgggcggac caacccgcga accgtaccat ctcccgcccc gatccatgtc
240
gtcggcggtc gcgtccgccg catccttcct cgcgctcgcg tcagcctccc ccgggagatc
300
acgcaggcgg gcgagggtga gcgcgcagcc accccacgcc ggggccggca ggttgcactg
360
gccgccgtgg ccgccgcagc gcacggctcg cgacggagct gtggcggcgc tcgccgccgg
420
gaagaaggac gcggggatcg acgacgccgc cgcgtccgtg aggcagcccc gcgcactccg
480
cggtggcgcc gccaccaagg tagttagtta tgaccaagtt atgacgcgtg cgcgcgcctc
540
gagatcatcg tcgtctcgct cacgaattgt ttatttatac aaaacgcacg cccgcgtgtg
600
caggtcgcgg agcgaaggga tcccgtcaag acgctcgacc gcgacgccgc ggaaggcggc
660
gggccgtccc cgccggcagc gaggcaggac gccgcccgtc cgccgagtat gaacggcatg
720
ccggtgaacg gcgagaacaa atctaccggc ggcggcggcg cgactaaaga cagcgggctg
780
cccacgcccg cacgcgcgcc ccatccgtcg acccagaaca gagcaccggt gaacggtgaa
840
aacaaagcta acgtcgcctc gccgccgacg agcatagccg aggccgcggc ttcggattcc
900
gcagctacca tttccatcag cgacaaggcg ccggagtccg ttgtcccagc tgagaagacg
960
ccgccgtcgt ccggctcaaa tttcgagtcc tcggcctctg ctcccgggtc tgacactgtc
1020
agcgacgtgg aacaagaact gaagaagggt gcggtcgttg tcgaagaagc tccaaagcca
1080
aaggctcttt cgccgcctgc agcccccgct gtacaagaag acctttggga tttcaagaaa
1140
tacattggtt tcgaggagcc cgtggaggcc aaggatgatg gccgggctgt cgcagatgat
1200
gcgggctcct ttgaacacca ccagaatcac gactccggac ctttggcagg ggagaatgtc
1260
atgaacgtgg tcgtcgtggc tgctgagtgt tctccctggt gcaaaacagg catggacatt
1320
acctcttcag tctctcttcc tgttgttcat aaaactttgc tcgaattact cataagaaca
1380
aacattgtgt tgcataggtg gtctgggaga tgttgcgggt gctctgccca aggctttggc
1440
aaagagagga catcgtgtta tggtactaca agctttcatt taactctgtt gggtccatat
1500
gttcgaataa tatcagtgag tagtataatg ttattaagtg caagacatga aagtgttctt
1560
ttgtcatact ccctccgtaa attaatataa gagcgtttag attactactt tagtgatcta
1620
aacgctctta tagtagttta cagacggagt agagtatttc atagccaacc ctggaggtta
1680
ggttgctgag gcctactggg tgggggaggg ggtttgaaac aagtggtggt tagcagccag
1740
atttcacaaa gaaggaggct gataaccaca ccatcagtga aggaatgaat gtcgggtacc
1800
cgatcgaccg ttttgcccaa cgtcgggttt acccgcccta tagatccgaa taagtagttc
1860
ctatcttcaa ttaggtacca aatatcgcca gcgcccgtgt gtgtatttat actactggat
1920
gatcaattta tcaacatttc cggttaatgg tttctatcat attcactgta attgttagta
1980
aacagtagat gtttgtaatg tagatgatgg ataaatgtat gttgtcgagc tttcatttca
2040
atgcaatttt gattgggagc tagtttcgcg gttcggttag agccatcaaa accccagaat
2100
ttttgggagt tggcttgtga gagagggttt tggggagtta actttcggga ttcagttaga
2160
gacgctctta ctagttccag taaagagtaa actattttct gcaggcatcc caattattct
2220
gtagaaatta gaagtggaaa atagttatgg tatcatataa accatatatt attcaaaatc
2280
tagaatcatg gacttggcta gactttgata atctgaaatt ttaaatttga tgataattga
2340
gaaatgatcc tttctatctt aggttgtggt accaaggtat ggggactatg aagaagccta
2400
cgatgtcgga gtccgaaaat actacaaggc tgctggacag gtaagcaaaa atgcaatcga
2460
aggggagctg aaattttatt gcttattgtc ataataaatc aatttttaag tgtttttttt
2520
gtcctgcagg atatggaagt gaattatttc catgcttata tcgatggagt tgattttgtg
2580
ttcattgacg ctcctctctt ccgacaccgt caggaagaca tttatggggg cagcagacag
2640
gttaatcttc tatatgttgg tgtttgattg cactgataaa ctgagaacaa gccaaggcct
2700
actgactggc atatgattac acattttatt ttttcaggaa attatgaagc gcatgatttt
2760
gttctgcaag gccgctgttg aggtatctct ccaactcaat tgacaaccta ttaccactat
2820
acaattatgt gtatgcatgt atttcaacag atacataatc tcttgtgaag tgcatatata
2880
ctaataacat ttcaatacct tacatgcaca tttggtcaag cgttatgatt taacttctga
2940
taatctattg cactgatgaa caattatctt gatgatcctt gttacttcat cgttatgttt
3000
ccatgttctc ttcaccgcga attgatttgg aaatagcatt tccacctgcc acaaacaata
3060
atatacactc ctactttcat ccaatttaga tattttcgta cttggcatat catcccatta
3120
aatattattg gtccatcatt tttattcctc tataatttgc aggttccatg gcacgttcca
3180
tgcggcggtg tcccttatgg ggatggaaat ctggtgttta ttgcaaatga ttggcacacg
3240
gcactcctgc ctgtctatct gaaagcatat tacagggacc atggtttgat gcagtacact
3300
cggtccatta tggtgataca taacatcgct caccaggttc cttttctcct aatcttgatt
3360
tttctctagt ctctactatt tactccacat tgtttgagga aactaaacgg gttgcaaaat
3420
tatgatggct tatgaaagtt atagtcttat agaggtaaat gcaccagtgg tgcttgaact
3480
tgtcacgcgt gttcactttg gtgcttacag ttgtagacta tgaaaaacgg gtgcaaaaac
3540
ttgctgttgt gtgccatacg gtgcattttc cgtatgtagg agtcaaacgt tgcctatgtg
3600
ggcattgtat tcccgtctat agctgttaga ccgtgcctac gtcgccattg ggcccacaca
3660
ctctctattt acatgtgggc cccacttgtc aacctatgac ataaataaat ggaaatttat
3720
aataaaaatg atggcctggg gtcttgaaaa tgggacctcg caggtatgct ggtagccagc
3780
acgccctaaa cattaatccc ctatgcactt catgtcttgt gtatgtgtgt gtctgtgtgg
3840
ggaggggggg ggtatgtatg cttatatcct ttgctccaag gctaccatcc tcaacaagcc
3900
cacctccgct tcaacacggc cagcgccttc atgatggccc aggtgctccg caccatcgct
3960
caaagcggca acgtcgttgt catgaccatc caccaaccca acacacaaaa tcctcaacat
4020
ccgcaaatag tgagcatgcc cctcttgtcc tttcccctcg tacccaaaca tgtcttgata
4080
acccttggag ctgcacaagt tgtgaccatc gcctgcgtcg cctcatagag cccgacctag
4140
ccggaccgtt atagaagcct acttgggagc ccatacctcc ctgcacatcc tcctctttcc
4200
ccatagatcg tgccgccatc gcaaaccaac ttctcctctc cttctcccac tctggccgtt
4260
tcccccgccg cgaagctgca atacatgccg agttggccat ggccctattc cccaattgct
4320
cgcactagga ggtcctcctc taagcctagc accttttccc ctcaccaatt gcaagttggg
4380
gagcccctcg cgagctccct acgtcggctg cagttgcctg ccgcctcaac tctgatccag
4440
acctcgttcc cgtggcctcg gcgacatctc ctcgacctcc cattccacac gtggcctggc
4500
gaggatcacc gcatgttcat ccatgtgaac cgaatcatca tagaactaac accggagagg
4560
tcatcccgac ggcgtcgcac tgttcctcta ttccccccaa gccgtgtcgc gtcataatat
4620
aagacggact tatttgtatc ccttgggtca tcggttcaat ggctatttct ttctcctgtc
4680
tactgataag tgggacccac acgccacact aagccctttc tttctcctac ccgttgataa
4740
gtgggaccca cacacagtac ttagccagag agagaacatg agcttgttgg tgccacgtcg
4800
gcaagccatg tcagcagtct taacggctac aaacaacgga tatggtgtca cgtgagcgtt
4860
tacgaatgga aagtgcatca tactgcatgc gagagccaga gccaggtttt tgcaccagtt
4920
ttctgtattt tacaactgcg agcatcaaag tgtacatatg ccgaaccaaa gtgaacatgg
4980
tgagtccatt cttttctggt gcggtgggtg gctcaaagac accccaatag aagctattgc
5040
ctccgacatt gccaattcgg tgccgaacca tattgaagtg gtgaggtcag ttgcttgtgc
5100
tatgactact aggtattgga tgagggacat aaaggatctc ataaatattg caatgttcat
5160
tcaaattctt aacatttgcg aagcgcttca tgatttccat ctcccctaga tcagagacac
5220
ttggtcgtgt acactgaatt tctcaggtcg cttctcgtct aaatccgcat atgtagctca
5280
cttcaatgac ttgcctttgg tccagctaac gccatttgcg tagcaaattt ttcatatggc
5340
tcgctctgcg caagaggatt tggatcacgg gcagacgcgc tagacaaggt cttccgcaca
5400
atgaacattg agttttttga tccgctcttc ccgaagacac ttgtgatctt attacgagtt
5460
gtgccatttc aaacatctgt ctctccatgg tcgccccagc catagatgcc ttgttctctg
5520
aatggtgggt ttcagctagg aacagggtgc caccttcgga caagaagttg cgtagtttgg
5580
tcgtcttaac tgcttggttg atttggaagg aacacaacaa cagtctttga aggcaaagct
5640
aattccttcg atcaagttat tagacggatc aagtgtgatg aatcctactg gtacaatgcc
5700
gttgctagtt gcttggagtc actatttggc taggtcgctt gccatcccgc tctgtgctaa
5760
gcgcttgggg tcgcttttgc tcaatttgta ttttgttgtt atgtgttttt agtaatgtaa
5820
cctgaacttt ctggactaag tagaaaaaaa ttctcctcca taatgatcac atacagttct
5880
cctgcatggt tcgaaaaaaa aatgagaaca tccgtggcaa gtttaagcac caccggtgca
5940
tttttacctc aaagttatat acaacactga catgccgaat tacatgcttt ggtcagttat
6000
tccattcttc ggtactccgt tgggctaatt ctttctcttc atgttgcatg cagggccgtg
6060
gccctgtaga tgaattcccg ttcaccgagt tgcctgagca ctacctggaa cacttcagac
6120
tgtacgaccc cgtgggtggt gaacacgcca actacttcgc cgccggcctg aagatggcgg
6180
accaggttgt cgtggtgagc cccgggtacc tgtgggagct gaagacggtg gagggcggct
6240
gggggcttca cgacatcata cggcagaacg actggaagac ccgcggcatc gtcaacggca
6300
tcgacaacat ggagtggaac cccgaggtgg acgcccacct caagtcggac ggctacacca
6360
acttctccct gaggacgctg gactccggca agcggcagtg caaggaggcc ctgcagcgcg
6420
agctgggcct gcaggtccgc gccgacgtgc cgctgctcgg cttcatcggc cgcctggacg
6480
ggcagaaggg cgtggagatc atcgcggacg ccatgccctg gatcgtgagc caggacgtgc
6540
agctggtgat gctgggcacc gggcgccacg acctggagag catgctgcag cacttcgagc
6600
gggagcacca cgacaaggtg cgcgggtggg tggggttctc cgtgcgcctg gcgcaccgga
6660
tcacggcggg ggcggacgcg ctcctcatgc cctcccggtt cgagccgtgc gggctgaacc
6720
agctctacgc catggcctac ggcaccgtcc ccgtcgtgca cgccgtcggc ggcctcaggg
6780
acaccgtgcc gccgttcgac cccttcaacc actccgggct cgggtggacg ttcgaccgcg
6840
ccgaggcgca caagctgatc gaggcgctcg ggcactgcct ccgcacctac cgagacttca
6900
aggagagctg gagggccctc caggagcgcg gcatgtcgca ggacttcagc
6950
<210> 10
<211> 676
<212> Белок
<213> Triticum aestivum
<400> 10
Met Leu Gly His Ile Ala Ser Ser Ser Ala Ala Phe Leu Leu Leu Val
1 5 10 15
Ala Ser Ser Ser Ser Ser Arg Arg Trp Arg Ser Ser Ser Pro Arg Ser
20 25 30
Phe Gly Ala Ala Gly Thr Arg Leu His Trp Glu Arg Arg Gly Phe Ser
35 40 45
Arg Asp Gly Ser Val Pro Cys Arg Arg Val Ser Ala Ala Ala Ala Val
50 55 60
Ala Gly Gly Glu Glu Gly Ala Gly Lys Ala Ile Ala Gly Glu Gly Ser
65 70 75 80
Arg Gln Ala Ala Ser Gly Gln Arg Gly Lys Leu Glu Ala Ala Glu Asn
85 90 95
Glu Asp Ala Val Ser Gln Lys Ser Val Ala Ser Ala Pro Arg Pro Asp
100 105 110
Ser Thr Val Ala Glu Gln His Trp Ala Ala Gly Ser Arg Ser Glu Val
115 120 125
Asp Pro Ser Ala Pro Val Ser Ala Ala Ala Ser Gly Tyr Trp Lys Asp
130 135 140
Val Val Val Ala Glu Gln Val Gly Ala Lys Val Asp Ala Gly Gly Asp
145 150 155 160
Ala Ala Lys Val Trp Ser Ser Pro Val Asp Ser Glu Asn Met Gly Ser
165 170 175
Ala Pro Leu Ala Gly Pro Asn Val Met Asn Val Ile Val Val Ala Ser
180 185 190
Glu Cys Ala Pro Phe Cys Lys Thr Gly Gly Leu Gly Asp Val Val Gly
195 200 205
Ala Leu Pro Lys Ala Leu Ala Arg Arg Gly His Arg Val Met Val Val
210 215 220
Ile Pro Lys Tyr Gly Asp Tyr Gly Glu Ala Arg Asp Leu Gly Val Arg
225 230 235 240
Lys Arg Tyr Lys Val Ala Gly Gln Asp Ser Glu Val Ser Tyr Phe His
245 250 255
Ser Tyr Ile Asp Gly Val Asp Phe Val Phe Leu Glu Ala Pro Pro Phe
260 265 270
Arg His Arg His Asn Asp Ile Tyr Gly Gly Glu Arg Pro Asp Val Leu
275 280 285
Lys Arg Met Ile Leu Phe Cys Lys Ala Ala Val Glu Val Pro Trp Tyr
290 295 300
Ala Pro Cys Gly Gly Thr Ile Tyr Gly Asp Gly Asn Leu Val Phe Ile
305 310 315 320
Ala Asn Asp Trp His Thr Ala Leu Leu Pro Val Tyr Leu Lys Ala Tyr
325 330 335
Tyr Arg Asp Asn Gly Leu Met Gln Tyr Thr Arg Ser Val Leu Val Ile
340 345 350
His Asn Ile Ala His Gln Gly Arg Gly Pro Val Asp Asp Phe Asn Ile
355 360 365
Met Asp Leu Pro Glu His Tyr Met Asp His Phe Lys Leu Tyr Asp Pro
370 375 380
Leu Gly Gly Gln His Asn Asn Val Phe Ala Ala Gly Leu Lys Met Ala
385 390 395 400
Asp Arg Val Val Thr Val Ser His Gly Tyr Met Trp Glu Leu Lys Thr
405 410 415
Met Glu Gly Gly Trp Gly Leu His Asp Ile Ile Asn Gln Asn Asp Trp
420 425 430
Lys Leu Asp Gly Ile Val Asn Gly Ile Asp Thr Ala Glu Trp Asn Pro
435 440 445
Ala Val Asp Val His Leu His Ser Asp Asp Tyr Thr Asn Tyr Thr Arg
450 455 460
Asp Thr Leu Asp Ile Gly Lys Arg Gln Cys Lys Ala Ala Leu Gln Arg
465 470 475 480
Glu Leu Gly Leu Gln Val Arg Asp Asp Val Pro Leu Ile Gly Phe Ile
485 490 495
Gly Arg Leu Asp His Gln Lys Gly Val Asp Ile Ile Ala Ala Ala Met
500 505 510
Pro Trp Ile Ala Gln Gln Asp Val Gln Leu Val Met Leu Gly Thr Gly
515 520 525
Arg Pro Asp Leu Glu Asp Met Leu Arg Arg Phe Glu Gly Glu His Arg
530 535 540
Asp Lys Val Arg Gly Trp Val Gly Phe Ser Val Arg Met Ala His Arg
545 550 555 560
Ile Thr Ala Gly Ala Asp Val Leu Leu Met Pro Ser Leu Phe Glu Pro
565 570 575
Cys Gly Leu Asn Gln Leu Tyr Ala Met Ala Tyr Gly Thr Val Pro Val
580 585 590
Val His Ala Val Gly Gly Leu Arg Asp Thr Val Ala Pro Phe Asp Pro
595 600 605
Phe Gly Gly Thr Gly Leu Gly Trp Thr Phe Asp Arg Ala Asp Ala Gly
610 615 620
Arg Met Ile Asp Ala Leu Gly His Cys Leu Asn Thr Tyr Trp Asn Tyr
625 630 635 640
Lys Glu Ser Trp Arg Gly Leu Gln Val Arg Gly Met Ser Gln Asp Leu
645 650 655
Ser Trp Asp Arg Ala Ala Glu Leu Tyr Glu Asn Val Leu Val Lys Ala
660 665 670
Lys Tyr Gln Trp
675
<210> 11
<211> 674
<212> Белок
<213> Triticum aestivum
<400> 11
Met Ser Gly Ala Ile Ala Ser Ser Ser Ala Ala Phe Leu Leu Leu Val
1 5 10 15
Ala Ser Ser Ser Cys Ser Ser Ser Ser Pro Arg Arg Trp Arg Ser Ser
20 25 30
Ser Pro Arg Ser Phe Ala Ala Ala Gly Thr Arg Leu His Trp Glu Arg
35 40 45
Arg Gly Phe Ser Arg Asp Gly Pro Val Pro Cys Arg Ser Pro Cys Ala
50 55 60
Ala Ala Gly Gly Glu Asp Gly Ala Ala Ala Gly Glu Ser Ser Lys Glu
65 70 75 80
Gly Val Ala Gly Leu Arg Gly Lys Leu Lys Ala Ala Glu Asn Glu Asp
85 90 95
Pro Val Ser Gln Lys Ser Val Ala Ser Ala Pro Arg Leu Asp Ser Ser
100 105 110
Val Ala Glu Gln Asn Gly Ala Ala Ala Thr Arg Ser Lys Ala Asp Pro
115 120 125
Ser Ala Pro Val Ser Ala Ala Ala Ser Gly Tyr Trp Lys Asp Val Val
130 135 140
Val Ala Glu Gln Val Gly Thr Lys Val Asp Thr Gly Gly Asp Ala Ala
145 150 155 160
Glu Val Ser Arg Ser Pro Val Asp Ser Glu Asn Lys Gly Ser Ala Pro
165 170 175
Leu Ala Gly Pro Asn Val Met Asn Val Ile Val Val Ala Ser Glu Cys
180 185 190
Ala Pro Phe Cys Lys Thr Gly Gly Leu Gly Asp Val Val Gly Ala Leu
195 200 205
Pro Lys Ala Leu Ala Arg Arg Gly His Arg Val Met Val Val Ile Pro
210 215 220
Lys Tyr Gly Asp Tyr Ala Glu Ala Arg Asp Leu Gly Val Arg Lys Arg
225 230 235 240
Tyr Lys Val Ala Gly Gln Asp Ser Glu Val Ser Tyr Phe His Ser Tyr
245 250 255
Ile Asp Gly Val Asp Phe Val Phe Leu Glu Ala Pro Pro Phe Arg His
260 265 270
Arg His Asn Asp Ile Tyr Gly Gly Glu Arg Pro Asp Val Leu Lys Arg
275 280 285
Met Ile Leu Phe Cys Lys Ala Ala Val Glu Val Pro Arg Tyr Ala Leu
290 295 300
Cys Gly Gly Thr Ile Tyr Gly Asp Gly Asn Leu Val Phe Ile Ala Asn
305 310 315 320
Asp Trp His Thr Ala Leu Leu Pro Val Tyr Leu Lys Ala Tyr Tyr Arg
325 330 335
Asp Asn Gly Leu Met Gln Tyr Thr Arg Ser Val Leu Val Ile His Asn
340 345 350
Ile Ala His Gln Gly Arg Gly Pro Val Asp Asp Phe Asn Ile Met Asp
355 360 365
Leu Pro Asp His Tyr Met Gly His Phe Lys Leu His Asp Pro Leu Gly
370 375 380
Gly Glu His Asn Asn Val Phe Ala Ala Gly Leu Lys Met Ala Asp Arg
385 390 395 400
Val Val Thr Val Ser His Gly Tyr Met Trp Glu Leu Lys Thr Val Glu
405 410 415
Gly Gly Trp Gly Leu His Asp Ile Ile Asn Gln Asn Asp Trp Lys Leu
420 425 430
Asp Gly Ile Val Asn Gly Ile Asp Thr Ala Glu Trp Asn Pro Ala Val
435 440 445
Asp Val His Leu His Ser Asp Asp Tyr Thr Asn Tyr Thr Arg Asp Thr
450 455 460
Leu Asp Ile Gly Lys Arg Gln Cys Lys Ala Ala Leu Gln Arg Glu Leu
465 470 475 480
Gly Leu Gln Val Arg Asp Asp Val Pro Leu Ile Gly Phe Ile Gly Arg
485 490 495
Leu Asp His Gln Lys Gly Val Asp Ile Ile Ala Ala Ala Met Pro Trp
500 505 510
Ile Ala Gln Gln Asp Val Gln Leu Val Met Leu Gly Thr Gly Arg Pro
515 520 525
Asp Leu Glu Asp Met Leu Arg Arg Phe Glu Gly Glu His Arg Asp Lys
530 535 540
Val Arg Gly Trp Val Gly Phe Ser Val Arg Met Ala His Arg Ile Thr
545 550 555 560
Ala Gly Ala Asp Val Leu Leu Met Pro Ser Leu Phe Glu Pro Cys Gly
565 570 575
Leu Asn Gln Leu Tyr Ala Val Ala Tyr Gly Thr Val Pro Val Val His
580 585 590
Ala Val Gly Gly Leu Arg Asp Thr Val Ala Pro Phe Asp Pro Phe Gly
595 600 605
Gly Thr Gly Leu Gly Trp Thr Phe Asp Arg Ala Asp Ala Gly Arg Met
610 615 620
Ile Asp Ala Leu Gly His Cys Leu Asn Thr Tyr Trp Asn Tyr Lys Glu
625 630 635 640
Ser Trp Arg Gly Leu Gln Val Arg Gly Met Ser Gln Asp Leu Ser Trp
645 650 655
Asp His Ala Ala Glu Leu Tyr Glu Asn Val Leu Val Lys Ala Lys Tyr
660 665 670
Gln Trp
<210> 12
<211> 2727
<212> ДНК
<213> Triticum aestivum
<400> 12
acccgtcgtc ttcctcggcg cgggcgctct agctcttccc agtctcggcc tccgagctcc
60
accacacaag ccgctcgcct gtccccggcc tccagttcct ccgcctcccg cccccccccc
120
cccccccgct ccgtaccgcc gcaaaaaacc tgcagccaca cgtagccagc gcagatcttt
180
cttccacccg cgcttaattt ccctcgtgct cgcgccgctc gccgtcgccc tcgtccacta
240
ctactctgcc ttgtttgtcc ggctgtttct gttcatcccc gaagacttct ggcgcgtcgg
300
atcccgggat gttggggcac atcgcttcct cgtccgcggc gttcctcttg ctcgtggcct
360
cctcctcgtc gtcgcggcgc tggcggagca gctcaccgcg ctctttcggt gccgccggta
420
cgcggctgca ttgggaacgg cgagggtttt ctcgggacgg atcggtgccg tgccgccgtg
480
tttcagcagc agcggcagtg gctggtggtg aggagggcgc ggggaaggca atagcagggg
540
agggctcgag gcaggcagcc tctgggcagc gcggcaagct cgaggctgct gaaaatgagg
600
atgctgtttc acaaaaatca gttgcatctg cacccaggcc agatagtacc gttgcagagc
660
aacattgggc agctgggagc agatccgaag tcgatccgtc agctcctgtc tcggcggcgg
720
catcaggtta ttggaaagac gtcgttgtcg ctgaacaggt tggggctaag gttgatgccg
780
gtggagatgc agcaaaagtg tggagttctc cggttgacag tgagaacatg gggtctgctc
840
ctttggctgg cccgaatgtg atgaatgtca tcgttgtggc ttctgaatgt gctcctttct
900
gtaaaacagg tgggcttgga gatgttgtgg gtgctttgcc gaaggctctg gcaagaagag
960
ggcatcgtgt tatggtcgtg ataccaaaat atggagatta cggagaagct cgtgatctag
1020
gtgttcgcaa acgttacaag gtagctggcc aggattcaga agtgagctac tttcattctt
1080
atatcgatgg agttgatttt gtgttcttag aggccccgcc cttccgccac cggcacaatg
1140
atatttatgg aggagaaaga ccggatgtgc tgaagcgcat gattttgttc tgcaaggctg
1200
ctgtggaggt tccttggtac gctccatgcg gtggtactat ctacggtgat ggcaatttag
1260
tcttcattgc aaacgattgg catactgcac ttctacctgt ttatctgaag gcgtattacc
1320
gagacaatgg cctgatgcag tatactcgtt ctgttctcgt gatccataac attgctcatc
1380
agggacgtgg ccctgtagat gacttcaaca tcatggactt gcctgagcac tacatggatc
1440
acttcaaact gtatgatccc cttggcggcc agcacaacaa cgtgttcgct gctggcctga
1500
agatggcaga ccgggtggtc accgtcagcc atggctacat gtgggagctg aagacgatgg
1560
aaggcggctg gggcctccac gacataataa accagaacga ctggaagctg gacggcatcg
1620
tgaacggcat cgacacggcc gagtggaacc ccgcagtcga cgtgcacctg cactccgacg
1680
actacaccaa ctacacccga gacacgctgg acatcggcaa gcggcagtgc aaggcggccc
1740
tgcagcgcga gctgggcctg caggtccgcg acgacgtgcc gctcatcggg ttcatcgggc
1800
ggctggacca ccagaagggc gtggacatca tcgcggcggc gatgccgtgg atcgcgcagc
1860
aggacgtgca gctggtgatg ctgggcacgg ggcggccgga cctggaggac atgctgcggc
1920
ggttcgaggg ggagcaccgg gacaaggtgc gcgggtgggt ggggttctcg gtgcggatgg
1980
cgcaccggat cacggcgggc gcggacgtgc tcctcatgcc gtcgctgttc gagccgtgcg
2040
ggctgaacca gctgtacgcg atggcgtacg ggaccgtgcc cgtggtgcac gccgtcggcg
2100
ggctccggga cacggtggcg ccgttcgacc cgttcggcgg caccgggctg gggtggacgt
2160
tcgaccgcgc ggacgccggc aggatgatcg acgcgctcgg gcactgcctc aacacgtact
2220
ggaactacaa ggagagctgg aggggcctgc aggtccgcgg catgtcgcag gacctcagct
2280
gggaccgcgc cgccgagctc tacgagaacg tcctcgtcaa ggccaagtac cagtggtgat
2340
gcggctgatg ctgacccctc tactgcaacg catgcacgta cttaggggac agccggaagt
2400
ggtgcccacg atcgcgatca ctggcgcccc ggagtagcca agtgtcacgc gatgccaccg
2460
gcggcagccg gacgacggtg gaggtagtga accgtgcccg tggcgccgcc caacttttgg
2520
gttcacgagt tgtacacacc agttcagtca ggttcgtggc ttctgtgaat taccgagtcg
2580
taggcgatca aataggaagt tgcagagttt ctatactgcc aattttctca gctcttggtg
2640
tggaaaaaca cagttctgag aaggttcatc actggacgct gaccacgttc acgttctgtt
2700
tcatgctcaa aaaaaaaaaa aaaacga
2727
<210> 13
<211> 1282
<212> ДНК
<213> Triticum aestivum
<400> 13
tggtgaggat ggcgcggcgg caggggagag ctcgaaggag ggggtcgctg ggctgcgcgg
60
caagctcaag gttggtaacg ctatcattcc ttcttctgat ggattccatt tcgtgctcag
120
gctgctgaaa atgaggatcc ggtttcacaa aaatcagttg catctgcacc caggctagac
180
agtagcgttg cagagcaaaa tggggcagct gcgaccagat ccaaagccga tccgtcagct
240
cctgtctcgg cggcagcatc aggttattgg aaagacgtcg ttgtcgctga acaggttgga
300
actaaggttg acaccggtgg agatgcagca gaagtgtcga gatctcccgt tgacagtgag
360
aacaaggggt ctgctccttt ggctggcccg aatgtgatga atgtcatcgt tgtggcttct
420
gagtgtgctc ctttctgtaa aacaggtgcg catacataaa ctgagcaatt tgaccaataa
480
tgatatcatg cataggcggg cttggagatg tcgtgggtgc tttgcccaag gctctggcca
540
gaagagggca tcgcgttatg gtacccactc ctttgctttt ctcttataca agtatttctt
600
tcaattttag gttgtgatac caaagtatgg cgattacgca gaagctcgtg atcttggtgt
660
tcgcaaacgt tacaaggtag ctggccaggt atgttaaata acgagtctgc agtaattgaa
720
ttgtgttctg gtttgcagga ttcagaagtg agttactttc actcttatat cgatggagtt
780
gattttgtat tcttagaggc cccgcccttc cgccaccggc acaatgatat ttatggagga
840
gaaagaccgg taagcgtctg tttccctaga gctttgtaca tttccatcat ttttggcagg
900
atgtgctgaa gcgcatgatt ttgttctgca aggctgctgt cgaggtacct tcacaaattg
960
tattgctatt gttcatctgt tcgagcattt gtaggttcct tggtacgctc catgtggtgg
1020
tactatctac ggagatggca atttggtctt cattgcaaac gattggcata ctgcacttct
1080
acctgtttat ctaaaggcat attaccgaga caatggcctg atgcagtata ctcgttctgt
1140
tctcgtgatc cataacattg ctcatcaggt tttacacctc aatctttaac tgctggacac
1200
taaaattttg ctttgcaggg acgtggccct gtagatgact tcaacatcat ggacttgcct
1260
gaccactaca tgggtcactt ca
1282
<210> 14
<211> 2025
<212> ДНК
<213> Triticum aestivum
<400> 14
atgtcggggg caatagcttc ctcgtccgcg gcgttcctct tgctcgtggc ctcctcctcc
60
tgctcctcct cgtcgccgcg gcgctggcgg agcagctcac cgcgctcttt cgctgccgcc
120
ggtacgcggc tgcattggga acggcgagga ttctctcggg acggaccggt gccgtgccgg
180
agcccctgcg cagcagctgg tggtgaggat ggcgcggcgg caggggagag ctcgaaggag
240
ggggtcgctg ggctgcgcgg caagctcaag gctgctgaaa atgaggatcc ggtttcacaa
300
aaatcagttg catctgcacc caggctagac agtagcgttg cagagcaaaa tggggcagct
360
gcgaccagat ccaaagccga tccgtcagct cctgtctcgg cggcagcatc aggttattgg
420
aaagacgtcg ttgtcgctga acaggttgga actaaggttg acaccggtgg agatgcagca
480
gaagtgtcga gatctcccgt tgacagtgag aacaaggggt ctgctccttt ggctggcccg
540
aatgtgatga atgtcatcgt tgtggcttct gagtgtgctc ctttctgtaa aacaggcggg
600
cttggagatg tcgtgggtgc tttgcccaag gctctggcca gaagagggca tcgcgttatg
660
gttgtgatac caaagtatgg cgattacgca gaagctcgtg atcttggtgt tcgcaaacgt
720
tacaaggtag ctggccagga ttcagaagtg agttactttc actcttatat cgatggagtt
780
gattttgtat tcttagaggc cccgcccttc cgccaccggc acaatgatat ttatggagga
840
gaaagaccgg atgtgctgaa gcgcatgatt ttgttctgca aggctgctgt cgaggttcct
900
aggtacgctc tatgtggtgg tactatctac ggagatggca atttggtctt cattgcaaac
960
gattggcata ctgcacttct acctgtttat ctaaaggcat attaccgaga caatggcctg
1020
atgcagtata ctcgttctgt tctcgtgatc cataacattg ctcatcaggg acgtggccct
1080
gtagatgact tcaacatcat ggacttgcct gaccactaca tgggtcactt caaactgcat
1140
gacccccttg gtggcgagca caacaacgtg ttcgccgctg gcctgaagat ggcagaccgg
1200
gtggtcaccg tcagccatgg ctacatgtgg gagctgaaga cggtggaagg cggctggggc
1260
ctccacgaca taataaacca gaacgactgg aaactggacg gcatcgtgaa cggcatcgac
1320
acggccgagt ggaaccccgc ggtcgacgtg cacctgcact ccgacgacta caccaactac
1380
acccgagaca cgctggacat cggcaagcgg cagtgcaagg cggccctgca gcgcgagctg
1440
ggcctgcagg tccgcgacga cgtgccgctc atcgggttca tcgggcggct ggaccaccag
1500
aagggcgtgg acatcatcgc ggcggcgatg ccgtggatcg cgcagcagga cgtgcagctg
1560
gtgatgctgg gcacggggcg gccggacctg gaggacatgc tgcggcggtt cgagggggag
1620
caccgggaca aggtgcgcgg gtgggtgggg ttctcggtgc ggatggcgca ccggatcacg
1680
gcgggcgcgg acgtcctgct gatgccgtcg ctgttcgagc cgtgcgggct gaaccagctg
1740
tacgcggtgg cgtacgggac cgtgcccgtg gtgcacgccg tcggcgggct ccgggacacg
1800
gtggcgccgt tcgacccgtt cggcggcacc gggctggggt ggacgttcga ccgcgcggac
1860
gccggcagga tgatcgacgc gctcgggcac tgcctcaaca cgtactggaa ctacaaggag
1920
agctggaggg gcctccaggt ccgcggcatg tcgcaggacc tcagctggga ccacgccgcc
1980
gagctctacg agaacgtcct cgtcaaggcc aagtaccagt ggtga
2025
<210> 15
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 15
tgcgtttacc ccacagagca
20
<210> 16
<211> 22
<212> ДНК
<213> Синтетическая последовательность
<400> 16
tgccaaaggt ccggaatcat gg
22
<210> 17
<211> 18
<212> ДНК
<213> Синтетическая последовательность
<400> 17
gcggaccagg ttgtcgtc
18
<210> 18
<211> 22
<212> ДНК
<213> Синтетическая последовательность
<400> 18
ctggctcacg atccagggca tc
22
<210> 19
<211> 24
<212> ДНК
<213> Синтетическая последовательность
<400> 19
gtaccaaggt atggggacta tgaa
24
<210> 20
<211> 22
<212> ДНК
<213> Синтетическая последовательность
<400> 20
gttggagaga tacctcaaca gc
22
<210> 21
<211> 23
<212> ДНК
<213> Синтетическая последовательность
<400> 21
aaggtctcca ccgtgtctcg aag
23
<210> 22
<211> 23
<212> ДНК
<213> Синтетическая последовательность
<400> 22
gacgtacagt ttgtcatgct tgg
23
<210> 23
<211> 23
<212> ДНК
<213> Синтетическая последовательность
<400> 23
ctgctggaca ggatatggaa gtg
23
<210> 24
<211> 23
<212> ДНК
<213> Синтетическая последовательность
<400> 24
gtatcaccat aacggagcga ctg
23
<210> 25
<211> 25
<212> ДНК
<213> Синтетическая последовательность
<400> 25
caatcactga tggtgtaacc aaagg
25
<210> 26
<211> 23
<212> ДНК
<213> Синтетическая последовательность
<400> 26
ccttcatgtt ggtcaatagc agc
23
<210> 27
<211> 25
<212> ДНК
<213> Синтетическая последовательность
<400> 27
cagaatggac aaagaatcat ccacg
25
<210> 28
<211> 24
<212> ДНК
<213> Синтетическая последовательность
<400> 28
gaaaatacat ccatgcctcc atcg
24
<210> 29
<211> 21
<212> ДНК
<213> Синтетическая последовательность
<400> 29
agggtacagg gtgggcgttc t
21
<210> 30
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 30
gtagggttgg tccacgaagg
20
<210> 31
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 31
ttcgacccct tcaaccactc
20
<210> 32
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 32
acgtcctcgt agagcttggc
20
<210> 33
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 33
tgacgaatct tggaaaatgg
20
<210> 34
<211> 23
<212> ДНК
<213> Синтетическая последовательность
<400> 34
ggcggcattt atcataacta ttg
23
<210> 35
<211> 22
<212> ДНК
<213> Синтетическая последовательность
<400> 35
gtagatgcgg tcgtttactt ga
22
<210> 36
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 36
ccagccacct tctgtttgtt
20
<210> 37
<211> 19
<212> ДНК
<213> Синтетическая последовательность
<400> 37
gggccttcat ggatcaacc
19
<210> 38
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 38
ccgcttcaag catcctcatc
20
<210> 39
<211> 23
<212> ДНК
<213> Синтетическая последовательность
<400> 39
ctggacagga tctggaagtg aaa
23
<210> 40
<211> 22
<212> ДНК
<213> Синтетическая последовательность
<400> 40
ggaacctcaa cagcagcctt ac
22
<210> 41
<211> 19
<212> ДНК
<213> Синтетическая последовательность
<400> 41
gccaatgcca ggaagatga
19
<210> 42
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 42
gcgcaacata ggatgggttt
20
<210> 43
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<400> 43
tacgaattct ccagcggaat gagaacacca
30
<210> 44
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<400> 44
tacggtaccc aagatgtaca gaagtgcaga
30
<210> 45
<211> 22
<212> ДНК
<213> Синтетическая последовательность
<400> 45
ggaaatacat ggcttgctgc tt
22
<210> 46
<211> 22
<212> ДНК
<213> Синтетическая последовательность
<400> 46
tctcttcgtc ttgatggttg ca
22
<210> 47
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 47
caggcttgta tcccaggtca
20
<210> 48
<211> 20
<212> ДНК
<213> Синтетическая последовательность
<400> 48
gcgtaggagg aaagcatgaa
20
<210> 49
<211> 17
<212> Белок
<213> Синтетическая последовательность
<400> 49
Ala Ala Ser Pro Gly Lys Val Leu Val Pro Asp Gly Glu Ser Asp Asp
1 5 10 15
Leu
<210> 50
<211> 10
<212> Белок
<213> Синтетическая последовательность
<400> 50
Ala Gly Gly Pro Ser Gly Glu Val Met Ile
1 5 10
<210> 51
<211> 16
<212> Белок
<213> Синтетическая последовательность
<400> 51
Val Ser Ala Pro Arg Asp Tyr Thr Met Ala Thr Ala Glu Asp Gly Val
1 5 10 15
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЛЮКОАМИЛАЗЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2802790C2 |
| ЭКСПРЕССИЯ ПОЛИПЕПТИДОВ НИТРОГЕНАЗЫ В РАСТИТЕЛЬНЫХ КЛЕТКАХ | 2018 |
|
RU2809244C2 |
| РАСТЕНИЯ С МОДИФИЦИРОВАННЫМИ ПРИЗНАКАМИ | 2017 |
|
RU2809117C2 |
| СПОСОБ СОЗДАНИЯ НОВЫХ МУТАЦИЙ В ОРГАНИЗМАХ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2833881C1 |
| СПОСОБ УВЕЛИЧЕНИЯ ФОТОСИНТЕТИЧЕСКОЙ ФИКСАЦИИ УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ БЕЛКА СЛИЯНИЯ ИЗ МНОГИХ СУБЪЕДИНИЦ ГЛИКОЛАТДЕГИДРОГЕНАЗЫ | 2011 |
|
RU2651501C2 |
| ИНСЕКТИЦИДНЫЕ ПОЛИПЕПТИДЫ С ШИРОКИМ СПЕКТРОМ АКТИВНОСТИ И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2750459C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОМЫШЛЕННЫХ ПРОДУКТОВ ИЗ РАСТИТЕЛЬНЫХ ЛИПИДОВ | 2015 |
|
RU2743384C2 |
| ЭКСПРЕССИЯ ПОЛИПЕПТИДОВ НИТРОГЕНАЗЫ В РАСТИТЕЛЬНЫХ КЛЕТКАХ | 2020 |
|
RU2833880C2 |
| ВЫСОКОАФФИННЫЙ Т-КЛЕТОЧНЫЙ РЕЦЕПТОР ДЛЯ РАСПОЗНАВАНИЯ АНТИГЕНА AFP | 2019 |
|
RU2836365C2 |
| ГЕН АХМ1554, КОДИРУЮЩИЙ ДЕЛЬТА-ЭНДОТОКСИН, И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2755282C2 |
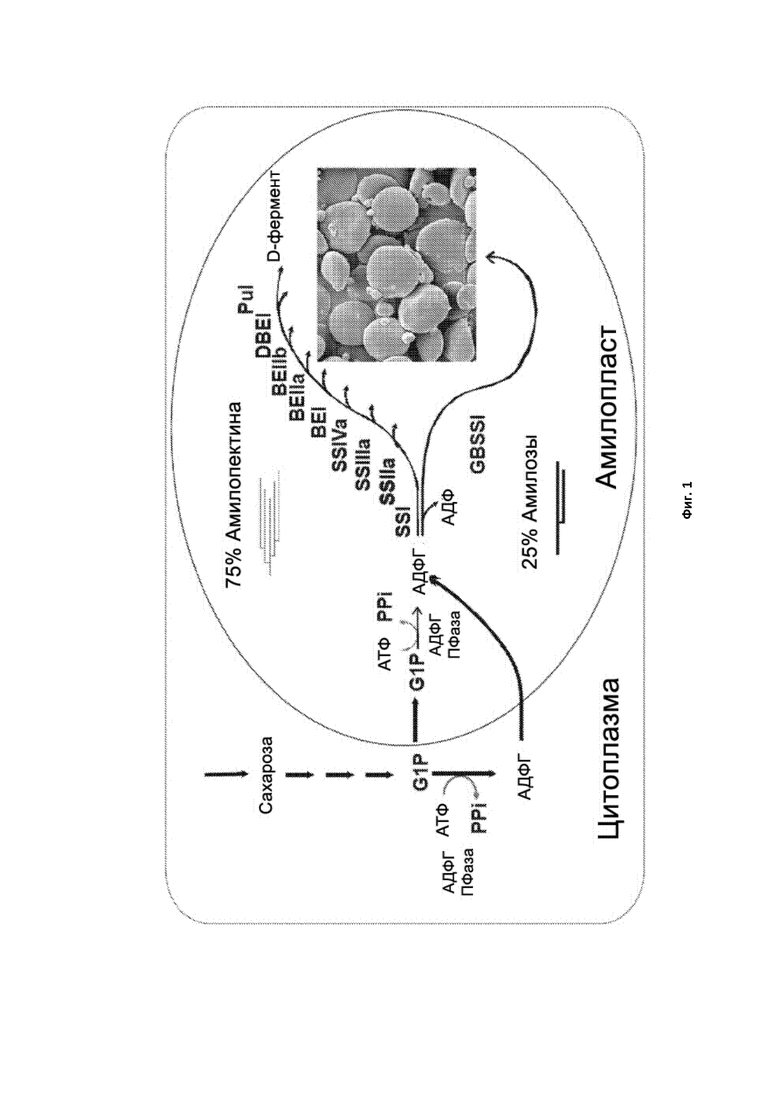
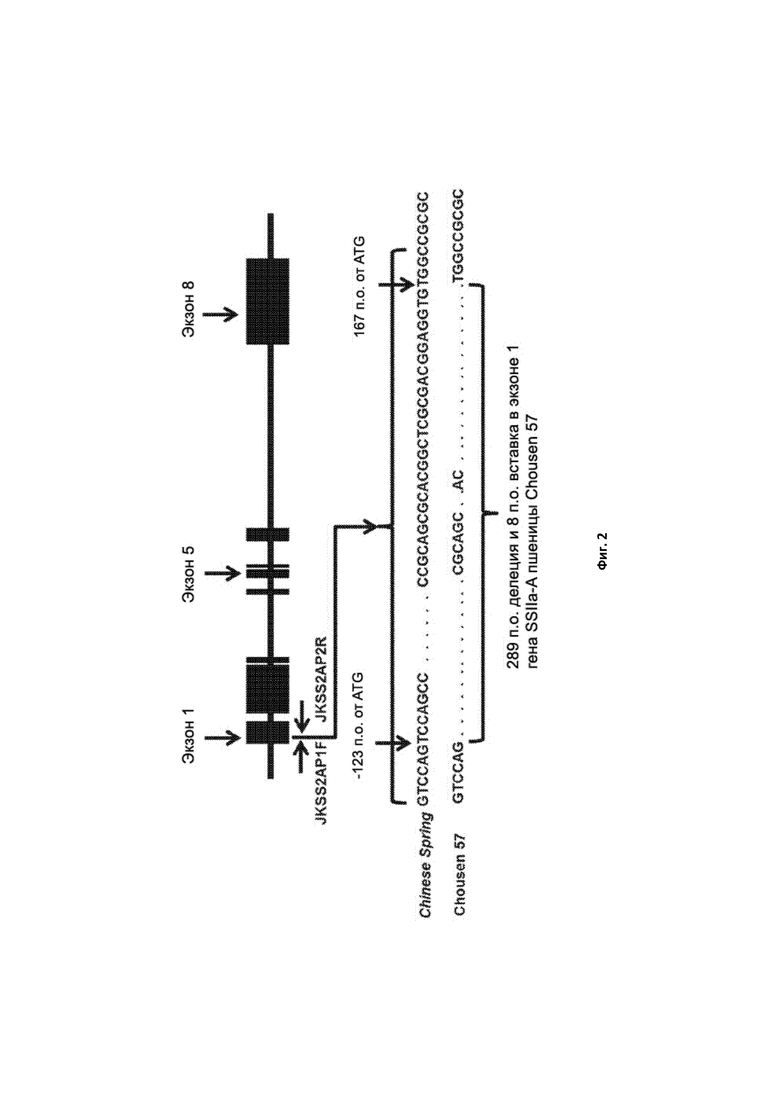
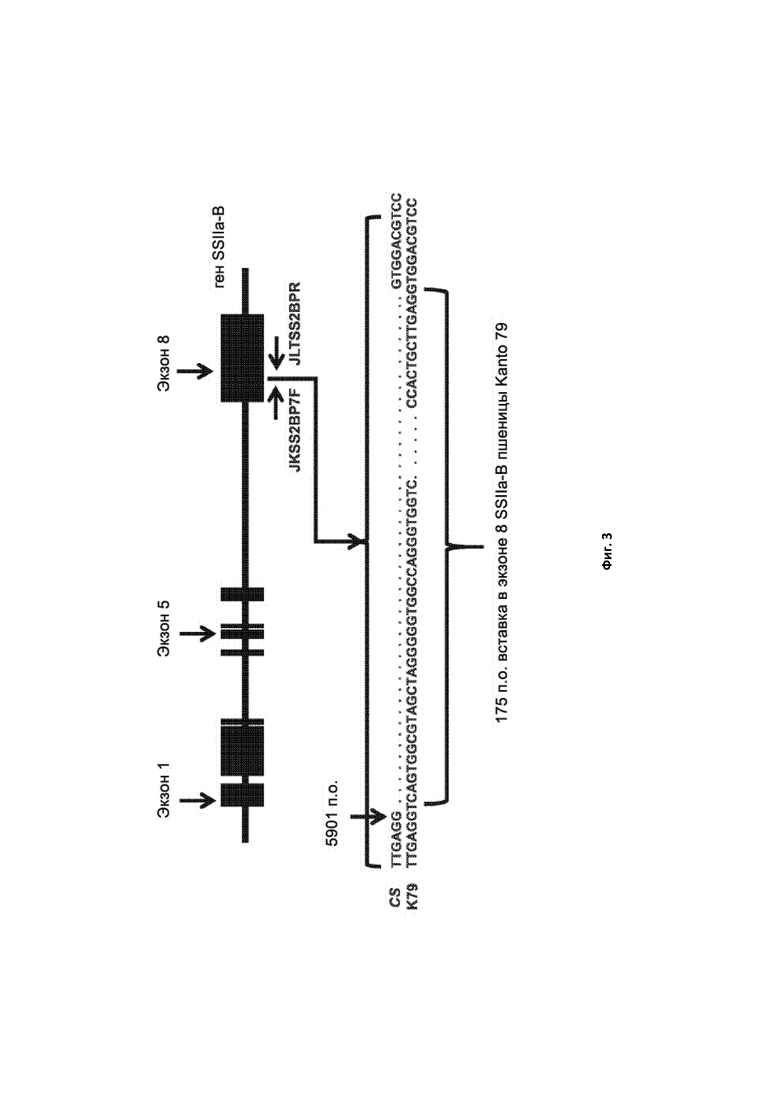
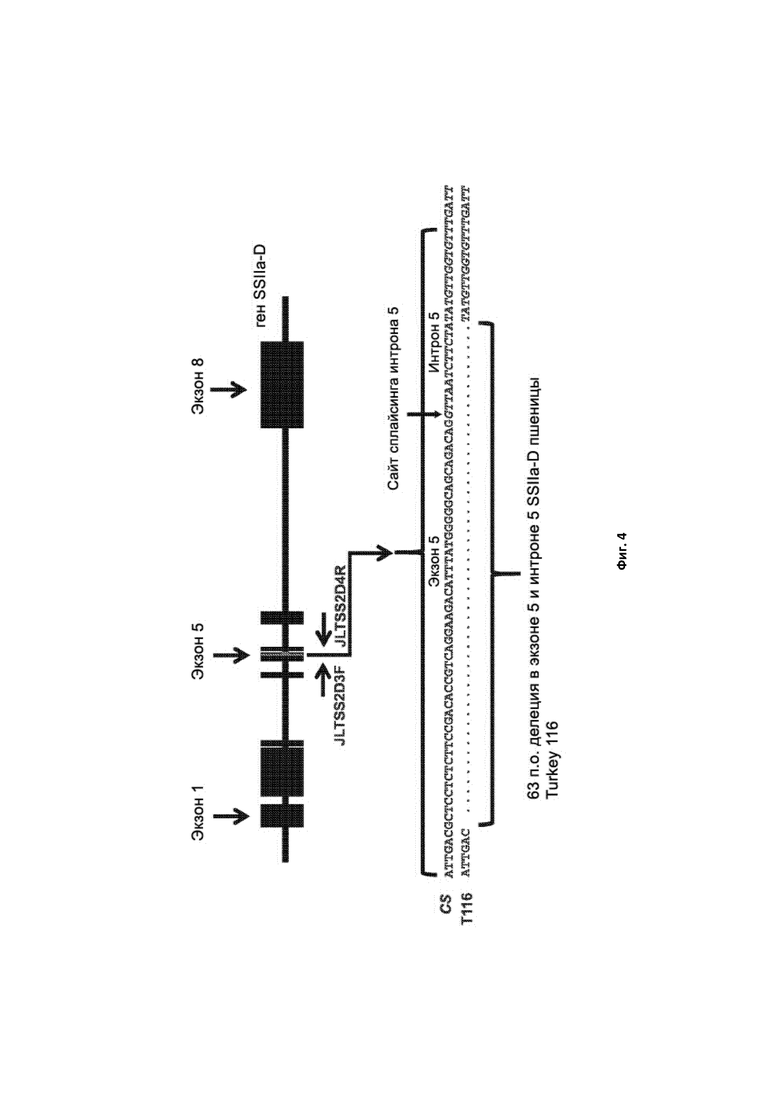
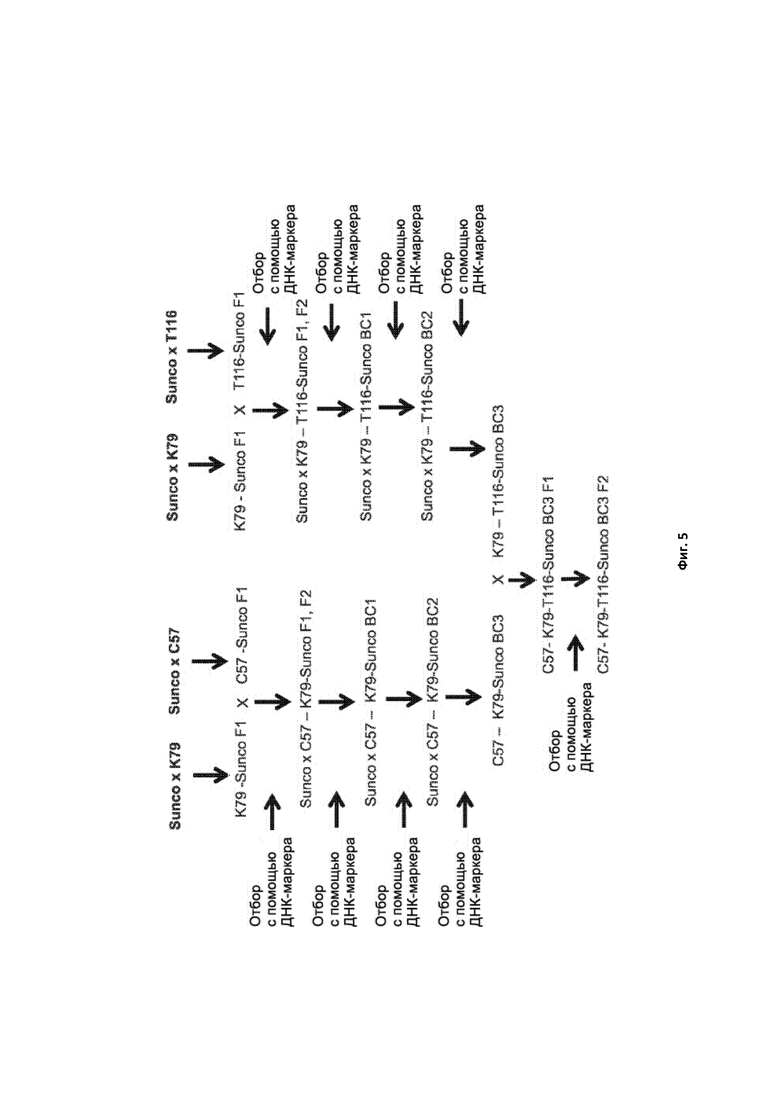

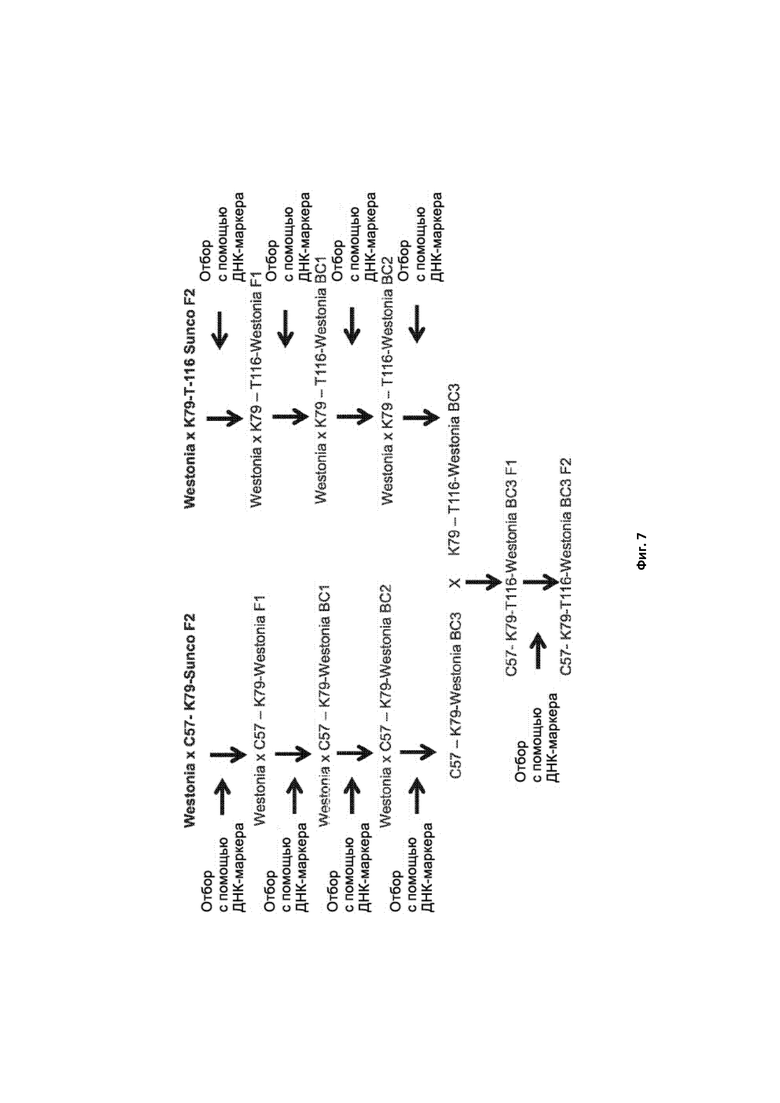

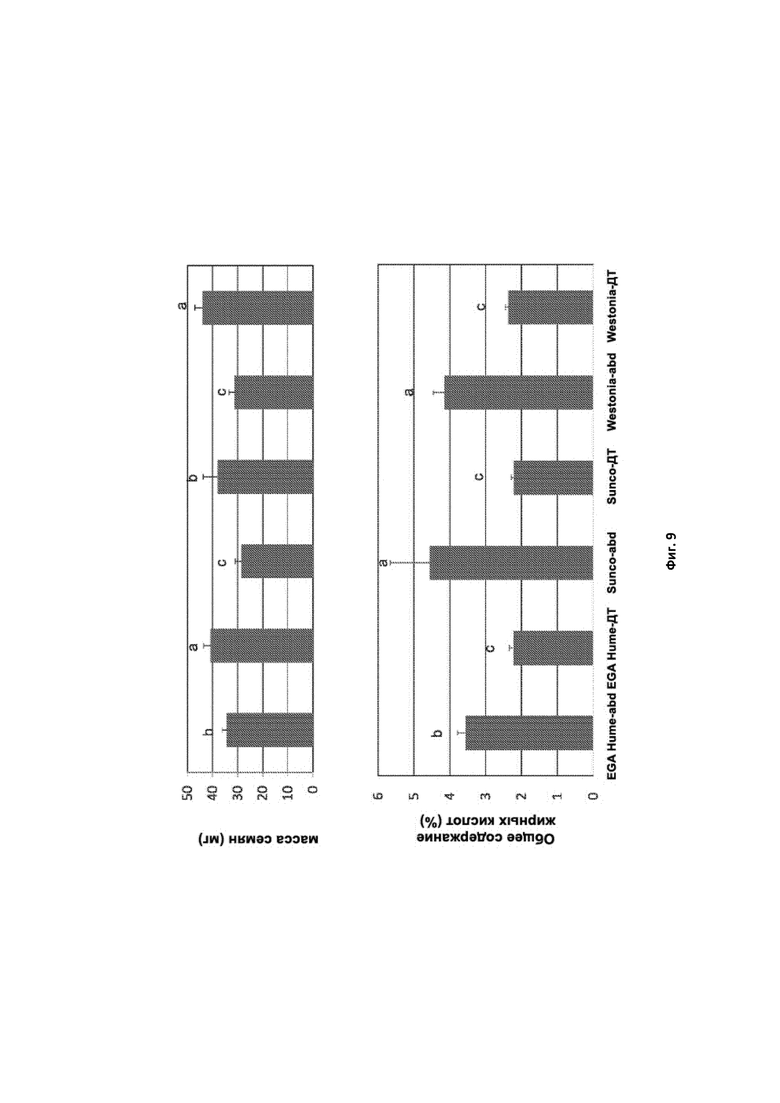



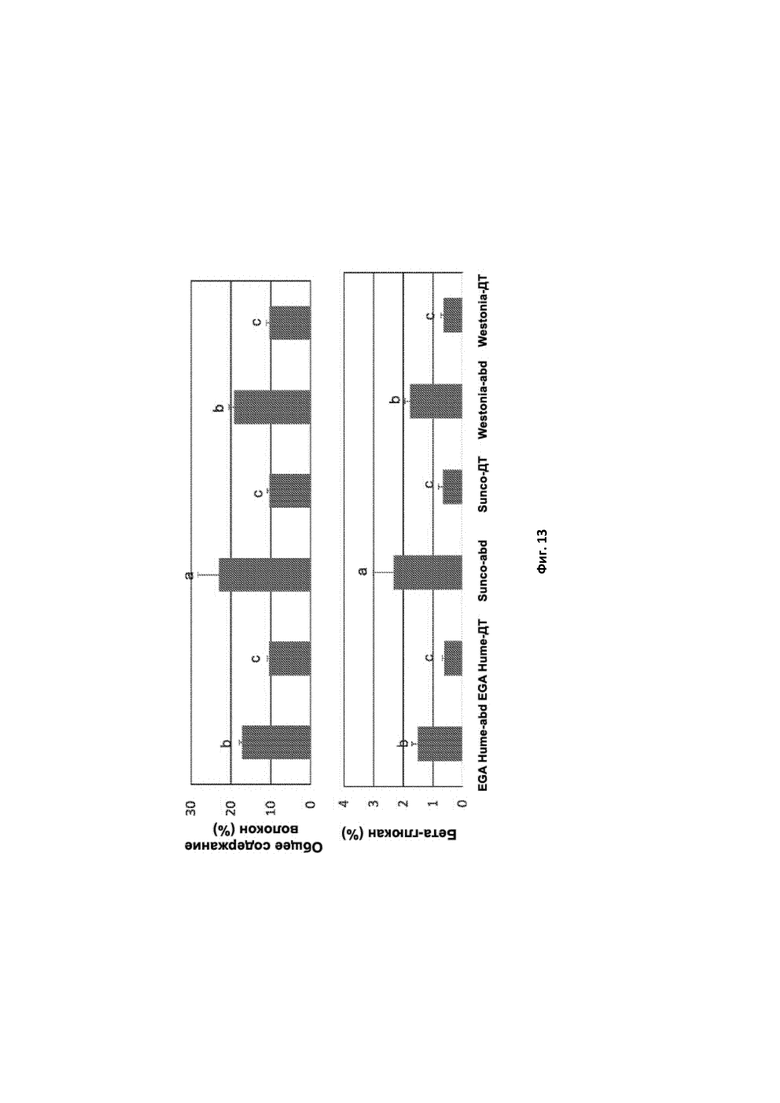


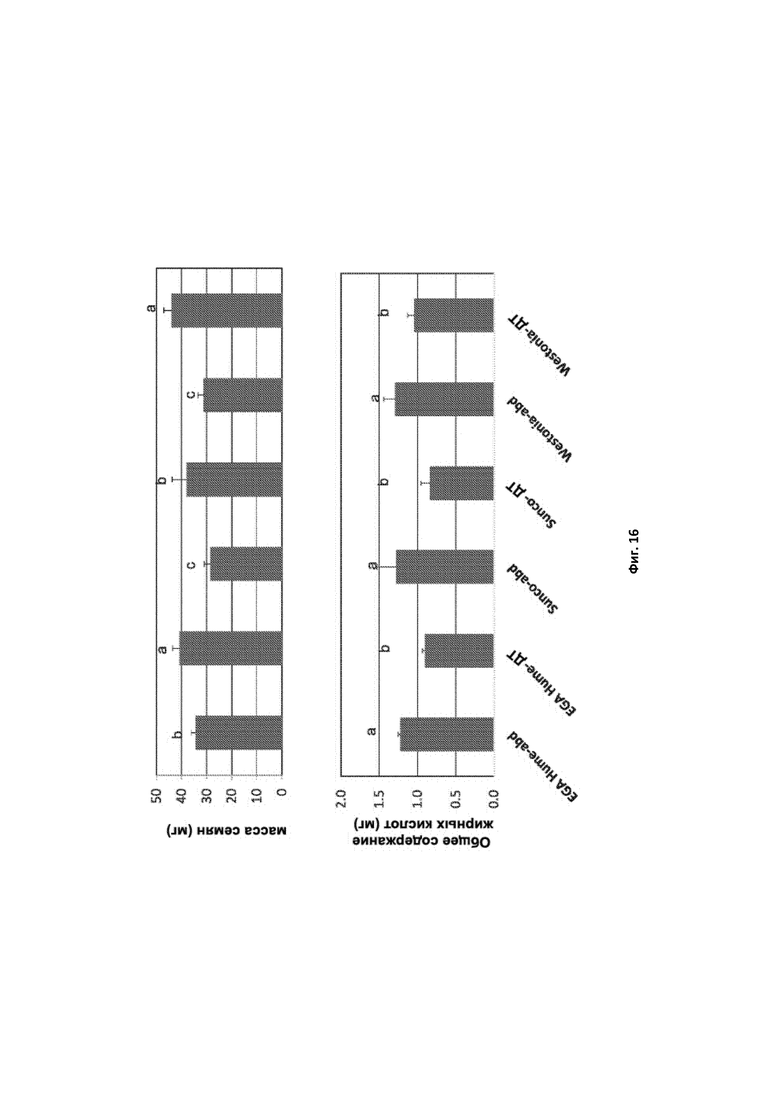

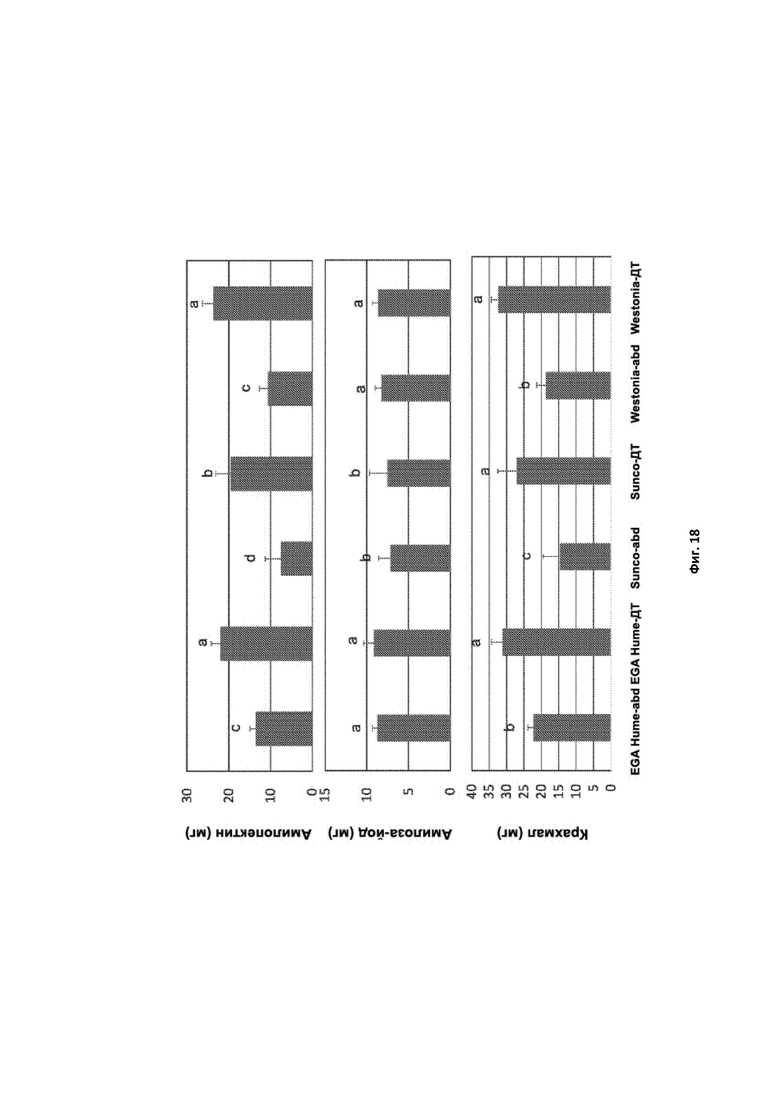

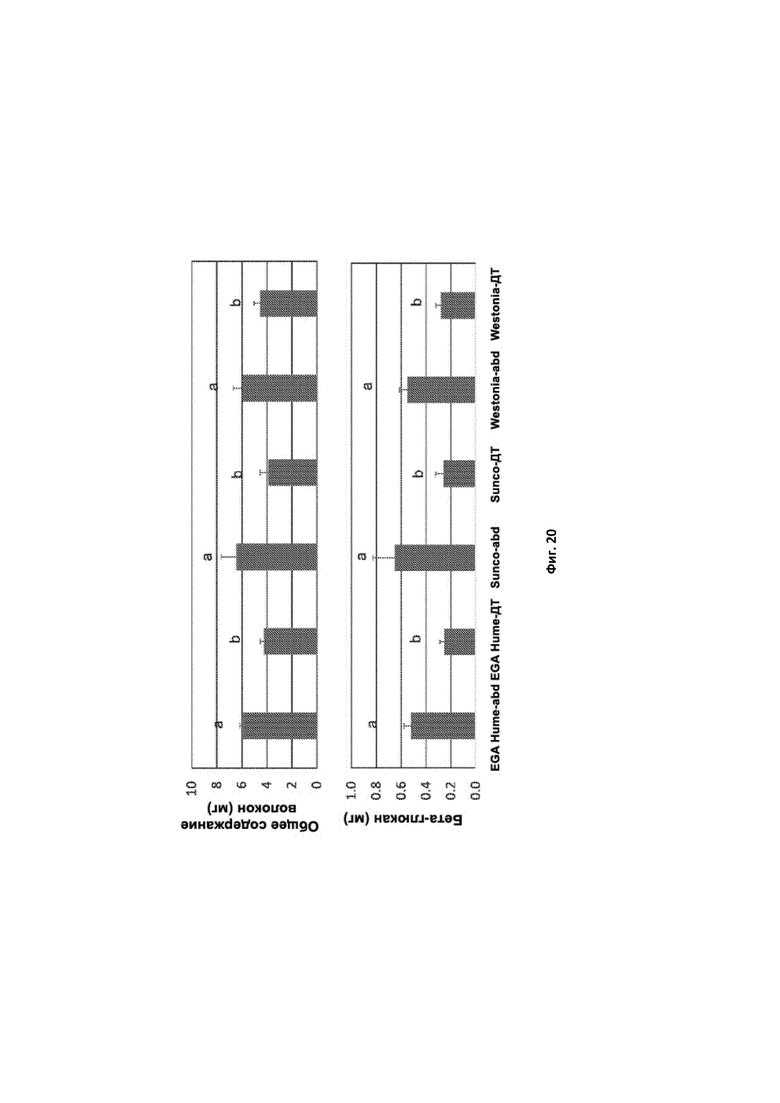

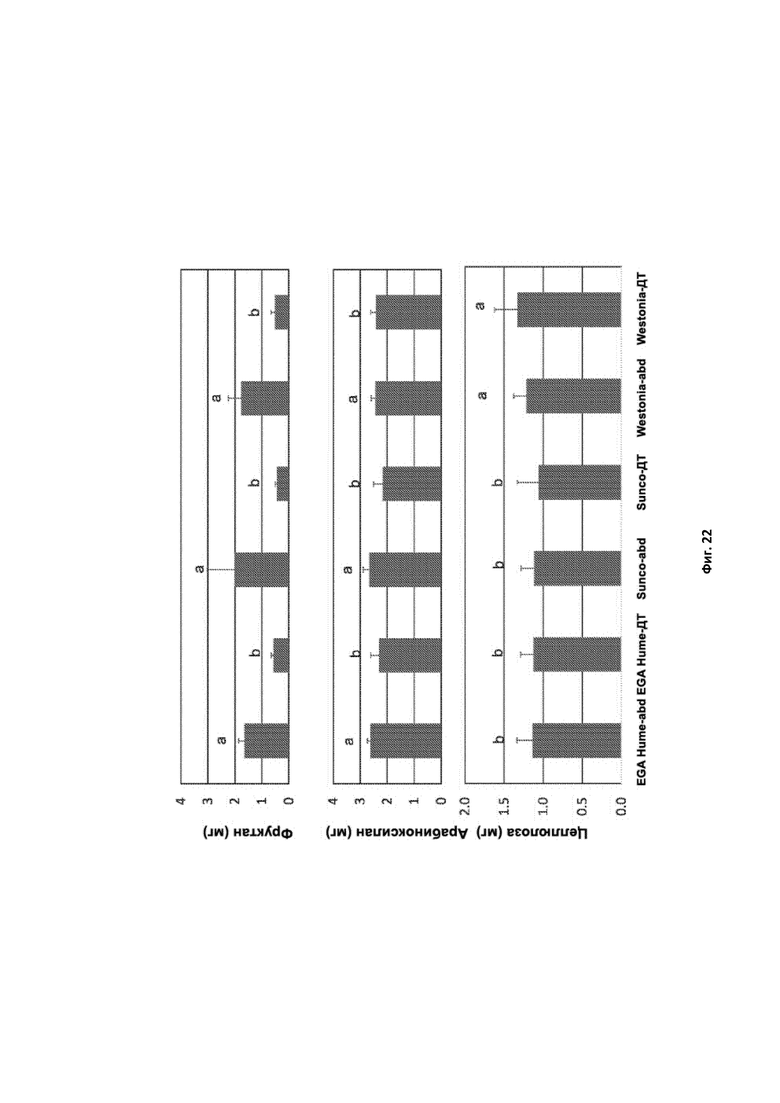
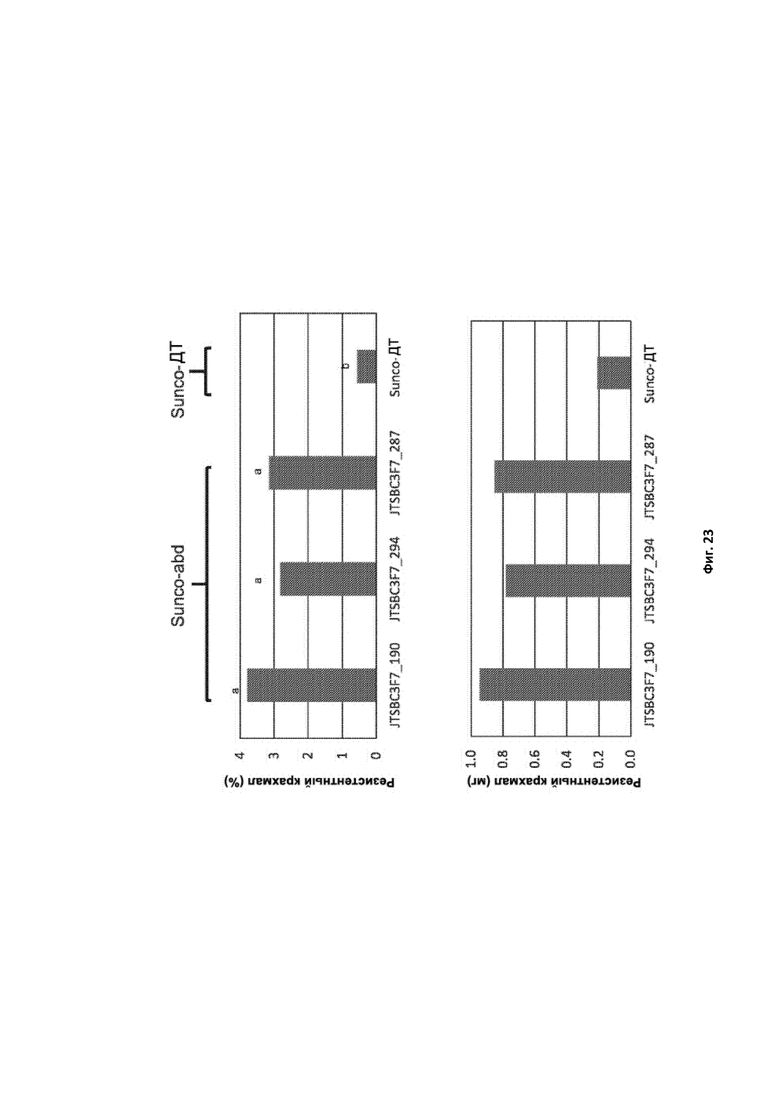
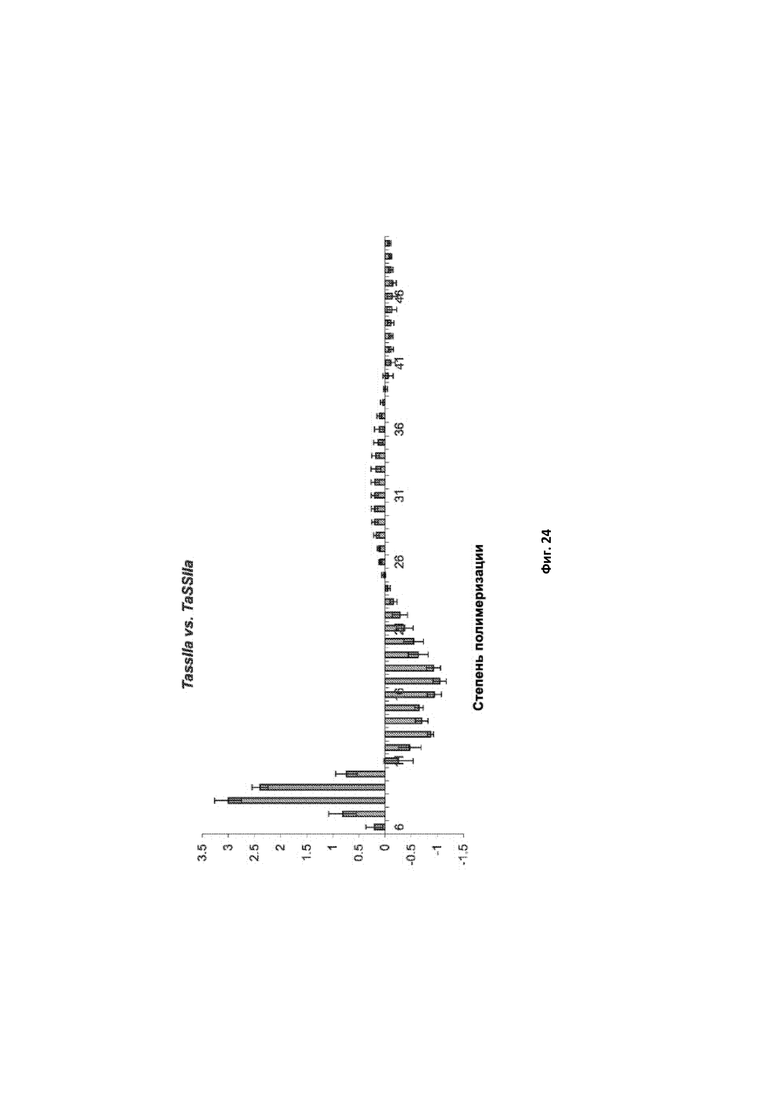
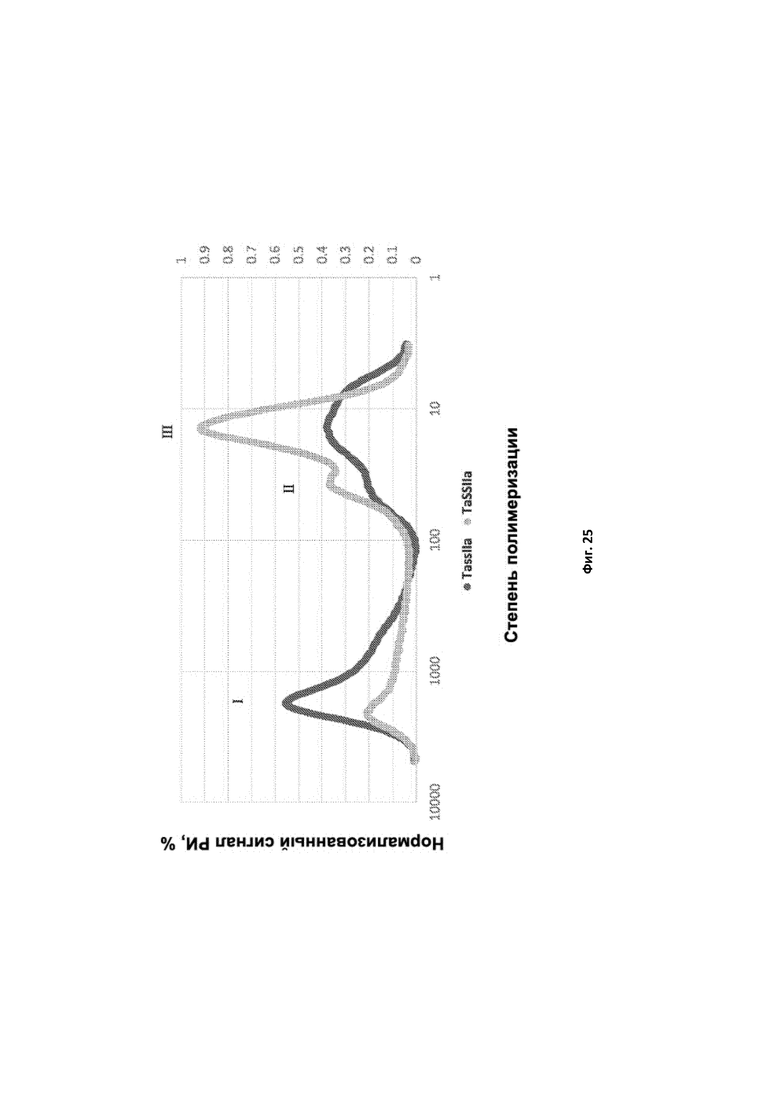
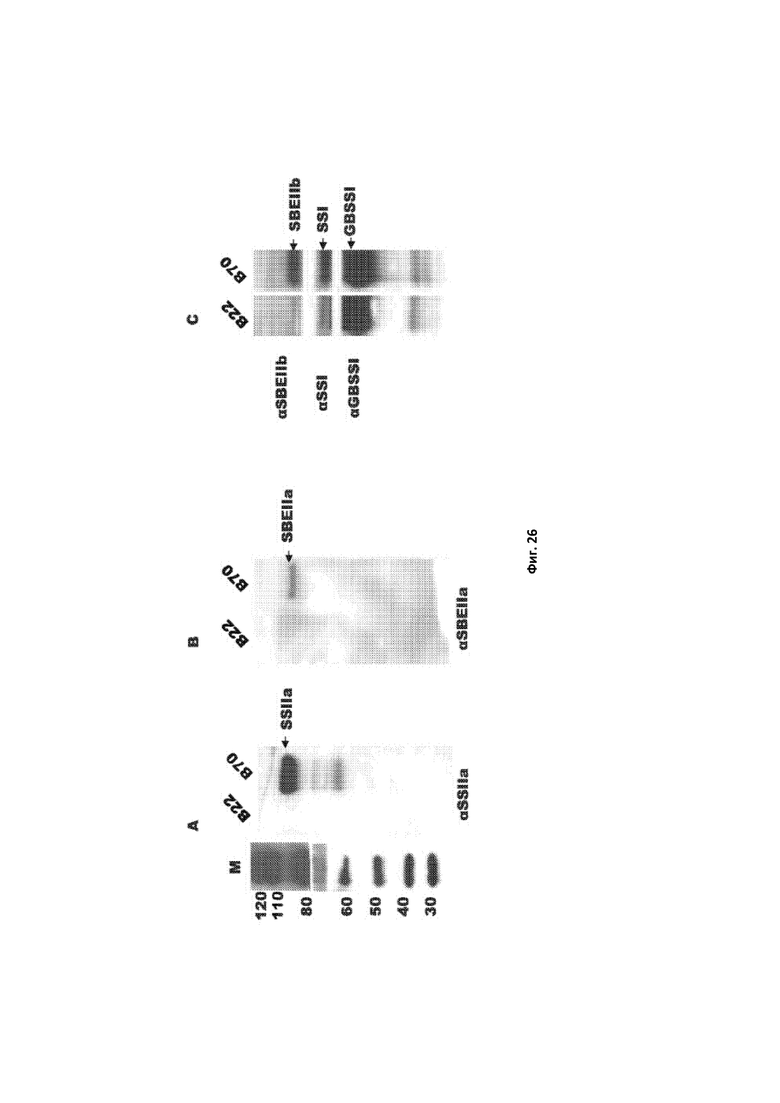
Изобретение относится к области биохимии, в частности к зерну пшеницы вида Triticum aestivum с повышенным содержанием амилозы, фруктана, β-глюкана, арабиноксилана и целлюлозы. Также раскрыты пищевой ингредиент и пищевой продукт, полученные из указанного зерна; композиция для получения указанного пищевого продукта или пищевого ингредиента. Раскрыты применение указанного зерна для получения муки; способ получения пшеницы; способ скрининга зерна пшеницы; способ получения пищевого продукта из указанного зерна; способ получения крахмала из указанного зерна. Изобретение позволяет эффективно получать зерно пшеницы вида Triticum aestivum с повышенным содержанием амилозы, фруктана, β-глюкана, арабиноксилана и целлюлозы по сравнению с зерном пшеницы дикого типа. 9 н. и 16 з.п. ф-лы, 26 ил., 9 табл., 12 пр.
1. Зерно пшеницы вида Triticum aestivum с повышенным содержанием амилозы, фруктана, β-глюкана, арабиноксилана и целлюлозы, содержащее
i) мутации в каждом из генов SSIIa, при этом зерно является гомозиготным в отношении мутации в гене SSIIa-A, гомозиготным в отношении нулевой мутации в гене SSIIa-B и гомозиготным в отношении нулевой мутации в гене SSIIa-D,
ii) общее содержание крахмала, включающее содержание амилозы и содержание амилопектина,
iii) содержание фруктана, которое повышено по сравнению с зерном пшеницы дикого типа в массовом отношении, предпочтительно от 3 до 12% массы зерна,
iv) содержание β-глюкана,
v) содержание арабиноксилана,
vi) содержание целлюлозы,
при этом зерно имеет массу зерновок от 25 до 60 мг, причем содержание амилозы составляет от 45 до 70% в массовом отношении от общего содержания крахмала зерна при определении анализом связывания йода, содержание амилопектина в массовом отношении снижено по сравнению с зерном пшеницы дикого типа, каждое из содержания β-глюкана, содержания арабиноксилана и содержания целлюлозы повышено по сравнению с зерном пшеницы дикого типа в массовом отношении так, что суммарное содержание фруктана, содержание β-глюкана, содержание арабиноксилана и содержание целлюлозы составляет от 15 до 30% массы зерна.
2. Зерно по п. 1, которое дополнительно характеризуется одним или более или всеми из следующих признаков:
i) содержание крахмала от 30 до 70% относительно массы зерна,
ii) содержание амилозы составляет от 45 до 65% по массе от общего содержания крахмала в зерне при определении анализом связывания йода,
iii) содержание крахмала имеет распределение по длинам цепей при определении методом капиллярного электрофореза с активацией флуоресценцией (FACE) после деветвления образцов крахмала, в котором увеличена доля длин цепей с СП (степенью полимеризации) 7-10 и снижена доля длин цепей с СП 11-24 по сравнению с крахмалом пшеницы дикого типа,
iv) содержание фруктана включает фруктан с СП 3-12 так, что по меньшей мере 50% содержания фруктана представлено СП 3-12,
v) содержание фруктана повышено в 2-10 раз по сравнению с зерном пшеницы дикого типа в массовом отношении,
vi) содержание β-глюкана и повышено на 1% или 2% по абсолютной величине и/или повышено в 2-7 раз по сравнению с зерном пшеницы дикого типа в массовом отношении,
vii) содержание β-глюкана составляет от 1 до 4% массы зерна,
viii) содержание арабиноксилана повышено на 1 – 5% по абсолютной величине,
ix) содержание целлюлозы повышено на 1 – 5% по абсолютной величине,
x) зерно имеет степень прорастания от около 70% до около 100% по сравнению с зерном пшеницы дикого типа,
xi) зерно при посеве дает растения пшеницы с мужской и женской фертильностью.
3. Зерно по п. 1 или 2, в котором отсутствует все из белка SSIIa-A, белка SSIIa-B и белка SSIIa-D.
4. Зерно по любому из пп. 1–3, в котором каждая нулевая мутация независимо выбрана из группы, состоящей из мутации с делецией, мутации со вставкой, стоп-кодона преждевременной терминации трансляции, мутации сайта сплайсинга и мутации с неконсервативной аминокислотной заменой, предпочтительно зерно при этом содержит мутации с делециями в каждом из двух или трех генов SSIIa.
5. Зерно по любому из пп. 1–4, которое дополнительно содержит мутацию с потерей функции в эндогенном гене, который кодирует полипептид синтеза крахмала, при этом указанный полипептид синтеза крахмала выбран из группы, состоящей из крахмальной синтазы I (SSI), крахмальной синтазы IIIa (SSIIIa) и крахмальной синтазы IV (SSIV), причем указанная мутация выбрана из группы, состоящей из мутации с делецией, мутации со вставкой, стоп-кодона преждевременной терминации трансляции, мутации сайта сплайсинга и мутации с неконсервативной аминокислотной заменой.
6. Зерно по любому из пп. 1–5, являющееся гомозиготным в отношении нулевой мутации в гене SSIIa-A, гомозиготным в отношении нулевой мутации в гене SSIIa-B и гомозиготным в отношении нулевой мутации в гене SSIIa-D.
7. Зерно по любому из пп. 1–6, в котором по меньшей мере одна мутация представляет собой i) внесенную мутацию, ii) была индуцирована в родительских растениях пшеницы или семенах посредством мутагенеза с помощью мутагенного агента, такого так химический агент, биологический агент или облучение, или iii) была внесена, чтобы модифицировать геном растения.
8. Зерно по любому из пп. 1–7, в котором содержание амилозы составляет около 60% по массе от общего содержания крахмала в зерне при определении анализом связывания йода.
9. Зерно по любому из пп. 1–8, в котором гранулы крахмала в зерне и/или крахмал в зерне характеризуются одним или более свойствами, выбранными из группы, состоящей из:
i) содержание по меньшей мере 2% резистентного крахмала;
ii) крахмал характеризуется сниженным гликемическим индексом (ГИ);
iii) гранулы крахмала имеют деформированную форму;
iv) гранулы крахмала имеют сниженное двулучепреломление при наблюдении в поляризованном свете;
v) крахмал характеризуется сниженным объемным разбуханием;
vi) модифицированные распределение по длинам цепей и/или частота ветвления в крахмале;
vii) крахмал характеризуется сниженной пиковой температурой желатинизации;
viii) крахмал характеризуется сниженной пиковой вязкостью;
ix) снижена температура клейстеризации крахмала;
x) снижена пиковая молекулярная масса амилозы при определении методом эксклюзионной хроматографии;
xi) снижена степень кристаллизации крахмала; и
xii) снижена доля крахмала A-типа и/или B-типа и/или повышена доля кристаллического крахмала V-типа;
при этом каждое свойство определяется в сравнении с гранулами крахмала пшеницы дикого типа или с крахмалом пшеницы дикого типа.
10. Зерно по любому из пп. 1–9, которое обработано таким образом, чтобы оно больше не было способно прорастать, например, как термически обработанное зерно или крупноразмолотое, дробленое, пропаренное, плющеное, рушенное, измельченное или молотое зерно.
11. Применение зерна по любому из пп. 1–10 для получения муки, которая предпочтительно представляет собой цельнозерновую муку или пшеничные отруби.
12. Применение зерна по любому из пп. 1–10 для получения гранул пшеничного крахмала.
13. Применение по п. 12, в котором гранулы пшеничного крахмала содержат от 45 до 70% амилозы по массе в виде доли от общего содержания крахмала гранул крахмала, причем гранулы крахмала предпочтительно содержат полипептид GBSSI пшеницы, и при этом гранулы крахмала характеризуются одним или более из:
i) отсутствие выявляемого полипептида SSIIa при определении иммунологическими способами;
ii) наличие деформированной формы; и
iii) наличие сниженного двулучепреломления при наблюдении в поляризованном свете;
при этом каждое свойство определяется в сравнении с гранулами крахмала пшеницы дикого типа.
14. Применение зерна по любому из пп. 1-10 для получения пшеничного крахмала.
15. Применение по п. 14, в котором пшеничный крахмал содержит от 45 до 70% амилозы по массе в виде доли от общего содержания крахмала гранул крахмала, причем гранулы крахмала предпочтительно содержат полипептид GBSSI пшеницы, и при этом гранулы крахмала характеризуются одним или более из:
i) отсутствие выявляемого полипептида SSIIa при определении иммунологическими способами;
ii) содержание по меньшей мере 2% резистентного крахмала в массовом отношении;
iii) сниженный гликемический индекс (ГИ);
iv) сниженное объемное разбухание;
v) модифицированное распределение по длинам цепей и/или частота ветвления;
vi) сниженная пиковая температура желатинизации;
vii) сниженная пиковая вязкость;
viii) сниженная температура клейстеризации крахмала;
ix) сниженная пиковая молекулярная масса амилозы при определении методом эксклюзионной хроматографии;
x) сниженная степень кристаллизации крахмала; и
xi) сниженная доля крахмала A-типа и/или B-типа и/или повышенная доля кристаллического крахмала V-типа;
при этом каждое свойство определяется в сравнении с крахмалом пшеницы дикого типа.
16. Пищевой ингредиент, который содержит зерно по любому из пп. 1–10 или муку, предпочтительно цельнозерновую, пшеничные отруби, гранулы пшеничного крахмала или пшеничный крахмал, полученные из зерна по любому из пп. 1-10, предпочтительно на уровне, составляющем по меньшей мере 10% на основании сухой массы.
17. Пищевой ингредиент по п.16, представляющий собой крупноразмолотое, дробленое, пропаренное, плющеное, рушенное, измельченное или молотое зерно или любую комбинацию этих вариантов.
18. Пищевой продукт, содержащий пищевой ингредиент на уровне, составляющем по меньшей мере 10% на основании сухой массы, при этом пищевой ингредиент представляет собой зерно пшеницы по любому из пп. 1–10 или муку, предпочтительно цельнозерновую, пшеничные отруби, гранулы пшеничного крахмала или пшеничный крахмал, полученные из зерна по любому из пп. 1-10.
19. Композиция для получения пищевого продукта или пищевого ингредиента с увеличенным содержанием амилозы, фруктана, β-глюкана, арабиноксилана и целлюлозы, содержащая зерно пшеницы по любому из пп. 1–10 или муку, предпочтительно цельнозерновую, пшеничные отруби, гранулы пшеничного крахмала или пшеничный крахмал, полученные из зерна по любому из пп. 1-10, на уровне, составляющем по меньшей мере 10% по массе, и зерно пшеницы, имеющее уровень амилозы менее 45% (масс./масс.), или полученные из него муку, цельнозерновую муку, гранулы крахмала или крахмал.
20. Способ получения растения пшеницы, которое дает зерно по любому из пп. 1–9, включающий этап (i) скрещивания двух родительских растений пшеницы, каждое из которых содержит нулевую мутацию в каждом из одного, двух или трех генов SSIIa, выбранных из группы, состоящей из SSIIa-A, SSIIa-B и SSIIa-D, или воздействие мутагенеза на родительское растение, содержащее указанные нулевые мутации; и этап (ii) скрининга растений или зерен, полученных при скрещивании или мутагенезе, или полученных от них дочерних растений или зерен с помощью анализа ДНК, РНК или белка, из растений или зерна, и этап (iii) отбора фертильного растения пшеницы, имеющего сниженную активность SSIIa по сравнению по меньшей мере с одним из родительских растений с этапа (i).
21. Способ скрининга зерна пшеницы или растения пшеницы, включающий (i) определение количества или активности SSIIa по сравнению с количеством или активностью в зерне пшеницы дикого типа или растении пшеницы дикого типа и отбор зерна или растения, которое дает зерно, по любому из пп. 1–9.
22. Способ получения пищевого продукта, включающий этапы (i) добавления пищевого ингредиента по п. 16 или 17 к другому пищевому ингредиенту и (ii) смешивания пищевых ингредиентов с получением, таким образом, пищевого продукта.
23. Способ по п. 22, который дополнительно включает этап обработки зерна по любому из пп. 1–10 для получения пищевого ингредиента перед этапом (i) или этап нагревания смешанных пищевых ингредиентов с этапа (ii) при температуре, составляющей по меньшей мере 100°C, в течение по меньшей мере 10 минут.
24. Пищевой продукт по п. 18 для применения для улучшения одного или более параметров метаболического здоровья, здоровья кишечника или здоровья сердечно-сосудистой системы или предотвращения или снижения тяжести или частоты случаев метаболического, кишечного или сердечно-сосудистого заболевания у субъекта.
25. Способ получения крахмала, включающий этапы i) получения зерна пшеницы по любому из пп. 1–10 и ii) выделения крахмала из зерна с получением, таким образом, крахмала.
| WO 2010006373 A1, 21.01.2010 | |||
| УСТОЙЧИВЫЕ К ГЕРБИЦИДАМ РАСТЕНИЯ ПОДСОЛНЕЧНИКА, ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ УСТОЙЧИВЫЕ К ГЕРБИЦИДАМ БЕЛКИ БОЛЬШОЙ СУБЪЕДИНИЦЫ АЦЕТОГИДРОКСИАЦИДСИНТАЗЫ, И СПОСОБЫ ПРИМЕНЕНИЯ | 2005 |
|
RU2415566C2 |
| WO 2005001098 A1, 12.10.2009. | |||
Авторы
Даты
2024-01-10—Публикация
2017-07-04—Подача