ОБЛАСТЬ ТЕХНИКИ
Заявленное изобретение относится к персонализированной медицине для онкологических заболеваний, а именно к системе обнаружения химерных продуктов генов во всех типах опухолевых образцов, основанной на анализе данных РНК-секвенирования, а именно детекции дисбаланса покрытия экзонов гена.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Химерные гены образуются в результате структурных изменений хромосом и являются характерной чертой генома раковых клеток. Такие изменения генома могут служить драйверными мутациями канцерогенеза, если в образовании химерного продукта принимает участие протоонкоген или ген-супрессор опухолевого роста. Особый интерес представляют химерные продукты, одним из партнеров которых является представитель генов рецепторных тирозинкиназ, в частности, ген ALK. Так, транслокации гена ALK - клинически значимый биомаркер (Hallberg, Palmer, 2013). Описано более 30 5'-генов-партнеров, которые объединяются с 3'-частью гена ALK (Hallberg, Palmer, 2013; Lovly et al., 2014). К опухолям, где детектированы химерные гены ALK, относятся крупноклеточная лимфома, диффузная крупноклеточная В-клеточная лимфома, глиома, немелкоклеточный рак легкого, колоректальный рак, рак молочной железы, яичников и пищевода (Hallberg, Palmer, 2013). Транслокации ALK не являются редкостью и обнаруживаются примерно в 8% случаев немелкоклеточного рака легкого (Kris et al., 2014).
Препараты Кризотиниб, церитиниб, алектиниб, бригатиниб и лоратиниб одобрены контролирующими инстанциями США для лечения немелкоклеточного рака легкого с химерным геном ALK. Ответ на терапию, ингибирующую ALK, также описан в исследованиях почечноклеточного рака и рака толстой кишки (Drilon et al., 2017).
Ввиду высокой значимости детекции транслокаций гена ALK для эффективного подбора противораковой терапии, было разработано несколько тестов для обнаружения данного биомаркера. «Классические» подходы основаны на методах ПЦР, флуоресцентной in situ гибридизации (FISH) или на иммуногистохимическом исследовании (ИГХ).
Предложен ряд способов анализа транслокаций ALK с геном-партнером EML4 с использованием специфических наборов праймеров, позволяющих амплифицировать исследуемый фрагмент и анализировать результаты с помощью полимеразной цепной реакции (ПЦР) в реальном времени, капиллярного электрофореза или гель-электрофореза в агарозном геле, а также детекции методом FISH (патентные заявки WO 2011087709, опубл. 21.07.2011; WO 2011095894, опубл. 11.08.2011, RU 2509153 C1, опубл. 10.03.2014). Также предложен метод детекции продуктов амплификации кДНК EML4-ALK с использованием флуоресцентной гибридизации с биочипами (патентная заявка WO 2010132888). Существенное ограничение всех предложенных методик - детекция ограничена наборами праймеров для ПЦР, то есть методы применимы для анализа только одного клинически значимого биомаркера: химерного гена ALK в паре с EML4.
Антитела для обнаружения транслокаций ALK Ventana ALK (D5F3) CDx Assay (Ventana Medical Systems, Tucson, AZ) методом ИГХ одобрены FDA США и зарегистрированы в РФ РУ № РЗН 2020/9786 от 25.03.2020. Стоит отметить, ИГХ детектирует уровень экспрессии целого белка ALK или его фрагментов, что служит лишь косвенным признаком наличия транслокации. Возможно, это является причиной частых несовпадений результатов анализа ИГХ с данными, полученными методами ПЦР или FISH (Mok T, Peters S, Camidge DR, et al. 2021).
Наиболее близким к заявляемому подходу является способ обнаружения химерных генов, основанный на детекции внутреннего дисбаланса экспресссии фрагментов генов методом амплификации в реальном времени 5' и 3'-частей гена (US 11021758 B2, опубл. 01.06.2021). При образовании химерных продуктов 5' и 3'-части гена оказываются под контролем разных геномных регуляторных элементов, что может приводить к повышению уровня транскрипции части гена, слитой с более сильным промотором. В частности, клинической значимостью при диагностике и выборе терапии онкологических заболеваний обладают химерные гены, образованные в результате слияния 3'-части потенциального протоонкогена с более сильным промотором. Поэтому авторы предлагают амплифицировать в реальном времени 5' и 3'-части гена (нетранслируемые области, UTR, untranslated region) набором разработанных праймеров и затем рассчитывать разницу экспрессии (IDE, Intragenic Differential Expression) по формуле:
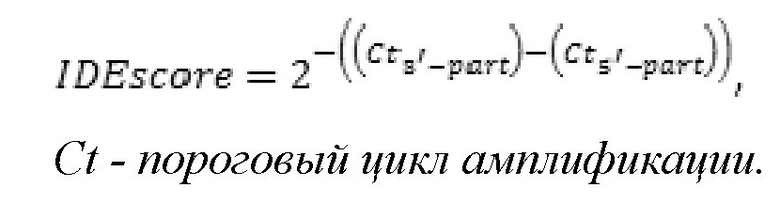
Превышение IDE порогового значения, определенного экспериментально, свидетельствует о значительной разнице в уровнях экспрессии 5' и 3'-частей гена и, следовательно, об образовании его химерных генов.
Описанный в патенте US 11021758 B2 метод обладает преимуществом, а именно возможностью детектировать все химерные продукты исследуемого гена, независимо от 5'-гена партнера и точного расположения точки химеризации. Однако этот метод не позволяет судить об экспрессии функционально значимой части гена ALK, кодирующей тирозинкиназный домен, поскольку детекция осуществляется заданным набором праймеров, специфичным к 3'-нетранслируемой области гена ALK. Описанный метод также не позволяет судить о транслокациях генов, отличных от ALK.
В настоящей заявке заявлен способ детекции транслокаций гена ALK в парафинизированных опухолевых образцах, основанный на анализе данных глубокого секвенирования тотальной мРНК. РНК-секвенирование не ограничено набором специфических праймеров и потенциально позволяет детектировать дисбаланс всех экспрессирующихся в образце генов. Также применение РНК-секвенирования позволяет объединить детекцию химерных генов ALK с определением других клинически значимых биомаркеров в одной экспериментальной процедуре.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
Техническим результатом данного изобретения является создание эффективного подхода к детекции структурных изменений гена ALK в раковых опухолях.
Описанный в настоящем изобретении подход заключается в анализе характера экспрессии гена ALK с целью детектировать дисбаланс экспрессии 5' и 3'-частей гена. Описанный в изобретении подход решает задачу детекции клинически значимого биомаркера - перестройки гена ALK, приведшей к его функциональному усилению, в различных типах опухолевых образцов, в том числе фиксированных в формалине парафинизированных образцах.
В качестве исходных данных представленный способ использует результаты транскриптомных исследований образцов клеток и тканей индивидуальных больных. В качестве биоматериала для исследования используются свежие, парафинизированные или законсервированные иным путем образцы опухолевой ткани или физиологических жидкостей, содержащих опухолевые клетки или фрагменты нуклеиновых кислот опухолевых клеток. Исследованием, предоставляющим исходные данные для способа, может быть транскриптомное профилирование: высокопроизводительное профилирование экспрессии генов на уровне РНК с использованием глубокого секвенирования тотальной мРНК.
На основе результатов транскриптомного профилирования, представленный способ детектирует дисбаланс экспрессии 5' и 3'-частей гена ALK, что свидетельствует о наличии в образце химерного продукта гена ALK.
Заявленный технический результат достигается посредством способа детекции транслокаций гена ALK в парафинизированных опухолевых образцах с помощью РНК-секвенирования путем оценки характера покрытия гена ALK прочтениями РНК-секвенирования, который состоит по меньшей мере из следующих этапов:
(а) получают образец ткани пациента, имеющей пролиферативный фенотип или образец физиологической жидкости, содержащей фрагменты нуклеиновых кислот опухолевых клеток;
(б) получают данные по экспрессии тотальной мРНК;
(в) получают данные из контрольной группы образцов ткани, не имеющей детектируемых химерных генов ALK, при этом контрольный образец получают из пролиферативной ткани того же типа, что и указанная ткань пациента, и тип данных, получаемых из контрольного образца, совпадает с типом данных, полученных на стадии (б);
(г) картируют прочтения РНК-секвенирования на экзоны гена ALK и нормализуют полученное число прочтений путем деления числа на длину соответствующего экзона и суммарное число прочтений в образце;
(д) сравнивают уровень покрытия экзонов 5' и 3'-частей гена ALK, при этом детекция статистически значимого различия - признак наличия химерного продукта гена ALK в образце: (i) применяют статистические тесты, например t-тест, для детекции значимой разницы покрытия 5' и 3'-частей гена ALK; (ii) проводят сравнение уровня покрытия экзонов 5' и 3'-частей гена ALK со средним уровнем покрытия соответствующих экзонов гена ALK контрольной группы.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
Сущность изобретения поясняется рисунками, на которых:
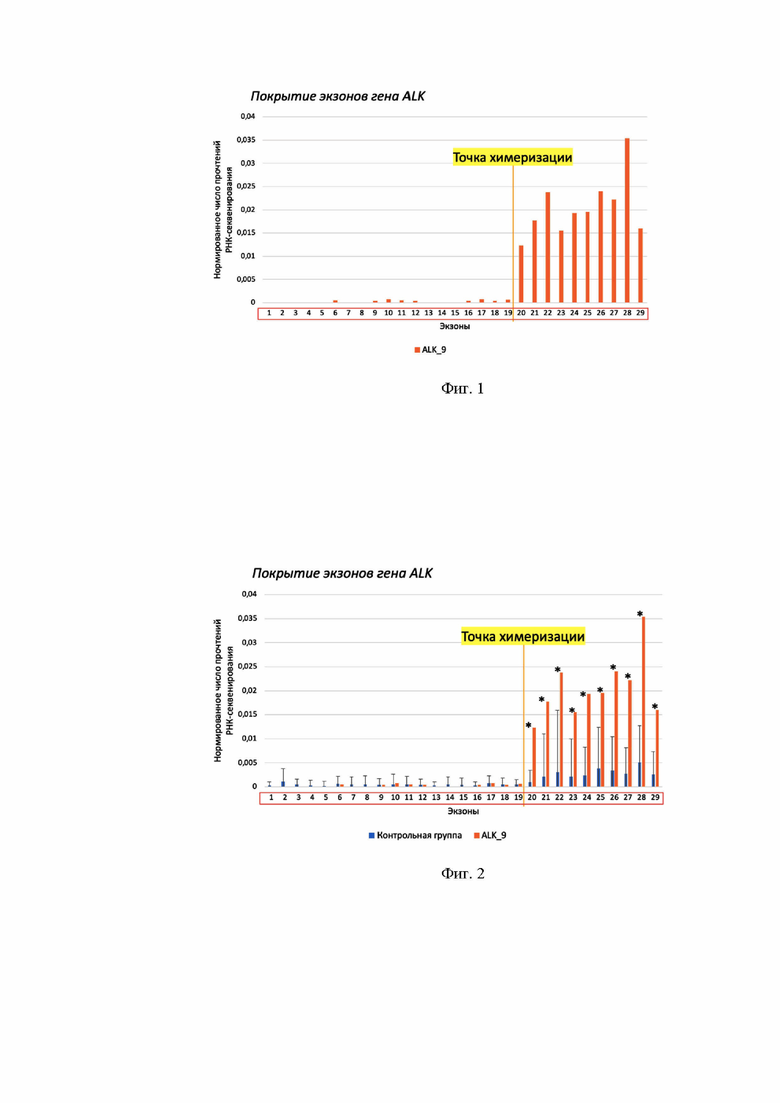
Фиг. 1. Диаграмма покрытия экзонов гена ALK прочтениями РНК-секвенирования в образце с химерным транскриптом ALK-9.
Фиг. 2. Диаграмма покрытия экзонов гена ALK в образце с химерным транскриптом ALK-9 и в образцах контрольной группы (среднее значение). * - превышение уровня покрытия экзона в образце ALK-9 95%-го процентиля уровня покрытия экзона контрольной группы.
Эти рисунки не охватывают и, кроме того, не ограничивают весь объем вариантов реализации данного технического решения, а представляют собой только иллюстративный материал частного случая его реализации.
ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее будет описан вариант выполнения способа детекции транслокаций гена ALK в парафинизированных опухолевых образцах с помощью РНК-секвенирования путем оценки характера покрытия гена ALK прочтениями РНК-секвенирования.
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Под «пациентом», следует понимать человека (предпочтительно) или другое млекопитающее. Под «тканью» пациента или субъекта следует понимать значение, принятое в медицинской литературе - это система клеток и межклеточного вещества, объединенных общим происхождением, строением и выполняемыми функциями. В описании данного изобретения это может быть кровь, твердая ткань различного происхождения (например, эпителиальная, соединительная, нервная или мышечная) или часть любого органа пациента или субъекта.
Под образцом ткани пациента, имеющим пролиферативный фенотип, понимают образец опухолевой ткани, клетки которой обладают способностью к неконтролируемому делению в результате патологического изменения (обычно в результате изменения генетического аппарата клеток). Такой образец может быть частью доброкачественной или злокачественной опухоли.
Под пролиферативным или онкологическим заболеванием понимают заболевание, характеризуемое патологическим изменением генетического аппарата клеток, приводящее к неконтролируемому делению определенной популяции клеток. Примерами пролиферативных заболеваний могут служить миелопролиферативные заболевания, лимфопролиферативные заболевания, пролиферативные заболевания соединительной ткани и другие заболевания.
Под данными по экспрессии тотальной мРНК следует понимать данные, показывающие абсолютное или относительное количество всех или более 300 видов молекул мРНК в образце.
Под “картированием прочтений” стоит понимать биоинформатический метод анализа результатов секвенирования, состоящий в определении позиций в референсном геноме, откуда с наибольшей вероятностью могло быть получено каждое конкретное прочтение.
Под “покрытием экзона” стоит понимать количество прочтений, которые частично или полностью картируются на некоторый участок экзона исследуемого гена.
Под “5'-частью” стоит понимать часть полинуклеотида (гена или транскрипта), расположенную ближе к 5'-концу полинуклеотида относительно 3'-части, но не обязательно включающую большую часть 5'-части гена. Применительно к химерным продуктам ALK и транслокациям “5'-часть” означает область, расположенную в направлении 5', то есть до точки химеризации/точки разрыва.
Под “3'-частью” стоит понимать часть полинуклеотида (гена или транскрипта), расположенную ближе к 3'-концу полинуклеотида относительно 5'-части, но не обязательно включающую большую часть 3'-части гена. Применительно к химерным продуктам ALK и транслокациям “3'-часть” означает область, расположенную в направлении 3', то есть после точки химеризации/точки разрыва.
При описании известных химерных генов ALK и их транскриптов “5'-часть” и “3'-часть” обозначают, как правило, регионы, расположенные по разные стороны от точки разрыва и являющиеся частями разных генов. При анализе неизвестных транскриптов следует предполагать, что точка химеризации максимально отдалена от 5'- и 3'-частей, чтобы охватить для анализа максимальное число потенциальных мест слияния. Такой подход позволяет включить в анализ как можно большее число потенциальных химерных продуктов ALK, которые могут возникнуть в любом месте между 5'- и 3'-частями.
Если не определено отдельно, технические и научные термины в данном описании имеют стандартные значения, общепринятые в научной и технической литературе.
Представленный подход решает задачу обнаружения химерных продуктов гена ALK в различных типах образцов пролиферативной ткани для более эффективного назначения противораковой терапии при помощи технологии, основанной на анализе дисбаланса покрытия экзонов генов прочтениями РНК-секвенирования.
В качестве образцов патологической ткани могут браться образцы свежей, парафинизированной или законсервированной иным способом ткани, либо образцы физиологических жидкостей пациента, содержащих фрагменты нуклеиновых кислот опухолевых клеток. В предпочтительном варианте осуществления изобретения анализ ткани производится у пациента с пролиферативным или онкологическим заболеванием ткани. Также для патологической ткани предпочтительно проводить анализ наиболее гистологически и цитологически гомогенного участка ткани пациента, имеющей пролиферативный фенотип. Для этого возможно проводить дополнительную очистку ткани, имеющей пролиферативный фенотип, от других окружающих ее тканей с помощью методов, известных специалистам.
Способ эффективен для анализа данных по экспрессии РНК генов в различных типах образцов.
Первой решаемой технической задачей (1) является картирование прочтений РНК-секвенирования на экзоны гена ALK исходя из полнотраскриптомных данных.
При этом первая техническая задача разделяется на ряд подзадач:
1.1. Получение транскриптомных данных для анализируемого образца.
1.2. Картирование прочтений на экзоны гена ALK и их нормализация.
Второй решаемой технической задачей (2) является анализ характера покрытия экзонов 5'- и 3'-частей гена ALK для детекции дисбаланса экспрессии.
Вторая техническая задача разделяется на следующие подзадачи:
2.1. Сравнение уровня покрытия экзонов 5'- и 3'-частей с помощью статистических методов, например, t-test.
2.2. Сравнение уровня покрытия отдельных экзонов со средним уровнем покрытия соответствующих экзонов в контрольной группе образцов (образцы того же типа пролиферативной ткани, в которых химерные продукты обнаружены не были) и детекция превышения 95% перцентиля покрытия экзонов 3'-части гена анализируемого образца.
Общая схема способа
В сравнении с существующим наиболее близким известным методом, представленное изобретение обладает рядом преимуществ. Во-первых, применение РНК-секвенирования позволяет анализировать характер экспрессии всех генов в образце, то есть потенциально возможно детектировать химерные продукты всех известных генов, в том числе ALK. В то время как анализ на основе ПЦР ограничен набором праймеров, комплиментарных к последовательностям конкретного гена или ограниченного набора генов. Во-вторых, способ РНК-секвенирования позволяет комбинировать определение различных биомаркеров в одной экспериментальной процедуре, что сокращает время анализа и подбора терапии. В-третьих, в отличие от алгоритмов, основанных на поиске химерных прочтений, представленный способ адаптирован для анализа в том числе парафинизированных материалов, степень деградации нуклеиновых кислот в которых повышена.
Анализ дисбаланса покрытия экзонов
Для детекции значимой разницы уровней экспрессии 5'- и 3'-частей гена ALK предложено два подхода:
1. Применение статистических тестов, например предлагается использовать t-тест, для сравнения уровня покрытия экзонов, составляющих 5'- и 3'-части гена ALK. Детекция в результате применения статистического критерия статистически значимого превышения уровня покрытия экзонов 3'-части над 5'-частью свидетельствует о дисбалансе экспрессии гена ALK и, следовательно, о наличии продуктов его перестройки в образце (фиг. 1). Данный подход не требует дополнительной информации о характере покрытия экзонов гена ALK в образцах контрольной группы без химерных продуктов, что позволяет применять его непосредственно для анализа любых полнотранскриптомных данных. Однако для применения данного подхода необходима предварительная информация об ожидаемом положении точки разрыва/химеризации для корректного объединения экзонов анализируемого гена в группы 5' и 3'-частей, то есть расположенных до и после точки химеризации. В настоящем изобретении указано, что в состав 3'-части гена ALK должен входить тирозинкиназный домен, картируемый экзонами 20-24. Кроме того, применение статистического t-теста невозможно для анализа химерных транскриптов, которые образованы в результате слияния первого экзона 3'-гена с экзонами 5'-партнера, а также второго экзона, поскольку в этом случае только один экзон оказывается расположен до точки химеризации и применение статистических тестов для детекции значимой разницы покрытия экзонов до/после точки химеризации невозможно.
2. Детекция экзонов ALK, превышающих 95% процентиль уровня покрытия соответствующих экзонов в образцах того же типа пролиферативной ткани, в которых химерных продуктов не обнаружено (фиг. 2). Данный подход основан на сравнении уровня покрытия каждого экзона со средним уровнем покрытия соответствующего экзона в контрольной группе. Если покрытие большинства экзонов 5'-части гена ALK значимо превышает средний уровень покрытия контрольной группы и в то же время уровень покрытия экзонов 3'-части гена ALK значимо не превышают средний уровень покрытия соответствующих экзонов контрольной группы, то следует сделать вывод о наличии в образце химерного продукта с 5'-частью гена ALK. Преимущество данного подхода - отсутствие необходимости в предварительно оценки положения точки химеризации, при этом разделение гена ALK на 5'- и 3'-части может быть основано на знании о клинической значимости химерных продуктов. Например, важным является критерий включения в химерных продукт, т.е. в 5'-часть, экзонов, кодирующих тирозинкиназный домен (экзоны 20-24 для гена ALK). Ограничение описываемого способа - необходимость в группе сравнения, то есть в транскриптомных данных, полученных и обработанных тем же способом, что и исследуемые данные, для группы образцов того же типа заболевания без химерных продуктов гена ALK.
Нижеследующие примеры работы способа приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример 1. Детекция дисбаланса покрытия экзонов гена ALK в образце рака легкого статистическим тестом.
Фиксированный в формалине парафинизированный образец рака легкого ALK-9 с подтвержденным в клинической лаборатории химерным геном EML4-ALK был получен для валидации представленного способа. Сначала была выделена тотальная РНК и проведено полнотраскриптомное секвенирование. Для удаления рРНК и приготовления библиотек использовали KAPA RNA HyperPrep Kit with RiboErase (HMR) (Roche Sequencing, США). Различные адаптеры KAPA UDI Primer Mix (Roche Sequencing, США) использовались для объединения образцов в одном запуске. Секвенирование проводили на приборе Illumina NextSeq 550 в режиме прочтения с одного конца, длина прочтения 50 пар оснований, расчетная глубина 30 миллионов «сырых» прочтений на образец. Качество запуска анализировалось программным обеспечением Illumina SAV. Для демультиплексирования использовали программу Illumina Bcl2fastq2 v2.17.
Для образца было получено 9490295 уникально картированных прочтений. Для расчета уровня покрытия экзонов использовали пакет программного обеспечения BEDtools multicov с параметрами «по умолчанию». В качестве входных файлов были BAM (Binary Alignment/Map) файл результатов РНК-секвенирования соответствующего образца и BED (Browser Extensible Data) файл, содержащий координаты экзонов транскрипта гена ALK ENST00000389048.8, входящего в проект MANE (Matched Annotation between NCBI and EBI). Полученные значения числа прочтений нормировали на длину соответствующего экзона и глубину секвенирования образца.
Получили картину распределения прочтений (фиг. 1). Обнаружена значимая разница уровней покрытия 5' и 3'-частей гена ALK, которая подтверждается статистическим тестом: t-test, p-value = 3*10-6. В область экзонов с амплифицированным сигналом попадают также и экзоны 20-24, кодирующие тирозинкиназный домен ALK. По итогам анализа сделан вывод о наличии перестройки гена ALK в исследованном образце.
Пример 2. Детекция дисбаланса покрытия экзонов гена ALK в образце рака легкого путем сравнения с покрытием экзонов контрольной группы.
Для исследуемого образца анализировали нормализованные данные покрытия экзонов гена ALK, полученные в примере 1. Группа сравнения - контрольная группа, содержащая 53 образца рака легкого, в которых не детектировано химерных транскриптов и для которых получены и нормированы транскриптомные данные, согласно описанию из примера 1. Затем сравнивали уровень покрытия каждого экзона гена ALK в исследуемом образце с 95-й перцентилью уровня покрытия соответствующего экзона в образцах контрольной группы.
Неравномерная экспрессия экзонов гена ALK, свидетельствующая о наличии химерного продукта, подтверждается: в то время как уровень покрытия экзонов 5'-части (т.е. расположенных до точки химеризации) не превышает 95% перцентиль, 10 из 10 экзонов 3'-части превышают эту границу. В область экзонов с амплифицированным сигналом попадают также и экзоны 20-24, кодирующие тирозинкиназный домен ALK. По итогам анализа сделан вывод о наличии перестройки гена ALK в исследованном образце.
Таким образом, применение обоих предложенных критериев позволяет детектировать химерные гены ALK в опухолевых образцах без предварительного знания о втором гене-партнере химерного продукта или точном положении точки химеризации.
При использовании изобретения достигается следующий технический результат: разработан новый, эффективный способ детекции химерных генов ALK в различных типах опухолевых образцов, включая фиксированные в формалине парафинизированные ткани. Данный способ может быть автоматизирован, что предотвращает потенциальные ошибки, связанные с ручным расчетом, и позволяет потенциально обнаружить продукты всех экспрессируемых в образце химерных генов ALK.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Настоящее изобретение предназначено для использования в персонализированной онкологии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДЕТЕКЦИИ ТРАНСЛОКАЦИЙ ГЕНОВ ТИРОЗИНКИНАЗНЫХ РЕЦЕПТОРОВ В ОБРАЗЦАХ ОПУХОЛЕВОЙ ТКАНИ С ИСПОЛЬЗОВАНИЕМ ДАННЫХ РНК-СЕКВЕНИРОВАНИЯ | 2023 |
|
RU2814710C1 |
| СПОСОБ ОЦЕНКИ СТАТУСА 14-ГО ЭКЗОНА ГЕНА MET ПО ДАННЫМ РНК СЕКВЕНИРОВАНИЯ | 2023 |
|
RU2817869C1 |
| Способ выявления химерного транскрипта DNAJB1-PRKACA в клинических образцах ткани пациентов с фиброламеллярной карциномой печени методом полимеразной цепной реакции в реальном времени | 2023 |
|
RU2807306C1 |
| Способ создания таргетной панели для исследования геномных регионов для выявления терапевтических биомаркеров ингибиторов иммунных контрольных точек (ИКТ) | 2023 |
|
RU2818360C1 |
| Способ выявления химерных транскриптов гена EWSR1, ассоциированных с саркомой Юинга | 2021 |
|
RU2759810C1 |
| ИНДИВИДУАЛИЗИРОВАННЫЕ ПРОТИВООПУХОЛЕВЫЕ ВАКЦИНЫ | 2012 |
|
RU2670745C9 |
| ИНДИВИДУАЛИЗИРОВАННЫЕ ПРОТИВООПУХОЛЕВЫЕ ВАКЦИНЫ | 2012 |
|
RU2779946C2 |
| Набор реактивов для оценки эффективности терапии ингибиторами тирозинкиназы при Ph-позитивных новообразованиях и способ его использования | 2020 |
|
RU2762356C2 |
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2330285C1 |
| ОПРЕДЕЛЕНИЕ СНИЖЕНИЯ УРОВНЯ мРНК ГЕНА ZG16 КАК СПОСОБ ДИАГНОСТИКИ РАКА ТОЛСТОЙ КИШКИ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2395234C1 |
Заявленное изобретение относится к персонализированной медицине для онкологических заболеваний, а именно к системе обнаружения химерных продуктов генов во всех типах опухолевых образцов, основанной на анализе данных РНК-секвенирования, а именно детекции дисбаланса покрытия экзонов гена. Изобретение описывает способ, позволяющий детектировать продукты экспрессии химерных генов ALK в широком спектре образцов патологических тканей пациентов на основе данных об экспрессии РНК. Способ основан на анализе характера экспрессии экзонов гена ALK и поиске дисбаланса покрытия экзонов, свидетельствующем о наличии структурной перестройки гена ALK. Подход основан на анализе полнотранскриптомных данных, что потенциально позволяет обнаружить химерные продукты также и других экспрессируемых в образце генов. Кроме того, данный способ может быть автоматизирован, что предотвращает потенциальные ошибки, связанные с ручным расчетом, и позволяет учитывать структурные перестройки, характерные для конкретного пациента, в сотнях и тысячах экспрессируемых генов. Применение данного способа позволит эффективно и точно детектировать химерные транскрипты ALK во всех типах опухолевых образцов, включая фиксированные в формалине парафинизированные образцы, степень деградации нуклеиновых кислот в которых повышена. Применение представленного подхода для быстрого и эффективного обнаружения потенциально всех клинически значимых химерных генов ALK повысит эффективность подбора противораковой терапии. 2 ил.
Способ детекции транслокаций гена ALK в парафинизированных опухолевых образцах с помощью РНК-секвенирования путем оценки характера покрытия гена ALK прочтениями РНК-секвенирования, состоящий по меньшей мере из следующих этапов:
(а) получают образец ткани пациента, имеющей пролиферативный фенотип или образец физиологической жидкости, содержащей фрагменты нуклеиновых кислот опухолевых клеток;
(б) получают данные по экспрессии тотальной мРНК;
(в) получают данные из контрольной группы образцов ткани, не имеющей детектируемых химерных генов ALK, при этом контрольный образец получают из пролиферативной ткани того же типа, что и указанная ткань пациента, и тип данных, получаемых из контрольного образца, совпадает с типом данных, полученных на стадии (б);
(г) картируют прочтения РНК-секвенирования на экзоны гена ALK и нормализуют полученное число прочтений путем деления числа на длину соответствующего экзона и суммарное число прочтений в образце;
(д) сравнивают уровень покрытия экзонов 5’ и 3’-частей гена ALK, детекция значимой разницы - признак наличия химерного продукта анализируемого гена в образце: (i) применяют статистические тесты, например t-тест, для детекции статистически значимой разницы покрытия 5’ и 3’-частей гена ALK; (ii) сравнение уровня покрытия экзонов 5’ и 3’-частей гена ALK со средним уровнем покрытия соответствующих экзонов гена ALK контрольной группы.
| RU 2020100096 A, 12.07.2021 | |||
| WO 2019231259 A1, 05.12.2019 | |||
| RU 2020142821 A, 12.07.2022. |
Авторы
Даты
2024-01-30—Публикация
2023-09-03—Подача