ОБЛАСТЬ ТЕХНИКИ
Заявленное изобретение относится к персонализированной медицине для онкологических заболеваний, а именно к способу поддержки принятия клинических решений с использованием анализа данных РНК секвенирования, основанного на детекции прочтений, картированных на стыки экзонов и асимметрии покрытия прочтениями гена MET.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Известны различные способы поддержки принятия клинических решений с использованием анализа данных РНК секвенирования на основе анализа транскриптов гена MET, например способ идентификации больного раком, который, вероятно, ответит на лечение антагонистом продукта гена MET (см. US2012089541A1, опубл.12.04.2012), включающий стадию определения уровня экспрессии C-MET. При высоком уровне этого биомаркера делается вывод, что пациент, вероятно, ответит на лечение антагонистом продукта этого гена.
На сегодняшний день наиболее надежным и не требующим дополнительных манипуляций с биологическим материалом способом оценки статуса 14-го экзона MET является способ, основанный на детекции прочтений, картированных на стыки экзонов и асимметрии покрытия прочтениями гена MET.
Делеция 14-го экзона в транскрипте гена MET может привести к онкотрансформации клетки по нескольким механизмам. Такая изоформа встречается приблизительно в 3% всех опухолей пациентов, страдающих немелкоклеточным раком легкого. В 2020 году были одобрены для клинического применения два препарата-конкуренты аденозинтрифосфата (АТФ), специфично ингибирующие MET с пропуском 14-го экзона капматиниб (capmatinib) и тепотиниб (tepotinib). Эффективность этих препаратов для лечения немелкоклеточного рака легкого с пропуском 14-го экзона MET была доказана в ходе клинических испытаний, и они были одобрены для лечения данной патологии в нескольких странах. [https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8290191/].
Поэтому для эффективной терапии этими и другими препаратами, специфично воздействующими на MET с пропуском 14-го экзона, необходимо корректно детектировать эту изоформу.
Существуют несколько методов детекции данной изоформы, а именно: основанная на секвенировании ДНК диагностическая платформа Illumina TruSight Tumor 26 assay [https://support.illumina.com/downloads/trusight_tumor_product_files.html], основанная на секвенировании РНК ArcherDx FusionPlex Solid Tumor assay [https://archerdx.com/research-products/solid-tumor-research/fusionplex-solid-tumor/] и система, основанная на ПЦР в реальном времени (см. US20170327887A1, опубл. 16.11.2017), выбранная заявителем в качестве наиболее близкого аналога. Все эти методики направлены на оценку мутационного статуса лишь малого числа геномных локусов, в число которых входит и ген MET, и уступают в количестве получаемой информации РНК-секвенированию опухолевого материала [https://www.sciencedirect.com/science/article/pii/S1556086419300073].
Соответственно, используя вышеупомянутые методы, невозможно одновременно оценить статус MET и уровень экспрессии большинства других генов - проведение процедуры РНК-секвенирования необходимо будет осуществлять отдельно, что, в частности, необходимо для работы систем персонализированной медицины, таких как Онкобокс [doi: 10.1007/978-1-0716-0138-9_17].
Предлагаемый способ является простым и надежным методом выявления пропуска 14-го экзона гена MET по данным РНК-секвенирования.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
Техническим результатом данного изобретения является улучшение детекции пропуска 14го экзона гена MET на основе данных РНК секвенирования. Изобретение призвано улучшить системы персонализированной медицины путем внедрения возможности детекции пропуска 14го экзона гена MET непосредственно по данным профилей тотального РНК-секвенирования библиотек опухолевых тканей.
Заявленный технический результат достигается посредством способа оценки выявления статуса 14 экзона гена MET по данным РНК секвенирования, который состоит по меньшей мере из следующих шагов:
а) получения биологического материала (образец ткани пациента или его физиологические жидкости), пригодного для РНК секвенирования;
б) получения данных РНК секвенирования из материала пункта (а);
в) получения из данных пункта (б) данных о картировании прочтений на экзоны гена MET человека, в том числе о картировании на стыки экзонов;
г) подсчета количества SJ прочтений, приходящихся на стык 13 и 15 экзонов и прошедших контроль качества, и сравнение его с выбранным порогом;
д) подсчета нормированного уровня асимметрии покрытия 13, 14 и 15-го экзонов, и сравнение его с выбранным порогом, абсолютное значение которого должно быть достаточно большим, для заключения о том, что 14-й экзон был пропущен;
е) анализа результатов пунктов (в) и (г), при котором при преодолении всех выбранных порогов, описанных в пунктах (в) и (г), делается вывод о наличии в образце гена MET с пропуском 14-го экзона.
В предпочтительном варианте выполнения при преодолении только одного из порогов (либо в пункте (в), либо в пункте (г)) биологический материал, из которого были получены данные РНК секвенирования, подвергается дополнительной проверке, позволяющей оценить статус 14-го экзона гена MET в этом биологическом материале. Если пороги пунктов (в) и (г) не были преодолены, делается вывод о том, что в образце нет транскриптов, соответствующих гену MET без 14-го экзона.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
Сущность изобретения поясняется рисунками, на которых;
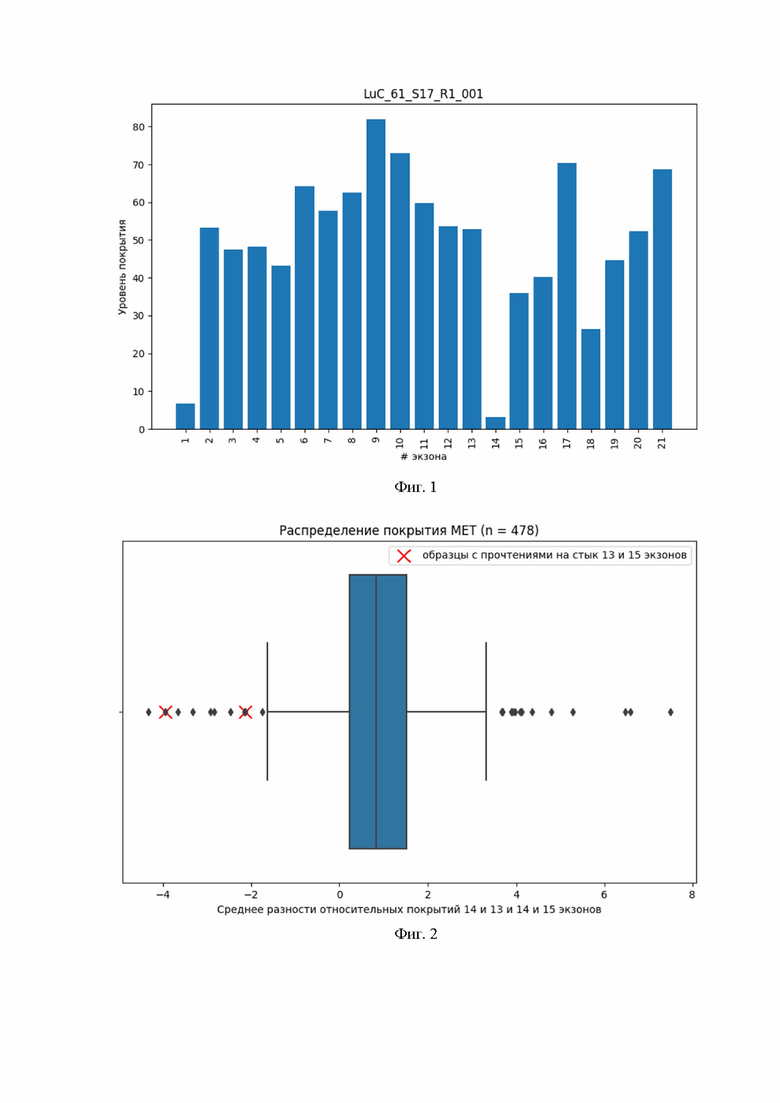
Фиг. 1. Визуализация уровня покрытия, полученная при обработке данных РНК секвенирования опухоли с экспрессией гена MET c пропущенным 14 экзоном (можно заметить низкую степень покрытия 14-го экзона по сравнению с соседними с ним экзонами)
Фиг. 2. Диаграмма размаха, показывающая распределение нормированных на длину средних разностей 14 и 13 и 14 и 15 экзонов. Красным отмечены образцы с прочтениями, приходящимися на стык 13 и 15 экзонов.
Эти рисунки не охватывают и, кроме того, не ограничивают весь объем вариантов реализации данного технического решения, а представляют собой только иллюстративный материал частного случая его реализации.
ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее будет описан вариант выполнения способа оценки статуса 14-го экзона гена MET по данным РНК секвенирования, который не ограничивает все варианты осуществления заявленного изобретения.
МЕТ представляет собой тирозинкиназу и протоонкоген, кодируемый на 7ой хромосоме. Активированный MET индуцирует сигнальные пути, участвующие в выживании и пролиферации клеток.
Мутации в MET связаны с рядом видов рака, включая рак почек, желудка, нервной системы, саркомы и рак легких. Мутации, которые приводят к более высокой экспрессии или делеции некоторых экзонов, часто связаны с этими видами рака. В частности, делеция 14-го экзона и связана со значительным процентом случаев немелкоклеточного рака легкого и аденокарциномы. MET обычно не деградирует при потере 14-го экзона. Возникающая в результате дисрегуляция MET вызывает устойчивую активацию нижестоящих путей пролиферации и выживания клеток. Мутации, которые вызывают делеции экзона 14 MET, являются гетерогенными, часто затрагивая акцепторные или донорные сайты сплайсинга.
Обнаружение пропуска 14-го экзона гена MET позволит назначить пациенту препараты, демонстрирующие высокую эффективность против этой изоформы, такие как капматиниб (capmatinib) и тепотиниб (tepotinib)
Системы персонализированной медицины, такие как Онкобокс [US11614434, опубл. 28.03.2023], применяют РНК секвенирование для предоставления рекомендаций по терапии пациентов со злокачественными новообразованиями.
Для картирования прочтений РНК секвенирования могут использоваться такие программы как STAR [https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3530905/], результатом работы которых являются геномные координаты, на которые картировалились те или иные прочтения, в том числе с разрывом внутри них. Ожидается, что большинство прочтений РНК секвенирования будет картироваться на экзоны, причем значения нормированных покрытий каждого экзона, входящего в конечную версию определенного транскрипта того или иного, экспрессирующегося в опухолевой ткани гена, не будет отличаться значительно (оценки допустимых разностей покрытий экзонов будут приведены ниже). В случае, если прочтение картировалось на референсный геном с разрывом, делается вывод о том, что оно пришло со стыка экзонов.
В заявленном изобретении используются эти данные для детекции прочтений, картированных на стык 13-го и 15-го экзона гена MET. Присутствие таких прочтений может свидетельствовать о том, что 14 экзон в транскрипте гена был пропущен.
Асимметрия покрытий 13, 14 и 15 экзона также проверяется. Неравномерность покрытия этих экзонов прочтениями зачастую связана с тем, что в зрелой мРНК пропущен 14 экзон, соответственно мы ожидаем обнаружить в исследуемом образце только небольшое количество прочтений, картированных на этот участок генома. Поэтому, при наличии пропуска 14-го экзона, средняя разность покрытий прочтениями 14го и 13го, и 14го и 15го экзонов будет детектируемо ниже, чем в случае без пропуска.
Детектирование двух вышеупомянутых признаков считается достаточным основанием для назначения Capmatinib-а или Tepotinib-а пациенту, страдающему немелкоклеточным раком легкого. Детектирование одного из них может послужить причиной для дальнейшей проверки при помощи ПЦР-РВ со специально подобранными условиями и праймерами или любого другого метода, позволяющего выявить пропуск 14 экзона гена MET.
Под образцом РНК, понимают РНК, извлеченную из каких бы то ни было клеток человека.
Под “картированием прочтений” стоит понимать биоинформатический метод анализа результатов секвенирования, состоящий в определении позиций в референсном геноме, откуда с наибольшей вероятностью могло быть получено каждое конкретное прочтение.
Под “SJ прочтениями” или “splice junction прочтениями” стоит понимать прочтения, отнесенные программами для картирования к вероятно картировавшимся на стык двух экзонов.
Под “геномными координатами” стоит понимать позицию в референсном геноме.
Под “флагом прочтения” стоит понимать характеристику прочтения, указываемую в файлах картирования (.sam, .bam) в виде комбинации бинарных флагов, несущих информацию об определенных свойствах прочтения.
Под “парой оснований” стоит понимать пару двух азотистых оснований нуклеотидов на комплементарных цепочках нуклеиновых кислот, соединенную с помощью водородных связей.
Под “покрытием прочтениями” стоит понимать количество прочтений, картированных на определенный участок референсного генома.
Если не определено отдельно, технические и научные термины в данном описании имеют стандартные значения, общепринятые в научной и технической литературе.
Данный способ детекции пропуска 14-го экзона в транскрипте гена MET призван улучшить системы для подбора терапии больных с онкологическими заболеваниями. Улучшение возможно если в системе используется секвенирование РНК.
Первой решаемой технической задачей (1) является анализ прочтений, картированных на стык экзонов. При этом в нее входят следующие подзадачи:
1.1 Детекция прочтений, приходящихся на стык экзонов 13 и 15 гена MET
1.2 Анализ качества задетектированных прочтений.
Второй решаемой задачей (2) является оценка уровня неравномерности покрытия прочтениями экзонов 13, 14, и 15. Данная задача также разбивается на подзадачи:
2.1 Нахождение прочтений, картированных на экзоны гена MET.
2.2 Анализ качества картирования каждого из найденных прочтений.
2.3 Подсчет покрытия прочтениями экзонов
2.4 Подсчет асимметрии покрытия экзонов 13, 14 и 15 гена MET
2.5 Определение границы разности покрытий, после преодоления которой можно считать, что в образце РНК присутствуют транскрипты, соответствующие гену MET c пропущенным 14 экзоном.
Задача пункта 1.1 решается при помощи программ для картирования прочтений, полученных в ходе РНК секвенирования, которые детектируют SJ прочтения. Прочтения, приходящиеся на стык 13 и 15-го экзонов, находятся согласно геномным координатам: геномные координаты одного конца прочтения должны приходиться на 13 экзон, координаты другого - на 15 экзон.
Контроль качества (пункт 1.2) выполнялся на уровне длины перекрытия: длина перекрытия прочтения с каждым из экзонов должна составлять не менее 10 пар оснований.
Для решения задачи 2 также используются данные, сгенерированные при картировании прочтений РНК секвенирования на геном человека.
Задача пункта 2.1 включает в себя нахождение всех прочтений, перекрывающихся с экзонами гена MET. Осуществляется это при помощи программ биоинформатического анализа последовательностей нуклеиновых кислот человека.
После нахождения требуемых прочтений происходит их анализ качества (пункт 2.2). Используется метрика качества картирования (mapping quality или MapQ). Прочтение должно преодолевать определенный порог по этой метрике. В зависимости от протокола РНК секвенирования может быть добавлен такой критерий, как направление прочтения (прямое или обратное). Если для выравнивания прочтений используются программы, дополнительно сигнализирующие о непрохождении внутреннего для программы контроля качества прочтения, прочтения, не прошедшие этот контроль также, не включаются в дальнейший анализ. Также на прочтения накладываются требования по качеству картирования: длина перекрытия прочтения с каждым из экзонов должна составлять не менее 10 пар оснований (аналогично пункту 1.2). Прочтения, не обладающие данными свойствами, не включаются в подсчет покрытия.
Вычисление покрытия экзона (пункт 2.3) происходит следующим образом: длины перекрытий с рассматриваемым экзоном всех прочтений, прошедших контроль качества, суммируются и делятся на длину экзона в парах оснований. Интуитивный смысл этой величины заключается в том, что она представляет собой среднее количество прочтений, приходящихся на 1 пару оснований экзона. Визуализацию вычисленных значений покрытия экзонов гена MET можно найти в Фиг. 1.
Для дальнейшей оценки асимметрии (пункт 2.4) берутся только те образцы, сумма покрытий по каждому из экзонов превышает 210 (данный порог соответствует среднему покрытию экзонов гена MET, равному 10). Образцы с более низким количеством картированных прочтений гена MET не подлежат анализу описываемым методом из-за сильной неравномерности покрытия.
Затем покрытия экзонов делятся на сумму покрытий всех экзонов гена MET и умножаются на 100 (последнее делается для удобства визуализации и документального представления). Таким образом достигается унификация оценки неравномерности - устраняется эффект от разного уровня экспрессии гена MET в разных образцах:
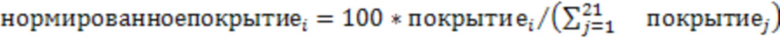 ,
,
где i и j - номера экзонов.
Далее вычисляется среднее арифметическое разности нормированных покрытий 14 и 13 и 14 и 15 экзонов. Полученная величина и является мерой асимметрии покрытия между этими экзонами.
После вычисления меры асимметрии покрытия необходимо понять, какую асимметрию считать достаточной, для заключения о том, что 14 экзон был пропущен (пункт 2.5). Для определения этого порога определяли асимметрию покрытия для 478 экспериментальных образцов РНК-секвенирования опухолевой ткани человека, ранее полученных компанией Онкобокс, со средним покрытием каждой пары оснований на экзонах больше 10. Предлагаемым в данном изобретении пограничным значением стало приблизительно значение внешнего нижнего ограничителя диаграммы размаха X1:
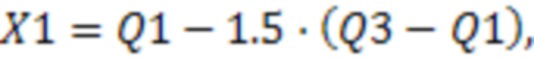
где Q1 и Q3 - первая и третья квартили распределения нормированных покрытий. Это значение оказалось близко к 2, что и было взято в качестве граничного значения (Фиг 2.)
Таким образом, после нахождения нужного количества SJ прочтений и вычисления асимметрии покрытия можно делать выводы о наличии пропуска 14 экзона гена MET. При наличии только одного из 2х этих признаков (наличие SJ ридов или наличие асимметрии) образец РНК секвенирования проверяется как либо другим методом на наличие пропуска 14го экзона гена MET. При наличии и асимметрии покрытия и достаточного количества SJ прочтений делается вывод о наличии в образце пропущенного 14-го экзона гена MET. При отсутствии всех вышеупомянутых признаков делается вывод о том, что пропуска 14-го экзона гена MET в образце нет.
Пример 1
Образец РНК-секвенирования А был взят у пациента А, страдающего немелкоклеточным раком легкого. После картирования прочтений РНК-секвенирования производился подсчет нормированного покрытия и асимметрии, как это описано выше. Асимметрия составила -3.95, что меньше выбранного порога, равного -2. Последнее свидетельствует о потенциальном наличии в образце транскрипта гена MET с пропуском 14го экзона. Среди прочтений РНК секвенирования также были найдены прочтения, картированные с высоким качеством на стык 13-го и 15-го экзонов гена MET. Это подтвердило экспрессию изоформы гена MET c пропуском 14-го экзона в рассматриваемом образце. Из этих фактов делается вывод, что в опухоли пациента происходит экспрессия изоформы гена MET с пропуском 14го экзона и есть основания назначить препарат, эффективный против данной изоформы.
Пример 2
Образец РНК-секвенирования Б был взят у пациента Б, страдающего немелкоклеточным раком легкого. После картирования прочтений РНК-секвенирования производился подсчет нормированного покрытия и асимметрии, как это описано выше. Асимметрия составила -2.1, что меньше выбранного порога, равного -2. Среди картированных прочтений РНК секвенирования НЕ нашлись таковые на стык экзонов 13 и 15 гена MET. Эти факты говорят о том, что требуется дополнительная проверка этого образца на предмет наличия пропуска 14-го экзона гена MET.
Для этого проводится 2 ПЦР в реальном времени (ПЦР-РВ). Первая ПЦР-РВ проводилась с 2-мя прамерами: прямым праймером F_13ex (последовательность: CAGAATTTCACAGGATTGATTG), картирующимся на 13 экзон гена MET, и обратным R_13-15ex (послеовательность: GATGAATTAGGAAACTGATCTTTAA), картирующимся на стык 13 и 15 экзонов. Длина ПЦР продукта 122 пар оснований. Вторая ПЦР-РВ проводилась со следующими праймерами: с прямым праймером F_13ex (последовательность: CAGAATTTCACAGGATTGATTG), картирующимся на 13 экзон гена MET, и обратным, картирующимся на стык 13 и 14 экзонов (К_13-14ex: TCACTGCCCAGATCTTTAA). Длина ПЦР продукта 116 пар оснований. Обе ПЦР проходили при следующих условиях: начальная денатурация 180 секунд при 95°С, затем 40 циклов 93°С 10 секунд, 58°С 30 секунд и 72°С 45 секунд, финальная элонгация длилась 2 минуты при 72°С. Для оценки качества продукта ПЦР использовали кривую плавления и секвенирование по Сэнгеру: в обоих случаях использовали праймер F_13ex. Пропуск 14 экзона считали верифицированным, если пороговый цикл обеих ПЦР не более 35. После проведения вышеописанных ПЦР-РВ с образцом Б мы получили пороговый цикл больше 35 только в контрольном ПЦР-РВ.
Из этих фактов делается вывод, что в опухоли пациента не происходит экспрессии изоформы гена MET с пропуском 14-го экзона и нет оснований назначить препарат, эффективный против данной изоформы.
Пример 3
Образец РНК-секвенирования В был взят у пациента В, страдающего немелкоклеточным раком легкого. После картирования прочтений РНК-секвенирования производился подсчет нормированного покрытия и асимметрии, как это описано выше. Асимметрия составила -1.6, что больше выбранного порога, равного -2. Среди прочтений РНК секвенирования были найдены прочтения, картированные с высоким качеством на стык 13-го и 15-го экзонов гена MET. Эти факты говорят о том, что требуется дополнительная проверка этого образца на предмет наличия пропуска 14-го экзона гена MET.
Для этого проводится 2 ПЦР в реальном времени (ПЦР-РВ). Первая ПЦР-РВ проводилась с 2мя прамерами: прямым праймером F_13ex (последовательность: CAGAATTTCACAGGATTGATTG), картирующимся на 13 экзон гена MET, и обратным R_13-15ex (послеовательность: GATGAATTAGGAAACTGATCTTTAA), картирующимся на стык 13 и 15 экзонов. Длина ПЦР продукта 122 пар оснований. Вторая ПЦР-РВ проводилась со следующими праймерами: с прямым праймером F_13ex (последовательность: CAGAATTTCACAGGATTGATTG), картирующимся на 13 экзон гена MET, и обратным, картирующимся на стык 13 и 14 экзонов (К_13-14ex: TCACTGCCCAGATCTTTAA). Длина ПЦР продукта 116 пар оснований. Обе ПЦР проходили при следующих условиях: начальная денатурация 180 секунд при 95°С, затем 40 циклов 93°С 10 секунд, 58°С 30 секунд и 72°С 45 секунд, финальная элонгация длилась 2 минуты при 72°С. Для оценки качества продукта ПЦР использовали кривую плавления и секвенирование по Сэнгеру: в обоих случаях использовали праймер F_13ex. Пропуск 14 экзона считали верифицированным, если пороговый цикл обеих ПЦР не более 35. После проведения вышеописанных ПЦР-РВ с образцом В мы получили пороговые циклы больше 35 во всех ПЦР-РВ.
Из этих фактов делается вывод, что в опухоли пациента происходит экспрессия изоформы гена MET с пропуском 14-го экзона и есть основания назначить препарат, эффективный против данной изоформы.
Пример 4
Образец РНК-секвенирования Г был взят у пациента Г, страдающего немелкоклеточным раком легкого. После картирования прочтений РНК-секвенирования производился подсчет нормированного покрытия и асимметрии, как это описано выше. Асимметрия составила -0.3, что больше выбранного порога, равного -2. Среди прочтений РНК секвенирования не были найдены прочтения, картированные с высоким качеством на стык 13го и 15го экзонов гена MET. Из этих фактов делается вывод, что в опухоли пациента не происходит экспрессии изоформы гена MET с пропуском 14го экзона и нет оснований назначить препарат, эффективный против данной изоформы.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Настоящее изобретение предназначено для использования в персонализированной онкологии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ ДЕТЕКЦИИ ТРАНСЛОКАЦИЙ ГЕНА ALK В ПАРАФИНИЗИРОВАННЫХ ОПУХОЛЕВЫХ ОБРАЗЦАХ С ПОМОЩЬЮ РНК-СЕКВЕНИРОВАНИЯ | 2023 |
|
RU2812346C1 |
| СПОСОБ ДЕТЕКЦИИ ТРАНСЛОКАЦИЙ ГЕНОВ ТИРОЗИНКИНАЗНЫХ РЕЦЕПТОРОВ В ОБРАЗЦАХ ОПУХОЛЕВОЙ ТКАНИ С ИСПОЛЬЗОВАНИЕМ ДАННЫХ РНК-СЕКВЕНИРОВАНИЯ | 2023 |
|
RU2814710C1 |
| Способ выявления вариаций и изменений числа копий в генах BRCA1 и BRCA2 по данным таргетного массового параллельного секвенирования генома | 2020 |
|
RU2759953C2 |
| Способ создания таргетной панели для исследования геномных регионов для выявления терапевтических биомаркеров ингибиторов иммунных контрольных точек (ИКТ) | 2023 |
|
RU2818360C1 |
| СПОСОБ НЕИНВАЗИВНОЙ ПРЕНАТАЛЬНОЙ ДИАГНОСТИКИ АНЕУПЛОИДИЙ ПЛОДА | 2015 |
|
RU2627673C2 |
| Тест-классификатор клинического ответа на лечение сорафенибом индивидуальных пациентов с раком почки | 2018 |
|
RU2747746C2 |
| СПОСОБ НЕИНВАЗИВНОЙ ПРЕНАТАЛЬНОЙ ДИАГНОСТИКИ АНЕУПЛОИДИЙ ПЛОДА | 2014 |
|
RU2583830C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КЛИНИЧЕСКОЙ ЭФФЕКТИВНОСТИ ПРИМЕНЕНИЯ ТАКСАНОВ ДЛЯ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2023 |
|
RU2836870C1 |
| СПОСОБ КВАНТИФИКАЦИИ СТАТИСТИЧЕСКОГО АНАЛИЗА АЛЬТЕРНАТИВНОГО СПЛАЙСИНГА В ДАННЫХ РНК-СЕК | 2020 |
|
RU2752663C1 |
| СПОСОБЫ И УСТРОЙСТВА ДЛЯ ОПРЕДЕЛЕНИЯ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ В РЕАЛЬНОМ ВРЕМЕНИ С ИСПОЛЬЗОВАНИЕМ НУКЛЕИНОВЫХ КИСЛОТ | 2018 |
|
RU2763969C2 |
Изобретение относится к области биотехнологии. Описан способ оценки статуса 14-го экзона гена MET по данным РНК секвенирования. Способ включает стадии получения биологического материала, пригодного для РНК секвенирования, получения данных РНК секвенирования из материала, получения данных о картировании прочтений на экзоны гена MET человека, подсчета количества SJ прочтений, приходящихся на стык 13 и 15-го экзонов и прошедших контроль качества, и сравнения его с порогом, определяемым пользователем и выбранным на основе требуемой строгости и точности определения наличия таких прочтений, подсчета нормированного уровня асимметрии покрытия 13, 14 и 15-го экзонов и сравнения его с порогом, определяемым пользователем и выбранным на основе анализа клинических образцов, и анализа результатов, при котором при преодолении всех выбранных порогов делается вывод о наличии в образце гена MET с пропуском 14-го экзона. Техническим результатом изобретения является улучшение детекции пропуска 14-го экзона гена MET на основе данных РНК секвенирования. 1 з.п. ф-лы, 2 ил., 4 пр.
1. Способ оценки статуса 14-го экзона гена MET по данным РНК секвенирования, который состоит, по меньшей мере, из следующих шагов:
а) получение биологического материала, пригодного для РНК секвенирования;
б) получение данных РНК секвенирования из материала пункта (а);
в) получение из данных пункта (б) данных о картировании прочтений на экзоны гена MET человека, в том числе о картировании на стыке экзонов;
г) подсчет количества SJ прочтений, приходящихся на стык 13 и 15-го экзонов и прошедших контроль качества, и сравнение его с порогом, определяемым пользователем и выбранным на основе требуемой строгости и точности определения наличия таких прочтений;
д) подсчет нормированного уровня асимметрии покрытия 13, 14 и 15-го экзонов и сравнение его с порогом, определяемым пользователем и выбранным на основе анализа клинических образцов;
е) анализ результатов пунктов (в) и (г), при котором при преодолении всех выбранных порогов, описанных в пунктах (в) и (г), делается вывод о наличии в образце гена MET с пропуском 14-го экзона.
2. Способ оценки по п.1, отличающийся тем, что при преодолении только одного из порогов, либо в пункте (в), либо в пункте (г), биологический материал, из которого были получены данные РНК секвенирования, подвергается дополнительной проверке, позволяющей оценить статус 14-го экзона гена MET в этом биологическом материале, если пороги пунктов (в) и (г) не были преодолены, делается вывод о том, что в образце нет транскриптов, соответствующих гену MET без 14-го экзона.
| Kim S | |||
| Y | |||
| et al | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Облицовка комнатных печей | 1918 |
|
SU100A1 |
| Холматов М.М | |||
| и др | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
Авторы
Даты
2024-04-22—Публикация
2023-09-03—Подача