Область техники, к которой относится изобретение
[0001]
Настоящее изобретение относится к соединению или фармацевтической композиции, применимых для лечения или предупреждения заболевания, ассоциированного с функцией потенциал-зависимого натриевого канала Nav1.7 (далее в данном документе называемого Nav1.7).
Уровень техники
[0002]
Потенциал-зависимые натриевые каналы (Nav) присутствуют в возбудимых клетках, в том числе в нейронных клетках центральной и периферической нервных систем, а также кардиомиоцитах. Их функция состоит в контроле возрастающей фазы потенциала действия, создаваемого деполяризацией потенциала клеточной мембраны, для участия в генерировании и распространении электрических сигналов. Nav необходимы для поддержания физиологических функций возбудимых клеток, таких как нейроны и клетки миокарда. Нарушения функции Nav связаны с такими заболеваниями, как эпилепсия (непатентный документ 1), аритмия (непатентный документ 2), миотония (непатентный документ 3) и хроническая боль (непатентный документ 4).
Nav состоят из α-субъединиц, которые образуют пору ионного канала, и β-субъединиц, которые действуют дополнительно. На сегодняшний день известно по меньшей мере девять α-субъединиц (от Nav1.1 до Nav1.9). Эти подтипы классифицируются на ТТХ-чувствительные Nav (Nav1.1, Nav1.2, Nav1.3, Nav1.4, Nav1.6, Nav1.7), которые функционально ингибируются токсином рыбы фугу тетродотоксином (TTX), и TTX-устойчивые Nav (Nav1.5, Nav1.8, Nav1.9). Известно, что Nav1.1, Nav1.2, Nav1.3 преимущественно экспрессируются в центральной нервной системе, Nav1.4 преимущественно экспрессируется в скелетных мышцах, Nav1.5 преимущественно экспрессируется в миокарде, Nav1.6 преимущественно экспрессируется в нервной системе, и Nav1.7, Nav1.8 и Nav1.9 преимущественно экспрессируются в периферической нервной системе (непатентный документ 5).
Nav1.7 представляет собой ТТХ-чувствительный натриевый канал, распределенный в периферической нервной системе, например, в автономных и сенсорных нейронах. Недавно было показано, что мутации в гене, кодирующем Nav1.7 (SCN9A), изменяют болевой порог. А именно, на основании анализа семейного анамнеза эритромелалгии с повышенным покраснением в дистальных отделах конечностей и болевыми ощущениями сообщалось о повышении частоты функциональной мутации в SCN9A (непатентный документ 6); а также сообщалось, что в SCN9A произошла мутация с потерей функции, на основании анализа происхождения нечувствительности к боли, при котором исчезло только болевое ощущение, хотя другие ощущения были нормальными (непатентный документ 7).
[0003]
Также из исследований с использованием антитела к Nav1.7 (непатентный документ 8) и соединений, ингибирующих Nav1.7 (непатентный документ 9, патентный документ 1 и патентный документ 2), известно, что ингибирование Nav1.7 обеспечивает обезболивающее действие в отношении ноцицептивной боли и невропатической боли.
Таким образом, поскольку предполагается, что Nav1.7 имеет отношение, в частности, к болевым ощущениям, ингибиторы Nav1.7 считаются применимыми в качестве терапевтических или профилактических лекарственных средств для заболеваний, связанных с болью, в частности, ноцицептивной болью и невропатической болью.
[0004]
Кроме того, поскольку ощущение зуда передается периферическими сенсорными нейронами, и Nav1.7 распределяется в периферической нервной системе, считается, что Nav1.7 участвует в остром и хроническом зуде; считается, что ингибирование Nav1.7 оказывает противозудный эффект в отношении острого или хронического зуда (непатентный документ 7).
[0005]
Ингибиторы Nav эффективны в лечении различных болезненных состояний. Например, неселективные ингибиторы Nav-подтипа включают лидокаин, местный анестетик, мексилетин, антиаритмическое лекарственное средство, и карбамазепин, противоэпилептическое лекарственное средство и так далее.
[0006]
Клинически известно, что неспецифические ингибиторы Nav-подтипа обладают обезболивающим действием и используются в качестве аналгетиков. Однако эти неселективные ингибиторы Nav-подтипа также оказывают ингибирующее действие в отношении Nav1.5, экспрессируемый в миокарде, и, таким образом, вызывают опасения по поводу неблагоприятного воздействия на сердечную функцию, которая особенно важна для жизнеобеспечения. На сегодняшний день не существует селективного ингибитора Nav1.7 для клинического применения.
[0007]
На основании вышеизложенного ингибиторы Nav1.7, которые являются селективными в отношении Nav1.5, считаются очень полезными в качестве терапевтических или профилактических лекарственных средств для различных болезненных патологий и вызывают меньшее беспокойство касательно побочных эффектов, связанных с ингибированием Nav1.5.
[0008]
К настоящему времени сообщалось о различных производных гетероароматических амидов, обладающих ингибирующим действием в отношении Nav1.7 (патентный документ 3 - патентный документ 10).
[0009]
Кроме того, в патентном документе 11 - патентном документе 15 раскрыты различные амидные соединения, обладающие ингибирующей активностью в отношении Nav1.7. Например, в патентном документе 15 описано соединение, представленное в виде:
[0010]
[Хим. 1]
 .
.
[0011]
В патентном документе 16 описано соединение, представленное в виде:
[0012]
[Хим. 2]
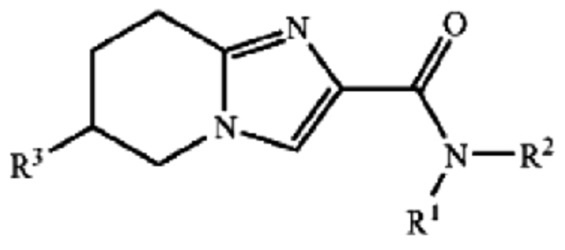
(где каждый символ имеет значение, определенное в патентном документе 16), в качестве соединения, характеризующегося сродством к калиевому каналу KCNQ2/3 и пригодного в качестве обезболивающего средства.
[0013]
В патентном документе 17 описано соединение, представленное в виде:
[0014]
[Хим. 3]

(где каждый символ имеет значение, определенное в патентном документе 17), обладающее ингибирующей активностью в отношении PDE4B и эффективное при различных нарушениях, включая боль.
[0015]
В непатентном документе 10 описано соединение, представленное в виде:
[0016]
[Хим. 4]

(где каждый символ имеет значения, указанные в патентном документе 10), в качестве отрицательного аллостерического модулятора метаботропного глутаматного рецептора 5 и соединение, применимое при хронической боли.
Документы предшествующего уровня техники
Патентные документы
[0017]
Патентный документ 1: WO2014/151472
Патентный документ 2: US20148883840A
Патентный документ 3: WO2008/008020
Патентный документ 4: WO2009/145720
Патентный документ 5: WO2009/145721
Патентный документ 6: WO2013/161928
Патентный документ 7: JP2014-101287A
Патентный документ 8: WO2015/119998
Патентный документ 9: WO2016/117647
Патентный документ 10: WO2008/130319
Патентный документ 11: WO2008/130320
Патентный документ 12: WO2008/130321
Патентный документ 13: WO2008/130322
Патентный документ 14: WO2008/130323
Патентный документ 15: WO2012/039657
Патентный документ 16: US20090186902A
Патентный документ 17: WO2017/145013
Непатентные документы
[0018]
Непатентный документ 1: Yogeeswari et al., Curr. Drug Targets 2004, 5 (7), 589-602.
Непатентный документ 2: Noble D., Proc Natl Acad Sci USA. 2002, 99 (9): 5755-5756.
Непатентный документ 3: Cannon SC, Kidney Int. 2000, 57 (3), 772-779.
Непатентный документ 4: Wood, JN et al., J. Neurobiol. 2004, 61 (1), 55-71.
Непатентный документ 5: Catterall, WA et al., Pharmacol Rev. 2005, 57: 397-409.
Непатентный документ 6: Waxman, SG Neurology. 2007, 7, 69 (6), 505-507.
Непатентный документ 7: Cox et al., Nature 2006, 444, 894-898.
Непатентный документ 8: Lee JH et al., Cell 2014, 157, 1393-1404.
Непатентный документ 9: Erin McGowan BS et al., Anesth Analg 2009, 109, 951-958.
Непатентный документ 10: G. Duvey et al., Bioorg. Med. Chem. Lett. 2013, 23 (16), 4523.
Раскрытие настоящего изобретения
Задачи, решаемые настоящим изобретением
[0019]
Целью настоящего изобретения является предоставление новых соединений, обладающих ингибирующим действием в отношении Nav1.7, и фармацевтических композиций, содержащих их.
Средства для решения задачи
[0020]
Авторы настоящего изобретения провели интенсивное исследование для решения вышеупомянутых задач, обнаружили, что следующее новое производное гетероароматического амида, представленное общей формулой (I), обладает ингибирующим действием в отношении Nav1.7, селективным по сравнению с Nav1.5, и реализовали настоящее изобретение.
[0021]
(0) Настоящее изобретение относится к производному гетероароматического амида, представленному общей формулой (I) или его фармацевтически приемлемой соли:
[0022]
[Хим. 5]

где
X1-X2 представляет собой N-C или C-N,
Y1, Y2, Y3 и Y4 независимо друг от друга представляют собой одинарную связь, -CH2-, -CH2CH2-, -CR4aR4b-, -CR4aH-, -CR4bH-, -CH2CR4aR4b-, -CH2CR4aH-, -NR4c-, -NH-, -S-, -SO2- или -O-,
Z1 представляет собой одинарную связь, -CR7aR7b-, -O-, -S-, -NH-, -NR7a-, -NR7aCH2-, -CH2NR7a-, -CO- или -SO2-,
кольцо A представляет собой 3-7-членное моноциклическое ароматическое кольцо или 8-12-членное бициклическое ароматическое кольцо,
R1a и R1b независимо друг от друга представляют собой атом водорода, атом галогена, гидроксильную группу, цианогруппу, C1-C4-алкильную группу, C1-C4-галогеналкильную группу, C1-C4-алкоксигруппу, C1-C4-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C1-C4-алкокси-C1-C4-алкильную группу или C1-C4-галогеналкокси-C1-C4-алкильную группу,
R2 представляет собой атом водорода, атом галогена, гидроксильную группу, цианогруппу, необязательно замещенную C1-C6-алкильную группу, необязательно замещенную C1-C6-галогеналкильную группу, необязательно замещенную C2-C6-алкенильную группу, необязательно замещенную C2-C6-алкинильную группу или необязательно замещенное насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо,
R3a, R3b и R3c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксильную группу, необязательно замещенную C1-C6-алкильную группу, необязательно замещенную C1-C6-галогеналкильную группу, необязательно замещенную C1-C6-алкоксигруппу, необязательно замещенную C1-C6-галогеналкоксигруппу, необязательно замещенную C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-алкокси-C1-C4-галогеналкильную группу, необязательно замещенную C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, необязательно замещенную C1-C6-алкилкарбонильную группу, необязательно замещенную C1-C6-алкоксикарбонильную группу, необязательно замещенную C1-C6-алкилкарбонилоксигруппу, необязательно замещенную C1-C6-галогеналкилкарбонильную группу, необязательно замещенную C1-C6-галогеналкоксикарбонильную группу, необязательно замещенную C1-C6-галогеналкилкарбонилоксигруппу, необязательно замещенную C3-C7-циклоалкильную группу, необязательно замещенную гетероциклоалкильную группу, необязательно замещенную C3-C7-циклоалкилоксигруппу, необязательно замещенную гетероциклоалкилоксигруппу, необязательно замещенную C2-C6-алкенильную группу, необязательно замещенную C2-C6-алкенилоксигруппу, необязательно замещенную C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную C2-C6-алкенилокси-C1-C4-галогеналкильную группу, необязательно замещенную C2-C6-алкинильную группу, необязательно замещенную C2-C6-алкинилоксигруппу, необязательно замещенную C2-C6-алкинилокси-C1-C4-алкильную группу, необязательно замещенную C2-C6-алкинилокси-C1-C4-галогеналкильную группу, необязательно замещенную C1-C4-алкокси-C1-C4-алкоксигруппу, необязательно замещенную C1-C4-галогеналкокси-C1-C4-алкоксигруппу, необязательно замещенную C2-C6-алкенилокси-C1-C4-алкоксигруппу, необязательно замещенную C2-C6-алкинилокси-C1-C4-алкоксигруппу, необязательно замещенную C2-C6-алкенилокси-C1-C4-галогеналкоксигруппу, необязательно замещенную C2-C6-алкинилокси-C1-C4-галогеналкоксигруппу, необязательно замещенную C1-C6-алкилтиогруппу, необязательно замещенную C1-C6-галогеналкилтиогруппу, необязательно замещенную C1-C4-алкилтио-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкилтио-C1-C4-алкильную группу, необязательно замещенную C1-C4-алкилтио-C1-C4-галогеналкильную группу, необязательно замещенную C1-C4-галогеналкилтио-C1-C4-галогеналкильную группу, необязательно замещенную C1-C6-алкилсульфонильную группу, -(CH2)pNRa1Ra2 (при этом Ra1 и Ra2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу, и p равняется 0, 1 или 2) или группу, представленную общей формулой (I-A),
[0023]
[Хим. 6]

где
кольцо B представляет собой насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо,
L1 представляет собой одинарную связь, -CRa3Ra4-, -O-, -NRa1-, -CRa3Ra4O-, -OCRa3Ra4-, -CH2CH2-, -CH=CH-, -C≡C- или -CH2OCH2- (при этом Ra3 и Ra4 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу),
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкильную группу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу или C2-C6-алкинильную группу,
R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксильную группу, необязательно замещенную C1-C6-алкильную группу, необязательно замещенную C1-C6-галогеналкильную группу, необязательно замещенную C1-C6-алкоксигруппу, необязательно замещенную C1-C6-галогеналкоксигруппу, необязательно замещенную C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-алкокси-C1-C4-галогеналкильную группу, необязательно замещенную C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, необязательно замещенную C1-C6-алкилкарбонильную группу, необязательно замещенную C1-C6-алкоксикарбонильную группу, необязательно замещенную C1-C6-алкилкарбонилоксигруппу, необязательно замещенную C1-C6-галогеналкилкарбонильную группу, необязательно замещенную C1-C6-галогеналкоксикарбонильную группу, необязательно замещенную C1-C6-галогеналкилкарбонилоксигруппу, необязательно замещенную C3-C7-циклоалкильную группу, необязательно замещенную гетероциклоалкильную группу, необязательно замещенную C3-C7-циклоалкилоксигруппу, необязательно замещенную гетероциклоалкилоксигруппу, необязательно замещенную C2-C6-алкенильную группу, необязательно замещенную C2-C6-алкенилоксигруппу, необязательно замещенную C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную C2-C6-алкенилокси-C1-C4-галогеналкильную группу, необязательно замещенную C2-C6-алкинильную группу, необязательно замещенную C2-C6-алкинилоксигруппу, необязательно замещенную C2-C6-алкинилокси-C1-C4-алкильную группу, необязательно замещенную C2-C6-алкинилокси-C1-C4-галогеналкильную группу, необязательно замещенную C1-C4-алкокси-C1-C4-алкоксигруппу, необязательно замещенную C1-C4-галогеналкокси-C1-C4-алкоксигруппу, необязательно замещенную C2-C6-алкенилокси-C1-C4-алкоксигруппу, необязательно замещенную C2-C6-алкинилокси-C1-C4-алкоксигруппу, необязательно замещенную C2-C6-алкенилокси-C1-C4-галогеналкоксигруппу, необязательно замещенную C2-C6-алкинилокси-C1-C4-галогеналкоксигруппу, необязательно замещенную C1-C6-алкилтиогруппу, необязательно замещенную C1-C6-галогеналкилтиогруппу, необязательно замещенную C1-C4-алкилтио-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкилтио-C1-C4-алкильную группу, необязательно замещенную C1-C4-алкилтио-C1-C4-галогеналкильную группу, необязательно замещенную C1-C4-галогеналкилтио-C1-C4-галогеналкильную группу, пентафторсульфанильную группу, -(CH2)qNRb1Rb2 (при этом Rb1 и Rb2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу, и q равняется 0, 1, 2 или 3) или группу общей формулы (I-B),
[0024]
[Хим. 7]

где
кольцо C представляет собой насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо или насыщенное, частично насыщенное или ненасыщенное 7-12-членное бициклическое кольцо,
L2 представляет собой одинарную связь, -CH=CH-, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CONRc(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRcCO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2S(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2SO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2SO2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2SO2NRc(CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2NRcSO2 (CR10eR10f)r3(CR10gR10h)r4-
(при этом Rc представляет собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу,
R10a, R10b, R10c, R10d, R10e, R10f, R10g и R10h независимо друг от друга представляют собой атом водорода, атом галогена, C1-C4-алкильную группу или C3-C7-циклоалкильную группу,
R10a и R10b вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо,
R10c и R10d вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо,
R10e и R10f вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо,
R10g и R10h вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо,
r1, r2, r3 и r4 независимо друг от друга равняются 0, 1 или 2),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксильную группу, цианогруппу, формильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-галогеналкилкарбонильную группу, C3-C7-циклоалкильную группу, гетероциклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу, -(CH2)sNRd1Rd2 (при этом Rd1 и Rd2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу, и s равняется 0, 1 или 2) или группу, представленную общей формулой (I-C),
[0025]
[Хим. 8]

где
кольцо D представляет собой 3-7-членное моноциклическое кольцо, необязательно замещенное атомом галогена, гидроксильной группой, C1-C4-алкильной группой, C1-C4-галогеналкильной группой, C1-C4-алкоксигруппой или C1-C4-галогеналкоксигруппой,
L3 представляет собой одинарную связь или атом кислорода, или
R4a и R4b вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо, или
R4a и R4b вместе необязательно образуют группу общей формулы (I-D),
[0026]
[Хим. 9]

(при этом R4d и R4e независимо друг от друга представляют собой атом водорода, атом галогена или C1-C4-алкильную группу, или R4d и R4e вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо),
R5a, R5b, R5c, R6a, R6b и n соответствуют одному из следующих положений, указанных в (i) - (v):
(i) R5b и R5c вместе образуют одинарную связь, -CH2-, -OCH2-, -CH2O-, -CH2S-, -SCH2-, -CH2NRe1-, -NRe1CH2-, -CH2CH2-, -CONRe1-, -NRe1CO-, -CRe1Re2O- или -OCRe1Re2- (при этом Re1 и Re2 представляют собой атом водорода или C1-C4-алкильную группу), и
R5a представляет собой атом водорода, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C3-C7-циклоалкильную группу, гетероциклоалкильную группу, C3-C7-циклоалкил-C1-C4-алкильную группу, гетероциклоалкил-C1-C4-алкильную группу или аралкильную группу, и
R6a и R6b независимо друг от друга представляют собой атом водорода, атом галогена, гидроксильную группу, цианогруппу, C1-C4-алкильную группу, C1-C4-галогеналкильную группу, C1-C4-алкоксигруппу или C1-C4-галогеналкоксигруппу, и
n равняется 1 или 2.
(ii) R5a и R6a вместе образуют -CH2-, -CH2CH2-, -CH2CRe1Re2-, -CRe1Re2CH2-, -CH2CH2CH2-, -CH2CH2O- или -CH2CH2CH2O- (при этом Re1 и Re2 соответствуют определению, приведенному в (i)), и
R5b представляет собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу,
R5c и R6b представляют собой атом водорода, атом галогена, гидроксильную группу, C1-C4-алкильную группу, C1-C4-галогеналкильную группу, C1-C4-алкоксигруппу, C1-C4-галогеналкоксигруппу, или
в качестве альтернативы R5c и R6b вместе образуют -(CH2)t-, -O(CH2)t-, -(CH2)tO-, -(CH2)tO(CH2)u-, -(CH2)tNRe3(CH2)u-, -(CH2)tCONRe3(CH2)u- или -(CH2)tNRe3CO(CH2)u- (при этом t и u независимо друг от друга равняются 0, 1, 2 или 3, и Re3 представляет собой атом водорода или C1-C4-алкильную группу), и
n равняется 1.
(iii) R5a представляет собой атом водорода, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C3-C7-циклоалкильную группу, гетероциклоалкильную группу, C3-C7-циклоалкил-C1-C4-алкильную группу, гетероциклоалкил-C1-C4-алкильную группу или аралкильную группу, и
R5b представляет собой атом водорода или C1-C4-алкильную группу,
R5c представляет собой атом водорода, C1-C4-алкильную группу или атом галогена,
R6a и R6b независимо друг от друга представляют собой атом водорода, атом галогена, C1-C6-алкильную группу, C3-C7-циклоалкильную группу или C1-C6-галогеналкильную группу, или
в качестве альтернативы R6a и R6b вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо, и
n равняется 1 или 2.
(iv) R5a и R5b вместе образуют -CH2CH2-, -CH2CH2CH2- или -CH2CH2CH2CH2-, и
R5c, R6a и R6b независимо друг от друга представляют собой атом водорода или атом галогена, и
n равняется 1 или 2.
(v) R6a и R5c вместе образуют -OCH2-, -CH2O-, -CH2S-, -SCH2-, -CH2NH-, -NHCH2- или -CH2CH2-, и
R5a и R5b представляют собой атом водорода, и
R6b представляет собой атом водорода или атом галогена, и
n равняется 1, и
R7a и R7b независимо друг от друга представляют собой атом водорода, атом галогена или C1-C4-алкильную группу.
[0027]
В частности, настоящее изобретение включает следующие объекты изобретения.
[0028]
(1) Фармацевтическая композиция, содержащая производное гетероароматического амида, представленное общей формулой (I), или его соль,
[0029]
[Хим. 10]

где
X1-X2, Y1, Y2, Y3, Y4, Z1 кольцо A, R1a, R1b, R2, R3a, R3b, R3c, R5a, R5b, R5c, R6a, R6b, n имеют такое же определение, что и в (0) (при условии, что кольцо C не является фенильным кольцом, если X1-X2 представляет собой N-C, Y1, Y2, Y3 и Y4 вместе образуют -CH2CR4aHCH2CH2-, R2 представляет собой атом водорода, R4a представляет собой группу, представленную общей формулой (I-B), и L2 представляет собой одинарную связь. В качестве альтернативы, если кольцо C представляет собой фенильное кольцо, X1-X2 представляет собой C-N).
[0030]
(4) Производное гетероароматического амида или его соль, представленное общей формулой (I),
[0031]
[Хим. 11]
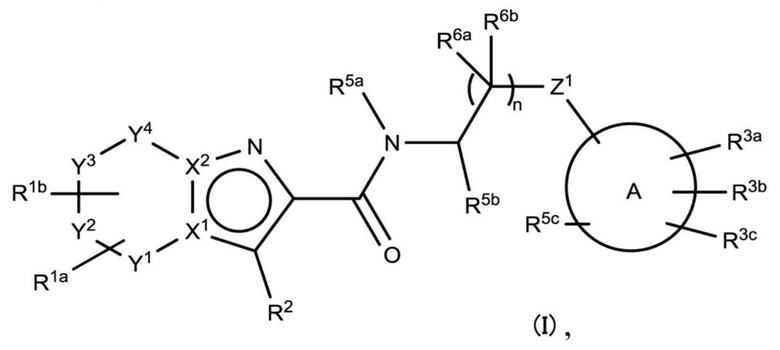
где
X1-X2, Y1, Y2, Y3, Y4, Z1, кольцо A, R1a, R1b, R2, R3a, R3b, R3c имеют такое же определение, что и в (0), при условии, что по меньшей мере один из Y1, Y2, Y3 или Y4 представляет собой -CR4aR4b-, -CR4aH-, -CH2CR4aR4b-, -CH2CR4aH- или -NR4c- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0), если R2 представляет собой атом водорода), и
R5a, R5b, R5c, R6a, R6b и n соответствуют одному из следующих положений (i) и (ii) (при условии, что Y1, Y2, Y3 и Y4 не образуют вместе -CH2NR4aHCH2CH2-, если R5a, R5b, R5c, R6a, R6b и n соответствуют положению (ii)).
[0032]
(5) Производное гетероароматического амида или его соль, описанные в (4) (при условии, что кольцо C не является фенильным кольцом, если X1-X2 представляет собой N-C, Y1, Y2, Y3 и Y4 вместе образуют -CH2CR4aHCH2CH2-, R2 представляет собой атом водорода, R4a представляет собой группу, представленную общей формулой (I-B), и L2 представляет собой одинарную связь. В качестве альтернативы, если кольцо C представляет собой фенильное кольцо, X1-X2 представляет собой C-N), где в общей формуле (I):
Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-, -OCH2CH2-, -OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCR4aR4bCH2CH2CH2-,
-OCH2CR4aHCH2CH2-, -OCH2CR4aR4bCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-, -CH2CH2OCH2-, -CH2CR4aHOCH2-
-CH2CH2CH2CH2-, -CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-,
-CH2CH2CR4aHCH2-, -CH2CH2CR4aR4bCH2-,
-CH2SCH2CH2-, -CH2SO2CH2CH2-,
-NHCH2CH2CH2-, -NR4cCH2CH2CH2-, -NR4cCR4aHCH2CH2-,
-NHCR4aHCH2CH2-,
-CH2NR4cCH2CH2-, -CH2NR4cCR4aHCH2-, -CH2NHCR4aHCH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)), и
R2 представляет собой атом водорода, атом галогена, гидроксильную группу, цианогруппу или необязательно замещенное насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо (при условии, что R2 представляет собой атом водорода, если X1-X2 представляет собой C-N, и Y1, Y2, Y3 и Y4 вместе образуют -OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-).
[0033]
(6) Производное гетероароматического амида или его соль, описанные в (4) или (5), где в общей формуле (I):
X1-X2 представляет собой C-N, и
Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-, -OCH2CH2-,
-OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCH2CR4aHCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-,
-CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-, -CH2CH2CR4aHCH2-,
-NHCH2CH2CH2-, -NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)),
R5a, R5b, R5c, R6a, R6b и n соответствуют положению (i) в (0).
[0034]
(7) Производное гетероароматического амида или его соль, представленное общей формулой (I-E2),
[0035]
[Хим. 12]
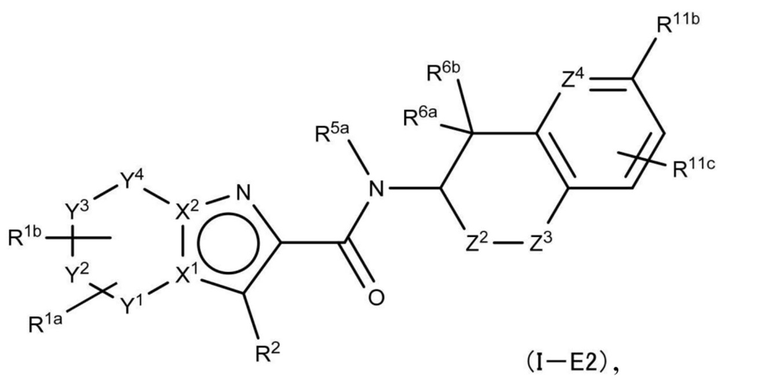
где
X1, X2, Y1, Y2, Y3, Y4, R1a, R1b, R2 имеют такое же определение, что и в (0),
Z2-Z3 представляет собой -CH2-, -OCH2-, -CH2O-, -SCH2-, -CH2S-, -CH2NRf1-, -NRf1CH2-, -CH2CH2-, -CONRf1-, -NRf1CO-, -OCRf1Rf2- или -CRf1Rf2O- (при этом Rf1 и Rf2 представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу),
R5a представляет собой атом водорода, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C3-C7-циклоалкильную группу, гетероциклоалкильную группу, C3-C7-циклоалкил-C1-C4-алкильную группу, гетероциклоалкил-C1-C4-алкильную группу или аралкильную группу,
R6a и R6b независимо друг от друга представляют собой атом водорода, атом галогена, гидроксильную группу, цианогруппу, C1-C4-алкильную группу, C1-C4-галогеналкильную группу, C1-C4-алкоксигруппу или C1-C4-галогеналкоксигруппу,
Z4 представляет собой C-R11a или атом азота,
R11a представляет собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкильную группу, C3-C7-циклоалкильную группу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкинильную группу или C2-C6-алкинилоксигруппу,
R11b соответствует определению, приведенному для R3b в (0), и
R11c соответствует определению, приведенному для R3c в (0),
при условии, что по меньшей мере один из Y1, Y2, Y3 или Y4 представляет собой -CR4aR4b-, -CR4aH-, -CH2CR4aR4b-, -CH2CR4aH- или -NR4c- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)), если R2 представляет собой атом водорода.
[0036]
(8) Производное гетероароматического амида или его соль, описанные в (7) (при условии, что R2 представляет собой атом водорода, если X1-X2 представляет собой C-N, и Y1, Y2, Y3 и Y4 вместе образуют -OCR4aHCH2CH2- или -OCR4aR4bCH2CH2-),
где в общей формуле (I-E2):
X1-X2 представляет собой C-N, и
Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-, -OCH2CH2-,
-OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCH2CR4aHCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-,
-CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-, -CH2CH2CR4aHCH2-,
-NHCH2CH2CH2-, -NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2-
(при этом R4a, R4b и R4c имеют такое же определение, что и в (0)).
[0037]
(9) Производное гетероароматического амида или его соль, описанные в (7) или (8), где в общей формуле (I-E2):
Z2-Z3 представляет собой -CH2O-,
R6a и R6b независимо друг от друга представляют собой атом водорода, атом фтора, гидроксильную группу или метоксигруппу,
каждый из R11a и R11c представляет собой атом водорода.
[0038]
(10) Производное гетероароматического амида или его соль, описанные в любом из (7) - (9), где в общей формуле (I-E2):
X1-X2 представляет собой C-N,
Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aHCH2-,
-OCR4aHCH2CH2CH2-, -CH2CR4aHCH2CH2-,
-NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2-, и
R4a представляет собой атом галогена, гидроксильную группу, цианогруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксильной группой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксильной группой, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-галогеналкилкарбонильную группу, C3-C7-циклоалкильную группу, C3-C7-циклоалкильную группу, необязательно замещенную атомом галогена или C1-C4-галогеналкильной группой, гетероциклоалкильную группу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкенилокси-C1-C4-алкильную группу, C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную атомом галогена, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C2-C6-алкинилокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или группу общей формулы (I-B),
[0039]
[Хим. 13]
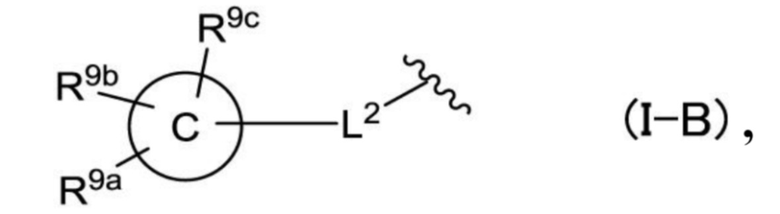
где
кольцо C представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L2 представляет собой одинарную связь, -CH=CH-, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2S(CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO(CR10eR10f)r3(CR10gR10h)r4- (при этом R10a, R10b, R10c, R10d, R10e, R10f, R10g, R10h, r1, r2, r3, r4 и Rc имеют такое же определение, что и в (0)), и
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксильную группу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкоксикарбонильную группу, гетероциклоалкилоксигруппу или -(CH2)sNRd1Rd2 (при этом s, Rd1 и Rd2 имеют такое же определение, что и в (0)).
[0040]
(11) Производное гетероароматического амида или его соль, описанные в (7) (при условии, что кольцо C не является фенильным кольцом, если Y1, Y2, Y3 и Y4 вместе образуют -CH2CR4aHCH2CH2-, R2 представляет собой атом водорода, R4a представляет собой группу, представленную общей формулой (I-B), и L2 представляет собой одинарную связь. В качестве альтернативы, если кольцо C представляет собой фенильное кольцо, X1-X2 представляет собой C-N), где в общей формуле (I-E2):
X1-X2 представляет собой N-C, и
Y1, Y2, Y3 и Y4 вместе образуют
-CH2CR4aHOCH2-, -CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)).
[0041]
(12) Производное гетероароматического амида или его соль, описанные в (7) или (11), где в общей формуле (I-E2):
Z2-Z3 представляет собой -CH2O-, и
каждый из R6a, R6b и R11c представляет собой атом водорода, и R11a представляет собой атом водорода или атом галогена.
[0042]
(13) Производное гетероароматического амида или его соль, описанные в любом из (7), (11) или (12), где в общей формуле (I-E2):
X1-X2 представляет собой N-C,
Y1, Y2, Y3 и Y4 вместе образуют
-CH2CR4aHOCH2-, -CH2CR4aHCH2CH2-, -CH2CH2NR4cCH2-,
-CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2-, и
R4a и R4c независимо друг от друга представляют собой атом галогена, гидроксильную группу, цианогруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксильной группой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксильной группой, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-галогеналкилкарбонильную группу, C3-C7-циклоалкильную группу, C3-C7-циклоалкильную группу, необязательно замещенную атомом галогена или C1-C4-галогеналкильной группой, гетероциклоалкильную группу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкенилокси-C1-C4-алкильную группу, C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную атомом галогена, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C2-C6-алкинилокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или группу общей формулы (I-B),
[0043]
[Хим. 14]
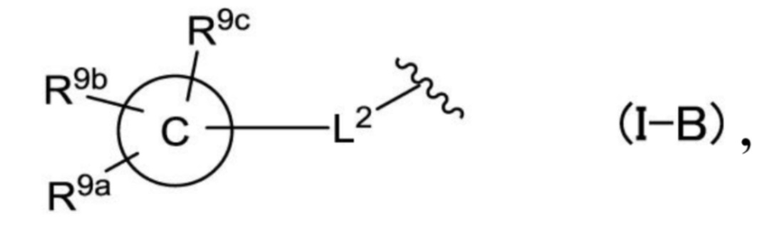
где
кольцо C представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L2 представляет собой одинарную связь, -CH=CH-, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2S(CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO(CR10eR10f)r3(CR10gR10h)r4- (при этом R10a, R10b, R10c, R10d, R10e, R10f, R10g, R10h, r1, r2, r3, r4 и Rc имеют такое же определение, что и в (0)),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксильную группу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкоксикарбонильную группу, гетероциклоалкилоксигруппу или -(CH2)sNRd1Rd2 (при этом s, Rd1 и Rd2 имеют такое же определение, что и в (0)).
[0044]
(14) Производное гетероароматического амида или его соль, описанные в любом из (7) - (13), где в общей формуле (I-E2):
R11b представляет собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную диметиламинокарбонильной группой или диметиламиногруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C2-C6-алкенильную группу, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, -(CH2)pNRa1Ra2 (при этом p, Ra1 и Ra2 имеют такое же определение, что и в (0)) или группу общей формулы (I-A),
[0045]
[Хим. 15]
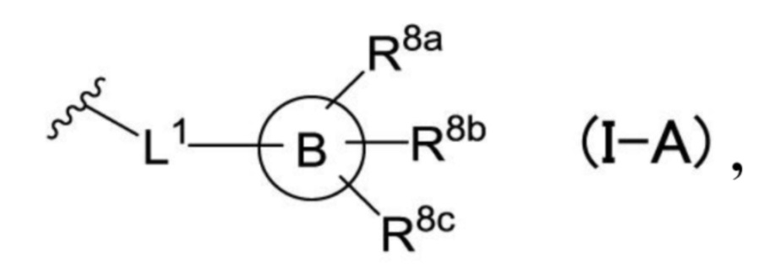
где
кольцо B представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил, тетразолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L1 представляет собой одинарную связь, -CH2-, -CH2O-, -OCH2-, -CH2CH2- или -CH2OCH2-,
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкильную группу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу или C2-C6-алкинильную группу.
[0046]
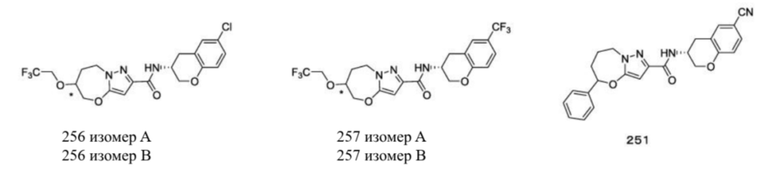
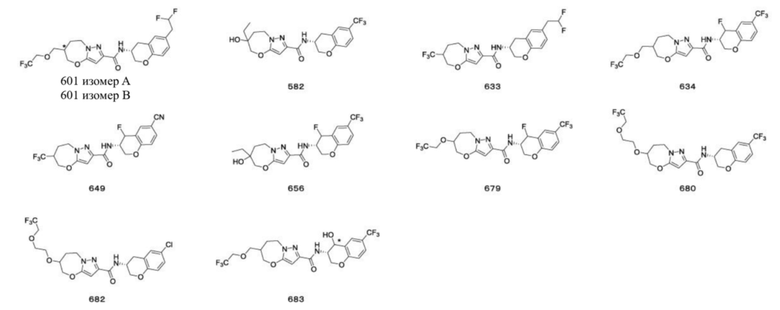
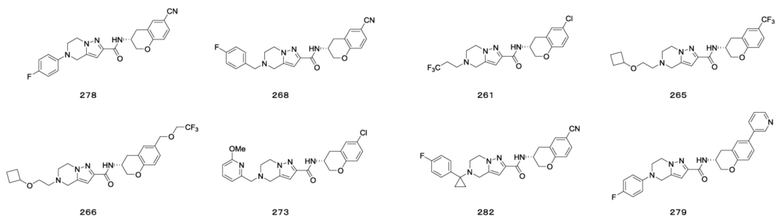
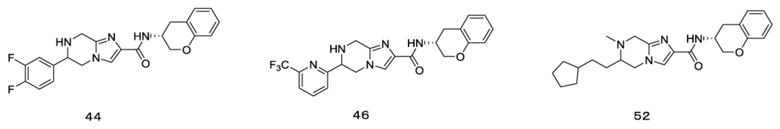
(15) Производное гетероароматического амида или его соль, описанные в (7), где соединение, представленное общей формулой (I-E2) (при этом звездочки (*), показанные в структурных формулах, означают, что соответствующий асимметричный атом углерода имеет единую стерическую структуру. Число указывает на номер примера. Что касается обозначений "изомер A", "изомер B", "изомер C" и "изомер D", среди множества соединений, обозначенных одним и тем же номером примера, изомеры указаны как "изомер A", "изомер B", "изомер C" и "изомер D" в соответствии с порядком получения с помощью высокоэффективной жидкостной хроматографии в примере), представляет собой любое из следующего:
[0047]
[Хим. 16]

[0048]
[Хим. 17]


[0049]
[Хим. 18]

[0050]
[Хим. 19]


[0051]
[Хим. 20]
[0052]
[Хим. 21]

[0053]
[Хим. 22]

[0054]
[Хим. 23]

[0055]
[Хим. 24]
[0056]
[Хим. 25]

[0057]
(16) Фармацевтическая композиция, содержащая производное гетероароматического амида или его соль, описанные в любом из (4) - (15).
(17) Фармацевтическая композиция для предупреждения или лечения нарушения, ассоциированного с функцией потенциал-зависимого натриевого канала Nav1.7, содержащая в качестве активного ингредиента производное гетероароматического амида, представленное общей формулой (I), или его соль, содержащиеся в фармацевтической композиции, описанной в (1), или производное гетероароматического амида или его соль, описанные в любом из (4) - (15) (далее в данном документе иногда называемые "производное гетероароматического амида или его соль, описанные в любом из (1) - (15)").
[0058]
(18) Средство для предупреждения или лечения нарушения, сопровождающегося болью, нарушения, сопровождающегося зудом, или нарушения вегетативной нервной системы, содержащее в качестве активного ингредиента производное гетероароматического амида или его соль, описанные в любом из (1) - (15).
(19) Средство для предупреждения или лечения нарушения, сопровождающегося болью, содержащее в качестве активного ингредиента производное гетероароматического амида или его соль, описанные в любом из (1) - (15).
(20) Обезболивающее средство, содержащее в качестве активного ингредиента производное гетероароматического амида или его соль, описанные в любом из (1) - (15).
(21) Средство для предупреждения или устранения ноцицептивной боли или невропатической боли, содержащее в качестве активного ингредиента производное гетероароматического амида или его соль, описанные в любом из (1) - (15).
(22) Применение производного гетероароматического амида или его соли, описанных в любом из (1) - (15) для изготовления фармацевтической композиции, применяемой для предупреждения или устранения боли.
(23) Применение производного гетероароматического амида или его соли, описанных в любом из (1) - (15) для изготовления обезболивающего средства.
Эффект настоящего изобретения
[0059]
Поскольку производное гетероароматического амида по настоящему изобретению или его соль обладают сильной ингибирующей активностью в отношении Nav1.7, их можно использовать в качестве активного ингредиента для терапевтического и/или профилактического средства при различных нарушениях, ассоциированных с функцией Nav1.7. Например, они применимы в качестве обезболивающего средства при заболеваниях, сопровождающимися различными видами боли.
Производное гетероароматического амида или его соль по настоящему изобретению не вызывают большого беспокойства касательно побочных эффектов, вызванных Nav1.5, и они являются применимыми в качестве активного ингредиента для терапевтических и/или профилактических средств при большом разнообразии патологий, связанных с функцией Nav1.7.
Соединения, описанные в патентном документе 3 - патентном документе 15, в значительной степени отличаются по структуре от соединений по настоящему изобретению.
Кроме того, в патентном документе 16, патентном документе 17 и непатентном документе 10 не описывается натриевый канал, а также не представлено ни описание, ни обеспечение соединений, обладающих ингибирующей активностью в отношении Nav1.7, селективной по сравнению с Nav1.5.
Варианты осуществления настоящего изобретения
[0060]
Далее настоящее изобретение объясняется более подробно.
Сначала описывается заместитель, который может иметь соединение по настоящему изобретению.
[0061]
Конкретными примерами "атома галогена" являются атом фтора, атом хлора, атом брома и атом йода.
Термин "C1-C6-алкильная группа" означает прямую или разветвленную алкильную группу, содержащую 1-6 атомов углерода, конкретные примеры включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, трет-бутильную группу, втор-бутильную группу, н-пентильную группу, трет-пентильную группу, 3-метилбутильную группу (изопентильную группу), неопентильную группу, н-гексильную группу, 3,3-диметилбутильную группу и так далее.
Термин "C1-C4-алкильная группа" означает прямую или разветвленную алкильную группу, содержащую 1-4 атома углерода, конкретные примеры включают метильную группу, этильную группу, н-пропильную группу, н-бутильную группу и так далее.
Термин "C1-C6-галогеналкильная группа" означает алкильную группу, в которой атомы водорода в вышеупомянутой "C1-C6-алкильной группе" замещены одним или несколькими атомами галогена, конкретные примеры включают монофторметильную группу, дифторметильную группу, трифторметильную группу, 2-фторэтильную группу, 2,2-дифторэтильную группу, 2,2,2-трифторэтильную группу, 1-фторэтильную группу, 1,1-дифторэтильную группу, 3,3,3-трифторпропильную группу, 3,3-дифторпропильную группу, 2-фторизопропильную группу, 2,3,3,3-тетрафторпропильную группу, 2,2,3,3-тетрафторпропильную группу, 2,2,3,3,3-пентафторпропильную группу, 1,1,2,2,3,3,3-гептафторпропильную группу, 1,1,1,3,3,3-гексафторизопропильную группу, 4,4,4-трифторбутильную группу, 2,2,3,4,4-пентафторбутильную группу, 2,2,3,4,4,4-гексафторбутильную группу, 2,2,3,3,4,4,4-гептафторбутильную группу, 3,3-дифторбутильную группу, 3,3,3-трифтор-2-(трифторметил)-пропильную группу, 3-фтор-3-метилбутильную группу и так далее.
Термин "C1-C4-галогеналкильная группа" означает алкильную группу, в которой один или несколько атомов водорода в вышеупомянутой "C1-C4-алкильной группе" замещены атомами галогена.
[0062]
Термин "C1-C6-алкоксигруппа" означает алкоксигруппу, в которой алкильный фрагмент соответствует определению, приведенному для "C1-C6-алкильной группы", конкретные примеры включают метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, н-бутоксигруппу, изобутоксигруппу, трет-бутоксигруппу, втор-бутоксигруппу, н-пентилоксигруппу, трет-амилоксигруппу, 3-метилбутоксигруппу, неопентилоксигруппу, н-гексилоксигруппу и так далее.
Термин "C1-C4-алкоксигруппа" означает алкоксигруппу, в которой алкильный фрагмент соответствует определению, приведенному для вышеупомянутой "C1-C4-алкильной группы".
Термин "C1-C6-галогеналкоксигруппа" означает галогеналкоксигруппу, в которой галогеналкильный фрагмент соответствует определению, приведенному для "C1-C6-галогеналкильной группы", конкретные примеры включают трифторметоксигруппу, дифторметоксигруппу, 2-фторэтоксигруппу, 2,2-дифторэтоксигруппу, 2,2,2-трифторэтоксигруппу, 3,3,3-трифторпропоксигруппу, 2,2,3,3-тетрафторпропоксигруппу, 2,2,3,3,3-пентафторпропоксигруппу, 1,1,1,3,3,3-гексафторизопропоксигруппу, 2,2,3,4,4,4-гексафторбутоксигруппу и так далее.
Термин "C1-C4-галогеналкоксигруппа" означает галогеналкоксигруппу, в которой галогеналкильный фрагмент соответствует определению, приведенному для вышеупомянутой "C1-C4-галогеналкильной группы".
[0063]
Термин "C1-C4-алкокси-C1-C4-алкильная группа" представляет собой вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "C1-C4-алкоксигруппой", и они могут связываться в любом замещаемом положении. Конкретные примеры включают метоксиметильную группу, этоксиметильную группу, изопропоксиметильную группу, н-пропоксиметильную группу, трет-бутоксиметильную группу, изобутоксиметильную группу, 2-метоксиэтильную группу, 2-этоксиэтильную группу, 1-этоксиэтильную группу, изобутоксиэтильную группу, трет-бутоксиэтильную группу и так далее.
Термин "C1-C4-галогеналкокси-C1-C4-алкильная группа" представляет собой вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "C1-C4-галогеналкоксигруппой", и они могут связываться в любом замещаемом положении. Конкретные примеры включают трифторметоксиметильную группу, дифторметоксиметильную группу, монофторметоксиметильную группу, 2,2,2-трифторэтоксиметильную группу, 2,2-дифторэтоксиметильную группу, 3,3,3-трифторпропоксиметильную группу, 4,4,4-трифторбутоксиметильную группу, 1,1,1,3,3,3-пентафторизопропоксиметильную группу, 3,3,3-трифтор-2-(трифторметил)-пропоксиметильную группу, 2-(трифторметокси)этильную группу, 2-(дифторметокси)этильную группу, 2-(2',2',2'-трифторэтокси)этильную группу, 2-(2',2'-дифторэтокси)этильную группу, 2-(1',1',1',3',3',3'-пентафторизопропокси)этильную группу, 3-(трифторметокси)пропильную группу, 3-(дифторметокси)пропильную группу, 3-(2',2',2'-трифторэтокси)пропильную группу, 3-(2',2'-дифторэтокси)пропильную группу, 3-(1',1',1',3',3',3'-пентафторизопропокси)пропильную группу и так далее.
Термин "C1-C4-алкокси-C1-C4-галогеналкильная группа" представляет собой вышеупомянутую "C1-C4-галогеналкильную группу", замещенную вышеупомянутой "C1-C4-алкоксигруппой", и они могут связываться в любом замещаемом положении. Конкретные примеры включают этоксимонофторметильную группу и так далее.
Термин "C1-C4-галогеналкокси-C1-C4-галогеналкильная группа" представляет собой вышеупомянутую "C1-C4-галогеналкильную группу", замещенную вышеупомянутой "C1-C4-галогеналкоксигруппой", и они могут связываться в любом замещаемом положении.
[0064]
Термин "C1-C6-алкилкарбонильная группа" означает алкилкарбонильную группу, в которой алкильный фрагмент представляет собой вышеупомянутую "C1-C6-алкильную группу", конкретные примеры включают метилкарбонильную группу, этилкарбонильную группу, н-пропилкарбонильную группу и так далее.
Термин "C1-C6-алкоксикарбонильная группа" означает алкоксикарбонильную группу, в которой алкоксифрагмент представляет собой вышеупомянутую "C1-C6-алкоксигруппу", конкретные примеры включают метоксикарбонильную группу, этоксикарбонильную группу, н-пропоксикарбонильную группу, трет-бутоксикарбонильную и так далее.
Термин "C1-C6-алкилкарбонилоксигруппа" означает алкилкарбонилоксигруппу, в которой алкилкарбонильный фрагмент представляет собой вышеупомянутую "C1-C6-алкилкарбонильную группу", конкретные примеры включают метилкарбонилоксигруппу, этилкарбонилоксигруппу, н-пропилкарбонилоксигруппу и так далее.
Термин "C1-C6-галогеналкилкарбонильная группа" означает галогеналкилкарбонильную группу, в которой галогеналкильный фрагмент представляет собой вышеупомянутую "C1-C6-галогеналкильную группу", в частности, представляет собой трифторметилкарбонильную группу и так далее.
Термин "C1-C6-галогеналкоксикарбонильная группа" означает галогеналкоксикарбонильную группу, в которой галогеналкоксифрагмент представляет собой вышеупомянутую "C1-C6-галогеналкоксигруппу".
Термин "C1-C6-галогеналкилкарбонилоксигруппа" означает галогеналкилкарбонилоксигруппу, в которой галогеналкилкарбонильный фрагмент представляет собой вышеупомянутую "C1-C6-галогеналкилкарбонильную группу".
[0065]
Термин "C3-C7-циклоалкильная группа" означает моноциклическую насыщенную углеродную кольцевую группу, содержащую от 3 до 7 атомов углерода. Конкретные примеры включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу и так далее.
[0066]
Термин "моноциклическое насыщенное гетероциклическое кольцо" означает 3-7-членное насыщенное моноциклическое кольцо, содержащее по меньшей мере один из атома кислорода, атома азота или атома серы, конкретные примеры включают азиридин, азетидин, пирролидин, пиперидин, пиперазин, азепан, оксетан, тетрагидрофуран, тетрагидропиран, морфолин, тиоморфолин и так далее.
Термин "гетероциклоалкильная группа" означает моноциклическую насыщенную гетероциклическую кольцевую группу, в которой по меньшей мере один из атомов углерода в "C3-C7-циклоалкильной группе" заменен атомом кислорода, атомом азота или атомом серы. Конкретные примеры "гетероциклоалкильной группы" включают азетидинильную группу, пирролидинильную группу, пиперидильную группу, пиперазинильную группу, морфолиногруппу и так далее.
[0067]
Термин "C3-C7-циклоалкилоксигруппа" означает циклоалкилоксигруппу, в которой циклоалкильный фрагмент представляет собой вышеупомянутую "C3-C7-циклоалкильную группу".
Термин "гетероциклоалкилоксигруппа" означает гетероциклоалкилоксигруппу, в которой гетероциклоалкильный фрагмент представляет собой вышеупомянутую "гетероциклоалкильную группу".
[0068]
Термин "C2-C6-алкенильная группа" означает прямую или разветвленную алкенильную группу, содержащую 2-6 атомов углерода и одну или несколько двойных связей. Положения двойных связей не ограничены. Конкретные примеры включают винильную группу, аллильную группу, 1-пропенильную группу, 2-пропенильную группу, изопропенильную группу, изобутенильную группу, 3-метил-3-бутенильную группу и так далее.
Термин "C2-C6-алкенилоксигруппа" означает алкенилоксигруппу, в которой алкенильный фрагмент представляет собой вышеупомянутую "C2-C6-алкенильную группу", конкретные примеры включают винилоксигруппу, аллилоксигруппу, 1-бутенилоксигруппу, 2-бутенилоксигруппу, 3-бутенилоксигруппу и так далее.
Термин "C2-C6-алкенилокси-C1-C4-алкильная группа" означает вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "C2-C6-алкенилоксигруппой", и они могут связываться в любом замещаемом положении. Например, можно указать винилоксиметильную группу, аллилоксиметильную группу и так далее.
Термин "C2-C6-алкенилокси-C1-C4-галогеналкильная группа" означает вышеупомянутую "C1-C4-галогеналкильную группу", замещенную вышеупомянутой "C2-C6-алкенилоксигруппой", и они могут связываться в любом замещаемом положении.
[0069]
Термин "C2-C6-алкинильная группа" означает прямую или разветвленную алкинильную группу, содержащую 2-6 атомов углерода и одну или несколько тройных связей. Положения тройных связей не ограничены. Конкретные примеры включают этинильную группу, 1-пропинильную группу, 2-пропинильную группу, 3-метил-1-бутинильную группу и так далее.
Термин "C2-C6-алкинилоксигруппа" означает алкинилоксигруппу, в которой алкинильный фрагмент представляет собой вышеупомянутую "C2-C6-алкинильную группу".
Термин "C2-C6-алкинилокси-C1-C4-алкильная группа" означает вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "C2-C6-алкинилоксигруппой", и они могут связываться в любом замещаемом положении.
Термин "C2-C6-алкинилокси-C1-C4-галогеналкильная группа" означает вышеупомянутую "C1-C4-галогеналкильную группу", замещенную вышеупомянутой "C2-C6-алкинилоксигруппой", и они могут связываться в любом замещаемом положении.
[0070]
Термин "C1-C4-алкокси-C1-C4-алкоксигруппа" означает вышеупомянутую "C1-C4-алкоксигруппу", замещенную вышеупомянутой "C1-C4-алкоксигруппой", и они могут связываться в любом замещаемом положении.
Термин "C1-C4-галогеналкокси-C1-C4-алкоксигруппа" означает вышеупомянутую "C1-C4-алкоксигруппу", замещенную вышеупомянутой "C1-C4-галогеналкоксигруппой", и они могут связываться в любом замещаемом положении. Конкретные примеры включают 2-(трифторметокси)этоксигруппу и так далее.
Термин "C2-C6-алкенилокси-C1-C4-алкоксигруппа" означает вышеупомянутую "C1-C4-алкоксигруппу", замещенную вышеупомянутой "C2-C6-алкенилоксигруппой", и они могут связываться в любом замещаемом положении.
Термин "C2-C6-алкинилокси-C1-C4-алкоксигруппа" означает вышеупомянутую "C1-C4-алкоксигруппу", замещенную вышеупомянутой "C2-C6-алкинилоксигруппой", и они могут связываться в любом замещаемом положении. Например, можно указать аллилоксиметоксигруппу и так далее.
Термин "C2-C6-алкенилокси-C1-C4-галогеналкоксигруппа" означает вышеупомянутую "C1-C4-галогеналкоксигруппу", замещенную вышеупомянутой "C2-C6-алкенилоксигруппой", и они могут связываться в любом замещаемом положении.
Термин "C2-C6-алкинилокси-C1-C4-галогеналкоксигруппа" означает вышеупомянутую "C1-C4-галогеналкоксигруппу", замещенную вышеупомянутой "C2-C6-алкинилоксигруппой", и они могут связываться в любом замещаемом положении.
[0071]
Термин "C1-C6-алкилтиогруппа" означает алкилтиогруппу, в которой алкильный фрагмент соответствует определению, приведенному для вышеупомянутой "C1-C6-алкильной группы", конкретные примеры включают метилтиогруппу, этилтиогруппу, н-пропилтиогруппу, изопропилтиогруппу, н-бутилтиогруппу и так далее.
Термин "C1-C4-алкилтиогруппа" означает алкилтиогруппу, в которой алкильный фрагмент соответствует определению, приведенному для вышеупомянутой "C1-C4-алкильной группы".
Термин "C1-C6-галогеналкилтиогруппа" означает алкилтиогруппу, в которой один или несколько атомов водорода в вышеупомянутой "C1-C6-алкилтиогруппе" замещены атомами галогена, конкретные примеры включают трифторметилтиогруппу, 2,2,2-трифторэтилтиогруппу и так далее.
Термин "C1-C4-галогеналкилтиогруппа" означает алкилтиогруппу, в которой один или несколько атомов водорода в вышеупомянутой "C1-C4-алкилтиогруппе" замещены атомами галогена.
Термин "C1-C4-алкилтио-C1-C4-алкильная группа" означает вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "C1-C4-алкилтиогруппой", и они могут связываться в любом замещаемом положении.
Термин "C1-C4-галогеналкилтио-C1-C4-алкильная группа" означает вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "C1-C4-галогеналкилтиогруппой", и они могут связываться в любом замещаемом положении. Конкретные примеры включают трифторметилтиометильную группу, ((2',2',2'-трифторэтил)тио)метильную группу, 2-((трифторметил)тио)этильную группу, 2-((2',2',2'-трифторэтил)тио)этильную группу и так далее.
Термин "C1-C4-алкилтио-C1-C4-галогеналкильная группа" означает вышеупомянутую "C1-C4-галогеналкильную группу", замещенную вышеупомянутой "C1-C4-алкилтиогруппой", и они могут связываться в любом замещаемом положении.
Термин "C1-C4-галогеналкилтио-C1-C4-галогеналкильная группа" означает вышеупомянутую "C1-C4-галогеналкильную группу", замещенную вышеупомянутой "C1-C4-галогеналкилтиогруппой", и они могут связываться в любом замещаемом положении.
Термин "C1-C6-алкилсульфонильная группа" означает вышеупомянутую "C1-C6-алкильную группу", замещенную сульфонильной группой, и они могут связываться в любом замещаемом положении.
[0072]
Термин "C3-C7-циклоалкил-C1-C4-алкильная группа" означает вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "C3-C7-циклоалкильной группой", и они могут связываться в любом замещаемом положении. Конкретные примеры включают циклопропилметильную группу и так далее.
Термин "гетероциклоалкил-C1-C4-алкильная группа" означает вышеупомянутую "C1-C4-алкильную группу", замещенную вышеупомянутой "гетероциклоалкильной группой", и они могут связываться в любом замещаемом положении. Конкретные примеры включают оксетанилметильную группу, пирролидинилметильную группу, морфолинометильную группу и так далее.
Термин "аралкильная группа" означает вышеупомянутую "C1-C6алкильную группу", замещенную фенильной группой, 5-членной гетероарильной группой или 6-членной гетероарильной группой. Они могут связываться по любому замещаемому положению. Конкретные примеры включают бензильную группу, фенэтильную группу и так далее.
[0073]
Термин "5-членный гетероарил" означает 5-членное моноциклическое ароматическое гетерокольцо, содержащее один или несколько (например, от одного до четырех) гетероатомов, выбранных из атома азота, атома серы и атома кислорода в дополнение к атомам углерода. Конкретные примеры включают пиррол, фуран, тиофен, имидазол, пиразол, оксазол, изоксазол, тиазол, изотиазол, тиадиазол, оксадиазол, триазол, тетразол и так далее.
Термин "5-членная гетероарильная группа" означает группу вышеупомянутого "5-членного гетероарила", при этом конкретные примеры включают пирролильную группу (например, 2-пирролильную группу), фурильную группу (например, 3-фурильную группу), тиенильную группу (например, 2-тиенильную группу), имидазолильную группу (например, 4-имидазолильную группу), пиразолильную группу (например, 3-пиразолильную группу) и так далее.
Термин "6-членный гетероарил" означает 6-членное моноциклическое ароматическое гетерокольцо, содержащее один или несколько (например, от одного до трех) атомов азота в дополнение к атомам углерода. Конкретные примеры включают пиридин, пиридазин, пиримидин, пиразин, триазин и так далее.
Термин "6-членная гетероарильная группа" означает группу "6-членного гетероарила", при этом конкретные примеры включают пиридильную группу (например, 2-пиридильную группу, 3-пиридильную группу, 4-пиридильную группу), пиридазинильную группу (например, 3-пиридазинильную группу), пиримидинильную группу (например, 5-пиримидинильную группу), пиразинильную группу (например, 2-пиразинильную группу) и так далее.
[0074]
В данном описании термин "моноциклическое кольцо" включает все из моноциклического насыщенного карбоциклического кольца, моноциклического частично насыщенного карбоциклического кольца, моноциклического ненасыщенного карбоциклического кольца, моноциклического насыщенного гетероциклического кольца, моноциклических частично насыщенных гетероциклов, моноциклического ненасыщенного гетероциклического кольца и моноциклического ароматического кольца, если не описано иное.
В данном описании термин "бициклическое кольцо" включает все из бициклического насыщенного карбоциклического кольца, бициклического частично насыщенного карбоциклического кольца, бициклического ненасыщенного карбоциклического кольца, бициклического насыщенного гетероциклического кольца, бициклического насыщенного гетероциклического кольца, бициклического частично насыщенного гетероциклического кольца, бициклических ненасыщенных гетероциклов и бициклического ароматического кольца, если не описано иное.
[0075]
В данном описании далее объясняется значение заместителей с термином "необязательно замещенные". При этом термин "замещенный" означает, что один или несколько атомов водорода в любом положении замещены атомом или функциональной группой, отличными от атома водорода, если не указано иное.
[0076]
В R2 из общей формулы (I) или общей формулы (I-E2) заместитель "необязательно замещенной C1-C6-алкильной группы", "необязательно замещенной C1-C6-галогеналкильной группы", "необязательно замещенной C2-C6-алкенильной группы", "необязательно замещенной C2-C6-алкинильной группы" или "необязательно замещенного насыщенного, частично насыщенного или ненасыщенного 3-7-членного моноциклического кольца" обозначает заместитель, выбранный из группы, состоящей из атома галогена, цианогруппы, карбоксильной группы, карбоксамидной группы, гидроксигруппы, C1-C4-алкильной группы, C1-C4-галогеналкильной группы, C1-C4-алкоксигруппы, C1-C4-галогеналкоксигруппы, C3-C7-циклоалкильной группы, гетероциклоалкильной группы, C3-C7-циклоалкилоксигруппы, гетероциклоалкилоксигруппы, C1-C4-алкилтиогруппы, C1-C4-галогеналкилтиогруппы и -NRd1Rd2 (при этом Rd1 и Rd2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу). Они могут замещаться по всем замещаемым положениям с помощью одного или нескольких заместителей.
[0077]
В R3a, R3b, R3c, R11b и R11c из общей формулы (I) или общей формулы (I-E2) заместитель "необязательно замещенной C1-C6-алкильной группы", "необязательно замещенной C1-C6-галогеналкильной группы", "необязательно замещенной C1-C6-алкоксигруппы", "необязательно замещенной C1-C6-галогеналкоксигруппы", "необязательно замещенной C1-C4-алкокси-C1-C4-алкильной группы", "необязательно замещенной C1-C4-галогеналкокси-C1-C4-алкильной группы", "необязательно замещенной C1-C4-алкокси-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C4-галогеналкокси-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C6-алкилкарбонильной группы", "необязательно замещенной C1-C6-алкоксикарбонильной группы", "необязательно замещенной C1-C6-алкилкарбонилоксигруппы", "необязательно замещенной C1-C6-галогеналкилкарбонильной группы", "необязательно замещенной C1-C6-галогеналкоксикарбонильной группы", "необязательно замещенной C1-C6-галогеналкилкарбонилоксигруппы", "необязательно замещенной C3-C7-циклоалкильной группы", "необязательно замещенной гетероциклоалкильной группы", "необязательно замещенной C3-C7-циклоалкилоксигруппы", "необязательно замещенной гетероциклоалкилоксигруппы", "необязательно замещенной C2-C6-алкенильной группы", "необязательно замещенной C2-C6-алкенилоксигруппы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-алкильной группы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-галогеналкильной группы", "необязательно замещенной C2-C6-алкинильной группы", "необязательно замещенной C2-C6-алкинилоксигруппы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-алкильной группы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C4-алкокси-C1-C4-алкоксигруппы", "необязательно замещенной C1-C4-галогеналкокси-C1-C4-алкоксигруппы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-алкоксигруппы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-алкоксигруппы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-галогеналкоксигруппы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-галогеналкоксигруппы", "необязательно замещенной C1-C6-алкилтиогруппы", "необязательно замещенной C1-C6-галогеналкилтиогруппы", "необязательно замещенной C1-C4-алкилтио-C1-C4-алкильной группы", "необязательно замещенной C1-C4-галогеналкилтио-C1-C4-алкильной группы", "необязательно замещенной C1-C4-алкилтио-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C4-галогеналкилтио-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C6-алкилсульфонильной группы" обозначает заместитель, выбранный из группы, состоящей из атома галогена, цианогруппы, карбоксильной группы, карбоксамидной группы, гидроксигруппы, C1-C4-алкильной группы, C1-C4-галогеналкильной группы, C1-C4-алкоксигруппы, C1-C4-галогеналкоксигруппы, C3-C7-циклоалкильной группы, гетероциклоалкильной группы, C3-C7-циклоалкилоксигруппы, гетероциклоалкилоксигруппы, C1-C4-алкилтиогруппы, C1-C4-галогеналкилтиогруппы, метиламиногруппы, диметиламиногруппы, этиламиногруппы, диэтиламиногруппы, этилметиламиногруппы, (2,2,2-трифторэтил)аминогруппы, метил-(2,2,2-трифторэтил)аминогруппы, этил-(2,2,2-трифторэтил)аминогруппы, бис(2,2,2-трифторэтил)аминогруппы, метиламинокарбонильной группы, диметиламинокарбонильной группы, этиламинокарбонильной группы, диэтиламинокарбонильной группы и этилметиламинокарбонильной группы. Они могут замещаться по всем замещаемым положениям с помощью одного или нескольких заместителей.
[0078]
В R4a, R4b или R4c из общей формулы (I) или общей формулы (I-E2) заместитель "необязательно замещенной C1-C6алкильной группы", "необязательно замещенной C1-C6-галогеналкильной группы", "необязательно замещенной C1-C6-алкоксигруппы", "необязательно замещенной C1-C6-галогеналкоксигруппы", "необязательно замещенной C1-C4-алкокси-C1-C4-алкильной группы", "необязательно замещенной C1-C4-галогеналкокси-C1-C4-алкильной группы", "необязательно замещенной C1-C4-алкокси-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C4-галогеналкокси-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C6-алкилкарбонильной группы", "необязательно замещенной C1-C6-алкоксикарбонильной группы", "необязательно замещенной C1-C6-алкилкарбонилоксигруппы", "необязательно замещенной C1-C6-алкоксикарбонилоксигруппы", "необязательно замещенной C1-C6-галогеналкилкарбонильной группы", "необязательно замещенной C1-C6-галогеналкоксикарбонильной группы", "необязательно замещенной C1-C6-галогеналкилкарбонилоксигруппы", "необязательно замещенной C3-C7-циклоалкильной группы", "необязательно замещенной гетероциклоалкильной группы", "необязательно замещенной C3-C7-циклоалкилоксигруппы", "необязательно замещенной гетероциклоалкилоксигруппы", "необязательно замещенной C2-C6-алкенильной группы", "необязательно замещенной C2-C6-алкенилоксигруппы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-алкильной группы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-галогеналкильной группы", "необязательно замещенной C2-C6-алкинильной группы", "необязательно замещенной C2-C6-алкинилоксигруппы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-алкильной группы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C4-алкокси-C1-C4-алкоксигруппы", "необязательно замещенной C1-C4-галогеналкокси-C1-C4-алкоксигруппы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-алкоксигруппы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-алкоксигруппы", "необязательно замещенной C2-C6-алкенилокси-C1-C4-галогеналкоксигруппы", "необязательно замещенной C2-C6-алкинилокси-C1-C4-галогеналкоксигруппы", "необязательно замещенной C1-C6-алкилтиогруппы", "необязательно замещенной C1-C6-галогеналкилтиогруппы", "необязательно замещенной C1-C4-алкилтио-C1-C4-алкильной группы", "необязательно замещенной C1-C4-галогеналкилтио-C1-C4-алкильной группы", "необязательно замещенной C1-C4-алкилтио-C1-C4-галогеналкильной группы", "необязательно замещенной C1-C4-галогеналкилтио-C1-C4-галогеналкильной группы" обозначает заместитель, выбранный из группы, состоящей из атома галогена, цианогруппы, карбоксильной группы, карбоксамидной группы, гидроксигруппы, C1-C4-алкильной группы, C1-C4-галогеналкильной группы, C1-C4-алкоксигруппы, C1-C4-галогеналкоксигруппы, C3-C7-циклоалкильной группы, гетероциклоалкильной группы, C3-C7-циклоалкилоксигруппы, гетероциклоалкилоксигруппы, C1-C4-алкилтиогруппы и C1-C4-галогеналкилтиогруппы. Они могут замещаться по всем замещаемым положениям с помощью одного или нескольких заместителей.
[0079]
В отношении производного гетероароматического амида по настоящему изобретению или его соли общей формулы (I) или общей формулы (I-E2) ниже в данном документе объясняются предпочтительные атомы, группы-заместители и кольца. Предпочтительным является соединение по настоящему изобретению, содержащее по меньшей мере одно из предпочтительных атомов, заместителей или колец; более предпочтительным является соединение по настоящему изобретению, содержащее несколько предпочтительных атомов, заместителей или колец.
[0080]
Предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-OCH2CH2CH2-, -OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-
-OCH2CH2-, -OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCR4aR4bCH2CH2CH2-,
-OCH2CR4aHCH2CH2-, -OCH2CR4aR4bCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-, -CH2CH2OCH2-, -CH2CR4aHOCH2-
-CH2CH2CH2CH2-, -CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-,
-CH2CH2CR4aHCH2-, -CH2CH2CR4aR4bCH2-,
-CH2SCH2CH2-, -CH2SO2CH2CH2-,
-NHCH2CH2CH2-, -NR4cCH2CH2CH2-, -NR4cCR4aHCH2CH2-,
-NHCR4aHCH2CH2-,
-CH2NR4cCH2CH2-, -CH2NR4cCR4aHCH2-, -CH2NHCR4aHCH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2-;
более предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-,
-OCH2CH2-, -OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCR4aR4bCH2CH2CH2-,
-OCH2CR4aHCH2CH2-, -OCH2CR4aR4bCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-, -CH2CH2OCH2-, -CH2CR4aHOCH2-
-CH2CH2CH2CH2-, -CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-,
-CH2CH2CR4aHCH2-, -CH2CH2CR4aR4bCH2-,
-CH2SCH2CH2-, -CH2SO2CH2CH2-,
-NHCH2CH2CH2-, -NR4cCH2CH2CH2-, -NR4cCR4aHCH2CH2-,
-NHCR4aHCH2CH2-,
-CH2NR4cCH2CH2-, -CH2NR4cCR4aHCH2-, -CH2NHCR4aHCH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2-.
При этом, например, "Y1, Y2, Y3 и Y4 вместе образуют -OCR4aHCH2CH2-" означает, что Y1 представляет собой -O-, Y2 представляет собой -CR4aH-, Y3 представляет собой -CH2-, и Y4 представляет собой -CH2-.
[0081]
Если X1-X2 представляет собой C-N (а именно, в случае, если X1 представляет собой атом углерода, и X2 представляет собой атом азота), предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-OCH2CH2CH2-, -OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-, -OCH2CH2-,
-OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCH2CR4aHCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-,
-CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-, -CH2CH2CR4aHCH2-,
-NHCH2CH2CH2-, -NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2-.
В данном случае более предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-, -OCH2CH2-,
-OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCH2CR4aHCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-,
-CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-, -CH2CH2CR4aHCH2-,
-NHCH2CH2CH2-, -NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2-.
В данном случае еще более предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-, -OCH2CH2-, -OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCH2CR4aHCH2CH2-, -CH2CR4aHCH2CH2-,
-NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2-.
В данном случае еще более предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-, -OCR4aHCH2-,
-OCR4aHCH2CH2CH2-, -CH2CR4aHCH2CH2-,
-NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2-.
В данном случае особенно предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-OCR4aHCH2CH2-.
Кроме того, в данном случае в другом аспекте настоящего изобретения особенно предпочтительные Y1, Y2, Y3 и Y4 вместе образуют -CH2NR4cCH2CH2-.
[0082]
Если X1-X2 представляет собой N-C (а именно, в случае, если X1 представляет собой атом азота, и X2 представляет собой атом углерода), предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-CH2CH2OCH2-, -CH2CR4aHOCH2-,
-CH2CH2CH2CH2-, -CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2-.
В данном случае более предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-CH2CH2OCH2-, -CH2CR4aHOCH2-, -CH2CR4aHCH2CH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2-.
В данном случае еще более предпочтительные Y1, Y2, Y3 и Y4 вместе образуют
-CH2CR4aHOCH2-, -CH2CR4aHCH2CH2-, -CH2CH2NR4cCH2-,
-CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2-.
[0083]
Z1 предпочтительно представляет собой одинарную связь, -CR7aR7b-, -O- или -S- и более предпочтительно - одинарную связь.
[0084]
Кольцо A представляет собой 3-7-членное моноциклическое ароматическое кольцо или 8-12-членное бициклическое ароматическое кольцо.
В одном варианте осуществления настоящего изобретения предпочтительное кольцо A представляет собой 3-7-членное моноциклическое ароматическое кольцо; например, в данном случае кольцо A представляет собой фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил, пиримидинил, тетразолил, изотиазолил, оксадиазолил, изоксазолил или тиадиазолил.
В данном случае предпочтительно кольцо A представляет собой фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил;
в данном случае более предпочтительно кольцо A представляет собой фенил, пиридил, пиразинил, пиридазинил или пиримидинил;
в данном случае еще более предпочтительно кольцо A представляет собой фенил.
[0085]
В одном варианте осуществления настоящего изобретения предпочтительное кольцо A представляет собой 8-12-членное бициклическое ароматическое кольцо;
например, в данном случае кольцо A представляет собой хинолинил, изохинолилфталадинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, бензоимидазолил, индолил, изоиндолил, бензооксазолинил, бензофуранил, изобензофуранил или индазолил.
В данном случае предпочтительно кольцо A представляет собой хинолил, бензоимидазолил, индолил или бензооксазолинил.
В данном случае более предпочтительно кольцо A представляет собой 8-хинолил, 1-бензоимидазолил, 3-индолил или 2-бензооксазолинил.
[0086]
R1a и R1b независимо друг от друга представляют собой атом водорода, атом галогена, гидроксигруппу, цианогруппу, C1-C4-алкильную группу, C1-C4-галогеналкильную группу, C1-C4-алкоксигруппу, C1-C4-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C1-C4-алкокси-C1-C4-алкильную группу или C1-C4-галогеналкокси-C1-C4-алкильную группу;
предпочтительно R1a и R1b независимо друг от друга представляют собой атом водорода, атом галогена, C1-C4-алкильную группу или C1-C4-галогеналкильную группу,
более предпочтительно R1a и R1b независимо друг от друга представляют собой атом водорода или атом галогена.
[0087]
R2 представляет собой атом водорода, атом галогена, гидроксигруппу, цианогруппу, необязательно замещенную C1-C6-алкильную группу, необязательно замещенную C1-C6-галогеналкильную группу, необязательно замещенную C2-C6-алкенильную группу, необязательно замещенную C2-C6-алкинильную группу или необязательно замещенное насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо.
Предпочтительно R2 представляет собой атом водорода, атом галогена, гидроксигруппу, цианогруппу или необязательно замещенное насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо;
более предпочтительно R2 представляет собой атом водорода или необязательно замещенное, насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо.
[0088]
В одном варианте осуществления настоящего изобретения предпочтительный R2 представляет собой атом водорода, атом галогена, гидроксигруппу или цианогруппу; в данном случае более предпочтительно R2 представляет собой атом водорода.
[0089]
Кроме того, в другом аспекте настоящего изобретения, если R2 представляет собой необязательно замещенное насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо, R2 предпочтительно представляет собой необязательно замещенное 3-7-членное моноциклическое ароматическое кольцо.
[0090]
Более того, в другом аспекте настоящего изобретения, если R2 представляет собой необязательно замещенное, насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо,
R2 предпочтительно представляет собой насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо, необязательно замещенное атомом галогена, цианогруппой, карбоксильной группой, карбоксамидной группой, гидроксигруппой, C1-C4-алкильной группой, C1-C4-галогеналкильной группой, C1-C4-алкоксигруппой, C1-C4-галогеналкоксигруппой, C3-C7-циклоалкильной группой, гетероциклоалкильной группой, C3-C7-циклоалкилоксигруппой, гетероциклоалкилоксигруппой, C1-C4-алкилтиогруппой, C1-C4-галогеналкилтиогруппой или -NRd1Rd2 (при этом Rd1 и Rd2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу).
В данном случае более предпочтительно R2 представляет собой ненасыщенное 3-7-членное моноциклическое кольцо, необязательно замещенное атомом галогена, цианогруппой, C1-C4-алкильной группой, C1-C4-галогеналкильной группой, C1-C4-алкоксигруппой, C1-C4-галогеналкоксигруппой или -NRd1Rd2 (при этом Rd1 и Rd2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу).
[0091]
Предпочтительно R3a, R3b и R3c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксигруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, замещенную гетероциклооксигруппой, C1-C6-алкильную группу, замещенную цианогруппой, C1-C6-алкильную группу, замещенную морфолиногруппой, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, замещенную диметиламиногруппой, C1-C4-алкокси-C1-C4-алкильную группу, замещенную диметиламинокарбонильной группой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-алкилкарбонилоксигруппу, C1-C6-галогеналкилкарбонильную группу, C1-C6-галогеналкоксикарбонильную группу, C1-C6-галогеналкилкарбонилоксигруппу, C3-C7-циклоалкильную группу, гетероциклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкенилокси-C1-C4-алкильную группу, C2-C6-алкенилокси-C1-C4-галогеналкильную группу, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена, C2-C6-алкинилоксигруппу, C2-C6-алкинилокси-C1-C4-алкильную группу, C2-C6-алкинилокси-C1-C4-галогеналкильную группу, C1-C4-алкокси-C1-C4-алкоксигруппу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C2-C6-алкенилокси-C1-C4-алкоксигруппу, C2-C6-алкинилокси-C1-C4-алкоксигруппу, C2-C6-алкенилокси-C1-C4-галогеналкоксигруппу, C2-C6-алкинилокси-C1-C4-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, C1-C4-алкилтио-C1-C4-галогеналкильную группу, C1-C4-галогеналкилтио-C1-C4-галогеналкильную группу, C1-C6-алкилсульфонильную группу, -(CH2)pNRa1Ra2 (при этом Ra1 и Ra2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу, и p равняется 0, 1 или 2) или группу, представленную общей формулой (I-A),
[0092]
[Хим. 26]
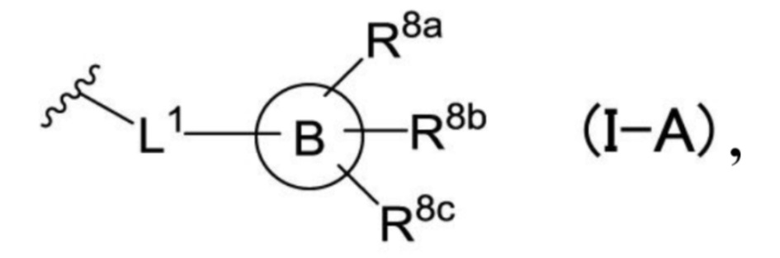
где
кольцо B, L1, R8a, R8b и R8c имеют такое же определение, что и в (0).
[0093]
Более предпочтительно R3a, R3b и R3c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксигруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную диметиламинокарбонильной группой или диметиламиногруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C2-C6-алкенильную группу, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, -(CH2)pNRa1Ra2 (при этом p, Ra1 и Ra2 имеют такое же определение, что и в (0)) или группу, представленную общей формулой (I-A),
[0094]
[Хим. 27]

где
кольцо B представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L1 представляет собой одинарную связь, -CH2-, -CH2O-, -OCH2-, -CH2CH2- или -CH2OCH2-,
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкильную группу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу или C2-C6-алкинильную группу.
[0095]
Более предпочтительно R3a, R3b и R3c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкильную группу, C2-C6-алкенильную группу, C2-C6-алкинильную группу, -(CH2)pNRa1Ra2 (при этом p равняется 1, и Ra1 и Ra2 независимо друг от друга представляют собой атом водорода, метильную группу, этильную группу или 2,2,2-трифторэтильную группу) или группу, представленную общей формулой (I-A),
[0096]
[Хим. 28]

где
кольцо B представляет собой C3-C7-циклоалкил, морфолино, фенил, пиразолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L1 представляет собой одинарную связь,
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу.
[0097]
Еще более предпочтительно R3a, R3b и R3c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу.
[0098]
Предпочтительно R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксигруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксигруппой, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-алкилкарбонилоксигруппу, C1-C6-галогеналкилкарбонильную группу, C1-C6-галогеналкоксикарбонильную группу, C1-C6-галогеналкилкарбонилоксигруппу, C3-C7-циклоалкильную группу, C3-C7-циклоалкильную группу, необязательно замещенную атомом галогена, гетероциклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкенилокси-C1-C4-алкильную группу, C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную атомом галогена, C2-C6-алкенилокси-C1-C4-галогеналкильную группу, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C2-C6-алкинилоксигруппу, C2-C6-алкинилокси-C1-C4-алкильную группу, C2-C6-алкинилокси-C1-C4-галогеналкильную группу, C1-C4-алкокси-C1-C4-алкоксигруппу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C2-C6-алкенилокси-C1-C4-алкоксигруппу, C2-C6-алкинилокси-C1-C4-алкоксигруппу, C2-C6-алкенилокси-C1-C4-галогеналкоксигруппу, C2-C6-алкинилокси-C1-C4-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, C1-C4-алкилтио-C1-C4-галогеналкильную группу, C1-C4-галогеналкилтио-C1-C4-галогеналкильную группу, пентафторсульфанильную группу, -(CH2)qNRb1Rb2 (при этом Rb1 и Rb2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу, и q равняется 0, 1, 2 или 3) или группу, представленную общей формулой (I-B),
[0099]
[Хим. 29]
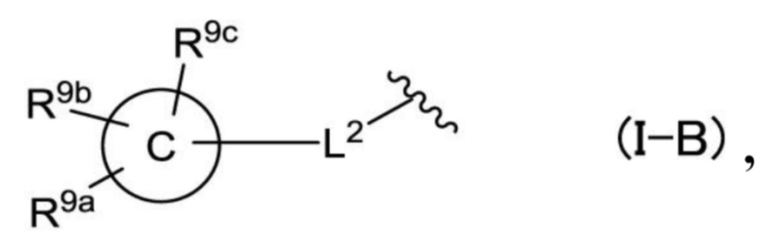
где
кольцо C, L2, R9a, R9b, R9c имеют такое же определение, что и в (0).
[0100]
Более предпочтительно R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксигруппой, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-галогеналкилкарбонильную группу, C3-C7-циклоалкильную группу, C3-C7-циклоалкильную группу, необязательно замещенную атомом галогена или C1-C4-галогеналкильной группой, гетероциклоалкильную группу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкенилокси-C1-C4-алкильную группу, C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную атомом галогена, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C2-C6-алкинилокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или группу общей формулы (I-B),
[0101]
[Хим. 30]

где
кольцо C представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L2 представляет собой одинарную связь, -CH=CH-, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2S(CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO(CR10eR10f)r3(CR10gR10h)r4- (при этом R10a, R10b, R10c, R10d, R10e, R10f, R10g, R10h, r1, r2, r3, r4 и Rc имеют такое же определение, что и в (0)),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкоксикарбонильную группу, гетероциклоалкилоксигруппу или -(CH2)sNRd1Rd2 (при этом s, Rd1 и Rd2 имеют такое же определение, что и в (0)).
[0102]
В одном варианте осуществления настоящего изобретения предпочтительные R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу или -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)),
более предпочтительно - атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой или C1-C4-галогеналкокси-C1-C4-алкильной группой, или C1-C4-галогеналкокси-C1-C4-алкоксигруппу.
[0103]
Кроме того, в другом аспекте настоящего изобретения, если R4a, R4b и R4c представляют собой группы, представленные общей формулой (I-B), более предпочтительно R4a, R4b и R4c представляют собой заместитель, выбранный из группы, состоящей из следующих формул:
[0104]
[Хим. 31]
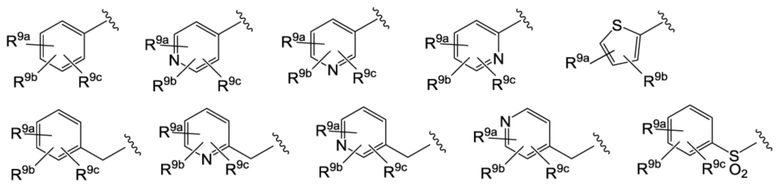
[0105]
[Хим. 32]

[0106]
[Хим. 33]
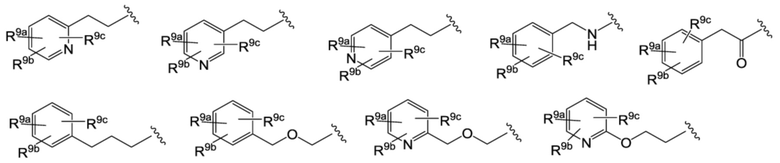
[0107]
[Хим. 34]

[0108]
[Хим. 35]

[0109]
[Хим. 36]

где R9a, R9b и R9c имеют такое же определение, что и в (0),
в данном случае более предпочтительно R4a, R4b и R4c представляют собой заместитель, выбранный из группы, состоящей из следующих формул:
[0110]
[Хим. 37]

где R9a, R9b и R9c имеют такое же определение, что и в (0),
в данном случае еще более предпочтительно R4a, R4b и R4c представляют собой заместитель, выбранный из группы, состоящей из следующего:
[0111]
[Хим. 38]
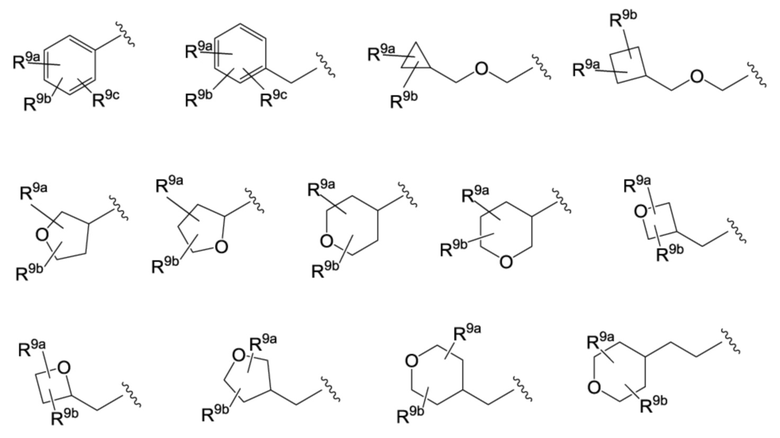
где R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу.
[0112]
Кроме того, в другом аспекте настоящего изобретения предпочтительные R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или заместитель, выбранный из группы, состоящей из следующих формул:
[0113]
[Хим. 39]
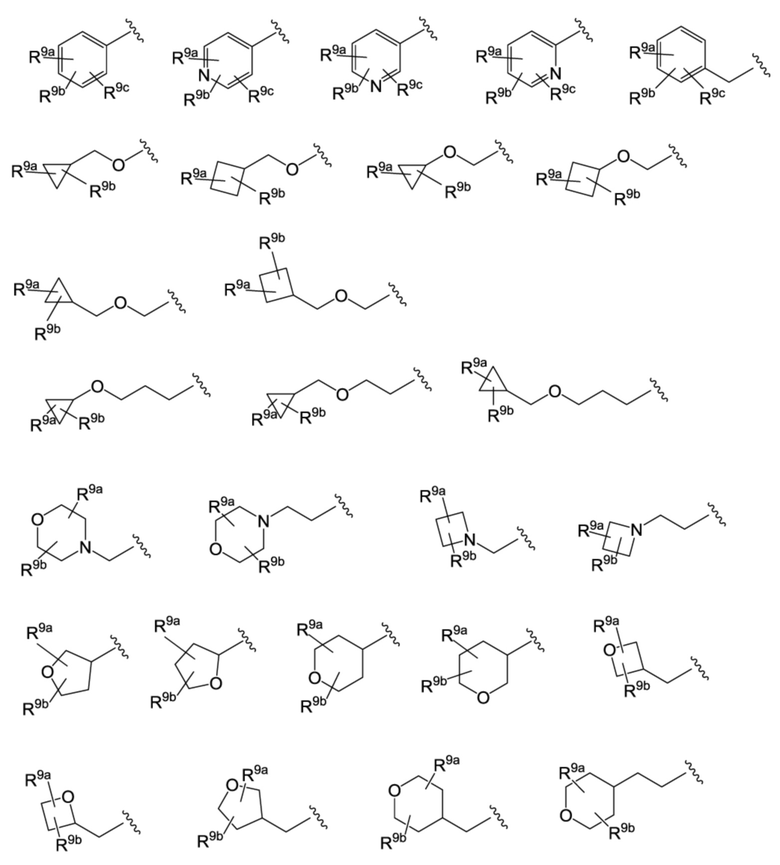
где R9a, R9b и R9c имеют такое же определение, что и в (0),
более предпочтительные R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу или заместитель, выбранный из группы, состоящей из следующих формул:
[0114]
[Хим. 40]

где R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу.
[0115]
Если R5a, R5b, R5c, R6a, R6b и n соответствуют положению (i) в (0), предпочтительными являются соединения по настоящему изобретению, где
R5b и R5c вместе образуют одинарную связь, -CH2O-, -CH2S-, -CH2NRe1-, -CH2CH2- или -CONRe1- (при этом Re1 и Re2 имеют такое же определение, что и в (0)),
R5a представляет собой атом водорода или C1-C6-алкильную группу,
R6a и R6b независимо друг от друга представляют собой атом водорода, атом фтора, гидроксигруппу или метоксигруппу, и
n равняется 1 или 2.
Более предпочтительно предпочтительными являются соединения по настоящему изобретению, где из R5a, R5b, R5c, R6a и R6b R5b и R5c вместе образуют -CH2O-, R5a, R6a и R6b представляют собой атомы водорода, и n равняется 1.
[0116]
В общей формуле (I-E2) Z2-Z3 предпочтительно представляет собой -CH2O-, -CH2S-, -CH2NRf1-, -CH2CH2- или -CONRf1- (при этом Rf1 и Rf2 представляют собой атом водорода или C1-C4-алкильную группу),
более предпочтительно Z2-Z3 образует -CH2O-.
[0117]
В общей формуле (I) или общей формуле (I-E2) R5a более предпочтительно представляет собой атом водорода, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C3-C7-циклоалкильную группу или гетероциклоалкильную группу,
более предпочтительно R5a представляет собой атом водорода.
[0118]
В общей формуле (I-E2), если Z4 представляет собой C-R11a, R11a предпочтительно представляет собой атом водорода, атом галогена, цианогруппу, цианометильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу,
более предпочтительно R11a представляет собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу или C1-C6-галогеналкильную группу,
более предпочтительно R11a представляет собой атом водорода.
[0119]
В общей формуле (I-E2) R11b соответствует R3b в (0); его предпочтительным заместителем является вышеупомянутый предпочтительный R3b.
В общей формуле (I-E2) R11c соответствует R3c в (0); его предпочтительным заместителем является вышеупомянутый предпочтительный R3c.
[0120]
В отношении производного гетероароматического амида по настоящему изобретению или его соли общей формулы (I-E2) ниже в данном документе объясняются предпочтительные комбинации атомов, группы-заместители или кольца.
[0121]
В одном варианте осуществления настоящего изобретения в соединении, представленном общей формулой (I-E2), содержащей R11a, R11b, R11c и по меньшей мере одно из R4a, R4b и R4c, предпочтительные комбинации таких заместителей выбраны из группы, состоящей из следующего:
R11a представляет собой атом водорода, атом галогена, цианогруппу, цианометильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу,
R11b и R11c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксигруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную диметиламинокарбонильной группой или диметиламиногруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C2-C6-алкенильную группу, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, -(CH2)pNRa1Ra2 (при этом p, Ra1 и Ra2 имеют такое же определение, что и в (0)) или группу, представленную общей формулой (I-A),
[0122]
[Хим. 41]
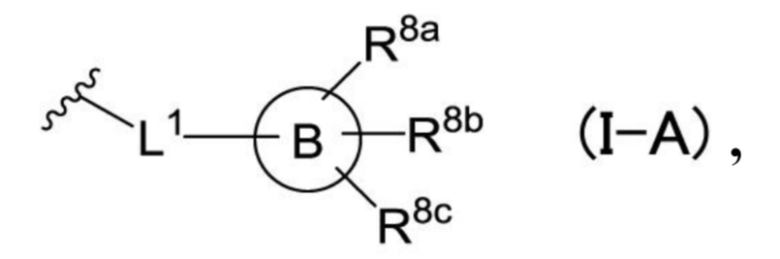
где
кольцо B представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L1 представляет собой одинарную связь, -CH2-, -CH2O-, -OCH2-, -CH2CH2- или -CH2OCH2-,
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкильную группу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу или C2-C6-алкинильную группу,
R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или заместитель, выбранный из группы, состоящей из следующих формул:
[0123]
[Хим. 42]

где R9a, R9b и R9c имеют такое же определение, что и в (0).
[0124]
В одном варианте осуществления настоящего изобретения в соединении, представленном общей формулой (I) или общей формулой (I-E2), содержащими R2 и по меньшей мере одно из R4a, R4b и R4c, предпочтительные комбинации таких заместителей выбраны из группы, состоящей из следующего:
R2 представляет собой атом водорода, атом галогена, гидроксигруппу или цианогруппу,
R4a, R4b и R4c независимо друг от друга представляют собой атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксигруппой, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-галогеналкилкарбонильную группу, C3-C7-циклоалкильную группу, C3-C7-циклоалкильную группу, необязательно замещенную атомом галогена или C1-C4-галогеналкильной группой, гетероциклоалкильную группу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкенилокси-C1-C4-алкильную группу, C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную атомом галогена, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C2-C6-алкинилокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или группу общей формулы (I-B),
[0125]
[Хим. 43]

где
кольцо C представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L2 представляет собой одинарную связь, -CH=CH-, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2S(CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO(CR10eR10f)r3(CR10gR10h)r4- (при этом R10a, R10b, R10c, R10d, R10e, R10f, R10g, R10h, r1, r2, r3, r4 и Rc имеют такое же определение, что и в (0)),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкоксикарбонильную группу, гетероциклоалкилоксигруппу или -(CH2)sNRd1Rd2 (при этом s, Rd1 и Rd2 имеют такое же определение, что и в (0)).
[0126]
В одном варианте осуществления настоящего изобретения в соединении, представленном общей формулой (I-E2), содержащей Z2-Z3, R6a, R6b, R11a, R11b и R11c, предпочтительные комбинации таких заместителей выбраны из группы, состоящей из следующего:
Z2-Z3 представляет собой -CH2O-, -CH2S-, -CH2NRf1-, -CH2CH2- или -CONRf1- (при этом Rf1 и Rf2 представляют собой атом водорода или C1-C4-алкильную группу),
R6a и R6b независимо друг от друга представляют собой атом водорода, атом фтора, гидроксигруппу или метоксигруппу,
R11a представляет собой атом водорода, атом галогена, цианогруппу, цианометильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу,
R11b и R11c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксигруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную диметиламинокарбонильной группой или диметиламиногруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C2-C6-алкенильную группу, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, -(CH2)pNRa1Ra2 (при этом p, Ra1 и Ra2 имеют такое же определение, что и в (0)) или группу общей формулы (I-A),
[0127]
[Хим. 44]

где
кольцо B представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L1 представляет собой одинарную связь, -CH2-, -CH2O-, -OCH2-, -CH2CH2- или -CH2OCH2-,
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкильную группу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу или C2-C6-алкинильную группу.
[0128]
В отношении производного гетероароматического амида по настоящему изобретению, представленного общей формулой (I) или (I-E2), далее объясняются предпочтительные соединения.
[0129]
В одном варианте осуществления настоящего изобретения предпочтительные соединения производного гетероароматического амида, представленного общей формулой (I-E2), представляют собой производные гетероароматического амида или их соль, представленные в вышеописанных (4) - (15).
[0130]
В другом варианте осуществления настоящего изобретения, например, соединения по настоящему изобретению, которые относятся к следующему "производному", являются предпочтительными в соединениях производного гетероароматического амида, представленного общей формулой (I) или общей формулой (I-E2). Любое "производное" включает его фармацевтически приемлемую соль, и одно соединение может относиться к нескольким группам "производных".
[0131]
Производное типа (a):
группа соединений, где в общей формуле (I) или в общей формуле (I-E2) X1-X2 представляет собой C-N, и Y1 представляет собой -O-; в частности, производное 2,3-дигидропиразоло[5,1-b]оксазола, производное 6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазина, производное 5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксепина и т. п.
Производное типа (b):
группа соединений, где в общей формуле (I) или в общей формуле (I-E2) X1-X2 представляет собой C-N, и Y1 представляет собой -CH2-; в частности, производное 4,5,6,7-тетрагидропиразоло[1,5-a]пиразина, производное 4,5,6,7-тетрагидропиразоло[1,5-a]пиридина, производное 6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазина и т. п.
Производное типа (c):
группа соединений, где в общей формуле (I) или в общей формуле (I-E2) X1-X2 представляет собой N-C, и Y1 представляет собой -CH2-; в частности, производное 5,6,7,8-тетрагидроимидазо[1,2-a]пиридина, производное 5,6,7,8-тетрагидроимидазо[1,2-a]пиразина, производное 5,6-дигидро-8H-имидазо[2,1-c][1,4]оксазина и т. п.
Производное типа (d):
производные гетероароматического амида общей формулы (I) или общей формулы (I-E2), где R2 представляет собой необязательно замещенное насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо.
[0132]
Каждое "производное" далее объясняется в отдельности для демонстрации соединений в предпочтительных вариантах осуществления. При этом любое соединение в каждом "производном" предусматривает оптически активные вещества и их фармацевтически приемлемые соли.
[0133]
В качестве производных типа (a) общей формулы (I) или общей формулы (I-E2) в соответствии с настоящим изобретением предпочтительными являются следующие соединения.
[0134]
a1) Производное гетероароматического амида или его соль, представленное общей формулой (I-G) ниже:
[0135]
[Хим. 45]

где
Y2, Y3, Y4, R1a, R1b, R6a и R6b имеют такое же определение, что и в (0),
Z2-Z3, Z4, R5a, R11b и R11c имеют такое же определение, что и в (7),
R2 представляет собой атом водорода, атом галогена, гидроксигруппу или цианогруппу,
при условии, что по меньшей мере один из Y2, Y3 или Y4 представляет собой -CR4aR4b-,
CR4aH-, -CH2CR4aR4b-, -CH2CR4aH- или -NR4c- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)).
[0136]
a2) Производное гетероароматического амида или его соль, описанные в a1), где в общей формуле (I-G):
Y2, Y3 и Y4 вместе образуют
-CR4aHCH2CH2-, -CR4aR4bCH2CH2-, -CH2CH2-, -CR4aHCH2-,
-CR4aR4bCH2-, -CH2CH2CH2CH2-, -CR4aHCH2CH2CH2- или -CH2CR4aHCH2CH2- (при этом R4a, R4b имеют такое же определение, что и в (0)).
[0137]
a3) Производное гетероароматического амида или его соль, описанные в a2) или a3), где в общей формуле (I-G):
Z2-Z3 представляет собой -CH2O-, -CH2S-, -CH2NRf1-, -CH2CH2- или -CONRf1- (при этом Rf1 и Rf2 имеют такое же определение, что и в (7)),
при этом R5a, R6a и R6b представляют собой атомы водорода.
[0138]
a4) Производное гетероароматического амида или его соль по любому из a1) - a3), где в общей формуле (I-G):
Z2-Z3 представляет собой -CH2O-,
R11a представляет собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу или C1-C6-галогеналкильную группу,
R11b и R11c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, формильную группу, нитрогруппу, карбоксамидную группу, гидроксигруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную диметиламинокарбонильной группой или диметиламиногруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C2-C6-алкенильную группу, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, -(CH2)pNRa1Ra2 (при этом p, Ra1 и Ra2 имеют такое же определение, что и в (0)) или группу, представленную общей формулой (I-A),
[0139]
[Хим. 46]
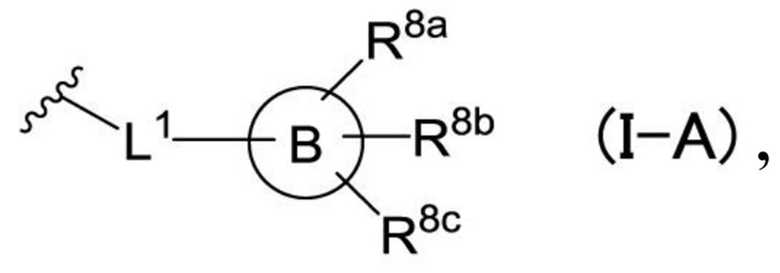
где
кольцо B представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L1 представляет собой одинарную связь, -CH2-, -CH2O-, -OCH2-, -CH2CH2- или -CH2OCH2- (при этом Ra1 и Ra2 имеют такое же определение, что и в (0)),
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C3-C7-циклоалкильную группу, C3-C7-циклоалкилоксигруппу, гетероциклоалкильную группу, гетероциклоалкилоксигруппу, C2-C6-алкенильную группу или C2-C6-алкинильную группу.
[0140]
a5) Производное гетероароматического амида или его соль по любому из a1) - a4), где в общей формуле (I-G):
R4a представляет собой атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксигруппой, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-галогеналкильную группу, C1-C4-галогеналкокси-C1-C4-галогеналкильную группу, C1-C6-алкилкарбонильную группу, C1-C6-алкоксикарбонильную группу, C1-C6-галогеналкилкарбонильную группу, C3-C7-циклоалкильную группу, C3-C7-циклоалкильную группу, необязательно замещенную атомом галогена или C1-C4-галогеналкильной группой, гетероциклоалкильную группу, C2-C6-алкенильную группу, C2-C6-алкенилоксигруппу, C2-C6-алкенилокси-C1-C4-алкильную группу, C2-C6-алкенилокси-C1-C4-алкильную группу, необязательно замещенную атомом галогена, C2-C6-алкинильную группу, C2-C6-алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C2-C6-алкинилокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или группу, представленную общей формулой (I-B),
[0141]
[Хим. 47]

где
кольцо C представляет собой C3-C7-циклоалкил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолино, фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L2 представляет собой одинарную связь, -CH=CH-, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2S(CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO(CR10eR10f)r3(CR10gR10h)r4 (при этом R10a, R10b, R10c, R10d, R10e, R10f, R10g, R10h, r1, r2, r3, r4 и Rc имеют такое же определение, что и в (0)),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкоксикарбонильную группу, гетероциклоалкилоксигруппу или -(CH2)sNRd1Rd2 (при этом s, Rd1 и Rd2 имеют такое же определение, что и в (0)).
[0142]
a6) Производное гетероароматического амида или его соль по любому из a1) - a5), где в общей формуле (I-G):
Y2, Y3 и Y4 вместе образуют -CR4aHCH2CH2-,
каждый R4a независимо представляет собой атом галогена, гидроксигруппу, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4-галогеналкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкоксигруппу, C1-C4-алкилтио-C1-C4-алкильную группу, C1-C4-галогеналкилтио-C1-C4-алкильную группу, -(CH2)qNRb1Rb2 (при этом q, Rb1 и Rb2 имеют такое же определение, что и в (0)) или заместители, выбранные из группы, состоящей из следующих формул:
[0143]
[Хим. 48]
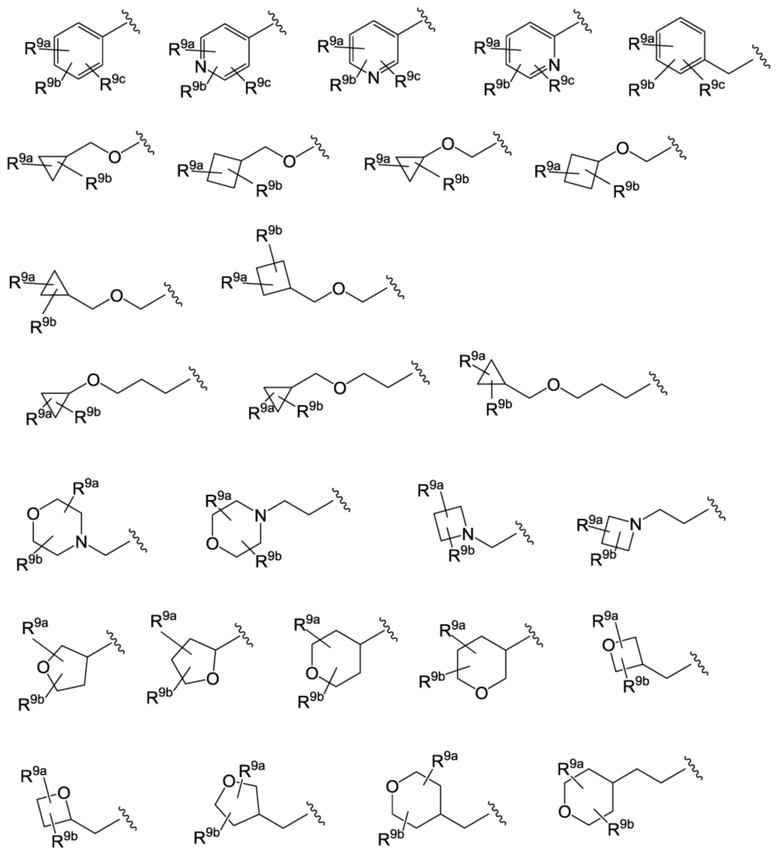
где R9a, R9b и R9c имеют такое же определение, что и в (0),
R11a представляет собой атом водорода,
R11b и R11c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, цианометильную группу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-галогеналкокси-C1-C4-алкильную группу, C2-C6-алкенильную группу, C2-C6-алкинильную группу, -(CH2)pNRa1Ra2 (при этом p равняется 1, и Ra1 и Ra2 независимо друг от друга представляют собой атом водорода, метильную группу, этильную группу или 2,2,2-трифторэтильную группу) или группу, представленную общей формулой (I-A),
[0144]
[Хим. 49]
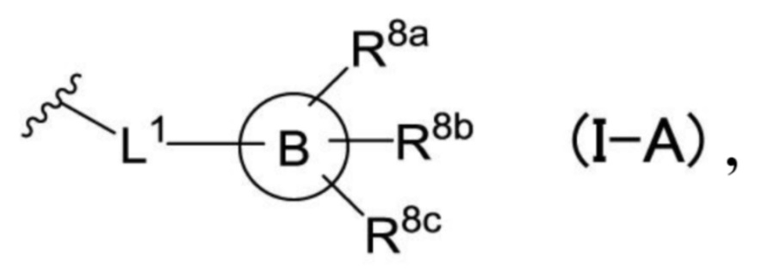
где
кольцо B представляет собой C3-C7-циклоалкил, морфолино, фенил, пиразолил, пиридил, пиразинил, пиридазинил или пиримидинил,
L1 представляет собой одинарную связь,
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6-алкоксигруппу или C1-C6-галогеналкоксигруппу.
[0145]
a7) Производное гетероароматического амида или его соль в a1), где соединение, представленное общей формулой (I-G), представляет собой следующее (при этом значения чисел и звездочек (*) являются такими, как приведено в (15)):
[0146]
[Хим. 50]

[0147]
[Хим. 51]


[0148]
[Хим. 52]

[0149]
[Хим. 53]


[0150]
[Хим. 54]

 .
.
[0151]
[Хим. 55]
 .
.
[0152]
В качестве производных типа (b) общей формулы (I) или общей формулы (I-E2) в соответствии с настоящим изобретением предпочтительными являются следующие соединения.
[0153]
b1) Производное гетероароматического амида или его соль, представленное общей формулой (I-I):
[0154]
[Хим. 56]
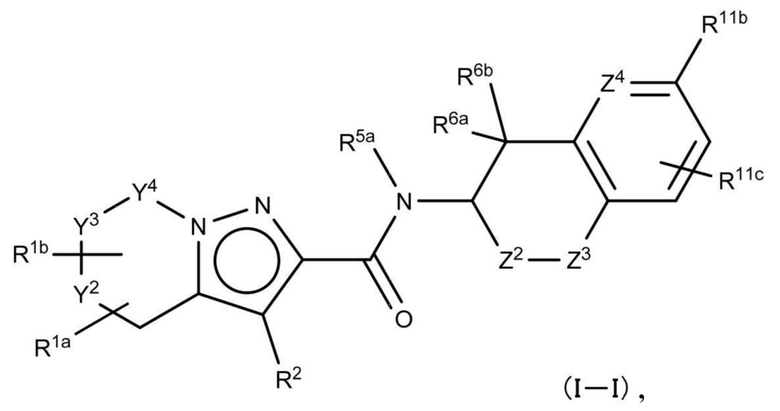
где
Y2, Y3, Y4, R1a, R1b, R2, R6a и R6b имеют такое же определение, что и в (0),
Z2-Z3, Z4, R5a, R11b, и R11c имеют такое же определение, что и в (7), при условии, что по меньшей мере один из Y2, Y3 или Y4 представляет собой -CR4aR4b-, -CR4aH-, -CH2CR4aR4b-, -CH2CR4aH- или -NR4c- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0).
[0155]
b2) Производное гетероароматического амида или его соль, приведенные в b1), где в общей формуле (I-I):
Y2, Y3 и Y4 вместе образуют
-OCH2CH2-, -OCH2CH2CH2-,
-CR4aHCH2CH2-, -CR4aR4bCH2CH2-, -CH2CR4aHCH2- или -NR4cCH2CH2- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)).
[0156]
b3) Производное гетероароматического амида или его соль из b1) или b2), где в общей формуле (I-I):
Z2-Z3 представляет собой -CH2O-, -CH2S-, -CH2NRf1-, -CH2CH2- или -CONRf1- (при этом Rf1 и Rf2 имеют такое же определение, что и в (7)),
при этом R5a, R6a и R6b представляют собой атомы водорода.
[0157]
b4) Производное гетероароматического амида или его соль, приведенные в b1), где соединение, представленное общей формулой (I-I), представляет собой следующее (при этом значения чисел являются такими, как приведено в (15)).
[0158]
[Хим. 57]

 [0159]
[0159]
В качестве производных типа (c) общей формулы (I) или общей формулы (I-E2) в соответствии с настоящим изобретением предпочтительными являются следующие соединения.
[0160]
c1) Производное гетероароматического амида или его соль, представленное общей формулой (I-K):
[0161]
[Хим. 58]

где
Y2, Y3, Y4, R1a, R1b, R2, R6a и R6b имеют такое же определение, что и в (0),
Z2-Z3, Z4, R5a, R11b и R11c имеют такое же определение, что и в (7) (при условии, что кольцо C не является фенильным кольцом, если Y2, Y3 и Y4 вместе образуют -CR4aHCH2CH2-, R2 представляет собой атом водорода, R4a представляет собой группу, представленную общей формулой (I-B), и L2 представляет собой одинарную связь, и
при условии, что по меньшей мере один из Y2, Y3 или Y4 представляет собой -CR4aR4b-, -CR4aH-, -CH2CR4aR4b-, -CH2CR4aH- или -NR4c- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)).
[0162]
c2) Производное гетероароматического амида или его соль, приведенные в c1), где в общей формуле (I-K):
Y2, Y3 и Y4 вместе образуют
-CR4aHOCH2-, -CR4aHCH2CH2-,
-CH2NR4cCH2-, -CR4aHNR4cCH2- или -CR4aHNHCH2- (при этом R4a и R4c имеют такое же определение, что и в (0)).
[0163]
c3) Производное гетероароматического амида или его соль из c1) или c2), где в общей формуле (I-K):
Z2-Z3 представляет собой -CH2O-, -CH2S-, -CH2NRf1-, -CH2CH2- или -CONRf1- (при этом Rf1 и Rf2 имеют такое же определение, что и в (7)),
при этом R5a, R6a и R6b представляют собой атом водорода.
[0164]
c4) Производное гетероароматического амида или его соль в c1), где соединение, представленное общей формулой (I-K), представляет собой следующее (при этом значения чисел являются такими, как приведено в (15)).
[0165]
[Хим. 59]
 .
.
[0166]
В качестве производных типа (d) общей формулы (I) или общей формулы (I-E2) в соответствии с настоящим изобретением предпочтительными являются следующие соединения.
[0167]
d1) Производное гетероароматического амида или его соль, представленное общей формулой (I-E2):
[0168]
[Хим. 60]

где
R1a, R1b, R6a и R6b имеют такое же определение, что и в (0),
Z2-Z3, Z4, R5a, R11b и R11c имеют такое же определение, что и в (7),
R2 представляет собой необязательно замещенное, насыщенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо, и
Y1, Y2, Y3 и Y4 вместе образуют
-OCH2CH2CH2-, -OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-
-OCH2CH2-, -OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-, -OCR4aR4bCH2CH2CH2-,
-OCH2CR4aHCH2CH2-, -OCH2CR4aR4bCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-, -CH2CH2OCH2-, -CH2CR4aHOCH2-
-CH2CH2CH2CH2-, -CH2CR4aHCH2CH2-, -CH2CR4aR4bCH2CH2-,
-CH2CH2CR4aHCH2-, -CH2CH2CR4aR4bCH2-,
-CH2SCH2CH2-, -CH2SO2CH2CH2-,
-NHCH2CH2CH2-, -NR4cCH2CH2CH2-, -NR4cCR4aHCH2CH2-, -NHCR4aHCH2CH2-,
-CH2NR4cCH2CH2-, -CH2NR4cCR4aHCH2-, -CH2NHCR4aHCH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2- (при этом R4a, R4b и R4c имеют такое же определение, что и в (0)),
X1-X2 представляет собой N-C или C-N, при условии, что Y1, Y2, Y3 и Y4 вместе не образуют -OCH2CH2CH2-, -OCR4aHCH2CH2- или -OCR4aR4bCH2CH2- в случае C-N.
[0169]
d2) Производное гетероароматического амида или его соль, приведенные в d1), где в общей формуле (I-E2):
Z2-Z3 представляет собой -CH2O-, -CH2S-, -CH2NRf1-, -CH2CH2- или -CONRf1- (при этом Rf1 и Rf2 имеют такое же определение, что и в (7)),
при этом R5a, R6a и R6b представляют собой атом водорода.
[0170]
d3) Производное гетероароматического амида или его соль, приведенные в любом из d1) - d2), где в общей формуле (I-E2):
R2 представляет собой фенил, пирролил, фурил, тиенил, имидазолил, пиразолил, оксазолил, тиазолил, триазолил, пиридил, пиразинил, пиридазинил, пиримидинил, тетразолил, изотиазолил, оксазолил, изоксазолил или тиадиазолил, где каждый из них необязательно замещен атомом галогена, цианогруппой, C1-C4-алкильной группой, C1-C4-галогеналкильной группой, C1-C4-алкоксигруппой, C1-C4-галогеналкоксигруппой или -NRd1Rd2 (при этом Rd1 и Rd2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу).
[0171]
d4) Производное гетероароматического амида или его соль, приведенные в любом из d1) - d3), где в общей формуле (I-E2):
R2 представляет собой фенил, пиразолил, триазолил, пиридил или пиразинил, где каждый из них необязательно замещен атомом галогена, цианогруппой, C1-C4-алкильной группой, C1-C4-галогеналкильной группой, C1-C4-алкоксигруппой, C1-C4-галогеналкоксигруппой или -NRd1Rd2 (при этом Rd1 и Rd2 независимо друг от друга представляют собой атом водорода, C1-C4-алкильную группу или C1-C4-галогеналкильную группу).
[0172]
d5) Производное гетероароматического амида или его соль, приведенные в любом из d1) - d4), где в общей формуле (I-E2):
R2 представляет собой фенил, пиразолил или пиридил, где каждый из них необязательно замещен атомом галогена, метильной группой, этильной группой, трифторметильной группой, трифторметоксигруппой, трифторэтильной группой, трифторэтоксигруппой или -NHRd2 (при этом Rd2 представляет собой метильную группу, этильную группу, трифторметильную группу или трифторэтильную группу).
[0173]
d6) Производное гетероароматического амида или его соль, приведенные в d1), где соединение, представленное общей формулой (I) или общей формулой (I-E2), представляет собой следующее (при этом значения чисел являются такими, как приведено в (15)).
[0174]
[Хим. 61].

[0175]
В качестве соли соединения по настоящему изобретению, представленного общей формулой (I), предпочтительной является фармацевтически приемлемая соль. "Фармакологически приемлемая соль" конкретно не ограничена при условии, что она представляет собой фармакологически приемлемую соль. Она предусматривает соли неорганических кислот, такие как гидрохлорид, гидробромид, нитрат, сульфат, фосфат; соли органических карбоновых кислот, такие как ацетат, оксалат, фумарат, малеат, малонат, цитрат, сукцинат, лактат, тартрат и малат; соли ароматических карбоновых кислот, такие как салицилат и бензоат; органические сульфонаты, такие как метансульфонат, тозилат и бензолсульфонат; соли щелочных металлов, такие как соль лития, соль натрия и соль калия; соли щелочноземельных металлов, такие как соль кальция, соль магния и т. д.
[0176]
Если в соединении по настоящему изобретению, представленном общей формулой (I), существует асимметричный углерод, то его рацемат, диастереоизомеры и все оптически активные вещества включены в настоящее изобретение, и если существуют геометрические изомеры, то любой из (E)-изомера, (Z)-изомера и их смесь включены в настоящее изобретение.
[0177]
Для соединения по настоящему изобретению, представленном общей формулой (I), сольваты, такие как гидрат и т. д., если они существуют, также включены в настоящее изобретение.
[0178]
Соединения, представленные общей формулой (I), т. е. производное гетероароматического амида по настоящему изобретению, можно получать различными способами; их можно получать, например, с помощью способов, представленных ниже, способов, подобных способам, представленным ниже, или путем соответствующего комбинирования способов, известных специалистам в данной области техники. Все исходные материалы и реакционные реагенты, применяемые в таких синтезах, являются коммерчески доступными или могут быть получены с применением коммерчески доступных соединений в соответствии со способами, общеизвестными специалистам в данной области техники. Кроме того, экстракцию, очистку и т. д. можно проводить в стандартных экспериментах органической химии. Кроме того, порядок, в котором следует проводить стадии, можно соответствующим образом изменять для всех следующих стадий.
[0179]
Соединение, представленное общей формулой (I), может быть получено, например, с помощью способа, показанного на следующей реакционной схеме-1.
<Реакционная схема-1>
[0180]
[Хим. 62]

где кольцо A, R1a, R1b, R2, R3a, R3b, R3c, R5a, R5b, R5c, R6a, R6b, n, X1, X2, Y1, Y2, Y3, Y4 и Z1 определены для общей формулы (I) в (0).
[0181]
(Стадия 1)
На стадии 1 соединение, представленное общей формулой (I), можно получать путем осуществления реакции конденсации соединения, представленного общей формулой (2), и соединения, представленного общей формулой (3), где в реакции конденсации применяют конденсирующий реагент в присутствии или при отсутствии основания. В качестве конденсирующих реагентов можно упомянуть N, N'-дициклогексилкарбодиимид (DCC), гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (EDC), 1,1'-карбонилдиимидазол (CDI), иодид 2-хлор-1-метилпиридиния, пропилфосфоновый ангидрид (циклический тример), гексафторфосфат O-(7-азабензотриазол-1-ил)-N, N,N',N'-тетраметилурония (HATU) и т. д.
В качестве основания можно упомянуть органические основания, такие как триметиламин, триэтиламин, диизопропилэтиламин, трипропиламин, триизопропиламин, трибутиламин, N-метилморфолин, пиридин, 4-(N, N-диметиламино)пиридин, N, N-диметиланилин, N, N-диэтиланилин, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,4-диазабицикло[2.2.2]октан (DABCO), 1,1,3,3-тетраметилгуанидин или 1,8-диазабицикло[5.4.0]-7-ундецен (DBU).
В качестве растворителя для реакционной смеси можно упомянуть галогенированные углеводородные растворители, такие как дихлорметан и т. д.; сложные эфиры, такие как этилацетат и т. д.; простые эфиры, такие как тетрагидрофуран и т. д.; амиды, такие как N, N-диметилформамид, N, N-диметилацетамид и т. д.; кетоны, такие как ацетон, метилэтилкетон и т. д.; ароматические углеводородные растворители, такие как толуол и т. д.; и смеси таких растворителей и т. д. При необходимости можно добавлять реакционный реагент, такой как 1-гидроксибензотриазол (HOBt) и т. д.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от 0°C до 100°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0182]
Кроме того, после дериватизации реакционного промежуточного соединения из соединения, представленного общей формулой (2), с применением активатора для карбоксильной группы соединение, представленное общей формулой (I), можно получать путем осуществления реакции с соединением, представленным общей формулой (3).
В качестве активатора для карбоксильной группы можно упомянуть тионилхлорид, оксалилхлорид, оксихлорид фосфора, фосген, трифосген, 1,1'-карбонилдиимидазол, этилхлоркарбонат и т. д.
В качестве растворителя для реакционной смеси можно упомянуть ароматические углеводородные растворители, такие как бензол, толуол хлорбензол, нитробензол, ксилол и т. д.; галогенированные углеводородные растворители, такие как хлороформ, дихлорметан и т. д.; простые эфиры, такие как тетрагидрофуран и т. д.; кетоны, такие как ацетон, метилэтилкетон и т. д.; нитрилы, такие как ацетонитрил, пропионитрил и т. д.; и смеси таких растворителей и т. д.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от 0°C до 100°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0183]
Среди соединений, представленных общей формулой (2) на реакционной схеме-1, соединение, представленное общей формулой (2-c), можно получать, например, с помощью способа, показанного на следующей реакционной схеме-3.
<Реакционная схема-3>
[0184]
[Хим. 63]
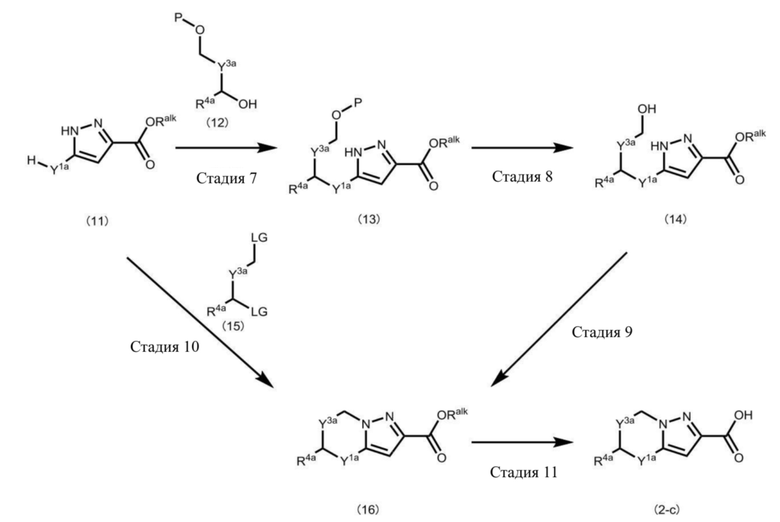
где
R4a является таковым, как определено для общей формулы (I) в (0);
Ralk представляет собой алкильную группу, содержащую от 1 до 8 атомов углерода, P представляет собой защитную группу, LG представляет собой уходящую группу (например, атом хлора, атом брома, атом йода, метансульфонилоксигруппу, трифторметансульфонилоксигруппу или п-толуолсульфонилоксигруппу и т. д.), Y1a представляет собой O или NH, и Y3a представляет собой одинарную связь, метилен или этилен.
[0185]
Защитная группа, представленная P, конкретно не ограничена при условии, что она является стандартно применяемой в качестве защитной группы для гидроксигруппы, следующее можно упомянуть в качестве примера: низшие алкильные группы, такие как метильная группа и т. д.; низшие алкоксиалкильные группы, такие как метоксиметильная группа, этоксиэтильная группа и т. д.; необязательно замещенные бензильные группы (в качестве заместителя можно упомянуть нитрогруппу, низшую алкоксигруппу и т. д.); низшие алкоксикарбонильные группы; низшие галогеналкоксикарбонильные группы; необязательно замещенные бензилоксикарбонильные группы (в качестве заместителя можно упомянуть нитрогруппу, низшую алкоксигруппу и т. д.); ацильные группы, такие как ацетильная группа, бензоильная группа и т. д.; трифенилметильную группу; тетрагидропиранильную группу; тризамещенные силильные группы, такие как триметилсилильная группа, триэтилсилильная группа, трет-бутилдиметилсилильная группа, триизопропилсилильная группа, диметилгексилсилильная группа, трет-бутилдифенилсилильная группа и т. д.
[0186]
(Стадия 7)
На стадии 7 соединение, представленное общей формулой (13), можно получать путем осуществления реакции соединения, представленного общей формулой (11), и соединения, представленного общей формулой (12), с производным азодикарбоновой кислоты и производным фосфина.
В качестве производного азодикарбоновой кислоты можно упомянуть этилазодикарбоксилат, изопропилазодикарбоксилат, 1,1'-(азодикарбонил)дипиперидин и т. д.
В качестве производного фосфина можно упомянуть трифенилфосфин, три-н-бутилфосфин и т. д. Кроме того, фосфорановый реагент, такой как цианометилентрибутилфосфоран, цианометилентриметилфосфоран и т. д., можно применять для проведения подобной реакции вместо производного азодикарбоновой кислоты и производного фосфина.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он представляет собой нейтральный растворитель; например, можно упомянуть тетрагидрофуран, толуол или их смесь.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от 0°C до 80°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0187]
Кроме того, соединение, представленное общей формулой (13), также можно получать путем осуществления реакции с соединением, представленным общей формулой (11), в присутствии основания после превращения гидроксигруппы в соединении, представленном общей формулой (12), в уходящую группу с помощью способа, общеизвестного специалистам в данной области техники.
В качестве реагента, превращающегося в уходящую группу, можно упомянуть следующее: тионилхлорид, сульфурилхлорид, оксалилхлорид, трихлорид фосфора, пентахлорид фосфора, трибромид фосфора, пентабромид фосфора, тетрабромметан, бромид диметилбромсульфония, тионилбромид, трииодид фосфора, п-толуолсульфонилхлорид, метансульфонилхлорид, трифторметансульфонилхлорид, трифторметансульфоновый ангидрид и т. д.
В качестве основания можно упомянуть следующее: неорганические основания, такие как карбонат калия, бикарбонат калия, ацетат калия, ацетат натрия, карбонат натрия, бикарбонат натрия, карбонат цезия, карбонат лития, фосфат трикалия, трет-бутоксид калия, трет-бутоксид натрия, фторид калия, гексаметилдисилазан калия или гидрид натрия и т. д.; органические основания, описанные выше (стадия 1).
В качестве растворителя для реакционной смеси можно упомянуть без ограничения ароматические углеводороды, такие как бензол, толуол, ксилол и т. д.; галогенированные углеводороды, такие как дихлорметан, хлороформ, 1,2-дихлорэтан и т. д.; нитрилы, такие как ацетонитрил, пропионитрил и т. д.; простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан и т. д.; апротонные полярные растворители, такие как N, N-диметилформамид, N, N-диметилацетамид, N-метилпирролидон, диметилсульфоксид и т. д. и смесь таких растворителей и т. д.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от комнатной температуры до 140°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0188]
(Стадия 8)
На стадии 8 соединение, представленное общей формулой (14), можно получать путем осуществления реакции удаления защитной группы для соединения, представленного общей формулой (13). Такие реакции удаления защитной группы можно проводить в соответствии со способами, общеизвестными специалистам в данной области техники (например, способами, описанными у Green и Wuts в "Protective Groups in Organic Synthesis" (3-е издание, 1999 г.)).
[0189]
(Стадия 9)
На стадии 9 соединение, представленное общей формулой (16), можно получать путем осуществления реакции соединения, представленного общей формулой (14), в присутствии или при отсутствии основания с галогенирующим реагентом и производным фосфина.
В качестве основания предпочтительным является, например, основание, описанное выше (стадия 7).
В качестве галогенирующего реагента можно упомянуть тетрахлорметан, тетрабромметан, гексахлорацетон, гексабромацетон, трифосген, бромид лития, метилиодид, бром и йод и т. д.
В качестве производного фосфина можно упомянуть трифенилфосфин, три-н-бутилфосфин и т. д.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, и для примера можно упомянуть растворители, описанные на (стадии 7).
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от комнатной температуры до 120°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0190]
(Стадия 10)
На стадии 10 соединение, представленное общей формулой (16), можно получать путем осуществления реакции циклизации соединения, представленного общей формулой (11), и соединения, представленного общей формулой (15), в присутствии или при отсутствии основания.
Предпочтительными являются, например, основания, описанные на (стадии 7) выше.
Для успешного проведения реакции можно дополнительно вводить добавку. В качестве добавки можно упомянуть иодид калия, иодид натрия, иодид тетрабутиламмония, бромид калия, бромид натрия, бромид тетрабутиламмония и т. д.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, и для примера можно упомянуть растворители, описанные на (стадии 7).
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от комнатной температуры до 120°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0191]
(Стадия 11)
На стадии 11 соединение, представленное общей формулой (2-c), можно получать путем гидролиза соединения, представленного общей формулой (16), в присутствии основания или кислоты, что представляет собой способ, подобный описанному на стадии 4 реакционной схемы-1.
[0192]
Среди соединений, представленных общей формулой (2) на реакционной схеме-1, соединение, представленное общей формулой (2-d), можно получать, например, с помощью способа, показанного на следующей реакционной схеме-5.
<Реакционная схема-5>
[0193]
[Хим. 64]
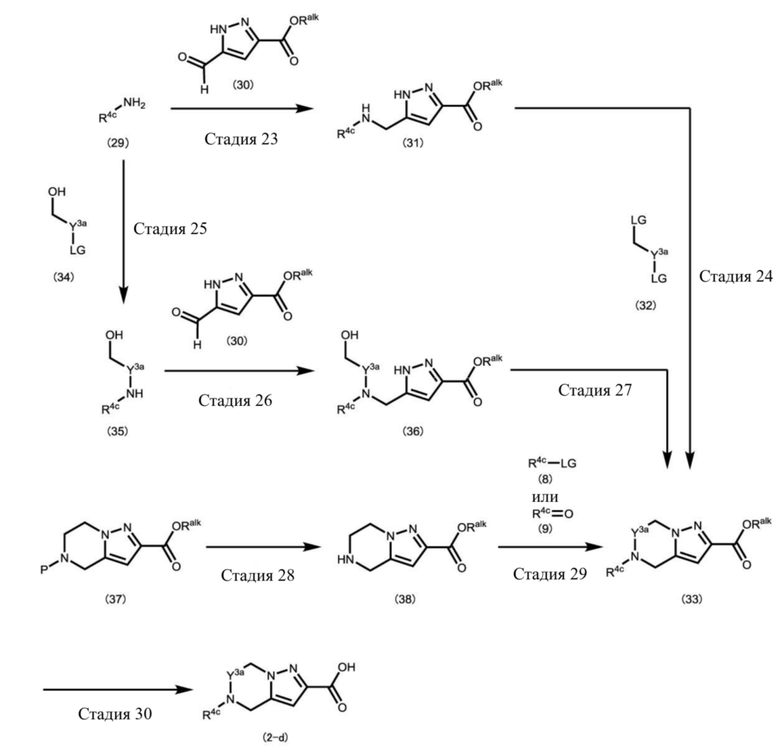
где R4c является таковым, как определено для общей формулы (I) в (0); кроме того, Ralk представляет собой алкильную группу, содержащую от 1 до 8 атомов углерода, P представляет собой защитную группу, LG представляет собой уходящую группу (например, атом хлора, атом брома, атом йода, метансульфонилоксигруппу, трифторметансульфонилоксигруппу или п-толуолсульфонилоксигруппу и т. д.), Y3a представляет собой метилен или этилен.
[0194]
Что касается защитной группы, представленной P, она конкретно не ограничена при условии, что ее обычно применяют в качестве защитной группы для аминогруппы; например, можно упомянуть следующее: трет-бутоксикарбонильную (Boc) группу, бензилоксикарбонил (Cbz), 9-флуоренилметилоксикарбонил (fmoc), ацетильную (Ac) группу, трифторацетильную группу, бензильную (Bn) группу, 4-метоксибензильную (PMB) группу и т. д.
[0195]
(Стадия 23)
На стадии 23 соединение, представленное общей формулой (31), можно получать путем осуществления реакции восстановительного алкилирования с соединением, представленным общей формулой (29), и соединением, представленным общей формулой (30), в присутствии или при отсутствии кислоты или основания, с применением восстанавливающего реагента.
В качестве основания предпочтительными являются, например, основания, описанные на (стадии 7) выше.
В качестве кислоты, подлежащей применению, можно упомянуть муравьиную кислоту, уксусную кислоту, пропионовую кислоту, изомасляную кислоту, гексановую кислоту, п-толуолсульфоновую кислоту или бензойную кислоту и т. д.
В качестве восстанавливающего реагента можно упомянуть борогидрид натрия, триацетоксиборогидрид натрия, цианоборогидрид натрия, диметиламин-боран, триэтиламин-боран, триметиламин-боран, трет-бутиламин-боран, N, N-диэтиланилин-боран или 2-пиколин-боран и т. д.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, и для примера можно упомянуть растворители, описанные на (стадии 7).
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от 0°C до 100°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0196]
(Стадия 24)
На стадии 24 соединение, представленное общей формулой (33), можно получать путем осуществления реакции циклизации с соединением, представленным общей формулой (31), и соединением, представленным общей формулой (32), в присутствии или при отсутствии основания, что представляет собой способ, подобный описанному на стадии 10 реакционной схемы-3.
[0197]
(Стадия 25)
На стадии 25 соединение, представленное общей формулой (35), можно получать путем осуществления реакции с соединением, представленным общей формулой (29), и соединением, представленным общей формулой (34), в присутствии или при отсутствии основания.
В качестве основания предпочтительным является, например, основание, описанное выше (стадия 7).
Для успешного проведения реакции можно дополнительно вводить добавку; в качестве добавки можно упомянуть добавку, описанную на (стадии 10).
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, и для примера можно упомянуть растворители, показанные на (стадии 7).
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от комнатной температуры до 120°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0198]
(Стадия 26)
На стадии 26 соединение, представленное общей формулой (36), можно получать путем осуществления реакции восстановительного алкилирования с соединением, представленным общей формулой (35), и соединением, представленным общей формулой (30), в присутствии или при отсутствии кислоты или основания с применением восстанавливающего реагента, что представляет собой способ, подобный описанному на стадии 23 реакционной схемы-5.
[0199]
(Стадия 27)
На стадии 27 соединение, представленное общей формулой (33), можно получать путем осуществления реакции соединения, представленного общей формулой (36), в присутствии или при отсутствии основания с галогенирующим реагентом и производным фосфина, что представляет собой способ, подобный описанному на стадии 9 реакционной схемы-3.
[0200]
(Стадия 28)
На стадии 28 соединение, представленное общей формулой (38), можно получать путем реакции удаления защитной группы с соединением, представленным общей формулой (37). Такие реакции удаления защитной группы можно проводить в соответствии со способами, общеизвестными специалистам в данной области техники (например, способами, описанными у Green и Wuts в "Protective Groups in Organic Synthesis" (3-е издание, 1999 г.)).
[0201]
(Стадия 29)
На стадии 29 соединение, представленное общей формулой (33), можно получать путем осуществления реакции соединения, представленного общей формулой (38), с соединением, представленным общей формулой (8), или с соединением, представленным общей формулой (9), что представляет собой способ, подобный описанному на стадии 5 схемы-2.
[0202]
(Стадия 30)
На стадии 30 соединение, представленное общей формулой (2-d), можно получать путем гидролиза соединения, представленного общей формулой (33), в присутствии основания или кислоты, что представляет собой способ, подобный описанному на стадии 4 схемы-2.
[0203]
Среди соединений, представленных общей формулой (2) на реакционной схеме-1, соединение, представленное общей формулой (2-e), можно получать, например, с помощью способа, показанного на следующей реакционной схеме-6.
<Реакционная схема-6>
[0204]
[Хим. 65]

где
R1a, R1b, X1, X2, Y1, Y2, Y3 и Y4 являются такими, как определено для общей формулы (I) в (0);
Ralk представляет собой алкильную группу, содержащую от 1 до 8 атомов углерода,
Rg и Rh независимо друг от друга представляют собой атом водорода или необязательно замещенную алкильную группу, или
Rg и Rh образуют необязательно замещенное неароматическое гетероциклическое кольцо, с которым связаны атомы кислорода, и при этом атом бора связан с атомом кислорода,
R2a представляет собой необязательно замещенное, частично насыщенное или ненасыщенное 3-7-членное моноциклическое кольцо,
Hal представляет собой атом галогена (например, атом хлора, атом брома, атом йода).
[0205]
(Стадия 31)
На стадии 31 соединение, представленное общей формулой (40), можно получать путем подвергания соединения, представленного общей формулой (39), действию галогенирующего реагента.
В качестве галогенирующего реагента можно упомянуть хлор, бром, йод, N-хлорсукцинимид, N-бромсукцинимид, N-йодсукцинимид, 1,3-дихлор-5,5-диметилгидантоин, 1,3-дибром-5,5-диметилгидантоин и т. д.
В данную реакцию можно добавлять соответствующую кислоту, такую как уксусная кислота, трифторуксусная кислота, хлористоводородная кислота и т. д.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, и для примера можно упомянуть растворители, описанные на (стадии 7).
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от комнатной температуры до 140°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0206]
(Стадия 32)
На стадии 32 соединение, представленное общей формулой (42), можно получать путем осуществления реакции соединения, представленного общей формулой (41), с соединением, представленным общей формулой (40), с дополнительным введением палладиевого катализатора и основания.
В качестве палладиевого катализатора можно упомянуть следующее: формы металлического палладия, такие как палладий на угле и палладиевая чернь и т. д.; органические соли палладия, такие как тетракис(трифенилфосфин)палладий, дихлорбис(трифенилфосфин)палладий, ацетат палладия, хлорид-1,1'-бис(дифенилфосфино)ферроценпалладия или бис(ди-трет-бутил-(4-диметиламинофенил)фосфин)дихлорпалладий(II); и органические комплексы палладия на полимерной подложке, такие как бис(ацетат)трифенилфосфинпалладий(II) на полимерной подложке и ди(ацетат)дициклогексилфенилфосфинпалладий(II) на полимерной подложке и т. д. Их можно применять в комбинации.
Добавляемое количество палладиевого катализатора относительно соединения, представленного общей формулой (40), обычно составляет от 1 до 50 мол. %, предпочтительно от 5 до 20 мол. %.
В качестве основания предпочтительным является, например, основание, описанное выше (стадия 7).
Для успешного проведения реакции можно дополнительно вводить добавку; в качестве добавки можно упомянуть следующее: триалкилфосфины, такие как триметилфосфин и три-трет-бутилфосфин и т. д.; трициклоалкилфосфины, такие как трициклогексилфосфин и т. д.; триарилфосфины, такие как трифенилфосфин и тритолилфосфин и т. д.; триалкилфосфиты, такие как триметилфосфит, триэтилфосфит и трибутилфосфит и т. д.; трициклоалкилфосфиты, такие как трициклогексилфосфит и т. д.; триарилфосфиты, такие как трифенилфосфит и т. д.; соль имидазолия, такую как хлорид 1,3-бис(2,4,6-триметилфенил)имидазолия и т. д.; дикетоны, такие как ацетилацетон и октафторацетилацетон и т. д.; амины, такие как триметиламин, триэтиламин, трипропиламин, триизопропиламин и трибутиламин и т. д.; 1,1'-бис(дифенилфосфино)ферроцен; 2,2'-бис(дифенилфосфино)-1,1'-бинафтил; 2-дициклогексилфосфино-2',6'-диметоксибифенил; 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил; 2-(ди-трет-бутилфосфино)-2',4',6'-триизопропилбифенил; 2-дициклогексилфосфино-2'-(N, N-диметиламино)бифенил; 4,5-бис(дифенилфосфино)-9,9-диметилксантен и 2-(ди-трет-бутилфосфино)бифенил. Такие добавки можно применять в комбинации.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, и для примера можно упомянуть растворители, описанные на (стадии 7).
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от комнатной температуры до 140°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0207]
(Стадия 33)
На стадии 33 соединение, представленное общей формулой (2-e), можно получать путем гидролиза соединения, представленного общей формулой (42), в присутствии основания или кислоты, что представляет собой способ, подобный описанному на стадии 4 схемы-2.
[0208]
Среди соединений, представленных общей формулой (3) на реакционной схеме-1, соединение, представленное общей формулой (3-a), можно получать, например, с помощью способа, показанного на следующей реакционной схеме-7.
<Реакционная схема-7>
[0209]
[Хим. 66]
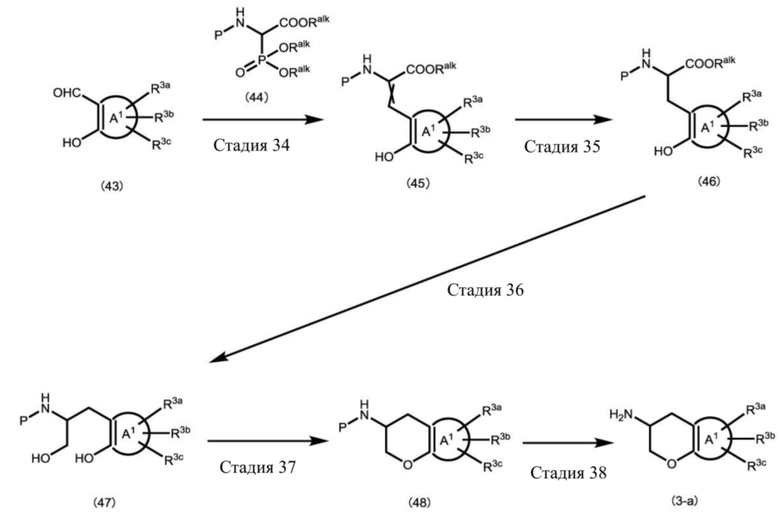
где
R3a, R3b, R3c являются таковыми, как определено для общей формулы (I) в (0);
кольцо A1 представляет собой 3-7-членное моноциклическое ароматическое кольцо, Ralk представляет собой алкильную группу, содержащую от 1 до 8 атомов углерода, и P представляет собой защитную группу.
[0210]
В качестве защитной группы, представленной P, можно упомянуть защитные группы, описанные в реакционной схеме-5.
[0211]
(Стадия 34)
На стадии 34 соединение, представленное общей формулой (45), можно получать путем осуществления реакции соединения, представленного общей формулой (44), с соединением, представленным общей формулой (43), в присутствии основания.
В качестве основания предпочтительными являются, например, основания, описанные на (стадии 1).
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию. Например, можно упомянуть растворители, описанные на (стадии 7), сложные эфиры, такие как этилацетат и т. д., и смесь таких растворителей.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от комнатной температуры до 120°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0212]
(Стадия 35)
На стадии 35 соединение, представленное общей формулой (46), можно получать путем осуществления реакции каталитического восстановления с соединением, представленным общей формулой (45), в присутствии катализатора на основе переходного металла и водорода.
В качестве катализатора на основе переходного металла можно упомянуть палладий на угле, гидроксид палладия, никель Ренея, оксид платины и т. д.
Добавляемое количество катализатора на основе переходного металла относительно веса соединения, представленного общей формулой (45), зачастую кратно пяти или меньшей величине и предпочтительно кратно 0,01-0,5.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, при этом можно упомянуть следующее: спирты, такие как метанол и этанол; сложные эфиры, такие как метилацетат и этилацетат; простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, 1,4-диоксан и 1,2-диметоксиэтан; апротонные полярные растворители, такие как N, N-диметилформамид, N, N-диметилацетамид, N-метилпирролидон и диметилсульфоксид; протонные полярные растворители, такие как уксусная кислота; воду и смесь таких растворителей.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от 0°C до 80°C при нормальном давлении или в условиях повышенного давления. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0213]
(Стадия 36)
На стадии 36, соединение, представленное общей формулой (47), можно получать путем восстановления сложного эфира соединения, представленного общей формулой (46), до спирта с применением восстанавливающего реагента.
В качестве восстановителя можно упомянуть алюмогидрид лития, борогидрид натрия, борогидрид лития, боран и т. д.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он не ингибирует в значительной степени реакцию, при этом можно упомянуть следующее: ароматические углеводороды, такие как бензол, толуол и ксилол; спирты, такие как метанол, этанол и 2-пропанол; простые эфиры, такие как диэтиловый эфир, тетрагидрофуран и 1,4-диоксан; апротонные полярные растворители, такие как N, N-диметилформамид, N, N-диметилацетамид, N-метилпирролидон и диметилсульфоксид; и смесь данных растворителей.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от 0°C до 100°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0214]
(Стадия 37)
На стадии 37 соединение, представленное общей формулой (48), можно получать путем осуществления реакции производного азодикарбоновой кислоты и производного фосфина с соединением, представленным общей формулой (47).
В качестве производного азодикарбоновой кислоты можно упомянуть этилазодикарбоксилат, изопропилазодикарбоксилат, 1,1'-(азодикарбонил)дипиперизин и т. д.
В качестве производного фосфина можно упомянуть трифенилфосфин, три-н-бутилфосфин и т. д.
Кроме того, фосфорановый реагент, такой как цианометилентрибутилфосфоран, цианометилентриметилфосфоран и т. д., можно применять для проведения подобной реакции вместо производного азодикарбоновой кислоты и производного фосфина.
Растворитель для реакционной смеси конкретно не ограничен при условии, что он представляет собой нейтральный растворитель; например, можно упомянуть тетрагидрофуран, толуол или их смесь.
Температура реакции конкретно не ограничена; реакцию обычно проводят при температуре в диапазоне от 0°C до 80°C. Время реакции конкретно не ограничено; предпочтительным является от 1 часа до 24 часов.
[0215]
(Стадия 38)
На стадии 38 соединение, представленное общей формулой (3-a), можно получать путем осуществления реакции удаления защитной группы из соединения, представленного общей формулой (48). Такие реакции удаления защитной группы можно проводить в соответствии со способами, общеизвестными специалистам в данной области техники (например, способами, описанными у Green и Wuts в "Protective Groups in Organic Synthesis" (3-е издание, 1999 г.)).
[0216]
В вышеописанном способе получения исходный материал, промежуточное соединение или конечный продукт также можно превращать в другие соединения по настоящему изобретению путем соответствующего превращения функциональной группы. Превращение функциональной группы можно проводить с помощью способа, общеизвестного специалистам в данной области техники (например, способа, описанного в "Comprehensive Organic Transformations", R.C. Larock, 1989 г. и т. д.).
[0217]
Соединение, представленное общей формулой (I), полученное с помощью вышеупомянутого способа, можно выделять и очищать в виде свободного соединения, его соли, его сольвата, такого как гидрат или сольват с этанолом, или кристаллического полиморфного вещества. Фармацевтически приемлемую соль соединения по настоящему изобретению можно получать с помощью стандартной реакции образования соли. Выделение и очистку можно проводить путем применения химических операций, таких как экстракционное разделение на фракции, кристаллизация и различные виды фракционной хроматографии.
[0218]
Кроме того, оптически активное соединение можно получать в виде стереохимически чистого изомера путем выбора соответствующего соединения исходного материала или путем стандартного оптического разделения рацемата. Например, в случае оптического разделения рацемата с применением хиральной колонки можно применять способ, известный специалистам в данной области техники (см., например, "Separation of optical isomers" Quarterly Chemical Review No. 6, 1989, Chemical Society of Japan, Society Publishing Center). Кроме того, в качестве хиральных колонок различные колонки являются коммерчески доступными, и из них можно соответствующим образом выбирать подходящую колонку; в качестве предпочтительных примеров можно упомянуть CHIRALPAK IA, CHIRALPAK IB и CHIRALPAK IC, изготовленные Daicel Corporation.
[0219]
Соединения по настоящему изобретению могут иметь оптические изомеры, стереоизомеры, таутомеры и/или геометрические изомеры; кроме того, соединения по настоящему изобретению включают все возможные изомеры, включая вышеупомянутые изомеры и их смеси. Аналогично исходные материалы и промежуточные соединения для синтезирования соединений по настоящему изобретению также могут иметь оптические изомеры, стереоизомеры, таутомеры и/или геометрические изомеры, и исходные материалы и промежуточные соединения для получения соединения по настоящему изобретению также включают все возможные изомеры, в том числе вышеупомянутые изомеры и их смеси.
[0220]
Пролекарства на основе соединения по настоящему изобретению можно получать, например, путем замещения соответствующей функциональной группы, присутствующей в соединении по настоящему изобретению, с помощью соответствующей защитной группы в соответствии со способом, известным специалистам в данной области техники (например, способом, описанным в "Design of Prodrugs", H. Bundgaard, Elsevier, 1985 г. и т. д.).
[0221]
Поскольку соединения по настоящему изобретению или их соли селективно ингибируют Nav1.7, но не Nav1.5, они вызывают меньше опасений в отношении побочных эффектов, обусловленных ингибированием Nav1.5, и очень эффективно действуют при широком диапазоне патологических состояний, ассоциированных с функцией Nav1.7. Несмотря на то, что с Nav1.7 ассоциированы различные патологические состояния, соединения по настоящему изобретению или их соли являются эффективными, например, для устранения или предупреждения боли. Более конкретно, соединения по настоящему изобретению или их соли являются применимыми, в частности, для устранения или предупреждения острой боли, хронической боли, ноцицептивной боли, невропатической боли и головной боли.
Кроме того, соединения по настоящему изобретению или их соли являются применимыми, в частности, для устранения или предупреждения острого или хронического зуда и нарушения вегетативной нервной системы.
[0222]
Ноцицептивная боль представляет собой боль, обусловленную повреждением ткани или интенсивными стимулами, которые могут вызывать повреждение, в том числе следующую боль:
периоперационную боль; хроническую послеоперационную боль; пост-травматическую боль; воспалительную боль; боль, связанную с раком; боль, ассоциированную с остеоартритом; боль, ассоциированную с опоясывающим лишаем; почечные колики; боль в мочевом пузыре; боль во внутренних органах; зубную боль; боль после удаления зуба; боль, связанную с заболеванием сердца; боль, ассоциированную с панкреатитом; боль, ассоциированную с контузией или растяжением; боль в спине; боль, ассоциированную с нарушениями скелетно-мышечной системы, и боль, ассоциированную с хронической артропатией.
Воспалительная боль включает боль, ассоциированную с патологическими состояниями, ассоциированными со следующими воспалительными факторами:
ревматоидный артрит; интерстициальный цистит; с заболеваниями кожи (например, солнечный ожог, ожоги, экзема, дерматит или псориаз); с заболеваниями глаз (например, глаукома, ретинит, ретинопатия, увеит или острые нарушения тканей глаза); с заболеваниями легких (например, астма, бронхит, аллергический ринит, хроническая обструктивная болезнь легкого, синдром острой дыхательной недостаточности или "легкое фермера"); с патологическими состояниями, ассоциированными с инфекциями, такими как грипп или простуда; с заболеваниями пищеварительного тракта (например, афтозная язва, синдром раздраженного кишечника, воспалительное заболевание кишечника, атопический гастрит, функциональное нарушение пищеварения, гастроэзофагеальная рефлюксная болезнь, болезнь Крона, илеит или язвенный колит); с дисменореей; с трансплантацией органов; с сосудистыми заболеваниями; с узелковым периартериитом; с тиреоидитом; с апластической анемией; с болезнью Ходжкина; со склеродермией; с миастенией гравис; с системной красной волчанкой; с болезнью Бехчета; с синдромом Шегрена; с нефротическим синдромом; с полимиозитом; с гингивитом и лихорадкой.
Боль, связанная с раком, включает боль, ассоциированную с опухолями, боль, ассоциированную с терапией рака.
Боль, ассоциированная с нарушениями скелетно-мышечной системы, включает миалгию, фибромиалгию, полимиозит, гнойный миозит, височно-нижнечелюстную миофасциальную боль. Боль в спине включает боль, обусловленную грыжей межпозвоночного диска, аномалиями суставов поясничного отдела позвоночника, крестцово-повздошного сустава, параспинальных мышц или задней продольной связки.
Хроническая артропатия включает ревматоидный артрит, остеоартрит, ревматоидный спондилит, подагрический артрит и хронический полиартрит у детей.
[0223]
Невропатическая боль представляет собой боль, обусловленную повреждением нервной системы в результате травмы или заболевания, и невропатическая боль включает множество нарушений, вызванных различными причинами. Невропатическая боль включает без ограничения следующую боль:
периферическую невропатическую боль; центральную невропатическую боль; постгерпетическую невралгию; диабетическую невропатию; невралгию тройничного нерва; неспецифичную боль в нижней части спины; невропатическую боль, связанную с раком; боль, ассоциированную с болезнью Паркинсона; боль, ассоциированную с рассеянным нейросклерозом; невропатическую боль, связанную с ВИЧ; боль, связанную с воспалением седалищного нерва; комплексный региональный болевой синдром; стеноз спинномозгового канала; синдром запястного канала; фантомную боль в ампутированных конечностях; пост-инсультную боль; боль, ассоциированную с повреждением спинного мозга; боль, ассоциированную с эпилепсией; боль, ассоциированную с конвульсиями; боль, ассоциированную с дефицитом витаминов; наследственную эритромелалгию; первичную эритромелалгию; нарушение, связанное с сильной пароксизмальной болью, ротолицевую боль и боль, вызванную синдромом жжения рта, токсинами или хроническими воспалительными состояниями.
Такая невропатическая боль включает самопроизвольную боль, сенсорные нарушения и сенсорные аномалии, гиперэстезию, высокую чувствительность к болевым стимулам (высокотемпературную, низкотемпературную, механическую гипералгезию), болезненное восприятие безвредных стимулов (динамическую, статическую, высокотемпературную или низкотемпературную аллодинию), гипоалгезию и т. д.
[0224]
Виды головной боли включают мигрень, кластерную головную боль, тензионную головную боль, комбинированную головную боль, головную боль, ассоциированную с сосудистыми нарушениями, вторичную головную боль, вегетативную цефалгию и т. д.
[0225]
Зуд включает кожный зуд, ассоциированный с заболеванием кожи, токсидермию, зуд при гемодиализе, зуд в глазах, зуд в ушах, зуд, обусловленный укусом насекомого, зуд, индуцированный опиоидами, зуд, ассоциированный с вирусной инфекцией и т. д., кожную лимфому и невропатический зуд.
[0226]
Нарушение вегетативной нервной системы включает вегетативную дисфункцию, неврологический гастрит, синдром раздраженного кишечника, болезнь Меньера, синдром гипервентиляции и вегетативную нейропатию.
Следует отметить, что заболевания, опосредованные действием Nav1.7, упомянуты выше в качестве примеров, и указанные заболевания не ограничены описанными выше.
[0227]
Лекарственный препарат, содержащий соединение по настоящему изобретению или его соль в качестве активного ингредиента, составляют из соединения по настоящему изобретению или его соли отдельно или в смеси с фармакологически приемлемым твердым или жидким носителем, подлежащим применению при получении составов. Его можно составлять с помощью способов, общепринятых в данной области техники. Примеры фармакологически приемлемого твердого или жидкого носителя, подлежащего применению при получении составов, включают следующее:
например, вспомогательные вещества, связующие, разрыхлители, добавки для улучшения распадаемости, флюидизирующие вещества, смазывающие средства, стабилизаторы, средства для нанесения покрытия, пластификаторы, отбеливатели, основания, эмульгаторы, загустители, суспендирующие средства, диспергирующие средства, растворители, солюбилизаторы, солюбилизирующие добавки, поверхностно-активные вещества, антиоксиданты, буферы, изотонические средства, регуляторы pH, консерванты, антисептические средства, отдушки, красящие вещества, подсластители, ароматизирующие средства и другие добавки.
[0228]
Лекарственный препарат по настоящему изобретению можно вводить перорально или парентерально млекопитающим (например, людям, обезьянам, коровам, лошадям, свиньям, собакам, кошкам, кроликам, морским свинкам, крысам, мышам и т. д.). В качестве примеров лекарственных форм для введения лекарственного препарата по настоящему изобретению можно упомянуть следующее:
например, таблетки (в том числе таблетки, покрытые сахарной оболочкой, таблетки, покрытые пленочной оболочкой), капсулы, гранулы, порошки, жидкие лекарственные препараты для перорального применения, сиропы, желеобразные средства для перорального применения, таблетки для применения в полости рта, жидкие препараты для применения в полости рта, спреи для применения в полости рта, полутвердые вещества для применения в полости рта, инъекционные препараты, средства для диализа, средства для ингаляции, глазные капли, глазные мази, ушные капли, назальные капли, суппозитории, полутвердые препараты для ректального применения, клизмы, таблетки для вагинального применения, суппозитории для вагинального применения, твердое средство для местного применения, жидкое средство для местного применения (в том числе жидкие мази и лосьоны), спреи, мази, кремы, гели, пластыри и т. д.
Кроме того, при необходимости можно смешивать другое лекарственное средство с лекарственным препаратом по настоящему изобретению.
[0229]
Если соединение по настоящему изобретению вводят перорально, то лекарственная форма конкретно не ограничена при условии, что лекарственную форму применяют в виде фармацевтической композиции для перорального введения; например, можно получать лекарственную форму, такую как таблетки, капсулы, гранулы или сиропы и т. д. Если получают лекарственный препарат по настоящему изобретению, предусматривающий такие лекарственные формы, то каждую лекарственную форму можно получать с помощью способа, общепринятого в данной области техники.
Кроме того, доза и частота введения лекарственного препарата по настоящему изобретению не ограничены, и их можно определять и/или регулировать с учетом возраста и веса субъекта, которому следует осуществить введение. Например, при пероральном введении взрослому пациенту активный ингредиент, соединение по настоящему изобретению или его соль, обычно вводят в дозе, составляющей от приблизительно 0,001 мг до приблизительно 1000 мг на кг веса тела за раз, и его можно вводить с нормальной частотой.
Примеры
[0230]
Ниже в данном документе признаки настоящего изобретения будут описаны более конкретно путем приведения примеров и тестовых примеров.
Материалы, применяемое количество, соотношения, содержание обработки, процедуры обработки и т. д., указанные в следующих примерах, можно соответствующим образом изменять при условии, что они не отклоняются от объекта настоящего изобретения.
Следовательно, объем настоящего изобретения не следует считать ограниченным конкретными примерами, показанными в данном документе ниже.
[0231]
Спектры 1H-ЯМР, показанные в данном документе ниже, измеряли с помощью спектрометра типа JNM-ECA400 (400 МГц, изготовленный JEOL Ltd.) или типа AVANCEIII HD400 (400 МГц, изготовленный Bruker BioSpin Co., Ltd.), с применением дейтерированного хлороформа (CDCl3), дейтерированного диметилсульфоксида (DMSO-d6), дейтерированного метанола (CD3OD) в качестве растворителей и тетраметилсилана (TMS) в качестве внутреннего стандарта. В результатах измерения химического сдвига значение δ было выражено в ppm, и значение J константы взаимодействия было выражено в Гц. В сокращениях "s" означает "синглет", "d" означает "дублет", "t" означает "триплет", "q" означает "квартет", "m" означает "мультиплет", и "br" означает "широкий". Масс-спектр (ESI-MS) измеряли путем ионизации электрораспылением с применением устройства Exactive (изготовленного Thermo Fisher Scientific Co., Ltd.). Химические структурные формулы и значения физических свойств соединений в каждом примере показаны в таблицах, показанных ниже.
[0232]
Ac: ацетил
ADDP: 1,1'-(азодикарбонил)дипиперидин
(AtaPhos)2PdCl2: бис(ди-трет-бутил-(4-диметиламинофенил)фосфин)дихлорпалладий(II)
Bn: бензил
Boc: трет-бутоксикарбонил
Bu: бутил
CAN: нитрат аммония-церия(IV)
DAST: трифторид N, N-диэтиламиносеры
DBU: диазабициклоундецен
DCE: 1,2-дихлорэтан
DCM: дихлорметан
DDQ: 2,3-дихлор-5,6-дициано-п-бензохинон
DIAD: диизопропилазодикарбоксилат
DIEA: N, N-диизопропилэтиламин
DMAP: N, N-диметил-4-аминопиридин
DME: 1,2-диметоксиэтан
DMF: N, N-диметилформамид
DMSO: диметилсульфоксид
Et: этил
EDCI: 1-(3-диметиламинопропил)-3-этилкарбодиимид
HATU: гексафторфосфат O-(7-азабензотриазол-1-ил)-N, N,N',N'-тетраметилурония
HOBt: 1-гидроксибензотриазол
HPLC: высокоэффективная жидкостная хроматография
i: изо
IPA: изопропиловый спирт
Me: метил
Ms: метансульфонил
н.: нормальный
NBS: N-бромсукцинимид
NCS: N-хлорсукцинимид
NIS: N-йодсукцинимид
NMM: N-метилморфолин
nor-AZADO: 9-аза-норадамантан-N-оксил
п: пара
Ph: фенил
PTSA: п-толуолсульфоновая кислота
TBAB: бромид тетрабутиламмония
TBA-HS: гидросульфат тетрабутиламмония
TBAI: йодид тетрабутиламмония
TBAF: фторид тетрабутиламмония
TBDPS: трет-бутилдифенилсилил
трет: третичный
tBuXphos: 2-ди-трет-бутилфосфино-2',4',6'-триизопропилбифенил
Tf: трифторметилсульфонил
TEA: триэтиламин
TFA: трифторуксусная кислота
TFAA: трифторуксусный ангидрид
THF: тетрагидрофуран
TMEDA: тетраметилэтилендиамин
TMS: триметилсилил
TMG: 1,1,3,3-тетраметилгуанидин
Ts: п-толуолсульфонил
Xantphos Pd G3: метансульфонат [(4,5'-бис(дифенилфосфино)-9,9'-диметилксантен)-2-(2'-амино-1,1'-бифенил)]палладия(II)
Звездочки (*), присутствующие в структурных формулах в примерах, указывают, что соответствующий асимметричный углерод имеет единственную стерическую структуру. Обозначения "изомер A", "изомер B", "изомер C" и "изомер D" при соединениях, обозначенных одним и тем же номером примера, указывают на изомеры, которые получают названия "изомер A", "изомер B", "изомер C" и "изомер D" в соответствии с порядком их сбора с помощью высокоэффективной жидкостной хроматографии в примере.
[0233]
Пример 1
Получение N-(6-фторхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида
[0234]
[Хим. 67]
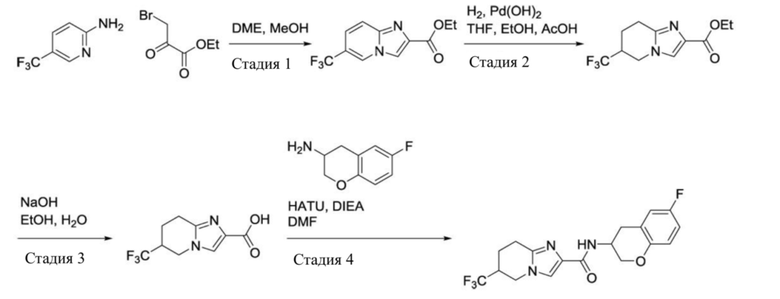
[0235]
Стадия 1
В смешанный раствор 5-(трифторметил)пиридин-2-амина (835 мг, 5,15 ммоль) в 1,2-диметоксиэтане (12,9 мл) и метаноле (12,9 мл) добавляли этилбромпируват (776 мкл, 6,18 ммоль) и смесь перемешивали в течение 14 часов при 80°C. После концентрирования реакционного раствора при пониженном давлении остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксилата (количество 557 мг, выход 42%).
[0236]
Стадия 2
В смешанный раствор этил-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксилата (5,96 г, 23,1 ммоль) в тетрагидрофуране (100 мл), этаноле (100 мл) и уксусной кислоте (11,9 мл) добавляли 20% гидроксид палладия на угле (2,43 г). Смесь перемешивали в условиях повышенного давления (приблизительно 3 атм.) в атмосфере водорода в течение 16 часов при комнатной температуре. Реакционный раствор фильтровали через целит и растворитель выпаривали при пониженном давлении. К остатку добавляли толуол и растворитель выпаривали при пониженном давлении с получением этил-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата (количество 6,42 г) в виде неочищенного продукта.
[0237]
Стадия 3
В раствор этил-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата (6,42 г, 24,5 ммоль) в этаноле (49 мл) добавляли 4 моль/л водный раствор гидроксида натрия (24,5 мл, 98,0 ммоль) и смесь перемешивали в течение 3 часов при комнатной температуре. В реакционный раствор добавляли 1 моль/л раствор хлористоводородной кислоты (98,0 мл, 98,0 ммоль) и затем растворитель выпаривали при пониженном давлении. К остатку добавляли толуол, растворитель выпаривали при пониженном давлении и процедуру повторяли три раза с получением 6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты (количество 11,2 г, выход 98%) в виде смеси с 4 эквивалентами хлорида натрия.
[0238]
Стадия 4
В суспензию 6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты (смесь с 4 эквивалентами хлорида натрия) (30,0 мг, 0,0641 ммоль) в N, N-диметилформамиде (641 мкл) добавляли HATU (29,2 мг, 0,0769 ммоль), N, N-диизопропилэтиламин (55 мкл, 0,32 ммоль) и гидрохлорид 6-фторхроман-3-амина (14,4 мг, 0,0705 ммоль) и смесь перемешивали в течение 6 часов при 40°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После этого органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом магния. После того, как растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением N-(6-фторхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида (количество 17,9 мг, выход 73%).
[0239]
Контрольный пример 1
Получение гидрохлорида (R)-6-хлорхроман-3-амина
[0240]
[Хим. 68]

[0241]
Стадия 1
В суспензию гидрохлорида (R)-хроман-3-амина (200 мг, 1,08 ммоль) в дихлорметане (11 мл) добавляли N, N-диизопропилэтиламин (555 мкл, 3,23 ммоль) и трифторуксусный ангидрид (180 мкл, 1,29 ммоль) и смесь перемешивали в течение 2 часов при комнатной температуре. После концентрирования реакционного раствора при пониженном давлении остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-N-(хроман-3-ил)-2,2,2-трифторацетамида (количество 245 мг, выход 93%).
[0242]
Стадия 2
В раствор (R)-N-(хроман-3-ил)-2,2,2-трифторацетамида (4,00 г, 16,3 ммоль) в ацетонитриле (100 мл) добавляли N-хлорсукцинимид (2,60 г, 19,5 ммоль) и смесь перемешивали в течение 6 часов при 70°C. В реакционный раствор добавляли насыщенный водный раствор гидрокарбоната натрия и этилацетат и смесь разделяли. После этого органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом магния. Растворитель выпаривали при пониженном давлении с получением (R)-N-(6-хлорхроман-3-ил)-2,2,2-трифторацетамида (количество 4,60 г, выход 100%).
[0243]
Стадия 3
В раствор (R)-N-(6-хлорхроман-3-ил)-2,2,2-трифторацетамида (297 мг, 1,06 ммоль) в хлороформе (2,7 мл) добавляли 4 моль/л водный раствор гидроксида натрия (2,7 мл, 10,8 ммоль) и смесь перемешивали в течение 17 часов при комнатной температуре. В реакционный раствор добавляли воду и хлороформ и смесь разделяли. Органический слой высушивали над безводным сульфатом натрия. Растворитель выпаривали при пониженном давлении и остаток очищали с помощью колоночной хроматографии на силикагеле. В раствор очищенного соединения в этилацетате добавляли 4 моль/л раствор хлороводорода в этилацетате и затем осажденное твердое вещество фильтровали с получением гидрохлорида (R)-6-хлорхроман-3-амина (количество 60,9 мг, выход 67%).
[0244]
Пример 2
Получение и разделение на изомеры N-((R)-6-хлорхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида
[0245]
[Хим. 69]

[0246]
Стадия 1
В суспензию 6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты (смесь с 4 эквивалентами хлорида натрия) (128 мг, 0,273 ммоль), синтезированного с помощью способа, описанного на стадии 3 в примере 1, в N, N-диметилформамиде (2,27 мл) добавляли HATU (95,0 мг, 0,250 ммоль), N, N-диизопропилэтиламин (195 мкл, 1,14 ммоль) и гидрохлорид (R)-6-хлорхроман-3-амина (50,0 мг, 0,227 ммоль), синтезированный с помощью способа, описанного в контрольном примере 1, и смесь перемешивали в течение 15 часов при комнатной температуре. В реакционный раствор добавляли воду и осажденное твердое вещество собирали путем фильтрации. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-6-хлорхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида (количество 60,9 мг, выход 67%).
[0247]
Стадия 2
Растворяли N-((R)-6-хлорхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамид (50,0 мг, 0,125 ммоль) в этаноле (20 мл) и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IB, проявляющий растворитель: этанол/н-гексан=50/50, расход: 5,0 мл/мин., комнатная температура) с получением изомера A (количество 16,8 мг, выход 34%) и изомера B (количество 14,3 мг, выход 29%).
[0248]
Соединение из примера 3 синтезировали из соединения из примера 2 (изомер A) в соответствии со схемой, изображенной на фигуре ниже.
[0249]
[Хим. 70]
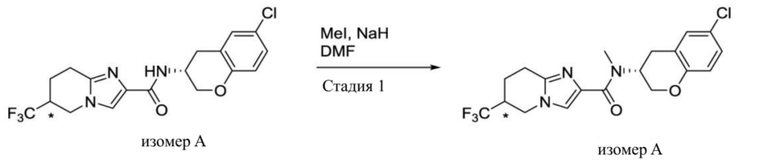
[0250]
Соединение из примера 4 синтезировали из соединения из примера 2 (изомер B) с помощью способа, подобного таковому для примера 3.
[0251]
Соединение из контрольного примера 2 (гидрохлорид (R)-6-бромхроман-3-амина) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0252]
[Хим. 71]
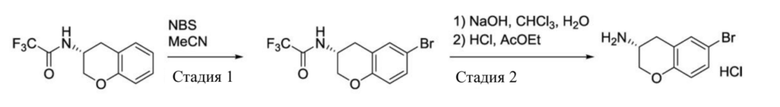
[0253]
Соединение из примера 5 синтезировали с помощью способов, подобных таковым, описанным в примере 1 и в контрольном примере 2.
[0254]
Контрольный пример 3
Получение гидрохлорида (R)-6-(дифторметил)хроман-3-амина
[0255]
[Хим. 72]

[0256]
Стадия 1
Перемешивали смешанную суспензию (R)-N-(6-бромхроман-3-ил)-2,2,2-трифторацетамида (6,47 г, 20,0 ммоль), винилтрифторбората калия (4,01 г, 29,9 ммоль), карбоната цезия (13,0 г, 39,9 ммоль) и бис(ди-трет-бутил-(4-диметиламинофенил)фосфин)дихлорпалладия(II) (707 мг, 0,998 ммоль) в 1,4-диоксане (167 мл) и воде (33 мл) в течение 15 часов при 100°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После этого органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом натрия. После того, как растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-винилхроман-3-ил)ацетофтор-N-(6-винилхроман-3-ил)ацетамида (количество 3,03 г, выход 56%).
[0257]
Стадия 2
В раствор (R)-2,2,2-трифтор-N-(6-винилхроман-3-ил)ацетамида (3,03 г, 11,2 ммоль) в 1,4-диоксане добавляли воду (37 мл), 2,6-лутидин (2,6 мл, 22,3 ммоль), перйодат натрия (9,56 г, 44,7 ммоль) и 2,5 вес/об. % раствор тетраоксида осмия в трет-бутаноле (5,7 мл, 0,56 ммоль) и смесь перемешивали в течение 3 часов при комнатной температуре. В реакционный раствор добавляли воду и этилацетат и смесь фильтровали. После того, как фильтрат разделяли, органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом натрия. После того, как растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-формилхроман-3-ил)ацетамида (количество 2,56 г, выход 84%).
[0258]
Стадия 3
К (R)-2,2,2-трифтор-N-(6-формилхроман-3-ил)ацетамиду (1,45 г, 5,31 ммоль) добавляли трифторид N, N-диэтиламиносеры (2,8 мл, 21,2 ммоль) и смесь перемешивали в течение 5 дней при комнатной температуре. Реакционный раствор разбавляли дихлорметаном, добавляли по каплям в жидкую смесь хлороформа и воды и затем смесь разделяли. Органический слой высушивали над безводным сульфатом магния и растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-N-(6-(дифторметил)хроман-3-ил)-2,2,2-трифторацетамида (количество 1,11 г, выход 71%).
[0259]
Стадия 4
Получали гидрохлорид (R)-6-(дифторметил)хроман-3-амина с помощью способа, подобного стадии 3 в контрольном примере 1, с применением (R)-N-(6-(дифторметил)хроман-3-ил)-2,2,2-трифторацетамида вместо (R)-N-(6-хлорхроман-3-ил)-2,2,2-трифторацетамида.
[0260]
Соединение из примера 6 синтезировали с помощью способов, подобных таковым, описанным в примере 1 и в контрольном примере 3.
[0261]
Соединения из примера 7 получали путем разделения соединения из примера 6.
[0262]
Соединение из контрольного примера 4 (гидрохлорид 5-хлорхроман-3-амина) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0263]
[Хим. 73]

[0264]
Соединение из примера 8 синтезировали с помощью способов, подобных таковым, описанным в примере 1 и в контрольном примере 4.
[0265]
Соединения из примера 9 (изомер A и изомер B) синтезировали с помощью способа, подобного таковому для примера 1.
[0266]
Соединение из примера 10 синтезировали из соединения из примера 9 в соответствии со схемой, изображенной на фигуре ниже.
[0267]
[Хим. 74]
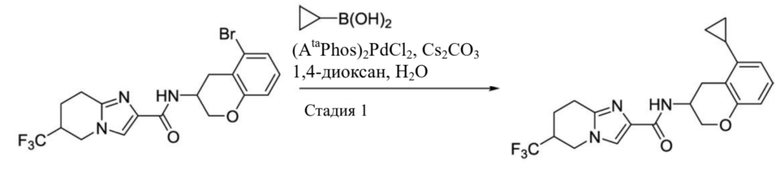
[0268]
Соединение из контрольного примера 5 (гидрохлорид (R)-6-этилхроман-3-амина) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0269]
[Хим. 75]
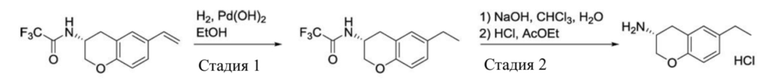
[0270]
Соединение из примера 11 синтезировали с помощью способов, подобных таковым, описанным в примере 1 и в контрольном примере 5.
[0271]
Соединение из примера 12 синтезировали с помощью способа, подобного таковому для примера 1.
[0272]
Соединение из примера 13 синтезировали из соединения из примера 12 в соответствии со схемой, изображенной на фигуре ниже.
[0273]
[Хим. 76]

[0274]
Соединение из контрольного примера 7 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для примера 1, с применением гидрохлорида (R)-хроман-3-амина вместо гидрохлорида 6-фторхроман-3-амина на стадии 4.
[0275]
[Хим. 77]

[0276]
Пример 14
Получение N-((R)-хроман-3-ил)-3-йод-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида
[0277]
[Хим. 78]
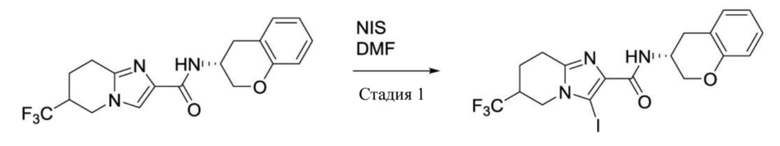
[0278]
В раствор N-((R)-хроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида, синтезированного с помощью способа, описанного в контрольном примере 7 (79,7 мг, 0,218 ммоль), в N, N-диметилформамиде (2,2 мл) добавляли N-йодсукцинимид (73,6 мг, 0,327 ммоль) и смесь перемешивали в течение 14 часов при 80°C. Дополнительно добавляли N-йодсукцинимид (73,6 мг, 0,327 ммоль) и смесь перемешивали в течение 8 часов при 100°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После этого органический слой промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия и растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-хроман-3-ил)-3-йод-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида (количество 97,5 мг, выход 91%).
[0279]
Соединение из примера 15 синтезировали из соединения из примера 14 в соответствии со схемой, изображенной на фигуре ниже.
[Хим. 79]

[0280]
Соединение из примера 16 синтезировали из соединения из контрольного примера 9 в соответствии со схемой, изображенной на фигуре ниже.
[0281]
[Хим. 80]

[0282]
Пример 17
Получение (R)-N-(6-хлорхроман-3-ил)-3-(6-метоксипиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида
[0283]
[Хим. 81]

[0284]
Стадия 1
Получали этил-3-йод-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилат с помощью способа, подобного таковому для примера 14, с применением этил-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата вместо N-((R)-хроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида.
[0285]
Стадия 2
Получали этил-3-(6-метоксипиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилат с помощью способа, подобного таковому для примера 15, с применением этил-3-йод-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата вместо N-((R)-хроман-3-ил)-3-йод-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида.
[0286]
Стадия 3
Получали 3-(6-метоксипиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновую кислоту в виде смеси с 4 эквивалентами хлорида натрия с помощью способа, подобного стадии 3 в примере 1, с применением этил-3-(6-метоксипиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата вместо этил-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата.
[0287]
Стадия 4
Получали (R)-N-(6-хлорхроман-3-ил)-3-(6-метоксипиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамид с помощью способа, подобного стадии 4 в примере 1, с применением 3-(6-метоксипиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты вместо 6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты и с применением гидрохлорида (R)-6-хлорхроман-3-амина, синтезированного с помощью способа, описанного в контрольном примере 1, вместо гидрохлорида 6-фторхроман-3-амина.
[0288]
Пример 18
Получение (R)-N-(6-хлорхроман-3-ил)-3-(пиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида
[0289]
[Хим. 82]

[0290]
Стадия 1
Получали этил-3-(6-хлорпиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилат с помощью способа, подобного стадии 2 в примере 17, с применением 6-(хлорпиридин-2-ил)бороновой кислоты вместо 6-метоксипиридин-2-бороновой кислоты.
[0291]
Стадия 2
В раствор этил-3-(6-хлорпиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата (1,05 г, 3,43 ммоль) в тетрагидрофуране (10 мл) добавляли этанол (10 мл), уксусную кислоту (1,8 мл) и 20% гидроксид палладия на угле (0,72 г) и смесь перемешивали в течение 2 часов в атмосфере водорода (при давлении, нагнетаемом с помощью баллона) при 50°C. Реакционный раствор фильтровали через целит и затем растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-3-(пиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата (количество 900 г, выход 97%).
[0292]
Стадия 3
Получали 3-(пиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновую кислоту в виде смеси с 4 эквивалентами хлорида натрия с помощью способа, подобного стадии 3 в примере 1, с применением этил-3-(пиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата вместо этил-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата.
[0293]
Стадия 4
В суспензию 3-(пиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты (4, смесь с хлоридом натрия) (15 мг, 0,031 ммоль), гидрохлорида (R)-6-хлорхроман-3-амина, синтезированного с помощью способа, описанного в контрольном примере 1 (6,9 мг, 0,031 ммоль), 1-гидроксибензотриазола (7,2 мг, 0,047 ммоль) и гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (9,0 мг, 0,047 ммоль) в дихлорметане (1 мл) добавляли 4-метилморфолин (21 мкл, 0,19 ммоль) и смесь перемешивали в течение 2 часов при комнатной температуре. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-N-(6-хлорхроман-3-ил)-3-(пиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида (количество 8,0 мг, выход 62%).
[0294]
Соединение из контрольного примера 8 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 2 - стадии 3 в примере 17.
[0295]
[Хим. 83]

[0296]
Соединение из примера 19 синтезировали из соединения из контрольного примера 8 и соединения из контрольного примера 43 с помощью способа, подобного стадии 4 в примере 18.
[0297]
Соединение из примера 20 синтезировали из соединения из контрольного примера 8 и соединения из контрольного примера 44 с помощью способа, подобного стадии 4 в примере 18.
[0298]
Соединение из примера 21 синтезировали с помощью способа, подобного таковому для примера 17.
[0299]
Соединение из примера 22 синтезировали с помощью способа, подобного таковому для примера 17.
[0300]
Соединение из контрольного примера 9 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 4 в примере 1.
[0301]
[Хим. 84]
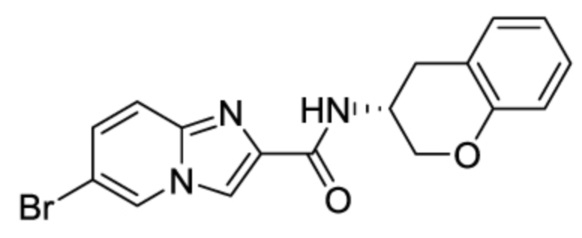
[0302]
Соединение из примера 23 синтезировали из соединения из контрольного примера 9 в соответствии со схемой, изображенной на фигуре ниже.
[0303]
[Хим. 85]

[0304]
Соединение из примера 24 синтезировали с помощью способа, подобного таковому для примера 23.
[0305]
Соединение из контрольного примера 10 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для примера 23.
[0306]
[Хим. 86]

[0307]
Соединение из примера 25 синтезировали из соединения из контрольного примера 10 в соответствии со схемой, изображенной на фигуре ниже.
[0308]
[Хим. 87]

[0309]
Соединение из контрольного примера 11 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 9.
[0310]
[Хим. 88]
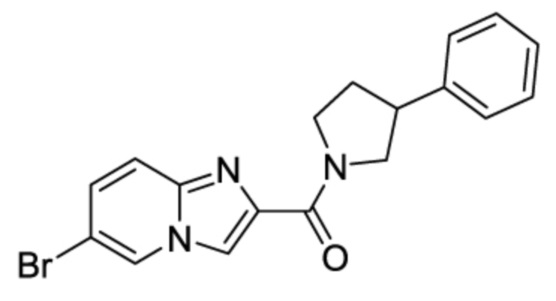
[0311]
Соединение из примера 26 синтезировали из соединения из контрольного примера 11 с помощью способа, подобного таковому для примера 23.
[0312]
Соединение из контрольного примера 12 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 4 в примере 1.
[0313]
[Хим. 89]

[0314]
Соединение из примера 27 синтезировали из соединения из контрольного примера 12 с помощью способа, подобного таковому для примера 23.
[0315]
Соединение из контрольного примера 13 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 12.
[0316]
[Хим. 90]
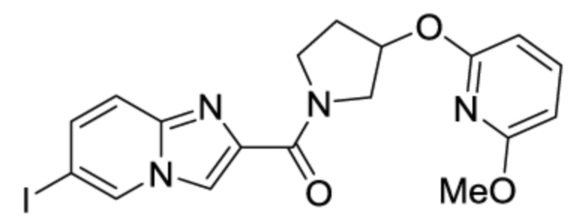
[0317]
Соединение из примера 28 синтезировали из соединения из контрольного примера 13 с помощью способа, подобного таковому для примера 23.
[0318]
Соединение из контрольного примера 14 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 12.
[0319]
[Хим. 91]
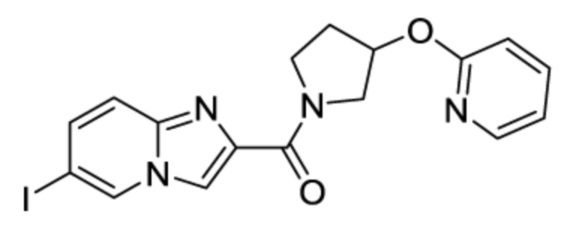
[0320]
Соединение из примера 29 синтезировали из соединения из контрольного примера 14 в соответствии со схемой, изображенной на фигуре ниже.
[0321]
[Хим. 92]

[0322]
Соединение из примера 30 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0323]
[Хим. 93]
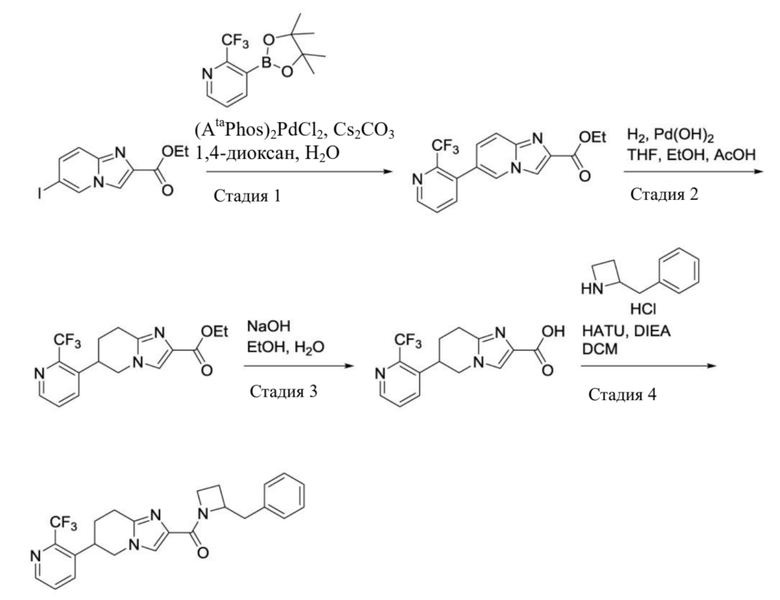
[0324]
Соединение из примера 31 получали в соответствии со схемой, изображенной на фигуре ниже.
[0325]
[Хим. 94]

[0326]
Соединение из контрольного примера 15 (2-(2,4-дифторфенил)морфолин) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0327]
[Хим. 95]
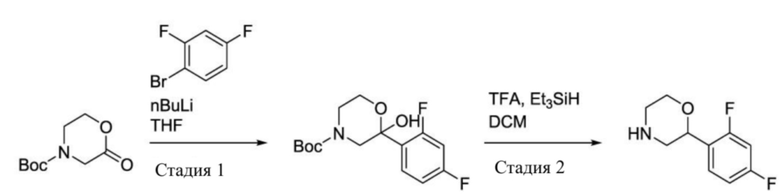
[0328]
Соединение из примера 32 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0329]
[Хим. 96]

[0330]
Соединение из примера 33 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0331]
[Хим. 97]
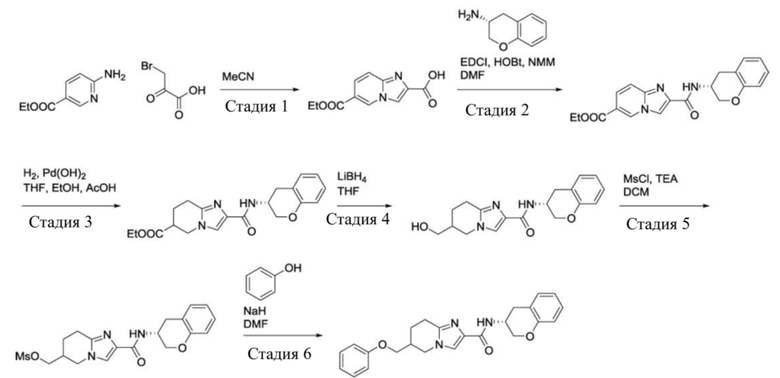
[0332]
Соединение из примера 34 синтезировали из соединения, синтезированного на стадии 4 в примере 33, в соответствии со схемой, изображенной на фигуре ниже.
[0333]
[Хим. 98]

[0334]
Соединение из примера 35 синтезировали из соединения из контрольного примера 9 в соответствии со схемой, изображенной на фигуре ниже.
[0335]
[Хим. 99]

[0336]
Соединение из примера 36 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0337]
[Хим. 100]

[0338]
Пример 37
Получение N-((R)-хроман-3-ил)-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида
[0339]
[Хим. 101]

[0340]
Стадия 1
Получали этил-6-гидроксиимидазо[1,2-a]пиридин-2-карбоксилат с помощью способа, подобного стадии 1 в примере 1, с применением 6-аминопиридин-3-ола вместо 5-(трифторметил)пиридин-2-амина.
[0341]
Стадия 2
В ледяной раствор этил-6-гидроксиимидазо[1,2-a]пиридин-2-карбоксилата (1,38 г, 6,69 ммоль) в N, N-диметилформамиде (34 мл) добавляли гидрид натрия (60% в масле) (535 мг, 13,4 ммоль). После перемешивания в течение 5 минут добавляли 2,2,2-трифторэтилтрифторметансульфонат (1,93 мл, 13,4 ммоль) и смесь перемешивали в течение 1 часа при 80°C. В реакционный раствор добавляли воду и этилацетат и затем смесь разделяли. Органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом натрия. Растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-6-(2,2,2-трифторэтокси)имидазо[1,2-a]пиридин-2-карбоксилата (количество 1,55 г, выход 80%).
[0342]
Стадия 3
Получали этил-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилат с помощью способа, подобного стадии 2 в примере 1, с применением этил-6-(2,2,2-трифторэтокси)имидазо[1,2-a]пиридин-2-карбоксилата вместо этил-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксилата.
[0343]
Стадия 4
Получали 6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновую кислоту с помощью способа, подобного стадии 3 в примере 1, с применением этил-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата вместо этил-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата.
[0344]
Стадия 5
Получали N-((R)-хроман-3-ил)-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамид с помощью способа, подобного стадии 4 в примере 1, с применением 6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты вместо 6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты и с применением гидрохлорида (R)-хроман-3-амина вместо гидрохлорида 6-фторхроман-3-амина.
[0345]
Соединение из примера 38 синтезировали из соединения, синтезированного на стадии 4 в примере 37, и соединения из контрольного примера 1 с помощью способа, подобного стадии 4 в примере 1.
[0346]
Соединения из примера 39 получали путем разделения соединения из примера 38.
[0347]
Соединение из примера 40 синтезировали из соединения, синтезированного на стадии 4 в примере 37, и соединения из контрольного примера 3 с помощью способа, подобного стадии 4 в примере 1.
[0348]
Соединение из примера 41 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0349]
[Хим. 102]

[0350]
Соединение из контрольного примера 16 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 1 в примере 1.
[0351]
[Хим. 103]

[0352]
Соединение из контрольного примера 17 (показано на фигуре ниже) синтезировали из соединения из контрольного примера 16 с помощью способа, подобного стадии 1 - стадии 2 в примере 41.
[0353]
[Хим. 104]
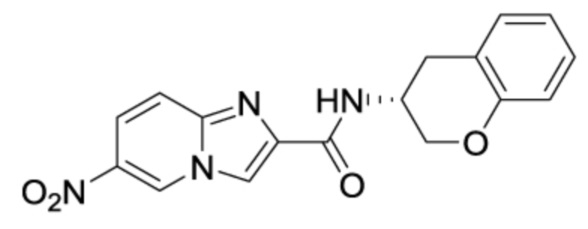
[0354]
Соединение из примера 42 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0355]
[Хим. 105]

[0356]
Соединение из примера 43 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0357]
[Хим. 106]
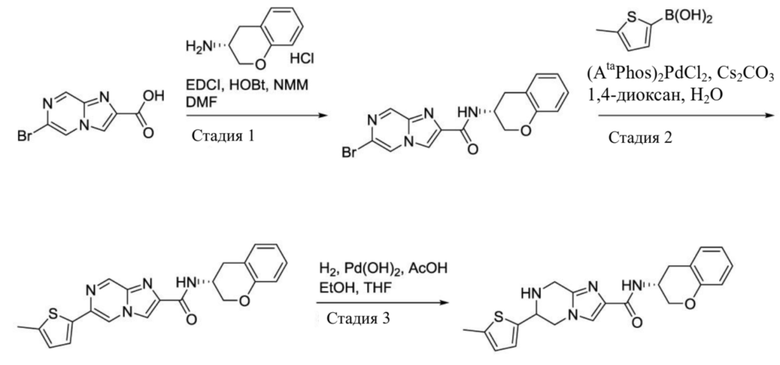
[0358]
Соединение из примера 44 синтезировали с помощью способа, подобного таковому для примера 43.
[0359]
Соединение из примера 45 синтезировали из соединения из примера 44 в соответствии со схемой, изображенной на фигуре ниже.
[0360]
[Хим. 107]
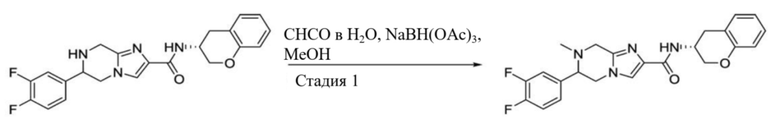
[0361]
Соединение из примера 46 синтезировали с помощью способа, подобного таковому для примера 43.
[0362]
Соединение из примера 47 синтезировали из соединения из примера 46 с помощью способа, подобного таковому для примера 45.
[0363]
Соединение из примера 48 синтезировали с помощью способа, подобного таковому для примера 43.
[0364]
Соединение из примера 49 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0365]
[Хим. 108]

[0366]
Соединение из примера 50 синтезировали из соединения из примера 49 с помощью способа, подобного таковому для примера 45.
[0367]
Соединение из примера 51 синтезировали с помощью способа, подобного таковому для примера 49.
[0368]
Соединение из примера 52 синтезировали из соединения из примера 51 с помощью способа, подобного таковому для примера 45.
[0369]
Соединение из примера 53 синтезировали с помощью способа, подобного таковому для примера 49.
[0370]
Соединение из примера 54 синтезировали из соединения из примера 53 с помощью способа, подобного таковому для примера 45.
[0371]
Соединение из примера 55 синтезировали с помощью способа, подобного таковому для примера 49.
[0372]
Соединение из примера 56 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0373]
[Хим. 109]
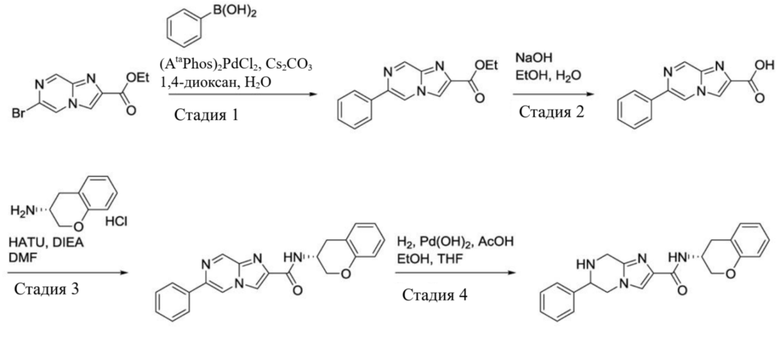
[0374]
Соединение из примера 57 синтезировали из соединения из примера 56 с помощью способа, подобного таковому для примера 45.
[0375]
Соединение из контрольного примера 18 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для примера 56.
[0376]
[Хим. 110]

[0377]
Соединение из примера 58 синтезировали из соединения из контрольного примера 18 с помощью способа, подобного таковому для примера 45.
[0378]
Соединение из примера 59 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0379]
[Хим. 111]
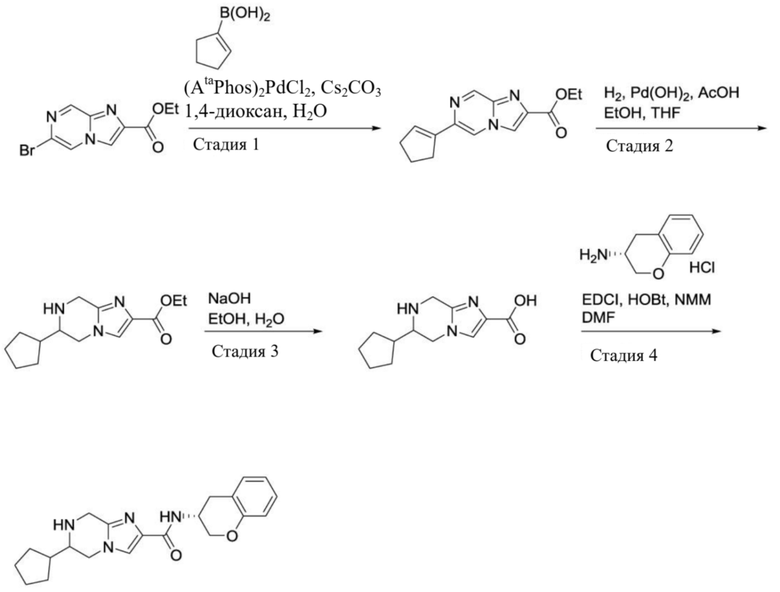
[0380]
Соединение из контрольного примера 19 синтезировали из соединения, синтезированного на стадии 1 в примере 56, в соответствии со схемой, изображенной на фигуре ниже.
[0381]
[Хим. 112]
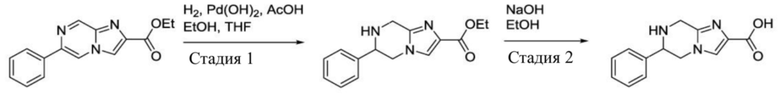
[0382]
Соединение из примера 60 синтезировали из соединения из контрольного примера 19 с помощью способа, подобного стадии 4 в примере 59.
[0383]
Соединение из контрольного примера 20 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 15.
[0384]
[Хим. 113]

[0385]
Соединение из примера 61 синтезировали из соединения из контрольного примера 19 и соединения из контрольного примера 20 с помощью способа, подобного стадии 4 в примере 59.
[0386]
Соединение из контрольного примера 21 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 19, с помощью способов, подобных описанным в примере 45 и стадии 2 в контрольном примере 19.
[0387]
[Хим. 114]

[0388]
Соединение из контрольного примера 22 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0389]
[Хим. 115]

[0390]
Соединение из примера 62 синтезировали из соединения из контрольного примера 21 и соединения из контрольного примера 22 с помощью способа, подобного стадии 3 в примере 56.
[0391]
Соединение из контрольного примера 23 (дигидрохлорид 2-(азетидин-3-илокси)-6-(трифторметил)пиридина) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0392]
[Хим. 116]

[0393]
Соединение из примера 63 синтезировали из соединения из контрольного примера 21 и соединения из контрольного примера 23 с помощью способа, подобного стадии 3 в примере 56.
[0394]
Соединение из примера 64 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0395]
[Хим. 117]

[0396]
Соединение из примера 65 синтезировали с помощью способов, подобных таковым, описанным в примере 64 и в контрольном примере 1.
[0397]
Соединение из примера 66 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0398]
[Хим. 118]

[0399]
Соединение из примера 67 синтезировали из соединения, синтезированного на стадии 4 в примере 66, и соединения из контрольного примера 43 с помощью способа, подобного стадии 4 в контрольном примере 18.
[0400]
Соединение из примера 68 синтезировали с помощью способа, подобного таковому для примера 32.
[0401]
Соединение из примера 69 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0402]
[Хим. 119]

[0403]
Контрольный пример 24
Получение (R)-3-аминохроман-6-карбонитрила
[0404]
[Хим. 120]

[0405]
Стадия 1
В раствор (R)-2,2,2-трифтор-N-(6-формилхроман-3-ил)ацетамида (1,43 г, 5,23 ммоль), синтезированного с помощью способа, описанного на стадии 2 в контрольном примере 3, в ацетонитриле (52,3 мл) добавляли азид натрия (524 мг, 8,06 ммоль) и трифторметансульфоновую кислоту (1,61 мл, 18,3 ммоль) и смесь перемешивали в течение 2 часов при комнатной температуре. В реакционный раствор добавляли насыщенный водный раствор гидрокарбоната натрия, воду и этилацетат и смесь разделяли. Органический слой промывали насыщенным солевым раствором и затем высушивали над безводным сульфатом натрия. Растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-N-(6-цианохроман-3-ил)-2,2,2-трифторацетамида (количество 1,40 г, выход 99%).
[0406]
Стадия 2
В раствор (R)-N-(6-цианохроман-3-ил)-2,2,2-трифторацетамида (1,40 г, 5,18 ммоль) в хлороформе (13 мл) добавляли 4 моль/л водный раствор гидроксида натрия (13,0 мл, 51,8 ммоль) и смесь перемешивали в течение 13 часов при комнатной температуре. В реакционный раствор добавляли воду и хлороформ и смесь разделяли. Органический слой промывали насыщенным солевым раствором и затем высушивали над безводным сульфатом натрия. Растворитель выпаривали при пониженном давлении с получением (R)-3-аминохроман-6-карбонитрила (количество 505 мг, выход 56%).
[0407]
Пример 70
Получение N-((R)-6-цианохроман-3-ил)-5-(2-фторфенил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0408]
[Хим. 121]
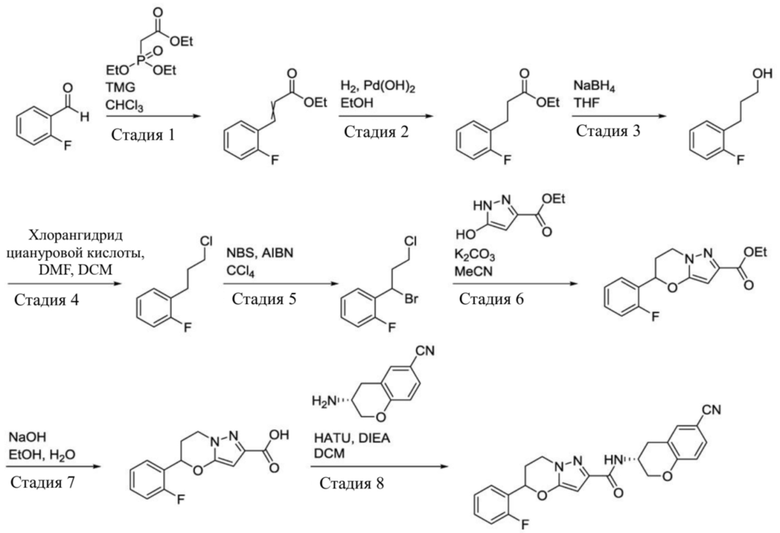
[0409]
Стадия 1
В раствор 2-фторбензальдегида (2,00 г, 16,1 ммоль) в хлороформе (32,2 мл) добавляли 1,1,3,3-тетраметилгуанидин (3,03 мл, 24,2 ммоль) и диэтилфосфоноэтилацетат (3,52 мл, 17,7 ммоль) и смесь перемешивали в течение 4 часов при 50°C. После выпаривания растворителя при пониженном давлении остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-3-(2-фторфенил)акрилата (количество 2,98 г, выход 95%).
[0410]
Стадия 2
В раствор этил-3-(2-фторфенил)акрилата (2,98 г, 15,3 ммоль) в этаноле (76,7 мл), добавляли 20% гидроксид палладия на угле (539 мг) и смесь перемешивали в условиях повышенного давления (приблизительно 3 атм.) в атмосфере водорода в течение 3 часов при 50°C. После того, как реакционный раствор фильтровали через целит, растворитель выпаривали при пониженном давлении с получением этил-3-(2-фторфенил)пропаноата (количество 2,79 г, выход 93%).
[0411]
Стадия 3
В раствор этил-3-(2-фторфенил)пропаноата (2,79 г, 14,2 ммоль) в тетрагидрофуране (71,1 мл) добавляли борогидрид лития (774 мг, 35,5 ммоль) и смесь перемешивали в течение 5 часов при комнатной температуре. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. Органический слой промывали насыщенным солевым раствором и затем высушивали над безводным сульфатом натрия. Растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением 3-(2-фторфенил)пропан-1-ола (количество 2,17 г, выход 99%).
[0412]
Стадия 4
В раствор хлорангидрида циануровой кислоты (2,86 г, 15,5 мл) в N, N-диметилформамиде (3,3 мл) добавляли раствор 3-(2-фторфенил)пропан-1-ола (2,17 г, 14,1 ммоль) в дихлорметане (70,4 мл) и смесь перемешивали в течение 13 часов при комнатной температуре. В реакционный раствор добавляли воду и хлороформ и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением 1-(3-хлорпропил)-2-фторбензола (количество 2,00 г, выход 82%).
[0413]
Стадия 5
В раствор 1-(3-хлорпропил)-2-фторбензола (2,00 г, 11,6 ммоль) в тетрахлорметане (39 мл) добавляли N-бромсукцинимид (2,27 г, 12,7 ммоль) и 2,2'-азобис(изобутиронитрил) (168 мкл, 1,16 ммоль) и смесь перемешивали в течение 2 часов при 90°C. В реакционный раствор добавляли воду и хлороформ и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением 1-(1-бром-3-хлорпропил)-2-фторбензола (количество 2,36 г, выход 81%).
[0414]
Стадия 6
В раствор 1-(1-бром-3-хлорпропил)-2-фторбензола (2,36 г, 9,38 ммоль) в ацетонитриле (31,3 мл) добавляли этил-5-гидрокси-1H-пиразол, 3-карбоксилат (1,47 г, 9,38 ммоль) и карбонат калия (3,89 г, 28,1 ммоль) и смесь перемешивали в течение 15 часов при 100°C. После концентрирования реакционного раствора при пониженном давлении остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-5-(2-фторфенил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата (количество 2,30 г, выход 84%).
[0415]
Стадия 7
В раствор этил-5-(2-фторфенил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата (2,30 г, 7,92 ммоль) в этаноле (15,8 мл) добавляли 4 моль/л водный раствор гидроксида натрия (7,92 мл, 31,7 ммоль) и смесь перемешивали в течение 24 часов при комнатной температуре. В реакционный раствор добавляли 2 моль/л раствор хлористоводородной кислоты и затем растворитель выпаривали при пониженном давлении. К остатку добавляли воду и этилацетат и смесь разделяли. Органический слой промывали насыщенным солевым раствором и затем высушивали над безводным сульфатом натрия и растворитель выпаривали при пониженном давлении с получением 5-(2-фторфенил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты (количество 1,80 г, выход 87%) в виде смеси с 4 эквивалентами хлорида натрия.
[0416]
Стадия 8
В суспензию 5-(2-фторфенил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты (смесь с 4 эквивалентами хлорида натрия) (36,1 мг, 0,138 ммоль) в дихлорметане (1,2 мл) добавляли HATU (48,0 мг, 0,126 ммоль), N, N-диизопропилэтиламин (99 мкл, 0,57 ммоль) и (R)-3-аминохроман-6-карбонитрил (20,0 мг, 0,115 ммоль) и смесь перемешивали в течение 2 часов при комнатной температуре. Реакционный раствор очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-6-цианохроман-3-ил)-5-(2-фторфенил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (количество 47,9 мг, выход 100%).
[0417]
Соединение из примера 71 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 2.
[0418]
Соединение из примера 72 синтезировали с помощью способа, подобного таковому для примера 70.
[0419]
Соединение из примера 73 синтезировали с помощью способа, подобного таковому для примера 70.
[0420]
Соединения из примера 74 получали путем разделения соединения из примера 73.
[0421]
Соединение из примера 75 синтезировали с помощью способа, подобного таковому для примера 70.
[0422]
Соединение из примера 76 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 5.
[0423]
Соединение из примера 77 синтезировали с помощью способа, подобного таковым, описанным на стадии 6 - стадии 8 в примере 70 и в контрольном примере 4.
[0424]
Соединение из контрольного примера 25 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 4.
[0425]
[Хим. 122]

[0426]
Соединение из примера 78 синтезировали с помощью способов, подобных таковым, описанным в примере 77 и в контрольном примере 25.
[0427]
Соединение из примера 79 синтезировали с помощью способа, подобного таковому для примера 77.
[0428]
Соединение из контрольного примера 27 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0429]
[Хим. 123]

[0430]
Соединение из примера 80 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 27.
[0431]
Контрольный пример 28
Получение дигидрохлорида (R)-6-(пиридин-2-ил)хроман-3-амина
[0432]
[Хим. 124]

[0433]
Стадия 1
В раствор (R)-N-(6-бромхроман-3-ил)-2,2,2,-трифторацетамида (500 мг, 1,54 ммоль), синтезированного с помощью способа, описанного на стадии 1 в контрольном примере 2, в 1,4-диоксане (10 мл) добавляли бис(пинаколато)дибор (800 мг, 3,15 ммоль), ацетат калия (300 мг, 7,87 ммоль) и [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (100 мг, 0,14 ммоль). Смесь перемешивали в течение 15 часов при 90°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)хроман-3-ил)ацетамида (количество 570 мг, выход 100%).
[0434]
Стадия 2
Перемешивали смешанную суспензию (R)-2,2,2-трифтор-N-(6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)хроман-3-ил)ацетамида (200 мг, 0,539 ммоль), 2-бромпиридина (130 мг, 0,823 ммоль), карбоната цезия (350 мг, 1,07 ммоль) и бис(ди-трет-бутил-(4-диметиламинофенил)фосфин)дихлорпалладия(II) (38,0 мг, 0,0537 ммоль) в 1,4-диоксане (2,5 мл) и воде (0,5 мл) в течение 5 часов при 100°C. В реакционный раствор добавляли насыщенный водный раствор хлорида аммония и этилацетат и смесь разделяли. Органический слой промывали насыщенным солевым раствором и затем высушивали над безводным сульфатом натрия. Растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-(пиридин-2-ил)хроман-3-ил)ацетамида (количество 82,0 мг, выход 47%).
[0435]
Стадия 3
Получали дигидрохлорид (R)-6-(пиридин-2-ил)хроман-3-амина с помощью способа, подобного стадии 3 в контрольном примере 1, с применением (R)-2,2,2-трифтор-N-(6-(пиридин-2-ил)хроман-3-ил)ацетамида вместо (R)-N-(6-хлорхроман-3-ил)-2,2,2-трифторацетамида.
[0436]
Соединение из примера 81 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 28.
[0437]
Соединение из примера 82 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0438]
[Хим. 125]

[0439]
Соединение из примера 83 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0440]
[Хим. 126]
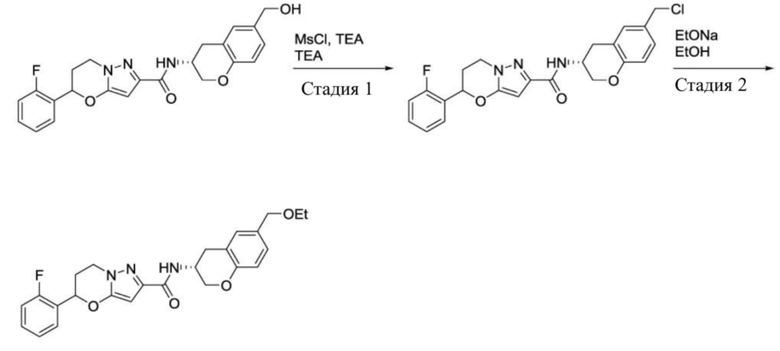
[0441]
Соединение из примера 84 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0442]
[Хим. 127]
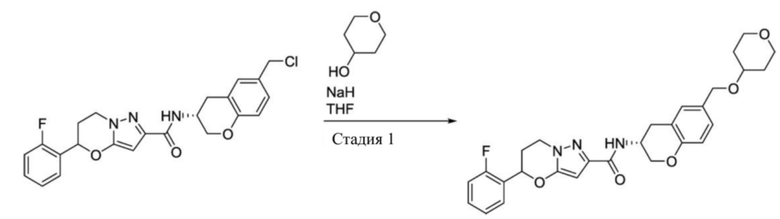
[0443]
Соединение из примера 85 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0444]
[Хим. 128]
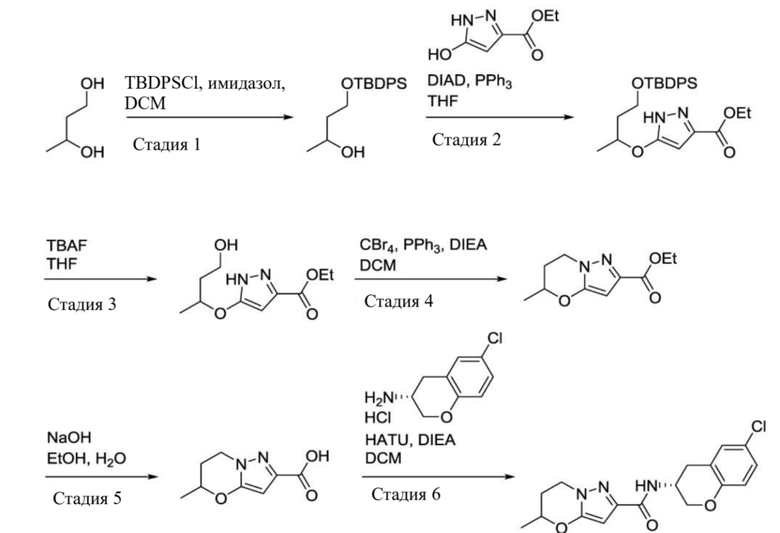
[0445]
Соединение из примера 86 синтезировали с помощью способа, подобного таковому для примера 85.
[0446]
Соединение из примера 87 синтезировали с помощью способа, подобного таковому для примера 85.
[0447]
Соединение из примера 88 синтезировали с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 2.
[0448]
Соединение из примера 89 синтезировали с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 2.
[0449]
Соединение из примера 90 синтезировали с помощью способа, подобного таковому для примера 85.
[0450]
Соединение из примера 91 синтезировали с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 24.
[0451]
Соединения из примера 92 получали путем разделения соединения из примера 91.
[0452]
Соединение из контрольного примера 29 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 27.
[0453]
[Хим. 129]

[0454]
Соединение из примера 93 синтезировали с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 29.
[0455]
Соединение из примера 94 синтезировали с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 24.
[0456]
Соединения из примера 95 получали путем разделения соединения из примера 94.
[0457]
Соединение из контрольного примера 30 (4-циклопропилбутан-1,3-диол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0458]
[Хим. 130]
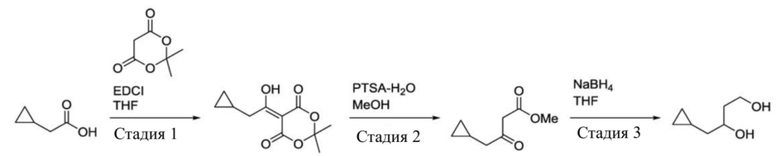
[0459]
Соединение из примера 96 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 30, в примере 85 и в контрольном примере 24.
[0460]
Соединения из примера 97 получали путем разделения соединения из примера 96.
[0461]
Контрольный пример 31
Получение этил-5-((бензилокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата
[0462]
[Хим. 131]

[0463]
Получали этил-5-((бензилокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилат с помощью способа, подобного стадии 1 - стадии 4 в примере 85, с применением 4-(бензилокси)бутан-1,3-диола вместо бутан-1,3-диола на стадии 1.
[0464]
Соединение из примера 98 синтезировали из соединения из контрольного примера 31 с помощью способов, подобных стадии 5 и стадии 6 в примере 85.
[0465]
Соединение из примера 99 синтезировали с помощью способов, подобных таковым из контрольного примера 31, стадии 5 и стадии 6 в примере 85 и примера 24.
[0466]
Пример 100
Получение N-((R)-6-цианохроман-3-ил)-5-(пропоксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0467]
[Хим. 132]
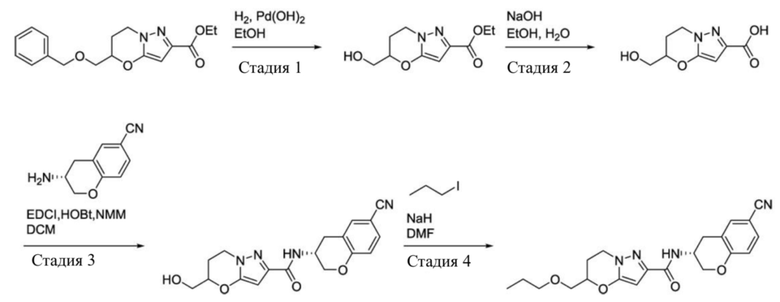
[0468]
Стадия 1
В раствор этил-5-((бензилокси)метил-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата (12,4 г, 18,4 ммоль), синтезированного с помощью способа, описанного в контрольном примере 31, в этаноле (61 мл) добавляли 20% гидроксид палладия на угле (2,59 мг). Смесь перемешивали в течение 23 часов при 40°C в условиях повышенного давления (приблизительно 3 атм.) в атмосфере водорода. После того, как реакционный раствор фильтровали через целит, растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата (количество 2,47 г, выход 59%).
[0469]
Стадия 2
В раствор этил-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата (1,97 г, 8,71 ммоль) в этаноле (44 мл) добавляли 4 моль/л водный раствор гидроксида натрия (8,7 мл, 35 ммоль) и смесь перемешивали в течение 15 часов при комнатной температуре. В реакционный раствор добавляли 2 моль/л раствор хлористоводородной кислоты и затем растворитель выпаривали при пониженном давлении с получением 5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты (количество 3,68 г, выход 98%) в виде смеси с 4 эквивалентами хлорида натрия.
[0470]
Стадия 3
В суспензию 5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты (смесь с 4 эквивалентами хлорида натрия) (450 мг, 1,04 ммоль), (R)-3-аминохроман-6-карбонитрила (200 мг, 1,15 ммоль), синтезированного с помощью способа, описанного в контрольном примере 24, 1-гидроксибензотриазола (169 мг, 1,25 ммоль) и гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (240 мг, 1,25 ммоль) в дихлорметане (10 мл) добавляли 4-метилморфолин (573 мкл, 5,21 ммоль) и смесь перемешивали в течение 24 часов при комнатной температуре. В реакционный раствор добавляли 1 моль/л раствор хлористоводородной кислоты и хлороформ и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-6-цианохроман-3-ил)-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (количество 300 мг, выход 81%).
[0471]
Стадия 4
В раствор N-((R)-6-цианохроман-3-ил)-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (330 мг, 0,931 ммоль) в N, N-диметилформамиде (8,8 мл) добавляли гидрид натрия (60% в масле) и 1-йодпропан (136 мкл, 1,39 ммоль). Смесь перемешивали в течение 13 часов при 90°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-6-цианохроман-3-ил)-5-(пропоксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (количество 73,3 мг, выход 20%).
[0472]
Пример 101
Разделение на изомеры N-((R)-6-цианохроман-3-ил)-5-(пропоксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0473]
[Хим. 133]

[0474]
Растворяли N-((R)-6-цианохроман-3-ил)-5-(пропоксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид (150 мг, 0,378 ммоль), синтезированный с помощью способа, описанного в примере 100, в этаноле (15 мл) и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IB, проявляющий растворитель: этанол, расход: 8,0 мл/мин., комнатная температура) с получением изомера A (количество 59,9 мг, выход 40%) и изомера B (количество 61,4 мг, выход 41%).
[0475]
Пример 102
Получение N-((R)-6-цианохроман-3-ил)-5-((циклопропилметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0476]
[Хим. 134]
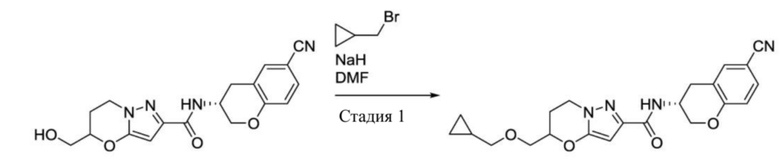
[0477]
В раствор N-((R)-6-цианохроман-3-ил)-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (397 мг, 1,12 ммоль), синтезированного с помощью способа, описанного на стадии 3 в примере 100, в N, N-диметилформамиде (11,2 мл) добавляли гидрид натрия (60% в масле) (179 мг, 4,48 ммоль). Смесь перемешивали в течение 10 минут при комнатной температуре. Дополнительно добавляли (бромметил)циклопропан (215 мкл, 2,24 ммоль) и смесь перемешивали в течение 16 часов при 90°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-6-цианохроман-3-ил)-5-((циклопропилметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (количество 136 мг, выход 30%).
[0478]
Пример 103
Разделение на изомеры N-((R)-6-цианохроман-3-ил)-5-((циклопропилметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0479]
[Хим. 135]

[0480]
Растворяли N-((R)-6-цианохроман-3-ил)-5-((циклопропилметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид (134 мг, 0,328 ммоль), синтезированный с помощью способа, описанного в примере 102, в этаноле (13 мл) и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IB, проявляющий растворитель: этанол, расход: 8,0 мл/мин., комнатная температура) с получением изомера A (количество 49,3 мг, выход 37%) и изомера B (количество 48,9 мг, выход 37%).
[0481]
Соединение из примера 104 синтезировали с помощью способа, подобного таковому для примера 100.
[0482]
Соединение из примера 105 синтезировали с помощью способов, подобных таковым, описанным в примере 100 и в контрольном примере 1.
[0483]
Соединение из примера 106 синтезировали с помощью способов, подобных таковым, описанным в примере 100 и в контрольном примере 1.
[0484]
Соединение из контрольного примера 32 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 27.
[0485]
[Хим. 136]

[0486]
Соединение из примера 107 синтезировали с помощью способов, подобных таковым, описанным в примере 100 и в контрольном примере 32.
[0487]
Соединение из контрольного примера 33 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для примера 100.
[0488]
[Хим. 137]
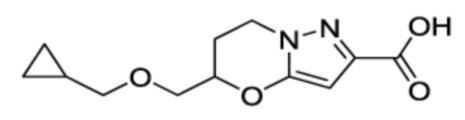
[0489]
Соединение из примера 108 синтезировали из соединения из контрольного примера 33 и соединения из контрольного примера 48 с помощью способа, подобного стадии 3 в примере 100.
[0490]
Соединения из примера 109 получали путем разделения соединения из примера 108.
[0491]
Соединение из примера 110 синтезировали из соединения из контрольного примера 33 и соединения из контрольного примера 28 с помощью способа, подобного стадии 3 в примере 100.
[0492]
Соединения из примера 111 получали путем разделения соединения из примера 110.
[0493]
Соединение из контрольного примера 34 (4-((1-метилциклопропил)метокси)бутан-1,3-диол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0494]
[Хим. 138]

[0495]
Соединение из примера 112 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 34, в примере 85 и в контрольном примере 24.
[0496]
Соединения из примера 113 получали путем разделения соединения из примера 112.
[0497]
Пример 114
Получение N-((R)-6-цианохроман-3-ил)-5-((2,2,2-трифторэтокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0498]
[Хим. 139]

[0499]
В раствор N-((R)-6-цианохроман-3-ил)-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (20,0 мг, 0,0564 ммоль), синтезированного с помощью способа, описанного на стадии 3 в примере 100, в толуоле (1,1 мл) добавляли трибутилфосфин (28,2 мкл, 0,113 ммоль), 2,2,2-трифторэтанол (40,6 мкл, 0,564 ммоль) и 1,1'-(азодикарбонил)дипиперизин (28,5 мг, 0,113 ммоль). Смесь перемешивали в течение 15 часов при 80°C.Реакционный раствор очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-6-цианохроман-3-ил)-5-((2,2,2-трифторэтокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида.
[0500]
Пример 115
Разделение на изомеры N-((R)-6-цианохроман-3-ил)-5-((2,2,2-трифторэтокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0501]
[Хим. 140]

[0502]
Растворяли N-((R)-6-цианохроман-3-ил)-5-((2,2,2-трифторэтокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид (178 мг, 0,408 ммоль), синтезированный с помощью способа, описанного в примере 114, в этаноле (18 мл) и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IB, проявляющий растворитель: этанол, расход: 8,0 мл/мин., комнатная температура) с получением изомера A (количество 74,7 мг, выход 42%) и изомера B (количество 70,5 мг, выход 40%).
[0503]
Соединение из примера 116 синтезировали с помощью способа, подобного таковому для примера 114.
[0504]
Соединение из примера 117 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0505]
[Хим. 141]

[0506]
Соединение из примера 118 синтезировали из соединения, синтезированного на стадии 3 в примере 100, с помощью способа, подобного стадии 2 в примере 117.
[0507]
Соединение из примера 119 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0508]
[Хим. 142]

[0509]
Соединение из примера 120 синтезировали из соединения, синтезированного на стадии 1 в примере 117, с помощью способа, подобного таковому для примера 119.
[0510]
Соединение из примера 121 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0511]
[Хим. 143]

[0512]
Соединение из примера 122 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0513]
[Хим. 144]

[0514]
Соединение из контрольного примера 35 синтезировали из соединения, синтезированного на стадии 1 в примере 122, в соответствии со схемой, изображенной на фигуре ниже.
[0515]
[Хим. 145]

[0516]
Соединение из примера 123 синтезировали из соединения из контрольного примера 35 и соединения из контрольного примера 28 с помощью способов, подобных стадии 3 и стадии 4 в примере 122.
[0517]
Соединения из примера 124 получали путем разделения соединения из примера 123.
[0518]
Соединение из примера 125 синтезировали из соединения из контрольного примера 35 и соединения из контрольного примера 32 с помощью способов, подобных стадии 3 и стадии 4 в примере 122.
[0519]
Контрольный пример 36
Этил-5-((2,2,2-трифторэтокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилат
[0520]
[Хим. 146]

[0521]
Получали этил-5-((2,2,2-трифторэтокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилат с помощью способа, подобного таковому для примера 114, с применением этил-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата, синтезированного с помощью способа, описанного на стадии 1 в примере 100, вместо N-((R)-6-цианохроман-3-ил)-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида.
[0522]
Соединение из примера 126 синтезировали из соединения из контрольного примера 36 и контрольного примера 48 с помощью способов, подобных стадии 2 и стадии 3 в примере 100.
[0523]
Соединения из примера 127 получали путем разделения соединения из примера 126.
[0524]
Пример 128
Получение 5-((2,2,2-трифторэтокси)метил)-N-((R)-6-((2,2,2-трифторэтокси)метил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0525]
[Хим. 147]

[0526]
Получали 5-((2,2,2-трифторэтокси)метил)-N-((R)-6-((2,2,2-трифторэтокси)метил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид с помощью способа, подобного стадии 3 и стадии 4 в примере 1, с применением этил-5-((2,2,2-трифторэтокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата, синтезированного с помощью способа, описанного в контрольном примере 36, вместо этил-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата на стадии 3, и с применением гидрохлорида (R)-6-((2,2,2-трифторэтокси)метил)хроман-3-амина, синтезированного с помощью способа, описанного в контрольном примере 44, вместо гидрохлорида 6-фторхроман-3-амина на стадии 4.
[0527]
Пример 129
Разделение на изомеры 5-((2,2,2-трифторэтокси)метил)-N-((R)-6-((2,2,2-трифторэтокси)метил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0528]
[Хим. 148]

[0529]
Растворяли 5-((2,2,2-трифторэтокси)метил)-N-((R)-6-((2,2,2-трифторэтокси)метил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид, синтезированный с помощью способа, описанного в примере 128, в этаноле и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IC, проявляющий растворитель: этанол/н-гексан=50/50, расход: 8,0 мл/мин., комнатная температура) с получением изомера A (количество 3,7 мг) и изомера B (количество 3,6 мг).
[0530]
Соединение из примера 130 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 28 с помощью способов, подобных стадии 2 и стадии 3 в примере 100.
[0531]
Соединения из примера 131 получали путем разделения соединения из примера 130.
[0532]
Соединение из примера 132 синтезировали из соединения из контрольного примера 36 и контрольного примера 32 с помощью способов, подобных стадии 3 и стадии 4 в примере 122.
[0533]
Соединение из контрольного примера 37 (5-((трифторметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0534]
[Хим. 149]

[0535]
Пример 133
Получение N-((R)-6-цианохроман-3-ил)-5-((трифторметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0536]
[Хим. 150]
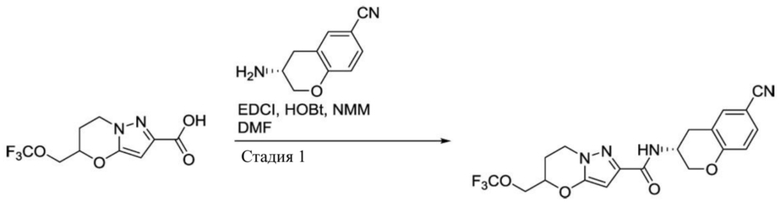
[0537]
В суспензию 5-((трифторметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты (смесь с 4 эквивалентами хлорида натрия) (267 мг, 0,534 ммоль), синтезированной с помощью способа, описанного в контрольном примере 37, (R)-3-аминохроман-6-карбонитрила (140 мг, 0,804 ммоль), синтезированного с помощью способа, описанного в контрольном примере 24, 1-гидроксибензотриазола (123 мг, 0,804 ммоль) и гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (154 мг, 0,804 ммоль) в N, N-диметилформамиде (5 мл) добавляли 4-метилморфолин (353 мкл, 3,21 ммоль). Смесь перемешивали в течение 15 часов при 40°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением N-((R)-6-цианохроман-3-ил)-5-((трифторметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (количество 182 мг, выход 81%).
[0538]
Пример 134
Разделение на изомеры N-((R)-6-цианохроман-3-ил)-5-((трифторметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0539]
[Хим. 151]

[0540]
Растворяли N-((R)-6-цианохроман-3-ил)-5-((трифторметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид (20 мг), синтезированный с помощью способа, описанного в примере 133, в этаноле (2 мл) и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IB, проявляющий растворитель: этанол, расход: 8,0 мл/мин., комнатная температура) с получением изомера A (количество 9,4 мг, выход 47%) и изомера B (количество 8,2 мг, выход 41%).
[0541]
Соединение из примера 135 синтезировали из соединения из контрольного примера 37 и соединения из контрольного примера 48 с помощью способа, подобного стадии 3 в примере 100.
[0542]
Соединения из примера 136 получали путем разделения соединения из примера 135.
[0543]
Соединение из контрольного примера 38 (5-((дифторметокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновую кислоту) синтезировали из соединения, синтезированного на стадии 1 в примере 100, в соответствии со схемой, изображенной на фигуре ниже.
[0544]
[Хим. 152]

[0545]
Соединение из примера 137 синтезировали из соединения из контрольного примера 38 и соединения из контрольного примера 48 с помощью способа, подобного стадии 3 в примере 100.
[0546]
Соединения из примера 138 получали путем разделения соединения из примера 137.
[0547]
Соединение из примера 139 синтезировали из соединения из контрольного примера 38 и соединения из контрольного примера 44 с помощью способа, подобного стадии 3 в примере 100.
[0548]
Соединения из примера 140 получали путем разделения соединения из примера 139.
[0549]
Соединение из примера 141 синтезировали из соединения из контрольного примера 38 и соединения из контрольного примера 45 с помощью способа, подобного стадии 3 в примере 100.
[0550]
Соединения из примера 142 получали путем разделения соединения из примера 141.
[0551]
Контрольный пример 39
Этил-5-(2-(бензилокси)этил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилат
[0552]
[Хим. 153]
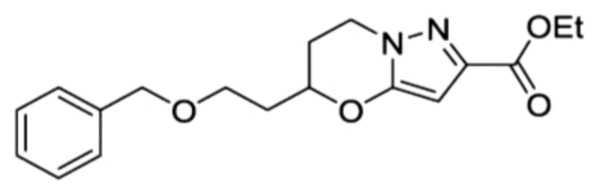
[0553]
Получали этил-5-(2-(бензилокси)этил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилат с помощью способа, подобного стадии 1 - стадии 4 в примере 85, с применением 5-(бензилокси)пентан-1,3-диола вместо бутан-1,3-диола на стадии 1.
[0554]
Контрольный пример 40
5-(2-(Трифторметокси)этил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновая кислота
[0555]
[Хим. 154]

[0556]
Стадия 1
Получали этил-5-(2-гидроксиэтил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилат с помощью способа, подобного стадии 1 в примере 100, с применением этил-5-(2-(бензилокси)этил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата, синтезированного с помощью способа, описанного в контрольном примере 39, вместо этил-5-((бензилокси)метил-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата.
[0557]
Стадия 2, стадия 3
Получали 5-(2-(трифторметокси)этил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновую кислоту в виде смеси с 2 эквивалентами хлорида натрия с помощью способа, подобного стадии 1 и стадии 2 в контрольном примере 37, с применением этил-5-(2-гидроксиэтил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата вместо этил-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата на стадии 1.
[0558]
Соединение из примера 143 синтезировали из соединения из контрольного примера 40 и соединения из контрольного примера 24 с помощью способа, подобного стадии 4 в примере 1.
[0559]
Соединения из примера 144 получали путем разделения соединения из примера 143.
[0560]
Соединение из контрольного примера 41 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 40, с помощью способа, подобного стадии 1 - стадии 2 в контрольном примере 38.
[0561]
[Хим. 155]
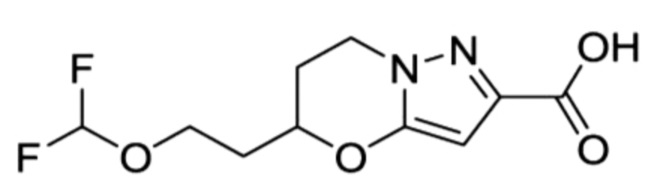
[0562]
Соединение из примера 145 синтезировали из соединения из контрольного примера 41 и соединения из контрольного примера 24 с помощью способа, подобного стадии 4 в примере 1.
[0563]
Соединения из примера 146 получали путем разделения соединения из примера 145.
[0564]
Соединение из примера 147 синтезировали из соединения из контрольного примера 41 и соединения из контрольного примера 48 с помощью способа, подобного стадии 4 в примере 1.
[0565]
Соединения из примера 148 получали путем разделения соединения из примера 147.
[0566]
Соединение из примера 149 синтезировали из соединения из контрольного примера 41 и соединения из контрольного примера 44 с помощью способа, подобного стадии 4 в примере 1.
[0567]
Соединения из примера 150 получали путем разделения соединения из примера 149.
[0568]
Соединение из контрольного примера 151 синтезировали из соединения, синтезированного на стадии 1 в примере 117, в соответствии со схемой, изображенной на фигуре ниже.
[0569]
[Хим. 156]

[0570]
Соединения из примера 152 получали путем разделения соединения из примера 151.
[0571]
Соединение из контрольного примера 42 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 2 - стадии 3 в примере 122.
[0572]
[Хим. 157]

[0573]
Соединение из примера 153 синтезировали из соединения из контрольного примера 42 в соответствии со схемой, изображенной на фигуре ниже.
[0574]
[Хим. 158]

[0575]
Соединение из примера 154 синтезировали из соединения из контрольного примера 42 в соответствии со схемой, изображенной на фигуре ниже.
[0576]
[Хим. 159]

[0577]
Соединение из примера 155 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0578]
[Хим. 160]
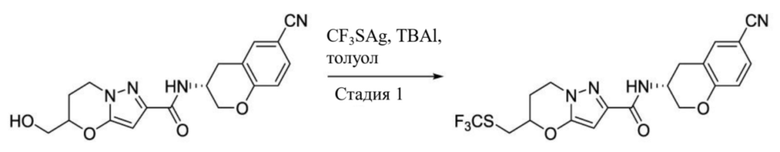
[0579]
Соединения из примера 156 получали путем разделения соединения из примера 155.
[0580]
Соединение из контрольного примера 157 синтезировали из соединения, синтезированного на стадии 1 в примере 151, в соответствии со схемой, изображенной на фигуре ниже.
[0581]
[Хим. 161]

[0582]
Соединения из примера 158 получали путем разделения соединения из примера 157.
[0583]
Пример 159
Получение N-((R)-6-бромхроман-3-ил)-5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0584]
[Хим. 162]
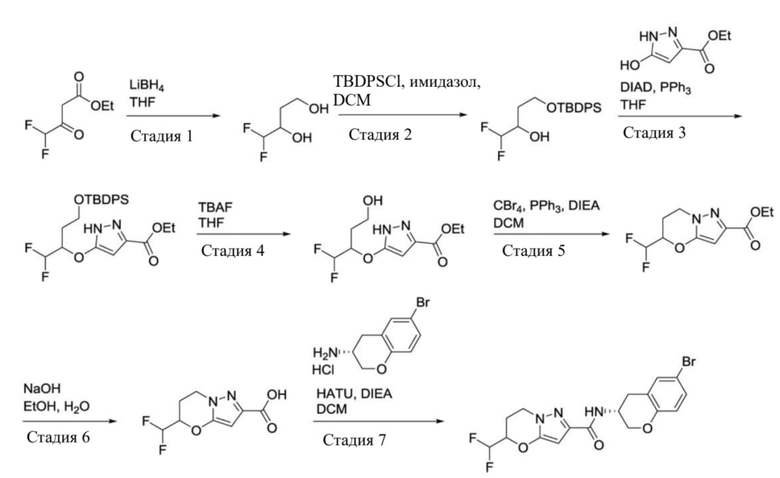
[0585]
Стадия 1
В раствор этил-4,4-дифтор-3-оксобутаноата (10,0 г, 60,2 ммоль) в тетрагидрофуране (300 мл) добавляли борогидрид лития (4,34 г, 199 ммоль) и смесь перемешивали в течение 15 часов при комнатной температуре. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. Органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом натрия. После того, как растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением 4,4-дифторбутан-1,3-диола (количество 3,37 г, выход 44%).
[0586]
Стадия 2
В раствор 4,4-дифторбутан-1,3-диола (128 мг, 1,02 ммоль) в дихлорметане (3,4 мл) добавляли имидазол (346 мг, 5,08 ммоль) и трет-бутилхлордифенилсилан (263 мкл, 1,01 ммоль) и смесь перемешивали в течение 6 часов при комнатной температуре. После того, как растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением 4-(трет-бутил(дифенил)силил)окси-1,1-дифторбутан-2-ола (количество 299 мг, выход 81%).
[0587]
Стадия 3
В раствор 4-(трет-бутил(дифенил)силил)окси-1,1-дифторбутан-2-ола (100 мг, 0,274 ммоль) в тетрагидрофуране (1,0 мл) добавляли этил-5-гидрокси-1H-пиразол-3-карбоксилат (42,8 мг, 0,274 ммоль), трифенилфосфин (93,6 мг, 0,357 ммоль) и 1,9 моль/л раствор азодикарбоновой кислоты в диизопропилтолуоле (190 мкл, 0,36 ммоль). Смесь перемешивали в течение 13 часов при комнатной температуре. Реакционный раствор очищали с помощью колоночной хроматографии на силикагеле с получением этил-5-(3-(трет-бутил(дифенилсилил)окси)-1-(дифторметил)пропокси)-1H-пиразол-3-карбоксилата (количество 33,3 мг, выход 24%).
Стадия 4
В раствор этил-5-(3-(трет-бутил(дифенилсилил)окси)-1-(дифторметил)пропокси)-1H-пиразол-3-карбоксилата (9,16 г, 18,2 ммоль) в тетрагидрофуране (180 мл) добавляли 1 моль/л раствор фторида тетрагидроаммония в тетрагидрофуране (37 мл, 37 ммоль) и смесь перемешивали в течение 1 часа при комнатной температуре. После концентрирования реакционного раствора при пониженном давлении остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-5-(1-(дифторметил)-3-гидроксипропокси)-1H-пиразол-3-карбоксилата (количество 4,75 г, выход 99%).
Стадия 5
В раствор этил-5-(1-(дифторметил)-3-гидроксипропокси)-1H-пиразол-3-карбоксилата (93,0 мг, 5,91 ммоль) в дихлорметане (3,5 мл) добавляли N, N-диизопропилэтиламин (363 мл, 2,11 ммоль), тетрабромметан (233 мг, 0,703 ммоль) и трифенилфосфин (120 мг, 0,703 ммоль). Смесь перемешивали в течение 22 часов при комнатной температуре. Добавляли 1 моль/л раствор хлористоводородной кислоты и хлороформ и смесь разделяли. Органический слой высушивали над безводным сульфатом натрия и затем растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата (219 мг) в виде смеси с трифенилфосфиноксидом.
Стадия 6
В раствор смеси этил-5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата и трифенилфосфиноксида (213 мг) в этаноле (1,7 мл) добавляли 4 моль/л водный раствор гидроксида натрия (346 мкл, 1,38 ммоль) и смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли 2 моль/л раствор хлористоводородной кислоты и толуол. После того, как растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением 5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты (20,1 мг).
[0588]
Стадия 7
Получали N-((R)-6-бромхроман-3-ил)-5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид с помощью способа, подобного стадии 3 в примере 100, с применением 5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты вместо 5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты и с применением гидрохлорида (R)-6-бромхроман-3-амина, синтезированного с помощью способа, описанного в контрольном примере 2, вместо (R)-3-аминохроман-6-карбонитрила.
[0589]
Контрольный пример 43
Получение гидрохлорида (R)-6-(трифторметил)хроман-3-амина
[0590]
[Хим. 163]

[0591]
Стадия 1
В раствор (R)-N-(хроман-3-ил)-2,2,2-трифторацетамида (2,50 г, 16,3 ммоль), синтезированного с помощью способа, описанного на стадии 1 в контрольном примере 1, в ацетонитриле (26 мл) добавляли моногидрат пара-толуолсульфоновой кислоты (2,13 г, 11,2 ммоль). Смесь перемешивали в течение 10 минут при комнатной температуре. Дополнительно добавляли раствор N-йодсукцинимида (2,52 г, 11,2 ммоль) в ацетонитриле (40 мл) и смесь перемешивали в течение 16 часов при комнатной температуре. После этого в реакционный раствор добавляли насыщенный водный раствор гидрокарбоната натрия, насыщенный водный раствор тиосульфата натрия и этилацетат и смесь разделяли. Органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом магния. К остатку добавляли н-гексан и этилацетат и остаток растворяли путем нагревания, и затем обеспечивали охлаждение раствора до комнатной температуры. Осажденное твердое вещество собирали путем фильтрации с получением (R)-2,2,2-трифтор-N-(6-йодхроман-3-ил)ацетамида (количество 1,19 г, выход 32%).
[0592]
Стадия 2
В раствор (R)-2,2,2-трифтор-N-(6-йодхроман-3-ил)ацетамида (1,19 г, 3,21 ммоль) в N, N-диметилформамиде (100 мл) добавляли йодид меди(I) (0,73 г, 3,8 ммоль), метил-2,2-дифтор-2-(фторсульфонил)ацетат (2,04 мл, 16 ммоль). Смесь перемешивали в течение 16 часов при 120°C. Обеспечивали охлаждение реакционного раствора до комнатной температуры, после чего его фильтровали через целит. После этого добавляли этилацетат, н-гексан и насыщенный водный раствор гидрокарбоната натрия и смесь разделяли. Органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом магния. После того, как растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-(трифторметил)хроман-3-ил)ацетамида (количество 949 мг, выход 95%).
[0593]
Стадия 3
В раствор (R)-2,2,2-трифтор-N-(6-(трифторметил)хроман-3-ил)ацетамида (133 мг, 0,425 ммоль) в метаноле (1,1 мл) добавляли 2 моль/л водный раствор гидроксида натрия (1,1 мл, 2,2 ммоль) и смесь перемешивали в течение 3 часов при комнатной температуре. В реакционный раствор добавляли воду и хлороформ и смесь разделяли. После этого органический слой высушивали над безводным сульфатом натрия. Растворитель выпаривали при пониженном давлении, остаток растворяли в этилацетате, добавляли 4 моль/л раствор хлороводорода в этилацетате и смесь перемешивали в течение 1 часа. Растворитель выпаривали при пониженном давлении с получением гидрохлорида ((R)-6-(трифторметил)хроман-3-амина (количество 93,8 мг, выход 87%).
[0594]
Пример 160
Получение 5-(дифторметил)-N-((R)-6-(трифторметил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0595]
[Хим. 164]

[0596]
В раствор 5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты (51,5 мг, 0,236 ммоль), синтезированной с помощью способа, описанного на стадии 6 в примере 159, гидрохлорида (R)-6-(трифторметил)хроман-3-амина (72,0 мг, 0,284 ммоль), синтезированного с помощью способа, описанного в контрольном примере 43, 1-гидроксибензотриазола (43,4 мг, 0,283 ммоль) и гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (54,5 мг, 0,284 ммоль) в N, N-диметилформамиде (787 мкл) добавляли 4-метилморфолин (158 мкл, 1,44 ммоль). Смесь перемешивали в течение 4 часов при комнатной температуре. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением 5-(дифторметил)-N-((R)-6-(трифторметил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида (количество 91,1 мг, выход 93%).
[0597]
Пример 161
Разделение на изомеры 5-(дифторметил)-N-((R)-6-(трифторметил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида
[0598]
[Хим. 165]

[0599]
Растворяли 5-(дифторметил)-N-((R)-6-(трифторметил)хроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид (14,7 мг, 0,035 ммоль), синтезированный с помощью способа, описанного в примере 160, в этаноле (7 мл) и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IC, проявляющий растворитель: этанол/н-гексан=50/50, расход: 20,0 мл/мин.) с получением изомера A (количество 6,2 мг, выход 42%) и изомера B (количество 5,2 мг, выход 35%).
[0600]
Контрольный пример 44
Получение гидрохлорида (R)-6-((2,2,2-трифторэтокси)метил)хроман-3-амина
[0601]
[Хим. 166]
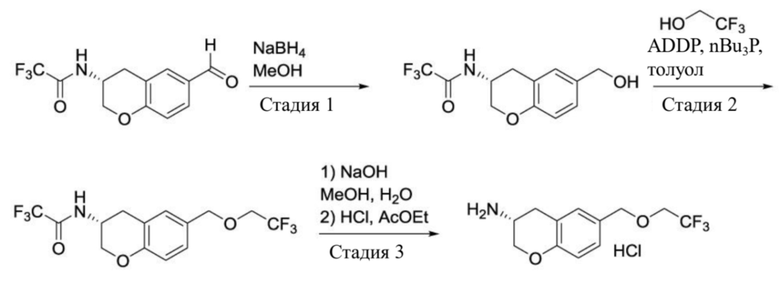
[0602]
Стадия 1
К ледяному (R)-2,2,2-трифтор-N-(6-формилхроман-3-ил)ацетамиду (3,89 г, 14,2 ммоль), синтезированному с помощью способа, описанного на стадии 2 в контрольном примере 3, в метаноле (70 мл) добавляли борогидрид натрия (1,08 г, 28,5 ммоль) и смесь перемешивали в течение 15 минут при охлаждении льдом. В реакционный раствор добавляли 1 моль/л раствор хлористоводородной кислоты и хлороформ и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-(гидроксиметил)хроман-3-ил)ацетамида (количество 2,34 г, выход 60%).
[0603]
Стадия 2
В раствор (R)-2,2,2-трифтор-N-(6-(гидроксиметил)хроман-3-ил)ацетамида (500 мг, 1,82 ммоль) в толуоле (18 мл) добавляли трибутилфосфин (908 мкл, 3,64 ммоль), 2,2,2-трифторэтанол (1,3 мл, 18 ммоль) и 1,1'-(азодикарбонил)дипиперидин (919 мг, 3,64 ммоль). Смесь перемешивали в течение 1 часа при 80°C. Обеспечивали охлаждение реакционного раствора до комнатной температуры, добавляли воду и этилацетат и смесь разделяли. Органический слой промывали насыщенным солевым раствором и затем высушивали над безводным сульфатом магния и растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-((2,2,2-трифторэтокси)метил)хроман-3-ил)ацетамида (количество 409 мг, выход 63%).
[0604]
Стадия 3
Получали гидрохлорид (R)-6-((2,2,2-трифторэтокси)метил)хроман-3-амина с помощью способа, подобного стадии 3 в контрольном примере 1, с применением (R)-2,2,2-трифтор-N-(6-((2,2,2-трифторэтокси)метил)хроман-3-ил)ацетамида вместо (R)-N-(6-хлорхроман-3-ил)-2,2,2-трифторацетамида вместо (R)-N-(6-хлорхроман-3-ил)-2,2,2-трифторацетамида.
[0605]
Соединение из примера 162 синтезировали с помощью способов, подобных таковым, описанным в примере 159 и в контрольном примере 44.
[0606]
Соединения из примера 163 получали путем разделения соединения из примера 162.
[0607]
Соединение из контрольного примера 45 (гидрохлорид (R)-6-(2-(дифторметокси)этил)хроман-3-амина) синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 3, в соответствии со схемой, изображенной на фигуре ниже.
[0608]
[Хим. 167]
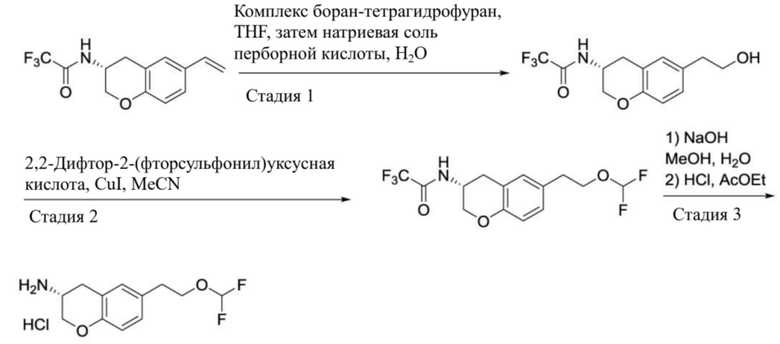
[0609]
Соединение из примера 164 синтезировали с помощью способов, подобных таковым, описанным в примере 159 и в контрольном примере 45.
[0610]
Соединения из примера 165 получали путем разделения соединения из примера 164.
[0611]
Соединения из контрольного примера 46 (N-((R)-6-хлорхроман-3-ил)-5-(2-гидроксипропан-2-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид и 5-ацетил-N-((R)-6-хлорхроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамид) синтезировали из соединения, синтезированного на стадии 1 в примере 117, в соответствии со схемой, изображенной на фигуре ниже.
[0612]
[Хим. 168]

[0613]
Соединение из примера 166 синтезировали из соединения из контрольного примера 46 (N-((R)-6-хлорхроман-3-ил)-5-(2-гидроксипропан-2-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида) с помощью способа, подобного таковому для примера 157.
[0614]
Соединение из примера 167 синтезировали из соединения из контрольного примера 46 (5-ацетил-N-((R)-6-хлорхроман-3-ил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида) с помощью способа, подобного таковому для примера 157.
[0615]
Соединение из примера 168 синтезировали из соединения, синтезированного на стадии 2 в контрольном примере 46, в соответствии со схемой, изображенной на фигуре ниже.
[0616]
[Хим. 169]

[0617]
Соединение из примера 169 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0618]
[Хим. 170]

[0619]
Соединения из примера 170 получали путем разделения соединения из примера 169.
[0620]
Соединение из примера 171 синтезировали с помощью способов, подобных таковым, описанным в примере 169 и в контрольном примере 2.
[0621]
Соединение из контрольного примера 47 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 4.
[0622]
[Хим. 171]
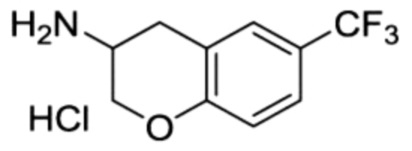
[0623]
Соединение из контрольного примера 48 (гидрохлорид (R)-6-(2,2-дифторэтил)хроман-3-амина) синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 45, в соответствии со схемой, изображенной на фигуре ниже.
[0624]
[Хим. 172]

[0625]
Соединение из примера 172 синтезировали с помощью способов, подобных таковым, описанным в примере 169 и в контрольном примере 48.
[0626]
Соединения из примера 173 получали путем разделения соединения из примера 172.
[0627]
Соединение из примера 174 синтезировали из соединения из примера 171 с помощью способа, подобного стадии 1 в контрольном примере 27.
[0628]
Соединение из примера 175 синтезировали с помощью способа, подобного таковому для примера 174.
[0629]
Соединение из примера 176 синтезировали с помощью способа, подобного таковому для примера 174.
[0630]
Соединение из примера 177 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0631]
[Хим. 173]

[0632]
Соединение из примера 178 синтезировали с помощью способов, подобных таковым, описанным в примере 177 и в контрольном примере 24.
[0633]
Соединение из примера 179 синтезировали с помощью способов, подобных таковым, описанным в примере 177 и в контрольном примере 32.
[0634]
Соединение из примера 180 синтезировали с помощью способов, подобных таковым, описанным в примере 177 и в контрольном примере 24.
[0635]
Соединение из примера 181 синтезировали с помощью способа, подобного стадии 6 - стадии 8 в примере 70.
[0636]
Соединение из примера 182 синтезировали с помощью способов, подобных таковым, описанным в примере 181 и в контрольном примере 24.
[0637]
Соединение из примера 183 синтезировали с помощью способов, подобных таковым, описанным в примере 169 и в контрольном примере 44.
[0638]
Соединения из примера 184 получали путем разделения соединения из примера 183.
[0639]
Соединение из контрольного примера 49 (3-(циклопропилметокси)пропан-1,2-диол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0640]
[Хим. 174]

[0641]
Соединение из контрольного примера 50 (показано на фигуре ниже) синтезировали из соединения из контрольного примера 49 с помощью способа, подобного стадии 1 - стадии 5 в примере 85.
[0642]
[Хим. 175]

[0643]
Соединение из примера 185 синтезировали из соединения из контрольного примера 50 и соединения из контрольного примера 44 с помощью способа, подобного стадии 3 в примере 100.
[0644]
Соединения из примера 186 получали путем разделения соединения из примера 185.
[0645]
Соединение из контрольного примера 51 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 1 - стадии 4 в примере 85.
[0646]
[Хим. 176]

[0647]
Пример 187
Получение 2-((2,2,2-трифторэтокси)метил)-N-((R)-6-((2,2,2-трифторэтокси)метил)хроман-3-ил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамида
[0648]
[Хим. 177]

[0649]
Стадия 1
Получали этил-2-(гидроксиметил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилат с помощью способа, подобного стадии 1 в примере 100, с применением этил-2-((бензилокси)метил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилата, синтезированного с помощью способа, описанного в контрольном примере 51, вместо этил-5-((бензилокси)метил-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата.
[0650]
Стадия 2
Получали этил-2-((2,2,2-трифторэтокси)метил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилат с помощью способа, подобного таковому для примера 114, с применением этил-2-(гидроксиметил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилата вместо N-((R)-6-цианохроман-3-ил)-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида.
[0651]
Стадия 3
Получали 2-((2,2,2-трифторэтокси)метил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновую кислоту в виде смеси с 4 эквивалентами хлорида натрия с помощью способа, подобного стадии 2 в примере 100, с применением этил-2-((2,2,2-трифторэтокси)метил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилата вместо этил-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата.
[0652]
Стадия 4
Получали 2-((2,2,2-трифторэтокси)метил)-N-((R)-6-((2,2,2-трифторэтокси)метил)хроман-3-ил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамид с помощью способа, подобного стадии 3 в примере 100, с применением 2-((2,2,2-трифторэтокси)метил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновой кислоты вместо 5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновой кислоты, и с применением гидрохлорида (R)-6-((2,2,2-трифторэтокси)метил)хроман-3-амина, синтезированного с помощью способа, описанного в контрольном примере 44, вместо (R)-3-аминохроман-6-карбонитрила.
[0653]
Соединения из примера 188 получали путем разделения соединения из примера 187.
[0654]
Соединение из примера 189 синтезировали с помощью способов, подобных таковым, описанным в примере 187 и в контрольном примере 45.
[0655]
Соединения из примера 190 получали путем разделения соединения из примера 189.
[0656]
Соединение из контрольного примера 52 (гидрохлорид (R)-6-(2,2,2-трифторэтил)хроман-3-амина) синтезировали из соединения, синтезированного на стадии 2 в контрольном примере 3, в соответствии со схемой, изображенной на фигуре ниже.
[0657]
[Хим. 178]

[0658]
Соединение из примера 191 синтезировали с помощью способов, подобных таковым, описанным в примере 187 и в контрольном примере 52.
[0659]
Соединения из примера 192 получали путем разделения соединения из примера 191.
[0660]
Контрольный пример 53
Получение (R)-6-(5-метилпиразин-2-ил)хроман-3-амина
[0661]
[Хим. 179]

[0662]
Стадия 1
В суспензию (R)-2,2,2-трифтор-N-(6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)хроман-3-ил)ацетамида (600 мг, 1,62 ммоль), синтезированного с помощью способа, описанного на стадии 1 в контрольном примере 28, 2-бром-5-метилпиразина (336 мг, 1,94 ммоль), карбоната цезия (1,00 г, 3,07 ммоль) в 1,4-диоксане (20 мл) добавляли Xantphos Pd G3 (15,0 мг, 0,0158 ммоль). Смесь перемешивали в течение 4 часов при 125°C. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После этого органический слой высушивали над безводным сульфатом натрия и растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-2,2,2-трифтор-N-(6-(5-метилпиразин-2-ил)хроман-3-ил)ацетамида (количество 224 мг, выход 41%).
[0663]
Стадия 2
Получали (R)-6-(5-метилпиразин-2-ил)хроман-3-амин с помощью способа, подобного стадии 3 в контрольном примере 1, с применением (R)-2,2,2-трифтор-N-(6-(5-метилпиразин-2-ил)хроман-3-ил)ацетамида вместо (R)-N-(6-хлорхроман-3-ил)-2,2,2-трифторацетамида.
[0664]
Соединение из примера 193 синтезировали с помощью способов, подобных таковым, описанным в примере 187 и в контрольном примере 52.
[0665]
Соединения из примера 194 получали путем разделения соединения из примера 193.
[0666]
Соединение из контрольного примера 54 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 1 в примере 187 с помощью способа, подобного таковому для контрольного примера 37.
[0667]
[Хим. 180]

[0668]
Соединение из примера 195 синтезировали из соединения из контрольного примера 54 и соединения из контрольного примера 44 с помощью способа, подобного стадии 3 в примере 100.
[0669]
Соединения из примера 196 получали путем разделения соединения из примера 195.
[0670]
Соединение из примера 197 синтезировали из соединения из контрольного примера 54 и соединения из контрольного примера 48 с помощью способа, подобного стадии 3 в примере 100.
[0671]
Соединения из примера 198 получали путем разделения соединения из примера 197.
[0672]
Соединение из примера 199 синтезировали с помощью способов, подобных таковым, описанным в примере 187 и в контрольном примере 24.
[0673]
Соединения из примера 200 получали путем разделения соединения из примера 199.
[0674]
Пример 201
Получение N-((R)-6-цианохроман-3-ил)-2-(2-(циклопропилметокси)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамида
[0675]
[Хим. 181]
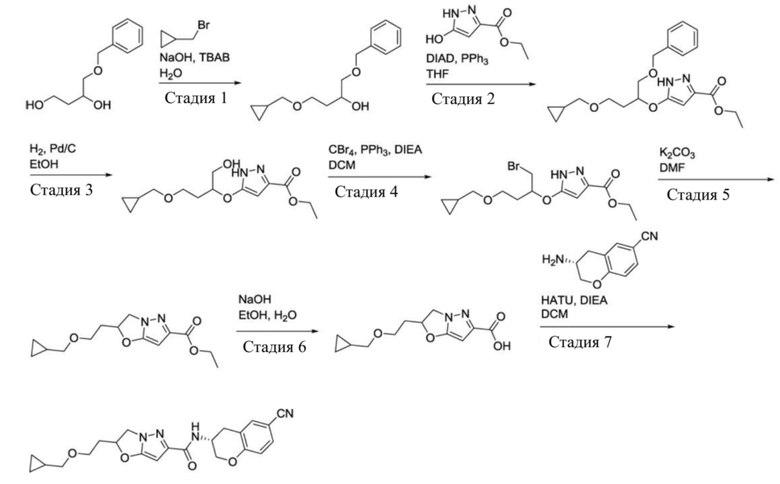
[0676]
Стадия 1
В 4 моль/л водный раствор гидроксида натрия (1 мл) добавляли бромид тетрабутиламмония (16,4 мг, 0,0509 ммоль), 4-бензилоксибутан-1,3-диол (100 мг, 0,510 ммоль) и (бромметил)циклопропан (0,15 мл, 1,6 ммоль). Смесь перемешивали в течение 2 часов при 50°C. В реакционный раствор добавляли насыщенный водный раствор хлорида аммония и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением 1-бензилокси-4-(циклопропилметокси)бутан-2-ола (количество 58 мг, выход 45%).
[0677]
Стадия 2
Получали этил-5-(1-бензилоксиметил)-3-(циклопропилметокси)пропокси)-1H-пиразол-3-карбоксилат с помощью способа, подобного таковому для примера 85, с применением 1-бензилокси-4-(циклопропилметокси)бутан-2-ола вместо 4-((трет-бутилдифенилсилил)окси)бутан-2-ола.
[0678]
Стадия 3
В раствор этил-5-(1-бензилоксиметил)-3-(циклопропилметокси)пропокси)-1H-пиразол-3-карбоксилата (1,3 г, 3,3 ммоль) в этаноле (50 мл) добавляли 5% палладий на угле (0,71 г) и смесь перемешивали в атмосфере водорода (давление с применением баллона) в течение 3 часов при комнатной температуре. После того, как реакционный раствор фильтровали через целит, растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-5-(3-(циклопропилметокси)-1-(гидроксиметил)пропокси)-1H-пиразол-3-карбоксилата (количество 0,91 г, выход 91%).
[0679]
Стадия 4
В раствор этил-5-(3-(циклопропилметокси)-1-(гидроксиметил)пропокси)-1H-пиразол-3-карбоксилата (0,91 г, 3,1 ммоль) в дихлорметане (20 мл) добавляли N, N-диизопропилэтиламин (3,1 мл, 18 ммоль), тетрабромметан (3,0 г, 9,0 ммоль) и трифенилфосфин (1,6 г, 6,1 ммоль). Смесь перемешивали в течение 15 часов при комнатной температуре. После концентрирования реакционного раствора при пониженном давлении остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-5-(1-(бромметил)-3-(циклопропилметокси)пропокси)-1H-пиразол-3-карбоксилата (количество 0,42 г, выход 38%).
[0680]
Стадия 5
В раствор этил-5-(1-(бромметил)-3-(циклопропилметокси)пропокси)-1H-пиразол-3-карбоксилата (0,42 г, 1,2 ммоль) в N, N-диметилформамиде (12 мл) добавляли карбонат калия (0,40 г, 2,9 ммоль) и смесь перемешивали в течение 3 часов при комнатной температуре. В реакционный раствор добавляли воду и хлороформ и смесь разделяли. После того, как органический слой высушивали над безводным сульфатом магния, растворитель выпаривали при пониженном давлении. Получали этил-2-(2-(циклопропилметокси)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилат (количество 195 мг, выход 60%).
[0681]
Стадия 6
Получали 2-(2-(циклопропилметокси)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновую кислоту в виде смеси с 4 эквивалентами хлорида натрия с помощью способа, подобного стадии 5 в примере 85, с применением этил-2-(2-(циклопропилметокси)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилата вместо этил-5-(2-фторфенил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата.
[0682]
Стадия 7
Получали N-((R)-6-цианохроман-3-ил)-2-(2-(циклопропилметокси)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамид с помощью способа, подобного стадии 4 в примере 1, с применением 2-(2-(циклопропилметокси)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновой кислоты вместо 6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты и с применением (R)-3-аминохроман-6-карбонитрила, синтезированного с помощью способа, описанного в контрольном примере 24, вместо гидрохлорида 6-фторхроман-3-амина.
[0683]
Соединения из примера 202 получали путем разделения соединения из примера 201.
[0684]
Пример 203
Получение 2-(2-(циклопропилметокси)этил)-N-((R)-6-(2-метоксипиримидин-5-ил)хроман-3-ил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамида
[0685]
[Хим. 182]
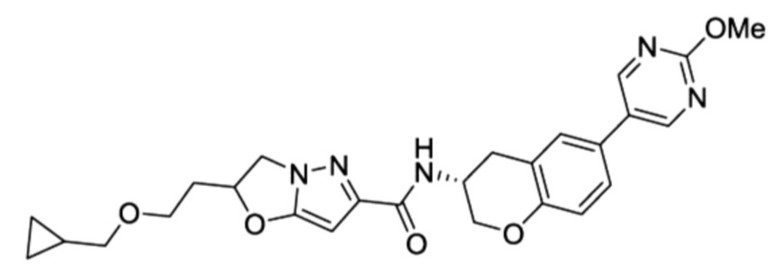
[0686]
Получали 2,2-(2-(циклопропилметокси)этил)-N-((R)-6-(2-метоксипиримидин-5-ил)хроман-3-ил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамид с помощью способа, подобного таковому для примера 201, с применением (R)-6-(2-метоксипиримидин-5-ил)хроман-3-амина, синтезированного с помощью способа, описанного в контрольном примере 29, вместо (R)-3-аминохроман-6-карбонитрила.
[0687]
Пример 204
Разделение на изомеры 2-(2-(циклопропилметокси)этил)-N-((R)-6-(2-метоксипиримидин-5-ил)хроман-3-ил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамида
[0688]
[Хим. 183]
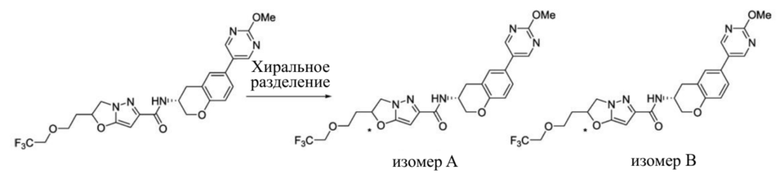
[0689]
Растворяли 2-(2-(циклопропилметокси)этил)-N-((R)-6-(2-метоксипиримидин-5-ил)хроман-3-ил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамид (22,0 мг, 0,045 ммоль), синтезированный с помощью способа, описанного в примере 203, в этаноле (7 мл), раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IB, проявляющий растворитель: этанол, расход: 8,0 мл/мин., комнатная температура) с получением изомера A (количество 6,4 мг, выход 29%) и изомера B (количество 8,5 мг, выход 39%).
[0690]
Соединение из контрольного примера 55 (2-(2-(2,2,2-трифторэтокси)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0691]
[Хим. 184]

[0692]
Соединение из контрольного примера 56 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 53.
[0693]
[Хим. 185]

[0694]
Соединение из примера 205 синтезировали из соединения из контрольного примера 55 и соединения из контрольного примера 56 с помощью способа, подобного стадии 3 в примере 100.
[0695]
Соединения из примера 206 получали путем разделения соединения из примера 205.
[0696]
Соединение из примера 207 синтезировали из соединения из контрольного примера 55 и соединения из контрольного примера 28 в соответствии со схемой, изображенной на фигуре ниже.
[0697]
[Хим. 186]

[0698]
Соединение из контрольного примера 57 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 5 в контрольном примере 55 с помощью способа, подобного таковому для контрольного примера 37.
[0699]
[Хим. 187]

[0700]
Соединение из примера 208 синтезировали из соединения из контрольного примера 57 и соединения из контрольного примера 24 с помощью способа, подобного стадии 4 в примере 1.
[0701]
Соединения из примера 209 получали путем разделения соединения из примера 208.
[0702]
Соединение из примера 210 синтезировали из соединения из контрольного примера 57 и соединения из контрольного примера 48 с помощью способа, подобного стадии 4 в примере 1.
[0703]
Соединения из примера 211 получали путем разделения соединения из примера 210.
[0704]
Соединение из примера 212 синтезировали из соединения из контрольного примера 57 и соединения из контрольного примера 56 с помощью способа, подобного стадии 4 в примере 1.
[0705]
Соединения из примера 213 получали путем разделения соединения из примера 212.
[0706]
Соединение из контрольного примера 58 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 5 в контрольном примере 55 с помощью способа, подобного таковому для контрольного примера 38.
[0707]
[Хим. 188]
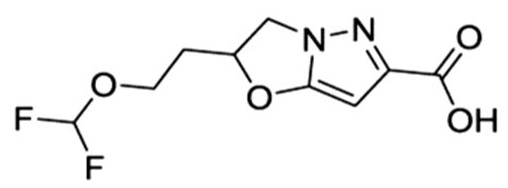
[0708]
Соединение из примера 214 синтезировали из соединения из контрольного примера 58 и соединения из контрольного примера 44 с помощью способа, подобного стадии 4 в примере 1.
[0709]
Соединения из примера 215 получали путем разделения соединения из примера 214.
[0710]
Соединение из примера 216 синтезировали из соединения из контрольного примера 58 и соединения из контрольного примера 45 с помощью способа, подобного стадии 4 в примере 1.
[0711]
Соединения из примера 217 получали путем разделения соединения из примера 216.
[0712]
Соединение из примера 218 синтезировали из соединения из контрольного примера 58 и соединения из контрольного примера 48 с помощью способа, подобного стадии 4 в примере 1.
[0713]
Соединения из примера 219 получали путем разделения соединения из примера 218.
[0714]
Соединение из контрольного примера 59 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для примера 53.
[0715]
[Хим. 189]
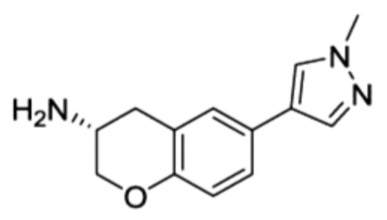
[0716]
Соединение из примера 220 синтезировали из соединения из контрольного примера 58 и соединения из контрольного примера 59 с помощью способа, подобного стадии 4 в примере 1.
[0717]
Соединения из примера 221 получали путем разделения соединения из примера 220.
[0718]
Соединение из контрольного примера 60 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 53.
[0719]
[Хим. 190]

[0720]
Соединение из примера 222 синтезировали из соединения из контрольного примера 58 и соединения из контрольного примера 60 с помощью способа, подобного стадии 4 в примере 1.
[0721]
Соединения из примера 223 получали путем разделения соединения из примера 222.
[0722]
Соединение из контрольного примера 61 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0723]
[Хим. 191]
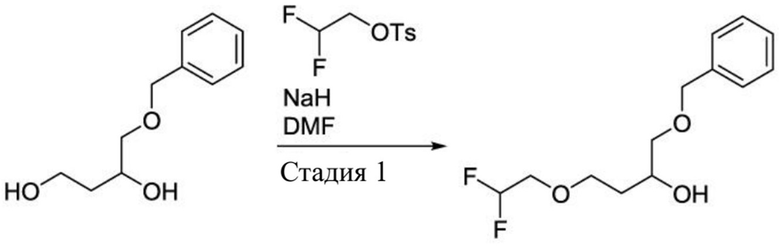
[0724]
Соединение из контрольного примера 62 (показано на фигуре ниже) синтезировали из соединения из контрольного примера 61 с помощью способа, подобного стадии 2 - стадии 6 в примере 201.
[0725]
[Хим. 192]

[0726]
Соединение из примера 224 синтезировали из соединения из контрольного примера 62 и соединения из контрольного примера 44 в соответствии со схемой, изображенной на фигуре ниже.
[0727]
[Хим. 193]
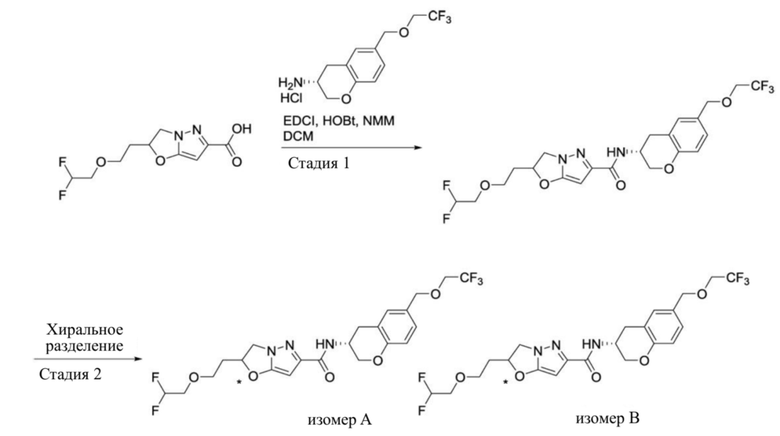
[0728]
Соединение из примера 225 синтезировали из соединения, синтезированного на стадии 5 в контрольном примере 55, в соответствии со схемой, изображенной на фигуре ниже.
[0729]
[Хим. 194]
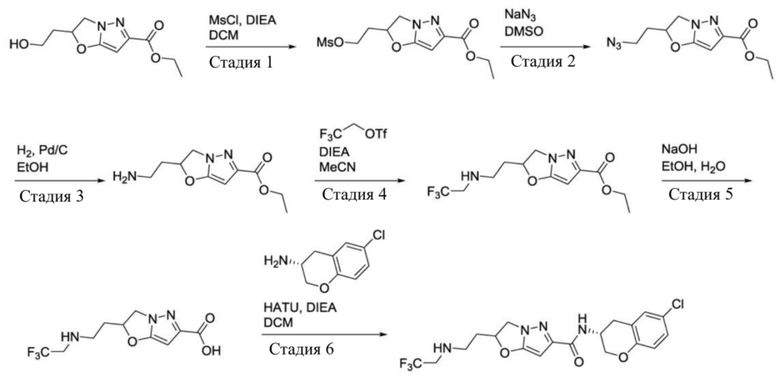
[0730]
Соединения из примера 226 получали путем разделения соединения из примера 225.
[0731]
Соединение из контрольного примера 63 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 27.
[0732]
[Хим. 195]
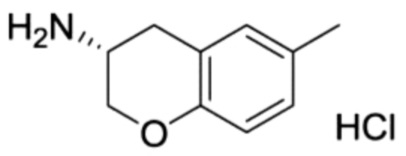
[0733]
Соединение из примера 227 синтезировали с помощью способов, подобных таковым, описанным в примере 225 и в контрольном примере 63.
[0734]
Соединения из примера 228 получали путем разделения соединения из примера 227.
[0735]
Соединение из примера 229 синтезировали с помощью способов, подобных таковым, описанным в примере 225 и в контрольном примере 43.
[0736]
Соединения из примера 230 получали путем разделения соединения из примера 229.
[0737]
Соединение из примера 231 синтезировали с помощью способов, подобных таковым, описанным в примере 225 и в контрольном примере 44.
[0738]
Соединения из примера 232 получали путем разделения соединения из примера 231.
[0739]
Соединение из контрольного примера 64 (2-(2-(3,3-дифторазетидин-1-ил)этил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновую кислоту) синтезировали из соединения, синтезированного на стадии 1 в примере 225, в соответствии со схемой, изображенной на фигуре ниже.
[0740]
[Хим. 196]
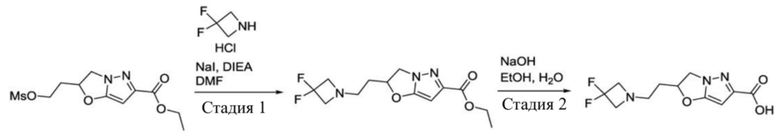
[0741]
Соединение из примера 233 синтезировали из соединения из контрольного примера 64 и соединения из контрольного примера 1 с помощью способа, подобного стадии 3 в примере 100.
[0742]
Соединения из примера 234 получали путем разделения соединения из примера 233.
[0743]
Соединение из примера 235 синтезировали из соединения из контрольного примера 64 и соединения из контрольного примера 43 с помощью способа, подобного стадии 3 в примере 100.
[0744]
Соединения из примера 236 получали путем разделения соединения из примера 235.
[0745]
Соединение из примера 237 синтезировали из соединения из контрольного примера 64 и соединения из контрольного примера 45 с помощью способа, подобного стадии 3 в примере 100.
[0746]
Соединения из примера 238 получали путем разделения соединения из примера 237.
[0747]
Соединение из контрольного примера 65 (гидрохлорид (R)-6-(2-(трифторметокси)этил)хроман-3-амина) синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 45, в соответствии со схемой, изображенной на фигуре ниже.
[0748]
[Хим. 197]

[0749]
Соединение из примера 239 синтезировали с помощью способов, подобных таковым, описанным в примере 233 и в контрольном примере 65.
[0750]
Соединения из примера 240 получали путем разделения соединения из примера 239.
[0751]
Соединение из контрольного примера 66 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 64.
[0752]
[Хим. 198]
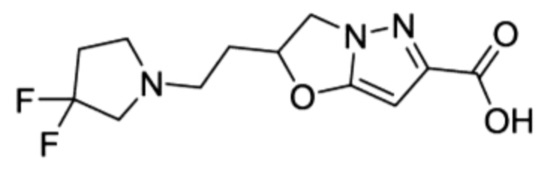
[0753]
Соединение из примера 241 синтезировали из соединения из контрольного примера 66 в соответствии со схемой, изображенной на фигуре ниже.
[0754]
[Хим. 199]
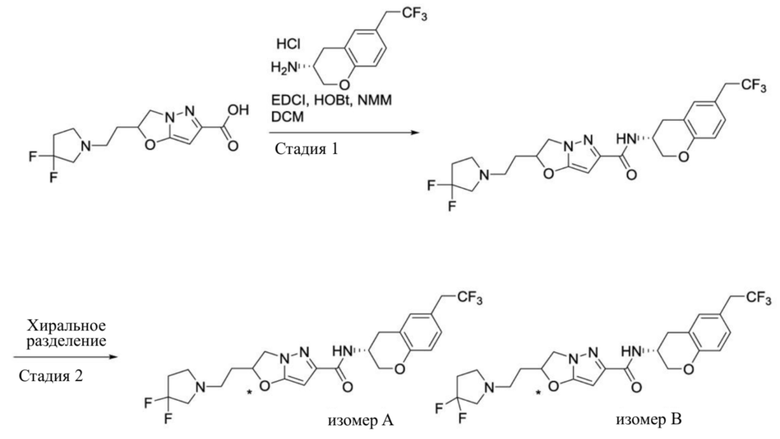
[0755]
Соединение из контрольного примера 67 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 64.
[0756]
[Хим. 200]
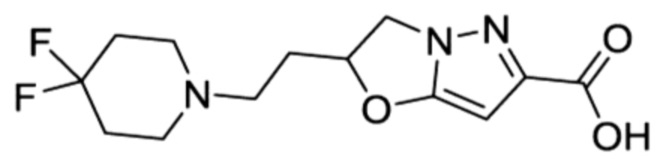
[0757]
Соединение из примера 242 синтезировали из соединения из контрольного примера 67 в соответствии со схемой, изображенной на фигуре ниже.
[0758]
[Хим. 201]

[0759]
Соединение из примера 243 синтезировали из соединения, синтезированного на стадии 5 в контрольном примере 55, и соединения из контрольного примера 24 с помощью способа, подобного стадии 2 - стадии 4 в примере 187.
[0760]
Соединения из примера 244 получали путем разделения соединения из примера 243.
[0761]
Соединение из примера 245 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0762]
[Хим. 202]

[0763]
Соединения из примера 246 получали путем разделения соединения из примера 245.
[0764]
Пример 247
Получение и разделение на изомеры N-((R)-6-цианохроман-3-ил)-2-(3-(трифторметокси)пропил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамида
[0765]
[Хим. 203]

[0766]
Стадия 1 - стадия 2
Получали 2-(3-(трифторметокси)пропил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновую кислоту с помощью способа, подобного стадии 1 - стадии 2 в контрольном примере 37, с применением этил-2-(3-гидроксипропил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилата, синтезированного с помощью способа, описанного на стадии 7 в примере 245, вместо этил-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата на стадии 1.
[0767]
Стадия 3
Получали N-((R)-6-цианохроман-3-ил)-2-(3-(трифторметокси)пропил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамид с помощью способа, подобного стадии 4 в примере 1, с применением 2-(3-(трифторметокси)пропил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновой кислоты вместо 6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоновой кислоты, и с применением (R)-3-аминохроман-6-карбонитрила, синтезированного с помощью способа, описанного в контрольном примере 24, вместо гидрохлорида 6-фторхроман-3-амина.
[0768]
Стадия 4
Растворяли N-((R)-6-цианохроман-3-ил)-2-(3-(трифторметокси)пропил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксамид (126 мг, 0,289 ммоль) в этаноле (12 мл) и раствор подвергали разделению на фракции с помощью HPLC (колонка: CHIRALPAK IB N-5, проявляющий растворитель: этанол, расход: 8,0 мл/мин., комнатная температура) с получением изомера A (количество 57,7 мг, выход 46%) и изомера B (количество 52,5 мг, выход 42%).
[0769]
Соединение из контрольного примера 248 синтезировали из соединения, синтезированного на стадии 7 в примере 245, в соответствии со схемой, изображенной на фигуре ниже.
[0770]
[Хим. 204]

[0771]
Соединение из примера 249 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0772]
[Хим. 205]
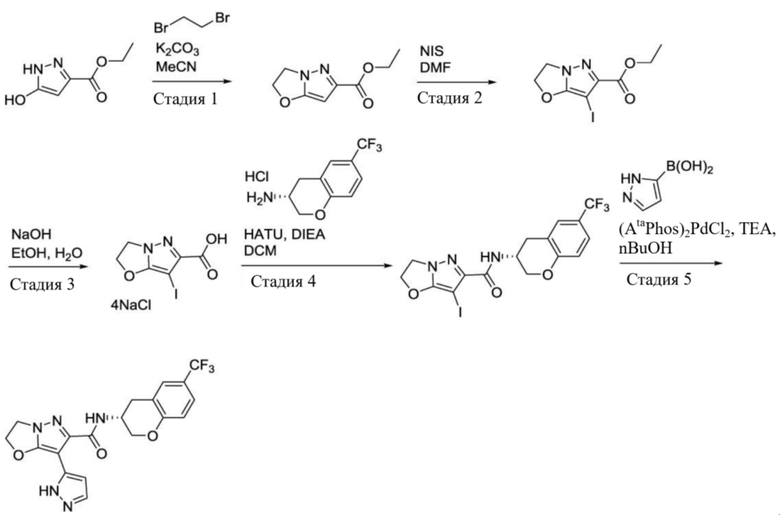
[0773]
Соединение из контрольного примера 68 (этил-2,2-диметил-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилат) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0774]
[Хим. 206]

[0775]
Соединение из примера 250 синтезировали из соединения из контрольного примера 68 с помощью способа, подобного стадии 2 - стадии 5 в примере 249.
[0776]
Соединение из примера 251 синтезировали с помощью способа, подобного стадии 5 - стадии 8 в примере 70.
[0777]
Пример 252
Получение N-((R)-6-цианохроман-3-ил)-6-(трифторметокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида
[0778]
[Хим. 207]
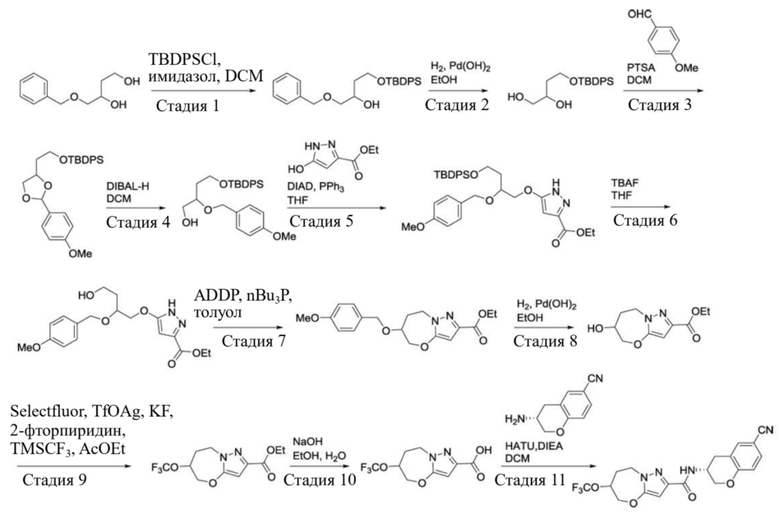
[0779]
Стадия 1
Получали 1-(бензилокси)-4-((трет-бутилдифенилсилил)окси)бутан-2-ол с помощью способа, подобного стадии 1 в примере 85, с применением 4-(бензилокси)бутан-1,3-диола вместо бутан-1,3-диола вместо бутан-1,3-диола.
[0780]
Стадия 2
Получали 4-((трет-бутилдифенилсилил)окси)бутан-1,2-диол с помощью способа, подобного стадии 1 в примере 100, с применением 1-(бензилокси)-4-((трет-бутилдифенилсилил)окси)бутан-2-ола вместо этил-5-((бензилокси)метил-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата.
[0781]
Стадия 3
В раствор 4-((трет-бутилдифенилсилил)окси)бутан-1,2-диола (2,00 г, 5,81 ммоль) в дихлорметане (24 мл) добавляли п-толуолсульфоновую кислоту (55 мг, 0,29 ммоль) и 4-метоксибензальдегид (2,37 г, 17,4 ммоль) и смесь перемешивали в течение 1 часа при комнатной температуре. В реакционный раствор добавляли насыщенный водный раствор гидрокарбоната натрия и хлороформ и смесь разделяли. После того, как органический слой промывали насыщенным солевым раствором и растворитель выпаривали при пониженном давлении, остаток очищали с помощью колоночной хроматографии на силикагеле с получением трет-бутил-(2-(2-(4-метоксифенил)-1,3-диоксолан-4-ил)этокси)дифенилсилана (количество 1,76 мг, выход 66%).
[0782]
Стадия 4
Раствор трет-бутил-(2-(2-(4-метоксифенил)-1,3-диоксолан-4-ил)этокси)дифенилсилана (1,76 г, 3,80 ммоль) в дихлорметане (20 мл) охлаждали до −78°C и в раствор добавляли 1 моль/л раствор гидрида диизобутилалюминия/н-гексана (5,33 мл, 5,33 ммоль). После перемешивания в течение 15 минут смесь нагревали до 0°C. В реакционный раствор добавляли водный раствор тартрата калия-натрия и хлороформ и смесь разделяли. После этого органический слой высушивали над безводным сульфатом натрия и растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением 4-(трет-бутил(дифенил)силил)окси-2-((4-метоксифенил)метокси)бутан-1-ола (количество 427 мг, выход 24%).
[0783]
Стадия 5 - стадия 6
Получали этил-5-(4-гидрокси-2-((4-метоксибензил)окси)бутокси)-1H-пиразол-3-карбоксилат с помощью способа, подобного стадии 2 - стадии 3 в примере 85, с применением 4-(трет-бутил(дифенил)силил)окси-2-((4-метоксифенил)метокси)бутан-1-ола вместо 4-((трет-бутилдифенилсилил)окси)бутан-2-ола на стадии 2.
[0784]
Стадия 7
В раствор этил-5-(4-гидрокси-2-((4-метоксибензил)окси)бутокси)-1H-пиразол-3-карбоксилата (274 мг, 0,752 ммоль) в толуоле (15 мл) добавляли три-N-бутилфосфин (376 мкл, 1,51 ммоль) и 1,1'-(азодикарбонил)дипиперидин (379 мг, 1,50 ммоль) и смесь перемешивали в течение 1,5 часа при 80°C. Обеспечивали охлаждение реакционного раствора до комнатной температуры, и добавляли воду и этилацетат, и смесь разделяли. Органический слой промывали насыщенным солевым раствором и высушивали над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-6-((4-метоксибензил)окси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата (количество 198 мг, выход 76%).
[0785]
Стадия 8
Получали этил-6-гидрокси-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилат с помощью способа, подобного стадии 1 в примере 100, с применением 6-((4-метоксибензил)окси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата вместо этил-5-((бензилокси)метил-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилата.
[0786]
Стадия 9 - стадия 11
С помощью способа, подобного таковому для примера 247, получали N-((R)-6-цианохроман-3-ил)-6-(трифторметокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамид с применением этил-6-гидрокси-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата вместо этил-2-(3-гидроксипропил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилата на стадии 1.
[0787]
Соединения из примера 253 получали путем разделения соединения из примера 252.
[0788]
Пример 254
Получение N-((R)-6-цианохроман-3-ил)-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида
[0789]
[Хим. 208]

[0790]
Стадия 1
С помощью способа, подобного таковому для примера 114, получали (4-(бензилокси)-3-(2,2,2-трифторэтокси)бутокси)(трет-бутил)дифенилсилан с применением 1-(бензилокси)-4-((трет-бутилдифенилсилил)окси)бутан-2-ола, синтезированного с помощью способа, описанного на стадии 1 в примере 252, вместо N-((R)-6-цианохроман-3-ил)-5-(гидроксиметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксамида.
[0791]
Стадия 2
С помощью способа, подобного стадии 2 в примере 252, получали 4-(трет-бутилдифенилсилил)окси)-2-(2,2,2-трифторэтокси)бутан-1-ол с применением (4-(бензилокси)-3-(2,2,2-трифторэтокси)бутокси)(трет-бутил)дифенилсилана вместо 1-(бензилокси)-4-((трет-бутилдифенилсилил)окси)бутан-2-ола.
[0792]
Стадия 3 - стадия 5
С помощью способа, подобного стадии 5 - стадии 7 в примере 252, получали этил-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилат с применением 4-(трет-бутилдифенилсилил)окси)-2-(2,2,2-трифторэтокси)бутан-1-ола вместо 4-(трет-бутил(дифенил)силил)окси-2-((4-метоксифенил)метокси)бутан-1-ола на стадии 5.
[0793]
Стадия 6 - стадия 7
С помощью способа, подобного стадии 10 - стадии 11 в примере 252, получали N-((R)-6-цианохроман-3-ил)-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамид с применением этил-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата вместо этил-6-(трифторметокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата на стадии 10.
[0794]
Соединения из примера 255 получали путем разделения соединения из примера 254.
[0795]
Пример 256
Получение N-((R)-6-хлорхроман-3-ил)-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида (изомер A и изомер B)
[0796]
[Хим. 209]
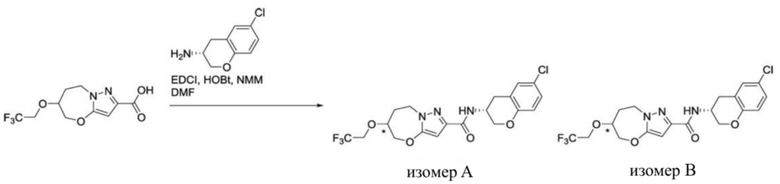
[0797]
В суспензию 6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоновой кислоты (смесь с 4 эквивалентами хлорида натрия) (26,0 мг, 0,0591 ммоль), синтезированной с помощью способа, описанного на стадии 6 в примере 254, (R)-6-хлорхроман-3-амина (14,1 мг, 0,0768 ммоль), 1-гидроксибензотриазола (14,2 мг, 0,0927 ммоль) и гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (17,8 мг, 0,0929 ммоль) в N, N-диметилформамиде (0,5 мл) добавляли 4-метилморфолин (41 мкл, 0,373 ммоль). Смесь перемешивали в течение 2 часов при комнатной температуре. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле и диастереомеры разделяли с получением N-((R)-6-хлорхроман-3-ил)-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида (изомер A) (количество 2,7 мг, выход 10%) и N-((R)-6-хлорхроман-3-ил)-6-(2,2,2-трифторэтокси)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида (изомер B) (количество 2,9 мг, выход 11%).
[0798]
Соединение из примера 257 синтезировали из соединения, синтезированного на стадии 6 в примере 254, в соответствии со схемой, изображенной на фигуре ниже.
[0799]
[Хим. 210]

[0800]
Пример 258
Получение (R)-3-(1H-пиразол-5-ил)-N-(6-(трифторметил)хроман-3-ил)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида
[0801]
[Хим. 211]

[0802]
Стадия 1
В раствор этил-5-гидрокси-1H-пиразол-3-карбоксилата (1,00 г, 6,40 ммоль) в ацетонитриле (13 мл) добавляли карбонат калия (2,66 г, 19,2 ммоль) и 1,4-дибромбутан (804 мкл, 6,73 ммоль). После герметизации смесь перемешивали в течение 15 часов при 100°C. Обеспечивали охлаждение реакционного раствора до комнатной температуры и после фильтрации фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата (количество 574 мг, выход 43%).
[0803]
Стадия 2
Получали этил-3-йод-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилат с помощью способа, подобного таковому для примера 14, с применением этил-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата вместо N-((R)-хроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида.
[0804]
Стадия 3 - стадия 4
Получали (R)-3-йод-N-(6-(трифторметил)хроман-3-ил)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамид с помощью способа, подобного стадии 3 - стадии 4 в примере 18, с применением этил-3-йод-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата вместо этил-3-(пиридин-2-ил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксилата на стадии 3 и с применением гидрохлорида (R)-6-(трифторметил)хроман-3-амина, синтезированного с помощью способа, описанного в контрольном примере 43, вместо гидрохлорида (R)-6-хлорхроман-3-амина на стадии 4.
[0805]
Стадия 5
В раствор (R)-3-йод-N-(6-(трифторметил)хроман-3-ил)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида (20 мг, 0,039 ммоль) в н-бутаноле (800 мкл) добавляли 1H-пиразол-5-илбороновую кислоту (8,8 мг, 0,079 ммоль), триэтиламин (22 мкл, 0,16 ммоль) и бис(ди-трет-бутил-(4-диметиламинофенил)фосфин)дихлорпалладий(II) (2,8 мг, 0,0040 ммоль). Смесь перемешивали в течение 1 часа при 120°C при микроволновом излучении. Реакционный раствор концентрировали при пониженном давлении и остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-3-(1H-пиразол-5-ил)-N-(6-(трифторметил)хроман-3-ил)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксамида (количество 13,6 мг, выход 77%).
[0806]
Пример 259
Получение (R)-3-(1H-пиразол-5-ил)-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамида
[0807]
[Хим. 212]

[0808]
Стадия 1 - стадия 4
Получали (R)-3-(1H-пиразол-5-ил)-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамид с помощью способа, подобного стадии 2 - стадии 5 в примере 258, с применением этил-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксилата вместо этил-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоксилата на стадии 2.
[0809]
Пример 260
Получение (R)-3-(пиридин-2-ил)-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамида
[0810]
[Хим. 213]
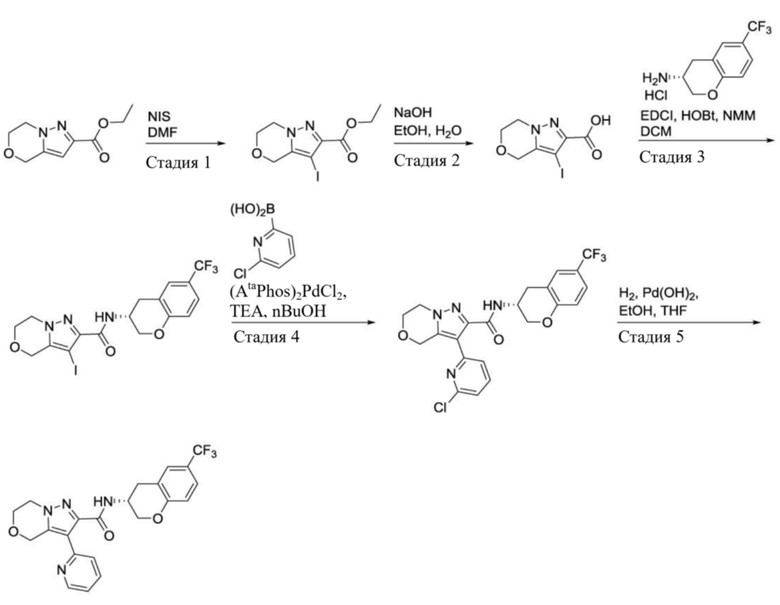
[0811]
Стадия 1
В раствор этил-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксилата (400 мг, 2,04 ммоль) в ацетонитриле (6,8 мл) добавляли N-йодсукцинимид (1,38 г, 6,13 ммоль) и смесь перемешивали в течение 14 часов при 70°C. В реакционный раствор добавляли водный раствор тиосульфата натрия и этилацетат и смесь разделяли. Органический слой высушивали над безводным сульфатом натрия и растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением этил-3-йод-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксилата (количество 650 мг, выход 99%).
[0812]
Стадия 2
В раствор этил-3-йод-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксилата (200 мг, 0,621 ммоль) в этаноле (6,2 мл) добавляли 4 моль/л водный раствор гидроксида натрия (0,62 мл, 2,5 ммоль) и смесь перемешивали в течение 2 часов при комнатной температуре. В реакционный раствор добавляли 2 моль/л раствор хлористоводородной кислоты и затем растворитель выпаривали при пониженном давлении. К остатку добавляли толуол и растворитель выпаривали при пониженном давлении с получением 3-йод-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоновой кислоты (количество 325 мг, выход 99%) в виде смеси с 4 эквивалентами хлорида натрия.
[0813]
Стадия 3
В суспензию 3-йод-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоновой кислоты (смесь с 4 эквивалентами хлорида натрия) (325 мг, 0,616 ммоль), гидрохлорида (R)-6-(трифторметил)хроман-3-амина (156 мг, 0,616 ммоль), синтезированного с помощью способа, описанного в контрольном примере 43, 1-гидроксибензотриазола (10,0 мг, 0,0739 ммоль) и гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (142 мг, 0,0739 ммоль) в дихлорметане (10 мл) добавляли 4-метилморфолин (203 мкл, 1,85 ммоль) и смесь перемешивали в течение 12 часов при комнатной температуре. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. После высушивания органического слоя с помощью безводного сульфата натрия растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-3-йод-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамида (количество 267 мг, выход 88%).
[0814]
Стадия 4
В смешанный раствор (R)-3-йод-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамида (60,0 мг, 0,122 ммоль) и (6-хлорпиридин-2-ил)бороновой кислоты (28,7 мг, 0,182 ммоль) в 1,4-диоксане (1 мл) и воде (1 мл) добавляли карбонат цезия (119 мг, 0,365 ммоль), бис(ди-трет-бутил-(4-диметиламинофенил)фосфин)дихлорпалладий(II) (8,6 мг, 0,012 ммоль). Смесь перемешивали в течение 1 часа при 140°C при микроволновом излучении. В реакционный раствор добавляли воду и этилацетат и смесь разделяли. Органический слой высушивали над безводным сульфатом магния и растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-3-(6-хлорпиридин-2-ил)-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамида (количество 9,4 мг, выход 33%).
[0815]
Стадия 5
В раствор (R)-3-(6-хлорпиридин-2-ил)-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамида (290 мг, 0,606 ммоль) в тетрагидрофуране (6 мл) добавляли этанол (6 мл) и 20% гидроксид палладия на угле (128 мг). Смесь перемешивали в условиях повышенного давления (давление с применением баллона) в атмосфере водорода в течение 2 часов при 50°C. После того, как реакционный раствор фильтровали через целит, растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-3-(пиридин-2-ил)-N-(6-(трифторметил)хроман-3-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоксамида (количество 204 мг, выход 76%).
[0816]
Соединение из примера 261 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0817]
[Хим. 214]
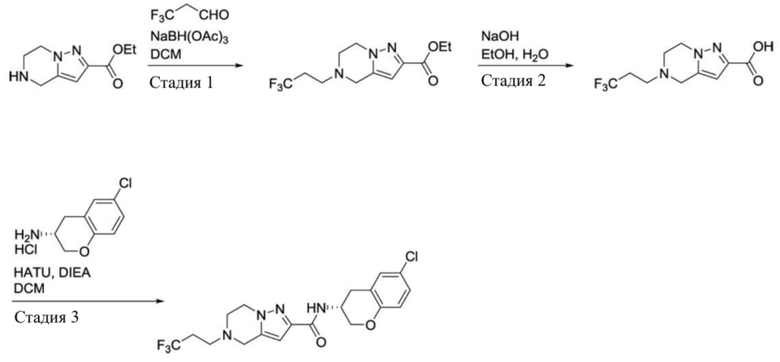
[0818]
Соединение из примера 262 синтезировали с помощью способа, подобного таковому для примера 261.
[0819]
Соединение из контрольного примера 69 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0820]
[Хим. 215]

[0821]
Соединение из примера 263 синтезировали с применением соединения из контрольного примера 69 и соединения из контрольного примера 1 с помощью способов, подобных стадии 2 и стадии 3 в примере 261.
[0822]
Соединение из примера 264 синтезировали с применением соединения из контрольного примера 69 и соединения из контрольного примера 47 с помощью способов, подобных стадии 2 и стадии 3 в примере 261.
[0823]
Соединение из контрольного примера 70 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 69.
[0824]
[Хим. 216]

[0825]
Соединение из примера 265 синтезировали с применением соединения из контрольного примера 70 и соединения из контрольного примера 43 с помощью способов, подобных стадии 2 и стадии 3 в примере 261.
[0826]
Соединение из примера 266 синтезировали с применением соединения из контрольного примера 70 и соединения из контрольного примера 44 с помощью способов, подобных стадии 2 и стадии 3 в примере 261.
[0827]
Соединение из примера 267 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0828]
[Хим. 217]

[0829]
Пример 268
Получение (R)-N-(6-цианохроман-3-ил)-5-(4-фторбензил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоксамида
[0830]
[Хим. 218]

[0831]
Стадия 1
В раствор 5-(трет-бутоксикарбонил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоновой кислоты (120 мг, 0,449 ммоль) в дихлорметане (3 мл) добавляли HATU (188 мг, 0,494 ммоль), N, N-диизопропилэтиламин (386 мкл, 2,24 ммоль) и (R)-3-аминохроман-6-карбонитрил (104 мг, 0,494 ммоль), синтезированный с помощью способа, описанного в контрольном примере 24. Смесь перемешивали в течение 12 часов при комнатной температуре. Реакционный раствор очищали с помощью колоночной хроматографии на силикагеле с получением (R)-трет-бутил-2-((6-цианохроман-3-ил)карбамоил)-6,7-дигидропиразоло[1,5-a]пиразин-5-(4H)-карбоксилата (количество 210 мг).
[0832]
Стадия 2
В раствор (R)-трет-бутил-2-((6-цианохроман-3-ил)карбамоил)-6,7-дигидропиразоло[1,5-a]пиразин-5-(4H)-карбоксилата (210 мг, 0,496 ммоль) в этилацетате (8 мл) добавляли 4 моль/л раствор хлороводорода в этилацетате (8,0 мл, 32 ммоль) и смесь перемешивали в течение 2 часов при комнатной температуре. Растворитель выпаривали при пониженном давлении с получением гидрохлорида (R)-N-(6-цианохроман-3-ил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоксамида (количество 178 мг, выход 100%).
[0833]
Стадия 3
В раствор (R)-N-(6-цианохроман-3-ил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоксамида (15,0 мг, 0,0417 ммоль) в N, N-диметилформамиде (208 мкл) добавляли N, N-диизопропилэтиламин (36 мкл, 0,21 ммоль) и 1-(бромметил)-4-фторбензол (15,8 мг, 0,0834 ммоль). Смесь перемешивали в течение 12 часов при 100°C. В реакционный раствор добавляли воду и хлороформ и смесь разделяли. После того, как органический слой высушивали над сульфатом натрия, растворитель выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением (R)-N-(6-цианохроман-3-ил)-5-(4-фторбензил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоксамида (количество 16,0 мг, выход 89%).
[0834]
Соединение из примера 269 синтезировали с помощью способа, подобного таковому для примера 268.
[0835]
Соединение из примера 270 синтезировали с помощью способа, подобного таковому для примера 268.
[0836]
Соединение из примера 271 синтезировали с помощью способа, подобного таковому для примера 268.
[0837]
Соединение из примера 272 синтезировали с помощью способов, подобных таковым, описанным в примере 268 и в контрольном примере 3.
[0838]
Соединение из контрольного примера 71 (показано на фигуре ниже) синтезировали с помощью способов, подобных таковым, описанным на стадии 1 - стадии 2 в примере 268 и в контрольном примере 1.
[0839]
[Хим. 219]

[0840]
Соединение из примера 273 синтезировали из соединения из контрольного примера 71 с помощью способа, подобного стадии 3 в примере 268.
[0841]
Соединение из примера 274 синтезировали из соединения из контрольного примера 71 в соответствии со схемой, изображенной на фигуре ниже.
[0842]
[Хим. 220]

[0843]
Соединение из примера 275 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0844]
[Хим. 221]

[0845]
Соединение из контрольного примера 72 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 1 - стадии 2 в примере 268.
[0846]
[Хим. 222]
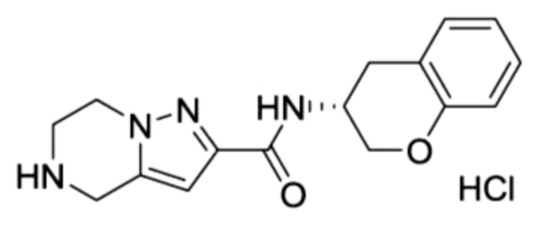
[0847]
Соединение из примера 276 синтезировали из соединения из контрольного примера 72 в соответствии со схемой, изображенной на фигуре ниже.
[0848]
[Хим. 223]

[0849]
Соединение из примера 277 синтезировали из соединения из контрольного примера 72 в соответствии со схемой, изображенной на фигуре ниже.
[0850]
[Хим. 224]

[0851]
Соединение из примера 278 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0852]
[Хим. 225]
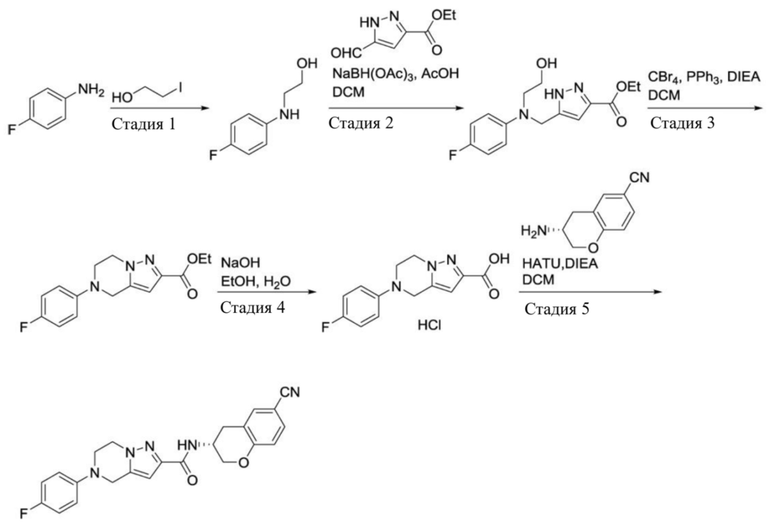
[0853]
Соединение из контрольного примера 73 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 27.
[0854]
[Хим. 226]

[0855]
Соединение из примера 279 синтезировали с помощью способов, подобных таковым, описанным в примере 278 и в контрольном примере 73.
[0856]
Соединение из примера 280 синтезировали из соединения из контрольного примера 71 в соответствии со схемой, изображенной на фигуре ниже.
[0857]
[Хим. 227]
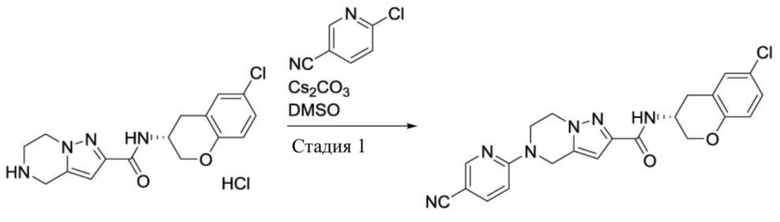
[0858]
Соединение из примера 281 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0859]
[Хим. 228]

[0860]
Соединение из примера 282 синтезировали с помощью способов, подобных таковым, описанным в примере 281 и в контрольном примере 24.
[0861]
Соединение из примера 283 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0862]
[Хим. 229]
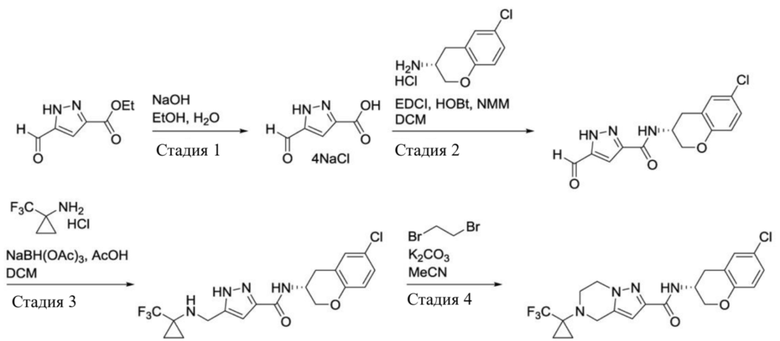
[0863]
Соединение из примера 284 синтезировали с помощью способа, подобного таковому для примера 283.
[0864]
Соединение из примера 285 синтезировали с помощью способа, подобного таковому для примера 283.
[0865]
Соединение из контрольного примера 74 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0866]
[Хим. 230]

[0867]
Соединение из примера 286 синтезировали с помощью способа, подобного таковому для примера 283, с применением соединения из контрольного примера 74 и соединения из контрольного примера 24.
[0868]
Соединение из примера 287 синтезировали с помощью способа, подобного стадии 6 - стадии 8 в примере 70.
[0869]
Пример 288
Получение гидрохлорида N-((R)-6-хлорхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида (изомер A)
[0870]
[Хим. 231]

[0871]
В раствор N-((R)-6-хлорхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида (изомер A) (170 мг, 0,425 ммоль), синтезированного с помощью способа, описанного в примере 2, в этилацетате (1 мл) добавляли 4 моль/л раствор хлороводорода в этилацетате (1 мл, 4 ммоль) и смесь перемешивали в течение 10 минут. Растворитель выпаривали при пониженном давлении с получением гидрохлорида N-((R)-6-хлорхроман-3-ил)-6-(трифторметил)-5,6,7,8-тетрагидроимидазо[1,2-a]пиридин-2-карбоксамида (изомер A) (количество 185 мг, выход 100%).
[0872]
Соединение из примера 289 синтезировали из соединения из примера 81 в соответствии со схемой, изображенной на фигуре ниже.
[0873]
[Хим. 232]

[0874]
Пример 290
Получение гидрохлорида (R)-N-(6-цианохроман-3-ил)-5-(4-фторбензил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоксамида
[0875]
[Хим. 233]

[0876]
В раствор (R)-N-(6-цианохроман-3-ил)-5-(4-фторбензил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоксамида (122 мг, 0,283 ммоль), синтезированного с помощью способа, описанного в примере 268, в этилацетате (2 мл) добавляли 4 моль/л раствор хлороводорода в этилацетате (141 мкл, 0,563 ммоль) и смесь перемешивали. Добавляли н-гексан (2 мл) осажденное твердое вещество фильтровали и затем твердое вещество высушивали при пониженном давлении с получением гидрохлорида (R)-N-(6-цианохроман-3-ил)-5-(4-фторбензил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-карбоксамида (количество 96,4 мг, выход 73%).
[0877]
В таблицах ниже показаны данные химических структур и инструментального анализа для соединений, синтезированных в примере 1 - примере 287. При этом в таблицах ниже звездочки (*), присутствующие в структурных формулах в примерах, указывают, что соответствующий асимметричный углерод имеет единственную стерическую структуру. Если конкретно не указано иное, "пример" в таблицах в каждом случае означает соединение, получение которого предусматривается в таком примере; например, данные, приведенные для примера 1, демонстрируют данные для соединения, получение которого предусматривается в примере 1.
[0878]
[Таблица 1]

(изомер A)
400 [M+H]+
(изомер B)
400 [M+H]+
414 [M+H]+
414 [M+H]+
444, 446
[M+H]+
(изомер A)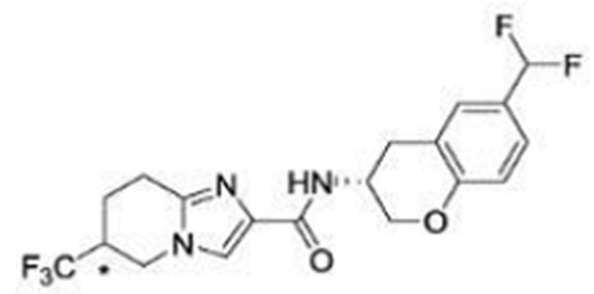
416 [M+H]+
(изомер B)
416 [M+H]+
[0879]
[Таблица 2]
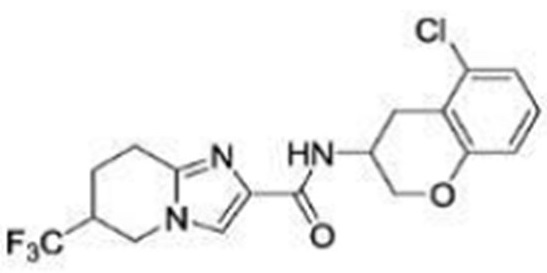
400 [M+H]+
(изомер A)
444, 446
[M+H]+
(изомер B)
444, 446
[M+H]+
406 [M+H]+
394 [M+H]+
444, 446
[M+H]+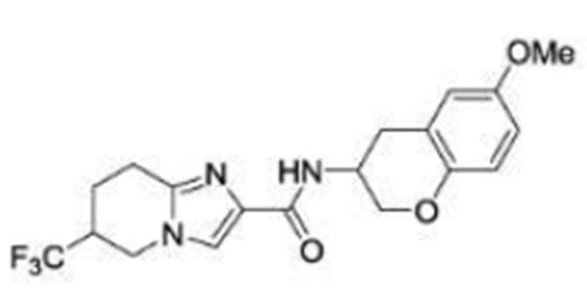
396 [M+H]+
492 [M+H]+
473 [M+H]+
[0880]
[Таблица 3]

374 [M+H]+
439 [M+H]+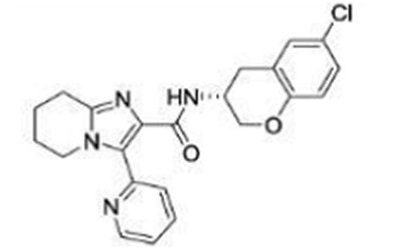
409 [M+H]+
432 [M+H]+
476 [M+H]+
397 [M+H]+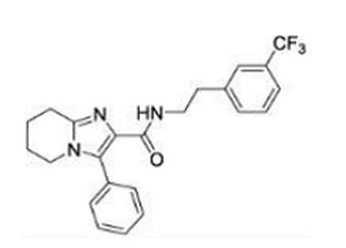
m), 3,58 (2H, q, J=7,1 Гц), 3,71 (2H, t, J=5,4 Гц), 7,38-7,46 (9H, m)..
414 [M+H]+
326 [M+H]+
366 [M+H]+
[0881]
[Таблица 4]

408 [M+H]+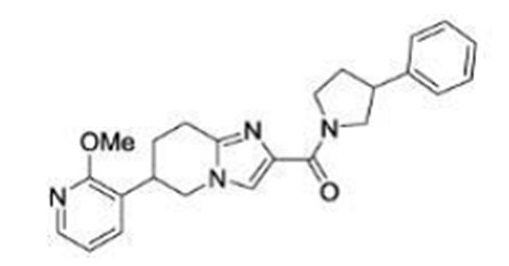
403 [M+H]+
405 [M+H]+
411 [M+H]+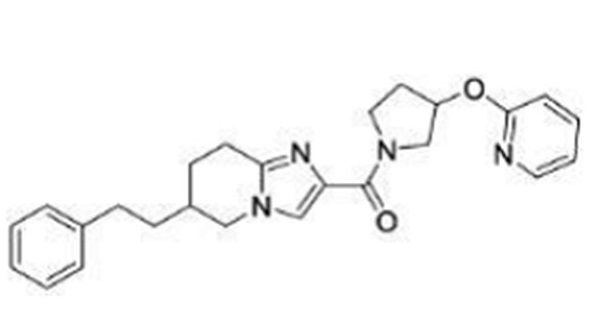
417 [M+H]+
441 [M+H]+
378 [M+H]+
523 [M+H]+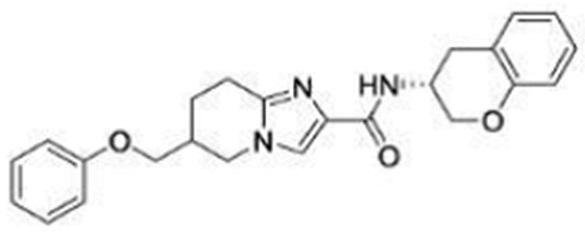
404 [M+H]+
[0882]
[Таблица 5]

384 [M+H]+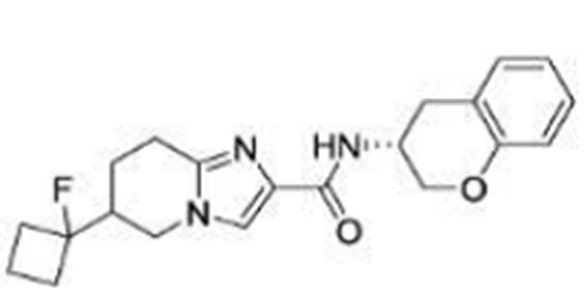
370 [M+H]+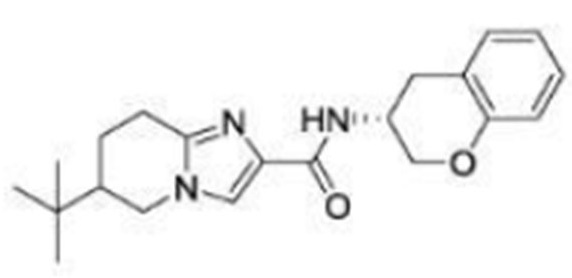
354 [M+H]+
396 [M+H]+
430 [M+H]+
(изомер A)
430 [M+H]+
(изомер B)
430 [M+H]+
446 [M+H]+
370 [M+H]+
[0883]
[Таблица 6]
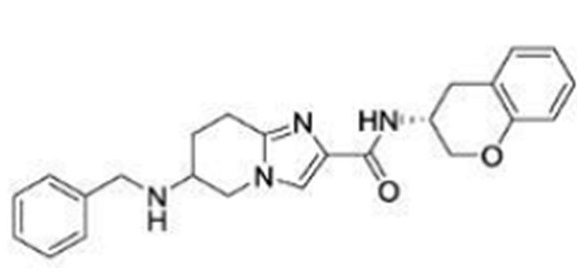
403 [M+H]+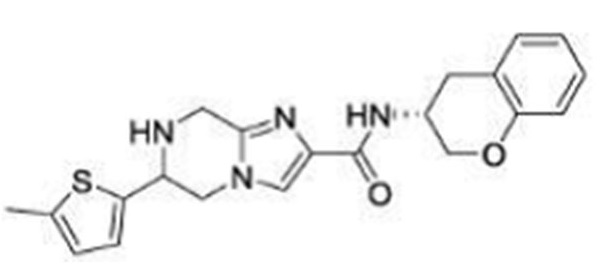
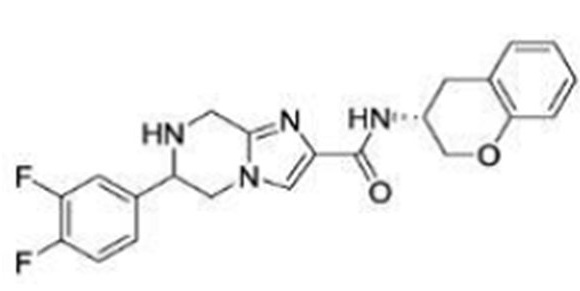
411 [M+H]+
425 [M+H]+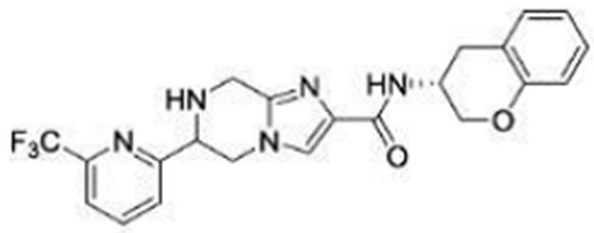
444 [M+H]+
476 [M+H]+
415 [M+H]+
369 [M+H]+
383 [M+H]+
[0884]
[Таблица 7]

395 [M+H]+
409 [M+H]+
421 [M+H]+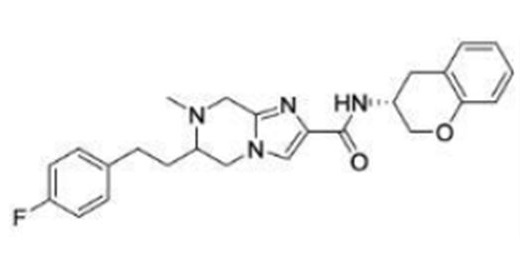
435 [M+H]+
417 [M+H]+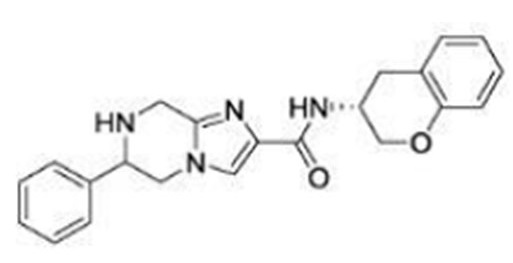
375 [M+H]+
389 [M+H]+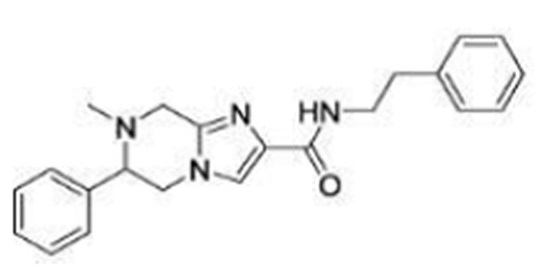
361 [M+H]+
367 [M+H]+
[0885]
[Таблица 8]

441 [M+H]+
457 [M+H]+
446 [M+H]+
458 [M+H]+
376 [M+H]+
441 [M+H]+
411 [M+H]+
445 [M+H]+
388 [M+H]+
[0886]
[Таблица 9]

405 [M+H]+
419 [M+H]+
472- 474
[M+H]+
426 [M+H]+
432 [M+H]+
(изомер A)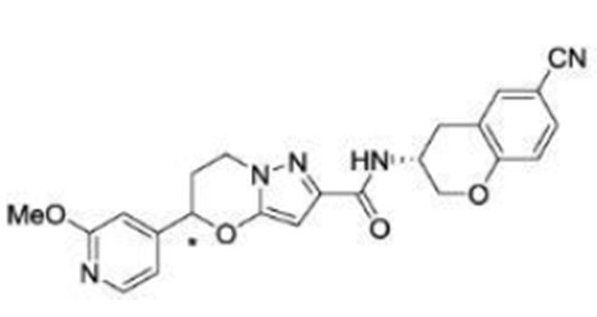
432 [M+H]+
(изомер B)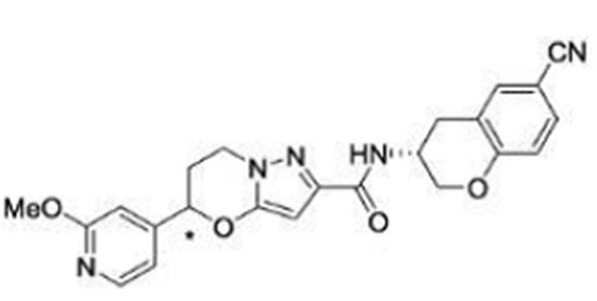
432 [M+H]+
432 [M+H]+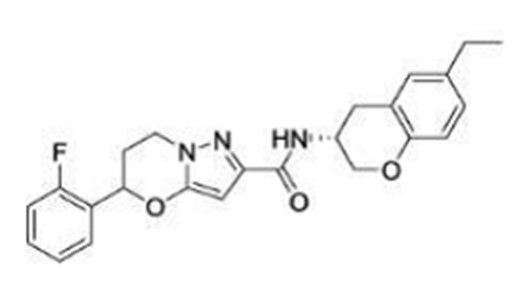
422 [M+H]+
[0887]
[Таблица 10]

410 [M+H]+
460 [M+H]+
392 [M+H]+
471 [M+H]+
471 [M+H]+
424 [M+H]+
452 [M+H]+
508 [M+H]+
348 [M+H]+
[0888]
[Таблица 11]

348 [M+H]+
348 [M+H]+
392, 394
[M+H]+
392, 394
[M+H]+
362 [M+H]+
353 [M+H]+
(изомер A)
353 [M+H]+
(изомер B)
353 [M+H]+
436 [M+H]+
[0889]
[Таблица 12]
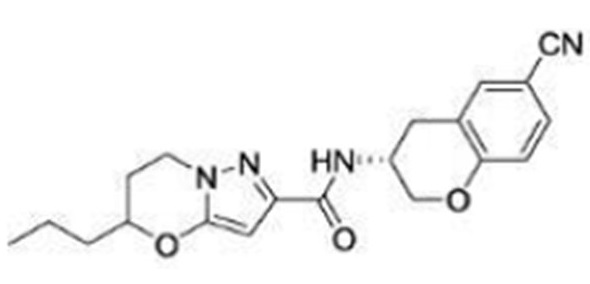
367 [M+H]+
(изомер A)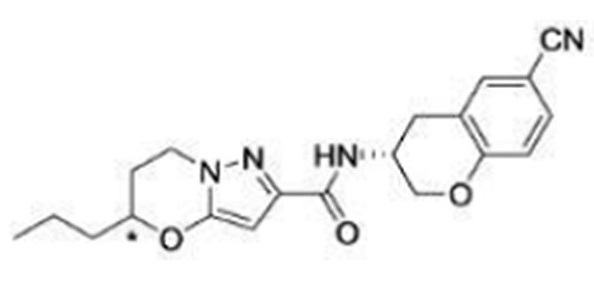
367 [M+H]+
(изомер B)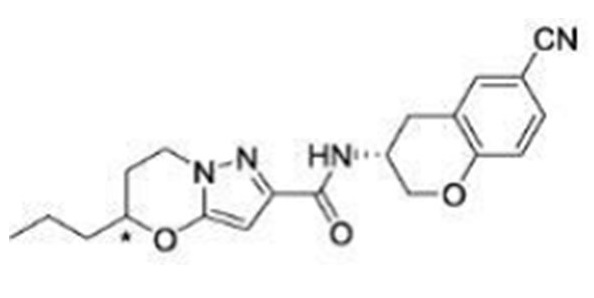
367 [M+H]+
379 [M+H]+
(изомер A)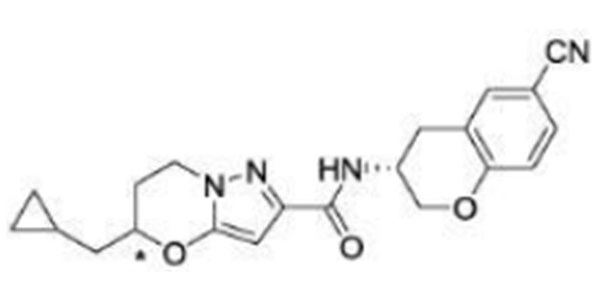
379 [M+H]+
(изомер B)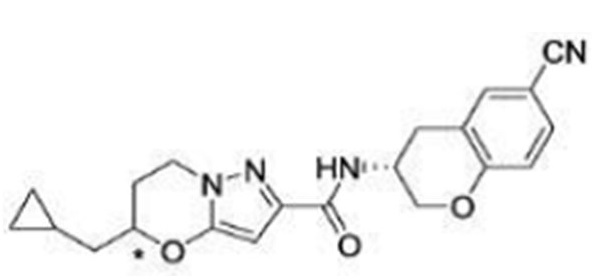
379 [M+H]+
454 [M+H]+
445 [M+H]+
397 [M+H]+
[0890]
[Таблица 13]
(изомер A)
397 [M+H]+
(изомер B)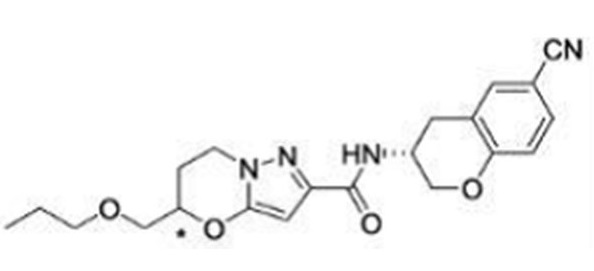
397 [M+H]+
409 [M+H]+
(изомер A)
409 [M+H]+
(изомер B)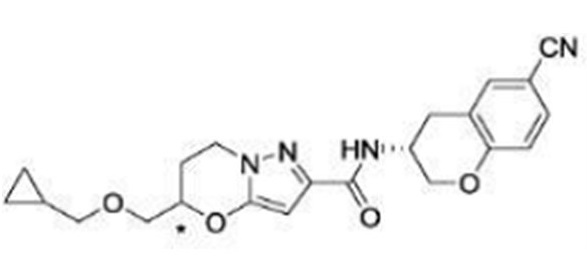
409 [M+H]+
463 [M+H]+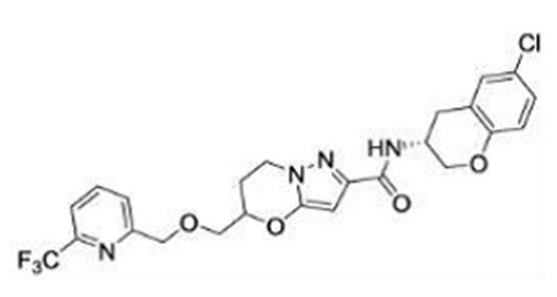
523 [M+H]+
418 [M+H]+
486 [M+H]+
[0891]
[Таблица 14]

448 [M+H]+
(изомер A)
448 [M+H]+
(изомер B)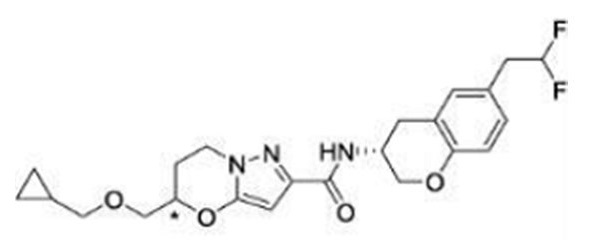
448 [M+H]+
461 [M+H]+
(изомер A)
461 [M+H]+
(изомер B)
461 [M+H]+
423 [M+H]+
(изомер A)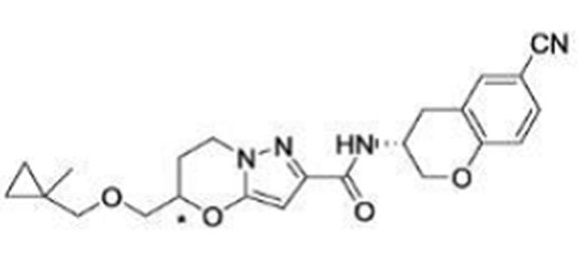
423 [M+H]+
(изомер B)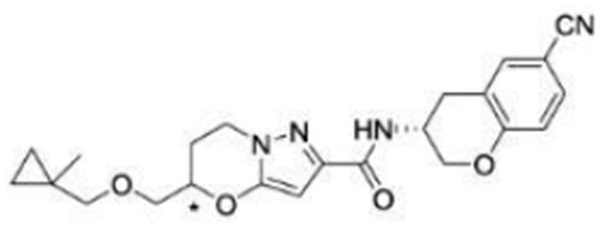
423 [M+H]+
[0892]
[Таблица 15]

437 [M+H]+
(изомер A)
437 [M+H]+
(изомер B)
437 [M+H]+
505 [M+H]+
441 [M+H]+
431 [M+H]+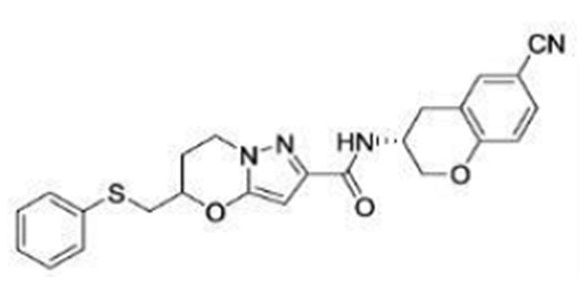
447 [M+H]+
441 [M+H]+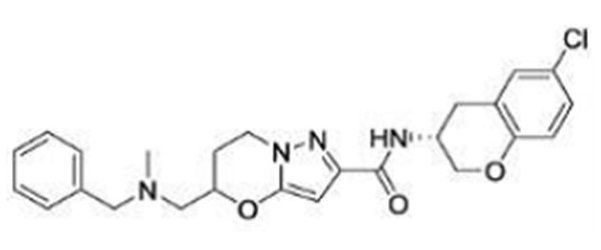
467 [M+H]+
[0893]
[Таблица 16]
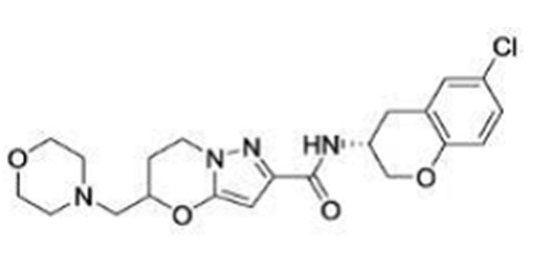
433 [M+H]+
435 [M+H]+
(изомер A)
435 [M+H]+
(изомер B)
435 [M+H]+
460 [M+H]+
476 [M+H]+
(изомер A)
476 [M+H]+
(изомер B)
476 [M+H]+
524 [M+H]+
[0894]
[Таблица 17]
(изомер A)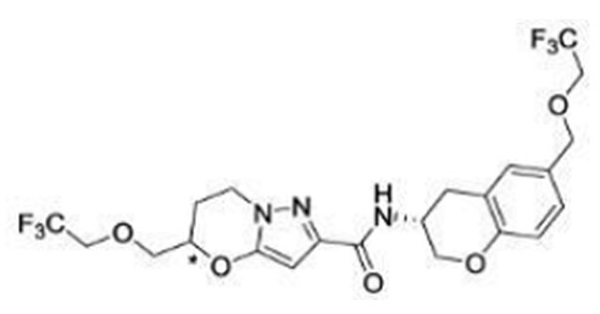
524 [M+H]+
(изомер B)
524 [M+H]+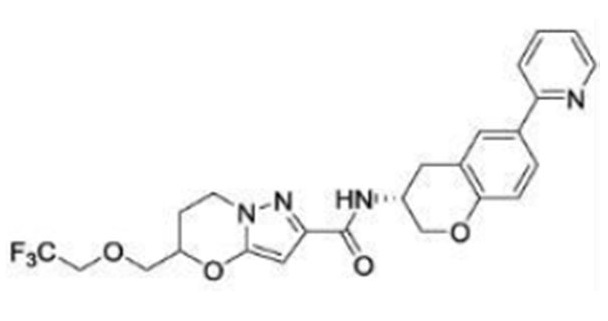
489 [M+H]+
(изомер A)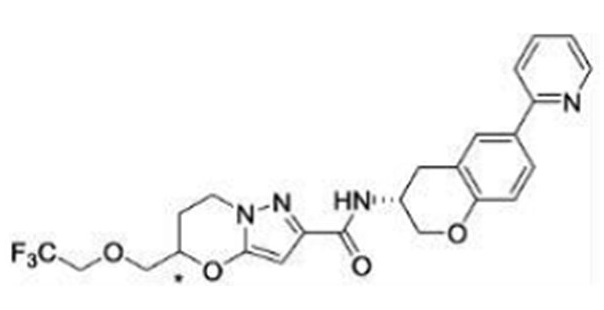
489 [M+H]+
(изомер B)
489 [M+H]+
514 [M+H]+
423 [M+H]+
(изомер A)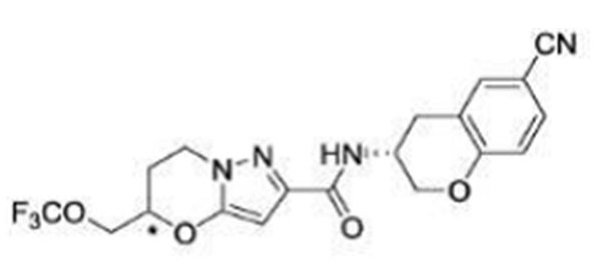
423 [M+H]+
(изомер B)
423 [M+H]+
[0895]
[Таблица 18]
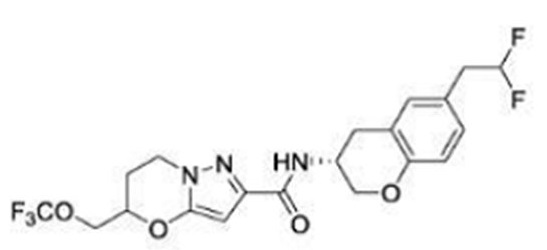
462 [M+H]+
(изомер A)
462 [M+H]+
(изомер B)
462 [M+H]+
444 [M+H]+
(изомер A)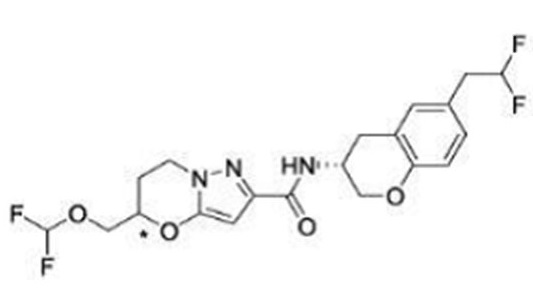
444 [M+H]+
(изомер B)
444 [M+H]+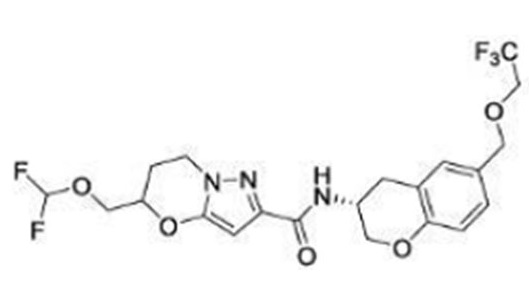
492 [M+H]+
(изомер A)
492 [M+H]+
(изомер B)
492 [M+H]+
[0896]
[Таблица 19]

474 [M+H]+
(изомер A)
474 [M+H]+
(изомер B)
474 [M+H]+
437 [M+H]+
(изомер A)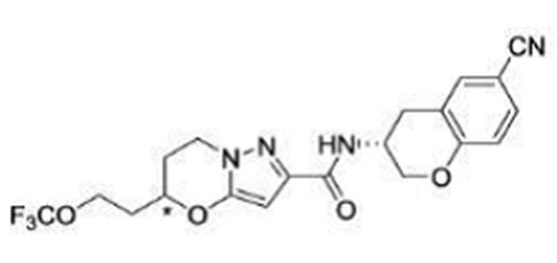
437 [M+H]+
(изомер B)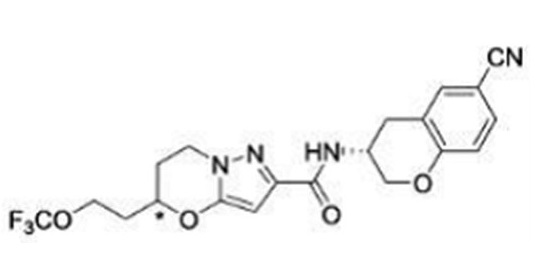
437 [M+H]+
419 [M+H]+
(изомер A)
419 [M+H]+
(изомер B)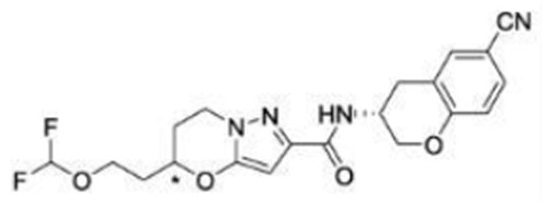
419 [M+H]+
[0897]
[Таблица 20]

458 [M+H]+
(изомер A)
458 [M+H]+
(изомер B)
458 [M+H]+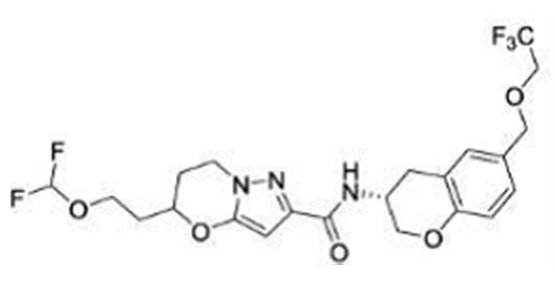
506 [M+H]+
(изомер A)
506 [M+H]+
(изомер B)
506 [M+H]+
445 [M+H]+
(изомер A)
445 [M+H]+
(изомер B)
445 [M+H]+
[0898]
[Таблица 21]
(изомер A)
453 [M+H]+
(изомер B)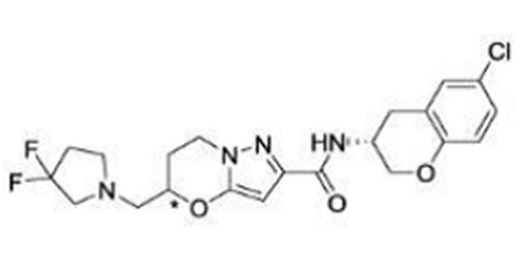
453 [M+H]+
(изомер A)
531 [M+H]+
439 [M+H]+
(изомер A)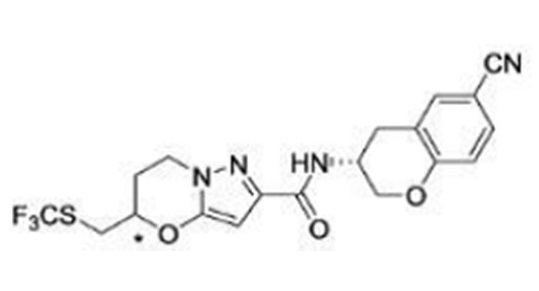
439 [M+H]+
(изомер B)
439 [M+H]+
384 [M+H]+
(изомер A)
384 [M+H]+
(изомер B)
384 [M+H]+
[0899]
[Таблица 22]

428, 430 [M+H]+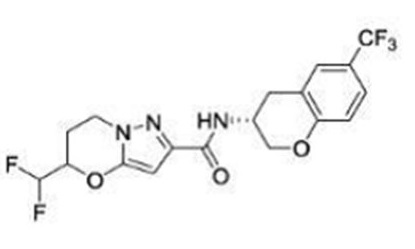
418 [M+H]+
(изомер A)
418 [M+H]+
(изомер B)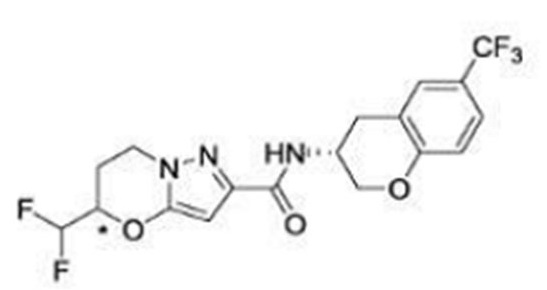
418 [M+H]+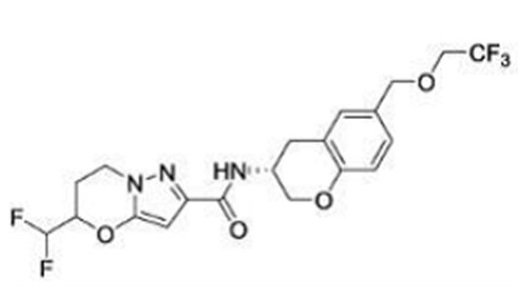
462 [M+H]+
(изомер A)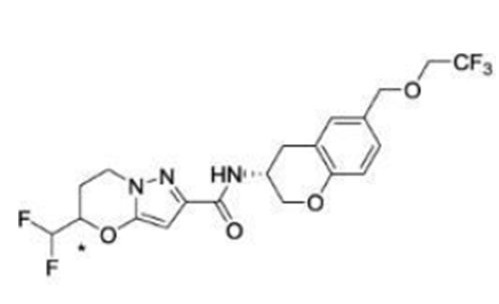
462 [M+H]+
(изомер B)
462 [M+H]+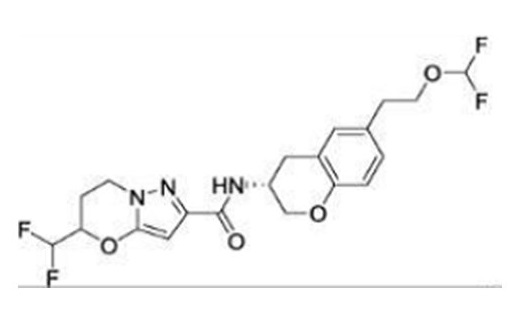
444 [M+H]+
(изомер A)
444 [M+H]+
[0900]
[Таблица 23]
(изомер B)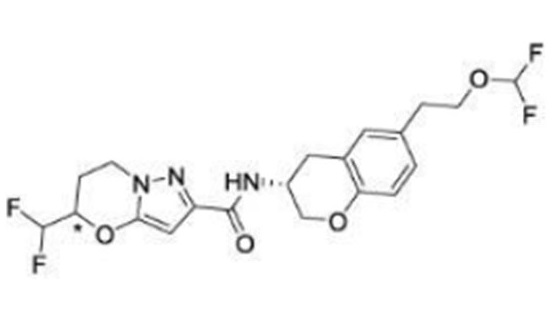
444 [M+H]+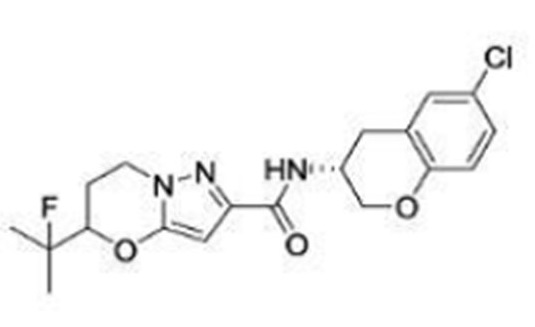
394 [M+H]+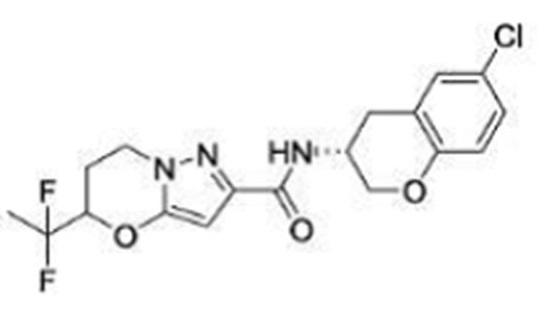
398 [M+H]+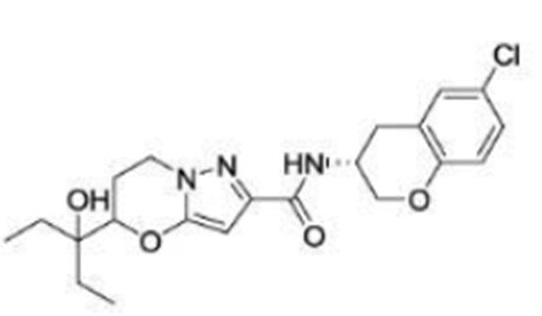
420 [M+H]+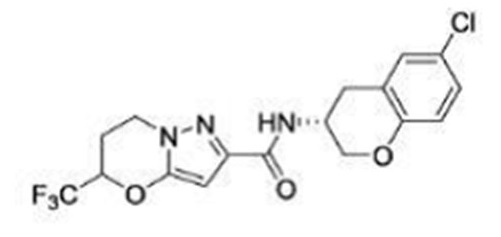
402 [M+H]+
(изомер A)
402 [M+H]+
(изомер B)
402 [M+H]+
446, 448 [M+H]+
432 [M+H]+
[0901]
[Таблица 24]
(изомер A)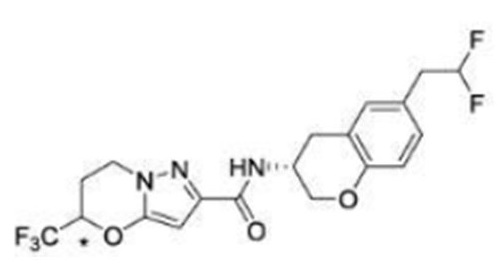
432 [M+H]+
(изомер B)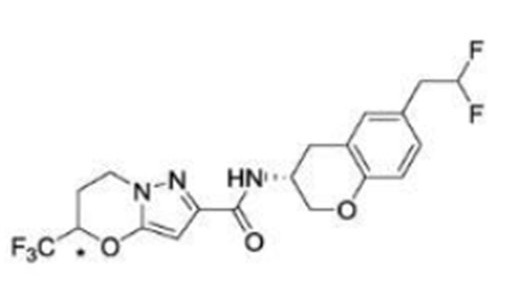
432 [M+H]+
470 [M+H]+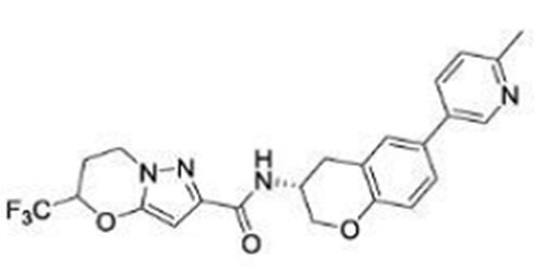
459 [M+H]+
476 [M+H]+
362 [M+H]+
353 [M+H]+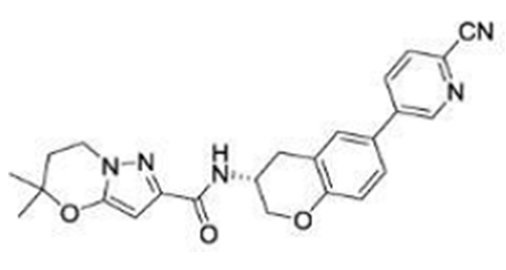
430 [M+H]+
365 [M+H]+
[0902]
[Таблица 25]

362 [M+H]+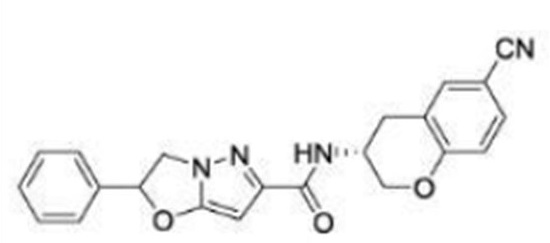
409 [M+H]+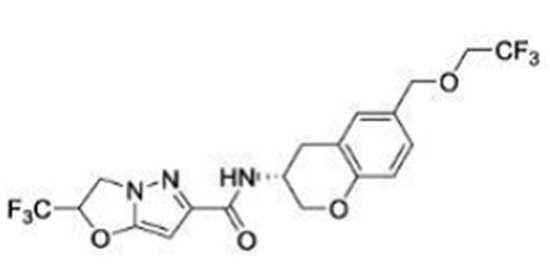
466 [M+H]+
(изомер A)
466 [M+H]+
(изомер B)
466 [M+H]+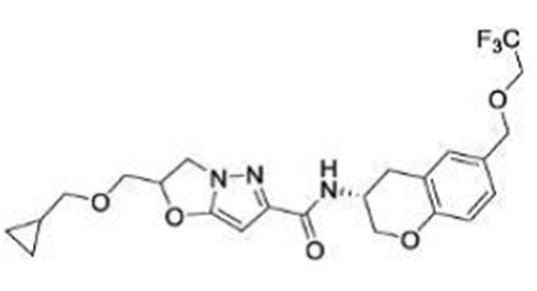
482 [M+H]+
(изомер A)
482 [M+H]+
(изомер B)
482 [M+H]+
510 [M+H]+
[0903]
[Таблица 26]
(изомер A)
510 [M+H]+
(изомер B)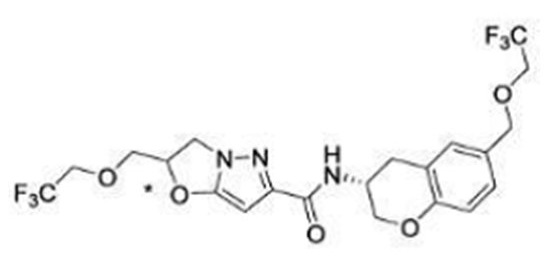
510 [M+H]+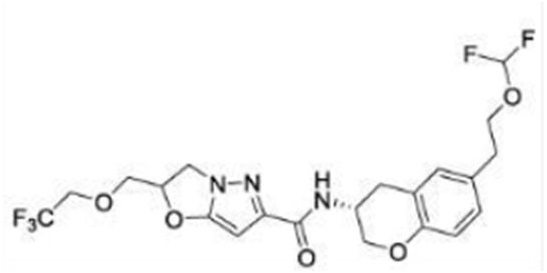
492 [M+H]+
(изомер A)
492 [M+H]+
(изомер B)
492 [M+H]+
480 [M+H]+
(изомер B)
480 [M+H]+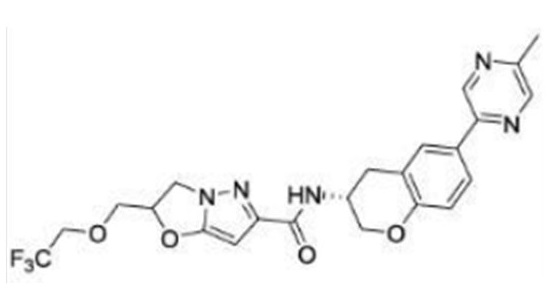
490 [M+H]+
(изомер A)
490 [M+H]+
[0904]
[Таблица 27]
(изомер B)
490 [M+H]+
496 [M+H]+
(изомер A)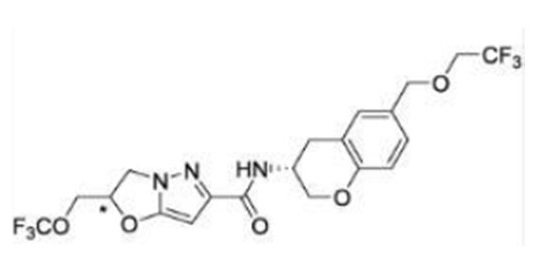
496 [M+H]+
(изомер B)
496 [M+H]+
448 [M+H]+
(изомер A)
448 [M+H]+
(изомер B)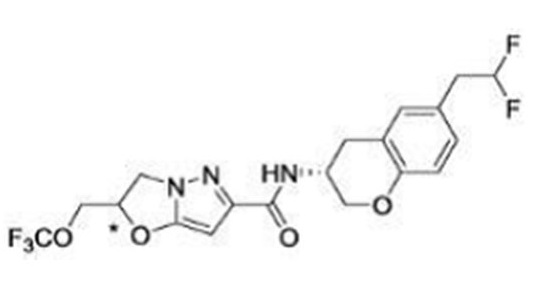
448 [M+H]+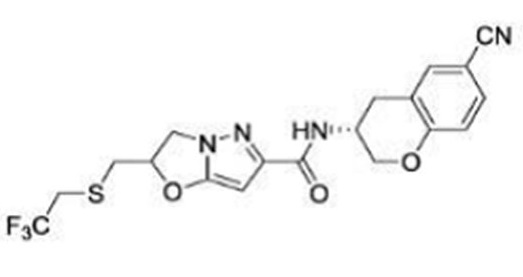
439 [M+H]+
(изомер A)
439 [M+H]+
[0905]
[Таблица 28]
(изомер B)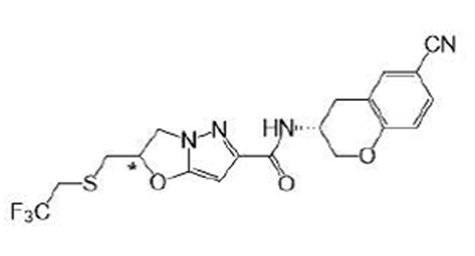
439 [M+H]+
409 [M+H]+
(изомер A)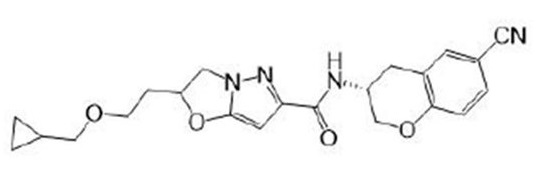
409 [M+H]+
(изомер B)
409 [M+H]+
492 [M+H]+
(изомер A)
492 [M+H]+
(изомер B)
492 [M+H]+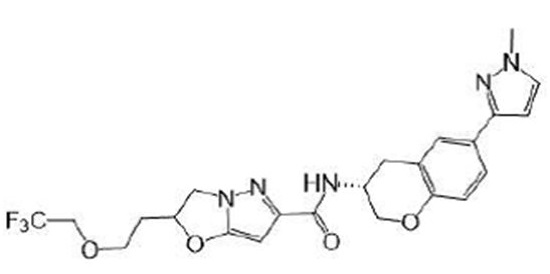
492 [M+H]+
(изомер A)
492 [M+H]+
[0906]
[Таблица 29]
(изомер B)
492 [M+H]+
(изомер A)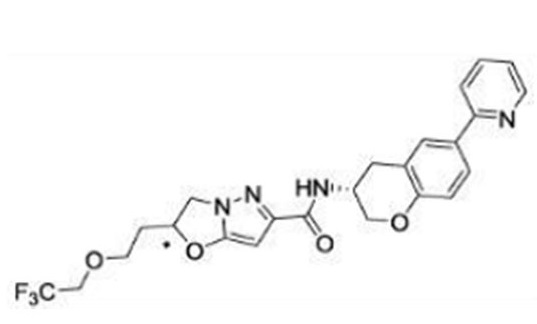
489 [M+H]+
(изомер B)
489 [M+H]+
423 [M+H]+
(изомер A)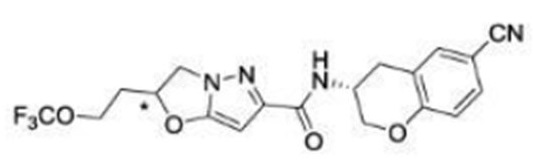
423 [M+H]+
(изомер B)
423 [M+H]+
462 [M+H]+
(изомер A)
462 [M+H]+
(изомер B)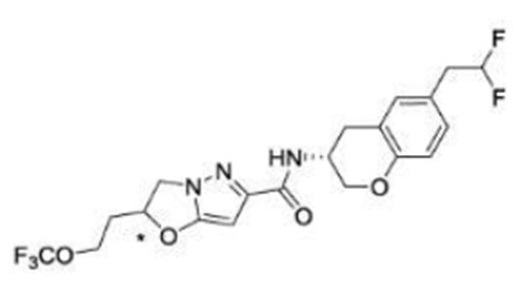
462 [M+H]+
[0907]
[Таблица 30]

478 [M+H]+
(изомер A)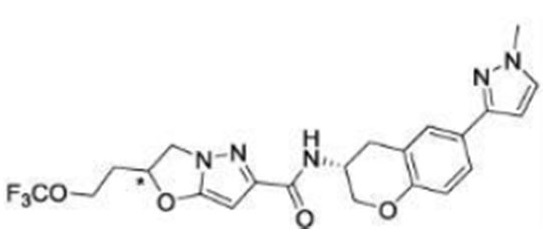
478 [M+H]+
(изомер B)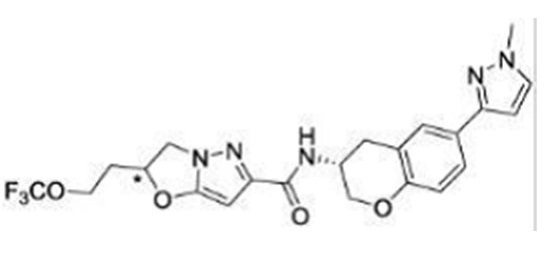
478 [M+H]+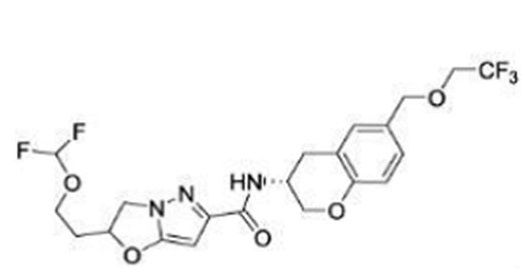
492 [M+H]+
(изомер A)
492 [M+H]+
(изомер B)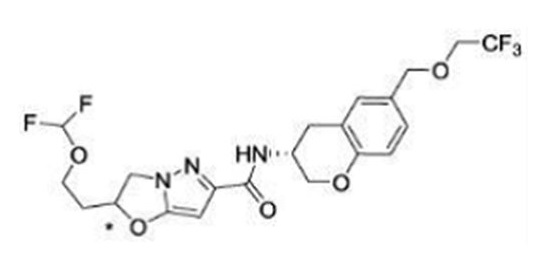
492 [M+H]+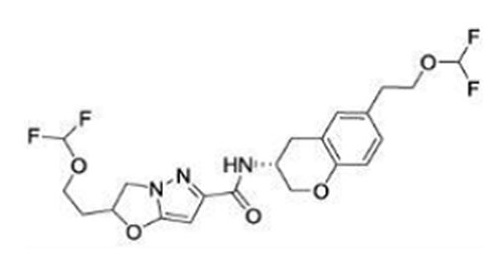
474 [M+H]+
(изомер A)
474 [M+H]+
(изомер B)
474 [M+H]+
[0908]
[Таблица 31]

444 [M+H]+
(изомер A)
444 [M+H]+
(изомер B)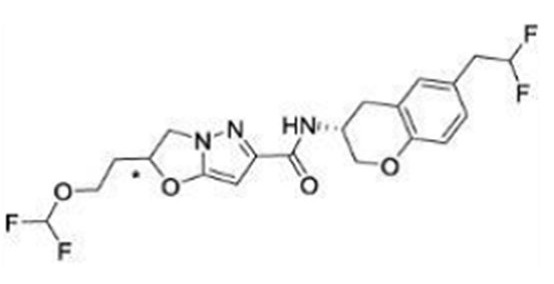
444 [M+H]+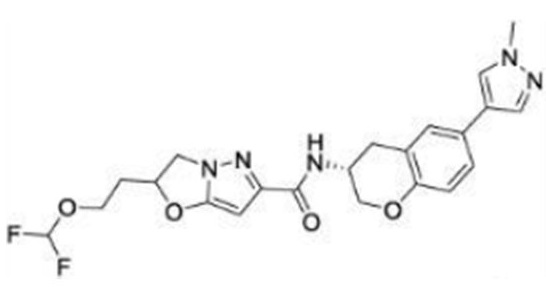
460 [M+H]+
(изомер A)
460 [M+H]+
(изомер B)
460 [M+H]+
458 [M+H]+
(изомер A)
458 [M+H]+
(изомер B)
458 [M+H]+
[0909]
[Таблица 32]
(изомер A)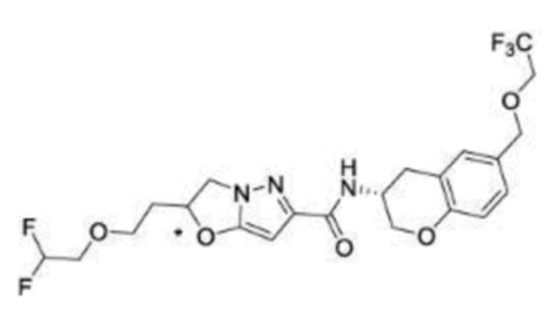
506 [M+H]+
(изомер B)
506 [M+H]+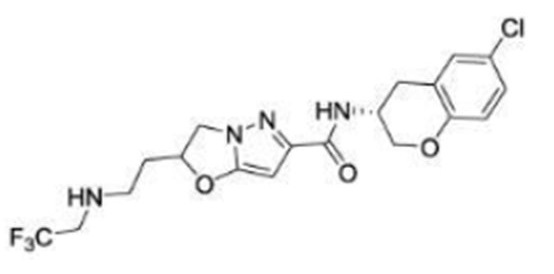
445 [M+H]+
(изомер A)
445 [M+H]+
(изомер B)
445 [M+H]+
425 [M+H]+
(изомер A)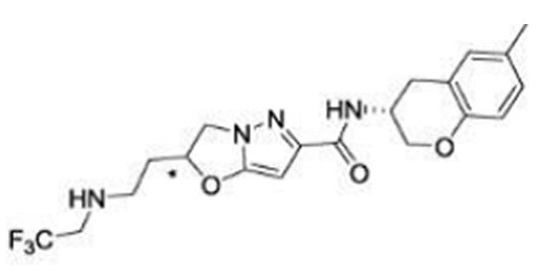
425 [M+H]+
(изомер B)
425 [M+H]+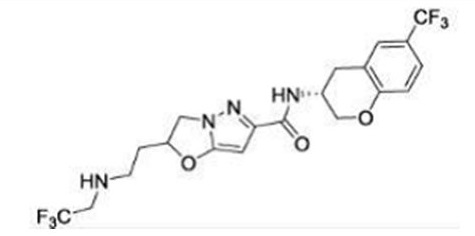
479 [M+H]+
[0910]
[Таблица 33]
(изомер A)
479 [M+H]+
(изомер B)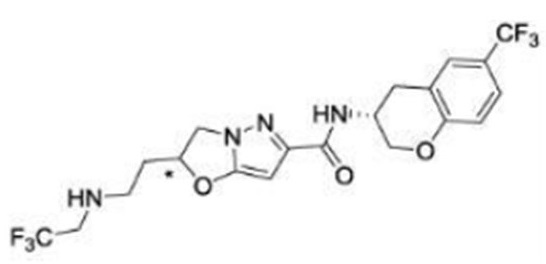
479 [M+H]+
523 [M+H]+
(изомер A)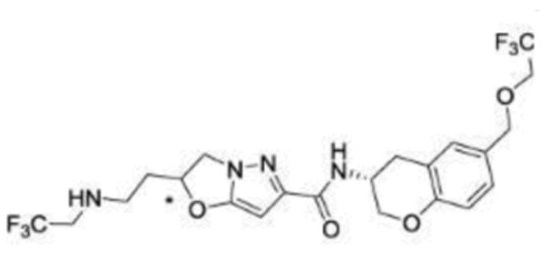
523 [M+H]+
(изомер B)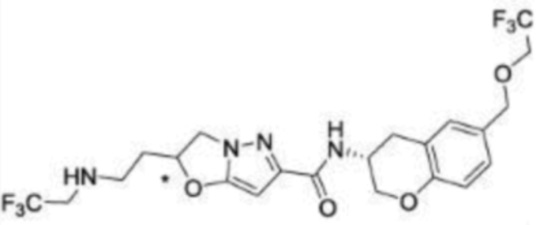
523 [M+H]+
439 [M+H]+
(изомер A)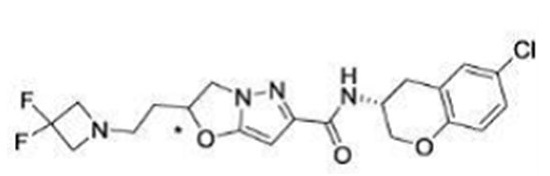
439 [M+H]+
(изомер B)
439 [M+H]+
473 [M+H]+
[0911]
[Таблица 34]
(изомер A)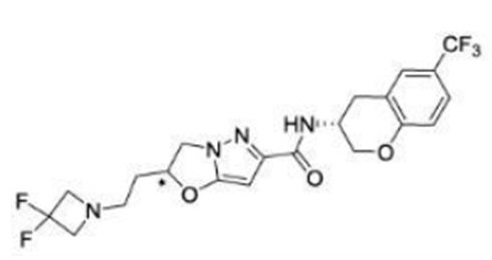
473 [M+H]+
(изомер B)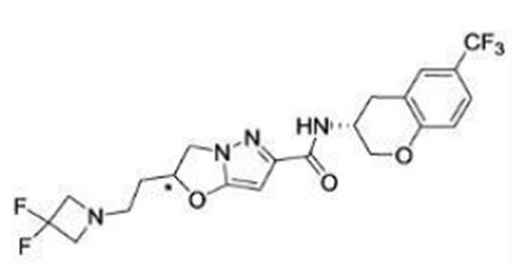
473 [M+H]+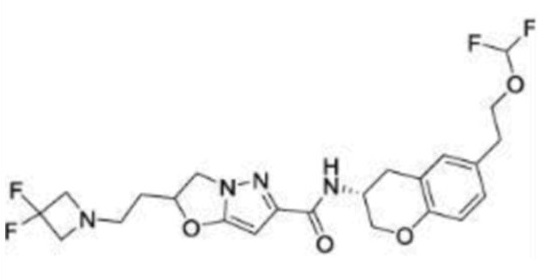
499 [M+H]+
(изомер A)
499 [M+H]+
(изомер B)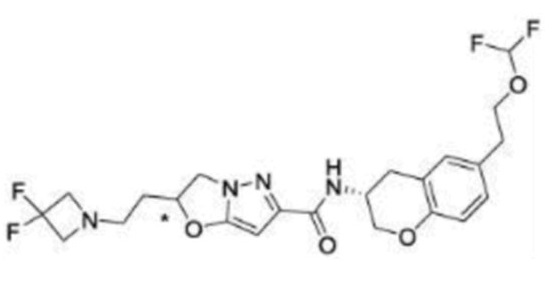
499 [M+H]+
517 [M+H]+
(изомер A)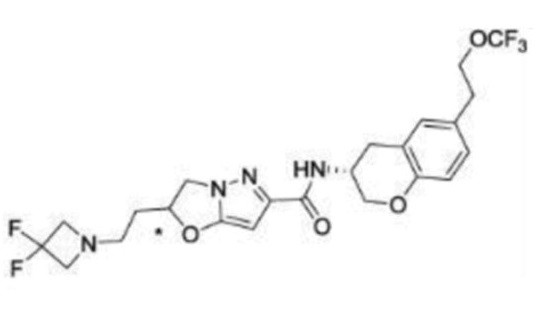
517 [M+H]+
(изомер B)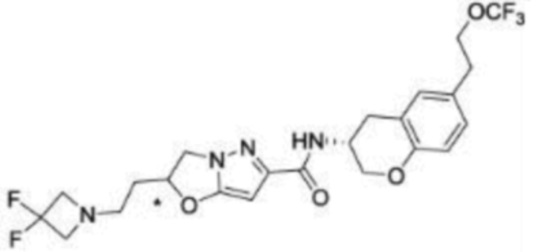
517 [M+H]+
(изомер A)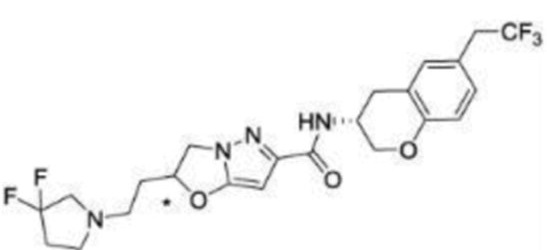
501 [M+H]+
[0912]
[Таблица 35]
(изомер B)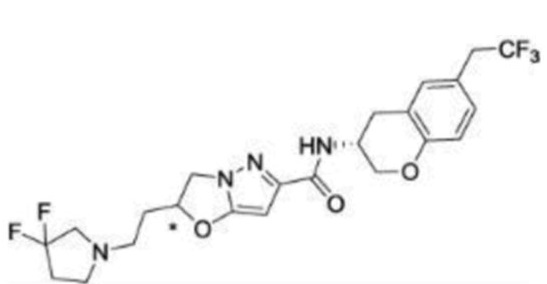
501 [M+H]+
(изомер A)
501 [M+H]+
(изомер B)
501 [M+H]+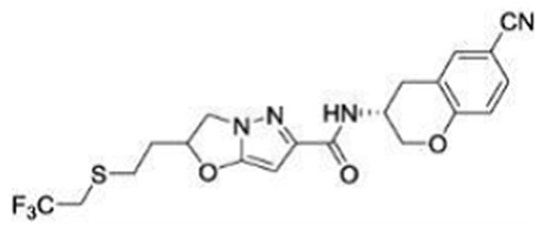
453 [M+H]+
(изомер A)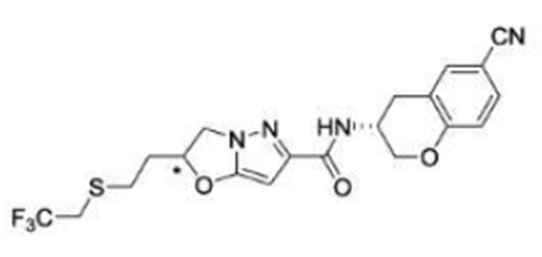
453 [M+H]+
(изомер B)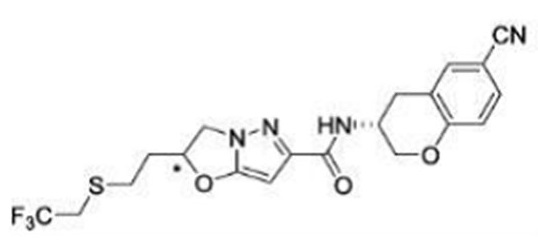
453 [M+H]+
451 [M+H]+
(изомер A)
451 [M+H]+
(изомер B)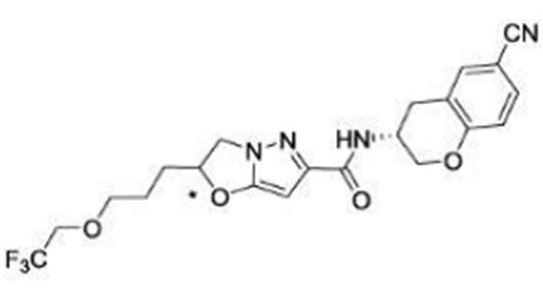
451 [M+H]+
[0913]
[Таблица 36]
(изомер A)
437 [M+H]+
(изомер B)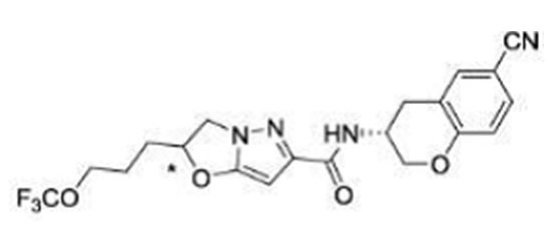
437 [M+H]+
(изомер A)
419 [M+H]+
(изомер B)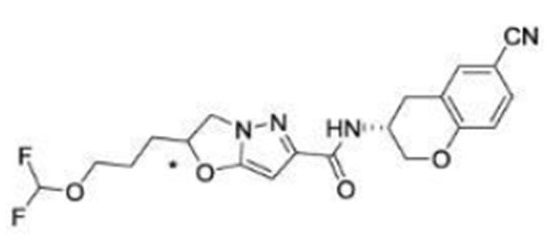
419 [M+H]+
420 [M+H]+
448 [M+H]+
415 [M+H]+
423 [M+H]+
(изомер A)
423 [M+H]+
[0914]
[Таблица 37]
(изомер B)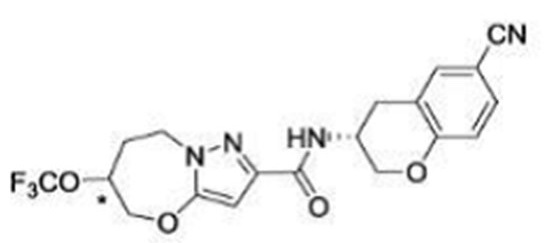
423 [M+H]+
437 [M+H]+
(изомер A)
437 [M+H]+
(изомер A)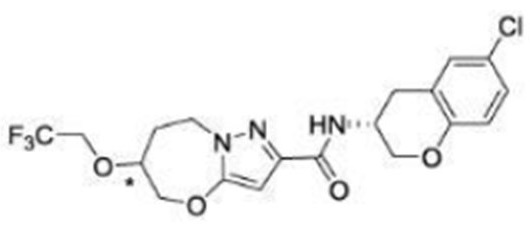
446 [M+H]+
(изомер B)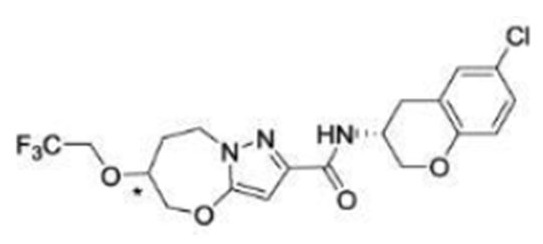
446 [M+H]+
(изомер A)
480 [M+H]+
(изомер B)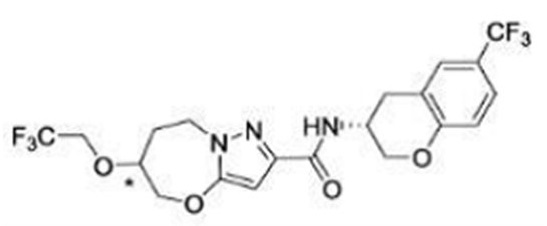
480 [M+H]+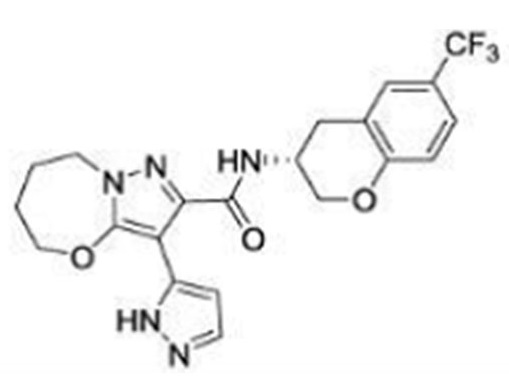
448 [M+H]+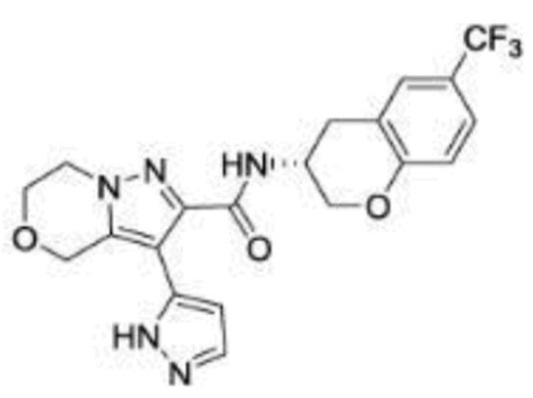
434 [M+H]+
[0915]
[Таблица 38]

445 [M+H]+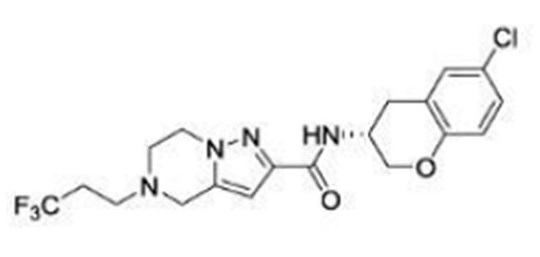
429 [M+H]+
429 [M+H]+
401 [M+H]+
435 [M+H]+
465 [M+H]+
509 [M+H]+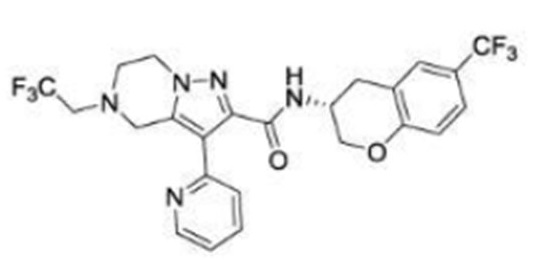
526 [M+H]+
432 [M+H]+
[0916]
[Таблица 39]

446 [M+H]+
380 [M+H]+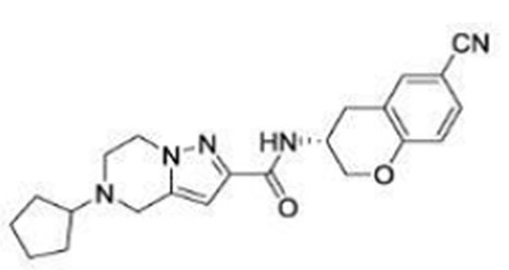
392 [M+H]+
449 [M+H]+
454 [M+H]+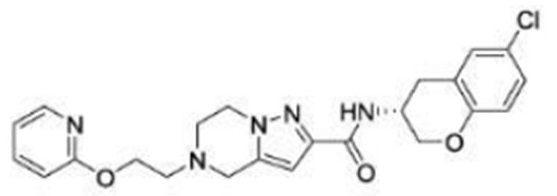
454 [M+H]+
457 [M+H]+
417 [M+H]+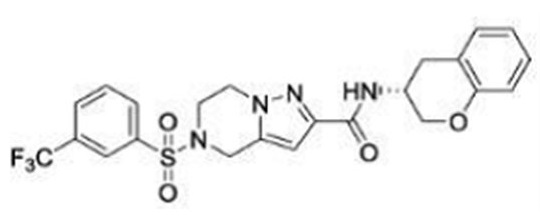
507 [M+H]+
[0917]
[Таблица 40]
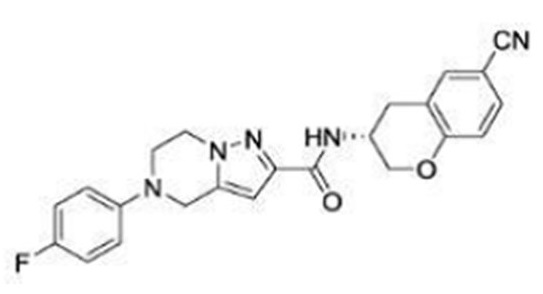


435 [M+H]+
389 [M+H]+
458 [M+H]+
441 [M+H]+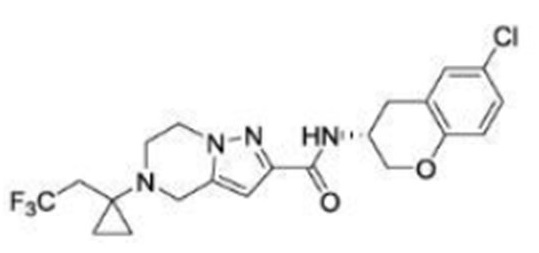
455 [M+H]+
452 [M+H]+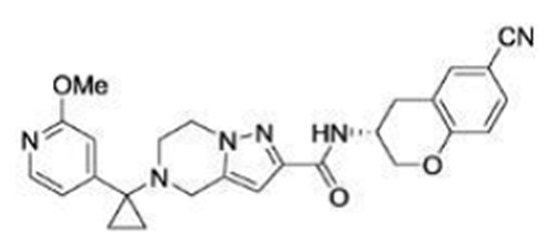
471 [M+H]+
[0918]
[Таблица 41]

375 [M+H]+
[0919]
Соединение из примера 291 синтезировали из соединения из примера 9 с помощью способа, подобного стадии 1 в контрольном примере 3.
[0920]
Соединение из примера 292 синтезировали из соединения из примера 9 с помощью способа, подобного стадии 1 - стадии 3 в контрольном примере 3.
[0921]
Соединение из примера 293 синтезировали из соединения из примера 9 с помощью способа, подобного стадии 1 в контрольном примере 3.
[0922]
Соединение из примера 294 синтезировали из соединения из примера 293 в соответствии со схемой, изображенной на фигуре ниже.
[0923]
[Хим. 234]
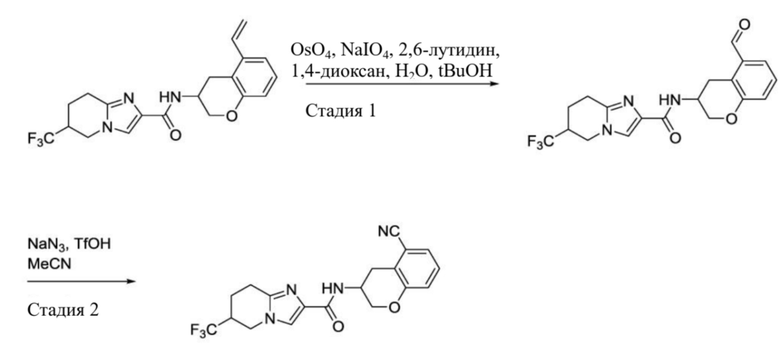
[0924]
Соединение из примера 295 синтезировали с помощью способа, подобного таковому для примера 11.
[0925]
Соединение из примера 296 синтезировали из соединения, синтезированного на стадии 1 в примере 294, в соответствии со схемой, изображенной на фигуре ниже.
[0926]
[Хим. 235]

[0927]
Соединение из примера 297 синтезировали из соединения, синтезированного на стадии 2 в примере 296, в соответствии со схемой, изображенной на фигуре ниже.
[0928]
[Хим. 236]

[0929]
Соединение из примера 298 синтезировали с помощью способов, подобных таковым, описанным в примере 1 и примере 3.
[0930]
Соединение из примера 299 синтезировали с помощью способа, подобного таковому для примера 15.
[0931]
Соединение из примера 300 синтезировали из соединения, синтезированного в примере 14 в соответствии со схемой, изображенной на фигуре ниже.
[0932]
[Хим. 237]

[0933]
Соединение из примера 301 синтезировали из соединения, синтезированного в примере 14, с помощью способа, подобного таковому для примера 29.
[0934]
Соединение из примера 302 синтезировали из соединения, синтезированного в примере 14, с помощью способа, подобного стадии 2 в контрольном примере 3.
[0935]
Соединение из примера 303 синтезировали с помощью способа, подобного таковому для примера 16.
[0936]
Соединение из примера 304 синтезировали с помощью способа, подобного таковому для примера 16.
[0937]
Соединение из примера 305 синтезировали с помощью способов, подобных таковым, описанным в примере 18 и в контрольном примере 43.
[0938]
Соединение из примера 306 синтезировали с помощью способов, подобных таковым, описанным в примере 18 и в контрольном примере 65.
[0939]
Соединение из контрольного примера 75 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для примера 26.
[0940]
[Хим. 238]

[0941]
Соединение из примера 307 синтезировали из соединения, синтезированного в контрольном примере 75 в соответствии со схемой, изображенной на фигуре ниже.
[0942]
[Хим. 239]
 [0943]
[0943]
Соединение из примера 308 синтезировали с помощью способа, подобного таковому для примера 307.
[0944]
Соединение из примера 309 синтезировали с помощью способа, подобного таковому для примера 307.
[0945]
Соединение из примера 310 синтезировали с помощью способа, подобного таковому для примера 307.
[0946]
Соединение из примера 311 синтезировали с помощью способа, подобного таковому для примера 307.
[0947]
Соединение из примера 312 синтезировали с помощью способов, подобных таковым, описанным в примере 307 и примере 102.
[0948]
Соединение из примера 313 синтезировали из соединения, синтезированного в контрольном примере 75 в соответствии со схемой, изображенной на фигуре ниже.
[0949]
[Хим. 240]
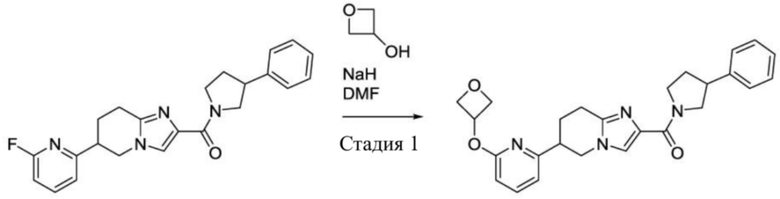
[0950]
Соединение из примера 314 синтезировали с помощью способа, подобного таковому для примера 27.
[0951]
Соединение из примера 315 синтезировали с помощью способа, подобного таковому для примера 26.
[0952]
Соединение из примера 316 синтезировали с помощью способа, подобного таковому для примера 26.
[0953]
Соединение из примера 317 синтезировали с помощью способа, подобного таковому для примера 29.
[0954]
Соединение из примера 318 синтезировали с помощью способа, подобного таковому для примера 30.
[0955]
Соединение из примера 319 синтезировали с помощью способов, подобных таковым, описанным в примере 41, в примере 168 и в примере 157.
[0956]
Соединение из примера 320 синтезировали с помощью способов, подобных таковым, описанным в примере 29 и примере 157.
[0957]
Соединение из примера 321 синтезировали с помощью способа, подобного таковому для примера 41.
[0958]
Соединение из примера 322 синтезировали из соединения, синтезированного на стадии 1 в примере 42, в соответствии со схемой, изображенной на фигуре ниже.
[0959]
[Хим. 241]
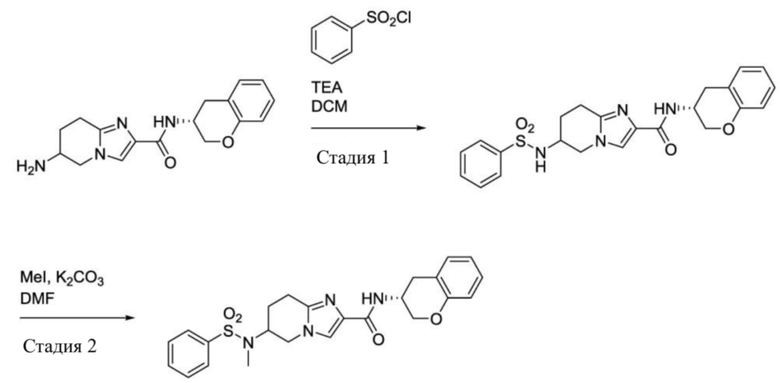
[0960]
Соединение из примера 323 синтезировали с помощью способа, подобного таковому для примера 62.
[0961]
Соединение из примера 324 синтезировали с помощью способа, подобного таковому для примера 43.
[0962]
Соединение из примера 325 синтезировали с помощью способов, подобных таковым, описанным в примере 62 и стадии 3 в примере 41.
[0963]
Соединение из примера 326 синтезировали с помощью способов, подобных таковым, описанным в примере 43 и примере 45.
[0964]
Соединение из примера 327 синтезировали с помощью способа, подобного таковому для примера 325.
[0965]
Соединение из примера 328 синтезировали с помощью способа, подобного таковому для примера 49.
[0966]
Соединение из контрольного примера 76 (гидрохлорид 3-(2-хлорфенил)-3-фторпирролидина) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0967]
[Хим. 242]

[0968]
Соединение из примера 329 синтезировали из соединения из контрольного примера 21 и соединения из контрольного примера 76 с помощью способа, подобного стадии 3 в примере 56.
[0969]
Соединение из примера 330 синтезировали с помощью способа, подобного таковому для примера 62.
[0970]
Соединение из примера 331 синтезировали с помощью способа, подобного таковому для примера 62.
[0971]
Соединение из примера 332 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 18, в примере 58 и в примере 3.
[0972]
Соединение из примера 333 синтезировали с помощью способов, подобных таковым, описанным в примере 59 и примере 45.
[0973]
Соединение из контрольного примера 77 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для контрольного примера 4.
[0974]
[Хим. 243]

[0975]
Соединение из примера 334 синтезировали из соединения из контрольного примера 21 и соединения из контрольного примера 77 с помощью способа, подобного стадии 3 в примере 100.
[0976]
Соединение из примера 335 синтезировали с помощью способов, подобных таковым, описанным в примере 43 и примере 45.
[0977]
Соединение из примера 336 синтезировали с помощью способа, подобного таковому для примера 43.
[0978]
Соединение из примера 337 синтезировали с помощью способа, подобного таковому для примера 43.
[0979]
Соединение из контрольного примера 78 ((R)-N-(хроман-3-ил)-3-фенил-5,6,7,8-тетрагидроимидазо[1,2-a]пиразин-2-карбоксамид) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0980]
[Хим. 244]

[0981]
Соединение из примера 338 синтезировали из соединения из контрольного примера 78 с помощью способа, подобного таковому для контрольного примера 69.
[0982]
Соединение из примера 339 синтезировали из соединения из контрольного примера 78 с помощью способа, подобного стадии 1 в контрольном примере 1.
[0983]
Соединение из контрольного примера 79 (6-фенил-5,6-дигидро-8H-имидазо[2,1-c][1,4]оксазин-2-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[0984]
[Хим. 245]
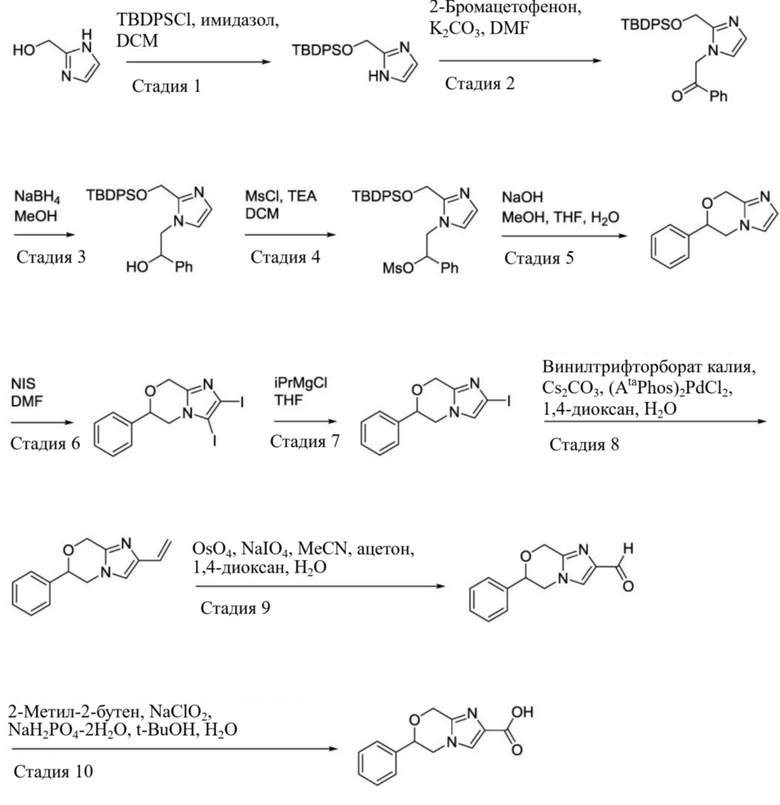
Соединение из примера 340 синтезировали из соединения из контрольного примера 79 с помощью способа, подобного стадии 3 в примере 100.
[0985]
Соединение из примера 341 синтезировали с помощью способа, подобного таковому для примера 64 и контрольного примера 24.
[0986]
Соединение из контрольного примера 80 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 1 и стадии 4 в контрольном примере 3.
[0987]
[Хим. 246]

[0988]
Соединение из примера 342 синтезировали с помощью способов, подобных таковым, описанным в примере 66 и в контрольном примере 80.
[0989]
Соединение из примера 343 синтезировали с помощью способов, подобных таковым, описанным в примере 66 и в контрольном примере 52.
[0990]
Соединение из примера 344 синтезировали с помощью способов, подобных таковым, описанным в примере 64 и в контрольном примере 1.
[0991]
Соединение из примера 345 синтезировали с помощью способов, подобных таковым, описанным в примере 64 и в контрольном примере 43.
[0992]
Соединение из примера 346 синтезировали с помощью способов, подобных таковым, описанным в примере 64 и в контрольном примере 43.
[0993]
Соединение из примера 347 синтезировали с помощью способа, подобного таковому для примера 69.
[0994]
Соединение из примера 348 синтезировали с помощью способов, подобных таковым, описанным в примере 69 и в контрольном примере 1.
[0995]
Соединение из примера 349 синтезировали с помощью способа, подобного таковому для примера 70.
[0996]
Соединение из примера 350 синтезировали с помощью способа, подобного таковому для примера 70.
[0997]
Соединение из примера 351 синтезировали с помощью способа, подобного таковому для примера 70.
[0998]
Соединение из примера 352 синтезировали с помощью способа, подобного таковому для примера 70.
[0999]
Соединение из примера 353 синтезировали с помощью способа, подобного таковому для примера 70.
[1000]
Соединение из примера 354 синтезировали с помощью способа, подобного таковому для примера 70.
[1001]
Соединение из примера 355 синтезировали с помощью способа, подобного таковому для примера 70.
[1002]
Соединение из примера 356 синтезировали с помощью способа, подобного таковому для примера 70.
[1003]
Соединение из примера 357 синтезировали из соединения из примера 71 с помощью способа, подобного стадии 1 в контрольном примере 27.
[1004]
Соединение из примера 358 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 1.
[1005]
Соединения из примера 359 и примера 360 получали путем разделения соединения из примера 70.
[1006]
Соединение из примера 361 синтезировали из соединения из примера 82 с помощью способа, подобного стадии 2 - стадии 3 в примере 296.
[1007]
Соединение из примера 362 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 1.
[1008]
Соединение из примера 363 синтезировали с помощью способа, подобного таковому для примера 70.
[1009]
Соединение из примера 364 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 24.
[1010]
Соединение из примера 365 синтезировали с помощью способа, подобного таковому для примера 361.
[1011]
Соединение из примера 366 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 24.
[1012]
Соединение из примера 367 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 1.
[1013]
Соединение из примера 368 синтезировали из соединения из примера 82 с помощью способов, подобных стадии 2 в примере 296 и стадии 1 в примере 122.
[1014]
Соединение из примера 369 синтезировали из соединения из примера 82 с помощью способа, подобного стадии 2 - стадии 3 в примере 296.
[1015]
Соединение из примера 370 синтезировали из соединения из примера 82 с помощью способа, подобного стадии 2 - стадии 3 в примере 296.
[1016]
Соединение из примера 371 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 1.
[1017]
Соединение из примера 372 синтезировали с помощью способов, подобных таковым, описанным в примере 70 и в контрольном примере 24.
[1018]
Соединение из примера 373 синтезировали с помощью способов, подобных таковым, описанным в примере 169 и в контрольном примере 24.
[1019]
Соединения из примера 374 получали путем разделения соединения из примера 373.
[1020]
Соединение из примера 375 синтезировали с помощью способов, подобных таковым, описанным в примере 169 и контрольном примере 73.
[1021]
Соединение из примера 376 синтезировали с помощью способов, подобных таковым, описанным в примере 169 и контрольном примере 23.
[1022]
Соединение из примера 377 синтезировали из соединения из примера 171 с помощью способа, подобного стадии 1 в контрольном примере 27.
[1023]
Соединение из примера 378 синтезировали из соединения из примера 171 с помощью способа, подобного стадии 1 в контрольном примере 27.
[1024]
Соединение из примера 379 синтезировали из соединения, синтезированного на стадии 1 в примере 120, в соответствии со схемой, изображенной на фигуре ниже.
[1025]
[Хим. 247]

[1026]
Соединение из примера 380 синтезировали из соединения из примера 171 с помощью способа, подобного стадии 1 в контрольном примере 27.
[1027]
Соединение из примера 381 синтезировали из соединения, синтезированного на стадии 1 в примере 117, с помощью способа, подобного таковому для примера 157.
[1028]
Соединение из примера 382 синтезировали из соединения из примера 171 с помощью способа, подобного стадии 1 в контрольном примере 27.
[1029]
Соединение из примера 383 синтезировали с помощью способов, подобных таковым, описанным в примере 177 и в контрольном примере 28.
[1030]
Соединение из примера 384 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 34, в примере 85 и в контрольном примере 24.
[1031]
Соединение из контрольного примера 81 (6,6-дифтор-5-метил-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1032]
[Хим. 248]

[1033]
Соединение из примера 385 синтезировали из соединения из контрольного примера 81 и соединения из контрольного примера 1 с помощью способа, подобного стадии 3 в примере 100.
[1034]
Соединение из примера 386 синтезировали из соединения, синтезированного на стадии 3 в примере 100, в соответствии со схемой, изображенной на фигуре ниже.
[1035]
[Хим. 249]

[1036]
Соединение из контрольного примера 82 (1-циклопропилпропан-1,3-диол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1037]
[Хим. 250]

[1038]
Соединение из примера 387 синтезировали из соединения из контрольного примера 82 с помощью способов, подобных таковым, описанным в примере 159 и в контрольном примере 1.
[1039]
Соединение из примера 388 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 82, в примере 159 и в контрольном примере 24.
[1040]
Соединение из примера 389 синтезировали с помощью способа, подобного таковому для примера 85.
[1041]
Соединение из контрольного примера 83 (5-((трет-бутилдифенилсилил)окси)-1-фенилпент-1-ин-3-ол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1042]
[Хим. 251]
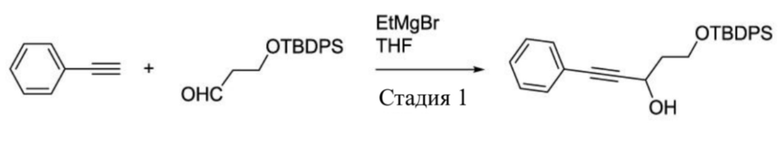
[1043]
Соединение из примера 390 синтезировали из соединения из контрольного примера 83 с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 24.
[1044]
Соединение из примера 391 синтезировали из соединения из примера 171 с помощью способов, подобных таковым, описанным в примере 82 и в примере 83.
[1045]
Соединение из примера 392 синтезировали из соединения из примера 171 с помощью способа, подобного стадии 2 в примере 117.
[1046]
Соединение из примера 393 синтезировали с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 24.
[1047]
Соединение из примера 394 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 83, в примере 85 и в контрольном примере 24.
[1048]
Соединение из примера 395 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 82, в примере 159 и в контрольном примере 1.
[1049]
Соединение из примера 396 синтезировали из соединения из примера 171 с помощью способа, подобного стадии 1 в контрольном примере 3.
[1050]
Соединение из примера 397 синтезировали из соединения из примера 396 с помощью способов, подобных таковым, описанным на стадии 1 в контрольном примере 45 и стадии 2 в контрольном примере 44.
[1051]
Соединение из контрольного примера 84 ((R)-6-(3-метокси-3-этилбут-1-ин-1-ил)хроман-3-амин) синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 2, в соответствии со схемой, изображенной на фигуре ниже.
[1052]
[Хим. 252]

[1053]
Соединение из примера 398 синтезировали с помощью способов, подобных таковым, описанным в примере 169 и в контрольном примере 84.
[1054]
Соединение из примера 399 синтезировали с помощью способа, подобного таковому для примера 391.
[1055]
Соединение из примера 400 синтезировали из соединения из примера 398 с помощью способа, подобного стадии 2 в примере 1.
[1056]
Соединение из примера 401 синтезировали с помощью способов, подобных таковым, описанным в примере 169, в контрольном примере 45 и в примере 122.
[1057]
Соединение из примера 402 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 83, в примере 85 и в контрольном примере 43.
[1058]
Соединение из примера 403 синтезировали с помощью способов, подобных таковым, описанным в примере 177 и в контрольном примере 65.
[1059]
Соединение из примера 404 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 83, в примере 85, в контрольном примере 3 и в контрольном примере 1.
[1060]
Соединение из примера 405 синтезировали из соединения, синтезированного на стадии 6 в примере 159, и соединения из контрольного примера 80 с помощью способа, подобного стадии 8 в примере 70.
[1061]
Соединение из контрольного примера 85 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 83, в примере 85 и в контрольном примере 1.
[Хим. 253]

[1062]
Соединения из примера 406 и примера 407 получали путем разделения соединения из контрольного примера 85.
[1063]
Соединение из примера 408 синтезировали с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 24.
[1064]
Соединение из примера 409 синтезировали с помощью способа, подобного таковому для примера 157.
[1065]
Соединение из примера 410 синтезировали с помощью способа, подобного таковому для примера 100.
[1066]
Соединение из примера 411 синтезировали с помощью способов, подобных таковым, описанным в примере 117 и в контрольном примере 24.
[1067]
Соединение из примера 412 синтезировали с помощью способа, подобного таковому для примера 114.
[1068]
Соединение из примера 413 синтезировали с помощью способов, подобных таковым, описанным в примере 100 и в контрольном примере 1.
[1069]
Соединение из примера 414 синтезировали с помощью способов, подобных таковым, описанным в примере 100 и в контрольном примере 28.
[1070]
Соединение из примера 415 синтезировали из соединения, синтезированного на стадии 1 в примере 117, с помощью способа, подобного стадии 1 - стадии 2 в примере 122.
[1071]
Соединение из контрольного примера 86 (2,3,5,6,6',7'-гексагидроспиро[пиран-4,5'-пиразоло[5,1-b][1,3]оксазин]-2'-карбоновую кислоту) синтезировали в соответствии со схемой ниже.
[1072]
[Хим. 254]

[1073]
Соединение из примера 416 синтезировали из соединения из контрольного примера 86 и соединения из контрольного примера 1 с помощью способа, подобного стадии 8 в примере 70.
[1074]
Соединение из примера 417 синтезировали из соединения, синтезированного на стадии 1 в примере 386, в соответствии со схемой, изображенной на фигуре ниже.
[1075]
[Хим. 255]

[1076]
Соединение из примера 418 синтезировали из соединения, синтезированного на стадии 3 в примере 100, в соответствии со схемой, изображенной на фигуре ниже.
[1077]
[Хим. 256]

[1078]
Соединение из контрольного примера 87 (5-(гидроксиметил)-5-метил-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1079]
[Хим. 257]

[1080]
Соединение из примера 419 синтезировали из соединения из контрольного примера 87 с помощью способов, подобных стадии 3 - стадии 4 в примере 100.
[1081]
Соединение из примера 420 синтезировали из соединения из контрольного примера 37 и соединения из контрольного примера 1 с помощью способа, подобного таковому для примера 133.
[1082]
Соединение из примера 421 синтезировали из соединения из контрольного примера 37 и соединения из контрольного примера 32 с помощью способа, подобного таковому для примера 133.
[1083]
Соединение из примера 422 синтезировали с помощью способа, подобного таковому для примера 114.
[1084]
Соединения из примера 423 и примера 424 получали путем разделения соединения из примера 422.
[1085]
Соединение из примера 425 синтезировали с помощью способов, подобных таковым из примера 100, контрольного примера 2 и стадии 1 в контрольном примере 27.
[1086]
Соединение из примера 426 синтезировали с помощью способа, подобного таковому для примера 425.
[1087]
Соединение из примера 427 синтезировали с помощью способа, подобного таковому для примера 425.
[1088]
Соединение из примера 428 синтезировали с помощью способа, подобного таковому для примера 425.
[1089]
Соединение из примера 429 синтезировали с помощью способа, подобного таковому для примера 425.
[1090]
Соединение из примера 430 синтезировали с помощью способа, подобного таковому для примера 425.
[1091]
Соединение из примера 431 синтезировали с помощью способа, подобного таковому для примера 425.
[1092]
Соединение из примера 432 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 43 с помощью способа, подобного стадии 5 - стадии 6 в примере 85.
[1093]
Соединение из примера 433 синтезировали из соединения из контрольного примера 41 и соединения из контрольного примера 43 с помощью способа, подобного стадии 6 в примере 85.
[1094]
Соединение из примера 434 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 24.
[1095]
Соединение из примера 435 синтезировали с помощью способов, подобных таковым, описанным в примере 434 и в контрольном примере 60.
[1096]
Соединение из примера 436 синтезировали из соединения из контрольного примера 36 с помощью способов, подобных таковым, описанным в контрольном примере 84 и стадии 5 - стадии 6 в примере 85.
[1097]
Соединение из примера 437 синтезировали с помощью способов, подобных таковым, описанным в примере 384 и в контрольном примере 48.
[1098]
Соединение из примера 438 синтезировали с помощью способов, подобных таковым, описанным в примере 384 и в контрольном примере 44.
[1099]
Соединение из примера 439 синтезировали с помощью способов, подобных таковым, описанным в примере 384, в примере 157 и в контрольном примере 24.
[1100]
Соединение из примера 440 синтезировали с помощью способов, подобных таковым, описанным в примере 122 и в контрольном примере 44.
[1101]
Соединение из примера 441 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 52 с помощью способа, подобного стадии 5 - стадии 6 в примере 85.
[1102]
Соединение из примера 442 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 1 с помощью способа, подобного стадии 5 - стадии 6 в примере 85.
[1103]
Соединение из примера 443 синтезировали с помощью способа, подобного таковому для примера 98.
[1104]
Соединение из примера 444 синтезировали с помощью способа, подобного таковым, описанным в примере 85 и в примере 69.
[1105]
Соединение из примера 445 синтезировали с помощью способов, подобных таковым, описанным в примере 183 и в контрольном примере 2.
[1106]
Соединение из примера 446 синтезировали из соединения, синтезированного в контрольном примере 68, с помощью способов, подобных таковым, описанным в примере 249 и в контрольном примере 1.
[1107]
Соединение из примера 447 синтезировали с помощью способов, подобных таковым, описанным в примере 183 и в контрольном примере 65.
[1108]
Соединение из примера 448 синтезировали из соединения, синтезированного на стадии 1 в примере 187, с помощью способа, подобного таковому для примера 225.
[1109]
Соединение из контрольного примера 88 (этил-2-(1,1-дифтор-2-гидроксиэтил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоксилат) синтезировали из соединения, синтезированного на стадии 4 в контрольном примере 81, в соответствии со схемой, изображенной на фигуре ниже.
[1110]
[Хим. 258]

[1111]
Соединение из примера 449 синтезировали из соединения из контрольного примера 88 с помощью способов, подобных таковым, описанным в контрольном примере 33 и стадии 6 в примере 85.
[1112]
Соединение из примера 450 синтезировали из соединения, синтезированного на стадии 1 в примере 187, с помощью способов, подобных таковым, описанным на стадии 2 в примере 117 и стадии 2 - стадии 3 в примере 100.
[1113]
Соединение из примера 451 синтезировали из соединения, синтезированного на стадии 5 в контрольном примере 55, с помощью способов, подобных таковым, описанным в контрольном примере 35 и стадии 5 - стадии 6 в примере 85.
[1114]
Соединение из примера 452 синтезировали из соединения, синтезированного на стадии 1 в примере 187, с помощью способов, подобных таковым, описанным в примере 225 и в контрольном примере 24.
[1115]
Соединение из примера 453 синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 187, с помощью способов, подобных таковым, описанным в контрольном примере 35 и стадии 5 - стадии 6 в примере 85.
[1116]
Соединение из примера 454 синтезировали из соединения из контрольного примера 50 с помощью способа, подобного стадии 3 в примере 100.
[1117]
Соединение из примера 455 синтезировали с помощью способов, подобных таковым, описанным в примере 451 и в контрольном примере 24.
[1118]
Соединение из примера 456 синтезировали из соединения из контрольного примера 55 и соединения из контрольного примера 60 с помощью способа, подобного стадии 3 в примере 100.
[1119]
Соединение из примера 457 синтезировали с помощью способов, подобных таковым, описанным в примере 243 и в контрольном примере 56.
[1120]
Соединение из примера 458 синтезировали из соединения, синтезированного на стадии 1 в примере 187, с помощью способов, подобных стадии 1 в примере 225, описанным в контрольном примере 64, в контрольном примере 43 и стадии 3 в примере 100.
[1121]
Соединение из примера 459 синтезировали с помощью способов, подобных таковым, описанным в примере 187 и в контрольном примере 48.
[1122]
Соединение из примера 460 синтезировали с помощью способов, подобных таковым, описанным в примере 203 и в контрольном примере 59.
[1123]
Соединение из примера 461 синтезировали с помощью способов, подобных таковым, описанным в примере 203 и в контрольном примере 56.
[1124]
Соединение из примера 462 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 38, в контрольном примере 65 и стадии 3 в примере 100.
[1125]
Соединение из примера 463 синтезировали с помощью способов, подобных таковым, описанным в примере 185 и в контрольном примере 80.
[1126]
Соединение из примера 464 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в контрольном примере 50, в контрольном примере 24 и стадии 3 в примере 100.
[1127]
Соединение из примера 465 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 24.
[1128]
Соединение из примера 466 синтезировали из соединения из контрольного примера 55 и соединения из контрольного примера 48 с помощью способа, подобного стадии 3 в примере 100.
[1129]
Соединение из примера 467 синтезировали с помощью способов, подобных таковым, описанным в примере 465 и в контрольном примере 60.
[1130]
Соединение из примера 468 синтезировали из соединения из контрольного примера 50 и соединения из контрольного примера 29 с помощью способа, подобного стадии 3 в примере 100.
[1131]
Соединение из примера 469 синтезировали из соединения из контрольного примера 50 и соединения из контрольного примера 1 с помощью способа, подобного стадии 3 в примере 100.
[1132]
Соединение из примера 470 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 24.
[1133]
Соединение из примера 471 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 48.
[1134]
Соединение из примера 472 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 44.
[1135]
Соединение из примера 473 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 59.
[1136]
Соединение из примера 474 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 60.
[1137]
Соединение из примера 475 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 49, в примере 85 и в контрольном примере 53.
[1138]
Соединения из примера 476 и примера 477 синтезировали с помощью способов, подобных таковым, описанным в примере 241 и в контрольном примере 43.
[1139]
Соединение из примера 478 синтезировали с помощью способов, подобных таковым, описанным на стадии 1 в примере 224 и в контрольном примере 48.
[1140]
Соединение из примера 479 синтезировали с помощью способов, подобных таковым, описанным на стадии 1 в примере 224 и в контрольном примере 52.
[1141]
Соединение из примера 480 синтезировали с помощью способов, подобных таковым, описанным в примере 251 и в контрольном примере 1.
[1142]
Соединение из примера 481 синтезировали с помощью способов, подобных таковым, описанным в примере 258 и в контрольном примере 1.
[1143]
Соединение из примера 482 синтезировали с помощью способов, подобных таковым, описанным в примере 254 и в контрольном примере 44.
[1144]
Соединение из контрольного примера 89 (4-((трет-бутилдифенилсилил)окси)-2-(трифторметил)бутан-1-ол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1145]
[Хим. 259]

[1146]
Соединение из примера 483 синтезировали из соединения из контрольного примера 89 с помощью способов, подобных таковым, описанным на стадии 2 - стадии 6 в примере 85 и в контрольном примере 24.
[1147]
Соединение из примера 484 синтезировали с помощью способа, подобного таковому для примера 259.
[1148]
Соединение из примера 485 синтезировали с помощью способа, подобного таковому для примера 259.
[1149]
Соединение из примера 486 синтезировали с помощью способов, подобных таковым, описанным в примере 16 и в контрольном примере 43.
[1150]
Соединение из примера 487 синтезировали из соединения из контрольного примера 72 с помощью способа, подобного стадии 1 в примере 266.
[1151]
Соединение из примера 488 синтезировали из соединения из контрольного примера 72 с помощью способа, подобного стадии 1 в примере 266.
[1152]
Соединение из примера 489 синтезировали с помощью способов, подобных таковым, описанным в примере 487 и в контрольном примере 24.
[1153]
Соединение из примера 490 синтезировали из соединения из контрольного примера 72 с помощью способа, подобного стадии 1 в примере 266.
[1154]
Соединение из примера 491 синтезировали с помощью способов, подобных таковым, описанным в примере 263 и в контрольном примере 24.
[1155]
Соединение из примера 492 синтезировали с помощью способов, подобных таковым, описанным в примере 268 и в контрольном примере 3.
[1156]
Соединение из примера 493 синтезировали из соединения из контрольного примера 71 с помощью способа, подобного стадии 1 в примере 266.
[1157]
Соединение из примера 494 синтезировали из соединения из контрольного примера 71 с помощью способов, подобных таковым, описанным в контрольном примере 69 и в примере 157.
[1158]
Соединение из примера 495 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 69, в примере 157 и стадии 2 - стадии 3 в примере 261.
[1159]
Соединение из примера 496 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 69 и стадии 2 - стадии 3 в примере 261.
[1160]
Соединение из примера 497 синтезировали с помощью способа, подобного таковому для примера 268.
[1161]
Соединение из примера 498 синтезировали с помощью способа, подобного таковому для примера 268.
[1162]
Соединение из примера 499 синтезировали с помощью способа, подобного таковому для примера 269.
[1163]
Соединение из примера 500 синтезировали с помощью способа, подобного таковому для примера 283.
[1164]
Соединение из примера 501 синтезировали с помощью способа, подобного таковому для примера 283.
[1165]
Соединение из примера 502 синтезировали с помощью способов, подобных таковым, описанным в примере 283 и в контрольном примере 24.
[1166]
Соединение из примера 503 синтезировали с помощью способов, подобных таковым, описанным в примере 283 и в контрольном примере 24.
[1167]
Соединение из примера 504 синтезировали из соединения из контрольного примера 69 с помощью способов, подобных таковым, описанным на стадии 2 - стадии 3 в примере 261 и в контрольном примере 48.
[1168]
Соединение из примера 505 синтезировали из соединения из контрольного примера 69 с помощью способов, подобных таковым, описанным на стадии 2 - стадии 3 в примере 261 и в контрольном примере 44.
[1169]
Соединение из примера 506 синтезировали с помощью способов, подобных таковым, описанным в примере 261 и в контрольном примере 43.
[1170]
Соединение из примера 507 синтезировали с помощью способов, подобных таковым, описанным в примере 261 и в контрольном примере 44.
[1171]
Соединение из примера 508 синтезировали с помощью способа, подобного таковому для примера 278.
[1172]
Соединение из примера 509 синтезировали с помощью способов, подобных таковым, описанным в примере 275 и в контрольном примере 1.
[1173]
Соединение из примера 510 синтезировали с помощью способа, подобного таковому для примера 276.
[1174]
Соединение из примера 511 синтезировали с помощью способа, подобного таковому для примера 277.
[1175]
Соединение из примера 512 синтезировали с помощью способов, подобных таковым, описанным в примере 64 и в контрольном примере 43.
[1176]
Соединение из примера 513 синтезировали с помощью способа, подобного таковому для примера 259.
[1177]
Соединение из примера 514 синтезировали с помощью способа, подобного таковому для примера 259.
[1178]
Соединение из примера 515 синтезировали с помощью способов, подобных таковым, описанным в примере 259 и в контрольном примере 1.
[1179]
Соединение из контрольного примера 90 (3-(6-этилпиридин-2-ил)-6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-карбоновую кислоту) синтезировали из соединения, синтезированного на стадии 1 в примере 259, в соответствии со схемой, изображенной на фигуре ниже.
[1180]
[Хим. 260]
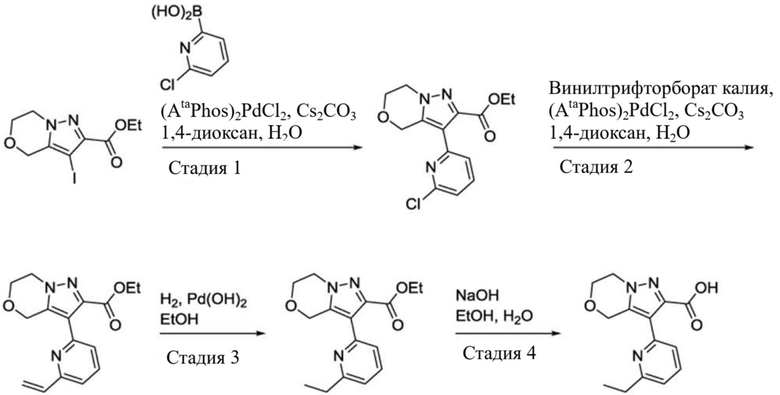
[1181]
Соединение из примера 516 синтезировали из соединения из контрольного примера 90 с помощью способа, подобного стадии 3 в примере 100.
[1182]
Соединение из примера 517 синтезировали с помощью способа, подобного таковому для примера 259.
[1183]
Соединение из примера 518 синтезировали с помощью способа, подобного таковому для примера 259.
[1184]
Соединение из примера 519 синтезировали из соединения из примера 514 в соответствии со схемой, изображенной на фигуре ниже.
[1185]
[Хим. 261]

[1186]
Соединение из примера 520 синтезировали из соединения из примера 519 с помощью способа, подобного таковому для примера 114.
[1187]
Соединение из примера 521 синтезировали из соединения из примера 519 в соответствии со схемой, изображенной на фигуре ниже.
[1188]
[Хим. 262]

[1189]
Соединение из примера 522 синтезировали из соединения, синтезированного на стадии 2 в примере 519, в соответствии со схемой, изображенной на фигуре ниже.
[1190]
[Хим. 263]

[1191]
Соединение из примера 523 синтезировали из соединения из примера 519 в соответствии со схемой, изображенной на фигуре ниже.
[1192]
[Хим. 264]
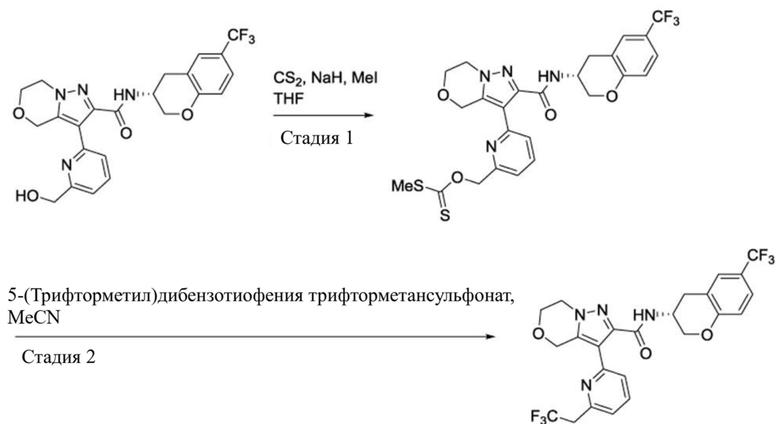
[1193]
Соединение из контрольного примера 91 (3-(6-метилпиридин-2-ил)-4,5,6,7-тетрагидропиразоло[1,5-a]пиримидин-2-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1194]
[Хим. 265]

[1195]
Соединение из примера 524 синтезировали из соединения из контрольного примера 91 и соединения из контрольного примера 43 с помощью способа, подобного стадии 3 в примере 100.
[1196]
Соединение из примера 525 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 91, в контрольном примере 44 и стадии 3 в примере 100.
[1197]
Соединение из примера 526 синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1198]
[Хим. 266]

[1199]
Соединение из примера 527 синтезировали из соединения, синтезированного на стадии 2 в примере 519, с помощью способа, подобного стадии 1 в контрольном примере 52.
[1200]
Соединение из примера 528 синтезировали с помощью способов, подобных таковым, описанным на стадиях 1-3 в примере 259 и в примере 260.
[1201]
Соединения из контрольного примера 92 ((3S)-3-амино-6-(трифторметил)хроман-4-ол (изомер A и изомер B)) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1202]
[Хим. 267]
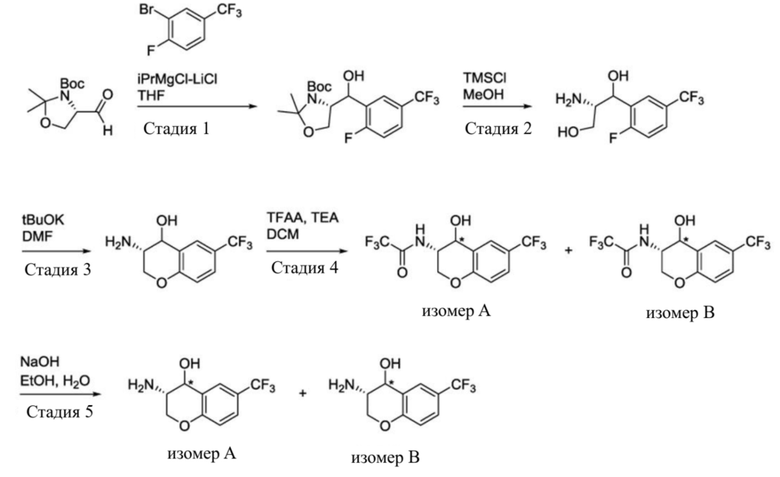
[1203]
Соединение из примера 529 синтезировали из соединения, синтезированного на стадии 1 в примере 259, и соединения, синтезированного в контрольном примере 92 (изомер A), с помощью способов, подобных таковым, описанным на стадии 2 - стадии 4 в примере 259.
[1204]
Соединение из примера 530 синтезировали из соединения, синтезированного на стадии 3 в примере 259, в соответствии со схемой, изображенной на фигуре ниже.
[1205]
[Хим. 268]
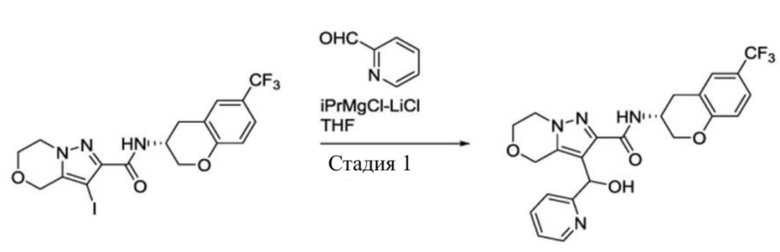
[1206]
Соединение из примера 531 синтезировали из соединения, синтезированного на стадии 3 в примере 259, в соответствии со схемой, изображенной на фигуре ниже.
[1207]
[Хим. 269]

[1208]
Соединение из примера 532 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 34, в примере 85 и в контрольном примере 24.
[1209]
Соединение из примера 533 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 34, в примере 85 и в контрольном примере 43.
[1210]
Соединения из контрольного примера 93 (5-(дифторметил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновую кислоту (изомер A и изомер B)) синтезировали из соединения, синтезированного на стадии 5 в примере 159 в соответствии со схемой, изображенной на фигуре ниже.
[1211]
[Хим. 270]

[1212]
Соединения из примера 534 (изомер A и изомер B) синтезировали из соединения из контрольного примера 93 (изомер A) и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 6 в примере 85.
[1213]
Соединение из примера 535 синтезировали из соединения из примера 534 (изомер A) в соответствии со схемой, изображенной на фигуре ниже.
[1214]
[Хим. 271]
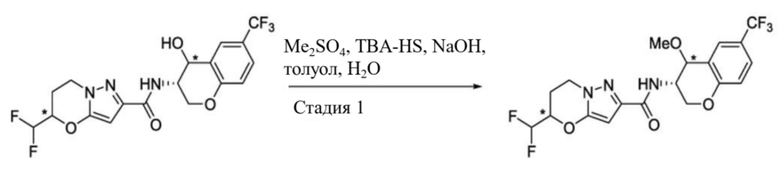
[1215]
Соединение из примера 536 синтезировали из соединения из примера 534 (изомер A) с помощью способа, подобного таковому для примера 114.
[1216]
Соединение из примера 537 синтезировали из соединения, синтезированного на стадии 7 в примере 70, с помощью способа, подобного стадии 3 в примере 100.
[1217]
Соединение из контрольного примера 94 (1-((2,4-дигидроксибутокси)метил)циклопропан-1-карбонитрил) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1218]
[Хим. 272]

[1219]
Соединение из примера 538 синтезировали из соединения из контрольного примера 94 с помощью способа, подобного таковому для примера 85.
[1220]
Соединение из контрольного примера 95 (этил-6-((бензилокси)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоксилат) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1221]
[Хим. 273]

[1222]
Соединение из примера 539 синтезировали из соединения из контрольного примера 95 с помощью способов, подобных таковым, описанным в примере 100 и в контрольном примере 43.
[1223]
Соединение из примера 540 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 34, в примере 169 и в контрольном примере 24.
[1224]
Соединение из примера 541 синтезировали с помощью способов, подобных таковым, описанным в примере 449 и в контрольном примере 24.
[1225]
Соединение из примера 542 синтезировали из соединения из контрольного примера 37 с помощью способа, подобного стадии 3 в примере 100.
[1226]
Соединение из контрольного примера 96 (4-((трет-бутилдифенилсилил)окси)-2-метилбутан-1-ол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1227]
[Хим. 274]
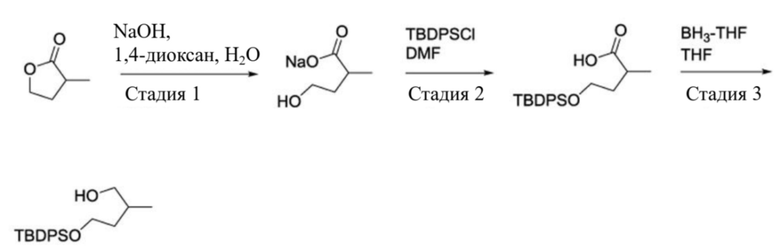
[1228]
Соединение из примера 543 синтезировали из соединения из контрольного примера 96 с помощью способов, подобных таковым, описанным в примере 85 и в контрольном примере 44.
[1229]
Соединение из примера 544 синтезировали из соединения из примера 534 в соответствии со схемой, изображенной на фигуре ниже.
[1230]
[Хим. 275]

[1231]
Соединение из примера 545 синтезировали с помощью способа, подобного таковому для примера 543.
[1232]
Соединение из примера 546 синтезировали из соединения из примера 534 (изомер A) с помощью способа, подобного стадии 1 в контрольном примере 37.
[1233]
Соединения из примера 547 (изомер A и изомер B) синтезировали путем разделения соединения из примера 540.
[1234]
Соединение из контрольного примера 97 (6-(((2,2,2-трифторэтил)амино)метил)-6,7-дигидро-5H-пиразоло[5,1-b][1,3]оксазин-2-карбоновую кислоту) синтезировали из соединения из контрольного примера 95 в соответствии со схемой, изображенной на фигуре ниже.
[1235]
[Хим. 276]

[1236]
Соединение из примера 548 синтезировали из соединения из контрольного примера 95 с помощью способа, подобного стадии 6 в примере 85.
[1237]
Соединение из контрольного примера 98 (гидрохлорид 6-(трифторметил)-3,4-дигидро-2H-пирано[3,2-b]пиридин-3-амина) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1238]
[Хим. 277]
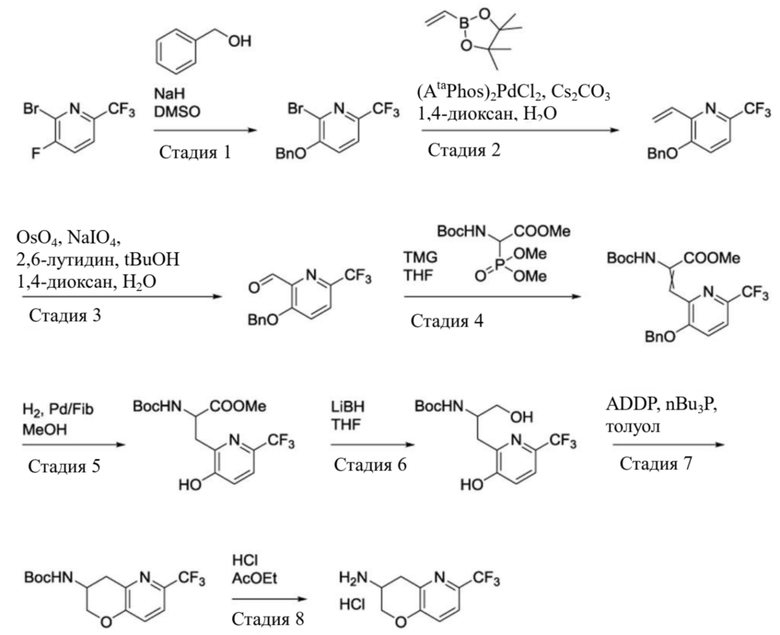
[1239]
Соединение из примера 549 синтезировали с помощью способов, подобных таковым, описанным в примере 90 и в контрольном примере 98.
[1240]
Соединение из примера 550 синтезировали из соединения, синтезированного на стадии 7 в примере 70, и соединения из контрольного примера 98 с помощью способа, подобного стадии 8 в примере 70.
[1241]
Соединение из примера 551 синтезировали из соединения из контрольного примера 93 (изомер A) с помощью способа, подобного стадии 6 в примере 85.
[1242]
Соединения из примера 552 (изомер A и изомер B) получали путем разделения соединения из примера 532.
[1243]
Соединение из примера 553 синтезировали с помощью способов, подобных таковым, описанным в примере 538 и в контрольном примере 43.
[1244]
Соединения из примера 554 (изомер A и изомер B) получали путем разделения соединения из примера 553.
[1245]
Соединение из контрольного примера 99 (6-((2,2,2-трифторэтокси)метил)-5,6,7,8-тетрагидропиразоло[5,1-b][1,3]оксазепин-2-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1246]
[Хим. 278]
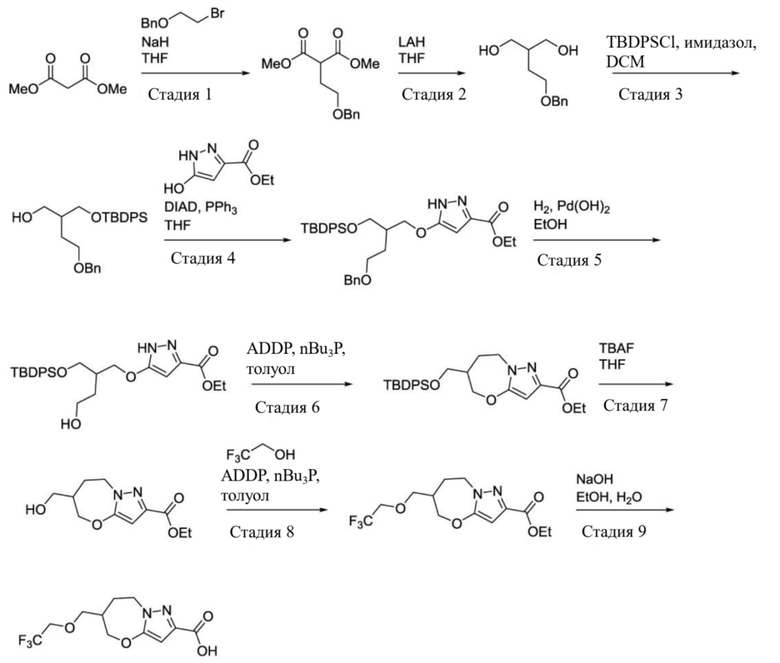
[1247]
Соединение из примера 555 синтезировали из соединения из контрольного примера 99 с помощью способа, подобного стадии 3 в примере 100.
[1248]
Соединение из примера 556 синтезировали из соединения из контрольного примера 99 и из соединения из контрольного примера 43 с помощью способа, подобного стадии 3 в примере 100.
[1249]
Соединение из примера 557 синтезировали из соединения из контрольного примера 99 и из соединения из контрольного примера 48 с помощью способа, подобного стадии 3 в примере 100.
[1250]
Соединение из примера 558 синтезировали из соединения из контрольного примера 33 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 8 в примере 70.
[1251]
Соединение из примера 559 синтезировали из соединения из контрольного примера 33 и соединения из контрольного примера 92 (изомер B) с помощью способа, подобного стадии 8 в примере 70.
[1252]
Соединение из примера 560 синтезировали из соединения из контрольного примера 50 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 8 в примере 70.
[1253]
Соединение из примера 561 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 7 - стадии 8 в примере 70.
[1254]
Соединения из примера 562 получали путем разделения соединения, синтезированного с помощью способов, подобных таковым, описанным на стадии 3 - стадии 5 в контрольном примере 34, в примере 169 и в контрольном примере 24.
[1255]
Соединения из примера 563 (изомер A и изомер B) получали путем разделения соединения из примера 538.
[1256]
Соединение из контрольного примера 100 (2-((тетрагидро-2H-пиран-4-ил)метил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1257]
[Хим. 279]

[1258]
Соединение из примера 564 синтезировали из соединения из контрольного примера 100 и соединения из контрольного примера 48 с помощью способа, подобного стадии 8 в примере 70.
[1259]
Соединение из примера 565 синтезировали из соединения из контрольного примера 100 и соединения из контрольного примера 24 с помощью способа, подобного стадии 8 в примере 70.
[1260]
Соединение из контрольного примера 101 ((R)-6-йодхроман-3-амин) синтезировали из соединения, синтезированного на стадии 1 в контрольном примере 1, в соответствии со схемой, изображенной на фигуре ниже.
[1261]
[Хим. 280]

[1262]
Соединение из примера 566 синтезировали из соединения из контрольного примера 93 (изомер A) и соединения из контрольного примера 101 с помощью способа, подобного стадии 8 в примере 70.
[1263]
Соединение из примера 567 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 34, в примере 85 и в контрольном примере 48.
[1264]
Соединение из примера 568 синтезировали из соединения из примера 534 (изомер B) с помощью способа, подобного таковому для примера 535.
[1265]
Соединение из примера 569 синтезировали из соединения, синтезированного на стадии 3 в примере 187, и соединения из контрольного примера 92 (изомер A) с помощью способов, подобных таковым, описанным на стадии 8 в примере 70 и в примере 535.
[1266]
Соединение из примера 570 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 92 (изомер A) с помощью способов, подобных таковым, описанным на стадии 7 - стадии 8 в примере 70 и в примере 535.
[1267]
Соединение из примера 571 синтезировали из соединения из контрольного примера 33 с помощью способа, подобного стадии 8 в примере 70.
[1268]
Соединения из примера 572 (изомер A и изомер B) получали путем разделения соединения из примера 555.
[1269]
Соединение из примера 573 синтезировали с помощью способа, подобного таковому для примера 70.
[1270]
Соединение из примера 574 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 4 с помощью способа, подобного стадии 5 - стадии 6 в примере 85.
[1271]
Соединения из примера 575 (изомер A и изомер B) получали путем разделения соединения из примера 559.
[1272]
Соединения из примера 576 (изомер A и изомер B) получали путем разделения соединения из примера 560.
[1273]
Соединения из примера 577 (изомер A и изомер B) получали путем разделения соединения из примера 565.
[1274]
Соединение из контрольного примера 102 (2-((циклопропилметокси)метил)-2,3-дигидроимидазо[2,1-b]оксазол-6-карбоновую кислоту) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1275]
[Хим. 281]

[1276]
Соединение из примера 578 синтезировали из соединения из контрольного примера 102 и соединения из контрольного примера 1 с помощью способа, подобного стадии 8 в примере 70.
[1277]
Соединения из примера 579 (изомер A и изомер B) синтезировали из соединения из контрольного примера 93 (изомер A) и контрольного примера 92 (изомер A) с помощью способов, подобных таковым, описанным на стадии 8 в примере 70 и в примере 114.
[1278]
Соединение из контрольного примера 103 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 1 в примере 259, с помощью способа, подобного таковому для контрольного примера 91.
[1279]
[Хим. 282]
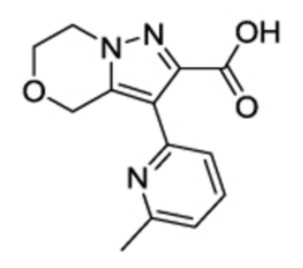
[1280]
Соединение из примера 580 синтезировали из соединения из контрольного примера 103 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 3 в примере 100.
[1281]
Соединение из примера 581 синтезировали из соединения из контрольного примера 90 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 3 в примере 100.
[1282]
Соединение из примера 582 синтезировали из соединения, синтезированного на стадии 8 в примере 252, в соответствии со схемой, изображенной на фигуре ниже.
[1283]
[Хим. 283]
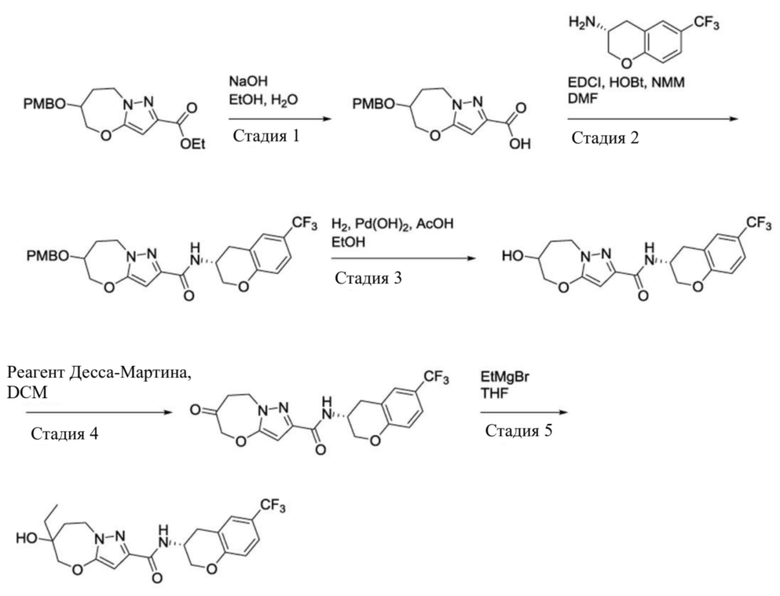
[1284]
Соединение из примера 583 синтезировали с помощью способов, подобных таковым, описанным на стадии 3 - стадии 5 в контрольном примере 34, в примере 85 и в контрольном примере 43.
[1285]
Соединение из примера 584 синтезировали с помощью способов, подобных таковым, описанным на стадии 3 - стадии 5 в контрольном примере 34, в примере 85 и в контрольном примере 1.
[1286]
Соединение из примера 585 синтезировали с помощью способов, подобных таковым, описанным на стадии 3 - стадии 5 в контрольном примере 34, в примере 85 и в контрольном примере 24.
[1287]
Соединение из примера 586 синтезировали с помощью способов, подобных таковым, описанным на стадии 3 - стадии 5 в контрольном примере 34, в примере 85 и в контрольном примере 48.
[1288]
Соединение из примера 587 синтезировали с применением соединения из контрольного примера 92 (изомер A) с помощью способа, подобного таковому, описанному в примере 199.
[1289]
Соединение из примера 588 синтезировали из соединения из контрольного примера 55 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 8 в примере 70.
[1290]
Соединение из примера 589 синтезировали из соединения из контрольного примера 55 и соединения из контрольного примера 92 (изомер B) с помощью способа, подобного стадии 8 в примере 70.
[1291]
Соединения из примера 590 (изомер A и изомер B) получали путем разделения соединения из примера 564.
[1292]
Соединение из контрольного примера 104 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 7 в примере 245 с помощью способов, подобных таковым, описанным в примере 114 и стадии 7 в примере 70.
[1293]
[Хим. 284]

[1294]
Соединение из примера 591 синтезировали из соединения из контрольного примера 104 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 8 в примере 70.
[1295]
Соединение из примера 592 синтезировали из соединения из контрольного примера 104 и соединения из контрольного примера 92 (изомер B) с помощью способа, подобного стадии 8 в примере 70.
[1296]
Соединение из примера 593 синтезировали из соединения из контрольного примера 92 (изомер A) с помощью способа, подобного таковому для примера 268.
[1297]
Соединение из примера 594 синтезировали из соединения из контрольного примера 92 (изомер A) с помощью способов, подобных таковым, описанным в примере 268 и в примере 261.
[1298]
Соединение из примера 595 синтезировали из соединения, синтезированного на стадии 6 в примере 201, и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 8 в примере 70.
[1299]
Соединение из примера 596 синтезировали из соединения, синтезированного на стадии 6 в примере 201, и соединения из контрольного примера 92 (изомер B) с помощью способа, подобного стадии 8 в примере 70.
[1300]
Соединения из примера 597 (изомер A и изомер B) получали путем разделения соединения из примера 569.
[1301]
Соединения из примера 598 (изомер A и изомер B) получали путем разделения соединения из примера 570.
[1302]
Соединение из примера 599 синтезировали с применением соединения из контрольного примера 92 (изомер B) с помощью способа, подобного таковому для примера 90.
[1303]
Соединения из примера 600 (изомер A и изомер B) получали путем разделения соединения из примера 588.
[1304]
Соединения из примера 601 (изомер A и изомер B) получали путем разделения соединения из примера 557.
[1305]
Соединения из примера 602 (изомер A и изомер B) получали путем разделения соединения, синтезированного из соединения из контрольного примера 99 и контрольного примера 44, с помощью способа, подобного стадии 3 в примере 100.
[1306]
Соединения из примера 603 (изомер A и изомер B) получали путем разделения соединения из примера 591.
[1307]
Соединение из контрольного примера 105 синтезировали из соединения, синтезированного на стадии 2 в примере 245, в соответствии со схемой, изображенной на фигуре ниже.
[1308]
[Хим. 285]

[1309]
Соединение из контрольного примера 106 (показано на фигуре ниже) синтезировали из соединения из контрольного примера 105 с помощью способа, подобного таковому, описанному на стадии 5 - стадии 8 в примере 245.
[1310]
[Хим. 286]

[1311]
Соединения из примера 604 (изомер A и изомер B) получали путем разделения соединения, синтезированного с применением соединения из контрольного примера 106 и контрольного примера 24, с помощью способа, подобного стадии 8 в примере 70.
[1312]
Соединение из примера 605 синтезировали из соединения из контрольного примера 100 и контрольного примера 44 с помощью способа, подобного стадии 8 в примере 70.
[1313]
Соединение из контрольного примера 107 (показано на фигуре ниже) синтезировали с помощью способов, подобных таковым, описанным на стадии 3 - стадии 5 в контрольном примере 34 и на стадии 1 - стадии 5 в примере 85.
[1314]
[Хим. 287]
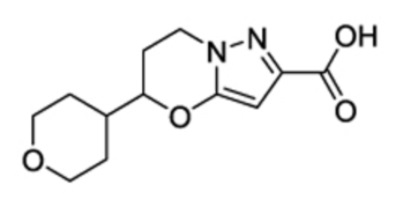
[1315]
Соединение из примера 606 синтезировали из соединения из контрольного примера 107 и соединения из контрольного примера 44 с помощью способа, подобного стадии 8 в примере 70.
[1316]
Соединение из примера 607 синтезировали с применением соединения из контрольного примера 106 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1317]
Соединения из примера 608 (изомер A и изомер B) получали путем разделения соединения из примера 607.
[1318]
Соединение из примера 609 синтезировали с применением соединения из контрольного примера 106 и соединения из контрольного примера 92 (изомер B) с помощью способа, подобного стадии 8 в примере 70.
[1319]
Соединения из примера 610 (изомер A и изомер B) получали путем разделения соединения из примера 609.
[1320]
Соединение из контрольного примера 108 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому для соединения из контрольного примера 107.
[1321]
[Хим. 288]

[1322]
Соединение из примера 611 синтезировали из соединения из контрольного примера 108 и соединения из контрольного примера 1 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1323]
Соединение из примера 612 синтезировали из соединения из контрольного примера 108 и соединения из контрольного примера 43 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1324]
Соединение из примера 613 синтезировали из соединения из контрольного примера 108 и соединения из контрольного примера 92 (изомер A) в соответствии со схемой, изображенной на фигуре ниже.
[1325]
[Хим. 289]

[1326]
Соединение из примера 614 синтезировали из соединения из контрольного примера 108 и контрольного примера 92 (изомер B) с помощью способа, подобного таковому для примера 613.
[1327]
Соединения из примера 615 (изомер A и изомер B) получали путем разделения соединения из примера 606.
[1328]
Соединения из примера 616 (изомер A и изомер B) получали путем разделения соединения из примера 592.
[1329]
Соединение из контрольного примера 109 ((3S)-3-амино-4-фторхроман-6-карбонитрил) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1330]
[Хим. 290]

[1331]
Соединения из примера 617 (изомер A, изомер B, изомер C и изомер D) получали путем разделения соединения, синтезированного из соединения из контрольного примера 33 и соединения из контрольного примера 109 с помощью способа, подобного стадии 8 в примере 70.
[1332]
Соединение из контрольного примера 110 (6-бром-2-((циклопропилметокси)метил)-2-метил-2,3-дигидропиразоло[5,1-b]оксазол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1333]
[Хим. 291]
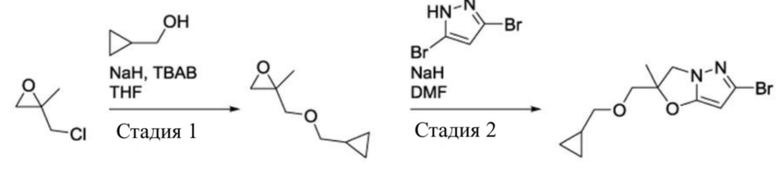
[1334]
Соединение из контрольного примера 111 (показано на фигуре ниже) синтезировали из соединения из контрольного примера 110 с помощью способа, подобного таковому, описанному на стадии 8 - стадии 10 в контрольном примере 79.
[1335]
[Хим. 292]

[1336]
Соединение из примера 618 синтезировали из соединения из контрольного примера 111 и соединения из контрольного примера 24 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1337]
Соединение из примера 619 синтезировали из соединения из контрольного примера 111 и соединения из контрольного примера 48 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1338]
Соединение из контрольного примера 112 (показано на фигуре ниже) синтезировали с помощью способов, подобных таковым, описанным на стадии 3 - стадии 5 в контрольном примере 34 и на стадии 1 - стадии 5 в примере 85.
[1339]
[Хим. 293]
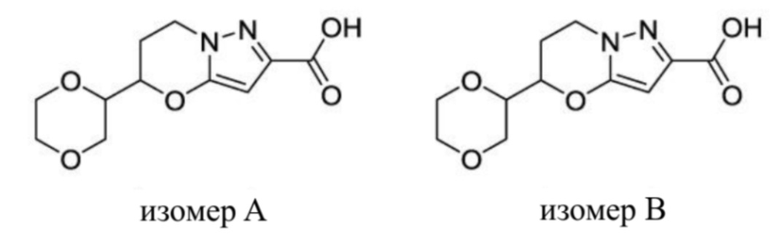
[1340]
Соединение из примера 620 синтезировали из соединения из контрольного примера 112 (изомеры A) и соединения из контрольного примера 43 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1341]
Соединение из примера 621 синтезировали из соединения из примера 588 с помощью способа, подобного таковому, описанному в примере 535.
[1342]
Соединения из примера 622 (изомер A и изомер B) получали путем разделения соединения из примера 605.
[1343]
Соединение из контрольного примера 113 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому, описанному в контрольном примере 100.
[1344]
[Хим. 294]

[1345]
Соединение из примера 623 синтезировали из соединения из контрольного примера 113 и соединения из контрольного примера 24 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1346]
Соединение из контрольного примера 114 (4-((трет-бутилдифенилсилил)окси)-1-(2,2-дифторэтокси)бутан-2-ол) синтезировали в соответствии со схемой, изображенной на фигуре ниже.
[1347]
[Хим. 295]

[1348]
Соединение из контрольного примера 115 (показано на фигуре ниже) синтезировали из соединения из контрольного примера 114 с помощью способов, подобных таковым, описанным на стадии 2 - стадии 5 в примере 85.
[1349]
[Хим. 296]

[1350]
Соединение из примера 624 синтезировали из соединения из контрольного примера 115 и соединения из контрольного примера 92 (изомер B) с помощью способов, подобных таковым, описанным на стадии 8 в примере 70 и на стадии 2 в примере 613.
[1351]
Соединение из примера 625 синтезировали из соединения из контрольного примера 70 и соединения из контрольного примера 92 (изомер A) с помощью способов, подобных таковым, описанным на стадии 7 - стадии 8 в примере 70 и на стадии 2 в примере 613.
[1352]
Соединение из контрольного примера 116 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому, описанному в контрольном примере 4.
[1353]
[Хим. 297]

[1354]
Соединение из примера 626 синтезировали из соединения, синтезированного на стадии 5 в примере 169, и соединения из контрольного примера 116 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1355]
Соединение из примера 627 синтезировали из соединения из контрольного примера 36 и соединения из контрольного примера 116 с помощью способа, подобного таковому, описанному на стадии 7 - стадии 8 в примере 70.
[1356]
Соединение из примера 628 синтезировали из соединения из контрольного примера 104 и соединения из контрольного примера 116 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1357]
Соединение из примера 629 синтезировали из соединения из контрольного примера 55 и соединения из контрольного примера 116 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1358]
Соединение из примера 630 синтезировали из соединения из контрольного примера 108 и соединения из контрольного примера 44 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1359]
Соединение из примера 631 синтезировали из соединения из контрольного примера 112 (изомеры A) и соединения из контрольного примера 44 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1360]
Соединение из примера 632 синтезировали из соединения из контрольного примера 89 с помощью способов, подобных таковым, описанным на стадии 2 - стадии 6 в примере 85 и в контрольном примере 44.
[1361]
Соединение из примера 633 синтезировали из соединения из контрольного примера 89 с помощью способов, подобных таковым, описанным на стадии 2 - стадии 6 в примере 85 и в контрольном примере 48.
[1362]
Соединение из примера 634 синтезировали из соединения из контрольного примера 99 и соединения из контрольного примера 92 (изомер A) с помощью способов, подобных таковым, описанным на стадии 8 в примере 70 и на стадии 2 в примере 613.
[1363]
Соединение из примера 635 синтезировали из соединения из контрольного примера 115 и контрольного примера 44 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1364]
Соединения из примера 636 (изомер A и изомер B) получали путем разделения соединения из примера 595.
[1365]
Соединение из контрольного примера 117 (показано на фигуре ниже) синтезировали с применением соединения из контрольного примера 92 (изомер A) с помощью способа, подобного таковому, описанному на стадии 1 - стадии 2 в примере 268.
[1366]
[Хим. 298]

[1367]
Соединение из примера 637 синтезировали из соединения из контрольного примера 117 с помощью способов, подобных таковым, описанным на стадии 1 в примере 261 и на стадии 2 в примере 613.
[1368]
Соединение из примера 638 синтезировали из соединения из контрольного примера 112 (изомеры B) и соединения из контрольного примера 44 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1369]
Соединение из примера 639 синтезировали из соединения, синтезированного на стадии 6 в примере 201, и соединения из контрольного примера 116 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1370]
Соединение из примера 640 синтезировали из соединения из контрольного примера 106 и соединения из контрольного примера 116 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1371]
Соединения из примера 641 (изомер A и изомер B) получали путем разделения соединения из примера 587.
[1372]
Соединение из примера 642 синтезировали из соединения из контрольного примера 117 с помощью способов, подобных таковым, описанным в контрольном примере 69 и стадии 2 в примере 613.
[1373]
Соединение из примера 643 синтезировали из соединения из контрольного примера 117 с помощью способа, подобного таковому для контрольного примера 637.
[1374]
Соединение из контрольного примера 118 (показано на фигуре ниже) синтезировали с помощью способа, подобного стадии 1 в примере 267.
[1375]
[Хим. 299]
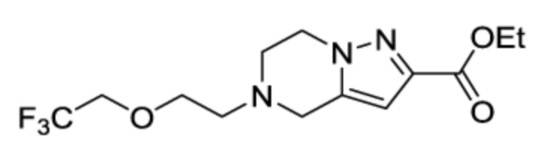
[1376]
Соединение из примера 644 синтезировали из соединения из контрольного примера 118 и соединения из контрольного примера 43 с помощью способа, подобного таковому, описанному на стадии 7 - стадии 8 в примере 70.
[1377]
Соединение из примера 645 синтезировали из соединения из контрольного примера 118 и соединения из контрольного примера 92 (изомер B) с помощью способов, подобных таковым, описанным на стадии 2 - стадии 3 в примере 100 и на стадии 2 в примере 613.
[1378]
Соединение из контрольного примера 119 (показано на фигуре ниже) синтезировали с применением соединения из контрольного примера 92 (изомер B) с помощью способов, подобных таковому, описанному на стадии 1 - стадии 2 в примере 268.
[1379]
[Хим. 300]

[1380]
Соединение из примера 646 синтезировали из соединения из контрольного примера 119 с помощью способов, подобных таковым, описанным в контрольном примере 69 и стадии 2 в примере 613.
[1381]
Соединение из примера 647 синтезировали из соединения из контрольного примера 119 с помощью способов, подобных таковым, описанным на стадии 1 в примере 261 и на стадии 2 в примере 613.
[1382]
Соединение из примера 648 синтезировали из соединения, синтезированного на стадии 5 в примере 169, и соединения из контрольного примера 109 с помощью способа, подобного таковому, описанному на стадии 8 в примере 70.
[1383]
Соединение из примера 649 синтезировали из соединения из контрольного примера 89 с помощью способов, подобных таковым, описанным на стадии 2 - стадии 6 в примере 85 и в контрольном примере 109.
[1384]
Соединение из примера 650 синтезировали из соединения, синтезированного на стадии 6 в примере 201, и соединения из контрольного примера 109 с помощью способа, подобного стадии 8 в примере 70.
[1385]
Соединение из контрольного примера 120 (показано на фигуре ниже) синтезировали с помощью способа, подобного таковому, описанному в соединении из контрольного примера 107.
[1386]
[Хим. 301]
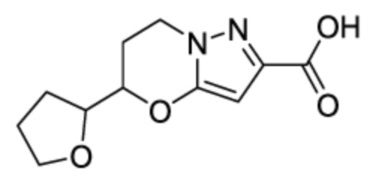
[1387]
Соединение из примера 651 синтезировали из соединения из контрольного примера 120 и соединения из контрольного примера 44 с помощью способа, подобного стадии 8 в примере 70.
[1388]
Соединение из примера 652 синтезировали из соединения из контрольного примера 117 с помощью способа, подобного таковому для контрольного примера 69.
[1389]
Соединение из примера 653 синтезировали с помощью способов, подобных таковым, описанным в примере 268 и в контрольном примере 43.
[1390]
Соединение из примера 654 синтезировали из соединения из примера 652 с помощью способа, подобного таковому, описанному на стадии 2 в примере 613.
[1391]
Соединение из примера 655 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 82, в примере 159 и в контрольном примере 44.
[1392]
Соединение из контрольного примера 121 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 3 в контрольном примере 92 с помощью способов, подобных таковым, описанным на стадии 1 и стадии 3 в контрольном примере 1 и на стадии 2 в примере 613.
[1393]
[Хим. 302]

[1394]
Соединение из примера 656 синтезировали из соединения, синтезированного на стадии 8 в примере 252, и соединения из контрольного примера 121 в соответствии со схемой, изображенной на фигуре ниже.
[1395]
[Хим. 303]

[1396]
Соединение из контрольного примера 122 (2-((2-(2,2,2-трифторэтокси)этокси)метил)-2,3-дигидропиразоло[5,1-b]оксазол-6-карбоновую кислоту) синтезировали из соединения, синтезированного на стадии 1 в примере 187, в соответствии со схемой, изображенной на фигуре ниже.
[1397]
[Хим. 304]

[1398]
Соединение из примера 657 синтезировали из соединения из контрольного примера 122 и соединения из контрольного примера 43 с помощью способа, подобного стадии 3 в примере 100.
[1399]
Соединение из примера 658 синтезировали из соединения из контрольного примера 122 и соединения из контрольного примера 1 с помощью способа, подобного стадии 3 в примере 100.
[1400]
Соединение из примера 659 синтезировали из соединения из контрольного примера 122 и соединения из контрольного примера 24 с помощью способа, подобного стадии 3 в примере 100.
[1401]
Соединение из примера 660 синтезировали из соединения из контрольного примера 122 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 3 в примере 100.
[1402]
Соединение из примера 661 синтезировали из соединения из контрольного примера 122 и соединения из контрольного примера 44 с помощью способа, подобного стадии 3 в примере 100.
[1403]
Соединение из контрольного примера 123 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 1 в примере 100, с помощью способа, подобного таковому для контрольного примера 122.
[1404]
[Хим. 305]

[1405]
Соединение из примера 662 синтезировали из соединения из контрольного примера 123 и соединения из контрольного примера 1 с помощью способа, подобного стадии 8 в примере 70.
[1406]
Соединение из примера 663 синтезировали из соединения из контрольного примера 123 и соединения из контрольного примера 43 с помощью способа, подобного стадии 8 в примере 70.
[1407]
Соединение из примера 664 синтезировали из соединения из контрольного примера 123 и соединения из контрольного примера 24 с помощью способа, подобного стадии 8 в примере 70.
[1408]
Соединение из примера 665 синтезировали из соединения из контрольного примера 123 и соединения из контрольного примера 92 (изомер B) с помощью способов, подобных таковым, описанным на стадии 8 в примере 70 и на стадии 2 в примере 613.
[1409]
Соединение из примера 666 синтезировали с помощью способов, подобных таковым, описанным в примере 268 и в контрольном примере 43.
[1410]
Соединение из примера 667 синтезировали из соединения из контрольного примера 118 и соединения из контрольного примера 44 с помощью способов, подобных таковым, описанным на стадии 7 - стадии 8 в примере 70.
[1411]
Соединение из примера 668 синтезировали из соединения из контрольного примера 120 и соединения из контрольного примера 48 с помощью способа, подобного стадии 8 в примере 70.
[1412]
Соединение из примера 669 синтезировали с помощью способов, подобных таковым, описанным в примере 268 и в контрольном примере 43.
[1413]
Соединение из примера 670 синтезировали из соединения из контрольного примера 119 с помощью способов, подобных таковым, описанным на стадии 1 в примере 261 и на стадии 2 в примере 613.
[1414]
Соединение из примера 671 синтезировали из соединения из контрольного примера 119 с помощью способов, подобных таковым, описанным в контрольном примере 69 и стадии 2 в примере 613.
[1415]
Соединение из примера 672 синтезировали из соединения из контрольного примера 119 с помощью способов, подобных таковым, описанным в контрольном примере 69 и стадии 2 в примере 613.
[1416]
Соединение из примера 673 синтезировали из соединения из контрольного примера 119 с помощью способов, подобных таковым, описанным в контрольном примере 69 и стадии 2 в примере 613.
[1417]
Соединение из примера 674 синтезировали с помощью способов, подобных таковым, описанным в контрольном примере 82, в примере 159 и в контрольном примере 48.
[1418]
Соединение из примера 675 синтезировали из соединения из контрольного примера 122 и соединения из контрольного примера 92 (изомер B) с помощью способа, подобного стадии 3 в примере 100.
[1419]
Соединение из примера 676 синтезировали из соединения из примера 660 с помощью способа, подобного таковому, описанному на стадии 2 в примере 613.
[1420]
Соединение из примера 677 синтезировали из соединения из контрольного примера 117 с помощью способа, подобного таковому для контрольного примера 69.
[1421]
Соединение из примера 678 синтезировали из соединения из контрольного примера 117 и соединения из примера 119 с помощью способов, подобных таковым, описанным в контрольном примере 69 и стадии 2 в примере 613.
[1422]
Соединение из примера 679 синтезировали из соединения, синтезированного на стадии 6 в примере 254, и соединения из контрольного примера 92 (изомер B) с помощью способов, подобных таковым, описанным на стадии 8 в примере 70 и на стадии 2 в примере 613.
[1423]
Соединение из контрольного примера 124 (показано на фигуре ниже) синтезировали из соединения, синтезированного на стадии 8 в примере 252, с помощью способа, подобного таковому для контрольного примера 122.
[1424]
[Хим. 306]
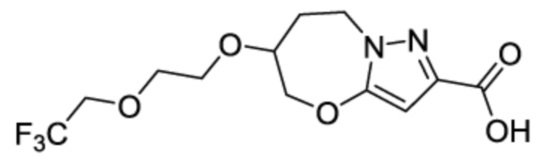
[1425]
Соединение из примера 680 синтезировали из соединения из контрольного примера 124 и соединения из контрольного примера 43 с помощью способа, подобного стадии 8 в примере 70.
[1426]
Соединение из примера 681 синтезировали из соединения из контрольного примера 124 и соединения из контрольного примера 92 (изомер A) с помощью способа, подобного стадии 8 в примере 70.
[1427]
Соединение из примера 682 синтезировали из соединения из контрольного примера 124 и соединения из контрольного примера 1 с помощью способа, подобного стадии 8 в примере 70.
[1428]
Соединение из примера 683 синтезировали из соединения из контрольного примера 99 и соединения из контрольного примера 92 (изомер A) с помощью способов, подобных таковым, описанным на стадии 3 в примере 100 и на стадии 2 в примере 613.
[1429]
В таблицах ниже показаны данные химических структур и инструментального анализа для соединений, синтезированных в примере 291 - примере 683.
[1430]
[Таблица 42]

442 [M+H]+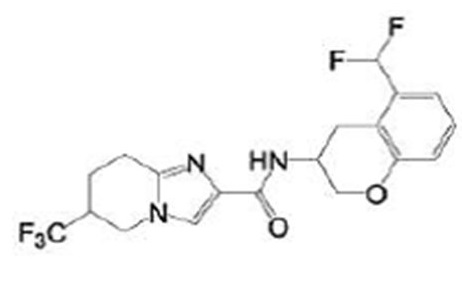
416 [M+H]+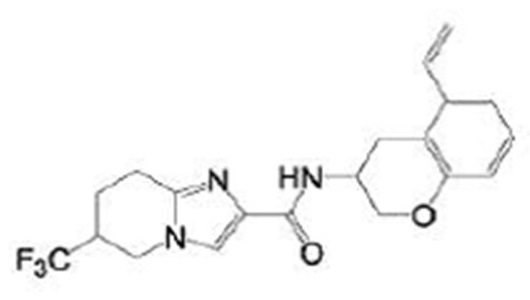
392 [M+H]+
391 [M+H]+
394 [M+H]+
424 [M+H]+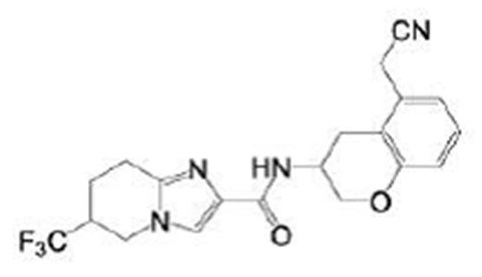
405 [M+H]+
534 [M+H]+
442 [M+H]+
[1431]
[Таблица 43]

391 [M+H]+
424 [M+H]+
392 [M+H]+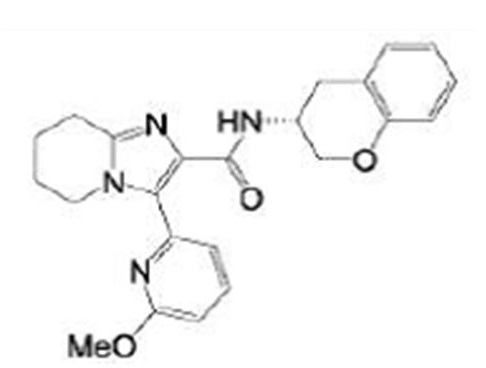
405 [M+H]+
472 [M+H]+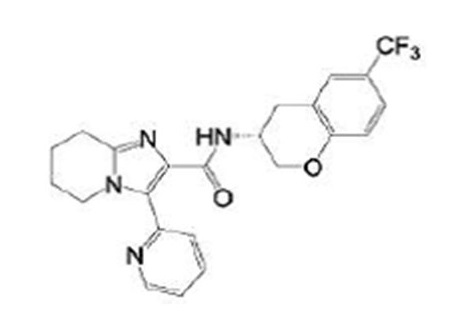
443 [M+H]+
487 [M+H]+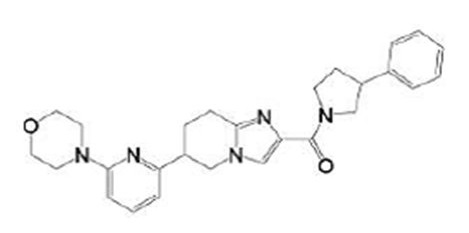
458 [M+H]+
416 [M+H]+
[1432]
[Таблица 44]
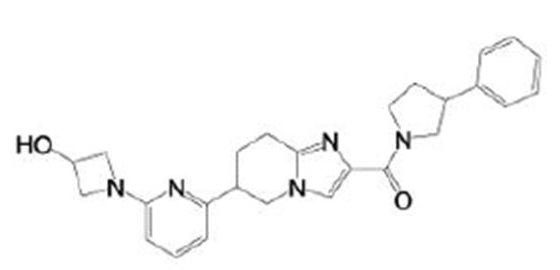
444 [M+H]+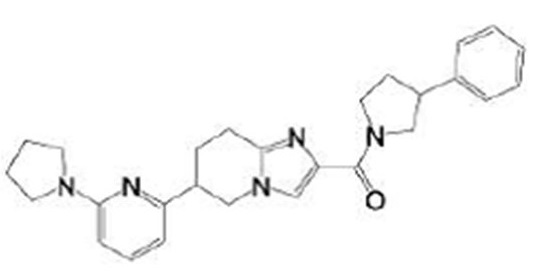
442 [M+H]+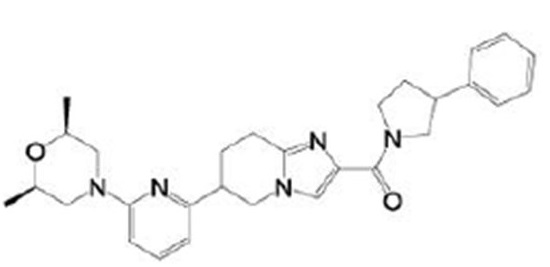
486 [M+H]+
486 [M+H]+
445 [M+H]+
443 [M+H]+
441 [M+H]+
471 [M+H]+
431 [M+H]+
[1433]
[Таблица 45]
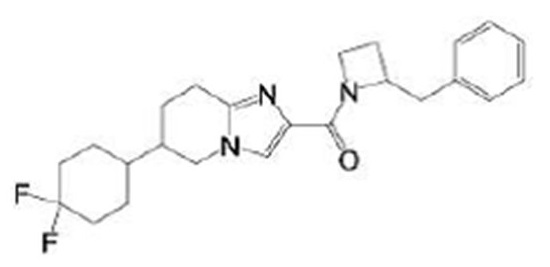
414 [M+H]+
386 [M+H]+
386 [M+H]+
426 [M+H]+
467 [M+H]+
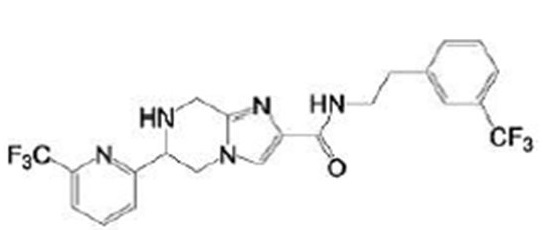
484 [M+H]+
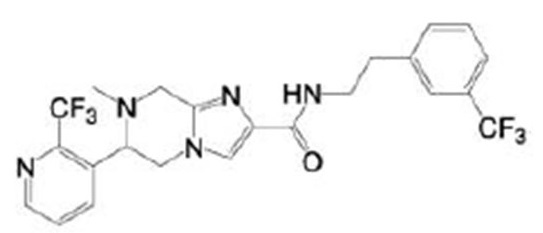
498 [M+H]+
[1434]
[Таблица 46]



439 [M+H]+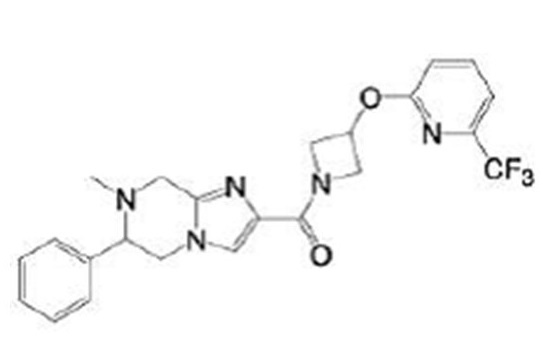
458 [M+H]+
465 [M+H]+
443 [M+H]+
516 [M+H]+
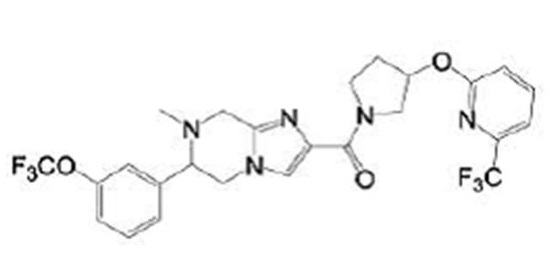
556 [M+H]+
[1435]
[Таблица 47]
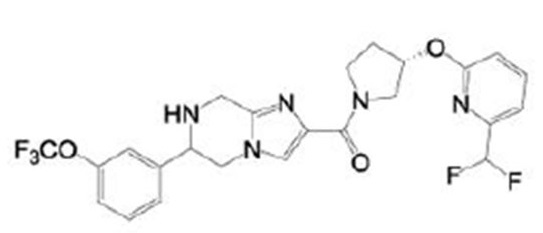
524 [M+H]+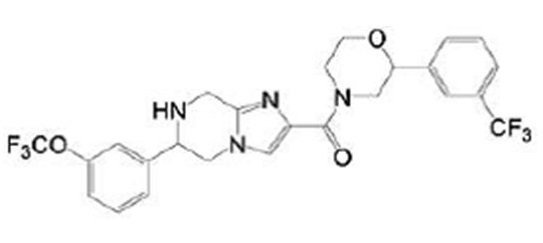
541 [M+H]+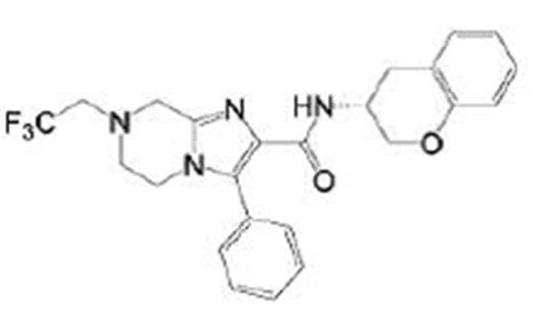
457 [M+H]+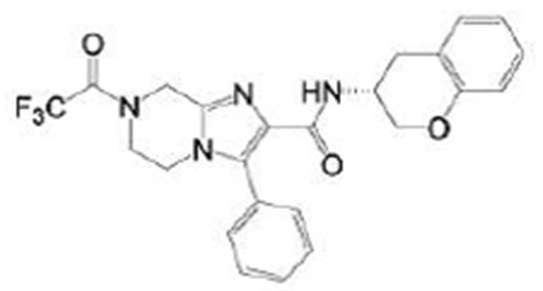
471 [M+H]+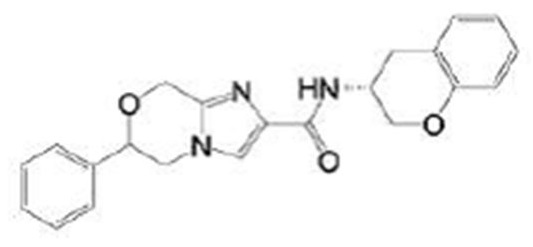

436 [M+H]+
417 [M+H]+
459 [M+H]+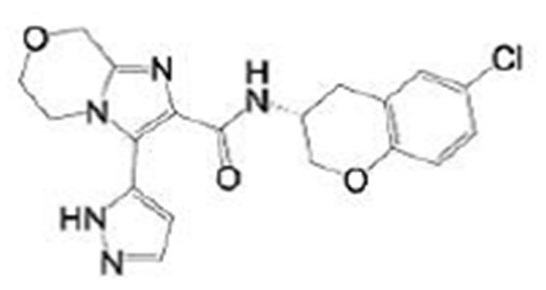
400 [M+H]+
[1436]
[Таблица 48]
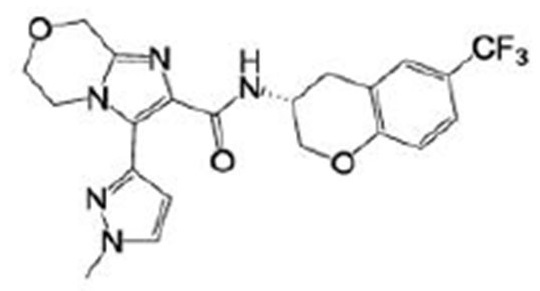
448 [M+H]+
543 [M+H]+
374 [M+H]+
439 [M+H]+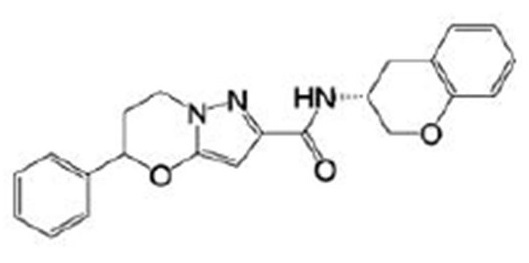
376 [M+H]+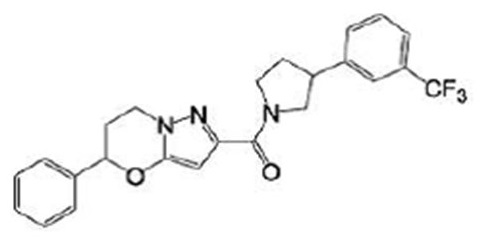
442 [M+H]+
406 [M+H]+
394 [M+H]+
454, 456 [M+H]+
[1437]
[Таблица 49]

412 [M+H]+
410 [M+H]+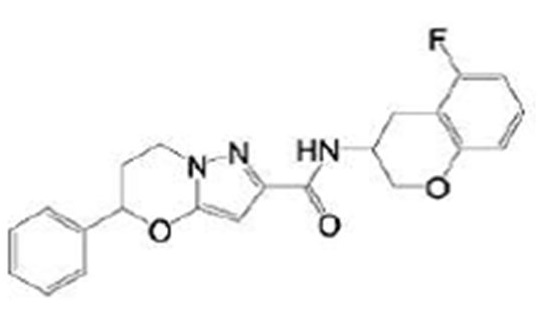
394 [M+H]+
472 [M+H]+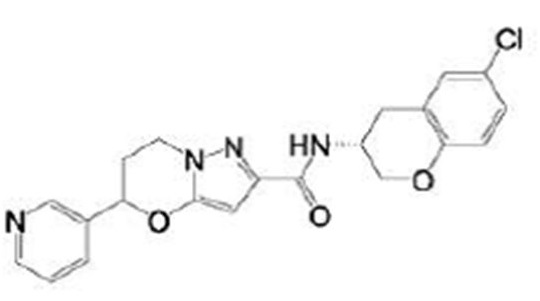
411 [M+H]+
419 [M+H]+
419 [M+H]+
438 [M+H]+
479 [M+H]+
[1438]
[Таблица 50]

445 [M+H]+
419 [M+H]+
466 [M+H]+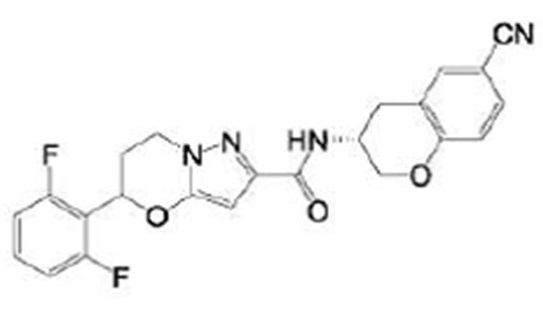
437 [M+H]+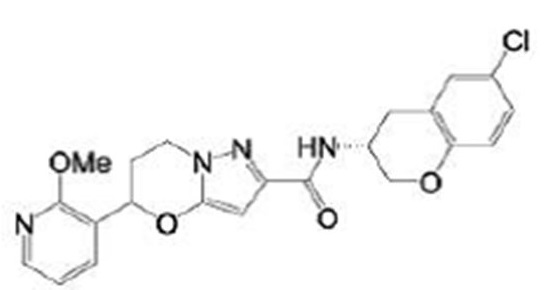
441 [M+H]+
493 [M+H]+
495 [M+H]+
509 [M+H]+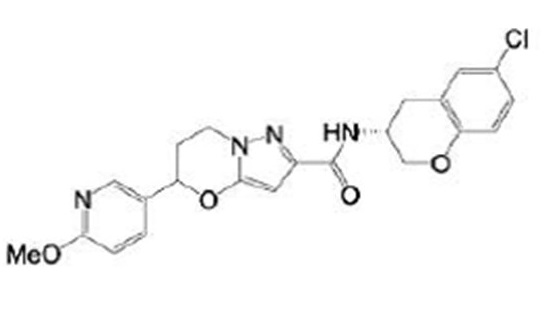
441 [M+H]+
[1439]
[Таблица 51]

446 [M+H]+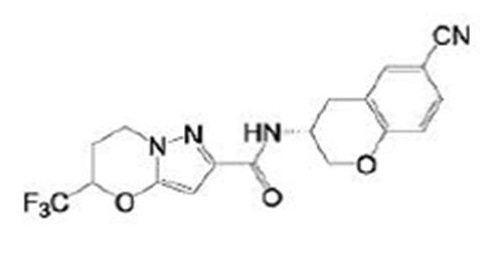
393 [M+H]+
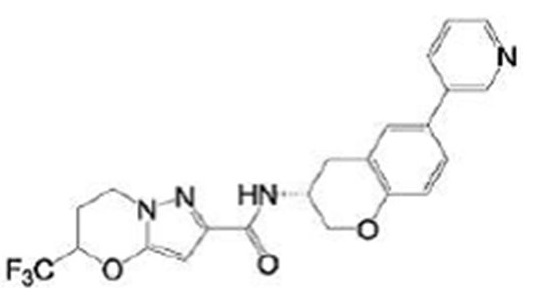
445 [M+H]+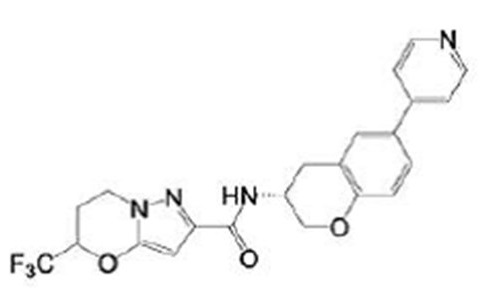
445 [M+H]+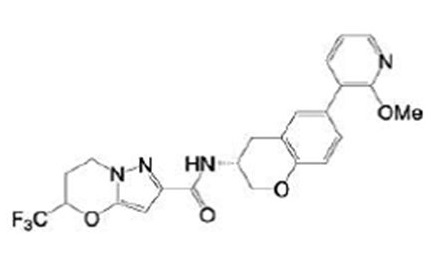
475 [M+H]+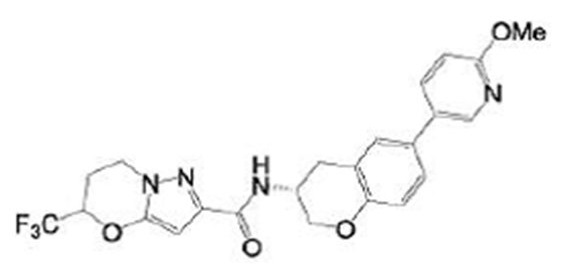
475 [M+H]+
346 [M+H]+
501 [M+H]+
[1440]
[Таблица 52]

366 [M+H]+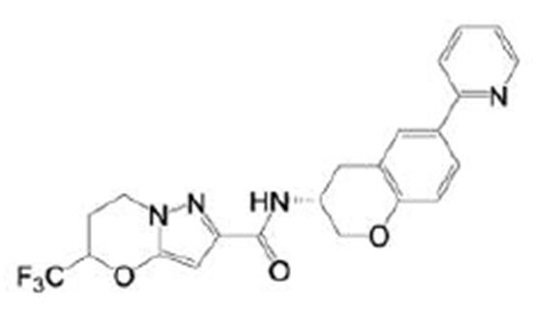
445 [M+H]+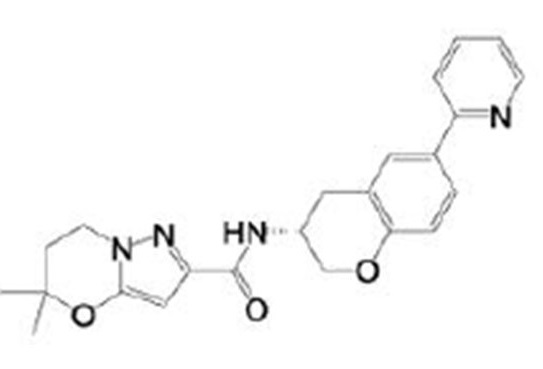
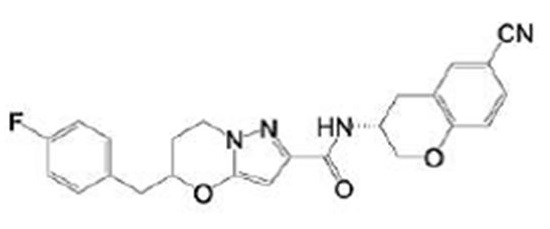
433 [M+H]+
384 [M+H]+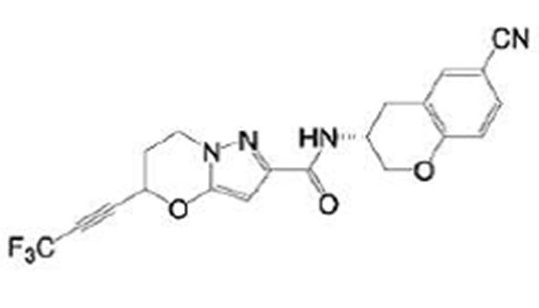
417 [M+H]+
374 [M+H]+

376 [M+H]+
[1441]
[Таблица 53]
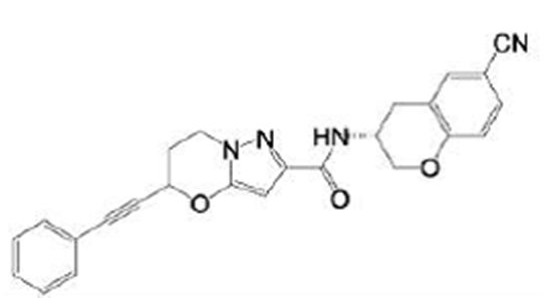
425 [M+H]+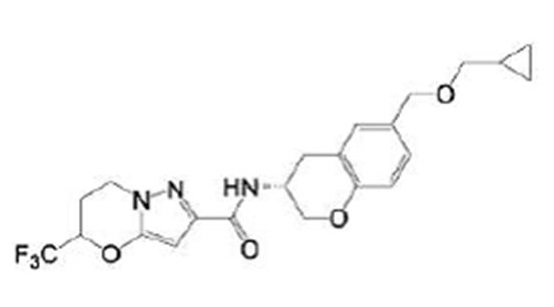
452 [M+H]+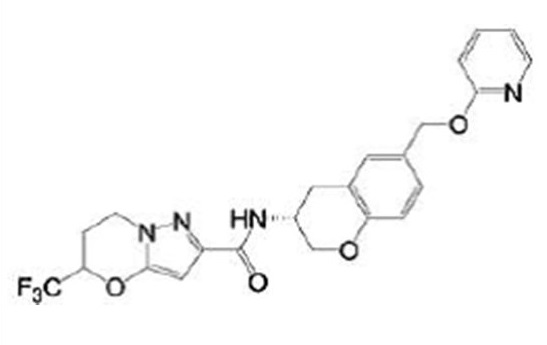
475 [M+H]+
367 [M+H]+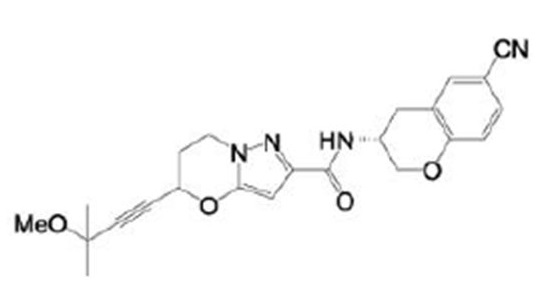
421 [M+H]+
432 [M+H]+
394 [M+H]+
494 [M+H]+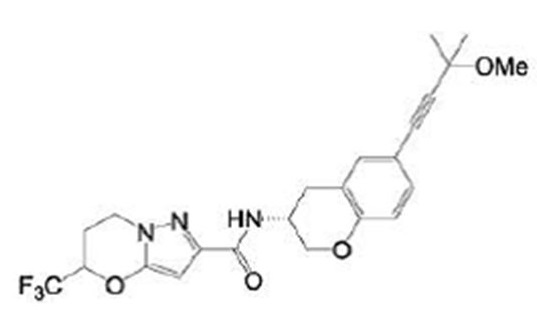
[1442]
[Таблица 54]

452 [M+H]+
468 [M+H]+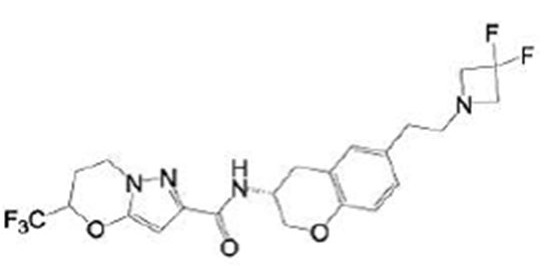
487 [M+H]+
432 [M+H]+
440 [M+H]+
398 [M+H]+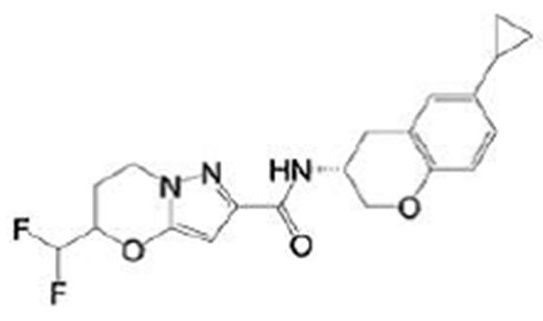
390 [M+H]+
398 [M+H]+
398 [M+H]+
[1443]
[Таблица 55]

398 [M+H]+
410 [M+H]+
423 [M+H]+
432 [M+H]+
487 [M+H]+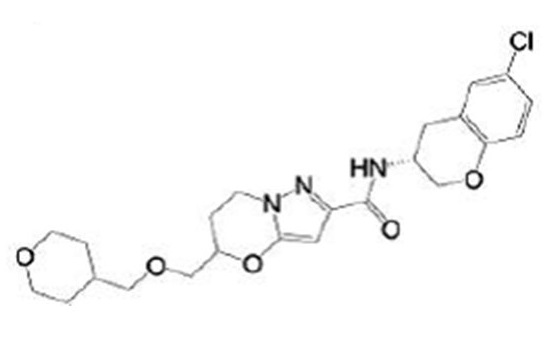
462 [M+H]+
547 [M+H]+
461 [M+H]+
404 [M+H]+
[1444]
[Таблица 56]
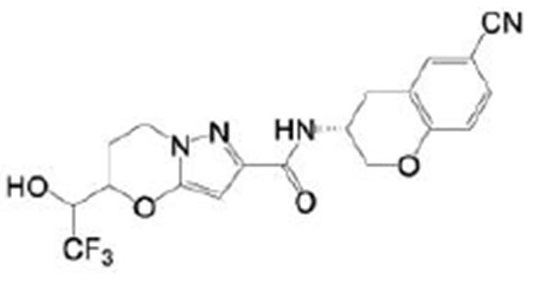
423 [M+H]+
451 [M+H]+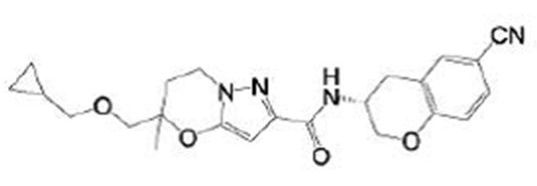
423 [M+H]+
432 [M+H]+
506 [M+H]+
453 [M+H]+
453 [M+H]+
453 [M+H]+
462 [M+H]+
[1445]
[Таблица 57]

464 [M+H]+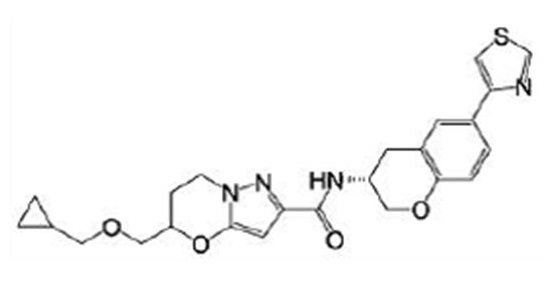
467 [M+H]+
467 [M+H]+
465 [M+H]+
532 [M+H]+
476 [M+H]+
480 [M+H]+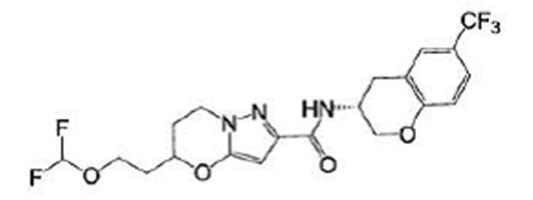
462 [M+H]+
477 [M+H]+
[1446]
[Таблица 58]

530 [M+H]+
436 [M+H]+
448 [M+H]+
496 [M+H]+
427 [M+H]+
517 [M+H]+
494 [M+H]+
446 [M+H]+
420 [M+H]+
[1447]
[Таблица 59]
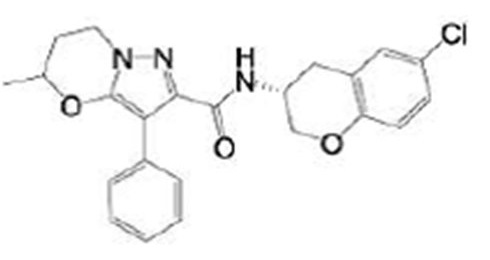
424 [M+H]+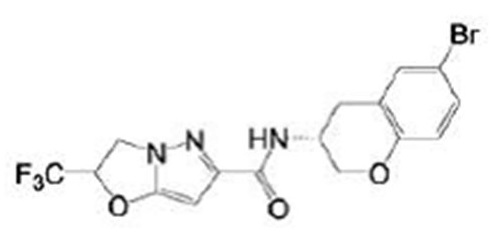
433 [M+H]+
362 [M+H]+
466 [M+H]+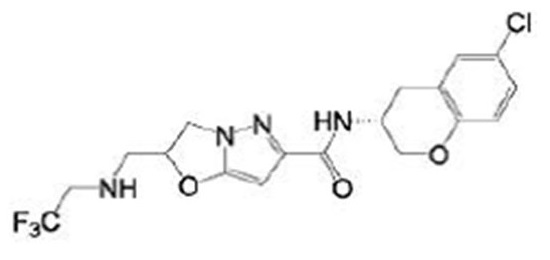
431 [M+H]+
454 [M+H]+
418 [M+H]+
414 [M+H]+
450 [M+H]+
[1448]
[Таблица 60]

400 [M+H]+
395 [M+H]+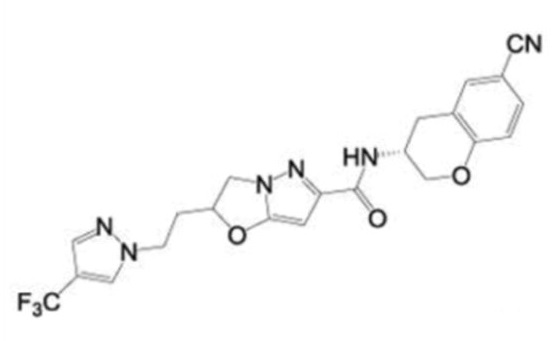
473 [M+H]+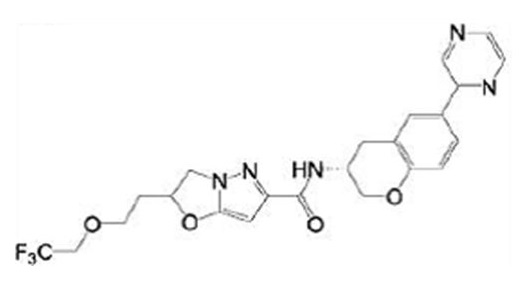
490 [M+H]+
508 [M+H]+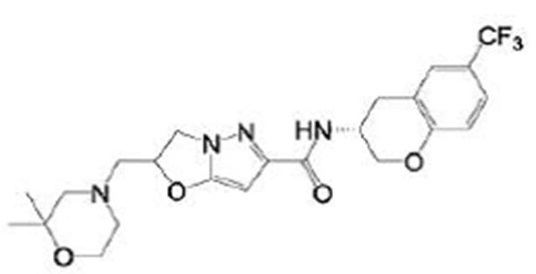
481 [M+H]+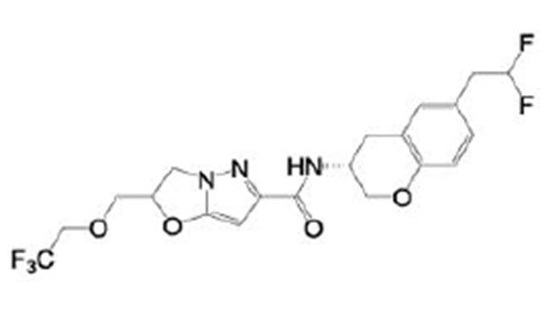
462 [M+H]+
464 [M+H]+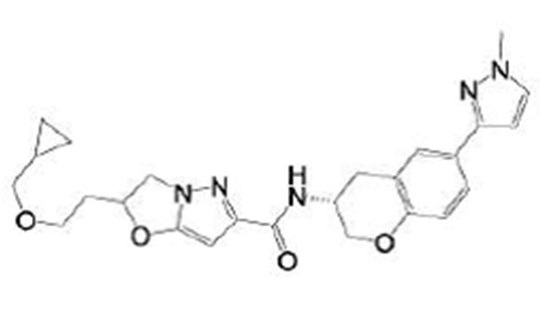
464 [M+H]+
[1449]
[Таблица 61]

478 [M+H]+
410 [M+H]+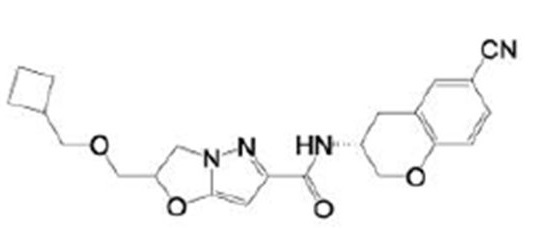
409 [M+H]+
477 [M+H]+
476 [M+H]+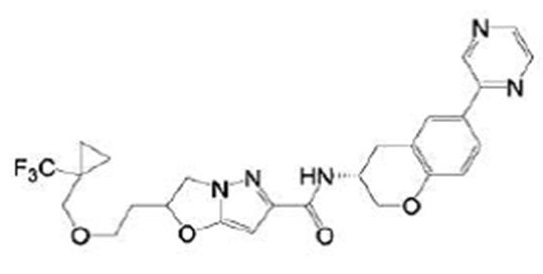
530 [M+H]+
478 [M+H]+
404 [M+H]+
409 [M+H]+
[1450]
[Таблица 62]

448 [M+H]+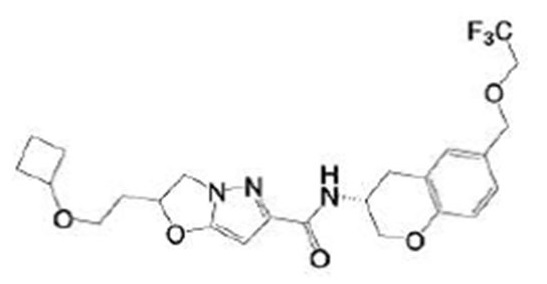
496 [M+H]+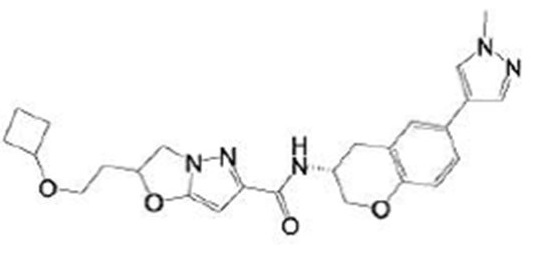
464 [M+H]+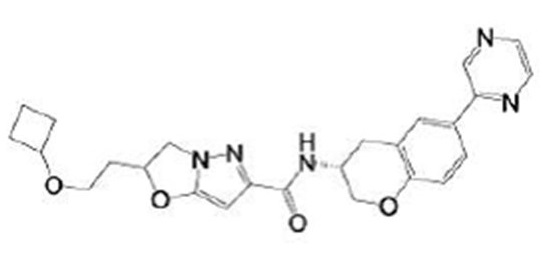
462 [M+H]+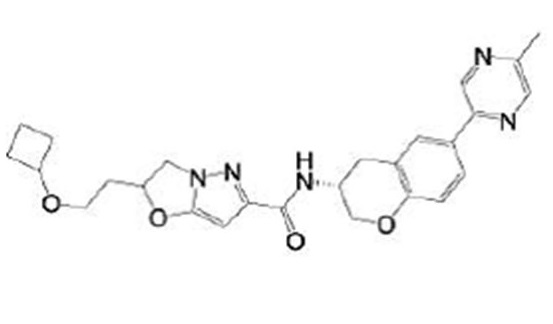
476 [M+H]+
487 [M+H]+
487 [M+H]+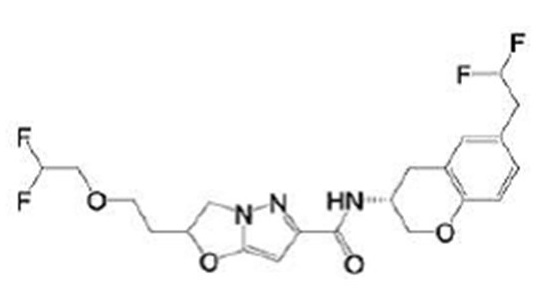
458 [M+H]+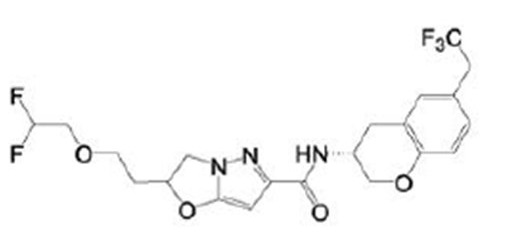
476 [M+H]+
[1451]
[Таблица 63]

424 [M+H]+
424 [M+H]+
524 [M+H]+
407 [M+H]+
475 [M+H]+
479 [M+H]+
434 [M+H]+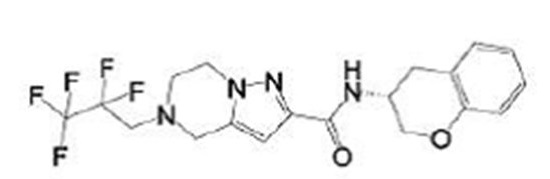
431 [M+H]+
403 [M+H]+
[1452]
[Таблица 64]

456 [M+H]+
407 [M+H]+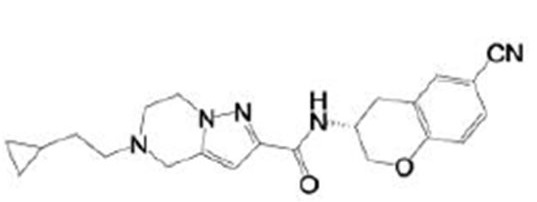
392 [M+H]+
440 [M+H]+
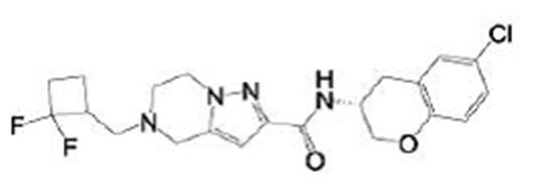
437 [M+H]+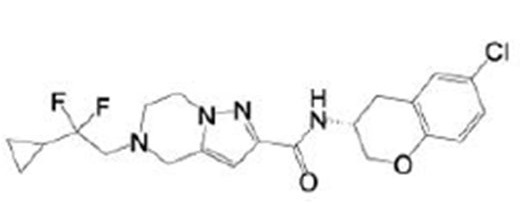
437 [M+H]+
406 [M+H]+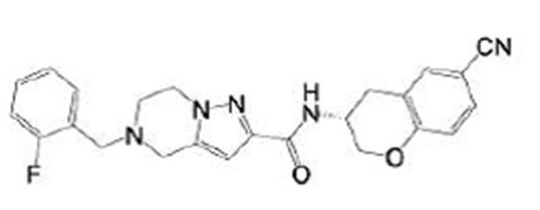
432 [M+H]+
[1453]
[Таблица 65]

392 [M+H]+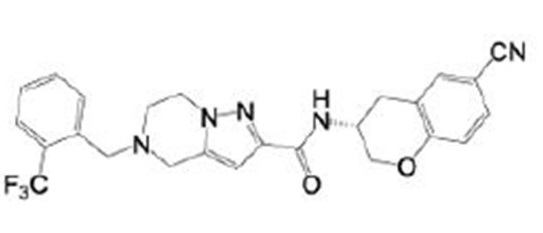
482 [M+H]+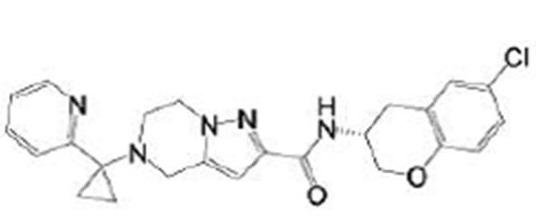
450 [M+H]+
443 [M+H]+
420 [M+H]+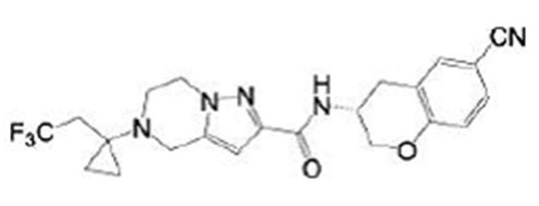
446 [M+H]+
431 [M+H]+
479 [M+H]+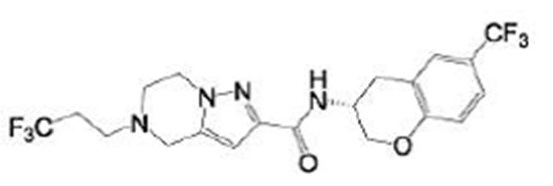
463 [M+H]+
[1454]
[Таблица 66]
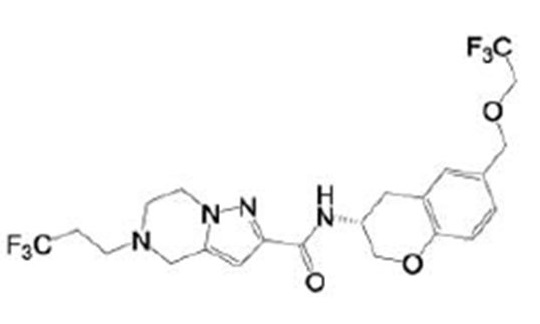
507 [M+H]+
393 [M+H]+
491 [M+H]+
431 [M+H]+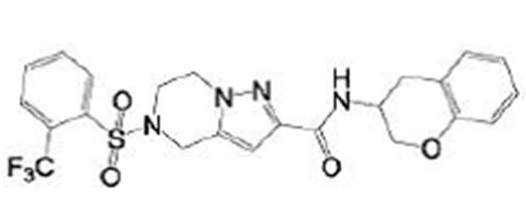
507 [M+H]+
448 [M+H]+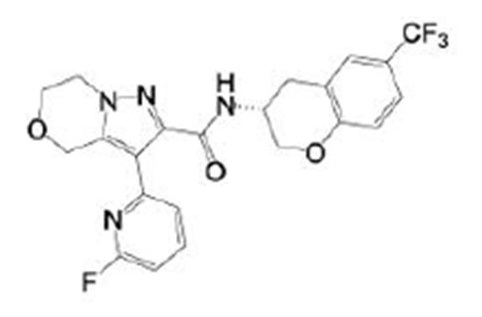
463 [M+H]+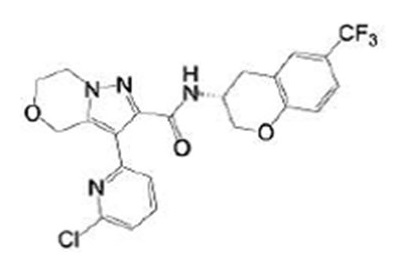
479 [M+H]+
411 [M+H]+
[1455]
[Таблица 67]
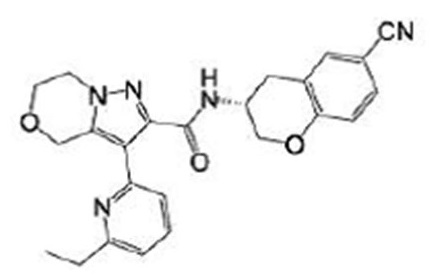
430 [M+H]+
495 [M+H]+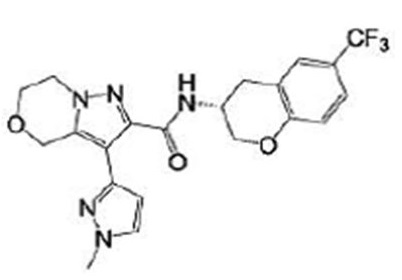
448 [M+H]+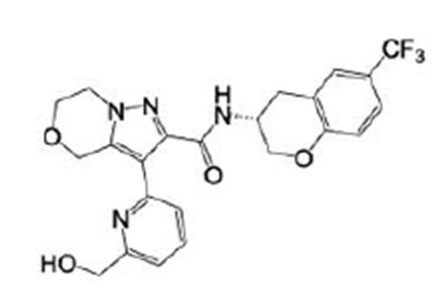
475 [M+H]+
557 [M+H]+
503 [M+H]+
489 [M+H]+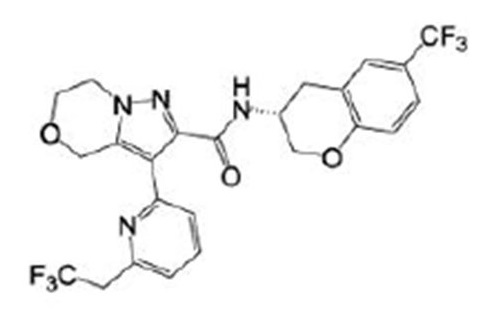
527 [M+H]+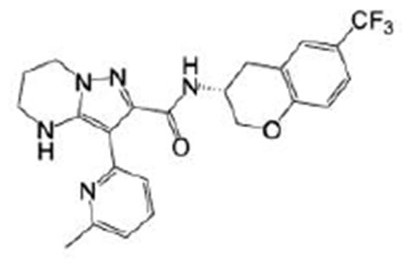
458 [M+H]+
[1456]
[Таблица 68]

488 [M+H]+
529 [M+H]+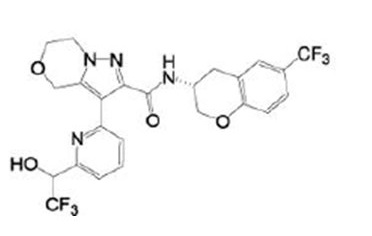
543 [M+H]+
459 [M+H]+
491 [M+H]+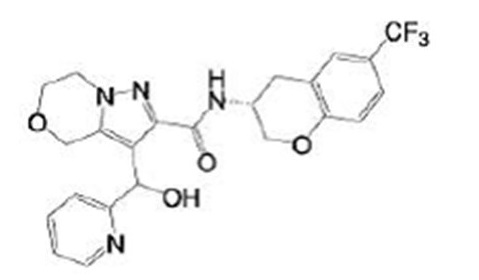
475 [M+H]+
473 [M+H]+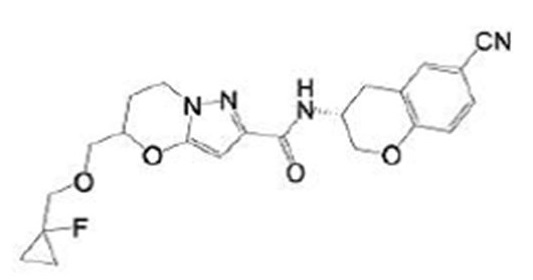

470 [M+H]+
[1457]
[Таблица 69]
(изомер A)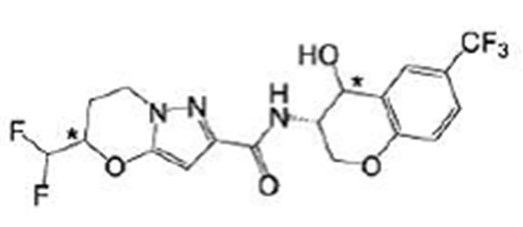
434 [M+H]+
(изомер B)
434 [M+H]+
448 [M+H]+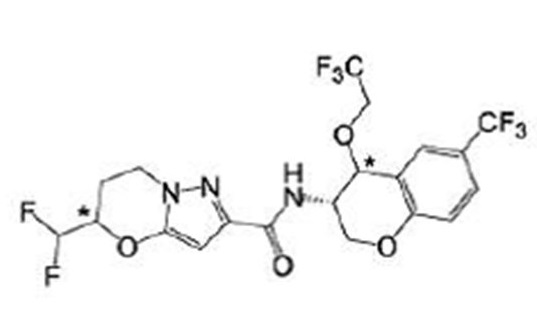
516 [M+H]+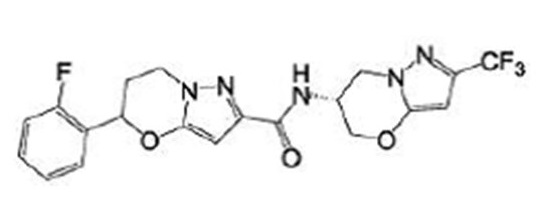
452 [M+H]+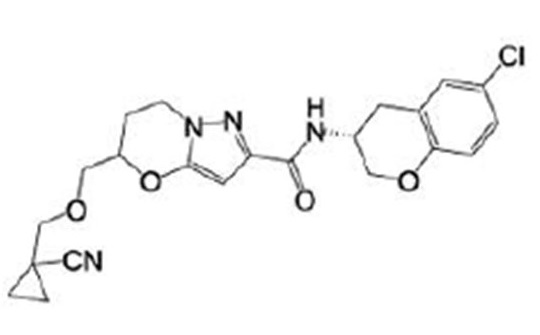
443 [M+H]+
452 [M+H]+

445 [M+H]+
[1458]
[Таблица 70]

446 [M+H]+
440 [M+H]+
462 [M+H]+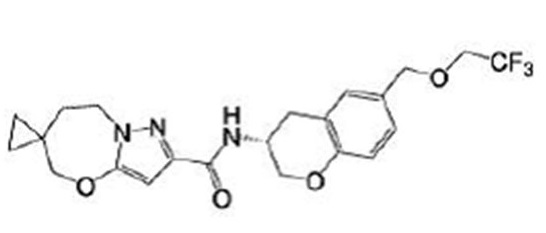
452 [M+H]+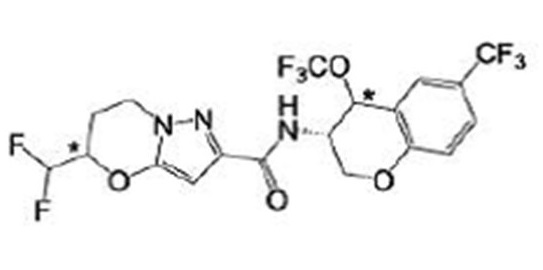
502 [M+H]+
(изомер A)
385 [M+H]+
(изомер B)
385 [M+H]+

397 [M+H]+
[1459]
[Таблица 71]

463 [M+H]+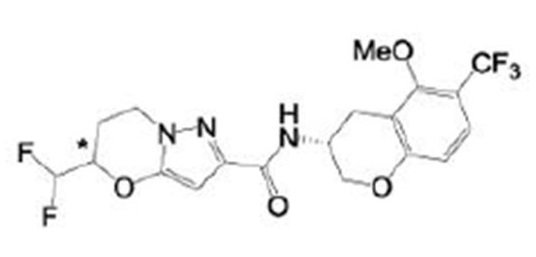
448 [M+H]+
(изомер A)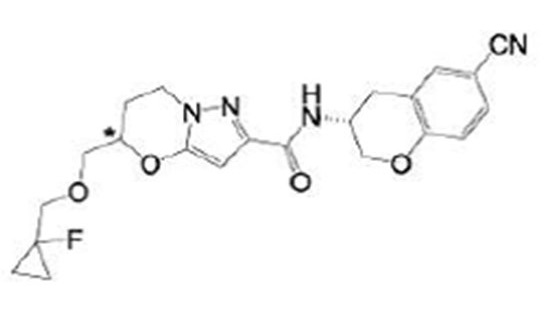
427 [M+H]+
(изомер B)
427 [M+H]+
477 [M+H]+
(изомер A)
477 [M+H]+
(изомер B)
477 [M+H]+

493 [M+H]+
[1460]
[Таблица 72]
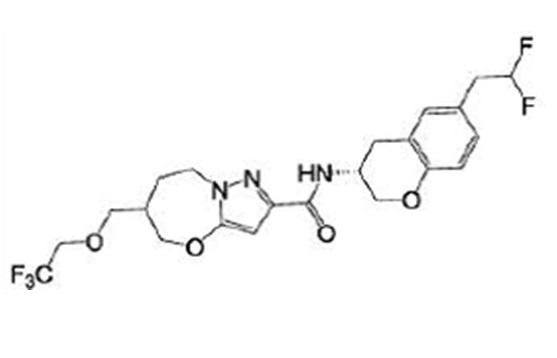
490 [M+H]+
468 [M+H]+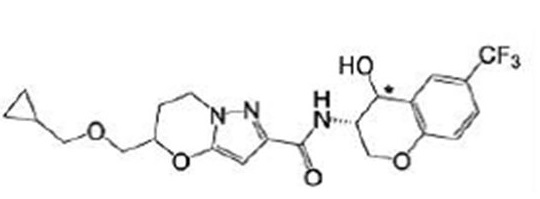
468 [M+H]+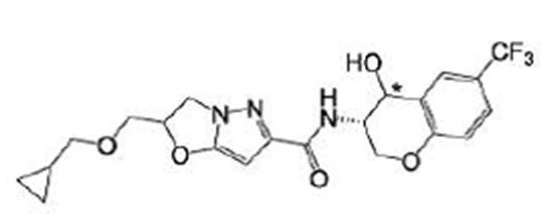
454 [M+H]+
496 [M+H]+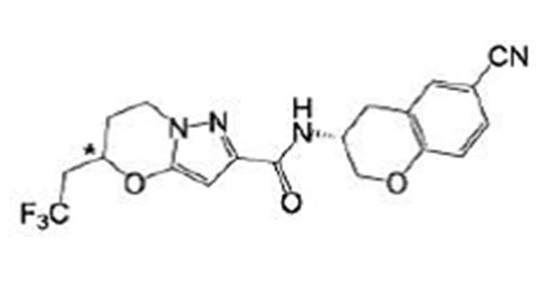
407 [M+H]+
(изомер A)
443 [M+H]+
(изомер B)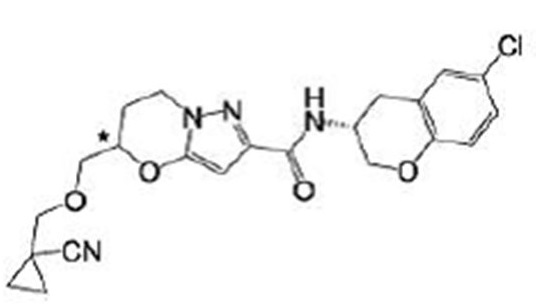

448 [M+H]+
[1461]
[Таблица 73]

409 [M+H]+
476 [M+H]+
466 [M+H]+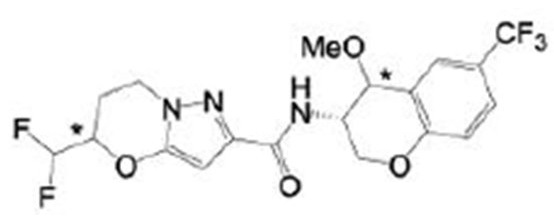
448 [M+H]+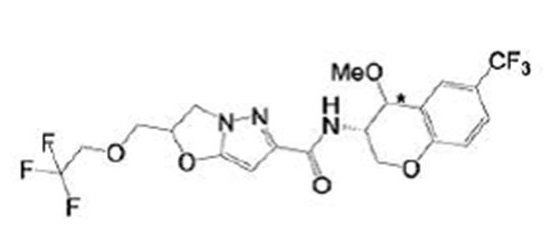
496 [M+H]+
510 [M+H]+
434 [M+H]+
(изомер A)
(изомер B)
451 [M+H]+
[1462]
[Таблица 74]

435 [M+H]+
446 [M+H]+
(изомер A)
468 [M+H]+
(изомер B)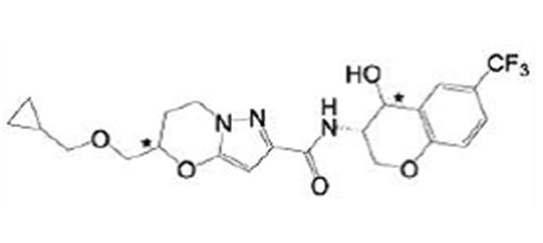
468 [M+H]+
(изомер A)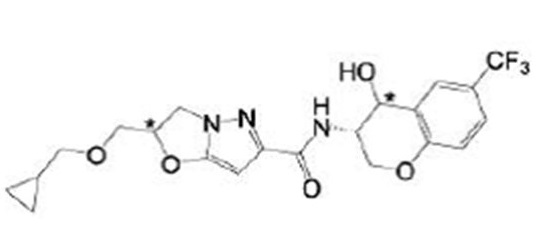
454 [M+H]+
(изомер B)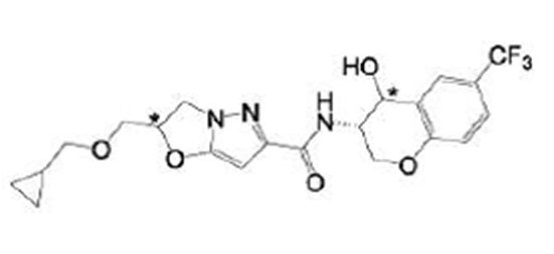
454 [M+H]+
(изомер A)
409 [M+H]+
(изомер B)

404 [M+H]+
[1463]
[Таблица 75]
(изомер A)
436 [M+H]+
(изомер B)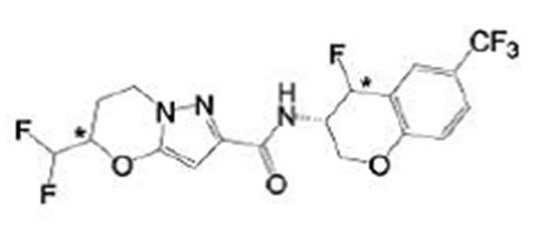
436 [M+H]+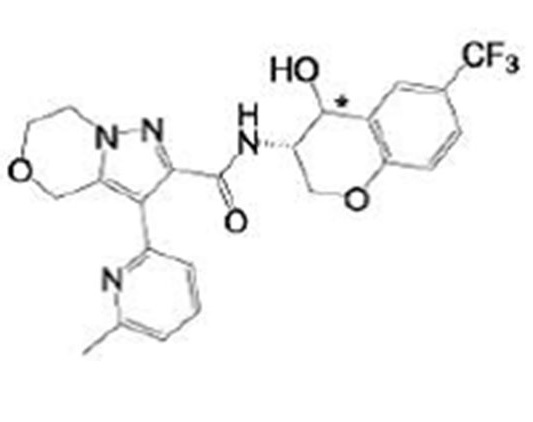
475 [M+H]+
489 [M+H]+
426 [M+H]+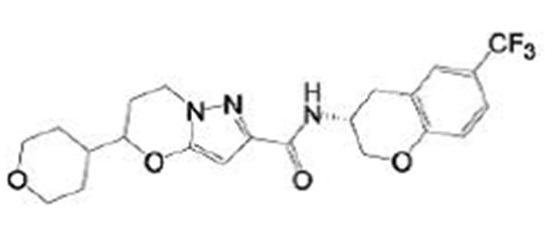
452 [M+H]+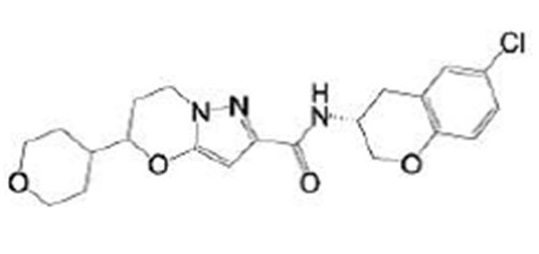
418 [M+H]+

448 [M+H]+
[1464]
[Таблица 76]
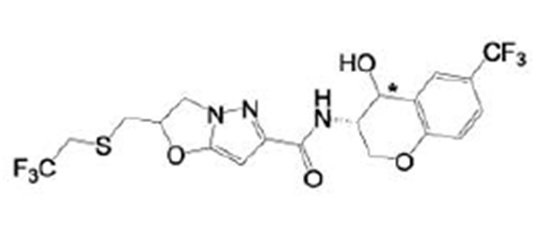
498 [M+H]+
496 [M+H]+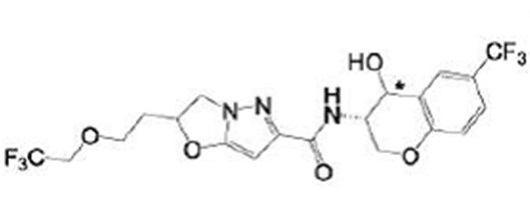
496 [M+H]+
(изомер A)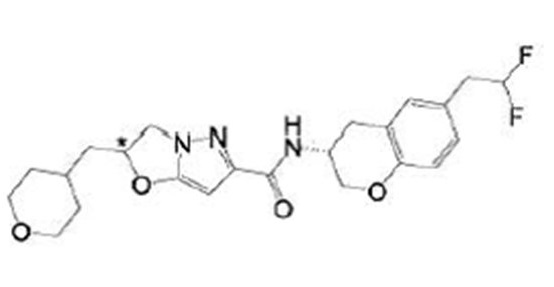
448 [M+H]+
(изомер B)
496 [M+H]+
510 [M+H]+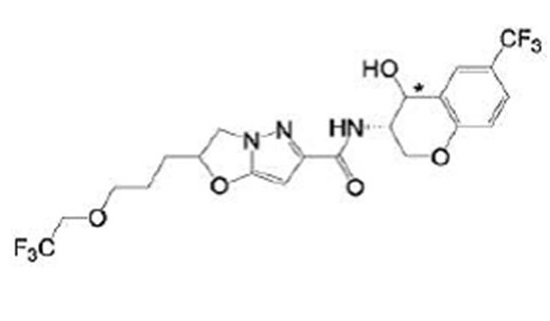
510 [M+H]+

478 [M+H]+
[1465]
[Таблица 77]

468 [M+H]+
468 [M+H]+
(изомер A)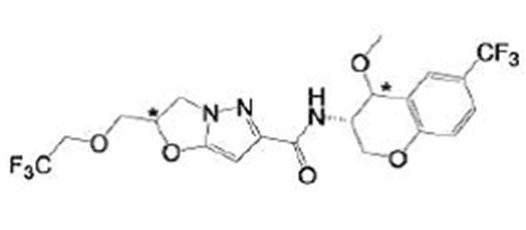
496 [M+H]+
(изомер B)
496 [M+H]+
(изомер A)
510 [M+H]+
(изомер B)
510 [M+H]+
412 [M+H]+
(изомер A)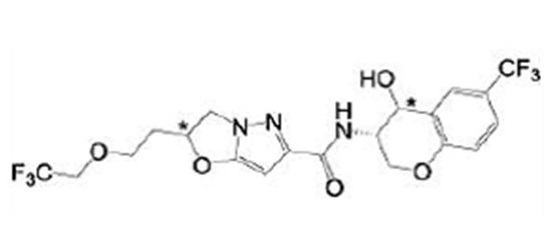
(изомер B)
496 [M+H]+
[1466]
[Таблица 78]
(изомер A)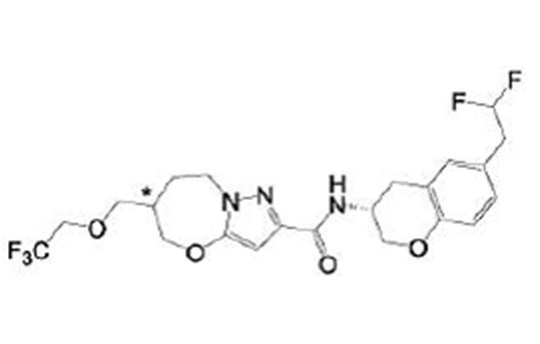
490 [M+H]+
(изомер B)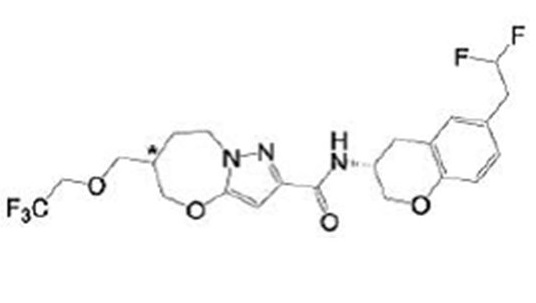
490 [M+H]+
(изомер A)
538 [M+H]+
(изомер B)
538 [M+H]+
(изомер A)
510 [M+H]+
(изомер B)
510 [M+H]+
(изомер A)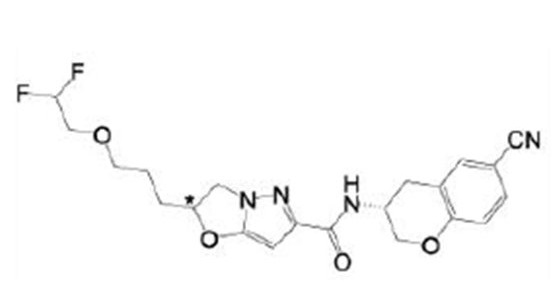
433 [M+H]+
(изомер B)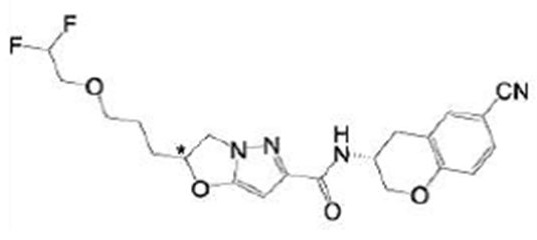

496 [M+H]+
[1467]
[Таблица 79]

496 [M+H]+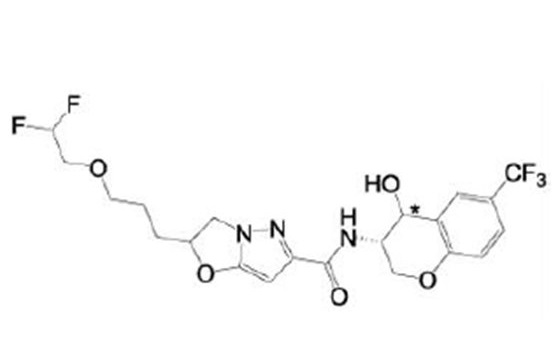
492 [M+H]+
(изомер A)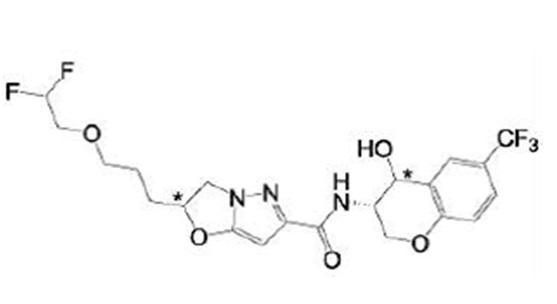
492 [M+H]+
(изомер B)
492 [M+H]+
492 [M+H]+
(изомер A)
492 [M+H]+
(изомер B)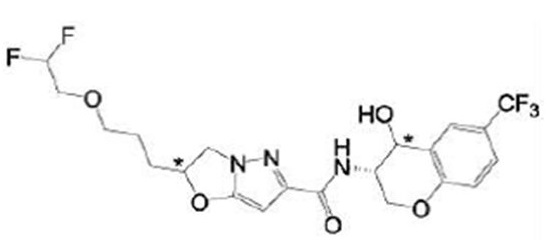
492 [M+H]+

438 [M+H]+
[1468]
[Таблица 80]

456 [M+H]+
456 [M+H]+
(изомер A)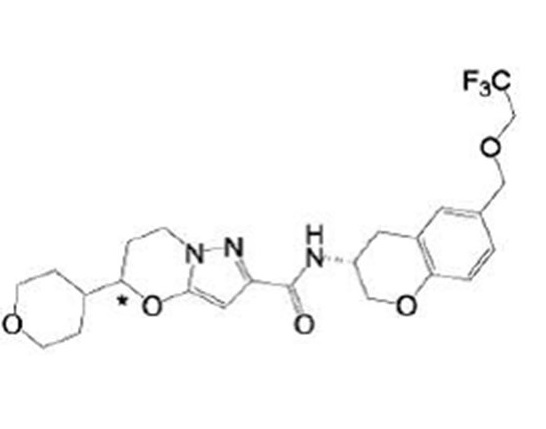
496 [M+H]+
(изомер B)
496 [M+H]+
(изомер A)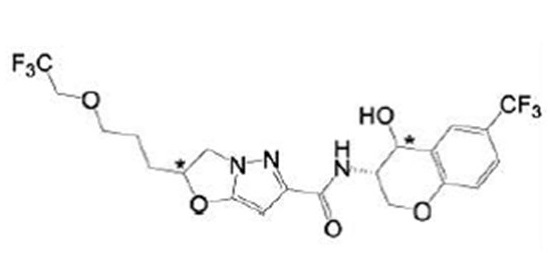
510 [M+H]+
(изомер B)
510 [M+H]+
(изомер A)
427 [M+H]+
(изомер B)
(изомер C)
427 [M+H]+
[1469]
[Таблица 81]
(изомер D)
427 [M+H]+
409 [M+H]+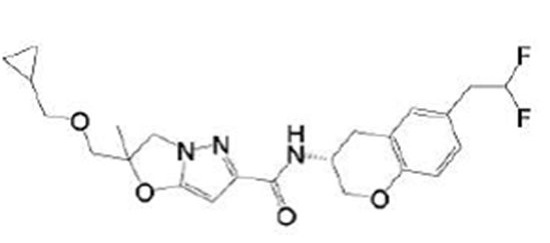
448 [M+H]+
454 [M+H]+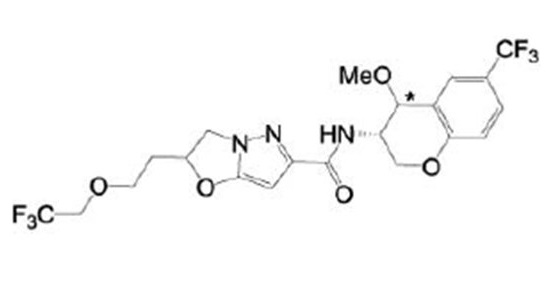
510 [M+H]+
(изомер A)
496 [M+H]+
(изомер B)
496 [M+H]+
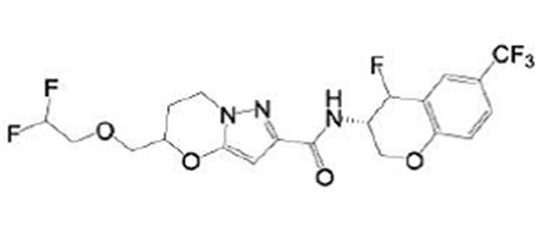
480 [M+H]+
[1470]
[Таблица 82]

483 [M+H]+
404 [M+H]+
448 [M+H]+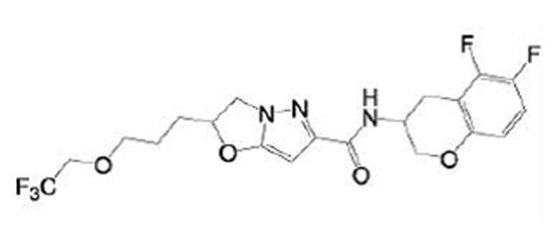
462 [M+H]+
448 [M+H]+
482 [M+H]+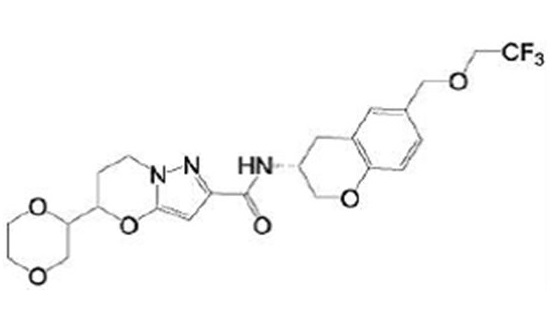
498 [M+H]+

446 [M+H]+
[1471]
[Таблица 83]
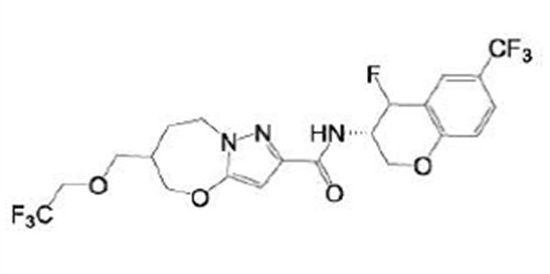
512 [M+H]+
506 [M+H]+
(изомер A)
468 [M+H]+
(изомер B)
468 [M+H]+
469 [M+H]+
498 [M+H]+
420 [M+H]+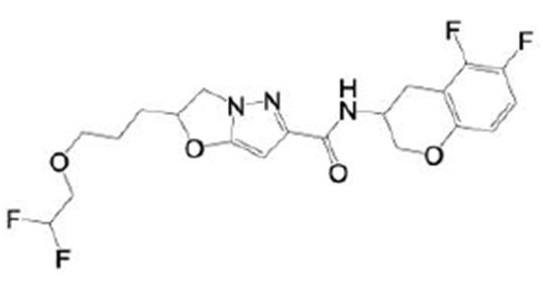
(изомер A)
498 [M+H]+
[1472]
[Таблица 84]
(изомер B)
498 [M+H]+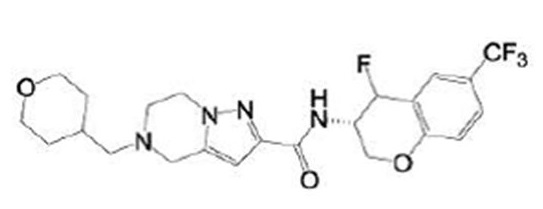
483 [M+H]+
441 [M+H]+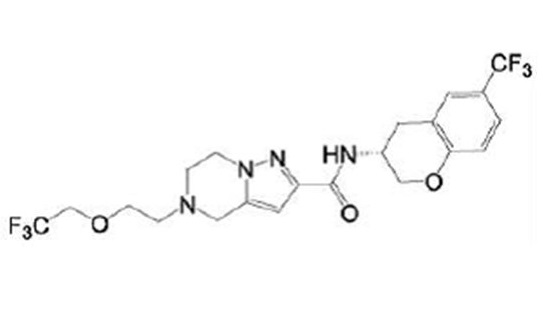
493 [M+H]+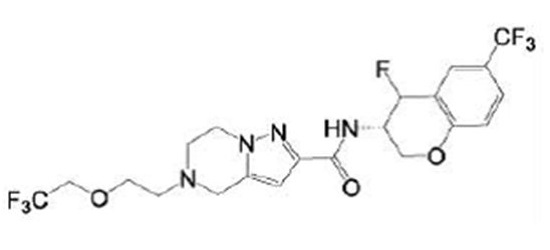
511 [M+H]+
455 [M+H]+
481 [M+H]+

425 [M+H]+
[1473]
[Таблица 85]

427 [M+H]+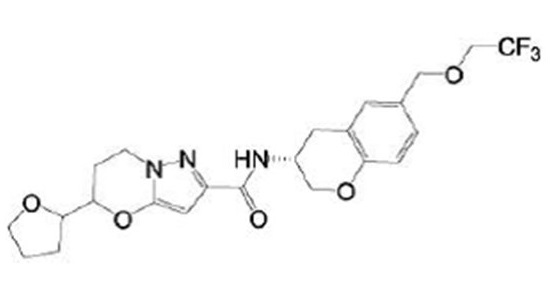
482 [M+H]+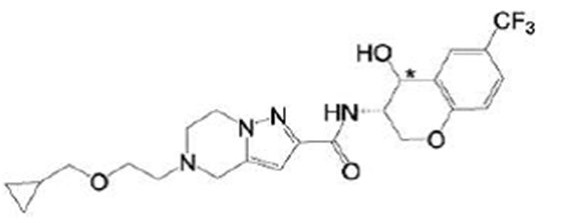
481 [M+H]+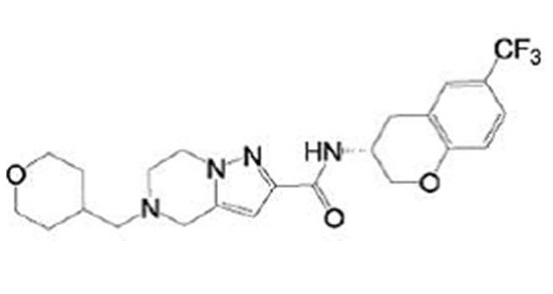
465 [M+H]+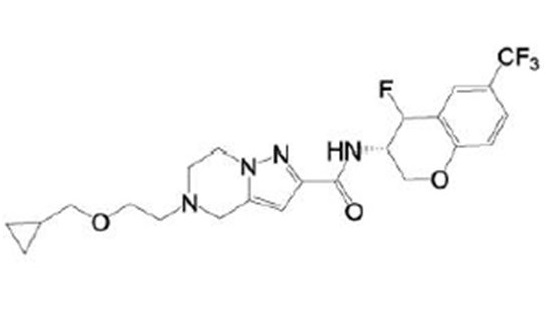
483 [M+H]+
510 [M+H]+
444 [M+H]+

476 [M+H]+
[1474]
[Таблица 86]
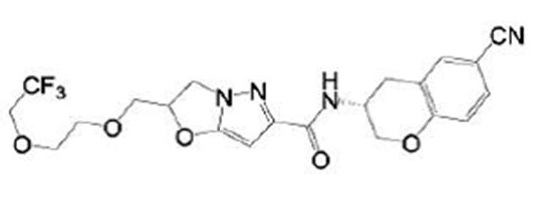
467 [M+H]+
526 [M+H]+
554 [M+H]+
490 [M+H]+
524 [M+H]+
481 [M+H]+
542 [M+H]+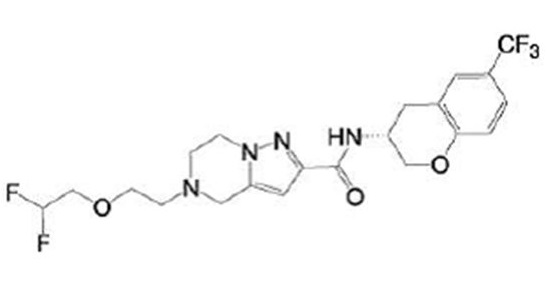

537 [M+H]+
[1475]
[Таблица 87]

434 [M+H]+
451 [M+H]+
455 [M+H]+
471 [M+H]+
483 [M+H]+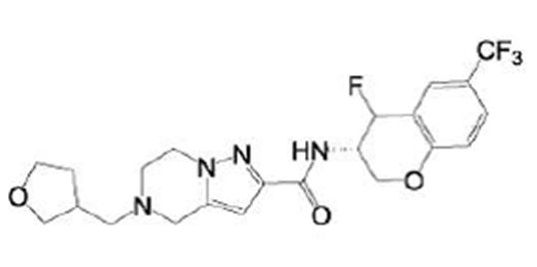
469 [M+H]+
462 [M+H]+

528 [M+H]+
[1476]
[Таблица 88]
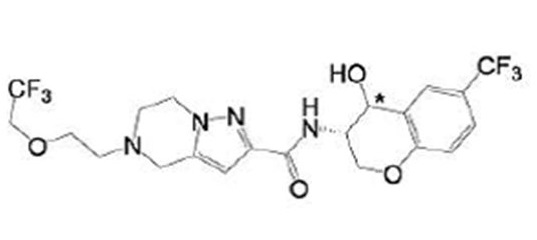
509 [M+H]+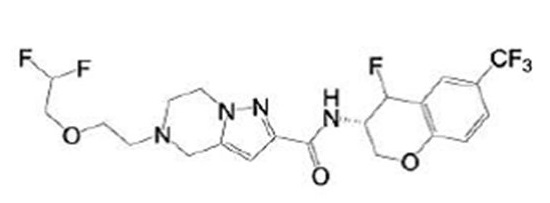
493 [M+H]+
498 [M+H]+
524 [M+H]+
540 [M+H]+
490 [M+H]+
510 [M+H]+
[1477]
Тестовый пример 1. Оценка ингибирующей активности в отношении Nav1.7 человека
Применяли клеточную линию, в которой субъединицы Nav1.7 человека и Navβ1 человека стабильно экспрессировались, представляющую собой клетки HEK293A. Применяли среду Игла, модифицированную Дульбекко (DMEM), дополненную 10% фетальной бычьей сыворотки, 600 мкг/мл генетицина и 2 мкг/мл бластицидина S, в качестве культуральной среды при условиях 37°C и 5% CO2 в колбах T175 для проведения культивирования. Когда достигали конфлюэнтности, составляющей 60-80%, клетки отделяли и получали клеточную суспензию с концентрацией приблизительно 0,5-5,0×106 клеток/мл. Величину тока через Nav1.7 человека записывали с применением полностью автоматического устройства для фиксации потенциала QPatch16X (Sophion Biosciences) при комнатной температуре. В качестве внеклеточной жидкости применяли раствор 145 мМ NaCl, 4 мМ KCl, 1 мМ MgCl2, 2 мМ CaCl2, 10 мМ глюкозы, 10 мМ 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновой кислоты (HEPES) при pH 7,4. В качестве внутриклеточной жидкости применяли раствор 135 мМ CsF, 1/5 мМ гликолевого эфира диаминтетрауксусной кислоты (EGTA)/CsOH, 10 мМ HEPES, 10 мМ NaCl при pH 7,3. Тестовые соединения растворяли в диметилсульфоксиде (DMSO) и разбавляли внеклеточной жидкостью с получением концентрации DMSO, составляющей 0,1% во время анализа.
[1478]
Ответ относительно тока получали при частоте дискретизации, составляющей 25 кГц, и шум удаляли с помощью 3 кГц-фильтра нижних частот. Потенциал фиксации составлял −100 мВ. Поправку на остаточный ток проводили путем применения ступенчатого импульса с напряжением −120 мВ перед тестовым импульсом. С целью исследования ингибирующего действия тестового соединения создавали следующий тестовый импульс: а именно, после применения деполяризующего импульса с напряжением −10 мВ в течение 50 миллисекунд его фиксировали на уровне −120 мВ в течение 500 миллисекунд; потенциал, при котором приблизительно 30-40% канала было инактивировано, поддерживали в течение 15 секунд, затем снова фиксировали на уровне −120 мВ в течение 100 миллисекунд и наконец создавали деполяризующий импульс с напряжением −10 мВ в течение 50 миллисекунд. Тестовые импульсы создавали до и после добавления тестового соединения.
Ингибирующую активность тестового соединения определяли на основе величины входящего тока, генерируемого вторым деполяризующим импульсом, и 50% ингибирующую концентрацию (IC50) рассчитывали на основе кривой зависимости ответа от концентрации. Значения IC50 показаны в таблицах 89-98 ниже.
Соединения со значениями IC50 менее 1 мкМ обозначены буквой "A", а соединения со значениями IC50 менее 10 мкМ обозначены буквой "B".
В то же время, если не указано иное, "пример" в таблице в каждом случае означает соединение, получение которого предусматривается в таком примере; например, результат оценки для примера 1 демонстрирует результат оценки для соединения, получение которого предусматривается в примере 1.
[1479]
Тестовый пример 2. Оценка ингибирующей активности в отношении Nav1.5 человека
Применяли клеточную линию, в которой Nav1.5 человека стабильно экспрессировался, представляющую собой клетки HEK293. Применяли DMEM, дополненную 15% фетальной бычьей сыворотки, 500 мкг/мл генетицина, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина, 20 мМ HEPES в качестве культуральной среды в условиях 37°C и 5% CO2 в колбах T175 для проведения культивирования. Когда достигали конфлюэнтности, составляющей 60-80%, получали клеточную суспензию с концентрацией приблизительно 0,5-5,0×106 клеток/мл. Величину тока через Nav1.5 человека записывали с применением полностью автоматического устройства для фиксации потенциала QPatch16X при комнатной температуре. В качестве внеклеточной жидкости применяли 145 мМ NaCl, 4 мМ KCl, 1 мМ MgCl2, 2 мМ CaCl2, 10 мМ глюкозы и 10 мМ HEPES при pH 7,4. В качестве внутриклеточной жидкости применяли 135 мМ CsF, 1/5 мМ EGTA/CsOH, 10 мМ HEPES и 10 мМ NaCl при pH 7,3. Тестовые соединения растворяли в DMSO и разбавляли внеклеточной жидкостью с получением концентрации DMSO, составляющей 0,1% во время анализа.
[1480]
Ответ относительно тока получали при частоте дискретизации, составляющей 25 кГц, и шум удаляли с помощью 3 кГц-фильтра нижних частот. Потенциал фиксации составлял −80 мВ. Поправку на остаточный ток проводили путем применения ступенчатого импульса с напряжением −100 мВ перед тестовым импульсом. С целью исследования ингибирующего эффекта тестового соединения в отношении Nav1.5 человека 20 раз непрерывно создавали тестовые импульсы, имитирующие потенциал действия кардиомиоцитов. Тестовые импульсы создавали до и после добавления тестового соединения.
[1481]
Ингибирующую активность тестового соединения определяли на основе величины входящего тока, генерируемого 20-м деполяризующим импульсом, и 50% ингибирующую концентрацию (IC50) рассчитывали на основе кривой зависимости ответа от концентрации.
Значения IC50 ингибирующего действия для тестовых соединений показаны в таблицах 89-98 ниже.
Соединения со значением IC50 менее 1 мкМ обозначены буквой "A", соединения со значением IC50 1 мкМ или больше и менее 3 мкМ обозначены буквой "B", и соединения со значением IC50 3 мкМ или больше обозначены буквой "C".
[1482]
Тестовый пример 3. Эффект в отношении острой боли
Для теста использовали самцов мышей линии ICR возрастом шесть недель. Тестовые соединения вводили перорально с концентрацией 1-10 мг/кг и обеспечивали привыкание мышей к прозрачной клетке для наблюдения в течение 60 минут. Мышей осторожно удерживали без анестезии и вводили подкожно 20 мкл раствора 80 мкг/мл капсаицина (0,8% этанола в физиологическом растворе) в подошвенную поверхность задней правой лапы мышей. Мышей возвращали в клетку для наблюдения и непосредственно после этого в виде времени реакции измеряли продолжительность связанного с болью поведения (зализывание, встряхивание) в отношении правой задней конечности в течение 5 минут.
Степень ингибирования для тестового соединения определяли с помощью следующей расчетной формулы.
Степень ингибирования для тестового соединения (%) = 100 × [1 − (время реакции в группе введения тестового соединения/время реакции в группе контроля со средой-носителем)]
Эффект тестового соединения в отношении острой боли показан в таблице 99 ниже. Соединения со степенью ингибирования 30% или больше обозначены буквой "A", и соединений со степенью ингибирования 20% или больше и менее 30% обозначены буквой "B", и соединения со степенью ингибирования 10% или больше, но менее 20% обозначены буквой "C".
[1483]
Тестовый пример 4. Эффект в отношении невропатической боли
Для теста использовали самцов мышей линии ICR возрастом пять недель. Кожу и мышцы разрезали, чтобы выделить шестой поясничный позвонок, под анестезией с применением изофлурана, и удаляли правый поперечный отросток. Выделяли спинномозговой нерв L5 из окружающей ткани, его удаляли и затем разрез зашивали.
Определяли 50% болевой порог подошвенной поверхности в соответствии со способом от Chaplan SR et al. (J Neurosci Methods 1994, 53: 55-63) с применением нитей фон Фрея (0,008 г, 0,02 г, 0,04 г, 0,07 г, 0,16 г, 0,4 г и 0,6 г). Сначала мышей помещали в клетку для измерений с решетчатой структурой и обеспечивали их привыкание, пока животные не успокаивались; нить 0,07 г прижимали к подошвенной поверхности в течение приблизительно 3 секунд. Если наблюдали поведение избегания, то применяли нить с интенсивностью стимуляции на один уровень ниже для создания стимуляции, и наоборот, если наблюдение избегания не наблюдали, то применяли нить с интенсивностью стимуляции на один уровень выше для создания стимуляции. Путем повторения данной операции с началом 2 раза до и после того, как менялось наличие или отсутствие поведения избегания, результаты записывали всего 6 раз для расчета 50% болевого порога с применением следующей расчетной формулы.
50% болевой порог (г)= (10[Xf+κδ]/10000)
Xf представляет собой значение интенсивности стимула нити, применяемой в последней стимуляции (логарифм значения), κ представляет собой значение, полученное из графика наличия/отсутствия поведения избегания за 6 раз, и δ представляет собой разницу в интенсивности стимула (логарифм значения) между применяемыми нитями (в данном случае 0,365).
Животных, которые демонстрировали 50% болевой порог подошвенной поверхности пораженной конечности, составляющий 0,16 г или больше до хирургической операции и 0,08 г или меньше через 1 неделю после хирургической операции, применяли в качестве животных с развитой аллодинией для оценки тестового вещества.
Каждое из соединений по настоящему изобретению, например, из примера 70, изомер A из примера 103, изомер A из примера 134, изомер A из примера 161 A, из примера 288 и из примера 290, увеличивало 50% болевой порог при дозе, составляющей 10 мг/кг или меньше, после одного перорального введения и демонстрировало противоаллодинический эффект.
[1484]
[Таблица 89]
[1485]
[Таблица 90]
[1486]
[Таблица 91]
[1487]
[Таблица 92]
[1488]
[Таблица 93]
[1489]
[Таблица 94]
[1490]
[Таблица 95]
[1491]
[Таблица 96]
[1492]
[Таблица 97]
[1493]
[Таблица 98]
[1494]
[Таблица 99]
[Промышленная применимость]
[1495]
Производное гетероароматического амида по настоящему изобретению, представленное общей формулой (I) или общей формулой (I-E2), или его соль характеризуются сильным ингибирующим эффектом в отношении Nav1.7 и более низким ингибирующим эффектом в отношении Nav1.5, так что они являются применимыми в качестве активного ингредиента терапевтического средства и/или профилактического средства при различных заболеваниях, ассоциированных с Nav1.7, с меньшими опасениями в отношении побочных эффектов, обусловленных Nav1.5. Например, производное гетероароматического амида по настоящему изобретению или его соль являются применимыми в качестве обезболивающего средства при различных заболеваниях, сопровождающихся болью.
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, ИХ КОМПОЗИЦИИ И ПРИМЕНЕНИЕ | 2014 |
|
RU2696585C2 |
| МОЛЕКУЛЫ С ПЕСТИЦИДНОЙ ФУНКЦИЕЙ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ, СВЯЗАННЫЕ С НИМИ | 2016 |
|
RU2735602C2 |
| МОЛЕКУЛЫ С ПЕСТИЦИДНОЙ ФУНКЦИЕЙ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ, СВЯЗАННЫЕ С НИМИ | 2016 |
|
RU2742119C2 |
| ПРОИЗВОДНОЕ НА ОСНОВЕ ДИГИДРОПИРИМИДО-КОЛЬЦА В КАЧЕСТВЕ ИНГИБИТОРА HBV | 2015 |
|
RU2693897C2 |
| МАКРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ, ВЫПОЛНЯЮЩЕЕ ФУНКЦИИ ИНГИБИТОРА WEE1, И ВАРИАНТЫ ЕГО ПРИМЕНЕНИЯ | 2018 |
|
RU2783243C2 |
| Соединения, полезные в качестве пестицидов, и промежуточные соединения, композиции и способы, связанные с ними | 2016 |
|
RU2821715C2 |
| СПОСОБ СИНТЕЗИРОВАНИЯ НОВОГО ХИРАЛЬНОГО ЛИГАНДА, ХЕЛАТА МЕТАЛЛА, РАЗЛИЧНЫХ НЕПРИРОДНЫХ АМИНОКИСЛОТ, МАРАВИРОКА И ЕГО ОСНОВНЫХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ | 2017 |
|
RU2727723C1 |
| ИНГИБИТОР PDE4 | 2017 |
|
RU2743126C2 |
| ПРОИЗВОДНЫЕ ФЕНОКСИФЕНИЛУКСУСНОЙ КИСЛОТЫ | 1994 |
|
RU2139273C1 |
| УСИЛИТЕЛЬ ПРОТИВООПУХОЛЕВОГО ВОЗДЕЙСТВИЯ, СОДЕРЖАЩИЙ СОЕДИНЕНИЕ ПИРРОЛОПИРИМИДИНА | 2016 |
|
RU2710380C1 |
Изобретение относится к производному гетероароматического амида, представленному общей формулой (I-E2), фармацевтическим композициям, средствам, обладающим ингибирующей активностью в отношении Nav1.7, а также примненению производного гетероароматического амида или его фармакологически приемлемой соли по любому из пп. 1-7 для изготовления фармацевтической композиции, обладающей ингибирующей активностью в отношении Nav1.7, применяемой для предупреждения или устранения боли. Технический результат: получены новые соединения, обладающие ингибирующей активностью в отношении Nav1.7, которые могут быть применимы для предупреждения или устранения боли. 12 н. и 5 з.п. ф-лы, 99 табл.
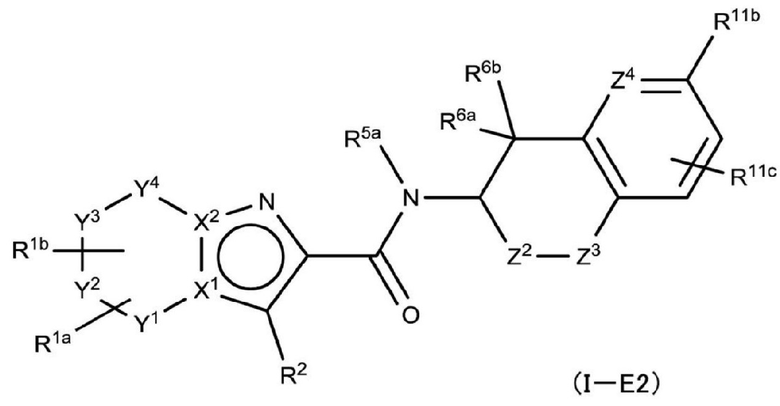
1. Производное гетероароматического амида или его фармакологически приемлемая соль, представленное общей формулой (I-E2),
[Хим. 1]

где
X1-X2 представляет собой C-N,
Y1, Y2, Y3 и Y4
вместе образуют
-OCH2CH2CH2-, -OCR4aHCH2CH2-, -OCR4aR4bCH2CH2-,
-OCH2CH2-, -OCR4aHCH2-, -OCR4aR4bCH2-,
-OCH2CH2CH2CH2-, -OCR4aHCH2CH2CH2-,
-OCH2CR4aHCH2CH2-, -OCH2CR4aR4bCH2CH2-,
-CH2OCH2CH2-, -CH2OCH2CH2CH2-,
-CH2CH2CH2CH2-, -CH2CR4aHCH2CH2-,
-NHCH2CH2CH2-, -NHCR4aHCH2CH2- или -CH2NR4cCH2CH2-,
R4a, R4b и R4c независимо друг от друга представляют собой гидроксигруппу, C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4 галогеналкокси-C1-C4 алкильную группу, C1-C4 алкокси-C1-C4 галогеналкильную группу, C3-C7 циклоалкильную группу, C3-C7 циклоалкильную группу, необязательно замещенную C1-C4 галогеналкильной группой, гетероциклоалкильную группу, C2-C6 алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C1-C4 галогеналкокси-C1-C4 алкоксигруппу, C1-C4 галогеналкилтио-C1-C4 алкильную группу, -(CH2)qNRb1Rb2 (Rb1 и Rb2 независимо друг от друга представляют собой атом водорода, C1-C4 алкильную группу, или C1-C4 галогеналкильную группу, и q равен 1, или 2), или группу, представленную общей формулой (I-B):
[Хим. 2]

где
кольцо C представляет собой C3-C7 циклоалкил, азетидинил, пирролидинил, пиперидил, морфолино, фенил, пиразолил, пиридил, оксетанил, тетрагидрофуранил, тетрагидропиранил или диоксанил,
L2 представляет собой одинарную связь, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O (CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc (CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO (CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2S (CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO2 (CR10eR10f)r3(CR10gR10h)r4-,
(Rc представляет собой C1-C4 алкильную группу,
R10a, R10b, R10c, R10d, R10e, R10f, R10g и R10h независимо друг от друга представляют собой атом водорода, атом галогена, C1-C4 алкильную группу или C3-C7 циклоалкильную группу,
R10a и R10b вместе со связанным с ними атомом углерода необязательно образуют циклопропан,
r1, r2, r3 и r4 независимо друг от друга представляют собой 0, 1 или 2),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атомом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу или C1-C6 алкоксигруппу,
R4a и R4b вместе со связанным с ними атомом углерода необязательно образуют 3-7-членное моноциклическое кольцо, или
R4a и R4b вместе необязательно образуют группу общей формулы (I-D):
[Хим. 3]

(R4d и R4e представляют собой атом водорода),
R1a и R1b независимо друг от друга представляют собой атом водорода, атомом галогена, или C1-C4 алкильную группу,
R2 представляет собой атом водорода, C1-C6-алкильную группу, необязательно замещенную пиридинилом, нафтилом, 5-6-членное моноциклическое ароматическое кольцо, необязательно замещенное метилом, этилом, 2,2,2-трифторэтилом, 1-гидрокси-2,2,2,-трифторэтилом, метокси, гидроксиметилом, 2,2,2-трифторэтоксиметилом, метоксиметилом, 2-гидрокси-2-прокси или атомом галогена,
Z2-Z3 представляет собой -CH2O-,
R5a представляет собой атом водорода или гетероциклоалкил-C1-C4 алкильную группу,
R6a и R6b независимо друг от друга представляют собой атом водорода, атомом галогена, гидроксигруппу, C1-C4 алкильную группу, C1-C4 алкоксигруппу или C1-C4-галогеналкоксигруппу,
Z4 представляет собой C-R11a или атом азота,
R11a представляет собой атом водорода, атомом галогена, C1-C6 алкоксигруппу или C1-C6-галогеналкоксигруппу,
R11b и R11c независимо друг от друга представляют собой атом водорода, атомом галогена, цианогруппу, C1-C6-алкильную группу, необязательно замещенную гидрокси, C1-C6-галогеналкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную диметиламинокарбонильной группой или диметиламино группой, C1-C4 галогеналкокси-C1-C4 алкильную группу, C2-C6 алкенильную группу, C2-C6 алкинильную группу, необязательно замещенную метокси, или группу, представленную общей формулой (I-B) (I-A):
[Хим. 4]

где
кольцо B представляет собой C3-C7 циклоалкил, азетидинил, морфолино, пиразолил, тиазолил, триазолил, пиридил, пиразинил, тетрагидроксипиранил или пиримидинил,
L1 представляет собой одинарную связь, -CRa3Ra4-, -CRa3Ra4O-, CH2CH2- или -CH2OCH2- (Ra3 и Ra4 представляют собой атом водорода),
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атомом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6 алкоксигруппу или гетероциклоалкильную группу,
(при условии, что Y1, Y2, Y3 и Y4 вместе не образуют -OCH2CH2CH2-, -OCH2CH2-, -OCH2CH2CH2CH2-, -CH2OCH2CH2-, -CH2OCH2CH2CH2-, -CH2CH2CH2CH2- или -NHCH2CH2CH2-, когда R2 представляет собой атом водорода).
2. Производное гетероароматического амида или его фармакологически приемлемая соль по п. 1, где в общей формуле (I-E2):
R4a представляет собой C1-C6-алкильную группу, C1-C6-алкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкильную группу, C1-C6-галогеналкильную группу, необязательно замещенную гидроксигруппой, C1-C6-галогеналкоксигруппу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную C1-C4-галогеналкоксигруппой, C1-C4 галогеналкокси-C1-C4 алкильную группу, C1-C4 алкокси-C1-C4 галогеналкильную группу, C3-C7 циклоалкильную группу, гетероциклоалкильную группу, C2-C6 алкинильную группу, необязательно замещенную атомом галогена или метоксигруппой, C1-C4 галогеналкокси-C1-C4 алкоксигруппу, C1-C4 галогеналкилтио-C1-C4 алкильную группу, -(CH2)qNRb1Rb2 (Rb1 и Rb2 независимо друг от друга представляют собой атом водорода, C1-C4 алкильную группу или C1-C4 галогеналкильную группу, и q равен 1 или 2), или группу, представленную общей формулой (I-B):
[Хим. 5]

где
кольцо C представляет собой C3-C7 циклоалкил, азетидинил, пирролидинил, пиперидил, морфолино, фенил, пиразолил, пиридил, тетрагидроксифуранил, тетрагидроксипиранил или диоксанил,
L2 представляет собой одинарную связь, -C≡C-,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O (CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc (CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2S (CR10eR10f)r3(CR10gR10h)r4-,
(Rc представляет собой C1-C4 алкильную группу,
R10a, R10b, R10c, R10d, R10e, R10f, R10g и R10h независимо друг от друга представляют собой атом водорода или атом галогена,
r1, r2, r3 и r4 независимо друг от друга представляют собой 0, 1 или 2),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атомом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу или C1-C6 алкоксигруппу},
R4b представляет собой гидроксигруппу, C1-C6-алкильную группу,
R4c представляет собой C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4 галогеналкокси-C1-C4 алкильную группу, C3-C7 циклоалкильную группу, C3-C7 циклоалкильную группу, необязательно замещенную C1-C4 галогеналкильной группой, или группу, представленную общей формулой (I-B):
[Хим. 6]

где
кольцо C представляет собой C3-C7 циклоалкил, фенил, пиридил, оксетанил, тетрагидроксифуранил или тетрагидроксипиранил,
L2 представляет собой одинарную связь,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O (CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2CO (CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO2 (CR10eR10f)r3(CR10gR10h)r4-,
(R10a, R10b, R10c, R10d, R10e, R10f, R10g, и R10h независимо друг от друга представляют собой атом водорода, атомом галогена, C1-C4 алкильную группу или C3-C7 циклоалкильную группу,
R10a и R10b вместе со связанным с ними атомом углерода необязательно образуют циклопропан,
r1, r2, r3 и r4 независимо друг от друга представляют собой 0, 1 или 2),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-галогеналкильную группу или C1-C6 алкоксигруппу,
R6a и R6b независимо представляют собой атом водорода, атом фтора, гидроксигруппу или метоксигруппу.
3. Производное гетероароматического амида или его фармакологически приемлемая соль по п. 1 или 2, где в общей формуле (I-E2):
Z4 представляет собой C-R11a,
R11a представляет собой атом водорода,
R11b представляет собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, необязательно замещенную гидрокси, C1-C6-галогеналкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, C1-C4-алкокси-C1-C4-алкильную группу, необязательно замещенную диметиламинокарбонильной группой или диметиламино группой, C1-C4 галогеналкокси-C1-C4 алкильную группу, C2-C6 алкенильную группу, C2-C6 алкинильную группу, необязательно замещенную метокси, или группу, представленную общей формулой (I-A):
[Хим. 7]

где
кольцо B представляет собой C3-C7 циклоалкил, азетидинил, морфолино, пиразолил, тиазолил, триазолил, пиридил, пиразинил, тетрагидроксипиранил или пиримидинил,
L1 представляет собой одинарную связь, -CRa3Ra4-, -CRa3Ra4O-, CH2CH2- или -CH2OCH2- (Ra3 и Ra4 представляют собой атом водорода),
R8a, R8b и R8c независимо друг от друга представляют собой атом водорода, атомы галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6 алкоксигруппу или гетероциклоалкильную группу,
R11c представляет собой атом водорода или атом галогена.
4. Производное гетероароматического амида или его фармакологически приемлемая соль по любому из пп. 1-3, где в общей формуле (I-E2):
R4a представляет собой гидроксигруппу, C1-C6-алкильную группу, пентильную группу, необязательно замещенную гидроксигруппой, C1-C5 галогеналкильную группу, 2,2,2-трифторэтильную группу, необязательно замещенную гидроксигруппой, C1-C2 галогеналкоксигруппу, C2-C4 алкокси-C1-C2 алкильную группу, необязательно замещенную 2,2,2-трифторэтоксигруппой, C1-C3 галогеналкокси-C1-C2 алкильную группу, этокси-монофторметильную группу, C3-C5 циклоалкильную группу, циклопропильную группу, необязательно замещенную C1-C2 галогеналкильной группой, C3 алкинильную группу, необязательно замещенную атомом галогена, C5 алкинильную группу, необязательно замещенную метоксигруппой, C1-C2 галогеналкокси-этокси группу, C1-C2 галогеналкилтио-C1-C2 алкильную группу или -(CH2)qNRb1Rb2 (Rb1 и Rb2 независимо друг от друга представляют собой атом водорода, C1-C2 алкильную группу или 2,2,2-трифторэтильную группу, и q равен 1 или 2),
R1a и R1b независимо друг от друга представляют собой атом водорода, атом фтора или C1-C2 алкильную группу,
R2 представляет собой атом водорода, C1-C2 алкильную группу, необязательно замещенную пиридинильной группой, нафтильной группой, 5-6-членное моноциклическое ароматическое кольцо, необязательно замещенное метилом, этилом, 2,2,2-трифторэтилом, 1-гидрокси-2,2,2,-трифторэтилом, метокси, гидроксиметилом, 2,2,2-трифторэтоксиметилом, метоксиметилом, 2-гидрокси-2-прокси, атомом фтора или атомом хлора,
R5a представляет собой атом водорода.
5. Производное гетероароматического амида или его фармакологически приемлемая соль, представленное общей формулой (I-E2),
[Хим. 8]

где
X1-X2 представляет собой N-C,
Y1, Y2, Y3 и Y4 вместе образуют
-CH2CH2OCH2-, -CH2CR4aHOCH2-,
-CH2CH2CH2CH2-, -CH2CR4aHCH2CH2-,
-CH2CH2NR4cCH2-, -CH2CR4aHNR4cCH2- или -CH2CR4aHNHCH2-,
R4a, R4b и R4c независимо друг от друга представляют собой C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6 алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6 галогеналкилкарбонильную группу, C3-C7 циклоалкильную группу, C3-C7 циклоалкильную группу, необязательно замещенную атомом галогена, C1-C4 галогеналкокси-C1-C4 алкоксигруппу, или группу, представленную общей формулой (I-B):
[Хим. 9]

где
кольцо C представляет собой C3-C7 циклоалкил, тиенил или пиридил,
L2 представляет собой одинарную связь,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O (CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc (CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO2NRc (CR10eR10f)r3(CR10gR10h)r4-
(Rc представляет собой атом водорода или C1-C4 алкильную группу,
R10a, R10b, R10c, R10d, R10e, R10f, R10g, и R10h представляют собой атом водорода,
r1, r2, r3 и r4 независимо друг от друга представляют собой 0, 1 или 2),
R9a, R9b и R9c независимо друг от друга представляют собой атом водорода, атом галогена, C1-C6-алкильную группу, C1-C6-галогеналкильную группу или C1-C6 алкоксигруппу,
R1a и R1b представляют собой атом водорода,
R2 представляет собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, необязательно замещенную гидроксигруппой, C2-C6 алкенильную группу или 5-6-членное моноциклическое ароматическое кольцо, необязательно замещенное метилом, метокси, 2,2,2-трифторэтокси или атомом галогена,
Z2-Z3 представляет собой -CH2O-,
R5a представляет собой атом водорода, C1-C6-алкильную группу или аралкильную группу,
R6a и R6b представляют собой атом водорода,
Z4 представляет собой C-R11a,
R11a представляет собой атом водорода, атом галогена, цианогруппу, цианометильную группу, C1-C6-галогеналкильную группу, C1-C4 алкокси-C1-C4 алкильную группу, C3-C7 циклоалкильную группу или C2-C6 алкенильную группу,
R11b и R11c независимо друг от друга представляют собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6 алкоксигруппу, C1-C4 галогеналкокси-C1-C4 алкильную группу, или группу, представленную общей формулой (I-A):
[Хим. 10]

где
кольцо B представляет собой C3-C7 циклоалкил,
L1 представляет собой одинарную связь,
R8a, R8b и R8c представляют собой атом водорода
(при условии, что кольцо C не является фенильным кольцом, если Y1, Y2, Y3 и Y4 вместе образуют -CH2CR4aHCH2CH2-, R2 представляет собой атом водорода, R4a представляет собой группу, представленную общей формулой (I-B), и L2 представляет собой одинарную связь,
(при условии, что Y1, Y2, Y3 и Y4 вместе не образуют, -CH2CH2OCH2-, или -CH2CH2CH2CH2-, когда R2 представляет собой атом водорода).
6. Производное гетероароматического амида или его фармакологически приемлемая соль по п. 5, где в общей формуле (I-E2):
R4a представляет собой C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6 алкоксигруппу, C1-C6-галогеналкоксигруппу, C3-C7 циклоалкильную группу, C3-C7 циклоалкильную группу, необязательно замещенную атомом галогена, C1-C4 галогеналкокси-C1-C4 алкоксигруппу, или группу, представленную общей формулой (I-B):
[Хим. 11]

где
кольцо C представляет собой C3-C7 циклоалкил, тиенил или пиридил,
L2 представляет собой одинарную связь,
-(CR10aR10b)r1(CR10cR10d)r2(CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2O (CR10eR10f)r3(CR10gR10h)r4-,
-(CR10aR10b)r1(CR10cR10d)r2NRc (CR10eR10f)r3(CR10gR10h)r4- или
-(CR10aR10b)r1(CR10cR10d)r2SO2NRc (CR10eR10f)r3(CR10gR10h)r4-
(Rc, R10a, R10b, R10c, R10d, R10e, R10f, R10g, R10h, r1, r2, r3, r4, R9a, R9b, и R9c имеют такое же определение, что и в п. 5),
R4c представляет собой C1-C6-алкильную группу, C1-C6-галогеналкильную группу или C1-C6 галогеналкилкарбонильную группу,
R11b представляет собой атом водорода, атом галогена, цианогруппу, C1-C6-алкильную группу, C1-C6-галогеналкильную группу, C1-C6 алкоксигруппу, C1-C4 галогеналкокси-C1-C4 алкильную группу или C3-C7 циклоалкильную группу.
7. Производное гетероароматического амида или его фармакологически приемлемая соль по п. 1 или 5, где соединение, представленное общей формулой (I-E2) (при этом звездочки (*) в структурных формулах означают, что стереоструктура соответствующего асимметричного атома углерода имеет единую стерическую структуру), представляет собой любое из следующего:
[Хим. 12]

[Хим. 11]


[Хим. 12]
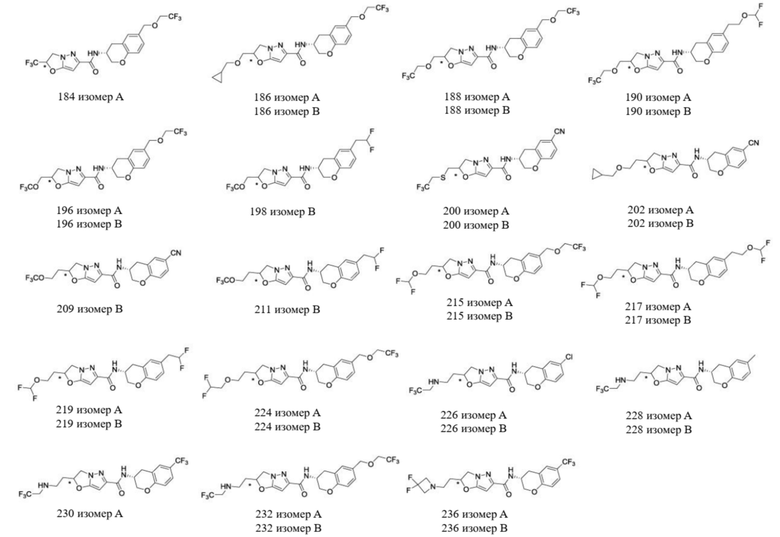
[Хим. 13]


[Хим. 14]

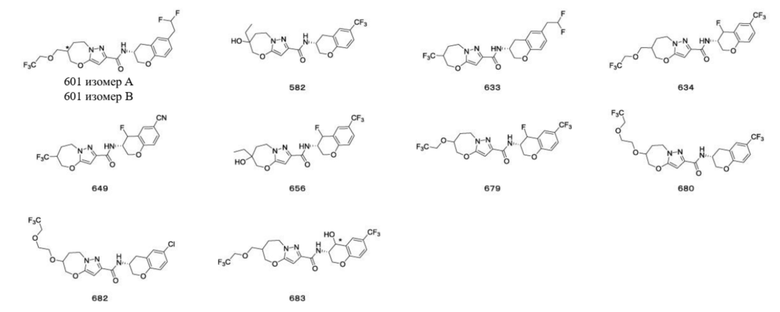
[Хим. 15]

[Хим. 16]


[Хим. 17]

[Хим. 18]
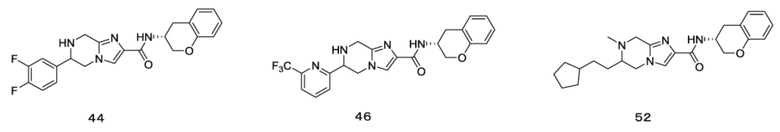
[Хим. 19]

8. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении Nav1.7, содержащая эффективное количество производного гетероароматического амида или его фармакологически приемлемой соли по любому из пп. 1-7.
9. Фармацевтическая композиция для предупреждения или лечения нарушения, ассоциированного с функцией потенциал-зависимого натриевого канала Nav1.7, содержащая в качестве активного ингредиента эффективное количество производного гетероароматического амида или его фармакологически приемлемой соли по любому из пп. 1-7.
10. Средство, обладающее ингибирующей активностью в отношении Nav1.7, для предупреждения или лечения нарушения, сопровождающегося болью, содержащее в качестве активного ингредиента производное гетероароматического амида или его фармакологически приемлемую соль по любому из пп. 1-7.
11. Средство, обладающее ингибирующей активностью в отношении Nav1.7, для предупреждения или лечения нарушения, сопровождающегося зудом, содержащее в качестве активного ингредиента производное гетероароматического амида или его фармакологически приемлемую соль по любому из пп. 1-7.
12. Средство, обладающее ингибирующей активностью в отношении Nav1.7, для предупреждения или лечения нарушения, ассоциированного с функцией вегетативных нервов, содержащее в качестве активного ингредиента производное гетероароматического амида или его фармакологически приемлемую соль по любому из пп. 1-7.
13. Обезболивающее средство, обладающее ингибирующей активностью в отношении Nav1.7, содержащее в качестве активного ингредиента производное гетероароматического амида или его фармакологически приемлемая соль по любому из пп. 1-7.
14. Средство, обладающее ингибирующей активностью в отношении Nav1.7, для предупреждения или устранения ноцицептивной боли, содержащее в качестве активного ингредиента производное гетероароматического амида или его фармакологически приемлемую соль по любому из пп. 1-7.
15. Средство, обладающее ингибирующей активностью в отношении Nav1.7, для предупреждения или устранения невропатической боли, содержащее в качестве активного ингредиента производное гетероароматического амида или его фармакологически приемлемую соль по любому из пп. 1-7.
16. Применение производного гетероароматического амида или его фармакологически приемлемой соли по любому из пп. 1-7 для изготовления фармацевтической композиции, обладающей ингибирующей активностью в отношении Nav1.7, применяемой для предупреждения или устранения боли.
17. Применение производного гетероароматического амида или его фармакологически приемлемой соли по любому из пп. 1-7 для изготовления обезболивающего средства, обладающего ингибирующей активностью в отношении Nav1.7.
| WO2018109097A1, 21.06.2018 | |||
| WO2017004500A1, 05.01.2017 | |||
| Высокочастотный фильтр-смеситель | 1965 |
|
SU1309257A1 |
| Электропривод постоянного тока | 1985 |
|
SU1309231A1 |
| Способ автоматического регулирования режима работы химических реакторов | 1986 |
|
SU1380773A1 |
| Способ измерения толщины покрытия на поверхности пленочного материала | 1990 |
|
SU1795267A1 |
| Глубиномер | 1990 |
|
SU1795259A1 |
| Способ определения выбросоопасности угольных пластов | 1991 |
|
SU1789032A3 |
Авторы
Даты
2024-02-06—Публикация
2019-09-09—Подача