Изобретение относится к области нефтепереработки и может быть использовано на нефте- и газоперерабатывающих заводах для утилизации кислых газов и синтеза сульфида натрия, в частности, предлагаемый способ может быть использован на установках, вырабатывающих кислый газ (газ регенерации аминов).
Изучением процесса получения сульфида натрия занимаются многие исследователи разных стран. Изучение этого процесса ведется по разным направлениям. Промышленный синтез данного вещества заключается в прокаливании глауберовой соли (минерала, известного под названием мирабилит). Это один из распространенных способов. Другой, не менее распространенный вариант получения заключается в восстановлении натриевой соли серной кислоты с помощью угля при температуре в диапазоне от 800 °C до 1000 °C. Для его реализации задействуют вращающиеся шахтные печи.
Преимущество получения Na2S абсорбцией сероводорода кислых газов регенерации амина обусловлено доступностью сырья, которое имеется практически на всех нефте- и газоперерабатывающих предприятиях. Для того чтобы абсорбция сероводорода гидроксидом натрия прошла с образованием конечного продукта сульфида натрия, необходимо использовать определенную концентрацию едкой щелочи (Федорова О.В. Абсорбция раствором гидроксида натрия сероводорода, выделяемого при воздействии серной кислотой на черный щелок сульфатцеллюлозного производства / О.В. Федорова, В.Г. Казаков, К.О. Субботина // Известия Санкт-Петербургской лесотехнической академии - 2019. - Вып. 226. - С.197-207). Аппаратура, предназначаемая для абсорбции сероводорода не специфична, поэтому поглощение сероводорода может быть произведено с помощью большинства абсорберов, применяемых в химической промышленности.
Известен способ получения сульфида натрия взаимодействием 20-30 %-ного раствора гидроксида натрия с сероводородсодержащим газом при температуре раствора +5-0 °С до рН 10,0-12,0 при непрерывном пропускании тока азота, описанный в патенте (Патент KZ № 12596, опубл. 13.11.2002). Выход готового продукта достигает 80-85 %.
Известен способ получения сульфида натрия (А.с. SU № 1810296, МПК С01В 17/22, опубл. 23.04.1993 г., Бюл. № 15) описывается способ получения сульфида натрия путем взаимодействия сероводородсодержащего газа с гидроксидом натрия и последующей кристаллизацией расплава сульфида натрия. Согласно изобретению, взаимодействие ведут в две стадии: на первой стадии абсорбируют сероводородсодержащий газ расплавленным гидроксидом натрия при температуре 110-140 °С. При этом вводят сероводород с 5-20 %-ным избытком от стехиометрически необходимого для образования сульфогидрата натрия в виде расплава и 95-105 % воды, которую выводят, конденсируя выделяющиеся пары. Контролируя выделившееся количество воды, судят об окончании первой стадии. На второй стадии расплав сульфогидрата натрия обрабатывают твердым гидроксидом натрия при температуре 160-180 °С. Полученный расплав кристаллизуют в виде чешуек при охлаждении.
Известен способ получения сульфида натрия (А.с. СССР SU № 1159880, МПК С01В 17/22, опубл. 07.06.1985 г., Бюл. № 21) из растворов сульфогидрата натрия и едкого натра, включающий предварительную очистку их от примесей металлов, осаждение основной соли сульфида натрия из раствора сульфогидрата натрия избытком едкого натра, отделение осадка и промывка его с образованием маточных и промывных вод, которые подвергают упариванию в присутствии металлического цинка до полного осаждения содержащихся в них примесей тяжелых металлов, восстановления тиосульфатов и полисульфидов, после чего упаренный раствор смешивают с сульфогидратом натрия до содержания последнего в растворе 60-70 г/л, подвергают двухстадийной очистке в присутствии свежеосажденного сульфида цинка и полиакриламида, а затем из очищенного раствора избытком едкого натра высаливают основную соль целевого продукта с последующей его промывкой.
Известен способ получения сульфида натрия (А.с. СССР SU № 712384, МПК С01В 17/22, опубл. 30.01.1980 г., Бюл. № 4) из бисульфидсодержащих растворов, являющихся отходом содовой очистки серосодержащих газов с концентрацией NaHS ~ 200 г/л. Сущность способа в том, что исходный NaHS-содержащий раствор подвергают взаимодействию с едким натром при избытке последнего, превышающем стехиометрическое количество на 60-70 г/л, с последующим выделением основной соли сульфида натрия и промывкой его насыщенным раствором сульфида натрия. Причем исходные растворы подвергают предварительной очистке: едкий натр очищают окисью кальция, гашеной в растворе полиакриламида, а бисульфид натрия обрабатывают окисью цинка, подкисленной уксусной кислотой.
Недостатком способа являются потери сульфида натрия, едкого натра с маточными и промывочными водами, поскольку переработка их не предусмотрена.
Этот недостаток исключает способ, описанный выше в патенте № 1159880. Предлагаемый способ позволяет получать товарный продукт из сульфидсодержащих выбросов, тем самым снизить потери Na2S со сточными водами. Продукт, полученный по этой технологии имеет следующий состав, масс.%: Na2Sx9H2O 97,2-99,8; тиосульфаты в пересчете на SO2 0,05-0,1; азотсодержащие примеси 0,002-0,004; тяжелые металлы 0,000-0,002.
Наиболее близким к предлагаемому способу по сущности и достигаемому результату является способ, описанный в (патент CN104709884, опубл. 17.06.2015). В изобретении CN104709884 предлагается система селективного производства сульфида натрия или гидросульфида натрия абсорбцией сероводорода щелоком. Предусмотрена система концентрированной кристаллизации сульфида натрия, система упаковки продукта. Сульфид натрия образуется при избытке щелочи, а гидросульфид натрия образуется при избытке сероводорода. В абсорбционную колонну вводят газообразный сероводород с содержанием 98 % из системы очистки сероводорода (содержание диоксида углерода контролируют на уровне менее 2 %, чтобы избежать реакции диоксида углерода с гидроксидом натрия с образованием карбоната натрия), чтобы увеличить скорость поглощения сероводородного газа, добавляют определенное количество азота, газовая нагрузка невелика, и азот может быть сброшен в сероводородный газ, чтобы равномерно заполнить пространство оборудования, и вакуумный насос можно поддерживать в вакууме, так что оборудование поддерживает микроотрицательное давление. Рабочее давление абсорбционной колонны составляет - 0,02 МПа.
Раствор сульфида натрия в резервуаре для хранения жидкости концентрируют выпариванием, а затем кристаллизуют в охлаждающем кристаллизационном резервуаре. В результате получают сульфид натрия с содержанием кристаллогидрата Na2Sx(5-9)H2O.
Содержание железа в производимом сегодня сульфиде натрия обычно достигает 150 ppm. Однако с развитием промышленности содержание железа в сульфиде натрия уже не может удовлетворять промышленный спрос. Поэтому существует острая необходимость в производстве сульфида натрия с содержанием железа менее 30 ppm.
Недостатками указанных выше способов являются:
1) очистка едкого натра окисью кальция, гашеной в растворе полиакриламида, что является дополнительным действием и повышает уровень капитальных и эксплуатационных затрат в процессе синтеза Na2S;
2) высокая температура (110-160 °С) при выпаривании раствора сульфида натрия;
3) обработка бисульфида натрия окисью цинка, подкисленной уксусной кислотой, что является дополнительным действием и повышает уровень капитальных и эксплуатационных затрат в процессе синтеза Na2S.
Технической задачей настоящего изобретения является синтез сульфида натрия c cодержанием основного вещества 63-67 % масс. (кристаллогидрат Na2Sх(2-3)H2O) и с содержанием железа менее 0,0030 ppm. Выполнение поставленной технической задачи позволяет устранить недостатки описанных выше предыдущих способов.
Техническая задача решается способом получения сульфида натрия абсорбцией сероводородсодержащего газа раствором гидроксида натрия, включающим получение сульфида натрия.
Новым является то, что 20-30 %-ный раствор гидроксида натрия насыщают сероводородсодержащим газом с содержанием сероводорода 97-99 % масс. до образования гидросульфида натрия, затем для получения сульфида натрия к полученному гидросульфиду натрия добавляют 40-46 %-ный раствор гидроксида натрия в количестве, соответствующем мольному соотношению NaSН/NaОН = 1:1, и одновременно с получением сульфида натрия производят сушку получаемого продукта в реакторе-сушилке под вакуумом при остаточном давлении 8-20 мм рт. ст. и при температуре 80-90 °С с получением 63-67 % масс. кристаллогидрата Na2Sх(2-3)H2O с содержанием железа менее 0,003 % масс., при этом глубина осушки сульфида натрия зависит от температурной депрессии, рассчитанной по формуле:
Δt = tp - tв,
где tp - рабочая температура процесса;
tв - температура кипения воды при рабочем давлении.
Для осуществления способа получения сульфида натрия абсорбцией сероводородсодержащего газа раствором гидроксида натрия используют:
- едкий натр, очищенный, марки А в соответствии с ГОСТ 11078-78 с содержанием железа 0,0005 % масс.;
- вода дистиллированная в соответствии с ГОСТ Р 58144-2018 с содержанием железа не более 0.05 мг/дм3;
- аргон газообразный в соответствии с ГОСТ 10157-79;
- азот газообразный повышенной чистоты в соответствии с ГОСТ 9293-74.
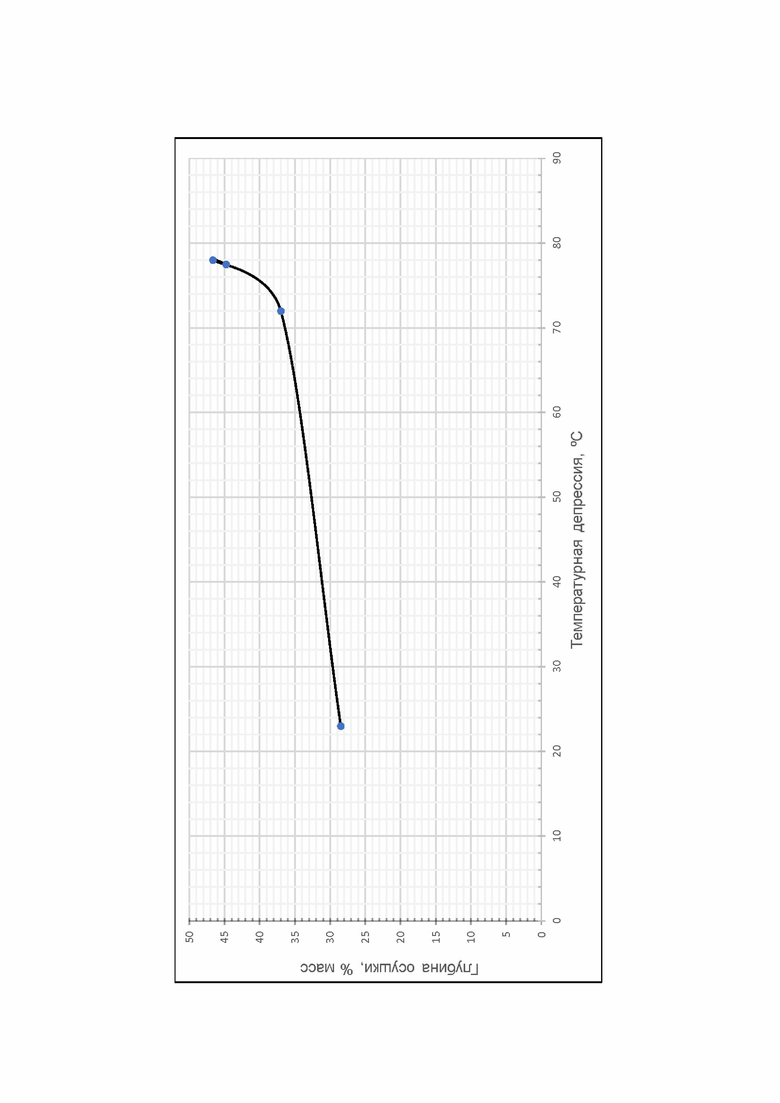
На фиг. показана зависимость глубины осушки сульфида натрия от температурной депрессии.
Способ осуществляют в следующей последовательности.
Насыщают 20-30 %-ный раствор гидроксида натрия сероводородсодержащим газом (с содержанием сероводорода 97-99 % масс.) до образования гидросульфида натрия. Для получения сульфида натрия к полученному гидросульфиду натрия добавляют 40-46 %-ный раствор гидроксида натрия в количестве, соответствующем мольному соотношению NaSН/NaОН = 1:1, и одновременно с получением сульфида натрия производят сушку получаемого продукта в одном аппарате - реакторе-сушилке под вакуумом при остаточном давлении 8-20 мм рт. ст. и при температуре 80-90 °С с получением 63-67 % масс. кристаллогидрата Na2Sх(2-3)H2O с содержанием железа менее 0,003 % масс.
При этом глубина осушки сульфида натрия зависит от температурной депрессии, рассчитанной по формуле:
Δt = tp - tв,
где tp - рабочая температура процесса;
tв - температура кипения воды при рабочем давлении.
Содержание сульфида натрия в синтезированном продукте определяют путем потенциометрического титрования по Методике выполнения измерений (МВИ) концентраций сульфидной и меркаптидной серы в щелочных растворах. Аттестована ФГУП ВНИИРасходометрии Государственный научно-метрологический центр. Свидетельство № 1106-02 от 25.12.2001 г.
Первую стадию процесса - получение гидросульфида натрия - проводили в режиме контактирования раствора едкого натра с сероводородсодержащим газом (кислый газ регенерации аминов) при температуре 17-40 °С, атмосферном давлении и концентрации раствора едкого натра 20-30 % масс. Для проведения опытов использовали стеклянный реактор объемом 150 мл, снабженный термометром и трубкой для подачи сероводородсодержащего газа. Расход газа контролировали по ротаметру. Перемешивание реакционной массы осуществляли магнитной мешалкой. На второй стадии полученный раствор гидросульфида натрия переливали в реактор-сушилку, предварительно заполненный аргоном, добавляли расчетное количество 42 %-ного раствора гидроксида натрия и сушили реакционную массу под вакуумом при остаточном давлении 8-20 мм рт.ст. и температуре 80-90 °С.
Пробу полученного сульфида натрия анализировали на содержание основного вещества и железа.
Пример конкретного выполнения.
В стеклянный реактор загружают 61-67 г 21-30 %-ного раствора едкого натра и при постоянном перемешивании через него пропускают 9 - 14 г кислого газа с концентрацией сероводорода 98,94 % масс. (до полного насыщения раствора). Температура абсорбции сероводорода равна 17-40 °С. Для лучшего поглощения сероводорода реактор охлаждают льдом. По завершению насыщения раствора гидроксида натрия сероводородом реакционную массу переливают в реактор-сушилку, предварительно заполненный аргоном, приливают расчетное количество 41,8 %-ного раствора гидроксида натрия. В одном аппарате одновременно протекает и кристаллизация, и сушка сульфида натрия под вакуумом при остаточном давлении 8-20 мм рт. ст. и температуре 80-90 °С. Полученный кристаллический продукт анализируют на содержание сульфида натрия потенциометрическим титрованием. Содержание железа в пробе определяют с использованием метода рентгенофлюоресцентной спектроскопии с применением Метода Фундаментальных Параметров на спектрометре Clever (режим съемки: ток трубки 200 мкА; напряжение трубки 45 кВ; фильтр Ti; время съемки 500 с; среда воздух). По результатам анализов установлено, что содержание железа в пробах сульфида натрия не превышает 17 ppm (3-17 ppm). Результаты проведенных опытов представлены в таблицах 1, 2 и 3.
NaHS
NaHS
NaHS
Результаты двухстадийного синтеза показали удовлетворительный выход Na2S, который в зависимости от условий проведения экспериментов составил 76-91 % (таблица 3). Выход основного продукта зависит от выхода промежуточного NaНS на первой стадии, который в свою очередь зависит от мольного соотношения NaOH/H2S, чем ниже это соотношение, тем выше выход NaНS и наоборот. Так в опыте № 4 таблица 3 при соотношении NaOH/H2S = 1,61 выход гидросульфида натрия снизился до 80 %, что объясняется реакцией образования Na2S.
Преимущество двухстадийного синтеза Na2S перед одностадийным заключается в том, что на первой стадии не образуется твердая фаза, реакционная масса жидкая и однофазная. В промышленном масштабе легко может осуществляться в колонных аппаратах без забивки газораспределительного устройства и без налипания кристаллов Na2S на поверхность аппаратов.
Для получения сульфида натрия с содержанием 63-67 % масс. (кристаллогидрат Na2Sх(2-3)Н2О) необходима сушка полученного сульфида натрия. Глубина осушки сульфида натрия зависит от термобарических условий процесса. Для выявления данной зависимости определены величины температурной депрессии, которые были рассчитаны по формуле:
Δt=tp - tв,
где tp - рабочая температура процесса;
tв - температура кипения воды при рабочем давлении.
На фиг. представлена зависимость глубины осушки (потеря массы) от температурной депрессии. На фиг. видно, что с ростом Δt до 70 °С зависимость имеет линейный характер, потеря массы плавно растет от 27 до 37 % с увеличением температурной депрессии. При Δt > 70 °С происходит резкое увеличение потери массы с 37 до 47 %, именно при данных условиях происходит вскипание расплавленного осадка.
При помощи способа получения сульфида натрия абсорбцией сероводородсодержащего газа раствором гидроксида натрия синтезируют сульфид натрия c cодержанием основного вещества 63-67 % масс. (кристаллогидрат Na2Sх(2-3)H2O) и с содержанием железа менее 0,0030 ppm.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения сульфида натрия | 1991 |
|
SU1810296A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОСУЛЬФИДА НАТРИЯ | 2004 |
|
RU2288169C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОСУЛЬФИДА НАТРИЯ | 2004 |
|
RU2281910C2 |
| СПОСОБ ОЧИСТКИ ПИРОГАЗА ОТ ДИОКСИДА УГЛЕРОДА И СЕРОВОДОРОДА | 1992 |
|
RU2019271C1 |
| Способ получения сульфида натрия | 1983 |
|
SU1159880A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ МОЛИБДЕНА ИЗ ПРОДУКТОВ КАТАЛИТИЧЕСКОГО ЭПОКСИДИРОВАНИЯ ОЛЕФИНОВ | 2007 |
|
RU2335499C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОГЕННОГО СЕРОВОДОРОДА | 2014 |
|
RU2577114C1 |
| СПОСОБ ОЧИСТКИ НЕФТИ И ГАЗОКОНДЕНСАТА ОТ СЕРОВОДОРОДА | 1996 |
|
RU2109033C1 |
| СПОСОБ ОЧИСТКИ ПИРОГАЗА ОТ ДИОКСИДА УГЛЕРОДА И СЕРОВОДОРОДА | 1992 |
|
RU2065319C1 |
| Способ очистки газа от сероводорода | 2023 |
|
RU2824351C1 |
Изобретение может быть использовано на нефте- и газоперерабатывающих заводах при утилизации кислых газов. Для получения сульфида натрия 20-30% раствор гидроксида натрия насыщают сероводородсодержащим газом с содержанием сероводорода 97-99% масс. до образования гидросульфида натрия. Затем к полученному гидросульфиду натрия добавляют 40-46% раствор гидроксида натрия в количестве, соответствующем мольному соотношению NaSН/NaОН=1:1. Одновременно с получением сульфида натрия проводят сушку получаемого продукта в реакторе-сушилке под вакуумом при остаточном давлении 8-20 мм рт. ст. и при температуре 80-90°С. Изобретение позволяет получить кристаллогидрат сульфида натрия Na2S⋅(2-3)H2O с содержанием основного вещества 63-67% масс. и содержанием железа менее 0,003% масс. 1 ил., 3 табл., 1 пр.
Способ получения сульфида натрия абсорбцией сероводородсодержащего газа раствором гидроксида натрия, включающий получение сульфида натрия, отличающийся тем, что 20-30%-ный раствор гидроксида натрия насыщают сероводородсодержащим газом с содержанием сероводорода 97-99% масс. до образования гидросульфида натрия, затем для получения сульфида натрия к полученному гидросульфиду натрия добавляют 40-46%-ный раствор гидроксида натрия в количестве, соответствующем мольному соотношению NaSН/NaОН=1:1, и одновременно с получением сульфида натрия производят сушку получаемого продукта в реакторе-сушилке под вакуумом при остаточном давлении 8-20 мм рт. ст. и при температуре 80-90°С с получением 63-67% масс. кристаллогидрата Na2S⋅(2-3)H2O с содержанием железа менее 0,003% масс., при этом глубина осушки сульфида натрия зависит от температурной депрессии, рассчитанной по формуле:
∆t=tp–tв,
где tp – рабочая температура процесса;
tв – температура кипения воды при рабочем давлении.
| CN 104709884 B, 24.08.2016 | |||
| СПОСОБ ПОЛУЧЕНИЯ СЕРПИСТОГО НАТРИЯ | 0 |
|
SU399455A1 |
| CN 1944241 B, 29.12.2010 | |||
| CN 105905871 B, 28.08.2018 | |||
| JP S63139007 A, 10.06.1988. | |||
Авторы
Даты
2024-02-19—Публикация
2023-09-05—Подача