Изобретение относится к области химической технологии, а именно, к высокотемпературным каталитическим окислительным способам превращения метана с получением синтез-газа: смеси Н2 и СО, являющегося исходным сырьем для получения водорода, моторных топлив, метанола, диметилового эфира, альдегидов, спиртов и других ценных веществ, а также к катализаторам и способу их получения для этой цели.
Процесс углекислотной конверсии природного газа протекает с образованием синтез-газа с соотношением Н2/СО~1, что позволяет без дополнительной обработки широкого использовать его в ряде промышленных синтезов компонентов топлив и ценных химических продуктов. Также данный процесс позволяет получать ценные продукты из двух основных парниковых газов.
Однако проблема создания высокоактивных и устойчивых к зауглероживанию катализаторов для данного процесса до сих пор не решена и остается одной из самых актуальных в гетерогенном окислительном катализе.
В качестве катализаторов углекислотной конверсии метана используют оксидные системы, которые в процессе катализа преобразуются в композиты, состоящие из металлических активных центров (никель, кобальт, металлы платиновой группы), диспергированных в матрице оксидных носителей (S. Bhattar, М.А. Abedin, S. Kanitkar, J.J. Spivey. A review on dry reforming of methane over perovskite derived catalysts. Catalysis Today, 2021, V. 365, P. 2-23.)
Известен катализатор и способ получения синтез-газа углекислотной конверсией метана, описанный в патенте RU 2453366, опубл. 2012. Катализатор углекислотной конверсии метана для получения синтез-газа представляет собой сложный носитель на основе церия-циркония, содержащего один или два металла, выбранные из группы редкоземельных элементов, таких как Pr, Sm, La, или их любую комбинацию, в качестве активного компонента содержит металл платиновой группы, выбранный из Pt или Ru; Pt или Ru с добавками Ni; La с добавками Ni; La с добавками Ni, Pt или Ru, при этом катализатор имеет общую формулу М1М2М3[АхВу Ce0.35Zr0.35]O2, где: х равен 0-0,3, у=0-0,3, А и/или В выбирают из металлов редкоземельных элементов Pr, La, Sm, M1 - выбирают из металлов платиновой группы - Pt или Ru; М2 - это Ni; М3 - La, при условии, если содержание металла М1=0, то содержание М2≠0, и если содержание М2=0, то содержание М1≠0. Для приготовления сложного оксидного носителя AxByCe0.35Zr0.35O2 используют 8-водный оксихлорид циркония (чда), 6-водный нитрат церия (чда), 6-водный нитрат празеодима (осч) и/или 6-водный нитрат самария (осч) и/или 6-водный нитрат лантана (чда), лимонную кислоту (ЛК, чда), этиленгликоль (ЭГ, ч), этилендиамин (ЭД). Реагенты берут в мольных соотношениях ЛК:ЭГ:ЭД:Ме ((Pr и/или Sm и/или La)+Ce+Zr)=3,75:11,25:3,75:1. Лимонную кислоту растворяют в этиленгликоле в соотношение ЛК:ЭГ=1:3 при перемешивании на водяной бане (60-80°С). Параллельно в 30 мл дистиллированной воды растворяют кристаллогидрат нитрата церия при перемешивании на водяной бане, при этом раствор был прозрачным, затем в него добавляют кристаллогидрат нитрата празеодима и/или самария, и/или лантана и перемешивают до полного растворения, образовавшийся раствор был бесцветный (салатовый - для празеодима). В смешанный раствор добавляют раствор лимонной кислоты в этиленгликоле, полученный ранее. При постоянном перемешивании без водяной бани добавляют этилендиамин, происходил разогрев раствора, и он становился темно-желтым (иногда темно-коричневым) и густым, при этом рН раствора повышается до ~ 5. Полученный раствор выдерживают при 80°С в течение 3 суток для удаления избытка растворителя, затем полученное вещество прокаливают в интервале температур до 900°С. На полученные допированные оксиды церия-циркония наносят платину или рутений в количестве 1-1,5 мас. % методом пропитки раствором H2PtCl6 или RuCl3 по влагоемкости. Полученные вещества сушат на воздухе и прокаливают при 900°С (для платины) или при 800°С (для рутения) в течение 1 ч. Катализатор, содержащий смешанный оксид церия-циркония в соотношении 1:1 и содержащий празеодим и/или самарий, празеодим и/или лантан с нанесенным активным компонентом - платиной или рутением, прессуют в таблетки диаметром 15 мм под давлением 2 МПа. Затем из таблетки, предварительно измельченной в агатовой ступке, используя сита с фиксируемым размером отверстий, готовят фракцию с размером частиц 0,25-0,5 мм. Способ получения синтез-газа в процессе углекислотной конверсии метана осуществляют с использованием катализатора при температуре 650-850°С. Реакционная смесь поступает в проточный реактор идеального вытеснения в соотношении 7% метана, 7% диоксида углерода и 86% азота. Наилучший результат получают на катализаторах RuNi/Pr0,3Ce0,35Zr0,35O2 и RuNi/Sm0,15Pr0,15Ce0,35Zr0,35O2. При 850°С конверсия СН4 составляет 97,1-99,6%, конверсия CO2 - 95,6-97,7%.
Несмотря на достигнутые высокие выходы синтез-газа, способ имеет недостатки: сильное разбавление продукта инертным газом- азотом, использование катализатора, характеризующегося сложной многостадийной процедурой приготовления и использованием дорогостоящих металлов платиновой группы.
Более близким к заявляемому является способ получения синтез-газа, описанный в патенте RU 2572530, опубл. 2016 г., высокотемпературным каталитическим окислительным превращением метана, заключающийся в подаче в реактор, в который помещен катализатор, исходной газовой смеси, содержащей смесь метана и углекислого газа с объемным отношением метан: CO2=1-1,1:1, при температуре на катализаторе 880-972°С, причем катализатор представляет из себя сложный оксид, включающий в свой состав ионы кобальта (Со), никеля (Ni), меди (Cu), неодима (Nd), кальция (Са), причем мольные соотношения веществ катализатора, соответствуют формулам NdaCabCucNidCoeOf, где а=0, 1, 2; b=0, 1, 2; с=0, 1; d=0, 1,2; е=0, 1, 2; f=3, 4, 5.
При этом получают катализатор путем растворения в воде, выпаривания раствора до загустения, высушивания в муфельной печи при 300°С и прокаливания 5 ч при 900°С, исходных веществ, содержащих растворимые в воде соединения Nd, Са, Со, Ni, Cu, образующих при прокаливании оксиды указанных металлов. Предпочтительно в качестве исходных веществ используют нитрат неодима Nd(NO3)3•6H2O, оксид кальция СаО, нитрат кобальта Co(NO3)2•6H2O, нитрат никеля Ni(NO3)2•6H2O, нитрат меди Cu(NO3)2•6H2O.
Получаемый технический результат заключается в повышении конверсии метана, выходов оксида углерода и водорода, в упрощении технологии проведения способа и сокращении затрат за счет проведения процесса в отсутствие инертных газов, а также использования катализатора, получаемого более простым способом.
Недостатком способа является недостаточно высокая производительность активных центров, описанных в способе катализаторов, по целевым продуктам - водороду и СО, образующим получаемый синтез-газ. Из описания изобретения следует, что в данном способе загрузка катализаторов составляет 0,2 г, в реактор подается метан-углекислотная смесь с объемным отношением метан: CO2, равным 1-1,1:1 со скоростью подачи от 7,2 до 12,9 л/г катализатора в час. При этом, несмотря на высокие выходы водорода и СО, достигающие 98-100%, производительность катализаторов по целевым продуктам не превышает 13 л СО/г катализатора в час и 13 л Н2/г катализатора в час. Данная максимальная производительность достигнута на катализаторе, образующемся из Ca2Co2O5, при 970°С.Другие описанные в способе катализаторы являются менее производительными.
Задача предлагаемого технического решения заключается в разработке способа получения синтез-газа углекислотной конверсией метана, обеспечивающего более высокие производительность катализатора и выходы СО и Н2, а также обеспечивающий быстрый выход катализатора на оптимальный режим его работы.
Поставленная задача решается тем, что предложен способ получения синтез-газа высокотемпературным каталитическим окислительным превращением метана, путем подачи исходной газовой смеси, содержащей смесь метана и углекислого газа, в реактор со сложнооксидным катализатором при повышенной температуре, отличающийся тем, что в качестве катализатора используют сложный оксид кобальта (Co) и самария (Sm), полученный смешением исходных соединений кобальта и самария, взятых в стехиометрических соотношениях, отвечающих содержанию кобальта в продукте после прокаливания равном 2% по массе, с прокаливанием полученной смеси при повышении температуры от комнатной до 800°С в течение 3 часов и выдерживают при данной температуре в течение 2 ч с получением сложного оксида кобальта (Со) и самария (Sm), расположенный в вертикальном реакторе на подложке из кварцевого волокна, перед катализатором помещают небольшое количество кварцевой крошки, выполняющей роль смесителя газов, катализатор разогревают в токе азота до 900°С, после чего отключают подачу азота и подают в реактор смесь метана и углекислого газа, поддерживая температуру катализатора 900°С в течение протекания всего процесса окислительного превращения метана.
Согласно изобретению в качестве исходной газовой смеси используют смесь метана и углекислого газа с объемным отношением метан: CO2, равным 0,98-1,04:1, подаваемой со скоростью 15-16 л/г катализатора в час.
По изобретению в качестве исходных соединений кобальта и самария при получении катализатора используют нитрат самария Sm(NO3)3*6H2O и нитрат кобальта Co(NO3)2*6H2O,
Технические результаты, которые могут быть получены от использования предлагаемого способа, заключаются
- в увеличении выхода продуктов синтез-газа - Н2 95-98% и СО 96-99%;
- в увеличении производительности по Н2 14,7-15,3 л/г катализатора в час и по СО 14,7-15,5 л/г катализатора в час;
- предлагаемый способ позволяет быстро выводить катализатор на оптимальный режим его работы;
- позволяет достигать стабильных показателей в течение 50 и более часов.
Способ получения катализатора по изобретению характеризуется простотой технологии и доступностью исходных компонентов. В качестве исходных веществ при получении катализатора возможно использовать различные водорастворимые соединения вышеуказанных металлов, такие, как, например, нитраты, хлориды, сульфаты, ацетаты, образующих при прокаливании оксиды и сложные оксиды металлов, в частности, используют Sm в виде нитрата Sm(NO3)3*6H2O, Со в виде нитрата Co(NO3)2*6H2O.
Исходные компоненты растворяют в воде, и образовавшийся раствор выпаривают, высушивают в муфельной печи и прокаливают при 800°С. Полученную массу измельчают и отсеивают фракцию 0,5-1 мм, которую в количестве 0,2±0,01 г загружают в реактор для использования в качестве катализатора высокотемпературного окислительного превращения метана в способе получения синтез-газа. Допустимо использование катализатора в виде порошка, частиц произвольного размера, либо в виде таблеток при проведении процесса в реакторе большего объема.
Приведенные ниже примеры иллюстрируют изобретение, но не ограничивают его.
Пример 1. Получение катализатора
Для приготовления катализатора в качестве исходных компонентов берут следующие соединения: Sm в виде нитрата Sm(NO3)3*6H2O, Со в виде нитрата Co(NO3)2*6H2O в стехиометрических количествах, соответствующих содержанию кобальта в продукте после прокаливания 2% по массе.
Исходные компоненты растворяют в воде, и образовавшийся раствор выпаривают до загустевания, высушивают в муфельной печи при 300°С и прокаливают, повышая температуру от комнатной до 800°С в течение 3 ч и выдерживают при данной температуре в течение 2 ч.
Образовавшийся сложный оксид используют в качестве катализатора углекислотной конверсии метана в синтез-газ.
Примеры 2-32. Углекислотная конверсия метана в синтез-газ.
В обогреваемый вертикально расположенный кварцевый реактор проточного типа, с карманом для термопары, расположенным в центре реактора, на подложку из кварцевого волокна помещают 0,2 г полученного катализатора в виде частиц размером 0,5-1 мм,
Перед катализатором помещают небольшое количество кварцевой крошки, выполняющей роль смесителя газов.
Катализатор разогревают в токе азота до 900°С, после чего отключают подачу азота и подают в реактор смесь метана и углекислого газа, поддерживая температуру катализатора 900°С в течение протекания всего процесса окислительного превращения метана. Исходное сырье представляет собой смесь метана и углекислого газа в объемном соотношении 0,98-1,04:1, причем возможно использование в качестве исходного сырья смеси магистрального природного газа и углекислого газа.
Метан и углекислый газ через расходомеры подают в реактор, где они, контактируя с кварцевой крошкой, образуют гомогенную смесь. Поток гомогенной метан-углекислотной смеси в реакторе достигает слоя катализатора.
Газовую смесь, образовавшуюся в результате реакции на катализаторе, охлаждают в конденсаторе для отделения паров воды, и часть смеси направляют в газовый хроматограф для определения состава продуктов реакции.
Анализ реакционной газовой смеси, выходящей из реактора, показал, что помимо целевых продуктов - смеси Н2 и СО, она может включать в свой состав следовые количества непрореагировавших метана, CO2 и воду.
Результаты проведения получения синтез-газа при варьировании значений мольного отношения метан: углекислый газ (СН4/CO2), скорости подачи метан-углекислотной смеси (W) приведены в таблице. В таблице в качестве показателей эффективности способа приведены данные по выходу целевых продуктов и производительности катализатора по Н2 и СО.
Выход монооксида углерода рассчитывают путем деления суммарного числа молей полученного СО на сумму числа молей поданных в реактор метана и углекислого газа.
Выход водорода рассчитывают по формуле wH2вых*100/(wCH4*2), где wH2 - количество водорода на выходе из реактора моль, wCH4 - скорость подачи метана на входе в реактор, моль.
Производительность катализатора рассчитывают путем умножения скорости подачи исходной газовой смеси (л/г катализатора в ч) на выход Н2 или СО (в %) деленный на 100%.
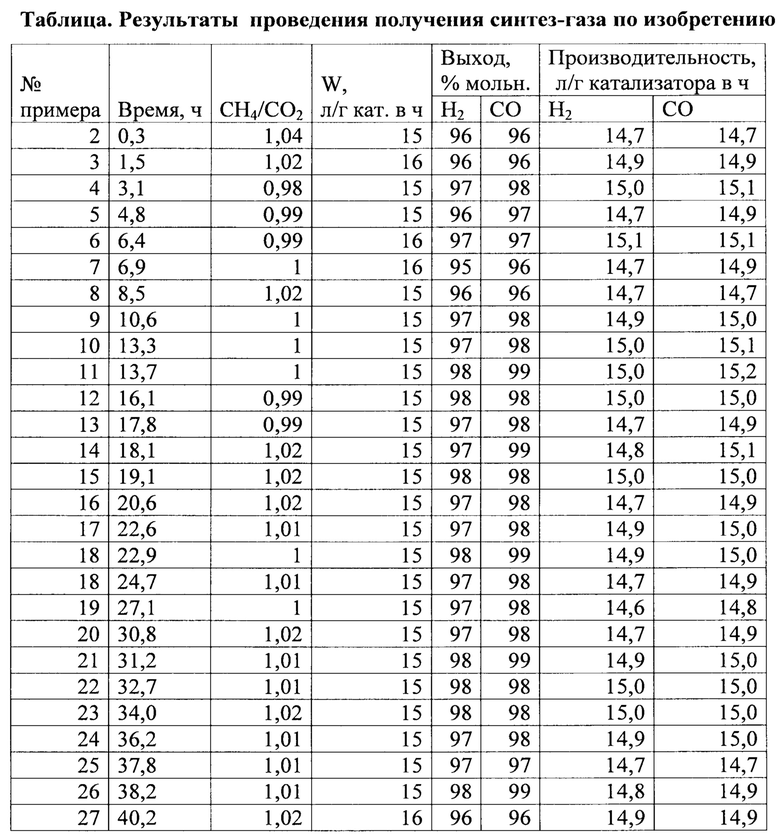

Согласно экспериментальным данным, приведенным в таблице, способ по изобретению обеспечивает выход Н2 95-98%, выход СО 96-99%, производительность по Н2 14,7-15,3 л/г катализатора в ч, по СО 14,7-15,5 л/г катализатора в час.
Таким образом, предлагаемый согласно изобретению способ, обеспечивает высокие выходы целевых продуктов и высокую производительность по целевым продуктам, причем способ обеспечивает как быстрый выход катализатора на оптимальный режим его работы, так и стабильность достигнутых показателей на протяжении не менее 50 часов его работы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2014 |
|
RU2572530C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2014 |
|
RU2573005C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2024 |
|
RU2834479C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА ВЫСОКОТЕМПЕРАТУРНЫМ КАТАЛИТИЧЕСКИМ ОКИСЛИТЕЛЬНЫМ ПРЕВРАЩЕНИЕМ МЕТАНА | 2015 |
|
RU2594161C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2019 |
|
RU2719176C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2010 |
|
RU2433950C1 |
| Способ приготовления катализаторов для получения синтез-газа путем углекислотной конверсии метана | 2018 |
|
RU2690496C1 |
| Способ получения синтез-газа из CO | 2017 |
|
RU2660139C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОБАЛЬТСОДЕРЖАЩЕГО КАТАЛИЗАТОРА СИНТЕЗА ФИШЕРА-ТРОПША | 2012 |
|
RU2602803C2 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2010 |
|
RU2453366C1 |
Изобретение относится к высокотемпературным каталитическим окислительным способам превращения метана с получением синтез-газа. Предложен способ получения синтез-газа высокотемпературным каталитическим окислительным превращением метана путем подачи исходной газовой смеси, содержащей смесь метана и углекислого газа, в реактор со сложнооксидным катализатором при повышенной температуре, отличающийся тем, что в качестве катализатора используют сложный оксид кобальта и самария, полученный смешением исходных соединений кобальта и самария, взятых в стехиометрических соотношениях, отвечающих содержанию кобальта в продукте после прокаливания равном 2% по массе, с прокаливанием полученной смеси при повышении температуры от комнатной до 800°С в течение 3 часов и выдерживают при данной температуре в течение 2 ч с получением сложного оксида кобальта и самария, расположенный в вертикальном реакторе на подложке из кварцевого волокна, перед катализатором помещают небольшое количество кварцевой крошки, выполняющей роль смесителя газов, катализатор разогревают в токе азота до 900°С, после чего отключают подачу азота и подают в реактор смесь метана и углекислого газа, поддерживая температуру катализатора 900°С в течение протекания всего процесса окислительного превращения метана. Технический результат - разработка способа получения синтез-газа углекислотной конверсией метана, обеспечивающего более высокие производительность катализатора и выходы СО и Н2, а также обеспечивающий быстрый выход катализатора на оптимальный режим его работы. 2 з.п. ф-лы, 1 табл., 32 пр.
1. Способ получения синтез-газа высокотемпературным каталитическим окислительным превращением метана путем подачи исходной газовой смеси, содержащей смесь метана и углекислого газа, в реактор со сложнооксидным катализатором при повышенной температуре, отличающийся тем, что
в качестве катализатора используют сложный оксид кобальта (Со) и самария (Sm), полученный смешением исходных соединений кобальта и самария, взятых в стехиометрических соотношениях, отвечающих содержанию кобальта в продукте после прокаливания равном 2% по массе,
с прокаливанием полученной смеси при повышении температуры от комнатной до 800°С в течение 3 часов и выдерживают при данной температуре в течение 2 ч с получением сложного оксида кобальта (Со) и самария (Sm),
расположенный в вертикальном реакторе на подложке из кварцевого волокна,
перед катализатором помещают небольшое количество кварцевой крошки, выполняющей роль смесителя газов,
катализатор разогревают в токе азота до 900°С, после чего отключают подачу азота и подают в реактор смесь метана и углекислого газа, поддерживая температуру катализатора 900°С в течение протекания всего процесса окислительного превращения метана.
2. Способ по п. 1, отличающийся тем, что в качестве исходной газовой смеси используют смесь метана и углекислого газа с объемным отношением метан: CO2, равным 0,98-1,04:1, подаваемой со скоростью 15-16 л/г катализатора в час.
3. Способ по п. 1, отличающийся тем, что в качестве исходных соединений кобальта и самария при получении катализатора используют нитрат самария Sm(NO3)3*6H2O и нитрат кобальта Co(NO3)2*6H2O.
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2010 |
|
RU2453366C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2014 |
|
RU2572530C1 |
| КАТАЛИЗАТОР РИФОРМИНГА УГЛЕВОДОРОДОВ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА С ИСПОЛЬЗОВАНИЕМ ТАКОВОГО | 2008 |
|
RU2475302C2 |
| JP 4335356 B2, 30.09.2009 | |||
| КОМПОЗИТНЫЙ ОКСИД КАТАЛИЗАТОРА РИФОРМИНГА УГЛЕВОДОРОДОВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА С ЕГО ИСПОЛЬЗОВАНИЕМ | 2009 |
|
RU2476267C2 |
Авторы
Даты
2024-02-28—Публикация
2023-05-25—Подача