Уровень техники
Галогены используются в нескольких отраслях промышленности, например, для антипиренов, биоцидов, буровых растворов и для новых областей применения, таких как накопление энергии. Элементарный бром является жидким при комнатной температуре и имеет высокое давление пара. Он является сильным окислителем, и случайное воздействие брома без средств защиты может вызвать в зависимости от степени воздействия раздражение, ожоги и отравление. Кроме того, утечка брома представляет опасность для окружающей среды.
Элементарный хлор при комнатной температуре представляет собой газ, обладающий коррозионными свойствами, и является одним из самых опасных из известных веществ. Он имеет зеленовато-желтый цвет с резким раздражающим запахом и тяжелее воздуха, поэтому газообразный хлор имеет свойство собираться в низинах. Неправильное обращение с газообразным хлором может привести к значительному ущербу. Согласно отчетам EPA (Агентство по охране окружающей среды США), ежегодно происходит более 1300 случаев выброса хлора, в среднем приводя к 300 травмам и 27 смертям, что больше, чем для любого другого химического вещества. Вдыхание является наиболее опасным путем воздействия газообразного хлора, вызывающим серьезное повреждение легких, которое может привести к смерти. В случае разлива хлор быстро распространяется, что делает такой выброс хлора предметом серьезной озабоченности.
На сегодняшний день процедура в случае аварийной утечки брома включает сложный и времязатратный метод, включающий параллельное действие нескольких различных химических веществ. Жидкую фазу брома часто обрабатывают Ca(OH)2 и водой, тогда как газовую фазу брома обрабатывают газообразным аммиаком, что может вызвать вторичный риск экологического загрязнения, вызванный аммиаком.
В случае разлива хлора в направлении облака газообразного хлора распыляют воду, чтобы замедлить его распространение и снизить его концентрацию.
Оперативная аварийная бригада должна включать несколько хорошо обученных членов для одновременной обработки газовой и жидкой фаз разлива. Обработка предполагает нахождение в непосредственной близости от источника утечки и контакт с ним, что требует использования подходящих личных средств защиты, таких как специальные защитные костюмы, защитные маски и респираторные средства.
Таким образом, существует потребность в легкой и простой процедуре, позволяющей быстро отреагировать в случае аварийной ситуации, чтобы предотвратить дальнейшее распространение галогенов и удалить образовавшиеся отходы безопасным и эффективным образом.
Краткое описание изобретения
Изобретение в первую очередь направлено на способ обработки аварийного разлива или утечки галогена (брома или хлора), включающий приведение водного раствора галогенида четвертичного аммония в контакт с указанным галогеном. Галогенид четвертичного аммония представляет собой бромид или хлорид и выбран из группы, состоящей из алифатических и циклических бромидов или хлоридов четвертичного аммония.
Способ согласно изобретению обеспечивает быструю нейтрализацию галогена и сбор продукта нейтрализации галогена в виде связанного в комплекс брома в форме жидкой или твердой массы, как подробно показано ниже.
Подробное описание изобретения
Поскольку элементарный бром имеет высокое давление пара, утечка брома требует быстрого реагирования, чтобы локализовать разлив и предотвратить дальнейшее распространение загрязнения. Таким образом, в одном из аспектов настоящего изобретения предложен способ изоляции разлива или утечки брома, предотвращающий дальнейшее испарение указанного брома и загрязнение им больших площадей. Соответственно, способ согласно изобретению может применяться к жидкой и/или газовой фазе загрязнения бромом путем нанесения водного раствора галоидной соли четвертичного аммония непосредственно на источник брома, который необходимо изолировать. Согласно изобретению раствор галоидной соли четвертичного аммония при нанесении на источник элементарного брома (Br2) вызывает связывание свободного брома в комплекс с указанной солью. Подразумевается, что связанный в комплекс бром не имеет высокого давления пара, и, таким образом, связанный в комплекс бром считается надежно локализованным.
В еще одном аспекте настоящего изобретения предложен способ изоляции/обработки газообразного хлора, предотвращающий дальнейшее распространение указанного хлора и загрязнение им больших площадей. Таким образом, способ согласно изобретению может применяться к газовой фазе загрязнения хлором путем нанесения водного раствора галоидной соли четвертичного аммония непосредственно на источник хлора, который необходимо изолировать. В некоторых вариантах осуществления водный раствор галоидной соли четвертичного аммония может быть распылен на/в направлении поступающего потока газообразного хлора.
В отдельных вариантах осуществления водный раствор галоидной соли четвертичного аммония согласно изобретению используют для обработки паров брома и предотвращения дальнейшего распространения брома в газовой фазе. Согласно изобретению водный раствор галоидной соли четвертичного аммония распыляют непосредственно на газовую фазу брома/пары брома. При контакте распыленных капель раствора галоидной соли четвертичного аммония с парами брома происходит связывание брома в комплекс с указанной солью, и он остается в жидкой форме, где образовавшийся комплекс брома и соли аммония не имеет высокого давления пара и, таким образом, связанный в комплекс бром считается локализованным и не распространяется дальше.
В других вариантах осуществления водный раствор галоидной соли четвертичного аммония согласно изобретению используют для обработки жидкого источника брома. Согласно изобретению водный раствор галоидной соли четвертичного аммония добавляют к жидкому источнику брома, выливают или распыляют на него. Указанное добавление водного раствора соли аммония к жидкому брому приводит к образованию двух жидких фаз; находящаяся сверху водная фаза (верхняя фаза) состоит в основном из воды и остаточных количеств соли четвертичного аммония и брома, в то время как находящаяся снизу органическая фаза (нижняя фаза) содержит большую часть брома в форме комплекса брома и соли четвертичного аммония. Понятно, что находящаяся снизу фаза, содержащая вещество связанного в комплекс брома, тяжелее, чем верхняя фаза на водной основе, что приводит к тому, что более тяжелая бромсодержащая органическая фаза локализуется и изолируется, тем самым обеспечивая устранение границы раздела между бромсодержащей жидкостью и воздухом.
Согласно изобретению после добавления раствора галоидной соли четвертичного аммония к жидкому брому поверхность находящейся сверху водной жидкости, находящаяся в контакте с воздухом, содержит только остаточное количество брома, и после добавления соли и образования комплекса с бромом пары брома не выделяются. Фазовое разделение, как описано выше, происходит в течение нескольких секунд после первоначального добавления раствора галоидной соли четвертичного аммония к жидкому источнику брома, тем самым обеспечивая быстрое образование комплекса и изоляцию брома.
Термин «галогенид четвертичного аммония» в контексте настоящего документа включает соединения, состоящие из катиона, в котором азот имеет положительный заряд, и противоаниона, представляющего собой галогенид. Азот может принимать положительный заряд, потому что он присоединен к четырем атомам углерода согласно формуле R1R2R3R4N+ X-, где R1, R2, R3 и R4 независимо выбраны из линейных или разветвленных C1-C5 алкильных групп и арильных групп, а X- обозначает противоанион, представляющий собой галогенид, например, бромид или хлорид, например, симметричные галоидные соли четвертичного аммония, где R1, R2, R3 и R4 являются одинаковыми (например, бромид тетраэтиламмония (TEAB) и бромид тетра-н-бутиламмония (TBAB)). Галоидные соли четвертичного аммония, в которых азот образует часть кольца, например, пяти- или шестичленных колец, включая ароматические кольца, также пригодны для настоящего изобретения, т. е. соли пиридиния, такие как бромиды 2-метил-1-алкилпиридиния, хлориды 2-метил-1-алкилпиридиния, бромиды 3-метил-1-алкилпиридиния и хлориды 3-метил-1-алкилпиридиния, где алкил в положении 1 кольца представляет собой линейную или разветвленную C1-C5 группу. Например, бромид 3-метил-1-н-бутилпиридиния (3-MBPy) и бромид 2-метил-1-этилпиридиния (2-MEPy). Синтез таких солей пиридиния описан в US 9722281 и US 9905874. То есть изобретение предполагает использование алифатических и циклических галогенидов четвертичного аммония, особенно бромидов.
В некоторых дополнительных вариантах осуществления концентрация раствора галоидной соли четвертичного аммония, используемого, как описано выше в настоящем документе, составляет не менее 30 мас.%, например, не менее 40 мас.%, и вплоть до насыщения (приблизительно 90 мас.%), например, от 40 мас.% до 60 мас.%.
Согласно изобретению концентрация раствора галоидной соли четвертичного аммония, добавляемого к жидкому брому, и, более конкретно, молярное соотношение между солью аммония и бромом влияет на физические свойства образующейся находящейся снизу фазы. Неожиданно было обнаружено, что конечное физическое состояние образующейся находящейся снизу фазы (которая состоит из связанного в комплекс брома) можно контролировать для облегчения безопасного удаления связанного в комплекс брома из места, в котором произошло загрязнение, в безопасную зону хранения отходов брома. Следует иметь в виду, что указанное выше молярное соотношение относится к соотношению четвертичный аммоний:бром при смешивании раствора галоидной соли четвертичного аммония с раствором брома, который требуется обработать, а затем удалить в отходы.
Следовательно, в еще одном аспекте настоящего изобретения предложен способ удаления бромсодержащих отходов, которые образуются из-за утечки или разлива брома. Согласно настоящему изобретению добавление раствора соли четвертичного аммония таким образом, чтобы соотношение четвертичный аммоний:бром находилось в диапазоне от 1:1 до приблизительно 1:8, будет способствовать образованию твердой фазы, гелеобразной фазы или жидкой фазы, содержащей связанный в комплекс бром, в течение нескольких часов после добавления раствора соли аммония, в зависимости от соли четвертичного аммония, используемой в водном растворе, смешиваемом с источником брома. Например, использование бромида тетраэтиламмония (TEAB) в качестве соли четвертичного аммония в растворе согласно изобретению при соотношении четвертичный аммоний:бром от 1:1 до приблизительно 1:4 приведет к образованию твердой фазы, содержащей связанный в комплекс бром, которая может быть легко удалена из исходного раствора и собран известными методами, например, путем фильтрации или вручную. Указанное твердое вещество, содержащее связанный в комплекс бром, характеризуется химической и структурной стабильностью в течение по меньшей мере 5 месяцев со дня образования комплекса с бромом.
В отдельных вариантах осуществления может быть достигнута переработка связанного в комплекс брома из гелеобразной формы или из твердой формы, и бром может быть отделен от соли аммония и повторно использован.
В дополнительном аспекте настоящего изобретения предложен способ изоляции и/или пассивации жидкого источника брома из окружающей среды путем образования стабильной пены на границе раздела между жидким источником брома и окружающей областью, где указанная пена предотвращает испарение газообразного брома с его поверхности. Пассивирующая пена согласно изобретению достигается путем использования водного раствора галоидной соли четвертичного аммония, содержащего пенообразователь, и распыления указанного раствора на поверхность жидкого источника брома, который требуется пассивировать и изолировать. Пена, которая образуется на поверхности жидкого брома, предотвращает испарение паров брома с поверхности брома и, следовательно, предотвращает дальнейшее загрязнение окружающей атмосферы и окружающей среды парами брома.
Согласно настоящему изобретению полученная пена затвердевает в течение нескольких часов, и образовавшаяся твердая фаза может быть безопасно удалена в отходы, как описано выше в настоящем документе.
В некоторых вариантах осуществления полученная пена и фаза источника брома образуют единую твердую фазу в течение нескольких часов после нанесения пены на поверхность жидкого источника брома.
В некоторых связанных вариантах осуществления пенообразователь, который используется в способе, описанном выше, представляет собой поверхностно-активное вещество типа водного плёнкообразующего пенообразователя (AFFF). Указанные пенообразователи обычно используются для пожаротушения. Соответственно, пены, которые используются в настоящем изобретении, представляют собой пенообразователи на водной основе, содержащие поверхностно-активные вещества на углеводородной основе, например, алкилсульфат натрия, или спиртоустойчивые водные плёнкообразующие пенообразователи (AR-AFFF). Неограничивающим примером такого спиртоустойчивого агента является FireAid-AR® 2000. Другие пены, которые могут быть использованы в настоящем изобретении, представляют собой C5-C10 короткоцепочечные амфотерные поверхностно-активные вещества, C5-C10 неионогенные поверхностно-активные вещества, анионные углеводородные поверхностно-активные вещества и фторированные поверхностно-активные вещества.
В некоторых других связанных вариантах осуществления концентрация указанного пенообразователя в растворе соли четвертичного аммония составляет от 5 до 30 мас.%. В некоторых других вариантах осуществления концентрация указанного пенообразователя составляет от 5 до 15 мас.%.
Растворы галоидных солей четвертичного аммония согласно изобретению химически стабильны и могут быть доступны для использования на месте работ. Таким образом, в настоящем изобретении дополнительно предложена аварийная система нейтрализации галогенов, содержащая распыляемый или разливаемый водный раствор галогенида четвертичного аммония с концентрацией не менее 40 мас.%, то есть, с описанными в настоящем документе составами.
Эта система, например, может представлять собой переносное устройство, содержащее водный раствор галоидной соли четвертичного аммония, готовый к использованию в случае аварийной ситуации. Например, мелкомасштабная система на 20 л водного раствора соли четвертичного аммония, имеющего концентрацию от приблизительно 40 мас.% до приблизительно 90 мас.% соли аммония, может быть собрана в виде рюкзака с ручным насосом для легкой подачи водного раствора соли четвертичного аммония согласно изобретению на открытый источник брома. В еще одном примере крупномасштабная система, содержащая вышеописанный раствор согласно изобретению, может быть установлена на транспортных средствах, имеющих требуемый формат, таких как буксировочное оборудование или специализированное подъемное оборудование, которое можно использовать в более удаленных местах разлива/утечки.
Кроме того, оборудование для пожаротушения может быть переоборудовано и использовано в тех же условиях, которые обычно используются для подавления огня, например, путем заполнения переносного блока раствором соли четвертичного аммония, имеющим концентрацию от 40 до 90 мас.%, и сжатия указанного раствора воздухом в соответствии со способами, известными специалисту в данной области техники.
Конкретный аспект изобретения относится к способу нейтрализации аварийной утечки газообразного хлора с помощью водной композиции, содержащей:
бромидную соль четвертичного аммония, например, алифатический и циклический бромид четвертичного аммония, как определено ранее; и
неорганический источник бромида, например, бромид щелочного или щелочноземельного металла.
Авторы изобретения обнаружили, что такая пара бромидных солей может быть растворена в воде для создания концентрированных, несколько вязких, но при этом легко перекачиваемых/распыляемых растворов, содержащих или состоящих из:
не менее 30 мас.%, например, более 40 мас.%, более 45 мас.% одной или более бромидных солей четвертичного аммония; и
не менее 30 мас.%, например, более 40 мас.%, более 45 мас.% одного или более бромидов щелочных или щелочноземельных металлов, таких как бромид натрия, бромид калия, бромид кальция или их смесь.
Вышеупомянутые растворы составляют дополнительный аспект изобретения, особенно растворы, полученные растворением в воде симметричной бромидной соли четвертичного аммония, в которой R1, R2, R3 и R4 являются одинаковыми, например, R1=R2=R3=R4=C1-C5 алкильная группа (например, бромид тетраэтиламмония, бромид тетрапропиламмония или бромид тетрабутиламмония), с бромидом натрия или бромидом кальция.
Соответственно, в изобретении, в частности, предложен нейтрализующий галогены водный раствор, содержащий:
от 30 до 60 мас.% (например, от 40 до 60 мас.%) бромида тетраалкиламмония, где алкил представляет собой линейный или разветвленный C1-C5 алкил; и
от 30 до 55 мас.% (например, от 40 до 55 мас.%) бромида натрия или от 30 до 60 мас.% (например, от 40 до 60 мас.%) бромида кальция.
Один предпочтительный водный раствор содержит или состоит из:
от 30 до 60 мас.% (например, от 40 до 60 мас.%) бромида тетраэтиламмония; и от 30 до 55 мас.% (например, от 40 до 55 мас.%) бромида натрия.
Один предпочтительный водный раствор содержит или состоит из:
от 30 до 60 мас.% (например, от 40 до 60 мас.%) бромида тетраэтиламмония; и от 30 до 60 мас.% (например, от 40 до 60 мас.%) бромида кальция.
Далее авторы изобретения используют номенклатуру QABr/Mn+(Br)n (M=Na, M=K и n=1; или M=Ca и n=2) для обозначения «смешанных» растворов. Эти растворы легко могут быть получены путем объединения насыщенных или близких к насыщению растворов отдельных солей (например, для приготовления «смешанных» растворов могут быть использованы приблизительно 50 мас.% водный раствор бромида тетраэтиламмония, приблизительно 45 мас.% водный раствор бромида натрия и приблизительно 52 мас.% водный раствор бромида кальция). Плотность раствора QABr/Mn+(Br)n находится в диапазоне от 1,2 до 1,7 г/см3. Растворы устойчивы к кристаллизации.
Экспериментальные результаты, представленные ниже, показывают, что газообразный хлор, который поступал нижнюю часть колонны и накапливался в ней, был эффективно нейтрализован путем распыления концентрированных растворов QABr/Mn+(Br)n с верхней части колонны (то есть, противотоком). Экспериментальная установка показана на фиг. 4 и подробно описана ниже. Расположенная ниже по потоку система улавливания, предназначенная для уравновешивания изменений давления в колонне и улавливания паров хлора, выходящих из колонны, не обнаружила испускаемого из колонны остаточного газообразного хлора.
Добавленный неорганический источник бромида поддерживает нейтрализующее действие бромида четвертичного аммония. Хлор – более сильный окислитель, чем бром:
Cl2(г.) + 2Br-(водн.) → 2Cl-(водн.) + Br2(ж.)
После поглощения раствором хлор восстанавливается бромид-ионами. Следовательно, хлорид-ионы могут замещать бромид-противоион, связанный с четвертичным аммонием, что приводит к образованию соответствующего хлорида, например, хлорида тетраэтиламмония. Экспериментальная работа, проведенная для подтверждения настоящего изобретения, показывает, что хлорид тетраэтиламмония является плохим комплексообразователем по отношению к элементарному хлору. Преимущество добавления неорганического источника бромида, такого как бромид натрия или бромид кальция, заключается в обеспечении бромид-иона для восстановления хлора, что позволяет четвертичному аммонию сохранять свои бромид-противоионы. Одновременно образующийся элементарный бром может прочно связываться с бромидом четвертичного аммония. Замещение бромида хлоридом в четвертичном аммонии до некоторой степени неизбежно, но это не должно умалять эффективность пары QABr/Mn+(Br)n, поскольку QACl достаточно хорошо действует как комплексообразователь для молекул брома: полученные авторами изобретения результаты показывают, что хлорид тетраэтиламмония достаточно эффективен в связывании с бромом.
Соответственно, конкретным аспектом изобретения является способ нейтрализации аварийной утечки хлора, например, из трубопроводов на химических заводах и других объектах, где хлор подается по трубопроводам к месту его предполагаемого использования (химический реактор и т. д.), где способ включает распыление вышеупомянутого раствора QABr/Mn+(Br)n над местом утечки и сбор продукта нейтрализации хлора в виде связанного в комплекс брома в форме жидкой или твердой массы.
Например, система нейтрализации на основе QABr/Mn+(Br)n может состоять из распылителей, расположенных над трубопроводами для хлора, для доставки раствора в ответ на обнаружение утечки хлора. Как отмечено выше и показано ниже в экспериментальном разделе, концентрированный QABr/Mn+(Br)n, испытанный в аналогичных условиях (распыление с верхней части колонны противотоком на газообразный хлор), продемонстрировал высокую эффективность.
В изобретении также предложено применение водного раствора галогенида четвертичного аммония, имеющего концентрацию не менее 40 мас.%, в качестве агента для нейтрализации галогенов в случае аварийной утечки галогена с конкретными составами, описанными выше. Для обработки аварийной утечки хлора водный раствор бромида четвертичного аммония предпочтительно дополнительно содержит один или более бромидов щелочных или щелочноземельных металлов с конкретными составами, подробно описанными выше.
В изобретении также предложена аварийная система нейтрализации галогенов, как упомянуто выше, содержащая водный раствор галогенида четвертичного аммония с концентрацией не менее 40 мас.% в немедленно распыляемой или разливаемой форме, например, с составами, подробно описанными выше. При установке в аварийной системе нейтрализации хлора распыляемый водный раствор дополнительно содержит один или более бромидов щелочных или щелочноземельных металлов с конкретными составами, подробно описанными выше.
Краткое описание графических материалов
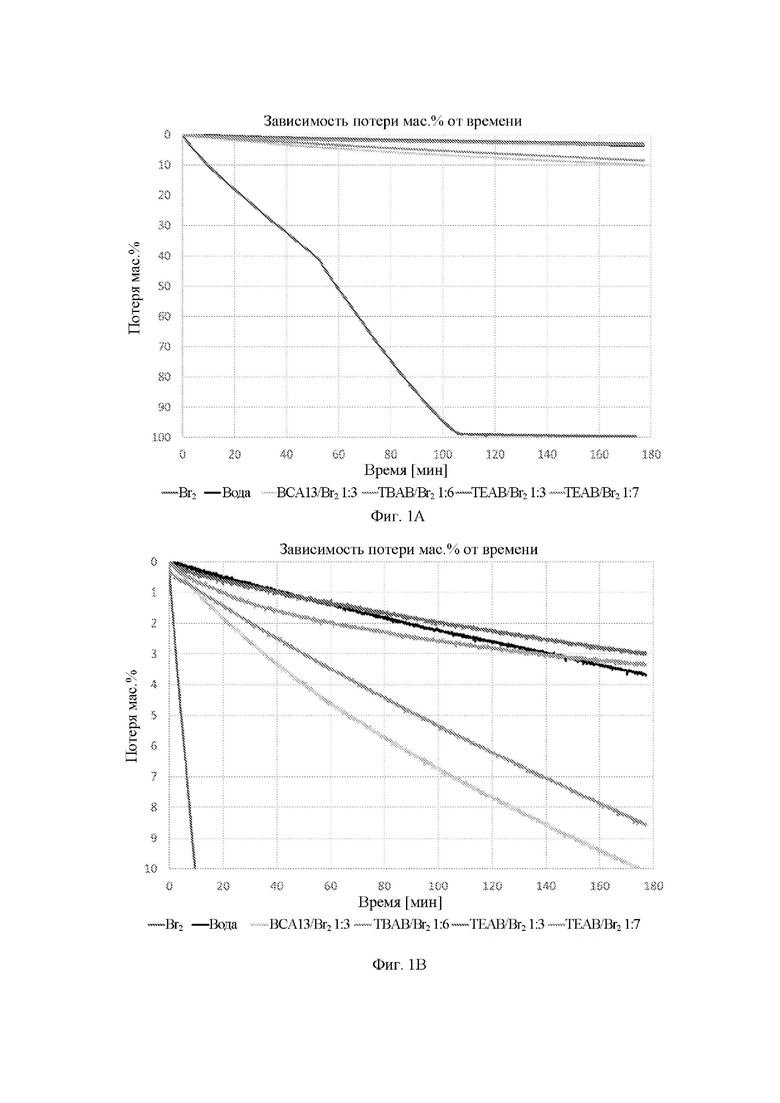
Фиг. 1: на 1A представлена зависимость изменения мас.% от времени, а на 1B представлена потеря массы для смесей четвертичных солей/брома в увеличенном масштабе.
На фиг. 2 изображен процесс улавливания Cl2, как описано в примере 8A. A – начальная точка эксперимента, B – после добавления 30 г хлора и D – достигнутое фазовое разделение в конце эксперимента.
На фиг. 3 изображен процесс улавливания Cl2, как описано в примере 8B. A – начальная точка эксперимента, B – после добавления 50 г хлора, C – после добавления 93 г хлора и D – после добавления 147 г хлора.
На фиг. 4 показана экспериментальная установка, использованная для нейтрализации хлора.
Примеры
Пример 1. Обработка паров брома
Два образца по 10 г жидкого брома (Br2) добавляли в стеклянные бутылки объемом 250 мл. Бутылки герметично закрывали, и внутри бутылок образовывались пары Br2.
В небольшую колбу с пульверизатором добавляли 50 мас.% водный раствор бромида тетраэтиламмония (TEAB).
Две запечатанные бутылки, содержащие Br2, открывали и переворачивали вертикально вниз, чтобы выпустить тяжелые пары Br2. Бутылку номер (1) использовали в качестве эталона, а бутылку номер (2) обрабатывали следующим образом: приблизительно 3 мл раствора TEAB, как описано выше, распыляли по направлению к отверстию бутылки номер (2).
Результаты: эталонная бутылка номер (1) продолжала выделять пары брома, в то время как из бутылки номер (2), на которую был распылен раствор TEAB, не наблюдалось выделения паров и наблюдались небольшие коричневые капли на внутренней поверхности бутылки.
Пример 2. Обработка разлива брома
A) 42 г 50 мас.% бромида 3-метил-1-н-бутилпиридиния (3-MBPy; также называемый BCA13) добавляли в делительную воронку, содержащую 32 г жидкого брома (молярное соотношение 1:2). Две жидкости смешивали встряхиванием делительной воронки и затем выдерживали. Сразу же образовались две фазы: верхняя водная фаза (слегка желтая) и нижняя органическая фаза (коричнево-красная). Эти две фазы сразу же собирали (по отдельности) и анализировали с помощью ВЭЖХ (высокоэффективная жидкостная хроматография) и титрования следующим образом:
Обе фазы анализировали на Br2 и 3-MBPy с помощью иодометрического титрования (при котором после окисления иодида проводили титрование тиосульфатом) и ВЭЖХ (HP 1100, оснащенный УФ-детектором и колонкой CROMASYL C-18 (2,1*250 мм), Agilent). Было обнаружено, что нижняя фаза (53,4 г) содержала 37 мас.% 3-MBPy и 58 мас.% брома. В верхней фазе (20,4 г) содержалось остаточное количество 3000 ppm 3-MBPy и 380 ppm брома.
B) Жидкий бром (160 г) вводили в стеклянный открытый сосуд объемом 1 л, и наблюдали пары брома. На поверхность жидкого брома выливали водный раствор бромида тетраэтиламмония (TEAB) (105 г 50 мас.% раствора).
Результаты: сразу после добавления раствора TEAB образовались две фазы, и после разделения фаз не наблюдалось паров брома. Нижняя фаза затвердела приблизительно через два часа.
C) Жидкий бром (120 г) добавляли в стеклянный открытый сосуд объемом 1 л, и наблюдали пары брома. На поверхность жидкого брома выливали водный раствор бромида тетрабутиламмония (TBAB) (161 г 50 мас.% раствора).
Результаты: сразу после добавления раствора бромида тетрабутиламмония образовались две фазы, и после разделения фаз не наблюдалось паров брома. Через два часа нижняя фаза превратилась в гелеобразную фазу. Полученную гелеобразную фазу переводили в жидкое состояние с использованием 40 г жидкого брома.
Пример 3. Пенная пассивация разлива брома
A) Жидкий бром (50 г) добавляли в стеклянный открытый сосуд объемом 1 л, и наблюдали пары брома. 25 г раствора, содержащего 92 мас.% раствора TEAB, представлявшего собой 50 мас.% бромид тетраэтиламмония, и 8 мас.% раствора пенообразователя AR-AFFF FireAid-AR® 2000, распыляли с помощью пульверизатора на поверхность жидкого брома.
Результаты: На поверхности брома сразу же образовалась пена, покрывающая границу раздела бром-воздух, и выделения паров брома не наблюдалось.
Поверх пены медленно добавляли еще 30 г жидкого брома, что не вызвало выделения паров.
Через несколько часов весь источник брома и фаза пены, покрывающей его поверхность, затвердели.
B) 50 г жидкого брома выливали в стеклянный открытый сосуд объемом 1 л, и наблюдали пары брома. 25 г раствора, содержащего 50 мас.% раствор бромида 3-метил-1-н-бутилпиридиния (3-MBPy) (80 мас.%) и 8 мас.% пенообразователя AR-AFFF FireAid-AR® 2000, распыляли с помощью пульверизатора на поверхность жидкого брома.
Результаты: На поверхности брома сразу же образовалась пена, покрывающая границу раздела бром-воздух, выделения паров брома не наблюдалось.
Поверх пены по каплям добавляли еще 30 г жидкого брома, что не вызвало выделения паров.
C) 50 г жидкого брома выливали в стеклянный открытый сосуд объемом 1 л. Дно сосуда было покрыто жидким бромом, и образовались пары брома. На поверхность жидкого брома распыляли 25 г 92 мас.% раствора 2-MEPy (50 мас.% бромид 2-метил-1-этилпиридиния (2-MEPy), смешанного с 8 мас.% раствора пенообразователя AR-AFFF FireAid-AR® 2000.
Результаты: На поверхности брома сразу же образовалась пена, покрывающая границу раздела бром-воздух, и выделения паров брома не наблюдалось.
Поверх пены по каплям добавляли еще 30 г жидкого брома, что не вызвало выделения паров.
Пример 4. Сбор обработанного твердого брома
Получали твердый продукт из обработанного жидкого брома, как описано в примерах 2B и 3. Твердое вещество собирали вручную шпателем в пластиковый контейнер. По прошествии 3 месяцев никаких изменений в продукте не наблюдалось.
Пример 5. Сбор обработанного жидкого брома
Жидкий продукт из обработанного жидкого брома, полученный, как описано в примере 2C, собирали вручную путем отсасывания в пластиковый контейнер. По прошествии 3 месяцев никаких изменений в продукте не наблюдалось.
Пример 6. Измерения скорости испарения
Целью исследования было проверить способность добавляемых к жидкому брому солей четвертичного аммония подавлять выделение паров брома. Исследование основано на мониторинге изменения массы образцов, содержащих жидкий бром (Br2; контроль), 3-MBPy/Br2, TBAB/Br2 и TEAB/ Br2 при различных молярных соотношениях, как описано в таблице 1 ниже. Потерю массы измеряли в тех же условиях, что и для эталона.
Образец (33 мл) помещали на весы (0,01 г) и устанавливали массу равной нулю. Изменение массы регистрировали каждые 5 секунд. Эксперимент проходил в условиях окружающей среды.
Результаты: Как показано на фиг. 1A и 1B и в таблице 1 ниже, было продемонстрировано, что даже при добавлении небольшого количества бромида четвертичного аммония к брому происходит значительное снижение образования паров брома. Скорость потери массы 50,04 г/ч была измерена для жидкого брома как такового, и она была снижена до 3,96 г/ч в системе, содержащей 3-MBPy и бром при молярном соотношении 1:3. Еще большее снижение скорости потери массы было достигнуто с использованием TEAB при том же молярном соотношении (1:3), что дало минимальную потерю массы 1,08 г/ч.
Таблица 1
Пример 7. Влияние соли четвертичного аммония на физическую форму связанного в комплекс брома
Были испытаны различные соли четвертичного аммония для определения их способности образовывать комплекс с бромом при различных молярных соотношениях. Растворы бромида 3-метил-1-н-бутилпиридиния (3-MBPy), бромида тетрабутиламмония (TBAB) и бромида тетраэтиламмония (TEAB) [50 мас.% раствор, всего 0,25 моль соли четвертичного аммония] смешивали с различной массой жидкого брома: 40, 80, 120, 160 и 200 г в стеклянном контейнере в молярном соотношении, как описано в таблице 2. Образовавшуюся находящуюся снизу фазу, полученную после смешивания, характеризовали в соответствии с физическим состоянием и тем, наблюдались ли пары брома после того, как произошло образование комплекса.
Таблица 2
Как можно видеть из таблицы 2, физическая форма связанного в комплекс брома зависит не только от типа соли четвертичного аммония, используемой для образования его комплекса, но также может зависеть от молярного соотношения между указанной солью четвертичного аммония и бромом. Кроме того, можно видеть, что для 3-MBPy, TBAB и TEAB образования паров брома не наблюдалось вплоть до молярного соотношения четвертичный аммоний:бром, равного 1:4.
Пример 8. Нейтрализация газообразного хлора (Cl2) бромидом четвертичного аммония в отдельности и бромидом четвертичного аммония/NaBr
A. 460 г 50 мас.% раствора 3-MBPy помещали в стеклянный сосуд. Из стеклянного сосуда отводили газы, раствор перемешивали и выделявшийся газ улавливали ловушкой с 20 мас.% NaOH.
В сосуд барботировали газообразный Cl2. Добавление газообразного Cl2 осуществляли из резервуара со сжатым газообразным хлором, его контролировали и регистрировали с использованием полуаналитических весов. Фазовое разделение наблюдали после добавления 30 г Cl2, как можно видеть на фиг. 2. По мере добавления Cl2 цвет раствора становился ярче.
В описанном растворе 3-MBPy в общей сложности было уловлено 2 моля (142 г) газообразного хлора.
B. 460 г 50 мас.% раствора 3-MBPy добавляли в стеклянный сосуд. В раствор добавляли 155 г NaBr. Из стеклянного сосуда отводили газы, раствор перемешивали и выделявшийся газ улавливали ловушкой с 26 мас.% NaOH.
В сосуд барботировали газообразный Cl2 (в течение 105 минут). Добавление газообразного Cl2 осуществляли из резервуара со сжатым газообразным хлором, его контролировали и регистрировали с использованием полуаналитических весов. По мере добавления Cl2 цвет раствора становился темнее, как можно видеть на фиг. 3. Добавление газообразного хлора прекращали после того, как наблюдалось выделение газа в ловушке.
В описанном растворе 3-MBPy:NaBr в общей сложности было уловлено 2,45 молей (174 г) газообразного хлора. Реакция была экзотермической, и после добавления 80 г хлора температура достигла 70,8°C. Дальнейшее добавление хлора не вызывало дальнейшего повышения температуры.
Примеры с 9 по 12. Устранение выброса газообразного Cl2 путем встречного распыления раствора для обработки, состоящего из бромида четвертичного аммония/неорганического бромида
Экспериментальная установка, использованная для следующего набора примеров, показана на фиг. 4. Экспериментальная установка состоит из трех основных частей: источников подачи (1) и (2), реакционной камеры (3) и системы улавливания газа (4). Из источников подачи регулируемые количества газообразного Cl2 (2) и раствора для обработки, состоящего из бромида четвертичного аммония и неорганической бромидной соли (1), по отдельности подают в реакционную камеру. Входное отверстие для Cl2 расположено в нижней части реакционной камеры (колонна 3, представляющая собой закрытый стеклянный сосуд объемом 30 л). Раствор подают из резервуара (1) в колонну (3) противотоком путем распыления через сопло (3o), расположенное в центре верхней части колонны (3).
Внутри колонны (3) происходит химическая реакция между газообразным Cl2 и реакционным раствором: восстановление Cl2 бромид-ионом и связывание элементарного брома в комплекс, образуемый галогенидом четвертичного аммония. Атмосферное давление внутри реакционной камеры уравновешивается за счет обеспечения двунаправленного потока газа через систему улавливания (4). Система улавливания состоит из трех улавливающих сосудов (M1, M2 и M3), соединенных последовательно от одного конца реакционной камеры (колонна 3) до выпускного отверстия. Первая ловушка M1 состоит из пустого сосуда и используется для предотвращения поступления потока улавливающего раствора в реакционную камеру (колонна 3), когда в колонне создается отрицательное давление. Две другие ловушки (M2 и M3) заполнены раствором гидроксида натрия (20-25 мас.%) для сбора и нейтрализации газообразного Cl2 или Br2, выходящего из колонны (3). На конце находится ловушка с активированным углем (M4).
Экспериментальную установку, показанную на фиг. 4, использовали для проведения серии испытаний, условия которых приведены в таблице 3 ниже. Вкратце, некоторое количество газообразного Cl2 (указано в таблице 3, столбец A) выпускали из баллона (2) в течение некоторого периода времени (указано в таблице 3, столбец B) через нижний соединительный узел пустого закрытого стеклянного сосуда объемом 30 л (колонна 3). Когда внутренняя часть сосуда начала снизу приобретать желтый цвет, что указывает на накопление газообразного хлора, раствор для обработки, состоящий из TEAB и неорганической бромидной соли, перекачивали из резервуара (1) и распыляли через сопло, расположенное в верхней части сосуда. Объем раствора TEAB/Mn+Brn, подаваемого в реакционный сосуд, и его состав указаны в таблице 3, столбец C).
Реакция между газообразным Cl2 и раствором для обработки TEAB/Mn+Brn привела к образованию продукта красного цвета в твердой или жидкой форме (фаза продукта указана в таблице 3, столбец D) и, следовательно, было создано внутреннее отрицательное давление. В результате 1-я ловушка (M1) была заполнена раствором гидроксида натрия, втянутым из 2-й и 3-й ловушек (M2 и M3 соответственно).
В таблице 3 ниже кратко изложены условия каждого эксперимента и образованный продукт.
Таблица 3
Cl2(г) (г)
[Состав раствора для обработки]
Фаза продукта
916 г раствора NaBr (45 мас.%)
3206 г раствора NaBr (45 мас.%) + 206 г NaBr(тв.)
1538 г CaBr2 (52 мас.%)
В 1-й (M1), 2-й (M2) и 3-й (M3) ловушках не было обнаружено остаточного газообразного Cl2 (менее 10 ppm), что указывает на полное поглощение газообразного хлора раствором для обработки, состоящим из TEAB/Mn+Brn, и превращение его в безвредный продукт, легко удаляемый из реакционного сосуда.
Пример 13 (сравнительный). Нейтрализация газообразного хлора (Cl2)
Для эксперимента использовали экспериментальную установку, показанную на фиг. 4 и подробно описанную выше. Газообразный Cl2 (107 г) в течение 5 минут выпускали (2) через нижний соединительный узел пустого закрытого стеклянного сосуда объемом 30 л (3). В течение первых пяти минут внутри ловушки с гидроксидом натрия M2 наблюдались пузырьки воздуха, поскольку Cl2 выталкивал воздух в стеклянном сосуде (3). В течение следующих девяти минут цвет раствора гидроксида натрия в первой ловушке с гидроксидом натрия (M2) изменился на желтовато-зеленый. В 3-й ловушке (M3) пузырьков не наблюдалось, так же как и изменения цвета. После перекрытия потока Cl2 стеклянный сосуд (3) продували газообразным N2 (5), чтобы вымыть весь оставшийся внутри реакционного сосуда газообразный Cl2.
По окончании эксперимента было определено положительное изменение массы на 97,7 г и 3,8 г в первой ловушке с NaOH (M2) и второй ловушке с NaOH (M3), соответственно.
Пример 14. Нейтрализация газообразного хлора (Cl2)
20 г порошка CaBr2 растворяли в 105 г водного раствора TEAB (50 мас.%) в стеклянном сосуде объемом 200 мл (соединенном с ловушкой с NaOH). Раствор барботировали газообразным Cl2 (32 г) из резервуара с регулируемым давлением с расходом 0,47 г/мин. Температура во время эксперимента находилась в пределах 30-40 oC. Через 68 минут в ловушке с NaOH наблюдалось выделение газообразного Cl2, что указывает на исчерпание реагента TEAB/CaBr2. Процесс останавливали, и раствор конечного продукта разделяли на две фазы – находящуюся сверху желтую водную фазу и красноватую органическую фазу снизу, что указывает на накопление элементарного брома в органической фазе. Органическая фаза затвердела через 1 час.
Пример 15 (согласно изобретению) и 16 (сравнительный). Тестирование хлорида четвертичного аммония в отношении образования комплексов с галогеном
Хлоридом четвертичного аммония, выбранным для экспериментов, был хлорид тетраэтиламмония (TEACl).
Было исследовано образование комплексов с бромом (пример 15). 0,4 моля жидкого брома (64 г) смешивали с 0,1 моль раствора TEACl (50 мас.%) (36 г). 3 эквивалента (48 г) брома были связаны в комплекс раствором TEACl, добавление 4-го эквивалента привело к появлению легкого выделения паров брома.
Было исследовано образование комплексов с хлором (пример 16). 10 г газообразного Cl2 барботировали через 108 г раствора TEACl (50 мас.%). Выделявшийся Cl2 собирали ловушкой с раствором гидроксида натрия (25 мас.%). В растворе TEACL не наблюдалось изменения массы, что указывает на то, что Cl2 полностью адсорбировался ловушкой (то есть, Cl2 не был уловлен TEACl).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения модифицированного диенсодержащего (cо)полимера | 2019 |
|
RU2732776C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ ПРИРОДНЫХ РАССОЛОВ | 1998 |
|
RU2157338C2 |
| СПОСОБ ОХЛАЖДЕНИЯ ТРОПОСФЕРЫ | 2010 |
|
RU2511252C2 |
| СПОСОБ ПОЛУЧЕНИЯ БРОМИДА АММОНИЯ | 2021 |
|
RU2789134C1 |
| ЭЛЕКТРОХИМИЧЕСКИЕ ГАЗОВЫЕ ДАТЧИКИ С ИОНОВЫМИ ЖИДКИМИ ЭЛЕКТРОЛИТИЧЕСКИМИ СИСТЕМАМИ | 2009 |
|
RU2502067C2 |
| СПОСОБ ПОЛУЧЕНИЯ БРОМИСТОГО ЛИТИЯ ИЗ РАССОЛОВ | 1998 |
|
RU2157339C2 |
| Способ получения 1-метилциклопропена | 2017 |
|
RU2667511C1 |
| МОДИФИЦИРОВАННЫЙ ДИЕНСОДЕРЖАЩИЙ (CО)ПОЛИМЕР, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИПИРЕНА | 2018 |
|
RU2782606C2 |
| МОДИФИЦИРОВАННЫЙ ДИЕНСОДЕРЖАЩИЙ (CО)ПОЛИМЕР, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИПИРЕНА | 2018 |
|
RU2795580C2 |
| АКТИВНЫЕ БРОМСОДЕРЖАЩИЕ БИОЦИДНЫЕ КОМПОЗИЦИИ И ИХ ПОЛУЧЕНИЕ | 2003 |
|
RU2339224C2 |



Изобретение относится к способам ликвидации аварийного разлива или утечки галогенов. Предложен способ обработки аварийного разлива или утечки элементарного галогена, представляющего собой бром или хлор, включающий приведение водного раствора галогенида четвертичного аммония в контакт с указанным галогеном, и сбор продукта нейтрализации галогена в виде связанного в комплекс брома в форме жидкой или твердой массы. Предложены также нейтрализующий элементарный хлор водный раствор, применение водного галогенида четвертичного аммония в качестве агента для нейтрализации элементарного галогена и варианты аварийной системы нейтрализации элементарных галогенов. Предложенный способ обеспечивает быструю нейтрализацию галогена в случае аварийного разлива или утечки и удобный сбор продуктов нейтрализации. 5 н. и 24 з.п. ф-лы, 4 ил., 3 табл., 16 пр.
1. Способ обработки аварийного разлива или утечки элементарного галогена, представляющего собой бром или хлор, включающий приведение водного раствора галогенида четвертичного аммония в контакт с указанным галогеном; и
сбор продукта нейтрализации галогена в виде связанного в комплекс брома в форме жидкой или твердой массы.
2. Способ по п. 1, где галогенид четвертичного аммония выбран из группы, состоящей из алифатических и циклических бромидов или хлоридов четвертичного аммония.
3. Способ по п. 2, где алифатический бромид четвертичного аммония имеет формулу R1R2R3R4N+ Br-, где R1, R2, R3 и R4 независимо выбраны из линейного или разветвленного C1-C5 алкила.
4. Способ по п. 3, где R1R2R3R4N+ Br- представляет собой симметричный бромид четвертичного аммония, так что R1, R2, R3 и R4 являются одинаковыми.
5. Способ по п. 4, где бромид четвертичного аммония представляет собой бромид тетраэтиламмония (TEAB), бромид тетрапропиламмония или бромид тетра-н-бутиламмония (TBAB).
6. Способ по п. 2, где циклический бромид или хлорид четвертичного аммония выбран из группы, состоящей из бромидов 2-метил-1-алкилпиридиния, хлоридов 2-метил-1-алкилпиридиния, бромидов 3-метил-1-алкилпиридиния и хлоридов 3-метил-1-алкилпиридиния, где алкил в положении 1 кольца представляет собой линейную или разветвленную C1-C5 группу.
7. Способ по п. 6, где бромид 2-метил-1-алкилпиридиния представляет собой бромид 2-метил-1-этилпиридиния (2-MEPy), а бромид 3-метил-1-алкилпиридиния представляет собой бромид 3-метил-1-н-бутилпиридиния (3-MBPy).
8. Способ по любому из пп. 1-7, где галоген представляет собой бром.
9. Способ по любому из пп. 1-7, где галоген представляет собой жидкий бром.
10. Способ по п. 9, где водный раствор галогенида четвертичного аммония содержит пенообразователь для образования пены поверх жидкого брома.
11. Способ по п. 10, где пенообразователь представляет собой водный плёнкообразующий пенообразователь (AFFF).
12. Способ по п.10, где галогенид четвертичного аммония представляет собой бромид тетраэтиламмония и пенообразователь представляет собой водный плёнкообразующий пенообразователь (AFFF).
13. Способ по любому из пп. 1-7, где галоген представляет собой газообразный бром.
14. Способ по любому из пп. 1-7, где галоген представляет собой газообразный хлор и где водный раствор галогенида четвертичного аммония дополнительно содержит один или более бромидов щелочных или щелочноземельных металлов.
15. Способ по п. 14, где водный раствор галогенида четвертичного аммония содержит не менее 40 мас.% галогенида четвертичного аммония и не менее 40 мас.% бромида щелочного или щелочноземельного металла.
16. Способ по п. 15, где водный раствор галогенида четвертичного аммония содержит:
симметричный бромид четвертичного аммония формулы R1R2R3R4N+ Br-, где R1, R2, R3 и R4 представляют собой одинаковые C1-C5 алкильные группы; и бромид натрия или бромид кальция.
17. Способ по п. 15, где водный раствор галогенида четвертичного аммония содержит бромид тетраэтиламмония, бромид тетрапропиламмония или бромид тетрабутиламмония.
18. Способ по п. 17, где водный раствор галогенида четвертичного аммония содержит бромид тетраэтиламмония.
19. Способ по п. 16, где водный раствор галогенида четвертичного аммония содержит бромид тетраэтиламмония и бромид кальция.
20. Способ по п. 14, включающий распыление раствора над местом утечки хлора и сбор продукта нейтрализации хлора в виде связанного в комплекс брома в форме жидкой или твердой массы.
21. Нейтрализующий элементарный хлор водный раствор, содержащий:
от 30 до 60 мас.% бромида тетраалкиламмония, где алкил представляет собой линейный или разветвленный C1-C5 алкил; и
от 30 до 55 мас.% бромида натрия или от 30 до 60 мас.% бромида кальция.
22. Нейтрализующий элементарный хлор водный раствор по п. 21, содержащий:
от 40 до 60 мас.% бромида тетраалкиламмония и
от 40 до 55 мас.% бромида натрия или от 40 до 60 мас.% бромида кальция.
23. Нейтрализующий элементарный хлор водный раствор по п. 21 или 22, где бромид тетраалкиламмония представляет собой бромид тетраэтиламмония.
24. Нейтрализующий элементарный хлор водный раствор по п. 21, содержащий:
от 40 до 60 мас.% бромида тетраэтиламмония и
от 40 до 60 мас.% бромида кальция.
25. Применение водного раствора галогенида четвертичного аммония с концентрацией не менее 40 мас.% в качестве агента для нейтрализации элементарного галогена в случае аварийной утечки элементарного галогена, где когда галоген представляет собой хлор, водный раствор галогенида четвертичного аммония дополнительно содержит один или более бромидов щелочных или щелочноземельных металлов.
26. Применение по п. 25, где галогенид четвертичного аммония представляет собой бромид тетраэтиламмония, и где бромид щелочноземельных металлов представляет собой бромид кальция.
27. Аварийная система нейтрализации элементарных галогенов, содержащая водный раствор галогенида четвертичного аммония с концентрацией не менее 40 мас.% в немедленно распыляемой или разливаемой форме, где система выбрана из:
мелкомасштабной системы, которая собрана в виде рюкзака с ручным насосом,
крупномасштабной системы, которая установлена на транспортных средствах, имеющих буксировочное или подъемное оборудование; и
оборудования для пожаротушения.
28. Аварийная система нейтрализации элементарного хлора, содержащая водный раствор галогенида четвертичного аммония с концентрацией не менее 40 мас.%, где галогенид представляет собой бромид или хлорид, где водный раствор галогенида четвертичного аммония дополнительно содержит один или более бромидов щелочных или щелочноземельных металлов, и где система нейтрализации состоит из распылителей, расположенных над трубопроводами для хлора, для доставки раствора в ответ на обнаружение утечки хлора.
29. Система по п. 28, где галогенид четвертичного аммония представляет собой бромид тетраэтиламмония, и где бромид щелочноземельных металлов представляет собой бромид кальция.
| WO 2017081358 A1, 18.05.2018 | |||
| WO 2012130803 A1, 01.10.2012 | |||
| Способ определения расхода выходных конвертерных газов | 1977 |
|
SU684067A1 |
| Способ очистки газовых выбросов от хлора | 1987 |
|
SU1692625A1 |
Авторы
Даты
2024-03-11—Публикация
2020-05-27—Подача