Изобретение относится к медицине, а именно к инфекционным болезням, заболеваниям ЛОР-органов, и может быть использовано для лечения аносмии при COVID-19.
Аносмия является одним из характерных симптомов SARS-CoV-2 (CoV-2, 2019-nCoV) и ряда других ОРВИ. Главным характерным отличием от аносмии, которая возникает при всех вирусных заболеваниях (например: риновирус, грипп и аденовирус), особенностью коронавирусной инфекции является внезапная потеря обоняния без признаков насморка и отеков слизистой носа.
Так, по результатам анализа данных, полученных после начала эпидемии COVID-19, была подтверждена корреляция между потерей обоняния и COVID-19, а также внезапное начало аносмии (Bagheri SH, Asghari A, Farhadi M, Shamshiri AR, Kabir A, Kamrava SK, et al. Coincidence of COVID-19 epidemic and olfactory dysfunction outbreak in Iran. Medical journal of the Islamic Republic of Iran. 2020;34:62). В ряде случаев аносмия являлась единственным симптомом коронавирусной инфекции (Hopkins C, Surda P, Whitehead E, Kumar BN. Early recovery following new onset anosmia during the COVID-19 pandemic – an observational cohort study. Journal of Otolaryngology - Head & Neck Surgery. 2020 May 4;49(1):26).
Возможными механизмами развития аносмии при COVID-19 являются: синдром обонятельной расщелины, местная воспалительная реакция в эпителии носовой полости, ранний апоптоз обонятельных клеток, структурные изменения обонятельных ресничек и нарушения передачи запаха, повреждение микроглии клеток, влияние на обонятельные луковицы, повреждения обонятельного эпителия, повреждении обонятельных нейронов и стволовых клеток. В качестве наиболее вероятной причины аносмии выделяют повреждение рецепторных клеток обонятельного нейроэпителия (Najafloo R, Majidi J, Asghari A, Aleemardani M, Kamrava SK, Simorgh S, et al. Mechanism of Anosmia Caused by Symptoms of COVID-19 and Emerging Treatments. ACS Chem Neurosci. 2021 Oct 20;12(20):3795–80).
Обонятельный нейроэпителий, включает в себя различные виды клеток: обонятельные биполярные нейроны, поддерживающие клетки, базальные стволовые клетки. Особенность биполярных нейронов состоит в том, что они постоянно растут, разрушаются и замещаются новыми нейронами. Базальная стволовая клетка будет превращаться в молодой биполярный обонятельный нейрон, срок жизни которого около месяца. Дендриты от биполярных нейронов обращены к апикальной поверхности, и представляют собой рецепторные окончания - обонятельные реснички. Поддерживающие клетки, помимо опорной функции, выполняют также фагоцитарную и секреторную (для того, чтобы поддержать местный солевой и водный баланс), а также осуществляют функцию детоксикации различных повреждающих агентов, которые проникают в эпителий из окружающей среды ( Najafloo R, Majidi J, Asghari A, Aleemardani M, Kamrava SK, Simorgh S, et al. Mechanism of Anosmia Caused by Symptoms of COVID-19 and Emerging Treatments. ACS Chem Neurosci. 2021 Oct 20;12(20):3795–808).
В свою очередь было показано, что коронавирус SARS-CoV заражает клетки посредством взаимодействия между его спайковым (S) белком и белком ACE2 (ангиотензинпревращающий фермент 2) на клетках-мишенях; это взаимодействие требует расщепления S белка протеазой клеточной поверхности TMPRSS2 (мембрано-связанная сериновая протеаза, продукт гена TMPRSS2). Результаты показывают, что только опорные и стволовые (но не рецепторные) клетки в обонятельном эпителии коэкспрессируют молекулы ACE2 и TMPRSS2. Следовательно, вирус напрямую не входит в сенсорные нейроны, а вместо этого нацеливается на опорные и стволовые клетки, инфицирование которых может быть причиной аносмии и связанной с ней обонятельной дисфункции у пациентов с COVID-19 (Choi R, Goldstein BJ. Olfactory epithelium: Cells, clinical disorders, and insights from an adult stem cell niche. Laryngoscope investigative otolaryngology. 2018;3(1):35–42).
В большинстве случаев обонятельные нарушения при COVID-19 являются транзиторными и длятся 2÷3 недели, поскольку обонятельный эпителий регулярно обновляется, замещая поврежденные клетки. При значительном повреждении обонятельного эпителия, особенно при вовлечении в процесс базальных клеток эпителия, которые экспрессируют большое количество АПФ2 рецепторов, хроническом воспалении и повышенном апоптозе клеток обонятельного эпителия, возможно развитие устойчивой аносмии, которая может персистировать до 12 мес. и больше ( Liang F, Wang DY. COVID-19 Anosmia: High Prevalence, Plural Neuropathogenic Mechanisms, and Scarce Neurotropism of SARS-CoV-2? Viruses. 2021 Nov;13(11):2225).
Задача, решаемая при создании настоящего изобретения, состоит в расширении арсенала средств для лечения аносмии при COVID-19. Техническим результатом, достигаемым при решении такой задачи, является повышение эффективности лечения последствий COVID-19 у человека.
Для достижения поставленного результата предлагается в качестве лечебного средства при аносмии, развивающейся на фоне COVID-19, применить пептид общей формулы Met-Glu-His-Phe-Pro-Gly-Pro (семакс).
Возможность реализации заявленного обозначения обусловлена следующим.
Основной причиной формирования аносмии при COVID-19 является повреждение клеток обонятельного эпителия, обонятельных луковиц и центральных мозговых структур. Следовательно, одним из возможных способов профилактики развития устойчивой, длительной аносмии является применение средств, обладающих цито- и нейропротекторными свойствами, как и в случае с терапией пациентов в остром периоде ишемического инсульта, для которых цитопротективную терапию в отношении всех клеток головного мозга (нейронов, глиальных и эндотелиальных клеток) определяют как одну из наиболее перспективных тактик лечения (Шетова И.М. Возможности нейропептидной цитопротекции при церебральном инсульте. Эффективная фармакотерапия. 2012;(1):16–9).
В настоящее время, единственным индивидуальным пептидом, применяемым в клинике как нейропротекторное средство, является Семакс - пептид общей формулы Met-Glu-His-Phe-Pro-Gly-Pro (Аубекова О.М., Климова Е.А. Терапевтическая эффективность «Семакса 1%» при ишемическом инсульте различной степени тяжести // Вестник неврологии, психиатрии и нейрохирургии, 2015, 2, 41-47; Полякова А.В. Нейропротективная терапия вне «терапевтического окна»: возможности семакса // Вестник неврологии, психиатрии и нейрохирургии, 2014, №5, с.54-60). Он является синтетическим олигопептидом, созданным на основе фрагмента АКТГ4-7 (Met-Glu-His-Phe), обладающего выраженной физиологической активностью в отношении центральной нервной системы (ЦНС) при отсутствии какой-либо гормональной активности. Для защиты от гидролизующего действия пептидаз к нему был присоединен трипептид Pro-Gly-Pro, обладающий, в свою очередь, нейропротективной активностью (Ашмарин И.П., Незавибатьков Н.Н., Мясоедов Н.Ф., Каменский А.А. и др. Ноотропный аналог адренокортикотропина 4-10 – Семакс (15-летний опыт разработки и изучения) //Журнал высшей нервной деятельности. -1997. –т.47. –с.419-425).
Как известно, нейропептиды, структурно связанные с АКТГ, могут влиять на текучесть синаптических мембран, модулировать рецепторные функции (воздействуя на процессы фосфорилирования белков), тормозить активацию микроглии и избыточный синтез нейротоксических цитокинов и лигантов к NMDA-рецепторам, обладать самостоятельным нейротрофическим эффектом (Зарубина И.В. Фармакологическая коррекция пептидами функционально-метаболических нарушений головного мозга в постишемическом периоде//Пептидная нейропротекция. Под редакцией М.М. Дьяконова, А.А. Каменского. – СПб.: Наука, 2009.- с.126-185). В качестве первичного нейропротектора Семакс оказывает влияние на одно из первых (и поэтому наиболее важных) звеньев патогенеза ишемического каскада: он подавляет глутаматную эксайтоксичность (повышает способность глиальных клеток захватывать свободный глутамат и аспартат из синаптической щели). Препарат также снижает интенсивность оксидантного стресса, повышая активность супероксиддисмутазы и подавляя образование свободных радикалов и избыточного количества NO-иона, а также препятствует нарушению структуры клеточных мембран. Как вторичный нейропротектор Семакс снижает интенсивность локального воспаления и отека мозговой ткани, вследствие устранения дисбаланса между уровнем про- и противовоспалительных цитокинов; активирует синтез нейротрофинов (регуляторов роста и дифференцировки нервной ткани: NGF, BDNF, NF-3 и -5), снижает скорость патологического апоптоза. Все это вместе взятое препятствует гибели нервных клеток и способствует восстановлению функциональной активности головного мозга (Левицкая Н.Г., Глазова Н.Ю., Себенцова Е.А., Манченко Д.М., Виленский Д.А., Андреева Л.А., Каменский А.А., Мясоедов Н.Ф. Исслелование спектра физиологической активности аналога АКТГ4-10 гептапептида семакс / Нейрохимия, 2008, т.25, №1, 111-118; Dolotov O.V., Karpenko E.A., Inozemtseva L.S., Seredenina T.S., Levitskaya N.G., Rozyczka J., Dubynina E.V., Novosadova E.V., Andreeva L.A., Alfeeva L.Y., Kamensky A.A., Grivennikov I.A., Myasoedov N.F., Engele J. Semax, an analog of ACTH(4-10) with cognitive effects, regulates BDNF and trkB expression in the rat hippocampus. Brain Res., 2006, v. 1117, №1, p. 54-60). Важными фармакологическими свойствами Семакса являются также нейрометаболическое и ноотропное действие. Так, его нейрометаболическое (антигипоксическое) действие связано со способностью препарата повышать эффективность метаболизма нервных клеток (в том числе и глиальных) в неблагоприятных условиях (гипоксия, ишемия, оксидантный стресс и др.) (Ашмарин И.П., Незавибатьков Н.Н., Мясоедов Н.Ф., Каменский А.А. и др. Ноотропный аналог адренокортикотропина 4-10 – Семакс (15-летний опыт разработки и изучения) //Журнал высшей нервной деятельности. -1997. – т.47. – с.419-425). Немаловажным для медицинской практики является его низкая токсичность и безопасность приема.
Вследствие всего вышесказанного представляется перспективным изучение препарата Семакс®, капли назальные 0,1%, производства АО «ИНПЦ «Пептоген», на пациентах с нарушением хемосенсорных функций, особенно с учетом фармакокинетики и фармакодинамики препарата.
Нижеследующие результаты многоцентрового рандомизированного двойного-слепого плацебо-контролируемого исследования, подтверждающего реализацию заявленного назначения, поясняются с учетом следующих графических материалов:
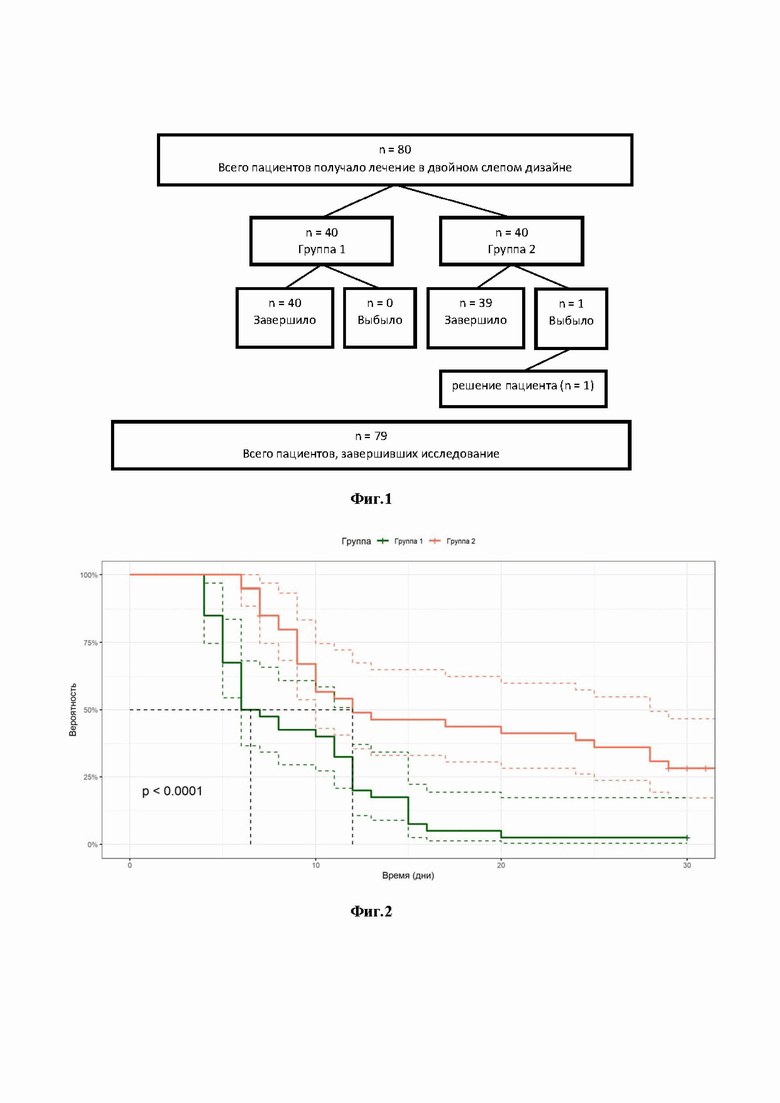
фиг.1 - схематическое участие пациентов в исследовании;
фиг.2 – график времени (в днях) от начала лечения до полного восстановления обоняния по данным субъективной оценки без учета времени отсутствия обоняния до включения в исследование: кривые выживаемости, метод Kaplan-Meier;
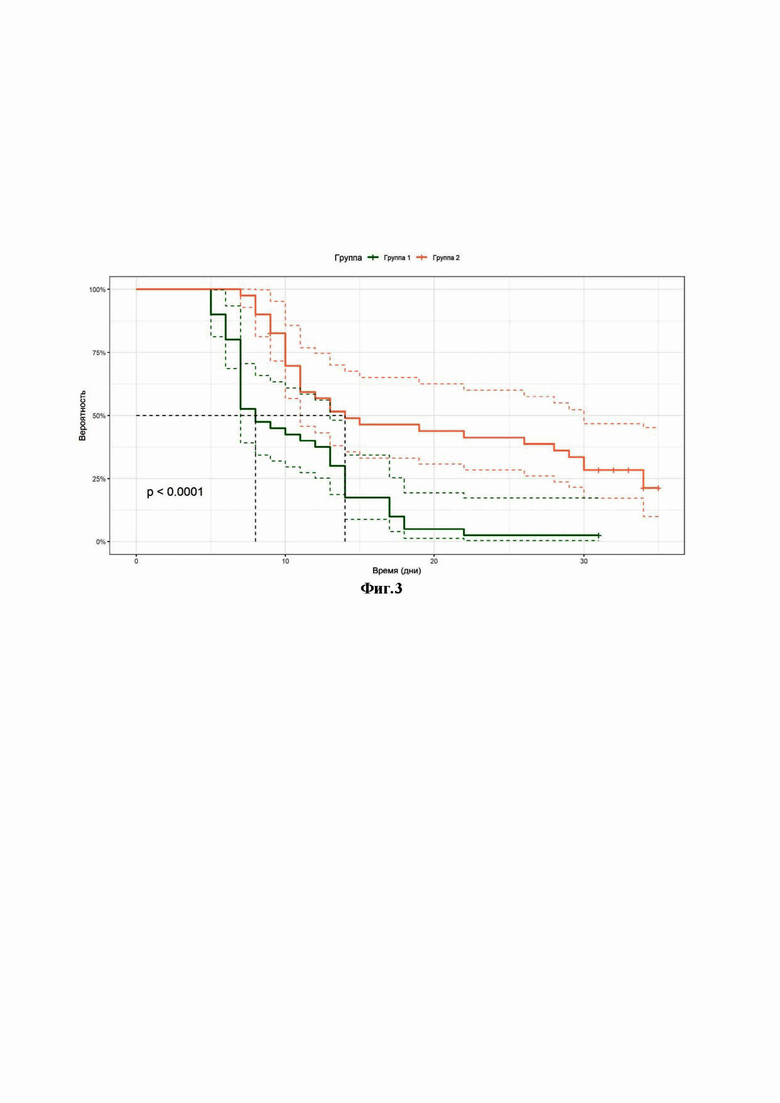
фиг.3 – график времени (в днях) от начала лечения до полного восстановления обоняния по данным субъективной оценки с учетом времени отсутствия обоняния до включения в исследование: кривые выживаемости, метод Kaplan-Meier
Со ссылкой на фиг.1, в исследовании был проведен скрининг, а затем рандомизация 80 пациентов, которые были распределены на группы следующим образом:
группа 1-40 пациентов, получавших Семакс®, капли назальные 0,1%, производства АО «ИНПЦ «Пептоген».
группа 2-40 пациентов, получавших плацебо (капли назальные производства АО «ИНПЦ «Пептоген»).
В ходе исследование все 40 пациентов из группы 1 завершили исследование. В группе 2 один из участников отказался от участия в исследовании после Визита 2 и соответственно завершил участие в исследовании преждевременно.
Полный набор данных для анализа включал в себя всех рандомизированных пациентов (по 40 (100%) пациентов в группе), все рандомизированные пациенты фактически получили лечение препаратов в соответствие с группой, назначенной при рандомизации. 79 из 80 пациентов в настоящем исследовании завершили все визиты исследования и не имели значимых отклонений от протокола.
Демографические и антропометрические исходные характеристики пациентов по группам представлены в таблице 1. Группы оказались высокосопоставимы по всем оцененным показателям, что говорит об успешности проведенной рандомизации, статистически значимых различий по возрасту, весу, росту и индексу массы тела (ИМТ) участников между группами выявлены не были.
Таблица 1
Половой состав групп также был сопоставим (таблица 2), между группами статистически значимых различий не выявлено (p=0,502, критерий «хи-квадрат»).
Таблица 2
Включенные в исследование пациенты не отличались по расовому составу. Подавляющее большинство пациентов относились к европеоидной расе (97,5% в группе 1 и 92,5% в группе 2 (p=0,612 точный тест Фишера).
При анализе медицинского анамнеза выявлено, что большинство пациентов не имели хирургических вмешательств в анамнезе (82,5% в группе 1, 85% в группе 2, p=1,000 (критерий «хи-квадрат»). Сопутствующие заболевания выявлены у 55% пациентов из группы 1 и у 52,5% пациентов из группы 2, к наиболее частым (частота 10% и более хотя бы в одной группе) относились: сопутствующая вирусная инфекция верхних дыхательных путей, остеохондроз, миопия и артериальная гипертензия. Частота применения сопутствующей терапии была сопоставимой (65% в группе 1, 60% в группе 2, p=0,817 (критерий «хи-квадрат»), ни у одного пациента не было выявлено отягощенного аллергического анамнеза, все пациенты участвовали в клинических исследованиях в первый раз в жизни.
Большинство пациентов обеих групп не употребляли алкоголь: 87,5% в группе 1 и 92,5% в группе 2 (p=0,282 точный тест Фишера); не курили: 97% в группе 1 и 95% в группе 2 (p=0,494 точный тест Фишера); ни один из участников исследования не употреблял наркотики.
10% участников в группе 1 и 5% участников в группе 2 не имели репродуктивного потенциала (p=0,675, точный тест Фишера), все пациенты с сохраненным репродуктивным потенциалом использовали надежные методы контрацепции. У всех участниц женского пола с сохраненным репродуктивным потенциалом тест на беременность был отрицательным и на момент включения в исследования, и на момент его планового либо преждевременного завершения.
Все пациенты, участвовавшие в исследовании, имели положительный результат исследования мазка на SARS-CoV-2. Приверженность назначенному лечению в исследовании была высокой: у всех пациентов она превышала 87% и в среднем составляла 97,8% в группе 1 и 98,77% в группе 2 (p=0,335, критерий Манна-Уитни).
Анализ эффективности
Препарат применялся согласно инструкции интраназально в суточной дозе 600 мкг (0,6 мг) в течение 5 дней. Если не было полного восстановления обоняния через 5 дней терапии, терапия продлевалась еще на 5 дней.
Первичным показателем (конечной точкой) эффективности в проведенном исследовании было среднее время полного восстановления обоняния в днях по данным субъективной оценки по группам без учета времени отсутствия обоняния до включения пациентов в исследование. Для анализа указанного первичного показателя эффективности применялся групповой последовательный дизайн (group sequential design) с одним промежуточным анализом. Промежуточный анализ был проведен в соответствии с протоколом после набора планируемого количества пациентов (40 рандомизаций в каждой группе).
Статистическая модель анализа, представленная в обосновании размера выборки, заключалась в сравнении рисков/опасностей (hazards) между группами (нулевая гипотеза H0: h1 – h2 ≤ 0; альтернативная гипотеза HA: h1 – h2 > 0) с последующим расчетом отношения рисков (hazard ratio), при этом предполагалось, что отношение рисков/опасностей будет равно или превысит значение 1,75, что приблизительно соответствует разнице в 3 дня во времени полного восстановления обоняния в днях по данным субъективной оценки по группам без учета времени отсутствия обоняния до включения пациентов в исследование.
Статистический анализ был выполнен в соответствии с руководством ICH E9 «Statistical Principles For Clinical Trials».
Контроль аносмии и динамики ее восстановления проводился с использованием ольфактометрии, которая проводилась дважды. Была использована методика «Sniff Magnitude test» (Brann Choi, R., Goldstein, B. J. Olfactory epithelium: Cells, clinical disorders, and insights from an adult stem cell niche. Laryngoscope Investigative Otolaryngology. 2018, Vol. 3, 1, pp. 35-42), суть которой заключается в количественном снижении объема вдыхаемого дурно пахнущего одоранта - пациент, имеющий нормальную обонятельную функцию, немедленно прекращает вдыхать этот запах, тогда как человек, страдающий нарушением обоняния, продолжает нормально или почти нормально дышать данным одорантом.
Данные по времени полного восстановления обоняния (в днях) по данным субъективной оценки по группам без учета времени отсутствия обоняния до включения пациентов в исследование по группам представлены в таблице 3, а также на фиг.2.
Таблица 3
Отношение рисков/опасностей (hazard ratio), доверительный интервал и значение p представлены в таблице 4. В качестве базовой группы использована группа 1 (Препарат Семакс®). Полученное значение – 2,953, 97,66% ДИ от 1,769 до 4,931, значение p<0,001. Таким образом, в результате анализа первичного показателя эффективности было получено значение, существенно превышающее запланированный порог (1,75), кроме того, запланированный порог превышала и нижняя граница доверительного интервала (1,762).
Таблица 4
Вторичные показатели (конечные точки) эффективности были представлены тремя параметрами:
среднее время полного восстановления обоняния в днях по данным субъективной оценки за время исследования по группам с учетом времени отсутствия обоняния до включения в исследование;
доля пациентов с полностью восстановившимся обонянием по данным субъективной оценки к 5, 11, 21 и 30 дням;
доля пациентов с частично восстановившимся обонянием по данным субъективной оценки к 5, 11, 21 и 30 дням.
Среднее время полного восстановления обоняния в днях по данным субъективной оценки за время исследования по группам с учетом времени отсутствия обоняния до включения в исследование данные представлены в таблице 5, а также на фиг.3. Как и для первичного показателя эффективности, необходимо отметить, что различия в среднем времени восстановления обоняния в днях по данным субъективной оценки за время исследования по группам с учетом времени отсутствия обоняния до включения в исследование достигли почти 9 дней, таким образом, выявленный эффект в отношении влияния на длительность аносмии не зависел от того, учитывается ли длительность потери обоснования до включения в исследование или же отсчитывается только от момента включения в исследование.
Таблица 5
Доля пациентов с полностью восстановившимся обонянием представлена в таблице 6. Необходимо отметить, что в группе 1 частота и скорость восстановления обоняния существенно выше по сравнению с группой 2 и в среднем время составляет 10 дней. Так, в группе 1 на моменты дня 5, дня 11 и дня 21 32,5% (13 участников), 67,5% (27 участников) и 97,5% пациентов (то есть 39 участников из 40) уже имели восстановившееся обоняние. В группе 2 на момент дня 5 отсутствовали пациенты с полным восстановлением обоняния; на моменты дня 11 и дня 21 полное восстановление обоняния наблюдалось лишь у 45,0% (18 участников) и 57,5% (то есть 23 участников из 39) пациентов. К дню 30 данные различия начали нивелироваться за счет того, что в группе 2 также началось восстановление обоняния.
Таблица 6
Доля пациентов с частично восстановившимся обонянием представлена в таблице 7. В обеих популяциях различия в пользу группы 1 выявлены на день 5 и на день 21.
Таблица 7
Таким образом, проведенное исследование продемонстрировало высокую клиническую эффективность исследуемого препарата Семакс® при лечении аносмии, развивающейся на фоне при COVID-19.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностики обонятельной дисфункции | 2024 |
|
RU2834954C1 |
| Применение способа получения кондиционной среды, обладающей регенераторным потенциалом для интраназального введения при лечении хронических поствирусных нарушений обоняния | 2023 |
|
RU2816357C1 |
| Способ оценки порога обоняния у детей | 2021 |
|
RU2770290C1 |
| Способ лечения дизосмии, вызванной коронавирусной инфекцией | 2021 |
|
RU2791808C2 |
| Способ физиотерапии аносмии после коронавирусной инфекции | 2021 |
|
RU2751823C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ОБОНЯТЕЛЬНОЙ ДИСФУНКЦИЕЙ ПРИ АТРОФИЧЕСКОМ РИНИТЕ | 2019 |
|
RU2713786C1 |
| Способ коррекции нарушения обоняния при патологии носа и околоносовых пазух | 2024 |
|
RU2830471C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ БОЛЕЗНИ ПАРКИНСОНА И ЭССЕНЦИАЛЬНОГО ТРЕМОРА | 2011 |
|
RU2467697C1 |
| СПОСОБ ДИАГНОСТИКИ ЗАБОЛЕВАНИЯ ПАРКИНСОНА У БОЛЬНЫХ С НАРУШЕНИЕМ ФУНКЦИИ ОБОНЯНИЯ | 2011 |
|
RU2478209C1 |
| Тест-система для диагностики обонятельной дисфункции | 2024 |
|
RU2831891C1 |
Изобретение относится к области фармацевтики и медицины, а именно к применению пептида формулы Met-Glu-His-Phe-Pro-Gly-Pro (семакс) в качестве лечебного средства при аносмии, развивающейся на фоне COVID-19. Технический результат заключается в повышении эффективности лечения последствий COVID-19 у человека, а именно аносмии. 3 ил., 7 табл., 1 пр.
Применение пептида формулы Met-Glu-His-Phe-Pro-Gly-Pro (семакс) в качестве лечебного средства при аносмии, развивающейся на фоне COVID-19.
Авторы
Даты
2024-04-02—Публикация
2023-09-29—Подача