Изобретение относится к анальгетическим средствам на основе 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов формулы (I, II, III):
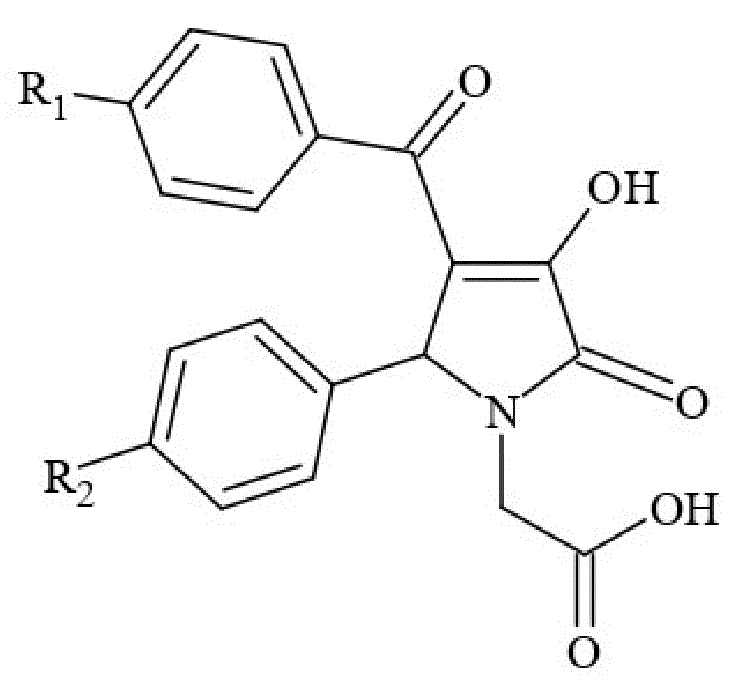
I, II, III,
R1 = H (I, II), CH3 (III); R2 = F (I, III), Cl (II)
Указанные соединения обладают выраженной антиноцицептивной активностью и низкой токсичностью, что позволяет предположить возможность их применения в медицине в качестве анальгетических лекарственных средств.
Ближайшими аналогами по структуре и действию заявляемому соединению являются 4-ацетил-3-гидрокси-1-карбоксиметил-5-(4-метилфенил)-3-пирролин-2-он (IV) и 4-ацетил-3-гидрокси-1-карбоксиметил-5-(4-этилфенил)-3-пирролин-2-он (V) [Синтез, анальгетическая и противовоспалительная активности 5-арил-4-ацетил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов / В.Л. Гейн, Е.В. Пастухова, С.В. Чащина // Химико-фармацевтический журнал. - 2022. - Т. 56, № 3. - С. 21-24] формулы:
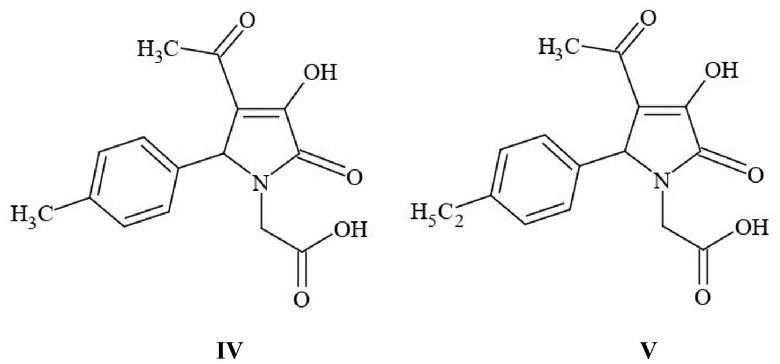
Структурные аналоги (IV, V) обладают анальгетической активностью (таблица 1).
В медицинской практике широко используется метамизол натрия (анальгин) в качестве анальгетического лекарственного средства, аналогичного по фармакологическому действию заявляемым соединениям (I, II, III), которое выбрано нами в качестве эталона сравнения (Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - С. 848).
Целью изобретения является поиск новых соединений с высокой анальгетической активностью и низкой токсичностью в ряду 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов.
Поставленная задача решается применением 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов формулы (I, II, III), которые обладают высокой анальгетической активностью и низкой токсичностью.
Заявляемые соединения (I II, III) синтезируют взаимодействием метиловых эфиров ароилпировиноградных кислот с гликоколом и ароматическими альдегидами в среде ледяной уксусной кислоты в присутствии безводного ацетата натрия по схеме:

R1 = H (I, II), CH3 (III); R2 = F (I, III), Cl (II)
Синтез соединений (I, II, III, IV, V) осуществлен согласно ранее описанных методик [Синтез 5-арил-4-ацил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов / В. Л. Гейн, Е. В. Пастухова // Бутлеровские сообщения, 2020. - Т. 64, № 11. С. 9 -12; Синтез 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов / В.Л. Гейн, Е.В. Пастухова // Журнал общей химии. - 2021. - Т. 91, № 7. - С. 987 -991; Синтез, анальгетическая и противовоспалительная активности 5-арил-4-ацетил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов / В.Л. Гейн, Е.В. Пастухова, С.В. Чащина // Химико-фармацевтический журнал. - 2022. - Т. 56, № 3. - С. 21-24]
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение соединения (I).
К смеси 10 ммоль безводного ацетата натрия и 10 ммоль гликокола в 10 мл ледяной уксусной кислоты добавляли по 10 ммоль метилового эфира бензоилпировиноградной кислоты и п-фторбензальдегида. Реакционную смесь нагревали до растворения компонентов и выдерживали при комнатной температуре в до выпадения осадка. Выпавший осадок отфильтровывали и перекристаллизовывали из этанола.
Выход 0.37 (11%). Т. пл. 222-224°С. Найдено, %: C 64.23; H 3.97; N 3.94. C19H14FNO5. Вычислено, %: C 64.25; H 3.96; N 3.97. ИК спектр (ИК-Фурье спектрометр IRAffinity-1 Shimadzu (Япония), в таблетках с KBr, ν, см-1): 3119 (OH), 1726 (COOН), 1695 (CON), 1626 (CO). Спектр ЯМР 1Н (Bruker AM-300, рабочая частота 500 МГц, DMSО-d6, ТМS, δ, м.д.): 4.25 д (1Н, CαНАНВ, J 20.00 Гц), 3.36 д (1Н, CαНАНВ, J 20.00 Гц), 5.48 с (1H, С5Н), 7.10-7.74 м (9H, CHAr), 12.90 c (1H, С3OH).
Соединение (I) - белое кристаллическое вещество, растворимое в ДМСО, ДМФА, при нагревании - в ледяной уксусной кислоте, диоксане, этаноле и не растворимые в воде.
Пример 2. Получение соединения (II).
К смеси 10 ммоль безводного ацетата натрия и 10 ммоль гликокола в 10 мл ледяной уксусной кислоты добавляли по 10 ммоль метилового эфира бензоилпировиноградной кислоты и п-хлорбензальдегида. Реакционную смесь нагревали до растворения компонентов и выдерживали при комнатной температуре в до выпадения осадка. Выпавший осадок отфильтровывали и перекристаллизовывали из этанола.
Выход 1.70 г (46%), Т. пл. 208-210°С. Найдено, %: C 61.38; H 3.80; N 3.77. C19H14ClNO5. Вычислено, %: C 61.09; H 3.54; N 3.49. ИК спектр (ИК-Фурье спектрометр IRAffinity-1 Shimadzu (Япония), в таблетках с KBr, ν, см-1): 3186 (OH), 1697 (COOН), 1668 (CON), 1624 (CO). Спектр ЯМР 1Н (Bruker AM-300, рабочая частота 500 МГц, DMSО-d6, ТМS, δ, м.д.): 4.27 д (1Н, CαНАНВ, J 20.00 Гц), 3.47 д (1Н, CαНАНВ, J 20.00 Гц), 5.54 с (1H, С5Н), 7.38-7.73 м (9H, CHAr), 12.94 c (1H, С3OH).
Соединение (II) - белое кристаллическое вещество, растворимое, растворимое в ДМСО, ДМФА, при нагревании - в ледяной уксусной кислоте, диоксане, этаноле и не растворимые в воде.
Пример 3. Получение соединения (III).
К смеси 10 ммоль безводного ацетата натрия и 10 ммоль гликокола в 10 мл ледяной уксусной кислоты добавляли по 10 ммоль метилового эфира 4-метилбензоилпировиноградной кислоты и п-фторбензальдегида. Реакционную смесь нагревали до растворения компонентов и выдерживали при комнатной температуре в до выпадения осадка. Выпавший осадок отфильтровывали и перекристаллизовывали из этанола. Выход 1.25 г (32%), Т. пл. 184-186°С. Найдено, %: C 65.04; H 4.37; N 3.79. C20H16FNO5. Вычислено, %: C 64.79; H 4.11; N 3.51. ИК спектр (ИК-Фурье спектрометр IRAffinity-1 Shimadzu (Япония), в таблетках с KBr, ν, см-1): 3250 (OH), 1736 (COOН), 1670 (CON), 1614 (CO). Спектр ЯМР 1Н (Bruker AM-300, рабочая частота 500 МГц, DMSО-d6, ТМS, δ, м.д.): 3.69 c (3H, CH3), 4.27 д (1Н, CαНАНВ, J 20.00 Гц), 3.48 д (1Н, CαНАНВ, J 20.00 Гц), 5.52 с (1H, С5Н), 7.25-7.65 м (8H, CHAr), 12.90 c (1H, С3OH).
Соединение (III) - белое кристаллическое вещество, растворимое, растворимое в ДМСО, ДМФА, при нагревании - в ледяной уксусной кислоте, диоксане, этаноле и не растворимые в воде.
Пример 4. Исследование анальгетической активности и острой токсичности соединений (I, II, III).
Исследования острой токсичности проведены на белых нелинейных мышах-самцах массой 20-28 г. Для определения средней летальной дозы использовали экспресс-метод Прозоровского В. Б. [В. Б. Прозоровский, Фармакология и токсикология, 41(7), 497 - 502 (1978).] Исследуемые соединения (I, II, III) вводили внутрижелудочно в виде взвеси в 1% растворе крахмала в возрастающих дозах. Каждую дозу вводили двум животным. Регистрировали общее состояние и поведение животных, состояние шерстного покрова, определяли массу тела. В каждой группе животных учитывали число летальных исходов за весь срок наблюдения (14 суток).
Рассчитывали острую токсичность, соблюдая рекомендации государственного фармакологического комитета по изучению общетоксического действия биологически активных веществ [Методические рекомендации по изучению общетоксического действия фармакологических средств. Утв. 25. 12. 97 / Вестн. фармакоп. комитета. - 1998. - №1. - С. 27-32].
Средняя летальная доза для соединений I и III составила 3680,0 мг/кг массы животного, для соединения II - 3550,0 мг/кг, что соответствует 4 классу токсичности (малотоксичные вещества) по классификации Hodge и Sterner (1943) и ГОСТ 32419-2013.
Исследование анальгетической активности (I, II, III) проводили в опытах на белых нелинейных мышах обоего пола массой 25-32 г по методу термического раздражения «горячая пластина» [Руководство по проведению доклинических исследований лекарственных средств / Под ред. А.Н. Миронова, Н.Д. Бунятян, А.Н. Васильева, О.Л. Верстаковой, М.В. Журавлевой, В.К. Лепахина, Н.В. Коробова, В.А. Меркулова, С.Н. Орехова, И.В. Сакаевой, Д.Б. Утешева, А.Н. Яворского. М.: Гриф и К, 2012. Ч. 1. 944 с.] Животных помещали на разогретую до 54оС металлическую поверхность, окруженную цилиндром. Регистрировали время с момента помещения на горячую поверхность до появления оборонительного рефлекса на болевое раздражение (облизывание задних лап, прыжки, отдергивание задней лапы). Критерием анальгетического эффекта считали достоверное увеличение латентного периода реакции по сравнению с контролем. Исследуемые соединения (I, II, III) вводили внутрибрюшинно за 30 мин до тестирования в дозе 50 мг/кг в виде взвеси в 1% растворе крахмала. В качестве эталона сравнения использовали метамизол натрия (ПАО Биосинтез», Россия) в дозе 50 мг/кг, который вводили аналогично исследуемым соединениям. В контрольные и опытные группы было включено по 8-10 мышей.
Анальгетическая активность 5-арил-4-ацил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов по методике «горячая пластина», (M±SD)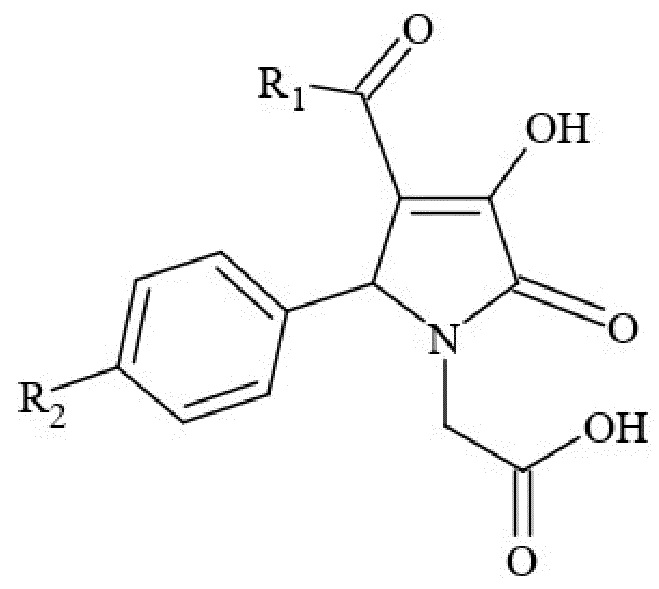
50 мг/кг
* - по сравнению с контролем
** - по сравнению с эталоном
Для альтернативной оценки анальгетической активности заявленных соединений была использована методика «уксусные корчи». Тест на висцеральную химическую ноцицепцию проводили в опытах на белых нелинейных половозрелых мышах-самцах массой 22-28 г. Специфическую болевую реакцию «корчи» вызывали внутрибрюшинным введением 0,75% водного раствора уксусной кислоты в дозе 0,1 мл/10 г массы тела животного. Подсчет числа «корчей» проводили сразу после введения уксусной кислоты в течение 15 минут [Руководство по проведению доклинических исследований лекарственных средств / Под ред. А.Н. Миронова, Н.Д. Бунятян, А.Н. Васильева, О.Л. Верстаковой, М.В. Журавлевой, В.К. Лепахина, Н.В. Коробова, В.А. Меркулова, С.Н. Орехова, И.В. Сакаевой, Д.Б. Утешева, А.Н. Яворского. М.: Гриф и К, 2012. Ч. 1. 944 с.]. В контрольную и опытные группы было включено по 6 животных. В качестве препарата сравнения использовали метамизол натрия (ОАО «Борисовский завод медицинских препаратов», Беларусь). Исследуемые соединения и эталонный препарат вводили внутрижелудочно через атравматичный металлический зонд в виде взвеси в 1% растворе крахмала в дозе 50 мг/кг за 60 мин до введения уксусной кислоты. Животные контрольной группы получали 1%-ный раствор крахмала, который вводили аналогично исследуемым соединениям. Критерием анальгетической активности исследуемых веществ считали уменьшение количества «корчей» у животных по сравнению с контрольной группой.
Анальгетическая активность 5-арил-4-ацил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов по методике «уксусные корчи», (M±SD)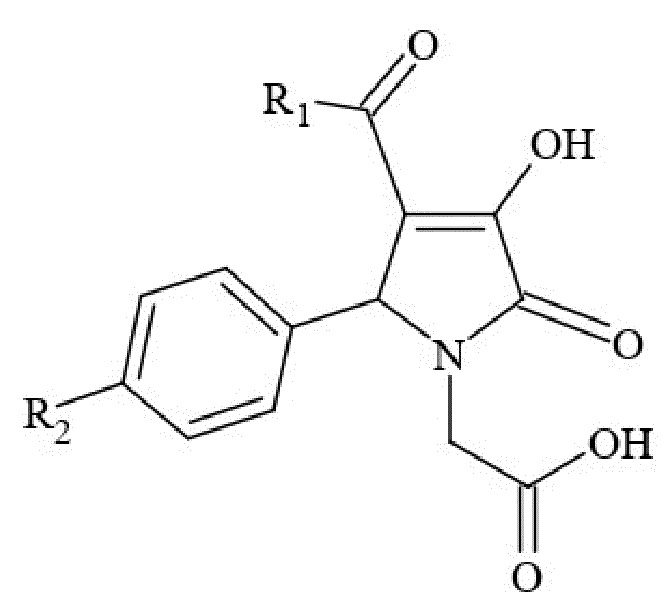
* - по сравнению с контролем
** - по сравнению с эталоном
Как видно из результатов, представленных в таблице 2, соединения ряда 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов (I, II, III) достоверно уменьшают количество «корчей» по сравнению с контролем. Представляет интерес соединение I, антиноцицептивная активность которого достоверно (при р <0.05) превосходит эффект препарата сравнения.
Проведенные исследования показали наличие анальгетической активности заявляемых соединений I, II, III превосходящей эффект эталона сравнения метамизола натрия и структурных аналогов IV и V (табл. 1, табл. 2).
Таким образом, соединения ряда 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов (I, II, III) проявляют более высокую анальгетическую активность по сравнению со структурными аналогами (IV, V) и эталоном сравнения метамизолом натрия, а также являются малотоксичными соединениями, и могут найти применение в медицине в качестве потенциальных лекарственных средств.
Исследование выполнено при финансовой поддержке Пермского научно-образовательного центра «Рациональное недропользование», 2022 год.
Изобретение относится области медицинской химии, а именно к применению 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов формулы (I, II, III), где R1=H (I, II), CH3 (III); R2=F (I, III), Cl (II), в качестве средств, обладающих анальгетической активностью. Технический результат изобретения заключается в проявлении высокой анальгетической активности и низкой токсичности соединений ряда 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов. 2 табл., 4 пр.
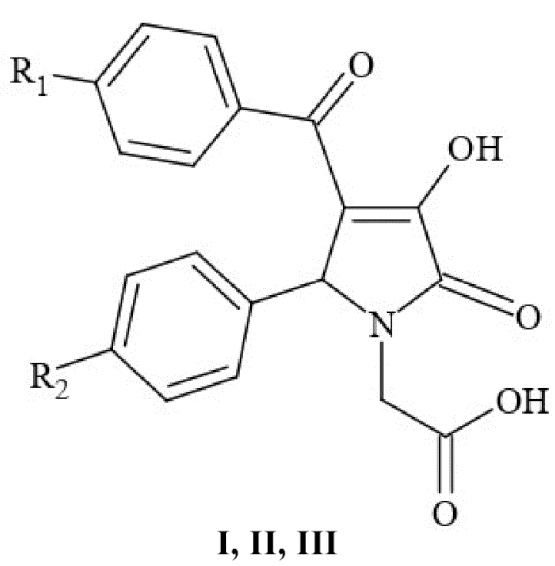
Применение 5-арил-4-ароил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов формулы (I, II, III)

R1=H (I, II), CH3 (III); R2=F (I, III), Cl (II),
в качестве средств, обладающих анальгетической активностью.
| ГЕЙН В.Л | |||
| и др | |||
| Синтез, анальгетическая и противовоспалительная активности 5-арил-4-ацетил-3-гидрокси-1-карбоксиметил-3-пирролин-2-онов, Химико-фармацевтический журнал, 2022, т.56, N 3, c.21-24 | |||
| ГЕЙН В.Л | |||
| и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| ГЕЙН В.Л | |||
| и др | |||
Авторы
Даты
2024-04-08—Публикация
2023-04-04—Подача