Область техники
[0001] Настоящее изобретение относится к комплексу гидроксида металла, содержащему модифицированную многослойную структуру гидроксида, которая содержит базовый слой, поверхностный слой и активный ингредиент, и к способу его получения.
Уровень техники
[0002] Активные ингредиенты для косметики, которые можно вводить в кожу и которые могут непосредственно проявлять свое действие, могут включать витамины и т.п. Витамины являются необходимыми веществами in vivo и обладают такими функциями, как ускорение метаболизма живых организмов, проявление антиоксидантного действия, защита клеточных стенок, усиление иммунитета, повышение стойкости к инфекциям и т.д., и у большинства приматов их биосинтез является невозможным, их необходимо получать вместе с пищей, а при недостаточном их употреблении возможен дефицит различных витаминов. Кроме того, в области ухода за кожей и ее лечения витамины играют важную роль для сохранения здоровой кожи, например, предотвращения пигментации, ускорения синтеза коллагена, блокирования УФ излучения, предотвращения высыхания и кератинизации кожи, предупреждения морщин, увлажнения кожи и т.п. Примеры витаминов включают ретинол (витамин A), аскорбиновую кислоту (витамин C), токоферол (витамин E) и их производные.
[0003] Помимо витаминов, активные ингредиенты для косметики могут включать α-гидроксикислоты (AHA), действующие для ускорения метаболизма в коже посредством удаления рогового слоя кожи, такие как молочная кислота, лимонная кислота и салициловая кислота; койевая кислота (5-гидрокси-2-(гидроксиметил)-4H-пиран-4-он), которая обладает действием отбеливания кожи посредством ингибирования биосинтеза меланина; индол-3-уксусная кислота (C10H9NO2), которая препятствует образованию морщин посредством ускорения пролиферации фибробластов; и салициловая кислота (2-гидроксибензойная кислота, C7H6O3), которая обладает действием антиоксиданта и активностью при лечении угрей, а также известны многие другие вещества для косметических ингредиентов.
[0004] Однако большинство вышеупомянутых материалов для косметических ингредиентов имеют ограниченное практическое применение вследствие проблем, связанных со стабильностью самого материала, раздражением кожи и токсичностью, устойчивостью высвобождения, диспергируемостью и т.д., и, следовательно, их функции или эффект проявляются недостаточно. Например, витамины являются физически и химически весьма нестабильными и легко разрушаются под действием нагревания, света, влаги, кислорода, щелочей и т.п., поэтому их функция и эффективность снижены, или происходит изменение цвета или возникает неприятный запах. Кроме того, α-гидроксикислоты, такие как молочная кислота, являются проблемными в том отношении, что они вызывают раздражение кожи. В случае койевой кислоты, меланиновые пигменты или меланоциты разрушаются вследствие ее проникновения в базальный слой и, следовательно, при использовании в высоких концентрациях она вызывает различные кожные заболевания, такие как дерматит, рак кожи и т.п., и может происходить изменение цвета вследствие окисления под действием света и высокой температуры. Индол-3-уксусная кислота также неустойчива в условиях окружающей среды, нагревания, света, влаги, кислорода и т.д., и особенно восприимчива к действию света, что вызывает проблемы изменения цвета и появления неприятного запаха.
[0005] Таким образом, проведены глубокие исследования для достижения эффекта стабилизации активных веществ, снижения раздражения кожи или токсичности и т.п. В частности, в корейском патенте №115076 описан способ получения нанокапсул витаминов посредством пропитывания и инкапсулирования в микроглобулы внутренней фазы витаминов и различных активных ингредиентов и их дополнительной стабилизации с использованием двухслойной липидной мембраны и диспергируемого в воде полимера. Кроме того, в публикации заявки на патент Кореи №2000-0048451 описан способ инкапсулирования липофильного сферического ядра активного ингредиента в синтетические и природные вододиспергируемые анионные полимеры, которые нерастворимы в воде.
[0006] Однако вышеупомянутые способы занимают много времени, поскольку такой способ, процесс и т.д. является сложным для обработки активного материала и, следовательно, экономически неэффективным. Кроме того, поскольку необходимо осуществлять дополнительное нанесение покрытия на активный ингредиент, действие самого активного ингредиента может быть снижено, и возникает проблема, связанная с тем, что активный материал не может быть в избытке включен в комплекс.
[0007] (Патентный документ 1) Патент Кореи №115076
[0008] (Патентный документ 2) Публикация заявки на патент Кореи №2000-0048451
Описание
Техническая задача
[0009] Настоящее изобретение сделано с учетом проблем, присутствующих в данной области техники, и настоящее изобретение направлено на обеспечение комплекса гидроксида металла, содержащего многослойную структуру гидроксида, которая содержит базовый слой, поверхностный слой и активный ингредиент, в которой сам активный ингредиент может быть стабильно включен в избыточном количестве в комплекс гидроксида металла, что обеспечивает возможность максимизации действия активного ингредиента, а также на обеспечение способа его получения, который является экономически эффективным благодаря сокращению технологического процесса, поскольку активный ингредиент может быть включен более стабильным и эффективным образом.
Техническое решение
[0010] В настоящем изобретении предложен комплекс гидроксида металла, содержащий модифицированную многослойную структуру гидроксида химической формулы 1, представленной ниже, которая содержит базовый слой, поверхностный слой и активный ингредиент.
[0011] [Химическая формула 1]
[0012] {[Mx(OH)z]B[My(OH)w]S}{(An)q}⋅m(H2O)
[0013] Здесь [Mx(OH)z]B представляет собой базовый слой многослойной структуры гидроксида, и [My(OH)w]S представляет собой поверхностный слой многослойной структуры гидроксида,
[0014] M представляет собой катион любого двухвалентного металла, выбранный из группы, состоящей из Ca2+, Mg2+, Cu2+, Zn2+, Ni2+, Co2+ и Fe2+,
[0015] x равен от 0,6 до 3,
[0016] y равен от 0 до 2,
[0017] z равен от 1 до 5,
[0018] w равен от 0 до 4,
[0019] z+w равно от 1 до 9,
[0020] q равен от 1 до 4,
[0021] m равен от 0,1 до 10,
[0022] n представляет собой зарядовое число A, и
[0023] активный ингредиент представлен символом A, где A представляет собой анионное соединение, содержащее в качестве функциональной группы, имеющей электростатическое притяжение в зависимости от pKa, по меньшей мере одну группу, выбранную из группы, состоящей из гидроксильной группы (-OH), карбонильной группы (-CO-), формильной группы (-CHO), карбоксильной группы (-COOH), сульфатной группы (-SO32-), дигидрофосфатной группы (-H2PO42-) и фосфатной группы (-PO43-).
[0024] В настоящем изобретении предложен комплекс гидроксида металла, получаемый посредством совместного осаждения активного ингредиента и гидроксида металла в реакции осаждения с использованием спирта и воды.
[0025] В настоящем изобретении предложен способ получения комплекса гидроксида металла, включающий совместное осаждение активного ингредиента и гидроксида металла в реакции осаждения с использованием спирта и воды.
Полезный эффект
[0026] В соответствии с настоящим изобретением, активный ингредиент может быть включен в многослойную структуру гидроксида в большем избытке, имеет превосходные характеристики устойчивого высвобождения и является включенным в комплекс гидроксида металла в стабильном состоянии и в большом количестве, что усиливает эффект доставляемого активного ингредиента.
[0027] Кроме того, предложенный комплекс гидроксида металла стабильно содержит нестабильный активный ингредиент, что обеспечивает возможность длительного хранения активного ингредиента и, при нанесении на кожу, минимизации раздражения, что усиливает эффект отсутствия раздражения.
[0028] Согласно настоящему изобретению, активный ингредиент включен в многослойную структуру гидроксида и, следовательно, демонстрирует превосходный эффект биосинтеза коллагена.
Краткое описание графических материалов
[0029] На фиг. 1 представлена картина рентгеновской дифракции каждого материала из таблицы 1, где  представляет собой кривую для MZLA,
представляет собой кривую для MZLA,  представляет собой эталонную кривую, и
представляет собой эталонную кривую, и  представляет собой кривую для основной соли цинка;
представляет собой кривую для основной соли цинка;
[0030] На фиг. 2 представлена картина рентгеновской дифракции гидроксида металла в зависимости от соотношения растворителей этанол : вода, причем если сумма массового соотношения EtOH и H2O равна 10, то  представляет собой кривую при соотношении EtOH 1,0 : H2O 9,0,
представляет собой кривую при соотношении EtOH 1,0 : H2O 9,0,  представляет собой кривую при соотношении EtOH 4,6 : H2O 5,4,
представляет собой кривую при соотношении EtOH 4,6 : H2O 5,4,  представляет собой кривую при соотношении EtOH 6,4 : H2O 3,6, и
представляет собой кривую при соотношении EtOH 6,4 : H2O 3,6, и  представляет собой кривую при соотношении EtOH 8,5 : H2O 1,5;
представляет собой кривую при соотношении EtOH 8,5 : H2O 1,5;
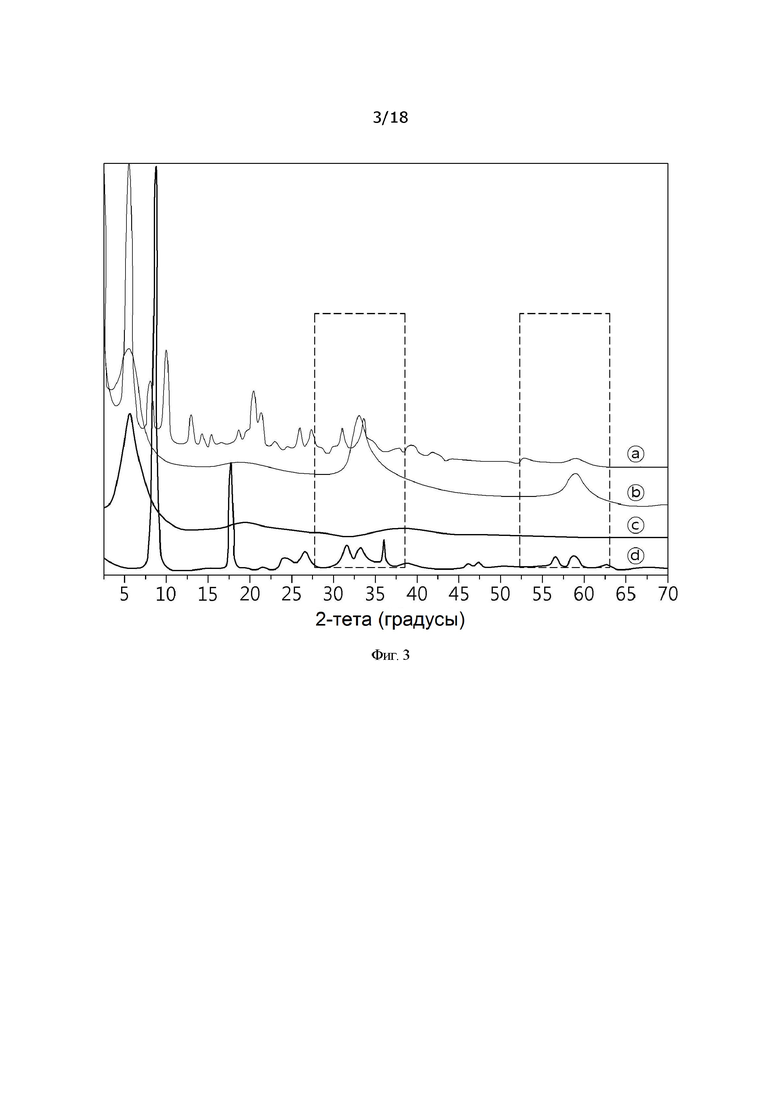
[0031] На фиг. 3 представлена картина рентгеновской дифракции, где  и
и  представляют собой картины рентгеновской дифракции гидроксида металла, полученного с использованием смешанного растворителя из этанола : воды (
представляют собой картины рентгеновской дифракции гидроксида металла, полученного с использованием смешанного растворителя из этанола : воды ( EtOH:H2O=85: 15, и
EtOH:H2O=85: 15, и  EtOH 4,6 : H2O 5,4),
EtOH 4,6 : H2O 5,4),  представляет собой картину рентгеновской дифракции гидроксида металла, полученного с использованием чистой воды в качестве растворителя, и
представляет собой картину рентгеновской дифракции гидроксида металла, полученного с использованием чистой воды в качестве растворителя, и  представляет собой картину рентгеновской дифракции ZBS-NO3;
представляет собой картину рентгеновской дифракции ZBS-NO3;
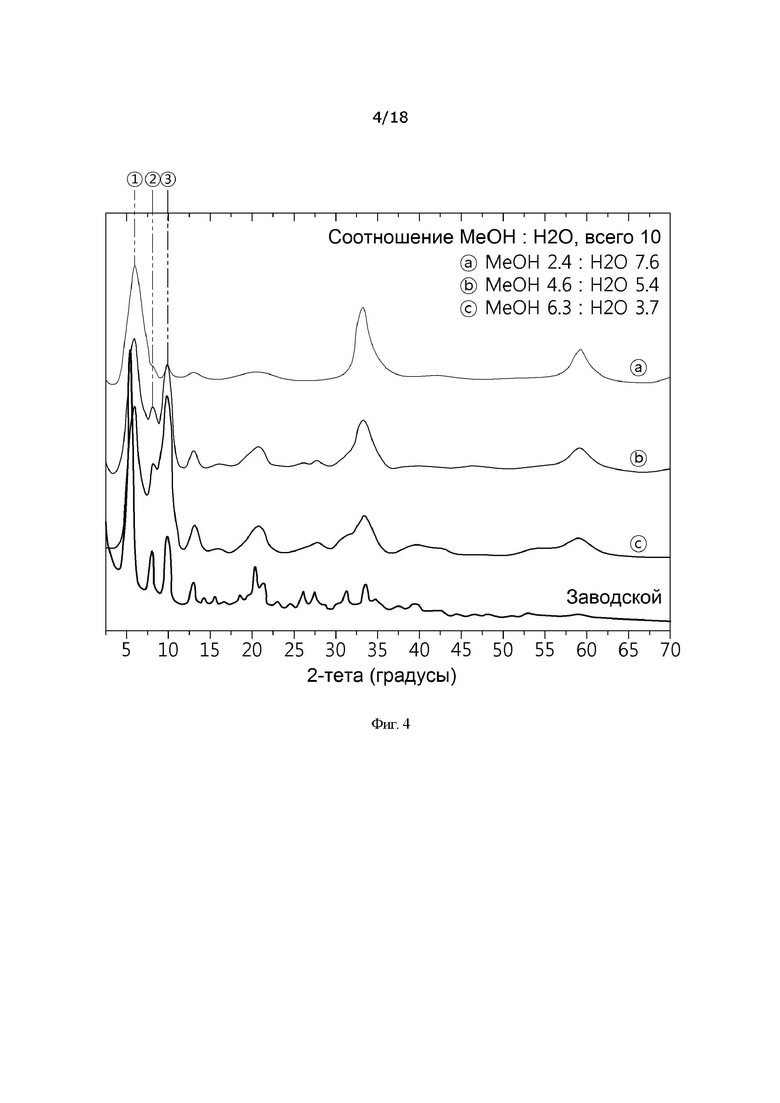
[0032] На фиг. 4 представлена картина рентгеновской дифракции гидроксида металла в зависимости от соотношения растворителей метанол : вода;
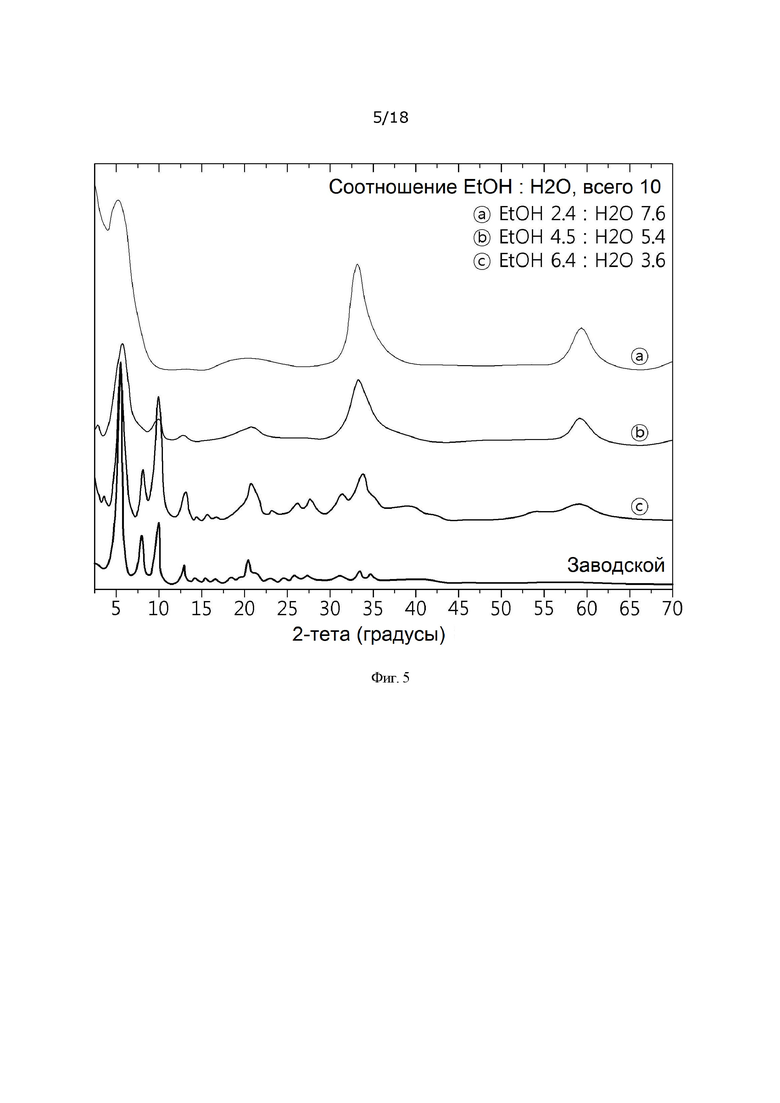
[0033] На фиг. 5 представлена картина рентгеновской дифракции гидроксида металла в зависимости от соотношения растворителей этанол : вода;
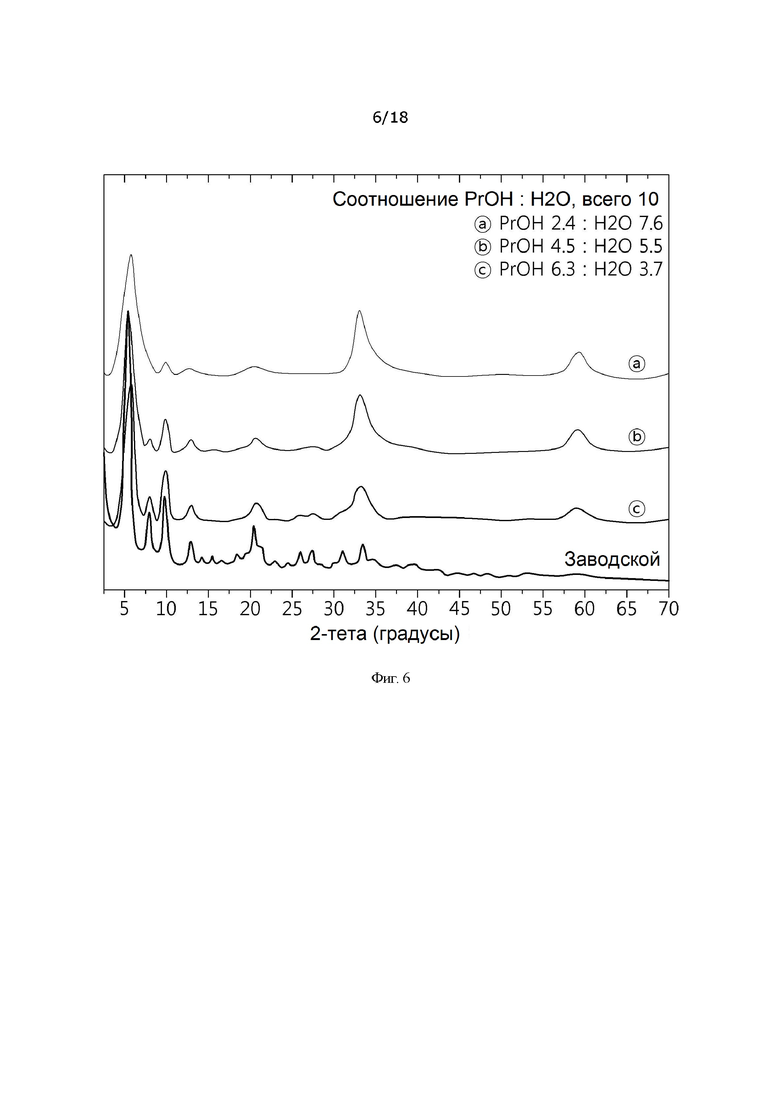
[0034] На фиг. 6 представлена картина рентгеновской дифракции гидроксида металла в зависимости от соотношения растворителей пропанол : вода;
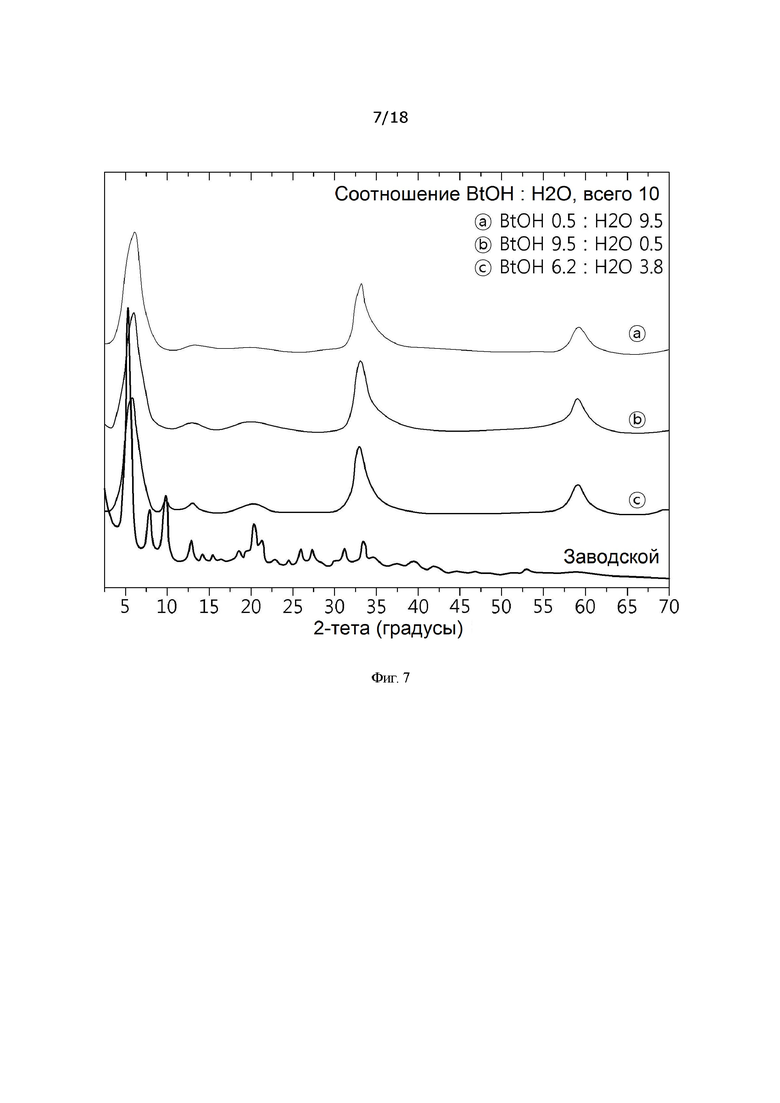
[0035] На фиг. 7 представлена картина рентгеновской дифракции гидроксида металла в зависимости от соотношения растворителей бутанол : вода;
[0036] На фиг. 8 представлено СЭМ изображение гидроксида металла в зависимости от соотношения растворителей этанол : вода, которое является увеличенным изображением части поверхности одиночных частиц;
[0037] На фиг. 9 представлено СЭМ изображение гидроксида металла в зависимости от соотношения растворителей этанол : вода;
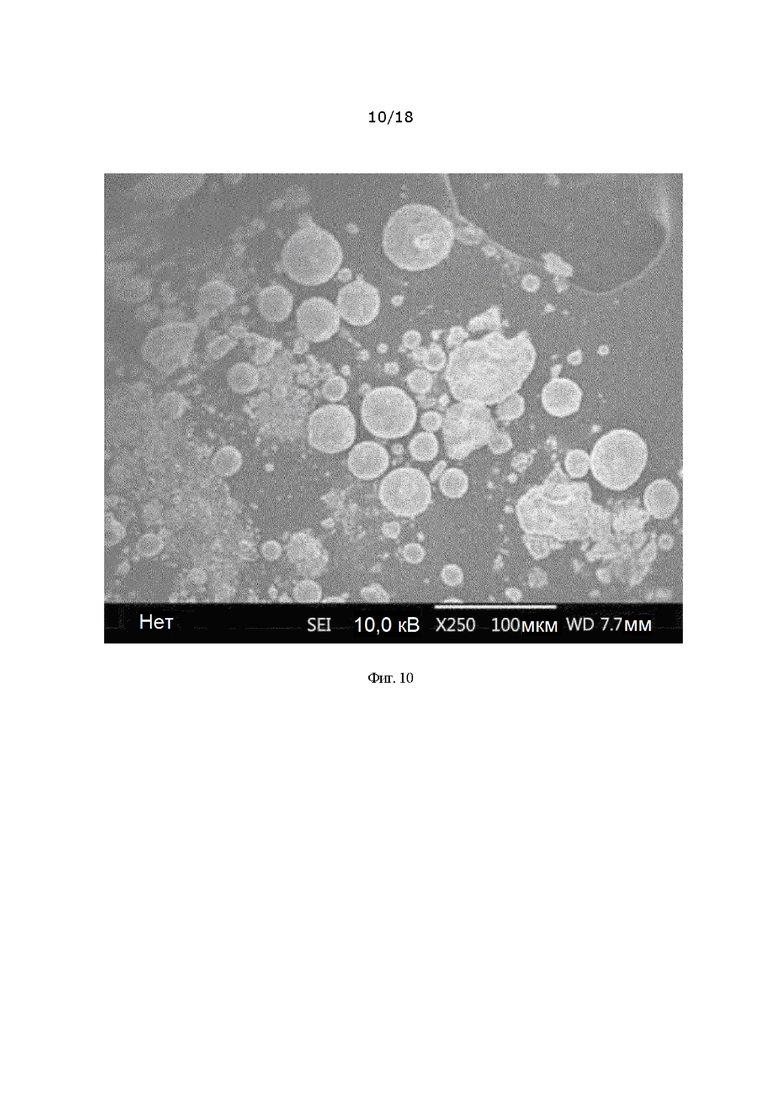
[0038] На фиг. 10 представлено СЭМ изображение гидроксида металла в зависимости от соотношения растворителей этанол : вода;
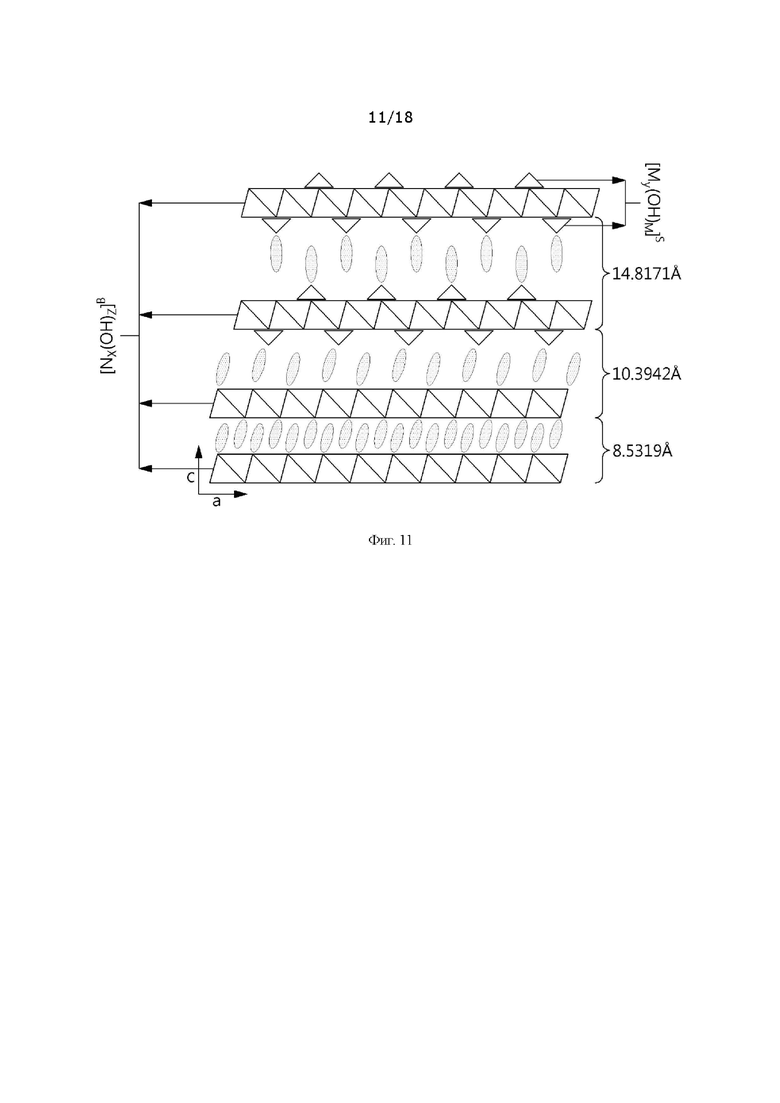
[0039] На фиг. 11 представлена специфическая конфигурация комплекса гидроксида металла согласно настоящему изобретению, [Mx(OH)z]B представляет собой базовый слой, и [My(OH)w]S представляет собой поверхностный слой;
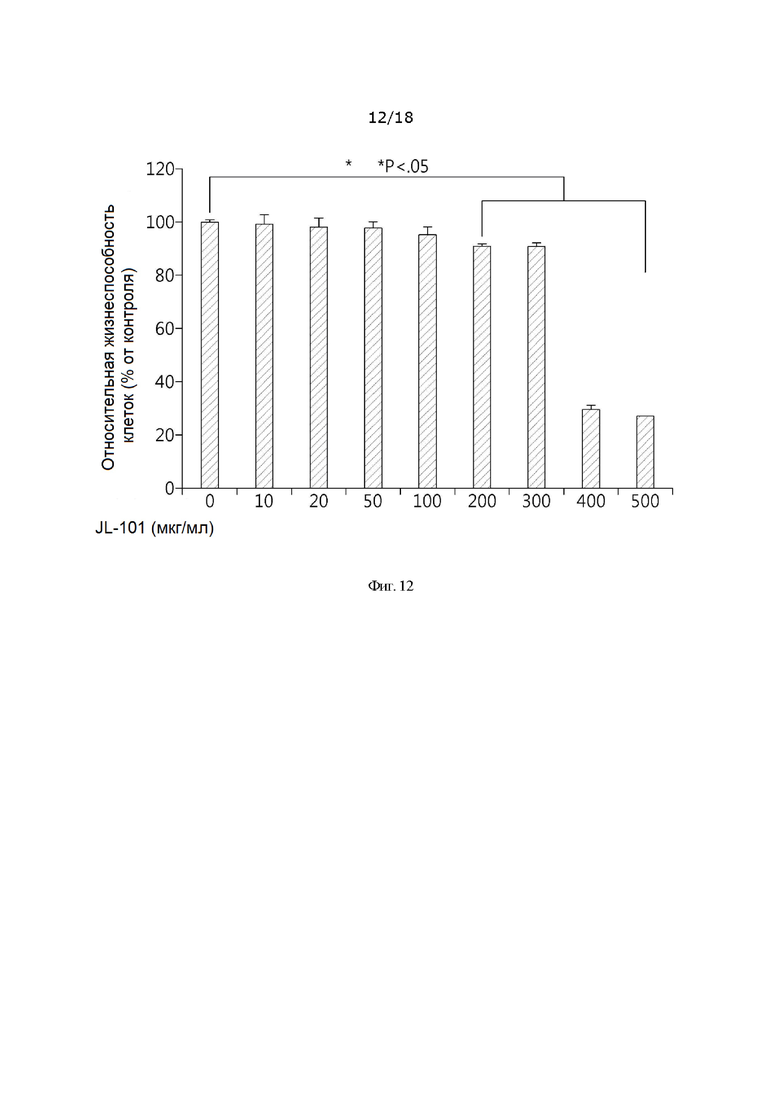
[0040] На фиг. 12 представлены результаты измерения жизнеспособности клеток фибробластов кожи человека, обработанных комплексом гидроксида металла согласно настоящему изобретению, по горизонтальной оси представлена концентрация обработанного образца материала, а по вертикальной оси представлена жизнеспособность клеток;
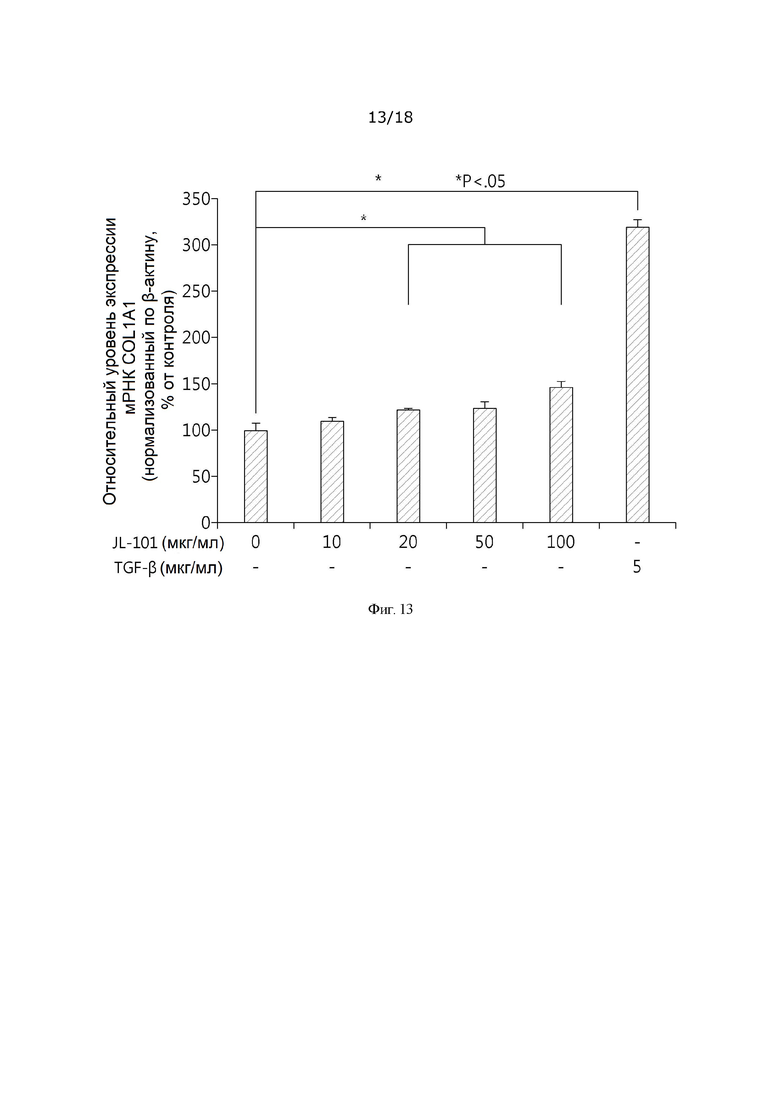
[0041] На фиг. 13 показано изменение экспрессии гена коллагена типа 1 (COL1A1) фибробластов кожи человека, обработанных комплексом гидроксида металла согласно настоящему изобретению, по горизонтальной оси представлена концентрация обработанного образца материала, а по вертикальной оси представлен уровень экспрессии мРНК COL1A1;
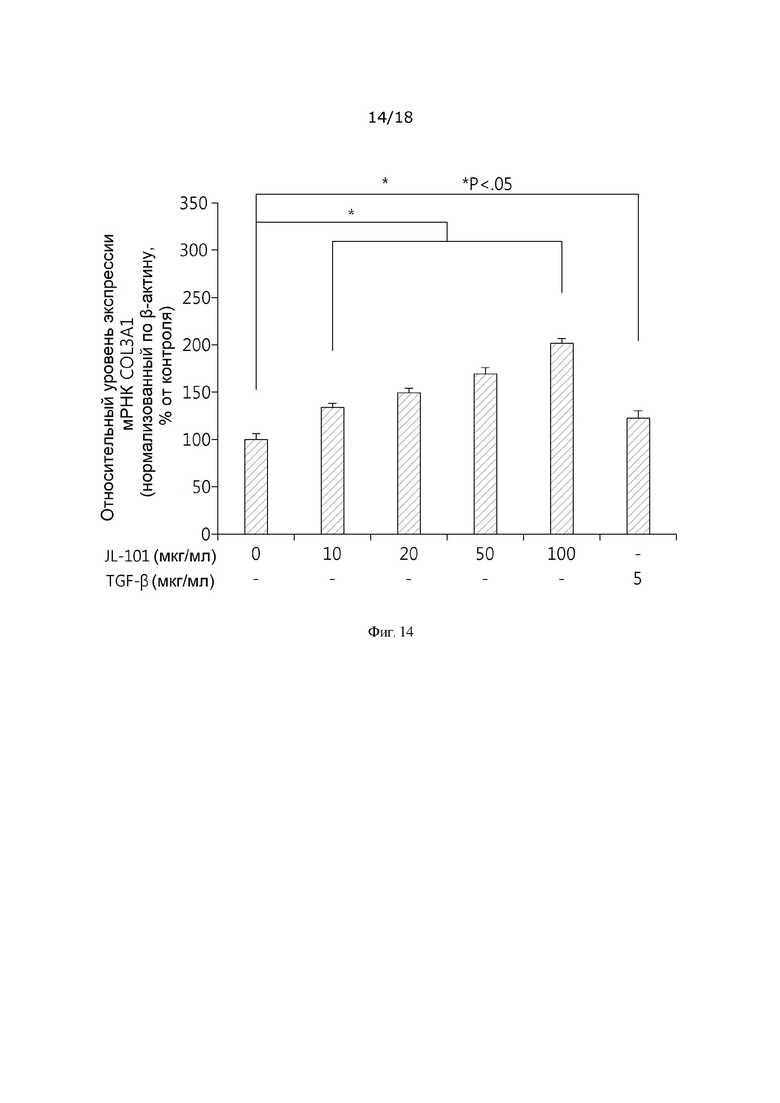
[0042] На фиг. 14 показано изменение экспрессии гена коллагена типа 3 (COL3A1) фибробластов кожи человека, обработанных комплексом гидроксида металла согласно настоящему изобретению, по горизонтальной оси представлена концентрация обработанного образца материала, а по вертикальной оси представлен уровень экспрессии мРНК COL3A1;
[0043] На фиг. 15 представлена растворимость Zn;
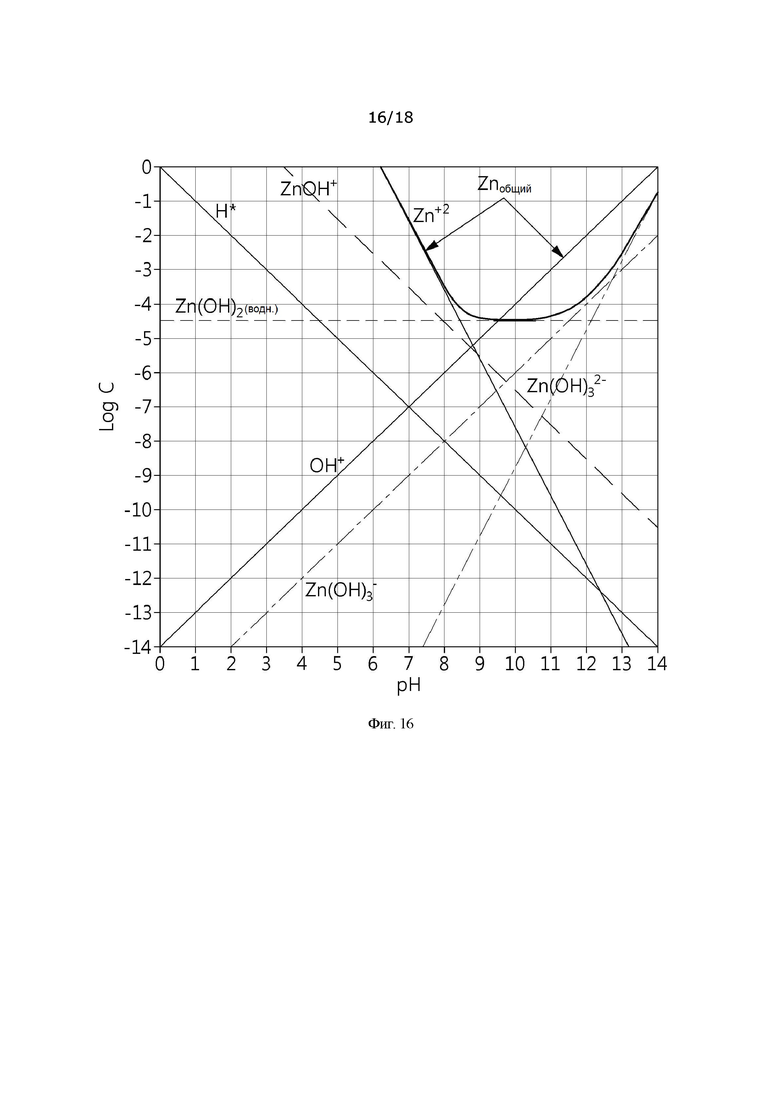
[0044] На фиг. 16 представлена кривая растворимости гидроксида цинка;
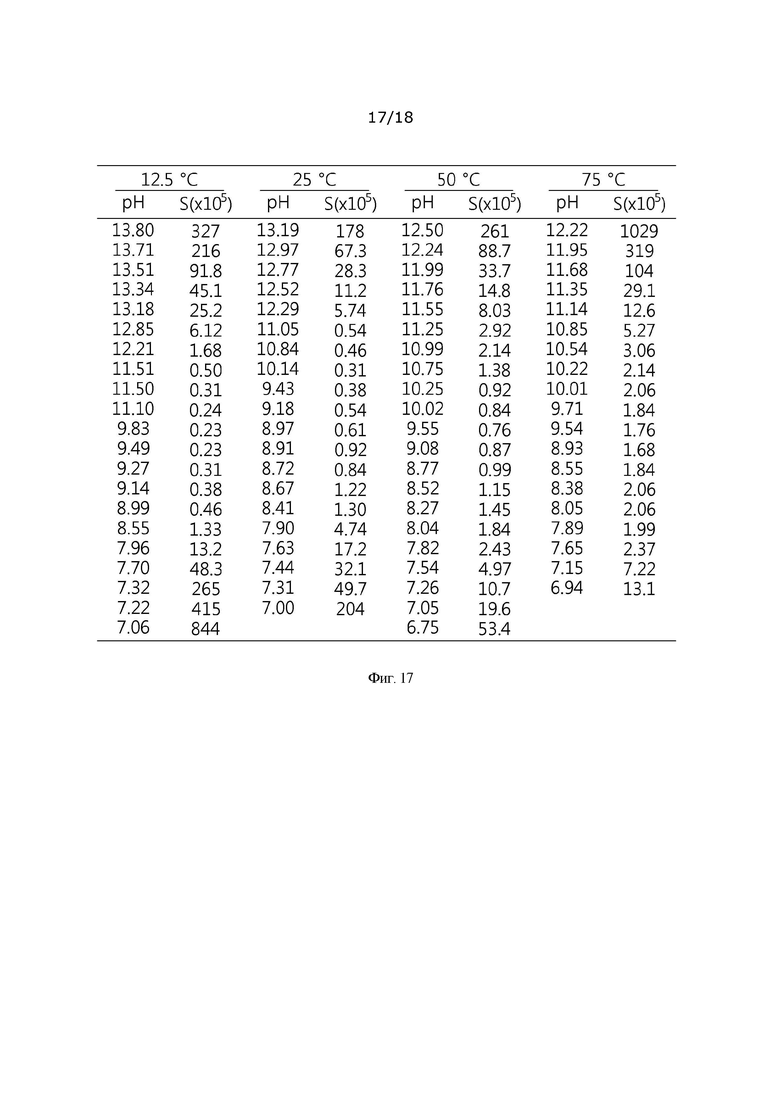
[0045] На фиг. 17 представлена растворимость гидроксида цинка, *S представляет собой растворимость, выраженную в моль цинка на кг воды; и
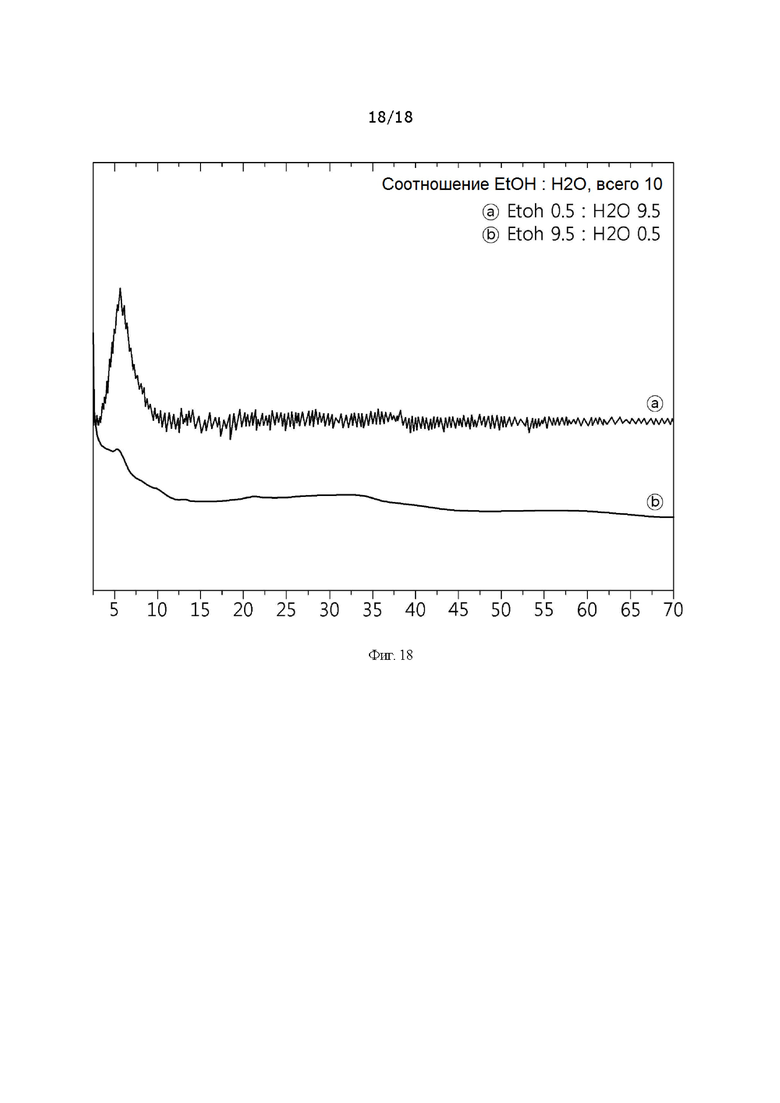
[0046] На фиг. 18 представлена картина рентгеновской дифракции гидроксида металла в зависимости от соотношения растворителей этанол : вода.
Наилучший способ реализации
[0047] Настоящее изобретение относится к комплексу гидроксида металла, содержащему модифицированную многослойную структуру гидроксида химической формулы 1, представленной ниже, которая содержит базовый слой, поверхностный слой и активный ингредиент.
[0048] [Химическая формула 1]
[0049] {[Mx(OH)z]B[My(OH)w]S}{(An)q}⋅m(H2O)
[0050] Здесь [Mx(OH)z]B представляет собой базовый слой многослойной структуры гидроксида, и [My(OH)w]S представляет собой поверхностный слой многослойной структуры гидроксида,
[0051] M представляет собой катион любого двухвалентного металла, выбранный из группы, состоящей из Ca2+, Mg2+, Cu2+, Zn2+, Ni2+, Co2+ и Fe2+,
[0052] x равен от 0,6 до 3,
[0053] y равен от 0 до 2,
[0054] z равен от 1 до 5,
[0055] w равен от 0 до 4,
[0056] z+w равно от 1 до 9,
[0057] q равен от 1 до 4.
[0058] m равен от 0,1 до 10,
[0059] n представляет собой зарядовое число A, и
[0060] активный ингредиент представлен символом A, где A представляет собой анионное соединение, содержащее в качестве функциональной группы, имеющей электростатическое притяжение в зависимости от pKa, по меньшей мере одну группу, выбранную из группы, состоящей из гидроксильной группы (-OH), карбонильной группы (-CO-), формильной группы (-CHO), карбоксильной группы (-COOH), сульфатной группы (-SO32-), дигидрофосфатной группы (-H2PO42-) и фосфатной группы (-PO43-).
[0061] Активный ингредиент, представленный символом A, может содержать по меньшей мере одну функциональную группу, выбранную из группы, состоящей из гидроксильной группы (-OH), карбонильной группы (-CO-), формильной группы (-CHO), карбоксильной группы (-COOH), сульфатной группы (-SO32-), дигидрофосфатной группы (-H2PO42-) и/или фосфатной группы (-PO43-).
[0062] Более конкретно, химическая формула 1 может быть представлена формулой
{[Zn3(OH)4]B[Zn2(OH)3]S}{(аскорбиновая кислота)2}⋅2(H2O),
{[Zn3(OH)4]B[Zn1(OH)2]S}{(аскорбиновая кислота)2}⋅3(H2O),
{[Zn3(OH)4]B[Zn1(OH)1]S}{(аскорбиновая кислота)2}⋅3(H2O) и
{[Zn3(OH)3]B[Zn1(OH)1]S}{(аскорбиновая кислота)2}⋅2(H2O).
[0063] A, который представляет собой активный ингредиент, может быть анионным, и примеры активного ингредиента, содержащего функциональную группу, имеющую электростатическое притяжение в зависимости от pKa, в частности, гидроксильную группу (-OH), могут включать аскорбиновую кислоту, 4-н-бутилрезорцин, токоферол, бакухиол, (+)-катехин, куркумин, гидрокситирозол, фитол, резорцин, картамин, лутеолин, корилагин, ресвератрол, ретинол, рутин, гидрохинон, азиатикозид, мадекассосид, гинзенозид, борнеол, диосметин, аспалатин, эвгенол, мангостин, пеларгонидин, цианидин, делфинидин, пеонидин, петунидин, малвидин, лутеин, кверцетин, аденозин, аскорбилпальмитат, аскорбилглюкозид, пиридоксин, тиамин, сапонин, секоизоларицирезинол, матаирезинол, пинорезинол, медиорезионл, ларицирезинол, сирингарезионл, артигенин, энтеролактон и энтеродиол.
[0064] Примеры активного ингредиента, содержащего карбоксильную группу (-COOH), могут включать арахидоновую кислоту, абиетиновую кислоту, абсцизиновую кислоту, α-липоевую кислоту, азелаиновую кислоту, кофеиновую кислоту, гидроксибензойную кислоту, протокатеховую кислоту, эллаговую кислоту, феруловую кислоту, фульвовую кислоту, олеаноловую кислоту, феноловую кислоту, гидроксикоричную кислоту, ванилиновую кислоту, протокатеховую кислоту, сальвианоловую кислоту, синаповую кислоту, транексамовую кислоту, валериановую кислоту, вератровую кислоту, хлорогеновую кислоту, азиатиковую кислоту, мадекассоновую кислоту, субериновую кислоту, гиалуроновую кислоту, урсоловую кислоту, аскорбиновую кислоту, сальвианоловую кислоту B, пиридин-3-карбоновую кислоту, аскорбилпальмитат, аскорбилглюкозид, карнитин, пантотеновую кислоту, биотин, фолиевую кислоту, аллиин, глутатион, серин, глицин, аланин, авенантрамид, треонин, цистеин, валин, лейцин, метионин, пролин, фенилаланин, тирозин, триптофан, аспарагиновую кислоту, глутаминовую кислоту, аспарагин, глутамин, гистидин, лизин, аргинин и т.п.
[0065] Примеры активного ингредиента, содержащего формильную группу (-CHO), могут включать деканаль, ретинальдегид, циннамальдегид, катехинальдегид, кониферилальдегид, сирингальдегид, ванилин и т.п.
[0066] Примеры активного ингредиента, содержащего карбонильную группу (-CO-), могут включать эдаравон, идебенон, коэнзим Q10, убиквинон, MitoQ, астаксантин, кофеин, параксантин, теофиллин, матаирезинол, фисцион, пропафенон, кумарин, генистеин, халькон, нарингенин, бергенин, аментофлавон, биоханин A, рибофлавин, сезамин и т.п.
[0067] Примеры анионного активного ингредиента, содержащего сульфатную группу (-SO32-), могут включать сульфат декстрана, сульфат железа (II), 4-O-сульфат феруловой кислоты, аскорбилсульфат и т.п.
[0068] Кроме того, примеры соединения, содержащего дигидрофосфатную группу (-H2PO42-), могут включать аденозинмонофосфат, фосфат ретинола, фосфат аскорбилпальмитата и т.п.
[0069] Кроме того, примеры соединения, содержащего дигидрофосфатную группу (-PO43-), могут включать аденозиндинофосфат, аденозинтрифосфат, аскорбилфосфат и т.п.
[0070] Более конкретно, активный ингредиент предпочтительно включает по меньшей мере одно соединение, выбранное из группы, состоящей из аскорбиновой кислоты, цистеина, салициловой кислоты, абсцизиновой кислоты, серина, аланина, глицина, карнитина, изолейцина, лейцина, субериновой кислоты, пролина, валина, азелаиновойк ислоты, фенилаланина, кофеиновой кислоты, триптофана, кумарина, тирозина, аспарагиновой кислоты, феруловой кислоты, глутаминовой кислоты, аргинина, пиридин-3-карбоновой кислоты, гистидина, лизина, аскорбилсульфата, треонина, протокатеховой кислоты, аскорбилфосфата, метионина, валериановой кислоты, аспарагина, глутамина, ванилиновой кислоты, гидроксибензойной кислоты, гидроксикоричной кислоты, коричного альдегида, пантотеновой кислоты, биотина, ретинола, α-липоевой кислоты, ресвератрола, 4-н-бутилрезорцина, гидрокситирозола, пиридоксина, синаповой кислоты, кониферилового альдегида, сирингальдегида и теофиллина, так что картина порошковой рентгеновской дифракции может иметь пиковые значения углов дифракции (2θ) 5,96±1°, 33,46±1° и 59,3±1°.
[0071] Согласно настоящему изобретению, многослойная структура означает, что базовый слой и/или поверхностный слой может быть модифицирован в структурной форме гидроксида металла, сформированной в целом, и, более конкретно, в такой структуре гидроксида металла, в которой структурная форма гидроксида металла поверхностного слоя может быть более изменчивой среди базового слоя и поверхностного слоя. В частности, базовый слой и поверхностный слой изображены на фиг. 11. Многослойная структура может содержать модифицированную многослойную структуру, имеющую такую конфигурацию, что обычная структура гидроксида металла, имеющая постоянное расположение двухслойной структуры, постепенно преобразуется в асимметричную слоистую структуру, что обусловливает модификацию такой двухслойной структуры. Это означает, что структура поверхностного слоя является модифицированной, так что сформированы отдельные структуры гидроксида металла разного размера, которые уложены друг на друга с образованием многослойной структуры. Многослойная структура может иметь от двух до пяти слоев, и предпочтительной является трехслойная структура.
[0072] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, которая имеет пиковые значения углов дифракции (2θ) 5,96±1°, 33,46±1° и 59,3±1°. В данном контексте многослойная структура гидроксида может содержать асимметричную и/или модифицированную слоистую структуру. Более предпочтительно, она может иметь пиковые значения (2θ) 5,96±0,5°, 33,46±0,5° и 59,3±0,5°, и предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме асимметричной и/или модифицированной слоистой структуры (от двух до пяти слоев).
[0073] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, имеющую пиковые значения углов дифракции (2θ) 5,96±1°, 8,5±1°, 10,36±1°, 13,36±1°, 19±1°, 20,84±1°, 21,7±1°, 26,34±1°, 37,68±1°, 31,48±1°, 33,78±1°, 34,88±1° и 59,3±1°. Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием этанола и/или воды в качестве растворителя. Асимметричная слоистая структура и/или модифицированная слоистая структура может быть получена подбором соотношения растворителей, и полученная асимметричная слоистая структура и/или модифицированная слоистая структура может представлять собой слоистую структуру, содержащую несколько слоев, например, от двух до пяти слоев.
[0074] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, которая имеет пиковые значения при углах дифракции (2θ) 6,28±1°, 8,88±1°, 10,32±1°, 13,42±1°, 21,04±1°, 28,14±1°, 33,5±1° и 59,16±1°. Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием метанола и/или воды в качестве растворителя. Посредством подбора соотношения растворителей может быть получена асимметричная слоистая структура и/или модифицированная слоистая структура, и полученная асимметричная слоистая структура и/или модифицированная слоистая структура может представлять собой слоистую структуру, содержащую несколько слоев, например, от двух до пяти слоев.
[0075] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, которая имеет пиковые значения при углах дифракции (2θ) 6,02±1°, 8,5±1°, 10,4±1°, 13,38±1°, 21,02±1°, 26,42±1°, 27,88±1°, 33,52±1° и 59,1±1°. Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием пропанола и/или воды в качестве растворителя. Предпочтительно, пропанол представляет собой н-пропанол.
[0076] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, которая имеет пиковые значения при углах дифракции (2θ) 6,22±1°, 10,5±1° и 13,36±1°, 20,94±1°, 33,46±1° и 59,28±1°. Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием бутанола и/или воды в качестве растворителя. Предпочтительно, бутанол представляет собой н-бутанол.
[0077] Более конкретно, согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, имеющую пиковые значения углов дифракции (2θ) 5,96±0,5°, 8,5±0,5°, 10,36±0,5°, 13,36±0,5°, 19±0,5°, 20,84±0,5°, 21,7±0,5°, 26,34±0,5°, 37,68±0,5°, 31,48±0,5°, 33,78±0,5°, 34,88±0,5° и 59,3±0,5° Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную и/или модифицированную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием этанола и/или воды в качестве растворителя.
[0078] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, которая имеет пиковые значения при углах дифракции (2θ) 6,28±0,5°, 8,88±0,5°, 10,32±0,5°, 13,42±0,5°, 21,04±0,5°, 28,14±0,5°, 33,5±0,5° и 59,16±0,5°. Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную и/или модифицированную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием метанола и/или воды в качестве растворителя.
[0079] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, которая имеет пиковые значения при углах дифракции (2θ) 6,02±0,5°, 8,5±0,5°, 10,4±0,5°, 13,38±0,5°, 21,02±0,5°, 26,42±0,5°, 27,88±0,5°, 33,52±0,5° и 59,1±0,5°. Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную и/или модифицированную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием пропанола и/или воды в качестве растворителя. Предпочтительно, пропанол представляет собой н-пропанол.
[0080] Согласно настоящему изобретению, многослойная структура гидроксида может иметь картину порошковой рентгеновской дифракции, которая имеет пиковые значения при углах дифракции (2θ) 6,22±0,5°, 10,5±0,5°, 13,36±0,5°, 20,94±0,5°, 33,46±0,5° и 59,28±0,5°. Предложенный комплекс гидроксида металла, удовлетворяющий требованиям приведенных выше пиковых значений, может быть представлен в форме слоистой структуры, и такая слоистая структура может содержать модифицированную асимметричную и/или модифицированную слоистую структуру. Более конкретно, слоистая структура может быть получена с использованием бутанола и/или воды в качестве растворителя. Предпочтительно, бутанол представляет собой н-бутанол.
[0081] Настоящее изобретение относится к комплексу гидроксида металла, полученному посредством совместного осаждения активного ингредиента и предшественника структуры гидроксида металла в реакции осаждения с использованием спирта и воды.
[0082] Более конкретно, структура гидроксида металла согласно настоящему изобретению может вызывать реакцию осаждения при использовании предшественника.
[0083] Согласно настоящему изобретению, конкретные примеры предшественника структуры гидроксида металла, которые могут вызывать реакцию осаждения, предпочтительно включают ZnO, ZnSO4, ZnCl2, ZnCO3, Zn(NO3)26H2O, Zn(CH3COO)2, CaO, CaCl2, Ca(NO3)26H2O, CaSO4, CaCO3, Ca(OH)2, MgO, MgCl2, MgSO4, Mg(NO3)26H2O, CuO, Cu(NO3)26H2O, CuCl2, CuSO4, Co(NO3)2, CoCO3, CoCl2, Co(OH)2, CoSO4, Co(CH3COO)2, NiO, NiCl2, Ni(NO3)2, NiSO4, NiCO3, Ni(OH)2, FeO, FeCl3, Fe(NO3)3, FeSO4, FeCO3 и Fe(OH)2, и могут предпочтительно включать ZnO, ZnSO4, ZnCl2, ZnCO3, Zn(NO3)26H2O и Zn(CH3COO)2.
[0084] Спирт может представлять собой по меньшей мере один, выбранный из группы, состоящей из метанола, этанола, пропанола и бутанола. Пропанол и/или бутанол может представлять собой н-пропанол и/или н-бутанол. На стадии совместного осаждения соотношение спирта и воды может составлять от 1:9 до 9:1, и предпочтительно от 2,4:7,6 до 6,2:3,8. Если соотношение спирта и воды входит в вышеуказанный диапазон, то образуется требуемая модифицированная многослойная структура.
[0085] Настоящее изобретение относится к способу получения комплекса гидроксида металла, включающему совместное осаждение активного ингредиента и структуры гидроксида металла в реакции осаждения с использованием спирта и воды. Спирт может представлять собой по меньшей мере один, выбранный из группы, состоящей из метанола, этанола, пропанола и бутанола. В данном контексте пропанол предпочтительно представляет собой н-пропанол, и бутанол предпочтительно представляет собой н-бутанол.
[0086] Более конкретно, способ согласно настоящему изобретению включает образование предшественника структуры гидроксида металла с использованием предшественника, получение раствора активного ингредиента посредством растворения активного ингредиента с применением спирта и воды и осуществление реакции осаждения предшественника структуры гидроксида металла и раствора активного ингредиента.
[0087] Согласно настоящему изобретению, если активный ингредиент и гидроксид металла осаждают с использованием спирта и воды, то сам активный ингредиент может внедряться в структуру гидроксида металла без необходимости в дополнительных процессах и/или стадиях, что обеспечивает возможность стабилизации активного ингредиента. Кроме того, использование спирта и воды в качестве растворителя может обеспечивать уменьшение количества технологических стадий, и общее время переработки комплекса гидроксида металла, получаемого согласно настоящему изобретению, сокращено до 3-5 часов, и предпочтительно от 3 часов 30 минут до 4 часов 30 минут. Традиционный способ получения таких же материалов занимает от 10 до 12 часов, и это означает, что может быть обеспечен эффект существенного сокращения технологического времени. Кроме того, может быть достигнут эффект дополнительного введения в комплекс гидроксида металла еще по меньшей мере от 5 до 15% активного ингредиента, по сравнению со стандартным количеством на основании рациональной формулы. В данном контексте спирт может представлять собой по меньшей мере один, выбранный из группы, состоящей из метанола, этанола, пропанола и бутанола, и предпочтительно используют этанол, поскольку активный ингредиент может быть весьма эффективно, в избытке включен в комплекс гидроксида металла.
[0088] Более конкретно, использование спирта в процессе синтеза обеспечивает возможность предотвращения разрушения (окисления, появления коричневой окраски и т.д.) активного материала, засорения фильтра ультрафильтрации (UF), используемого для промывания суспензии, получаемой после синтеза, и разрушения материала во время трехкратного процесса UF промывания. Более того, может быть сокращено время высушивания по сравнению со способом, в котором используют только воду, посредством высушивания с использованием распылительной сушилки после промывания, и разрушение активного материала может быть предотвращено благодаря высушиванию при 65-75°С, и предпочтительно 70°С (при использовании воды сушку осуществляют при 95°С или более). В частности, в качестве спирта предпочтительно используют этанол, поэтому может быть эффективно достигнут эффект описанного выше способа.
Способ осуществления изобретения
[0089] Согласно настоящему изобретению, базовый принцип синтеза гидроксида металла представляет собой реакцию осаждения. Реакция осаждения может быть определена в соответствии с уравнением 1, представленным ниже, и она связана со стабильностью продукта, получаемого по уравнению 1, представленному ниже. В отношении получения осадка, может образовываться насыщенный раствор, если концентрация образующихся ионов равна растворимости образующегося осадка, и может происходить образование осадка при избытке концентрации насыщения, если концентрация образующихся ионов превышает растворимость образующегося осадка. Если концентрация образующихся ионов, необходимая для осаждения, меньше растворимости образующегося осадка, то может образовываться ненасыщенный раствор, и, следовательно, не происходит образование осадка. Таким образом, для получения осадка необходимо использовать предшественник в заранее определенном количестве или в большем количестве, чтобы преодолеть растворимость образующегося осадка. Однако при использовании предшественника в слишком большом количестве следует соблюдать осторожность, поскольку может возникать проблема, связанная с повторным растворением осадка под действием противоионов или вследствие образования комплексных соединений. Подробности реакции осаждения, связанные с настоящим изобретением, представлены на фиг. 15-17.
[0090] [Уравнение 1]
[0091] [Ksp]=[Zn2+][OH-]2
[0092] Продукт растворения может быть представлен как Zn2+ (водн.), Zn(OH)+ (водн.), Zn(OH)2 (водн.), Zn(OH)3- (водн.) и Zn(OH)42- (водн.), и представлен во взаимосвязи с данными о растворимости на основании равновесия и константы равновесия на фиг. 15, упрощая возможность соотнесения перечисленных частиц с другими частицами.
[0093] Пример синтеза 1: Получение 1 многослойного кристалла гидроксида металла, в котором витамин C (аскорбиновая кислота) внедрен между слоями слоистой соли металла
[0094] 30 г ZnO и 1197 мл деионизированной воды, не содержащей карбонат-ионов (CO32-), перемешивали (400 об./мин.) при комнатной температуре в атмосфере азота в главном реакторе, и к полученной смеси медленно, по каплям добавляли концентрированный раствор HCl, так чтобы ее оттированный рН составлял от 0,5 до 1. 26 г витамина C растворяли в 230 мл деионизированной воды и 175 мл этанола во вспомогательной емкости 1, и раствор витамина C из вспомогательной емкости 1 добавляли в главный реактор и перемешивали в течение 30 минут в атмосфере азота. Поддерживая скорость перемешивания (700 об./мин.) в главном реакторе, в него вводили 5 М водный раствор гидроксида натрия из вспомогательной емкости 2, так чтобы оттитрованный рН смеси составлял примерно 6,5-7,5, после чего инициировали реакцию осаждения при перемешивании (700 об./мин.) в течение 3 часов. После реакции измеренный рН составлял 6,5-7,0, и после прекращения реакции получали белый взвешенный осадок. Осадок центрифугировали и три раза промывали этанолом (50%) для удаления непрореагировавших солей и витамина C. После центрифугирования осадок отделяли от надосадочного раствора и сушили в сушилке с горячим воздухом (температура на входе: 70°C), используя этанол (95%), с получением 35,4 г бледно-бежевого продукта витамин C-гидроксид цинка (выход: 58,8%, содержание аскорбиновой кислоты: 42,24%). {[Zn3(OH)4]B[Zn2(OH)3]S}{(аскорбиновая кислота)2}⋅2(H2O)
[0095] Пример синтеза 2: Получение 2 многослойного кристалла гидроксида металла, в котором витамин C внедрен между слоями слоистой соли металла
[0096] 30 г ZnO, 549 мл деионизированной воды, не содержащей карбонат-ионов (CO32-), и 628 мл этанола (>98%) перемешивали (400 об./мин.) при комнатной температуре в атмосфере азота в главном реакторе, и к полученной смеси медленно, по каплям добавляли концентрированный раствор HCl, так чтобы ее оттированный рН составлял от 0,5 до 1. 26 г витамина C растворяли в 230 мл деионизированной воды и 175 мл этанола во вспомогательной емкости 1, и раствор витамина C из вспомогательной емкости 1 добавляли в главный реактор и перемешивали в течение 30 минут в атмосфере азота. Поддерживая скорость перемешивания (700 об./мин.) в главном реакторе, в него вводили 5 М водный раствор гидроксида натрия из вспомогательной емкости 2, так чтобы оттитрованный рН смеси составлял примерно 6,5-7,5, после чего инициировали реакцию осаждения при перемешивании (700 об./мин.) в течение 3 часов. После реакции измеренный рН составлял 6,5-7,0, и после прекращения реакции получали белый взвешенный осадок. Осадок центрифугировали и три раза промывали этанолом (50%) для удаления непрореагировавших солей и витамина C. После центрифугирования осадок отделяли от надосадочного раствора и сушили в сушилке с горячим воздухом (температура на входе: 70°C), используя этанол (95%), с получением 37,6 г продукта витамин C-гидроксид цинка, имеющего цвет бледной слоновой кости, близкий к белому (выход: 62,4%, содержание аскорбиновой кислоты: 45,19%). {[Zn3(OH)4]B[Zn1(OH)2]S}{(аскорбиновая кислота)2}⋅3(H2O)
[0097] Пример синтеза 3: Получение 3 многослойного кристалла гидроксида металла, в котором витамин C внедрен между слоями слоистой соли металла
[0098] 30 г ZnO, 254 мл деионизированной воды, не содержащей карбонат-ионов (CO32-), и 943 мл этанола (>98%) перемешивали (400 об./мин.) при комнатной температуре в атмосфере азота в главном реакторе, и к полученной смеси медленно, по каплям добавляли концентрированный раствор HCl, так чтобы ее оттированный рН составлял от 0,5 до 1. 26 г витамина C растворяли в 230 мл деионизированной воды и 175 мл этанола во вспомогательной емкости 1, и раствор витамина C добавляли в главный реактор и перемешивали в течение 30 минут в атмосфере азота. Поддерживая скорость перемешивания (700 об./мин.) в главном реакторе, в него вводили 5 М водный раствор гидроксида натрия из вспомогательной емкости 2, так чтобы оттитрованный рН смеси составлял примерно 6,5-7,5, после чего инициировали реакцию осаждения при перемешивании (700 об./мин.) в течение 3 часов. После реакции измеренный рН составлял 6,5-7,0, и после прекращения реакции получали белый взвешенный осадок. Осадок центрифугировали и три раза промывали этанолом (50%) для удаления непрореагировавших солей и витамина C. После центрифугирования осадок отделяли от надосадочного раствора и сушили в сушилке с горячим воздухом (температура на входе: 70°C), используя этанол (95%), с получением 39,5 г продукта, имеющего цвет бледной слоновой кости, близкий к белому (выход: 65,6%, содержание аскорбиновой кислоты: 46,35%). {[Zn3(OH)4]B[Zn1(OH)1]S}{(аскорбиновая кислота)2}⋅3(H2O)
[0099] Пример синтеза 4: Получение 4 многослойного кристалла гидроксида металла, в котором витамин C внедрен между слоями слоистой соли металла
[00100] 30 г ZnO, 68 мл деионизированной воды, не содержащей карбонат-ионов (CO32-), и 1129 мл этанола (>98%) перемешивали (400 об./мин.) при комнатной температуре в атмосфере азота в главном реакторе, и к полученной смеси медленно, по каплям добавляли концентрированный раствор HCl, так чтобы ее оттированный рН составлял от 0,5 до 1. 26 г витамина C растворяли в 50 мл деионизированной воды и 355 мл этанола во вспомогательной емкости 1, и раствор витамина C добавляли в главный реактор и перемешивали в течение 30 минут в атмосфере азота. Поддерживая скорость перемешивания (700 об./мин.) в главном реакторе, в него вводили 5 М водный раствор гидроксида натрия из вспомогательной емкости 2, так чтобы оттитрованный рН смеси составлял примерно 6,5-7,5, после чего инициировали реакцию осаждения при перемешивании (700 об./мин.) в течение 3 часов. После реакции измеренный рН составлял 6,5-7,0, и после прекращения реакции получали белый взвешенный осадок. Осадок центрифугировали и три раза промывали этанолом (50%) для удаления непрореагировавших солей и витамина C. После центрифугирования осадок отделяли от надосадочного раствора и сушили в сушилке с горячим воздухом (температура на входе 70°C), используя этанол (95%), с получением 39,5 г продукта, имеющего цвет бледной слоновой кости, близкий к белому (выход: 67,8%, содержание аскорбиновой кислоты: 48,84%). {[Zn3(OH)3]B[Zn1(OH)1]S}{(аскорбиновая кислота)2}⋅2(H2O)
[00101] Метод анализа и критерии оценки
[00102] Для подтверждения структуры многослойного гидроксида металла проводили анализ, используя следующий метод анализа.
[00103] Метод анализа 1: Картина порошковой рентгеновской дифракции
[00104] - Прибор: Рентгеновский дифрактометр для порошковой рентгеновской дифракции (ПРД) (D/MAXPRINT 2200-Ultima, Rigaku, Япония)
[00105] Излучение Cu-Kα (λ=1,5418 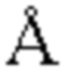 )
)
[00106] Напряжение разрядной лампы: 40 кВ, ток: 30 мА
[00107] В качестве рентгеновского дифрактометра использовали прибор D/MAXPRINT 2200-Ultima производства компании Rigaku (Япония). Анод, генерирующий рентгеновские лучи, был изготовлен из металлической Cu, и измерение проводили с использованием Kα лучей (λ=1,5418 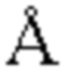 ) при 2θ от 3 до 70°, скорости сканирования 0,02°/0,2 с, и размером щели расходимости, щели рассеивания и приемной щели 0,1, 1 и 1 мм, соответственно. Напряжение разрядной лампы составляло 40 кВ, ток 30 мА.
) при 2θ от 3 до 70°, скорости сканирования 0,02°/0,2 с, и размером щели расходимости, щели рассеивания и приемной щели 0,1, 1 и 1 мм, соответственно. Напряжение разрядной лампы составляло 40 кВ, ток 30 мА.
[00108] Критерий оценки 1
[00109] Одномерную (1D) электронную плотность по оси z диаграммы ПРД (порошковой рентгеновской дифракции) рассчитывали по следующему уравнению 2.
[00110] [Уравнение 2]
[00111] 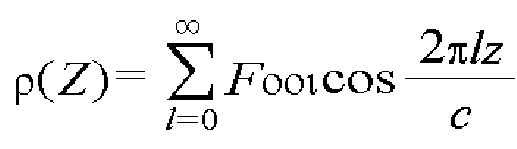
[00112] Проводили сравнительный анализ порошка, полученного в результате синтеза, с помощью картины рентгеновской дифракции, и рассчитывали расстояние между слоями по уравнению Брэгга (ниже, уравнение 3). Пик, расположенный ближе всего, представляет собой расстояние между слоями, включая расстояние между слоем синтезированного гидроксида металла и анионным слоем, которое называют главным межслоевым расстоянием.
[00113] [Уравнение 3]
[00114] nλ=2dsinθ
[00115] (λ = длина волны рентгеновского излучения, d = шаг кристаллической решетки, θ = угол падения)
[00116] Метод анализа 2: Анализ ВЭЖХ
[00117] - Прибор: Прибор для высокоэффективной жидкостной хроматографии (ВЭЖХ) серии Agilent 1100 (Agilent Technologies, США)
[00118] УФ детектор (λmax=240)
[00119] Колонка Zorbax C18 (4,6 мм x 150 мм, 5 мкм, Agilent Technologies, США)
[00120] Скорость потока: 0,65 мл/мин.
[00121] Объем ввода пробы: 10 мкл
[00122] Температура колонки: 35°C
[00123] Для анализа ВЭЖХ использовали прибор серии Agilent 1100 (Agilent Technologies, США). λmax измеряли при 240 нм и проводили измерение с помощью колонки Zorbax C18 (4,6 мм x 150 мм, 5 мкм, Agilent Technologies, США) в условиях 0,65 мл/мин., при объеме ввода пробы 10 мкл и температуре колонки 35°C.
[00124] Буфер подвижной фазы содержал 0,1% раствор трифторуксусной кислоты (ReagentPlus®, 99%) в ацетонитриле (безводный, 99,8%) и деионизированную воду в объемном соотношении 2:8.
[00125] Для обработки образца смешивали 40 мг образца с 100 мл буферного растворителя, обрабатывали ультразвуком в течение 10 минут и затем быстро перемешивали в течение 10 минут. Полученный раствор отфильтровывали с помощью нейлонного шприц-фильтра (размер пор 0,2 мкм) и проводили измерения полученного образца.
[00126] Экспериментальный пример 1
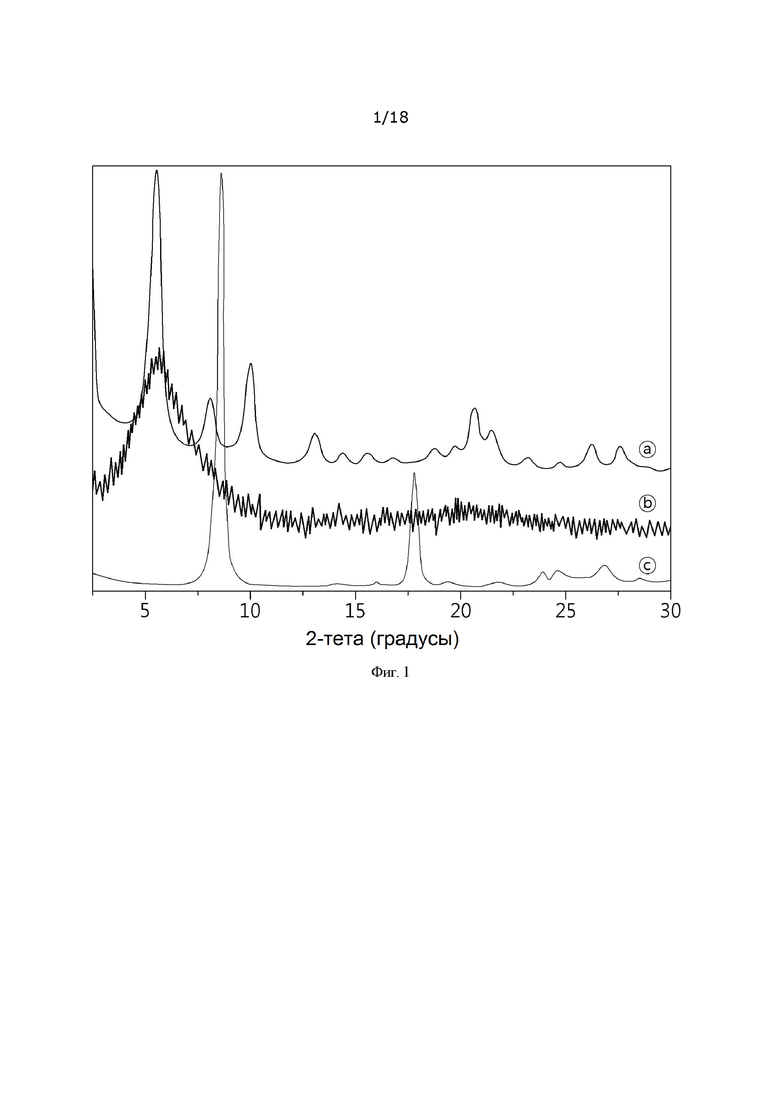
[00127] Диаграмма, которую анализировали описанным выше методом анализа, представлена на фиг. 1 и ниже в таблице 1.
[00128] Способ получения эталонного соединения (Zn5(OH)8(аскорбиновая кислота)2⋅2H2O)
[00129] 6 г Zn(NO3)2⋅H2O и 1,42 г витамина C растворяли в деионизированной воде, не содержащей карбонат-ионов (CO32-), титровали до рН примерно 6-7 с использованием 0,2 M NaOH, и затем оставляли взаимодействовать в течение 12 часов с получением осадка витамина C-основной соли цинка. Оттитрованный раствор центрифугировали для отделения надосадочного раствора и шесть раз промывали для удаления непрореагировавших солей и витамина C с получением 2,9 г продукта (выход: 65%, и содержание витамина C: 39%).
[00130] Способ получения MZLA {[Zn3(OH)4]B[Zn1(OH)2]S}{(аскорбиновая кислота)2}⋅3(H2O)
[00131] MZLA согласно настоящему изобретению получали таким же образом, как в примере синтеза 2.
[00132] Способ получения основной соли цинка (Zn5(OH)8(NO3)2⋅2H2O)
[00133] 5 г Zn(NO3)2⋅6H2O растворяли в деионизированной воде, не содержащей карбонат-ионы (CO32-), а затем титровали до рН примерно 6-7 с использованием 0,2 M NaOH, с получением осадка основной соли цинка. Оттитрованный таким образом раствор центрифугировали и промывали для удаления непрореагировавших солей с получением 2,6 г белого порошка (выход: 70%).
[00134] [Таблица 1]
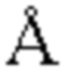 )
)
Таблица. Картины порошковой рентгеновской дифракции, соответствующие межплоскостному расстоянию.
[00135] Как показано на картине рентгеновской дифракции на фиг. 1, изменение физической структуры координационного центра металла в металлическом листе проявляется как изменение единичного заряда базовой площади, а количество, размер, прочность связывания и ориентация аскорбата определяются такими физическими свойствами, как стерическое затруднение, электронная плотность, ион-дипольный момент и т.д. аскорбата, связанного со слоем металла внутри слоистого листа, с образованием высоты между слоями.
[00136] Межслоевые расстояния гидроксида металла (MZLA) в данном эксперименте составляли 14,82 Å, 10,4 Å и 8,53 Å при 5,96°, 8,5° и 10,36°, соответственно. Значения d для трех положений пиков, расположенных при 15° или менее, отличались друг от друга, и с учетом отношения порядка упаковки уравнения межслоевого расстояния (уравнения Брэгга) к оси c, имеют место различные типы упаковки. Это обусловлено формированием другого базового слоя (межплоскостного расстояния) для отражения (0,0,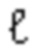 ) и образованием отдельных пиков из разных структур. Кроме того, с учетом толщины слоя (толщины слоя брусита, 7,4 Å) и длины аскорбат-иона (4,9 Å), пик вблизи 8,5° (10,394 Å) дополнительно снизился на примерно 4,4 Å по сравнению с 5,96°, а пик вблизи 10,36° (8,6419 Å) снизился на 6,29 Å и стал меньше, чем межслоевое расстояние (9,82 Å) за счет ионов NO3- в ZBS, что указывает на изменение координационного центра металла, образованного металлическим слоем и аскорбатом, что обусловливает уменьшение межслоевого расстояния.
) и образованием отдельных пиков из разных структур. Кроме того, с учетом толщины слоя (толщины слоя брусита, 7,4 Å) и длины аскорбат-иона (4,9 Å), пик вблизи 8,5° (10,394 Å) дополнительно снизился на примерно 4,4 Å по сравнению с 5,96°, а пик вблизи 10,36° (8,6419 Å) снизился на 6,29 Å и стал меньше, чем межслоевое расстояние (9,82 Å) за счет ионов NO3- в ZBS, что указывает на изменение координационного центра металла, образованного металлическим слоем и аскорбатом, что обусловливает уменьшение межслоевого расстояния.
[00137] Кристалличность пика, отображающего промежутки в слоистой структуре по сравнению с обычной структурой гидроксида, была увеличена, и образовался новый пик. Межслоевое расстояние обычного гидроксида металла составило 14,67 Å, но в MZLA (модифицированном слоистом аскорбате цинка) образовался новый пик, и рассчитанное межслоевое пространство составило 14,81 Å, 10,39 Å и 8,53 Å, что обусловливает изменение дифрактограммы и увеличение кристалличности.
[00138] Экспериментальный пример 2: Картина рентгеновской дифракции и измерение содержания витамина C в зависимости от содержания этанола и воды
[00139] Примеры 1-4
[00140] Пример 1, пример 2, пример 3 и пример 4 синтезировали таким же образом, как описано в примере синтеза 1, примере синтеза 2, примере синтеза 3 и примере синтеза 4, соответственно, с использованием количеств, представленных ниже в таблице 2.
[00141] [Таблица 2]
(a) EtOH 1,0 : H2O 9,0
(b) EtOH 4,6 : H2O 5,4
(с) EtOH 6,4 : H2O 3,6
(d) EtOH 8,5 : H2O 1,5
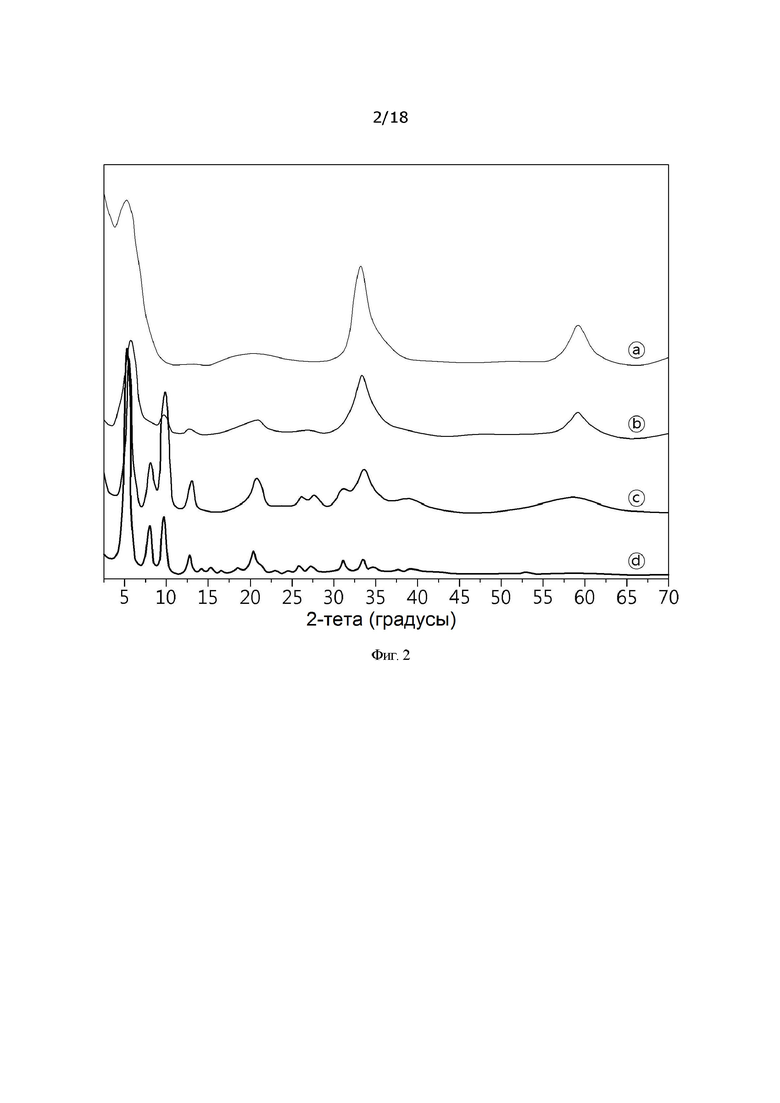
[00142] Как показано в таблице 2 и на фиг. 2, изменилась кристалличность пика, а межслоевое расстояние варьировалось в зависимости от отношения этанола к деионизированной воде во время синтеза. При низком содержании этанола (пример 1 (a)) дифракционная картина аскорбата, в целом, проявлялась вблизи 5-6°, а при постепенном увеличении содержания этанола кристалличность пика повышалась и возникала новая дифракционная картина с образованием четких пиков вблизи 8° и 10°.
[00143] Кроме того, при увеличении содержания этанола количество аскорбата в гидроксиде металла постепенно увеличивалось до 44,24%, 45,19% и 48,84%, и порошок также демонстрировал цвет бледной слоновой кости, близкий к белому.
[00144] Экспериментальный пример 3: Анализ изменений рентгеновской дифрактограммы в зависимости от  соотношения EtOH:H2O=85:15,
соотношения EtOH:H2O=85:15,  соотношения EtOH:H2O=10:90,
соотношения EtOH:H2O=10:90,  H2O= 100 (эталон) и
H2O= 100 (эталон) и  ZBS-NO3
ZBS-NO3
[00145] Zn сайт, образующий тетраэдрическую структуру в слоистой структуре, находится в нестабильной форме с положительным зарядом и взаимодействует с ионной молекулой для уравновешивания заряда, соответствующего ему, а молекула воды, связанная с Zn сайтом дипольным моментом, образует металлический слой посредством связывания с анионом через водородные связи и ион-дипольные взаимодействия. В данном случае, при использовании EtOH в заранее определенном количестве или в большем количестве, конкуренция между молекулами растворителя, имеющими одинаковые дипольные моменты, способствует нестабильности молекул воды, связывающихся с Zn сайтом, что приводит к изменению структурного положения Zn, образующего тетраэдрическую структуру в слое ZBS. Аскорбат в ZBS-аскорбате присутствует благодаря связыванию молекул воды, связанных с Zn, и аскорбиновой кислоты (в дегидратированной форме), а структурная нестабильность, обусловленная этанолом, нарушает связь аскорбата с молекулой воды.
[00146] Описанная тенденция подтверждена на фиг. 3, и по той же причине, которая описана выше, для сохранения структурно стабильной формы при использовании этанола в заранее определенном количестве, образуется скрученная асимметричная слоистая структура по типу нанолистов (турбостатическая структура), и возникают пики вблизи 33° и 58° в форме широкого горба ( ). При увеличении количества этанола положение анионов в слоистом листе изменяется для сохранения структурно более стабильной формы, и появляются и изменяются пики, отображающие межслоевое расстояние, при 15° или менее. Кроме того, при исчезновении асимметричной структуры исчезают также пики вблизи 33° и 58°, и появляется слоистая структура (
). При увеличении количества этанола положение анионов в слоистом листе изменяется для сохранения структурно более стабильной формы, и появляются и изменяются пики, отображающие межслоевое расстояние, при 15° или менее. Кроме того, при исчезновении асимметричной структуры исчезают также пики вблизи 33° и 58°, и появляется слоистая структура ( ) многослойного типа.
) многослойного типа.
[00147] Асимметричная слоистая структура (турбостатическая структура) дифракционной картины при 30°<θ<40° и 55°<θ<65° не обнаруживается в ZBS-NO3 ( ), но обнаруживается в структурах, содержащих другие анионы в ZBS. В случае обычной ZBS-аскорбиновой кислоты он не возникает, как на графике
), но обнаруживается в структурах, содержащих другие анионы в ZBS. В случае обычной ZBS-аскорбиновой кислоты он не возникает, как на графике  на фиг. 3, но представляет собой физическое явление, искусственно создаваемое посредством регулирования содержания EtOH, демонстрируя структуру и форму, отличную от пиков рентгеновской дифракции, представленных в качестве эталона.
на фиг. 3, но представляет собой физическое явление, искусственно создаваемое посредством регулирования содержания EtOH, демонстрируя структуру и форму, отличную от пиков рентгеновской дифракции, представленных в качестве эталона.
[00148] Экспериментальный пример 4: Сканирующая электронная микроскопия гидроксида металла из примера синтеза 2
[00140] Фиг. 8-10 представляют собой изображения сканирующей электронной микроскопии (СЭМ) гидроксида металла, полученного в примере синтеза 2. Данный гидроксид металла имеет средний размер частиц от 10 до 20 мкм и сферическую форму. Размер его частиц отличается от эталонного образца, и известно, что эталонный образец имеет размер частиц примерно 200-300 нм или 0,5 мкм, или менее.
[00150]
[00151] Экспериментальный пример 5: Картина рентгеновской дифракции и измерение содержания витамина C в зависимости от содержания этанола и воды
[00152] Примеры 5-7
[00153] Пример 5, пример 6 и пример 7 получали таким же образом, как в примере синтеза 2, примере синтеза 3 и примере синтеза 4, соответственно, за исключением того, что использовали количества, представленные ниже в таблице 3.
[00154] Конкретные значения рентгеновской дифракции для примеров 5-7 представлены на фиг. 4.
[00155] [Таблица 3]
(a)
(b)
(с)
[00156] Экспериментальный пример 6: Картина рентгеновской дифракции и измерение содержания витамина C в зависимости от содержания метанола и воды
[00157] Примеры 8-10
[00158] Пример 8, пример 9 и пример 10 получали таким же образом, как в примере синтеза 2, примере синтеза 3 и примере синтеза 4, соответственно, за исключением того, что использовали метанол вместо этанола и использовали количества, представленные ниже в таблице 4.
[00159] Конкретные значения рентгеновской дифракции для примеров 8-10 представлены на фиг. 5 и в следующей таблице 5.
[00160] [Таблица 4]
(a)
(b)
(с)
[00161] [Таблица 5]
[00162] Экспериментальный пример 7: Картина рентгеновской дифракции и измерение содержания витамина C в зависимости от содержания пропанола и воды
[00163] Примеры 11-13
[00164] Пример 11, пример 12 и пример 13 получали таким же образом, как в примере синтеза 2, примере синтеза 3 и примере синтеза 4, соответственно, за исключением того, что использовали н-пропанол вместо этанола и использовали количества, представленные ниже в таблице 6.
[00165] Конкретные значения рентгеновской дифракции для примеров 11-13 представлены на фиг. 6.
[00166] [Таблица 6]
(a)
(b)
(с)
[00167] [Таблица 7]
[00168] Экспериментальный пример 8: Картина рентгеновской дифракции и измерение содержания витамина C в зависимости от содержания бутанола и воды
[00169] Примеры 14-17
[00170] Пример 14, пример 15 и пример 16 получали таким же образом, как в примере синтеза 2, примере синтеза 3 и примере синтеза 4, соответственно, за исключением того, что использовали н-бутанол вместо этанола и использовали количества, представленные ниже в таблице 8.
[00171] Конкретные значения рентгеновской дифракции для примеров 14-16 представлены на фиг. 7.
[00172] [Таблица 8]
(a)
(b)
(с)
[00173] [Таблица 9]
[00174] Экспериментальный пример 9: Влияние примера 3 на экспрессию коллагена
[00175] - Экспериментальный способ
[00176] Для испытания увеличения in-vitro выработки коллагена под действием примера 3 (здесь и далее упоминаемого как «порошок JL-101) использовали фибробласты кожи здорового человека (HDF). Чтобы установить концентрацию экспериментального раствора образца, HDF обрабатывали экспериментальным соединением в течение 24 часов, и диапазон концентрации, в котором не наблюдали цитотоксичность, подтверждали в испытании цитотоксичности. HDF обрабатывали «порошком JL-101» в установленной концентрации экспериментального раствора таким же образом, а уровни экспрессии COL1A1 и мРНК COL3A1, которые представляют собой гены коллагена, сравнивали и анализировали с помощью ПЦР в реальном времени (РВ-ПЦР).
[00177] - Выбор клеточной линии и выращивание клеток
[00178] Для данного испытания использовали фибробласты кожи здорового человека (nHDF; Lonza, Базель, Швейцария). Клетки выращивали в инкубаторе с 5% CO2 при 37°C, используя среду, содержащую базовую среду для фибробластов (cc-3181, Lonza, Волкерсвилл, штат Мэриленд, США) и FGM™-2 SingleQuots™ (hGFG, инсулин, FBS и гентамицин/амфотерицин-B; cc-4126, Lonza, Волкерсвилл, штат Мэриленд, США).
[00179] - Экспериментальный материал
[00180] В качестве экспериментального материала получали «JL-101» в форме порошка и растворяли его в фосфатно-солевом буферном растворе (PBS; Biosesang, Соннам, Корея), и использовали для обработки клеток. В качестве положительного контроля использовали трансформирующий фактор роста бета (TGF-β; T7039, Sigma-Aldrich, штат Миссури, США), который растворяли в PBS и использовали для обработки клеток.
[00181] - Определение концентрации экспериментального материала
[00182] Фибробласты кожи человека высевали в количестве 4×10³ клеток/лунка в 96-луночный планшет, выращивали в течение 24 часов, обрабатывали соответствующей концентрацией экспериментального материала и выращивали еще 24 часа. Затем клетки обрабатывали аналитическим буфером WST-1 в 10% от количества среды и доставляли для дальнейшего взаимодействия при 37°С на 0,5-1 час, после чего измеряли их поглощение при 450 нм на микропланшет-ридере iMark microplate reader (Bio-Rad, Геркулес, штат Калифорния, США). Эталонное поглощение измеряли при 650 нм для коррекции полученного значения. Полученные значения выражали как среднее значение ± стандартное отклонение для трех независимых экспериментов. P<0,05 проверяли по t-критерию Стьюдента, чтобы показать значимость полученного значения. Диапазон концентрации, в котором жизнеспособность клеток в результате обработки экспериментальным материалом не уменьшалась, которую сравнивали с контрольным образцом на основании полученных значений, задавали в качестве концентрации экспериментального раствора для следующего эксперимента.
[00183] - Измерение уровня экспрессии гена коллагена
[00184] Уровень экспрессии гена коллагена определяли посредством измерения уровней экспрессии гена COL1A1, который является репрезентативным компонентом коллагена 1 типа, и гена COL3A1, который является репрезентативным компонентом коллагена 3 типа, используя количественную ПЦР в реальном времени (кРВ-ПЦР) (Peter, 2008). Фибробласты кожи человека высевали в количестве 2×105 клеток/лунка в 6-луночный планшет для выращивания культур, выращивали в течение 24 часов, обрабатывали заранее определенной концентрацией экспериментального материала и затем выращивали еще 24 часа. Выращенные клетки собирали и лизировали, используя 1 мл реагента TRIzol (Life Technologies), и экстрагировали общую мРНК. Концентрацию и чистоту (отношение A260/A280 и A260/A230) общей мРНК измеряли с помощью спектрофотометра для микрообъемов MaestroNano® (Maestrogen, Лас-Вегас, штат Невада, США) и выбирали только общую мРНК, имеющую высокую чистоту 2,0 или более.
[00185] Общую мРНК заменяли на кДНК, используя обратную транскриптазу M-MLV (Life Technologies), и использовали для кРВ-ПЦР. кРВ-ПЦР проводили с помощью набора реактивов HOT FIREPol EvaGreen PCR Mix Plus (Solis BioDyne, Эстония), и анализировали экспрессию соответствующего гена с помощью программного обеспечения Line-Gene K (Bioer Technology Co. Ltd., Ханчжоу, Китай). В качестве положительного контроля для экспериментального измерения содержания мРНК коллагена и коллагеназы использовали TGF-β (Chung et al., 1997). ПЦР проводили посредством денатурации при 94°С в течение 5 минут и 40 циклов денатурации (94°C, 30 с), отжига (60°C, 30 с) и полимеризации (72°C, 30 с). Изменение экспрессии гена измеряли посредством сравнения с уровнем экспрессии контрольного гена β-ACTIN. Значения Cт для COL1A1 и COL3A1 нормализовали к значению Cт для β-ACTIN, и рассчитывали относительные уровни экспрессии COL1A1 и COL3A1 методом 2-ΔΔCt. Полученные значения выражали как среднее значение ± стандартное отклонение для трех независимых экспериментов. P<0,05 проверяли по t-критерию Стьюдента, чтобы показать значимость полученного значения. Информация о праймерах, использованных для кРВ-ПЦР, представлена ниже в таблице 10.
[00186] [Таблица 10]

[00187] - Определение экспериментальной концентрации раствора экспериментального материала
[00188] Концентрацию экспериментального раствора «порошка JL-101» в качестве экспериментального материала определяли с помощью анализа WST-1. Фибробласты кожи человека обрабатывали в течение 24 часов «порошком JL-101» в концентрации от 0 до 500 мкг/мл и измеряли жизнеспособность клеток с помощью анализа WST-1. Результаты представлены на фиг. 12. Жизнеспособность клеток, если концентрация «порошка JL-101», использованного для обработки клеток, составляла 100 мкг/мл или менее (10, 20, 50 и 100 мкг/мл), существенно не отличалась от отрицательного контроля. Однако если концентрация составляла 200 мкг/мл или более (200, 300, 400 и 500 мкг/мл), то жизнеспособность клеток снижалась на 5% или более по сравнению с отрицательным контролем. Таким образом, в следующем испытании эффективности в качестве концентрации экспериментального раствора задавали концентрацию 100 мкг/мл или менее «порошка JL-101» (фиг. 12).
[00189] - Измерение уровня экспрессии мРНК коллагена 1 типа
[00190] Наличие увеличения или снижения экспрессии коллагена в фибробластах кожи человека под действием обработки экспериментальным «порошком JL-101» оценивали посредством измерения изменений уровня экспрессии мРНК COL1A1 и мРНК COL3A1, которые являются генами коллагена 1 типа и коллагена 3 типа, главным образом присутствующих в коже, и сначала измеряли степень экспрессии мРНК COL1A1 при обработке «порошком JL-101». Фибробласты кожи человека обрабатывали экспериментальным «порошком JL-101» в максимальной концентрации экспериментального раствора 100 мкг/мл или менее (10, 20, 50 и 100 мкг/мл), установленной в описанном выше испытании цитотоксичности, и затем выращивали в течение 24 часов, после чего экстрагировали общую РНК и синтезировали кДНК. Затем измеряли уровень экспрессии мРНК COL1A1 с помощью кРВ-ПЦР, используя набор праймеров COL1A1 и набор праймеров β-ACTIN, представленные в таблице 11. В качестве положительного контроля использовали TGF-β для повышения достоверности результатов испытания. Как показано на фиг. 13, экспрессия мРНК COL1A1 увеличивалась в зависимости от концентрации при обработке с использованием 100 мкг/мл или менее «порошка JL-101». В частности, экспрессия мРНК COL1A1 при обработке с использованием 100 мкг/мл увеличилась на 45,88±6,79% по сравнению с отрицательным контролем. На основании результатов обработки положительным контролем TGF-β (5,0 нг/мл), экспрессия мРНК COL1A1 увеличилась на 219,65±7,25% по сравнению с отрицательным контролем (фиг. 13).
[00191] - Измерение уровня экспрессии мРНК коллагена 3 типа
[00192] Как показано на фиг. 14, экспрессию мРНК COL3A1 при обработке «порошком JL-101» анализировали на основании анализа экспрессии мРНК COL1A1 при обработке «порошком JL-101». Фибробласты кожи человека обрабатывали экспериментальным «порошком JL-101» в диапазоне концентрации экспериментального раствора (10, 20, 50 и 100 мкг/мл), установленном таким же образом, как в испытании измерения уровня экспрессии мРНК коллагена 1 типа, и выращивали в течение 24 часов, после чего экстрагировали общую РНК и синтезировали кДНК, и измеряли уровень экспрессии мРНК COL3A1 с помощью кРВ-ПЦР, используя набор праймеров COL3A1 и набор праймеров β-ACTIN, представленные в таблице 1. В качестве положительного контроля использовали TGF-β для повышения достоверности результатов испытания. Как показано на фиг. 14, экспрессия мРНК COL3A1 увеличивалась в зависимости от концентрации при обработке с использованием от 0 до 100 мкг/мл «порошка JL-101». В частности, экспрессия мРНК COL3A1 при обработке с использованием 100 мкг/мл «порошка JL-101» увеличилась на 100,98±5,49% по сравнению с отрицательным контролем. На основании результатов обработки положительным контролем TGF-β (5,0 нг/мл), экспрессия мРНК COL3A1 увеличилась на 22,93±6,21% по сравнению с отрицательным контролем.
[00193] - Результаты измерений
[00194] В Корейском Исследовательском Институте дерматологии проводили испытание эффективности в отношении увеличения выработки коллагена в фибробластах кожи человека под действием экспериментального «порошка JL-101), по запросу компании C & Pharm.
[00195] На основании результатов анализа жизнеспособности фибробластов кожи человека под действием экспериментального «порошка JL-101», предоставленного компанией C & Pharm, жизнеспособность клеток не снижалась в условиях выращивания в течение 24 часов после обработки с использованием концентрации 100 мкг/мл или менее (10, 20, 50 и 100 мкг/мл) по сравнению с отрицательным контролем «порошка JL-101». В испытании эффективности в отношении увеличения экспрессии коллагена, экспрессия мРНК COL1A1 существенно увеличивалась при обработке с использованием 20, 50 и 100 мкг/мл «порошка JL-101» по сравнению с отрицательным контролем. В частности, экспрессия мРНК COL1A1 при обработке с использованием 100 мкг/мл «порошка JL-101» увеличилась на 45,88±6,79% по сравнению с отрицательным контролем без обработки. На основании результатов обработки фибробластов кожи человека положительным контролем TGF-β в концентрации 5,0 нг/мл, экспрессия мРНК COL1A1 увеличилась на 219,65±7,25% по сравнению с отрицательным контролем. Экспрессия мРНК COL3A1 увеличивалась в зависимости от концентрации при обработке с использованием 100 мкг/мл или менее «порошка JL-101». В частности, экспрессия мРНК COL3A1 при обработке с использованием 100 мкг/мл «порошка JL-101» увеличилась на 100,98±5,49% по сравнению с отрицательным контролем без обработки. На основании результатов обработки фибробластов кожи человека положительным контролем TGF-β в концентрации 5,0 нг/мл, экспрессия мРНК COL3A1 увеличилась на 22,82±6,21% по сравнению с отрицательным контролем.
[00196] Таким образом, при обработке фибробластов кожи человека экспериментальным материалом, предоставленным компанией C & Pharm, экспрессия мРНК COL1A1 была увеличена на 45,88±6,79%, а экспрессия мРНК COL3A1 была увеличена на 100,98±5,49% по сравнению с отрицательным контролем. Соответствующие уровни экспрессии коллагена составляли примерно 45,64% и 163,50% от уровня экспрессии коллагена с положительным контролем (TGF-β). Таким образом, установлено, что «порошок JL-101» увеличивает экспрессию коллагена в фибробластах кожи человека.
[00197] Эталонные примеры 1 и 2
[00198] Получение эталонного примера 1
[00199]  EtOH 0,5 : H2O 9,5
EtOH 0,5 : H2O 9,5
[00200] 3 г ZnO и 148,3 мл деионизированной воды, не содержащей карбонат-ионов (CO32-), перемешивали (400 об./мин.) при комнатной температуре в атмосфере азота в главном реакторе, и к полученной смеси медленно, по каплям добавляли концентрированный раствор HCl, так чтобы ее оттированный рН составлял от 0,5 до 1. 2,6 г витамина C (аскорбиновой кислоты) растворяли в 10 мл деионизированной воды и 8,69 мл этанола во вспомогательной емкости 1, и раствор витамина C из вспомогательной емкости 1 добавляли в главный реактор и перемешивали в течение 30 минут в атмосфере азота. Поддерживая скорость перемешивания (700 об./мин.) в главном реакторе, в него вводили 1,6 М водный раствор гидроксида натрия из вспомогательной емкости 2, так чтобы оттитрованный рН смеси составлял примерно 6,5-7,5, после чего инициировали реакцию осаждения при перемешивании (700 об./мин.) в течение 3 часов. После реакции измеренный рН составлял 6,5-7,0, и после прекращения реакции получали белый взвешенный осадок. Осадок центрифугировали и три раза промывали, удаляя непрореагировавшие соли и витамин C. После центрифугирования осадок, отделенный от надосадочного раствора, охлаждали жидким азотом и затем лиофилизировали с получением 3,5 г бледно-бежевого витамина C-гидроксида цинка (выход: 58,1%, содержание аскорбиновой кислоты: 38,66%).
[00201] Получение эталонного примера 2
[00202]  EtOH 9,5 : H2O 0,5
EtOH 9,5 : H2O 0,5
[00203] 30 г ZnO и 125,15 мл этанола, не содержащего карбонат-ионов (CO32-), перемешивали (400 об./мин.) при комнатной температуре в атмосфере азота в главном реакторе, и к полученной смеси медленно, по каплям добавляли концентрированный раствор HCl, так чтобы ее оттированный рН составлял от 0,5 до 1. 2,6 г витамина C растворяли в 1,84 мл деионизированной воды и 40 мл этанола во вспомогательной емкости 1, и раствор витамина C из вспомогательной емкости 1 добавляли в главный реактор и перемешивали в течение 30 минут в атмосфере азота. Поддерживая скорость перемешивания (700 об./мин.) в главном реакторе, в него вводили 1,6 М водный раствор гидроксида натрия из вспомогательной емкости 2, так чтобы оттитрованный рН смеси составлял примерно 6,5-7,5, после чего инициировали реакцию осаждения при перемешивании (700 об./мин.) в течение 3 часов. После реакции измеренный рН составлял 6,5-7,0, и после прекращения реакции получали белый взвешенный осадок. Осадок центрифугировали и три раза промывали, удаляя непрореагировавшие соли и витамин C. После центрифугирования осадок, отделенный от надосадочного раствора, охлаждали жидким азотом и затем лиофилизировали с получением 3,41 г бледно-бежевого витамина C-гидроксида цинка (выход: 56,6%, содержание аскорбиновой кислоты: 34,24%).
[00204] Полученные таким образом эталонные примеры 1 и 2 представлены ниже в таблице 11, а конкретные значения рентгеновской дифракции для эталонных примеров 1 и 2 представлены на фиг. 18.
[00205] [Таблица 11]
(a)
(b)
[00206] Промышленная применимость
[00207] В соответствии с настоящим изобретением, комплекс гидроксида металла построен так, что активный ингредиент включен в модифицированную многослойную структуру гидроксида, демонстрируя превосходные характеристики устойчивого высвобождения и улучшая эффект доставленного активного ингредиента благодаря стабильном включению активного ингредиента в высокой концентрации в указанный комплекс гидроксида металла. Кроме того, предложенный комплекс гидроксида металла стабильно содержит нестабильный активный ингредиент, что обеспечивает возможность длительного хранения активного ингредиента и, при нанесении на кожу, минимизации раздражения, что усиливает эффект отсутствия раздражения, и может демонстрировать превосходный эффект экспрессии коллагена.
[00208] Кроме того, в настоящем изобретении предложен способ получения предложенного комплекса гидроксида металла, обладающего превосходным действием, как описано выше.



Изобретение относится к комплексу гидроксида металла, содержащему многослойную структуру гидроксида, которая содержит базовый слой, поверхностный слой и активный ингредиент, и к способу его получения. Комплекс гидроксида металла содержит многослойную структуру гидроксида химической формулы {[Mx(OH)z]B[My(OH)w]S}{(An)q}⋅m(H2O), где [Mx(OH)z]B - базовый слой многослойной структуры гидроксида и [My(OH)w]S - поверхностный слой многослойной структуры гидроксида, M представляет собой Zn2+, А - активный ингредиент, представляет собой анионное соединение, содержащее аскорбиновую кислоту в качестве функциональной группы. Комплекс гидроксида металла включает асимметричную ламинированную структуру. Комплекс гидроксида металла получен совместным осаждением активного ингредиента и предшественника структуры гидроксида металла в реакции осаждения с использованием спирта и воды. Обеспечивается возможность максимизации действия активного ингредиента. 5 н. и 4 з.п. ф-лы, 18 ил., 11 табл., 28 пр.
1. Комплекс гидроксида металла, содержащий модифицированную многослойную структуру гидроксида химической формулы 1, представленной ниже, которая содержит базовый слой, поверхностный слой и активный ингредиент:
[Химическая формула 1]
{[Mx(OH)z]B[My(OH)w]S}{(An)q}⋅m(H2O),
где [Mx(OH)z]B представляет собой базовый слой модифицированной многослойной структуры гидроксида и [My(OH)w]S представляет собой поверхностный слой модифицированной многослойной структуры гидроксида,
М представляет собой Zn2+,
х равен от 0,6 до 3,
у равен от 0 до 2,
z равен от 1 до 5,
w равен от 0 до 4,
z+w равно от 1 до 9,
q равен от 1 до 4,
m равен от 0,1 до 10,
n представляет собой зарядовое число А, и
активный ингредиент представлен символом А, где А представляет собой анионное соединение, содержащее аскорбиновую кислоту в качестве функциональной группы, имеющей электростатическое притяжение в зависимости от pKa;
где указанный комплекс гидроксида металла включает асимметричную ламинированную структуру,
где указанная модифицированная многослойная структура гидроксида имеет профиль порошковой рентгеновской дифракции с пиковыми значениями углов дифракции (2θ) 5,96±1°, 33,46±1° и 59,3±1°.
2. Комплекс гидроксида металла по п. 1, в котором указанная многослойная структура гидроксида содержит от двух до пяти слоев.
3. Комплекс гидроксида металла, содержащий модифицированную многослойную структуру гидроксида химической формулы 1, представленной ниже, которая содержит базовый слой, поверхностный слой и активный ингредиент:
[Химическая формула 1]
{[Mx(OH)z]B[My(OH)w]S}{(An)q}⋅m(H2O),
где [Mx(OH)z]B представляет собой базовый слой модифицированной многослойной структуры гидроксида и [My(OH)w]S представляет собой поверхностный слой модифицированной многослойной структуры гидроксида,
М представляет собой Zn2+,
х равен от 0,6 до 3,
у равен от 0 до 2,
z равен от 1 до 5,
w равен от 0 до 4,
z+w равно от 1 до 9,
q равен от 1 до 4,
m равен от 0,1 до 10,
n представляет собой зарядовое число А, и
активный ингредиент представлен символом А, где А представляет собой анионное соединение, содержащее аскорбиновую кислоту в качестве функциональной группы, имеющей электростатическое притяжение в зависимости от pKa; где указанная модифицированная многослойная структура гидроксида имеет профиль порошковой рентгеновской дифракции с пиковыми значениями углов дифракции (2θ) 5,96±1°, 8,5±1°, 10,36±1°, 13,36±1°, 19±1°, 20,84±1°, 21,7±1°, 26,34±1°, 37,68±1°, 31,48±1°, 33,78±1°, 34,88±1° и 59,3±1°.
4. Комплекс гидроксида металла, содержащий модифицированную многослойную структуру гидроксида химической формулы 1, представленной ниже, которая содержит базовый слой, поверхностный слой и активный ингредиент:
[Химическая формула 1]
{[Mx(OH)z]B[My(OH)w]S}{(An)q}⋅m(H2O),
где [Mx(OH)z]B представляет собой базовый слой модифицированной многослойной структуры гидроксида и [My(OH)w]S представляет собой поверхностный слой модифицированной многослойной структуры гидроксида,
М представляет собой Zn2+,
х равен от 0,6 до 3,
у равен от 0 до 2,
z равен от 1 до 5,
w равен от 0 до 4,
z+w равно от 1 до 9,
q равен от 1 до 4,
m равен от 0,1 до 10,
n представляет собой зарядовое число А, и
активный ингредиент представлен символом А, где А представляет собой анионное соединение, содержащее аскорбиновую кислоту в качестве функциональной группы, имеющей электростатическое притяжение в зависимости от pKa; где указанная модифицированная многослойная структура гидроксида имеет профиль порошковой рентгеновской дифракции с пиковыми значениями при углах дифракции (2θ) 6,28±1°, 8,88±1°, 10,32±1°, 13,42±1°, 21,04±1°, 28,14±1°, 33,5±1° и 59,16±1°.
5. Комплекс гидроксида металла по любому из пп. 1, 3 или 4, в котором указанная многослойная структура гидроксида получена совместным осаждением по реакции осаждения с использованием спирта и воды в качестве растворителя.
6. Комплекс гидроксида металла по п. 5, в котором указанный спирт представляет собой по меньшей мере один спирт, выбранный из группы, состоящей из метанола, этанола, пропанола и бутанола.
7. Комплекс гидроксида металла, содержащий модифицированную многослойную структуру гидроксида, полученный посредством совместного осаждения активного ингредиента и предшественника структуры гидроксида металла в реакции осаждения с использованием спирта и воды с получением асимметричной ламинированной структуры,
где указанная модифицированная многослойная структура гидроксида имеет профиль порошковой рентгеновской дифракции с пиковыми значениями углов дифракции (2θ) 5,96±1°, 33,46±1° и 59,3±1°,
где указанный активный ингредиент представляет собой анионное соединение, содержащее аскорбиновую кислоту, и указанный спирт представляет собой по меньшей мере один спирт, выбранный из группы, состоящей из метанола, этанола, пропанола и бутанола.
8. Комплекс гидроксида металла по п. 7, в котором соотношение спирта и воды при совместном осаждении составляет от 1:9 до 9:1.
9. Способ получения комплекса гидроксида металла, включающий совместное осаждение активного ингредиента и предшественника структуры гидроксида металла в реакции осаждения с использованием спирта и воды с получением асимметричной ламинированной структуры,
где указанный комплекс гидроксида металла включает модифицированную многослойную структуру гидроксида,
где указанная модифицированная многослойная структура гидроксида имеет профиль порошковой рентгеновской дифракции с пиковыми значениями углов дифракции (2θ) 5,96±1°, 33,46±1° и 59,3±1°,
где указанный активный ингредиент представляет собой анионное соединение, содержащее аскорбиновую кислоту, и указанный спирт представляет собой по меньшей мере один спирт, выбранный из группы, состоящей из метанола, этанола, пропанола и бутанола.
| KR 101082391 B1, 11.11.2011 | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| KR 100998354 B1, 03.12.2010 | |||
| KR 20030012641 A, 12.02.2003 | |||
| ФАРМАЦЕВТИЧЕСКИ АКТИВНЫЕ СОЕДИНЕНИЯ, ИХ ПОЛУЧЕНИЕ, СОДЕРЖАЩИЕ ИХ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2420297C2 |
Авторы
Даты
2024-04-25—Публикация
2019-09-23—Подача