ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
Настоящая заявка испрашивает приоритет в соответствии с предварительной заявкой на патент США № 62/560955, поданной 20 сентября 2017 года и включенной таким образом в данный документ посредством ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к области иммунотерапии. Более конкретно, настоящее изобретение относится к способам проведения курса иммунотерапии у пациентов, опухоли которых характеризуются высокой нагрузкой пассажирскими генными мутациями.
УРОВЕНЬ ТЕХНИКИ
В тексте описания упоминаются различные публикации, в том числе патенты, патентные заявки, опубликованные патентные заявки, номера доступа, технические статьи и научные статьи. Каждая из данных упоминаемых публикаций включена в данный документ посредством ссылки во всей своей полноте и для всех целей.
Недавние исследования показали, что пациенты, у которых опухоли характеризуются более высоким показателем общей мутационной нагрузки опухоли (TMB), с большей вероятностью получат пользу от иммунотерапии ввиду повышенного презентирования неоантигенов, которые могут вызывать иммунный ответ. Однако общая мутационная нагрузка включает драйверные генные мутации, которые фактически могут подавлять иммуногенность и снижать чувствительность к лечению.
Не существует какого-либо разработанного способа, предназначенного для идентификации пассажирских генов и мутаций в них и оценки иммуногенности. Эти и другие недостатки решены в настоящем изобретении.
КРАТКОЕ ОПИСАНИЕ
Следует понимать, что и нижеследующее общее описание, и нижеследующее подробное описание являются лишь иллюстративными и поясняющими, но не являются ограничивающими.
В первом аспекте настоящего изобретения представлен способ, предусматривающий получение данных о генетической последовательности, где данные о генетической последовательности охватывают множество генов и получены для множества биологических образцов, отобранных у субъектов, имеющих множество типов заболеваний, идентификацию множества мутантных генов для каждого из множества биологических образцов, где каждый из мутантных генов содержит генетическую последовательность, имеющую по меньшей мере одну не являющуюся синонимичной соматическую мутацию, определение мутационной нагрузки опухоли для каждого биологического образца исходя из числа мутантных генов в каждом биологическом образце для каждого типа заболевания, определение средней мутационной нагрузки опухоли для множества мутантных генов во множестве биологических образцов исходя из определенного числа мутантных генов в каждом биологическом образце для каждого мутантного гена и каждого типа заболевания, определение доли биологических образцов, содержащих мутантный ген, для каждого мутантного гена, определение коэффициента корреляции между средней мутационной нагрузкой опухоли и долей биологических образцов, содержащих мутантный ген. Более высокий коэффициент корреляции указывает на то, что конкретный ген с большей вероятностью приобретет соматические мутации при типах рака с более высокой общей частотой появления мутаций (например, пассажирский ген), тогда как более низкий коэффициент корреляции указывает на то, что конкретный ген c меньшей вероятностью приобретет соматические мутации при типах рака, характеризующихся более высокой общей частотой появления мутаций (например, ген, не являющийся пассажирским).
В другом аспекте настоящего изобретения представлены способы отбора пациента с раком для иммунотерапии. Как правило, данные способы предусматривают определение общей нагрузки пассажирскими генными мутациями опухоли у пациента с раком, получение фонового распределения для мутационной нагрузки опухоли, нормализацию общей нагрузки пассажирскими генными мутациями относительно фонового распределения и отнесение пациента с раком к категории респондеров на иммунотерапию, если общая нагрузка пассажирскими генными мутациями на по меньшей мере приблизительно полторы величины стандартного отклонения превышает среднее значение фонового распределения.
Получение фонового распределения может предусматривать определение мутационной нагрузки для случайным образом выбранных генов во множестве образцов, полученных из опухоли, однако число случайным образом выбранных генов в каждом образце предпочтительно равняется числу пассажирских генов, используемому для вычисления общей нагрузки пассажирскими генными мутациями. Нормализация общей нагрузки пассажирскими генными мутациями относительно фонового распределения может предусматривать получение z-показателя, указывающего на число стандартных отклонений от среднего значения фонового распределения.
Способы могут дополнительно предусматривать определение того, относится ли мутантный ген опухоли к категории пассажирских генов. Отнесение мутантного гена опухоли к категории пассажирских генов, может предусматривать отбор мутантного гена опухоли и сопоставление мутантного гена со структурированным набором данных, охватывающим пассажирские гены, определенные в соответствии с индексом пассажирских генов. Индекс пассажирских генов может предусматривать коэффициент корреляции между долей образцов, содержащих мутантный ген, полученных от когорты пациентов с раком, и медианным числом мутантных генов для каждого типа опухоли в когорте пациентов с раком.
Способы могут дополнительно предусматривать проведение курса иммунотерапии у пациента с раком. Курс иммунотерапии может предусматривать введение пациенту ингибитора T-клеточного ингибиторного рецептора. Курс иммунотерапии может предусматривать введение пациенту активатора T-клеточного активирующего рецептора.
Курс иммунотерапии может предусматривать введение пациенту антитела, которое связывается с PD1. Антитело, которое связывается с PD1, может содержать по меньшей мере последовательность вариабельного участка тяжелой цепи (HCVR) под SEQ ID NO: 21 и вариабельный участок легкой цепи или может содержать по меньшей мере последовательность вариабельного участка легкой цепи (LCVR) под SEQ ID NO: 22 и вариабельный участок тяжелой цепи. Антитело, которое связывается с PD1, может содержать HCVR или SEQ ID NO: 21 и LCVR или SEQ ID NO: 22. Данное антитело, которое связывается с PD1, можно вводить в комбинации с антителом, которое связывается с LAG3.
Курс иммунотерапии может предусматривать введение пациенту антитела, которое связывается с PDL1. Антитело, которое связывается с PDL1, может содержать по меньшей мере последовательность HCVR под SEQ ID NO: 122 и LCVR или может содержать по меньшей мере последовательность LCVR под SEQ ID NO: 123 и HCVR. Антитело, которое связывается с PDL1, может содержать HCVR или SEQ ID NO: 122 и LCVR или SEQ ID NO: 123. Данное антитело, которое связывается с PDL1, можно вводить в комбинации с антителом, которое связывается с LAG3.
Курс иммунотерапии может предусматривать введение пациенту антитела, которое связывается с LAG3. Антитело, которое связывается с LAG3, может содержать по меньшей мере последовательность HCVR под SEQ ID NO: 93 и LCVR или может содержать по меньшей мере последовательность LCVR под SEQ ID NO: 94 и HCVR. Антитело, которое связывается с LAG3, может содержать HCVR или SEQ ID NO: 93 и LCVR или SEQ ID NO: 94. Данное антитело, которое связывается с LAG3, можно вводить в комбинации с антителом, которое связывается с PD1, или с антителом, которое связывается с PDL1.
Дополнительные преимущества будут частично изложены в нижеследующем описании или могут быть получены в ходе практического осуществления. Преимущества будут реализованы и достигнуты с помощью признаков и комбинаций, конкретно указанных в прилагаемой формуле изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Прилагаемые графические материалы, которые включены в настоящее описание и составляют его часть, иллюстрируют варианты осуществления и вместе с описанием служат для пояснения принципов способов и систем.
На фигуре 1 показана блок-схема, иллюстрирующая пример способа.
На фигуре 2 показана блок-схема, иллюстрирующая пример способа.
На фигуре 3 показана блок-схема, иллюстрирующая еще один пример способа.
На фигуре 4 показана блок-схема, иллюстрирующая еще один пример способа.
На фигуре 5 представлен общий обзор характеристик пассажирских генов.
На фигуре 6 показаны диаграммы рассеяния для доли пациентов с вариантом гена (ось y) и среднего общего числа мутантных генов (ось x) при каждом типе рака.
На фигуре 7 показана насыщенность по шкале индекса пассажирских генов (PGI) для раковых драйверных генов и различных других групп генов.
На фигуре 8 показаны гены из CGC с наиболее высокими (слева) и наиболее низкими (справа) значениями PGI и соответствующий им тип рака с наиболее высокой процентной долей (>2%) образцов с мутациями.
На фигурах 9A-C графически представлены a) показатели местной иммунной цитолитической активности, b) число ридов для TCR и c) клинический исход в когортах пациентов.
На фигуре 10 показана блок-диаграмма, демонстрирующая иллюстративную операционную среду, предназначенную для выполнения раскрытых способов.
На фигуре 11 показана TMB в когорте пациентов в клиническом исследовании фазы 1.
На фигуре 12 показаны 500 основных пассажирских генов с наиболее высоким индексом пассажирских генов (PGI).
ПОДРОБНОЕ ОПИСАНИЕ
Различные термины, относящиеся к аспектам настоящего изобретения, используются по всему описанию и в формуле изобретения. Если не указано иное, такие термины следует понимать в их обычным значении в данной области техники. Другие конкретно определенные термины следует интерпретировать в соответствии с определением, представленным в данном документе.
Используемые в описании и прилагаемой формуле изобретения формы единственного числа включают ссылки на форму множественного числа, если контекст явно не указывает на иное.
Ингибирование предусматривает уменьшение, снижение, блокирование, предупреждение, замедление, инактивацию, уменьшение чувствительности, остановку и/или понижающую регуляцию активности или экспрессии представляющих интерес молекулы или сигнального пути.
Варианты осуществления способов и систем описаны ниже со ссылкой на блок-диаграммы и блок-схемы, иллюстрирующие способы, системы, устройства и компьютерные программные продукты. Будет понятно, что каждый блок иллюстраций в виде блок-диаграмм и блок-схем и комбинации блоков на иллюстрациях в виде блок-диаграмм и блок-схем соответственно могут быть реализованы посредством команд компьютерных программ. Данные команды компьютерных программ могут быть загружены на компьютер общего назначения, компьютер специализированного назначения или другое программируемое устройство обработки данных, представляющее собой машину, за счет которых команды, выполняемые компьютером или другим программируемым устройством обработки данных, обеспечивают реализацию функций, указанных в блоке или блоках блок-схемы.
Такие команды компьютерных программ также могут храниться в машиночитаемом запоминающем устройстве, которое может управлять компьютером или другим программируемым устройством обработки данных для выполнения их функций надлежащим образом, за счет чего команды, хранящиеся в машиночитаемом запоминающем устройстве, обеспечивают получение готового изделия, включая машиночитаемые команды, предназначенные для реализации функции, указанной в блоке или блоках блок-схемы. Команды компьютерных программ также могут быть загружены на компьютер или другое программируемое устройство обработки данных для обеспечения выполнения ряда технологических стадий на компьютере или другом программируемом устройстве с получением реализуемого с помощью компьютера процесса, за счет чего команды, выполняемые на компьютере или другом программируемом устройстве, обеспечивают стадии для реализации функций, указанных в блоке или блоках блок-схемы.
Соответственно, блоки иллюстраций в виде блок-диаграмм и блок-схем обеспечивают комбинации средств, предназначенных для выполнения указанных функций, комбинации стадий, предназначенных для выполнения указанных функций, и средства, представленные командами программ, предназначенные для выполнения указанных функций. Также следует понимать, что каждый блок иллюстраций в виде блок-диаграмм и блок-схем и комбинации блоков иллюстраций в виде блок-диаграмм и блок-схем могут быть реализованы с помощью аппаратных компьютерных систем специализированного назначения, которые выполняют указанные функции или стадии, или комбинаций аппаратных средств специализированного назначения и компьютерных программ.
Термины «субъект» и «пациент» используют взаимозаменяемо, при этом они включают любой животное. Предпочтительными являются млекопитающие, в том числе млекопитающие-компаньоны (например, кошка, собака) и сельскохозяйственные млекопитающие (например, свинья, лошадь, корова), а также грызуны, в том числе мыши, кролики и крысы, морские свинки и другие грызуны. Приматы, отличные от человека, являются более предпочтительными, при этом люди являются особо предпочтительными.
В соответствии с настоящим изобретением было обнаружено, что при раке общая нагрузка пассажирскими генными мутациями в отличие от общей мутационной нагрузки для всех генов служит в качестве точного индикатора того, существует ли вероятность положительного ответа на иммунотерапию у пациента с раком. Мутационная нагрузка опухоли (TMB) может указывать на число мутаций в пределах кодирующего участка генома опухоли. Мутантные гены оценивали и классифицировали в соответствии с их статусом в качестве пассажирского гена с помощью индекса пассажирских генов, который использовали в широкомасштабном анализе ракового генома. Было отмечено, что среди идентифицированных пассажирских генов преобладали семейства генов, известные избыточным количеством пассажирских мутаций, в том числе генов, кодирующих крупные белки, генов с низким уровнем экспрессии и генов с поздним временем репликации ДНК. Общая нагрузка пассажирскими генными мутациями положительно коррелирует с иммуногенностью опухоли и благоприятным прогнозом клинических исходов у пациентов. Соответственно, в настоящем изобретении представлены способы классификации пациентов по их показателю нагрузки пассажирскими генными мутациями как часть курса иммунотерапии.
В биологии рака считается, что драйверные мутации по меньшей мере в некоторой степени вовлечены в канцерогенез или трансформацию клеток. При этом пассажирские мутации считаются такими мутациями, которые не обеспечивают преимущества в росте или не способствуют развитию рака. См. Stratton MR et al. (2009) Nature. 458:719-24. Таким образом, пассажирские гены включают в себя те гены, которые содержат пассажирские мутации. Неограничивающие примеры мутаций включают замены, инверсии, вставки и делеции одного или более нуклеотидов, кодонов, генов или хромосом, а также изменение числа копий.
В одном аспекте настоящего изобретения представлены способы и системы идентификации или классификации пассажирских генов. Среди идентифицированных пассажирских генов преобладают семейства, известные избыточным количеством пассажирских мутаций, как, например, особо крупные белки и гены с низким уровнем экспрессии или с поздним временем репликации ДНК. В некоторых вариантах осуществления пассажирские гены можно идентифицировать или классифицировать в соответствии с индексом пассажирских генов (PGI). Таким образом, например, пассажирские гены можно идентифицировать или классифицировать в соответствии с PGI, который представляет собой коэффициент корреляции между долей образцов, полученных от когорты пациентов с раком, которые содержат мутантный ген, и медианным числом мутантных генов для каждого типа опухоли в когорте пациентов с раком. На основе идентификации пассажирских генов может быть составлен структурированный набор данных, охватывающий пассажирские гены.
У отдельных пациентов с раком можно проводить скрининг, чтобы определить, содержат ли их опухоли пассажирские гены, а также, чтобы определить общую нагрузку пассажирскими генными мутациями их опухолей. Исходя из нагрузки пассажирскими генными мутациями у пациента, пациента можно классифицировать в соответствии с его способностью проявлять положительный ответ на иммунотерапию. Иммунотерапия, как правило, повышает естественный иммунный ответ организма на злокачественные опухоли и включает без ограничения повышение T-клеточного ответа на опухоль.
Пример подхода, с помощью которого пациента с раком можно оценивать в отношении отвечаемости на иммунотерапию показан на фиг. 1. В общих чертах способы предусматривают определение общей нагрузки пассажирскими генными мутациями опухоли у пациента с раком (110), получение фонового распределения для мутационной нагрузки опухоли (120), нормализацию общей нагрузки пассажирскими генными мутациями относительно фонового распределения (130) и отнесение пациента с раком к категории респондеров на иммунотерапию (140).
Также раскрыты способы лечения пациента с раком с помощью иммунотерапии после проведения его оценки в отношении отвечаемости на иммунотерапию. Например, раскрыты способы лечения пациента с раком посредством иммунотерапии, предусматривающие определение того, является ли пациент с раком респондером на иммунотерапию, предусматривающее определение общей нагрузки пассажирскими генными мутациями опухоли у пациента; получение фонового распределения для мутационной нагрузки опухоли; нормализацию общей нагрузки пассажирскими генными мутациями относительно фонового распределения и отнесение пациента с раком к категории имеющих генотип респондера на иммунотерапию, если общая нагрузка пассажирскими генными мутациями на по меньшей мере приблизительно полторы величины стандартного отклонения превышает среднее значение фонового распределения; и проведение иммунотерапии у пациента с раком, отнесенного к категории респондеров на иммунотерапию.
Дополнительно раскрыты способы лечения пациента с помощью ингибитора T-клеточного ингибиторного рецептора, или рецептора на опухолевой клетке, или средства для лечения, отличного от иммунотерапевтического, где пациент страдает от рака, при этом способ предусматривает следующие стадии: определение того, является ли пациент респондером на иммунотерапию посредством получения или полученного биологического образца опухоли пациента; выполнения или выполненного анализа генотипирования биологического образца для определения того, имеется ли у пациента генотип респондера на иммунотерапию, выполняемого с помощью секвенирования биологического образца с получением данных о последовательности; определения на основе данных о последовательности общей нагрузки пассажирскими генными мутациями опухоли у пациента; получения на основе данных о последовательности фонового распределения для мутационной нагрузки опухоли; нормализации общей нагрузки пассажирскими генными мутациями относительно фонового распределения и отнесения пациента к категории респондеров на иммунотерапию, если общая нагрузка пассажирскими генными мутациями на по меньшей мере приблизительно полторы величины стандартного отклонения превышает среднее значение фонового распределения; при этом если у пациента имеется генотип респондера на иммунотерапию, то осуществляют введение терапевтически эффективного количества ингибитора T-клеточного ингибиторного рецептора или рецептора на опухолевой клетке, при этом если у пациента отсутствует генотип респондера на иммунотерапию, то осуществляют введение средства для лечения, отличного от иммунотерапевтического. В некоторых вариантах осуществления уровень риска неблагоприятного клинического исхода для пациента с генотипом респондера на иммунотерапию является более низким после введения терапевтически эффективного количества ингибитора T-клеточного ингибиторного рецептора или рецептора на опухолевой клетке по сравнению риском, который может быть при введении пациенту средства для лечения, отличного от иммунотерапевтического. В некоторых вариантах осуществления активация T-клеток и/или иммунная цитолитическая активность у пациента с генотипом респондера на иммунотерапию является более высокой после введения терапевтически эффективного количества ингибитора T-клеточного ингибиторного рецептора или рецептора на опухолевой клетке, чем она может быть при введении пациенту средства для лечения, отличного от иммунотерапевтического.
Раскрыты иммунотерапевтические средства, предназначенные для применения в способе лечения пациента с раком, при этом способ предусматривает определение того, относится ли пациент с раком к категории респондеров на иммунотерапию, что осуществляют путем определения общей нагрузки пассажирскими генными мутациями опухоли у пациента; получения фонового распределения для мутационной нагрузки опухоли; нормализации общей нагрузки пассажирскими генными мутациями относительно фонового распределения; отнесения пациента с раком к категории имеющих генотип респондера на иммунотерапию, если общая нагрузка пассажирскими генными мутациями на по меньшей мере приблизительно полторы величины стандартного отклонения превышает среднее значение фонового распределения; и введение иммунотерапевтического средства пациенту с раком, отнесенному к категории респондеров на иммунотерапию
В некоторых предпочтительных вариантах осуществления определение общей нагрузки пассажирскими генными мутациями опухоли у пациента с раком (110) может предусматривать определение общей нагрузки пассажирскими генными мутациями с помощью любого способа секвенирования, который используют для определения кодирующих участков («экзома») в геноме опухоли. Также можно использовать способы полногеномного секвенирования.
Мутации в экзоме можно определять с использованием способов секвенирования, известных из уровня техники. Например, в патентном документе US 2013/0040863, включенном в данный документ посредством ссылки, описаны способы определения последовательности нуклеиновой кислоты целевой молекулы нуклеиновой кислоты, включающие секвенирование путем синтеза, секвенирование путем лигирования или секвенирование путем гибридизации, в том числе с целью выявления мутаций, проведения полногеномного секвенирования и секвенирования экзонов. При необходимости можно использовать различные способы амплификации с получением более высоких количеств, в частности небольших образцов нуклеиновых кислот, до проведения секвенирования.
Секвенирование посредством синтеза (SBS) и секвенирование посредством лигирования можно осуществлять с использованием ePCR, которая используется в 454 Lifesciences (Бренфорд, Коннектикут) и Roche Diagnostics (Базель, Швейцария). Нуклеиновые кислоты, такие как геномная ДНК или другие, представляющие интерес, можно разделять на фрагменты, диспергировать в эмульсиях типа «вода-в-масле» и разбавлять, в результате чего отдельный фрагмент нуклеиновой кислоты отделяется от других фрагментов в капле эмульсии. Можно использовать гранулу, например, несущую множество копий праймера, и проводить амплификацию, в результате чего каждая капля эмульсии служит в качестве реакционного «сосуда» для амплификации одного фрагмента нуклеиновой кислоты с получением множества копий. Можно использовать другие способы, такие как мостиковая ПЦР (Illumina, Inc.; Сан-Диего, Калифорния) или полони-амплификация (Agencourt/Applied Biosystems). US 2009/0088327; US 2010/0028885 и US 2009/0325172, каждый из которых включен в данный документ посредством ссылки.
Способы ручного или автоматизированного секвенирования хорошо известны в данной области техники и включают без ограничения секвенирование по Сэнгеру, пиросеквенирование, секвенирование путем гибридизации, секвенирование путем лигирования и т. п. Способы секвенирования можно осуществлять вручную или с использованием автоматизированных способов. Кроме того, способы амплификации, изложенные в данном документе, можно использовать для подготовки нуклеиновых кислот к секвенированию с использованием коммерчески доступных способов, таких как автоматизированное секвенирование по Сэнгеру (доступное от Applied Biosystems, Фостер-Сити, Калифорния) или пиросеквенирование (доступное от 454 Lifesciences, Бренфорд, Коннектикут и Roche Diagnostics, Базель, Швейцария); для способов секвенирования с помощью синтеза, коммерчески доступных от Illumina, Inc. (Сан-Диего, Калифорния) или Helicos (Кембридж, Массачусетс), или способов секвенирования путем лигирования, разрабатываемых Applied Biosystems на основе их платформы Agencourt (см. также Ronaghi et al., Science 281:363 (1998); Dressman et al., Proc. Natl. Acad. Sci. USA 100:8817-8822 (2003); Mitra et al., Proc. Natl. Acad. Sci. USA 100:55926-5931 (2003)), которые включены в данный документ посредством ссылки.
Совокупность нуклеиновых кислот, в которой праймер гибридизируется с каждой нуклеиновой кислотой таким образом, что образуются матрицы нуклеиновых кислот и осуществляется модификация праймера, направляемая матрицей. Модификацию можно выявить для определения последовательности матрицы. Например, праймеры можно модифицировать путем удлинения с использованием полимеразы, при этом удлинение праймеров можно отслеживать в условиях, которые позволяют устанавливать идентичность и местоположение конкретных нуклеотидов. Например, можно отслеживать удлинение и определять последовательность матриц нуклеиновых кислот с использованием пиросеквенирования, которое описано в патентных документах US 2005/0130173, US 2006/0134633, патенте США № 4971903; патенте США № 6258568 и патенте США № 6210891, каждый из которых включен в данный документ посредством ссылки, и которое также является коммерчески доступным. Удлинение также можно отслеживать в соответствии с добавлением нуклеотидных аналогов, меченых полимеразой, с использованием способов, описанных, например, в патенте США № 4863849; патенте США № 5302509; патенте США № 5763594; патенте США № 5798210; патенте США № 6001566; патенте США № 6664079; патентном документе U.S. 2005/0037398 и патенте США № 7057026, каждый из которых включен в данный документ посредством ссылки. Полимеразы, применимые в способах секвенирования, как правило, представляют собой ферменты с полимеразной активностью, полученные из природных источников. Будет понятно, что полимеразы можно модифицировать с изменением их специфичности в отношении модифицированных нуклеотидов, как это описано, например, в патентном документе WO 01/23411; патенте США № 5939292 и патентном документе WO 05/024010, каждый из которых включен в данный документ посредством ссылки. Кроме того, полимеразы не обязательно должны быть получены из биологических систем. Полимеразы, которые применимы в настоящем изобретении, включают любое средство, способное катализировать удлинение праймера на основе нуклеиновой кислоты, направляемое последовательностью матрицы, с которой гибридизируется праймер. Как правило, полимеразы будут представлять собой белковые ферменты, выделенные из биологических систем.
В качестве альтернативы последовательности экзонов можно определять с использованием секвенирования путем лигирования, как это описано, например, в Shendure et al. Science 309:1728-1732 (2005); патенте США № 5599675 и патенте США № 5750341, каждый из которых включен в данный документ посредством ссылки. Последовательности матриц нуклеиновых кислот можно определять с использованием способов секвенирования путем гибридизации, таких как способы, описанные в патенте США № 6090549; патенте США № 6401267 и патенте США № 6620584, каждый из которых включен в данный документ посредством ссылки.
При необходимости продукты последовательности экзонов выявляют с использованием анализа лигирования, такого как анализ олигонуклеотидного лигирования (OLA). Выявление с помощью OLA предусматривает зависимое от матрицы лигирование двух зондов меньшего размера в один длинный зонд с использованием целевой последовательность в ампликоне в качестве матрицы. В конкретном варианте осуществления однонитевая целевая последовательность включает первый целевой домен и второй целевой домен, которые граничат и являются смежными. Первый зонд OLA и второй зонд OLA можно гибридизировать с комплементарными последовательностями соответствующих целевых доменов. Два зонда OLA затем ковалентно соединяют друг с другом с образованием модифицированного зонда. В определенных вариантах осуществления, в которых зонды гибридизируются непосредственно смежно друг с другом, с помощью лигазы может образовываться ковалентная связь. Один или оба зонда могут включать нуклеозид с меткой, как, например, связанная с пептидом метка. Соответственно, присутствие лигированного продукта может быть определено путем выявления метки. В конкретных вариантах осуществления лигируемые зонды могут включать сайты праймирования, сконструированные с возможностью обеспечения амплификации продукта лигированных зондов с использованием праймеров, которые гибридизируются с сайтами праймирования, например, в ходе реакции ПЦР.
В качестве альтернативы лигируемые зонды можно использовать в анализе удлинения-лигирования, где гибридизированные зонды не являются смежными, а один или более нуклеотидов добавляют наряду с одним или более средствами, которые обеспечивают соединение зондов посредством добавленных нуклеотидов. Кроме того, анализ лигирования или анализ удлинения-лигирования можно проводить с помощью одного запирающего зонда вместо двух отдельных лигируемых зондов.
В некоторых предпочтительных вариантах осуществления получение фонового распределения (120) предусматривает определение мутационной нагрузки для случайным образом выбранных генов во множестве образцов, полученных из опухоли, при условии, что число случайным образом выбранных генов в каждом образце равняется числу пассажирских генов, используемому для вычисления общей нагрузки пассажирскими генными мутациями.
В некоторых предпочтительных вариантах осуществления нормализация общей нагрузки пассажирскими генными мутациями относительно фонового распределения (130) предусматривает получение z-показателя, указывающего на число стандартных отклонений от среднего значения фонового распределения. В альтернативном варианте осуществления можно использовать p-значения. Можно осуществлять корреляцию z-показателей с p-значениями. Например, z-показатель, составляющий 1,65, равняется p-значению p<0,05, и z-показатель, составляющий 2,3, равняется p-значению p<0,01.
Отнесение пациента с раком к категории респондеров на иммунотерапию можно осуществлять в соответствии с соотношением общей нагрузки пассажирскими генными мутациями и среднего значения фонового распределения. Например, пациента можно отнести к категории респондеров на иммунотерапию в том случае, если общая нагрузка пассажирскими генными мутациями на по меньшей мере определенную величину стандартного отклонения превышает среднее значение фонового распределения. Величина стандартного отклонения может, например, превышать на по меньшей мере приблизительно 1, по меньшей мере приблизительно 1,5, по меньшей мере приблизительно 2, по меньшей мере приблизительно 2,5, по меньшей мере приблизительно 3 или более 3 стандартных отклонений среднее значение фонового распределения.
В некоторых вариантах осуществления пациент с раком может страдать от плоскоклеточного рака кожи (CSCC), уротелиальной карциномы мочевого пузыря (BLCA), инвазивной карциномы молочной железы (BRCA), плоскоклеточной карциномы шейки матки и эндоцервикальной аденокарциномы (CESC), аденокарциномы толстой кишки/прямой кишки (CORE), мультиформной глиобластомы (GBM), плоскоклеточной карциномы головы и шеи (HNSC), светлоклеточной карциномы почки (KIRC), папиллярной почечно-клеточной карциномы почки (KIRP), острого миелоидного лейкоза (LAML), гепатоцеллюлярной карциномы печени (LIHC), глиомы головного мозга низкой степени злокачественности (LGG), аденокарциномы легкого (LUAD), плоскоклеточной карциномы легкого (LUSC), серозной цистаденокарциномы яичника (OV), феохромоцитомы и параганглиомы (PCPG), аденокарцинома предстательной железы (PRAD), меланомы кожи (SKCM), аденокарциномы желудка.
В некоторых вариантах осуществления способы дополнительно предусматривают отнесение мутантного гена опухоли к категории пассажирских генов. Отнесение мутантного гена опухоли к категории пассажирских генов, может предусматривать отбор мутантного гена опухоли и сопоставление мутантного гена со структурированным набором данных, охватывающим пассажирские гены, определенные в соответствии с индексом пассажирских генов. Индекс пассажирских генов может предусматривать коэффициент корреляции между долей образцов, содержащих мутантный ген, полученных от когорты пациентов с раком, и медианным числом мутантных генов для каждого типа опухоли в когорте пациентов с раком.
Если пациента с раком относят к категории респондеров на иммунотерапию, то способ может дополнительно предусматривать проведение курса иммунотерапии у пациента с раком. В некоторых вариантах осуществления курс иммунотерапии предусматривает введение пациенту ингибитора T-клеточного ингибиторного рецептора или рецептора на опухолевой клетке. В некоторых вариантах осуществления ингибитор T-клеточного ингибиторного рецептора или рецептора на опухолевой клетке может предусматривать антитело или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления курс иммунотерапии предусматривает введение пациенту активатора T-клеточного рецептора, который стимулирует активацию T-клеток и пролонгирует иммунную цитолитическую активность.
В некоторых вариантах осуществления T-клеточные ингибиторные рецепторы или рецепторы, располагающиеся на опухолевой клетке, на которые можно целенаправленно воздействовать с помощью ингибиторов с целью иммунотерапии, предусматривают один или более из PD1, PDL1, CTLA4, LAG3 и TIM3. Таким образом, в некоторых вариантах осуществления ингибитор T-клеточного ингибиторного рецептора или рецептора на опухолевой клетке предусматривает антитело или его антигенсвязывающий фрагмент, которые специфически связываются с одним или более из PD1, PDL1, CTLA4, LAG3 и TIM3. В качестве части курса иммунотерапии пациенту с раком можно вводить антитело или его антигенсвязывающий фрагмент, которые специфически связываются с одним или более из PD1, PDL1, CTLA4, LAG3 и TIM3, или можно вводить любую комбинацию из двух или более таких антител или их антигенсвязывающих фрагментов.
В некоторых вариантах осуществления курс иммунотерапии предусматривает введение пациенту антитела, которое связывается с PD1. В некоторых предпочтительных вариантах осуществления антитело, которое связывается с PD1, содержит по меньшей мере последовательность вариабельного участка тяжелой цепи (HCVR) под SEQ ID NO:21 и последовательность вариабельного участка легкой цепи (LCVR) под SEQ ID NO:22. В некоторых вариантах осуществления любое из антител или их антигенсвязывающих фрагментов, которые связывают PD1, может представлять собой любое из антител или их антигенсвязывающих фрагментов, описанных в заявке на патент США № 14/603776 (публикация № US 2015-0203579), которая тем самым включена в данный документ посредством ссылки. Например, в некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с PD1, содержат HCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 1, и LCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с PD1, содержат LCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 1, и HCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с PD1, содержат пару HCVR и LCVR, которая показана в таблице 1. Можно использовать другие антитела, которые связываются с PD1 (или их антигенсвязывающие фрагменты), и они включают без ограничения пембролизумаб, ниволумаб, дурвалумаб, атезолизумаб, пидилизумаб, камрелизумаб, PDR001, MED10680, JNJ-63723283 и MCLA-134.
SEQ ID NO:
SEQ ID NO:
SEQ ID NO:
SEQ ID NO:
В некоторых вариантах осуществления курс иммунотерапии предусматривает введение пациенту антитела, которое связывается с белком LAG3 (также известным как CD223). В некоторых вариантах осуществления антитело, которое связывается с LAG3, содержит по меньшей мере последовательность HCVR под SEQ ID NO:93 и последовательность LCVR под SEQ ID NO:94. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, которые связывают LAG3, могут представлять собой любые из антител или их антигенсвязывающих фрагментов, описанных в заявке на патент США № 15/289032 (публикация № US 2017-0101472), которая тем самым включена в данный документ посредством ссылки. Например, в некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с LAG3, содержат HCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 2, и LCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с LAG3, содержат LCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 2, и HCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с LAG3, содержат пару HCVR и LCVR, которая показана в таблице 2. Можно использовать другие антитела, которые связываются с LAG3 (или их антигенсвязывающие фрагменты), и они включают без ограничения BMS-986016 и GSK2381781.
SEQ ID NO:
SEQ ID NO:
SEQ ID NO:
SEQ ID NO:
В некоторых вариантах осуществления курс иммунотерапии предусматривает введение пациенту антитела, которое связывается с PDL1. В некоторых предпочтительных вариантах осуществления антитело, которое связывается с PDL1, содержит по меньшей мере последовательность HCVR под SEQ ID NO:122 и последовательность LCVR под SEQ ID NO:123. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, которые связывают PDL1, могут представлять собой любые из антител или их антигенсвязывающих фрагментов, описанных в заявке на патент США № 14/603808 (публикация № US 2015-0203580), которая тем самым включена в данный документ посредством ссылки. Например, в некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с PDL1, содержат HCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 3, и LCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с PDL1, содержат LCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 3, и HCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с PDL1, содержат пару HCVR и LCVR, которая показана в таблице 3. Можно использовать другие антитела, которые связываются с PDL1 (или их антигенсвязывающие фрагменты), и они включают без ограничения одно или более из авелумаба, атезолизумаба и дурвалумаба.
SEQ ID NO:
SEQ ID NO:
SEQ ID NO:
SEQ ID NO:
В некоторых вариантах осуществления курс иммунотерапии предусматривает введение пациенту антитела, которое связывается с CTLA4. В некоторых вариантах осуществления антитела или их антигенсвязывающие фрагменты, которые связывают CTLA4, могут представлять собой любые из антител или их антигенсвязывающих фрагментов, описанных в предварительной заявке на патент США № 62/537753, поданной 27 июля 2017 г., которая тем самым включена в данный документ посредством ссылки. Например, в некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с CTLA4, содержат HCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 4, и LCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с CTLA4, содержат LCVR, характеризующийся аминокислотной последовательностью, выбранной из последовательностей, перечисленных в таблице 4, и HCVR. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, которые связываются с CTLA4, содержат пару HCVR и LCVR, которая показана в таблице 4. Можно использовать другие антитела, которые связываются с CTLA4 (или их антигенсвязывающие фрагменты), и они включают без ограничения одно или более из ипилимумаба и тремелимумаба, а также любое из антител или их антигенсвязывающих фрагментов, раскрытых в патентах США №№ 6984720; 7605238 или 7034121, все из которых тем самым включены в данный документ посредством ссылки.
В некоторых вариантах осуществления курс иммунотерапии может предусматривать введение пациенту комбинации одного или более ингибиторов T-клеточного ингибиторного рецептора. Комбинация может предусматривать комбинацию антител, или комбинацию антигенсвязывающих частей таких антител, или комбинацию антител и антигенсвязывающих частей. Таким образом, например, курс иммунотерапии может предусматривать введение пациенту антитела, которое связывается с PD1, в комбинации со вторым курсом иммунотерапии, в частности с антителом, которое связывается с LAG3, или антителом, которое связывается с PDL1, или антителом, которое связывается с CTLA. Курс иммунотерапии может предусматривать введение пациенту антитела, которое связывается с PDL1, в комбинации со вторым курсом иммунотерапии, в частности с антителом, которое связывается с LAG3, или антителом, которое связывается с PD1, или антителом, которое связывается с CTLA. Курс иммунотерапии может предусматривать введение пациенту антитела, которое связывается с LAG3, в комбинации со вторым курсом иммунотерапии, в частности с антителом, которое связывается с PD1, или антителом, которое связывается с PDL1, или антителом, которое связывается с CTLA. Курс иммунотерапии может предусматривать введение пациенту антитела, которое связывается с CTLA4, в комбинации со вторым курсом иммунотерапии, в частности антителом, которое связывается с LAG3, или антителом, которое связывается с PDL1, или антителом, которое связывается с PD1. Антитело, которое связывается с PD1, может предусматривать любое антитело или антигенсвязывающий домен, описанные или приведенные в качестве примера в данном документе. Антитело, которое связывается с PD1, может предусматривать любое антитело или антигенсвязывающий домен, описанные или приведенные в качестве примера в данном документе. Антитело, которое связывается с PDL1, может предусматривать любое антитело или антигенсвязывающий домен, описанные или приведенные в качестве примера в данном документе. Антитело, которое связывается с LAG3, может предусматривать любое антитело или антигенсвязывающий домен, описанные или приведенные в качестве примера в данном документе. Антитело, которое связывается с CTLA4, может предусматривать любое антитело или антигенсвязывающий домен, описанные или приведенные в качестве примера в данном документе.
В некоторых предпочтительных вариантах осуществления курс иммунотерапии предусматривает введение пациенту комбинации антитела или его антигенсвязывающей части, которые связываются с PD1, и антитела или его антигенсвязывающей части, которые связываются с LAG3. В некоторых предпочтительных вариантах осуществления антитело, которое связывается с PD1, содержит по меньшей мере последовательность вариабельного участка тяжелой цепи (HCVR) под SEQ ID NO:21 и последовательность вариабельного участка легкой цепи (LCVR) под SEQ ID NO:22 и антитело, которое связывается с LAG3, содержит по меньшей мере последовательность HCVR под SEQ ID NO:93 и последовательность LCVR под SEQ ID NO:94.
В некоторых предпочтительных вариантах осуществления курс иммунотерапии предусматривает введение пациенту комбинации антитела или его антигенсвязывающей части, которые связываются с PDL1, и антитела или его антигенсвязывающей части, которые связываются с LAG3. В некоторых предпочтительных вариантах осуществления антитело, которое связывается с PDL1, содержит по меньшей мере последовательность вариабельного участка тяжелой цепи (HCVR) под SEQ ID NO:122 и последовательность вариабельного участка легкой цепи (LCVR) под SEQ ID NO:123 и антитело, которое связывается с LAG3, содержит по меньшей мере последовательность HCVR под SEQ ID NO:93 и последовательность LCVR под SEQ ID NO:94.
В некоторых вариантах осуществления иммунотерапевтическое средство может представлять собой любое из известных иммунотерапевтических средств, используемых для лечения рака. Например, иммунотерапевтическое средство может представлять собой цемиплимаб, ниволумаб, пембролизумаб, атезолизумаб, дурвалумаб, авелумаб, ипилимумаб, IFN-альфа, IL-2 или их комбинацию. В некоторых вариантах осуществления иммунотерапевтическое средство может представлять собой ингибитор иммунной контрольной точки, описанный в тексте данного документа, или такие средства, которые хорошо известны в данной области техники. Например, цемиплимаб, ниволумаб, пембролизумаб, атезолизумаб, дурвалумаб, авелумаб являются известными ингибиторами иммунных контрольных точек.
В некоторых альтернативных вариантах осуществления курс иммунотерапии предусматривает введение пациенту активатора T-клеточного активирующего рецептора. В некоторых предпочтительных вариантах осуществления T-клеточный активирующий рецептор, на который можно целенаправленно воздействовать с помощью иммунотерапевтических активаторов, предусматривает один или более из CD28, CD40L, ICOS и 4-1BB.
Пример подхода, предназначенного для определения общей нагрузки пассажирскими генными мутациями для опухоли у пациента с раком показан на фиг. 2 и фиг. 3. Генетический образец может быть отобран/получен (202). Генетический образец может представлять собой образец от пациента с раком. Генетический образец может быть получен из опухоли пациента с раком. Генетический образец можно подвергать секвенированию с получением в результате данных о генетической последовательности.
В некоторых вариантах осуществления данные о последовательности могут быть получены или собраны с помощью любого способа, описанного в данном документе. Например, данные о последовательности могут быть получены непосредственно путем проведения процесса секвенирования образца. В качестве альтернативы или дополнительно данные о последовательности могут быть получены опосредованно, например, от третьей стороны, из базы данных и/или публикации. В некоторых вариантах осуществления данные о последовательности получают с помощью компьютерной системы, например, из устройства для хранения данных или из отдельной компьютерной системы.
В некоторых вариантах осуществления данные о последовательности могут представлять собой массив данных о последовательности. Термины «массовое секвенирование», или «секвенирование следующего поколения», или «массовое параллельное секвенирование» относится к любой технологии высокопроизводительного секвенирования, при которой процессы секвенирования ДНК и/или РНК осуществляются параллельно. Например, способы массового секвенирования, как правило, способны обеспечивать получение более одного миллиона ампликонов полинуклеиновой кислоты в одном анализе. Термины «массовое секвенирование», «массовое параллельное секвенирование» и «секвенирование следующего поколения» относятся только к общим способам, необязательно предусматривающим получение более 1 миллиона маркерных последовательностей за один цикл. Любой способ массового секвенирования может быть реализован в раскрытых способах и системах, как, например секвенирование с использованием химии обратимых терминаторов (например, Illumina), пиросеквенирование с использованием эмульсионных капель с полониями (например, Roche), ионное полупроводниковое секвенирование (IonTorrent), одномолекулярное секвенирование (например, Pacific Biosciences), массивно-параллельное опознавательное секвенирование и т. д.
В некоторых вариантах осуществления данные о последовательности можно получать посредством любого способа секвенирования, известного в данной области техники. Например, в некоторых вариантах осуществления данные секвенирования получают с использованием секвенирования по методике терминации цепи, секвенирования путем лигирования, секвенирования путем синтеза, пиросеквенирования, ионного полупроводникового секвенирования, одномолекулярного секвенирования в режиме реального времени, секвенирования с использованием меток, секвенирования Dilute-`N`-Go и/или секвенирования 454.
В некоторых вариантах осуществления данные о последовательности являются результатом осуществления способа, в ходе которого осуществляют способ амплификации нуклеиновых кислот для амплификации по меньшей мере части одного или более геномного локуса или транскрипта с последующим секвенированием полученного продукта амплификации. Примеры способов амплификации нуклеиновых кислот, применимых в реализации способов, раскрытых в данном документе, включают без ограничения полимеразную цепную реакцию (ПЦР), LATE-PCR, лигазную цепную реакцию (LCR), амплификацию с вытеснением цепи (SDA), амплификацию, опосредованную транскрипцией (TMA), самоподдерживающуюся репликацию последовательности (3SR), амплификацию c репликазой Qβ, амплификацию на основе последовательности нуклеиновой кислоты (NASBA), репаративную цепную реакцию (RCR), амплификацию ДНК по методу бумеранга (BDA) и/или амплификацию по типу катящегося кольца (RCA).
В некоторых вариантах осуществления способ включает стадию проведения процесса секвенирования образца. Можно использовать любой образец при условии, что образец содержит ДНК и/или РНК из опухоли пациента. Источником образца может служить, например, плотная ткань, как, например, полученная из свежего, замороженного и/или подвергнутого консервации органа, образца ткани, биоптата или аспирата; кровь или любые составляющие компоненты крови, сыворотка крови, цельная кровь; физиологические жидкости, такие как спинномозговая жидкость, амниотическая жидкость, перитонеальная жидкость или интерстициальная жидкость.
Данные о генетической последовательности можно анализировать (204) посредством вычислительного устройства для идентификации драйверных генов и для определения числа мутаций в драйверных генах. Если число мутаций в драйверных генах является высоким (206), то это может быть показателем того, что пациент будет отвечать на иммунотерапию (210). Если число мутаций в драйверных генах является низким (206), то это может быть показателем того, что ответ на иммунотерапию будет слабым или будет отсутствовать (208). Мутации в драйверных генах могут обеспечивать «ключевые фенотипические признаки рака», например ускользание от иммунного ответа.
В альтернативном варианте осуществления данные о генетической последовательности можно анализировать (212) посредством вычислительного устройства для идентификации пассажирских генов и для определения числа мутаций в пассажирских генах. Если число мутаций в пассажирских генах является высоким (216), то это может быть показателем (210) того, что пациент будет отвечать на иммунотерапию. Если число мутаций в пассажирских генах является низким (216), то это может быть показателем (208) того, что ответ на иммунотерапию будет слабым или будет отсутствовать. Хотя пассажирские гены не имеют какой-либо причинной связи c онкогенезом, мутации в пассажирских генах можно использовать для оценки иммуногенности. В некоторых вариантах осуществления данные о генетической последовательности можно анализировать (212) для идентификации пассажирских генов, определения числа мутаций в пассажирских генах и определения фонового распределения для мутационной нагрузки опухоли. Число мутаций в пассажирских генах можно анализировать относительно фонового распределения для определения того, на сколько стандартных отклонений (если вообще отличается) число мутаций в пассажирских генах отличается от среднего значения. Если число стандартных отклонений является высоким (например, по меньшей мере 1, 1,5, 2, 2,5) (216), то пациента с раком можно отнести к категории респондеров с наилучшим ответом на иммунотерапию (210). Если число стандартных отклонений является низким (216), то пациента с раком можно отнести к категории респондеров со слабым ответом на иммунотерапию (208).
В некоторых вариантах осуществления пассажирские гены можно идентифицировать в широкомасштабном анализе ракового генома в соответствии с критерием, названном в данном документе как индекс пассажирских генов (PGI) (212). В некоторых вариантах осуществления PGI основан на высокой корреляции показателей частоты появления генетических мутаций (GMR) в пассажирских генах c показателями общей частоты появления мутаций при раке, также называемыми мутационной нагрузкой опухоли (214). Среди идентифицированных пассажирских генов преобладают семейства, известные избыточным количеством пассажирских мутаций, как, например, особо крупные белки и гены с низким уровнем экспрессии или с поздним временем репликации ДНК. Накопление большего количества пассажирских генных мутаций будет иметь место в образцах/типах рака, характеризующихся более высокими показателями частоты появления мутаций, при этом среднее число мутантных генов на образец при каждом типе рака может выступать в качестве суррогатного показателя для вероятности появления пассажирских мутаций при данном типе рака. Таким образом, для каждого гена Xi PGI может быть определен как показатель корреляции между процентной долей образцов с мутацией гена Xi и средним числом мутантных генов на образец при каждом типе рака. Более высокий PGI указывает на то, что конкретный ген с большей вероятностью приобретет соматические мутации при типах рака, характеризующихся более высокой общей частотой появления мутаций. Гены с низким значением PGI демонстрируют слабую ассоциацию между двумя переменными (что, например, можно наблюдать в случае канонических раковых драйверных генов, таких как TP53, PIK3CA и KRAS). Среди генов, характеризующихся наивысшим PGI, преобладают семейства генов, известные избыточным количеством пассажирских мутаций, например, особо крупные белки (>4000 аминокислот), гены, охватывающие большие геномные локусы (>1 Мб), гены с низким уровнем экспрессии, гены с поздним временем репликации ДНК и т. п. Интегральная функция распределения (CDF) для данных семейств генов демонстрирует резкую тенденцию к повышению при PGI>0,7, в то время как гены в каталоге соматических мутаций при раке (COSMIC) из реестра генов рака (CGC) характеризуются более равномерным распределением. Двухвыборочные тесты Колмогорова-Смирнова демонстрируют значимое различие в ранговом распределении семейств пассажирских генов по сравнению с таким распределением для генов из CGC (p=8,3×10-19 для крупных белков; p=2,9×10-12 для генов, охватывающих геномный локус >1 Мб; p=6,4×10-35 для генов с низким уровнем экспрессии; p=2,7×10-29 для генов с поздней репликацией). Подобные результаты получают при группировке образцов по показателю частоты появления мутаций (вместо типа рака) для вычисления PGI.
Наиболее значимые пассажирские гены на основе их наивысших значений PGI могут являться нейтральными по отношению к типу опухоли или специфичными для каждого типа опухоли. Таким образом, в некоторых случаях наиболее значимые пассажирские гены можно использовать в общем независимо от типа опухоли. Хотя данные наиболее значимые пассажирские гены не изменяются независимо от типа опухоли, наиболее значимые пассажирские гены могут изменяться со временем из-за доступности дополнительных образцов. В некоторых случаях наиболее значимые пассажирские гены могут изменяться среди типов опухолей. В некоторых случаях наиболее значимые пассажирские гены могут являться идентичными среди типов опухолей. Кроме того, если наиболее значимые пассажирские гены являются идентичными среди типов опухолей, то ранжирование в пределах данного перечня наиболее значимых пассажирских генов может варьировать. Например, наиболее значимые 50 пассажирских генов для рака молочной железы могут быть идентичными наиболее значимым 50 пассажирским генам для рака легкого, однако занимающий первое место пассажирский ген (что означает наивысший PGI) для рака молочной железы может быть пассажирским геном для рака легкого, занимающим пятое место. В некоторых случаях наиболее значимые 50 пассажирских генов для одного типа опухоли могут включать 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50 и до 100 процентов включительно наиболее значимых 50 пассажирских генов для второго типа опухоли. В зависимости от того, какой предусмотрен диапазон значений PGI, перечень наиболее значимых 25, 50, 100, 150, 200, 250, 300, 350, 400, 450, 500 или даже свыше 2000 пассажирских генов может быть представлен в качестве перечня наиболее значимых пассажирских генов. В некоторых случаях наиболее значимые пассажирские гены неизменны среди пациентов. Для всех пациентов можно использовать один и тот же перечень пассажирских генов, и при этом каждый пациент будет иметь разную TMB.
В одном варианте осуществления, проиллюстрированном на фиг. 3, раскрыт способ (300), предусматривающий получение данных о генетической последовательности (310). Данные о генетической последовательности могут охватывать множество генов и могут быть получены из множества биологических образцов, отобранных у субъектов со множеством типов заболеваний. Множество типов заболеваний может предусматривать виды рака.
В некоторых вариантах осуществления способ (300) может предусматривать идентификацию множества мутантных генов для каждого множества биологических образцов (320), где каждый из мутантных генов содержит генетическую последовательность, характеризующуюся присутствием по меньшей мере одной несинонимичной соматической мутации.
В некоторых вариантах осуществления с помощью способа (300) можно определять мутационную нагрузку опухоли для каждого биологического образца исходя из числа мутантных генов в каждом биологическом образце (330). В предпочтительном варианте осуществления определение мутационной нагрузки опухоли для каждого биологического образца, исходя из числа мутантных генов в каждом биологическом образце, может предусматривать сложение числа мутантных генов в каждом образце от пациента.
С помощью способа (300) можно идентифицировать мутации в гене (пассажирском или драйверном), например, путем выравнивания мутантных последовательностей с последовательностями дикого типа или эталонными последовательностями. Различные программы и алгоритмы выравнивания описаны в Smith and Waterman (1981) Adv. Appl. Math. 2:482; Needleman and Wunsch (1970) J. Mol. Biol. 48:443; Pearson and Lipman (1988) Proc. Natl. Acad. Sci. USA 85:2444; Higgins and Sharp (1988) Gene 73:237-244; Higgins and Sharp (1989) CABIOS 5:151-153; Corpet et al. (1988) Nucl. Acids Res. 16:10881-90; Huang et al. (1992) Computer Appl. in the Biosci. 8:155-65 и Pearson et al. (1994). Meth. Mol. Biol. 24:307-31, которые включены в данный документ посредством ссылки. В Altschul et al. (1994) Nature Genet. 6:119-29 (включенной в данный документ посредством ссылки) представлено подробное рассмотрение способов выравнивания последовательностей и расчетов гомологии.
Средство поиска основного локального выравнивания (BLAST) NCBI (Altschul et al. 1990) доступно из нескольких источников, в том числе из Национального центра биологической информации (NCBI, Бетесда, Мэриленд) и в сети интернет, для применения в сочетании с программами для анализа последовательностей blastp, blastn, blastx, tblastn и tblastx. Доступ к нему можно получить по адресу <//www.ncbi.nlmn.ih.gov/BLAST/>. Описание того, как определять идентичность последовательности с помощью данной программы, доступно по адресу <//www.nebi.rlm.nih.gov/BLAST/blast-help.html>.
В некоторых вариантах осуществления для каждого типа заболевания способ (300) может предусматривать определение средней мутационной нагрузки опухоли для множества мутантных генов во множестве биологических образцов исходя из установленного числа мутантных генов в каждом биологическом образце (340). В предпочтительном варианте осуществления определение средней мутационной нагрузки опухоли для множества мутантных генов во множестве биологических образцов, исходя из определенного числа мутантных генов в каждом биологическом образце, может предусматривать сложение показателей мутационной нагрузки опухоли для каждого образца от пациента и деление этой суммы на число образцов от пациентов для каждого типа заболевания.
В некоторых вариантах осуществления для каждого мутантного гена и каждого типа заболевания способ (300) может предусматривать определение доли биологических образцов, содержащих мутантный ген (350).
В некоторых вариантах осуществления для каждого мутантного гена способ (300) может предусматривать определение коэффициента корреляции между средней мутационной нагрузкой опухоли и долей биологических образцов, содержащих мутантный ген (360).
В некоторых вариантах осуществления способ (300) может предусматривать определение того, является ли мутантный ген пассажирским геном исходя из коэффициента (370) корреляции. Более высокий коэффициент корреляции указывает на то, что конкретный ген с большей вероятностью приобретет соматические мутации при типах рака c более высокой общей частотой появления мутаций (например, пассажирский ген), тогда как более низкий коэффициент корреляции указывает на то, что конкретный ген c меньшей вероятностью приобретет соматические мутации при типах рака, характеризующихся более высокой общей частотой появления мутаций (например, ген, не являющийся пассажирским).
В альтернативном варианте осуществления способ (300) может дополнительно предусматривать создание перечня мутантных генов, идентифицированных в качестве пассажирских генов. В определенном аспекте предпочтительного варианта осуществления перечень может представлять профиль иммуногенности для выбранного заболевания.
В некоторых вариантах осуществления, проиллюстрированных на фиг. 4, раскрыт способ отбора пациента для противораковой терапии (400), предусматривающий определение множества пассажирских генов, присутствующих в образце опухоли пациента с заболеванием (410).
В некоторых вариантах осуществления способ (400) может предусматривать сравнение множества пассажирских генов с профилем иммуногенности для заболевания (420). В предпочтительном варианте осуществления профиль иммуногенности можно получать путем выполнения стадий, предусматривающих получение данных о генетической последовательности, где данные о генетической последовательности охватывают множество генов и получены для множества биологических образцов, отобранных у субъектов, имеющих множество типов заболеваний, идентификацию множества мутантных генов для каждого из множества биологических образцов, где каждый из мутантных генов содержит генетическую последовательность, имеющую по меньшей мере одну не являющуюся синонимичной соматическую мутацию, определение мутационной нагрузки опухоли для каждого биологического образца исходя из числа мутантных генов в каждом биологическом образце для каждого типа заболевания, определение средней мутационной нагрузки опухоли для множества мутантных генов во множестве биологических образцов исходя из определенного числа мутантных генов в каждом биологическом образце для каждого мутантного гена и каждого типа заболевания, определение доли биологических образцов, содержащих мутантный ген, для каждого мутантного гена, определение коэффициента корреляции между средней мутационной нагрузкой опухоли и долей биологических образцов, содержащих мутантный ген. В некоторых вариантах осуществления мутантный ген может быть определен как пассажирский ген на основе коэффициента корреляции. Более высокий коэффициент корреляции указывает на то, что конкретный ген с большей вероятностью приобретет соматические мутации при типах рака с более высокой общей частотой появления мутаций (например, пассажирский ген), тогда как более низкий коэффициент корреляции указывает на то, что конкретный ген c меньшей вероятностью приобретет соматические мутации при типах рака, характеризующихся более высокой общей частотой появления мутаций (например, ген, не являющийся пассажирским).
Может быть создан перечень мутантных генов, идентифицированных в качестве пассажирских генов, при этом перечень представляет собой профиль иммуногенности для выбранного заболевания. В предпочтительном варианте осуществления определение мутационной нагрузки опухоли для каждого биологического образца, исходя из числа мутантных генов в каждом биологическом образце, может предусматривать сложение числа мутантных генов в каждом образце от пациента. В предпочтительном варианте осуществления определение средней мутационной нагрузки опухоли для множества мутантных генов во множестве биологических образцов, исходя из определенного числа мутантных генов в каждом биологическом образце, может предусматривать сложение показателей мутационной нагрузки опухоли для каждого образца от пациента и деление этой суммы на число образцов от пациентов для каждого типа заболевания.
В некоторых вариантах осуществления PGI может использоваться для идентификации пассажирских генов для конкретных видов рака, а затем с использованием показателя TMB для пассажирских генов можно идентифицировать пациентов, которые являются респондерами на конкретные средства для лечения, как, например, без ограничения на антитело к PD-1 или на комбинацию антитела к PD-1 и другого противоракового терапевтического средства. TMB для пассажирских генов также можно использовать для идентификации респондеров на другие антитела, предназначенные для лечения рака, такие как без ограничения антитело к CD20 (хронический лимфоцитарный лейкоз), антитело к HER2 (рак молочной железы), антитело к EGFR (колоректальный рак и рак головы и шеи), антитело к CD19 (виды В-клеточного рака) и антитело к CD20 (лимфома), или на комбинации антитела, предназначенного для лечения, и другого противоракового терапевтического средства. В некоторых вариантах осуществления другое средство противораковой терапии может представлять собой химиотерапевтическое средство, иммуномодулирующее средство (например, второе антитело, цитокин), лучевую терапию или хирургическое вмешательство.
В некоторых вариантах осуществления сравнение множества пассажирских генов с профилем иммуногенности для заболевания может предусматривать определение числа совпадений между множеством мутантных генов и перечнем мутантных генов в профиле.
В некоторых вариантах осуществления, если множество пассажирских генов совпадает с профилем иммуногенности для заболевания (430), то с помощью способа (400) можно идентифицировать пациента в качестве кандидата для иммунотерапии.
В некоторых вариантах осуществления, если множество пассажирских генов не совпадает с профилем иммуногенности для заболевания (440), то с помощью способа (400) можно идентифицировать пациента как не являющегося кандидатом для иммунотерапии.
В альтернативном варианте осуществления способ (400) может дополнительно предусматривать включение пациента в программу иммунотерапии в том случае, если пациент был идентифицирован в качестве кандидата для иммунотерапии.
Раскрытые иммунотерапевтические средства можно использовать в комбинации с другим антителом или его антигенсвязывающими фрагментами, а также с другими противораковыми терапевтическими средствами. Средства комбинированной терапии можно вводить одновременно или последовательно. В некоторых вариантах осуществления два или более терапевтических средств могут быть составлены вместе с фармацевтически приемлемым носителем для получения в результате фармацевтической композиции. В некоторых вариантах осуществления два или более терапевтических средств составляются по отдельности с фармацевтически приемлемым носителем для получения в результате двух или более фармацевтических композиций. Под «фармацевтически приемлемым» подразумевают материал или носитель, который может быть выбран для сведения к минимуму любой деградации активного ингредиента и для сведения к минимуму любых неблагоприятных побочных эффектов у субъекта, как это будет хорошо известно специалисту в данной области техники. Примеры носителей включают димиристоилфосфатидил (DMPC), фосфатно-буферный солевой раствор или мультивезикулярную липосому. Например, в качестве носителей в настоящем изобретении можно использовать PG:PC:холестерин:пептид или PC:пептид. Другие подходящие фармацевтически приемлемые носители и составы на их основе описаны в Remington: The Science and Practice of Pharmacy (19th ed.) ed. A.R. Gennaro, Mack Publishing Company, Easton, PA 1995. Как правило, в составе используют соответствующее количество фармацевтически приемлемой соли, необходимое для придания изотоничности составу. Другие примеры фармацевтически приемлемого носителя включают без ограничения солевой раствор, раствор Рингера и раствор декстрозы. Значение pH раствора может составлять от приблизительно 5 до приблизительно 8 или от приблизительно 7 до приблизительно 7,5. Дополнительные носители включают препараты с замедленным высвобождением, такие как полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие композицию, при этом матрицы представлены в форме формованных изделий, например, пленок, стентов (которые имплантируют в сосуды в ходе процедуры ангиопластики), липосом или микрочастиц. Для специалистов в данной области техники будет очевидно, что некоторые носители могут являться более предпочтительными в зависимости, например, от пути введения и концентрации вводимой композиции. Они чаще всего будут представлять собой стандартные носители, предназначенные для введения лекарственных средств людям, в том числе такие растворы, как стерильная вода, солевой раствор и забуференные растворы с физиологическим значением pH.
Фармацевтические композиции также могут включать носители, загустители, разбавители, буферы, консерванты и т. п. при условии того, что предполагаемая активность иммунотерапевтического средства по настоящему изобретению не ухудшится. Фармацевтические композиции также могут включать один или более активных ингредиентов (в дополнение к композиции по настоящему изобретению), таких как противомикробные средства, противовоспалительные средства, анестетики и т. п. Фармацевтическую композицию можно вводить с помощью ряда способов в зависимости от того, требуется местное или системное лечение, и в зависимости от участка, подлежащего лечению.
Препараты для парентерального введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, как, например, оливковое масло, и инъекционные органические сложные эфиры, как, например, этилолеат. Водные носители включают воду, спиртовые/водные растворы, эмульсии или суспензии, в том числе физиологический солевой раствор и забуференные среды. Среды-носители для парентерального введения включают раствор хлорида натрия, раствор Рингера с декстрозой, декстрозу и хлорид натрия, раствор Рингера с лактатом или нелетучие масла. Среды-носители для внутривенного введения включают растворы для восполнения жидкостей и питательных веществ, растворы для восполнения электролитов (как, например, растворы на основе раствора Рингера с декстрозой) и т. п. Также могут присутствовать консерванты и другие добавки, такие как, например, противомикробные вещества, антиоксиданты, хелатирующие средства и инертные газы и т. п.
Составы для глазного введения могут включать мази, лосьоны, кремы, гели, капли, суппозитории, спреи, жидкости и порошки. Могут быть необходимы или желательны традиционные фармацевтический носители, водные, порошкообразные или масляные основы, загустители и т. п.
Композиции для перорального введения включают порошки или гранулы, суспензии или растворы в воде или неводных средах, капсулы, саше или таблетки. Могут потребоваться загустители, ароматизаторы, разбавители, эмульгаторы, диспергирующие средства или связующие. Некоторые из композиций потенциально можно вводить в виде фармацевтически приемлемой соли присоединения кислоты или основания, образованной путем реакции с неорганическими кислотами, с такими как хлористоводородная кислота, бромистоводородный кислота, перхлорная кислота, азотная кислота, тиоциановая кислота, серная кислота и фосфорная кислота, и с органическими кислотами, такими как муравьиная кислота, уксусная кислота, пропионовая кислота, гликолевая кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота и фумаровая кислота, или путем реакции с неорганическим основанием, таким как гидроксид натрия, гидроксид аммония, гидроксид калия, и с органическими основаниями, такими как моно-, ди-, триалкил- и ариламины и замещенные этаноламины.
Фармацевтические композиции по настоящему изобретению, подходящие для инъекционного использования, включают стерильные водные растворы или дисперсии. Кроме того, композиции могут быть в форме стерильных порошков, предназначенных для экстемпорального приготовления стерильных инъекционных растворов или дисперсий. Как правило, конечная инъекционная форма должна быть стерильной и должна характеризоваться соответствующим уровнем текучести, чтобы обеспечивать возможность введения через шприц. Фармацевтические композиции должны быть стабильными в условиях изготовления и хранения; таким образом, предпочтительно они должны быть защищены от контаминирующего действия микроорганизмов, таких как бактерии и грибы. Носителем может быть растворитель или дисперсионная среда содержащая, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль), растительные масла и их подходящие смеси.
Например, можно получать инъекционные растворы, в которых носитель представляет собой солевой раствор, раствор глюкозы или смесь физиологического солевого раствора и раствора глюкозы. Можно также получать инъекционные суспензии, в случае которых можно использовать подходящие жидкие носители, суспендирующие средства и т. п. Также включены препараты в твердой форме, которые предназначены для превращения непосредственно перед применением в препараты в жидкой форме.
Препараты для парентерального введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, как, например, оливковое масло, и инъекционные органические сложные эфиры, как, например, этилолеат. Водные носители включают воду, спиртовые/водные растворы, эмульсии или суспензии, в том числе физиологический солевой раствор и забуференные среды. Среды-носители для парентерального введения включают раствор хлорида натрия, раствор Рингера с декстрозой, декстрозу и хлорид натрия, раствор Рингера с лактатом или нелетучие масла. Среды-носители для внутривенного введения включают растворы для восполнения жидкостей и питательных веществ, растворы для восполнения электролитов (как, например, растворы на основе раствора Рингера с декстрозой) и т. п. Также могут присутствовать консерванты и другие добавки, такие как, например, противомикробные вещества, антиоксиданты, хелатирующие средства и инертные газы и т. п.
Фармацевтические композиции по настоящему изобретению могут быть в форме, подходящей для местного применения, в такой как, например, аэрозоль, крем, мазь, лосьон, присыпка, ополаскиватели для полости рта, ополаскиватели для горла и т. п. Кроме того, композиции могут быть в форме, подходящей для применения в трансдермальных устройствах. Такие составы можно получать с использованием соединения по настоящему изобретению или его фармацевтически приемлемых солей с помощью традиционных технологических способов. В качестве примера крем или мазь получают путем смешивания гидрофильного материала и воды вместе с соединением в количестве, составляющем от приблизительно 5 вес. % до приблизительно 10 вес. %, с получением крема или мази, характеризующихся требуемой консистенцией.
В композициях, подходящих для чрескожного введения, носитель необязательно предусматривает средство, усиливающее проникновение, и/или подходящее смачивающее средство, необязательно объединяемое с подходящими добавками любой природы в малых пропорциях, при этом добавки не оказывают существенного вредного воздействия на кожу. Указанные добавки могут облегчать накожное введение и/или могут быть применимы для получения необходимых композиций. Данные композиций можно вводить посредством разных средств, например, в виде трансдермального пластыря, в виде точечного нанесения, в виде мази.
Фармацевтические композиции по настоящему изобретению могут быть в форме, подходящей для ректального введения, где носитель является твердым. Предпочтительно, чтобы смесь была в форме суппозиториев с однократной дозой. Подходящие носители включают масло какао и другие материалы, обычно используемые в данной области техники. Суппозитории можно подходящим образом формировать путем предварительного смешивания композиции с размягченным или расплавленным носителем (носителями) с последующим охлаждением и формованием в формах.
В дополнение к вышеупомянутым ингредиентам, представляющим собой носители, описанные выше фармацевтические составы могут включать, если это необходимо, один или более дополнительных ингредиентов, представляющих собой носители, таких как разбавители, буферы, вкусоароматические средства, связующие, поверхностно-активные вещества, загустители, смазывающие средства, консерванты (в том числе антиоксиданты) и т. п. Кроме того, могут быть включены другие вспомогательные средства с целью придания изотоничности составу по отношению к крови предполагаемого реципиента. Композиции, содержащие раскрытое иммунотерапевтическое средство и/или его фармацевтически приемлемые соли, также можно получать в форме порошка или жидкого концентрата.
Точная дозировка и частота введения зависят от конкретного раскрытого пептида, продукта раскрытого способа получения, его фармацевтически приемлемой соли, сольвата или полиморфа, его гидрата, его сольвата, его полиморфа или его стереохимически изомерной формы; конкретного состояния, подлежащего лечению, и тяжести состояния, подлежащего лечению; от различных факторов, являющихся специфическими для анамнеза субъекта, которому вводят дозу, таких как возраст, вес, пол, степень нарушения и общее физическое состояние конкретного субъекта, а также от другого лекарственного препарата, который может принимать индивидуум; что хорошо известно специалистам в данной области техники. Кроме того, очевидно, что указанное эффективное суточное количество может быть уменьшено или увеличено в зависимости от ответа субъекта, подвергаемого лечению, и/или в зависимости от оценки лечащего врача, назначающего композиции.
В зависимости от режима введения фармацевтическая композиция будет содержать активный ингредиент в количестве от 0,05 до 99% по весу, предпочтительно от 0,1 до 70% по весу, более предпочтительно от 0,1 до 50% по весу и фармацевтически приемлемый носитель в количестве от 1 до 99,95% по весу, предпочтительно от 30 до 99,9% по весу, более предпочтительно от 50 до 99,9% по весу, при этом все количества в процентах приведены из расчета на общий вес композиции.
В иллюстративном варианте осуществления некоторые или все из способов и систем могут быть реализованы посредством одного или более компьютеров, как, например, компьютера (1001), проиллюстрированного на фиг. 10 и описанного ниже. В некоторых вариантах осуществления в раскрытых способах и системах может использоваться один или более компьютеров для выполнения одной или более функций в одном или более местоположениях. На фиг. 10 показана блок-диаграмма, демонстрирующая иллюстративную операционная среду, предназначенную для выполнения раскрытых способов. Данная иллюстративная операционная среда является лишь примером операционной среды и не предполагает каких-либо ограничений в отношении объема применения или функциональности архитектуры операционной среды. Также не следует истолковывать операционную среду как каким-либо образом зависящую от или требующую наличия любого из компонентов или их комбинации, показанных в иллюстративной операционной среде.
В некоторых вариантах осуществления способы и системы по настоящему изобретению могут функционировать с многочисленными другими средами или конфигурациями вычислительных систем общего назначения или специализированного назначения. Примеры хорошо известных вычислительных систем, сред и/или конфигураций, которые могут быть подходящими для использования с системами и способами, включают без ограничения персональные компьютеры, серверные компьютеры, портативные компьютеры и многопроцессорные системы. Дополнительные примеры включают компьютерные приставки, программируемую бытовую электронную технику, сетевые компьютеры, миникомпьютеры, суперкомпьютеры, распределенные вычислительные среды, которые содержат любые из вышеперечисленных систем или устройств и т. п.
В некоторых вариантах осуществления вычисление, предусматриваемое раскрытыми способами и системами, можно выполнять с помощью компонентов программного обеспечения. Раскрытые системы и способы могут быть описаны в общем контексте выполняемых компьютером команд, как, например, блоки программ, выполняемые одним или более компьютерами или другими устройствами. Как правило, блоки программ включают программный код, рутинные операции, программы, объекты, компоненты, структурированные наборы данных и т. д., которые выполняют конкретные задачи или обеспечивают реализацию конкретных типов абстрактных данных. Раскрытые способы также можно осуществлять на практике с помощью сетевых и распределенных вычислительных сред, в которых задачи выполняются устройствами дистанционной обработки данных, которые связаны посредством коммуникационной сети. В распределенной вычислительной среде блоки программ могут быть расположены как в локальной, так и в удаленной компьютерной среде хранения информации, в том числе в запоминающем устройстве.
Кроме того, специалисту в данной области техники будет понятно, что системы и способы, раскрытые в данном документе, могут быть реализованы посредством вычислительного устройства общего назначения в виде компьютера 1001. Компоненты компьютера 1001 могут предусматривать без ограничения один или более процессоров 1003, системную память 1012 и системную шину 1013, которая соединяет разные компоненты системы, в том числе один или более процессоров 1003 с системной памятью 1012. Система может использовать параллельную вычислительную обработку.
Системная шина 1013 представляет собой один или более из нескольких возможных типов шинных структур, в том числе шину памяти или контроллер памяти, периферийную шину, ускоренный графический порт или локальную шину с использованием любой из множества шинных архитектур. Шина 1013 и все шины, указанные в данном описании, могут быть также реализованы посредством проводного или беспроводного сетевого соединения, при этом каждая из подсистем, в том числе один или более процессоров 1003, запоминающее устройство 1004 большой емкости, операционная система 1005, программное обеспечение 1006 для PGI, данные 1007 о PGI, сетевой адаптер 1008, системная память 1012, интерфейс 1010 ввода/вывода, графический адаптер 1009, устройство 1011 отображения и интерфейс 1002 «пользователь-машина», может находиться в пределах одного или более удаленных вычислительных устройств 1014 a, b, c, находящихся в физически отделенных местоположениях, соединенных посредством шин данного типа, в результате чего реализуется полностью распределенная система.
Компьютер 1001, как правило, содержит ряд различных машиночитаемых носителей. Иллюстративные носители данных могут представлять собой любые доступные носители, доступ к которым осуществляется с помощью компьютера 1001, и они предусматривают, например, без ограничения как энергозависимые, так и энергонезависимые носители, съемные и несъемные носители. Системная память 1012 содержит машиночитаемые носители в виде энергозависимого запоминающего устройства, такого как запоминающее устройство с произвольным доступом (RAM), и/или энергонезависимого запоминающего устройства, такого как запоминающее устройство с постоянным доступом (ROM). Системная память 1012, как правило, содержит данные, как, например, данные о PGI 1007, и/или блоки программ, как, например, операционная система 1005 и программное обеспечение для PGI 1006, которые непосредственно доступны для одного или более процессоров 1003 и/или в данный момент подвергаются обработке с их помощью. Данные 1007 о PGI могут предусматривать данные об охвате и/или данные об ожидаемом охвате.
В некоторых вариантах осуществления компьютер 1001 также может содержать другой съемный/несъемный энергозависимый/энергонезависимый компьютерный носитель информации. В качестве примера на фиг. 10 показано запоминающее устройство 1004 большой емкости, которое может обеспечивать энергонезависимое хранение программного кода, машиночитаемых команд, структурированных наборов данных, блоков программ и других данных для компьютера 1001. Например, без ограничения запоминающее устройство 1004 большой емкости может представлять собой жесткий диск, съемный магнитный диск, съемный оптический диск, кассеты с магнитной лентой или другие магнитные запоминающие устройства, карты флэш-памяти, CD-ROM, универсальные цифровые диски (DVD) или другое оптическое запоминающее устройство, запоминающие устройства с произвольным доступом (RAM), запоминающие устройства с постоянным доступом (ROM), электрически стираемое программируемое постоянное запоминающее устройство (EEPROM) и т. п.
Необязательно любое число блоков программ может храниться на запоминающем устройстве 1004 большой емкости, в том числе в качестве примера операционная система 1005 и программное обеспечение 1006 для PGI. Как операционная система 1005, так и программное обеспечение 1006 для PGI (или какая-либо их комбинация) могут содержать элементы программ и программное обеспечение 1006 для PGI. Данные 1007 о PGI также могут храниться на запоминающем устройстве 1004 большой емкости. Данные 1007 о PGI могут храниться в любой одной или более баз данных, известных в данной области техники. Примеры таких баз данных включают DB2®, Microsoft® Access, Microsoft® SQL Server, Oracle®, mySQL, PostgreSQL и т. п. Базы данных могут быть централизованными или распределенными между несколькими системами.
В альтернативном варианте осуществления пользователь может вводить команды и информацию в компьютер 1001 с помощью устройства ввода данных (не показано). Примеры таких устройств ввода данных включают без ограничения клавиатуру, указательное устройство (например, «мышь»), микрофон, джойстик, сканер, устройства тактильного ввода, как, например, перчатки и другие покрывающие тело предметы и т. п. Эти и другие устройства ввода данных могут быть соединены с одним или более процессорами 1003 посредством интерфейса 1002 «пользователь-машина», которые соединены с системной шиной 1013, но могут быть соединены посредством другого интерфейса и шинных структур, таких как параллельный порт, игровой порт, порт IEEE 1394 (также известный как порт Firewire), последовательный порт или универсальная последовательная шина (USB).
В альтернативном варианте осуществления устройство 1011 отображения также может быть соединено с системной шиной 1013 посредством интерфейса, такого как графический адаптер 1009. Предполагается, что компьютер 1001 может иметь более одного графического адаптера 1009, и компьютер 1001 может иметь более одного устройства 1011 отображения. Например, устройство отображения может представлять собой монитор, LCD (жидкокристаллический дисплей) или проектор. В дополнение к устройству 1011 отображения другие периферийные устройства вывода могут предусматривать такие компоненты, как громкоговорители (не показаны) и принтер (не показан), которые могут быть соединены с компьютером 1001 посредством интерфейса 1010 ввода/вывода. Любая стадия и/или результат способов могут быть выведены в любой форме на устройство вывода. Такой выводимый результат может быть представлен в любой форме визуального представления, в том числе без ограничения в текстовой, графической, анимационной, звуковой, тактильной формах и т. п. Дисплей 1011 и компьютер 1001 могут быть частью одного устройства или отдельными устройствами.
Компьютер 1001 может функционировать в сетевой среде с использованием логических соединений с одним или более удаленными вычислительными устройствами 1014 a, b, c. В качестве примера удаленное вычислительное устройство может представлять собой персональный компьютер, портативный компьютер, смартфон, сервер, маршрутизатор, сетевой компьютер, одноранговое устройство или другой общий узел сети и т. д. Логические соединения между компьютером 1001 и удаленным вычислительным устройством 1014 a, b, c могут быть установлены посредством сети 1015, такой как локальная вычислительная сеть (LAN) и/или общая глобальная вычислительная сеть (WAN). Такие сетевые соединения могут быть осуществлены посредством сетевого адаптера 1008. Сетевой адаптер 1008 может быть реализован как в проводной, так и беспроводной средах. Такие сетевые среды являются традиционными и общеупотребительными для жилых помещений, офисов, компьютерных сетей масштаба предприятия, внутренних сетей и сети Интернет.
В целях иллюстрации прикладные программы и другие выполняемые компоненты программ, как, например, операционная система 1005, проиллюстрированы в данном документе в виде дискретных блоков, хотя понятно, что такие программы и компоненты находятся в различные моменты времени в разных компонентах памяти вычислительного устройства 1001 и их выполнение реализуется одним или более процессорами 1003 компьютера. В одном аспекте по меньшей мере часть программного обеспечения 1006 для PGI и/или данных 1007 о PGI может храниться на и/или выполняться в одном или более из вычислительного устройства 1001, удаленных вычислительных устройств 1014 a, b, c и/или их комбинаций. Таким образом, использование программного обеспечения 1006 для PGI и/или данных 1007 о PGI может быть реализовано в пределах среды облачных вычислений, где доступ к программному обеспечению 1006 для PGI и/или данным 1007 о PGI можно получать по сети 1015 (например, сети Интернет). Более того, в одном аспекте данные 1007 о PGI можно синхронизировать между одним или более из вычислительного устройства 1001, удаленных вычислительных устройств 1014 a, b, c и/или их комбинаций.
Вариант реализации программного обеспечения 1006 для PGI может храниться на машиночитаемых носителях или передаваться посредством какого-либо типа машиночитаемых носителей. Любой из раскрытых способов можно осуществлять посредством машиночитаемых команд, реализованных на машиночитаемых носителях. Машиночитаемые носители могут представлять собой любые доступные носители, доступ к которым может быть получен с помощью компьютера. В качестве примера и без ограничения машиночитаемые носители могут предусматривать «компьютерные носители информации» и «средства связи». «Компьютерные носители информации» содержат энергозависимые и энергонезависимые съемные и несъемные носители, реализованные посредством любых способов или технологии хранения информации, такой как машиночитаемые команды, структурированные наборы данных, блоки программ или другие данные. Иллюстративные компьютерные носители информации включают без ограничения RAM, ROM, EEPROM, флеш-память или другую технологию хранения информации, CD-ROM, универсальные цифровые диски (DVD) или другое оптическое запоминающее устройство, кассеты с магнитной лентой, магнитную ленту, запоминающее устройство на магнитных дисках или другие магнитные запоминающие устройства или любой другой носитель, который можно использовать для хранения требуемой информации и доступ к которому может быть получен с помощью компьютера.
В способах и системах могут использоваться методики искусственного интеллекта, такие как машинное обучение и итеративное обучение. Примеры таких методик включают без ограничения экспертные системы, рассуждение на основе аналогичных случаев, Байесовские сети, поведенческий искусственный интеллект, нейронные сети, системы на основе нечеткой логики, эволюционное моделирование (например, генетические алгоритмы), роевый интеллект (например, алгоритмы муравьиной колонии) и гибридные интеллектуальные системы (например, экспертные правила вывода, полученные посредством нейронной сети, или продукционные правила, полученные в результате статистического обучения).
Если четко не указано иное, ни в коем случае не предполагается, что любой способ, изложенный в данном документе, должен истолковываться как требующий выполнения его стадий в определенном порядке. Соответственно, если в формуле изобретения в действительности не указан порядок стадий или в формуле изобретения или в описании конкретно не указано, что стадии должны ограничиваться конкретным порядком, то никоим образом не предполагается, что порядок таким образом выводится из контекста. Это справедливо для любого возможного неявного основания для интерпретации, в том числе логики порядка стадий или последовательности выполнения технологических операций; общеупотребительного значения, полученного на основе грамматической конструкции или пунктуации; числа или типа вариантов осуществления, описанных в описании.
Следующие примеры представлены для более подробного описания настоящего изобретения. Они предназначены для иллюстрации изобретения, но не для его ограничения.
Пример 1
Индекс пассажирских генов
Способ с использованием индекса пассажирских генов (PGI) включает все образцы согласно TCGA, сгруппированные по типу рака, при этом медианное число мутантных генов определяли для каждой группы. Мутации ограничивали только соматическими мутациями, не являющимися молчащими, путем сравнения плотных опухолей с аналогичными образцами неизмененных крови или плотных тканей за исключением острого миелоидного лейкоза, при котором опухолевые клетки крови сравнивали с нормальной плотной тканью. Профили мутаций составляли в виде бинарной матрицы таким образом, что в том случае, если какой-либо локус, соответствующий гену, несет мутацию у данного пациента, то устанавливается бит. PGI рассчитывали для каждого гена Xi в виде показателя корреляции Пирсона между долей образцов с мутацией гена Xi и медианным числом мутантных генов при каждом типе рака. Перед проведением расчета показателей корреляции к доле образцов с мутацией прибавляли чрезвычайно малое количество равномерно распределенного шума, чтобы избежать проблем, обусловленных всеми нулевыми вводимыми значениями.
Пример 2
Z-показатель для нагрузки опухоли драйверными и пассажирскими генными мутациями
Способ определения z-показателя для TMB драйверными/пассажирскими генами предусматривает следующее. Для вычисления z-показателя для TMB сначала определяли фоновое распределение для TMB с использованием 1000 случайным образом выбранных наборов генов равного размера. Затем сравнивали числа мутантных драйверных/пассажирских генов с фоновым распределением для вычисления z-показателя, указывающего на то, на сколько стандартных отклонений данное число отличается от среднего значения фонового уровня. Драйверные гены загружали из реестра раковых генов COSMIC 22 января 2015 года, а пассажирские гены определяли как n наиболее значимых генов, ранжированных по PGI, полученному на основе данных TCGA.
Пример 3
Нагрузка опухоли пассажирскими генными мутациями и отвечаемость на иммунотерапию
Для вычисления индекса пассажирских генов (PGI) составляли перечень соматических мутаций, не являющихся молчащими, для 6685 образцов 20 типов опухолей согласно TCGA. Соматические мутации определяли путем сравнения генома опухоли с геномом зародышевой линии, например, полученного из образца нормальной крови от одного и того же пациента. Медианное число измененных генов на образец варьировало от 9 при остром миелоидном лейкозе до 289 при меланоме кожи, что составляло более чем 32-кратное различие между типами рака с наиболее низкой и наиболее высокой частотой появления мутаций (фиг. 5). Это согласуется с предыдущими наблюдениями, что образцы рака кожи и легкого характеризуются наиболее высокими показателями частоты появления мутаций вследствие воздействия мутагенов окружающей среды. На фиг. 5 показано число соматических мутаций, не являющихся молчащими, на образец в 6685 экзомах рака согласно TCGA.
20 типов рака, включенных в данное исследование, представляли собой уротелиальную карциному мочевого пузыря (BLCA), инвазивную карциному молочной железы (BRCA), плоскоклеточную карциному шейки матки и эндоцервикальную аденокарциному (CESC), аденокарциному толстой кишки/прямой кишки (CORE), мультиформную глиобластому (GBM), плоскоклеточную карциному головы и шеи (HNSC), светлоклеточную карциному почки (KIRC), папиллярную почечно-клеточную карциному почки (KIRP), острый миелоидный лейкоз (LAML), гепатоцеллюлярную карциному печени (LIHC), глиому головного мозга низкой степени злокачественности (LGG), аденокарциному легкого (LUAD), плоскоклеточную карциному легкого (LUSC), серозную цистаденокарциному яичника (OV), феохромоцитому и параганглиому (PCPG), аденокарциному предстательной железы (PRAD), меланому кожи (SKCM), аденокарциному желудка (STAD), карциному щитовидной железы (THCA) и эндометриоидную карциному тела матки (UCEC).
Было высказано предположение о том, что накопление большего количества мутаций пассажирских генов будет происходить при типах рака, характеризующихся более высокими общими показателями частоты появления мутаций, и при этом среднее число измененных генов на образец при каждом типе рака может выступать в качестве суррогатного показателя для вероятности появления пассажирских мутаций при данном типе рака. Для каждого гена Xi определяли PGI как показатель корреляции между процентной долей образцов с вариантом гена Xi и средним числом измененных генов на образец при каждом типе рака. Более высокий показатель PGI указывал на то, что конкретный ген с большей вероятностью приобретет соматические мутации при типах рака, характеризующихся более высокой общей частотой появления мутаций. Пассажирские гены демонстрируют сильную линейную зависимость двух переменных, хотя слабые ассоциации наблюдали для канонических генов рака, таких как TP53, PIK3CA и KRAS (фиг. 6). На фиг. 6 проиллюстрированы диаграммы рассеяния для доли пациентов с вариантом гена (ось y) и среднего общего числа мутантных генов (ось x) при каждом типе рака. Верхний ряд демонстрирует высокую линейную зависимость для наиболее значимых пассажирских генов (MUC16, r=0,979; ADAM2, r=0,972; COL5A2, r=0,968), а нижний ряд демонстрирует слабую ассоциацию 2 переменных для канонических раковых генов (TP53, r=0,301; PIK3CA, r=0,120; KRAS, r=0,222).
Среди генов, характеризующихся наивысшими значениями PGI, преобладают семейства генов, известные избыточным количеством пассажирских мутаций, например, особо крупные белки (>4000 аминокислот), гены, охватывающие большие геномные локусы (>1 Мб), гены с низким уровнем экспрессии и гены с поздним временем репликации ДНК. Интегральная функция распределения (CDF) для данных семейств генов демонстрирует резкую тенденцию к повышению при PG>I0,7, в то время как драйверные гены в каталоге соматических мутаций при раке (COSMIC) из реестра генов рака (CGC) характеризуются более равномерным распределением (фиг. 7). На фиг. 7 проиллюстрирована насыщенность по шкале PGI для драйверных генов рака и различных других групп генов. Пунктирные линии (вверху) показывают долю генов при различных значениях PGI, а вертикальные линии (ниже) указывают на ранг отдельных генов. Для исследования различия в распределении генов для каждой группы по сравнению с распределением раковых генов использовали двухвыборочный тест Колмогорова-Смирнова. Двухвыборочные тесты Колмогорова-Смирнова продемонстрировали значимое различие в ранговом распределении семейств пассажирских генов по сравнению с таким распределением для генов из CGC (p=8,3×10-19 для крупных белков; p=2,9×10-12 для генов, охватывающих геномный локус >1 Мб; p=6,4×10-35 для генов с низким уровнем экспрессии; p=2,7×10-29 для генов с поздней репликацией). Подобные результаты наблюдали после проведения группирования образцов по показателю частоты появления мутаций (вместо типа рака) для вычисления PGI. Несмотря на то, что некоторые гены из CGC также обладают высоким значением PGI, они не валидированы для их включения в наиболее значимые измененные гены для типов рака согласно TCGA. Например, KDR (рецептор с доменом, содержащим киназную вставку) характеризуется наиболее высокой частотой появления мутаций при меланоме (14% при SKCM), но причинная связь для KDR известна только в отношении развития немелкоклеточной карциномы легкого и ангиосаркомы. Аналогичным образом не выявили каких-либо валидированных случаев при типе рака с наиболее высоким значением измененных генов для наиболее значимых 30 генов из CGC. И наоборот, 16 из 30 драйверных генов из CGC с наиболее низким значением PGI валидированы для их соответствующего типа рака с измененными генами (фиг. 8). На фиг. 8 показано, что гены из CGC с низким PGI с большей вероятностью будут валидированы для типа рака с измененными генами. На фиг. 8 показаны гены согласно CGC с наиболее высокими (слева) и наиболее низкими (справа) значениями PGI и их соответствующий тип рака с наиболее высокой процентной долей (>2%) образцов с мутациями. Сокращения, отмеченные звездочкой, представляют собой тип рака, валидированный CGC для гена. Ни один из типов рака с генами из CGC с наиболее высоким PGI не валидировали, при этом 16/30 типов рака с генами из CGC с наиболее низким PGI являются валидированными.
PGI использовали в качестве критерия для отбора пассажирских генов, а мутационную нагрузку опухоли (TMB) выбранными пассажирскими генами использовали для стратификации когорты пациентов, которая характеризуется более высокой вероятностью ответа на иммунотерапию. Для демонстрации данного подхода показатели местной иммунной цитолитической активности и количество ридов для T-клеточных рецепторов (TCR) использовали в качестве суррогатного показателя для иммуногенности, при этом проводили тестирование на предмет того, имеется ли какое-либо различие в иммуногенности у пациентов с высокими и низкими TMB в данным TCGA. Для каждого пациента вычисляли TMB с помощью 3 различных подходов, а именно (i) традиционный показатель общей TMB, (ii) TMB драйверными генами и (iii) TMB пассажирскими генами. Для количественной оценки цитолитической активности авторы настоящего изобретения использовали простой критерий на основе РНК, который основан на уровне экспрессии генов двух ключевых цитолитических эффекторов, - гранзима A (GZMA) и перфорина (PRF1). Было обнаружено, что показатели цитолитической активности значимо отличались (p<0,05 согласно U-критерию Манна-Уитни) у пациентов с высокими и низкими TMB пассажирскими генами при 7 различных типах рака (аденокарцинома толстой кишки, p<4,6×10-11; инвазивная карцинома молочной железы, p<5,0×10-4; аденокарцинома легкого, p<7,7×10-4; эндометриоидная карцинома тела матки, p<9,9×10-4; плоскоклеточная карцинома шейки матки, p<2,2×10-3; плоскоклеточная карцинома легкого, p<5,7×10-3; аденокарцинома предстательной железы, p<2,1×10-2), при этом различия являются более значимыми по сравнению с такими, которые получены при использовании общей TMB и TMB драйверными генами при соответствующих типах рака (фиг. 9A).
TCR отвечают за распознавание комплексов пептид-MHC, и их многообразие непосредственно связано с числом чужеродных или мутантных белков, например, неоантигенов раковых клеток. Анализ β репертуара TCR проводили с использованием данных TCGA по секвенированию РНК, и сравнивали β количество ридов для TCR между пациентами с высокими и низкими TMB пассажирскими генами. На фиг. 9B показано, что выявленное количество ридов для TCR β значимо различалось между пациентами с высокими и низкими TMB при 8 различных типах рака (эндометриоидная карцинома тела матки, p<3,2×10-6; аденокарцинома толстой кишки, p<4,5×10-6; плоскоклеточная карцинома шейки матки, p<2,4×10-3; инвазивная карцинома молочной железы, p<7,3×10-3; меланома кожи, p<9,2×10-3; аденокарцинома легкого, p<1,5×10-2; серозная цистаденокарцинома яичника, p<2,7×10-2; аденокарцинома предстательной железы, p<3,8×10-2). В соответствии с наблюдениями в отношении цитолитической активности различия в TCR β являются более значимыми между группами, сформированными по показателю TMB пассажирскими генами, по сравнению с такими группами, которые сформированы с использованием общей TMB и TMB драйверными генами.
И наконец, проводили тестирование для определения того, существует ли какое-либо преимущество в отношении выживаемости, ассоциированное с TMB на основе данных TCGA. При плоскоклеточной карциноме шейки матки и легкого (CESC и LUSC) общая TMB, хотя и не является статистически значимой, демонстрирует тенденцию к положительной корреляции с лучшим исходом в отношении выживаемости, тогда как TMB драйверными генами ассоциирован с неблагоприятным прогнозом (фиг. 9C). На фиг. 9C показано, что клинический исход для когорт пациентов, сгруппированных по показателям мутационной нагрузки (i) всеми генами, (ii) драйверными генами и (iii) пассажирскими генами при меланоме кожи (SKCM), плоскоклеточной карциноме шейки матки (CESC) и эндоцервикальной аденокарциноме и плоскоклеточной карциноме легкого (LUSC), демонстрирует значимые различия в выживаемости только в когортах пациентов, сгруппированных по TMB пассажирскими генами, но не по общей TMB/TMB для драйверными генами. SKCM демонстрирует значимое различие в отношении выживаемости пациентов между группами с высокими и низкими общей TMB/TMB пассажирскими генами.
Только при использовании TMB пассажирскими генами различие в исходе в отношении выживаемости между группами пациентов с высокими и низкими TMB было статистически значимым как для CESC, так и для LUSC. При меланоме кожи (SKCM) стратификация пациентов с использованием как TMB пассажирскими генами, так и общей TMB демонстрирует аналогичное значимое разделение в кривых выживаемости, указывая на то, что драйверные генные мутации, которые оказывают сильное влияние на подавление иммуногенности при меланоме, присутствуют в очень низком количестве или отсутствуют. 110 пациентов распределяли в две группы равного размера по мутационной нагрузке с использованием независимого набора данных о блокировании CTLA-4 при метастатической меланоме. Стратификация с использованием TMB для 200 пассажирских генов повысила показатель клинической пользы для выбранной группы пациентов от исходного уровня 24,55% до 36,36% (точный критерий Фишера, p=0,0035). Стратификация пациентов с использованием общей TMB обеспечивает такое же повышение клинической пользы, дополнительно подтверждая наблюдения в отношении цитолитической активности, выявления TCR и преимущества в отношении выживаемости при меланоме с использованием данных TCGA.
На фиг. 11 представлены показатели TMB для когорты пациентов в клиническом исследовании фазы 1 ингибирования PD1. Замкнутые окружности, замкнутые квадраты и замкнутые треугольники обозначают пациентов с частичным ответом (PR), стабильным заболеванием (SD) и прогрессирующим заболеванием (PD) соответственно. Незакрашенные фигуры представляют данные для отдельных пациентов, а закрашенные фигуры представляют среднее значение в каждой из групп PR/SD/PD. Показатели общей TMB приведены в виде общего числа мутантных генов (левая ось y), а показатели TMB для драйверных/пассажирских генов приведены в виде z-показателя (правая ось y). Сравнение как PR с PD, так и PR с PD+SD демонстрирует статистически значимые отличия в показателе TMB для пассажирских генов независимо от используемого числа наиболее значимых пассажирских генов (50/100/1000). Для группы PR значимое различие в показателях общей TMB или TMB для драйверных генов получено не было.
Пример 4
Нагрузка опухоли пассажирскими генными мутациями и клинический ответ на иммунотерапию
Для оценки клинического ответа различных злокачественных новообразований на иммунотерапевтическое средство использовали данные о соматических мутациях из исследования фазы 1 моноклонального человеческого антитела к PD-1 (белку запрограммированной смерти клетки 1) в качестве средства монотерапии и в комбинации с другими противораковыми терапевтическими средствами. В общем данные о клиническом ответе получены от 74 пациентов со злокачественными новообразованиями на поздней стадии (n=8 с частичным ответом, PR; n=29 со стабильным заболеванием, SD; n=37 с прогрессирующим заболеванием, PD). Общая TMB определена как общее число мутантных генов, при этом показатели TMB драйверными/пассажирскими генами представлены z-показателями с целью нормализации в отношении показателя общей TMB у пациентов. Z-показатели вычисляли путем сравнения числа мутантных драйверных/пассажирских генов с фоновым распределением с использованием случайным образом выбранных генов одинакового размера. Более высокие z-показатели указывают на более высокую нагрузку мутациями в выбранных группах драйверных/пассажирских генов независимо от фонового показателя общей TMB. Общая TMB и z-показатель для TMB драйверными генами не обеспечивают установления различия между PR и другими группами пациентов, тогда как значения z-показателей для TMB пассажирскими генами у пациентов с PR в значительной степени выше по сравнению с такими у пациентов в группах PD или PD+SD. Результаты согласуются со значениями TMB, рассчитанными с использованием 50, 100, 500 (фиг. 12) и 1000 наиболее значимых пассажирских генов.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Ридженерон
<120> Способы иммунотерапии пациентов, опухоли которых
характеризуются высокой нагрузкой пассажирскими
генными мутациями
<130> 37595.0015P1
<150> 62/560,955
<151> 2017-09-20
<160> 217
<170> PatentIn версии 3.5
<210> 1
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 1
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Asp Thr Gly Gly Asn Thr Tyr Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ser Lys Asn Thr Leu Ser
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Gln Gly Gly Ser Tyr Pro Tyr Tyr Phe His Tyr Trp Gly
100 105 110
Gln Gly Ser Leu Val Thr Val Ser Ser
115 120
<210> 2
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 2
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Ile Trp Tyr Gln Gln Lys Pro Gly Thr Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Cys Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 3
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 3
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Asn Asn
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Tyr Ser Gly Gly Phe Thr Tyr Tyr Thr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg His Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Tyr Tyr Tyr Asp Thr Ser Asp Tyr Trp Thr Phe Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 4
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 4
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Gly Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn
100 105
<210> 5
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 5
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Asn Asn
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Tyr Ser Gly Gly Phe Thr Tyr Tyr Thr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg His Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Tyr Tyr Tyr Asp Thr Ser Asp Tyr Trp Thr Phe Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 6
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 6
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Gly Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn
100 105
<210> 7
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 7
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Ser Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Ile Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Ala Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly His Trp Asn Tyr Phe Phe Glu Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 8
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 8
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Thr Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Gln Leu Glu Ile Lys
100 105
<210> 9
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 9
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Gly Ala Ser Gly Phe Thr Phe Arg Asn Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ile Thr Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Ser Ala Gly Asp Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Val Gly Asp Thr Ala Val Tyr Tyr Cys Thr
85 90 95
Arg Asp Ile His Cys Ser Ser Thr Arg Cys Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 10
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 10
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 11
<211> 130
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 11
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Lys Phe Ser Asn Glu
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Asp Gln Asp Phe Trp Ser Gly Tyr Tyr Thr Gly Ala
100 105 110
Asp Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr Val
115 120 125
Ser Ser
130
<210> 12
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 12
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 13
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 13
Gln Met Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Val Val Tyr Gly Gly Ser Leu Asn Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Asn Arg Val Thr Met Ser Val Asp Thr Ser Lys Ile Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Val Thr Val Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Leu Leu Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 14
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 14
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Val Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr Ser Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Asn Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Ala Ala Ser Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Tyr Ala Thr Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 15
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 15
Gln Leu Gln Leu Gln Glu Ser Gly Pro Asp Leu Val Lys Pro Ser Asp
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asp Ser Ile Ser Ser Thr
20 25 30
Thr Tyr Tyr Trp Ala Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Met Ser Tyr Asn Gly Asn Asn Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Ala Ile Ser Ala Gly Thr Ser Gln Lys Gln Phe
65 70 75 80
Ser Leu Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr His
85 90 95
Cys Ala Arg His Leu Gly Tyr Asn Gly Asn Trp Tyr Pro Phe Asp Phe
100 105 110
Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser
115 120
<210> 16
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 16
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Thr Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 17
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 17
Glu Val Gln Val Val Glu Ser Gly Gly Gly Leu Val Glu Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Lys Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Thr Pro Gly Lys Ala Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Trp Ser Gly Asn Asn Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Lys Asp Asp Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Thr Lys Asp Ile Ser Ile Thr Gly Thr Leu Asp Ala Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 18
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 18
Asp Ile Gln Met Thr Gln Ser Pro Ile Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Ile Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Arg Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Gly Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala His Ser Phe Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 19
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 19
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ile Ile Trp Ser Asp Gly Asp Ser Glu Tyr Asn Leu Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Asp Leu Glu Asp Ile Trp Gly Gln Gly Thr Met Val
100 105 110
Thr Val Ser Ser
115
<210> 20
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 20
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 21
<211> 117
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 21
Glu Val Gln Leu Leu Glu Ser Gly Gly Val Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Gly Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Gly Gly Gly Arg Asp Thr Tyr Phe Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Gly Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Lys Trp Gly Asn Ile Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 22
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 22
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Ser Ile Thr Ile Thr Cys Arg Ala Ser Leu Ser Ile Asn Thr Phe
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu His Gly Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Thr Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Ser Asn Thr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Val Val Asp Phe Arg
100 105
<210> 23
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 23
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Asp Gly Lys Thr Val Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Glu Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Trp Gln Tyr Leu Ile Glu Arg Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 24
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 24
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 25
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 25
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Gly Ile Gly Trp Thr Gly Gly Arg Ser Ser Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Gly Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Gln Trp Leu Val Gln Trp Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 26
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 26
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 27
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Arg Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Leu Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gly Ile Ser Trp Asn Asp Gly Lys Thr Val Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu His
65 70 75 80
Leu Glu Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Trp Gln Tyr Leu Ile Asp Arg Tyr Phe Asp Phe Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 28
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 28
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Gly Trp Ser Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Ser Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ala Tyr Thr Phe Met Ile Thr Leu Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 29
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 29
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ser Gly Trp Asn Arg Gly Ser Leu Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Lys Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Val Arg Val Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Gly Phe Val Val Val Ser Ala Ala Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 30
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 30
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Val Thr Phe Arg Asn Phe
20 25 30
Ala Ile Ile Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Phe Phe Ser Ala Ala Asn Tyr Ala Gln Ser Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Pro Asp Glu Ser Thr Ser Thr Ala Phe
65 70 75 80
Met Glu Leu Ala Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Glu Arg Gly His Thr Tyr Gly Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 31
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 31
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ser Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Trp Asn Arg Gly Arg Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Asp Leu Arg Val Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Ala Glu Gln Trp Leu Asp Glu Gly Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 32
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 32
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Arg Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Ser
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Gln Gly Gly Ser Tyr Pro Tyr Tyr Phe His Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 33
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 33
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Glu Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Gly Trp Ser Asn Val Lys Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Val Arg Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Phe Tyr Tyr Cys
85 90 95
Val Lys Ala Tyr Thr Ser Met Leu Thr Leu Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 34
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 34
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Phe
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Asp Gly Ser Thr Ser Asn Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Val Ala Gly Asp Ile Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 35
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 35
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
His Trp Asn Trp Ile Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ile Gly Ser Thr Asp Tyr Asn Pro Ser Leu Glu
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Pro Val Gly Ala Thr Gly Ala Ser Asp Val Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser
115
<210> 36
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 36
Glu Val Gln Leu Val Glu Ser Gly Gly Ser Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Val Ser Gly Phe Thr Phe Glu Asp Tyr
20 25 30
Gly Leu Ser Trp Val Arg Gln Ile Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Thr Gly Gly Asn Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr His Cys
85 90 95
Thr Arg Asp Arg Gln Trp Leu Met Gln Trp Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 37
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 37
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Ala Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Ser Tyr Gly Gly Ser Asp Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ser Ala His Trp Asn Phe Phe Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 38
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 38
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Ala Leu His Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Trp Asn Ser Gly Val Ile Gly Tyr Ala Asp Ser Leu
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Gly Ser Gly Ser Tyr Tyr Val Ser Trp Phe Asp Pro Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 39
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 39
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Thr
20 25 30
Ala Tyr His Trp Asp Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Thr Ile Thr Tyr Asn Gly Asn Thr Tyr Phe Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Leu Ser Met Thr Ala Ala Glu Thr Ala Val Phe Tyr
85 90 95
Cys Ala Arg His Leu Gly Tyr Asn Ser Asp Phe Phe Pro Phe Asp Phe
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 40
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 40
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Ala Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Gly Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Asp Ser Thr Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Ser Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Lys Val Arg Asn Tyr Asp Gly Ser Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser
115
<210> 41
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 41
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Met Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Gly Ser Gly Arg Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Glu Ser Val Thr Gly Thr Ser Ser Tyr Tyr Tyr Gly Val Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 42
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 42
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr His Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Ser Tyr Arg Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 43
<211> 128
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 43
Gln Val Gln Leu Glu Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Trp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Leu Ile Trp Tyr Asp Gly Thr Asn Lys Lys Tyr Gly Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Cys Gly His Ser Gly Asn Asp Arg Gly Thr Tyr Tyr Tyr
100 105 110
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
<210> 44
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 44
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 45
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 45
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Glu Ile Ser His Arg Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ser
85 90 95
Arg Asp Glu Glu Leu Glu Phe Arg Phe Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 46
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 46
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Val
35 40 45
Tyr Gly Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Phe Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 47
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 47
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ile Ser Asn
20 25 30
Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Asn Phe Phe Tyr Thr Gly Ala Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Ala Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Leu Tyr Tyr
85 90 95
Cys Ala Ser Tyr Asn Arg Asn Tyr Arg Phe Asp Pro Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 48
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 48
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 49
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 49
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Thr Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Ser Gly Asn Ala Asp Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Ala Gly Tyr Cys Ser Ser Pro Thr Cys Tyr Ser Tyr Tyr Tyr Phe
100 105 110
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 50
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 50
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ile Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Phe Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asn Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 51
<211> 129
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 51
Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu Val Lys Pro Thr Glu
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Ala
20 25 30
Gly Met Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala His Ile Phe Ser Asn Asp Glu Lys Ser Tyr Ser Thr Ser
50 55 60
Leu Arg Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Ser Gln Val
65 70 75 80
Val Leu Thr Val Thr Asn Leu Asp Pro Val Asp Thr Ala Thr Tyr Phe
85 90 95
Cys Ala Arg Ile Pro Glu Phe Thr Ser Ser Ser Trp Ala Leu Tyr Tyr
100 105 110
Phe Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser
<210> 52
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 52
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Thr Ser Thr
20 25 30
Tyr Phe Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Ala Thr Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Asp Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Arg Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Val Lys
100 105
<210> 53
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 53
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Asp Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Val Arg Trp Asn Trp Gly Ser Val Tyr Trp Tyr Phe Asp Leu Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 54
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 54
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ile Ile Ser Ser Ser
20 25 30
Tyr Phe Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Val Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Met Tyr Phe Cys Gln Gln Tyr Gly Asn Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 55
<211> 117
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 55
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Asn Thr His
20 25 30
Arg Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Tyr Gly Asn Asp Val Lys Asn Tyr Ser Pro Ser
50 55 60
Leu Glu Thr Arg Leu Thr Ile Ala Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Phe
85 90 95
Cys Ser Tyr Ile Thr Gly Glu Gly Met Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 56
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 56
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Ser Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Asn Leu Met Tyr Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Asn Trp Phe His Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Tyr Lys Val Ser Asn Arg Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly
85 90 95
Thr His Trp Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 57
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 57
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Asn Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Lys Gln Phe Ser Leu
65 70 75 80
Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Met Tyr Tyr Cys Thr
85 90 95
Arg Asp Glu Glu Gln Glu Leu Arg Phe Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 58
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 58
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Thr Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Arg Ala Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Phe Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Glu Val Glu Ile Lys
100 105
<210> 59
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 59
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Val Val His Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Asn Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Val Ser Glu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Leu Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val
85 90 95
Arg Gly Glu Asp Tyr Asp Phe Trp Ser Asp Tyr Tyr Asn Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 60
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 60
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Thr Ile Ser Ser Tyr
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Lys Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 61
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 61
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Pro Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Ile Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ala Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ser
85 90 95
Arg Gly Glu Asp Tyr Tyr Asp Ser Ser Gly Tyr Ser Tyr Tyr Phe Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 62
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 62
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 63
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 63
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Arg Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Ser Pro Gly Thr Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Asn Ile Asn Phe Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Glu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Asp Tyr Asp Ile Trp Ser Gly Tyr Tyr Arg Glu Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 64
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 64
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Lys Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 65
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 65
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Glu Phe
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Glu Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Asn Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Met Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Gln Leu Asn Ser Val Thr Val Ala Asp Thr Ala Leu Tyr Tyr Cys Ala
85 90 95
Phe Gly Tyr Asp Phe Arg Ser Ser Tyr Glu Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 66
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 66
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Thr Tyr
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Gln Pro Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ser Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 67
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 67
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Gly Gly Gly Arg Thr Tyr Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Ser Met Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Lys Glu Arg Val Thr Gly Ile Asp His Tyr Tyr Tyr Gly Val Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 68
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 68
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Thr Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Ala Ser Gly Thr Asp Phe Thr Leu Ala Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Thr Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 69
<211> 130
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 69
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Asn Thr Lys Asp Tyr Ala Gly Ser Val
50 55 60
Lys Gly Arg Val Thr Ile Ser Arg Asp Asn Ala Lys Asn Leu Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr His Cys
85 90 95
Ala Arg Asp Gly Gly His Tyr Asp Ile Leu Thr Gly Ser Met Ser Tyr
100 105 110
Tyr Tyr Tyr Ala Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
115 120 125
Ser Ser
130
<210> 70
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 70
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 71
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 71
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Lys Thr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Gly Ser Gly Ser Thr Ser Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Tyr Lys Lys Thr Leu Ser
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Leu Asp Ile Met Ala Thr Val Gly Gly Leu Phe Asn Asn Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 72
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 72
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 73
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 73
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg His
20 25 30
Thr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala His Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Thr Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Pro Tyr Thr Arg Gln Gly Tyr Phe Asp Leu Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 74
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 74
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Asp Tyr Ser Thr Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 75
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 75
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Asp Trp Met
35 40 45
Gly Ile Ile Asn Pro Gly Gly Gly Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Leu Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Thr Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Glu Asn Trp Asn Ser Tyr Phe Asp Asn Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 76
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 76
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Leu Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Gly Ala Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 77
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 77
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Thr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Ile Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Thr Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Ala Arg Tyr Gly Ser Gly Ser Tyr Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 78
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 78
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Thr
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Thr Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 79
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 79
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Asn
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Gly Ile Ile Tyr Trp Asn Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Arg Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala His Arg Gly Leu Phe Gly Gly Trp Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 80
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 80
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Phe Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Ser Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 81
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 81
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ile Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Ala Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Gly Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ser Lys Val Ala Ala Ala Asn Asn Tyr Tyr Tyr Ala Leu Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 82
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 82
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Lys Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Val Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 83
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 83
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Asn Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Val Ser Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Glu Val Glu Tyr Ser Ser Ser Asn Tyr Asn Tyr Tyr
100 105 110
Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 84
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 84
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Val Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Leu Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 85
<211> 125
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 85
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe His Asn Phe
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Thr Gly Ser Gly Thr Ser Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Lys Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Gly Tyr Asp Tyr Ser Gly Ser Tyr Tyr Asn Trp Phe
100 105 110
Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 86
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 86
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Ile Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Phe Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Ser
85 90 95
Leu Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 87
<211> 128
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 87
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser His Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Met Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Asn Ile Trp Ser Gly Tyr Tyr Ala Ala Tyr Tyr Phe
100 105 110
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 88
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 88
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Ser Trp Leu Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Ile Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Ile Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Val Gln Phe Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 89
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 89
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Asn Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ala Phe Ser Asp Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Met Ser Ser Val Thr Ala Ala Asp Ala Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Asp Tyr Asp Ile Trp Asn Gly Tyr Tyr Gln Glu Lys Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 90
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 90
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Lys Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Val Val Tyr Tyr Cys His Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 91
<211> 117
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 91
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Phe Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Leu Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Phe Tyr Ser Gly Ser Thr Asp Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Lys Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Thr Ile Ser Thr Trp Trp Phe Ala Pro Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 92
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 92
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Gly Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Asn Asn
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Gly Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Ser Cys Gln Gln Tyr Asn Asn Trp Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 93
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 93
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ile Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Gln Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Val Ala Thr Ser Gly Asp Phe Asp Tyr Tyr Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 94
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 94
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Thr Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Thr Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Lys Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 95
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 95
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Asn Tyr
20 25 30
Trp Ile Val Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Thr Ile Phe Pro Ser Tyr Pro Leu Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 96
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 96
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Asn Gly Tyr Asn Phe Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Val Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Ile Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 97
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 97
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Asn
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Thr Leu Ile Tyr Trp Asn Glu Asn Lys His Tyr Ser Pro Ser
50 55 60
Leu Lys Asn Arg Ile Thr Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Leu Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Val His Arg Gly Trp Leu Gly Ala Ile Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 98
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 98
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 99
<211> 126
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 99
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asp Ile Ser Gly Ser Gly Gly Arg Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Met Leu Tyr
65 70 75 80
Leu Gln Met Asn Ile Leu Arg Ala Glu Asp Thr Ala Val Tyr His Cys
85 90 95
Ala Lys Gly Thr Gly Gln Gln Val Asp Leu Tyr Asn Tyr Tyr Tyr Ala
100 105 110
Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 100
<211> 129
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 100
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Tyr Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Lys Gly Ile Ser Gly Ile Lys Gly Gly Ser Tyr Tyr Tyr
100 105 110
Tyr Tyr Ala Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser
<210> 101
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 101
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Asn Lys Ile Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ser Thr Val Asp Tyr Asn Trp Tyr Phe Asp Phe Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 102
<211> 129
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 102
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Phe Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Leu Ile Trp Tyr Asp Gly Thr Asn Glu Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Gly Val Ala Thr Phe Thr Arg Gly Asn Tyr Tyr Tyr
100 105 110
Asn Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser
<210> 103
<211> 129
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 103
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Phe Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Gly Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Met Leu Tyr
65 70 75 80
Leu Gln Met Thr Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Lys Thr Gly Thr Gly Ile Thr Gly Tyr Ser Tyr
100 105 110
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser
<210> 104
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 104
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ile Thr Asn
20 25 30
Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Arg Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Glu Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Ile Tyr Tyr
85 90 95
Cys Ala Arg Glu Gly Asp Pro Ser Leu Asp Pro Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 105
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 105
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 106
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 106
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser His Ile Ser Gly Ser Gly Gly Asn Ser Tyr Ser Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ser Leu Asp Ile Met Ala Thr Val Gly Gly Leu Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 107
<211> 131
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 107
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Ile Phe Ser Phe Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Asp Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Glu Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Arg Asp Gln Gly Ile Ser Tyr Tyr Asp Ile Leu Thr Gly Asn Tyr
100 105 110
Asn Tyr Tyr Tyr Gly Val Asp Val Trp Gly Gln Gly Thr Thr Val Thr
115 120 125
Val Ser Ser
130
<210> 108
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 108
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Glu Ile Ser His Arg Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ser
85 90 95
Arg Asp Glu Glu Leu Glu Phe Arg Phe Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 109
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 109
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Val
35 40 45
Tyr Gly Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Phe Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 110
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 110
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Leu Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Gly Ser Gly Gly Gly Thr Tyr Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Asp Asp Thr Ala Val Phe Tyr Cys
85 90 95
Thr Lys Glu Ser Thr Thr Gly Thr Tyr Ser Tyr Phe Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 111
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 111
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Thr Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Leu Ser Gly Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 112
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 112
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Phe
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Asn Gln Asp Gly Thr Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Asn Thr Tyr Tyr Asp Phe Trp Ser Gly His Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 113
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 113
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr His Ser Tyr Ser Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 114
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 114
Gln Glu His Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Leu Trp Ser Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Val Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Arg Gly Ala Pro Gly Ile Pro Ile Phe Gly Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 115
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 115
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Thr Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Ala Ile Lys
100 105
<210> 116
<211> 130
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 116
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Arg Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu His Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Asp Asp Ile Val Val Val Pro Ala Val Met Arg Glu
100 105 110
Tyr Tyr Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
115 120 125
Ser Ser
130
<210> 117
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 117
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Thr Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Asn Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 118
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 118
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Gln Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Thr Lys Lys Tyr Ala His Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Asp Thr Ala Tyr
65 70 75 80
Met Ile Leu Ser Ser Leu Ile Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Asp Trp Asn Phe Gly Ser Trp Phe Asp Ser Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 119
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 119
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Thr Leu Val His Gly
20 25 30
Asp Gly Asn Thr Tyr Leu Ser Trp Ile Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Gln Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Leu Tyr Phe Cys Met Gln Ala
85 90 95
Thr His Phe Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 120
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 120
Gln Val His Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly His Gly Leu Glu Trp Met
35 40 45
Gly Trp Leu Asn Pro Asn Thr Gly Thr Thr Lys Tyr Ile Gln Asn Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Thr Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Asp Trp Asn Tyr Gly Ser Trp Phe Asp Thr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 121
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 121
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Pro Ser Leu Val His Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Ser Trp Leu Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Ile Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Thr His Phe Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Arg
100 105 110
<210> 122
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 122
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Gly Met Thr Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile His Trp His Gly Lys Arg Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Lys Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Gly Glu Asp Thr Ala Leu Tyr His Cys
85 90 95
Val Arg Gly Gly Met Ser Thr Gly Asp Trp Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Ile Val Ser Ser
115 120
<210> 123
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 123
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 124
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 124
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Gly Met Thr Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile His Trp Ser Gly Arg Ser Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Met Ser Thr Gly Asp Trp Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 125
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 125
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 126
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 126
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Gly Ser Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Leu Thr Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 127
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 127
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Thr Ile Asn Ile Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Arg Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys His Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 128
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 128
Glu Glu Arg Leu Val Glu Ser Gly Gly Asp Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Val Gly Thr Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Ser Gly Gly Asn Thr His Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Ile Met Ser Arg Gln Thr Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Glu Thr Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Leu Asp Val Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 129
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 129
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Met Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
Phe Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 130
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 130
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Met Pro Gly Ser
1 5 10 15
Ser Val Arg Val Ser Cys Lys Ala Ser Gly Gly Ile Phe Ser Ser Ser
20 25 30
Thr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Ile Pro Val Phe Gly Thr Val Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Ile Phe Thr Ala Asp Glu Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Lys Ser Gly Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Asn Trp Gly Leu Gly Ser Phe Tyr Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 131
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 131
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Phe Asn Phe Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Gly Val Phe Tyr Cys Gln Gln Tyr Glu Ser Ala Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 132
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 132
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val His Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Pro Phe Asp Glu Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ser Asn Asn Asn Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Phe Tyr Tyr Cys
85 90 95
Ala Lys Ser Gly Ile Phe Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 133
<211> 105
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 133
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Leu Leu Ile Tyr Ala Ala
35 40 45
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Gly Gly Ser
50 55 60
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Arg Pro Glu Asp Phe
65 70 75 80
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Cys Thr Pro Pro Ile Thr Phe
85 90 95
Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 134
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 134
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Leu Ile Ser Tyr Glu Gly Arg Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Thr Leu Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 135
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 135
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Thr Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Asn
20 25 30
Arg Met Cys Val Thr Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Arg Ile Asp Trp Asp Gly Val Lys Tyr Tyr Asn Thr Ser
50 55 60
Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Phe Tyr
85 90 95
Cys Ala Arg Ser Thr Ser Leu Thr Phe Tyr Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 136
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 136
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 137
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 137
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Glu Phe Thr Val Gly Thr Asn
20 25 30
His Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Tyr Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg His Thr Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Thr Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Leu Gly Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 138
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 138
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Val Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Arg Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 139
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 139
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Arg Gly Glu
1 5 10 15
Ser Leu Arg Leu Tyr Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gly Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Trp Gly Ser Gly Tyr Tyr Phe Asp Phe Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 140
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 140
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asn Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Phe Gln Asn Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 141
<211> 130
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 141
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asp Ile Val Val Val Pro Ala Pro Met Gly Tyr Tyr Tyr
100 105 110
Tyr Tyr Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
115 120 125
Ser Ser
130
<210> 142
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 142
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 143
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 143
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Phe
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Thr Gly Gly Asn Met Asp Tyr Ala Asn Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Glu Asp Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Ala Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Asp Ile Arg Gly Ile Val Ala Thr Gly Gly Ala Phe Asp Ile
100 105 110
Trp Gly Arg Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 144
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 144
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Thr Ile Ser Thr Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Val Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 145
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 145
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Gly Thr Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Val Ile Tyr Ser Gly Gly Ser Thr Phe Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Gln Thr Ser Gln Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 146
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 146
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 147
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 147
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Ile Ser Thr Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Tyr Ser Ser Gly Ser Thr Tyr Tyr Ile Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Leu Thr Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Asn Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 148
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 148
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Ile Asp Asp Ser
20 25 30
Ala Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Asp Ile Arg Gly Asn Trp Asn Tyr Gly Gly Asn Trp Phe Asp
100 105 110
Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 149
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 149
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe Thr Val Gly Val Asn
20 25 30
His Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Phe Ser Ser Gly Arg Thr Phe Tyr Gly Asp Tyr Val Lys
50 55 60
Gly Arg Leu Thr Ile Phe Arg Gln Thr Ser Gln Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Gly Gly Leu Asp Ile Trp Gly Arg Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 150
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 150
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Leu His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Thr Gly Gly Thr Ile Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Thr Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Thr Arg Asp Ile Arg Gly Asn Trp Lys Tyr Gly Gly Trp Phe Asp Pro
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 151
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 151
Gln Val Gln Leu Val Gln Ser Gly Thr Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ala Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Asp Trp Met
35 40 45
Gly Trp Ile Ser Pro Asn Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Asn Thr Phe Tyr
65 70 75 80
Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Ser Thr His His Asn Ser Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 152
<211> 114
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 152
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Gly Thr Asn
20 25 30
Phe Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Tyr Ser Gly Gly Thr Ala Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Thr Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Gly Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser
<210> 153
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 153
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asn Thr Tyr
20 25 30
Val Leu Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Ile Pro Ile Leu Gly Ala Ala Asn Tyr Ala Gln Asn Phe
50 55 60
Gln Gly Arg Val Thr Phe Thr Thr Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Thr Ser Gly Gly Phe Asp Pro Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 154
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 154
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr His Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Ser Pro Tyr Asn Gly Tyr Thr Asp Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Leu Thr Thr Asp Thr Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Asn Leu Arg Ser Asp Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ser Arg Gly Arg Gly Pro Tyr Trp Ser Phe Asp Leu Trp Gly Arg Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 155
<211> 117
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 155
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Asp Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Val Tyr Asn Gly Asn Ile Asn Tyr Ala Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Met Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Thr Gln Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 156
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 156
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Asn
20 25 30
Leu Asn Trp Tyr Gln Gln Asn Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Thr Thr Ser Ser Leu Gln Gly Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Phe Arg Thr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 157
<211> 128
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 157
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ser
20 25 30
Ala Met His Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Gly Lys Ala Asn Ser Phe Ala Thr Ala Tyr Ser Ala
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Ser Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr
85 90 95
Phe Cys Thr Arg Glu Asp Gln Gln Leu Val Arg Pro Tyr Tyr Tyr His
100 105 110
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 158
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 158
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Thr Ser Gln Ser Ile Thr Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Thr Ala Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Glu Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 159
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 159
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Ser Pro Gly Arg Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Tyr Trp Asn Asp His Glu Arg Tyr Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Asn Leu Val
65 70 75 80
Val Leu Ala Met Ala Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Phe
85 90 95
Cys Ala His Arg Asn Ile Glu Tyr Arg Arg Ser Tyr Phe Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 160
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 160
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Arg
1 5 10 15
Asp Arg Val Thr Val Thr Cys Arg Ala Ser Gln Asp Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Thr Phe Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 161
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 161
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Asn Ser Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Val Tyr Tyr Ser Gly Ser Thr Thr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Phe Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ala Ala Glu Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Thr Leu Gly Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 162
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 162
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Phe Ser Asn Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Thr Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Ala Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Arg Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 163
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 163
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Thr Trp Tyr Asp Gly Ser Asn Lys His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Tyr Ser Leu Arg Ala Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Val Arg Gly Gly His Leu Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 164
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 164
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Gly Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 165
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 165
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Asn Gly Val Ser Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Ile Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Ala Ser Trp Asp Tyr Asn Gly Val Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 166
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 166
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Ser Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly
85 90 95
Leu Gln Pro Pro Asn Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 167
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 167
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ile Val Ser Gly Gly Ser Thr Ser Ser Asn
20 25 30
Thr Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Thr Ile His Tyr Ser Gly Asn Pro Tyr Tyr Asp Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn His Phe
65 70 75 80
Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Thr Arg Gln Tyr Ile Asn Phe Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 168
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 168
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Val Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Arg Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Val Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Asp Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 169
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 169
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Leu Thr Phe Ser Tyr Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Ala Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Leu Gly Gly Asp Asp Tyr Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 170
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 170
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 171
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 171
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Thr Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Gly Asn Ile Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Gly Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Leu Glu Pro Tyr His Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 172
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 172
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln His Tyr Asp Asn Leu Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 173
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 173
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Asn Tyr
20 25 30
Val Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Arg Gly Gly Asn Ser Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ser Ile Ser Arg Asp His Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Val Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ala Glu Arg Gly Tyr Ser Tyr Gly Phe Asn Trp Phe Asp Pro
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 174
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 174
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Gly Asn Asn Phe Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 175
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 175
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Val Ile Trp Tyr Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Asn Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Gly Arg Leu Ser Tyr Tyr His Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 176
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 176
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Phe
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Gly Thr Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ala Tyr Tyr Cys Gln Gln Thr Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 177
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 177
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Met Ser Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Thr Ala Tyr Asn Gly Asn Ser Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Asp Tyr Leu Gly Val Phe Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 178
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 178
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Thr Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 179
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 179
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Glu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Arg Thr Ser Gly Thr Thr Lys Tyr Tyr Ala Asp Ser Met
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Gly Gly Gly Thr Phe Leu His Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 180
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 180
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ala Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Lys Ser Phe Pro Met
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 181
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 181
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Thr Ser Gly
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Phe Tyr Ser Gly Ile Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Thr Tyr Asn Ser Leu Arg Leu Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 182
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 182
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Ile Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Tyr Gly
20 25 30
Asp Gly Asn Thr Tyr Leu Asn Trp Phe Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Tyr Lys Val Ser Asn Arg Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ser
85 90 95
Thr His Trp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 183
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 183
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ala Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Asp Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ser Arg Asp Lys Ala Asn Ser Phe Thr Thr Glu Tyr Val Ala
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Glu Asp Ser Lys Asn Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ala Arg Thr Asn Tyr Asp Phe Ser Leu Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 184
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 184
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Ala Trp Phe Gln Gln Lys Pro Gly Asn Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Lys Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Thr Tyr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 185
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 185
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
His Trp Ser Trp Ile Arg Gln Pro Leu Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Gly Ser Ser Ile Trp Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 186
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 186
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Lys Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ile Tyr Ser Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 187
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 187
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Val Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys Arg Phe Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala His Arg Arg Leu Gly Leu Tyr Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 188
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 188
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Trp Ala Ser Gln Gly Ile Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Val His Ile Tyr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 189
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 189
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Leu Ser Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Leu Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Asp Gly Pro Phe Lys Ile Ser Phe Phe Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 190
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 191
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 191
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Arg Asn Lys His Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Val Arg Gly Gly Gln Leu Gly Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 192
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 192
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 193
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 193
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Ser Ser Ser Tyr
20 25 30
Gly Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Trp Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 194
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 194
Asp Ile Arg Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Thr Val Asn Thr Phe
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Phe Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Gly Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Ser Tyr Ser Val Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Glu
100 105
<210> 195
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 195
Gln Val Gln Leu His Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Ser Gly Gly Ser Ile Ser Asn Gly
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Gln Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ile Gly Asn Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Glu Ser Arg Val Thr Met Ser Ile Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Ile Tyr Tyr
85 90 95
Cys Ala Arg Gln Glu Phe Val Pro Gly Ala Glu Tyr Phe Leu His Trp
100 105 110
Gly Gln Gly Ile Leu Val Thr Val Ser Ser
115 120
<210> 196
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 196
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Asp
20 25 30
Leu Gly Trp His Gln Gln Lys Ser Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Ala Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ser Ala Thr Tyr Tyr Cys Leu Gln Gln Asn Ser Tyr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 197
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 197
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Gly Thr Gly Phe Ile Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Asn Ser Leu Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Lys Ser Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Asp Val Thr Arg Leu Glu Leu Arg Gly Phe Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Gln Val Thr Val Ser Ser
115 120
<210> 198
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 198
Glu Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Arg Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Ala Ile Lys
100 105
<210> 199
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 199
Asp Arg Gln Met Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ile Ala Ser Gly Phe Ile Ile Ser Arg Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Arg Asn Lys Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Glu Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Arg Val His Gln Phe Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 200
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 200
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Ile Thr Ile Thr Cys Arg Gly Ser Gln Asn Ile Gly Ser Phe
20 25 30
Leu Ser Trp Tyr Gln Gln Arg Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Phe Gly Ala Tyr Asn Leu Gln Gly Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 201
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 201
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Asn Asn Gly
20 25 30
Gly His Tyr Trp Thr Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ile Gly Thr Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Glu Ser Arg Leu Ser Leu Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Ile Tyr Tyr
85 90 95
Cys Ala Arg Ser Ser Leu Ser Val Ser Glu Ala Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 202
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 202
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Phe Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gly Ser Phe
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Asn Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 203
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 203
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Asn Gly
20 25 30
Gly Tyr Tyr Trp Thr Trp Ile Arg Gln Asn Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ile Gly Thr Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Glu Ser Arg Leu Ser Leu Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Ser Ser Leu Ala Val Ser Glu Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 204
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 204
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Thr Ile Ser Thr Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Arg Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Thr Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 205
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 205
Gln Val Gln Leu Val Gln Ser Gly Thr Glu Val Lys Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Thr Gly Tyr
20 25 30
Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro His Ser Gly Gly Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Asn Thr Ala Tyr
65 70 75 80
Leu Asp Leu Ile Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ile Gly Gly Gly Gly Tyr Ser Ser Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 206
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 206
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Thr Thr Ala Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Phe
85 90 95
Thr Phe Gly Ser Gly Thr Lys Val Asp Ile Lys
100 105
<210> 207
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 207
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asp Ile Ser Gly Ser Gly Leu Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ser Lys Asn Met Leu Tyr
65 70 75 80
Leu Gln Met Asn Arg Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Glu Pro Ser His Trp Asn Gly Glu Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 208
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 208
Glu Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Thr Val Ser Asn Ser
20 25 30
His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Thr Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Ser Leu Thr Ile Ile Arg Leu Glu
65 70 75 80
Pro Asp Asp Phe Ala Val Tyr Phe Cys Gln Gln His Glu Ser Ser Pro
85 90 95
Pro Thr Phe Gly Gln Gly Ala Lys Leu Glu Ile Lys
100 105
<210> 209
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 209
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Phe Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asn
20 25 30
Tyr Tyr Tyr Trp Gly Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr His Thr Gly Asn Ala Tyr Asp Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Ile Tyr Tyr
85 90 95
Cys Ala Arg His His Ser Ser Ser Ser Trp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Arg Gly Thr Leu Val Ile Val Ser Ser
115 120
<210> 210
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 210
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Trp Ile Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Pro Gly Ile Pro Gly Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Asn
100 105
<210> 211
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 211
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Leu Thr Ser Tyr Asp Gly Ser Lys Lys Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Lys Gly Gly Asp Asp Tyr Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 212
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 212
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Gly Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Asn
100 105
<210> 213
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 213
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Asn Asn
20 25 30
Gly Ile Ser Trp Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Pro Tyr Asn Gly Asn Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Thr Thr Val Tyr
65 70 75 80
Met Asp Val Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Asp Gly Pro Ile Thr Ile Ser Tyr Phe Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 214
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 214
Glu Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ala Gly Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Thr
100 105
<210> 215
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 215
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Asn Arg Tyr
20 25 30
Gly Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Thr Trp Tyr Asp Gly Arg Asn Lys Tyr Phe Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ser Phe Ser Arg Asp Ser Ser Thr Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Phe Gly Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 216
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 216
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Ile Leu Thr Ile Asn Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Asn Ser Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 217
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> синтетическая конструкция; антигенсвязывающий домен
<400> 217
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Gly Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr His Cys
85 90 95
Ala Arg Ser Gly Asn Phe Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛО ПРОТИВ LILRB1 И ЕГО ПРИМЕНЕНИЯ | 2021 |
|
RU2813373C1 |
| АНТИ-LILRB1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2801535C1 |
| ПОЛИПЕПТИД, ВКЛЮЧАЮЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2018 |
|
RU2815452C2 |
| CD47-АНТИГЕНСВЯЗЫВАЮЩАЯ ЕДИНИЦА И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2780859C2 |
| ИНДУЦИРУЮЩИЙ ЦИТОТОКСИЧНОСТЬ ТЕРАПЕВТИЧЕСКИЙ АГЕНТ | 2015 |
|
RU2743464C2 |
| АНТИТЕЛА К ТАУ И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2787779C2 |
| HPV-СПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2018 |
|
RU2804664C2 |
| АНТИГЕНСВЯЗЫВАЮЩАЯ МОЛЕКУЛА, СОДЕРЖАЩАЯ ДВА АНТИГЕНСВЯЗЫВАЮЩИХ ДОМЕНА, КОТОРЫЕ СВЯЗАНЫ ДРУГ С ДРУГОМ | 2019 |
|
RU2838581C2 |
| НОВОЕ АНТИ-С-МЕТ АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2751720C2 |
| Антитело против FXI/FXIA, его антигенсвязывающий фрагмент и фармацевтическое применение | 2021 |
|
RU2838408C1 |
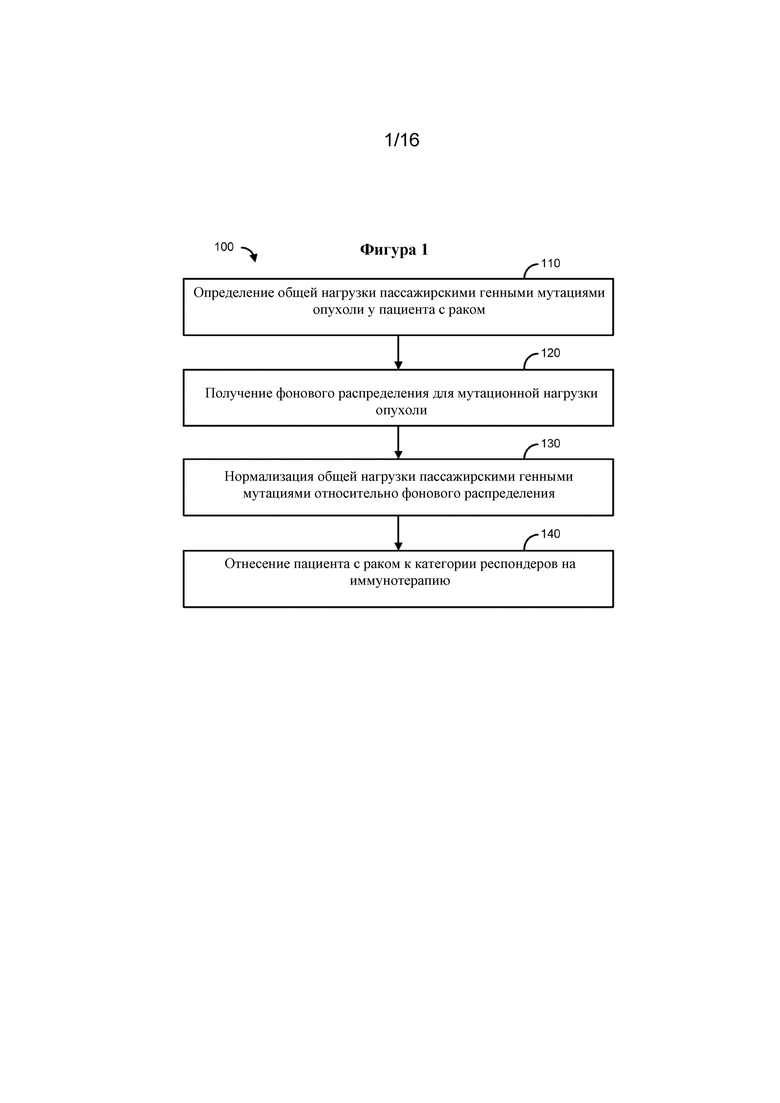
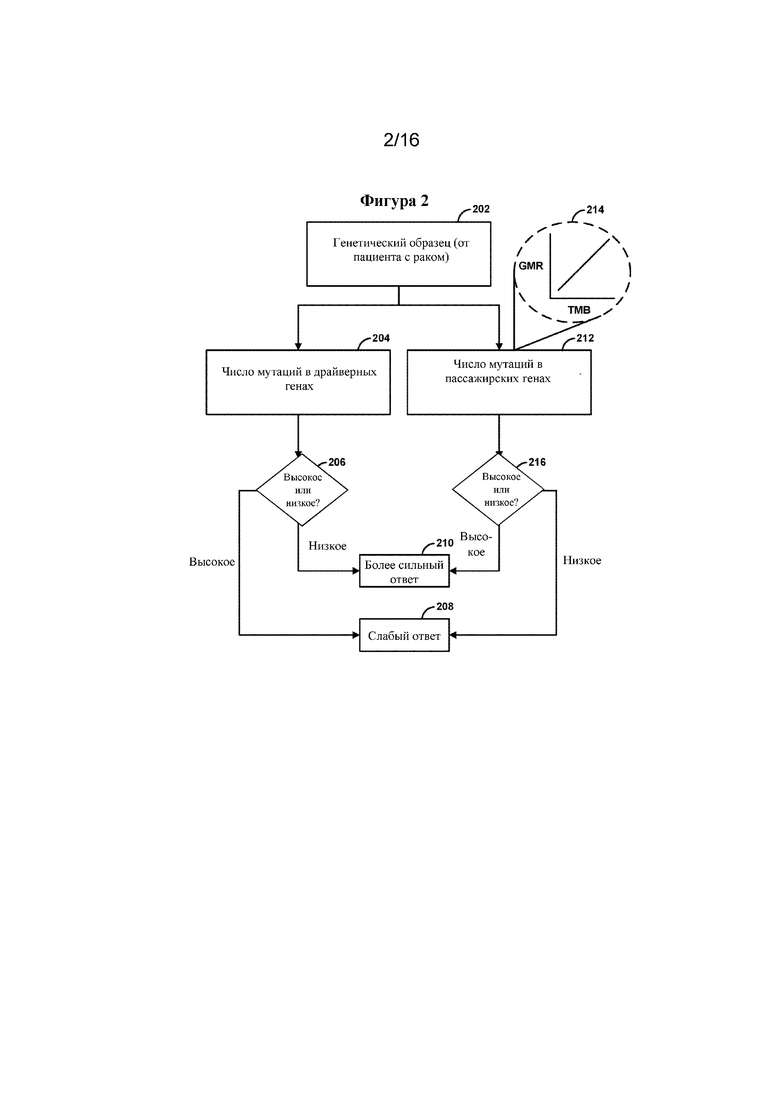
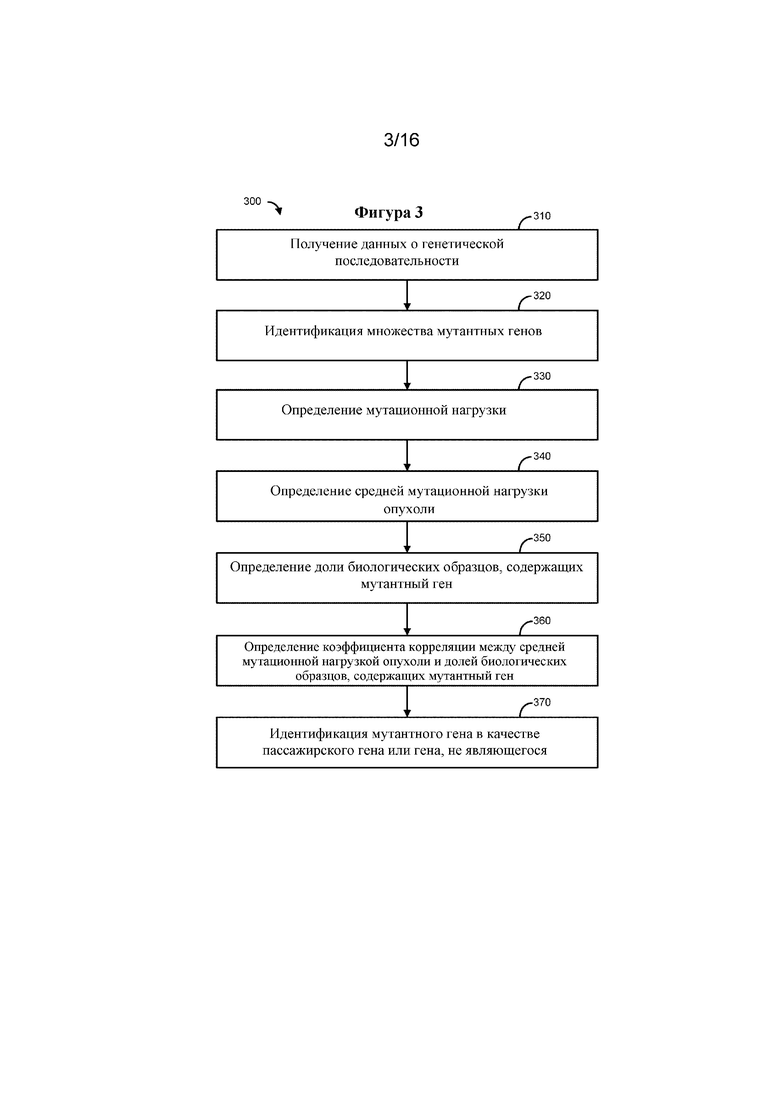
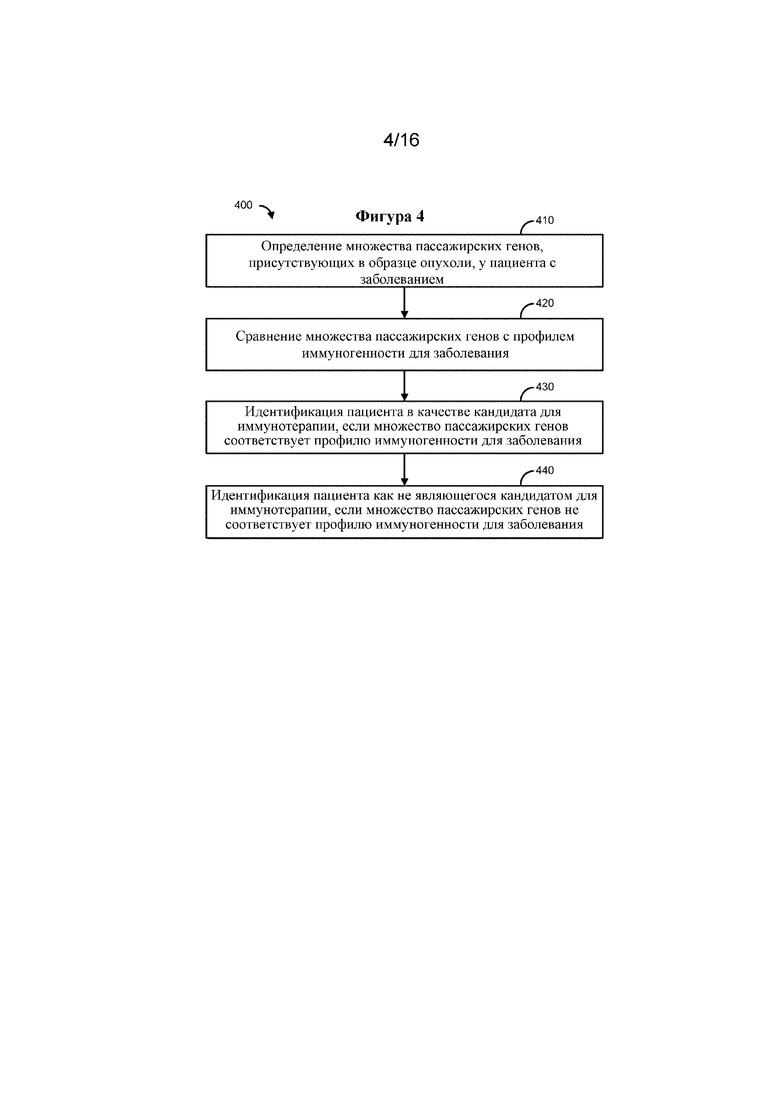
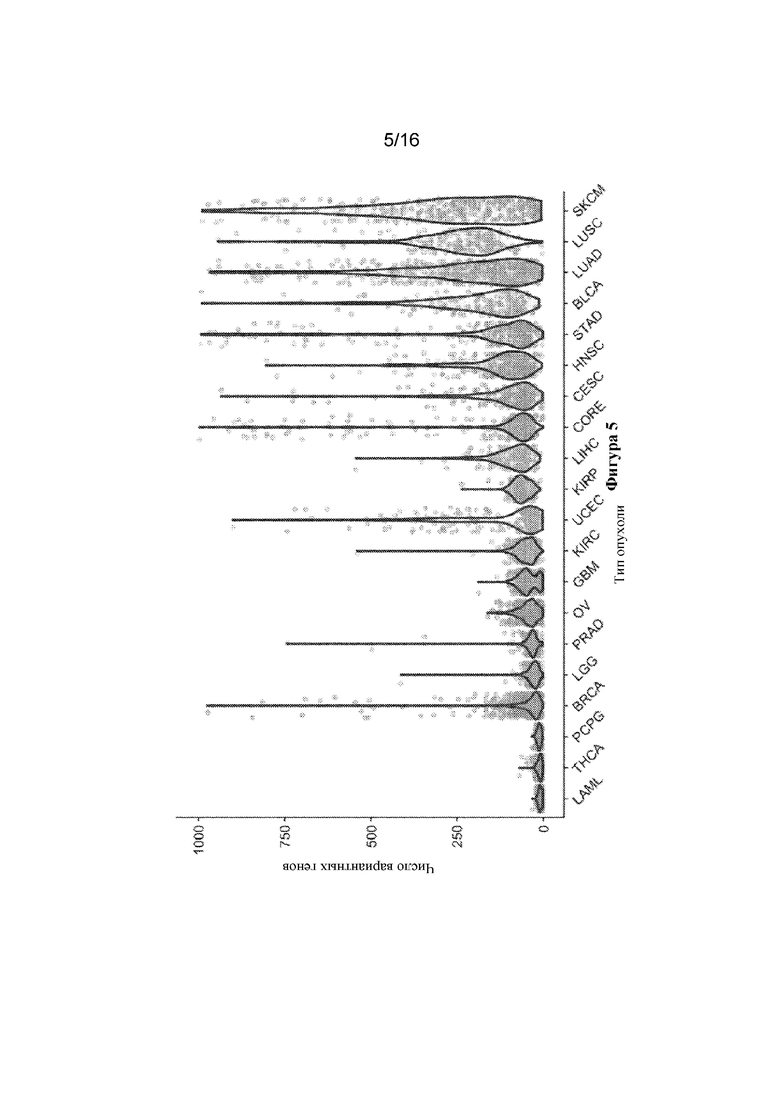
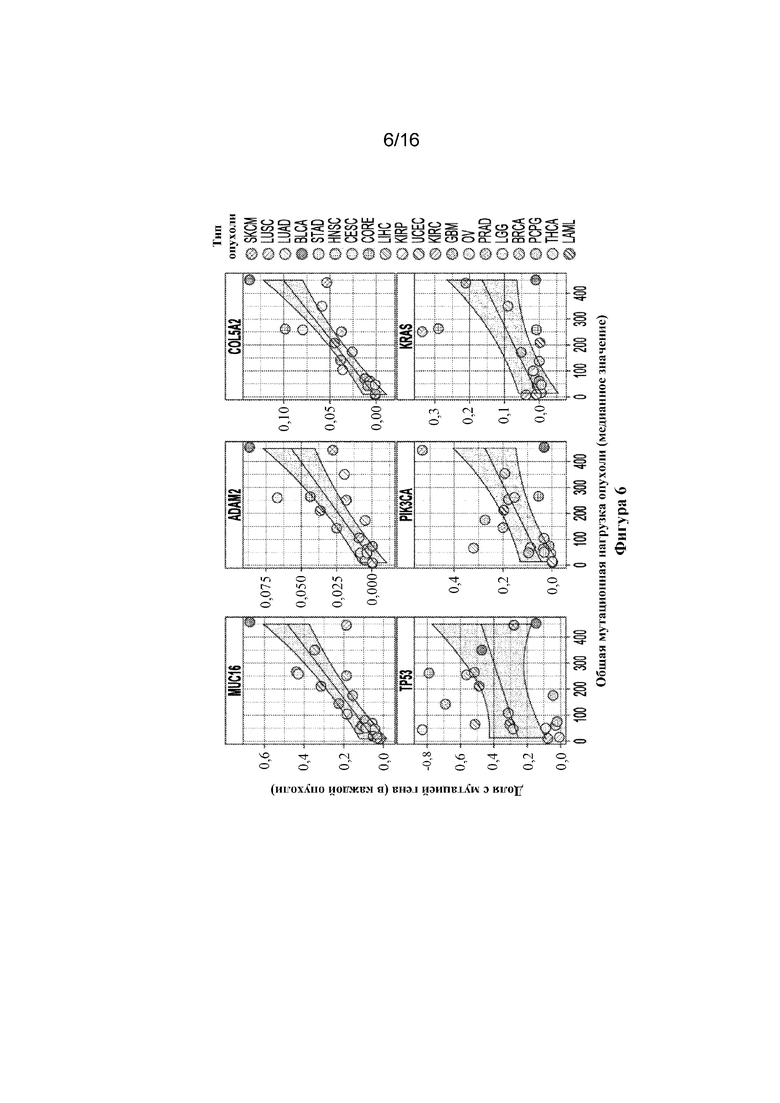
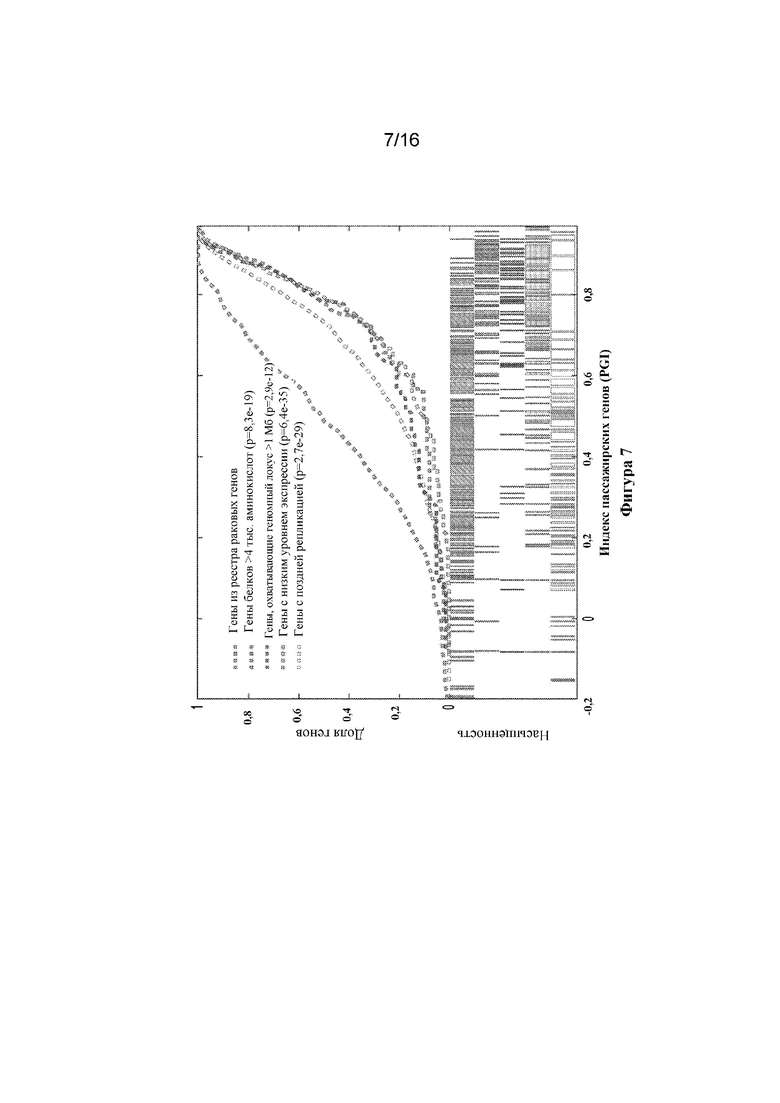
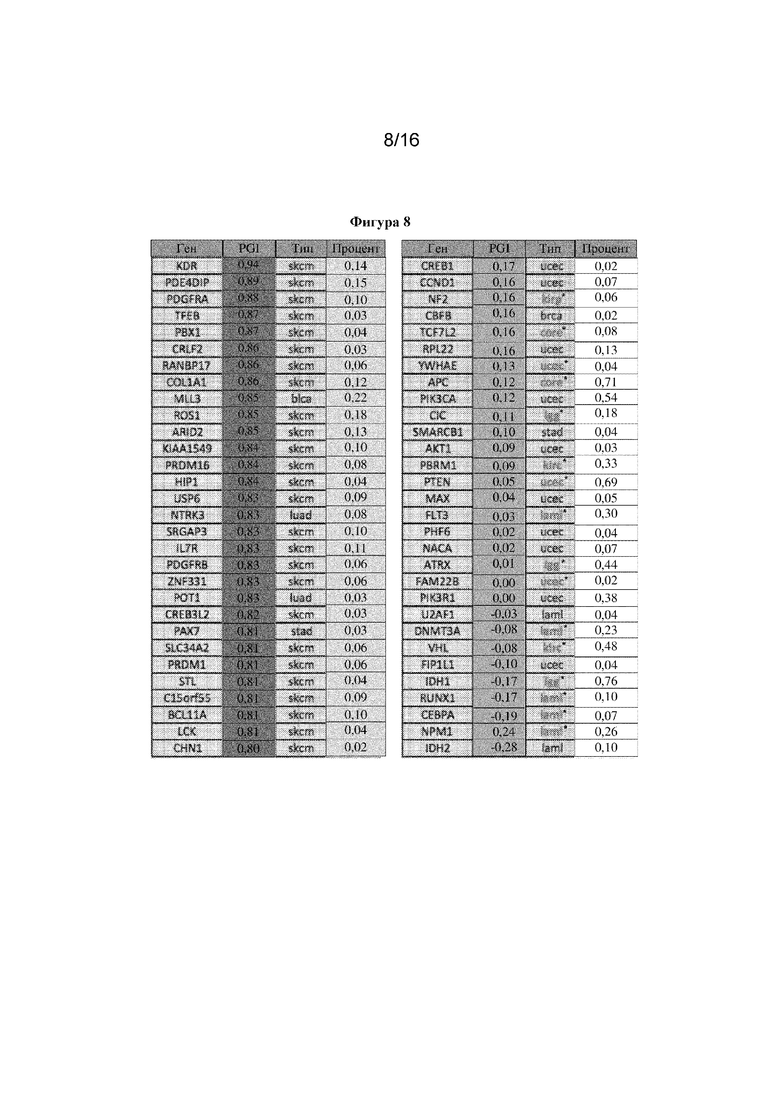
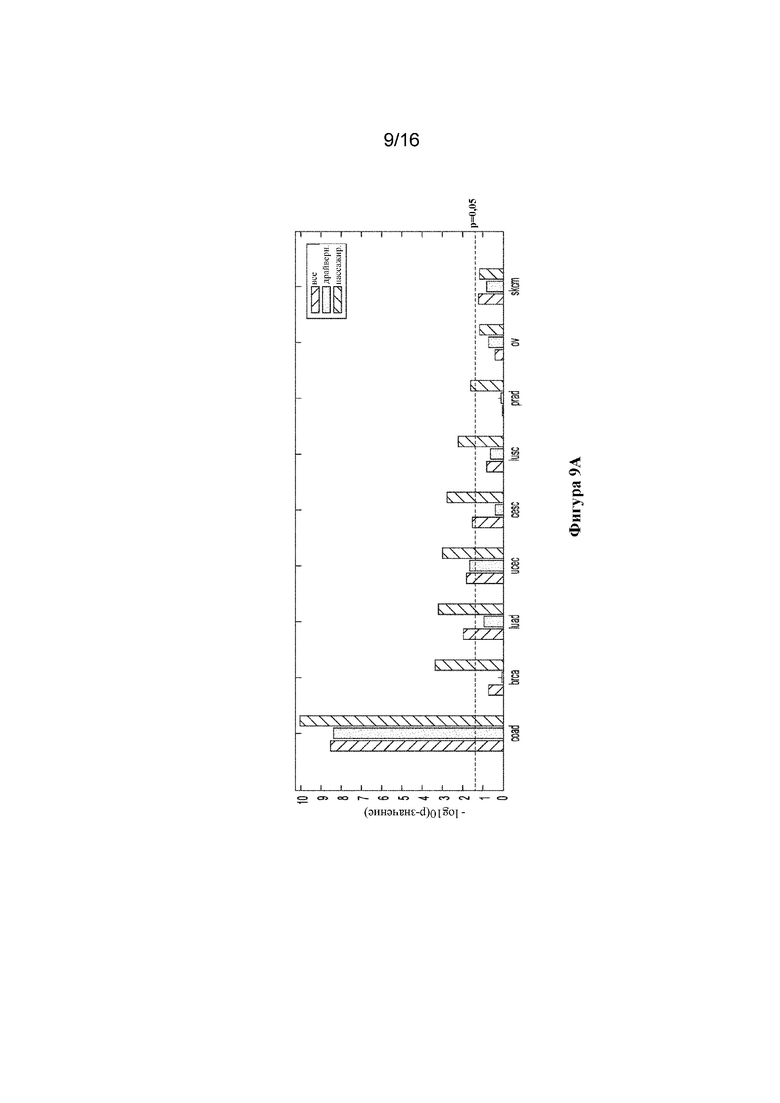
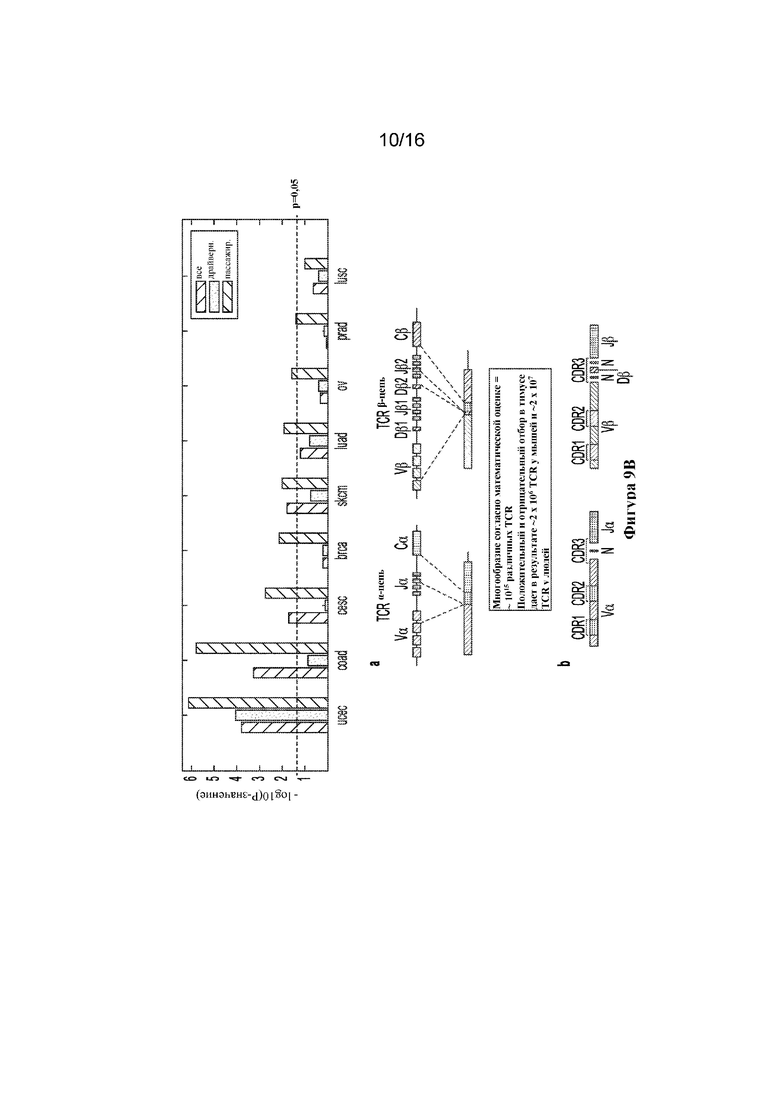
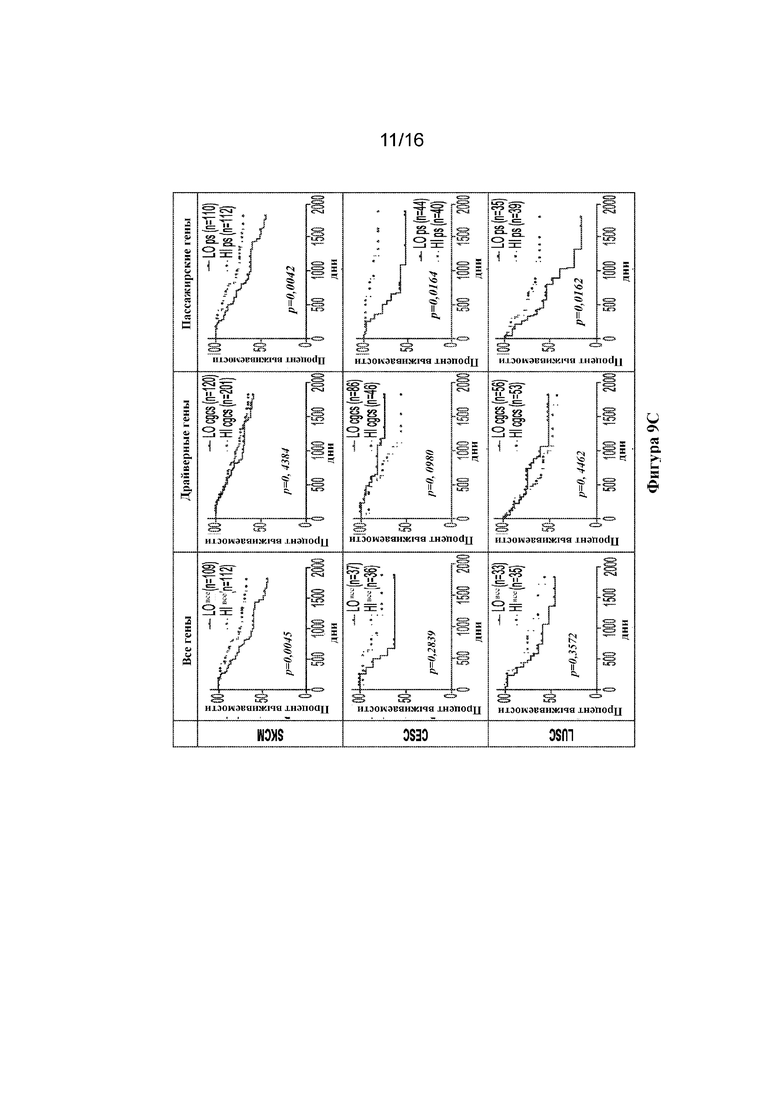
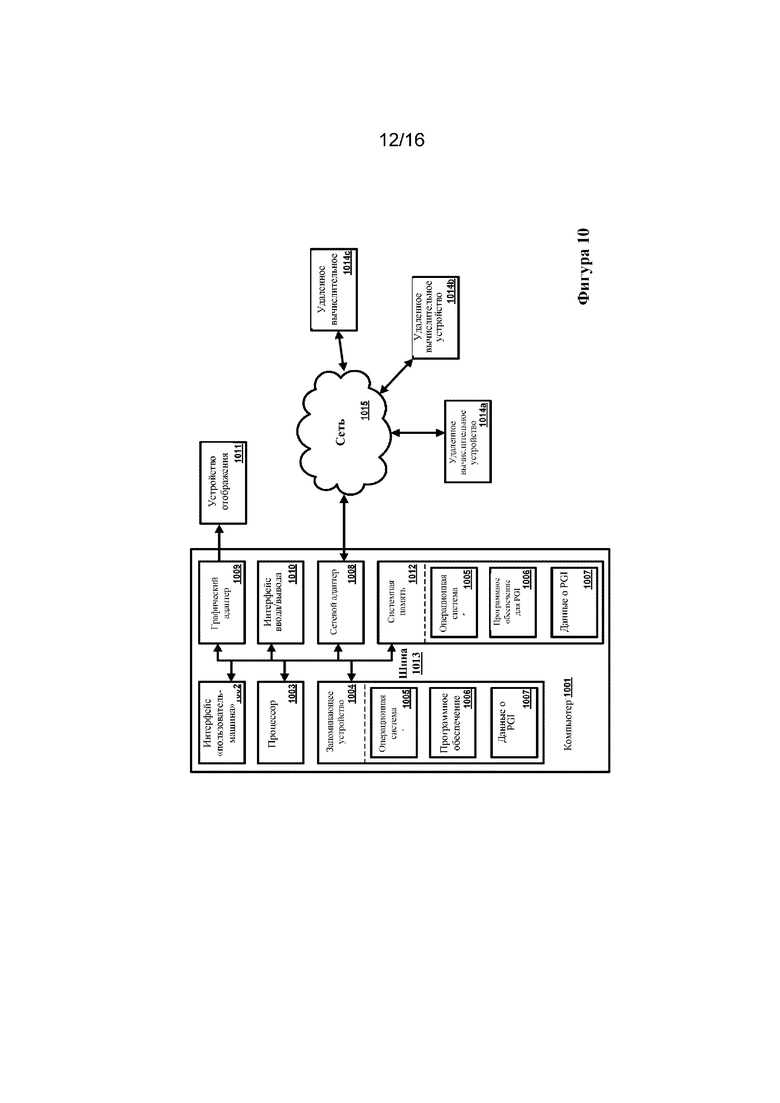

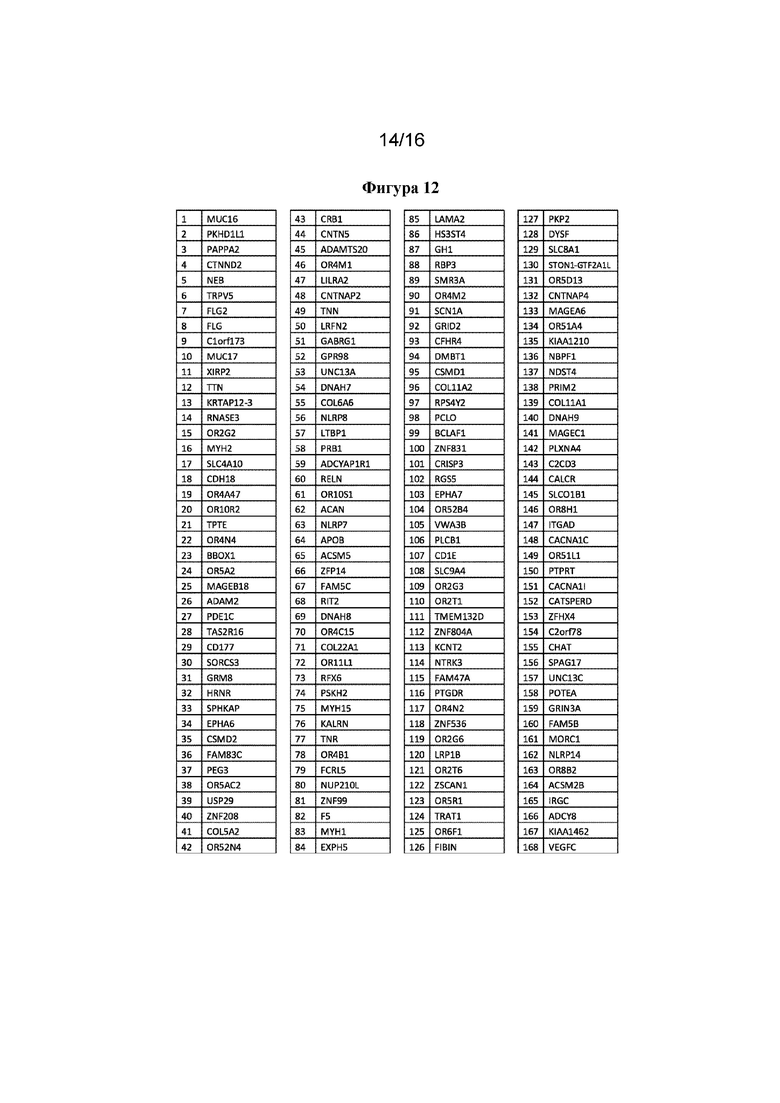
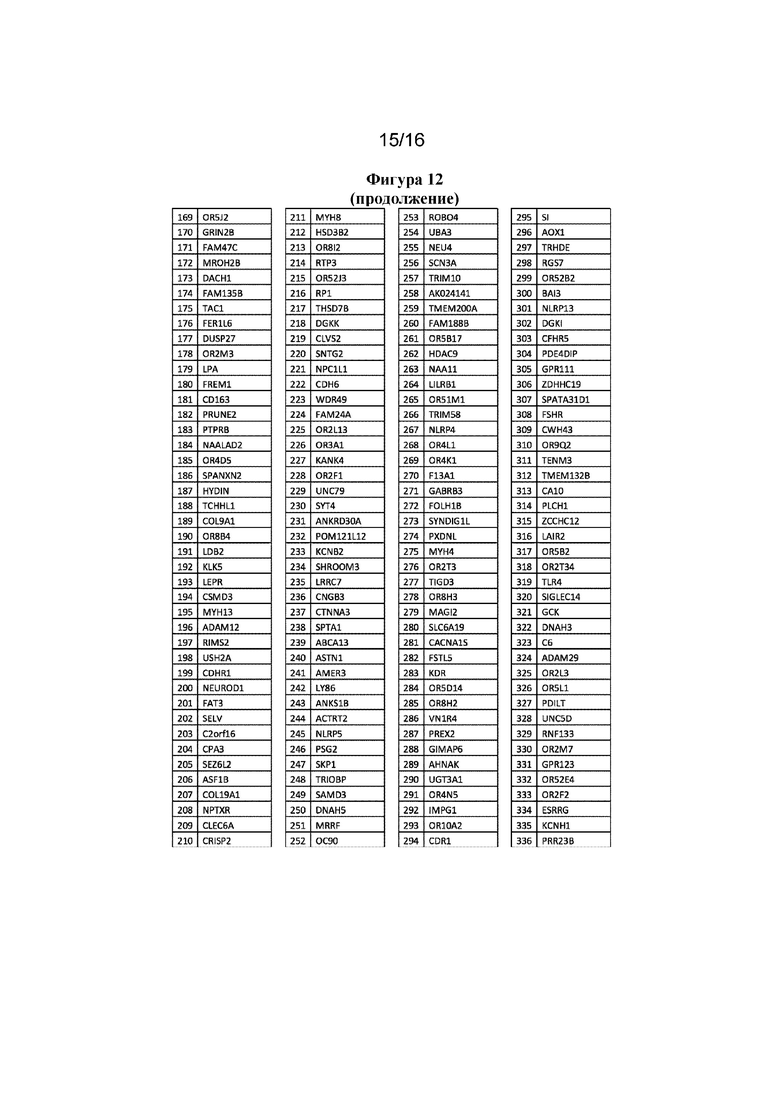
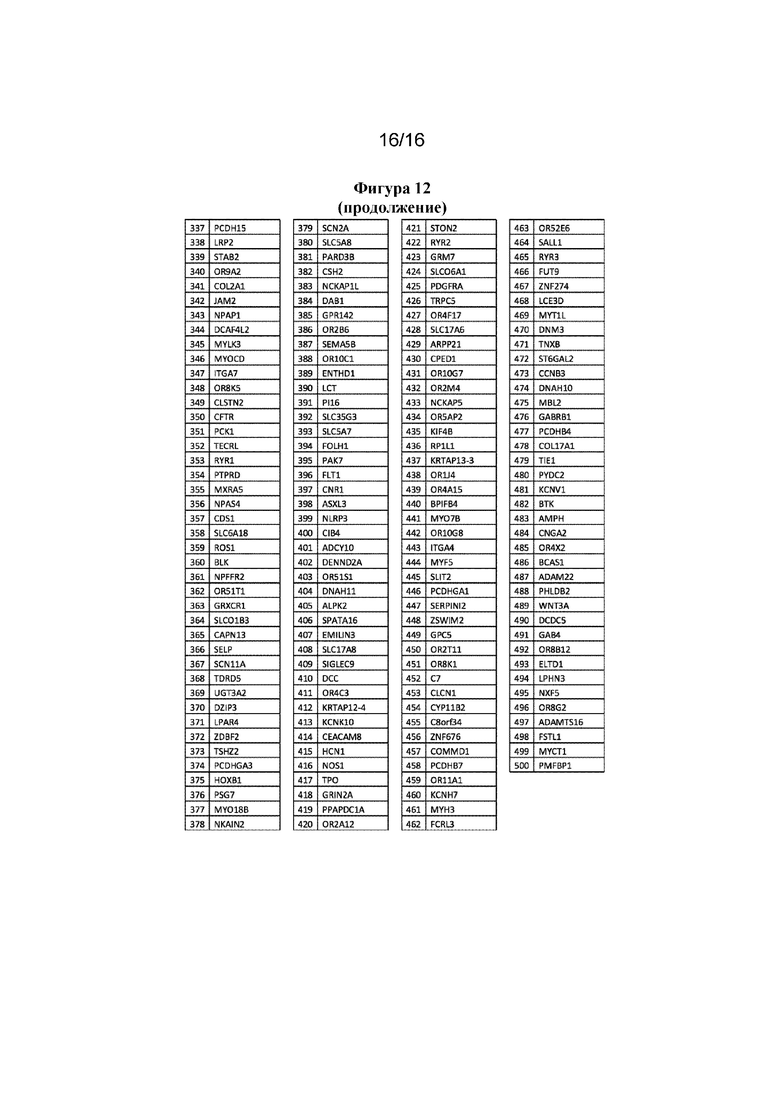
Изобретение относится к области биотехнологии. Предложено применение антитела, которое связывается с PD1 и ингибирует его, при производстве лекарственного средства для лечения субъекта с раком. При этом у субъекта было определено наличие опухоли с общей нагрузкой пассажирскими генными мутациями, превышающей фоновую мутационную нагрузку опухоли. Отбор пациента с раком для иммунотерапии предусматривает определение общей нагрузки пассажирскими генными мутациями опухоли у пациента с раком, получение фонового распределения для мутационной нагрузки опухоли, нормализацию общей нагрузки пассажирскими генными мутациями относительно фонового распределения и отнесение пациента с раком к категории респондеров на иммунотерапию, если общая нагрузка пассажирскими генными мутациями превышает среднее значение фонового распределения. Изобретение обеспечивает эффективный отбор пациентов – респондеров на иммунотерапию рака. 42 з.п. ф-лы, 14 ил., 4 табл., 4 пр.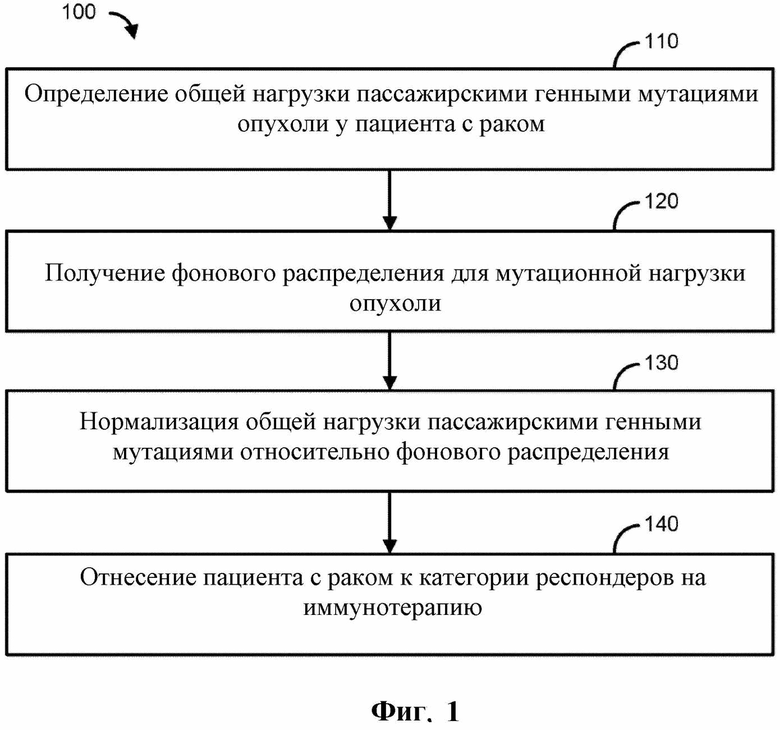
1. Применение антитела, которое связывается с PD1 и ингибирует его, при производстве лекарственного средства для лечения субъекта с раком, при этом у субъекта было определено наличие опухоли с общей нагрузкой пассажирскими генными мутациями, превышающей фоновую мутационную нагрузку опухоли.
2. Применение по п. 1, где нагрузка пассажирскими генными мутациями определяется как большая, чем фоновая мутационная нагрузка, посредством:
определения общей нагрузки пассажирскими генными мутациями опухоли;
создания фоновой мутационной нагрузки опухоли; и
нормализации общей нагрузки пассажирскими генными мутациями по отношению к фоновой мутационной нагрузке.
3. Применение по п. 2, отличающееся тем, что фоновая мутационная нагрузка определяется на основе случайно выбранных генов опухоли, и где количество случайно выбранных генов равно количеству пассажирских генов, используемых для определения общей нагрузки пассажирскими генными мутациями.
4. Применение по любому из пп. 2, 3, отличающееся тем, что нормализация общей нагрузки пассажирскими генными мутациями по отношению к фоновой мутационной нагрузке включает получение z-показателя, указывающего количество стандартных отклонений от среднего значения фоновой мутационной нагрузки.
5. Применение по любому из пп. 2-4, дополнительно включающее классификацию мутантного гена в опухоли в качестве пассажирского гена.
6. Применение по п. 5, отличающееся тем, что классификация мутантного гена в опухоли в качестве пассажирского гена включает выбор мутантного гена из опухоли и сопоставление мутантного гена со структурой данных, содержащей пассажирские гены, определенные в соответствии с индексом пассажирских генов.
7. Применение по п. 6, отличающееся тем, что индекс пассажирских генов предусматривает коэффициент корреляции между долей образцов, содержащих мутантный ген, полученных от когорты пациентов с раком, и медианным числом мутантных генов для каждого типа опухоли в когорте пациентов с раком.
8. Применение по любому из пп. 1-7, отличающееся тем, что антитело, которое связывается с PD1 и ингибирует его, включает последовательность вариабельного участка тяжелой цепи (HCVR), содержащую аминокислотную последовательность SEQ ID NO: 21.
9. Применение по п. 2, дополнительно включающее получение данных о генетической последовательности, где данные о генетической последовательности содержат множество генов и получены из опухоли пациента.
10. Применение по п. 2, где нагрузка пассажирскими генными мутациями больше, чем фоновая мутационная нагрузка, когда нормализованная нагрузка пассажирскими генными мутациями составляет по меньшей мере примерно 1, по меньшей мере примерно 1,5, по меньшей мере примерно 2, по меньшей мере примерно 2,5, по меньшей мере примерно 3 или более 3 стандартных отклонений, превышающих среднее значение фоновой мутационной нагрузки.
11. Применение по п. 1, где нагрузка пассажирскими генными мутациями определяется на основе одного или более пассажирских генов с частотой генетических мутаций, которая сильно коррелирует с общей частотой мутаций опухоли.
12. Применение по п. 1, где рак представляет собой плоскоклеточный рак кожи (CSCC), уротелиальную карциному мочевого пузыря (BLCA), инвазивную карциному молочной железы (BRCA), плоскоклеточную карциному шейки матки и эндоцервикальную аденокарциному (CESC), аденокарциному толстой кишки/прямой кишки (CORE), мультиформную глиобластому (GBM), плоскоклеточную карциному головы и шеи (HNSC), светлоклеточную карциному почки (KIRC), папиллярную почечно-клеточную карциному почки (KIRP), острый миелоидный лейкоз (LAML), гепатоцеллюлярную карциному печени (LIHC), глиому головного мозга низкой степени злокачественности (LGG), аденокарциному легкого (LUAD), плоскоклеточную карциному легкого (LUSC), серозную цистаденокарциному яичника (OV), феохромоцитому и параганглиому (PCPG), аденокарциному предстательной железы (PRAD), меланому кожи (SKCM) эндометриоидную карциному тела матки или аденокарциному желудка.
13. Применение по п. 1, где рак включает рак легкого.
14. Применение по п. 13, где рак легкого включает немелкоклеточную карциному легкого.
15. Применение по п. 1, где рак включает рак кожи.
16. Применение по п. 15, где рак кожи включает плоскоклеточный рак кожи (CSCC).
17. Применение по п. 1, где рак включает рак шейки матки.
18. Применение по п. 8, где рак представляет собой cutaneous плоскоклеточный рак кожи (CSCC), уротелиальную карциному мочевого пузыря (BLCA), инвазивную карциному молочной железы (BRCA), плоскоклеточную карциному шейки матки и эндоцервикальную аденокарциному (CESC), аденокарциному толстой кишки/прямой кишки (CORE), мультиформную глиобластому (GBM), плоскоклеточную карциному головы и шеи (HNSC), светлоклеточную карциному почки (KIRC), папиллярную почечно-клеточную карциному почки (KIRP), острый миелоидный лейкоз (LAML), гепатоцеллюлярную карциному печени (LIHC), глиому головного мозга низкой степени злокачественности (LGG), аденокарциному легкого (LUAD), плоскоклеточную карциному легкого (LUSC), серозную цистаденокарциному яичника (OV), феохромоцитому и параганглиому (PCPG), аденокарциному предстательной железы (PRAD), меланому кожи (SKCM), эндометриоидную карциному тела матки или аденокарциному желудка.
19. Применение по п. 8, где рак включает рак легкого.
20. Применение по п. 19, где рак легкого включает немелкоклеточную карциному легкого.
21. Применение по п. 8, где рак включает рак кожи.
22. Применение по п. 21, где рак кожи включает плоскоклеточный рак кожи (CSCC).
23. Применение по п. 8, где рак включает рак шейки матки.
24. Применение по п. 8, где антитело, которое связывается с PD1 и ингибирует его, дополнительно включает последовательность вариабельного участка легкой цепи (LCVR), содержащую аминокислотную последовательность SEQ ID NO: 22.
25. Применение по п. 24, где рак представляет собой плоскоклеточный рак кожи (CSCC), уротелиальную карциному мочевого пузыря (BLCA), инвазивную карциному молочной железы (BRCA), плоскоклеточную карциному шейки матки и эндоцервикальную аденокарциному (CESC), аденокарциному толстой кишки/прямой кишки (CORE), мультиформную глиобластому (GBM), плоскоклеточную карциному головы и шеи (HNSC), светлоклеточную карциному почки (KIRC), папиллярную почечно-клеточную карциному почки (KIRP), острый миелоидный лейкоз (LAML), гепатоцеллюлярную карциному печени (LIHC), глиому головного мозга низкой степени злокачественности (LGG), аденокарциному легкого (LUAD), плоскоклеточную карциному легкого (LUSC), серозную цистаденокарциному яичника (OV), феохромоцитому и параганглиому (PCPG), аденокарциному предстательной железы (PRAD), меланому кожи (SKCM) эндометриоидную карциному тела матки или аденокарциному желудка.
26. Применение по п. 24, где рак включает рак легкого.
27. Применение по п. 26, где рак легкого включает немелкоклеточную карциному легкого.
28. Применение по п. 24, где рак включает рак кожи.
29. Применение по п. 28, где рак кожи включает плоскоклеточный рак кожи (CSCC).
30. Применение по п. 24, где рак включает рак шейки матки.
31. Применение по п. 24, где антитело, которое связывается с PD1 и ингибирует его, включает цемиплимаб.
32. Применение по п. 31, где рак представляет собой плоскоклеточный рак кожи (CSCC), уротелиальную карциному мочевого пузыря (BLCA), инвазивную карциному молочной железы (BRCA), плоскоклеточную карциному шейки матки и эндоцервикальную аденокарциному (CESC), аденокарциному толстой кишки/прямой кишки (CORE), мультиформную глиобластому (GBM), плоскоклеточную карциному головы и шеи (HNSC), светлоклеточную карциному почки (KIRC), папиллярную почечно-клеточную карциному почки (KIRP), острый миелоидный лейкоз (LAML), гепатоцеллюлярную карциному печени (LIHC), глиому головного мозга низкой степени злокачественности (LGG), аденокарциному легкого (LUAD), плоскоклеточную карциному легкого (LUSC), серозную цистаденокарциному яичника (OV), феохромоцитому и параганглиому (PCPG), аденокарциному предстательной железы (PRAD), меланому кожи (SKCM) эндометриоидную карциному тела матки или аденокарциному желудка.
33. Применение по п. 31, где рак включает рак легкого.
34. Применение по п. 33, где рак легкого включает немелкоклеточную карциному легкого.
35. Применение по п. 31, где рак включает рак кожи.
36. Применение по п. 35, где рак кожи включает плоскоклеточный рак кожи (CSCC).
37. Применение по п. 31, где рак включает рак шейки матки.
38. Применение антитела по любому из пп. 1-37, где применение также включает антитело, которое связывается с LAG3 и ингибирует его.
39. Применение по п. 38, где антитело, которое связывается с LAG3 и ингибирует его, содержит вариабельный участок тяжелой цепи (HCVR), включающий аминокислотную последовательность SEQ ID NO: 93.
40. Применение по п. 38 или 39, где антитело, которое связывается с LAG3 и ингибирует его, также содержит вариабельный участок легкой цепи (LCVR), включающий аминокислотную последовательность SEQ ID NO: 94.
41. Применение антитела по любому из пп. 1-37, где применение также включает антитело, которое связывается с PDL1 и ингибирует его.
42. Применение по п. 41, где антитело, которое связывается с PDL1 и ингибирует его, содержит по меньшей мере последовательность HCVR SEQ ID NO: 122 и последовательность LCVR SEQ ID NO: 123.
43. Применение антитела по любому из пп. 1-37, где применение также включает антитело, которое связывается с CTLA4 и ингибирует его.
| WO 2017151517 A1, 08.09.2017 | |||
| WO 2017151524 A1, 08.09.2017 | |||
| TOPALIAN S.L | |||
| et al | |||
| Mechanism-driven biomarkers to guide immune checkpoint blockade in cancer therapy, NATURE REVIEWS | |||
| CANCER, 2016, vol.16, no.5, pp.275-287 | |||
| RIZVI N.A | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2024-05-21—Публикация
2018-09-19—Подача