ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к антителу к ВСМА (антиген созревания В-клеток), его антигенсвязывающему фрагменту и их медицинскому применению. Кроме того, настоящее изобретение относится к антителу к ВСМА и его антигенсвязывающему фрагменту, и к содержащей их фармацевтической композиции, для применения для обнаружения или лечения ВСМА-опосредованных заболеваний или состояний.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
В-клетки представляют собой лимфоциты, играющие важную роль в адаптивном гуморальном иммунитете и выработке антител, специфически распознающих антигены. Три подтипа В-клеток представляют собой наивные В-клетки, В-клетки памяти и плазматические клетки. В процессе рекомбинации VDJ два или три фрагмента ДНК, выбранные из геномной библиотеки, рекомбинируются для получения комбинаторного массива вариабельных доменов антител, таким образом, создается не более 109 уникальных линий В-клеток путем дальнейшего изменения вариабельных доменов, кодируемых В-клетками разных линий, что приводит к антителам, специфичным к уникальным мишеням. В-клетки участвуют во многих заболеваниях. Злокачественная трансформация В-клеток приводит к раку, в том числе к некоторым лимфомам, таким как множественная миелома и лимфома Ходжкина. В-клетки также участвуют в аутоиммунных заболеваниях, включая системную красную волчанку (СКВ) и IgA-нефропатию. Рак, связанный с В-клетками, и аутоиммунные заболевания можно рассматривать как нарушение функции В-клеток, поэтому возможной стратегией контроля таких заболеваний является применение антител, нацеленных на патологические В-клетки.
ВСМА (CD269 (антиген 269 кластера дифференцировки) или TNFRSF 17 (рецептор 17 надсемейства рецепторов фактора некроза опухоли)) является членом суперсемейства рецепторов TNF (фактор некроза опухоли), который представляет собой негликозилированный внутренний мембранный рецептор для лигандов BAFF (активатор В-клеток) и APRIL (лиганд, индуцирующий пролиферацию). ВСМА и его соответствующие лиганды могут регулировать различные функции гуморального иммунитета, развитие В-клеток и гомеостаз. ВСМА обнаружен в селезенке, лимфатических узлах, тимусе, надпочечниках и печени. Он экспрессируется плазмобластами человека, плазматическими клетками миндалевидной железы, селезенки и костного мозга, а также В-клетками памяти миндалевидной железы и В-клетками герминативного центра, и различные анализы линий В-клеток показывают, что уровень экспрессии ВСМА увеличивается после созревания. ВСМА высоко экспрессируется при В-клеточной лимфоме и множественной миеломе.
Антитела к ВСМА описаны, например, в Gras М-Р. et al. Lit Immunol. 7 (1995) 1093-1106, WO200124811, WO200124812, WO2010104949 и WO2012163805. Антитела к ВСМА и их применение для лечения лимфомы и множественной миеломы описаны, например, в WO2002066516 и WO2010104949. WO2013154760 относится к химерному рецептору антигена, содержащему фрагмент, распознающий ВСМА, и фрагмент, активирующий Т-клетки.
В US9273141 описан антигенсвязывающий белок, способный интернализоваться, который специфически связывается с ВСМА и ингибирует связывание BAFF и/или APRIL с ВСМА, а также описан конъюгат, содержащий указанный антигенсвязывающий белок и цитотоксический агент.
Согласно настоящему изобретению предложено антитело к ВСМА с высокой аффинностью, высокой специфичностью, низкой иммуногенностью, высокой биологической активностью, значительным противоопухолевым действием и усиленным эндоцитозом, а также цитотоксический конъюгат, содержащий указанное антитело, и их применение для ингибирования опухолей.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно некоторым вариантам осуществления настоящего изобретения предложено антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемая соль, содержащие:
вариабельную область тяжелой цепи антитела, содержащую по меньшей мере одну HCDR (определяющая комплементарность область тяжелой цепи), представленную в последовательности, выбранной из группы, состоящей из SEQ ID NO: 3, SEQ ID NO: 4 и SEQ ID NO: 5; и
вариабельную область легкой цепи антитела, содержащую по меньшей мере одну LCDR (определяющая комплементарность область легкой цепи), представленную в последовательности, выбранной из группы, состоящей из SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8.
В предпочтительном варианте осуществления настоящего изобретения вариабельная область тяжелой цепи антитела к ВСМА или его антигенсвязывающего фрагмента содержат:
HCDR1, представленную в SEQ ID NO: 3,
HCDR2, представленную в SEQ ID NO: 4 и
HCDR3, представленную в SEQ ID NO: 5.
В предпочтительном варианте осуществления настоящего изобретения вариабельная область легкой цепи антитела к ВСМА или его антигенсвязывающего фрагмента содержат:
LCDR1, представленную в SEQ ID NO: 6,
LCDR2, представленную в SEQ ID NO: 7 и
LCDR3, представленную в SEQ ID NO: 8.
В предпочтительном варианте осуществления настоящего изобретения антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи и вариабельную область легкой цепи, причем вариабельная область тяжелой цепи содержит:
HCDR1, представленную в SEQ ID NO: 3,
HCDR2, представленную в SEQ ID NO: 4 и
HCDR3, представленную в SEQ ID NO: 5; и
вариабельная область легкой цепи содержит:
LCDR1, представленную в SEQ ID NO: 6,
LCDR2, представленную в SEQ ID NO: 7 и
LCDR3, представленную в SEQ ID NO: 8.
В соответствии с некоторыми вариантами осуществления настоящего изобретения предложены антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемая соль, причем антитело к ВСМА или его антигенсвязывающий фрагмент содержат по меньшей мере одну HCDR, выбранную из SEQ ID NO: 3, SEQ ID NO: 4 и SEQ ID NO: 5, или их мутантные последовательности.
В соответствии с некоторыми вариантами осуществления настоящего изобретения предложены антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемая соль, причем антитело к ВСМА или его антигенсвязывающий фрагмент содержат по меньшей мере одну LCDR, выбранную из SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, или их мутантные последовательности.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи, которая содержит:
HCDR1, представленную в SEQ ID NO: 3, или ее мутантную последовательность,
HCDR2, представленную в SEQ ID NO: 4, или ее мутантную последовательность, и
HCDR3, представленную в SEQ ID NO: 5, или ее мутантную последовательность.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, вариабельная область легкой цепи антитела к ВСМА или его антигенсвязывающего фрагмента содержит:
LCDR1, представленную в SEQ ID NO: 6, или ее мутантную последовательность,
LCDR2, представленную в SEQ ID NO: 7, или ее мутантную последовательность, и
LCDR3, представленную в SEQ ID NO: 8, или ее мутантную последовательность.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи антитела и вариабельную область легкой цепи антитела, причем вариабельная область тяжелой цепи содержит:
HCDR1, представленную в мутантной последовательности SEQ ID NO: 3,
HCDR2, представленную в мутантной последовательности SEQ ID NO: 4 и
HCDR3, представленную в мутантной последовательности SEQ ID NO: 5; и
вариабельная область легкой цепи содержит:
LCDR1, представленную в мутантной последовательности SEQ ID NO: 6,
LCDR2, представленную в мутантной последовательности SEQ ID NO: 7 и
LCDR3, представленную в мутантной последовательности SEQ ID NO: 8.
В предпочтительном варианте осуществления настоящего изобретения предложены антитело к ВСМА или его антигенсвязывающий фрагмент или его фармацевтически приемлемая соль, как описано выше, где мутантная последовательность имеет от 1 до 3 аминокислотных мутаций в области CDR (определяющая комплементарность область), которые оптимизируют активность антитела, стабильность антитела или снижение иммуногенности.
В предпочтительном варианте осуществления настоящего изобретения антитело к ВСМА или его антигенсвязывающий фрагмент представляет собой мышиное антитело.
В предпочтительном варианте осуществления настоящего изобретения антитело к ВСМА или его антигенсвязывающий фрагмент представляет собой химерное антитело.
В предпочтительном варианте осуществления настоящего изобретения антитело к ВСМА или его антигенсвязывающий фрагмент представляет собой человеческое антитело.
В предпочтительном варианте осуществления настоящего изобретения антитело к ВСМА или его антигенсвязывающий фрагмент представляет собой гуманизированное антитело.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент дополнительно содержат константную область тяжелой цепи, полученную из человеческого IgG1 (иммуноглобулин G1) или его варианта, IgG2 или его варианта, IgG3 или его варианта или IgG4 или его варианта.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент дополнительно содержат константную область тяжелой цепи, полученную из человеческого IgG1, IgG2 или IgG4.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент дополнительно содержат константную область тяжелой цепи IgG1, с повышенной ADCC-токсичность (антителозависимая клеточная цитотоксичность) после аминокислотной мутации.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент дополнительно содержат константную область тяжелой цепи, представленную в SEQ ID: 22.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент дополнительно содержат константную область легкой цепи, полученную из человеческой κ-цепи или ее варианте, λ-цепи или ее варианта.
В предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент дополнительно содержат константную область легкой цепи, представленную в SEQ ID: 23.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА, или его антигенсвязывающего фрагмента, или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА, или его антигенсвязывающий фрагмент, или его фармацевтически приемлемая соль содержат вариабельную область тяжелой цепи, представленную в последовательности, выбранной из группы, состоящей из SEQ ID NO: 9, SEQ ID NO: 10 и SEQ ID NO: 11.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи, идентичную по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99% SEQ ID NO: 9, SEQ ID NO: 10 или SEQ ID NO: 11.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА, или его антигенсвязывающего фрагмента, или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА, или его антигенсвязывающий фрагмент, содержат вариабельную область легкой цепи, представленную в последовательности, выбранной из группы, состоящей из SEQ ID NO: 12, SEQ ID NO: 13 и SEQ ID NO: 14.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область легкой цепи, идентичную по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99% SEQ ID NO: 12, SEQ ID NO: 13 или SEQ ID NO: 14.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь, представленную в SEQ ID NO: 15, SEQ ID NO: 16 или SEQ ID NO: 17.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь, идентичную по меньшей мере на 80%, 85%, 90%, 95% или 99% SEQ Ш NO: 15, SEQ ID NO: 16 или SEQ ID NO: 17.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат легкую цепь, представленную в SEQ ID NO: 18, SEQ ID NO: 19 или SEQ ID NO: 20.
В дополнительном предпочтительном варианте осуществления антитела к ВСМА или его антигенсвязывающего фрагмента или его фармацевтически приемлемой соли по настоящему изобретению, антитело к ВСМА или его антигенсвязывающий фрагмент содержат легкую цепь, идентичную по меньшей мере на 80%, 85%, 90%, 95% или 99% SEQ ID NO: 18, SEQ ID NO: 19 или SEQ ID NO: 20.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи, представленную в SEQ ID NO: 9 и вариабельную область легкой цепи, представленную в SEQ ID NO: 12.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, причем вариабельная область тяжелой цепи выбрана из SEQ ID NO: 9 или идентичной ей по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99%, и вариабельная область легкой цепи выбрана из SEQ ID NO: 12 или идентичной ей по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99%.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи, представленную в SEQ ID NO: 10 и вариабельную область легкой цепи, представленную в SEQ ID NO: 13.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи и вариабельную область легкой цепи, причем вариабельная область тяжелой цепи выбрана из SEQ ID NO: 10 или идентичной ей по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99%, и вариабельная область легкой цепи выбрана из SEQ ID NO: 13 или идентичной ей по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99%.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи, представленную в SEQ ID NO: 11 и вариабельную область легкой цепи, представленную в SEQ ID NO: 14.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи и вариабельную область легкой цепи, причем вариабельная область тяжелой цепи выбрана из SEQ ID NO: 11 или идентичной ей по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99%, и вариабельная область легкой цепи выбрана из SEQ ID NO: 14 или идентичной ей по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95% или 99%.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь, представленную в SEQ ID NO: 15 и легкую цепь, представленную в SEQ ID NO: 18.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь и легкую цепь, причем тяжелая цепь выбрана из SEQ ID NO: 15 или идентичной ей по меньшей мере на 80%, 85%, 90%, 95% или 99%, и легкая цепь выбрана из SEQ ID NO: 18 или идентичной ей по меньшей мере на 80%, 85%, 90%, 95% или 99%.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь, представленную в SEQ ID NO: 16 и легкую цепь, представленную в SEQ ID NO: 19.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь и легкую цепь, причем тяжелая цепь выбрана из SEQ ID NO: 16 или идентичной ей по меньшей мере на 80%, 85%, 90%, 95% или 99%, и легкая цепь выбрана из SEQ ID NO: 19 или идентичной ей по меньшей мере на 80%, 85%, 90%, 95% или 99%.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь, представленную в SEQ ID NO: 17 и легкую цепь, представленную в SEQ ID NO: 20.
В более предпочтительном варианте осуществления настоящего изобретения, антитело к ВСМА или его антигенсвязывающий фрагмент содержат тяжелую цепь и легкую цепь, причем тяжелая цепь выбрана из SEQ ID NO: 17 или идентичной ей по меньшей мере на 80%, 85%, 90%, 95% или 99%, и легкая цепь выбрана из SEQ ID NO: 20 или идентичной ей по меньшей мере на 80%, 85%, 90%, 95% или 99%.
В еще одном варианте осуществления настоящего изобретения предложен полинуклеотид, кодирующий антитело к ВСМА или его антигенсвязывающий фрагмент по настоящему изобретению.
В еще одном варианте осуществления настоящего изобретения предложен вектор экспрессии, содержащий полинуклеотид по настоящему изобретению.
В еще одном варианте осуществления настоящего изобретения предложена клетка-хозяин, в которую введен или которая содержит вектор экспрессии по настоящему изобретению.
В еще одном варианте осуществления настоящего изобретения предложена клетка-хозяин, трансформированная вектором экспрессии по настоящему изобретению.
В предпочтительном варианте осуществления настоящего изобретения, клетка-хозяин представляет собой бактерию, предпочтительно Escherichia coli.
В предпочтительном варианте осуществления настоящего изобретения, клетка-хозяин представляет собой дрожжи, предпочтительно Pichia pastoris.
В предпочтительном варианте осуществления настоящего изобретения, клетка-хозяин представляет собой клетку млекопитающего, предпочтительно клетку СНО (яичник китайского хомячка) или клетку НЕК293 (эмбриональная почка человека).
В другом аспекте настоящего изобретения предложен способ получения антитела к ВСМА, включающий этапы:
культивирования клетки-хозяина по настоящему изобретением;
выделения антитела из культуры; и
очистки антител.
Способ получения антитела к ВСМА, предложенного по настоящему изобретению, где:
культивирование клетки-хозяина по настоящему изобретению, предпочтительно клетки НЕК293;
выделение антитела из культуры, предпочтительно из культуральной жидкости; и очистка антитела аффинной хроматографией, предпочтительно методом хроматографии.
В еще одном варианте осуществления настоящего изобретения предложена фармацевтическая композиция, содержащая антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемую соль по настоящему изобретению, а также фармацевтически приемлемый эксципиент, разбавитель или носитель.
В еще одном варианте осуществления настоящего изобретения предложен реагент для обнаружения или диагностики, содержащий антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемую соль по настоящему изобретению.
В еще одном варианте осуществления настоящего изобретения предложен набор для обнаружения или диагностики, содержащий антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемую соль по настоящему изобретению, а также меченое вторичное антитело, буфер и субстрат, пригодный для обнаружения или диагностики.
В другом варианте осуществления настоящего изобретения предложен набор для обнаружения или диагностики, содержащий антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемую соль по настоящему изобретению, и один или более реагентов, способных обнаруживать связывание антитела к ВСМА или его антигенсвязывающего фрагмента с ВСМА.
В другом аспекте настоящего изобретения предложено антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемая соль, или содержащая их фармацевтическая композиция согласно настоящему изобретению, для применения для лечения или профилактики ВСМА-опосредованных заболеваний или состояний.
В другом аспекте настоящего изобретения предложено применение антитела к ВСМА или его антигенсвязывающего фрагмента, или его фармацевтически приемлемой соли, или содержащей их фармацевтической композиции по настоящему изобретению, для получения лекарственного препарата для лечения или профилактики ВСМА-опосредованных заболеваний или состояний.
В другом аспекте настоящего изобретения предложено антитело к ВСМА или его антигенсвязывающий фрагмент, или его фармацевтически приемлемая соль, или реагент для обнаружения или диагностики, содержащий указанные объекты по настоящему изобретению, для применения для обнаружения, диагностики и прогнозирования ВСМА-опосредованных заболеваний или состояний.
В другом аспекте настоящего изобретения предложено применение антитела к ВСМА или его антигенсвязывающего фрагмента, или его фармацевтически приемлемой соли, или реагента для обнаружения или диагностики, содержащего указанные объекты по настоящему изобретению, для получения набора для обнаружения, диагностики и прогнозирования ВСМА-опосредованных заболеваний или состояний.
В частном варианте осуществления ВСМА-опосредованное заболевание или состояние представляет собой рак, предпочтительно рак, экспрессирующий ВСМА, более предпочтительно лимфому, лейкоз или миелому, наиболее предпочтительно множественную миелому.
В частном варианте осуществления ВСМА-опосредованное заболевание или состояние представляет собой аутоиммунное заболевание, предпочтительно красную волчанку, IgA-нефропатию и ревматический артрит.
В другом аспекте настоящего изобретения предложен конъюгат антитело-лекарственное средство, содержащий антитело к ВСМА или его антигенсвязывающий фрагмент по настоящему изобретению, связанный с цитотоксическим агентом, предпочтительно где цитотоксический агент выбран из группы, состоящей из MMAF (монометил ауристатин F), SN-38 (7-этил-10-гидроксикамптотецин) и эксатекана (Exatecan). Кроме того, предпочтительно, чтобы конъюгат антитело-лекарственное средство по настоящему изобретению имел структурную формулу, выбранную из группы, состоящей из:
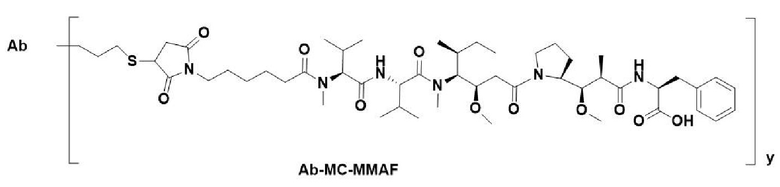 ,
,
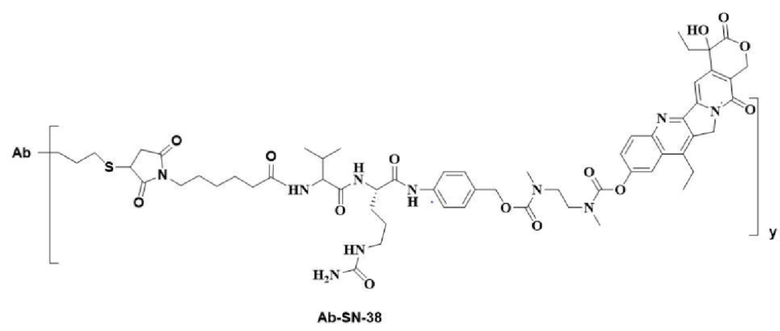 , и
, и
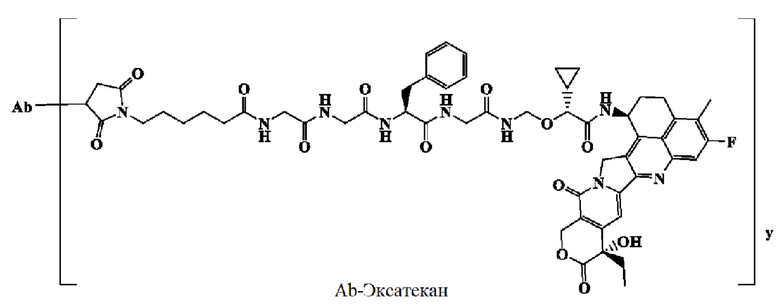 ,
,
где Ab представляет собой антитело к ВСМА или его антигенсвязывающий фрагмент, как описано выше по настоящему изобретению.
Кроме того, в настоящем изобретении предложено применение конъюгата антитело-лекарственное средство по настоящему изобретению для получения лекарственного препарата для лечения ВСМА-опосредованных заболеваний или состояний, причем ВСМА-опосредованное заболевание или состояние выбрано группы, состоящей из рака и аутоиммунного заболевания, предпочтительно рак представляет собой рак, экспрессирующий ВСМА, более предпочтительно лимфому, лейкоз или миелому, наиболее предпочтительно множественную миелому. Предпочтительно аутоиммунное заболевание выбрано из группы, состоящей из красной волчанки, IgA-нефропатии и ревматического артрита.
В другом аспекте настоящего изобретения предложен способ лечения ВСМА-опосредованных заболеваний или состояний у субъекта, нуждающегося в этом, который включает введение субъекту терапевтически эффективного количества антитела к ВСМА или его антигенсвязывающего фрагмента, или его фармацевтически приемлемой соли по настоящему изобретению, содержащей его фармацевтической композиции или конъюгата антитело-лекарственное средство по настоящему изобретению.
Антитело к ВСМА или его антигенсвязывающий фрагмент, предложенный в настоящем изобретении, обладают высокой аффинностью, высокой специфичностью, низкой иммуногенностью, высокой биологической активностью и значительным противоопухолевым действием. В то же время, антитела по настоящему изобретению могут быть быстро интернализованы после связывания с антигеном ВСМА, что указывает на то, что они подходят для применения в форме ADC (конъюгат антитело-лекарственное средство) для терапевтических применений или других применений, требующих быстрой интернализации. Антитела по настоящему изобретению в форме ADC могут эффективно уничтожать опухолевые клетки, экспрессирующие ВСМА.
Подробное описание Термины
Чтобы облегчить понимание настоящего изобретения, некоторые технические и научные термины конкретным образом определены ниже. Если иное четко не определено где-либо в данном документе, все другие технические и научные термины, используемые в данном описании, имеют значения, обычно понятные специалистам в области техники, к которой относится настоящее изобретение.
Трехбуквенные коды и однобуквенные коды аминокислот, используемые в настоящем изобретении, описаны в J. Biol. Chem., 243, стр. 3558 (1968).
Термин «антитело», описанный в настоящем описании, относится к иммуноглобулину, который представляет собой тетрапептидную цепную структуру, состоящую из двух идентичных тяжелых цепей и двух идентичных легких цепей, связанных межцепочечными дисульфидными связями. Аминокислотный состав и порядок расположения константных областей тяжелой цепи иммуноглобулина различны, поэтому их антигенность также различна. В соответствии с этим иммуноглобулины можно разделить на пять типов или известных как изотипы иммуноглобулинов, а именно IgM, IgD, IgG, IgA и IgE, и соответствующие им тяжелые цепи представляют собой μ-цепь, δ-цепь, γ-цепь, α-цепь и ε-цепь, соответственно. Один и тот же тип Ig может быть отнесен к разным подклассам в соответствии с разницей в аминокислотном составе шарнирной области, а также в количестве и положении дисульфидных связей тяжелой цепи. Например, IgG можно разделить на IgG1, IgG2, IgG3 и IgG4. Легкая цепь классифицируется как κ-цепь или λ-цепь в соответствии с отличием в константной области. Каждый из пяти типов Ig может иметь κ-цепь или λ-цепь.
В настоящем изобретении легкая цепь антитела по настоящему изобретению может дополнительно содержать константную область легкой цепи, которая включает человеческую или мышиную κ-, λ-цепь или их варианты.
В настоящем описании тяжелая цепь антитела по настоящему изобретению может дополнительно содержать константную область тяжелой цепи, которая включает человеческие или мышиные IgG1, IgG2, IgG3, IgG4 или их варианты.
Последовательность приблизительно из 110 аминокислот вблизи N-конца тяжелой и легкой цепей антитела сильно варьирует и представляет собой вариабельную область (V-область); остальная аминокислотная последовательность вблизи С-конца относительно стабильна и представляет собой константную область (С-область). Вариабельная область включает 3 гипервариабельные области (HVR) и 4 каркасные области (FR) с относительно консервативными последовательностями. Три гипервариабельные области, которые определяют специфичность антитела, также известны как области, определяющие комплементарность (CDR). Каждая из вариабельной области легкой цепи (VL) и вариабельной области тяжелой цепи (VH) состоит из 3 областей CDR и 4 областей FR. Порядок расположения от амино-конца к карбоксильному концу следующий: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Три области CDR легкой цепи относятся к LCDR1, LCDR2 и LCDR3, три области CDR тяжелой цепи относятся к HCDR1, HCDR2 и HCDR3. Количество и положение аминокислотных остатков CDR области VL и области VH антитела или антигенсвязывающего фрагмента по настоящему изобретению соответствуют известным критериям нумерации по Кабату и критериям определения по базам данных на веб-сайтах AbM или IMGT и по Кабату (http://bioinf.org.uk/abs/).
Термин «антигенпрезентирующая клетка» или «АПК» представляет собой клетку, которая презентирует чужеродный антиген в комплексе с ГКГС (главный комплекс гистосовместимости) на своей поверхности. Т-клетки используют рецепторы Т-клеток (TCR) для распознавания таких комплексов. Примеры АПК включают, без ограничений, дендритные клетки (ПК), мононуклеарные клетки периферической крови (МКПК), моноциты, В-лимфобласты и дендритные клетки, происходящие из моноцитов.
Термин «презентирование антигена» относится к процессу захвата антигенов АПК и обеспечения возможности их узнавания Т-клетками, например, в качестве компонента конъюгата ГКГС-I/ГКГС-II.
Термин «ВСМА» включает любой вариант или изоформу ВСМА, которые естественным образом экспрессируются клетками. Антитела по настоящему изобретению могут перекрестно реагировать с ВСМА, полученным от видов, отличных от человека. Альтернативно, антитела также могут быть специфичными для ВСМА человека и могут не проявлять перекрестной реактивности с ВСМА, полученным от других видов. ВСМА или любой его вариант или изоформа могут быть выделены из клеток или тканей, экспрессирующих его в природе, или получены с помощью рекомбинантных методов с использованием методов, обычно используемых в данной области, и тех, которые описаны в настоящем документе. Предпочтительно антитело к ВСМА нацелено на ВСМА человека, который имеет нормальный профиль гликозилирования.
Термин «рекомбинантное человеческое антитело» включает человеческие антитела, полученные, экспрессированные, созданные или выделенные с помощью рекомбинантных методов, и применяемые методы и способы хорошо известны в данной области, такие как:
1. антитела, выделенные из трансгенных и трансхромосомных животных (например, мышей) с генами иммуноглобулина человека или из полученных из них гибридом;
2. антитела, выделенные из клеток-хозяев, трансформированных для экспрессии антител, таких как трансфектомы;
3. антитела, выделенные из библиотек рекомбинантных комбинаторных человеческих антител; и
4. антитела, полученные, экспрессированные, созданные или выделенные такими способами, как сплайсинг последовательностей генов человеческого иммуноглобулина с другими последовательностями ДНК.
Такие рекомбинантные человеские антитела содержат вариабельную область и константную область, в которых используются специфические последовательности иммуноглобулина зародышевой линии человека, кодируемые генами зародышевой линии, но также содержащие последующие перестройки и мутации, такие как те, которые происходят во время созревания антитела.
Термин «мышиное антитело» в настоящем изобретении представляет собой моноклональное антитело к ВСМА человека, полученное в соответствии со знаниями и навыками в данной области. Во время получения испытуемому вводят антиген к ВСМА, а затем выделяют гибридомы, экспрессирующие антитело с желаемой последовательностью или функциональными свойствами. В предпочтительном варианте осуществления настоящего изобретения мышиное антитело к ВСМА или его антигенсвязывающий фрагмент могут дополнительно содержать константную область легкой цепи *к-, *-цепи мыши или их варианта или дополнительно содержать константную область тяжелой цепи мышиного IgG1, IgG2, IgG3 или IgG4 или их вариант.
Термин «человеческое антитело» включает антитела, имеющие вариабельную область и константную область последовательностей иммуноглобулина зародышевой линии человека. Человеческие антитела по настоящему изобретению могут включать аминокислотные остатки, которые не кодируются последовательностями иммуноглобулина зародышевой линии человека (например, мутации, введенные случайным или сайт-специфическим мутагенезом in vitro или соматическими мутациями in vivo). Однако термин «человеческое антитело» не включает антитела, в которых последовательности CDR, полученные из зародышевой линии других видов млекопитающих (таких как мыши), были привиты к человеческим каркасным последовательностям (а именно, «гуманизированные антитела»).
Термин «гуманизированное антитело», также известное как антитело с привитым CDR, относится к антителу, полученному путем прививания последовательностей CDR мыши в каркасные области вариабельной области человеческого антитела. Гуманизированное антитело может преодолеть недостатки сильного иммунного ответа, индуцированного химерными антителами, которые несут большое количество белковых компонентов мыши. Чтобы избежать снижения активности, вызванного снижением иммуногенности, вариабельные области человеческих антител могут быть подвержены минимальной обратной мутации для поддержания активности.
Термин «химерное антитело» представляет собой антитело, образованное путем слияния вариабельной области антитела мыши с константной областью человеческого антитела, что может облегчать иммунный ответ, индуцированный мышиным антителом. Создание химерного антитела требует сначала создания гибридомы, которая секретирует специфичное моноклональное антитело мыши, затем клонирования гена вариабельной области из клеток мышиной гибридомы, а затем, при необходимости, клонирования гена константной области человеческого антитела, связывая ген вариабельной области мыши с геном константной области человека для формирования химерного гена, который встраивают в вектор экспрессии человека и, наконец, экспрессирования молекулы химерного антитела в эукариотической промышленной системе или прокариотической промышленной системе. Константная область человеческого антитела может быть выбрана из константной области тяжелой цепи человеческих IgG1, IgG2, IgG3 или IgG4 или их варианта, предпочтительно константной области тяжелой цепи человеческих IgG1, IgG2 или IgG4, или константной области тяжелой цепи IgG1 с усиленной ADCC после аминокислотной мутации.
Термин «антигенсвязывающий фрагмент» относится к антигенсвязывающему фрагменту антитела и аналогу антитела, которые обычно содержат по меньшей мере часть антигенсвязывающей области или вариабельной области (например, одну или более CDR) исходного антитела. Фрагмент антитела сохраняет, по меньше мере, часть специфичности связывания исходного антитела. Как правило, когда активность представлена в виде молей, фрагмент антитела сохраняет по меньшей мере 10% исходной связывающей активности. Предпочтительно фрагмент антитела сохраняет по меньшей мере 20%, 50%, 70%, 80%, 90%, 95% или 100% или более аффинности связывания исходного антитела с мишенью. Примеры антигенсвязывающих фрагментов включают, но не ограничиваются ими: Fab, Fab', F(ab')2 (Fab - антигенсвязывающий фрагмент), фрагмент Fv (вариабельный фрагмент), линейное антитело, одноцепочечное антитело, нанотело, доменное антитело и мультиспецифическое антитело. Обзор сконструированных вариантов антител представлен в Holliger and Hudson, 2005, Nat. Biotechnol. 23: 1126-1136.
«Fab-фрагмент» состоит из одной легкой цепи и СН1 (домен 1 константной области тяжелой цепи) и вариабельных областей одной тяжелой цепи. Тяжелая цепь молекулы Fab не может образовывать дисульфидные связи с другой молекулой тяжелой цепи.
Область «Fc» (кристаллизующийся фрагмент) содержит два фрагмента тяжелой цепи антитела, содержащие домены СН1 и СН2. Два фрагмента тяжелой цепи удерживаются вместе двумя или более дисульфидными связями и за счет гидрофобного взаимодействия домена СН3.
«Fab'-фрагмент» содержит легкую цепь и часть тяжелой цепи, включающую домен VH (домен вариабельной области тяжелой цепи), домен СН1 и область между доменами СН1 и СН2, так что межцепочечные дисульфидные связи могут образовываться между двумя тяжелыми цепями двух Fab'-фрагментов, тем самым образуя молекулу F(ab')2.
«Фрагмент F(ab')2» содержит две легкие цепи и две тяжелые цепи, включающие часть константной области между доменами СН1 и СН2, тем самым образуя межцепочечные дисульфидные связи между двумя тяжелыми цепями. Следовательно, фрагмент F(ab')2 состоит из двух фрагментов Fab', удерживаемых вместе дисульфидными связями между двумя тяжелыми цепями.
«Fv-область» содержит вариабельные области как тяжелой цепи, так и легкой цепи, но не содержит константных областей.
Термин «мультиспецифическое антитело» используется в самом широком смысле, включая антитела, обладающие специфичностью в отношении нескольких эпитопов. Данные мультиспецифические антитела включают, без ограничений: антитела, содержащие вариабельную область тяжелой цепи VH и вариабельную область легкой цепи VL, где единица VH-VL обладает специфичностью в отношении нескольких эпитопов; антитела с двумя или более областями VL и VH, каждая единица VH-VL связывается с разными мишенями или разными эпитопами одной и той же мишени; антитела с двумя или более отдельными вариабельными областями, причем каждая отдельная вариабельная область связывается с разными мишенями или разными эпитопами одной и той же мишени; полноразмерные антитела, фрагменты антител, диатела, биспецифические диатела и триатела, ковалентно или нековалентно связанные фрагменты антител и т.п.
Термин «одноцепочечное антитело» представляет собой одноцепочечный рекомбинантный белок, образованный путем связывания вариабельной области тяжелой цепи VH и вариабельной области легкой цепи VL антитела через линкерный пептид. Это минимальный фрагмент антитела с полным антигенсвязывающим сайтом.
Термин «фрагмент доменного антитела» представляет собой фрагмент иммуноглобулина, обладающий иммунологическими функциональными фрагментами, который содержит либо вариабельную область тяжелой цепи, либо вариабельную область легкой цепи. В некоторых случаях две или более областей VH ковалентно связаны пептидным линкером с образованием фрагмента двухвалентного домена антитела. Две области VH фрагмента антитела с двухвалентным доменом могут быть нацелены на один и тот же антиген или на разные антигены.
Термин «связывание с ВСМА» в настоящем изобретении относится к способности взаимодействовать с ВСМА человека.
Термин «антигенсвязывающий сайт» в настоящем изобретении относится к трехмерному сайту, который распознается антителом или антигенсвязывающим фрагментом по настоящему изобретению.
Термин «эпитоп» относится к участку на антигене, который специфически связывается с иммуноглобулином или антителом. Эпитопы могут быть образованы соседними аминокислотами или несмежными аминокислотами, которые соприкасаются в результате третичной укладки белка. Эпитопы, образованные соседними аминокислотами, обычно сохраняются после воздействия денатурирующего растворителя, в то время как эпитопы, образованные третичной укладкой, обычно исчезают после обработки денатурирующим растворителем. Эпитопы обычно содержат по меньшей мере 3-15 аминокислот в уникальной пространственной конформации. Способы определения того, какой эпитоп связан с данным антителом, хорошо известны в данной области, включая иммуноблоттинг, анализ обнаружения методом иммунопреципитации и т.п.Способы определения пространственной конформации эпитопа включают методы, известные в данной области, и способы, описанные в настоящем документе, например, рентгеноструктурный анализ, двумерный ядерно-магнитный резонанс и т.п.
Термины «специфически связывается» и «селективно связывается», используемые в настоящем описании, относятся к связыванию антитела с эпитопом на заданном антигене. Как правило, когда рекомбинантный ВСМА человека используется в качестве аналита, а антитело используется в качестве лиганда, при измерении с помощью технологии поверхностного плазмонного резонанса (SPR) в приборе, антитело связывается с заданным антигеном при равновесной константе диссоциации (KD) примерно менее 10-7 М или даже меньше, и его аффинность связывания с заданным антигеном по меньшей мере в два раза выше, чем его аффинность связывания с неспецифическими антигенами (такими как BSA (бычий сывороточный альбумин) и т.п.), отличными от заданного антигена или близкородственного антигена. Термин «антитело, которое распознает антиген» может быть использован здесь взаимозаменяемо с термином «антитело, которое специфически связывается с антигеном».
Термин «перекрестная реакция» относится к способности антител по настоящему изобретению связываться с ВСМА, полученными из разных видов. Например, антитело по настоящему изобретению, которое связывается с ВСМА человека, может также связываться с ВСМА другого вида. Перекрестную реактивность измеряют в анализах связывания (например, SPR и ELISA (иммуноферментный анализ)) путем обнаружения специфической реактивности с очищенным антигеном или связывания или функционального взаимодействия с клетками, которые физиологически экспрессируют ВСМА. Способы определения перекрестной реактивности включают стандартные анализы связывания, как описано в настоящем документе, например, анализ поверхностного плазмонного резонанса (SPR) или проточную цитометрию.
Термины «ингибирование» или «блокировка» могут использоваться взаимозаменяемо и охватывают как частичное, так и полное ингибирование/блокирование. Ингибирование/блокирование лиганда предпочтительно снижает или изменяет нормальный уровень или тип активности, который имеет место, когда связывание лиганда происходит без ингибирования или блокирования. Под ингибированием и блокированием также подразумевается любое измеримое снижение аффинности связывания лиганда при контакте с антителом к ВСМА по сравнению с лигандом, не контактирующим с антителом к ВСМА.
Предполагается, что термин «ингибирование роста» (например, клеток) включает любое измеримое снижение роста клеток.
Термины «индуцированный иммунный ответ» и «усиленный иммунный ответ» могут использоваться взаимозаменяемо и относиться к иммунному ответу, стимулируемому (т.е. пассивному или адаптивному) специфическим антигеном. Термин «индуцировать» для индуцирования CDC (комплемент-зависимая цитотоксичность) или ADCC относится к стимуляции конкретного механизма прямого уничтожения клеток.
«ADCC» в настоящем изобретении, т.е. антителозависимая клеточно-опосредованная цитотоксичность, означает, что клетки, экспрессирующие Fc-рецепторы, непосредственно убивают клетки-мишени, покрытые антителами, путем распознавания Fc-сегмента антител. Действие ADCC антител может быть усилена, уменьшена или устранена путем модификации Fc-сегмента IgG. Модификация относится к мутации в константной области тяжелой цепи антитела.
Способы получения и очистки антител и антигенсвязывающих фрагментов хорошо известны и могут быть найдены в предшествующем уровне техники, например, в Antibodies: A Laboratory Manual, Cold Spring Harbor, главы 5-8 и 15. Например, мышей можно иммунизировать ВСМА человека или его фрагментом, и полученные антитела можно ренатурировать и очистить, а также секвенировать аминокислоты с использованием обычных способов. Антигенсвязывающие фрагменты также могут быть получены с использованием общепринятых способов. Антитело или его антигенсвязывающий фрагмент по настоящему изобретению генетически сконструированы для добавления одной или более областей FR человека к нечеловеческим областям CDR. Последовательности зародышевой линии FR человека можно получить с веб-сайта ImmunoGeneTics (IMGT) http://imgt.cines.fr или из The Immunoglobulin FactsBook, 2001ISBN012441351.
Сконструированные антитела или антигенсвязывающие фрагменты по настоящему изобретению могут быть получены и очищены обычными способами. Последовательности кДНК (комплементарная дезоксирибонуклеиновая кислота) соответствующих антител можно клонировать и рекомбинировать в векторы экспрессии GS (глутаминовая синтетаза). Векторы экспрессии рекомбинантного иммуноглобулина могут стабильно трансфецировать клетки СНО. В качестве более рекомендуемого предшествующего уровня техники системы экспрессии млекопитающих могут приводить к гликозилированию антител, особенно на высококонсервативном N-конце Fc-области. Стабильные клоны получают путем экспрессии антител, которые специфически связываются с человеческим антигеном. Положительные клоны размножаются в бессывороточной среде биореакторов для получения антител. Культуральная жидкость, в которую секретируются антитела, может быть очищена и собрана обычными способами. Антитела могут быть отфильтрованы и концентрированы общепринятыми способами. Растворимые смеси и мультимеры также могут быть удалены общепринятыми способами, например молекулярными ситами и ионным обменом. Полученный продукт необходимо немедленно заморозить, например, при -70°С, или лиофилизировать.
Антитело по настоящему изобретению относится к моноклональному антителу. Моноклональное антитело (mAb) в настоящем изобретении относится к антителу, полученному из одного клонированного клеточного штамма, который не ограничивается эукариотическим, прокариотическим или фагово-клонированным клеточным штаммом. Моноклональные антитела или антигенсвязывающие фрагменты могут быть получены путем рекомбинации с использованием, например, гибридомной технологии, технологии рекомбинации, технологии фагового дисплея, синтетической технологии (такой как CDR-прививание) или других существующих технологий.
«Введение», «вводить» и «лечение» применительно к животным, людям, экспериментальным субъектам, клеткам, тканям, органам или биологическим жидкостям, относятся к контактированию экзогенного лекарственного препарата, терапевтического средства, диагностического средства или композиции с животными, людьми, субъектами, клетками, тканями, органами или биологическими жидкостями. «Введение», «вводить» и «лечение» могут относиться, например, к лечению, фармакокинетике, диагностике, исследовательским и экспериментальным методам. Лечение клеток включает приведение в контакт реагентов с клетками и приведение в контакт реагентов с жидкостями, где жидкости контактируют с клетками. «Введение», «вводить» и «лечение» также относятся к лечению, например, клеток реагентами, диагностическими агентами, связующими композициями или другой клеткой in vitro и ex vivo. «Лечение» применительно к людям, ветеринарным или исследовательским субъектам, относится к терапевтическим, предупредительным или профилактическим мерам, исследовательским и диагностическим применениям.
«Лечение» относится к введению внутреннего или наружного терапевтического агента, например, содержащего любое из антител по настоящему изобретению, пациенту, имеющему один или более симптомов заболевания, на которые, как известно, терапевтический агент оказывает терапевтическое действие. Как правило, терапевтическое средство вводят в количестве, эффективном для облегчения одного или более симптомов заболевания у субъекта или популяции, получающих лечение, либо для индукции регрессии таких симптомов, либо для ингибирования развития таких симптомов до любой клинически измеримой степени. Количество терапевтического агента, которое является эффективным для облегчения любого конкретного симптома заболевания (также называемое «терапевтически эффективным количеством»), может варьироваться в зависимости от множества факторов, например, от состояния заболевания, возраста и массы тела пациента, и способность лекарственного средства оказывать желаемый терапевтический эффект у больного. Облегчение симптомов заболевания можно определить с помощью любых методов клинических испытаний, обычно используемых врачами или другими медицинскими работниками для оценки тяжести или прогрессирования симптомов. Несмотря на то, что варианты осуществления настоящего изобретения (например, способы лечения или продукты) могут быть неэффективными для облегчения каждого интересующего симптома заболевания, они должны уменьшать интересующий симптом заболевания у статистически значимого числа пациентов, что определяется любыми методами статистического тестирования, такие как t-критерий Стьюдента, критерий хи-квадрат, U-критерий Манна и Уитни, критерий Крускала-Уоллиса (Н-критерий), критерий Джонкхира-Терпстры и критерий Уилкоксона.
Термин «состоящий по существу из...» или его вариант, используемый в описании и формуле изобретения, означает, что он содержит все описанные элементы или группы элементов и необязательно содержит другие элементы, сходные или отличные по своей природе с описанными элементами, что существенно не изменят основные или новые свойства данного режима дозирования, метода или композиции.
Термин «встречающийся в природе», применяемый к определенному объекту в настоящем изобретении, относится к тому факту, что объект можно найти в природе. Например, полипептидная последовательность или полинуклеотидная последовательность, существующая в организмах (включая вирусы), которые могут быть выделены из природных источников и не были преднамеренно искусственно модифицированы в лаборатории, являются встречающимися в природе.
«Эффективное количество» включает количество, достаточное для облегчения или предотвращения симптома или состояния медицинского состояния. Эффективное количество также относится к количеству, достаточному для возможности или облегчения диагностики. Эффективное количество для конкретного пациента или ветеринарного субъекта может варьироваться в зависимости от следующих факторов: таких как состояние, подлежащее лечению, общее состояние здоровья пациента, способ, путь и доза введения лекарственного средства, а также тяжесть побочных эффектов. Эффективное количество может быть максимальной дозировкой или схемой дозирования, позволяющей избежать значительных побочных или токсических эффектов.
«Экзогенные» относятся к веществам, вырабатываемым вне организмов, клеток или человеческого тела в зависимости от фона.
«Эндогенные» относятся к веществам, вырабатываемым внутри клеток, организмов или человеческого тела в зависимости от происхождения.
«Идентичный» относится к сходству последовательностей между двумя полинуклеотидными последовательностями или между двумя полипептидами. Когда положения в двух выровненных последовательностях заняты одним и тем же основанием или субъединицей мономера аминокислоты, например, каждое положение двух молекул ДНК занято аденином, тогда молекулы считаются гомологичными в этом положении. Процент идентичности между двумя последовательностями является функцией количества совпадающих или гомологичных положений, общих для двух последовательностей, деленного на количество положений для сравнения × 100%. Например, при оптимальном выравнивании последовательностей, если 6 из 10 позиций в двух последовательностях совпадают или гомологичны, то эти две последовательности гомологичны на 60%. Как правило, выравнивание совершено, когда две последовательности выравнивают для получения максимального процента идентичности.
Используемые в настоящем документе выражения «клетка», «клеточная линия» и «клеточная культура» могут использоваться взаимозаменяемо, и все такие названия включают их потомство. Следовательно, слова «трансформант» и «трансформированная клетка» включают первичные тестовые клетки и полученные из них культуры независимо от количества пассажей. Также следует понимать, что из-за преднамеренных или непреднамеренных мутаций все потомство не может быть абсолютно одинаковым по содержанию ДНК. Включено мутантное потомство с той же функцией или биологической активностью, что и в исходных трансформированных клетках. Это хорошо видно из контекста, когда упоминаются разные наименования.
«Необязательный» или «необязательно» означает, что событие или обстоятельство, описанное впоследствии, может, но не обязательно, произойти, и описание включает случаи, когда событие или обстоятельство происходит или не происходит. Например, «необязательно содержащий от 1 до 3 вариабельных областей тяжелой цепи антитела» означает, что вариабельные области тяжелой цепи антитела конкретных последовательностей могут, но не обязательно должны присутствовать.
«Фармацевтическая композиция» означает, что она включает одно или более антител или антигенсвязывающих фрагментов, описанных в настоящем документе, а также другие компоненты, такие как физиологически/фармацевтически приемлемые носители и эксципиенты. Функция фармацевтической композиции состоит в том, чтобы облегчить введение соединения в организм, что способствует абсорбции активного ингредиента, необходимой для проявления биологической активности.
«Лекарственная нагрузка» (DAR) представлена у, который представляет собой среднее количество цитотоксических препаратов на одно антитело в конъюгате антитело-лекарственное средство. Лекарственная нагрузка (DAR) конъюгата антитело-лекарственное средство, полученного в результате реакции связывания, может быть охарактеризована обычными способами, например, масс-спектрометрией, HPLC(высокоэффективная жидкостная хроматография) и ELISA. С помощью этих методов можно определить количественное распределение конъюгата антитело-лекарственное средство по значению у.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение будет дополнительно описано со ссылкой на следующие примеры, которые не следует рассматривать как ограничивающие объем настоящего изобретения. Экспериментальные способы без конкретных условий в примерах по настоящему изобретению обычно следуют обычным условиям, таким как Antibodies: А Laboratory Manual and Molecular Cloning: A Laboratory Manual, Cold Spring Harbor; или в соответствии с условиями, рекомендованными производителем сырья или продукта.
Реагенты без указания источника являются обычными реагентами, приобретаемыми на рынке.
Пример 1: Получение антигенов
Белок, кодирующий His-меченный (His-полигистидин) внеклеточный домен ВСМА человека (BCMA-His), синтезируют SinoBiologics (кат. №: 10620-Н08Н). Последовательность BCMA-His:
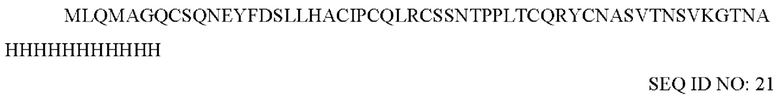
Пример 2: Получение мышиных гибридом и последовательностей антител В общей сложности 5 самок мышей Balb/c и 5 А/J в возрасте 10 недель иммунизируют человеческим антигеном BCMA-His. Используют полный адъювант Фрейнда Sigma (CFA) и неполный адъювант Фрейнда Sigma (IFA). Иммуноген и иммунный адъювант тщательно смешивают в соотношении 1:1 и эмульгируют с получением стабильной жидкости типа «вода в масле». Инъекционная доза составляла 25 мкг/200 мкл/мышь.

Титр сыворотки и способность связываться с антигенами поверхности клетки сыворотки иммунизированных мышей оценивают с помощью непрямого метода ELISA по Примеру 3. Начало слияния клеток определяют по результатам определения титра (разведение более 100000 раз). Иммунизированных мышей с высоким титром сыворотки, аффинностью и связыванием FACS отбирают для одной заключительной иммунизации и затем умерщвляют. Клетки селезенки сливают с клетками миеломы SP2/0 и высеивают для получения гибридом. Интересующие гибридомы подвергают скринингу с помощью непрямого ELISA и устанавливают их как моноклональные клеточные штаммы методом серийных разведений. Полученные антитело-положительные штаммы подвергают дополнительному скринингу с помощью непрямого ELISA, чтобы отобрать гибридомы, которые связываются с рекомбинантным белком. Собирают гибридомные клетки в логарифмической фазе роста. РНК (рибонуклеиновая кислота) экстрагируют тризолом (Invitrogen, 15596-018) и подвергают обратной транскрипции (обратная транскриптаза PrimeScriptTM, Takara #2680А). кДНК, полученную путем обратной транскрипции, амплифицируют с помощью ПЦР с использованием набора мышиных Ig-праймеров (Novagen, ТВ326 Rev.B 0503). Наконец, была получена последовательность мышиного антитела М1.
Последовательности вариабельных областей тяжелой (HCVR) и легкой цепей (LCVR) мышиного моноклонального антитела M1 следующие:

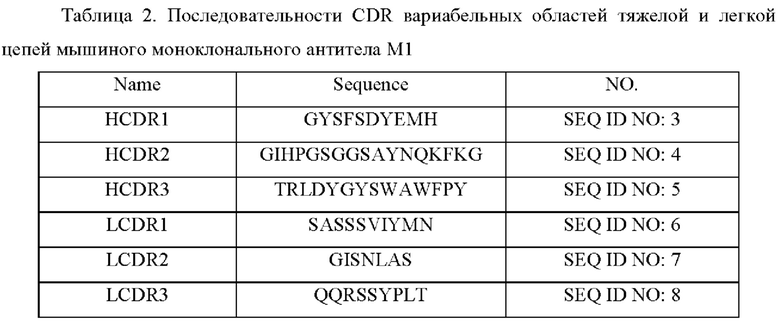
Примеры 3: Способ определения связывающей активности антител in vitro. (1) Непрямой анализ связывания ELISA in vitro:
Белок ВСМА His (Sino Biological Inc., кат.№10620-H08H) разбавляют PBS (фосфатно-солевой буферный раствор) с рН 7,4 до концентрации 1 мкг/мл, добавляют в 96-луночный планшет для высокоаффинного ELISA в количестве 100 мкл/лунку и инкубируют в холодильнике при 4°С в течение ночи (16-20 ч). После промывания планшета 4 раза PBST (рН 7,4 PBS, содержащего 0,05% Tween-20), добавляют блокирующий раствор 3% бычьего сывороточного альбумина (BSA), разбавленный PBST, в количестве 150 мкл/лунку и инкубируют при комнатной температуре в течение 1 ч для блокирования. После завершения блокирования блокирующий раствор удаляют, а планшет промывают 4 раза буфером PBST.
Исследуемое антитело разбавляют в 10-кратном градиенте PBST, содержащем 3% BSA, с исходной концентрацией 1 мкМ, для 10 разведений, добавляют в микротитровальный планшет по 100 мкл/лунку и инкубируют при комнатной температуре в течение 1 ч. После завершения инкубации планшет промывают 4 раза PBST. Козье античеловеческое вторичное антитело, меченное HRP (Abcam, кат. №ab97225), разбавленное PBST, содержащем 3% BSA, добавляют по 100 мкл/лунку и инкубируют при комнатной температуре в течение 1 ч. Планшет промывают 4 раза PBST, а затем добавляют хромогенный субстрат ТМВ (Cell Signaling Technology, кат. №7004S) по 100 мкл/лунку и инкубируют при комнатной температуре в темноте в течение 1 мин. Стоп-раствор (Cell Signaling Technology, кат. №7002S) добавляют в количестве 100 мкл/лунку для прекращения реакции. Величину абсорбции при 450 нм считывают с помощью устройства для считывания микропланшетов (BioTek, модель Synergy H1). Данные анализируют. Результаты анализируют путем построения кривой концентрация-сигнал, как показано в следующей таблице:

(2) Анализ связывания клеток in vitro:
Собирают культивируемые клетки с высокой экспрессией ВСМА (клетки НЕК-293Т, сверхэкспрессирующие ВСМА; опухолевые клетки, экспрессирующие ВСМА, NCI-Н929, депозитный номер АТСС (Американская коллекция типовых культур) CRL-9068). Плотность клеток регулируют и клетки высеивают на 96-луночный планшет с U-образным дном в количестве от 1×105 до 2×105 клеток на лунку. Планшет центрифугируют при 1200 g в течение 5 мин и удаляют супернатант. Добавляют 100 мкл градиентно разведенного раствора антител или сыворотки иммунизированных мышей и инкубируют при 4°С в течение 60 мин. Планшет центрифугируют при 1200 g в течение 5 мин и удаляют супернатант. Клетки дважды промывают PBS. Добавляют флуоресцентно меченное вторичное антитело (РЕ-GAM или PE-GAH) по 100 мкл на лунку и инкубируют при 4°С в течение 60 мин. Планшет центрифугируют при 1200 g в течение 5 мин и удаляют супернатант. Клетки дважды промывают PBS и затем повторно суспендируют в PBS. Сигнал обнаруживают с помощью проточного цитометра, и для анализа результатов строят кривую концентрации.
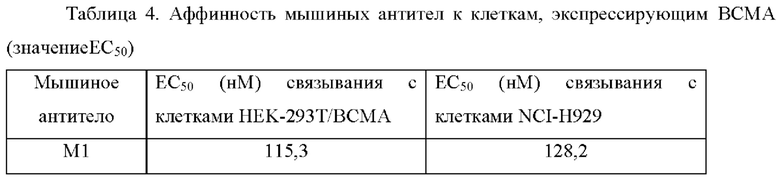
Пример 4: Эксперимент по гуманизации мышиных антител
Гуманизацию мышиных моноклональных антител к ВСМА человека проводят в соответствии со способами, опубликованными во многих документах в данной области. Вкратце, исходные константные домены (мышиное антитело) заменяют константными доменами человека. Последовательности антител зародышевой линии человека отбирают в соответствии с идентичностью между антителом мыши и человеческим антителом. В настоящем изобретении мышиное антитело M1 гуманизируют.
На основе типичной структуры CDR VH/VL полученного мышиного антитела, последовательности вариабельных областей тяжелой и легкой цепей выравнивают с базой данных зародышевой линии человеческого антител для получения высокоидентичных матриц зародышевой линии человека.
Области CDR мышиного антитела M1 прививают к выбранным соответствующим матрицам для гуманизации. Затем, исходя из трехмерной структуры мышиного антитела, обратной мутации подвергают встроенные остатки, остатки, непосредственно взаимодействующие с областями CDR, и остатки, оказывающие существенное влияние на конформацию VL и VH, и оптимизируют химически нестабильные аминокислотные остатки областей CDR. После тестирования экспрессии и сравнения количества обратных мутаций отбирают и конструируют следующие последовательности гуманизированных вариабельных областей тяжелой цепи HCVR:

Сконструированные последовательности вариабельной области тяжелой цепи и легкой цепи связывают с последовательностями константной области (С) тяжелой цепи и легкой цепи IgG1 соответственно. Примеры последовательностей константных областей тяжелой цепи и легкой цепи соответственно следующие:

Примеры последовательностей тяжелой и легкой цепей, полученных после связывания, следующие:


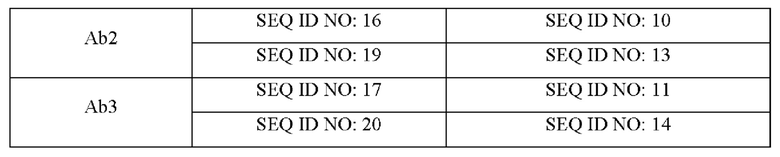
Фрагменты кДНК синтезируют в соответствии с аминокислотными последовательностями легкой цепи и тяжелой цепи каждого гуманизированного антитела, указанного выше, и встраивают в вектор экспрессии pcDNA3.1 (Life Technologies Cat. №V790-20). Вектор экспрессии используют вместе с реагентом для трансфекции PEI (подиэтиламин) (Polysciences, Inc. Cat. №23966) в соотношении 1:2 для трансфекции клеток НЕК293 (Life Technologies Cat. №11625019). Клетки инкубируют в CO2-инкубаторе в течение 4-5 дней. Жидкость клеточной культуры собирают, центрифугируют и фильтруют. Затем образцы наносят на аффинную колонку для очистки антител. Колонку промывают фосфатным буфером. Образцы элюируют глицин-солянокислотным буфером (рН 2,7, 0,1 М Gly-HCl), нейтрализуют 1 М трис-соляной кислотой, рН 9,0, и подвергают диализу против фосфатного буфера с получением гуманизированных белков антител по настоящему изобретению.
Пример 5: Анализ аффинности связывания in vitro и кинетический анализ Аффинность (ЕС50) каждого гуманизированного антитела к человеческому антигену ВСМА определяют с использованием непрямого анализа связывания ELISA in vitro в соответствии с Примером 3 (1), и она показана в Таблице 6 ниже:
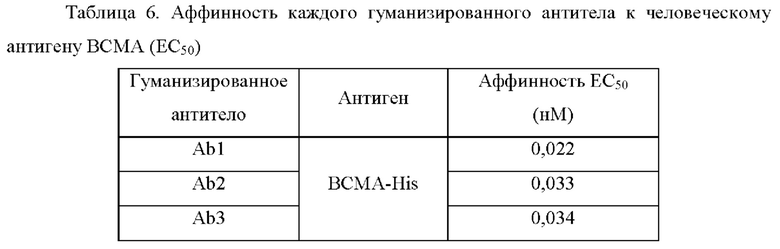
Аффинность (ЕС50) каждого гуманизированного антитела к опухолевым клеткам NCI-H929 определяют с использованием анализа связывания клеток in vitro в соответствии с Примером 3 (2), и она показана в Таблице 7 ниже:
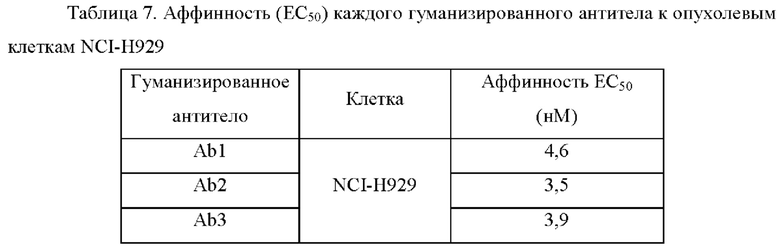
Пример 6: Эндоцитоз антител
NCI-H929 (депозитный номер АТСС CRL-9068) используют для оценки того, могут ли антитела по настоящему изобретению подвергаться эндоцитозу в клетках вместе с ВСМА человека после связывания с ВСМА. Клетки NCI-H929 расщепляют трипсином (после однократной промывки PBS при 37°С в течение примерно 2 мин), собирают и повторно суспендируют в предварительно охлажденном буфере FACS (PBS + фетальная бычья сыворотка). Концентрацию клеток доводят до 1×106 клеток/мл. 1 мл клеточной суспензии добавляют в пробирку Эппендорфа, центрифугируют при 1500 об/мин в течение 5 мин и удаляют супернатант. 1 мл полученного тестируемого антитела добавляют для повторного суспендирования клеток, и конечная концентрация антитела составляла 20 мкг/мл. Клетки инкубируют на шейкере при 4°С в течение 1 ч, центрифугируют (4°С, 1500 об/мин × 5 мин) и сбрасывают супернатант. Клетки дважды промывают буфером FACS и удаляют супернатант. В каждую пробирку добавляют 100 мкл рабочего раствора флуоресцентных вторичных антител для повторного суспендирования клеток. Клетки инкубируют на шейкере при 4°С в течение 30 мин, центрифугируют (4°С, 1500 об/мин × 5 мин) и сбрасывают супернатант. Клетки дважды промывают буфером FACS и удаляют супернатант. В каждую пробирку добавляют 1,0 мл предварительно нагретой полной клеточной среды NCI-H929 для повторного суспендирования клеток и тщательно перемешивают. Суспензию клеток разделяют на аликвоты в 4 пробирки по 200 мкл на пробирку, соответственно, в виде группы 0 мин, контрольной группы, группы 30 мин и группы 2 ч. 0 мин и контрольную группы помещают на лед, а остальные группы помещают в инкубатор при 37°С для эндоцитоза на 30 мин и 2 ч соответственно. В соответствующий момент времени пробирку Эппендорфа извлекают и помещают на лед для предварительного охлаждения на 5 мин. Все экспериментальные группы центрифугируют (4°С, 1500 об/мин × 5 мин) и удаляют супернатант. Клетки дважды промывают буфером FACS и удаляют супернатант.250 мкл полоскового буфера добавляют в пробирки Эппендорфа всех групп лечения, кроме группы 0 мин. Клетки инкубируют при комнатной температуре в течение 8 мин, центрифугируют (4°С, 1500 об/мин × 5 мин) и сбрасывают супернатант. Клетки дважды промывают буфером FACS и удаляют супернатант. Во все группы лечения добавляют 100 мкл фиксирующего раствора, помещают при 4°С на более чем 30 мин для иммуноокрашивания и определяют с помощью проточного питометра DxFlex. Процент эндоцитоза антитела ВСМА (%) = (значение интенсивности флуоресценции в каждый момент времени - среднее значение интенсивности флуоресценции контрольной группы)/среднее значение интенсивности флуоресценции в нулевой точке - среднее значение интенсивности флуоресценции контрольной группы. Результаты приведены в Таблице 8 ниже:
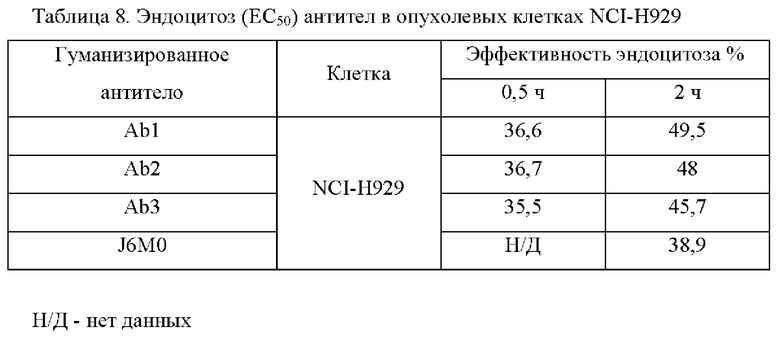
Результаты показывают, что по сравнению с антителом J6M0 к ВСМА (описанным в патенте US 9273141) антитела по настоящему изобретению обладают более высокой эффективностью эндоцитоза.
Пример 7: Конъюгация антител к MC-MMAF (Малеимидокапроил монометил ауристатин F)
Антитела по настоящему изобретению обладают клеточно-аффинной активностью и эндоцитозной активностью, что делает их подходящими для связывания с лекарственными средствами с образованием конъюгатов антитело-лекарственное средство для лечения ВСМА-опосредованных заболеваний. Антитела по настоящему изобретению были связаны с MC-MMAF с образованием конъюгатов антитело-лекарственное средство. Процесс связывания показан в следующем уравнении, где Ab представляет собой антитело Ab2 или Ab3:
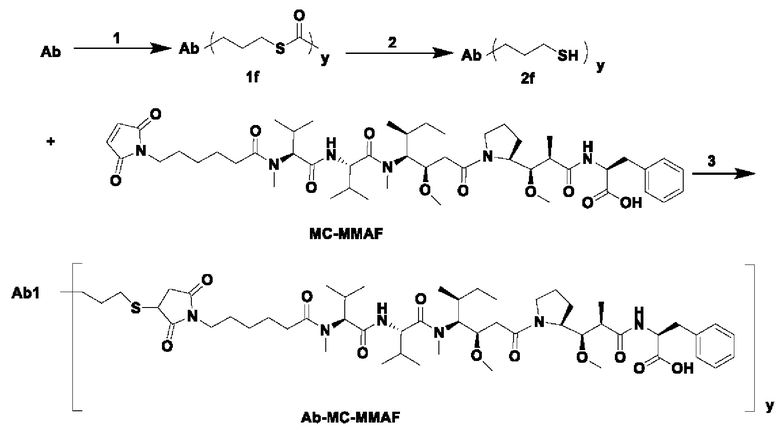
На первом этапе S-(3-гидроксипропил)тиоацетат (0,7 мг, 5,3 моль) растворяют в 0,9 мл раствора ацетонитрила для последующего использования. Предварительно полученный указанный выше раствор в ацетонитриле, содержащем S-(3-гидроксипропил) тиоацетат, добавляют к буферу уксусная кислота/ацетат натрия, содержащему антитело, рН составляет 4,3 (10,35 мг/мл, 9,0 мл, 0,97 моль). Затем по каплям добавляют 1,0 мл водного раствора, содержащего цианоборгидрид натрия (14,1 мг, 224 моль), и проводят реакцию при встряхивании при 25°С в течение 2 ч. После завершения реакции реакционную смесь обессоливают и очищают с использованием гелевой колонки Sephadex G25 (фаза элюирования: 0,05 М раствор PBS, рН 6,5) с получением раствора, содержащего продукт 1f. Раствор концентрируют до 10 мг/мл и сразу используют в следующей реакции.
На втором этапе к раствору 1f (11,0 мл) добавляют 0,35 мл 2,0 М раствора гидрохлорида карбоксамида и проводят реакцию при встряхивании при 25°С в течение 30 мин. Затем реакционный раствор обессоливают и очищают с использованием гелевой колонки Sephadex G25 (фаза элюирования: 0,05 М раствор PBS, рН 6,5) с получением раствора, содержащего продукт 2f (концентрация 6,17 мг/мл, 14,7 мл).
На третьем этапе соединение MC-MMAF (1,1 мг, 1,2 моль, получают по способу, описанному в патенте РСТ WO 2005081711) растворяют в 0,3 мл ацетонитрила, добавляют в раствор 2f (концентрация 6,17 мг/мл, 3,0 мл) и подвергают реакции при встряхивании при 25°С в течение 4 ч. Затем реакционный раствор обессоливают и очищают с использованием гелевой колонки Sephadex G25 (фаза элюирования: 0,05 М раствор PBS, рН 6,5) и фильтруют в стерильных условиях на фильтре с получением продукта Ab2-МС-MMAF. Среднее значение DAR, у, продукта Ab2-MC-MMAF, определенное методом HIC-HPLC (гидрофобная интерактивная высокоэффективная жидкостная хроматография), составляло 4, и конъюгат антитело-лекарственное средство в буфере PBS (3,7 мг/мл, 4,7 мл) хранят в холодильнике при 4°С. Продукт Ab3-MC-MMAF получают описанным выше способом. Среднее значение DAR у, продукта Ab3-MC-MMAF, определенное методом HIC-HPLC, составило 4,1, а конъюгат антитело-лекарственное средство в буфере PBS (3,5 мг/мл, 5,0 мл) хранят в холодильнике при 4°С.
Пример 8: Конъюгация антител к SN-38
Лекарственные средства, конъюгированные с антителами, получают с помощью следующего процесса связывания, в котором Ab представляет собой Ab2:
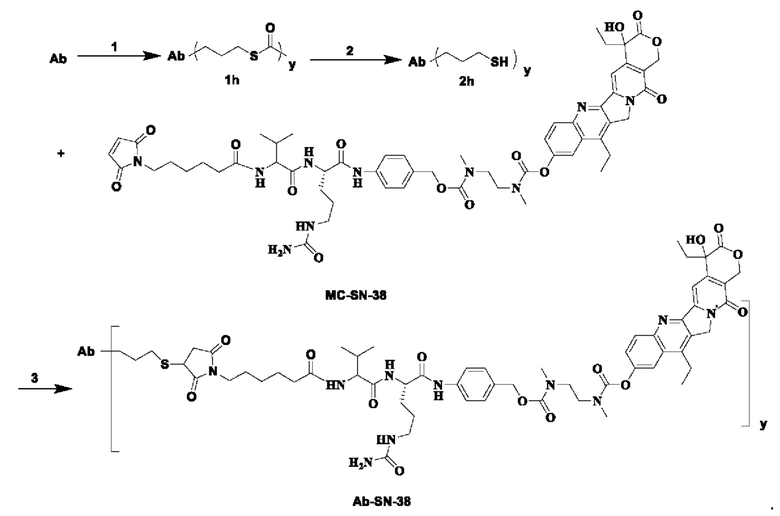
На первом этапе S-(3-гидроксипропил)тиоацетат (0,7 мг, 5,3 моль) растворяют в 0,9 мл раствора ацетонитрила для последующего использования. Предварительно полученный указанный выше раствор в ацетонитриле, содержащем S-(3-гидроксипропил) тиоацетат, добавляют к буферу уксусная кислота/ацетат натрия, содержащему антитело, рН составляет 4,3 (10,35 мг/мл, 9,0 мл, 0,97 моль). Затем по каплям добавляют 1,0 мл водного раствора, содержащего цианоборгидрид натрия (14,1 мг, 224 моль), и проводят реакцию при встряхивании при 25°С в течение 2 ч. После завершения реакции реакционную смесь обессоливают и очищают с использованием гелевой колонки Sephadex G25 (фаза элюирования: 0,05 М раствор PBS, рН 6,5) с получением раствора, содержащего продукт 1h. Раствор концентрируют до 10 мг/мл и сразу используют в следующей реакции.
На втором этапе к раствору 1h (11,0 мл) добавляют 0,35 мл 2,0 М раствора гидрохлорида карбоксамида и проводят реакцию при встряхивании при 25°С в течение 30 мин. Затем реакционный раствор обессоливают и очищают с использованием гелевой колонки Sephadex G25 (фаза элюирования: 0,05 М раствор PBS, рН 6,5) с получением раствора, содержащего продукт 2h (концентрация 6,2 мг/мл, 15,0 мл). Раствор концентрируют до 10 мг/мл и сразу используют в следующей реакции.
На третьем этапе соединение MC-SN-38 (1,3 мг, 1,2 моль) растворяют в 0,3 мл ацетонитрила, добавляют к 2h (концентрация 6,2 мг/мл, 3,0 мл) и подвергаются реакции при встряхивании при 25°С в течение 4 ч. Затем реакционный раствор обессоливают и очищают на гелевой колонке Sephadex G25 (фаза элюирования: 0,05 М раствор PBS, рН 6,5) и фильтруют в стерильных условиях на фильтре с получением конъюгата антитело-лекарственное средство Ab-SN-38 в PBS буфере (3,7 мг/мл, 4,7 мл), который хранят в холодильнике при 4°С. Среднее значение у определяют по ультрафиолетовому (УФ) излучению. Кюветы, заполненные сукцинатным буфером натрия, помещают соответственно в эталонную абсорбционную ячейку и абсорбционную ячейку для определения образца, и после вычета контрольного растворителя кюветы, заполненные тестируемым раствором, помещают в абсорбционную ячейку для определения образца. Абсорбцию измеряют при 280 нм и 370 нм.
Обработка данных:
Содержание антител Cmab определяют путем построения стандартной кривой и измерения абсорбции при длине волны 280 нм. Содержание малых молекул CDrug определяют путем измерения абсорбции при длине волны 370 нм.
Среднее значение лекарственной нагрузки у = CDdrug/Cmab.
Среднее значение DAR у конъюгата антитело-лекарственное средство Ab2-SN-38, определенное вышеуказанным способом, составило 3,9.
Пример 9: Конъюгация антител с эксатеканом
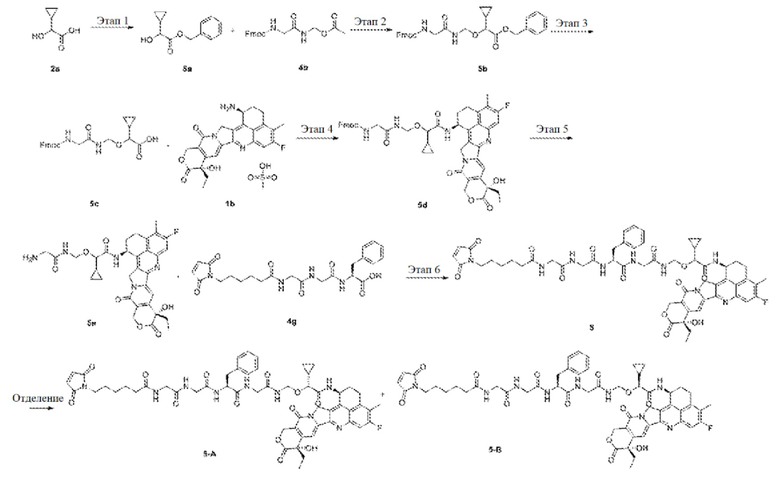 .
.
На первом этапе 2а (2 г, 17,2 ммоль) растворяют в 75 мл ацетонитрила и добавляют последовательно карбонат калия (9,27 г, 67,2 ммоль), бензилбромид (20 мл, 167,2 ммоль) и иодид тетрабутиламмония (620 мг, 1,68 г ммоль). Реакционный раствор перемешивают при комнатной температуре в течение 48 ч и фильтруют через диатомовую землю. Осадок на фильтре промывают этилацетатом (20 мл). Фильтрат объединяют и концентрируют при пониженном давлении. Полученные остатки очищают хроматографией на колонке с силикагелем с проявляющей системой растворителей С с получением продукта 5а (3,2 г, выход: 90,1%).
На втором этапе в реакционную колбу добавляют соединения 5а (181,3 мг, 0,879 ммоль) и 4b (270 мг, 0,733 ммоль). Добавляют 6 мл тетрагидрофурана. Реакционную смесь трижды заменяют аргоном и охлаждают до 0-5°С на бане со льдом и водой. Добавляют трет-бутоксид калия (164 мг, 1,46 ммоль). Ледяную баню удаляют, реакционную смесь нагревают до комнатной температуры и перемешивают в течение 40 мин. Добавляют 15 мл ледяной воды и реакционную смесь экстрагируют этилацетатом (40 мл × 2) и хлороформом (20 мл × 5). Органические фазы объединяют и концентрируют.Полученные остатки растворяют в 6 мл диоксана, добавляют 3 мл воды, бикарбоната натрия (73,8 мг, 0,879 ммоль) и 9-флуоренилметилхлорформиата (190 мг, 0,734 ммоль) и перемешивают при комнатной температуре в течение 2 ч. Добавляют 30 мл воды и реакционную смесь экстрагируют этилацетатом (20 мл × 3). Органические фазы объединяют, промывают насыщенным раствором хлорида натрия, сушат над безводным сульфатом натрия и фильтруют. Фильтрат концентрируют при пониженном давлении. Полученные остатки очищают колоночной хроматографией на силикагеле с проявляющей системой растворителей C с получением продукта 5b бензил-10-циклопропил-1-(9Н-флуорен-9-ил)-3,6-диоксо-2,9-диокса-4,7-диазаундек-11-карбоксилата (73 мг, выход: 19,4%).
МС m/z (ESI (ионизация электроспреем): 515,0 [М+1].
На третьем этапе 5b (30 мг, 0,058 ммоль) растворяют в 6,75 мл смешанного растворителя тетрагидрофурана и этилацетата (об. : об. = 2:1). Добавляют палладий на угле (18 мг, содержание 10%, сухой), реакционную смесь трижды заменяют водородом и проводят реакцию при перемешивании при комнатной температуре в течение 1 ч. Реакционный раствор фильтруют через диатомовую землю. Осадок на фильтре промывают этилацетатом. Фильтрат концентрируют с получением сырого продукта 5 с 10-циклопропил-1-(9Н-флуорен-9-ил)-3,6-диоксо-2,9-диокса-4,7-диазаундек-11-кислота (20 мг), который непосредственно используют в следующей реакции без очистки.
МС m/z (ESI): 424,9 [М+1].
На четвертом этапе в реакционную колбу добавляют 1b (15 мг, 28,2 мкмоль). Добавляют 1,5 мл N, N-диметилформамида. Реакционную смесь трижды заменяют аргоном и охлаждают до 0-5°С на бане со льдом и водой. Добавляют каплю триэтиламина, сырой продукт 5 с (20 мг, 47,1 мкмоль), 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилхлорморфолин (25,4 мг, 86,2 мкмоль) и реакционную смесь подвергают реакции при перемешивании на бане со льдом в течение 40 мин. Добавляют 15 мл воды и реакционную смесь экстрагируют этилацетатом (20 мл × 3). Органические фазы объединяют. Органические фазы промывают насыщенным раствором хлорида натрия (20 мл × 2), сушат над безводным сульфатом натрия и фильтруют. Фильтрат концентрируют при пониженном давлении. Полученные остатки очищают тонкослойной хроматографией с проявляющей системой растворителей В с получением указанного в заголовке продукта 5d (9Н-флуорен-9-ил)метил(2-(((1-циклопропил-2-(((1S,9S)-9-этил-5-фтор-9-гидрокси-4-метил-10,13-диоксо-2,3,9,10,13,15-гексагидро-1H, 12Н-бензо[де]пирано[3',4':6,7]индолозино[1,2-b]хинолин-1-ил)амино)-2-оксоэтокси)метил)амино)-2-оксоэтил)карбамат (23,7 мг, выход: 78,9%).
MC m/z (ESI): 842,1 [М+1].
На пятом этапе 5d (30 мг, 35,7 мкмоль) растворяют в 3 мл дихлорметана. Добавляют 1,5 мл диэтиламина и реакционную смесь перемешивают при комнатной температуре в течение 2 ч. Реакционный раствор концентрируют при пониженном давлении. Добавляют 1,5 мл толуола и реакционную смесь концентрируют при пониженном давлении, повторяют дважды. К остаткам добавляют 4,5 мл н-гексана и гомогенизируют. Супернатант выливают после того, как ее оставляют в покое, а твердое вещество оставляют. Твердые остатки концентрируют при пониженном давлении и сушат выкачиванием, получая сырой продукт 5е 2-((2-аминоацетамидо)метокси)-2-циклопропил-N-((1S,9S)-9-этил-5-фтор-9-гидроксил-4-метил-10,13-диоксо-2,3,9,10,13,15-гексагидро-1Н,12Н-бензо[де]пирано[3',4':6,7]индолозино[1,2-b]хинолин-1-ил)ацетамид (23 мг), который непосредственно используют в следующей реакции без очистки.
МС m/z (ESI): 638,0 [М+18].
На шестом этапе сырой продукт 5е (20 мг, 32,3 мкмоль) растворяют в 1 мл N, N-диметилформамида и трижды заменяют аргоном. Реакционную смесь охлаждают до 0-5°С на бане со льдом и водой. Добавляют 0,5 мл 4g раствора N,N-диметилформамида (31,8 мг, 67,3 мкмоль), 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилхлорморфолин (27,8 мг, 94,3 мкмоль) добавляют и подвергают реакции при перемешивании на бане со льдом в течение 10 мин. Ледяную баню удаляют, реакционную смесь нагревают до комнатной температуры и проводят реакцию при перемешивании в течение 1 ч с получением соединения 5. Реакционный раствор очищают высокоэффективной жидкостной хроматографией (условия разделения: колонка: XBridge Prep C18 OBD 5 мкм 19*250 мм; подвижная фаза: А-вода (10 ммоль NH4OAc): В-ацетонитрил, градиентное элюирование, скорость потока: 18 мл/мин). Соответствующие компоненты собирают и концентрируют при пониженном давлении с получением продуктов 5-А и 5-В (3,6 мг, 2,6 мг).
МС m/z (ESI): 1074,4 [М+1].
Соединение одинарной конфигурации 5-А (с более коротким временем удерживания):
Анализ UPLC (сверхэффективная жидкостная хроматография): время удерживания: 1,14 мин, чистота: 85% (колонка: ACQUITY UPLC ВЕНС18 1,7 мкм 2,1*50
мм, подвижная фаза: А-вода (5 ммоль NH4OAc), В-ацетонитрил).
1Н ЯМР (400 МГц, ДМСО-d6): δ 8,60 (t, 1H), 8,51-8,49 (d, 1Н), 8,32-8,24 (m, 1Н), 8,13-8,02 (га, 2Н), 8,02-7,96 (m, 1Н), 7,82-7,75 (m, 1Н), 7,31 (s, 1Н), 7,26-7,15 (m, 4Н), 6,99 (s, 1H), 6,55-6,48 (m, 1Н), 5,65-5,54 (m, 1Н), 5,41 (s, 2Н), 5,35-5,15 (m, 3Н), 4,74-4,62 (m, 2Н), 4,54-4,40 (m, 2Н), 3,76-3,64 (m, 4Н), 3,62-3,48 (m, 2Н), 3,20-3,07 (m, 2Н), 3,04-2,94 (m, 2Н), 2,80-2,62 (m, 2Н), 2,45-2,30 (m, 3Н), 2,25-2,15 (m, 2Н), 2,15-2,04 (m, 2Н), 1,93-1,78 (m, 2Н), 1,52-1,39 (m, 3Н), 1-34-1,12 (m, 5Н), 0,87 (t, 3Н), 0,64-0,38 (m, 4Н)
Соединение одинарной конфигурации 5-В (с более длительным временем удерживания):
Анализ UPLC: время удерживания: 1,16 мин, чистота: 89% (колонка: ACQUITY UPLC ВЕНС18 1,7 мкм 2,1*50 мм, подвижная фаза: А-вода (5 ммоль NH4OAc), В-ацетонитрил).
1Н ЯМР (400 МГц, ДМСО-d6): δ 8,68-8,60 (m, 1Н), 8,58-8,50 (m, 1Н), 8,32-8,24 (m, 1Н), 8,13-8,02 (m, 2Н), 8,02-7,94 (m, 1Н), 7,82-7,75 (m, 1Н), 7,31 (s, 1H), 7,26-7,13 (m, 4Н), 6,99 (s, 1Н), 6,55-6,48 (m, 1Н), 5,60-5,50 (m, 1H), 5-41 (s, 2Н), 5,35-5,15 (m, 3Н), 4,78-4,68 (m, 1Н), 4,60-4,40 (m, 2Н), 3,76-3,58 (m, 4Н), 3,58-3,48 (m, 1Н), 3,20-3,10 (m, 2Н), 3,08-2,97 (m, 2Н), 2,80-2,72 (m, 2Н), 2,45-2,30 (m, 3Н), 2,25-2,13 (m, 2Н), 2,13-2,04 (m, 2Н), 2,03-1,94 (m, 2Н), 1,91-1,78 (m, 2Н), 1,52-1,39 (m, 3Н), 1,34-1,12 (m, 5Н), 0,91-0,79 (m, 3Н), 0,53-0,34 (m, 4Н)
Способы получения других промежуточных продуктов аналогичны промежуточным продуктам 5.
Получений водный раствор, содержащий трис(2-карбоксиэтил)фосфин (10 мМ, 0,347 мл, 3,47 мкмоль), добавляют к забуференному PBS водному раствору, содержащему антитело Ab2 (рН составляет 6,5) 0,05 М водному раствору, забуференному PBS; 7,3 мл, 13,8 мг/мл, 0,681 мкмоль) при 37°С. Реакционную смесь помещают в шейкер с водяной баней и подвергают реакции при встряхивании при 37°С в течение 3 ч. Реакцию останавливают, реакционный раствор охлаждают до 25°С на водяной бане, разбавляют до 14,0 мл и отбирают 3,3 мл раствора для следующей реакции.
Соединение 5-А (3,0 мг, 3,72 мкмоль) растворяют в 0,15 мл ДМСО (диметилсульфоксид) и добавляют к 3,3 мл вышеуказанного раствора. Реакционную смесь помещают в шейкер с водяной баней и подвергают реакции при встряхивании при 25°С в течение 3 ч. Реакцию останавливают. Реакционный раствор обессоливают и очищают с использованием гелевой колонки с сефадексом G25 (фаза элюирования: рН 6,5, 0,05 М водный раствор, забуференный PBS, содержащий 0,001 М ЭДТА (этилендиаминтетрауксусная кислота)) с получением типичного продукта Ab-эксатекан, Ab2-эксатекан в буфере PBS (1,35 мг/мл, 13 мл), который хранят в замороженном виде при 4°С.
Среднее значение у определяют по абсорбции в ультрафиолетовом диапазоне. Кюветы, заполненные сукцинатным буфером натрия, помещают соответственно в эталонную абсорбционную ячейку и абсорбционную ячейку для определения образца, и после вычета контрольного растворителя кюветы, заполненные тестируемым раствором, помещают в абсорбционную ячейку для определения образца. Абсорбцию измеряют при 280 нм и 370 нм.
Обработка данных:
Содержание антител Cmab определяют путем построения стандартной кривой и измерения абсорбции при длине волны 280 нм. Содержание малых молекул CDrug определяют путем измерения абсорбции при длине волны 370 нм.
Среднее значение лекарственной нагрузки у = CDdrug/Cmab.
Что касается типичного продукта Ab2-эксатекан, то его значение определено 7,6 вышеописанным способом. Образцы Ab2-эксатекан (у составляет 8) получают очисткой УФ-ВЭЖХ (ВЭЖХ с ультрафиолетовым матричным фотодиодным детектором).
Пример 10: Опухолелизирующая активность конъюгатов антитело-лекарственное средство
Для дальнейшего исследования цитотоксического эффекта конъюгатов антитело-лекарственное средство на опухоли, формирующийся in vivo, противоопухолевый эффект конъюгатов антитело-лекарственное средство по настоящему изобретению оценивают после формирования трансплантированных опухолей клетками NCI-H929 у мышей.
(1) 9×106 клеток NCI-H929 вводят подкожно 8-недельным иммунодефицитным бестимусным мышам (NOD-SCID). Внутривенное введение конъюгатов антитело-лекарственное средство Ab2-MC-MMAF (Пример 7, у составляет 4) и Ab2-экзатекана (Пример 9, у составляет 8) начинают через 8 дней один раз в неделю в дозе 1 мг/кг. Белок человеческого IgGl используют в качестве контроля в дозе 1 мг/кг. В контрольной группе и группе лечения было по 5 мышей. Степень ингибирования опухоли рассчитывают путем измерения объема опухоли. Степень ингибирования опухоли составляет 100% - (объем опухоли в группе лечения на 14-й день - объем опухоли в группе лечения на 0-й день)/(объем опухоли в контрольной группе на 14-й день - объем опухоли в контрольной группе на 0-й день). Результаты исследования приведены в Таблице 9. Конъюгаты антитело-лекарственное средство Ab2-MC-MMAF (Пример 7, у составляет 4) и Ab2-эксатекан (Пример 9, у составляет 8) проявляют ингибирующее действие на опухоль.
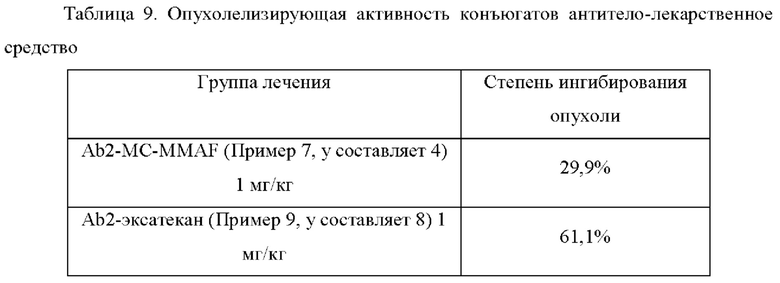
(1) 9×106 клеток NCI-H929 вводят подкожно 8-недельным бестимусным мышам с иммунодефицитом (NOD-SCID). Внутривенную инъекцию конъюгатов антитело-лекарственное средство Ab2-MC-MMAF (Пример 7, у составляет 4) и Ab3-MC-MMAF (Пример 7, у составляет 4,1) начинают проводить через 8 дней два раза в неделю и в дозировке 3 мг/кг. Белок человеческого IgG1 используют в качестве контроля в дозировке 1 мг/кг. В контрольной группе и группе лечения было по 5 мышей. Степень ингибирования опухоли рассчитывают путем измерения объема опухоли. Степень ингибирования опухоли TGI составляет 100% - (объем опухоли в группе лечения на 14-й день - объем опухоли в группе лечения на 0-й день)/(объем опухоли в контрольной группе на 14-й день - объем опухоли в контрольной группе на 0-й день). Результаты исследования приведены в Таблице 10. Ab2-MC-MMAF (Пример 7, у составляет 4) и Ab3-MC-MMAF (Пример 7, у составляет 4,1) оба проявляют цитотоксический эффект в отношении опухолей.
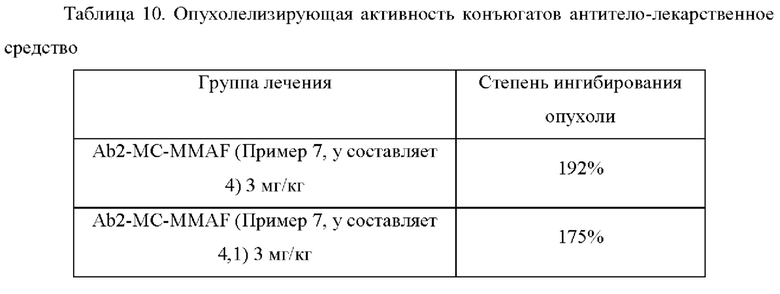
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ШАНХАЙ ХЭНСОХ БИОМЕДИКАЛ КО., ЛТД., ЦЗЯНСУ ХЭНСОХ
ФАРМАСЬЮТИКАЛ ГРУП КО., ЛТД.
<120> АНТИТЕЛО К BCMA, ЕГО АНТИГЕН-СВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ
МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ
<130> 702071CPCT
<150> CN 201910695597.9
<151> 2019-07-30
<160> 23
<170> SIPOSequenceListing 1.0
<210> 1
<211> 121
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(121)
<223> Вариабельная область тяжелой цепи мышиного mab M1
<400> 1
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Leu Gly Tyr Ser Phe Ser Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Thr Pro Val His Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 2
<211> 106
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(106)
<223> Вариабельный домен легкой цепи мышиного mab M1
<400> 2
Glu Ile Leu Leu Thr Gln Ser Pro Ala Ile Ile Val Thr Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ile Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Ile Trp Ile Tyr
35 40 45
Gly Ile Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Phe Ser Phe Thr Ile Asn Ser Met Glu Ala Glu
65 70 75 80
Asp Val Ala Thr Tyr Tyr Cys Gln Gln Arg Ser Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 3
<211> 10
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(10)
<223> HCDR1 мышиного mab M1
<400> 3
Gly Tyr Ser Phe Ser Asp Tyr Glu Met His
1 5 10
<210> 4
<211> 17
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(17)
<223> HCDR2 мышиного mab M1
<400> 4
Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 5
<211> 14
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(14)
<223> HCDR3 мышиного mab M1
<400> 5
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr
1 5 10
<210> 6
<211> 10
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(10)
<223> LCDR1 мышиного mab M1
<400> 6
Ser Ala Ser Ser Ser Val Ile Tyr Met Asn
1 5 10
<210> 7
<211> 7
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(7)
<223> LCDR2 мышиного mab M1
<400> 7
Gly Ile Ser Asn Leu Ala Ser
1 5
<210> 8
<211> 9
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(9)
<223> LCDR3 мышиного mab M1
<400> 8
Gln Gln Arg Ser Ser Tyr Pro Leu Thr
1 5
<210> 9
<211> 121
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(121)
<223> Гуманизированная вариабельная область тяжелой цепи HCVR1
<400> 9
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 10
<211> 121
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(121)
<223> Гуманизированная вариабельная область тяжелой цепи HCVR2
<400> 10
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 11
<211> 121
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(121)
<223> Гуманизированная вариабельная область тяжелой цепи HCVR3
<400> 11
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 12
<211> 106
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(106)
<223> Вариабельная область гуманизированной легкой цепи LCVR1
<400> 12
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ile Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Gly Ile Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 13
<211> 106
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(106)
<223> Вариабельная область гуманизированной легкой цепи LCVR2
<400> 13
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ile Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Ile Trp Ile Tyr
35 40 45
Gly Ile Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 14
<211> 106
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(106)
<223> Вариабельная область гуманизированной легкой цепи LCVR3
<400> 14
Glu Ile Leu Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ile Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Ile Trp Ile Tyr
35 40 45
Gly Ile Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 15
<211> 451
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ЦЕПЬ
<222> (1)..(451)
<223> Ab1 HC
<400> 15
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 16
<211> 451
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ЦЕПЬ
<222> (1)..(451)
<223> Ab2 HC
<400> 16
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 17
<211> 451
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ЦЕПЬ
<222> (1)..(451)
<223> Ab3 HC
<400> 17
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile His Pro Gly Ser Gly Gly Ser Ala Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Asp Tyr Gly Tyr Ser Trp Ala Trp Phe Pro Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 18
<211> 213
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ЦЕПЬ
<222> (1)..(213)
<223> Ab1 LC
<400> 18
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ile Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Gly Ile Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 19
<211> 213
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ЦЕПЬ
<222> (1)..(213)
<223> Ab2 LC
<400> 19
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ile Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Ile Trp Ile Tyr
35 40 45
Gly Ile Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 20
<211> 213
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ЦЕПЬ
<222> (1)..(213)
<223> Ab3 LC
<400> 20
Glu Ile Leu Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ile Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Ile Trp Ile Tyr
35 40 45
Gly Ile Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 21
<211> 65
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ПЕПТИД
<222> (1)..(65)
<223> Внеклеточная область His-меченного BCMA человека
<400> 21
Met Leu Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser
1 5 10 15
Leu Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr
20 25 30
Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser
35 40 45
Val Lys Gly Thr Asn Ala His His His His His His His His His His
50 55 60
His
65
<210> 22
<211> 330
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(330)
<223> Константная область тяжелой цепи
<400> 22
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 23
<211> 107
<212> ПРТ
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> Константная область легкой цепи
<400> 23
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛО К B7-H4, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2792748C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО ПРОТИВ CD3E/BCMA И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800164C2 |
| КОНЪЮГАТ АНТИТЕЛА К B7-H4 И ЛЕКАРСТВЕННОГО СРЕДСТВА И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2827531C2 |
| АНТИТЕЛО ПРОТИВ СТОЛБНЯЧНОГО ТОКСИНА И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2815280C1 |
| АНТИТЕЛО ПРОТИВ КЛАУДИНА 18.2 И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2822550C2 |
| АНТИТЕЛО К CLDN-18.2 И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2829997C1 |
| АНТИТЕЛО, СВЯЗЫВАЮЩЕЕ ЧЕЛОВЕЧЕСКИЙ IL-4R, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2779649C1 |
| АНТИТЕЛА, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2766094C2 |
| Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с BCMA, и его применение | 2022 |
|
RU2820350C2 |
| КОНЪЮГАТ АНТИТЕЛА ПРОТИВ CEA И АНАЛОГА ЭКСАТЕКАНА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2833323C1 |
Группа изобретений относится к области иммунологии, в частности к антителу к ВСМА, его антигенсвязывающему фрагменту и их медицинскому применению. Предложены антитело к ВСМА или его антигенсвязывающий фрагмент, его получение, фармацевтическая композиция, цитотоксический конъюгат и их применение в качестве лекарственного средства для лечения или для обнаружения и диагностики ВСМА-опосредованных заболеваний или состояний. Антитело обладает высокой аффинностью, высокой специфичностью, низкой иммуногенностью, высокой биологической активностью, значительным противоопухолевым действием и усиленным эндоцитозом. Данное изобретение может найти дальнейшее применение в терапии различных ВСМА-опосредованных заболеваний или состояний. 10 н. и 25 з.п. ф-лы, 10 табл., 9 пр.
1. Антитело к BCMA (антиген созревания B-клеток) или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи и вариабельную область легкой цепи, где вариабельная область тяжелой цепи содержит HCDR1, представленную в SEQ ID NO: 3, HCDR2, представленную в SEQ ID NO: 4, и HCDR3, представленную в SEQ ID NO: 5; и вариабельная область легкой цепи содержит LCDR1, представленную в SEQ ID NO: 6, LCDR2, представленную в SEQ ID NO: 7, и LCDR3, представленную в SEQ ID NO: 8.
2. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 1, где антитело к BCMA представляет собой мышиное антитело, химерное антитело, человеческое антитело или гуманизированное антитело.
3. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 1 или 2, где антитело к BCMA или его антигенсвязывающий фрагмент дополнительно содержит константную область тяжелой цепи, полученную из человеческого IgG1 (иммуноглобулин G1), IgG2, IgG3 или IgG4, или их варианта.
4. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 3, где антитело к BCMA или его антигенсвязывающий фрагмент дополнительно содержит константную область тяжелой цепи, полученную из человеческого IgG1, IgG2 или IgG4.
5. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 3, где антитело к BCMA или его антигенсвязывающий фрагмент дополнительно содержит константную область тяжелой цепи IgG1 с повышенной ADCC-токсичностью (антителозависимая клеточная цитотоксичность) после аминокислотной мутации.
6. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 3, где антитело к BCMA или его антигенсвязывающий фрагмент дополнительно содержит константную область тяжелой цепи IgG1, представленную в SEQ ID NO: 22.
7. Антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-6, где антитело к BCMA или его антигенсвязывающий фрагмент дополнительно содержит константную область легкой цепи, полученную из человеческой κ-цепи, λ-цепи или их варианта.
8. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 7, где антитело к BCMA или его антигенсвязывающий фрагмент дополнительно содержит константную область легкой цепи, представленную в SEQ ID NO: 23.
9. Антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-8, где антитело к BCMA или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 9, SEQ ID NO: 10 и SEQ ID NO: 11, или вариабельную область тяжелой цепи, идентичную им по меньшей мере на 95% или 99%.
10. Антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-9, где антитело к BCMA или его антигенсвязывающий фрагмент содержит вариабельную область легкой цепи, выбранную из группы, состоящей из SEQ ID NO: 12, SEQ ID NO: 13 и SEQ ID NO: 14, или вариабельную область легкой цепи, идентичную им по меньшей мере на 95% или 99%.
11. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 9 или 10, где антитело к BCMA или его антигенсвязывающий фрагмент содержит тяжелую цепь, выбранную из группы, состоящей из SEQ ID NO: 15, SEQ ID NO: 16 и SEQ ID NO: 17, или тяжелую цепь, идентичную им по меньшей мере на 95% или 99%.
12. Антитело к BCMA или его антигенсвязывающий фрагмент по п. 9 или 10, где антитело к BCMA или его антигенсвязывающий фрагмент содержит легкую цепь, выбранную из группы, состоящей из SEQ ID NO: 18, SEQ ID NO: 19 и SEQ ID NO: 20, или легкую цепь, идентичную им по меньшей мере на 95% или 99%.
13. Антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-12, где
антитело к BCMA или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, представленную в SEQ ID NO: 9, и вариабельную область легкой цепи, представленную в SEQ ID NO: 12; или
антитело к BCMA или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, представленную в SEQ ID NO: 10, и вариабельную область легкой цепи, представленную в SEQ ID NO: 13; или
антитело к BCMA или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, представленную в SEQ ID NO: 11, и вариабельную область легкой цепи, представленную в SEQ ID NO: 14.
14. Антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-13, где
антитело к BCMA содержит тяжелую цепь, представленную в SEQ ID NO: 15, и легкую цепь, представленную в SEQ ID NO: 18; или
антитело к BCMA содержит тяжелую цепь, представленную в SEQ ID NO: 16, и легкую цепь, представленную в SEQ ID NO: 19; или
антитело к BCMA содержит тяжелую цепь, представленную в SEQ ID NO: 17, и легкую цепь, представленную в SEQ ID NO: 20.
15. Полинуклеотид, кодирующий антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-14.
16. Вектор экспрессии, содержащий полинуклеотид по п. 15.
17. Клетка-хозяин для получения антитела к BCMA или его антигенсвязывающего фрагмента по любому из пп. 1-14, в которую введен или которая содержит вектор экспрессии по п. 16.
18. Клетка-хозяин по п. 17, где клетка-хозяин представляет собой клетку бактерии, дрожжей или млекопитающего.
19. Клетка-хозяин по п. 18, которая представляет собой клетку Escherichia coli, Pichia pastoris, клетку CHO (яичник китайского хомячка) или клетку HEK293 (эмбриональная почка человека).
20. Способ получения антитела к BCMA по любому из пп. 1-14, включающий этапы:
культивирования клетки-хозяина по любому из пп. 17-19;
выделения антитела из культуры; и
очистки антитела.
21. Способ по п. 20, включающий этапы:
культивирования клетки НЕК293;
выделения антитела из культуральной жидкости; и
очистки антитела хроматографическим методом.
22. Фармацевтическая композиция для лечения или профилактики BCMA-опосредованного заболевания или состояния, содержащая антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-14, а также фармацевтически приемлемый эксципиент или носитель.
23. Набор для обнаружения или диагностики, предназначенный для обнаружения, диагностики или прогнозирования BCMA-опосредованного заболевания или состояния, содержащий антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-14, необязательно, где набор для обнаружения или диагностики также содержит один или более реагентов, способных обнаруживать связывание антитела к BCMA или его антигенсвязывающего фрагмента с BCMA.
24. Конъюгат антитело-лекарственное средство для лечения или профилактики BCMA-опосредованного заболевания или состояния, содержащий антитело к BCMA или его антигенсвязывающий фрагмент по любому из пп. 1-14, связанные с цитотоксическим агентом.
25. Конъюгат антитело-лекарственное средство по п. 24, где цитотоксический агент выбран из группы, состоящей из MMAF (монометил ауристатин F), SN-38 (7-этил-10-гидроксикамптотецин) и эксатекана.
26. Применение антитела к BCMA или его антигенсвязывающего фрагмента по любому из пп. 1-14, или фармацевтической композиции по п. 22, или конъюгата антитело-лекарственное средство по п. 24 для получения лекарственного препарата для лечения или профилактики BCMA-опосредованного заболевания или состояния.
27. Применение по п. 26, где BCMA-опосредованное заболевание или состояние представляет собой рак или аутоиммунное заболевание.
28. Применение по п. 27, где рак представляет собой рак, экспрессирующий BCMA, и аутоиммунное заболевание выбрано из группы, состоящей из красной волчанки, IgA-нефропатии и ревматического артрита.
29. Применение по п. 28, где рак, экспрессирующий BCMA, представляет собой лимфому, лейкоз или миелому.
30. Применение по п. 29, где миелома представляет собой множественную миелому.
31. Применение антитела к BCMA или его антигенсвязывающего фрагмента по любому из пп. 1-14 для получения набора для обнаружения, диагностики или прогнозирования BCMA-опосредованного заболевания или состояния.
32. Применение по п. 31, где BCMA-опосредованное заболевание или состояние представляет собой рак или аутоиммунное заболевание.
33. Применение по п. 32, где рак представляет собой рак, экспрессирующий BCMA, и аутоиммунное заболевание выбрано из группы, состоящей из красной волчанки, IgA-нефропатии и ревматического артрита.
34. Применение по п. 33, где рак, экспрессирующий BCMA, представляет собой лимфому, лейкоз или миелому.
35. Применение по п. 34, где миелома представляет собой множественную миелому.
| CN 109293772 A, 01.02.2019 | |||
| WO 2019025983 A1, 07.02.2019 | |||
| US 2019023801 A1, 24.01.2019 | |||
| WO 2017083511 A1, 18.05.2017 | |||
| US 2018171018 A1, 21.06.2018 | |||
| US 9273141 B2, 01.03.2016 | |||
| RU 2017133826 A, 13.05.2019 | |||
| HECHLER T | |||
| ET AL | |||
| Спускная труба при плотине | 0 |
|
SU77A1 |
| CANCER RESEARCH, 2017, v.77, | |||
Авторы
Даты
2024-05-22—Публикация
2020-07-29—Подача