ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к антителу к B7-H4, его антигенсвязывающему фрагменту, обладающему иммунореактивностью в отношении человеческого рецептора B7-H4, химерным антителам и гуманизированным антителам, содержащим области CDR (complementary determining region - определяющая комплементарность область) указанного антитела к B7-H4, фармацевтическим композициям, содержащим человеческое антитело против B7-H4 и его антигенсвязывающий фрагмент, и их применению в качестве противораковых агентов.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Иммунотерапия опухолей представляет собой «проблемное место» в долгосрочном исследований и разработок в области лечения рака и среди которых T-клеточная иммунотерапия опухолей занимает центральное положение. Ускользание опухоли от иммунологического надзора является огромным препятствием, с которым сталкивается иммунотерапия опухолей. Большинство экспрессирующих опухолей может распознаваться в различной степени иммунной системой хозяина, но во многих случаях опухолевый рост стимулируется ингибированием иммунной системы, вызванным собственно опухолевыми клетками, вследствие неудовлетворительного иммунного ответа, вызываемого неэффективной активацией эффекторных T-клеток. Иммунотерапия опухолей предполагает использование в полной мере и рекрутинг киллерных T-клеток и/или других клеток иммунной системы у пациентов с опухолью для уничтожения опухолей.
Исследования на CD28 рецепторе и его лигандах привели к характеризации родственных молекул, известных как суперсемейство B7. Члены семейства B7 представляют собой класс иммуноглобулинов с иммуноглобулин V-подобным доменом (IgV) и иммуноглобулин C-подобным доменом (IgC), члены которого включают костимулирующие факторы B7.1 (CD80) и B7.2 (CD86), индуцибельный лиганд для фактора стимуляции (ICOS-L/B7-H2), лиганд запрограммированной гибели клеток-1 (PD-L1/B7-H1), лиганд запрограммированной гибели клеток-2 (PD-L2/B7-DC), B7-H4 и B7-H4, и т.д.
Человеческий B7-H4 представляет собой трансмембранный белок типа I, состоящий из 282 аминокислот, кодирующий ген которого расположен в области p11.1 хромосомы 1 (Choi IH et al., J Immunol. 2003 Nov 1; 171(9): 4650-4). B7-H4 играет роль в негативной регуляции T-клеточного иммунного ответа. B7-H4 оказывает сильное ингибирующее действие на дифференциацию, развитие, прохождение по клеточному циклу и продукцию цитокинов CD4+ и CD8+ T-клеток (Sica GL et al. Immunity. 2003 Jun; 18(6): 849-61). Нарушения клеток иммунной системы и аутоиммунные явления не обнаруживались в мышах, нокаутированных по B7-H4 (Zhu G et al, Blood. 2009 Feb 19; 113(8): 1759-67; Suh WK et al., Blood. Mol Cell Biol. 2006 Sep; 26(17):6403-11). B7-H4 рецепторы и их сигнальные пути в настоящее время все еще остаются неясными.
При недавних исследованиях обнаружили, что белок B7-H4 в большом количестве экспрессируется в разных опухолевых тканях, делая возможным избегание опухолевыми клетками атаки со стороны иммунной системы организма. В качестве мишени для терапии опухолей молекула B7-H4 предоставляет новый способ иммунотерапии опухолей.
В настоящее время, известно, что человеческий B7-H4 экспрессируется на разных раковых клетках, таких как клетки рака молочной железы, рака яичника, рака легкого, рака шейки матки, рака почки, рака мочевого пузыря и рака печени. Экспрессия мРНК (матричная РНК) B7-H4 была обнаружена в селезенке, легком, тимусе, печени, скелетной мышце, почке, поджелудочной железе, яичке и яичнике. Низкий уровень экспрессии B7-H4 на уровне белка обнаруживали в тканях, таких как молочная железа (катетерная или дольковая), эпителий маточных труб и железа эндометрия. Связанные с этим исследования также показали, что B7-H4 сверхэкспрессируется в макрофагах, ассоциированных с опухолью (TAM - tumor-associated macrophage) (Kryczek, I. et al., J. Exp. Med. 2006, 203(4): 871-881), наряду с тем, что макрофаги являются важным компонентом микроокружения опухоли и могут обуславливать вплоть до 50 % массы опухоли.
В настоящее время многочисленные национальные фармацевтические компании занимаются разработкой моноклональных антител против B7-H4 и/или их лекарственных средств-конъюгатов для улучшения собственного иммунного ответа пациента на опухоли и достижения непосредственного уничтожения опухолевых клеток. Родственные патенты представляют собой, например, WO2013025779, US20140322129 и тому подобное. Моноклональные антитела к B7-H4, имеющиеся у компаний, таких как Medimmune и FivePrime, в настоящее время находятся на доклинической фазе; конъюгаты антитело против B7-H4 - лекарственное средство Genentech также находятся на доклинической фазе разработки.
Согласно настоящему изобретению предложены антитела против B7-H4 с высокой аффинностью, высокой селективностью и высокой биологической активностью, для применения в иммунотерапии на основе моноклональных антител в отношении опухолей и связанные с ними применения. Также предложены лекарственные средства, композиции и способы лечения B7-H4-позитивных опухолей.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, содержащее:
вариабельную область легкой цепи антитела, содержащую по меньшей мере одну LCDR (определяющая комплементарность область легкой цепи), выбранную из группы, состоящей из:
SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8;
SEQ ID NO: 14, SEQ ID NO: 15, SEQ ID NO: 16;
SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 24;
SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32;
SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40;
SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 48;
SEQ ID NO: 54, SEQ ID NO: 55, SEQ ID NO: 56;
SEQ ID NO: 62, SEQ ID NO: 63, SEQ ID NO: 64;
SEQ ID NO: 70, SEQ ID NO: 71, SEQ ID NO: 72; и
вариабельную область тяжелой цепи антитела, содержащую по меньшей мере одну HCDR (определяющая комплементарность область тяжелой цепи, выбранную из группы, состоящей из:
SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5;
SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13;
SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21;
SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO:29;
SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37;
SEQ ID NO: 43, SEQ ID NO: 44, SEQ ID NO: 45;
SEQ ID NO: 51, SEQ ID NO: 52, SEQ ID NO: 53;
SEQ ID NO: 59, SEQ ID NO: 60, SEQ ID NO: 61;
SEQ ID NO: 67, SEQ ID NO: 68, SEQ ID NO: 69;
SEQ ID NO: 73, SEQ ID NO: 74.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где вариабельная область тяжелой цепи указанного антитела содержит:
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 3, SEQ ID NO: 4 и SEQ ID NO: 5, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 11, SEQ ID NO: 12 и SEQ ID NO: 13, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 19, SEQ ID NO: 20 и SEQ ID NO: 21, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 27, SEQ ID NO: 28 и SEQ ID NO: 29, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 35, SEQ ID NO: 36 и SEQ ID NO: 37, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 43, SEQ ID NO: 44 и SEQ ID NO: 45, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 51, SEQ ID NO: 52 и SEQ ID NO: 53, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61, соответственно;
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 67, SEQ ID NO: 68 и SEQ ID NO: 69, соответственно; или
HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 73, SEQ ID NO: 74 и SEQ ID NO: 21, соответственно.
В предпочтительном воплощении изобретения предложено антитело против B7-H4 или его антигенсвязывающий фрагмент, где вариабельная область легкой цепи указанного антитела содержит:
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно;
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, соответственно;
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 22, SEQ ID NO: 23 и SEQ ID NO: 24, соответственно;
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 30, SEQ ID NO: 31 и SEQ ID NO: 32, соответственно;
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 38, SEQ ID NO: 39 и SEQ ID NO: 40, соответственно;
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 46, SEQ ID NO: 47 и SEQ ID NO: 48, соответственно;
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 54, SEQ ID NO: 55 и SEQ ID NO: 56, соответственно;
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 62, SEQ ID NO: 63 и SEQ ID NO: 64, соответственно; или
LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 70, SEQ ID NO: 71 и SEQ ID NO: 72, соответственно.
Особенно предпочтительное антитело к B7-H4 или его антигенсвязывающий фрагмент может представлять собой любое антитело или его фрагмент, выбранное из группы, состоящей из нижеследующего, содержащее одну или более из следующих последовательностей CDR областей или последовательностей, демонстрирующих по меньшей мере 95%-ную идентичность с этими последовательностями:
(1) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO:3, SEQ ID NO:4 и SEQ ID NO:5, соответственно;
(2) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 11, SEQ ID NO: 12 и SEQ ID NO: 13, соответственно;
(3) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 22, SEQ ID NO: 23 и SEQ ID NO: 24, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 19, SEQ ID NO: 20 и SEQ ID NO:21, соответственно;
(4) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 30, SEQ ID NO: 31 и SEQ ID NO: 32, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 27, SEQ ID NO: 28 и SEQ ID NO: 29, соответственно;
(5) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 38, SEQ ID NO: 39 и SEQ ID NO: 40, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 35, SEQ ID NO: 36 и SEQ ID NO: 37, соответственно;
(6) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 46, SEQ ID NO: 47 и SEQ ID NO: 48, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 43, SEQ ID NO: 44 и SEQ ID NO: 45, соответственно;
(7) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 54, SEQ ID NO: 55 и SEQ ID NO: 56, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 51, SEQ ID NO: 52 и SEQ ID NO: 53, соответственно;
(8) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 62, SEQ ID NO: 63 и SEQ ID NO: 64, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61, соответственно;
(9) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 70, SEQ ID NO: 71 и SEQ ID NO: 72, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 67, SEQ ID NO: 68 и SEQ ID NO: 69, соответственно; и
(10) вариабельная область легкой цепи антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 22, SEQ ID NO: 23 и SEQ ID NO: 24, соответственно; и вариабельная область тяжелой цепи антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 73, SEQ ID NO: 74 и SEQ ID NO: 21, соответственно.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где данное антитело или его антигенсвязывающий фрагмент представляет собой мышиное антитело или его фрагмент.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, где данное антитело или его антигенсвязывающий фрагмент представляет собой химерное антитело или его фрагмент.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где данное антитело или его антигенсвязывающий фрагмент представляет собой человеческое антитело или его фрагмент.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где данное антитело или его антигенсвязывающий фрагмент представляет собой гуманизированное антитело или его фрагмент.
В предпочтительном воплощении изобретения предложено антитело против B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где вариабельная область легкой цепи гуманизированного антитела представляет собой вариабельную область легкой цепи, содержащую последовательность(и), выбранную(ые) из группы, состоящей из SEQ ID NO: 76, SEQ ID NO: 78, SEQ ID NO: 80 или SEQ ID NO: 82.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где вариабельная область тяжелой цепи гуманизированного антитела представляет собой вариабельную область тяжелой цепи, содержащую последовательность(и), выбранную(ые) из группы, состоящей из SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79 или SEQ ID NO: 81.
В предпочтительном воплощении изобретения предложено антитело против B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где вариабельная область тяжелой цепи гуманизированного антитела дополнительно содержит FR (framework region- каркасная область) область(и) тяжелой цепи человеческого IgG1, IgG2, IgG3 или IgG4 или ее вариант, предпочтительно содержит FR область(и) тяжелой цепи человеческого IgG1, IgG2 или IgG4; более предпочтительно содержит FR область(и) тяжелой цепи IgG1, которые подвергались аминокислотной мутации для усиления ADCC (antibody-dependent cellular cytotoxicity - антителозависимая клеточная цитотоксичность) токсичности.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где легкая цепь гуманизированного антитела представляет собой легкую цепь, содержащую последовательность, выбранную из группы, состоящей из SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 88 или SEQ ID NO: 90.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где тяжелая цепь гуманизированного антитела представляет собой тяжелую цепь, содержащую последовательность, выбранную из группы, состоящей из SEQ ID NO: 83, SEQ ID NO:85, SEQ ID NO: 87 или SEQ ID NO: 89.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где вариабельная область легкой цепи гуманизированного антитела представляет собой вариабельную область легкой цепи, содержащую последовательность, выбранную из группы, состоящей из SEQ ID NO: 76 или SEQ ID NO: 80.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где вариабельная область тяжелой цепи гуманизированного антитела представляет собой вариабельную область тяжелой цепи, содержащую последовательность, выбранную из группы, состоящей из SEQ ID NO: 75 или SEQ ID NO: 79.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где легкая цепь гуманизированного антитела содержит последовательность, выбранную из группы, состоящей из SEQ ID NO: 84 или SEQ ID NO: 88.
В предпочтительном воплощении изобретения предложено антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где тяжелая цепь гуманизированного антитела содержит последовательность, выбранную из группы, состоящей из SEQ ID NO: 83 или SEQ ID NO: 87.
В более предпочтительном воплощении изобретения гуманизированное антитело выбрано из любых следующих антител, содержащих:
(1) вариабельную область легкой цепи SEQ ID NO: 76 и вариабельную область тяжелой цепи SEQ ID NO: 75;
(2) вариабельную область легкой цепи SEQ ID NO: 78 и вариабельную область тяжелой цепи SEQ ID NO: 77;
(3) вариабельную область легкой цепи SEQ ID NO: 80 и вариабельную область тяжелой цепи SEQ ID NO: 79 или
(4) вариабельную область легкой цепи SEQ ID NO: 82 и вариабельную область тяжелой цепи SEQ ID NO: 81.
В еще одном предпочтительном воплощении изобретения гуманизированное антитело выбрано из любого из следующих антител, содержащих:
(1) легкую цепь SEQ ID NO: 84 и тяжелую цепь SEQ ID NO: 83;
(2) легкую цепь SEQ ID NO: 86 и тяжелую цепь SEQ ID NO: 85;
(3) легкую цепь SEQ ID NO: 88 и тяжелую цепь SEQ ID NO: 87 или
(4) легкую цепь SEQ ID NO: 90 и тяжелую цепь SEQ ID NO:89.
Антитело к B7-H4 или его антигенсвязывающий фрагмент, имеющее по меньшей мере одну из следующих характеристик: (1) связывание с эпитопом B7-H4, содержащим аминокислоты 41-60 в SEQ ID NO: 100; и (2) связывание с эпитопом B7-H4, содержащим аминокислоты 53-59 в SEQ ID NO: 100.
Антитело к B7-H4 или его антигенсвязывающий фрагмент, имеющее по меньшей мере одну из следующих характеристик: (1) связывание с эпитопом B7-H4, содержащим аминокислоту 53 в SEQ ID NO: 100; (2) связывание с эпитопом B7-H4, содержащим аминокислоту 54 в SEQ ID NO: 100; (3) связывание с эпитопом B7-H4, содержащим аминокислоту 56 в SEQ ID NO: 100; (4) связывание с эпитопом B7-H4, содержащим аминокислоту 57 в SEQ ID NO: 100; (5) связывание с эпитопом B7-H4, содержащим аминокислоту 58 в SEQ ID NO: 100; и (2) связывание с эпитопом B7-H4, содержащим аминокислоту 59 в SEQ ID NO: 100.
В предпочтительном воплощении изобретения предложено антитело против B7-H4 или его антигенсвязывающий фрагмент, как описано выше, где антигенсвязывающий фрагмент представляет собой Fab, Fv, sFv, F(ab')2, линейное антитело, одноцепочечное антитело, нанотело, доменное антитело или мультиспецифичное антитело.
Настоящее изобретение дополнительно предлагает последовательность ДНК, кодирующая антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше.
Настоящее изобретение дополнительно предлагает экспрессионный вектор, содержащий последовательность ДНК, как описано выше.
Изобретению дополнительно предлагает клетку-хозяина, в которую вводят или которая содержит экспрессионный вектор, как указано выше.
В предпочтительном воплощении изобретения клетка-хозяин, как описано выше, характеризуется тем, что клетка-хозяин представляет собой бактерию, предпочтительно Escherichia coli.
В предпочтительном воплощении изобретения клетка-хозяин, как описано выше, представляет собой дрожжи, предпочтительно Pichia pastoris.
В предпочтительном воплощении изобретения клетка-хозяин, как описано выше, представляет собой клетку млекопитающего, предпочтительно клетку яичника китайского хомяка (CHO - Chinese Hamster Ovary) или клетку эмбриональной почки человека (HEK - human embryonic kidney) 293.
Изобретению также предлагает способ получения антитела к B7-H4, включающий культивирование клетки-хозяина, как описано выше, выделение антитела из культуры и очистку данного антитела.
Изобретению также предлагает мультиспецифичное антитело, содержащее вариабельную область легкой цепи и вариабельную область тяжелой цепи, как описано выше.
Изобретению также предлагает одноцепочечное антитело, содержащее вариабельную область легкой цепи и вариабельную область тяжелой цепи, как описано выше.
Изобретению также предлагает реагент для выявления или диагностическое средство, содержащее антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше.
Настоящее изобретение также предлагает способ иммунодетекции или определения B7-H4, который включает использование антитела против B7-H4 или его антигенсвязывающего фрагмента по настоящему изобретению.
Настоящее изобретение также предлагает способ диагностирования заболеваний, ассоциированных с B7-H4 позитивными клетками, который включает выявление или измерение уровня B7-H4 или B7-H4 позитивных клеток посредством использования антитела к B7-H4 или его антигенсвязывающего фрагмента согласно настоящему изобретению.
Изобретение дополнительно предлагает фармацевтическую композицию, содержащую антитело к B7-H4 или его антигенсвязывающий фрагмент, как описано выше, и фармацевтически приемлемый эксципиент, разбавитель или носитель.
Настоящее изобретение дополнительно предлагает применение антитела к B7-H4 или его антигенсвязывающего фрагмента, как описано выше, в изготовлении лекарственного средства для лечения B7-H4-опосредованного заболевания или состояния; где заболевания предпочтительно представляет собой рак; предпочтительно, заболевание представляет собой рак с экспрессией B7-H4; рак наиболее предпочтительно выбран из группы, состоящей из рака молочной железы, рака яичника, рака предстательной железы, рака поджелудочной железы, рака почки, рака легкого, рака печени, рака желудка, рака толстой кишки, рака мочевого пузыря, рака пищевода, рака шейки матки, рака желчного пузыря, глиобластомы и меланомы.
Настоящее изобретение дополнительно предлагает способ лечения и предупреждения B7-H4-опосредованных заболеваний или состояний, включающий введение субъекту, нуждающемуся в этом, терапевтически эффективного количества антитела к B7-H4 или его антигенсвязывающего фрагмента или фармацевтической композиции, содержащей вышеуказанное, где заболевание предпочтительно представляет собой рак; предпочтительно заболевание представляет собой рак с экспрессией B7-H4; рак наиболее предпочтительно выбран из группы, состоящей из рака молочной железы, рака яичника, рака предстательной железы, рака поджелудочной железы, рака почки, рака легкого, рака печени, рака желудка, рака толстой кишки, рака мочевого пузыря, рака пищевода, рака желчного пузыря, рака шейки матки, глиобластомы и меланомы.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1: ELISA (enzyme-linked immunosorbent assay - твердофазный иммуноферментный анализ) анализ связывания in vitro антител, показывающий, что все семь химерных антител обладают активностью связывания с очищенным человеческим антигеном B7-H4, где химерные антитела 2F7 и 2F8 имеют EC50 (полумаксимальная эффективная концентрация) примерно 0,1 нМ.
Фиг. 2: Непрямые ELISA анализы связывания, демонстрирующие антигенный эпитоп, с которым связывается антитело против B7-H4 hu2F7.
Фиг. 3: Фармакологический анализ у мышей, демонстрирующий противоопухолевое действие антитела против B7-H4 hu1C9.
Фиг. 4: Тест иммунной функции, демонстрирующий действие антител к B7-H4 hu1C9 и hu2G6 в усилении иммунитета (пролиферация T-клеток).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
1. Терминология
Для более легкого понимания изобретения некоторые технические и научные термины конкретно определены ниже. Если где-либо в данном документе конкретно не указано иное, все другие технические и научные термины, используемые в данном документе, имеют значение, обычно подразумеваемое одним из рядовых специалистов в данной области, к которой принадлежит данное изобретение.
В том виде, в котором он используется в данном документе, однобуквенный код и трехбуквенный код для аминокислот представляет собой такой, как описано в J. Biol. Chem, 243, p 3558 (1968).
В том виде, в котором он используется в данном документе, термин «антитело» относится к иммуноглобулину, структуре четырех пептидных цепей, образованной посредством соединенных вместе двух идентичных тяжелых цепей и двух идентичных легких цепей межцепочечной(ыми) дисульфидной(ыми) связью(ями). Разные константные области тяжелой цепи иммуноглобулина демонстрируют разные аминокислотные составы и последовательности, представляя, вследствие этого, разную антигенность. Соответственно, иммуноглобулины могут быть подразделены на пять категорий или так называемых изотипов иммуноглобулинов, а именно IgM, IgD, IgG, IgA и IgE, их тяжелые цепи представляют собой цепь μ, цепь δ, цепь γ, цепь α и цепь ε, соответственно. В соответствии со своим аминокислотным составом шарнирной области и числом и локализацией дисульфидных связей тяжелой цепи, один и тот же тип Ig может быть подразделен на разные подкатегории, например, IgG может быть подразделен на IgG1, IgG2, IgG3 и IgG4. Легкая цепь может быть подраздела на цепь κ или λ, в соответствии с разными константными областями. Каждый из пяти Ig может иметь цепь κ или λ.
В настоящем изобретении вариабельная область легкой цепи антитела, описанная в данном документе, дополнительно содержит константную область легкой цепи, которая содержит цепь κ, λ человека или мыши или ее вариант.
В настоящем изобретении вариабельная область тяжелой цепи антитела, описанная в данном документе, дополнительно содержит константную область тяжелой цепи, которая содержит IgG1, 2, 3, 4 человека или мыши или ее вариант.
Последовательности из примерно 110 аминокислот, расположенные рядом с N-концом тяжелых цепей и легких цепей антитела, сильно меняются, данная область известна как вариабельная область (область V); остальная часть аминокислотной последовательности рядом с C-концом является относительно стабильной, известная как константная область (C область). Вариабельная область содержит три гипервариабельные области (HVR - hypervariable region) и четыре каркасные области (FR - framework region), имеющие относительно консервативную последовательность. Три гипервариабельные области определяют специфичность антитела, также известные как определяющая комплементарность область (CDR). Каждая вариабельная область легкой цепи (LCVR - light chain variable region) и каждая вариабельная область тяжелой цепи (HCVR - heavy chain variable region) состоят из трех CDR и четырех FR, причем порядок от N-конца до С-конца является следующим: FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Три CDR легкой цепи относятся к LCDR1, LCDR2 и LCDR3; три CDR тяжелой цепи относятся к HCDR1, HCDR2 и HCDR3. Число и положение аминокислотных остатков CDR в VL и VH антитела или антигенсвязывающего фрагмента в данном документе соответствуют известным критериям нумерации Kabat и критериям определения Kabat или AbM (http://bioinf.org.uk/abs/).
Термин «антигенпрезентирующая клетка» или «АПК» представляет собой клетку, которая экспонирует на своей поверхности чужеродные антигены в комплексе с MHC (major histocompatibility complex - главный комплекс гистосовместимости). T-клетки распознают такой комплекс посредством T-клеточных рецепторов (TCR - T cell receptor). Примеры АПК включают дендритные клетки (DC -dendritic cell), мононуклеарные клетки периферической крови (PBMC - peripheral blood mononuclear cell), моноциты, B-лимфобласты и дендритные клетки моноцитарного происхождения (DC), но не ограничиваются ими. Термин «презентация антигена» относится к процессу, во время которого АПК захватывают антигены и делают возможным их распознавание T-клетками, например, в виде компонента конъюгатов MHC-I/MHC-II.
Термин «B7-H4» относится к члену семейства белков B7 человека, также известному как CD276, который представляет собой трансмембранный белок типа I, имеющий четыре Ig-подобных внеклеточных домена. B7-H4 является одним из белков иммунной контрольной точки, экспрессируемых на поверхности антигенпрезентирующих клеток или раковых клеток, и он оказывает ингибирующее действие активацию T-клеток. Термин «B7-H4» включает любой вариант или изоформу B7-H4, экспрессируемую клетками в природе. Антитела по настоящему изобретению могут вступать в перекрестную реакцию с B7-H4, полученными из видов, не являющихся человеком. В качестве альтернативы, антитела могут быть специфичными в отношении человеческого B7-H4 и могут не демонстрировать перекрестной реактивности с другими видами. B7-H4 или любой его вариант или изотип может быть выделен из клеток или тканей, в которых они экспрессируются в природе, или получен посредством методов генной инженерии с использованием методик, обычно используемых в данной области, и методик, описанных в данном документе. Предпочтительно, антитела против B7-H4 нацелены на человеческий B7-H4 с нормальным профилем гликозилирования.
Термин «рекомбинантное человеческое антитело» включает человеческие антитела, получаемые, экспрессируемые, создаваемые или выделяемые посредством методов генной инженерии, и данные используемые методики и способы хорошо известны в данной области, такие как: (1) антитело, выделенное из животного (например, мыши), трансгенного или трансхромосомного в отношении человеческого гена иммуноглобулина, или полученной гибридомы; (2) антитело, выделенное из трансформированных клеток-хозяев, экспрессирующих данное антитело, таких как трансфектома; (3) антитело, выделенное из комбинаторной библиотеки рекомбинантных человеческих антител; и (4) антитело, полученное, экспрессируемое, созданное или выделенное в результате сплайсинга последовательностей генов человеческого иммуноглобулина на других ДНК-последовательностях или т. п. Такое рекомбинантное человеческое антитело содержит вариабельную область и константную область в результате включения конкретных последовательностей иммуноглобулина зародышевой линии человека, кодируемых генами зародышевой линии, а также последующих перестроек и мутаций, таких как перестройки и мутации, происходящие во время созревания антитела.
Термин «мышиное антитело» в настоящем изобретении относится к моноклональному антителу к человеческому B7-H4, полученному в соответствии со знанием и умениями в данной области. Во время получения объекту испытания инъецируют антиген B7-H4, и затем выделяют гибридому, экспрессирующую антитело, которое имеет желаемую последовательность или функциональные характеристики. В предпочтительном воплощении настоящего изобретения мышиное антитело к B7-H4 или его антигенсвязывающий фрагмент дополнительно сдержит константную область легкой цепи мышиной цепи κ, λ или ее вариант, или дополнительно содержит константную область тяжелой цепи мышиного IgG1, IgG2, IgG3 или IgG4 или ее вариант.
Термин «человеческое антитело» включает антитела, имеющие вариабельные и константные области из последовательностей иммуноглобулина зародышевой линии человека. Человеческие антитела по настоящему изобретению могут включать аминокислотные остатки, которые не кодируются последовательностями иммуноглобулина зародышевой линии человека (например, мутации, вводимые посредством случайного или сайт-направленного мутагенеза in vitro или посредством соматической мутации in vivo). Однако, термин «человеческое антитело» не включает антитело, в котором последовательности CDR, происходящие из зародышевой линии млекопитающего другого вида, такой как зародышевая линия мыши, были привиты на последовательность каркасной области человека (то есть «гуманизированное антитело»).
Термин «гуманизированное антитело», также известное как антитело с привитыми CDR, относится к антителу, созданному посредством прививания мышиных последовательностей CDR в каркас вариабельной области человеческого антитела. Гуманизированные антитела преодолевают нежелательный сильный гуморальный ответ, вызываемый химерными антителами, которые несут большое количество мышиных белковых компонентов. Для того, чтобы избежать снижения активности, вызванного сниженной иммуногенностью, вариабельная область человеческого антитела может подвергаться минимальной обратной мутации с сохранением активности.
Термин «химерное антитело» представляет собой антитело, которое образовано слиянием вариабельной области мышиного антитела с константной областью человеческого антитела, и химерное антитело может облегчить иммунный ответ, вызываемый мышиным антителом. Для создания химерного антитела сначала создают гибридому, секретирующую специфичное мышиное моноклональное антитело, ген вариабельной области клонируют из клеток гибридомы мыши, затем ген константной области человеческого антитела клонируют при желании, ген вариабельной области мыши лигируют с геном константной области человека с образованием химерного гена, который затем может быть вставлен в человеческий вектор, и, наконец, молекула химерного антитела экспрессируется в эукариотической или прокариотической промышленной системе. Константная область человеческого антитела выбрана из константной области тяжелой цепи человеческого IgG1, IgG2, IgG3 или IgG4, или ее варианта, предпочтительно представляет собой константную область тяжелой цепи человеческого IgG2 или IgG4, или константную область тяжелой цепи IgG1, которая демонстрирует повышенную ADCC (антителозависимую клеточную цитотоксичность) из-за аминокислотной мутации.
Термин «антигенсвязывающий фрагмент» относится к антигенсвязывающим фрагментам антитела или аналогов антитела, которые обычно включают по меньшей мере часть антигенсвязывающей области или вариабельной области (например, одной или более CDR) исходного антитела. Фрагменты антитела сохраняют по меньшей мере некоторую специфичность связывания исходного антитела. Обычно, когда активность выражена в молях, фрагменты антитела сохраняют по меньшей мере 10%-ную активность связывания исходного антитела. Предпочтительно, фрагменты антитела сохраняют по меньшей мере 20%-ную, 50%-ную, 70%-ную, 80%-ную, 90%-ную, 95%-ную или 100%-ную или более высокую аффинность связывания исходного антитела в отношении мишени. Примеры антигенсвязывающих фрагментов включают Fab, Fab', F(ab')2, Fv фрагменты, линейные антитела, одноцепочечные антитела, нанотела, доменные антитела и мультиспецифичные антитела, но не ограничиваются ими. Сконструированные варианты антител рассмотрены в Holliger and Hudson (2005) Nat. Biotechnol. 23: 1126-1136.
«Fab-фрагмент» состоит из CH1 и вариабельных областей легкой цепи и тяжелой цепи. Тяжелая цепь молекулы Fab не может образовывать дисульфидную связь с другой тяжелой цепью молекулы.
«Fc» область содержит два фрагмента тяжелой цепи, содержащих домены CH1 и CH2 антитела. Данные два фрагмента тяжелой цепи удерживаются вместе за счет двух или более дисульфидных связей и гидрофобного взаимодействия CH3 домена.
«Fab' фрагмент» содержит легкую цепь и часть тяжелой цепи, содержащую домен VH, домен CH1 и область между доменами CH1 и CH2, и, вследствие этого, F(ab')2-молекула может быть образована двумя тяжелыми цепями двух Fab'-фрагментов, связанных посредством межцепочечных дисульфидных связей.
«F(ab')2 фрагмент» содержит две легкие цепи и часть тяжелых цепей, содержащие константную область между доменами CH1 и CH2, вследствие этого, межцепочечные дисульфидные связи образуются между двумя тяжелыми цепями. Таким образом, F(ab')2-фрагмент состоит из двух Fab'-фрагментов, удерживаемых вместе посредством дисульфидных связей между двумя тяжелыми цепями.
«Fv область» содержит вариабельные области от обеих тяжелой и легкой цепей, но без константных областей.
Термин «мультиспецифичное антитело» используется в своем самом широком смысле и охватывает антитела с мультиэпитопной специфичностью. Данные мультиспецифичные антитела включают, но не ограничиваются антителами, содержащими вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), где VH-VL единица обладает мультиэпитопной специфичностью; антителами, содержащими две или более областей VL и VH, где каждая VH-VL единица связывается с разными мишенями или с разными эпитопами одной и той же мишени; антителами, содержащими две или более одиночных вариабельных областей, где каждая отдельная вариабельная область связывается с разными мишенями или с разными эпитопами одной и той же мишени; полноразмерными антителами; фрагментами антитела; диателами; биспецифичными диателами и триателами, фрагментами антитела, которые были ковалентно или нековалентно связаны вместе.
Термин «одноцепочечное антитело» представляет собой одноцепочечный рекомбинантный белок, состоящий из вариабельной области тяжелой цепи антитела (VH) и вариабельной области легкой цепи антитела (VL), соединенных пептидным линкером, и одноцепочечное антитело представляет собой наименьший фрагмент антитела с интактными антигенсвязывающими сайтами.
Термин «фрагмент доменного антитела» представляет собой фрагмент иммуноглобулина, обладающий иммунологическими функциями, и он содержат только вариабельную область тяжелой цепи или вариабельную область легкой цепи. В некоторых случаях две или более VH областей ковалентно связаны с пептидным линкером с образованием бивалентного фрагмента доменного антитела. Данные две VH области бивалентного фрагмента доменного антитела могут нацеливаться на одни и те же или разные антигены.
Термин «связывание с B7-H4» относится к взаимодействию с человеческим B7-H4. Термин «антигенсвязывающий сайт», в том виде, в котором он используется в данном документе, относится к дискретным трехмерным сайтам на антигене, распознаваемым антителом или его антигенсвязывающим фрагментом по настоящей заявке.
Термин «эпитоп» относится к сайтам на антигене, которые специфично связываются с иммуноглобулином или антителом. Эпитоп может быть образован смежными аминокислотами или несмежными аминокислотами, а приведен к закрытому состоянию благодаря третичной укладки белка. Эпитоп, образованный смежными аминокислотами, обычно сохраняется после воздействия денатурирующих растворителей, тогда как эпитоп, образованный третичной укладкой, обычно утрачивается после обработки денатурирующими растворителями. Эпитопы обычно включают по меньшей мере 3-15 аминокислот в единственной пространственной конформации. Способы определения того, что эпитоп связан данным антителом, хорошо известны в данной области, включая анализы иммуноблоттинг и иммунопреципитация и т. п. Способы определения пространственной конформации эпитопа включают методики в данной области и методики, описанные в данной области, такие как рентгеноструктурный анализ и двумерный ядерный магнитный резонанс.
Термин «специфично связывается с», «селективно связывается с» в том виде, в котором он используется в данном документе, относится к связыванию антитела с эпитопом на заданном антигене. Обычно, когда рекомбинантный человеческий B7-H4 используется в качестве аналита, и антитело используется в качестве лиганда, антитело связывается с заданным антигеном с константой равновесия диссоциации (KD) приблизительно меньше чем 10-7 M или даже меньше, и аффинность антитела в отношении связывания с заданным антигеном по меньшей мере в два раза выше чем в случае неспецифичных антигенов (отличных от заданного антигена или близкородственных антигенов) (как например, БСА (Бычий сывороточный альбумин)), как измерено на приборе посредством методик поверхностного плазмонного резонанса (SPR - surface plasmon resonance). Термин «антитело, которое распознает антиген» может использоваться в данном документе взаимозаменяемо с термином «специфично связывающее антитело».
Термин «перекрестная реакция» относится к способности антитела по настоящему изобретению связываться с B7-H4, происходящим из разных видов. Например, антитело по настоящему изобретению, которое связывается с человеческим B7-H4, может также связываться с B7-H4, происходящим из другого вида. Перекрестную реактивность измеряют посредством выявления специфичной реактивности с очищенным антигеном в анализах связывания (например, SPR и ELISA), или посредством выявления связывания или функционального взаимодействия с клетками, физиологически экспрессирующими B7-H4. Способы определения перекрестной реактивности включают стандартные анализы связывания, как описано в данном документе, такие как анализ поверхностный плазмонный резонанс (SPR) или проточная цитометрия.
Термины «ингибирование» или «блокада» используются взаимозаменяемо и охватывают как частичное, так и полное ингибирование/блокаду. Ингибирование/блокада лиганда предпочтительно снижает нормальный уровень связывания лиганда или изменяет тип лиганд-связывающей активности, по сравнению с лиганд-связывающей активностью в отсутствии ингибирования или блокады. Также предполагается, что ингибирование и блокада включают любое ощутимое уменьшение в аффинности связывания, где лиганд приводится в контакт с антителом к B7-H4, при сравнении с аффинностью связывания в отсутствии антитела к B7-H4.
Предполагается, что термин «ингибирование роста» (например, в контексте клеток) включает любое поддающееся измерению уменьшение в росте клеток.
Термины «вызывающий иммунный ответ» и «усиливающий иммунный ответ» используются взаимозаменяемо и относятся к иммунному ответу на стимуляцию конкретным антигеном (а именно, пассивному или адаптивному). В отношении индукции CDC (complement-dependent cytotoxicity - комплемент-зависимая цитотоксичность) или ADCC, термин «вызывающий» означает стимуляцию конкретного механизма для прямого уничтожения клеток.
В том виде, в котором он используется в данном документе, термин «ADCC», а именно антителозависимая клеточная цитотоксичность, относится к клеткам, экспрессирующим Fc-рецепторы, которые непосредственно уничтожают клетки-мишени, покрытые антителом, в результате распознавания Fc-сегмента антитела. ADCC эффекторная функция антитела может ослабляться или исключаться в результате модификации Fc-сегмента IgG. Модификация относится к мутации(ям) константной области тяжелой цепи антитела.
Способы получения и очистки антител и антигенсвязывающих фрагментов хорошо известны в данной области и могут быть найдены, например, в руководстве по лабораторным технологиям с антителами Колд-Спринг-Харбор, глава 5-8 и 15. Например, мыши могут быть иммунизированы человеческим B7-H4 или его фрагментами, и полученные антитела могут быть затем ренатурированы, очищены и секвенированы с использованием общепринятых способов, хорошо известных в данной области. Антигенсвязывающие фрагменты можно также получать общепринятыми способами. Антитело или антигенсвязывающий фрагмент по настоящему изобретению можно получить в результате введения одной или более человеческих каркасных областей (FR) в не являющиеся человеческими производные CDR, используя методы генной инженерии. Последовательности FR зародышевой линии человека могут быть получены из ImMunoGeneTics (IMGT), на веб-сайте http://imgt.cines.fr, или из The Immunoglobulin FactsBook, 2001ISBN012441351.
Сконструированное антитело или антигенсвязывающий фрагмент по настоящему изобретению может быть получено или очищено, используя традиционные способы. Например, последовательности кДНК, кодирующие соответствующие антитела, могут быть клонированы и рекомбинированы в экспрессионный вектор GS. Затем клетки CHO можно подвергать стабильной трансфекции рекомбинантным экспрессионным вектором иммуноглобулина. В качестве более рекомендованного способа, хорошо известного в данной области, экспрессионные системы млекопитающих могут приводить к гликозилированию антител, особенно на высоко консервативном N-конце в FC области. Стабильные клоны могут быть получены в результате экспрессии антитела, специфично связывающегося с человеческим антигеном. Позитивные клоны могут быть размножены в культуральной среде, не содержащей сыворотку, для получения антител в биореакторах. Культуральная среда, в которую антитело секретировалось, может быть очищена и собрана посредством общепринятых методик. Антитело может быть отфильтровано и концентрировано с применением стандартных методик. Растворимые смеси и агрегаты могут быть эффективно удалены стандартными методиками, такими как молекулярное сито или ионный обмен. Полученный продукт должен быть немедленно заморожен, например, при минус 70 °C, или может быть лиофилизирован.
Антитела по настоящему изобретению относятся к моноклональным антителам. Моноклональное антитело или mAb, в том виде, в котором оно используется в данном документе, относится к антителу, которое происходит из одиночного клона, включая эукариотический, прокариотический или фаговый одиночный клон, но, не ограничиваясь ими. Моноклональные антитела или их антигенсвязывающие фрагменты могут быть получены, например, посредством технологий на основе гибридомы, методов генной инженерии, технологий фагового дисплея, технологий синтеза (например, CDR-прививка) или других технологий, известных в данной области.
Термин «введение» и «обработка» при применении к животному, человеку, экспериментальному субъекту, клетке, ткани, органу или биологической жидкости, относится к приведению экзогенного фармацевтического, терапевтического, диагностического средства или композиции в контакт с животным, человеком, субъектом, клеткой, тканью, органом или биологической жидкостью. Термины «введение» и «обработка» могут относиться, например, к терапевтическим, фармакокинетическим, диагностическим, исследовательским и экспериментальным способам. Обработка клетки охватывает приведение реагента в контакт с клеткой, а также приведение реагента в контакт с жидкостью, где данная жидкость находится в контакте с клеткой. Термины «введение» и «обработка» также означают обработки in vitro и ex vivo, например клетки, реагентом, диагностическим средством, связывающей композицией или другой клеткой. Термин «лечение», при применении к субъекту-человеку, субъекту ветеринарии или исследования, относится к терапевтическому лечению, профилактическим или превентивным мерам, к исследовательским и диагностическим применениям.
Термин «лечить» означает вводить терапевтическое средство, такое как композиция, содержащая любое из связывающих соединений по настоящему изобретению, внутрь или наружно, пациенту, страдающему от одного или более симптомов заболевания, в отношении которого данное средство обладает известной терапевтической активностью. Типично терапевтическое средство вводят в количестве, эффективном для облегчения одного или более симптомов заболевания у пациента или популяции, подлежащих лечению, или вызывая регрессию симптома(ов) или ингибируя прогрессирование такого(их) симптома(ов) до какой-либо клинически измеряемой степени. Количество терапевтического средства, которое является эффективным для облегчения какого-либо определенного симптома заболевания (также называемое «терапевтически эффективным количеством»), может варьировать в зависимости от факторов, таких как течение заболевания, возраст и масса пациента, и способности средства вызывать желаемый ответ у пациента. Был ли облегчен симптом заболевания можно оценить посредством клинического измерения, обычно используемого лечащими врачами или другими квалифицированными медицинскими работниками, для оценки тяжести или статуса прогрессирования указанного симптома. В то время как воплощение (например, способ лечения или продукт производства) настоящего изобретения может не быть эффективным в облегчении исследуемого(ых) симптома(ов) заболевания у каждого пациента, оно должно облегчать исследуемый(е) симптом(ы) заболевания у статистически значимого числа пациентов, как определено любым статистическим критерием, известным в данной области, таким как t-критерий Стьюдента, критерий хи-квадрат, U-критерий Манна - Уитни, критерий Краскела - Уоллиса (H-критерий), критерий Джонкхира-Терпстры и критерий Уилкоксона.
Термин «по существу состоящий из» или его варианты, используемые на протяжении всего описания изобретения и формулы изобретения, означает включение всех элементов или групп элементов, и необязательно других элементов, демонстрирующих похожие свойства или даже свойство, отличное от свойства указанных элементов. Указанные другие элементы не значительно меняют существующее или новое свойство данной схемы дозирования, способа или композиции. В качестве неограничивающего примера, связывающее соединение, по существу состоящее из описанной аминокислотной последовательности, может также включать одну или более аминокислот, которые значимо не влияют на свойства связывающего соединения.
Термин «встречающийся в природе», при применении к объекту в настоящем изобретении, относится к тому факту, что данный объект может быть обнаружен в природе. Например, полипептидные последовательности или полинуклеотидные последовательности, которые существуют в организмах (включая вирусы) и не были искусственно модифицированы в лаборатории, встречаются в природе, где указанный организм может быть выделен из природных источников.
Термин «эффективное количество» охватывает количество, достаточное для смягчения или предупреждения симптома или признака медицинского состояния. Эффективное количество также означает количество, достаточное для обеспечения возможности или облегчения диагностирования. Эффективное количество для конкретного пациента или субъекта ветеринарии может варьировать в зависимости от факторов, таких как состояние, подлежащее лечению, общее здоровье пациента, путь и доза введения, и тяжесть побочных эффектов. Эффективное количество может представлять собой максимальную дозу или схему дозирования, которая позволяет избежать значимых побочных эффектов или токсичных действий.
Термин «экзогенный» относится к веществу, которое образуются вне организма, клетки или организма человека, в зависимости от контекста. Термин «эндогенный» относится к веществам, которые образуются в клетке, организме или теле человека, в зависимости от контекста.
Термин «гомология» относится к сходству последовательностей между двумя полинуклеотидными последовательностями или между двумя полипептидами. Когда положение в двух последовательностях, подлежащих сравнению, занято одной и той же мономерной субъединицей - основанием или аминокислотой - например, если положение в каждой из двух молекул ДНК занято аденином, тогда данные молекулы являются гомологичными в данном положении. Процент гомологии двух последовательностей является функцией, где число совпадающих или гомологичных положений, являющихся общими у двух последовательностей, разделено на число сравниваемых положений и затем умножено на 100. Например, при оптимальном выравнивании последовательностей, если 6 из 10 положений в двух последовательностях совпадают или являются гомологичными, тогда данные две последовательности считаются гомологичными на 60 %. В общем, сравнение осуществляют, когда получают максимальный процент гомологии при выравнивании двух последовательностей.
В том виде, в котором они используются в данном документе, выражения «клетка», «клеточная линия» и «клеточная культура» используются взаимозаменяемо, и все такие обозначения включают их потомство. Таким образом, слова «трансформанты» и «трансформированные клетки» включают первичную исследуемую клетку и полученные из нее культуры без учета числа пассажей. Также следует понимать, что все потомство не может быть с точностью идентичным по содержанию ДНК вследствие целенаправленных или случайных мутаций. Также учитывается потомство с мутациями, таким образом подвергавшееся скринингу, что демонстрирует такую же функцию или биологическую активность, как функция или биологическая активность исходно трансформированной клетки. Где подразумеваются отдельные обозначения, это будет очевидно из контекста.
Термин «необязательный» или «необязательно» означает, что событие или обстоятельство, которое следует, может происходить, но не обязательно происходит, и описание включает пример, в котором событие или ситуация будет происходить или не будет происходить. Например, фраза «необязятально содержащий 1-3 вариабельные области тяжелой цепи антитела» означает, что вариабельная область тяжелой цепи антитела, имеющая конкретную последовательность, может присутствовать, но не обязательно присутствует.
Термин «фармацевтическая композиция» относится к смеси, содержащей одно или более соединений согласно настоящему изобретению или его(их) физиологически/фармацевтически приемлемую соль или пролекарство вместе с другими химическими компонентами, а также дополнительными компонентами, такими как физиологически/фармацевтически приемлемые носители и эксципиенты. Целью фармацевтической композиции является содействие введению в организм и облегчение поглощения активного вещества, и оказание, таким образом, биологического действия.
Настоящее изобретение дополнительно описано ниже в данном документе со ссылкой на примеры; однако объем настоящего изобретения не ограничивается ими. В примерах настоящего изобретения, где не описаны конкретные условия, эксперименты обычно проводят в общепринятых условиях, как описано в руководстве по лабораторным технологиям с антителами, молекулярному клонированию, Колд-Спринг-Харбор (Antibodies A Laboratory Manual, Molecular Cloning, Cold Spring Harbor) или в условиях, предложенных производителями сырья или продуктов. Где источник реагентов конкретным образом не приведен, реагенты представляют собой имеющиеся в продаже традиционные реагенты.
Пример 1: Получение антигенов и конструирование стабильных клеточных линий
Последовательность, кодирующую человеческий B7-H4 с HisFlag-меткой (huB7-H4-HF), и последовательность, кодирующую человеческий B7-H4 с huFc-меткой (h-B7-H4-Fc), синтезировали посредством технологии интегрированной ДНК CRO (IDT - Integrated DNA Technology) (последовательность матрицы для каждого из приведенных выше рекомбинантных белков B7-H4 была сконструирована авторами изобретения), и клонировали в вектор pTT5 (Biovector),соответственно. Рекомбинантные белки B7-H4 экспрессировали в клетках 293T и очищали в соответствии с Примером 2.
Очищенные белки использовали в следующих примерах.
Последовательность huB7-H4-Fc:
FGISGRHSITVTTVASAGNIGEDGILSCTFEPDIKLSDIVIQWLKEGVLGLVHEFKEGKDELSEQDEMFRGRTAVFADQVIVGNASLRLKNVQLTDAGTYKCYIITSKGKGNANLEYKTGAFSMPEVNVDYNASSETLRCEAPRWFPQPTVVWASQVDQGANFSEVSNTSFELNSENVTMKVVSVLYNVTINNTYSCMIENDIAKATGDIKVTESEIKRRSHLQLLNSKAGSGGGGDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO: 99
Последовательность huB7-H4-his:
MASLGQILFWSIISIIIILAGAIALIIGFGISGRHSITVTTVASAGNIGEDGILSCTFEPDIKLSDIVIQWLKEGVLGLVHEFKEGKDELSEQDEMFRGRTAVFADQVIVGNASLRLKNVQLTDAGTYKCYIITSKGKGNANLEYKTGAFSMPEVNVDYNASSETLRCEAPRWFPQPTVVWASQVDQGANFSEVSNTSFELNSENVTMKVVSVLYNVTINNTYSCMIENDIAKATGDIKVTESEIKRRSHLQLLNSKADYKDDDDKGSHHHHHHHH
SEQ ID NO: 100
Стадии очистки для huB7-H4-his:
Образцы супернатанта, экспрессируемые клетками, центрифугировали с высокой скоростью для удаления примесей, подвергали замене буфера на PBS (phosphate buffered saline - фосфатно-солевой буферный раствор) и добавляли к ним имидазол до конечной концентрации 5 мМ. Никелевую колонку уравновешивали раствором PBS, содержащим 5мМ имидазол, и промывали 2-5 объемами колонки. После замены буфера образцы супернатанта наносили на колонку. Колонку промывали PBS, содержащим 5 мМ имидазол до тех пор, пока измеренное значение A280 не возвращалось к исходному уровню. Затем колонку промывали PBS плюс 10 мМ имидазол, удаляли неспецифично связанные белки-примеси и собирали элюат. Целевой белок элюировали PBS, содержащим 300 мМ имидазол, и собирали пик элюирования. Собранный элюат дополнительно очищали посредством ионного обмена (колонка SP). Маточный раствор A: 0,01 M PB, pH 8,0. Маточный раствор B: Раствор A плюс 1 M NaCl. Для элюирования целевого белка раствор PBS-имидазола заменяли Раствором A, и колонку SP уравновешивали раствором A. И затем образцы наносили на колонку. Затем колонку промывали раствором B в концентрационном градиенте от 0 до 100 % 10 объемами колонки, и собирали пик элюирования. Полученный белок идентифицировали как желательный белок посредством электрофореза и разделяли на аликвоты для применения. Получали человеческий B7-H4 с HisFlag-меткой (hu-B7-H4 his).
Стадии очистки для huB7-H4-Fc:
Образцы супернатанта, экспрессируемые клетками HEK293, центрифугировали с высокой скоростью для удаления примесей и подвергали замене буфера на PBS. Колонку с Белком A для аффинной хроматографии уравновешивали 10 мМ фосфатным буфером и промывали 2-5 объемами колонки. После замены буфера образцы супернатанта наносили на колонку. Колонку промывали буфером в количестве 25 объемов колонки до тех пор, пока измеренное значение A280 не возвращалось к исходному уровню. Целевой белок элюировали 0,8 % ацетатным буфером, pH 3,5, и собирали пик элюирования. В аликвоты сразу же добавляли буфер 1 M Tris-Cl, pH 8,0, для нейтрализации. И затем раствор заменяли PBS посредством колонки-фильтра Amico-15 Millipore. Полученный белок идентифицировали посредством электрофореза, пептидного картирования и ЖХ (жидкостная хроматография)-МС (масс-спектрометрия) и разделяли на аликвоты для применения.
Конструирование стабильного пула клеток CHO-S:
Полноразмерную последовательность, кодирующую белок B7-H4 человека или яванского макака (huB7-H4 или cyB7-H4), синтезировали посредством технологии интегрированной ДНК (IDT) (приведенные выше рекомбинантные белки B7-H3 конструировали авторы настоящего изобретения) и клонировали в сконструированный вектор pcDNA3.1, pcDNA3.1/puro (Invitrogen #V79020), соответственно. Клетки CHO-S (ATCC) культивировали в культуральной среде CD-CHO (Life Technologies, #10743029) до достижения 0,5×106/мл. 10 мкг вектора, кодирующего ген huB7H3 или cyB7H3, смешивали с 50 мкл LF-LTX (Life Technologies, #A12621) в 1 мл среды Opti-MEM (Life Technologies, #31985088), инкубировали при комнатной температуре в течение 20 минут, дополняли культуральной средой для клеток CHO и помещали в инкубатор с CO2 для культивации. После 24 часов среду заменяли свежей средой, и добавляли 10 мкг/мл пуромицина. После этого, культуральную среду меняли каждые 2-3 суток, и, спустя 10-12 суток, посредством осуществления скрининга получали стабильный пул клеток CHO-S.
Пример 2: Получение мышиных гибридом и последовательностей антител
Животных иммунизировали человеческим антигеном huB7-H4-Fc. Использовали пять мышей Balb/c и пять мышей A/J (самки, возраст 10 недель). Иммуноген и иммуноадъювант (Полный адъювант Фрейнда Sigma (CFA - Complete Freund's Adjuvant) или неполный адъювант Фрейнда Sigma (IFA - Incomplete Freund's Adjuvant)) тщательно смешивали в соотношении 1:1 и эмульгировали с получением стабильной жидкости «вода в масле»; Доза для инъекции составляла 25 мкг/200 мкл/мышь.
Титр сыворотки и способность к связыванию с антигенами клеточной поверхности оценивали с помощью сывороток от иммунизированных мышей посредством метода непрямого ELISA и ELISA с захватом, как описано в Примере 3. Слияние клеток инициировали, в зависимости от результатов анализа титра (более чем 100000-кратное разведение). Мышей с высоким титром сыворотки, аффинностью и сильным FACS (fluorescent-activated cell sorting - сортировка клеток с активированной флуоресценцией) связыванием подвергали конечной иммунизации и затем умерщвляли. Клетки селезенки и клетки миеломы SP2/0 сливали и высевали в планшет с получением гибридом, скрининг которых осуществляли посредством непрямого ELISA и ELISA с захватом с получением целевых гибридом. Моноклональные клеточные линии создавали посредством предельного разведения. Клетки CHO-S, стабильно экспрессирующие B7-H4, дополнительно трансфицировали полученными позитивными в отношении антител линиями. Пустые клетки CHO-S использовали в качестве контроля для исключения гибридомных линий неспецифичных связывающих антител. Восемь гибридомных линий, которые не только связываются с рекомбинантными белками, но также связываются с антигенами, которые экспрессируются клетками, получали посредством проточной сортировки. Гибридомные клетки собирали в логарифмическую фазу роста, РНК выделяли с помощью Тризола (Invitrogen, 15596-018) и осуществляли обратную транскрипцию (Обратная транскриптаза PrimeScript™, Takara #2680A). кДНК, полученные в результате обратной транскрипции, амплифицировали посредством ПЦР (полимеразная цепная реакция)-амплификации с использованием набора праймеров Mouse Ig-Primer Set (Novagen, TB326 Rev. B 0503) и секвенировали, и в конечном итоге получали последовательности 8 мышиных антител.
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 2F7 выглядят следующим образом:
HCVR 2F7
EVQLVESGGGLVQPGGSLKLSCAASGFTFSNYYMSWVRQTPEKRLEWVAYVSSGGGSTYYSDSVKGRFTISRDNAKNTLYLQMSSLKPEDTAMYYCTRESYSQGNYFDYWGQGTTLTVSS
SEQ ID NO: 1
LCVR 2F7
DIVMTQSPATLSVTPGDRVSLSCRASQSISDYLHWYQQKSHESPRLLIKFASQSISGIPSRFSGSGSGSDFTLSINSVEPEDVGVYYCQNGHSFSLTFGAGTKLELK
SEQ ID NO: 2
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей M1 выглядят следующим образом:
HCVR M1
EIQLQQSGPELVMPGASVKVSCTASGYPFTTYNMYWVKQSHGKSLEWIAYIDPYNGGTSYNQKFKGKATLTVDKSSSTAYMHLNSLTSEDSAVYYCARSGFYDGYYAWYFDVWGAGTTVTVSS
SEQ ID NO: 9
LCVR M1
DVVMTQTPLSLPVSLGDQASISCRSSQSLVHSGGNTYLHWYLQKPGQSPKLLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYFCSQSTHVPLTFGAGTKLELK
SEQ ID NO: 10
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 2F8 выглядят следующим образом:
HCVR 2F8
QVQLQQPGSVLVRPGASVKLSCKASGYTFTNSWMNWAKLRPGQGLEWIGGIYPNSGNIEYNEKFKGKATLTVDTSSSTAYMDLTSLTSEDSAVYYCARDSRFSYWGQGTLVTVSA
SEQ ID NO: 17
LCVR 2F8
DIVMTQSHKFMSTSVGDRVSITCKASQDVRTAVAWYQQKPGQSPKLLISSTSYRYTGVPDRFTGSGSGTDFTFIISSVQAEDLAVYYCQQHYSTPLTFGAGTKLELK
SEQ ID NO: 18
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 2F4 выглядят следующим образом:
HCVR 2F4
EVQLVESGGGLVKPGGSLKLSCAASGLTFSRYAMSWVRQTPEKRLEWVAGISSGGSYTYYSDTVKGRFTISRDNVRNTLYLQMSSLRSEDTAMYYCGREYGRDYWGQGTSVTVSS
SEQ ID NO: 25
LCVR 2F4
DILMTQSPSSMSVSLGDTVSITCHASQGINSNIGWLQQKPGKSFKGLIYHGTNLEDGVPSRFSGSGSGTDYSLTISSLESEDFADYYCVQYAQFPRTFGGGTTLEIK
SEQ ID NO: 26
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 2A10 выглядят следующим образом:
HCVR 2A10
EVQLVESGGGFVKPGGSLKLSCAASGFTFSTFGMSWVRQTPDKRLEWVAGISPGGSYTYYPDTVKGRFTISRDNARNTLYLQMSSLRSEDSAMYYCTRGRSVWGTGTTVTVSS
SEQ ID NO: 33
LCVR 2A10
DILMTQSPSSMSVSLGDTVSITCHASQDISSNIGWLQQKPGKSFKGLIYHGTTLEDGIPSRFSGSGSGADYSLTISSLESEDFADYYCVQSAQFPWTFGGGTKLEIK
SEQ ID NO: 34
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 2E4 выглядят следующим образом:
HCVR 2E4
QVQLQQPGSVLVRPGTSVKLSCKASGYTFTSSWMNWVKQRPGQGLEWIGGIYPNRGTTEYNEKFKGKATLTVDTSSSTAFMDLNRLTSEDSAVYYCARDSRFADWGQGTLVTVSA
SEQ ID NO: 41
LCVR 2E4
DIMLTQSHKFMSTSVGDRVSITCKASQDVSAAVAWYQQKPGQSPKLLISSASYRYTGVPDRFTGSGSGTDFTFTISSVQAEDLAVYYCQQHYNTPLTFGAGTKLELK
SEQ ID NO: 42
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 1E4 выглядят следующим образом:
HCVR 1E4
EVQLVESGGGLVKPGGSLKLSCAASGFTFSRYAMSWVRQTPEKRLEWVAGISSGGSYTYYPDTLKGRFTVSRDNARNTLYLQMSSLRSEDTAKYFCASQGSNHYFDYWGQGTTLTVSS
SEQ ID NO: 49
LCVR 1E4
DTLMTQSPSSMSVSLGDTVSITCHASQGIHNNIGWLQQKPGKSFKALIYHGTNLEDGVPSRFSGSGSGADYSLIISSLESEDFADYYCVQYAQFPYTFGGGTKLEIK
SEQ ID NO: 50
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 2G6 выглядят следующим образом:
HCVR 2G6
EVQLVESGGGLVKPGGSLKLSCAASGFTFSRYGMSWVRQTPEKRLEWVAGINGGGSYTYYLDTVKGRFTISRDNSRNTLYLQMSSLRSEDTAMYYCVSQGSNYYFDYWGQGTTLTVSS
SEQ ID NO: 57
LCVR 2G6
DIRMTQSPSSMSVSLGDTVSITCHASQGISSNIGWLQQKPGKSFKALIYHGTNLEDGVPSRFSGSGSGADYSLTISSLESEDFADYYCVQYAQFPYTFGGGTKLEIK
SEQ ID NO: 58
Содержатся следующие последовательности CDR:
Последовательности вариабельных областей тяжелой и легкой цепей мышиного mAb 1C9 выглядят следующим образом:
HCVR 1C9
QVQLQQPGSVLVRPGASVKLSCKASGDTFTTYWMNWVKQRPGQGLEWIGGIYLNSGSSEYNEKFKGKATLSVDTSSSTAYMDLSSLTSEDSAVYYCARDSRFSYWGQGTLVTVSA
SEQ ID NO: 65
LCVR 1C9
DIVMTQSHKFLSTSVGDRVSITCKASQDVSTAVAWYQQKPGQSPELLISSASYRYTGVPDRFTGSGSGTDFTFTISSVQAEDLAVYYCQQHYNTPLTFGAGTQLELK
SEQ ID NO: 66
Содержатся следующие последовательности CDR:
Вариабельные области тяжелой и легкой цепей каждого мышиного mAb клонировали в константную область тяжелой цепи человеческого IgG1 и константную область легкой цепи каппа, соответственно, и затем очищали, идентифицировали и тестировали на активность, как описано в Примере 4.
Пример 3: Выявление in vitro связывающей активности антител
(1) Непрямой анализ связывания ELISA in vitro:
Белок HuB7-H4 His (Sino Biological Inc., кат. № 10738-H08H) разводили до концентрации 1 мкг/мл с помощью PBS, pH 7,4, добавляли в 96-луночный планшет для микротитрования с высокой аффинностью в объеме 100 мкл/лунка и инкубировали при 4 °C в течение ночи (16-20 часов). Планшет промывали PBST (PBS, содержащий 0,05 % Tween-20, pH 7,4) четыре раза, и затем в него добавляли 150 мкл/лунка 3%-ого блокирующего раствора бычьего сывороточного альбумина (BSA), разбавленного в PBST, и инкубировали при комнатной температуре в течение 1 часа для блокирования. После окончания блокирования, блокирующий раствор отбрасывали, и планшет промывали 4 раза буфером PBST.
Антитела, подлежащие тестированию, разводили PBST, содержащим 3 % BSA, получая градиент 10-кратного разведения, начиная с 1 мкМ в общей сложности с 10 дозами. Разведения добавляли в планшет в количестве 100 мкл/лунка и инкубировали при комнатной температуре в течение 1 часа. После окончания инкубации планшет промывали 4 раза PBST, добавляли в него 100 мкл/лунка вторичного антитела козы к человеческому антителу, меченному HRP (horseradish peroxidase - пероксидаза хрена) (Abeam, кат. № ab97225), разведенного в PBST, содержащем 3 % BSA, и инкубировали при комнатной температуре в течение 1 часа. Планшет промывали 4 раза PBST, в него добавляли 100 мкл/лунка хромогенного субстрата TMB (tetramethylbenzidine - тетраметилбензидин) (Cell Signaling Technology, кат. № 7004S), инкубировали при комнатной температуре в темноте в течение 1 минуты и добавляли в него 100 мкл/лунка останавливающего раствора (Cell Signaling Technology, кат. № 7002S) для окончания реакции. Поглощение считывали при 450 нм с использованием микропланшет-ридера (BioTek, модель Synergy H1), и анализировали данные. Строили кривую зависимости концентрации от значения сигнала, и результаты анализировали, как показано в следующей таблице:
(2) Конкурентный анализ ELISA:
Белок HuB7-H4 His (Sino Biological Inc., кат. № 10738-H08H) разводили до концентрации 1 мкг/мл с помощью PBS, pH 7,4, добавляли в 96-луночный планшет для микротитрования с высокой аффинностью в объеме 100 мкл/лунка и инкубировали при 4°C в течение ночи (16-20 часов). Планшет промывали 4 раза PBST (PBS, содержащий 0,05% Tween-20, pH 7,4), в него добавляли 150 мкл/лунка 3%-ого блокирующего раствора бычьего сывороточного альбумина (BSA), разведенного в PBST, и инкубировали при комнатной температуре в течение 1 часа. После окончания блокирования блокирующий раствор отбрасывали, и планшет промывали 4 раза буфером PBST.
0,1 нМ эталонное химерное антитело получали с PBST, содержащим 3 % BSA, и использовали в качестве раствора для разведения мышиных антител, подлежащих тестированию, получая градиент 10-кратного разведения, начиная с 100 нМ в общей сложности с 10 дозами. Разведенные антитела добавляли в планшет в количестве 100 мкл/лунка и инкубировали в течение 1 часа при комнатной температуре. После окончания инкубации планшет промывали 4 раза PBST, и добавляли 100 мкл/лунка меченного HRP вторичного антитела козы против человеческого антитела (Abcam, кат.№ ab97225), разведенного в PBST, содержащем 3% BSA, и инкубировали в течение 1 часа при комнатной температуре. Планшет промывали 4 раза PBST, и затем добавляли 100 мкл/лунка хромогенного субстрата TMB (Cell Signaling Technology, кат. № 7004S), и инкубировали при комнатной температуре в течение 1 минуты в темноте. 100 мкл/лунка останавливающего раствора (Cell Signaling Technology, кат. № 7002S) добавляли для окончания реакции, и поглощение считывали при 450 нм с использованием микропланшет-ридера (BioTek, модель Synergy H1). Осуществляли анализ данных. Степень конкурентного ингибирования = ((поглощение в случае эталонного антитела - поглощение в случае конкурентного антитела)/поглощение в случае антитела Abv)*100.
(3) Анализ связывания ELISA с захватом in vitro:
Вторичное антитело козы r мышиному IgG (Jackson Immuno Research, кат. № 115-006-071) разводили до концентрации 2 мкг/мл буфером PBS, pH 7,4, добавляли в 96-луночный планшет для микротитрования в объеме 100 мкл/лунка и инкубировали в инкубаторе при 37 °C в течение 2 часов. Планшет промывали один раз PBST, добавляли в него блокирующий раствор, содержащий 5 % обезжиренного молока (Bright Dairy, Обезжиренное молоко в порошке), разведенного в PBST в количестве 200 мкл/лунка, и инкубировали при 37 °C в течение 2 часов или при 4 °C в течение ночи (16-18 часов) для блокирования. После окончания блокирования блокирующий раствор отбрасывали, и планшет промывали 4 раза PBST.
Мышиные сыворотки или очищенные рекомбинантные антитела, подлежащие тестированию, разводили до разных концентраций раствором для разведения образца, содержащим 5 % NHS (PBST с 2,5 % обезжиренным молоком), инкубировали в течение 40 минут при комнатной температуре, добавляли в планшет в количестве 100 мкл/лунка и инкубировали в инкубаторе в течение 40 минут при 37 °C. После окончания инкубации, планшет промывали 4 раза PBST, добавляли в него 100 мкл/лунка белкового раствора биотинилированного huB7-H4-his (Sino Biological #10738-H08H), разведенного в растворе для разведения образца, и инкубировали при 37 °C в течение 40 минут. После окончания инкубации планшет промывали 4 раза PBST, добавляли в него 100 мкл/лунка HRP-меченного стрептавидина (Jackson Immuno Research, кат. № 016-030-084), разведенного в PBST, и инкубировали при 37 °C в течение 40 минут. После 4-кратной промывки планшета PBST добавляли 100 мкл/лунка хромогенного субстрата TMB (InnoReagents Biotechnology Co., Ltd.), инкубировали при комнатной температуре в течение 10-15 мин в темноте, добавляли 50 мкл/лунка 1M H2SO4 для остановки реакции. Поглощение считывали при 450 нм с использованием микропланшет-ридера (Beijing Perlong New Technology Co., Ltd., модель DNM-9602), и осуществляли анализ данных.
(4) Анализ связывания с клеткой in vitro:
Культивируемые клетки SK-BR3 или клетки, стабильно трансфицированные CHO-huB7-H4, собирали и затем высевали в 96-луночный планшет с U-образным дном при плотности клеток 1×105 - 2×105 клеток на лунку. Супернатант удаляли посредством центрифугирования при 1200 g в течение 5 мин, добавляли 100 мкл серийно разведенных растворов антител или мышиных иммунных сывороток и инкубировали при 4°C в течение 60 мин, и удаляли супернатант посредством центрифугирования при 1200 g в течение 5 мин. Клетки дважды промывали PBS, добавляли к ним флуоресцентно меченое вторичное антитело (PE-GAM или PE-GAH) в количестве 100 мкл на лунку, инкубировали в течение 60 мин при 4 °C и центрифугировали при 1200 g в течение 5 мин для удаления супернатанта. Клетки дважды промывали PBS и затем ресуспендировали в PBS. Сигналы выявляли, используя проточный цитометр, и чертили кривую концентрации, и анализировали результаты.
Пример 4: Конструирование и экспрессия рекомбинантных химерных антител к B7-H4
Сайт-направленные аминокислотные мутации осуществляли в FR области(ях) (каркасные области) вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL) для каждого мышиного антитела по настоящему изобретению. Различные тяжелые и легкие цепи гуманизированных антител конструировали в соответствии с разными комбинациями аминокислотных мутаций. Клетки, трансфицированные плазмидами разных комбинаций тяжелой и легкой цепей, стали использовать для получения гуманизированных антител.
Вектор тяжелой цепи конструировали следующим образом: сигнальный пептид плюс мутантная последовательность вариабельной области тяжелой цепи плюс человеческая последовательность константной области IgG1.
Вектор легкой цепи конструировали следующим образом: сигнальный пептид плюс мутантная последовательность вариабельной области легкой цепи плюс человеческая последовательность константной области каппа.
Приведенные выше последовательности вставляли в вектор pCEP4, соответственно. Экспрессионные векторы синтезировали в соответствии с вышеприведенной конструкцией, полученные векторные плазмиды экстрагировали посредством набора для выделения maxi, и проверяли посредством секвенирования. Подтвержденными плазмидами трансфицировали клетки 293F человека с PEI (Polyethylenimine - полиэтиленимин) и непрерывно культивировали. Клетки 293F культивировали в среде, не содержащей сыворотку (Shanghai opmbiosciences, OPM-293CD03), до логарифмической фазы роста для трансфекции клеток. 21,4 мкг плазмиды с легкой цепью гуманизированного антитела и 23,6 мкг плазмиды с тяжелой цепью гуманизированного антитела растворяли в 10 мл среды восстановленной сыворотки Opti-MEM® I (GIBCO, 31985-070), хорошо перемешивали, затем к ним добавляли 200 мкг PEI, хорошо перемешивали, инкубировали в течение 15 мин при RT (комнатная температура) добавляли в 50 мл клеток. Условия культивирования клеток выглядели следующим образом: 5 % CO2, 37 °C, 125 об/мин. На протяжении периода культивирования среду восполняли в сутки 1 и сутки 3, до тех пор, пока жизнеспособность клеток не достигала менее чем 70 %. Клеточный супернатант собирали и центрифугировали для фильтрования. После центрифугирования клеточную культуру наносили на колонку для аффинной хроматографии для очистки антител. Очищенные химерные антитела в конечном итоге получали после промывки колонки фосфатным буфером, элюировали глицин гидрохлоридным буфером (0,1 M Gly-HCl, pH 2,7), нейтрализовали 1 M Tris-HCl, pH 9,0, и осуществляли диализ против фосфатного буфера.
Пример 5: Анализ аффинности связывания и кинетики in vitro
Способ Biacore признан способом объективного выявления аффинности и кинетики у белков. Аффинность и кинетику связывания антител против B7-H4 по изобретению, подлежащих тестированию, анализировали посредством Biacore T200 (GE).
Антитело к B7-H4 по настоящему изобретению, подлежащее тестированию, ковалентно связывалось с чипом CM5 (GE) посредством стандартного способа на основе связывания аминогрупп NHS с использованием набора, предоставленного Biacore. Затем,
а) 50 нМ человеческого белка huB7-H4-his (Sino Biological #10738-H08H), разведенного тем же буфером, загружали со скоростью потока 10 мкл/мин, и чип регенерировали посредством регенерирующего реагента, предоставленного в наборе. Кинетику связывания антигена с антителом записывали на протяжении 3 минут и кинетику диссоциации записывали в течение 10 минут. Полученные данные анализировали посредством программного обеспечения BIAevaluation GE с использованием 1:1 модели связывания (Ленгмюра). Данные по kd (koff) каждого мышиного антитела, оцениваемые данным способом, показаны в следующей таблице.
kd (1/с)
б) Серию концентраций человеческого белка huB7-H4-his, разведенного тем же буфером, соответственно загружали со скоростью потока 10 мкл/мин, и чип регенерировали регенерирующим реагентом, предоставленным в наборе. Кинетику связывания антиген-антитело записывали на протяжении 3 минут и кинетику диссоциации записывали на протяжении 10 мин. Полученные данные анализировали посредством программного обеспечения BIAevaluation GE с использованием 1:1 модели связывания (Ленгмюра). Значения ka(kon), kd (koff) и KD для каждого химерного антитела, оцениваемые данным способом, показаны в следующей таблице:
kd (1/с)
KD
Пример 6: Гуманизация мышиных антител
Гуманизацию мышиных моноклональных антител к человеческому B7-H4 проводили, как раскрыто во многих литературных источниках в данной области. Кратко, родительский (мышиное антитело) константный домен заменяли человеческим константным доменом, и человеческие последовательности антител отбирали на основе гомологии между мышиным антителом и человеческим антителом. В настоящем изобретении мышиные молекулы кандидатов 2F7, 2F8, 2G6 и 1C9 подвергали гуманизации.
На основе типичной структуры CDR VH/VL полученного мышиного антитела, последовательности вариабельной области тяжелой и легкой цепей сравнивали с базой данных антител зародышевой линии человека с получением матрицы зародышевой линии человека с высокой гомологией.
CDR области мышиных антител 2F7, 2F8, 2G6 и 1C9 прививали на выбранную соответствующую гуманизированную матрицу. В случае 2F8, область HCDR1 (GYTFTNSWMN, SEQ ID NO: 19) и область HCDR2 (GIYPNSGNIEYNEKFKG, SEQ ID NO: 20) заменяли GYTFTSSWMN (SEQ ID NO: 73) и GIYPNRGNIEYNEKFKG (SEQ ID NO: 74), соответственно, для удаления возможных нестабильных сайтов деацетилирования. Гуманизированные вариабельные области заменяли и рекомбинировали с константной областью IgG (предпочтительно IgG1 для тяжелой цепи и κ для легкой цепи). Затем, на основе трехмерной структуры мышиного антитела, обратные мутации осуществляли на включенных остатках, остатках, которые непосредственно взаимодействовали с CDR, и остатках, которые оказывают важное влияние на конформацию VL и VH. Химически нестабильные аминокислотные остатки в областях CDR оптимизировали. Получали и выявляли антитела, полученные вследствие комбинации гуманизированных последовательностей вариабельных областей легкой и тяжелой цепей.
Молекулы гуманизированных антител hu2F7, hu2F8, hu2G6 и hu1C9 в конечном итоге отбирали посредством тестирования экспрессии и сравнения числа обратных мутаций, и соответствующие последовательности вариабельных областей тяжелой и легкой цепей показаны в SEQ ID NO: 75-82, и соответствующие последовательности тяжелой и легкой цепей показаны в SEQ ID NO: 83-90.
HCVR hu2F7
EVQLVESGGGLVQPGGSLRLSCAASGFTFSNYYMSWVRQAPGKGLEWVAYVSSGGGSTYYSDSVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCTRESYSQGNYFDYWGQGTTVTVSS
SEQ ID NO: 75
EVQLVESGGGLVQPGGSLRLSCAASGFTFSNYYMSWVRQAPGKGLEWVAYVSSGGGSTYYSDSVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCARESYSQGNYFDYWGQGTTVTVSS
SEQ ID NO: 91
LCVR hu2F7
EIVMTQSPATLSLSPGERATLSCRASQSISDYLHWYQQKPGQSPRLLIKFASQSISGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQNGHSFSLTFGQGTKLEIK
SEQ ID NO: 76
EIVLTQSPATLSLSPGERATLSCRASQSISDYLHWYQQKPGQAPRLLIYFASQSISGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQNGHSFSLTFGQGTKLEIK
SEQ ID NO: 92
EIVLTQSPATLSLSPGERATLSCRASQSISDYLHWYQQKPGQAPRLLIKFASQSISGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQNGHSFSLTFGQGTKLEIK
SEQ ID NO: 93
EIVMTQSPATLSLSPGERATLSCRASQSISDYLHWYQQKPGQAPRLLIKFASQSISGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQNGHSFSLTFGQGTKLEIK
SEQ ID NO: 94
HCVR hu2F8
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSSWMNWVRQAPGQRLEWMGGIYPNRGNIEYNEKFKGRVTLTVDTSASTAYMELSSLRSEDTAVYYCARDSRFSYWGQGTLVTVSS
SEQ ID NO: 77
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSSWMNWVRQAPGQRLEWMGGIYPNRGNIEYNEKFKGRVTITVDTSASTAYMELSSLRSEDTAVYYCARDSRFSYWGQGTLVTVSS
SEQ ID NO: 95
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSSWMNWVRQAPGQGLEWMGGIYPNRGNIEYNEKFKGRVTLTVDTSASTAYMELSSLRSEDTAVYYCARDSRFSYWGQGTLVTVSS
SEQ ID NO: 96
LCVR hu2F8
DIQMTQSPSSLSASVGDRVTITCKASQDVRTAVAWYQQKPGKAPKLLISSTSYRYTGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQHYSTPLTFGGGTKVEIK
SEQ ID NO: 78
DIVMTQSPSSLSASVGDRVTITCKASQDVRTAVAWYQQKPGKAPKLLISSTSYRYTGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQHYSTPLTFGGGTKVEIK
SEQ ID NO: 97
DIVMTQSPSSLSASVGDRVTITCKASQDVRTAVAWYQQKPGKSPKLLISSTSYRYTGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQHYSTPLTFGGGTKVEIK
SEQ ID NO: 98
HCVR hu2G6
EVQLLESGGGLVQPGGSLRLSCAASGFTFSRYGMSWVRQAPGKGLEWVSGINGGGSYTYYLDTVKGRFTISRDNARNTLYLQMSSLRAEDTAVYYCVSQGSNYYFDYWGQGTLVTVSS
SEQ ID NO: 79
LCVR hu2G6
DIRMTQSPSSLSASVGDRVTITCHASQGISSNIGWLQQKPGKAPKALIYHGTNLEDGVPSRFSGSGSGADYTLTISSLQPEDFATYYCVQYAQFPYTFGGGTKVEIK
SEQ ID NO: 80
HCVR hu1C9
EVQLVQSGAEVKKPGASVKVSCKASGDTFTTYWMNWVRQAPGQRLEWMGGIYLNRGSSEYNEKFKGRVTLTVDTSASTAYMELSSLRSEDTAVYYCARDSRFSYWGQGTLVTVSS
SEQ ID NO: 81
LCVR hu1C9
DIQMTQSPSSLSASVGDRVTITCKASQDVSTAVAWYQQKPGKAPKLLISSASYRYTGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQHYNTPLTFGGGTKVEIK
SEQ ID NO: 82
HC hu2F7
EVQLVESGGGLVQPGGSLRLSCAASGFTFSNYYMSWVRQAPGKGLEWVAYVSSGGGSTYYSDSVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCTRESYSQGNYFDYWGQGTTVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO: 83
LC hu2F7
EIVMTQSPATLSLSPGERATLSCRASQSISDYLHWYQQKPGQSPRLLIKFASQSISGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQNGHSFSLTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 84
HC hu2F8
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSSWMNWVRQAPGQRLEWMGGIYPNRGNIEYNEKFKGRVTLTVDTSASTAYMELSSLRSEDTAVYYCARDSRFSYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO: 85
LC hu2F8
DIQMTQSPSSLSASVGDRVTITCKASQDVRTAVAWYQQKPGKAPKLLISSTSYRYTGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQHYSTPLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 86
HC hu2G6
EVQLLESGGGLVQPGGSLRLSCAASGFTFSRYGMSWVRQAPGKGLEWVSGINGGGSYTYYLDTVKGRFTISRDNARNTLYLQMSSLRAEDTAVYYCVSQGSNYYFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO: 87
LC hu2G6
DIRMTQSPSSLSASVGDRVTITCHASQGISSNIGWLQQKPGKAPKALIYHGTNLEDGVPSRFSGSGSGADYTLTISSLQPEDFATYYCVQYAQFPYTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 88
HC hu1C9
EVQLVQSGAEVKKPGASVKVSCKASGDTFTTYWMNWVRQAPGQRLEWMGGIYLNRGSSEYNEKFKGRVTLTVDTSASTAYMELSSLRSEDTAVYYCARDSRFSYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO: 89
LC hu1C9
DIQMTQSPSSLSASVGDRVTITCKASQDVSTAVAWYQQKPGKAPKLLISSASYRYTGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQHYNTPLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 90
Фрагменты кДНК синтезировали на основе аминокислотных последовательностей упомянутых выше легкой и тяжелой цепей гуманизированных антител и вставляли в экспрессионные векторы pcDNA3.1 (Life Technologies, кат. № V790-20). Экспрессионными векторами и реагентом для трансфекции PEI (Polysciences, Inc., кат. № 23966) трансфицировали клетки HEK293 (Life Technologies, кат. № 11625019) в соотношении 1:2 и инкубировали в CO2 инкубаторе в течение 4-5 суток. Экспрессируемые антитела выделяли посредством центрифугирования, и очистку антител проводили в соответствии со способом Примера 4 с получением гуманизированных белков-антител hu2F7 и hu2F8 по настоящему изобретению.
Пример 7: Определение активности гуманизированных антител
Следующие анализы in vitro проводили на гуманизированных антителах hu2F7 и hu2F8:
1. Анализ связывания с клетками in vitro:
Культивируемые клетки MX-1 собирали, плотность клеток регулировали посредством PBS, pH 7,4, затем высевали в 96-луночный планшет с V-образным дном с 1×105 клеток на лунку и центрифугировали при 2000 об/мин в течение 5 минут для удаления супернатанта. Добавляли 100 мкл серийно разведенного раствора химерного антитела (разведенного 0,5 % BSA в PBS с получением градиента 3-кратных разведений, начиная с 1 мкМ, в общей сложности с 10 дозами) в каждую лунку, перемешивали и инкубировали в течение 1 часа при 4 °C при встряхивании; культуру центрифугировали при 2000 об/мин в течение 5 минут для удаления супернатанта, и клетки дважды промывали PBS, и в каждую лунку добавляли 100 мкл FITC-меченного вторичного антитела козы против человеческого антитела (Abeam, кат.№ ab97224), разведенного 0,5 % BSA в PBS, хорошо перемешивали и инкубировали в течение 30 минут при 4 °C на качалке. Центрифугирование проводили при 2000 об/мин в течение 5 минут, и супернатант удаляли. Клетки дважды промывали PBS и ресуспендировали в PBS. Сигналы выявляли, используя проточный цитометр (BECKMANCOULTER, модель DxFLEX), и чертили кривую концентрации, и анализировали результаты. Как показано в таблице и на фигуре, гуманизированные антитела 2F7, 2F8, 2G6 и 1C9 демонстрируют позитивное связывание с клетками MX-1, на которых B7-H4 экспрессировался на высоком уровне.
2. Кинетический анализ аффинности (процедуры способа были такими же, как процедуры, описанные в Примере 5). Результаты показаны ниже в таблице. Все гуманизированные антитела hu2F7, hu2F8, hu2G6 и hu1C9 демонстрируют сильную аффинность в отношении человеческого белка-антигена B7-H4.
kd (1/с)
KD
Пример 8: Определение эпитопов связывания, распознаваемых гуманизированными антителами
Процедуры способа были такими же, как описано в Примере 3 (1): непрямой анализ связывания ELISA in vitro. Осуществляли деградацию B7-H4 SEQ ID NO: 100 на фрагменты антигена из 20 аминокислот в длину, и фрагмент антигена P12 (аминокислотная последовательность: TVASAGNIGEDGILSCTFEP), как было обнаружено, специфично связывался гуманизированным антителом против B7-H4 hu2F7, в непрямом анализе связывания ELISA in vitro. Результаты показаны на Фиг. 2. Для дополнительного подтверждения эпитопа, с которым связывается антитело, проводили сканирование аланином на фрагменте антигена P12, то есть, каждую отдельную аминокислоту, расположенную в P12, мутировали до аланина, соответственно. В непрямом анализе связывания ELISA in vitro обнаружили, что мутации в части аминокислотной последовательности ILSCTFE значимо ослабляли связывание антитела с фрагментом антигена, демонстрируя, что эпитоп связывания с антителом был расположен в части аминокислотной последовательности ILSCTFE (SEQ ID NO: 109), содержащейся в аминокислотной последовательности TVASAGNIGEDGILSCTFEP. Результаты показаны в следующей таблице:
В непрямом анализе связывания ELISA in vitro обнаружили, что фрагмент антигена P12 (аминокислотная последовательность: TVASAGNIGEDGILSCTFEP) специфично связывался гуманизированным антителом против B7-H4, hu1C9. Результаты показаны ниже в таблице. Для дополнительного подтверждения эпитопа, с которым связывается антитело, сканирование аланином проводили на фрагменте антигена P12, то есть, каждую отдельную аминокислоту, расположенную в P12, мутировали до аланина, соответственно. В непрямом анализе связывания ELISA in vitro обнаружили, что мутации в части аминокислотной последовательности LSCTF значимо ослабляли связывание антитела с фрагментом антигена, демонстрируя, что эпитоп связывания с антителом был расположен в части аминокислотной последовательности LSCTF (SEQ ID NO: 110), содержащейся в аминокислотной последовательности TVASAGNIGEDGILSCTFEP. Результаты показаны в следующей таблице:
В непрямом анализе связывания ELISA in vitro обнаружили, что фрагмент антигена P12 (аминокислотная последовательность: TVASAGNIGEDGILSCTFEP) специфично связывался гуманизированным антителом против B7-H4, hu2G6. Результаты показаны ниже в таблице. Для дополнительного подтверждения эпитопа, с которым связывается антитело, проводили сканирование аланином на фрагменте антигена P12, то есть, каждую отдельную аминокислоту, расположенную в P12, мутировали до аланина, соответственно. В непрямом анализе связывания ELISA in vitro обнаружили, что мутации в части аминокислотной последовательности ILSCTFEP значимо ослабляли связывание антитела с фрагментом антигена, демонстрируя, что эпитоп связывания с антителом был расположен в части аминокислотной последовательности ILSCTFEP (SEQ ID NO: 111), содержащейся в аминокислотной последовательности TVASAGNIGEDGILSCTFEP. Результаты показаны в следующей таблице:
Пример 9: Противоопухолевое действие гуманизированных антител
Опухолевые клетки MC38 имплантировали в мышей, в которые вводили человеческий ген B7-H4 посредством технологии редактирования генома. Когда опухоль достигала в среднем 100 мм3, мышам инъецировали контроль или гуманизированное антитело против B7-H4 hu1C9 (10 мг/кг или 30 мг/кг) каждые 3 суток. Наблюдая за размером опухоли, обнаружили, что hu1C9 оказывает значимое действие на ингибирование роста опухоли и оказывает противоопухолевое действие. Конкретные результаты показаны на Фиг. 3 и в следующей таблице:
Пример 10: Воздействие гуманизированных антител на усиление иммунитета
Противоопухолевое действие антитела против B7-H4 может быть опосредовано эффектом усиления иммунитета в отношении опухолей. Для проверки достоверности данного механизма CD4-позитивные T-клетки выделяли из периферической крови человека. Разные концентрации антител к B7-H4, включая гуманизированное антитело hu2G6 и hu1C9, добавляли в культивируемые T-клетки. Конкретные результаты показаны на Фиг. 4 и ниже в таблице. Гуманизированное антитело hu2G6 и гуманизированное антитело hu1C9 оказывают действие на усиление пролиферации T-клеток и могут достигать противоопухолевого действия посредством эффектов усиления иммунитета в отношении опухолей.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ЦЗЯНСУ ХЭНСОХ ФАРМАСЬЮТИКАЛ ГРУП КО., ЛТД.
ШАНХАЙ ХЭНСОХ БИОМЕДИКАЛ КО., ЛТД.
<120> АНТИТЕЛО К B7-H4, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО
ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ
<130> 719011CPCT
<160> 111
<170> SIPOSequenceListing 1,0
<210> 1
<211> 120
<212> БЕЛОК
<213> Мышь домовая
<400> 1
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Tyr Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Tyr Val Ser Ser Gly Gly Gly Ser Thr Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Lys Pro Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Thr Arg Glu Ser Tyr Ser Gln Gly Asn Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 2
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 2
Asp Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Thr Pro Gly
1 5 10 15
Asp Arg Val Ser Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Ser His Glu Ser Pro Arg Leu Leu Ile
35 40 45
Lys Phe Ala Ser Gln Ser Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ser Asp Phe Thr Leu Ser Ile Asn Ser Val Glu Pro
65 70 75 80
Glu Asp Val Gly Val Tyr Tyr Cys Gln Asn Gly His Ser Phe Ser Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 3
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 3
Gly Phe Thr Phe Ser Asn Tyr Tyr Met Ser
1 5 10
<210> 4
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 4
Tyr Val Ser Ser Gly Gly Gly Ser Thr Tyr Tyr Ser Asp Ser Val Lys
1 5 10 15
Gly
<210> 5
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 5
Glu Ser Tyr Ser Gln Gly Asn Tyr Phe Asp Tyr
1 5 10
<210> 6
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 6
Arg Ala Ser Gln Ser Ile Ser Asp Tyr Leu His
1 5 10
<210> 7
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 7
Phe Ala Ser Gln Ser Ile Ser
1 5
<210> 8
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 8
Gln Asn Gly His Ser Phe Ser Leu Thr
1 5
<210> 9
<211> 123
<212> БЕЛОК
<213> Мышь домовая
<400> 9
Glu Ile Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Met Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Thr Ala Ser Gly Tyr Pro Phe Thr Thr Tyr
20 25 30
Asn Met Tyr Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Asp Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Phe Tyr Asp Gly Tyr Tyr Ala Trp Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 10
<211> 112
<212> БЕЛОК
<213> Мышь домовая
<400> 10
Asp Val Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Gly Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 11
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 11
Gly Tyr Pro Phe Thr Thr Tyr Asn Met Tyr
1 5 10
<210> 12
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 12
Tyr Ile Asp Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 13
<211> 14
<212> БЕЛОК
<213> Мышь домовая
<400> 13
Ser Gly Phe Tyr Asp Gly Tyr Tyr Ala Trp Tyr Phe Asp Val
1 5 10
<210> 14
<211> 16
<212> БЕЛОК
<213> Мышь домовая
<400> 14
Arg Ser Ser Gln Ser Leu Val His Ser Gly Gly Asn Thr Tyr Leu His
1 5 10 15
<210> 15
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 15
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 16
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 16
Ser Gln Ser Thr His Val Pro Leu Thr
1 5
<210> 17
<211> 115
<212> БЕЛОК
<213> Мышь домовая
<400> 17
Gln Val Gln Leu Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Ser
20 25 30
Trp Met Asn Trp Ala Lys Leu Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Pro Asn Ser Gly Asn Ile Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Thr Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 18
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 18
Asp Ile Val Met Thr Gln Ser His Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Arg Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Ser Ser Thr Ser Tyr Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Ile Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 19
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 19
Gly Tyr Thr Phe Thr Asn Ser Trp Met Asn
1 5 10
<210> 20
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 20
Gly Ile Tyr Pro Asn Ser Gly Asn Ile Glu Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 21
<211> 6
<212> БЕЛОК
<213> Мышь домовая
<400> 21
Asp Ser Arg Phe Ser Tyr
1 5
<210> 22
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 22
Lys Ala Ser Gln Asp Val Arg Thr Ala Val Ala
1 5 10
<210> 23
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 23
Ser Thr Ser Tyr Arg Tyr Thr
1 5
<210> 24
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 24
Gln Gln His Tyr Ser Thr Pro Leu Thr
1 5
<210> 25
<211> 115
<212> БЕЛОК
<213> Мышь домовая
<400> 25
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu Thr Phe Ser Arg Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Gly Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Ser Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Val Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Gly Arg Glu Tyr Gly Arg Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr
100 105 110
Val Ser Ser
115
<210> 26
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 26
Asp Ile Leu Met Thr Gln Ser Pro Ser Ser Met Ser Val Ser Leu Gly
1 5 10 15
Asp Thr Val Ser Ile Thr Cys His Ala Ser Gln Gly Ile Asn Ser Asn
20 25 30
Ile Gly Trp Leu Gln Gln Lys Pro Gly Lys Ser Phe Lys Gly Leu Ile
35 40 45
Tyr His Gly Thr Asn Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Ser
65 70 75 80
Glu Asp Phe Ala Asp Tyr Tyr Cys Val Gln Tyr Ala Gln Phe Pro Arg
85 90 95
Thr Phe Gly Gly Gly Thr Thr Leu Glu Ile Lys
100 105
<210> 27
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 27
Gly Leu Thr Phe Ser Arg Tyr Ala Met Ser
1 5 10
<210> 28
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 28
Gly Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Ser Asp Thr Val Lys
1 5 10 15
Gly
<210> 29
<211> 6
<212> БЕЛОК
<213> Мышь домовая
<400> 29
Glu Tyr Gly Arg Asp Tyr
1 5
<210> 30
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 30
His Ala Ser Gln Gly Ile Asn Ser Asn Ile Gly
1 5 10
<210> 31
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 31
His Gly Thr Asn Leu Glu Asp
1 5
<210> 32
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 32
Val Gln Tyr Ala Gln Phe Pro Arg Thr
1 5
<210> 33
<211> 113
<212> БЕЛОК
<213> Мышь домовая
<400> 33
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Phe
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Asp Lys Arg Leu Glu Trp Val
35 40 45
Ala Gly Ile Ser Pro Gly Gly Ser Tyr Thr Tyr Tyr Pro Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Ser Ala Met Tyr Tyr Cys
85 90 95
Thr Arg Gly Arg Ser Val Trp Gly Thr Gly Thr Thr Val Thr Val Ser
100 105 110
Ser
<210> 34
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 34
Asp Ile Leu Met Thr Gln Ser Pro Ser Ser Met Ser Val Ser Leu Gly
1 5 10 15
Asp Thr Val Ser Ile Thr Cys His Ala Ser Gln Asp Ile Ser Ser Asn
20 25 30
Ile Gly Trp Leu Gln Gln Lys Pro Gly Lys Ser Phe Lys Gly Leu Ile
35 40 45
Tyr His Gly Thr Thr Leu Glu Asp Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Ser
65 70 75 80
Glu Asp Phe Ala Asp Tyr Tyr Cys Val Gln Ser Ala Gln Phe Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 35
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 35
Gly Phe Thr Phe Ser Thr Phe Gly Met Ser
1 5 10
<210> 36
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 36
Gly Ile Ser Pro Gly Gly Ser Tyr Thr Tyr Tyr Pro Asp Thr Val Lys
1 5 10 15
Gly
<210> 37
<211> 4
<212> БЕЛОК
<213> Мышь домовая
<400> 37
Gly Arg Ser Val
1
<210> 38
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 38
His Ala Ser Gln Asp Ile Ser Ser Asn Ile Gly
1 5 10
<210> 39
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 39
His Gly Thr Thr Leu Glu Asp
1 5
<210> 40
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 40
Val Gln Ser Ala Gln Phe Pro Trp Thr
1 5
<210> 41
<211> 115
<212> БЕЛОК
<213> Мышь домовая
<400> 41
Gln Val Gln Leu Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Thr
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Pro Asn Arg Gly Thr Thr Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Phe
65 70 75 80
Met Asp Leu Asn Arg Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ala Asp Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 42
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 42
Asp Ile Met Leu Thr Gln Ser His Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ala Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Ser Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 43
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 43
Gly Tyr Thr Phe Thr Ser Ser Trp Met Asn
1 5 10
<210> 44
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 44
Gly Ile Tyr Pro Asn Arg Gly Thr Thr Glu Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 45
<211> 6
<212> БЕЛОК
<213> Мышь домовая
<400> 45
Asp Ser Arg Phe Ala Asp
1 5
<210> 46
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 46
Lys Ala Ser Gln Asp Val Ser Ala Ala Val Ala
1 5 10
<210> 47
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 47
Ser Ala Ser Tyr Arg Tyr Thr
1 5
<210> 48
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<220>
<221> ДОМЕН
<222> (1)..(10)
<223> мутантная область HCDR1 2F8
<400> 48
Gln Gln His Tyr Asn Thr Pro Leu Thr
1 5
<210> 49
<211> 118
<212> БЕЛОК
<213> Мышь домовая
<400> 49
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Gly Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Pro Asp Thr Leu
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Lys Tyr Phe Cys
85 90 95
Ala Ser Gln Gly Ser Asn His Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 50
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 50
Asp Thr Leu Met Thr Gln Ser Pro Ser Ser Met Ser Val Ser Leu Gly
1 5 10 15
Asp Thr Val Ser Ile Thr Cys His Ala Ser Gln Gly Ile His Asn Asn
20 25 30
Ile Gly Trp Leu Gln Gln Lys Pro Gly Lys Ser Phe Lys Ala Leu Ile
35 40 45
Tyr His Gly Thr Asn Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Ser Leu Ile Ile Ser Ser Leu Glu Ser
65 70 75 80
Glu Asp Phe Ala Asp Tyr Tyr Cys Val Gln Tyr Ala Gln Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 51
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 51
Gly Phe Thr Phe Ser Arg Tyr Ala Met Ser
1 5 10
<210> 52
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 52
Gly Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Pro Asp Thr Leu Lys
1 5 10 15
Gly
<210> 53
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 53
Gln Gly Ser Asn His Tyr Phe Asp Tyr
1 5
<210> 54
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 54
His Ala Ser Gln Gly Ile His Asn Asn Ile Gly
1 5 10
<210> 55
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 55
His Gly Thr Asn Leu Glu Asp
1 5
<210> 56
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 56
Val Gln Tyr Ala Gln Phe Pro Tyr Thr
1 5
<210> 57
<211> 118
<212> БЕЛОК
<213> Мышь домовая
<400> 57
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Gly Ile Asn Gly Gly Gly Ser Tyr Thr Tyr Tyr Leu Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Val Ser Gln Gly Ser Asn Tyr Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 58
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 58
Asp Ile Arg Met Thr Gln Ser Pro Ser Ser Met Ser Val Ser Leu Gly
1 5 10 15
Asp Thr Val Ser Ile Thr Cys His Ala Ser Gln Gly Ile Ser Ser Asn
20 25 30
Ile Gly Trp Leu Gln Gln Lys Pro Gly Lys Ser Phe Lys Ala Leu Ile
35 40 45
Tyr His Gly Thr Asn Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Ser
65 70 75 80
Glu Asp Phe Ala Asp Tyr Tyr Cys Val Gln Tyr Ala Gln Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 59
<211> 10
<212> БЕЛОК
<213> Мышь домовая
<400> 59
Gly Phe Thr Phe Ser Arg Tyr Gly Met Ser
1 5 10
<210> 60
<211> 17
<212> БЕЛОК
<213> Мышь домовая
<400> 60
Gly Ile Asn Gly Gly Gly Ser Tyr Thr Tyr Tyr Leu Asp Thr Val Lys
1 5 10 15
Gly
<210> 61
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 61
Gln Gly Ser Asn Tyr Tyr Phe Asp Tyr
1 5
<210> 62
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 62
His Ala Ser Gln Gly Ile Ser Ser Asn Ile Gly
1 5 10
<210> 63
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 63
His Gly Thr Asn Leu Glu Asp
1 5
<210> 64
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 64
Val Gln Tyr Ala Gln Phe Pro Tyr Thr
1 5
<210> 65
<211> 115
<212> БЕЛОК
<213> Мышь домовая
<400> 65
Gln Val Gln Leu Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Asp Thr Phe Thr Thr Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Leu Asn Ser Gly Ser Ser Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Ser Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 66
<211> 107
<212> БЕЛОК
<213> Мышь домовая
<400> 66
Asp Ile Val Met Thr Gln Ser His Lys Phe Leu Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Glu Leu Leu Ile
35 40 45
Ser Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Gln Leu Glu Leu Lys
100 105
<210> 67
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 67
Gly Asp Thr Phe Thr Thr Tyr
1 5
<210> 68
<211> 6
<212> БЕЛОК
<213> Мышь домовая
<400> 68
Tyr Leu Asn Ser Gly Ser
1 5
<210> 69
<211> 6
<212> БЕЛОК
<213> Мышь домовая
<400> 69
Asp Ser Arg Phe Ser Tyr
1 5
<210> 70
<211> 11
<212> БЕЛОК
<213> Мышь домовая
<400> 70
Lys Ala Ser Gln Asp Val Ser Thr Ala Val Ala
1 5 10
<210> 71
<211> 7
<212> БЕЛОК
<213> Мышь домовая
<400> 71
Ser Ala Ser Tyr Arg Tyr Thr
1 5
<210> 72
<211> 9
<212> БЕЛОК
<213> Мышь домовая
<400> 72
Gln Gln His Tyr Asn Thr Pro Leu Thr
1 5
<210> 73
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(10)
<223> гуманизированная HCDR1 2F8
<400> 73
Gly Tyr Thr Phe Thr Ser Ser Trp Met Asn
1 5 10
<210> 74
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(17)
<223> гуманизированная HCDR2 2F8
<400> 74
Gly Ile Tyr Pro Asn Arg Gly Asn Ile Glu Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 75
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(120)
<223> hu2F7 HCVR
<400> 75
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Val Ser Ser Gly Gly Gly Ser Thr Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Glu Ser Tyr Ser Gln Gly Asn Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 76
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2F7 LCVR
<400> 76
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
35 40 45
Lys Phe Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Asn Gly His Ser Phe Ser Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 77
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(115)
<223> hu2F8 HCVR
<400> 77
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Pro Asn Arg Gly Asn Ile Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 78
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2F8 LCVR
<400> 78
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Arg Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Ser Thr Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 79
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(118)
<223> hu2G6 HCVR
<400> 79
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Gly Gly Gly Ser Tyr Thr Tyr Tyr Leu Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Ser Gln Gly Ser Asn Tyr Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 80
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2G6 LCVR
<400> 80
Asp Ile Arg Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys His Ala Ser Gln Gly Ile Ser Ser Asn
20 25 30
Ile Gly Trp Leu Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile
35 40 45
Tyr His Gly Thr Asn Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Val Gln Tyr Ala Gln Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 81
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(115)
<223> hu1C9 HCVR
<400> 81
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Asp Thr Phe Thr Thr Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Asn Arg Gly Ser Ser Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 82
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu1C9 LCVR
<400> 82
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 83
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(450)
<223> hu2F7 HC
<400> 83
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Val Ser Ser Gly Gly Gly Ser Thr Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Glu Ser Tyr Ser Gln Gly Asn Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 84
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(214)
<223> hu2F7 LC
<400> 84
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
35 40 45
Lys Phe Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Asn Gly His Ser Phe Ser Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 85
<211> 445
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(445)
<223> hu2F8 HC
<400> 85
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Pro Asn Arg Gly Asn Ile Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 86
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(214)
<223> hu2F8 LC
<400> 86
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Arg Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Ser Thr Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 87
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(448)
<223> hu2G6 HC
<400> 87
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Gly Gly Gly Ser Tyr Thr Tyr Tyr Leu Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Ser Gln Gly Ser Asn Tyr Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 88
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(214)
<223> hu2G6 LC
<400> 88
Asp Ile Arg Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys His Ala Ser Gln Gly Ile Ser Ser Asn
20 25 30
Ile Gly Trp Leu Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile
35 40 45
Tyr His Gly Thr Asn Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Val Gln Tyr Ala Gln Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 89
<211> 445
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(445)
<223> hu1C9 HC
<400> 89
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Asp Thr Phe Thr Thr Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Asn Arg Gly Ser Ser Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 90
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(214)
<223> hu1C9 LC
<400> 90
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 91
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(120)
<223> hu2F7 HCVR
<400> 91
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Val Ser Ser Gly Gly Gly Ser Thr Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Tyr Ser Gln Gly Asn Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 92
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2F7 LCVR
<400> 92
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Phe Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Asn Gly His Ser Phe Ser Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 93
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2F7 LCVR
<400> 93
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Phe Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Asn Gly His Ser Phe Ser Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 94
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2F7 LCVR
<400> 94
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Phe Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Asn Gly His Ser Phe Ser Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 95
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(115)
<223> hu2F8 HCVR
<400> 95
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Pro Asn Arg Gly Asn Ile Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 96
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(115)
<223> hu2F8 HCVR
<400> 96
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Pro Asn Arg Gly Asn Ile Glu Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Arg Phe Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 97
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2F8 LCVR
<400> 97
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Arg Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Ser Thr Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 98
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ДОМЕН
<222> (1)..(107)
<223> hu2F8 LCVR
<400> 98
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Arg Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ser Pro Lys Leu Leu Ile
35 40 45
Ser Ser Thr Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 99
<211> 463
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ПЕПТИД
<222> (1)..(463)
<223> huB7-H4-Fc
<400> 99
Phe Gly Ile Ser Gly Arg His Ser Ile Thr Val Thr Thr Val Ala Ser
1 5 10 15
Ala Gly Asn Ile Gly Glu Asp Gly Ile Leu Ser Cys Thr Phe Glu Pro
20 25 30
Asp Ile Lys Leu Ser Asp Ile Val Ile Gln Trp Leu Lys Glu Gly Val
35 40 45
Leu Gly Leu Val His Glu Phe Lys Glu Gly Lys Asp Glu Leu Ser Glu
50 55 60
Gln Asp Glu Met Phe Arg Gly Arg Thr Ala Val Phe Ala Asp Gln Val
65 70 75 80
Ile Val Gly Asn Ala Ser Leu Arg Leu Lys Asn Val Gln Leu Thr Asp
85 90 95
Ala Gly Thr Tyr Lys Cys Tyr Ile Ile Thr Ser Lys Gly Lys Gly Asn
100 105 110
Ala Asn Leu Glu Tyr Lys Thr Gly Ala Phe Ser Met Pro Glu Val Asn
115 120 125
Val Asp Tyr Asn Ala Ser Ser Glu Thr Leu Arg Cys Glu Ala Pro Arg
130 135 140
Trp Phe Pro Gln Pro Thr Val Val Trp Ala Ser Gln Val Asp Gln Gly
145 150 155 160
Ala Asn Phe Ser Glu Val Ser Asn Thr Ser Phe Glu Leu Asn Ser Glu
165 170 175
Asn Val Thr Met Lys Val Val Ser Val Leu Tyr Asn Val Thr Ile Asn
180 185 190
Asn Thr Tyr Ser Cys Met Ile Glu Asn Asp Ile Ala Lys Ala Thr Gly
195 200 205
Asp Ile Lys Val Thr Glu Ser Glu Ile Lys Arg Arg Ser His Leu Gln
210 215 220
Leu Leu Asn Ser Lys Ala Gly Ser Gly Gly Gly Gly Asp Lys Thr His
225 230 235 240
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
245 250 255
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
260 265 270
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
275 280 285
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
290 295 300
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
305 310 315 320
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
325 330 335
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
340 345 350
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
355 360 365
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
370 375 380
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
385 390 395 400
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
405 410 415
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
420 425 430
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
435 440 445
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455 460
<210> 100
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ПЕПТИД
<222> (1)..(276)
<223> huB7-H4-his
<400> 100
Met Ala Ser Leu Gly Gln Ile Leu Phe Trp Ser Ile Ile Ser Ile Ile
1 5 10 15
Ile Ile Leu Ala Gly Ala Ile Ala Leu Ile Ile Gly Phe Gly Ile Ser
20 25 30
Gly Arg His Ser Ile Thr Val Thr Thr Val Ala Ser Ala Gly Asn Ile
35 40 45
Gly Glu Asp Gly Ile Leu Ser Cys Thr Phe Glu Pro Asp Ile Lys Leu
50 55 60
Ser Asp Ile Val Ile Gln Trp Leu Lys Glu Gly Val Leu Gly Leu Val
65 70 75 80
His Glu Phe Lys Glu Gly Lys Asp Glu Leu Ser Glu Gln Asp Glu Met
85 90 95
Phe Arg Gly Arg Thr Ala Val Phe Ala Asp Gln Val Ile Val Gly Asn
100 105 110
Ala Ser Leu Arg Leu Lys Asn Val Gln Leu Thr Asp Ala Gly Thr Tyr
115 120 125
Lys Cys Tyr Ile Ile Thr Ser Lys Gly Lys Gly Asn Ala Asn Leu Glu
130 135 140
Tyr Lys Thr Gly Ala Phe Ser Met Pro Glu Val Asn Val Asp Tyr Asn
145 150 155 160
Ala Ser Ser Glu Thr Leu Arg Cys Glu Ala Pro Arg Trp Phe Pro Gln
165 170 175
Pro Thr Val Val Trp Ala Ser Gln Val Asp Gln Gly Ala Asn Phe Ser
180 185 190
Glu Val Ser Asn Thr Ser Phe Glu Leu Asn Ser Glu Asn Val Thr Met
195 200 205
Lys Val Val Ser Val Leu Tyr Asn Val Thr Ile Asn Asn Thr Tyr Ser
210 215 220
Cys Met Ile Glu Asn Asp Ile Ala Lys Ala Thr Gly Asp Ile Lys Val
225 230 235 240
Thr Glu Ser Glu Ile Lys Arg Arg Ser His Leu Gln Leu Leu Asn Ser
245 250 255
Lys Ala Asp Tyr Lys Asp Asp Asp Asp Lys Gly Ser His His His His
260 265 270
His His His His
275
<210> 101
<211> 20
<212> БЕЛОК
<213> Человек разумный
<400> 101
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ile Leu Ser Cys
1 5 10 15
Thr Phe Glu Pro
20
<210> 102
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ВАРИАНТ
<222> (1)..(20)
<223> вариант фрагмента антигена P12
<400> 102
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ala Leu Ser Cys
1 5 10 15
Thr Phe Glu Pro
20
<210> 103
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ВАРИАНТ
<222> (1)..(20)
<223> вариант фрагмента антигена P12
<400> 103
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ile Ala Ser Cys
1 5 10 15
Thr Phe Glu Pro
20
<210> 104
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ВАРИАНТ
<222> (1)..(20)
<223> вариант фрагмента антигена P12
<400> 104
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ile Leu Ser Ala
1 5 10 15
Thr Phe Glu Pro
20
<210> 105
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ВАРИАНТ
<222> (1)..(20)
<223> вариант фрагмента антигена P12
<400> 105
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ile Leu Ser Cys
1 5 10 15
Ala Phe Glu Pro
20
<210> 106
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ВАРИАНТ
<222> (1)..(20)
<223> вариант фрагмента антигена P12
<400> 106
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ile Leu Ser Cys
1 5 10 15
Thr Ala Glu Pro
20
<210> 107
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ВАРИАНТ
<222> (1)..(20)
<223> вариант фрагмента антигена P12
<400> 107
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ile Leu Ser Cys
1 5 10 15
Thr Phe Ala Pro
20
<210> 108
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> ВАРИАНТ
<222> (1)..(20)
<223> вариант фрагмента антигена P12
<400> 108
Thr Val Ala Ser Ala Gly Asn Ile Gly Glu Asp Gly Ile Leu Ser Cys
1 5 10 15
Thr Phe Glu Ala
20
<210> 109
<211> 7
<212> БЕЛОК
<213> Человек разумный
<400> 109
Ile Leu Ser Cys Thr Phe Glu
1 5
<210> 110
<211> 5
<212> БЕЛОК
<213> Человек разумный
<400> 110
Leu Ser Cys Thr Phe
1 5
<210> 111
<211> 8
<212> БЕЛОК
<213> Человек разумный
<400> 111
Ile Leu Ser Cys Thr Phe Glu Pro
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Антитело к BCMA, его антигенсвязывающий фрагмент и их медицинское применение | 2020 |
|
RU2819660C2 |
| КОНЪЮГАТ АНТИТЕЛА К B7-H4 И ЛЕКАРСТВЕННОГО СРЕДСТВА И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2827531C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО ПРОТИВ ВИРУСА БЕШЕНСТВА И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2764740C1 |
| БИСПЕЦИФИЧНЫЙ СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2801528C2 |
| АНТИТЕЛО ПРОТИВ В7-Н3, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2765306C2 |
| АНТИТЕЛО К CD3 И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2802272C2 |
| АНТИТЕЛО К PD-1, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2807484C2 |
| СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800923C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО ПРОТИВ CD3E/BCMA И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800164C2 |
| АНТИТЕЛО ПРОТИВ СТОЛБНЯЧНОГО ТОКСИНА И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2815280C1 |
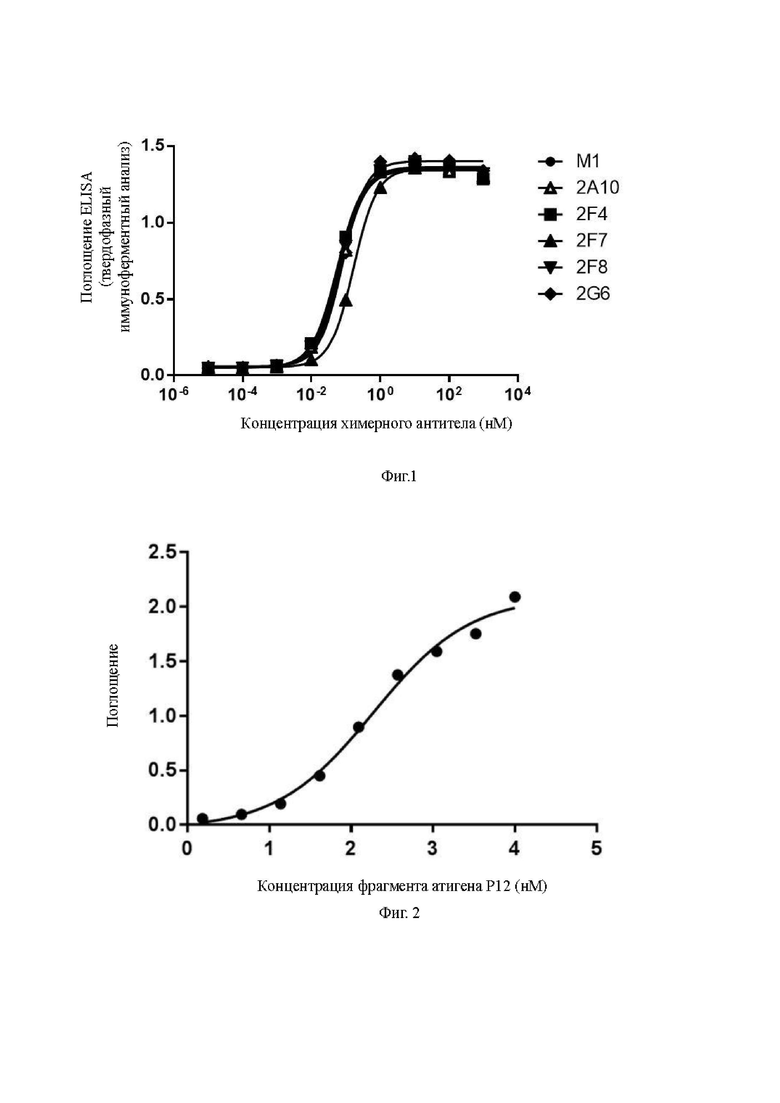
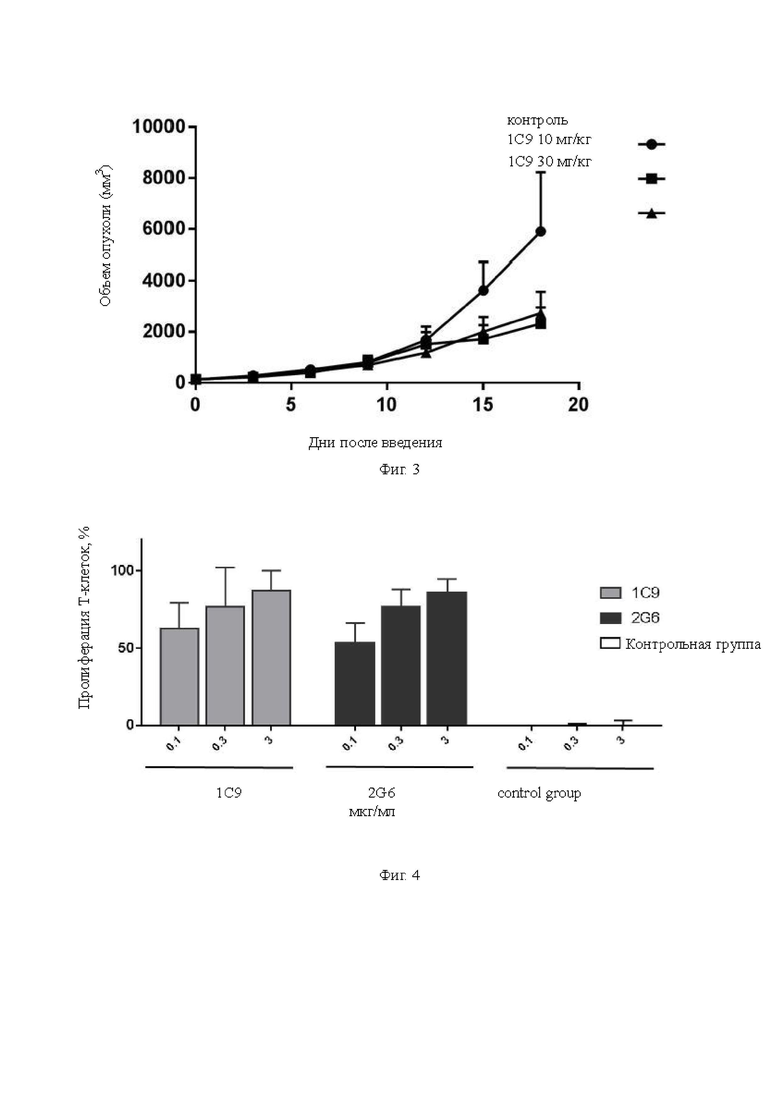
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая антитело к B7-H4 или его антигенсвязывающий фрагмент, молекулу ДНК, кодирующую антитело или его антигенсвязывающий фрагмент, экспрессионный вектор, содержащий молекулу ДНК, клетку-хозяин для экспрессии антитела к B7-H4 или его антигенсвязывающего фрагмента, способ получения антитела, включающий культивирование клетки-хозяина и выделение антитела, фармацевтическую композицию для лечения B7-H4-опосредованных заболеваний или состояний, содержащую антитело к B7-H4 или его антигенсвязывающий фрагмент, реагент для выявления, предназначенный для иммунодетекции или определения B7-H4, диагностическое средство для диагностики B7-H4-опосредованных заболеваний или состояний, и применение антитела к B7-H4 или его антигенсвязывающего фрагмента или фармацевтической композиции в изготовлении лекарственного средства для лечения или предупреждения B7-H4-опосредованного заболевания или состояния. Изобретение расширяет арсенал средств, связывающихся с B7-H4. 9 н. и 14 з.п. ф-лы, 4 ил., 23 табл., 10 пр.
1. Антитело к B7-H4 или его антигенсвязывающий фрагмент, содержащее:
вариабельную область легкой цепи антитела и вариабельную область тяжелой цепи антитела, где
1) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 3, SEQ ID NO: 4 и SEQ ID NO: 5, соответственно;
2) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 11, SEQ ID NO: 12 и SEQ ID NO: 13, соответственно;
3) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 22, SEQ ID NO: 23 и SEQ ID NO: 24, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 19, SEQ ID NO: 20 и SEQ ID NO: 21, соответственно;
4) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 30, SEQ ID NO: 31 и SEQ ID NO: 32, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 27, SEQ ID NO: 28 и SEQ ID NO: 29, соответственно;
5) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 38, SEQ ID NO: 39 и SEQ ID NO: 40, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 35, SEQ ID NO: 36 и SEQ ID NO: 37, соответственно;
6) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 46, SEQ ID NO: 47 и SEQ ID NO: 48, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 43, SEQ ID NO: 44 и SEQ ID NO: 45, соответственно;
7) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 54, SEQ ID NO: 55 и SEQ ID NO: 56, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 51, SEQ ID NO: 52 и SEQ ID NO: 53, соответственно;
8) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 62, SEQ ID NO: 63 и SEQ ID NO: 64, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61, соответственно;
9) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 70, SEQ ID NO: 71 и SEQ ID NO: 72, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 67, SEQ ID NO: 68 и SEQ ID NO: 69, соответственно; или
10) вариабельная область легкой цепи указанного антитела содержит LCDR1, LCDR2 и LCDR3, как показано в SEQ ID NO: 22, SEQ ID NO: 23 и SEQ ID NO: 24, соответственно; и вариабельная область тяжелой цепи данного антитела содержит HCDR1, HCDR2 и HCDR3, как показано в SEQ ID NO: 73, SEQ ID NO: 74 и SEQ ID NO: 21, соответственно.
2. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 1, где антитело или его антигенсвязывающий фрагмент выбрано из группы, состоящей из мышиного антитела или его фрагмента, химерного антитела или его фрагмента, человеческого антитела или его фрагмента и гуманизированного антитела или его фрагмента.
3. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 2, где вариабельная область тяжелой цепи гуманизированного антитела содержит константную(ые) область(и) тяжелой цепи человеческого IgG1, IgG2, IgG3 или IgG4 или ее вариант, предпочтительно содержит константную(ые) область(и) тяжелой цепи человеческого IgG1, IgG2 или IgG4; более предпочтительно содержит константную(ые) область(и) тяжелой цепи IgG1, которая подвергалась аминокислотной мутации для усиления ADCC (антителозависимая клеточная цитотоксичность) токсичности.
4. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 2, где вариабельная область легкой цепи гуманизированного антитела представляет собой вариабельную область легкой цепи, содержащую последовательность, выбранную из группы, состоящей из: SEQ ID NO: 76, SEQ ID NO: 78, SEQ ID NO: 80 или SEQ ID NO: 82, предпочтительно SEQ ID NO: 76 или SEQ ID NO: 80.
5. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 2, где вариабельная область тяжелой цепи гуманизированного антитела представляет собой вариабельную область тяжелой цепи, содержащую последовательность, выбранную из группы, состоящей из: SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79 или SEQ ID NO: 81, предпочтительно SEQ ID NO: 75 или SEQ ID NO: 79.
6. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 2, где легкая цепь гуманизированного антитела представляет собой легкую цепь, содержащую последовательность, выбранную из группы, состоящей из: SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 88 или SEQ ID NO: 90, предпочтительно SEQ ID NO: 84 или SEQ ID NO: 88.
7. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 2, где тяжелая цепь гуманизированного антитела представляет собой тяжелую цепь, содержащую последовательность, выбранную из группы, состоящей из: SEQ ID NO: 83, SEQ ID NO: 85, SEQ ID NO: 87 или SEQ ID NO: 89, предпочтительно SEQ ID NO: 83 или SEQ ID NO: 87.
8. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 2, где гуманизированное антитело содержит:
(1) вариабельную область легкой цепи SEQ ID NO: 76 и вариабельную область тяжелой цепи SEQ ID NO: 75;
(2) вариабельную область легкой цепи SEQ ID NO: 78 и вариабельную область тяжелой цепи SEQ ID NO: 77;
(3) вариабельную область легкой цепи SEQ ID NO: 80 и вариабельную область тяжелой цепи SEQ ID NO: 79; или
(4) вариабельную область легкой цепи SEQ ID NO: 82 и вариабельную область тяжелой цепи SEQ ID NO: 81.
9. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 2, где гуманизированное антитело содержит:
(1) легкую цепь SEQ ID NO: 84 и тяжелую цепь SEQ ID NO: 83;
(2) легкую цепь SEQ ID NO: 86 и тяжелую цепь SEQ ID NO: 85;
(3) легкую цепь SEQ ID NO: 88 и тяжелую цепь SEQ ID NO: 87; или
(4) легкую цепь SEQ ID NO: 90 и тяжелую цепь SEQ ID NO: 89.
10. Антитело к B7-H4 или его антигенсвязывающий фрагмент по любому из пп. 2-9, где гуманизированное антитело имеет следующую характеристику: связывание с эпитопом, содержащим аминокислоты 41-60 в SEQ ID NO: 100 B7-H4.
11. Антитело к B7-H4 или его антигенсвязывающий фрагмент по п. 10, где гуманизированное антитело имеет следующую характеристику: связывание с эпитопом, содержащим аминокислоты 53-59 в SEQ ID NO: 100 B7-H4.
12. Молекула ДНК, кодирующая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-11.
13. Экспрессионный вектор, содержащий молекулу ДНК по п. 12.
14. Клетка-хозяин для экспрессии антитела к B7-H4 или его антигенсвязывающего фрагмента, в которую вводят или которая содержит экспрессионный вектор по п. 13.
15. Клетка-хозяин по п. 14, которая представляет собой бактерию, предпочтительно Escherichia coli.
16. Клетка-хозяин по п. 14, которая представляет собой дрожжи, предпочтительно Pichia pastoris.
17. Клетка-хозяин по п. 14, которая представляет собой клетку млекопитающего, предпочтительно клетку яичника китайского хомяка (CHO) или клетку эмбриональной почки человека (HEK) 293.
18. Способ получения антитела, включающий культивирование клетки-хозяина по пп. 14-17, выделение антитела из культуры и очистку антитела.
19. Фармацевтическая композиция для лечения B7-H4-опосредованных заболеваний или состояний, содержащая антитело к B7-H4 или его антигенсвязывающий фрагмент по любому из пп. 1-11, и фармацевтически приемлемый эксципиент, разбавитель или носитель.
20. Реагент для выявления, предназначенный для иммунодетекции или определения B7-H4, содержащий антитело к B7-H4 или его антигенсвязывающий фрагмент по любому из пп. 1-11.
21. Диагностическое средство для диагностики B7-H4-опосредованных заболеваний или состояний, содержащее антитело к B7-H4 или его антигенсвязывающий фрагмент по любому из пп. 1-11.
22. Применение антитела к B7-H4 или его антигенсвязывающего фрагмента по любому из пп. 1-11 или фармацевтической композиции по п. 19 в изготовлении лекарственного средства для лечения или предупреждения B7-H4-опосредованного заболевания или состояния.
23. Применение по п. 22, где заболевание представляет собой рак; предпочтительно заболевание представляет собой рак с экспрессией B7-H4; рак наиболее предпочтительно выбран из группы, состоящей из рака молочной железы, рака яичника, рака предстательной железы, рака поджелудочной железы, рака почки, рака легкого, рака печени, рака желудка, рака толстой кишки, рака мочевого пузыря, рака пищевода, рака шейки матки, рака желчного пузыря, глиобластомы и меланомы.
| RU 2015129551 A 25.01.2017 | |||
| EP 2934576 A1 28.10.2015 | |||
| WO 2009073533 A3 11.06.2009 | |||
| Yun Qian et al | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Exp | |||
| Med., 2011, vol | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Деревянное стыковое устройство | 1920 |
|
SU163A1 |
Авторы
Даты
2023-03-23—Публикация
2019-02-01—Подача