Область техники, к которой относится изобретение
Настоящее изобретение относится к области биотехнологии и медицины, а именно к моноклональному антителу или его антигенсвязывающему фрагменту, которое специфически связывается с ВСМА. Изобретение также относится к нуклеиновым кислотам, кодирующим указанное антитело, векторам экспрессии, клеткам-хозяевам и способам их получения, способам получения антител по изобретению, фармацевтическим композициям, содержащим антитело по изобретению, фармацевтическим композициям, содержащим антитело по изобретению и другие терапевтически активные соединения, способам лечения заболеваний или нарушений, опосредованных ВСМА, применениям антител или их фармацевтических композиций для лечения заболеваний или нарушений, опосредованных ВСМА, и применениям антител по изобретению и других терапевтически активных соединений для лечения заболеваний или нарушений, опосредованных ВСМА.
Уровень техники
В-клеточный антиген созревания (ВСМА, B-cell maturation antigen; TNFRSF17 и CD269) является представителем суперсемейства рецепторов фактора некроза опухоли (TNF). Его нативными лигандами являются В-клеточный активирующий фактор (BAFF; также называемый BLyS или TALL-1, TNFSF13B) и индуцирующий пролиферацию лиганд (APRIL, TNFSF13, CD256), которые вовлечены в регуляцию различных аспектов гуморального иммунитета, развитие В-клеток и гомеостаз. Однако APRIL связывается с ВСМА со значительно более высокой аффинностью (10-9 М), чем BAFF (10-7 М) (Yu-Tzu Tai ЕТ ALL, APRIL and ВСМА promote human multiple myeloma growth and immunosuppression in the bone marrow microenvironment, Blood, 2016, 127, 25, pp.3225-3236, https://doi.org/10.1182/blood-2016-01-691162).
ВСМА экспрессируется на поздних стадиях дифференцировки В-клеток: плазмобластах и плазмоцитах (плазматических клетках, PC). При множественной миеломе (ММ) экспрессия ВСМА значительно увеличивается на злокачественных плазмоцитах по сравнению с нормальными клетками, а активация ВСМА способствует росту и выживаемости плазматических клеток посредством активации MEK/ERK, AKT, NFκB, JNK, р38 и Elk-1 (Shih-Feng Cho ЕТ ALL, Targeting В Cell Maturation Antigen (BCMA) in Multiple Myeloma: Potential Uses of BCMA-Based Immunotherapy, Front Immunol, 2018, 9, 1821, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6095983).
ВСМА является перспективной мишенью для иммунотерапевтических препаратов при различных онкологических заболеваниях, например, лейкемии, лимфоме или множественной миеломе, т.к. данный антиген отличается ограниченной представленностью и повышенной экспрессией на злокачественных плазматических клетках, по сравнению с нормальными плазмацитами.
В патентных документах WO2012163805, WO2013072406, WO2014089335, WO2017143069 описаны различные антитела к ВСМА.
На данный момент в мире всего одно антитело к ВСМА в составе конъюгата антитела с лекарственным средством одобрено к терапевтическому использованию (белантамаб мафодотин). В связи с вышесказанным, актуальным является создание новых антител, которые специфически связываются с ВСМА.
Раскрытие сущности изобретения
Авторами данной группы изобретений были разработаны антитела, которые специфически связываются с ВСМА, и обладают высокими параметрами аффинности связывания с антигеном ВСМА.
Определения и общие методы
Если иное не определено в настоящем документе, научные и технические термины, используемые в связи с настоящим изобретением, будут иметь значения, которые обычно понятны специалистам в данной области.
Кроме того, если по контексту не требуется иное, термины в единственном числе включают в себя термины во множественном числе, и термины во множественном числе включают в себя термины в единственном числе. Как правило, используемая классификация и методы культивирования клеток, молекулярной биологии, иммунологии, микробиологии, генетики, аналитической химии, химии органического синтеза, медицинской и фармацевтической химии, а также гибридизации и химии белка и нуклеиновых кислот, описанные в настоящем документе, хорошо известны специалистам и широко применяются в данной области. Ферментативные реакции и способы очистки осуществляют в соответствии с инструкциями производителя, как это обычно осуществляется в данной области, или как описано в настоящем документе.
Термин «KD» в данном описании относится к константе аффинности (или константе равновесия), которую получают из отношения Kd к Ka (т.е. Kd/Ka), и ее выражают в виде молярной концентрации (М).
«Аффинность связывания» обычно относится к силе совокупных нековалентных взаимодействий между единичным сайтом связывания молекулы (например, антитела) и ее партнером по связыванию (например, антигеном). Если не указано иначе, «аффинность связывания» относится к внутренней (характерной, истинной) аффинности связывания, которая отражает 1:1 взаимодействие между членами пары связывания (например, антителом и антигеном). Аффинность молекулы X к своему партнеру Y обычно можно представить константой аффинности (KD). Желательно, чтобы величина KD составляла, примерно, 200 нМ, 150 нМ, 100 нМ, 60 нМ, 50 нМ, 40 нМ, 30 нМ, 20 нМ, 10 нМ, 8 нМ, 6 нМ, 4 нМ, 2 нМ, 1 нМ или менее. Аффинность можно измерять обычными методами, известными в уровне техники, включая методы по данному описанию. Низкоаффинные антитела обычно медленно связываются с антигеном и имеют тенденцию легко диссоциировать, тогда как высокоаффинные антитела обычно быстрее связывают антиген и имеют тенденцию дольше оставаться в связанном состоянии. В уровне техники известны различные методы измерения аффинности связывания, любой из этих методов можно использовать для целей настоящего изобретения.
Термин «Kd», «koff» или «kdis» относится к константе скорости диссоциации конкретного взаимодействия связывающей молекулы и антигена. Константу скорости диссоциации koff можно измерить посредством биослойной интерферометрии, например, с помощью системы Octet™.
Термин «Ka», «kon» или «on-rate» относится к константе скорости ассоциации.
Термин «R2» относится к коэффициенту детерминации.
Термин «Response» относится к сигналу связывания антитела с антигеном.
Термин «in vitro» относится к биологическому объекту, биологическому процессу или биологической реакции вне организма, смоделированному в искусственных условиях. Например, рост клеток in vitro должен пониматься как рост клеток в среде вне организма, например, в пробирке, культуральном флаконе или микропланшете.
Термин ED50 (ЕС50) (50% эффективная доза/концентрация) относится к концентрациям препарата, при которых измеряемый биологический эффект достигается на 50% (может включать цитотоксичность).
В настоящем описании и в последующей формуле изобретения, если контекстом не предусмотрено иное, слова «включать» и «содержать» или их вариации, такие как «включает», «включающий», «содержит» или «содержащий», следует понимать как включение указанного целого или группы целых, но не исключение любого другого целого или группы целых.
Антитело
Настоящее изобретение относится к моноклональному антителу или его антигенсвязывающему фрагменту, которое специфически связывается с ВСМА (B-cell maturation antigen; другое название TNFRSF17 и CD269).
Термин «моноклональное антитело» или «mAb» относится к антителу, которое синтезировано и выделено отдельной клональной популяцией клеток.
Антитело по изобретению является рекомбинантным антителом.
Термин «рекомбинантное антитело» означает антитело, которое экспрессируется в клетке или клеточной линии, содержащей нуклеотидную последовательность (нуклеотидные последовательности), которая кодирует антитело, при этом указанная нуклеотидная последовательность (нуклеотидные последовательности) не ассоциирована с клеткой в природе.
В одном из аспектов настоящее изобретение относится к выделенному моноклональному антителу или его антигенсвязывающему фрагменту, которое специфически связывается с ВСМА, включающее:
(а) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 с аминокислотной последовательностью SX1X2MS, где
X1=S или G;
X2=A, L или V;
(ii) CDR2 с аминокислотной последовательностью X3YNGGSDRAGX4X5DSVX6G, где
X3=G или С;
X4=F или Y;
Х5=А или Т;
Х6=Е или K; и
(iii) CDR3 с аминокислотной последовательностью SEQ ID NO: 7;
и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 с аминокислотной последовательностью X7GX8X9SNIGX10X11X12X13VX14, где
X7=S или Т;
X8=S, G или Т;
X9=S, Т, I или R;
Х10=0 или А;
X11=S, Н, N, G или Т;
X12=N, R или Y;
X13=T, А, I или D;
X14=N или Н;
(ii) CDR2 с аминокислотной последовательностью X15X16X17X18RPS, где
X15=N, R, K, S или G;
X16=D, N, G, Т или Н;
X17=S, N или Т;
X18=Q или N; и
(iii) CDR3 с аминокислотной последовательностью X19X20WDX21X22X23X24X25WX26, где
Х19=А или S;
Х20=А, S, Т или V;
X21=G, D, Н или S;
X22=S, D или R;
Х23=L или V;
X24=N, T, R или S;
X25=V, A, G или N;
Х26=М, V или L.
Определение «выделенный», применяемое для описания различных антител по данному описанию, означает антитело, идентифицированное и выделенное и/или регенерированное из клетки или клеточной культуры, в которой оно экспрессируется. Примеси (загрязняющие компоненты) из природной среды представляют собой материалы, которые, как правило, мешают диагностическому или терапевтическому применению полипептида, и могут включать ферменты, гормоны и другие белковые или небелковые растворенные вещества. Обычно выделенный полипептид получают в результате по меньшей мере одной стадии очистки.
Термин «антитело» или «иммуноглобулин» (Ig), как использовано в данном описании, включает целые антитела. Термин «антитело» относится к гликопротеину, содержащему по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, взаимосвязанные дисульфидными связями. Каждая тяжелая цепь содержит вариабельную область тяжелой цепи (сокращенно называемую в данном описании как VH) и константную область тяжелой цепи. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно называемой в данном описании как VL) и константной области легкой цепи. Предпочтительно легкая цепь представляет собой легкую каппа (κ)-цепь, а константный домен CL предпочтительно представляет собой С-каппа (κ).
Антитела согласно изобретению могут представлять собой антитела любого класса (например, IgA, IgD, IgE, IgG и IgM, предпочтительно IgG) или подкласса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2, предпочтительно IgG1).
Области VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые определяющими комплементарность областями (CDR), разбросанные между областями, которые являются более консервативными, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат домен связывания, который взаимодействует с антигеном.
Константные области антител могут опосредовать связывание иммуноглобулина с тканями хозяина или факторами, включая различные клетки иммунной системы (например, эффекторными клетками), и первый компонент (C1q) классической системы комплемента.
Термин «антигенсвязывающая часть» антитела или «антигенсвязывающий фрагмент», как использовано в данном описании, относится к одному или нескольким фрагментам антитела, которые сохраняют способность специфически связываться с антигеном. Было показано, что антигенсвязывающая функция антитела может выполняться фрагментами полноразмерного антитела. Примеры связывающих фрагментов, включенных в термин «антигенсвязывающая часть» антитела включают (i) Fab-фрагмент, одновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) F(ab')2-фрагмент, двухвалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области; (iii) Fd-фрагмент, состоящий из доменов VH и CH1; (iv) Fv-фрагмент, состоящий из доменов VL и VH в едином плече антитела, (v) dAb-фрагмент (Ward et al., (1989) Nature 341:544-546), который состоит из домена VH/VHH. Кроме того, две области Fv-фрагмента, VL и VH, кодируются разными генами, они могут быть соединены при помощи рекомбинантных способов с использованием синтетического линкера, который дает возможность получать их в виде единой белковой цепи, в которой области VL и VH спариваются с образованием одновалентных молекул (известных как одноцепочечный Fv (scFv); см., например, Bird et al. (1988) Science 242:423-426; и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Предполагается, что такие одноцепочечные молекулы также включены в термин «антигенсвязывающая часть» антитела. Такие фрагменты антител получают с использованием общепринятых способов, известных специалистам в данной области, и эти фрагменты подвергают скринингу таким же образом, как и интактные антитела.
«Kabat номенклатура» или «номенклатура по Kabat» применяются в данной заявке к системе нумерации аминокислотных остатков, которые являются более вариабельными (т.е. гипервариабельными), чем остальные аминокислотные остатки в вариабельных участках тяжелой и легкой цепи антитела (Kabat et al. Ann. N.Y. Acad. Sci., 190:382-93 (1971); Kabat et al. Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242(1991)).
Антитело по данному изобретению, «которое специфически связывается» целевой антиген, представляет собой антитело, которое связывает антиген с достаточной аффинностью так, что антитело можно применять в качестве диагностического и/или терапевтического агента при нацеливании на белок или клетку или ткань, экспрессирующую антиген, и в незначительной степени перекрестно реагирует с другими белками.
Термин «специфически связывается с» конкретным полипептидом или эпитопом на конкретном полипептиде-мишени можно характеризовать на примере молекулы, имеющей KD к мишени по меньшей мере около 200 нМ, или же по меньшей мере около 150 нМ, или же по меньшей мере около 100 нМ, или же по меньшей мере около 60 нМ, или же по меньшей мере около 50 нМ, или же по меньшей мере около 40 нМ, или же по меньшей мере около 30 нМ, или же по меньшей мере около 20 нМ, или же по меньшей мере около 10 нМ, или же по меньшей мере около 8 нМ, или же по меньшей мере около 6 нМ, или же по меньшей мере около 4 нМ, или же по меньшей мере около 2 нМ, или же по меньшей мере около 1 нМ или выше.
В одном варианте изобретения термин «специфическое связывание» относится к связыванию, при котором молекула связывается с конкретным полипептидом или эпитопом на конкретном полипептиде, практически не связываясь с каким-либо другим полипептидом или эпитопом на полипептиде.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен тяжелой цепи, который содержит CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен тяжелой цепи, который содержит CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 4, SEQ ID NO: 5 или SEQ ID NO: 6.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен легкой цепи, который содержит CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен легкой цепи, который содержит CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен легкой цепи, который содержит CDR3 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34 или SEQ ID NO: 35.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3;
CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 4, SEQ ID NO: 5 или SEQ ID NO: 6;
и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает:
(i) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7;
(ii) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 1;
(iii) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 3,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7;
(iv) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7;
или
(v) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 6 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15;
CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24;
и
CDR3 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34 или SEQ ID NO: 35.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает:
(i) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 8,
CDR2 с аминокислотной последовательностью SEQ ID NO: 16 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 25;
(ii) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 9,
CDR2 с аминокислотной последовательностью SEQ ID NO: 17 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 26;
(iii) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 10,
CDR2 с аминокислотной последовательностью SEQ ID NO: 18 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 27;
(iv) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 11,
CDR2 с аминокислотной последовательностью SEQ ID NO: 19 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 28;
(v) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 29;
(vi) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 30;
(vii) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 10,
CDR2 с аминокислотной последовательностью SEQ ID NO: 21 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 31;
(viii) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 13,
CDR2 с аминокислотной последовательностью SEQ ID NO: 22 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 32;
(ix) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 14,
CDR2 с аминокислотной последовательностью SEQ ID NO: 23 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 33;
(x) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 8,
CDR2 с аминокислотной последовательностью SEQ ID NO: 24 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 34;
или
(xi) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 15,
CDR2 с аминокислотной последовательностью SEQ ID NO: 17 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 35.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает:
(a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3;
CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 4, SEQ ID NO: 5 или SEQ ID NO: 6;
и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15;
CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24;
и
CDR3 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34 или SEQ ID NO: 35.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает:
(i) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 8,
CDR2 с аминокислотной последовательностью SEQ ID NO: 16 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 25;
(ii) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 9,
CDR2 с аминокислотной последовательностью SEQ ID NO: 17 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 26;
(iii) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 3,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 10,
CDR2 с аминокислотной последовательностью SEQ ID NO: 18 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 27;
(iv) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 11,
CDR2 с аминокислотной последовательностью SEQ ID NO: 19 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 28;
(v) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 29;
(vi) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 6 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 30;
(vii) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 10,
CDR2 с аминокислотной последовательностью SEQ ID NO: 21 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 31;
(viii) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 13,
CDR2 с аминокислотной последовательностью SEQ ID NO: 22 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 32;
(ix) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 30;
(x) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 14,
CDR2 с аминокислотной последовательностью SEQ ID NO: 23 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 33;
(xi) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 8,
CDR2 с аминокислотной последовательностью SEQ ID NO: 24 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 34; или
(xii) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 15,
CDR2 с аминокислотной последовательностью SEQ ID NO: 17 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 35.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 41, SEQ ID NO: 42 или SEQ ID NO: 43.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает вариабельный домен легкой цепи, который содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 48, SEQ ID NO: 49, SEQ ID NO: 50, SEQ ID NO: 51, SEQ ID NO: 52, SEQ ID NO: 53 или SEQ ID NO: 54.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 41, SEQ ID NO: 42 или SEQ ID NO: 43; и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 48, SEQ ID NO: 49, SEQ ID NO: 50, SEQ ID NO: 51, SEQ ID NO: 52, SEQ ID NO: 53 или SEQ ID NO: 54.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающий фрагмент включает:
(i) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 36 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 44;
(ii) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 37 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 45;
(iii) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 38 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 46;
(iv) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 39 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 47;
(v) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 48;
(vi) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 41 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 49;
(vii) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 50;
(viii) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 51;
(ix) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 49;
(x) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 42 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 52;
(xi) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 43 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 53; или
(xii) (а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 54.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой полноразмерное антитело IgG.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой полноразмерное антитело IgG, которое относится к изотипу IgG1, IgG2, IgG3 или IgG4 человека.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой полноразмерное антитело IgG, которое относится к изотипу IgG1 человека.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело содержит мутации L234A и L235A (или L247A и L248A по Kabat) в СН2 согласно нумерации аминокислот антител EU (Edelman G.M. и др., Proc. Natl. Acad. Sci. USA 63, 1969, pp. 78 - 85; Kabat Е.А. и др., Sequences of Proteins of Immunological Interest, 5-ое изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991).
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело включает тяжелую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 55, SEQ ID NO: 56, SEQ ID NO: 57, SEQ ID NO: 58, SEQ ID NO: 59, SEQ ID NO: 60, SEQ ID NO: 61 или SEQ ID NO: 62.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело включает легкую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 65, SEQ ID NO: 66, SEQ ID NO: 67, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 70, SEQ ID NO: 71, SEQ ID NO: 72 или SEQ ID NO: 73.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело включает:
(i) (а) тяжелую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 55, SEQ ID NO: 56, SEQ ID NO: 57, SEQ ID NO: 58, SEQ ID NO: 59, SEQ ID NO: 60, SEQ ID NO: 61 или SEQ ID NO: 62, и
(b) легкую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 65, SEQ ID NO: 66, SEQ ID NO: 67, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 70, SEQ ID NO: 71, SEQ ID NO: 72 или SEQ ID NO: 73.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело включает:
(i) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 55, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 63;
(ii) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 56, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 64;
(iii) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 57, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 65;
(iv) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 58, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 66;
(v) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 67;
(vi) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 60, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 68;
(vii) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 69;
(viii) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59,
и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 70;
(ix) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 68,
(x) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 61, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 71;
(xi) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 62, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 72;
или
(xii) (а) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 73.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-001.
Антитело 01-001 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 55; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 63.
Антитело 01-001 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 36;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 44.
Антитело 01-001 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 1,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 4,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 8,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 16,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 25.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-006. Антитело 01-006 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 56; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 64.
Антитело 01-006 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 37;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 45.
Антитело 01-006 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 5,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 9,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 17,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 26.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-016.
Антитело 01-016 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 57; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 65.
Антитело 01-016 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 38;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 46.
Антитело 01-016 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 3,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 4,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 10,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 18,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 27.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-021.
Антитело 01-021 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 58; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 66.
Антитело 01-021 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 39;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 47.
Антитело 01-021 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 4,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 11,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 19,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 28.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-022.
Антитело 01-022 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 67.
Антитело 01-022 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 48.
Антитело 01-022 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 5,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 12,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 20,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 29.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-024.
Антитело 01-024 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 60; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 68.
Антитело 01-024 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 41;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 49.
Антитело 01-024 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 6,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 12,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 20,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 30.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-025.
Антитело 01-025 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 69.
Антитело 01-025 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 50.
Антитело 01-025 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 5,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 10,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 21,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 31.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-026.
Антитело 01-026 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 70.
Антитело 01-026 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 51.
Антитело 01-026 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 5,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 13,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 22,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 32.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-027.
Антитело 01-027 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 68.
Антитело 01-027 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 49.
Антитело 01-027 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 5,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 12,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 20,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 30.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-030.
Антитело 01-030 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 61; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 71.
Антитело 01-030 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 42;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 52.
Антитело 01-030 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 4,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 14,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 23,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 33.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-033.
Антитело 01-033 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 62; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 72.
Антитело 01-033 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 43;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 53.
Антитело 01-033 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 4,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 8,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 24,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 34.
В некоторых вариантах осуществления изобретения выделенное моноклональное антитело, которое специфично связывается с ВСМА, представляет собой антитело 01-037.
Антитело 01-037 включает:
(a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59; и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 73.
Антитело 01-037 включает:
(a) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 40;
(b) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 54.
Антитело 01-037 включает:
(a) вариабельный домен тяжелой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 2,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 5,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
(i) CDR1 (Kabat) с аминокислотной последовательностью SEQ ID NO: 15,
(ii) CDR2 (Kabat) с аминокислотной последовательностью SEQ ID NO: 17,
(iii) CDR3 (Kabat) с аминокислотной последовательностью SEQ ID NO: 35.
Молекула нуклеиновой кислоты
В одном из аспектов настоящее изобретение относится к нуклеиновой кислоте, которая кодирует любое вышеуказанное антитело или его антигенсвязывающий фрагмент которое специфически связывается с ВСМА.
В любом из указанных вариантов осуществления изобретения молекулы нуклеиновых кислот могут быть выделенными.
Термины «нуклеиновая кислота», «нуклеиновая последовательность» или «нуклеиновокислотная последовательность», «полинуклеотид», «олигонуклеотид», «полинуклеотидная последовательность» и «нуклеотидная последовательность», которые используются равнозначно в данном описании, обозначают четкую последовательность нуклеотидов, модифицированных или не модифицированных, определяющую фрагмент или участок нуклеиновой кислоты, содержащую или не содержащую неприродные нуклеотиды и являющуюся либо двухцепочечной ДНК или РНК, либо одноцепочечной ДНК или РНК, либо продуктами транскрипции указанных ДНК.
Термин нуклеотидная последовательность охватывает его комплемент, если не указано иное. Таким образом, нуклеиновую кислоту, имеющую определенную последовательность следует понимать как охватывающие ее комплементарную цепь с ее комплементарной последовательностью.
«Выделенная» молекула нуклеиновой кислоты представляет собой молекулу нуклеиновой кислоты, которая идентифицирована и отделена от по меньшей мере одной молекулы нуклеиновой кислоты-примеси. Выделенная молекула нуклеиновой кислоты отличается от той формы или набора, в которых она находится в естественных условиях. Таким образом, выделенная молекула нуклеиновой кислоты отличается от молекулы нуклеиновой кислоты, существующей в клетках в естественных условиях.
В одном из аспектов настоящее изобретение относится к молекуле нуклеиновой кислоты, содержащей нуклеотидную последовательность, которая кодирует аминокислотную последовательность, выбранную из SEQ ID NO: 1-73. Молекула нуклеиновой кислоты может также содержать любую комбинацию указанных нуклеотидных последовательностей.
Специалисту в данной области будет очевидно, что аминокислотная последовательность легкой или тяжелой цепи антитела по изобретению или их фрагментов (VH, VL, CDR и так далее) может быть кодирована широким рядом различных ДНК-последовательностей с учетом вырожденности генетического кода. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота представляет собой ДНК.
Молекула нуклеиновой кислоты по данному изобретению может быть выделена из любого источника, который продуцирует моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА. В определенных вариантах осуществления изобретения молекула нуклеиновой кислоты по данному изобретению может быть синтезирована путем химического синтеза, а не выделена.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-001, и включает нуклеотидную последовательность с SEQ ID NO: 74.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-001, и включает нуклеотидную последовательность с SEQ ID NO: 82.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-001, и включает нуклеотидную последовательность с SEQ ID NO: 93.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-001, и включает нуклеотидную последовательность с SEQ ID NO: 101.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-006, и включает нуклеотидную последовательность с SEQ ID NO: 75.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-006, и включает нуклеотидную последовательность с SEQ ID NO: 83.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-006, и включает нуклеотидную последовательность с SEQ ID NO: 94.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-006, и включает нуклеотидную последовательность с SEQ ID NO: 102.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-016, и включает нуклеотидную последовательность с SEQ ID NO: 76.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-016, и включает нуклеотидную последовательность с SEQ ID NO: 84.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-016, и включает нуклеотидную последовательность с SEQ ID NO: 95.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-016, и включает нуклеотидную последовательность с SEQ ID NO: 103.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-021, и включает нуклеотидную последовательность с SEQ ID NO: 77.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-021, и включает нуклеотидную последовательность с SEQ ID NO: 85.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-021, и включает нуклеотидную последовательность с SEQ ID NO: 96.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-021, и включает нуклеотидную последовательность с SEQ ID NO: 104.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-022, и включает нуклеотидную последовательность с SEQ ID NO: 78.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-022, и включает нуклеотидную последовательность с SEQ ID NO: 86.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-022, и включает нуклеотидную последовательность с SEQ ID NO: 97.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-022, и включает нуклеотидную последовательность с SEQ ID NO: 105.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-024, и включает нуклеотидную последовательность с SEQ ID NO: 79.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-024, и включает нуклеотидную последовательность с SEQ ID NO: 87.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-024, и включает нуклеотидную последовательность с SEQ ID NO: 98.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-024, и включает нуклеотидную последовательность с SEQ ID NO: 106.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-025, и включает нуклеотидную последовательность с SEQ ID NO: 78.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-025, и включает нуклеотидную последовательность с SEQ ID NO: 88.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-025, и включает нуклеотидную последовательность с SEQ ID NO: 97.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-025, и включает нуклеотидную последовательность с SEQ ID NO: 107.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-026, и включает нуклеотидную последовательность с SEQ ID NO: 78.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-026, и включает нуклеотидную последовательность с SEQ ID NO: 89.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-026, и включает нуклеотидную последовательность с SEQ ID NO: 97.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-026, и включает нуклеотидную последовательность с SEQ ID NO: 108.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-027, и включает нуклеотидную последовательность с SEQ ID NO: 78.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-027, и включает нуклеотидную последовательность с SEQ ID NO: 87.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-027, и включает нуклеотидную последовательность с SEQ ID NO: 97.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-027, и включает нуклеотидную последовательность с SEQ ID NO: 106.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-030, и включает нуклеотидную последовательность с SEQ ID NO: 80.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-030, и включает нуклеотидную последовательность с SEQ ID NO: 90.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-030, и включает нуклеотидную последовательность с SEQ ID NO: 99.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-030, и включает нуклеотидную последовательность с SEQ ID NO: 109.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-033, и включает нуклеотидную последовательность с SEQ ID NO: 81.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-033, и включает нуклеотидную последовательность с SEQ ID NO: 91.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-033, и включает нуклеотидную последовательность с SEQ ID NO: 100.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-033, и включает нуклеотидную последовательность с SEQ ID NO: 110.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена тяжелой цепи антитела 01-037, и включает нуклеотидную последовательность с SEQ ID NO: 78.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность вариабельного домена легкой цепи антитела 01-037, и включает нуклеотидную последовательность с SEQ ID NO: 92.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность тяжелой цепи антитела 01-037, и включает нуклеотидную последовательность с SEQ ID NO: 97.
В некоторых вариантах осуществления изобретения нуклеиновая кислота представляет собой нуклеиновую кислоту, которая кодирует аминокислотную последовательность легкой цепи антитела 01-037, и включает нуклеотидную последовательность с SEQ ID NO: 111.
Молекулы нуклеиновой кислоты могут использоваться для экспрессии рекомбинантного моноклонального антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА.
Вектор
В одном из аспектов настоящее изобретение относится к экспрессионному вектору, содержащему любую из вышеуказанных молекул нуклеиновых кислот, которые кодируют соответствующие аминокислотные последовательности антитела, которое специфически связывается с ВСМА, или его части (например, последовательностей связывающих доменов тяжелой цепи и/или легкой цепи). Настоящее изобретение относится к вектору, подходящему для экспрессии любой из нуклеотидных последовательностей, описанных в настоящем документе.
Термин «вектор» при использовании в настоящем документе означает молекулу нуклеиновой кислоты, способную транспортировать другую нуклеиновую кислоту, с которой она соединена.
Как применяют в настоящем описании, термин «экспрессия» определяют как транскрипцию и/или трансляцию конкретной нуклеотидной последовательности, запускаемую ее промотором.
В некоторых вариантах осуществления изобретения вектор представляет собой плазмиду, т.е. кольцевую двухцепочечную часть ДНК, в которую могут быть вставлены дополнительные сегменты ДНК.
В некоторых вариантах осуществления изобретения вектор представляет собой вирусный (экспрессионный) вектор, в котором дополнительные сегменты ДНК могут быть вставлены в вирусный геном.
В некоторых вариантах осуществления изобретения векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, имеющие бактериальный сайт инициации репликации и эписомные векторы). В других вариантах осуществления изобретения векторы (например, неэписомальные векторы) могут быть интегрированы в геном клетки-хозяина при введении в клетку-хозяина, и таким образом реплицируются вместе с геном хозяина. Более того, некоторые векторы способны направлять экспрессию генов, с которыми они функционально соединены. Такие векторы упоминаются в данном документе как «рекомбинантные экспрессирующие векторы» (или просто «экспрессирующие векторы» («вектор экспрессии» или «экспрессионный вектор»)).
В некоторых вариантах осуществления изобретения экспрессионные векторы включают плазмиды, ретровирусы, аденовирусы, аденоассоциированные вирусы (AAV), вирусы растений, такие как вирус мозаики цветной капусты, вирусы табачной мозаики, космиды, YAC и тому подобное. Молекулы ДНК могут быть вставлены в вектор таким образом, что последовательности, контролирующие транскрипцию и трансляцию в векторе, выполняют предусмотренную функцию регуляции транскрипции и трансляции ДНК. Экспрессионный вектор и последовательности контроля экспрессии могут быть выбраны таким образом, чтобы быть совместимыми с используемой экспрессирующей клеткой-хозяином.
В одном варианте осуществления изобретения молекулы ДНК, кодирующие частично или по всей длине последовательности первого и второго связывающих доменов (например, последовательности тяжелой и легкой цепи, где связывающий домен содержит последовательность тяжелой и легкой цепи) могут быть введены в отдельные векторы.
В одном варианте осуществления изобретения любая комбинация указанных выше молекул ДНК вводится в тот же экспрессионный вектор.
В одном варианте осуществления изобретения молекулы ДНК могут быть введены в экспрессионный вектор стандартными способами (например, лигированием комплементарных сайтов рестрикции на фрагменте гена антитела и вектора или лигированием тупых концов, если сайты рестрикции отсутствуют).
В некоторых вариантах осуществления изобретения подходящим вектором является тот, который включает места рестрикции так, что любая последовательность VH или VL может быть легко включена и экспрессирована, как описано выше. Прекращение полиаденилирования и транскрипции может произойти вниз по ходу сайта нативной хромосомы кодируемых участков. Рекомбинантный экспрессионный вектор также может кодировать сигнальный пептид, который облегчает выработку цепочки антитела клеткой-хозяином. Ген цепочки антитела может быть клонирован в вектор таким образом, что сигнальный пептид соединен с рамкой считывания аминоконца цепи иммуноглобулина. Сигнальным пептидом может быть сигнальный пептид иммуноглобулина или гетерологичный сигнальный пептид (то есть, сигнальный пептид белка не иммуноглобулиновой природы).
В некоторых вариантах осуществления изобретения вектор может включать последовательность контроля экспрессии. Термин «последовательность контроля экспрессии», используемый в данном описании, означает полинуклеотидные последовательности, которые необходимы для воздействия на экспрессию и процессинг кодирующих последовательностей, к которым они вставлены. Специалистам в этой области будет понятно, что дизайн экспрессионного вектора, включая выбор последовательностей контроля экспрессии, может зависеть от таких факторов, как выбор типа клетки-хозяина для трансформации, требуемый уровень экспрессии антитела, и т.д. Контролирующие экспрессию последовательности включают соответствующие последовательности инициации транскрипции, терминации, промотора и энхансера; эффективные сигналы процессинга РНК, такие как сплайсинг и сигналы полиаденилирования; последовательности, которые стабилизируют цитоплазматическую мРНК; последовательности, которые повышают эффективность трансляции (т.е. консенсусная последовательность Козака); последовательности, которые повышают стабильность белка; и, при желании, последовательности, которые усиливают секрецию белка. Характер таких последовательностей контроля экспрессии различается в зависимости от организма-хозяина; в прокариотах такие последовательности контроля экспрессии, как правило, включают промотор, сайт связывания рибосомы, а также последовательности терминации транскрипции; в эукариотах, как правило, такие последовательности контроля экспрессии включают промоторы и последовательности терминации транскрипции. Предпочтительные последовательности контроля экспрессии для экспрессирующей клетки-хозяина млекопитающего включают вирусные элементы обеспечивающие высокий уровень экспрессии белков в клетках млекопитающих, таких как промоторы и/или энхансеры, полученные из ретровирусной LTR, цитомегаловируса (CMV) (например, CMV промотора/энхансера), обезьяньего вируса 40 (SV40) (например, SV40 промотора/энхансера), аденовируса, (например, большого позднего промотора аденовируса (AdMLP)), вирус полиомы, а также сильных промоторов млекопитающих, таких как TTR промотор, промотор нативных иммуноглобулинов или промотор актина. Последовательности контроля экспрессии включают, как минимум, все компоненты, наличие которых имеет важное значение для экспрессии и процессинга.
В некоторых вариантах осуществления изобретения в дополнение к генам цепи антитела и последовательностям контроля экспрессии, рекомбинантные векторы экспрессии изобретения могут нести дополнительные последовательности, такие как последовательности, которые регулируют репликацию вектора в клетках-хозяевах (например, точки начала репликации) и гены селектируемого маркера. Ген селектируемого маркера облегчает селекцию клеток-хозяев, в которые был введен вектор.
Клетка-хозяин
В одном из аспектов настоящее изобретение относится к способу получения клетки-хозяина для получения любого вышеуказанного антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, и включает трансформирование клетки вышеуказанным вектором.
В одном из аспектов настоящее изобретение относится к клетке-хозяину для получения любого вышеуказанного антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, которая содержит любую из вышеуказанных нуклеиновых кислот.
Термин «клетка-хозяин» при использовании в данном документе означает клетку, в которую введен рекомбинантный экспрессионный вектор. Настоящее изобретение относится к клеткам-хозяевам, которые могут включать, например, вектор в соответствии с настоящим изобретением, описанным выше. Настоящее изобретение относится также к клеткам-хозяевам, которые включают, например, нуклеотидную последовательность, кодирующую тяжелую цепь или ее антигенсвязывающие части, нуклеотидную последовательность, кодирующую легкую цепь или ее антигенсвязывающие части, или обе из них. Следует понимать, что «клетка-хозяин» означают не только конкретную заявленную клетку, но также и потомство такой клетки. Поскольку модификации могут проходить в последующих поколениях вследствие мутации или воздействий окружающей среды, такое потомство не может, на самом деле, быть идентичным родительской клетке, но такие клетки по-прежнему включены в объем термина «клетка-хозяин» при использовании в настоящем документе.
Молекулы нуклеиновой кислоты, кодирующие моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, по изобретению и векторы, содержащие эти молекулы нуклеиновой кислоты, могут быть использованы для трансфекции клетки млекопитающего, клетки растения, бактериальной клетки или дрожжевой клетки. Трансфекция может происходить любым известным способом для введения полинуклеотидов в клетку хозяина. Способы введения гетерологичных полинуклеотидов в клетки млекопитающих хорошо известны в данной области и включают декстран опосредованную трансфекцию, трансфекцию комплексом нуклеиновой кислоты и позитивно заряженного полимера, трансфекцию преципитатом нуклеиновой кислоты и фосфата кальция, полибрен опосредованную трансфекцию, слияние протопластов, трансфекцию инкапсулированными в липосомы полинуклеотидами и прямую микроинъекцию ДНК в ядра. В дополнение молекулы нуклеиновых кислот могут быть введены в клетки млекопитающих вирусными (экспрессионными) векторами.
Клеточные линии млекопитающих, используемые в качестве хозяев для трансформации, хорошо известны в данной области и включают множество иммортализованных доступных клеточных линий. К ним относятся, например, клетки яичников китайского хомячка (СНО), NS0 клетки, клетки SP2, HEK-293Т клетки, 293 Фристайл клетки (Invitrogen), NIH-3T3 клетки, клетки HeLa, клетки почек хомячка (BHK), клетки почек африканских зеленых мартышек (COS), клетки гепатоцеллюлярной карциномы человека (например, Hep G2), А549, SK-HEP1, HUH7, Hep-RG клетки и ряд других клеточных линий. Клеточные линии выбираются путем определения, какие клеточные линии имеют высокие уровни экспрессии и обеспечивают необходимые характеристики продуцируемого белка. Другими клеточными линиями, которые могут быть использованы, являются клеточные линии насекомых, такие как Sf9 или Sf21 клетки. Когда векторы рекомбинантной экспрессии, кодирующие моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, вводятся в клетки-хозяева млекопитающих, антитела или их фрагменты продуцируются путем культивирования клеток-хозяев в течение времени, достаточного для экспрессии антител или их фрагментов в клетках-хозяевах или, предпочтительнее, выделения антител или их фрагментов в питательную среду, в которой выращиваются клетки-хозяева. Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может быть выделено из питательной среды с использованием стандартных методов очистки белка. Клетки-хозяева растений, например, включают Nicotiana, Arabidopsis, ряску, кукурузу, пшеницу, картофель и т.д. Клетки бактерий хозяина включают виды Escherichia и Streptomyces. Дрожжевые клетки-хозяева включают Schizosaccharomyces pombe, Saccharomyces cerevisiae и Pichia pastoris.
Кроме того, уровень продукции моноклонального антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, из продуцирующей клеточной линии можно усилить с помощью ряда известных методов. Например, система экспрессии гена глутамин синтетазы (система GS) является достаточно распространенной для усиления экспрессии при определенных условиях.
Вполне вероятно, что моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, различных клеточных линий будут отличаться друг от друга профилем гликозилирования. Однако моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, кодируемые молекулами нуклеиновой кислоты, описанными в данном документе, или содержащее аминокислотные последовательности, приведенные в настоящем документе, являются частью данного изобретения, независимо от состояния гликозилирования связывающих молекул и в целом, независимо от наличия или отсутствия пост-трансляционных модификаций.
Вышеуказанная клетка-хозяин не относится к клетке-хозяину, полученной с использованием человеческих эмбрионов.
Вышеуказанная клетка-хозяин не относится к клетке-хозяину, полученной с модификации генетической целостности клеток зародышевой линии человека.
Способ получения антитела
В одном из аспектов настоящее изобретение относится к способу получения антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, заключающемуся в культивировании описанной выше клетки-хозяина в культуральной среде в условиях, достаточных для получения указанного антитела или его фрагмента, при необходимости, с последующим выделением и очисткой полученного антитела или его фрагмента.
Фармацевтические композиции
Другим аспектом изобретения является фармацевтическая композиция, содержащая в качестве активного ингредиента (или в качестве единственного активного ингредиента) моноклональное антитело по настоящему изобретению или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА.
В одном из аспектов настоящее изобретение относится к фармацевтической композиции для лечения заболевания или нарушения, опосредованного ВСМА, которая содержит любое вышеуказанное антитело или его антигенсвязывающий фрагмент в терапевтически эффективном количестве в сочетании с одним или несколькими фармацевтически приемлемыми эксципиентами.
«Фармацевтическая композиция» обозначает композицию, включающую в себя антитело согласно изобретению и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки.
Термин «фармацевтически приемлемый» означает один или несколько совместимых жидких или твердых компонентов, которые подходят для введения млекопитающему, предпочтительно человеку.
Термин «эксципиент» или «вспомогательное вещество» используется в данном документе для описания любого компонента, отличающегося от антитела по данному изобретению. Это вещества неорганического или органического происхождения, используемые в процессе производства, изготовления лекарственных препаратов для придания им необходимых физико-химических свойств.
В некоторых вариантах осуществления композиции предназначены для улучшения, профилактики или лечения заболеваний или нарушений, которые могут быть опосредованы ВСМА.
Термин «заболевание или нарушение, опосредованное ВСМА», подразумевает все заболевания или нарушения, которые либо прямо, либо косвенно связаны с ВСМА, включая этиологию, развитие, прогресс, персистентность или патологию заболевания или нарушения.
«Лечить», «лечение» и «терапия» относятся к методу смягчения или устранения биологического расстройства и/или по меньшей мере одного из сопутствующих ему симптомов. Кроме того, содержащиеся в данном документе ссылки на «лечение» включает ссылки на лечебную, паллиативную и профилактическую терапию.
Термин «нарушение» означает любое состояние, которое можно улучшить в результате лечения по настоящему изобретению. В определение данного термина входят хронические и острые нарушения или заболевания, включающие в себя патологические состояния, которые вызывают предрасположенность млекопитающего к возникновению данного нарушения.
«Терапевтически эффективным количеством» считается количество вводимого в процессе лечения терапевтического агента, которое избавит в определенной степени от одного или нескольких симптомов заболевания, по поводу которого проводится лечение. Терапевтически эффективное количество может изменяться в зависимости от таких факторов, как конкретное состояние, по поводу которого проводится лечение, возраста, пола и веса пациента, а также является ли введение моноклонального антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, самостоятельным лечением или оно проводится в комбинации с одним или более дополнительных препаратов или методов лечения.
В одном аспекте субъект лечения или пациент является млекопитающим, предпочтительно человеческим субъектом. Вышеупомянутый субъект может быть мужского или женского пола любого возраста.
Фармацевтические композиции по настоящему изобретению и способы их изготовления будут бесспорно очевидными для специалистов в этой области. Производство фармацевтических композиций предпочтительно должно соответствовать требованиям GMP (надлежащей производственной практики).
В некоторых вариантах осуществления фармацевтической композиции она может включать буферную композицию, тонические агенты (осмолитик или осмотический агент), стабилизаторы и/или солюбилизаторы.
Фармацевтическая композиция по изобретению является стабильной.
Фармацевтическая композиция является «стабильной», если активный агент сохраняет свою физическую стабильность и/или химическую стабильность и/или биологическую активность в течение заявленного срока годности при температуре хранения, например, при 2-8°С. Предпочтительно, чтобы активный агент сохранял и физическую, и химическую стабильность, а также биологическую активность. Период хранения выбирается на основании результатов исследования стабильности при ускоренном и естественном хранении.
Фармацевтическая композиция по настоящему изобретению пригодна для парентерального введения в виде стерильных лекарственных средств, предназначенных для введения в организм субъекта с нарушением целостности кожных покровов или слизистых оболочек, минуя желудочно-кишечный тракт путем инъекций, инфузий или имплантации. В частности, предполагается, что парентеральное введение включает, помимо прочего, подкожную, внутрибрюшинную, внутримышечную, внутривенную, внутриартериальную, интратекальную, внутрижелудочковую, интрауретральную, внутричерепную, внутрисуставнную, трансдермальную инъекцию или инфузию; и почечные диализные инфузионные методики. Внутриопухолевая доставка, например, внутриопухолевая инъекция, также может быть применима. Также предусмотрена региональная перфузия.
В некоторых вариантах осуществления фармацевтическую композицию вводят внутривенно.
В некоторых вариантах осуществления внутривенное введение проводят при помощи инфузии, пролонгированной инфузии или длительной непрерывной инфузии.
В некоторых вариантах осуществления фармацевтическую композицию вводят подкожно.
В некоторых вариантах осуществления подкожное введение проводят при помощи подкожной инъекции.
В некоторых вариантах осуществления фармацевтическая композиция представляет собой инъекционную лекарственную форму.
В некоторых вариантах осуществления инъекционная лекарственная форма представляет собой раствор для инфузии.
В некоторых вариантах осуществления инъекционная лекарственная форма представляет собой раствор для подкожного введения.
Инъекционные лекарственные формы могут быть изготовлены в стандартной лекарственной форме, например, в ампулах, флаконах, полимерных контейнерах, преднаполненных шприцах, устройствах для автоинжекции, но, не ограничиваясь ими.
В некоторых вариантах осуществления фармацевтическая композиция представляет собой фармацевтическую композицию, предоставленную в сухой форме, то есть, порошка или гранул для растворения в подходящем растворителе (например, стерильной апирогенной воде) перед введением. Такое лекарственное средство может быть получено, например, с помощью лиофилизации, т.е. процесса, известного в данной области техники как сушка из замороженного состояния, включающая в себя замораживание препарата и последующее удаление растворителя из замороженного содержимого.
В некоторых вариантах осуществления фармацевтическая композиция представляет собой лиофилизат для приготовления раствора для инфузии.
В некоторых вариантах осуществления фармацевтическая композиция представляет собой лиофилизат для приготовления раствора для подкожного введения.
В некоторых вариантах осуществления фармацевтическая композиция представляет собой концентрат для приготовления раствора для инфузии.
В некоторых вариантах осуществления фармацевтическая композиция представляет собой концентрат для приготовления раствора для подкожного введения.
В одном из аспектов настоящее изобретение относится к фармацевтической композиции, которая содержит моноклональное антитело по настоящему изобретению или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, и по меньшей мере одно другое терапевтически активное соединение.
В одном из аспектов настоящее изобретение относится к фармацевтической композиции для лечения заболевания или нарушения, опосредованного ВСМА, которая содержит любое вышеуказанное антитело или его антигенсвязывающий фрагмент и по меньшей мере одно другое терапевтически активное соединение.
В одном из аспектов настоящее изобретение относится к фармацевтической, которая содержит любое вышеуказанное антитело или его антигенсвязывающий фрагмент и, дополнительно, по меньшей мере одно другое терапевтически активное соединение.
В одном из аспектов настоящее изобретение относится к фармацевтической композиции для лечения заболевания или нарушения, опосредованного ВСМА, которая содержит любое вышеуказанное антитело или его антигенсвязывающий фрагмент и, дополнительно, по меньшей мере одно другое терапевтически активное соединение.
В одном из аспектов настоящее изобретение относится к фармацевтической композиции для лечения заболевания или нарушения, опосредованного ВСМА, которая содержит любое вышеуказанное антитело или его антигенсвязывающий фрагмент и по меньшей мере одно другое терапевтически активное соединение, которое представляет собой антитело, малую молекулу, средство для гормональной терапии или их комбинация.
В некоторых вариантах осуществления фармацевтической композиции заболевание или нарушение, опосредованное ВСМА, выбрано из группы: множественная миелома, хронический лимфолейкоз, острый В-лимфобластный лейкоз, неходжкинская лимфома, лимфома Ходжкина.
Терапевтическое применение моноклоналъного антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА
В одном аспекте антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, применяется в лечении нарушений, опосредованного с активностью с ВСМА.
В одном аспекте субъект лечения или пациент является млекопитающим, предпочтительно человеческим субъектом. Вышеупомянутый субъект может быть мужского или женского пола и любого возраста.
В одном из аспектов настоящее изобретение относится к способу лечения заболевания или нарушения, опосредованного ВСМА, включающий введение субъекту, нуждающемуся в таком лечении, любого вышеуказанного антитела или его антигенсвязывающего фрагмента или вышеуказанной фармацевтической композиции в терапевтически эффективном количестве.
В одном из аспектов настоящее изобретение относится к способу лечения заболевания или нарушения, опосредованного ВСМА, включающий введение субъекту, нуждающемуся в таком лечении, любого вышеуказанного антитела или его антигенсвязывающего фрагмента и по меньшей мере одно другого терапевтически активного соединения в терапевтически эффективном количестве.
В некоторых вариантах осуществления способа лечения заболевание или нарушение, опосредованное ВСМА, выбрано из группы: множественная миелома, хронический лимфолейкоз, острый В-лимфобластный лейкоз, неходжкинская лимфома, лимфома Ходжкина.
В некоторых вариантах осуществления способа лечения другое терапевтически активное соединение представляет собой антитело, малую молекулу, средство для гормональной терапии или их комбинация.
В одном из аспектов настоящее изобретение относится к применению вышеуказанного антитела или его антигенсвязывающего фрагмента или вышеуказанной фармацевтической композиции для лечения у субъекта, нуждающегося в таком лечении, заболевания или нарушения, опосредованного ВСМА.
В одном из аспектов настоящее изобретение относится к применению вышеуказанного антитела или его антигенсвязывающего фрагмента и по меньшей мере одно другого терапевтически активного соединения для лечения заболевания или нарушения, опосредованного ВСМА.
В некоторых вариантах осуществления применения заболевание или нарушение, опосредованное ВСМА, выбрано из группы: множественная миелома, хронический лимфолейкоз, острый В-лимфобластный лейкоз, неходжкинская лимфома, лимфома Ходжкина.
В некоторых вариантах осуществления применения другое терапевтически активное соединение представляет собой антитело, малую молекулу, средство для гормональной терапии или их комбинация.
Используемые в данном документе применения или способы, относящиеся к антителу или его антигенсвязывающему фрагменту, которое специфически связывается с ВСМА, с одним или более другими терапевтическими агентами, как предполагают, означают, ссылаются или включают:
1) одновременное введение такой комбинации антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы вместе в одной лекарственной форме, из которой указанные компоненты высвобождаются практически одновременно указанному пациенту,
2) одновременное введение такой комбинации антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы отдельно в разных лекарственных формах, введение которых происходит практически в одно и то же время указанному пациенту, после чего указанные компоненты высвобождаются практически одновременно указанному пациенту,
3) последовательное введение такой комбинации антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы отдельно друг от друга в отдельных лекарственных формах, которые принимаются в последовательно по времени указанным пациентом со значимым временным интервалом между каждым введением, после чего указанные компоненты высвобождаются в практически разное время указанному пациенту; а также
4) последовательное введение такой комбинации антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы вместе в единый лекарственной форме, из которой высвобождение указанных компонентов происходит контролируемым образом, после чего они одновременно, последовательно или совместно высвобождаются в одно и то же время и/или разное время указанному пациенту, где каждая часть может быть введена одним или разными путями.
Антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться без дополнительного терапевтического лечения, т.е. в качестве самостоятельной терапии.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с ингибиторы протеасом.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с противоопухолевыми иммуномодуляторами (например, леналидомид, помалидомид).
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с цитостатической химиотерапией (циклофосфамид, этопозид и др.).
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с тирозинкиназными ингибиторами.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с препаратами ингибиторами BCL2.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с препаратами антагонистами экспортина 1.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с глюкокортикостеройдами.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с противоопухолевыми моноклональными антителами (например, даратамумаб).
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с таргетной терапией.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с моноклональными антителами агонистами цитокинов (например, IL15SA, IL2).
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с моноклональными антителами антагонистами цитокинов (например, anti-IL6R, anti-TNF).
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комбинации с препаратами Г-КСФ (Гранулоцитарный колониестимулирующий фактор).
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комплексе трансплантацией гемопоэтических стволовых клеток.
В некоторых вариантах осуществления способа лечения или применения антитело или его антигенсвязывающий фрагмент, которое специфически связывается с ВСМА, может назначаться в комплексе с лучевой терапией.
В некоторых вариантах осуществления способа лечения или применения подходящая доза моноклонального антитела или его антигенсвязывающего фрагмента, которое специфически связывается с ВСМА, по данному изобретению будет в диапазоне от 0,1-200 мг/кг.
Краткое описание чертежей
Фигура 1 представляет собой карту экспрессиоиного вектора, несущего генетическую последовательность вариабельных доменов.
Фигура 2 представляет собой карту экспрессионного вектора, несущего генетическую последовательность вариабельных доменов.
Фигура 3 представляет собой карту вектора, несущего генетическую последовательность тяжелой цепи антитела.
Фигура 4 представляет собой карту вектора, несущего генетическую последовательность легкой цепи антитела.
Фигура 5 представляет собой электрофореграмму кандидатов 01, 06, 016, 021 и 022 в полиакриламидном геле 7,5% в денатурирующих нередуцирующих условиях после первой стадии очистки на сорбенте с Protein А.
М - маркер молекулярного веса.
1 - кандидат 01.
2 - кандидат 06.
3 - кандидат 016.
4 - кандидат 021.
5 - кандидат 022
Фигура 6 представляет собой электрофореграмму кандидатов 024, 025, 026, 027, 030, 033 и 037 в полиакриламидном геле 7,5% в денатурирующих нередуцирующих условиях после первой стадии очистки на сорбенте с Protein А.
М - маркер молекулярного веса.
1 - кандидат 024.
2 - кандидат 025.
3 - кандидат 026.
4 - кандидат 027.
5 - кандидат 030.
6 - кандидат 033.
7 - кандидат 037. Примеры
Для наилучшего понимания изобретения приводятся следующие примеры. Эти примеры приведены только в иллюстративных целях и не должны толковаться как ограничивающие сферу применения изобретения в любой форме.
Все публикации, патенты и патентные заявки, указанные в этой спецификации включены в данный документ путем отсылки. Хотя вышеупомянутое изобретение было довольно подробно описано путем иллюстрации и примера в целях исключения двусмысленного толкования, специалистам в данной области на основе идей, раскрытых в данном изобретении, будет вполне понятно, что могут быть внесены определенные изменения и модификации без отклонения от сущности и объема прилагаемых вариантов осуществления изобретения.
Материалы и общие методы
Общая информация, касающаяся нуклеотидных последовательностей легких и тяжелых цепей человеческого иммуноглобулина, представлена у: Kabat Е.А. и др., Sequences of Proteins of Immunological Interest, 5-ое изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991. Аминокислоты цепей антител пронумерованы согласно нумерации EU (Edelman G.M. и др., Proc. Natl. Acad. Sci. USA 63, 1969, ее. 78- 85; Kabat Е.А. и др., Sequences of Proteins of Immunological Interest, 5-ое изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991).
Методы рекомбинантной ДНК
Для манипуляций с ДНК использовали стандартные методы, описанные у Sambrook J. и др., Molecular cloning: A laboratory manual; Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, 1989. Реагенты для молекулярной биологии использовали согласно инструкциям производителей.
Синтез генов
Требуемые сегменты генов получали из олигонуклеотидов, созданных путем химического синтеза. Генные сегменты длиной от 300 до 1400 п. н., которые фланкированы уникальными сайтами рестрикции, собирали путем отжига и лигирования олигонуклеотидов, включая ПНР-амплификацию и последующее клонирование через сайты рестрикции. Последовательности ДНК субклонированных генных фрагментов подтверждали путем секвенирования ДНК.
Определение последовательностей ДНК
Последовательности ДНК определяли путем секвенирования по Сенгеру.
Анализ последовательностей ДНК и белков и обработка данных о последовательностях
Применяли пакет программ фирмы Unipro UGENE версия 1.29 и SnapGene Viewer для создания, картирования, анализа, аннотирования и иллюстрации последовательностей.
Экспрессионные векторы
Для экспрессии описанных в материалах заявки антител применяли варианты экспрессионных плазмид, предназначенных для экспрессии антител в клетках прокариот (E.coli) кратковременной экспрессии в клетках эукариот (например, в клетках СНО). Помимо экспрессионной кассеты антитела векторы содержали: сайт инициации репликации, обеспечивающий репликацию указанной плазмиды в E.coli, гены, придающие устойчивость в E.coli к различным антибиотикам (например, к ампициллину, канамицину).
Слияние генов, содержащих описанные цепи антитела, как указано ниже, осуществляли с помощью ПЦР и/или синтеза и сборки генов с использованием известных методов и процедур рекомбинации путем соединения соответствующих сегментов нуклеиновых кислот, например, с использованием уникальных сайтов рестрикции в соответствующих векторах. Субклонированные нуклеотидные последовательности подтверждали секвенированием ДНК. Для кратковременных трансфекций создавали большие количества плазмид посредством получения плазмид из трансформированных культур Е. coli.
Пример 1. Продукция рекомбинантных антигенов в суспензионной культуре клеток млекопитающих
Последовательности экстраклеточных доменов человека рецептора ВСМА (SEQ https://www.uniprot.org/uniprot/Q02223 (1-54 а.к)) клонировали в плазмиды рЕЕ для наработки белка в клетках млекопитающих с тагами TEV-Fc, Avi-His, Avi-His-TEV-HSA по сайтам рестрикции Sa1I/NotI. Плазмиды нарабатывали в необходимых количествах в клетках E.Coli и очищали при помощи набора Qiagen.
Антигены продуцировали в клетках постоянной клеточной линии, полученной из клеток яичника китайского хомячка (линия СНО-Т). Суспензионное культивирование осуществляли в колбах на орбитальном шейкере-инкубаторе. Для экспрессии целевых антигенов, клетки трансфецировали с помощью линейного полиэтиленимина. Через 9 дней после трансфекций культуральную жидкость отделяли от клеток фильтрацией через глубинный фильтр с размером пор 0,5/0,22 мкм.
Антиген BCMA-TEV-Fc из культуральной жидкости выделяли и очищали, используя колонку с сорбентом для аффинной хроматографии с Protein А. Осветленную культуральную жидкость пропускали через колонку, уравновешенную фосфатно-солевым буфером (ФСБ, рН 7,4). Связанный антиген элюировали, используя 0,1 М глициновый буфер рН 2.5. Далее полученный целевой белок переводили в ФСБ (рН 7,4) с помощью диализа и добавляли DTT, фильтровали через Millex GP 0,22 мкм, переносили в пробирки и хранили при -70°С. Антигены BCMA-Avi-His, ВСМА-Avi-His-TEV-HSA из культуральной жидкости выделяли и очищали, используя колонку с сорбентом для аффинной хроматографии с Ni-NTA. Осветленную культуральную жидкость пропускали через колонку, уравновешенную фосфатно-солевым буфером (ФСБ, рН 7,4). Связанный антиген элюировали, используя ФСБ с добавлением 500 мМ имидазола (рН 7,4). Далее белок переводили в ФСБ с помощью диализа. После этого белок наносили на гель-фильтрационную колонку. Полученный белок фильтровали через Millex GP 0,22 мкм, переносили в пробирки и хранили при -70°С.
Пример 2. Клонирование генов вариабельных доменов антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 в экспрессионную плазмиду
Клонирование генов вариабельных доменов антител в экспрессионные плазмиды pLL (фиг. 1) и рЕТ22 (фиг. 2) осуществляли по стандартному протоколу с применением рестриктазно-лигазного метода.
В последующем экспрессионные вектора, содержащие фрагменты антител, трансформировали в штаммы E.coli BL21-DE3 и BL21-Gold для проведения сравнительного анализа аффинности вариабельных фрагментов антител из дисплейных библиотек к антигену методом ИФА с использованием автоматизированной платформы.
Пример 3. Наработка и первичный анализ Fab-фрагментов и scFv-фрагментов антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037, специфически связывающих ВСМА человека
Наработку Fab и scFv проводили по стандартной методике: бактериальные клетки E.coli BL21-DE3 и BL21-Gold трансформировали экспрессионными векторами, содержащими гены scFv и Fab соответственно, а последующее добавление индуктора запускало транскрипцию 1ас-оперона, что при культивировании полученных трансформантов вызывало экспрессию scFv и Fab, которые экспортировались в периплазматическое пространство клеток. Далее проводили ИФА для проверки связывания scFv и Fab с иммобилизованным на подложке антигеном hBCMA-Avi-His в концентрации 0,2 мкг/мл в 0,1 М NaHCO3 (рН 9,0) (антиген иммобилизовали в течение ночи при +4°С). Все последующие этапы проводили при комнатной температуре по стандартному протоколу ИФА с использованием высокопроизводительной автоматизированной платформы на базе роботизированных систем. После каждого этапа проводили отмывку 300 мкл на лунку 1х ФСБТ в трех повторностях. Проводили блокирования неспецифических участков связывания на планшете 1% обезжиренным молоком в 1х ФСБТ, после отмывки добавляли аналит, в качестве которого выступали супернатанты клеток Е. coli в объеме 60 мкл на лунку. Детекция иммунных комплексов осуществляли при помощи козьих анти-Myc-tag антител конъгюированных с пероксидазой в разведении 1:20000. Окрашивание субстрат-хромогенной смеси проводили добавлением субстратного раствора ТМБ в объеме 50 мкл на 15 минут. Остановку реакции осуществляли 25 мкл H2SO4 1%. Цветовой сигнал измеряли при длине волны 450 нм. Степень связывания антитела была пропорциональна продуцированию цветового сигнала. Клоны, у которых цветовой сигнал превышал сигнал от контрольного антитела, проверяли в ИФА на неспецифическое связывание.
Таким образом, все анализируемые Fab-фрагменты и scFv-фрагменты антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 показывают специфическое связывание с hBCMA-Avi-His.
Пример 4. Анализ неспецифического связывания Fab-фрагментов и scFv-фрагментов антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 с другими антигенами
ИФА использовали также для анализа неспецифического связывания исследуемых scFv- и Fab-фрагментов с другими антигенами. Исследование проводили, как описано выше, но в качестве антигенов для иммобилизации использовали hCD16-Avi-His-FLAG, cynoIL4R-Fc в 0,1 М NaHCO3 (рН 9,0) (антигены иммобилизовали в течение ночи при 4°С). В качестве контроля специфического связывания использовали hBCMA-Avi-His, rhesusBCMA (антигены иммобилизовали в течение ночи при 4°С). Все последующие этапы проводили по стандартному протоколу ИФА с использованием высокопроизводительной автоматизированной платформы.
Все анализируемые Fab-фрагменты и scFv-фрагменты антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 показывают специфическое связывание с hBCMA-Avi-His, rhesusBCMA и не показывают неспецифическое взаимодействие с hCD16-Avi-His-FLAG и cynoIL4R-Fc.
Пример 5. Анализ Fab-фрагментов и scFv-фрагментов антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 по скорости диссоциации на ForteBio
Измерения Fab фрагментов проводились на приборе ForteBio Octet RED 384 с применением FAB2G биосенсоров (ForteBio). Образцы Fab загружались на сенсоры из супернатантов в течение 16-18 часов при температурном режиме (5±3)°С. После загрузки сенсоры перемещались в кинетический буферный раствор с 500 мМ NaCl (4,3 мМ Na2HPO4; 500 мМ NaCl, 1,5 мМ KH2PO4; 2,7 мМ KCl; объемная доля добавленного Tween 20 составляла 0,1%; массовая доля добавленного БСА составляла 0,1%; рН 7,4), данный буферный раствор применялся для приготовления всех последующих шагов экспериментов с образцами Fab. Измерения проводились при температуре 30°С. Уравновешивание сенсоров в кинетическом буферном растворе проводилось не менее 10 мин., затем записывалась базовая линия (60 с). После записи базовой линии сенсоры с иммобилизованными Fab погружали в лунки с раствором аналита (рекомбинантный антиген BCMA-Avi-His-TEV-HSA человека, где происходила ассоциация комплекса антиген-Fab в течение 300 секунд. Концентрация антигена ВСМА человека составляла 391,2 нМ (30 мкг/мл). Затем детектировалась диссоциация комплекса в кинетическом буферном растворе в течение 600 секунд. Для проверки неспецифического взаимодействия аналита с сенсорами (отрицательный контроль) применялись сенсоры, не загруженные Fab фрагментами кандидатов. На этапе загрузки сенсоры для отрицательного контроля погружались в супернатант, не содержащий Fab, все остальные этапы были аналогичны загруженным образцами Fab сенсорорам.
Измерения scFv фрагментов проводились на приборе Forte Bio Octert RED 384 с применением SAX биосенсоров (ForteBio). Для измерений было проведено биотинилирование антигена ВСМА человека в мольном соотношении антиген к биотину 1:1,5. Анализ кинетики взаимодействия проводили при 30°С. Для проведения анализа применялся кинетический буферный раствор (4,3 мМ Na2HPO4; 136,9 мМ NaCl, 1,5 мМ KH2PO4; 2,7 мМ KCl; объемная доля добавленного Tween 20 составляла 0,1%; массовая доля добавленного БСА составляла 0,1%; рН 7,4). Биотинилированный антиген ВСМА человека загружался на сенсоры в течение 600 секунд, концентрация раствора антигена в кинетическом буферном растворе составляла 20 мкг/мл. Базовая линия после загрузки записывалась в течение 120 с. После записи базовой линии сенсоры с иммобилизованным антигеном погружали в лунки с раствором аналита (кандидаты scFv), где происходила ассоциация комплекса антиген-scFv в течение 150 секунд (образцы scFv для этапа ассоциации разбавлялись кинетическим буферным раствором до концентрации 1200 нМ). Затем детектировалась диссоциация комплекса антиген-scFv в кинетическом буферном растворе в течение 600 секунд. Референсный сигнал записывался параллельно с записью сенсограм кандидатов и вычитался при обработке сенсограмм. В качестве референсного сигнала применялся сигнал сенсора, погружавшегося в кинетический буферный раствор без аналита на этапе ассоциации, все остальные этапы аналогичны сенсорам, записывавшим исследуемый сигнал. Для проверки неспецифического взаимодействия аналита (кандидаты scFv) с сенсорами применялись сенсоры, не загруженные антигеном. На этапе загрузки сенсоры для отрицательного контроля погружались в кинетический буферный раствор, не содержащий антигена, все остальные этапы были аналогичны сенсорам с загруженным антигеном.
Кривые связывания анализировались с помощью программы Octet Data Analysis (версия 9.0) с использованием модели взаимодействия 1:1. Результат анализа для Fab- и scFv-фрагментов антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 приведен в таблице 1. Данные Fab- и scFv-фрагменты в дальнейшем использовались для создания полноразмерных антител.
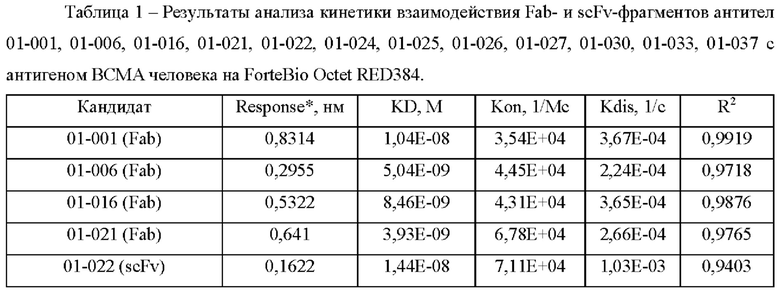
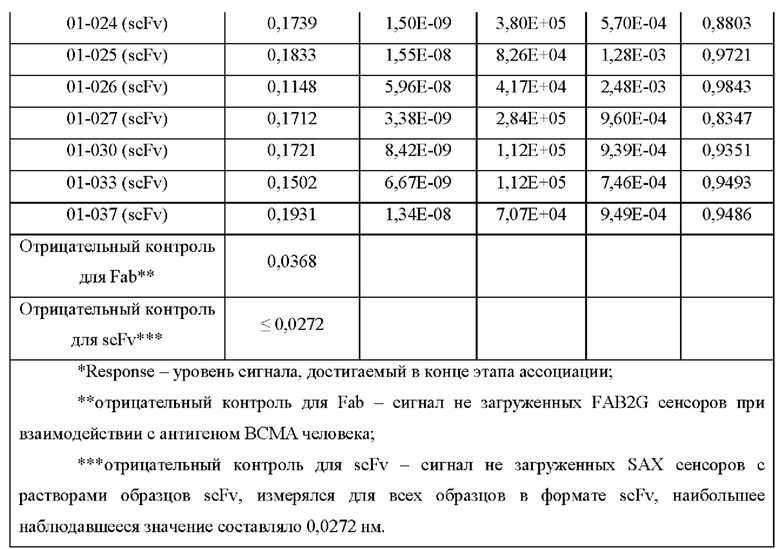
Пример 6. Получение генетических конструкций для синтеза полноразмерных антител Клонирование проводили по стандартной методике. Нарабатывали ПНР-продукты, содержащие гены вариабельных доменов тяжелой и легкой цепей антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 с праймерами содержащими сайты рестрикции. Вариабельный домен тяжелой цепи клонировали в вектор pEE-HCLALA IgG1 (фиг. 3) по сайтам рестрикции Sal1/Nhe1. Вариабельный домен легкой цепи клонировали в вектор рЕЕ-CK (фиг. 4) по сайтам рестрикции Sal1/BsiW1. Полученные генетические конструкции передали на транзиентную наработку белков в клеточной линии СНО-Т.
Пример 7. Получение полноразмерных антител
Полноразмерные антитела 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 продуцировали в клетках постоянной клеточной линии, полученной из клеток яичника китайского хомячка (линия СНО-Т) с помощью транзиентной трансфекций в двух повторностях. Суспензионное культивирование осуществляли в биореакторах на орбитальном шейкере, с использованием бессывороточных сред. Для транзиентной экспрессии клетки в концентрации 2-2,2×106 кл/мл трансфецировали с помощью линейного полиэтиленимина. Соотношение ДНК/ПЭИ составляло 1:7. На 10 день культивирования клеточную суспензию центрифугировали при 2000 g в течение 15 минут и фильтровали через фильтр с размером пор 0,22 мкм.
Антитела очищали путем аффинной хроматографии на колонках с помощью роботизированной станции. Колонку уравновешивали буфером 50 mM NaPB (Натрий фосфатный буфер), 150 mM NaCl (рН 7,5), наносили фильтрованную культуральную жидкость с антителами, затем колонку промывали 8 объемами буфера 50 mM NaPB, 150 mM NaCl и 4 объемами 50 тМ NaPB (рН 7,5). Элюцию белка проводили раствором 50 mM NaPB, 100 mM NaCl (рН 3) за 6 объемов колонок. Полученные образцы нейтрализовали 25 мкл 1М фосфатным буфером (рН 8).
Для контроля чистоты кандидатов использовали электрофорез в полиакриламидном геле и эксклюзионную ВЭЖХ. Электрофорез проводили в полиакриламидном геле 7,5% в денатурирующих нередуцирующих условиях. Определение чистоты белка проводили по интенсивности окрашивания бенда при нагрузке белка на дорожку 10 мкг. Электрофореграммы представлены на фиг. 5 и фиг. 6. Эксклюзионную ВЭЖХ проводили на колонке в подвижной фазе 0,05М NaH2PO4, 0,3 М NaCl рН=7,0.
Пример 8. Определение аффинности полноразмерных антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 к ВСМА человека на Forte Bio
Эксперименты по исследованию аффинности связывания антител 01-001, 01-006, 01-016,01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 к антигену ВСМА человека проводили на приборе ForteBio Octet RED 384. Антитела в концентрации 20 мкг/мл иммобилизировались на поверхности Protein Абиосенсоров (ForteBio). Анализ проводили при 30°С, с использованием кинетического буферного раствора (4,3 мМ Na2HPO4; 136,9 мМ NaCl, 1,5 мМ KH2PO4; 2,7 мМ KCl; объемная доля добавленного Tween 20 составляла 0,1%; массовая доля добавленного БСА составляла 0,1%; рН 7,4). После того как в кинетическом буферном растворе прописывали базовую линию, сенсоры с иммобилизованными антителом погружали в лунки с раствором аналита (ВСМА), где происходила ассоциация комплекса в течение 300 секунд. Для каждого исследуемого антитела записывались сенсограмма для раствора ВСМА человека с концентрацией 10 мкг/мл (130,4 нМ) и референсный сигнал (референсная сенсограмма) кинетического буферного раствора без ВСМА. Затем детектировалась диссоциация комплекса в буферном растворе в течение 600 секунд. Для проверки неспецифического взаимодействия аналита с сенсорами (отрицательный контроль) применялись сенсоры, не загруженные антителами. На этапе загрузки сенсоры для отрицательного контроля погружались в кинетический буферный раствор, не содержавший антител, все остальные этапы были аналогичны загруженным антителами сенсорам.
Кривые связывания с вычетом референсного сигнала анализировались с помощью программы Octet Data Analysis (версия 9.0) с использованием модели взаимодействия 1:1 (таблица 2).
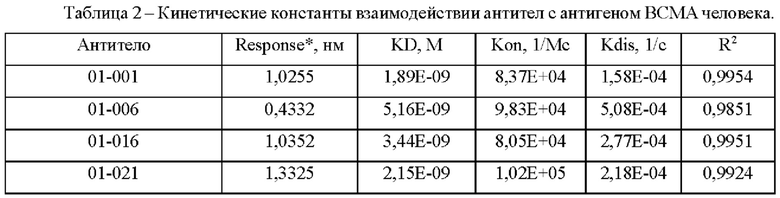
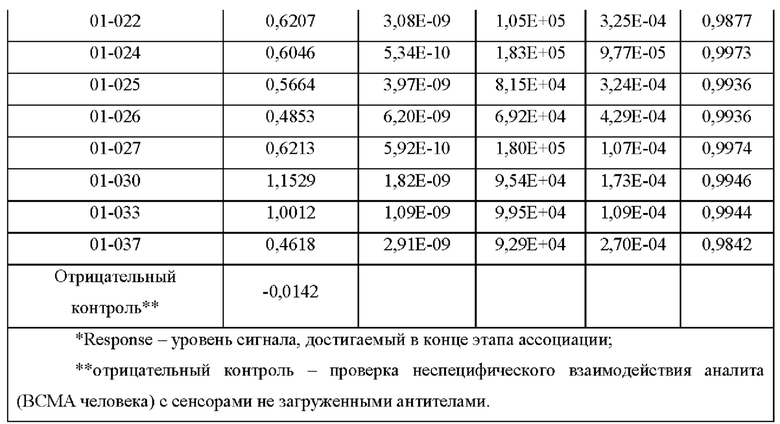
Таким образом, все анализируемые анти-ВСМА антитела специфически связываются с антигеном ВСМА человека и обладают высокими параметрами аффинности связывания с антигеном ВСМА человека (таблица 3).
Пример 13. Проверка взаимодействий полноразмерных антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 с ВСМА резус на приборе Forte Bio.
Целью данного эксперимента было подтверждение взаимодействия антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 с антигеном резус ВСМА. Проверка взаимодействия антител с антигеном резус ВСМА проводилась на приборе ForteBio Octet RED384 с применением биосенсоров AR2G (ForteBio). Эксперимент состоял из следующих этапов: активация сенсоров, загрузка белка на сенсоры, тушение непрореагировавших активированных групп, запись базовой линии, запись ассоциации аналита, записи диссоциации. Измерения проводились при температуре 30°С. Активация сенсоров осуществлялась в водном растворе, содержащем 20 мМ EDC и 10 мМ sNHS в течении 300 с. Загрузка антигена резус ВСМА на поверхность биосенсоров осуществлялась в 10 мМ натрий-ацетатном буферном растворе с рН 5,0 в течении 300 с. Концентрация белка для загрузки составляла 10 мкг/мл. Тушение непрореагировавших активных центров на поверхности сенсоров осуществлялось в течение 300 с в 1М водном растворе этаноламина с рН 8,5 (значение рН доводилось добавлением соляной кислоты). Для проверки неспецифического взаимодействия аналита с сенсорами (отрицательный контроль) применялся сенсор, не загруженный антигеном (на этапе загрузки сенсор погружался в 10 мМ натрий-ацетатный буферный раствор с рН 5,0, все остальные этапы аналогичны загруженным антигеном сенсорорам). Базовая линия и все последующие шаги эксперимента проводились в кинетическом буферном растворе (4,3 мМ Na2HPO4; 136,9 мМ NaCl, 1,5 мМ KH2PO4; 2,7 мМ KCl; объемная доля добавленного Tween 20 составляла 0,1%; массовая доля добавленного БСА составляла 0,1%; рН 7,4). На этапе ассоциации (продолжительность этапа 300 с) сенсоры с загруженным резус ВСМА погружались в лунки с раствором аналита (исследуемое антитело), приготовленного в кинетическом буферном растворе. Концентрация аналита составляла 2,5 мкг/мл. На этапе диссоциации сенсоры погружались в лунки с кинетическим буфером, в которых записывалась базовая линия.
Кривые связывания обрабатывались с помощью программы Octet Data Analysis (версия 9.0) с использованием модели взаимодействия 1:1. Результаты обработки представлены в таблице 4 (значение kdis <1.0Е-07 (1/с) и соответствующее ему значение KD <1.0Е-12 (М) означает, что в рамках примененной методики измерения и обработки для данного образца превышен предел чувствительности по константе скорости диссоциации для описывающей сенсограмму модельной кривой). Полученные значения кинетических констант носят оценочный характер в связи с применением бивалентного аналита (антител) и могут применяться только для сравнения образцов. Для всех анти-ВСМА антител наблюдается сигнал связывания с антигеном резус ВСМА на этапе ассоциации и медленный спад сигнала на этапе диссоциации, что подтверждает высокую авидность при взаимодействии с данным антигеном. Таким образом, все анализируемые анти-ВСМА антитела специфически связываются с антигеном резус ВСМА (таблица 3).
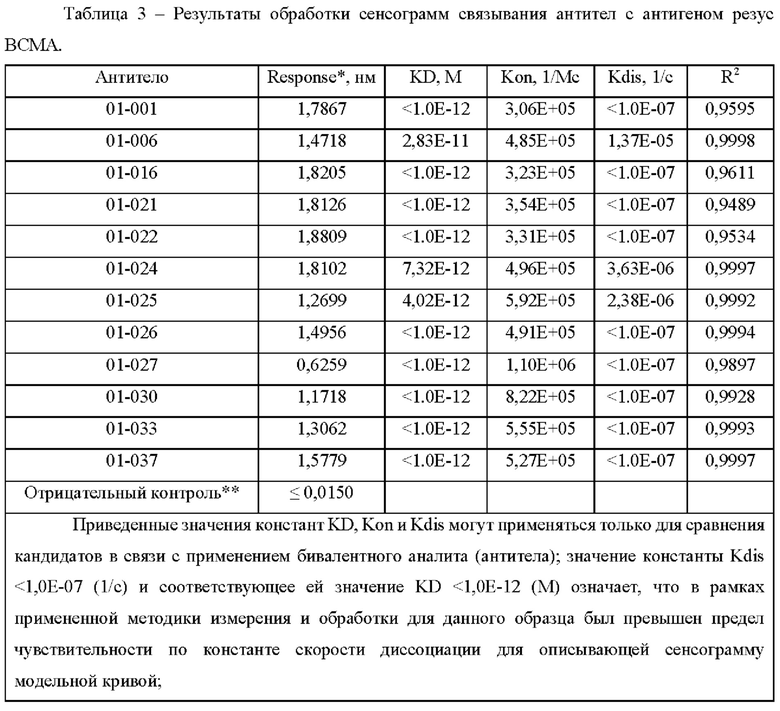

Пример 14. Проверка блокирования взаимодействия APRIL с ВСМА человека антителами 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 на приборе Forte Bio.
Исследование проводили на приборе ForteBio Octet RED 384 с применением биосенсоров AR2G (ForteBio). Эксперимент состоял из следующих основных этапов: загрузка антигена человека APRIL/TNFSF13 на сенсоры, проверка связывания антигена APRIL/TNFSF13 со смесью ВСМА человека и проверяемого антитела (премикс). В качестве положительного контроля применялся раствор ВСМА человека без добавления антител. Заключение о блокировании взаимодействия проводилось на основании сравнения сигнала (response) премикса и сигнала положительного контроля.
Активация сенсоров осуществлялась в водном растворе, содержащем 20 мМ EDC и 10 мМ sNHS в течении 300 с. Загрузка антигена APRIL/TNFSF13 на поверхность биосенсоров осуществлялась в 10 мМ натрий-ацетатном буфере с рН 5,0 в течении 900 с. Концентрация белка APRIL/TNFSF13 для загрузки составляла 10 мкг/мл. Для проверки неспецифического взаимодействия аналита с сенсорами применялся сенсор, не загруженный антигеном (на этапе загрузки сенсор погружался в натрий-ацетатный буфере с рН 5,0, все остальные этапы были аналогичны загруженному антигеном сенсору). Тушение непрореагировавших активных центров на поверхности сенсоров осуществлялось в 1М водном растворе этаноламина с рН 8,5 (рН доводился добавлением соляной кислоты) в течение 300 с. Все шаги эксперимента после этапа тушения проводились в кинетическом буфере: 4,3 мМ Na2HPO4; 136,9 мМ NaCl, 1,5 мМ KH2PO4; 2,7 мМ KCl; объемная доля добавленного Tween 20 составляла 0,1%; массовая доля добавленного БСА (бычий сывороточный альбумин) составляла 0,1%, рН 7,4. На этапе ассоциации (продолжительность этапа 300 с) сенсоры с загруженным белком погружались в лунки с раствором аналита. В качестве аналита на этапе ассоциации применялся раствор, содержащий 710 нМ исследуемого антитела и 71 нМ ВСМА человека в кинетическом буферном растворе. В качестве положительного контроля применялся раствор (аналит) с концентрацией ВСМА человека 71 нМ. Измерения проводились при температуре 30°С. Референсные сенсоры проходили все этапы аналогично сенсорам, применяемым для записи сенсограмм аналита, за исключением этапа ассоциации - на этапе ассоциации данные сенсоры погружались в кинетический буфер без аналита (измерение сигнала референсных сенсоров осуществлялось параллельно с записью основных сенсограмм). Референсный сигнал вычитался из анализируемого сигнала при обработке сенсограмм.
Обработка сенсограмм проводилась с применением программного обеспечения ForteBio Octet Data Analysisn 9.0. Результаты эксперимента представлены в таблице 4. Исследованные антитела 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 блокируют связывание загруженного на сенсоры APRIL/TNFSF13 с антигеном ВСМА человека.
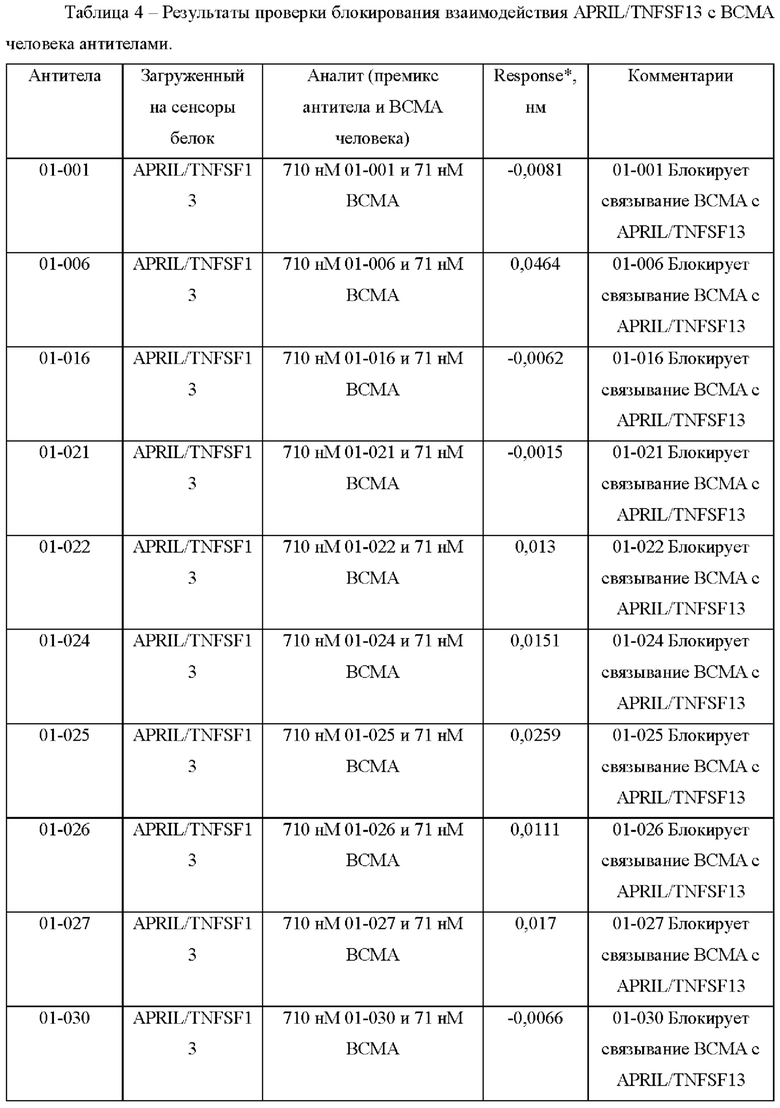
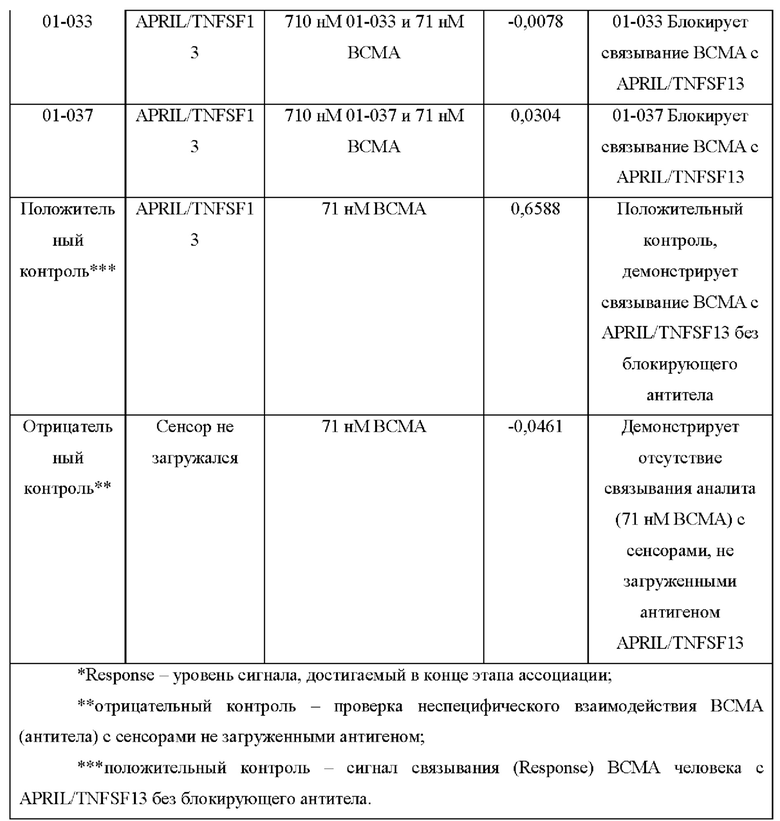
Пример 15. Анализ связывания анти-ВСМА антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 с человеческим ВСМА на поверхности клеток RPMI8226 методом проточной цитометрии.
Способность анти-ВСМА антител 01-001, 01-006, 01-016,01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 связываться с человеческим антигеном ВСМА на поверхности клеток оценивали методом проточной цитометрии на клеточной линии RPMI8226 (множественная миелома), стабильно экспрессирующей рецептор ВСМА на своей поверхности.
25 000 клеток в лунке инкубировали в буфере для окрашивания (PBS+NaN3+5% BSA) в течение 30 минут при +4°C с серийными разведениями анализируемых антител. После истечения указанного времени клетки отмывали 2 раза холодным (+4°С) буфером для окрашивания и связавшиеся антитела детектировали путем окрашивания вторичными антителами против человеческого Fc-фрагмента с фикоэритриновой меткой в течение 30 минут при +4°С. В качестве контроля были использованы лунки без внесения антител и только с вторичными антителами. По истечению времени клетки отмывали 2 раза холодным (+4°С) буфером для окрашивания и ресуспендировали в 150 мкл холодного (+4°С) буфера для окрашивания. Затем образцы анализировали на проточном цитометре. Проводили гейтирование по параметрам прямого и бокового светорассеяния (FSC и SSC) для нахождения целевой клеточной популяции, далее проводили гейтирование по параметрам высоты и площади прямого светорассеяния (FSC-H и FSC-А) для обозначения одиночных (синглетных) клеток в популяции.
Половина от эффективной концентрации ЕС50 была рассчитана с помощью построения четырехпараметрической регрессионной логистической модели, данные представлены в таблице 5.
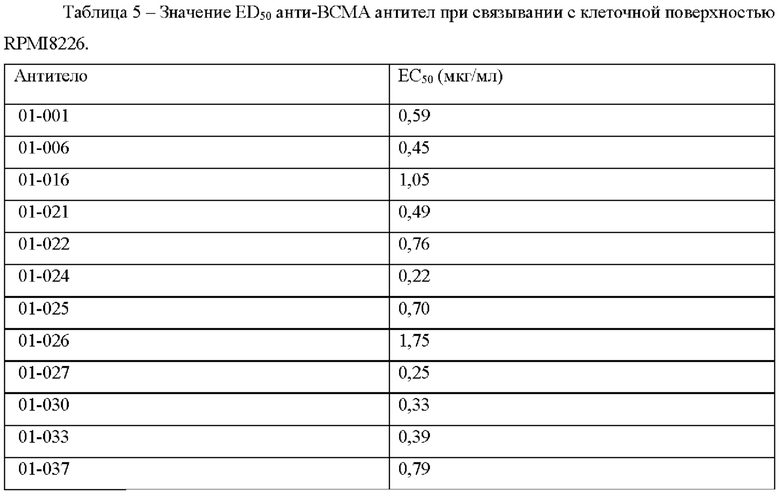
Вывод: исходя из полученных данных все проанализированные антитела связываются с мишенью ВСМА на поверхности клеток множественной миеломы.
Пример 16. Анализ неспецифического связывания анти-ВСМА антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 на поверхности ВСМА-отрицательных клеток K562 методом проточной цитометрии.
Наличие неспецифического связывания анти-ВСМА антител 01-001, 01-006, 01-016, 01-021, 01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037 оценивали методом проточной цитометрии на клеточной линии K562 (хроническая миелогенная лейкемия), которая характеризуется отсутствием экспрессии ВСМА на своей поверхности.
25 000 клеток K562 в лунке инкубировали в буфере для окрашивания (PBS+NaN3+5% BSA) в течение 30 минут при +4°C с разведенными анализируемыми антителами. После истечения указанного времени клетки отмывали 2 раза холодным (+4°С) буфером для окрашивания и связавшиеся антитела детектировали путем окрашивания вторичными антителами против человеческого Fc-фрагмента с фикоэритриновой меткой в течение 30 минут при +4°С. В качестве контроля были использованы лунки без внесения антител и только с вторичными антителами. По истечению времени клетки отмывали 2 раза холодным (+4°С) буфером для окрашивания и ресуспендировали в 150 мкл холодного (+4°С) буфера для окрашивания. Затем образцы анализировали на проточном цитометре. Проводили гейтирование по параметрам прямого и бокового светорассеяния (FSC и SSC) для нахождения целевой клеточной популяции, далее проводили гейтирование по параметрам высоты и площади прямого светорассеяния (FSC-H и FSC-А) для обозначения одиночных (синглетных) клеток в популяции.
RPMI8226 брали в качестве положительного контроля связывания анализируемых антител с ВСМА на поверхности клетки. Пробоподготовку проводили аналогично вышеописанной для K562.
Оценку неспецифического связывания антител проводили путем сравнения уровней флуоресцентного сигнала от антител в одной концентрации в вариантах для клеточных линий K562 и RPMI8226, данные представлены в таблице 6.
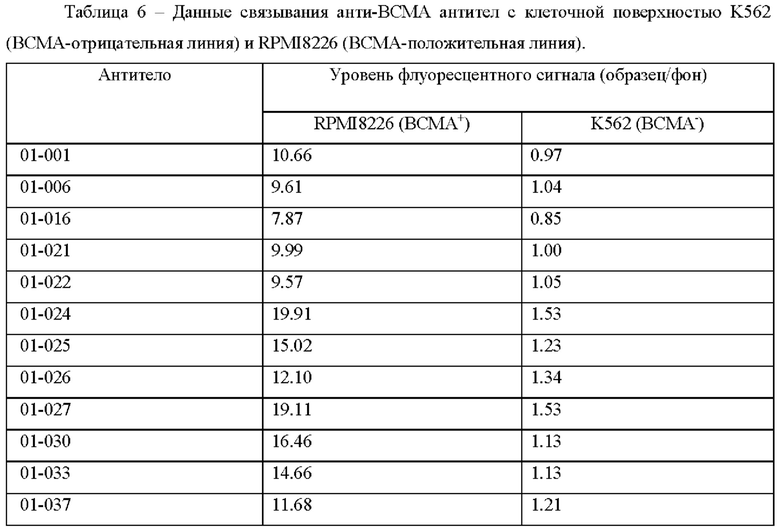
Вывод: исходя из полученных результатов все проанализированные антитела не проявляют неспецифического связывания с ВСМА-отрицательной клеточной линией.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
--->
<110> АО "БИОКАД"
<120> Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с BCMA, и его применение
<160> 111
<170> BiSSAP 1.3.6
<210> 1
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена тяжелой цепи антитела 01-001
<400> 1
Ser Ser Ala Met Ser
1 5
<210> 2
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена тяжелой цепи антител 01-006, 01-021, 01-022, 01-024,
01-025, 01-026, 01-027, 01-030, 01-033, 01-037
<400> 2
Ser Gly Leu Met Ser
1 5
<210> 3
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена тяжелой цепи антитела 01-016
<400> 3
Ser Ser Val Met Ser
1 5
<210> 4
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена тяжелой цепи антител 01-001, 01-016, 01-021, 01-030,
01-033
<400> 4
Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val Glu
1 5 10 15
Gly
<210> 5
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена тяжелой цепи антител 01-006, 01-022, 01-025, 01-026,
01-027, 01-037
<400> 5
Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val Lys
1 5 10 15
Gly
<210> 6
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена тяжелой цепи антитела 01-024
<400> 6
Cys Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val Lys
1 5 10 15
Gly
<210> 7
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена тяжелой цепи антител 01-001, 01-006, 01-016, 01-021,
01-022, 01-024, 01-025, 01-026, 01-027, 01-030, 01-033, 01-037
<400> 7
Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr
1 5 10
<210> 8
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антител 01-001, 01-033
<400> 8
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Thr Val Asn
1 5 10
<210> 9
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антитела 01-006
<400> 9
Ser Gly Ser Thr Ser Asn Ile Gly His Arg Thr Val Asn
1 5 10
<210> 10
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антител 01-016, 01-025
<400> 10
Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Ala Val Asn
1 5 10
<210> 11
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антитела 01-021
<400> 11
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Ile Val Asn
1 5 10
<210> 12
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антител 01-022, 01-024, 01-027
<400> 12
Ser Gly Gly Ile Ser Asn Ile Gly Ser Asn Ile Val Asn
1 5 10
<210> 13
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антитела 01-026
<400> 13
Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly Tyr Asp Val His
1 5 10
<210> 14
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антитела 01-030
<400> 14
Ser Gly Ser Ile Ser Asn Ile Gly Ser Asn Thr Val Asn
1 5 10
<210> 15
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR1 (Kabat) вариабельного
домена легкой цепи антитела 01-037
<400> 15
Ser Gly Thr Arg Ser Asn Ile Gly Thr Asn Thr Val Asn
1 5 10
<210> 16
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антитела 01-001
<400> 16
Asn Asp Ser Gln Arg Pro Ser
1 5
<210> 17
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антител 01-006, 01-037
<400> 17
Arg Asn Asn Gln Arg Pro Ser
1 5
<210> 18
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антитела 01-016
<400> 18
Lys Asn Asn Gln Arg Pro Ser
1 5
<210> 19
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антитела 01-021
<400> 19
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 20
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антител 01-022, 01-024, 01-027
<400> 20
Ser Gly Asn Gln Arg Pro Ser
1 5
<210> 21
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антитела 01-025
<400> 21
Ser Thr Asn Gln Arg Pro Ser
1 5
<210> 22
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антитела 01-026
<400> 22
Gly Asn Thr Asn Arg Pro Ser
1 5
<210> 23
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антитела 01-030
<400> 23
Asn His Asn Gln Arg Pro Ser
1 5
<210> 24
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR2 (Kabat) вариабельного
домена легкой цепи антитела 01-033
<400> 24
Ser Asp Asn Gln Arg Pro Ser
1 5
<210> 25
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-001
<400> 25
Ala Ala Trp Asp Gly Ser Leu Asn Val Trp Met
1 5 10
<210> 26
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-006
<400> 26
Ala Ala Trp Asp Asp Ser Leu Thr Ala Trp Val
1 5 10
<210> 27
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-016
<400> 27
Ala Ala Trp Asp Gly Ser Leu Asn Ala Trp Met
1 5 10
<210> 28
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-021
<400> 28
Ser Ala Trp Asp His Ser Leu Asn Ala Trp Val
1 5 10
<210> 29
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-022
<400> 29
Ala Ser Trp Asp Asp Ser Leu Asn Gly Trp Val
1 5 10
<210> 30
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антител 01-024 и 01-027
<400> 30
Ser Ser Trp Asp Ser Asp Leu Arg Asn Trp Val
1 5 10
<210> 31
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-025
<400> 31
Ala Ala Trp Asp Asp Arg Val Ser Ala Trp Leu
1 5 10
<210> 32
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-026
<400> 32
Ala Ala Trp Asp Asp Ser Leu Asn Gly Trp Val
1 5 10
<210> 33
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-030
<400> 33
Ala Thr Trp Asp Asp Ser Leu Ser Ala Trp Leu
1 5 10
<210> 34
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-033
<400> 34
Ala Ala Trp Asp Gly Ser Leu Asn Ala Trp Leu
1 5 10
<210> 35
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность CDR3 (Kabat) вариабельного
домена легкой цепи антитела 01-037
<400> 35
Ala Val Trp Asp Asp Arg Val Ser Ala Trp Leu
1 5 10
<210> 36
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антитела 01-001
<400> 36
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Leu Ser Ser Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 37
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антитела 01-006
<400> 37
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 38
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антитела 01-016
<400> 38
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Phe Ser Ser Ser
20 25 30
Val Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 39
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антитела 01-021
<400> 39
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 40
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антител 01-022, 01-025, 01-026, 01-027 и 01-037
<400> 40
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Val Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 41
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антитела 01-024
<400> 41
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Val Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Cys Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 42
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антитела 01-030
<400> 42
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Val Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 43
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена тяжелой
цепи антитела 01-033
<400> 43
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Gly Phe Glu Trp Val Ser
35 40 45
Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val Glu
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 44
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-001
<400> 44
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asn Asp Ser Gln Arg Pro Ser Gly Val Pro Asp Gln Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Asp Asn Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Val Trp Met Phe Gly Gly Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 45
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-006
<400> 45
Gln Ala Val Leu Thr Gln Pro Pro Ser Val Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Thr Ser Asn Ile Gly His Arg
20 25 30
Thr Val Asn Trp Tyr Gln Gln Phe Pro Gly Ala Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr His Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Thr Ala Trp Val Phe Gly Gly Gly Thr Gln Leu Thr Val Leu
100 105 110
<210> 46
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-016
<400> 46
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Phe Lys Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Val Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Ala Trp Met Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 47
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-021
<400> 47
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Ile Val Asn Trp Tyr Gln Gln Phe Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Phe Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Leu Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala Trp Asp His Ser Leu
85 90 95
Asn Ala Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 48
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-022
<400> 48
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Ser Ile Ser Cys Ser Gly Gly Ile Ser Asn Ile Gly Ser Asn
20 25 30
Ile Val Asn Trp Tyr Gln His Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Gly Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ser Trp Asp Asp Ser Leu
85 90 95
Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 49
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антител 01-024 и 01-027
<400> 49
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Ser Ile Ser Cys Ser Gly Gly Ile Ser Asn Ile Gly Ser Asn
20 25 30
Ile Val Asn Trp Tyr Gln His Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Gly Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Trp Asp Ser Asp Leu
85 90 95
Arg Asn Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 50
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-025
<400> 50
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Arg Val
85 90 95
Ser Ala Trp Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 51
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-026
<400> 51
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Val Ile Tyr Gly Asn Thr Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu
65 70 75 80
Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser
85 90 95
Leu Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 52
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-030
<400> 52
Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ile Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln His Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asn His Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Thr Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Phe Cys Ala Thr Trp Asp Asp Ser Leu
85 90 95
Ser Ala Trp Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 53
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-033
<400> 53
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asp Asn Gln Arg Pro Ser Gly Val Pro Glu Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Leu
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Ala Trp Leu Phe Gly Gly Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 54
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность вариабельного домена легкой
цепи антитела 01-037
<400> 54
Ser Tyr Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Thr Arg Ser Asn Ile Gly Thr Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Val Trp Asp Asp Arg Val
85 90 95
Ser Ala Trp Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 55
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антитела 01-001
<400> 55
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Leu Ser Ser Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 56
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антитела 01-006
<400> 56
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 57
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антитела 01-016
<400> 57
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Phe Ser Ser Ser
20 25 30
Val Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 58
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антитела 01-021
<400> 58
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 59
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антител 01-022,
01-025, 01-026, 01-027 и 01-037
<400> 59
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Val Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 60
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антитела 01-024
<400> 60
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Val Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Cys Tyr Asn Gly Gly Ser Asp Arg Ala Gly Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 61
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антитела 01-030
<400> 61
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Val Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Phe Glu Trp Val
35 40 45
Ser Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 62
<211> 450
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность тяжелой цепи антитела 01-033
<400> 62
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Gly
20 25 30
Leu Met Ser Trp Val Arg Gln Ala Pro Gly Gly Phe Glu Trp Val Ser
35 40 45
Gly Tyr Asn Gly Gly Ser Asp Arg Ala Gly Phe Ala Asp Ser Val Glu
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Tyr Ile Ala Asn Ser Gly Thr Tyr Tyr Trp Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 63
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-001
<400> 63
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asn Asp Ser Gln Arg Pro Ser Gly Val Pro Asp Gln Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Asp Asn Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Val Trp Met Phe Gly Gly Gly Thr Lys Val Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 64
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-006
<400> 64
Gln Ala Val Leu Thr Gln Pro Pro Ser Val Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Thr Ser Asn Ile Gly His Arg
20 25 30
Thr Val Asn Trp Tyr Gln Gln Phe Pro Gly Ala Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr His Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Thr Ala Trp Val Phe Gly Gly Gly Thr Gln Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 65
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-016
<400> 65
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Phe Lys Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Val Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Ala Trp Met Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 66
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-021
<400> 66
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Ile Val Asn Trp Tyr Gln Gln Phe Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Phe Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Leu Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala Trp Asp His Ser Leu
85 90 95
Asn Ala Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 67
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-022
<400> 67
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Ser Ile Ser Cys Ser Gly Gly Ile Ser Asn Ile Gly Ser Asn
20 25 30
Ile Val Asn Trp Tyr Gln His Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Gly Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ser Trp Asp Asp Ser Leu
85 90 95
Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 68
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антител 01-024 и
01-027
<400> 68
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Ser Ile Ser Cys Ser Gly Gly Ile Ser Asn Ile Gly Ser Asn
20 25 30
Ile Val Asn Trp Tyr Gln His Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Gly Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Trp Asp Ser Asp Leu
85 90 95
Arg Asn Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 69
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-025
<400> 69
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Arg Val
85 90 95
Ser Ala Trp Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 70
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-026
<400> 70
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Val Ile Tyr Gly Asn Thr Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu
65 70 75 80
Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser
85 90 95
Leu Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 71
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-030
<400> 71
Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ile Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln His Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asn His Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Thr Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Phe Cys Ala Thr Trp Asp Asp Ser Leu
85 90 95
Ser Ala Trp Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 72
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-033
<400> 72
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asp Asn Gln Arg Pro Ser Gly Val Pro Glu Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Leu
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Ala Trp Leu Phe Gly Gly Gly Thr Lys Val Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 73
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность легкой цепи антитела 01-037
<400> 73
Ser Tyr Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Thr Arg Ser Asn Ile Gly Thr Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Val Trp Asp Asp Arg Val
85 90 95
Ser Ala Trp Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 74
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антитела
01-001
<400> 74
gaagtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag tctctggatt caccttgagt agcagtgcca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcgaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agt 363
<210> 75
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антитела
01-006
<400> 75
gaagtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgttcag catctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggctat 180
acagactccg tgaagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agt 363
<210> 76
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антитела
01-016
<400> 76
gaggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag tctctggatt caccttcagt agcagtgtca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agt 363
<210> 77
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антитела
01-021
<400> 77
caggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agt 363
<210> 78
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антител
01-022, 01-025, 01-026, 01-027 и 01-037
<400> 78
gaagtgcagc tggtgcagtc tgggggaggg ttggtgcagt ctggggggtc tctgagagtc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggctac 180
acagactccg tgaagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcgaatagcg gtacttacta ctgggactac tggggccagg ggaccacggt caccgtctcg 360
agt 363
<210> 79
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антитела
01-024
<400> 79
gaagtgcagc tggtgcagtc tgggggaggg ttggtgcagt ctggggggtc tctgagagtc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcatgc tataatggtg gtagtgatag ggcaggctac 180
acagactccg tgaagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcgaatagcg gtacttacta ctgggactac tggggccagg ggaccacggt caccgtctcg 360
agt 363
<210> 80
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антитела
01-030
<400> 80
gaggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagagtc 60
tcctgtgcag cctctggatt cagcttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtctcg 360
agt 363
<210> 81
<211> 363
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена тяжелой цепи антитела
01-033
<400> 81
gaggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagacgccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccacggt caccgtctcg 360
agt 363
<210> 82
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-001
<400> 82
cagcctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caatatcggg agtaatactg tcaattggta tcagcaactc 120
ccaggaacgg cccccaaact cctcatctat aatgatagtc agcggccctc aggggtccct 180
gaccaattct ctgggtccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgacaatg aggctgatta ttactgtgca gcatgggatg gcagcctgaa tgtctggatg 300
ttcggcggag ggaccaaggt caccgtccta 330
<210> 83
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-006
<400> 83
caggctgtgc tgactcagcc cccctcagtg tctgggaccc ccggacagag ggtcaccatc 60
tcttgttctg gaagcacctc caacatcgga cataggactg taaactggta tcagcaattt 120
ccaggagcgg cccccaaact cctcatctat aggaataatc agcggccctc aggggtccct 180
gcccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta tcactgtgca gcatgggatg acagcctgac tgcttgggtg 300
ttcggcggag ggacccagct caccgtttta 330
<210> 84
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-016
<400> 84
cagcctgtgc tgactcagcc accctcggtg tctgaagccc ccaggcagag ggtcaccatc 60
tcctgttctg gaagcagctc caacatcgga aataatgctg taaactggta ccagcagctc 120
ccaggaaagg ctcccaaact cctcatcttt aagaataatc agcggccctc aggggtccct 180
gaccggttct ctggctccaa gtctggcacc tcagcctccc tggtcatcag tgggctccag 240
tctgaggatg aggctgatta ctactgtgca gcatgggatg gcagcctgaa tgcttggatg 300
ttcggcgggg ggaccaagct gaccgtccta 330
<210> 85
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-021
<400> 85
cagtctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agtaatattg taaactggta ccagcagttc 120
ccaggaacgg cccccaaact cctcattttt agtaataatc agcggccctc aggggtccct 180
gaccgattat ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgttca gcatgggatc acagcctgaa tgcctgggtg 300
ttcggcggag ggaccaagct gaccgtccta 330
<210> 86
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-022
<400> 86
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcagcatc 60
tcttgttctg gaggcatctc caacatcgga agtaatattg taaactggta ccaacacctc 120
ccaggaacgg cccccaaact cctcatatat agtggtaatc aacggccctc aggagtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgtgca tcgtgggatg acagcctgaa tggctgggta 300
ttcggcggag ggaccaagct gaccgtccta 330
<210> 87
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антител
01-024 и 01-027
<400> 87
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcagcatc 60
tcttgttctg gaggcatctc caacatcgga agtaatattg taaactggta ccaacacctc 120
ccaggaacgg cccccaaact cctcatatat agtggtaatc aacggccctc aggagtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tggactccag 240
tccgaggatg aggctgacta ttactgctca tcatgggaca gcgacctcag gaattgggtg 300
ttcggcgggg ggaccaagct gaccgtccta 330
<210> 88
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-025
<400> 88
cagcctgtgc tgactcagcc accctcggtg tctgaagccc ccaggcagag ggtcaccatc 60
tcctgttctg gaagcagctc caacatcgga aataatgctg taaactggta ccagcagctc 120
ccaggaaagg ctcccaaact cctcatctat agtactaatc agcggccctc aggggtccct 180
gaccgattct ctggttccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg acagagtgag tgcttggctg 300
tttggcggag ggaccaagct gaccgtccta 330
<210> 89
<211> 333
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-026
<400> 89
cagtctgtgt tgacgcagcc gccctcagtg tctggggccc cagggcagag ggtcaccatc 60
tcctgcactg ggagcagctc caacatcggg gcaggttatg atgtacactg gtaccagcaa 120
cttccaggaa cagcccccaa actcgtcatc tatggtaaca ccaatcggcc ctcaggggtc 180
cctgaccgat tctctggctc caagtctggc acctcagcct ccctggccat cagtgggctc 240
cagtctgagg atgaggctga ttattactgt gcagcatggg atgacagcct gaatggttgg 300
gtattcggcg gaggcaccaa gctgaccgtc cta 333
<210> 90
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-030
<400> 90
cagtctgccc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcatctc caacatcgga agtaatactg taaactggta ccagcatctc 120
ccaggaacgg cccccaaact cctcatctat aatcataatc agcggccctc aggggtccct 180
gaccgattct ctggctccac gtctggcacg tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta tttctgtgca acatgggatg acagcctgag tgcttggctg 300
ttcggcggag ggaccaagct gaccgtccta 330
<210> 91
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-033
<400> 91
cagtctgtgc tgacgcagcc gccctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agtaatactg tgaactggta ccagcagctc 120
ccaggaacgg cccccaaact cctcatctat agtgataatc agcggccctc aggtgtccct 180
gaacgcttct ctggctccaa gtctggcacc tcagcctccc tggccatcag tggcctcctg 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg gcagcctgaa tgcttggcta 300
ttcggcggtg ggaccaaggt caccgtccta 330
<210> 92
<211> 330
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность вариабельного домена легкой цепи антитела
01-037
<400> 92
tcctatgtgc tgacacagcc accctcagcg tctgggaccc ccggacagag ggtcaccatc 60
tcttgttctg ggaccaggtc caacatcgga actaatactg ttaactggta ccagcagctc 120
ccaggaacgg cccccaaact cctcatctat agaaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ctactgtgca gtatgggatg acagagtgag tgcttggctg 300
tttggcggag ggaccaagct gaccgtccta 330
<210> 93
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антитела 01-001
<400> 93
gaagtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag tctctggatt caccttgagt agcagtgcca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcgaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 94
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антитела 01-006
<400> 94
gaagtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgttcag catctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggctat 180
acagactccg tgaagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 95
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антитела 01-016
<400> 95
gaggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag tctctggatt caccttcagt agcagtgtca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 96
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антитела 01-021
<400> 96
caggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtgtcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 97
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антител 01-022, 01-025, 01-026,
01-027 и 01-037
<400> 97
gaagtgcagc tggtgcagtc tgggggaggg ttggtgcagt ctggggggtc tctgagagtc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggctac 180
acagactccg tgaagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcgaatagcg gtacttacta ctgggactac tggggccagg ggaccacggt caccgtctcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 98
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антитела 01-024
<400> 98
gaagtgcagc tggtgcagtc tgggggaggg ttggtgcagt ctggggggtc tctgagagtc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcatgc tataatggtg gtagtgatag ggcaggctac 180
acagactccg tgaagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcgaatagcg gtacttacta ctgggactac tggggccagg ggaccacggt caccgtctcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 99
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антитела 01-030
<400> 99
gaggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagagtc 60
tcctgtgcag cctctggatt cagcttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagactccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccctggt caccgtctcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 100
<211> 1353
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность тяжелой цепи антитела 01-033
<400> 100
gaggtgcagc tggtgcagtc tgggggaggc ttggtgcagc ctggggggtc tctgagactc 60
tcctgtgcag cctctggatt caccttcagt agcggtctca tgagctgggt ccgccaggct 120
ccaggaaagg ggttcgagtg ggtctcaggc tataatggtg gtagtgatag ggcaggcttt 180
gcagacgccg tggagggccg attcaccatc tccagagaca acgccaagaa cacgctgtat 240
ctgcaaatga acagcctgaa acctgaggac acggccgtgt attactgtgc aagatatata 300
gcaaatagcg gtacttacta ctgggactac tggggccagg ggaccacggt caccgtctcg 360
agtgctagca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccagctgt ccttcagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga agccgcaggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtccccgggt aaa 1353
<210> 101
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-001
<400> 101
cagcctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caatatcggg agtaatactg tcaattggta tcagcaactc 120
ccaggaacgg cccccaaact cctcatctat aatgatagtc agcggccctc aggggtccct 180
gaccaattct ctgggtccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgacaatg aggctgatta ttactgtgca gcatgggatg gcagcctgaa tgtctggatg 300
ttcggcggag ggaccaaggt caccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 102
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-006
<400> 102
caggctgtgc tgactcagcc cccctcagtg tctgggaccc ccggacagag ggtcaccatc 60
tcttgttctg gaagcacctc caacatcgga cataggactg taaactggta tcagcaattt 120
ccaggagcgg cccccaaact cctcatctat aggaataatc agcggccctc aggggtccct 180
gcccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta tcactgtgca gcatgggatg acagcctgac tgcttgggtg 300
ttcggcggag ggacccagct caccgtttta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 103
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-016
<400> 103
cagcctgtgc tgactcagcc accctcggtg tctgaagccc ccaggcagag ggtcaccatc 60
tcctgttctg gaagcagctc caacatcgga aataatgctg taaactggta ccagcagctc 120
ccaggaaagg ctcccaaact cctcatcttt aagaataatc agcggccctc aggggtccct 180
gaccggttct ctggctccaa gtctggcacc tcagcctccc tggtcatcag tgggctccag 240
tctgaggatg aggctgatta ctactgtgca gcatgggatg gcagcctgaa tgcttggatg 300
ttcggcgggg ggaccaagct gaccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 104
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-021
<400> 104
cagtctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agtaatattg taaactggta ccagcagttc 120
ccaggaacgg cccccaaact cctcattttt agtaataatc agcggccctc aggggtccct 180
gaccgattat ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgttca gcatgggatc acagcctgaa tgcctgggtg 300
ttcggcggag ggaccaagct gaccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 105
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-022
<400> 105
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcagcatc 60
tcttgttctg gaggcatctc caacatcgga agtaatattg taaactggta ccaacacctc 120
ccaggaacgg cccccaaact cctcatatat agtggtaatc aacggccctc aggagtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgtgca tcgtgggatg acagcctgaa tggctgggta 300
ttcggcggag ggaccaagct gaccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 106
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антител 01-024 и 01-027
<400> 106
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcagcatc 60
tcttgttctg gaggcatctc caacatcgga agtaatattg taaactggta ccaacacctc 120
ccaggaacgg cccccaaact cctcatatat agtggtaatc aacggccctc aggagtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tggactccag 240
tccgaggatg aggctgacta ttactgctca tcatgggaca gcgacctcag gaattgggtg 300
ttcggcgggg ggaccaagct gaccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 107
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-025
<400> 107
cagcctgtgc tgactcagcc accctcggtg tctgaagccc ccaggcagag ggtcaccatc 60
tcctgttctg gaagcagctc caacatcgga aataatgctg taaactggta ccagcagctc 120
ccaggaaagg ctcccaaact cctcatctat agtactaatc agcggccctc aggggtccct 180
gaccgattct ctggttccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg acagagtgag tgcttggctg 300
tttggcggag ggaccaagct gaccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 108
<211> 654
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-026
<400> 108
cagtctgtgt tgacgcagcc gccctcagtg tctggggccc cagggcagag ggtcaccatc 60
tcctgcactg ggagcagctc caacatcggg gcaggttatg atgtacactg gtaccagcaa 120
cttccaggaa cagcccccaa actcgtcatc tatggtaaca ccaatcggcc ctcaggggtc 180
cctgaccgat tctctggctc caagtctggc acctcagcct ccctggccat cagtgggctc 240
cagtctgagg atgaggctga ttattactgt gcagcatggg atgacagcct gaatggttgg 300
gtattcggcg gaggcaccaa gctgaccgtc ctacgtacgg tggctgcacc atctgtcttc 360
atcttcccgc catctgatga gcagttgaaa tctggaactg cctctgttgt gtgcctgctg 420
aataacttct atcccagaga ggccaaagta cagtggaagg tggataacgc cctccaatcg 480
ggtaactccc aggagagtgt cacagagcag gacagcaagg acagcaccta cagcctcagc 540
agcaccctga cgctgagcaa agcagactac gagaaacaca aagtctacgc ctgcgaagtc 600
acccatcagg gcctgagctc gcccgtcaca aagagcttca acaggggaga gtgt 654
<210> 109
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-030
<400> 109
cagtctgccc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcatctc caacatcgga agtaatactg taaactggta ccagcatctc 120
ccaggaacgg cccccaaact cctcatctat aatcataatc agcggccctc aggggtccct 180
gaccgattct ctggctccac gtctggcacg tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta tttctgtgca acatgggatg acagcctgag tgcttggctg 300
ttcggcggag ggaccaagct gaccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 110
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-033
<400> 110
cagtctgtgc tgacgcagcc gccctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agtaatactg tgaactggta ccagcagctc 120
ccaggaacgg cccccaaact cctcatctat agtgataatc agcggccctc aggtgtccct 180
gaacgcttct ctggctccaa gtctggcacc tcagcctccc tggccatcag tggcctcctg 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg gcagcctgaa tgcttggcta 300
ttcggcggtg ggaccaaggt caccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<210> 111
<211> 651
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует аминокислотную
последовательность легкой цепи антитела 01-037
<400> 111
tcctatgtgc tgacacagcc accctcagcg tctgggaccc ccggacagag ggtcaccatc 60
tcttgttctg ggaccaggtc caacatcgga actaatactg ttaactggta ccagcagctc 120
ccaggaacgg cccccaaact cctcatctat agaaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ctactgtgca gtatgggatg acagagtgag tgcttggctg 300
tttggcggag ggaccaagct gaccgtccta cgtacggtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ИЛИ ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ, КОТОРОЕ СПЕЦИФИЧЕСКИ СВЯЗЫВАЕТСЯ С IL-4Rα, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2808563C2 |
| АНТИТЕЛО, СПОСОБНОЕ СВЯЗЫВАТЬСЯ С ТИМИЧЕСКИМ СТРОМАЛЬНЫМ ЛИМФОПОЭТИНОМ, И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2825304C2 |
| АНТИГЕНСВЯЗЫВАЮЩИЙ ПОЛИПЕПТИД, СВЯЗЫВАЮЩИЙСЯ С CD47, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2833294C2 |
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО, КОТОРОЕ СПЕЦИФИЧЕСКИ СВЯЗЫВАЕТСЯ С CSF-1R | 2020 |
|
RU2751249C1 |
| АНТИТЕЛА, КОТОРЫЕ СВЯЗЫВАЮТСЯ С СОРТИЛИНОМ И ПОДАВЛЯЮТ СВЯЗЫВАНИЕ ПРОГРАНУЛИНА | 2016 |
|
RU2735639C2 |
| АНТИТЕЛО, СВЯЗЫВАЮЩЕЕ ЧЕЛОВЕЧЕСКИЙ IL-4R, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2779649C1 |
| АНТИТЕЛО ПРОТИВ БЕТА-АМИЛОИДА, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2777844C1 |
| ТРИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ, ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2822200C2 |
| КОНЪЮГАТ АНТИТЕЛА ПРОТИВ CEA И АНАЛОГА ЭКСАТЕКАНА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2833323C1 |
| АНТИ-PCSK9 АНТИТЕЛО, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2739208C2 |
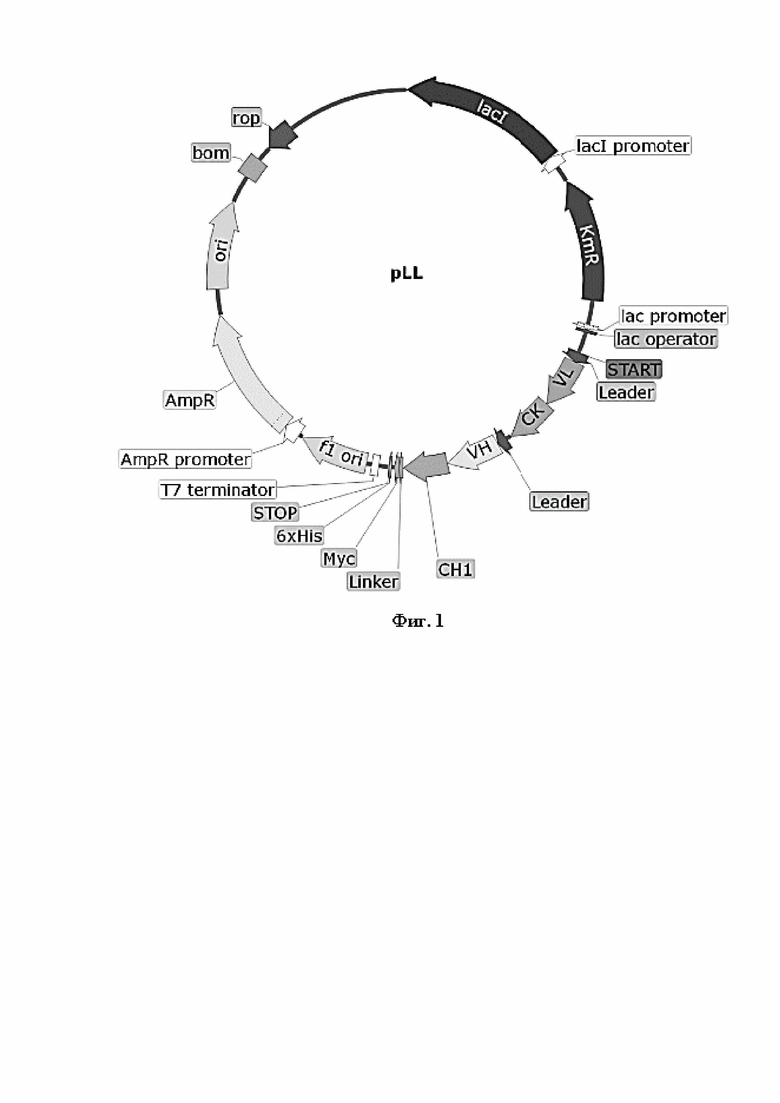
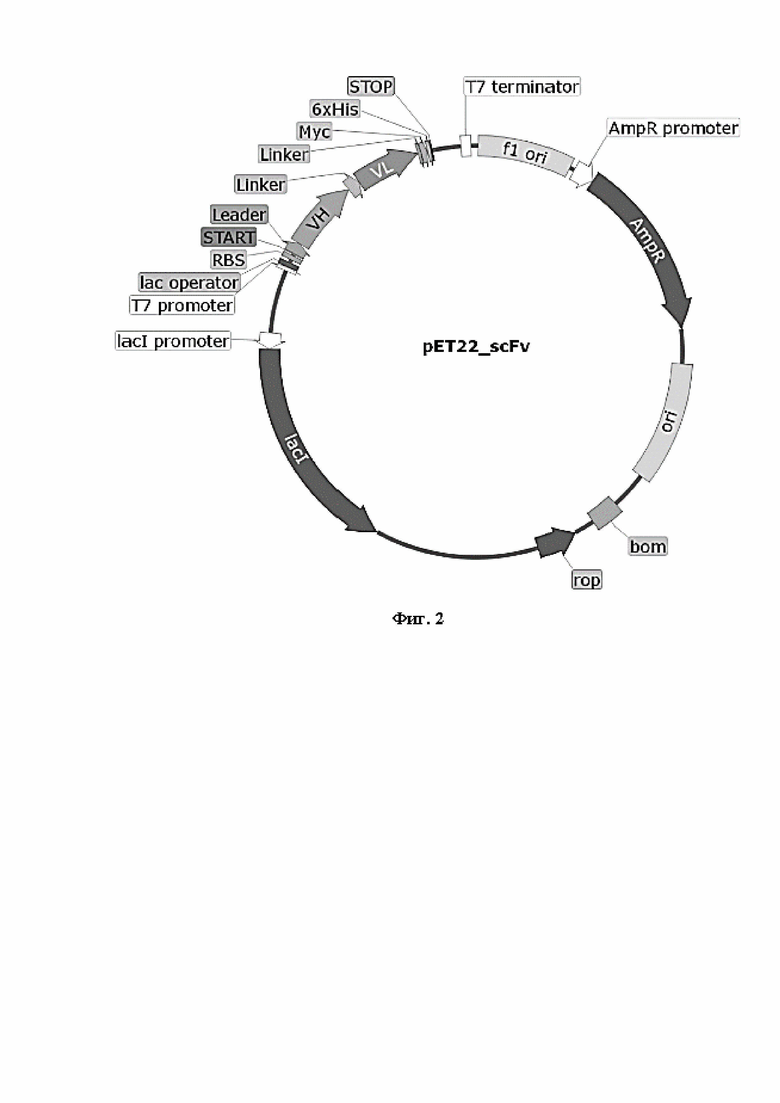
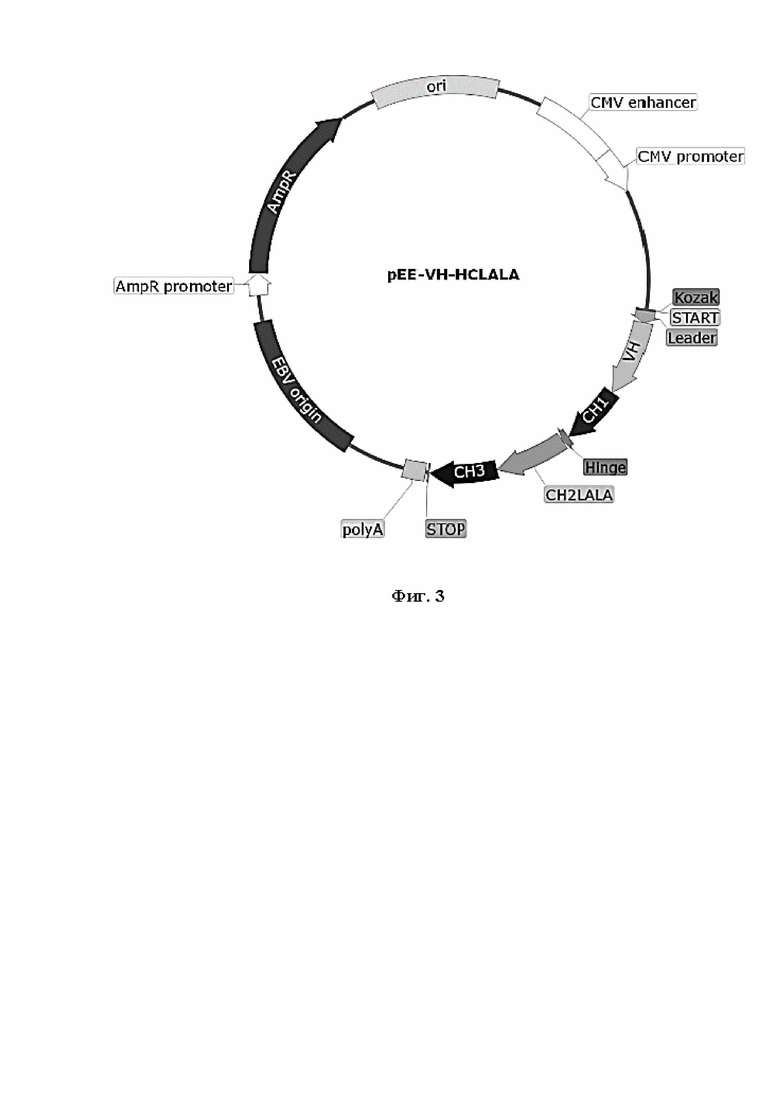
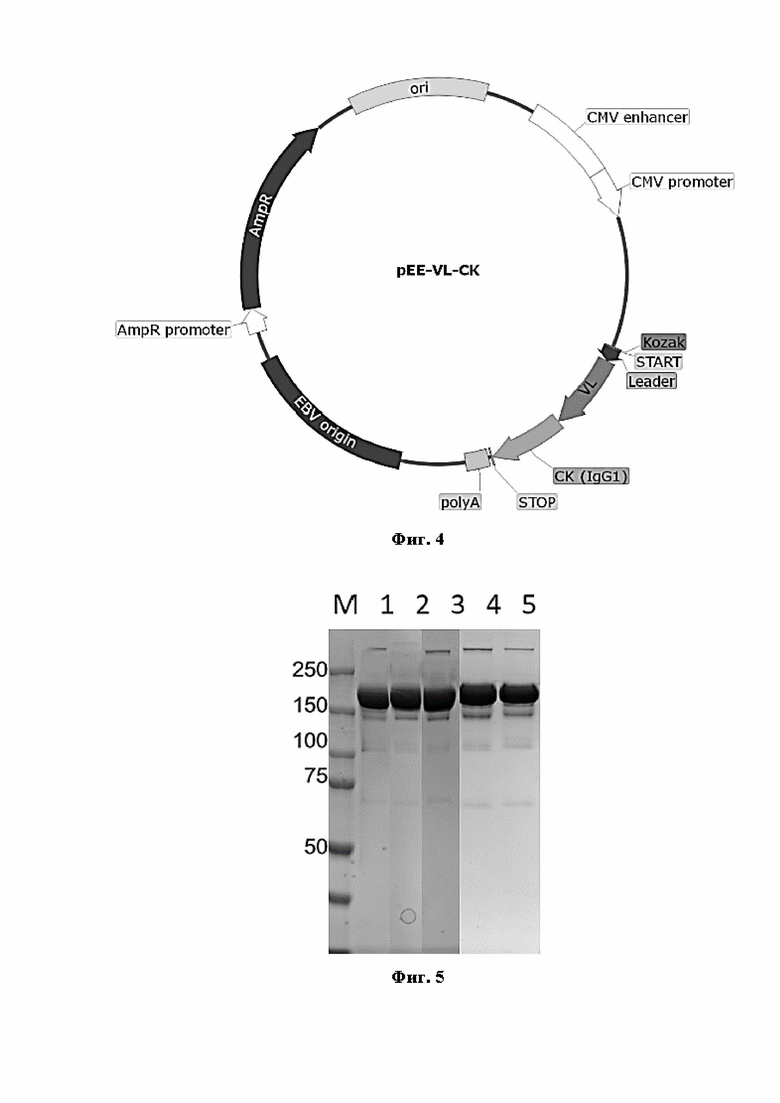
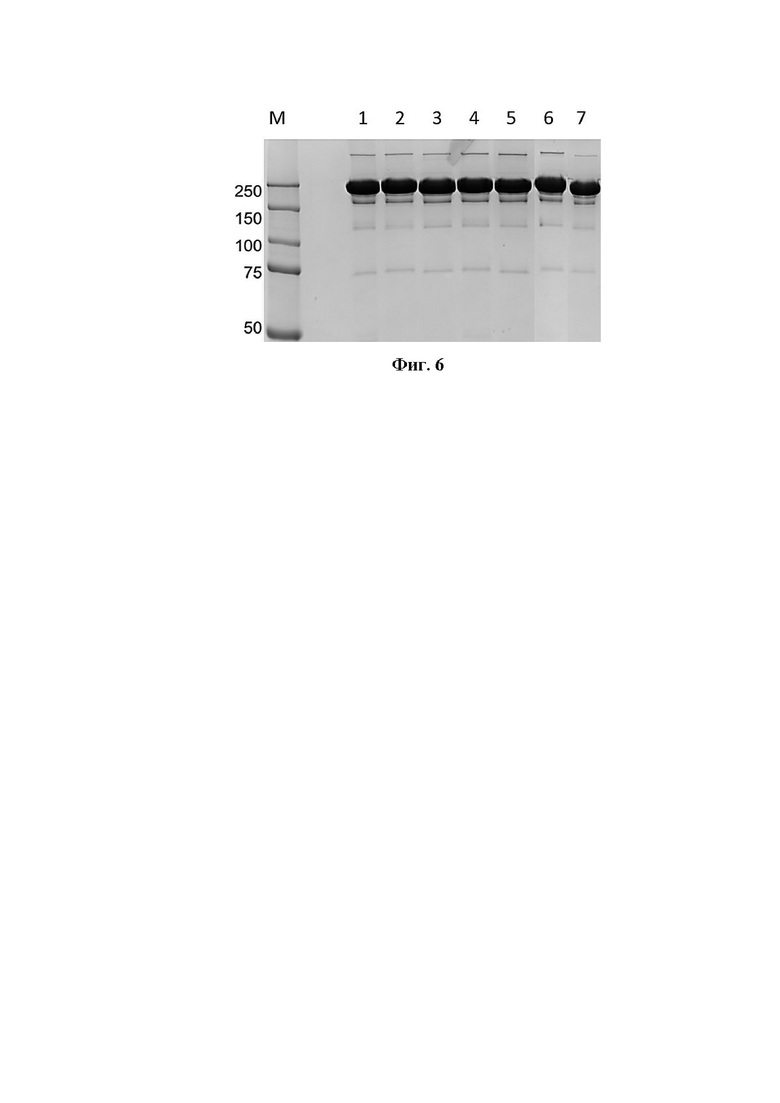
Изобретение относится к области биохимии, в частности к выделенному моноклональному антителу или его антигенсвязывающему фрагменту, которое специфически связывается с BCMA. Изобретение позволяет получать антитело, которое эффективно специфически связывается с BCMA. 12 з.п. ф-лы, 6 ил., 6 табл., 8 пр.
1. Выделенное моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с BCMA, включающее:
(a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3;
CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 4, SEQ ID NO: 5 или SEQ ID NO: 6;
и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15;
CDR2 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24;
и
CDR3 с аминокислотной последовательностью, которую выбирают из группы: SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34 или SEQ ID NO: 35.
2. Выделенное моноклональное антитело или его антигенсвязывающий фрагмент по п. 1, включающее:
(i) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 8,
CDR2 с аминокислотной последовательностью SEQ ID NO: 16 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 25;
(ii) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 9,
CDR2 с аминокислотной последовательностью SEQ ID NO: 17 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 26;
(iii) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 3,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 10,
CDR2 с аминокислотной последовательностью SEQ ID NO: 18 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 27;
(iv) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 11,
CDR2 с аминокислотной последовательностью SEQ ID NO: 19 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 28;
(v) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 29;
(vi) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 6 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 30;
(vii) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 10,
CDR2 с аминокислотной последовательностью SEQ ID NO: 21 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 31;
(viii) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7, и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 13,
CDR2 с аминокислотной последовательностью SEQ ID NO: 22 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 32;
(ix) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 12,
CDR2 с аминокислотной последовательностью SEQ ID NO: 20 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 30;
(x) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 14,
CDR2 с аминокислотной последовательностью SEQ ID NO: 23 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 33;
(xi) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 4 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 8,
CDR2 с аминокислотной последовательностью SEQ ID NO: 24 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 34;
или
(xii) (a) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 2,
CDR2 с аминокислотной последовательностью SEQ ID NO: 5 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 7; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 15,
CDR2 с аминокислотной последовательностью SEQ ID NO: 17 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 35.
3. Выделенное моноклональное антитело или его антигенсвязывающий фрагмент по п. 1, где вариабельный домен тяжелой цепи содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 41, SEQ ID NO: 42 или SEQ ID NO: 43.
4. Выделенное моноклональное антитело или его антигенсвязывающий фрагмент по п. 1, где вариабельный домен легкой цепи содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 48, SEQ ID NO: 49, SEQ ID NO: 50, SEQ ID NO: 51, SEQ ID NO: 52, SEQ ID NO: 53 или SEQ ID NO: 54.
5. Выделенное моноклональное антитело или его антигенсвязывающий фрагмент по п. 1, где:
(а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 41, SEQ ID NO: 42 или SEQ ID NO: 43; и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 48, SEQ ID NO: 49, SEQ ID NO: 50, SEQ ID NO: 51, SEQ ID NO: 52, SEQ ID NO: 53 или SEQ ID NO: 54.
6. Выделенное моноклональное антитело или его антигенсвязывающий фрагмент по п. 5, где:
(i) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 36 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 44;
(ii) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 37 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 45;
(iii) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 38 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 46;
(iv) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 39 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 47;
(v) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 48;
(vi) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 41 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 49;
(vii) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 50;
(viii) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 51;
(ix) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 49;
(x) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 42 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 52;
(xi) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 43 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 53;
или
(xii) (а) вариабельный домен тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 40 и
(b) вариабельный домен легкой цепи содержит аминокислотную последовательность SEQ ID NO: 54.
7. Выделенное моноклональное антитело по любому из пп. 1-6, где антитело, которое специфично связывается с BCMA, представляет собой полноразмерное антитело IgG.
8. Выделенное моноклональное антитело по п. 7, где полноразмерное антитело IgG относится к изотипу IgG1, IgG2, IgG3 или IgG4 человека.
9. Выделенное моноклональное антитело по п. 8, где полноразмерное антитело IgG относится к изотипу IgG1 человека.
10. Выделенное моноклональное антитело по п. 9, где антитело содержит мутации L234A и L235A согласно нумерации аминокислот антител EU в CH2 участке.
11. Выделенное моноклональное антитело по п. 1, включающее тяжелую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 55, SEQ ID NO: 56, SEQ ID NO: 57, SEQ ID NO: 58, SEQ ID NO: 59, SEQ ID NO: 60, SEQ ID NO: 61 или SEQ ID NO: 62.
12. Выделенное моноклональное антитело по п. 1, включающее легкую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 65, SEQ ID NO: 66, SEQ ID NO: 67, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 70, SEQ ID NO: 71, SEQ ID NO: 72 или SEQ ID NO: 73.
13. Выделенное моноклональное антитело по п. 1, включающее:
(i) (a) тяжелую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 55, SEQ ID NO: 56, SEQ ID NO: 57, SEQ ID NO: 58, SEQ ID NO: 59, SEQ ID NO: 60, SEQ ID NO: 61 или SEQ ID NO: 62, и
(b) легкую цепь, содержащую аминокислотную последовательность, которую выбирают из группы: SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 65, SEQ ID NO: 66, SEQ ID NO: 67, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 70, SEQ ID NO: 71, SEQ ID NO: 72 или SEQ ID NO: 73.
14. Выделенное моноклональное антитело по п. 13, включающее:
(i) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 55, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 63;
(ii) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 56, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 64;
(iii) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 57, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 65;
(iv) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 58, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 66;
(v) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 67;
(vi) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 60, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 68;
(vii) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 69;
(viii) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 70;
(ix) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 68,
(x) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 61, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 71;
(xi) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 62, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 72;
или
(xii) (a) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
(b) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 73.
| WO 2021248005 A1, 09.12.2021 | |||
| WO 2018201051 A1, 01.11.2018 | |||
| RU 2019123366 A, 24.02.2021 | |||
| A.K | |||
| SHRINER and et.al., Comparison of the human immune response to conjugate and polysaccharide pneumococcal vaccination using a reconstituted SCID mouse model, Vaccine, 24 (2006), pp | |||
| Автомобиль с двумя направляющими осями | 1925 |
|
SU7197A1 |
Авторы
Даты
2024-06-03—Публикация
2022-06-09—Подача