Изобретение относится к способам модификации лигнина и касается нитрозирования сульфатного лигнина, что расширяет возможности для его практического использования, например, в качестве усилителя синтетического каучука; при производстве керамики, пластических масс; диметилсульфида [1].
Реакция нитрозирования относится к реакциям электрофильного замещения атомов водорода бензольного ядра на нитрозогруппу. Она является широко применяемой в органическом синтезе и в аналитической химии. Электрофильным реагентом при нитрозировании является катион нитрозония, который образуется из азотистой кислоты. Так как азотистая кислота является неустойчивым соединением, то ее генерируют из устойчивых солей прямо в реакционной смеси путем подкисления. То есть нитрозирование проводится в кислой среде.
Благодаря высокой химической активности, мягким условиям проведения реакций с помощью азотистой кислоты и ее производных получают различные классы соединений [2], [3], [4].
Каталитические свойства азотистой кислоты ускоряют проведение некоторых органических реакций [5], [6].
В качестве аналитического реагента азотистая кислота используется для определения огромного числа органических соединений [7].
В химии древесины азотистая кислота и нитриты также нашли разнообразное применение. Известны предложения использовать нитритные обработки в схемах отбелки целлюлозы [8], модификации лигносульфоновых кислот с целью получения комплексонатов с катионами биогенных металлов [9], [10], [11], [12].
Сульфатный лигнин (СЛ) является одним из видов технических лигнинов. Он образуется в процессе сульфатной варки целлюлозы. В отличие от лигносульфоновых кислот сульфатный лигнин не растворяется в воде и водных растворах кислот. То есть при нитрозировании реакция будет проходить в гетерогенных условиях.
Наиболее близким к заявляемому решению является способ нитрозирования сульфатного лигнина путем смешения нитрита натрия и сульфатного лигнина и последующей выдержки реакционной смеси [13]. Нитрозирование проводится гомогенных условиях в водно-диоксановом растворе. Для подкисления используются водные растворы кислотных реагентов [прототип] Недостатком способа является то, что после проведения реакции реакционная смесь содержит примеси неорганических солей, образующихся в результате реакции образования азотистой кислоты, выступающей в роли нитрозирующего реагента:
NaNO2 + HX = NaX + HNO2
где X – анион кислотного реагента.
Задача изобретения заключается в получении нитрозированного сульфатного лигнина, не содержащего примесей катионов и проведение реакции в гомогенных условиях с высокой эффективностью процесса.
Это достигается тем, что модификация сульфатного лигнина включает приготовление растворов исходных реагентов, их смешение, подкисление, выдержку и проводится в водно-органическом растворителе.
Для этого первоначально готовят раствор сульфатного лигнина в органическом растворителе. В полученный раствор добавляют заданный объем водного раствора нитрита натрия. Полученную реакционную смесь подкисляют с помощью катионообменной смолы (катионита) и выдерживают в течение заданного времени. О протекании нитрозирования судят по изменению электронных спектров.
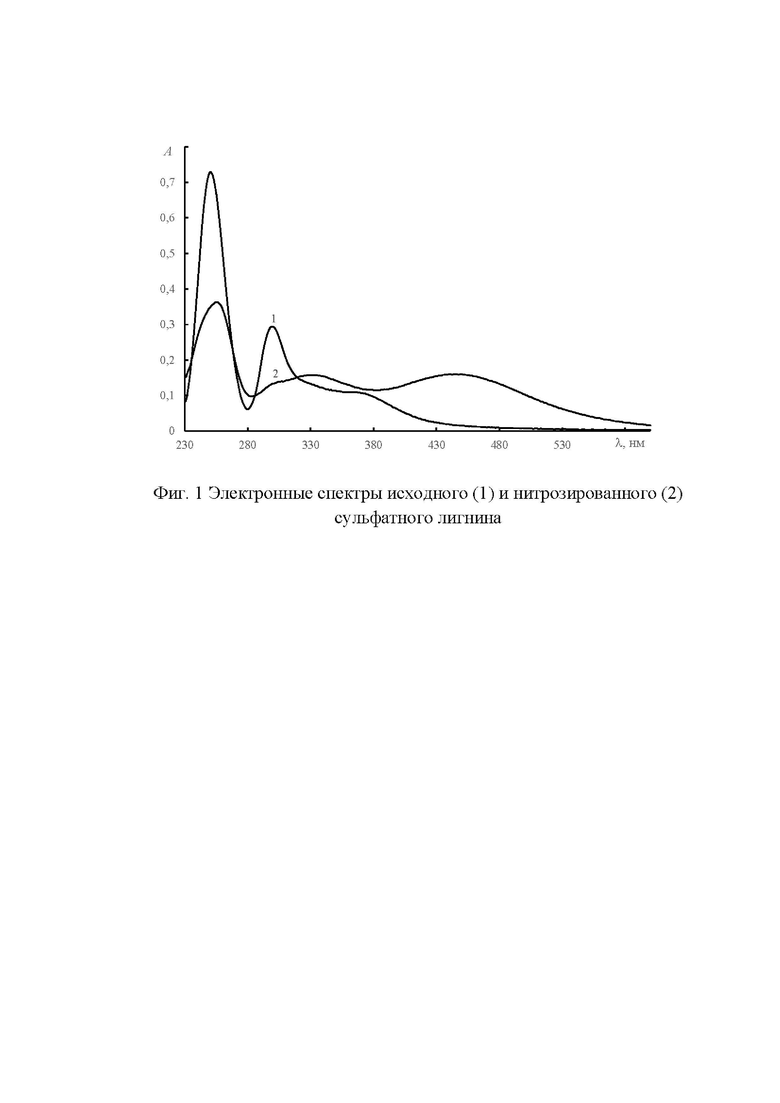
При нитрозировании сульфатного лигнина в его молекуле появляется нитрозогруппы. Нитрозогруппы значительно изменяют характер электронных спектров поглощения. При подщелачивании раствора на спектре щелочного раствора нитрозированного лигнина в области 400…500 нм появляется дополнительная полоса поглощения, вызванная таутомерной хинон-монооксимной формой нитрозированной молекулы (Фиг. 1).
Пример 1. Предварительно были приготовлены растворы сульфатного лигнина в диоксане концентрацией 100 мг/мл и нитрита натрия в воде концентрацией 133 мг/мл. В микрореактор помещают 5 мл раствора сульфатного лигнина в диоксане, добавляют 1,5 мл водного раствора нитрита натрия. Затем добавляют 3 г катионита КУ-2-8. Через заданные промежутки времени (3, 5, 18, 30, 45 и 60 мин) отбирают по 0,1 мл реакционной смеси и переносят в мерную колбу вместимостью 25 мл, куда предварительно вносят 2,5 мл 1 М раствора гидроксида натрия для прекращения реакции нитрозирования. Объем раствора доводят до метки дистиллированной водой. Измеряют оптическую плотность при 430 нм (А430). Выделения осадка в условиях реакции не наблюдалось, т.е. реакция проходит в гомогенных условиях. Результаты приведены в таблице 1.
Таблица 1
Пример 2. Предварительно были приготовлены растворы сульфатного лигнина в диоксане концентрацией 33,3 мг/мл и нитрита натрия в воде концентрации 33,7 мг/мл. В микрореактор помещают 3 мл раствора сульфатного лигнина в диоксане, добавляют 1,5 мл водного раствора нитрита натрия. Затем добавляют 1 г катионита КУ-2-8. Через заданные промежутки времени (0, 5, 10, 15, 20, 30 мин) отбирают по 0,1 мл реакционной смеси и переносят в мерную колбу вместимостью 25 мл, куда предварительно вносят 2,5 мл 1 М раствора гидроксида натрия. Объем раствора доводят до метки дистиллированной водой. Измеряют оптическую плотность при 430 нм (А430). Выделения осадка в условиях реакции не наблюдалось, т.е. реакция проходит в гомогенных условиях. Результаты измерения оптической приведены в таблице 2.
Таблица 2
Пример 3. Способ нитрозирования сульфатного лигнина в условиях примера 2, отличающийся тем, что объем раствора нитрита составил 0,9 мл, а масса катионита КУ-2-8 составила 0,75 г. Выделения осадка в условиях реакции не наблюдалось, т.е. реакция проходит в гомогенных условиях. Результаты измерения оптической приведены в таблице 3.
Таблица 3
Пример 4. Способ нитрозирования сульфатного лигнина в условиях примера 2, отличающийся тем, что в качестве органического растворителя использовали диметилсульфоксид (ДМСО). Объем раствора сульфатного лигнина в ДМСО 3,5 мл, концентрация 20 мг/мл. Объем нитрита натрия составил 1 мл, концентрация 28 мг/мл. Масса катионита КУ-2-8 составила 0,8 г. Выделения осадка в условиях реакции не наблюдалось, т.е. реакция проходит в гомогенных условиях. Результаты измерения оптической приведены в таблице 4.
Таблица 4
Пример 5. Способ нитрозирования сульфатного лигнина в условиях примера 4, отличающийся тем, что объем раствора сульфатного лигнина составил 3,2 мл, а нитрита натрия 0,7 мл. Вместо катионита КУ-2-8 был использован катионит - вофатит, масса которого составила 0,7 г. Выделения осадка в условиях реакции не наблюдалось, т.е. реакция проходит в гомогенных условиях. Результаты измерения оптической показали прирост оптической плотности в 1,3 раза.
Таким образом, полученные результаты свидетельствуют о том, что проведение модификации сульфатного лигнина с помощью реакции нитрозирования в водно-органической среде позволяет провести реакцию в гомогенных условиях и добиться высокой эффективности процесса без примесей катионов.
По результатам экспериментов оптимальная продолжительность нитрозирования сульфатного лигнина в зависимости от расхода реагентов 15 - 30 минут.
Источники:
[1] Химия нитро- и нитрозогрупп. Под ред. Г. Фойера. Пер. с англ. Под ред. С.С. Новикова. Т. 1. – М.: Мир, 1972. – 536 с. Feuer H. (ed.) The chemistry of nitro and nitroso groups. Part 1. – N.Y.: John Wiley & Sons, 1969. – 771 p.
[2] Общая органическая химия. Под ред. Д. Бартона и У.Д. Оллиса. Т. 3. Азотсодержащие соединения. Под ред. И.О. Сазерленда. – Пер. с англ. Под ред. Н.К. Кочеткова и Л.В. Бакинского. – М.: Химия, 1982. – 736 с.
[3] Товбис М.С., Субоч Г.А. Нитрозофенолы и нитрозоанилины – синтез, свойства. – Красноярск: СибГТУ, 2013. – 159 с.
[4] Беляев Е.Ю., Гидаспов Б.В. Ароматические нитрозосоединения. – Л.: Химия, 1989. – 176 с.
[5] Ингольд К. Теоретические основы органической химии. – Пер. с англ. К.П. Бутина; под ред. проф. И.П. Белецкой. – М.: Мир, 1973. – 1056 с.
[6] Коренман И.М. Фотометрический анализ. Методы определения органических соединений. – М.: Химия, 1975. – 360 с.
[7] Гоготов А.Ф. Нитритные обработки небеленых целлюлоз с последующей кислородно-щелочной делигнификацией // Химия растительного сырья. – 1999. – № 1. – С 89-97.
[8] Khabarov Yu.G., Koshutina N.N. Complex formation by the modified lignosulfonic acids with cations of various metals. – Sixth European Workshop on Lignocel-lulosics and Pulp "Advanced in Lignocellulosics Chemistry Towards High Quality Processes and Products". – France. Bordeaux, 2000. – P. 391-393.
[9] Пат. 2165936 РФ. Способ получения щелочерастворимого хелата железа / Ю.Г. Хабаров, Н.Н. Кошутина, А.Е. Шергин // Открытия. Изобретения. – 2001. – № 12.
[10] Pat. 5169931 US. Int. Cl. C08H 5/02. Nitrite-oxidized lignosulfonates and method of making the same and use of these as dispersants / K.D. Sears, G.J. Byrd. – Publ. Dec. 8, 1992.
[11] Гоготов А.Ф. Нитриты в процессах модификации, переработки и исследования лигнина и лигноцеллюлозных материалов // Химия в интересах устойчивого развития. – 1999. – № 7. – C. 223-227.
[12] Гоготов А.Ф. Нитрозолигнин в качестве стабилизатора целлюлозы при гипохлоритной отбелке // Химия растительного сырья. – 1999. – № 4. – С. 9-12.
[13] Пат. 2566503 РФ. МПК C07G 1/00 (2011.01), C08H 7/00 (2011.01). Способ нитрозирования сульфатного лигнина / Ю.Г. Хабаров, И.М. Бабкин, А.А. Рекун, О.В. Максименко // Бюл. – 2015. – № 30.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ НИТРОЗИРОВАНИЯ СУЛЬФАТНОГО ЛИГНИНА | 2014 |
|
RU2566503C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРОЗОПРОИЗВОДНЫХ ЛИГНОСУЛЬФОНАТОВ | 2007 |
|
RU2363702C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЩЕЛОЧЕРАСТВОРИМОГО ХЕЛАТА ЖЕЛЕЗА | 1998 |
|
RU2165936C2 |
| Способ модификации сульфатного лигнина | 2020 |
|
RU2753533C1 |
| Термогазохимический бинарный состав и способ применения для обработки призабойной и удаленной зон нефтегазоносного пласта | 2015 |
|
RU2637259C2 |
| Стабилизатор коллоидного раствора серебра | 2022 |
|
RU2794897C1 |
| 3-МЕТИЛ-4-НИТРОЗОПИРАЗОЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2440343C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАГНИТОАКТИВНОГО СОЕДИНЕНИЯ | 2011 |
|
RU2453500C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4,6-ТРИАМИНО-5-НИТРОЗОПИРИМИДИНА | 1993 |
|
RU2054423C1 |
| СПОСОБ СИНТЕЗА п-НИТРОЗОФЕНОЛА И УСТРОЙСТВО ДЛЯ ПОЛУЧЕНИЯ п-НИТРОЗОФЕНОЛА ЭТИМ СПОСОБОМ | 2023 |
|
RU2813692C1 |
Изобретение относится к способу модификации лигнина и касается нитрозирования сульфатного лигнина, что расширяет возможности для его практического использования, например, в качестве усилителя синтетического каучука при производстве керамики, пластических масс, диметилсульфида. Способ нитрозирования сульфатного лигнина заключается в смешении водного раствора нитрита натрия, раствора сульфатного лигнина в органическом растворителе и добавлении кислотного реагента с последующей выдержкой реакционной смеси, при этом в качестве органического растворителя используют диметилсульфоксид, а в качестве кислотного реагента используют катионообменную смолу. Технический результат изобретения заключается в получении нитрозированного сульфатного лигнина, не содержащего примесей катионов, и проведении реакции в гомогенных условиях с высокой эффективностью процесса. 1 ил., 4 табл., 5 пр.
Способ нитрозирования сульфатного лигнина путем смешения водного раствора нитрита натрия, раствора сульфатного лигнина в органическом растворителе и добавления кислотного реагента с последующей выдержкой реакционной смеси, отличающийся тем, что в качестве органического растворителя используют диметилсульфоксид, а в качестве кислотного реагента используют катионообменную смолу.
| СПОСОБ НИТРОЗИРОВАНИЯ СУЛЬФАТНОГО ЛИГНИНА | 2014 |
|
RU2566503C1 |
| Скрипников Е.А | |||
| и др | |||
| ИЗУЧЕНИЕ НИТРОЗИРОВАНИЯ ЛИГНОСУЛЬФОНОВЫХ КИСЛОТ МЕТОДОМ ЭЛЕКТРОННОЙ СПЕКТРОСКОПИИ | |||
| ФИЗИКОХИМИЯ РАСТИТЕЛЬНЫХ ПОЛИМЕРОВ | |||
| Материалы IX международной конференции | |||
| Архангельск, 30 июня - 02 июля 2021, Издательство: Северный (Арктический) федеральный университет имени М.В | |||
| Ломоносова, 196-200 с | |||
| Гоготов | |||
Авторы
Даты
2024-05-22—Публикация
2023-07-28—Подача