ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к антигенсвязывающему полипептиду, в частности к антигенсвязывающему полипептиду, который связывается с CD47, и его антигенсвязывающей части, и к способу применения таких антигенсвязывающих полипептидов и их антигенсвязывающих частей.
УРОВЕНЬ ТЕХНИКИ
CD47, также известный как белок, ассоциированный с интегрином, представляет собой трансмембранный гликопротеин, широко экспрессируемый среди множества видов и тканей. Он является членом суперсемейства иммуноглобулинов. CD47 весит около 50 кД и содержит 1 внеклеточный Ig-подобный вариабельный домен, 5 сильно гидрофобных удлиненных трансмембранных сегментов и 1 короткий альтернативно сплайсированный карбоксиконцевой цитоплазматический хвост.
Ингибиторный рецептор сигнально-регуляторного белка α (SIRPα) является одним из лигандов CD47, который связывается с NH2-концевым IgV-подобным доменом SIRPα. SIRPα экспрессируется преимущественно в клетках миелоидного происхождения, включая макрофаги, гранулоциты, DC-клетки, тучные клетки и их предшественники, включая гемопоэтические стволовые клетки. Например, CD47 может ингибировать фагоцитарную функцию макрофагов путем связывания с белком SIRPα на поверхности макрофагов. Было показано, что блокирование CD47-опосредованного связывания с SIRPα на фагоцитах или потеря экспрессии у мышей с нокаутом CD47 может вызывать удаление жизнеспособных клеток и несостарившихся эритроцитов. Для тех клеток, в которых все еще присутствуют префагоцитарные сигналы, блокирование SIRPα также позволяет осуществлять фагоцитоз мишеней, которые в норме не фагоцитируются.
Запрограммированная гибель клеток (ЗГК, PCD) и фагоцитарное удаление представляют собой обычные способы, с помощью которых организмы отвечают на наличие и осуществляют удаление поврежденных, предраковых или инфицированных клеток. Таким образом, у клеток, которые выживают после такого ответа организма, (раковых клеток, хронически инфицированных клеток и т.д.), есть способы как избежать ЗГКи фагоцитарное удаление. CD47 конститутивно активируется в различных типах больных, раковых и инфицированных клеток, что позволяет этим клеткам уклоняться от фагоцитоза. Соединения против CD47, которые блокируют взаимодействие между CD47 на одной клетке (раковой клетке, хронически инфицированной клетке и т.д.) и SIRPα на другой клетке (фагоците), могут противодействовать увеличению экспрессии CD47 и способствовать фагоцитозу раковых клеток и/или инфицированных клеток.
Экспрессия и/или активность CD47 связаны с рядом заболеваний и нарушений. Различные исследования продемонстрировали, что почти все опухолевые клетки и опухолевые ткани в высокой степени экспрессируют CD47. CD47, высоко экспрессируемый на поверхности опухолевых клеток, связывается с SIRPα на поверхности макрофагов, посылая сигнал «не ешь меня», так что макрофаги в области инфильтрации опухолевой ткани хорошо ладят с опухолевыми клетками и даже способствуют экспансии и росту опухолевых клеток путем облегчения пролиферации кровеносных сосудов в опухолях и подавления эффекторных Т-клеток. Таким образом, существует потребность в CD47-направленной терапии.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В данном изобретении предложены новый выделенный антигенсвязывающий полипептид, который связывается с CD47, и его антигенсвязывающая часть в качестве решения для CD47-направленной терапии.
В одном аспекте в данном изобретении предложены выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, при этом антигенсвязывающий полипептид содержит следующие области, определяющие комплементарность:
CDR1 тяжелой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 1, 2, 3, 4 и 5;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 6, 7, 8, 9 и 10;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 11, 12, 13, 14 и 15;
CDR1 легкой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 16, 17, 18, 19 и 20;
CDR2 легкой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 21, 22, 23, 24 и 25; и
CDR3 легкой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 26, 27, 28, 30 и 32;
При этом последовательность, указанная в SEQ ID NO: 32, представляет собой QQFSX2STWT, где X2 представляет собой D или E.
В другом аспекте в данном изобретении предложены выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, при этом антигенсвязывающий полипептид содержит следующие области, определяющие комплементарность:
CDR1 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 1, 2, 3, 4 и 5, или их консервативно модифицированных форм;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 6, 7, 8, 9 и 10, или их консервативно модифицированных форм;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 11, 12, 13, 14 и 15, или их консервативно модифицированных форм;
CDR1 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 16, 17, 18, 19 и 20, или их консервативно модифицированных форм;
CDR2 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 21, 22, 23, 24 и 25, или их консервативно модифицированных форм; и
CDR3 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 26, 27, 28, 30 и 32, или их консервативно модифицированных форм.
В другом аспекте в данном изобретении предложены выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, при этом антигенсвязывающий полипептид содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 33, 35, 37, 39, 41, 83, 85 и 87, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 34, 36, 38, 40, 42, 84, 86 и 88,
при этом последовательность, представленная в SEQ ID NO: 83, представляет собой:
QVQLVQSGAEVKKPGSSVKVSCKASGYTFSRYWIEWVRQAPGQGLEWMGEFIPGSDTTNYAQKFQGRVTITAX3X4STX5TAYMELSSLRSEDTAVYYCARGGLRRMDYWGQGTLVTVSS, где X3 представляет собой D или E, X4 представляет собой I или E, а X5 представляет собой S или N;
последовательность, представленная в SEQ ID NO: 84, представляет собой:
DIQMTQSPSSLSASVGDRVTITCRASSSVSSTYLHWYQQKPGKAPKLX6IYTTSTLASGVPSRFSGSGSGTX7X8TLTISSLQPEDFATYYCQQFSX2STWTFGQGTKLEIK, где X6 представляет собой L или W, X7 представляет собой D или S, X8 представляет собой F или Y, а X2 представляет собой D или E;
последовательность, представленная в SEQ ID NO: 85, представляет собой:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTNYGMNWVRQAPGQGLX9WMGWIN TNTGEPTYAQX10LQGRVTMTX11DTSTX12TAYMELRSLRSDDTAVYYCX13RFSHLRGPMD YWGQGTLVTVSS, где X9 представляет собой E или K, X10 представляет собой K или E, X11 представляет собой L или T, X12 представляет собой R или S, и X13 представляет собой A или T;
последовательность, представленная в SEQ ID NO: 86, представляет собой:
DX14QMTQSPSSLSASVGDRVTITCRSSQSLVHSNGYTYLHWYQQKPGKAPKLLIYKVSNRFSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCSQSTHVPPTFGQGTKLEIK, где X14 представляет собой I или A;
последовательность, представленная в SEQ ID NO: 87, представляет собой:
QVQLVQSGAEVKKPGASVKVSCKX15SGFNIEDDYIEWVRQAPGQGLEWMGRIDPANDKTKYAQKFQGRVTMTX16DTSTX17TVYMELSSLRSEDTAVYYCX18RPGLRRYYSMDYWGQGTLVTVSS, где X15 представляет собой A или V, X16 представляет собой R или G, X17 представляет собой S или N, и X18 представляет собой A или T;
последовательность, представленная в SEQ ID NO: 88, представляет собой:
DIQMTQSPSSLSASVGDRVTITCKASENVVSYVSWYQQKPGKAPKLLIYGASNRYTGVPSRFX19GSGSX20TDFTLTISSLQPEDFATYYCGQSYSYPLTFGQGTKLEIK, где X19 представляет собой S или I, и X20 представляет собой S или G.
В другом аспекте в данном изобретении предложены выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, при этом антигенсвязывающий полипептид или его антигенсвязывающая часть обладают одним или комбинацией нескольких из следующих свойств:
(a) связывание с CD47 со значением KD 1,89E-08 или менее (например, 1,53E-08 или менее);
(b) блокирование связывания CD47 с SIRPα;
(c) стимулирование опосредованного макрофагами фагоцитоза CD47-экспрессирующих клеток;
(d) не вызывает значимого апоптоза CD4+Т-клеток;
(e) не вызывает существенной гематоцитопении, анемии или агглютинации эритроцитов; и
(f) антигенсвязывающий полипептид или его антигенсвязывающая часть имеют температуру плавления T ≥ 62°C и температуру агрегации Tagg ≥ 61°C.
В другом аспекте в данном изобретении предложены выделенный антигенсвязывающий полипептид или его антигенсвязывающая часть, при этом антигенсвязывающий полипептид или его антигенсвязывающая часть связываются с тем же эпитопом на CD47, что и любой из иллюстративных антигенсвязывающих полипептидов или их антигенсвязывающих частей, представленных в данном документе.
В другом аспекте в данном изобретении предложены выделенный антигенсвязывающий полипептид или его антигенсвязывающая часть, при этом антигенсвязывающий полипептид или его антигенсвязывающая часть конкурируют за связывание с CD47 с любым из иллюстративных антигенсвязывающих полипептидов или их антигенсвязывающих частей, представленных в данном документе, при этом конкуренцию измеряют с помощью ИФА, проточной цитометрии или анализа поверхностного плазмонного резонанса.
В данном документе антигенсвязывающая часть может быть выбрана из Fab-фрагмента, Fab'-фрагмента, F(ab')2-фрагмента, Fd-фрагмента, Fv-фрагмента, dAb-фрагмента, изолированной области, определяющей комплементарность, и нанотела, но не ограничивается этим.
В другом аспекте в данном изобретении предложен иммуноконъюгат, содержащий антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающую часть, описанные в данном документе, и терапевтический агент, связанный или конъюгированный с антигенсвязывающим полипептидом или его антигенсвязывающей частью.
В контексте данного документа антигенсвязывающий полипептид или его антигенсвязывающая часть могут быть связаны с терапевтическим агентом с помощью линкера. Линкер может быть расщепляемым или нерасщепляемым.
В контексте данного документа терапевтический агент может быть выбран из цитотоксических препаратов, радиоизотопов или иммуномодуляторов, например, химиотерапевтических агентов, иммунодепрессантов, иммуностимуляторов, антиметаболитов, алкилирующих агентов, антибиотиков, антиангиогенных агентов, антимитотических агентов, токсинов и апоптотических агентов.
В другом аспекте в данном изобретении предложена композиция, содержащая компонент А и фармацевтически приемлемый носитель, при этом компонент А представляет собой антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающую часть, описанные в данном документе, или иммуноконъюгат, описанный в данном документе.
В другом аспекте в данном изобретении предложена выделенная клеточная линия гибридомы, выбранная из группы, состоящей из 2B2, 2H8, 3F10, 16E5 и 14A9.
В другом аспекте в данном изобретении предложена выделенная нуклеиновая кислота, кодирующая антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающую часть, описанные в данном документе.
В другом аспекте в данном изобретении предложен вектор, содержащий нуклеиновую кислоту, описанную в данном документе.
В другом аспекте в данном изобретении предложена клетка-хозяина, содержащая вектор, описанный в данном документе, или в геном которой интегрирована выделенная нуклеиновая кислота, описанная в данном документе. Предпочтительно вектор представляет собой вектор экспрессии.
В еще одном аспекте в данном изобретении предложен способ получения антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части, который включает: культивирование клетки-хозяина, описанной в данном документе, в условиях, подходящих для экспрессии нуклеиновой кислоты, кодирующей антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающей части, описанные в данном документе, и выделение экспрессированного антигенсвязывающего полипептида или его антигенсвязывающей части.
В еще одном аспекте в данном изобретении предложен способ уменьшения опухоли или ингибирования роста опухолевых клеток у субъекта, который включает введение субъекту терапевтически эффективного количества антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части, описанных в данном документе, иммуноконъюгата, описанного в данном документе, или композиции, описанной в данном документе.
В еще одном аспекте в данном изобретении предложен способ лечения онкологического заболевания у нуждающегося в этом субъекта, который включает введение субъекту терапевтически эффективного количества антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части, описанных в данном документе, иммуноконъюгата, описанного в данном документе, или композиции, описанной в данном документе.
В еще одном аспекте в данном изобретении предложен способ стимуляции фагоцитоза макрофагами у субъекта, который включает введение субъекту эффективного количества антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части, описанных в данном документе, иммуноконъюгата, описанного в данном документе, или композиции, описанной в данном документе.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 представлено влияние химерных антител против CD47 на агглютинацию эритроцитов, при этом образцы (антитела или контроли) в одном ряду относятся к одному типу, но имеют разные концентрации, а образцы в одном столбце имеют одинаковую концентрацию, но относятся к разным типам; концентрации образцов в разных столбцах слева направо составляют 10000 нг/мл, 3333,33 нг/мл, 1111,11 нг/мл, 370,37 нг/мл, 123,46 нг/мл, 41,15 нг/мл, 13,72 нг/мл и 4,57 нг/мл, соответственно; образцы в разных рядах представляют собой, сверху вниз, Xi2B2, Xi2H8, Xi3F10, Xi16E5, Xi14A9, Xi16E5-2 (еще один повтор Xi16E5), Hu5F9, IgG4 и ФСБ соответственно.
На Фиг. 2 представлено влияние некоторых гуманизированных антител против CD47 на агглютинацию эритроцитов, при этом образцы в одной колонке относятся к одному типу, но имеют разные концентрации, а образцы в одном ряду имеют одинаковую концентрацию, но относятся к разным видам; концентрации антител в разных рядах сверху вниз составляют 10000 нг/мл, 3333,33 нг/мл, 1111,11 нг/мл, 370,37 нг/мл, 123,46 нг/мл, 41,15 нг/мл, 13,72 нг/мл и 4,57 нг/мл, соответственно; антитела в столбцах 1-12, слева направо: hz3F10-1.1, hz3F10-2.1, hz3F10-3.1, hz3F10-4.1, hz3F10-5.1, hz3F10-6.1, hz3F10-1.2, hz3F10-2.2, hz3F10-3.2, hz3F10-4.2, hz3F10-5.2 и hz3F10-6.2, соответственно.
На Фиг. На Фиг. 3 представлено влияние некоторых гуманизированных антител против CD47 на агглютинацию эритроцитов, при этом образцы в одной колонке относятся к одному типу, но имеют разные концентрации, а образцы в одном ряду имеют одинаковую концентрацию, но относятся к разным видам; концентрации антител в разных рядах сверху вниз составляют 10000 нг/мл, 3333,33 нг/мл, 1111,11 нг/мл, 370,37 нг/мл, 123,46 нг/мл, 41,15 нг/мл, 13,72 нг/мл и 4,57 нг/мл, соответственно; антитела в столбцах 1-8, слева направо: hz16E5-1.1, hz16E5-3.1, hz16E5-1.2, hz16E5-3.2, hz16E5-1.3, hz16E5-3.3, hz14A9-2.3 и hz14A9-2.4, соответственно.
На Фиг. 4 представлено влияние антител против CD47 на выживаемость мышей.
На Фиг. 5 представлено изменения массы тела мыши с течением времени после однократного введения антител против CD47.
На Фиг. 6 представлено скорости изменения массы тела мыши в различные моменты времени после однократного введения антител против CD47.
На Фиг. 7 представлены изменения количества эритроцитов у мышей с течением времени после однократного введения антител против CD47.
На Фиг. 8 представлены скорости изменения количества эритроцитов у мышей в разные моменты времени после однократного введения антител против CD47.
На Фиг. 9 представлены изменения содержания гемоглобина у мышей с течением времени после однократного введения антител против CD47.
На Фиг. 10 представлены скорости изменения содержания гемоглобина у мышей в разные моменты времени после однократного введения антител против CD47.
На Фиг. 11 представлены изменения среднего объема опухоли с течением времени после введения антител против CD47 в мышиной модели клеток острого миелоидного лейкоза человека - MOLM-16.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Иллюстративные варианты реализации данного изобретения будут описаны ниже; однако специалистам в данной области техники будет понятно, что объем правовой охраны данного изобретения не ограничивается ими и что могут быть сделаны различные модификации, поправки или изменения на основе сущности и концепции данного изобретения, и содержание с этими модификациями, поправками или изменениями по-прежнему попадает в объем данного изобретения.
Терминология
Используемый в контексте данного документа термин «антигенсвязывающий полипептид» относится к полипептидам и белкам, имеющим, по меньшей мере, один антигенсвязывающий домен. Примеры антигенсвязывающего полипептида включают, но не ограничиваются ими, моноклональные антитела, мультиспецифические антитела или слитые белки. Используемый в контексте данного документа термин «антигенсвязывающая часть» антигенсвязывающего полипептида относится к одному или более фрагментам антигенсвязывающего полипептида, которые сохраняют способность специфически связываться с антигеном (например, белком CD47). Показано, что антигенсвязывающую функцию антигенсвязывающих полипептидов могут выполнять их фрагменты. Примеры, охватываемые термином «антигенсвязывающая часть» антигенсвязывающего полипептида, включают: (i) Fab-фрагменты, моновалентные фрагменты, состоящие из доменов VL, VH, CL и CH1; (ii) "Fab'-фрагменты", отличающиеся от Fab-фрагментов наличием нескольких дополнительных остатков, включая один или более цистеинов из шарнирной области антитела, на карбокси-конце домена CH1 тяжелой цепи; (iii) F(ab')2-фрагменты, бивалентные фрагменты, содержащие два Fab-фрагмента, соединенных дисульфидным мостиком шарнирной области; (iv) Fd-фрагменты, состоящие из доменов VH и CH1; (v) Fv-фрагменты, состоящие из доменов VL и VH одного плеча антитела; (vi) dAb-фрагменты (Ward et al., (1989) Nature 341:544-546), состоящие из доменов VH; (vii) изолированные области, определяющие комплементарность (CDR); и (viii) нанотела, содержащие вариабельную область тяжелой цепи, один вариабельный домен и два константных домена. Кроме того, хотя два домена Fv-фрагмента, VL и VH, кодируются разными генами, их можно соединить синтетическим линкером с использованием рекомбинантных способов, тем самым образуя единую белковую цепь, в которой области VL и VH спарены, в результате чего образуется моновалентная молекула (известная как одноцепочечное Fv (scFv) антитело; см., например, Bird et al., (1988) Science 242: 423-426, и Huston et al., (1988) Proc. Natl. Acad. USA 85:5879-5883). Предполагается также, что такие одноцепочечные антитела охватываются термином антигенсвязывающий полипептид. Описанная в данном документе антигенсвязывающая часть может быть получена с использованием обычных способов, хорошо известных специалистам в данной области техники, и фрагменты могут быть подвергнуты скринингу на возможность применения таким же образом, как и интактные антигенсвязывающие полипептиды.
Термин «изотип» относится к классу антител, кодируемых геном константной области тяжелой цепи. Антигенсвязывающий полипептид, который связывается с CD47, и его антигенсвязывающая часть по данному изобретению могут быть получены из любых видов, включая, но не ограничиваясь ими, мышей, крыс, кроликов, приматов, отличных от человека (например, шимпанзе, яванских макак, паукообразных обезьян, макак), лам и людей. Антигенсвязывающий полипептид, который связывается с CD47, и его антигенсвязывающая часть могут быть химерными, гуманизированными или полностью человеческими антителами. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, представляет собой антитело, продуцируемое линией гибридомных клеток мышиного происхождения. Таким образом, в некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, представляет собой мышиное антитело. В некоторых других вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело. В некоторых вариантах реализации данного изобретения химерное антитело представляет собой химерное антитело мыши-человека. В некоторых других вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело. В некоторых других вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, получен из мышиного антитела и является гуманизированным.
Термин «химерное антитело» относится к антителу, имеющему, по меньшей мере, часть вариабельной области тяжелой цепи и часть вариабельной области легкой цепи, полученные от одного вида, и, по меньшей мере, часть константной области, полученную от другого вида. Например, в некоторых вариантах реализации данного изобретения химерное антитело может содержать мышиную вариабельную область и человеческую константную область.
Термин «гуманизированное антитело» относится к антителу, содержащему области, определяющие комплементарность (CDR), полученные из нечеловеческого антитела, и каркасные и константные области, полученные из антитела человека. Например, предложенное в данном документе гуманизированное антитело, которое связывается с CD47, может содержать CDR, полученные из одного или более мышиных антител, а также каркасные и константные области антитела человека. Таким образом, в некоторых вариантах реализации данного изобретения гуманизированное антитело, предложенное в данном документе, связывается с тем же эпитопом на CD47, что и мышиное антитело, из которого получены CDR гуманизированного антитела. Иллюстративные гуманизированные антитела описаны в данном документе. Дополнительные гуманизированные антитела, которые связываются с CD47 или его вариантами, содержащими CDR тяжелой и легкой цепей, предложенные в данном документе, могут быть созданы с использованием любых каркасных последовательностей антитела человека, и они также включены в данное раскрытие. В некоторых вариантах реализации данного изобретения каркасные последовательности, подходящие для использования по данному раскрытию, включают последовательности, сходные по структуре с каркасными последовательностями, предложенными в данном документе. Дополнительные модификации могут быть сделаны в каркасных областях для улучшения свойств антител, предложенных в данном документе. Такие дополнительные модификации каркасных областей могут включать: химические модификации, точечные мутации для снижения иммуногенности или удаления эпитопов Т-клеток, или модификации, возвращающие мутации к остаткам исходных последовательностей зародышевой линии. В некоторых вариантах реализации данного изобретения такие модификации включают модификации, соответствующие мутациям, приведенным в качестве примеров в данном документе, включая реверсии последовательностей зародышевой линии. Например, в некоторых вариантах реализации данного изобретения одна или более аминокислот в каркасных областях VH и/или VL человека гуманизированных антител, предложенных в данном документе, возвращаются к соответствующим аминокислотам в исходных мышиных антителах. Например, для VH и VL гуманизированных антител 3F10, 14A9 и 16E5 несколько сайтов каркасных аминокислот матричных антител человека, описанных выше, возвращаются к соответствующим аминокислотным последовательностям мышиных антител 3F10, 14A9 и 16E5. В некоторых вариантах реализации данного изобретения аминокислоты в положении 2 и/или положении 33 и/или положении 48 и/или положении 63 и/или положении 68 и/или положении 71 и/или положении 72 и/или положении 94 вариабельной области легкой цепи возвращаются к соответствующим аминокислотам, обнаруженных в положениях вариабельной области легкой цепи мышиных 3F10, 14A9 или 16E5. В некоторых других вариантах реализации данного изобретения аминокислоты в положении 24 и/или положении 46 и/или положении 63 и/или положении 72 и/или положении 73 и/или положении 74 и/или положении 77 и/или положении 97 вариабельной области тяжелой цепи возвращаются к соответствующим аминокислотам, обнаруженных в положениях вариабельной области тяжелой цепи мышиных 3F10, 14A9 или 16E5. В некоторых вариантах реализации данного изобретения гуманизированное антитело 3F10 содержит вариабельную область тяжелой цепи, типы мутаций которой выбраны из одной или более из следующих мутаций: положение 73, в котором аминокислота мутирована с Asp (D) на Glu (E), положение 74, в котором аминокислота мутирована с Glu (E) на Ile (I), и положение 77, в котором аминокислота мутирована с Ser (S) на Asn (N); и гуманизированное антитело 3F10 содержит вариабельную область легкой цепи, типы мутаций которой выбраны из одной или более из следующих мутаций: положение 48, в котором аминокислота мутирована с Leu (L) на Trp (W), положение 71, в котором аминокислота мутирована с Asp (D) на Ser (S), положение 72, в котором аминокислота мутирована с Phe (F) на Tyr (Y), и положение 94, в котором аминокислота мутирована с Asp (D) на Glu (E). В некоторых вариантах реализации данного изобретения гуманизированное антитело 14A9 содержит вариабельную область тяжелой цепи, типы мутаций которой выбраны из одной или более из следующих мутаций: положение 24, в котором аминокислота мутирована с Ala (A) на Val (V), положение 72, в котором аминокислота мутирована с Arg (R) на Gly (G), положение 77, в котором аминокислота мутирована с Ser (S) на Asn (N), и положение 97, в котором аминокислота мутирована с Ala (A) до Thr (Т); и гуманизированное антитело 14A9 содержит вариабельную область легкой цепи, типы мутаций которой выбраны из одной или более из следующих мутаций: положение 63, в котором аминокислота мутирована с Ser (S) на Ile (I), и положение 68, в котором аминокислота мутирована с Gly (G) на Ser (S). В некоторых вариантах реализации данного изобретения гуманизированное антитело 16E5 содержит вариабельную область тяжелой цепи, типы мутаций которой выбраны из одной или более из следующих мутаций: положение 46, в котором аминокислота мутирована с Glu (E) на Lys (K), положение 63, в котором аминокислота мутирована с Lys (K) на Glu (E), положение 72, котором аминокислота мутирована с Thr (T) в Leu (L), положение 77, в котором аминокислота мутирована с Ser (S) на Arg (R), и положение 97, в котором аминокислота мутирована с Ala (A) на Thr (T); и гуманизированное антитело 16E5 содержит вариабельную область легкой цепи, типы мутаций которой выбраны из одной или более из следующих мутаций: положение 2, в котором аминокислота мутирована с Ile (I) на Ala (A), и положение 33, в котором аминокислота мутирована с Asn (N) на Gln (Q). Если не указано иное, описанные в данном документе мутации нумеруются, начиная с первой аминокислоты вариабельной области по порядку. Дополнительные или альтернативные реверсивные мутации могут быть сделаны в каркасных областях гуманизированных антител, предложенных в данном документе, для улучшения свойств антител. Данное раскрытие также включает гуманизированные антитела, которые связываются с CD47 и содержат модификации каркаса, соответствующие иллюстративным модификациям, раскрытым в данном документе, относительно любой подходящей каркасной последовательности и другим модификациям каркаса, которые иным образом улучшают свойства антитела.
Используемый в контексте данного документа термин «полученный», когда он используется для обозначения молекулы или полипептида, связанного с референтным антителом или другими связывающими белками, означает молекулу или полипептид, которые могут специфически связываться с тем же эпитопом, что и референтное антитело или другие связывающие белки.
Термин «выделенный» означает, что представляющее интерес соединение (например, антитело или нуклеиновая кислота) было выделено из его природной среды.
Используемый в контексте данного документа термин «EC50» относится к эффективной концентрации, составляющей 50% от максимального ответа антитела. Используемый в контексте данного документа термин «IC50» относится к ингибирующей концентрации, составляющей 50% от максимального ответа антитела. Как EC50, так и IC50 можно измерить с помощью анализа ИФА или FACS или любого другого способа, известного в данной области техники.
Используемый в контексте данного документа термин «KD» относится к константе диссоциации, выраженной в молярной концентрации (М). Величина KD антитела может быть определена с использованием способов, хорошо известных в данной области техники. Одним из предпочтительных способов определения KD антител является использование поверхностного плазмонного резонанса, более предпочтительно использование биосенсорной системы, такой как система Biacore.
Термин «лечение» относится к мере, предпринятой для статистически значимого лечения, излечения, облегчения, купирования, преобразования, устранения, нормализации, улучшения или воздействия на болезнь (например, расстройство) и симптом болезни, или предотвращения или отсрочки появление симптома, осложнения и биохимических показателей или иным образом предотвращения или ингибирования дальнейшего прогрессирования заболевания, болезни или расстройства.
Используемый в контексте данного документа термин «терапевтически эффективное количество» относится к количеству соединения или композиции, необходимого для обеспечения терапевтического эффекта и/или профилактического эффекта у субъекта.
Используемый в контексте данного документа термин «субъект» включает любого человека или животное, не являющееся человеком. Термин «животное, не являющееся человеком» включает всех позвоночных, например, млекопитающих и животных, не являющихся млекопитающими, таких как приматы, не являющиеся человеком, овцы, собаки, кошки, лошади, коровы, куры, амфибии и рептилии. Предпочтительно субъект по данному раскрытию представляет собой человека. Термины «пациент» и «субъект» используются в данном документе взаимозаменяемо.
Используемый в контексте данного документа термин «около» означает нахождение в допустимом диапазоне ошибок, определенном специалистами в данной области техники для конкретного значения, которое будет частично зависеть от того, как значение измеряется или определяется, т.е. от ограничений, налагаемых системой измерения. Например, «около» может означать нахождение в пределах 1 или более 1 стандартного отклонения, как это практикуется в данной области техники. В качестве альтернативы «около» может означать диапазон до ±5%, например, колеблющийся в пределах конкретного числового диапазона, заданного ±2%, ±1% или ±0,5%. Когда конкретное значение приводится в данном раскрытии или в формуле изобретения, если не указано иное, «около» следует рассматривать как означающее нахождение в допустимом диапазоне ошибок для этого конкретного значения. В этом контексте, если не указано иное, все значения параметров или условий в рамках этапа по умолчанию изменяются с помощью «около».
Термин «идентичность» также известен как соответствие. Процент идентичности между двумя последовательностями представляет собой функцию количества идентичных положений, общих для последовательностей (т.е. % идентичности=количество идентичных положений/общее количество положений × 100), при этом следует учитывать количество пропусков, которые необходимо ввести для получения оптимального выравнивания двух последовательностей, и длину каждого пропуска. Сравнение последовательностей и определение процента идентичности между двумя последовательностями может быть достигнуто с использованием математического алгоритма. Например, процент идентичности между двумя нуклеотидными последовательностями может быть определен с помощью алгоритма Майерса и Миллера (Comput. Appl. Biosci., 4:11-17 (1988)), который был включен в программу ALIGN (версия 2.0) и использует таблицу массы остатков PAM120 со штрафом за удлинение пропуска 12 и штрафом за внесения пропуска 4. Кроме того, процент идентичности двух аминокислотных последовательностей можно определить с помощью алгоритма Нидлмана и Вунша (J. Mol. Biol. 484-453 (1970)), который был включен в программу GAP в программном пакете GCG (доступен на www.gcg.com) и использует матрицу Blossum 62 или матрицу PAM250 со штрафом за внесение пропуска 16, 14, 12, 10, 8, 6 или 4 и штрафом за удлинение пропуска 1, 2, 3, 4, 5 или 6.
Термины «Xn» и «Хаа» эквивалентны и относятся к неуказанной аминокислоте, область применения которой определяется последующими определениями в соответствующем описании.
Термин «включать», «состоять из» или «содержать» и его варианты следует понимать как «включая, но не ограничиваясь этим», что означает, что другие элементы, компоненты и этапы, которые не указаны, охватываются в дополнение к элементам, компонентам и этапам, которые перечислены.
В контексте данного документа термины в единственном числе охватывают референты во множественном числе и наоборот, если в контексте явно не указано иное.
Все патенты, патентные заявки и другие указанные публикации прямо включены в данный документ в полном объеме посредством ссылки для целей описания и раскрытия данного изобретения. Данные публикации предоставлены исключительно потому, что они были раскрыты до даты подачи данной заявки. Все заявления относительно дат этих документов или описание содержания этих документов основаны на информации, доступной заявителю, и не являются признанием правильности дат или содержания этих документов. Кроме того, в любой стране или регионе любая ссылка на эти публикации в данном документе не должна рассматриваться как признание того, что публикации являются частью общепризнанных знаний в данной области техники. Различные аспекты данного изобретения будут описаны более подробно в следующих разделах.
Антигенсвязывающий Полипептид, Который Связывается с CD47, и Его Антигенсвязывающая Часть
В контексте данного документа термины «CD47», «белок, ассоциированный с интегрином», «IAP», «OA3» и «MER6» используются взаимозаменяемо. Термины «CD47 человека» и «hCD47» и т.п. используются в данном документе взаимозаменяемо и относятся к CD47 человека и вариантам или изотипам CD47 человека. В контексте данного документа термины «антитело, которое связывается с CD47» и «антитело против CD47» используются взаимозаменяемо.
В данном изобретении предложены антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, что обеспечивает новое решение для CD47-направленной терапии. Предложенный в данном документе антигенсвязывающий полипептид также обладает рядом других желательных свойств для таргетной терапии, помимо связывания с CD47 человека или/и CD47 яванской макаки. В частности, эти желательные признаки могут представлять собой, например, по меньшей мере, одно из следующего: связывание с CD47 со значением KD 1,53E-08 или менее; блокирование связывания CD47 с SIRPα; стимулирование опосредованного макрофагами фагоцитоза CD47-экспрессирующих клеток; незначительно индуцирует апоптоз CD4+Т-клеток; не вызывает существенной гематоцитопении, анемии или агглютинации эритроцитов; и антигенсвязывающий полипептид или его антигенсвязывающая часть имеют температуру плавления T ≥ 62°C и температуру агрегации Tagg ≥ 61°C. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, обладает лучшим терапевтическим эффектом; в некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, обладает уменьшенными побочными действиями.
В другом аспекте в данном изобретении предложены антигенсвязывающий полипептид, который связывается с CD47, и его антигенсвязывающая часть, содержащие специфические последовательности.
В некоторых вариантах реализации данного изобретения предложены выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, содержащие одну или более CDR, выбранных из группы, состоящей из последовательностей SEQ ID NO: 1-32.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть содержат последовательность CDR1 тяжелой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 1, 2, 3, 4 и 5.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть содержат CDR2 тяжелой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 6, 7, 8, 9 и 10.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть содержат CDR3 тяжелой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 11, 12, 13, 14 и 15.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть содержат CDR1 легкой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 16, 17, 18, 19 и 20.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть содержат CDR2 легкой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 21, 22, 23, 24 и 25.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть содержат CDR3 легкой цепи, содержащую аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 26, 27, 28, 30 и 32.
Специалистам в данной области техники будет понятно, что CDR тяжелой цепи и CDR легкой цепи антигенсвязывающего полипептида, предложенного в данном документе, могут быть независимо выбраны или смешаны и сопоставлены для образования антигенсвязывающего полипептида или его антигенсвязывающей части, содержащих любые CDR1, CDR2 и CDR3 тяжелой цепи и любые CDR1, CDR2 и CDR3 легкой цепи антигенсвязывающего полипептида, предложенного в данном документе. Таким образом, в некоторых вариантах реализации данного изобретения предложен выделенный антигенсвязывающий полипептид, который связывается с CD47 и содержит три CDR тяжелой цепи (CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи) и три CDR легкой цепи (CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи), при этом:
CDR1 тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 1, 2, 3, 4 и 5;
CDR2 тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 6, 7, 8, 9 и 10;
CDR3 тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 11, 12, 13, 14 и 15;
CDR1 легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 16, 17, 18, 19 и 20;
CDR2 легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 21, 22, 23, 24 и 25; и
CDR3 легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 26, 27, 28, 30 и 32.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит следующие области, определяющие комплементарность: CDR1 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 1, 2, 3, 4 и 5; CDR2 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 6, 7, 8, 9 и 10; CDR3 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 11, 12, 13, 14 и 15; CDR1 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 16, 17, 18, 19 и 20; CDR2 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 21, 22, 23, 24 и 25; и CDR3 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 26, 27, 28, 30 и 32.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 1, 6 и 11, соответственно; CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичность, по меньшей мере, 94% идентичность, по меньшей мере, 95% идентичность, по меньшей мере, 96% идентичность, по меньшей мере, 97% идентичность, по меньшей мере, 98% идентичность, по меньшей мере, 99% идентичность или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 16, 21 и 26, соответственно. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит следующие области, определяющие комплементарность: CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 1; CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 6; CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 11; CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 16; CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 21; и CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 26.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 2, 7 и 12, соответственно; CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 17, 22 и 27, соответственно. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит следующие области, определяющие комплементарность: CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 2; CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 7; CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 12; CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 17; CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 22; и CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 27.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 3, 8 и 13, соответственно; CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 18, 23 и 28, соответственно. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит следующие области, определяющие комплементарность: CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 3; CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 8; CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 13; CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 18; CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 23; и CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 28.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 4, 9 и 14, соответственно; CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 19, 24 и 32, соответственно. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит следующие области, определяющие комплементарность: CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 4; CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 9; CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 14; CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 19; CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 24; и CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 32.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 5, 10 и 15, соответственно; CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи содержат аминокислотные последовательности, имеющие, по меньшей мере, 80% идентичности, по меньшей мере, 81% идентичности, по меньшей мере, 82% идентичности, по меньшей мере, 83% идентичности, по меньшей мере, 84% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотными последовательностями, представленными в последовательностях SEQ ID NO: 20, 25 и 30, соответственно. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит следующие области, определяющие комплементарность: CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 5; CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 10; CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 15; CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 20; CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 25; и CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 30.
В данном изобретении также предложена консервативно модифицированная форма антигенсвязывающего полипептида и его антигенсвязывающей части. Специалистам в данной области техники будет понятно, что консервативная аминокислотная замена относится к замене одной аминокислоты другой аминокислотой, имеющей аналогичную структуру или аналогичные химические свойства (например, аналогичную боковую цепь). Иллюстративные консервативные замены описаны в данной области техники, например, в Watson et al., Molecular Biology of the Gene, the Bengamin/Cummings Publication Company, 4th Edition (1987).
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит: CDR1 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 1, 2, 3, 4 и 5, или ее консервативно модифицированную форму; CDR2 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 6, 7, 8, 9 и 10, или ее консервативно модифицированную форму; CDR3 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 11, 12, 13, 14 и 15, или ее консервативно модифицированную форму; CDR1 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 16, 17, 18, 19 и 20, или ее консервативно модифицированную форму; CDR2 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 21, 22, 23, 24 и 25, или ее консервативно модифицированную форму; и CDR3 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 26, 27, 28, 30 и 32, или ее консервативно модифицированную форму. Консервативные модификации существуют в любой одной или более CDR легкой цепи или CDR тяжелой цепи.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит: CDR1 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 3, 4 и 5; CDR2 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 8, 9 и 10; CDR3 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 13, 14 и 15; CDR1 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 18, 19 и 20; CDR2 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 23, 24 и 25; и CDR3 легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 28, 30 и 32.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 1 или ее консервативно модифицированную форму; CDR2 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 6 или ее консервативно модифицированную форму; CDR3 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 11 или ее консервативно модифицированную форму; CDR1 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 16 или ее консервативно модифицированную форму; CDR2 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 21 или ее консервативно модифицированную форму; и CDR3 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 26 или ее консервативно модифицированную форму.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 2 или ее консервативно модифицированную форму; CDR2 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 7 или ее консервативно модифицированную форму; CDR3 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 12 или ее консервативно модифицированную форму; CDR1 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 17 или ее консервативно модифицированную форму; CDR2 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 22 или ее консервативно модифицированную форму; CDR3 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 27 или ее консервативно модифицированную форму.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 3 или ее консервативно модифицированную форму; CDR2 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 8 или ее консервативно модифицированную форму; CDR3 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 13 или ее консервативно модифицированную форму; CDR1 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 18 или ее консервативно модифицированную форму; CDR2 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 23 или ее консервативно модифицированную форму; CDR3 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 28 или ее консервативно модифицированную форму.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 4 или ее консервативно модифицированную форму; CDR2 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 9 или ее консервативно модифицированную форму; CDR3 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 14 или ее консервативно модифицированную форму; CDR1 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 19 или ее консервативно модифицированную форму; CDR2 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 24 или ее консервативно модифицированную форму; CDR3 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 32 или ее консервативно модифицированную форму.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 5 или ее консервативно модифицированную форму; CDR2 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 10 или ее консервативно модифицированную форму; CDR3 тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 15 или ее консервативно модифицированную форму; CDR1 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 20 или ее консервативно модифицированную форму; CDR2 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 25 или ее консервативно модифицированную форму; CDR3 легкой цепи содержит аминокислотную последовательность SEQ ID NO: 30 или ее консервативно модифицированную форму.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, предложенный в данном документе, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи; вариабельные области тяжелой и легкой цепей содержат области CDR и каркасные области FR (включая FR1, FR2, FR3 и FR4), которые образуют последовательность вариабельной области в порядке FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4.
Таким образом, в другом аспекте в данном изобретении предложен выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, при этом антигенсвязывающий полипептид содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 33, 35, 37, 39, 41, 83, 85 и 87; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 34, 36, 38, 40, 42, 84, 86 и 88.
при этом последовательность, указанная в SEQ ID NO: 83, представляет собой:
QVQLVQSGAEVKKPGSSVKVSCKASGYTFSRYWIEWVRQAPGQGLEWMGEFIPGSDTTNYAQKFQGRVTITAX3X4STX5TAYMELSSLRSEDTAVYYCARGGLRRMDYWGQGTLVTVSS, где X3 представляет собой D или E, X4 представляет собой I или E, и X5 представляет собой S или N;
последовательность, указанная в SEQ ID NO: 84, представляет собой:
DIQMTQSPSSLSASVGDRVTITCRASSSVSSTYLHWYQQKPGKAPKLX6IYTTSTLASGVPSRFSGSGSGTX7X8TLTISSLQPEDFATYYCQQFSX2STWTFGQGTKLEIK, где X6 представляет собой L или W, X7 представляет собой D или S, X8 представляет собой F или Y, и X2 представляет собой D или E;
последовательность, указанная в SEQ ID NO: 85, представляет собой:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTNYGMNWVRQAPGQGLX9WMGWIN TNTGEPTYAQX10LQGRVTMTX11DTSTX12TAYMELRSLRSDDTAVYYCX13RFSHLRGPMD YWGQGTLVTVSS, где X9 представляет собой E или K, X10 представляет собой K или E, X11 представляет собой L или T, X12 представляет собой R или S, и X13 представляет собой A или T;
последовательность, указанная в SEQ ID NO: 86, представляет собой:
DX14QMTQSPSSLSASVGDRVTITCRSSQSLVHSNGYTYLHWYQQKPGKAPKLLIYKVSNRFSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCSQSTHVPPTFGQGTKLEIK, где X14 представляет собой I или A;
последовательность, указанная в SEQ ID NO: 87, представляет собой:
QVQLVQSGAEVKKPGASVKVSCKX15SGFNIEDDYIEWVRQAPGQGLEWMGRIDPANDKTKYAQKFQGRVTMTX16DTSTX17TVYMELSSLRSEDTAVYYCX18RPGLRRYYSMDYWGQGTLVTVSS, где X15 представляет собой A или V, X16 представляет собой R или G, X17 представляет собой S или N, и X18 представляет собой A или T;
последовательность, указанная в SEQ ID NO: 88, представляет собой:
DIQMTQSPSSLSASVGDRVTITCKASENVVSYVSWYQQKPGKAPKLLIYGASNRYTGVPSRFX19GSGSX20TDFTLTISSLQPEDFATYYCGQSYSYPLTFGQGTKLEIK, где X19 представляет собой S или I, и X20 представляет собой S или G.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 33, 35, 37, 39, 41, 83, 85 и 87; и вариабельная область легкой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 34, 36, 38, 40, 42, 84, 86 и 88.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 35, 39, 41, 83, 85 и 87; и вариабельная область легкой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 36, 40, 42, 84, 86 и 88. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит или состоит из аминокислотной последовательности SEQ ID NO: 79; и вариабельная область легкой цепи содержит или состоит из аминокислотной последовательности SEQ ID NO: 80. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит или состоит из аминокислотной последовательности SEQ ID NO: 81; и вариабельная область легкой цепи содержит или состоит из аминокислотной последовательности SEQ ID NO: 82.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 33; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 34. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 33, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 34.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 35; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 36. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 35, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 36.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 37; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 38. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, предложенный в данном документе, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 37, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 38.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 39; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 40. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, предложенный в данном документе, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 39, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 40.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 41; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 42. В некоторых вариантах реализации данного изобретения в выделенном антигенсвязывающем полипептиде, который связывается с CD47, представленном в данном документе, вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 41, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 42.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 83; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 84. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 83, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 84.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 85; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 86. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 85, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 86.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 87; и вариабельная область легкой цепи содержит аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 86% идентичности, по меньшей мере, 87% идентичности, по меньшей мере, 88% идентичности, по меньшей мере, 89% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 91% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью SEQ ID NO: 88. В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 87, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 88.
В некоторых вариантах реализации данного изобретения вариабельная область тяжелой цепи и вариабельная область легкой цепи, описанные в данном документе, имеют характеристики последовательностей CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, описанных в данном документе.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представленный в данном документе, содержит тяжелую цепь и легкую цепь, которые содержат константную область в дополнение к вариабельной области тяжелой цепи и вариабельной области легкой цепи, описанным в данном документе. В некоторых вариантах реализации данного изобретения константная область является гуманизированной. В некоторых вариантах реализации данного изобретения каркасные области FR как константной области, так и вариабельной области являются гуманизированными. Иммуногенность снижается за счет конструирования химерных антител (например, гуманизированных константных областей и вариабельных областей антитела, не являющегося человеческим) или гуманизированных антител (например, гуманизированных константных областей и FR).
В некоторых вариантах реализации данного изобретения константная область легкой цепи антигенсвязывающего полипептида представляет собой константную область κ-цепи антитела человека. В некоторых вариантах реализации данного изобретения константная область легкой цепи антигенсвязывающего полипептида представляет собой константную область λ-цепи антитела человека.
Константная область тяжелой цепи антигенсвязывающего полипептида может принадлежать любому типу константной области, например, IgG, IgM, IgD, IgA и IgE, и любому подклассу, например, IgG1, IgG2, IgG3 и IgG4. В некоторых других вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, относится к подклассу IgG1. В некоторых других вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, относится к подклассу IgG4.
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид содержит модифицированную константную область. В некоторых вариантах реализации данного изобретения шарнирная область в константной области IgG4 человека модифицирована, чтобы избежать или уменьшить замену цепей; например, антитело IgG4 имеет мутацию Ser228Pro (S228P) в соответствии с индексом нумерации EU.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело, содержащее вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 33, 35, 37, 39 и 41; и вариабельная область легкой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 34, 36, 38, 40 и 42.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело, содержащее тяжелую цепь и легкую цепь, при этом тяжелая цепь имеет аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 89, 93, 97, 101 и 105; и легкая цепь имеет аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 91, 95, 99, 103 и 107. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 89 и легкую цепь в соответствии с последовательностью SEQ ID NO: 91. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 93 и легкую цепь в соответствии с последовательностью SEQ ID NO: 95. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 97 и легкую цепь в соответствии с последовательностью SEQ ID NO: 99. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 101 и легкую цепь в соответствии с последовательностью SEQ ID NO: 103. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой химерное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 105 и легкую цепь в соответствии с последовательностью SEQ ID NO: 107.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 83, 85 и 87; и вариабельная область легкой цепи содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 84, 86 и 88.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, при этом тяжелая цепь имеет аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98% идентичности, по меньшей мере, 99% идентичности или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 109, 113, 117, 121, 125, 129, 133, 137, 141, 145, 149, 153, 157, 161, 165, 169, 173, 177, 181 и 185; и легкая цепь имеет аминокислотную последовательность, имеющую, по меньшей мере, 80% идентичности, по меньшей мере, 85% идентичности, по меньшей мере, 90% идентичности, по меньшей мере, 92% идентичности, по меньшей мере, 93% идентичности, по меньшей мере, 94% идентичности, по меньшей мере, 95% идентичности, по меньшей мере, 96% идентичности, по меньшей мере, 97% идентичности, по меньшей мере, 98%, идентичности, по меньшей мере, 99% или 100% идентичности с аминокислотной последовательностью, выбранной из последовательностей SEQ ID NO: 111, 115, 119, 123, 127, 131, 135, 139, 143, 147, 151, 155, 159, 163, 167, 171, 175, 179, 183 и 187. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 109 и легкую цепь в соответствии с последовательностью SEQ ID NO: 111. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 113 и легкую цепь в соответствии с последовательностью SEQ ID NO: 115. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 117 и легкую цепь в соответствии с последовательностью SEQ ID NO: 119. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 121 и легкую цепь в соответствии с последовательностью SEQ ID NO: 123. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 125 и легкую цепь в соответствии с последовательностью SEQ ID NO: 127. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 129 и легкую цепь в соответствии с последовательностью SEQ ID NO: 131. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 133 и легкую цепь в соответствии с последовательностью SEQ ID NO: 135. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 137 и легкую цепь в соответствии с последовательностью SEQ ID NO: 139. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 141 и легкую цепь в соответствии с последовательностью SEQ ID NO: 143. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 145 и легкую цепь в соответствии с последовательностью SEQ ID NO: 147. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 149 и легкую цепь в соответствии с последовательностью SEQ ID NO: 151. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 153 и легкую цепь в соответствии с последовательностью SEQ ID NO: 155. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 157 и легкую цепь в соответствии с последовательностью SEQ ID NO: 159. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 161 и легкую цепь в соответствии с последовательностью SEQ ID NO: 163. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 165 и легкую цепь в соответствии с последовательностью SEQ ID NO: 167. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 169 и легкую цепь в соответствии с последовательностью SEQ ID NO: 171. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 173 и легкую цепь в соответствии с последовательностью SEQ ID NO: 175. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 177 и легкую цепь в соответствии с последовательностью SEQ ID NO: 179. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 181 и легкую цепь в соответствии с последовательностью SEQ ID NO: 183. В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, представляет собой гуманизированное антитело, содержащее тяжелую цепь в соответствии с последовательностью SEQ ID NO: 185 и легкую цепь в соответствии с последовательностью SEQ ID NO: 187.
В одном варианте реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, содержит тяжелую цепь и легкую цепь, при этом тяжелая цепь содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 93, 101, 105, 109, 113, 117, 121, 125, 129, 133, 137, 141, 145, 149, 153, 157, 161, 165, 169, 173, 177, 181 и 185; и легкая цепь содержит или состоит из следующей последовательности: аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 95, 103, 107, 111, 115, 119, 123, 127, 131, 135, 139, 143, 147, 151, 155, 159, 163, 167, 171, 175, 179, 183 и 187.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть связываются с CD47 со значением KD 1,53E-08 M или менее. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть связываются с CD47 человека. В некоторых других вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть связываются с CD47 яванской макаки. В некоторых других вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть связываются с CD47 человека или CD47 яванской макаки. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть имеют аффинность связывания (KD) в диапазоне от около 1E-12 М до около 1Е-05 М, от около 1Е-12 М до около 1,89Е-06 М, от около 1Е-12 М до около 1,89Е-07 М, от около 1Е-11 М до около 1,89Е-07 М, от около 9,46Е-10 М до около 1,89Е-07 М, от около 9,46Е-10 М до около 1,89Е-08 М, от около 2,04Е-10 М до около 1,53Е-07 М или от около 2,04Е-10 М до около 1,89Е-08 М для CD47 человека. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть имеют аффинность связывания (KD) около 1Е-05 М или менее, около 1,89Е-06 М или менее, около 1,89Е-07 М или менее, около 1,89Е-08 М или менее, около 1,53E-08 М или менее, около 9,31E-08 М или менее, около 9,31E-09 М или менее, около 8,55E-09 М или менее, около 2,35E-09 М или менее или около 2,04E-010 М или менее для CD47 человека. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть имеют аффинность связывания (KD) около 7,48Е-09 М, около 3,50Е-10 М, около 7,67Е-10 М, около 9,06Е-09 М, около 2,35Е-09 М, около 9,46E-10 М, около 8,36E-10 М, около 1,53E-09 М, около 1,42E-09 М, около 9,60E-10 М, около 5,92E-10 М, около 9,04E-10 М, около 7,79Е-10 М, о 1,15Е-09 М, около 1,34Е-09 М, около 8,96Е-10 М, около 7,65Е-10 М, около 1,89Е-08 М, около 6,28Е-09 М, около 9,31Е-09 М, около 1,71Е-08 М, около 1,53Е-08 М, около 7,13Е-09 М, около 2,04Е-10 М или около 8,55Е-09 М для CD47 человека. В некоторых вариантах реализации данного изобретения аффинность связывания kD антигенсвязывающего полипептида, который связывается с CD47, и его антигенсвязывающей части, предложенных в данном документе, измеряют с помощью Biacore.
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть имеют EC50 связывания от около 1 нг/мл до около 2000 нг/мл, от около 1 нг/мл до около 1500 нг/мл, от около 1 нг/мл до около 1106 нг/мл, от около 1 нг/мл до около 699 нг/мл, от около 1 нг/мл до около 340 нг/мл, от около 30 нг/мл до около 340 нг/мл, от около 50 нг/мл до около 340 нг/мл или от около 100 нг/мл до около 340 нг/мл для CD47 человека. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть имеют ЕС50 связывания около 2000 нг/мл или менее, около 1500 нг/мл или менее, около 1106 нг/мл или менее, около 699 нг/мл или менее или около 340 нг/мл или менее для CD47 человека. В некоторых вариантах реализации данного изобретения EC50 антигенсвязывающего полипептида, который связывается с CD47, и его антигенсвязывающей части, предложенных в данном документе, измеряют с помощью ИФА или FACS.
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть блокируют связывание CD47 с SIRPα. Сигнальный регуляторный белок α (SIRPα) представляет собой один из лигандов, связывающихся с CD47, и экспрессируется на гемопоэтических клетках, включая макрофаги и дендритные клетки. CD47 взаимодействует с SIRPα на макрофагах, посылая макрофагам сигнал «не ешь меня». В случае лечения использование антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части для блокирования взаимодействия SIRPα с CD47, может способствовать поглощению и удалению раковых клеток иммунной системой хозяина. Следовательно, способность блокировать взаимодействие CD47 с SIRPα и, таким образом, давать возможность макрофагам фагоцитировать CD47-экспрессирующие опухолевые клетки, является важной функциональной особенностью некоторых антигенсвязывающих полипептидов, которые связываются с CD47. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид (например, химерные антитела Xi2B2, Xi2H8, Xi3F10, Xi16E5, Xi14A9) и/или его антигенсвязывающая часть имеют блокирующую IC50 от около 358,5 нг/мл до около 26966 нг/мл, от около 358,5 нг/мл до около 4861 нг/мл, от около 358,5 нг/мл до около 631,2 нг/мл или от около 358,5 нг/мл до около 1283 нг/мл при использовании клеток Jurkat и анализа проточной цитометрии. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть имеют блокирующую IC50 около 26966 нг/мл или менее, около 15000 нг/мл или менее, около 10000 нг/мл или менее, около 8000 нг/мл или менее, около 6000 нг/мл или менее, около 4861 нг/мл или менее, около 3000 нг/мл или менее, около 2500 нг/мл или менее, около 2000 нг/мл или менее, около 1500 нг/мл или менее, около 1283 нг/мл или менее, около 1000 нг/мл или менее, около 800 нг/мл или менее, около 500 нг/мл или менее или около 358,5 нг/мл или менее.
В некоторых вариантах реализации данного изобретения, на основе анализа ИФА, антигенсвязывающий полипептид, который связывается с CD47 (например, химерные антитела Xi2B2, Xi2H8 и Xi3F10 или их гуманизированные антитела, Xi16E5 или его гуманизированные антитела и Xi14A9 или его гуманизированные антитела), и/или его антигенсвязывающая часть имеют блокирующую IC50 от около 4,682 нг/мл до около 15246 нг/мл, от около 621,1 нг/мл до около 15246 нг/мл, от около 621,1 нг/мл до около 7910 нг/мл, от около 621,1 нг/мл до около 2939 нг/мл, от около 621,1 нг/мл до около 2500 нг/мл, от около 621,1 нг/мл до около 2051 нг/мл, от около 621,1 нг/мл до около 1738 нг/мл, от около 621,1 нг/мл до около 1500 нг/мл, от около 621,1 нг/мл до около 1400 нг/мл, от около 621,1 нг/мл до около 1300 нг/мл, от около 621,1 нг /мл до около 1200 нг/мл, от около 621,1 нг/мл до около 1100 нг/мл, от около 621,1 нг/мл до около 1000 нг/мл, от около 621,1 нг/мл до около 900 нг/мл, от около 621,1 нг/мл до около 800 нг/мл или от около 621,1 нг/мл до около 703,2 нг/мл. В некоторых вариантах реализации данного изобретения, на основании анализа ИФА, антигенсвязывающий полипептид и/или его антигенсвязывающая часть имеют блокирующую IC50 около 15246 нг/мл или менее, около 7910 нг/мл или менее, около 2939 нг/мл или менее, около 2500 нг/мл или менее, около 2051 нг/мл или менее, около 1738 нг/мл или менее, около 1500 нг/мл или менее, около 1400 нг/мл или менее, около 1300 нг/мл или менее, около 1200 нг/мл или менее, около 1100 нг/мл или менее, около 1000 нг/мл или менее, около 900 нг/мл или менее, около 800 нг/мл или менее, около 703,2 нг/мл или менее, около 621,1 нг/мл или менее, около 450 нг/мл или менее, около 350 нг/мл или менее, около 250 нг/мл или менее, около 150 нг/мл или менее, около 100 нг/мл или менее, около 50 нг/мл или менее, около 40 нг/мл или менее, около 30 нг/мл или менее, около 20 нг/мл или менее, около 10 нг/мл или менее или около 4,682 нг/мл или менее.
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть способствуют опосредованному макрофагами фагоцитозу CD47-экспрессирующих клеток. Как описано ранее, фагоцитоз CD47-экспрессирующих клеток, таких как раковые клетки (конкретными примерами являются клетки HL60 и т.п.), макрофагами усиливается за счет блокирования связывания SIRPα с CD47 с помощью антигенсвязывающего полипептида, который связывается с CD47. В некоторых вариантах реализации данного изобретения при использовании антигенсвязывающего полипептида, который связывается с CD47, в концентрации от около 1 мкг/мл до около 10 мкг/мл, скорость фагоцитоза макрофагами составляет от около 3,5% до около 65,7%, от около 11,5% до около 65,7%, от около 28,8% до около 65,7% или от около 44,67% до около 65,7%. В некоторых вариантах реализации данного изобретения при концентрации антигенсвязывающего полипептида от около 1 мкг/мл до около 10 мкг/мл скорость фагоцитоза макрофагами составляет от около 1,34% до около 81,66%, от около 2% до около 81,66%, от около 11,95% до около 81,66%, от около 24,19% до около 81,66% или от около 71,48% до около 81,66%.
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть не вызывают значимого апоптоза CD4+Т-клеток. В некоторых вариантах реализации данного изобретения анализ апоптоза проводили с помощью проточной цитометрии. В контексте данного документа значимый апоптоз означает отсутствие статистически значимого отличия (P ≤ 0,05) от отрицательного контроля в пределах допустимого диапазона (например, не оказывающего влияния на субъект или в пределах контролируемого диапазона); например, в некоторых вариантах реализации данного изобретения нет значимых отличий от IgG отрицательного контроля.
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть имеют Tm (температура плавления) около 62°C или более, около 63°C или более, около 64°C или более, около 65°C или более, около 66°C или более, около 67°С или более, около 68°С или более, около 69°С или более или около 70°С или более. В некоторых вариантах реализации данного изобретения антитело и/или его фрагмент имеют Tagg (температуру агрегации) около 61°C или более, около 62°C или более, около 63°C или более, около 64°C или более, около 65°C или более, около 66°C или более, около 67°С или более, около 68°С или более, около 69°С или более, около 70°С или более, около 71°С или более, около 72°С или более или около 73°С или более. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть имеют Tm от около 62°C до около 75°C, от около 63°C до около 70,6°C, от около 64°C до около 70,6°C, от около 65°C до около 70,6°C, от около 67°С до около 70,6°С или от около 68°С до около 70,6°С. В некоторых вариантах реализации данного изобретения антитело и/или его фрагмент имеют Tagg от около 60°С до около 73,81°С, от около 61°С до около 73,81°С, от около 62°С до около 73,81°С, от около 63°С до около 73,81°С, от около 64°C до около 73,81°C, от около 65°C до около 73,81°C, от около 67°C до около 73,81°C или от около 68°C до около 73,81°C. В некоторых вариантах реализации данного изобретения Tm и Tagg определяются с помощью нано-ДСФ (DSF).
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть не вызывают существенной гематоцитопении, анемии или агглютинации эритроцитов. Термины «красное кровяное тельце» и «эритроцит» являются синонимами и используются взаимозаменяемо. Термин «агглютинация» означает слипание клеток. Поскольку эритроциты также экспрессируют CD47, некоторые антигенсвязывающие полипептиды, которые связываются с CD47, связываются с эритроцитами, тем самым вызывая агглютинацию. Таким образом, ожидается, что предотвращение или снижение вредного воздействия антигенсвязывающих полипептидов, которые связываются с CD47, на эритроциты уменьшит побочные эффекты при лечении.
Таким образом, в другом аспекте данного изобретения предложены антигенсвязывающий полипептид, который связывается с CD47, и его антигенсвязывающая часть, обладающие одним из следующих свойств или комбинацией нескольких из них:
(a) связывание с CD47 со значением KD 1,89E-08 или менее (например, 1,53E-08);
(b) блокирование связывания CD47 с SIRPα;
(c) стимулирование опосредованного макрофагами фагоцитоза CD47-экспрессирующих клеток;
(d) не вызывает значимого апоптоза CD4+Т-клеток;
(e) не вызывает существенной гематоцитопении, анемии или агглютинации эритроцитов; и
(f) антигенсвязывающий полипептид или его антигенсвязывающая часть имеют температуру плавления T ≥ 62°C и температуру агрегации Tagg ≥ 61°C.
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть обладают одним, двумя, тремя, четырьмя, пятью или шестью свойствами (a)-(f). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (а), (b) и (с). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (а), (b) и (e). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (а), (c) и (e). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (a), (b), (c) и (d). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (a), (b), (c) и (e). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (a), (b), (c) и (f). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (a), (b), (c), (d) и (f). В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид и/или его антигенсвязывающая часть обладают свойствами (a), (b), (c), (d), (e) и (f).
В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, и/или его антигенсвязывающая часть представляют собой антитело против CD47 или его антигенсвязывающую часть.
В некоторых других вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, предложенный в данном документе, представляет собой моноклональное антитело.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, предложенный в данном документе, представляет собой моноспецифическое антитело.
В некоторых вариантах реализации данного изобретения выделенный антигенсвязывающий полипептид, который связывается с CD47, предложенный в данном документе, представляет собой мультиспецифическое антитело, например, биспецифическое антитело или триспецифическое антитело.
В некоторых вариантах реализации данного изобретения в данном изобретении предложен антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, которые связываются с тем же эпитопом на CD47, что и любое из иллюстративных антител, предложенных в данном документе, например, связываются с тем же эпитопом, что и химерное или гуманизированное антитело 16E5, например, связывается с тем же эпитопом, что и химерное или гуманизированное антитело 3F10, и, например, связывается с тем же эпитопом, что и химерное или гуманизированное антитело 14A9. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид или его антигенсвязывающая часть конкурируют с любым из иллюстративных антител, предложенных в данном документе, за связывание с CD47, например, конкурируют с химерным или гуманизированным антителом 16E5 за связывание с CD47, например, конкурируют с химерным или гуманизированным антителом 3F10 за связывание с CD47 и, например, конкурируют с химерным или гуманизированным антителом 14A9 за связывание с CD47. Связывание с CD47 можно измерить с помощью ИФА, проточной цитометрии или анализа поверхностного плазмонного резонанса (ППР, SPR) или любого другого способа, известного в данной области техники.
В данном описании предложены некоторые иллюстративные моноклональные антитела, которые связываются с CD47, включая химерные версии антител 2B2, 2H8, 3F10, 16E5 и 14A9 (Xi2B2, Xi2H8, Xi3F10, Xi16E5 и Xi14A9) и гуманизированные варианты 3F10, 16E5 и 14A9. Аминокислотные последовательности CDR тяжелой цепи (CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи) иллюстративных антител, которые связываются с CD47, предложенные в данном документе, представлены в Таблице S1 ниже. Аминокислотные последовательности CDR легкой цепи (CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи) представлены в Таблице S2 ниже. Аминокислотные последовательности вариабельных областей и полноразмерных тяжелых и легких цепей представлены в Таблицах S3 и S4 ниже.
(SEQ ID NO: 1)
(SEQ ID NO: 6)
(SEQ ID NO: 11)
(SEQ ID NO: 2)
(SEQ ID NO: 7)
(SEQ ID NO: 12)
(SEQ ID NO: 3)
(SEQ ID NO: 8)
(SEQ ID NO: 13)
(SEQ ID NO: 4)
(SEQ ID NO: 9)
(SEQ ID NO: 14)
(SEQ ID NO: 5)
(SEQ ID NO: 10)
(SEQ ID NO: 15)
(SEQ ID NO: 4)
(SEQ ID NO: 9)
(SEQ ID NO: 14)
(SEQ ID NO: 3)
(SEQ ID NO: 8)
(SEQ ID NO: 13)
(SEQ ID NO: 5)
(SEQ ID NO: 10)
(SEQ ID NO: 15)
(SEQ ID NO: 16)
(SEQ ID NO: 21)
(SEQ ID NO: 26)
(SEQ ID NO: 17)
(SEQ ID NO: 22)
(SEQ ID NO: 27)
(SEQ ID NO: 18)
(SEQ ID NO: 23)
(SEQ ID NO: 28)
(SEQ ID NO: 19)
(SEQ ID NO: 24)
(SEQ ID NO: 29)
(SEQ ID NO: 20)
(SEQ ID NO: 25)
(SEQ ID NO: 30)
(SEQ ID NO: 19)
(SEQ ID NO: 24)
(SEQ ID NO: 29)
(SEQ ID NO: 19)
(SEQ ID NO: 24)
(SEQ ID NO: 31)
(SEQ ID NO: 18)
(SEQ ID NO: 23)
(SEQ ID NO: 28)
(SEQ ID NO: 20)
(SEQ ID NO: 25)
(SEQ ID NO: 30)
(SEQ ID NO: 19)
(SEQ ID NO: 24)
(SEQ ID NO: 32)
где X3 представляет собой D или E, X4 представляет собой I или E, и X5 представляет собой S или N
где X6 представляет собой L или W, X7 представляет собой D или S, X8 представляет собой F или Y, и X2 представляет собой D или E
DDTAVYYC X13RFSHLRGPMDYWGQGTLVTVSS
где X9 представляет собой E или K, X10 представляет собой K или E, X11 представляет собой L или T, X12 представляет собой R или S, и X13 представляет собой A или T
где X14 представляет собой I или A
где X15 представляет собой A или V, X16 представляет собой R или G, X17 представляет собой S или N, X18 представляет собой A или T
где X19 представляет собой S или I, и X20 представляет собой S или G
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Иммуноконъюгаты
В некоторых вариантах реализации данного изобретения в данном изобретении предложен иммуноконъюгат антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части. Терапевтические агенты, которые могут быть связаны или конъюгированы с антигенсвязывающим полипептидом, который связывается с CD47, или его антигенсвязывающей частью, могут включать, но не ограничиваются ими, цитотоксические лекарственные препараты, радиоизотопы, иммуномодуляторы или антитела. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, непосредственно конъюгированы с терапевтическим агентом. В некоторых вариантах реализации данного изобретения антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, конъюгированы с терапевтическим агентом через линкер.
Композиция
В данном изобретении предложена фармацевтическая композиция, содержащая выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающую часть, или нуклеиновую кислоту, кодирующую антитело или его фрагмент, или иммуноконъюгат, описанный в данном документе, и дополнительно один или более фармацевтически приемлемых носителей. В некоторых вариантах реализации данного изобретения композиция содержит любые моноклональные антитела, химерные и гуманизированные антитела, антитела 2B2, 2H8, 3F10, 16E5 и 14A9, а также фармацевтически приемлемый носитель. Фармацевтически приемлемые носители включают, например, эксципиенты, разбавители, инкапсулирующие материалы, наполнители, буферы или другие агенты.
Гибридома
В данном изобретении предложена выделенная клеточная линия гибридомы, выбранная из группы, состоящей из 2B2, 2H8, 3F10, 16E5 и 14A9. Клеточные линии гибридомы 2B2, 2H8, 3F10, 16E5 и 14A9 секретируют моноклональные антитела, которые связываются с CD47.
Выделенная Нуклеиновая Кислота
В данном изобретении предложена выделенная нуклеиновая кислота, содержащая последовательность, кодирующую антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающую часть, описанные в данном документе. В некоторых вариантах реализации данного изобретения нуклеиновая кислота может кодировать аминокислотную последовательность, содержащую вариабельную область тяжелой цепи антигенсвязывающего полипептида и/или вариабельную область легкой цепи, описанные в данном документе. В некоторых вариантах реализации данного изобретения нуклеиновая кислота может кодировать аминокислотную последовательность, содержащую тяжелую цепь антигенсвязывающего полипептида и/или легкую цепь антигенсвязывающего полипептида, описанного в данном документе. Нуклеотидные последовательности некоторых вариабельных областей и тяжелой и легкой цепей антигенсвязывающего полипептида перечислены в списке последовательностей.
Вектор
В данном изобретении предложен вектор, содержащий выделенную нуклеиновую кислоту. В некоторых вариантах реализации данного изобретения вектор представляет собой вектор для клонирования; в некоторых других вариантах реализации данного изобретения вектор представляет собой вектор экспрессии.
Вектор экспрессии необязательно представляет собой любой вектор экспрессии, способный экспрессировать антигенсвязывающий полипептид или его антигенсвязывающую часть, описанные в данном документе.
Клетка-хозяин
В некоторых вариантах реализации данного изобретения в данном изобретении предложена клетка-хозяин, содержащая вектор, при этом клетка-хозяин является подходящей клеткой-хозяином для клонирования или кодирования антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части. В некоторых вариантах реализации данного изобретения клетка-хозяина представляет собой прокариотическую клетку. В других вариантах реализации данного изобретения клетка-хозяина представляет собой эукариотическую клетку. В некоторых вариантах реализации данного изобретения клетка-хозяин выбрана из клеток дрожжей, клеток млекопитающих или других клеток, подходящих для получения антигенсвязывающего полипептида или его антигенсвязывающей части. Клетки млекопитающих представляют собой, например, клетки яичника китайского хомячка (СНО).
Способ Получения Антигенсвязывающих Полипептидов, Связывающихся с CD47
В некоторых вариантах реализации данного изобретения в данном изобретении предложен способ получения выделенного антигенсвязывающего полипептида, который связывается с CD47, который включает: культивирование клетки-хозяина, содержащей нуклеиновую кислоту, кодирующую антигенсвязывающий полипептид, в условиях, подходящих для экспрессии антигенсвязывающего полипептида, и выделение антигенсвязывающего полипептида из клетки-хозяина или среды для культивирования клеток-хозяев. Для получения антигенсвязывающего полипептида, который связывается с CD47, нуклеиновую кислоту, кодирующую антитело, выделяют и встраивают в один или более векторов для дальнейшего клонирования и/или экспрессии в клетке-хозяине. Нуклеиновую кислоту можно получить с использованием различных способов, известных в данной области техники, таких как клонирование генов, сплайсинг генов и химический синтез.
Применение
В данном изобретении предложено применение выделенного антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части. В некоторых вариантах реализации данного изобретения введение субъекту терапевтически эффективного количества выделенного антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части, описанных в данном документе, может снижать или ингибировать рост опухолевых клеток. В некоторых вариантах реализации данного изобретения введение субъекту терапевтически эффективного количества выделенного антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части, описанных в данном документе, может быть эффективным при лечении онкологического заболевания. Субъекты, нуждающиеся в лечении, включают пациентов с заболеванием или состоянием, а также тех, у кого может быть выявлено заболевание или состояние, и целью которых является предотвращение, отсрочка или облегчение заболевания или состояния. В контексте данного документа «онкологическое заболевание» относится к физиологическому состоянию у млекопитающих, которое обычно характеризуется нерегулируемым ростом клеток. Примеры онкологического заболевания включают, но не ограничиваются ими, лейкемию, лимфому, рак яичников, рак молочной железы, рак эндометрия, рак толстой кишки, рак прямой кишки, рак мочевого пузыря, рак уротелия, рак легких, рак бронхов, рак костей, рак предстательной железы, рак поджелудочной железы, рак желудка, печеночноклеточный рак, рак желчного пузыря, рак желчных протоков, рак пищевода, почечно-клеточный рак, рак щитовидной железы, рак головы и шеи, рак яичек, эндокринную аденокарциному, рак надпочечников, рак гипофиза, рак кожи, рак мягких тканей, рак сосудов, рак головного мозга, рак нервной системы, рак глаза, рак мозговых оболочек, рак ротоглотки, рак гортаноглотки, рак шейки матки и рак матки, глиобластому, медуллобластому, астроцитому, глиому, менингиому, гастриному, нейробластому, меланому, острый миелоидный лейкоз, миелодиспластический синдром и саркому.
В некоторых вариантах реализации данного изобретения введение субъекту эффективного количества выделенного антигенсвязывающего полипептида, который связывается с CD47, или его антигенсвязывающей части, описанных в данном документе, стимулирует фагоцитоз макрофагами у субъекта.
Хотя предыдущее раскрытие было описано довольно подробно с помощью иллюстраций и примеров с целью ясного понимания, специалистам в данной области техники в свете идей данного раскрытия будет очевидно, что в данное раскрытие могут быть внесены определенные изменения и модификации без отклонения от сущности или объема прилагаемой формулы изобретения. Следующие примеры приведены исключительно в иллюстративных целях и не ограничивают объем изобретения. Специалисты в данной области техники легко определят ряд некритических параметров, которые можно изменить или модифицировать для получения по существу аналогичных результатов. Положительный контроль Hu5F9, используемый в конкретных примерах в данном документе, представляет собой гуманизированное антитело и имеет ту же последовательность, что и антитело «5F9» патента США №US2015/0183874A1.
Если не указано иное, в практике данного изобретения используются способы традиционной молекулярной биологии, клеточной биологии, биохимии и иммунологии, хорошо известные в данной области техники и описанные ниже: например, Methods in Molecular Biology, Humana Press; Molecular Cloning: A Laboratory Manual, 2nd Edition (Sambrook et al., 1989); Current Protocols in Immunology (J. E. Coligan et al., 1991); Immunobiology (C. A. Janeway and P. Travers, 1997); Antibodies (P. Finch, 1997); Antibodies: a practical approach (Ed. D. Catty, IRL Press, 1988-1989); Monoclonal antibodies: a practical approach (Ed. P. Shepherd and C. Dean, Oxford University Press, 2000); Phage display: a laboratory manual (C. Barbas III et al., Cold Spring Harbor Laboratory Press, 2001); и Using antibodies: a laboratory manual (E. Harlow and D. Lane, Cold Spring Harbor Laboratory Press, 1999).
Пример 1: Получение Моноклональных Антител Против CD47
Иммунизация мышей белком CD47:
Для получения антител против CD47 мышей Balb/c иммунизировали подкожно равными объемами полного адъюванта Фрейнда (первая иммунизация) или неполного адъюванта Фрейнда (бустерная иммунизация), эмульгированного рекомбинантным белком с гистидиновой меткой hCD47-His Tag (ACRObiosystems, кат.№CD7-H5227) (50 мг/Balb/c на мышь) или hCD47-mFc (ACRObiosystems, кат.№CD7-H52A5), каждые 2 недели в течение 6 недель, сделав всего 3 иммунизации. При четвертой иммунизации каждой мыши внутримышечно вводили 20 мкг белка hCD47-mFc (ACRObiosystems, кат.№CD7-H52A5) (в водном адъюванте). За три дня до слияния клеток мышам внутривенно вводили антиген без адъюванта для усиления иммунизации. Клетки селезенки (1×108) иммунизированных мышей сливали с клетками миеломы SP2/0 (1,5×107) с использованием полиэтиленгликоля 1500 (Roche, кат.№10783641001). После слияния клетки распределяли по лункам 96-луночного планшета по 0,1 мл/лунку и инкубировали в инкубаторе при 37°С 5% СО2. В День 1 клетки подпитывали, добавляя в каждую лунку дополнительно 0,1 мл среды ГАТ, содержащей сыворотку и 2× метотрексата. На День 3 и 7, 0,1 мл среды из каждой лунки заменяли 0,1 мл свежей среды ГАТ. Скрининг обычно проводили между Днем 9 и 14, и скрининг, направленный на супернатанты тестовых культур антител, которые реагировали с hCD47-His Tag (ACRObiosystems, кат.№CD7-H5227), выполняли с помощью ИФА для положительных лунок.
Клонирование клеток гибридомы проводили способом предельного разведения. Отобранные положительные смешанные клоны подвергали предельному разведению. Один штамм положительных смешанных клонов высевали в два 96-луночных планшета (100 клеток/планшет, 200 клеток/планшет). Клетки гибридомы культивировали в среде RPMI 1640 (Hyclone, кат.№SH30809.01), содержащей 10% фетальной бычьей сыворотки. Через 10 дней субклоны после предельного разведения также подвергали анализу ИФА для исследования культуральных супернатантов и отбирали положительные субклоны. Клонированные клетки гибридомы сохраняли и использовали для выделения кДНК.
Выделение кДНК и получение последовательности вариабельной области антител против CD47 человека:
Тотальную РНК выделяли из отобранной клеточной линии гибридомы, продуцирующей антитело hCD47, с использованием набора для выделения РНК (Takara, кат. №9767), и первую цепь кДНК синтезировали с использованием набора для обратной транскрипции (Thermo Fisher, кат.№K1652) в соответствии с инструкциями производителя с использованием тотальной РНК в качестве матрицы. Затем синтезированную кДНК использовали для амплификации связанных с антителами последовательностей in vitro с помощью ПЦР с использованием вырожденных праймеров к IgG мыши.
Продукты ПЦР-амплификации разделяли электрофоретически в 1% агарозном/трис-ацетатном геле. Фрагмент ДНК ожидаемого размера (около 450 п. н. для тяжелой и легкой цепей) удаляли из геля и очищали. 3 мкл очищенного ПЦР-продукта клонировали в вектор pMD-19T (Takara, кат.№6013) и трансформировали в химически компетентные клетки DH5α Escherichia coli (Takara, кат.№9057). В каждой реакции лигирования случайным образом отбирали 10 положительных клонов и проводили секвенирование ДНК с использованием прямого праймера М13.
Последовательности вариабельной области тяжелой цепи (VH) и последовательности вариабельной области легкой цепи (VL) пяти мышиных моноклональных антител (антител 2B2, 2H8, 3F10, 16E5 и 14A9) были получены из соответствующих клонов гибридом (2B2, 2H8, 3F10, 16E5 и 14А9) путем амплификации и секвенирования, и представлены ниже:
Конструирование и экспрессия химерных антител:
Посредством химического синтеза генов вариабельных областей мышиных антител область VL каждого антитела мыши была связана с константной областью κ-цепи антитела человека для создания химерной легкой цепи, и область VH антитела мыши была связана с константной областью IgG4 (с S228P согласно нумерации EU) для создания химерной тяжелой цепи. Плазмиды экспрессии для химерной легкой цепи и химерной тяжелой цепи конструировали с использованием стандартных способов генной инженерии. Клетки CHO (система объемом 200 мл при 106 клеток/мл) трансфицировали с использованием 100 мкг каждого типа плазмид экспрессии химерной тяжелой цепи и химерной легкой цепи и культивировали в течение 6 дней. Затем химерное антитело в супернатанте очищали с использованием колонки с белком А.
Путем конструирования и экспрессии было получено пять химерных антител, и их полноразмерные последовательности химерных тяжелых цепей и химерных легких цепей и нуклеиновых кислот, кодирующих их, были следующими: Xi2H8 (химерная тяжелая цепь и нуклеиновая кислота, кодирующая их: SEQ ID NO: 89-90; химерная легкая цепь и нуклеиновая кислота, кодирующая одинаковые: SEQ ID NO: 91-92), Xi2B2 (химерная тяжелая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 97-98; химерная легкая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 99-100), Xi3F10 (химерная тяжелая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 101-102; химерная легкая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 103-104), Xi16E5 (химерная тяжелая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 93-94; химерная легкая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 95-96) и Xi14A9 (химерная тяжелая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 105-106; химерная легкая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO: 107-108).
Схема гуманизации антител:
Химерные антитела человека и мыши 3F10, 14A9 и 16E5 гуманизировали путем прививки CDR (см., например, патент США №5225539). Мышиные антитела 3F10, 14A9 и 16E5 гомологично моделировали с использованием MOE (Molecular Operating Environment) для получения структурных моделей белков Fv-доменов. Аминокислотные последовательности VH и VL мышиных антител 3F10, 14A9 и 16E5 были введены на веб-сайт инструмента, связанного с международной информационной системой ImMunoGeneTics (http://www.imgt.org/3Dstructure-DB/cgi/DomainGapAlign.cgi), из которых были отобраны последовательности антител зародышевой линии человека, высоко гомологичные вариабельным областям антител мыши 3F10, 14A9 и 16E5. Области, определяющие комплементарность (CDR) в VH и VL мышиных антител 3F10, 14A9 и 16E5 прививали к матричным антителам человека. Для 3F10 выбранная матрица VH человека представляла собой комбинацию IGHV1-69*01 и IGHJ4*01, а выбранная матрица VL человека представляла собой комбинацию IGKV1-39*01 и IGKJ2*01. Для 14A9 выбранная матрица VH человека представляла собой комбинацию IGHV1-46*01 и IGHJ4*01, а выбранная матрица VL человека представляла собой комбинацию IGKV1-39*01 и IGKJ2*01. Для 16E5 выбранная матрица VH человека представляла собой комбинацию IGHV1-18*01 и IGHJ4*01, а выбранная матрица VL человека представляла собой комбинацию IGKV1-39*01 и IGKJ2*01.
Аминокислотные последовательности CDR указанных выше матричных антител человека были заменены CDR гибридомных (мышиных) антител 3F10, 14A9 и 16E5. Последовательности незаменимых аминокислот из VH и VL мышиных антител 3F10, 14A9 и 16E5 прививают к каркасам VH и VL вышеуказанных матричных антител зародышевой линии человека для получения функциональных гуманизированных антител. Для VH и VL антител 3F10, 14A9 и 16E5 несколько сайтов каркасных аминокислот матричных антител человека, описанных выше, были заменены на соответствующие аминокислотные последовательности мышиных антител 3F10, 14A9 и 16E5. Мутации проводили в некоторых областях CDR.
Для вариабельной области тяжелой цепи гуманизированного антитела 3F10 выбор и сочетание типов мутаций производились из следующих сайтов: положение 73, в котором аминокислота была мутирована с Asp (D) на Glu (E), положение 74, в котором аминокислота кислота была заменена с Glu (E) на Ile (I), и положение 77, в котором аминокислота была мутирована с Ser (S) на Asn (N); и для вариабельной области легкой цепи гуманизированного антитела 3F10 выбор и сочетание типов мутаций производились из следующих сайтов: положение 48, в котором аминокислота была мутирована с Leu (L) на Trp (W), положение 71, в котором аминокислота была мутирована с Asp (D) на Ser (S), положение 72, в котором аминокислота была мутирована с Phe (F) на Tyr (Y), и положение 94, в котором аминокислота была мутирована с Asp (D) на Glu (Е). Для вариабельной области тяжелой цепи гуманизированного антитела 14A9 выбор и сочетание типов мутаций производились из следующих сайтов: положение 24, в котором аминокислота была мутирована с Ala (A) на Val (V), положение 72, в котором аминокислота кислота была заменена с Arg (R) на Gly (G), положение 77, в котором аминокислота была заменена с Ser (S) на Asn (N), и положение 97, в котором аминокислота была заменена с Ala (A) на Thr (Т); и для вариабельной области легкой цепи гуманизированного антитела 14A9 выбор и сочетание типов мутаций производились из следующих сайтов: положение 63, в котором аминокислота была мутирована с Ser (S) на Ile (I), и положение 68, в котором аминокислота была мутирована с Gly (G) на Ser (S). Для вариабельной области тяжелой цепи гуманизированного антитела 16E5 выбор и сочетание типов мутаций производились из следующих сайтов: положение 46, в котором аминокислота была мутирована с Glu (E) на Lys (K), положение 63, в котором аминокислота кислота была мутирована с Lys (K) на Glu (E), положение 72, в котором аминокислота была мутирована с Thr (T) на Leu (L), положение 77, в котором аминокислота была мутирована с Ser (S) на Arg (R) и положение 97, в котором аминокислота была заменена с Ala (A) на Thr (T); и для вариабельной области легкой цепи гуманизированного антитела 16E5 выбор и сочетание типов мутаций производились из следующих сайтов: положение 2, в котором аминокислота была мутирована с Ile (I) на Ala (A), и положение 33, в котором аминокислота была мутирована с Asn (N) на Gln (Q). Сайты мутаций, описанные в данном документе, нумеруются, начиная с первой аминокислоты вариабельной области по порядку.
Последовательности гуманизированных антител 3F10, 14A9 и 16E5 и кодирующие их нуклеиновые кислоты были следующими: hz3F10-1.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 109-110; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 111-112), hz3F10-2.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 113-114; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 115-116), hz3F10-3.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 117-118; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 119-120), hz3F10-4.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 121- 122; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 123-124), hz3F10-5.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 125-126; легкая цепь и нуклеиновая кислота, кодирующая ее: SEQ ID NO 127-128), hz3F10-6.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 129-130; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 131-132), hz3F10-1.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 133-134; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 135-136), hz3F10-2.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 137-138; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 139 -140), hz3F10-3.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 141-142; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 143-144), hz3F10-4.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 145-146; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 147-148), hz3F10-5.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 149-150; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 151-152), hz3F10-6.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 153-154; легкие цепи и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 155-156), hz16E5-1.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 157-158; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 159-160), hz16E5-1.3 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 161-162; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 163-164), hz16E5-1.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 165-166; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 167 -168), hz16E5-3.2 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 169-170; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 171-172), hz16E5-3.1 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 173-174; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 175-176), hz16E5-3.3 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 177-178; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 179-180), hz14A9-2.3 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 181-182; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 183-184) и hz14A9-2.4 (тяжелая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 185-186; легкая цепь и нуклеиновые кислоты, кодирующие ее: SEQ ID NO 187-188).
Конструирование и экспрессия гуманизированных антител 3F10, 14A9 и 16E5:
ДНК, кодирующую полноразмерную легкую цепь и полноразмерную тяжелую цепь гуманизированных антител 3F10, 14A9 и 16E5, синтезировали и клонировали в векторы экспрессии (включая, например, вектор pcDNA3.1, описанный в CN107001463A, и вектор pCHO1.0, описанный в CN109422811A). Клетки СНО (система объемом 200 мл при 106 клеток/мл) трансфицировали 100 мкг каждого типа плазмид экспрессии тяжелой цепи гуманизированного антитела и плазмиды экспрессии легкой цепи и культивировали в среде ExpiCHO (Gibco, кат.№A29100-01) в инкубаторе при 37°С с 5% CO2 в течение 6 дней. После центрифугирования получали супернатант, и гуманизированное антитело в супернатанте очищали с использованием колонки с белком А.
Пример 2: Анализ Аффинности Антител Против CD47 на Основе Biacore
Равновесные константы диссоциации KD (в единицах М) были получены с помощью Biacore, измеряющего кинетику связывания белка CD47 человека (белок CD47 человека, с гистидиновой меткой; ACRObiosystems, кат.№CD7-H5227) и белка CD47 яванской макаки (белок CD47 яванской макаки/макаки-резус, с гистидиновой меткой; ACRObiosystems, кат.№CD7-C52H1) с антителами против CD47 (химерными или гуманизированными); анализ Biacore проводили при 25°C и данные регистрировали со скоростью 1 Гц.
Поликлональный кроличий антимышиный IgG (GE, BR-1008-38) разбавляли 10 мМ ацетатом натрия, pH 5,0, и иммобилизовали на референтной проточной ячейке и экспериментальной проточной ячейке биосенсорного чипа CM5 с использованием набора для связывания амина (GE, BR10050), и было достигнуто около 15000 RM. В начале каждого цикла разведенное исследуемое антитело (1,5 мг/мл) вводили в экспериментальную проточную кювету и выдерживали в течение 1 мин, чтобы оно было захвачено. Эти данные демонстрируют, что антитела против CD47 (химерные и гуманизированные) связывались с CD47, как было измерено с помощью Biacore.
Пример 3: Анализ Связывания Антител Против CD47 на Основе ИФА
Анализ связывания ИФА проводили на основе белка CD47 человека и химерных антител против CD47 или гуманизированных антител против CD47. 96-луночный планшет (Costar, кат.№9018) покрывали в течение ночи при 4°C 100 мкл/лунку покрывающего буфера, содержащего 2 мкг/мл CD47-His (белок CD47 человека, меченый гистидином; ACRObiosystems, кат.№CD7-H5227) в ФСБ (PBS). Лунки аспирировали и сайты неспецифического связывания блокировали, добавляя 100 мкл/лунку блокирующего раствора (ФСБ с 1% (масс./об.) бычим сывороточным альбумином (БСА, Sigma, кат.№B2064-100G)) и инкубируя планшет при 37°C в течение 1 часа. После трехкратной промывки 96-луночного планшета промывочным буфером (ФСБ с 0,01% (масс./об.) Твин 20 (Sigma, кат.№P9416-100ML)) добавляли по 100 мкл/лунку серийных разведений 1:4 (от 30 мкг/мл) антител против CD47 (см. Таблицу 3 для химерных антител и см. Таблицу 4 для гуманизированных антител) в блокирующем растворе и инкубировали планшет при комнатной температуре в течение 2 ч. 96-луночный планшет промывали, а затем инкубировали со вторичным антителом HRP-античеловеческим IgG (BD, кат.№555788) в течение 20 мин в темноте. После промывания 96-луночного планшета добавляли 100 мкл/лунку субстратного раствора ТМБ (TIANGEN, кат.№PA107-01) и инкубировали 96-луночный планшет при комнатной температуре в течение 10 мин. Для остановки реакции добавляли 100 мкл/лунку стоп-раствора (1 M H2SO4). Колориметрические сигналы генерировали и считывали при 450 нм с помощью многофункционального устройства для считывания микропланшетов (производитель: PerkinElmer; модель: EnVision). Данные анализировали с помощью GraphPad Prism5 и рассчитывали EC50. Эти данные демонстрируют, что антитела против CD47, связанные с CD47, и гуманизированные антитела показали хорошие результаты, как подтверждают результаты ИФА.
Пример 4: Анализ Связывания Антител Против CD47 на Основе Анализа с Применением Клеток
Клеточный анализ связывания антител против CD47 (химерных или гуманизированных) проводили на основе связывания с клеточной линией CHO-K1, стабильно экспрессирующей CD47. Клетки CHO-K1-CD47 (клетки CHO-K1, экспрессирующие белок CD47 человека) добавляли в каждую лунку 96-луночного планшета (Eppendorf, кат.№C030730.119) (по 1,2 × 104 клеток на лунку) и инкубировали с антителами против CD47 (20 мкг/мл, разведение 1:4 в ФСБ) при комнатной температуре в течение 1-2 часов. Затем клетки трижды промывали буфером ФСБ и вторичное антитело, меченный Alexa Fluor 488 козий античеловеческий IgG (Jackson ImmunoResearch Inc., кат.№109-545-088), разводили 1:200 с ФСБ и добавляли к клеткам по 100 мкл/лунку. Клетки инкубировали при комнатной температуре в течение 30 мин. Клетки трижды промывали буфером ФСБ. Ядерный краситель Hoechst (Sigma, кат.№B2261) разводили буфером ФСБ в соотношении 1:500, а затем добавляли в каждую лунку по 100 мкл/лунку для окрашивания в течении 10 мин. Клетки промывали 3 раза ФСБ и анализировали с использованием системы одновременного многопараметрического анализа (производитель: PerkinElmer; модель: Operetta). Результаты представлены в Таблицах 5 и 6. Эти данные демонстрируют, что антитела против CD47 связывались с CD47, как показывает анализ связывания на основе клеток.
Пример 5: Анализ Ингибирования Химерными Антителами Против CD47 на Основе Анализа с Применением Клеток
Блокирующие воздействия химерных антител против CD47 на связывание CD47 с SIRPα оценивали на основе анализа проточной цитометрии.
Клетки Jurkat (Банк клеток Китайской академии наук, кат.№TCHU123) добавляли в 96-луночный U-планшет по 5 × 105 клеток на лунку, и в каждую лунку добавляли 100 мкл разведения 1 мкг/мл лиганда CD47 Human-SIRPα-mFC (белок SIRP альфа/CD172a человека, меченый Fc IgG1 мыши, ACRObiosystems, кат.№SIA-H52A8) в буфере ФСБ. Раствор инкубировали при комнатной температуре в течение 1 часа. После двукратной промывки планшета буфером ФСБ в каждую лунку добавляли по 100 мкл химерных антител против CD47 (Таблица 7). 4-кратное разведение проводили буфером ФСБ от начальной концентрации 20 мкг/мл с получением 8 градиентов. Раствор инкубировали при комнатной температуре в течение 1-2 часов. После 3-кратного промывания планшета буфером ФСБ в качестве вторичного антитела для анализа использовали меченный Alexa Fluor 488 козий антимышиный IgG (Jackson ImmunoResearch Inc., кат.№115-545-062), и в каждую лунку добавляли 100 мкл вторичного антитела для анализа, разбавленного буфером ФСБ в соотношении 1:200. Планшет инкубировали при комнатной температуре в течение 1 ч и промывали 3 раза буфером ФСБ. Блокирующие воздействия химерных антител против CD47 на связывание CD47 с SIRPα определяли с использованием проточного цитометра (BD, модель: C6). Результаты представлены в Таблице 7. Химерные антитела против CD47 могут блокировать связывание CD47 с SIRPα. Среди всех антител Xi3F10, Xi16E5 и Xi14A9 обладают лучшим ингибирующим воздействием.
Пример 6: Анализ Ингибирования Антителами Против CD47 на Основе ИФА
Блокирующие воздействия антител против CD47 на связывание CD47 с SIRPα оценивали на основе анализа ИФА.
В 96-луночном микропланшете (Costar, кат.№9018) с CD47-His (белок CD47 человека, меченый гистидином; ACRObiosystems, кат. №CD7-H5227) в качестве захватывающего антигена в каждую лунку добавляли 100 мкл покрывающего буфера ФСБ, содержащего 2 мкг/мл захватывающего антигена. Планшет оставляли на ночь при температуре 2-8°C. Лунки аспирировали для удаления покрывающего буфера и блокировали 100 мкл/лунку блокирующего раствора (ФСБ с 1% (масс./об.) бычьего сывороточного альбумина (БСА, Sigma, кат.№B2064-100G)) путем инкубации при 37°С в течение 1 часа. 96-луночный планшет промывали промывочным буфером (ФСБ с 0,01% (масс./об.) Твин 20 (Sigma, кат.№P9416-100ML)). Затем добавляли 100 мкл/лунку 1 мкг/мл лиганда CD47 Human-SIRPα-mFC (белок SIRP альфа/CD172a человека, меченый Fc IgG1 мыши, ACRObiosystems, кат.№SIA-H52A8), и планшет инкубировали при 25±2°C в течение 1,5 ч. После того как 96-луночный планшет промывали промывочным буфером ФСБ, добавляли химерные антитела против CD47 или гуманизированные антитела против CD47 (см. Таблицу 8 для химерных антител и см. Таблицу 9 для гуманизированных антител). 4-кратное разведение проводили буфером ФСБ от начальной концентрации 20 мкг/мл с получением 8 градиентов. Раствор инкубировали при комнатной температуре в течение 1,5 часа. После того как планшет промывали буфером ФСБ, добавляли 100 мкл/лунку меченого HRP козьего антимышиного IgG (BD, кат.№554002), разбавленного 1:2000 буфером ФСБ, и планшет инкубировали при 25±2°С в течение 1 часа. После того, как 96-луночный планшет промывали буфером ФСБ, добавляли 100 мкл/лунку субстратного раствора ТМБ (TIANGEN, кат.№PA107-01), и планшет инкубировали при комнатной температуре для развития окрашивания в течение 10 мин. Для остановки реакции добавляли 100 мкл/лунку 1 М H2SO4. Колориметрические сигналы генерировали и считывали при 450 нм с помощью многофункционального устройства для считывания микропланшетов (производитель: PerkinElmer; модель: EnVision). Данные анализировали с помощью GraphPad Prism5 и рассчитывали EC50. Результаты представлены в Таблице 8 и Таблице 9. Химерные антитела (Xi3F10, Xi16E5, Xi14A9) и гуманизированные антитела 14A9, 16E5 и 3F10 обладали хорошими блокирующими эффектами, как продемонстрировал анализ на основе ИФА.
Пример 7: Анализ Антител Против CD47 на Основе Стимуляции Фагоцитоза Макрофагами
Способность антител против CD47 стимулировать фагоцитоз опухолевых клеток макрофагами, имеющими SIRPα на клеточной поверхности, определяли на основе проточной цитометрии.
Моноциты выделяли из мононуклеарных клеток периферической крови человека (PBMC, Sailybio, кат.№190056) с использованием набора для выделения моноцитов (STEMCELL, кат.№19058), помещали в 24-луночный планшет (Greiner bio-one, кат.№662-160) в количестве 5×105 клеток на лунку и индуцировали под действием 100 нг/мл стимулирующего фактора M-CSF (R&D Systems, кат.№216-MC-010) в течение 7 дней для образования макрофагов. 1 × 106 клеток-мишеней HL60 (Шанхайский институт биохимии и клеточной биологии Китайской академии наук, кат.№TCHu23) суспендировали в 5 мкмоль/л CFSE (BD, кат.№565082) флуоресцентного красителя (разбавленного буфером ФСБ до желаемой концентрации), инкубировали на водяной бане при 37°C в темноте в течение 15 минут и промывали буфером ФСБ для получения клеток HL60, меченных CFSE, которые затем инкубировали с 10 мкг/мл и 1 мкг/мл каждого антитела против CD47 (см. Таблицу 10 для химерных антител и см. Таблицу 11 для гуманизированных антител) в инкубаторе при 37°C с 5% CO2 в течение 1-2 часов. Культивируемые клетки HL60 промывали 3 раза буфером ФСБ и добавляли к макрофагам. Клетки инкубировали в инкубаторе при 37°C с 5% СО2 в течение 2-4 ч. После 3-кратного промывания клеток буфером ФСБ в каждую лунку добавляли смесь из 260 мкл ФСБ, 20 мкл антитела против CD14 АПК - (APC Mouse Anti-Human CD14, BD, кат.№555399) и 20 мкл антитела PE-CD11b (PE Mouse Anti-Human CD11b/Mac-1, BD, кат.№555388). Клетки инкубировали при 4°С в темноте в течение 30 мин, промывали 3 раза буфером ФСБ и расщепляли трипсином (Gibco, кат.№12604-013). Скорость фагоцитоза (%) макрофагами определяли с помощью проточного цитометра (BD, модель: C6).
Влияния химерных антител против CD47 и гуманизированных антител против CD47 на фагоцитоз макрофагов представлены в Таблицах 10 и 11. Среди антител химерные антитела Xi3F10, Xi16E5 и Xi14A9 и гуманизированные антитела против CD47 обладали хорошими стимулирующими эффектами на фагоцитоз, и эффективность гуманизированных антител hz14A9-2.3 и hz14A9-2.4 была более высокой.
Пример 8: Воздействие Антител Против CD47 на CD4+Т-Клетки
Воздействие антител против CD47 на CD4+Т-клетки определяли на основе анализа проточной цитометрии.
CD4+Т-клетки выделяли из мононуклеарных клеток периферической крови человека (PBMC, Sailybio, кат.№190056) с использованием набора для выделения Т-клеток (Miltenyi Biotech, кат.№130-094-131) и помещали в 24-луночный планшет (Greiner bio-one, кат.№662106) по 5×105 клеток на лунку. Антитела против CD47 (см. Таблицу 12 для химерных антител и см. Таблицу 13 для гуманизированных антител) добавляли по отдельности в одно и тоже время так, чтобы конечные концентрации составляли 10 мкг/мл и 1 мкг/мл. Добавляли полную среду 1640 и инкубировали клетки в инкубаторе при 37°С с 5% CO2 в течение 20 ч и окрашивали с использованием набора для апоптоза (STEMCELL, кат.№556547) при комнатной температуре в течение 15 мин. Скорость апоптоза клеток (%) определяли с помощью проточного цитометра (BD, модель: C6). Скорость апоптоза рассчитывали на основе суммы раннего апоптоза и позднего апоптоза. Результаты демонстрируют, что антитела против CD47 (см. Таблицу 12 для химерных антител и см. Таблицу 13 для гуманизированных антител) не оказывали значимого влияния на апоптоз Т-клеток.
Пример 9: Анализ Термостабильности Антител Против CD47 на Основе Нано-ДСФ
Высокопроизводительный анализатор стабильности белка Prometheus NT.48 представляет собой прибор для получения различных типов данных, таких как стабильность молекулярной структуры белка, стабильность агрегации и стабильность коллоидной дисперсии. С помощью этого прибора измеряли температуры плавления (Tm) и температуры агрегации (Tagg) химерных антител против CD47 и гуманизированных антител против CD47. Результаты представлены в Таблицах 14 и 15 и демонстрируют, что антитела против CD47 обладают хорошей термостабильностью.
Пример 10: Воздействие Антител Против CD47 на Агглютинацию Эритроцитов
Некоторые опубликованные исследования продемонстрировали, что поверхность эритроцитов содержит определенное количество белка CD47, который вызывает связывание некоторых антител против CD47 с эритроцитами после их добавления и, таким образом, может вызывать агглютинацию эритроцитов. Таким образом, исследовали влияние антител против CD47 на агглютинацию эритроцитов.
Собирали антикоагулированную кровь и тщательно смешивали с равным количеством физиологического раствора. Смесь центрифугировали при 2000 об./мин в течение 5 минут и супернатант удаляли. Эритроциты промывали 3 раза сбалансированным солевым раствором Хенкса, не содержащим кальция и магния (Thermo Fisher Scientific, кат.№14175-095). При первых двух промывках смесь центрифугировали при 2000 об./мин в течение 5 мин, при последней промывке смесь центрифугировали при 2000 об./мин в течение 10 мин и удаляли супернатант. Эритроциты разводили в 10 раз буфером ФСБ с образованием 10% суспензии эритроцитов, которую добавляли в 96-луночный U-планшет (eppendorf, кат.№003073119) по 100 мкл/лунку. Различные концентрации антител против CD47 добавляли по 100 мкл/лунку. Антитела разводили в 3 раза буфером ФСБ от исходной концентрации 10 мкг/мл, получая 8 градиентов концентрации. Планшет инкубировали при 37°С в течение 2-6 часов. Эритроциты фиксировали и фотографировали. Там, где происходила агглютинация, эритроциты полностью слипались, оседали на дно и распластывались в виде куска сетки; там, где агглютинации не происходило, эритроциты оседали на дно лунки и присутствовали в виде точек.
Влияние химерных антител против CD47 на агглютинацию эритроцитов представлено на Фиг. 1. Влияние гуманизированных антител против CD47 на агглютинацию эритроцитов представлено на Фиг. 2 и 3. Все химерные антитела Xi3F10, Xi16E5 и Hu5F9 вызывали агглютинацию крови. Xi3F10 вызывало агглютинацию крови при 1111,1 нг/мл, а Xi16E5 и Hu5F9 вызывали агглютинацию крови при 123,46 нг/мл. Все химерные антитела Xi2B2, Xi2H8 и Xi14A9 не вызывали агглютинации крови при всех исследованных концентрациях. Гуманизированные антитела hz3F10-3.1, hz3F10-4.1, hz3F10-3.2 и hz3F10-4.2 вызывали агглютинацию крови с 3,3 мкг/мл, а hz16E5-1.1, hz16E5-3.1, hz16E5-1.2, hz16E5-3.2, hz16E5-1.3 и hz16E5- 3.3 вызывали агглютинацию крови при 3,3 мкг/мл. Другие гуманизированные антитела не вызывали агглютинации крови при всех исследованных концентрациях.
Пример 11: Анализ Связывания Антител Против CD47 с Эритроцитами
На основании того факта, что определенное количество CD47 на поверхности эритроцитов может связываться с некоторыми антителами против CD47, оценивали связывание антител против CD47 с эритроцитами.
Собирали антикоагулированную кровь и тщательно смешивали с равным количеством физиологического раствора. Смесь центрифугировали при 2000 об./мин в течение 5 минут и супернатант удаляли. Эритроциты промывали 3 раза сбалансированным солевым раствором Хенкса, не содержащим кальция и магния (Thermo Fisher Scientific, кат.№14175-095). При первых двух промывках смесь центрифугировали при 2000 об./мин в течение 5 мин, при последней промывке смесь центрифугировали при 2000 об./мин в течение 10 мин и удаляли супернатант.Выделенные эритроциты фиксировали 4% полиоксиметиленом (Sangon Biotech (Shanghai) Co., Ltd., кат.№E672002-0500) в течение ночи, инкубировали с 10 мкг/мл или 1 мкг/мл антител против CD47 при комнатной температуре на следующий день в течение 1-2 ч, промывали буфером ФСБ, инкубировали со вторичным антителом, меченным Alexa Fluor 488 козьим античеловеческим IgG (Jackson ImmunoResearch Inc., кат.№109-545-088), разведенным 1:200 с буфером ФСБ при комнатной температуре в течение 1 часа, и промывали буфером ФСБ, и связывание эритроцитов с химерными антителами против CD47 (см. Таблицу 16) или гуманизированными антителами (см. Таблицу 17) оценивали с использованием проточного цитометра (BD, модель: C6) по средней интенсивности флуоресценции (СИФ, MFI).
Пример 12. Фармакодинамическая Активность Антител Против CD47 в Мышиной Модели Гематологической Опухоли с Использованием Клеток Раджи (Raji)
Мышиная модель гематологической опухоли была создана с использованием клеток Раджи гематологической опухоли. В модели применяли антитела против CD47 и оценивали фармакодинамическую активность антител.
Суспензию клеток Раджи в буфере ФСБ готовили в концентрации 5×106 клеток/мл, и вводили самкам мышей NOD/SCID через хвостовую вену в дозе 0,1 мл/мышь. Через 7 дней мышей рандомизировали на 4 группы по 10 особей, которые представляли собой группу 1: группу IgG4; группу 2: группа Hu5F9; группу 3: hz3F10-6.1; и группу 4: hz14A9-2.3. Введение осуществляли внутрибрюшинно в дозах 10 мг/кг в течение 21 дня подряд. Наблюдали за выживаемостью животных.
Как представлено на Фиг. 4, антитела против CD47 hz14A9-2.3 и hz3F10-6.1 продемонстрировали противоопухолевую активность в модели гематологической опухоли на клетках Раджи. Показатели выживаемости мышей демонстрируют, что: все животные в группе IgG4 погибли на День 17, при медиане выживаемости 13,5 дней; все животные в группе Hu5F9 погибли на День 30, при медиане выживания 18,5 дня; все животные в группе hz14A9-2.3 погибли на День 34, при медиане выживания 28,5 дня; все животные в группе hz3F10-6.1 погибли на День 21, при медиане выживания 17,5 дней. Эти данные демонстрируют, что антитело hz14A9-2.3 обладает большей эффективностью в отношении увеличения продолжительности жизни животных, в сравнении с другими группами, а антитела hz3F10-6.1 и Hu5F9 обладают в основном эквивалентными эффектами.
Пример 13. Анализ Токсичности Антител Против CD47 при Однократном Введении
Поскольку CD47 экспрессируется на эритроцитах и играет роль в очищении организма от старых эритроцитов, сравнивали токсическое влияние антител против CD47 у мышей B-hCD47.
Мыши B-hCD47 были рандомизированы на 3 группы: группа Hu5F9 из 3 мышей, группа hz14A9-2.3 из 4 мышей и группа hz3F10-6.1 из 3 мышей. Мышам B-hCD47 вводили антитело Hu5F9, антитело hz14A9-2.3 или антитело hz3F10-6.1 через хвостовую вену в однократной дозе 10 мг/кг, и изменения числа эритроцитов (RBC), уровня гемоглобина (HGB) и массы тела измеряли через 2, 4, 7, 10 и 14 дней после введения.
Как представлено в Таблице 18 и на Фиг. 5 и 6, только в группе hz14A9-2.3 масса тела мышей постоянно увеличивалась, а масса тела мышей в группах Hu5F9 и hz3F10-6.1 сначала уменьшалась, а затем увеличивалась после введения; в группе hz3F10-6.1 снижение было больше, чем в группе Hu5F9. Как представлено в Таблицах 19-20 и на Фиг. 7-10, уровни RBC и HGB у животных всех трех групп снижались до минимальных значений через 4 дня после введения, а затем начинали повышаться. Уровни RBC и HGB в группе hz14A9-2.3, по существу, вернулись к норме через 7 дней после введения, а уровни в двух других группах, по существу, вернулись к норме, по меньшей мере, через 10 дней после введения. Три группы расположены в порядке убывания в соответствии со снижением уровня RBC и HGB через 4 дня после введения: hz3F10-6.1>Hu5F9>hz14A9-2.3. Видно, что антитело hz14A9-2.3 не обладает значимой токсичностью и превосходит за свойствами положительное антитело Hu5F9.
Пример 14
Противоопухолевую активность антител исследовали с использованием мышиной модели клеток острого миелоидного лейкоза человека MOLM-16. Каждой мыши NOD-SCID подкожно инокулировали клетки MOLM-16, и после роста опухоли до 80-150 мм3, животных рандомизировали на 5 групп: (1) модельная группа (группа отрицательного контроля, получавшая человеческий IgG4, 5 мг/мл), кол-во=10 мышей; (2) группа hz14A9-2.3, 0,5 мг/кг, кол-во=6 мышей; (3) группа hz14A9-2.3, 1,5 мг/кг, кол-во=6 мышей; (4) группа hz14A9-2.3, 5 мг/кг, кол-во=6 мышей; и (5) группа Hu5F9, 5 мг/кг, кол-во=6 мышей. В день 0 (D0) мышей разделяли на группы и вводили внутривенно один раз в 3 дня, всего две дозы. Диаметры опухолей измеряли два раза в неделю, а терапевтические эффекты определяли в зависимости от объема опухоли.
Объем опухоли (V) рассчитывали следующим образом: V=(a × b2)/2, где a и b обозначают длину и ширину, соответственно.
T/C (%)=(Т - Т0)/(C - C0) × 100, где T и C представляют собой средние объемы опухоли в конце эксперимента в группе лечения и группе отрицательного контроля, соответственно; T0 и C0 представляют собой средние объемы опухоли в начале эксперимента в группе лечения и группе отрицательного контроля, соответственно.
Ингибирование роста опухоли (TGI) (%)=100% - T/C (%).
Результаты представлены в Таблице 21 и 11. Антитело hz14A9-2.3 способно эффективно ингибировать рост опухоли в дозе 1,5 мг/кг, при этом ингибирование роста опухоли (или TGI) достигает 93% на День 17 (D17). Ингибирование роста опухоли антителом hz14A9-2.3 достигало 125% в дозе 5 мг/кг.
D0
D0
D17
D17
D17
D17
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> CHIA TAI TIANQING PHARMACEUTICAL GROUP CO., LTD.
<120> АНТИГЕНСВЯЗЫВАЮЩИЙ ПОЛИПЕПТИД, СВЯЗЫВАЮЩИЙСЯ С CD47, И ЕГО ПРИМЕНЕНИЕ
<160> 198
<170> SIPOSequenceListing 1.0
<210> 1
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 1
Gly Phe Ser Leu Thr Asn Tyr Gly Val His
1 5 10
<210> 2
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 2
Gly Phe Thr Phe Ser Asn Tyr Tyr Met Ser
1 5 10
<210> 3
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 3
Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn
1 5 10
<210> 4
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 4
Gly Tyr Thr Phe Ser Arg Tyr Trp Ile Glu
1 5 10
<210> 5
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 5
Gly Phe Asn Ile Glu Asp Asp Tyr Ile Glu
1 5 10
<210> 6
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 6
Ile Ile Trp Ala Gly Gly Ser Thr Asn
1 5
<210> 7
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 7
Tyr Ile Ser Ser Gly Gly Gly Ser Thr Tyr
1 5 10
<210> 8
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 8
Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr
1 5 10
<210> 9
<211> 8
<212> БЕЛОК
<213> Mus musculus
<400> 9
Glu Phe Ile Pro Gly Ser Asp Thr
1 5
<210> 10
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 10
Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys
1 5 10
<210> 11
<211> 8
<212> БЕЛОК
<213> Mus musculus
<400> 11
Asp Asp Tyr Ala Ser Met Asp Tyr
1 5
<210> 12
<211> 3
<212> БЕЛОК
<213> Mus musculus
<400> 12
Phe Ala Tyr
1
<210> 13
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 13
Phe Ser His Leu Arg Gly Pro Met Asp Tyr
1 5 10
<210> 14
<211> 8
<212> БЕЛОК
<213> Mus musculus
<400> 14
Gly Gly Leu Arg Arg Met Asp Tyr
1 5
<210> 15
<211> 11
<212> БЕЛОК
<213> Mus musculus
<400> 15
Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr
1 5 10
<210> 16
<211> 16
<212> БЕЛОК
<213> Mus musculus
<400> 16
Arg Ser Ser Gln Ser Leu Val His Ser Asn Gly Asn Thr Tyr Leu His
1 5 10 15
<210> 17
<211> 16
<212> БЕЛОК
<213> Mus musculus
<400> 17
Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn
1 5 10 15
<210> 18
<211> 16
<212> БЕЛОК
<213> Mus musculus
<400> 18
Arg Ser Ser Gln Ser Leu Val His Ser Asn Gly Tyr Thr Tyr Leu His
1 5 10 15
<210> 19
<211> 12
<212> БЕЛОК
<213> Mus musculus
<400> 19
Arg Ala Ser Ser Ser Val Ser Ser Thr Tyr Leu His
1 5 10
<210> 20
<211> 11
<212> БЕЛОК
<213> Mus musculus
<400> 20
Lys Ala Ser Glu Asn Val Val Ser Tyr Val Ser
1 5 10
<210> 21
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 21
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 22
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 22
Leu Val Ser Lys Leu Asp Ser
1 5
<210> 23
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 23
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 24
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 24
Thr Thr Ser Thr Leu Ala Ser
1 5
<210> 25
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 25
Gly Ala Ser Asn Arg Tyr Thr
1 5
<210> 26
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 26
Ser Gln Ser Thr His Val Pro Tyr Thr
1 5
<210> 27
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 27
Gly Thr His Phe Pro Leu Thr
1 5
<210> 28
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 28
Ser Gln Ser Thr His Val Pro Pro Thr
1 5
<210> 29
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 29
Gln Gln Phe Ser Asp Ser Thr Trp Thr
1 5
<210> 30
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 30
Gly Gln Ser Tyr Ser Tyr Pro Leu Thr
1 5
<210> 31
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<400> 31
Gln Gln Phe Ser Glu Ser Thr Trp Thr
1 5
<210> 32
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> UNSURE
<222> (5)
<223> Xaa представляет собой D или E
<400> 32
Gln Gln Phe Ser Xaa Ser Thr Trp Thr
1 5
<210> 33
<211> 116
<212> БЕЛОК
<213> Mus musculus
<400> 33
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Ala Gly Gly Ser Thr Asn Tyr Asn Ser Ala Leu Met
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Asp Asp Tyr Ala Ser Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser
115
<210> 34
<211> 112
<212> БЕЛОК
<213> Mus musculus
<400> 34
Asp Ala Phe Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Tyr Thr Leu Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 35
<211> 119
<212> БЕЛОК
<213> Mus musculus
<400> 35
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Val Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Glu Glu Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Arg Thr Ala Phe
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Thr Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Ala Ser Val Thr Val Ser Ser
115
<210> 36
<211> 112
<212> БЕЛОК
<213> Mus musculus
<400> 36
Asp Ala Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Leu Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 37
<211> 112
<212> БЕЛОК
<213> Mus musculus
<400> 37
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Tyr Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Ser Gly Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Lys Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
100 105 110
<210> 38
<211> 112
<212> БЕЛОК
<213> Mus musculus
<400> 38
Asp Ala Val Val Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 39
<211> 117
<212> БЕЛОК
<213> Mus musculus
<400> 39
Glu Val Gln Leu Gln Gln Ser Val Ala Glu Leu Met Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Tyr Cys Lys Ala Thr Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Lys Gln Arg Pro Gly His Gly Leu Glu Trp Ile
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Phe Thr Ala Glu Ile Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Ser
100 105 110
Val Thr Val Ser Ser
115
<210> 40
<211> 108
<212> БЕЛОК
<213> Mus musculus
<400> 40
Asp Ile Val Met Thr Gln Thr Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Ser Gly Ala Ser Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Val Glu
65 70 75 80
Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 41
<211> 120
<212> БЕЛОК
<213> Mus musculus
<400> 41
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Val Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Val Ser Gly Phe Asn Ile Glu Asp Asp
20 25 30
Tyr Ile Glu Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys Tyr Ala Pro Lys Phe
50 55 60
Gln Asp Lys Ala Thr Ile Thr Gly Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 42
<211> 107
<212> БЕЛОК
<213> Mus musculus
<400> 42
Asn Ile Val Leu Thr Gln Ser Pro Lys Ser Met Ser Met Ser Val Gly
1 5 10 15
Glu Arg Val Thr Leu Ser Cys Lys Ala Ser Glu Asn Val Val Ser Tyr
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Glu Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Ile Gly
50 55 60
Ser Gly Ser Ser Thr Asp Phe Thr Leu Ile Ile Ser Ser Phe Gln Pro
65 70 75 80
Glu Asp Leu Ala Asp Tyr His Cys Gly Gln Ser Tyr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 43
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 43
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 44
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 44
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 45
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 45
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 46
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 46
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 47
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 47
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 48
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 48
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 49
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 49
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 50
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 50
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 51
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 51
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 52
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 52
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 53
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 53
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 54
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 54
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 55
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 55
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 56
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 56
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 57
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 57
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 58
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 58
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 59
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 59
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 60
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 60
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 61
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 61
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 62
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 62
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 63
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 63
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 64
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 64
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 65
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<400> 65
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 66
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<400> 66
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 67
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<400> 67
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 68
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<400> 68
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 69
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<400> 69
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 70
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<400> 70
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 71
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<400> 71
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 72
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<400> 72
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 73
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<400> 73
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 74
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<400> 74
Asp Ala Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 75
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<400> 75
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 76
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<400> 76
Asp Ala Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 77
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<400> 77
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 78
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<400> 78
Asp Ala Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 79
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<400> 79
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Phe Asn Ile Glu Asp Asp
20 25 30
Tyr Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Gly Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 80
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<400> 80
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asn Val Val Ser Tyr
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Ser Arg Phe Ile Gly
50 55 60
Ser Gly Ser Ser Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gln Ser Tyr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 81
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<400> 81
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Phe Asn Ile Glu Asp Asp
20 25 30
Tyr Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Gly Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 82
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<400> 82
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asn Val Val Ser Tyr
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Ser Arg Phe Ile Gly
50 55 60
Ser Gly Ser Ser Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gln Ser Tyr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 83
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> UNSURE
<222> (73)
<223> Xaa представляет собой D или E
<220>
<221> UNSURE
<222> (74)
<223> Xaa представляет собой I или E
<220>
<221> UNSURE
<222> (77)
<223> Xaa представляет собой S или N
<400> 83
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Xaa Xaa Ser Thr Xaa Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 84
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> UNSURE
<222> (48)
<223> Xaa представляет собой L или W
<220>
<221> UNSURE
<222> (71)
<223> Xaa представляет собой D или S
<220>
<221> UNSURE
<222> (72)
<223> Xaa представляет собой F или Y
<220>
<221> UNSURE
<222> (94)
<223> Xaa представляет собой D или E
<400> 84
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Xaa
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Xaa Xaa Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Xaa Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 85
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> UNSURE
<222> (46)
<223> Xaa представляет собой E или K
<220>
<221> UNSURE
<222> (63)
<223> Xaa представляет собой E или K
<220>
<221> UNSURE
<222> (72)
<223> Xaa представляет собой L или T
<220>
<221> UNSURE
<222> (77)
<223> Xaa представляет собой R или S
<220>
<221> UNSURE
<222> (97)
<223> Xaa представляет собой A или T
<400> 85
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Xaa Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Xaa Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Xaa Asp Thr Ser Thr Xaa Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Xaa Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 86
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> UNSURE
<222> (2)
<223> Xaa представляет собой I или A
<400> 86
Asp Xaa Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 87
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> UNSURE
<222> (24)
<223> Xaa представляет собой A или V
<220>
<221> UNSURE
<222> (72)
<223> Xaa представляет собой R или G
<220>
<221> UNSURE
<222> (77)
<223> Xaa представляет собой S или N
<220>
<221> UNSURE
<222> (97)
<223> Xaa представляет собой A или T
<400> 87
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Xaa Ser Gly Phe Asn Ile Glu Asp Asp
20 25 30
Tyr Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Xaa Asp Thr Ser Thr Xaa Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Xaa Arg Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 88
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> UNSURE
<222> (63)
<223> Xaa представляет собой S или I
<220>
<221> UNSURE
<222> (68)
<223> Xaa представляет собой S или G
<400> 88
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asn Val Val Ser Tyr
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Ser Arg Phe Xaa Gly
50 55 60
Ser Gly Ser Xaa Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gln Ser Tyr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 89
<211> 443
<212> БЕЛОК
<213> Искусственная последовательность
<400> 89
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Ala Gly Gly Ser Thr Asn Tyr Asn Ser Ala Leu Met
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Asp Asp Tyr Ala Ser Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 90
<211> 1332
<212> ДНК
<213> Искусственная последовательность
<400> 90
caggtgcagc tgaaggagtc tggaccagga ctggtggctc catctcagtc cctgagcatc 60
acctgcacag tgtccggctt cagcctgacc aactacggag tgcactgggt gaggcagcca 120
cctggcaagg gactggagtg gctgggcatc atctgggctg gcggctccac aaactataat 180
tctgccctga tgtcccggct gtctatctcc aaggacaaca gcaagtctca ggtgtttctg 240
aagatgaata gcctgcagac cgacgataca gccatgtact attgtgctag ggacgattac 300
gccagcatgg attattgggg ccagggcacc tctgtgacag tgtccagcgc ctctacaaag 360
ggcccttccg tgttcccact ggctccctgc tccagaagca catctgagtc caccgccgct 420
ctgggctgtc tggtgaagga ctacttccct gagccagtga ccgtgtcctg gaacagcggc 480
gccctgacat ctggcgtgca cacctttcca gctgtgctgc agtccagcgg cctgtactcc 540
ctgtcttccg tggtgacagt gcccagctct tccctgggca ccaagacata tacctgcaac 600
gtggaccata agccttccaa taccaaggtg gataagaggg tggagagcaa gtacggacca 660
ccttgcccac catgtccagc tcctgagttt ctgggaggac catccgtgtt cctgtttcct 720
ccaaagccta aggacaccct gatgatcagc cggacacctg aggtgacctg cgtggtggtg 780
gacgtgtctc aggaggatcc agaggtgcag ttcaactggt acgtggatgg cgtggaggtg 840
cacaatgcta agaccaagcc aagagaggag cagtttaatt ccacataccg cgtggtgagc 900
gtgctgaccg tgctgcatca ggattggctg aacggcaagg agtataagtg caaggtgtcc 960
aataagggcc tgcccagctc tatcgagaag acaatcagca aggctaaggg acagcctagg 1020
gagccacagg tgtacaccct gcccccttct caggaggaga tgacaaagaa ccaggtgtcc 1080
ctgacctgtc tggtgaaggg cttctatcca agcgacatcg ctgtggagtg ggagtctaat 1140
ggccagcccg agaacaatta caagaccaca ccacccgtgc tggactctga tggctccttc 1200
tttctgtatt ctaggctgac agtggataag tcccggtggc aggagggcaa cgtgtttagc 1260
tgctctgtga tgcacgaggc cctgcacaat cattataccc agaagtccct gagcctgtct 1320
ctgggcaagt ga 1332
<210> 91
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 91
Asp Ala Phe Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Tyr Thr Leu Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 92
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 92
gacgccttca tgacccagac accactgtcc ctgcctgtga gcctgggcga tcaggcttct 60
atctcctgca gatccagcca gtctctggtg cactccaacg gcaatacata cctgcattgg 120
tatctgcaga agccaggcca gtcccccaag ctgctgatct acaaggtgag caacaggttc 180
tctggcgtgc ctgaccggtt tagcggctct ggctccggca ccgatttcac actgaagatc 240
tccagggtgg aggctgagga cctgggcgtg tacttttgta gccagtctac ccacgtgcca 300
tatacactgg gcggcggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 93
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<400> 93
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Val Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Glu Glu Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Arg Thr Ala Phe
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Thr Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Ala Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 94
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<400> 94
gaggtgcagc tgcagcagtc tggccccgag ctgaagaagc ctggcgagac cgtgaagatc 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaagcaggtg 120
ccaggcaagg gcctgaagtg gatgggctgg atcaacacca atacaggcga gcccacatac 180
gccgaggagt tcaagggcag attcgctttt agcctggaga cctctgcccg cacagctttt 240
ctgcagatca acaatctgaa gaacgaggac accgccacat acttctgtac caggttttcc 300
cacctgcggg gccccatgga ttattggggc cagggcgcta gcgtgacagt gtccagcgcc 360
tctacaaagg gcccttccgt gttcccactg gctccctgct ccagaagcac atctgagtcc 420
accgccgctc tgggctgtct ggtgaaggac tacttccctg agccagtgac cgtgtcctgg 480
aacagcggcg ccctgacatc tggcgtgcac acctttccag ctgtgctgca gtccagcggc 540
ctgtactccc tgtcttccgt ggtgacagtg cccagctctt ccctgggcac caagacatat 600
acctgcaacg tggaccataa gccttccaat accaaggtgg ataagagggt ggagagcaag 660
tacggaccac cttgcccacc atgtccagct cctgagtttc tgggaggacc atccgtgttc 720
ctgtttcctc caaagcctaa ggacaccctg atgatcagcc ggacacctga ggtgacctgc 780
gtggtggtgg acgtgtctca ggaggatcca gaggtgcagt tcaactggta cgtggatggc 840
gtggaggtgc acaatgctaa gaccaagcca agagaggagc agtttaattc cacataccgc 900
gtggtgagcg tgctgaccgt gctgcatcag gattggctga acggcaagga gtataagtgc 960
aaggtgtcca ataagggcct gcccagctct atcgagaaga caatcagcaa ggctaaggga 1020
cagcctaggg agccacaggt gtacaccctg cccccttctc aggaggagat gacaaagaac 1080
caggtgtccc tgacctgtct ggtgaagggc ttctatccaa gcgacatcgc tgtggagtgg 1140
gagtctaatg gccagcccga gaacaattac aagaccacac cacccgtgct ggactctgat 1200
ggctccttct ttctgtattc taggctgaca gtggataagt cccggtggca ggagggcaac 1260
gtgtttagct gctctgtgat gcacgaggcc ctgcacaatc attataccca gaagtccctg 1320
agcctgtctc tgggcaagtg a 1341
<210> 95
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 95
Asp Ala Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Leu Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 96
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 96
gacgccgtga tgacccagac accactgtcc ctgcccgtga gcctgggcga tcaggcttct 60
atctcctgca gatccagcca gtctctggtg cactccaacg gctacacata tctgcattgg 120
tacctgcaga agcctggcca gtccccaaag ctgctgatct ataaggtgag caataggttc 180
tctggagtgc cagaccggtt tagcggatct ggatccggca ccgatttcac actgaagatc 240
tccaggctgg aggctgagga cctgggcgtg tacttctgta gccagtctac ccacgtgccc 300
cctacatttg gcggcggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 97
<211> 439
<212> БЕЛОК
<213> Искусственная последовательность
<400> 97
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Tyr Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Ser Gly Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Lys Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
100 105 110
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
115 120 125
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
130 135 140
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
145 150 155 160
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
165 170 175
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
180 185 190
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
195 200 205
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
210 215 220
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
225 230 235 240
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
245 250 255
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
260 265 270
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
275 280 285
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
290 295 300
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
305 310 315 320
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
325 330 335
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
340 345 350
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
355 360 365
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
370 375 380
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
385 390 395 400
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
405 410 415
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
420 425 430
Leu Ser Leu Ser Leu Gly Lys
435
<210> 98
<211> 1320
<212> ДНК
<213> Искусственная последовательность
<400> 98
gaagtgatgc tggtggagag cggaggagga ctggtgcagc caggaggcag cctgaagctg 60
tcttgcgccg cttccggctt cacctttagc aactactata tgtcttgggt gagacagaca 120
cccgagaagc gcctggagtg ggtggcttac atctccagcg gaggaggatc cacctactat 180
cctgacagcg tgaagggcag gttcaccatc tctcgggata acgccaagaa tacactgtac 240
ctgcagatgt cttccctgaa gtccgaggac acagctatgt actattgtgc ctggtttgct 300
tattggggcc agggcaccct ggtgacagtg tctgctgcct ctacaaaggg cccttccgtg 360
ttcccactgg ctccctgctc cagaagcaca tctgagtcca ccgccgctct gggctgtctg 420
gtgaaggact acttccctga gccagtgacc gtgtcctgga acagcggcgc cctgacatct 480
ggcgtgcaca cctttccagc tgtgctgcag tccagcggcc tgtactccct gtcttccgtg 540
gtgacagtgc ccagctcttc cctgggcacc aagacatata cctgcaacgt ggaccataag 600
ccttccaata ccaaggtgga taagagggtg gagagcaagt acggaccacc ttgcccacca 660
tgtccagctc ctgagtttct gggaggacca tccgtgttcc tgtttcctcc aaagcctaag 720
gacaccctga tgatcagccg gacacctgag gtgacctgcg tggtggtgga cgtgtctcag 780
gaggatccag aggtgcagtt caactggtac gtggatggcg tggaggtgca caatgctaag 840
accaagccaa gagaggagca gtttaattcc acataccgcg tggtgagcgt gctgaccgtg 900
ctgcatcagg attggctgaa cggcaaggag tataagtgca aggtgtccaa taagggcctg 960
cccagctcta tcgagaagac aatcagcaag gctaagggac agcctaggga gccacaggtg 1020
tacaccctgc ccccttctca ggaggagatg acaaagaacc aggtgtccct gacctgtctg 1080
gtgaagggct tctatccaag cgacatcgct gtggagtggg agtctaatgg ccagcccgag 1140
aacaattaca agaccacacc acccgtgctg gactctgatg gctccttctt tctgtattct 1200
aggctgacag tggataagtc ccggtggcag gagggcaacg tgtttagctg ctctgtgatg 1260
cacgaggccc tgcacaatca ttatacccag aagtccctga gcctgtctct gggcaagtga 1320
<210> 99
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 99
Asp Ala Val Val Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 100
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 100
gacgccgtgg tgacccagac accactgacc ctgtccgtga caatcggcca gcccgcttct 60
atctcctgca agtccagcca gtccctgctg gacagcgatg gcaagacata cctgaactgg 120
ctgctgcaga ggccaggaca gagccctaag cggctgatct atctggtgtc taagctggac 180
tccggcgtgc ctgatagatt caccggcagc ggctctggca ccgactttac actgaagatc 240
tctcgcgtgg aggccgagga tctgggcgtg tactattgtt ggcagggcac ccacttccca 300
ctgacatttg gcgctggcac caagctggag ctgaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 101
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 101
Glu Val Gln Leu Gln Gln Ser Val Ala Glu Leu Met Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Tyr Cys Lys Ala Thr Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Lys Gln Arg Pro Gly His Gly Leu Glu Trp Ile
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Phe Thr Ala Glu Ile Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Ser
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 102
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 102
gaggtgcagc tgcagcagtc tgtggccgag ctgatgaagc caggcgcttc cgtgaagatc 60
tactgcaagg ccaccggcta cacattcagc agatattgga tcgagtgggt gaagcagagg 120
ccaggacacg gactggagtg gatcggcgag ttcatccctg gctctgacac cacaaacttc 180
aatgagaagt ttaagggcaa ggccaccttt acagctgaga tctccagcaa caccgcttat 240
atgcagctgt cttccctgac atccgaggac agcgccgtgt acttttgtgc taggggcggc 300
ctgaggcgga tggattattg gggccagggc acctccgtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 103
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 103
Asp Ile Val Met Thr Gln Thr Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Ser Gly Ala Ser Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Val Glu
65 70 75 80
Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 104
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 104
gacatcgtga tgacccagac acccgccatc atgtccgcct ctcctggcga gaaggtgacc 60
atgacatgca gggcctccag ctccgtgtcc agcacctacc tgcactggta tcagcagaag 120
agcggcgctt ctccaaagct gtggatctac accacatcca cactggctag cggagtgcca 180
gctcggttct ccggaagcgg atctggcacc tcctatagcc tgacaatctc ttccgtggag 240
gccgaggacg ccgctaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
ggcggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 105
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<400> 105
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Val Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Val Ser Gly Phe Asn Ile Glu Asp Asp
20 25 30
Tyr Ile Glu Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys Tyr Ala Pro Lys Phe
50 55 60
Gln Asp Lys Ala Thr Ile Thr Gly Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 106
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<400> 106
gaggtgcagc tgcagcagtc tggagctgag gtggctaggc caggagcttc cgtgaagctg 60
agctgcaccg tgtctggctt caacatcgag gacgattaca tcgagtgggt gaagcagaga 120
ccagagcagg gactggagtg gatcggaagg atcgaccccg ccaacgataa gacaaagtac 180
gctcctaagt ttcaggacaa ggccaccatc acaggcgata cctccagcaa tacagcttat 240
ctgcagctgt cttccctgac ctccgaggac acagccgtgt actattgtac cagacccggc 300
ctgaggcggt actattccat ggattattgg ggccagggca ccagcgtgac agtgagctct 360
gcctctacaa agggcccttc cgtgttccca ctggctccct gctccagaag cacatctgag 420
tccaccgccg ctctgggctg tctggtgaag gactacttcc ctgagccagt gaccgtgtcc 480
tggaacagcg gcgccctgac atctggcgtg cacacctttc cagctgtgct gcagtccagc 540
ggcctgtact ccctgtcttc cgtggtgaca gtgcccagct cttccctggg caccaagaca 600
tatacctgca acgtggacca taagccttcc aataccaagg tggataagag ggtggagagc 660
aagtacggac caccttgccc accatgtcca gctcctgagt ttctgggagg accatccgtg 720
ttcctgtttc ctccaaagcc taaggacacc ctgatgatca gccggacacc tgaggtgacc 780
tgcgtggtgg tggacgtgtc tcaggaggat ccagaggtgc agttcaactg gtacgtggat 840
ggcgtggagg tgcacaatgc taagaccaag ccaagagagg agcagtttaa ttccacatac 900
cgcgtggtga gcgtgctgac cgtgctgcat caggattggc tgaacggcaa ggagtataag 960
tgcaaggtgt ccaataaggg cctgcccagc tctatcgaga agacaatcag caaggctaag 1020
ggacagccta gggagccaca ggtgtacacc ctgccccctt ctcaggagga gatgacaaag 1080
aaccaggtgt ccctgacctg tctggtgaag ggcttctatc caagcgacat cgctgtggag 1140
tgggagtcta atggccagcc cgagaacaat tacaagacca caccacccgt gctggactct 1200
gatggctcct tctttctgta ttctaggctg acagtggata agtcccggtg gcaggagggc 1260
aacgtgttta gctgctctgt gatgcacgag gccctgcaca atcattatac ccagaagtcc 1320
ctgagcctgt ctctgggcaa gtga 1344
<210> 107
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<400> 107
Asn Ile Val Leu Thr Gln Ser Pro Lys Ser Met Ser Met Ser Val Gly
1 5 10 15
Glu Arg Val Thr Leu Ser Cys Lys Ala Ser Glu Asn Val Val Ser Tyr
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Glu Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Ile Gly
50 55 60
Ser Gly Ser Ser Thr Asp Phe Thr Leu Ile Ile Ser Ser Phe Gln Pro
65 70 75 80
Glu Asp Leu Ala Asp Tyr His Cys Gly Gln Ser Tyr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 108
<211> 645
<212> ДНК
<213> Искусственная последовательность
<400> 108
aacatcgtgc tgacccagtc ccctaagagc atgtctatgt ccgtgggcga gagggtgaca 60
ctgtcttgca aggcctccga gaacgtggtg tcctacgtga gctggtatca gcagaagccc 120
gagcagagcc ctaagctgct gatctacggc gcttctaata ggtataccgg agtgccagac 180
cggttcatcg gatccggctc cagcaccgat ttcacactga tcatctcttc ctttcagcca 240
gaggacctgg ccgattacca ctgtggccag agctactctt atcccctgac ctttggcgct 300
ggcacaaagc tggagctgaa gcgtacggtg gccgctccca gcgtgttcat ctttccccct 360
tctgacgagc agctgaagtc tggcaccgct tccgtggtgt gcctgctgaa caatttctac 420
cccagagagg ccaaggtgca gtggaaggtg gataacgctc tgcagtccgg caatagccag 480
gagtctgtga ccgagcagga ctccaaggat agcacatatt ctctgtcttc caccctgaca 540
ctgtctaagg ccgactacga gaagcacaag gtgtatgctt gcgaggtgac ccatcagggc 600
ctgagctctc ctgtgacaaa gtcctttaat cgcggcgagt gttga 645
<210> 109
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 109
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 110
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 110
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcttgcaagg cttccggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgata tctccaccag cacagcttat 240
atggagctgt cttccctgag gagcgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 111
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 111
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 112
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 112
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca gactttaccc tgacaatcag ctctctgcag 240
cccgaggact tcgccaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 113
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 113
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 114
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 114
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcttgcaagg cttccggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgata tctccaccag cacagcttat 240
atggagctgt cttccctgag gagcgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 115
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 115
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 116
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 116
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca gactttaccc tgacaatcag ctctctgcag 240
cccgaggatt tcgccaccta ctattgtcag cagttctctg agtccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 117
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 117
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 118
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 118
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcttgcaagg cttccggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgata tctccaccag cacagcttat 240
atggagctgt cttccctgag gagcgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 119
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 119
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 120
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 120
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 121
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 121
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 122
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 122
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcttgcaagg cttccggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgata tctccaccag cacagcttat 240
atggagctgt cttccctgag gagcgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 123
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 123
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 124
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 124
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg agtccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 125
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 125
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 126
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 126
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcttgcaagg cttccggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgata tctccaccag cacagcttat 240
atggagctgt cttccctgag gagcgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 127
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 127
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 128
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 128
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gtggatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 129
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 129
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Ile Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 130
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 130
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcttgcaagg cttccggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgata tctccaccag cacagcttat 240
atggagctgt cttccctgag gagcgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 131
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 131
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 132
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 132
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gtggatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg agtccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 133
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 133
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 134
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 134
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcctgcaagg ctagcggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgaga tctctaccaa tacagcttat 240
atggagctgt cttccctgag gtccgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 135
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 135
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 136
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 136
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca gactttaccc tgacaatcag ctctctgcag 240
cccgaggact tcgccaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 137
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 137
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 138
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 138
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcctgcaagg ctagcggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgaga tctctaccaa tacagcttat 240
atggagctgt cttccctgag gtccgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 139
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 139
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 140
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 140
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca gactttaccc tgacaatcag ctctctgcag 240
cccgaggatt tcgccaccta ctattgtcag cagttctctg agtccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 141
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 141
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 142
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 142
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcctgcaagg ctagcggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgaga tctctaccaa tacagcttat 240
atggagctgt cttccctgag gtccgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 143
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 143
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 144
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 144
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 145
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 145
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 146
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 146
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcctgcaagg ctagcggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgaga tctctaccaa tacagcttat 240
atggagctgt cttccctgag gtccgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 147
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 147
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 148
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 148
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg agtccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 149
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 149
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 150
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 150
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcctgcaagg ctagcggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgaga tctctaccaa tacagcttat 240
atggagctgt cttccctgag gtccgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 151
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 151
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Asp Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 152
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 152
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gtggatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 153
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<400> 153
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Arg Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Phe Ile Pro Gly Ser Asp Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Glu Ile Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Leu Arg Arg Met Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 154
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<400> 154
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggctccag cgtgaaggtg 60
tcctgcaagg ctagcggcta caccttctct agatattgga tcgagtgggt gcgccaggct 120
ccaggacagg gactggagtg gatgggcgag ttcatccctg gctccgacac cacaaactac 180
gctcagaagt ttcagggcag ggtgaccatc acagccgaga tctctaccaa tacagcttat 240
atggagctgt cttccctgag gtccgaggac acagccgtgt actattgtgc tagaggcggc 300
ctgaggcgga tggattactg gggccagggc accctggtga cagtgagctc tgcctctaca 360
aagggccctt ccgtgttccc actggctccc tgctccagaa gcacatctga gtccaccgcc 420
gctctgggct gtctggtgaa ggactacttc cctgagccag tgaccgtgtc ctggaacagc 480
ggcgccctga catctggcgt gcacaccttt ccagctgtgc tgcagtccag cggcctgtac 540
tccctgtctt ccgtggtgac agtgcccagc tcttccctgg gcaccaagac atatacctgc 600
aacgtggacc ataagccttc caataccaag gtggataaga gggtggagag caagtacgga 660
ccaccttgcc caccatgtcc agctcctgag tttctgggag gaccatccgt gttcctgttt 720
cctccaaagc ctaaggacac cctgatgatc agccggacac ctgaggtgac ctgcgtggtg 780
gtggacgtgt ctcaggagga tccagaggtg cagttcaact ggtacgtgga tggcgtggag 840
gtgcacaatg ctaagaccaa gccaagagag gagcagttta attccacata ccgcgtggtg 900
agcgtgctga ccgtgctgca tcaggattgg ctgaacggca aggagtataa gtgcaaggtg 960
tccaataagg gcctgcccag ctctatcgag aagacaatca gcaaggctaa gggacagcct 1020
agggagccac aggtgtacac cctgccccct tctcaggagg agatgacaaa gaaccaggtg 1080
tccctgacct gtctggtgaa gggcttctat ccaagcgaca tcgctgtgga gtgggagtct 1140
aatggccagc ccgagaacaa ttacaagacc acaccacccg tgctggactc tgatggctcc 1200
ttctttctgt attctaggct gacagtggat aagtcccggt ggcaggaggg caacgtgttt 1260
agctgctctg tgatgcacga ggccctgcac aatcattata cccagaagtc cctgagcctg 1320
tctctgggca agtga 1335
<210> 155
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<400> 155
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Thr
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Glu Ser Thr
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 156
<211> 648
<212> ДНК
<213> Искусственная последовательность
<400> 156
gacatccaga tgacacagag cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc gggcttcttc cagcgtgtct tccacctacc tgcactggta tcagcagaag 120
cccggcaagg cccctaagct gtggatctac accacaagca ccctggcttc tggcgtgcca 180
tccaggttct ctggctccgg cagcggcaca tcttataccc tgacaatcag ctctctgcag 240
cccgaggact ttgccaccta ctattgtcag cagttctctg agtccacctg gacatttggc 300
cagggcacaa agctggagat caagcgtacg gtggccgctc ccagcgtgtt catctttccc 360
ccttctgacg agcagctgaa gtctggcacc gcttccgtgg tgtgcctgct gaacaatttc 420
taccccagag aggccaaggt gcagtggaag gtggataacg ctctgcagtc cggcaatagc 480
caggagtctg tgaccgagca ggactccaag gatagcacat attctctgtc ttccaccctg 540
acactgtcta aggccgacta cgagaagcac aaggtgtatg cttgcgaggt gacccatcag 600
ggcctgagct ctcctgtgac aaagtccttt aatcgcggcg agtgttga 648
<210> 157
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<400> 157
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 158
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<400> 158
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaggcaggct 120
ccaggacagg gactggagtg gatgggctgg atcaacacca atacaggcga gcctacatac 180
gcccagaagc tgcagggcag ggtgaccatg acactggaca ccagcacaag aaccgcttat 240
atggagctga ggtctctgcg gtccgacgat accgccgtgt actattgtgc tagattttct 300
cacctgaggg gaccaatgga ttactgggga cagggcacac tggtgaccgt gtccagcgcc 360
tctacaaagg gcccttccgt gttcccactg gctccctgct ccagaagcac atctgagtcc 420
accgccgctc tgggctgtct ggtgaaggac tacttccctg agccagtgac cgtgtcctgg 480
aacagcggcg ccctgacatc tggcgtgcac acctttccag ctgtgctgca gtccagcggc 540
ctgtactccc tgtcttccgt ggtgacagtg cccagctctt ccctgggcac caagacatat 600
acctgcaacg tggaccataa gccttccaat accaaggtgg ataagagggt ggagagcaag 660
tacggaccac cttgcccacc atgtccagct cctgagtttc tgggaggacc atccgtgttc 720
ctgtttcctc caaagcctaa ggacaccctg atgatcagcc ggacacctga ggtgacctgc 780
gtggtggtgg acgtgtctca ggaggatcca gaggtgcagt tcaactggta cgtggatggc 840
gtggaggtgc acaatgctaa gaccaagcca agagaggagc agtttaattc cacataccgc 900
gtggtgagcg tgctgaccgt gctgcatcag gattggctga acggcaagga gtataagtgc 960
aaggtgtcca ataagggcct gcccagctct atcgagaaga caatcagcaa ggctaaggga 1020
cagcctaggg agccacaggt gtacaccctg cccccttctc aggaggagat gacaaagaac 1080
caggtgtccc tgacctgtct ggtgaagggc ttctatccaa gcgacatcgc tgtggagtgg 1140
gagtctaatg gccagcccga gaacaattac aagaccacac cacccgtgct ggactctgat 1200
ggctccttct ttctgtattc taggctgaca gtggataagt cccggtggca ggagggcaac 1260
gtgtttagct gctctgtgat gcacgaggcc ctgcacaatc attataccca gaagtccctg 1320
agcctgtctc tgggcaagtg a 1341
<210> 159
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 159
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 160
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 160
gacatccaga tgacacagtc cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc ggtcttccca gagcctggtg cactctaacg gctacaccta tctgcattgg 120
taccagcaga agccaggcaa ggctcccaag ctgctgatct ataaggtgtc caatagattc 180
agcggcgtgc cttctcgctt ttctggctcc ggcagcggca cagacttcac cctgacaatc 240
agctctctgc agccagagga ttttgccacc tactattgtt ctcagtccac ccacgtgccc 300
cctacattcg gccagggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 161
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<400> 161
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 162
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<400> 162
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaggcaggct 120
ccaggacagg gcctgaagtg gatgggatgg atcaacacca atacaggcga gcctacatac 180
gcccaggagc tgcagggcag ggtgaccatg acactggaca ccagcacaag aaccgcctat 240
atggagctga ggtctctgcg gtccgacgat acagccgtgt actattgtac cagattttct 300
cacctgaggg gaccaatgga ttactgggga cagggcacac tggtgaccgt gtccagcgcc 360
tctacaaagg gcccttccgt gttcccactg gctccctgct ccagaagcac atctgagtcc 420
accgccgctc tgggctgtct ggtgaaggac tacttccctg agccagtgac cgtgtcctgg 480
aacagcggcg ccctgacatc tggcgtgcac acctttccag ctgtgctgca gtccagcggc 540
ctgtactccc tgtcttccgt ggtgacagtg cccagctctt ccctgggcac caagacatat 600
acctgcaacg tggaccataa gccttccaat accaaggtgg ataagagggt ggagagcaag 660
tacggaccac cttgcccacc atgtccagct cctgagtttc tgggaggacc atccgtgttc 720
ctgtttcctc caaagcctaa ggacaccctg atgatcagcc ggacacctga ggtgacctgc 780
gtggtggtgg acgtgtctca ggaggatcca gaggtgcagt tcaactggta cgtggatggc 840
gtggaggtgc acaatgctaa gaccaagcca agagaggagc agtttaattc cacataccgc 900
gtggtgagcg tgctgaccgt gctgcatcag gattggctga acggcaagga gtataagtgc 960
aaggtgtcca ataagggcct gcccagctct atcgagaaga caatcagcaa ggctaaggga 1020
cagcctaggg agccacaggt gtacaccctg cccccttctc aggaggagat gacaaagaac 1080
caggtgtccc tgacctgtct ggtgaagggc ttctatccaa gcgacatcgc tgtggagtgg 1140
gagtctaatg gccagcccga gaacaattac aagaccacac cacccgtgct ggactctgat 1200
ggctccttct ttctgtattc taggctgaca gtggataagt cccggtggca ggagggcaac 1260
gtgtttagct gctctgtgat gcacgaggcc ctgcacaatc attataccca gaagtccctg 1320
agcctgtctc tgggcaagtg a 1341
<210> 163
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 163
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 164
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 164
gacatccaga tgacacagtc cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc ggtcttccca gagcctggtg cactctaacg gctacaccta tctgcattgg 120
taccagcaga agccaggcaa ggctcccaag ctgctgatct ataaggtgtc caatagattc 180
agcggcgtgc cttctcgctt ttctggctcc ggcagcggca cagacttcac cctgacaatc 240
agctctctgc agccagagga ttttgccacc tactattgtt ctcagtccac ccacgtgccc 300
cctacattcg gccagggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 165
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<400> 165
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 166
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<400> 166
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaggcaggct 120
ccaggacagg gcctgaagtg gatgggatgg atcaacacca atacaggcga gcctacatac 180
gcccaggagc tgcagggcag ggtgaccatg acactggaca ccagcacaag aaccgcttat 240
atggagctga ggtctctgcg gtccgacgat accgccgtgt actattgtgc tagattttct 300
cacctgaggg gaccaatgga ttactgggga cagggcacac tggtgaccgt gtccagcgcc 360
tctacaaagg gcccttccgt gttcccactg gctccctgct ccagaagcac atctgagtcc 420
accgccgctc tgggctgtct ggtgaaggac tacttccctg agccagtgac cgtgtcctgg 480
aacagcggcg ccctgacatc tggcgtgcac acctttccag ctgtgctgca gtccagcggc 540
ctgtactccc tgtcttccgt ggtgacagtg cccagctctt ccctgggcac caagacatat 600
acctgcaacg tggaccataa gccttccaat accaaggtgg ataagagggt ggagagcaag 660
tacggaccac cttgcccacc atgtccagct cctgagtttc tgggaggacc atccgtgttc 720
ctgtttcctc caaagcctaa ggacaccctg atgatcagcc ggacacctga ggtgacctgc 780
gtggtggtgg acgtgtctca ggaggatcca gaggtgcagt tcaactggta cgtggatggc 840
gtggaggtgc acaatgctaa gaccaagcca agagaggagc agtttaattc cacataccgc 900
gtggtgagcg tgctgaccgt gctgcatcag gattggctga acggcaagga gtataagtgc 960
aaggtgtcca ataagggcct gcccagctct atcgagaaga caatcagcaa ggctaaggga 1020
cagcctaggg agccacaggt gtacaccctg cccccttctc aggaggagat gacaaagaac 1080
caggtgtccc tgacctgtct ggtgaagggc ttctatccaa gcgacatcgc tgtggagtgg 1140
gagtctaatg gccagcccga gaacaattac aagaccacac cacccgtgct ggactctgat 1200
ggctccttct ttctgtattc taggctgaca gtggataagt cccggtggca ggagggcaac 1260
gtgtttagct gctctgtgat gcacgaggcc ctgcacaatc attataccca gaagtccctg 1320
agcctgtctc tgggcaagtg a 1341
<210> 167
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 167
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 168
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 168
gacatccaga tgacacagtc cccatccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgcc ggtcttccca gagcctggtg cactctaacg gctacaccta tctgcattgg 120
taccagcaga agccaggcaa ggctcccaag ctgctgatct ataaggtgtc caatagattc 180
agcggcgtgc cttctcgctt ttctggctcc ggcagcggca cagacttcac cctgacaatc 240
agctctctgc agccagagga ttttgccacc tactattgtt ctcagtccac ccacgtgccc 300
cctacattcg gccagggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 169
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<400> 169
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 170
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<400> 170
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaggcaggct 120
ccaggacagg gcctgaagtg gatgggatgg atcaacacca atacaggcga gcctacatac 180
gcccaggagc tgcagggcag ggtgaccatg acactggaca ccagcacaag aaccgcttat 240
atggagctga ggtctctgcg gtccgacgat accgccgtgt actattgtgc tagattttct 300
cacctgaggg gaccaatgga ttactgggga cagggcacac tggtgaccgt gtccagcgcc 360
tctacaaagg gcccttccgt gttcccactg gctccctgct ccagaagcac atctgagtcc 420
accgccgctc tgggctgtct ggtgaaggac tacttccctg agccagtgac cgtgtcctgg 480
aacagcggcg ccctgacatc tggcgtgcac acctttccag ctgtgctgca gtccagcggc 540
ctgtactccc tgtcttccgt ggtgacagtg cccagctctt ccctgggcac caagacatat 600
acctgcaacg tggaccataa gccttccaat accaaggtgg ataagagggt ggagagcaag 660
tacggaccac cttgcccacc atgtccagct cctgagtttc tgggaggacc atccgtgttc 720
ctgtttcctc caaagcctaa ggacaccctg atgatcagcc ggacacctga ggtgacctgc 780
gtggtggtgg acgtgtctca ggaggatcca gaggtgcagt tcaactggta cgtggatggc 840
gtggaggtgc acaatgctaa gaccaagcca agagaggagc agtttaattc cacataccgc 900
gtggtgagcg tgctgaccgt gctgcatcag gattggctga acggcaagga gtataagtgc 960
aaggtgtcca ataagggcct gcccagctct atcgagaaga caatcagcaa ggctaaggga 1020
cagcctaggg agccacaggt gtacaccctg cccccttctc aggaggagat gacaaagaac 1080
caggtgtccc tgacctgtct ggtgaagggc ttctatccaa gcgacatcgc tgtggagtgg 1140
gagtctaatg gccagcccga gaacaattac aagaccacac cacccgtgct ggactctgat 1200
ggctccttct ttctgtattc taggctgaca gtggataagt cccggtggca ggagggcaac 1260
gtgtttagct gctctgtgat gcacgaggcc ctgcacaatc attataccca gaagtccctg 1320
agcctgtctc tgggcaagtg a 1341
<210> 171
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 171
Asp Ala Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 172
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 172
gacgcccaga tgacacagtc cccatccagc ctgtccgcta gcgtgggcga tagggtgacc 60
atcacatgcc ggtcttccca gagcctggtg cactctaacg gctacaccta tctgcattgg 120
taccagcaga agccaggcaa ggcccccaag ctgctgatct ataaggtgtc caatagattc 180
agcggcgtgc cttctcgctt ttctggctcc ggcagcggca cagacttcac cctgacaatc 240
agctctctgc agccagagga ttttgctacc tactattgtt ctcagtccac ccacgtgccc 300
cctacattcg gccagggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 173
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<400> 173
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 174
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<400> 174
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaggcaggct 120
ccaggacagg gactggagtg gatgggctgg atcaacacca atacaggcga gcctacatac 180
gcccagaagc tgcagggcag ggtgaccatg acactggaca ccagcacaag aaccgcttat 240
atggagctga ggtctctgcg gtccgacgat accgccgtgt actattgtgc tagattttct 300
cacctgaggg gaccaatgga ttactgggga cagggcacac tggtgaccgt gtccagcgcc 360
tctacaaagg gcccttccgt gttcccactg gctccctgct ccagaagcac atctgagtcc 420
accgccgctc tgggctgtct ggtgaaggac tacttccctg agccagtgac cgtgtcctgg 480
aacagcggcg ccctgacatc tggcgtgcac acctttccag ctgtgctgca gtccagcggc 540
ctgtactccc tgtcttccgt ggtgacagtg cccagctctt ccctgggcac caagacatat 600
acctgcaacg tggaccataa gccttccaat accaaggtgg ataagagggt ggagagcaag 660
tacggaccac cttgcccacc atgtccagct cctgagtttc tgggaggacc atccgtgttc 720
ctgtttcctc caaagcctaa ggacaccctg atgatcagcc ggacacctga ggtgacctgc 780
gtggtggtgg acgtgtctca ggaggatcca gaggtgcagt tcaactggta cgtggatggc 840
gtggaggtgc acaatgctaa gaccaagcca agagaggagc agtttaattc cacataccgc 900
gtggtgagcg tgctgaccgt gctgcatcag gattggctga acggcaagga gtataagtgc 960
aaggtgtcca ataagggcct gcccagctct atcgagaaga caatcagcaa ggctaaggga 1020
cagcctaggg agccacaggt gtacaccctg cccccttctc aggaggagat gacaaagaac 1080
caggtgtccc tgacctgtct ggtgaagggc ttctatccaa gcgacatcgc tgtggagtgg 1140
gagtctaatg gccagcccga gaacaattac aagaccacac cacccgtgct ggactctgat 1200
ggctccttct ttctgtattc taggctgaca gtggataagt cccggtggca ggagggcaac 1260
gtgtttagct gctctgtgat gcacgaggcc ctgcacaatc attataccca gaagtccctg 1320
agcctgtctc tgggcaagtg a 1341
<210> 175
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 175
Asp Ala Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 176
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 176
gacgcccaga tgacacagtc cccatccagc ctgtccgcta gcgtgggcga tagggtgacc 60
atcacatgcc ggtcttccca gagcctggtg cactctaacg gctacaccta tctgcattgg 120
taccagcaga agccaggcaa ggcccccaag ctgctgatct ataaggtgtc caatagattc 180
agcggcgtgc cttctcgctt ttctggctcc ggcagcggca cagacttcac cctgacaatc 240
agctctctgc agccagagga ttttgctacc tactattgtt ctcagtccac ccacgtgccc 300
cctacattcg gccagggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 177
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<400> 177
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Asn Thr Gly Glu Pro Thr Tyr Ala Gln Glu Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Leu Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Ser His Leu Arg Gly Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 178
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<400> 178
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaggcaggct 120
ccaggacagg gcctgaagtg gatgggatgg atcaacacca atacaggcga gcctacatac 180
gcccaggagc tgcagggcag ggtgaccatg acactggaca ccagcacaag aaccgcctat 240
atggagctga ggtctctgcg gtccgacgat acagccgtgt actattgtac cagattttct 300
cacctgaggg gaccaatgga ttactgggga cagggcacac tggtgaccgt gtccagcgcc 360
tctacaaagg gcccttccgt gttcccactg gctccctgct ccagaagcac atctgagtcc 420
accgccgctc tgggctgtct ggtgaaggac tacttccctg agccagtgac cgtgtcctgg 480
aacagcggcg ccctgacatc tggcgtgcac acctttccag ctgtgctgca gtccagcggc 540
ctgtactccc tgtcttccgt ggtgacagtg cccagctctt ccctgggcac caagacatat 600
acctgcaacg tggaccataa gccttccaat accaaggtgg ataagagggt ggagagcaag 660
tacggaccac cttgcccacc atgtccagct cctgagtttc tgggaggacc atccgtgttc 720
ctgtttcctc caaagcctaa ggacaccctg atgatcagcc ggacacctga ggtgacctgc 780
gtggtggtgg acgtgtctca ggaggatcca gaggtgcagt tcaactggta cgtggatggc 840
gtggaggtgc acaatgctaa gaccaagcca agagaggagc agtttaattc cacataccgc 900
gtggtgagcg tgctgaccgt gctgcatcag gattggctga acggcaagga gtataagtgc 960
aaggtgtcca ataagggcct gcccagctct atcgagaaga caatcagcaa ggctaaggga 1020
cagcctaggg agccacaggt gtacaccctg cccccttctc aggaggagat gacaaagaac 1080
caggtgtccc tgacctgtct ggtgaagggc ttctatccaa gcgacatcgc tgtggagtgg 1140
gagtctaatg gccagcccga gaacaattac aagaccacac cacccgtgct ggactctgat 1200
ggctccttct ttctgtattc taggctgaca gtggataagt cccggtggca ggagggcaac 1260
gtgtttagct gctctgtgat gcacgaggcc ctgcacaatc attataccca gaagtccctg 1320
agcctgtctc tgggcaagtg a 1341
<210> 179
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<400> 179
Asp Ala Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Tyr Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 180
<211> 660
<212> ДНК
<213> Искусственная последовательность
<400> 180
gacgcccaga tgacacagtc cccatccagc ctgtccgcta gcgtgggcga tagggtgacc 60
atcacatgcc ggtcttccca gagcctggtg cactctaacg gctacaccta tctgcattgg 120
taccagcaga agccaggcaa ggcccccaag ctgctgatct ataaggtgtc caatagattc 180
agcggcgtgc cttctcgctt ttctggctcc ggcagcggca cagacttcac cctgacaatc 240
agctctctgc agccagagga ttttgctacc tactattgtt ctcagtccac ccacgtgccc 300
cctacattcg gccagggcac caagctggag atcaagcgta cggtggccgc tcccagcgtg 360
ttcatctttc ccccttctga cgagcagctg aagtctggca ccgcttccgt ggtgtgcctg 420
ctgaacaatt tctaccccag agaggccaag gtgcagtgga aggtggataa cgctctgcag 480
tccggcaata gccaggagtc tgtgaccgag caggactcca aggatagcac atattctctg 540
tcttccaccc tgacactgtc taaggccgac tacgagaagc acaaggtgta tgcttgcgag 600
gtgacccatc agggcctgag ctctcctgtg acaaagtcct ttaatcgcgg cgagtgttga 660
<210> 181
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<400> 181
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Phe Asn Ile Glu Asp Asp
20 25 30
Tyr Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Gly Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 182
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<400> 182
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg tgtccggctt caacatcgag gacgattaca tcgagtgggt gaggcaggct 120
ccaggacagg gactggagtg gatgggaagg atcgaccctg ccaacgataa gacaaagtac 180
gctcagaagt ttcagggcag agtgaccatg acaggcgaca ccagcacaaa taccgtgtat 240
atggagctgt ccagcctgcg ctctgaggat accgccgtgt actattgtgc taggcccggc 300
ctgagacgct actattccat ggactattgg ggccagggca cactggtgac cgtgtcttcc 360
gcctctacaa agggcccttc cgtgttccca ctggctccct gctccagaag cacatctgag 420
tccaccgccg ctctgggctg tctggtgaag gactacttcc ctgagccagt gaccgtgtcc 480
tggaacagcg gcgccctgac atctggcgtg cacacctttc cagctgtgct gcagtccagc 540
ggcctgtact ccctgtcttc cgtggtgaca gtgcccagct cttccctggg caccaagaca 600
tatacctgca acgtggacca taagccttcc aataccaagg tggataagag ggtggagagc 660
aagtacggac caccttgccc accatgtcca gctcctgagt ttctgggagg accatccgtg 720
ttcctgtttc ctccaaagcc taaggacacc ctgatgatca gccggacacc tgaggtgacc 780
tgcgtggtgg tggacgtgtc tcaggaggat ccagaggtgc agttcaactg gtacgtggat 840
ggcgtggagg tgcacaatgc taagaccaag ccaagagagg agcagtttaa ttccacatac 900
cgcgtggtga gcgtgctgac cgtgctgcat caggattggc tgaacggcaa ggagtataag 960
tgcaaggtgt ccaataaggg cctgcccagc tctatcgaga agacaatcag caaggctaag 1020
ggacagccta gggagccaca ggtgtacacc ctgccccctt ctcaggagga gatgacaaag 1080
aaccaggtgt ccctgacctg tctggtgaag ggcttctatc caagcgacat cgctgtggag 1140
tgggagtcta atggccagcc cgagaacaat tacaagacca caccacccgt gctggactct 1200
gatggctcct tctttctgta ttctaggctg acagtggata agtcccggtg gcaggagggc 1260
aacgtgttta gctgctctgt gatgcacgag gccctgcaca atcattatac ccagaagtcc 1320
ctgagcctgt ctctgggcaa gtga 1344
<210> 183
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<400> 183
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asn Val Val Ser Tyr
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Ser Arg Phe Ile Gly
50 55 60
Ser Gly Ser Ser Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gln Ser Tyr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 184
<211> 645
<212> ДНК
<213> Искусственная последовательность
<400> 184
gacatccaga tgacccagag cccttccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgca aggcttctga gaacgtggtg tcctacgtga gctggtatca gcagaagccc 120
ggcaaggccc ctaagctgct gatctacggc gcttctaata ggtataccgg agtgccatcc 180
cggttcatcg gatccggctc ttccacagac tttaccctga caatcagctc tctgcagcca 240
gaggatttcg ccacatacta ttgtggccag agctactctt atcccctgac ctttggccag 300
ggcacaaagc tggagatcaa gcgtacggtg gccgctccca gcgtgttcat ctttccccct 360
tctgacgagc agctgaagtc tggcaccgct tccgtggtgt gcctgctgaa caatttctac 420
cccagagagg ccaaggtgca gtggaaggtg gataacgctc tgcagtccgg caatagccag 480
gagtctgtga ccgagcagga ctccaaggat agcacatatt ctctgtcttc caccctgaca 540
ctgtctaagg ccgactacga gaagcacaag gtgtatgctt gcgaggtgac ccatcagggc 600
ctgagctctc ctgtgacaaa gtcctttaat cgcggcgagt gttga 645
<210> 185
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<400> 185
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Phe Asn Ile Glu Asp Asp
20 25 30
Tyr Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Ala Asn Asp Lys Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Gly Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Pro Gly Leu Arg Arg Tyr Tyr Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 186
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<400> 186
caggtgcagc tggtgcagtc cggagctgag gtgaagaagc caggagctag cgtgaaggtg 60
tcttgcaagg tgtccggctt caacatcgag gacgattaca tcgagtgggt gaggcaggct 120
ccaggacagg gactggagtg gatgggaagg atcgaccctg ccaacgataa gacaaagtac 180
gctcagaagt ttcagggcag agtgaccatg acaggcgaca ccagcacaaa taccgtgtat 240
atggagctgt ccagcctgcg ctctgaggat acagccgtgt actattgtac caggcccggc 300
ctgagacgct actattccat ggactattgg ggccagggca cactggtgac cgtgtcttcc 360
gcctctacaa agggcccttc cgtgttccca ctggctccct gctccagaag cacatctgag 420
tccaccgccg ctctgggctg tctggtgaag gactacttcc ctgagccagt gaccgtgtcc 480
tggaacagcg gcgccctgac atctggcgtg cacacctttc cagctgtgct gcagtccagc 540
ggcctgtact ccctgtcttc cgtggtgaca gtgcccagct cttccctggg caccaagaca 600
tatacctgca acgtggacca taagccttcc aataccaagg tggataagag ggtggagagc 660
aagtacggac caccttgccc accatgtcca gctcctgagt ttctgggagg accatccgtg 720
ttcctgtttc ctccaaagcc taaggacacc ctgatgatca gccggacacc tgaggtgacc 780
tgcgtggtgg tggacgtgtc tcaggaggat ccagaggtgc agttcaactg gtacgtggat 840
ggcgtggagg tgcacaatgc taagaccaag ccaagagagg agcagtttaa ttccacatac 900
cgcgtggtga gcgtgctgac cgtgctgcat caggattggc tgaacggcaa ggagtataag 960
tgcaaggtgt ccaataaggg cctgcccagc tctatcgaga agacaatcag caaggctaag 1020
ggacagccta gggagccaca ggtgtacacc ctgccccctt ctcaggagga gatgacaaag 1080
aaccaggtgt ccctgacctg tctggtgaag ggcttctatc caagcgacat cgctgtggag 1140
tgggagtcta atggccagcc cgagaacaat tacaagacca caccacccgt gctggactct 1200
gatggctcct tctttctgta ttctaggctg acagtggata agtcccggtg gcaggagggc 1260
aacgtgttta gctgctctgt gatgcacgag gccctgcaca atcattatac ccagaagtcc 1320
ctgagcctgt ctctgggcaa gtga 1344
<210> 187
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<400> 187
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asn Val Val Ser Tyr
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Ser Arg Phe Ile Gly
50 55 60
Ser Gly Ser Ser Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gln Ser Tyr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 188
<211> 645
<212> ДНК
<213> Искусственная последовательность
<400> 188
gacatccaga tgacccagag cccttccagc ctgtccgcca gcgtgggcga tagggtgacc 60
atcacatgca aggcttctga gaacgtggtg tcctacgtga gctggtatca gcagaagccc 120
ggcaaggccc ctaagctgct gatctacggc gcttctaata ggtataccgg agtgccatcc 180
cggttcatcg gatccggctc ttccacagac tttaccctga caatcagctc tctgcagcca 240
gaggatttcg ccacatacta ttgtggccag agctactctt atcccctgac ctttggccag 300
ggcacaaagc tggagatcaa gcgtacggtg gccgctccca gcgtgttcat ctttccccct 360
tctgacgagc agctgaagtc tggcaccgct tccgtggtgt gcctgctgaa caatttctac 420
cccagagagg ccaaggtgca gtggaaggtg gataacgctc tgcagtccgg caatagccag 480
gagtctgtga ccgagcagga ctccaaggat agcacatatt ctctgtcttc caccctgaca 540
ctgtctaagg ccgactacga gaagcacaag gtgtatgctt gcgaggtgac ccatcagggc 600
ctgagctctc ctgtgacaaa gtcctttaat cgcggcgagt gttga 645
<210> 189
<211> 348
<212> ДНК
<213> Mus musculus
<400> 189
caggtgcagc tgaaggagtc tggaccagga ctggtggctc catctcagtc cctgagcatc 60
acctgcacag tgtccggctt cagcctgacc aactacggag tgcactgggt gaggcagcca 120
cctggcaagg gactggagtg gctgggcatc atctgggctg gcggctccac aaactataat 180
tctgccctga tgtcccggct gtctatctcc aaggacaaca gcaagtctca ggtgtttctg 240
aagatgaata gcctgcagac cgacgataca gccatgtact attgtgctag ggacgattac 300
gccagcatgg attattgggg ccagggcacc tctgtgacag tgtccagc 348
<210> 190
<211> 336
<212> ДНК
<213> Mus musculus
<400> 190
gacgccttca tgacccagac accactgtcc ctgcctgtga gcctgggcga tcaggcttct 60
atctcctgca gatccagcca gtctctggtg cactccaacg gcaatacata cctgcattgg 120
tatctgcaga agccaggcca gtcccccaag ctgctgatct acaaggtgag caacaggttc 180
tctggcgtgc ctgaccggtt tagcggctct ggctccggca ccgatttcac actgaagatc 240
tccagggtgg aggctgagga cctgggcgtg tacttttgta gccagtctac ccacgtgcca 300
tatacactgg gcggcggcac caagctggag atcaag 336
<210> 191
<211> 357
<212> ДНК
<213> Mus musculus
<400> 191
gaggtgcagc tgcagcagtc tggccccgag ctgaagaagc ctggcgagac cgtgaagatc 60
tcttgcaagg cctccggcta caccttcaca aactatggca tgaattgggt gaagcaggtg 120
ccaggcaagg gcctgaagtg gatgggctgg atcaacacca atacaggcga gcccacatac 180
gccgaggagt tcaagggcag attcgctttt agcctggaga cctctgcccg cacagctttt 240
ctgcagatca acaatctgaa gaacgaggac accgccacat acttctgtac caggttttcc 300
cacctgcggg gccccatgga ttattggggc cagggcgcta gcgtgacagt gtccagc 357
<210> 192
<211> 336
<212> ДНК
<213> Mus musculus
<400> 192
gacgccgtga tgacccagac accactgtcc ctgcccgtga gcctgggcga tcaggcttct 60
atctcctgca gatccagcca gtctctggtg cactccaacg gctacacata tctgcattgg 120
tacctgcaga agcctggcca gtccccaaag ctgctgatct ataaggtgag caataggttc 180
tctggagtgc cagaccggtt tagcggatct ggatccggca ccgatttcac actgaagatc 240
tccaggctgg aggctgagga cctgggcgtg tacttctgta gccagtctac ccacgtgccc 300
cctacatttg gcggcggcac caagctggag atcaag 336
<210> 193
<211> 336
<212> ДНК
<213> Mus musculus
<400> 193
gaagtgatgc tggtggagag cggaggagga ctggtgcagc caggaggcag cctgaagctg 60
tcttgcgccg cttccggctt cacctttagc aactactata tgtcttgggt gagacagaca 120
cccgagaagc gcctggagtg ggtggcttac atctccagcg gaggaggatc cacctactat 180
cctgacagcg tgaagggcag gttcaccatc tctcgggata acgccaagaa tacactgtac 240
ctgcagatgt cttccctgaa gtccgaggac acagctatgt actattgtgc ctggtttgct 300
tattggggcc agggcaccct ggtgacagtg tctgct 336
<210> 194
<211> 336
<212> ДНК
<213> Mus musculus
<400> 194
gacgccgtgg tgacccagac accactgacc ctgtccgtga caatcggcca gcccgcttct 60
atctcctgca agtccagcca gtccctgctg gacagcgatg gcaagacata cctgaactgg 120
ctgctgcaga ggccaggaca gagccctaag cggctgatct atctggtgtc taagctggac 180
tccggcgtgc ctgatagatt caccggcagc ggctctggca ccgactttac actgaagatc 240
tctcgcgtgg aggccgagga tctgggcgtg tactattgtt ggcagggcac ccacttccca 300
ctgacatttg gcgctggcac caagctggag ctgaag 336
<210> 195
<211> 351
<212> ДНК
<213> Mus musculus
<400> 195
gaggtgcagc tgcagcagtc tgtggccgag ctgatgaagc caggcgcttc cgtgaagatc 60
tactgcaagg ccaccggcta cacattcagc agatattgga tcgagtgggt gaagcagagg 120
ccaggacacg gactggagtg gatcggcgag ttcatccctg gctctgacac cacaaacttc 180
aatgagaagt ttaagggcaa ggccaccttt acagctgaga tctccagcaa caccgcttat 240
atgcagctgt cttccctgac atccgaggac agcgccgtgt acttttgtgc taggggcggc 300
ctgaggcgga tggattattg gggccagggc acctccgtga cagtgagctc t 351
<210> 196
<211> 324
<212> ДНК
<213> Mus musculus
<400> 196
gacatcgtga tgacccagac acccgccatc atgtccgcct ctcctggcga gaaggtgacc 60
atgacatgca gggcctccag ctccgtgtcc agcacctacc tgcactggta tcagcagaag 120
agcggcgctt ctccaaagct gtggatctac accacatcca cactggctag cggagtgcca 180
gctcggttct ccggaagcgg atctggcacc tcctatagcc tgacaatctc ttccgtggag 240
gccgaggacg ccgctaccta ctattgtcag cagttctctg attccacctg gacatttggc 300
ggcggcacaa agctggagat caag 324
<210> 197
<211> 360
<212> ДНК
<213> Mus musculus
<400> 197
gaggtgcagc tgcagcagtc tggagctgag gtggctaggc caggagcttc cgtgaagctg 60
agctgcaccg tgtctggctt caacatcgag gacgattaca tcgagtgggt gaagcagaga 120
ccagagcagg gactggagtg gatcggaagg atcgaccccg ccaacgataa gacaaagtac 180
gctcctaagt ttcaggacaa ggccaccatc acaggcgata cctccagcaa tacagcttat 240
ctgcagctgt cttccctgac ctccgaggac acagccgtgt actattgtac cagacccggc 300
ctgaggcggt actattccat ggattattgg ggccagggca ccagcgtgac agtgagctct 360
<210> 198
<211> 321
<212> ДНК
<213> Mus musculus
<400> 198
aacatcgtgc tgacccagtc ccctaagagc atgtctatgt ccgtgggcga gagggtgaca 60
ctgtcttgca aggcctccga gaacgtggtg tcctacgtga gctggtatca gcagaagccc 120
gagcagagcc ctaagctgct gatctacggc gcttctaata ggtataccgg agtgccagac 180
cggttcatcg gatccggctc cagcaccgat ttcacactga tcatctcttc ctttcagcca 240
gaggacctgg ccgattacca ctgtggccag agctactctt atcccctgac ctttggcgct 300
ggcacaaagc tggagctgaa g 321
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| CD47-АНТИГЕНСВЯЗЫВАЮЩАЯ ЕДИНИЦА И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2780859C2 |
| Терапевтические антитела к CD47 | 2016 |
|
RU2748401C2 |
| СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800923C2 |
| АНТИТЕЛА ПРОТИВ СИГНАЛ-РЕГУЛЯТОРНОГО БЕЛКА АЛЬФА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2771964C2 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2837821C1 |
| Белки, связывающие NKG2D, CD16 и опухолеассоциированный антиген | 2018 |
|
RU2816716C2 |
| БИСПЕЦИФИЧНЫЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2800779C2 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2808030C2 |
| СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2811120C2 |
| АНТИТЕЛО ПРОТИВ SIRPα | 2019 |
|
RU2791002C2 |


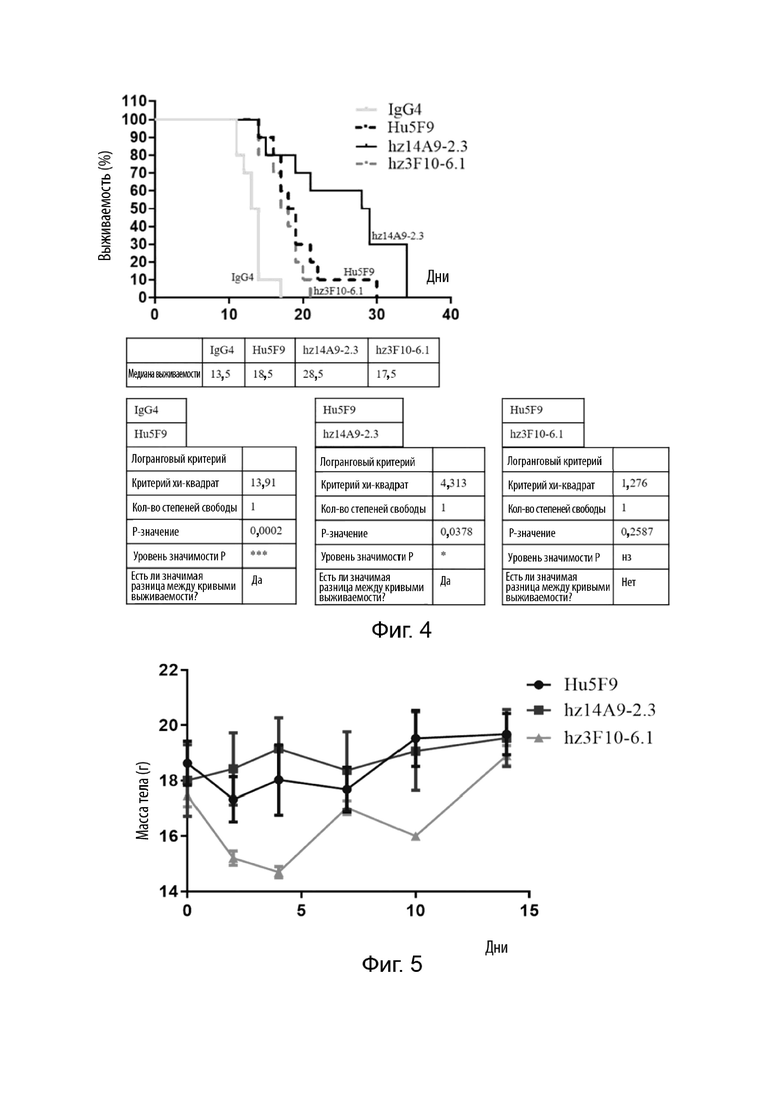
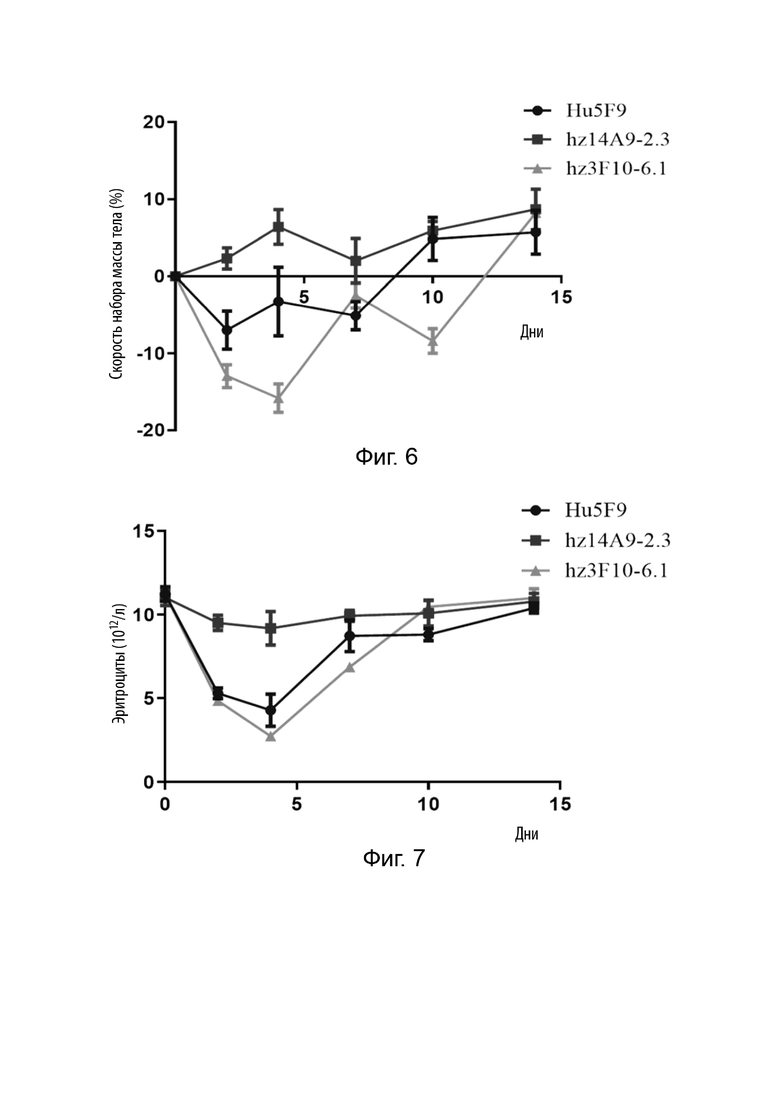
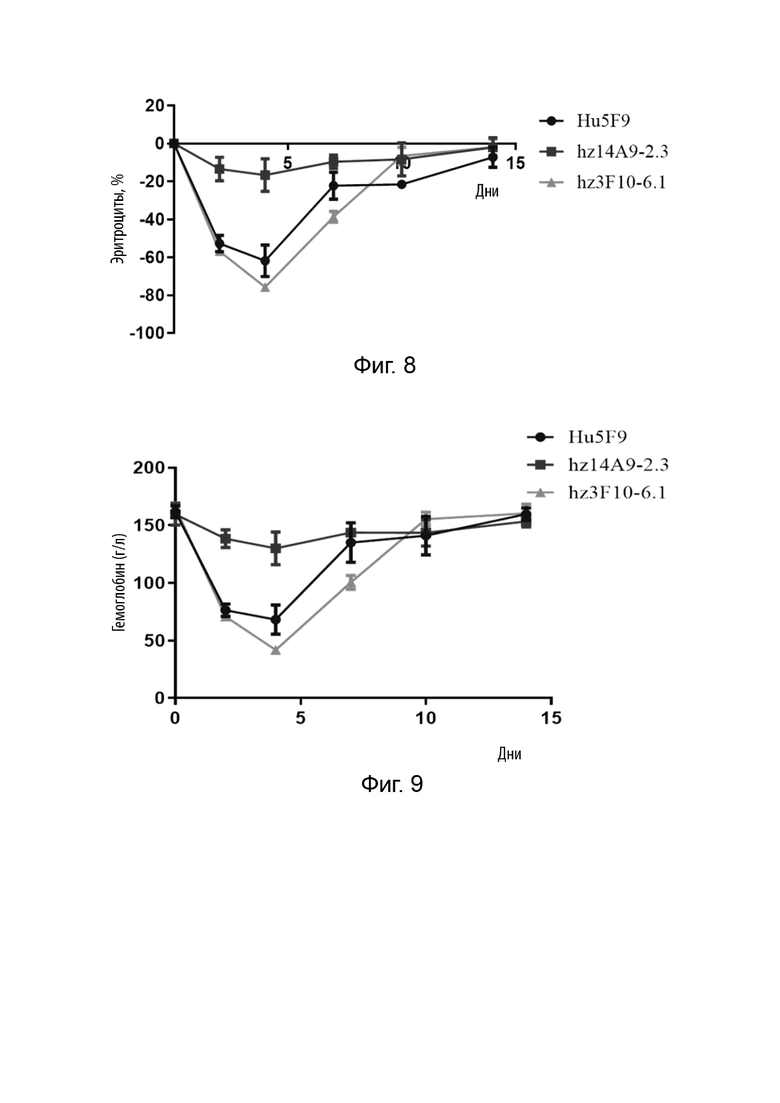
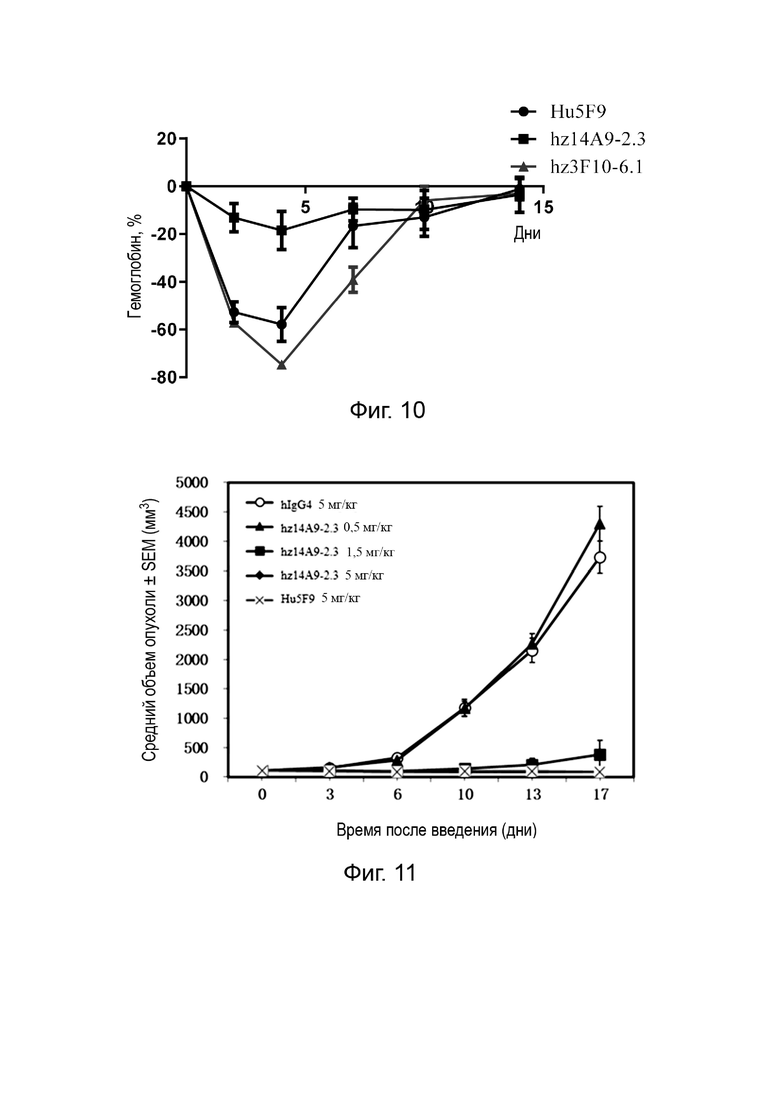
Изобретение относится к области биотехнологии, а именно к выделенному антигенсвязывающему полипептиду, который связывается с CD47, и его антигенсвязывающей части, а также к иммуноконъюгату и композиции, их содержащим. Изобретение эффективно для уменьшения опухоли у нуждающегося в этом субъекта, а также для лечения онкологического заболевания у нуждающегося в этом субъекта. 6 н. и 16 з.п. ф-лы, 11 ил., 21 табл., 14 пр.
1. Выделенный антигенсвязывающий полипептид, который связывается с CD47, или его антигенсвязывающая часть, отличающиеся тем, что антигенсвязывающий полипептид содержит одну из следующих областей, определяющих комплементарность:
(1)
CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 5;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 10;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 15;
CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 20;
CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 25; и
CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 30;
(2)
CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 2;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 7;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 12;
CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 17;
CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 22; и
CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 27;
(3)
CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 3;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 8;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 13;
CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 18;
CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 23; и
CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 28;
(4)
CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 4;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 9;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 14;
CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 19;
CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 24; и
CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 32; или
(5)
CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 1;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 6;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 11;
CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 16;
CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 21; и
CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 26.
2. Антигенсвязывающий полипептид или его антигенсвязывающая часть по п. 1, отличающиеся тем, что указанный антигенсвязывающий полипептид содержит:
CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 5;
CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 10;
CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 15;
CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 20;
CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 25; и
CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 30.
3. Антигенсвязывающий полипептид или его антигенсвязывающая часть по п. 1, отличающиеся тем, что указанный антигенсвязывающий полипептид содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 33, 35, 37, 39, 41, 83, 85 и 87, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 34, 36, 38, 40, 42, 84, 86 и 88.
4. Антигенсвязывающий полипептид или его антигенсвязывающая часть по п. 1 или 3, отличающиеся тем, что антигенсвязывающий полипептид содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом:
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 79, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 80;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 33, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 34;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 35, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 36;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 37, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 38;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 39, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 40;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 41, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 42;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 83, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 84;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 85, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 86;
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 87, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 88; или
вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 81, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 82.
5. Антигенсвязывающий полипептид или его антигенсвязывающая часть по любому из пп. 1-4, отличающиеся тем, что указанный антигенсвязывающий полипептид содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 79, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 80.
6. Антигенсвязывающий полипептид или его антигенсвязывающая часть по любому из пп. 1 и 3, 4, отличающиеся тем, что:
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 181 и легкую цепь в соответствии с последовательностью SEQ ID NO: 183;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 89 и легкую цепь в соответствии с последовательностью SEQ ID NO: 91;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 93 и легкую цепь в соответствии с последовательностью SEQ ID NO: 95;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 97 и легкую цепь в соответствии с последовательностью SEQ ID NO: 99;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 101 и легкую цепь в соответствии с последовательностью SEQ ID NO: 103;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 105 и легкую цепь в соответствии с последовательностью SEQ ID NO: 107;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 109 и легкую цепь в соответствии с последовательностью SEQ ID NO: 111;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 113 и легкую цепь в соответствии с последовательностью SEQ ID NO: 115;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 117 и легкую цепь в соответствии с последовательностью SEQ ID NO: 119;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 121 и легкую цепь в соответствии с последовательностью SEQ ID NO: 123;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 125 и легкую цепь в соответствии с последовательностью SEQ ID NO: 127;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 129 и легкую цепь в соответствии с последовательностью SEQ ID NO: 131;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 133 и легкую цепь в соответствии с последовательностью SEQ ID NO: 135;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 137 и легкую цепь в соответствии с последовательностью SEQ ID NO: 139;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 141 и легкую цепь в соответствии с последовательностью SEQ ID NO: 143;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 145 и легкую цепь в соответствии с последовательностью SEQ ID NO: 147;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 149 и легкую цепь в соответствии с последовательностью SEQ ID NO: 151;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 153 и легкую цепь в соответствии с последовательностью SEQ ID NO: 155;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 157 и легкую цепь в соответствии с последовательностью SEQ ID NO: 159;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 161 и легкую цепь в соответствии с последовательностью SEQ ID NO: 163;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 165 и легкую цепь в соответствии с последовательностью SEQ ID NO: 167;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 169 и легкую цепь в соответствии с последовательностью SEQ ID NO: 171;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 173 и легкую цепь в соответствии с последовательностью SEQ ID NO: 175;
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 177 и легкую цепь в соответствии с последовательностью SEQ ID NO: 179; или
антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 185 и легкую цепь в соответствии с последовательностью SEQ ID NO: 187.
7. Антигенсвязывающий полипептид или его антигенсвязывающая часть по п. 6, отличающиеся тем, что указанный антигенсвязывающий полипептид содержит тяжелую цепь в соответствии с последовательностью SEQ ID NO: 181 и легкую цепь в соответствии с последовательностью SEQ ID NO: 183.
8. Антигенсвязывающий полипептид или его антигенсвязывающая часть по любому из пп. 1-7, отличающиеся тем, что антигенсвязывающий полипептид является химерным, гуманизированным или полностью человеческим.
9. Антигенсвязывающий полипептид или его антигенсвязывающая часть по любому из пп. 1-8, отличающиеся тем, что антигенсвязывающий полипептид или его антигенсвязывающая часть выбраны из группы, состоящей из моноклональных антител, слитых белков, Fab-фрагментов, Fab'-фрагментов, F(ab')2-фрагментов, Fd-фрагментов, Fv-фрагментов, dAb-фрагментов, изолированных областей CDR и scFv.
10. Антигенсвязывающий полипептид или его антигенсвязывающая часть по любому из пп. 1-9, отличающиеся тем, что антигенсвязывающий полипептид относится к подклассу IgG1, IgG2, IgG3 или IgG4.
11. Антигенсвязывающий полипептид или его антигенсвязывающая часть по п. 10, отличающиеся тем, что антигенсвязывающий полипептид подкласса IgG4 имеет мутацию S228P согласно индексу нумерации EU.
12. Антигенсвязывающий полипептид или его антигенсвязывающая часть по любому из пп. 1-11, отличающиеся тем, что антигенсвязывающий полипептид или его антигенсвязывающая часть обладают одним или комбинацией нескольких из следующих свойств:
(a) связывание с CD47 со значением KD 1,89E-08 или менее;
(b) блокирование связывания CD47 с SIRPα;
(c) стимулирование опосредованного макрофагами фагоцитоза CD47-экспрессирующих клеток;
(d) не вызывает значимого апоптоза CD4+ Т-клеток;
(e) не вызывает существенной гематоцитопении, анемии или агглютинации эритроцитов; и
(f) антигенсвязывающий полипептид или его антигенсвязывающая часть имеют температуру плавления T ≥ 62°C и температуру агрегации Tagg ≥ 61°C.
13. Иммуноконъюгат, который обладает способностью связываться с CD47, содержащий антигенсвязывающий полипептид или его антигенсвязывающую часть по любому из пп. 1-12 и терапевтический агент, который связан или конъюгирован с указанным антигенсвязывающим полипептидом или его антигенсвязывающей частью.
14. Иммуноконъюгат по п. 13, отличающийся тем, что терапевтический агент представляет собой цитотоксический лекарственный препарат, радиоизотоп, иммуномодулятор или антитело.
15. Композиция для лечения онкологического заболевания, содержащая компонент А и фармацевтически приемлемый носитель, при этом компонент А представляет собой антигенсвязывающий полипептид или его антигенсвязывающую часть по любому из пп. 1-12 или иммуноконъюгат по п. 13 или 14.
16. Способ уменьшения опухоли у нуждающегося в этом субъекта, включающий введение указанному субъекту терапевтически эффективного количества антигенсвязывающего полипептида или его антигенсвязывающей части по любому из пп. 1-12 или иммуноконъюгата по п. 13 или 14.
17. Способ по п. 16, при котором опухоль уменьшают в результате ингибирования роста опухолевых клеток у субъекта.
18. Способ по п. 16, при котором опухоль уменьшают в результате стимулирования фагоцитоза макрофагами у субъекта.
19. Способ лечения онкологического заболевания у нуждающегося в этом субъекта, включающий введение указанному субъекту терапевтически эффективного количества антигенсвязывающего полипептида или его антигенсвязывающей части по любому из пп. 1-12 или иммуноконъюгата по п. 13 или 14.
20. Способ по п. 19, отличающийся тем, что онкологическое заболевание выбрано из группы, состоящей из лейкемии, лимфомы, рака яичников, рака молочной железы, рака эндометрия, рака толстой кишки, рака прямой кишки, рака мочевого пузыря, рака уротелия, рака легких, рака бронхов, рака костей, рака предстательной железы, рака поджелудочной железы, рака желудка, печёночноклеточного рака, рака желчного пузыря, рака желчных протоков, рака пищевода, почечно-клеточного рака, рака щитовидной железы, рака головы и шеи, рака яичек, эндокринной аденокарциномы, рака надпочечников, рака гипофиза, рака кожи, рака мягких тканей, рака сосудов, рака головного мозга, рака нервной системы, рака глаза, рака мозговых оболочек, рака ротоглотки, рака гортаноглотки, рака шейки матки и рака матки, глиобластомы, медуллобластомы, астроцитомы, глиомы, менингиомы, гастриномы, нейробластомы, меланомы, острого миелоидного лейкоза, миелодиспластического синдрома и саркомы.
21. Применение антигенсвязывающего полипептида или его антигенсвязывающей части по любому из пп. 1-12 при приготовлении лекарственного средства для лечения онкологического заболевания у нуждающегося в этом субъекта.
22. Применение по п. 21, отличающееся тем, что онкологическое заболевание выбрано из группы, состоящей из лейкемии, лимфомы, рака яичников, рака молочной железы, рака эндометрия, рака толстой кишки, рака прямой кишки, рака мочевого пузыря, рака уротелия, рака легких, рака бронхов, рака костей, рака предстательной железы, рака поджелудочной железы, рака желудка, печёночноклеточного рака, рака желчного пузыря, рака желчных протоков, рака пищевода, почечно-клеточного рака, рака щитовидной железы, рака головы и шеи, рака яичек, эндокринной аденокарциномы, рака надпочечников, рака гипофиза, рака кожи, рака мягких тканей, рака сосудов, рака головного мозга, рака нервной системы, рака глаза, рака мозговых оболочек, рака ротоглотки, рака гортаноглотки, рака шейки матки и рака матки, глиобластомы, медуллобластомы, астроцитомы, глиомы, менингиомы, гастриномы, нейробластомы, меланомы, острого миелоидного лейкоза, миелодиспластического синдрома и саркомы.
| WO 2014093678 A2, 19.06.2014 | |||
| WO 2018095428 A1, 31.05.2018 | |||
| DADI ZENG et al., A fully human anti-CD47 blocking antibody with therapeutic potential for cancer, Oncotarget, 2016, Vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Устройство для выпрямления многофазного тока | 1923 |
|
SU50A1 |
| Разборный контейнер | 1949 |
|
SU83040A1 |
| JIE LIU et al., Pre-Clinical Development of a Humanized Anti-CD47 Antibody with Anti-Cancer Therapeutic Potential, PLoS ONE 10(9): | |||
Авторы
Даты
2025-01-16—Публикация
2021-04-01—Подача