Изобретение относится к области определения и оценки антиоксидантной активности (АОА) биологически активных препаратов и может быть использовано в фармацевтике и пищевой промышленности, а также иметь отношение к биологической химии.
Известны способы оценки АОА с помощью спектрофотометрического метода, основанные на восстановлении Fe(III) полифенолами с последующим построением градуировочного графика (Бриленок Н.С., Вершинин В.И., Бахарева М.В. и др. Оценка антиоксидантной активности полифенолов по методу FRAP в присутствии комплексонатов // Аналитика и контроль. - 2016. - Т. 20, №3. - С. 209-217; Колбас Н.Ю., Решетников В.Н. Оценка антиоксидантной активности водно-этанольных экстрактов некоторых представителей рода Rubus II Труды БГУ (Биохимия). - 2011. - Т. 6 (Часть 1). - С. 136-143).
Указанные способы имеют следующие недостатки:
- применимы для соединений полифенольного типа;
- в присутствии некоторых соединений возникает погрешность. Известен запатентованный способ оценки АОА биологически активных
препаратов спектрофотометрическим методом по величине оптической плотности продукта аутоокисления адреналина (Малютина И.Г. с соавт. Способ оценки антиоксидантной активности биологически активных препаратов: Пат. 2738302 от 08.06.2020, опубл. 11.12.2020). Известный способ имеет следующие недостатки:
- применим к жидким водорастворимым формам соединений;
- не позволяет дать оценку выраженности АОА (путем сравнения относительно выбранного стандарта).
Известен способ оценки АОА природных соединений в крови по патенту 2392623 (Лисовская И.Л. с соавт. Способ оценки антиоксидантной активности: Пат. 2392623 от 16.02.2009; опубл. 20.06.2010. Бюл. №17).
Указанный способ имеет следующие недостатки:
- антиоксиданты (АО) добавляются в кровь непосредственно перед индукцией аутоокисления (до забора крови АО не принимались перорально);
- не дается интерпретация (оценка) выраженности АОА по полученному показателю АОА;
- для получения относительного показателя АОА используются величины концентраций АО, а не интегрированные индексы АОА;
- оценка АОА дается лишь по кинетическим показателям, что может характеризовать свойства АО и вне биологических тканей (в биологических жидкостях, например).
Известен способ оценки АОА путем определения перекисного гемолиза эритроцитов у экспериментальных животных (Батуева Ю.А., Торопова А.А., Мондодоев А.Г., Шантанова Л.Н. Мембраностабилизирующее и антиоксидантное действие комплексного растительного средства «Литофит» в тест-системах in vitro // Сибирский медицинский журнал (Иркутск). - 2015; 136(5): 122-124). Указанный способ имеет недостатки:
- для индуцирования СРО используется смесь Н2О2 с солями железа (II) (Реактив Фентона), хотя можно использовать и более дешевые индукторы, например, перекись водорода;
- оценка АОА давалась на основе определения абсолютной величины перекисного гемолиза эритроцитов, что позволяет давать лишь сравнительную оценку АОА вводимых соединений.
Известен способ спектрофотометрического определения АОА природных соединений через антиоксидантную емкость в эквивалентах тролокса, принятого за стандарт (Miller N.J., Rice-Evans С, Davies M.J. et al. A novel method for measuring antioxidant capacity and its application to monitoring the antioxidant status in premature neonates / Clin Sci (London). - 1993. - Vol. 84, №4. - P. 407-412). Однако данный способ имеет следующие недостатки:
- идуцируемый в методике катион-радикал реагента-красителя (ABTS) имеет высокий молярный коэффициент поглощения, что вносит вклад в погрешность при измерении оптической плотности;
- измерение АОА природных соединений производится вне живого объекта;
- указанный способ не позволяет качественно оценить АОА природных соединений (по принципу «повышенная/пониженная АОА»).
Известен способ-прототип спектрофотометрического определения в крови антиоксидантной активности природных соединений, которые перорально вводили животным, по данным перекисной резистентности эритроцитов по патенту 2801864 (Логинов П.В. с соавт. Способ определения антиоксидантной активности природных соединений в эксперименте: Пат. 2801864 от 31.10.2022; опубл. 17.08.2023. Бюл. №23). Данный прототип имеет следующий недостаток:
- названный способ не позволяет качественно оценить АОА природных соединений, поскольку отсутствует стандарт сравнения.
Предлагаемое изобретение направлено на то, чтобы дать качественную оценку антиоксидантной активности (АОА) природных соединений путем использования вычисленной величины индекса антиоксидантной активности (ИАА) для расчета выраженности АОА по силе действия. Предлагаемый способ позволяет оценить АОА соединений различной природы.
Указанный технический результат достигается тем, что показатели антиоксидантной активности природных соединений относят к таковому тролокса, и рассчитывают выраженность антиоксидантной активности по формуле:
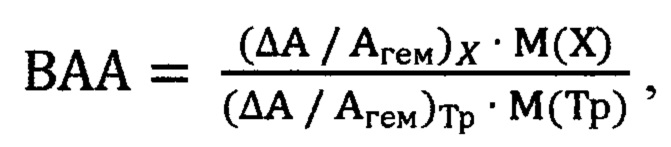
где BAA - выраженность антиоксидантной активности; (ΔА/Агем)Х - перекисная резистентность эритроцитов в присутствии природного соединения X; (ΔА/Агем)Тр - перекисная резистентность эритроцитов в присутствии тролокса Тр; ΔА - понижение оптической плотности образца крови: ΔА=Агем - Аоп; Агем - оптическая плотность пробы гемолизованной крови, Аоп - оптическая плотность опытной пробы; М (X) и М (Тр) - молярные массы соответственно природного соединения X и тролокса; и при величине ВАА ниже 1 судят о пониженной относительно тролокса антиоксидантной активности, а при величине ВАА больше 1 судят о повышенной относительно тролокса антиоксидантной активности соединения.
Неферментативные антиоксидантные системы (АОС) включают в себя жиро- и водорастворимые АО. Жирорастворимые АО эффективно встраиваются во все биомембраны клеток, защищая их таким образом от негативного воздействия свободных радикалов. Водорастворимые АО (например, аскорбиновая кислота) эффективно функционируют в межклеточном пространстве, блокируя приближение радикалов к поверхностям клеток (Николаев А.А., Логинов П.В., Мавлютова Е.Б., Белявская А.А. Свободные радикалы и био-антиоксиданты в репродуктивных процессах (обзор литературы) // Проблемы репродукции. - 2018. - Т. 24, №1. - С. 21-26).
По патенту 2801864 (Логинов П.В. с соавт. Способ определения антиоксидантной активности природных соединений в эксперименте: Пат. 2801864 от 31.10.2022; опубл. 17.08.2023. Бюл. №23) был предложен способ определения антиоксидантной активности природных соединений путем вычисления индекса антиоксидантной активности по формуле:

где ИАА - индекс антиоксидантной активности, у.е.; ΔА/Агем - перекисная резистентность эритроцитов (ПРЭ), вычисляемая по модифицированной методике А.А. Покровского и А.А. Абрарова; ΔА - понижение оптической плотности образца крови: ΔА=Агем - Аоп; Агем - оптическая плотность пробы гемолизованной крови, Аоп - оптическая плотность опытной пробы; п - количество вещества вводимого природного соединения (антиоксиданта), ммоль.
В то же самое время для качественной оценки выраженности антиоксидантной активности природных соединений указанного индекса не достаточно. Для оценки выраженности АОА, однако, необходима выработка некого стандарта, который сочетал бы в себе признаки водо- и жирорастворимых антиоксидантов преимущественно фенольного типа, тем более что значительная часть природных АО именно фенольного типа (токоферолы, полифенолы, эстрогены и т.д.). В иных водорастворимых АО, как правило, присутствует гидроксогруппа (аскорбиновая кислота), либо тиольная, например, в эрготионеине, цистеине (структурный аналог гидроксогруппы). Более того, между фенольными и гидроксотиольными водорастворимыми АО существует взаимосвязь, которая обозначается как неферментативная АОС: тиолы в этой цепи восстанавливают аскорбаты, а последние восстанавливают токоферолы. Таким образом, в качестве «усредненного» стандарта, сочетающего признаки всех звеньев неферментативной АОС, принят водорастворимый аналог токоферола - Тролокс, в структуре которого отсутствует боковая фитильная цепь (обусловливает водораствормость), присутствует гидроксогруппа, связанная с бензольным кольцом (фенольная часть). В этой связи в настоящее время принято оценивать антиоксидантную емкость в эквивалентах тролокса, принятого за стандарт (Иванова А.В. Потенциометрия в исследовании антиоксидантных и антирадикальных свойств веществ: диссертация... доктора хим. наук. - Екатеринбург: ФГАОУ ВО «Уральский федеральный университет имени первого Президента России Б.Н. Ельцина», 2019. - 350 с.). Тролокс является водорастворимым аналогом а-токоферола и сочетает, таким образом, в себе признаки водо- и жирорастворимых АО (структура тролокса приводится в отдельном разделе полученных результатов).
Таким образом, относя индексы антиоксидантной активности природных соединений к таковому тролокса на основе формулы (1), можно дать качественную оценку выраженности природных соединений по формуле:
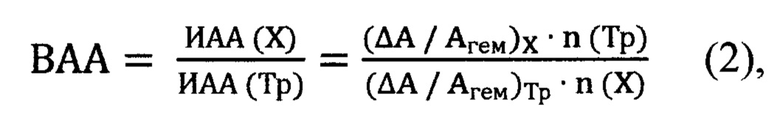
где ВАА - выраженность антиоксидантной активности, n (Тр) и n (X) - количества веществ соответственно тролокса и природного соединения X.
Учитывая, что количество вещества вычисляется по формуле: n=m/М (где m - масса, М - молярная масса), формула (2) приобретает следующий
вид: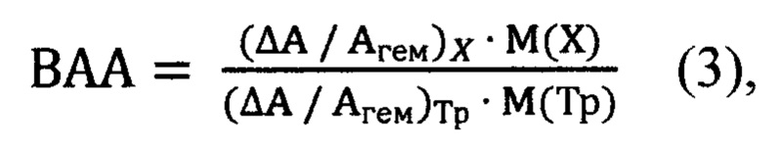
где М (X) и М (Тр) - молярные массы соответственно природного соединения X и тролокса. Выведенная формула позволяет судить, насколько выражена антиоксидантная активность по отношению к тролоксу, принятому за стандарт. В случае если АОА природного соединения окажется ниже таковой тролокса (ВАА будет ниже 1), следует говорить о пониженной антиоксидантной активности; в противоположном случае, когда ВАА будет выше 1, следует говорить о повышенной антиоксидантной активности.
Создание способа оценки антиоксидантной активности природных соединений осуществлялось на базе кафедры Фундаментальной химии ФГБОУ ВО «Астраханский государственный медицинский университет» Минздрава России. Для этого использовались беспородные белые крысы линии Wistar массой 210±15 г (30 шт. ), которые были поделены на три группы по 10 шт. в каждой. Первую группу использовали для оценки АОА α-токоферола (α-ТФ) и цистеина (Цис). Вторую группу животных использовали для оценки АОА полифенольных соединений (ПФС) имбиря, полученных и выделенных по патенту №2740997 (Логинов П.В., Николаев А.А., Мавлютова Е.Б., Голубкина С.А. Способ выделения полифенолов из корневищ имбиря: Пат. 2740997 от 05.11.2019, опубл. 22.01.2021) и водорастворимого АО - аскорбиновой кислоты (АсК) в сравнительном аспекте. Третья группа животных получала в качестве добавки в пищу тролокс. Все антиоксиданты вводили per os в течение двух недель в дозах 2,5 мг в сутки. В первых двух группах вначале животным вводили водорастворимые природные соединения (Цис в первой группе и АсК во второй группе), затем через 30 дней вводили α-ТФ (1 группа) и экстракт ПФС (2 группа) (для полного вымывания из крови животных водорастворимых соединений). Эксперимент проходил в течение двух месяцев в осенний период времени года (сентябрь-октябрь) во избежание сезонных влияний: Цистеин и АсК вводили параллельно в двух группах в первой половине сентября, α-ТФ и ПФС вводили во второй половине октября. Забор крови производили из хвостовой вены с соблюдением этических норм о гуманном отношении к животным в соответствии с Женевской конвенцией (1985). При заборе крови пипетку предварительно обрабатывали гепариновым раствором во избежание свертывания крови.
Для осуществления названного способа использовались следующие реактивы и оборудование: 1/15 М фосфатный буфер (рН 7,4), физиологический раствор, пергидроль (30% Н2О2), пипетка для забора крови и отбора рабочего раствора перекиси водорода емкостью 0,2 мл с грушей, водяная баня, термостат, центрифуга, спектрофотоколориметр КФК-3 (Россия). Для приготовления буферно-физиологической смеси использовали приготовленный фосфатный буфер и физраствор в соотношении 1:9. Рабочий раствор перекиси (10%) готовили путем смешивания пергидроля и физраствора в соотношении 1: 2. Далее определяли показатель ПРЭ по модифицированной методике Покровского А.А. и Абрарова А.А. (1964). Для этого к 4 мл буферно-физиологической смеси (рН 7,4) добавляют 0,1 мл крови и полученный раствор помещают в термостат на 15 минут при t=37°С, затем добавляют 0,2 мл рабочего раствора перекиси водорода, после чего пробирки вновь помещают в термостат на 30 минут при t=37°С. Пробу, в которой происходит полный гемолиз, готовят путем добавления 0,1 мл крови к 4 мл дистиллированной воды. Затем пробирки вынимают, дают им остыть 25 минут при комнатной температуре, и центрифугируют в течение 5 минут при 3000 об/мин; надосадочную жидкость сливают в кювету с толщиной фотометрируемого слоя 0,5 см и измеряют оптические плотности обоих проб при длине волны λ=536 нм против раствора сравнения (дистиллированная вода). Далее производится расчет показателя ПРЭ и индекса ВАА.
Апробация. В предлагаемом способе достигнуты следующие результаты. На основе измерений оптических плотностей контрольной и опытной проб были вычислены показатели ВАА для следующих антиоксидантных природных соединений: α-токоферола (α-ТФ), аскорбиновой кислоты (АсК), экстракта полифенольных соединений (ПФС) и цистеина (Цис). Ниже приводятся примеры расчетов ВАА для вышеуказанных природных АО.
Пример 1. Оценка АОА α-ТФ.
Были получены следующие значения оптических плотностей при полном гемолизе крови Агем: 0,450; 0,490; 0,420; 0,530; 0,520; 0,550; 0,602; 0,480; 0,540; 0,480. Показатели оптических плотностей опытных проб Аоп оказались следующими: 0,120; 0,150; 0,110; 0,175; 0,205; 0,215; 0,150; 0,120; 0,130; 0,125. Далее вычисляли показатели ПРЭ для α-ТФ:
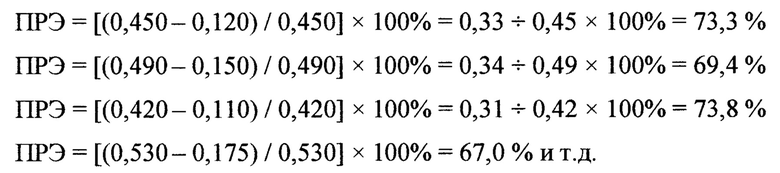
В среднем показатель ПРЭ для α-ТФ оказался равным 71,1α3,54% (или в долях 0,71).
Показатели оптической плотности при полном гемолизе крови для тролокса Агем следующие: 0,504; 0,500; 0,510; 0,490; 0,508; 0,495; 0,505; 0,510; 0,503; 0,512. Показатели оптических плотностей опытных проб Аоп оказались следующими: 0,252; 0,240; 0,254; 0,225; 0,260; 0,255; 0,247; 0,250; 0,244; 0,250. Далее вычисляли показатели ПРЭ для тролокса Тр в долях:
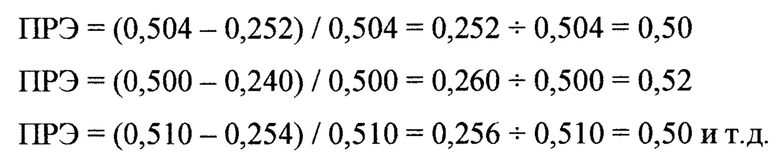
В среднем показатель ПРЭ для Тр оказался равным 0,52. Молярные массы для α-ТФ и Тр равны соответственно 430 и 250 г/моль. Вычислим показатель ВАА для α-ТФ:
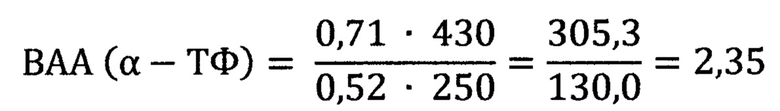
(Величину ИАА для тролокса 130,0 в знаменателе формулы для вычисления ВАА будем использовать в последующих примерах расчета индексов ВАА).
Таким образом показатель ВАА для α-ТФ 2,35 оказался выше 1, что свидетельствует о повышенной антиоксидантной активности α-токоферола.
Пример 2. Оценка АОА АсК.
Были получены следующие значения оптических плотностей при полном гемолизе крови Агем: 0,525; 0,500; 0,550; 0,605; 0,520; 0,480; 0,600; 0,630; 0,600; 0,565. Показатели оптических плотностей опытных проб Аоп оказались следующими: 0,385; 0,355; 0,370; 0,480; 0,400; 0,300; 0,300; 0,350; 0,390; 0,405. Далее вычисляли показатели ПРЭ для АсК:
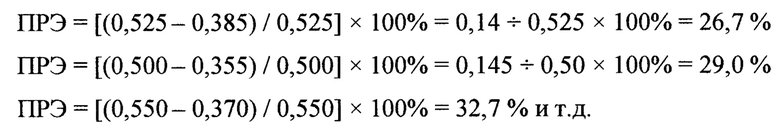
В среднем показатель ПРЭ для АсК оказался равным 30,2±1,90% (или в долях 0,30). Молярная масса аскорбиновой кислоты 176 г/моль. Вычислим показатель ВАА для АсК:
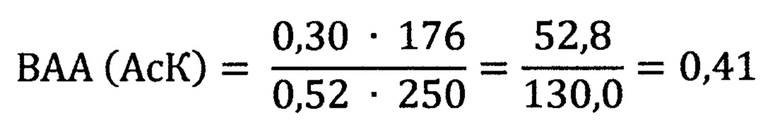
Таким образом показатель ВАА для АсК 0,41 оказался ниже 1, что свидетельствует о пониженной антиоксидантной активности аскорбиновой кислоты.
Пример 3. Оценка АОА ПФС.
Были получены следующие значения оптических плотностей при полном гемолизе крови Агем: 0,525; 0,500; 0,550; 0,605; 0,520; 0,480; 0,600; 0,630; 0,600; 0,565. Показатели оптических плотностей опытных проб Аоп оказались следующими: 0,200; 0,170; 0,180; 0,240; 0,175; 0,140; 0,240; 0,245; 0,180; 0,190. Далее вычисляли показатели ПРЭ для ПФС:
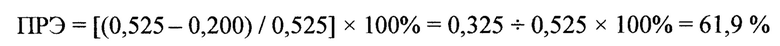
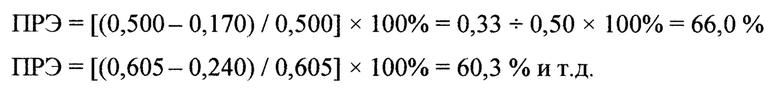
В среднем показатель ПРЭ для ПФС оказался равным 62,1±1,14% (или в долях 0,62). Средняя молярная масса ПФС составляет 285 г/моль. Вычислим показатель ВАА для ПФС:
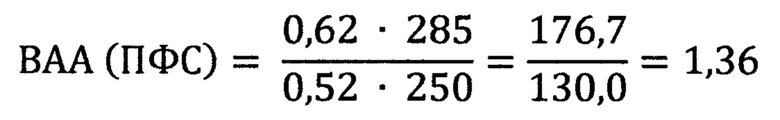
Таким образом, показатель ВАА для ПФС 1,36 оказался выше 1, что свидетельствует о повышенной антиоксидантной активности полифенольных соединений.
Пример 4. Оценка АОА цистеина.
Были получены следующие значения оптических плотностей при полном гемолизе крови Агем: 0,522; 0,510; 0,508; 0,515; 0,525; 0,495; 0,530; 0,527; 0,520; 0,530. Показатели оптических плотностей опытных проб Аоп оказались следующими: 0,365; 0,378; 0,365; 0,370; 0,400; 0,300; 0,386; 0,384; 0,390; 0,371. Далее вычисляли показатели ПРЭ для цистеина (Цис):
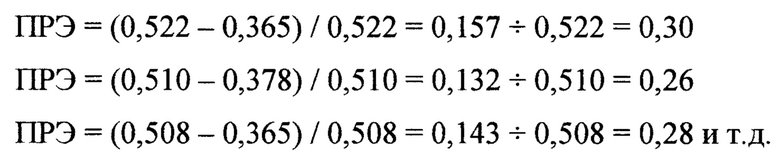
В среднем показатель ПРЭ для Цис оказался равным 0,28. Средняя молярная масса Цис составляет 107 г/моль. Вычислим показатель ВАА для Цис:
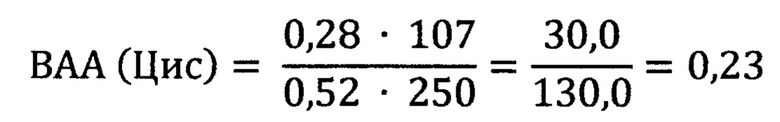
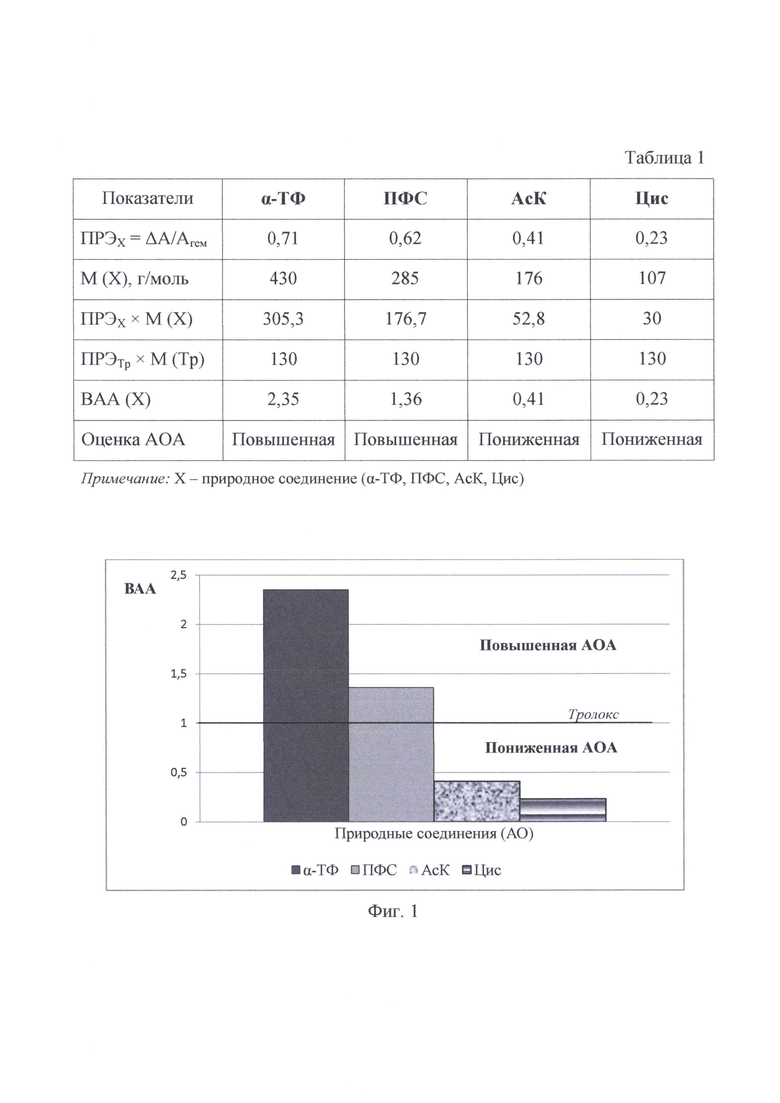
Таким образом, показатель ВАА для Цис 0,23 оказался ниже 1, что свидетельствует о пониженной антиоксидантной активности цистеина. Все полученные данные в описанных выше примерах обобщены в таблице 1 и наглядно представлены на Фиг. 1. Структура тролокса следующая:
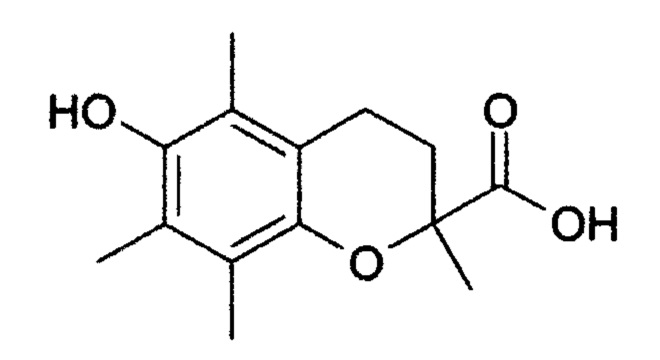
Из таблицы 1 следует, что показатель ПРЭ положительно коррелирует с величиной молярной массы антиоксидантов: чем выше молярная масса, тем выше величина ПРЭ. Указанное обстоятельство вполне объяснимо, поскольку высокая молекулярность означает способность вещества гидрофобно взаимодействовать с подобными макромолеклами в живой клетке. Такие макромолекулы встречаются, в частности, в биомембранах клеток. Поэтому жирорастворимые АО, в которых помимо бензольного кольца имеются длинные боковые фитильные цепи, способны «растворяться» в липидном бислое клеток за счет гидрофобных взаимодействий.
Как видно из графика (Фиг. 1), наиболее выраженной антиоксидантной активностью обладает а-токоферол (α-ТФ): его выраженность антиоксидантной активности (ВАА) превышаегтаковую ПФС более чем в 1,7 раза (на 72%), АсК - почти в 6 раз. Наименее выражена АОА у аминокислоты цистеина, что вполне естественно, учитывая ее низкую молекулярность. ПФС, в отличие от α-ТФ, обладают средней длиной боковой фитильной цепи, поэтому по своей «растворимости» в биомембранах клеток уступают токоферолу.
Аскорбиновая кислота (аскорбат, или витамин С), как и аминокислота цистеин, является водорастворимым АО и преимущественно циркулирует в крови, нежели внедряется в липидный бислой биомембран клеток. Кроме того, аскорбиновая кислота оказывает свое АО-действие главным образом опосредованно, восстанавливая иные АО в антиокислительной цепочке, например, α-токоферол, a N-ацетилцистеин (производный метаболит цистеина), в свою очередь, восстанавливает аскорбат.Поэтому индивидуальное АО-действие АсК и Цис менее выражено, чем у токоферола, который возглавляет неферментативную цепочку антиоксидантной системы АОС (П.В. Логинов. Функциональные особенности и пути коррекции репродуктивных процессов при стрессогенных воздействиях: Дисс. … доктора биол. наук. - Астрахань, 2016. - 260 с.). На основе выявленных закономерностей можно построить ряд по возрастанию АОА рассмотренных соединений:
Цистеин < Аскорбиновая кислота < ПФС < α-токоферол (витамин Е)
Созданный способ позволяет дать качественную оценку АОА природных соединений вне зависимости от их природы (жирорастворимые или водорастворимые, фенольного или нефенольного типа), что сочетается с простой технологией и методологией. Более того, данный способ позволяет также давать оценку АОА природных соединений в пределах живого организма, а не изолированно на основе изучения их физико-химических характеристик. Кроме того, описанный способ эффективно работает при использовании минимальных количеств биопроб.
Таким образом, предлагаемый способ можно в дальнейшем адаптировать для клинических исследований после соответствующих дополнительных испытаний, поскольку он позволяет давать точную качественную оценку антиоксидантной активности различных природных соединений вне зависимости от их природы, а также характеризовать выраженность их действия в организме в сравнительном аспекте.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ АКТИВНОСТИ ПРИРОДНЫХ СОЕДИНЕНИЙ В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2801864C1 |
| СПОСОБ ДИАГНОСТИКИ ОКИСЛИТЕЛЬНОГО СТРЕССА ОРГАНИЗМА ЧЕЛОВЕКА | 2003 |
|
RU2236008C1 |
| СПОСОБ ОЦЕНКИ АНТИОКСИДАНТНОЙ АКТИВНОСТИ | 2009 |
|
RU2392623C1 |
| Средство, обладающее антиагрегантной, цитопротекторной и антиоксидантной активностью | 2018 |
|
RU2694061C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЛИПИДКОРРИГИРУЮЩИМИ, ГИПОКОАГУЛЯЦИОННЫМИ И АНТИОКСИДАНТНЫМИ СВОЙСТВАМИ | 2005 |
|
RU2302248C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКИСЛИТЕЛЬНОЙ АКТИВНОСТИ АНТИОКСИДАНТНЫХ ПРЕПАРАТОВ | 1999 |
|
RU2160898C1 |
| СПОСОБ ЛЕЧЕНИЯ ЖЕЛЧНОГО ПЕРИТОНИТА | 2004 |
|
RU2285522C2 |
| СПОСОБ ОЦЕНКИ АНТИОКСИДАНТНОЙ ЗАЩИТЫ ОРГАНИЗМА ЧЕЛОВЕКА | 2013 |
|
RU2538081C1 |
| АНТИОКСИДАНТНОЕ СРЕДСТВО С ГЕПАТОПРОТЕКТОРНЫМ ЭФФЕКТОМ НА ОСНОВЕ НАНОСТРУКТУРИРОВАННОГО СЕЛЕНА И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2013 |
|
RU2557992C1 |
| КОМПОЗИЦИЯ ДЛЯ КОРРЕКЦИИ ПАТОЛОГИЧЕСКИХ НАРУШЕНИЙ УГЛЕВОДНОГО, ЛИПИДНОГО ОБМЕНА И АНТИОКСИДАНТНОГО СТАТУСА ОРГАНИЗМА | 2008 |
|
RU2360683C1 |
Изобретение относится к медицине, а именно к фармацевтике, биологической химии, и может быть использовано для оценки антиоксидантной активности природных соединений. В крови животных, которым вводят природное соединение, производят спектрофотометрическое определение показателей антиоксидантной активности природных соединений по данным перекисной резистентности эритроцитов. Показатели антиоксидантной активности природных соединений относят к таковому тролокса. Рассчитывают выраженность антиоксидантной активности по формуле: 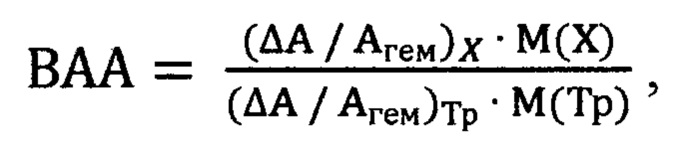 где ВАА - выраженность антиоксидантной активности; (ΔА/Агем)х - перекисная резистентность эритроцитов в присутствии природного соединения X; (ΔА/Агем)Тр - перекисная резистентность эритроцитов в присутствии тролокса Тр; ΔА - понижение оптической плотности образца крови: ΔА=Агем - Аоп; Агем - оптическая плотность пробы гемолизованной крови, Аоп - оптическая плотность опытной пробы; М (X) и М (Тр) - молярные массы соответственно природного соединения X и тролокса. При величине ВАА ниже 1 определяют пониженную относительно тролокса антиоксидантную активность соединения. При величине ВАА больше 1 определяют повышенную относительно тролокса антиоксидантную активность соединения. Способ обеспечивает возможность дать качественную оценку антиоксидантной активности природных соединений за счет использования вычисленной величины индекса антиоксидантной активности для расчета выраженности антиоксидантной активности по силе действия. 1 ил., 1 табл., 4 пр.
где ВАА - выраженность антиоксидантной активности; (ΔА/Агем)х - перекисная резистентность эритроцитов в присутствии природного соединения X; (ΔА/Агем)Тр - перекисная резистентность эритроцитов в присутствии тролокса Тр; ΔА - понижение оптической плотности образца крови: ΔА=Агем - Аоп; Агем - оптическая плотность пробы гемолизованной крови, Аоп - оптическая плотность опытной пробы; М (X) и М (Тр) - молярные массы соответственно природного соединения X и тролокса. При величине ВАА ниже 1 определяют пониженную относительно тролокса антиоксидантную активность соединения. При величине ВАА больше 1 определяют повышенную относительно тролокса антиоксидантную активность соединения. Способ обеспечивает возможность дать качественную оценку антиоксидантной активности природных соединений за счет использования вычисленной величины индекса антиоксидантной активности для расчета выраженности антиоксидантной активности по силе действия. 1 ил., 1 табл., 4 пр.
Способ оценки антиоксидантной активности природных соединений, заключающийся в том, что в крови животных, которым вводят природное соединение, производят спектрофотометрическое определение показателей антиоксидантной активности природных соединений по данным перекисной резистентности эритроцитов, отличающийся тем, что показатели антиоксидантной активности природных соединений относят к таковому тролокса, и рассчитывают выраженность антиоксидантной активности по формуле:
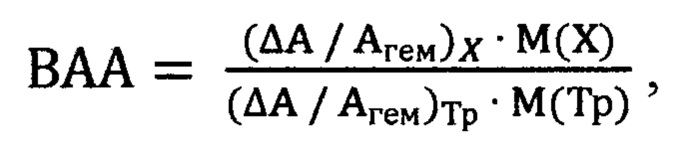
где ВАА - выраженность антиоксидантной активности; (ΔА/Агем)х - перекисная резистентность эритроцитов в присутствии природного соединения X; (ΔА/Агем)Тр - перекисная резистентность эритроцитов в присутствии тролокса Тр; ΔА - понижение оптической плотности образца крови: ΔА=Агем - Аоп; Агем - оптическая плотность пробы гемолизованной крови, Аоп - оптическая плотность опытной пробы; М (X) и М (Тр) - молярные массы соответственно природного соединения X и тролокса; и при величине ВАА ниже 1 определяют пониженную относительно тролокса антиоксидантную активность, а при величине ВАА больше 1 определяют повышенную относительно тролокса антиоксидантную активность соединения.
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ АКТИВНОСТИ ПРИРОДНЫХ СОЕДИНЕНИЙ В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2801864C1 |
| СПОСОБ ОЦЕНКИ АНТИОКСИДАНТНОЙ АКТИВНОСТИ | 2009 |
|
RU2392623C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОКСИДАНТНОЙ/АНТИОКСИДАНТНОЙ АКТИВНОСТИ ВЕЩЕСТВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2012 |
|
RU2486499C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ АКТИВНОСТИ ВЕЩЕСТВА | 2009 |
|
RU2419794C2 |
| Способ оценки антиоксидантной активности биологически активных препаратов | 2020 |
|
RU2738302C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ АКТИВНОСТИ С ИСПОЛЬЗОВАНИЕМ МЕТОДА ЭЛЕКТРОННО-ПАРАМАГНИТНОЙ РЕЗОНАНСНОЙ СПЕКТРОСКОПИИ | 2015 |
|
RU2614365C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНТЕГРАЛЬНОЙ АНТИОКСИДАНТНОЙ АКТИВНОСТИ С ИСПОЛЬЗОВАНИЕМ ИНДИКАТОРНОЙ СИСТЕМЫ МЕДЬ(II) - НЕОКУПРОИН | 2016 |
|
RU2625038C1 |
| WO 2010045986 A1, 29.04.2010 | |||
| US 20230341364 A1, 26.10.2023. | |||
Авторы
Даты
2024-06-20—Публикация
2023-10-02—Подача