ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Данная заявка подается в электронном виде через EFS-Web и включает представленный в электронном виде список последовательностей в формате.txt. Файл.txt содержит список последовательностей под названием «PC72591_PROV2 _ST25.txt», созданный 28 января 2021 и имеющий размер 152 КБ. Перечень последовательностей, содержащийся в этом файле.txt, является частью описания и полностью включен в настоящее описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к композициям Escherichia coli и способам их получения.
УРОВЕНЬ ТЕХНИКИ
Угроза для здоровья населения, создаваемая растущей устойчивостью к противомикробным лекарственным средствам, описана в недавних отчетах, опубликованных ВОЗ и CDC (Thelwall SN, et al. Annual Epidemiological Commentary Mandatory MRSA, MSSA и E. coli bacteraemia and C. difficile infection data 2015/16. 2016; Russo TA, et al. Microbes and infection 2003; 5:449-56). Приоритетные патогены, описанные обоими агентствами, включают Enterobacteriaceae, резистентные к цефалоспоринам третьего поколения за счет продуцирования бета-лактамаз расширенного спектра (ESBL), и к карбапенемам за счет продуцирования ферментов карбапенемаз. По данным CDC, Enterobacteriaceae, экспрессирующие ESBL, представляют собой серьезную угрозу, в то время как резистентность Enterobacteriaceae к карбапенемным антибиотикам последней линии считается неотложной угрозой. Штаммы E. coli ESBL становятся все более распространенными, и неизлечимые инфекции, вызванные Klebsiella pneumoniae, продуцирующей как ESBL, так и карбапенемазы, становятся все более распространенными, особенно в развивающихся странах.
Escherichia coli является одним из наиболее распространенных бактериальных патогенов человека с клиническими проявлениями, которые включают инфекции кровотока (70/100000 в США) (Marder EP, et al. Foodborne pathogens and disease 2014; 11:593-5), инфекции мочевыводящих путей (связанные с катетером (25000-525000 случаев в год в США) (Al-Hasan MN, et al. The Journal of antimicrobial chemotherapy 2009; 64:169-7); не связанные с катетером (6-8 миллионов случаев в год в США) (там же)); инфекции в области хирургического вмешательства (127500 случаев в год в США), пневмония (14100-23400 случаев в год в США) (там же) и диарея, связанная с серьезными пищевыми отравлениями (63000 случаев в год в США) (Zowawi HM, et al. Nature review Urology 2015; 12:570-84). Они классифицируются серологически по различиям в структуре связанного с липополисахаридом О-антигена (>180 известных серотипов), капсульного полисахаридного К-антигена (>80 серотипов) и жгутикового Н-антигена (>50 серотипов).
Инфекции мочевыводящих путей (UTI) чаще всего проявляются в виде цистита, который у некоторых людей может повторяться неоднократно после выздоровления. При отсутствии лечения они могут прогрессировать до пиелонефрита и инфекций кровотока. Инфекции E. coli связаны с высоким уровнем резистентности к антибиотикам (Rogers BA, et al. The Journal of antimicrobial chemotherapy 2011; 66:1-14), при этом многие штаммы резистентны ко многим антибиотикам, включая антибиотики последнего поколения, такие как карбапенемы и полимиксины (Nicolas-Chanoine M-H, et al. Clinical Microbiology Reviews 2014; 27:543-74). В частности, мультилокусный тип последовательности серотипа O25b (MLST) 131 стал всемирным пандемическим клоном, вызывающим преимущественно внебольничные инфекции с высокой степенью резистентности к цефалоспоринам расширенного спектра (ESBL) и фторхинолонам (Poolman JT, et al. The Journal of infectious diseases 2016; 213:6-13; Podschun R, et al. Clin Microbiol Rev 1998; 11:589-603). Штаммы, инфицирующие E. coli BSI и UTI, также известны как инвазивные внекишечные патогенные E. coli (ExPEC) или уропатогенные E. coli (UPEC). Сообщается, что из >180 идентифицированных серотипов О-антигена E. coli среди штаммов ExPEC, на подгруппу из 10-12 О-серотипов приходится >60% случаев бактериемии (Yinnon AM, et al. QJM : monthly journal of the Association of Physicians 1996; 89:933-41).
После E.coli, Klebsiella spp. (включая K. pneumoniae и K. oxytoca) являются следующими наиболее распространенными грамотрицательными патогенами, связанными с инвазивными инфекциями, включая UTI, пневмонию, внутрибрюшную инфекцию и инфекцию кровотока (BSI) (Podschun R, et al. Clin Microbiol Rev 1998; 11:589-603; Anderson DJ, et al. PLoS One 2014; 9:e91713; Chen L, et al. Trends Microbiol 2014; 22:686-96; Iredell J, et al. Bmj 2016; 352:h6420). Klebsiella сохраняют глубокую способность приобретать резистентность к антибиотикам за счет горизонтально передающихся ESBL и генов, придающих резистентность к карбапенемам (Follador R, et al. Microbial Genomics 2016; 2:e000073; Schrag SJ, Farley MM, Petit S, et al. Epidemiology of Invasive Early-Onset Neonatal Sepsis, 2005 to 2014. 2016; 138:e20162013). Соответственно, за последнее десятилетие во всем мире резко возросла распространенность резистентных к ESBL клебсиелл, продуцирующих бета-лактамазы расширенного спектра (ESBL). Klebsiella spp. могут экспрессировать до 8 различных O-типов и >80 K-типов. В то время как существует множество К-антигенов, связанных с вирулентными штаммами клебсиелл, только четыре серотипа О-антигена составляют >80% клинических изолятов Klebsiella, независимо от места взятия образца (кровь, моча, мокрота), инфекционного статуса (инвазивная или неинвазивная) или характера приобретения (внебольничная или внутрибольничная) (Stoll BJ, et al. Pediatrics 2011; 127:817-26).
Повышенный уровень инвазивных инфекций E. coli и Klebsiella с множественной лекарственной резистентностью (МЛУ) среди уязвимых новорожденных и пожилых людей подчеркивает необходимость применения подходов, основанных на вакцинах, в качестве альтернативы стандартным антибиотикам, которые становятся менее эффективными.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Для удовлетворения этих и других потребностей настоящее изобретение относится к композициям и способам их применения для индукции иммунных ответов против серотипов E.coli и K.pneumoniae.
В одном варианте осуществления изобретение предлагает композицию, содержащую полипептид, полученный из FimH, или его фрагмента; и сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
В одном аспекте, композиция дополнительно содержит, по меньшей мере, один сахарид, полученный из любой одной K. pneumoniae, выбранный из группы, состоящей из O1, O2, O3 и O5.
В другом аспекте, композиция дополнительно содержит сахарид, полученный из K. pneumoniae, который конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгированный с белком-носителем.
В другом варианте осуществления, изобретение предлагает композицию, содержащую полипептид, полученный из FimH, или его фрагмент; и, по меньшей мере, один сахарид, полученный из любой одной K. pneumoniae, выбранный из группы, состоящей из O1, O2, O3 и O5. В одном аспекте, композиция дополнительно содержит, по меньшей мере, один сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
В другом аспекте, где сахарид, полученный из K. pneumoniae, конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгирован с белком-носителем.
В другом варианте осуществления изобретение предлагает композицию, содержащую, по меньшей мере, один сахарид, полученный из любого одного K. pneumoniae, выбранный из группы, состоящей из О1, О2, О3 и О5; и, по меньшей мере, один сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
В одном аспекте, композиция дополнительно содержит полипептид, полученный из FimH, или его фрагмент. В другом аспекте, сахарид E. coli содержит Формулу O8. В другом аспекте, сахарид E. coli содержит Формулу O9.
В другом варианте осуществления, изобретение относится к способу индукции иммунного ответа против Escherichia coli у млекопитающего, включающему введение млекопитающему эффективного количества композиции по любому из приведенных выше вариантов осуществления и их аспектов.
В другом варианте осуществления изобретение относится к способу индукции иммунного ответа против Klebsiella pneumoniae у млекопитающего, включающему введение млекопитающему эффективного количества композиции по любому из приведенных выше вариантов осуществления и их аспектов.
В одном аспекте, изобретение относится к рекомбинантной клетке млекопитающего, включающей полинуклеотид, кодирующий полипептид, полученный из E.coli, или его фрагмент. В некоторых вариантах осуществления, полинуклеотид кодирует полипептид, полученный из фимбриального полипептида H (fimH) E. coli или его фрагмента. В некоторых вариантах осуществления, полипептид, полученный из FimH E. coli, или его фрагмент включает остаток фенилаланина на N-конце полипептида.
В одном аспекте, изобретение относится к способу получения полипептида, полученного из E.coli, или его фрагмента в рекомбинантной клетке млекопитающего. Способ включает культивирование рекомбинантной клетки млекопитающего в подходящих условиях, тем самым экспрессируя полипептид или его фрагмент; и сбор полипептида или его фрагмента. В некоторых вариантах осуществления, способ дополнительно включает очистку полипептида или его фрагмента. В некоторых вариантах осуществления, выход полипептида составляет, по меньшей мере, 0,05 г/л. В некоторых вариантах осуществления, выход полипептида составляет, по меньшей мере, 0,10 г/л.
В одном аспекте, изобретение относится к композиции, включающей полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80% 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29 или любой их комбинацией.
В другом аспекте, изобретение относится к композиции, которая включает полипептид, содержащий, по меньшей мере, n последовательных аминокислот из любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29, где n равно 7 или более (например, 8, 10, 12, 14, 16, 18, 20 и более). В некоторых вариантах осуществления композиция дополнительно включает сахарид, выбранный из любой Формулы в Таблице 1, предпочтительно, Формулы O1A, Формулы O1B, Формулы O2, Формулы O6 и Формулы O25B, где n представляет собой целое число от 1 до 100, предпочтительно, от 31 до 100.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На ФИГ. 1А-1Н изображены аминокислотные последовательности, включая аминокислотные последовательности для типовых полипептидов, полученных из E. coli или их фрагментов; и аминокислотные последовательности для типовых последовательностей wzzB.
На ФИГ. 2A-2T изображены карты типовых векторов экспрессии.
На ФИГ. 3 показаны результаты экспрессии и очистки.
На ФИГ. 4 показаны результаты экспрессии и очистки.
На ФИГ. 5 показаны результаты экспрессии.
На ФИГ. 6A-6C показаны пулы SEC pSB02083 и pSB02158 и аффинности; включая выходы.
На ФИГ. 7 показаны результаты экспрессии мутантной конструкции pSB2198 FimH dscG Lock.
На ФИГ. 8 показаны результаты экспрессии pSB2307 FimH dscG дикого типа.
На ФИГ. 9А-9С показаны структуры О-антигенов, синтезированных полимеразно-зависимым путем с четырьмя или менее остатками в остове.
На ФИГ. 10А-10В: на ФИГ. 10А показаны структуры О-антигенов, синтезируемых полимеразно-зависимым путем с пятью или шестью остатками в остове; на ФИГ. 10В показаны О-антигены, которые, как предполагается, синтезируются с помощью ABC-транспортер-зависимого пути.
На ФИГ. 11 показано компьютерное сканирование мутагенеза Phe1 с другими аминокислотами, имеющими алифатические гидрофобные боковые цепи, например, Ile, Leu и Val, которые могут стабилизировать белок FimH и обеспечить связывание маннозы.
На ФИГ. 12A-12B показаны плазмиды: плазмида репликона pUC, 500-700x копий на клетку, регулятор длины цепи (ФИГ. 12A); и плазмида репликона Р15а, 10-12х копий на клетку, О-антигенный оперон (ФИГ. 12В).
На ФИГ. 13A-13B показана модуляция длины цепи О-антигена в штаммах серотипов O25a и O25b посредством экспрессии на основе плазмид гетерологичных регуляторов длины цепи wzzB и fepE. Показана генетическая комплементация экспрессии LPS в плазмидных трансформантах нокаутных штаммов wzzB O25K5H1 (O25a) и GAR2401 (O25b). На левой стороне ФИГ. 13A показаны профили LPS плазмидных трансформантов O25a O25K5HΔwzzB; и справа аналогичные профили трансформантов O25b GAR 2401ΔwzzB. Иммуноблот репликата геля, зондированного O25-специфической сывороткой (Statens Serum Institut), показан на ФИГ. 13В. O25a Δ wxxB (нокаут) фон, связанный с дорожками 1-7; O25b 2401 ΔwzzB (нокаут) фон, связанный с дорожками 8-15.
На ФИГ. 14 показана экспрессия длинноцепочечного О-антигена, обеспечиваемая плазмидами E. coli и Salmonella fepE в организме хозяина O25K5H1ΔwzzB.
На ФИГ. 15 показано, что экспрессия Salmonella fepE генерирует LPD длинного О-антигена в различных клинических изолятах.
На ФИГ. 16A-16B изображена опосредованная плазмидой индуцируемая арабинозой экспрессия O25b длинного O-антигена LPS в штамме-хозяине с нокаутом O25b O-антигена. Результаты SPS PAGE показаны на ФИГ. 16A, и результаты иммуноблота O25 показаны на ФИГ. 16B, где дорожка 1 соответствует клону 1, без арабинозы; дорожка 2 соответствует клону 1, 0,2% арабинозы; дорожка 3 соответствует клону 9, без арабинозы; дорожка 4 соответствует клону 9, 0,2% арабинозы; дорожка 5 соответствует стандарту O55 E. coli LPS; и дорожка 6 соответствует стандарту O111 E. coli LPS, как на ФИГ. 16А и на ФИГ. 16В.
На ФИГ. 17 показана опосредованная плазмидой индуцируемая арабинозой экспрессия LPS длинного О-антигена в обычном штамме-хозяине.
На ФИГ. 18 показана экспрессия LPS О25 О-антигена в штаммах Exploratory Bioprocess.
На ФИГ. 19A-19B показаны профили SEC и свойства короткого (ФИГ. 19A, штамм 1 O25b wt 2831) и длинного O25b O-антигенов (ФИГ. 19B, штамм 2 O25b 2401Δ wzzB /LT2 FepE), очищенных от штаммов GAR2831 и '2401ΔwzzB/ fepE.
На ФИГ. 20A-20B показаны схемы вакцинации кроликов: (ФИГ. 20A) информация относительно схемы вакцинации для исследования кроликов 1 VAC-2017-PRL-EC-0723; (ФИГ. 20B) схема вакцинации для исследования на кроликах 2 VAC-2018-PRL-EC-077.
На ФИГ. 21A-21C показаны ответы IgG гликоконъюгата O25b, где -●- означает результаты перед сбором крови; -■- сбор крови 1 (6 недель); -▲- сбор крови 2 (8 недель); -♦- сбор крови 3 (12 недель). На ФИГ. 21А показаны результаты для кролика 1-3 (средняя активация); На ФИГ. 21B показаны результаты для кролика 2-3 (низкая активация); На ФИГ. 21C показаны результаты для кролика 3-1 (высокая активация).
На ФИГ. 22A-22F показаны IgG-ответы на гликоконъюгат O25b длинного O-антигена, т. е. конъюгат O25b-CRM197 с низкой активацией (ФИГ. 22D - 22F, где -●- означает результаты предварительного отбора крови от кролика 2-1, -■- 12-я неделя антисыворотки от кролика 2-1) по сравнению с неконъюгированным полисахаридом, т.е. свободным полисахаридом O25b (ФИГ. 22A-22C, где -●- означает результаты предварительного отбора крови от кролика A-1, -■- антисыворотка на 6 неделе от кролика A-1, -▲- антисыворотка на 8 неделе от кролика A-1). Обратите внимание, что MFI нанесены на график в логарифмической шкале, чтобы выделить различия между предиммунными и иммунными антителами в диапазоне <1000 MFI. На ФИГ. 22А показаны результаты для кролика А-1 (неконъюгированный поли); на ФИГ. 22В показаны результаты для кролика А-3 (неконъюгированный поли); на ФИГ. 22С показаны результаты для кролика А-4 (неконъюгированный поли); на ФИГ. 22D показаны результаты для кролика 2-1 (низкая активация); на ФИГ. 22E показаны результаты для кролика 2-2 (низкая активация); и на ФИГ. 22F показаны результаты для кролика 2-3 (низкая активация).
На ФИГ. 23A-23C показана поверхностная экспрессия нативного O-антигена по сравнению с длинным O25b O-антигеном, обнаруженным с помощью антисыворотки O25b. На ФИГ. 23A показаны результаты, где -●- означает результаты сравнения O25b 2831 с PD3 антисывороткой; -■- представляет результаты O25b 2831 wt по сравнению с перед сбором крови; -▲- представляет результаты исследования O25b 2831/fepE по сравнению с PD3 антисывороткой; -▼- представляет результаты O25b 2831/fepE по сравнению с перед сбором крови. На ФИГ. 23B показаны результаты, где -●- представляет результаты O25b 2401 по сравнению с PD3 антисывороткой; -■- представляет результаты O25b 2401 по сравнению с перед сбором крови; -▲- представляет результаты O25b 2401/fepE по сравнению с PD3 антисывороткой; -▼- представляет результаты O25b 2401/fepE по сравнению с перед сбором крови. На ФИГ. 23C показаны результаты, где -●- представляет результаты E. coli K12 по сравнению с PD3 антисывороткой; и -■- представляет результаты E. coli K12 по сравнению с перед сбором крови.
На ФИГ. 24 представлены обобщенные структуры углеводного остова олигосахаридов внешнего ядра пяти известных хемотипов. Все глюкозы находятся в α-аномерной конфигурации, если не указано иное. Гены, продукты которых катализируют образование каждой связи, указаны пунктирными стрелками. Звездочкой обозначен остаток корового олигосахарида, к которому происходит присоединение О-антигена.
На ФИГ. 25 показано, что неконъюгированный свободный полисахарид O25b не является иммуногенным (dLIA), где -●- представляет результаты недели 18 (1 нед=PD4) с антисывороткой из 4-1; -■- представляет результаты недели 18 (1 нед=PD4) с антисывороткой из 4-2; -▲- представляет результаты недели 18 (1 нед=PD4) с антисывороткой из 5-1; -▼- представляет результаты недели 18 (1 нед=PD4) с антисывороткой из 5-2; -*- представляет результаты недели 18 (1 нед=PD4) с антисывороткой из 6-1; - - представляет результаты недели 18 (1 нед=PD4) с антисывороткой из 6-2.
- представляет результаты недели 18 (1 нед=PD4) с антисывороткой из 6-2.
На ФИГ. 26A-26C представлены графики, иллюстрирующие специфичность титров OPA конъюгированных иммунных сывороток BRC Rabbit O25b RAC. На ФИГ. 26A показаны титры OPA в сыворотке кролика 2-3 до иммунизации (-●-) и в сыворотке после иммунизации через 13 недель (-■-). На ФИГ. 26B показаны титры OPA в сыворотке кролика 1-2 до иммунизации (-●-) и сыворотке после иммунизации через 19 недель (-■-). На ФИГ. 26C показана специфичность титра OPA кролика 1-2 через 19 недель, при котором активность OPA иммунной сыворотки кролика 1-2 блокируется предварительной инкубацией со 100 мкг/мл очищенного неконъюгированного O25b длинного полисахарида O-антигена, где -■- представляет результаты для иммунной сыворотки кролика 1-2, неделя 19; и -▼- представляет результаты для кролика 1-2, неделя 19 w/R1 Long-OAg.
На ФИГ. 27А-27С на ФИГ. 27A представлена иллюстрация типовой схемы введения. На ФИГ. 27В и ФИГ. 27C представлены графики, изображающие уровни O-антигена O25b IgG, индуцированные неконъюгированным полисахаридом O25b длинного O-антигена (ФИГ. 27B, O25b Free Poly (2 мкг)) и полученного гликоконъюгата O25b RAC/DMSO длинного O-антигена (ФИГ. 27C, O25b-CRM197 RAC Long (2 мкг)), где -… - (пунктирная линия) представляет уровень наивного CD1 O25b IgG.
На ФИГ. 28A-28B представлены графики, показывающие OPA иммуногенность RAC, длинных гликоконъюгатов eTEC O25b и гликоконъюгатов с одним концом после введения дозы 2 (ФИГ. 28A) и после введения дозы 3 (ФИГ. 28B), где -○- представляет результаты для короткого гликоконъюгата с одним концом 2 мкг; -●- одноконцевой длинный 2 мкг; -▲- RAC/ДМСО длинный 2 мкг; -▼- eTEC длинный 2 мкг; * Фоновый контроль (n=20).  Показатели пациентов, ответивших на лечение, представляют собой % мышей с титрами >2х от исходного уровня до вакцинации.
Показатели пациентов, ответивших на лечение, представляют собой % мышей с титрами >2х от исходного уровня до вакцинации.
На ФИГ. 29 представлен график, показывающий иммуногенность ОРА химического состава eTEC и измененные уровни активации полисахарида.  Показатели пациентов, ответивших на лечение, представляют собой % мышей с титрами >2х от исходного уровня до вакцинации.
Показатели пациентов, ответивших на лечение, представляют собой % мышей с титрами >2х от исходного уровня до вакцинации.
На ФИГ. 30A-30B показана типовая схема введения (ФИГ. 30A); и график, изображающий защиту мышей, иммунизированных дозами конъюгатов eTEC E. coli, от летального заражения изолятом O25b (ФИГ. 30B), где -◊- представляет активацию eTEC с длинной цепью 17%; -Δ- eTEC представляет 10% активацию длинной цепи; -∇- представляет активацию eTEC с длинной цепью 4%; -□- представляет собой полисахарид O25b; -○- представляет собой невакцинированные контроли.
На ФИГ. 31 представлена схема, иллюстрирующая пример получения конъюгатов с одним концом, где процесс конъюгации включает селективную активацию 2-кето-3-дезоксиоктановой кислоты (KDO) дисульфид-аминовым линкером при демаскировании тиоловой функциональной группы. Затем KDO конъюгируют с активированным бромом белком CRM 197, как показано на ФИГ. 31 (Получение односторонних конъюгатов).
На ФИГ. 32A-32B представлена типовая блок-схема процессов активации (ФИГ. 32A) и конъюгации (ФИГ. 32B), используемых при получении гликоконъюгата E. coli с CRM197.
На ФИГ. 33 изображены структуры повторяющейся единицы (RU) полиманнановых О-антигенов E.coli и K.pneumoniae. Условные обозначения: тримерные E. coli O8 и K. pneumoniae O5 идентичны, как и терамерные E. coli O9A/ K. pneumoniae O3a и пентамерные E. coli O9/ K. pneumoniae O3. Дифференциация подтипов O3 K. pneumoniae на уровне биосинтетических ферментных последовательностей описана в Guachalla LM et al. (Scientific Reports 2017; 7:6635).
На ФИГ. 34A-34B показана иммунная сыворотка E. coli серотипа O8, обладающая бактерицидным действием против инвазивных штаммов K. pneumoniae серотипа O5. Условные обозначения: иммунную сыворотку кролика, индуцированную конъюгатом E.coli серотипа O8-антиген CRM197, оценивают в бактерицидных анализах со штаммом E.coli O8 (ФИГ. 34A) и штаммом K. pneumoniae O5 (ФИГ. 34B). Сильная опсонофагоцитарная активность (OPA) против штамма E. coli O8 наблюдалась после двух доз вакцины (неделя 15), которая отсутствовала после предварительной адсорбции с неконъюгированным полисахаридом O8 (O8-OAg) или с подобранной предиммунизированной сывороткой (неделя 0). Та же иммунная сыворотка кролика показала антигенспецифическую бактерицидную активность сыворотки (SBA) против штамма K. pneumoniae O5. BRC - комплемент крольчат, hC - обедненная IgG/IgM сыворотка человека в качестве источника комплемента.
На ФИГ. 35A-35 изображена иммунная сыворотка E. coli серотипа O9 О-антигена, обладающая бактерицидным действием против инвазивного изолята K. pneumoniae O3. Условные обозначения: Иммунную сыворотку кролика, полученную с помощью конъюгата E. coli серотипа O9a O-антигена CRM197, оценивают в анализе опсонофагоцитов (OPA) со штаммом E. coli O9a (ФИГ. 35A) и штаммом K. pneumoniae O3b (ФИГ. 35B). Активность OPA против штамма E. coli O9 наблюдалась после введения двух доз вакцины (15 неделя), которая отсутствовала после предварительной адсорбции с неконъюгированным полисахаридом O9 (O9-OAg) или с подобранной предиммунизированной сывороткой (0 неделя). Та же иммунная сыворотка кролика также показала мощную антигенспецифическую бактерицидную активность сыворотки (SBA) против штамма K. pneumoniae O3b. BRC, комплемент для крольчат; hC, обедненная IgG/IgM сыворотка человека, используемая в качестве источника комплемента.
ИДЕНТИФИКАТОРЫ ПОСЛЕДОВАТЕЛЬНОСТИ
SEQ ID NO: 1 представляет аминокислотную последовательность D-манноза-специфичного адгезина фимбрии 1 дикого типа [Escherichia coli FimH J96].
SEQ ID NO: 2 представляет собой аминокислотную последовательность фрагмента FimH, соответствующую остаткам 22-300 а.к. SEQ ID NO: 1 (зрелый белок FimH).
SEQ ID NO: 3 представляет аминокислотную последовательность лектинового домена FimH.
SEQ ID NO: 4 представляет аминокислотную последовательность пилинового домена FimH.
SEQ ID NO: 5 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH (pSB02198 - FimH mIgK сигнальный пептид/F22..Q300 J96 FimH N28S V48C L55C N91S N249Q/7 АК линкер/FimG A1..K14/ GGHis8 в pcDNA3.1(+))
SEQ ID NO: 6 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH (pSB02307 - FimH mIgK signal pept/F22..Q300 J96 FimH N28S N91S N249Q/His8 в pcDNA3.1(+))
SEQ ID NO: 7 представляет аминокислотную последовательность фрагмента полипептида, полученного из FimH E. coli (конструкция pSB02083 FimH лектиновый домен дикого типа)
SEQ ID NO: 8 представляет аминокислотную последовательность фрагмента полипептида, полученного из E. coli FimH (pSB02158 FimH замкнутого мутанта лектинового домена).
SEQ ID NO: 9 представляет аминокислотную последовательность фрагмента полипептида, полученного из E. coli FimG (FimG A1..K14).
SEQ ID NO: 10 представляет аминокислотную последовательность фрагмента полипептида, полученного из E. coli FimC.
SEQ ID NO: 11 представляет аминокислотную последовательность линкера из 4 а.к.
SEQ ID NO: 12 представляет аминокислотную последовательность линкера из 5 а.к.
SEQ ID NO: 13 представляет аминокислотную последовательность линкера из 6 а.к.
SEQ ID NO: 14 представляет аминокислотную последовательность линкера из 7 а.к.
SEQ ID NO: 15 представляет аминокислотную последовательность линкера из 8 а.к.
SEQ ID NO: 16 представляет аминокислотную последовательность линкера из 9 а.к.
SEQ ID NO: 17 представляет аминокислотную последовательность линкера из 10 а.к.
SEQ ID NO: 18 представляет аминокислотную последовательность для сигнальной последовательности FimH J96.
SEQ ID NO: 19 представляет собой аминокислотную последовательность сигнального пептида SEQ ID NO: 5 (pSB02198 - сигнальный пептид FimH mIgK/F22..Q300 J96 FimH N28S V48C L55C N91S N249Q/линкер 7 А.К./FimG A1..K14/GGHis8 в pcDNA3.1(+)).
SEQ ID NO: 20 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH, в соответствии с SEQ ID NO: 5 (зрелый белок pSB02198 - сигнальный белок FimH mIgK/F22..Q300 J96 FimH N28S V48C L55C N91S N249Q/линкер 7 А.К./FimG A1..K14/GGHis8 в pcDNA3.1(+)).
SEQ ID NO: 21 представляет аминокислотную последовательность полипептида, полученного из E. coli FimG.
SEQ ID NO: 22 представляет аминокислотную последовательность сигнального пептида SEQ ID NO: 6 (pSB02307 - сигнальный пептид FimH mIgK/F22..Q300 J96 FimH N28S N91S N249Q/His8 в pcDNA3.1(+)).
SEQ ID NO: 23 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH, в соответствии с SEQ ID NO: 6 (зрелый белок сигнального белка FimH mIgK/F22..Q300 J96 FimH N28S N91S N249Q/His8 в pcDNA3. 1(+)).
SEQ ID NO: 24 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH, в соответствии с SEQ ID NO: 7 (зрелый белок конструкция pSB02083 лектинового домена FimH дикого типа).
SEQ ID NO: 25 представляет последовательность аминокислот для His-метки.
SEQ ID NO: 26 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH, в соответствии с SEQ ID NO: 8 (зрелый белок pSB02158 замкнутый мутант лектинового домена FimH).
SEQ ID NO: 27 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH (pSB01878).
SEQ ID NO: 28 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH (K12).
SEQ ID NO: 29 представляет аминокислотную последовательность полипептида, полученного из E. coli FimH (UTI89).
SEQ ID NO: 30 представляет аминокислотную последовательность O25b 2401 WzzB.
SEQ ID NO: 31 представляет аминокислотную последовательность O25a:K5:H1 WzzB.
SEQ ID NO: 32 представляет аминокислотную последовательность O25a ETEC ATCC WzzB.
SEQ ID NO: 33 представляет аминокислотную последовательность K12 W3110 WzzB.
SEQ ID NO: 34 представляет аминокислотную последовательность WzzB Salmonella LT2.
SEQ ID NO: 35 представляет аминокислотную последовательность O25b 2401 FepE.
SEQ ID NO: 36 представляет аминокислотную последовательность O25a:K5:H1 FepE.
SEQ ID NO: 37 представляет аминокислотную последовательность O25a ETEC ATCC FepE.
SEQ ID NO: 38 представляет аминокислотную последовательность O157 FepE.
SEQ ID NO: 39 представляет аминокислотную последовательность FepE Salmonella LT2.
SEQ ID NO: 40 представляет последовательность праймеров для LT2wzzB_S.
SEQ ID NO: 41 представляет последовательность праймеров для LT2wzzB_AS.
SEQ ID NO: 42 представляет последовательность праймеров для O25bFepE_S.
SEQ ID NO: 43 представляет последовательность праймеров для O25bFepE_A.
SEQ ID NO: 44 представляет последовательность праймеров для wzzB P1_S.
SEQ ID NO: 45 представляет последовательность праймеров для wzzB P2_AS.
SEQ ID NO: 46 представляет последовательность праймеров для wzzB P3_S.
SEQ ID NO: 47 представляет последовательность праймеров для wzzB P4_AS.
SEQ ID NO: 48 представляет последовательность праймеров для O157 FepE_S.
SEQ ID NO: 49 представляет последовательность праймеров для O157 FepE_AS.
SEQ ID NO: 50 представляет последовательность праймеров для pBAD33_adaptor_S.
SEQ ID NO: 51 представляет последовательность праймеров для pBAD33_adaptor_AS.
SEQ ID NO: 52 представляет последовательность праймеров для JUMPSTART_r.
SEQ ID NO: 53 представляет последовательность праймеров для gnd_f.
SEQ ID NO: 54 представляет аминокислотную последовательность для сигнальной последовательности мышиного IgK.
SEQ ID NO: 55 представляет аминокислотную последовательность сигнального пептида большой субъединицы p51 FcRn рецептора IgG человека.
SEQ ID NO: 56 представляет аминокислотную последовательность сигнального пептида белка IL-10 человека.
SEQ ID NO: 57 представляет аминокислотную последовательность сигнального пептида слияния гликопротеина F0 респираторно-синцитиального вируса А человека (штамм А2).
SEQ ID NO: 58 представляет аминокислотную последовательность сигнального пептида гемагглютинина вируса гриппа А.
SEQ ID NO: 59-101 представляют последовательности аминокислот и нуклеиновых кислот для родственного наноструктуре полипептида, или его фрагмента.
SEQ ID NO: 102-109 представляют последовательности SignalP 4.1 (DTU Bioinformatics) из различных видов, используемые для прогнозирования сигнальных пептидов.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном варианте осуществления, изобретение предлагает композицию, содержащую полипептид, полученный из FimH, или его фрагмент; и сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
В одном аспекте, композиция дополнительно содержит, по меньшей мере, один сахарид, полученный из любой одной K. pneumoniae, выбранный из группы, состоящей из O1, O2, O3 и O5. В другом аспекте, композиция дополнительно содержит сахарид, полученный из Klebsiella pneumoniae типа O1. В другом аспекте, композиция дополнительно содержит сахарид, полученный из K. pneumoniae типа О2. В другом аспекте, композиция дополнительно содержит сахарид, полученный из K. pneumoniae типа О3. В другом аспекте, композиция дополнительно содержит сахарид, полученный из K. pneumoniae типа О5. В другом аспекте, композиция дополнительно содержит сахарид, полученный из K. pneumoniae типа O1 и сахарид, полученный из K. pneumoniae типа О2.
В другом аспекте, композиция дополнительно содержит сахарид, полученный из K. pneumoniae, который конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгированный с белком-носителем.
В другом аспекте, композиция дополнительно содержит полипептид, полученный из K. pneumoniae.
В другом варианте осуществления изобретение предлагает композицию, содержащую полипептид, полученный из FimH, или его фрагмент; и, по меньшей мере, один сахарид, полученный из любой одной K. pneumoniae, выбранный из группы, состоящей из O1, O2, O3 и O5. В одном аспекте, композиция дополнительно содержит, по меньшей мере, один сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
В другом аспекте, где сахарид, полученный из K. pneumoniae, конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгирован с белком-носителем.
В еще одном аспекте, композиция дополнительно содержит полипептид, полученный из K. pneumoniae.
В другом варианте осуществления, изобретение предлагает композицию, содержащую, по меньшей мере, один сахарид, полученный из любого одного K. pneumoniae, выбранный из группы, состоящей из О1, О2, О3 и О5; и, по меньшей мере, один сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
В одном аспекте, композиция дополнительно содержит полипептид, полученный из FimH, или его фрагмент. В другом аспекте, сахарид E. coli содержит Формулу O8. В другом аспекте, сахарид E. coli содержит Формулу O9.
В еще одном аспекте, композиция дополнительно содержит полипептид, полученный из K. pneumoniae.
В одном аспекте вышеупомянутых вариантов осуществления, сахарид ковалентно связан с белком-носителем. В одном аспекте, сахарид дополнительно содержит группу 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO). В другом аспекте, где белок-носитель выбран из любого из CRM197, группы B дифтерийного токсина (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C TT, коклюшного анатоксина, холерного анатоксина или экзотоксина А из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы холерного токсина B (CTB), Streptococcus pneumoniae пневмолизина и его детоксицированных вариантов, AcrA C. jejuni, природных гликопротеинов C. jejuni и стрептококковой пептидазы C5a (SCP).
В другом варианте осуществления, изобретение относится к способу индукции иммунного ответа против Escherichia coli у млекопитающего, включающему введение млекопитающему эффективного количества композиции в соответствии с любым из приведенных выше вариантов осуществления и их аспектов. В одном аспекте, иммунный ответ включает опсонофагоцитарные антитела против E. coli. В другом аспекте, иммунный ответ защищает млекопитающее от инфекции E.coli.
В другом варианте осуществления, изобретение относится к способу индукции иммунного ответа против Klebsiella pneumoniae у млекопитающего, включающему введение млекопитающему эффективного количества композиции в соответствии с любым из приведенных выше вариантов осуществления и их аспектов. В одном аспекте, иммунный ответ включает опсонофагоцитарные антитела против Klebsiella pneumoniae. В другом аспекте, иммунный ответ защищает млекопитающее от инфекции Klebsiella pneumoniae.
Изобретатели преодолели трудности продуцирования полипептидов, полученных из белков адгезинов E. coli, путем использования клеток млекопитающих для экспрессии. Как показано в настоящем описании, на протяжении всего описания и в разделе «Примеры», было обнаружено, что экспрессия рекомбинантных полипептидов в клетках млекопитающих неизменно обеспечивает высокие выходы по сравнению с экспрессией полипептидов в E. coli. Кроме того, изобретатели неожиданно идентифицировали мутации и конструкции экспрессии для стабилизации рекомбинантных полипептидов и их фрагментов в желаемой конформации.
Блокирование первичных стадий инфекции, а именно прикрепления бактерий к рецепторам клеток-хозяев и колонизации поверхности слизистой оболочки, важно для профилактики, лечения и/или снижения вероятности бактериальных инфекций. Бактериальное прикрепление может включать взаимодействие между поверхностным бактериальным белком, называемым адгезином, и рецептором клетки-хозяина. Предыдущие доклинические исследования адгезина FimH (полученного из уропатогенной E. coli) подтвердили, что против адгезина вырабатываются антитела. Успехи в идентификации, характеризации и выделении адгезинов необходимы для профилактики инфекций, от среднего отита и кариеса до пневмонии и сепсиса.
Для продуцирования адгезивных белков, таких как FimH и их фрагменты, в промышленных масштабах необходимо идентифицировать подходящие конструкции и подходящие хозяева, чтобы полипептид и его фрагменты могли экспрессироваться в достаточных количествах в течение продолжительного периода времени и в предпочтительной конформации. Например, в некоторых вариантах осуществления, предпочтительная конформация рекомбинантного полипептида проявляет низкую аффинность (например, Kd ~ 300 мкМ) к мономаннозе. В некоторых вариантах осуществления, предпочтительная конформация проявляет высокую аффинность (например, Kd <1,2 мкМ) к мономаннозе.
Адгезиновые белки, полученные из E.coli, были рекомбинантно экспрессированы в клетках E.coli. Однако выходы были менее 10 мг/л. Очистка больших количеств адгезина, связанного с ворсинками, может быть сложной задачей, если он продуцируется в E. coli. Не ограничиваясь какой-либо теорией или механизмом, было высказано предположение, что продукт, экспрессируемый в E. coli, может иметь конформацию, которая не оптимальна для индукции эффективного иммунного ответа у млекопитающих.
В одном аспекте, изобретение включает рекомбинантную клетку млекопитающего, которая включает полинуклеотидную последовательность, кодирующую полипептид, полученный из бактериального адгезинового белка или его фрагмента.
В другом аспекте, изобретение включает способ получения полипептида или его фрагмента в клетке млекопитающего, включающий: (i) культивирование клетки млекопитающего в подходящих условиях, тем самым экспрессируя указанный полипептид или его фрагмент; и (ii) сбор указанного полипептида или его фрагмента из культуры. Способ может дополнительно включать очистку полипептида или его фрагмента. Также в настоящем документе описан полипептид или его фрагмент, полученный этим способом.
В другом аспекте, изобретение включает композицию, включающую описанный в настоящем документе полипептид или его фрагмент. Композиция может включать полипептид или его фрагмент, который подходит для введения in vivo. Например, полипептид или его фрагмент в такой композиции может иметь чистоту, по меньшей мере, 85%, по меньшей мере, 86%, по меньшей мере, 87%, по меньшей мере, 88%, по меньшей мере, 89%, по меньшей мере, 90%, по меньшей мере, 91%, по меньшей мере, 92%, по меньшей мере, 93%, по меньшей мере, 94%, по меньшей мере, 95%, по меньшей мере, 96%, по меньшей мере, 97%, по меньшей мере, 98% или по меньшей мере, 99% массовых. Композиция может дополнительно содержать адъювант.
В еще одном аспекте, изобретение включает композицию для индукции иммунного ответа против E. coli. Также описано применение композиции, описанной в настоящем документе, для индуцирования иммунного ответа против E.coli, и применение композиции, описанной в настоящем документе, в производстве лекарственного средства для индуцирования иммунного ответа против E.coli.
I. Полипептиды, полученные из E. coli, и их фрагменты
В одном аспекте, в настоящем документе описана клетка млекопитающего, которая включает полинуклеотид, кодирующий полипептид, полученный из E. coli, или его фрагмент. Используемый в настоящем документе термин «полученный из» относится к полипептиду, который содержит аминокислотную последовательность полипептида FimH или полипептидного комплекса FimCH или его фрагмента, как описано в настоящем документе, который был изменен путем введения замены, делеции или добавления аминокислотного остатка. Предпочтительно, полипептид, полученный из E.coli, или его фрагмент включает последовательность, имеющую, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность последовательности соответствующего полипептида или фрагмента FimH E. coli дикого типа. В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент имеет такую же общую длину аминокислот, что и соответствующий полипептид FimH дикого типа или полипептидный комплекс FimCH или их фрагмент.
Фрагменты должны включать, по меньшей мере, n последовательных аминокислот из последовательностей и, в зависимости от конкретной последовательности, n равно 7 или более (например, 8, 10, 12, 14, 16, 18, 20 или более). Предпочтительно, фрагменты включают эпитоп из последовательности. В некоторых вариантах осуществления фрагмент включает аминокислотную последовательность из, по меньшей мере, 50 последовательных аминокислотных остатков, по меньшей мере, 100 последовательных аминокислотных остатков, по меньшей мере, 125 последовательных аминокислотных остатков, по меньшей мере, 150 последовательных аминокислотных остатков, по меньшей мере, 175 последовательных аминокислотных остатков, по меньшей мере, 200 последовательных аминокислотных остатков или, по меньшей мере, 250 последовательных аминокислотных остатков аминокислотной последовательности полипептида, полученного из E.coli.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент включает одну или несколько неклассических аминокислот по сравнению с соответствующим полипептидом или фрагментом FimH E. coli дикого типа.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент обладают аналогичной или идентичной функцией соответствующего полипептида FimH дикого типа или его фрагмента.
В предпочтительном варианте осуществления, полипептиды или полипептидные комплексы или их фрагменты по изобретению выделяют или очищают.
В некоторых вариантах осуществления, полинуклеотид, кодирующий полипептид, полученный из E. coli, или его фрагмент интегрируется в геномную ДНК клетки млекопитающего, и, при культивировании в подходящих условиях, указанный полипептид, полученный из E. coli, или его фрагмент экспрессируется клеткой млекопитающего.
В предпочтительном варианте осуществления, полипептид, полученный из E. coli, или его фрагмент растворим.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент секретируется из клетки-хозяина млекопитающего.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент могут включать дополнительные аминокислотные остатки, такие как N-концевые или C-концевые удлинения. Такие удлинения могут включать одну или несколько меток, которые могут облегчить обнаружение (например, эпитопную метку для обнаружения моноклональными антителами) и/или очистку (например, полигистидиновую метку, позволяющую проводить очистку на никельхелатирующей смоле) полипептида или его фрагмента.. В некоторых вариантах осуществления, метка включает аминокислотную последовательность, выбранную из любой из SEQ ID NO: 21 и SEQ ID NO: 25. Такие метки для аффинной очистки известны в данной области техники. Примеры меток аффинной очистки включают, например, метку His (гексагистидин, который может, например, связываться с ионом металла), белок, связывающий мальтозу (MBP), который может, например, связываться с амилозой, глутатион-S-трансферазу (GST), которая может, например, связываться с глутатионом, метку FLAG, которая может, например, связываться с анти-flag антителом), метку Strep, которая может, например, связываться со стрептавидином или его производным). В предпочтительных вариантах осуществления, полипептид, полученный из E.coli, или его фрагмент не включает дополнительные аминокислотные остатки, такие как N-концевые или С-концевые удлинения. В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент, описанный в настоящем документе, не включает последовательность экзогенной метки.
Хотя в настоящем документе могут быть указаны конкретные штаммы E.coli, следует понимать, что полипептид, полученный из E.coli, или его фрагмент не ограничиваются конкретными штаммами, если не указано иное.
В некоторых вариантах осуществления, полипептид, полученный из E. coli FimH, или его фрагмент включает остаток фенилаланина на N-конце полипептида. В некоторых вариантах осуществления, полипептид, полученный из FimH или его фрагмента, включает остаток фенилаланина в пределах первых 20 положений остатков на N-конце. Предпочтительно, остаток фенилаланина расположен в положении 1 полипептида. Например, в некоторых вариантах осуществления полипептид, полученный из E.coli FimH, или его фрагмент не включает дополнительный остаток глицина на N-конце полипептида, полученного из E.coli FimH, или его фрагмента.
В некоторых вариантах осуществления, фенилаланиновый остаток в положении 1 зрелого FimH E. coli дикого типа заменен алифатической гидрофобной аминокислотой, такой как, например, любой из остатков Ile, Leu и Val.
В некоторых вариантах осуществления, сигнальный пептид может применяться для экспрессирования полипептида, полученного из E. coli или его фрагмента. Сигнальные последовательности и кассеты экспрессии для продуцирования белков известны в данной области техники. Как правило, лидерные пептиды имеют длину от 5 до 30 аминокислот и обычно присутствуют на N-конце вновь синтезированного полипептида. Сигнальный пептид обычно содержит длинный участок гидрофобных аминокислот, который имеет тенденцию к образованию одиночной альфа-спирали. Кроме того, многие сигнальные пептиды начинаются с короткого положительно заряженного участка аминокислот, что может помочь обеспечить правильную топологию полипептида во время транслокации. На конце сигнального пептида обычно находится участок аминокислот, который распознается и расщепляется сигнальной пептидазой. Сигнальная пептидаза может расщепляться во время или после завершения транслокации с образованием свободного сигнального пептида и зрелого белка. В некоторых вариантах осуществления, сигнальный пептид включает аминокислотную последовательность, имеющую, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 99,9% или 100% идентичность любой из SEQ ID NO: 9, SEQ ID NO: 18, SEQ ID NO: 19 и SEQ ID NO: 22.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент описанный в настоящем документе, может включать расщепляемый линкер. Такие линкеры позволяют отделить метку от очищенного комплекса, например, путем добавления агента, способного расщеплять линкер. Расщепляемые линкеры известны в данной области техники. Такие линкеры могут быть расщеплены, например, путем облучения фотолабильной связи или гидролиза, катализируемого кислотой. Другой пример расщепляемого линкера включает полипептидный линкер, который включает сайт распознавания протеазы и может быть расщеплен путем добавления подходящего фермента протеазы.
В некоторых вариантах осуществления полипептид, полученный из E. coli, или его фрагмент включает модификацию по сравнению с соответствующим полипептидом или фрагментом FimH E. coli дикого типа. Модификация может включать ковалентное присоединение молекулы к полипептиду. Например, такие модификации могут включать гликозилирование, ацетилирование, пэгилирование, фосфорилирование, амидирование, дериватизацию известными защитными/блокирующими группами, протеолитическое расщепление, связывание с клеточным лигандом или другим белком и т.д. В некоторых вариантах осуществления полипептид, полученный из E. coli или его фрагмент может включать модификацию, такую как химическая модификация с использованием способов, известных специалистам в данной области техники, включая, но не ограничиваясь ими, специфическое химическое расщепление, ацетилирование, формилирование, метаболический синтез туникамицина и т.д. по сравнению с соответствующим полипептидом FimH E. coli дикого типа или его фрагментом. В другом варианте осуществления, модификация может включать ковалентное присоединение молекулы липида к полипептиду. В некоторых вариантах осуществления, полипептид не включает ковалентное присоединение молекулы к полипептиду по сравнению с соответствующим полипептидом FimH E. coli дикого типа, или его фрагментом.
Например, белки и полипептиды, продуцируемые в клеточной культуре, могут быть гликопротеинами, которые содержат ковалентно связанные углеводные структуры, включая олигосахаридные цепи. Эти олигосахаридные цепи связаны с белком либо N-связями, либо O-связями. Олигосахаридные цепи могут составлять значительную часть массы гликопротеина. Как правило, N-связанный олигосахарид добавляют к аминогруппе на боковой цепи остатка аспарагина в целевой консенсусной последовательности Asn-X-Ser/Thr, где X может быть любой аминокислотой, кроме пролина. В некоторых вариантах осуществления, сайт гликозилирования включает аминокислотную последовательность, выбранную из любой из следующих: аспарагин-глицин-треонин (NGT), аспарагин-изолейцин-треонин (NIT), аспарагин-глицин-серин (NGS), аспарагин-серин-треонин (NST) и аспарагин-треонин-серин (NTS). Полипептид, полученный из E.coli, или его фрагмент, продуцируемый в клетках млекопитающих, может быть гликозилирован. Гликозилирование может происходить по N-связанному сигналу гликозилирования Asn-Xaa-Ser/Thr в последовательности полипептида, полученного из E.coli, или его фрагмента. «N-связанное гликозилирование» относится к присоединению углеводного фрагмента через GIcNAc к аспарагиновому остатку в полипептидной цепи. N-связанный углевод содержит обычную структуру ядра Man 1-6(Man1-3)Manβ1-4GlcNAcβ1-4GlcNAcβ-R, где R представляет собой аспарагиновый остаток продуцируемого полипептида, полученного из E. coli, или его фрагмента.
В некоторых вариантах осуществления, сайт гликозилирования в полипептиде, полученном из E.coli, или его фрагменте удален посредством мутации в последовательности полипептида, полученного из E.coli, или его фрагмента. Например, в некоторых вариантах осуществления остаток Asn мотива гликозилирования (Asn-Xaa-Ser/Thr) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления замена остатка выбрана из любого из Ser, Asp, Thr и Gln.
В некоторых вариантах осуществления, остаток Ser мотива гликозилирования может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, замена остатка выбрана из любого из Asp, Thr и Gln.
В некоторых вариантах осуществления, остаток Thr мотива гликозилирования может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления замена остатка выбрана из любого из Ser, Asp и Gln.
В некоторых вариантах осуществления, сайт гликозилирования (такой как Asn-Xaa-Ser/Thr) в полипептиде, полученном из E. coli, или его фрагменте не удаляют и не модифицируют. В некоторых вариантах осуществления, в среду для культивирования клеток можно добавить соединение для снижения или ингибирования гликозилирования. В таких вариантах осуществления, полипептид или белок содержит, по меньшей мере, еще один негликозилированный (т.е. агликозилированный) сайт, то есть полностью незанятый гликановый сайт, к которому не присоединена углеводная группа, или содержит, по меньшей мере, на один углеводный фрагмент меньше в том же потенциальном сайте гликозилирования, чем идентичный полипептид или белок, который продуцируется клеткой в идентичных условиях, но в отсутствие соединения, ингибирующего гликозилирование. Такие соединения известны в данной области техники и могут включать, помимо прочего, туникамицин, гомологи туникаймицина, стрептовирудин, микоспоцидин, амфомицин, цусимицин, антибиотик 24010, антибиотик ММ 19290, бацитрацин, коринетоксин, шоудомицин, дуимицин, 1-дезоксиманноноджиримицин, дезоксиноджиримицин, N-метил-1-дексойманноджиримицин, брефельдин А, аналоги глюкозы и маннозы, 2-дезокси-D-глюкозу, 2-дезоксиглюкозу, D-(+)-маннозу, D-(+) галактозу, 2-дезокси-2-фтор-D-глюкозу, 1,4-дидезокси-1,4-имино-D-маннит (DIM), фторглюкозу, фторманнозу, UDP-2-дезоксиглюкозу, GDP-2-дезоксиглюкозу, ингибиторы гидроксиметилглутарил-СоА-редуктазы, 25-гидроксихолестерин, гидроксихолестерин, свайнсонин, циклогексимид, пуромицин, актиномицин D, монензин, м-хлоркарбонилцианид фенилгидразон (CCCP), компактин, долихил-фосфорил-дезоксиглюкозу, N-ацетил-D-глюкозамин, гигоксантин, тимидин, холестерин, глюкозамин, маннозамин, кастаноспермин, глутамин, бромокондурит, кондуритол эпоксид и производные кондуритола, гликозилметил-п-нитрофенилтриазены, β-гидроксинорвалин, трео-β-фтораспарагин, δ-лактон D-(+)-глюконовой кислоты, ди(2-этилгексил)фосфат, трибутилфосфат, додецилфосфат, 2-диметиламиноэтиловый эфир (дифенилметил)-фосфорной кислоты, йодид [2-(дифенилфосфинилокси)этил]триметиламмония, йодоацетат и/или фторацетат. Специалист в данной области техники легко распознает или сможет определить ингибирующие гликозилирование вещества, которые могут использоваться в соответствии со способами и композициями по настоящему изобретению без ненужных экспериментов. В таких вариантах осуществления, гликозилирование полипептида или его фрагмента можно контролировать без введения аминокислотной мутации в полипептид или его фрагмент.
В некоторых вариантах осуществления, уровень гликозилирования (например, количество гликановых сайтов, которые заняты на полипептиде или его фрагменте, размер и/или сложность гликоформы в этом сайте и подобные) полипептида или его фрагмента, продуцируемого клетки млекопитающих, ниже, чем уровни гликозилирования полипептида или его фрагмента, продуцируемые в идентичных во всем остальном условиях в идентичной во всем остальном среде, в которой отсутствует такое соединение, ингибирующее гликолиз, и/или мутация.
В некоторых вариантах осуществления, последовательность полипептида, полученного из E.coli, или его фрагмента не включает сайт гликозилирования N-связанного белка. В некоторых вариантах осуществления, последовательность полипептида, полученного из E.coli, или его фрагмента не включает, по меньшей мере, один сайт гликозилирования N-связанного белка. В некоторых вариантах осуществления, последовательность полипептида, полученного из E.coli, или его фрагмента не включает какие-либо сайты гликозилирования N-связанного белка. В некоторых вариантах осуществления, последовательность полипептида, полученного из E. coli, или его фрагмента включает сайт гликозилирования N-связанного белка. В некоторых вариантах осуществления, последовательность полипептида, полученного из E. coli, или его фрагмента включает не более 1 сайта гликозилирования N-связанного белка. В некоторых вариантах осуществления, последовательность полипептида, полученного из E. coli, или его фрагмента включает не более 2 сайтов гликозилирования N-связанного белка.
Полипептид, полученный из E.coli, или его фрагмент, экспрессируемый различными клеточными линиями или у трансгенных животных, может иметь различные по сравнению друг с другом занятости гликановых сайтов, гликоформы и/или паттерны гликозилирования. В некоторых вариантах осуществления, изобретение охватывает полипептид, полученный из E.coli, или его фрагмент, независимо от гликозилирования, присутствия гликана или структуры гликоформ полипептида, полученного из E.coli, или его фрагмента, продуцируемого в клетке млекопитающего.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент может быть получен из полипептида E. coli FimH, где аминокислотный остаток в положении 1 полипептида представляет собой фенилаланин, а не метионин, например, полипептид, имеющий аминокислотную последовательность SEQ ID NO: 2. Предпочтительно, полипептид, полученный из E.coli FimH, содержит фенилаланин в положении 1 аминокислотной последовательности полипептида, полученного из E.coli. В другом предпочтительном варианте осуществления, полипептид, полученный из E.coli FimH, содержит аминокислотную последовательность SEQ ID NO: 3, где, предпочтительно, остаток в положении 1 аминокислотной последовательности полипептида, полученного из E.coli, представляет собой фенилаланин. В некоторых вариантах осуществления, полипептид, полученный из E.coli, или его фрагмент может включать аминокислотную последовательность SEQ ID NO: 4, которая может быть получена из полипептида FimH E.coli.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент включает аминокислотную последовательность, имеющую, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 99,9% или 100% идентичность любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28 и SEQ ID NO: 29. В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент может быть получен из FimG полипептида E. coli, например, имеющего аминокислотную последовательность SEQ ID NO: 9. В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент может быть получен из FimC полипептида E. coli, например, имеющего аминокислотную последовательность SEQ ID NO: 10.
А. Полипептиды, полученные из FimH E. coli, и их фрагменты
Бактериальные фимбриальные адгезины FimH и FmlH позволяют Escherichia coli использовать различные микросреды мочевыводящих путей посредством распознавания специфических гликопротеинов клеток-хозяев. FimH связывается с манозилированными рецепторами уроплакина в уроэпителии, тогда как FmlH связывается с галактозой или N-ацетилгалактозамин-О-гликанами на эпителиальных поверхностных белках в почках и воспаленном мочевом пузыре. Фимбрии FimH также играют роль в колонизации энтеротоксигенной E.coli (ETEC) и инвазивной E.coli с множественной лекарственной резистентностью в кишечнике посредством связывания с высокоманнозилированными белками на кишечном эпителии.
Полноразмерный FimH состоит из двух доменов: N-концевого лектинового домена и С-концевого пилинового домена, которые соединены коротким линкером. Лектиновый домен FimH содержит домен распознавания углеводов, который отвечает за связывание с маннозилированным уроплакином 1a на поверхности уротелиальных клеток. Пилиновый домен прикрепляется к ядру пилуса через донорную цепь последующей субъединицы FimG, что представляет собой процесс, называемый комплементацией донорной цепи.
Конформация и лиганд-связывающие свойства лектинового домена FimH находятся под аллостерическим контролем пилинового домена FimH. В статических условиях, взаимодействие двух доменов полноразмерного FimH стабилизирует лектиновый домен в области низкой аффинности к мономаннозе (например, Kd ~ 300 мкМ), которое характеризуется неглубоким карманом связывания. Связывание с маннозидным лигандом вызывает конформационные изменения, ведущие к состоянию средней аффинности, при котором лектиновый и пилиновый домены остаются в тесном контакте. Однако при напряжении сдвига лектиновый и пилиновый домены разделяются, тем самым вызывая состояние высокой аффинности (например, Kd <1,2 мкМ).
Из-за отсутствия отрицательной аллостерической регуляции, осуществляемой пилиновым доменом, выделенный лектиновый домен FimH заблокирован в высокоаффинном состоянии. Выделенный рекомбинантный лектиновый домен, который заблокирован в высокоаффинном состоянии, проявляет высокую стабильность. Однако блокировка адгезина в конформации с низким уровнем связывания индуцирует выработку ингибирующих адгезию антител. Соответственно, существует интерес к стабилизации лектинового домена в низкоаффинном состоянии.
Существует дополнительный интерес к способам экспрессии FimH с высокими выходами, достаточными для разработки продукта. Препятствием для разработки композиций, содержащих FimH, является низкий выход, достигаемый при экспрессии FimH в нативном состоянии в периплазме E. coli. Типовые выходы, указанные в лабораторных условиях, составляют 3-5 мг/л для очищенного комплекса FimCH и 4-10 мг/л для FimH(LD), что ниже уровней, которые считаются масштабируемыми для производства материала для клинических испытаний. Конформация FimH in vivo отличается от конформации очищенной рекомбинантной формы белка. В общем, FimH имеет нативную конформацию, которая, по меньшей мере, частично определяется взаимодействием in vivo FimH с его периплазматическим белком теплового шока, называемым FimC.
Рекомбинантное продуцирование FimH остается сложной задачей. Экспрессия и очистка белков не является рутинным процессом.
В предпочтительном варианте осуществления, полипептид или его фрагмент происходят из FimH E. coli. В некоторых вариантах осуществления, полипептид или его фрагмент включает полноразмерный FimH E. coli. Полноразмерный FimH включает два домена: N-концевой лектиновый домен и С-концевой пилиновый домен, которые соединены коротким линкером. В некоторых вариантах осуществления, полная длина FimH E.coli включает 279 аминокислот, что включает полную длину зрелого белка FimH E.coli. В некоторых вариантах осуществления, полная длина FimH E.coli включает 300 аминокислот, что включает полную длину зрелого белка FimH E.coli и последовательность сигнального пептида, имеющую длину 21 аминокислоту. Первичная структура FimH дикого типа длиной 300 аминокислот высоко консервативна во всех штаммах E. coli.
Типовой последовательностью для полноразмерного FimH E. coli является SEQ ID NO: 1. Полноразмерная последовательность FimH включает последовательность лектинового домена и последовательность пилинового домена. Лектиновый домен FimH содержит домен распознавания углеводов, который отвечает за связывание с маннозилированным уроплакином 1a на поверхности уротелиальных клеток. Пилиновый домен прикрепляется к ядру пилуса через донорную цепь последующей субъединицы FimG, что представляет собой процесс, называемый комплементацией донорной цепи.
Начиная с N-конца, названия и в скобках иллюстративные аминокислотные последовательности каждого домена полноразмерного FimH следующие: лектин FimH (SEQ ID NO: 2) и пилин FimH (SEQ ID NO: 3).
Другие подходящие полипептиды и их фрагменты, полученные из E. coli FimH, включают варианты, которые имеют различную степень идентичности с любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29, такую, как, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29. В некоторых вариантах осуществления, варианты белков FimH: (i) образуют часть FimH-FimC; (ii) содержат, по меньшей мере, один эпитоп из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29; и/или (iii) могут индуцировать антитела in vivo, которые иммунологически перекрестно реагируют с FimH E. coli.
В некоторых вариантах осуществления композиция включает полипептид, содержащий, по меньшей мере, n последовательных аминокислот из любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29, где n равно 7 или более (например, 8, 10, 12, 14, 16, 18, 20 и более). Предпочтительно, фрагменты включают эпитоп из последовательности. В некоторых вариантах осуществления, композиция включает полипептид, содержащий, по меньшей мере, 50 последовательных аминокислотных остатков, по меньшей мере, 100 последовательных аминокислотных остатков, по меньшей мере, 125 последовательных аминокислотных остатков, по меньшей мере, 150 последовательных аминокислотных остатков, по меньшей мере, 175 последовательных аминокислотных остатков, по меньшей мере, по меньшей мере, 200 последовательных аминокислотных остатков или по меньшей мере, 250 последовательных аминокислотных остатков аминокислотной последовательности любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29.
В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 1. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 2. В некоторых вариантах осуществления, композиция включает полипептид, имеющий по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 3. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 4. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 20. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 23. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность SEQ ID NO: 24. В некоторых вариантах осуществления, композиция включает полипептид, содержащий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 26. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 28. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 30.
Другой пример подходящего полипептида и его фрагментов, полученных из E. coli FimH, описанных в настоящем документе, показан как SEQ ID NO: 2, в котором отсутствует N-концевая сигнальная последовательность дикого типа, и он соответствует аминокислотным остаткам 22-300 SEQ ID NO: 1. Другой пример фрагмента FimH включает всю N-концевую сигнальную последовательность и зрелый белок, как указано в SEQ ID NO: 1.
В некоторых вариантах осуществления, сайт гликозилирования в полипептиде, полученном из E.coli, или его фрагменте, удален посредством мутации в последовательности полипептида, полученного из E.coli, или его фрагмента. Например, в некоторых вариантах осуществления, остаток Asn в положении 7 зрелого полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 2) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, остаток Asn в положении 7 лектинового домена полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 3) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления замена остатка выбрана из любого из Ser, Asp, Thr и Gln.
В некоторых вариантах осуществления, остаток Thr в положении 10 зрелого полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 2) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, остаток Thr в положении 7 лектинового домена полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 3) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, замена остатка выбрана из любого из Ser, Asp и Gln.
В некоторых вариантах осуществления, остаток Asn в положении N235 зрелого полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 2) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, остаток Asn в положении N228 зрелого полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 2) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, замена остатка выбрана из любого из Ser, Asp, Thr и Gln.
В некоторых вариантах осуществления, остаток Asn в положении 70 зрелого полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 2) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, остаток Asn в положении 70 лектинового домена полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 3) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, замена остатка выбрана из любого из Ser, Asp, Thr и Gln.
В некоторых вариантах осуществления, остаток Ser в положении 72 зрелого полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 2) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, остаток Ser в положении 72 лектинового домена полипептида FimH E. coli (например, в соответствии с нумерацией SEQ ID NO: 3) может быть мутирован, предпочтительно путем замены. В некоторых вариантах осуществления, замена остатка выбрана из любого из Asp, Thr и Gln.
Используемый в настоящем документе термин «фрагмент» относится к полипептиду и определяется как любая дискретная часть данного полипептида, которая уникальна или характерна для этого полипептида. Используемый в настоящем документе термин также относится к любой отдельной части данного полипептида, которая сохраняет, по меньшей мере, часть активности полноразмерного полипептида. В некоторых вариантах осуществления, доля сохраняемой активности составляет, по меньшей мере, 10% активности полноразмерного полипептида. В некоторых вариантах осуществления, доля сохраняемой активности составляет, по меньшей мере, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% активности полноразмерного полипептида. В некоторых вариантах осуществления, доля сохраняемой активности составляет, по меньшей мере, 95%, 96%, 97%, 98% или 99% активности полноразмерного полипептида. В некоторых вариантах осуществления, доля сохраняемой активности составляет 100% или более от активности полноразмерного полипептида. В некоторых вариантах осуществления, фрагмент включает, по меньшей мере, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более последовательных аминокислот полноразмерного полипептида.
В. Комплекс FimH, FimC и их фрагментов
В некоторых вариантах осуществления, полипептид, полученный из E.coli FimH, или его фрагмент присутствует в комплексе с полипептидом, полученным из E.coli. FimC или его фрагментом. В предпочтительном варианте осуществления, полипептид, полученный из E. coli FimH или его фрагмент, и полипептид, полученный из E. coli FimC или его фрагмент присутствуют в комплексе, предпочтительно, в соотношении 1:1 в комплексе. Не ограничиваясь какой-либо теорией или механизмом, полноразмерный FimH может быть стабилизирован в активной конформации с помощью периплазматического белка теплового шока FimC, что делает возможным очистку полноразмерного белка FimH. Соответственно, в некоторых вариантах осуществления, полипептид или его фрагмент включает полноразмерный FimH и полноразмерный FimC.
В некоторых вариантах осуществления, полипептид или его фрагмент включает фрагмент FimH и фрагмент FimC. В некоторых вариантах осуществления, полипептид или его фрагмент включает полноразмерный FimH и фрагмент FimC. Типовая последовательность FimC E.coli представлена в SEQ ID NO: 10. В некоторых вариантах осуществления, полипептид, полученный из E.coli, или его фрагмент включает комплексообразующие фрагменты FimH.
Комплексообразующий фрагмент FimH может представлять собой любую часть или часть белка FimH, которые сохраняют способность образовывать комплекс с FimC или его фрагментом. Подходящий комплексообразующий фрагмент FimH также может быть получен или определен с помощью стандартных анализов, известных в данной области техники, таких как ко-иммунопреципитация, перекрестное связывание или совместная локализация с помощью флуоресцентного окрашивания и т.д. SDS-PAGE или вестерн-блотинг также могут быть использованы. (например, показывая, что фрагмент FimH и FimC или его фрагмент находятся в комплексе, что подтверждается гель-электрофорезом). В некоторых вариантах осуществления, комплексообразующий фрагмент FimH (i) образует часть комплекса FimH-FimC; (ii) содержит, по меньшей мере, один эпитоп из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 10, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29; и/или (iii) может индуцировать антитела in vivo, которые иммунологически перекрестно реагируют с FimH E. coli.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент включает полноразмерный FimH, где FimH не находится в комплексе с FimC. В дополнительных вариантах осуществления, полипептид или его фрагмент включает фрагмент FimH, где фрагмент не образует комплекс с FimC. В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент FimC включает SEQ ID NO: 10. В некоторых вариантах осуществления, комплекс может быть экспрессирован из одной и той же плазмиды, предпочтительно, под контролем отдельных промоторов для каждого полипептида или его фрагмента.
В некоторых вариантах осуществления, полипептид, полученный из FimH E. coli, или его фрагмента, связывается с полипептидом, полученным из FimC E. coli, или его фрагментом, который может быть встроен в структуру полипептида, полученного из E. coli. FimH или его фрагмента. Часть молекулы FimC, которая связывается с FimH в комплексе, называется «донорной цепью», и механизм образования нативной структуры FimH с использованием цепи из FimC, которая связывается с FimH в комплексе FimCH, известен как «комплементация донорной цепи».
В некоторых вариантах осуществления, полипептид, полученный из FimH E. coli, или его фрагмент может быть экспрессирован соответствующей версией FimH, комплементированной донорной цепью, где аминокислотная последовательность FimC, которая взаимодействует с FimH в комплексе FimCH, сама сконструирована в C-конце FimH для обеспечения нативной конформации без необходимости присутствия остатка молекулы FimC. В некоторых вариантах осуществления, полипептид, полученный из FimH E. coli, или его фрагмент может быть экспрессирован в форме комплекса, который включает его изолированные домены, такие как лектинсвязывающий домен и пилиновый домен, и такие домены могут быть связаны друг с другом ковалентно или нековалентно. Например, в некоторых вариантах осуществления, связывающий сегмент может включать аминокислотные последовательности или другие олигомерные структуры, в том числе, простые полимерные структуры.
Способы и композиции по изобретению могут включать описанные в настоящем документе комплексы, в которых указанные полипептиды или их фрагменты, полученные из E. coli, коэкспрессируются или образуются в комбинированном состоянии.
С. Лектиновый домен, пилиновый домен и их варианты
Конформация и лиганд-связывающие свойства лектинового домена FimH могут находиться под аллостерическим контролем пилинового домена FimH. В статических условиях, взаимодействие двух доменов полноразмерного FimH стабилизирует лектиновый домен в состоянии с низким сродством к мономаннозе (например, Kd ~ 300 мкМ), для которого характерен неглубокий карман связывания. Связывание с маннозидным лигандом может вызывать конформационные изменения, ведущие к состоянию средней аффинности, при котором лектиновый и пилиновый домены остаются в тесном контакте. Однако при напряжении сдвига лектиновый и пилиновый домены могут разделяться и индуцировать состояние высокого сродства (например, Kd <1,2 мкМ).
Из-за отсутствия отрицательной аллостерической регуляции, осуществляемой пилиновым доменом, изолированный лектиновый домен FimH заблокирован в высокоаффинном состоянии (например, Kd <1,2 мкМ). Изолированный рекомбинантный лектиновый домен, который заблокирован в высокоаффинном состоянии. Блокировка адгезина в низкоаффинной конформации (например, Kd ~ 300 мкМ), однако, индуцирует выработку ингибирующих адгезию антител. Соответственно, существует интерес к стабилизации лектинового домена в низкоаффинном состоянии.
В некоторых вариантах осуществления, полипептид, полученный из E.coli, или его фрагмент включает лектиновый домен FimH E.coli. Примеры последовательностей лектинового домена включают любую из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 24 и SEQ ID NO: 26. В некоторых вариантах осуществления, лектиновый домен E. coli FimH включает цистеиновые замены. В предпочтительном варианте осуществления, лектиновый домен FimH E. coli включает цистеиновые замены в первых 50 аминокислотных остатках лектинового домена. В некоторых вариантах осуществления, лектиновый домен может включать 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 цистеиновых замен. Предпочтительно, лектиновый домен включает 2 цистеиновых замены. См., например, pSB02158 и pSB02198.
Другие подходящие полипептиды и их фрагменты, полученные из FimH E. coli, включают варианты лектинового домена FimH, которые имеют различную степень идентичности с SEQ ID NO: 3, такую как, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность последовательности, указанной в SEQ ID NO: 3. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность SEQ ID NO: 3. В некоторых вариантах осуществления, полипептид, полученный из E.coli, или его фрагмент включает пилиновый домен FimH E.coli. Другие подходящие полипептиды и их фрагменты, полученные из FimH E. coli, включают варианты пилинового домена FimH, которые имеют различную степень идентичности с SEQ ID NO: 7, такую как, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность последовательности, указанной в SEQ ID NO: 7. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность SEQ ID NO: 4. Другие подходящие полипептиды и их фрагменты, полученные из FimH E. coli, включают варианты лектинового домена FimH, которые имеют различную степень идентичности с SEQ ID NO: 8, такую как, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность к последовательности, указанной в SEQ ID NO: 8. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность с SEQ ID NO: 8. В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент включает пилиновый домен FimH E. coli. Другие подходящие полипептиды и их фрагменты, полученные из FimH E. coli, включают варианты пилинового домена FimH, которые имеют различную степень идентичности с SEQ ID NO: 24, такую как, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность последовательности, указанной в SEQ ID NO: 24. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность SEQ ID NO: 24. Другие подходящие полипептиды и их фрагменты, полученные из FimH E. coli, включают варианты лектинового домена FimH, которые имеют различную степень идентичности с SEQ ID NO: 26, такую как, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность последовательности SEQ ID NO: 26. В некоторых вариантах осуществления, композиция включает полипептид, имеющий, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 99,9% идентичность SEQ ID NO: 26.
В некоторых вариантах осуществления, композиция включает полипептид, содержащий, по меньшей мере, n последовательных аминокислот из любой из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 24 и SEQ ID NO: 26., где n равно 7 или более (например, 8, 10, 12, 14, 16, 18, 20 или более). Предпочтительно, фрагменты включают эпитоп из последовательности. В некоторых вариантах осуществления, композиция включает полипептид, содержащий, по меньшей мере, 50 последовательных аминокислотных остатков, по меньшей мере, 100 последовательных аминокислотных остатков, по меньшей мере, 125 последовательных аминокислотных остатков, по меньшей мере, 150 последовательных аминокислотных остатков, по меньшей мере, 175 последовательных аминокислотных остатков, по меньшей мере, 200 последовательных аминокислотных остатков или, по меньшей мере, 250 последовательных аминокислотных остатков аминокислотной последовательности любой из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 24 и SEQ ID NO: 26.
Расположение и длину лектинового домена E. coli FimH или его гомолога или варианта можно предсказать на основе попарного выравнивания его последовательности с любой из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 24 и SEQ ID NO: 26, например, путем сопоставления аминокислотной последовательности FimH с SEQ ID NO: 1 и идентификации последовательности, которая соответствует остаткам 22-179 SEQ ID NO: 1.
D. N-концевая сигнальная последовательность дикого типа
В некоторых вариантах осуществления, N-концевая сигнальная последовательность дикого типа полноразмерного FimH расщепляется в клетке-хозяине с образованием зрелого полипептида FimH. Таким образом, FimH, экспрессируемый клеткой-хозяином, может не иметь N-концевой сигнальной последовательности. В предпочтительных вариантах осуществления полипептид, полученный из E. coli, или его фрагмент могут кодироваться нуклеотидной последовательностью, в которой отсутствует кодирующая последовательность для N-концевой сигнальной последовательности дикого типа.
В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент включает фрагменты FimH, образующие комплекс FimH-FimC, N-концевую сигнальную последовательность (например, остатки 1-21 SEQ ID NO: 1) или их сочетание. Комплексообразующий фрагмент FimH может представлять собой любую часть или участок белка FimH, который сохраняет способность образовывать комплекс с FimC.
В некоторых вариантах осуществления, в полипептиде, полученном из E. coli, или его фрагменте может отсутствовать от 1 до 21 аминокислотного остатка (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 аминокислотный остаток или отсутствовать 1-21 остаток, 1-20 остатков, 1-15 остатков, 1-10 остатков, 2-20 остатков, 2-15 остатков, 2-10 остатков, 5-20 остатков, 5-15 остатков или 5-10 остатков) на N-конце и/или С-конце полноразмерного полипептида FimH, который может включать сигнальную последовательность, лектиновый домен и пилиновый домен.
II. Нуклеиновые кислоты
В одном аспекте, описаны нуклеиновые кислоты, кодирующие полипептид, полученный из E.coli, или его фрагмент. Одну или несколько конструкций нуклеиновых кислот, кодирующих полипептид, полученный из E.coli, или его фрагмент, можно использовать для геномной интеграции и последующей экспрессии полипептида, полученного из E.coli, или его фрагмента. Например, в клетку-хозяин можно ввести единственную конструкцию нуклеиновой кислоты, кодирующую полипептид, полученный из E. coli, или его фрагмент. Альтернативно, кодирующие последовательности для полипептида, полученного из E. coli, или его фрагмента могут быть перенесены двумя или несколькими конструкциями нуклеиновой кислоты, которые затем вводятся в клетку-хозяин одновременно или последовательно.
Например, в одном иллюстративном варианте осуществления, одна конструкция нуклеиновой кислоты кодирует лектиновый домен и пилиновый домен FimH E. coli. В другом типовом варианте осуществления, одна конструкция нуклеиновой кислоты кодирует лектиновый домен, и вторая конструкция нуклеиновой кислоты кодирует пилиновый домен FimH E. coli. В некоторых вариантах осуществления, достигается геномная интеграция.
Конструкция нуклеиновой кислоты может содержать геномную ДНК, содержащую один или несколько интронов, или кДНК. Некоторые гены экспрессируются более эффективно, когда присутствуют интроны. В некоторых вариантах осуществления, последовательность нуклеиновой кислоты пригодна для экспрессии экзогенных полипептидов в указанной клетке млекопитающего.
В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая полипептид или его фрагмент, является кодон-оптимизированной для повышения уровня экспрессии в любой конкретной клетке.
В некоторых вариантах осуществления, конструкция нуклеиновой кислоты включает сигнальную последовательность, которая кодирует пептид, управляющий секрецией полипептида, полученного из E. coli, или его фрагмента. В некоторых вариантах осуществления, нуклеиновая кислота включает нативную сигнальную последовательность полипептида, полученного из E. coli FimH. В некоторых вариантах осуществления, где полипептид, полученный из E. coli, или его фрагмент включает эндогенную сигнальную последовательность, последовательность нуклеиновой кислоты, кодирующая сигнальную последовательность, может быть кодон-оптимизированной для повышения уровня экспрессии белка в клетке-хозяине.
В некоторых вариантах осуществления сигнальная последовательность имеет любую из следующих длин: 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 и 30 аминокислот. В некоторых вариантах осуществления, длина сигнальной последовательности составляет 20 аминокислот. В некоторых вариантах осуществления, длина сигнальной последовательности составляет 21 аминокислоту.
В некоторых вариантах осуществления, где полипептид или его фрагмент включает сигнальную последовательность, эндогенная сигнальная последовательность, ассоциированная с полипептидом в природе, может быть заменена сигнальной последовательностью, не связанной с полипептидом дикого типа, для повышения уровня экспрессии полипептида или его фрагмента в культивируемых клетках. Соответственно, в некоторых вариантах осуществления, нуклеиновая кислота не включает нативную сигнальную последовательность полипептида, полученного из E. coli, или его фрагмента. В некоторых вариантах осуществления, нуклеиновая кислота не включает нативную сигнальную последовательность полипептида, полученного из FimH E. coli. В некоторых вариантах осуществления, полипептид, полученный из E. coli, или его фрагмент может быть экспрессирован гетерологичным пептидом, который предпочтительно представляет собой сигнальную последовательность, или другим пептидом, имеющим специфический сайт расщепления на N-конце зрелого белка или полипептида, полученного из E. coli, или ее фрагмент. Например, полипептид, полученный из FimH E. coli или его фрагмент может быть экспрессирован гетерологичным пептидом (например, сигнальной последовательностью IgK), который предпочтительно представляет собой сигнальную последовательность или другой пептид, имеющий специфический сайт расщепления на N-конце зрелого белка FimH E. coli. В предпочтительных вариантах осуществления, специфический сайт расщепления на N-конце зрелого белка FimH E.coli находится непосредственно перед исходным остатком фенилаланина зрелого белка E.coli FimH. Выбранная гетерологичная последовательность, предпочтительно, является той, которая распознается и процессируется (т.е. расщепляется сигнальной пептидазой) клеткой-хозяином.
В предпочтительных вариантах осуществления, сигнальная последовательность представляет собой сигнальную последовательность IgK. В некоторых вариантах осуществления, нуклеиновая кислота кодирует аминокислотную последовательность SEQ ID NO: 18. В некоторых вариантах осуществления, нуклеиновая кислота кодирует аминокислотную последовательность SEQ ID NO: 19. В некоторых вариантах осуществления, нуклеиновая кислота кодирует аминокислотную последовательность SEQ ID NO: NO: 22. В предпочтительных вариантах осуществления, сигнальная последовательность представляет собой сигнальную последовательность мышиного IgK.
Подходящие векторы экспрессии млекопитающих для продуцирования полипептида, полученного из E. coli или его фрагментов, известны в данной области техники и могут быть коммерчески доступными, например вектор экспрессии pSecTag2 от Invitrogen™. Типовая последовательность сигнального пептида Ig каппа мыши включает последовательность ETDTLLLWVLLLWVPGSTG (SEQ ID NO: 54). В некоторых вариантах осуществления, вектор включает вектор экспрессии млекопитающих pBudCE4.1 от Thermo Fisher. Дополнительные типовые и подходящие векторы включают вектор экспрессии млекопитающих pcDNA™ 3.1 (Thermo Fisher).
В некоторых вариантах осуществления, сигнальная последовательность не включает сигнальную последовательность гемагглютинина.
В некоторых вариантах осуществления, нуклеиновая кислота включает нативную сигнальную последовательность полипептида, полученного из E. coli, или ее фрагмент. В некоторых вариантах осуществления сигнальная последовательность не является сигнальной последовательностью IgK. В некоторых вариантах осуществления сигнальная последовательность включает сигнальную последовательность гемагглютинина.
В одном аспекте в настоящем документе раскрыты векторы, которые включают кодирующие последовательности для полипептида, полученного из E. coli, или его фрагмента. Примеры векторов включают плазмиды, которые способны реплицироваться автономно или реплицироваться в клетке млекопитающего. Типовые векторы экспрессии содержат подходящие промоторы, энхансеры и терминаторы, которые можно использовать для регуляции экспрессии кодирующей последовательности(ей) в конструкции экспрессии. Векторы могут также включать маркеры селекции для обеспечения фенотипического признака для селекции трансформированных клеток-хозяев (например, придания резистентности к антибиотикам, таким как ампициллин или неомицин).
Подходящие промоторы известны в данной области техники. Примеры промоторов включают, например, промотор CMV, аденовируса, EF1a, промотор металлотионина GAPDH, ранний промотор SV-40, более поздний промотор SV-40, промотор вируса опухоли молочной железы мышей, промотор вируса саркомы Рауса, промотор полиэдрина и т.д. Промоторы могут быть конститутивными или индуцибельными. Можно использовать один или несколько векторов (например, один вектор, кодирующий все субъединицы, или домены, или их фрагменты, или несколько векторов, вместе кодирующих субъединицы, или домены, или их фрагменты).
Также можно использовать внутренний сайт посадки рибосомы (IRES) и пептидные последовательности 2А. IRES и пептид 2A обеспечивают альтернативные подходы к совместной экспрессии нескольких последовательностей. IRES представляет собой нуклеотидную последовательность, которая позволяет инициировать трансляцию в середине последовательности матричной РНК (мРНК) как часть более крупного процесса синтеза белка. Обычно у эукариот трансляция может инициироваться только на 5'-конце молекулы мРНК. Элементы IRES позволяют экспрессировать несколько генов в одном транскрипте. Полицистронные векторы на основе IRES, которые экспрессируют несколько белков из одного транскрипта, могут уменьшать ускользание неэкспрессирующих клонов от селекции. Пептид 2А позволяет транслировать несколько белков в одной открытой рамке считывания в полипротеин, который впоследствии расщепляется на отдельные белки с помощью механизма проскока рибосом. Пептид 2A может обеспечивать более сбалансированную экспрессию множества белковых продуктов. Примеры последовательностей IRES включают, например, IRES EV71, IRES EMCV, IRES HCV. Для геномной интеграции, интеграция может быть сайт-специфической или случайной. Сайт-специфическая рекомбинация может быть достигнута путем введения гомологичной последовательности (последовательностей) в конструкции нуклеиновых кислот, описанные в настоящем документе. Такая гомологичная последовательность по существу соответствует эндогенной последовательности в конкретном сайте-мишени в геноме хозяина. В качестве альтернативы можно использовать случайное интегрирование. Иногда уровень экспрессии белка может варьироваться в зависимости от сайта интеграции. Следовательно, может быть желательно выбрать ряд клонов в соответствии с уровнем экспрессии рекомбинантного белка, чтобы идентифицировать клон, который достигает желаемого уровня экспрессии.
Примеры конструкций нуклеиновых кислот дополнительно описаны на фигурах, таких как любая из фиг. 2А- 2Т.
В одном аспекте, последовательность нуклеиновой кислоты кодирует аминокислотную последовательность, имеющую, по меньшей мере, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 99,9% или 100% идентичность любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28 и SEQ ID NO: 29.
III. Клетки-хозяева
В одном аспекте, изобретение относится к клеткам, в которых последовательности, кодирующие полипептид, полученный из E.coli, или его фрагмент, экспрессируются в клетке-хозяине млекопитающего. В одном варианте осуществления, полипептид, полученный из E. coli, или его фрагмент временно экспрессируется в клетке-хозяине. В другом варианте осуществления, полипептид, полученный из E.coli, или его фрагмент стабильно интегрируется в геном клеток-хозяев и при культивировании в подходящих условиях экспрессирует полипептид, полученный из E.coli, или его фрагмент. В предпочтительном варианте осуществления, полинуклеотидная последовательность экспрессируется с высокой эффективностью и геномной стабильностью.
Подходящие клетки-хозяева млекопитающих известны в данной области техники. Предпочтительно клетка-хозяин пригодна для продуцирования белка в промышленных масштабах. Примеры клеток-хозяев млекопитающих включают любые из следующих клеток и их производные: клетки яичника китайского хомяка (CHO), клетки COS (линия клеток, полученная из почки обезьяны (африканская зеленая мартышка), клетки Vero, клетки Hela, клетки почки детеныша хомячка (BHK), клетки эмбриональной почки человека (HEK), клетки NSO (линия клеток миеломы мыши) и клетки C127 (линия клеток неопухолевой мыши). Дополнительные типовые клетки-хозяева млекопитающих включают Сертоли мыши (TM4), печень серой крысы (BRL 3A), опухоль молочной железы мыши (MMT), гепатому крысы (HTC), миелому мыши (NSO), гибридому мыши (Sp2/0), тимому мыши (EL4), яичник китайского хомячка (CHO) и производные клеток CHO, эмбрион мыши (NIH/3T3, 3T3 Li), миокард крысы (H9c2), миобласт мыши (C2C12) и почку мыши (miMCD-3). Другие примеры клеточных линий млекопитающих включают NS0/1, Sp2/0, Hep G2, PER.C6, COS-7, TM4, CV1, VERO-76, MDCK, BRL 3A, W138, MMT 060562, TR1, MRC5 и FS4.
Любая клетка, восприимчивая к клеточной культуре, может быть использована в соответствии с настоящим изобретением. В некоторых вариантах осуществления, клетка представляет собой клетку млекопитающего. Неограничивающие примеры клеток млекопитающих, которые можно использовать в соответствии с настоящим изобретением, включают линию миеломы мыши BALB/c (NSO/1, ЕСАСС №: 85110503); ретинобласты человека (PER.C6, Leiden, The Netherlands); линию почки обезьяны CV1, трансформированные SV40 (COS-7, ATCC CRL 1651); линию почек эмбриона человека (клетки 293 или 293, субклонированные для роста в суспензионной культуре, Graham et al., J. Gen Virol., 36:59, 1977); клетки почек детенышей хомячков (BHK, ATCC CCL 10); клетки яичника китайского хомячка +/-DHFR (CHO, Urlaub and Chasin, Proc. Natl. Acad. Sci. USA, 77:4216, 1980); клетки Сертоли мыши (TM4, Mather, Biol. Reprod., 23:243-251, 1980); клетки почки обезьяны (CV1 ATCC CCL 70); клетки почки африканской зеленой мартышки (VERO-76, ATCC CRL-1 587); клетки карциномы шейки матки человека (HeLa, ATCC CCL 2); клетки почек собак (MDCK, ATCC CCL 34); клетки печени серой крысы (BRL 3A, ATCC CRL 1442); клетки легкого человека (W138, ATCC CCL 75); клетки печени человека (Hep G2, HB 8065); опухоль молочной железы мыши (MMT 060562, ATCC CCL51); клетки TRI (Mather et al., Annals NY Acad. Sci., 383:44-68, 1982); клетки МРС 5; клетки FS4; и линию гепатомы человека (Hep G2). В некоторых предпочтительных вариантах осуществления, клетки представляют собой клетки СНО. В некоторых предпочтительных вариантах осуществления, клетки представляют собой GS-клетки.
Кроме того, в соответствии с настоящим изобретением, можно использовать любое количество коммерчески доступных и некоммерческих клеточных линий гибридомы. Термин «гибридома», используемый в настоящем документе, относится к клетке или потомству клетки, полученному в результате слияния иммортализованной клетки и клетки, продуцирующей антитело. Такая полученная гибридома представляет собой иммортализованную клетку, продуцирующую антитела. Отдельные клетки, используемые для создания гибридомы, могут быть получены из любого млекопитающего, включая, но не ограничиваясь ими, крысу, свинью, кролика, овцу, свинью, козу и человека. В некоторых вариантах осуществления, гибридома представляет собой клеточную линию триомы, которая возникает, когда потомство слияний гетерогибридной миеломы, которые являются продуктом слияния между клетками человека и клеточной линией миеломы мыши, впоследствии сливают с плазматической клеткой. В некоторых вариантах осуществления гибридома представляет собой любую иммортализованную гибридную клеточную линию, которая продуцирует антитела, такую как, например, квадромы (см., например, Milstein et al., Nature, 537:3053, 1983). Специалисту в данной области техники будет понятно, что клеточные линии гибридомы могут иметь различные требования к питанию и/или могут требовать различных условий культивирования для оптимального роста, и он сможет модифицировать условия по мере необходимости.
В некоторых вариантах осуществления, клетка содержит первый представляющий интерес ген, где первый представляющий интерес ген является хромосомно интегрированным. В некоторых вариантах осуществления, первый представляющий интерес ген содержит репортерный ген, селекционный ген, представляющий интерес ген (например, кодирующий полипептид, полученный из E. coli, или его фрагмент), вспомогательный ген или их комбинацию. В некоторых вариантах осуществления, ген, представляющий терапевтический интерес, содержит ген, кодирующий трудно экспрессируемый белок (DtE).
В некоторых вариантах осуществления, первый представляющий интерес ген расположен между двумя отдельными сайтами-мишенями рекомбинации (RTS) в клетке млекопитающего с сайт-специфической интеграцией (SSI), где два RTS являются хромосомно интегрированными в локус NL1 или локус NL2. См., например, публикацию патентной заявки США № 20200002727 для описания локуса NL1, локуса NL2, локуса NL3, локуса NL4, локуса NL5 и локуса NL6. В некоторых вариантах осуществления, первый представляющий интерес ген расположен в локусе NL1. В некоторых вариантах осуществления, клетка содержит второй представляющий интерес ген, где второй представляющий интерес ген является хромосомно интегрированным. В некоторых вариантах осуществления, второй представляющий интерес ген содержит репортерный ген, селекционный ген, представляющий терапевтический интерес ген (такой как полипептид, полученный из E. coli или его фрагмент), вспомогательный ген или их комбинацию. В некоторых вариантах осуществления, ген, представляющий терапевтический интерес, содержит ген, кодирующий белок DtE. В некоторых вариантах осуществления, второй представляющий интерес ген расположен между двумя RTS. В некоторых вариантах осуществления второй представляющий интерес ген расположен в локусе NL1 или локусе NL2. В некоторых вариантах осуществления, первый представляющий интерес ген расположен в локусе NL1, и второй представляющий интерес ген расположен в пределах локуса NL2. В некоторых вариантах осуществления клетка содержит третий представляющий интерес ген, где третий представляющий интерес ген является хромосомно интегрированным. В некоторых вариантах осуществления третий представляющий интерес ген содержит репортерный ген, селекционный ген, представляющий терапевтический интерес ген (такой как полипептид, полученный из E. coli или его фрагмент), вспомогательный ген или их комбинацию. В некоторых вариантах осуществления ген, представляющий терапевтический интерес, содержит ген, кодирующий белок DtE. В некоторых вариантах осуществления третий представляющий интерес ген расположен между двумя RTS. В некоторых вариантах осуществления, третий представляющий интерес ген расположен в пределах локуса NL1 или локуса NL2. В некоторых вариантах осуществления, третий представляющий интерес ген расположен в локусе, отличном от локуса NL1 и локуса NL2. В некоторых вариантах осуществления первый представляющий интерес ген, второй представляющий интерес ген и третий представляющий интерес ген находятся в пределах трех отдельных локусов. В некоторых вариантах осуществления, по меньшей мере, один из первого представляющего интерес гена, второго представляющего интерес гена и третьего представляющего интерес гена находится в локусе NL1, и, по меньшей мере, один из первого представляющего интерес гена, второго представляющего интерес гена и третьего представляющего интерес гена находится в локусе NL2. В некоторых вариантах осуществления, клетка содержит сайт-специфический ген рекомбиназы. В некоторых вариантах осуществления, сайт-специфический ген рекомбиназы встроен в хромосому.
В некоторых вариантах осуществления, настоящее изобретение относится к клетке млекопитающего, содержащей, по меньшей мере, четыре различных RTS, где клетка содержит (a) по меньшей мере, два различных RTS, хромосомно интегрированных в локус NL1 или локус NL2; (b) первый представляющий интерес ген встроен между, по меньшей мере, двумя RTS из (а), где первый представляющий интерес ген содержит репортерный ген, ген, кодирующий белок DtE, вспомогательный ген или их комбинацию; (c) и второй представляющий интерес ген интегрирован во второй хромосомный локус, отличный от локуса (a), где второй представляющий интерес ген содержит репортерный ген, ген, кодирующий белок DtE (такой как полипептид, полученный из E. coli или его фрагмент), вспомогательный ген или их комбинацию. В некоторых вариантах осуществления, настоящее изобретение относится к клетке млекопитающего, содержащей, по меньшей мере, четыре различных RTS, где клетка содержит (a) по меньшей мере, два различных RTS, интегрированных в хромосому в пределах локуса Fer1L4; (b) по меньшей мере, два различных RTS хромосомно интегрированных в локус NL1 или локус NL2; (c) первый представляющий интерес ген является хромосомно интегрированным в локус Fer1L4, при этом первый представляющий интерес ген содержит репортерный ген, ген, кодирующий белок DtE, вспомогательный ген или их комбинацию; и (d) второй представляющий интерес ген встроен в хромосому внутри локуса NL1 или локуса NL2 из (b), где второй представляющий интерес ген содержит репортерный ген, ген, кодирующий белок DtE (например, полученный из полипептида из E. coli или его фрагмента), вспомогательный ген или их комбинацию.
В некоторых вариантах осуществления, настоящее изобретение относится к клетке млекопитающего, содержащей, по меньшей мере, шесть различных RTS, где клетка содержит (а) по меньшей мере, два различных RTS и первый представляющий интерес ген, интегрированные в хромосому в пределах локуса Fer1L4; (b) по меньшей мере, два различных RTS и второй интересующий ген, хромосомно интегрированные в локус NL1; и (c) по меньшей мере, два различных RTS и третий представляющий интерес ген, хромосомно интегрированные в локус NL2.
Как упоминается в настоящем документе, термины «в функциональной комбинации», «в функциональном порядке» и «функционально связанный» относятся к связыванию последовательностей нуклеиновых кислот таким образом, что молекула нуклеиновой кислоты способна направлять транскрипцию данного гена и/или синтез желаемой продуцируемой белковой молекулы. Этот термин также относится к соединению аминокислотных последовательностей таким образом, что образуется функциональный белок. В некоторых вариантах осуществления, представляющий интерес ген функционально связан с промотором, где представляющий интерес ген встроен в хромосому клетки-хозяина. В некоторых вариантах осуществления, представляющий интерес ген функционально связан с гетерологичным промотором; где представляющий интерес ген хромосомно интегрирован в клетку-хозяина. В некоторых вариантах осуществления, вспомогательный ген функционально связан с промотором, где вспомогательный ген хромосомно интегрирован в геном клетки-хозяина. В некоторых вариантах осуществления, вспомогательный ген функционально связан с гетерологичным промотором; где вспомогательный ген хромосомно интегрирован в геном клетки-хозяина. В некоторых вариантах осуществления ген, кодирующий белок DtE, функционально связан с промотором, где ген, кодирующий белок DtE, хромосомно интегрирован в геном клетки-хозяина. В некоторых вариантах осуществления, ген, кодирующий белок DtE, функционально связан с гетерологичным промотором, где ген, кодирующий белок DtE, хромосомно интегрирован в геном клетки-хозяина. В некоторых вариантах осуществления ген рекомбиназы функционально связан с промотором, где ген рекомбиназы встроен в хромосому клетки-хозяина. В некоторых вариантах осуществления ген рекомбиназы функционально связан с промотором, где ген рекомбиназы не интегрирован в геном клетки-хозяина. В некоторых вариантах осуществления ген рекомбиназы функционально связан с гетерологичным промотором, где ген рекомбиназы не встроен в хромосому в геном клетки-хозяина. В некоторых вариантах осуществления, ген рекомбиназы функционально связан с гетерологичным промотором, где ген рекомбиназы не встроен в хромосому в геном клетки-хозяина.
Используемый в настоящем документе термин «хромосомно-интегрированный» или «хромосомная интеграция» относится к стабильному включению последовательности нуклеиновой кислоты в хромосому клетки-хозяина, например клетки млекопитающего. т.е. последовательности нуклеиновой кислоты, которая хромосомно интегрирована в геномную ДНК (гДНК) клетки-хозяина, например клетки млекопитающего. В некоторых вариантах осуществления, последовательность нуклеиновой кислоты, интегрированная в хромосому, является стабильной. В некоторых вариантах осуществления, последовательность нуклеиновой кислоты, интегрированная в хромосому, не расположена на плазмиде или векторе. В некоторых вариантах осуществления последовательность нуклеиновой кислоты, интегрированная в хромосому, не вырезается. В некоторых вариантах осуществления хромосомная интеграция опосредована сгруппированными короткими палиндромными повторами с регулярными промежутками (CRISPR) и системой редактирования генов CRISPR-ассоциированного белка (Cas) (CRISPR/CAS).
В некоторых вариантах осуществления, клетки-хозяева подходят для выращивания в суспензионных культурах. Суспензионно-компетентные клетки-хозяева обычно являются монодисперсными или растут рыхлыми агрегатами без существенной агрегации. Суспензионно-компетентные клетки-хозяева включают клетки, подходящие для суспензионного культивирования без адаптации или манипуляций (например, гемопоэтические клетки, лимфоидные клетки), и клетки, которые сделали суспензионно-компетентными путем модификации или адаптации зависимых от прикрепления клеток (например, эпителиальные клетки, фибробласты).
В некоторых вариантах осуществления, уровень экспрессии или активность полипептида, полученного из E. coli, или его фрагмента увеличивается, по меньшей мере, в 2 раза, по меньшей мере, в 3 раза, по меньшей мере, в 5 раз, по меньшей мере, в 10 раз, по меньшей мере, в 20 раз, при по меньшей мере, в 30 раз, по меньшей мере, в 40 раз, по меньшей мере, в 50 раз, по меньшей мере, в 60 раз, по меньшей мере, в 70 раз, по меньшей мере, в 75 раз, по меньшей мере, в 80 раз, по меньшей мере, в 90 раз, по меньшей мере, в 100 раз по сравнению с экспрессией полипептида, полученного из E.coli, или его фрагмента в бактериальной клетке, такой как, например, клетка-хозяин E.coli.
Описанные в настоящем документе клетки-хозяева подходят для крупномасштабного культивирования. Например, клеточные культуры могут иметь объем 10 л, 30 л, 50 л, 100 л, 150 л, 200 л, 300 л, 500 л, 1000 л, 2000 л, 3000 л, 4000 л, 5000 л, 10000 л или больше. В некоторых вариантах осуществления, размер клеточной культуры может составлять от 10 л до 5000 л, от 10 л до 10000 л, от 10 л до 20000 л, от 10 л до 50000 л, от 40 л до 50000 л, от 100 л. до 50000 л, от 500 л до 50000 л, от 1000 л до 50000 л, от 2000 л до 50000 л, от 3000 л, до 50000 л, от 4000 л до 50000 л, от 4500 л до 50000 л, от 1000 л до 10000 л, от 1000 л до 20000 л, от 1000 л до 25000 л, от 1000 л до 30000 л, от 15 л до 2000 л, от 40 л до 1000 л, от 100 л до 500 л, от 200 л до 400 л или любое целое число между ними. Компоненты среды для клеточной культуры известны в данной области техники и могут включать, например, буфер, содержание аминокислот, содержание витаминов, содержание солей, содержание минералов, содержание сыворотки, содержание источника углерода, содержание липидов, содержание нуклеиновой кислоты, содержание гормонов, содержание микроэлементов, содержание аммиака, содержание кофакторов, содержание индикаторов, содержание малых молекул, содержание гидролизатов и содержание модуляторов ферментов.
Используемые в настоящем документе термины «среда», «среда для культивирования клеток» и «среда для культивирования» относятся к раствору, содержащему питательные вещества, которые питают растущие клетки млекопитающих. Как правило, такие растворы содержат незаменимые и заменимые аминокислоты, витамины, источники энергии, липиды и микроэлементы, необходимые клетке для минимального роста и/или выживания. Такой раствор может также содержать дополнительные компоненты, которые усиливают рост и/или выживаемость выше минимальной скорости, включая, помимо прочего, гормоны и/или другие факторы роста, определенные ионы (такие как натрий, хлорид, кальций, магний и фосфат), буферы, витамины, нуклеозиды или нуклеотиды, микроэлементы (неорганические соединения, обычно присутствующие в очень низких конечных концентрациях), неорганические соединения, присутствующие в высоких конечных концентрациях (например, железо), аминокислоты, липиды и/или глюкоза или другой источник энергии. В некоторых вариантах осуществления среда преимущественно составлена с рН и концентрацией соли, оптимальными для выживания и пролиферации клеток. В некоторых вариантах осуществления среда представляет собой питательную среду, которую добавляют после начала культивирования клеток.
В некоторых вариантах осуществления, клетки можно выращивать в одной из множества сред с определенным химическим составом, где компоненты сред известны и контролируются. В некоторых вариантах осуществления клетки можно выращивать в сложной среде, в которой не все компоненты среды известны и/или контролируются. Среды для выращивания культур клеток млекопитающих с определенным химическим составом широко разрабатывались и публиковались в течение последних нескольких десятилетий. Все компоненты определенных сред хорошо охарактеризованы, поэтому определенные среды не содержат сложных добавок, таких как сыворотка или гидролизаты. Ранние составы сред были разработаны для обеспечения роста клеток и поддержания их жизнеспособности практически без учета продуцирования белка. Совсем недавно составы сред были разработаны специально для поддержки высокопродуктивных клеточных культур, продуцирующих рекомбинантный белок. Такие среды предпочтительны для использования в способе изобретения. Такие среды обычно содержат большое количество питательных веществ и, в частности, аминокислот для поддержки роста и/или поддержания высокой плотности клеток. При необходимости эти среды могут быть модифицированы специалистом в данной области техники для использования в способе по изобретению. Например, специалист в данной области техники может уменьшить количество фенилаланина, тирозина, триптофана и/или метионина в этих средах для их использования в качестве основных сред или питательных сред в способе, описанном в настоящем документе.
Не все компоненты сложных сред хорошо охарактеризованы, поэтому сложные среды могут содержать добавки, такие как простые и/или сложные источники углерода, простые и/или сложные источники азота и сыворотку, среди прочего. В некоторых вариантах комплексная среда, подходящая для настоящего изобретения, содержит добавки, такие как гидролизаты, в дополнение к другим компонентам определенной среды, как описано в настоящем документе. В некоторых вариантах осуществления определенная среда обычно включает примерно пятьдесят химических соединений в известных концентрациях в воде. Большинство из них также содержат один или несколько хорошо охарактеризованных белков, таких как инсулин, IGF-1, трансферрин или BSA, но другие не требуют белковых компонентов и поэтому называются средами с определенными свойствами, не содержащими белков. Типовые химические компоненты среды делятся на пять широких категорий: аминокислоты, витамины, неорганические соли, микроэлементы и другие категории, не поддающиеся четкой категоризации.
Среда для культивирования клеток может быть необязательно дополнена дополнительными компонентами. Используемый в настоящем документе термин «дополнительные компоненты» относится к компонентам, которые усиливают рост и/или выживаемость выше минимальной скорости, включая, помимо прочего, гормоны и/или другие факторы роста, определенные ионы (такие как натрий, хлорид, кальций, магний и фосфат), буферы, витамины, нуклеозиды или нуклеотиды, микроэлементы (неорганические соединения, обычно присутствуют в очень низких конечных концентрациях), аминокислоты, липиды и/или глюкозу или другой источник энергии. В некоторых вариантах осуществления, к исходной культуре клеток могут быть добавлены дополнительные компоненты. В некоторых вариантах осуществления дополнительные компоненты могут быть добавлены после начала культивирования клеток. Как правило, микроэлементы относятся к различным неорганическим солям, содержащимся в микромолярных или более низких количествах. Например, часто включаемыми микроэлементами являются цинк, селен, медь и другие. В некоторых вариантах осуществления железо (двухвалентное железо или соли трехвалентного железа) может быть включено в качестве микроэлемента в исходную среду для культивирования клеток в микромолярных концентрациях. Марганец также часто включается в число микроэлементов в виде двухвалентного катиона (MnCl2 или MnSO4) в диапазоне концентраций от наномолярных до микромолярных. Многочисленные менее распространенные микроэлементы обычно добавляют в наномолярных концентрациях.
В некоторых вариантах осуществления, среда, используемая в способе по изобретению, представляет собой среду, пригодную для поддержания высокой плотности клеток, например, 1х106 клеток/мл, 5х106 клеток/мл, 1х107 клеток/мл, 5х107 клеток/мл, 1х108 клеток/мл или 5х108 клеток/мл в культуре клеток. В некоторых вариантах осуществления, клеточная культура представляет собой периодическую культуру клеток млекопитающих, предпочтительно периодическую культуру клеток СНО.
В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит тирозин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит триптофан в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления среда для культивирования клеток содержит метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит лейцин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит серин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит треонин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит глицин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит два компонента: фенилаланин, тирозин, триптофан, метионин, лейцин, серин, треонин и глицин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ. или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин и тирозин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин и триптофан в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин и метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит тирозин и триптофан в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит тирозин и метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит триптофан и метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит три из фенилаланина, тирозина, триптофана, метионина, лейцина, серина, треонина и глицина в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ. или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин, тирозин и триптофан в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин, тирозин и метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин, триптофан и метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит тирозин, триптофан и метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит четыре из фенилаланина, тирозина, триптофана, метионина, лейцина, серина, треонина и глицина в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ. или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин, тирозин, триптофан и метионин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит пять из фенилаланина, тирозина, триптофана, метионина, лейцина, серина, треонина и глицина в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ. или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит шесть из фенилаланина, тирозина, триптофана, метионина, лейцина, серина, треонина и глицина в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ. или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит семь из фенилаланина, тирозина, триптофана, метионина, лейцина, серина, треонина и глицина в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ. или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит фенилаланин, тирозин, триптофан, метионин, лейцин, серин, треонин и глицин в концентрации ниже 2 мМ, ниже 1 мМ, от 0,1 до 2 мМ, от 0,1 до 1 мМ, от 0,5 до 1,5 мМ или от 0,5 до 1 мМ. В некоторых вариантах осуществления, среда для культивирования клеток дополнительно содержит, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 глицина, валина, лейцина, изолейцина, пролина, серина, треонина, лизина, аргинина, гистидина, аспартата, глутамата и аспарагина в концентрации выше 2 мМ, 3 мМ, 4 мМ, 5 мМ, 10 мМ, 15 мМ, предпочтительно, 2 мМ. В некоторых вариантах осуществления, среда для культивирования клеток дополнительно содержит, по меньшей мере, 5 из глицина, валина, лейцина, изолейцина, пролина, серина, треонина, лизина, аргинина, гистидина, аспартата, глутамата и аспарагина в концентрации выше 2 мМ, 3 мМ, 4 мМ, 5 мМ, 10 мМ, 15 мМ, предпочтительно, 2 мМ. В некоторых вариантах осуществления, среда для культивирования клеток дополнительно содержит глицин, валин, лейцин, изолейцин, пролин, серин, треонин, лизин, аргинин, гистидин, аспартат, глутамат и аспарагин в концентрации выше 2 мМ, 3 мМ, 4 мМ, 5 мМ, 10 мМ, 15 мМ, предпочтительно, 2 мМ. В некоторых вариантах осуществления, среда для культивирования клеток дополнительно содержит по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8 или 9 валина, изолейцина, пролина, лизина, аргинина, гистидина, аспартата, глутамата и аспарагина в концентрации концентрация выше 2 мМ, 3 мМ, 4 мМ, 5 мМ, 10 мМ, 15 мМ, предпочтительно, 2 мМ. В некоторых вариантах осуществления, среда для культивирования клеток дополнительно содержит, по меньшей мере, 5 из валина, изолейцина, пролина, лизина, аргинина, гистидина, аспартата, глутамата и аспарагина в концентрации выше 2 мМ, 3 мМ, 4 мМ, 5 мМ, 10 мМ, 15 мМ, предпочтительно, 2 мМ. В некоторых вариантах осуществления, среда для культивирования клеток дополнительно содержит валин, изолейцин, пролин, лизин, аргинин, гистидин, аспартат, глутамат и аспарагин в концентрации выше 2 мМ, 3 мМ, 4 мМ, 5 мМ, 10 мМ, 15 мМ, предпочтительно, 2 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит серин в концентрации выше 3 мМ, 5 мМ, 7 мМ, 10 мМ, 15 мМ или 20 мМ, предпочтительно, 10 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит валин в концентрации выше 3 мМ, 5 мМ, 7 мМ, 10 мМ, 15 мМ или 20 мМ, предпочтительно 10 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит цистеин в концентрации выше 3 мМ, 5 мМ, 7 мМ, 10 мМ, 15 мМ или 20 мМ, предпочтительно, 10 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит изолейцин в концентрации выше 3 мМ, 5 мМ, 7 мМ, 10 мМ, 15 мМ или 20 мМ, предпочтительно, 10 мМ. В некоторых вариантах осуществления, среда для культивирования клеток содержит лейцин в концентрации выше 3 мМ, 5 мМ, 7 мМ, 10 мМ, 15 мМ или 20 мМ, предпочтительно, 10 мМ. В некоторых вариантах осуществления, указанная выше среда для культивирования клеток предназначена для использования в способе, описанном в настоящем документе. В некоторых вариантах осуществления, вышеуказанная среда для культивирования клеток используется в описанном в настоящем документе способе в качестве базовой среды. В некоторых вариантах осуществления, описанную выше среду для культивирования клеток используют в качестве питательной среды описанным в настоящем документе способом.
IV. Способ производства
В одном аспекте, изобретение включает способ получения полипептида, полученного из E.coli, или его фрагмента. Способ включает культивирование клетки млекопитающего в подходящих условиях, тем самым экспрессируя полипептид, полученный из E. coli, или его фрагмент. Способ может дополнительно включать сбор полипептида, полученного из E. coli, или его фрагмента из культуры. Способ может дополнительно включать очистку полипептида, полученного из E. coli, или его фрагмента.
В некоторых вариантах осуществления, способ дает полипептид или его фрагмент с выходом от 0,1 г/л до 0,5 г/л.
В некоторых вариантах осуществления, клетки можно выращивать в периодических культурах или культурах с подпиткой, где культивирование останавливают после достаточной экспрессии полипептида, после чего экспрессированный полипептид собирают и, необязательно, очищают. В некоторых вариантах осуществления, клетки можно выращивать в перфузионных культурах, где культивирование не останавливается, и к культуре периодически или непрерывно добавляются новые питательные вещества и другие компоненты, во время которых периодически или непрерывно собирают экспрессированный полипептид.
В некоторых вариантах осуществления, клетки можно выращивать в небольших реакционных сосудах объемом от нескольких миллилитров до нескольких литров. В некоторых вариантах осуществления, клетки можно выращивать в крупномасштабных коммерческих биореакторах объемом от приблизительно, по меньшей мере, 1 литра до 10, 100, 250, 500, 1000, 2500, 5000, 8000, 10000, 12000 литров или более или любого другого объема между указанными.
Температуру клеточной культуры выбирают, прежде всего, исходя из диапазона температур, при которых клеточная культура остается жизнеспособной, при которой вырабатывается высокий уровень полипептида, температуру, при которой образование или накопление продуктов метаболизма сводится к минимуму, и/ или любую комбинацию этих или других факторов, которые практикующий специалист считает важными. В качестве одного неограничивающего примера, клетки CHO хорошо растут и продуцируют высокие уровни белка или полипептида при температуре приблизительно 37°C. В целом, большинство клеток млекопитающих хорошо растут и/или могут продуцировать высокие уровни белка или полипептида в диапазоне приблизительно от 25°C до 42°C, хотя способы, изложенные в настоящем описании, не ограничиваются этими температурами. Некоторые клетки млекопитающих хорошо растут и/или могут продуцировать высокие уровни белка или полипептида в диапазоне примерно от 35°C до 40°C. В некоторых вариантах осуществления, клеточную культуру выращивают при температуре 20°C, 21°C, 22°C, 23°С, 24°C, 25°C, 26°C, 27℃, 28°C, 29°C, 30°C, 31°C, 32°C, 33°C, 34°C, 35°C, 36°C, 37°C, 38°C, 39°C, 40°C, 41°C, 42°C, 43°C, 44°C или 45°C, один или несколько раз в процессе культивирования клеток.
Термины «культура» и «культура клеток», используемые в настоящем документе, относятся к клеточной популяции, которая суспендирована в среде в условиях, подходящих для выживания и/или роста клеточной популяции. Как будет понятно специалистам в данной области техники, в некоторых вариантах осуществления, эти термины, используемые в настоящем документе, относятся к комбинации, включающей клеточную популяцию и среду, в которой популяция суспендирована. В некоторых вариантах осуществления, клетки клеточной культуры включают клетки млекопитающих.
Настоящее изобретение можно использовать с любым способом культивирования клеток, который подходит для желаемого процесса (например, продуцирования рекомбинантного белка (например, антитела)). В качестве неограничивающего примера, клетки можно выращивать в периодических культурах или культурах с подпиткой, где культивирование останавливают после достаточной экспрессии рекомбинантного белка (например, антитела), после чего собирают экспрессированный белок (например, антитело). Альтернативно, в качестве еще одного неограничивающего примера, клетки можно выращивать с периодической подпиткой, при которой культивирование не прекращают, и новые питательные вещества и другие компоненты периодически или постоянно добавляют в культуру, во время чего экспрессированный рекомбинантный белок (например, антитело) собирают периодически или постоянно. Другие подходящие способы (например, культивирование в центрифужных пробирках) известны в данной области техники и могут быть использованы для практического применения настоящего изобретения.
В некоторых вариантах осуществления, клеточная культура, подходящая для настоящего изобретения, представляет собой культуру с подпиткой. Используемый в настоящем документе термин «культура с подпиткой» относится к способу культивирования клеток, при котором дополнительные компоненты добавляют в культуру в момент или в моменты после начала процесса культивирования. Такие предоставленные компоненты обычно содержат питательные компоненты для клеток, которые были истощены в процессе культивирования. Культуру с подпиткой обычно останавливают в какой-то момент, и клетки и/или компоненты среды собирают и, необязательно, очищают. В некоторых вариантах осуществления, культура с подпиткой содержит базовую среду с добавлением питательной среды.
Клетки можно выращивать в любом удобном объеме, выбранном практикующим врачом. Например, клетки можно выращивать в небольших реакционных сосудах объемом от нескольких миллилитров до нескольких литров. Альтернативно, клетки можно выращивать в крупномасштабных коммерческих биореакторах объемом приблизительно от 1 литра до 10, 50, 100, 250, 500, 1000, 2500, 5000, 8000, 10000, 12000, 15000, 20000 или 25000 литров или больше или любого объема между указанными.
Температуру клеточной культуры выбирают, прежде всего, исходя из диапазона температур, при котором клеточная культура остается жизнеспособной, и диапазона, при котором продуцируется высокий уровень желаемого продукта (например, рекомбинантного белка). В общем, большинство клеток млекопитающих хорошо растут и могут продуцировать желаемые продукты (например, рекомбинантные белки) в диапазоне температур примерно от 25°С до 42°С, хотя способы, описанные в настоящем изобретении, не ограничиваются этими температурами. Некоторые клетки млекопитающих хорошо растут и могут продуцировать желаемые продукты (например, рекомбинантные белки или антитела) в диапазоне температур примерно от 35°С до 40°С. В некоторых вариантах осуществления, культуру клеток выращивают при температуре 20°C, 21°C, 22°C, 23°C, 24°C, 25°C, 26°C, 27°C, 28°C, 29°C, 30°C, 31°C, 32°С, 33°C, 34°C, 35°C, 36°C, 37°C, 38°C, 39°C, 40°C, 41°C, 42°C, 43°C, 44°C или 45°C, один или несколько раз в течение процесса культивирования клеток. Специалисты в данной области техники смогут выбрать подходящую температуру или температуры для выращивания клеток в зависимости от конкретных потребностей клеток и конкретных требований к продуцированию от практикующего специалиста. Клетки можно выращивать в течение любого периода времени, в зависимости от потребностей практикующего специалиста и требований самих клеток. В некоторых вариантах осуществления, клетки выращивают при 37°C. В некоторых вариантах осуществления, клетки выращивают при 36,5°C.
В некоторых вариантах осуществления, клетки можно выращивать во время начальной фазы роста (или фазы роста) в течение большего или меньшего времени, в зависимости от потребностей практикующего специалиста и требований самих клеток. В некоторых вариантах осуществления, клетки выращивают в течение периода времени, достаточного для достижения заданной плотности клеток. В некоторых вариантах осуществления, клетки выращивают в течение периода времени, достаточного для достижения плотности клеток, которая представляет собой заданную долю от максимальной плотности клеток, которой, в конечном итоге, достигли бы клетки, если бы им давали возможность расти без помех. Например, клетки можно выращивать в течение периода времени, достаточного для достижения желаемой плотности жизнеспособных клеток 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 99 процентов от максимальной плотности клеток. В некоторых вариантах осуществления, клетки выращивают до тех пор, пока плотность клеток не увеличится более чем на 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% в день культивирования. В некоторых вариантах осуществления, клетки выращивают до тех пор, пока плотность клеток не увеличится более чем на 5% в день культивирования.
В некоторых вариантах осуществления, клетки могут расти в течение определенного периода времени. Например, в зависимости от исходной концентрации клеточной культуры, температуры, при которой выращивают клетки, и собственной скорости роста клеток, клетки можно выращивать в течение 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более дней, предпочтительно, от 4 до 10 дней. В некоторых случаях, клеткам может быть позволено расти в течение месяца или более. Практикующий специалист по настоящему изобретению сможет выбрать продолжительность начальной фазы роста в зависимости от требований к продуцированию белка и потребностей самих клеток.
Культуру клеток можно перемешивать или встряхивать во время начальной фазы культивирования, чтобы увеличить оксигенацию и диспергирование питательных веществ в клетках. В соответствии с настоящим изобретением, специалисту в данной области техники будет понятно, что может быть полезно контролировать или регулировать определенные внутренние условия биореактора во время начальной фазы роста, включая, помимо прочего, рН, температуру, оксигенацию и т.д.
В конце начальной фазы роста, по меньшей мере, одно из условий культивирования может быть изменено таким образом, что применяется второй набор условий культивирования, и в культуре происходит метаболический сдвиг. Метаболический сдвиг может быть достигнут, например, путем изменения температуры, pH, осмоляльности или уровня химической индукции клеточной культуры. В одном неограничивающем варианте осуществления, условия культивирования изменяют путем изменения температуры культивирования. Однако, как известно в данной области техники, изменение температуры не является единственным механизмом, с помощью которого может быть достигнут соответствующий метаболический сдвиг. Например, такой метаболический сдвиг также может быть достигнут путем изменения других условий культивирования, включая, но не ограничиваясь ими, рН, осмоляльность и уровни бутирата натрия. Время культурального сдвига будет определять специалист, практикующий настоящее изобретение, исходя из требований к продуцированию белка или потребностей самих клеток.
При смещении температуры культивирования, сдвиг температуры может быть относительно постепенным. Например, для полного изменения температуры может потребоваться несколько часов или дней. Альтернативно, температурный сдвиг может быть относительно резким. Например, изменение температуры может быть завершено менее чем за несколько часов. При наличии соответствующего производственного и контрольного оборудования, которое является стандартным для промышленного крупномасштабного производства полипептидов или белков, изменение температуры может быть завершено менее чем за час.
В некоторых вариантах осуществления, после изменения условий клеточной культуры, как обсуждалось выше, клеточную культуру поддерживают для последующей фазы продуцирования при втором наборе условий культивирования, способствующих выживанию и жизнеспособности клеточной культуры и подходящих для экспрессии желаемого полипептида или белка в коммерчески приемлемых количествах.
Как обсуждалось выше, культура может быть изменена путем изменения одного или нескольких условий культивирования, включая, но не ограничиваясь ими, температуру, рН, осмоляльность и уровни бутирата натрия. В некоторых вариантах осуществления, сдвигается температура культуры. В соответствии с этим вариантом осуществления, во время последующей фазы продуцирования культуру поддерживают при температуре или диапазоне температур, которые ниже, чем температура или диапазон температур начальной фазы роста. Как обсуждалось выше, для увеличения плотности или жизнеспособности клеток или для увеличения экспрессии рекомбинантного белка можно использовать множественные дискретные температурные сдвиги.
В некоторых вариантах осуществления, клетки можно поддерживать на последующей фазе продуцирования до тех пор, пока не будет достигнута желаемая плотность клеток или титр продуцирования. В другом варианте осуществления настоящего изобретения, клеткам позволяют расти в течение определенного периода времени во время последующей фазы продуцирования. Например, в зависимости от концентрации клеточной культуры в начале последующей фазы роста, температура, при которой выращивают клетки, и собственная скорость роста клеток клетки могут расти в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 и более дней. В некоторых случаях, клеткам может быть позволено расти в течение месяца или более. Специалист, практикующий настоящее изобретение, сможет выбрать продолжительность последующей фазы продуцирования в зависимости от требований к продуцированию полипептидов или белков и потребностей самих клеток.
Культуру клеток можно перемешивать или встряхивать во время последующей фазы продуцирования, чтобы увеличить оксигенацию и распределение питательных веществ в клетках. В соответствии с настоящим изобретением, специалист в данной области техники поймет, что может быть полезно контролировать или регулировать определенные внутренние условия биореактора во время последующей фазы роста, включая, помимо прочего, рН, температуру, оксигенацию и т. д.
В некоторых вариантах осуществления, клетки экспрессируют рекомбинантный белок, и способ культивирования клеток по изобретению включает фазу роста и фазу продуцирования.
В некоторых вариантах осуществления, стадия (ii) любого из способов, описанных в настоящем документе, применяется в течение всего способа культивирования клеток. В некоторых вариантах осуществления, стадия (ii) любого из способов, описанных в настоящем документе, применяется во время части способа культивирования клеток. В некоторых вариантах осуществления, стадию (ii) применяют до тех пор, пока не будет достигнута заданная плотность жизнеспособных клеток.
В некоторых вариантах осуществления, способ культивирования клеток по изобретению включает фазу роста и фазу продуцирования, и стадию (ii) применяют во время фазы роста. В некоторых вариантах осуществления, способ культивирования клеток по изобретению включает фазу роста и фазу продуцирования, и стадию (ii) применяют в течение части фазы роста. В некоторых вариантах осуществления, способ культивирования клеток по изобретению включает фазу роста и фазу продуцирования, и стадию (ii) применяют во время фазы роста и фазы продуцирования.
На стадии (ii) любого из описанных в настоящем документе способов, термин «поддерживание» может относиться к поддерживанию концентрации аминокислоты или метаболита ниже C1 или C2 в течение всего процесса культивирования (до сбора) или в течение части процесса культивирования, такой как, например, фаза роста, часть фазы роста или до тех пор, пока не будет получена заданная плотность клеток.
В некоторых вариантах осуществления любого из вышеупомянутых способов, рост и/или продуктивность клеток увеличиваются по сравнению с контрольной культурой, где указанная контрольная культура идентична, за исключением того, что она не включает стадию (ii).
В некоторых вариантах осуществления любого из вышеупомянутых способов, способ по изобретению представляет собой способ улучшения роста клеток. В некоторых вариантах осуществления, способ по изобретению представляет собой способ улучшения роста клеток в культуре клеток высокой плотности при высокой плотности клеток.
Высокая плотность клеток, используемая в настоящем документе, относится к плотности клеток выше 1х106 клеток/мл, 5х106 клеток/мл, 1х107 клеток/мл, 5х107 клеток/мл, 1х108 клеток/мл или 5х108 клеток/мл, предпочтительно, выше 1х107 клеток/мл, более предпочтительно, выше 5х107 клеток/мл.
В некоторых вариантах осуществления, способ по изобретению представляет собой способ улучшения роста клеток в клеточной культуре, где плотность клеток превышает 1х106 клеток/мл, 5х106 клеток/мл, 1х107 клеток/мл, 5x107 клеток/мл, 1х108 клеток/мл или 5х108 клеток/мл. В некоторых вариантах осуществления, способ по изобретению представляет собой способ улучшения роста клеток в клеточной культуре, где максимальная плотность клеток превышает 1х106 клеток/мл, 5х106 клеток/мл, 1х107 клеток/мл, 5х107 клеток/мл, 1х108 клеток/мл или 5х108 клеток/мл.
В некоторых вариантах осуществления, рост клеток определяется плотностью жизнеспособных клеток (VCD), максимальной плотностью жизнеспособных клеток или интегрированным подсчетом жизнеспособных клеток (IVCC). В некоторых вариантах осуществления, рост клеток определяется максимальной плотностью жизнеспособных клеток.
Используемый в настоящем документе термин «плотность жизнеспособных клеток» относится к числу клеток, присутствующих в данном объеме среды. Плотность жизнеспособных клеток может быть измерена любым способом, известным специалисту в данной области техники. Предпочтительно, плотность жизнеспособных клеток измеряют с использованием автоматического счетчика клеток, такого как Bioprofile Flex®. Используемый в настоящем документе термин «максимальная плотность клеток» относится к максимальной плотности клеток, достигаемой во время культивирования клеток. Используемый в настоящем документе термин «жизнеспособность клеток» относится к способности клеток в культуре выживать при заданном наборе условий культивирования или экспериментальных вариациях. Специалистам в данной области техники будет понятно, что в настоящее изобретение включен один из многих способов определения жизнеспособности клеток. Например, для определения жизнеспособности клетки можно использовать краситель (например, трипановый синий), который не проходит через мембрану живой клетки, но может проходить через разрушенную мембрану мертвой или умирающей клетки.
Термин «интегрированный подсчет жизнеспособных клеток (IVCC)», используемый в настоящем документе, относится к площади под кривой плотности жизнеспособных клеток (VCD). IVCC можно рассчитать по следующей формуле: IVCCt+1=IVCCt+(VCDt+VCDt+1)*(Δt)/2, где Δt означает разницу во времени между моментами времени t и t+1. IVCCt=0 можно не принимать в расчет. VCDt и VCDt+1 означают плотности жизнеспособных клеток в моменты времени t и t+1.
Используемый в настоящем документе термин «титр» относится, например, к общему количеству рекомбинантно экспрессированного белка, продуцируемого клеточной культурой в заданном количестве объема среды. Титр обычно выражается в граммах белка на литр среды.
В некоторых вариантах осуществления, рост клеток увеличивается, по меньшей мере, на 5%, 10%, 15%, 20% или 25% по сравнению с контрольной культурой. В некоторых вариантах осуществления, рост клеток увеличивается, по меньшей мере, на 10% по сравнению с контрольной культурой. В некоторых вариантах осуществления, рост клеток увеличивается, по меньшей мере, на 20% по сравнению с контрольной культурой.
В некоторых вариантах осуществления, продуктивность определяют по титру и/или объемной продуктивности.
Используемый в настоящем документе термин «титр» относится, например, к общему количеству рекомбинантно экспрессированного белка, продуцируемого клеточной культурой в заданном количестве объема среды. Титр обычно выражается в граммах белка на литр среды.
В некоторых вариантах продуктивность определяют по титру. В некоторых вариантах осуществления, продуктивность повышается, по меньшей мере, на 5%, 10%, 15%, 20% или 25% по сравнению с контрольной культурой. В некоторых вариантах осуществления, продуктивность увеличивается, по меньшей мере, на 10% по сравнению с контрольной культурой. В некоторых вариантах осуществления, продуктивность увеличивается, по меньшей мере, на 20% по сравнению с контрольной культурой.
В некоторых вариантах осуществления, максимальная плотность клеток клеточной культуры превышает 1х106 клеток/мл, 5х106 клеток/мл, 1х107 клеток/мл, 5х107 клеток/мл, 1х108 клеток/мл или 5х108 клеток/мл. В некоторых вариантах осуществления, максимальная плотность клеток клеточной культуры превышает 5х106 клеток/мл. В некоторых вариантах осуществления, максимальная плотность клеток в клеточной культуре превышает 1х108 клеток/мл.
V. Очистка
В некоторых вариантах осуществления, способ получения полипептида, полученного из E.coli, или его фрагмента включает выделение и/или очистку полипептида, полученного из E.coli, или его фрагмента. В некоторых вариантах осуществления, экспрессированный полипептид, полученный из E. coli, или его фрагмент секретируется в среду, и, таким образом, клетки и другие твердые вещества могут быть удалены путем центрифугирования и/или фильтрации.
Полипептид, полученный из E.coli, или его фрагмент, полученный в соответствии с описанными в настоящем документе способами, может быть получен из клеток-хозяев и очищен любым подходящим способом. Подходящие способы очистки полипептида или его фрагмента включают преципитацию и различные типы хроматографии, такие как гидрофобное взаимодействие, ионный обмен, аффинность, хелатирование и эксклюзионную хроматографию, все из которых известны в данной области техники. Подходящие схемы очистки могут включать два или несколько из этих или других подходящих способов. В некоторых вариантах осуществления, один или несколько полипептидов или их фрагментов, происходящих из E. coli может включать «метку», облегчающую очистку, такую как эпитопная метка или HIS метка, Strep метка. Такие меченые полипептиды могут быть легко очищены, например, из кондиционированных сред с помощью хелатирующей хроматографии или аффинной хроматографии. Необязательно, последовательность метки может быть расщеплена после очистки.
В некоторых вариантах осуществления, полипептид, полученный из E.coli, или его фрагмент может включать метку для аффинной очистки. Метки аффинной очистки известны в данной области техники. Примеры включают, например, His метку (связывается с ионом металла), антитело, мальтозо-связывающий белок (MBP) (связывается с амилозой), глутатион-S-трансферазу (GST) (связывается с глутатионом), FLAG метку, Strep метку (связывается со стрептавидином или его производным).
В предпочтительном варианте осуществления, полипептид, полученный из E.coli, или его фрагмент не включает метку очистки.
В некоторых вариантах осуществления, выход полипептида, полученного из E. coli, или его фрагмента составляет, по меньшей мере, примерно 1 мг/л, по меньшей мере, примерно 2 мг/л, по меньшей мере, примерно 3 мг/л, по меньшей мере, примерно 4 мг/л, по меньшей мере, примерно 5 мг/л, по меньшей мере, примерно 6 мг/л, по меньшей мере, примерно 7 мг/л, по меньшей мере, примерно 8 мг/л, по меньшей мере, примерно 9 мг/л, по меньшей мере, примерно 10 мг/л, при по меньшей мере, примерно 11 мг/л, по меньшей мере, примерно 12 мг/л, по меньшей мере, примерно 13 мг/л, по меньшей мере, примерно 14 мг/л, по меньшей мере, примерно 15 мг/л, по меньшей мере, примерно 16 мг/л, по меньшей мере, примерно 17 мг/л, по меньшей мере, примерно 18 мг/л, по меньшей мере, примерно 19 мг/л, по меньшей мере, примерно 20 мг/л, по меньшей мере, примерно 25 мг/л, по меньшей мере, примерно 30 мг/л, по меньшей мере, примерно 35 мг /л, по меньшей мере, примерно 40 мг/л, по меньшей мере, примерно 45 мг/л, по меньшей мере, примерно 50 мг/л, по меньшей мере, примерно 55 мг/л, по меньшей мере, примерно 60 мг/л, по меньшей мере, примерно 65 мг/л, по меньшей мере, примерно 70 мг/л, по меньшей мере, примерно 75 мг/л, по меньшей мере, примерно 80 мг/л, по меньшей мере, примерно 85 мг/л, по меньшей мере, примерно 90 мг/л, по меньшей мере, примерно 95 мг/л, или по меньшей мере, около 100 мг/л.
В некоторых вариантах осуществления, культура имеет размер, по меньшей мере, примерно 10 л, например, объем, по меньшей мере, примерно 10 л, по меньшей мере, примерно 20 л, по меньшей мере, примерно 30 л, по меньшей мере, примерно 40 л, по меньшей мере, примерно 50 л, по меньшей мере, примерно 60 л, по меньшей мере, примерно 70 л, по меньшей мере, примерно 80 л, по меньшей мере, примерно 90 л, по меньшей мере, примерно 100 л, по меньшей мере, примерно 150 л, по меньшей мере, примерно 200 л, по меньшей мере, примерно 250 л, по меньшей мере, примерно 300 л, по меньшей мере, примерно 400 л, по меньшей мере, примерно 500 л, по меньшей мере, примерно 600 л, по меньшей мере, примерно 700 л, по меньшей мере, примерно 800 л, по меньшей мере, примерно 900 л, по меньшей мере, примерно 1000 л, по меньшей мере, примерно 2000 л, по меньшей мере, примерно 3000 л, по меньшей мере, примерно 4000 л, по меньшей мере, примерно 5000 л, по меньшей мере, примерно 6000 л, по меньшей мере, примерно 10000 л, по меньшей мере, примерно 15000 л, по меньшей мере, примерно 20000 л, по меньшей мере, примерно 25000 л, по меньшей мере, примерно 30000 л, по меньшей мере, примерно 35000 л, по меньшей мере, примерно 40000 л, при по меньшей мере, примерно 45000 л, по меньшей мере, примерно 50000 л, по меньшей мере, примерно 55000 л, по меньшей мере, примерно 60000 л, по меньшей мере, примерно 65000 л, по меньшей мере, примерно 70000 л, по меньшей мере, примерно 75000 л, по меньшей мере, примерно 80000 л, по меньшей мере, примерно 85000 л, по меньшей мере, примерно 90000 л, по меньшей мере, примерно 95000 л, по меньшей мере, примерно 100000 л и т.д.
VI. Композиции и составы
В одном аспекте, изобретение включает композицию, которая включает полипептид, полученный из E. coli, или его фрагмент. В некоторых вариантах осуществления, композиция вызывает иммунный ответ, включая антитела, которые могут придавать иммунитет к патогенным видам E. coli.
В некоторых вариантах осуществления, композиция включает полипептид, полученный из E. coli, или его фрагмент в качестве единственного антигена. В некоторых вариантах осуществления, композиция не включает конъюгат.
В некоторых вариантах осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент и дополнительный антиген. В некоторых вариантах осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент и дополнительный антиген E.coli. В некоторых вариантах осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент, и гликоконъюгат из E.coli.
В некоторых вариантах осуществления, полипептид или его фрагмент происходят из FimH E. coli.
В некоторых вариантах осуществления, композиция включает полипептид, полученный из FimC E. coli, или его фрагмент.
В некоторых вариантах осуществления, композиция включает полипептид, полученный из FimH E. coli, или его фрагмент; и полипептид, полученный из FimC E. coli, или его фрагмент.
В одном аспекте, изобретение включает композицию, включающую полипептид, полученный из FimH E. coli, или его фрагмент; и сахарид, имеющий структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 1 до 100.
В некоторых вариантах осуществления, композиция включает один или несколько сахаридов, которые являются или получены из одного или нескольких серотипов K. pneumoniae, выбранных из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac, О3, О4, О5, О7, О8 и О12. В некоторых вариантах осуществления, композиция включает сахарид из одного или нескольких серотипов O1, O2, O3 и O5 или их комбинацию или полученный из них. В некоторых вариантах осуществления, композиция включает сахарид из каждого из серотипов K. pneumoniae O1, O2, O3 и O5 или полученный из них.
В некоторых вариантах осуществления, композиция дополнительно включает, по меньшей мере, один сахарид, полученный из любого типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5. В некоторых вариантах осуществления, композиция дополнительно включает, по меньшей мере, один сахарид, полученный из K. pneumoniae типа O1. В некоторых вариантах осуществления, композиция дополнительно включает, по меньшей мере, один сахарид, полученный из K. pneumoniae типа O2. В некоторых вариантах осуществления, композиция включает комбинацию сахаридов, где сахарид получен из любого одного из типов K. pneumoniae, выбранных из группы, состоящей из O1, O2, O3 и O5. Например, в некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, полученный из K. pneumoniae типа O1, и по меньшей мере, один сахарид, полученный из K. pneumoniae типа O2. В предпочтительном варианте осуществления, сахарид, полученный из K. pneumoniae, конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгирован с белком-носителем.
В некоторых вариантах осуществления, композиция включает любой из описанных в настоящем документе сахаридов. В предпочтительных вариантах осуществления, композиция включает любой из описанных в настоящем документе конъюгатов.
В некоторых вариантах осуществления, композиция включает, по меньшей мере, один гликоконъюгат из серотипа O25 E. coli, предпочтительно, серотипа O25b. В одном варианте осуществления, композиция включает, по меньшей мере, один гликоконъюгат из серотипа О1 Е. coli, предпочтительно, серотипа О1а. В одном варианте осуществления, композиция включает, по меньшей мере, один гликоконъюгат из серотипа О2 Е. coli. В одном варианте осуществления, композиция включает, по меньшей мере, один гликоконъюгат из серотипа О6 Е. coli.
В одном варианте осуществления, композиция включает, по меньшей мере, один гликоконъюгат, выбранный из любого из следующих серотипов O25, O1, O2 и O6 E. coli, предпочтительно, O25b, O1a, O2 и O6. В одном варианте осуществления, композиция включает, по меньшей мере, два гликоконъюгата, выбранных из любого из следующих серотипов O25, O1, O2 и O6 E. coli, предпочтительно, O25b, O1a, O2 и O6. В одном варианте осуществления, композиция включает, по меньшей мере, три гликоконъюгата, выбранных из любого из следующих серотипов O25, O1, O2 и O6 E. coli, предпочтительно, O25b, O1a, O2 и O6. В одном варианте осуществления, композиция включает гликоконъюгат каждого из следующих серотипов O25, O1, O2 и O6 E. coli, предпочтительно, O25b, O1a, O2 и O6.
В предпочтительном варианте осуществления, гликоконъюгат любой из вышеуказанных композиций индивидуально конъюгирован с CRM197.
Соответственно, в некоторых вариантах осуществления, композиция включает полипептид, полученный из E. coli, или его фрагмент; и О-антиген, по меньшей мере, из одного серотипа E.coli. В предпочтительном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из более чем 1 серотипа E. coli. Например, композиция может включать О-антиген от двух разных серотипов E.coli (или «v», валентность) до 12 различных серотипов (12v). В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 3 разных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 4 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-антиген из 5 различных серотипов E.coli. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 6 различных серотипов E. coli. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 7 различных серотипов E. coli. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 8 различных серотипов E. coli. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 9 различных серотипов E. coli. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 10 различных серотипов E. coli. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 11 различных серотипов E. coli. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 12 различных серотипов. В одном варианте осуществления композиция, включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 13 различных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 14 различных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 15 различных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 16 различных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 17 различных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 18 различных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 19 различных серотипов. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 20 различных серотипов.
Предпочтительно, количество сахаридов E. coli может варьироваться от 1 серотипа (или «v», валентности) до 26 различных серотипов (26v). В одном варианте осуществления, имеется один серотип. В одном варианте осуществления, имеется 2 различных серотипа. В одном варианте осуществления, имеется 3 различных серотипа. В одном варианте осуществления, имеется 4 различных серотипа. В одном варианте осуществления, имеется 5 различных серотипов. В одном варианте осуществления, имеется 6 различных серотипов. В одном варианте осуществления, имеется 7 различных серотипов. В одном варианте осуществления, имеется 8 различных серотипов. В одном варианте осуществления, имеется 9 различных серотипов. В одном варианте осуществления, имеется 10 различных серотипов. В одном варианте осуществления, имеется 11 различных серотипов. В одном варианте осуществления, имеется 12 различных серотипов. В одном варианте осуществления, имеется 13 различных серотипов. В одном варианте осуществления, имеется 14 различных серотипов. В одном варианте осуществления, имеется 15 различных серотипов. В одном варианте осуществления, имеется 16 различных серотипов. В одном варианте осуществления, имеется 17 различных серотипов. В одном варианте осуществления, имеется 18 различных серотипов. В одном варианте осуществления, имеется 19 различных серотипов. В одном варианте осуществления, имеется 20 различных серотипов. В одном варианте осуществления, имеется 21 различный серотип. В одном варианте осуществления, имеется 22 различных серотипа. В одном варианте осуществления, имеется 23 различных серотипа. В одном варианте осуществления, имеется 24 различных серотипа. В варианте осуществления, существует 25 различных серотипов. В одном варианте осуществления, имеется 26 различных серотипов. Сахариды конъюгируют с белком-носителем с образованием гликоконъюгатов, как описано в настоящем документе.
В одном аспекте, композиция включает полипептид, полученный из E.coli, или его фрагмент; и гликоконъюгат, который включает О-антиген, по меньшей мере, из одной серогруппы E. coli, где О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из более чем 1 серотипа E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 2 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 3 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 4 различных серотипов E.coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 5 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 6 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 7 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 8 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 9 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-антиген из полипептида, полученного из E. coli, или его фрагмент; и 10 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-антиген из полипептида, полученного из E. coli, или его фрагмент; и 11 различных серотипов E. coli, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 12 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 13 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 14 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 15 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 16 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 17 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 18 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 19 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-антиген из 20 различных серотипов, где каждый О-антиген конъюгирован с белком-носителем.
В другом аспекте, композиция включает О-полисахарид, по меньшей мере, одного серотипа E.coli. В предпочтительном варианте композиция включает О-полисахарид из более чем 1 серотипа E. coli. Например, композиция может включать О-полисахарид из от двух различных серотипов E.coli до 12 различных серотипов E.coli. В одном варианте осуществления, композиция включает О-полисахарид из 3 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 4 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 5 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 6 различных серотипов E.coli. В одном варианте осуществления, композиция включает О-полисахарид из 7 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 8 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 9 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 10 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 11 различных серотипов E. coli. В одном варианте осуществления, композиция включает О-полисахарид из 12 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 13 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 14 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 15 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 16 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 17 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 18 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 19 различных серотипов. В одном варианте осуществления, композиция включает О-полисахарид из 20 различных серотипов.
В предпочтительном варианте осуществления, композиция включает О-полисахарид, по меньшей мере, из одного серотипа E. coli, где О-полисахарид конъюгирован с белком-носителем. В предпочтительном варианте осуществления, композиция включает О-полисахарид из более чем 1 серотипа E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. Например, композиция может включать О-полисахарид от двух различных серотипов E.coli до 12 различных серотипов E.coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 3 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 4 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 5 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 6 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 7 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 8 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 9 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 10 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 11 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 12 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 13 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 14 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 15 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 16 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 17 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 18 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 19 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем. В одном варианте осуществления, композиция включает О-полисахарид из 20 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем.
В наиболее предпочтительном варианте осуществления, композиция включает O-полисахарид, по меньшей мере, из одного серотипа E. coli, где О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В предпочтительном варианте осуществления, композиция включает О-полисахарид из более чем 1 серотипа E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. Например, композиция может включать О-полисахарид от двух разных серотипов E. coli до 12 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и основной сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 3 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 4 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 5 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 6 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 7 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 8 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 9 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 10 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 11 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 12 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и при этом О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 13 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и при этом О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 14 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 15 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 16 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и при этом О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 17 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и при этом О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 18 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 19 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает О-полисахарид из 20 различных серотипов, где каждый О-полисахарид конъюгирован с белком-носителем, и при этом О-полисахарид включает О-антиген и коровый сахарид. В предпочтительном варианте осуществления, белок-носитель представляет собой CRM197.
В другом предпочтительном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O25a, где n равно, по меньшей мере, 40, и коровый сахарид. В предпочтительном варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O25b, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O1a, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О2, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О6, где n равно, по меньшей мере, 40, и коровый сахарид.
В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О17, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает O-полисахарид, конъюгированный с CRM197, где O-полисахарид включает формулу O15, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O18A, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О75, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О4, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O16, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O13, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О7, где n равно, по меньшей мере, 40, и основной сахарид.
В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О8, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, О-полисахарид включает формулу О8, где n равно 1-20, предпочтительно, 2-5, более предпочтительно, 3. Формула О8 показана, например, на ФИГ. 10В. В другом варианте осуществления, композиция дополнительно включает О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О9, где n равно, по меньшей мере, 40, и коровый сахарид. В другом варианте осуществления, О-полисахарид включает формулу О9, где n равно 1-20, предпочтительно, 4-8, более предпочтительно, 5. Формула О9 показана, например, на ФИГ. 10В. В другом варианте осуществления, О-полисахарид включает формулу O9a, где n равно 1-20, предпочтительно, 4-8, более предпочтительно, 5. Формула O9a показана, например, на ФИГ. 10В.
В некоторых вариантах осуществления изобретения, О-полисахарид выбран из Формулы O20ab, Формулы O20ac, Формулы O52, Формулы O97 и Формулы O101, где n равно 1-20, предпочтительно, 4-8, более предпочтительно, 5. См., например, ФИГ. 10В.
Как описано выше, композиция может включать полипептид, полученный из E.coli, или его фрагмент; и любую комбинацию конъюгированных О-полисахаридов (антигенов). В одном примерном варианте осуществления, композиция включает полисахарид, который включает Формулу O25b, полисахарид, который включает Формулу O1A, полисахарид, который включает Формулу O2, и полисахарид, который включает Формулу O6. Более конкретно, такая композиция, которая включает: (i) О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O25b, где n равно, по меньшей мере, 40, и основной сахарид; (ii) О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу O1a, где n равно, по меньшей мере, 40, и коровый сахарид; (iii) О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает Формулу О2, где n равно, по меньшей мере, 40, и коровый сахарид; и (iv) О-полисахарид, конъюгированный с CRM197, где О-полисахарид включает формулу О6, где n равно, по меньшей мере, 40, и основной сахарид.
В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и, по меньшей мере, один O-полисахарид, полученный из любого серотипа E. coli, где серотип не является O25a. Например, в одном варианте осуществления, композиция не включает сахарид, который включает Формулу O25a. Такая композиция может включать, например, О-полисахарид, который включает Формулу O25b, О-полисахарид, который включает Формулу O1A, О-полисахарид, который включает Формулу O2, и О-полисахарид, который включает Формулу O6.
В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 2 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 3 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 4 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 5 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 6 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 7 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 8 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 9 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 10 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 11 различных серотипов E. coli, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 12 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 13 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 14 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 15 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 16 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 17 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 18 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 19 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид. В одном варианте осуществления, композиция включает полипептид, полученный из E.coli, или его фрагмент; и О-полисахарид из 20 различных серотипов, где каждый О-полисахарид конъюгирован с CRM197, и где О-полисахарид включает О-антиген и коровый сахарид.
В одном аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E.coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает Формулу O25b, где n равно 15 ± 2. В одном аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E. coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает Формулу O25b, где n равно 17 ± 2. В одном аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E. coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает Формулу O25b, где n равно 55 ± 2. В другом аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E. coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает Формулу O25b, где n равно 51 ± 2. В одном варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R1. В другом варианте осуществления, сахарид дополнительно включает коровую сахаридную часть E. coli K12. В другом варианте осуществления, сахарид дополнительно включает фрагмент KDO. Предпочтительно, белок-носитель представляет собой CRM197. В одном варианте осуществления, конъюгат получают путем односторонне-связанной конъюгации. В одном варианте осуществления, конъюгат получают химическим методом восстановительного аминирования, предпочтительно в ДМСО буфере. В одном варианте осуществления, сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC). Предпочтительно, композиция дополнительно включает фармацевтически приемлемый разбавитель.
В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны связывать полисахарид E. coli серотипа O25B в концентрации, по меньшей мере, 0,2 пг/мл, 0,3 пг/мл, 0,35 пг/мл, 0,4 пг/мл или 0,5 пг/мл по данным анализа ELISA. Таким образом, можно провести сравнение активности OPA в сыворотке до и после иммунизации с иммуногенной композицией по изобретению и сравнить их реакцию на серотип O25B, чтобы оценить потенциальное увеличение числа пациентов, ответивших на лечение. В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны убивать E. coli серотипа O25B по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция вырабатывает функциональные антитела у людей, где указанные антитела способны убивать серотип O25B E. coli по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению увеличивает долю пациентов, ответивших на лечение против серотипа O25B E. coli (т.е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция вызывает титр, по меньшей мере, 1:8 против серотипа O25B E. coli, по меньшей мере, у 50% субъектов по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению вызывает титр, по меньшей мере, 1:8 против серотипа O25B E. coli, по меньшей мере, у 60%, 70%, 80% или, по меньшей мере, 90% субъектов, по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает долю пациентов, ответивших на лечение против серотипа O25B E. coli (т.е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает титры ОРА у людей против серотипа O25B E. coli по сравнению с предварительно иммунизированной популяцией.
В одном аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E.coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O1a, где n равно 39 ± 2. В другом аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E. coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O1a, где n равно 13 ± 2. В одном варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R1. В одном варианте осуществления, сахарид дополнительно включает фрагмент KDO. Предпочтительно, белок-носитель представляет собой CRM197. В одном варианте осуществления, конъюгат получают путем односторонне-связанной конъюгации. В одном варианте осуществления, конъюгат получают химическим способом восстановительного аминирования, предпочтительно в ДМСО буфере. В одном варианте осуществления, сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC). Предпочтительно, композиция дополнительно включает фармацевтически приемлемый разбавитель.
В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны связывать полисахарид серотип O1A E. coli в концентрации, по меньшей мере, 0,2 пг/мл, 0,3 пг/мл, 0,35 пг/мл, 0,4 пг/мл или 0,5 пг/мл по данным анализа ELISA. Таким образом, можно провести сравнение ОРА активности сыворотки до и после иммунизации иммуногенной композицией по изобретению и сравнить их ответ на серотип О1А, чтобы оценить потенциальное увеличение числа пациентов, ответивших на лечение. В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны убивать серотип O1A E. coli по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция индуцирует функциональные антитела у людей, где указанные антитела способны убивать серотип О1А Е. coli по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению увеличивает долю пациентов, ответивших на лечение против серотипа O1A E. coli (т.е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция вызывает титр, по меньшей мере, 1:8 против серотипа O1A E. coli, по меньшей мере, у 50% субъектов по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению вызывает титр, по меньшей мере, 1:8 против серотипа O1A E. coli, по меньшей мере, у 60%, 70%, 80% или, по меньшей мере, 90% субъектов по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает долю пациентов, ответивших на лечение против серотипов O1A E. coli (т.е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает титры ОРА у людей против серотипа О1А Е. coli по сравнению с предварительно иммунизированной популяцией.
В одном аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E.coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O2, где n равно 43 ± 2. В другом аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E. coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O2, где n равно 47 ± 2. В другом аспекте, изобретение относится к композиции, которая включает конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O2, где n равно 17 ± 2. В другом аспекте, изобретение относится к композиции, которая включает конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O2, где n равно 18 ± 2. В одном варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R1. В другом варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R4. В другом варианте осуществления, сахарид дополнительно включает фрагмент KDO. Предпочтительно, белок-носитель представляет собой CRM197. В одном варианте осуществления, конъюгат получают путем односторонне-связанной конъюгации. В одном варианте осуществления, конъюгат получают химическим способом восстановительного аминирования, предпочтительно в ДМСО буфере. В одном варианте осуществления, сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC). Предпочтительно, композиция дополнительно включает фармацевтически приемлемый разбавитель.
В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны связывать полисахарид серотип O2 E. coli в концентрации, по меньшей мере, 0,2 пг/мл, 0,3 пг/мл, 0,35 пг/мл, 0,4 пг/мл или 0,5 пг/мл по данным анализа ELISA. Таким образом, можно провести сравнение ОРА активности сыворотки до и после иммунизации с иммуногенной композицией по изобретению и сравнить их ответ на серотип О2, чтобы оценить потенциальное увеличение пациентов, ответивших на лечение. В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны убивать серотип О2 Е. coli по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция вырабатывает у людей функциональные антитела, где указанные антитела способны убивать серотип О2 Е. coli по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению увеличивает долю пациентов, ответивших на лечение против серотипа О2 E. coli (т.е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция вызывает титр, по меньшей мере, 1:8 против серотипа О2 Е. coli, по меньшей мере, у 50% субъектов по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению вызывает титр, по меньшей мере, 1:8 против серотипа О2 E. coli, по меньшей мере, у 60%, 70%, 80% или, по меньшей мере, 90% субъектов по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает долю пациентов, ответивших на лечение против серотипа O2 E. coli (т.е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает титры ОРА у людей против серотипа О2 Е. coli по сравнению с предварительно иммунизированной популяцией.
В одном аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E.coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает Формулу O6, где n равно 42 ± 2. В другом аспекте, изобретение относится к композиции, которая включает полипептид, полученный из E. coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O6, где n равно 50 ± 2. В другом аспекте, изобретение относится к композиции, которая включает конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O6, где n равно 17 ± 2. В другом аспекте, изобретение относится к композиции, которая включает конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид включает формулу O6, где n равно 18 ± 2. В одном варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R1. В одном варианте осуществления, сахарид дополнительно включает фрагмент KDO. Предпочтительно белок-носитель представляет собой CRM197. В одном варианте осуществления, конъюгат получают путем односторонне-связанной конъюгации. В одном варианте осуществления, конъюгат получают химическим способом восстановительного аминирования, предпочтительно в ДМСО буфере. В одном варианте осуществления, сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC). Предпочтительно, композиция дополнительно включает фармацевтически приемлемый разбавитель.
В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны связывать полисахарид серотипа O6 E. coli в концентрации, по меньшей мере, 0,2 пг/мл, 0,3 пг/мл, 0,35 пг/мл, 0,4 пг/мл или 0,5 пг/мл по данным анализа ELISA. Таким образом, можно провести сравнение ОРА активности сыворотки до и после иммунизации с иммуногенной композицией по изобретению и сравнить их ответ на серотип О6, чтобы оценить потенциальное увеличение числа пациентов, ответивших на лечение. В одном варианте осуществления, иммуногенная композиция индуцирует антитела IgG у людей, где указанные антитела способны убивать серотип О6 Е. coli по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция вырабатывает у людей функциональные антитела, где указанные антитела способны убивать серотип О6 Е. coli по данным опсонофагоцитарного анализа in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению увеличивает долю пациентов, ответивших на лечение против серотипа О6 E. coli (т. е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция вызывает титр, по меньшей мере, 1:8 против серотипа О6 Е. coli, по меньшей мере, у 50% субъектов по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению вызывает титр, по меньшей мере, 1:8 против серотипа О6 E. coli, по меньшей мере, у 60%, 70%, 80% или, по меньшей мере, 90% субъектов по данным анализа опсонофагоцитарного уничтожения in vitro. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает долю пациентов, ответивших на лечение против серотипов O6 E. coli (т.е. индивидуумов с сывороткой, имеющей титр, по меньшей мере, 1:8 по данным OPA in vitro) по сравнению с предварительно иммунизированной популяцией. В одном варианте осуществления, иммуногенная композиция по изобретению значительно увеличивает титры ОРА у людей против серотипа О6 Е. coli по сравнению с предварительно иммунизированной популяцией.
В одном аспекте, композиция включает полипептид, полученный из E.coli, или его фрагмент; и конъюгат, включающий сахарид, ковалентно связанный с белком-носителем, где сахарид имеет структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 1 до 100. В одном варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R1. В одном варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R2. В одном варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R3. В другом варианте осуществления, сахарид дополнительно включает коровую сахаридную группу E. coli R4. В одном варианте осуществления, сахарид дополнительно включает сахаридную часть ядра E. coli K12. В другом варианте осуществления, сахарид дополнительно включает фрагмент KDO. Предпочтительно белок-носитель представляет собой CRM197. В одном варианте осуществления, конъюгат получают путем односторонне-связанной конъюгации. В одном варианте осуществления, конъюгат получают химическим способом восстановительного аминирования, предпочтительно в ДМСО буфере. В одном варианте осуществления, сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC). Предпочтительно, композиция дополнительно включает фармацевтически приемлемый разбавитель. В одном варианте осуществления, композиция дополнительно включает, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 дополнительных конъюгатов до не более чем 30 дополнительных конъюгатов, где каждый конъюгат включает сахарид, ковалентно связанный с белком-носителем, где сахарид включает структуру, выбранную из любой из указанных Формул.
А. Сахарид
В одном варианте осуществления, сахарид получают путем экспрессии (не обязательно сверхэкспрессии) различных белков Wzz (например, WzzB) для контроля размера сахарида.
Используемый в настоящем документе термин «сахарид» относится к одной сахарной группе или моносахаридной единице, а также к комбинациям двух или нескольких отдельных сахарных групп или моносахаридных единиц, ковалентно связанных с образованием дисахаридов, олигосахаридов и полисахаридов. Сахарид может быть линейным или разветвленным.
В одном варианте осуществления, сахарид продуцируется рекомбинантной грамотрицательной бактерией. В одном варианте осуществления, сахарид продуцируется в рекомбинантной клетке E.coli. В одном варианте осуществления, сахарид продуцируется в рекомбинантной клетке Salmonella. Примеры бактерий включают E. coli O25K5H1, E. coli BD559, E. coli GAR2831, E. coli GAR865, E. coli GAR868, E. coli GAR869, E. coli GAR872, E. coli GAR878, E. coli GAR896, E. coli GAR1902, E. coli O25a ETC NR-5, E. coli O157:H7:K-, Salmonella enterica серотип Typhimurium, штамм LT2, E. coli GAR2401, Salmonella enterica серотип Enteritidis CVD 1943, Salmonella enterica серотип Typhimurium CVD 1925, Salmonella enterica серотип Paratyphi A CVD 1902 и Shigella flexneri CVD 1208S. В одном варианте осуществления, бактерия не является E.coli GAR2401. Этот генетический подход к продуцированию сахаридов позволяет эффективно производить О-полисахариды и молекулы О-антигена в качестве компонентов вакцины.
Термин «белок wzz», используемый в настоящем документе, относится к полипептиду, определяющему длину цепи, такому как, например, wzzB, wzz, wzzSF, wzzST, fepE, wzzfepE, wzzl и wzz2. Номера доступа GenBank для типовых последовательностей генов wzz: AF011910 для E4991/76, AF011911 для F186, AF011912 для M70/1-1, AF011913 для 79/311, AF011914 для Bi7509- 41, AF011915 для C664-1992, AF011916 для C258-94, AF011917 для C722-89 и AF011919 для EDL933. Номера доступа GenBank для последовательностей генов G7 и Bi316-41 wzz: U39305 и U39306, соответственно. Дополнительные номера доступа в GenBank для типовых последовательностей генов wzz: NP_459581 для Salmonella enterica подвид enterica, серовар Typhimurium str. LT2 FepE; AIG66859 для штамма E. coli O157:H7 EDL933 FepE; NP_461024 для Salmonella enterica подвид enterica, серовар Typhimurium str. LT2 WzzB. NP_416531 для E. coli K-12 подштамм MG1655 WzzB, NP_415119 для E. coli K-12 подштамм MG1655 FepE. В предпочтительных вариантах осуществления, белок семейства wzz представляет собой любой из белков wzzB, wzz, wzzSF, wzzST, fepE, wzzfepE, wzz1 и wzz2, наиболее предпочтительно, wzzB, более предпочтительно, fepE.
Примеры последовательностей wzzB включают последовательности, представленные в SEQ ID No: 30-34. Примеры последовательностей FepE включают последовательности, представленные в SEQ ID No: 35-39.
В некоторых вариантах осуществления, модифицированный сахарид (модифицированный по сравнению с соответствующим сахаридом дикого типа) может быть получен путем экспрессии (не обязательно сверхэкспрессии) белка семейства wzz (например, fepE) из грамотрицательной бактерии в грамотрицательной бактерии и/или путем выключения (т.е. репрессии, делеции, удаления) второго гена wzz (например, wzzB) для получения высокомолекулярных сахаридов, таких как липополисахариды, содержащие промежуточные или длинные цепи О-антигена. Например, модифицированные сахариды могут быть получены путем экспрессии (не обязательно сверхэкспрессии) wzz2 и выключения wzzl. Или, альтернативно, модифицированные сахариды могут быть получены путем экспрессии (не обязательно сверхэкспрессии) wzzfepE и выключения wzzB. В другом варианте осуществления, модифицированные сахариды могут быть получены путем экспрессии (не обязательно сверхэкспрессии) wzzB, но отключения wzzfepE. В другом варианте осуществления, модифицированные сахариды могут быть получены путем экспрессии fepE. Предпочтительно, белок семейства wzz получают из штамма, гетерологичного клетке-хозяину.
В некоторых вариантах осуществления сахарид получают путем экспрессии белка семейства wzz, имеющего аминокислотную последовательность, которая имеет, по меньшей мере, 30%, 50%, 70%, 75%, 80%, 85%, 90%, 95%, 98% 99% или 100% идентичность последовательности любой из SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38 и SEQ ID NO: 39. В одном варианте осуществления, белок семейства wzz включает последовательность, выбранную из любой из SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38 и SEQ ID NO: 39. Предпочтительно, белок семейства wzz имеет, по меньшей мере, 30%, 50%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% идентичность последовательности с SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34. В некоторых вариантах осуществления, сахарид получают путем экспрессии белка, аминокислотная последовательность которого имеет, по меньшей мере, 30%, 50% 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% идентичность последовательности белка fepE.
В одном аспекте, изобретение относится к сахаридам, полученным путем экспрессии белка семейства wzz, предпочтительно fepE, в грамотрицательной бактерии с образованием высокомолекулярных сахаридов, содержащих промежуточные или длинные цепи О-антигена, которые имеют увеличение, по меньшей мере, на 1, 2, 3, 4 или 5 повторяющихся единиц по сравнению с соответствующим О-полисахаридом дикого типа. В одном аспекте, изобретение относится к сахаридам, продуцируемым грамотрицательной бактерией в культуре, которая экспрессирует (не обязательно сверхэкспрессирует) белок семейства wzz (например, wzzB) из грамотрицательной бактерии для получения высокомолекулярных сахаридов, содержащих короткие или промежуточные или длинные цепи О-антигена, которые имеют увеличение, по меньшей мере, на 1, 2, 3, 4 или 5 повторяющихся единиц по сравнению с соответствующим О-антигеном дикого типа. См. описание О-полисахаридов и О-антигенов ниже для дополнительных иллюстративных сахаридов, имеющих увеличенное количество повторяющихся единиц по сравнению с соответствующими сахаридами дикого типа. Желаемой длиной цепи является длина цепи, обеспечивающая улучшенную или максимальную иммуногенность в контексте данной конструкции вакцины.
В другом варианте осуществления, сахарид включает любую Формулу, выбранную из Таблицы 1, где количество повторяющихся звеньев n в сахариде больше, чем количество повторяющихся звеньев в соответствующем O-полисахариде дикого типа на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 или более повторяющихся единиц. Предпочтительно, сахарид включает увеличение, по меньшей мере, на 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50 повторяющихся единиц по сравнению с соответствующим О-полисахаридом дикого типа. См., например, Таблицу 24. Способы определения длины сахаридов известны в данной области техники. Такие способы включают ядерный магнитный резонанс, масс-спектроскопию и эксклюзионную хроматографию, как описано в примере 13.
В предпочтительном варианте осуществления, изобретение относится к сахариду, продуцируемому в рекомбинантной клетке-хозяине E. coli, где ген эндогенного регулятора длины О-антигена wzz (например, wzzB) удален и заменен (вторым) геном wzz из грамотрицательной бактерии, гетерологичной рекомбинантной клетке-хозяину E. coli (например, Salmonella fepE), с образованием высокомолекулярных сахаридов, таких как липополисахариды, содержащие промежуточные или длинные цепи О-антигена. В некоторых вариантах осуществления, рекомбинантная клетка-хозяин E.coli включает ген wzz из Salmonella, предпочтительно из Salmonella enterica. В других вариантах осуществления, изобретение применимо ко всем штаммам E.coli, экспрессирующим О-антигены, регулируемые wzzB. В одном аспекте, штаммы E. coli серотипа O8 и O9, которые продуцируют О-антигены, состоящие из гомополимерных маннанов, не продуцируются в соответствии с этим вариантом осуществления, поскольку они используют разные механизмы для регуляции длины цепи и транспорта LPS к наружной мембране (J Biol Chem 2009; 284:30662-72; J Biol Chem 2012; 287:35078-91; Proceedings of the National Academy of Sciences 2014; 111:6407-12). В дополнительном варианте осуществления, гомополимерные галактаны полисахариды Klebsiella серотипов О1 и О2 получают в соответствии со способом, изложенным в этом варианте осуществления.
В одном варианте осуществления, клетка-хозяин включает гетерологичный ген белка семейства wzz в виде стабильно поддерживаемого плазмидного вектора. В другом варианте осуществления, клетка-хозяин включает гетерологичный ген белка семейства wzz в качестве встроенного гена в хромосомную ДНК клетки-хозяина. Способы стабильной экспрессии плазмидного вектора в клетке-хозяине E.coli и способы интеграции гетерологичного гена в хромосому клетки-хозяина E.coli известны в данной области техники. В одном варианте осуществления, клетка-хозяин включает гетерологичные гены О-антигена в виде стабильно поддерживаемого плазмидного вектора. В другом варианте осуществления, клетка-хозяин включает гетерологичные гены О-антигена в виде встроенного гена в хромосомную ДНК клетки-хозяина. Способы стабильной экспрессии плазмидного вектора в клетке-хозяине E.coli и клетке-хозяине Salmonella известны в данной области техники. Способы интеграции гетерологичного гена в хромосому клетки-хозяина E.coli и клетки-хозяина Salmonella известны в данной области техники.
В одном аспекте, рекомбинантную клетку-хозяин культивируют в среде, содержащей источник углерода. Источники углерода для культивирования E.coli известны в данной области техники. Примеры источников углерода включают сахарные спирты, полиолы, альдольные сахара или кетосахара, включая арабинозу, целлобиозу, фруктозу, глюкозу, глицерин, инозит, лактозу, мальтозу, маннит, маннозу, рамнозу, раффинозу, сорбит, сорбозу, сахарозу, трегалозу, пируват, сукцинат и метиламин. В предпочтительном варианте осуществления, среда включает глюкозу. В некоторых вариантах осуществления, среда включает полиол или альдольный сахар, например, маннит, инозит, сорбозу, глицерин, сорбит, лактозу и арабинозу в качестве источника углерода. Все источники углерода могут быть добавлены в среду до начала культивирования, либо их можно добавлять поэтапно или непрерывно во время культивирования.
Типовая культуральная среда для рекомбинантной клетки-хозяина включает элемент, выбранный из любого из KH2PO4, K2HPO4, (NH4)2SO4, цитрата натрия, Na2SO4, аспарагиновой кислоты, глюкозы, MgSO4, FeSO4-7H2O, Na2MoO4-2H2O, H3BO3, CoCl2-6H2O, CuCl2-2H2O, MnCl2-4H2O, ZnCl2 и CaCl2-2H2O. Предпочтительно, среда включает KH2PO4, K2HPO4, (NH4)2SO4, цитрат натрия, Na2SO4, аспарагиновую кислоту, глюкозу, MgSO4, FeSO4-7H2O, Na2MoO4-2H2O, H3BO3, CoCl2-6H2O, CuCl2-2H2O, MnCl2-4H2O, ZnCl2 и CaCl2-2H2O.
Используемая в настоящем документе среда может быть твердой или жидкой, синтетической (т.е. искусственной) или природной, и может включать достаточное количество питательных веществ для культивирования рекомбинантной клетки-хозяина. Предпочтительно, среда представляет собой жидкую среду.
В некоторых вариантах осуществления, среда может дополнительно включать подходящие неорганические соли. В некоторых вариантах осуществления, среда может дополнительно включать микроэлементы питательных веществ. В некоторых вариантах осуществления, среда может дополнительно включать факторы роста. В некоторых вариантах осуществления, среда может дополнительно включать дополнительный источник углерода. В некоторых вариантах осуществления, среда может дополнительно включать подходящие неорганические соли, микроэлементы, факторы роста и дополнительный источник углерода. Неорганические соли, следовые питательные вещества, факторы роста и дополнительные источники углерода, подходящие для культивирования E. coli, известны в данной области техники.
В некоторых вариантах осуществления, среда может включать дополнительные компоненты, по мере необходимости, такие как пептон, N-Z амин, ферментативный гидрозилат сои, дополнительный дрожжевой экстракт, солодовый экстракт, дополнительные источники углерода и различные витамины. В некоторых вариантах осуществления, среда не включает такие дополнительные компоненты, как пептон, N-Z амин, ферментативный гидрозилат сои, дополнительный дрожжевой экстракт, солодовый экстракт, дополнительные источники углерода и различные витамины.
Иллюстративные примеры подходящих дополнительных источников углерода включают, но не ограничены ими, другие углеводы, такие как глюкоза, фруктоза, маннит, крахмал или гидролизат крахмала, гидролизат целлюлозы и меласса; органические кислоты, такие как уксусная кислота, пропионовая кислота, молочная кислота, муравьиная кислота, яблочная кислота, лимонная кислота и фумаровая кислота; и спирты, такие как глицерин, инозит, маннит и сорбит.
В некоторых вариантах осуществления, среда дополнительно включает источник азота. Источники азота, подходящие для культивирования E.coli, известны в данной области техники. Иллюстративные примеры подходящих источников азота включают, но не ограничены ими, аммиак, включая газообразный аммиак и водный раствор аммиака; аммониевые соли неорганических или органических кислот, такие как хлорид аммония, нитрат аммония, фосфат аммония, сульфат аммония и ацетат аммония; мочевину; нитратные или нитритные соли и другие азотсодержащие материалы, включая аминокислоты в чистом или неочищенном виде, мясной экстракт, пептон, рыбную муку, рыбный гидролизат, кукурузный экстракт, гидролизат казеина, гидролизат соевого жмыха, дрожжевой экстракт, сухие дрожжи, этанол-дрожжевой дистиллят, соевую муку, хлопковую муку и подобные.
В некоторых вариантах осуществления, среда включает неорганическую соль. Иллюстративные примеры подходящих неорганических солей включают, но не ограничены ими, соли калия, кальция, натрия, магния, марганца, железа, кобальта, цинка, меди, молибдена, вольфрама и других микроэлементов, и фосфорную кислоту.
В некоторых вариантах осуществления, среда включает соответствующие факторы роста. Иллюстративные примеры подходящих микроэлементов, факторов роста и подобных включают, но не ограничены ими, коэнзим А, пантотеновую кислоту, пиридоксин-HCl, биотин, тиамин, рибофлавин, флавин мононуклеотид, флавин адениндинуклеотид, DL-6,8-тиоктовую кислоту, фолиевую кислоту, витамин B12, другие витамины, аминокислоты, такие как цистеин и гидроксипролин, основания, такие как аденин, урацил, гуанин, тимин и цитозин, тиосульфат натрия, п- или р-аминобензойную кислоту, ниацинамид, нитрилоацетат и другие например, в виде чистых или частично очищенных химических соединений или в виде природных материалов. Количества могут быть определены эмпирически специалистом в данной области техники в соответствии со способами и методиками, известными в данной области техники.
В другом варианте осуществления, описанный в настоящем документе модифицированный сахарид (по сравнению с соответствующим сахаридом дикого типа) получают синтетическим путем, например, in vitro. Синтетическое продуцирование или синтез сахаридов может способствовать отказу от дорогостоящих и длительных процессов продуцирования. В одном варианте осуществления, сахарид синтезируется синтетическим путем, например, с использованием стратегии последовательного гликозилирования или комбинации последовательного гликозилирования и стратегии [3+2] блока синтеза из подходящим образом защищенных моносахаридных промежуточных соединений. Например, тиогликозиды и производные гликозилтрихлорацетимидата могут быть использованы в качестве доноров гликозила при гликозилировании. В одном варианте осуществления, сахарид, который синтетически синтезирован in vitro, имеет структуру, идентичную сахариду, полученному рекомбинантными способами, такими как манипулирование белком семейства wzz, описанным выше.
Сахарид, полученный (с помощью рекомбинантных или синтетических средств), имеет структуру, полученную из любого серотипа E. coli, включая, например, любой из следующих серотипов E. coli: O1 (например, O1A, O1B и O1C), O2, O3, O4 (например, O4:K52 и O4:K6), O5 (например, O5ab и O5ac (штамм 180/C3)), O6 (например, O6:K2; K13; K15 и O6:K54), O7, O8, O9, O10, O11, O12, O13, O14, O15, O16, O17, O18 (например, O18A, O18ac, O18A1, O18B и O18B1), O19, O20, O21, O22, O23 (например, O23A), O24, O25 (например, O25a и O25b), O26, O27, O28, O29, O30, O32, O33, O34, O35, O36, O37, O38, O39, O40, O41, O42, O43, O44, O45 (например, O45 и O45rel), O46, O48, O49, O50, O51, O52, O53, O54, O55, O56, O57, O58, O59, O60, O61, O62, 62D1, O63, O64, O65, O66, O68, O69, O70, O71, O73 (например, O73 (штамм 73-1)), O74, O75, O76, O77, O78, O79, O80, O81, O82, O83, O84, O85, O86, O87, O88, O89, O90, O91, O92, O93, O95, O96, O97, O98, O99, O100, O101, O102, O103, O104, O105, O106, O107, O108, O109, O110, 0111, O112, O113, O114, O115, O116, O117, O118, O119, O120, O121, O123, O124, O125, O126, O127, O128, O129, O130, O131, O132, O133, O134, O135, O136, O137, O138, O139, O140, O141, O142, O143, O144, O145, O146, O147, O148, O149, O150, O151, O152, O153, O154, O155, O156, O157, O158, O159, O160, O161, O162, O163, O164, O165, O166, O167, O168, O169, O170, O171, O172, O173, O174, O175, O176, O177, O178, O179, O180, O181, O182, O183, O184, O185, O186 и O187.
Индивидуальные полисахариды обычно очищают (обогащают по отношению к количеству конъюгата полисахарид-белок) способами, известными в данной области техники, такими как, например, диализ, операции концентрирования, операции диафильтрации, фильтрация в тангенциальном потоке, осаждение, элюирование, центрифугирование, преципитация, ультрафильтрация, глубинная фильтрация и/или колоночная хроматография (ионообменная хроматография, мультимодальная ионообменная хроматография, ДЭАЭ и хроматография гидрофобного взаимодействия). Полисахариды предпочтительно очищают способом, который включает фильтрацию с тангенциальным потоком.
Очищенные полисахариды могут быть активированы (например, химически активированы), чтобы сделать их способными реагировать (например, либо непосредственно с белком-носителем, либо через линкер, такой как спейсер eTEC), и затем включаться в гликоконъюгаты по изобретению, как дополнительно описано в настоящем документе.
В одном предпочтительном варианте осуществления, сахарид по изобретению получают из серотипа E. coli, где серотип представляет собой O25a. В другом предпочтительном варианте осуществления, серотип представляет собой O25b. В другом предпочтительном варианте осуществления, серотип представляет собой O1A. В другом предпочтительном варианте осуществления, серотип представляет собой О2. В другом предпочтительном варианте осуществления, серотип представляет собой О6. В другом предпочтительном варианте осуществления, серотип представляет собой O17. В другом предпочтительном варианте осуществления, серотип представляет собой O15. В другом предпочтительном варианте осуществления, серотип представляет собой O18A. В другом предпочтительном варианте осуществления, серотип представляет собой O75. В другом предпочтительном варианте осуществления, серотип представляет собой О4. В другом предпочтительном варианте осуществления, серотип представляет собой O16. В другом предпочтительном варианте осуществления, серотип представляет собой O13. В другом предпочтительном варианте осуществления, серотип представляет собой О7. В другом предпочтительном варианте осуществления, серотип представляет собой О8. В другом предпочтительном варианте осуществления, серотип представляет собой О9.
Используемая в настоящем документе ссылка на любой из перечисленных выше серотипов относится к серотипу, который включает в себя структуру повторяющихся единиц (О-единица, как описано ниже), известную в данной области техники, и является уникальной для соответствующего серотипа. Например, термин серотип «O25a» (также известный в данной области техники как серотип «O25») относится к серотипу, который охватывает Формулу O25, показанную в таблице 1. В качестве другого примера, термин серотип «O25b» относится к серотипу, который охватывает Формулу O25b, показанную в таблице 1.
Используемые в настоящем документе серотипы упоминаются в настоящем документе в общем, если не указано иное, так что, например, термин «формула «O18» в общем относится к Формуле O18A, Формуле O18ac, Формуле 18A1, Формуле O18B и Формуле O18B1.
Используемый в настоящем документе термин «O1» в общем относится к видам формулы, которые включают общий термин «O1» в названии формулы в соответствии с таблицей 1, такой как любая из Формулы O1A, Формулы O1A1, Формулы O1B и Формулы O1C, каждая из которых показана в таблице 1. Соответственно, «серотип O1» в общем относится к серотипу, который охватывает любую из Формулы O1A, Формулы O1A1, Формулы O1B и Формулы O1C.
Используемый в настоящем документе термин «О6» в общем относится к разновидностям Формулы, которые включают общий термин «О6» в названии Формулы в соответствии с таблице 1, такой как любая из Формулы О6:К2; К13; К15; и O6:K54, каждая из которых показана в таблице 1. Соответственно, «серотип O6» в общем относится к серотипу, который охватывает любую из формул O6:K2; К13; К15; и О6:К54.
Другие примеры терминов, которые в общем относятся к разновидностям Формулы, которые включают общий термин в название Формулы в соответствии с таблицей 1, включают: «O4», «O5», «O18» и «O45».
Используемый в настоящем документе термин «О2» относится к формуле О2, показанной в таблице 1. Термин «О-антиген О2» относится к сахариду, который охватывает формулу О2, показанную в таблице 1.
Используемая в настоящем документе ссылка на О-антиген серотипа, перечисленного выше, относится к сахариду, который охватывает формулу, помеченную соответствующим названием серотипа. Например, термин «О-антиген O25B» относится к сахариду, который охватывает Формулу O25B, показанную в таблице 1.
В качестве другого примера, термин «О1-О-антиген» в общем относится к сахариду, который охватывает Формулу, включающую термин «О1», такую как Формула О1А, Формула О1А1, Формула О1В и Формула О1С, каждая из которых показана в таблице 1.
В качестве другого примера, термин «О6-О-антиген» в общем относится к сахариду, который охватывает Формулу, включающую термин «О6», такую как Формула О6:К2; Формула O6:K13; Формула O6:K15 и Формула O6:K54, каждая из которых показана в таблице 1.
В. O-полисахарид
Используемый в настоящем документе термин «О-полисахарид» относится к любой структуре, которая включает О-антиген, при условии, что структура не включает целую клетку или липид А. Например, в одном варианте осуществления, О-полисахарид включает липополисахарид где липид А не связан. Стадия удаления липида А известна в данной области техники и включает, например, термическую обработку с добавлением кислоты. Пример процесса включает обработку 1% уксусной кислотой при 100°С в течение 90 минут. Этот процесс сочетается с процессом выделения липида А как удаленного. Типовой способ выделения липида А включает ультрацентрифугирование.
В одном варианте осуществления, О-полисахарид относится к структуре, состоящей из О-антигена, и в этом случае О-полисахарид является синонимом термина О-антиген. В одном предпочтительном варианте осуществления, О-полисахарид относится к структуре, которая включает повторяющиеся звенья О-антигена без корового сахарида. Соответственно, в одном варианте осуществления, О-полисахарид не включает коровую группу E. coli R1. В другом варианте осуществления, О-полисахарид не включает коровую группу E. coli R2. В другом варианте осуществления, О-полисахарид не включает коровую группу E. coli R3. В другом варианте осуществления, О-полисахарид не включает коровую группу E. coli R4. В другом варианте осуществления, O-полисахарид не включает коровую группу E. coli K12. В другом предпочтительном варианте осуществления, О-полисахарид относится к структуре, которая включает О-антиген и коровый сахарид. В другом варианте осуществления, О-полисахарид относится к структуре, которая включает О-антиген, коровый сахарид и фрагмент KDO.
Способы очистки О-полисахарида, который включает коровый олигосахарид, от LPS известны в данной области техники. Например, после очистки LPS, очищенный LPS можно гидролизовать путем нагревания в 1% (об./об.) уксусной кислоте в течение 90 минут при 100 градусах Цельсия с последующим ультрацентрифугированием при 142000 х g в течение 5 часов при 4 градусах Цельсия. Супернатант, содержащий О-полисахарид, сушат вымораживанием и хранят при 4 градусах Цельсия. В некоторых вариантах осуществления, описана делеция генов синтеза капсулы для обеспечения простой очистки О-полисахарида.
О-полисахарид может быть выделен способами, включая, но не ограничиваясь ими, мягкий кислотный гидролиз для удаления липида А из LPS. Другие варианты осуществления могут включать использование гидразина в качестве агента для получения О-полисахарида. Получение LPS можно осуществить известными в данной области техники способами.
В некоторых вариантах осуществления О-полисахариды, очищенные от штаммов грамотрицательных бактерий дикого типа, модифицированных или аттенуированных, которые экспрессируют (не обязательно сверхэкспрессируют) белок Wzz (например, wzzB), предназначены для использования в конъюгированных вакцинах. В предпочтительных вариантах осуществления, О-полисахаридная цепь очищается из штамма грамотрицательных бактерий, экспрессирующих (не обязательно сверхэкспрессирующих) белок wzz, для использования в качестве вакцинного антигена либо в виде конъюгата, либо в виде комплексной вакцины.
В одном варианте осуществления, О-полисахарид имеет молекулярную массу, которая увеличивается примерно в 1-кратно, 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 11-кратно, 12-кратно, 13-кратно, 14-кратно, 15-кратно, 16-кратно, 17-кратно, 18-кратно, 19-кратно, 20-кратно, 21-кратно, 22-кратно, 23-кратно, 24-кратно, 25-кратно, 26-кратно, 27-кратно, 28-кратно, 29-кратно, 30-кратно, 31-кратно, 32-кратно, 33-кратно, 34-кратно, 35-кратно, 36-кратно, 37-кратно, 38-кратно, 39-кратно, 40-кратно, 41-кратно, 42-кратно, 43-кратно, 44-кратно, 45-кратно, 46-кратно, 47-кратно, 48-кратно, 49-кратно, 50-кратно, 51-кратно, 52-кратно, 53-кратно, 54-кратно, 55-кратно, 56-кратно, 57-кратно, 58-кратно, 59-кратно, 60-кратно, 61-кратно, 62-кратно, 63-кратно, 64-кратно, 65-кратно, 66-кратно, 67-кратно, 68-кратно, 69-кратно, 70-кратно, 71-кратно, 72-кратно, 73-кратно, 74-кратно, 75-кратно, 76-кратно, 77-кратно, 78-кратно, 79-кратно, 80-кратно, 81-кратно, 82-кратно, 83-кратно, 84-кратно, 85-кратно, 86-кратно, 87-кратно, 88-кратно, 89-кратно, 90-кратно, 91-кратно, 92-кратно, 93-кратно, 94-кратно, 95-кратно, 96-кратно, 97-кратно, 98-кратно, 99-кратно, 100-кратно или более по сравнению с соответствующим O-полисахаридом дикого типа. В предпочтительном варианте осуществления, О-полисахарид имеет молекулярную массу, увеличенную по меньшей мере, 1-кратно и не более чем 5-кратно по сравнению с соответствующим О-полисахаридом дикого типа. В другом варианте осуществления, О-полисахарид имеет молекулярную массу, увеличенную по меньшей мере, 2-кратно и не более чем 4-кратно по сравнению с соответствующим О-полисахаридом дикого типа. Увеличение молекулярной массы О-полисахарида по сравнению с соответствующим О-полисахаридом дикого типа предпочтительно связано с увеличением количества повторяющихся единиц О-антигена. В одном варианте осуществления, увеличение молекулярной массы О-полисахарида обусловлено белком семейства wzz.
В одном варианте осуществления, O-полисахарид имеет молекулярную массу, которая увеличена примерно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 кДа или более по сравнению с соответствующим О-полисахаридом дикого типа. В одном варианте осуществления, О-полисахарид по изобретению имеет молекулярную массу, увеличенную, по меньшей мере, на 1 и не более чем на 200 кДа по сравнению с соответствующим О-полисахаридом дикого типа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 5 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 12 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 15 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 18 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 21 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 22 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 30 и не более чем на 200 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 1 и не более чем на 100 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 5 и не более чем на 100 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 100 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 12 и не более чем на 100 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 15 и не более чем на 100 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 100 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 1 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 5 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 12 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 15 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 18 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 30 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 90 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 12 и не более чем на 85 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 75 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 70 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 60 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 50 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 49 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 48 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 47 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 10 и не более чем на 46 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 45 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 44 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 43 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 42 кДа. В одном варианте осуществления, молекулярная масса увеличивается, по меньшей мере, на 20 и не более чем на 41 кДа. Такое увеличение молекулярной массы О-полисахарида по сравнению с соответствующим О-полисахаридом дикого типа предпочтительно связано с увеличением количества повторяющихся единиц О-антигена. В одном варианте осуществления, увеличение молекулярной массы О-полисахарида обусловлено белком семейства wzz. См., например, Таблицу 21.
В другом варианте осуществления, О-полисахарид включает любую Формулу, выбранную из Таблицы 1, где количество повторяющихся звеньев n в О-полисахариде больше, чем количество повторяющихся звеньев в соответствующем О-полисахариде дикого типа на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 или более повторяющихся единиц. Предпочтительно, сахарид включает увеличение, по меньшей мере, на 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50 повторяющихся единиц по сравнению с соответствующим О-полисахаридом дикого типа. См., например, Таблицу 21.
С. О-антиген
О-антиген входит в состав липополисахарида (LPS) внешней мембраны грамотрицательных бактерий. О-антиген находится на поверхности клетки и является вариабельным компонентом клетки. Вариабельность О-антигена служит основой для серотипирования грамотрицательных бактерий. Текущая схема серотипирования E. coli включает О-полисахариды с 1 по 181.
О-антиген включает олигосахаридные повторяющиеся единицы (О-единицы), структура дикого типа которых обычно содержит от двух до восьми остатков из широкого спектра сахаров. О-единицы типовых О-антигенов E. coli показаны в таблице 1, см. также ФИГ. 9А-9С и ФИГ. 10А-10В.
В одном варианте осуществления, сахарид по изобретению может представлять собой одну олигосахаридную единицу. В одном варианте осуществления, сахарид по изобретению представляет собой одну повторяющуюся олигосахаридную единицу соответствующего серотипа. В таких вариантах осуществления, сахарид может включать структуру, выбранную из Формулы O8, Формулы O9a, Формулы O9, Формулы O20ab, Формулы O20ac, Формулы O52, Формулы O97 и Формулы O101.
В одном варианте осуществления, сахарид по изобретению может представлять собой олигосахариды. Олигосахариды имеют небольшое количество повторяющихся единиц (обычно, 5-15 повторяющихся единиц) и обычно получают синтетическим путем или путем гидролиза полисахаридов. В таких вариантах осуществления сахарид может включать структуру, выбранную из Формулы O8, Формулы O9a, Формулы O9, Формулы O20ab, Формулы O20ac, Формулы O52, Формулы O97 и Формулы O101.
Предпочтительно, чтобы все сахариды по настоящему изобретению и в иммуногенных композициях по настоящему изобретению были полисахаридами. Высокомолекулярные полисахариды могут индуцировать определенные иммунные ответы антител из-за эпитопов, присутствующих на антигенной поверхности. Выделение и очистка высокомолекулярных полисахаридов предпочтительно рассматриваются для использования в конъюгатах, композициях и способах по настоящему изобретению.
В некоторых вариантах осуществления, количество повторяющихся единиц O в каждом отдельном полимере O-антигена (и, следовательно, длина и молекулярная масса полимерной цепи) зависит от регулятора длины цепи wzz, белка внутренней мембраны. Разные белки wzz придают разные диапазоны модальной длины (от 4 до >100 повторяющихся единиц). Термин «модальная длина» относится к количеству повторяющихся O-единиц. Грамотрицательные бактерии часто имеют два разных белка Wzz, которые обеспечивают две различные длины модальных цепей OAg: одну длиннее, и другую короче. Экспрессия (не обязательно сверхэкспрессия) белков семейства wzz (например, wzzB) в грамотрицательных бактериях может позволить манипулировать длиной О-антигена, сдвигать или смещать бактериальное продуцирование О-антигенов определенных диапазонов длины и для увеличения продуцирования высокопродуктивных липополисахаридов с большой молекулярной массой. В одном варианте осуществления, «короткая» модальная длина, используемая в настоящем документе, относится к небольшому количеству повторяющихся O-единиц, например, 1-20. В одном варианте осуществления, «длинная» модальная длина, используемая в настоящем документе, относится к количеству повторяющихся O-единиц, превышающему 20 и максимальному количеству 40. В одном варианте осуществления, «очень длинная» модальная длина, используемая в настоящем документе, относится к более чем 40 повторяющихся О-единиц.
В одном варианте осуществления, полученный сахарид имеет увеличение, по меньшей мере, на 10 повторяющихся единиц, 15 повторяющихся единиц, 20 повторяющихся единиц, 25 повторяющихся единиц, 30 повторяющихся единиц, 35 повторяющихся единиц, 40 повторяющихся единиц, 45 повторяющихся единиц, 50 повторяющихся единиц, 55 повторяющиеся единицы, 60 повторяющихся единиц, 65 повторяющихся единиц, 70 повторяющихся единиц, 75 повторяющихся единиц, 80 повторяющихся единиц, 85 повторяющихся единиц, 90 повторяющихся единиц, 95 повторяющихся единиц или 100 повторяющихся единиц по сравнению с соответствующим O-полисахаридом дикого типа.
В другом варианте осуществления, сахарид по изобретению имеет увеличение на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 или более повторяющихся единиц по сравнению с соответствующим О-полисахаридом дикого типа. Предпочтительно, сахарид включает увеличение, по меньшей мере, на 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50 повторяющихся единиц по сравнению с соответствующим О-полисахаридом дикого типа. См., например, Таблицу 21. Способы определения длины сахаридов известны в данной области техники. Такие способы включают ядерный магнитный резонанс, масс-спектроскопию и эксклюзионную хроматографию, как описано в примере 13.
Способы определения количества повторяющихся единиц в сахариде также известны в данной области техники. Например, количество повторяющихся единиц (или «n» в Формуле) можно рассчитать путем деления молекулярной массы полисахарида (без молекулярной массы основного сахарида или остатка KDO) на молекулярную массу повторяющейся единицы (т.е. молекулярную масса структуры в соответствующей Формуле, показанной, например, в таблице 1, которая теоретически может быть рассчитана как сумма молекулярной массы каждого моносахарида в Формуле). Молекулярная масса каждого моносахарида в формуле известна в данной области техники. Молекулярная масса повторяющейся единицы Формулы O25b, например, составляет около 862 Да. Молекулярная масса повторяющейся единицы Формулы O1a, например, составляет около 845 Да. Молекулярная масса повторяющейся единицы Формулы O2, например, составляет около 829 Да. Молекулярная масса повторяющейся единицы Формулы O6, например, составляет около 893 Да. При определении количества повторяющихся единиц в конъюгате, в расчете учитываются молекулярная масса белка-носителя и соотношение белок:полисахарид. Как определено в настоящем документе, «n» относится к количеству повторяющихся единиц (представленных в скобках в таблице 1) в молекуле полисахарида. Как известно в данной области техники, в биологических макромолекулах повторяющиеся структуры могут перемежаться областями несовершенных повторов, такими как, например, отсутствующие ответвления. Кроме того, в данной области техники известно, что полисахариды, выделенные и очищенные из природных источников, таких как бактерии, могут быть гетерогенными по размеру и разветвлению. В таком случае n может представлять собой среднее или медианное значение n для молекул в популяции.
В одном варианте осуществления, О-полисахарид имеет увеличение, по меньшей мере, на одну повторяющуюся единицу О-антигена по сравнению с соответствующим О-полисахаридом дикого типа. Повторяющиеся единицы О-антигенов показаны в таблице 1. В одном варианте осуществления, О-полисахарид включает 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 или более повторяющихся единиц. Предпочтительно, сахарид имеет в общей сложности от, по меньшей мере, 3 до не более 80 повторяющихся единиц. В другом варианте осуществления, О-полисахарид имеет увеличение на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 или более повторяющихся единиц по сравнению с соответствующим О-полисахаридом дикого типа.
В одном варианте осуществления, сахарид включает О-антиген, где n в любой из формул О-антигена (такой как, например, формулы, показанные в таблице 1 (см. также ФИГ. 9A-9C и ФИГ. 10A-10B)) представляет собой целое число, по меньшей мере, 1, 2, 3, 4, 5, 10, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, и не более 200, 100, 99, 98, 97, 96, 95, 94, 93, 92, 91, 90, 89, 88, 87, 86, 81, 80, 79, 78, 77, 76, 75, 74, 73, 72, 71, 70, 69, 68, 67, 66, 65, 60, 59, 58, 57, 56, 55, 54, 53, 52, 51 или 50. Любое минимальное значение и любое максимальное значение могут быть объединены для определения диапазона. Типовые диапазоны включают, например, от, по меньшей мере, 1 до не более 1000; от, по меньшей мере, 10 до не более 500; и от, по меньшей мере, 20 до не более 80, предпочтительно, не более 90. В одном предпочтительном варианте осуществления, n составляет от, по меньшей мере, 31 до не более 90. В предпочтительном варианте осуществления, n составляет от 40 до 90, более предпочтительно, от 60 до 85.
В одном варианте осуществления, сахарид включает О-антиген, где n в любой из формул О-антигена составляет, по меньшей мере, 1 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 5 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 10 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 25 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 50 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 75 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 100 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 125 и не более 200. В одном варианте осуществления, n в любой в формулах О-антигена составляет, по меньшей мере, 150 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 175 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 175 и не более 200. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 1 и не более 100. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 5 и не более 100. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 10 и не более 100. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 25 и не более 100. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 50 и не более 100. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 75 и не более 100. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 1 и не более 75. В одном из вариантов осуществления n в любой из формул О-антигена составляет, по меньшей мере, 5 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 10 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 20 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 25 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 30 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 40 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 50 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 30 и не более 90. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 85. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 75. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 70. В одном варианте осуществления, n в любой из формул одна из формул О-антигена составляет, по меньшей мере, 35 и не более 60. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 50. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 49. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 48. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 47. В о В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 35 и не более 46. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 36 и не более 45. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 37 и не более 44. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 38 и не более 43. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 39 и не более 42. В одном варианте осуществления, n в любой из формул О-антигена составляет, по меньшей мере, 39 и не более 41.
Например, в одном варианте осуществления, n в сахариде составляет 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89 или 90, наиболее предпочтительно, 40. В другом варианте осуществления, n составляет от, по меньшей мере, 35 до не более 60. Например, в одном варианте осуществления, n составляет любое из 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59 и 60, предпочтительно, 50. В другом предпочтительном варианте осуществления, n составляет от, по меньшей мере, 55 до не более 75. Например, в одном варианте осуществления, n составляет 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68 или 69, наиболее предпочтительно, 60.
Структура сахарида может быть определена способами и инструментами, известными из уровня техники, такими как, например, ЯМР, включая 1D, 1H и/или 13C, 2D TOCSY, DQF-COSY, NOESY и/или HMQC.
В некоторых вариантах осуществления, очищенный полисахарид перед конъюгацией имеет молекулярную массу от 5 кДа до 400 кДа. В других таких вариантах осуществления, сахарид имеет молекулярную массу от 10 кДа до 400 кДа; от 5 кДа до 400 кДа; от 5 кДа до 300 кДа; от 5 кДа до 200 кДа; от 5 кДа до 150 кДа; от 10 кДа до 100 кДа; от 10 кДа до 75 кДа; от 10 кДа до 60 кДа; от 10 кДа до 40 кДа; от 10 кДа до 100 кДа; 10 кДа до 200 кДа; от 15 кДа до 150 кДа; от 12 кДа до 120 кДа; от 12 кДа до 75 кДа; от 12 кДа до 50 кДа; от 12 и 60 кДа; от 35 кДа до 75 кДа; от 40 кДа до 60 кДа; от 35 кДа до 60 кДа; от 20 кДа до 60 кДа; от 12 кДа до 20 кДа; или от 20 кДа до 50 кДа. В дополнительных вариантах осуществления, полисахарид имеет молекулярную массу от 7 кДа до 15 кДа; 8 кДа до 16 кДа; 9 кДа до 25 кДа; 10 кДа до 100; 10 кДа до 60 кДа; 10 кДа до 70 кДа; 10 кДа до 160 кДа; 15 кДа до 600 кДа; 20 кДа до 1000 кДа; 20 кДа до 600 кДа; 20 кДа до 400 кДа; 30 кДа до 1000 КДа; 30 кДа до 60 кДа; 30 кДа до 50 кДа или 5 кДа до 60 кДа. Любое целое число в любом из вышеуказанных диапазонов рассматривается как вариант осуществления изобретения.
Используемый в настоящем документе термин «молекулярная масса» полисахарида или конъюгата белок-носитель-полисахарид относится к молекулярной массе, рассчитанной с помощью эксклюзионной хроматографии (SEC) в сочетании с детектором многоуглового лазерного светорассеяния (MALLS).
Полисахарид может немного уменьшиться в размерах во время обычных процедур очистки. Кроме того, как описано в настоящем документе, полисахарид можно подвергнуть классификации по размерам перед конъюгацией. Может быть использована механическая или химическая классификация по размерам. Химический гидролиз можно проводить с использованием уксусной кислоты. Механическая калибровка может быть проведена с использованием сдвигов гомогенизации под высоким давлением. Упомянутые выше диапазоны молекулярных масс относятся к очищенным полисахаридам перед конъюгацией (например, перед активацией).
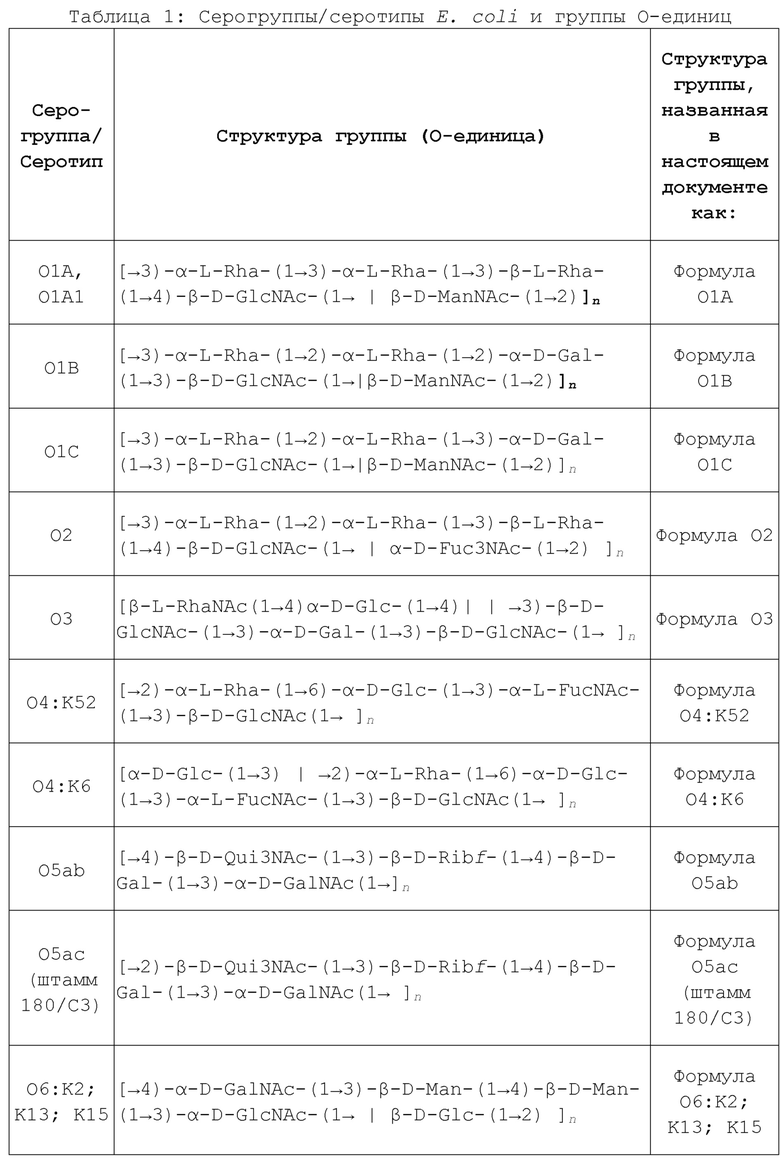
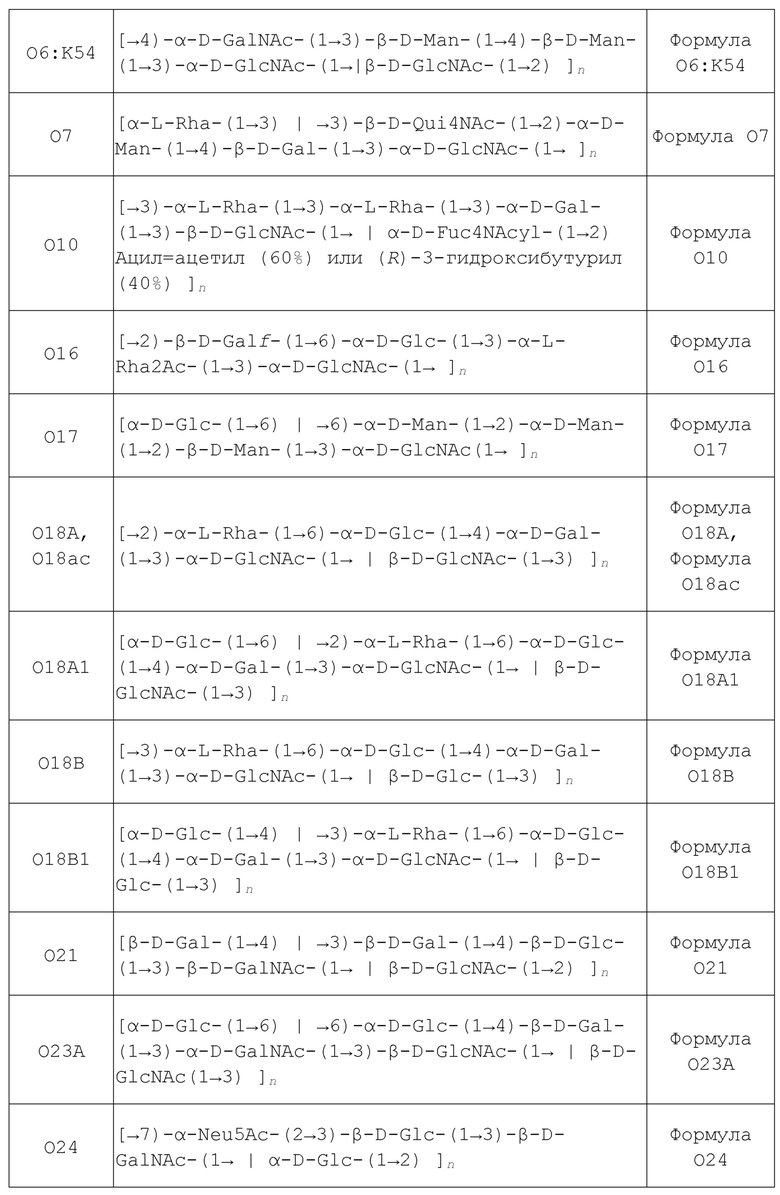
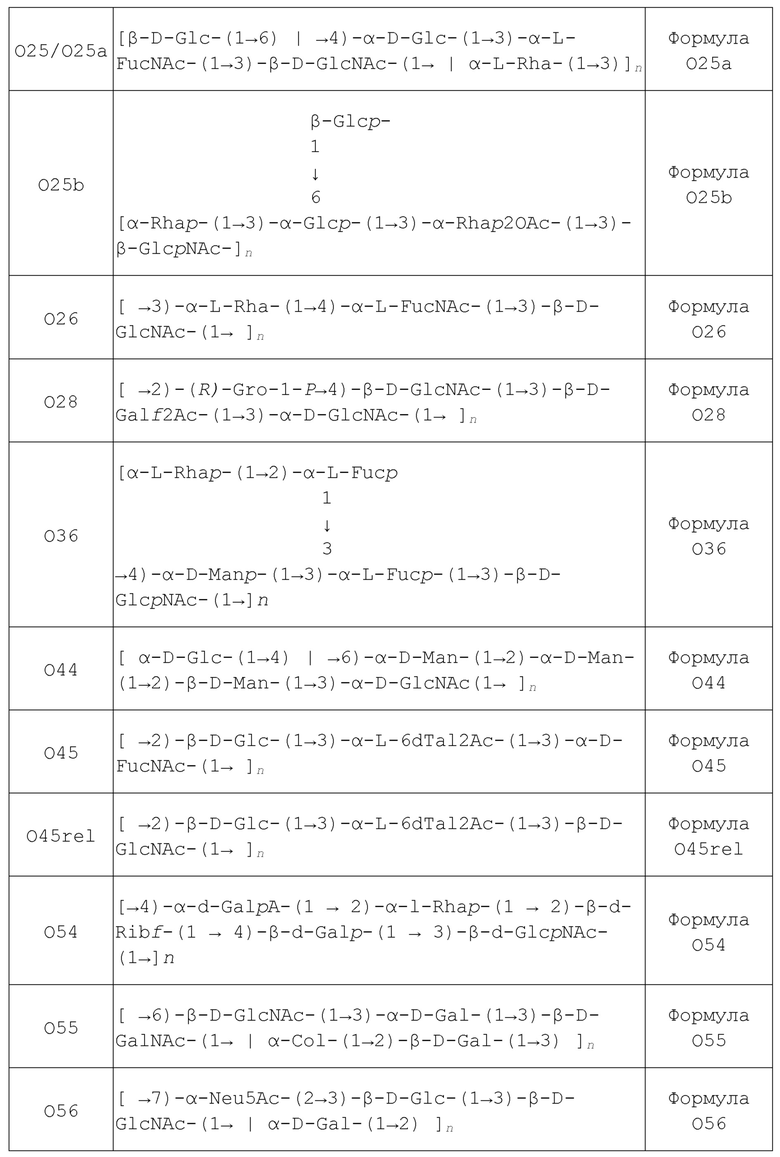

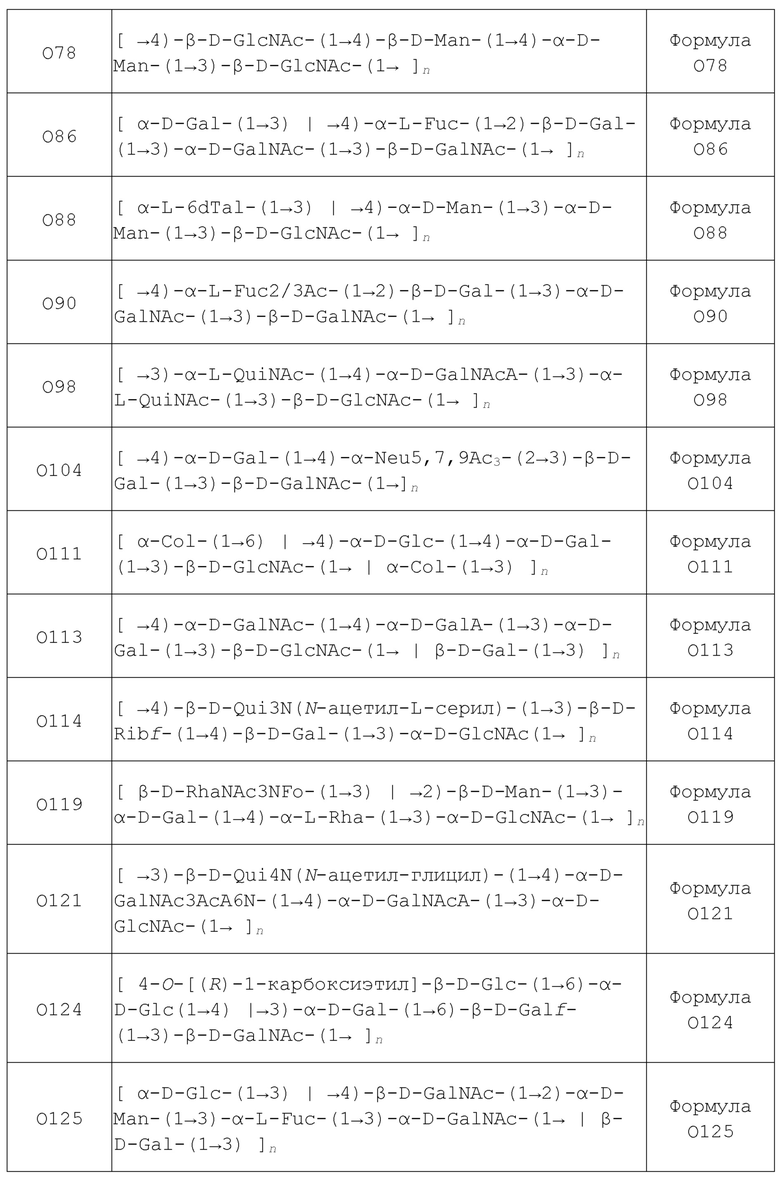
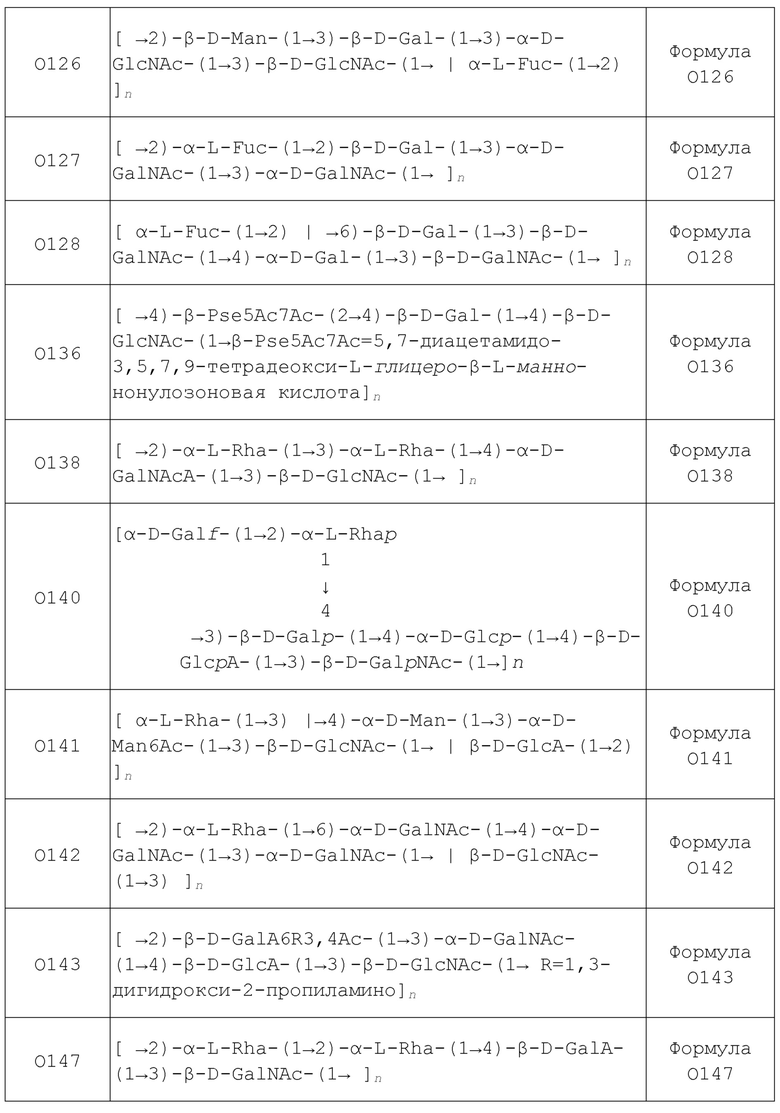
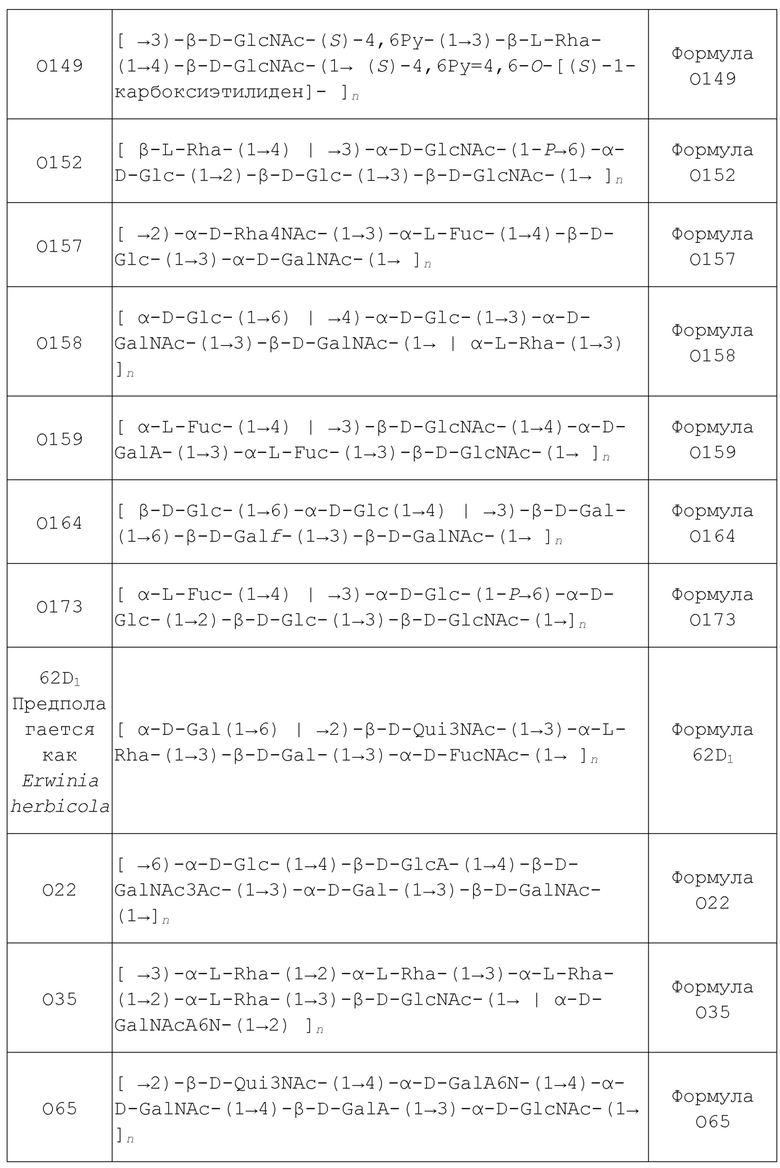
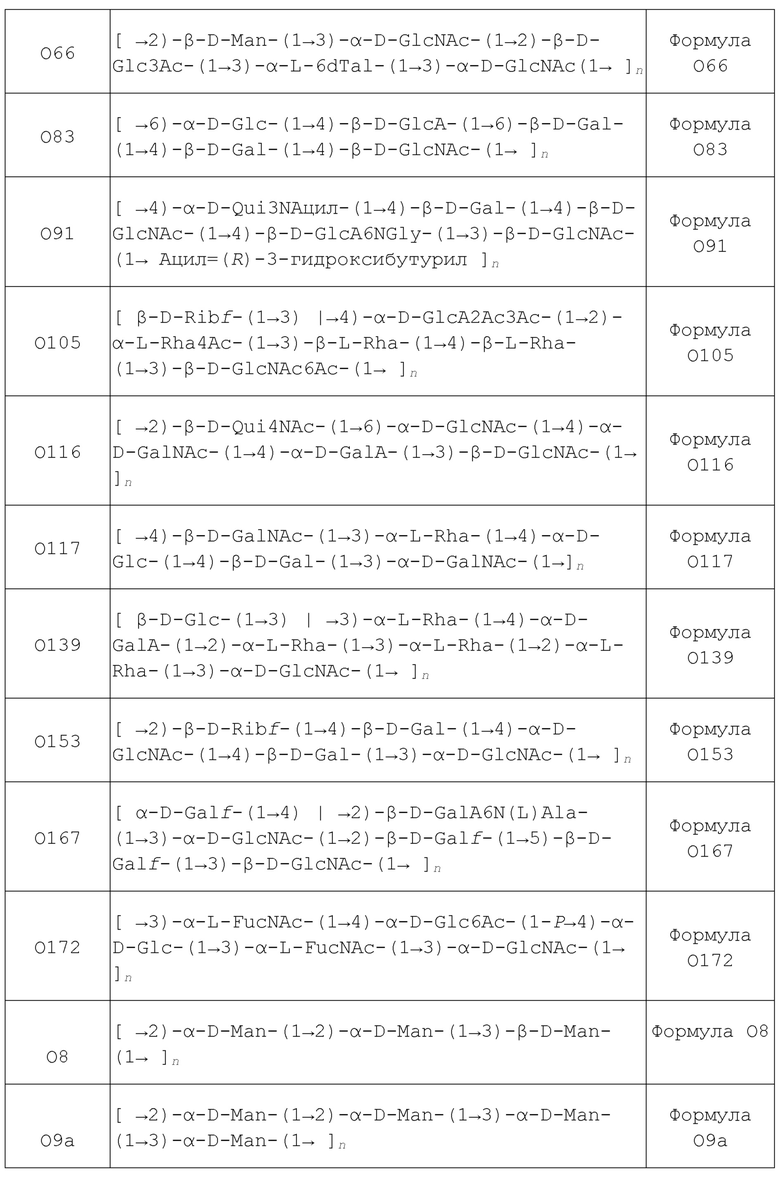

D. Коровый олигосахарид
Основной олигосахарид расположен между липидом А и внешней областью О-антигена в LPS E. coli дикого типа. Более конкретно, коровый олигосахарид представляет собой часть полисахарида, которая включает связь между О-антигеном и липидом А в E. coli дикого типа. Эта связь включает кетозидную связь между полукетальной функцией самого внутреннего остатка 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO)) и гидроксильной группой остатка GlcNAc липида А. Основной олигосахарид регион демонстрирует высокую степень сходства среди штаммов E. coli дикого типа. Обычно он включает ограниченное количество сахаров. Коровый олигосахарид включает внутреннюю коровую область и внешнюю коровую область.
Более конкретно, внутреннее ядро состоит в основном из L-глицеро-D-манно-гептозы (гептозы) и остатков KDO. Внутреннее ядро очень консервативно. Остаток KDO включает следующую формулу KDO:
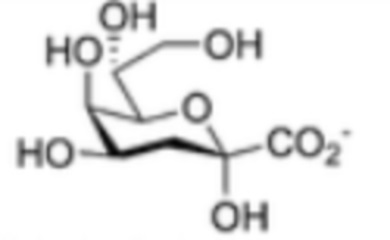
Внешняя область корового олигосахарида демонстрирует больше вариаций, чем внутренняя коровая область, и различия в этой области отличают пять хемотипов E. coli: R1, R2, R3, R4 и K-12. См. ФИГ. 24, которая иллюстрирует обобщенные структуры углеводного остова внешних коровых олигосахаридов пяти известных хемотипов. HepII является последним остатком внутреннего корового олигосахарида. В то время как все внешние коровые олигосахариды имеют общую структурную тему, с (гексозным)3 углеводным остовом и двумя остатками боковой цепи, порядок гексоз в основной цепи, а также природа, положение и связь остатков боковой цепи могут варьироваться. Структуры внешних коровых олигосахаридов R1 и R4 очень похожи, различаясь только одним β-связанным остатком.
Коровые олигосахариды E. coli дикого типа классифицируются в данной области техники на основе структур дистального олигосахарида на пять различных хемотипов: E. coli R1, E. coli R2, E. coli R3, E. coli R4 и E. coli К12.
В предпочтительном варианте осуществления, композиции, описанные в настоящем документе, включают гликоконъюгаты, в которых О-полисахарид включает коровый олигосахарид, связанный с О-антигеном. В одном варианте осуществления, композиция индуцирует иммунный ответ, по меньшей мере, против любого из коровых хемотипов E.coli: E.coli R1, E.coli R2, E.coli R3, E.coli R4 и E.coli K12. В другом варианте осуществления, композиция индуцирует иммунный ответ, по меньшей мере, против двух коровых хемотипов E. coli. В другом варианте осуществления, композиция индуцирует иммунный ответ, по меньшей мере, против трех коровых хемотипов E. coli. В другом варианте осуществления, композиция индуцирует иммунный ответ, по меньшей мере, против четырех коровых хемотипов E. coli. В другом варианте осуществления, композиция индуцирует иммунный ответ против всех пяти коровых хемотипов E. coli.
В другом предпочтительном варианте осуществления, композиции, описанные в настоящем документе, включают гликоконъюгаты, в которых О-полисахарид не включает коровый олигосахарид, связанный с О-антигеном. В одном варианте осуществления, такая композиция индуцирует иммунный ответ, по меньшей мере, против любого из коровых хемотипов E.coli: E.coli R1, E.coli R2, E.coli R3, E.coli R4 и E.coli K12, несмотря на гликоконъюгат, содержащий О-полисахарид, который не включает коровый олигосахарид.
Серотипы E. coli можно охарактеризовать в соответствии с одним из пяти хемотипов. В таблице 2 перечислены типовые серотипы, охарактеризованные в соответствии с хемотипом. Серотипы, выделенные жирным шрифтом, представляют собой серотипы, которые чаще всего связаны с указанным коровым хемотипом. Соответственно, в предпочтительном варианте осуществления, композиция индуцирует иммунный ответ, по меньшей мере, против любого из коровых хемотипов E.coli: E.coli R1, E.coli R2, E.coli R3, E.coli R4 и E.coli K12, который включает иммунный ответ против любого из соответствующих серотипов E. coli.
В некоторых вариантах осуществления, композиция включает сахарид, имеющий структуру, полученную из серотипа, имеющего хемотип R1, например, выбранный из сахарида, имеющего Формулу O25a, Формулу O6, Формулу O2, Формулу O1, Формулу O75, Формулу O4, Формулу O16, Формулу O8, Формулу O18, Формулу O9, Формулу O13, Формулу O20, Формулу O21, Формулу O91 и Формулу O163, где n составляет от 1 до 100. В некоторых вариантах осуществления, сахарид в указанной композиции дополнительно включает коровую группу E. coli R1., например, показанную на ФИГ. 24.
В некоторых вариантах осуществления композиция, включает сахарид, имеющий структуру, полученную из серотипа, имеющего хемотип R1, например, выбранный из сахарида, имеющего Формулу O25a, Формулу O6, Формулу O2, Формулу O1, Формулу O75, Формулу O4, Формулу O16, Формулу O18, Формулу O13, Формулу O20, Формулу O21, Формулу O91 и Формулу O163, где n составляет от 1 до 100, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65. В некоторых вариантах осуществления сахарид в указанной композиции дополнительно включает коровую группу E. coli R1 в сахариде.
В некоторых вариантах осуществления, композиция включает сахарид, имеющий структуру, полученную из серотипа, имеющего хемотип R2, например, выбранный из сахарида, имеющего Формулу O21, Формулу O44, Формулу O11, Формулу O89, Формулу O162 и Формулу O9, где n составляет от 1 до 100, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65. В некоторых вариантах осуществления сахарид в указанной композиции дополнительно включает коровую группу E. coli R2, например, показанную на ФИГ. 24.
В некоторых вариантах осуществления, композиция включает сахарид, имеющий структуру, полученную из серотипа, имеющего хемотип R3, например, выбранный из сахарида, имеющего Формулу O25b, Формулу O15, Формулу O153, Формулу O21, Формулу O17, Формулу O11, Формулу O159, Формулу O22, Формулу O86 и Формулу O93, где n составляет от 1 до 100, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65. В некоторых вариантах осуществления сахарид в указанной композиции дополнительно включает коровую группу E. coli R3, например, показанную на ФИГ. 24.
В некоторых вариантах осуществления, композиция включает сахарид, имеющий структуру, полученную из серотипа, имеющего хемотип R4, например, выбранный из сахарида, имеющего Формулу O2, Формулу O1, Формулу O86, Формулу O7, Формулу O102, Формулу O160 и Формулу O166, где n составляет от 1 до 100, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65. В некоторых вариантах осуществления сахарид в указанной композиции дополнительно включает коровую группу E. coli R4, например, показанную на ФИГ. 24.
В некоторых вариантах осуществления, композиция включает сахарид, имеющий структуру, полученную из серотипа, имеющего хемотип К-12 (например, выбранного из сахарида, имеющего формулу O25b, и сахарида, имеющего формулу O16), где n составляет от 1 до 1000, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65. В некоторых вариантах осуществления, сахарид в указанной композиции дополнительно включает коровую группу E. coli K-12, например, показанную на ФИГ. 24.
В некоторых вариантах осуществления, сахарид включает коровый сахарид. Соответственно, в одном варианте осуществления, О-полисахарид дополнительно включает коровую группу E. coli R1. В другом варианте осуществления, О-полисахарид дополнительно включает коровую группу E. coli R2. В другом варианте осуществления, О-полисахарид дополнительно включает коровую группу E. coli R3. В другом варианте осуществления, О-полисахарид дополнительно включает коровую группу R4 E. coli. В другом варианте осуществления, О-полисахарид дополнительно включает коровую группу E. coli K12.
В некоторых вариантах осуществления, сахарид не включает коровый сахарид. Соответственно, в одном варианте осуществления, О-полисахарид не включает коровую группу E. coli R1. В другом варианте осуществления, О-полисахарид не включает коровую группу E. coli R2. В другом варианте осуществления, О-полисахарид не включает коровую группу E. coli R3. В другом варианте осуществления, О-полисахарид не включает коровую группу E. coli R4. В другом варианте осуществления, O-полисахарид не включает коровую группу E. coli K12.
Е. Конъюгированные О-антигены
Химическая связь О-антигенов или, предпочтительно, О-полисахаридов с белковыми носителями может улучшить иммуногенность О-антигенов или О-полисахаридов. Однако изменчивость размера полимера представляет собой практическую проблему для производства. При коммерческом использовании, размер сахарида может влиять на совместимость с различными стратегиями синтеза конъюгации, однородность продукта и иммуногенность конъюгата. Контроль экспрессии регулятора длины цепи белка семейства Wzz посредством манипулирования путями синтеза О-антигена позволяет производить цепи О-антигена желаемой длины в различных штаммах грамотрицательных бактерий, включая E. coli.
В одном варианте осуществления, очищенные сахариды химически активируют для получения активированных сахаридов, способных реагировать с белком-носителем. После активации, каждый сахарид отдельно конъюгируется с белком-носителем с образованием конъюгата, а именно, гликоконъюгата. Используемый в настоящем документе термин «гликоконъюгат» относится к сахариду, ковалентно связанному с белком-носителем. В одном варианте осуществления, сахарид связан непосредственно с белком-носителем. В другом варианте осуществления, сахарид связан с белком через спейсер/линкер. Конъюгаты могут быть получены по схемам, которые связывают носитель с О-антигеном в одном или нескольких сайтах вдоль О-антигена, или по схемам, которые активируют, по меньшей мере, один остаток корового олигосахарида.
В одном варианте осуществления, каждый сахарид конъюгирован с одним и тем же белком-носителем. Если белок-носитель является одинаковым для 2 или нескольких сахаридов в композиции, сахариды могут быть конъюгированы с одной и той же молекулой белка-носителя (например, молекулы-носители имеют конъюгированные с ней 2 или несколько различных сахаридов).
В предпочтительном варианте осуществления, каждый из сахаридов индивидуально конъюгирован с разными молекулами белкового носителя (каждая молекула белкового носителя имеет конъюгированный с ней только один тип сахарида). В указанном варианте осуществления, сахариды, как говорят, индивидуально конъюгированы с белком-носителем.
Химическая активация сахаридов и последующая конъюгация с белком-носителем могут быть достигнуты описанными в настоящем документе способами активации и конъюгации. После конъюгации полисахарида с белком-носителем, гликоконъюгаты очищают (обогащают по отношению к количеству конъюгата полисахарид-белок) различными методами. Эти методы включают операции концентрации/диафильтрации, осаждения/элюирования, колоночной хроматографии и глубинной фильтрации. После очистки отдельных гликоконъюгатов их смешивают с получением иммуногенной композиции по настоящему изобретению.
Активация. Настоящее изобретение дополнительно относится к активированным полисахаридам, полученным в соответствии с любым из вариантов осуществления, описанных в настоящем документе, где полисахарид активируют химическим реагентом с образованием реакционноспособных групп для конъюгации с линкером или белком-носителем. В некоторых вариантах осуществления, сахарид по изобретению активируют перед конъюгацией с белком-носителем. В некоторых вариантах осуществления, степень активации не приводит к значительному снижению молекулярной массы полисахарида. Например, в некоторых вариантах осуществления, степень активации не расщепляет полисахаридный остов. В некоторых вариантах осуществления степень активации не оказывает существенного влияния на степень конъюгации, измеряемую количеством остатков лизина, модифицированных в белке-носителе, таком как CRM197 (по данным аминокислотного анализа). Например, в некоторых вариантах осуществления, степень активации не приводит к значительному увеличению количества модифицированных остатков лизина (по данным аминокислотного анализа) в белке-носителе в 3 раза по сравнению с количеством лизиновых остатков, модифицированных в белке-носителе конъюгата с эталонным полисахаридом при той же степени активации. В некоторых вариантах осуществления, степень активации не увеличивает уровень неконъюгированного свободного сахарида. В некоторых вариантах осуществления, степень активации не снижает оптимальное соотношение сахарид/белок.
В некоторых вариантах осуществления, активированный сахарид имеет долю активации, при котором количество молей тиола на повторяющуюся единицу сахарида активированного сахарида составляет от 1 до 100%, например, от 2 до 80%, от 2 до 50%, 3-30% и 4-25%. Степень активации составляет, по меньшей мере, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, ≥20%, ≥30%, ≥40%, ≥50%, ≥60%, ≥70%, ≥80%, или ≥90%, или около 100%. Предпочтительно, степень активации составляет, самое большее, 50%, более предпочтительно, самое большее, 25%. В одном варианте осуществления, степень активации составляет, самое большее, 20%. Любое минимальное значение и любое максимальное значение могут быть объединены для определения диапазона.
В одном варианте осуществления, полисахарид активируют тетрафторборатом 1-циано-4-диметиламинопиридиния (CDAP) с образованием цианатного эфира. Активированный полисахарид затем связывают напрямую или через спейсерную (линкерную) группу с аминогруппой на белке-носителе (предпочтительно CRM197 или столбнячном анатоксине).
Например, спейсером может быть цистамин или цистеамин для получения тиолированного полисахарида, который может быть сопряжен с носителем через тиоэфирную связь, полученную после реакции с малеимид-активированным белком-носителем (например, с использованием сложного эфира N-[Y-малеимидобутирокси]сукцинимида (GMBS)) или галоацетилированным белком-носителем (например, с использованием йодацетимида, N-сукцинимидилбромацетата (SBA; SIB), N-сукцинимидил(4-йодацетил)аминобензоата (SIAB), сульфосукцинимидил(4-йодацетил)аминобензоата (сульфо-SIAB), N-сукцинимидилиодацетата (SIA) или сукцинимидил-3-[бромацетамидо]пропионата (SBAP)). В одном варианте осуществления, цианатный эфир (необязательно полученный с помощью CDAP химии) сочетают с гександиамином или дигидразидом адипиновой кислоты (ADH), и аминопроизводный сахарид конъюгируют с белком-носителем (например, CRM197) с использованием карбодиимида (например, EDAC или EDC) через карбоксильную группу на белковом носителе.
В других подходящих методиках конъюгации используют карбодиимиды, гидразиды, активные сложные эфиры, норборан, п-нитробензойную кислоту, N-гидроксисукцинимид, S-NHS, EDC, TSTU. Конъюгация может включать карбонильный линкер, который может быть образован реакцией свободной гидроксильной группы сахарида с CDI с последующей реакцией с белком с образованием карбаматной связи. Это может включать восстановление аномерного конца до первичной гидроксильной группы, необязательную защиту/снятие защиты первичной гидроксильной группы, реакцию первичной гидроксильной группы с CDI с образованием карбаматного промежуточного соединения CDI и связывание карбаматного промежуточного соединения CDI с аминогруппой на белке (CDI химия).
Молекулярная масса. В некоторых вариантах осуществления, гликоконъюгат содержит сахарид с молекулярной массой от 10 кДа до 2000 кДа. В других вариантах осуществления, сахарид имеет молекулярную массу от 50 кДа до 1000 кДа. В других вариантах осуществления, сахарид имеет молекулярную массу от 70 кДа до 900 кДа. В других вариантах осуществления, сахарид имеет молекулярную массу от 100 кДа до 800 кДа. В других вариантах осуществления, сахарид имеет молекулярную массу от 200 кДа до 600 кДа. В дополнительных вариантах осуществления, сахарид имеет молекулярную массу от 100 кДа до 1000 кДа; до 100 кДа до 900 кДа; до 100 кДа до 800 кДа; до 100 кДа до 700 кДа; до 100 кДа до 600 кДа; до 100 кДа до 500 кДа; до 100 кДа до 400 кДа; до 100 кДа до 300 кДа; до 150 кДа до 1,000 кДа; до 150 кДа до 900 кДа; до 150 кДа до 800 кДа; до 150 кДа до 700 кДа; до 150 кДа до 600 кДа; до 150 кДа до 500 кДа; до 150 кДа до 400 кДа; до 150 кДа до 300 кДа; до 200 кДа до 1,000 кДа; до 200 кДа до 900 кДа; до 200 кДа до 800 кДа; до 200 кДа до 700 кДа; до 200 кДа до 600 кДа; до 200 кДа до 500 кДа; до 200 кДа до 400 кДа; до 200 кДа до 300; 250 кДа до 1,000 кДа; до 250 кДа до 900 кДа; до 250 кДа до 800 кДа; до 250 кДа до 700 кДа; до 250 кДа до 600 кДа; до 250 кДа до 500 кДа; до 250 кДа до 400 кДа; до 250 кДа до 350 кДа; до 300 кДа до 1,000 кДа; до 300 кДа до 900 кДа; до 300 кДа до 800 кДа; до 300 кДа до 700 кДа; до 300 кДа до 600 кДа; до 300 кДа до 500 кДа; до 300 кДа до 400 кДа; до 400 кДа до 1,000 кДа; до 400 кДа до 900 кДа; до 400 кДа до 800 кДа; до 400 кДа до 700 кДа; до 400 кДа до 600 кДа; до 500 кДа до 600 кДа. В одном варианте осуществления, гликоконъюгат, имеющий такую молекулярную массу, получают односторонней конъюгацией. В другом варианте осуществления, гликоконъюгат, имеющий такую молекулярную массу, получают с помощью химии восстановительного аминирования (RAC), приготовленного в водном буфере. Любое целое число в любом из вышеуказанных диапазонов рассматривается как вариант осуществления изобретения.
В некоторых вариантах осуществления, гликоконъюгат по изобретению имеет молекулярную массу от 400 кДа до 15000 кДа; от 500 кДа до 10000 кДа; от 2000 кДа до 10000 кДа; от 3000 кДа до 8000 кДа; или от 3000 кДа до 5000 кДа. В других вариантах осуществления, гликоконъюгат имеет молекулярную массу от 500 кДа до 10000 кДа. В других вариантах осуществления, гликоконъюгат имеет молекулярную массу от 1000 кДа до 8000 кДа. В других вариантах осуществления, гликоконъюгат имеет молекулярную массу от 2000 кДа до 8000 кДа или от 3000 кДа до 7000 кДа. В дополнительных вариантах осуществления, гликоконъюгат по изобретению имеет молекулярную массу от 200 кДа до 20000 кДа; от 200 кДа до 15000 кДа; от 200 кДа до 10000 кДа; от 200 кДа до 7,500 кДа; от 200 кДа до 5000 кДа; от 200 кДа до 3000 кДа; от 200 кДа до 1000 кДа; от 500 кДа до 20000 кДа; от 500 кДа до 15000 кДа; от 500 кДа до 12,500 кДа; от 500 кДа до 10000 кДа; от 500 кДа до 7,500 кДа; от 500 кДа до 6000 кДа; от 500 кДа до 5000 кДа; от 500 кДа до 4000 кДа; от 500 кДа до 3000 кДа; от 500 кДа до 2000 кДа; от 500 кДа до 1,500 кДа; от 500 кДа до 1000 кДа; от 750 кДа до 20000 кДа; от 750 кДа до 15000 кДа; от 750кДа до 12,500 кДа; от 750кДа до 10000 кДа; от 750кДа до 7,500 кДа; от 750 кДа до 6000 кДа; от 750 кДа до 5000 кДа; от 750 кДа до 4000 кДа; от 750 кДа до 3000 кДа; от 750 кДа до 2000 кДа; от 750 кДа до 1,500 кДа; от 1000 кДа до 15000 кДа; от 1000 кДа до 12,500 кДа; от 1000 кДа до 10000 кДа; от 1000 кДа до 7,500 кДа; от 1000 кДа до 6000 кДа; от 1000 кДа до 5000 кДа; от 1000 кДа до 4000 кДа; от 1000 кДа до 2,500 кДа; от 2000 кДа до 15000 кДа; от 2000 кДа до 12,500 кДа; от 2000 кДа до 10000 кДа; от 2000 кДа до 7,500 кДа; от 2000 кДа до 6000 кДа; от 2000 кДа до 5000 кДа; от 2000 кДа до 4000 кДа; или от 2000 кДа до 3000 кДа. В одном варианте осуществления, гликоконъюгат, имеющий такую молекулярную массу, получают конъюгацией eTEC, описанной в настоящем документе. В другом варианте осуществления, гликоконъюгат, имеющий такую молекулярную массу, получают с помощью химии восстановительного аминирования (RAC). В другом варианте осуществления, гликоконъюгат, имеющий такую молекулярную массу, получают с помощью химии восстановительного аминирования (RAC) в ДМСО.
В дополнительных вариантах осуществления, гликоконъюгат по изобретению имеет молекулярную массу от 1000 кДа до 20000 кДа; от 1000 кДа до 15000 кДа; от 2000 кДа до 10000 кДа; от 2000 кДа до 7500 кДа; от 2000 кДа до 5000 кДа; от 3000 кДа до 20000 кДа; от 3000 кДа до 15000 кДа; от 3000 кДа до 12500 кДа; от 4000 кДа до 10000 кДа; от 4000 кДа до 7500 кДа; от 4000 кДа до 6000 кДа; или между 5000 кДа и 7000 кДа. В одном варианте осуществления, гликоконъюгат, имеющий такую молекулярную массу, получают с помощью химии восстановительного аминирования (RAC). В другом варианте осуществления, гликоконъюгат, имеющий такую молекулярную массу, получают с помощью химии восстановительного аминирования (RAC) в ДМСО. В другом варианте осуществления, гликоконъюгат с такой молекулярной массой получают с помощью описанной в настоящем документе конъюгации eTEC.
В дополнительных вариантах осуществления, гликоконъюгат по изобретению имеет молекулярную массу от 5000 кДа до 20000 кДа; от 5000 кДа до 15000 кДа; от 5000 кДа до 10000 кДа; от 5000 кДа до 7500 кДа; от 6000 кДа до 20000 кДа; от 6000 кДа до 15000 кДа; от 6000 кДа до 12500 кДа; от 6000 кДа до 10000 кДа или от 6000 кДа до 7500 кДа.
Молекулярную массу гликоконъюгата можно измерить с помощью SEC-MALLS. Любое целое число в любом из вышеуказанных диапазонов рассматривается как вариант осуществления изобретения. Гликоконъюгаты по изобретению также могут характеризоваться отношением (масса/масса) сахарида к белку-носителю. В некоторых вариантах осуществления, отношение полисахарида к белку-носителю в гликоконъюгате (масс./масс.) составляет от 0,5 до 3 (например, примерно 0,5, примерно 0,6, примерно 0,7, примерно 0,8, примерно 0,9, примерно 1,0, примерно 1,1, примерно 1,2, примерно 1,3, примерно 1,4, примерно 1,5, примерно 1,6, примерно 1,7, примерно 1,8, примерно 1,9, примерно 2,0, примерно 2,1, примерно 2,2, примерно 2,3, примерно 2,4, примерно 2,5, примерно 2,6, примерно 2,7, примерно 2,8, примерно 2,9 или примерно 3,0). В других вариантах осуществления, отношение сахарида к белку-носителю (масс./масс.) составляет от 0,5 до 2,0, от 0,5 до 1,5, от 0,8 до 1,2, от 0,5 до 1,0, от 1,0 до 1,5 или от 1,0 до 2,0. В дополнительных вариантах осуществления, отношение сахарида к белку-носителю (масс./масс.) составляет от 0,8 до 1,2. В предпочтительном варианте осуществления, отношение полисахарида к белку-носителю в конъюгате составляет от 0,9 до 1,1. В некоторых таких вариантах осуществления, белок-носитель представляет собой CRM197.
Гликоконъюгаты также могут быть охарактеризованы распределением их молекул по размерам (Kd). Среду эксклюзионной хроматографии (CL-4B) можно использовать для определения относительного распределения молекул конъюгата по размерам. Эксклюзионную хроматографию (ЭХ) используют в колонках с гравитационной подачей для профилирования распределения молекул конъюгатов по размерам. Крупные молекулы, исключенные из пор среды, элюируются быстрее, чем мелкие. Сборщики фракций используют для сбора элюата колонки. Фракции тестируют колориметрически с помощью анализа сахаридов. Для определения Kd колонки калибруют, чтобы установить долю, при которой молекулы полностью исключаются (V0), (Kd=0), и долю, представляющую максимальное удержание (Vi), (Kd=1). Доля, при которой достигается указанный признак образца (Ve), связана с Kd выражением Kd=(Ve - Vo)/ (Vi - V0).
Свободный сахарид. Гликоконъюгаты и иммуногенные композиции по изобретению могут включать свободный сахарид, который нековалентно конъюгирован с белком-носителем, но, тем не менее, присутствует в композиции гликоконъюгата. Свободный сахарид может быть нековалентно связан с (т.е. нековалентно связан, адсорбирован или захвачен) гликоконъюгатом. В предпочтительном варианте осуществления, гликоконъюгат содержит не более 50%, 45%, 40%, 35%, 30%, 25%, 20% или 15% свободного полисахарида по сравнению с общим количеством полисахарида. В предпочтительном варианте осуществления, гликоконъюгат содержит менее примерно 25% свободного полисахарида по сравнению с общим количеством полисахарида. В предпочтительном варианте осуществления, гликоконъюгат содержит не более примерно 20% свободного полисахарида по сравнению с общим количеством полисахарида. В предпочтительном варианте осуществления, гликоконъюгат содержит не более примерно 15% свободного полисахарида по сравнению с общим количеством полисахарида. В другом предпочтительном варианте осуществления, гликоконъюгат содержит не более примерно 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% свободного полисахарида по сравнению с общим количеством полисахарида. В предпочтительном варианте осуществления, гликоконъюгат содержит менее примерно 8% свободного полисахарида по сравнению с общим количеством полисахарида. В предпочтительном варианте осуществления, гликоконъюгат содержит не более примерно 6% свободного полисахарида по сравнению с общим количеством полисахарида. В предпочтительном варианте осуществления, гликоконъюгат содержит не более примерно 5% свободного полисахарида по сравнению с общим количеством полисахарида. См., например, Таблицу 19, Таблицу 20, Таблицу 21, Таблицу 22, Таблицу 23, Таблицу 24 и Таблицу 25.
Ковалентная связь. В других вариантах осуществления, конъюгат содержит, по меньшей мере, одну ковалентную связь между белком-носителем и сахаридом на каждые 5-10 повторяющихся единиц сахарида; каждые 2-7 сахаридных повторяющихся единиц; каждые 3-8 сахаридных повторяющихся единиц; каждые 4-9 сахаридных повторяющихся единиц; каждые 6-11 сахаридных повторяющихся единиц; каждые 7-12 сахаридных повторяющихся единиц; каждые 8-13 сахаридных повторяющихся единиц; каждые 9-14 сахаридных повторяющихся единиц; каждые 10-15 сахаридных повторяющихся единиц; каждые 2-6 сахаридных повторяющихся единиц, каждые 3-7 сахаридных повторяющихся единиц; каждые 4-8 сахаридных повторяющихся единиц; каждые 6-10 сахаридных повторяющихся единиц; каждые 7-11 сахаридных повторяющихся единиц; каждые 8-12 сахаридных повторяющихся единиц; каждые 9-13 сахаридных повторяющихся единиц; каждые 10-14 сахаридных повторяющихся единиц; каждые 10-20 сахаридных повторяющихся единиц; каждые 4-25 сахаридных повторяющихся единиц или каждые 2-25 сахаридных повторяющихся единиц. В частых вариантах осуществления, белок-носитель представляет собой CRM197. В другом варианте осуществления, по меньшей мере, одна связь между белком-носителем и сахаридом возникает на каждые 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 сахаридных повторяющихся единиц полисахарида. В одном варианте осуществления, белок-носитель представляет собой CRM197. Любое целое число в любом из вышеуказанных диапазонов рассматривается как вариант осуществления изобретения.
Лизиновые остатки. Другой способ охарактеризовать гликоконъюгаты по изобретению заключается в количестве лизиновых остатков в белке-носителе (например, CRM197), которые становятся конъюгированными с сахаридом, что может быть охарактеризовано как ряд конъюгированных лизинов (степень конъюгации). Доказательства лизиновой модификации белка-носителя вследствие ковалентных связей с полисахаридами могут быть получены с помощью аминокислотного анализа с использованием обычных методов, известных специалистам в данной области техники. Конъюгация приводит к уменьшению количества восстановленных лизиновых остатков по сравнению с исходным материалом белка-носителя, используемым для получения материалов конъюгата. В предпочтительном варианте осуществления, степень конъюгации гликоконъюгата по изобретению составляет от 2 до 15, от 2 до 13, от 2 до 10, от 2 до 8, от 2 до 6, от 2 до 5, от 2 до 4, от 3 до 15, от 3 до 13, от 3 до 10, от 3 до 8, от 3 до 6, от 3 до 5, от 3 до 4, от 5 до 15, от 5 до 10, от 8 до 15, от 8 до 12, от 10 до 15 или от 10 до 12. В одном варианте осуществления, степень конъюгации гликоконъюгата по изобретению составляет примерно 2, примерно 3, примерно 4, примерно 5, примерно 6, примерно 7, примерно 8, примерно 9, примерно 10, примерно 11, примерно 12, примерно 13, примерно 14 или примерно 15. В предпочтительном варианте осуществления, степень конъюгации гликоконъюгата по изобретению составляет от 4 до 7. В некоторых таких вариантах осуществления, белок-носитель представляет собой CRM197.
Частота присоединения сахаридной цепи к лизину на белке-носителе является еще одним параметром для характеристики гликоконъюгатов по изобретению. Например, в некоторых вариантах осуществления, по меньшей мере, одна ковалентная связь между белком-носителем и полисахаридом приходится на каждые 4 сахаридных повторяющихся единицы полисахарида. В другом варианте осуществления, ковалентная связь между белком-носителем и полисахаридом возникает, по меньшей мере, один раз на каждые 10 сахаридных повторяющихся единиц полисахарида. В другом варианте осуществления, ковалентная связь между белком-носителем и полисахаридом возникает по меньшей мере, один раз на каждые 15 сахаридных повторяющихся единиц полисахарида. В другом варианте осуществления, ковалентная связь между белком-носителем и полисахаридом возникает, по меньшей мере, один раз на каждые 25 сахаридных повторяющихся единиц полисахарида.
О-ацетилирование. В некоторых вариантах осуществления, сахариды по изобретению являются O-ацетилированными. В некоторых вариантах осуществления, гликоконъюгат содержит сахарид, который имеет степень O-ацетилирования между 10-100%, между 20-100%, между 30-100%, между 40-100%, между 50-100%, между 60-100%, между 70-100%, между 75-100%, 80-100%, 90-100%, 50-90%, 60-90%, 70-90% или 80-90%. В других вариантах осуществления, степень ацетилирования составляет ≥10%, ≥20%, ≥30%, ≥40%, ≥50%, ≥60%, ≥70%, ≥80%, или ≥90%, или около 100%. Под % О-ацетилирования подразумевается доля данного сахарида по отношению к 100% (где каждая повторяющаяся единица полностью ацетилирована относительно ее ацетилированной структуры).
В некоторых вариантах осуществления, гликоконъюгат получают восстановительным аминированием. В некоторых вариантах осуществления, гликоконъюгат представляет собой односторонне-связанный конъюгированный сахарид, где сахарид ковалентно связан непосредственно с белком-носителем. В некоторых вариантах осуществления, гликоконъюгат ковалентно связан с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC).
ВОССТАНОВИТЕЛЬНОЕ АМИНИРОВАНИЕ. В одном варианте осуществления, сахарид конъюгирован с белком-носителем посредством восстановительного аминирования (например, как описано в публикациях патентных заявок США №№ 2006/0228380, 2007/0231340, 2007/0184071 и 2007/0184072, WO 2006/110381, WO 2008/079653 и WO 2008/143709).
Восстановительное аминирование включает (1) окисление сахарида, (2) восстановление активированного сахарида и белка-носителя с образованием конъюгата. Перед окислением сахарид необязательно гидролизуют. Можно использовать механический или химический гидролиз. Химический гидролиз можно проводить с использованием уксусной кислоты.
Стадия окисления может включать реакцию с периодатом. Используемый в настоящем документе термин «периодат» относится как к периодату, так и к йодной кислоте. Этот термин также включает как метапериодат (IO4-), так и ортопериодат (IO65-), а также различные соли периодата (например, периодат натрия и периодат калия). В одном варианте осуществления, полисахарид окисляют в присутствии метапериодата, предпочтительно, в присутствии периодата натрия (NaIO4). В другом варианте осуществления, полисахарид окисляют в присутствии ортопериодата, предпочтительно, в присутствии йодной кислоты.
В одном варианте осуществления, окисляющий агент представляет собой стабильное нитроксильное или нитроксидное радикальное соединение, такое как соединения пиперидин-N-окси или пирролидин-N-окси, в присутствии окислителя для селективного окисления первичных гидроксилов. В указанной реакции, фактическим окислителем является соль N-оксоаммония в каталитическом цикле. В одном аспекте, указанное стабильное нитроксильное или нитроксидное радикальное соединение представляет собой соединения пиперидин-N-окси или пирролидин-N-окси. В одном аспекте, указанное стабильное нитроксильное или нитроксидное радикальное соединение несет группу TEMPO (2,2,6,6-тетраметил-1-пиперидинилокси) или PROXYL (2,2,5,5-тетраметил-1-пирролидинилокси). В одном аспекте, указанное стабильное нитроксильное радикальное соединение представляет собой TEMPO или его производное. В одном аспекте, указанный окислитель представляет собой молекулу, несущую фрагмент N-галогена. В одном аспекте, указанный окислитель выбран из любого из N-хлорсукцинимида, N-бромсукцинимида, N-лодосукцинимида, дихлоризоциануровой кислоты, 1,3,5-трихлор-1,3,5-триазинан-2,4,6-триона, дибромизоциануровой кислоты, 1,3,5-трибром-1,3,5-триазинан-2,4,6-триона, дийодизоциануровой кислоты и 1,3,5-трииод-1,3,5-триазинан-2,4,6-триона. Предпочтительно, указанный окислитель представляет собой N-хлорсукцинимид.
После стадии окисления сахарида, говорят, что сахарид активирован, и далее в настоящем описании он упоминается как «активированный». Активированный сахарид и белок-носитель могут быть лиофилизированы (высушены вымораживанием) либо независимо (дискретная лиофилизация), либо вместе (совместно лиофилизированы). В одном варианте осуществления, активированный сахарид и белок-носитель лиофилизируют совместно. В другом варианте осуществления, активированный полисахарид и белок-носитель лиофилизируют независимо.
В одном варианте осуществления, лиофилизация происходит в присутствии невосстанавливающего сахара, возможные невосстанавливающие сахара включают сахарозу, трегалозу, раффинозу, стахиозу, мелецитозу, декстран, маннит, лактит и палатинит.
Следующей стадией процесса конъюгации является восстановление активированного сахарида и белка-носителя с образованием конъюгата (так называемое восстановительное аминирование) с использованием восстанавливающего агента. Подходящие восстанавливающие агенты включают цианоборгидриды, такие как цианоборгидрид натрия, триацетоксиборгидрид натрия или боргидрид натрия или цинка в присутствии кислот Бренстеда или Льюиса), аминобораны, такие как пиридинборан, 2-пиколинборан, 2,6-диборанметанол, диметиламинборан, t-BuMe'PrN-BH3, бензиламин-BH3 или 5-этил-2-метилпиридинборан (PEMB), боран-пиридин или борогидрид-обменная смола. В одном варианте осуществления, восстановителем является цианоборгидрид натрия.
В одном варианте осуществления, реакцию восстановления проводят в водном растворителе (например, выбранном из PBS, MES, HEPES, Bis-tris, ADA, PIPES, MOPSO, BES, MOPS, DIPSO, MOBS, HEPPSO, POPSO, TEA, EPPS, Bicine или HEPB, при pH от 6,0 до 8,5, от 7,0 до 8,0 или от 7,0 до 7,5), в другом варианте осуществления, реакцию проводят в апротонном растворителе. В одном варианте осуществления, реакцию восстановления проводят в растворителе ДМСО (диметилсульфоксиде) или в ДМФ (диметилформамиде). Растворитель ДМСО или ДМФ можно использовать для восстановления активированного полисахарида и белка-носителя, которые были лиофилизированы.
В конце реакции восстановления, в конъюгатах могут остаться непрореагировавшие альдегидные группы, которые можно блокировать с помощью подходящего защитного агента. В одном варианте осуществления, этот защитный агент представляет собой боргидрид натрия (NaBH4). После конъюгации (реакции восстановления и, необязательно, кэпирования) гликоконъюгаты могут быть очищены (обогащены по отношению к количеству конъюгата полисахарид-белок) различными методами, известными специалисту в данной области техники. Эти методы включают диализ, операции концентрирования/диафильтрации, осаждение/элюирование тангенциальной проточной фильтрацией, колоночную хроматографию (DEAE или хроматографию гидрофобного взаимодействия) и глубинную фильтрацию. Гликоконъюгаты могут быть очищены диафильтрацией и/или ионообменной хроматографией и/или эксклюзионной хроматографией. В одном варианте осуществления, гликоконъюгаты очищают диафильтрацией или ионообменной хроматографией или эксклюзионной хроматографией. В одном варианте осуществления, гликоконъюгаты подвергают стерильной фильтрации.
В предпочтительном варианте осуществления, гликоконъюгат из серотипа E. coli выбран из любого из O25B, O1, O2 и O6, получен восстановительным аминированием. В предпочтительном варианте осуществления, гликоконъюгаты из E. coli серотипов O25B, O1, O2 и O6 получают восстановительным аминированием.
В одном аспекте, изобретение относится к конъюгату, который включает белок-носитель, например, CRM197, связанный с сахаридом формулы O25B, представленной 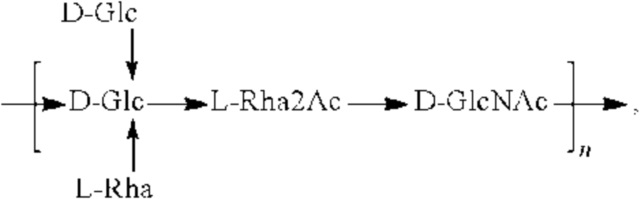 ,
,
где n представляет собой любое целое число, большее или равное 1. В предпочтительном варианте осуществления, n является целым числом, равным, по меньшей мере, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40 и не более 200, 100, 99, 98, 97, 96, 95, 94, 93, 92, 91, 90, 89, 88, 87, 86, 81, 80, 79, 78, 77, 76, 75, 74, 73, 72, 71, 70, 69, 68, 67, 66, 65, 60, 59, 58, 57, 56, 55, 54, 53, 52, 51 или 50. Любое минимальное значение и любое максимальное значение могут быть объединены для определения диапазона. Типовые диапазоны включают, например, по меньшей мере, от 1 до не более 1000; по меньшей мере, от 10 до не более 500; и по меньшей мере, от 20 до не более 80. В одном предпочтительном варианте осуществления, n составляет, по меньшей мере, от 31 до не более 90, более предпочтительно, от 40 до 90, наиболее предпочтительно, от 60 до 85.
В другом аспекте, изобретение относится к конъюгату, который включает белок-носитель, например, CRM197, связанный с сахаридом, имеющим любую из следующих структур, показанных в таблице 1 (см. также ФИГ. 9A-9C и ФИГ. 10A-10B), где n представляет собой целое число, большее или равное 1.
Без привязки к какой-либо теории или механизму, в некоторых вариантах осуществления, считается, что стабильный конъюгат требует такого уровня модификации сахаридного антигена, который уравновешивает сохранение структурной целостности критических иммуногенных эпитопов антигена.
Активация и образование альдегида. В некоторых вариантах осуществления, сахарид по изобретению активируется, что приводит к образованию альдегида. В таких вариантах осуществления, где сахарид активирован, доля (%) активации (или степень окисления (DO)) (см., например, пример 31) относится к молям повторяющейся единицы сахарида на моль альдегида активированного полисахарида. Например, в некоторых вариантах осуществления, сахарид активируется периодатным окислением вицинальных диолов на повторяющейся единицу полисахарида, что приводит к образованию альдегида. Изменение молярных эквивалентов (мэкв) периодата натрия по отношению к сахаридному повторяющемуся звену и температуре во время окисления приводит к различным уровням степени окисления (DO).
Концентрации сахаридов и альдегидов обычно определяют с помощью колориметрических анализов. Альтернативным реагентом является комбинация TEMPO (2,2,6,6-тетраметилпиперидин 1-оксильный радикал)-N-хлорсукцинимида (NCS), которая приводит к образованию альдегидов из первичных спиртовых групп.
В некоторых вариантах осуществления, активированный сахарид имеет степень окисления, при которой количество молей повторяющейся единицы сахарида на моль альдегида активированного сахарида составляет между 1-100, например, между 2-80, между 2-50, между 3-30 и между 4-25. Степень активации, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, ≥20, ≥30, ≥40, ≥50, ≥60, ≥70, ≥80 или ≥90 или примерно 100. Предпочтительно, степень окисления (DO) составляет, по меньшей мере, 5 и не более 50, более предпочтительно, по меньшей мере, 10 и не более 25. В одном варианте осуществления, степень активации составляет, по меньшей мере, 10 и не более 25. Любое минимальное значение и любое максимальное значение могут быть объединены для определения диапазона. Степень окисления может быть представлена в долях (%) активации. Например, в одном варианте осуществления, значение DO, равное 10, относится к одной повторяющейся единице активированного сахарида из общего числа 10 повторяющихся единиц сахарида в активированном сахариде, и в этом случае значение DO, равное 10, может быть представлено как 10% активации.
В некоторых вариантах осуществления, конъюгат, полученный с помощью восстановительного аминирования, включает белок-носитель и сахарид, где сахарид имеет структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187. В некоторых вариантах осуществления, сахарид в конъюгате включает Формулу, где n представляет собой целое число от 1 до 1000, от 5 до 1000, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65.
ОДНОСТОРОННЕ-СВЯЗАННЫЕ КОНЬЮГАТЫ
В некоторых вариантах осуществления, конъюгат представляет собой конъюгированный сахарид с односторонней связью, где сахарид ковалентно связан на одном конце сахарида с белком-носителем. В некоторых вариантах осуществления, односторонне-связанный конъюгированный полисахарид имеет концевой сахарид. Например, конъюгат является односторонне-связанным, если один из концов (концевой сахаридный остаток) полисахарида ковалентно связан с белком-носителем. В некоторых вариантах осуществления, конъюгат является односторонне-связанным, если концевой сахаридный остаток полисахарида ковалентно связан с белком-носителем через линкер. Такие линкеры могут включать, например, цистаминовый линкер (А1), 3,3'-дитиобис(пропановый дигидразидный) линкер (А4) и 2,2'-дитио-N,N'-бис(этан-2,1-диил)бис(2-(аминоокси)ацетамидный) линкер (А6).
В некоторых вариантах осуществления, сахарид конъюгирован с белком-носителем через остаток 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO) с образованием односторонне-связанного конъюгата. См., например, пример 26, пример 27, пример 28 и ФИГ. 17.
В некоторых вариантах осуществления, конъюгат предпочтительно не является биоконъюгатом. Термин «биоконъюгат» относится к конъюгату между белком (например, белком-носителем) и антигеном, например, О-антигеном (например, О25В), полученным на фоне клетки-хозяина, где механизм клетки-хозяина связывает антиген с белком (например, N-ссылки). Гликоконъюгаты включают биоконъюгаты, а также конъюгаты сахарный антиген (например, олиго- и полисахариды)-белок, полученные способами, не требующими приготовления конъюгата в клетке-хозяине, например конъюгированием путем химической связи белка и сахарида.
Тиолактивированные сахариды. В некоторых вариантах осуществления, сахарид по изобретению активирован тиолом. В таких вариантах осуществления, где сахарид активирован тиолом, доля (%) активации относится к молям тиола на сахаридную повторяющуюся единицу активированного полисахарида. Концентрации сахарида и тиола обычно определяют с помощью анализа Эллмана для количественного определения сульфгидрилов. Например, в некоторых вариантах осуществления, сахарид включает активацию 2-кето-3-дезоксиоктановой кислоты (KDO) дисульфид-аминовым линкером. См., например, пример 10 и ФИГ. 31. В некоторых вариантах осуществления, сахарид ковалентно связан с белком-носителем через двухвалентный гетеробифункциональный линкер (также называемый в настоящем документе «спейсером»). Линкер предпочтительно обеспечивает тиоэфирную связь между сахаридом и белком-носителем, что приводит к образованию гликоконъюгата, называемого в настоящем документе «тиоэфирным гликоконъюгатом». В некоторых вариантах осуществления, линкер дополнительно обеспечивает карбаматные и амидные связи, такие как, например, (2-((2-оксоэтил)тио)этил)карбамат (eTEC). См., например, Пример 21.
В некоторых вариантах осуществления односторонне-связанный конъюгат включает белок-носитель и сахарид, где сахарид имеет структуру, выбранную из любой из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187. В некоторых вариантах осуществления, сахарид в конъюгате включает Формулу, где n представляет собой целое число от 1 до 1000, от 5 до 1000, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65.
Например, в одном варианте осуществления, односторонне-связанный конъюгат включает белок-носитель и сахарид, имеющий структуру, выбранную из Формулы O8, Формулы O9a, Формулы O9, Формулы O20ab, Формулы O20ac, Формулы O52, Формулы O97 и Формулы O101, где n представляет собой целое число от 1 до 10.
F. КОНЪЮГАТЫ eTEC
В одном аспекте, изобретение в целом относится к гликоконъюгатам, содержащим сахарид, полученный из описанной выше E. coli, ковалентно конъюгированный с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC) (как описано, например, в патенте США 9517274 и публикации международной патентной заявки WO 2014027302, полностью включенных в настоящее описание посредством ссылки), включая иммуногенные композиции, содержащие такие гликоконъюгаты, и способы получения и применения таких гликоконъюгатов и иммуногенных композиций. Указанные гликоконъюгаты содержат сахарид, ковалентно конъюгированный со спейсером eTEC через один или несколько спейсеров eTEC, где сахарид ковалентно конъюгирован со спейсером eTEC посредством карбаматной связи, и где белок-носитель ковалентно конъюгирован со спейсером eTEC посредством амидной связи. Спейсер eTEC включает семь линейных атомов (т.е. -C(O)NH(CH2)2SCH2C(O)-) и обеспечивает стабильные тиоэфирные и амидные связи между сахаридом и белком-носителем.
Гликоконъюгаты, связанные с eTEC, по изобретению могут быть представлены общей формулой (I):
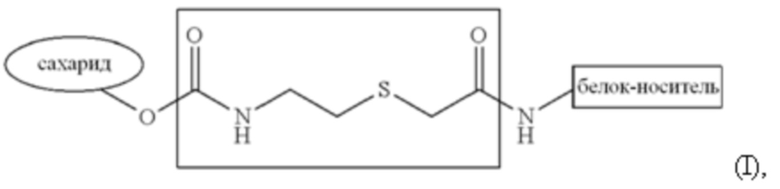
где атомы, составляющие спейсер eTEC, содержатся в центральной рамке.
В указанных гликоконъюгатах по изобретению сахарид может представлять собой полисахарид или олигосахарид.
Белки-носители, включенные в гликоконъюгаты по изобретению, выбраны из группы белков-носителей, обычно подходящих для таких целей, как описано в настоящем документе далее или известно специалистам в данной области техники. В конкретных вариантах осуществления, белок-носитель представляет собой CRM197.
В другом аспекте, изобретение предлагает способ получения гликоконъюгата, содержащего сахарид, описанный в настоящем документе, конъюгированного с белком-носителем через спейсер eTEC, включающий стадии а) реакции сахарида с производным угольной кислоты в органическом растворителе с получением активированного сахарида; b) взаимодействие активированного сахарида с цистамином или цистеамином или их солью с получением тиолированного сахарида; c) взаимодействие тиолированного сахарида с восстанавливающим агентом с получением активированного тиолированного сахарида, содержащего один или несколько свободных сульфгидрильных остатков; d) взаимодействие активированного тиолированного сахарида с активированным белком-носителем, содержащим одну или несколько α-галогенацетамидных групп, с получением конъюгата тиолированный сахарид-белок-носитель; и e) взаимодействие конъюгата тиолированный сахарид-белок-носитель с (i) первым кэпирующим реагентом, способным кэпировать неконъюгированные α-галогенацетамидные группы активированного белка-носителя; и/или (ii) вторым кэпирующим реагентом, способным кэпировать неконъюгированные свободные сульфгидрильные остатки активированного тиолированного сахарида; в результате чего образуется гликоконъюгат, связанный с eTEC.
В частых вариантах осуществления, производное угольной кислоты представляет собой 1,1'-карбонил-ди-(1,2,4-триазол) (CDT) или 1,1'-карбонилдиимидазол (CDI). Предпочтительно, производное угольной кислоты представляет собой CDT, и органический растворитель представляет собой полярный апротонный растворитель, такой как диметилсульфоксид (ДМСО). В предпочтительных вариантах осуществления, тиолированный сахарид получают реакцией активированного сахарида с бифункциональным симметричным тиоалкиламиновым реагентом, цистамином или его солью. Альтернативно, тиолированный сахарид может быть образован реакцией активированного сахарида с цистеамином или его солью. Гликоконъюгаты, связанные с eTEC, полученные способами по изобретению, могут быть представлены общей формулой (I).
В частых вариантах осуществления, первым кэпирующим реагентом является N-ацетил-L-цистеин, который реагирует с неконъюгированными α-галогенацетамидными группами на остатках лизина белка-носителя с образованием остатка S-карбоксиметилцистеина (СМС), ковалентно связанного с активированным остатком лизина через тиоэфирную связь.
В других вариантах осуществления, второй кэпирующий реагент представляет собой йодацетамид (IAA), который взаимодействует с неконъюгированными свободными сульфгидрильными группами активированного тиолированного сахарида с получением кэпированного тиоацетамида. Часто стадия е) включает кэпирование как первым кэпирующим реагентом, так и вторым кэпирующим реагентом. В некоторых вариантах осуществления, стадия e) включает кэпирование с помощью N-ацетил-L-цистеина в качестве первого кэпирующего реагента и IAA в качестве второго кэпирующего реагента.
В некоторых вариантах осуществления, стадия кэпирования e) дополнительно включает реакцию с восстанавливающим агентом, например, DTT, TCEP или меркаптоэтанолом, после реакции с первым и/или вторым реагентом кэпирования.
Гликоконъюгаты, связанные с eTEC, и иммуногенные композиции по изобретению могут включать свободные сульфгидрильные остатки. В некоторых случаях, активированные тиолированные сахариды, образованные способами, предложенными в настоящем документе, будут включать несколько свободных сульфгидрильных остатков, некоторые из которых могут не подвергаться ковалентной конъюгации с белком-носителем на стадии конъюгации. Такие остаточные свободные сульфгидрильные остатки кэпируются реакцией с атиол-реактивным блокирующим реагентом, например, йодацетамидом (IAA), для блокирования потенциально реакционноспособной функциональной группы. Другие тиол-реакционноспособные кэпирующие реагенты, например малеимидсодержащие реагенты и подобные, также рассматриваются.
Кроме того, гликоконъюгаты, связанные с eTEC, и иммуногенные композиции по изобретению могут включать остаточный неконъюгированный белок-носитель, который может включать активированный белок-носитель, который претерпел модификацию во время стадий процесса кэпирования.
В некоторых вариантах осуществления, стадия d) дополнительно включает получение активированного белка-носителя, содержащего одну или несколько α-галогенацетамидных групп, перед реакцией активированного тиолированного сахарида с активированным белком-носителем. В частых вариантах осуществления, активированный белок-носитель содержит одну или несколько α-бромацетамидных групп.
В другом аспекте, изобретение относится к гликоконъюгату, связанному с eTEC, содержащему описанный в настоящем документе сахарид, конъюгированный с белком-носителем через спейсер eTEC, полученный в соответствии с любым из описанных в настоящем документе способов.
В некоторых вариантах осуществления, белок-носитель представляет собой CRM197, и ковалентная связь через спейсер eTEC между CRM197 и полисахаридом происходит, по меньшей мере, один раз в каждых 4, 10, 15 или 25 сахаридных повторяющихся единицах полисахарида.
Для каждого из аспектов изобретения, в конкретных вариантах осуществления способов и композиций, описанных в настоящем документе, гликоконъюгат, связанный с eTEC, содержит сахарид, описанный в настоящем документе, например, сахарид, полученный из E. coli.
В другом аспекте, изобретение предлагает способ профилактики, лечения или облегчения бактериальной инфекции, заболевания или состояния у субъекта, включающий введение субъекту иммунологически эффективного количества иммуногенной композиции по изобретению, где указанная иммуногенная композиция содержит связанный с eTEC гликоконъюгат, содержащий описанный в настоящем документе сахарид. В некоторых вариантах осуществления, сахарид получают из E. coli.
В некоторых вариантах осуществления, гликоконъюгат, связанный с eTEC, содержит белок-носитель и сахарид, в котором указанный сахарид имеет структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 and Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187. В некоторых вариантах осуществления, сахарид в конъюгате включает Формулу, где n представляет собой целое число от 1 до 1000, от 5 до 1000, предпочтительно, от 31 до 100, более предпочтительно, от 35 до 90, наиболее предпочтительно, от 35 до 65.
Количество лизиновых остатков в белке-носителе, которые становятся конъюгированными с сахаридом, можно охарактеризовать как диапазон конъюгированных лизинов. Например, в некоторых вариантах осуществления иммуногенных композиций, CRM197 может содержать от 4 до 16 лизиновых остатков из 39, ковалентно связанных с сахаридом. Другой способ выражения этого параметра состоит в том, что примерно от 10% до примерно 41% лизинов CRM197 ковалентно связаны с сахаридом. В других вариантах осуществления, CRM197 может содержать от 2 до 20 лизиновых остатков из 39, ковалентно связанных с сахаридом. Другой способ выражения этого параметра заключается в том, что примерно от 5% до примерно 50% лизинов CRM197 ковалентно связаны с сахаридом.
В частых вариантах осуществления, белок-носитель представляет собой CRM197, и ковалентная связь через спейсер eTEC между CRM197 и полисахаридом происходит, по меньшей мере, один раз в каждых 4, 10, 15 или 25 сахаридных повторяющихся единицах полисахарида.
В других вариантах осуществления, конъюгат содержит, по меньшей мере, одну ковалентную связь между белком-носителем и сахаридом на каждые 5-10 повторяющихся единиц сахарида; каждые 2-7 повторяющихся единиц сахарида; каждые 3-8 повторяющихся единиц сахарида; каждые 4-9 повторяющихся единиц сахарида; каждые 6-11 повторяющихся единиц сахарида; каждые 7-12 повторяющихся единиц сахарида; каждые 8-13 повторяющихся единиц сахарида; каждые 9-14 повторяющихся единиц сахарида; каждые 10-15 повторяющихся единиц сахарида; каждые 2-6 повторяющихся единиц сахарида, каждые 3-7 повторяющихся единиц сахарида; каждые 4-8 повторяющихся единиц сахарида; каждые 6-10 повторяющихся единиц сахарида; каждые 7-11 повторяющихся единиц сахарида; каждые 8-12 повторяющихся единиц сахарида; каждые 9-13 повторяющихся единиц сахарида; каждые 10-14 повторяющихся единиц сахарида; каждые 10-20 повторяющихся единиц сахарида; или каждые 4-25 повторяющихся единиц сахарида.
В другом варианте осуществления, по меньшей мере, одна связь между белком-носителем и сахаридом возникает на каждые 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 повторяющихся единиц сахарида полисахарида.
G. БЕЛКИ-НОСИТЕЛИ
Компонент гликоконъюгата по изобретению представляет собой белок-носитель, с которым конъюгирован сахарид. Термины «белок-носитель» или «белок-носитель» или «носитель» могут использоваться в настоящем документе взаимозаменяемо. Белки-носители должны поддаваться стандартным процедурам конъюгации.
Одним из компонентов конъюгата является белок-носитель, с которым конъюгирован О-полисахарид. В одном варианте осуществления, конъюгат включает белок-носитель, конъюгированный с сердцевинным олигосахаридом О-полисахарида (см. ФИГ. 24). В одном варианте осуществления, конъюгат включает белок-носитель, конъюгированный с О-антигеном О-полисахарида.
Термины «белок-носитель» или «белок-носитель» или «носитель» могут использоваться в настоящем документе взаимозаменяемо. Белки-носители должны поддаваться стандартным процедурам конъюгации.
В предпочтительном варианте осуществления, белок-носитель конъюгатов независимо выбран из любого одного из мутантов TT, DT, DT (таких как CRM197), белка D H.influenzae, слитых белков PhtX, PhtD, PhtDE (в частности, описанных в WO 01/98334 и WO 03/54007), детоксицированного пневмолизина, PorB, белка N19, PspA, OMPC, токсина A или B C. Difficile и PsaA. В одном варианте осуществления, белок-носитель конъюгатов по изобретению представляет собой DT (дифтерийный анатоксин). В другом варианте осуществления, белок-носитель конъюгатов по изобретению представляет собой ТТ (столбнячный анатоксин). В другом варианте осуществления, белок-носитель конъюгатов по изобретению представляет собой PD (белок D Haemophilus influenzae - см., например, ЕР 0 594 610 В). В некоторых вариантах осуществления, белок-носитель включает поли(L-лизин) (PLL). В другом варианте осуществления, белком-носителем конъюгатов по изобретению является SCP (стрептококковая пептидаза C5a) (Brown, C.K. et al., 2005, PNAS 102(51): 18391-18396).
В предпочтительном варианте осуществления, сахариды конъюгированы с белком CRM197. Белок CRM197 представляет собой нетоксичную форму дифтерийного токсина, но иммунологически неотличим от дифтерийного токсина. CRM197 продуцируется C. diphtheriae, инфицированным нетоксигенным фагом β197tox, созданным в результате нитрозогуанидинового мутагенеза токсигенного коринефага бета. Белок CRM197 имеет ту же молекулярную массу, что и дифтерийный токсин, но отличается от него одной заменой основания (гуанин на аденин) в структурном гене. Это единственное изменение основания вызывает аминокислотную замену глицина на глутаминовую кислоту в зрелом белке и устраняет токсические свойства дифтерийного токсина. Белок CRM197 является безопасным и эффективным носителем сахаридов, зависящим от Т-клеток.
Соответственно, в некоторых вариантах осуществления, конъюгаты по изобретению включают CRM197 в качестве белка-носителя, где сахарид ковалентно связан с CRM197.
В предпочтительном варианте осуществления, белок-носитель гликоконъюгатов выбран из группы, состоящей из DT (дифтерийного токсина), TT (столбнячного анатоксина) или фрагмента C из TT, CRM197 (нетоксичного, но антигенно идентичного варианта дифтерийного токсина), других мутантов DT (таких как CRM176, CRM228, CRM 45 (Uchida et al. J. Biol. Chem. 218; 3838-3844, 1973), CRM9, CRM45, CRM102, CRM103 или CRM107; и другие мутации, описанные Nicholls and Youle in Genetically Engineered Toxins, Ed: Frankel, Maecel Dekker Inc, 1992; делеции или мутации Glu-148 в Asp, Gln или Ser и/или Ala 158 в GIy и другие мутации, описанные в US 4709017 или US 4950740; мутации, по меньшей мере, одного или нескольких остатков Lys 516, Lys 526, Phe 530 и/или Lys 534 и другие мутации, описанные в US 5917017 или US 6455673; или фрагмент, описанный в US 5843711), пневмококкового пневмолизина (Kuo et al (1995) Infect lmmun 63; 2706-13) включая детоксицированный каким-либо образом слой, например, dPLY-GMBS (WO 04081515, PCT/EP2005/010258) или dPLY-формол, PhtX, включая PhtA, PhtB, PhtD, PhtE (последовательности PhtA, PhtB, PhtD или PhtE описаны в WO 00/37105 или WO 00/39299) и слияния белков Pht, например слияния PhtDE, слияния PhtBE, Pht AE (WO 01/98334, WO 03/54007, WO 2009/000826), OMPC (менингококкового белка наружной мембраны - обычно экстрагируется из N. meningitidis серогруппы B - EP0372501), PorB (из N. meningitidis), PD (белок Haemophilus influenzae D - см., например, ЕР 0594610 В) или их иммунологически функциональных эквивалентов, синтетических пептидов (ЕР0378881, ЕР0427347), белков теплового шока (WO 93/17712, WO 94/03208), белков коклюша (WO 98/58668, ЕР0471177), цитокинов, лимфокинов, факторов роста или гормонов (WO 91/01146), искусственных белков, содержащих множественные CD4+ Т-клеточные эпитопы человека из различных антигенов, происходящих от патогенов (Falugi et al (2001) Eur J Immunol 31; 3816-3824), например белка N19 (Baraldoi et al. (2004) Infect lmmun 72; 4884-7), поверхностного белка пневмококка PspA (WO 02/091998), белков, поглощающих железо (WO 01/72337), токсина A или B или C. difficile (WO 00/61761), трансферрин-связывающих белков, белка пневмококковой адгезии (PsaA), рекомбининатного экзотоксина А Pseudomonas aeruginosa (в частности, его нетоксических мутантов (таких как экзотоксин A, несущий замену на глутаминовой кислоте 553 (Uchida Cameron DM, RJ Collier. 1987. J. Bacteriol. 169:4967-4971)). Другие белки, такие как овальбумин, гемоцианин лимфы улитки (KLH), бычий сывороточный альбумин (BSA) или очищенное белковое производное туберкулина (PPD), также могут быть использованы в качестве белков-носителей. Другие подходящие белки-носители включают инактивированные бактериальные токсины, такие как холерный анатоксин (например, как описано в международной патентной заявке № WO 2004/083251), E.coli LT, E.coli ST и экзотоксин A из Pseudomonas aeruginosa.
В некоторых вариантах осуществления, белок-носитель выбран из любого из, например, CRM197, фрагмента B дифтерийного токсина (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C из TT, коклюшного анатоксина, холерного анатоксина или экзотоксина А из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), флагеллина, детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы холерного токсина B (CTB), пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, C. jejuni AcrA и природных гликопротеинов C. jejuni. В одном варианте осуществления, белок-носитель представляет собой детоксицированный экзотоксин Pseudomonas (EPA). В другом варианте осуществления, белок-носитель представляет собой не детоксицированный экзотоксин Pseudomonas (EPA). В одном варианте осуществления, белок-носитель представляет собой флагеллин. В другом варианте осуществления, белок-носитель не является флагеллином.
В предпочтительном варианте осуществления, белок-носитель гликоконъюгатов независимо выбран из группы, состоящей из мутантов ТТ, DT, DT (таких как CRM197), белка D H. influenzae, слияний PhtX, PhtD, PhtDE (в частности, описанных в WO 01/98334 и WO 03/54007), детоксицированного пневмолизина, PorB, белка N19, PspA, OMPC, токсина A или B C. Difficile и PsaA. В одном варианте осуществления, белок-носитель гликоконъюгатов по изобретению представляет собой DT (дифтерийный анатоксин). В другом варианте осуществления, белок-носитель гликоконъюгатов по изобретению представляет собой ТТ (столбнячный анатоксин). В другом варианте осуществления, белок-носитель гликоконъюгатов по изобретению представляет собой PD (белок D Haemophilus influenzae - см., например, ЕР 0 594 610 В).
В предпочтительном варианте осуществления, капсульные сахариды по изобретению конъюгированы с белком CRM197. Белок CRM197 представляет собой нетоксичную форму дифтерийного токсина, но иммунологически неотличим от дифтерийного токсина. CRM197 продуцируется C. diphtheriae, инфицированным нетоксигенным фагом β197tox, созданным нитрозогуанидиновым мутагенезом токсигенного коринефага бета (Uchida, T. et al. 1971, Nature New Biology 233:8-11). Белок CRM197 имеет ту же молекулярную массу, что и дифтерийный токсин, но отличается от него одной заменой основания (гуанин на аденин) в структурном гене. Это единственное изменение основания вызывает аминокислотную замену глицина на глутаминовую кислоту в зрелом белке и устраняет токсические свойства дифтерийного токсина. Белок CRM197 является безопасным и эффективным носителем сахаридов, зависящим от Т-клеток. Более подробную информацию о CRM197 и его продуцировании можно найти, например, в US 5,614,382.
Соответственно, в частых вариантах осуществления, гликоконъюгаты по изобретению содержат CRM197 в качестве белка-носителя, где капсулярный полисахарид ковалентно связан с CRM197.
Н. ДОЗИРОВКИ КОМПОЗИЦИЙ
Схемы дозирования могут быть скорректированы для обеспечения оптимального желаемого ответа. Например, можно вводить одну дозу полипептида, полученного из E. coli, или его фрагмента, можно вводить несколько разделенных доз в течение времени, или дозу можно пропорционально уменьшать или увеличивать в зависимости от остроты ситуации. Следует отметить, что значения дозировки могут варьироваться в зависимости от типа и тяжести состояния, подлежащего облегчению, и могут включать однократные или многократные дозы. Кроме того, следует понимать, что для любого конкретного субъекта конкретные схемы дозирования должны корректироваться с течением времени в соответствии с индивидуальными потребностями и профессиональным мнением лица, вводящего или контролирующего введение композиций, и что диапазоны дозировок, указанные в настоящем документе, являются только типовыми и не предназначены для ограничения объема или применения заявленной композиции. Определение подходящих дозировок и схем введения терапевтического белка хорошо известно в соответствующей области техники, и будут поняты специалистом в данной области техники после предоставления описанных в настоящем документе идей.
В некоторых вариантах осуществления, количество полипептида, полученного из E.coli, или его фрагмента в композиции может составлять от примерно 10 мкг до примерно 300 мкг каждого белка-антигена. В некоторых вариантах осуществления, количество полипептида, полученного из E. coli, или его фрагмента в композиции может составлять от примерно 20 мкг до примерно 200 мкг каждого белкового антигена.
Количество гликоконъюгата(ов) в каждой дозе выбирают как количество, которое индуцирует иммунозащитный ответ без существенных неблагоприятных побочных эффектов в типовых вакцинах. Такое количество будет варьироваться в зависимости от того, какой конкретный иммуноген используется и как он презентирован.
Количество конкретного гликоконъюгата в иммуногенной композиции можно рассчитать на основе общего количества полисахаридов для этого конъюгата (конъюгированного и не конъюгированного). Например, гликоконъюгат с 20% свободного полисахарида будет содержать около 80 г конъюгированного полисахарида и около 20 г не конъюгированного полисахарида в дозе 100 г полисахарида. Количество гликоконъюгата может варьироваться в зависимости от серотипа E. coli. Концентрацию сахарида можно определить с помощью анализа уроновой кислоты.
«Иммуногенное количество» различных полисахаридных компонентов в иммуногенной композиции может различаться, и каждое из них может составлять примерно 1,0 г, примерно 2,0 г, примерно 3,0 г, примерно 4,0 г, примерно 5,0 г, примерно 6,0 г, примерно 7,0 г, примерно 8,0 г, примерно 9,0 г, примерно 10,0 г, примерно 15,0 г, примерно 20,0 г, примерно 30,0 г, примерно 40,0 пг, примерно 50,0 пг, примерно 60,0 пг, примерно 70,0 пг, примерно 80,0 пг, примерно 90,0 пг или примерно 100,0 г любого конкретного полисахаридного антигена. Как правило, каждая доза будет содержать от 0,1 г до 100 г полисахарида для данного серотипа, в частности, от 0,5 г до 20 г, более конкретно, от 1 г до 10 г, и еще более конкретно, от 2 г до 5 г. Любое целое число в любом из вышеуказанных диапазонов рассматривается как вариант осуществления изобретения. В одном варианте осуществления, каждая доза будет содержать 1 г, 2 г, 3 г, 4 г, 5 г, 6 г, 7 г, 8 г, 9 г, 10 г, 15 г или 20 г полисахарида для данного серотипа.
Количество белка-носителя. Как правило, каждая доза будет содержать от 5 г до 150 г белка-носителя, в частности, от 10 г до 100 г белка-носителя, более конкретно, от 15 г до 100 г белка-носителя, более конкретно, от 25 до 75 г белка-носителя, более конкретно, от 30 г до 70 г белка-носителя, более конкретно, от 30 до 60 г белка-носителя, более конкретно, от 30 г до 50 г белка-носителя, и еще более конкретно, от 40 до 60 г белка-носителя. В одном варианте осуществления, указанный белок-носитель представляет собой CRM197. В одном варианте осуществления, каждая доза будет содержать примерно 25 г, примерно 26 г, примерно 27 г, примерно 28 г, примерно 29 г, примерно 30 г, примерно 31 г, примерно 32 г, примерно 33 г, примерно 34 г, примерно 35 г, примерно 36 г, примерно 37 г, примерно 38 г, примерно 39 г, примерно 40 г, примерно 41 г, примерно 42 г, примерно 43 г, примерно 44 г, примерно 45 г, примерно 46 г, примерно 47 г, примерно 48 г, примерно 49 г, примерно 50 г, примерно 51 г, примерно 52 г, примерно 53 г, примерно 54 г, примерно 55 г, примерно 56 г, примерно 57 г, примерно 58 г, примерно 59 г, примерно 60 г, примерно 61 г, примерно 62 г, примерно 63 г, примерно 64 г, примерно 65 г, примерно 66 г, примерно 67 г, 68 г, примерно 69 г, примерно 70 г, примерно 71 г, примерно 72 г, примерно 73 г, примерно 74 г или примерно 75 г белка-носителя. В одном варианте осуществления, указанный белок-носитель представляет собой CRM197.
I. АДЪЮВАНТ
В некоторых вариантах осуществления, описанные в настоящем документе иммуногенные композиции могут дополнительно содержать, по меньшей мере, один, два или три адъюванта. Термин «адъювант» относится к соединению или смеси, которые усиливают иммунный ответ на антиген. Антигены могут действовать в первую очередь как система доставки, в первую очередь как иммуномодулятор или иметь сильные черты обоих. Подходящие адъюванты включают адъюванты, подходящие для применения у млекопитающих, включая человека.
Примеры известных подходящих адъювантов типа системы доставки, которые можно использовать у людей, включают, но не ограничены ими, квасцы (например, фосфат алюминия, сульфат алюминия или гидроксид алюминия), фосфат кальция, липосомы, эмульсии масло-в-воде, такие как MF59 (4,3% масс./об. сквалена, 0,5% масс./об. полисорбата 80 (Tween 80), 0,5% масс./об. сорбитантриолеата (Span 85)), эмульсии вода-в-масле, такие как Монтанид, и микрочастицы или наночастицы поли(D,L-лактид-со-гликолид) (PLG).
В одном варианте осуществления, иммуногенные композиции, описанные в настоящем документе, содержат соли алюминия (квасцы) в качестве адъюванта (например, фосфат алюминия, сульфат алюминия или гидроксид алюминия). В предпочтительном варианте осуществления, иммуногенные композиции, описанные в настоящем документе, содержат фосфат алюминия или гидроксид алюминия в качестве адъюванта. В одном варианте осуществления, иммуногенные композиции, описанные в настоящем документе, содержат от 0,1 мг/мл до 1 мг/мл или от 0,2 мг/мл до 0,3 мг/мл элементарного алюминия в форме фосфата алюминия. В одном варианте осуществления, иммуногенные композиции, описанные в настоящем документе, содержат примерно 0,25 мг/мл элементарного алюминия в форме фосфата алюминия. Примеры известных подходящих адъювантов иммуномодулирующего типа, которые можно использовать у людей, включают, но не ограничены ими, сапониновые экстракты из коры дерева Aquilla (QS21, Quil A), агонисты TLR4, такие как MPL (монофосфорил липид A), 3DMPL (3-O-деацилированный MPL) или GLA-AQ, мутанты LT/CT, цитокины, такие как различные интерлейкины (например, IL-2, IL-12) или GM-CSF, AS01 и подобные.
Примеры известных подходящих адъювантов иммуномодулирующего типа, с признаками как доставки, так и иммуномодуляции, которые могут быть использованы у людей, включают, но не ограничены ими, ISCOMS (см., например, Sjölander et al. (1998) J. Leukocyte Biol. 64:713; WO 90/03184, WO 96/11711, WO 00/48630, WO 98/36772, WO 00/41720, WO 2006/134423 и WO 2007/026190) или GLA-EM, который представляет собой комбинацию агониста TLR4 и эмульсии масло-в-воде.
Для ветеринарных применений, включая, помимо прочего, эксперименты на животных, можно использовать полный адъювант Фрейнда (CFA), неполный адъювант Фрейнда (IFA), Эмульсиген, N-ацетилмурамил-L-треонил-D-изоглутамин (thr-MDP), N-ацетил-нор-мурамил-L-аланил-D-изоглутамин (CGP 11637, обозначаемый как нор-MDP), N-ацетилмурамил-L-аланил-D-изоглутаминил-L-аланин-2-(1'-2'-дипальмитоил-sn-глицеро-3-гидроксифосфорилокси)-этиламин (CGP 19835A, обозначаемый как MTP-PE) и RIBI, который содержит три компонента, экстрагированные из бактерий, монофосфориловый липид A, димиколат трегалозы и скелет клеточной стенки (MPL+TDM+CWS) в 2% эмульсии сквалена/Tween 80.
Дополнительные типовые адъюванты для повышения эффективности иммуногенных композиций, описанных в настоящем документе, включают, но не ограничены ими, (1) составы эмульсий типа «масло в воде» (с или без других специфических иммуностимулирующих агентов, таких как мурамиловые пептиды (см. ниже) или компонентов клеточной стенки бактерий)), такие как, например, (а) SAF, содержащий 10% сквалана, 0,4% Tween 80, 5% блокированного плюроником полимера L121 и thr-MDP, либо микрофлюидизированного в субмикронную эмульсию, либо перемешанного для получения эмульсии большего размера, и (b) адъювантная система RIBI™ (RAS) (Ribi Immunochem, Hamilton, Mont.), содержащая 2% сквалена, 0,2% Tween 80 и один или несколько компонентов бактериальной клеточной стенки, таких как монофосфорилипид A (MPL), трегалозодимиколат (TDM) и скелет клеточной стенки (CWS), предпочтительно MPL+CWS (DETOX™); (2) сапониновые адъюванты, такие как QS21, STIMULON™ (Cambridge Bioscience, Worcester, Mass.), ABISCO® (Isconova, Sweden) или ISCOMATRIX® (Commonwealth Serum Laboratories, Australia), или полученные из них частицы, такие как ISCOM (иммуностимулирующие комплексы), где ISCOMS могут быть лишены дополнительного детергента (например, WO 00/07621); (3) полный адъювант Фрейнда (CFA) и неполный адъювант Фрейнда (IFA); (4) цитокины, такие как интерлейкины (например, IL-1, IL-2, IL-4, IL-5, IL-6, IL-7, IL-12 (например, WO 99/44636)), интерфероны (например, гамма-интерферон), макрофагальный колониестимулирующий фактор (M-CSF), фактор некроза опухоли (TNF) и т.д.; (5) монофосфориллипид А (MPL) или 3-O-деацилированный MPL (3dMPL) (см., например, GB2220211, EP0689454) (см., например, WO 00/56358); (6) комбинации 3dMPL, например, с QS21 и/или эмульсиями масло-в-воде (см., например, ЕР0835318, ЕР0735898, ЕР0761231); (7) полиоксиэтиленовый эфир или полиоксиэтиленовый эфир (см., например, WO 99/52549); (8) поверхностно-активное вещество на основе сложного эфира полиоксиэтиленсорбитана в комбинации с октоксинолом (например, WO 01/21207) или поверхностно-активное вещество на основе алкилового или сложного эфира полиоксиэтилена в сочетании, по меньшей мере, с одним дополнительным неионным поверхностно-активным веществом, таким как октоксинол (например, WO 01/21152); (9) сапонин и иммуностимулирующий олигонуклеотид (например, олигонуклеотид CpG) (например, WO 00/62800); (10) иммуностимулятор и частицу соли металла (см., например, WO 00/23105); (11) сапонин и эмульсию масло-в-воде (например, WO 99/11241); (12) сапонин (например, QS21) + 3dMPL+IM2 (необязательно+стерол) (например, WO 98/57659); (13) другие вещества, которые действуют как иммуностимулирующие агенты для повышения эффективности композиции. Мурамиловые пептиды включают N-ацетилмурамил-L-треонил-D-изоглутамин (thr-MDP), N-25-ацетил-нормурамил-L-аланил-D-изоглутамин (nor-MDP), N-ацетилмурамил-L-аланил-D-изоглутарнинил-L-аланин-2-(1'-2'-дипальмитоил-sn-глицеро-3-гидроксифосфорилокси)-этиламин MTP-PE) и т.д.
В варианте осуществления настоящего изобретения, иммуногенные композиции, описанные в настоящем документе, содержат олигонуклеотид CpG в качестве адъюванта. Олигонуклеотид CpG, используемый в настоящем документе, относится к иммуностимулирующему олигодезоксинуклеотиду CpG (CpG ODN), и, соответственно, эти термины используются взаимозаменяемо, если не указано иное. Иммуностимулирующие олигодезоксинуклеотиды CpG содержат один или несколько иммуностимулирующих мотивов CpG, которые представляют собой неметилированные цитозин-гуаниновые динуклеотиды, необязательно в определенных предпочтительных контекстах оснований. Статус метилирования иммуностимулирующего мотива CpG обычно относится к остатку цитозина в динуклеотиде. Иммуностимулирующий олигонуклеотид, содержащий, по меньшей мере, один неметилированный динуклеотид CpG, представляет собой олигонуклеотид, который содержит 5' неметилированный цитозин, связанный фосфатной связью с 3' гуанином, и который активирует иммунную систему посредством связывания с Toll-подобным рецептором 9 (TLR-9). В другом варианте осуществления, иммуностимулирующий олигонуклеотид может содержать один или несколько метилированных динуклеотидов CpG, которые будут активировать иммунную систему через TLR9, но не так сильно, как если бы мотив(ы) CpG был/были неметилированы. Иммуностимулирующие олигонуклеотиды CpG могут содержать один или несколько палиндромов, которые, в свою очередь, могут охватывать динуклеотид CpG. Олигонуклеотиды CpG описаны в ряде выданных патентов, опубликованных патентных заявках и других публикациях, включая патенты США №№ 6,194,388; 6,207,646; 6,214,806; 6,218,371; 6,239,116; и 6,339,068.
В варианте осуществления, настоящего изобретения, иммуногенные композиции, описанные в настоящем документе, содержат любой из олигонуклеотидов CpG, описанных на странице 3, строка 22, до страницы 12, строка 36 WO 2010/125480.
Были идентифицированы различные классы иммуностимулирующих олигонуклеотидов CpG. Они обозначаются как классы А, В, С и Р и более подробно описаны на стр. 3, строка 22, на стр. 12, строка 36, WO 2010/125480. Способы по изобретению охватывают использование этих различных классов иммуностимулирующих олигонуклеотидов CpG.
VII. Наночастицы
В другом аспекте, в настоящем документе описан иммуногенный комплекс, включающий 1) наноструктуру; и 2) по меньшей мере, один фимбриальный полипептидный антиген или его фрагмент. Предпочтительно, фимбриальный полипептид или его фрагмент получают из фимбриального H E. coli (fimH). В предпочтительном варианте осуществления, фимбриальный полипептид выбран из любого из фимбриальных полипептидов, описанных выше. Например, фимбриальный полипептид может содержать любую аминокислотную последовательность, выбранную из SEQ ID NO: 1-10, 18, 20, 21, 23, 24 и 26-29.
В некоторых вариантах осуществления, антиген слит или конъюгирован с внешней частью наноструктуры для стимуляции развития адаптивных иммунных ответов на отображаемые эпитопы. В некоторых вариантах осуществления, иммуногенный комплекс дополнительно включает адъювант или другие иммуномодулирующие соединения, прикрепленные к внешней стороне и/или инкапсулированные внутри клетки, чтобы помочь адаптировать тип иммунного ответа, генерируемого для каждого патогена.
В некоторых вариантах осуществления, наноструктура включает единую сборку, включающую множество идентичных первых родственных наноструктуре полипептидов.
В альтернативных вариантах осуществления, наноструктура включает множество сборок, включая множество идентичных первых родственных наноструктуре полипептидов, и множество вторых сборок, где каждая вторая сборка содержит множество идентичных вторых родственных наноструктуре полипептидов.
Для создания описанных в настоящем документе иммуногенных композиций можно использовать различные платформы наноструктур. В некоторых вариантах осуществления, используемые наноструктуры образованы множеством копий одной субъединицы. В некоторых вариантах осуществления, используемые наноструктуры образованы множеством копий множества различных субъединиц.
Наноструктуры обычно имеют шарообразную форму и/или имеют вращательную симметрию (например, с 3-кратной и 5-кратной осью), например, с икосаэдрической структурой, приведенной в настоящем документе в качестве примера.
В некоторых вариантах осуществления, антиген представлен на самособирающихся наночастицах, таких как самособирающиеся наноструктуры, полученные из ферритина (FR), E2p, Qβ и I3-01. E2p представляет собой переконструированный вариант дигидролипоилацилтрансферазы из Bacillus stearothermophilus. I3-01 представляет собой сконструированный белок, который может самособираться в гиперстабильные наночастицы. Последовательности субъединиц этих белков известны в данной области техники. В первом аспекте, в настоящем документе описан родственный наноструктуре полипептид, содержащий аминокислотную последовательность, которая, по меньшей мере, на 75% идентична по своей длине и идентична, по меньшей мере, в одном идентифицированном положении интерфейса аминокислотной последовательности родственного наноструктуре полипептида, выбранной из группы, состоящей из SEQ ID NO: 59-92. Родственные наноструктуре полипептиды можно использовать, например, для получения наноструктур. Родственные наноструктуре полипептиды были сконструированы благодаря их способности к самосборке в пары с образованием наноструктур, таких как икосаэдрические наноструктуры.
В некоторых вариантах осуществления, наноструктура включает (а) множество первых сборок, каждая первая сборка содержит множество идентичных первых родственных наноструктуре полипептидов, где первые родственные наноструктуре полипептиды содержат аминокислотную последовательность родственного наноструктуре полипептида, выбранного из группы, состоящей из SEQ ID NO: 59-92; и (b) множество вторых сборок, каждая вторая сборка содержит множество идентичных вторых родственных наноструктуре полипептидов, где вторые родственные наноструктуре полипептиды содержат аминокислотную последовательность родственного наноструктуре полипептида, выбранного из группы, состоящей из SEQ ID NOS: 59-92, и где второй родственный наноструктуре полипептид отличается от первого родственного наноструктуре полипептида; где множество первых сборок нековалентно взаимодействует с множеством вторых сборок с образованием наноструктуры;
Наноструктуры включают симметрично повторяющиеся, неприродные, нековалентные поверхности раздела полипептид-полипептид, которые ориентируют первую сборку и вторую сборку в наноструктуру, такую как структура с икосаэдрической симметрией.
SEQ ID NO: 59-92 предоставляют аминокислотную последовательность иллюстративных родственных наноструктуре полипептидов. Количество остатков интерфейса для типовых родственных наноструктуре полипептидов, SEQ ID NO: 59-92 находится в диапазоне от 4 до 13 остатков. В различных вариантах осуществления, родственные наноструктуре полипептиды содержат аминокислотную последовательность, имеющую, по меньшей мере, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность по длине и идентичность, по меньшей мере, в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 идентифицированных положениях интерфейса (в зависимости от количество остатков интерфейса для данного родственного наноструктуре полипептида), к аминокислотной последовательности родственного наноструктуре полипептида, выбранного из группы, состоящей из SEQ ID NO: 59-92. В других вариантах осуществления, родственные наноструктуре полипептиды содержат аминокислотную последовательность, имеющую, по меньшей мере, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность по длине и идентичность, по меньшей мере, на 20%, 25%, 33%, 40%, 50%, 60%, 70%, 75%, 80%, 90% или 100% идентифицированных положений интерфейса к аминокислотной последовательности родственного наноструктуре полипептида, выбранного из группы, состоящей из SEQ ID NO: 59-92. В дополнительных вариантах осуществления, родственные наноструктуре полипептиды включают родственный наноструктуре полипептид, имеющий аминокислотную последовательность родственного наноструктуре полипептида, выбранного из группы, состоящей из SEQ ID NO: 59-98.
В одном неограничивающем варианте осуществления, полипептиды, относящиеся к наноструктуре, могут быть модифицированы для облегчения ковалентной связи с представляющим интерес «грузом». В одном неограничивающем примере, родственные наноструктуре полипептиды могут быть модифицированы, например, путем введения различных цистеиновых остатков в определенные положения для облегчения связывания с одним или несколькими представляющими интерес антигенами, так что наноструктура родственных наноструктуре полипептидов, будет обеспечивать каркас для предоставления большого количества антигенов для доставки в качестве вакцины для создания улучшенного иммунного ответа.
В некоторых вариантах осуществления, некоторые или все нативные остатки цистеина, которые присутствуют в полипептидах, связанных с наноструктурой, но не предназначены для использования для конъюгации, могут быть заменены другими аминокислотами для облегчения конъюгации в определенных положениях. В другом неограничивающем варианте осуществления, родственные наноструктуре полипептиды могут быть модифицированы путем связывания (ковалентного или нековалентного) с фрагментом для облегчения «эндосомального высвобождения». Для применений, которые включают доставку молекул, представляющих интерес, в клетку-мишень, таких как адресная доставка, критическим шагом может быть высвобождение из эндосомы - мембраносвязанной органеллы, которая является точкой входа средства доставки в клетку. Эндосомы созревают в лизосомы, которые разлагают свое содержимое. Таким образом, если средство доставки каким-то образом не «высвободится» из эндосомы до того, как станет лизосомой, оно будет деградировать и не будет выполнять свою функцию. Существует множество липидов или органических полимеров, которые разрушают эндосомы и позволяют проникнуть в цитозоль. Таким образом, в этом варианте осуществления, родственные наноструктуре полипептиды могут быть модифицированы, например, путем введения цистеиновых остатков, которые сделают возможной химическую конъюгацию такого липида или органического полимера с мономером или полученной поверхностью сборки. В другом неограничивающем примере, полипептиды, связанные с наноструктурой, могут быть модифицированы, например, путем введения цистеиновых остатков, которые сделают возможной химическую конъюгацию флуорофоров или других визуализирующих агентов, позволяющих визуализировать наноструктуры in vitro или in vivo.
Поверхностные аминокислотные остатки на полипептидах, связанных с наноструктурой, могут быть мутированы для улучшения стабильности или растворимости белковых субъединиц или собранных наноструктур. Как должно быть известно специалистам в данной области техники, если родственный наноструктуре полипептид имеет значительную гомологию последовательности с существующим семейством белков, можно использовать множественное выравнивание последовательностей других белков из этого семейства для выбора аминокислотных мутаций в неконсервативных положения, которые могут повышать стабильность и/или растворимость белка, процесс, называемый консенсусным дизайном белка (9).
Поверхностные аминокислотные остатки на полипептидах, связанных с наноструктурой, могут быть мутированы в положительно заряженные (Arg, Lys) или отрицательно заряженные (Asp, Glu) аминокислоты, чтобы придать поверхности белка общий положительный или общий отрицательный заряд. В одном неограничивающем варианте осуществления, поверхностные аминокислотные остатки на полипептидах, связанных с наноструктурой, могут быть мутированы, чтобы придать внутренней поверхности самособирающейся наноструктуры высокий суммарный заряд. Затем такую наноструктуру можно использовать для упаковки или инкапсуляции молекулы груза с противоположным суммарным зарядом из-за электростатического взаимодействия между внутренней поверхностью наноструктуры и молекулой груза. В одном неограничивающем варианте осуществления, поверхностные аминокислотные остатки на полипептидах, связанных с наноструктурой, могут быть мутированы, в первую очередь аргининовыми или лизиновыми остатками, чтобы придать внутренней поверхности самособирающейся наноструктуры суммарный положительный заряд. Затем растворы, содержащие родственные наноструктуре полипептиды, можно смешивать в присутствии молекулы-носителя нуклеиновой кислоты, такой как дцДНК, оцДНК, дцРНК, оцРНК, кДНК, миРНК, киРНК, кшРНК, пиРНК или другая нуклеиновая кислота, чтобы инкапсулировать нуклеиновую кислоту внутри самособирающейся наноструктуры. Такую наноструктуру можно использовать, например, для защиты, доставки или концентрирования нуклеиновых кислот.
В одном варианте осуществления, наноструктура имеет икосаэдрическую симметрию. В этом варианте осуществления, наноструктура может содержать 60 копий первого родственного наноструктуре полипептида и 60 копий второго родственного наноструктуре полипептида. В одном из таких вариантов осуществления, количество идентичных первых родственных наноструктуре полипептидов в каждой первой сборке отличается от количества идентичных вторых родственных наноструктуре полипептидов в каждой второй сборке. Например, в одном варианте осуществления, наноструктура содержит двенадцать первых сборок и двадцать вторых сборок; в этом варианте осуществления, каждая первая сборка может; например, содержат пять копий идентичного первого родственного наноструктуре полипептида, и каждая вторая сборка может, например, содержать три копии идентичного второго родственного наноструктуре полипептида. В другом варианте осуществления, наноструктура содержит двенадцать первых сборок и тридцать вторых сборок; в этом варианте осуществления, каждая первая сборка может, например, содержать пять копий идентичного первого родственного наноструктуре полипептида, и каждая вторая сборка может, например, содержать две копии идентичного второго родственного наноструктуре полипептида. В другом варианте осуществления, наноструктура содержит двадцать первых сборок и тридцать вторых сборок; в этом варианте осуществления, каждая первая сборка может, например, содержать три копии идентичного первого родственного наноструктуре полипептида, и каждая вторая сборка может, например, содержать две копии идентичного второго родственного наноструктуре полипептида. Все эти варианты осуществления способны формировать синтетические наноматериалы с правильной икосаэдрической симметрией.
VIII. КОМБИНАЦИЯ С САХАРИДОМ И/ИЛИ ПОЛИПЕПТИДОМ ИЛИ ЕГО ФРАГМЕНТОМ, ПОЛУЧЕННЫМ ИЗ KLEBSIELLA PNEUMONIAE
Klebsiella pneumoniae представляет собой грамотрицательный патоген, вызывающий инфекции мочевыводящих путей, бактериемию и сепсис. В одном аспекте, любая из композиций, описанных в настоящем документе, может дополнительно включать, по меньшей мере, один сахарид, который является или получен из, по меньшей мере, одного серотипа K. pneumoniae, выбранного из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac, O3, O4, O5, O7, O8 и O12. В предпочтительном варианте осуществления, любая из описанных в настоящем документе композиций может дополнительно включать полипептид, полученный из K. pneumoniae, выбранный из полипептида, полученного из фимбриального белка типа I K. pneumoniae, или его иммуногенного фрагмента; и полипептид, полученный из фимбриального белка типа III K. pneumoniae или его иммуногенного фрагмента.
Как известно в данной области техники, антигены O1 и O2 K. pneumoniae содержат гомополимерные галактозные звенья (или галактаны). Каждый из антигенов O1 и O2 K. pneumoniae содержит единицы D-галактана I (иногда называемые повторяющейся единицей O2a), но антигены O1 отличаются тем, что антигены O1 имеют структуру кэпа D-галактана II. D-галактан III (d-Gal-III) представляет собой вариант D-галактана I. В некоторых вариантах осуществления, сахарид, полученный из K. pneumoniae O1, включает повторяющуюся единицу [→3)-β-D-Galf-(1→3)-α-D-Galp-(1→]. В некоторых вариантах осуществления, сахарид, полученный из K. pneumoniae O1, включает повторяющуюся единицу [→3)-α-D-Galp-(1→3)-β-D-Galp-(1→]. В некоторых вариантах осуществления, сахарид, полученный из K. pneumoniae O1, включает повторяющуюся единицу [→3)-β-D-Galf-(1→3)-α-D-Galp-(1→] и повторяющуюся единицу [→3)-α-D- Galp-(1→3)-β-D-Galp-(1→]. В некоторых вариантах осуществления, сахарид, полученный из K. pneumoniae O1, включает повторяющуюся единицу →3)-β-D-Galf -(1→3)-[α-D-Galp-(1→4)]-α-D-Galp-(1→] (упоминающуюся как повторяющаяся единица D-Gal-III).
В некоторых вариантах осуществления сахарид, полученный из K. pneumoniae O2, включает повторяющуюся единицу [→3)-α-ᴅ-Galp-(1→3)-β-ᴅ-Galf-(1→] (которая может быть элементом антигена O2a серотипа K. pneumoniae). В некоторых вариантах осуществления, сахарид, полученный из K. pneumoniae O2, включает повторяющуюся единицу [→3)-β-ᴅ-GlcpNAc-(1→5)-β-ᴅ-Galf-(1→] (которая может быть элементом антигена O2c серотипа K. pneumoniae). В некоторых вариантах осуществления, сахарид, полученный из O2 K. pneumoniae, включает модификацию повторяющейся единицы O2a путем добавления боковой цепи (1→4)-связанных остатков Galp (которые могут быть элементом антигена O2afg K. pneumoniae). В некоторых вариантах осуществления, сахарид, полученный из O2 K. pneumoniae, включает модификацию повторяющейся единицы O2a путем добавления боковой цепи (1→2)-связанных остатков Galp (которые могут быть элементом антигена O2aeh K. pneumoniae).
Без привязки к механизму или теории, структура полисахарида О-антигена серотипов O3 и O5 K. pneumoniae описана в данной области техники как идентичная таковой у серотипов E. coli O9a (формула O9a) и O8 (формула O8), соответственно.
В некоторых вариантах осуществления сахарид, полученный из K. pneumoniae O4, включает повторяющуюся единицу [→4)-α-D-Galp-(1→2)-β-D-Ribf-(1→)]. В некоторых вариантах осуществления, сахарид, полученный из K. pneumoniae O7, включает повторяющуюся единицу [→2-a-L-Rhap-(1→2)-β-D-Ribf-(1→3)-α-L-Rhap-(1→3)-α-L-Rhap-(1→]. В некоторых вариантах осуществления, сахарид, полученный из серотипа K. pneumoniae O8, включает ту же структуру повторяющихся единиц, что и K. pneumoniae O2a, но нестехиометрически O-ацетилированную. В некоторых вариантах осуществления, сахарид, полученный из K. pneumoniae серотипа O12, включает повторяющуюся единицу [α-Rhap-(1→3)-β-GlcpNAc] дисахаридной повторяющейся единицы.
В одном аспекте, изобретение включает композицию, включающую полипептид, полученный из E. coli FimH, или его фрагмент; и, по меньшей мере, один сахарид, который является или получен из, по меньшей мере, одного серотипа K. pneumoniae, выбранного из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac, O3, O4, O5, О7, О8 и О12. В некоторых вариантах осуществления, композиция включает сахариды одного или нескольких серотипов O1, O2, O3 и O5 или их комбинации или полученные из них. В некоторых вариантах осуществления, композиция включает сахариды каждого из серотипов O1, O2, O3 и O5 или производные от них.
В другом аспекте, изобретение включает композицию, включающую, по меньшей мере, один сахарид, который является или получен из, по меньшей мере, одного серотипа K. pneumoniae, выбранного из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac, O3, O4, O5, O7, O8 и O12; и сахарид, имеющий структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 1 до 100. В некоторых вариантах осуществления, композиция включает сахарид из или полученный из одного или нескольких серотипов O1, O2, O3 и O5 K. pneumoniae или их комбинации. В некоторых вариантах осуществления, композиция включает сахарид из или полученный из каждого из серотипов O1, O2, O3 и O5 K. pneumoniae. В некоторых вариантах осуществления, композиция включает сахарид формулы O9 и не включает сахарид, полученный из серотипа O3 K. pneumoniae. В некоторых вариантах осуществления, композиция включает сахарид формулы O8 и не включает сахарид, полученный из серотипа O5 K. pneumoniae.
В другом аспекте, изобретение относится к композиции, включающей композицию, включающую полипептид, полученный из E. coli FimH, или его фрагмент; по меньшей мере, один сахарид, который является или получен из, по меньшей мере, одного серотипа K. pneumoniae, выбранного из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac, O3, O4, O5, О7, О8 и О12; и сахарид, имеющий структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 1 до 100. В некоторых вариантах осуществления, композиция включает сахарид, имеющий формулу O9, и не включает сахарид, полученный из серотипа O3 K. pneumoniae. В некоторых вариантах осуществления, композиция включает сахарид формулы O8 и не включает сахарид, полученный из серотипа O5 K. pneumoniae.
В некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, полученный из любого типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5. В некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, полученный из типа O1 K. pneumoniae. В некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, полученный из типа O2 K. pneumoniae.
В некоторых вариантах осуществления, композиция включает комбинацию сахаридов, полученных из K. pneumoniae, где первый сахарид получают из любого одного из типов K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5; и второй сахарид получают из сахарида, полученного из любого одного из типов K. pneumoniae, выбранного из группы, состоящей из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac, O3, О4, О5, О7, О8 и О12. Например, в некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, полученный из типа O1 K. pneumoniae, и, по меньшей мере, один сахарид, полученный из типа O2 K. pneumoniae. В предпочтительном варианте осуществления, сахарид, полученный из K. pneumoniae, конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгирован с белком-носителем.
В другом аспекте, изобретение включает композицию, включающую полипептид, полученный из E.coli FimH, или его фрагмент; и, по меньшей мере, один сахарид, полученный из любого типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5.
В другом аспекте, изобретение включает по меньшей мере, один сахарид, полученный из любого типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5; и, по меньшей мере, один сахарид, полученный из E. coli, имеющий структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187. В некоторых вариантах осуществления, композиция включает сахарид формулы O9 и не включает сахарид, полученный из серотипа O3 K. pneumoniae. В некоторых вариантах осуществления, композиция включает сахарид формулы O8 и не включает сахарид, полученный из серотипа O5 K. pneumoniae.
В некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, полученный из типа O1 K. pneumoniae; и, по меньшей мере, один сахарид, полученный из E.coli, имеющий структуру, выбранную из группы, состоящей из Формулы O8 и Формулы O9. В другом варианте осуществления, композиция включает, по меньшей мере, один сахарид, полученный из типа О2 К. pneumoniae; и, по меньшей мере, один сахарид, полученный из E.coli, имеющий структуру, выбранную из группы, состоящей из Формулы O8 и Формулы O9. В другом варианте осуществления, композиция включает, по меньшей мере, один сахарид, полученный из типа О1 К. pneumoniae; по меньшей мере, один сахарид, полученный из типа О2 К. pneumoniae; и, по меньшей мере, один сахарид, полученный из E.coli, имеющий структуру, выбранную из группы, состоящей из Формулы O8 и Формулы O9.
В некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, который является или получен из, по меньшей мере, одного серотипа K. pneumoniae, выбранного из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac, О3, О4, О5, О7, О8 и О12; по меньшей мере, один сахарид, полученный из E.coli, имеющий структуру, выбранную из группы, состоящей из Формулы O8 и Формулы O9. В некоторых вариантах осуществления, композиция включает, по меньшей мере, один сахарид, который является или получен из, по меньшей мере, одного серотипа K. pneumoniae, выбранного из O1 (и вариантов d-Gal-III), O2 (и вариантов d-Gal-III), O2ac., О3, О4, О5, О7, О8 и О12; по меньшей мере, один сахарид, полученный из E.coli, имеющий структуру, выбранную из группы, состоящей из формулы O1A, формулы O1B, формулы O2, формулы O6 и формулы O25B.
В некоторых вариантах осуществления композиция дополнительно включает полипептид, полученный из K. pneumoniae, выбранный из полипептида, полученного из фимбриального белка типа I K. pneumoniae, или его иммуногенного фрагмента; и полипептид, полученный из фимбриального белка типа III K. pneumoniae или его иммуногенного фрагмента. Последовательности таких полипептидов известны в данной области техники.
ПРИМЕРЫ
Для лучшего понимания настоящего изобретения приведены следующие примеры. Эти примеры предназначены только для целей иллюстрации и не должны рассматриваться как ограничивающие каким-либо образом объем изобретения. Следующие примеры иллюстрируют некоторые варианты осуществления изобретения.
ПРИМЕР 1: Сущность конструкций
pCAG вектор
pCAG вектор
Наблюдаемая не пониженная масса, с His-меткой: 18117.90
Масса без метки:
17022.08
Вектор с двойным промотором (CMV & EF1α)
Вектор с двойным промотором (CMV & EF1α)
Вектор с двойным промотором (CMV & EF1α)
Все исследованные конструкции FimH представляют собой мономерные белки ожидаемой молекулярной массы.
Ожидаемая молекулярная масса комплекса FimC-FimH составляет 53,1 кДа;
Ожидаемая молекулярная масса FimC составляет 24 кДа.
ПРИМЕР 2: Экспрессия связывающего домена лектина FimH у млекопитающих
Настоящий неограничивающий пример относится к получению полипептида, полученного из E.coli, или его фрагмента в клеточной линии НЕК. Выходы являются относительно высокими по сравнению с экспрессией полипептида, полученного из E.coli, или его фрагмента в клетке-хозяине E.coli.
Для продуцирования вариантов FimH из клеток млекопитающих используют алгоритм прогнозирования SignalP для анализа различных гетерологичных сигнальных последовательностей для секреции белков и фрагментов. Также анализируют лидерную последовательность FimH дикого типа. Прогнозы показывают, что лидерная последовательность FimH дикого типа может работать для секреции вариантов FimH в клетках млекопитающих, однако было предсказано, что секретируемый вариант расщепляется на остатке W20 полноразмерного FimH дикого типа (см. SEQ ID NO: 1), а не на остатке F22 полноразмерного FimH дикого типа (см. SEQ ID NO: 1). Было предсказано, что сигнальная последовательность гемагглютинина не работает. Было предсказано, что сигнальная последовательность IgK мыши продуцирует N-конец F22 SEQ ID NO: 1 или остаток F1 зрелого белка.
На основании этих анализов синтезируют ДНК и рекомбинантно получают конструкции для экспрессии лектин-связывающего домена FimH с FimH-лидером дикого типа. Также получают конструкции для экспрессии лектин-связывающего домена FimH с сигнальной последовательностью mIgK. Метки аффинной очистки, такие как His-метка, вводят на С-конце полипептида, полученного из E. coli, или его фрагмента для облегчения очистки.
Экспрессионную плазмиду трансфицируют в клетки-хозяева НЕК, а именно в клетки млекопитающих EXPI293.
Полипептиды или их фрагменты, полученные из E.coli, успешно экспрессируют. Например, предпочтительная N-концевая обработка с использованием сигнальной последовательности mIgK, слитой со зрелым началом FimH в F22, продемонстрируют для конструкции pSB01892 FimHdscG с помощью МС. Считается, что обработка корректирует конструкцию домена лектина pSB01878, и данные масс-спектра подтверждают это.
Предпочтительная N-концевая обработка (т.е. обработка в F22 SEQ ID NO: 1) не показана для нативного лидерного пептида FimH.
Конструкции pSB01877 и pSB01878 находятся в векторах экспрессии pcDNA3.1(+) млекопитающих. Клетки разводят и затем используют для трансфекции по 20 мл. Используют 1 мкг/мл ДНК для каждой конструкции и трансфицируют клетки в 125 мл колбах с использованием протокола Expifectamine. Через 72 часа, жизнеспособность клеток все еще остается хорошей, поэтому экспрессию продолжают до 96 часов. Образцы берут через 72 часа и анализируют по 10 мкл каждого на гелях SDS PAGE для проверки экспрессии.
Через 96 часов, кондиционированную среду собирают и добавляют 0,25 мл смолы Nickel Excel с периодическим связыванием O/N при 4℃ при вращении. Элюируют TrisCl pH 8,0, NaCl, имидазолом. См. ФИГ. 4.
Ожидаемая масса pSB01878 соответствует N-концевому F22. Гликозилирование присутствует на 1 или 2 сайтах (+1 масса от каждого дезамидирования N-D).
Конструируют мутанты гликозилирования. См., например, pSB02081, pSB02082, pSB02083, pSB02088 и pSB02089. Мутанты гликозилирования экспрессируют представляющие интерес полипептиды. Результаты см. на ФИГ. 5.
Также конструируют замкнутый мутант лектинового домена FimH. См., например, pSB02158. Результаты экспрессии конструкции pSB02158 показаны на ФИГ. 6В.
Анализ поляризации флуоресценции с использованием 0,5 пмолей аминофенил-маннопиранозида, конъюгированного с флуоресцеином (APMP). Анализ проводят при комнатной температуре, 300 об/мин в течение 64 ч. Результаты, показаны на ФИГ. 6С.
ПРИМЕР 3: Экспрессия комплекса FimH/C у млекопитающих, pSB01879 и pSB01880
Для получения комплекса FimH/C получают конструкции с двойной экспрессией FimC под промотором EF1alpha и FimH с сигнальным пептидом либо дикого типа, либо mIgK. Их клонируют в вектор экспрессии млекопитающих pBudCE4.1 (ThermoFisher) и к FimC добавляли His-метку C-конца. Вариант FimC разрабатывают для секреции с использованием сигнального пептида mIgK, поскольку это приводит к положительному прогнозу образования FimC G37 в качестве первого остатка зрелого белка на основе анализа SignalP.
Более конкретно, эти конструкции конструируют таким образом, чтобы фрагмент FimC находился под промотором EF1alpha в векторе pBudCE4.1, и фрагмент FimH был вставлен под промотором CMV в том же векторе. Вектор pBudCE4.1 представляет собой вектор экспрессии от Thermo Fisher, который имеет 2 промотора для экспрессии в клетках млекопитающих. Вставку фрагмента FimC (вставку pSB01881) субклонируют путем расщепления NotI и XhoI и субклонирования в вектор pBudCE4.1 в тех же сайтах. Их высевают на чашки с 2xYT зеоцином в количестве 50 мкг/мл. Колонии инокулируют в 2xYT с 50 мкг/мл зеоцина, выращивают в течение ночи при 37℃ и готовят плазмиду. Их расщепляют NotI и XhoI для проверки наличия вставки, и все колонии имеют размер вставки ~722 п.н.
pSB01881 расщепляют HindIII и BamHI, и ДНК вставки pSB01879 и вставки pSB01880 расщепляют HindIII и BamHI. Эти фрагменты выделяют из геля и субклонируют в вектор pSB01881 и высевают на планшеты 2xYT zeo 50 мкг/мл. Колонии от каждого инокулируют в 2xYT zeo 50 мкг/мл, выращивают в течение ночи при 37℃, готовят плазмиду и расщепляют с помощью NotI и XhoI для тестирования вставки FimC и HindIII и BamHI для тестирования вставки FimH. Все клоны имеют вставки ожидаемого размера в обоих сайтах клонирования. Клоны pSB01879-1 и pSB01880-1 впоследствии используют для экспрессии.
Было показано, что комплекс FimH/FimC также экспрессируется в клетках EXPI293. Экспрессию можно оптимизировать, переключая промоторы, такие как EF1α, CAG, Ub, Tub или другие промоторы.
Предпочтительная N-концевая обработка (т.е. обработка на F22 SEQ ID NO: 1) не показана для нативного лидерного пептида FimH.
Типовые результаты SignalP 4.1 (DTU Bioinformatics), используемые для прогнозирования сигнальных пептидов, показаны ниже. Предполагается, что дополнительные сигнальные пептиды будут продуцировать предпочтительный N-конец Phe в положении 1 зрелого полипептида FimH или его фрагмента. Ниже приведен только типовой набор из 4 общих сигнальных последовательностей.
Прогнозируют, что следующие последовательности сигнальных пептидов дают предпочтительный N-конец Phe в положении 1 зрелого полипептида FimH или его фрагмента:
Не было спрогнозировано, что следующие последовательности сигнальных пептидов будут давать предпочтительный N-конец Phe в положении 1 зрелого полипептида FimH или его фрагмента:
MGVPRPQPWALGLLLFLLPGSLGAESHLSLLYHLTAVSSPAPGTPAFWVSGWLGPQQYLSYNSLRGEAEPCGAWVWENQVSWYWEKETTDLRIKEKLFLEAFKALGGKGPYTLQGLLGCELGPDNTSVPTAKFALNGEEFMNFDLKQGTWGGDWPEALAISQRWQQQDKAANKELTFLLFSCPHRLREHLERGRGNLEWKEPPSMRLKARPSSPGFSVLTCSAFSFYPPELQLRFLRNGLAAGTGQGDFGPNSDGSFHASSSLTVKSGDEHHYCCIVQHAGLAQPLRVELESPAKSSVLVVGIVIGVLLLTAAAVGGALLWRRMRSGLPAPWISLRGDDTGVLLPTPGEAQDADLKDVNV IPATA (SEQ ID NO: 102)
MGVPRPQPWALGLLLFLLPGSLGfacktangtaipigggsanvyvnlapvvnvgqnlvvdls (SEQ ID NO: 103)
MELLILKANAITTILTAVTFCFASGQNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPPTNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVSKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTSKVLDLKNYIDKQLLPIVNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMSIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEINLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGMDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRKSDELLHNVNAGKSTTNIMITTIIIVIIVILLSLIAVGLLLYCKARSTPVTLSKDQLSGINNIAFSN (SEQ ID NO: 104)
MELLILKANAITTILTAVTFCFASGfacktangtaipigggsanvyvnlapvvnvgqnlvvdls (SEQ ID NO: 105)
Max. С 28 0,188
Max. Y 28 0,263
Max. S 11 0,478
среднее S 1-27 0,387
D 1-27 0,312 0,500 НЕТ
Название=Последовательность SP='НЕТ' D=0,312 D-отсечка=0,500 Сети=SignalP-TM
MHSSALLCCLVLLTGVRASPGQGTQSENSCTHFPGNLPNMLRDLRDAFSRVKTFFQMKDQLDNLLLKESLLEDFKGYLGCQALSEMIQFYLEEVMPQAENQDPDIKAHVNSLGENLKTLRLRLRRCHRFLPCENKSKAVEQVKNAFNKLQEKGIYKAMSEFDIFINYIEAYMTMKIRN (SEQ ID NO: 106)
MHSSALLCCLVLLTGVRAfacktangtaipigggsanvyvnlapvvnvgqnlvvdls (SEQ ID NO: 107)
Max. С 19 0,726
Max. Y 19 0,829
Max. S 4 0,973
среднее S 1-18 0,947
D 1-18 0,893 0,450 ДА
Наименование=Последовательность SP='ДА' Сайт расщепления между положениями 18 и 19: VRA-FA D=0,893 D-отсечка=0,450 Сети=SignalP-безТМ
MAIIYLILLFTAVRGDQICIGYHANNSTEKVDTNLERNVTVTHAKDILEKTHNGKLCKLNGIPPLELGDCSIAGWLLGNPECDRLLSVPEWSYIMEKENPRDGLCYPGSFNDYEELKHLLSSVKHFEKVKILPKDRWTQHTTTGGSRACAVSGNPSFFRNMVWLTKEGSDYPVAKGSYNNTSGEQMLIIWGVHHPIDETEQRTLYQNVGTYVSVGTSTLNKRSTPEIATRPKVNGQGGRMEFSWTLLDMWDTINFESTGNLIAPEYGFKISKRGSSGIMKTEGTLENCETKCQTPLGAINTTLPFHNVHPLTIGECPKYVKSEKLVLATGLRNVPQIESRGLFGAIAGFIEGGWQGMVDGWYGYHHSNDQGSGYAADKESTQKAFDGITNKVNSVIEKMNTQFEAVGKEFGNLERRLENLNKRMEDGFLDVWTYNAELLVLMENERTLDFHDSNVKNLYDKVRMQLRDNVKELGNGCFEFYHKCDDECMNSVKNGTYDYPKYEEESKLNRNEIKGVKLSSMGVYQILAIYATVAGSLSLAIMMAGISFWMCSNGSLQCRICI (SEQ ID NO: 108)
MAIIYLILLFTAVRGfacktangtaipigggsanvyvnlapvvnvgqnlvvdls (SEQ ID NO: 109)
Max. С 18 0,524
Max. Y 18 0,690
Max. S 1 0,951
среднее S 1-17 0,895
D 1-17 0,800 0,450 ДА
Наименование=Последовательность SP='ДА' Сайт расщепления между положениями 17 и 18: GFA-CK D=0,800 D-отсечка=0,450 Сети=SignalP-безТМ
ПРИМЕР 4: Экспрессия слияния комплемента донорной цепи FimH с пептидом FimG у млекопитающих.
Тестируют несколько длин линкера. Получают рекомбинантную экспрессию с этими линкерами, слитыми FimH с N-концевым пептидом FimG как в FimH дикого типа, так и в сигнальном пептиде mIgK, слитом с F22 FimH.
Также показано, что конструкции FimG комплемента донорной цепи FimH обладают устойчивой экспрессией в клетках EXPI293.
Предпочтительная N-концевая обработка (т.е. обработка на F22 SEQ ID NO: 1) не показана для нативного лидерного пептида FimH.
Для комплементарных конструкций донорной цепи конструируют олигонуклеотиды для получения базовых конструкций в pcDNA3.1(+), которые содержат различные линкеры и пептид FimG. Уникальный сайт BstEII вставляют на остатках G294 V295 T296 в соответствии с нумерацией SEQ ID NO: 1 FimH. Тот же самый сайт BstEII вставляют в линкеры для получения базовых конструкций.
Конструируют базовые конструкции для pSB01882-01895. Праймеры используют для ПЦР-амплификации pcDNA3.1(+) с ДНК полимеразой ACCUPRIME PFX (Thermo Fisher), расщепления продуктов ПЦР с помощью NdeI (в промоторе CMV) и BamHI и клонирования в pcDNA3.1(+), который расщепляют с помощью NdeI и BamHI и гель выделяют для удаления фрагмента.
Другую временную трансфекцию проводят с pSB01877, 01878, 01879, 01880, 01885 и 01892 вместе с клетками EXPI293 в качестве контроля.
Конструкции pSB01882 - pSB01895 используют при тестировании экспрессии временной трансфекции в клетках EXPI293 от Thermo Fisher в соответствии с протоколом производителя. См. ФИГ. 3, которая показывает результаты после экспрессии в 20 мл клеток EXPI293, 72 часа, с 10 мкл загруженной кондиционированной среды; наблюдается высокий уровень экспрессии; комплекс FimH/FimC присутствует после экспрессии из конструкций pSB01879 и pSB01880; 20 мл партии кондиционированных сред, связанных с Nickel Excel, промывка 40 CV, элюирование имдидазолом.
Получают дополнительные конструкции комплемента FimH-донорной цепи. См., например, конструкции pSB02198, pSB02199, pSB02200, pSB02304, pSB02305, pSB02306, pSB02307, pSB02308. Экспрессия конструкции замкнутого мутанта pSB2198 FimH dscG показана на ФИГ. 7. Замкнутый мутант pSB2198 FimH dscG дает 12 мг/л в результате временной экспрессии.
В соответствии с Vi-CELL XR 2.04 (Beckman Coulter, Inc.) наблюдается следующее (фактический тип клеток, используемых для экспрессии, представляет собой клетки HEK):
ПРИМЕР 5: Фрагменты молекулярной массы с обработанным сигнальным пептидом
pSB02083
pSB02198
1,45 мг/мл
5 мл
20190918 SS
pSB02307
0,48 мг/мл
5 мл
20190918 SS
ПРИМЕР 6: N-концевая α-аминогруппа Phe1 (в соответствии с нумерацией SEQ ID NO: 2) в зрелом белке FimH обеспечивает критическое полярное распознавание D-маннозы.
Не привязываясь к какой-либо теорией или механизму, предполагается, что правильное расщепление сигнального пептида непосредственно перед Phe1 (согласно нумерации SEQ ID NO: 2) зрелого белка FimH важно для экспрессии функционального белка FimH. Изменения в N-концевой α-аминогруппе, такие как добавление аминокислоты на N-конце перед Phe1 белка FimH, могут отменить взаимодействия водородных связей с атомами O2, O5 и O6 D-маннозы и ввести стерическое отталкивание с D-маннозой, тем самым блокируя связывание маннозы. Это подтверждается нашим экспериментальным наблюдением, что добавление дополнительного остатка Gly перед Phe1 в SEQ ID NO: 2 не приводит к обнаружению связывания маннозы.
После анализа кристаллической структуры FimH, связанного с D-маннозой, наблюдается следующее: N-концевая α-аминогруппа Phe1 вместе с боковыми цепями Asp54 FimH в соответствии с нумерацией SEQ ID NO: 2 и Gln133 FimH в соответствии с нумерацией SEQ ID NO: 2 обеспечивают критические полярные мотивы распознавания для D-маннозы, и мутации и изменения этих полярных взаимодействий приводят к отсутствию связывания маннозы.
ПРИМЕР 7: Боковая цепь Phe1 в FimH не взаимодействует напрямую с D-маннозой, а скорее спрятана внутри FimH, что позволяет предположить, что Phe1 может быть заменен другими остатками, например алифатическими гидрофобными остатками (Ile, Leu или Val)
Анализ кристаллических структур FimH в комплексе с D-маннозой и ее аналогами (например, PDB ID: 1QUN) показывает, что боковая цепь Phe1 (согласно нумерации SEQ ID NO: 2) взаимодействует не напрямую с D-маннозой, а скорее стабилизирует карман связывания путем укладки его ароматических колец с боковыми цепями Val56, Tyr95, Gln133 и Phe144 (в соответствии с нумерацией SEQ ID NO: 2).
Альтернативный N-концевой остаток вместо Phe может стабилизировать белок FimH, обеспечивать связывание маннозы и обеспечивать правильное расщепление сигнального пептида. Такие остатки могут быть идентифицированы подходящим способом, известным в данной области техники, например, путем визуального осмотра кристаллической структуры FimH или более количественного отбора с использованием программного обеспечения для компьютерного дизайна белков, такого как BioLuminate™ [BioLuminate, Schrodinger LLC, New York, 2017], Discovery Studio™ [Discovery Studio Modeling Environment, Dassault Systèmes, San Diego, 2017], MOE™ [Molecular Operating Environment, Chemical Computing Group Inc., Montreal, 2017] и Rosetta™ [Rosetta, University of Washington, Seattle, 2017]. Иллюстративный пример показан на ФИГ. 9А-9С. Замещающие аминокислоты могут быть алифатическими гидрофобными аминокислотами (например, Ile, Leu и Val). На ФИГ. 11 показано компьютерное сканирование мутагенеза Phe1 с другими аминокислотами, имеющими алифатические гидрофобные боковые цепи, например, Ile, Leu и Val, которые могут стабилизировать белок FimH и обеспечить связывание маннозы.
ПРИМЕР 8: Мутации Asn7 в соответствии с нумерацией SEQ ID NO: 2 в белке FimH могут удалять предполагаемый сайт N-гликозилирования и предотвращать дезамидирование, не влияя на связывание маннозы, mAb21 или mAb475
Сверхэкспрессия секретируемого E. coli FimH из клеточных линий млекопитающих, может приводить к N-связанному гликозилированию по остатку Asn7 в соответствии с нумерацией SEQ ID NO: 2. Кроме того, остаток Asn7 подвергается воздействию растворителя, и за ним следует остаток Gly, делая его очень склонным к дезамидированию.
Анализ кристаллических структур FimH в комплексе с D-маннозой и ее аналогами (например, PDB ID: 1QUN) показывает, что Asn7 находится более чем в 20 Å от сайта связывания маннозы, и мутация в этом сайте не должна влиять на связывание маннозы. Таким образом, мутации Asn7 в другие аминокислоты (например, Ser, Asp и Gln) могут эффективно удалять предполагаемый сайт N-гликозилирования и предотвращать дезамидирование.
ПРИМЕР 9: Штаммы E.coli и S.enterica
Клинические штаммы и производные перечислены в Таблице 10. Дополнительные эталонные штаммы включают: O25K5H1, и клинический штамм серотипа O25a; и штамм LT2 серовара Typhimurium S. enterica.
Конструируют нокауты генов в штаммах E. coli, удаляющие таргетируемую открытую рамку считывания, но оставляющие короткую рубцовую последовательность.
Гидролизованная цепь O-антигена и основные сахара обозначены далее как O-полисахарид (OPS) для простоты.
штамм LT2
ПРИМЕР 10: Олигонуклеотидные праймеры для клонирования кластера генов wzzB, fepE и О-антигена
Salmonella enterica, серовар Typhimurium, штамм LT2
Сборка штамма ST131 O25b EC958 и данные WGS O25b GAR2401
(UDP-глюкоза-6-дегидрогеназа)
(Фосфорибозил-AMP циклогидролаза/фосфорибозил-ATP пирофосфогидролаза)
ПРИМЕР 11: Плазмиды
Плазмидные векторы и субклоны перечислены в таблице 12. Фрагменты ПЦР, содержащие различные гены E. coli и Salmonella wzzB и fepE амплифицируют из очищенной геномной ДНК и субклонируют в высококопийную плазмиду, представленную в наборе для клонирования Invitrogen PCR®Blunt. Фиг. 12А-12В. Эта плазмида основана на репликоне pUC. Праймеры P3 и P4 используют для амплификации генов wzzB E. coli с их нативным промотором, и они предназначены для связывания с областями в проксимальных и дистальных генах, кодирующих UDP-глюкоза-6-дегидрогеназу и фосфорибозиладениннуклеотидгидролазу, соответственно (аннотации в Genbank MG1655 NC_000913. 3). Фрагмент ПЦР, содержащий ген Salmonella fepE и промотор, амплифицируют с использованием ранее описанных праймеров. Аналогичные праймеры fepE E. coli разрабатывают на основе доступных последовательностей генома Genbank или данных о полном геноме, полученных внутри (в случае GAR2401 и O25K5H1). Низкокопийную плазмиду pBAD33 используют для экспрессии генов биосинтеза О-антигена под контролем промотора арабинозы. Плазмиду сначала модифицируют для облегчения клонирования (методом Гибсона) длинных ПЦР фрагментов, амплифицированных с использованием универсальных праймеров, гомологичных 5'-промотору и гену 3'-6-фосфоглюконатдегидрогеназы (gnd). Таблица 12. Субклон pBAD33, содержащий оперон биосинтеза O25b, показан на ФИГ. 12А-12В.
Матрица гДНК
ПРИМЕР 12: Очистка О-антигена
Ферментативный бульон обрабатывают уксусной кислотой до конечной концентрации 1-2% (конечный рН 4,1). Экстракцию OAg и делипидирование проводят путем нагревания обработанного кислотой бульона до 100°C в течение 2 часов. В конце кислотного гидролиза смесь охлаждают до температуры окружающей среды и добавляют 14% NH4OH до конечного значения pH 6,1. Нейтрализованный бульон центрифугируют и собирают центрифугат. К центрифугату добавляют CaCl2 в фосфате натрия, и полученную взвесь инкубируют в течение 30 минут при комнатной температуре. Твердые вещества удаляют центрифугированием, и фугат 12-кратно концентрируют с использованием мембраны 10 кДа с последующими двумя диафильтрациями против воды. Затем ретентат, содержащий OAg, очищают с помощью угольного фильтра. Угольный фильтрат разводят 1:1 (об./об.) 4,0М сульфатом аммония. Конечная концентрация сульфата аммония составляет 2М. Угольный фильтрат, обработанный сульфатом аммония, дополнительно очищают с использованием мембраны с 2М сульфатом аммония в качестве рабочего буфера. OAg собирают в потоке. Для длинного OAg, фильтрат HIC концентрируют, и затем заменяют буфер на воду (20 диаобъемов) с использованием мембраны 5 кДа. Для короткого (нативного) полисахарида OAg, MWCO дополнительно снижают для увеличения выхода.
ПРИМЕР 13: Конъюгация длинного О-антигена O25b с CRM197
Первый набор конъюгатов длинноцепочечного полисахарида O25b-CRM197 получают с использованием периодатного окисления с последующим конъюгированием с использованием химии восстановительного аминирования (RAC) (таблица 14). Конъюгированные варианты с тремя уровнями активации (низкий, средний и высокий) за счет варьирования уровней окисления. Конъюгаты получают реакцией лиофилизированных активированных полисахаридов с лиофилизированным CRM197, восстановленным в среде ДМСО, с использованием цианоборогидрида натрия в качестве восстанавливающего агента. Реакции конъюгации проводят при 23℃ в течение 24 часов с последующим кэпированием с применением боргидрида натрия в течение 3 ч. После стадии гашения конъюгации, конъюгаты очищают ультрафильтрацией/диафильтрацией с регенерированной целлюлозной мембраной 100K MWCO, используя 5 мМ сукцината/0,9% NaCl, pH 6,0. Окончательную фильтрацию конъюгатов проводят с использованием мембраны 0,22 мкм.
Если прямо не указано иное, конъюгаты, описанные в следующих примерах, включают коровую сахаридную группу.
1.1. Экспрессия длинного О-антигена, обеспечиваемая регуляторами длины цепи гетерологичной полимеразы
Первоначальная конструкция штамма E. coli сфокусирована на серотипе O25. Цель состоит в том, чтобы сверхэкспрессировать гетерологичные гены wzzB или fepE, чтобы увидеть, придают ли они большую длину цепи в нокаутных штаммах O25 wzzB. Сначала изоляты крови подвергают скринингу с помощью ПЦР для идентификации штаммов подтипов O25a и O25b. Далее штаммы подвергают скринингу на чувствительность к ампициллину. Идентифицируют единственный чувствительный к ампициллину изолят O25b, GAR2401, в который введена делеция wzzB. Точно так же, делецию wzzB проводят в штамме O25a, O25K5H1. Для генетической комплементарности этих мутаций, гены wzzB из GAR 2401 и O25K5H1 субклонируют в высококопийный клонирующий вектор PCR-Blunt II и вводят в оба штамма электропорацией. Аналогичным образом клонируют и переносят дополнительные гены wzzB из E. coli K-12 и S. enterica серовара Typhimurium LT2; аналогично, гены fepE из E. coli O25K5H1, GAR 2401, O25a ETEC NR-5, O157: H7: K- и S. enterica серовара Typhimurium LT2.
Бактерии выращивают в течение ночи в среде LB, и LPS экстрагируют фенолом, разделяют с помощью SDS PAGE (4-12% акриламида) и окрашивают. В каждую лунку геля загружают LPS, экстрагированный из одинакового количества бактериальных клеток (приблизительно 2 единицы OD600). Размер LPS оценивают по внутреннему нативному стандарту LPS E. coli и путем подсчета лестницы, различимой в подмножестве образцов, показывающих широкое распределение длин цепей (отличающихся одной повторяющейся единицей). На левой стороне ФИГ. 13A показаны профили LPS плазмидных трансформантов O25a O25K5HΔwzzB; и справа, аналогичные профили трансформантов O25b GAR 2401ΔwzzB. Иммуноблот репликата геля, зондированного O25-специфической сывороткой, показан на ФИГ. 13В.
Результаты этого эксперимента показывают, что введение гомологичного гена wzzB в хозяина E. coli O25aΔwzzB восстанавливает экспрессию короткого O25 LPS (10-20x), как это делает Salmonella LT2 wzzB. Введение гена O25b wzzB из GAR2401 не дает, что позволяет предположить, что фермент WzzB из этого штамма является дефектным. Сравнение аминокислотных последовательностей WzzB E. coli позволяет предположить, что за это могут быть ответственны замены A210E и P253S. Примечательно, что Salmonella LT2 fepE и E. coli fepE из O25a O25K5H1 придают способность экспрессировать очень длинные (VL) OAg LPS, при этом Salmonella LT2 fepE приводит к OAg, превышающему по размеру размер, придаваемый E. coli fepE.
Аналогичная картина экспрессии наблюдается с трансформантами GAR2401Δ wzzB: E. coli O25a или штамм K12 wzzB восстанавливают способность продуцировать короткие LPS. Salmonella LT2 fepE создает самый длинный LPS, E. coli fepE немного короче LPS, тогда как Salmonella LT2 wzzB дает длинный LPS среднего размера (L). Способность других генов fepE E. coli продуцировать очень длинные LPS оценивают в отдельном эксперименте с трансформантами E. coli O25aΔwzzB. Гены fepE из GAR2401, штамма O25a ETEC и штамма-продуцента токсина Shigella O157 также придают способность создавать очень длинный LPS, но не такой длинный, как LPS, создаваемый Salmonella LT2 fepE (ФИГ. 14).
Установив на штаммах серотипа O25a и O25b, что Salmonella LT2 fepE создает самый длинный LPS среди изученных регуляторов полимеразы, мы попытались определить, будет ли он также продуцировать очень длинный LPS у других серотипов E. coli. Изоляты бактериемии дикого типа серотипов O1, O2, O6, O15 и O75 трансформируют плазмидой Salmonella fepE и экстрагируют LPS. Результаты, показанные на ФИГ. 15, подтверждают, что Salmonella fepE может придавать способность очень долго вырабатывать LPS в других распространенных серотипах, связанных с инфекциями крови. Результаты также показывают, что экспрессия Salmonella fepE на основе плазмиды, по-видимому, подавляет контроль длины цепи, обычно осуществляемый эндогенным wzzB в этих штаммах.
1.2. Плазмидная экспрессия О-антигенов в обычном штамме хозяина E. coli.
С точки зрения развития биопроцессов, возможность продуцировать О-антигены разных серотипов в общем хозяине E. coli вместо нескольких штаммов значительно упростила бы производство индивидуальных антигенов. С этой целью кластеры генов О-антигена из разных серотипов амплифицируют с помощью ПЦР и клонируют в низкокопийную плазмиду (pBAD33) под контролем промотора, регулируемого арабинозой. Эта плазмида совместима (может сосуществовать) с плазмидой Salmonella LT2 fepE в E. coli, поскольку она содержит другой репликон (p15a) и другой селектируемый маркер (хлорамфеникол или канамицин). В первом эксперименте, субклон плазмиды оперона pBAD33 O25b котрансфицируют плазмидой Salmonella LT2 fepE в GAR 2401ΔwzzB, и трансформанты, выращенные в присутствии или в отсутствие 0,2% арабинозы. Результаты, показанные на ФИГ. 16A-16B, демонстрируют, что очень длинный LPS О-антигена продуцируется арабинозозависимым образом.
Аналогичным образом оценивают кластеры генов О-антигена, клонированные из других серотипов, и результаты, показаны на ФИГ. 17. Совместная экспрессия плазмид Salmonella LT2 fepE и pBAD33-OAg приводит к обнаруживаемому длинноцепочечному LPS, соответствующему серотипам O1, O2 (для двух из четырех клонов), O16, O21 и O75. По неизвестным причинам, плазмида pBAD33-O6 не дает обнаруживаемых LPS во всех четырех обработанных изолятах. Хотя уровень экспрессии был переменным, результаты показывают, что экспрессия длинноцепочечных О-антигенов возможна у обычного хозяина. Однако в некоторых случаях может потребоваться дополнительная оптимизация для улучшения экспрессии, например, путем модификации последовательностей плазмидного промотора.
Профили LPS из различных штаммов E.coli серотипа O25 с или без плазмиды Salmonella LT2 fepE показаны на ФИГ. 18. Изучают два штамма для ферментации, экстракции и очистки О-антигенов: GAR2831, для продуцирования нативного короткого O25b OAg; и GAR2401ΔwzzB/fepE для продуцирования длинного O25b OAg. Соответствующие короткие и длинные формы LPS, показанные на ФИГ. 18 геля SDS-PAGE, выделены красным цветом. Полисахариды экстрагируют непосредственно из ферментированных бактерий уксусной кислотой и очищают. Профили эксклюзионной хроматографии очищенных коротких и длинных или очень длинных полисахаридов O25b показаны на ФИГ. 19А-19В. Свойства двух партий короткого полисахарида (из GAR2831) сравнивают с одним препаратом очень длинного полисахарида (из штамма GAR2401ΔwzzB/fepE). Молекулярная масса длинного О-антигена в 3,3 раза больше, чем у короткого О-антигена, и количество повторяющихся единиц оценивают как ~65 (очень длинные) против ~20. См. Таблицу 13.
Очень длинный полисахарид O25b O-антигена конъюгируют с дифтерийным токсоидом CRM197 с использованием обычного процесса восстановительного аминирования. Получают три разные партии гликоконъюгата с разной степенью активации периодатом: средняя (5,5%), низкая (4,4%) и высокая (8,3%). Было показано, что полученные препараты и неконъюгированный полисахарид не содержат эндотоксин (таблица 14).
Каждую группа из четырех кроликов (самки New Zealand White) вакцинируют 10 мкг гликоконъюгата и 20 мкг адъюванта QS21, и берут образцы сыворотки (VAC-2017-PRL-EC-0723) в соответствии со схемой, показанной на ФИГ. 20А. Стоит отметить, что доза 10 мкг находится на нижней границе диапазона, обычно назначаемого кроликам при оценке бактериальных гликоконъюгатов (более типично, 20-50 мкг). Группу кроликов также вакцинируют в отдельном исследовании (VAC-2017-PRL-GB-0698) неконъюгированным полисахаридом с использованием той же дозы (10 мкг полисахарида+20 мкг адъюванта QS21) и идентичной схемы введения.
Реакции антител кроликов на три препарата гликоконъюгатов O25b оценивают в анализе LUMINEX, в котором карбоксигранулы покрывают метилированным сывороточным альбумином человека, предварительно связанным с неконъюгированным длинным полисахаридом O25b. Присутствие O25b-специфических IgG-антител в образцах сыворотки определяют с помощью вторичных анти-IgG-антител, меченных фикоэритрином (PE). Профили иммунного ответа, наблюдаемые в сыворотке, взятой на неделе 0 (до иммунизации), неделе 6 (после введения дозы 2, PD2), неделе 8 (после введения дозы 3, PD3) и неделе 12 (после введения дозы 4, PD4) у наиболее отвечающих кроликов (по одному из каждой группы из четырех) показаны на ФИГ. 21А-21С. Ни у одного из 12 кроликов не было обнаружено значительных титров IgG в сыворотке до иммунизации. В отличие от этого, ответы антигенспецифических антител O25b обнаружены в поствакцинальной сыворотке кроликов во всех трех группах, при этом ответы группы с низкой активацией гликоконъюгата имеют более высокую тенденцию, чем группы со средней или высокой активацией гликоконъюгата. Максимальные ответы наблюдаются в момент времени после введения дозы 3. Один кролик из группы с низкой активацией и один кролик из группы с высокой активацией не ответили на вакцинацию (пациенты, не ответившие на лечение).
Для оценки влияния конъюгации белка-носителя CRM197 на иммуногенность длинного полисахарида O25b OAg, присутствие антител в сыворотке кроликов, вакцинированных неконъюгированным полисахаридом, сравнивают с сывороткой кроликов, вакцинированных гликоконъюгатом CRM197 низкой активации, ФИГ. 22А-22F. Примечательно, что свободный полисахарид не является иммуногенным, практически не вызывая ответов IgG в иммунных и предиммунных сыворотках (ФИГ. 22А). Напротив, средние значения интенсивности флуоресценции (MFI) O25b OAg-специфических IgG, примерно в десять раз превышающие уровни в сыворотке до иммунизации, наблюдают в сыворотках PD4 от трех из четырех кроликов, вакцинированных O25b OAg-CRM197, в диапазоне разведения сывороток (от 1:100 до 1:6400). Эти результаты демонстрируют необходимость конъюгации белка-носителя для получения антител IgG к полисахариду O25b OAg при уровне дозы 10 мкг.
Бактерии, выращенные на TSA планшетах, суспендируют в PBS, доводят до OD600 2,0, и фиксируют в 4% параформальдегиде в PBS. После блокирования в 4% BSA/PBS в течение 1 ч, бактерии инкубируют с серийными разведениями предиммунной сыворотки и иммунной сыворотки PD3 в 2% BSA/PBS и определяют связанный IgG с помощью PE-меченого вторичного F(ab) антитела.
Специфичность антител O25b, индуцированных O25b OAg-CRM197, демонстрируют в экспериментах по проточной цитометрии с интактными бактериями. Связывание IgG с целыми клетками определяют с помощью PE-конъюгированного фрагмента F(ab')2 антикроличьего IgG козы в проточном цитометре Accuri.
Как показано на ФИГ. 23A-23C, предиммунные кроличьи антитела не связываются с изолятами серотипа O25b дикого типа GAR2831 и GAR2401 или со штаммом K-12 E. coli, тогда как соответствующие PD3 антитела окрашивают бактерии O25b зависимым от концентрации образом. Отрицательный контрольный штамм К-12, у которого отсутствует способность экспрессировать OAg, показывает очень слабое связывание PD3 антител, скорее всего, из-за присутствия на его поверхности открытых эпитопов внутренних коровых олигосахаридов. Введение плазмиды Salmonella fepE в изоляты O25b дикого типа приводит к значительному усилению окрашивания, что согласуется с более высокой плотностью иммуногенных эпитопов, обеспечиваемой более длинным полисахаридом OAg.
Вывод: Описанные результаты показывают, что Salmonella fepE не только является детерминантой очень длинных полисахаридов О-антигена у видов Salmonella, но также может придавать штаммам E. coli различных серотипов О-антигена способность производить очень длинные OAg. Это свойство можно использовать для получения вакцинных полисахаридов О-антигена с улучшенными свойствами для разработки биопроцессов, облегчая очистку и химическую конъюгацию с соответствующими белками-носителями, и потенциально повышая иммуногенность за счет образования комплексов с более высокой молекулярной массой.
ПРИМЕР 14: Первоначальные исследования на кроликах позволяют получить первые реагенты поликлональных антител и ответы IgG на RAC O25b OAg-CRM197
Конъюгаты длинноцепочечного полисахарида O25b-CRM197 получают с использованием периодатного окисления с последующим конъюгированием с использованием химии восстановительного аминирования (RAC) (таблица 14). См. также таблицу 24.
Средняя активация 5,5%
Низкая активация 4,5%
Высокая активация 8,3%
Свободный полисахарид O25b
В исследовании на кроликах 1 (VAC-2017-PRL-EC-0723) (также описанном выше в примере 13) - пять (5) кроликов/группу с 10 мкг L-, M- или H-активацией RAC (+QS21) получают композиции по схеме, показанной на ФИГ. 20А. Было обнаружено, что неконъюгированный свободный полисахарид O25b не является иммуногенным в последующем исследовании на кроликах (VAC-2017-PRL-GB-0698) (см. ФИГ. 25).
В исследовании на кроликах 2 (VAC-2018-PRL-EC-077) - 2 кролика/группу с L-RAC (AlOH3, QS21 или без адъюванта) получают композицию в соответствии со схемой, показанной на ФИГ. 20В.
Кролики 4-1, 4-2, 5-1, 5-2, 6-1 и 6-2 получают очень длинный неконъюгированный полисахарид O25b, описанный в примере 13, и тестируют сыворотку на 18 неделе.
Более конкретно, кролику 4-1 вводят композицию, включающую 50 мкг неконъюгированного O25b, 100 мкг адъюванта AlOH3. Кролику 4-2 вводят композицию, включающую 50 мкг неконъюгированного O25b, 100 мкг адъюванта AlOH3. Кролику 5-1 вводят композицию, включающую 50 мкг неконъюгированного O25b, 50 мкг адъюванта QS-21. Кролику 5-2 вводят композицию, включающую 50 мкг неконъюгированного O25b, 50 мкг адъюванта QS-21. Кролику 6-1 вводят композицию, включающую 50 мкг неконъюгированного O25b без адъюванта. Кролику 6-2 вводят композицию, включающую 50 мкг неконъюгированного O25b без адъюванта.
ПРИМЕР 15: Исследования на кроликах с конъюгатом O25b RAC: титры разведения сыворотки dLIA
Исследование 2 на кроликах (VAC-2018-PRL-EC-077) титры разведения сыворотки O25b dLIA по сравнению с кроликами с наилучшим ответом из исследования 1 (VAC-2017-PRL-EC-0723). Для этих экспериментов проводят модифицированный анализ прямого связывания Luminex, в котором полилизиновый конъюгат O25b длинного O-антигена пассивно адсорбируют на карбоксигранулах Luminex вместо смеси метилированного сывороточного альбумина длинного O-антигена, описанной ранее. Использование конъюгата полилизин-O25b улучшает чувствительность анализа и качество ответов, зависящих от концентрации IgG, что позволяет определить титры разведения сыворотки с помощью аппроксимации кривой (нелинейное уравнение с четырьмя параметрами). Титры IgG O25b в сыворотке кролика с самым высоким титром из первого исследования сравнивают с сывороткой кролика из второго исследования в таблице 15.
Более высокие дозы во втором исследовании на кроликах (50/20 мкг против 10 мкг) не улучшают титры IgG.
Двухмесячный отдых усиливает ответы IgG (не наблюдается при более коротких интервалах).
По-видимому, квасцы усиливают ответ IgG у кроликов по сравнению с QS21 или без адъюванта.
Опсонофагоцитарный анализ (OPA) с комплементом крольчат (BRC) и клетками HL60 в качестве источника нейтрофилов проводят для измерения функциональной иммуногенности гликоконъюгатов O-антигена. Предварительно замороженные бактериальные исходные E. coli GAR2831 выращивают в бульоне Луриа (LB) при 37°С. Клетки осаждают и суспендируют до концентрации 1 OD600 единиц на мл в PBS с добавлением 20% глицерина и замораживают. Предварительно титрованные размороженные бактерии разводят до 0,5х105 КОЕ/мл в HBSS (сбалансированный солевой раствор Хэнка) с 1% желатина) и 10 мкл (103 КОЕ) в сочетании с 20 мкл серийно разведенной сыворотки в микропланшете для тканевых культур с U-образным дном, и смесь встряхивают (700 об/мин на шейкере BELLCO) в течение 30 мин при 37℃ в инкубаторе с 5% CO2. 10 мкл 2,5% комплемента (сыворотка Baby Rabbit Serum, PEL-FREEZ 31061-3, предварительно разведенная в HBG) и 20 мкл клеток HL-60 (0,75х107/мл) и 40 мкл HBG добавляют к микропланшет с U-образным дном для культивирования ткани, и смесь встряхивают на шейкере BELLCO со скоростью 700 об/мин в течение 45 мин при 37°С в инкубаторе с 5% CO2. Затем 10 мкл каждых 100 мкл реакционной смеси переносят в соответствующие лунки предварительно смоченного фильтровального планшета MILLIPORE MULTISCREENHTS HV, приготовленного путем нанесения 100 мкл воды, фильтр вакуумируют и наносят 150 мкл 50% LB. Фильтровальный планшет фильтруют под вакуумом и инкубируют в течение ночи при 37°С в инкубаторе с 5% CO2. На следующий день колонии подсчитывают после фиксации, окрашивания и обесцвечивания красителем COOMASSIE и растворами Destain с использованием анализатора IMMUNOSPOT® и программного обеспечения IMMUNOCAPTURE. Чтобы установить специфичность активности OPA, иммунную сыворотку предварительно инкубируют со 100 мкг/мл очищенного длинного O-антигена O25b перед объединением с другими компонентами анализа в реакции OPA. Анализ OPA включает контрольные реакции без клеток HL60 или комплемента, чтобы продемонстрировать зависимость любого наблюдаемого уничтожения от этих компонентов.
Совпадающие образцы сыворотки до и после вакцинации от типовых кроликов из обоих исследований на кроликах оценивают в анализе и определяют титры разведения сыворотки (таблица 16, ФИГ. 26A-26B). Предварительная инкубация с неконъюгированным полисахаридом длинного O-антигена O25b блокирует бактерицидную активность, демонстрируя специфичность OPA (ФИГ. 19C). Таблица 16, титры ОРА.
Кролика 2-3 дозируют следующим образом: дозирование кролика 2-3: 10/10/10/10 мкг конъюгата RAC+QS21, после введения дозы (PD) 4 сбора крови. Кролику 1-2 вводят следующие дозы: 50/20/20/20 мкг конъюгата RAC+Al(OH)3, PD4 сбор крови.
ПРИМЕР 16. Уровни IgG О-антигена O25b, вызванные неконъюгированным полисахаридом длинного О-антигена O25b и полученным гликоконъюгатом длинного О-антигена O25b RAC/ДМСО
Группам из десяти мышей CD-1 путем подкожной инъекции вводят 0,2 или 2,0 мкг/животное гликоконъюгата длинного О-антигена O25b RAC/ДМСО на 0, 5 и 13 неделях с взятием крови на 3 неделе (после введения дозы 1, PD1), 6 неделе (после введения дозы 2, PD2) и 13 неделе (после введения дозы 3, PD3) для тестирования иммуногенности. Уровни антигенспецифического IgG определяют количественным анализом Luminex (подробности см. в примере 15) с O25b-специфическим mAb мыши в качестве внутреннего стандарта. Исходные уровни IgG (пунктирная линия) определяют в сыворотке крови 20 случайно выбранных невакцинированных мышей. Свободный неконъюгированный полисахаридный иммуноген длинного О-антигена O25b не индуцирует IgG выше исходного уровня ни в какой момент времени. В отличие от этого, ответы IgG наблюдаются после двух доз гликоконъюгата длинного конъюгата O25b-CRM197 RAC: сильные однородные ответы IgG наблюдаются при PD3 с промежуточными и более вариабельными уровнями IgG при PD2. Значения GMT IgG (нг/мл) указаны с погрешностями 95% ДИ. См. ФИГ. 27А-27С.
ПРИМЕР 17: Специфичность комплемента крольчат O25b (BRC) OPA
A-B) Постиммунная сыворотка O25b RAC/ДМСО с длинным О-антигеном от кроликов 2-3 и 1-2 (но не соответствующая предиммунной контрольной сыворотке) проявляет бактерицидную ОРА активность. C) Активность OPA иммунной сыворотки кролика 1-2 блокируют путем предварительной инкубации с 100 мкг/мл длинного полисахарида O-антигена O25b. Бактерии штамма GAR2831 инкубируют с HL60, 2,5% BRC и серийными разведениями сыворотки в течение 1 ч при 37℃, и выжившие бактерии подсчитывают путем подсчета микроколоний (КОЕ) на фильтровальных планшетах. См. ФИГ. 26А-26С.
ПРИМЕР 18: Длинные гликоконъюгаты RAC и eTEC O25b являются более иммуногенными, чем гликоконъюгаты с одним концом
Анализ BRC OPA с резистентным к карбапенему, резистентным к фторхинолону штаммом MDR Atlas187913. Группы из 20 мышей CD-1 вакцинируют 2 мкг гликоконъюгата в соответствии с той же схемой, которая показана на ФИГ. 28A-28B, и ответы OPA определяют в моменты времени после введения дозы 2 (PD2) (ФИГ. 28A) и после введения дозы 3 (PD3) (ФИГ. 28B). Столбцы обозначают GMT с 95% ДИ. Указаны показатели пациентов, ответивших на лечение, выше исходного уровня без вакцинации. Log преобразованные данные из разных групп оценивают, чтобы определить, были ли различия статистически значимыми, с использованием непарного t-критерия с поправкой Уэлча (Graphpad Prism). Результаты суммированы в таблице 17. См. ФИГ. 28А-28В. У мышей, вакцинированных 2 мкг длинных гликоконъюгатов eTEC O1a, титры ОРА против O1a, PD2 и PD3 (данные не показаны) превышают титры ОРА против O25b, PD2 и PD3, соответственно, как показано в таблице 17.
ПРИМЕР 19: Иммуногенность OPA в химии eTEC можно улучшить путем изменения уровней активации полисахарида
Анализ BRC OPA с резистентным к карбапенему, резистентным к фторхинолону штаммом MDR Atlas187913. Группы из 20 мышей CD-1 вакцинируют 0,2 мкг или 2 мкг указанного длинного гликоконъюгата O25b eTEC, и ответы OPA определяют в момент времени PD2. Совокупные log преобразованные данные для групп с 4% активацией по сравнению с 17% активацией оценивают для подтверждения того, что различия в ответах OPA были статистически значимыми, с использованием непарного t-критерия с поправкой Уэлча (Graphpad Prism). GMT и долю пациентов, ответивших на лечение, для отдельных групп приведены в таблице 18. См. ФИГ. 29.
ПРИМЕР 20: Исследование заражения показывает, что длинные конъюгаты E. coli O25b eTEC вызывают защиту после трех доз
Группы из 20 мышей CD-1, иммунизированных дозой 2 мкг в соответствии с указанным графиком, подвергают внутрибрюшинному заражению 1х109 бактериями штамма GAR2831. Последующую выживаемость отслеживают в течение шести дней. Группы мышей, вакцинированных гликоконъюгатами eTEC, активированными на уровне 4%, 10% или 17%, защищены от летальной инфекции, тогда как невакцинированные контрольные мыши или мыши, вакцинированные 2 мкг неконъюгированного длинного полисахарида O25b, не защищены. См. ФИГ. 30А-30В.
ПРИМЕР 21: Способ получения eTEC-связанных гликоконъюгатов
Активация сахарида и тиолирование дигидрохлоридом цистамина. Сахарид восстанавливают в безводном диметилсульфоксиде (ДМСО). Содержание влаги в растворе определяют с помощью анализа Карла Фишера (KF) и доводят до содержания влаги 0,1 и 1,0%, обычно 0,5%.
Для инициации активации готовят свежеприготовленный раствор 1,1'-карбонил-ди-1,2,4-триазола (CDT) или 1,1'-карбонилдиимидазола (CDI) в концентрации 100 мг/мл в ДМСО. Сахарид активируют различными количествами CDT/CDI (1-10 молярных эквивалентов) и дают возможность протекать реакции в течение 1-5 часов при комнатной температуре или 35℃. Добавляют воду, чтобы погасить любой остаточный CDI/CDT в растворе реакции активации. Расчеты выполняют для определения добавляемого количества воды и допущения конечного содержания влаги в пределах 2-3% от общего количества воды. Реакции дают протекать в течение 0,5 часа при комнатной температуре. Дигидрохлорид цистамина готовят на месте в безводном ДМСО в концентрации 50 мг/мл. Активированный сахарид подвергают реакции с 1-2 мол. экв. дигидрохлорида цистамина. Альтернативно активированный сахарид подвергают реакции с 1-2 мол. экв. гидрохлорида цистеамина. Реакция тиолирования протекает в течение 5-20 часов при комнатной температуре с получением тиолированного сахарида. Уровень тиолирования определяют добавленным количеством CDT/CDI.
Восстановление и очистка активированного тиолированного сахарида. К реакционной смеси тиолированного сахарида добавляют раствор трис(2-карбоксиэтил)фосфина (ТСЕР), 3-6 мол. экв. и оставляют на 3-5 часов при кт. Реакционную смесь затем разводят 5-10-кратно добавлением предварительно охлажденного 10 мМ одноосновного фосфата натрия и фильтруют через 5 мкм фильтр. Дифильтрацию тиолированного сахарида проводят против 30-40-кратного диаобъема предварительно охлажденного 10 мМ одноосновного фосфата натрия. Аликвоту ретентата активированного тиолированного сахарида отбирают для определения концентрации сахарида и анализа содержания тиола (Эллман).
Активация и очистка бромацетилированного белка-носителя. Свободные аминогруппы белка-носителя бромацетилируют реакцией с бромацетилирующим агентом, таким как N-гидроксисукцинимидный эфир бромуксусной кислоты (BAANS), бромацетилбромид или другим подходящим реагентом.
Белок-носитель (в 0,1 М фосфате натрия, pH 8,0 ± 0,2) сначала выдерживают при 8 ± 3°С, примерно при pH 7 перед активацией. К белковому раствору добавляют N-гидроксисукцинимидный эфир бромуксусной кислоты (BAANS) в виде исходного раствора диметилсульфоксида (ДМСО) (20 мг/мл) в соотношении 0,25-0,5 BAANS: белок (масс./масс.). Реакционную смесь осторожно перемешивают при 5 ± 3°С в течение 30-60 минут. Полученный бромацетилированный (активированный) белок очищают, например, ультрафильтрацией/диафильтрацией с использованием 10 кДа мембраны MWCO с использованием 10 мМ фосфатного (pH 7,0) буфера. После очистки, концентрацию белка в бромацетилированном белке-носителе оценивают с помощью анализа белка по Лоури.
Степень активации определяют анализом общего содержания бромида с помощью ионообменной жидкостной хроматографии в сочетании с обнаружением по подавленной электропроводности (ионная хроматография). Связанный бромид на активированном бромацетилированном белке отщепляют от белка в образце для анализа и количественно определяют вместе с любым свободным бромидом, который может присутствовать. Любой оставшийся ковалентно связанный бром на белке высвобождают путем превращения в ионный бромид при нагревании образца в щелочном 2-меркаптоэтаноле.
Активация и очистка бромацетилированного CRM197. CRM197 разводят до 5 мг/мл 10 мМ фосфатом, забуференным 0,9% NaCl, pH 7 (PBS), и затем готовят 0,1 М NaHCO3, pH 7,0, используя 1 М исходный раствор. BAANS добавляют в соотношении СО197:BAANS 1:0,35 (масс.:масс.), используя исходный раствор BAANS 20 мг/мл ДМСО. Реакционную смесь инкубируют при температуре от 3°C до 11°C в течение 30 минут - 1 часа, затем очищают ультрафильтрацией/диафильтрацией с использованием 10K мембраны MWCO и 10 мМ фосфата натрия/0,9% NaCl, pH 7,0. Очищенный активированный CRM197 анализируют с помощью анализа Лоури для определения концентрации белка, и затем разводят PBS до 5 мг/мл. Добавляют сахарозу до 5% масс./об. в качестве криопротектора, и активированный белок замораживают и хранят при -25°С до тех пор, пока он не потребуется для конъюгации.
Бромацетилирование лизиновых остатков CRM197 является очень последовательным, приводя к активации от 15 до 25 лизинов из 39 доступных лизинов. Реакция дает высокие выходы активированного белка.
Конъюгация активированного тиолированного сахарида с бромацетилированным белком-носителем. Затем добавляют бромацетилированный белок-носитель и активированный тиолированный сахарид. Исходное соотношение сахарид/белок составляет 0,8 ± 0,2. рН реакции доводят до 9,0 ± 0,1 с помощью 1 М раствора NaOH. Реакции конъюгации дают протекать при 5°С в течение 20 ± 4 часов.
Кэпирование остаточных реакционноспособных функциональных групп. Непрореагировавшие бромацетилированные остатки на белке-носителе гасят реакцией с 2 мол. экв. N-ацетил-L-цистеина в качестве кэпирующего реагента в течение 3-5 часов при 5°C. Остаточные свободные сульфгидрильные группы кэпируют 4 мол. экв. йодацетамида (IAA) в течение 20-24 часов при 5°C.
Очистка eTEC-связанного гликоконъюгата. Смесь реакции конъюгации (после IAA-кэпирования) фильтруют через фильтр 0,45 мкм. Ультрафильтрацию/диафильтрацию гликоконъюгата проводят против 5 мМ сукцината - 0,9% солевого раствора, рН 6,0. Затем ретентат гликоконъюгата фильтруют через 0,2 мкм фильтр. Аликвоту гликоконъюгата берут для анализов. Оставшийся гликоконъюгат хранят при 5°С. См. таблицу 21, таблицу 22, таблицу 23, таблицу 24 и таблицу 25.
ПРИМЕР 22: ПОЛУЧЕНИЕ КОНЮГАТОВ E.COLI-O25B ETEC
Процесс активации - Активация липополисахарида E. coli-O25b. Лиофилизированный полисахарид E. coli-O25b восстанавливают в безводном диметилсульфоксиде (ДМСО). Содержание влаги в лиофилизированном растворе O25b/ДМСО определяют с помощью анализа Карла Фишера (KF). Содержание влаги регулируют добавлением воды для инъекций к раствору O25b/ДМСО до достижения содержания влаги 0,5%.
Для инициации активации, на месте получают 1,1'-карбонилдиимидазол (CDI) в виде 100 мг/мл в растворе ДМСО. Полисахарид E. coli-O25b активируют различными количествами CDI перед стадией тиолирования. Активацию CDI проводят при комнатной температуре или 35°C в течение 1-3 часов. Добавляют воду, чтобы погасить любой остаточный CDI в реакционном растворе для активации. Расчеты выполняют для определения добавляемого количества воды и допущения конечного содержания влаги в пределах 2-3% от общего количества воды. Реакции дают протекать в течение 0,5 часа при комнатной температуре.
Тиолирование активированного полисахарида E. coli-O25b. Цистамин-дигидрохлорид получают на месте в безводном ДМСО, и 1-2 мол. экв. дигидрохлорида цистамина добавляют к реакционному раствору активированного полисахарида. Реакции дают протекать в течение 20 ± 4 часов при кт.
Восстановление и очистка активированного тиолированного полисахарида E. coli-O25b. К реакционной смеси тиолированного сахарида добавляют раствор трис(2-карбоксиэтил)фосфина (ТСЕР), добавляют 3-6 мол. экв. и оставляют на 3-5 часов при комнатной температуре. Затем реакционную смесь разводят 5-10-кратно добавлением предварительно охлажденного 10 мМ одноосновного фосфата натрия и фильтруют через 5 мкм фильтр. Диафильтрацию тиолированного сахарида проводят против 40-кратного диаобъема предварительно охлажденного 10 мМ одноосновного фосфата натрия с кассетами ультрафильтрационных мембран 5K MWCO. Ретентат тиолированного полисахарида O25b берут как для анализа концентрации сахарида, так и для анализа тиола (Эллман). Блок-схема процесса активации представлена на ФИГ. 32А).
Процесс конъюгации - конъюгация тиолированного полисахарида E. coli-O25b с бромацетилированным CRM197. Белок-носитель CRM197 отдельно активируют бромацетилированием, как описано в примере 21, и затем подвергают реакции с активированным полисахаридом E. coli-O25b для реакции конъюгации. Бромацетилированный CRM197 и тиолированный полисахарид O25b смешивают вместе в реакционном сосуде. Соотношение входа сахарид/белок составляет 0,8 ± 0,2. рН реакции доводят до 8,0-10,0. Реакции конъюгации дают протекать при 5°C в течение 20 ± 4 часов.
Кэпирование реакционноспособных групп на бромацетилированном CRM197 и тиолированном полисахариде E. coli-O25b. Непрореагировавшие бромацетилированные остатки на белках CRM197 кэпируют, подвергая реакции с 2 мол. экв. N-ацетил-L-цистеина в течение 3-5 часов при 5°C с последующим кэпированием любых остаточных свободных сульфгидрильных групп тиолированного O25b-полисахарида с 4 мол. экв. йодацетамида (IAA) в течение 20-24 часов при 5°C.
Очистка eTEC-связанного гликоконъюгата E. coli-O25b. Раствор конъюгации фильтруют через 0,45 мкм или 5 мкм фильтр. Диафильтрацию гликоконъюгата O25b проводят с использованием кассет ультрафильтрационных мембран 100K MWCO. Диафильтрацию проводят против 5 мМ сукцината - 0,9% солевого раствора, рН 6,0. Затем 100K ретентат гликоконъюгата E. coli-O25b фильтруют через 0,22 мкм фильтр и хранят при 5°C.
Блок-схема процесса конъюгации представлена на ФИГ. 32В.
Результаты
Параметры реакции и данные о характеристиках для нескольких партий гликоконъюгатов E. coli-O25b eTEC показаны в таблице 19. Активация-тиолирование CDI с дигидрохлоридом цистамина приводит к получению гликоконъюгатов с выходом сахаридов от 41 до 92% и содержанием свободных сахаридов от <5 до 14%. См. также Таблицу 21, Таблицу 22, Таблицу 23, Таблицу 24 и Таблицу 25.
ПРИМЕР 23: Процедура приготовления конъюгатов полисахарида-CRM197 eTEC О-антигена E. coli (применительно к О-антигенам из серотипов O25b, O1a, O2 и O6 E. coli
Активация полисахаридов.
О-антиген E. coli восстанавливают в безводном диметилсульфоксиде (ДМСО). Чтобы инициировать активацию, к раствору полисахарида добавляют различные количества 1,1'-карбонилдиимидазола (CDI) (1-10 молярных эквивалентов) и выдерживают реакцию в течение 1-5 часов при комнатной температуре или 35°С. Затем добавляют воду (2-3%, об./об.) для гашения любого остаточного CDI в реакционном растворе активации. После того как реакции дают возможность протекать в течение 0,5 часа при кт, добавляют 1-2 мол. экв. дигидрохлорида цистамина. Реакции дают протекать в течение 5-20 часов при кт, и затем обрабатывают 3-6 мол. экв. трис(2-карбоксиэтил)фосфина (TCEP) с получением тиолированного сахарида. Уровень тиолирования определяют добавленным количеством CDI.
Реакционную смесь затем разводят 5-10-кратно добавлением предварительно охлажденного 10 мМ одноосновного фосфата натрия и фильтруют через 5 мкм фильтр. Дифильтрацию тиолированного сахарида проводят против 30-40-кратного диаобъема предварительно охлажденного 10 мМ одноосновного фосфата натрия. Аликвоту ретентата активированного тиолированного сахарида отбирают для определения концентрации сахарида и содержания тиола (Эллман).
Активация белка-носителя (CRM197)
CRM197 (в 0,1 М фосфате натрия, pH 8,0 ± 0,2) перед активацией сначала выдерживают при 8 ± 3°С примерно при pH 8. К белковому раствору добавляют N-гидроксисукцинимидный эфир бромуксусной кислоты (BAANS) в виде исходного раствора диметилсульфоксида (ДМСО) (20 мг/мл) в соотношении 0,25-0,5 BAANS:белок (масс./масс.). Реакционную смесь осторожно перемешивают при 5 ± 3°С в течение 30-60 минут. Полученный бромацетилированный (активированный) белок очищают, например, ультрафильтрацией/диафильтрацией с использованием 10 кДа мембраны MWCO с использованием 10 мМ фосфатного (pH 7,0) буфера. После очистки, концентрацию белка в бромацетилированном белке-носителе оценивают с помощью анализа белка по Лоури.
Конъюгация
Затем в реактор добавляют активированный CRM197 и активированный полисахарид O-антигена E. coli и перемешивают. Входящее соотношение сахаридов/белков составляет 1 ± 0,2. рН реакции доводят до 9,0 ± 0,1 с 1 М раствором NaOH. Реакции конъюгации дают протекать при 5°С в течение 20 ± 4 часов. Непрореагировавшие бромацетилированные остатки на белке-носителе гасят реакцией с 2 мол. экв. N-ацетил-L-цистеина в качестве кэпирующего реагента в течение 3-5 часов при 5°C. Остаточные свободные сульфгидрильные группы кэпируют 4 мол. экв. йодацетамида (IAA) в течение 20-24 часов при 5°C. Затем реакционную смесь очищают с помощью ультрафильтрации/диафильтрации, проводимой против 5 мМ сукцината - 0,9% солевого раствора, рН 6,0. Затем очищенный конъюгат фильтруют через 0,2 мкм фильтр. См. Таблицу 21, Таблицу 22, Таблицу 23, Таблицу 24 и Таблицу 25.
ПРИМЕР 24: Общая методика - Конъюгация О-антигена (из серотипов O1, O2, O6, 25b E. coli) с полисахаридом с помощью восстановительного химического анализа (RAC)
Конъюгация в диметилсульфоксиде (RAC/ДМСО)
Активирующий полисахарид
Окисление полисахаридов проводят в 100 мМ натрий-фосфатном буфере (рН 6,0 ± 0,2) путем последовательного добавления расчетного количества 500 мМ натрий-фосфатного буфера (рН 6,0) и воды для инъекций (WFI) до конечной концентрации полисахарида 2,0 г/л. При необходимости pH реакции доводят приблизительно до pH 6,0. После корректировки рН, температуру реакции снижают до 4°С. Окисление инициируют добавлением примерно 0,09-0,13 молярных эквивалентов периодата натрия. Реакцию окисления проводят при 5 ± 3°С в течение приблизительно 20 ± 4 ч.
Концентрирование и диафильтрацию активированного полисахарида проводят с использованием ультрафильтрационных кассет 5K MWCO. Диафильтрацию проводят против 20-кратного диаобъема WFI. Затем очищенный активированный полисахарид хранят при 5 ± 3°С. Очищенный активированный сахарид характеризуется, среди прочего, (i) концентрацией сахарида по колориметрическому анализу; (ii) концентрацией альдегида по колориметрическому анализу; (iii) степенью окисления; и (iv) молекулярной массой по SEC-MALLS.
Смешивание активированного полисахарида с сахарозным эксципиентом и лиофилизация
Активированный полисахарид смешивают с сахарозой в соотношении 25 граммов сахарозы на грамм активированного полисахарида. Бутылку с перемешанной смесью затем лиофилизируют. После лиофилизации, флаконы, содержащие лиофилизированный активированный полисахарид, хранят при температуре -20 ± 5°С. Рассчитанное количество белка CRM197 замораживают в резервуаре и отдельно лиофилизируют. Лиофилизированный CRM197 хранят при -20 ± 5°С.
Восстановление лиофилизированного активированного полисахарида и белка-носителя
Лиофилизированный активированный полисахарид восстанавливают в безводном диметилсульфоксиде (ДМСО). После полного растворения полисахарида к лиофилизированному CRM197 добавляют равное количество безводного ДМСО для восстановления.
Конъюгация и кэпирование
Восстановленный активированный полисахарид объединяют с восстановленным CRM197 в реакционном сосуде с последующим тщательным перемешиванием с получением прозрачного раствора перед началом конъюгации с цианоборгидридом натрия. Конечная концентрация полисахарида в реакционном растворе составляет примерно 1 г/л. Конъюгацию инициируют добавлением к реакционной смеси 0,5-2,0 МЭкв цианоборгидрида натрия и инкубацией при 23 ± 2°C в течение 20-48 ч. Реакцию конъюгации останавливают добавлением 2 МЭкв боргидрида натрия (NaBH4), чтобы кэпировать непрореагировавшие альдегиды. Эта реакция кэпирования продолжается при 23 ± 2°С в течение 3 ± 1 часа.
Очистка конъюгата
Раствор конъюгата разводят 1:10 охлажденным 5 мМ сукцинатом - 0,9% солевым раствором (pH 6,0) при подготовке к очистке тангенциальной проточной фильтрацией с использованием мембран 100-300K MWCO. Разведенный раствор конъюгата пропускают через 5-мкм фильтр и проводят диафильтрацию с использованием 5 мМ сукцината/0,9% солевого раствора (pH 6,0) в качестве среды. После завершения диафильтрации, ретентат конъюгата пропускают через фильтр 0,22 мкм. Конъюгат дополнительно разводят 5 мМ сукцинатом/0,9% солевым раствором (pH 6) до целевой концентрации сахарида приблизительно 0,5 мг/мл. Альтернативно, конъюгат очищают, используя 20 мМ гистидина - 0,9% солевого раствора (pH 6,5) путем фильтрации с тангенциальным потоком с использованием мембран 100-300 K MWCO. Заключительную стадию фильтрации через 0,22 мкм проводят с получением иммуногенного конъюгата. См. Таблицу 21, Таблицу 22, Таблицу 23, Таблицу 24 и Таблицу 25.
ПРИМЕР 25: Конъюгация в водном буфере (RAC/водный), применительно к серотипам O25B, O1A, O2 и O6 E. coli
Активацию полисахаридов и диафильтрацию проводят так же, как и для конъюгации на основе ДМСО.
Отфильтрованный активированный сахарид смешивают с CRM197 при массовом отношении полисахарида к белку в диапазоне от 0,4 до 2 масс./масс. в зависимости от серотипа. Это входное соотношение выбрано для регулирования отношения полисахарида к CRM197 в полученном конъюгате.
Полученную смесь затем лиофилизируют. После конъюгации, смесь полисахарида и белка растворяют в 0,1 М натрий-фосфатном буфере с концентрацией полисахарида в диапазоне от 5 до 25 г/л в зависимости от серотипа, рН доводят от 6,0 до 8,0 в зависимости от серотипа. Конъюгацию инициируют добавлением к реакционной смеси 0,5-2,0 МЭкв цианоборгидрида натрия и инкубацией при 23 ± 2°C в течение 20-48 часов. Реакцию конъюгации останавливают добавлением 1-2 МЭкв боргидрида натрия (NaBH4), чтобы кэпировать непрореагировавшие альдегиды.
Альтернативно, отфильтрованный активированный сахарид и расчетное количество белка CRM197 замораживают и лиофилизируют по отдельности, и затем объединяют при растворении в 0,1 М фосфатно-натриевом буфере, затем проводят последующую конъюгацию, как описано выше.
ПРИМЕР 26: Процедура получения односторонних конъюгатов полисахарид-CRM197 О-антигена E. coli
Липополисахариды (LPS), которые являются обычными компонентами внешней мембраны грамотрицательных бактерий, содержат липид А, коровую область и О-антиген (также называемый О-специфическим полисахаридом или О-полисахаридом). Различные серотипы повторяющихся единиц О-антигена различаются по своему составу, структуре и серологическим особенностям. О-антиген, используемый в настоящем изобретении, присоединен к коровому домену, который содержит сахарную единицу, называемую 2-кето-3-дезоксиоктановой кислотой (KDO), на конце своей цепи. В отличие от некоторых способов конъюгации, основанных на случайной активации полисахаридной цепи (например, активации периодатом натрия или карбодиимидом). Это изобретение описывает процесс конъюгации, включающий селективную активацию KDO с помощью дисульфид-аминового линкера, после демаскирования тиоловой функциональной группы, он затем конъюгируется с активированным бромом белком CRM197, как показано на ФИГ. 31 (Получение односторонних конъюгатов).
Конъюгация на основе цистаминового линкера (А1)
Полисахарид О-антигена и цистамин (50-250 мол. экв. KDO) смешивают в фосфатном буфере, доводя рН до 6,0-7,0. К смеси добавляют цианоборгидрид натрия (NaCNBH3) (5-30 мол. экв. KDO) и смесь перемешивают при 37°С в течение 48-72 ч. После охлаждения до комнатной температуры и разведения равным объемом фосфатного буфера, смесь обрабатывают трис(2-карбоксиэтил)фосфином (TCEP) (добавляют 1,2 моль, экв. цистамина). Затем смесь очищают посредством диафильтрации с использованием 5 кДа мембраны MWCO против 10 мМ одноосновного раствора фосфата натрия с получением тиолсодержащего полисахарида О-антигена. Содержание тиола определяют с помощью анализа Эллмана.
Затем проводят конъюгацию путем смешивания полисахарида О-антигена, активированного тиолом, с активированным бромом белком CRM197 в соотношении 0,5-2,0. рН реакционной смеси доводят до 8,0-10,0 с помощью 1 М раствора NaOH. Реакцию конъюгации проводят при 5°С в течение 24 ± 4 ч. Непрореагировавшие остатки брома на белке-носителе гасят взаимодействием с 2 мол. экв. N-ацетил-L-цистеина в течение 3-5 часов при 5°С. Затем добавляют 3 мол. экв. йодацетамида (относительно добавленного N-ацетил-L-цистеина) для кэпирования оставшихся свободных сульфгидрильных групп. Эта реакция кэпирования продолжается в течение еще 3-5 часов при 5°C, и рН обеих стадий кэпирования поддерживают на уровне 8,0-10,0 добавлением 1М NaOH. Полученный конъюгат получали после ультрафильтрации/диафильтрации с использованием 30 кДа мембраны MWCO против 5 мМ сукцината - 0,9% солевого раствора, рН 6,0. См. Таблицу 21, Таблицу 22, Таблицу 23, Таблицу 24 и Таблицу 25.
ПРИМЕР 27: Конъюгация на основе линкера 3,3'-дитиобис(пропанового дигидразида) (А4)
Полисахарид О-антигена и 3,3'-дитиобис(пропановый дигидразид) (5-50 мол. экв. KDO) смешивают в ацетатном буфере, доводят рН до 4,5-5,5. К смеси добавляют цианоборогидрид натрия (NaCNBH3) (5-30 мол. экв. KDO) и смесь перемешивают при 23-37°С в течение 24-72 часов. Затем смесь обрабатывают трис(2-карбоксиэтил)фосфином (TCEP) (добавляют 1,2 моль, экв. линкера 3,3'-дитиобис(пропанового дигидразида)). Затем смесь очищают посредством диафильтрации с использованием 5 кДа мембраны MWCO против 10 мМ одноосновного раствора фосфата натрия с получением тиолсодержащего полисахарида О-антигена. Содержание тиола определяют с помощью анализа Эллмана.
Затем проводят конъюгацию путем смешивания полисахарида О-антигена, активированного тиолом, с активированным бромом белком CRM197 в соотношении 0,5-2,0. рН реакционной смеси доводят до 8,0-10,0 1 М раствором NaOH. Реакцию конъюгации проводят при 5°С в течение 24 ± 4 часов. Непрореагировавшие остатки брома на белке-носителе гасят взаимодействием с 2 мол. экв. N-ацетил-L-цистеина в течение 3-5 часов при 5°С. Затем добавляют 3 мол. экв. йодацетамида (относительно добавленного N-ацетил-L-цистеина) для кэпирования оставшихся свободных сульфгидрильных групп. Эту реакцию кэпирования проводят в течение еще 3-5 часов при 5°C, и рН обеих стадий кэпирования поддерживают на уровне 8,0-10,0 добавлением 1М NaOH. Полученный конъюгат получают после ультрафильтрации/диафильтрации с использованием 30 кДа мембраны MWCO против 5 мМ сукцината - 0,9% солевого раствора, рН 6,0.
ПРИМЕР 28: Конъюгация на основе линкера 2,2'-дитио-N,N'-бис(этан-2,1-диил)бис(2-(аминоокси)ацетамид) (А6)
Полисахарид O-антигена и 2,2'-дитио-N,N'-бис(этан-2,1-диил)бис(2-(аминоокси)ацетамид) (5-50 мол. экв. KDO) смешивают в ацетатном буфере, доводят pH до 4,5-5,5. Затем смесь перемешивают при 23-37℃ в течение 24-72 часов с последующим добавлением цианоборгидрида натрия (NaCNBH3) (5-30 мол. экв. KDO), и смесь перемешивают еще 3-24 часа. Затем смесь обрабатывают трис(2-карбоксиэтил)фосфином (TCEP) (1,2 моль, экв. добавленного линкера). Затем смесь очищают посредством диафильтрации с использованием 5 кДа мембраны MWCO против 10 мМ одноосновного раствора фосфата натрия с получением тиолсодержащего полисахарида О-антигена. Содержание тиола определяют с помощью анализа Эллмана.
Затем проводят конъюгацию путем смешивания полисахарида О-антигена, активированного тиолом, с активированным бромом белком CRM197 в соотношении 0,5-2,0. рН реакционной смеси доводят до 8,0-10,0 1 М раствором NaOH. Реакцию конъюгации проводят при 5°С в течение 24 ± 4 ч. Непрореагировавшие остатки брома на белке-носителе гасят взаимодействием с 2 мол. экв. N-ацетил-L-цистеина в течение 3-5 часов при 5°С. Затем добавляют 3 мол. экв. йодацетамида (относительно добавленного N-ацетил-L-цистеина) для кэпирования остаточных свободных сульфгидрильных групп. Эту реакцию кэпирования продолжают в течение еще 3-5 часов при 5°C, и рН обеих стадий кэпирования поддерживают на уровне 8,0-10,0 добавлением 1М NaOH. Полученный конъюгат получают после ультрафильтрации/диафильтрации с использованием 30 кДа мембраны MWCO против 5 мМ сукцината - 0,9% солевого раствора, рН 6,0.
ПРИМЕР 29: Получение активированного бромом CRM197
CRM197 получают в 0,1 М растворе фосфата натрия, pH 8,0 ± 0,2, и охлаждают до 5 ± 3°С. К раствору белка добавляют N-гидроксисукцинимидный эфир бромуксусной кислоты (BAANS) в виде исходного раствора диметилсульфоксида (ДМСО) (20 мг/мл) в соотношении 0,25-0,5 BAANS:белок (масс./масс.). Реакцию осторожно перемешивают при 5 ± 3°С в течение 30-60 минут. Полученный бромацетилированный (активированный) белок очищают, например, ультрафильтрацией/диафильтрацией с использованием 10 кДа мембраны MWCO с использованием 10 мМ фосфатного (pH 7,0) буфера. После очистки, концентрацию белка в бромацетилированном белке-носителе оценивают с помощью анализа белка по Лоури.
ПРИМЕР 29: Получение конъюгатов E. coli O-Ag-TT
Длинный полисахарид серотипа O25b E. coli, партия № 709766-30 (примерно 6,92 мг/мл, ММ: примерно 39 кДа), 50 мг, лиофилизированный, используют для конъюгации столбнячного анатоксина (ТТ).
Длинный полисахарид серотипа O1a E. coli, 710958-142-3 (примерно 6,3 мг/мл, ММ: примерно 44,3 кДа) (50 мг, 7,94 мл) лиофилизируют.
Длинный полисахарид серотипа O6 E. coli, 710758-121-1 (примерно 16,8 мг/мл, ММ: примерно 44 кДа) (50 мг, 2,98 мл) лиофилизируют.
Каждый из перечисленных выше лиофилизированных полисахаридов растворяют в воде для инъекций с получением примерно 5-10 мг/мл, добавляют 0,5 мл (100 мг раствора (1-циано-4-диметиламинопиридина тетрафторбората (CDAP) в 1 мл ацетонитрила) и перемешивают при КТ. Добавляют 0,2 М триэтиламина (TEA) (2 мл) и перемешивают при КТ.
Приготовление столбнячного анатоксина (ТТ): ТТ (100 мг, 47 мл) концентрируют приблизительно до 20 мл и дважды промывают солевым раствором (2х50 мл) с использованием фильтровальных пробирок. После этого его разводят HEPES и солевым раствором, чтобы получить конечную концентрацию HEPES примерно 0,25 М.
ТТ готовят, как описано выше, и pH реакционной смеси доводят примерно до 9,1-9,2. Реакционную смесь перемешивают при КТ.
Через 20-24 часа реакцию гасят глицином (0,5 мл). После этого ее концентрируют с использованием мембран из регенерированной целлюлозы MWCO и проводят диафильтрацию против солевого раствора. Фильтруют и анализируют. См. таблицу 26.
Конц. сахарида (Anthrone): 1,122 мг/мл (выход 92%).
Концентрация белка (Lowry): 1,133 мг/мл
SP отношение: 0,99
Свободный сахарид (DOC): 74,7%
Полученный продукт концентрируют до 15 мл, используя мембраны из регенерированной целлюлозы MWCO, и проводят диафильтрацию против солевого раствора (диаобъемы 40X). Фильтруют через фильтр 0,22 мкм и анализируют.
Объем: 27 мл
Конц. сахарида (Anthrone): 1,041 мг/мл (выход 56%).
Концентрация белка (Lowry): 1,012 мг/мл
SP отношение: 1,03
Свободный сахарид (DOC): 60,6% (восстановление поли 100%)
Конц. сахарида (Anthrone): 0,790 мг/мл (выход 66%).
Концентрация белка (Lowry): 1,895 мг/мл
SP отношение: 0,42
Свободный сахарид (DOC): <5%
ММ (кДа): 1192
Эндотоксин (ЕОП/мкг): 0,022
ПРИМЕР 30: Дополнительные результаты ферментации, очистки и конъюгации О-антигена
Типовые процессы, описанные ниже, обычно применимы ко всем серотипам E. coli. Получение каждого полисахарида включает периодическую ферментацию с последующей химической инактивацией перед последующей очисткой.
Штаммы и хранение. Штаммы, используемые для биосинтеза короткоцепочечного О-антигена, представляют собой клинические штаммы E. coli дикого типа. Длинноцепочечный О-антиген получают с производными короткоцепочечных продуцентов, которые сконструированы методом Ваннера-Даценко с делецией нативного гена wzzb и комплементированы «длинноцепочечной» удлиняющей функцией fepE из Salmonella. Функция fepE экспрессируется из его нативного промотора либо на высококопийном векторе «topo» на основе colE1, либо на низкокопийном производном вектора pET30a на основе colE1, из которого была удалена промоторная область Т7.
Банки клеток получают путем выращивания клеток либо в среде LB без животных компонентов, либо в минимальной среде до OD600, по меньшей мере, 3,0. Затем бульон разводят свежей средой и смешивают с 80% глицерином для получения конечной концентрации глицерина 20% с 2,0 OD600/мл.
Среда, используемая для культивирования посева и ферментации. Используемая среда для посева и ферментации имеет следующий состав: KH2PO4, K2HPO4, (NH4)2SO4, цитрат натрия, Na2SO4, аспарагиновая кислота, глюкоза, MgSO4, FeSO4-7H2O, Na2MoO4-2H2O, H3BO3, CoCl2-6H2O, CuCl2-2H2O, MnCl2-4H2O, ZnCl2 и CaCl2-2H2O.
Условия посева и ферментации. Затравку инокулируют при 0,1% из одной пробирки с затравкой. Колбу с затравкой инкубируют при 37℃ в течение 16-18 часов и обычно получают 10-20 OD600/мл.
Ферментацию проводят в 10-литровом ферментере из нержавеющей стали с паром на месте.
Инокуляцию ферментера обычно проводят в соотношении 1:1000 из 10 OD600 затравки. Порционная фаза, представляющая собой период, в течение которого происходит рост на 10 г/л порционной глюкозе, обычно длится 8 часов. После истощения глюкозы, происходит внезапное повышение содержания растворенного кислорода, и в этот момент глюкоза питается до ферментации. Затем ферментация обычно продолжается в течение 16-18 часов с выходом >120 OD600/мл.
Первоначальная оценка продуцирования О-антигена с короткой/длинной цепью для серотипов O1a, O2, O6 и O25b. Штаммы дикого типа для O1a, O2, O6 и O25b ферментируют в дополненной минимальной среде в периодическом режиме до OD600=15-20. При истощении глюкозы, приводящем к резкому снижению потребления кислорода, в течение 16-18 часов вводили ограничивающую рост подкормку глюкозой из раствора глюкозы. Достигают плотности клеток 124-145 OD600 единиц/мл. pH бульона для сбора затем доводят до примерно 3,8 и нагревают до 95°С в течение 2 часов. Затем гидролизованный бульон охлаждают до 25°С, доводят до pH 6,0 и центрифугируют для удаления твердых веществ. Полученный супернатант затем наносят на колонку эксклюзионной ВЭЖХ для количественного определения О-антигена. Получают продуктивность в диапазоне 2240-4180 мг/л. Обнаруживают, что молекулярная масса очищенного короткоцепочечного О-антигена из этих партий находится в диапазоне 10-15 кДа. Также отмечают, что эксклюзионная хроматография гидролизатов O2 и O6 выявила отчетливый и отделимый загрязняющий полисахарид, который не был очевиден в гидролизатах O1a и O25b.
Длинноцепочечные версии O-антигенов O1a, O2, O6 и O25b получают путем ферментации версии с делецией wzzb каждого штамма, несущего гетерологичный, комплементарный ген fepE на высококопийной, селективной к канамицину topo плазмиде. Ферментацию проводят так же, как и для короткоцепочечных, хотя и с селекцией канамицина. Конечная плотность клеток, наблюдаемая при 124-177 OD600/мл, связана с продуктивностью О-антигена 3500-9850 мг/л. Основанный на комплементации синтез длинноцепочечного О-антигена является, по меньшей мере, таким же продуктивным, как и у родительского штамма с короткой цепью, и в некоторых случаях, даже более продуктивным. Молекулярная масса очищенного полисахарида О-антигена составляет 33-49 кДа или примерно в 3 раза превышает размер соответствующей короткой цепи.
Отмечено, что гидролизаты с длинной цепью для О2 и О6 демонстрируют признаки загрязняющего полисахаридного пика, который в случае длинноцепочечного антигена наблюдается как плечо на основном пике О-антигена; O1 и O25b не показывают признаков продуцирования загрязняющего полисахарида, как это было замечено ранее с короткоцепочечным родительским белком.
Обнаружено, что подавление скорости роста связано с наличием topo-репликона в отсутствие fepE. Кроме того, мутация Δwzzb сама по себе не оказывает неблагоприятного воздействия на скорость роста, что указывает на то, что нарушенная скорость роста передается плазмидным вектором.
Оценка штаммов на продуцирование О-антигенов О11, О13, О16, О21 и О75. Несколько штаммов дикого типа серотипов O11, O13, O16, O21 и O75 оценивают на их склонность к продуцированию нежелательных полисахаридов при ферментации с помощью эксклюзионной ВЭЖХ. Штаммы для О11, О13, О16, О21 и О75 отобраны по отсутствию загрязняющего полисахарида, а также по их способности продуцировать >1000 мг/л О-антигена и по проявлению профиля чувствительности к антибиотикам, что позволяет рекомбинацию Ваннера-Даценко для введения признака Δwzzb.
Конструируют селектируемые по хлорамфениколу версии topo-fepE и pET-fepE, что позволяет ввести fepE в штаммы O11, O13, O16, O21 и O75 Δwzzb, которые в целом являются резистентными к канамицину. Полученные штаммы, несущие topo-fepE и pET-fepE, ферментируют с селекцией по хлорамфениколу, и надосадочную жидкость из кислотно-гидролизованного бульона оценивают с помощью эксклюзионной ВЭЖХ. Конструкции как с высоко- (topo), так и с низкокопийным (pET) fepE направляют синтез О-антигена с продуктивностью для каждой из них, которая эквивалентна родительскому дикому типу. Экспрессии потенциально мешающих полисахаридов не наблюдается.
Оценка скоростей роста штаммов, несущих плазмиду wzzb, показывает, что O11, O13 и O21 замедляются в присутствии topo-fepE, но не pET-fepE; штаммы O16 и O75 показывают приемлемую скорость роста независимо от выбора репликона.
Процесс очистки полисахаридов включает кислотный гидролиз для высвобождения О-антигенов. Неочищенную суспензию серотипспецифичной культуры E. coli в ферментационном реакторе непосредственно обрабатывают уксусной кислотой до конечного рН 3,5 ± 0,5 и нагревают подкисленный бульон до температуры 95 ± 5°С в течение, по меньшей мере, одного часа. Эта обработка расщепляет лабильную связь между KDO на проксимальном конце олигосахарида и липида А, таким образом высвобождая цепь O-Ag. Подкисленный бульон, содержащий высвободившийся O-Ag, охлаждают до 20 ± 10℃ перед нейтрализацией до pH 7 ± 1,0 с использованием NH4OH. Процесс дополнительно включает несколько стадий центрифугирования, фильтрации и концентрирования/диафильтрации.
(основ ной)

O25a wzzB



(RAC/ДМСО)






132242-137
Пример 31: Исследованная конъюгация с О-антигеном (О4, О11, О21, О75) (RAC/ДМСО)
Пример 32: Получение конъюгатов PLL
Пример 33: Стабильная экспрессия полипептидов E. coli в клетках млекопитающих
Стабильные клоны CHO, экспрессирующие FimH GSD или FimH LD, создают с использованием системы стабильной экспрессии SSI (сайт-специфической интеграции).
Клетка-хозяин CHO представляет собой сконструированную клеточную линию из фона CHOK1SV GS-KO (см., например, патентную заявку США 20200002727 для описания линии клеток-хозяев CHOK1SV GS-KO). Коротко, посадочную площадку с геном зеленого флуоресцентного белка (GFP), окруженную двумя сайтами FRT, таргетируют в «горячую точку» транскрипции в геноме клетки-хозяина. Ген GFP можно заменить геном GS и представляющим интерес геном, которые также окружены сайтами FRT из вектора LVEC, коэкспрессируемого с рекомбиназой флиппазы (FLPe). Эта система не только имеет профили роста и продуктивности, которые выгодно отличаются от случайной интеграции, но также демонстрирует генотипическую и фенотипическую стабильность, по меньшей мере, в 100 поколениях.
Как упоминается в настоящем документе, термин «сайт FRT» относится к нуклеотидной последовательности, при которой продукт гена флиппазы (FLP) 2 мкм плазмиды дрожжей, рекомбиназа FLP, может катализировать сайт-специфическую рекомбинацию. В данной области техники известно множество неидентичных сайтов FRT. Последовательности различных сайтов FRT сходны тем, что все они содержат идентичные инвертированные повторы из 13 пар оснований, фланкирующие асимметричную коровую область из 8 пар оснований, в которой происходит рекомбинация. Именно асимметричная коровая область отвечает за направленность сайта и за различия между различными сайтами FRT. Их иллюстративные (не ограничивающие) примеры включают встречающийся в природе FRT (F) и несколько мутантных или вариантных сайтов FRT, таких как FRT F1 и FRT F2.
Как упоминается в настоящем документе, термин «посадочная площадка» относится к последовательности нуклеиновой кислоты, содержащей первый сайт-мишень рекомбинации, хромосомно интегрированный в клетку-хозяин. В некоторых вариантах осуществления, сайт посадки содержит два или несколько сайтов-мишеней рекомбинации, хромосомно интегрированных в клетку-хозяин. В некоторых вариантах осуществления, клетка содержит 1, 2, 3, 4, 5, 6, 7 или 8 посадочных площадок. В некоторых вариантах осуществления, клетка содержит 1, 2 или 3 посадочные площадки. В некоторых вариантах осуществления, клетка содержит 4 посадочные площадки. В некоторых вариантах осуществления, посадочные площадки интегрированы в 1, 2, 3, 4, 5, 6, 7 или 8 различных хромосомных локусов. В некоторых вариантах осуществления, посадочные площадки интегрированы в 1, 2 или 3 различных хромосомных локуса. В некоторых вариантах осуществления, посадочные площадки встроены в 4 различных хромосомных локуса.
Вектор экспрессии LVEC для FimH GSD или FimH LD и вектор экспрессии FLPe совместно трансфицируют в клетку-хозяин SSI путем электропорации либо с помощью BioRad Gene Pulser Xcell, либо с помощью Amaxa 4D-Nucleofector. Затем клетки культивируют в среде без глутамина, чтобы селектировать клетки, которые имеют ген GS, интегрированный в сайт посадочной площадки. Обычно клетки восстанавливаются через 2-3 недели. Затем проводят клонирование одиночных клеток в 96-луночных планшетах либо с помощью FACS, либо с помощью лимитирующих разведений. Титры из лунок с клетками ранжируют, чтобы сузить до 48 лучших клонов. Проводят второй раунд скрининга с подпиткой в 24 глубоколуночных планшетах, чтобы сузить количество клонов до 12 лучших. Третий раунд скрининга с подпиткой в Ambr15 проводят, чтобы сузить количество клонов до 3 лучших. Эксперименты с Ambr250 используют для идентификации лучшего клона. Основной банк клеток и рабочий банк клеток создают для лучшего клона после его идентификации.
Пример 34: Разработка линии клеток и экспрессия в продуцирующем реакторе белков FimH-DSG WT и FimHLD WT
Пример, описанный в настоящем документе, описывает типовое продуцирование обоих, FimH-DSG WT и FimHLD WT из стабильных клеточных линий CHO, где кодирующие последовательности для каждого белка стабильно интгерированы в геном CHO.
В условиях продуцирующего биореактора, выбранные стабильные клеточные линии CHO способны продуцировать белок-мишень в количестве примерно 1 грамм на литр культуры для FimH-DSG WT и 250 миллиграммов на литр культуры для FimHLD WT. Систему посевных ферментеров для продуцирующего реактора непрерывно увеличивают в масштабе после размораживания флаконов рабочего банка клеток и размножают во встряхиваемых колбах с использованием плотности жизнеспособных клеток для инокуляции 0,3×106 клеток/мл в течение трех циклов пассажей во встряхиваемых колбах, чтобы обеспечить достаточное количество клеток для продуцирующего реактора. Клетки выращивают при 36,5°С, 5% СО2 в течение трех-четырех дней.
Продуцирующий реактор засевают из последней встряхиваемой колбы с целевой плотностью инокуляции клеток 1×106 клеток/мл. Продуцирующий реактор выращивают при 36,5°C в течение семи дней, используя pH 7,05 (+/-0,15) и ориентируясь на насыщение CO2 5-10%. pH контролируют бикарбонатом натрия/калия для контроля основания, и барботажем CO2 для контроля кислоты. Растворенный кислород контролируют на заданном уровне 40% с использованием чистого кислорода через барботаж. Температуру доводят до 31°С на седьмой день. Реактор подпитывают в первый день с использованием стратегии подпитки, при которой подпитку добавляют в соответствии с плотностью жизнеспособных клеток. Это достигается за счет использования коэффициента подпитки 0,75, чтобы гарантировать, что компоненты подпитки не закончатся во время цикла. Затем подпитку добавляют непрерывно, чтобы обеспечить желаемый объем подпитки в течение дня.
Продуцирующий реактор собирают на 13 день, собранную культуру центрифугируют и фильтруют через 0,22 мкм фильтр перед последующей обработкой.
Пример 35. Антитела, индуцированные CRM197. Конъюгаты O-антигенов E.coli серотипов O8 и O9 проявляют перекрестную защитную бактерицидную активность против инвазивных изолятов серотипов O5 и O3 K.pneumoniae
Этот пример демонстрирует, что антитела, индуцированные короткими односторонними нативными CRM197 полиманнановыми конъюгатами O-антигенов серотипов O8 и O9 E. coli, являются бактерицидными и перекрестно защищающими от штаммов O5 и O3 Klebsiella, которые экспрессируют эквивалентные или родственные O-антигены.
E. coli и K. pneumoniae имеют общие полиманнановые О-антигены, которые синтезируются ферментами, кодируемыми высоко гомологичными кластерами биосинтетических генов. Полисахариды O-антигена O8 и O9 E. coli представляют собой линейные гомополимеры маннозы, повторяющиеся единицы которых отличаются моносахаридными связями и количеством остатков. Их аналогами в K. pneumoniae являются О-антигены серотипов О5 и О3. Биосинтез полиманнановых О-антигенов E. coli и K. pneumoniae включает другой механизм транслокации О-единиц и синтеза цепи, чем у других О-антигенов E. coli. В этом случае, удлинение цепи регулируется биосинтетическим комплексом WbdA-WbdD (King JD, Berry S, et al. Proceedings of the National Academy of Sciences 2014; 111:6407-12), который отличается от Wzx/Wzy-зависимого пути, где длина цепи контролируется ферментами WzzB или FepE. Как следствие, нативные полиманнановые О-антигены могут быть получены только в их короткой форме, что требует иных методов биопроцессов для очистки и конъюгации белков-носителей, чем для сконструированных длинных О-антигенов E. coli. Тот же механизм и ограничения относятся к преобладающим O-антигенам серотипов O1 и O2K. pneumoniae, которые представляют собой полигалактаны, состоящие из остатков галактозы.
Структурная взаимосвязь между этими О-антигенами и их подтипами показана на ФИГ. 33. О-антигены O8 E.coli и O5 K.pneumoniae идентичны (Vinogradov E, et al. J Biol Chem 2002; 277:25070-81). O-антигены E. coli O9 и K. pneumoniae O3 имеют общие тетрамерные O9a/O3a и пентамерные O9/O3 подтипы повторяющихся единиц, в то время как тримерный подтип O3b обнаружен только у K. pneumoniae. Эти подтипы можно идентифицировать серологически и генотипически (Guachalla LM, et al. Scientific Reports 2017; 7:6635). Локусы серотипа O3a отличаются единственной точечной мутацией в wbdA (C80R). Аналогичная точечная мутация в ферменте E. coli O9 wbdA (C55R) превращает полисахарид O9 в O9a (Kido N, Kobayashi H. Journal of bacteriology 2000; 182:2567-73). Подтип O3b имеет достаточную дивергенцию нуклеотидов в последовательности фермента WbdD, что требует отдельной эталонной последовательности. Веб-алгоритм Kaptive (Wick RR, et al. J Clin Microbiol 2018; 56), реализованный в конвейере Pfizer BigSdb для полногеномного секвенирования (WGS), обозначает локусы O3 либо как O3/O3a (охватываемые одной и той же эталонной последовательностью), либо как O3b.
Материалы и способы
а. Получение иммунных сывороток E. coli серотипов O8 и O9 CRM197 у кроликов
Две группы по четыре самки кроликов New Zealand White в каждой используют для проведения исследования в Covance. Животные получают 10 мкг/животное конъюгата серотипа O8 или O9 CRM197 на дозу с CFA/IFA в качестве адъюванта. Нативные О-антигены О8 и О9 конъюгируют с использованием односторонней химии. Каждую 1 мл дозу 10 мкг антигена делят на два участка подкожной вакцинации. Вакцинации проводят на 0, 6 и 14 неделях с забором крови на 7 и 15 неделях, что соответствует временным точкам после введения второй дозы (PD2) и после введения третьей дозы (PD3).
b. Бактериальные штаммы
E. coli и K. pneumoniae получают из спонсируемой Pfizer коллекции Antimicrobial Testing Leadership and Surveillance (ATLAS), которая поддерживается клинической лабораторией International Health Management Associates (IHMA). Штаммы генотипически характеризуют полногеномным секвенированием (WGS) с использованием платформы Miseq (Illumina). Данные WGS используют для получения информации о многолокусных последовательностях (MLST) с использованием установленных схем E. coli и K. pneumoniae, интегрированных в платформу BigDdb (Wirth T, et al. Molecular microbiology 2006; 60:1136-51; Jolley KA, et al. Wellcome Open Res 2018; 3:124; Diancourt L, et al. Journal of clinical microbiology 2005; 43:4178-82). Встроенные in silico алгоритмы серотипирования E. coli и K. pneumoniae используют для прогнозирования серотипа О-антигена (Wick RR, et al. J Clin Microbiol 2018; 56; Joensen KG, et al. J Clin Microbiol 2015; 53:2410-26).
c. Конъюгаты E. coli O8 и O9 CRM197
Полисахариды O-антигена серотипа O8 и O9a экстрагируют и очищают из штаммов EC0130 и EC0423, соответственно (таблица 34). Процесс конъюгации включает селективную активацию моносахарида Kdo, присутствующего на восстанавливающем конце коротких нативных O-антигенов O8 и O9 E. coli, с помощью дисульфид-аминового линкера. После демаскирования тиоловой функциональной группы, ее затем конъюгируют с активированным бромом белком CRM197, как описано в примере 26, изложенном в настоящем документе.
d. Бактерицидные анализы
Предварительно замороженные исходные растворы E. coli и K. pneumoniae готовят путем выращивания штаммов в средах DMEM или LB до OD600 от 0,5 до 1,0, и перед замораживанием добавляют глицерин до конечной концентрации 20%. Конкретные условия анализа варьируются в зависимости от условий, оптимизированных для каждого бактериального штамма. Предварительно титрованные размороженные бактерии разводят до 1х105 КОЕ/мл в ОРА-буфере (сбалансированный солевой раствор Хэнкса (Life Technologies) и 0,1% желатина), и 20 мкл (103 КОЕ) бактериальной суспензии опсонизируют с 20 мкл серийно разбавленной сыворотки в течение 30 мин при комнатной температуре в микропланшете для тканевых культур. Затем, 10 мкл комплемента (сыворотка крольчат или сыворотка человека, обедненная IgG/IgM, Pel-Freez) и 20 мкл клеток HL-60 (в соотношении 100-200:1) добавляют в каждую лунку с ОРА буфером до конечного объема 100 мкл. Реакционную смесь встряхивают в течение 60 мин при 37°С в инкубаторе с 5% СО2. В некоторых случаях, бактерии напрямую объединяют с комплементом и HL60 без стадии предварительной опсонизации и встряхивают в течение 60 мин при 37°C в атмосфере 5% CO2. После инкубации, 10 мкл каждой реакционной смеси переносят в соответствующие лунки предварительно смоченного фильтрующего планшета Millipore MultiScreen HTS HV, содержащего 100 мкл воды. После вакуумной фильтрации жидкости, применяют 100 мкл 50% среды для роста бактерий и фильтруют, и планшет инкубируют в течение ночи при 37°С в герметичном пакете с застежкой-молнией. На следующий день подсчитывают микроколонии после окрашивания красителем Coomassie с использованием анализатора ImmunoSpot® и программного обеспечения ImmunoCapture. В случае анализа серотипа O9 E. coli, OPA миниатюризируют для реакционных объемов 50 мкл в 384-луночном формате. Для установления специфичности активности ОРА, иммунные сыворотки предварительно инкубируют с очищенным полисахаридом О-антигена перед стадией опсонизации. Анализ OPA включает контрольные реакции без клеток HL60 или комплемента, чтобы продемонстрировать зависимость любого наблюдаемого уничтожения от этих компонентов. Для анализа серотипа O5 Klebsiella, где присутствие HL60 не оказывает влияния, бактерицидные реакции в сыворотке проводят в отсутствие эффекторных клеток.
Результаты
а. Селекция штаммов E. coli и K. pneumoniae для бактерицидных анализов
Бактериальные клинические штаммы первоначально отбирают после подтверждения экспрессии О-антигена с помощью профилирования LPS (путем эксклюзионной ВЭЖХ) и доступности поверхности О-антигена с помощью проточной цитометрии с О-антиген-специфической антисывороткой кролика. Затем проводят эмпирический скрининг сывороточного комплемента для определения отдельных совместимых партий в диапазоне концентраций, которые обеспечивают подходящий баланс низких уровней неспецифического уничтожения в сочетании с высокой степенью чувствительности в присутствии иммунных сывороток. Дополнительные параметры оптимизации анализа включают корректировку соотношения эффекторных клеток HL60 и бактерий, скорость шейкера, наличие/отсутствие герметика для планшетов и включение стадии предварительной инкубации с опсонизацией.
b. Перекрестная защита и специфичность О-антигена иммунной сыворотки O8 E. coli и O5 K. pneumoniae
O8 EC0305 E. coli и штамм O5 KP0121 K. pneumoniae выбирают для разработки анализа. Оба являются изолятами крови. EC0305 является резистентным к цефалоспоринам и тетрациклину, и KP0121 является резистентным к ампициллину. Анализ OPA разрабатывают для штамма O8 EC0305 E. coli с условиями, включающими 3,0% BRC, соотношение бактерий к HL60 1:100 и одностадийную 60-минутную реакцию инкубации OPA. Поскольку обнаружено, что бактерицидная активность штамма KP0121 O5 K. pneumoniae в присутствии иммунных сывороток не зависит от эффекторных клеток HL60, разрабатывают SBA. В этом случае, реакция SBA требует использования 10% обедненной сыворотки человека в качестве источника комплемента. Результаты бактерицидных анализов с этими штаммами O8 E. coli и O5 K. pneumoniae показаны на ФИГ. 34А-34В. В OPA серотипа O8 E. coli, кроличья иммунная сыворотка, полученная после двух доз конъюгата O8-CRM197, показывает сильное специфическое уничтожение O-антигена, которое заблокировано предварительной адсорбцией иммунной сыворотки свободным полисахаридом O8 O-антигена. Полное уничтожение наблюдается при разведении сыворотки менее 1:1000. Совпадающие предиммунные сыворотки от того же кролика оказались неактивными. Ту же кроличью сыворотку оценивают в SBA O5 K. pneumoniae и находят, что она аналогично бактерицидная при разведении сыворотки 1:2000. Уничтожение блокируется свободным O8 О-антигеном и отсутствует с предиммунной сывороткой. В этом случае, сывороточная матрица прозона маскирует активность SBA при разведении сыворотки менее 1:1000.
с. перекрестная защита и специфичность иммунной сыворотки O9 E. coli и O3 K. pneumoniae OPA O-антигена
O9a EC0611 E. coli и штамм O3b KP0009 K. pneumoniae выбирают для разработки анализа. EC0611 является резистентным к ампициллину, и KP0009 является резистентным к цефалоспоринам, фторхинолонам и тетрациклину. Оба являются изолятами UTI из инфекций почек и мочевого пузыря соответственно. O-антиген O9a, использованный для создания конъюгата CRM197 и полученной иммунной сыворотки, имеет структуру тетраметического полиманнанового повтора и идентичен O-антигену штамма O9a EC0611 для анализа; однако он структурно гетерологичен тестируемому штамму O3b O-антигена KP0009 K. pneumoniae, который, как предполагается, экспрессирует более короткую трехмерную повторяющуюся единицу на основании последовательности его гена wbdD (см. ФИГ. 33). Результаты OPA со штаммами O9a E.coli и O3b K.pneumoniae показывают, что иммунная сыворотка против O9a E.coli эффективна против обоих (ФИГ. 35A-35B). Полное уничтожение ОРА наблюдается при разведении сыворотки менее 1:8000 для штамма O9a E. coli и менее 1:1600 для штамма O3b Klebsiella. Специфичность демонстрируют отсутствием активности при преадсорбции сыворотки со свободным О-антигеном О9а и с соответствующей предиммунной сывороткой.
Вывод
Конъюгаты серотипа O8 и O9 E. coli полиманнана CRM197 вырабатывают функциональные антитела, которые способны убивать не только гомологичные клинические штаммы E. coli, но и штаммы серотипа O5 и O3 Klebsiella в бактерицидных анализах. Результаты подтверждают, что эти конъюгаты продуцируют антитела, обладающие перекрестной защитой против изолятов обоих видов, экспрессирующих структурно родственные полиманнановые О-антигены.
Следующие пункты описывают дополнительные варианты осуществления изобретения:
С. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид, имеющий структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 1 до 100.
С2. Композиция по п. С1, отличающаяся тем, что сахарид имеет структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O10, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O21, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O28, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O55, Формулы O56, Формулы O58, Формулы O64, Формулы O69, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O75, Формулы O77, Формулы O78, Формулы O86, Формулы O88, Формулы O90, Формулы O98, Формулы O104, Формулы 0111, Формулы O113, Формулы O114, Формулы O119, Формулы O121, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O136, Формулы O138, Формулы O141, Формулы O142, Формулы O143, Формулы O147, Формулы O149, Формулы O152, Формулы O157, Формулы O158, Формулы O159, Формулы O164, Формулы O173, Формулы 62D1, Формулы O22, Формулы O35, Формулы O65, Формулы O66, Формулы O83, Формулы O91, Формулы O105, Формулы O116, Формулы O117, Формулы O139, Формулы O153, Формулы O167 и Формулы O172, где n представляет собой целое число. от 20 до 100.
С3. Композиция по п. С2, отличающаяся тем, что сахарид имеет структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O3, Формулы O4 (например, Формулы O4:K52 и Формулы O4:K6), Формулы O5 (например, Формулы O5ab и Формулы O5ac (штамм 180/C3)), Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O7, Формулы O10, Формулы O16, Формулы O17, Формулы O18 (например, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B и Формулы O18B1), Формулы O21, Формулы O23 (например, Формулы O23A), Формулы O24, Формулы O25 (например, Формулы O25a и Формулы O25b), Формулы O26, Формулы O28, Формулы O44, Формулы O45 (например, Формулы O45 и Формулы O45rel), Формулы O55, Формулы O56, Формулы O58, Формулы O64, Формулы O69, Формулы O73 (например, Формулы O73 (штамм 73-1)), Формулы O75, Формулы O77, Формулы O78, Формулы O86, Формулы O88, Формулы O90, Формулы O98, Формулы O104, Формулы 0111, Формулы O113, Формулы O114, Формулы O119, Формулы O121, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O136, Формулы O138, Формулы O141, Формулы O142, Формулы O143, Формулы O147, Формулы O149, Формулы O152, Формулы O157, Формулы O158, Формулы O159, Формулы O164, Формулы O173 и Формулы 62D1, где n представляет собой целое число от 20 до 100.
С4. Композиция по п. С2, содержащая структуру, выбранную из Формулы O1 (например, Формулы O1A, Формулы O1B и Формулы O1C), Формулы O2, Формулы O6 (например, Формулы O6:K2; K13; K15 и Формулы O6:K54), Формулы O15, Формулы O16, Формулы O21, Формулы O25 (например, Формулы O25a и Формулы O25b) и Формулы O75.
С5. Композиция по п. С2, содержащая структуру, выбранную из Формулы O4, Формулы O11, Формулы O21 и Формулы O75.
С6. Композиция по п. С1, отличающаяся тем, что сахарид не имеет структуру, выбранную из Формулы O8, Формулы O9a, Формулы O9, Формулы O20ab, Формулы O20ac, Формулы O52, Формулы O97 и Формулы O101.
С7. Композиция по п. С1, отличающаяся тем, что сахарид не имеет структуру, выбранную из Формулы O12.
С8. Композиция по п. С4, отличающаяся тем, что сахарид получают путем экспрессии белка семейства wzz в грамотрицательной бактерии с образованием указанного сахарида.
С9. Композиция по п. С8, отличающаяся тем, что белок семейства wzz выбран из группы, состоящей из wzzB, wzz, wzzSF, wzzST, fepE, wzzfepE, wzz1 и wzz2.
С10. Композиция по п. С8, отличающаяся тем, что белок семейства wzz представляет собой wzzB.
С11. Композиция по п. С8, отличающаяся тем, что белок семейства wzz представляет собой fepE.
С12. Композиция по п. С8, отличающаяся тем, что белок семейства wzz представляет собой wzzB и fepE.
С13. Композиция по п. С8, отличающаяся тем, что белок семейства wzz получен из Salmonella enterica.
С14. Композиция по п. С8, отличающаяся тем, что белок семейства wzz содержит последовательность, выбранную из любой из SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38 и SEQ ID NO: 39.
С15. Композиция по п. С8, отличающаяся тем, что белок семейства wzz содержит последовательность, по меньшей мере, на 90% идентичную любой из последовательностей SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34.
С16. Композиция по п. С8, отличающаяся тем, что белок семейства wzz содержит последовательность, выбранную из любой из SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38 и SEQ ID NO: 39.
С17. Композиция по п. С1, отличающаяся тем, что сахарид синтезирован синтетическим путем.
С18. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно содержит группу R1 E. coli.
С19. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно содержит группу R2 E. coli.
С20. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно содержит группу R3 E. coli.
С21. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно содержит группу R4 E. coli.
С22. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно содержит группу K-12 E. coli.
С23. Композиция по любому из пп. С1-С22, отличающаяся тем, что сахарид дополнительно содержит группу 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO).
С24. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно не содержит группу R1 E. coli.
С25. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно не содержит группу R2 E. coli.
С26. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно не содержит группу R3 E. coli.
С27. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно не содержит группу R4 E. coli.
С28. Композиция по любому из пп. С1-С17, отличающаяся тем, что сахарид дополнительно не содержит группу K-12 E. coli.
С29. Композиция по любому из пп. С1-С22, отличающаяся тем, что сахарид дополнительно не содержит группу 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO).
С30. Композиция по любому из пунктов С1-С23, отличающаяся тем, что сахарид не содержит липид А.
С31. Композиция по любому из пп. С1-С30, отличающаяся тем, что полисахарид имеет молекулярную массу от 10 кДа до 2000 кДа или от 50 кДа до 2000 кДа.
С32. Композиция по любому из пп. С1-С31, отличающаяся тем, что сахарид имеет среднюю молекулярную массу 20-40 кДа.
С33. Композиция по любому из пп. С1-С32, отличающаяся тем, что сахарид имеет среднюю молекулярную массу от 40000 до 60000 кДа.
С34. Композиция по любому из пунктов С1-С33, где n равно целому числу от 31 до 90.
С35. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и конъюгат, содержащий сахарид, ковалентно связанный с белком-носителем, где сахарид получен из E. coli.
С36. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и конъюгат, содержащий сахарид по любому из пунктов С1-С, ковалентно связанный с белком-носителем.
С37. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и конъюгат по любому из пунктов С35-С36, отличающийся тем, что белок-носитель выбран из любого из поли(L-лизина), CRM197, фрагмента дифтерийного токсина B (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C TT, коклюшного анатоксина, холерного анатоксина или экзотоксина A из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы B холерного токсина (CTB), пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni, природных гликопротеинов C. jejuni и стрептококковой пептидазы C5a (SCP).
С38. Композиция по любому из пунктов C35-C37, отличающаяся тем, что белок-носитель представляет собой CRM197.
С39. Композиция по любому из пунктов C35-C37, отличающаяся тем, что белок-носитель представляет собой столбнячный анатоксин (ТТ).
С40. Композиция по любому из пунктов C35-C37, отличающаяся тем, что белок-носитель представляет собой поли(L-лизин).
С41. Композиция по любому из пунктов C35-C39, отличающаяся тем, что конъюгат получают восстановительным аминированием.
С42. Композиция по любому из пп. C35-C39, отличающаяся тем, что конъюгат получен с помощью химии CDAP.
С43. Композиция по любому из пунктов C35-C39, отличающаяся тем, что конъюгат представляет собой односторонне-связанный конъюгированный сахарид.
С44. Композиция по любому из пп. C35-C39, отличающаяся тем, что сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC).
С45. Композиция по п. C44, отличающаяся тем, что сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC), где сахарид ковалентно связан со спейсером eTEC через карбаматную связь, и где белок-носитель ковалентно связан со спейсером eTEC посредством амидной связи.
С46. Композиция по любому из пп. C44-C45, отличающаяся тем, что CRM197 содержит от 2 до 20 или от 4 до 16 лизиновых остатков, ковалентно связанных с полисахаридом через спейсер eTEC.
С47. Композиция по любому из пунктов C35-C46, отличающаяся тем, что соотношение сахарид:белок-носитель (масс./масс.) составляет от 0,2 до 4.
С48. Композиция по любому из пп. C35-C46, отличающаяся тем, что отношение сахарида к белку составляет, по меньшей мере, 0,5 и не более 2.
С49. Композиция по любому из пп. C35-C46, отличающаяся тем, что отношение сахарида к белку составляет от 0,4 до 1,7.
С50. Композиция по любому из пп. C43-C49, отличающаяся тем, что сахарид конъюгирован с белком-носителем через остаток 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO).
С51. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и конъюгат, содержащий сахарид, ковалентно связанный с белком-носителем, где сахарид имеет структуру, выбранную из Формулы O8, Формулы O9a, Формулы O9, Формулы O20ab, Формулы O20ac, Формулы O52, Формулы O97 и Формулы O101, где n представляет собой целое число. от 1 до 10.
С52. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид по любому из пп. C1-C34, и фармацевтически приемлемый разбавитель.
С53. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и конъюгат по любому из пп. C35-C51 и фармацевтически приемлемый разбавитель.
С54. Композиция по п. C53, содержащая не более примерно 25% свободного сахарида по сравнению с общим количеством сахарида в композиции.
С55. Композиция по любому из пп. C52-C53, дополнительно содержащая адъювант.
С56. Композиция по любому из пп. C52-C53, дополнительно содержащая алюминий.
С57. Композиция по любому из пп. C52-C53, дополнительно содержащая QS-21.
С58. Композиция по любому из пп. C52-C53, дополнительно содержащая олигонуклеотид CpG.
С59. Композиция по любому из пп. C52-C53, отличающаяся тем, что композиция не включает адъювант.
С60. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид, полученный из E. coli, конъюгированный с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC), где полисахарид ковалентно связан со спейсером eTEC через карбаматную связь, и где белок-носитель ковалентно связан со спейсером eTEC через амидную связь.
С61. Композиция по п. C60, отличающаяся тем, что сахарид представляет собой О-антиген, полученный из E. coli.
С62. Композиция по п. C60, дополнительно содержащая фармацевтически приемлемый эксципиент, носитель или разбавитель.
С63. Композиция по п. C60, отличающаяся тем, что сахарид представляет собой О-антиген, полученный из E. coli.
С64. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид по любому из пунктов C1-C17, конъюгированный с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC), где полисахарид ковалентно связан со спейсером eTEC через карбаматную связь, и где белок-носитель ковалентно связан со спейсером eTEC через амидную связь.
С65. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и (i) конъюгат антигена O25B E. coli, ковалентно связанный с белком-носителем, (ii) конъюгат антигена O1A E. coli, ковалентно связанный с белком-носителем, (iii) конъюгат антигена O2 E. coli, ковалентно связанный с белком-носителем, и (iv) конъюгат антигена O6, ковалентно связанный с белком-носителем, где антиген O25B E. coli имеет структуру Формулы O25B, где n представляет собой целое число больше 30.
С66. Композиция по пп. C65, отличающаяся тем, что белок-носитель выбран из любого из поли(L-лизина), CRM197, фрагмента B дифтерийного токсина (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C TT, коклюшного анатоксина, холерного анатоксина или экзотоксина A из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы холерного токсина B (CTB), Пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni и природных гликопротеинов C. jejuni.
С67. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и (i) конъюгат антигена O25B E. coli, ковалентно связанный с белком-носителем, (ii) конъюгат антигена O4 E. coli, ковалентно связанный с белком-носителем, (iii) конъюгат антигена O11 E. coli, ковалентно связанный с белком-носителем, и (iv) конъюгат антигена O21, ковалентно связанный с белком-носителем, где антиген O25B E. coli имеет структуру Формулы O75, где n представляет собой целое число больше 30.
С68. Композиция по п. C67, отличающаяся тем, что белок-носитель выбран из любого из поли(L-лизина), CRM197, фрагмента B дифтерийного токсина (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C TT, коклюшного анатоксина, холерного анатоксина, или экзотоксина A из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы холерного токсина B (CTB), пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni, природных гликопротеинов C. jejuni и стрептококковой пептидазы C5a (SCP).
С69. Способ получения композиции, содержащей полипептид, полученный из FimH, или его фрагмент; и конъюгат, содержащий сахарид, конъюгированный с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC), включающий стадии а) взаимодействия сахарида с 1,1'-карбонил-ди-(1,2,4-триазолом) (CDT) или 1,1'-карбонилдиимидазолом (CDI) в органическом растворителе с получением активированного сахарида; b) взаимодействия активированного сахарида с цистамином или цистеамином или их солью с получением тиолированного сахарида; c) взаимодействия тиолированного сахарида с восстанавливающим агентом с получением активированного тиолированного сахарида, содержащего один или несколько свободных сульфгидрильных остатков; d) взаимодействия активированного тиолированного сахарида с активированным белком-носителем, содержащим одну или несколько α-галогенацетамидных групп, с получением конъюгата тиолированный сахарид-белок-носитель; и e) взаимодействия конъюгата тиолированный сахарид-белок-носитель с (i) первым кэпирующим реагентом, способным кэпировать неконъюгированные α-галогенацетамидные группы активированного белка-носителя; и/или (ii) вторым кэпирующим реагентом, способным кэпировать неконъюгированные свободные сульфгидрильные остатки; где получают гликоконъюгат, связанный с eTEC, где сахарид получают из E. coli; дополнительно включающий экспрессию полинуклеотида, кодирующего полипептид, полученный из FimH, или его фрагмента в рекомбинантной клетке млекопитающего, и выделение указанного полипептида или его фрагмента.
С70. Способ по п. C69, включающий приготовление композиции по любому из пп. C1-C34.
С71. Способ по любому из пп. C69-C70, отличающийся тем, что стадия кэпирования е) включает реакцию конъюгата тиолированный сахарид-белок-носитель с (i) N-ацетил-L-цистеином в качестве первого кэпирующего реагента, и/или (ii) йодацетамидом в качестве второго кэпирующего реагента.
С72. Способ по любому из пп. C69-C71, дополнительно включающий стадию смешивания сахарида путем взаимодействия с триазолом или имидазолом с получением смешанного сахарида, где смешанный сахарид замораживают, лиофилизируют и восстанавливают в органическом растворителе перед стадией а).
С73. Способ по любому из пп. C69-C72, дополнительно включающий очистку тиолированного полисахарида, полученного на стадии c), где стадия очистки включает диафильтрацию.
С74. Способ по любому из пп. C69-C73, отличающийся тем, что способ дополнительно включает очистку гликоконъюгата, связанного с eTEC, путем диафильтрации.
С75. Способ по любому из пп. C69-C74, отличающийся тем, что органический растворитель на стадии а) представляет собой полярный апротонный растворитель, выбранный из любого из следующих: диметилсульфоксида (ДМСО), диметилформамида (ДМФ), диметилацетамида (ДМА), N-метил-2-пирролидона (NMP), ацетонитрила, 1,3-диметил-3,4,5,6-тетрагидро-2(1H)-пиримидинона (DMPU) и гексаметилфосфорамида (HMPA) или их смеси.
С76. Среда, содержащая KH2PO4, K2HPO4, (NH4)2SO4, цитрат натрия, Na2SO4, аспарагиновую кислоту, глюкозу, MgSO4, FeSO4-7H2O, Na2MoO4-2H2O, H3BO3, CoCl2-6H2O, CuCl2-2H2O, MnCl2-4H2O, ZnCl2 и CaCl2-2H2O.
С77. Среда по п. C76, отличающаяся тем, что указанная среда используется для культивирования E. coli.
С78. Способ получения сахарида по любому из пп. C1-C34, включающий культивирование рекомбинантной E. coli в среде; получение указанного сахарида путем культивирования указанной клетки в указанной среде; где указанная клетка продуцирует указанный сахарид.
С79. Способ по п. C78, отличающийся тем, что среда содержит элемент, выбранный из любого из KH2PO4, K2HPO4, (NH4)2SO4, цитрата натрия, Na2SO4, аспарагиновой кислоты, глюкозы, MgSO4, FeSO4-7H2O, Na2MoO4-2H2O, H3BO3, CoCl2-6H2O, CuCl2-2H2O, MnCl2-4H2O, ZnCl2 и CaCl2-2H2O.
С80. Способ по п. C78, отличающийся тем, что среда содержит гидролизат сои.
С81. Способ по п. C78, отличающийся тем, что среда содержит дрожжевой экстракт.
С82. Способ по п. C78, отличающийся тем, что среда дополнительно не содержит гидролизат сои и дрожжевой экстракт.
С83. Способ по п. C78, отличающийся тем, что клетка E. coli содержит гетерологичный белок семейства wzz, выбранный из любого из wzzB, wzz, wzzSF, wzzST, fepE, wzzfepE, wzz1 и wzz2.
С84. Способ по п. C78, отличающийся тем, что клетка E. coli содержит белок семейства wzz Salmonella enterica, выбранный из любого из wzzB, wzz, wzzSF, wzzST, fepE, wzzfepE, wzz1 и wzz2.
С85. Способ по п. C84, отличающийся тем, что белок семейства wzz содержит последовательность, выбранную из любой из SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
С86. Способ по п. C78, отличающийся тем, что культивирование дает выход >120 OD600/мл.
С87. Способ по п. C78, дополнительно включающий очистку сахарида.
С88. Способ по п. C78, отличающийся тем, что стадия очистки включает любую из следующих: диализа, операций концентрирования, операций диафильтрации, фильтрации с тангенциальным потоком, осаждения, элюирования, центрифугирования, осаждения, ультрафильтрации, глубинной фильтрации и колоночной хроматографии (ионообменной хроматографии, мультимодальной ионообменной хроматографии, DEAE и хроматографии гидрофобного взаимодействия).
С89. Способ индукции иммунного ответа у млекопитающего, включающий введение субъекту композиции по любому из пп. C1-C68.
С90. Способ по п. C89, отличающийся тем, что иммунный ответ включает индукцию анти-E. coli O-специфических полисахаридных сывороточных антител.
С91. Способ по п. C89, отличающийся тем, что иммунный ответ включает индукцию анти-E. coli антитела IgG.
С92. Способ по п.С89, отличающийся тем, что иммунный ответ включает индукцию бактерицидной активности против E.coli.
С93. Способ по п. C89, отличающийся тем, что иммунный ответ включает индукцию опсонофагоцитарных антител против E. coli.
С94. Способ по п. C89, отличающийся тем, что иммунный ответ включает уровень среднего геометрического титра (GMT) по меньшей мере, от 1000 до 200000 после первоначального дозирования.
С95. Способ по п. C89, отличающийся тем, что композиция содержит сахарид, содержащий Формулу O25, где n представляет собой целое число от 40 до 100, где иммунный ответ включает уровень среднего геометрического титра (GMT), по меньшей мере, от 1000 до 200000 после первоначального дозирования.
С96. Способ по п. C89, отличающийся тем, что млекопитающее подвержено риску любого из состояний, выбранных из инфекции мочевыводящих путей, холецистита, холангита, диареи, гемолитико-уремического синдрома, неонатального менингита, уросепсиса, внутрибрюшинной инфекции, менингита, осложненной пневмонии, раневой инфекции, инфекцией, связанной с биопсией простаты, неонатального/младенческого сепсиса, нейтропенической лихорадки и других инфекций кровотока; пневмонии, бактериемии и сепсиса.
С97. Способ по п. C89, отличающийся тем, что у млекопитающего имеется одно из состояний, выбранных из инфекции мочевыводящих путей, холецистита, холангита, диареи, гемолитико-уремического синдрома, неонатального менингита, уросепсиса, внутрибрюшинной инфекции, менингита, осложненной пневмонии, раневой инфекции, инфекции, связанной с биопсией простаты, неонатального/младенческого сепсиса, нейтропенической лихорадки и других инфекций кровотока; пневмонии, бактериемии и сепсиса.
С98. Способ (i) индукции иммунного ответа у субъекта против внекишечной патогенной Escherichia coli, (ii) индукции иммунного ответа у субъекта против внекишечной патогенной Escherichia coli, или (iii) индукции продуцирования опсонофагоцитарных антител у субъекта, которые специфичны в отношении внекишечной патогенной Escherichia coli, где способ включает введение субъекту эффективного количества композиции в соответствии с любым из пп. C1-С68.
С99. Способ по п. С98, отличающийся тем, что у субъекта имеется риск развития инфекции мочевыводящих путей.
С100. Способ по п. С98, отличающийся тем, что у субъекта имеется риск развития бактериемии.
С101. Способ по п. С98, отличающийся тем, что у субъекта существует риск развития сепсиса.
С102. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и (i) конъюгат антигена O25B E. coli, ковалентно связанный с белком-носителем, (ii) конъюгат антигена O1A E. coli, ковалентно связанный с белком-носителем, (iii) конъюгат O2 E. coli, ковалентно связанный с белком-носителем, и (iv) конъюгат O6-антигена, ковалентно связанный с белком-носителем, где антиген O25B E. coli имеет структуру Формулы O25B, где n представляет собой целое число больше 30.
С103. Композиция по п. С102, отличающаяся тем, что белок-носитель выбран из группы, состоящей из поли(L-лизина), детоксицированного экзотоксина А P. aeruginosa (EPA), CRM197, белка, связывающего мальтозу (MBP), дифтерийного анатоксина, столбнячного анатоксина, детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы B холерного токсина (CTB), холерного токсина, детоксицированных вариантов холерного токсина, пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni и природных гликопротеинов C. jejuni.
С104. Способ (i) индукции иммунного ответа у субъекта против внекишечной патогенной Escherichia coli, (ii) индукции иммунного ответа у субъекта против внекишечной патогенной Escherichia coli или (iii) индукции продуцирования опсонофагоцитарных антител у субъекта, специфичных к внекишечной патогенной Escherichia coli, где способ включает введение субъекту эффективного количества композиции по п. С1.
С105. Способ по п. С104, отличающийся тем, что у субъекта имеется риск развития инфекции мочевыводящих путей.
С106. Способ по п. С104, отличающийся тем, что у субъекта имеется риск развития бактериемии.
С107. Способ по п. С104, отличающийся тем, что у субъекта существует риск развития сепсиса.
С108. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид, имеющий увеличение, по меньшей мере, на 5 повторяющихся единиц по сравнению с соответствующим O-полисахаридом дикого типа E. coli.
С109. Композиция по п. С108, отличающаяся тем, что сахарид содержит Формулу O25a, и E. coli представляет собой серотип O25a E. coli.
С110. Композиция по п. С108, отличающаяся тем, что сахарид содержит Формулу O25b, и E. coli представляет собой серотип O25b E. coli.
С111. Композиция по п. С108, отличающаяся тем, что сахарид содержит Формулу O2, и E. coli представляет собой серотип O2 E. coli.
С112. Композиция по п. С108, отличающаяся тем, что сахарид содержит Формулу O6, и E. coli представляет собой серотип O6 E. coli.
С113. Композиция по п. С108, отличающаяся тем, что сахарид содержит Формулу O1, и E. coli представляет собой серотип O1 E. coli.
С114. Композиция по п. С108, отличающаяся тем, что сахарид содержит Формулу O17, и E. coli представляет собой серотип O17 E. coli.
С115. Композиция по п. С108, отличающаяся тем, что сахарид имеет структуру, выбранную из: Формулы O1, Формулы O2, Формулы O3, Формулы O4, Формулы O5, Формулы O6, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O24, Формулы O25, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144,O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 5 до 1000.
С116. Композиция по п. С108, отличающаяся тем, что E.coli представляет собой E.coli серотипа, выбранного из группы, состоящей из: O1, O2, O3, O4, O5, O6, O7, O8, O9, O10, O11, O12, O13, O14, O15, O16, O17, O18, O19, O20, O21, O22, O23, O24, O25, O25b, O26, O27, O28, O29, O30, O32, O33, O34, O35, O36, O37, O38, O39, O40, O41, O42, O43, O44, O45, O46, O48, O49, O50, O51, O52, O53, O54, O55, O56, O57, O58, O59, O60, O61, O62, O63, O64, O65, O66, O68, O69, O70, O71, O73, O74, O75, O76, O77, O78, O79, O80, O81, O82, O83, O84, O85, O86, O87, O88, O89, O90, O91, O92, O93, O95, O96, O97, O98, O99, O100, O101, O102, O103, O104, O105, O106, O107, O108, O109, O110, 0111, O112, O113, O114, O115, O116, O117, O118, O119, O120, O121, O123, O124, O125, O126, O127, O128, O129, O130, O131, O132, O133, O134, O135, O136, O137, O138, O139, O140, O141, O142, O143, O144,O145, O146, O147, O148, O149, O150, O151, O152, O153, O154, O155, O156, O157, O158, O159, O160, O161, O162, O163, O164, O165, O166, O167, O168, O169, O170, O171, O172, O173, O174, O175, O176, O177, O178, O179, O180, O181, O182, O183, O184, O185, O186 и O187.
С117. Композиция по п. С108, отличающаяся тем, что сахарид получают путем увеличения количества повторяющихся единиц О-полисахаридов, продуцируемых грамотрицательной бактерией в культуре, включающей сверхэкспрессию белков семейства wzz в грамотрицательной бактерии, с получением указанного сахарида.
С118. Композиция по п. С117, отличающаяся тем, что сверхэкспрессированный белок семейства wzz выбран из группы, состоящей из wzzB, wzz, wzzSF, wzzST, fepE, wzzfepE, wzz1 и wzz2.
С119. Композиция по п. С117, отличающаяся тем, что белок семейства wzz со сверхэкспрессией представляет собой wzzB.
С120. Композиция по п. С117, отличающаяся тем, что сверхэкспрессированный белок семейства wzz представляет собой fepE.
С121. Композиция по п. С117, отличающаяся тем, что сверхэкспрессированный белок семейства wzz представляет собой wzzB и fepE.
С122. Композиция по п. С108, отличающаяся тем, что сахарид синтезирован синтетическим путем.
С123. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и конъюгат, содержащий сахарид по п. С108, ковалентно связанный с белком-носителем.
С124. Композиция по п. С123, отличающаяся тем, что белок-носитель представляет собой CRM197.
С125. Композиция по п. С123, отличающаяся тем, что сахарид имеет структуру, выбранную из: Формулы O1, Формулы O2, Формулы O3, Формулы O4, Формулы O5, Формулы O6, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O24, Формулы O25, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144,O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 5 до 1000.
С126. Композиция по п. С123, отличающаяся тем, что указанный сахарид содержит увеличение, по меньшей мере, на 5 повторяющихся единиц по сравнению с соответствующим O-полисахаридом дикого типа.
С127. Композиция по п. С1, дополнительно содержащая фармацевтически приемлемый разбавитель.
С128. Композиция по п. С127, дополнительно содержащая адъювант.
С129. Композиция по п. С127, дополнительно содержащая алюминий.
С130. Композиция по п. С127, дополнительно содержащая QS-21.
С131. Композиция по п. С127, отличающаяся тем, что композиция не включает адъювант.
С132. Способ индукции иммунного ответа у субъекта, включающий введение субъекту композиции по п. С127.
С133. Композиция по п. С123, дополнительно содержащая фармацевтически приемлемый разбавитель.
С134. Способ индукции иммунного ответа у субъекта, включающий введение субъекту композиции по п. С133.
С135. Способ по п. С132 или С134, отличающийся тем, что иммунный ответ включает индукцию сывороточного антитела против O-специфического полисахарида E. coli.
С136. Способ по п. С135, отличающийся тем, что сывороточное антитело против O-специфического полисахарида E. coli представляет собой антитело IgG.
С137. Способ по п. С135, отличающийся тем, что сывороточное антитело против O-специфического полисахарида E. coli представляет собой антитело IgG, обладающее бактерицидной активностью против E. coli.
С138. Иммуногенная композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид, полученный из E. coli, конъюгированный с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC), где полисахарид ковалентно связан со спейсером eTEC через карбаматную связь, и где белок-носитель ковалентно связан со спейсером eTEC через амидную связь.
С139. Иммуногенная композиция по п. С138, дополнительно содержащая фармацевтически приемлемый эксципиент, носитель или разбавитель.
С140. Иммуногенная композиция по п. С138, отличающаяся тем, что сахарид представляет собой О-антиген, полученный из E. coli.
С141. Иммуногенная композиция по п. С138, отличающаяся тем, что сахарид имеет структуру, выбранную из: Формулы O1, Формулы O2, Формулы O3, Формулы O4, Формулы O5, Формулы O6, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O24, Формулы O25, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144,O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 5 до 1000.
С142. Иммуногенная композиция по п. С138, отличающаяся тем, что сахарид имеет степень O-ацетилирования от 75 до 100%.
С143. Иммуногенная композиция по п. С138, отличающаяся тем, что белок-носитель представляет собой CRM197.
С144. Иммуногенная композиция по п. С143, отличающаяся тем, что CRM197 содержит от 2 до 20 лизиновых остатков, ковалентно связанных с полисахаридом через спейсер eTEC.
С145. Иммуногенная композиция по п. С143, отличающаяся тем, что CRM197 содержит от 4 до 16 лизиновых остатков, ковалентно связанных с полисахаридом через спейсер eTEC.
С146. Иммуногенная композиция по п. С138, дополнительно содержащая дополнительный антиген.
С147. Иммуногенная композиция по п. С138, дополнительно содержащая адъювант.
С148. Иммуногенная композиция по п. С147, отличающаяся тем, что адъювант представляет собой адъювант на основе алюминия, выбранный из группы, состоящей из фосфата алюминия, сульфата алюминия и гидроксида алюминия.
С149. Иммуногенная композиция по п. С138, отличающаяся тем, что композиция не содержит адъювант.
С150. Иммуногенная композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и гликоконъюгат, содержащий сахарид, полученный из E. coli, конъюгированный с белком-носителем, где гликоконъюгат получают с использованием восстановительного аминирования.
С151. Иммуногенная композиция по п. С150, дополнительно содержащая фармацевтически приемлемый эксципиент, носитель или разбавитель.
С152. Иммуногенная композиция по п. С150, отличающаяся тем, что сахарид представляет собой О-антиген, полученный из E. coli.
С153. Иммуногенная композиция по п. С150, отличающаяся тем, что сахарид имеет структуру, выбранную из: Формулы O1, Формулы O2, Формулы O3, Формулы O4, Формулы O5, Формулы O6, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O24, Формулы O25, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144,O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186 и Формулы O187, где n представляет собой целое число от 5 до 1000.
С154. Иммуногенная композиция по п. С150, отличающаяся тем, что сахарид имеет степень O-ацетилирования от 75 до 100%.
С155. Иммуногенная композиция по п. С150, отличающаяся тем, что белок-носитель представляет собой CRM197.
С156. Иммуногенная композиция по п. С150, дополнительно содержащая дополнительный антиген.
С157. Иммуногенная композиция по п. С150, дополнительно содержащая адъювант.
С158. Иммуногенная композиция по п. С157, отличающаяся тем, что адъювант представляет собой адъювант на основе алюминия, выбранный из группы, состоящей из фосфата алюминия, сульфата алюминия и гидроксида алюминия.
С159. Иммуногенная композиция по п. С150, отличающаяся тем, что композиция не содержит адъювант.
С160. Способ индукции иммунного ответа у субъекта, включающий введение субъекту композиции по любому из пп. С138-С159.
С161. Способ по п. С160, отличающийся тем, что иммунный ответ включает индукцию сывороточного антитела, специфичного к O-специфическому полисахариду E. coli.
С162. Способ по п. С135, отличающийся тем, что сывороточное антитело против O-специфического полисахарида E. coli представляет собой антитело IgG.
С163. Способ по п. С135, отличающийся тем, что сывороточное антитело против O-специфического полисахарида E. coli представляет собой антитело IgG, обладающее бактерицидной активностью против E. coli.
С164. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187, где n больше, чем число повторяющихся единиц в соответствующем полисахариде E. coli дикого типа.
С165. Композиция по п. С164, где n представляет собой целое число от 31 до 100.
С166. Композиция по п. С164, отличающаяся тем, что сахарид имеет структуру, соответствующую любой из Формулы O1A, Формулы O1B и Формулы O1C, Формулы O2, Формулы O6 и Формулы O25B.
С167. Композиция по п. С164, отличающаяся тем, что сахарид продуцируется в рекомбинантной клетке-хозяине, которая экспрессирует белок семейства wzz, имеющий по меньшей мере, 90% идентичность последовательности любой из SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38 и SEQ ID NO: 39.
С168. Композиция по п. С167, отличающаяся тем, что белок содержит любую из SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34.
С169. Сахарид по п. С164, отличающийся тем, что сахарид синтезирован синтетическим путем.
С170. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и конъюгат, содержащий белок-носитель, ковалентно связанный с сахаридом, где указанный сахарид имеет структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187, где n представляет собой целое число от 1 до 100.
С171. Композиция по п. С170, отличающаяся тем, что сахарид включает любую из следующих Формулы O25b, Формулы O1A, Формулы O2 и Формулы O6.
С172. Композиция по п. С170, отличающаяся тем, что сахарид дополнительно содержит любой из группы R1 E. coli, группы R2 E. coli, группы R3 E. coli, группы R4 E. coli и группы K-12 E. coli.
С173. Композиция по п. С170, отличающаяся тем, что сахарид дополнительно не содержит какой-либо из группы R1 E. coli, группы R2 E. coli, группы R3 E. coli, группы R4 E. coli и группы K-12 E. coli. Композиция по п. С170, отличающаяся тем, что сахарид дополнительно не содержит группу R2 E. coli.
С174. Композиция по п. С170, отличающаяся тем, что сахарид дополнительно содержит фрагмент 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO).
С175. Композиция по п. С170, отличающаяся тем, что белок-носитель выбран из любого из CRM197, группы B дифтерийного токсина (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C TT, коклюшного анатоксина, холерного анатоксина или экзотоксина А из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы холерного токсина B (CTB), пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni, природных гликопротеинов C. jejuni.
С176. Композиция по п. С170, отличающаяся тем, что белок-носитель представляет собой CRM197.
С177. Композиция по п. С170, отличающаяся тем, что белок-носитель представляет собой столбнячный анатоксин.
С178. Композиция по п. С170, отличающаяся тем, что отношение сахарида к белку составляет от, по меньшей мере, 0,5 до не более 2.
С179. Композиция по п. С170, отличающаяся тем, что конъюгат получен восстановительным аминированием.
С180. Композиция по п. С170, отличающаяся тем, что сахарид конъюгирован с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC).
С181. Композиция по п. С170, отличающаяся тем, что сахарид представляет собой односторонне-связанный конъюгированный сахарид.
С182. Композиция по п. С174, отличающаяся тем, что сахарид конъюгирован с белком-носителем через остаток 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO).
С183. Композиция по п. С170, отличающаяся тем, что конъюгат получают с помощью химии CDAP.
С184. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и (а) конъюгат, содержащий белок-носитель, ковалентно связанный с сахаридом, включающим Формулу O25b, где n представляет собой целое число от 31 до 90, (b) конъюгат, содержащий белок-носитель, ковалентно связанный с сахаридом, включающим Формулу O1A, где n представляет собой целое число от 31 до 90, (c) конъюгат, содержащий белок-носитель, ковалентно связанный с сахаридом, включающим Формулу O2, где n представляет собой целое число от 31 до 90, и (d) конъюгат, содержащий белок-носитель, ковалентно связанный с сахаридом, включающим Формулу O6, где n представляет собой целое число от 31 до 90.
С185. Композиция по п. С184, дополнительно содержащая конъюгат, содержащий белок-носитель, ковалентно связанный с сахаридом, имеющий структуру, выбранную из любой из следующих: Формулы O15, Формулы O16, Формулы O17, Формулы O18 и Формулы O75, где n представляет собой целое число от 31 до 90.
С186. Композиция по п. С184, содержащая не более 25% свободного сахарида по сравнению с общим количеством сахарида в композиции.
С187. Способ индукции иммунного ответа против Escherichia coli у млекопитающего, включающий введение млекопитающему эффективного количества композиции по любому из пп. С184-С186.
С188. Способ по п. С187, отличающийся тем, что иммунный ответ включает опсонофагоцитарные антитела против E. coli.
С189. Способ по п. С187, отличающийся тем, что иммунный ответ защищает млекопитающее от инфекции E. coli.
С190. Клетка млекопитающего, содержащая (а) первый представляющий интерес ген, кодирующий полипептид, полученный из E. coli, или его фрагмент, где ген интегрирован, по меньшей мере, между двумя сайтами-мишенями рекомбинации (RTS).
С191. Вариант осуществления по п. С190, отличающийся тем, что два RTS являются хромосомно интегрированными в локус NL1 или локус NL2.
С192. Вариант осуществления по п. С190, отличающийся тем, что первый представляющий интерес ген дополнительно содержит репортерный ген, ген, кодирующий трудно экспрессируемый белок, вспомогательный ген или их комбинацию.
С193. Вариант осуществления по п. С190, дополнительно содержащий второй представляющий интерес ген, интегрированный во второй хромосомный локус, отличный от локуса (a), где второй представляющий интерес ген содержит репортерный ген, ген, кодирующий трудно экспрессируемый белок, вспомогательный ген или их комбинацию.
С194. Рекомбинантная клетка млекопитающего, содержащая полинуклеотид, кодирующий полипептид, полученный из E. coli, или его фрагмент.
С195. Рекомбинантная клетка по С194, отличающаяся тем, что полипептид получен из фимбриального H E. coli (FimH).
С196. Рекомбинантная клетка по С195, отличающаяся тем, что полипептид содержит остаток фенилаланина на N-конце полипептида.
С197. Рекомбинантная клетка по С195, отличающаяся тем, что полипептид содержит остаток фенилаланина в пределах первых 20 положений остатков на N-конце.
С198. Рекомбинантная клетка по С195, отличающаяся тем, что полипептид содержит остаток фенилаланина в положении 1 полипептида.
С199. Рекомбинантная клетка по С198, отличающаяся тем, что полипептид не содержит глициновый остаток непосредственно перед фенилаланиновым остатком в положении 1 полипептида.
С200. Рекомбинантная клетка по С195, отличающаяся тем, что полипептид не содержит сайт N-гликозилирования в положении 7 полипептида.
С201. Рекомбинантная клетка по С199, где полипептид не содержит остаток Asn в положении 7 полипептида.
С202. Рекомбинантная клетка по C201, отличающаяся тем, что полипептид содержит остаток, выбранный из группы, состоящей из Ser, Asp, Thr и Gln в положении 7.
С203. Рекомбинантная клетка по С198, отличающаяся тем, что полипептид не содержит сайт N-гликозилирования в положении 70 полипептида.
С204. Рекомбинантная клетка по C203, отличающаяся тем, что полипептид не содержит остаток Asn в положении 70 полипептида.
С205. Рекомбинантная клетка по C203, где полипептид не содержит остаток Ser в положении 70 полипептида.
С206. Рекомбинантная клетка по C194, отличающаяся тем, что полипептид содержит замену остатка, выбранного из группы, состоящей из Ser, Asp, Thr и Gln в сайте N-гликозилирования полипептида.
С207. Рекомбинантная клетка по С206, где сайт N-гликозилирования содержит положение N235 полипептида.
С208. Рекомбинантная клетка по С206, где сайт N-гликозилирования содержит положение N228 полипептида.
С209. Рекомбинантная клетка по С206, отличающаяся тем, что сайт N-гликозилирования содержит положения N235 и положения N228 полипептида.
С210. Рекомбинантная клетка по C195, отличающаяся тем, что полипептид содержит SEQ ID NO: 3.
С211. Рекомбинантная клетка по C195, отличающаяся тем, что полипептид содержит SEQ ID NO: 2.
С212. Рекомбинантная клетка по С194, отличающаяся тем, что полипептид содержит алифатический гидрофобный аминокислотный остаток в положении 1 полипептида.
С213. Рекомбинантная клетка по C212, отличающаяся тем, что алифатический гидрофобный аминокислотный остаток выбран из группы, состоящей из Ile, Leu и Val.
С214. Рекомбинантная клетка по C194, где полипептид содержит фрагмент FimH.
С215. Рекомбинантная клетка по C214, отличающаяся тем, что полипептид содержит лектиновый домен FimH.
С216. Рекомбинантная клетка по C215, отличающаяся тем, что лектиновый домен имеет массу примерно 17022 дальтон.
С217. Рекомбинантная клетка по С194, где полипептид находится в комплексе с полипептидом FimC или его фрагментом.
С218. Рекомбинантная клетка по C217, отличающаяся тем, что полипептид FimC или его фрагмент содержит глициновый остаток в положении 37 полипептида FimC или его группы.
С219. Рекомбинантная клетка по С195, где полипептид находится в конформации с низким сродством.
С220. Рекомбинантная клетка по С195, отличающаяся тем, что полипептид стабилизирован с помощью FimG.
С221. Рекомбинантная клетка по C195, где полипептид стабилизирован пептидом донорной цепи FimG (DsG).
С222. Рекомбинантная клетка по C221, отличающаяся тем, что полинуклеотидная последовательность дополнительно кодирует линкерную последовательность.
С223. Рекомбинантная клетка по C222, отличающаяся тем, что линкер содержит, по меньшей мере, 4 аминокислотных остатка и не более 15 аминокислотных остатков.
С224. Рекомбинантная клетка по C222, отличающаяся тем, что линкер содержит, по меньшей мере, 5 аминокислотных остатков и не более 10 аминокислотных остатков.
С225. Рекомбинантная клетка по C222, отличающаяся тем, что линкер содержит 7 аминокислотных остатков.
С226. Рекомбинантная клетка по C194, отличающаяся тем, что полипептид не содержит сигнальный пептид, выбранный из группы, состоящей из нативного лидерного пептида FimH, сигнального пептида гемагглютинина гриппа и сигнального пептида слияния гликопротеина F0 респираторно-синцитиального вируса A (штамм A2) человека.
С227. Рекомбинантная клетка по C194, отличающаяся тем, что указанный полипептид содержит последовательность сигнального пептида IgK мыши.
С228. Рекомбинантная клетка по C194, отличающаяся тем, что полипептид содержит любую последовательность сигнального пептида, выбранную из сигнального пептида большой субъединицы p51 FcRn рецептора IgG человека и сигнального пептида белка IL10 человека.
С229. Рекомбинантная клетка по C195, отличающаяся тем, что полипептид содержит мутацию аргинина в пролин в положении аминокислоты 60 (R60P) в соответствии с нумерацией SEQ ID NO: 3.
С230. Рекомбинантная клетка по С194, отличающаяся тем, что уровень экспрессии полипептида превышает уровень экспрессии соответствующего полипептида дикого типа, экспрессируемого в периплазме клетки E.coli дикого типа.
С231. Рекомбинантная клетка по С194, отличающаяся тем, что уровень экспрессии полипептида превышает 10 мг/л.
С232. Рекомбинантная клетка по С194, отличающаяся тем, что полинуклеотидная последовательность интегрирована в геномную ДНК указанной клетки млекопитающего.
С233. Рекомбинантная клетка по C194, отличающаяся тем, что полинуклеотидная последовательность кодон-оптимизирована для экспрессии в клетке.
С234. Рекомбинантная клетка по С194, где клетка представляет собой клетку почки эмбриона человека.
С235. Рекомбинантная клетка по C234, отличающаяся тем, что клетка почки эмбриона человека содержит клетку HEK293.
С236. Рекомбинантная клетка по C235, отличающаяся тем, что клетка HEK293 выбрана из любой из клеток HEK293T, клеток HEK293TS и клеток HEK293E.
С237. Рекомбинантная клетка по С195, где клетка представляет собой клетку СНО.
С238. Рекомбинантная клетка по C237, где указанная клетка CHO представляет собой клетку CHO-K1, клетку CHO-DUXB11, CHO-DG44 или клетку CHO-S.
С239. Рекомбинантная клетка по С194, отличающаяся тем, что полипептид является растворимым.
С240. Рекомбинантная клетка по С194, где полипептид секретируется из клетки.
С241. Рекомбинантная клетка по C195, где полипептид содержит замену N28Q в соответствии с нумерацией SEQ ID NO: 1.
С242. Рекомбинантная клетка по C195, отличающаяся тем, что полипептид содержит замену N28D в соответствии с нумерацией SEQ ID NO: 1.
С243. Рекомбинантная клетка в соответствии с C195, где полипептид содержит замену N28S в соответствии с нумерацией SEQ ID NO: 1.
С244. Рекомбинантная клетка по C195, где полипептид содержит замену, выбранную из любой из N28Q, V48C и L55C, в соответствии с нумерацией SEQ ID NO: 1.
С245. Рекомбинантная клетка в соответствии с C195, где полипептид содержит замену N92S в соответствии с нумерацией SEQ ID NO: 1.
С246. Рекомбинантная клетка по C194, отличающаяся тем, что полипептид, полученный из FimH, или его фрагмент содержит замену, выбранную из любой из V48C и L55C, в соответствии с нумерацией SEQ ID NO: 1.
С247. Культура, содержащая рекомбинантную клетку по C194, где указанная культура имеет размер, по меньшей мере, 5 литров.
С248. Культура по С242, отличающаяся тем, что выход полипептида или его группы составляет, по меньшей мере, 0,05 г/л.
С249. Культура по С248, отличающаяся тем, что выход полипептида или его группы составляет, по меньшей мере, 0,10 г/л.
С250. Способ получения полипептида, полученного из E.coli, или его фрагмента, включающий культивирование рекомбинантной клетки млекопитающего по C194 в подходящих условиях, тем самым экспрессируя полипептид или его фрагмент; и сбор полипептида или его фрагмента.
С251. Способ по С250, дополнительно включающий очистку полипептида или его фрагмента.
С252. Способ по C250, отличающийся тем, что клетка содержит нуклеиновую кислоту, кодирующую любую из SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 27.
С253. Способ по С250, отличающийся тем, что выход полипептида или его фрагмента составляет, по меньшей мере, 0,05 г/л.
С254. Способ по С250, отличающийся тем, что выход полипептида или его группы составляет, по меньшей мере, 0,10 г/л.
С255. Композиция, содержащая полипептид, имеющий, по меньшей мере, 70% идентичность любой из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 20, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 28 и SEQ ID NO: 29.
С256. Композиция по C255, дополнительно содержащая сахарид, имеющий структуру, выбранную из любой Формулы в таблице 1.
С257. Композиция по C256, отличающаяся тем, что сахарид ковалентно связан с белком-носителем.
С258. Композиция по C257, отличающаяся тем, что белок-носитель выбран из любого из поли(L-лизина), CRM197, группы дифтерийного токсина B (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), группы C TT, коклюшного анатоксина, холерного анатоксина или экзотоксина A из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы B холерного токсина (CTB), пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni и природных гликопротеинов C. jejuni.
С259. Композиция по C257, отличающаяся тем, что белок-носитель представляет собой CRM197.
С260. Композиция по С257, отличающаяся тем, что белок-носитель представляет собой столбнячный анатоксин (ТТ).
С261. Композиция по C257, отличающаяся тем, что белок-носитель представляет собой поли(L-лизин).
С262. Композиция по C257, отличающаяся тем, что сахарид ковалентно связан с белком-носителем посредством восстановительного аминирования.
С263. Композиция по C257, отличающаяся тем, что сахарид ковалентно связан с белком-носителем с помощью CDAP химии.
С264. Композиция по C257, отличающаяся тем, что сахарид ковалентно связан с белком-носителем посредством односторонне-связанной конъюгации.
С265. Композиция по C257, отличающаяся тем, что сахарид ковалентно связан с белком-носителем через спейсер (2-((2-оксоэтил)тио)этил)карбамат (eTEC).
С266. Полипептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 27.
С267. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
С268. Композиция по п. C267, дополнительно содержащая, по меньшей мере, один сахарид, полученный из любого типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5.
С269. Композиция по п. C267, дополнительно содержащая сахарид, полученный из Klebsiella pneumoniae типа O1.
С270. Композиция по п. C267, дополнительно содержащая сахарид, полученный из K. pneumoniae типа O2.
С271. Композиция по п. C267, дополнительно содержащая сахарид, полученный из K. pneumoniae типа O3.
С272. Композиция по п. C267, дополнительно содержащая сахарид, полученный из K. pneumoniae типа O5.
С273. Композиция по п. C267, дополнительно содержащая сахарид, полученный из K. pneumoniae типа O1, и сахарид, полученный из K. pneumoniae типа O2.
С274. Композиция по п. C268, отличающаяся тем, что сахарид, полученный из K. pneumoniae, конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгирован с белком-носителем.
С275. Композиция по п. C267, дополнительно содержащая полипептид, полученный из K. pneumoniae.
С276. Композиция, содержащая полипептид, полученный из FimH, или его фрагмент; и, по меньшей мере, один сахарид, полученный из любого типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5.
С277. Композиция по п. C276, дополнительно содержащая по меньшей мере, один сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
С278. Композиция по п. C277, отличающаяся тем, что сахарид, полученный из K. pneumoniae, конъюгирован с белком-носителем; и сахарид, полученный из E. coli, конъюгирован с белком-носителем.
С279. Композиция по п. C277, дополнительно содержащая полипептид, полученный из K. pneumoniae.
С280. Композиция, содержащая по меньшей мере, один сахарид, полученный из любого типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5; и, по меньшей мере, один сахарид, имеющий структуру, выбранную из Формулы O1, Формулы O1A, Формулы O1B, Формулы O1C, Формулы O2, Формулы O3, Формулы O4, Формулы O4:K52, Формулы O4:K6, Формулы O5, Формулы O5ab, Формулы O5ac, Формулы O6, Формулы O6:K2; K13; K15, Формулы O6:K54, Формулы O7, Формулы O8, Формулы O9, Формулы O10, Формулы O11, Формулы O12, Формулы O13, Формулы O14, Формулы O15, Формулы O16, Формулы O17, Формулы O18, Формулы O18A, Формулы O18ac, Формулы O18A1, Формулы O18B, Формулы O18B1, Формулы O19, Формулы O20, Формулы O21, Формулы O22, Формулы O23, Формулы O23A, Формулы O24, Формулы O25, Формулы O25a, Формулы O25b, Формулы O26, Формулы O27, Формулы O28, Формулы O29, Формулы O30, Формулы O32, Формулы O33, Формулы O34, Формулы O35, Формулы O36, Формулы O37, Формулы O38, Формулы O39, Формулы O40, Формулы O41, Формулы O42, Формулы O43, Формулы O44, Формулы O45, Формулы O45, Формулы O45rel, Формулы O46, Формулы O48, Формулы O49, Формулы O50, Формулы O51, Формулы O52, Формулы O53, Формулы O54, Формулы O55, Формулы O56, Формулы O57, Формулы O58, Формулы O59, Формулы O60, Формулы O61, Формулы O62, Формулы 62D1, Формулы O63, Формулы O64, Формулы O65, Формулы O66, Формулы O68, Формулы O69, Формулы O70, Формулы O71, Формулы O73, Формулы O73, Формулы O74, Формулы O75, Формулы O76, Формулы O77, Формулы O78, Формулы O79, Формулы O80, Формулы O81, Формулы O82, Формулы O83, Формулы O84, Формулы O85, Формулы O86, Формулы O87, Формулы O88, Формулы O89, Формулы O90, Формулы O91, Формулы O92, Формулы O93, Формулы O95, Формулы O96, Формулы O97, Формулы O98, Формулы O99, Формулы O100, Формулы O101, Формулы O102, Формулы O103, Формулы O104, Формулы O105, Формулы O106, Формулы O107, Формулы O108, Формулы O109, Формулы O110, Формулы 0111, Формулы O112, Формулы O113, Формулы O114, Формулы O115, Формулы O116, Формулы O117, Формулы O118, Формулы O119, Формулы O120, Формулы O121, Формулы O123, Формулы O124, Формулы O125, Формулы O126, Формулы O127, Формулы O128, Формулы O129, Формулы O130, Формулы O131, Формулы O132, Формулы O133, Формулы O134, Формулы O135, Формулы O136, Формулы O137, Формулы O138, Формулы O139, Формулы O140, Формулы O141, Формулы O142, Формулы O143, Формулы O144, Формулы O145, Формулы O146, Формулы O147, Формулы O148, Формулы O149, Формулы O150, Формулы O151, Формулы O152, Формулы O153, Формулы O154, Формулы O155, Формулы O156, Формулы O157, Формулы O158, Формулы O159, Формулы O160, Формулы O161, Формулы O162, Формулы O163, Формулы O164, Формулы O165, Формулы O166, Формулы O167, Формулы O168, Формулы O169, Формулы O170, Формулы O171, Формулы O172, Формулы O173, Формулы O174, Формулы O175, Формулы O176, Формулы O177, Формулы O178, Формулы O179, Формулы O180, Формулы O181, Формулы O182, Формулы O183, Формулы O184, Формулы O185, Формулы O186, Формулы O187.
С281. Композиция по п. C280, дополнительно содержащая полипептид, полученный из FimH, или его фрагмент.
С282. Композиция по п. C280, отличающаяся тем, что сахарид E. coli содержит Формулу O8.
С283. Композиция по п. C280, отличающаяся тем, что сахарид E. coli содержит Формулу O9.
С284. Композиция по п. C280, дополнительно содержащая полипептид, полученный из K. pneumoniae.
С285. Композиция по любому из пп. C267-C284, отличающаяся тем, что сахарид ковалентно связан с белком-носителем.
С286. Композиция по п. C285, отличающаяся тем, что сахарид дополнительно содержит группу 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO).
С2987. Композиция по п. C285, отличающаяся тем, что сахарид содержит липид А.
С288. Композиция по любому из пп. C285-C287, отличающаяся тем, что сахарид синтезирован синтетическим путем.
С289. Композиция по п. C285, отличающаяся тем, что белок-носитель выбран из любого из CRM197, группы B дифтерийного токсина (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C TT, коклюшного анатоксина, холерного анатоксина или экзотоксина А из Pseudomonas aeruginosa; детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы холерного токсина B (CTB), пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni, природных гликопротеинов C. jejuni и стрептококковой пептидазы C5a (SCP).
С290. Способ индукции иммунного ответа против Escherichia coli у млекопитающего, включающий введение млекопитающему эффективного количества композиции по любому из пп. C267-C289.
С291. Способ по п. C290, отличающийся тем, что иммунный ответ включает опсонофагоцитарные антитела против E. coli.
С292. Способ по п. C290, отличающийся тем, что иммунный ответ защищает млекопитающее от инфекции E. coli.
С293. Способ индукции иммунного ответа против Klebsiella pneumoniae у млекопитающего, включающий введение млекопитающему эффективного количества композиции по любому из пп. C267-C289.
С294. Способ по п. C293, отличающийся тем, что иммунный ответ включает опсонофагоцитарные антитела против Klebsiella pneumoniae.
С295. Способ по п. C293, отличающийся тем, что иммунный ответ защищает млекопитающее от инфекции Klebsiella pneumoniae.
С296. Композиции и способы по любому из пп. C1-C266, дополнительно содержащие, по меньшей мере, один сахарид, полученный из любого одного типа K. pneumoniae, выбранного из группы, состоящей из O1, O2, O3 и O5.
С297. Композиции и способы по п. C296, отличающиеся тем, что K. pneumoniae типа O1 содержит вариант O1V1 или O1V2.
С298. Композиции и способы по п. C296, отличающиеся тем, что K. pneumoniae типа O2 содержит вариант O2V1 или O2V2.
С299. Использование композиций, указанных в любом из пп. C1-C298, как указано в настоящем документе.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Pfizer Inc.
Donald, Robert G.K.
<120> КОМПОЗИЦИИ ESCHERICHIA COLI И СПОСОБЫ НА ИХ ОСНОВЕ
<130> PC072591A
<160> 109
<170> PatentIn version 3.5
<210> 1
<211> 300
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 1
Met Lys Arg Val Ile Thr Leu Phe Ala Val Leu Leu Met Gly Trp Ser
1 5 10 15
Val Asn Ala Trp Ser Phe Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile
20 25 30
Pro Ile Gly Gly Gly Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val
35 40 45
Val Asn Val Gly Gln Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe
50 55 60
Cys His Asn Asp Tyr Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln
65 70 75 80
Arg Gly Ser Ala Tyr Gly Gly Val Leu Ser Asn Phe Ser Gly Thr Val
85 90 95
Lys Tyr Ser Gly Ser Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro
100 105 110
Arg Val Val Tyr Asn Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu
115 120 125
Tyr Leu Thr Pro Val Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly
130 135 140
Ser Leu Ile Ala Val Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser
145 150 155 160
Asp Asp Phe Gln Phe Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val
165 170 175
Val Pro Thr Gly Gly Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr
180 185 190
Leu Pro Asp Tyr Pro Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys
195 200 205
Ala Lys Ser Gln Asn Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp
210 215 220
Ala Gly Asn Ser Ile Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln
225 230 235 240
Gly Val Gly Val Gln Leu Thr Arg Asn Gly Thr Ile Ile Pro Ala Asn
245 250 255
Asn Thr Val Ser Leu Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly
260 265 270
Leu Thr Ala Asn Tyr Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn
275 280 285
Val Gln Ser Ile Ile Gly Val Thr Phe Val Tyr Gln
290 295 300
<210> 2
<211> 279
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 2
Phe Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val Gly Gln
20 25 30
Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Asn Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu Pro Asp Tyr Pro
165 170 175
Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala Lys Ser Gln Asn
180 185 190
Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala Gly Asn Ser Ile
195 200 205
Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly Val Gly Val Gln
210 215 220
Leu Thr Arg Asn Gly Thr Ile Ile Pro Ala Asn Asn Thr Val Ser Leu
225 230 235 240
Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu Thr Ala Asn Tyr
245 250 255
Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val Gln Ser Ile Ile
260 265 270
Gly Val Thr Phe Val Tyr Gln
275
<210> 3
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 3
Phe Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val Gly Gln
20 25 30
Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Asn Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val
145 150 155
<210> 4
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 4
Gly Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu Pro Asp Tyr
1 5 10 15
Pro Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala Lys Ser Gln
20 25 30
Asn Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala Gly Asn Ser
35 40 45
Ile Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly Val Gly Val
50 55 60
Gln Leu Thr Arg Asn Gly Thr Ile Ile Pro Ala Asn Asn Thr Val Ser
65 70 75 80
Leu Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu Thr Ala Asn
85 90 95
Tyr Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val Gln Ser Ile
100 105 110
Ile Gly Val Thr Phe Val Tyr Gln
115 120
<210> 5
<211> 330
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 5
Val Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro
20 25 30
Ile Gly Gly Gly Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Cys Val
35 40 45
Asn Val Gly Gln Asn Cys Val Val Asp Leu Ser Thr Gln Ile Phe Cys
50 55 60
His Asn Asp Tyr Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg
65 70 75 80
Gly Ser Ala Tyr Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys
85 90 95
Tyr Ser Gly Ser Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg
100 105 110
Val Val Tyr Asn Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr
115 120 125
Leu Thr Pro Val Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser
130 135 140
Leu Ile Ala Val Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp
145 150 155 160
Asp Phe Gln Phe Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val
165 170 175
Pro Thr Gly Gly Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu
180 185 190
Pro Asp Tyr Pro Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala
195 200 205
Lys Ser Gln Asn Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala
210 215 220
Gly Asn Ser Ile Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly
225 230 235 240
Val Gly Val Gln Leu Thr Arg Gln Gly Thr Ile Ile Pro Ala Asn Asn
245 250 255
Thr Val Ser Leu Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu
260 265 270
Thr Ala Asn Tyr Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val
275 280 285
Gln Ser Ile Ile Gly Val Thr Phe Val Tyr Gln Gly Gly Ser Ser Gly
290 295 300
Gly Gly Ala Asp Val Thr Ile Thr Val Asn Gly Lys Val Val Ala Lys
305 310 315 320
Gly Gly His His His His His His His His
325 330
<210> 6
<211> 330
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 6
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro
20 25 30
Ile Gly Gly Gly Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val
35 40 45
Asn Val Gly Gln Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys
50 55 60
His Asn Asp Tyr Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg
65 70 75 80
Gly Ser Ala Tyr Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys
85 90 95
Tyr Ser Gly Ser Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg
100 105 110
Val Val Tyr Asn Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr
115 120 125
Leu Thr Pro Val Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser
130 135 140
Leu Ile Ala Val Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp
145 150 155 160
Asp Phe Gln Phe Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val
165 170 175
Pro Thr Gly Gly Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu
180 185 190
Pro Asp Tyr Pro Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala
195 200 205
Lys Ser Gln Asn Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala
210 215 220
Gly Asn Ser Ile Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly
225 230 235 240
Val Gly Val Gln Leu Thr Arg Gln Gly Thr Ile Ile Pro Ala Asn Asn
245 250 255
Thr Val Ser Leu Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu
260 265 270
Thr Ala Asn Tyr Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val
275 280 285
Gln Ser Ile Ile Gly Val Thr Phe Val Tyr Gln Gly Gly Ser Ser Gly
290 295 300
Gly Gly Ala Asp Val Thr Ile Thr Val Asn Gly Lys Val Val Ala Lys
305 310 315 320
Gly Gly His His His His His His His His
325 330
<210> 7
<211> 188
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 7
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro
20 25 30
Ile Gly Gly Gly Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val
35 40 45
Asn Val Gly Gln Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys
50 55 60
His Asn Asp Tyr Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg
65 70 75 80
Gly Ser Ala Tyr Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys
85 90 95
Tyr Ser Gly Ser Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg
100 105 110
Val Val Tyr Asn Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr
115 120 125
Leu Thr Pro Val Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser
130 135 140
Leu Ile Ala Val Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp
145 150 155 160
Asp Phe Gln Phe Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val
165 170 175
Pro Thr Gly Gly His His His His His His His His
180 185
<210> 8
<211> 188
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 8
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro
20 25 30
Ile Gly Gly Gly Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Cys Val
35 40 45
Asn Val Gly Gln Asn Cys Val Val Asp Leu Ser Thr Gln Ile Phe Cys
50 55 60
His Asn Asp Tyr Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg
65 70 75 80
Gly Ser Ala Tyr Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys
85 90 95
Tyr Ser Gly Ser Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg
100 105 110
Val Val Tyr Asn Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr
115 120 125
Leu Thr Pro Val Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser
130 135 140
Leu Ile Ala Val Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp
145 150 155 160
Asp Phe Gln Phe Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val
165 170 175
Pro Thr Gly Gly His His His His His His His His
180 185
<210> 9
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 9
Ala Asp Val Thr Ile Thr Val Asn Gly Lys Val Val Ala Lys
1 5 10
<210> 10
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 10
Met Ser Asn Lys Asn Val Asn Val Arg Lys Ser Gln Glu Ile Thr Phe
1 5 10 15
Cys Leu Leu Ala Gly Ile Leu Met Phe Met Ala Met Met Val Ala Gly
20 25 30
Arg Ala Glu Ala Gly Val Ala Leu Gly Ala Thr Arg Val Ile Tyr Pro
35 40 45
Ala Gly Gln Lys Gln Val Gln Leu Ala Val Thr Asn Asn Asp Glu Asn
50 55 60
Ser Thr Tyr Leu Ile Gln Ser Trp Val Glu Asn Ala Asp Gly Val Lys
65 70 75 80
Asp Gly Arg Phe Ile Val Thr Pro Pro Leu Phe Ala Met Lys Gly Lys
85 90 95
Lys Glu Asn Thr Leu Arg Ile Leu Asp Ala Thr Asn Asn Gln Leu Pro
100 105 110
Gln Asp Arg Glu Ser Leu Phe Trp Met Asn Val Lys Ala Ile Pro Ser
115 120 125
Met Asp Lys Ser Lys Leu Thr Glu Asn Thr Leu Gln Leu Ala Ile Ile
130 135 140
Ser Arg Ile Lys Leu Tyr Tyr Arg Pro Ala Lys Leu Ala Leu Pro Pro
145 150 155 160
Asp Gln Ala Ala Glu Lys Leu Arg Phe Arg Arg Ser Ala Asn Ser Leu
165 170 175
Thr Leu Ile Asn Pro Thr Pro Tyr Tyr Leu Thr Val Thr Glu Leu Asn
180 185 190
Ala Gly Thr Arg Val Leu Glu Asn Ala Leu Val Pro Pro Met Gly Glu
195 200 205
Ser Thr Val Lys Leu Pro Ser Asp Ala Gly Ser Asn Ile Thr Tyr Arg
210 215 220
Thr Ile Asn Asp Tyr Gly Ala Leu Thr Pro Lys Met Thr Gly Val Met
225 230 235 240
Glu
<210> 11
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 11
Asp Asn Lys Gln
1
<210> 12
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 12
Gly Gly Ser Gly Gly
1 5
<210> 13
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 13
Gly Gly Ser Ser Gly Gly
1 5
<210> 14
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 14
Gly Gly Ser Ser Gly Gly Gly
1 5
<210> 15
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 15
Gly Gly Gly Ser Ser Gly Gly Gly
1 5
<210> 16
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 16
Gly Gly Gly Ser Gly Ser Gly Gly Gly
1 5
<210> 17
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 17
Gly Gly Gly Ser Gly Gly Ser Gly Gly Gly
1 5 10
<210> 18
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 18
Met Lys Arg Val Ile Thr Leu Phe Ala Val Leu Leu Met Gly Trp Ser
1 5 10 15
Val Asn Ala Trp Ser
20
<210> 19
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 19
Val Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly
20
<210> 20
<211> 279
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 20
Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Cys Val Asn Val Gly Gln
20 25 30
Asn Cys Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu Pro Asp Tyr Pro
165 170 175
Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala Lys Ser Gln Asn
180 185 190
Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala Gly Asn Ser Ile
195 200 205
Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly Val Gly Val Gln
210 215 220
Leu Thr Arg Gln Gly Thr Ile Ile Pro Ala Asn Asn Thr Val Ser Leu
225 230 235 240
Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu Thr Ala Asn Tyr
245 250 255
Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val Gln Ser Ile Ile
260 265 270
Gly Val Thr Phe Val Tyr Gln
275
<210> 21
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 21
Ala Asp Val Thr Ile Thr Val Asn Gly Lys Val Val Ala Lys Gly Gly
1 5 10 15
His His His His His His His His
20
<210> 22
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 22
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly
20
<210> 23
<211> 279
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 23
Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val Gly Gln
20 25 30
Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu Pro Asp Tyr Pro
165 170 175
Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala Lys Ser Gln Asn
180 185 190
Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala Gly Asn Ser Ile
195 200 205
Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly Val Gly Val Gln
210 215 220
Leu Thr Arg Gln Gly Thr Ile Ile Pro Ala Asn Asn Thr Val Ser Leu
225 230 235 240
Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu Thr Ala Asn Tyr
245 250 255
Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val Gln Ser Ile Ile
260 265 270
Gly Val Thr Phe Val Tyr Gln
275
<210> 24
<211> 160
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 24
Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val Gly Gln
20 25 30
Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
<210> 25
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 25
His His His His His His His His
1 5
<210> 26
<211> 160
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 26
Phe Ala Cys Lys Thr Ala Ser Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Cys Val Asn Val Gly Gln
20 25 30
Asn Cys Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
<210> 27
<211> 168
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 27
Phe Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val Gly Gln
20 25 30
Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Asn Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
His His His His His His His His
165
<210> 28
<211> 279
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 28
Phe Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val Gly Gln
20 25 30
Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ser Ala Tyr
50 55 60
Gly Gly Val Leu Ser Asn Phe Ser Gly Thr Val Lys Tyr Ser Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu Pro Asp Tyr Pro
165 170 175
Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala Lys Ser Gln Asn
180 185 190
Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala Gly Asn Ser Ile
195 200 205
Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly Val Gly Val Gln
210 215 220
Leu Thr Arg Asn Gly Thr Ile Ile Pro Ala Asn Asn Thr Val Ser Leu
225 230 235 240
Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu Thr Ala Asn Tyr
245 250 255
Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val Gln Ser Ile Ile
260 265 270
Gly Val Thr Phe Val Tyr Gln
275
<210> 29
<211> 279
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 29
Phe Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile Pro Ile Gly Gly Gly
1 5 10 15
Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Ala Val Asn Val Gly Gln
20 25 30
Asn Leu Val Val Asp Leu Ser Thr Gln Ile Phe Cys His Asn Asp Tyr
35 40 45
Pro Glu Thr Ile Thr Asp Tyr Val Thr Leu Gln Arg Gly Ala Ala Tyr
50 55 60
Gly Gly Val Leu Ser Ser Phe Ser Gly Thr Val Lys Tyr Asn Gly Ser
65 70 75 80
Ser Tyr Pro Phe Pro Thr Thr Ser Glu Thr Pro Arg Val Val Tyr Asn
85 90 95
Ser Arg Thr Asp Lys Pro Trp Pro Val Ala Leu Tyr Leu Thr Pro Val
100 105 110
Ser Ser Ala Gly Gly Val Ala Ile Lys Ala Gly Ser Leu Ile Ala Val
115 120 125
Leu Ile Leu Arg Gln Thr Asn Asn Tyr Asn Ser Asp Asp Phe Gln Phe
130 135 140
Val Trp Asn Ile Tyr Ala Asn Asn Asp Val Val Val Pro Thr Gly Gly
145 150 155 160
Cys Asp Val Ser Ala Arg Asp Val Thr Val Thr Leu Pro Asp Tyr Pro
165 170 175
Gly Ser Val Pro Ile Pro Leu Thr Val Tyr Cys Ala Lys Ser Gln Asn
180 185 190
Leu Gly Tyr Tyr Leu Ser Gly Thr Thr Ala Asp Ala Gly Asn Ser Ile
195 200 205
Phe Thr Asn Thr Ala Ser Phe Ser Pro Ala Gln Gly Val Gly Val Gln
210 215 220
Leu Thr Arg Asn Gly Thr Ile Ile Pro Ala Asn Asn Thr Val Ser Leu
225 230 235 240
Gly Ala Val Gly Thr Ser Ala Val Ser Leu Gly Leu Thr Ala Asn Tyr
245 250 255
Ala Arg Thr Gly Gly Gln Val Thr Ala Gly Asn Val Gln Ser Ile Ile
260 265 270
Gly Val Thr Phe Val Tyr Gln
275
<210> 30
<211> 325
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 30
Met Arg Val Glu Asn Asn Asn Val Ser Gly Gln Asn His Asp Pro Glu
1 5 10 15
Gln Ile Asp Leu Ile Asp Leu Leu Val Gln Leu Trp Arg Gly Lys Met
20 25 30
Thr Ile Ile Ile Ser Val Ile Val Ala Ile Ala Leu Ala Ile Gly Tyr
35 40 45
Leu Ala Val Ala Lys Glu Lys Trp Thr Ser Thr Ala Ile Ile Thr Gln
50 55 60
Pro Asp Val Gly Gln Ile Ala Gly Tyr Asn Asn Ala Met Asn Val Ile
65 70 75 80
Tyr Gly Gln Ala Ala Pro Lys Val Ser Asp Leu Gln Glu Thr Leu Ile
85 90 95
Gly Arg Phe Ser Ser Ala Phe Ser Ala Leu Ala Glu Thr Leu Asp Asn
100 105 110
Gln Glu Glu Pro Glu Lys Leu Thr Ile Glu Pro Ser Val Lys Asn Gln
115 120 125
Gln Leu Pro Leu Thr Val Ser Tyr Val Gly Gln Thr Ala Glu Gly Ala
130 135 140
Gln Met Lys Leu Ala Gln Tyr Ile Gln Gln Val Asp Asp Lys Val Asn
145 150 155 160
Gln Glu Leu Glu Lys Asp Leu Lys Asp Asn Ile Ala Leu Gly Arg Lys
165 170 175
Asn Leu Gln Asp Ser Leu Arg Thr Gln Glu Val Val Ala Gln Glu Gln
180 185 190
Lys Asp Leu Arg Ile Arg Gln Ile Gln Glu Ala Leu Gln Tyr Ala Asn
195 200 205
Gln Glu Gln Val Thr Lys Pro Gln Val Gln Gln Thr Glu Asp Val Thr
210 215 220
Gln Asp Thr Leu Phe Leu Leu Gly Ser Glu Ala Leu Glu Ser Met Ile
225 230 235 240
Lys His Glu Ala Thr Arg Pro Leu Val Phe Ser Ser Asn Tyr Tyr Gln
245 250 255
Thr Arg Gln Asn Leu Leu Asp Ile Glu Ser Leu Lys Val Asp Asp Leu
260 265 270
Asp Ile His Ala Tyr Arg Tyr Val Met Lys Pro Thr Leu Pro Ile Arg
275 280 285
Arg Asp Ser Pro Lys Lys Ala Ile Thr Leu Ile Leu Ala Val Leu Leu
290 295 300
Gly Gly Met Val Gly Ala Gly Ile Val Leu Gly Arg Asn Ala Leu Arg
305 310 315 320
Asn Tyr Asn Ala Lys
325
<210> 31
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 31
Met Arg Val Glu Asn Asn Asn Val Ser Gly Gln Asn Asn Asp Pro Glu
1 5 10 15
Gln Ile Asp Leu Ile Asp Leu Leu Val Gln Leu Trp Arg Gly Lys Met
20 25 30
Thr Ile Ile Ile Ser Val Ile Val Ala Ile Ala Leu Ala Ile Gly Tyr
35 40 45
Leu Ala Val Ala Lys Glu Lys Trp Thr Ser Thr Ala Ile Ile Thr Gln
50 55 60
Pro Asp Val Gly Gln Ile Ala Gly Tyr Asn Asn Ala Met Asn Val Ile
65 70 75 80
Tyr Gly Gln Ala Ala Pro Lys Val Ser Asp Leu Gln Glu Thr Leu Ile
85 90 95
Gly Arg Phe Ser Ser Ala Phe Ser Ala Leu Ala Glu Thr Leu Asp Asn
100 105 110
Gln Asp Glu Pro Glu Lys Leu Thr Ile Glu Pro Ser Val Lys Asn Gln
115 120 125
Gln Leu Pro Leu Thr Val Ser Tyr Val Gly Gln Thr Ala Glu Gly Ala
130 135 140
Gln Met Lys Leu Ala Gln Tyr Ile Gln Gln Val Asp Asp Lys Val Asn
145 150 155 160
Gln Glu Leu Glu Lys Asp Leu Lys Asp Asn Ile Ala Leu Gly Arg Lys
165 170 175
Asn Leu Gln Asp Ser Leu Arg Thr Gln Glu Val Val Ala Gln Glu Gln
180 185 190
Lys Asp Leu Arg Ile Arg Gln Ile Gln Glu Ala Leu Gln Tyr Ala Asn
195 200 205
Gln Ala Gln Val Thr Lys Pro Gln Ile Gln Gln Thr Gly Glu Asp Ile
210 215 220
Thr Gln Asp Thr Leu Phe Leu Leu Gly Ser Glu Ala Leu Glu Ser Met
225 230 235 240
Ile Lys His Glu Ala Thr Arg Pro Leu Val Phe Ser Pro Asn Tyr Tyr
245 250 255
Gln Thr Arg Gln Asn Leu Leu Asp Ile Glu Ser Leu Lys Val Asp Asp
260 265 270
Leu Asp Ile His Ala Tyr Arg Tyr Val Met Lys Pro Thr Leu Pro Ile
275 280 285
Arg Arg Asp Ser Pro Lys Lys Ala Ile Thr Leu Ile Leu Ala Val Leu
290 295 300
Leu Gly Gly Met Val Gly Ala Gly Ile Val Leu Gly Arg Asn Ala Leu
305 310 315 320
Arg Asn Tyr Asn Ala Lys
325
<210> 32
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 32
Met Arg Val Glu Asn Asn Asn Val Ser Gly Gln Asn His Asp Pro Glu
1 5 10 15
Gln Ile Asp Leu Ile Asp Leu Leu Val Gln Leu Trp Arg Gly Lys Met
20 25 30
Thr Ile Ile Ile Ser Val Val Val Ala Ile Ala Leu Ala Ile Gly Tyr
35 40 45
Leu Ala Val Ala Lys Glu Lys Trp Thr Ser Thr Ala Ile Ile Thr Gln
50 55 60
Pro Asp Val Gly Gln Ile Ala Gly Tyr Asn Asn Ala Met Asn Val Ile
65 70 75 80
Tyr Gly Gln Ala Ala Pro Lys Val Ser Asp Leu Gln Glu Thr Leu Ile
85 90 95
Gly Arg Phe Ser Phe Ala Phe Ser Ala Leu Ala Glu Thr Leu Asp Asn
100 105 110
Gln Lys Glu Pro Glu Lys Leu Thr Ile Glu Pro Ser Val Lys Asn Gln
115 120 125
Gln Leu Pro Leu Thr Val Ser Tyr Val Gly Gln Thr Ala Glu Asp Ala
130 135 140
Gln Met Lys Leu Ala Gln Tyr Ile Gln Gln Val Asp Asp Lys Val Asn
145 150 155 160
Gln Glu Leu Glu Lys Asp Leu Lys Asp Asn Leu Ala Leu Gly Arg Lys
165 170 175
Asn Leu Gln Asp Ser Leu Arg Thr Gln Glu Val Val Ala Gln Glu Gln
180 185 190
Lys Asp Leu Arg Ile Arg Gln Ile Gln Glu Ala Leu Gln Tyr Ala Asn
195 200 205
Gln Ala Gln Val Thr Lys Pro Gln Ile Gln Gln Thr Gly Glu Asp Ile
210 215 220
Thr Gln Asp Thr Leu Phe Leu Leu Gly Ser Glu Ala Leu Glu Ser Met
225 230 235 240
Ile Lys His Glu Ala Thr Arg Pro Leu Val Phe Ser Pro Asn Tyr Tyr
245 250 255
Gln Thr Arg Gln Asn Leu Leu Asp Ile Glu Asn Leu Lys Val Asp Asp
260 265 270
Leu Asp Ile His Ala Tyr Arg Tyr Val Met Lys Pro Thr Leu Pro Ile
275 280 285
Arg Arg Asp Ser Pro Lys Lys Ala Ile Thr Leu Ile Leu Ala Val Leu
290 295 300
Leu Gly Gly Met Val Gly Ala Gly Ile Val Leu Gly Arg Asn Ala Leu
305 310 315 320
Arg Asn Tyr Asn Ser Lys
325
<210> 33
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 33
Met Arg Val Glu Asn Asn Asn Val Ser Gly Gln Asn His Asp Pro Glu
1 5 10 15
Gln Ile Asp Leu Ile Asp Leu Leu Val Gln Leu Trp Arg Gly Lys Met
20 25 30
Thr Ile Ile Ile Ser Val Ile Val Ala Ile Ala Leu Ala Ile Gly Tyr
35 40 45
Leu Ala Val Ala Lys Glu Lys Trp Thr Ser Thr Ala Ile Ile Thr Gln
50 55 60
Pro Asp Val Gly Gln Ile Ala Gly Tyr Asn Asn Ala Met Asn Val Ile
65 70 75 80
Tyr Gly Gln Ala Ala Pro Lys Val Ser Asp Leu Gln Glu Thr Leu Ile
85 90 95
Gly Arg Phe Ser Ser Ala Phe Ser Ala Leu Ala Glu Thr Leu Asp Asn
100 105 110
Gln Glu Glu Arg Glu Lys Leu Thr Ile Glu Pro Ser Val Lys Asn Gln
115 120 125
Gln Leu Pro Leu Thr Val Ser Tyr Val Gly Gln Thr Ala Glu Gly Ala
130 135 140
Gln Met Lys Leu Ala Gln Tyr Ile Gln Gln Val Asp Asp Lys Val Asn
145 150 155 160
Gln Glu Leu Glu Lys Asp Leu Lys Asp Asn Ile Ala Leu Gly Arg Lys
165 170 175
Asn Leu Gln Asp Ser Leu Arg Thr Gln Glu Val Val Ala Gln Glu Gln
180 185 190
Lys Asp Leu Arg Ile Arg Gln Ile Gln Glu Ala Leu Gln Tyr Ala Asn
195 200 205
Gln Ala Gln Val Thr Lys Pro Gln Ile Gln Gln Thr Gly Glu Asp Ile
210 215 220
Thr Gln Asp Thr Leu Phe Leu Leu Gly Ser Glu Ala Leu Glu Ser Met
225 230 235 240
Ile Lys His Glu Ala Thr Arg Pro Leu Val Phe Ser Pro Asn Tyr Tyr
245 250 255
Gln Thr Arg Gln Asn Leu Leu Asp Ile Glu Ser Leu Lys Val Asp Asp
260 265 270
Leu Asp Ile His Ala Tyr Arg Tyr Val Met Lys Pro Met Leu Pro Ile
275 280 285
Arg Arg Asp Ser Pro Lys Lys Ala Ile Thr Leu Ile Leu Ala Val Leu
290 295 300
Leu Gly Gly Met Val Gly Ala Gly Ile Val Leu Gly Arg Asn Ala Leu
305 310 315 320
Arg Asn Tyr Asn Ala Lys
325
<210> 34
<211> 327
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 34
Met Thr Val Asp Ser Asn Thr Ser Ser Gly Arg Gly Asn Asp Pro Glu
1 5 10 15
Gln Ile Asp Leu Ile Glu Leu Leu Leu Gln Leu Trp Arg Gly Lys Met
20 25 30
Thr Ile Ile Val Ala Val Ile Ile Ala Ile Leu Leu Ala Val Gly Tyr
35 40 45
Leu Met Ile Ala Lys Glu Lys Trp Thr Ser Thr Ala Ile Ile Thr Gln
50 55 60
Pro Asp Ala Ala Gln Val Ala Thr Tyr Thr Asn Ala Leu Asn Val Leu
65 70 75 80
Tyr Gly Gly Asn Ala Pro Lys Ile Ser Glu Val Gln Ala Asn Phe Ile
85 90 95
Ser Arg Phe Ser Ser Ala Phe Ser Ala Leu Ser Glu Val Leu Asp Asn
100 105 110
Gln Lys Glu Arg Glu Lys Leu Thr Ile Glu Gln Ser Val Lys Gly Gln
115 120 125
Ala Leu Pro Leu Ser Val Ser Tyr Val Ser Thr Thr Ala Glu Gly Ala
130 135 140
Gln Arg Arg Leu Ala Glu Tyr Ile Gln Gln Val Asp Glu Glu Val Ala
145 150 155 160
Lys Glu Leu Glu Val Asp Leu Lys Asp Asn Ile Thr Leu Gln Thr Lys
165 170 175
Thr Leu Gln Glu Ser Leu Glu Thr Gln Glu Val Val Ala Gln Glu Gln
180 185 190
Lys Asp Leu Arg Ile Lys Gln Ile Glu Glu Ala Leu Arg Tyr Ala Asp
195 200 205
Glu Ala Lys Ile Thr Gln Pro Gln Ile Gln Gln Thr Gln Asp Val Thr
210 215 220
Gln Asp Thr Met Phe Leu Leu Gly Ser Asp Ala Leu Lys Ser Met Ile
225 230 235 240
Gln Asn Glu Ala Thr Arg Pro Leu Val Phe Ser Pro Ala Tyr Tyr Gln
245 250 255
Thr Lys Gln Thr Leu Leu Asp Ile Lys Asn Leu Lys Val Thr Ala Asp
260 265 270
Thr Val His Val Tyr Arg Tyr Val Met Lys Pro Thr Leu Pro Val Arg
275 280 285
Arg Asp Ser Pro Lys Thr Ala Ile Thr Leu Val Leu Ala Val Leu Leu
290 295 300
Gly Gly Met Ile Gly Ala Gly Ile Val Leu Gly Arg Asn Ala Leu Arg
305 310 315 320
Ser Tyr Lys Pro Lys Ala Leu
325
<210> 35
<211> 377
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 35
Met Ser Ser Leu Asn Ile Lys Gln Gly Ser Asp Ala His Phe Pro Asp
1 5 10 15
Tyr Pro Leu Ala Ser Pro Ser Asn Asn Glu Ile Asp Leu Leu Asn Leu
20 25 30
Ile Ser Val Leu Trp Arg Ala Lys Lys Thr Val Met Ala Val Val Phe
35 40 45
Ala Phe Ala Cys Ala Gly Leu Leu Ile Ser Phe Ile Leu Pro Gln Lys
50 55 60
Trp Thr Ser Ala Ala Val Val Thr Pro Pro Glu Pro Val Gln Trp Gln
65 70 75 80
Glu Leu Glu Lys Ser Phe Thr Lys Leu Arg Val Leu Asp Leu Asp Ile
85 90 95
Lys Ile Asp Arg Thr Glu Ala Phe Asn Leu Phe Ile Lys Lys Phe Gln
100 105 110
Ser Val Ser Leu Leu Glu Glu Tyr Leu Arg Ser Ser Pro Tyr Val Met
115 120 125
Asp Gln Leu Lys Glu Ala Lys Ile Asp Glu Leu Asp Leu His Arg Ala
130 135 140
Ile Val Ala Leu Ser Glu Lys Met Lys Ala Val Asp Asp Asn Ala Ser
145 150 155 160
Lys Lys Lys Asp Glu Pro Ser Leu Tyr Thr Ser Trp Thr Leu Ser Phe
165 170 175
Thr Ala Pro Thr Ser Glu Glu Ala Gln Thr Val Leu Ser Gly Tyr Ile
180 185 190
Asp Tyr Ile Ser Thr Leu Val Val Lys Glu Ser Leu Glu Asn Val Arg
195 200 205
Asn Lys Leu Glu Ile Lys Thr Gln Phe Glu Lys Glu Lys Leu Ala Gln
210 215 220
Asp Arg Ile Lys Thr Lys Asn Gln Leu Asp Ala Asn Ile Gln Arg Leu
225 230 235 240
Asn Tyr Ser Leu Asp Ile Ala Asn Ala Ala Gly Ile Lys Lys Pro Val
245 250 255
Tyr Ser Asn Gly Gln Ala Val Lys Asp Asp Pro Asp Phe Ser Ile Ser
260 265 270
Leu Gly Ala Asp Gly Ile Glu Arg Lys Leu Glu Ile Glu Lys Ala Val
275 280 285
Thr Asp Val Ala Glu Leu Asn Gly Glu Leu Arg Asn Arg Gln Tyr Leu
290 295 300
Val Glu Gln Leu Thr Lys Ala His Val Asn Asp Val Asn Phe Thr Pro
305 310 315 320
Phe Lys Tyr Gln Leu Ser Pro Ser Leu Pro Val Lys Lys Asp Gly Pro
325 330 335
Gly Lys Ala Ile Ile Val Ile Leu Ser Ala Leu Ile Gly Gly Met Val
340 345 350
Ala Cys Gly Gly Val Leu Leu Arg Tyr Ala Met Ala Ser Arg Lys Gln
355 360 365
Asp Ala Met Met Ala Asp His Leu Val
370 375
<210> 36
<211> 377
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 36
Met Ser Ser Leu Asn Ile Lys Gln Gly Ser Glu Ala His Phe Pro Glu
1 5 10 15
Tyr Pro Leu Ala Ser Pro Ser Asn Asn Glu Ile Asp Leu Leu Asn Leu
20 25 30
Ile Glu Val Leu Trp Arg Ala Lys Lys Thr Val Met Ala Val Val Phe
35 40 45
Ala Phe Ala Cys Ala Gly Leu Leu Ile Ser Phe Ile Leu Pro Gln Lys
50 55 60
Trp Thr Ser Ala Ala Val Val Thr Pro Pro Glu Pro Val Gln Trp Gln
65 70 75 80
Glu Leu Glu Lys Thr Phe Thr Lys Leu Arg Val Leu Asp Leu Asp Ile
85 90 95
Lys Ile Asp Arg Thr Glu Ala Phe Asn Leu Phe Ile Lys Lys Phe Gln
100 105 110
Ser Val Ser Leu Leu Glu Glu Tyr Leu Arg Ser Ser Pro Tyr Val Met
115 120 125
Asp Gln Leu Lys Glu Ala Lys Ile Asp Pro Leu Asp Leu His Arg Ala
130 135 140
Ile Val Ala Leu Ser Glu Lys Met Lys Ala Val Asp Asp Asn Ala Ser
145 150 155 160
Lys Lys Lys Asp Glu Ser Ala Leu Tyr Thr Ser Trp Thr Leu Ser Phe
165 170 175
Thr Ala Pro Thr Ser Glu Glu Ala Gln Lys Val Leu Ala Gly Tyr Ile
180 185 190
Asp Tyr Ile Ser Ala Leu Val Val Lys Glu Ser Ile Glu Asn Val Arg
195 200 205
Asn Lys Leu Glu Ile Lys Thr Gln Phe Glu Lys Glu Lys Leu Ala Gln
210 215 220
Asp Arg Ile Lys Thr Lys Asn Gln Leu Asp Ala Asn Ile Gln Arg Leu
225 230 235 240
Asn Tyr Ser Leu Asp Ile Ala Asn Ala Ala Gly Ile Lys Lys Pro Val
245 250 255
Tyr Ser Asn Gly Gln Ala Val Lys Asp Asp Pro Asp Phe Ser Ile Ser
260 265 270
Leu Gly Ala Asp Gly Ile Glu Arg Lys Leu Glu Ile Glu Lys Ala Val
275 280 285
Thr Asp Val Ala Glu Leu Asn Gly Glu Leu Arg Asn Arg Gln Tyr Leu
290 295 300
Val Glu Gln Leu Thr Lys Thr Asn Ile Asn Asp Val Asn Phe Thr Pro
305 310 315 320
Phe Lys Tyr Gln Leu Arg Pro Ser Leu Pro Val Lys Lys Asp Gly Gln
325 330 335
Gly Lys Ala Ile Ile Val Ile Leu Ser Ala Leu Val Gly Gly Met Val
340 345 350
Ala Cys Gly Gly Val Leu Leu Arg His Ala Met Ala Ser Arg Lys Gln
355 360 365
Asp Ala Met Met Ala Asp His Leu Val
370 375
<210> 37
<211> 377
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 37
Met Ser Ser Leu Asn Ile Lys Gln Gly Ser Asp Ala His Phe Pro Asp
1 5 10 15
Tyr Pro Leu Ala Ser Pro Ser Asn Asn Glu Ile Asp Leu Leu Asn Leu
20 25 30
Ile Ser Val Leu Trp Arg Ala Lys Lys Thr Val Met Ala Val Val Phe
35 40 45
Ala Phe Ala Cys Ala Gly Leu Leu Ile Ser Phe Ile Leu Pro Gln Lys
50 55 60
Trp Thr Ser Ala Ala Val Val Thr Pro Pro Glu Pro Val Gln Trp Gln
65 70 75 80
Glu Leu Glu Lys Ser Phe Thr Lys Leu Arg Val Leu Asp Leu Asp Ile
85 90 95
Lys Ile Asp Arg Thr Glu Ala Phe Asn Leu Phe Ile Lys Lys Phe Gln
100 105 110
Ser Val Ser Leu Leu Glu Glu Tyr Leu Arg Ser Ser Pro Tyr Val Met
115 120 125
Asp Gln Leu Lys Glu Ala Lys Ile Asp Glu Leu Asp Leu His Arg Ala
130 135 140
Ile Val Ala Leu Ser Glu Lys Met Lys Ala Val Asp Asp Asn Ala Ser
145 150 155 160
Lys Lys Lys Asp Glu Pro Ser Leu Tyr Thr Ser Trp Thr Leu Ser Phe
165 170 175
Thr Ala Pro Thr Ser Glu Glu Ala Gln Thr Val Leu Ser Gly Tyr Ile
180 185 190
Asp Tyr Ile Ser Thr Leu Val Val Lys Glu Ser Leu Glu Asn Val Arg
195 200 205
Asn Lys Leu Glu Ile Lys Thr Gln Phe Glu Lys Glu Lys Leu Ala Gln
210 215 220
Asp Arg Ile Lys Thr Lys Asn Gln Leu Asp Ala Asn Ile Gln Arg Leu
225 230 235 240
Asn Tyr Ser Leu Asp Ile Ala Asn Ala Ala Gly Ile Lys Lys Pro Val
245 250 255
Tyr Ser Asn Gly Gln Ala Val Lys Asp Asp Pro Asp Phe Ser Ile Ser
260 265 270
Leu Gly Ala Asp Gly Ile Glu Arg Lys Leu Glu Ile Glu Lys Ala Val
275 280 285
Thr Asp Val Ala Glu Leu Asn Gly Glu Leu Arg Asn Arg Gln Tyr Leu
290 295 300
Val Glu Gln Leu Thr Lys Ala His Val Asn Asp Val Asn Phe Thr Pro
305 310 315 320
Phe Lys Tyr Gln Leu Ser Pro Ser Leu Pro Val Lys Lys Asp Gly Pro
325 330 335
Gly Lys Ala Ile Ile Val Ile Leu Ser Ala Leu Ile Gly Gly Met Val
340 345 350
Ala Cys Gly Gly Val Leu Leu Arg Tyr Ala Met Ala Ser Arg Lys Gln
355 360 365
Asp Ala Met Met Ala Asp His Leu Val
370 375
<210> 38
<211> 377
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 38
Met Ser Ser Leu Asn Ile Lys Gln Gly Ser Asp Ala His Phe Pro Asp
1 5 10 15
Tyr Pro Leu Ala Ser Pro Ser Asn Asn Glu Ile Asp Leu Leu Asn Leu
20 25 30
Ile Ser Val Leu Trp Arg Ala Lys Lys Thr Val Met Ala Val Val Phe
35 40 45
Ala Phe Ala Cys Ala Gly Leu Leu Ile Ser Phe Ile Leu Pro Gln Lys
50 55 60
Trp Thr Ser Ala Ala Val Val Thr Pro Pro Glu Pro Val Gln Trp Gln
65 70 75 80
Glu Leu Glu Lys Thr Phe Thr Lys Leu Arg Val Leu Asp Leu Asp Ile
85 90 95
Lys Ile Asp Arg Thr Glu Ala Phe Asn Leu Phe Ile Lys Lys Phe Gln
100 105 110
Ser Val Ser Leu Leu Glu Glu Tyr Leu Arg Ser Ser Pro Tyr Val Met
115 120 125
Asp Gln Leu Lys Glu Ala Lys Ile Asp Glu Leu Asp Leu His Arg Ala
130 135 140
Ile Val Ala Leu Ser Glu Lys Met Lys Ala Val Asp Asp Asn Ala Ser
145 150 155 160
Lys Lys Lys Asp Glu Pro Ser Leu Tyr Thr Ser Trp Thr Leu Ser Phe
165 170 175
Thr Ala Pro Thr Ser Glu Glu Ala Gln Thr Val Leu Ser Gly Tyr Ile
180 185 190
Asp Tyr Ile Ser Ala Leu Val Val Lys Glu Ser Ile Glu Asn Val Arg
195 200 205
Asn Lys Leu Glu Ile Lys Thr Gln Phe Glu Lys Glu Lys Leu Ala Gln
210 215 220
Asp Arg Ile Lys Met Lys Asn Gln Leu Asp Ala Asn Ile Gln Arg Leu
225 230 235 240
Asn Tyr Ser Leu Asp Ile Ala Asn Ala Ala Gly Ile Lys Lys Pro Val
245 250 255
Tyr Ser Asn Gly Gln Ala Val Lys Asp Asp Pro Asp Phe Ser Ile Ser
260 265 270
Leu Gly Ala Asp Gly Ile Glu Arg Lys Leu Glu Ile Glu Lys Ala Val
275 280 285
Thr Asp Val Ala Glu Leu Asn Gly Glu Leu Arg Asn Arg Gln Tyr Leu
290 295 300
Val Glu Gln Leu Thr Lys Ala Asn Ile Asn Asp Val Asn Phe Thr Pro
305 310 315 320
Phe Lys Tyr Gln Leu Ser Pro Ser Leu Pro Val Lys Lys Asp Gly Pro
325 330 335
Gly Lys Ala Ile Ile Val Ile Leu Ser Ala Leu Ile Gly Gly Met Val
340 345 350
Ala Cys Gly Ser Val Leu Leu Arg Tyr Ala Met Ala Ser Arg Lys Gln
355 360 365
Asp Ala Met Met Ala Asp His Leu Val
370 375
<210> 39
<211> 378
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 39
Met Pro Ser Leu Asn Val Lys Gln Glu Lys Asn Gln Ser Phe Ala Gly
1 5 10 15
Tyr Ser Leu Pro Pro Ala Asn Ser His Glu Ile Asp Leu Phe Ser Leu
20 25 30
Ile Glu Val Leu Trp Gln Ala Lys Arg Arg Ile Leu Ala Thr Val Phe
35 40 45
Ala Phe Ala Cys Val Gly Leu Leu Leu Ser Phe Leu Leu Pro Gln Lys
50 55 60
Trp Thr Ser Gln Ala Ile Val Thr Pro Ala Glu Ser Val Gln Trp Gln
65 70 75 80
Gly Leu Glu Arg Thr Leu Thr Ala Leu Arg Val Leu Asp Met Glu Val
85 90 95
Ser Val Asp Arg Gly Ser Val Phe Asn Leu Phe Ile Lys Lys Phe Ser
100 105 110
Ser Pro Ser Leu Leu Glu Glu Tyr Leu Arg Ser Ser Pro Tyr Val Met
115 120 125
Asp Gln Leu Lys Gly Ala Gln Ile Asp Glu Gln Asp Leu His Arg Ala
130 135 140
Ile Val Leu Leu Ser Glu Lys Met Lys Ala Val Asp Ser Asn Val Gly
145 150 155 160
Lys Lys Asn Glu Thr Ser Leu Phe Thr Ser Trp Thr Leu Ser Phe Thr
165 170 175
Ala Pro Thr Arg Glu Glu Ala Gln Lys Val Leu Ala Gly Tyr Ile Gln
180 185 190
Tyr Ile Ser Asp Ile Val Val Lys Glu Thr Leu Glu Asn Ile Arg Asn
195 200 205
Gln Leu Glu Ile Lys Thr Arg Tyr Glu Gln Glu Lys Leu Ala Met Asp
210 215 220
Arg Val Arg Leu Lys Asn Gln Leu Asp Ala Asn Ile Gln Arg Leu His
225 230 235 240
Tyr Ser Leu Glu Ile Ala Asn Ala Ala Gly Ile Lys Arg Pro Val Tyr
245 250 255
Ser Asn Gly Gln Ala Val Lys Asp Asp Pro Asp Phe Ser Ile Ser Leu
260 265 270
Gly Ala Asp Gly Ile Ser Arg Lys Leu Glu Ile Glu Lys Gly Val Thr
275 280 285
Asp Val Ala Glu Ile Asp Gly Asp Leu Arg Asn Arg Gln Tyr His Val
290 295 300
Glu Gln Leu Ala Ala Met Asn Val Ser Asp Val Lys Phe Thr Pro Phe
305 310 315 320
Lys Tyr Gln Leu Ser Pro Ser Leu Pro Val Lys Lys Asp Gly Pro Gly
325 330 335
Lys Ala Ile Ile Ile Ile Leu Ala Ala Leu Ile Gly Gly Met Met Ala
340 345 350
Cys Gly Gly Val Leu Leu Arg His Ala Met Val Ser Arg Lys Met Glu
355 360 365
Asn Ala Leu Ala Ile Asp Glu Arg Leu Val
370 375
<210> 40
<211> 22
<212> DNA
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 40
gaagcaaacc gtacgcgtaa ag 22
<210> 41
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 41
cgaccagctc ttacacggcg 20
<210> 42
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 42
gaaataggac cactaataaa tacacaaatt aataac 36
<210> 43
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 43
ataattgacg atccggttgc c 21
<210> 44
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 44
gctatttacg ccctgattgt cttttgt 27
<210> 45
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 45
attgagaacc tgcgtaaacg gc 22
<210> 46
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 46
tgaagagcgg ttcagataac ttcc 24
<210> 47
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 47
cgatccggaa acctcctaca c 21
<210> 48
<211> 26
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 48
gattattcgc gcaacgctaa acagat 26
<210> 49
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 49
tgatcattga cgatccggta gcc 23
<210> 50
<211> 70
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 50
cggtagctgt aaagccaggg gcggtagcgt ggtttaaacc caagcaacag atcggcgtcg 60
tcggtatgga 70
<210> 51
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 51
agcttccata ccgacgacgc cgatctgttg cttgggttta aaccacgcta ccgcccctgg 60
ctttacagct accgagct 78
<210> 52
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 52
ggtagctgta aagccagggg cggtagcgtg 30
<210> 53
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 53
ccataccgac gacgccgatc tgttgcttgg 30
<210> 54
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 54
Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro Gly
1 5 10 15
Ser Thr Gly
<210> 55
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 55
Met Gly Val Pro Arg Pro Gln Pro Trp Ala Leu Gly Leu Leu Leu Phe
1 5 10 15
Leu Leu Pro Gly Ser Leu Gly
20
<210> 56
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 56
Met His Ser Ser Ala Leu Leu Cys Cys Leu Val Leu Leu Thr Gly Val
1 5 10 15
Arg Ala
<210> 57
<211> 25
<212> БЕЛОК
<213> Респираторный синцитиальный вирус А человека (штамм A2)
<400> 57
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly
20 25
<210> 58
<211> 15
<212> БЕЛОК
<213> Вирус гриппа A (штамм A/Japan/305/1957 H2N2)
<400> 58
Met Ala Ile Ile Tyr Leu Ile Leu Leu Phe Thr Ala Val Arg Gly
1 5 10 15
<210> 59
<211> 207
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 59
Met Glu Gly Met Asp Pro Leu Ala Val Leu Ala Glu Ser Arg Leu Leu
1 5 10 15
Pro Leu Leu Thr Val Arg Gly Gly Glu Asp Leu Ala Gly Leu Ala Thr
20 25 30
Val Leu Glu Leu Met Gly Val Gly Ala Leu Glu Ile Thr Leu Arg Thr
35 40 45
Glu Lys Gly Leu Glu Ala Leu Lys Ala Leu Arg Lys Ser Gly Leu Leu
50 55 60
Leu Gly Ala Gly Thr Val Arg Ser Pro Lys Glu Ala Glu Ala Ala Leu
65 70 75 80
Glu Ala Gly Ala Ala Phe Leu Val Ser Pro Gly Leu Leu Glu Glu Val
85 90 95
Ala Ala Leu Ala Gln Ala Arg Gly Val Pro Tyr Leu Pro Gly Val Leu
100 105 110
Thr Pro Thr Glu Val Glu Arg Ala Leu Ala Leu Gly Leu Ser Ala Leu
115 120 125
Lys Phe Phe Pro Ala Glu Pro Phe Gln Gly Val Arg Val Leu Arg Ala
130 135 140
Tyr Ala Glu Val Phe Pro Glu Val Arg Phe Leu Pro Thr Gly Gly Ile
145 150 155 160
Lys Glu Glu His Leu Pro His Tyr Ala Ala Leu Pro Asn Leu Leu Ala
165 170 175
Val Gly Gly Ser Trp Leu Leu Gln Gly Asp Leu Ala Ala Val Met Lys
180 185 190
Lys Val Lys Ala Ala Lys Ala Leu Leu Ser Pro Gln Ala Pro Gly
195 200 205
<210> 60
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 60
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Glu Ala Ala Ile Arg Thr Leu Lys Ala Leu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Ala Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Asp Glu Leu Asp
100 105 110
Ile Leu Ala Leu Val Arg Ala Ile Glu His Ala Ala Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Arg Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 61
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 61
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Ser Ala Ala Ile Leu Thr Leu Lys Met Glu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Ala Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Ala Glu Leu Lys
100 105 110
Ile Leu Ala Ala Arg Arg Ala Ile Glu His Ala Leu Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Phe Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 62
<211> 209
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 62
Met Ser Thr Ile Asn Asn Gln Leu Lys Ala Leu Lys Val Ile Pro Val
1 5 10 15
Ile Ala Ile Asp Asn Ala Glu Asp Ile Ile Pro Leu Gly Lys Val Leu
20 25 30
Ala Glu Asn Gly Leu Pro Ala Ala Glu Ile Thr Phe Arg Ser Ser Ala
35 40 45
Ala Val Lys Ala Ile Met Leu Leu Arg Ser Ala Gln Pro Glu Met Leu
50 55 60
Ile Gly Ala Gly Thr Ile Leu Asn Gly Val Gln Ala Leu Ala Ala Lys
65 70 75 80
Glu Ala Gly Ala Thr Phe Val Val Ser Pro Gly Phe Asn Pro Asn Thr
85 90 95
Val Arg Ala Cys Gln Ile Ile Gly Ile Asp Ile Val Pro Gly Val Asn
100 105 110
Asn Pro Ser Thr Val Glu Ala Ala Leu Glu Met Gly Leu Thr Thr Leu
115 120 125
Lys Phe Phe Pro Ala Glu Ala Ser Gly Gly Ile Ser Met Val Lys Ser
130 135 140
Leu Val Gly Pro Tyr Gly Asp Ile Arg Leu Met Pro Thr Gly Gly Ile
145 150 155 160
Thr Pro Ser Asn Ile Asp Asn Tyr Leu Ala Ile Pro Gln Val Leu Ala
165 170 175
Cys Gly Gly Thr Trp Met Val Asp Lys Lys Leu Val Thr Asn Gly Glu
180 185 190
Trp Asp Glu Ile Ala Arg Leu Thr Arg Glu Ile Val Glu Gln Val Asn
195 200 205
Pro
<210> 63
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 63
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Thr Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Lys Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Ser Lys Asn Arg Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Asn Leu Asn Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 64
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 64
Met Asn Gln His Ser His Lys Asp Tyr Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Ser Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Ala Glu His His Arg
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 65
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 65
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn
145 150 155 160
Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Ser Ala Leu Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys
180 185 190
Ala Lys Ala Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
195 200 205
<210> 66
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 66
Met Asn Gln His Ser His Lys Asp Tyr Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Ala Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Ser Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Asp Ala His Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 67
<211> 177
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 67
Met Phe Thr Lys Ser Gly Asp Asp Gly Asn Thr Asn Val Ile Asn Lys
1 5 10 15
Arg Val Gly Lys Asp Ser Pro Leu Val Asn Phe Leu Gly Asp Leu Asp
20 25 30
Glu Leu Asn Ser Phe Ile Gly Phe Ala Ile Ser Lys Ile Pro Trp Glu
35 40 45
Asp Met Lys Lys Asp Leu Glu Arg Val Gln Val Glu Leu Phe Glu Ile
50 55 60
Gly Glu Asp Leu Ser Thr Gln Ser Ser Lys Lys Lys Ile Asp Glu Ser
65 70 75 80
Tyr Val Leu Trp Leu Leu Ala Ala Thr Ala Ile Tyr Arg Ile Glu Ser
85 90 95
Gly Pro Val Lys Leu Phe Val Ile Pro Gly Gly Ser Glu Glu Ala Ser
100 105 110
Val Leu His Val Thr Arg Ser Val Ala Arg Arg Val Glu Arg Asn Ala
115 120 125
Val Lys Tyr Thr Lys Glu Leu Pro Glu Ile Asn Arg Met Ile Ile Val
130 135 140
Tyr Leu Asn Arg Leu Ser Ser Leu Leu Phe Ala Met Ala Leu Val Ala
145 150 155 160
Asn Lys Arg Arg Asn Gln Ser Glu Lys Ile Tyr Glu Ile Gly Lys Ser
165 170 175
Trp
<210> 68
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 68
Met Asn Gln His Ser His Lys Asp Tyr Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Gln Cys Val Arg Ala
20 25 30
Phe Glu Glu Ala Met Ala Asp Ala Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Ser Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Ser Ser Arg Glu His His Glu
115 120 125
Phe Phe Arg Glu His Phe Met Val Lys Gly Val Glu Ala Ala Ala Ala
130 135 140
Cys Ile Thr Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 69
<211> 201
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 69
Met Gly His Thr Lys Gly Pro Thr Pro Gln Gln His Asp Gly Ser Ala
1 5 10 15
Leu Arg Ile Gly Ile Val His Ala Arg Trp Asn Lys Thr Ile Ile Met
20 25 30
Pro Leu Leu Ile Gly Thr Ile Ala Lys Leu Leu Glu Cys Gly Val Lys
35 40 45
Ala Ser Asn Ile Val Val Gln Ser Val Pro Gly Ser Trp Glu Leu Pro
50 55 60
Ile Ala Val Gln Arg Leu Tyr Ser Ala Ser Gln Leu Gln Thr Pro Ser
65 70 75 80
Ser Gly Pro Ser Leu Ser Ala Gly Asp Leu Leu Gly Ser Ser Thr Thr
85 90 95
Asp Leu Thr Ala Leu Pro Thr Thr Thr Ala Ser Ser Thr Gly Pro Phe
100 105 110
Asp Ala Leu Ile Ala Ile Gly Val Leu Ile Lys Gly Glu Thr Met His
115 120 125
Phe Glu Tyr Ile Ala Asp Ser Val Ser His Gly Leu Met Arg Val Gln
130 135 140
Leu Asp Thr Gly Val Pro Val Ile Phe Gly Val Leu Thr Val Leu Thr
145 150 155 160
Asp Asp Gln Ala Lys Ala Arg Ala Gly Val Ile Glu Gly Ser His Asn
165 170 175
His Gly Glu Asp Trp Gly Leu Ala Ala Val Glu Met Gly Val Arg Arg
180 185 190
Arg Asp Trp Ala Ala Gly Lys Thr Glu
195 200
<210> 70
<211> 237
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 70
Met Tyr Glu Val Asp His Ala Asp Val Tyr Asp Leu Phe Tyr Leu Gly
1 5 10 15
Arg Gly Lys Asp Tyr Ala Ala Glu Ala Ser Asp Ile Ala Asp Leu Val
20 25 30
Arg Ser Arg Thr Pro Glu Ala Ser Ser Leu Leu Asp Val Ala Cys Gly
35 40 45
Thr Gly Thr His Leu Glu His Phe Thr Lys Glu Phe Gly Asp Thr Ala
50 55 60
Gly Leu Glu Leu Ser Glu Asp Met Leu Thr His Ala Arg Lys Arg Leu
65 70 75 80
Pro Asp Ala Thr Leu His Gln Gly Asp Met Arg Asp Phe Gln Leu Gly
85 90 95
Arg Lys Phe Ser Ala Val Val Ser Met Phe Ser Ser Val Gly Tyr Leu
100 105 110
Lys Thr Val Ala Glu Leu Gly Ala Ala Val Ala Ser Phe Ala Glu His
115 120 125
Leu Glu Pro Gly Gly Val Val Val Val Glu Pro Trp Trp Phe Pro Glu
130 135 140
Thr Phe Ala Asp Gly Trp Val Ser Ala Asp Val Val Arg Arg Asp Gly
145 150 155 160
Arg Thr Val Ala Arg Val Ser His Ser Val Arg Glu Gly Asn Ala Thr
165 170 175
Arg Met Glu Val His Phe Thr Val Ala Asp Pro Gly Lys Gly Val Arg
180 185 190
His Phe Ser Asp Val His Leu Ile Thr Leu Phe His Gln Arg Glu Tyr
195 200 205
Glu Ala Ala Phe Met Ala Ala Gly Leu Arg Val Glu Tyr Leu Glu Gly
210 215 220
Gly Pro Ser Gly Arg Gly Leu Phe Val Gly Val Pro Ala
225 230 235
<210> 71
<211> 138
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 71
Met Gly Met Lys Glu Lys Phe Val Leu Ile Ile Thr His Gly Asp Phe
1 5 10 15
Gly Lys Gly Leu Leu Ser Gly Ala Glu Val Ile Ile Gly Lys Gln Glu
20 25 30
Asn Val His Thr Val Gly Leu Asn Leu Gly Asp Asn Ile Glu Lys Val
35 40 45
Ala Lys Glu Val Met Arg Ile Ile Ile Ala Lys Leu Ala Glu Asp Lys
50 55 60
Glu Ile Ile Ile Val Val Asp Leu Phe Gly Gly Ser Pro Phe Asn Ile
65 70 75 80
Ala Leu Glu Met Met Lys Thr Phe Asp Val Lys Val Ile Thr Gly Ile
85 90 95
Asn Met Pro Met Leu Val Glu Leu Leu Thr Ser Ile Asn Val Tyr Asp
100 105 110
Thr Thr Glu Leu Leu Glu Asn Ile Ser Lys Ile Gly Lys Asp Gly Ile
115 120 125
Lys Val Ile Glu Lys Ser Ser Leu Lys Met
130 135
<210> 72
<211> 154
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 72
Met Lys Tyr Asp Gly Ser Lys Leu Arg Ile Gly Ile Leu His Ala Arg
1 5 10 15
Trp Asn Leu Glu Ile Ile Ala Ala Leu Val Ala Gly Ala Ile Lys Arg
20 25 30
Leu Gln Glu Phe Gly Val Lys Ala Glu Asn Ile Ile Ile Glu Thr Val
35 40 45
Pro Gly Ser Phe Glu Leu Pro Tyr Gly Ser Lys Leu Phe Val Glu Lys
50 55 60
Gln Lys Arg Leu Gly Lys Pro Leu Asp Ala Ile Ile Pro Ile Gly Val
65 70 75 80
Leu Ile Lys Gly Ser Thr Met His Phe Glu Tyr Ile Cys Asp Ser Thr
85 90 95
Thr His Gln Leu Met Lys Leu Asn Phe Glu Leu Gly Ile Pro Val Ile
100 105 110
Phe Gly Val Leu Thr Cys Leu Thr Asp Glu Gln Ala Glu Ala Arg Ala
115 120 125
Gly Leu Ile Glu Gly Lys Met His Asn His Gly Glu Asp Trp Gly Ala
130 135 140
Ala Ala Val Glu Met Ala Thr Lys Phe Asn
145 150
<210> 73
<211> 164
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 73
Met Ala Val Lys Gly Leu Gly Glu Val Asp Gln Lys Tyr Asp Gly Ser
1 5 10 15
Lys Leu Arg Ile Gly Ile Leu His Ala Arg Trp Asn Arg Lys Ile Ile
20 25 30
Leu Ala Leu Val Ala Gly Ala Val Leu Arg Leu Leu Glu Phe Gly Val
35 40 45
Lys Ala Glu Asn Ile Ile Ile Glu Thr Val Pro Gly Ser Phe Glu Leu
50 55 60
Pro Tyr Gly Ser Lys Leu Phe Val Glu Lys Gln Lys Arg Leu Gly Lys
65 70 75 80
Pro Leu Asp Ala Ile Ile Pro Ile Gly Val Leu Ile Lys Gly Ser Thr
85 90 95
Met His Phe Glu Tyr Ile Cys Asp Ser Thr Thr His Gln Leu Met Lys
100 105 110
Leu Asn Phe Glu Leu Gly Ile Pro Val Ile Phe Gly Val Leu Thr Cys
115 120 125
Leu Thr Asp Glu Gln Ala Glu Ala Arg Ala Gly Leu Ile Glu Gly Lys
130 135 140
Met His Asn His Gly Glu Asp Trp Gly Ala Ala Ala Val Glu Met Ala
145 150 155 160
Thr Lys Phe Asn
<210> 74
<211> 175
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 74
Met Gly Ala Asn Trp Tyr Leu Asp Asn Glu Ser Ser Arg Leu Ser Phe
1 5 10 15
Thr Ser Thr Lys Asn Ala Asp Ile Ala Glu Val His Arg Phe Leu Val
20 25 30
Leu His Gly Lys Val Asp Pro Lys Gly Leu Ala Glu Val Glu Val Glu
35 40 45
Thr Glu Ser Ile Ser Thr Gly Ile Pro Leu Arg Asp Met Leu Leu Arg
50 55 60
Val Leu Val Phe Gln Val Ser Lys Phe Pro Val Ala Gln Ile Asn Ala
65 70 75 80
Gln Leu Asp Met Arg Pro Ile Asn Asn Leu Ala Pro Gly Ala Gln Leu
85 90 95
Glu Leu Arg Leu Pro Leu Thr Val Ser Leu Arg Gly Lys Ser His Ser
100 105 110
Tyr Asn Ala Glu Leu Leu Ala Thr Arg Leu Asp Glu Arg Arg Phe Gln
115 120 125
Val Val Thr Leu Glu Pro Leu Val Ile His Ala Gln Asp Phe Asp Met
130 135 140
Val Arg Ala Phe Asn Ala Leu Arg Leu Val Ala Gly Leu Ser Ala Val
145 150 155 160
Ser Leu Ser Val Pro Val Gly Ala Val Leu Ile Phe Thr Ala Arg
165 170 175
<210> 75
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 75
Met Thr Asp Tyr Ile Arg Asp Gly Ser Ala Ile Lys Ala Leu Ser Phe
1 5 10 15
Ala Ile Ile Leu Ala Glu Ala Asp Leu Arg His Ile Pro Gln Asp Leu
20 25 30
Gln Arg Leu Ala Val Arg Val Ile His Ala Cys Gly Met Val Asp Val
35 40 45
Ala Asn Asp Leu Ala Phe Ser Glu Gly Ala Gly Lys Ala Gly Arg Asn
50 55 60
Ala Leu Leu Ala Gly Ala Pro Ile Leu Cys Asp Ala Arg Met Val Ala
65 70 75 80
Glu Gly Ile Thr Arg Ser Arg Leu Pro Ala Asp Asn Arg Val Ile Tyr
85 90 95
Thr Leu Ser Asp Pro Ser Val Pro Glu Leu Ala Lys Lys Ile Gly Asn
100 105 110
Thr Arg Ser Ala Ala Ala Leu Asp Leu Trp Leu Pro His Ile Glu Gly
115 120 125
Ser Ile Val Ala Ile Gly Asn Ala Pro Thr Ala Leu Phe Arg Leu Phe
130 135 140
Glu Leu Leu Asp Ala Gly Ala Pro Lys Pro Ala Leu Ile Ile Gly Met
145 150 155 160
Pro Val Gly Phe Val Gly Ala Ala Glu Ser Lys Asp Glu Leu Ala Ala
165 170 175
Asn Ser Arg Gly Val Pro Tyr Val Ile Val Arg Gly Arg Arg Gly Gly
180 185 190
Ser Ala Met Thr Ala Ala Ala Val Asn Ala Leu Ala Ser Glu Arg Glu
195 200 205
<210> 76
<211> 128
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 76
Met Ile Thr Val Phe Gly Leu Lys Ser Lys Leu Ala Pro Arg Arg Glu
1 5 10 15
Lys Leu Ala Glu Val Ile Tyr Ser Ser Leu His Leu Gly Leu Asp Ile
20 25 30
Pro Lys Gly Lys His Ala Ile Arg Phe Leu Cys Leu Glu Lys Glu Asp
35 40 45
Phe Tyr Tyr Pro Phe Asp Arg Ser Asp Asp Tyr Thr Val Ile Glu Ile
50 55 60
Asn Leu Met Ala Gly Arg Ser Glu Glu Thr Lys Met Leu Leu Ile Phe
65 70 75 80
Leu Leu Phe Ile Ala Leu Glu Arg Lys Leu Gly Ile Arg Ala His Asp
85 90 95
Val Glu Ile Thr Ile Lys Glu Gln Pro Ala His Cys Trp Gly Phe Arg
100 105 110
Gly Arg Thr Gly Asp Ser Ala Arg Asp Leu Asp Tyr Asp Ile Tyr Val
115 120 125
<210> 77
<211> 235
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 77
Met Gly Ser Asp Leu Gln Lys Leu Gln Arg Phe Ser Thr Cys Asp Ile
1 5 10 15
Ser Asp Gly Leu Leu Asn Val Tyr Asn Ile Pro Thr Gly Gly Tyr Phe
20 25 30
Pro Asn Leu Thr Ala Ile Ser Pro Pro Gln Asn Ser Ser Ile Val Gly
35 40 45
Thr Ala Tyr Thr Val Leu Phe Ala Pro Ile Asp Asp Pro Arg Pro Ala
50 55 60
Val Asn Tyr Ile Asp Ser Val Pro Pro Asn Ser Ile Leu Val Leu Ala
65 70 75 80
Leu Glu Pro His Leu Gln Ser Gln Phe His Pro Phe Ile Lys Ile Thr
85 90 95
Gln Ala Met Tyr Gly Gly Leu Met Ser Thr Arg Ala Gln Tyr Leu Lys
100 105 110
Ser Asn Gly Thr Val Val Phe Gly Arg Ile Arg Asp Val Asp Glu His
115 120 125
Arg Thr Leu Asn His Pro Val Phe Ala Tyr Gly Val Gly Ser Cys Ala
130 135 140
Pro Lys Ala Val Val Lys Ala Val Gly Thr Asn Val Gln Leu Lys Ile
145 150 155 160
Leu Thr Ser Asp Gly Val Thr Gln Thr Ile Cys Pro Gly Asp Tyr Ile
165 170 175
Ala Gly Asp Asn Asn Gly Ile Val Arg Ile Pro Val Gln Glu Thr Asp
180 185 190
Ile Ser Lys Leu Val Thr Tyr Ile Glu Lys Ser Ile Glu Val Asp Arg
195 200 205
Leu Val Ser Glu Ala Ile Lys Asn Gly Leu Pro Ala Lys Ala Ala Gln
210 215 220
Thr Ala Arg Arg Met Val Leu Lys Asp Tyr Ile
225 230 235
<210> 78
<211> 162
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 78
Met Ser Gly Met Arg Val Tyr Leu Gly Ala Asp His Ala Gly Tyr Glu
1 5 10 15
Leu Lys Gln Ala Ile Ile Ala Phe Leu Lys Met Thr Gly His Glu Pro
20 25 30
Ile Asp Cys Gly Ala Leu Arg Tyr Asp Ala Asp Asp Asp Tyr Pro Ala
35 40 45
Phe Cys Ile Ala Ala Ala Thr Arg Thr Val Ala Asp Pro Gly Ser Leu
50 55 60
Gly Ile Val Leu Gly Gly Ser Gly Asn Gly Glu Gln Ile Ala Ala Asn
65 70 75 80
Lys Val Pro Gly Ala Arg Cys Ala Leu Ala Trp Ser Val Gln Thr Ala
85 90 95
Ala Leu Ala Arg Glu His Asn Asn Ala Gln Leu Ile Gly Ile Gly Gly
100 105 110
Arg Met His Thr Leu Glu Glu Ala Leu Arg Ile Val Lys Ala Phe Val
115 120 125
Thr Thr Pro Trp Ser Lys Ala Gln Arg His Gln Arg Arg Ile Asp Ile
130 135 140
Leu Ala Glu Tyr Glu Arg Thr His Glu Ala Pro Pro Val Pro Gly Ala
145 150 155 160
Pro Ala
<210> 79
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 79
Met Gly Asp Asp Ala Arg Ile Ala Ala Ile Gly Asp Val Asp Glu Leu
1 5 10 15
Asn Ser Gln Ile Gly Val Leu Leu Ala Glu Pro Leu Pro Asp Asp Val
20 25 30
Arg Ala Ala Leu Ser Ala Ile Gln His Asp Leu Phe Asp Leu Gly Gly
35 40 45
Glu Leu Cys Ile Pro Gly His Ala Ala Ile Thr Glu Asp His Leu Leu
50 55 60
Arg Leu Ala Leu Trp Leu Val His Tyr Asn Gly Gln Leu Pro Pro Leu
65 70 75 80
Glu Glu Phe Ile Leu Pro Gly Gly Ala Arg Gly Ala Ala Leu Ala His
85 90 95
Val Cys Arg Thr Val Cys Arg Arg Ala Glu Arg Ser Ile Lys Ala Leu
100 105 110
Gly Ala Ser Glu Pro Leu Asn Ile Ala Pro Ala Ala Tyr Val Asn Leu
115 120 125
Leu Ser Asp Leu Leu Phe Val Leu Ala Arg Val Leu Asn Arg Ala Ala
130 135 140
Gly Gly Ala Asp Val Leu Trp Asp Arg Thr Arg Ala His
145 150 155
<210> 80
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 80
Met Ile Leu Ser Ala Glu Gln Ser Phe Thr Leu Arg His Pro His Gly
1 5 10 15
Gln Ala Ala Ala Leu Ala Phe Val Arg Glu Pro Ala Ala Ala Leu Ala
20 25 30
Gly Val Gln Arg Leu Arg Gly Leu Asp Ser Asp Gly Glu Gln Val Trp
35 40 45
Gly Glu Leu Leu Val Arg Val Pro Leu Leu Gly Glu Val Asp Leu Pro
50 55 60
Phe Arg Ser Glu Ile Val Arg Thr Pro Gln Gly Ala Glu Leu Arg Pro
65 70 75 80
Leu Thr Leu Thr Gly Glu Arg Ala Trp Val Ala Val Ser Gly Gln Ala
85 90 95
Thr Ala Ala Glu Gly Gly Glu Met Ala Phe Ala Phe Gln Phe Gln Ala
100 105 110
His Leu Ala Thr Pro Glu Ala Glu Gly Glu Gly Gly Ala Ala Phe Glu
115 120 125
Val Met Val Gln Ala Ala Ala Gly Val Thr Leu Leu Leu Val Ala Met
130 135 140
Ala Leu Pro Gln Gly Leu Ala Ala Gly Leu Pro Pro Ala
145 150 155
<210> 81
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 81
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Ser Ala Ala Ile Leu Thr Leu Lys Met Glu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Lys Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Ala Glu Leu Lys
100 105 110
Ile Leu Ala Ala Arg Arg Ala Ile Glu His Ala Leu Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Phe Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 82
<211> 209
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 82
Met Asp Asp Ile Asn Asn Gln Leu Lys Arg Leu Lys Val Ile Pro Val
1 5 10 15
Ile Ala Ile Asp Asn Ala Glu Asp Ile Ile Pro Leu Gly Lys Val Leu
20 25 30
Ala Glu Asn Gly Leu Pro Ala Ala Glu Ile Thr Phe Arg Ser Ser Ala
35 40 45
Ala Val Lys Ala Ile Met Leu Leu Arg Ser Ala Gln Pro Glu Met Leu
50 55 60
Ile Gly Ala Gly Thr Ile Leu Asn Gly Val Gln Ala Leu Ala Ala Lys
65 70 75 80
Glu Ala Gly Ala Asp Phe Val Val Ser Pro Gly Phe Asn Pro Asn Thr
85 90 95
Val Arg Ala Cys Gln Ile Ile Gly Ile Asp Ile Val Pro Gly Val Asn
100 105 110
Asn Pro Ser Thr Val Glu Gln Ala Leu Glu Met Gly Leu Thr Thr Leu
115 120 125
Lys Phe Phe Pro Ala Glu Ala Ser Gly Gly Ile Ser Met Val Lys Ser
130 135 140
Leu Val Gly Pro Tyr Gly Asp Ile Arg Leu Met Pro Thr Gly Gly Ile
145 150 155 160
Thr Pro Asp Asn Ile Asp Asn Tyr Leu Ala Ile Pro Gln Val Leu Ala
165 170 175
Cys Gly Gly Thr Trp Met Val Asp Lys Lys Leu Val Arg Asn Gly Glu
180 185 190
Trp Asp Glu Ile Ala Arg Leu Thr Arg Glu Ile Val Glu Gln Val Asn
195 200 205
Pro
<210> 83
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 83
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Asp Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Lys Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Asp Lys Asn Arg Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Asn Leu Asn Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 84
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 84
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Asp Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Glu Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Asp Lys Asn Glu Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Asp Leu Asp Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 85
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 85
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Asp Glu His His Arg
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Asn Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 86
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 86
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asp Gly Gly Ile Tyr Asp His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Glu Tyr Glu Asp Ser Asp Glu Asp His Glu
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Asn Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 87
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 87
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Asp Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn
145 150 155 160
Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Asp Ala Leu Val Lys Gly Asp Pro Asp Glu Val Arg Glu Lys
180 185 190
Ala Lys Lys Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
195 200 205
<210> 88
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 88
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Asp Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Glu Phe Val Glu Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asp
145 150 155 160
Leu Asp Asp Val Cys Glu Trp Phe Asp Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Asp Ala Leu Val Glu Gly Asp Pro Asp Glu Val Arg Glu Asp
180 185 190
Ala Lys Glu Phe Val Glu Glu Ile Arg Gly Cys Thr Glu
195 200 205
<210> 89
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 89
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Asp Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn
145 150 155 160
Leu Asp Asn Val Cys Lys Trp Phe Lys Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Lys Ala Leu Val Lys Gly Lys Pro Asp Glu Val Arg Glu Lys
180 185 190
Ala Lys Lys Phe Val Lys Lys Ile Arg Gly Cys Thr Glu
195 200 205
<210> 90
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 90
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Arg Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Asp Ala His Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 91
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 91
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Arg Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asp Gly Gly Ile Tyr Asp His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Glu Tyr Glu Asp Ser Asp Ala Asp Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 92
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 92
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Arg Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asn Gly Met Met Asn Val Gln Leu Asn Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Asn Tyr Asp Lys Ser Lys Ala His Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 93
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (70)..(70)
<223> Xaa является A или K
<400> 93
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Ser Ala Ala Ile Leu Thr Leu Lys Met Glu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Xaa Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Ala Glu Leu Lys
100 105 110
Ile Leu Ala Ala Arg Arg Ala Ile Glu His Ala Leu Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Phe Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 94
<211> 209
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Xaa является S или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Xaa является T или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (10)..(10)
<223> Xaa является A или R
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (85)..(85)
<223> Xaa является T или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (119)..(119)
<223> Xaa является A или Q
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (163)..(163)
<223> Xaa является S или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (189)..(189)
<223> Xaa является T или R
<400> 94
Met Xaa Xaa Ile Asn Asn Gln Leu Lys Xaa Leu Lys Val Ile Pro Val
1 5 10 15
Ile Ala Ile Asp Asn Ala Glu Asp Ile Ile Pro Leu Gly Lys Val Leu
20 25 30
Ala Glu Asn Gly Leu Pro Ala Ala Glu Ile Thr Phe Arg Ser Ser Ala
35 40 45
Ala Val Lys Ala Ile Met Leu Leu Arg Ser Ala Gln Pro Glu Met Leu
50 55 60
Ile Gly Ala Gly Thr Ile Leu Asn Gly Val Gln Ala Leu Ala Ala Lys
65 70 75 80
Glu Ala Gly Ala Xaa Phe Val Val Ser Pro Gly Phe Asn Pro Asn Thr
85 90 95
Val Arg Ala Cys Gln Ile Ile Gly Ile Asp Ile Val Pro Gly Val Asn
100 105 110
Asn Pro Ser Thr Val Glu Xaa Ala Leu Glu Met Gly Leu Thr Thr Leu
115 120 125
Lys Phe Phe Pro Ala Glu Ala Ser Gly Gly Ile Ser Met Val Lys Ser
130 135 140
Leu Val Gly Pro Tyr Gly Asp Ile Arg Leu Met Pro Thr Gly Gly Ile
145 150 155 160
Thr Pro Xaa Asn Ile Asp Asn Tyr Leu Ala Ile Pro Gln Val Leu Ala
165 170 175
Cys Gly Gly Thr Trp Met Val Asp Lys Lys Leu Val Xaa Asn Gly Glu
180 185 190
Trp Asp Glu Ile Ala Arg Leu Thr Arg Glu Ile Val Glu Gln Val Asn
195 200 205
Pro
<210> 95
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (13)..(13)
<223> Xaa является T или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (33)..(33)
<223> Xaa является K или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (71)..(71)
<223> Xaa является S или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (74)..(74)
<223> Xaa является R или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (101)..(101)
<223> Xaa является N или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (103)..(103)
<223> Xaa является N или D
<400> 95
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Xaa Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Xaa Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Xaa Lys Asn Xaa Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Xaa Leu Xaa Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 96
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> Xaa является Y или H
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (82)..(82)
<223> Xaa является N или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (87)..(87)
<223> Xaa является R или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (105)..(105)
<223> Xaa является S или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (119)..(119)
<223> Xaa является R или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (121)..(121)
<223> Xaa является R или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (124)..(124)
<223> Xaa является A или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (126)..(126)
<223> Xaa является H или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (128)..(128)
<223> Xaa является R или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (150)..(150)
<223> Xaa является A или N
<400> 96
Met Asn Gln His Ser His Lys Asp Xaa Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Xaa Gly Gly Ile Tyr Xaa His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Xaa Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Xaa Tyr Xaa Asp Ser Xaa Glu Xaa His Xaa
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Xaa Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 97
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (126)..(126)
<223> Xaa является T или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (139)..(139)
<223> Xaa является Q или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (142)..(142)
<223> Xaa является K или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (160)..(160)
<223> Xaa является N или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (163)..(163)
<223> Xaa является N или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (166)..(166)
<223> Xaa является E или K
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (169)..(169)
<223> Xaa является D или K
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (179)..(179)
<223> Xaa является S, D или K
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (183)..(183)
<223> Xaa является K или E
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (185)..(185)
<223> Xaa является T, D, или K
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (192)..(192)
<223> Xaa является D или K
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (195)..(195)
<223> Xaa является A, E, или K
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (198)..(198)
<223> Xaa является E или K
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (199)..(199)
<223> Xaa является E или K
<400> 97
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Xaa Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Xaa Phe Val Xaa Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Xaa
145 150 155 160
Leu Asp Xaa Val Cys Xaa Trp Phe Xaa Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Xaa Ala Leu Val Xaa Gly Xaa Pro Asp Glu Val Arg Glu Xaa
180 185 190
Ala Lys Xaa Phe Val Xaa Xaa Ile Arg Gly Cys Thr Glu
195 200 205
<210> 98
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> Xaa является Y или H
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (38)..(38)
<223> Xaa является A или R
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (82)..(82)
<223> Xaa является N или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (87)..(87)
<223> Xaa является R или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (97)..(97)
<223> Xaa является N или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (105)..(105)
<223> Xaa является S, N, или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (119)..(119)
<223> Xaa является R, E, или N
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (121)..(121)
<223> Xaa является R, E, или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (122)..(122)
<223> Xaa является K или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (124)..(124)
<223> Xaa является K или D
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (126)..(126)
<223> Xaa является H или D
<400> 98
Met Asn Gln His Ser His Lys Asp Xaa Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Xaa Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Xaa Gly Gly Ile Tyr Xaa His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Xaa Gly Met Met Asn Val Gln Leu Xaa Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Xaa Tyr Xaa Xaa Ser Xaa Ala Xaa Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 99
<211> 142
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 99
taatgcttaa gtcgaacaga aagtaatcgt attgtacacg gccgcataat cgaaattaat 60
acgactcact ataggggaat tgtgagcgga taacaattcc ccatcttagt atattagtta 120
agtataagaa ggagatatac tt 142
<210> 100
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 100
taaagaagga gatatcat 18
<210> 101
<211> 17
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 101
tgagaaggag atatcat 17
<210> 102
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 102
Met Gly Val Pro Arg Pro Gln Pro Trp Ala Leu Gly Leu Leu Leu Phe
1 5 10 15
Leu Leu Pro Gly Ser Leu Gly Ala Glu Ser His Leu Ser Leu Leu Tyr
20 25 30
His Leu Thr Ala Val Ser Ser Pro Ala Pro Gly Thr Pro Ala Phe Trp
35 40 45
Val Ser Gly Trp Leu Gly Pro Gln Gln Tyr Leu Ser Tyr Asn Ser Leu
50 55 60
Arg Gly Glu Ala Glu Pro Cys Gly Ala Trp Val Trp Glu Asn Gln Val
65 70 75 80
Ser Trp Tyr Trp Glu Lys Glu Thr Thr Asp Leu Arg Ile Lys Glu Lys
85 90 95
Leu Phe Leu Glu Ala Phe Lys Ala Leu Gly Gly Lys Gly Pro Tyr Thr
100 105 110
Leu Gln Gly Leu Leu Gly Cys Glu Leu Gly Pro Asp Asn Thr Ser Val
115 120 125
Pro Thr Ala Lys Phe Ala Leu Asn Gly Glu Glu Phe Met Asn Phe Asp
130 135 140
Leu Lys Gln Gly Thr Trp Gly Gly Asp Trp Pro Glu Ala Leu Ala Ile
145 150 155 160
Ser Gln Arg Trp Gln Gln Gln Asp Lys Ala Ala Asn Lys Glu Leu Thr
165 170 175
Phe Leu Leu Phe Ser Cys Pro His Arg Leu Arg Glu His Leu Glu Arg
180 185 190
Gly Arg Gly Asn Leu Glu Trp Lys Glu Pro Pro Ser Met Arg Leu Lys
195 200 205
Ala Arg Pro Ser Ser Pro Gly Phe Ser Val Leu Thr Cys Ser Ala Phe
210 215 220
Ser Phe Tyr Pro Pro Glu Leu Gln Leu Arg Phe Leu Arg Asn Gly Leu
225 230 235 240
Ala Ala Gly Thr Gly Gln Gly Asp Phe Gly Pro Asn Ser Asp Gly Ser
245 250 255
Phe His Ala Ser Ser Ser Leu Thr Val Lys Ser Gly Asp Glu His His
260 265 270
Tyr Cys Cys Ile Val Gln His Ala Gly Leu Ala Gln Pro Leu Arg Val
275 280 285
Glu Leu Glu Ser Pro Ala Lys Ser Ser Val Leu Val Val Gly Ile Val
290 295 300
Ile Gly Val Leu Leu Leu Thr Ala Ala Ala Val Gly Gly Ala Leu Leu
305 310 315 320
Trp Arg Arg Met Arg Ser Gly Leu Pro Ala Pro Trp Ile Ser Leu Arg
325 330 335
Gly Asp Asp Thr Gly Val Leu Leu Pro Thr Pro Gly Glu Ala Gln Asp
340 345 350
Ala Asp Leu Lys Asp Val Asn Val Ile Pro Ala Thr Ala
355 360 365
<210> 103
<211> 62
<212> БЕЛОК
<213> Homo sapiens
<400> 103
Met Gly Val Pro Arg Pro Gln Pro Trp Ala Leu Gly Leu Leu Leu Phe
1 5 10 15
Leu Leu Pro Gly Ser Leu Gly Phe Ala Cys Lys Thr Ala Asn Gly Thr
20 25 30
Ala Ile Pro Ile Gly Gly Gly Ser Ala Asn Val Tyr Val Asn Leu Ala
35 40 45
Pro Val Val Asn Val Gly Gln Asn Leu Val Val Asp Leu Ser
50 55 60
<210> 104
<211> 574
<212> БЕЛОК
<213> Респираторный синцитиальный вирус A человека (штамм A2)
<400> 104
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Pro Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Ser Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Ser Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Val Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Ser Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Ile Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Met Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu His Asn Val Asn Ala Gly Lys Ser Thr Thr Asn Ile Met Ile Thr
515 520 525
Thr Ile Ile Ile Val Ile Ile Val Ile Leu Leu Ser Leu Ile Ala Val
530 535 540
Gly Leu Leu Leu Tyr Cys Lys Ala Arg Ser Thr Pro Val Thr Leu Ser
545 550 555 560
Lys Asp Gln Leu Ser Gly Ile Asn Asn Ile Ala Phe Ser Asn
565 570
<210> 105
<211> 64
<212> БЕЛОК
<213> Респираторный синцитиальный вирус A человека(штамм A2)
<400> 105
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Phe Ala Cys Lys Thr Ala Asn
20 25 30
Gly Thr Ala Ile Pro Ile Gly Gly Gly Ser Ala Asn Val Tyr Val Asn
35 40 45
Leu Ala Pro Val Val Asn Val Gly Gln Asn Leu Val Val Asp Leu Ser
50 55 60
<210> 106
<211> 178
<212> БЕЛОК
<213> Homo sapiens
<400> 106
Met His Ser Ser Ala Leu Leu Cys Cys Leu Val Leu Leu Thr Gly Val
1 5 10 15
Arg Ala Ser Pro Gly Gln Gly Thr Gln Ser Glu Asn Ser Cys Thr His
20 25 30
Phe Pro Gly Asn Leu Pro Asn Met Leu Arg Asp Leu Arg Asp Ala Phe
35 40 45
Ser Arg Val Lys Thr Phe Phe Gln Met Lys Asp Gln Leu Asp Asn Leu
50 55 60
Leu Leu Lys Glu Ser Leu Leu Glu Asp Phe Lys Gly Tyr Leu Gly Cys
65 70 75 80
Gln Ala Leu Ser Glu Met Ile Gln Phe Tyr Leu Glu Glu Val Met Pro
85 90 95
Gln Ala Glu Asn Gln Asp Pro Asp Ile Lys Ala His Val Asn Ser Leu
100 105 110
Gly Glu Asn Leu Lys Thr Leu Arg Leu Arg Leu Arg Arg Cys His Arg
115 120 125
Phe Leu Pro Cys Glu Asn Lys Ser Lys Ala Val Glu Gln Val Lys Asn
130 135 140
Ala Phe Asn Lys Leu Gln Glu Lys Gly Ile Tyr Lys Ala Met Ser Glu
145 150 155 160
Phe Asp Ile Phe Ile Asn Tyr Ile Glu Ala Tyr Met Thr Met Lys Ile
165 170 175
Arg Asn
<210> 107
<211> 57
<212> БЕЛОК
<213> Homo sapiens
<400> 107
Met His Ser Ser Ala Leu Leu Cys Cys Leu Val Leu Leu Thr Gly Val
1 5 10 15
Arg Ala Phe Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile Pro Ile Gly
20 25 30
Gly Gly Ser Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val
35 40 45
Gly Gln Asn Leu Val Val Asp Leu Ser
50 55
<210> 108
<211> 562
<212> БЕЛОК
<213> Вирус гриппа A (штамм A/Japan/305/1957 H2N2)
<400> 108
Met Ala Ile Ile Tyr Leu Ile Leu Leu Phe Thr Ala Val Arg Gly Asp
1 5 10 15
Gln Ile Cys Ile Gly Tyr His Ala Asn Asn Ser Thr Glu Lys Val Asp
20 25 30
Thr Asn Leu Glu Arg Asn Val Thr Val Thr His Ala Lys Asp Ile Leu
35 40 45
Glu Lys Thr His Asn Gly Lys Leu Cys Lys Leu Asn Gly Ile Pro Pro
50 55 60
Leu Glu Leu Gly Asp Cys Ser Ile Ala Gly Trp Leu Leu Gly Asn Pro
65 70 75 80
Glu Cys Asp Arg Leu Leu Ser Val Pro Glu Trp Ser Tyr Ile Met Glu
85 90 95
Lys Glu Asn Pro Arg Asp Gly Leu Cys Tyr Pro Gly Ser Phe Asn Asp
100 105 110
Tyr Glu Glu Leu Lys His Leu Leu Ser Ser Val Lys His Phe Glu Lys
115 120 125
Val Lys Ile Leu Pro Lys Asp Arg Trp Thr Gln His Thr Thr Thr Gly
130 135 140
Gly Ser Arg Ala Cys Ala Val Ser Gly Asn Pro Ser Phe Phe Arg Asn
145 150 155 160
Met Val Trp Leu Thr Lys Glu Gly Ser Asp Tyr Pro Val Ala Lys Gly
165 170 175
Ser Tyr Asn Asn Thr Ser Gly Glu Gln Met Leu Ile Ile Trp Gly Val
180 185 190
His His Pro Ile Asp Glu Thr Glu Gln Arg Thr Leu Tyr Gln Asn Val
195 200 205
Gly Thr Tyr Val Ser Val Gly Thr Ser Thr Leu Asn Lys Arg Ser Thr
210 215 220
Pro Glu Ile Ala Thr Arg Pro Lys Val Asn Gly Gln Gly Gly Arg Met
225 230 235 240
Glu Phe Ser Trp Thr Leu Leu Asp Met Trp Asp Thr Ile Asn Phe Glu
245 250 255
Ser Thr Gly Asn Leu Ile Ala Pro Glu Tyr Gly Phe Lys Ile Ser Lys
260 265 270
Arg Gly Ser Ser Gly Ile Met Lys Thr Glu Gly Thr Leu Glu Asn Cys
275 280 285
Glu Thr Lys Cys Gln Thr Pro Leu Gly Ala Ile Asn Thr Thr Leu Pro
290 295 300
Phe His Asn Val His Pro Leu Thr Ile Gly Glu Cys Pro Lys Tyr Val
305 310 315 320
Lys Ser Glu Lys Leu Val Leu Ala Thr Gly Leu Arg Asn Val Pro Gln
325 330 335
Ile Glu Ser Arg Gly Leu Phe Gly Ala Ile Ala Gly Phe Ile Glu Gly
340 345 350
Gly Trp Gln Gly Met Val Asp Gly Trp Tyr Gly Tyr His His Ser Asn
355 360 365
Asp Gln Gly Ser Gly Tyr Ala Ala Asp Lys Glu Ser Thr Gln Lys Ala
370 375 380
Phe Asp Gly Ile Thr Asn Lys Val Asn Ser Val Ile Glu Lys Met Asn
385 390 395 400
Thr Gln Phe Glu Ala Val Gly Lys Glu Phe Gly Asn Leu Glu Arg Arg
405 410 415
Leu Glu Asn Leu Asn Lys Arg Met Glu Asp Gly Phe Leu Asp Val Trp
420 425 430
Thr Tyr Asn Ala Glu Leu Leu Val Leu Met Glu Asn Glu Arg Thr Leu
435 440 445
Asp Phe His Asp Ser Asn Val Lys Asn Leu Tyr Asp Lys Val Arg Met
450 455 460
Gln Leu Arg Asp Asn Val Lys Glu Leu Gly Asn Gly Cys Phe Glu Phe
465 470 475 480
Tyr His Lys Cys Asp Asp Glu Cys Met Asn Ser Val Lys Asn Gly Thr
485 490 495
Tyr Asp Tyr Pro Lys Tyr Glu Glu Glu Ser Lys Leu Asn Arg Asn Glu
500 505 510
Ile Lys Gly Val Lys Leu Ser Ser Met Gly Val Tyr Gln Ile Leu Ala
515 520 525
Ile Tyr Ala Thr Val Ala Gly Ser Leu Ser Leu Ala Ile Met Met Ala
530 535 540
Gly Ile Ser Phe Trp Met Cys Ser Asn Gly Ser Leu Gln Cys Arg Ile
545 550 555 560
Cys Ile
<210> 109
<211> 54
<212> БЕЛОК
<213> Вирус гриппа A (штамм A/Japan/305/1957 H2N2)
<400> 109
Met Ala Ile Ile Tyr Leu Ile Leu Leu Phe Thr Ala Val Arg Gly Phe
1 5 10 15
Ala Cys Lys Thr Ala Asn Gly Thr Ala Ile Pro Ile Gly Gly Gly Ser
20 25 30
Ala Asn Val Tyr Val Asn Leu Ala Pro Val Val Asn Val Gly Gln Asn
35 40 45
Leu Val Val Asp Leu Ser
50
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МУТАНТЫ FIMH E. COLI И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2831010C1 |
| КОМПОЗИЦИИ ESCHERICHIA COLI И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2788526C2 |
| ВЫДЕЛЕННОЕ АНТИТЕЛО (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ АНТИТЕЛА, ВЫДЕЛЕННАЯ НУКЛЕИНОВАЯ КИСЛОТА, ЭКСПРЕССИОННАЯ КАССЕТА (ВАРИАНТЫ), ПЛАЗМИДА (ВАРИАНТЫ), КЛЕТКА-ХОЗЯИН, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, НАБОР, СПОСОБ ЛЕЧЕНИЯ БОЛЬНОГО, ПОДВЕРЖЕННОГО РИСКУ ИЛИ СТРАДАЮЩЕГО ОТ ИНФЕКЦИИ E.COLI, И СПОСОБ ДИАГНОСТИКИ ОПРЕДЕЛЕНИЯ ИНФЕКЦИЙ E.COLI | 2014 |
|
RU2724530C2 |
| Композиции с Neisseria meningitidis и способы их применения | 2020 |
|
RU2839906C1 |
| КОМПОЗИЦИИ NEISSERIA MENINGITIDIS И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2739504C2 |
| СПОСОБ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ БЕЛКОВОГО/ПЕПТИДНОГО АНТИГЕНА | 2021 |
|
RU2830627C1 |
| ПРИМЕНЕНИЕ ГЛИКОЗИДАЗ В ПОЛУЧЕНИИ ОЛИГОСАХАРИДОВ | 2019 |
|
RU2810730C2 |
| ФЕРМЕНТАТИВНЫЙ СИНТЕЗ N-АЦЕТИЛНЕЙРАМИНОВОЙ КИСЛОТЫ | 2018 |
|
RU2809787C2 |
| ФЕРМЕНТАТИВНОЕ ПОЛУЧЕНИЕ СИАЛИЛИРОВАННЫХ САХАРИДОВ | 2019 |
|
RU2819876C2 |
| СПОСОБ СНИЖЕНИЯ ОШИБОЧНОГО ВКЛЮЧЕНИЯ НЕКАНОНИЧЕСКИХ АМИНОКИСЛОТ С РАЗВЕТВЛЕННОЙ ЦЕПЬЮ | 2019 |
|
RU2816654C2 |








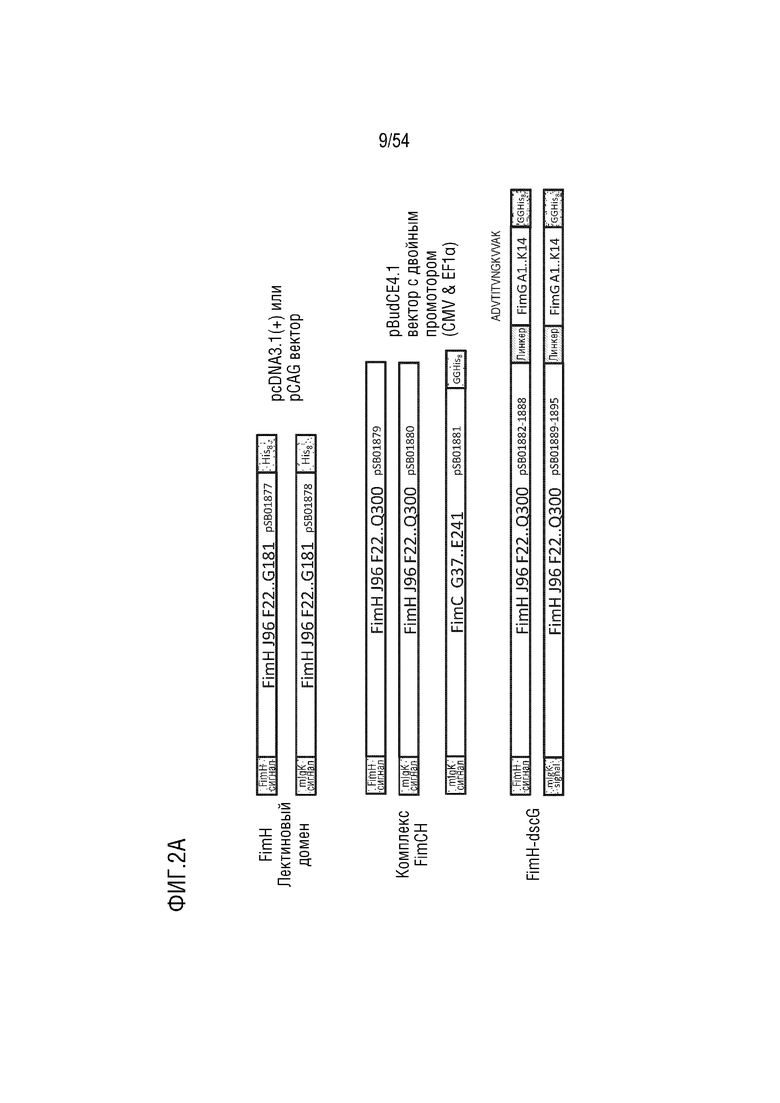
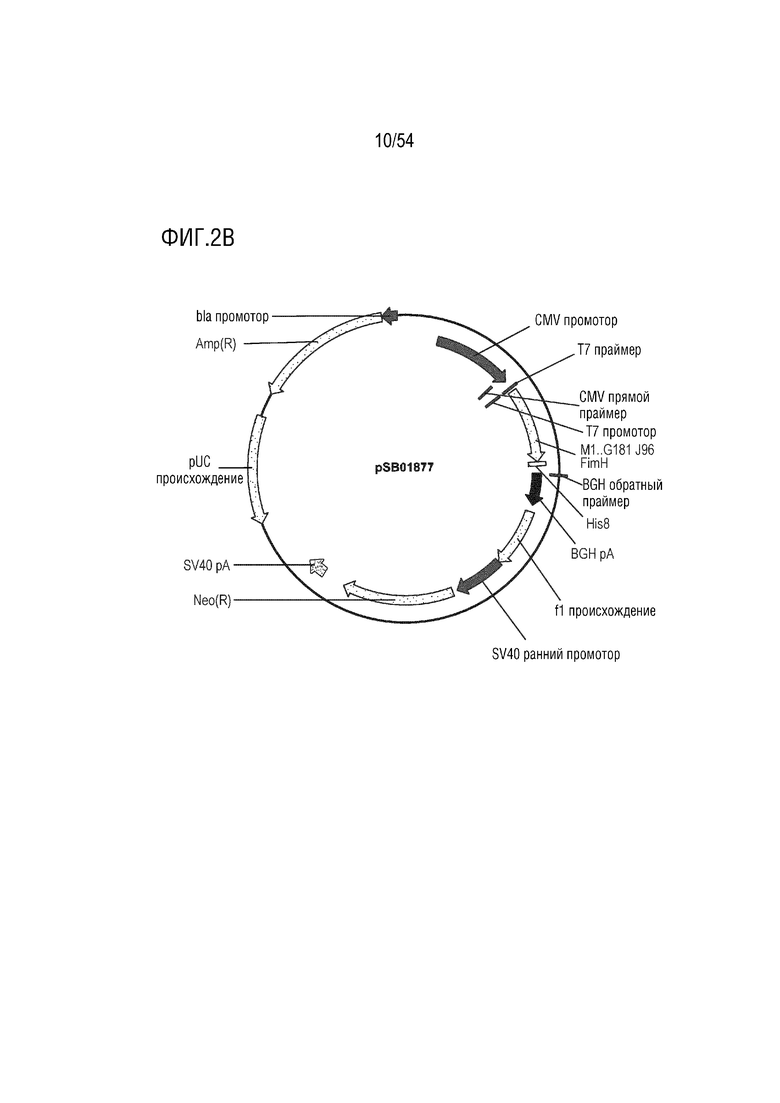
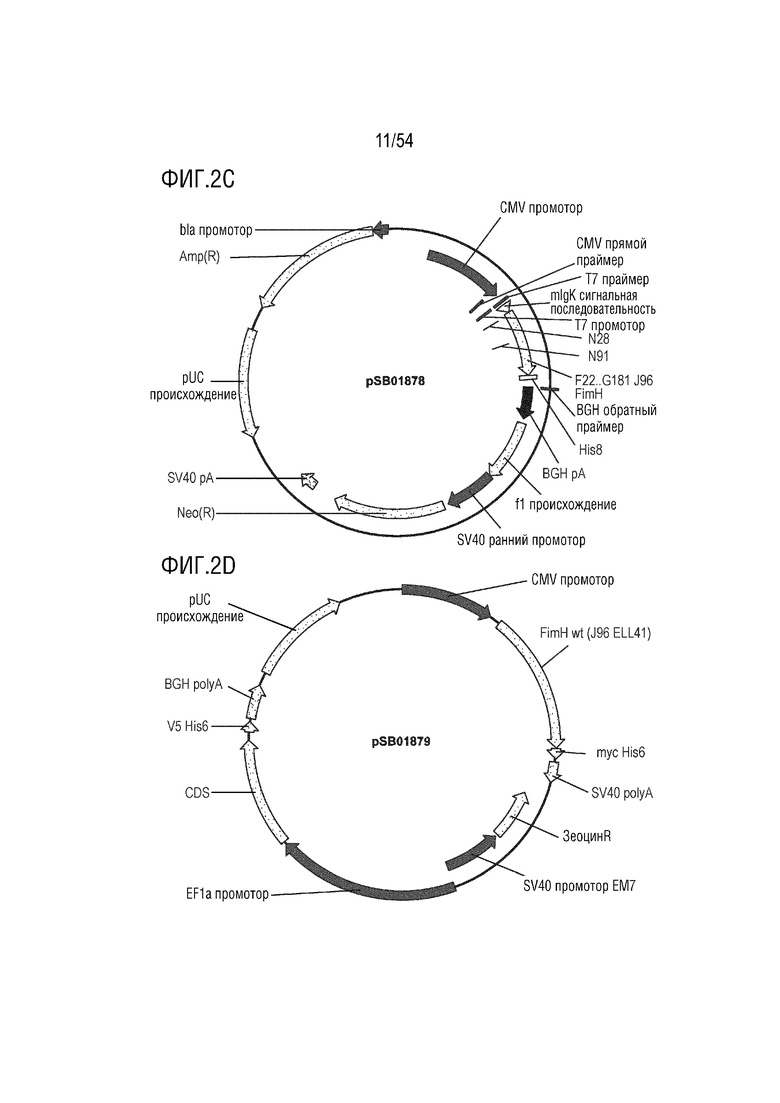
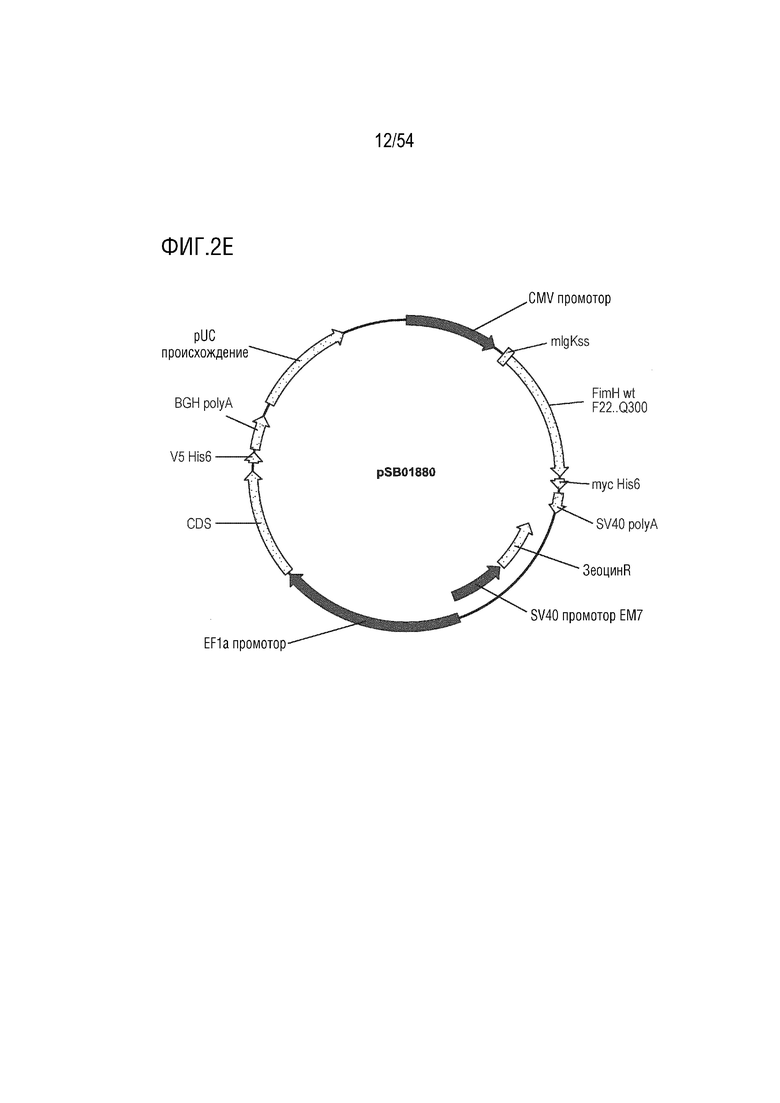
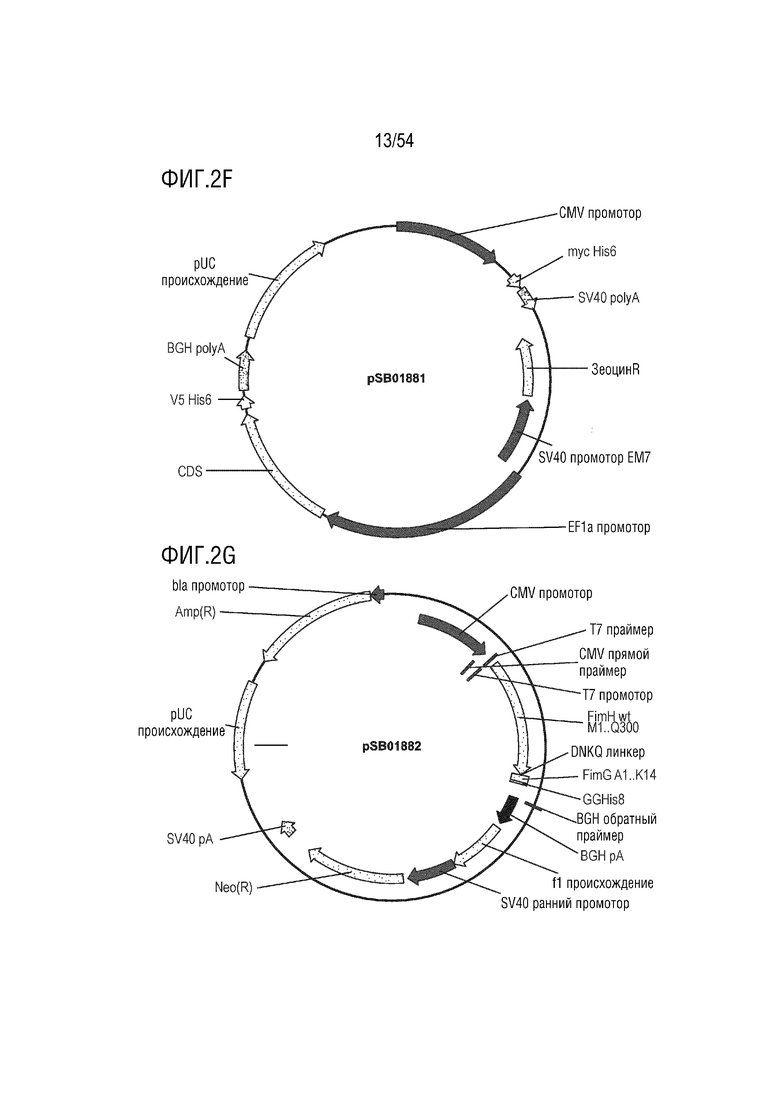
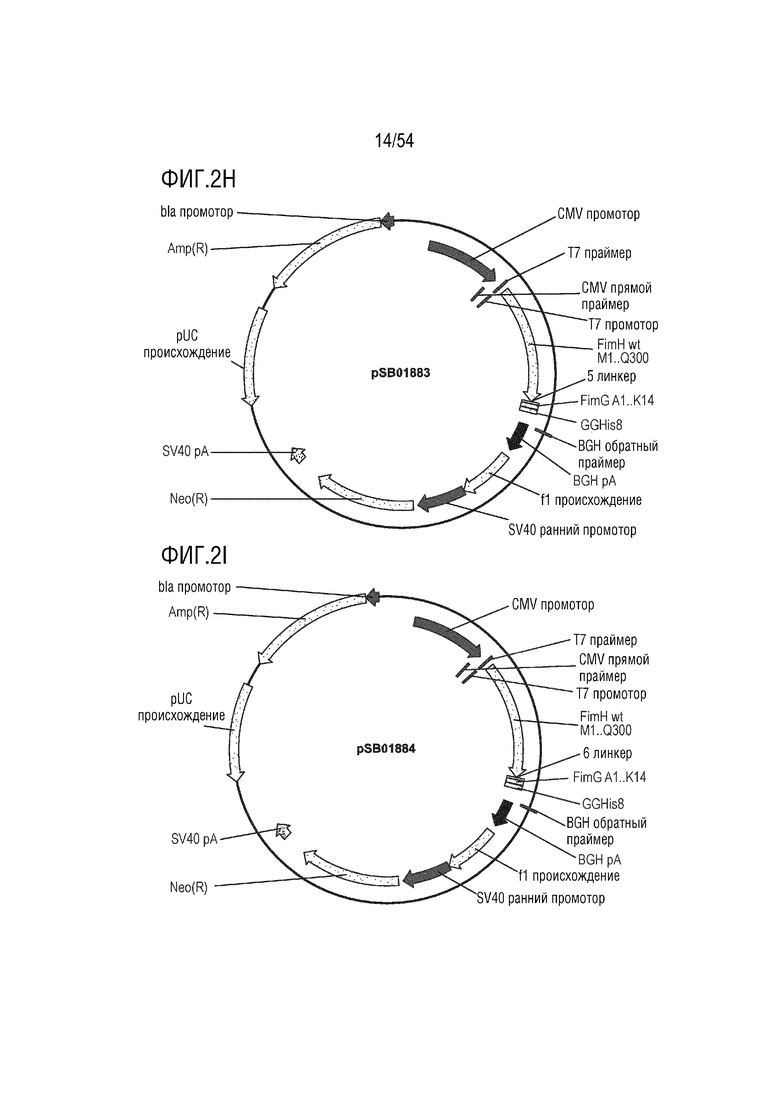
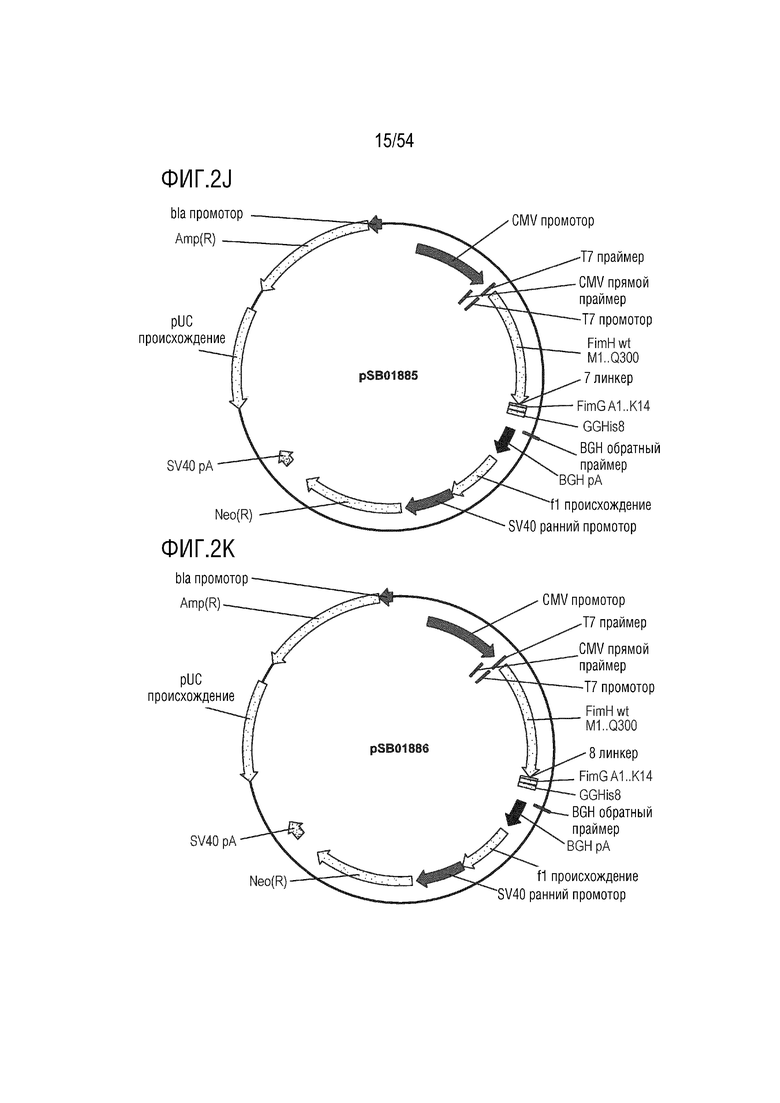
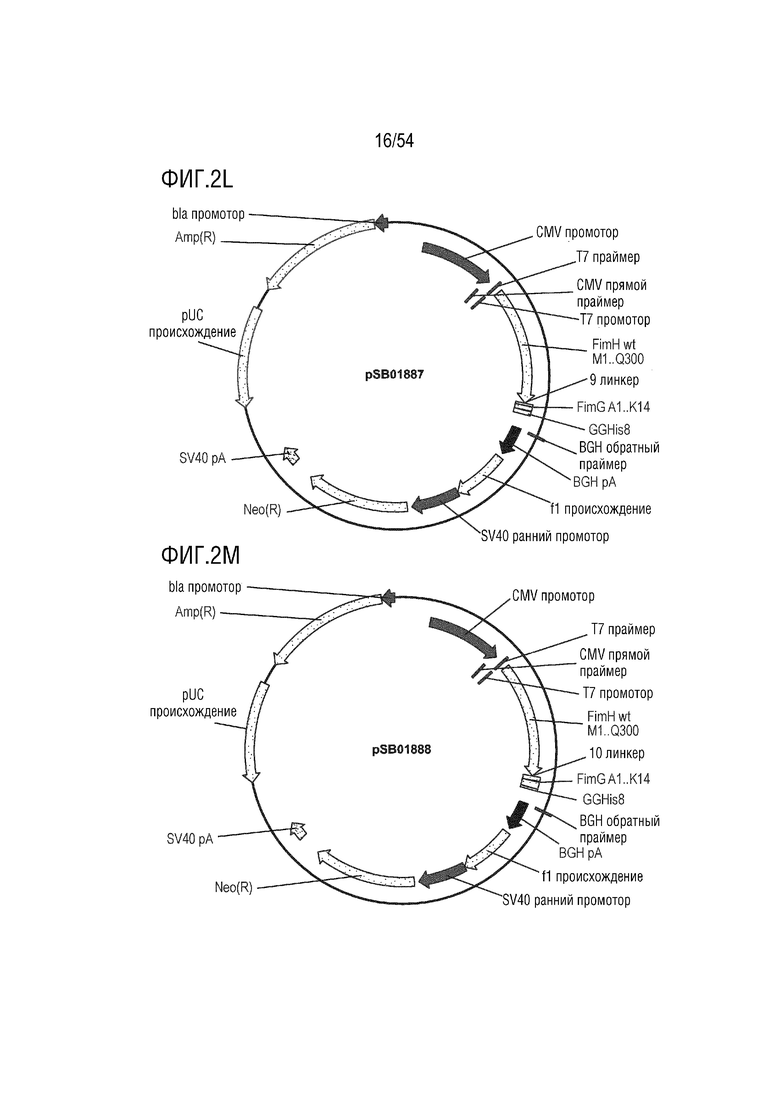
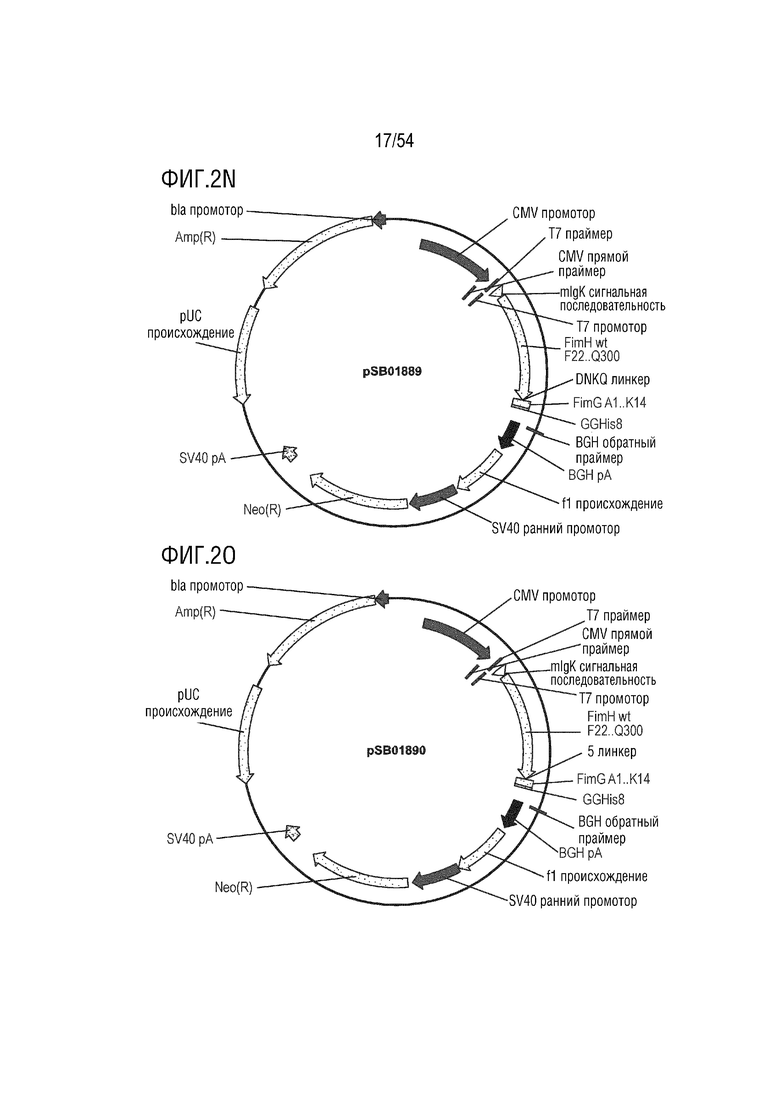
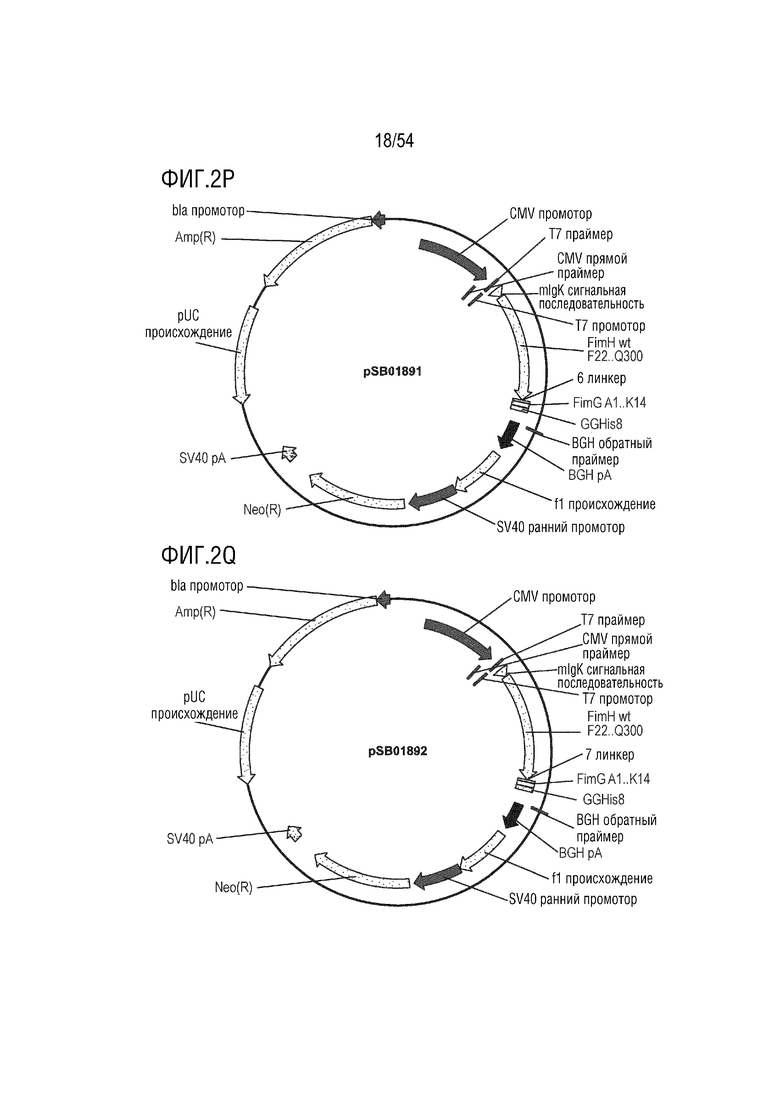
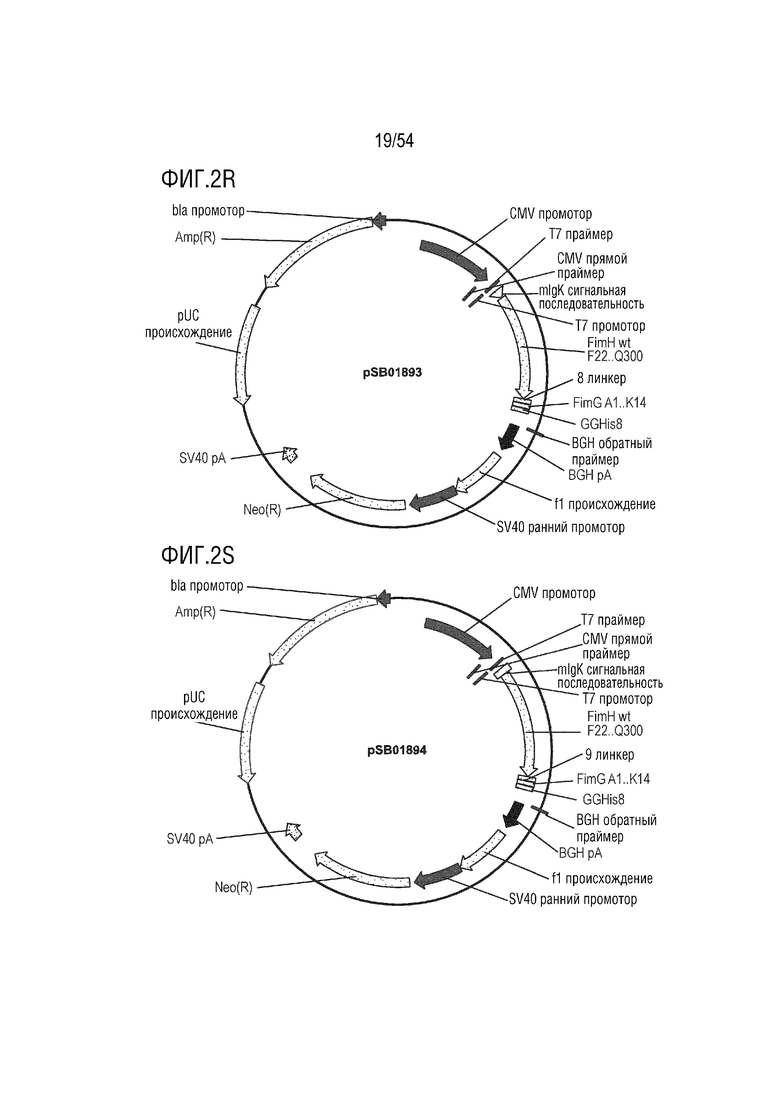
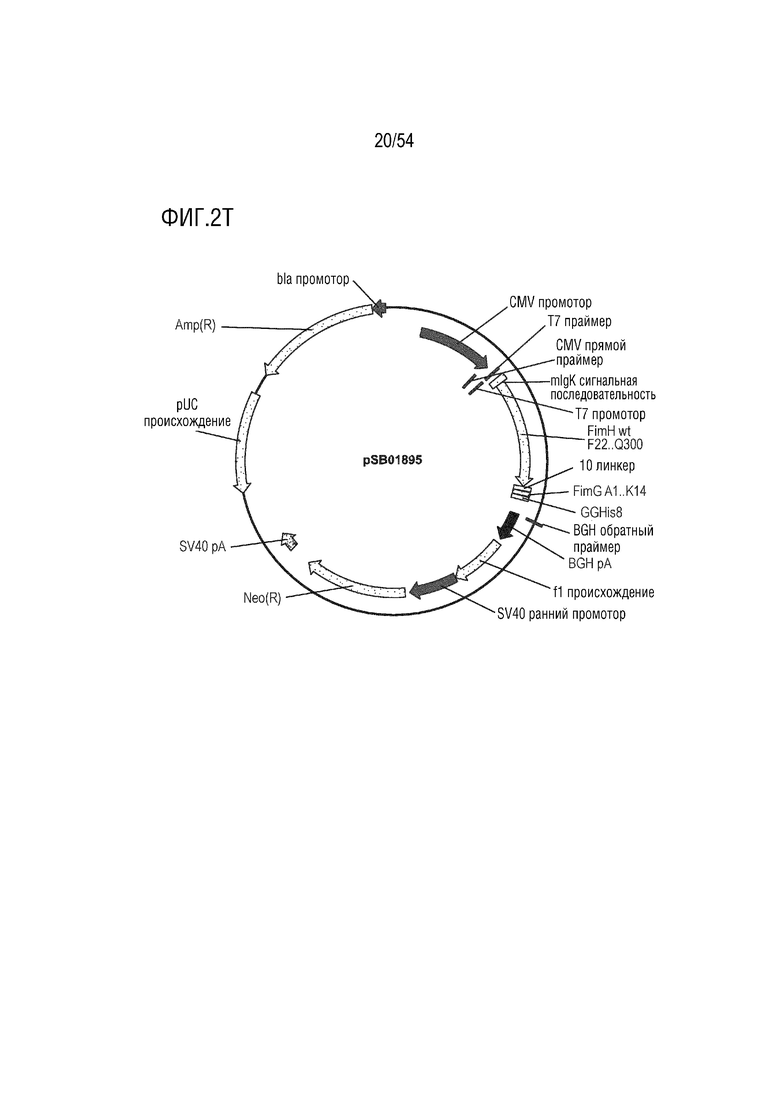
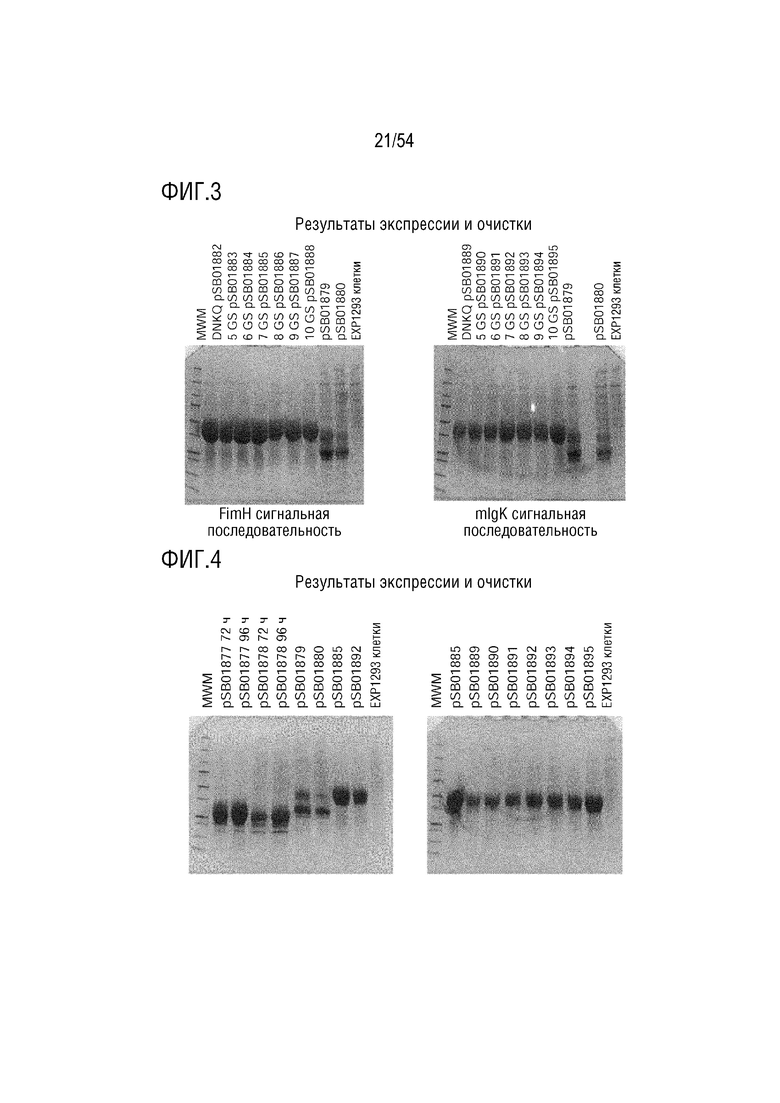
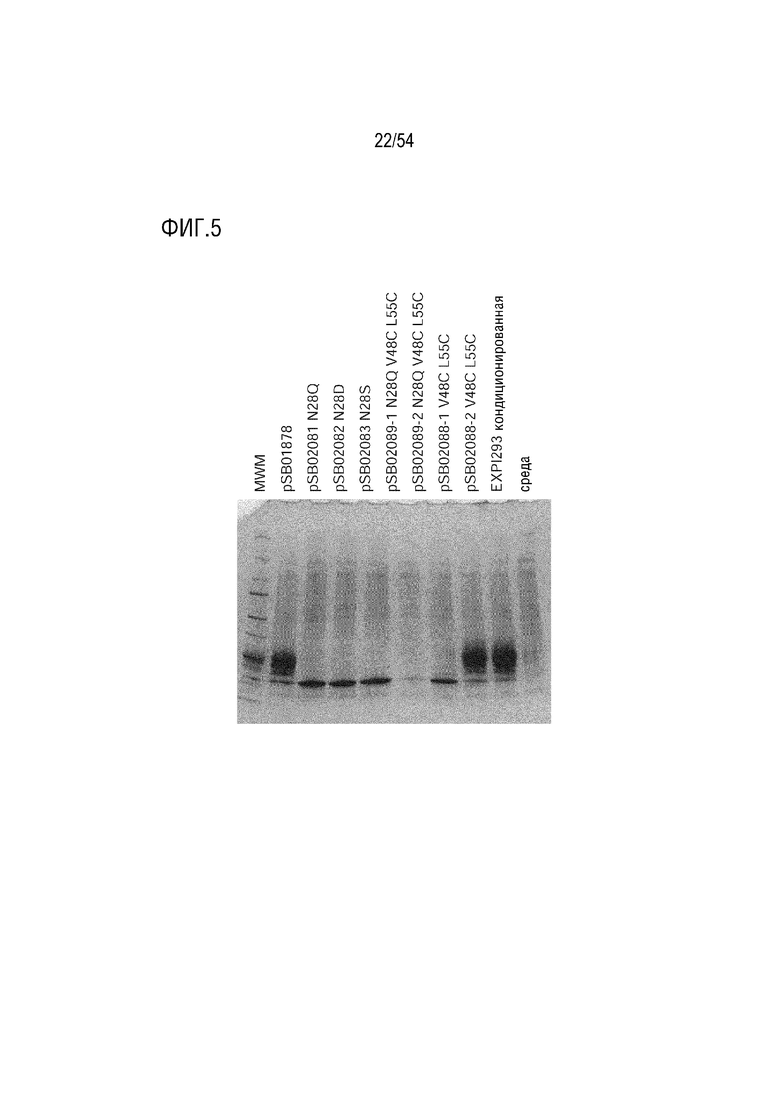

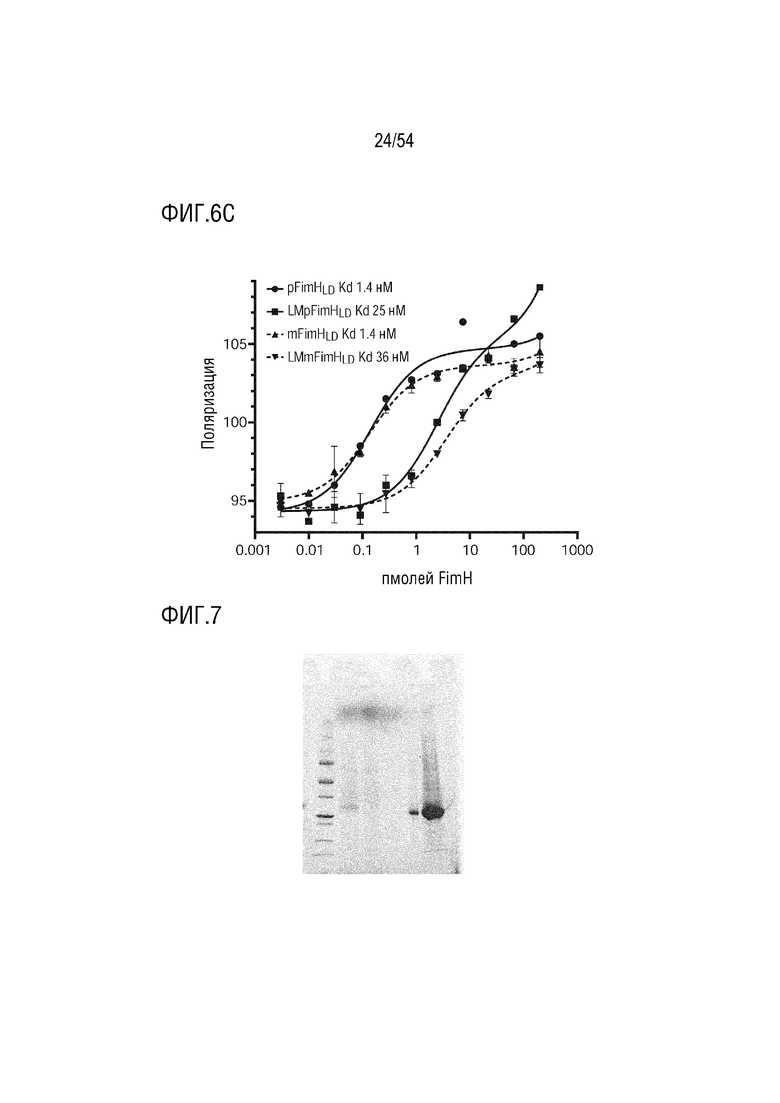
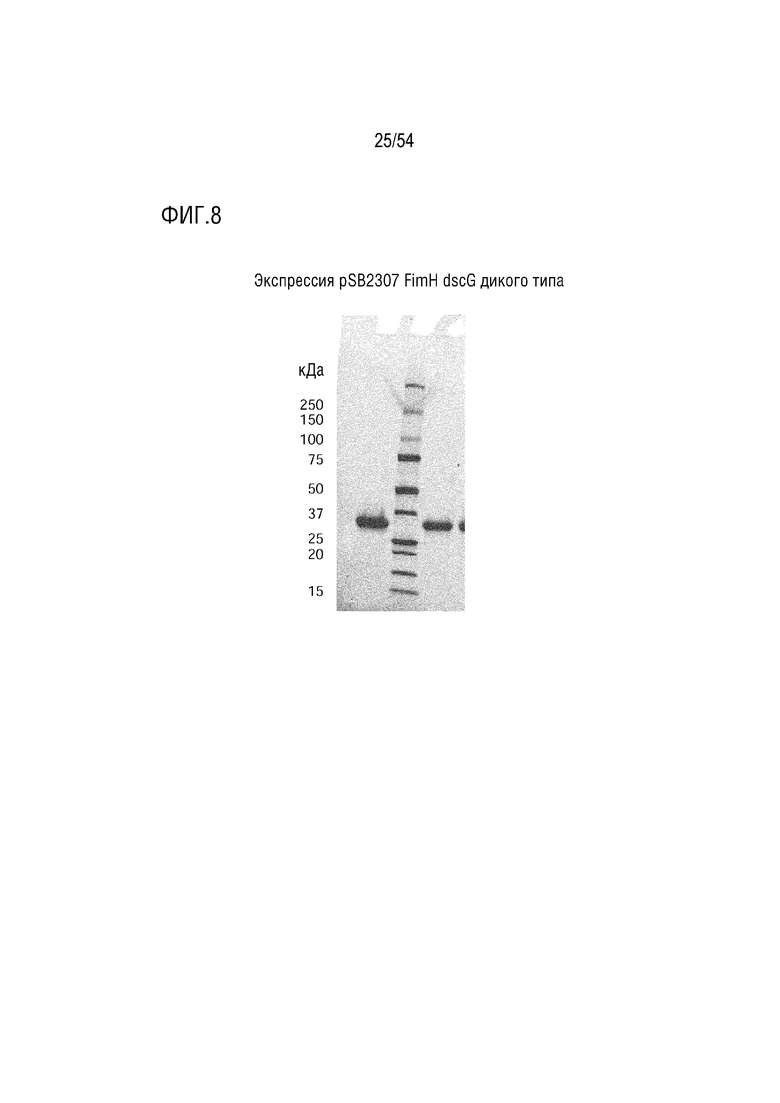




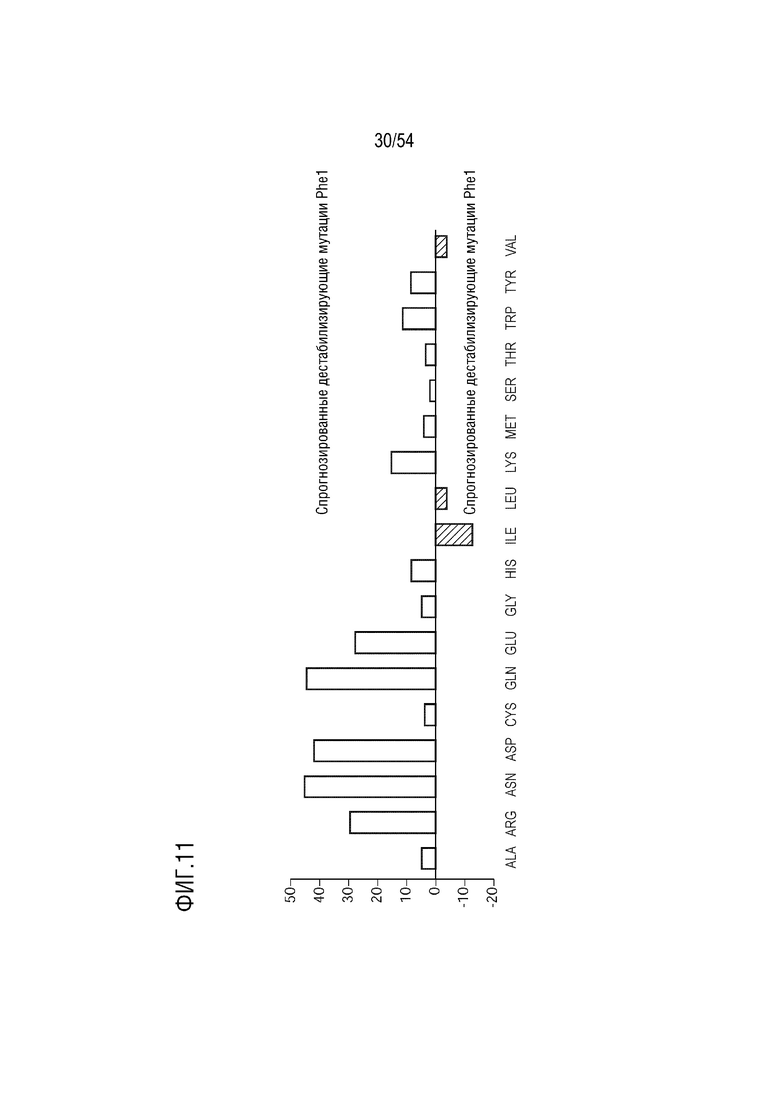
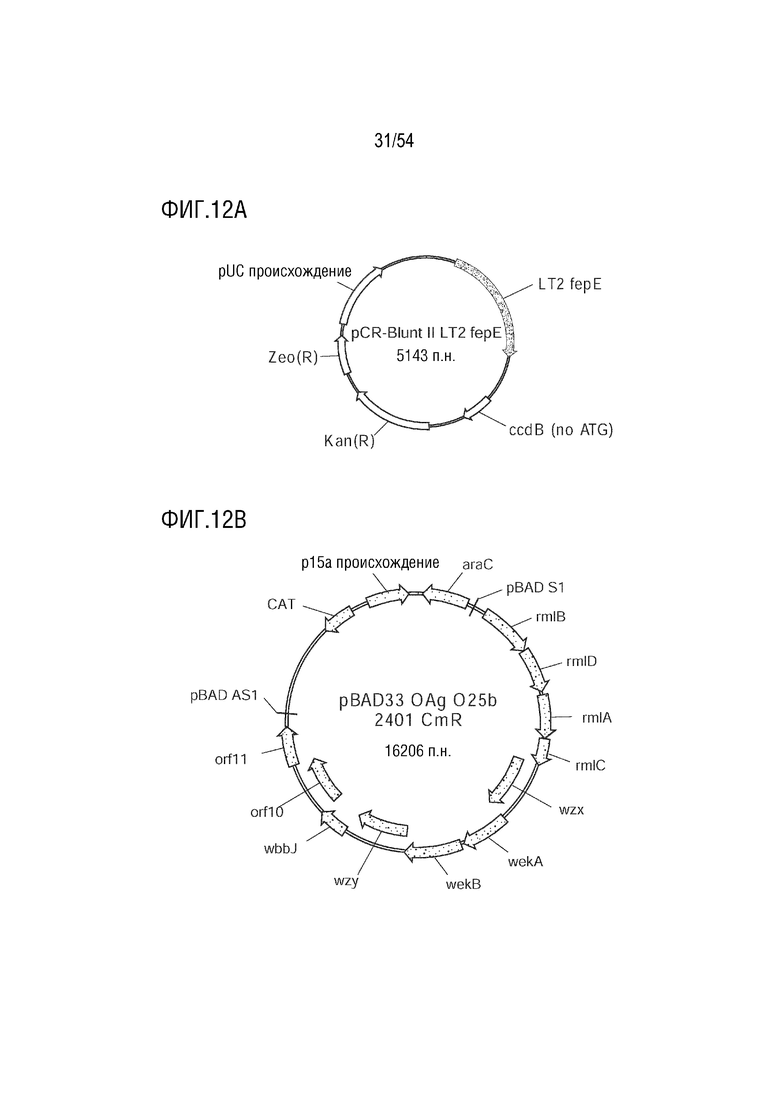
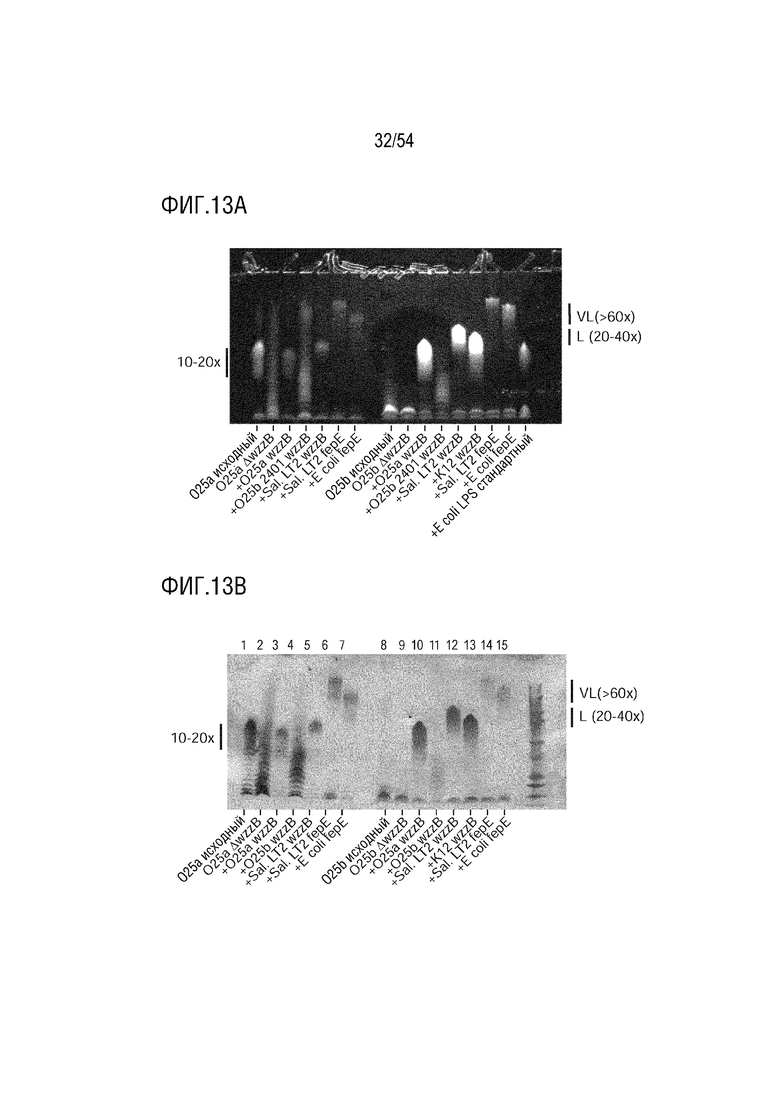
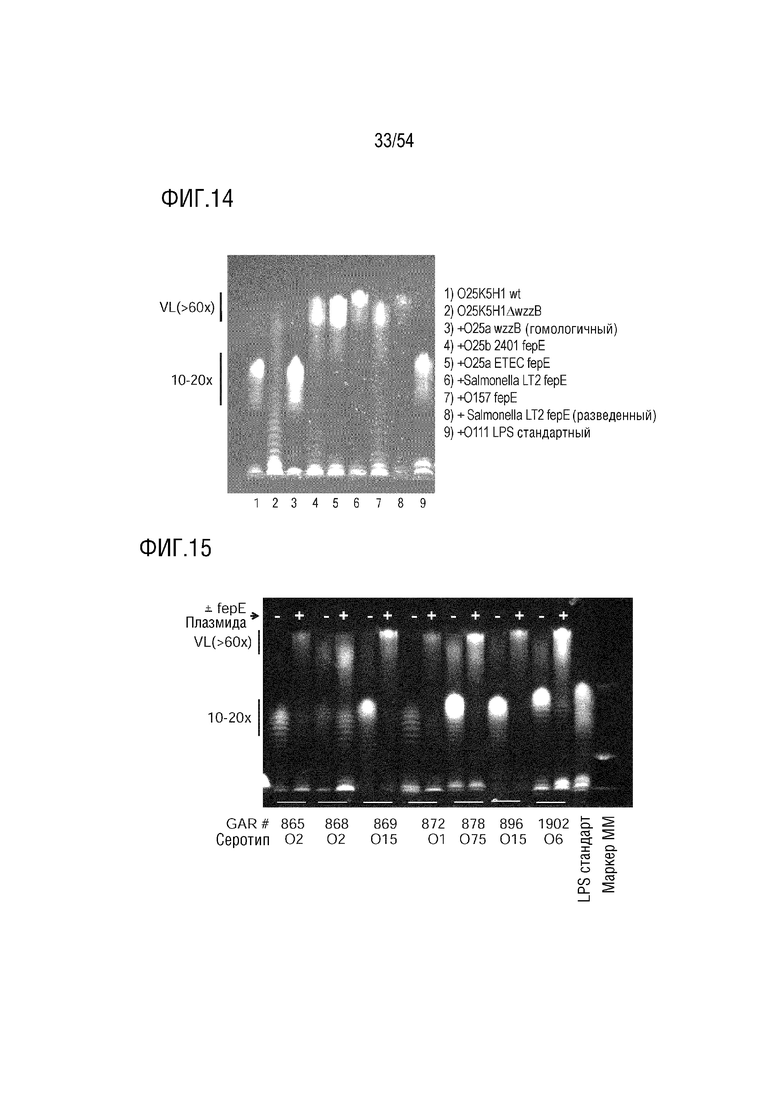
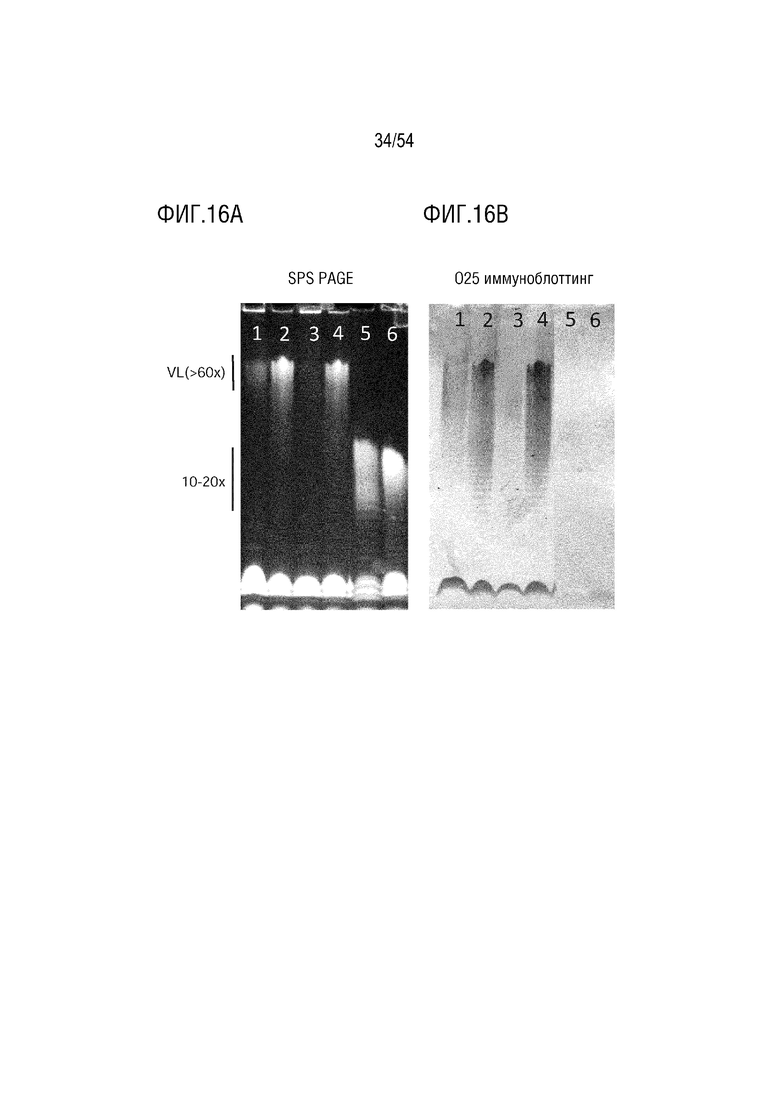


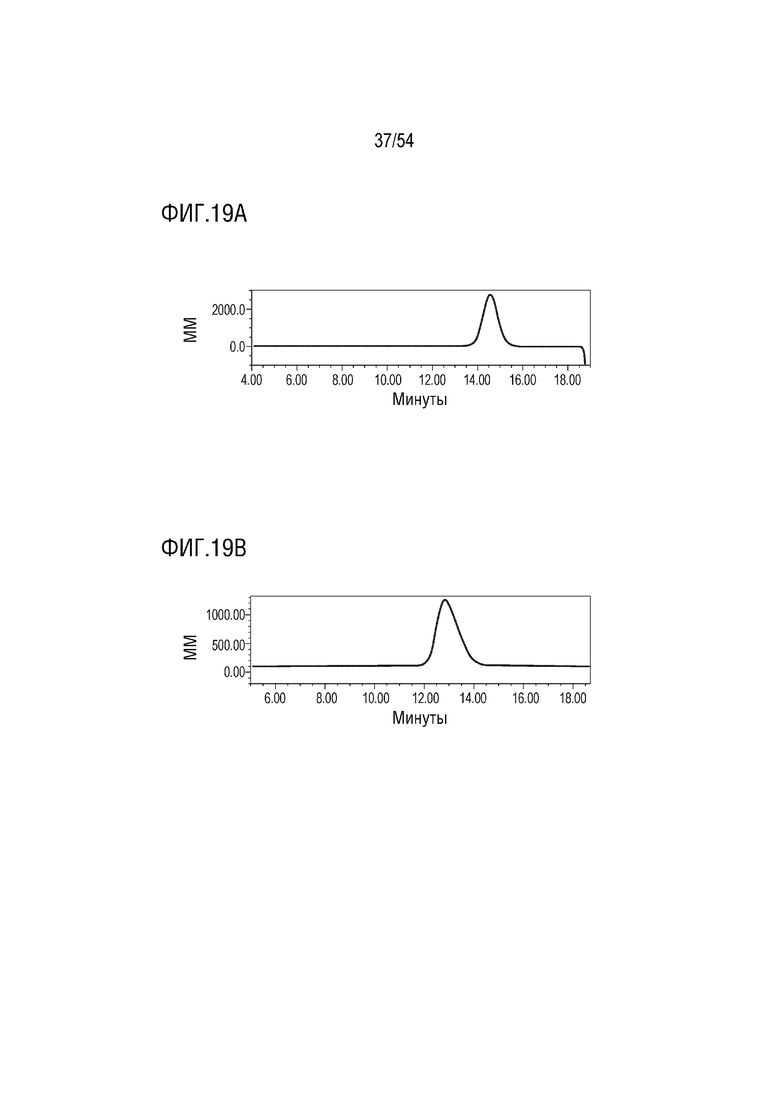
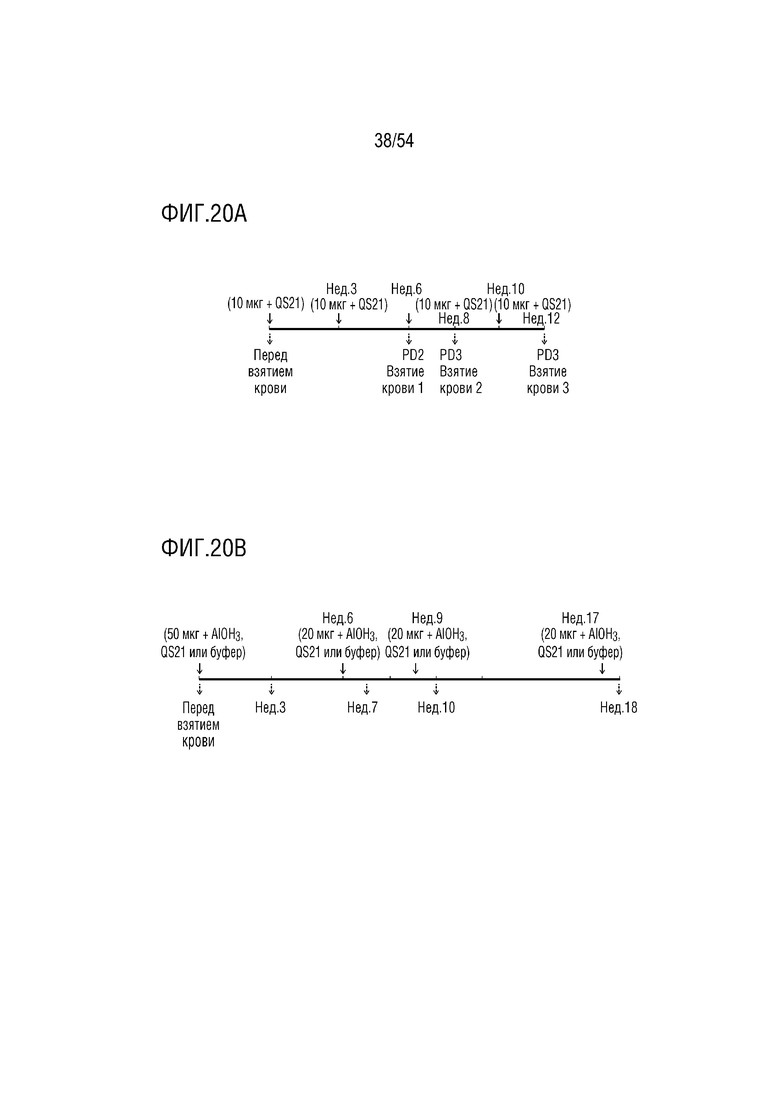
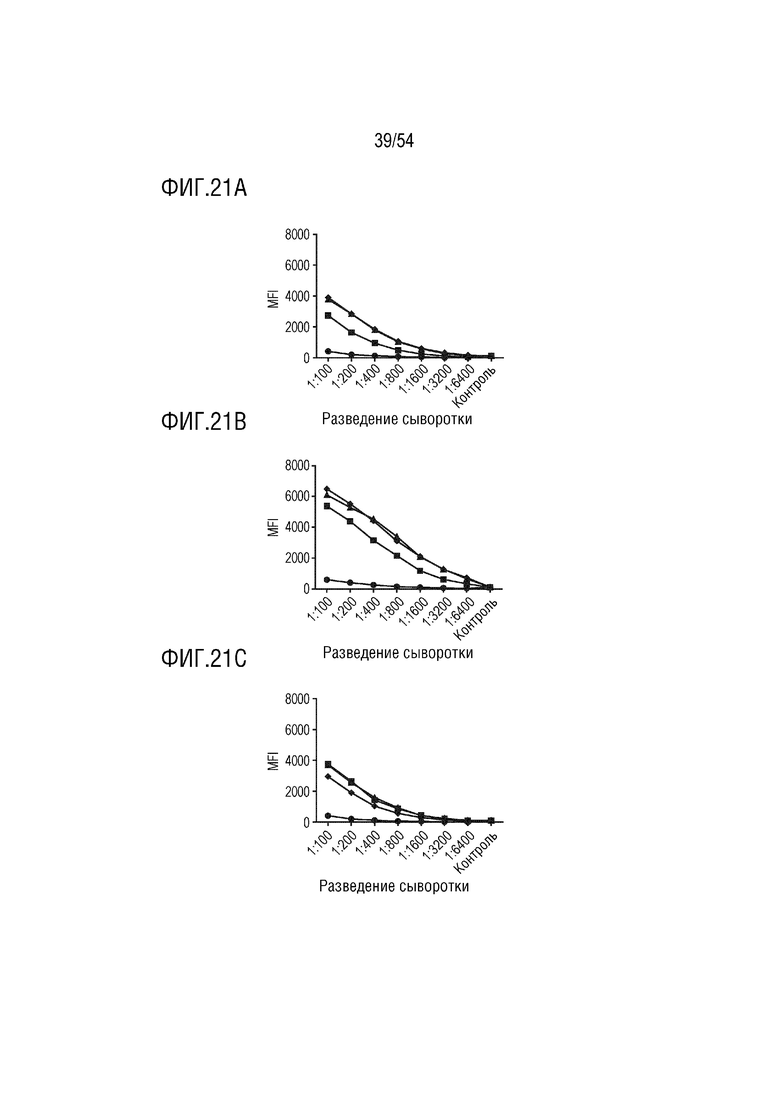
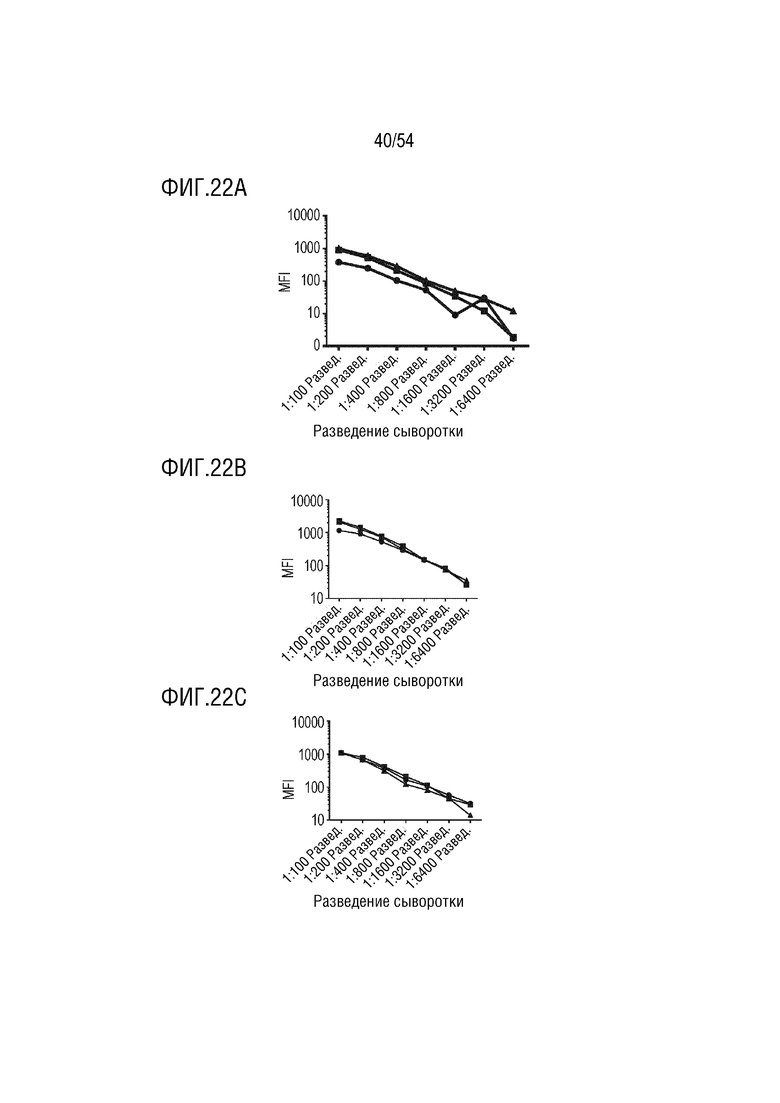
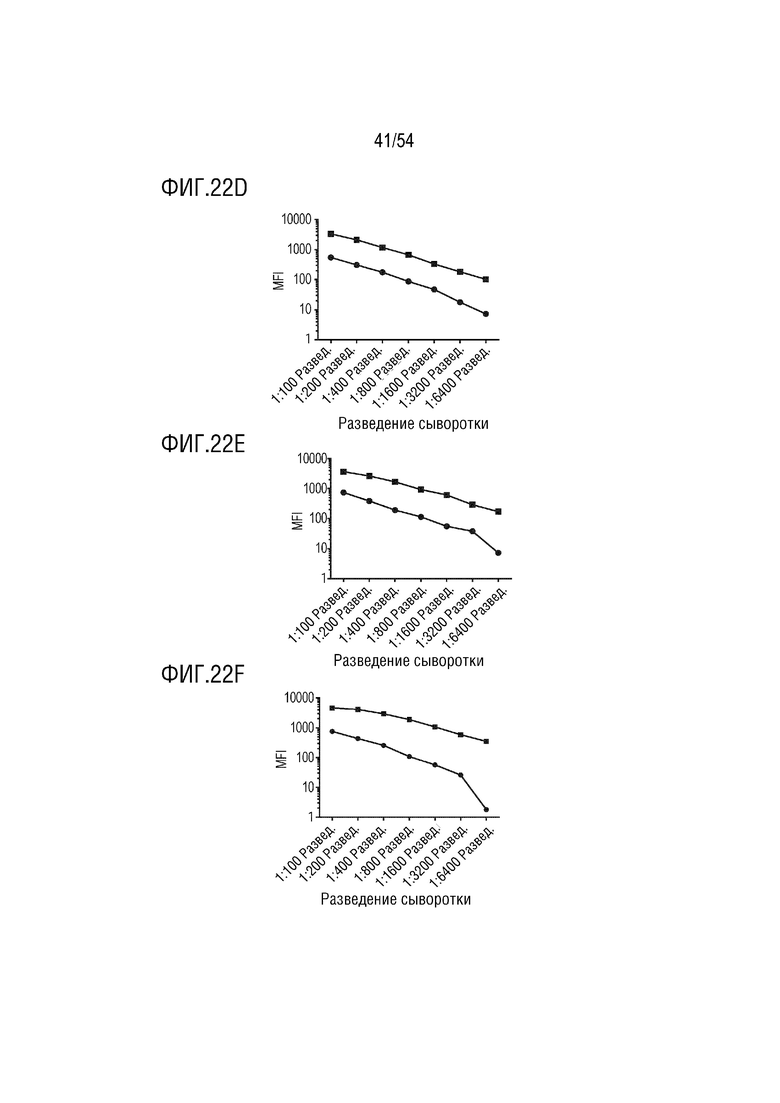
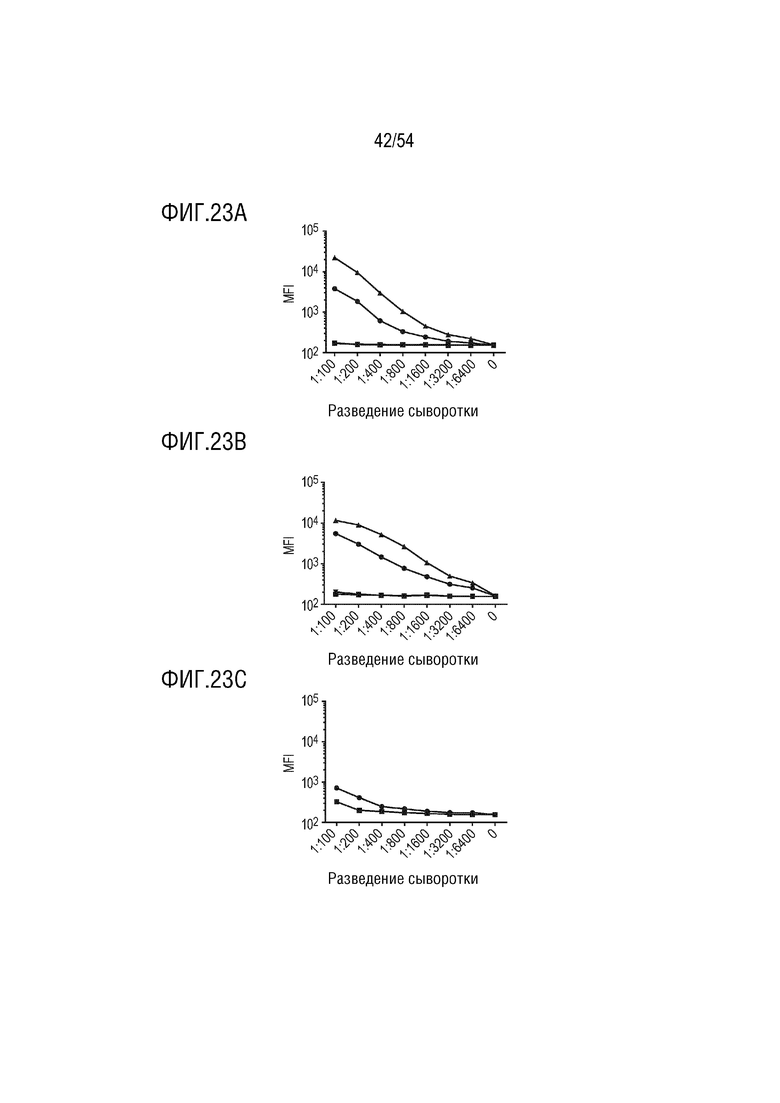
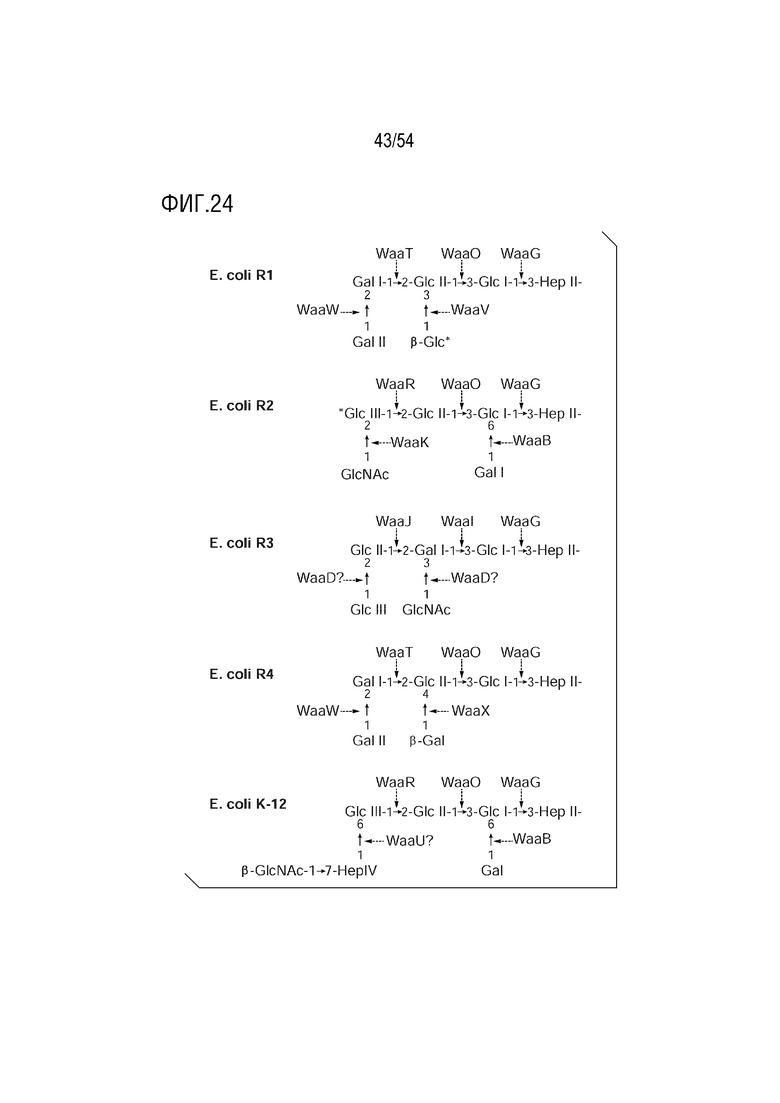
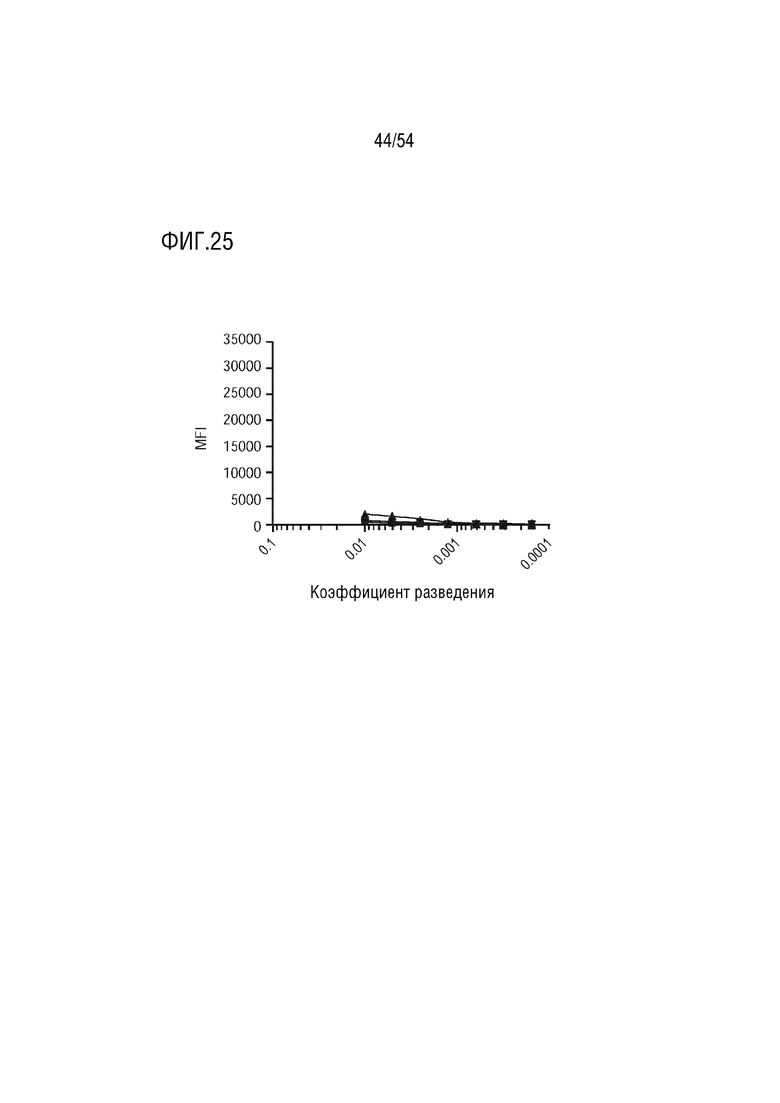
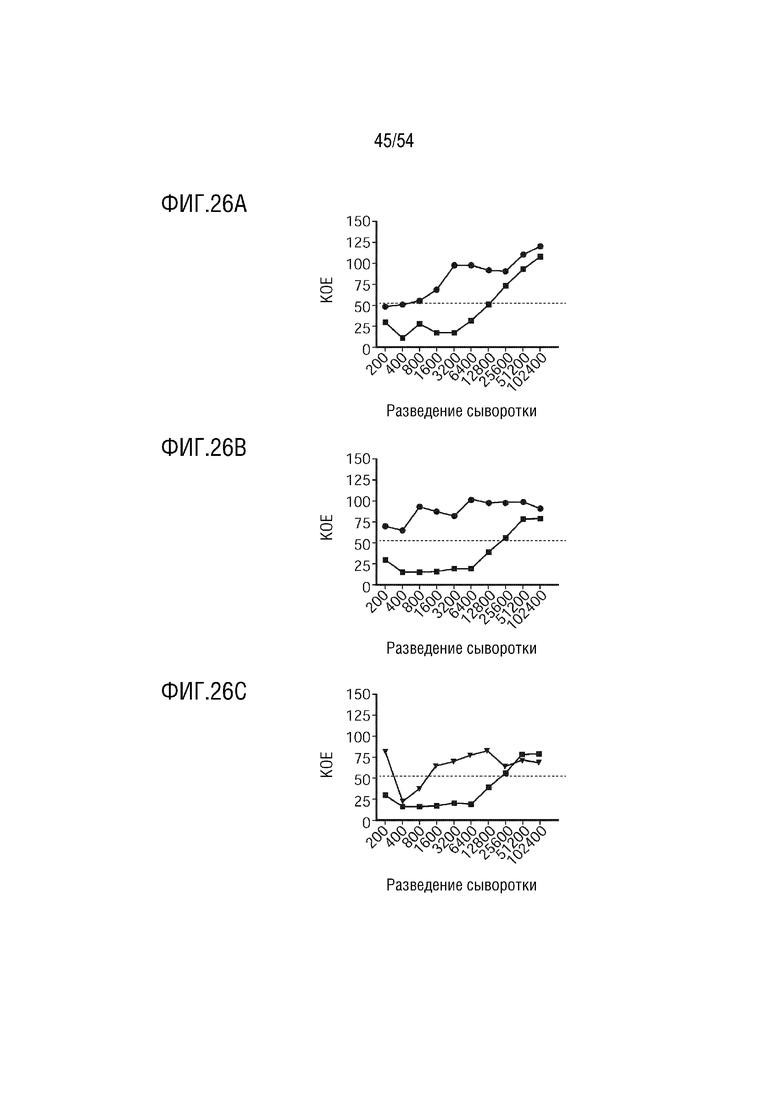
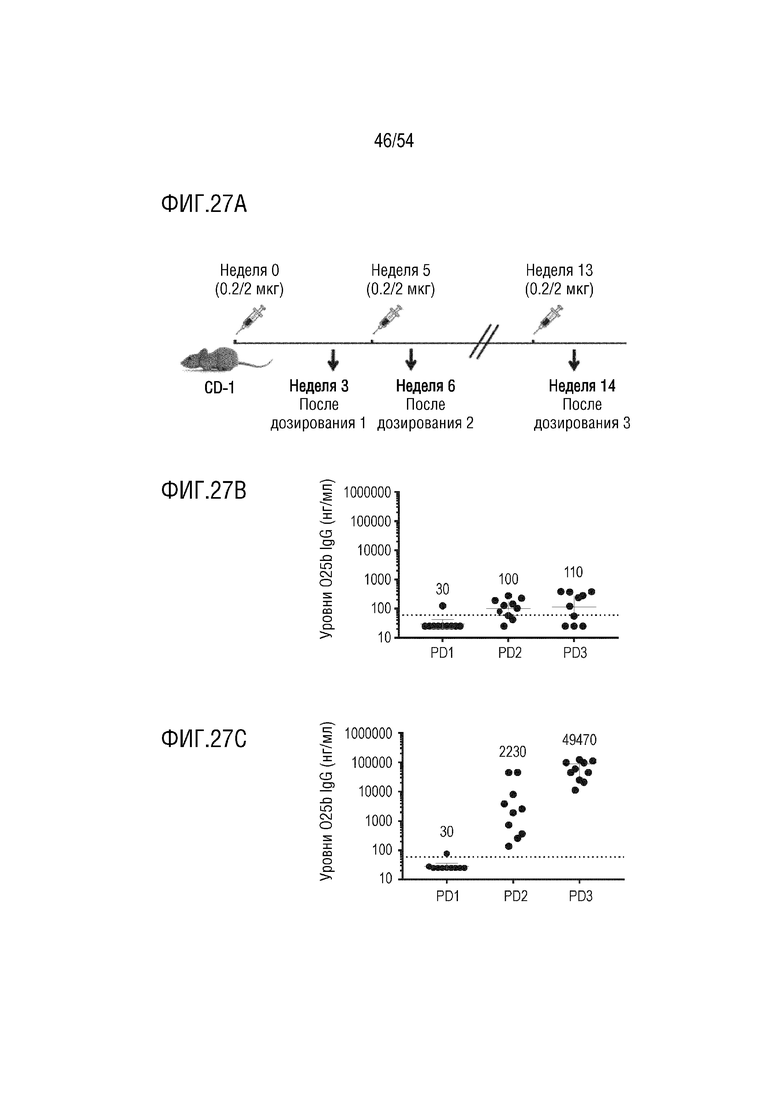
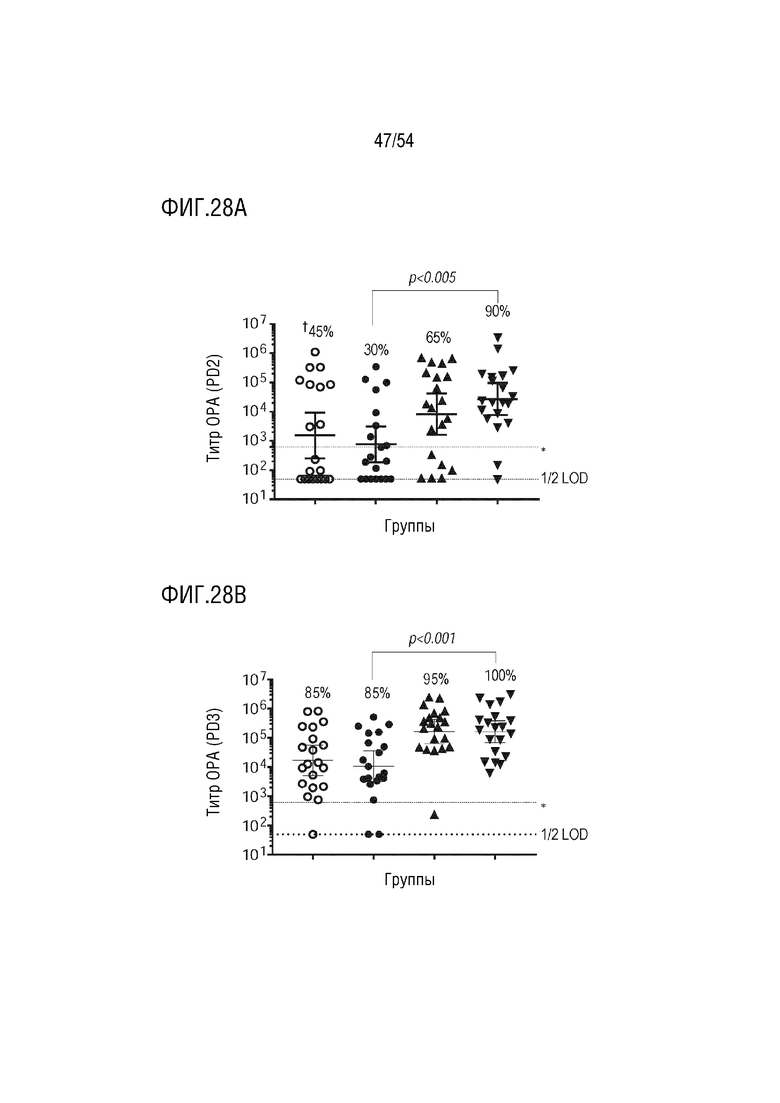
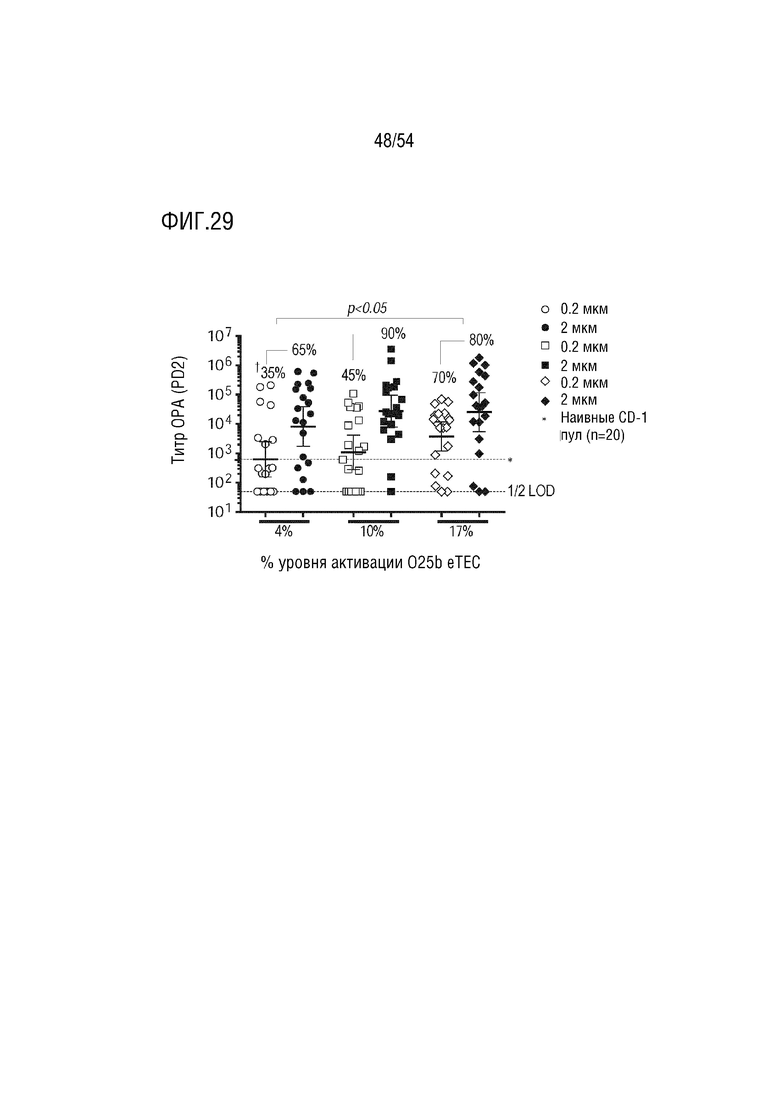
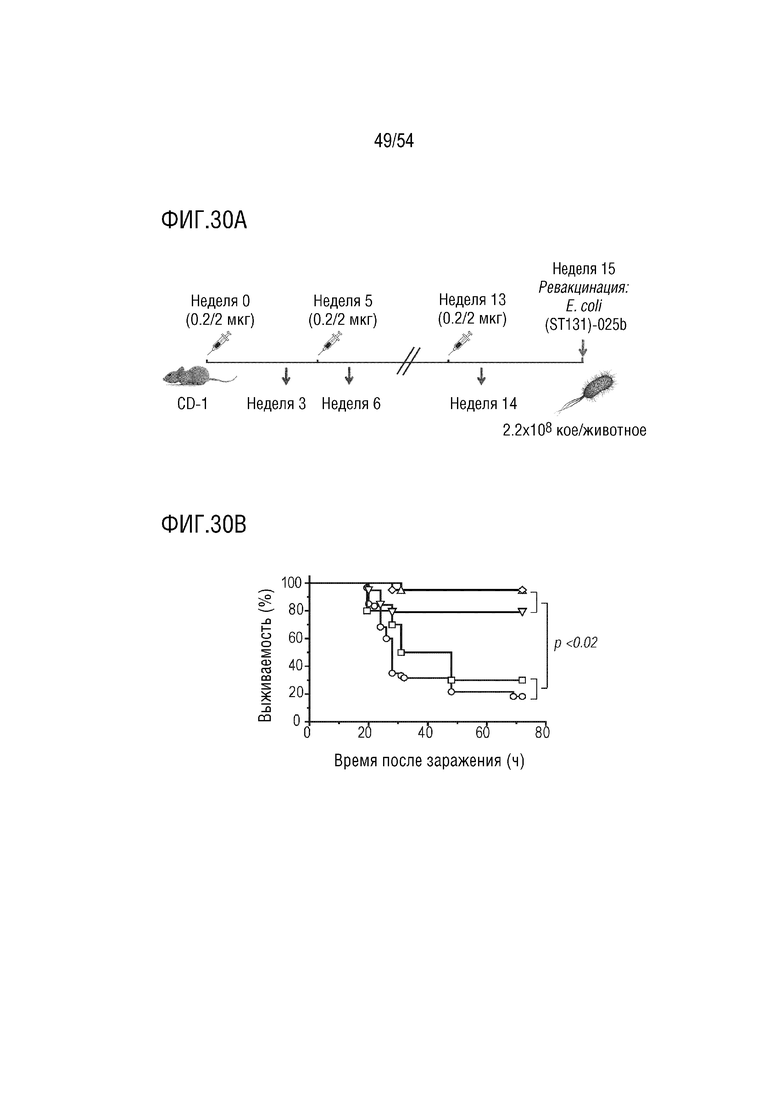
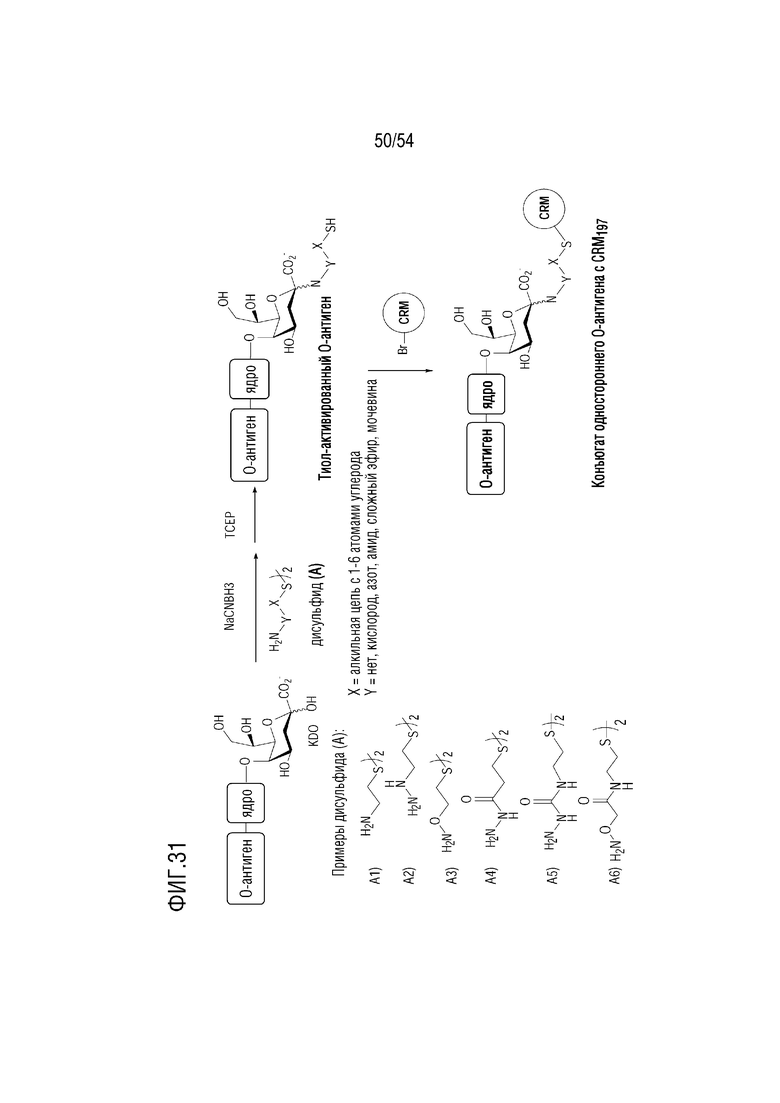
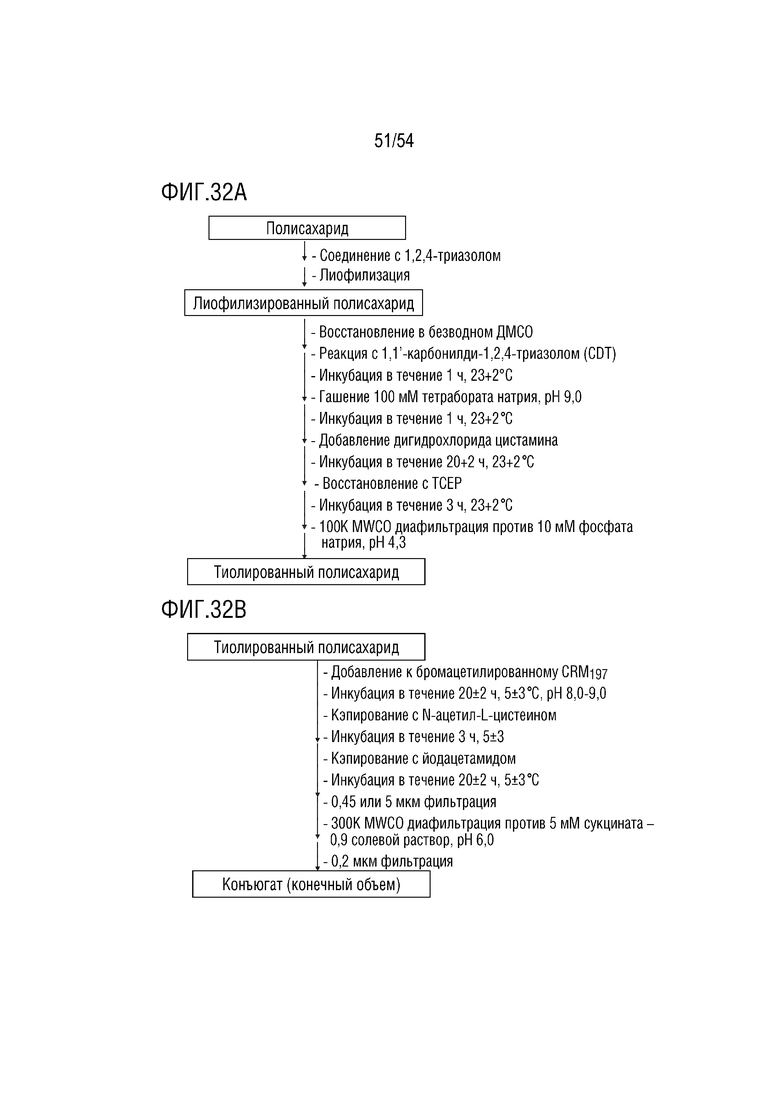

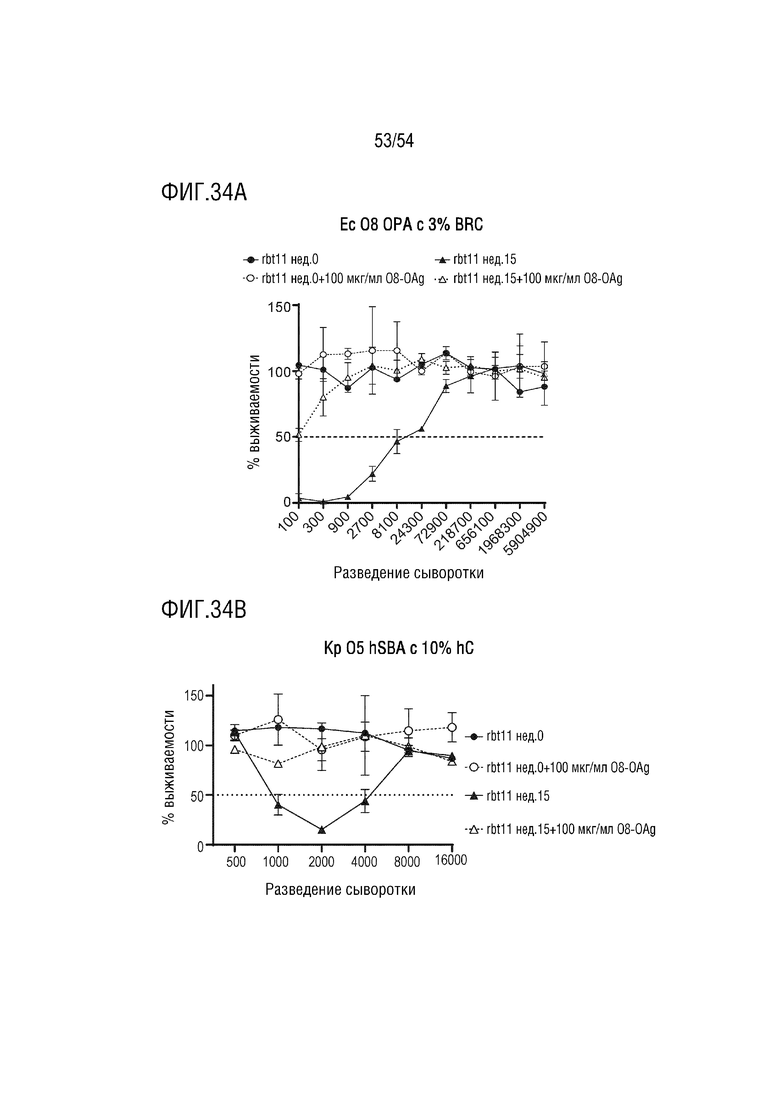
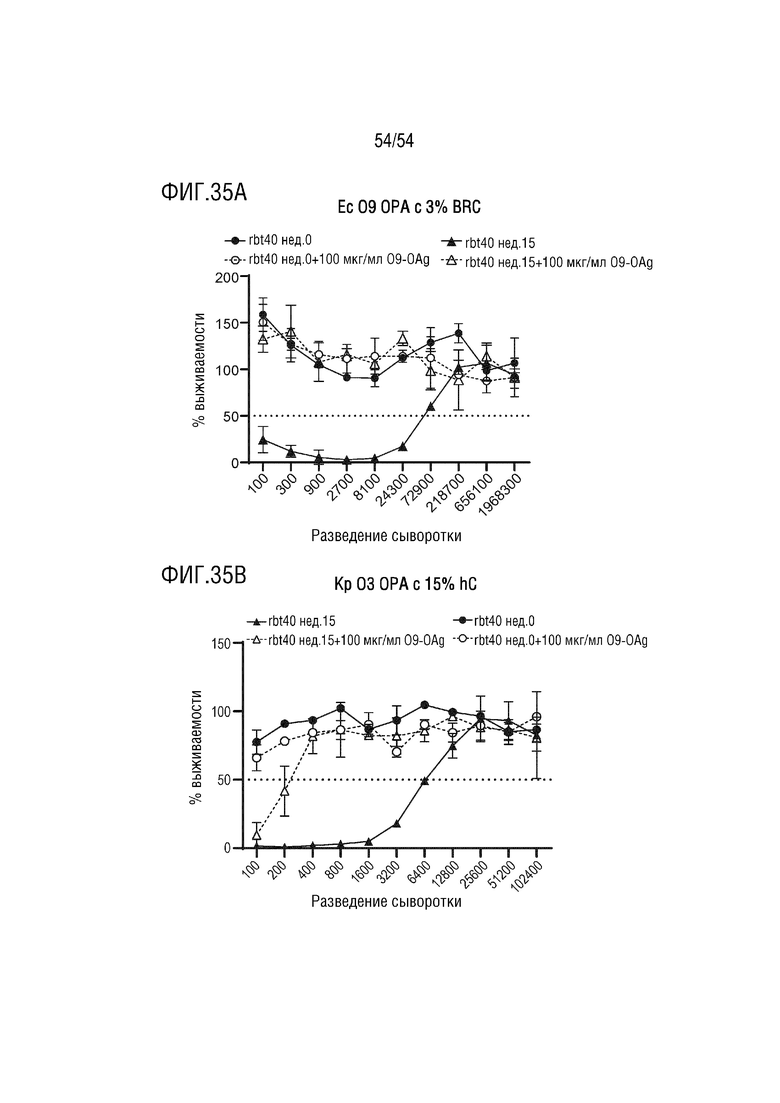
Настоящее изобретение относится к области биотехнологии, в частности к области иммунологии. Изобретение раскрывает композицию модифицированных на белке-носителе О-полисахаридов, полученных из бактерий Escherichia coli (E. coli) и Klebsiella pneumoniae (K. pneumoniae). Изобретение может быть применимо в медицинской практике для индукции иммунного ответа к E. coli и к K. pneumoniae у субъекта. 4 н. и 12 з.п. ф-лы, 34 табл., 35 ил., 35 пр.
1. Композиция для индукции иммунного ответа против Escherichia coli (E. coli) и Klebsiella pneumoniae (K. pneumoniae) у млекопитающего, содержащая сахарид, полученный из E.coli, содержащий Формулу, выбранную из группы, состоящей из
Формулы O1, содержащей структуру [→3)-α-L-Rha-(1→3)-α-L-Rha-(1→3)-β-L-Rha-(1→4)-β-D-GlcNAc-(1→ | β-D-ManNAc-(1→2)]n;
Формулы O2, содержащей структуру [→3)-α-L-Rha-(1→2)-α-L-Rha-(1→3)-β-L-Rha-(1→4)-β-D-GlcNAc-(1→ | α-D-Fuc3NAc-(1→2)]n;
Формулы O6, содержащей структуру [→4)-α-D-GalNAc-(1→3)-β-D-Man-(1→4)-β-D-Man-(1→3)-α-D-GlcNAc-(1→ | β-D-Glc-(1→2)]n или [→4)-α-D-GalNAc-(1→3)-β-D-Man-(1→4)-β-D-Man-(1→3)-α-D-GlcNAc-(1→|β-D-GlcNAc-(1→2)]n; и
Формулы O25, содержащей структуру [β-d-Glc-(1→6) | →4)-α-d-Glc-(1→3)-α-l-FucNAc-(1→3)-β-d-GlcNAc-(1→ | α-l-Rha-(1→3)]n или
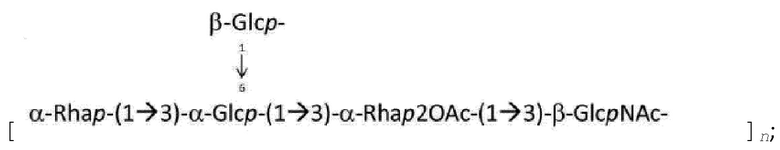
и сахарид, полученный из K. pneumoniae, содержащий Формулу, выбранную из группы, состоящей из
Формулы O1, содержащей структуру [→3)-β-D-Galf-(1→3)-α-D-Galp-(1→]n, [→3)-α-D-Galp-(1→3)-β-D-Galp-(1→]n, как [→3)-β-D-Galf-(1→3)-α-D-Galp-(1→]n, так и [→3)-α-D-Galp-(1→3)-β-D-Galp-(1→]n, или [→3)-β-D-Galf-(1→3)-[α-D-Galp-(1→4)]-α-D-Galp-(1→]n;
Формулы O2, содержащей структуру [→3)-α-ᴅ-Galp-(1→3)-β-D -Galf-(1→]n или [→3)-β-D -GlcpNAc-(1→5)-β-D-Galf-(1→]n;
Формулы O3, содержащей структуру [→2)-α-d-Man-(1→2)-α-d-Man-(1→3)-α-d-Man-(1→3)-α-d-Man-(1→]n; и
Формулы O5, содержащей структуру [→2)-α-d-Man-(1→2)-α-d-Man-(1→3)-β-d-Man-(1→]n.
2. Композиция по п.1, содержащая сахарид, полученный из Klebsiella pneumoniae, содержащий Формулу O1.
3. Композиция по п. 1, содержащая сахарид, полученный из K. pneumoniae, содержащий Формулу О2.
4. Композиция по п. 1, содержащая сахарид, полученный из K. pneumoniae, содержащий Формулу О3.
5. Композиция по п. 1, содержащая сахарид, полученный из K. pneumoniae, содержащий Формулу О5.
6. Композиция по п. 1, содержащая сахарид, полученный из K. pneumoniae, содержащий Формулу O1, и сахарид, полученный из K. pneumoniae, содержащий Формулу О2.
7. Композиция по п. 1, где композиция содержит структуру сахаридов E. coli, содержащую каждую из следующих Формул: Формула O25, Формула O1A, Формула O2 и Формула O6.
8. Композиция для индукции иммунного ответа против Escherichia coli (E. coli) и Klebsiella pneumoniae (K. pneumoniae) у млекопитающего, содержащая сахарид, полученный из E.coli, содержащий Формулу, выбранную из группы, состоящей из
Формулы O1, содержащей структуру [→3)-α-L-Rha-(1→3)-α-L-Rha-(1→3)-β-L-Rha-(1→4)-β-D-GlcNAc-(1→ | β-D-ManNAc-(1→2)]n;
Формулы O2, содержащей структуру [→3)-α-L-Rha-(1→2)-α-L-Rha-(1→3)-β-L-Rha-(1→4)-β-D-GlcNAc-(1→ | α-D-Fuc3NAc-(1→2)]n;
Формулы O6, содержащей структуру [→4)-α-D-GalNAc-(1→3)-β-D-Man-(1→4)-β-D-Man-(1→3)-α-D-GlcNAc-(1→ | β-D-Glc-(1→2)]n или [→4)-α-D-GalNAc-(1→3)-β-D-Man-(1→4)-β-D-Man-(1→3)-α-D-GlcNAc-(1→|β-D-GlcNAc-(1→2)]n; и
Формулы O25, содержащей структуру [β-d-Glc-(1→6) | →4)-α-d-Glc-(1→3)-α-l-FucNAc-(1→3)-β-d-GlcNAc-(1→ | α-l-Rha-(1→3)]n или
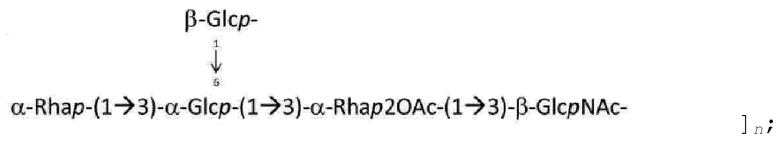
и сахарид, полученный из K. pneumoniae, содержащий Формулу, выбранную из группы, состоящей из
Формулы O1, содержащей структуру [→3)-β-D-Galf-(1→3)-α-D-Galp-(1→]n, [→3)-α-D-Galp-(1→3)-β-D-Galp-(1→]n, как [→3)-β-D-Galf-(1→3)-α-D-Galp-(1→]n, так и [→3)-α-D-Galp-(1→3)-β-D-Galp-(1→]n, или [→3)-β-D-Galf-(1→3)-[α-D-Galp-(1→4)]-α-D-Galp-(1→]n;
Формулы O2, содержащей структуру [→3)-α-D-Galp-(1→3)-β-D-Galf-(1→]n или [→3)-β-D-GlcpNAc-(1→5)-β-D-Galf-(1→]n;
Формулы O3, содержащей структуру [→2)-α-d-Man-(1→2)-α-d-Man-(1→3)-α-d-Man-(1→3)-α-d-Man-(1→]n; и
Формулы O5, содержащей структуру [→2)-α-d-Man-(1→2)-α-d-Man-(1→3)-β-d-Man-(1→]n, где сахарид, полученный из K. pneumoniae конъюгирован с белком-носителем, и где сахарид, полученный из E. coli, конъюгирован с белком-носителем.
9. Композиция по п. 8, отличающаяся тем, что сахарид дополнительно содержит группу 3-дезокси-d-манно-окт-2-улозоновой кислоты (KDO).
10. Композиция по п. 8, отличающаяся тем, что белок-носитель выбран из любого из перекрестно-реагирующего материала 197 (CRM197), группы B дифтерийного токсина (DTFB), DTFB C8, дифтерийного анатоксина (DT), столбнячного анатоксина (TT), фрагмента C TT, коклюшного анатоксина, холерного анатоксина, экзотоксина А из Pseudomonas aeruginosa, детоксицированного экзотоксина A P. aeruginosa (EPA), белка, связывающего мальтозу (MBP), детоксицированного гемолизина A S. aureus, фактора слипания A, фактора слипания B, субъединицы B холерного токсина (CTB), пневмолизина Streptococcus pneumoniae и его детоксицированных вариантов, AcrA C. jejuni, природных гликопротеинов C. jejuni и стрептококковой пептидазы C5a (SCP).
11. Способ индукции иммунного ответа против Escherichia coli у млекопитающего, включающий введение млекопитающему эффективного количества композиции по любому из пп. 1-10.
12. Способ по п. 11, отличающийся тем, что иммунный ответ включает опсонофагоцитарные антитела против E. coli.
13. Способ по п. 11, отличающийся тем, что иммунный ответ защищает млекопитающее от инфекции E. coli.
14. Способ индукции иммунного ответа против Klebsiella pneumoniae у млекопитающего, включающий введение млекопитающему эффективного количества композиции по любому из пп. 1-10.
15. Способ по п. 14, отличающийся тем, что иммунный ответ включает опсонофагоцитарные антитела против Klebsiella pneumoniae.
16. Способ по п. 14, отличающийся тем, что иммунный ответ защищает млекопитающее от инфекции Klebsiella pneumoniae.
| WO 2015052344 A1, 16.04.2015 | |||
| STENUTZ R | |||
| et al.: "The structures of Escherichia coli O-polysaccharide antigens", FEMS Microbiology Reviews, 2006, v | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| OSAWA K | |||
| Соломорезка | 1918 |
|
SU157A1 |
| IMMUNOL., 2013, v | |||
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
Авторы
Даты
2024-06-27—Публикация
2021-02-20—Подача