Изобретение относится к области получения наноразмерных частиц (далее - НЧ) методом импульсной лазерной абляции в жидкости и может быть использовано для получения НЧ висмута, морфология которых зависит от рН среды и которые могут найти применение в качестве переносчиков лекарственных препаратов для их триггерной доставки в клетки раковых опухолей, отличающиеся пониженным значением рН (по сравнению с значением рН здоровых клеток).
Известен способ получения НЧ висмута со средним размером 50 нм (см. Y. Zhao, Z. Zhang, Н. Dang. «А simple way to prepare bismuth nanoparticles», Materials Letters, 2004, №58, pp.790-793 [1]).
В известном способе 0,5 г гранул висмута (чистота 99,5%) смешивают с 30 мл парафинового масла в герметичном сосуде, нагревают до 280°С и перемешивают в течение 10 часов. Затем надосадочную жидкость переливают в другой сосуд и остужают до комнатной температуры. После этого надосадочную жидкость центрифугируют и промывают хлороформом до получения черно-коричневого порошка. Получаемые таким способом сферические НЧ висмута имеют средний размер 50 нм, хорошо растворимы в маслах, однако участие химически активных веществ в процессе синтеза и, как следствие, загрязнение этими веществами поверхности висмута затрудняет их применение в качестве активных компонентов для противораковой терапии в биомедицине.
Известен способ получения НЧ висмута методом лазерной абляции (см. L. Torrisia, L. Silipignia, N. Restucciaa, S. Cuzzocreab, M. Cutroneoc, F. Barrecaa, B. Faziod, G. Di Marcod, S. Guglielminoe. «Laser-generated bismuth nanoparticles for applications in imaging and radiotherapy», Journal of Physics and Chemistry of Solids, 2018, №119, pp. 62-70 [2]).
В известном способе образец мишени висмута площадью 3 см2 и толщиной 1 мм погружают на дно стеклянной кюветы, заполненной 5 мл дистиллированной воды, и затем облучают лазерными импульсами с длиной волны 1064 нм, частотой повторения импульсов 10 Гц, длительностью импульсов 3 нс, энергией в импульсе 100 мДж, диаметром лазерного пучка 1 мм от 5 до 30 минут, что позволяет получить концентрацию раствора от 0,5 мг/мл до 2 мг/мл, соответственно. Получаемые таким способом НЧ висмута имеют средний размер 25 нм.
К недостаткам способа можно отнести то, что получаемые НЧ висмута не обладают рН- зависимыми морфологическими, в том числе, размерными и структурными, свойствами, что исключает возможность использования их в качестве триггерных доставщиков лекарственных препаратов для противораковой терапии.
Техническая проблема, решаемая заявленным изобретением, состоит в устранении указанных недостатков.
При этом достигается технический результат, заключающийся в возможности получения НЧ висмута, морфологические, в том числе, размерные и структурные, и оптические свойства которых могут изменяться в условиях пониженного pH среды, характерного для раковых клеток.
Техническая проблема решается, а указанный технический результат достигается в результате создания способа получения НЧ висмута с триггерной рН-зависимой трансформацией для биомедицинских применений, включающий облучение поверхности мишени висмута, погруженной в ацетон или изопропанол, лазерными импульсами с частотой повторения импульсов от 100 Гц до 100 МГц и энергией в импульсе от 5 до 400 мкДж в течение не менее 1 мин до получения коллоидного раствора, центрифугирование полученного коллоидного раствора с ускорением от 5000 до 15000 g в течение от 30 секунд до 3 минут до получения надосадочной жидкости с НЧ висмута, покрытие НЧ висмута биосовместимым полимером Pluronic F127 путем добавления не менее 60 мае. % порошка биосовместимого полимера Pluronic F127 в полученную надосадочную жидкость и перемешивания полученного раствора в течение не менее 5 мин, в котором покрытые НЧ висмута отмывают от избытков биосовместимого полимера Pluronic F127 путем центрифугирования полученного раствора с ускорением не менее 3000 g в течение не менее 10 мин.
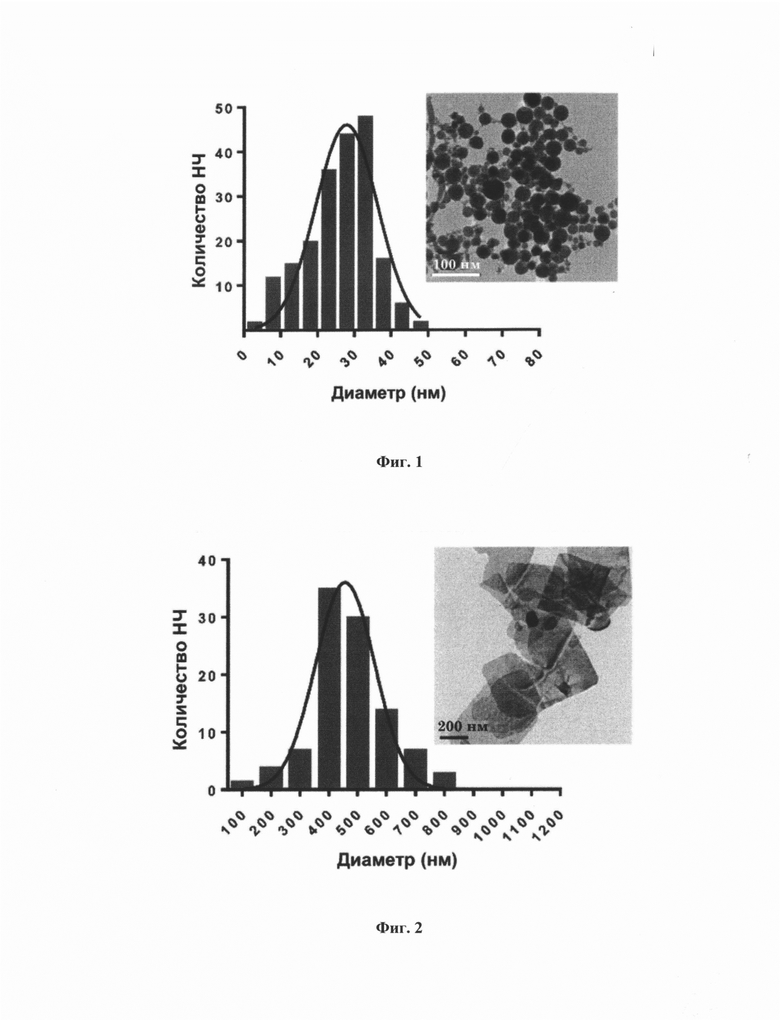
На фиг. 1 представлено электронное изображение и размерное распределение НЧ висмута в среде с pH, равным 7.
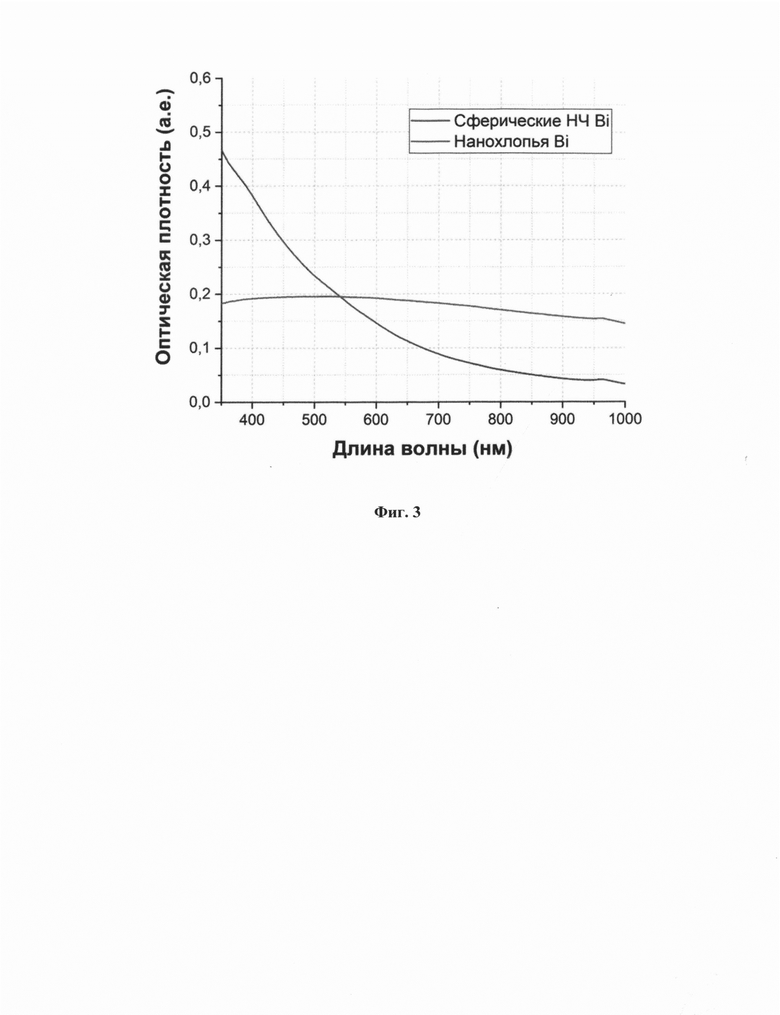
На фиг. 2 представлено электронное изображение и размерное распределение наночастиц висмута в среде с pH, равным 6,6.
На фиг. 3 представлены оптические спектры сферических наночастиц висмута и трансформированных нанолистов висмута.
Заявленный способ реализуют посредством выполнения следующей последовательности действий.
1. Поверхность мишени висмута, погруженной в органический растворитель, облучают лазерными импульсами с частотой повторения импульсов от 100 Гц до 100 МГц и энергией в импульсе от 5 до 400 мкДж в течение не менее 1 мин до получения коллоидного раствора. Облучение поверхности мишени висмута в иных, чем органический,
растворителях приведет к преждевременному изменению морфологии НЧ висмута. Использование импульсов с частотой повторения за пределами указанного диапазона не позволит добиться требуемой производительности синтеза. Энергии ниже 5 мкДж не будет достаточно для отрыва материала с поверхности мишени, а использование энергии выше 400 мкДж приведет к откалыванию крупных кусков мишени во время синтеза. Облучение поверхности мишени висмута в течение менее одной минуты не позволит наработать минимально необходимый объем НЧ.
2. Полученный коллоидный раствор центрифугируют с ускорением от 5000 до 15000 g в течение от 30 секунд до 3 минут до получения надосадочной жидкости с НЧ висмута. Центрифугирование с ускорением ниже 5000 g приведет к недостаточному осаждению крупных субмикронных частиц висмута, а центрифугирование с ускорением выше 15000 g приведет к осаждению мелких НЧ висмута, что не позволит отделить их в дальнейшем. Центрифугирование за пределами указанного временного диапазона не позволит отделить крупные субмикронные частицы висмута от наноразмерных частиц.
3. Покрывают НЧ висмута биосовместимым полимером путем добавления не менее 60 мас. % порошка биосовместимого полимера в полученную надосадочную жидкость и перемешивания полученного раствора в течение не менее 5 мин. При добавлении менее 60 мас. % полимера и перемешивании менее 5 минут не все НЧ висмута будут покрыты.
4. Покрытые НЧ висмута отмывают от избытков биосовместимого полимера путем центрифугирования полученного раствора с ускорением не менее 3000 g в течение не менее 10 мин и подвергают воздействию ультразвуковых колебаний в течение 1-15 минут. Центрифугирование с ускорением менее 3000 g менее 10 минут не позволит отделить НЧ висмута, покрытые полимером, от растворенных полимерных молекул. Воздействие ультразвуковых колебаний за пределами указанного временного диапазона не позволит достигнуть оптимальной степени редиспергирования НЧ.
Получаемые НЧ висмута обладают химически чистой поверхностью, средним гидродинамическим размером от 25 до 100 нм и могут менять свою морфологические, в том числе, размерные и структурные, и оптические свойства при попадании в среду с рН не более 6,8 (характерную для клеток раковых опухолей).
Использование при синтезе в качестве буферной жидкости деионизованной воды приводит к постепенной полиморфной трансформации сферических НЧ металлического висмута в субмикронные и наноразмерные частицы, состоящие в основном из субкарбонатов висмута (BiO)2СО3 и (BiO)4СО3(ОН)2 в течение периода времени от 30 до 80 минут. В результате такой трансформации преждевременно изменяются как морфология (размеры и структура НЧ), так и их оптические свойства. Вместе с тем, синтезированные в органическом растворителе НЧ висмута остаются стабильными и сохраняют свои морфологические (размерные и структурные) и оптические, свойства не менее 3 месяцев. Покрытие НЧ висмута, синтезированных в органическом растворителе, биосовместимым полимером дополнительно позволяет сохранить их стабильность в водных и физиологических растворах, при этом при попадании такой покрытой НЧ висмута в среду с рН не более 6,8 запускается процесс полиморфной трансформации, что делает данные частицы перспективными в биомедицине.
Ниже приведены примеры осуществления изобретения.
Пример 1.
Мишень кристаллического висмута (чистота 99,99%) подвергали ультразвуковой очистке в химически чистом ацетоне в течение 5 минут. После очистки мишень фиксировали в вертикальном положении и размещали внутри стеклянной кюветы, заполненной 15 мл химически чистого ацетона, и подвергали воздействию фемтосекундных лазерных импульсов с длиной волны 1030 нм, длительностью импульсов 270 фс, частотой повторения импульсов 200 кГц, энергией в импульсе 30 мкДж в течение 15 минут. Лазерное излучение на поверхности образца мишени висмута фокусировали при помощи плоскопольной линзы с фокусным расстоянием 160 мм. Сканирование сфокусированным пучком лазерного излучения поверхности образца мишени висмута осуществлялось при помощи гальванометрической установки.
Полученный коллоидный раствор центрифугировали в течение 1,5 минут с ускорением 10000 g. В результате центрифугирования требуемая размерная фракция НЧ оставалась в верхних слоях жидкости. Полученную таким образом надосадочную жидкость отделяли и добавляли в нее порошок биосовместимого полимера Pluronic F127 так, чтобы итоговая массовая концентрация полимера в растворе составляла 70%. Полученный раствор тщательно перемешивали в течение 10 минут и затем центрифугировали с ускорением 5000 g в течение 10 минут. Надосадочную жидкость с остатками полимера, полученную в результате центрифугирования, удаляли. Полученный осадок редиспергировали в физрастворе с рН, равным 7, после чего образец НЧ висмута в физрастворе анализировали с помощью растровой электронной микроскопии (РЭМ). Как видно из фиг. 1, средний размер НЧ висмута, покрытых полимерной оболочкой, составлял 28 нм со стандартным отклонением 4 нм.
НЧ висмута, покрытые полимерной оболочкой, переводили из физраствора в раствор с пониженным рН, равным 6,6, характерным для раковых клеток астроцитомы мозга. Полученный раствор исследовали с помощью РЭМ. Как видно из фиг. 2, средний размер НЧ висмута увеличился и составил 455 нм со стандартным отклонением 50 нм. Также изменилась форма НЧ со сферической на вытянутую (нанолисты).
Полученные результаты подтверждают возможность использования полученных НЧ висмута в качестве рН-зависимых триггерных доставщиков лекарственных препаратов в противораковой терапии.
Пример 2.
Мишень кристаллического висмута (чистота 99,99%) подвергали ультразвуковой очистке в химически чистом изопропаноле в течение 5 минут. После очистки мишень фиксировали в вертикальном положении и размещали внутри стеклянной кюветы, заполненной 15 мл химически чистого изопропанола, и подвергали воздействию фемтосекундных лазерных импульсов с длиной волны 1063 нм, длительностью импульсов 540 фс, частотой повторения импульсов 10 кГц, энергией в импульсе 150 мкДж в течение 30 минут. Лазерное излучение на поверхности образца мишени висмута фокусировали при помощи плоскопольной линзы с фокусным расстоянием 100 мм. Сканирование сфокусированным пучком лазерного излучения поверхности мишени висмута осуществлялось при помощи гальванометрической установки.
Полученный коллоидный раствор центрифугировали в течение 2,5 минут с ускорением 5000 g. В результате центрифугирования требуемая размерная фракция наноразмерных частиц оставалась в верхних слоях жидкости. Полученную таким образом надосадочную жидкость отделяли и добавляли в нее порошок биосовместимого полимера Pluronic F127 так, чтобы итоговая массовая концентрация полимера в растворе составляла 80%. Полученный раствор тщательно перемешивали в течение 15 минут и затем центрифугировали с ускорением 5000 g в течение 12 минут. Надосадочную жидкость с остатками полимера, полученную в результате центрифугирования, удаляли. Полученный осадок редиспергировали в физрастворе с рН равным 7,2, после чего образец НЧ висмута в физрастворе анализировали с помощью РЭМ. В результате средний размер НЧ висмута, покрытых полимерной оболочкой, составлял 36 нм со стандартным отклонением 7 нм.
НЧ висмута, покрытые полимерной оболочкой, переводили из физраствора в раствор с пониженным рН, равным 6,4, характерным для раковых клеток легких. Полученный раствор исследовали с помощью РЭМ. В результате средний размер наночастиц висмута увеличился и составил 421 нм со стандартным отклонением 42 нм. Также изменилась форма наночастиц со сферической на вытянутую (нанолисты).
Полученные результаты подтверждают возможность использования наночастиц висмута в качестве рН-зависимых триггерных доставщиков лекарственных препаратов в противораковой терапии.
Пример 3
Мишень кристаллического висмута (чистота 99,99%) подвергали ультразвуковой очистке в химически чистом изопропаноле в течение 6 минут. После очистки мишень фиксировали в вертикальном положении и размещали внутри стеклянной кюветы, заполненной 15 мл химически чистого изопропанола, и подвергали воздействию фемтосекундных лазерных импульсов с длиной волны 1064 нм, длительностью импульсов 270 фс, частотой повторения импульсов 100 кГц, энергией в импульсе 75 мкДж в течение 25 минут. Лазерное излучение на поверхности образца мишени висмута фокусировали при помощи плоскопольной линзы с фокусным расстоянием 160 мм. Сканирование сфокусированным пучком лазерного излучения поверхности образца мишени висмута осуществлялось при помощи гальванометрической установки.
Полученный коллоидный раствор центрифугировали в течение 1 минуты с ускорением 15000 g. В результате центрифугирования требуемая размерная фракция наноразмерных частиц оставалась в верхних слоях жидкости. Полученную таким образом надосадочную жидкость отделяли и добавляли в нее порошок биосовместимого полимера Pluronic F127 (либо любого иного подходящего биосовместимого полимера) так, чтобы итоговая массовая концентрация полимера в растворе составляла 75%. Полученный раствор тщательно перемешивали в течение 12 минут и затем центрифугировали с ускорением 4000 g в течение 11 минут. Надосадочную жидкость с остатками полимера, полученную в результате центрифугирования, удаляли. Полученный осадок редиспергировали в физрастворе с рН равным 7, после чего образец НЧ висмута в физрастворе анализировали с помощью РЭМ. В результате средний размер НЧ висмута, покрытых полимерной оболочкой, составлял 68 нм со стандартным отклонением 12 нм.
НЧ висмута, покрытые полимерной оболочкой, переводили из физраствора в раствор с пониженным рН, равным 6,9, характерным для раковых клеток злокачественной меланомы. Полученный раствор исследовали с помощью РЭМ. В результате средний размер наночастиц висмута увеличился и составил 79 нм со стандартным отклонением 18 нм. Однако форма наночастиц не изменялась.
НЧ висмута, покрытые полимерной оболочкой, переводили из физраствора в раствор с пониженным рН, равным 6,8, характерным для раковых клеток матки. Полученный раствор исследовали с помощью РЭМ. В результате средний размер наночастиц висмута увеличился и составил 433 нм со стандартным отклонением 49 нм. Также изменилась форма наночастиц со сферической на вытянутую (нанолисты).
Полученные результаты подтверждают возможность использования наночастиц висмута в качестве рН-зависимых триггерных доставщиков лекарственных препаратов в противораковой терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОТОННОЙ ТЕРАПИИ СОЛИДНОЙ КАРЦИНОМЫ ЭРЛИХА | 2023 |
|
RU2808984C1 |
| СПОСОБ ПОЛУЧЕНИЯ СФЕРИЧЕСКИХ КОЛЛОИДНЫХ НАНОРАЗМЕРНЫХ ЧАСТИЦ ЗОЛОТА МЕТОДОМ ИМПУЛЬСНОЙ ЛАЗЕРНОЙ АБЛЯЦИИ | 2023 |
|
RU2825640C1 |
| Способ получения стабильного высококонцентрированного коллоидного раствора на основе лазерно-аблированных наночастиц золота диаметром до 10 нм для биомедицинского применения | 2023 |
|
RU2834959C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛОИДНО-СТАБИЛЬНЫХ СУБМИКРОННЫХ И НАНОРАЗМЕРНЫХ ЧАСТИЦ БОРА СО СРЕДНИМ РАЗМЕРОМ МЕНЕЕ 200 НАНОМЕТРОВ | 2022 |
|
RU2797422C1 |
| СПОСОБ СИНТЕЗА ПОКРЫТИЙ ИЗ ДИОКСИДА КРЕМНИЯ ДЛЯ КОЛЛОИДНЫХ НАНОЧАСТИЦ ЗОЛОТА РАЗЛИЧНОЙ ГЕОМЕТРИИ | 2020 |
|
RU2769057C1 |
| Оптический сенсор для тушения флуоресценции оптически активных аминокислот тромбоцитов и способ его получения | 2022 |
|
RU2787689C1 |
| Планарный наноструктурированный сенсор на основе поверхностного плазмонного резонанса для усиления комбинационного рассеяния света тромбоцитов человека и способ его получения | 2022 |
|
RU2788479C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЧАСТИЦЫ РЕЗВЕРАТРОЛА, И СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2008 |
|
RU2373926C1 |
| СПОСОБ ЛАЗЕРНО-ИНДУЦИРОВАННОЙ МОДИФИКАЦИИ ХИМИЧЕСКОГО СОСТАВА НАНОЧАСТИЦ ДИСУЛЬФИДА МОЛИБДЕНА | 2023 |
|
RU2812405C1 |
| Метод получения стабилизированных линейных цепочек углерода в жидкости | 2019 |
|
RU2744089C1 |
Изобретение может быть использовано для получения наночастиц висмута, которые могут найти применение в качестве переносчиков лекарственных препаратов для их триггерной доставки в клетки раковых опухолей. Способ получения наночастиц висмута с триггерной рН-зависимой трансформацией включает облучение поверхности мишени висмута, погруженной в ацетон или изопропанол, лазерными импульсами в течение не менее 1 мин до получения коллоидного раствора. Частота повторения импульсов от 100 Гц до 100 МГц, энергия в импульсе от 5 до 400 мкДж. Осуществляют центрифугирование полученного коллоидного раствора с ускорением от 5000 до 15000 g в течение от 30 с до 3 мин до получения надосадочной жидкости с наночастицами висмута. Полученные наночастицы висмута покрывают биосовместимым полимером, добавляя не менее 60 мас.% порошка биосовместимого полимера Pluronic F127 в полученную надосадочную жидкость и перемешивая полученный раствор в течение не менее 5 мин. Покрытые наночастицы висмута отмывают от избытков биосовместимого полимера путем центрифугирования раствора с ускорением не менее 3000 g в течение не менее 10 мин. Изобретение позволяет получить наночастицы висмута, морфологические и оптические свойства которых могут изменяться в условиях пониженного рН среды, характерного для раковых клеток. 3 ил., 3 пр.
Способ получения наночастиц висмута с триггерной рН-зависимой трансформацией для биомедицинских применений, включающий облучение поверхности мишени висмута, погруженной в ацетон или изопропанол, лазерными импульсами с частотой повторения импульсов от 100 Гц до 100 МГц и энергией в импульсе от 5 до 400 мкДж в течение не менее 1 мин до получения коллоидного раствора, центрифугирование полученного коллоидного раствора с ускорением от 5000 до 15000 g в течение от 30 с до 3 мин до получения надосадочной жидкости с наночастицами висмута, покрытие наночастиц висмута биосовместимым полимером Pluronic F127 путем добавления не менее 60 мас. % порошка биосовместимого полимера Pluronic F127 в полученную надосадочную жидкость и перемешивания полученного раствора в течение не менее 5 мин, в котором покрытые наночастицы висмута отмывают от избытков биосовместимого полимера Pluronic F127 путем центрифугирования полученного раствора с ускорением не менее 3000 g в течение не менее 10 мин.
| BULMAHN J | |||
| C | |||
| et al., Laser-Ablative Synthesis of Stable Aqueous Solutions of Elemental Bismuth Nanoparticles for Multimodal Theranostic Applications, Nanomaterials, 2020, N 10(8), 1463 | |||
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ ВИСМУТА | 2013 |
|
RU2545342C2 |
| CN 107137358 A, 08.09.2017 | |||
| ПРОМЫВНОЙ АППАРАТ | 1923 |
|
SU1080A1 |
| ТИХОНОВСКИЙ Г | |||
| В | |||
| и др., Лазерный синтез наночастиц висмута для мультимодальной | |||
Авторы
Даты
2024-08-22—Публикация
2023-10-13—Подача