[0001] В данной заявке заявляется приоритет по предварительной заявке на патент США № 62/799513, поданной 31 января 2019 года, и предварительной заявке на патент США № 62/678878, поданной 31 мая 2018 года, раскрытие которых явным образом полностью включено в данный документ посредством ссылки.
[0002] В данном документе раскрыты Т-клетки с химерным антигенным рецептором (CAR-T) с редактированным геномом и способы их использования для иммунотерапии. В частности, изобретение относится к Т-клеткам, которые могут быть генетически модифицированы для экспрессии одного или более химерных антигенных рецепторов (CAR), и к способам их использования для лечения рака.
[0003] Т-клетки, тип лимфоцитов, играют центральную роль в клеточно-опосредованном иммунитете. Т-клетки можно отличить от других лимфоцитов, таких как В-клетки и NK-клетки, по присутствию Т-клеточного рецептора (ТКР) на клеточной поверхности. Т-клетки хелперы (ТH), также называемые CD4+ T или CD4 T-клетками, экспрессируют гликопротеин CD4 на своей поверхности. Т-клетки хелперы активируются при воздействии пептидных антигенов, представленных молекулами ГКГ (главный комплекс гистосовместимости) II класса После активации эти клетки быстро размножаются и секретируют цитокины, регулирующие иммунный ответ. Цитотоксические T-клетки (TC), также известные как CD8+ T-клетки или CD8 T-клетки, экспрессируют гликопротеин CD8 на поверхности клетки. CD8+ T-клетки активируются при воздействии пептидных антигенов, представленных молекулами ГКГ I класса. Т-клетки памяти, подмножество Т-клеток, сохраняются в течение длительного времени и реагируют на свой распознанный антиген, тем самым обеспечивая иммунную систему «памятью» против прошлых инфекций и/или опухолевых клеток. Гамма-дельта (γδ) Т-клетки являются прототипом «нетрадиционных» Т-клеток и представляют собой относительно небольшое подмножество Т-клеток в периферической крови. Они определяются экспрессией гетеродимерных Т-клеточных рецепторов (TCR), состоящих из γ и δ цепей. Это отличает их от CD4+ Т-клеток хелперов и CD8+ цитотоксических Т-клеток. Вирусоспецифические цитотоксические Т-лимфоциты представляют собой Т-клетки, обладающие реактивностью против вирусных антигенов, в частности вируса Эпштейна-Барра (EBV) и цитомегаловируса (CMV).
[0004] Описанные в данном документе Т-клетки могут быть генетически модифицированы для экспрессии химерных антигенных рецепторов (CAR), которые представляют собой слитые белки, состоящие из фрагмента распознавания антигена и доменов активации Т-клеток. Т-клетки, экспрессирующие CAR, могут распознавать определенный белок, то есть антиген на опухолевых клетках. Эти Т-клетки, экспрессирующие CAR, могут быть размножены в лаборатории перед инфузией пациенту.
[0005] Клинические испытания показали высокую частоту ответа после инфузии анти-CD19 CAR у пациентов с В-клеточными злокачественными новообразованиями, включая диффузную В-крупноклеточную лимфому (ДВККЛ) и острый лимфобластный лейкоз предшественников B-клеток (ОЛЛ), что привело к появлению двух лекарственных средств, одобренных FDA Yescarta™ (axicabtagene ciiloleucel, Kite Pharma/Gilead) и Kymriah™ (tisagenlecleucel, Novartis). Несмотря на эти успехи, разработка CAR-T-клеточной терапии против Т-клеточных злокачественных новообразований оказалась проблематичной, отчасти из-за общей экспрессии целевых антигенов между злокачественными Т-клетками и эффекторными Т-клетками. Среди наиболее общих проблем: (1) антигенная мишень(и) для химерного антигенного рецептора(ов); (2) конструкция CAR, т.е. моно CAR, двойные CAR, тандемные CAR; и (3) неоднородность опухоли, в частности, вариация поверхностной экспрессии опухолевых антигенов. Следовательно, остается потребность в улучшенных иммунотерапевтических средствах на основе химерных антигенных рецепторов (CAR), которые используют редактирование генома и создание моно, двойных и тандемных CAR для более эффективного, безопасного и действенного нацеливания на рак, включая Т-клетки, сопутствующие злокачественные новообразования.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0006] На Фиг. 1 представлена схема двойной CAR T-клетки (dCAR T-клетки).
[0007] На Фиг. 2 представлена схема тандемной CAR T-клетки (tCAR T-клетки).
[0008] На Фиг. 3 представлена схема двойной и тандемной конструкций CAR.
[0009] На Фиг. 4 представлена схема тандемных нацеленных конструкций CAR.
[0010] На Фиг. 5 продемонстрирована чистота продукта CAR-T без механического истощения CAR-T клеток CD3+ или CD2+. Как показал анализ FACS, CAR T-клетки CD3- и CD2- обладают высокой чистотой без необходимости магнитного истощения CD3+ клеток. Типовые графики FACS демонстрируют окрашивание FITC CD3 (ось y) и CD2 (ось x). Показаны клоны 5 (вверху) и 6 (внизу).
[0011] На Фиг. 6 продемонстрирована чистота продукта CAR-T без механического истощения CAR-T клеток CD3+ или CD2+. Как показал анализ FACS, CAR T-клетки CD3- и CD2- обладают высокой чистотой без необходимости отбора CD3+ клеток с помощью магнитного истощения. Типовые графики FACS демонстрируют окрашивание FITC CD3 (ось y) и CD2 (ось x). Показаны клоны 7 (вверху) и 8 (внизу).
[0012] На Фиг. 7 продемонстрирована чистота продукта CAR-T без механического истощения CAR-T клеток CD3+ или CD2+. Как показал анализ FACS, CAR T-клетки CD3- и CD2- обладают высокой чистотой без необходимости отбора CD3+ клеток с помощью магнитного истощения. Типовые графики FACS демонстрируют окрашивание FITC CD3 (ось y) и CD2 (ось x). Показаны клоны 13 (вверху) и 14 (внизу).
[0013] На Фиг. 8 продемонстрирована чистота продукта CAR-T без механического истощения CAR-T клеток CD3+ или CD2+. Как показал анализ FACS, CAR T-клетки CD3- и CD2- обладают высокой чистотой без необходимости отбора CD3+ клеток с помощью магнитного истощения. Типовые графики FACS демонстрируют окрашивание FITC CD3 (ось y) и CD2 (ось x). Показаны клоны 15 (вверху) и 16 (внизу).
[0014] На Фиг. 9А продемонстрировано уничтожение опухолевых клеток тандемных CD2-CD3 CAR-T клонов 5 (вверху) и 6 (внизу); легенда демонстрирует соотношение эффекторных клеток к клеткам-мишеням (соотношение E:T).
[0015] На Фиг. 9В продемонстрировано уничтожение опухолевых клеток тандемных CD2-CD3 CAR-T клонов 7 (вверху) и 8 (внизу); легенда демонстрирует соотношение эффекторных клеток к клеткам-мишеням (соотношение E:T).
[0016] На Фиг. 9С продемонстрировано уничтожение опухолевых клеток тандемных CD2-CD3 CAR-T клонов 13 (вверху) и 14 (внизу); легенда демонстрирует соотношение эффекторных клеток к клеткам-мишеням (соотношение E:T).
[0017] На Фиг. 9D продемонстрировано уничтожение опухолевых клеток тандемных CD2-CD3 CAR-T клонов 15 (вверху) и 16 (внизу); легенда демонстрирует соотношение эффекторных клеток к клеткам-мишеням (соотношение E:T).
[0018] На Фиг. 10А продемонстрирована схема конструкции BCMA CAR, трансдуцируемой в Т-клетки, которые будут нацелены на BCMA.
[0019] На Фиг. 10B продемонстрировано уничтожение опухолевых клеток BCMA-CAR T-клеток в анализе высвобождения 51Cr. Эффективное уничтожение BCMA-CAR T-клеток наблюдали при множественных соотношениях эффектор к цели (E:T). Нетрансдуцированные активированные Т-клетки и CD19-CAR T-клетки использовали в качестве отрицательного контроля и не вызывали гибели клеток MM.1S-CG.
[0020] На Фиг. 10С продемонстрирована in vivo эффективность ВСМА CAR T-клеток. Все семь мышей, получавших BCMA CAR-T, прожили почти 150 дней или более по сравнению с контрольными мышами, которые умерли на около 50 день.
[0021] На Фиг. 10D продемонстрирована последовательная биолюминесцентная визуализация (BLI), измеренная в фотопотоке, выявившая устойчивое снижение сигнала до фоновых уровней, которые никогда не увеличивались на протяжении всего эксперимента у мышей, получавших лечение BCMA CAR T-клетками.
[0022] На Фиг. 11A продемонстрирована схема конструкции CS1-CAR, трансдуцируемой в Т-клетки, которые будут нацелены на CS1.
[0023] На Фиг. 11В продемонстрирована in vivo эффективность CS1-CAR T-клеток. Мышам прививали клетки MM.1S-CG и клетки MM.1S-CG, лишенные CS1 (с использованием технологии CAS9/CRISPR; MM.1S-CGΔCS1), в качестве способа проверки специфичности CS1-CAR T-клеток. Все мыши, получавшие CS1-CAR T-клетки (n=10), жили > 90 дней, в то время как средняя выживаемость мышей CD19-контроля (n=8) составляла 43 дня.
[0024] На Фиг. 11С продемонстрировано серийное биолюминесцентное изображение (BLI), показывающее, что у мышей, обработанных CS1-CAR T-клетками, наблюдалось трехлогарифмическое снижение потока фотонов и клиренса опухоли костного мозга (от эксперимента 1 до эксперимента 3).
[0025] На Фиг. 12А продемонстрирована схема моно (CD19, CS1) и тандемных (BCMA-CS1) конструкций.
[0026] На Фиг. 12В продемонстрирован FACS-анализ клеток Jurkat, экспрессирующих CD19 CAR, которые не связывались ни с белком BCMA, ни с CS1 (нижний левый квадрант каждого графика). Клетки Jurkat, экспрессирующие белок BCMA CAR, связанный с белком BCMA (верхний левый квадрант каждого графика). Клетки Jurkat, экспрессирующие белок CS1 CAR, связанный с белком CS1 (нижний правый квадрант каждого графика). Клетки Jurkat, экспрессирующие тандемный белок BCMA-CS1 CAR, связанный с обоими рекомбинантными белками (верхний правый квадрант каждого графика), что свидетельствует об экспрессии обоих scFv.
[0027] На Фиг. 12С продемонстрирована in vitro эффективность одиночных и тандемных CAR T-клеток с использованием стандартных четырехчасовых анализов высвобождения хрома (51Cr). BCMA-CS1 tCAR T-клетки убивали клетки MM.1S-CG с такой же эффективностью, как и отдельные BCMA, так и CS1 CAR T-клетки нацеленные на антиген.
[0028] На Фиг. 13 продемонстрирована тестирование эффективности CD2*CD3Δ-dCARTΔCD2ΔCD3ε на ксеногенной модели T-ОЛЛ.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0029] В нижеследующем описании будут подробно описаны варианты реализации, альтернативы и использование сконструированных клеток, а также использование sch-клеток, например, в иммунотерапии и адоптивном переносе клеток для лечения заболеваний. Соответственно, в данном документе представлены следующие варианты реализации.
[0030] Вариант реализации данного изобретения 1. CAR T-клетка, которая содержит один или более химерных антигенных рецепторов (CAR), нацеленных на один или более антигенов, при этом CAR T-клетка дефицитна по субъединице рецепторного комплекса T-клеток и/или дефицитна по меньшей мере по одному или более антигенам, с которыми специфически связывается один или более CAR.
[0031] Вариант реализации данного изобретения 2. CAR T-клетка, которая содержит один или более химерных антигенных рецепторов (CAR), нацеленных на один или более антигенов, при этом CAR T-клетка дефицитна по одному или более антигенам, с которыми специфически связывается один или более CAR.
[0032] Вариант реализации данного изобретения 3. CAR T-клетка по варианту реализации данного изобретения 1, в котором субъединица рецепторного комплекса Т-клеток выбрана из TCRα, TCRβ, TCRδ, TCRγ, CD3ε, CD3γ, CD3δ, и CD3ζ.
[0033] Вариант реализации данного изобретения 4. CAR T-клетка по любому из вариантов реализации данного изобретения 1-2, в котором химерный антигенный рецептор (CAR) специфически связывает один или более антигенов, экспрессируемых на поверхности злокачественной Т-клетки или клетке миеломы
[0034] Вариант реализации данного изобретения 5. CAR T-клетка, по любому из вариантов реализации данного изобретения 1-4, в котором последовательность химерного антигенного рецептора (CAR) по меньшей мере на 95% идентична аминокислотной последовательности, выбранной из SEQ ID NO:32, SEQ ID NO:33, SEQ ID NO:34, SEQ ID NO:35, SEQ ID NO:36, SEQ ID NO:37, SEQ ID NO:38 или SEQ ID NO:39.
[0035] Вариант реализации данного изобретения 6. CAR T-клетка, по любому из вариантов реализации данного изобретения 1-4, в котором последовательность химерного антигенного рецептора (CAR) по меньшей мере на 98% идентична аминокислотной последовательности, выбранной из SEQ ID NO:32, SEQ ID NO:33, SEQ ID NO:34, SEQ ID NO:35, SEQ ID NO:36, SEQ ID NO:37, SEQ ID NO:38 или SEQ ID NO:39.
[0036] Вариант реализации данного изобретения 7. CAR T-клетка, по любому из вариантов реализации данного изобретения 1-4, в котором химерный антигенный рецептор (CAR) представляет собой аминокислотную последовательность, выбранную из SEQ ID NO:32, SEQ ID NO:33, SEQ ID NO:34, SEQ ID NO:35, SEQ ID NO:36, SEQ ID NO:37, SEQ ID NO:38 или SEQ ID NO:39.
[0037] Вариант реализации данного изобретения 8. CAR T-клетка по любому из вариантов реализации данного изобретения 1-4, в котором химерный антигенный рецептор специфически связывает один или более антигенов, выбранных из BCMA, CS1, CD38, CD138, CD19, CD33, CD123, CD371, CD117, CD135, Tim-3, CD5, CD7, CD2, CD4, CD3, CD79A, CD79B, APRIL, CD56 и CD1a.
[0038] Вариант реализации данного изобретения 9. CAR T-клетка по любому из вариантов реализации данного изобретения 1-5, в котором химерный антигенный рецептор(ы) специфически связывает по меньшей мере один антиген, экспрессируемый на поверхности злокачественной Т-клетки.
[0039] Вариант реализации данного изобретения 10. CAR T-клетка по варианту реализации данного изобретения 9, в котором антиген, экспрессируемый на поверхности злокачественной T-клетки, выбран из CD2, CD3, CD4, CD5, CD7, TCRA и TCRβ.
[0040] Вариант реализации данного изобретения 11. CAR T-клетка по любому из вариантов реализации данного изобретения 1-5, в котором химерный антигенный рецептор специфически связывает по меньшей мере один антиген, экспрессируемый на поверхности злокачественной плазматической клетки.
[0041] Вариант реализации данного изобретения 12. CAR T-клетка по варианту реализации данного изобретения 11, в котором антиген, экспрессируемый на поверхности злокачественной плазматической клетки, выбран из BCMA, CS1, CD38, CD79A, CD79B, CD138 и CD19.
[0042] Вариант реализации данного изобретения 13. CAR T-клетка по любому из вариантов реализации данного изобретения 1-5, в котором химерный антигенный рецептор(ы) специфически связывает по меньшей мере один антиген, экспрессируемый на поверхности злокачественной В-клетки.
[0043] Вариант реализации данного изобретения 14. CAR T-клетка по варианту реализации данного изобретения 13, в котором антиген, экспрессируемый на поверхности злокачественной В-клетки, выбран из CD19, CD20, CD21, CD22, CD23, CD24, CD25, CD27, CD38 и CD45.
[0044] Вариант реализации данного изобретения 15. CAR T-клетка по варианту реализации данного изобретения 14, в котором антиген, экспрессируемый на поверхности злокачественной В-клетки, выбран из CD19 и CD20.
[0045] Вариант реализации данного изобретения 16. CAR T-клетка по любому из вариантов реализации 1-15, в котором CAR T-клетка дополнительно содержит «суицидный» ген.
[0046] Вариант реализации данного изобретения 17. CAR T-клетка по любому из вариантов реализации 1-16, в котором передача сигналов, опосредованная эндогенным Т-клеточным рецептором, заблокирована в CAR-T-клетке.
[0047] Вариант реализации данного изобретения 18. CAR T-клетка по любому из вариантов реализации 1-17, в котором CAR T-клетки не индуцируют аллореактивность или реакцию «трансплантат против хозяина».
[0048] Вариант реализации данного изобретения 19. CAR T-клетка по любому из вариантов реализации 1-18, в котором CAR T-клетки не индуцируют взаимное уничтожение.
[0049] Вариант реализации данного изобретения 20. Двойная или тандемная CAR T-клетка по любому из вариантов реализации 1-19.
[0050] Вариант реализации данного изобретения 21. CAR T-клетка по варианту реализации 20, в котором CAR специфически связывает (связывают) две разные мишени, выбранные из CD2xCD3ε, CD2xCD4, CD2xCD5, CD2xCD7, CD3εxCD4, CD3εxCD5, CD3εxCD7, CD4xCD5, CD4xCD7, CD5xCD7, TRACxCD2, TRACxCD3ε, TRACxCD4, TRACxCD5, TRACxCD7, TCRβxCD2, TCRβxCD3ε, TCRβxCD4, TCRβxCD7, CD2xCD3ε, CD2xCD4, CD2xCD5, CD2xCD7, CD3εxCD4, CD3εxCD5, CD3εxCD7, CD4xCD5, CD4xCD7, CD5xCD7, TRACxCD2, TRACxCD3ε, TRACxCD4, TRACxCD5, TRACxCD7, TCRβxCD2, TCRβxCD3ε, TCRβxCD4, TCRβxCD5, TCRβxCD7, BCMAxCS1, BCMAxCD19, BCMAxCD38, CS1xCD19, CD19xCD38, APRILxCS1, APRILxBCMA, APRILxCD19, APRILxCD38, CS1xCD38, CD79AxBCMA, CD79AxCS1, CD79AxCD19, CD79AxCD38, CD79AxCD38, CD79AxAPRIL, CD79AxCD79B, CD79BxBCMA, CD79BxCS1, CD79BxCD19, CD79BxCD38, CD79BxAPRIL, CD79BxCD79A, CD138xBCMA, CD138xCS1, CD138xCD19, CD138xCD38, CD138xAPRIL, CD138xCD79A, CD138xCD79B, CD138xBCMA и CD138xCS1.
[0051] Вариант реализации данного изобретения 22. CAR T-клетка по варианту реализации 21, в котором CAR специфически связывает (связывают) две разные мишени, выбранные из CD2xCD3ε, CD2xCD4, CD2xCD5, CD2xCD7, CD3εxCD4, CD3εxCD5, CD3εxCD7, CD4xCD5, CD4xCD7, CD5xCD7, TRACxCD2, TRACxCD3ε, TRACxCD4, TRACxCD5, TRACxCD7, TCRβxCD2, TCRβxCD3ε, TCRβxCD4, TCRβxCD7, CD2xCD3ε, CD2xCD4, CD2xCD5, CD2xCD7, CD3εxCD4, CD3εxCD5, CD3εxCD7, CD4xCD5, CD4xCD7, CD5xCD7, TRACxCD2, TRACxCD3ε, TRACxCD4, TRACxCD5, TRACxCD7, TCRβxCD2, TCRβxCD3ε, TCRβxCD4, TCRβxCD5 и TCRβxCD7.
[0052] Вариант реализации данного изобретения 23. CAR T-клетка по варианту реализации 21, в котором CAR специфически связывает (связывают) две разные мишени, выбранные из BCMAxCS1, BCMAxCD19, BCMAxCD38, CS1xCD19, CD19xCD38, APRILxCS1, APRILxBCMA, APRILxCD19, APRILxCD38, CS1xCD38, CD79AxBCMA, CD79AxCS1, CD79AxCD19, CD79AxCD38, CD79AxCD38, CD79AxAPRIL, CD79AxCD79B, CD79BxBCMA, CD79BxCS1, CD79BxCD19, CD79BxCD38, CD79BxAPRIL, CD79BxCD79A, CD138xBCMA, CD138xCS1, CD138xCD19, CD138xCD38, CD138xAPRIL, CD138xCD79A, CD138xCD79B, CD138xBCMA и CD138xCS1.
[0053] Вариант реализации данного изобретения 24. CAR T-клетка по варианту реализации 21, в котором CAR специфически связывает (связывают) две разные мишени, выбранные из CD123xCD371, CD123xCLEC12A, CD123xCD117, CD123xFLT3, CD123xCD7, CD123xTim3, CD371xCLEC12A, CD371xCD117, CD371xFLT3, CD371xCD7, CD371xTim3, CLEC12AxCD117, CLEC12AxFLT3, CLEC12AxCD7, CLEC12AxTim3, CD117xFLT3, CD117xCD7, CD117xTim3, FLT3xCD7, FLT3xTim3 и CD7xTim3.
[0054] Вариант реализации данного изобретения 25. Двойная CAR T-клетка по любому из вариантов реализации 21-24.
[0055] Вариант реализации данного изобретения 26. Тандемная CAR T-клетка по любому из вариантов реализации 21-34.
[0056] Вариант реализации данного изобретения 27. CAR T-клетка по любому из вариантов реализации 1-26, в котором CAR T-клетка дополнительно содержит «суицидный» ген.
[0057] Вариант реализации данного изобретения 28. CAR T-клетка по любому из вариантов реализации 1-26, в котором передача сигналов, опосредованная эндогенным Т-клеточным рецептором, заблокирована в CAR-T-клетке.
[0058] Вариант реализации данного изобретения 29. CAR T-клетка по любому из вариантов реализации 1-26, в котором CAR T-клетки не индуцируют аллореактивность или реакцию «трансплантат против хозяина».
[0059] Вариант реализации данного изобретения 30. CAR T-клетка по любому из вариантов реализации 1-26, в котором CAR T-клетки не индуцируют взаимное уничтожение.
[0060] Вариант реализации данного изобретения 31. Двойной или тандемный химерный антигенный рецептор (dCAR или tCAR), нацеленный на два или более антигенов клеток плазмы.
[0061] Вариант реализации данного изобретения 32. CAR по варианту реализации 31, в котором антиген(ы) клеток плазмы выбран(ы) из BCMA, CS1, CD38, CD79A, CD79B, CD138 и CD19.
[0062] Вариант реализации данного изобретения 33. CAR по варианту реализации 32, в котором CAR специфически связывает (связывают) две разные мишени, выбранные из BCMAxCS1, BCMAxCD19, BCMAxCD38, CS1xCD19, CD19xCD38, APRILxCS1, APRILxBCMA, APRILxCD19, APRILxCD38, CS1xCD38, CD79AxBCMA, CD79AxCS1, CD79AxCD19, CD79AxCD38, CD79AxCD38, CD79AxAPRIL, CD79AxCD79B, CD79BxBCMA, CD79BxCS1, CD79BxCD19, CD79BxCD38, CD79BxAPRIL, CD79BxCD79A, CD138xBCMA, CD138xCS1, CD138xCD19, CD138xCD38, CD138xAPRIL, CD138xCD79A, CD138xCD79B, CD138xBCMA и CD138xCS1.
[0063] Вариант реализации данного изобретения 34. CAR по любому из вариантов реализации 31-33, в котором CAR представляет собой dCAR.
[0064] Вариант реализации данного изобретения 35. CAR по любому из вариантов реализации 31-33, в котором CAR представляет собой tCAR.
[0065] Вариант реализации данного изобретения 36. Двойной или тандемный химерный антигенный рецептор (dCAR или tCAR), нацеленный на два или более антигенов лейкозной клетки.
[0066] Вариант реализации данного изобретения 37. CAR по варианту реализации 36, в котором антиген(ы) клеток плазмы выбран(ы) из CD123, CLEC12A, CD117, FLT3, CD7 и Tim3.
[0067] Вариант реализации данного изобретения 38. CAR по варианту реализации 37, в котором CAR специфически связывает (связывают) две разные мишени, выбранные из CD123xCD371, CD123xCLEC12A, CD123xCD117, CD123xFLT3, CD123xCD7, CD123xTim3, CD371xCLEC12A, CD371xCD117, CD371xFLT3, CD371xCD7, CD371xTim3, CLEC12AxCD117, CLEC12AxFLT3, CLEC12AxCD7, CLEC12AxTim3, CD117xFLT3, CD117xCD7, CD117xTim3, FLT3xCD7, FLT3xTim3 и CD7xTim3.
[0068] Вариант реализации данного изобретения 39. CAR по любому из вариантов реализации 36-38, в котором CAR представляет собой dCAR.
[0069] Вариант реализации данного изобретения 40. CAR по любому из вариантов реализации 36-38, в котором CAR представляет собой tCAR.
[0070] Вариант реализации данного изобретения 41. Тандемный химерный антигенный рецептор (tCAR), нацеленный на два или более антигенов Т-клетки.
[0071] Вариант реализации данного изобретения 42. tCAR по варианту реализации 41, в котором Т-клеточные антигены выбраны из CD5, CD7, CD2, CD4 и CD3.
[0072] Вариант реализации данного изобретения 43. tCAR по варианту реализации 42, нацелен на пару (т.е. два) антигена.
[0073] Вариант реализации данного изобретения 44. tCAR по варианту реализации 43, в котором пара антигенов выбрана из CD2xCD3ε, CD2xCD4, CD2xCD5, CD2xCD7, CD3εxCD4, CD3εxCD5, CD3εxCD7, CD4xCD5, CD4xCD7, CD5xCD7, TRACxCD2, TRACxCD3ε, TRACxCD4, TRACxCD5, TRACxCD7, TCRβxCD2, TCRβxCD4, TCRβxCD7, CD2xCD3ε, CD2xCD4, CD2xCD5, CD2xCD7, CD3εxCD4, CD3εxCD5, CD4xCD5, CD4xCD7, CD5xCD7, TRACxCD2, TRACxCD3ε, TRACxCD4, TRACxCD5, TRACxCD7, TCRβxCD2, TCRβxCD3ε, TCRβxCD4, TCRβxCD5 и TCRβxCD7.
[0074] Вариант реализации данного изобретения 45. tCAR по варианту реализации 43, в котором пара антигенов выбрана из CD2xCD3ε, CD2xCD4, CD2xCD5, CD2xCD7, CD3εxCD4, CD3εxCD5, CD3εxCD7, CD4xCD5, CD4xCD7 и CD5xCD7.
[0075] Вариант реализации данного изобретения 46. tCAR по любому из вариантов реализации 35 и 40-45, в котором конструкция CAR представляет собой линейную конструкцию tCAR.
[0076] Вариант реализации данного изобретения 47. tCAR по варианту реализации данного изобретения 46, в котором линейная конструкция tCAR содержит первый вариабельный фрагмент тяжелой цепи (VH) и первый вариабельный фрагмент легкой цепи (VL), обозначенные VH1 и VL1, соединенные (GGGGS)2-6 линкером ко второму вариабельному фрагменту легкой цепи (VL) и первому вариабельному фрагменту тяжелой цепи (VH), обозначенные как VL2 и VH2.
[0077] Вариант реализации данного изобретения 48. tCAR по варианту реализации данного изобретения 46, в котором линейная конструкция tCAR содержит первый вариабельный фрагмент тяжелой цепи (VH) и первый вариабельный фрагмент легкой цепи (VL), обозначенные VH2 и VL2, соединенные (GGGGS)2-6 линкером ко второму вариабельному фрагменту легкой цепи (VL) и первому вариабельному фрагменту тяжелой цепи (VH), обозначенные как VH1 и VL1.
[0078] Вариант реализации данного изобретения 49. tCAR по варианту реализации данного изобретения 46, в котором линейная конструкция tCAR содержит первый вариабельный фрагмент легкой цепи (VL) и первый вариабельный фрагмент тяжелой цепи (VH), обозначенные VL1 и VH1, соединенные (GGGGS)2-6 линкером ко второму вариабельному фрагменту тяжелой цепи (VH) и первому вариабельному фрагменту легкой цепи (VL), обозначенные как VH2 и VL2.
[0079] Вариант реализации данного изобретения 50. tCAR по варианту реализации данного изобретения 46, в котором линейная конструкция tCAR содержит первый вариабельный фрагмент легкой цепи (VL) и первый вариабельный фрагмент тяжелой цепи (VH), обозначенные VL2 и VH2, соединенные (GGGGS)2-6 линкером ко второму вариабельному фрагменту тяжелой цепи (VH) и первому вариабельному фрагменту легкой цепи (VL), обозначенные как VH1 и VL1.
[0080] Вариант реализации данного изобретения 51. tCAR по варианту реализации 46, в котором линейная конструкция tCAR содержит структуру, выбранную из 7-I - 7-XXXII.
[0081] Вариант реализации данного изобретения 52. tCAR по любому из вариантов реализации 35 и 40-45, в котором конструкция CAR представляет собой шпилечную конструкцию tCAR.
[0082] Вариант реализации данного изобретения 53. tCAR по варианту реализации данного изобретения 52, в котором шпилечная конструкция tCAR содержит первый вариабельный фрагмент тяжелой цепи (VH), полученный из первого scFv, и второй вариабельный фрагмент тяжелой цепи (VH), полученный из второго scFv, обозначенные VH1 и VH2, соединенные линкером (GGGGS)2-6 с первым вариабельным фрагментом легкой цепи (VL), полученным из второго scFv, и вторым вариабельным фрагментом легкой цепи (VL), полученным из первого scFv, обозначенные как VL2 и V12.
[0083] Вариант реализации данного изобретения 54. tCAR по варианту реализации данного изобретения 52, в котором шпилечная конструкция tCAR содержит второй вариабельный фрагмент тяжелой цепи (VH), полученный из второго scFv, и первый вариабельный фрагмент тяжелой цепи (VH), полученный из первого scFv, обозначенные VH2 и VH1, соединенные линкером (GGGGS)2-6 с первым вариабельным фрагментом легкой цепи (VL), полученным из первого scFv, и вторым вариабельным фрагментом легкой цепи (VL), полученным из второго scFv, обозначенные как VL1 и VL2.
[0084] Вариант реализации данного изобретения 55. tCAR по варианту реализации данного изобретения 52, в котором шпилечная конструкция tCAR содержит первый вариабельный фрагмент легкой цепи (VL), полученный из первого scFv, и второй вариабельный фрагмент легкой цепи (VL), полученный из второго scFv, обозначенные VL1 и VL2, соединенные линкером (GGGGS)2-6 с первым вариабельным фрагментом тяжелой цепи (VH), полученным из первого scFv, и вторым вариабельным фрагментом тяжелой цепи (VL), полученным из второго scFv, обозначенные как VH2 и VH1.
[0085] Вариант реализации данного изобретения 56. tCAR по варианту реализации данного изобретения 52, в котором шпилечная конструкция tCAR содержит второй вариабельный фрагмент легкой цепи (VL), полученный из второго scFv, и первый вариабельный фрагмент легкой цепи (VL), полученный из первого scFv, обозначенные VL2 и VL1, соединенные линкером (GGGGS)2-6 с первым вариабельным фрагментом тяжелой цепи (VH), полученным из первого scFv, и вторым вариабельным фрагментом тяжелой цепи (VH), полученным из второго scFv, обозначенные как VH1 и VH2.
[0086] Вариант реализации данного изобретения 57. tCAR по варианту реализации 52, в котором шпилечная конструкция tCAR содержит структуру, выбранную из 9-I - 9-XXXII.
[0087] Вариант реализации данного изобретения 58. tCAR по любому из вариантов реализации 35 и 40-45, в котором конструкция CAR представляет собой шпилечную конструкцию tCAR DSB с (Cys=Cys) двухцепочечной связью (DSB) в линкере.
[0088] Вариант реализации данного изобретения 59. tCAR по варианту реализации данного изобретения 58, в котором шпилечная конструкция tCAR содержит первый вариабельный фрагмент тяжелой цепи (VH), полученный из первого scFv, и второй вариабельный фрагмент тяжелой цепи (VH), полученный из второго scFv, обозначенные VH1 и VH2, соединенные линкером (GGGGS)0-1-(GGGGC)1-(GGGGS)1-2-(GGGGP)1-(GGGGS)2-3-(GGGGC)1-(GGGGS)0-1с первым вариабельным фрагментом легкой цепи (VL), полученным из второго scFv, и вторым вариабельным фрагментом легкой цепи (VL), полученным из первого scFv, обозначенные как VL2 и V12.
[0089] Вариант реализации данного изобретения 60. tCAR по варианту реализации данного изобретения 58, в котором шпилечная конструкция tCAR содержит второй вариабельный фрагмент тяжелой цепи (VH), полученный из второго scFv, и первый вариабельный фрагмент тяжелой цепи (VH), полученный из первого scFv, обозначенные VH2 и VH1, соединенные линкером (GGGGS)0-1-(GGGGC)1-(GGGGS)1-2-(GGGGP)1-(GGGGS)2-3-(GGGGC)1-(GGGGS)0-1с первым вариабельным фрагментом легкой цепи (VL), полученным из первого scFv, и вторым вариабельным фрагментом легкой цепи (VL), полученным из второго scFv, обозначенные как VL1 и VL2.
[0090] Вариант реализации данного изобретения 61. tCAR по варианту реализации данного изобретения 58, в котором шпилечная конструкция tCAR содержит первый вариабельный фрагмент легкой цепи (VL), полученный из первого scFv, и второй вариабельный фрагмент легкой цепи (VL), полученный из второго scFv, обозначенные VL1 и VL2, соединенные линкером (GGGGS)0-1-(GGGGC)1-(GGGGS)1-2-(GGGGP)1-(GGGGS)2-3-(GGGGC)1-(GGGGS)0-1с первым вариабельным фрагментом тяжелой цепи (VH), полученным из первого scFv, и вторым вариабельным фрагментом тяжелой цепи (VL), полученным из второго scFv, обозначенные как VH2 и VH1.
[0091] Вариант реализации данного изобретения 62. tCAR по варианту реализации данного изобретения 58, в котором шпилечная конструкция tCAR содержит второй вариабельный фрагмент легкой цепи (VL), полученный из второго scFv, и первый вариабельный фрагмент легкой цепи (VL), полученный из первого scFv, обозначенные VL2 и VL1, соединенные линкером (GGGGS)0-1-(GGGGC)1-(GGGGS)1-2-(GGGGP)1-(GGGGS)2-3-(GGGGC)1-(GGGGS)0-1с первым вариабельным фрагментом тяжелой цепи (VH), полученным из первого scFv, и вторым вариабельным фрагментом тяжелой цепи (VH), полученным из второго scFv, обозначенные как VH1 и VH2.
[0092] Вариант реализации данного изобретения 63. tCAR по варианту реализации 58, в котором шпилечная конструкция DSB tCAR содержит структуру, выбранную из 11-I - 11-XXXII.
[0093] Вариант реализации данного изобретения 64. tCAR по любому из вариантов реализации 41-63, в котором каждая из цепей VH и VL полученная из scFv, который распознает другой антиген, выбранный из CD5, CD7, CD2, CD4 и CD3.
[0094] Вариант реализации данного изобретения 65. tCAR по варианту реализации данного изобретения 64, в котором каждая из цепей VH и VL отличается и по меньшей мере на 95% идентична аминокислотной последовательности, выбранной из от SEQ ID NO:12 - SEQ ID NO:31.
[0095] Вариант реализации данного изобретения 66. tCAR по варианту реализации данного изобретения 64, в котором каждая из цепей VH и VL отличается и по меньшей мере на 98% идентична аминокислотной последовательности, выбранной из от SEQ ID NO:12 - SEQ ID NO:31.
[0096] Вариант реализации данного изобретения 67. tCAR по варианту реализации данного изобретения 64, в котором каждая из цепей VH и VL отличается и представляет собой последовательность, выбранную из SEQ ID NO:12 - SEQ ID NO:31.
[0097] Вариант реализации данного изобретения 68. tCAR по любому из вариантов реализации 35, 39 и 41-67 содержит по меньшей мере один костимулирующий домен, выбранный из CD28 и 4-1BB.
[0098] Вариант реализации данного изобретения 69. tCAR по варианту реализации данного изобретения 68, в котором костимулирующий домен представляет собой CD28.
[0099] Вариант реализации данного изобретения 70. tCAR по любому из вариантов реализации данного изобретения 35 и 40-69, содержащий сигнальный домен CD3ζ.
[00100] Вариант реализации данного изобретения 71. tCAR по любому из вариантов реализации данного изобретения 41-63 и 68-70, в котором каждая из цепей VH и VL, происходит от scFv, распознающего CD2 или scFv, распознающего CD3.
[00101] Вариант реализации данного изобретения 72. tCAR по варианту реализации данного изобретения 64, в котором конструкция tCAR выбрана из Клона 5, Клона 6, Клона 7, Клона 8, Клона 13, Клона 14, Клона 15 и Клона 16.
[00102] Вариант реализации данного изобретения 73. tCAR по варианту реализации данного изобретения 64, в котором конструкция tCAR имеет последовательность по меньшей мере на 95% идентичную аминокислотной последовательности, выбранной из SEQ ID NO:41 - SEQ ID NO:46.
[00103] Вариант реализации данного изобретения 74. Тандемная Т-клетка химерного антигенного рецептора (CAR) (tCAR T-клетка), которая содержит tCAR, нацеленную на два или более Т-клеточных антигена по любому из вариантов реализации 35 и 40-73.
[00104] Вариант реализации данного изобретения 75. tCAR T-клетка по варианту реализации данного изобретения 74, в котором клетка дефицитна по одному или более антигенам, с которыми специфически связывается один или более CAR.
[00105] Вариант реализации данного изобретения 76. tCAR T-клетка по любому из вариантов реализации данного изобретения 74 и 75, в котором tCAR T-клетка дефицитна по субъединице рецепторного комплекса T-клеток.
[00106] Вариант реализации данного изобретения 77. tCAR T-клетка по варианту реализации данного изобретения 76, в котором субъединица рецепторного комплекса Т-клетки выбрана из TCRα(TRAC), TCRβ, TCRδ, TCRγ, CD3ε, CD3γ, CD3δ, и CD3ζ.
[00107] Вариант реализации данного изобретения 78. tCAR-T по варианту реализации данного изобретения 77, в котором субъединица рецепторного комплекса Т-клетки выбрана из TCRα(TRAC) и CD3ε.
[00108] Вариант реализации данного изобретения 79. tCAR-T по варианту реализации данного изобретения 78, в котором субъединица рецепторного комплекса Т-клетки представляет собой TRAC.
[00109] Вариант реализации данного изобретения 80. tCAR T-клетка по любому из вариантов реализации 35 и 40-79, в котором CAR T-клетка дополнительно содержит «суицидный» ген.
[00110] Вариант реализации данного изобретения 81. tCAR T-клетка по любому из вариантов реализации 35 и 40-80, в котором передача сигналов, опосредованная эндогенным Т-клеточным рецептором, заблокирована в CAR-T-клетке.
[00111] Вариант реализации данного изобретения 82. tCAR T-клетка по любому из вариантов реализации 35 и 40-81, в котором CAR T-клетки не индуцируют аллореактивность или реакцию «трансплантат против хозяина».
[00112] Вариант реализации данного изобретения 83. tCAR T-клетка по любому из вариантов реализации 35 и 40-82, в котором CAR T-клетки не индуцируют взаимное уничтожение.
[00113] Вариант реализации данного изобретения 84. Тандемная CAR T-клетка, имеющая CAR, нацеленную на CD2 и CD3, при этом CAR T-клетка дефицитна по субъединице рецепторного комплекса Т-клеток и дефицитна по CD2.
[00114] Вариант реализации данного изобретения 85. CAR-T по варианту реализации данного изобретения 85, в котором CAR имеет последовательность по меньшей мере на 95% идентичную аминокислотной последовательности, выбранной из SEQ ID NO:41 - SEQ ID NO:44.
[00115] Вариант реализации данного изобретения 86. CAR-T по варианту реализации данного изобретения 85, в котором CAR имеет последовательность по меньшей мере на 98% идентичную аминокислотной последовательности, выбранной из SEQ ID NO:41 - SEQ ID NO:44.
[00116] Вариант реализации данного изобретения 87. CAR-T по варианту реализации данного изобретения 85, в котором CAR представляет собой аминокислотную последовательность, выбранную из SEQ ID NO:41 - SEQ ID NO:44.
[00117] Вариант реализации данного изобретения 88. Тандемная CAR T-клетка, имеющая CAR, нацеленную на CD2 и CD7, при этом CAR T-клетка дефицитна по субъединице рецепторного комплекса T-клетки и дефицитна по CD2 и CD7.
[00118] Вариант реализации данного изобретения 89. CAR-T по варианту реализации данного изобретения 88, в котором CAR имеет последовательность по меньшей мере на 95% идентичную аминокислотной последовательности, выбранной из SEQ ID NO:45 - SEQ ID NO:46.
[00119] Вариант реализации данного изобретения 90. CAR-T по варианту реализации данного изобретения 88, в котором CAR имеет последовательность по меньшей мере на 98% идентичную аминокислотной последовательности, выбранной из SEQ ID NO:45 - SEQ ID NO:46.
[00120] Вариант реализации данного изобретения 91. CAR-T по варианту реализации данного изобретения 88, в котором CAR представляет собой аминокислотную последовательность, выбранную из SEQ ID NO:45 - SEQ ID NO:46.
[00121] Вариант реализации данного изобретения 92. CAR T-клетка, которая содержит химерный антигенный рецептор (CAR), нацеленный на CD7, где CAR T-клетка дефицитна по TRAC и дефицитна по CD7, и содержит костимулирующий домен CD28 и сигнальный домен CD3ζ.
[00122] Вариант реализации данного изобретения 93. CAR-T по варианту реализации данного изобретения 92, в котором CAR имеет последовательность по меньшей мере на 95% идентичную аминокислотной последовательности, выбранной из SEQ ID NO:32 - SEQ ID NO:39.
[00123] Вариант реализации данного изобретения 94. CAR-T по варианту реализации данного изобретения 92, в котором CAR имеет последовательность по меньшей мере на 98% идентичную аминокислотной последовательности, выбранной из SEQ ID NO:32 - SEQ ID NO:39.
[00124] Вариант реализации данного изобретения 95. CAR-T по варианту реализации данного изобретения 92, в котором CAR представляет собой аминокислотную последовательность, выбранную из SEQ ID NO:32 - SEQ ID NO:39.
[00125] Терапевтическая композиция, содержащая популяцию CAR T-клеток по любому из вариантов реализации 1-30 и 74-95, или содержащую популяцию CAR T-клеток, содержащих CAR по любому из вариантов реализации 31-73, и по меньшей мере один терапевтически приемлемый носитель и/или адъювант.
[00126] Вариант реализации данного изобретения 96. Способ лечения рака у пациента, включающий введение отредактированного геномом CAR T-клетки, популяции отредактированных геномом CAR T-клеток, двойных CAR T-клеток или тандемного CAR-T по любому из вариантов реализации 1- 30 и 74-95, или содержащих популяцию CAR T-клеток, содержащих CAR (ы) по любому из вариантов реализации 31-73, пациенту, нуждающемуся в этом.
[00127] Вариант реализации данного изобретения 97. Способ по варианту реализации 97, в котором рак представляет собой гематологическое злокачественное новообразование.
[00128] Вариант реализации данного изобретения 98. Способ по варианту реализации 98, в котором гематологическое злокачественное новообразование представляет собой злокачественное новообразование Т-клеток.
[00129] Вариант реализации данного изобретения 99. Способ по варианту реализации 99, в котором Т-клеточная злокачественная опухоль представляет собой Т-клеточный острый лимфобластный лейкоз (Т-ОЛЛ).
[00130] Вариант реализации данного изобретения 100. Способ по варианту реализации 99, в котором злокачественная опухоль Т-клеток представляет собой неходжкинскую лимфому.
[00131] Вариант реализации данного изобретения 101. Способ по варианту реализации 99, в котором Т-клеточная злокачественная опухоль представляет собой Т-клеточный хронический лимфоцитарный лейкоз (Т-ХЛЛ).
[00132] Вариант реализации данного изобретения 102. Способ по варианту реализации 98, в котором гематологическое злокачественное новообразование представляет собой множественную миелому.
[00133] Вариант реализации данного изобретения 103. Способ по варианту реализации 98, в котором гематологическое злокачественное новообразование представляет собой острый миелоидный лейкоз (ОМЛ).
[00134] Вариант реализации данного изобретения 104. Способ получения CAR T-клетки по любому из варианту реализации выше или данного документа, с использованием Cas9-CRISPR и гРНК, выбранной из тех, что раскрыты в данном документе.
[00135] Вариант реализации данного изобретения 105. Способ получения CAR T-клетки по любому из варианту реализации выше или данного документа, с использованием Cas9-CRISPR и гРНК, выбранной из тех, что раскрыты в Таблице 12 и Таблицах 15-47.
[00136] Вариант реализации данного изобретения 106. Способ получения CAR T-клетки по любому из варианту реализации выше или данного документа, с использованием Cas9-CRISPR и гРНК, выбранной из тех, что раскрыты в Таблице 12 и тех, которые выделены жирным шрифтом в Таблицах 15-47.
[00137] Вариант реализации данного изобретения 107. Способ получения CAR T-клетки по любому из варианту реализации выше или данного документа, с использованием Cas9-CRISPR и гРНК, выбранной из тех, что раскрыты в Таблице 12.
[00138] M
[00139] В данном документе описывается редактированная геномом CAR T-клетка, полученная из хелперной Т-клетки, цитотоксической Т-клетки, вирусоспецифической цитотоксической Т-клетки, Т-клетки памяти или гамма-дельта (γδ) Т-клетки, которые включают один или более химерных антигенных рецепторов (CAR), нацеленных на один или более антигенам, при этом CAR T-клетка дефицитна по одному или более антигенам, с которыми специфически связывается один или более CAR.
[00140] Также предлагается редактированная геномом CAR T-клетка, полученная из хелперной Т-клетки, цитотоксической Т-клетки, вирусоспецифической цитотоксической Т-клетки, Т-клетки памяти или гамма-дельта (γδ) Т-клетки, которые включают один или более химерных антигенных рецепторов (CAR), нацеленных на один или более антигенов, при этом CAR T-клетка дефицитна по субъединице рецепторного комплекса Т-клеток и одному, или более антигенам, с которыми специфически связывается один или более CAR.
[00141] Также предлагается CAR T-клетка, полученная из хелперной Т-клетки, цитотоксической Т-клетки, вирусоспецифической цитотоксической Т-клетки, Т-клетки памяти или гамма-дельта (γδ) Т-клетки, в которой недостаточная субъединица рецепторного комплекса Т-клеток выбрана из TCRα, TCRβ, TCRδ, TCRγ, CD3ε, CD3γ, CD3δ, и CD3ζ.
[00142] В некоторых вариантах реализации, химерный антигенный рецептор специфически связывает по меньшей мере один антиген, экспрессируемый на поверхности злокачественной Т-клетки.
[00143] В некоторых вариантах реализации, один или более антигенов выбраны из BCMA, CS1, CD38, CD138, CD19, CD33, CD123, CD371, CD117, CD135, Tim-3, CD5, CD7, CD2, CD4, CD3, CD79A, CD79B, APRIL, CD56 и CD1a.
[00144] В некоторых вариантах реализации, CAR T-клетка дополнительно содержит систему суицидальной генной терапии.
[00145] В некоторых вариантах реализации, передача сигналов, опосредованная эндогенным Т-клеточным рецептором, блокируется в CAR-T-клетке.
[00146] В некоторых вариантах реализации, CAR T-клетка не индуцирует аллореактивность или реакцию «трансплантат против хозяина».
[00147] В некоторых вариантах реализации, CAR T-клетки не индуцируют взаимное уничтожение.
[00148] Также предлагается двойная или тандемная CAR T-клетка.
[00149] Также предлагается фармацевтическая композиция, содержащая популяцию CAR T-клеток, как описано в данном документе, и по меньшей мере один терапевтически приемлемый носитель и/или адъювант.
[00150] Также предлагаются способы лечения гематологических злокачественных новообразований, включающие введение редактируемой геномом CAR T-клетки, популяции редактируемых геномом CAR T-клеток, при этом популяция редактируемых геномом CAR T-клеток представляет собой моно CAR T-клетки, двойные CAR T-клетки или тандемные CAR T-клетки, как описано в данном документе, или фармацевтические композиции, содержащие их, как описано в данном документе, пациенту, нуждающемуся в этом.
[00151] В некоторых вариантах реализации, гематологическое злокачественное новообразование представляет собой злокачественное новообразование Т-клеток.
[00152] В некоторых вариантах реализации, Т-клеточная злокачественная опухоль представляет собой Т-клеточный острый лимфобластный лейкоз (T-ОЛЛ).
[00153] В некоторых вариантах реализации, Т-клеточная злокачественная опухоль представляет собой неходжкинскую лимфому.
[00154] В некоторых вариантах реализации, Т-клеточная злокачественная опухоль представляет собой Т-клеточный хронический лимфоцитарный лейкоз (T-ХЛЛ).
[00155] В некоторых вариантах реализации изобретения гематологическое злокачественное новообразование представляет собой множественную миелому.
[00156] В некоторых вариантах реализации изобретения гематологическое злокачественное новообразование представляет собой острый миелоидный лейкоз (ОМЛ).
CAR T-клетки
[00157] В данном изобретении предлагаются Т-клетки, несущие химерный антигенный рецептор (CAR T-клетки), фармацевтические композиции, содержащие их, и способы иммунотерапии для лечения рака, в частности гематологических злокачественных новообразований.
[00158] CAR T-клетка представляет собой T-клетку, которая экспрессирует химерный антигенный рецептор. Т-клетка, экспрессирующая молекулу CAR, может быть хелперной Т-клеткой, цитотоксической Т-клеткой, вирусоспецифичной цитотоксической Т-клеткой, Т-клеткой памяти или гамма-дельта (γδ) Т-клеткой.
[00159] Химерный антигенный рецептор (CAR) представляет собой рекомбинантный слитый белок, содержащий: 1) внеклеточный лиганд-связывающий домен, т.е. антигенраспознающий домен, 2) трансмембранный домен и 3) сигнальный трансдуцирующий домен.
[00160] Внеклеточный лиганд-связывающий домен представляет собой олиго- или полипептид, способный связывать лиганд. Предпочтительно внеклеточный лиганд-связывающий домен будет способен взаимодействовать с молекулой клеточной поверхности, которая может быть антигеном, рецептором, пептидным лигандом, белковым лигандом мишени или полипептидом мишени. Внеклеточный лиганд-связывающий домен может специфически связываться с антигеном с константой аффинности или аффинностью взаимодействия (KD) от около 0,1 пМ до около 10 пМ, от около 0,1 пМ до около 1 пМ, или более предпочтительно от около 0,1 пМ до около 100 нМ. Способы определения константы аффинности или аффинности взаимодействия (KD) хорошо известны в данной области техники. В некоторых случаях внеклеточный лиганд-связывающий домен выбирается для распознавания лиганда, который действует как маркер клеточной поверхности на клетках-мишенях, связанных с определенными болезненными состояниями.
[00161] В одном варианте реализации, внеклеточный лиганд-связывающий домен содержит фрагмент одноцепочечного антитела (scFv), содержащий вариабельные фрагменты легкой (VL) и тяжелой (VH) цепи, соединенные линкером (например, GGGGS(2-6)), и придает специфичность либо для Т-клеточного антигена, либо для антигена, не специфичного к Т-клетке. В одном варианте реализации, химерный антигенный рецептор CAR T-клетки может связываться с Т-клеточно-специфическим антигеном, экспрессируемым или сверхэкспрессируемым на поверхности злокачественной Т-клетки, для которой CAR T-клетка является дефицитной по антигену (например, геном-отредактированная CAR T-клетка).
[00162] Неограничивающие примеры CAR-нацеленных антигенов, экспрессируемых на поверхностях злокачественных Т-клеток, включают CD5, CD7, CD2, CD4 и CD3. В одном варианте реализации, CAR T-клетка согласно данному изобретению содержит химерный антигенный рецептор с внеклеточным лиганд-связывающим доменом, который специфически связывается с CD5.
[00163] В другом варианте реализации, CAR T-клетка согласно данному изобретению содержит химерный антигенный рецептор с внеклеточным лиганд-связывающим доменом, который специфически связывается с CD7. Другими словами, CAR, который специфически связывает CD7, включает внеклеточный лиганд-связывающий домен, содержащий полипептидную последовательность по меньшей мере на 80%, 90%, 95%, 97% или 99% идентичную аминокислотной последовательности, выбранной из SEQ ID NO: 20 и SEQ ID NO: 21, и связаны вместе гибким линкером, содержащим последовательность (GGGGS)3-4.
[00164] В другом варианте реализации, CAR T-клетка согласно данному изобретению содержит химерный антигенный рецептор с внеклеточным лиганд-связывающим доменом, который специфически связывается с CD2. Другими словами, CAR, который специфически связывает CD2, включает внеклеточный лиганд-связывающий домен, содержащий полипептидную последовательность по меньшей мере на 80%, 90%, 95%, 97% или 99% идентичную аминокислотной последовательности, выбранной из SEQ ID NO: 12 и SEQ ID NO: 13, или SEQ ID NO: 14 и SEQ ID NO: 15, и связаны вместе гибким линкером, содержащим последовательность (GGGGS)3-4.
[00165] В еще одном варианте реализации, CAR T-клетка согласно данному изобретению содержит химерный антигенный рецептор с внеклеточным лиганд-связывающим доменом, который специфически связывается с CD4.
[00166] В еще одном варианте реализации, CAR T-клетка согласно данному изобретению содержит внеклеточный лиганд-связывающий домен химерного антигенного рецептора, который специфически связывается с CD3. Другими словами, CAR, который специфически связывает CD3, включает внеклеточный лиганд-связывающий домен, содержащий полипептидную последовательность по меньшей мере на 80%, 90%, 95%, 97% или 99% идентичную аминокислотной последовательности, выбранной из SEQ ID NO: 16 и SEQ ID NO: 17, или SEQ ID NO: 18 и SEQ ID NO: 19, и связаны вместе гибким линкером, содержащим последовательность (GGGGS)3-4.
[00167] Неограничивающие примеры антигенов, нацеленных на CAR, экспрессируемых на поверхности лейкозных клеток (например, аномальных миелобластов, красных кровяных телец или тромбоцитов), включают CD123 (IL3RA), CD371 (CLL-1; CLEC12A), CD117 (c-kit) и CD135 (FLT3), CD7 и Tim3. CAR может быть сконструирован с внеклеточным лиганд-связывающим доменом для нацеливания на эти антигены для лечения лейкоза, то есть острого миелоидного лейкоза (ОМЛ).
[00168] Неограничивающие примеры антигенов, нацеленных на CAR, экспрессируемых на поверхности клетки множественной миеломы (например, злокачественной плазматической клетки), включают BCMA, CS1, CD38, CD79A, CD79B, CD138 и CD19. CAR может быть сконструирован с внеклеточным лиганд-связывающим доменом для нацеливания на эти антигены для лечения множественной миеломы. В другом варианте реализации, CAR может быть сконструирован с частью белка APRIL, нацеленным на лиганд для антигена созревания B-клеток (BCMA) и трансмембранного активатора, и партнера CAML (TACI), эффективно нацеливая как BCMA, так и TACI на лечение множественной миеломы. Сигнальный пептид направляет транспорт секретируемого или трансмембранного белка к клеточной мембране и/или поверхности клетки, чтобы обеспечить правильную локализацию полипептида. В частности, сигнальный пептид согласно данному изобретению направляет присоединенный полипептид, то есть рецептор CAR, к клеточной мембране, где внеклеточный лиганд-связывающий домен присоединенного полипептида отображается на поверхности клетки, трансмембранный домен присоединенного полипептида охватывает клеточная мембрана, и сигнальный трансдуцирующий домен присоединенного полипептида находится в цитоплазматической части клетки. В одном варианте реализации, сигнальный пептид представляет собой сигнальный пептид CD8α человека (SEQ ID NO:1). В одном варианте реализации, сигнальный пептид представляет собой функциональный фрагмент сигнального пептида CD8α Функциональный фрагмент определяется как фрагмент из по меньшей мере 10 аминокислот сигнального пептида CD8α, который направляет присоединенный полипептид к клеточной мембране и/или поверхности клетки. Примеры функциональных фрагментов сигнального пептида CD8α человека включают аминокислотные последовательности MALPVTALLLPLALLLHAA, MALPVTALLLP, PVTALLLPLALL и LLLPLALLLHAARP.
[00169] Обычно внеклеточный лиганд-связывающий домен связан с сигнальным трансдуцирующим доменом химерного антигенного рецептора (CAR) посредством трансмембранного домена (Tm). Трансмембранный домен пересекает клеточную мембрану, прикрепляет CAR к поверхности Т-клеток и соединяет внеклеточный лиганд-связывающий домен с доменом, передающим сигнал, что влияет на экспрессию CAR на поверхности Т-клеток.
[00170] Отличительной особенностью трансмембранного домена в данном описании является способность экспрессироваться на поверхности иммунной клетки, чтобы направлять ответ иммунной клетки против заранее определенной клетки-мишени. Трансмембранный домен можно получить либо из природного, либо из синтетического источника. Альтернативно, трансмембранный домен согласно данному изобретению может происходить из любого мембраносвязанного или трансмембранного белка.
[00171] Неограничивающие примеры трансмембранных полипептидов согласно данному изобретению представляют собой альфа, бета или дзета-цепь Т-клеточного рецептора, CD28, CD3 эпсилон, CD45, CD4, CDS, CDS, CD9, CD16, CD22, CD33, CD37, CD64, CDS0, CD86, CD134, CD137 и CD154. Альтернативно, трансмембранный домен может быть синтетическим и содержать преимущественно гидрофобные аминокислотные остатки (например, лейцин и валин). В одном варианте реализации, трансмембранный домен происходит из предшественника изоформы 1 альфа-цепи гликопротеина CD8 поверхности Т-клетки (NP_001139345.1) (SEQ ID NO: 4), и более предпочтительно CD28 (SEQ ID NO: 3). Трансмембранный домен может дополнительно включать шарнирную область между внеклеточным лиганд-связывающим доменом и указанным трансмембранным доменом. Термин «шарнирная область» обычно означает любой олиго- или полипептид, который функционирует, чтобы связывать трансмембранный домен с внеклеточным лиганд-связывающим доменом. В частности, шарнирная область используется для обеспечения большей гибкости и доступности для внеклеточного лиганд-связывающего домена. Шарнирная область может содержать до 300 аминокислот, предпочтительно от 10 до 100 аминокислот и наиболее предпочтительно от 25 до 50 аминокислот. Шарнирная область может происходить из всех или частей встречающихся в природе молекул, таких как CD28, 4-1BB (CD137), OX-40 (CD134), CD3ζ, рецептор Т-клетки α или β-цепи, CD45, CD4, CD5, CD8, CD8α, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, ICOS, CD154 или из всей или части константной области антитела. В качестве альтернативы, шарнирная область может быть синтетической последовательностью, которая соответствует встречающейся в природе шарнирной последовательности, или шарнирная область может быть полностью синтетической шарнирной последовательностью. В одном варианте реализации, шарнирный домен содержит часть CD8 α (SEQ ID NO:2) человека, рецептор FcγRIIIα или IgG1 и по меньшей мере на 80%, 90%, 95%, 97% или 99% идентичную к ней последовательность.
[00172] Химерный антигенный рецептор (CAR) согласно данному изобретению содержит трансдукционный сигнальный домен или внутриклеточный сигнальный домен CAR, который отвечает за внутриклеточную передачу сигналов после связывания внеклеточного лиганд-связывающего домена с мишенью, что приводит к активации иммунной клетки и иммунной реакции. Внутриклеточный сигнальный домен отвечает за активацию по меньшей мере одной из нормальных эффекторных функций иммунной эффекторной клетки, экспрессирующей CAR. Эффекторной функцией Т-клетки, например, может быть цитолитическая активность или хелперная активность, включая секрецию цитокинов. Таким образом, термин "цитоплазматическая сигнальная область" относится к части белка, которая трансдуцирует сигнал эффекторной функции и направляет клетку для выполнения специализированной функции.
[00173] Примерами доменов сигнальной трансдукции для использования в CAR могут быть цитоплазматическими последовательностями Т-клеточного рецептора и корецепторов, которые действуют совместно, инициируя сигнальную трансдукцию после взаимодействия антигенного рецептора, а также любые производные или варианты этих последовательностей и любой синтетической последовательности, имеющей такие же функциональные возможности. Домен сигнальной трансдукции включает два разных класса цитоплазматических сигнальных последовательностей: те, которые инициируют антиген-зависимую первичную активацию, и те, которые действуют антиген-независимым образом, обеспечивая вторичный или костимулирующий сигнал. Первичная цитоплазматическая сигнальная последовательность может содержать сигнальные мотивы, которые известны как иммунорецепторные тирозиновые активирующие мотивы ITAM. ITAM представляют собой четко определенные сигнальные мотивы, обнаруженные в внутрицитоплазматическом хвосте множества рецепторов, которые служат сайтами связывания для тирозинкиназ класса syk/zap70. Неограничивающие примеры ITAM, которые могут быть использованы в данном изобретении, могут включать те, которые получены из TCRζ, FcRγ, FcRβ, FcRε, CD3γ, CD3δ, CD3ε, CDS, CD22, CD79a, CD79b и CD66d. В одном варианте реализации сигнальный трансдуцирующий домен CAR может включать сигнальный домен CD3ζ с аминокислотной последовательностью по меньшей мере на 80%, 90%, 95%, 97% или 99% идентичной к ней последовательности.
[00174] Кроме того, CAR T-клетки по данному изобретению могут дополнительно содержать одну или более систем суицидальной генной терапии. Подходящие системы суицидальной генной терапии, известные в данной области техники, включают, но не ограничиваются ими, несколько тимидинкиназ вируса простого герпеса (HSVtk)/ганцикловир (GCV) или индуцибельные белки каспазы 9. В одном варианте реализации, суицидный ген представляет собой химерную CD34/тимидинкиназу.
[00175] Описанные в данном документе Т-клетки могут быть дефицитными по антигену, с которым химерный антигенный рецептор специфически связывается, и поэтому устойчивы к взаимному уничтожению. В некоторых вариантах реализации, антиген Т-клетки модифицирован таким образом, что химерный антигенный рецептор больше не связывает специфически модифицированный антиген. Например, эпитоп антигена, распознаваемый химерным антигенным рецептором, может быть модифицирован с помощью одной или более изменениями аминокислоты (например, заменами или делециями), или эпитоп может быть удален из антигена. В других вариантах реализации, экспрессия антигена снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более. Способы снижения экспрессии белка известны в данной области техники и включают, но не ограничиваются ими, модификацию или замену промотора, функционально связанного с последовательностью нуклеиновой кислоты, кодирующей белок. В других вариантах реализации, Т-клетка модифицируется таким образом, что антиген не экспрессируется, например, путем делеции или разрушения гена, кодирующего антиген. В каждом из вышеупомянутых вариантов реализации, Т-клетка может быть дефицитной по одному или предпочтительно по всем антигенам, с которыми специфически связывается химерный антигенный рецептор. Способы генетической модификации Т-клетки, чтобы она была дефицитной по антигену хорошо известны в данной области техники, и выше приведены неограничивающие примеры. В типовом варианте реализации редактирование гена CRISPR/cas9 может быть использовано для модификации Т-клетки, чтобы она была дефицитной по антигену, например, как описано ниже. В качестве альтернативы для редактирования генов могут быть использованы TALEN.
[00176] В варианте вышеописанного способа конструкция, кодирующая один или более блокаторов экспрессии белка (PEBL), может быть трансдуцирована в клетку либо на этапе редактирования, либо как часть этапа редактирования, либо как часть трансдукции CAR. Например, может быть трансдуцирована конструкция, кодирующая одноцепочечный вариабельный фрагмент, полученный из антитела, специфичный для CD3ε, например, лентивирусным вектором. После экспрессии PEBL внутриклеточно колокализуется с CD3ε, блокируя поверхностную экспрессию CD3 и TCRαβ. Соответственно, PEBL-блокада поверхностной экспрессии CD3/TCRαβ является альтернативным способом получения аллогенных CAR T-клеток. Кроме того, экспрессию PEBL и CAR можно комбинировать в одной конструкции. Любой из этих способов может быть реализован с использованием способов, раскрытых в данном документе, и PEBL могут быть получены для блокирования любой из целей супрессии гена, раскрытых в данном документе.
[00177] Описанные выше способы можно адаптировать для вставки CAR в локус гена, кодирующего антиген, белок клеточной поверхности или секретируемый белок, такой как цитокин. Таким образом, редактирование генома осуществляется путем трансфекции CAR. После этого клетки можно активировать, как описано в данном документе, исключая отдельный этап редактирования генома в некоторых вариантах реализации. В идеале такой шаг следует выполнять, пока клетки активно делятся. Ожидается, что такие способы также приведут к устойчивому увеличению количества сконструированных клеток.
[00178] В определенных обстоятельствах Т-клетка может быть выбрана из-за дефицита антигена, с которым специфически связывается химерный антигенный рецептор. Определенные Т-клетки будут производить и отображать меньше данного поверхностного белка; вместо этого при делеции или нефункционализации антигена, который будет мишенью T-CAR, T-клетка может быть выбрана из-за дефицита антигена, и популяция антиген-дефицитных клеток увеличится для трансдукции CAR. Такая клетка также будет устойчивой к взаимному уничтожению.
[00179] Таблица 1. Аминокислотные последовательности различных компонентов CAR.
[00180] Таблица 2. Аминокислотные последовательности вариабельной тяжелой (VH) и вариабельной легкой (VL) цепей scFv.
Моно CAR T-клетки (mCAR-T)
[00181] CAR T-клетки, охватываемые данным описанием, имеют дефицит по одному или более антигенам, с которыми химерный антигенный рецептор специфически связывается, и поэтому устойчивы к взаимному уничтожению. В некоторых вариантах реализации один или более антигенов Т-клетки модифицированы таким образом, что химерный антигенный рецептор больше не связывает специфически один или более модифицированных антигенов. Например, эпитоп одного или более антигенов, распознаваемый химерным антигенным рецептором, может быть модифицирован с помощью одной или более изменениями аминокислоты (например, заменами или делециями), или эпитоп может быть удален из антигена. В других вариантах реализации, экспрессия одного или более антигенов снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более. Способы снижения экспрессии белка известны в данной области техники и включают, но не ограничиваются ими, модификацию или замену промотора, функционально связанного с последовательностью нуклеиновой кислоты, кодирующей белок. В других вариантах реализации, Т-клетка модифицируется таким образом, что один или более антигенов не экспрессируется, например, путем делеции или разрушения гена, кодирующего один или более антигенов. В каждом из вышеупомянутых вариантов реализации, CAR T-клетка может быть дефицитной по одному или предпочтительно по всем антигенам, с которыми специфически связывается химерный антигенный рецептор. Способы генетической модификации Т-клетки, чтобы она была дефицитной по одному или более антигенам хорошо известны в данной области техники и в данном документе приведены неограничивающие примеры. В вариантах реализации, описанных в Примерах 1-6, система CRISPR-Cas9 используется для модификации Т-клетки таким образом, чтобы она была дефицитной по одному или более антигенам.
[00182] CAR T-клетки, охватываемые данным раскрытием, могут, кроме того, быть дефицитными по передаче сигналов эндогенного Т-клеточного рецептора (TCR) в результате удаления части рецепторного комплекса T-клеток (TCR)-CD3. В различных вариантах реализации может быть желательно устранить или подавить эндогенную передачу сигналов, опосредованную эндогенным TCR в CAR T-клетках, описанных в данном документе. Например, уменьшение или устранение передачи сигналов, опосредованной эндогенным TCR в CAR T-клетках может предотвратить или уменьшить реакцию трансплантат против хозяина (GvHD), когда аллогенные Т-клетки используются для продуцирования CAR T-клеток. Способы устранения или подавления передачи сигналов, опосредованной эндогенным TCR известны в данной области техники и включают, но не ограничиваются этим, удаление части рецепторного комплекса TCR-CD3, например, альфа-цепи рецептора TCR (TRAC), бета-цепи рецептора TCR (TCRβ), TCRδ, TCRγ, CD3ε, CD3γ и/или CD3δ. Удаление части рецепторного комплекса TCR может блокировать передачу сигналов, опосредованную TCR, и, таким образом, может позволить безопасное использование аллогенных Т-клеток в качестве источника CAR T-клеток, не вызывая опасную для жизни реакцию ТПХ.
[00183] Кроме того, CAR T-клетки, охватываемые данным изобретением могут дополнительно содержать одну или более суицидных генов, описанных в данном документе.
[00184] В одном варианте реализации данное изобретение предлагает Т-клетку, содержащую химерный антигенный рецептор, который специфически связывает CD5, при этом Т-клетка дефицитна по CD5, например, CD5ΔCART5 клетке В неограничивающих примерах дефицит в CD5 вызван (а) модификацией CD5, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD5, (b) модификацией Т-клетки, при которой экспрессия антигена снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD5 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD5). В дополнительных вариантах реализации Т-клетка содержит суицидный ген и/или модификацию таким образом, что передача сигналов, опосредованная эндогенным Т-клеточным рецептором (TCR), заблокирована в Т-клетке. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека экспрессируется в CD5ΔCART5 клетках.
[00185] В другом варианте реализации данное изобретение предлагает Т-клетку, содержащую химерный антигенный рецептор, который специфически связывает CD7, при этом Т-клетка дефицитна по CD7, например, CD7ΔCART7 клетке. В неограничивающих примерах дефицит в CD7 вызван (а) модификацией CD7, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD7, (b) модификацией Т-клетки, при которой экспрессия антигена снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD7 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD7). В дополнительных вариантах реализации Т-клетка содержит суицидный ген и/или модификацию таким образом, что передача сигналов, опосредованная эндогенным Т-клеточным рецептором (TCR), заблокирована в Т-клетке. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека экспрессируется в CD7ΔCART7 клетках.
[00186] В другом варианте реализации данное изобретение предлагает Т-клетку, содержащую химерный антигенный рецептор, который специфически связывает CD2, при этом Т-клетка дефицитна по CD2, например, CD2ΔCART2 клетке. В неограничивающих примерах дефицит в CD2 вызван (а) модификацией CD2, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD2, (b) модификацией Т-клетки, при которой экспрессия антигена снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD2 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD2). В дополнительных вариантах реализации Т-клетка содержит суицидный ген и/или модификацию таким образом, что передача сигналов, опосредованная эндогенным Т-клеточным рецептором (TCR), заблокирована в Т-клетке. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека экспрессируется в CD2ΔCART2 клетках.
[00187] В другом варианте реализации данное изобретение предлагает Т-клетку, содержащую химерный антигенный рецептор, который специфически связывает CD4, при этом Т-клетка дефицитна по CD4, например, CD4ΔCART4 клетке. В неограничивающих примерах дефицит в CD4 вызван (а) модификацией CD4, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD4, (b) модификацией Т-клетки, при которой экспрессия антигена снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD4 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD4). В дополнительных вариантах реализации Т-клетка содержит суицидный ген и/или модификацию таким образом, что передача сигналов, опосредованная эндогенным Т-клеточным рецептором (TCR), заблокирована в Т-клетке. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека экспрессируется в CD4ΔCART4 клетках.
[00188] В другом варианте реализации данное изобретение предлагает Т-клетку, содержащую химерный антигенный рецептор, который специфически связывает CD3, при этом Т-клетка дефицитна по CD3ε, например, CD3ΔCART3e клетке. В неограничивающих примерах дефицит в CD3 вызван (а) модификацией CD3, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD3, (b) модификацией Т-клетки, при которой экспрессия антигена снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD3 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD3ε). В дополнительных вариантах реализации Т-клетка содержит суицидный ген и/или модификацию таким образом, что передача сигналов, опосредованная эндогенным Т-клеточным рецептором (TCR), заблокирована в Т-клетке. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека экспрессируется в CD3ΔCART3ε клетках.
[00189] Раскрыты варианты реализации аминокислотных последовательностей CAR, которые могут экспрессироваться на поверхности редактируемой геномом CAR T-клетки, полученной из цитотоксической Т-клетки, Т-клетки памяти или гамма-дельта (γδ) T-клетки.
[00190] Таблица 3. Аминокислотные последовательности монохимерных антигенных рецепторов (CAR).
[00191] Аналогичным образом могут быть сконструированы другие моно-CAR-T клетки, которые приведены ниже в Таблице 4.
[00192] Таблица 4. Моно-CAR и CAR-T.
подавление антигена
Двойные CAR T-клетки (dCAR-T)
[00193] Двойная CAR T-клетка (dCAR-T) может быть получена путем клонирования последовательности, кодирующей белок первого внеклеточного лиганд-связывающего домена, в лентивирусный вектор, содержащий один или более костимулирующих доменов и домен передачи сигнала, и клонирование второй последовательности, кодирующей белок второго внеклеточного лиганд-связывающего домена в один и тот же лентивирусный вектор, содержащий дополнительный один или более костимулирующих доменов и сигнальный трансдуцирующий домен, в результате чего получается плазмида, из которой две конструкции CAR экспрессируются из одного и того же вектора.
[00194] В одном варианте реализации в описании предложена сконструированная Т-клетка, содержащая двойной Химерный Aнтигенный Рецептор (dCAR), т.е. последовательность, кодирующую белок двух CAR, экспрессируемых из одной лентивирусной конструкции, которая специфически связывает альфа-цепь рецептора CD5 и TCR (TRAC ), где Т-клетка дефицитна по CD5 и TRAC (например, CD5*TRAC-dCARTΔCD5ΔTRAC клетка). В неограничивающих примерах дефицит по CD5 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD5 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что рецептор химерного антигена больше не связывается специфически модифицированный CD5 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD5 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке как минимум на 50%, как минимум на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD5 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD5 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD5*TRAC-CARTΔCD5ΔTRAC клетках.
[00195] Во втором варианте реализации в описании представлена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD7 и альфа-цепь рецептора TCR (TRAC), при этом Т-клетка дефицитна по CD7 и TRAC, например, CD7*TRAC-dCARTΔCD7ΔTRAC клетке. В неограничивающих примерах дефицит по CD7 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD5 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что рецептор химерного антигена больше не связывается специфически модифицированный CD7 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD7 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке как минимум на 50%, как минимум на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD7 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD7 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*TRAC-dCARTΔCD7Δ клетках.
[00196] В третьем варианте реализации в описании представлена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD2 и альфа-цепь рецептора TCR (TRAC), при этом Т-клетка дефицитна по CD2 и TRAC, например, CD2*TRAC-dCARTΔCD2ΔTRAC клетке. В неограничивающих примерах дефицит по CD2 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD2 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что рецептор химерного антигена больше не связывается специфически модифицированный CD2 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD7 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке как минимум на 50%, как минимум на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD2 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*TRAC-dCARTΔCD2ΔTRAC клетках.
[00197] В другом варианте реализации в описании представлена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD4 и альфа-цепь рецептора TCR (TRAC), при этом Т-клетка дефицитна по CD4 и TRAC, например, CD4*TRAC-dCARTΔCD4ΔTRAC клетке. В неограничивающих примерах дефицит по CD4 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD4 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что рецептор химерного антигена больше не связывается специфически модифицированный CD4 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD7 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке как минимум на 50%, как минимум на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD4 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD4 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD4*TRAC-dCARTΔCD4ΔTRAC клетках.
[00198] В другом варианте реализации в описании представлена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD3 и альфа-цепь рецептора TCR (TRAC), при этом Т-клетка дефицитна по CD3 и TRAC, например, CD3*TRAC-dCARTΔCD3TRAC клетке. В неограничивающих примерах дефицит по CD3 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD3 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что рецептор химерного антигена больше не связывается специфически модифицированный CD3 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD3 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке как минимум на 50%, как минимум на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD3 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD3 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD3*TRAC-dCARTΔCD3ΔTRAC клетках.
[00199] В другом варианте реализации данное изобретение предлагает сконструированную Т-клетку, содержащую dCAR, которая специфически связывает CD2 и CD3-эпсилон (ε) цепь, где Т-клетка дефицитна по CD2 и CD3-эпсилон, например, CD2*CD3ε-dCARTΔCD2ΔCD3ε клетка. В неограничивающих примерах дефицит по CD2 и CD3-эпсилон (ε) цепь является результатом (а) модификации CD2 и CD3-эпсилон, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD2 и CD3-эпсилон, (b) модификации Т-клетки таким образом, что экспрессия CD2- и CD3-эпсилон снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD2 и CD3-эпсилон не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или CD3-эпсилон. В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*CD3ε-dCARTΔCD2ΔCD3εклетках.
[00200] В другом варианте реализации данное изобретение предлагает сконструированную Т-клетку, содержащую dCAR, которая специфически связывает CD4 и CD3-эпсилон (ε) цепь, где Т-клетка дефицитна по CD2 и CD3ε, например, CD4*CD3ε-dCARTΔCD4ΔCD3ε клетке. В неограничивающих примерах дефицит по CD4 и CD3ε цепи является результатом (а) модификации CD4 и CD3 эпсилон, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD4 и CD3ε, (b) модификации Т-клетки таким образом, что экспрессия CD4 и CD3ε снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD4 и CD3ε не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD4 и/или CD3ε. В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD4*CD3ε-dCARTΔCD4ΔCD3εклетках.
[00201] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD5 и TCR бета (β) цепь, при этом Т-клетка дефицитна по CD5 и TCRβ, например, CD5*TCRβ-dCARTΔCD5ΔTCRβ клетке. В неограничивающих примерах дефицит по CD5 и TCRβ цепь является результатом (а) модификации CD5 и TCRβ, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD5 и TCRβ, (b) модификации Т-клетки таким образом, что экспрессия CD5 и TCRβ снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD5 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD5 и/или TCRβ. В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека экспрессируется в CD5*TCRβ-dCARTΔCD5ΔTCRβ клетках.
[00202] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD7 и TCR бета(β) цепь, при этом Т-клетка дефицитна по CD5 и TCR beta, например, CD7*TCRβ-dCARTΔCD7ΔTCRβ клетке. В неограничивающих примерах дефицит по CD7 и TCRβ цепь является результатом (а) модификации CD7 и TCRβ, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD7 и TCRβ, (b) модификации Т-клетки таким образом, что экспрессия CD7 и TCRβ снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD7 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD7 и/или TCRβ. В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека экспрессируется в CD7*TCRβ-dCARTΔCD7ΔTCRβ клетках.
[00203] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD2 и TCR бета (β) цепь, при этом Т-клетка дефицитна по CD2 и TCRβ, например, CD2*TCRβ-dCARTΔCD7ΔTCRβ клетке. В неограничивающих примерах дефицит по CD2 и TCRβ цепь является результатом (а) модификации CD2 и TCRβ, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD2 и TCRβ, (b) модификации Т-клетки таким образом, что экспрессия CD2 и TCRβ снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD2 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или TCRβ. В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*TCRβ-dCARTΔCD2ΔTCRβ клетках.
[00204] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD4 и TCR бета (β) цепь, при этом Т-клетка дефицитна по CD2 и TCRβ, например, CD4*TCRβ-dCARTΔCD4ΔTCRβ клетке. В неограничивающих примерах дефицит по CD4 и TCRβ цепь является результатом (а) модификации CD4 и TCRβ, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD4 и TCRβ, (b) модификации Т-клетки таким образом, что экспрессия CD4 и TCRΒснижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD4 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD4 и/или TCRβ. В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD4*TCRβ-dCARTΔCD4ΔTCRβ клетках.
[00205] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD7 и CD2, при этом Т-клетка дефицитна по CD7 и CD2, например, CD7*CD2-dCARTΔCD7ΔCD2 клетке. В неограничивающих примерах дефицит в CD7 и CD2 вызван (а) модификацией CD7 и CD2, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD7 и CD2, (b) модификацией Т-клетки, при которой экспрессия CD7 и CD2 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD7 и CD2 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD7 и/или CD2. В дополнительных вариантах реализации Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*CD2-dCARTΔCD7ΔCD2 клетках.
[00206] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD7 и CD5, при этом Т-клетка дефицитна по CD7 и CD5, например, CD7*CD5-dCARTΔCD7ΔCD5 клетке. В неограничивающих примерах дефицит в CD7 и CD5 вызван (а) модификацией CD7 и CD5, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD7 и CD5, (b) модификацией Т-клетки, при которой экспрессия CD7 и CD5 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD7 и CD5 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD7 и/или CD5. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*CD5-dCARTΔCD7ΔCD5 клетках.
[00207] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD7 и CD4, при этом Т-клетка дефицитна по CD7 и CD4, например, CD7*CD4-dCARTΔCD7ΔCD4 клетке. В неограничивающих примерах дефицит в CD7 и CD4 вызван (а) модификацией CD7 и CD4, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD7 и CD4, (b) модификацией Т-клетки, при которой экспрессия CD7 и CD4 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD7 и CD4 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD7 и/или CD4. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах суицидный ген, экспрессируемый в клетках CD7*CD4-dCARTΔCD7ΔCD4, кодирует модифицированный ген 1-тимидинкиназы (TK) вируса простого герпеса человека, слитый внутри рамки считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*CD4-dCARTΔCD7ΔCD4 клетках.
[00208] В другом варианте реализации данное изобретение предлагает сконструированную Т-клетку, содержащую dCAR, которая специфически связывает CD2 и CD5, при этом Т-клетка дефицитна по CD2, CD5 и TRAC, например, CD2*CD5-dCARTΔCD2ΔCD5ΔTRAC клетке. В неограничивающих примерах дефицит в CD2 и CD5 вызван (а) модификацией CD2 и CD5, экспрессируемой Т-клеткой таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD2 и CD5, (b) модификацией Т-клетки, при которой экспрессия CD2 и CD5 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификацией Т-клетки таким образом, что CD2 и CD5 не экспрессируется (например, путем удаления или разрушения гена, кодирующего CD2 и/или CD5. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*CD5-dCARTΔCD2ΔCD5 клетках.
[00209] В другом варианте реализации данное изобретение предлагает сконструированную Т-клетку, содержащую dCAR, которая специфически связывает CD2 и CD4, при этом Т-клетка дефицитна по CD2, CD4 и TRAC, например, CD2*CD4-dCARTΔCD2ΔCD4ΔTRAC клетке. В неограничивающих примерах дефицит в CD2 и CD4 в вызван (а) модификацией CD2 и CD4 экспрессирующих Т-клеток таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD2 и CD4, (b) модификацией Т-клетки, при которой экспрессия CD2 и CD4 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD2 и CD4 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или CD4. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*CD4-dCARTΔCD2ΔCD4 клетках.
[00210] В другом варианте реализации в описании предложена сконструированная Т-клетка, содержащая dCAR, которая специфически связывает CD5 и CD4, при этом Т-клетка дефицитна по CD5 и CD4, например, CD5*CD4-dCARTΔCD5ΔCD4 клетке. В неограничивающих примерах дефицит в CD5 и CD4 в вызван (а) модификацией CD5 и CD4 экспрессирующих Т-клеток таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD5 и CD4, (b) модификацией Т-клетки, при которой экспрессия CD5 и CD4 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD5 и CD4 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD5 и/или CD4. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD5*CD4-dCARTΔCD5ΔCD4 клетках.
[00211] В одном варианте реализации двойная CAR T-клетка содержит (i) первый полипептид химерного антигенного рецептора (CAR), содержащий первый сигнальный пептид, первый внеклеточный лиганд-связывающий домен, первую шарнирную область, первый трансмембранный домен, один или больше костимулирующих доменов и первый сигнальный трансдуцирующий домен; и (ii) второй полипептид химерного антигенного рецептора, содержащий второй сигнальный пептид, второй внеклеточный лиганд-связывающий домен, вторую шарнирную область, второй трансмембранный домен, один или более костимулирующих доменов и второй сигнальный трансдуцирующий домен; где первый внеклеточный лиганд-связывающий домен и второй внеклеточный лиганд-связывающий домен обладают аффинностью к различным молекулам клеточной поверхности; и где двойная CAR T-клетка обладает одним или более генетическими нарушениями, приводящими к снижению экспрессии молекулы клеточной поверхности в двойной CAR-T-клетке.
[00212] Во втором варианте реализации первый сигнальный пептид представляет собой сигнальную последовательность CD8α.
[00213] В третьем варианте реализации первый внеклеточный лиганд-связывающий домен представляет собой гибридный белок вариабельных областей тяжелой и легкой цепей иммуноглобулина, обозначенный VH1 и VL1, и связанный коротким линкерным пептидом из 5 аминокислот (GGGGS). В некоторых вариантах реализации этот линкерный пептид повторяется 3 или 4 раза. В некоторых вариантах реализации первый домен распознавания антигена может быть выбран из VH1 - (GGGGS)3-4 - VL1 или VL1 - (GGGGS)3-4 - VH1.
[00214] В другом варианте реализации первая шарнирная область содержит CD8α.
[00215] В другом варианте реализации первый трансмембранный домен представляет собой CD8 или CD28.
[00216] В некоторых вариантах реализации первый костимулирующий домен содержит 4-1BB, CD28 или их комбинацию в любом порядке, то есть 4-1BB-CD28 или CD28-4-1BB.
[00217] В некоторых вариантах реализации первый сигнальный домен представляет собой би-пептид CD3ζ или CD3ζ, то есть CD3ζ - CD3ζ..
[00218] Во втором варианте реализации первый сигнальный пептид представляет собой сигнальную последовательность CD8α SEQ NO:1.
[00219] В некотором варианте реализации второй внеклеточный лиганд-связывающий домен представляет собой слитый белок вариабельных областей тяжелой и легкой цепей иммуноглобулина, обозначенный VH2 и VL2, и связанный коротким линкерным пептидом из 5 аминокислот (GGGGS). В некоторых вариантах реализации этот линкерный пептид повторяется 3 или 4 раза. В некоторых вариантах реализации второй домен распознавания антигена может быть выбран из VH2 - (GGGGS)3-4 - VL2 или VL2 - (GGGGS)3-4 - VH2.
[00220] В другом варианте реализации вторая шарнирная область содержит CD8α.
[00221] В другом варианте реализации второй трансмембранный домен представляет собой CD8 или CD28.
[00222] В некоторых вариантах реализации второй костимулирующий домен содержит 4-1BB, CD28 или их комбинацию в любом порядке, то есть 4-1BB-CD28 или CD28-4-1BB.
[00223] В некоторых вариантах реализации второй сигнальный домен представляет собой би-пептид CD3ζ или CD3ζ, то есть CD3ζ - CD3ζ..
[00224] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VH1 -(GGGGS) 3-4 - VL1 и второй слитый белок внеклеточного лиганд-связывающего домена VH2 - (GGGGS)3-4 - VL2.
[00225] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VL1 - (GGGGS)3-4 - VH1 и второй слитый белок внеклеточного лиганд-связывающего домена VL2 - (GGGGS)3-4 - VH2.
[00226] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VH2 -(GGGGS) 3-4 - VL2 и второй слитый белок внеклеточного лиганд-связывающего домена VH1 - (GGGGS)3-4 - VL1.
[00227] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VL2 -(GGGGS) 3-4 - VH2 и второй слитый белок внеклеточного лиганд-связывающего домена VL1 - (GGGGS)3-4 - VH1.
[00228] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VH1 - (GGGGS)3-4 - VL1 и второй слитый белок внеклеточного лиганд-связывающего домена VL2 - (GGGGS)3-4 - VH2.
[00229] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VL1 - (GGGGS)3-4 - VH1 и второй слитый белок внеклеточного лиганд-связывающего домена VН2 - (GGGGS)3-4 - VL2.
[00230] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VH2 -(GGGGS) 3-4 - VL2 и второй слитый белок внеклеточного лиганд-связывающего домена VL1 - (GGGGS)3-4 - VН1.
[00231] В некоторых вариантах реализации полипептид CAR содержит первый слитый белок внеклеточного лиганд-связывающего домена VL2 - (GGGGS)3-4 - VH2 и второй слитый белок внеклеточного лиганд-связывающего домена VH1 - (GGGGS)3-4 - VL1.
[00232] В некоторых вариантах реализации полипептид CAR содержит по меньшей мере один сайт высокоэффективного расщепления, причем сайт высокоэффективного расщепления выбран из P2A, T2A, E2A и F2A.
[00233] В некоторых вариантах реализации полипептид CAR содержит суицидный ген.
[00234] В некоторых вариантах реализации полипептид CAR содержит мутантный рецептор к цитокинам.
[00235] В некоторых вариантах реализации, двойная CAR T-клетка нацелена на два антигена, выбранных из CD5, CD7, CD2, CD4, CD3, CD33, CD123 (IL3RA), CD371 (CLL-1; CLEC12A), CD117 (c-kit), CD135 (FLT3), BCMA, CS1, CD38, CD79A, CD79B, CD138, и CD19, APRIL, и TACI.
[00236] Дополнительные примеры двойных CAR приведены ниже в Таблице 5.
[00237] Таблица 5. Двойные CAR и dCAR-T
Тандемные клетки CAR-T (tCAR-T)
[00238] Тандемная CAR T-клетка (tCAR-T) представляет собой T-клетку с одним химерным антигенным полипептидом, содержащим два отдельных внеклеточных лиганд-связывающих домена, способных взаимодействовать с двумя разными молекулами клеточной поверхности, при этом внеклеточные лиганд-связывающие домены связаны вместе посредством гибкого линкера и совместно используют один или более костимулирующих доменов, причем связывание первого или второго внеклеточного лиганд-связывающего домена будет передавать сигнал через один или более костимулирующих доменов и сигнальный трансдуцирующий домен.
[00239] В одном из вариантов реализации сконструированная Т-клетка содержит в свою очередь Тандемный Химерный Антигенный Рецептор (tCAR), где один внеклеточный лиганд-связывающий домен специфически связывает CD5, а второй внеклеточный лиганд-связывающий домен связывает альфа-цепь рецептора TCR (TRAC), где Т-клетка дефицитна по CD5 и TRAC, например, CD5*TRAC-tCARTΔCD5ΔTRAC клетке. В неограничивающих примерах дефицит по CD5 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD5 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что tCAR больше не связывает специфически модифицированный CD5 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD5 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD5 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD5 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD5*TRAC-tCARTΔCD5ΔTRAC клетках.
[00240] Во втором варианте реализации сконструированная Т-клетка содержит в свою очередь тандемный Химерный Aнтигенный Рецептор (tCAR), где один внеклеточный лиганд-связывающий домен специфически связывает CD7, а второй внеклеточный лиганд-связывающий домен связывает альфа-цепь рецептора TCR (TRAC), где Т-клетка дефицитна по CD7 и TRAC, например, CD7*TRAC-tCARTΔCD7ΔTRAC клетке. В неограничивающих примерах дефицит по CD7 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD7 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что tCAR больше не связывает специфически модифицированный CD7 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD7 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD7 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD7 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*TRAC-tCARTΔCD7ΔTRAC клетках.
[00241] Во втором варианте реализации сконструированная Т-клетка содержит в свою очередь тандемный Химерный Aнтигенный Рецептор (tCAR), где один внеклеточный лиганд-связывающий домен специфически связывает CD2, а второй внеклеточный лиганд-связывающий домен связывает альфа-цепь рецептора TCR (TRAC), где Т-клетка дефицитна по CD2 и TRAC, например, CD2*TRAC-tCARTΔCD2ΔTRAC клетке. В неограничивающих примерах дефицит по CD2 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD2 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что tCAR больше не связывает специфически модифицированный CD2 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD2 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD2 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*TRAC-tCARTΔCD2ΔTRAC клетках.
[00242] В другом варианте реализации сконструированная Т-клетка содержит в свою очередь тандемный Химерный Aнтигенный Рецептор (tCAR), где один внеклеточный лиганд-связывающий домен специфически связывает CD4, а второй внеклеточный лиганд-связывающий домен связывает альфа-цепь рецептора TCR (TRAC), где Т-клетка дефицитна по CD4 и TRAC, например, CD4*TRAC-tCARTΔCD4ΔTRAC клетке. В неограничивающих примерах дефицит по CD4 и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD4 и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что tCAR больше не связывает специфически модифицированный CD4 и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD4 и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD4 и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD4 и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD4*TRAC-tCARTΔCD4ΔTRAC клетках.
[00243] В другом варианте реализации сконструированная Т-клетка содержит в свою очередь тандемный Химерный Aнтигенный Рецептор (tCAR), где один внеклеточный лиганд-связывающий домен специфически связывает) цепь CD3 эпсилон (ε), а второй внеклеточный лиганд-связывающий домен связывает альфа-цепь рецептора TCR (TRAC), где Т-клетка дефицитна по CD3ε и TRAC, например, CD3ε*TRAC-tCARTΔCD3εΔTRAC клетке. В неограничивающих примерах дефицит по CD3ε и альфа-цепи рецептора TCR (TRAC) возник в результате (а) модификации CD3ε и альфа-цепи рецептора TCR (TRAC), экспрессируемой Т-клеткой, так что tCAR больше не связывает специфически модифицированный CD3ε и альфа-цепь рецептора TCR (TRAC), (b) модификации Т-клетки таким образом, что экспрессия CD3ε и альфа-цепи рецептора TCR (TRAC) снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или более, или (c) модификации Т-клетки, так что CD3ε и альфа-цепь рецептора TCR (TRAC) не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD3ε и/или альфа-цепь рецептора TCR (TRAC). В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD3ε*TRAC-tCARTΔCD3εΔTRAC клетках.
[00244] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Aнтигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD2 и второй внеклеточный лиганд-связывающий домен связывает CD3 эпсилон (ε)цепь, при этом Т-клетки имеют дефицит по CD2 и CD3ε, например, CD2*CD3ε-tCARTΔCD2ΔCD3ε клетке. В неограничивающих примерах дефицит по CD2 и CD3εявляется результатом (а) модификации CD2 и CD3ε, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD2 и CD3ε, (b) модификации Т-клетки таким образом, что экспрессия CD2 и CD3ε снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD2 и CD3ε не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или CD3ε. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*CD3ε-tCARTΔCD2ΔCD3ε клетках.
[00245] В другом варианте реализации, сконструированная Т-клетка содержит тандемный Химерный Aнтигенный Рецептор (tCAR), где один внеклеточный лиганд-связывающий домен специфически связывает CD4, а второй внеклеточный лиганд-связывающий домен связывает (ε) цепь CD3 эпсилон, при этом Т-клетка дефицитна по CD4 и CD3ε, например, CD4*CD3ε-tCARTΔCD4ΔCD3ε клетке. В неограничивающих примерах дефицит по CD4 и CD3εявляется результатом (а) модификации CD4 и CD3ε, экспрессируемой Т-клеткой, так что химерный антигенный рецептор больше не связывает специфически модифицированные CD4 и CD3ε, (b) модификации Т-клетки таким образом, что экспрессия CD4 и CD3ε снижается в Т-клетке по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или больше, или (c) модификации Т-клетки, так что CD4 и CD3ε не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD4 и/или CD3ε. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах кодирующая белок последовательность модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD4*CD3ε-tCARTΔCD4ΔCD3ε клетках.
[00246] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD5 и второй внеклеточный лиганд-связывающий домен связывает цепь TCRβ , в котором Т- клетка дефицитная по цепи CD5 и TCRβ , например, CD5*TCRβ-tCARTΔCD5ΔTCRβ клетка. В неограничивающих примерах дефицит в CD5 и цепи TCRβ в вызван (а) модификацией CD5 и TCRβ экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD5 и TCRβ, (b) модификацией Т-клетки, при которой экспрессия CD5 и TCRβ снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD5 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD5 и/или TCRβ. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD5*TCRβ-tCARTΔCD5ΔTCRβ клетках.
[00247] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD7 и второй внеклеточный лиганд-связывающий домен связывает цепь TCRβ , в котором Т- клетка дефицитная по цепи CD7 и TCRβ , например, CD7*TCRβ-tCARTΔCD7ΔTCRβ клетка. В неограничивающих примерах дефицит в CD7 и цепи TCRβ в вызван (а) модификацией CD7 и TCRβ экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD7 и TCRβ, (b) модификацией Т-клетки, при которой экспрессия CD7 и TCRβ снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD7 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD7 и/или TCRβ. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*TCRβ-tCARTΔCD7ΔTCRβ клетках.
[00248] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD2 и второй внеклеточный лиганд-связывающий домен связывает цепь TCRβ , в котором Т- клетка дефицитная по цепи CD2 и TCRβ , например, CD2*TCRβ-tCARTΔCD7ΔTCRβ клетка. В неограничивающих примерах дефицит в CD2 и цепи TCRβ в вызван (а) модификацией CD2 и TCRβ экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD2 и TCRβ, (b) модификацией Т-клетки, при которой экспрессия CD2 и TCRβ снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD2 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или TCRβ. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*TCRβ-tCARTΔCD2ΔTCRβ клетках.
[00249] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD4 и второй внеклеточный лиганд-связывающий домен связывает цепь TCRβ , в котором Т- клетка дефицитная по цепи CD4 и TCRβ , например, CD4*TCRβ-tCARTΔCD4ΔTCRβ клетка. В неограничивающих примерах дефицит в CD4 и цепи TCRβ в вызван (а) модификацией CD4 и TCRβ экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD4 и TCRβ, (b) модификацией Т-клетки, при которой экспрессия CD4 и TCRβ снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD4 и TCRβ не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD4 и/или TCRβ. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD4*TCRβ-tCARTΔCD4ΔTCRβ клетках.
[00250] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD7 и второй внеклеточный лиганд-связывающий домен связывает CD2, в котором Т- клетка дефицитная по CD7 и CD2, например, CD7*CD2-tCARTΔCD7ΔCD2 клетка. В неограничивающих примерах дефицит в CD7 и CD2 в вызван (а) модификацией CD7 и CD2 экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD7 и CD2, (b) модификацией Т-клетки, при которой экспрессия CD7 и CD2 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD7 и CD2 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD7 и/или CD2. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*CD2-tCARTΔCD7ΔCD2 клетках.
[00251] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD7 и второй внеклеточный лиганд-связывающий домен связывает CD5, в котором Т- клетка дефицитная по CD7 и CD5, например, CD7*CD5-tCARTΔCD7ΔCD5 клетка. В неограничивающих примерах дефицит в CD7 и CD5 в вызван (а) модификацией CD7 и CD5 экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD7 и CD5, (b) модификацией Т-клетки, при которой экспрессия CD7 и CD5 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD7 и CD5 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD7 и/или CD5. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*CD5-tCARTΔCD7ΔCD5 клетках.
[00252] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD7 и второй внеклеточный лиганд-связывающий домен связывает CD4, в котором Т- клетка дефицитная по CD7 и CD4, например, CD7*CD4-tCARTΔCD7ΔCD4 клетка. В неограничивающих примерах дефицит в CD7 и CD4 в вызван (а) модификацией CD7 и CD4 экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD7 и CD4, (b) модификацией Т-клетки, при которой экспрессия CD7 и CD4 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD7 и CD4 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD7 и/или CD4. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD7*CD4-tCARTΔCD7ΔCD4 клетках.
[00253] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD2 и второй внеклеточный лиганд-связывающий домен связывает CD5, в котором Т- клетка дефицитная по CD2 и CD5, например, CD2*CD5-tCARTΔCD2ΔCD5 клетка. В неограничивающих примерах дефицит в CD2 и CD5 в вызван (а) модификацией CD2 и CD5 экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD2 и CD5, (b) модификацией Т-клетки, при которой экспрессия CD2 и CD5 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или более, или (с) модификацией Т-клеток таким образом, что CD2 и CD5 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или CD5. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*CD5-tCARTΔCD2ΔCD5 клетках.
[00254] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD2 и второй внеклеточный лиганд-связывающий домен связывает CD4, в котором Т- клетка дефицитная по CD2 и CD4, например, CD2*CD4-tCARTΔCD2ΔCD4 клетка. В неограничивающих примерах дефицит в CD2 и CD4 в вызван (а) модификацией CD2 и CD4 экспрессирующих Т-клеток таким образом, что tCAR больше специфично не связывает модифицированный CD2 и CD4, (b) модификацией Т-клетки, при которой экспрессия CD2 и CD4 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или более, или (с) модификацией Т-клеток таким образом, что CD2 и CD4 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD2 и/или CD4. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD2*CD4-tCARTΔCD2ΔCD4 клетках.
[00255] В другом варианте реализации, сконструированная Т-клетка включает в себя тандемный Химерный Антигенный Рецептор (tCAR), в котором один внеклеточный лиганд-связывающий домен специфически связывает CD5 и второй внеклеточный лиганд-связывающий домен связывает CD4, в котором Т- клетка дефицитная по CD5 и CD4, например, CD5*CD4-tCARTΔCD5ΔCD4 клетка. В неограничивающих примерах дефицит в CD5 и CD4 в вызван (а) модификацией CD5 и CD4 экспрессирующих Т-клеток таким образом, что химерный антигенный рецептор больше специфично не связывает модифицированный CD5 и CD4, (b) модификацией Т-клетки, при которой экспрессия CD5 и CD4 снижается в Т-клетке по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере , 90% или более, или (с) модификацией Т-клеток таким образом, что CD5 и CD4 не экспрессируются (например, путем удаления или разрушения гена, кодирующего CD5 и/или CD4. В дополнительных вариантах реализации, Т-клетка содержит суицидный ген. В неограничивающих примерах, последовательность, кодирующая белок модифицированного гена тимидинкиназы (TK) вируса простого герпеса-1 человека, слита в рамке считывания с внеклеточными и трансмембранными доменами кДНК CD34 человека и экспрессируется в CD5*CD4-tCARTΔCD5ΔCD4 клетках.
[00256] В другом варианте реализации, линейная тандемная CAR T-клетка содержит полипептид химерного антигенного рецептора (CAR), содержащий первый сигнальный пептид, первый внеклеточный лиганд-связывающий домен, второй внеклеточный лиганд-связывающий домен, шарнирную область, трансмембранный домен, один или более костимулирующих доменов и сигнальный трансдуцирующий домен, в которых первый внеклеточный лиганд-связывающий домен распознавания антигена и второй внеклеточный лиганд-связывающий домен распознавания антигена обладают сродством к различным молекулам клеточной поверхности, то есть антигенам на раковой клетке, например, злокачественной Т-клетке, злокачественной В-клетке или злокачественная плазматической клетке; и в котором линейная тандемная CAR T-клетка обладает одной или более генетическими модификациями, делециями или нарушениями, приводящими к снижению экспрессии молекул клеточной поверхности в линейной тандемной CAR T-клетке.
[00257] В другом варианте реализации, сигнальный пептид представляет собой сигнальный пептид из CD8α человека (SEQ ID NO:1).
[00258] В третьем варианте реализации, первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий легкий (VL) и тяжелый (VH) вариабельные фрагменты, обозначенные VH1 и VL1 и соединенные линкером (например, GGGGS). В некоторых вариантах реализации, этот пептидный линкер повторяется 2, 3, 4, 5 или 6 раз . В некоторых вариантах реализации, первый домен распознавания антигена может быть выбран из: 1) VH1 - (GGGGS)3-4 - VL1 или 2) VL1 - (GGGGS)3-4 -VH1.
[00259] В некоторых вариантах реализации, второй внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий легкий (VL) и тяжелый (VH) вариабельные фрагменты, обозначенные VH2 и VL2 и соединенные линкером (например, GGGGS). В некоторых вариантах реализации, этот пептидный линкер повторяется 2, 3, 4, 5 или 6 раз. В некоторых вариантах реализации, первый домен распознавания антигена может быть выбран из: 1) VH2 - (GGGGS)3-4 - VL2 или 2) VL2 - (GGGGS)3-4 -VH2.
[00260] В дополнительных вариантах реализации, первый домен распознавания антигена и второй домен распознавания антигена соединены коротким линкерным пептидом из 5 аминокислот (GGGGS). В некоторых вариантах реализации, этот пептидный линкер повторяется 2, 3, 4, 5 или 6 раз.
Конструкции линейных тандемных CAR
[00261] В одном варианте реализации, линейной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий тяжелый (VH) и легкий (VL) вариабельные фрагменты, обозначенные VH1 и VL1 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий легкий (VL) и тяжелый (VH) вариабельные фрагменты, обозначенные VL2 и VH2 и соединенные линкером (например, GGGGS)2-6.
[00262] В втором варианте реализации, линейной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий тяжелый (VH) и легкий (VL) вариабельные фрагменты, обозначенные VH2 и VL2 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий легкий (VL) и тяжелый (VH) вариабельные фрагменты, обозначенные VL1 и VH1 и соединенные линкером (например, GGGGS)2-6.
[00263] В третьем варианте реализации, линейной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий тяжелый (VL) и легкий (VH) вариабельные фрагменты, обозначенные VL1 и VH1 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий легкий (VH) и тяжелый (VL) вариабельные фрагменты, обозначенные VH2 и VL2 и соединенные линкером (например, GGGGS)2-6.
[00264] В четвертом варианте реализации, линейной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий тяжелый (VL) и легкий (VH) вариабельные фрагменты, обозначенные VL2 и VH2 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий легкий (VH) и тяжелый (VL) вариабельные фрагменты, обозначенные VH1 и VL1 и соединенные линкером (например, GGGGS)2-6.
[00265] Для каждого из вариантов реализации, линейной тандемной конструкции CAR первый и второй внеклеточные лиганд-связывающие домены нацелены на поверхностную молекулу, т.е. антиген, экспрессируемый на поверхности злокачественной Т-клетки, выбран, но не ограничиваясь ими, из BCMA, CS1, CD38, CD138, CD19, CD33, CD123, CD371, CD117, CD135, Tim-3, CD5, CD7, CD2, CD4, CD3, CD79A, CD79B, APRIL, CD56 и CD1a.
[00266] Дополнительные примеры линейных тандемных CAR приведены ниже в Таблице 6.
Таблица 6. Тандемные CAR и CAR-Т (линейные или шпилечные).
[00267] Например, в настоящем документе представлены линейные тандемные конструкции CAR, которые могут включать домены VH и VL scFv, нацеленных на любую из пар антигенов, представленных в Таблице 6 выше.
Таблица 7. Конструкции линейных тандемных CAR.
Конструкции шпилечных тандемных CAR
[00268] В одном варианте реализации, шпилечной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента тяжелой цепи, обозначенные VH1 и VH2 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента легкой цепи, обозначенные VL2 и VL1 и соединенные линкером (например, GGGGS)2-6.
[00269] Во втором варианте реализации, шпилечной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента тяжелой цепи, обозначенные VH2 и VH1 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента легкой цепи, обозначенные VL1 и VL2 и соединенные линкером (например, GGGGS)2-6.
[00270] В третьем варианте реализации, шпилечной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента легкой цепи, обозначенные VL1 и VL2 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента тяжелой цепи, обозначенные VH2 и VH1 и соединенные линкером (например, GGGGS)2-6.
[00271] В четвертом варианте реализации, шпилечной тандемной конструкции CAR первый внеклеточный лиганд-связывающий домен содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента легкой цепи, обозначенные VL2 и VL1 и соединенные линкером (например, GGGGS)2-6. Второй внеклеточный лиганд-связывающий домен распознавания антигена содержит одноцепочечный фрагмент антитела (scFv), содержащий два вариабельных фрагмента тяжелой цепи, обозначенные VH1 и VH2 и соединенные линкером (например, GGGGS)2-6.
[00272] Для каждого из вариантов реализации, шпилечной тандемной конструкции CAR первый и второй внеклеточные лиганд-связывающие домены нацелены на поверхностную молекулу, т.е. антиген, экспрессируемый на поверхности злокачественной Т-клетки, выбран, но не ограничиваясь ими, из BCMA, CS1, CD38, CD138, CD19, CD33, CD123, CD371, CD117, CD135, Tim-3, CD5, CD7, CD2, CD4, CD3, CD79A, CD79B, APRIL, CD56 и CD1a.
[00273] Дополнительные примеры тандемных шпилечных CAR приведены выше в Таблице 6.
[00274] Кроме того, в данном документе представлены конструкции CAR и CAR T-клетки, которые могут включать домены VH и VL scFv, нацеленные на (1) CD2 и CD3; и (2) CD2 и CD7, которые представлены ниже в Таблице 8.
Таблица 8. Аминокислотные последовательности шпилечных тандемных химерных антигенных рецепторов (CAR).
[00275] Кроме того, в настоящем документе представлены шпилечные тандемные конструкции CAR, которые могут включать домены VH и VL scFv, нацеленных на любую из пар антигенов, представленных в Таблице 6.
Таблица 9. Конструкции шпилечных тандемных CAR
[00276] Например, в Таблице 10 представлены тандемные шпилечные конструкции CAR, которые включают домены VH и VL scFv CD2 и CD3.
[00277] Таблица 10. Шпилечные тандемные конструкции CAR нацеленные на CD2 и CD3.
[00278] В Таблице 11 также представлены шпилечные тандемные конструкции CAR с (Cys=Cys) двухцепочечной связью (DSB), которые могут включать домены VH и VL scFv, нацеленные на любую из пар антигенов, представленных в Таблице 6.
Таблица 11. Шпилечные тандемные конструкции DSB CAR с (Cys=Cys) двухцепочечной связью (DSB).
Способы конструирования CAR в двойной или тандемной конструкции с использованием редактирования генов
[00279] В дополнительном аспекте может быть создан контроль CAR T-клеток. Например, контрольная CAR T-клетка может включать внеклеточный домен, который связывается с антигеном, не экспрессирующимся на злокачественной T-клетке. Например, если терапевтическая CAR T-клетка нацелена на Т-клеточный антиген, такой как CD7, или множественные Т-клеточные антигены, такие как CD2 и CD3, антигеном, с которым связывается контрольная CAR T-клетка, может быть CD19. CD19 представляет собой антиген, экспрессируемый на В-клетках, но не на Т-клетках, поэтому CAR T-клетка с внеклеточным доменом, адаптированным для связывания с CD19, не будет связываться с Т-клетками. Эти CAR T-клетки можно использовать в качестве контроля для анализа эффективности связывания и неспецифического связывания CAR T-клеток, нацеленных на представляющий интерес рак и/или распознающих интересующий антиген.
[00280] CAR могут быть дополнительно сконструированы, как описано в WO2018027036A1, необязательно с использованием вариаций, которые будут известны специалистам в данной области техники. Могут быть получены лентивирусные векторы и клеточные линии, а также разработаны, проверены и синтезированы направляющие РНК, как раскрыто в вышеуказанном документе, а также с помощью способов, известных в данной области техники и из коммерческих источников.
[00281] Сконструированные CAR могут быть введены в Т-клетки с использованием ретровирусов, которые эффективно и стабильно интегрируют последовательность нуклеиновой кислоты, кодирующую химерный антигенный рецептор, в геном клетки-мишени. Другие способы, известные в данной области техники, включают, но не ограничиваются ими, лентивирусную трансдукцию, системы на основе транспозонов, прямую трансфекцию РНК и системы CRISPR/Cas (например, системы типа I, типа II или типа III с использованием подходящего белка Cas, такого как Cas3, Cas4, Cas5, Cas5e (или CasD), Cas6, Cas6e, Cas6f, Cas7, Cas8a1 , Cas8a2, Cas8b, Cas8c, Cas9, Cas10, Casl Od, CasF, CasG, CasH, Csy1 , Csy2, Csy3, Cse1 (или CasA), Cse2 (или CasB), Cse3 (или CasE), Cse4 (или CasC), Csc1 , Csc2, Csa5, Csn2, Csm2, Csm3, Csm4, Csm5, Csm6, Cmr1 , Cmr3, Cmr4, Cmr5, Cmr6, Csb1 , Csb2, Csb3,Csx17, Csx14, Csx1 0, Csx16, CsaX, Csx3, Csz1 , Csx15, Csf1 , Csf2, Csf3, Csf4 и Cu1966, и т.п.). Также могут быть использованы цинк-пальцевые нуклеазы (ZFN) и аналогичные активатору транскрипции эффекторные нуклеазы (TALEN). См., например, Shearer RF and Saunders DN, “Experimental design for stable genetic manipulation in mammalian cell lines: lentivirus and alternatives,” Genes Cells 2015 Jan; 20(1):1-10.
[00282] Манипуляции с передачей сигналов PI3K можно использовать для предотвращения дифференциирования измененных CAR T-клеток из-за конститутивной самосигнализации CAR и стимулирования развития Т-клеток долгоживущей памяти. фармакологическая блокада PI3K во время производства CAR-T и экспансии ex vivo может отменить предпочтительное развитие эффекторных Т-клеток и восстановить соотношение эффектор/память CAR-T, наблюдаемое в пустых векторных трансдуцированных Т-клетках, что может улучшить устойчивость и терапевтическую активность Т-клеток in vivo. Ингибирование p110δ PI3K может повысить эффективность и память в опухолеспецифических терапевтических CD8 T-клетках, в то время как ингибирование p110α PI3K может увеличить выработку цитокинов и противоопухолевый ответ.
Предполагается, что это связано с тем, что присутствие CAR на поверхности Т-клетки может изменять ее активацию и дифференциирование даже в отсутствие лиганда. Конститутивная самосигнализация через CAR, связанная как с каркасом scFv, так и с сигнальными доменами, может приводить к аберрантному поведению Т-клеток, включая измененное дифференциирование и снижение выживаемости. Это важно, поскольку эффективность CAR T-клеток у пациентов напрямую связана с их продолжительностью жизни in vivo. Присутствие костимулирующего домена CD28 увеличивало истощение CAR T-клеток, вызванное постоянной передачей самосигналов CAR; костимулирующий домен 4-1BB имел меньший эффект. Кроме того, CD3-zeta значительно усиливает конститутивную активацию PI3K, AKT, mTOR и путей гликолиза и способствует образованию короткоживущих эффекторных клеток по сравнению с центральными/стволовыми клетками памяти. См., например, Zhang W. et al., "Modulation of PI3K signaling to improve CAR T cell function," Oncotarget, 2018 Nov 9; 9(88): 35807-35808.
Удаление или подавление гена цитокинов
[00283] В дополнение к редактированию генов TCR и белков и антигенов клеточной поверхности, можно редактировать гены секретируемых белков, таких как цитокины и хемокины. Такое редактирование может быть выполнено, например, для уменьшения или предотвращения развития или поддержания синдрома высвобождения цитокинов (CRS). CRS вызывается большим и быстрым высвобождением цитокинов из иммунных клеток в ответ на иммунотерапию (или другой иммунологический стимул). Модификация, разрушение или удаление одного или более генов цитокинов или хемокинов может быть выполнено с использованием способов, известных в данной области техники, таких как генетическая абляция (подавление гена), при которой экспрессия генов отменяется посредством изменения или удаления информации о генетической последовательности. Это может быть достигнуто с использованием известных в данной области техники инструментов генной инженерии, таких как аналогичные активатору транскрипции эффекторные нуклеазы (TALEN), цинк-пальцевые нуклеазы (ZFN), CRISPR, путем трансдукции малых шпилечных РНК (shРНК) путем направленной трансдукции CAR в последовательность гена цитокина и т.п.
[00284] Цитокины или хемокины, которые могут быть удалены из иммунных эффекторных клеток, как описано в данном документе, например, с использованием Cas9-CRISPR или путем направленной трансдукции CAR в последовательность гена цитокина, включают, без ограничения, следующее: XCL1, XCL2, CCL1, CCL2, CCL3, CCL4, CCL5, CCL7, CCL8, CCL11, CCL13, CCL14, CCL15, CCL16, CCL17, CCL18, CCL19, CCL20, CCL21, CCL22, CCL23, CCL24, CCL25, CCL26, CCL27, CXCL1, CXCL2, CXCL3, CXCL4, CXCL5, CXCL6, CXCL7, CXCL8, CXCL9, CXCL10, CXCL11, CXCL12, CXCL13, CXCL14, CX3CL1, IL-1α, IL-1β, IL-1RA, IL-18, IL-2, IL-4, IL-7, IL-9, IL-13, IL-15, IL-3, IL-5, GM-CSF, IL-6, IL-11, G-CSF, IL-12, LIF, OSM, IL-10, IL-20, IL-14, IL-16, IL-17, IFN-α, IFN-β, IFN-γ, CD154, LT-β, TNF-α,TNF-β, 4-1BBL, APRIL, CD70, CD153, CD178, GITRL, LIGHT, OX40L, TALL-1, TRAIL, TWEAK, TRANCE, TGF-β1, TGF-β2, TGF-β3, Epo, Tpo, Flt-3L, SCF, M-CSF, MSP, A2M, ACKR1, ACKR2, ACKR3, ACVR1, ACVR2B, ACVRL1, ADIPOQ, AGER, AGRN, AIMP1, AREG, BMP1, BMP10, BMP15, BMP2, BMP3, BMP4, BMP5, BMP6, BMP7, BMP8A, BMP8B, BMPR2, C10orf99, C1QTNF4, C5, CCL28, CCR1, CCR2, CCR3, CCR5, CCR6, CCR7, CD109, CD36, CD4, CD40LG, CD74, CER1, CHRD, CKLF, CLCF1, CMTM1, CMTM2, CMTM3, CMTM4, CMTM5, CMTM6, CMTM7, CMTM8, CNTF, CNTFR, COPS5, CRLF1, CSF1, CSF1R, CSF2, CSF3, CSF3R, CTF1, CX3CR1, CXCL16, CXCL17, CXCR1, CXCR2, CXCR3, CXCR4, CXCR6, EBI3, EDN1, ELANE, ENG, FAM3B, FAM3C, FAM3D, FAS, FASLG, FGF2, FLT3LG, FZD4, GBP1, GDF1, GDF10, GDF11, GDF15, GDF2, GDF3, GDF5, GDF6, GDF7, GDF9, GPI, GREM1, GREM2, GRN, HAX1, HFE2, HMGB1, HYAL2, IFNA10, IFNA14, IFNA16, IFNA2, IFNA5, IFNA6, IFNA8, IFNAR1, IFNAR2, IFNB1, IFNE, IFNG, IFNGR1, IFNK, IFNL1, IFNL3, IFNW1, IL10RA, IL11RA, IL12A, IL12B, IL12RB1, IL17A, IL17B, IL17C, IL17D, IL17F, IL18BP, IL-19, IL1F10, IL1R1, IL1R2, IL1RAPL1, IL1RL1, IL1RN, IL20RA, IL20RB, IL21, IL22, IL22RA1, IL22RA2, IL23A, IL23R, IL24, IL25, IL26, IL27, IL2RA, IL2RB, IL2RG, IL31, IL31RA, IL32, IL33, IL34, IL36A, IL36B, IL36G, IL36RN, IL37, IL6R, IL6ST, INHA, INHBA, INHBB, INHBC, INHBE, ITGA4, ITGAV, ITGB1, ITGB3, KIT, KITLG, KLHL20, LEFTY1, LEFTY2, LIFR, LTA, LTB, LTBP1, LTBP3, LTBP4, MIF, MINOS1-, MSTN, NAMPT, NBL1, NDP, NLRP7, NODAL, NOG, NRG1, NRP1, NRP2, OSMR, PARK7, PDPN, PF4, PF4V1, PGLYRP1, PLP2, PPBP, PXDN, SCG2, SCGB3A1, SECTM1, SLURP1, SOSTDC1, SP100, SPP1, TCAP, TGFBR1, TGFBR2, TGFBR3, THBS1, THNSL2, THPO, TIMP1, TNF, TNFRSF11, TNFRSF1A, TNFRSF9, TNFRSF10, TNFSF11, TNFSF12, TNFSF12-, TNFSF13, TNFSF13B, TNFSF14, TNFSF15, TNFSF18, TNFSF4, TNFSF8, TNFSF9, TRIM16, TSLP, TWSG1, TXLNA, VASN, VEGFA, VSTM1, WFIKKN1, WFIKKN2, WNT1, WNT2, WNT5A, WNT7A и ZFP36.
[00285] Последовательности этих генов известны и доступны в данной области техники.
Показания и стандарты лечения при терапии ACT (CAR-T)
[00286] В некоторых вариантах реализации, иммунные эффекторные клетки с редактированием генома, раскрытые в данном документе и/или созданные с использованием способов, раскрытых в данном документе, экспрессируют один или более химерных антигенных рецепторов (CAR) и могут использоваться в качестве лекарственного средства, т.е. для лечения заболевания. В некоторых вариантах осуществления клетки представляют собой клетки СНО.
[00287] Клетки, раскрытые в данном документе и/или полученные с использованием раскрытых в данном документе способов, могут использоваться в иммунотерапии и переносе адоптивных клеток, для лечения или производства лекарственного средства для лечения рака, аутоиммунных заболеваний, инфекционных заболеваний и других состояний.
[00288] Рак может быть гематологической злокачественным новообразованием или солидной опухолью. Гематологические злокачественные новообразования включают лейкозы, лимфомы, множественную миелому и их подтипы. Лимфомы можно классифицировать по-разному, часто на основе основного типа злокачественных клеток, включая лимфому Ходжкина (часто виды рака клеток Рида-Штернберга, но также иногда происходящие из В-клеток; все другие лимфомы относятся к неходжкинским лимфомам), В-клеточные лимфомы, Т-клеточные лимфомы, лимфомы из мантийных клеток, лимфому Беркитта, фолликулярную лимфому и другие, как они определены в данном документе и известны в данной области техники.
[00289] В-клеточные лимфомы включают, но не ограничиваются ими, диффузную крупноклеточную B-клеточную лимфому (ДКВКЛ), хронический лимфоцитарный лейкоз (ХЛЛ)/малую лимфоцитарную лимфому (МЛЛ) и другие, как определено в данном документе и известно в данной области техники.
[00290] Т-клеточные лимфомы включают Т-клеточный острый лимфобластный лейкоз/лимфому (Т-ОЛЛ), Т-клеточную периферическую лимфому (Т-ПЛ), Т-клеточный хронический лимфоцитарный лейкоз (Т-ХЛЛ), синдром Сезари и другие, как определено в данном документе и известно в данной области техники.
[00291] Лейкозы включают острый миелоидный (или миелогенный) лейкоз (ОМЛ), хронический миелоидный (или миелогенный) лейкоз (ХМЛ), острый лимфоцитарный (или лимфобластный) лейкоз (ОЛЛ), хронический лимфоцитарный лейкоз (ХЛЛ) волосатоклеточный лейкоз (иногда классифицируется как лимфома) и другие, как определено в данном документе и известно в данной области техники.
[00292] Злокачественные новообразования клеток плазмы включают лимфоплазмоцитарную лимфому, плазмоцитому и множественную миелому.
[00293] В некоторых вариантах реализации, лекарственное средство можно использовать для лечения рака у пациента, в частности, для лечения солидных опухолей, таких как меланомы, нейробластомы, глиомы или карциномы, такие как опухоли мозга, головы и шеи, груди, легких (например, не-мелкоклеточный рак легкого, НМРЛ), репродуктивного тракта (например, яичника), верхних отделов пищеварительного тракта, поджелудочной железы, печени, почечной системы (например, почек), мочевого пузыря, простаты и толстой кишки.
[00294] В другом варианте реализации, лекарственное средство можно использовать для лечения рака у пациента, в частности, для лечения гематологических злокачественных новообразований, выбранных из множественной миеломы и острого миелоидного лейкоза (ОМЛ), и злокачественных опухолей Т-клеток, выбранных из Т-клеточного острого лимфобластного лейкоза, неходжкинской лимфомы и Т-клеточного хронического лимфоцитарного лейкоза (T-ХЛЛ).
[00295] В некоторых вариантах реализации, клетки можно использовать для лечения аутоиммунных заболеваний, таких как волчанка, аутоиммунный (ревматоидный) артрит, рассеянный склероз, отторжение трансплантата, болезнь Крона, язвенный колит, дерматит и т.п. В некоторых вариантах реализации, клетки представляют собой Т-клетки с химерным рецептором аутоантител или CAR-T, отображающие антигены или их фрагменты вместо фрагментов антител; в этой версии адаптивного переноса клеток В-клетки, вызывающие аутоиммунные заболевания, будут пытаться атаковать сконструированные Т-клетки, которые ответят, убивая их.
[00296] В некоторых вариантах реализации, клетки можно использовать для лечения инфекционных заболеваний, таких как ВИЧ и туберкулез.
[00297] В другом варианте реализации, CAR T-клетки по данному изобретению могут подвергаться устойчивой экспансии Т-клеток in vivo и могут сохраняться в течение продолжительного времени.
[00298] В некоторых вариантах реализации, лечение пациента CAR T-клетками согласно настоящему раскрытию может быть улучшающим, лечебным или профилактическим. Это может быть либо частью аутологичной иммунотерапии, либо частью лечения аллогенной иммунотерапией. Под аутологичными подразумевается, что клетки, линия клеток или популяция клеток, используемые для лечения пациентов, происходят от указанного пациента или от донора, совместимого с лейкоцитарным антигеном человека (HLA). Термин «аллогенный» означает, что клетки или популяция клеток, используемые для лечения пациентов, происходят не от пациента, а от донора.
[00299] Лечение рака CAR T-клетками по настоящему раскрытию может осуществляться в сочетании с одним или более видами лечения, выбранными из терапии антителами, химиотерапии, цитокинотерапии, терапии дендритными клетками, генной терапии, гормональной терапии, лучевой терапии, лазерной светотерапии и облучения.
[00300] Введение CAR T-клеток или популяции CAR T-клеток в соответствии с настоящим раскрытием может осуществляться путем аэрозольной ингаляции, инъекции, приема внутрь, переливания, имплантации или трансплантации. Композиции можно вводить пациенту трансартериально, подкожно, внутрикожно, внутриопухолево, интранодально, интрамедуллярно, внутримышечно, внутривенно или внутрибрюшинно. В некоторых вариантах осуществления настоящего изобретения композиции вводят путем внутривенной инъекции.
[00301] Введение CAR T-клеток или популяции CAR T-клеток может состоять из введения 104 -109 клеток на кг массы тела, предпочтительно от 105 до 106 клеток/кг массы тела, включая все целые значения количества клеток. в пределах этих диапазонов. CAR T-клетки или популяция CAR T-клеток можно вводить в одной или более дозах. В другом варианте реализации, эффективное количество CAR T-клеток или популяции CAR T-клеток вводят в виде разовой дозы. В другом варианте эффективное количество клеток вводят в виде более чем одной дозы в течение определенного периода времени. Время введения определяется на усмотрение врача и зависит от клинического состояния пациента. CAR T-клетки или популяция CAR T-клеток могут быть получены из любого источника, такого как банк крови или донор. Хотя потребности пациентов меняются, определение оптимальных диапазонов эффективных количеств данной популяции (популяций) клеток CAR-T для конкретного заболевания или состояния находится в пределах компетенции специалистов в данной области техники. Эффективное количество означает количество, которое обеспечивает терапевтический или профилактический эффект. Вводимая доза будет зависеть от возраста, состояния здоровья и массы тела пациента-реципиента, типа сопутствующего лечения, если таковое имеется, частоты лечения и характера желаемого эффекта.
[00302] В другом варианте реализации, эффективное количество CAR T-клеток или популяции CAR T-клеток или композиции, содержащей эти CAR T-клетки, вводят парентерально. Введение может быть внутривенным. Введение CAR T-клеток или популяции CAR T-клеток или композиции, содержащей эти CAR T-клетки, можно осуществлять непосредственно путем инъекции в опухоль.
[00303] В одном варианте реализации, настоящего раскрытия CAR T-клетки или популяция CAR T-клеток вводятся пациенту в сочетании, например, до, одновременно или после, любого количества подходящих способов лечения, включая, но не ограничиваясь, лечением цитокинами или экспрессией цитокинов внутри CAR-T, которые усиливают пролиферацию и устойчивость Т-клеток, и включают, но не ограничиваются ими, IL-2, IL-7 и IL-15 или их аналоги.
[00304] В некоторых вариантах реализации, CAR T-клетки или популяция CAR T-клеток по настоящему раскрытию могут использоваться в комбинации с агентами, которые ингибируют иммуносупрессивные пути, включая, помимо прочего, ингибиторы TGFβ, интерлейкин 10 (IL-10), аденозин, VEGF, индоламин-2,3-диоксигеназу 1 (IDO1), индоламин-2,3-диоксигеназу 2 (IDO2), триптофан-2-3-диоксигеназу (TDO), лактат, гипоксию, аргиназу и простагландин E2.
[00305] В другом варианте реализации, CAR T-клетки или популяция CAR T-клеток по настоящему раскрытию могут быть использованы в комбинации с ингибиторами контрольных точек T-клеток, включая, но не ограничиваясь ими, анти-CTLA4 (ипилимумаб) анти-PD1 (пембролизумаб), ниволумаб, цемиплимаб, анти-PDL1 (атезолизумаб, авелумаб, дурвалумаб), анти-PDL2, анти-BTLA, анти-LAG3, анти-TIM3, анти-VISTA, анти-TIGIT и анти-KIR.
[00306] В другом варианте реализации, CAR T-клетки или популяция CAR T-клеток по настоящему раскрытию могут использоваться в комбинации с агонистами Т-клеток, включая, но не ограничиваясь ими, антитела, которые стимулируют CD28, ICOS, OX-40, CD27, 4-1BB, CD137, GITR и HVEM.
[00307] В другом варианте реализации, CAR T-клетки или популяция CAR T-клеток по настоящему раскрытию могут использоваться в сочетании с терапевтическими онколитическими вирусами, включая, но не ограничиваясь ими, ретровирусы, пикорнавирусы, рабдовирусы, парамиксовирусы, реовирусы, парвовирусы, аденовирусы, герпесвирусы и поксвирусы.
[00308] В другом варианте реализации, CAR T-клетки или популяция CAR T-клеток по настоящему раскрытию могут использоваться в комбинации с иммуностимулирующими терапиями, такими как агонисты толл-подобных рецепторов, включая, но не ограничиваясь ими, TLR3, TLR4, TLR7 и агонисты TLR9.
[00309] В другом варианте реализации, CAR T-клетки или популяция CAR T-клеток по настоящему раскрытию могут использоваться в комбинации со стимулятором агонистов гена интерферона (STING), такими как циклическая ГМФ-AМФ-синтаза (cGAS).
[00310] Аплазия иммунных эффекторных клеток, в частности аплазия Т-клеток, также вызывает беспокойство после терапии адоптивным переносом клеток. Когда излечиваемая злокачественная опухоль является Т-клеточной злокачественной опухолью, а CAR T-клетки нацелены на Т-клеточный антиген, нормальные Т-клетки и их предшественники, экспрессирующие антиген, истощаются, и иммунная система оказывается под угрозой. Соответственно, способы лечения этих побочных эффектов сопровождаются терапией. Такие способы включают отбор и сохранение незлокачественных Т-клеток или предшественников, аутологичных или аллогенных (необязательно сконструированных так, чтобы не вызывать отторжения или отторжения), для последующего размножения и повторной инфузии пациенту после истощения или деактивации CAR T-клеток. Альтернативно, CAR T-клетки, которые распознают и убивают подмножества TCR-несущих клеток, таких как нормальные и злокачественные TRBC1+, но не TRBC2+ клетки, или, альтернативно, TRBC2+, но не TRBC1+ клетки, могут быть использованы для искоренения T-клеточной злокачественной опухоли при сохранении достаточного количества нормальных Т-клеток для поддержания нормальной функции иммунной системы.
Определения
[00311] Если в данном документе не указано иное, все используемые технические и научные термины имеют то же значение, которое обычно понимается квалифицированным специалистом в области генной терапии, биохимии, генетики и молекулярной биологии. Хотя способы и материалы, аналогичные или эквивалентные описанным в данном документе, которые могут быть использованы в практике или испытании данного изобретения, подходящие способы и материалы описаны ниже.
[00312] Используемые в данном документе термины имеют указанные значения. Когда раскрываются диапазоны значений и используются обозначения «от n1 … до n2 » или «между n1 … и n2 », где n1 и n2 представляют собой числа, тогда, если не указано иное, это обозначение предназначены для включения самих чисел и диапазона между ними. Этот диапазон может быть целым или непрерывным между конечными значениями включительно. В качестве примера предполагается, что диапазон «от 2 до 6 атомов углерода» включает два, три, четыре, пять и шесть атомов углерода, поскольку атомы углерода представлены в целых единицах. Сравните, в качестве примера, диапазон «от 1 до 3 мкМ (микромолярный)», который предназначен для включения 1 мкМ, 3 мкМ и всего, что находится между ними, с любым количеством значащих цифр (например, 1,255 мкМ, 2,1 мкМ, 2,9999 мкМ и т.п.).
[00313] Используемый в данном документе термин «около» предназначен для определения числовых значений, которые он модифицирует, обозначая такое значение как переменную в пределах погрешности. Когда не указывается конкретная погрешность, такая как стандартное отклонение от среднего значения, указанного в диаграмме или таблице данных, термин «около» следует понимать как обозначающий диапазон, который будет охватывать указанное значение, и диапазон, который будет включен путем округления в большую или меньшую сторону до этой цифры с учетом значащих цифр.
[00314] Термин «активация» (и другие его варианты) применительно к клеткам обычно понимается как синоним «стимуляции» и, как он используется в данном документе, относится к лечению клеток, которое приводит к увеличению популяций клеток. В Т-клетках активация часто достигается воздействием агонистов CD2 и CD28 (а иногда также CD2), обычно антител, необязательно нанесенных на магнитные шарики или конъюгированных с коллоидным полимерным матриксом.
[00315] Используемый в данном документе термин «антиген» означает белок клеточной поверхности, распознаваемый (т.е. являющийся мишенью) рецептором Т-клеток или химерным антигенным рецептором. В классическом смысле антигены представляют собой вещества, обычно белки, которые распознаются антителами, но определения частично совпадают, поскольку CAR включает производные от доменов антител, таких как легкая (VL) и тяжелая (VH) цепи, распознающие один или более антигенов.
[00316] Термин «рак» относится к злокачественному новообразованию или аномальному росту клеток в организме. Многие различные виды рака можно охарактеризовать или идентифицировать с помощью определенных белков или молекул клеточной поверхности. Таким образом, в общих чертах, рак в соответствии с настоящим раскрытием может относиться к любому злокачественному новообразованию, которое можно лечить с помощью иммунной эффекторной клетки, такой как CAR T-клетка, как описано в данном документе, при этом иммунная эффекторная клетка распознает и связывается с белком клеточной поверхности на раковой клетке. В контексте настоящего описания «рак» может относиться к гематологическому злокачественному новообразованию, такому как множественная миелома, Т-клеточное злокачественное образование или В-клеточное злокачественное образование. Т-клеточные злокачественные новообразования могут включать, помимо прочего, Т-клеточный острый лимфобластный лейкоз (Т-ОЛЛ) или неходжкинскую лимфому. Рак может также относиться к солидной опухоли, такой как, но не ограничиваясь этим, рак шейки матки, рак поджелудочной железы, рак яичников, мезотелиома и рак легких.
[00317] Используемый в данном документе «белок клеточной поверхности» представляет собой белок (или белковый комплекс), экспрессируемый клеткой, по меньшей мере, частично на поверхности клетки. Примеры белков клеточной поверхности включают TCR (и его субъединицы) и CD7.
[00318] «Химерный антигенный рецептор» или «CAR», как используется в данном документе и обычно используется в данной области, относится к рекомбинантному слитому белку, который имеет внеклеточный лиганд-связывающий домен, трансмембранный домен и сигнальный трансдуцирующий домен, который заставляет клетку выполнять специализированную функцию при связывании внеклеточного лиганд-связывающего домена с компонентом, присутствующим на клетке-мишени. Например, CAR может обладать специфичностью на основе антител к желаемому антигену (например, опухолевому антигену) с внутриклеточным доменом, активирующим Т-клеточный рецептор, для генерации химерного белка, который проявляет специфическую клеточную иммунную активность по отношению к мишени. CAR первого поколения включают внеклеточный лиганд-связывающий домен и сигнальный трансдуцирующий домен, обычно CD3ζ или FcεRIγ. CAR второго поколения построены на основе конструкций CAR первого поколения путем включения внутриклеточного костимулирующего домена, обычно 4-1BB или CD28. Эти костимулирующие домены помогают повысить цитотоксичность и пролиферацию CAR T-клеток по сравнению с CAR первого поколения. CAR третьего поколения включают в себя несколько костимулирующих доменов, в первую очередь для увеличения пролиферации и персистенции CAR T-клеток. Химерные антигенные рецепторы отличаются от других антигенсвязывающих агентов своей способностью как связывать ГКГ-независимые антигены, так и передавать сигналы активации через свой внутриклеточный домен.
[00319] «Несущая CAR иммунная эффекторная клетка» представляет собой иммунную эффекторную клетку, трансдуцированную по меньшей мере одним CAR. «CAR T-клетка» представляет собой T-клетку, трансдуцированную по меньшей мере одним CAR; CAR T-клетки могут быть моно, двойными или тандемными CAR T-клетками. CAR T-клетки могут быть аутологичными, что означает, что они созданы из собственных клеток субъекта, или аллогенными, что означает, что клетки получены от здорового донора и, во многих случаях, сконструированы таким образом, чтобы не спровоцировать реакцию "хозяин против трансплантата» или реакцию "трансплантат против хозяина". Донорские клетки также могут быть получены из пуповинной крови или получены из индуцированных плюрипотентных стволовых клеток.
[00320] Двойная CAR T-клетка (dCAR-T) может быть определена как T-клетка с двумя различными полипептидами химерного антигенного рецептора, имеющими сродство к разным антигенам-мишеням, экспрессируемым в одной и той же эффекторной клетке, где каждый CAR функционирует независимо. CAR может быть экспрессирован из одной или более полинуклеотидных последовательностей.
[00321] Тандемная CAR T-клетка (tCAR-T) может быть определена как T-клетка с одним химерным антигенным полипептидом, содержащим два различных внеклеточных лигандсвязывающих домена со сродством к различным мишеням, где внеклеточный лиганд-связывающие домены связаны через пептидный линкер и имеют один или более общих костимулирующих доменов, где связывание любого внеклеточного лиганд-связывающего домена будет сигнализировать через один или более общих костимулирующих доменов и передающий сигнал домен.
[00322] Термин «комбинированная терапия» означает введение двух или более терапевтических агентов для лечения терапевтического состояния или расстройства, описанного в настоящем раскрытии. Такое введение включает совместное введение этих терапевтических агентов практически одновременно, например, в одной капсуле с фиксированным соотношением активных ингредиентов или в нескольких отдельных капсулах для каждого активного ингредиента. Кроме того, такое введение также включает последовательное применение каждого типа терапевтического агента. В любом случае схема лечения будет обеспечивать благоприятные эффекты комбинации лекарственных средств при лечении состояний или расстройств, описанных в данном документе.
[00323] Используемый в данном документе термин «композиция» относится к комбинации популяций иммунотерапевтических клеток с одним или более терапевтически приемлемыми носителями.
[00324] Термин «заболевание», используемый в данном документе, в целом является синонимом и используется взаимозаменяемо с терминами «расстройство», «синдром» и «состояние» (как медицинское состояние), поскольку все они отражают ненормальное состояние тела человека или животного или одной из его частей, которая нарушает нормальное функционирование, и обычно проявляется в виде отличительных признаков и симптомов и приводит к сокращению продолжительности или качества жизни человека или животного.
[00325] Используемый в данном документе термин «взаимное уничтожение» означает процесс, который происходит, когда CAR T-клетка становится мишенью для другой CAR T-клетки, содержащей тот же химерный антигенный рецептор, что и мишень для CAR T-клетки, и уничтожается ею, поскольку клетка-мишень экспрессирует антиген, специфически распознаваемый химерным антигенным рецептором на обеих клетках. CAR T-клетка, содержащая химерный антигенный рецептор, дефицитная по антигену, с которым специфически связывается рецептор химерный антигенный рецептор, будет «устойчивой к взаимному уничтожению».
[00326] Термин «редактированный геномом» в контексте данного документа означает добавление, удаление или изменение гена, чтобы он не функционировал. Таким образом, в некоторых вариантах реализации, «CAR T-клетка с редактированным геномом» представляет собой CAR T-клетку, которая имеет такой ген, как CAR, распознающий по меньшей мере один добавленный антиген; и/или имеет ген, такой как ген(ы) антигена(ов), которые распознаются с помощью делеции CAR; и/или имеет такой ген, как TCR, или его субъединицу (например, α- или β-цепь), удаленную или модифицированную, чтобы быть нефункциональной, или субъединица связанного комплекса передачи сигнала CD3, или его субъединица (например, цепи γ, δ, ε или ζ) удалены или изменены, чтобы быть нефункциональными.
[00327] Используемый в данном документе термин «суицидный ген» относится к последовательности нуклеиновой кислоты, введенной в CAR T-клетку стандартными способами, известными в данной области, которые при активации приводят к гибели CAR T-клетки. При необходимости суицидные гены могут способствовать отслеживанию и удалению, то есть уничтожению CAR T-клеток in vivo. Облегченное уничтожение CAR T-клеток путем активации суицидного гена может быть выполнено стандартными способами, известными в данной области техники. Системы суицидных генов, известные в данной области техники, включают, но не ограничиваются ими, включают (а) вирус простого герпеса (HSV)-tk, который превращает нетоксичное пролекарство ганцикловир (GCV) в GCV-трифосфат, что приводит к гибели клеток за счет остановки репликации ДНК, (b) iCasp9 может связываться с небольшой молекулой AP1903 и приводить к димеризации, которая активирует внутренний путь апоптоза, и (c) целевой поверхностный антиген, экспрессируемый в трансдуцированных Т-клетках (например, CD20 и усеченный EGFR), позволяя удалить модифицированные клетки эффективно путем дополнения/антитело-зависимой клеточной цитотоксичности (CDC/ADCC) после введения ассоциированного моноклонального антитела.
[00328] «Раковая клетка», например, представляет собой злокачественную Т-клетку, злокачественную В-клетку или злокачественную плазматическую клетку.
[00329] «Злокачественная В-клетка» представляет собой В-клетку, полученную из В-клеточного злокачественного образования. В-клеточные злокачественные новообразования включают, без ограничения, (ДКВКЛ), хронический лимфоцитарный лейкоз (ХЛЛ)/малую лимфоцитарную лимфому (МЛЛ) и острый лимфобластный лейкоз предшественников B-клеток (ОЛЛ).
[00330] «Злокачественная Т-клетка» представляет собой Т-клетку, полученную из Т-клеточного злокачественного образования.
[00331] Термин «Т-клеточное злокачественное образование» относится к широкой, весьма гетерогенной группе злокачественных новообразований, происходящих от предшественников Т-клеток, зрелых Т-клеток или естественных клеток-киллеров. Неограничивающие примеры Т-клеточных злокачественных новообразований включают Т-клеточный острый лимфобластный лейкоз/лимфому (T-ОЛЛ), Т-клеточный вирусный лейкоз человека, положительный тип 1 (HTLV-1 +), Т-клеточный лейкоз/лимфому взрослых (ТЛВ), Т-клеточный пролимфоцитарный лейкоз (T-ПЛЛ), Т-клеточная лимфома/лейкоз взрослых (ассоциированный с HTLV-1), агрессивный лейкоз NK-клеток, анапластическую крупноклеточную лимфому (ALCL), ALK-положительную, анапластическую крупноклеточную лимфому (ALCL), ALK-отрицательную, ангиоиммунобластную Т-клеточная лимфому (AITL), анапластическую крупноклеточную лимфому, связанную с грудным имплантатом, хроническое лимфопролиферативное заболевание NK-клеток, экстраузловую NK/T-клеточную лимфому, носовой тип, энтеропатический тип T- клеточной лимфомы, фолликулярную Т-клеточную лимфому, гепатоспленическую Т-клеточную лимфому, индолентное Т-клеточное лимфопролиферативное заболевание желудочно-кишечного тракта, мономорфную эпителиотрофную кишечную Т-клеточную лимфому, грибовидный микоз, узловую периферическую Т-клеточную лимфому с TFH фенотипом, периферическую Т-клеточную лимфому (PTCL), NOS, первичную кожную γδ Т-клеточную лимфому, первичную поверхностную акральную CD8+ агрессивную эпидермотропую цитотоксическую Т-клеточную лимфому, первичную поверхностную акральную CD8+ T-клеточную лимфому, первичные поверхностные CD4+ малые/средние Т-клеточные лимфопролиферативные нарушения [первичная поверхностная анапластическая крупноклеточная лимфома (C-ALCL), лимфоидный папулезный синдром], синдром Сезари, подкожную, панникулитоподобную Т-клеточную лимфому, системную EBV+ Т-клеточную лимфому детского возраста и Т-клеточный крупногранулярный лимфоцитарный лейкоз (LGL).
[00332] «Здоровый донор», как используется в данном документе, представляет собой таковой, у кого нет гематологического злокачественного новообразования (например, злокачественного новообразования Т-клеток).
[00333] В данном контексте термин "фармацевтически приемлемая соль" относится к таким солям, которые с медицинской точки зрения подходят для применения в контакте с тканями субъекта без чрезмерной токсичности, раздражения, аллергической реакции и/или тому подобного, и имеют разумное соотношение польза/риск.
[00334] Термин «терапевтически эффективный» предназначен для определения количества активных ингредиентов, используемых при лечении заболевания или нарушения, или для воздействия на клиническую конечную точку.
[00335] Используемый в данном документе термин «секретируемый белок» означает белок, секретируемый клеткой, который оказывает влияние на другие клетки. В качестве примера секретируемые белки включают цитокины, хемокины и факторы транскрипции.
[00336] Термин «донорская матрица» относится к эталонному геномному материалу, который клетка использует в качестве матрицы для восстановления двухцепочечного разрыва через путь репарации ДНК, направленный на гомологию (HDR). Донорская матрица содержит фрагмент ДНК, который необходимо вставить в геном (содержащий ген, который должен быть экспрессирован, CAR или маркер), с двумя плечами гомологии, фланкирующими участок двухцепочечного разрыва. В некоторых вариантах реализации, донорская матрица может быть аденоассоциированным вирусом, одноцепочечной ДНК или двухцепочечной ДНК.
[00337] Термин «воздействие», используемый в данном документе, в контексте приведения композиций вещества (например, антител) в тесный контакт с другими композициями вещества (такими как клетки), означает синоним «инкубировать с» и использование одного термина вместо другого не предполагает более продолжительного периода контакта.
[00338] Термин «пациент» обычно является синонимом термина «субъект» и включает всех млекопитающих, включая человека.
[00339] Следующие примеры дополнительно иллюстрируют настоящее изобретение.
ПРИМЕРЫ
Пример 1 - Способ получения и тестирования клеток CAR-T с редактированным геномом путем вставки CAR в локусы CD3e
[00340] Следующие шаги могут быть предприняты для получения CAR T-клетки с редактированным геномом, в которой car экспрессируется из локусов, редактируемого гена (CAR-T), описанных в данном документе. Этот пример описывает создание CD7CART ΔCD7 ΔCD3ε клетки. Специалисты в данной области техники поймут, что некоторые из стадий могут выполняться последовательно или в порядке, не указанном ниже, хотя, возможно, это приведет к различной эффективности.
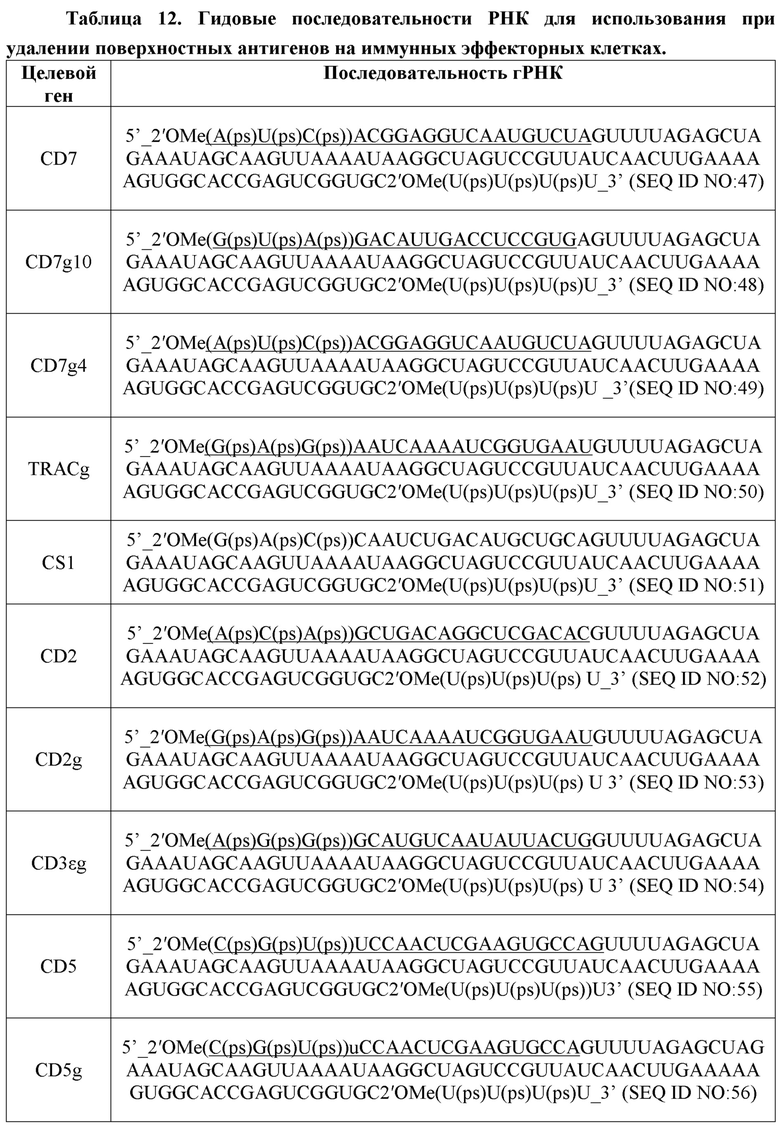
РНК; (ps) обозначают фосфоротиоат. Подчеркнутые основания обозначают целевую последовательность.
Стадия 1 - Активация Т-клеток (День 0).
[00341] Очистите Т-клетки из камеры лейкафереза, используя набор для выделения Miltenyi human PanT. Ресуспендируйте в среде. Подсчитывали клетки ММ. Определите количество бусин CD3/CD28, активирующих Т-клетки человека, необходимое для получения соотношения бусы: клетки 3: 1. Промойте бусы 2 раза средой для Т-клеток. Разбавьте клетки до 1256 клеток/мл в среде hXcyte. Добавьте бусы CD3/CD28 активации человеческих Т-клеток. Аликвотируйте 4 мл/лунку раствора 1256 клеток/мл в 6-луночный планшет. Инкубируйте клетки при 37 °C.
Стадия 2 - CRISPR (День 2).
[00342] Целевой ген генетически удален, а CAR вставлен в редактируемые локусы гена. Двухцепочечный разрыв ДНК может быть восстановлен с помощью гомологически направленного восстановления с использованием донорной матрицы для восстановления разрыва и вставки желаемой последовательности в редактируемые локусы. Делеция мишени может быть достигнута путем электропорации мРНК и гРНК Cas9 против мишени(ей). Донорная матрица может быть ДНК-плазмидой или двухцепочечной линейной ДНК, содержащей гомологию с ДНК, окружающей двухцепочечные разрывы, подвергнутые электропорированию с Cas9/гРНК. Кроме того, вирусный вектор, такой как ААВ, может использоваться в качестве источника донорской матрицы. Однако другие способы могут быть использованы для индукции двухцепочечных разрывов ДНК. К ним относятся другие способы редактирования генома, такие как TALEN и мегануклеазы.
Таблица 13. CRISPR протокол
[00343] Протокол - Nucleofection с использованием нуклеофектора 4D - 4×106 клеток на реакцию. Программа EO-115 - объем трансфекции 100 мкл. Вся добавка должна быть добавлена в раствор Nucleofector™ P3. Подготовьте планшеты для культивирования клеток, заполнив соответствующее количество лунок желаемым объемом рекомендуемой питательной среды (2 мл в 6-луночном планшете) и предварительно инкубируйте/уравновешивайте планшеты в увлажненном инкубаторе при 37 °C/5% CO2. Магнитно удалите бусы (сделайте это дважды, чтобы полностью удалить). Подсчитайте клетки и определите плотность клеток. Центрифугируйте необходимое количество клеток при 90xg в течение 10 минут при комнатной температуре. Полностью удалите супернатант. Ресуспендируйте в ФСБ (1 мл), перенесите в пробирку для микроцентрифуги и центрифугируйте необходимое количество клеток при 90xg в течение 10 минут при комнатной температуре. Полностью удалите супернатант. Осторожно ресуспендируйте клеточный осадок в полном растворе 4DNucleofector™ P3 при комнатной температуре (4×106 на 100 мкл). Добавьте 20мкг каждой гРНК (gCD7 и gCD3ε) в каждую пробирку 15 мкг cas9. Добавьте 100 мкл клеток в каждую пробирку с Cas9/гРНК, осторожно перемешайте и перенесите все в Nucleocuvette™. Осторожно постучите, чтобы удалить пузырьки. Электропорируйте с помощью программы (Human T-cell stim EO-115). После завершения цикла осторожно извлеките сосуд Nucleocuvette™ из фиксатора с помощью специального приспособления. Ресуспендируйте клетки с предварительно нагретой средой. Отберите среду из лунки назначения, добавьте в кювету и осторожно пипетируйте вверх и вниз два-три раза. Перенесите в лунку. Повторите то же самое со средой из той же лунки. Инкубируйте при 37 oC.
Стадия 3 - Трансдукция Т-клеток вектором ААВ, содержащим репарационную конструкцию HDR.
[00344] Рекомбинантный донорный вектор ААВ6 добавляли к культуре клеток через 2-4 часа после электропорации с MOI между 1e4 и 1e6.
Стадия 4 - Оценка активности CRISPR и эффективности Td (10 День).
[00345] Возьмите 5×105 клеток из каждого образца и проанализируйте с помощью проточной цитометрии. Промойте образцы RB. Добавьте 3 мкл антитела к CD34 PE (это обнаруживает CAR, поскольку наша конструкция содержит усеченный CD34 человека). Добавьте 5 мкл CD3 APC и 2 мкл CD2 BV421. Промойте. Выполните проточную цитометрию. Клетки должны быть CD3ε отрицательными, CD7 отрицательными. Соберите Т-клетки (11 день) .
[00346] Очистите CAR T-клетки. CD34+ (CAR+) и TCR-отрицательные клетки могут быть очищены в одну стадию с использованием положительного отбора клеток CD34+ на Miltenyi Automacs. Это обогащает клетки CAR+ и удаляет клетки TCR+ (поскольку вставка CAR нарушает передачу сигналов TCR)
Стадия 5 - Оценка активности CAR-T in vivo
[00347] Введите опухоль в мышей NSG (5e5 MOLT3 или HH: содержащие люциферазу) при выполнении эксперимента визуализации in vivo. День 7:
[00348] Определите опухолевую нагрузку у мышей с помощью биолюминесцентной визуализации. Введите 2×106 CD34+CAR-T на мышь с помощью в./в. через хвостовую вену или проведите 4-часовой анализ высвобождения хрома для клеток-мишеней (MOLT3 или HH) (11 день) . Специалисты в данной области техники поймут, что возможна некоторая гибкость во временных рамках, указанных в Примере 1.
Пример 2 - Способ получения тандемных tCAR T-клеток с редактированным геномом
[00349] В варианте протокола из Примера 1 может быть получена тандемная CAR T-клетка, распознающая два антигена. На Стадии 2 два антигена могут быть удалены с поверхности клетки или подавлены, как описано выше, путем электропорации с гРНК для каждой из двух мишеней и мРНК Cas9. На Стадии 3 эта CAR T-клетка затем трансдуцируется с помощью CAR, который распознает две мишени. Варианты тандемной CAR T-клетки, представлены на схеме на Фиг. 2. Дополнительные примеры tCAR T-клеток представлены в Таблице 6.
Пример 3 - Двойные CAR T-клетки с редактированным геномом или тандемные CAR T-клетки с редактированным геномом
[00350] Несколько типов двойных или тандемных CAR T-клеток с редактированным геномом можно получить с использованием описанных выше способов. Фиг. 1 и Фиг. 2 иллюстрируют примеры тандемных и двойных CAR T-клеток. Цифры указывают на антигены-мишени, и не указывают порядок экспрессии scFv в тандемной конструкции CAR. Дополнительные примеры представлены ниже в Таблицах 6-11.
[00351] В настоящем документе представлены дополнительные примеры тандемных и двойных CAR T-клеток с делецией, без делеции или подавлением одного или более поверхностных белков, которые являются антигенами-мишенями CAR и экспрессируются на CAR T-клетках. В целом, примеры с делецией или подавлением более чем одного антигена с большей вероятностью будут иметь преимущество большей устойчивости к взаимному уничтожению для этих CAR T-клеток. Следует также отметить, что порядок, в котором scFv, ориентированы в тандемных CAR приведены в Таблицах 6-11, и не является ограничивающим. Например, CD2*CD3ε охватывает tCAR с ориентацией CD2*CD3ε или ориентацией CD3ε*CD2.
[00352] Дополнительные примеры моно-, тандемных и двойных CAR T-клеток, нацеленных на экспрессию антигенов на множественных миеломных клетках, представлены в данном документе без делеции, с делецией или подавлением одного или более поверхностных белков, которые являются антигенами-мишенями для CAR и экспрессируются на CAR Т-клетках. В целом, примеры с делецией или подавлением более чем одного антигена с большей вероятностью будут иметь преимущество большей устойчивости к взаимному уничтожению для этих CAR T-клеток.
Пример 4 - Лечение пациента(ов) двойными или тандемными CAR T-клетками, с редактированным геномом
[00353] Пациентов можно лечить с использованием клеток, полученных указанными выше способами, как представлено на Фиг. 1 и Фиг. 2. Например, пациенту можно вливать увеличенную популяцию двойных или тандемных CAR T-клеток.
[00354] Двойные или тандемные клетки CAR-T нацелены на раковые клетки, не вызывая аллореактивности. Например, CD2*CD3ε-dCARTΔCD2ΔCD3ε клетки будут нацелены на раковые клетки (и другие не-раковые клетки), несущие поверхностные антигены CD2 и CDε.
Пример 5- Тестирование эффективности CD2*CD3Δ-dCARTΔCD2ΔCD3ε на ксеногенной модели T-ОЛЛ
[00355] Тестирование эффективности CD2*CD3Δ-dCARTΔCD2ΔCD3ε на ксеногенной модели T-ОЛЛ: 5×105 клеток Jurkat (T-ОЛЛ-99% CD2+, 99%% CD3% по данным FACS) меченных красной люциферазой щелкунчика (CBR), вводили внутривенно реципиентам NSG перед инфузией CD2*CD3ε-dCARTΔCD2ΔCD3ε (WC5 или WC13), CD3CARTΔCD2ΔCD3ε (UCART3), CD2CARTΔCD2ΔCD3ε (UCART2) или нецелевых CD19-CARΔCD2ΔCD3ε (UCART19) контрольных клеток в./в. на +4 день. В отличие от мышей, получавших CD19-CARΔCD2ΔCD3ε, или мышей, которым инъецировали только опухоль, мыши, получавшие CD2*CD3ε-dCARTΔCD2ΔCD3ε, демонстрировали значительно более длительную выживаемость и снижение опухолевой нагрузки, как определено с помощью биолюминесцентного изображения, представленного на Фиг. 13. В будущих моделях CD2 * CD3ε-dCARTΔCD2ΔCD3ε будет обеспечивать преимущество в выживаемости по сравнению с CD3CARTΔCD2ΔCD3ε, CD2CARTΔCD2ΔCD3ε и уменьшать опухолевую нагрузку в версии этой модели, в которой в целевой клетке отсутствует либо CD2 (CD2CARTΔCD2ΔCD3ε), либо CD3 (CD3CARTΔCD2ΔCD3ε).
Пример 6 - Моно CAR T-клетки с редактированным геномом
[00356] Примеры моно CAR T-клеток с редактированным геномом, нацеленных на антигены, экспрессируемые на гематологических злокачественных новообразованиях, представлены ниже без делеции, с делецией или подавлением одного или более поверхностных белков, которые являются антигенами-мишенями CAR и экспрессируются на CAR T-клетках. В целом, примеры с делецией или подавлением более чем одного антигена с большей вероятностью будут иметь преимущество большей устойчивости к взаимному уничтожению для этих CAR T-клеток.
Пример 7 - Клетки UCART2/3, с редактированным геномом, созданные путем редактирования перед активацией
[00357] В 0 день клетки оттаивали в оттаивающем буфере. После этого клетки ресуспендировали в среде и давали отдохнуть в течение двух часов. Клетки собирали и подсчитывали. Необходимое количество клеток центрифугировали при 100×g в течение 10 минут при комнатной температуре. Супернатант полностью удаляли, клетки ресуспендировали в ФСБ (1 мл) и переносили в микроцентрифужную пробирку и центрифугировали при 100×g в течение 10 минут при комнатной температуре. Супернатант удаляли полностью, а затем клетки ресуспендировали в буфере P3, подсчитывали и доводили количество до 5×107 на мл. Объем пула клеток 100 мкл добавляли в пробирку, содержащую Cas9/гРНК, осторожно перемешивали и все переносили в Nucleocuvette™, по которой осторожно постукивали для удаления пузырьков. После этого начинали электропорацию с использованием программы (Human T cell stim EO-115). После этой процедуры активированные клетки переносили в предварительно нагретую среду и распределяли аликвотами по 2 мл в 12-луночном планшете. Аликвотные образцы выдерживали в течение 24 часов.
[00358] В день 1 клетки были активированы T Cell TransAct™, как показано в Таблице 14.
[00359] Таблица 14. Активация T Cell TransAct™.
[00360] На 2 день добавляли 1 мкл полибрена на каждый мл среды (8 мг/мл исходного раствора). Требуемое количество вируса было добавлено для получения требуемой M.O.I (множественности заражения). Клетки и вирус были смешаны и помещены обратно в инкубатор при 37 °C.
[00361] На 3 день активированные клетки промывали для снятия стимуляции.
[00362] На 12 день анализ FACS показал высокую чистоту клеток CD3-CD2-/CAR-T; см. Фиг. 5 (клон 5 и клон 6), Фиг. 6 (клон 7 и клон 8), Фиг. 7 (клон 13 и клон 14) и Фиг. 8 (клон 15 и клон 16). Стандартные анализы четырехчасового высвобождения хрома (51Cr) были выполнены с использованием (51Cr) меченных геном-редактированных клеток Jurkat (ΔCD2, ΔCD3 и ΔCD2ΔCD3. Эти эксперименты показали, что функциональные реакции уничтожения опухоли с мишенями CD2 и CD3 независимы друг от друга (см. Фиг. 9A, Фиг. 9B, Фиг. 9C и Фиг. 9D).
Пример 8 - Уничтожение опухолевых клеток клетками BCMA-CAR-T
[00363] BCMA CAR-T были сначала протестированы in vitro на эффективность с использованием стандартных четырехчасовых анализов по высвобождению хрома (51Cr) с использованием меченных 51Cr клеток-мишеней MM.1S. Чтобы обеспечить отслеживание in vivo, клеточная линия миеломы человека (BCMA +/CD19-) была модифицирована для экспрессии красной люциферазы щелкунчика, слитой с GFP (MM.1S-CG). CAR T-клетки инкубировали с 51Cr-меченными клетками MM.1S-CG в течение четырех часов при различных соотношениях эффекторного (CAR-T) и целевого (MM.1S-CG) и высвобожденный 51Cr измеряли как маркер гибели клеток MM.1S-CG (Фиг. 10В). Эффективное уничтожение наблюдали при множественных соотношениях эффектор к цели (E:T). Нетрансдуцированные активированные Т-клетки и CD19-CAR-T использовали в качестве отрицательного контроля и не вызывали гибели клеток MM.1S-CG. Затем эффективность in vivo тестировали путем приживления мышам NSG 500000 клеток миеломы человека MM.1S-CG (в./в.). Двадцать восемь дней спустя, когда опухолевая нагрузка была высокой, мышей оставляли без лечения или лечили 2 × 106 CD19-CAR-T или BCMA CAR-T. Все семь мышей, получавших BCMA CAR-T, прожили почти 150 дней или более по сравнению с контрольными мышами, которые умерли на около 50 день (Фиг. 10С). Причина смерти одной мыши, которая умерла в когорте BCMA CAR-T, неизвестна. Анализ проточной цитометрии не выявил опухолевых клеток GFP+ у этой мыши. Последовательная биолюминесцентная визуализация (BLI) выявила устойчивое снижение сигнала до фоновых уровней, которые никогда не повышались на протяжении всего эксперимента (Фиг. 10D).
Пример 9 - Уничтожение опухолевых клеток клетками CS1-CAR-T
[00364] Эффективность клеток CS1-CAR-T in vivo путем инъекции 5 × 105 MM.1S-CG мышам NSG и 28 дней спустя, когда опухолевая нагрузка была высокой (поток фотонов BLI 1010), инъецировали 2 × 106 клеток CS1-CAR-T или отрицательные контрольные клетки CD19-CAR-T. Мышам также прививали клетки MM.1S-CG без CS1 (с использованием технологии CAS9/CRISPR; MM.1S-CGΔCS1) в качестве способа проверки специфичности клеток CS1-CAR-T. Все мыши, получавшие CS1-CAR T-клетки (n=10), жили > 90 дней (Фиг. 11B), в то время как средняя выживаемость мышей CD19-контроля (n=8) составляла 43 дня. Мы лечили мышей с привитыми MM.1S-CGΔCS1 с помощью CS1-CAR-T или CD19 CAR-T, как указано выше. Выживаемость этих мышей была аналогична таковой у контрольных мышей (49 дней), демонстрируя специфичность in vivo. Последовательная биолюминесцентная визуализация (BLI) показала, что у мышей, обработанных CS1-CAR-T, наблюдалось трехлогарифмическое снижение потока фотонов и клиренса опухоли костного мозга (Фиг. 11С). У подгруппы мышей CS1-CAR-T развились экстрамедуллярные опухоли, которые сохранили экспрессию CS1, что позволяет предположить, что ускользания антигена не произошло.
Пример 10 - Эффективность и уничтожение клеток тандемом (tCAR), нацеленным на BCMA и CS1
[00365] Двунаправленный CAR-T, который экспрессирует два scFv в тандеме (tCAR), нацеленный на BCMA и CS1, был разработан в попытке повысить эффективность и уничтожить миеломные клетки CAR-T. В качестве контроля тандемный CAR тестировался бок о бок с однонаправленными клетками BCMA-CAR-T и однонаправленными клетками CS1-CAR-T. Клетки CD19-CAR-T использовали в качестве отрицательного контроля. Во-первых, было подтверждено, что каждый scFv экспрессируется в tCAR. Для этого клетки Jurkat инфицировали лентивирусом, экспрессирующим каждую конструкцию CAR, как представлено на Фиг. 12А. Клетки CAR-T инкубировали с рекомбинантными белками BCMA и CS1 человека, каждый из которых был помечен отдельными флуоресцентными флуофорами. Отрицательные контрольные CAR T-клетки гейтировали (синий цвет), а экспериментальные CAR T-клетки накладывали друг на друга (красный цвет). Как и ожидалось, клетки Jurkat, экспрессирующие CD19-CAR, не связывались ни с белком BCMA, ни с CS1 (нижний левый квадрант, Фиг. 12В). Клетки Jurkat, экспрессирующие белок BCMA CAR, связанный с белком BCMA (верхний левый квадрант, Фиг. 12В). Клетки Jurkat, экспрессирующие белок CS1 CAR, связанный с белком CS1 (нижний правый квадрант, Фиг. 12В). Клетки Jurkat, экспрессирующие тандемный белок BCMA-CS1 CAR, связанный с обоими рекомбинантными белками (верхний правый квадрант, Фиг. 12B), предполагает экспрессию обоих scFv.
[00366] Одиночные и тандемные CAR T-клетки тестировали на эффективность in vitro с помощью стандартных четырехчасовых анализов высвобождения хрома (51Cr). Для этих экспериментов CAR T-клетки инкубировали с рядом эффекторных клеток-мишеней (соотношение E:T). BCMA-CS1 tCAR T-клетки убивали клетки MM.1S-CG с такой же эффективностью, как и отдельные клетки-мишени CAR-T. Дополнительные эксперименты позволят оптимизировать двунаправленные клетки BCMA-CS1 CAR-T для обеспечения эффективности in vivo .
Пример 11 - Анализ отклонения от цели для отбора гРНК
[00367] Направляющие РНК были разработаны и проверены на предмет активности Washington University Genome Engineering & iPSC. Направляющие РНК были разработаны и проверены на предмет активности Washington University Genome Engineering & iPSC. Последовательности, комплементарные данной гРНК, могут существовать по всему геному, включая, но не ограничиваясь этим, целевой локус. Короткая последовательность с большей вероятностью гибридизуется вне мишени. Точно так же некоторые длинные последовательности внутри гРНК могут иметь точные совпадения (long_0) или близкие совпадения (long_1, long_2, представляющие, соответственно, одно- или двухнуклеотидное различие) по всему геному. Они также могут гибридизоваться не по назначению, что приводит к редактированию неправильного гена и снижению эффективности редактирования.
[00368] Анализ отклонения от цели выбранной гРНК выполняли для 2 экзонов hCD2 (CF58 и CF59), чтобы определить количество сайтов в геноме человека, которые точно совпадают или содержат до 1 или 2 несовпадений, которые могут включать целевой сайт. Результаты приведены в Таблице 15 для экзона CF58 и в Таблице 16 для экзона CF59.
Таблица 15. Анализ отклонения от цели гидовой РНК (гРНК) для hCD2 (экзон CF58)
Таблица 16. Анализ отклонения от цели гидовой РНК (гРНК) для hCD2 (CF59)
[00369] Последовательности гРНК в Таблице 15 и Таблице 16 были нормализованы (% нормализации к NHEJ) на активность гРНК посредством секвенирования следующего поколения (NGS). GFP использовали в качестве контроля. После анализа секвенирования были рекомендованы следующие гРНК на основе профиля отклонения от цели: CF58.CD2.g1 (41,2%), CF58.CD2.g23 (13,2%), CF59.CD2.g20 (26,6%), CF59.CD2.g13 (66,2%), CF59.CD2.g17 (17,5%). Гидовая РНК (гRNA) с нормализованными частотами NHEJ, равными или превышающими 15%, является хорошим кандидатом для проектов создания линий клеток и моделей животных.
[00370] Анализ отклонения от цели выбранной гРНК был выполнен для hCD3E для определения количества сайтов в геноме человека, которые являются точным совпадением или содержат до 1 или 2 несовпадений, которые могут включать целевой сайт. Результаты представлены в Таблице 17 hCD3E.
Таблица 17. Анализ отклонения от цели гидовой РНК (гРНК) для hCD3E
[00371] Последовательности гРНК в Таблице 17 были нормализованы (% нормализации к NHEJ) на активность гРНК посредством секвенирования следующего поколения (NGS). GFP использовали в качестве контроля. После анализа секвенирования были рекомендованы следующие гРНК на основе профиля отклонения от цели: MS1044.CD3E.sp28 (> 15%) и MS1044.CD3E.sp12 (> 15%). Гидовая РНК (гРНК) с нормализованными частотами NHEJ, равными или превышающими 15%, является хорошим кандидатом для проектов создания линий клеток и моделей животных.
[00372] Анализ отклонения от цели выбранной гРНК выполняли для 3 экзонов hCD5 (Экзон 3, Экзон 4, и Экзон 5), чтобы определить количество сайтов в геноме человека, которые точно совпадают или содержат до 1 или 2 несовпадений, которые могут включать целевой сайт. Результаты приведены в Таблице 18 для Экзона 3, в Таблице 19 для Экзона 4 и в Таблице 20 для Экзона 5.
Таблица 18. Анализ отклонения от цели гидовой РНК (гРНК) для hCD5 (Экзон 3)
Таблица 19. Анализ отклонения от цели гидовой РНК (гРНК) для hCD5 (Экзон 4)
Таблица 20. Анализ отклонения от цели гидовой РНК (гРНК) для hCD5 (Экзон 5)
[00373] Последовательности гРНК в Таблице 18, Таблице 19 и Таблице 20 были нормализованы (% нормализации к NHEJ) на активность гРНК посредством секвенирования следующего поколения (NGS). GFP использовали в качестве контроля. После анализа секвенирования были рекомендованы следующие гРНК на основе профиля отклонения от цели: Экзон 3: SP597.hCD5.g2 (76,5%), SP597.hCD5.g22 (36,3%), SP597.hCD5.g39 (16,0%), SP597.hCD5.g46. Экзон4: SP598.hCD5.g7, SP598.hCD5.g10 (58,5%). Экзон5: SP599.hCD5.g5 (51,0%), SP599.hCD5.g30, SP599.hCD5.g42, SP599.hCD5.g58 (41,0%)
[00374] Анализ отклонения от цели выбранной гРНК был выполнен для hCSF2 для определения количества сайтов в геноме человека, которые являются точным совпадением или содержат до 1 или 2 несовпадений, которые могут включать целевой сайт. Результаты представлены в Таблице 21 для hCSF2.
Таблица 21. Анализ отклонения от цели гидовой РНК (гРНК) для hCSF2
[00375] Последовательности гРНК в Таблице 21 были нормализованы (% нормализации к NHEJ) на активность гРНК посредством секвенирования следующего поколения (NGS). GFP использовали в качестве контроля. После анализа секвенирования были рекомендованы следующие гРНК на основе профиля отклонения от цели: MS1086.CSF2.sp8 (> 15%) и MS1086.CSF2.sp10 (> 15%).
[00376] Анализ отклонения от цели выбранной гРНК выполняли для 2 экзонов hCTLA4 (Экзон 1 и Экзон 2), чтобы определить количество сайтов в геноме человека, которые точно совпадают или содержат до 1 или 2 несовпадений, которые могут включать целевой сайт. Результаты приведены в Таблице 22 для Экзона 1, в Таблице 23 для Экзона 2 для hCTLA4.
Таблица 22. Анализ отклонения от цели гидовой РНК (гРНК) для hCTLA4 (Экзон 1)
Таблица 23. Анализ отклонения от цели гидовой РНК (гРНК) для hCTLA4 (Экзон 2)
[00377] Последовательности гРНК в Таблице 22 и Таблице 23 были нормализованы (% нормализации к NHEJ) на активность гРНК посредством секвенирования следующего поколения (NGS). GFP использовали в качестве контроля. После анализа секвенирования были рекомендованы следующие гРНК на основе профиля отклонения от цели: Экзон 1: SP621.hCTLA4.g2 (> 15%) и SP621.hCTLA4.g12 (> 15%). Экзон 2: SP622.hCTLA4.g2 (> 15%), SP622.hCTLA4.g9 (> 15%) и SP622.hCTLA4.g33 (> 15%).
[00378] Анализ отклонения от цели выбранной гРНК выполняли для 2 экзонов hPDCD1 (CF60 и CF61), чтобы определить количество сайтов в геноме человека, которые точно совпадают или содержат до 1 или 2 несовпадений, которые могут включать целевой сайт. Результаты приведены в Таблице 24 для Экзона CF60 и в Таблице 25 для Экзона CF61.
Таблица 24. Анализ отклонения от цели гидовой РНК (гРНК) для hPDCD1 (Экзон CF60)
Таблица 25. Анализ отклонения от цели гидовой РНК (гРНК) для hPDCD1 (CF61)
[00379] Последовательности гРНК в Таблице 24 и Таблице 25 были нормализованы (% нормализации к NHEJ) на активность гРНК посредством секвенирования следующего поколения (NGS). GFP использовали в качестве контроля. После анализа секвенирования были рекомендованы следующие гРНК на основе профиля отклонения от цели: CF60.PDCD1.g12 (65,6%), CF60.PDCD1.g3 (69,2%), CF61.PDCD1.g6, CF61.PDCD1.g2 (72,7%) и CF61.PDCD1.g35 (24,0%).
[00380] Анализ отклонения от цели выбранной гРНК выполняли для 2 экзонов hTIM3 (Экзон 2 и Экзон 3), чтобы определить количество сайтов в геноме человека, которые точно совпадают или содержат до 1 или 2 несовпадений, которые могут включать целевой сайт. Результаты приведены в Таблице 26 для Экзона 2, в Таблице 27 для Экзона 3.
Таблица 26. Анализ отклонения от цели гидовой РНК (гРНК) для hTIM3 (Экзон 2)
Таблица 27. Анализ отклонения от цели гидовой РНК (гРНК) для hTIM3 (Экзон 3)
[00381] Последовательности гРНК в Таблице 26 и Таблице 27 были нормализованы (% нормализации к NHEJ) на активность гРНК посредством секвенирования следующего поколения (NGS). GFP использовали в качестве контроля. После анализа секвенирования были рекомендованы следующие гРНК на основе профиля отклонения от цели: Экзон 2: SP619.hTIM3.g12 (45,0%), SP619.hTIM3.g20 (60,9%) и SP619.hTIM3.g49 (45,4%). Экзон 3: SP620.hTIM3.g5 (58,0%) и SP620.hTIM3.g7 (2,9%).
[00382] Описанные выше способы могут быть соответствующим образом изменены специалистами в данной области техники для получения и подтверждения активности других моно, двойных и тандемных CAR T-клеток, описанных в данном документе.
[00383] Хотя настоящее изобретение было описано со ссылкой на конкретные детали некоторых вариантов его реализации, в приведенных выше примерах, следует понимать, что модификации и изменения охватываются духом и объемом изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ВАШИНГТОН ЮНИВЕРСИТИ
<120> Т-КЛЕТКИ С ХИМЕРНЫМИ АНТИГЕННЫМИ РЕЦЕПТОРАМИ (CAR-T) ДЛЯ
ЛЕЧЕНИЯ РАКА
<130> WGN0001-401-PC
<140> PCT/US19/035010
<141> 2019-05-31
<150> 62/678,878
<151> 2018-05-31
<150> 62/799,513
<151> 2019-01-31
<160> 452
<170> PatentIn version 3.5
<210> 1
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 1
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 2
<211> 45
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 2
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 3
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 4
<211> 235
<212> Белок
<213> Homo sapiens
<400> 4
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Gln Phe Arg Val Ser Pro Leu Asp Arg Thr
20 25 30
Trp Asn Leu Gly Glu Thr Val Glu Leu Lys Cys Gln Val Leu Leu Ser
35 40 45
Asn Pro Thr Ser Gly Cys Ser Trp Leu Phe Gln Pro Arg Gly Ala Ala
50 55 60
Ala Ser Pro Thr Phe Leu Leu Tyr Leu Ser Gln Asn Lys Pro Lys Ala
65 70 75 80
Ala Glu Gly Leu Asp Thr Gln Arg Phe Ser Gly Lys Arg Leu Gly Asp
85 90 95
Thr Phe Val Leu Thr Leu Ser Asp Phe Arg Arg Glu Asn Glu Gly Tyr
100 105 110
Tyr Phe Cys Ser Ala Leu Ser Asn Ser Ile Met Tyr Phe Ser His Phe
115 120 125
Val Pro Val Phe Leu Pro Ala Lys Pro Thr Thr Thr Pro Ala Pro Arg
130 135 140
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
145 150 155 160
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
165 170 175
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
180 185 190
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His
195 200 205
Arg Asn Arg Arg Arg Val Cys Lys Cys Pro Arg Pro Val Val Lys Ser
210 215 220
Gly Asp Lys Pro Ser Leu Ser Ala Arg Tyr Val
225 230 235
<210> 5
<211> 42
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 5
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 6
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 6
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 7
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 7
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 8
<211> 22
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 8
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 9
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 9
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 10
<211> 308
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 10
Met Pro Arg Gly Trp Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser
1 5 10 15
Gly Phe Met Ser Leu Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro
20 25 30
Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu
35 40 45
Thr Thr Thr Pro Ser Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser
50 55 60
Gln His Gly Asn Glu Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys
65 70 75 80
Phe Thr Ser Thr Ser Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser
85 90 95
Ser Val Gln Ser Gln Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro
100 105 110
Ala Asn Val Ser Thr Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro
115 120 125
Gly Asn Val Ser Asp Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser
130 135 140
Pro Thr Lys Pro Tyr Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys
145 150 155 160
Ala Glu Ile Lys Cys Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly
165 170 175
Ile Cys Leu Glu Gln Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys
180 185 190
Asp Arg Gly Glu Gly Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala
195 200 205
Asp Ala Asp Ala Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser
210 215 220
Glu Val Arg Pro Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu
225 230 235 240
Ile Ser Ser Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys
245 250 255
Lys Leu Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln
260 265 270
Ser Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu
275 280 285
Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser
290 295 300
Trp Ser Pro Ile
305
<210> 11
<211> 710
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 11
Met Pro Arg Gly Trp Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser
1 5 10 15
Gly Phe Met Ser Leu Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro
20 25 30
Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu
35 40 45
Thr Thr Thr Pro Ser Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser
50 55 60
Gln His Gly Asn Glu Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys
65 70 75 80
Phe Thr Ser Thr Ser Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser
85 90 95
Ser Val Gln Ser Gln Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro
100 105 110
Ala Asn Val Ser Thr Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro
115 120 125
Gly Asn Val Ser Asp Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser
130 135 140
Pro Thr Lys Pro Tyr Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys
145 150 155 160
Ala Glu Ile Lys Cys Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly
165 170 175
Ile Cys Leu Glu Gln Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys
180 185 190
Asp Arg Gly Glu Gly Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala
195 200 205
Asp Ala Asp Ala Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser
210 215 220
Glu Val Arg Pro Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu
225 230 235 240
Ile Ser Ser Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys
245 250 255
Lys Leu Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln
260 265 270
Ser Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu
275 280 285
Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser
290 295 300
Trp Ser Pro Thr Gly Glu Gly Gly Gly Gly Gly Asp Leu Gly Gly Val
305 310 315 320
Lys Leu Pro His Leu Phe Gly Lys Arg Leu Val Glu Ala Arg Met Ala
325 330 335
Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala Ala Arg
340 345 350
Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg Arg Gln
355 360 365
Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr Leu Leu
370 375 380
Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr Thr Thr
385 390 395 400
Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr Val Pro
405 410 415
Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr Ile Ala
420 425 430
Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile Ser Ala
435 440 445
Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met Gly Met
450 455 460
Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly Gly Glu
465 470 475 480
Ala Gly Ser Ser His Ala Pro Pro Pro Ala Leu Thr Leu Leu Leu Asp
485 490 495
Arg His Pro Ile Ala Val Met Leu Cys Tyr Pro Ala Ala Arg Tyr Leu
500 505 510
Met Gly Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala Leu Ile
515 520 525
Pro Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu Pro Glu
530 535 540
Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly Glu Arg
545 550 555 560
Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly Leu Leu
565 570 575
Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp Glu Asp
580 585 590
Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly Ala Glu Pro
595 600 605
Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp Thr Leu Phe Thr
610 615 620
Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn Gly Asp Leu Tyr Asn
625 630 635 640
Val Phe Ala Trp Ala Leu Asp Val Leu Ala Lys Arg Leu Arg Pro Met
645 650 655
His Val Phe Ile Leu Asp Tyr Asp Gln Ser Pro Ala Gly Cys Arg Asp
660 665 670
Ala Leu Leu Gln Leu Thr Ser Gly Met Val Gln Thr His Val Thr Thr
675 680 685
Pro Gly Ser Ile Pro Thr Ile Cys Asp Leu Ala Arg Thr Phe Ala Arg
690 695 700
Glu Met Gly Glu Ala Asn
705 710
<210> 12
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 12
Glu Val Lys Leu Glu Glu Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Arg Thr Ser Gly Phe Asn Leu Lys Asp Thr
20 25 30
Ile His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Lys Trp Ile Gly
35 40 45
Arg Ile Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp Pro Lys Phe Gln
50 55 60
Asp Lys Ala Thr Val Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr Leu
65 70 75 80
Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys Val
85 90 95
Thr Tyr Ala Tyr Asp Gly Asn Trp Tyr Phe Asp Val Trp Gly Ala Gly
100 105 110
Thr Ala Val Thr Val Ser Ser
115
<210> 13
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 13
Asp Ile Lys Asn Ile Thr Gln Ser Pro Ser Ser Met Tyr Val Ser Leu
1 5 10 15
Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser
20 25 30
Phe Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu
35 40 45
Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Tyr Glu Asp Met Glu Ile Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro
85 90 95
Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met Lys Arg
100 105
<210> 14
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 14
Glu Val Gln Leu Glu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Thr
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Ile Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Glu Lys Phe
50 55 60
Lys Asp Lys Ala Ile Leu Ser Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Ile Gln Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Arg Asp Ala Lys Tyr Asp Gly Tyr Ala Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 15
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 15
Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val Pro Val Thr Pro Gly
1 5 10 15
Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Thr Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asn Arg Phe Ser Gly Ser Gly Ser Glu Thr Thr Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Glu
100 105 110
Arg
<210> 16
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 16
Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro
1 5 10 15
Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
20 25 30
Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln
50 55 60
Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr
65 70 75 80
Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr
85 90 95
Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 17
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 17
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala His Phe Arg Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Gly Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn Arg
100 105
<210> 18
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 18
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
35 40 45
Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 19
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 19
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp
85 90 95
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
100 105
<210> 20
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 20
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Phe Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Asp Glu Val Arg Gly Tyr Leu Asp Val Trp Gly Ala Gly Thr Thr
100 105 110
Val Thr Val Ser
115
<210> 21
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 21
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Ser Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Lys Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 22
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 22
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Val Gly Ala His Asp Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 23
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 23
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Asp Thr Asp Phe Thr Leu Gln Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly
85 90 95
Thr His Pro Ala Ile Ser Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 24
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 24
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Phe Ala Leu Phe Gly Phe Arg Glu Gln Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 25
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Leu Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 26
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 26
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Ala Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Val Ala Ala Ala Val Ala Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 27
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 27
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ser
85 90 95
Leu Gln Thr Pro Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105 110
<210> 28
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 28
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Thr Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Met Ile Ala Thr Arg Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 29
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 29
Asp Ile Val Met Thr Gln Ser Gln Lys Ser Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Ile Thr Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Asn Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 30
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 30
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Ile Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Val Ile Tyr Pro Gly Asn Asp Asp Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Val Arg Leu Arg Tyr Phe Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ser Gly
115 120
<210> 31
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 31
Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Ser Leu Ala Val Ser
1 5 10 15
Pro Gly Glu Arg Val Thr Met Ser Cys Lys Ser Ser Gln Ser Val Phe
20 25 30
Phe Ser Ser Ser Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Ile Pro
35 40 45
Gly Gln Ser Pro Arg Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser
50 55 60
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
65 70 75 80
Leu Thr Ile Ser Ser Val Gln Pro Glu Asp Leu Ala Ile Tyr Tyr Cys
85 90 95
His Gln Tyr Leu Ser Ser Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu
100 105 110
Ile Lys Arg
115
<210> 32
<211> 832
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 32
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln
35 40 45
Gly Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr Tyr Thr Ser Ser Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr
100 105 110
Ser Lys Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
115 120 125
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
145 150 155 160
Val Lys Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu
165 170 175
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys
180 185 190
Arg Leu Glu Trp Val Ala Ser Ile Ser Ser Gly Gly Phe Thr Tyr Tyr
195 200 205
Pro Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg
210 215 220
Asn Ile Leu Tyr Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Asp Glu Val Arg Gly Tyr Leu Asp Val Trp
245 250 255
Gly Ala Gly Thr Thr Val Thr Val Ser Pro Arg Ala Ser Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val
305 310 315 320
Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe
325 330 335
Ile Ile Phe Trp Val Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg
485 490 495
Thr Asp Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly
500 505 510
Asp Val Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly
515 520 525
Trp Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser
530 535 540
Leu Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr
545 550 555 560
Phe Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro
565 570 575
Ser Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn
580 585 590
Glu Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr
595 600 605
Ser Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser
610 615 620
Gln Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser
625 630 635 640
Thr Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser
645 650 655
Asp Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro
660 665 670
Tyr Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys
675 680 685
Cys Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu
690 695 700
Gln Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu
705 710 715 720
Gly Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala
725 730 735
Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro
740 745 750
Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys
755 760 765
Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu Gly Ile
770 775 780
Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser Tyr Ser Gln
785 790 795 800
Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu Ala Val Leu
805 810 815
Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp Ser Pro Ile
820 825 830
<210> 33
<211> 1234
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 33
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln
35 40 45
Gly Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr Tyr Thr Ser Ser Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr
100 105 110
Ser Lys Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
115 120 125
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
145 150 155 160
Val Lys Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu
165 170 175
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys
180 185 190
Arg Leu Glu Trp Val Ala Ser Ile Ser Ser Gly Gly Phe Thr Tyr Tyr
195 200 205
Pro Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg
210 215 220
Asn Ile Leu Tyr Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Asp Glu Val Arg Gly Tyr Leu Asp Val Trp
245 250 255
Gly Ala Gly Thr Thr Val Thr Val Ser Pro Arg Ala Ser Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val
305 310 315 320
Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe
325 330 335
Ile Ile Phe Trp Val Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg
485 490 495
Thr Asp Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly
500 505 510
Asp Val Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly
515 520 525
Trp Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser
530 535 540
Leu Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr
545 550 555 560
Phe Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro
565 570 575
Ser Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn
580 585 590
Glu Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr
595 600 605
Ser Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser
610 615 620
Gln Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser
625 630 635 640
Thr Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser
645 650 655
Asp Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro
660 665 670
Tyr Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys
675 680 685
Cys Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu
690 695 700
Gln Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu
705 710 715 720
Gly Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala
725 730 735
Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro
740 745 750
Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys
755 760 765
Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu Gly Ile
770 775 780
Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser Tyr Ser Gln
785 790 795 800
Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu Ala Val Leu
805 810 815
Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp Ser Pro Thr
820 825 830
Gly Glu Gly Gly Gly Gly Gly Asp Leu Gly Gly Val Lys Leu Pro His
835 840 845
Leu Phe Gly Lys Arg Leu Val Glu Ala Arg Met Ala Ser Tyr Pro Cys
850 855 860
His Gln His Ala Ser Ala Phe Asp Gln Ala Ala Arg Ser Arg Gly His
865 870 875 880
Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg Arg Gln Gln Glu Ala Thr
885 890 895
Glu Val Arg Leu Glu Gln Lys Met Pro Thr Leu Leu Arg Val Tyr Ile
900 905 910
Asp Gly Pro His Gly Met Gly Lys Thr Thr Thr Thr Gln Leu Leu Val
915 920 925
Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr Val Pro Glu Pro Met Thr
930 935 940
Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr Ile Ala Asn Ile Tyr Thr
945 950 955 960
Thr Gln His Arg Leu Asp Gln Gly Glu Ile Ser Ala Gly Asp Ala Ala
965 970 975
Val Val Met Thr Ser Ala Gln Ile Thr Met Gly Met Pro Tyr Ala Val
980 985 990
Thr Asp Ala Val Leu Ala Pro His Val Gly Gly Glu Ala Gly Ser Ser
995 1000 1005
His Ala Pro Pro Pro Ala Leu Thr Leu Leu Leu Asp Arg His Pro
1010 1015 1020
Ile Ala Val Met Leu Cys Tyr Pro Ala Ala Arg Tyr Leu Met Gly
1025 1030 1035
Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala Leu Ile Pro
1040 1045 1050
Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu Pro Glu
1055 1060 1065
Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly Glu
1070 1075 1080
Arg Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly
1085 1090 1095
Leu Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp
1100 1105 1110
Trp Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln
1115 1120 1125
Gly Ala Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly
1130 1135 1140
Asp Thr Leu Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro
1145 1150 1155
Asn Gly Asp Leu Tyr Asn Val Phe Ala Trp Ala Leu Asp Val Leu
1160 1165 1170
Ala Lys Arg Leu Arg Pro Met His Val Phe Ile Leu Asp Tyr Asp
1175 1180 1185
Gln Ser Pro Ala Gly Cys Arg Asp Ala Leu Leu Gln Leu Thr Ser
1190 1195 1200
Gly Met Val Gln Thr His Val Thr Thr Pro Gly Ser Ile Pro Thr
1205 1210 1215
Ile Cys Asp Leu Ala Arg Thr Phe Ala Arg Glu Met Gly Glu Ala
1220 1225 1230
Asn
<210> 34
<211> 831
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 34
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln
35 40 45
Gly Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr Tyr Thr Ser Ser Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr
100 105 110
Ser Lys Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
115 120 125
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
145 150 155 160
Val Lys Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu
165 170 175
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys
180 185 190
Arg Leu Glu Trp Val Ala Ser Ile Ser Ser Gly Gly Phe Thr Tyr Tyr
195 200 205
Pro Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg
210 215 220
Asn Ile Leu Tyr Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Asp Glu Val Arg Gly Tyr Leu Asp Val Trp
245 250 255
Gly Ala Gly Thr Thr Val Thr Val Ser Pro Arg Ala Ser Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val
305 310 315 320
Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe
325 330 335
Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp
340 345 350
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
355 360 365
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr
485 490 495
Asp Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp
500 505 510
Val Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp
515 520 525
Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu
530 535 540
Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe
545 550 555 560
Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser
565 570 575
Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn Glu
580 585 590
Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser
595 600 605
Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln
610 615 620
Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr
625 630 635 640
Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp
645 650 655
Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr
660 665 670
Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys
675 680 685
Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln
690 695 700
Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly
705 710 715 720
Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly
725 730 735
Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro Gln
740 745 750
Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys Leu
755 760 765
Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu Gly Ile Leu
770 775 780
Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser Tyr Ser Gln Lys
785 790 795 800
Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu Ala Val Leu Gly
805 810 815
Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp Ser Pro Ile
820 825 830
<210> 35
<211> 1233
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 35
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln
35 40 45
Gly Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr Tyr Thr Ser Ser Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr
100 105 110
Ser Lys Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
115 120 125
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
145 150 155 160
Val Lys Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu
165 170 175
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys
180 185 190
Arg Leu Glu Trp Val Ala Ser Ile Ser Ser Gly Gly Phe Thr Tyr Tyr
195 200 205
Pro Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg
210 215 220
Asn Ile Leu Tyr Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Asp Glu Val Arg Gly Tyr Leu Asp Val Trp
245 250 255
Gly Ala Gly Thr Thr Val Thr Val Ser Pro Arg Ala Ser Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val
305 310 315 320
Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe
325 330 335
Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp
340 345 350
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
355 360 365
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr
485 490 495
Asp Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp
500 505 510
Val Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp
515 520 525
Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu
530 535 540
Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe
545 550 555 560
Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser
565 570 575
Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn Glu
580 585 590
Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser
595 600 605
Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln
610 615 620
Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr
625 630 635 640
Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp
645 650 655
Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr
660 665 670
Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys
675 680 685
Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln
690 695 700
Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly
705 710 715 720
Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly
725 730 735
Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro Gln
740 745 750
Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys Leu
755 760 765
Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu Gly Ile Leu
770 775 780
Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser Tyr Ser Gln Lys
785 790 795 800
Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu Ala Val Leu Gly
805 810 815
Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp Ser Pro Thr Gly
820 825 830
Glu Gly Gly Gly Gly Gly Asp Leu Gly Gly Val Lys Leu Pro His Leu
835 840 845
Phe Gly Lys Arg Leu Val Glu Ala Arg Met Ala Ser Tyr Pro Cys His
850 855 860
Gln His Ala Ser Ala Phe Asp Gln Ala Ala Arg Ser Arg Gly His Ser
865 870 875 880
Asn Arg Arg Thr Ala Leu Arg Pro Arg Arg Gln Gln Glu Ala Thr Glu
885 890 895
Val Arg Leu Glu Gln Lys Met Pro Thr Leu Leu Arg Val Tyr Ile Asp
900 905 910
Gly Pro His Gly Met Gly Lys Thr Thr Thr Thr Gln Leu Leu Val Ala
915 920 925
Leu Gly Ser Arg Asp Asp Ile Val Tyr Val Pro Glu Pro Met Thr Tyr
930 935 940
Trp Gln Val Leu Gly Ala Ser Glu Thr Ile Ala Asn Ile Tyr Thr Thr
945 950 955 960
Gln His Arg Leu Asp Gln Gly Glu Ile Ser Ala Gly Asp Ala Ala Val
965 970 975
Val Met Thr Ser Ala Gln Ile Thr Met Gly Met Pro Tyr Ala Val Thr
980 985 990
Asp Ala Val Leu Ala Pro His Val Gly Gly Glu Ala Gly Ser Ser His
995 1000 1005
Ala Pro Pro Pro Ala Leu Thr Leu Leu Leu Asp Arg His Pro Ile
1010 1015 1020
Ala Val Met Leu Cys Tyr Pro Ala Ala Arg Tyr Leu Met Gly Ser
1025 1030 1035
Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala Leu Ile Pro Pro
1040 1045 1050
Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu Pro Glu Asp
1055 1060 1065
Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly Glu Arg
1070 1075 1080
Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly Leu
1085 1090 1095
Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp
1100 1105 1110
Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly
1115 1120 1125
Ala Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp
1130 1135 1140
Thr Leu Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn
1145 1150 1155
Gly Asp Leu Tyr Asn Val Phe Ala Trp Ala Leu Asp Val Leu Ala
1160 1165 1170
Lys Arg Leu Arg Pro Met His Val Phe Ile Leu Asp Tyr Asp Gln
1175 1180 1185
Ser Pro Ala Gly Cys Arg Asp Ala Leu Leu Gln Leu Thr Ser Gly
1190 1195 1200
Met Val Gln Thr His Val Thr Thr Pro Gly Ser Ile Pro Thr Ile
1205 1210 1215
Cys Asp Leu Ala Arg Thr Phe Ala Arg Glu Met Gly Glu Ala Asn
1220 1225 1230
<210> 36
<211> 1248
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 36
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser
20 25 30
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala
35 40 45
Ser Gln Ser Val Asp Tyr Glu Gly Asp Ser Phe Leu Asn Trp Tyr Gln
50 55 60
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Asn
65 70 75 80
Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
85 90 95
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
100 105 110
Tyr Tyr Cys Gln Gln Ser Asn Glu Asp Pro Leu Thr Phe Gly Gln Gly
115 120 125
Thr Lys Val Glu Ile Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
165 170 175
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
180 185 190
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
195 200 205
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
210 215 220
Lys Gly Arg Ala Thr Phe Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
225 230 235 240
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
245 250 255
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr Trp Gly Gln Gly Thr Leu
260 265 270
Val Thr Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro Ala Pro Arg
275 280 285
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
290 295 300
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
305 310 315 320
Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val Val Gly Gly Val
325 330 335
Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp
340 345 350
Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met
355 360 365
Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala
370 375 380
Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg
385 390 395 400
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
405 410 415
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
420 425 430
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
435 440 445
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
450 455 460
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
465 470 475 480
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
485 490 495
Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp Gly Ser Gly
500 505 510
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
515 520 525
Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr Ala Leu Cys
530 535 540
Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp Asn Asn Gly
545 550 555 560
Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser
565 570 575
Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr Leu Gly Ser
580 585 590
Thr Ser Leu His Pro Val Ser Gln His Gly Asn Glu Ala Thr Thr Asn
595 600 605
Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val Ile Thr Ser
610 615 620
Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr Ser Val Ile
625 630 635 640
Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro Glu Thr Thr
645 650 655
Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu Ser Thr Thr
660 665 670
Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr Ser Ser Ser
675 680 685
Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser Gly Ile Arg
690 695 700
Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn Lys Thr Ser
705 710 715 720
Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly Leu Ala Arg Val
725 730 735
Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly Ala Gln Val Cys
740 745 750
Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro Gln Cys Leu Leu Leu
755 760 765
Val Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys Leu Gln Leu Met Lys
770 775 780
Lys His Gln Ser Asp Leu Lys Lys Leu Gly Ile Leu Asp Phe Thr Glu
785 790 795 800
Gln Asp Val Ala Ser His Gln Ser Tyr Ser Gln Lys Thr Leu Ile Ala
805 810 815
Leu Val Thr Ser Gly Ala Leu Leu Ala Val Leu Gly Ile Thr Gly Tyr
820 825 830
Phe Leu Met Asn Arg Arg Ser Trp Ser Pro Thr Gly Glu Gly Gly Gly
835 840 845
Gly Gly Phe Lys Arg Asp Leu Gly Gly Val Lys Leu Pro His Leu Phe
850 855 860
Gly Lys Arg Leu Val Glu Ala Arg Met Ala Ser Tyr Pro Cys His Gln
865 870 875 880
His Ala Ser Ala Phe Asp Gln Ala Ala Arg Ser Arg Gly His Ser Asn
885 890 895
Arg Arg Thr Ala Leu Arg Pro Arg Arg Gln Gln Glu Ala Thr Glu Val
900 905 910
Arg Leu Glu Gln Lys Met Pro Thr Leu Leu Arg Val Tyr Ile Asp Gly
915 920 925
Pro His Gly Met Gly Lys Thr Thr Thr Thr Gln Leu Leu Val Ala Leu
930 935 940
Gly Ser Arg Asp Asp Ile Val Tyr Val Pro Glu Pro Met Thr Tyr Trp
945 950 955 960
Gln Val Leu Gly Ala Ser Glu Thr Ile Ala Asn Ile Tyr Thr Thr Gln
965 970 975
His Arg Leu Asp Gln Gly Glu Ile Ser Ala Gly Asp Ala Ala Val Val
980 985 990
Met Thr Ser Ala Gln Ile Thr Met Gly Met Pro Tyr Ala Val Thr Asp
995 1000 1005
Ala Val Leu Ala Pro His Val Gly Gly Glu Ala Gly Ser Ser His
1010 1015 1020
Ala Pro Pro Pro Ala Leu Thr Leu Leu Leu Asp Arg His Pro Ile
1025 1030 1035
Ala Val Met Leu Cys Tyr Pro Ala Ala Arg Tyr Leu Met Gly Ser
1040 1045 1050
Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala Leu Ile Pro Pro
1055 1060 1065
Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu Pro Glu Asp
1070 1075 1080
Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly Glu Arg
1085 1090 1095
Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly Leu
1100 1105 1110
Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp
1115 1120 1125
Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly
1130 1135 1140
Ala Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp
1145 1150 1155
Thr Leu Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn
1160 1165 1170
Gly Asp Leu Tyr Asn Val Phe Ala Trp Ala Leu Asp Val Leu Ala
1175 1180 1185
Lys Arg Leu Arg Pro Met His Val Phe Ile Leu Asp Tyr Asp Gln
1190 1195 1200
Ser Pro Ala Gly Cys Arg Asp Ala Leu Leu Gln Leu Thr Ser Gly
1205 1210 1215
Met Val Gln Thr His Val Thr Thr Pro Gly Ser Ile Pro Thr Ile
1220 1225 1230
Cys Asp Leu Ala Arg Thr Phe Ala Arg Glu Met Gly Glu Ala Asn
1235 1240 1245
<210> 37
<211> 841
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 37
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val
20 25 30
Pro Val Thr Pro Gly Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys
35 40 45
Thr Leu Leu His Ser Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln
50 55 60
Arg Pro Gly Gln Ser Pro Gln Val Leu Ile Tyr Arg Met Ser Asn Leu
65 70 75 80
Ala Ser Gly Val Pro Asn Arg Phe Ser Gly Ser Gly Ser Glu Thr Thr
85 90 95
Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr
100 105 110
Tyr Cys Met Gln His Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
115 120 125
Lys Leu Glu Ile Glu Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Glu Glu
145 150 155 160
Ser Gly Ala Glu Leu Val Arg Pro Gly Thr Ser Val Lys Leu Ser Cys
165 170 175
Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met His Trp Ile Lys
180 185 190
Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile Gly Arg Ile Asp Pro Tyr
195 200 205
Asp Ser Glu Thr His Tyr Asn Glu Lys Phe Lys Asp Lys Ala Ile Leu
210 215 220
Ser Val Asp Lys Ser Ser Ser Thr Ala Tyr Ile Gln Leu Ser Ser Leu
225 230 235 240
Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys Ser Arg Arg Asp Ala Lys
245 250 255
Tyr Asp Gly Tyr Ala Leu Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr
260 265 270
Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
275 280 285
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
290 295 300
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
305 310 315 320
Phe Ala Cys Asp Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala
325 330 335
Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg
340 345 350
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
355 360 365
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
370 375 380
Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala
385 390 395 400
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
405 410 415
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
420 425 430
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
435 440 445
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
450 455 460
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
465 470 475 480
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
485 490 495
His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp Gly Ser Gly Ala Thr
500 505 510
Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly
515 520 525
Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr Ala Leu Cys Leu Leu
530 535 540
Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp Asn Asn Gly Thr Ala
545 550 555 560
Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn
565 570 575
Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr Leu Gly Ser Thr Ser
580 585 590
Leu His Pro Val Ser Gln His Gly Asn Glu Ala Thr Thr Asn Ile Thr
595 600 605
Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val Ile Thr Ser Val Tyr
610 615 620
Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr Ser Val Ile Ser Thr
625 630 635 640
Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro Glu Thr Thr Leu Lys
645 650 655
Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu Ser Thr Thr Ser Thr
660 665 670
Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr Ser Ser Ser Pro Ile
675 680 685
Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser Gly Ile Arg Glu Val
690 695 700
Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn Lys Thr Ser Ser Cys
705 710 715 720
Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly Leu Ala Arg Val Leu Cys
725 730 735
Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly Ala Gln Val Cys Ser Leu
740 745 750
Leu Leu Ala Gln Ser Glu Val Arg Pro Gln Cys Leu Leu Leu Val Leu
755 760 765
Ala Asn Arg Thr Glu Ile Ser Ser Lys Leu Gln Leu Met Lys Lys His
770 775 780
Gln Ser Asp Leu Lys Lys Leu Gly Ile Leu Asp Phe Thr Glu Gln Asp
785 790 795 800
Val Ala Ser His Gln Ser Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val
805 810 815
Thr Ser Gly Ala Leu Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu
820 825 830
Met Asn Arg Arg Ser Trp Ser Pro Ile
835 840
<210> 38
<211> 842
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 38
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val
20 25 30
Pro Val Thr Pro Gly Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys
35 40 45
Thr Leu Leu His Ser Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln
50 55 60
Arg Pro Gly Gln Ser Pro Gln Val Leu Ile Tyr Arg Met Ser Asn Leu
65 70 75 80
Ala Ser Gly Val Pro Asn Arg Phe Ser Gly Ser Gly Ser Glu Thr Thr
85 90 95
Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr
100 105 110
Tyr Cys Met Gln His Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
115 120 125
Lys Leu Glu Ile Glu Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Glu Glu
145 150 155 160
Ser Gly Ala Glu Leu Val Arg Pro Gly Thr Ser Val Lys Leu Ser Cys
165 170 175
Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met His Trp Ile Lys
180 185 190
Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile Gly Arg Ile Asp Pro Tyr
195 200 205
Asp Ser Glu Thr His Tyr Asn Glu Lys Phe Lys Asp Lys Ala Ile Leu
210 215 220
Ser Val Asp Lys Ser Ser Ser Thr Ala Tyr Ile Gln Leu Ser Ser Leu
225 230 235 240
Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys Ser Arg Arg Asp Ala Lys
245 250 255
Tyr Asp Gly Tyr Ala Leu Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr
260 265 270
Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
275 280 285
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
290 295 300
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
305 310 315 320
Phe Ala Cys Asp Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala
325 330 335
Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Lys
340 345 350
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
355 360 365
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
370 375 380
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
385 390 395 400
Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu
405 410 415
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
420 425 430
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
435 440 445
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
450 455 460
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
465 470 475 480
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
485 490 495
Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp Gly Ser Gly Ala
500 505 510
Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro
515 520 525
Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr Ala Leu Cys Leu
530 535 540
Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp Asn Asn Gly Thr
545 550 555 560
Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr
565 570 575
Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr Leu Gly Ser Thr
580 585 590
Ser Leu His Pro Val Ser Gln His Gly Asn Glu Ala Thr Thr Asn Ile
595 600 605
Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val Ile Thr Ser Val
610 615 620
Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr Ser Val Ile Ser
625 630 635 640
Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro Glu Thr Thr Leu
645 650 655
Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu Ser Thr Thr Ser
660 665 670
Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr Ser Ser Ser Pro
675 680 685
Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser Gly Ile Arg Glu
690 695 700
Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn Lys Thr Ser Ser
705 710 715 720
Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly Leu Ala Arg Val Leu
725 730 735
Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly Ala Gln Val Cys Ser
740 745 750
Leu Leu Leu Ala Gln Ser Glu Val Arg Pro Gln Cys Leu Leu Leu Val
755 760 765
Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys Leu Gln Leu Met Lys Lys
770 775 780
His Gln Ser Asp Leu Lys Lys Leu Gly Ile Leu Asp Phe Thr Glu Gln
785 790 795 800
Asp Val Ala Ser His Gln Ser Tyr Ser Gln Lys Thr Leu Ile Ala Leu
805 810 815
Val Thr Ser Gly Ala Leu Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe
820 825 830
Leu Met Asn Arg Arg Ser Trp Ser Pro Ile
835 840
<210> 39
<211> 835
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 39
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Ala
20 25 30
Glu Leu Ala Arg Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser
35 40 45
Gly Tyr Thr Phe Thr Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro
50 55 60
Gly Gln Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr
65 70 75 80
Thr Asn Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp
85 90 95
Lys Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu
100 105 110
Asp Ser Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys
115 120 125
Leu Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser
165 170 175
Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser
180 185 190
Tyr Met Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp
195 200 205
Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala His Phe Arg
210 215 220
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Gly Met Glu
225 230 235 240
Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro
245 250 255
Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn Arg Pro Arg Ala
260 265 270
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp
305 310 315 320
Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val
325 330 335
Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu
340 345 350
Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr
355 360 365
Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr
370 375 380
Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg Arg Thr Asp Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
500 505 510
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met
515 520 525
Pro Arg Gly Trp Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly
530 535 540
Phe Met Ser Leu Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr
545 550 555 560
Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr
565 570 575
Thr Thr Pro Ser Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln
580 585 590
His Gly Asn Glu Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe
595 600 605
Thr Ser Thr Ser Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser
610 615 620
Val Gln Ser Gln Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala
625 630 635 640
Asn Val Ser Thr Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly
645 650 655
Asn Val Ser Asp Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro
660 665 670
Thr Lys Pro Tyr Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala
675 680 685
Glu Ile Lys Cys Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile
690 695 700
Cys Leu Glu Gln Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp
705 710 715 720
Arg Gly Glu Gly Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp
725 730 735
Ala Asp Ala Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu
740 745 750
Val Arg Pro Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile
755 760 765
Ser Ser Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys
770 775 780
Leu Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser
785 790 795 800
Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu
805 810 815
Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp
820 825 830
Ser Pro Ile
835
<210> 40
<211> 835
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 40
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Ala
20 25 30
Glu Leu Ala Arg Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser
35 40 45
Gly Tyr Thr Phe Thr Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro
50 55 60
Gly Gln Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr
65 70 75 80
Thr Asn Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp
85 90 95
Lys Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu
100 105 110
Asp Ser Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys
115 120 125
Leu Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser
165 170 175
Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser
180 185 190
Tyr Met Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp
195 200 205
Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala His Phe Arg
210 215 220
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Gly Met Glu
225 230 235 240
Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro
245 250 255
Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn Arg Pro Arg Ala
260 265 270
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp
305 310 315 320
Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val
325 330 335
Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu
340 345 350
Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr
355 360 365
Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr
370 375 380
Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg Arg Thr Asp Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
500 505 510
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met
515 520 525
Pro Arg Gly Trp Thr Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly
530 535 540
Phe Met Ser Leu Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr
545 550 555 560
Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr
565 570 575
Thr Thr Pro Ser Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln
580 585 590
His Gly Asn Glu Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe
595 600 605
Thr Ser Thr Ser Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser
610 615 620
Val Gln Ser Gln Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala
625 630 635 640
Asn Val Ser Thr Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly
645 650 655
Asn Val Ser Asp Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro
660 665 670
Thr Lys Pro Tyr Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala
675 680 685
Glu Ile Lys Cys Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile
690 695 700
Cys Leu Glu Gln Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp
705 710 715 720
Arg Gly Glu Gly Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp
725 730 735
Ala Asp Ala Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu
740 745 750
Val Arg Pro Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile
755 760 765
Ser Ser Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys
770 775 780
Leu Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser
785 790 795 800
Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu
805 810 815
Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp
820 825 830
Ser Pro Ile
835
<210> 41
<211> 1133
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 41
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met
20 25 30
Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser
35 40 45
Ser Val Ser Tyr Met Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro
50 55 60
Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala
65 70 75 80
His Phe Arg Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser
85 90 95
Gly Met Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser
100 105 110
Ser Asn Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn Arg
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Lys Asn Ile Thr Gln Ser Pro Ser Ser Met
145 150 155 160
Tyr Val Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln
165 170 175
Asp Ile Asn Ser Phe Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser
180 185 190
Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro
195 200 205
Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile
210 215 220
Ser Ser Leu Glu Tyr Glu Asp Met Glu Ile Tyr Tyr Cys Leu Gln Tyr
225 230 235 240
Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met Lys
245 250 255
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
275 280 285
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
290 295 300
Gly Gly Ser Glu Val Lys Leu Glu Glu Ser Gly Ala Glu Leu Val Lys
305 310 315 320
Pro Gly Ala Ser Val Lys Leu Ser Cys Arg Thr Ser Gly Phe Asn Leu
325 330 335
Lys Asp Thr Ile His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Lys
340 345 350
Trp Ile Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp Pro
355 360 365
Lys Phe Gln Asp Lys Ala Thr Val Thr Ala Asp Thr Ser Ser Asn Thr
370 375 380
Ala Tyr Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr
385 390 395 400
Tyr Cys Val Thr Tyr Ala Tyr Asp Gly Asn Trp Tyr Phe Asp Val Trp
405 410 415
Gly Ala Gly Thr Ala Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
420 425 430
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Ser
435 440 445
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
450 455 460
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
465 470 475 480
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
485 490 495
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
500 505 510
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
515 520 525
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
530 535 540
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
545 550 555 560
Thr Thr Leu Thr Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro Ala
565 570 575
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
580 585 590
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
595 600 605
Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val Val Gly
610 615 620
Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile
625 630 635 640
Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met
645 650 655
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
660 665 670
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe
675 680 685
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
690 695 700
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
705 710 715 720
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
725 730 735
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
740 745 750
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
755 760 765
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
770 775 780
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp Gly
785 790 795 800
Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu
805 810 815
Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr Ala
820 825 830
Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp Asn
835 840 845
Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn
850 855 860
Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr Leu
865 870 875 880
Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn Glu Ala Thr
885 890 895
Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val Ile
900 905 910
Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr Ser
915 920 925
Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro Glu
930 935 940
Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu Ser
945 950 955 960
Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr Ser
965 970 975
Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser Gly
980 985 990
Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn Lys
995 1000 1005
Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly Leu
1010 1015 1020
Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly
1025 1030 1035
Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro
1040 1045 1050
Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser
1055 1060 1065
Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu
1070 1075 1080
Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser
1085 1090 1095
Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu
1100 1105 1110
Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg
1115 1120 1125
Ser Trp Ser Pro Ile
1130
<210> 42
<211> 1134
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 42
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Trp Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Lys Asn Ile Thr Gln Ser Pro Ser Ser Met
145 150 155 160
Tyr Val Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln
165 170 175
Asp Ile Asn Ser Phe Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser
180 185 190
Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro
195 200 205
Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile
210 215 220
Ser Ser Leu Glu Tyr Glu Asp Met Glu Ile Tyr Tyr Cys Leu Gln Tyr
225 230 235 240
Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met Lys
245 250 255
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
275 280 285
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
290 295 300
Gly Gly Ser Glu Val Lys Leu Glu Glu Ser Gly Ala Glu Leu Val Lys
305 310 315 320
Pro Gly Ala Ser Val Lys Leu Ser Cys Arg Thr Ser Gly Phe Asn Leu
325 330 335
Lys Asp Thr Ile His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Lys
340 345 350
Trp Ile Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp Pro
355 360 365
Lys Phe Gln Asp Lys Ala Thr Val Thr Ala Asp Thr Ser Ser Asn Thr
370 375 380
Ala Tyr Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr
385 390 395 400
Tyr Cys Val Thr Tyr Ala Tyr Asp Gly Asn Trp Tyr Phe Asp Val Trp
405 410 415
Gly Ala Gly Thr Ala Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
420 425 430
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
435 440 445
Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
450 455 460
Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met
465 470 475 480
Asn Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Leu
485 490 495
Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp
500 505 510
Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln
515 520 525
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
530 535 540
Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln
545 550 555 560
Gly Thr Leu Val Thr Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro
565 570 575
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
580 585 590
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
595 600 605
Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val Val
610 615 620
Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile
625 630 635 640
Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr
645 650 655
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
660 665 670
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys
675 680 685
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
690 695 700
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
705 710 715 720
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
725 730 735
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
740 745 750
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
755 760 765
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
770 775 780
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp
785 790 795 800
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
805 810 815
Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr
820 825 830
Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp
835 840 845
Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser
850 855 860
Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr
865 870 875 880
Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn Glu Ala
885 890 895
Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val
900 905 910
Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr
915 920 925
Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro
930 935 940
Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu
945 950 955 960
Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr
965 970 975
Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser
980 985 990
Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn
995 1000 1005
Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly
1010 1015 1020
Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala
1025 1030 1035
Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg
1040 1045 1050
Pro Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser
1055 1060 1065
Ser Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys
1070 1075 1080
Leu Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln
1085 1090 1095
Ser Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala
1100 1105 1110
Leu Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg
1115 1120 1125
Arg Ser Trp Ser Pro Ile
1130
<210> 43
<211> 1134
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 43
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Lys Asn Ile Thr Gln Ser Pro Ser Ser
20 25 30
Met Tyr Val Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser
35 40 45
Gln Asp Ile Asn Ser Phe Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys
50 55 60
Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val
65 70 75 80
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr
85 90 95
Ile Ser Ser Leu Glu Tyr Glu Asp Met Glu Ile Tyr Tyr Cys Leu Gln
100 105 110
Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met
115 120 125
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
145 150 155 160
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
165 170 175
Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
180 185 190
Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val
195 200 205
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr
210 215 220
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
225 230 235 240
Gly Asn Thr Leu Pro Trp Thr Phe Gly Cys Gly Thr Lys Val Glu Ile
245 250 255
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
275 280 285
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
290 295 300
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
305 310 315 320
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe
325 330 335
Thr Gly Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
340 345 350
Glu Trp Val Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn
355 360 365
Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn
370 375 380
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
385 390 395 400
Tyr Tyr Cys Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe
405 410 415
Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
435 440 445
Ser Glu Val Lys Leu Glu Glu Ser Gly Ala Glu Leu Val Lys Pro Gly
450 455 460
Ala Ser Val Lys Leu Ser Cys Arg Thr Ser Gly Phe Asn Leu Lys Asp
465 470 475 480
Thr Ile His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Lys Trp Ile
485 490 495
Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp Pro Lys Phe
500 505 510
Gln Asp Lys Ala Thr Val Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
515 520 525
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
530 535 540
Val Thr Tyr Ala Tyr Asp Gly Asn Trp Tyr Phe Asp Val Trp Gly Ala
545 550 555 560
Gly Thr Ala Val Thr Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro
565 570 575
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
580 585 590
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
595 600 605
Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val Val
610 615 620
Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile
625 630 635 640
Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr
645 650 655
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
660 665 670
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys
675 680 685
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
690 695 700
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
705 710 715 720
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
725 730 735
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
740 745 750
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
755 760 765
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
770 775 780
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp
785 790 795 800
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
805 810 815
Glu Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr
820 825 830
Ala Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp
835 840 845
Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser
850 855 860
Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr
865 870 875 880
Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn Glu Ala
885 890 895
Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val
900 905 910
Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr
915 920 925
Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro
930 935 940
Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu
945 950 955 960
Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr
965 970 975
Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser
980 985 990
Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn
995 1000 1005
Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly
1010 1015 1020
Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala
1025 1030 1035
Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg
1040 1045 1050
Pro Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser
1055 1060 1065
Ser Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys
1070 1075 1080
Leu Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln
1085 1090 1095
Ser Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala
1100 1105 1110
Leu Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg
1115 1120 1125
Arg Ser Trp Ser Pro Ile
1130
<210> 44
<211> 1133
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 44
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Lys Asn Ile Thr Gln Ser Pro Ser Ser
20 25 30
Met Tyr Val Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser
35 40 45
Gln Asp Ile Asn Ser Phe Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys
50 55 60
Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val
65 70 75 80
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr
85 90 95
Ile Ser Ser Leu Glu Tyr Glu Asp Met Glu Ile Tyr Tyr Cys Leu Gln
100 105 110
Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met
115 120 125
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gln Ile Val Leu Thr Gln Ser Pro Ala Ile
145 150 155 160
Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser
165 170 175
Ser Ser Val Ser Tyr Met Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser
180 185 190
Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro
195 200 205
Ala His Phe Arg Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile
210 215 220
Ser Gly Met Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp
225 230 235 240
Ser Ser Asn Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn
245 250 255
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
275 280 285
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
290 295 300
Gly Gly Ser Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu
305 310 315 320
Ala Arg Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
325 330 335
Thr Phe Thr Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro Gly Gln
340 345 350
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn
355 360 365
Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser
370 375 380
Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser
385 390 395 400
Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp
405 410 415
Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly
420 425 430
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
435 440 445
Glu Val Lys Leu Glu Glu Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
450 455 460
Ser Val Lys Leu Ser Cys Arg Thr Ser Gly Phe Asn Leu Lys Asp Thr
465 470 475 480
Ile His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Lys Trp Ile Gly
485 490 495
Arg Ile Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp Pro Lys Phe Gln
500 505 510
Asp Lys Ala Thr Val Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr Leu
515 520 525
Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys Val
530 535 540
Thr Tyr Ala Tyr Asp Gly Asn Trp Tyr Phe Asp Val Trp Gly Ala Gly
545 550 555 560
Thr Ala Val Thr Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro Ala
565 570 575
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
580 585 590
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
595 600 605
Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Val Leu Val Val Val Gly
610 615 620
Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile
625 630 635 640
Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met
645 650 655
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
660 665 670
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe
675 680 685
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
690 695 700
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
705 710 715 720
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
725 730 735
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
740 745 750
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
755 760 765
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
770 775 780
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp Gly
785 790 795 800
Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu
805 810 815
Glu Asn Pro Gly Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr Ala
820 825 830
Leu Cys Leu Leu Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp Asn
835 840 845
Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn
850 855 860
Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr Leu
865 870 875 880
Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly Asn Glu Ala Thr
885 890 895
Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val Ile
900 905 910
Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr Ser
915 920 925
Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro Glu
930 935 940
Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu Ser
945 950 955 960
Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr Ser
965 970 975
Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser Gly
980 985 990
Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn Lys
995 1000 1005
Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly Leu
1010 1015 1020
Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly
1025 1030 1035
Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro
1040 1045 1050
Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser
1055 1060 1065
Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu
1070 1075 1080
Gly Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser
1085 1090 1095
Tyr Ser Gln Lys Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu
1100 1105 1110
Leu Ala Val Leu Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg
1115 1120 1125
Ser Trp Ser Pro Ile
1130
<210> 45
<211> 1129
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 45
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln
35 40 45
Gly Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr Tyr Thr Ser Ser Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr
100 105 110
Ser Lys Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
115 120 125
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Asp Ile Lys Asn Ile Thr Gln Ser Pro Ser Ser
145 150 155 160
Met Tyr Val Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser
165 170 175
Gln Asp Ile Asn Ser Phe Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys
180 185 190
Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val
195 200 205
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr
210 215 220
Ile Ser Ser Leu Glu Tyr Glu Asp Met Glu Ile Tyr Tyr Cys Leu Gln
225 230 235 240
Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met
245 250 255
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
260 265 270
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
275 280 285
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
290 295 300
Gly Gly Gly Ser Glu Val Lys Leu Glu Glu Ser Gly Ala Glu Leu Val
305 310 315 320
Lys Pro Gly Ala Ser Val Lys Leu Ser Cys Arg Thr Ser Gly Phe Asn
325 330 335
Leu Lys Asp Thr Ile His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu
340 345 350
Lys Trp Ile Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp
355 360 365
Pro Lys Phe Gln Asp Lys Ala Thr Val Thr Ala Asp Thr Ser Ser Asn
370 375 380
Thr Ala Tyr Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val
385 390 395 400
Tyr Tyr Cys Val Thr Tyr Ala Tyr Asp Gly Asn Trp Tyr Phe Asp Val
405 410 415
Trp Gly Ala Gly Thr Ala Val Thr Val Ser Ser Gly Gly Gly Gly Ser
420 425 430
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
435 440 445
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly Ser
450 455 460
Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu Thr Phe Ser Ser Tyr Ala
465 470 475 480
Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val Ala
485 490 495
Ser Ile Ser Ser Gly Gly Phe Thr Tyr Tyr Pro Asp Ser Val Lys Gly
500 505 510
Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu Gln
515 520 525
Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala Arg
530 535 540
Asp Glu Val Arg Gly Tyr Leu Asp Val Trp Gly Ala Gly Thr Thr Val
545 550 555 560
Thr Val Ser Pro Arg Ala Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
565 570 575
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
580 585 590
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
595 600 605
Phe Ala Cys Asp Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala
610 615 620
Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg
625 630 635 640
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
645 650 655
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
660 665 670
Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala
675 680 685
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
690 695 700
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
705 710 715 720
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
725 730 735
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
740 745 750
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
755 760 765
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
770 775 780
His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp Gly Ser Gly Ala Thr
785 790 795 800
Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly
805 810 815
Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr Ala Leu Cys Leu Leu
820 825 830
Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp Asn Asn Gly Thr Ala
835 840 845
Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn
850 855 860
Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr Leu Gly Ser Thr Ser
865 870 875 880
Leu His Pro Val Ser Gln His Gly Asn Glu Ala Thr Thr Asn Ile Thr
885 890 895
Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val Ile Thr Ser Val Tyr
900 905 910
Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr Ser Val Ile Ser Thr
915 920 925
Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro Glu Thr Thr Leu Lys
930 935 940
Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu Ser Thr Thr Ser Thr
945 950 955 960
Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr Ser Ser Ser Pro Ile
965 970 975
Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser Gly Ile Arg Glu Val
980 985 990
Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn Lys Thr Ser Ser Cys
995 1000 1005
Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly Leu Ala Arg Val Leu
1010 1015 1020
Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly Ala Gln Val Cys
1025 1030 1035
Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro Gln Cys Leu Leu
1040 1045 1050
Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys Leu Gln Leu
1055 1060 1065
Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu Gly Ile Leu Asp
1070 1075 1080
Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser Tyr Ser Gln Lys
1085 1090 1095
Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu Ala Val Leu
1100 1105 1110
Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp Ser Pro
1115 1120 1125
Ile
<210> 46
<211> 1129
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 46
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Lys Asn Ile Thr Gln Ser Pro Ser Ser
20 25 30
Met Tyr Val Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser
35 40 45
Gln Asp Ile Asn Ser Phe Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys
50 55 60
Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val
65 70 75 80
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr
85 90 95
Ile Ser Ser Leu Glu Tyr Glu Asp Met Glu Ile Tyr Tyr Cys Leu Gln
100 105 110
Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met
115 120 125
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Thr Thr Ser Ser
145 150 155 160
Leu Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Ser Ala Ser
165 170 175
Gln Gly Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly
180 185 190
Thr Val Lys Leu Leu Ile Tyr Tyr Thr Ser Ser Leu His Ser Gly Val
195 200 205
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr
210 215 220
Ile Ser Asn Leu Glu Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln
225 230 235 240
Tyr Ser Lys Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
245 250 255
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
260 265 270
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
275 280 285
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
290 295 300
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
305 310 315 320
Lys Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Leu Thr
325 330 335
Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg
340 345 350
Leu Glu Trp Val Ala Ser Ile Ser Ser Gly Gly Phe Thr Tyr Tyr Pro
355 360 365
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn
370 375 380
Ile Leu Tyr Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met
385 390 395 400
Tyr Tyr Cys Ala Arg Asp Glu Val Arg Gly Tyr Leu Asp Val Trp Gly
405 410 415
Ala Gly Thr Thr Val Thr Val Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Lys Leu
435 440 445
Glu Glu Ser Gly Ala Glu Leu Val Lys Pro Gly Ala Ser Val Lys Leu
450 455 460
Ser Cys Arg Thr Ser Gly Phe Asn Leu Lys Asp Thr Ile His Trp Val
465 470 475 480
Lys Gln Arg Pro Glu Gln Gly Leu Lys Trp Ile Gly Arg Ile Asp Pro
485 490 495
Ala Asn Gly Asn Thr Lys Tyr Asp Pro Lys Phe Gln Asp Lys Ala Thr
500 505 510
Val Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr Leu Gln Leu Ser Ser
515 520 525
Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys Val Thr Tyr Ala Tyr
530 535 540
Asp Gly Asn Trp Tyr Phe Asp Val Trp Gly Ala Gly Thr Ala Val Thr
545 550 555 560
Val Ser Ser Pro Arg Ala Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
565 570 575
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
580 585 590
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
595 600 605
Phe Ala Cys Asp Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala
610 615 620
Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg
625 630 635 640
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
645 650 655
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
660 665 670
Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala
675 680 685
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
690 695 700
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
705 710 715 720
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
725 730 735
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
740 745 750
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
755 760 765
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
770 775 780
His Met Gln Ala Leu Pro Pro Arg Arg Thr Asp Gly Ser Gly Ala Thr
785 790 795 800
Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly
805 810 815
Pro Val Ser Glu Ala Met Pro Arg Gly Trp Thr Ala Leu Cys Leu Leu
820 825 830
Ser Leu Leu Pro Ser Gly Phe Met Ser Leu Asp Asn Asn Gly Thr Ala
835 840 845
Thr Pro Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn
850 855 860
Val Ser Tyr Gln Glu Thr Thr Thr Pro Ser Thr Leu Gly Ser Thr Ser
865 870 875 880
Leu His Pro Val Ser Gln His Gly Asn Glu Ala Thr Thr Asn Ile Thr
885 890 895
Glu Thr Thr Val Lys Phe Thr Ser Thr Ser Val Ile Thr Ser Val Tyr
900 905 910
Gly Asn Thr Asn Ser Ser Val Gln Ser Gln Thr Ser Val Ile Ser Thr
915 920 925
Val Phe Thr Thr Pro Ala Asn Val Ser Thr Pro Glu Thr Thr Leu Lys
930 935 940
Pro Ser Leu Ser Pro Gly Asn Val Ser Asp Leu Ser Thr Thr Ser Thr
945 950 955 960
Ser Leu Ala Thr Ser Pro Thr Lys Pro Tyr Thr Ser Ser Ser Pro Ile
965 970 975
Leu Ser Asp Ile Lys Ala Glu Ile Lys Cys Ser Gly Ile Arg Glu Val
980 985 990
Lys Leu Thr Gln Gly Ile Cys Leu Glu Gln Asn Lys Thr Ser Ser Cys
995 1000 1005
Ala Glu Phe Lys Lys Asp Arg Gly Glu Gly Leu Ala Arg Val Leu
1010 1015 1020
Cys Gly Glu Glu Gln Ala Asp Ala Asp Ala Gly Ala Gln Val Cys
1025 1030 1035
Ser Leu Leu Leu Ala Gln Ser Glu Val Arg Pro Gln Cys Leu Leu
1040 1045 1050
Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser Lys Leu Gln Leu
1055 1060 1065
Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu Gly Ile Leu Asp
1070 1075 1080
Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser Tyr Ser Gln Lys
1085 1090 1095
Thr Leu Ile Ala Leu Val Thr Ser Gly Ala Leu Leu Ala Val Leu
1100 1105 1110
Gly Ile Thr Gly Tyr Phe Leu Met Asn Arg Arg Ser Trp Ser Pro
1115 1120 1125
Ile
<210> 47
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 47
aucacggagg ucaaugucua guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 48
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 48
guagacauug accuccguga guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 49
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 49
aucacggagg ucaaugucua guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 50
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 50
gagaaucaaa aucggugaau guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 51
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 51
gaccaaucug acaugcugca guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 52
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 52
acagcugaca ggcucgacac guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 53
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 53
gagaaucaaa aucggugaau guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 54
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 54
agggcauguc aauauuacug guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 55
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 55
cguuccaacu cgaagugcca guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 56
<211> 100
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 56
cguuccaacu cgaagugcca guuuuagagc uagaaauagc aaguuaaaau aaggcuaguc
60
cguuaucaac uugaaaaagu ggcaccgagu cggugcuuuu
100
<210> 57
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 57
caaagagatt acgaatgcct ngg
23
<210> 58
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 58
caaggcattc gtaatctctt ngg
23
<210> 59
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 59
cttgtagata tcctgatcat ngg
23
<210> 60
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 60
cttgggtcag gacatcaact ngg
23
<210> 61
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 61
cgatgatcag gatatctaca ngg
23
<210> 62
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 62
ttacgaatgc cttggaaacc ngg
23
<210> 63
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 63
tacgaatgcc ttggaaacct ngg
23
<210> 64
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 64
acgaatgcct tggaaacctg ngg
23
<210> 65
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 65
tgatattgac gatataaaat ngg
23
<210> 66
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 66
atgatattga cgatataaaa ngg
23
<210> 67
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 67
gcatctgaag accgatgatc ngg
23
<210> 68
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 68
aacctggggt gccttgggtc ngg
23
<210> 69
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 69
ttggaaacct ggggtgcctt ngg
23
<210> 70
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 70
gtatcaatat atgatacaaa ngg
23
<210> 71
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 71
caaggcaccc caggtttcca ngg
23
<210> 72
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 72
cttggaaacc tggggtgcct ngg
23
<210> 73
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 73
tcatcactca tttgaaaact ngg
23
<210> 74
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 74
caagttgatg tcctgaccca ngg
23
<210> 75
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 75
gtcctgaccc aaggcacccc ngg
23
<210> 76
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 76
atatttgatt tgaagattca ngg
23
<210> 77
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 77
tacaaaagga aaaaatgtgt ngg
23
<210> 78
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 78
acatataagc tatttaaaaa ngg
23
<210> 79
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 79
aaaagagaaa gagactttca ngg
23
<210> 80
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 80
cttgatacag gtttaattcg ngg
23
<210> 81
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 81
acagctgaca ggctcgacac ngg
23
<210> 82
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 82
gatgtttccc atcttgatac ngg
23
<210> 83
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 83
gtcgagcctg tcagctgtcc ngg
23
<210> 84
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 84
caaaattcaa gtgcacagca ngg
23
<210> 85
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 85
gaattttgca ctcaggctgg ngg
23
<210> 86
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 86
gaattaaacc tgtatcaaga ngg
23
<210> 87
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 87
aattaaacct gtatcaagat ngg
23
<210> 88
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 88
agttccattc attacctcac ngg
23
<210> 89
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 89
agagggtcat cacacacaag ngg
23
<210> 90
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 90
atacaagtcc aggagatctt ngg
23
<210> 91
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 91
tcttgataca ggtttaattc ngg
23
<210> 92
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 92
ctgacctgtg aggtaatgaa ngg
23
<210> 93
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 93
acatctaaaa ctttctcaga ngg
23
<210> 94
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 94
gcaaaattca agtgcacagc ngg
23
<210> 95
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 95
ggttgtgttg atacaagtcc ngg
23
<210> 96
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 96
atcttgatac aggtttaatt ngg
23
<210> 97
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 97
attcattacc tcacaggtca ngg
23
<210> 98
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 98
aacatctaaa actttctcag ngg
23
<210> 99
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 99
agcagggaac aaagtcagca ngg
23
<210> 100
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 100
caacacaacc ctgacctgtg ngg
23
<210> 101
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 101
cttgaatttt gcactcaggc ngg
23
<210> 102
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 102
cattcattac ctcacaggtc ngg
23
<210> 103
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 103
tgcacttgaa ttttgcactc ngg
23
<210> 104
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 104
tctcaaaacc aaagatctcc ngg
23
<210> 105
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 105
ttgacatgcc ctcagtatcc ngg
23
<210> 106
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 106
ctggattacc tcttgccctc ngg
23
<210> 107
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 107
gagatggaga ctttatatgc ngg
23
<210> 108
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 108
agatggagac tttatatgct ngg
23
<210> 109
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 109
agggcatgtc aatattactg ngg
23
<210> 110
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 110
gatggagact ttatatgctg ngg
23
<210> 111
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 111
tattatgtct gctaccccag ngg
23
<210> 112
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 112
tgccatagta tttcagatcc ngg
23
<210> 113
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 113
agataaaagt tcgcatcttc ngg
23
<210> 114
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 114
ctgaaaattc cttcagtgac ngg
23
<210> 115
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 115
ctgagggcaa gaggtaatcc ngg
23
<210> 116
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 116
tttcagatcc aggatactga ngg
23
<210> 117
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 117
tatctctacc tgagggcaag ngg
23
<210> 118
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 118
tgaggatcac ctgtcactga ngg
23
<210> 119
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 119
aatcatctgc tacggacaac ngg
23
<210> 120
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 120
gcagactttt gacgcttgac ngg
23
<210> 121
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 121
ccgttccaac tcgaagtgcc ngg
23
<210> 122
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 122
cgttccaact cgaagtgcca ngg
23
<210> 123
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 123
ctggcacttc gagttggaac ngg
23
<210> 124
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 124
gtctgccagc ggctgaactg ngg
23
<210> 125
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 125
atcatctgct acggacaact ngg
23
<210> 126
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 126
agacttttga cgcttgactg ngg
23
<210> 127
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 127
cagacttttg acgcttgact ngg
23
<210> 128
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 128
cctggcactt cgagttggaa ngg
23
<210> 129
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 129
gcaccccaca gttcagccgc ngg
23
<210> 130
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 130
ccttgaggta gacctccagc ngg
23
<210> 131
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 131
aggtctacct caaggacgga ngg
23
<210> 132
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 132
tggaacgggt gagccttgcc ngg
23
<210> 133
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 133
tgtggggtgc ccttaagcct ngg
23
<210> 134
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 134
aagcgtcaaa agtctgccag ngg
23
<210> 135
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 135
tagcagatga ttgagctctg ngg
23
<210> 136
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 136
gattgagctc tgaggtgtgt ngg
23
<210> 137
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 137
ggggccggag ctccaagcag ngg
23
<210> 138
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 138
ggtgtgtagg tgacaaggaa ngg
23
<210> 139
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 139
ccggagctcc aagcagtggg ngg
23
<210> 140
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 140
ggtagacctc cagctggccc ngg
23
<210> 141
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 141
ctcgaagtgc cagggccagc ngg
23
<210> 142
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 142
ctggccctgg cacttcgagt ngg
23
<210> 143
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 143
tctgccagcg gctgaactgt ngg
23
<210> 144
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 144
ccatgtgcca tccgtccttg ngg
23
<210> 145
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 145
ccagctggag gtctacctca ngg
23
<210> 146
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 146
tctgaggtgt gtaggtgaca ngg
23
<210> 147
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 147
aggaaggggc caaggcttaa ngg
23
<210> 148
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 148
cagagctcaa tcatctgcta ngg
23
<210> 149
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 149
gggccggagc tccaagcagt ngg
23
<210> 150
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 150
cctcccactg cttggagctc ngg
23
<210> 151
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 151
tggagctccg gccccagctc ngg
23
<210> 152
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 152
gtgtgtaggt gacaaggaag ngg
23
<210> 153
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 153
atggtttgca gccagagctg ngg
23
<210> 154
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 154
ctggaggtct acctcaagga ngg
23
<210> 155
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 155
ctgccagcgg ctgaactgtg ngg
23
<210> 156
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 156
aatgacatgt gtcactctct ngg
23
<210> 157
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 157
acatggtttg cagccagagc ngg
23
<210> 158
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 158
catggtttgc agccagagct ngg
23
<210> 159
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 159
gacacatgtc atttctgctg ngg
23
<210> 160
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 160
actggggtcc tcccactgct ngg
23
<210> 161
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 161
cctcaaggac ggatggcaca ngg
23
<210> 162
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 162
aggtgtgtag gtgacaagga ngg
23
<210> 163
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 163
aaggaagggg ccaaggctta ngg
23
<210> 164
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 164
gaagtgccag ggccagctgg ngg
23
<210> 165
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 165
tttgcagcca gagctggggc ngg
23
<210> 166
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 166
aaatgacatg tgtcactctc ngg
23
<210> 167
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 167
aggtgacaag gaaggggcca ngg
23
<210> 168
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 168
atttctgctg tggctgcagt ngg
23
<210> 169
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 169
gctgtggctg cagttggaga ngg
23
<210> 170
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 170
ggcgggggcc ttgtcgttgg ngg
23
<210> 171
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 171
ctctggagtt gtggtgggcg ngg
23
<210> 172
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 172
tctggagttg tggtgggcgg ngg
23
<210> 173
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 173
cgttggaggt gttgtcttct ngg
23
<210> 174
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 174
agacaacacc tccaacgaca ngg
23
<210> 175
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 175
gtgggcgggg gccttgtcgt ngg
23
<210> 176
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 176
tcgttggagg tgttgtcttc ngg
23
<210> 177
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 177
accacaactc cagagcccac ngg
23
<210> 178
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 178
gctctggagt tgtggtgggc ngg
23
<210> 179
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 179
gtgggctctg gagttgtggt ngg
23
<210> 180
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 180
tgtgggctct ggagttgtgg ngg
23
<210> 181
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 181
gttggaggtg ttgtcttctg ngg
23
<210> 182
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 182
ggctctggag ttgtggtggg ngg
23
<210> 183
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 183
catagctgat ggtacccccc ngg
23
<210> 184
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 184
cggccagcac tgtgccggcg ngg
23
<210> 185
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 185
caagaactcg gccacttttc ngg
23
<210> 186
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 186
ggtgttcccg tggctcccct ngg
23
<210> 187
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 187
ccagcactgt gccggcgtgg ngg
23
<210> 188
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 188
ggcaagggct ggtgttcccg ngg
23
<210> 189
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 189
ggcgtggtgg agttctacag ngg
23
<210> 190
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 190
ccaccacgcc ggcacagtgc ngg
23
<210> 191
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 191
ggagttctac agcggcagcc ngg
23
<210> 192
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 192
gttctacagc ggcagcctgg ngg
23
<210> 193
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 193
accagccctt gccaatccaa ngg
23
<210> 194
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 194
agttctacag cggcagcctg ngg
23
<210> 195
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 195
ccaggtcctg ggtcttgtcc ngg
23
<210> 196
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 196
tggtgttccc gtggctcccc ngg
23
<210> 197
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 197
gagttctaca gcggcagcct ngg
23
<210> 198
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 198
gaactcaagc tgtacctccc ngg
23
<210> 199
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 199
aagaactcgg ccacttttct ngg
23
<210> 200
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 200
tccattggat tggcaagggc ngg
23
<210> 201
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 201
ttctacagcg gcagcctggg ngg
23
<210> 202
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 202
agaactcggc cacttttctg ngg
23
<210> 203
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 203
gcttcaagaa ggagccacac ngg
23
<210> 204
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 204
gatcttccat tggattggca ngg
23
<210> 205
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 205
gctgtagaac tccaccacgc ngg
23
<210> 206
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 206
gtcctgggcc tcatagctga ngg
23
<210> 207
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 207
taccatcagc tatgaggccc ngg
23
<210> 208
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 208
ggggggtacc atcagctatg ngg
23
<210> 209
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 209
cctgaagcaa tgctccaggg ngg
23
<210> 210
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 210
ttttcctgaa gcaatgctcc ngg
23
<210> 211
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 211
ctctggcaga tgcttcaaga ngg
23
<210> 212
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 212
agaggaagtt ctccaggtcc ngg
23
<210> 213
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 213
tctggcggcc agcactgtgc ngg
23
<210> 214
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 214
ttgagttctg gatcttccat ngg
23
<210> 215
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 215
ttctggatct tccattggat ngg
23
<210> 216
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 216
atcttccatt ggattggcaa ngg
23
<210> 217
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 217
tcaagaagga gccacactgg ngg
23
<210> 218
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 218
gggaggtaca gcttgagttc ngg
23
<210> 219
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 219
cccgtggctc ccctgggtct ngg
23
<210> 220
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 220
ccaggacaag acccaggacc ngg
23
<210> 221
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 221
ctctgcaaca acctccagtg ngg
23
<210> 222
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 222
tgttgcagag gaagttctcc ngg
23
<210> 223
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 223
caggtcctgg gtcttgtcct ngg
23
<210> 224
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 224
tgaggcccag gacaagaccc ngg
23
<210> 225
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 225
ctgtgccacc agctgcagcc ngg
23
<210> 226
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 226
tgtgccacca gctgcagcct ngg
23
<210> 227
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 227
catctgccag agactgaggc ngg
23
<210> 228
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 228
ctgcagctgg tggcacagtc ngg
23
<210> 229
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 229
cacactggag gttgttgcag ngg
23
<210> 230
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 230
cagctggtgg cacagtctgg ngg
23
<210> 231
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 231
agcaaaggag ggcaagaact ngg
23
<210> 232
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 232
gaggaagttc tccaggtcct ngg
23
<210> 233
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 233
gccaccagct gcagcctggg ngg
23
<210> 234
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 234
gcaggcagag cccaagaccc ngg
23
<210> 235
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 235
caggcagagc ccaagaccca ngg
23
<210> 236
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 236
tcctcccagg ctgcagctgg ngg
23
<210> 237
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 237
gctctgcctg cctcagtctc ngg
23
<210> 238
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 238
cctccctgga gcattgcttc ngg
23
<210> 239
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 239
tttcctgaag caatgctcca ngg
23
<210> 240
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 240
ccgtggctcc cctgggtctt ngg
23
<210> 241
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 241
aaaatcaagc cccagaaaag ngg
23
<210> 242
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 242
gaagcatctg ccagagactg ngg
23
<210> 243
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 243
gaagcatctg ccagagactg ngg
23
<210> 244
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 244
aggcagagcc caagacccag ngg
23
<210> 245
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 245
cccaagaccc aggggagcca ngg
23
<210> 246
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 246
tactcaggtt caggagacgc ngg
23
<210> 247
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 247
tcaggagacg ccgggcctcc ngg
23
<210> 248
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 248
actcaggttc aggagacgcc ngg
23
<210> 249
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 249
cagtgtctct actcaggttc ngg
23
<210> 250
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 250
atgctcccag ggctgcgtgc ngg
23
<210> 251
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 251
gagacgccgg gcctcctgga ngg
23
<210> 252
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 252
cagcagcagt gtctctactc ngg
23
<210> 253
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 253
gatggcattc acatgctccc ngg
23
<210> 254
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 254
ggagcatgtg aatgccatcc ngg
23
<210> 255
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 255
tagagacact gctgctgaga ngg
23
<210> 256
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 256
gcatgtgaat gccatccagg ngg
23
<210> 257
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 257
atggcattca catgctccca ngg
23
<210> 258
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 258
tgaatgccat ccaggaggcc ngg
23
<210> 259
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 259
tgctcccagg gctgcgtgct ngg
23
<210> 260
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 260
cagccccagc acgcagccct ngg
23
<210> 261
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 261
gctcccaggg ctgcgtgctg ngg
23
<210> 262
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 262
ccttggattt cagcggcaca ngg
23
<210> 263
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 263
ccttgtgccg ctgaaatcca ngg
23
<210> 264
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 264
tgaacctggc taccaggacc ngg
23
<210> 265
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 265
agggccaggt cctggtagcc ngg
23
<210> 266
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 266
ctcagctgaa cctggctacc ngg
23
<210> 267
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 267
agaaaaaaca ggagagtgca ngg
23
<210> 268
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 268
gcacaaggct cagctgaacc ngg
23
<210> 269
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 269
tggcttgcct tggatttcag ngg
23
<210> 270
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 270
aaacaggaga gtgcagggcc ngg
23
<210> 271
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 271
gagagtgcag ggccaggtcc ngg
23
<210> 272
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 272
ggatgaagag aagaaaaaac ngg
23
<210> 273
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 273
aagaaaaaac aggagagtgc ngg
23
<210> 274
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 274
ccgggtgaca gtgcttcggc ngg
23
<210> 275
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 275
acacaaagct ggcgatgcct ngg
23
<210> 276
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 276
ccctcagtcc ttggatagtg ngg
23
<210> 277
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 277
gtgcggcaac ctacatgatg ngg
23
<210> 278
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 278
ctgtgcggca acctacatga ngg
23
<210> 279
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 279
ggcccagcct gctgtggtac ngg
23
<210> 280
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 280
gttcacttga tttccactgg ngg
23
<210> 281
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 281
caactcattc cccatcatgt ngg
23
<210> 282
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 282
ccgcacagac ttcagtcacc ngg
23
<210> 283
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 283
tgtgcggcaa cctacatgat ngg
23
<210> 284
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 284
cctcactatc caaggactga ngg
23
<210> 285
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 285
cggacctcag tggctttgcc ngg
23
<210> 286
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 286
gaggttcact tgatttccac ngg
23
<210> 287
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 287
ccaggtgact gaagtctgtg ngg
23
<210> 288
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 288
actggaggtg cccgtgcaga ngg
23
<210> 289
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 289
caagtgaacc tcactatcca ngg
23
<210> 290
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 290
gtggtactgg ccagcagccg ngg
23
<210> 291
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 291
aggtccgggt gacagtgctt ngg
23
<210> 292
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 292
atctgcacgg gcacctccag ngg
23
<210> 293
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 293
ccgtgcagat ggaatcatct ngg
23
<210> 294
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 294
ctagatgatt ccatctgcac ngg
23
<210> 295
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 295
acctcactat ccaaggactg ngg
23
<210> 296
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 296
cctgccgaag cactgtcacc ngg
23
<210> 297
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 297
tggccagtac cacagcaggc ngg
23
<210> 298
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 298
atctccaggc aaagccactg ngg
23
<210> 299
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 299
gcacgtggcc cagcctgctg ngg
23
<210> 300
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 300
gtgtgtgagt atgcatctcc ngg
23
<210> 301
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 301
cactgtcacc cggacctcag ngg
23
<210> 302
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 302
gctggcgatg cctcggctgc ngg
23
<210> 303
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 303
ctgctggcca gtaccacagc ngg
23
<210> 304
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 304
aggcaaagcc actgaggtcc ngg
23
<210> 305
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 305
gcagatggaa tcatctagga ngg
23
<210> 306
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 306
cctagatgat tccatctgca ngg
23
<210> 307
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 307
ggccagtacc acagcaggct ngg
23
<210> 308
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 308
tgcatactca cacacaaagc ngg
23
<210> 309
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 309
gcttcggcag gctgacagcc ngg
23
<210> 310
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 310
caggcaaagc cactgaggtc ngg
23
<210> 311
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 311
tgtagcaccg cccagacgac ngg
23
<210> 312
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 312
ggcgccctgg ccagtcgtct ngg
23
<210> 313
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 313
cgtctgggcg gtgctacaac ngg
23
<210> 314
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 314
aggcgccctg gccagtcgtc ngg
23
<210> 315
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 315
caccgcccag acgactggcc ngg
23
<210> 316
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 316
accgcccaga cgactggcca ngg
23
<210> 317
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 317
gggcggtgct acaactgggc ngg
23
<210> 318
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 318
gtctgggcgg tgctacaact ngg
23
<210> 319
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 319
cgactggcca gggcgcctgt ngg
23
<210> 320
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 320
cggtgctaca actgggctgg ngg
23
<210> 321
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 321
tggcggccag gatggttctt ngg
23
<210> 322
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 322
acgactggcc agggcgcctg ngg
23
<210> 323
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 323
ctacaactgg gctggcggcc ngg
23
<210> 324
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 324
gccctggcca gtcgtctggg ngg
23
<210> 325
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 325
tgcagatccc acaggcgccc ngg
23
<210> 326
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 326
aactgggctg gcggccagga ngg
23
<210> 327
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 327
cggagagctt cgtgctaaac ngg
23
<210> 328
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 328
gcgtgacttc cacatgagcg ngg
23
<210> 329
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 329
atgtggaagt cacgcccgtt ngg
23
<210> 330
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 330
gccctgctcg tggtgaccga ngg
23
<210> 331
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 331
cacgaagctc tccgatgtgt ngg
23
<210> 332
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 332
cctgctcgtg gtgaccgaag ngg
23
<210> 333
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 333
tgacacggaa gcggcagtcc ngg
23
<210> 334
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 334
ccccttcggt caccacgagc ngg
23
<210> 335
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 335
cagcaaccag acggacaagc ngg
23
<210> 336
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 336
gcagttgtgt gacacggaag ngg
23
<210> 337
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 337
cccttcggtc accacgagca ngg
23
<210> 338
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 338
ccgggctggc tgcggtcctc ngg
23
<210> 339
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 339
aggcggccag cttgtccgtc ngg
23
<210> 340
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 340
cagcttgtcc gtctggttgc ngg
23
<210> 341
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 341
cggtcaccac gagcagggct ngg
23
<210> 342
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 342
gtgtcacaca actgcccaac ngg
23
<210> 343
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 343
ctgcagcttc tccaacacat ngg
23
<210> 344
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 344
caagctggcc gccttccccg ngg
23
<210> 345
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 345
cgtgtcacac aactgcccaa ngg
23
<210> 346
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 346
cgttgggcag ttgtgtgaca ngg
23
<210> 347
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 347
gcttgtccgt ctggttgctg ngg
23
<210> 348
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 348
cggaagcggc agtcctggcc ngg
23
<210> 349
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 349
cgatgtgttg gagaagctgc ngg
23
<210> 350
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 350
catgtggaag tcacgcccgt ngg
23
<210> 351
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 351
ccctgctcgt ggtgaccgaa ngg
23
<210> 352
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 352
cgggctggct gcggtcctcg ngg
23
<210> 353
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 353
agcttgtccg tctggttgct ngg
23
<210> 354
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 354
gaaggtggcg ttgtcccctt ngg
23
<210> 355
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 355
acttccacat gagcgtggtc ngg
23
<210> 356
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 356
gccgggctgg ctgcggtcct ngg
23
<210> 357
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 357
tcggtcacca cgagcagggc ngg
23
<210> 358
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 358
tctggttgct ggggctcatg ngg
23
<210> 359
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 359
acggaagcgg cagtcctggc ngg
23
<210> 360
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 360
cccgaggacc gcagccagcc ngg
23
<210> 361
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 361
ctggctgcgg tcctcgggga ngg
23
<210> 362
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 362
catgagcccc agcaaccaga ngg
23
<210> 363
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 363
agtcctggcc gggctggctg ngg
23
<210> 364
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 364
gggggttcca gggcctgtct ngg
23
<210> 365
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 365
ggtcaccacg agcagggctg ngg
23
<210> 366
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 366
gctgcggtcc tcggggaagg ngg
23
<210> 367
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 367
ggaccgcagc cagcccggcc ngg
23
<210> 368
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 368
gagaaggtgg gggggttcca ngg
23
<210> 369
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 369
ggagaaggtg ggggggttcc ngg
23
<210> 370
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 370
agcggcagtc ctggccgggc ngg
23
<210> 371
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 371
ggggttccag ggcctgtctg ngg
23
<210> 372
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 372
cttctcccca gccctgctcg ngg
23
<210> 373
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 373
gttggagaag ctgcaggtga ngg
23
<210> 374
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 374
ggggggttcc agggcctgtc ngg
23
<210> 375
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 375
ggagaagctg caggtgaagg ngg
23
<210> 376
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 376
cacgagcagg gctggggaga ngg
23
<210> 377
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 377
gcagggctgg ggagaaggtg ngg
23
<210> 378
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 378
cagggctggg gagaaggtgg ngg
23
<210> 379
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 379
gagcagggct ggggagaagg ngg
23
<210> 380
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 380
agcagggctg gggagaaggt ngg
23
<210> 381
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 381
agggctgggg agaaggtggg ngg
23
<210> 382
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 382
gggctgggga gaaggtgggg ngg
23
<210> 383
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 383
agaagtggaa tacagagcgg ngg
23
<210> 384
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 384
aatgtggcaa cgtggtgctc ngg
23
<210> 385
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 385
ctaaatgggg atttccgcaa ngg
23
<210> 386
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 386
catccagata ctggctaaat ngg
23
<210> 387
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 387
cagacgggca cgaggttccc ngg
23
<210> 388
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 388
gcggctgggg tgtagaagca ngg
23
<210> 389
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 389
gaacctcgtg cccgtctgct ngg
23
<210> 390
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 390
gacgggcacg aggttccctg ngg
23
<210> 391
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 391
atccccattt agccagtatc ngg
23
<210> 392
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 392
gtggaataca gagcggaggt ngg
23
<210> 393
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 393
agacgggcac gaggttccct ngg
23
<210> 394
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 394
ggaacctcgt gcccgtctgc ngg
23
<210> 395
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 395
gagtcacatt ctctatggtc ngg
23
<210> 396
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 396
atgtgactct agcagacagt ngg
23
<210> 397
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 397
ttttcatcat tcattatgcc ngg
23
<210> 398
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 398
aatgtgactc tagcagacag ngg
23
<210> 399
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 399
atccagatac tggctaaatg ngg
23
<210> 400
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 400
tgctgccgga tccaaatccc ngg
23
<210> 401
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 401
tctacacccc agccgcccca ngg
23
<210> 402
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 402
ttatgcctgg gatttggatc ngg
23
<210> 403
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 403
cgctctgtat tccacttctg ngg
23
<210> 404
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 404
gaggttccct ggggcggctg ngg
23
<210> 405
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 405
tgccccagca gacgggcacg ngg
23
<210> 406
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 406
acagtgggat ctactgctgc ngg
23
<210> 407
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 407
tgtgtttgaa tgtggcaacg ngg
23
<210> 408
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 408
tgaaaaattt aacctgaagt ngg
23
<210> 409
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 409
acatccagat actggctaaa ngg
23
<210> 410
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 410
atgaaaggga tgtgaattat ngg
23
<210> 411
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 411
tggtgctcag gactgatgaa ngg
23
<210> 412
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 412
ggtgtagaag cagggcagat ngg
23
<210> 413
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 413
acgttgccac attcaaacac ngg
23
<210> 414
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 414
acgaggttcc ctggggcggc ngg
23
<210> 415
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 415
gcctgtcctg tgtttgaatg ngg
23
<210> 416
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 416
gtgcccgtct gctggggcaa ngg
23
<210> 417
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 417
aacctcgtgc ccgtctgctg ngg
23
<210> 418
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 418
ggcggctggg gtgtagaagc ngg
23
<210> 419
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 419
agtcacattc tctatggtca ngg
23
<210> 420
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 420
ctggtttgat gaccaacttc ngg
23
<210> 421
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 421
cattcattat gcctgggatt ngg
23
<210> 422
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 422
tgctagagtc acattctcta ngg
23
<210> 423
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 423
gggcacgagg ttccctgggg ngg
23
<210> 424
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 424
ggctcctttg ccccagcaga ngg
23
<210> 425
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 425
attattggac atccagatac ngg
23
<210> 426
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 426
tttcatcatt cattatgcct ngg
23
<210> 427
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 427
ttctacaccc cagccgcccc ngg
23
<210> 428
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 428
tcagggacac atctcctttg ngg
23
<210> 429
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 429
gctcctttgc cccagcagac ngg
23
<210> 430
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 430
ctcagaagtg gaatacagag ngg
23
<210> 431
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 431
cgaggttccc tggggcggct ngg
23
<210> 432
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 432
gccacattca aacacaggac ngg
23
<210> 433
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 433
ggtgctcagg actgatgaaa ngg
23
<210> 434
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 434
aggtcacccc tgcaccgact ngg
23
<210> 435
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 435
ctctctgccg agtcggtgca ngg
23
<210> 436
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 436
tctctctgcc gagtcggtgc ngg
23
<210> 437
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 437
ccaaggatgc ttaccaccag ngg
23
<210> 438
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 438
tctctgccga gtcggtgcag ngg
23
<210> 439
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 439
cccctggtgg taagcatcct ngg
23
<210> 440
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 440
tccaaggatg cttaccacca ngg
23
<210> 441
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 441
ggtggtaagc atccttggaa ngg
23
<210> 442
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 442
gtgaagtctc tctgccgagt ngg
23
<210> 443
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 443
atgcttacca ccaggggaca ngg
23
<210> 444
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 444
ttccaaggat gcttaccacc ngg
23
<210> 445
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 445
agtcggtgca ggggtgacct ngg
23
<210> 446
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой a, c, g или t
<400> 446
acttcactgc agcctttcca ngg
23
<210> 447
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<220>
<221> MISC_FEATURE
<223> Эта последовательность может охватывать 2-6 "Gly Gly Gly Gly
Ser" повторяющихся единиц
<400> 447
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25 30
<210> 448
<211> 50
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<220>
<221> MISC_FEATURE
<223> Эта последовательность может охватывать 1-3 "Gly Gly Gly Gly
Ser" повторяющихся единиц, 1 "Gly Gly Gly Gly Pro" повторяющуюся
единицу и 1 "Gly Gly Gly Gly Cys" повторяющуюся единицу.
<220>
<221> MISC_FEATURE
<223> Эта последовательность может охватывать 1-3 "Gly Gly Gly Gly
Ser" повторяющихся единиц, 1 "Gly Gly Gly Gly Pro" единицу и 1 "Gly
Gly Gly Gly Cys" единицу.
<400> 448
Gly Gly Gly Gly Ser Gly Gly Gly Gly Cys Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Pro Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Cys Gly Gly Gly
35 40 45
Gly Ser
50
<210> 449
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<220>
<221> MISC_FEATURE
<223> Эта последовательность может охватывать 3-4 "Gly Gly Gly Gly
Ser" повторяющихся единиц
<400> 449
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 450
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 450
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 451
<211> 50
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 451
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
35 40 45
Gly Ser
50
<210> 452
<211> 45
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 452
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Pro Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
35 40 45
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Т-КЛЕТКИ С КОСТИМУЛИРУЮЩИМ ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ, НАЦЕЛЕННЫЕ НА IL13Rα2 | 2015 |
|
RU2749922C2 |
| ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К МЕЗОТЕЛИНУ И ИММУННЫЕ ЭФФЕКТОРНЫЕ КЛЕТКИ, НАЦЕЛЕННЫЕ НА МЕЗОТЕЛИН | 2016 |
|
RU2748281C2 |
| Химерные антигенные рецепторы, нацеливающиеся на CD70 | 2019 |
|
RU2801824C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) С АНТИГЕНСВЯЗЫВАЮЩИМИ ДОМЕНАМИ К КОНСТАНТНОЙ ОБЛАСТИ β Т-КЛЕТОЧНОГО РЕЦЕПТОРА | 2015 |
|
RU2744046C2 |
| Т-КЛЕТКИ, МОДИФИЦИРОВАННЫЕ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА, НАЦЕЛЕННЫМ НА CS1 | 2015 |
|
RU2727451C2 |
| АНТИ-HLA-A2 АНТИТЕЛА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2782276C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2829097C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2017 |
|
RU2826270C2 |
| АНТИТЕЛО ПРОТИВ ГЛИПИКАНА-3 И ЕГО ПРИМЕНЕНИЕ | 2016 |
|
RU2744245C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
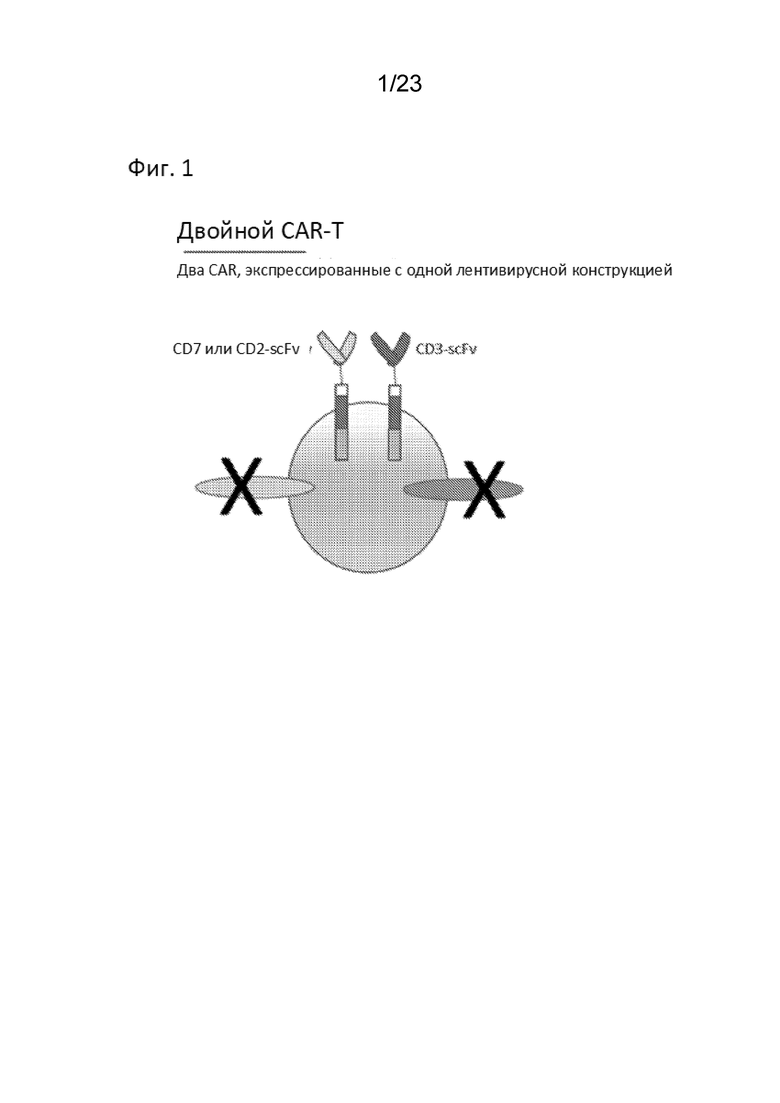
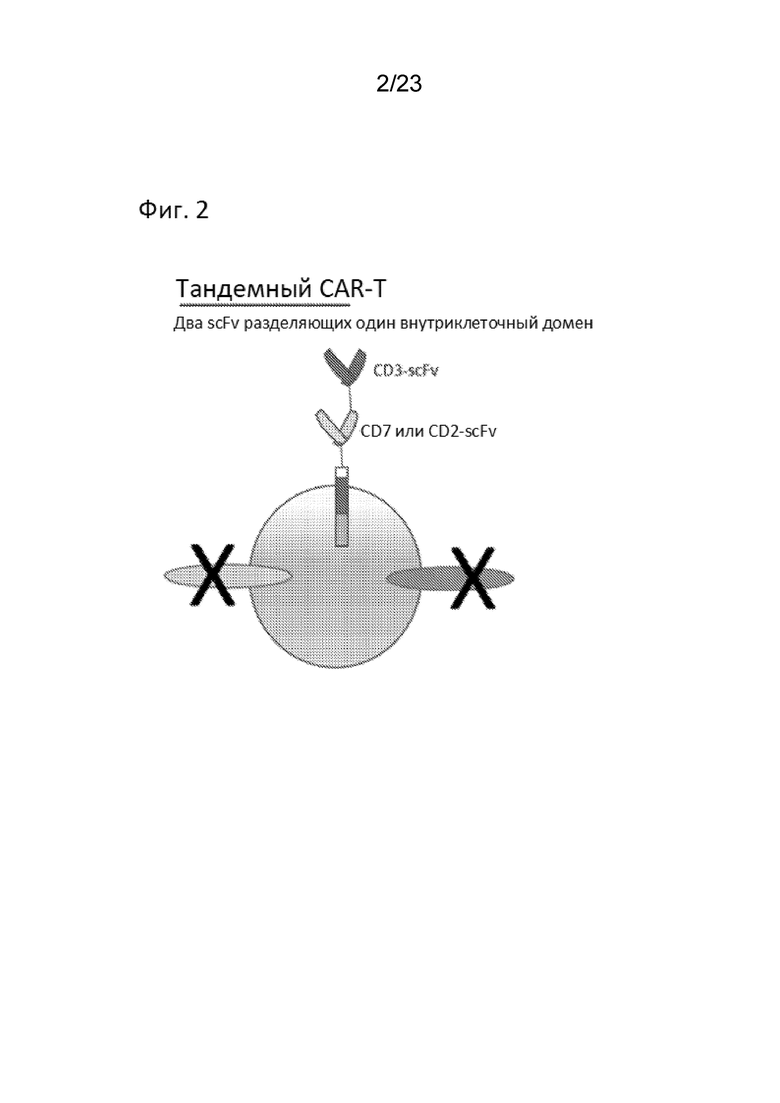

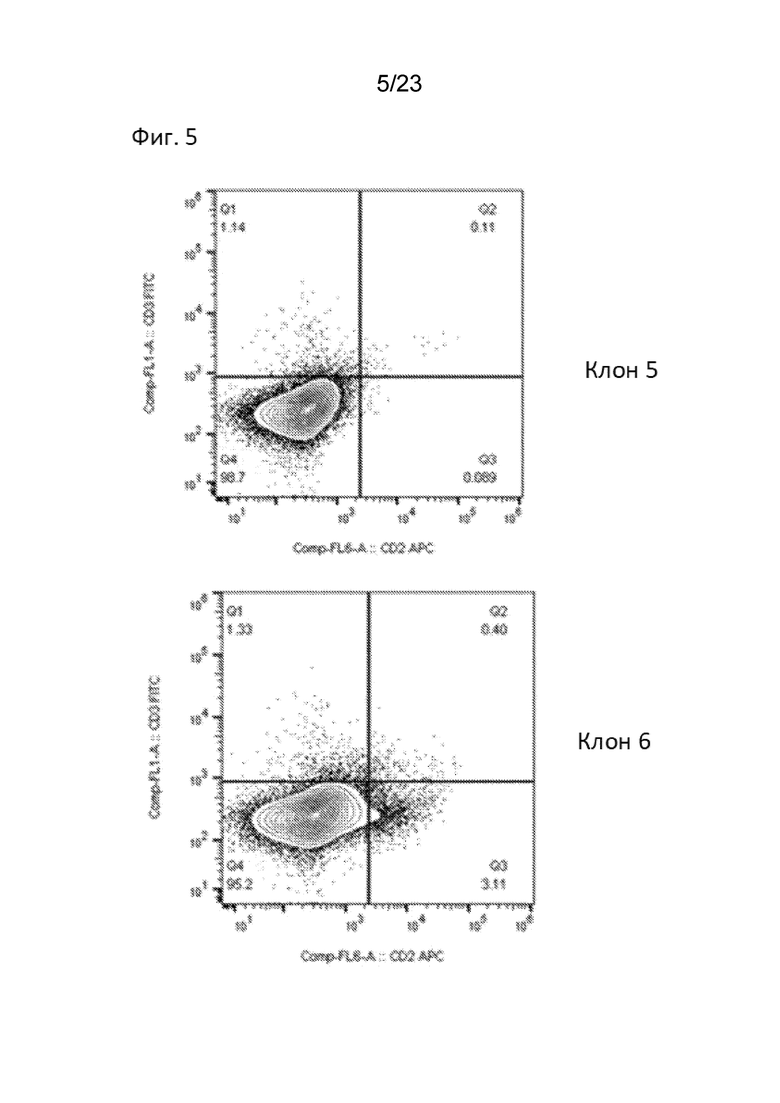
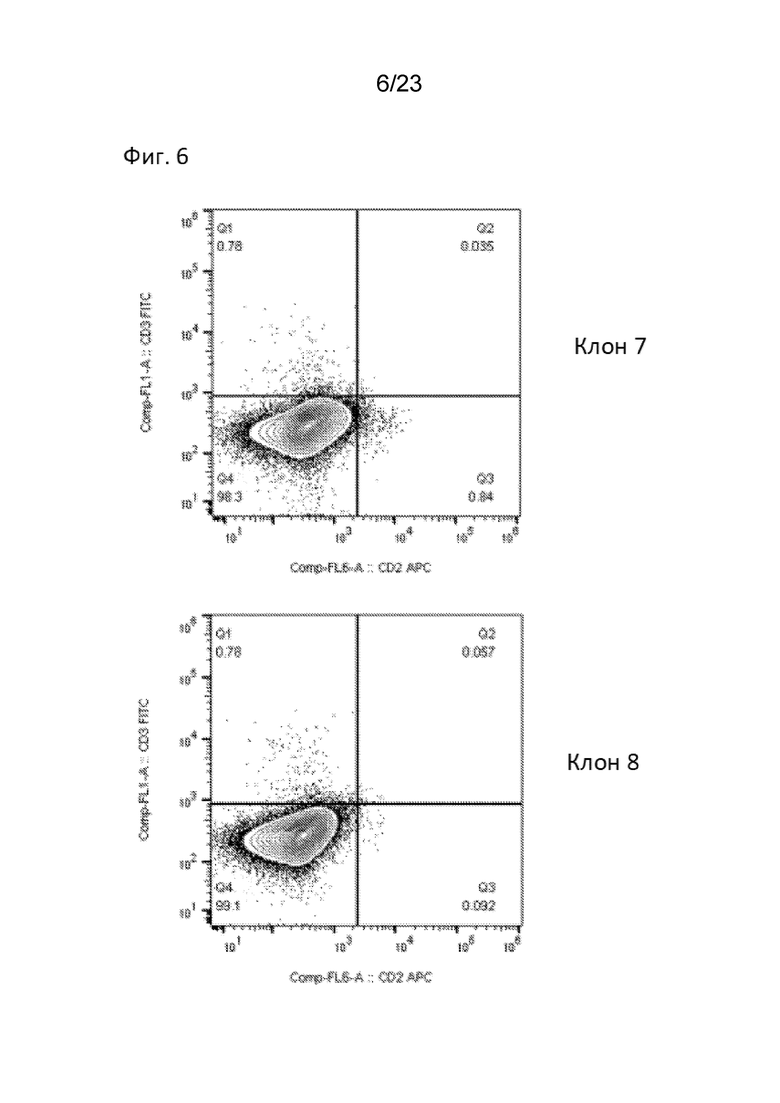
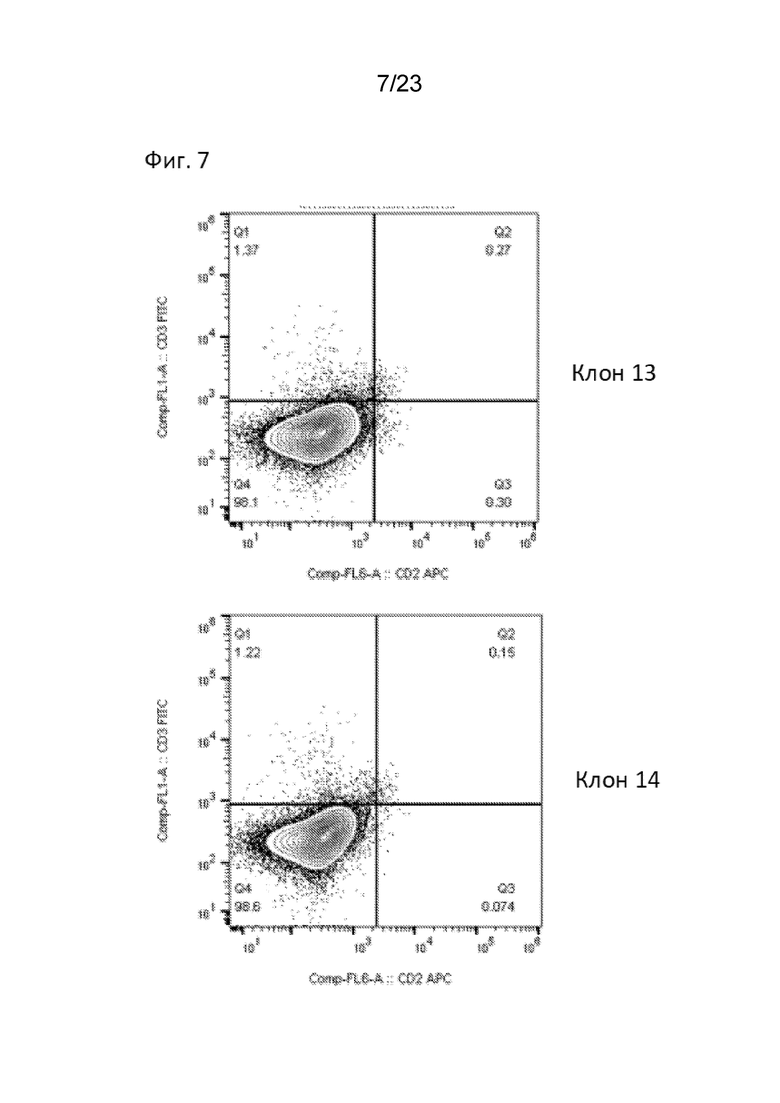
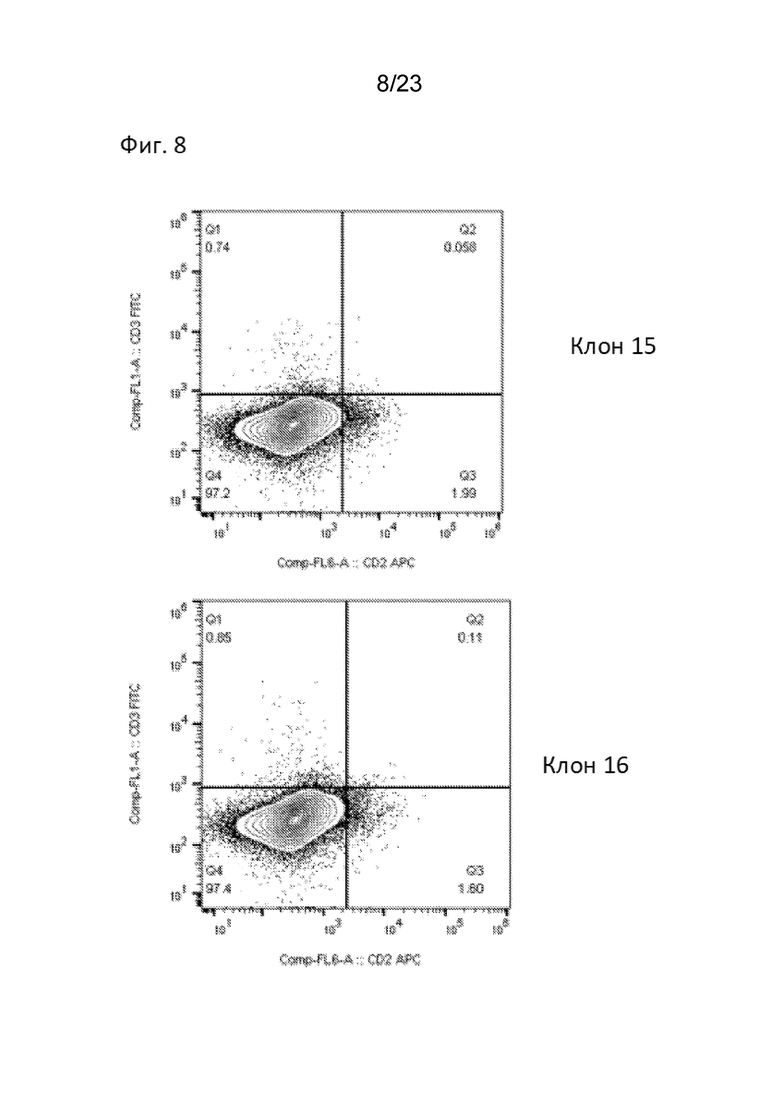
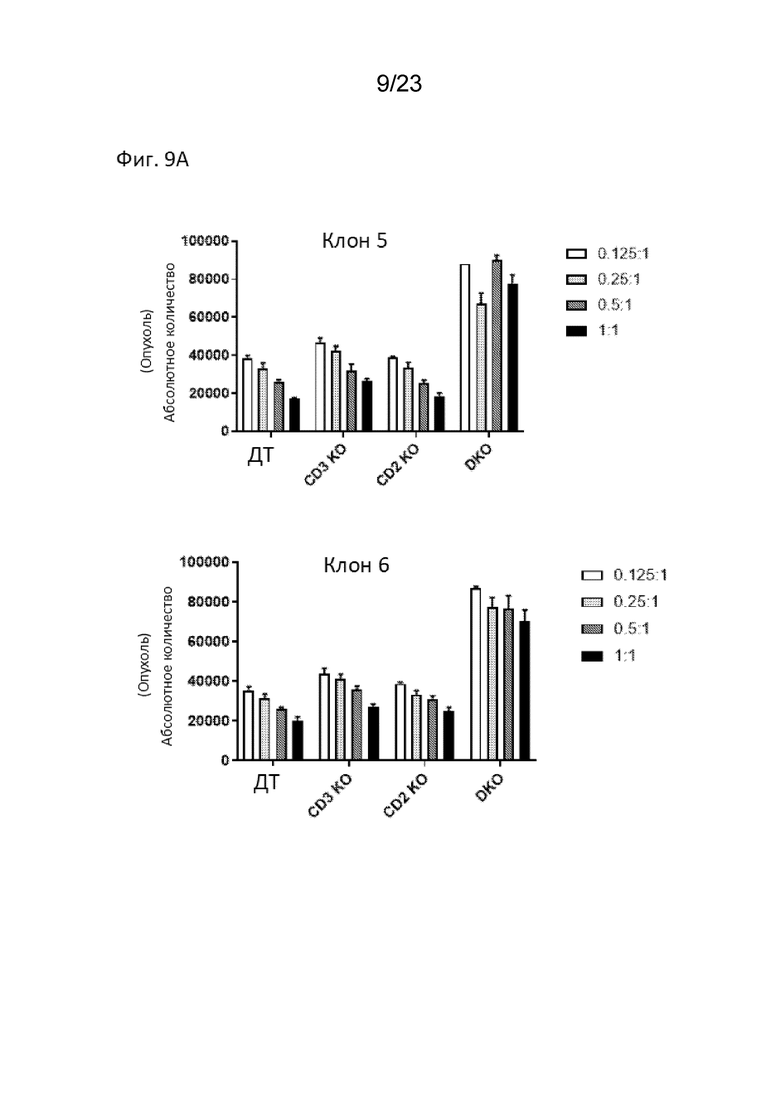
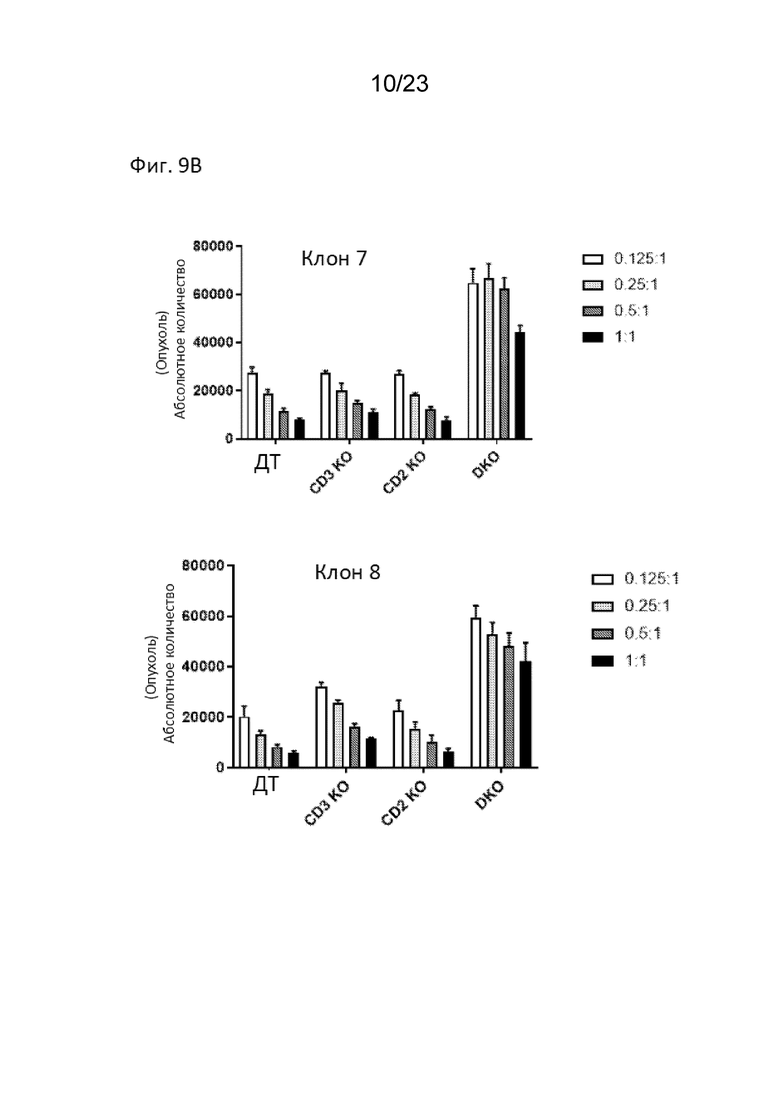
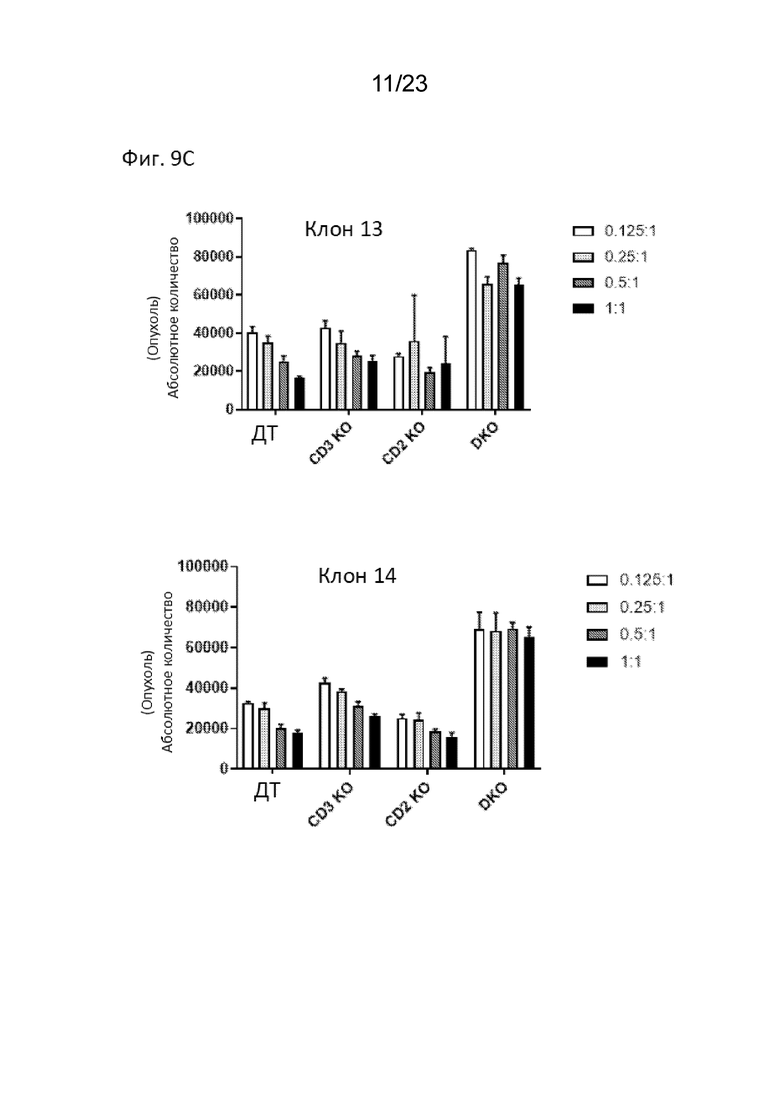
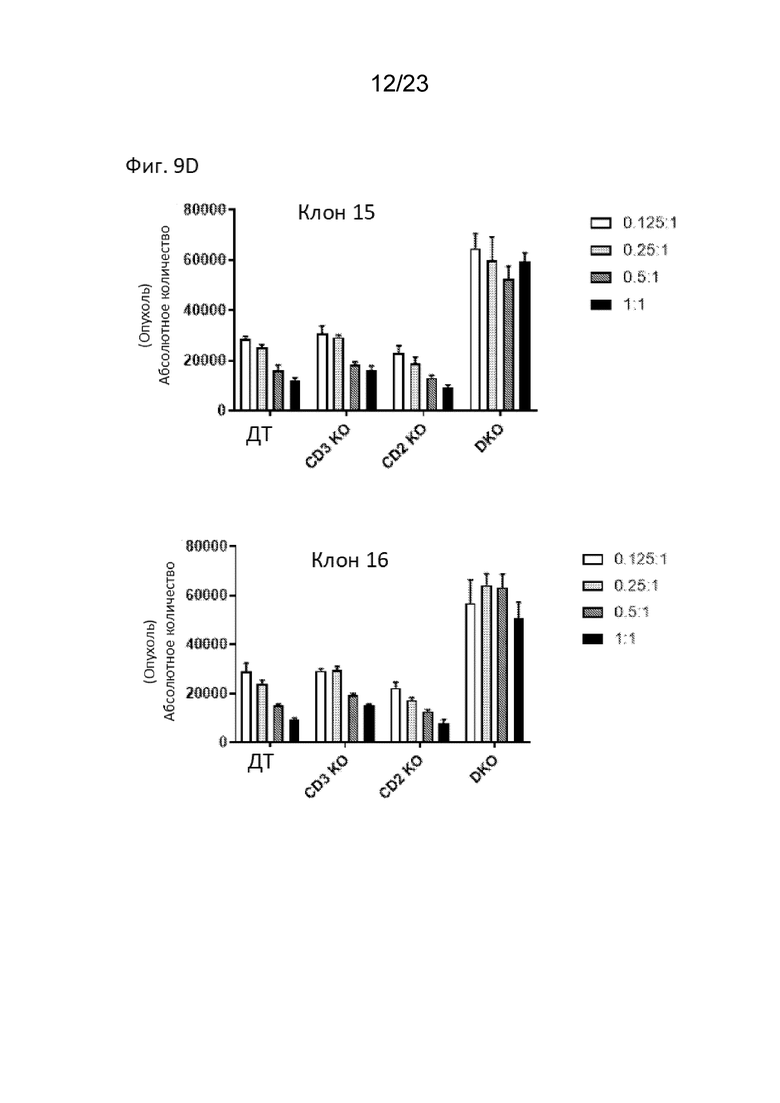

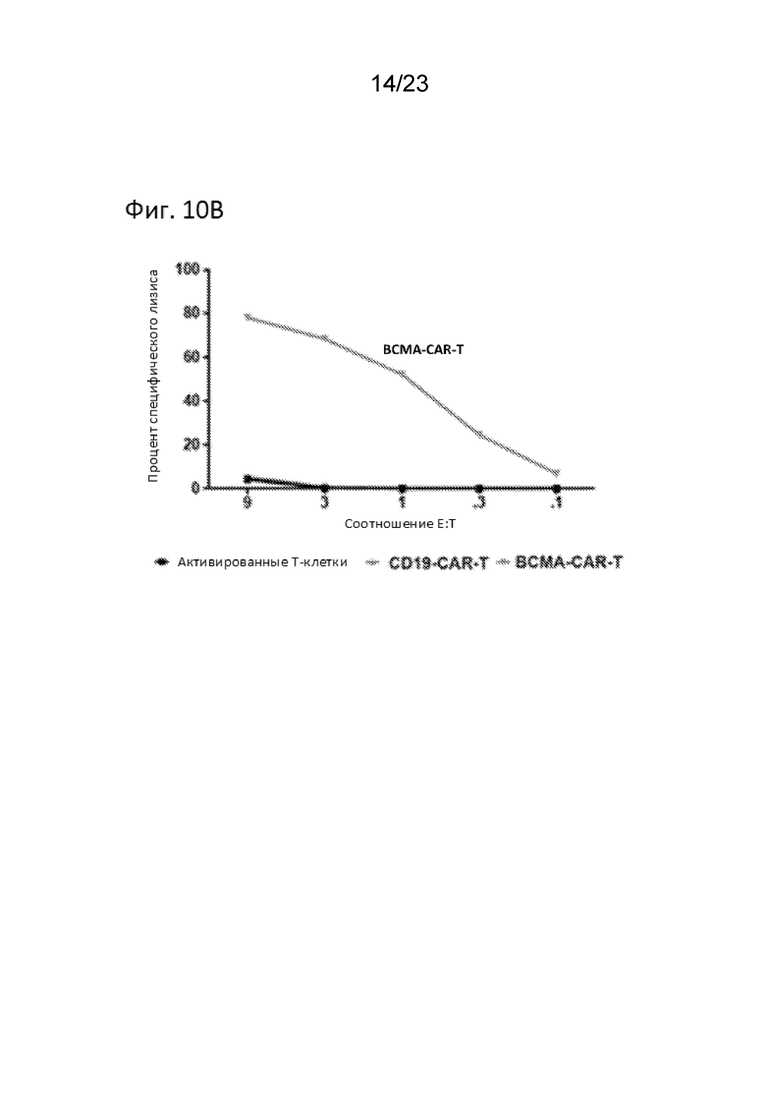
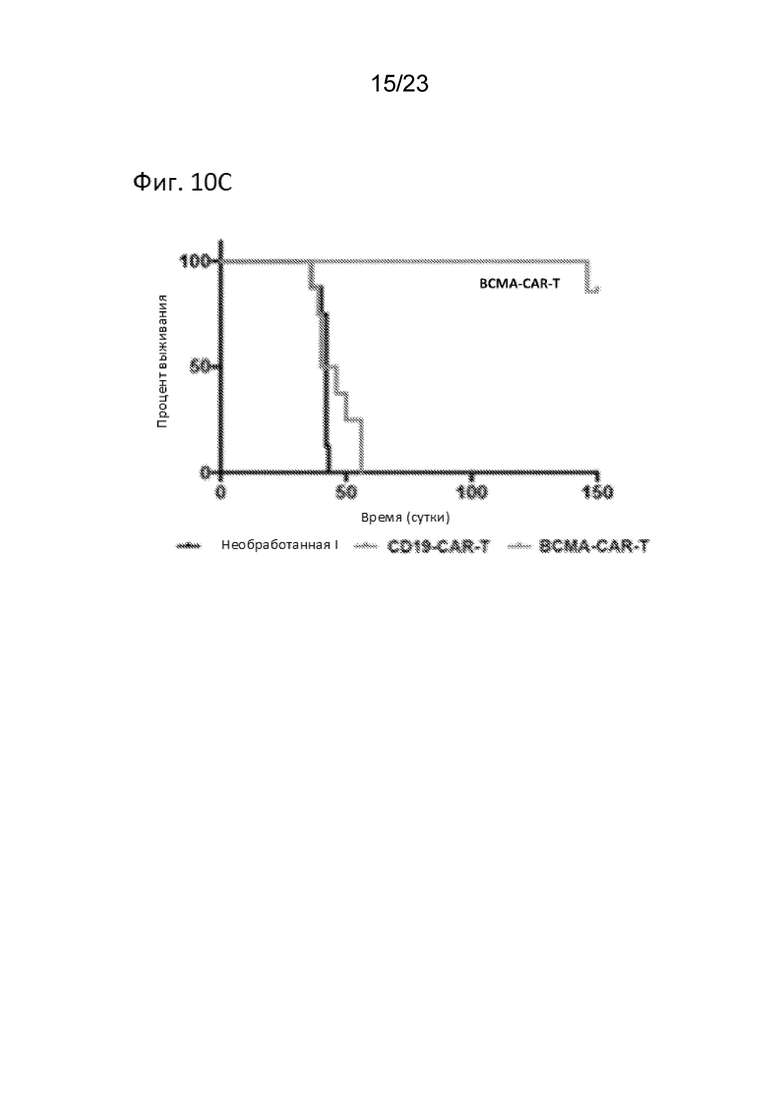
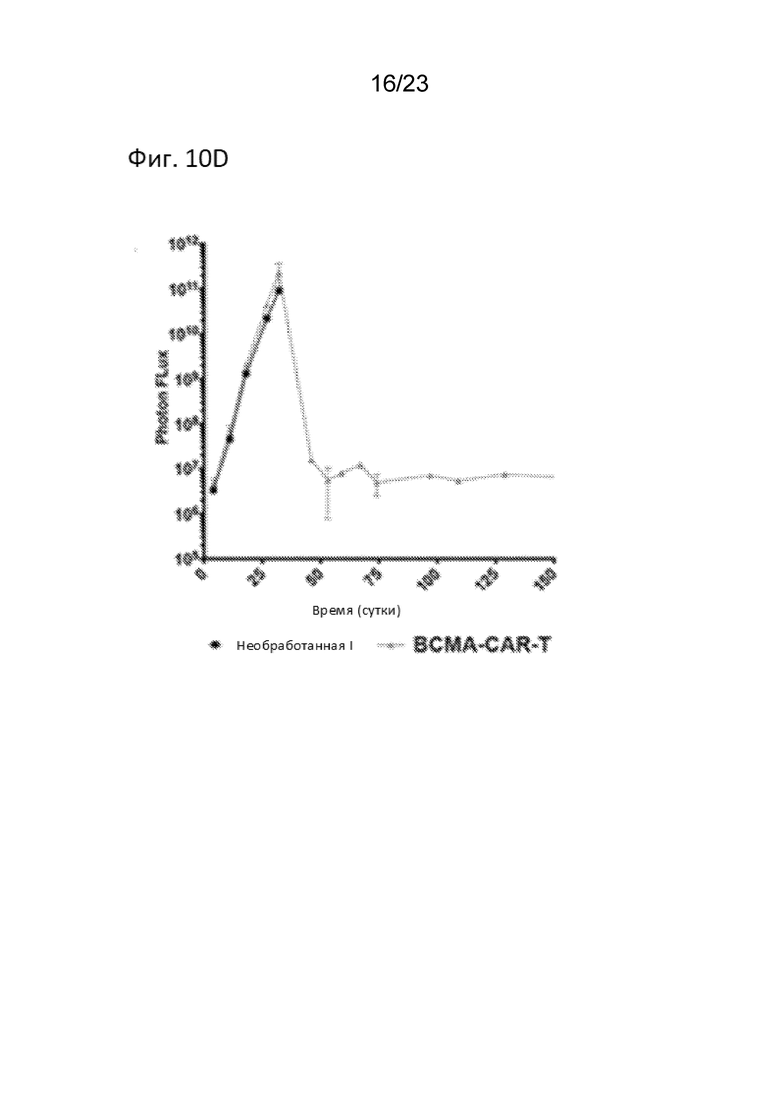

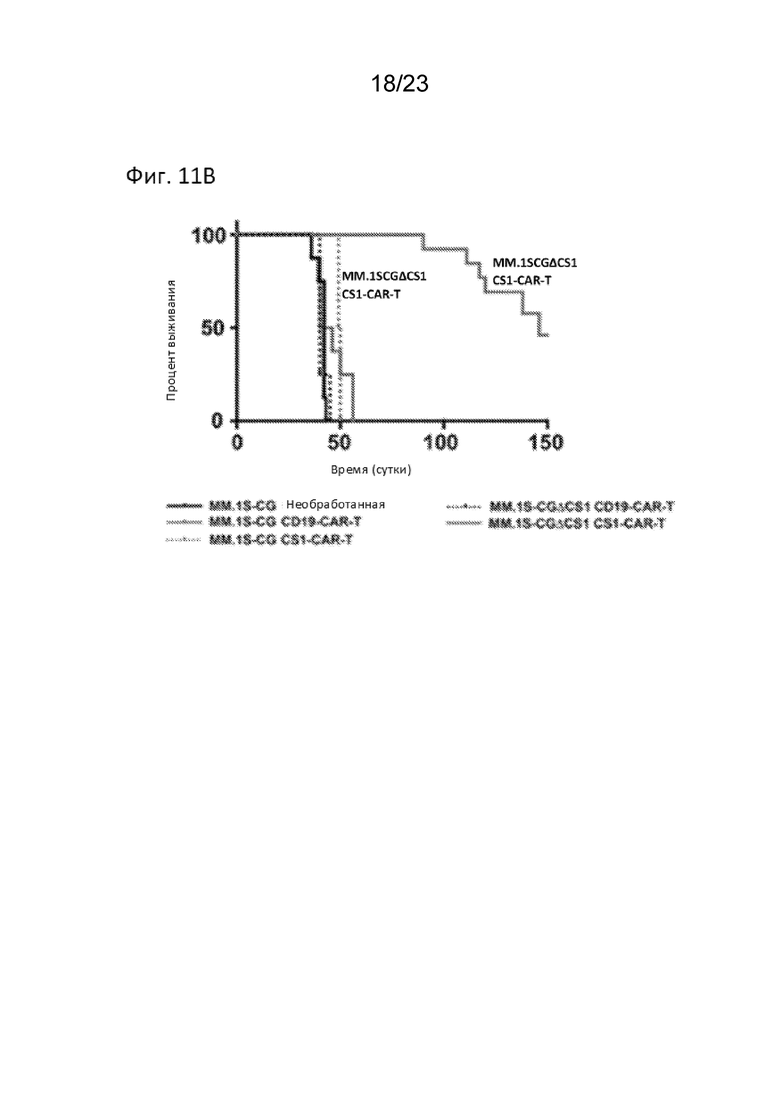
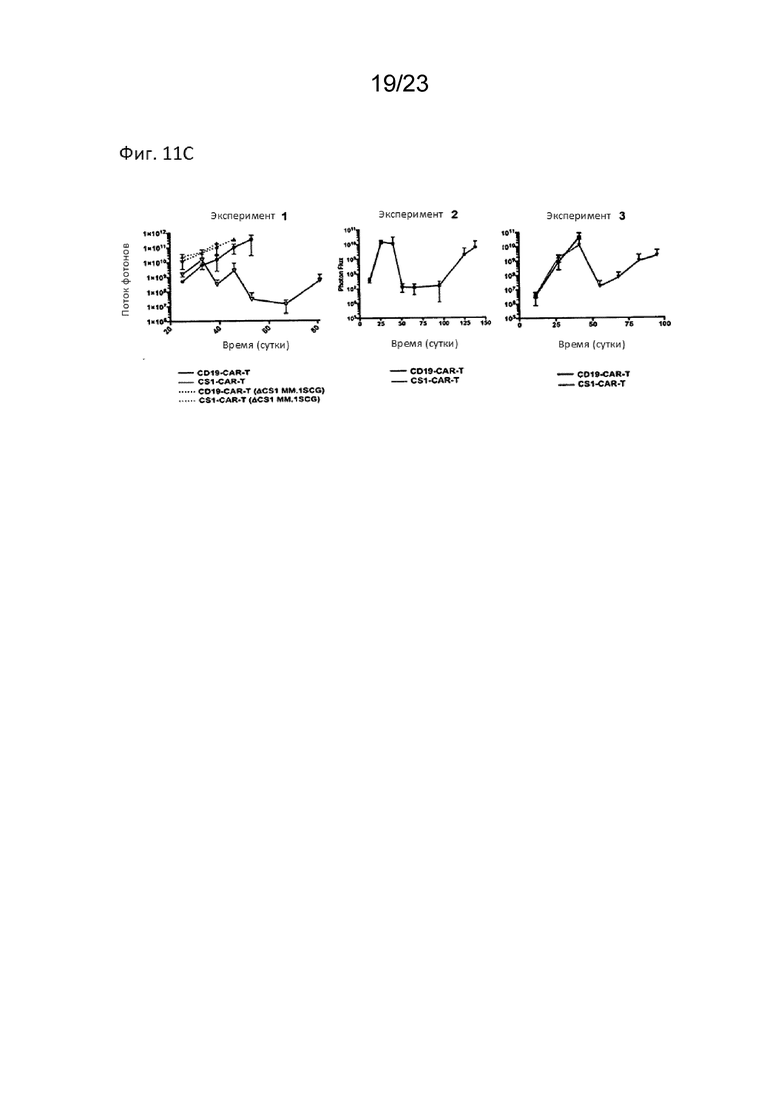

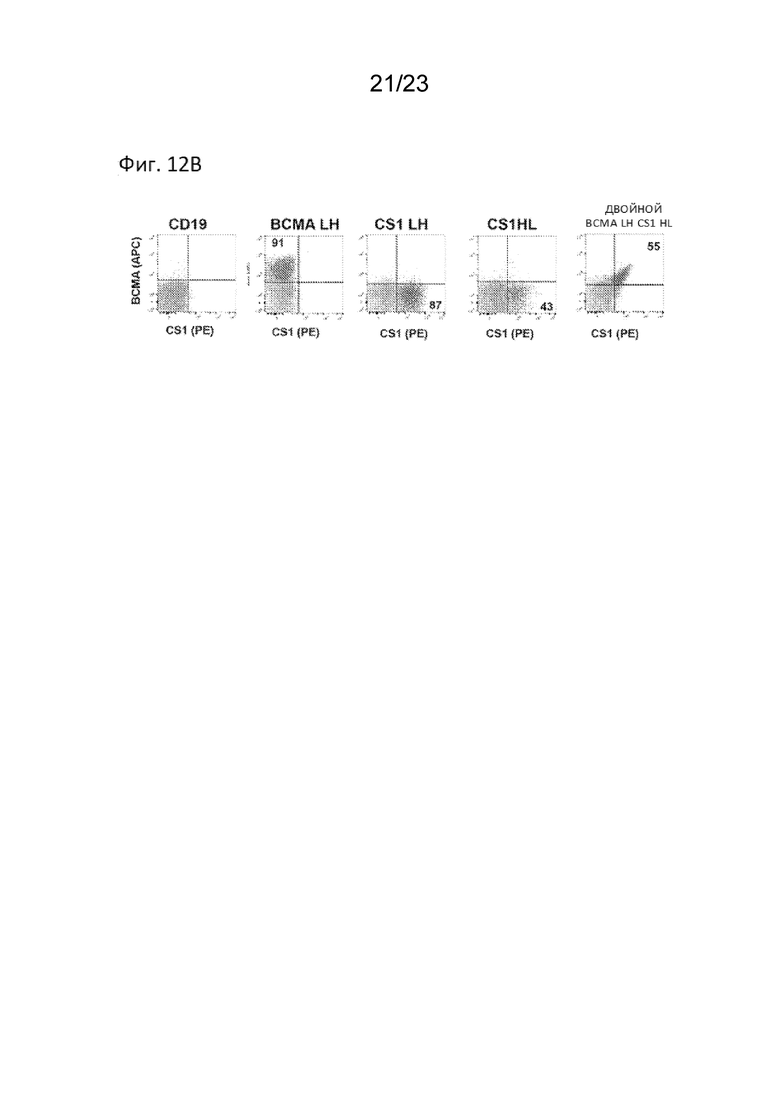
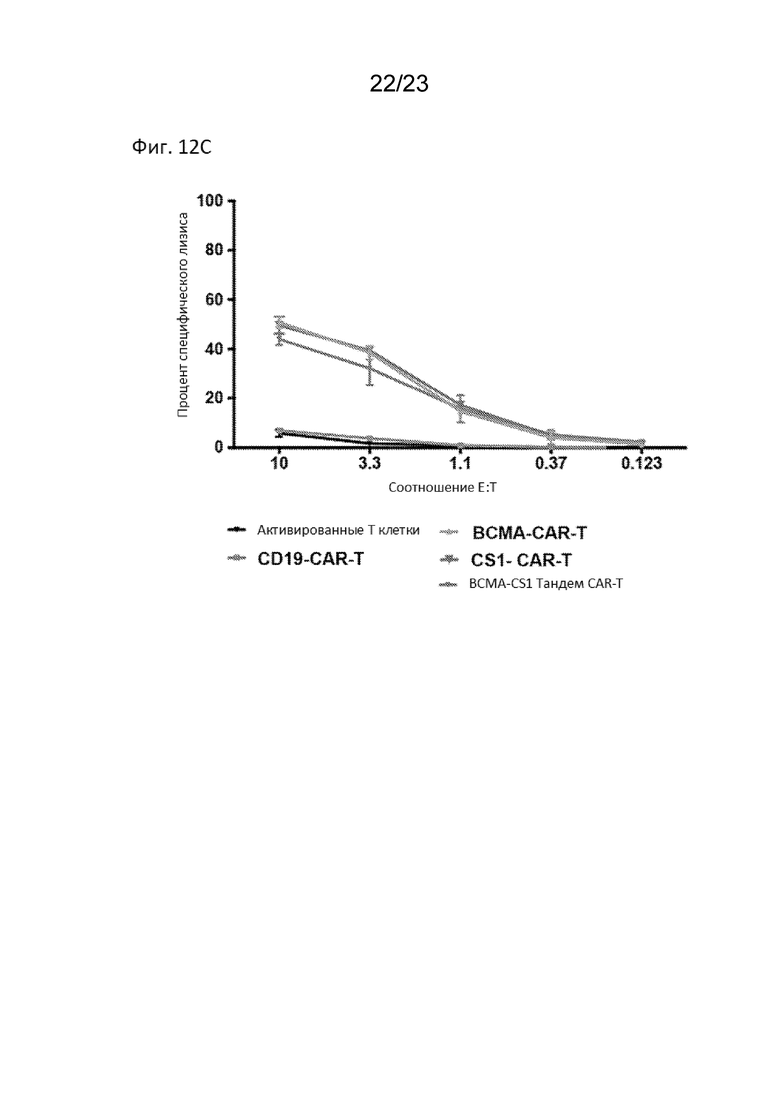
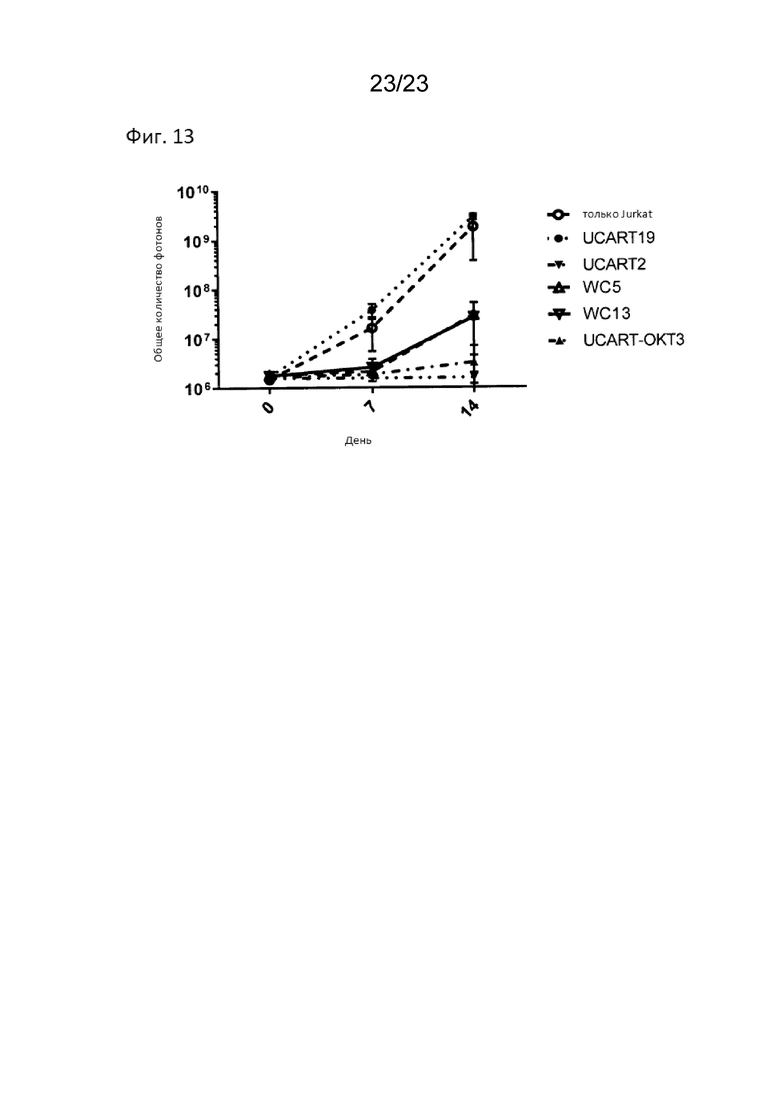
Изобретение относится к области биохимии, клеточной биологии и иммунотерапии. Предложены Т-клетки с химерным антигенным рецептором (CAR-T) с редактированным геномом, которые могут быть получены из цитотоксических Т-клеток, вирусоспецифичной цитотоксической Т-клетки, Т-клеток памяти или гамма-дельта (γδ) Т-клеток и содержат один или более химерных антигенных рецепторов (CAR), нацеленных на один или более антигенов, при этом CAR T-клетка дефицитна по одному или более антигенам, с которыми специфически связывается один или более CAR. В частности, данное изобретение относится к сконструированным Т-клеткам (CAR-T), несущим моно, двойные и тандемные химерные антигенные рецепторы (CAR), и способам иммунотерапии для лечения рака. Изобретение обеспечивает CAR Т-клетки для более эффективного, безопасного и действенного нацеливания на рак. 3 н. и 13 з.п. ф-лы, 13 ил., 27 табл., 11 пр.
1. CAR T-клетка для лечения гематологического злокачественного новообразования, которая содержит один или более химерных антигенных рецепторов (CAR), которые специфически связывают CD7, при этом CAR T-клетка дефицитна по субъединице альфа цепи Т-клеточного рецептора рецепторного комплекса T-клеток (TRAC) и дефицитна по CD7, где CAR содержит:
сигнальный пептид CD8α, содержащий SEQ ID NO: 1;
вариабельную область легкой цепи, содержащую SEQ ID NO: 21;
пептидный линкер, содержащий SEQ ID NO: 9;
вариабельную область тяжелой цепи, содержащую SEQ ID NO: 20;
шарнирную область CD8α, содержащую SEQ ID NO: 2;
костимулирующий домен, выбранный из 4-1BB, содержащего SEQ ID NO: 5; и
сигнальный домен CD3 дзета, содержащий SEQ ID NO: 7.
2. CAR T-клетка по п. 1, отличающаяся тем, что CAR содержит:
MALPVTALLLPLALLLHAARPDIQMTQTTSSLSASLGDRVTISCSASQGISNYLNWYQQKPDGTVKLLIYYTSSLHSGVPSRFSGSGSGTDYSLTISNLEPEDIATYYCQQYSKLPYTFGGGTKLEIKRGGGGSGGGGSGGGGSGGGGSEVQLVESGGGLVKPGGSLKLSCAASGLTFSSYAMSWVRQTPEKRLEWVASISSGGFTYYPDSVKGRFTISRDNARNILYLQMSSLRSEDTAMYYCARDEVRGYLDVWGAGTTVTVSPRASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDFWVLVVVGGVLACYSLLVTVAFIIFWVKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR.
3. CAR T-клетка по п. 1, отличающаяся тем, что последовательность химерного антигенного рецептора (CAR) по меньшей мере на 95% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38 или SEQ ID NO: 39.
4. CAR T-клетка по любому из пп. 1-3, отличающаяся тем, что CAR Т-клетка содержит нуклеиновую кислоту, кодирующую аминокислотную последовательность, выбранную из SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38 или SEQ ID NO: 39.
5. CAR T-клетка по любому из пп. 1-4, отличающаяся тем, что передача сигналов, опосредованная эндогенным Т-клеточным рецептором, заблокирована в CAR T-клетке.
6. CAR T-клетка по любому из пп. 1-5, отличающаяся тем, что CAR T-клетки не индуцируют аллореактивность или реакцию «трансплантат против хозяина».
7. CAR T-клетка по любому из пп. 1-6, отличающаяся тем, что CAR T-клетки не индуцируют взаимное уничтожение.
8. Терапевтическая композиция для лечения гематологического злокачественного новообразования, содержащая популяцию CAR T-клеток по любому из пп. 1-7 и по меньшей мере один терапевтически приемлемый носитель и/или адъювант.
9. Способ лечения гематологического злокачественного новообразования у пациента, включающий введение CAR T-клетки по любому из пп. 1-7 или терапевтической композиции по п. 8 пациенту, нуждающемуся в этом.
10. Способ по п. 9, отличающийся тем, что гематологическое злокачественное новообразование представляет собой злокачественное новообразование Т-клеток.
11. Способ по п. 10, отличающийся тем, что злокачественное новообразование Т-клеток представляет собой Т-клеточный острый лимфобластный лейкоз (Т-ОЛЛ).
12. Способ по п. 10, отличающийся тем, что злокачественное новообразование Т-клеток представляет собой неходжкинскую лимфому.
13. Способ по п. 10, отличающийся тем, что злокачественное новообразование Т-клеток представляет собой Т-клеточный хронический лимфоцитарный лейкоз (Т-ХЛЛ).
14. Способ по п. 9, отличающийся тем, что гематологическое злокачественное новообразование представляет собой множественную миелому.
15. Способ по п. 9, отличающийся тем, что гематологическое злокачественное новообразование представляет собой острый миелоидный лейкоз (ОМЛ).
16. CAR T-клетка по п. 1, содержащая нуклеиновую кислоту, кодирующую SEQ ID NO: 32.
| 0 |
|
SU254141A1 | |
| GOMES-SILVA D | |||
| et al., CD7-edited T cells expressing a CD7-specific CAR for the therapy of T-cell malignancies, Blood, 2017, vol | |||
| Реверсивный дисковый культиватор для тросовой тяги | 1923 |
|
SU130A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| ПЕРЕДВИЖНАЯ ДИАГРАММА ДЛЯ СРАВНЕНИЯ ЦЕННОСТИ РАЗЛИЧНЫХ ПРОДУКТОВ ПО ИХ КАЛОРИЙНОСТИ | 1919 |
|
SU285A1 |
| RAPPL G | |||
| et al., The CD3-zeta chimeric antigen receptor overcomes TCR Hypo-responsiveness of human terminal late-stage T cells, PLoS One, 2012, vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2024-01-12—Публикация
2019-05-31—Подача