ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет по предварительной заявке на патент США № 62/686982, поданной 19 июня 2018 г. Все содержание вышеупомянутой заявки включено в настоящую заявку посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Заявка, рассматриваемая в данный момент, содержит Перечень последовательностей, который был предоставлен в электронном виде в формате ASCII и указанный Перечень полностью включен в настоящую заявку посредством ссылки. Упомянутая копия файла в формате ASCII, созданная 19 июня 2019 г., имеет название A2176-7000WO_SL, размер файла составляет 101767 байт.
УРОВЕНЬ ТЕХНИКИ
Белки комплемента являются частью врожденного иммунного ответа. Они выполняют ряд биологических функций, таких как опсонизация (покрытие чужеродных патогенов), формирование мембраноатакующего комплекса и усиление воспаления путем активации различных путей: классического, лектинового и альтернативного. Пути комплемента сходятся в общий путь, приводящий к расщеплению или активации C3 с образованием C3a или C3b, что в свою очередь приводит к образованию различных биологически активных молекул, таких как C5a и C5b. Экспериментальные исследования продемонстрировали, что блокирование расщепления C5 на C5a и C5b может оказывать противовоспалительное действие, не оказывая влияния на активацию и функцию предшествующих компонентов (например, Rother RP et al., Nature Biotechnology 2007; 25(11): 1256-1264, Fukuzawa T et al., Sci Rep. 2017; 7(1): 1080; все содержание каждого из указанных литературных источников включено в настоящую заявку посредством ссылки). Существует потребность в разработке новых подходов к лечению, предотвращению и диагностике нарушений, связанных с комплементом, и других нарушений, имеющих схожие механизмы развития заболевания.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложены, по меньшей мере частично, молекулы антител, связывающиеся с компонентом 5 комплемента (C5), например, С5 человека (например, C5 человека, содержащий аминокислотную последовательность SEQ ID NO: 53) и которые включают одно или более функциональных свойств и структурных характеристик, раскрытых в настоящей заявке. В одном варианте реализации изобретения молекула антитела связывается с и/или снижает (например, ингибирует, блокирует или нейтрализует) одну или более активностей C5. В одном варианте реализации изобретения молекула антитела выбрана из Таблицы 1 или конкурирует за связывание с C5 с молекулой антитела, выбранной из Таблицы 1. В одном варианте реализации изобретения молекула антитела связывается с таким же или перекрывающимся эпитопом, что и эпитоп, распознаваемый молекулой антитела, выбранной из Таблицы 1. В одном варианте реализации изобретения молекула антитела содержит одну или более вариабельных областей тяжелой цепи и/или одну или более вариабельных областей легкой цепи, описанных в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит один или более участков, определяющих комплементарность (CDR) тяжелой цепи и/или один или более участков, определяющих комплементарность (CDR) легкой цепи, описанных в Таблице 1. В одном варианте реализации изобретения также предложены молекулы нуклеиновых кислот, кодирующие молекулы антител, векторы экспрессии, клетки-хозяева, композиции (например, фармацевтические композиции), наборы, контейнеры и способы получения молекул антител. Раскрытые в настоящей заявке молекулы антител пригодны для применения с целью снижения или ингибирования нежелательной активации системы комплемента или ее компонента. Раскрытые в настоящей заявке молекулы антител можно применять (самостоятельно или в комбинации с другими агентами или терапевтическими средствами) для лечения, предотвращения и/или диагностики нарушений, связанных с комплементом.
Соответственно, в аспекте настоящего изобретения предложена молекула антитела, например, описанная в настоящей заявке молекула антитела, обладающая одним или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или всеми) из следующих свойств:
связывается с C5 (например, C5 человека) с высокой аффинностью, например, константа диссоциации (KD’) составляет примерно 50 нМ или менее, например, примерно 20 нМ или менее, 10 нМ или менее, 9 нМ или менее, 8 нМ или менее, 7 нМ или менее, 6 нМ или менее, 5 нМ или менее, 4 нМ или менее, 3 нМ или менее, 2 нМ или менее, 1 нМ или менее, 0,5 нМ или менее, 0,2 нМ или менее, 0,1 нМ или менее, 0,05 нМ или менее, 0,02 нМ или менее, 0,01 нМ или менее, 0,005 нМ или менее, 0,002 нМ или менее или 0,001 нМ или менее, например, от 0,001 нМ до 10 нМ, от 0,001 нМ до 5 нМ, от 0,001 нМ до 2 нМ, от 0,001 нМ до 1 нМ, от 0,001 нМ до 0,5 нМ, от 0,001 нМ до 0,2 нМ, от 0,001 нМ до 0,1 нМ, от 0,001 до 0,05 нМ, от 0,001 до 0,02 нМ, от 0,001 до 0,005 нМ, от 5 нМ до 10 нМ, от 2 нМ до 10 нМ, от 1 нМ до 10 нМ, от 0,5 нМ до 10 нМ, от 0,2 нМ до 10 нМ, от 0,1 нМ до 10 нМ, от 0,05 нМ до 10 нМ, от 0,02 нМ до 10 нМ, от 0,01 нМ до 10 нМ, от 0,005 нМ до 10 нМ, от 0,002 до 10 нМ, от 0,002 нМ до 5 нМ, от 0,005 нМ до 2 нМ, от 0,01 нМ до 1 нМ, от 0,02 нМ до 0,5 нМ, от 0,05 нМ до 0,2 нМ, от 0,001 нМ до 0,002 нМ, от 0,002 нМ до 0,005 нМ, от 0,005 нМ до 0,01 нМ, от 0,01 нМ до 0,02 нМ, от 0,02 нМ до 0,05 нМ, от 0,05 нМ до 0,1 нМ, от 0,1 нМ до 0,2 нМ, от 0,2 нМ до 0,5 нМ, от 0,5 нМ до 1 нМ, от 1 нМ до 2 нМ, от 2 нМ до 5 нМ или от 5 нМ до 10 нМ, например, от 0,1 нМ до 0,6 нМ или от 0,2 нМ до 0,53 нМ, например, как определено описанным в настоящей заявке способом;
связывается с C5 (например, C5 человека) при нейтральном значении pH с аффинностью по меньшей мере превышающей в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 раз аффинность при кислом значении pH, например, при значении pH ниже 7, 6,5, 6, 5,5, 5 или менее;
связывается с C5 (например, C5 человека) с высокой аффинностью, например, с полумаксимальной эффективной концентрацией (EC50), составляющей примерно 2 мкг/мл или менее, например, примерно 1 мкг/мл или менее, 0,9 мкг/мл или менее, 0,8 мкг/мл или менее, 0,7 мкг/мл или менее, 0,6 мкг/мл или менее, 0,5 мкг/мл или менее, 0,4 мкг/мл или менее, 0,3 мкг/мл или менее, 0,2 мкг/мл или менее, 0,1 мкг/мл или менее, 0,09 мкг/мл или менее, 0,08 мкг/мл или менее, 0,07 мкг/мл или менее, 0,06 мкг/мл или менее, 0,05 мкг/мл или менее, 0,04 мкг/мл или менее, 0,03 мкг/мл или менее, 0,02 мкг/мл или менее, 0,01 мкг/мл или менее, 0,005 мкг/мл или менее, 0,002 мкг/мл или менее, 0,001 мкг/мл или менее, например, от 0,001 мкг/мл до 2 мкг/мл, например, от 0,001 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 0,5 мкг/мл, от 0,001 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,1 мкг/мл, от 0,001 мкг/мл до 0,05 мкг/мл, от 0,001 мкг/мл до 0,02 мкг/мл, от 0,001 мкг/мл до 0,01 мкг/мл, от 0,001 мкг/мл до 0,005 мкг/мл, от 0,002 мкг/мл до 1 мкг/мл, от 0,005 мкг/мл до 1 мкг/мл, от 0,01 мкг/мл до 1 мкг/мл, от 0,02 мкг/мл до 1 мкг/мл, от 0,05 мкг/мл до 1 мкг/мл, от 0,1 мкг/мл до 1 мкг/мл, от 0,2 мкг/мл до 1 мкг/мл, от 0,5 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 1 мкг/мл, от 0,002 мкг/мл до 0,5 мкг/мл, от 0,005 мкг/мл до 0,2 мкг/мл, от 0,01 мкг/мл до 0,1 мкг/мл или от 0,02 мкг/мл до 0,05 мкг/мл, например, как определено описанным в настоящей заявке способом;
специфически связывается с эпитопом С5 (например, C5 человека), например, таким же, схожим или перекрывающимся эпитопом, что и эпитоп, распознаваемый моноклональным антителом, описанным в Таблице 1, например, каким-либо моноклональным антителом ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012, или ATG-013;
снижает (например, ингибирует, блокирует или нейтрализует) одну или более биологических активностей C5 (например, C5 человека), в условиях in vitro, ex vivo или in vivo;
снижает (например, ингибирует, блокирует или нейтрализует) одну или более биологических активностей C5 (например, C5 человека), например, с концентрацией полумаксимального ингибирования (IC50), составляющей примерно 50 мкг/мл или менее, например, примерно 20 мкг/мл или менее, 10 мкг/мл или менее, 9 мкг/мл или менее, 8 мкг/мл или менее, 7 мкг/мл или менее, 6 мкг/мл или менее, 5 мкг/мл или менее, 4 мкг/мл или менее, 3 мкг/мл или менее, 2 мкг/мл или менее, 1 мкг/мл или менее, 0,5 мкг/мл или менее, 0,2 мкг/мл или менее, 0,1 мкг/мл или менее, 0,05 мкг/мл или менее, 0,02 мкг/мл или менее, 0,01 мкг/мл или менее, 0,005 мкг/мл или менее, 0,002 мкг/мл или менее или 0,001 мкг/мл или менее, например, от 0,001 мкг/мл до 10 мкг/мл, от 0,001 мкг/мл до 5 мкг/мл, от 0,001 мкг/мл до 2 мкг/мл, от 0,001 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 0,5 мкг/мл, от 0,001 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,1 мкг/мл, от 0,001 до 0,05 мкг/мл, от 0,001 до 0,02 мкг/мл, от 0,001 до 0,005 мкг/мл, от 5 мкг/мл до 10 мкг/мл, от 2 мкг/мл до 10 мкг/мл, от 1 мкг/мл до 10 мкг/мл, от 0,5 мкг/мл до 10 мкг/мл, от 0,2 мкг/мл до 10 мкг/мл, от 0,1 мкг/мл до 10 мкг/мл, от 0,05 мкг/мл до 10 мкг/мл, от 0,02 мкг/мл до 10 мкг/мл, от 0,01 мкг/мл до 10 мкг/мл, от 0,005 мкг/мл до 10 мкг/мл, от 0,002 до 10 мкг/мл, от 0,002 мкг/мл до 5 мкг/мл, от 0,005 мкг/мл до 2 мкг/мл, от 0,01 мкг/мл до 1 мкг/мл, от 0,02 мкг/мл до 0,5 мкг/мл, от 0,05 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,002 мкг/мл, от 0,002 мкг/мл до 0,005 мкг/мл, от 0,005 мкг/мл до 0,01 мкг/мл, от 0,01 мкг/мл до 0,02 мкг/мл, от 0,02 мкг/мл до 0,05 мкг/мл, от 0,05 мкг/мл до 0,1 мкг/мл, от 0,1 мкг/мл до 0,2 мкг/мл, от 0,2 мкг/мл до 0,5 мкг/мл, от 0,5 мкг/мл до 1 мкг/мл, от 1 мкг/мл до 2 мкг/мл, от 2 мкг/мл до 5 мкг/мл, или от 5 мкг/мл до 10 мкг/мл, например, от 1 мкг/мл до 8 мкг/мл или от 2 мкг/мл до 6 мкг/мл, например, как определено описанным в настоящей заявке способом;
демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и моноклональное антитело, описанное в Таблице 1, например, какое-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013;
демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая вариабельную область тяжелой цепи и/или вариабельную область легкой цепи, описанную в Таблице 1, например, вариабельную область тяжелой цепи и/или вариабельную область легкой цепи какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013;
демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая один или более (например, два или три) участков, определяющих комплементарность (CDR) тяжелой цепи и/или один или более (например, два или три) участков, определяющих комплементарность (CDR) легкой цепи, описанных в Таблице 1, например, один или более (например, два или три) участков, определяющих комплементарность (CDR) тяжелой цепи и/или один или более (два или три) участков, определяющих комплементарность (CDR) легкой цепи какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013;
демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая аминокислотную последовательность, представленную в Таблице 1;
демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая аминокислотную последовательность, кодируемую нуклеотидной последовательностью, представленной в Таблице 5;
ингибирует, например, конкурентно ингибирует связывание второй молекулы антитела с С5 (например, C5 человека), например, C5 человека, при этом вторая молекула антитела является молекулой антитела, выбранной из Таблицы 1, например, каким-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013;
конкурирует со второй молекулой антитела за связывание с C5 (например, C5 человека), при этом вторая молекула антитела является моноклональным антителом, выбранным из Таблицы 1, например, каким-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013;
обладает одним или более биологическими свойствами моноклонального антитела, выбранного из Таблицы 1, например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013;
обладает одной или более структурными характеристиками моноклонального антитела, выбранного из Таблицы 1, например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013; или
обладает одной или более фармакокинетическими характеристиками моноклонального антитела, выбранного из Таблицы 1, например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела связывается с C5 (например, C5 человека) с высокой аффинностью, например, с KD’, составляющим примерно 50 нМ или менее, например, примерно 20 нМ или менее, 10 нМ или менее, 9 нМ или менее, 8 нМ или менее, 7 нМ или менее, 6 нМ или менее, 5 нМ или менее, 4 нМ или менее, 3 нМ или менее, 2 нМ или менее, 1 нМ или менее, 0,5 нМ или менее, 0,2 нМ или менее, 0,1 нМ или менее, 0,05 нМ или менее, 0,02 нМ или менее, 0,01 нМ или менее, 0,005 нМ или менее, 0,002 нМ или менее или 0,001 нМ или менее, например, от 0,001 нМ до 10 нМ, от 0,001 нМ до 5 нМ, от 0,001 нМ до 2 нМ, от 0,001 нМ до 1 нМ, от 0,001 нМ до 0,5 нМ, от 0,001 нМ до 0,2 нМ, от 0,001 нМ до 0,1 нМ, от 0,001 до 0,05 нМ, от 0,001 до 0,02 нМ, от 0,001 до 0,005 нМ, от 5 нМ до 10 нМ, от 2 нМ до 10 нМ, от 1 нМ до 10 нМ, от 0,5 нМ до 10 нМ, от 0,2 нМ до 10 нМ, от 0,1 нМ до 10 нМ, от 0,05 нМ до 10 нМ, от 0,02 нМ до 10 нМ, от 0,01 нМ до 10 нМ, от 0,005 нМ до 10 нМ, от 0,002 до 10 нМ, от 0,002 нМ до 5 нМ, от 0,005 нМ до 2 нМ, от 0,01 нМ до 1 нМ, от 0,02 нМ до 0,5 нМ, от 0,05 нМ до 0,2 нМ, от 0,001 нМ до 0,002 нМ, от 0,002 нМ до 0,005 нМ, от 0,005 нМ до 0,01 нМ, от 0,01 нМ до 0,02 нМ, от 0,02 нМ до 0,05 нМ, от 0,05 нМ до 0,1 нМ, от 0,1 нМ до 0,2 нМ, от 0,2 нМ до 0,5 нМ, от 0,5 нМ до 1 нМ, от 1 нМ до 2 нМ, от 2 нМ до 5 нМ, или от 5 нМ до 10 нМ, например, от 0,1 нМ до 0,6 нМ или от 0,2 нМ до 0,53 нМ, например, как определено описанным в настоящей заявке способом.
В одном варианте реализации изобретения молекула антитела связывается с C5 (например, C5 человека) при нейтральном значении pH с аффинностью по меньшей мере превышающей в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 раз аффинность при кислом значении pH, например, при значении pH ниже 7, 6,5, 6, 5,5, 5 или менее.
В одном варианте реализации изобретения молекула антитела связывается с C5 (например, C5 человека) с высокой аффинностью, например, с EC50, составляющей примерно 2 мкг/мл или менее, например, примерно 1 мкг/мл или менее, 0,9 мкг/мл или менее, 0,8 мкг/мл или менее, 0,7 мкг/мл или менее, 0,6 мкг/мл или менее, 0,5 мкг/мл или менее, 0,4 мкг/мл или менее, 0,3 мкг/мл или менее, 0,2 мкг/мл или менее, 0,1 мкг/мл или менее, 0,09 мкг/мл или менее, 0,08 мкг/мл или менее, 0,07 мкг/мл или менее, 0,06 мкг/мл или менее, 0,05 мкг/мл или менее, 0,04 мкг/мл или менее, 0,03 мкг/мл или менее, 0,02 мкг/мл или менее, 0,01 мкг/мл или менее, 0,005 мкг/мл или менее, 0,002 мкг/мл или менее, 0,001 мкг/мл или менее, например, от 0,001 мкг/мл до 2 мкг/мл, например, от 0,001 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 0,5 мкг/мл, от 0,001 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,1 мкг/мл, от 0,001 мкг/мл до 0,05 мкг/мл, от 0,001 мкг/мл до 0,02 мкг/мл, от 0,001 мкг/мл до 0,01 мкг/мл, от 0,001 мкг/мл до 0,005 мкг/мл, от 0,002 мкг/мл до 1 мкг/мл, от 0,005 мкг/мл до 1 мкг/мл, от 0,01 мкг/мл до 1 мкг/мл, от 0,02 мкг/мл до 1 мкг/мл, от 0,05 мкг/мл до 1 мкг/мл, от 0,1 мкг/мл до 1 мкг/мл, от 0,2 мкг/мл до 1 мкг/мл, от 0,5 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 1 мкг/мл, от 0,002 мкг/мл до 0,5 мкг/мл, от 0,005 мкг/мл до 0,2 мкг/мл, от 0,01 мкг/мл до 0,1 мкг/мл или от 0,02 мкг/мл до 0,05 мкг/мл, например, как определено описанным в настоящей заявке способом.
В одном варианте реализации изобретения молекула антитела специфически связывается с эпитопом С5 (например, C5 человека), например, таким же, схожим или перекрывающимся эпитопом, что и эпитоп, распознаваемый моноклональным антителом, описанным в Таблице 1, например, каким-либо моноклональным антителом ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела снижает (например, ингибирует, блокирует или нейтрализует) одну или более биологических активностей C5 (например, C5 человека) в условиях in vitro, ex vivo или in vivo.
В одном варианте реализации изобретения молекула антитела снижает (например, ингибирует, блокирует или нейтрализует) одну или более биологических активностей C5 (например, С5 человека), например, с IC50, составляющей примерно 50 мкг/мл или менее, например, примерно 20 мкг/мл или менее, 10 мкг/мл или менее, 9 мкг/мл или менее, 8 мкг/мл или менее, 7 мкг/мл или менее, 6 мкг/мл или менее, 5 мкг/мл или менее, 4 мкг/мл или менее, 3 мкг/мл или менее, 2 мкг/мл или менее, 1 мкг/мл или менее, 0,5 мкг/мл или менее, 0,2 мкг/мл или менее, 0,1 мкг/мл или менее, 0,05 мкг/мл или менее, 0,02 мкг/мл или менее, 0,01 мкг/мл или менее, 0,005 мкг/мл или менее, 0,002 мкг/мл или менее или 0,001 мкг/мл или менее, например, от 0,001 мкг/мл до 10 мкг/мл, от 0,001 мкг/мл до 5 мкг/мл, от 0,001 мкг/мл до 2 мкг/мл, от 0,001 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 0,5 мкг/мл, от 0,001 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,1 мкг/мл, от 0,001 до 0,05 мкг/мл, от 0,001 до 0,02 мкг/мл, от 0,001 до 0,005 мкг/мл, от 5 мкг/мл до 10 мкг/мл, от 2 мкг/мл до 10 мкг/мл, от 1 мкг/мл до 10 мкг/мл, от 0,5 мкг/мл до 10 мкг/мл, от 0,2 мкг/мл до 10 мкг/мл, от 0,1 мкг/мл до 10 мкг/мл, от 0,05 мкг/мл до 10 мкг/мл, от 0,02 мкг/мл до 10 мкг/мл, от 0,01 мкг/мл до 10 мкг/мл, от 0,005 мкг/мл до 10 мкг/мл, от 0,002 до 10 мкг/мл, от 0,002 мкг/мл до 5 мкг/мл, от 0,005 мкг/мл до 2 мкг/мл, от 0,01 мкг/мл до 1 мкг/мл, от 0,02 мкг/мл до 0,5 мкг/мл, от 0,05 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,002 мкг/мл, от 0,002 мкг/мл до 0,005 мкг/мл, от 0,005 мкг/мл до 0,01 мкг/мл, от 0,01 мкг/мл до 0,02 мкг/мл, от 0,02 мкг/мл до 0,05 мкг/мл, от 0,05 мкг/мл до 0,1 мкг/мл, от 0,1 мкг/мл до 0,2 мкг/мл, от 0,2 мкг/мл до 0,5 мкг/мл, от 0,5 мкг/мл до 1 мкг/мл, от 1 мкг/мл до 2 мкг/мл, от 2 мкг/мл до 5 мкг/мл, или от 5 мкг/мл до 10 мкг/мл, например, от 1 мкг/мл до 8 мкг/мл или от 2 мкг/мл до 6 мкг/мл, например, как определено описанным в настоящей заявке способом.
В одном варианте реализации изобретения молекула антитела демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и моноклональное антитело, описанное в Таблице 1, например, какое-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая вариабельную область тяжелой цепи и/или вариабельную область легкой цепи, описанную в Таблице 1, например, вариабельную область тяжелой цепи и/или вариабельную область легкой цепи какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая один или более (например, два или три) участков, определяющих комплементарность (CDR) тяжелой цепи и/или один или более (например, два или три) участков, определяющих комплементарность (CDR) легкой цепи, описанных в Таблице 1, например, один или более (например, два или три) участков, определяющих комплементарность (CDR) тяжелой цепи и/или один или более (два или три) участков, определяющих комплементарность (CDR) легкой цепи какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая аминокислотную последовательность, представленную в Таблице 1.
В одном варианте реализации изобретения молекула антитела демонстрирует такую же или схожую аффинность связывания или специфичность, или оба параметра, что и молекула антитела, содержащая аминокислотную последовательность, кодируемую нуклеотидной последовательностью, представленной в Таблице 5.
В одном варианте реализации изобретения молекула антитела ингибирует, например, конкурентно ингибирует связывание второй молекулы антитела с С5 (например, C5 человека), при этом вторая молекула антитела является молекулой антитела, выбранной из Таблицы 1, например, каким-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела конкурирует со второй молекулой антитела за связывание с C5 (например, C5 человека), при этом вторая молекула антитела является моноклональным антителом, выбранным из Таблицы 1, например, каким-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела обладает одним или более биологическими свойствами моноклонального антитела, выбранного из Таблицы 1, например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела обладает одной или более структурными характеристиками моноклонального антитела, выбранного из Таблицы 1, например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела обладает одной или более фармакокинетическими характеристиками моноклонального антитела, выбранного из Таблицы 1, например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела является синтетической молекулой антитела. В одном варианте реализации изобретения молекула антитела является выделенной молекулой антитела. В одном варианте реализации изобретения молекула антитела является молекулой рекомбинантного антитела. В одном варианте реализации изобретения молекула антитела является гуманизированным антителом. В одном варианте реализации изобретения молекула антитела является молекулой моноспецифического антитела. В одном варианте реализации изобретения молекула антитела является молекулой мультиспецифического антитела.
В некоторых вариантах воплощения изобретения молекула антитела содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3),
при этом VH содержит одно, два или все из следующего:
(i) HCDR1, содержащий аминокислотную последовательность:
GX1X2FX3X4X5Y,
где X1 является Y, F или H;
X2 является I или T;
X3 является S или T;
X4 является N, S, D или G и
X5 является F, N или отсутствует
(SEQ ID NO: 87);
(ii) HCDR2, содержащий аминокислотную последовательность:
X1X2X3X4GX5,
где X1 является L или N;
X2 является A или P;
X3 является G, T или K;
X4 является S, D, N, T или S и
X5 является S, H или D
(SEQ ID NO: 88);
(iii) HCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6X7X8X9X10X11X12X13,
где X1 является Y или G;
X2 является P, Y, S, F или W;
X3 является F, S или W;
X4 является G или P;
X5 является S, N или M;
X6 является S, W, T или D;
X7 является P, A или V;
X8 является N, M или отсутствует;
X9 является W, D или отсутствует;
X10 является E, Y, A или отсутствует;
X11 является F, M или отсутствует;
X12 является D или отсутствует и
X13 является Y, V или отсутствует
(SEQ ID NO: 89) и
при этом VL содержит одно, два или все из следующего:
(iv) LCDR1, содержащий аминокислотную последовательность:
X1AX2X3X4IX5X6X7LX8,
где X1 является R или G;
X2 является S или T;
X3 является Q или E;
X4 является N, S или G;
X5 является N или Y;
X6 является N или G;
X7 является Y или A и
X8 является H, N или A
(SEQ ID NO: 90);
(v) LCDR2, содержащий аминокислотную последовательность:
X1ASX2X3X4X5,
где X1 является A, G или D;
X2 является N или T;
X3 является L или R;
X4 является Q, A, Y или E, или
X5 является G, D, T или S
(SEQ ID NO: 91); и
(vi) LCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6PX7X8,
где X1 является L или Q;
X2 является Q или N;
X3 является T или V;
X4 является H или L;
X5 является A, N или S;
X6 является Y или T;
X7 является L, V, W или Y, или
X8 является T или S;
(SEQ ID NO: 92).
В вариантах воплощения изобретения молекула антитела содержит VH и VL, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3),
при этом VH содержит одно, два или все из следующего:
(i) HCDR1, содержащий аминокислотную последовательность:
X1X2X3X4X5
где X1 является N, D, S или G;
X2 является Y, F или N;
X3 является W или Y;
X4 является M или I; и
X5 является Q или Н
(SEQ ID NO: 94);
(ii) HCDR2, содержащий аминокислотную последовательность:
X1X2X3X4X5X6GX7TX8YX9QKFX10G
где X1 является E или W;
X2 является I или V;
X3 является L или N;
X4 является P или A;
X5 является G, T или K;
X6 является T, S, D или N;
X7 является S, H или D;
X8 является Е или N;
X9 является A или S и
X10 является Q или R
(SEQ ID NO: 95);
(iii) HCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6X7X8WX9X10DX11
где X1 является Y или G;
X2 является F, P, Y или W;
X3 является F или отсутствует;
X4 является G или отсутствует;
X5 является S или отсутствует;
X6 является Т, S или отсутствует;
X7 является Р или отсутствует;
X8 является N или отсутствует;
X9 является Y, E, A или G;
X10 является F или M и
X11 является V или Y
(SEQ ID NO: 96) и
при этом VL содержит одно, два или все из следующего:
(iv) LCDR1, содержащий аминокислотную последовательность:
X1AX2X3X4IX5X6X7LX8
где X1 является G или R;
X2 является T или S;
X3 является Е или Q;
X4 является N, G или S;
X5 является Y или N;
X6 является G или N;
X7 является A или Y; и
X8 является N, A или H
(SEQ ID NO: 97);
(v) LCDR2, содержащий аминокислотную последовательность:
X1ASX2X3X4X5
где X1 является G, D или A;
X2 является N или T;
X3 является L или R;
X4 является A, Y, E или Q и
X5 является D, T, S или G
(SEQ ID NO: 98) и
(vi) LCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6PX7X8
где X1 является Q или L;
X2 является N или Q;
X3 является V или T;
X4 является L или H;
X5 является N, S или A;
X6 является T или Y;
X7 является L, V, W или Y, или
X8 является S или T
(SEQ ID NO: 99).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом VH содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 19); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 28) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 43) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 20); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 28) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 43) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 21); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 29) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 43) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 22); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 29) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 43) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 19); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 28) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 44) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 20); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 28) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 44) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 21); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 29) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 44) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 22); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 29) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 44) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 22); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 29) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 44) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 20); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 28) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 35).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 38); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 44) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 54); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 59) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 76) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 55); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 59) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 76) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 54); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 60) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 76) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 55); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 60) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 76) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 54); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 59) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 77) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 55); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 59) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 77) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 54); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 60) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 77) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 55); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 60) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 77) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 55); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 60) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 77) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит VH, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: (i) HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 55); (ii) HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 59) или (iii) HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 66).
В одном варианте реализации изобретения молекула антитела содержит VL, при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: (i) LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 71); (ii) LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 77) или (iii) LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-001 (например, SEQ ID NO: 1).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-001 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-001 (например, SEQ ID NO: 1) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-001 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-001 (например, SEQ ID NO: 1), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-001 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-002 (например, SEQ ID NO: 2).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-002 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-002 (например, SEQ ID NO: 2) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-002 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-002 (например, SEQ ID NO: 2), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-002 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-003 (например, SEQ ID NO: 3).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-003 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-003 (например, SEQ ID NO: 3) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-003 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-003 (например, SEQ ID NO: 3), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-003 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-004 (например, SEQ ID NO: 4).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-004 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-004 (например, SEQ ID NO: 4) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-004 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-004 (например, SEQ ID NO: 4), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-004 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-005 (например, SEQ ID NO: 1).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-005 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-005 (например, SEQ ID NO: 1) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-005 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-005 (например, SEQ ID NO: 1), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-005 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-006 (например, SEQ ID NO: 2).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-006 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-006 (например, SEQ ID NO: 2) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-006 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-006 (например, SEQ ID NO: 2), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-006 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-007 (например, SEQ ID NO: 3).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-007 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-007 (например, SEQ ID NO: 3) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-007 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-007 (например, SEQ ID NO: 3), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-008 (например, SEQ ID NO: 4).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-008 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-008 (например, SEQ ID NO: 4) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-008 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-008 (например, SEQ ID NO: 4), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-008 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-012 (например, SEQ ID NO: 4).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-012 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-012 (например, SEQ ID NO: 4) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-012 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-012 (например, SEQ ID NO: 4), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-012 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-013 (например, SEQ ID NO: 2).
В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-013 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-013 (например, SEQ ID NO: 2) и (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-013 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую аминокислотную последовательность VH моноклонального антитела ATG-013 (например, SEQ ID NO: 2), и (ii) VL, содержащую аминокислотную последовательность VL моноклонального антитела ATG-013 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела является моноклональным антителом ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела содержит одну или более каркасных областей, полученных из последовательности каркасной области зародышевой линии человека.
В одном варианте реализации изобретения молекула антитела содержит VH, описанную в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит VL, описанную в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит VH и VL, описанные в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит один, два или три участка, определяющих комплементарность (CDR) VH, описанной в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит один, два или три участка, определяющих комплементарность (CDR) VL, описанной в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит один, два или три участка, определяющих комплементарность (CDR) VH, описанной в Таблице 1, и один, два или три участка, определяющих комплементарность (CDR) VL, описанной в Таблице 1.
В одном варианте реализации изобретения молекула антитела содержит две VH и две VL. В одном варианте реализации изобретения молекула антитела содержит антигенсвязывающий фрагмент. В одном варианте реализации изобретения молекула антитела содержит Fab, F(ab')2, Fv, scFv или Fd.
В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG, например, содержащей константную область тяжелой цепи IgG, например, выбранная из IgG1, IgG2, IgG3 или IgG4, например, IgG2 или IgG4. В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG1, например, имеющей описанную в настоящей заявке константную область IgG1. В другом варианте воплощения изобретения молекула антитела является молекулой антитела IgG2, например, имеющей описанную в настоящей заявке константную область IgG2. В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG3, например, имеющей описанную в настоящей заявке константную область IgG3. В другом варианте воплощения изобретения молекула антитела является молекулой антитела IgG4, например, имеющей описанную в настоящей заявке константную область IgG4. В другом варианте воплощения изобретения молекула антитела содержит химерную константную область, включающую изотипы IgG2, IgG3 и/или IgG4. В одном варианте реализации изобретения константная область тяжелой цепи содержит одну или более модификаций аминокислот в шарнирном участке, в CH2 или CH3 участке. В одном варианте реализации изобретения молекула антитела содержит константную область легкой цепи каппа или лямбда легкой цепи.
В одном варианте реализации изобретения молекула антитела содержит Fc-участок. В одном варианте реализации изобретения Fc-участок содержит одно или оба из замещений Met-428-Leu и Asn-434-Ser в остатках, соответствующих метионину 428 и аспарагину 434, соответственно, нумерация каждого согласно нумерации ЕС. В одном варианте реализации изобретения Fc-участок содержит одно, два или три из замещений Met-252-Tyr, Ser-254-Thr и Thr-256-Glu в остатках, соответствующих метионину 252, серину 254 и треонину 256, соответственно, нумерация каждого согласно нумерации ЕС.
В аспекте изобретение определяет отличительные признаки молекулы антитела к C5, описанной в настоящей заявке, например, синтетической или выделенной молекулы антитела к C5, описанной в настоящей заявке.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 19 или 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 28 или 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 43 или 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 48 или 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 20 или 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 28 или 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 43 или 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 48 или 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 21 или 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 29 или 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 43 или 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 48 или 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 22 или 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 29 или 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 43 или 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 48 или 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 19 или 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 28 или 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 44 или 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 49 или 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 20 или 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 28 или 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 44 или 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 49 или 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 21 или 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 29 или 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 44 или 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 49 или 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 22 или 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 29 или 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 44 или 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 49 или 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 22 или 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 29 или 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 44 или 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 49 или 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 20 или 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 28 или 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 35 или 66) и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 38 или 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 44 или 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 49 или 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 43) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 43) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 48).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 19); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 21); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 29) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 22); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 29) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 28) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 35) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 44) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 20); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 28) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 35), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 38); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 44) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 49).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-001 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-001 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-001 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-002 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-002 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-002 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-003 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-003 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-003 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 76) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-004 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-004 (например, SEQ ID NO: 76) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-004 (например, SEQ ID NO: 81).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-005 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-005 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-005 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-006 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-006 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-006 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 54); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-007 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-007 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-007 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-008 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-008 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-008 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 60) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 60) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-012 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-012 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-012 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит:
(i) VH, содержащую одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 59) или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 66) и
(ii) VL, содержащую одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 77) или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит: (i) VH, содержащую: HCDR1, содержащий аминокислотную последовательность HCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 55); HCDR2, содержащий аминокислотную последовательность HCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 59) и HCDR3, содержащий аминокислотную последовательность HCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 66), и (ii) VL, содержащую: LCDR1, содержащий аминокислотную последовательность LCDR1 моноклонального антитела ATG-013 (например, SEQ ID NO: 71); LCDR2, содержащий аминокислотную последовательность LCDR2 моноклонального антитела ATG-013 (например, SEQ ID NO: 77) и LCDR3, содержащий аминокислотную последовательность LCDR3 моноклонального антитела ATG-013 (например, SEQ ID NO: 82).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-001 (например, SEQ ID NO: 1) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-001 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-002 (например, SEQ ID NO: 2) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-002 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-003 (например, SEQ ID NO: 3) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-003 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-004 (например, SEQ ID NO: 4) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-004 (например, SEQ ID NO: 10).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-005 (например, SEQ ID NO: 1) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-005 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-006 (например, SEQ ID NO: 2) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-006 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-007 (например, SEQ ID NO: 3) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-007 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-008 (например, SEQ ID NO: 4) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-008 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-012 (например, SEQ ID NO: 4) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-012 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит одно или оба из: (i) VH, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VH моноклонального антитела ATG-013 (например, SEQ ID NO: 2) или (ii) VL, содержащую аминокислотную последовательность, которая отличается не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 11, 12, 13, 14 или 15 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 96, 97, 98, 99 или 100% аминокислотной последовательности VL моноклонального антитела ATG-013 (например, SEQ ID NO: 11).
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 100 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 101 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 102 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 103 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 104 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 105 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 106 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 107 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 108 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 109 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 110 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 111 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 112 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 113 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеотидной последовательностью SEQ ID NO: 114 (или нуклеотидной последовательностью по существу идентичной ей) или VL, кодируемую нуклеотидной последовательностью SEQ ID NO: 115 (или нуклеотидной последовательностью по существу идентичной ей) или обе последовательности.
В одном варианте реализации изобретения молекула антитела является моноклональным антителом ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую какую-либо аминокислотную последовательность из SEQ ID NO: 1-9, VL, содержащую какую-либо аминокислотную последовательность из SEQ ID NO: 10-15 или обе последовательности.
В одном варианте реализации изобретения молекула антитела является каким-либо из антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела является синтетической молекулой антитела. В одном варианте реализации изобретения молекула антитела является выделенной молекулой антитела. В одном варианте реализации изобретения молекула антитела является молекулой рекомбинантного антитела. В одном варианте реализации изобретения молекула антитела является гуманизированным антителом. В одном варианте реализации изобретения молекула антитела является молекулой моноспецифического антитела. В одном варианте реализации изобретения молекула антитела является молекулой мультиспецифического антитела.
В одном варианте реализации изобретения молекула антитела содержит две вариабельные области тяжелой цепи и две вариабельные области легкой цепи. В одном варианте реализации изобретения молекула антитела содержит антигенсвязывающий фрагмент. В одном варианте реализации изобретения молекула антитела содержит Fab, F(ab')2, Fv, scFv или Fd.
В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG, например, содержащей константную область тяжелой цепи IgG, например, выбранную из IgG1, IgG2, IgG3 или IgG4, например, IgG2 или IgG4. В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG1, например, имеющей описанную в настоящей заявке константную область IgG1. В другом варианте воплощения изобретения молекула антитела является молекулой антитела IgG2, например, имеющей описанную в настоящей заявке константную область IgG2. В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG3, например, имеющей описанную в настоящей заявке константную область IgG3. В другом варианте воплощения изобретения молекула антитела является молекулой антитела IgG4, например, имеющей описанную в настоящей заявке константную область IgG4. В другом варианте воплощения изобретения молекула антитела содержит химерную константную область, включающую изотипы IgG2, IgG3 и/или IgG4. В одном варианте реализации изобретения константная область тяжелой цепи содержит одну или более модификаций аминокислот в шарнирном участке, в CH2 или CH3 участке. В одном варианте реализации изобретения молекула антитела содержит константную область легкой цепи каппа или лямбда легкой цепи.
В одном варианте реализации изобретения молекула антитела содержит Fc-участок. В одном варианте реализации изобретения Fc-участок содержит одну или более мутаций. В одном варианте реализации изобретения Fc-участок содержит замещения Met-428-Leu и Asn-434-Ser в остатках, соответствующих метионину 428 и аспарагину 434, нумерация каждого согласно нумерации ЕС. В одном варианте реализации изобретения Fc-участок содержит одно, два или три из замещений Met-252-Tyr, Ser-254-Thr и Thr-256-Glu в остатках, соответствующих метионину 252, серину 254 и треонину 256, соответственно, нумерация каждого согласно нумерации ЕС.
В аспекте изобретение определяет отличительные признаки молекулы антитела, которая:
a) конкурирует за связывание с C5 с молекулой антитела к C5, содержащей участки, определяющие комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3) и участки, определяющие комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3) какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013, например, как описано в Таблице 1; или
b) связывается или по существу связывается с эпитопом, который полностью или частично перекрывается с эпитопом молекулы антитела к C5, содержащей участки, определяющие комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3) и участки, определяющие комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3) какого-либо из моноклональных антител ATG-001 (например, SEQ ID №№: 19, 28, 35, 38, 43 и/или 48, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 54, 59, 66, 71, 76 и/или 81, соответственно, согласно нумерации по Кабат/Kabat), ATG-002 (например, SEQ ID №№: 20, 28, 35, 38, 43 и/или 48, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 55, 59, 66, 71, 76 и/или 81, соответственно, согласно нумерации по Кабат/Kabat), ATG-003 (например, SEQ ID №№: 21, 29, 35, 38, 43 и/или 48, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 54, 60, 66, 71, 76 и/или 81, соответственно, согласно нумерации по Кабат/Kabat), ATG-004 (например, SEQ ID №№: 22, 29, 35, 38, 43, и/или 48, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 55, 60, 66, 71, 76 и/или 81, соответственно, согласно нумерации по Кабат/Kabat), ATG-005 (например, SEQ ID №№: 19, 28, 35, 38, 44 и/или 49, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 54, 59, 66, 71, 77 и/или 82, соответственно, согласно нумерации по Кабат/Kabat), ATG-006 (например, SEQ ID №№: 20, 28, 35, 38, 44 и/или 49, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 55, 59, 66, 71, 77 и/или 82, соответственно, согласно нумерации по Кабат/Kabat), ATG-007 (например, SEQ ID №№: 21, 29, 35, 38, 44 и/или 49, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 54, 60, 66, 71, 77, и/или 82, соответственно, согласно нумерации по Кабат/Kabat), ATG-008 (например, SEQ ID №№: 22, 29, 35, 38, 44 и/или 49, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 55, 60, 66, 71, 77 и/или 82, соответственно, согласно нумерации по Кабат/Kabat), ATG-012 (например, SEQ ID №№: 22, 29, 35, 38, 44 и/или 49, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 55, 60, 66, 71, 77, и/или 82, соответственно, согласно нумерации по Кабат/Kabat) или ATG-013 (например, SEQ ID №№: 22, 29, 35, 38, 44 и/или 49, соответственно, согласно нумерации по Чотиа/Chothia или SEQ ID №№: 55, 60, 66, 71, 77 и/или 82, соответственно, согласно нумерации по Кабат/Kabat), например, как описано в Таблице 1.
В одном варианте реализации изобретения молекула антитела конкурирует за связывание с молекулой антитела к C5, содержащей VH и VL какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела связывается или, по существу, связывается с эпитопом, который полностью или частично перекрывается с эпитопом молекулы антитела к C5, содержащей VH и VL какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела является синтетической молекулой антитела. В одном варианте реализации изобретения молекула антитела является выделенной молекулой антитела. В одном варианте реализации изобретения молекула антитела является молекулой рекомбинантного антитела. В одном варианте реализации изобретения молекула антитела является гуманизированным антителом. В одном варианте реализации изобретения молекула антитела является молекулой моноспецифического антитела. В одном варианте реализации изобретения молекула антитела является молекулой мультиспецифического антитела.
В одном варианте реализации изобретения молекула антитела конкурирует за связывание с двумя, тремя, четырьмя, пятью, шестью, семью или всеми молекулами антител к C5, содержащими НCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3 какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела конкурирует за связывание с двумя, тремя, четырьмя, пятью, шестью, семью или всеми молекулами антител к C5, содержащими VH и VL какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела связывается или по существу связывается с эпитопом, который полностью или частично перекрывается с эпитопами двух, трех, четырех, пяти, шести, семи или всех молекул антител к C5, содержащих HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3 какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела связывается или по существу связывается с эпитопом, который полностью или частично перекрывается с эпитопами двух, трех, четырех, пяти, шести, семи или всех молекул антител к C5, содержащих VH и VL какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела связывается или по существу связывается с эпитопом, который полностью или частично перекрывается с эпитопами двух, трех, четырех, пяти, шести, семи или всех молекул антител, содержащих HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3 какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела, содержит HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3 какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела связывается или по существу связывается с эпитопом, который полностью или частично перекрывается с эпитопами двух, трех, четырех, пяти, шести, семи или всех молекул антител, содержащих VH и VL какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013.
В одном варианте реализации изобретения молекула антитела является синтетической молекулой антитела. В одном варианте реализации изобретения молекула антитела является выделенной молекулой антитела. В одном варианте реализации изобретения молекула антитела является молекулой рекомбинантного антитела. В одном варианте реализации изобретения молекула антитела является гуманизированным антителом. В одном варианте реализации изобретения молекула антитела является молекулой моноспецифического антитела. В одном варианте реализации изобретения молекула антитела является молекулой мультиспецифического антитела.
В одном варианте реализации изобретения молекула антитела содержит две вариабельные области тяжелой цепи и две вариабельные области легкой цепи. В одном варианте реализации изобретения молекула антитела содержит антигенсвязывающий фрагмент. В одном варианте реализации изобретения молекула антитела содержит Fab, F(ab')2, Fv, scFv или Fd.
В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG, например, содержащей константную область тяжелой цепи IgG, например, выбранную из IgG1, IgG2, IgG3 или IgG4, например, IgG2 или IgG4. В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG1, например, имеющей описанную в настоящей заявке константную область IgG1. В другом варианте воплощения изобретения молекула антитела является молекулой антитела IgG2, например, имеющей описанную в настоящей заявке константную область IgG2. В одном варианте реализации изобретения молекула антитела является молекулой антитела IgG3, например, имеющей описанную в настоящей заявке константную область IgG3. В другом варианте воплощения изобретения молекула антитела является молекулой антитела IgG4, например, имеющей описанную в настоящей заявке константную область IgG4. В другом варианте воплощения изобретения молекула антитела содержит химерную константную область, включающую изотипы IgG2, IgG3 и/или IgG4. В одном варианте реализации изобретения константная область тяжелой цепи содержит одну или более модификаций аминокислот в шарнирном участке, в CH2 или CH3 участке. В одном варианте реализации изобретения молекула антитела содержит константную область легкой цепи каппа или лямбда легкой цепи.
В одном варианте реализации изобретения молекула антитела содержит Fc-участок. В одном варианте реализации изобретения Fc-участок содержит одну или более мутаций. В одном варианте реализации изобретения Fc-участок содержит замещения Met-428-Leu и Asn-434-Ser в остатках, соответствующих метионину 428 и аспарагину 434, нумерация каждого согласно нумерации ЕС. В одном варианте реализации изобретения Fc-участок содержит одно, два или три из замещений Met-252-Tyr, Ser-254-Thr и Thr-256-Glu в остатках, соответствующих метионину 252, серину 254 и треонину 256, соответственно, нумерация каждого согласно нумерации ЕС.
В аспекте изобретение определяет отличительные признаки композиции, например, фармацевтической композиции, содержащей описанную в настоящей заявке молекулу антитела. В одном варианте реализации изобретения композиция дополнительно содержит фармацевтически приемлемый носитель.
В аспекте изобретение определяет отличительные признаки молекулы нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи (VH), вариабельную область легкой цепи (VL) или обе области описанной в настоящей заявке молекулы антитела.
В аспекте изобретение определяет отличительные признаки вектора, содержащего описанную в настоящей заявке молекулу нуклеиновой кислоты.
В аспекте изобретение определяет отличительные признаки клетки, например, выделенной клетки, содержащей описанную в настоящей заявке молекулу нуклеиновой кислоты или описанный в настоящей заявке вектор.
В аспекте изобретение определяет отличительные признаки набора, содержащего описанную в настоящей заявке молекулу антитела и инструкции по применению молекулы антитела.
В аспекте изобретение определяет отличительные признаки контейнера, содержащего описанную в настоящей заявке молекулу нуклеиновой кислоты.
В аспекте изобретение определяет отличительные признаки способа получения молекулы антитела к C5, способ, включающий культивирование описанной в настоящей заявке клетки в условиях, позволяющих продуцировать молекулу антитела, тем самым получая молекулу антитела.
В одном варианте реализации изобретения способ дополнительно включает выделение молекулы антитела.
В аспекте изобретение определяет отличительные признаки способа лечения нарушения, связанного с комплементом, например, описанного в настоящей заявке нарушения, связанного с комплементом, способа, включающего введение субъекту, нуждающемуся в этом, эффективного количества описанной в настоящей заявке молекулы антитела или описанной в настоящей заявке композиции, посредством чего происходит лечение нарушения, связанного с комплементом.
В одном варианте реализации изобретения нарушение, связанное с комплементом, является воспалением. В одном варианте реализации изобретения нарушение, связанное с комплементом, выбрано из группы, состоящей из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aГУС), типичного или инфекционного гемолитико-уремического синдрома (тГУС), болезни плотных депозитов (БПД), пароксизмальной ночной гемоглобинурии (ПНГ), оптического нейромиелита (НМО), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (ТТП); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита и тромботической микроангиопатии (ТМА). В одном варианте реализации изобретения нарушение, связанное с комплементом, является ПНГ. В одном варианте реализации изобретения нарушение, связанное с комплементом, является аГУС.
В одном варианте реализации изобретения субъект является человеком. В одном варианте реализации изобретения молекулу антитела вводят субъекту внутривенно.
В одном варианте реализации изобретения молекулу антитела вводят субъекту в дозе от 0,1 мг/кг до 50 мг/кг, например, от 0,2 мг/кг до 25 мг/кг, от 0,5 мг/кг до 10 мг/кг, от 0,5 мг/кг до 5 мг/кг, от 0,5 мг/кг до 3 мг/кг, от 0,5 мг/кг до 2,5 мг/кг, от 0,5 мг/кг до 2 мг/кг, от 0,5 мг/кг до 1,5 мг/кг, от 0,5 мг/кг до 1 мг/кг, от 1 мг/кг до 1,5 мг/кг, от 1 мг/кг до 2 мг/кг, от 1 мг/кг до 2,5 мг/кг, от 1 мг/кг до 3 мг/кг, от 1 мг/кг до 2,5 мг/кг или от 1 мг/кг до 5 мг/кг.
В одном варианте реализации изобретения молекулу антитела вводят субъекту в фиксированной дозе от 10 мг до 1000 мг, например, от 10 мг до 500 мг, от 10 мг до 250 мг, от 10 мг до 150 мг, от 10 мг до 100 мг, от 10 мг до 50 мг, от 250 мг до 500 мг, от 150 мг до 500 мг, от 100 мг до 500 мг, от 50 мг до 500 мг, от 25 мг до 250 мг, от 50 мг до 150 мг, от 50 мг до 100 мг, от 100 мг до 150 мг, от 100 мг до 200 мг или от 150 мг до 250 мг.
В одном варианте реализации изобретения молекулу антитела вводят один раз в неделю, два раза в неделю, один раз в две недели, один раз в три недели, один раз в четыре недели, один раз в восемь недель, один раз в месяц, один раз в два месяца или один раз в три месяца.
В одном варианте реализации изобретения введение молекулы антитела снижает активность C5 в ткани, например, в крови или в клетках крови (например, эритроцитах).
В одном варианте реализации изобретения способ дополнительно включает введение субъекту второго лекарственного средства в связи с нарушением, связанным с комплементом.
В аспекте изобретение определяет отличительные признаки способа снижения активности C5 в клетке или субъекте, способа, включающего приведение в контакт с клеткой или субъектом или введение субъекту, нуждающемуся в этом, эффективного количества описанной в настоящей заявке молекулы антитела или описанной в настоящей заявке композиции, посредством чего снижается активность C5.
В одном варианте реализации изобретения клетка является клеткой человека. В одном варианте реализации изобретения субъект является человеком.
В одном варианте реализации изобретения стадия приведения в контакт происходит в условиях in vitro, ex vivo или in vivo. В одном варианте реализации изобретения молекулу антитела вводят субъекту внутривенно.
В одном варианте реализации изобретения молекулу антитела вводят субъекту в дозе от 0,1 мг/кг до 50 мг/кг, например, от 0,2 мг/кг до 25 мг/кг, от 0,5 мг/кг до 10 мг/кг, от 0,5 мг/кг до 5 мг/кг, от 0,5 мг/кг до 3 мг/кг, от 0,5 мг/кг до 2,5 мг/кг, от 0,5 мг/кг до 2 мг/кг, от 0,5 мг/кг до 1,5 мг/кг, от 0,5 мг/кг до 1 мг/кг, от 1 мг/кг до 1,5 мг/кг, от 1 мг/кг до 2 мг/кг, от 1 мг/кг до 2,5 мг/кг, от 1 мг/кг до 3 мг/кг, от 1 мг/кг до 2,5 мг/кг или от 1 мг/кг до 5 мг/кг.
В одном варианте реализации изобретения молекулу антитела вводят субъекту в фиксированной дозе от 10 мг до 1000 мг, например, от 10 мг до 500 мг, от 10 мг до 250 мг, от 10 мг до 150 мг, от 10 мг до 100 мг, от 10 мг до 50 мг, от 250 мг до 500 мг, от 150 мг до 500 мг, от 100 мг до 500 мг, от 50 мг до 500 мг, от 25 мг до 250 мг, от 50 мг до 150 мг, от 50 мг до 100 мг, от 100 мг до 150 мг, от 100 мг до 200 мг или от 150 мг до 250 мг.
В одном варианте реализации изобретения молекулу антитела вводят один раз в неделю, два раза в неделю, один раз в две недели, один раз в три недели, один раз в четыре недели, один раз в восемь недель, один раз в месяц, один раз в два месяца, один раз в три месяца.
В одном варианте реализации изобретения введение молекулы антитела снижает активность C5 в ткани, например, в крови или в клетках крови (например, эритроцитах).
В аспекте изобретение определяет отличительные признаки применения описанной в настоящей заявке молекулы антитела или описанной в настоящей заявке композиции для лечения или при получении лекарственного средства для лечения описанного в настоящей заявке расстройства.
В другом аспекте изобретение определяет отличительные признаки описанной в настоящей заявке молекулы антитела или описанной в настоящей заявке композиции для использования при лечении описанного в настоящей заявке расстройства
В аспекте изобретение определяет отличительные признаки способа обнаружения молекулы C5, способа, включающего контакт клетки или образца, отобранного у субъекта, с описанной в настоящей заявке молекулой антитела, посредством чего обнаруживается молекула C5.
В одном варианте реализации изобретения молекула антитела конъюгирована с детектируемой меткой. В одном варианте реализации изобретения молекулу C5 обнаруживают в условиях in vitro или ex vivo. В другом варианте воплощения изобретения молекулу C5 обнаруживают в условиях in vivo.
Изобретение предполагает все комбинации какого-либо одного или более из вышеупомянутых аспектов и/или вариантов воплощения изобретения, а также комбинации с каким-либо одним или более вариантами воплощения изобретения, изложенными в подробном описании изобретения и примерах.
Другие отличительные признаки, цели и преимущества композиций и способов в настоящей заявке будут очевидны из описания и чертежей, а также из формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГУРЫ 1A-1B являются набором диаграмм, демонстрирующих оценку чистоты и целостности указанных иллюстративных моноклональных антител к C5 с использованием (ФИГ. 1A) способа ДСН-ПААГ в невосстанавливающих или восстанавливающих условиях и (ФИГ. 1B) способа эксклюзионной хроматографии (SEC). ATG-001, ATG-002, ATG-003, ATG-005, ATG-006, ATG-007 содержат их соответствующие последовательности VH и VL, представленные в Таблице 1, в сочетании с последовательностью константной области тяжелой цепи IgG-1; ATG-004 и ATG-008 содержат их соответствующие последовательности VH и VL, представленные в Таблице 1, в сочетании с последовательностью константной области тяжелой цепи IgG2/4-LS; и ATG-012 и ATG-013 содержат их соответствующие последовательности VH и VL, представленные в Таблице 1, в сочетании с последовательностью константной области тяжелой цепи IgG2/4-YTE.
ФИГУРЫ 2A-2B являются набором диаграмм, демонстрирующих функциональную оценку сконструированных моноклональных антител к C5. ФИГ. 2A демонстрирует связывание указанных иллюстративных моноклональных антител к C5 с C5 человека. ФИГ. 2B демонстрирует ингибирование гемолиза cRBC указанными иллюстративными моноклональными антителами к C5. ATG-001, ATG-002, ATG-003, ATG-005, ATG-006, ATG-007 содержат их соответствующие последовательности VH и VL, представленные в Таблице, 1 в сочетании с последовательностью константной области тяжелой цепи IgG-1; ATG-004 и ATG-008 содержат их соответствующие последовательности VH и VL, представленные в Таблице 1, в сочетании с последовательностью константной области тяжелой цепи IgG2/4-LS; и ATG-012 содержит их соответствующие последовательности VH и VL, представленные в Таблице 1, в сочетании с последовательностью константной области тяжелой цепи IgG2/4-YTE.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящей заявке раскрыты молекулы антител, связывающиеся с С5, например, C5 человека, с высокой аффинностью и специфичностью. Преимущество состоит в том, что несколько из описанных в настоящей заявке молекул антител обладают улучшенной способностью снижать (например, ингибировать, блокировать или нейтрализовать) одну или более биологических активностей C5. Также предложены молекулы нуклеиновых кислот, кодирующие молекулы антител, векторы экспрессии, клетки-хозяева, композиции (например, фармацевтические композиции), наборы и способы создания молекул антител. Раскрытые в настоящей заявке молекулы антител и фармацевтические композиции возможно использовать (отдельно или в комбинации с другими агентами или терапевтическими средствами) для лечения, предотвращения и/или диагностики расстройств и состояний, например, расстройств и состояний, связанных с активацией C5.
Определения
Термины, используемые в настоящей заявке в единственном числе обозначают одно или более чем одно (например, по меньше мере один).
Используемый в настоящей заявке термин «или» обозначает и используется взаимозаменяемо с термином «и/или», если контекст однозначно не указывает иное.
«Примерно» и «приблизительно», как правило, будут обозначать приемлемую степень погрешности измеряемой величины с учетом характера или точности измерений. Иллюстративными степенями погрешности являются значения в пределах 20 процентов (%), как правило, в пределах 10% и, большей частью в пределах 5% (например, в пределах 4%, 3%, 2% или 1%) от заданного значения или диапазона значений.
Раскрытые в настоящей заявке композиции и способы охватывают полипептиды и нуклеиновые кислоты, содержащие указанные последовательности, или последовательности по существу идентичные или схожие с ними, например, последовательности по меньшей мере на 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более идентичные указанной последовательности.
В отношении аминокислотной последовательности термин «по существу идентичный» в настоящей заявке обозначает первую аминокислоту, содержащую достаточное или минимальное количество аминокислотных остатков, которые являются а) идентичными или б) консервативными заменами выровненных аминокислотных остатков во второй аминокислотной последовательности, таким образом, что первая и вторая аминокислотные последовательности могут иметь общий структурный домен и/или общую функциональную активность. Например, аминокислотные последовательности, содержащие общий структурный домен по меньшей мере на примерно 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичный эталонной последовательности, например, последовательности, предоставленной в настоящей заявке.
В отношении нуклеотидной последовательности термин «по существу идентичный» в настоящей заявке обозначает последовательность первой нуклеиновой кислоты, содержащую достаточное или минимальное количество нуклеотидов, которые являются идентичными выровненным нуклеотидам в последовательности второй нуклеиновой кислоты, таким образом, что первая и вторая нуклеотидные последовательности кодируют полипептид, обладающий общей функциональной активностью, или кодируют общий структурный домен полипептида, или общую функциональную активность полипептида. Например, нуклеотидные последовательности по меньшей мере на примерно 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичные эталонной последовательности, например, последовательности, предоставленной в настоящей заявке.
Термин «функциональный вариант» обозначает полипептиды, содержащие аминокислотную последовательность по существу идентичную последовательности, встречающейся в природе, или они кодируются по существу идентичной нуклеотидной последовательностью и способны обладать одной или более активностями последовательности, встречающейся в природе.
Определение гомологичности или идентичности между последовательностями (термины используют в настоящей заявке взаимозаменяемо) проводят следующим образом.
Для определения процента идентичности двух аминокислотных последовательностей или двух последовательностей нуклеиновых кислот последовательности выравнивают для оптимального сравнения (например, гэпы (пробелы) могут быть введены в одну или обе из первой и второй аминокислотной последовательности или последовательности нуклеиновых кислот для оптимального выравнивания, а негомологичные последовательности возможно не учитывать при сравнении). В иллюстративном варианте воплощения изобретения длина эталонной последовательности, выровненной для сравнения, составляет по меньшей мере 30%, например, по меньшей мере 40%, 50%, 60%, 70%, 80%, 90% или 100% от длины эталонной последовательности. Затем сравнивают аминокислотные остатки или нуклеотиды в соответствующих аминокислотных или нуклеотидных положениях. Если положение в первой последовательности занято тем же аминокислотным остатком или нуклеотидом, что и соответствующее положение во второй последовательности, тогда молекулы идентичны по этому положению.
Процент идентичности двух последовательностей является функцией количества идентичных положений, общих для последовательностей, с учетом количества гэпов (пробелов) и длины каждого гэпа (пробела), которые необходимо ввести для оптимального выравнивания двух последовательностей.
Сравнение последовательностей и определение процента идентичности двух последовательностей могут быть выполнены с использованием математического алгоритма. В одном варианте реализации изобретения процент идентичности двух аминокислотных или нуклеотидных последовательностей определяют с использованием Clustal Omega (Sievers et al. Mol Syst Biol. 2011; 7:539). В одном варианте реализации изобретения процент идентичности двух аминокислотных или нуклеотидных последовательностей определяют с использованием Kalign2 (Lassmann et al. Nucleic Acids Res. 2009; 37(3):858-65; Lassmann and Sonnhammer BMC Bioinformatics. 2005; 6:298). В одном варианте реализации изобретения процент идентичности двух аминокислотных или нуклеотидных последовательностей определяют с использованием MAFFT (Katoh and Standley Mol Biol Evol. 2013; 30(4):772-80). В одном варианте реализации изобретения процент идентичности двух аминокислотных или нуклеотидных последовательностей определяют с использованием MUSCLE (Edgar Nucleic Acids Res. 2004; 32(5):1792-7; Edgar BMC Bioinformatics. 2004; 5:113). В одном варианте реализации изобретения процент идентичности двух аминокислотных или нуклеотидных последовательностей определяют с использованием MView (Brown et al. Bioinformatics. 1998; 14(4):380-1). Также описаны другие способы определения процента идентичности двух последовательностей, например, в Li et al. Nucleic Acids Res. 2015; 43(W1):W580-4; McWilliam et al. Nucleic Acids Res. 2013; 41(Web Server issue):W597-600.
В одном варианте реализации изобретения процент идентичности двух аминокислотных последовательностей определяют с использованием алгоритма Нидлмана и Вунша/Needleman and Wunsch (J Mol Biol. 1970; 48(3):443-53), который включен в программу GAP в пакете программного обеспечения GCG (доступен на сайте www.gcg.com), с использованием либо матрицы Blossum 62, либо матрицы PAM250 и вес гэпа (пробела) составляет 16, 14, 12, 10, 8, 6 или 4 и вес длины составляет 1, 2, 3, 4, 5 или 6. В одном варианте реализации изобретения процент идентичности двух нуклеотидных последовательностей определяют с использованием программы GAP в пакете программного обеспечения GCG (доступен на сайте www.gcg.com) с использованием NWSgapdna. Матрица CMP и вес гэпа (пробела) составляет 40, 50, 60, 70 или 80 и длина гэпа (пробела) составляет 1, 2, 3, 4, 5 или 6. Подходящим набором параметров (и таким, который необходимо использовать, если не указано иное) является матрица замен Blossum 62 со штрафом за гэп (пробел), составляющим 12, штрафом за продолжение гэпа (пробела), составляющим 4, и штрафом за гэп (пробел) со сдвигом рамки считывания, составляющим 5.
Процент идентичности двух аминокислотных или нуклеотидных последовательностей возможно определить с использованием алгоритма Мейерса и Миллера/Meyers and Miller (Comput Appl Biosci. 1988; 4(1):11-7), который включен в программу ALIGN (версия 2.0) с использованием таблицы веса остатков PAM120, штраф за длину гэпа (пробела) составляет 12 и штраф за гэп (пробел) составляет 4.
Описанные в настоящей заявке последовательности нуклеиновых кислот и белков возможно использовать в качестве «запрашиваемой последовательности» для проведения поиска в общедоступных базах данных, например, для идентификации других представителей семейства или родственных последовательностей. Указанные виды поиска возможно выполнить с помощью программ NBLAST и XBLAST (версия 2.0) согласно Altschul, et al. 1990; J. Mol. Biol. 215:403-10. Поиск нуклеотидов в BLAST возможно выполнить с помощью программы NBLAST, очки=100, длина слова=12 для получения нуклеотидных последовательностей, гомологичных описанной в настоящей заявке нуклеиновой кислоте. Поиск белков в BLAST возможно выполнить с помощью программы XBLAST, очки=50, длина слова=3 для получения аминокислотных последовательностей, гомологичных описанным в настоящей заявке молекулам белка. Для получения выравниваний с гэпами (пропусками) для сравнения возможно использовать Gapped BLAST, как описано у Altschul et al., Nucleic Acids Res. 1997; 25:3389-3402. При использовании программ BLAST и Gapped BLAST возможно использовать параметры по умолчанию соответствующих программ (например, XBLAST и NBLAST). См. www.ncbi.nlm.nih.gov.
Используемый в настоящей заявке термин «гибридизуется в условиях «низкой жесткости», «средней жесткости», «высокой жесткости» или «очень высокой жесткости»» описывают условия гибридизации и отмывки. Руководство по проведению реакций гибридизации возможно найти в литературном источнике Current Protocols in Molecular Biology, John Wiley & Sons, N.Y. (1989), 6.3.1-6.3.6, который включен в данный документ посредством ссылки. В указанном источнике описаны водные и неводные способы, и какой-либо из них может быть использован. Конкретные условия гибридизации, указанные в настоящей заявке, следующие: 1) гибридизация в условиях «низкой жесткости» в 6X натрия хлориде/натрия цитрате (SSC) при примерно 45°C с последующими двумя отмывками в 0,2X SSC, 0,1% SDS при по меньшей мере 50°C (температуру отмывки возможно увеличить до 55°C для условий «низкой жесткости»); 2) гибридизация в условиях «средней жесткости» в 6X SSC при примерно 45°C с последующими одной или более отмывками в 0,2X SSC, 0,1% SDS при 60°C; 3) гибридизация в условиях «высокой жесткости» в 6X SSC при примерно 45°C с последующими одной или более отмывками в 0,2X SSC, 0,1% при 65°C и предпочтительно 4) гибридизация в условиях «очень высокой жесткости»: 0,5 M натрия фосфат, 7% SDS при 65°C с последующими одной или более отмывками в 0,2X SSC, 1% SDS при 65°C. Условия «очень высокой жесткости» 4) являются подходящими условиями и такими, которые необходимо использовать, если не указано иное.
Подразумевается, что описанные в настоящей заявке молекулы могут иметь дополнительные консервативные замены или замены заменимых аминокислот, не оказывающие существенного влияния на их функции.
Термин «аминокислота» предназначен для охвата всех молекул, как природных, так и синтетических, которые включают как функциональную аминогруппу, так и функциональную кислотную группу и могут быть включены в полимер аминокислот, встречающихся в природе. Иллюстративные аминокислоты включают аминокислоты, встречающиеся в природе; их аналоги, производные и родственные им аминокислоты; аналоги аминокислот, содержащие разные боковые цепи, и все стереоизомеры какой-либо из вышеперечисленных молекул. Используемый в настоящей заявке термин «аминокислота» включает как D- или L-оптические изомеры, так и пептидомиметики.
«Консервативная аминокислотная замена» является заменой, при которой аминокислотный остаток заменяется аминокислотным остатком, имеющим схожую боковую цепь. Семейства аминокислотных остатков, имеющих схожие боковые цепи, известны в данной области техники. Указанные семейства включают аминокислоты с боковыми цепями, обладающими основными свойствами (например, лизин, аргинин, гистидин), с боковыми цепями, обладающими кислотными свойствами (например, аспарагиновая кислота, глутаминовая кислота), с незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин), с неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), с бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и с ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин).
В настоящей заявке термины «полипептид», «пептид» и «белок» (если он одноцепочечный) используют взаимозаменяемо для обозначения полимеров аминокислот какой-либо длины. Полимер может быть линейным или разветвленным, может содержать модифицированные аминокислоты и может прерываться кислотами, отличными от аминокислот. Термины также включают аминокислотный полимер, который был модифицирован, например, образование дисульфидной связи, гликозилирование, липидирование, ацетилирование, фосфорилирование или какая-либо иная манипуляция, такая как конъюгация с метящим компонентом. Полипептид может быть выделен из природных источников, может быть получен рекомбинантными способами из эукариотического или прокариотического хозяина или может являться продуктом синтетических способов.
Термины «нуклеиновая кислота», «последовательность нуклеиновой кислоты», «нуклеотидная последовательность» или «полинуклеотидная последовательность» и «полинуклеотид» используют взаимозаменяемо. Они обозначают полимерную форму нуклеотидов какой-либо длины, дезоксирибонуклеотидов или рибонуклеотидов или их аналогов. Полинуклеотид может быть одноцепочечным или двухцепочечным, и если он является одноцепочечным, он может быть кодирующей цепью или некодирующей (антисмысловой) цепью. Полинуклеотид может содержать модифицированные нуклеотиды, такие как метилированные нуклеотиды и аналоги нуклеотидов. Последовательность нуклеотидов может прерываться компонентами, отличными от нуклеотидов. Полинуклеотид может быть дополнительно модифицированным после полимеризации, например, путем конъюгации с метящим компонентом. Нуклеиновая кислота может быть рекомбинантным полинуклеотидом или полинуклеотидом геномного происхождения, полинуклеотидом из кДНК, полинуклеотидом полусинтетического или синтетического происхождения, который либо не встречается в природе, либо конъюгирован с другим полинуклеотидом, имеющим структуру, не встречающуюся в природе.
В настоящей заявке термин «выделенный» обозначает материал, который удален из его исходного или нативного окружения (например, естественного окружения, если он встречается в природе). Например, полинуклеотид, встречающийся в природе, или полипептид, присутствующий в живом животном, не изолируют, однако изолируют тот же полинуклеотид или полипептид, отделенный вмешательством человека от некоторых или всех сосуществующих материалов в естественной системе. Такие полинуклеотиды могут быть частью вектора и/или такие полинуклеотиды или полипептиды могут входить в состав композиции и при этом бытьвыделенными, поскольку такой вектор или композиция не являются частью среды, в которой они встречаются в природе.
В настоящей заявке термин «лечить», например, комплемент-опосредованное расстройство, обозначает, что субъект (например, человек), имеющий расстройство, например, комплемент-опосредованное расстройство, и/или у которого есть симптом расстройства, например, комплемент-опосредованного расстройства, в одном варианте реализации изобретения будет иметь симптомы в меньшей степени тяжелые и/или у него быстрее будет наступать выздоровление при введении молекулы антитела, чем если бы молекула антитела никогда не вводилась. В одном варианте реализации изобретения при лечении комплемент-опосредованного расстройства, уровень C5a и/или C5b может быть ниже у субъекта, получающего лечение в сравнении с сопоставимым субъектом, не получающим лечение. Например, диагностическое исследование способом иммунофлуоресценции или электронной микроскопии будет обнаруживать C5a и/или C5b в биологическом образце субъекта после введения описанной в настоящей заявке молекулы антитела для эффективного лечения воспалительного заболевания. Другие способы определения, например, анализы мочи, анализы крови, ультразвуковое обследование, рентгенография или цистоскопия также могут быть использованы для контроля лечения у пациента или для обнаружения наличия, например, уменьшения (или отсутствия) симптома расстройства, например, комплемент-опосредованного расстройства, после лечения расстройства у субъекта. Лечение может, например, частично или полностью облегчить, нормализовать, ослабить, ингибировать или уменьшить тяжесть, и/или уменьшить частоту, и, необязательно, отсрочить начало одного или более проявлений эффектов или симптомов, особенностей и/или причин расстройства, например, комплемент-опосредованного расстройства. В одном варианте реализации изобретения лечение проводится для субъекта, у которого не проявляются определенные признаки расстройства, например, комплемент-опосредованного расстройства, и/или субъекта, у которого проявляются только ранние признаки расстройства, например, комплемент-опосредованного расстройства. В одном варианте реализации изобретения проводится лечение субъекта, у которого проявляются один или более установленных признаков расстройства, например, комплемент-опосредованного расстройства. В одном варианте реализации изобретения проводится лечение субъекта, у которого диагностировано расстройство, например, комплемент-опосредованное расстройство. В одном варианте реализации изобретения расстройство является описанным в настоящей заявке расстройством, связанным с комплементом.
В настоящей заявке термин «предотвращает» расстройство, например, комплемент-опосредованное расстройство, обозначает, что субъект (например, человек) с меньшей вероятностью будет иметь расстройство, например, комплемент-опосредованное расстройство, если субъект получает молекулу антитела. В одном варианте реализации изобретения у субъекта есть риск развития расстройства, например, комплемент-опосредованного расстройства. В одном варианте реализации изобретения расстройство является описанным в настоящей заявке расстройством, связанным с комплементом.
Различные аспекты описанных в настоящей заявке композиций и способов более подробно описаны ниже. Дополнительные определения приведены в описании.
Компонент 5 комплемента
Компонент 5 комплемента, также известный как C5, C5D, C5a, C5b, CPAMD4, ECLZB или комплемент C5, является белком, кодируемым у человека геном C5.
С5 является пятым компонентом системы комплемента, который принимает участие в процессах воспаления и уничтожения клеток. C5 состоит из альфа- и бета-полипептидных цепей, соединенных дисульфидным мостиком. C5 расщепляется на C5a и C5b. Активирующий пептид C5a, который является анафилатоксином, обладающим спазмогенной и хемотаксической активностью, синтезируется из альфа-полипептида посредством расщепления C5-конвертазой. Продукт макромолекулярного расщепления C5b может образовывать комплекс с компонентом C6 комплемента и указанный комплекс является основой для образования мембраноатакующего комплекса, который включает дополнительные компоненты комплемента.
Иллюстративные пути комплемента, включая типы, функции и регуляцию описаны, например, Srijana Khanal на microbeonline.com/complement-system-pathways-functions-regulation/ 5 ноября 2017 г.
Иллюстративные аминокислотные и нуклеотидные последовательности C5 человека описаны, например, в SEQ ID NO: 53.
Аминокислотная последовательность C5 человека предоставлена следующим образом.
C5 человека (SEQ ID NO: 53)
MGLLGILCFLIFLGKTWGQEQTYVISAPKIFRVGASENIVIQVYGYTEAFDATISIKSYPDKKFSYSSGHVHLSSENKFQNSAILTIQPKQLPGGQNPVSYVYLEVVSKHFSKSKRMPITYDNGFLFIHTDKPVYTPDQSVKVRVYSLNDDLKPAKRETVLTFIDPEGSEVDMVEEIDHIGIISFPDFKIPSNPRYGMWTIKAKYKEDFSTTGTAYFEVKEYVLPHFSVSIEPEYNFIGYKNFKNFEITIKARYFYNKVVTEADVYITFGIREDLKDDQKEMMQTAMQNTMLINGIAQVTFDSETAVKELSYYSLEDLNNKYLYIAVTVIESTGGFSEEAEIPGIKYVLSPYKLNLVATPLFLKPGIPYPIKVQVKDSLDQLVGGVPVTLNAQTIDVNQETSDLDPSKSVTRVDDGVASFVLNLPSGVTVLEFNVKTDAPDLPEENQAREGYRAIAYSSLSQSYLYIDWTDNHKALLVGEHLNIIVTPKSPYIDKITHYNYLILSKGKIIHFGTREKFSDASYQSINIPVTQNMVPSSRLLVYYIVTGEQTAELVSDSVWLNIEEKCGNQLQVHLSPDADAYSPGQTVSLNMATGMDSWVALAAVDSAVYGVQRGAKKPLERVFQFLEKSDLGCGAGGGLNNANVFHLAGLTFLTNANADDSQENDEPCKEILRPRRTLQKKIEEIAAKYKHSVVKKCCYDGACVNNDETCEQRAARISLGPRCIKAFTECCVVASQLRANISHKDMQLGRLHMKTLLPVSKPEIRSYFPESWLWEVHLVPRRKQLQFALPDSLTTWEIQGVGISNTGICVADTVKAKVFKDVFLEMNIPYSVVRGEQIQLKGTVYNYRTSGMQFCVKMSAVEGICTSESPVIDHQGTKSSKCVRQKVEGSSSHLVTFTVLPLEIGLHNINFSLETWFGKEILVKTLRVVPEGVKRESYSGVTLDPRGIYGTISRRKEFPYRIPLDLVPKTEIKRILSVKGLLVGEILSAVLSQEGINILTHLPKGSAEAELMSVVPVFYVFHYLETGNHWNIFHSDPLIEKQKLKKKLKEGMLSIMSYRNADYSYSVWKGGSASTWLTAFALRVLGQVNKYVEQNQNSICNSLLWLVENYQLDNGSFKENSQYQPIKLQGTLPVEARENSLYLTAFTVIGIRKAFDICPLVKIDTALIKADNFLLENTLPAQSTFTLAISAYALSLGDKTHPQFRSIVSALKREALVKGNPPIYRFWKDNLQHKDSSVPNTGTARMVETTAYALLTSLNLKDINYVNPVIKWLSEEQRYGGGFYSTQDTINAIEGLTEYSLLVKQLRLSMDIDVSYKHKGALHNYKMTDKNFLGRPVEVLLNDDLIVSTGFGSGLATVHVTTVVHKTSTSEEVCSFYLKIDTQDIEASHYRGYGNSDYKRIVACASYKPSREESSSGSSHAVMDISLPTGISANEEDLKALVEGVDQLFTDYQIKDGHVILQLNSIPSSDFLCVRFRIFELFEVGFLSPATFTVYEYHRPDKQCTMFYSTSNIKIQKVCEGAACKCVEADCGQMQEELDLTISAETRKQTACKPEIAYAYKVSITSITVENVFVKYKATLLDIYKTGEAVAEKDSEITFIKKVTCTNAELVKGRQYLIMGKEALQIKYNFSFRYIYPLDSLTWIEYWPRDTTCSSCQAFLANLDEFAEDIFLNGC
Другой вариант и альтернативные последовательности C5 человека предложены, например, как Genbank Accession Nos. NP_001304092.1 (изоформа 2), NP_001304093.1 (прекурсор изоформы 3) и NP_001726.2 (препротеин изоформы 1) по состоянию на 11 июня 2018 г. Соответствующие нуклеотидные последовательности, кодирующие перечисленные выше последовательности C5 человека, предложены как Genbank Accession Nos. NM_001317163.1, NM_001317164.1 и NM_001735.2 по состоянию на 11 июня 2018 г.
Иллюстративные аминокислотные и нуклеотидные последовательности C5 мыши (также называемые гемолитическим комплементом, Hc, He, C5a или Hfib2) описаны, например, в Genbank Accession Nos. NP_034536.2 и NM_010406.2, соответственно, по состоянию на 11 июня 2018 г.
Аминокислотная последовательность C5 мыши предоставлена следующим образом.
SEQ ID NO: 93
MPLPAMGLWGILCLLIFLDKTWGQEQTYVISAPKILRVGSSENVVIQVHGYTEAFDATLSLKSYPDKKVTFSSGYVNLSPENKFQNAALLTLQPNQVPREESPVSHVYLEVVSKHFSKSKKIPITYNNGILFIHTDKPVYTPDQSVKIRVYSLGDDLKPAKRETVLTFIDPEGSEVDIVEENDYTGIISFPDFKIPSNPKYGVWTIKANYKKDFTTTGTAYFEIKEYVLPRFSVSIELERTFIGYKNFKNFEITVKARYFYNKVVPDAEVYAFFGLREDIKDEEKQMMHKATQAAKLVDGVAQISFDSETAVKELSYNSLEDLNNKYLYIAVTVTESSGGFSEEAEIPGVKYVLSPYTLNLVATPLFVKPGIPFSIKAQVKDSLEQAVGGVPVTLMAQTVDVNQETSDLETKRSITHDTDGVAVFVLNLPSNVTVLKFEIRTDDPELPEENQASKEYEAVAYSSLSQSYIYIAWTENYKPMLVGEYLNIMVTPKSPYIDKITHYNYLILSKGKIVQYGTREKLFSSTYQNINIPVTQNMVPSARLLVYYIVTGEQTAELVADAVWINIEEKCGNQLQVHLSPDEYVYSPGQTVSLDMVTEADSWVALSAVDRAVYKVQGNAKRAMQRVFQALDEKSDLGCGAGGGHDNADVFHLAGLTFLTNANADDSHYRDDSCKEILRSKRNLHLLRQKIEEQAAKYKHSVPKKCCYDGARVNFYETCEERVARVTIGPLCIRAFNECCTIANKIRKESPHKPVQLGRIHIKTLLPVMKADIRSYFPESWLWEIHRVPKRKQLQVTLPDSLTTWEIQGIGISDNGICVADTLKAKVFKEVFLEMNIPYSVVRGEQIQLKGTVYNYMTSGTKFCVKMSAVEGICTSGSSAASLHTSRPSRCVFQRIEGSSSHLVTFTLLPLEIGLHSINFSLETSFGKDILVKTLRVVPEGVKRESYAGVILDPKGIRGIVNRRKEFPYRIPLDLVPKTKVERILSVKGLLVGEFLSTVLSKEGINILTHLPKGSAEAELMSIAPVFYVFHYLEAGNHWNIFYPDTLSKRQSLEKKIKQGVVSVMSYRNADYSYSMWKGASASTWLTAFALRVLGQVAKYVKQDENSICNSLLWLVEKCQLENGSFKENSQYLPIKLQGTLPAEAQEKTLYLTAFSVIGIRKAVDICPTMKIHTALDKADSFLLENTLPSKSTFTLAIVAYALSLGDRTHPRFRLIVSALRKEAFVKGDPPIYRYWRDTLKRPDSSVPSSGTAGMVETTAYALLASLKLKDMNYANPIIKWLSEEQRYGGGFYSTQDTINAIEGLTEYSLLLKQIHLDMDINVAYKHEGDFHKYKVTEKHFLGRPVEVSLNDDLVVSTGYSSGLATVYVKTVVHKISVSEEFCSFYLKIDTQDIEASSHFRLSDSGFKRIIACASYKPSKEESTSGSSHAVMDISLPTGIGANEEDLRALVEGVDQLLTDYQIKDGHVILQLNSIPSRDFLCVRFRIFELFQVGFLNPATFTVYEYHRPDKQCTMIYSISDTRLQKVCEGAACTCVEADCAQLQAEVDLAISADSRKEKACKPETAYAYKVRITSATEENVFVKYTATLLVTYKTGEAADENSEVTFIKKMSCTNANLVKGKQYLIMGKEVLQIKHNFSFKYIYPLDSSTWIEYWPTDTTCPSCQAFVENLNNFAEDLFLNSCE
В одном варианте реализации изобретения, когда молекула антитела к C5 связывается или, по существу, связывается с C5, она связывается или, по существу, связывается с одной или более изоформами C5, например, одной или более изоформами C5 человека, описанными в настоящей заявке. В одном варианте реализации изобретения молекула антитела связывается или, по существу, связывается с C5, имеющим аминокислотную последовательность SEQ ID NO: 53.
Молекулы антител
В настоящей заявке раскрыты молекулы антител, которые связываются с C5, например, описанная в настоящей заявке молекула антитела к C5.
В настоящей заявке термин «молекула антитела» обозначает белок, например, цепь иммуноглобулина или ее фрагмент, содержащий по меньшей мере одну последовательность вариабельной области иммуноглобулина. Термин «молекула антитела» включает, например, полноразмерное антитело и антигенсвязывающий фрагмент антитела.
Например, молекула антитела может включать последовательность вариабельной области тяжелой (H) цепи (в настоящей заявке сокращенно VH) и последовательность вариабельной области легкой (L) цепи (в настоящей заявке сокращенно VL). В другом примере молекула антитела включает две последовательности вариабельной области тяжелой (H) цепи и две последовательности вариабельной области легкой (L) цепи, тем самым формируя два антигенсвязывающих сайта, такие как Fab, Fab', F(ab')2, Fc, Fd, Fd', Fv, одноцепочечные антитела (например, scFv или sc (Fv)2), антитела с одним вариабельным доменом, диатела (Dab) (двухвалентные и биспецифические) и химерные (например, гуманизированные) антитела, которые могут быть получены модификацией полноразмерных антител или антител, синтезированных de novo с использованием технологий рекомбинантной ДНК. Указанные функциональные фрагменты антител сохраняют способность селективно связываться со своим соответствующим антигеном или рецептором. Антитела и фрагменты антител могут быть из какого-либо класса антител, включая, но не ограничиваясь ими, IgG, IgA, IgM, IgD и IgE, и из какого-либо подкласса (например, IgG1, IgG2, IgG3 и IgG4) антител. Молекулы антител могут быть моноклональными или поликлональными. В вариантах воплощения изобретения молекула антитела является полноразмерным антителом IgG. Молекула антитела также может быть антителом человека, гуманизированным антителом, CDR-привитым антителом или антителом, полученным в условиях in vitro. Молекула антитела может иметь константную область тяжелой цепи, выбранную, например, из IgG1, IgG2, IgG3, IgG4 или химеры двух или более изотипов. Молекула антитела также может иметь легкую цепь, выбранную, например, из каппа или лямбда. Термин «иммуноглобулин» (Ig) используется в настоящей заявке взаимозаменяемо с термином «антитело». В вариантах воплощения изобретения молекула антитела является молекулой мультиспецифического антитела (например, молекула биспецифического антитела).
Примеры антигенсвязывающих фрагментов включают: (i) Fab-фрагмент, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) F(ab')2-фрагмент, двухвалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области; (iii) Fd-фрагмент, состоящий из доменов VH и CH1; (iv) Fv-фрагмент, состоящий из доменов VL и VH одного плеча антитела, (v) фрагмент диатела (dAb), который состоит из домена VH; (vi) верблюжий или камелизированный вариабельный домен; (vii) одноцепочечный Fv (scFv), см., например, Bird et al. (1988) Science 242:423-426 и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883); (viii) однодоменное антитело. Указанные фрагменты антител могут быть получены с использованием какого-либо подходящего способа, включая несколько традиционных способов, известных специалистам в данной области техники, и оценка пригодности фрагментов может быть проведена аналогичным для интактных антител образом.
Термин «антитело» включает интактные молекулы, а также их функциональные фрагменты. Константные области антител могут быть изменены, например, может быть внесена мутация, с целью модификации свойств антитела (например, с целью увеличения или уменьшения одного или более из: связывания Fc-рецептора, гликозилирования антитела, количества остатков цистеина, функции эффекторных клеток или функции комплемента).
В одном варианте реализации изобретения молекула антитела является одноцепочечным антителом. Одноцепочечное антитело (scFv) может быть сконструировано (см., например, Colcher, D. et al. (1999) Ann N Y Acad Sci 880:263-80 и Reiter, Y. (1996) Clin Cancer Res 2:245-52). Может быть получен димер или мультимер одноцепочечного антитела для создания мультивалентных антител, обладающих специфичностью к различным эпитопам одного и того же белка-мишени.
В одном варианте реализации изобретения молекула антитела является однодоменным антителом. Однодоменные антитела могут включать антитела, чьи участки, определяющие комплементарность, являются частью однодоменного полипептида. Примеры включают, но не ограничены ими, тяжелоцепочечные антитела, антитела, естественным образом лишенные легких цепей, однодоменные антитела, полученные из обычных 4-цепочечных антител, сконструированные антитела и однодоменные каркасы, отличные от тех, которые получены из антител. Однодоменные антитела могут быть какими-либо из известных в данной области техники или какими-либо однодоменными антителами, полученными в будущем. Однодоменные антитела могут быть получены из любого вида, включая, но не ограничиваясь ими, мышь, человека, верблюда, ламу, рыбу, акулу, козу, кролика и крупный рогатый скот. В одном варианте реализации изобретения однодоменное антитело является однодоменным антителом, встречающимся в природе, известным как тяжелоцепочечное антитело, лишенное легких цепей. Такие однодоменные антитела раскрыты, например, в WO 94/04678. Для ясности необходимо сказать, что указанный вариабельный домен, полученный из тяжелоцепочечного антитела, естественным образом лишенного легкой цепи, известен в настоящей заявке как VHH или нанотело, чтобы отличить его от традиционной VH четырехцепочечных иммуноглобулинов. Такая молекула VHH может быть получена из антител, продуцируемых видами Camelidae, например, верблюдом, ламой, дромадером, альпакой и гуанако. Другие виды, кроме Camelidae, могут продуцировать тяжелоцепочечные антитела, естественным образом лишенные легкой цепи; такие VHH также входят в объем изобретения.
Области VH и VL могут подразделяться на области гипервариабельности, называемые «участками, определяющими комплементарность» (CDR), чередующиеся с более консервативными областями, называемыми «каркасными областями» (FR или FW). В настоящей заявке термины «участок, определяющий комплементарность» и «CDR» обозначают последовательности аминокислот в вариабельных областях антитела, обеспечивающих антигенную специфичность и аффинность связывания. Как правило, существует три участка, определяющих комплементарность (CDR) в каждой вариабельной области тяжелой цепи (HCDR1, HCDR2, HCDR3) и три участка, определяющих комплементарность (CDR) в каждой вариабельной области легкой цепи (LCDR1, LCDR2, LCDR3). В настоящей заявке термины «каркас», «FW» и «FR» используют взаимозаменяемо.
Размер каркасной области и участков, определяющих комплементарность (CDR), были точно определены рядом способов (см., Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242 (система нумерации по Кабат/Kabat); Chothia, C. et al. 1987; J. Mol. Biol. 196:901-917 (система нумерации по Чотиа/Chothia) и определение AbM, используемое программным обеспечением Oxford Molecular AbM antibody modeling. См., в целом, например, Protein Sequence and Structure Analysis of Antibody Variable Domains. In: Antibody Engineering Lab Manual (Ed.: Duebel, S. and Kontermann, R., Springer-Verlag, Heidelberg). В настоящей заявке участки, определяющие комплементарность (CDR), определенные в соответствии с нумерацией по Чотиа/Chothia, также иногда называют «гипервариабельными петлями». Согласно всем определениям каждая VH и VL обычно включает три участка, определяющих комплементарность (CDR), и четыре FR, расположенные от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4.
Например, согласно Кабат/Kabat, аминокислотные остатки участка, определяющего комплементарность (CDR) вариабельной области тяжелой цепи (VH) пронумерованы 31-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3), а аминокислотные остатки участка, определяющего комплементарность (CDR) вариабельной области легкой цепи (VL) пронумерованы 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3). Согласно Чотиа/Chothia, аминокислоты участка, определяющего комплементарность (CDR) VH пронумерованы 26-32 (HCDR1), 52-56 (HCDR2) и 95-102 (HCDR3), а аминокислотные остатки в VL пронумерованы 26-32 (LCDR1), 50-52 (LCDR2) и 91-96 (LCDR3). Путем объединения определений участков, определяющих комплементарность (CDR) согласно как Кабат/Kabat, так и Чотиа/Chothia, участки, определяющие комплементарность (CDR) состоят из аминокислотных остатков 26-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3) в VH человека и аминокислотных остатков 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3) в VL человека.
В целом, если конкретно не указано иное, описанные в настоящей заявке молекулы антител к C5 могут включать какую-либо комбинацию из одного или более участков, определяющих комплементарность (CDR) по Кабат/Kabat и/или гипервариабельных петель по Чотиа/Chothia, например, описанных в Таблице 1.
В настоящей заявке «последовательность вариабельной области иммуноглобулина» обозначает аминокислотную последовательность, которая может формировать структуру вариабельной области иммуноглобулина. Например, последовательность может включать всю или часть аминокислотной последовательности вариабельной области, встречающейся в природе. Например, последовательность может включать или может не включать одну, две или более N- или C-концевых аминокислот или может включать другие альтерации, совместимые с образованием структуры белка.
Термин «антигенсвязывающий фрагмент» обозначает часть молекулы антитела, которая содержит детерминанты, формирующие взаимосвязь с антигеном, например, C5, например, C5 человека или его эпитопом. Применимо к белкам (или миметикам белков) антигенсвязывающий фрагмент, как правило, включает одну или более петель (из по меньшей мере, например, четырех аминокислот или миметиков аминокислот), формирующих поверхность, которая связывается с антигеном, например, C5, например, C5 человека. Как правило, антигенсвязывающий фрагмент молекулы антитела включает по меньшей мере один или два участка, определяющих комплементарность (CDR) и/или гипервариабельные петели, или, более типично, по меньшей мере три, четыре, пять или шесть участков, определяющих комплементарность (CDR) и/или гипервариабельных петель.
В настоящей заявке термины «конкурировать» или «перекрестно конкурировать» используют взаимозаменяемо для обозначения способности молекулы антитела препятствовать связыванию молекулы антитела к C5, например, молекулы антитела к C5, описанной в настоящей заявке, с мишенью, например, C5, например, C5 человека. Препятствование связыванию может быть прямым или непрямым (например, через аллостерическую модуляцию молекулы антитела или мишени). Степень, с которой молекула антитела способна препятствовать связыванию другой молекулы антитела с мишенью, и, следовательно, можно ли сказать, что она конкурирует, возможно определить с помощью анализа конкурентного связывания, например, FACS анализа, ELISA или анализа BIACORE. В одном варианте реализации изобретения анализ конкурентного связывания является количественным конкурентным анализом. В одном варианте реализации изобретения считается, что первая молекула антитела к C5 конкурирует со второй молекулой антитела к C5 за связывание с мишенью, когда связывание первой молекулы антитела с мишенью снижается на 10% или более, например, 20% или более, 30% или более, 40% или более, 50% или более, 55% или более, 60% или более, 65% или более, 70% или более, 75% или более, 80% или более, 85% или более, 90% или более, 95% или более, 98% или более, 99% или более в условиях анализа конкурентного связывания (например, в описанном в настоящей заявке анализе конкурентного связывания).
В настоящей заявке термины «моноклональное антитело» или «композиция моноклонального антитела» обозначают препарат молекул антитела одномолекулярной композиции. Композиция моноклонального антитела демонстрирует одну специфичность связывания и аффинность к конкретному эпитопу. Моноклональные антитела возможно получить с помощью гибридомной технологии или способами, не использующими гибридомную технологию (например, рекомбинантные способы).
«Эффективно человеческий» белок является белком, который не индуцирует ответ нейтрализующих антител, например, ответ, опосредованный человеческими антителами к антителам мыши (HAMA). HAMA может быть проблематичным в ряде случаев, например, если молекулу антитела вводят повторно, например, при лечении хронического или рецидивирующего состояния. Ответ HAMA может сделать повторное введение антител потенциально неэффективным ввиду повышенного клиренса антител из сыворотки и потенциальных аллергических реакций (см., например, Saleh et al., Cancer Immunol. Immunother., 32:180-190 (1990); LoBuglio et al., Hybridoma, 5:5117-5123 (1986)).
Молекула антитела может быть поликлональным или моноклональным антителом. В одном варианте реализации изобретения антитело может быть получено рекомбинантным способом, например, получено каким-либо подходящим способом фагового дисплея или комбинаторными способами.
В данной области техники известны различные способы генерации антител способом фагового дисплея и комбинаторными способами (как описано в, например, Ladner et al. патент США № 5223409; Kang et al. международная публикация № WO 92/18619; Dower et al. международная публикация № WO 91/17271; Winter et al. международная публикация WO 92/20791; Markland et al. международная публикация № WO 92/15679; Breitling et al. международная публикация WO 93/01288; McCafferty et al. международная публикация № WO 92/01047; Garrard et al. международная публикация № WO 92/09690; Ladner et al. международная публикация № WO 90/02809; Fuchs et al. (1991) Bio/Technology 9:1370-1372; Hay et al. (1992) Hum Antibod Hybridomas 3:81-85; Huse et al. (1989) Science 246:1275-1281; Griffths et al. (1993) EMBO J 12:725-734; Hawkins et al. (1992) J Mol Biol 226:889-896; Clackson et al. (1991) Nature 352:624-628; Gram et al. (1992) PNAS 89:3576-3580; Garrad et al. (1991) Bio/Technology 9:1373-1377; Hoogenboom et al. (1991) Nuc Acid Res 19:4133-4137 и Barbas et al. (1991) PNAS 88:7978-7982, содержание которых включено в настоящую заявку посредством ссылки).
В одном варианте реализации изобретения молекула антитела является полностью человеческим антителом (например, антитело, полученное в организме мыши, который был генетически сконструирован для продуцирования антитела из последовательности человеческого иммуноглобулина) или нечеловеческим антителом, например, антителом грызуна (например, мышь или крыса), козы, примата (например, обезьяна), верблюда. В одном варианте реализации изобретения нечеловеческое антитело является антителом грызуна (например, антитело мыши или крысы). Способы получения антител грызунов известны в данной области техники.
Человеческие моноклональные антитела могут быть получены с использованием трансгенных мышей, несущих гены человеческих иммуноглобулинов вместо мышиных систем. Спленоциты таких трансгенных мышей, которые были иммунизированы представляющим интерес антигеном, используют для получения гибридом, секретирующих человеческие mAb со специфической аффинностью к эпитопам человеческого белка (см., например, Wood et al. международная публикация WO 91/00906; Kucherlapati et al. публикация PCT WO 91/10741; Lonberg et al. международная заявка WO 92/03918; Kay et al. международная заявка 92/03917; Lonberg, N. et al. 1994 Nature 368:856-859; Green, L.L. et al. 1994 Nature Genet. 7:13-21; Morrison, S.L. et al. 1994 Proc. Natl. Acad. Sci. USA 81:6851-6855; Bruggeman et al. 1993 Year Immunol 7:33-40; Tuaillon et al. 1993 PNAS 90:3720-3724; Bruggeman et al. 1991 Eur J Immunol 21:1323-1326).
Антитело может быть антителом, в котором вариабельная область или ее часть, например, участки, определяющие комплементарность (CDR) образуются в организме, отличном от человеческого, например, организмe крысы или мыши. В объем изобретения входят химерные, CDR-привитые и гуманизированные антитела. В объем изобретения входят антитела, образующиеся в организме, отличном от человеческого, например, организмe крысы или мыши, а затем модифицированные, например, по каркасному участку вариабельной области или константной области, для уменьшения антигенности у человека.
Химерные антитела возможно получить каким-либо подходящим способом рекомбинантных ДНК. Несколько из них известны в данной области техники (см., Robinson et al., публикация Международной заявки на патент № WO1987/002671; Akira, et al., публикация европейской заявки на патент № 184187; Taniguchi, M., публикация европейской заявки на патент № 171496; Morrison et al., публикация европейской заявки на патент № 173494; Neuberger et al., публикация европейской заявки на патент № WO 86/01533; Cabilly et al. заявка на патент США № 4816567; Cabilly et al., публикация европейской заявки на патент № 125023; Better et al. (1988 Science 240:1041-1043); Liu et al. (1987) PNAS 84:3439-3443; Liu et al., 1987, J. Immunol. 139:3521-3526; Sun et al. (1987) PNAS 84:214-218; Nishimura et al., 1987, Canc. Res. 47:999-1005; Wood et al. (1985) Nature 314:446-449 и Shaw et al., 1988, J. Natl Cancer Inst. 80:1553-1559).
Гуманизированное или CDR-привитое антитело будет содержать по меньшей мере один или два, но обычно все три реципиентных участка, определяющих комплементарность (CDR) (тяжелых и/или легких цепей иммуноглобулина), которые заменены донорским участком, определяющим комплементарность (CDR). Антитело может быть заменено по меньшей мере частью нечеловеческого участка, определяющего комплементарность (CDR) или только некоторые участки, определяющие комплементарность (CDR), могут быть заменены нечеловеческими участками, определяющими комплементарность (CDR). Необходимо заменить только то количество участков, определяющих комплементарность (CDR), которое необходимо для связывания гуманизированного антитела с липополисахаридом. В одном варианте реализации изобретения донором будет выступать антитело грызуна, например, антитело крысы или мыши, а реципиентом будет выступать каркас человека или консенсусный каркас человека. Как правило, иммуноглобулин, предоставляющий участки, определяющие комплементарность (CDR), называется «донором», а иммуноглобулин, предоставляющий каркас, называется «акцептором». В одном варианте реализации изобретения донорский иммуноглобулин является нечеловеческим иммуноглобулином (например, иммуноглобулином грызуна). Как правило, акцепторный каркас является каркасом, встречающимся в природе (например, человеческим), или консенсусным каркасом, или последовательностью примерно на 85% или более, например, на 90%, 95%, 99% или более.
В настоящей заявке термин «консенсусная последовательность» обозначает последовательность, образованную из наиболее часто встречающихся аминокислот (или нуклеотидов) в семействе родственных последовательностей (См., например, Winnaker, From Genes to Clones (Verlagsgesellschaft, Weinheim, Germany 1987). В семействе белков каждое положение консенсусной последовательности занято аминокислотой, наиболее часто встречающейся в этом положении в семействе. Если две аминокислоты встречаются одинаково часто, какая-либо из них может быть включена в консенсусную последовательность. «Консенсусный каркас» обозначает каркасную область в консенсусной последовательности иммуноглобулина.
Антитело возможно гуманизировать каким-либо подходящим способом, и несколько таких способов известны в данной области техники (см., например, Morrison, S. L., 1985, Science 229:1202-1207, Oi et al., 1986, BioTechniques 4:214, и Queen et al. US 5585089, US 5693761 и US 5693762, содержание которых включено в настоящую заявку посредством ссылки).
Гуманизированные или CDR-привитые антитела возможно получить путем прививания участка, определяющего комплементарность (CDR), или замены участка, определяющего комплементарность (CDR), при этом возможно заменить один, два или все участки, определяющие комплементарность (CDR) цепи иммуноглобулина. См, например, патент США 5225539; Jones et al. (1986) Nature 321:552-525; Verhoeyan et al. (1988) Science 239:1534; Beidler et al. 1988; J. Immunol. 141:4053-4060; Winter US 5225539, содержание которых включено в настоящую заявку посредством ссылки. Винтер/Winter описывает способ прививания участка, определяющего комплементарность (CDR), который возможно использовать для получения гуманизированных антител (заявка на патент Великобритании GB 2188638A, подана 26 марта 1987 г.; Winter US 5225539), содержание которой включено в настоящую заявку посредством ссылки.
Также предложены гуманизированные антитела, в которых конкретные аминокислоты были заменены, удалены или добавлены. Критерии выбора аминокислот из донора описаны, например, в патенте США 5585089, например, в параграфах 12-16 патента США 5585089, содержание которых включено в настоящую заявку посредством ссылки. Другие способы гуманизации антител описаны в Padlan et al. EP 519596 A1, опубликованном 23 декабря 1992 г.
В одном варианте реализации изобретения молекула антитела содержит константную область тяжелой цепи, выбранную из, например, константных областей тяжелых цепей IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE; в частности, выбранную из, например, константных областей тяжелых цепей (например, человеческих) IgG1, IgG2, IgG3 и IgG4. В другом варианте воплощения изобретения молекула антитела содержит константную область легкой цепи, выбранную из, например, константных областей легкой цепи (например, человеческих) каппа или лямбда. Константная область может быть изменена, например, может быть внесена мутация, с целью модификации свойств молекулы антитела (например, с целью увеличения или уменьшения одного или более из: связывания Fc-рецептора, гликозилирования антитела, количества остатков цистеина, функции эффекторных клеток и/или функции комплемента). В одном варианте реализации изобретения молекула антитела обладает эффекторной функцией и способна фиксировать комплемент. В другом варианте воплощения изобретения молекула антитела не рекрутирует эффекторные клетки или не фиксирует комплемент. В одном варианте реализации изобретения молекула антитела обладает сниженной способностью или не обладает способностью связывать Fc-рецептор. Например, молекула антитела может быть изотипом или подтипом, фрагментом или другим мутантом, который не сохраняет способность связываться с Fc-рецептором, например, молекула антитела содержит мутированную или удаленную область, связывающую Fc-рецептор.
В одном варианте реализации изобретения в константную область молекулы антитела внесены изменения. Способы изменения константной области антитела известны в данной области техники. Молекулы антител с измененной функцией, например, с измененным сродством к эффекторному лиганду, такому как FcR на клетке или компонент С1 комплемента, могут быть получены путем замены по меньшей мере одного аминокислотного остатка в константной области антитела на другой остаток (см., например., EP 388151 A1, патент США № 5624821 и патент США № 5648260, содержание которых включено в настоящую заявку посредством ссылки). Также предусмотрены аминокислотные мутации, стабилизирующие структуру антитела, такие как S228P (номенклатура ЕС, S241P в номенклатуре Кабат/Kabat) в человеческом IgG4. Возможно описать изменения подобного типа, которые при реализации в мышином иммуноглобулине или иммуноглобулине другого вида приведут к уменьшению или устранению этих функций.
В одном варианте реализации изобретения единственными аминокислотами в молекуле антитела являются канонические аминокислоты. В одном варианте реализации изобретения молекула антитела содержит аминокислоты, встречающиеся в природе, их аналоги, производные и родственные им соединения; аналоги аминокислот, содержащие разные боковые цепи, и/или все стереоизомеры какой-либо из вышеперечисленных молекул. Молекула антитела может содержать D- или L-оптические изомеры аминокислот и пептидомиметики.
В одном варианте реализации изобретения молекула антитела содержит моноклональное антитело (например, полноразмерное антитело, которое содержит Fc-участок иммуноглобулина). В одном варианте реализации изобретения молекула антитела содержит полноразмерное антитело или полноразмерную цепь иммуноглобулина. В одном варианте реализации изобретения молекула антитела содержит антигенсвязывающий фрагмент или функциональный фрагмент полноразмерного антитела или полноразмерной цепи иммуноглобулина.
В одном варианте реализации изобретения молекула антитела является молекулой моноспецифического антитела, например, молекула антитела связывает единственный эпитоп. Например, молекула моноспецифического антитела может содержать множество последовательностей вариабельной области иммуноглобулина, каждая из которых связывает один и тот же эпитоп.
В одном варианте реализации изобретения молекула антитела является молекулой мультиспецифического антитела, например, она содержит множество последовательностей вариабельной области иммуноглобулина, при этом первая последовательность вариабельной области иммуноглобулина из множества обладает специфичностью связывания в отношении первого эпитопа и вторая последовательность вариабельной области иммуноглобулина из множества обладает специфичностью связывания в отношении второго эпитопа. В одном варианте реализации изобретения первый и второй эпитопы находятся на одном и том же антигене, например, на одном и том же белке (или на субъединице мультимерного белка). В одном варианте реализации изобретения первый и второй эпитопы перекрываются. В одном варианте реализации изобретения первый и второй эпитопы не перекрываются. В одном варианте реализации изобретения первый и второй эпитопы находятся на разных антигенах, например, на разных белках (или на разных субъединицах мультимерного белка). В одном варианте реализации изобретения молекула мультиспецифического антитела содержит третью, четвертую или пятую вариабельную область иммуноглобулина. В одном варианте реализации изобретения молекула мультиспецифического антитела является молекулой биспецифического антитела, молекулой триспецифического антитела или молекулой тетраспецифического антитела.
В одном варианте реализации изобретения молекула мультиспецифического антитела является молекулой биспецифического антитела. Биспецифическое антитело обладает специфичностью не более чем к двум антигенам. Как правило, молекула биспецифического антитела характеризуется первой последовательностью вариабельной области иммуноглобулина, которая обладает специфичностью связывания в отношении первого эпитопа, и второй последовательностью вариабельной области иммуноглобулина, которая обладает специфичностью связывания в отношении второго эпитопа. В одном варианте реализации изобретения первый и второй эпитопы находятся на одном и том же антигене, например, на одном и том же белке (или на субъединице мультимерного белка). В одном варианте реализации изобретения первый и второй эпитопы перекрываются. В одном варианте реализации изобретения первый и второй эпитопы не перекрываются. В одном варианте реализации изобретения первый и второй эпитопы находятся на разных антигенах, например, на разных белках (или на разных субъединицах мультимерного белка). В одном варианте реализации изобретения молекула биспецифического антитела содержит последовательность вариабельной области тяжелой цепи и последовательность вариабельной области легкой цепи, которые обладают специфичностью связывания в отношении первого эпитопа, и последовательность вариабельной области тяжелой цепи и последовательность вариабельной области легкой цепи, которые обладают специфичностью связывания в отношении второго эпитопа. В одном варианте реализации изобретения молекула биспецифического антитела содержит половину антитела, обладающего специфичностью связывания в отношении первого эпитопа, и половину антитела, обладающего специфичностью связывания в отношении второго эпитопа. В одном варианте реализации изобретения молекула биспецифического антитела содержит половину антитела или его фрагмент, обладающий специфичностью связывания в отношении первого эпитопа, и половину антитела или его фрагмент, обладающий специфичностью связывания в отношении второго эпитопа. В одном варианте реализации изобретения молекула биспецифического антитела содержит scFv или его фрагмент, обладающий специфичностью связывания в отношении первого эпитопа, и scFv или его фрагмент обладают специфичностью связывания в отношении второго эпитопа.
Протоколы создания молекул биспецифических или гетеродимерных антител известны в данной области техники; включая, но не ограничиваясь ими, например, подход «выступ во впадину», описанный в, например, US5731168; конъюгация Fc при электростатическом взаимодействии, как описано в, например, WO 09/089004, WO 06/106905 и WO 2010/129304; образование гетеродимеров с доменами, сконструированными путем обмена между цепями (SEED), как описано в, например, WO 07/110205; обмен Fab-фрагментами, как описано в, например, WO 08/119353, WO 2011/131746 и WO 2013/060867; двойной конъюгат антитела, например, путем сшивания антител для получения биспецифической структуры с использованием гетеробифункционального реагента, содержащего реакционноспособную аминогруппу и реакционноспособную сульфгидрильную группу, как описано в, например, US4433059; детерминанты биспецифических антител, полученные рекомбинацией полуантител (пар тяжелой-легкой цепей или Fab) из различных антител через цикл восстановления и окисления дисульфидных связей между двумя тяжелыми цепями, как описано в, например, US 4444878; трифункциональные антитела, например, три Fab'-фрагмента, сшитые через реакционноспособные сульфгидрильные группы, как описано в, например, US5273743; биосинтетические связывающие белки, например, пара scFv, сшитая посредством C-концевых хвостов, предпочтительно посредством химического перекрестного сшивания дисульфидными или реакционноспособными аминогруппами, как описано в, например, US5534254; бифункциональные антитела, например, Fab-фрагменты с различной специфичностью связывания, димеризованные посредством лейциновых «застежек» (например, c-fos и c-jun), которые заменили константный домен, как описано в, например, US5582996; биспецифические и олигоспецифические моно- и олиговалентные рецепторы, например, области VH-CH1 двух антител (двух Fab-фрагментов), связанных через полипептидный спейсер между областью CH1 одного антитела и областью VH другого антитела, как правило, со связанными легкими цепями, как описано в, например, US5591828; биспецифические конъюгаты ДНК-антитело, например, сшивание антител или Fab-фрагментов через двухцепочечный участок ДНК, как описано в, например, US5635602; биспецифические слитые белки, например, экспрессирующая конструкция, содержащая два scFv с гидрофильным спиральным пептидным линкером между ними и полной константной областью, как описано в, например, US5637481; мультивалентные и мультиспецифические связывающие белки, например, димер полипептидов, содержащих первый домен со связывающей областью вариабельной области тяжелой цепи Ig и второй домен со связывающей областью вариабельной области легкой цепи Ig, как правило, называемых диателами (также раскрыты структуры высшего порядка, создающие биспецифические, триспецифические или тетраспецифические молекулы, как описано в, например, US5837242; конструкции минител со связанными VL и VH цепями, дополнительно соединенные пептидными спейсерами с шарнирной областью антитела и областью CH3, которые возможно подвергать димеризации с образованием биспецифических/мультивалентных молекул, как описано в, например, US5837821; домены VH и VL, связанные с коротким пептидным линкером (например, 5 или 10 аминокислотами) или вообще без линкера в какой-либо ориентации, которые могут образовывать димеры с образованием биспецифических диател; тримеры и тетрамеры, как описано в, например, US5844094; нить доменов VH (или доменов VL в представителях семейства), соединенных пептидными связями с перекрестно сшиваемыми группами на С-конце, дополнительно связанными с доменами VL с образованием серии FV (или scFv), как описано в, например, US5864019 и одноцепочечные связывающие полипептиды с доменами VH и VL, связанными через пептидный линкер, объединяют в мультивалентные структуры посредством нековалентного или химического сшивания с образованием, например, гомобивалентных, гетеробивалентных, трехвалентных и четырехвалентных структур с использованием формата как scFV, так и диатела, как описано в, например, US5869620. Все содержание упомянутых выше литературных источников включено в настоящую заявку посредством ссылки.
Дополнительные способы получения молекул мультиспецифических или биспецифических антител возможно найти, например, в US5910573, US5932448, US5959083, US5989830, US6005079, US6239259, US6294353, US6333396, US6476198, US6511663, US6670453, US6743896, US6809185, US6833441, US7129330, US7183076, US7521056, US7527787, US7534866, US7612181, US2002/004587, US2002/076406, US2002/103345, US2003/207346, US2003/211078, US2004/219643, US2004/220388, US2004/242847, US2005/003403, US2005/004352, US2005/069552, US2005/079170, US2005/100543, US2005/136049, US2005/136051, US2005/163782, US2005/266425, US2006/083747, US2006/120960, US2006/204493, US2006/263367, US2007/004909, US2007/087381, US2007/128150, US2007/141049, US2007/154901, US2007/274985, US2008/050370, US2008/069820, US2008/152645, US2008/171855, US2008/241884, US2008/254512, US2008/260738, US2009/130106, US2009/148905, US2009/155275, US2009/162359, US2009/162360, US2009/175851, US2009/175867, US2009/232811, US2009/234105, US2009/263392, US2009/274649, EP346087, WO00/06605, WO02/072635, WO04/081051, WO06/020258, WO2007/044887, WO2007/095338A2, WO2007/137760A2, WO2008/119353, WO2009/021754, WO2009/068630, WO91/03493, WO93/23537, WO94/09131, WO94/12625, WO95/09917, WO96/37621, WO99/64460. Все содержание упомянутых выше литературных источников включено в настоящую заявку посредством ссылки.
Полипептид описанной в настоящей заявке молекулы антитела может быть линейным или разветвленным, он может содержать модифицированные аминокислоты и может прерываться кислотами, отличными от аминокислот. Молекула антитела также может быть модифицирована, например, путем образования дисульфидной связи, гликозилирования, липидирования, ацетилирования, фосфорилирования или какой-либо иной манипуляцией, такой как конъюгация с метящим компонентом. Полипептид может быть выделен из природных источников, может быть получен рекомбинантными способами из эукариотического или прокариотического хозяина или может являться продуктом синтетических способов.
Описанную в настоящей заявке молекулу антитела возможно использовать отдельно в неконъюгированной форме или она может быть конъюгирована с веществом, например, с токсином или фрагментом (например, терапевтический агент; соединение, испускающее излучение; молекулы растительного, грибкового или бактериального происхождения или биологический белок (например, белковый токсин) или частицей (например, рекомбинантная вирусная частица, например, через белок оболочки вируса). Например, антитело к C5 может быть конъюгировано с радиоактивным изотопом, таким как α-, β- или γ-излучатель, или β- и γ-излучатель.
Молекулу антитела возможно дериватизировать или присоединить к другой функциональной молекуле (например, другому пептиду или белку). В настоящей заявке «дериватизированная» молекула антитела обозначает молекулу, которая была модифицирована. Способы дериватизации включают, но не ограничены ими, присоединение флуоресцентного фрагмента, радионуклеотида, токсина, фермента или аффинного лиганда, такого как биотин. Соответственно, предполагается, что молекулы антител включают дериватизированные и иным образом модифицированные формы описанных в настоящей заявке антител, включая молекулы иммуноадгезии. Например, молекула антитела может быть функционально связана (путем химического присоединения, генетической гибридизации, нековалентной ассоциации или иным образом) с одним или более другими молекулярными объектами, такими как другое антитело (например, биспецифическое антитело или диатело), детектируемый агент, токсин, фармацевтический агент и/или белок или пептид, который может опосредовать ассоциацию антитела или части антитела с другой молекулой (такой как активный центр стрептавидина или полигистидиновая метка).
Некоторые типы дериватизированных молекул антител получают сшиванием двух или более антител (одного или разных типов, например, для создания биспецифических антител). Подходящие сшивающие агенты включают агенты, являющиеся гетеробифункциональными, содержащими две отдельные реакционные группы, разделенные подходящим спейсером (например, сложный эфир м-малеимидобензоил-N-гидроксисукцинимида), или гомобифункциональными (например, дисукцинимидил суберат). Такие линкеры возможно приобрести у Пирс Кемикал Компани, Рокфорд, Ill/Pierce Chemical Company, Rockford, Ill.
Подходящие детектируемые агенты, с помощью которых молекула антитела к денге может быть дериватизирована (или помечена) для включения флуоресцентных соединений, различных ферментов, простетических групп, люминесцентных материалов, биолюминесцентных материалов, флуоресцирующих атомов металлов, например, европия (Eu) и других антаноидов и радиоактивных материалов (описаны ниже). Иллюстративные флуоресцентные детектируемые агенты включают флуоресцеин, флуоресцеина изотиоцианат, родамин, 5-диметиламин-1-нафталинсульфонилхлорид, фикоэритрин и т.п. Антитело также может быть дериватизировано с помощью детектируемых ферментов, таких как щелочная фосфатаза, пероксидаза хрена, β-галактозидаза, ацетилхолинэстераза, глюкозооксидаза и т.п. Когда антитело дериватизировано с помощью детектируемого фермента, его обнаружение осуществляют при добавлении дополнительных реагентов, которые используются ферментом для продуцирования детектируемого продукта реакции. Например, когда присутствует детектируемый агент пероксидаза хрена, добавление перекиси водорода и диаминобензидина приводит к получению детектируемого окрашенного продукта реакции. Молекула антитела также может быть дериватизирована простетической группой (например, стрептавидин/биотин и авидин/биотин). Например, антитело может быть дериватизировано биотином и обнаружено посредством непрямого определения связывания авидина или стрептавидина. Примеры подходящих флуоресцентных материалов включают умбеллиферон, флуоресцеин, флуоресцеина изотиоцианат, родамин, флуоресцеина дихлортриазиниламин, дансилхлорид или фикоэритрин; пример люминесцентного материала включает люминол, и примеры биолюминесцентных материалов включают люциферазу, люциферин и экворин.
Меченые молекулы антител возможно использовать, например, в диагностических и/или исследовательских целях в ряде случаев, включая (i) выделение предетерминированного антигена стандартными способами, такими как аффинная хроматография или иммунопреципитация; (ii) обнаружение предетерминированного антигена (например, в клеточном лизате или супернатанте клеток) для оценки количества и профиля экспрессии белка; (iii) мониторинг уровней белка в ткани в рамках процедуры клинического обследования, например, для определения эффективности данного режима лечения.
Описанная в настоящей заявке молекула антитела может быть конъюгирована с другим молекулярным объектом, как правило, с меткой или терапевтическим (например, противомикробным (например, антибактериальным или бактерицидным), иммуномодулирующим, иммуностимулирующим, цитотоксическим или цитостатическим) агентом или фрагментом. Радиоактивные изотопы возможно использовать в диагностических или терапевтических целях. Радиоактивные изотопы, которые могут быть конъюгированы с молекулами антител, включают, но не ограничены ими, α-, β- или γ-излучатели или β- и γ-излучатели. Такие радиоактивные изотопы включают, но не ограничены ими, йод (131I или 125I), иттрий (90Y), лютеций (177Lu), актиний (225Ac), празеодим, астат (211At), рений (186Re), висмут (212Bi или 213Bi), индий (111In), технеций (99 mTc), фосфор (32P), родий (188Rh), серу (35S), углерод (14C), тритий (3H), хром (51Cr), хлор (36Cl), кобальт (57Co или 58Co), железо (59Fe), селен (75Se) или галлий (67Ga). Радиоизотопы, подходящие в качестве терапевтических агентов, включают: иттрий (90Y), лютеций (177Lu), актиний (225Ac), празеодим, астат (211At), рений (186Re), висмут (212или 213Bi) и родий (188Rh). Радиоизотопы, подходящие в качестве меток, например, для применения в диагностике, включают йод (131I или 125I), индий (111In), технеций (99mTc), фосфор (32P), углерод (14C) и тритий (3H) или один или более из терапевтических изотопов, перечисленных выше.
Настоящее изобретение предоставляет молекулы антител, меченные радиоактивной меткой, и способы их мечения. В одном варианте реализации изобретения раскрыт способ мечения молекулы антитела. Способ включает приведение в контакт молекулы антитела с хелатирующим агентом с получением конъюгированного антитела. Конъюгированное антитело метят радиоактивным изотопом, например,111Индием, 90Иттрием и 177Лютецием, с получением меченой молекулы антитела.
В одном варианте реализации изобретения молекула антитела конъюгирована с терапевтическим агентом. В настоящей заявке раскрыты терапевтически активные радиоизотопы. Примеры других терапевтических агентов включают, но не ограничены ими, таксол, цитохалазин B, грамицидин D, бромид этидия, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол, пуромицин, майтанзиноиды, например, майтансинол (см., например, патент США № 5208020), CC-1065 (см., например, патенты США №№ 5475092, 5585499, 5846545) и их аналоги или гомологи. Терапевтические агенты включают, но не ограничены ими, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацилдекарбазин), алкилирующие агенты (например, мехлорэтамин, тиоэпахлорамбуцил, CC-1065, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклотосфосфамид, бусульфан, диброманнитол, стрептозотоцин, митомицин C и цис-дихлордиамин платины (II) (DDP) цисплатин), антрациклины (например, даунорубицин (ранее дауномицин ) и доксорубицин), антибиотики (например, дактиномицин (ранее актиномицин), блеомицин, митрамицин и антрамицин (AMC)) и антимитотические агенты (например, винкристин, винбластин, таксол и майтанзиноиды).
В одном варианте реализации изобретения молекула антитела к C5 (например, молекула моноспецифического, биспецифического или мультиспецифического антитела) ковалентно связана, например, слита, с другим партнером, например, белком, например, в форме слитой молекулы (например, слитой белок).
В настоящей заявке «слитой белок» и «слитой полипептид» обозначают полипептид, содержащий по меньшей мере две части, ковалентно соединенные между собой, где каждая из частей является полипептидом. В одном варианте реализации изобретения каждая из частей является полипептидом, обладающим разными свойствами. Свойство может быть биологическим свойством, таким как активность в условиях in vitro или in vivo. Свойство также может быть простым химическим или физическим свойством, таким как связывание с молекулой-мишенью, катализ реакции и т.д. Две части могут быть непосредственно связаны одной пептидной связью или могут быть связаны через линкер (например, пептидный линкер), но находятся в рамке считывания друг с другом.
В одном аспекте изобретение определяет отличительные признаки способа, предоставляющего связывающий целевой агент, который специфически связывается с C5 (например, C5 человека). Например, целевая связывающая молекула является молекулой антитела. Способ включает: предоставление целевого белка, который содержит по меньшей мере часть нечеловеческого белка, часть гомологична (например, по меньшей мере идентична на 70, 75, 80, 85, 87, 90, 92, 94, 95, 96, 97, 98%) соответствующей части целевого человеческого белка, но отличается по меньшей мере одной аминокислотой (например, по меньшей мере одной, двумя, тремя, четырьмя, пятью, шестью, семью, восьмью или девятью аминокислотами); получение связывающего агента (например, молекулы антитела), который специфически связывается с целевым белком, и оценку эффективности связывающего агента относительно модулирования активности целевого белка. Способ может дополнительно включать введение связывающего агента (например, молекулы антитела) или производного (например, молекулы гуманизированного антитела) субъекту (например, субъекту-человеку).
В другом аспекте настоящее изобретение предоставляет способ получения раскрытой в настоящей заявке молекулы антитела. Способ включает: предоставление антигена, например, C5 (например, C5 человека) или его фрагмента; получение молекулы антитела, которая специфически связывается с антигеном; оценку эффективности молекулы антитела относительно модулирования активности антигена и/или организма, экспрессирующего антиген, например, C5, например, C5 человека. Способ может дополнительно включать введение молекулы антитела, включая ее производное (например, молекулу гуманизированного антитела) субъекту, например, человеку.
В настоящем изобретении предложена выделенная молекула нуклеиновой кислоты, кодирующая указанную выше молекулу антитела, ее векторы и клетки-хозяева. Молекула нуклеиновой кислоты включает, но не ограничена ими, РНК, геномную ДНК и кДНК.
Аминокислотные и нуклеотидные последовательности иллюстративных молекул антител представлены в Таблицах 1-5.
HCDR1
HCDR2
HCDR3
LCDR1
LCDR2
LCDR3
HCDR1
HCDR2
HCDR3
LCDR1
LCDR2
LCDR3
agctgcaaagcgagcggctatatttttaccaactattggatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggcagcaccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaacctggcggatggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagaacgtgctgaacaccccgctgagctttggcggc
ggcaccaaagtggatattaaa
agctgcaaagcgagcggctatatttttaccgatttttatatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggcagcaccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaacctggcggatggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagaacgtgctgaacaccccgctgagctttggcggc
ggcaccaaagtggatattaaa
agctgcaaagcgagcggccatatttttaccaactattggatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggccataccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaacctggcggatggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagaacgtgctgaacaccccgctgagctttggcggc
ggcaccaaagtggatattaaa
agctgcaaagcgagcggccatatttttaccgatttttatatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggccataccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaacctggcggatggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagaacgtgctgaacaccccgctgagctttggcggc
ggcaccaaagtggatattaaa
agctgcaaagcgagcggctatatttttaccaactattggatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggcagcaccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaaccgctataccggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagcaggtgctgaacaccccggtgagctttggcggc
ggcaccaaagtggatattaaa
agctgcaaagcgagcggctatatttttaccgatttttatatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggcagcaccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaaccgctataccggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagcaggtgctgaacaccccggtgagctttggcggc
ggcaccaaagtggatattaaa
agctgcaaagcgagcggccatatttttaccaactattggatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggccataccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaaccgctataccggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagcaggtgctgaacaccccggtgagctttggcggc
ggcaccaaagtggatattaaa
agctgcaaagcgagcggccatatttttaccgatttttatatgcagtgggtgcgccaggcg
ccgggccagggcctggaatggatgggcgaaattctgccgggcaccggccataccgaatat
gcgcagaaatttcagggccgcgtgaccatgacccgcgataccagcattagcaccgtgtat
atggaagtgcgccgcctgcgcagcgatgataccgcggtgtattattgcgcgcgctatttt
tttggcagcaccccgaactggtattttgatgtgtggggccagggcaccctggtgaccgtg
agcagc
attacctgcggcgcgaccgaaaacatttatggcgcgctgaactggtatcagcatgaaccg
ggcaaagcgccgaaactgctgatttatggcgcgagcaaccgctataccggcgtgaccagc
cgctttagcggcagcggcagcggcaccgattttaccctgaccattagcaccctgcagccg
gaagattttgcgacctattattgccagcaggtgctgaacaccccggtgagctttggcggc
ggcaccaaagtggatattaaa
В одном варианте реализации изобретения молекула антитела содержит один, два или три участка, определяющих комплементарность (CDR) области VH описанной в настоящей заявке молекулы антитела, например, в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013), участки, определяющие комплементарность (CDR), определены по номенклатуре Кабат/Kabat или Чотиа/Chothia. В одном варианте реализации изобретения молекула антитела содержит один, два или три участка, определяющих комплементарность (CDR) области VL описанной в настоящей заявке молекулы антитела, например, в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013), участки, определяющие комплементарность (CDR), определены по номенклатуре Кабат/Kabat или Чотиа/Chothia. В одном варианте реализации изобретения молекула антитела содержит один или более (например, два или три) участков, определяющих комплементарность (CDR) области VH и/или один или более (например, два или три) участков, определяющих комплементарн ость (CDR) области VL какой-либо описанной в настоящей заявке молекулы антитела, например, в Таблице 1 (например, кого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013), участки, определяющие комплементарность (CDR), определены по номенклатуре Кабат/Kabat или Чотиа/Chothia.
В одном варианте реализации изобретения молекула антитела содержит один, два или три участка, определяющих комплементарность (CDR) VH, описанных в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит один, два или три участка, определяющих комплементарность (CDR) VL, описанных в Таблице 1. В одном варианте реализации изобретения молекула антитела содержит один или более (например, два или три) участков, определяющих комплементарность (CDR) VH и/или один или более (например, два или три) участков, определяющих комплементарность (CDR) VL, описанных в Таблице 1.
В одном варианте реализации изобретения молекула антитела содержит один, два, три или четыре каркаса области VH молекулы антитела, описанной в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013). В одном варианте реализации изобретения молекула антитела содержит один, два, три или четыре каркаса области VL молекулы антитела, описанной в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013). В одном варианте реализации изобретения молекула антитела содержит один или более (например, два, три или четыре) каркаса области VH и/или один или более (например, два, три или четыре) каркаса области VL молекулы антитела, описанной в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013).
В одном варианте реализации изобретения молекула антитела содержит вариабельную область тяжелой цепи молекулы антитела, описанной в настоящей заявке, например, в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013). В одном варианте реализации изобретения молекула антитела содержит вариабельную область легкой цепи молекулы антитела, описанной в настоящей заявке, например, в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013). В одном варианте реализации изобретения молекула антитела содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи молекулы антитела, описанной в настоящей заявке, например, в Таблице 1 (например, какого-либо из моноклональных антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013).
В одном варианте реализации изобретения молекула антитела содержит вариабельную область тяжелой цепи, имеющую аминокислотную последовательность, представленную в Таблице 1, или аминокислотную последовательность по существу идентичную ей. В одном варианте реализации изобретения молекула антитела содержит вариабельную область легкой цепи, имеющую аминокислотную последовательность, представленную в Таблице 1, или аминокислотную последовательность, по существу идентичную ей. В одном варианте реализации изобретения молекула антитела содержит вариабельную область тяжелой цепи, имеющую аминокислотную последовательность, представленную в Таблице 1 (или аминокислотную последовательность по существу идентичную ей) и вариабельную область легкой цепи, имеющую аминокислотную последовательность, представленную в Таблице 1 (или аминокислотную последовательность, по существу идентичную ей).
Иллюстративные аминокислотные последовательности VH и VL также представлены в Таблице 2. Иллюстративные аминокислотные последовательности участка, определяющего комплементарность (CDR) по Чотиа/Chothia и Кабат/Kabat также представлены в Таблицах 3-4, соответственно.
В одном варианте реализации изобретения молекула антитела содержит вариабельную область тяжелой цепи, кодируемую нуклеотидной последовательностью, представленной в Таблице 5, или нуклеотидной последовательностью, по существу идентичной ей. В одном варианте реализации изобретения молекула антитела содержит вариабельную область легкой цепи, кодируемую нуклеотидной последовательностью, представленной в Таблице 5, или нуклеотидной последовательностью, по существу идентичной ей. В одном варианте реализации изобретения молекула антитела содержит вариабельную область тяжелой цепи, кодируемую нуклеотидной последовательностью, представленной в Таблице 5 (или нуклеотидной последовательностью, по существу идентичной ей) и вариабельную область легкой цепи, кодируемую нуклеотидной последовательностью, представленной в Таблице 5 (или нуклеотидной последовательностью, по существу идентичной ей).
В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область тяжелой цепи. В одном варианте реализации изобретения константная область тяжелой цепи является константной областью IgG1 или ее функциональной частью. В другом варианте воплощения изобретения константная область тяжелой цепи является константной областью IgG2 или ее функциональной частью. В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область легкой цепи. В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область тяжелой цепи. В одном варианте реализации изобретения константная область тяжелой цепи является константной областью IgG3 или ее функциональной частью. В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область тяжелой цепи. В одном варианте реализации изобретения константная область тяжелой цепи является константной областью IgG4 или ее функциональной частью. В одном варианте реализации изобретения молекула антитела содержит химерную константную область, содержащую изотипы IgG2, IgG3 и/или IgG4. В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область тяжелой цепи и константную область легкой цепи. В одном варианте реализации изобретения молекула антитела содержит константную тяжелой цепи, константную область легкой цепи и вариабельные области тяжелой и легкой цепей молекулы антитела, описанной в Таблице 1. В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область тяжелой цепи, константную область легкой цепи и вариабельные области, содержащие один, два, три, четыре, пять или шесть участков, определяющих комплементарность (CDR) молекулы антитела, описанной в Таблице 1.
Иллюстративные константные области тяжелой и легкой цепей описаны ниже.
>IgG2/4 тяжелая-константная (IgG2/4)
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSNFGTQTYTCNVDHKPSNTKVDKTVERKCCVECPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK (SEQ ID NO: 116)
>IgG2/4 тяжелая-константная с замещениями Met-252-Tyr, Ser-254-Thr и Thr-256-Glu (IgG2/4-YTE)
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSNFGTQTYTCNVDHKPSNTKVDKTVERKCCVECPPCPAPPVAGPSVFLFPPKPKDTLYITREPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK (SEQ ID NO: 117)
>IgG2/4 тяжелая-константная с замещениями Met-429-Leu и Asn-435-Ser (IgG2/4-LS)
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSNFGTQTYTCNVDHKPSNTKVDKTVERKCCVECPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVLHEALHSHYTQKSLSLSLGK (SEQ ID NO: 118)
>IgG1 тяжелая-константная (IgG1)
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 119)
> легкая-константная
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO: 120)
В одном варианте реализации изобретения молекула антитела содержит один или более (например, все) участков, определяющих комплементарность (CDR) ATG-004 или ATG-008, и химерную константную область тяжелой цепи человеческого IgG2/4 с замещениями Met-429-Leu и/или Asn-435-Ser, как описано в настоящей заявке. В одном варианте реализации изобретения молекула антитела содержит один или более (например, все) участков, определяющих комплементарность (CDR) ATG-001, ATG-002, ATG-003, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013, и константную область человеческого IgG1, как описано в настоящей заявке.
В некоторых вариантах воплощения изобретения молекула антитела содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3),
при этом VH содержит одно, два или все из следующего:
(i) HCDR1, содержащий аминокислотную последовательность:
GX1X2FX3X4X5Y,
где X1 является Y, F или H;
X2 является I или T;
X3 является S или T;
X4 является N, S, D или G и
X5 является F, N или отсутствует
(SEQ ID NO: 87);
(ii) HCDR2, содержащий аминокислотную последовательность:
X1X2X3X4GX5,
где X1 является L или N;
X2 является A или P;
X3 является G, T или K;
X4 является S, D, N, T или S и
X5 является S, H или D
(SEQ ID NO: 88);
(iii) HCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6X7X8X9X10X11X12X13,
где X1 является Y или G;
X2 является P, Y, S, F или W;
X3 является F, S или W;
X4 является G или P;
X5 является S, N или M;
X6 является S, W, T или D;
X7 является P, A или V;
X8 является N, M или отсутствует;
X9 является W, D или отсутствует;
X10 является E, Y, A или отсутствует;
X11 является F, M или отсутствует;
X12 является D или отсутствует и
X13 является Y, V или отсутствует
(SEQ ID NO: 89), и
при этом VL содержит одно, два или все из следующего:
(iv) LCDR1, содержащий аминокислотную последовательность:
X1AX2X3X4IX5X6X7LX8,
где X1 является R или G;
X2 является S или T;
X3 является Q или E;
X4 является N, S или G;
X5 является N или Y;
X6 является N или G;
X7 является Y или A и
X8 является H, N или A
(SEQ ID NO: 90);
(v) LCDR2, содержащий аминокислотную последовательность:
X1ASX2X3X4X5,
где X1 является A, G или D;
X2 является N или T;
X3 является L или R;
X4 является Q, A, Y или E, или
X5 является G, D, T или S
(SEQ ID NO: 91), и
(vi) LCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6PX7X8,
где X1 является L или Q;
X2 является Q или N;
X3 является T или V;
X4 является H или L;
X5 является A, N или S;
X6 является Y или T;
X7 является L, V, W или Y, или
X8 является T или S
(SEQ ID NO: 92).
В одном варианте реализации изобретения VH содержит HCDR1, содержащий аминокислотную последовательность: GX1X2FX3X4X5Y (SEQ ID NO: 87), которая не содержит одно, два, три, четыре или все из следующего: X1 является Y, X2 является I, X3 является S, X4 является S или X5 является N. В одном варианте реализации изобретения X1 не является Y. В одном варианте реализации изобретения X2 не является I. В одном варианте реализации изобретения X3 не является S. В одном варианте реализации изобретения X4 не является S. В одном варианте реализации изобретения X5 не является N. В одном варианте реализации изобретения HCDR1 не содержит аминокислотную последовательность SEQ ID NO: 16.
В одном варианте реализации изобретения VH содержит HCDR2, содержащий аминокислотную последовательность: X1X2X3X4GX5 (SEQ ID NO: 88), которая не содержит одно, два, три, четыре или все из следующего: X1 является L, X2 является P, X3 является G, X4 является S или X5 является S. В одном варианте реализации изобретения X1 не является L. В одном варианте реализации изобретения X2 не является P. В одном варианте реализации изобретения X3 не является G. В одном варианте реализации изобретения X4 не является S. В одном варианте реализации изобретения X5 не является S. В одном варианте реализации изобретения HCDR1 не содержит аминокислотную последовательность SEQ ID NO: 56.
В одном варианте реализации изобретения VH содержит HCDR3, содержащий аминокислотную последовательность: X1X2X3X4X5X6X7X8X9X10X11X12X13 (SEQ ID NO: 89), которая не содержит одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять одиннадцать, двенадцать или все из следующего: X1 является Y, X2 является F, X3 является F, X4 является G, X5 является S, X6 является S, X7 является P, X8 является N, X9 является W, X10 является Y, X11 является F, X12 является D или X13 является V. В одном варианте реализации изобретения X1 не является Y. В одном варианте реализации изобретения X2 не является F. В одном варианте реализации изобретения X3 не является F. В одном варианте реализации изобретения X4 не является G. В одном варианте реализации изобретения X5 не является S. В одном варианте реализации изобретения X6 не является S. В одном варианте реализации изобретения X7 не является P. В одном варианте реализации изобретения X8 не является N. В одном варианте реализации изобретения X9 не является W. В одном варианте реализации изобретения X10 не является Y. В одном варианте реализации изобретения X11 не является F. В одном варианте реализации изобретения X12 не является D. В одном варианте реализации изобретения или X13 не является V.
В одном варианте реализации изобретения VL содержит LCDR1, содержащий аминокислотную последовательность: X1AX2X3X4IX5X6X7LX8 (SEQ ID NO: 90), которая не содержит одно, два, три, четыре, пять, шесть, семь или все из следующего: X1 является G, X2 является S, X3 является E, X4 является N, X5 является Y, X6 является G, X7 является A или X8 является N. В одном варианте реализации изобретения X1 не является G. В одном варианте реализации изобретения X2 не является S. В одном варианте реализации изобретения X3 не является E. В одном варианте реализации изобретения X4 не является N. В одном варианте реализации изобретения X5 не является Y. В одном варианте реализации изобретения X6 не является G. В одном варианте реализации изобретения X7 не является A. В одном варианте реализации изобретения или X8 не является N.
В одном варианте реализации изобретения VL содержит LCDR2, содержащий аминокислотную последовательность: X1ASX2X3X4X5 (SEQ ID NO: 91), которая не содержит одно, два, три, четыре или все из следующего: X1 является G, X2 является N, X3 является L, X4 является А или X5 является D. X1 не является G, X2 не является N, X3 не является L, X4 не является A или X5 не является D.
В одном варианте реализации изобретения VL содержит LCDR3, содержащий аминокислотную последовательность: X1X2X3X4X5X6PX7X8 (SEQ ID NO: 92), которая не содержит одно, два, три, четыре, пять, шесть, семь или все из следующего: X1 является Q, X2 является N, X3 является V, X4 является L, X5 является N, X6 является T, X7 является L или X8 является T. В одном варианте реализации изобретения X1 не является Q. В одном варианте реализации изобретения X2 не является N. В одном варианте реализации изобретения X3 не является V. В одном варианте реализации изобретения X4 не является L. В одном варианте реализации изобретения X5 не является N. В одном варианте реализации изобретения X6 не является Т. В одном варианте реализации изобретения X7 не является L. В одном варианте реализации изобретения X8 не является Т.
В вариантах воплощения изобретения молекула антитела содержит VH и VL, при этом VH содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом VL содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3),
при этом VH содержит одно, два или все из следующего:
(i) HCDR1, содержащий аминокислотную последовательность:
X1X2X3X4X5
где X1 является N, D, S или G;
X2 является Y, F или N;
X3 является W или Y;
X4 является M или I и
X5 является Q или Н
(SEQ ID NO: 94);
(ii) HCDR2, содержащий аминокислотную последовательность:
X1X2X3X4X5X6GX7TX8YX9QKFX10G
где X1 является E или W;
X2 является I или V;
X3 является L или N;
X4 является P или A;
X5 является G, T или K;
X6 является T, S, D или N;
X7 является S, H или D;
X8 является Е или N;
X9 является A или S и
X10 является Q или R
(SEQ ID NO: 95);
(iii) HCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6X7X8WX9X10DX11
где X1 является Y или G;
X2 является F, P, Y или W;
X3 является F или отсутствует;
X4 является G или отсутствует;
X5 является S или отсутствует;
X6 является Т, S или отсутствует;
X7 является Р или отсутствует;
X8 является N или отсутствует;
X9 является Y, E, A или G;
X10 является F или M и
X11 является V или Y
(SEQ ID NO: 96), и
при этом VL содержит одно, два или все из следующего:
(iv) LCDR1, содержащий аминокислотную последовательность:
X1AX2X3X4IX5X6X7LX8
где X1 является G или R;
X2 является T или S;
X3 является Е или Q;
X4 является N, G или S;
X5 является Y или N;
X6 является G или N;
X7 является A или Y и
X8 является N, A или H
(SEQ ID NO: 97);
(v) LCDR2, содержащий аминокислотную последовательность:
X1ASX2X3X4X5
где X1 является G, D или A;
X2 является N или T;
X3 является L или R;
X4 является A, Y, E или Q и
X5 является D, T, S или G
(SEQ ID NO: 98), и
(vi) LCDR3, содержащий аминокислотную последовательность:
X1X2X3X4X5X6PX7X8
где X1 является Q или L;
X2 является N или Q;
X3 является V или T;
X4 является L или H;
X5 является N, S или A;
X6 является T или Y;
X7 является L, V, W или Y и
X8 является S или T
(SEQ ID NO: 99).
В одном варианте реализации изобретения VH содержит HCDR1, содержащий аминокислотную последовательность: X1X2X3X4X5 (SEQ ID NO: 94), которая не содержит одно, два, три, четыре или все из следующего: X1 является N, X2 является Y, X3 является W, X4 является I или X5 является Q. В одном варианте реализации изобретения X1 не является N. В одном варианте реализации изобретения X2 не является Y. В одном варианте реализации изобретения X3 не является W. В одном варианте реализации изобретения X4 не является I. В одном варианте реализации изобретения X5 не является Q.
В одном варианте реализации изобретения VH содержит HCDR2, содержащий аминокислотную последовательность: X1X2X3X4X5X6GX7TX8YX9QKFX10G (SEQ ID NO: 95), которая не содержит одно, два, три, четыре, пять, шесть, семь или все из следующего: X1 является E, X2 является I, X3 является L, X4 является P, X5 является G, X6 является S, X7 является S или X8 является E. В одном варианте реализации изобретения X1 не является E. В одном варианте реализации изобретения X2 не является I. В одном варианте реализации изобретения X3 не является L. В одном варианте реализации изобретения X4 не является P. В одном варианте реализации изобретения X5 не является G. В одном варианте реализации изобретения X6 не является S. В одном варианте реализации изобретения X7 не является S. В одном варианте реализации изобретения или X8 не является E.
В одном варианте реализации изобретения VH содержит HCDR3, содержащий аминокислотную последовательность: X1X2X3X4X5X6X7X8WX9X10DX11 (SEQ ID NO: 96), которая не содержит одно, два, три, четыре или все из следующего: X1 является Y, X2 является F, X3 является F, X4 является G, X5 является S, X6 является S, X7 является P, X8 является N, X9 является Y, X10 является F или X11 является V. В одном варианте реализации изобретения X1 не является Y. В одном варианте реализации изобретения X2 не является F. В одном варианте реализации изобретения X3 не является F. В одном варианте реализации изобретения X4 не является G. В одном варианте реализации изобретения X5 не является S. В одном варианте реализации изобретения X6 не является S. В одном варианте реализации изобретения X7 не является P. В одном варианте реализации изобретения X8 не является N. В одном варианте реализации изобретения X9 не является Y. В одном варианте реализации изобретения X10 не является F. В одном варианте реализации изобретения или X11 не является V.
В одном варианте реализации изобретения VL содержит LCDR1, содержащий аминокислотную последовательность: X1AX2X3X4IX5X6X7LX8 (SEQ ID NO: 97), которая не содержит одно, два, три, четыре, пять, шесть, семь или все из следующего: X1 является G, X2 является S, X3 является E, X4 является N, X5 является Y, X6 является G, X7 является A или X8 является N. В одном варианте реализации изобретения X1 не является Y. В одном варианте реализации изобретения X2 не является F. В одном варианте реализации изобретения X3 не является F. В одном варианте реализации изобретения X4 не является G. В одном варианте реализации изобретения X5 не является S. В одном варианте реализации изобретения X6 не является S. В одном варианте реализации изобретения X7 не является P. В одном варианте реализации изобретения X8 не является N. В одном варианте реализации изобретения X9 не является Y. В одном варианте реализации изобретения X10 не является F. В одном варианте реализации изобретения или X11 не является V.
В одном варианте реализации изобретения VL содержит LCDR2, содержащий аминокислотную последовательность: X1ASX2X3X4X5 (SEQ ID NO: 98), которая не содержит одно, два, три, четыре или все из следующего: X1 является G, X2 является N, X3 является L, X4 является A или X5 является D. В одном варианте реализации изобретения X1 не является G. В одном варианте реализации изобретения X2 не является N. В одном варианте реализации изобретения X3 не является L. В одном варианте реализации изобретения X4 не является A. В одном варианте реализации изобретения или X5 не является D.
В вариантах воплощения изобретения VL содержит LCDR3, содержащий аминокислотную последовательность: X1X2X3X4X5X6PX7X8 (SEQ ID NO: 99), которая не содержит одно, два, три, четыре, пять, шесть, семь или все из следующего: X1 является Q, X2 является N, X3 является V, X4 является L, X5 является N, X6 является T, X7 является L или X8 является T. В одном варианте реализации изобретения X1 не является Q. В одном варианте реализации изобретения X2 не является N. В одном варианте реализации изобретения X3 не является V. В одном варианте реализации изобретения X4 не является L. В одном варианте реализации изобретения X5 не является N. В одном варианте реализации изобретения X6 не является Т. В одном варианте реализации изобретения X7 не является L. В одном варианте реализации изобретения или X8 не является T.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43 или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28, и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38, LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28; и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38, LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59, и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 1. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 10. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 1, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 100. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 101. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 100, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 101.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28, и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28; и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 2. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 10. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 2, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 102. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 103. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 102, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 103.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43, или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29, и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 3. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 10. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 3, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 104. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 105. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 104, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 105.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29, и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 43; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 48.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 76; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 81.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 4. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 10. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 106. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 107. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 106, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 107.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28; и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 19; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28; и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 1. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 11. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 1, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 108. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 109. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 108, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 109.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28; и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28; и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1, SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59, и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 2. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 11. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 2, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 110. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 111. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 110, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 111.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 21; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 54; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 3. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO 11. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 3, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 112. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 113. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 112, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 113.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность LCDR1 SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 29; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 22; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 29; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 60; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 60; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 28; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 35 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 20; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 28; и HCDR3, содержащий аминокислотную последовательность SEQ ID NO: 35, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 38; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 44; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 49.
В одном варианте реализации изобретения молекула антитела содержит одно или оба из:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит одно, два или все из следующего: HCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 59; или HCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 66 или
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит одно, два или все из следующего: LCDR1, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность, которая отличается не более чем 1, 2, или 3 аминокислотными остатками от, или которая гомологична по меньшей мере на 85, 90, 95, 99 или 100% аминокислотной последовательности SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит:
(i) вариабельную область тяжелой цепи (VH), при этом вариабельная область тяжелой цепи содержит три участка, определяющих комплементарность тяжелой цепи (HCDR1, HCDR2 и HCDR3), при этом вариабельная область тяжелой цепи содержит: HCDR1, содержащий аминокислотную последовательность SEQ ID NO: 55; HCDR2, содержащий аминокислотную последовательность SEQ ID NO: 59; и HCDR3 содержащий аминокислотную последовательность SEQ ID NO: 66, и
(ii) вариабельную область легкой цепи (VL), при этом вариабельная область легкой цепи содержит три участка, определяющих комплементарность легкой цепи (LCDR1, LCDR2 и LCDR3), при этом вариабельная область легкой цепи содержит: LCDR1, содержащий аминокислотную последовательность SEQ ID NO: 71; LCDR2, содержащий аминокислотную последовательность SEQ ID NO: 77; или LCDR3, содержащий аминокислотную последовательность SEQ ID NO: 82.
В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 4. В одном варианте реализации изобретения молекула антитела содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 11. В одном варианте реализации изобретения молекула антитела содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 114. В одном варианте реализации изобретения молекула антитела содержит VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 115. В одном варианте реализации изобретения молекула антитела содержит VH, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 114, и VL, кодируемую нуклеиновой кислотой, которая содержит нуклеотидную последовательность SEQ ID NO: 115.
В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область тяжелой цепи, например, описанную в настоящей заявке константную область тяжелой цепи. В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область легкой цепи, например, описанную в настоящей заявке константную область легкой цепи. В одном варианте реализации изобретения молекула антитела дополнительно содержит константную область тяжелой цепи, например, описанную в настоящей заявке константную область тяжелой цепи, и константную область легкой цепи, например, описанную в настоящей заявке константную область легкой цепи.
В одном варианте реализации изобретения описанная в настоящей заявке молекула антитела обладает одним или более (например, 2, 3, 4, 5 или всеми) из следующих свойств: специфически связывается с C5 (например, C5 человека); препятствует расщеплению C5, например, на C5a и C5b; препятствует C5-опосредованному разрушению эритроцитов; препятствует хроническому разрушению эритроцитов или гемолизу; снижает воспаление; или какую-либо их комбинацию. В одном варианте реализации изобретения молекула антитела содержит один или более (например, 2, 3, 4, 5 или все) участков, определяющих комплементарность (CDR), одну или обе из вариабельной области тяжелой цепи или вариабельных областей легкой цепи или одну или обе из тяжелой цепи или легкой цепи какой-либо из молекул антител ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013. В одном варианте реализации изобретения молекула антитела пригодна для применения при лечении заболевания почек, например, IgA-нефропатии. В другом варианте воплощения изобретения молекула антитела пригодна для применения при лечении заболевания или расстройства, например, комплемент-опосредованного расстройства, например, описанного в настоящей заявке комплемент-опосредованного расстройства.
Описанные в настоящей заявке молекулы антител могут обладать несколькими преимуществами. Например, молекулы антител возможно использовать для эффективного лечения, предотвращения или диагностики расстройства, связанного с C5, например, описанного в настоящей заявке расстройства, например, комплемент-опосредованного расстройства, например, описанного в настоящей заявке комплемент-опосредованного расстройства.
В одном варианте реализации изобретения молекула антитела связывается с C5, например, C5 человека, с высокой аффинностью, например, KD’ составляет примерно 50 нМ или менее, например, примерно 20 нМ или менее, 10 нМ или менее, 9 нМ или менее, 8 нМ или менее, 7 нМ или менее, 6 нМ или менее, 5 нМ или менее, 4 нМ или менее, 3 нМ или менее, 2 нМ или менее, 1 нМ или менее, 0,5 нМ или менее, 0,2 нМ или менее, 0,1 нМ или менее, 0,05 нМ или менее, 0,02 нМ или менее, 0,01 нМ или менее, 0,005 нМ или менее, 0,002 нМ или менее или 0,001 нМ или менее, например, от 0,001 нМ до 10 нМ, от 0,001 нМ до 5 нМ, от 0,001 нМ до 2 нМ, от 0,001 нМ до 1 нМ, от 0,001 нМ до 0,5 нМ, от 0,001 нМ до 0,2 нМ, от 0,001 нМ до 0,1 нМ, от 0,001 до 0,05 нМ, от 0,001 до 0,02 нМ, от 0,001 до 0,005 нМ, от 5 нМ до 10 нМ, от 2 нМ до 10 нМ, от 1 нМ до 10 нМ, от 0,5 нМ до 10 нМ, от 0,2 нМ до 10 нМ, от 0,1 нМ до 10 нМ, от 0,05 нМ до 10 нМ, от 0,02 нМ до 10 нМ, от 0,01 нМ до 10 нМ, от 0,005 нМ до 10 нМ, от 0,002 до 10 нМ, от 0,002 нМ до 5 нМ, от 0,005 нМ до 2 нМ, от 0,01 нМ до 1 нМ, от 0,02 нМ до 0,5 нМ, от 0,05 нМ до 0,2 нМ, от 0,001 нМ до 0,002 нМ, от 0,002 нМ до 0,005 нМ, от 0,005 нМ до 0,01 нМ, от 0,01 нМ до 0,02 нМ, от 0,02 нМ до 0,05 нМ, от 0,05 нМ до 0,1 нМ, от 0,1 нМ до 0,2 нМ, от 0,2 нМ до 0,5 нМ, от 0,5 нМ до 1 нМ, от 1 нМ до 2 нМ, от 2 нМ до 5 нМ или от 5 нМ до 10 нМ.
В одном варианте реализации изобретения молекула антитела связывается с C5 с Koff, составляющей менее 1×10-4, 5×10-5 или 1×10-5 с-1. В одном варианте реализации изобретения молекула антитела связывается с C5 с Kon, составляющей более 1×104, 5×104, 1×105 или 5×105 M-1с-1.
В одном варианте реализации изобретения молекула антитела связывается с C5, например, C5 человека, с высокой аффинностью, например, EC50 составляет примерно 2 мкг/мл или менее, например, примерно 1 мкг/мл или менее, 0,9 мкг/мл или менее, 0,8 мкг/мл или менее, 0,7 мкг/мл или менее, 0,6 мкг/мл или менее, 0,5 мкг/мл или менее, 0,4 мкг/мл или менее, 0,3 мкг/мл или менее, 0,2 мкг/мл или менее, 0,1 мкг/мл или менее, 0,09 мкг/мл или менее, 0,08 мкг/мл или менее, 0,07 мкг/мл или менее, 0,06 мкг/мл или менее, 0,05 мкг/мл или менее, 0,04 мкг/мл или менее, 0,03 мкг/мл или менее, 0,02 мкг/мл или менее, 0,01 мкг/мл или менее, 0,005 мкг/мл или менее, 0,002 мкг/мл или менее, 0,001 мкг/мл или менее, например, от 0,001 мкг/мл до 2 мкг/мл, например, от 0,001 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 0,5 мкг/мл, от 0,001 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,1 мкг/мл, от 0,001 мкг/мл до 0,05 мкг/мл, от 0,001 мкг/мл до 0,02 мкг/мл, от 0,001 мкг/мл до 0,01 мкг/мл, от 0,001 мкг/мл до 0,005 мкг/мл, от 0,002 мкг/мл до 1 мкг/мл, от 0,005 мкг/мл до 1 мкг/мл, от 0,01 мкг/мл до 1 мкг/мл, от 0,02 мкг/мл до 1 мкг/мл, от 0,05 мкг/мл до 1 мкг/мл, от 0,1 мкг/мл до 1 мкг/мл, от 0,2 мкг/мл до 1 мкг/мл, от 0,5 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 1 мкг/мл, от 0,002 мкг/мл до 0,5 мкг/мл, от 0,005 мкг/мл до 0,2 мкг/мл, от 0,01 мкг/мл до 0,1 мкг/мл или от 0,02 мкг/мл до 0,05 мкг/мл, например, как определено описанным в настоящей заявке способом.
В одном варианте реализации изобретения молекула антитела снижает (например, ингибирует, блокирует или нейтрализует) одну или более биологических активностей C5 (например, C5 человека), например, IC50 составляет примерно 50 мкг/мл или менее, например, примерно 20 мкг/мл или менее, 10 мкг/мл или менее, 9 мкг/мл или менее, 8 мкг/мл или менее, 7 мкг/мл или менее, 6 мкг/мл или менее, 5 мкг/мл или менее, 4 мкг/мл или менее, 3 мкг/мл или менее, 2 мкг/мл или менее, 1 мкг/мл или менее, 0,5 мкг/мл или менее, 0,2 мкг/мл или менее, 0,1 мкг/мл или менее, 0,05 мкг/мл или менее, 0,02 мкг/мл или менее, 0,01 мкг/мл или менее, 0,005 мкг/мл или менее, 0,002 мкг/мл или менее или 0,001 мкг/мл или менее, например, от 0,001 мкг/мл до 10 мкг/мл, от 0,001 мкг/мл до 5 мкг/мл, от 0,001 мкг/мл до 2 мкг/мл, от 0,001 мкг/мл до 1 мкг/мл, от 0,001 мкг/мл до 0,5 мкг/мл, от 0,001 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,1 мкг/мл, от 0,001 до 0,05 мкг/мл, от 0,001 до 0,02 мкг/мл, от 0,001 до 0,005 мкг/мл, от 5 мкг/мл до 10 мкг/мл, от 2 мкг/мл до 10 мкг/мл, от 1 мкг/мл до 10 мкг/мл, от 0,5 мкг/мл до 10 мкг/мл, от 0,2 мкг/мл до 10 мкг/мл, от 0,1 мкг/мл до 10 мкг/мл, от 0,05 мкг/мл до 10 мкг/мл, от 0,02 мкг/мл до 10 мкг/мл, от 0,01 мкг/мл до 10 мкг/мл, от 0,005 мкг/мл до 10 мкг/мл, от 0,002 до 10 мкг/мл, от 0,002 мкг/мл до 5 мкг/мл, от 0,005 мкг/мл до 2 мкг/мл, от 0,01 мкг/мл до 1 мкг/мл, от 0,02 мкг/мл до 0,5 мкг/мл, от 0,05 мкг/мл до 0,2 мкг/мл, от 0,001 мкг/мл до 0,002 мкг/мл, от 0,002 мкг/мл до 0,005 мкг/мл, от 0,005 мкг/мл до 0,01 мкг/мл, от 0,01 мкг/мл до 0,02 мкг/мл, от 0,02 мкг/мл до 0,05 мкг/мл, от 0,05 мкг/мл до 0,1 мкг/мл, от 0,1 мкг/мл до 0,2 мкг/мл, от 0,2 мкг/мл до 0,5 мкг/мл, от 0,5 мкг/мл до 1 мкг/мл, от 1 мкг/мл до 2 мкг/мл, от 2 мкг/мл до 5 мкг/мл или от 5 мкг/мл до 10 мкг/мл, например, как определено описанным в настоящей заявке способом.
В одном варианте реализации изобретения молекула антитела связывается с линейным или конформационным эпитопом на C5. В одном варианте реализации изобретения молекула антитела связывается или по существу связывается с таким же, схожим или перекрывающимся эпитопом на C5, что и вторая молекула антитела (например, моноклональное антитело, представленное в Таблице 1). В одном варианте реализации изобретения молекула антитела конкурирует со второй молекулой антитела (например, моноклональное антитело, представленное в Таблице 1) за связывание с C5. В одном варианте реализации изобретения эпитоп является конформационным эпитопом.
В одном варианте реализации изобретения LCDR1, LCDR2, LCDR3, HCDR1 и HCDR2 принадлежат к каноническим классам 2, 1, 1, 1 и 2, соответственно, участков, определяющих комплементарность (CDR) по Чотиа/Chothia. В одном варианте реализации изобретения молекула антитела содержит по меньшей мере один из контактов паратоп-паратоп, представленных в Таблице 6.
Эпитоп
Описанная в настоящей заявке молекула антитела может связываться с эпитопом на C5 (например, C5 человека). Например, эпитоп, связываемый описанной в настоящей заявке молекулой антитела, может содержать одну или более точек контакта с эпитопом в последовательности белка C5, описанной в настоящей заявке.
Животные модели
Описанные в настоящей заявке молекулы антител возможно оценить в условиях in vivo, например, в различных животных моделях. Например, животную модель возможно использовать для оценки эффективности описанной в настоящей заявке молекулы антитела для ингибирования расщепления C5 и/или для лечения или профилактики описанного в настоящей заявке расстройства, например, комплемент-опосредованного расстройства, например, описанного в настоящей заявке комплемент-опосредованного расстройства. Животные модели также возможно использовать, например, для изучения побочных эффектов, определения концентраций молекул антител в условиях in situ, демонстрации корреляции между функцией C5 и комплемент-опосредованным расстройством, например, описанным в настоящей заявке комплемент-опосредованным расстройством.
Иллюстративные животные модели комплемент-опосредованного расстройства, например, описанного в настоящей заявке комплемент-опосредованного расстройства, которые возможно использовать для оценки описанной в настоящей заявке молекулы антитела, включают, но не ограничены ими, мышей с дефицитом C5, например, восстановленных C5 человека.
Иллюстративные животные модели других описанных в настоящей заявке расстройств также известны в данной области техники. Иллюстративные виды животных, которые возможно использовать для оценки описанных в настоящей заявке молекул антител, включают, но не ограничены ими, мышей, крыс, кроликов, морских свинок и обезьян.
Фармацевтические композиции и наборы
В аспекте настоящее изобретение предоставляет композиции, например, фармацевтически приемлемые композиции, включающие описанную в настоящей заявке молекулу антитела (например, описанную в настоящей заявке молекулу гуманизированного антитела) в сочетании с фармацевтически приемлемым носителем.
В настоящей заявке «фармацевтически приемлемый носитель» включает какой-либо и все растворители, дисперсионные среды, изотонические агенты и агенты, замедляющие абсорбцию, и тому подобное, которые являются физиологически совместимыми. Носитель может быть пригодным для внутривенного, внутримышечного, подкожного, парентерального, ректального, спинального или эпидермального введения (например, путем инъекции или инфузии). В одном варианте реализации изобретения менее примерно 5%, например, менее примерно 4%, 3%, 2% или 1% молекул антител в фармацевтической композиции присутствуют в виде агрегатов. В других вариантах воплощения изобретения по меньшей мере примерно 95%, например, по меньшей мере примерно 96%, 97%, 98%, 98,5%, 99%, 99,5%, 99,8% или более молекул антител в фармацевтической композиции присутствуют в виде мономеров. В одном варианте реализации изобретения уровень агрегатов или мономеров определяют хроматографией, например, высокоэффективной эксклюзионной хроматографией (HP-SEC).
Представленные в настоящей заявке композиции могут быть в различных формах. К ним относятся, например, жидкие, полутвердые и твердые лекарственные формы, такие как жидкие растворы (например, растворы для инъекций и инфузий), дисперсии или суспензии, липосомы и суппозитории. Подходящая форма зависит от предполагаемого способа введения и терапевтического применения. Типичные подходящие композиции находятся в форме растворов для инъекций или инфузий. Одним подходящим способом введения является парентеральный (например, внутривенный, подкожный, внутрибрюшинный, внутримышечный). В одном варианте реализации изобретения молекулу антитела вводят путем внутривенной инфузии или инъекции. В одном варианте реализации изобретения молекулу антитела вводят путем внутримышечной или подкожной инъекции.
В настоящей заявке фразы «парентеральное введение» и «вводимый парентерально» обозначают способы введения, отличные от энтерального и местного, как правило, путем инъекции, и включают, без ограничения, внутривенную, внутримышечную, внутриартериальную, интратекальную, интрарикапсулярную, интраорбитальную, внутрисердечную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, подкапсульную, субарахноидальную, внутриспинальную, эпидуральную и внутригрудинную инъекцию и инфузию.
Терапевтические композиции, как правило, должны быть стерильными и стабильными в условиях получения и хранения. Композиция может быть приготовлена в виде раствора, микроэмульсии, дисперсии, липосомы или другой упорядоченной структуры, пригодной для высокой концентрации антител. Стерильные растворы для инъекций могут быть приготовлены путем включения необходимого количества активного соединения (т.е. антитела или фрагмента антитела) в соответствующий растворитель с одним или с комбинацией перечисленных выше ингредиентов, при необходимости, с последующей стерилизацией фильтрованием. Как правило, дисперсии готовят путем включения активного соединения в стерильный носитель, который содержит основную дисперсионную среду и другие необходимые ингредиенты из перечисленных выше. В случае стерильных порошков для приготовления стерильных растворов для инъекций предпочтительными способами получения являются вакуумная сушка и сублимационная сушка, при использовании которых получают порошок активного ингредиента в сочетании с каким-либо дополнительным желаемым ингредиентом из его раствора, предварительно стерилизованного фильтрованием. Подходящую текучесть раствора возможно поддерживать, например, использованием покрытия, такого как лецитин, путем поддержания необходимого размера частиц в случае дисперсии и путем использования поверхностно-активных веществ. Пролонгированную абсорбцию композиций для инъекций возможно достичь включением в композицию агента, замедляющего абсорбцию, например, солей моностеарата и желатина.
Описанные в настоящей заявке молекулы антител возможно вводить различными способами. Некоторые из них известны в данной области техники и для многих терапевтических, профилактических или диагностических применений пригодным путем/способом введения является внутривенная инъекция или инфузия. Например, молекулы антител возможно вводить путем внутривенной инфузии со скоростью, составляющей менее 10 мг/мин; предпочтительно, оставляющей менее или равной 5 мг/мин для достижения дозы от примерно 1 до 100 мг/м2, предпочтительно примерно от 5 до 50 мг/м2, примерно от 7 до 25 мг/м2 и более предпочтительно примерно 10 мг/м2. Как будет понятно специалисту в данной области техники, путь и/или способ введения будут варьировать в зависимости от желаемых результатов. В одном варианте реализации изобретения активное соединение может быть приготовлено с носителем, который будет защищать соединение от быстрого высвобождения, таким как состав с контролируемым высвобождением, включая имплантаты, трансдермальные пластыри и микроинкапсулированные системы доставки. Возможно использовать биоразлагаемые биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, сложные полиортоэфиры и полимолочная кислота. Многие способы приготовления таких составов запатентованы или хорошо известны специалистам в данной области техники. См., например, Sustained and Controlled Release Drug Delivery Systems, J. R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
В одном варианте реализации изобретения молекулу антитела возможно вводить перорально, например, с инертным разбавителем или усваиваемым пищевым носителем. Молекула антитела (и другие ингредиенты, если это желательно) также может быть заключена в желатиновую капсулу с твердой или мягкой оболочкой, спрессована в таблетки или включена непосредственно в рацион субъекта. Для перорального терапевтического введения молекула антитела может быть включена с вспомогательными веществами и может быть использована в форме таблеток для приема внутрь, буккальных таблеток, пастилок, капсул, эликсиров, суспензий, сиропов, облаток и т.п. Для введения молекулы антитела способом, отличным от парентерального введения, может потребоваться нанесение покрытия на соединение или совместное введение соединения с веществом, предотвращающим его инактивацию. Терапевтические, профилактические или диагностические композиции также возможно вводить с помощью медицинских устройств и несколько известны в данной области техники.
Режимы дозирования корректируют для достижения желаемого ответа (например, терапевтический, профилактический или диагностический ответ). Например, возможно ввести один болюс, возможно ввести несколько разделенных доз в течение периода времени, или дозу возможно пропорционально уменьшить или увеличить, в зависимости от терапевтической ситуации. Особенно предпочтительно готовить парентеральные композиции в виде единичной дозированной формы, обеспечивающей простоту введения и однородность дозирования. Используемая в настоящей заявке единичная дозированная форма обозначает физически дискретные единицы, пригодные в качестве единичных доз для субъектов, подлежащих лечению; каждая единица содержит предетерминированное количество активного соединения, рассчитанное для получения желаемого терапевтического эффекта, в сочетании с необходимым фармацевтическим носителем. Характеристики единичных дозированных форм определяются и непосредственно зависят от (a) уникальных характеристик молекулы антитела и конкретного терапевтического, профилактического или диагностического эффекта, который необходимо достичь, и (б) ограничений, которые имеются в области приготовления такой молекулы антитела для лечения чувствительности у индивидуумов.
Иллюстративный, неограничивающий диапазон терапевтически, профилактически или диагностически эффективного количества молекулы антитела составляет примерно 0,1-50 мг/кг веса тела субъекта, например, примерно 0,1-30 мг/кг, например, примерно 1- 30, 1-15, 1-10, 1-5, 5-10 или 1-3 мг/кг, например, примерно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40 или 50 мг/кг. Молекулу антитела возможно вводить путем внутривенной инфузии со скоростью, составляющей менее 10 мг/мин, например, составляющей менее или равной 5 мг/мин для достижения дозы от примерно 1 до 100 мг/м2, например, примерно от 5 до 50 мг/м2, примерно от 7 до 25 мг/м2, например, 10 мг/м2. Необходимо отметить, что значения дозировки могут варьировать в зависимости от типа и тяжести состояния, которое необходимо облегчить. Также следует понимать, что для какого-либо конкретного субъекта конкретные режимы дозирования необходимо корректировать с течением времени в соответствии с индивидуальной потребностью и профессиональным суждением лица, вводящего или контролирующего введение композиций, и что диапазоны дозировки, представленные в настоящей заявке, являются исключительно иллюстративными и не предназначены для ограничения объема или применения заявленных композиций.
Фармацевтические композиции настоящей заявки могут включать «терапевтически эффективное количество», «профилактически эффективное количество» или «диагностически эффективное количество» описанной в настоящей заявке молекулы антитела.
«Терапевтически эффективное количество» обозначает количество, эффективное в дозировках и в течение периодов времени, необходимых для достижения желаемого терапевтического результата. Терапевтически эффективное количество молекулы антитела может варьировать в зависимости от таких факторов, таких как патологическое состояние, возраст, пол и масса индивидуума, и способность антитела или фрагмента антитела вызывать желаемый ответ у индивидуума. Терапевтически эффективное количество также является количеством, при котором терапевтически благоприятные эффекты преобладают над токсическими или вредными эффектами молекулы антитела. «Терапевтически эффективная дозировка», как правило, ингибирует поддающийся измерению параметр на по меньшей мере примерно 20%, например, на по меньшей мере примерно 40%, на по меньшей мере примерно 60% или на по меньшей мере примерно 80% по сравнению с субъектами, не получающими лечение. Поддающимся измерению параметром может быть, например, гематурия, окрашенная моча, пенистая моча, боль, отек (отечность) рук и ступней или высокое кровяное давление. Способность молекулы антитела ингибировать поддающийся измерению параметр возможно оценить на животной модели, позволяющей прогнозировать эффективность для лечения или профилактики IgA-нефропатии. Альтернативно данное свойство композиции возможно оценить путем определения способности молекулы антитела ингибировать расщепление C5, например, с помощью анализа в условиях in vitro, например, путем измерения уровней C5b.
«Профилактически эффективное количество» обозначает количество, эффективное в дозировках и в течение периодов времени, необходимых для достижения желаемого профилактического результата. Как правило, поскольку профилактическую дозу используют у индивидуумов до появления заболевания, или на ранней стадии заболевания, профилактически эффективное количество будет меньше терапевтически эффективного количества.
«Диагностически эффективное количество» обозначает количество, эффективное в дозировках и в течение периодов времени, необходимых для достижения желаемого диагностического результата. Как правило, диагностически эффективным количеством является количество, при котором расстройство, например, описанное в настоящей заявке расстройство, например, IgA-нефропатия, может быть диагностировано в условиях in vitro, ex vivo или in vivo.
Также в объем настоящего изобретения входит набор, содержащий описанную в настоящей заявке молекулу антитела. Набор может включать один или более иных элементов, включающих: инструкции по применению; другие реагенты, например, метку, терапевтический агент или агент, пригодный для хелатирования или присоединения иным способом молекулы антитела к метке или терапевтическому агенту, или радиопротекторную композицию; устройства или иные вещества для получения молекулы антитела для введения; фармацевтически приемлемые носители, а также устройства или иные вещества для введения субъекту.
Нуклеиновые кислоты
Настоящее изобретение также определяет отличительные признаки нуклеиновых кислот, которые содержат нуклеотидные последовательности, кодирующие молекулы антител (например, вариабельные области тяжелой и легкой цепей и участки, определяющие комплементарность (CDR) молекул антитела), как описано в настоящей заявке.
Например, настоящее изобретение определяет отличительные признаки первой и второй нуклеиновых кислот, кодирующих вариабельные области тяжелой и легкой цепи, соответственно, молекулы антитела, выбранной из одной или более молекул антител, описанных в настоящей заявке, например, молекулы антитела из Таблицы 1, или фрагмента молекулы антитела, например, вариабельных областей из Таблицы 1. Нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую какую-либо из аминокислотных последовательностей в таблицах в настоящей заявке, или последовательность по существу идентичную им (например, последовательность, идентичную им по меньшей мере на 85%, 90%, 95%, 99% или более, или которая отличается не более чем 3, 6, 15, 30 или 45 нуклеотидами от последовательностей, представленных в таблицах в настоящей заявке).
В одном варианте реализации изобретения нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере один, два или три участка, определяющих комплементарность (CDR) вариабельной области тяжелой цепи, имеющую аминокислотную последовательность, представленную в таблицах в настоящей заявке, или последовательность по существу гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или имеющую одну или более замен, например, консервативные замены). В одном варианте реализации изобретения нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере один, два или три участка, определяющих комплементарность (CDR) вариабельной области легкой цепи, имеющую аминокислотную последовательность, представленную в таблицах в настоящей заявке, или последовательность по существу гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или имеющую одну или более замен, например, консервативные замены). В одном варианте реализации изобретения нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере один, два, три, четыре, пять или шесть участков, определяющих комплементарность (CDR) вариабельных областей тяжелой и легкой цепи, имеющую аминокислотную последовательность, представленную в таблицах в настоящей заявке, или последовательность по существу гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или имеющую одну или более замен, например, консервативные замены).
В одном варианте реализации изобретения нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере один, два или три участка, определяющих комплементарность (CDR) вариабельной области тяжелой цепи, имеющую нуклеотидную последовательность, указанную в Таблице 5, последовательность по существу гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или способную к гибридизации в условиях жесткости, описанных в настоящей заявке). В одном варианте реализации изобретения нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере один, два или три участка, определяющих комплементарность (CDR) вариабельной области легкой цепи, имеющую нуклеотидную последовательность, указанную в Таблице 5, или последовательность по существу гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или способную к гибридизации в условиях жесткости, описанных в настоящей заявке). В одном варианте реализации изобретения нуклеиновая кислота может содержать нуклеотидную последовательность, кодирующую по меньшей мере один, два, три, четыре, пять или шесть участков, определяющих комплементарность (CDR) вариабельных областей тяжелой и легкой цепи, имеющую нуклеотидную последовательность, указанную в Таблице 5, или последовательность по существу гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или способную к гибридизации в условиях жесткости, описанных в настоящей заявке).
В одном варианте реализации изобретения нуклеиновая кислота содержит нуклеотидную последовательность, указанную в Таблице 5, или последовательность, по существу, гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или способную к гибридизации в условиях жесткости, описанных в настоящей заявке). В одном варианте реализации изобретения нуклеиновая кислота содержит фрагмент нуклеотидной последовательности, указанной в Таблице 5, или последовательность, по существу, гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или способную к гибридизации в условиях жесткости, описанных в настоящей заявке). Фрагмент может кодировать, например, вариабельную область (например, VH или VL); один, два или три, или более CDR, или одну, две, три или четыре, или более каркасных областей.
Раскрытые в настоящей заявке нуклеиновые кислоты включают дезоксирибонуклеотиды или рибонуклеотиды, или их аналоги. Полинуклеотид может быть одноцепочечным или двухцепочечным, и если он является одноцепочечным, он может быть кодирующей цепью или некодирующей (антисмысловой) цепью. Полинуклеотид может содержать модифицированные нуклеотиды, такие как метилированные нуклеотиды и аналоги нуклеотидов. Последовательность нуклеотидов может прерываться компонентами, отличными от нуклеотидов. Полинуклеотид может быть дополнительно модифицированным после полимеризации, например, путем конъюгации с метящим компонентом. Нуклеиновая кислота может быть рекомбинантным полинуклеотидом или полинуклеотидом геномного происхождения, полинуклеотидом из кДНК, полинуклеотидом полусинтетического или синтетического происхождения, который либо не встречается в природе, либо конъюгирован с другим полинуклеотидом, имеющим структуру, не встречающуюся в природе.
В аспекте заявка определяет отличительные признаки клеток-хозяев и векторов, содержащих описанные в настоящей заявке нуклеиновые кислоты. Нуклеиновые кислоты могут присутствовать в одном векторе или в отдельных векторах, присутствующих в одной и той же клетке-хозяине или в отдельной клетке-хозяине, как более подробно описано ниже.
Векторы
Дополнительно в настоящей заявке предложены векторы, содержащие нуклеотидные последовательности, кодирующие описанную в настоящей заявке молекулу антитела.
В одном варианте реализации изобретения вектор содержит нуклеотид, кодирующий описанную в настоящей заявке молекулу антитела, например, как описано в Таблице 1. В другом варианте воплощения изобретения вектор содержит описанную в настоящей заявке нуклеотидную последовательность, например, в Таблице 5. Векторы включают, но не ограничены ими, вирус, плазмиду, космиду, фаг лямбда или искусственную хромосому дрожжей (YAC).
Возможно использовать разные векторные системы. Например, один класс векторов использует элементы ДНК, полученные из вирусов животных, таких как, например, вирус папилломы крупного рогатого скота, вирус полиомы, аденовирус, вирус коровьей оспы, бакуловирус, ретровирусы (вирус саркомы Рауса, MMTV или MOMLV) или вирус SV40. Другой класс векторов использует элементы РНК, полученные из РНК-вирусов, таких как вирус леса Семлики, вирус восточного лошадиного энцефалита и флавивирусы.
Дополнительно, путем введения одного или нескольких маркеров, позволяющих отобрать трансфицированные клетки-хозяева, возможно выбрать клетки, содержащие ДНК, стабильно интегрированную в их хромосомы. Маркер может обеспечивать, например, прототропию к ауксотрофному хозяину, резистентность к биоцидам (например, антибиотикам) или резистентность к тяжелым металлам, таким как медь, и т.п. Селектируемый маркерный ген может быть либо непосредственно связан с экспрессируемыми последовательностями ДНК, либо может быть введен в ту же клетку путем котрансформации. Также могут потребоваться дополнительные элементы для оптимального синтеза мРНК. Такие элементы могут включать сигналы сплайсинга, а также промоторы транскрипции, энхансеры и сигналы терминации.
Как только вектор экспрессии или последовательность ДНК, содержащая конструкции, подготовлены для экспрессии, векторы экспрессии возможно трансфицировать или ввести в соответствующую клетку-хозяина. Указанную процедуру возможно осуществить различными способами, например, слиянием протопластов, осаждением кальция фосфатом, электропорацией, трансдукцией ретровирусом, вирусной трансфекцией, способом генной пушки, липидной трансфекцией или другими традиционными способами. В случае слияния протопластов клетки выращивают в среде и проводят скрининг соответствующей активности.
Способы и условия культивирования полученных трансфицированных клеток, а также выделения продуцируемой молекулы антитела, известны специалистам в данной области техники, и их возможно изменить или оптимизировать в зависимости от конкретного вектора экспрессии и используемой клетки-хозяина млекопитающего в соответствии с настоящим описанием.
Клетки
Настоящее изобретение также предоставляет клетки (например, клетки-хозяева), содержащие нуклеиновую кислоту, кодирующую описанную в настоящей заявке молекулу антитела. Например, клетки-хозяева могут содержать молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, представленную в Таблице 5, последовательность, по существу, гомологичную ей (например, последовательность по меньшей мере примерно на 85%, 90%, 95%, 99% или более идентичную ей и/или способную к гибридизации в условиях жесткости, описанных в настоящей заявке), или фрагмент одной из указанных нуклеиновых кислот. Дополнительно клетки-хозяева могут содержать молекулу нуклеиновой кислоты, кодирующую аминокислотную последовательность из Таблицы 1, последовательность, по существу, гомологичную ей (например, последовательность по меньшей мере примерно на 80%, 85%, 90%, 95%, 99% или более идентичную ей) или фрагмент одной из указанных последовательностей.
В одном варианте реализации изобретения клетки-хозяева являются генетически сконструированными и содержат нуклеиновые кислоты, кодирующие описанную в настоящей заявке молекулу антитела.
В одном варианте реализации изобретения клетки-хозяева генетически сконструированы с использованием кассеты экспрессии. Фраза «кассета экспрессии» обозначает нуклеотидные последовательности, способные оказывать влияние на экспрессию гена в хозяевах, совместимых с такими последовательностями. Такие кассеты могут включать промотор, открытую рамку считывания с интронами или без них и сигнал терминации. Также возможно использовать дополнительные факторы, необходимые или подходящие для влияния на экспрессию, такие как, например, индуцируемый промотор.
Изобретение также предоставляет клетки-хозяева, содержащие описанные в настоящей заявке векторы.
Клетка может быть, но не ограничена ими, эукариотической клеткой, бактериальной клеткой, клеткой насекомого или клеткой человека. Подходящие эукариотические клетки включают, но не ограничены ими, клетки Vero, клетки HeLa, клетки COS, клетки CHO, клетки HEK293, клетки BHK и клетки MDCKII. Подходящие клетки насекомых включают, но не ограничены ими, клетки Sf9. В одном варианте реализации изобретения клетка (например, клетка-хозяин) является выделенной клеткой.
Применение молекул антител
Раскрытые в настоящей заявке молекулы антител, а также раскрытые в настоящей заявке фармацевтические композиции имеют терапевтическое, профилактическое и/или диагностическое применение в условиях in vitro, ex vivo и in vivo.
В одном варианте реализации изобретения молекула антитела снижает (например, ингибирует, блокирует или нейтрализует) одну или более биологических активностей C5 (например, расщепление С5). Например, указанные молекулы антител возможно вводить в клетки в культуре, в условиях in vitro или ex vivo, или субъекту, например, субъекту-человеку, например, в условиях in vivo, для снижения (например, ингибирования, блокирования или нейтрализации) одной или более биологических активностей C5. В одном варианте реализации изобретения молекула антитела ингибирует или, по существу, ингибирует расщепление C5, например, C5 человека, например, для образования C5a и C5b. Соответственно, в аспекте изобретение предоставляет способ лечения, предотвращения или диагностики расстройства, например, описанного в настоящей заявке расстройства (например, IgA-нефропатии) у субъекта, включающий введение субъекту описанной в настоящей заявке молекулы антитела, при этом осуществляется лечение, предотвращение или диагностика расстройства. Например, изобретение предоставляет способ, включающий приведение в контакт описанной в настоящей заявке молекулы антитела с клетками в культуре, например, в условиях in vitro или ex vivo, или введение описанной в настоящей заявке молекулы антитела субъекту, например, в условиях in vivo, для лечения, предотвращения или диагностики расстройства, например, расстройства, связанного с комплемент-опосредованным расстройством, например, описанного в настоящей заявке комплемент-опосредованного расстройства.
В настоящей заявке термин «субъект» предназначен для обозначения человека и животных, отличных от человека. В одном варианте реализации изобретения субъект является субъектом-человеком, например, пациентом-человеком, имеющим комплемент-опосредованное расстройство, например, описанное в настоящей заявке комплемент-опосредованное расстройство, или имеющим риск развития комплемент-опосредованного расстройства, например, описанного в настоящей заявке комплемент-опосредованного расстройства. Термин «животные, отличные от человека» включает млекопитающих и животных, отличных от млекопитающих, таких как нечеловеческие приматы. В одном варианте реализации изобретения субъект является человеком. Описанные в настоящей заявке способы и композиции подходят для лечения пациентов-людей, имеющих комплемент-опосредованное расстройство, например, описанное в настоящей заявке комплемент-опосредованное расстройство. Пациенты, имеющие комплемент-опосредованное расстройство, например, описанное в настоящей заявке комплемент-опосредованное расстройство, включают тех, у кого развилось комплемент-опосредованное расстройство, например, описанное в настоящей заявке комплемент-опосредованное расстройство, но которые (по меньшей мере временно) являются бессимптомными, пациентов, у которых проявился симптом комплемент-опосредованного расстройства, например, описанного в настоящей заявке комплемент-опосредованного расстройства, или пациентов, имеющих расстройство на фоне или связанное с комплемент-опосредованным расстройством, например, с описанным в настоящей заявке комплемент-опосредованным расстройством.
Способы лечения или предотвращения расстройств
Описанные в настоящей заявке молекулы антител возможно использовать для лечения или предотвращения комплемент-опосредованных расстройств, или их симптомов.
В одном варианте реализации изобретения расстройство связано с аберрантными уровнями C5. В одном варианте реализации изобретения молекулу антитела используют для лечения субъекта, имеющего описанное в настоящей заявке расстройство, или имеющего риск развития описанного в настоящей заявке расстройства.
Иллюстративные комплемент-опосредованные расстройства, включают, но не ограничены ими, расстройства, связанные с АР и/или расстройства, связанные с CP. Такие расстройства включают, без ограничения, ревматоидный артрит (РА); синдром антифосфолипидных антител; волчаночный нефрит; повреждение, вызванное ишемией/реперфузией; атипичный гемолитико-уремический синдром (аГУС); типичный или инфекционный гемолитико-уремический синдром (тГУС); болезнь плотных депозитов (БПД); пароксизмальную ночную гемоглобинурию (ПНГ); оптический нейромиелит (НМО); мультифокальную моторную нейропатию (ММН); рассеянный склероз (РС); макулярную дегенерацию (например, возрастная макулярная дегенерация (ВМД)); гемолиз, повышение активности печеночных ферментов и тромбоцитопению (HELLP-синдром); тромботическую тромбоцитопеническую пурпуру (ТТП); спонтанную потерю плода; Паучиммунный васкулит; буллезный эпидермолиз; рецидивирующую потерю плода; миастению гравис и черепно-мозговую травму.
В одном варианте реализации изобретения комплемент-опосредованное расстройство, является заболеванием сосудов, связанным с комплементом, таким как, но не ограниченным ими, заболевание сосудов, связанное с сахарным диабетом (например, глаза), окклюзия центральной вены сетчатки, сердечно-сосудистое заболевание, миокардит, цереброваскулярная болезнь, периферическое сосудистое заболевание (например, скелетно-мышечное), реноваскулярное заболевание, заболевание мезентериальных сосудов/сосудов кишечника, реваскуляризация трансплантатов и/или реплантов, васкулит, пурпурный нефрит Геноха-Шенлейна, васкулит, ассоциированный с системной красной волчанкой, васкулит, ассоциированный с ревматоидным артритом, васкулит, обусловленный иммунными комплексами, болезнь Такаясу, дилатационная кардиомиопатия, диабетическая ангиопатия, болезнь Кавасаки (артериит), венозная газовая эмболия (ВГЭ) и рестеноз после установки стента, ротационной атерэктомии и чрескожной транслюминальной коронарной ангиопластики (ЧТКА).
Дополнительные комплемент-опосредованные расстройства включают, без ограничения, миастению гравис, болезнь холодовых агглютининов, дерматомиозит, болезнь Грейвса, атеросклероз, болезнь Альцгеймера, синдром Гийена-Барре, болезнь Дегоса, отторжение ткани (например, отторжение трансплантата), сепсис, ожог (например, ожог тяжелой степени), системный воспалительный ответ, сепсис, септический шок, повреждение спинного мозга, гломерулонефрит, тиреоидит Хашимото, сахарный диабет I типа, псориаз, пузырчатку, аутоиммунную гемолитическую анемию (АИГА), идиопатическую тромбоцитопеническую пурпуру (ИТП), синдром Гудпасчера, антифосфолипидный синдром (АФС) и катастрофический АФС (КАФС). В некоторых вариантах воплощения изобретения описанные в настоящей заявке растворы с высокой концентрацией антител можно применять в способах лечения тромботической микроангиопатии (ТМА), например, ТМА, ассоциированной с комплемент-опосредованным расстройством, таким как какое-либо из описанных в настоящей заявке комплемент-опосредованных расстройств.
Комплемент-опосредованные расстройства, также включают заболевания легких, связанные с комплементом, такие как, астма, бронхит, хроническая обструктивная болезнь легких (ХОБЛ), интерстициальное заболевание легких, дефицит α-1-антитрипсина, эмфизема, бронхоэктазы, облитерирующий бронхиолит, альвеолит, саркоидоз, легочный фиброз и коллагеновые сосудистые заболевания, но не ограниченные ими.
В одном варианте реализации изобретения комплемент-опосредованное расстройство, выбрано из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aГУС), типичного или инфекционного гемолитико-уремического синдрома (тГУС), болезни плотных депозитов (БПД), пароксизмальной ночной гемоглобинурии (ПНГ), оптического нейромиелита (НМО), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (ТТП); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита или тромботической микроангиопатии (ТМА).
Описанные в настоящей заявке молекулы антител, как правило, вводят с частотой, поддерживающей терапевтически эффективный уровень молекул антител в системе пациента до выздоровления пациента. Например, молекулы антитела возможно вводить с частотой, обеспечивающей концентрацию в сыворотке, достаточную для по меньшей мере примерно 1, 2, 5, 10, 20, 30 или 40 молекул антител для связывания каждой молекулы C5. В одном варианте реализации изобретения молекулы антител вводят каждые 1, 2, 3, 4, 5, 6 или 7 дней, каждые 1, 2, 3, 4, 5 или 6 недель или каждые 1, 2, 3, 4, 5 или 6 месяцев.
Способы введения различных молекул антител известны в данной области техники и описаны ниже. Подходящие дозировки используемых молекул антител будут зависеть от возраста и веса субъекта и конкретного применяемого лекарственного средства.
В одном варианте реализации изобретения молекула антитела вводится субъекту (например, субъекту-человеку) внутривенно. В одном варианте реализации изобретения молекулу антитела вводят субъекту в дозе от 0,1 мг/кг до 50 мг/кг, например, от 0,2 мг/кг до 25 мг/кг, от 0,5 мг/кг до 10 мг/кг, от 0,5 мг/кг до 5 мг/кг, от 0,5 мг/кг до 3 мг/кг, от 0,5 мг/кг до 2,5 мг/кг, от 0,5 мг/кг до 2 мг/кг, от 0,5 мг/кг до 1,5 мг/кг, от 0,5 мг/кг до 1 мг/кг, от 1 мг/кг до 1,5 мг/кг, от 1 мг/кг до 2 мг/кг, от 1 мг/кг до 2,5 мг/кг, от 1 мг/кг до 3 мг/кг, от 1 мг/кг до 2,5 мг/кг или от 1 мг/кг до 5 мг/кг. В одном варианте реализации изобретения молекулу антитела вводят субъекту в фиксированной дозе от 10 мг до 1000 мг, например, от 10 мг до 500 мг, от 10 мг до 250 мг, от 10 мг до 150 мг, от 10 мг до 100 мг, от 10 мг до 50 мг, от 250 мг до 500 мг, от 150 мг до 500 мг, от 100 мг до 500 мг, от 50 мг до 500 мг, от 25 мг до 250 мг, от 50 мг до 150 мг, от 50 мг до 100 мг, от 100 мг до 150 мг, от 100 мг до 200 мг или от 150 мг до 250 мг. В одном варианте реализации изобретения молекулу антитела вводят один раз в неделю, два раза в неделю, один раз в две недели, один раз в три недели, один раз в четыре недели, один раз в восемь недель, один раз в месяц, один раз в два месяца или один раз в три месяца. В одном варианте реализации изобретения молекулу антитела вводят от 0,5 до 3 мг/кг или от 50 до 150 мг один раз в неделю, два раза в неделю, один раз каждые две недели или один раз каждые четыре недели.
Молекулы антител возможно использовать самостоятельно или они могут быть конъюгированы со вторым агентом, например, бактериальным агентом, токсином или белком, например, со второй молекулой антитела к C5. Данный способ включает: введение только молекулы антитела или молекулы антитела, конъюгированной со вторым агентом субъекту, нуждающемуся в таком лечении. Молекулы антител возможно использовать для доставки различных терапевтических агентов, например, токсина или их смесей.
Воспалительные заболевания
В одном варианте реализации изобретения комплемент-опосредованное расстройство, является воспалительным заболеванием, например, ПНГ или aГУС. В одном варианте реализации изобретения молекулу антитела используют для лечения симптома, связанного с воспалительным заболеванием, например, ПНГ или aГУС, или их комбинацией.
Пароксизмальная ночная гемоглобинурия (ПНГ), как правило, характеризуется разрушением эритроцитов (гемолитическая анемия), тромбами (тромбоз) и расстройством функции костного мозга (например, выработка недостаточного количества компонентов крови).
Атипичный гемолитико-уремический синдром (аГУС), как правило, связан с хронической неконтролируемой активацией системы комплемента. Как правило, аГУС характеризуется системной тромботической микроангиопатией (ТМА), образованием тромбов в мелких сосудах по всему телу, что может привести к инсульту, сердечному приступу, почечной недостаточности и смерти.
Комбинированное лечение
Молекулы антител возможно использовать в сочетании с другими лекарственными средствами. Например, комбинированное лечение может включать молекулу антитела, входящую в состав в комбинации с и/или вводимую совместно с одним или более дополнительными терапевтическими агентами, например, одним или более дополнительными терапевтическими агентами, описанными в настоящей заявке. В других вариантах воплощения изобретения молекулы антител вводят в комбинации с другими терапевтическими средствами лечения, например, описанными в настоящей заявке другими терапевтическими средствами лечения. Преимуществом указанного комбинированного лечения может быть использование более низких дозировок вводимых терапевтических агентов, что позволяет избежать возможных токсических эффектов или осложнений, связанных с различными монотерапиями.
В настоящей заявке вводимый «в комбинации» обозначает, что два (или более) различных лечения предоставляют субъекту до или во время поражения субъекта расстройством. В одном варианте реализации изобретения два или более лечения предоставляют с профилактической целью, например, до того, как у субъекта разовьется расстройство или у пациента будет диагностировано расстройство. В другом варианте воплощения изобретения два или более лечения предоставляют после того, как у субъекта развилось или было диагностировано расстройство. В одном варианте реализации изобретения предоставление одного лечения все еще происходит, когда начинается предоставление второго, так что происходит перекрытие. В настоящей заявке такое явление иногда упоминается как «одновременное» или «сопутствующее предоставление». В других вариантах воплощения изобретения предоставление одного лечения заканчивается до того, как начинают предоставлять другое лечение. В одном варианте реализации того или иного случая лечение более эффективно ввиду сочетанного введения. Например, второе лечение является более эффективным, например, наблюдается эквивалентный эффект при менее интенсивном втором лечении или второе лечение уменьшает симптомы в большей степени по сравнению с тем, что возможно было бы наблюдать, если бы второе лечение предоставляли в отсутствие первого лечения, или аналогичная ситуация наблюдается с первым лечением. В одном варианте реализации изобретения предоставление таково, что уменьшение симптома или другого параметра, связанного с расстройством, превышает таковое, которое наблюдалось бы при предоставлении одного лечения в отсутствие другого. Эффект двух лечений может быть частично аддитивным, полностью аддитивным или более чем аддитивным. Предоставление может быть таковым, что эффект первого предоставленного лечения все еще обнаруживается при предоставлении второго.
В одном варианте реализации изобретения дополнительный агент является второй молекулой антитела, например, молекулой антитела, отличной от первой молекулы антитела. Иллюстративные молекулы антител, которые возможно использовать в комбинации, включают, но не ограничены ими, какую-либо комбинацию молекул антител, перечисленных в Таблице 1.
В одном варианте реализации изобретения молекулу антитела вводят в комбинации со вторым лечением для лечения или предотвращения комплемент-опосредованного расстройства, например, описанного в настоящей заявке комплемент-опосредованного расстройства.
Иллюстративные виды лечения, которые возможно использовать в комбинации с молекулой антитела или композицией, описанными в настоящей заявке, для лечения или предотвращения других расстройств, также описаны в настоящей заявке в разделе «Способы лечения или предотвращения расстройств».
Способы диагностики
В некоторых аспектах настоящее изобретение предоставляет способ диагностики для обнаружения наличия C5 (например, C5 человека) в условиях in vitro (например, в биологическом образце, таком как биопсия или образец крови) или в условиях in vivo (например, визуализация у субъекта в условиях in vivo). Способ включает: (i) приведение в контакт образца с описанной в настоящей заявке молекулой антитела или введение субъекту молекулы антитела; (необязательно) (ii) контакт эталонного образца, например, контрольного образца (например, контрольного биологического образца, такого как биопсия или образец крови) или контрольного субъекта с описанной в настоящей заявке молекулой антитела; и (iii) обнаружение образования комплекса молекулы антитела и C5 в образце или субъекте, или контрольном образце или субъекте, при этом изменение, например, статистически значимое изменение, образования комплекса в образце или субъекте относительно контрольного образца или субъекта свидетельствует о наличии C5 в образце. Молекула антитела может быть прямо или косвенно помечена детектируемым веществом для облегчения обнаружения связанного или несвязанного антитела. Подходящие детектируемые вещества включают различные ферменты, простетические группы, флуоресцентные вещества, люминесцентные вещества и радиоактивные вещества, как описано выше и более подробно описано ниже.
Термин «образец», обозначающий образцы, используемые для обнаружения полипептида (например, C5) или нуклеиновой кислоты, кодирующей полипептид, включает, но не ограничен ими, клетки, клеточные лизаты, белки или мембранные экстракты клеток, биологические жидкости, такие как кровь или образцы тканей, такие как биопсии.
Образование комплекса молекулы антитела и C5 может быть обнаружено путем измерения или визуализации либо молекулы антитела, связанной с C5, либо несвязанной молекулы антитела. Возможно использовать какие-либо подходящие анализы на обнаружение и типичные анализы на обнаружение включают твердофазные иммуноферментные анализы (ELISA), радиоиммуноанализ (РИА) или иммуногистохимию. В качестве альтернативы мечению молекулы антитела, наличие C5 возможно определить в образце конкурентным иммуноанализом с использованием стандартов, меченных детектируемым веществом, и немеченой молекулы антитела. В таком анализе объединяют биологический образец, меченые стандарты и молекулу антитела и определяют количество меченого стандарта, связанного с немеченой связывающей молекулой. Количество C5 в образце обратно пропорционально количеству меченого стандарта, связанного с молекулой антитела.
Описанные в настоящей заявке молекулы антител можно применять для диагностики расстройств, которые зможно лечить или предотвращать с помощью описанных в настоящей заявке молекул антител. Описанные в настоящей заявке способы обнаружения или диагностики возможно использовать в сочетании с другими описанными в настоящей заявке способами для лечения или предотвращения расстройства, описанного в настоящей заявке.
Настоящее изобретение также включает какой-либо из следующих пронумерованных пунктов.
1. Выделенная молекула антитела, способная связываться с компонентом 5 (C5) комплемента, которая содержит:
(a) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 87, аминокислотную последовательность HCDR2 SEQ ID NO: 88 и аминокислотную последовательность HCDR3 SEQ ID NO: 89; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 90, аминокислотную последовательность LCDR2 SEQ ID NO: 91 и аминокислотную последовательность LCDR3 SEQ ID NO: 92 или
(б) VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 94, аминокислотную последовательность HCDR2 SEQ ID NO: 95 и аминокислотную последовательность HCDR3 SEQ ID NO: 96; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 97, аминокислотную последовательность LCDR2 SEQ ID NO: 98 и аминокислотную последовательность LCDR3 SEQ ID NO: 99.
2. Молекула антитела по п. 1, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 87, аминокислотную последовательность HCDR2 SEQ ID NO: 88 и аминокислотную последовательность HCDR3 SEQ ID NO: 89; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 90, аминокислотную последовательность LCDR2 SEQ ID NO: 91 и аминокислотную последовательность LCDR3 SEQ ID NO: 92.
3. Молекула антитела по п. 1, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 94, аминокислотную последовательность HCDR2 SEQ ID NO: 95 и аминокислотную последовательность HCDR3 SEQ ID NO: 96; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 97, аминокислотную последовательность LCDR2 SEQ ID NO: 98 и аминокислотную последовательность LCDR3 SEQ ID NO: 99.
4. Молекула антитела по любому из пп. 1-3, которая содержит VH, содержащую какую-либо аминокислотную последовательность HCDR1 из SEQ ID NO: 16-23; какую-либо аминокислотную последовательность HCDR2 из SEQ ID NO: 24-30 и какую-либо аминокислотную последовательность HCDR3 из SEQ ID NO: 31-36; и VL, содержащую какую-либо аминокислотную последовательность LCDR1 из SEQ ID NO: 37-41, какую-либо аминокислотную последовательность LCDR2 из SEQ ID NO: 42-46 и какую-либо аминокислотную последовательность LCDR3 из SEQ ID NO: 47-52.
5. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 19, аминокислотную последовательность HCDR2 SEQ ID NO: 28 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 43 и аминокислотную последовательность LCDR3 SEQ ID NO: 48.
6. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 20, аминокислотную последовательность HCDR2 SEQ ID NO: 28 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 43 и аминокислотную последовательность LCDR3 SEQ ID NO: 48.
7. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 21, аминокислотную последовательность HCDR2 SEQ ID NO: 29 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 43 и аминокислотную последовательность LCDR3 SEQ ID NO: 48.
8. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 22, аминокислотную последовательность HCDR2 SEQ ID NO: 29 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 43 и аминокислотную последовательность LCDR3 SEQ ID NO: 48.
9. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 19, аминокислотную последовательность HCDR2 SEQ ID NO: 28 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 44 и аминокислотную последовательность LCDR3 SEQ ID NO: 49.
10. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 20, аминокислотную последовательность HCDR2 SEQ ID NO: 28 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 44 и аминокислотную последовательность LCDR3 SEQ ID NO: 49.
11. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 21, аминокислотную последовательность HCDR2 SEQ ID NO: 29 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 44 и аминокислотную последовательность LCDR3 SEQ ID NO: 49.
12. Молекула антитела по п. 4, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 22, аминокислотную последовательность HCDR2 SEQ ID NO: 29 и аминокислотную последовательность HCDR3 SEQ ID NO: 35; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 38, аминокислотную последовательность LCDR2 SEQ ID NO: 44 и аминокислотную последовательность LCDR3 SEQ ID NO: 49.
13. Молекула антитела по любому из пп. 1-3, которая содержит VH, содержащую какую-либо аминокислотную последовательность HCDR1 из SEQ ID NO: 54-58; какую-либо аминокислотную последовательность HCDR2 из SEQ ID NO: 59-65 и какую-либо аминокислотную последовательность HCDR3 из SEQ ID NO: 66-70; и VL, содержащую какую-либо аминокислотную последовательность LCDR1 из SEQ ID NO: 71-75, какую-либо аминокислотную последовательность LCDR2 из SEQ ID NO: 76-80 и какую-либо аминокислотную последовательность LCDR3 из SEQ ID NO: 81-86.
14. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 54, аминокислотную последовательность HCDR2 SEQ ID NO: 59 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 76 и аминокислотную последовательность LCDR3 SEQ ID NO: 81.
15. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 55, аминокислотную последовательность HCDR2 SEQ ID NO: 59 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 76 и аминокислотную последовательность LCDR3 SEQ ID NO: 81.
16. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 54, аминокислотную последовательность HCDR2 SEQ ID NO: 60 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 76 и аминокислотную последовательность LCDR3 SEQ ID NO: 81.
17. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 55, аминокислотную последовательность HCDR2 SEQ ID NO: 60 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 76 и аминокислотную последовательность LCDR3 SEQ ID NO: 81.
18. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 54, аминокислотную последовательность HCDR2 SEQ ID NO: 59 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 77 и аминокислотную последовательность LCDR3 SEQ ID NO: 82.
19. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 55, аминокислотную последовательность HCDR2 SEQ ID NO: 59 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 77 и аминокислотную последовательность LCDR3 SEQ ID NO: 82.
20. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 54, аминокислотную последовательность HCDR2 SEQ ID NO: 60 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 77 и аминокислотную последовательность LCDR3 SEQ ID NO: 82.
21. Молекула антитела по п. 13, которая содержит VH, содержащую аминокислотную последовательность HCDR1 SEQ ID NO: 55, аминокислотную последовательность HCDR2 SEQ ID NO: 60 и аминокислотную последовательность HCDR3 SEQ ID NO: 66; и VL, содержащую аминокислотную последовательность LCDR1 SEQ ID NO: 71, аминокислотную последовательность LCDR2 SEQ ID NO: 77 и аминокислотную последовательность LCDR3 SEQ ID NO: 82.
22. Молекула антитела по любому из пп. 1-21, которая содержит VH, содержащую аминокислотную последовательность по меньшей мере на 85%, 90% или 95% идентичную какой-либо из SEQ ID NO: 1-9.
23. Молекула антитела по п. 22, которая содержит VH, содержащую какую-либо аминокислотную последовательность из SEQ ID NO: 1-9.
24. Молекула антитела по любому из пп. 1-21, которая содержит VL, содержащую аминокислотную последовательность по меньшей мере на 85%, 90% или 95% идентичную какой-либо из SEQ ID NO: 10-15.
25. Молекула антитела по п. 24, которая содержит VL, содержащую какую-либо аминокислотную последовательность из SEQ ID NO: 10-15.
26. Молекула антитела по любому из пп. 1-21, которая содержит VH, содержащую аминокислотную последовательность по меньшей мере на 85%, 90% или 95% идентичную какой-либо из SEQ ID NO: 1-9, и VL, содержащую аминокислотную последовательность по меньшей мере на 85%, 90% или 95% идентичную какой-либо из SEQ ID NO: 10-15.
27. Молекула антитела по п. 26, которая содержит VH, содержащую какую-либо аминокислотную последовательность из SEQ ID NO: 1-9, и VL, содержащую какую-либо аминокислотную последовательность из SEQ ID NO: 10-15.
28. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 1, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
29. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 2, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
30. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 3, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
31. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
32. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 1, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
33. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 2, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
34. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 3, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
35. Молекула антитела по любому из пп. 1-27, которая содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
36. Молекула антитела по любому из предыдущих пунктов, которая содержит антигенсвязывающий фрагмент.
37. Молекула антитела по п. 36, при этом антигенсвязывающий фрагмент содержит Fab, F(ab')2, Fv или scFv.
38. Молекула антитела по любому из предыдущих пунктов, которая содержит константную область тяжелой цепи, выбранную из константных областей тяжелой цепи IgG1, IgG2, IgG3 или IgG4, или химеру двух или более изотипов (например, IgG2/4), и необязательно, при этом константная область тяжелой цепи содержит одну или более модификаций аминокислот в шарнирном участке, CH2 или CH3 участке, как указано в IgG2/4-LS или IgG2/4-YTE.
39. Молекула антитела по любому из предыдущих пунктов, которая содержит константную область легкой цепи, выбранную из константных областей легкой цепи каппа или лямбда.
40. Молекула антитела по любому из предыдущих пунктов, которая содержит константную область тяжелой цепи, выбранную из константных областей тяжелой цепи IgG1, IgG2, IgG3, IgG4 или химеру двух или более изотипов (например, IgG2 и IgG4), и константную область легкой цепи, выбранную из константных областей легкой цепи каппа или лямбда.
41. Молекула антитела по любому из предыдущих пунктов, которая содержит Fc-участок.
42. Молекула антитела по п. 41, при этом Fc-участок содержит одно или оба из замещений Met-429-Leu и Asn-435-Ser в остатках, соответствующих метионину 428 и аспарагину 434, соответственно, нумерация каждого согласно нумерации ЕС.
43. Молекула антитела по п. 41 или 42, при этом Fc-участок содержит одно, два или три из замещений Met-252-Tyr, Ser-254-Thr и Thr-256-Glu в остатках, соответствующих метионину 252, серину 254 и треонину 256, соответственно, нумерация каждого согласно нумерации ЕС.
44. Молекула антитела по любому из предыдущих пунктов, содержащая две VH и две VL.
45. Молекула антитела по любому из предыдущих пунктов, при этом указанная молекула антитела является молекулой гуманизированного антитела.
46. Молекула антитела по любому из предыдущих пунктов, при этом указанная молекула антитела является молекулой моноклонального антитела.
47. Молекула антитела по любому из предыдущих пунктов, при этом указанная молекула антитела является синтетической молекулой антитела.
48. Молекула антитела по любому из предыдущих пунктов, при этом указанная молекула антитела является молекулой моноспецифического антитела.
49. Молекула антитела по любому из предыдущих пунктов, которая является молекулой мультиспецифического антитела.
50. Молекула антитела по любому из предыдущих пунктов, которая является молекулой биспецифического антитела.
51. Молекула антитела по любому из предыдущих пунктов, при этом C5 является C5 человека.
52. Молекула антитела по любому из предыдущих пунктов, которая связывается с C5 человека с KD’, составляющей менее 0,1 мкг/мл или 0,6 нМ.
53. Молекула антитела по любому из предыдущих пунктов, которая связывается с C5 человека с KD’, составляющей от 0,03 до 0,08 мкг/мл или от 0,2 нМ до 0,53 нМ.
54. Молекула антитела по любому из предыдущих пунктов, которая связывается с C5 человека с EC50, составляющей менее 2 мкг/мл (например, менее 0,5 мкг/мл), как определено методом ELISA.
55. Молекула антитела по любому из предыдущих пунктов, которая связывается с C5 человека с EC50, составляющей от 0,01 мкг/мл до 2 мкг/мл (например, от 0,02 мкг/мл до 0,2 мкг/мл), как определено методом ELISA.
56. Молекула антитела по любому из предыдущих пунктов, которая связывается с C5 человека с EC50, составляющей от 0,03 мкг/мл до 0,8 мкг/мл (например, от 0,03 мкг/мл до 0,16 мкг/мл), как определено методом ELISA.
57. Молекула антитела по любому из предыдущих пунктов, которая ингибирует гемолиз при IC50, составляющей менее 10 мкг/мл, как определено способом оценки гемолиза в условиях in vitro.
58. Молекула антитела по любому из предыдущих пунктов, которая ингибирует гемолиз при IC50, составляющей от 0,5 мкг/мл до 6 мкг/мл (например, от 2 мкг/мл до 6 мкг/мл), как определено способом оценки гемолиза в условиях in vitro.
59. Молекула антитела по любому из предыдущих пунктов, которая ингибирует гемолиз при IC50, составляющей от 0,5 мкг/мл до 3,3 мкг/мл (например, от 2,3 мкг/мл до 3,3 мкг/мл), как определено способом оценки гемолиза в условиях in vitro.
60. Молекула антитела по любому из предыдущих пунктов, которая связывается с C5 человека, содержащим аминокислотную последовательность SEQ ID NO: 53.
61. Молекула антитела по любому из предыдущих пунктов, при этом:
(1) LCDR1, LCDR2, LCDR3, HCDR1 и HCDR2 принадлежат к каноническим классам 2, 1, 1, 1 и 2, соответственно, участков, определяющих комплементарность (CDR) по Чотиа/Chothia, и
(2) молекула антитела содержит по меньшей мере один из контактов паратоп-паратоп, представленных в Таблице 6.
62. Молекула антитела, способная связываться с C5, которая содержит VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, при этом:
(1) LCDR1, LCDR2, LCDR3, HCDR1 и HCDR2 принадлежат к каноническим классам 2, 1, 1, 1 и 2, соответственно, участков, определяющих комплементарность (CDR) по Чотиа/Chothia, и
(2) молекула антитела содержит по меньшей мере один из контактов паратоп-паратоп, представленных в Таблице 6.
63. Молекула антитела, которая конкурирует за связывание с C5 с молекулой антитела по любому из предыдущих пунктов.
64. Молекула антитела, которая связывается с тем же или перекрывающимся эпитопом, что и эпитоп, распознаваемый молекулой антитела по любому из предыдущих пунктов.
65. Фармацевтическая композиция, содержащая выделенную молекулу антитела по любому из предыдущих пунктов и фармацевтически приемлемый носитель, вспомогательное вещество или стабилизатор.
66. Выделенная нуклеиновая кислота, кодирующая VH, VL или обе молекулы антитела по любому из пп. 1-65.
67. Вектор экспрессии, содержащий нуклеиновую кислоту по п. 66.
68. Клетка-хозяин, содержащая нуклеиновую кислоту по п. 66 или вектор по п. 67.
69. Способ получения молекулы антитела, включающий культивирование клетки-хозяина по п. 68 в условиях, подходящих для экспрессии гена.
70. Способ ингибирования C5, включающий приведение в контакт C5 с молекулой антитела по любому из пп. 1-64 или фармацевтической композицией по п. 65.
71. Способ по пункту 70, при этом стадия приведения в контакт происходит в условиях in vitro, ex vivo или in vivo.
72. Способ лечения расстройства, включающий введение субъекту, нуждающемуся в этом, молекулы антитела по любому из пп. 1-64 или фармацевтической композиции по п. 65 в количестве, эффективном для лечения расстройства.
73. Способ по п. 72, при этом расстройство является комплемент-опосредованным расстройством, необязательно, при этом комплемент-опосредованное расстройство, выбрано из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aГУС), типичного или инфекционного гемолитико-уремического синдрома (тГУС), болезни плотных депозитов (БПД), пароксизмальной ночной гемоглобинурии (ПНГ), оптического нейромиелита (НМО), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (ТТП); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита или тромботической микроангиопатии (ТМА).
74. Способ по п. 72 или 73, при этом молекулу антитела вводят субъекту в дозе от 0,1 мг/кг до 50 мг/кг.
75. Способ по любому из пп. 72-74, дополнительно включающий введение второго терапевтического агента или средства.
76. Способ по п. 75, при этом второй терапевтический агент или средство вводят до, во время или после введения молекулы антитела.
77. Способ предотвращения расстройства, включающий введение субъекту, нуждающемуся в этом, молекулы антитела по любому из пп. 1-64 или фармацевтической композиции по п. 65 в количестве, эффективном для лечения расстройства.
78. Способ по п. 77, при этом расстройство является комплемент-опосредованным расстройством, необязательно, при этом комплемент-опосредованное расстройство, выбрано из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aГУС), типичного или инфекционного гемолитико-уремического синдрома (тГУС), болезни плотных депозитов (БПД), пароксизмальной ночной гемоглобинурии (ПНГ), оптического нейромиелита (НМО), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (ТТП); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита или тромботической микроангиопатии (ТМА).
79. Способ обнаружения C5, включающий (i) приведение в контакт образца или субъекта с молекулой антитела по любому из пп. 1-64 в условиях, которые делают возможным взаимодействие молекулы антитела и C5, и (ii) обнаружение образования комплекса молекулы антитела и образца или субъекта.
80. Способ по п. 79, дополнительно включающий приведение в контакт эталонного образца или субъекта с молекулой антитела по любому из пп. 1-64 в условиях, которые делают возможным взаимодействие молекулы антитела и C5, и (ii) обнаружение образования комплекса молекулы антитела и образца или субъекта.
81. Молекула антитела по любому из пп. 1-64 или фармацевтическая композиция по п. 66 для применения для лечения расстройства у субъекта.
82. Молекула антитела или фармацевтическая композиция для применения по п. 84, при этом расстройство является комплемент-опосредованным расстройством, необязательно, при этом комплемент-опосредованное расстройство, выбрано из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aГУС), типичного или инфекционного гемолитико-уремического синдрома (тГУС), болезни плотных депозитов (БПД), пароксизмальной ночной гемоглобинурии (ПНГ), оптического нейромиелита (НМО), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (ТТП); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита или тромботической микроангиопатии (ТМА).
83. Применение молекулы антитела по любому из пп. 1-64 или фармацевтической композиции по п. 66 при получении лекарственного средства для лечения расстройства у субъекта.
84. Применение по п. 83, при этом расстройство является комплемент-опосредованным расстройством, необязательно, при этом комплемент-опосредованное расстройство, выбрано из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aГУС), типичного или инфекционного гемолитико-уремического синдрома (тГУС), болезни плотных депозитов (БПД), пароксизмальной ночной гемоглобинурии (ПНГ), оптического нейромиелита (НМО), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (ТТП); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита или тромботической микроангиопатии (ТМА).
ПРИМЕРЫ
Пример 1: Получение и характеристика моноклонального антитела (mAb) к C5
Получение моноклональных антител к C5
Белок комплемента сходится в общий путь, приводящий к расщеплению или активации C3 с образованием C3a или C3b, что в свою очередь приводит к образованию различных биологически активных молекул, таких как C5a и C5b.
Был создан ряд иллюстративных mAb к C5 (обозначаемых как ATG-001, ATG-002, ATG-003, ATG-004, ATG-005, ATG-006, ATG-007, ATG-008, ATG-012 или ATG-013).
Функциональный анализ моноклональных антител к C5
Иллюстративные mAb к C5 экспрессировали в клетках Expi CHO и определяли их чистоту способом ДНС-ПААГ в восстанавливающих и невосстанавливающих условиях. В восстанавливающих условиях mAb мигрировали в виде двух отдельных треков 25 кДа и 50 кДа, что соответствовало молекулярным массам легкоцепочечных и тяжелоцепочечных полипептидов, соответственно. В невосстанавливающих условиях mAb наблюдали как один трек 150 кДа, что соответствовало молекулярной массе интактного антитела (ФИГ. 1A). Анализ моноклональных антител способом эксклюзионной хроматографии (SEC) продемонстрировал, что большинство антител были мономерными (ФИГ. 1B).
Оценку связывания иллюстративных антител с C5 человека при pH 7,4 проводили способом ELISA. Значения ЕС50 иллюстративных антител демонстрируют, что иллюстративные антитела проявляют высокую аффинность связывания с C5 человека (ФИГ. 2A). Кроме того, иллюстративные антитела дозозависимо ингибировали гемолиз куриных эритроцитов с концентрацией полумаксимального ингибирования (IC50) в диапазоне 0,5-6 мкг/мл, демонстрируя, что иллюстративные антитела подавляли активность C5 (ФИГ. 2B).
Полученные данные подтверждают, что сконструированные антитела проявляли активность против C5 в биохимических исследованиях и исследованиях в условиях in vitro.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
Все упомянутые в настоящей заявке публикации, патенты и номера доступа включены в настоящую заявку во всей их полноте посредством ссылки, как если бы каждая отдельная публикация или патент были конкретно и индивидуально указаны как включенные посредством ссылки.
ЭКВИВАЛЕНТЫ
Хотя обсуждались конкретные варианты воплощения настоящего изобретения, приведенное выше описание носит иллюстративный и неограничивающий характер. Многие вариации изобретения будут очевидны специалистам в данной области техники после ознакомления с настоящим описанием и приведенной ниже формулой изобретения. Полный объем изобретения должен определяться путем ссылки на формулу изобретения в сочетании с полным объемом их эквивалентов и описанием вместе с такими вариациями.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ATARGA, LLC
<120> МОЛЕКУЛЫ АНТИТЕЛ К КОМПОНЕНТУ 5 КОМПЛЕМЕНТА И ИХ ПРИМЕНЕНИЕ
<130> A2176-7000WO
<140>
<141>
<150> 62/686,982
<151> 2018-06-19
<160> 120
<170> Патентная версия 3.5
<210> 1
<211> 122
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 1
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Asn Tyr
20 25 30
Trp Met Gln Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Leu Pro Gly Thr Gly Ser Thr Glu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Val Arg Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Phe Phe Gly Ser Thr Pro Asn Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 2
<211> 122
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 2
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Asp Phe
20 25 30
Tyr Met Gln Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Leu Pro Gly Thr Gly Ser Thr Glu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Val Arg Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Phe Phe Gly Ser Thr Pro Asn Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 3
<211> 122
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 3
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Asn Tyr
20 25 30
Trp Met Gln Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Leu Pro Gly Thr Gly His Thr Glu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Val Arg Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Phe Phe Gly Ser Thr Pro Asn Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 4
<211> 122
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 4
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Asp Phe
20 25 30
Tyr Met Gln Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Leu Pro Gly Thr Gly His Thr Glu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Val Arg Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Phe Phe Gly Ser Thr Pro Asn Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 5
<211> 123
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 5
Gln Val Lys Leu Leu Glu Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
1 5 10 15
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Ser Asn
20 25 30
Tyr Trp Ile Gln Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp
35 40 45
Met Gly Glu Ile Leu Ala Gly Ser Gly Ser Thr Glu Tyr Ser Gln Lys
50 55 60
Phe Arg Gly Arg Val Thr Phe Thr Arg Asp Thr Ser Ala Thr Thr Ala
65 70 75 80
Tyr Met Gly Leu Ser Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Tyr Pro Phe Gly Ser Ser Pro Asn Trp Glu Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 6
<211> 123
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 6
Gln Val Lys Leu Leu Glu Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
1 5 10 15
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Ile Phe Ser Asn
20 25 30
Tyr Trp Ile Gln Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp
35 40 45
Met Gly Glu Val Leu Pro Gly Ser Gly Ser Thr Glu Tyr Ser Gln Lys
50 55 60
Phe Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ala Thr Thr Ala
65 70 75 80
Tyr Met Gly Leu Ser Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Tyr Tyr Phe Gly Ser Ser Pro Asn Trp Tyr Phe Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 7
<211> 123
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 7
Gln Val Lys Leu Leu Glu Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
1 5 10 15
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ser
20 25 30
Tyr Trp Ile Gln Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp
35 40 45
Met Gly Glu Ile Leu Pro Gly Asp Gly Ser Thr Glu Tyr Ser Gln Lys
50 55 60
Phe Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ala Thr Thr Ala
65 70 75 80
Tyr Met Gly Leu Ser Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Tyr Phe Phe Gly Ser Ser Pro Asn Trp Ala Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 8
<211> 123
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 8
Gln Val Lys Leu Leu Glu Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
1 5 10 15
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ser
20 25 30
Tyr Trp Ile Gln Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp
35 40 45
Met Gly Glu Ile Leu Pro Thr Asn Gly Ser Thr Glu Tyr Ser Gln Lys
50 55 60
Phe Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ala Thr Thr Ala
65 70 75 80
Tyr Met Gly Leu Ser Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Tyr Phe Phe Gly Ser Ser Pro Asn Trp Ala Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 9
<211> 116
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 9
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Asn
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Tyr Met
35 40 45
Gly Trp Ile Asn Pro Lys Ser Gly Asp Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Val Arg Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Gly Trp Trp Gly Met Asp Val Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 10
<211> 107
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 10
Glu Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gly Ala Thr Glu Asn Ile Tyr Gly Ala
20 25 30
Leu Asn Trp Tyr Gln His Glu Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Leu Ala Asp Gly Val Thr Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Asn Val Leu Asn Thr Pro Leu
85 90 95
Ser Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105
<210> 11
<211> 107
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 11
Glu Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gly Ala Thr Glu Asn Ile Tyr Gly Ala
20 25 30
Leu Asn Trp Tyr Gln His Glu Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Thr Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Val Leu Asn Thr Pro Val
85 90 95
Ser Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105
<210> 12
<211> 107
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 12
Glu Leu Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Asn Ile Ala Cys Arg Ala Ser Glu Gly Ile Tyr Gly Ala
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Val Leu Asn Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 13
<211> 107
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 13
Glu Leu Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Asn Ile Ala Cys Arg Ala Ser Glu Ser Ile Tyr Gly Ala
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Asn Val Leu Ser Thr Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 14
<211> 107
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 14
Glu Leu Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Asn Ile Ala Cys Gly Ala Ser Glu Asn Ile Tyr Gly Ala
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Asn Val Leu Asn Thr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 15
<211> 107
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 15
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asn Ile Asn Asn Tyr
20 25 30
Leu His Trp Tyr Gln His Glu Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Asn Leu Gln Gly Gly Val Thr Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Thr His Ala Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105
<210> 16
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 16
Gly Tyr Ile Phe Ser Asn Tyr
1 5
<210> 17
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 17
Gly Phe Ile Phe Ser Asn Tyr
1 5
<210> 18
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 18
Gly Tyr Ile Phe Thr Ser Tyr
1 5
<210> 19
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 19
Gly Tyr Ile Phe Thr Asn Tyr
1 5
<210> 20
<211> 8
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 20
Gly Tyr Ile Phe Thr Asp Phe Tyr
1 5
<210> 21
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 21
Gly His Ile Phe Thr Asn Tyr
1 5
<210> 22
<211> 8
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 22
Gly His Ile Phe Thr Asp Phe Tyr
1 5
<210> 23
<211> 8
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 23
Gly Tyr Thr Phe Thr Gly Asn Tyr
1 5
<210> 24
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 24
Leu Ala Gly Ser Gly Ser
1 5
<210> 25
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 25
Leu Pro Gly Ser Gly Ser
1 5
<210> 26
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 26
Leu Pro Gly Asp Gly Ser
1 5
<210> 27
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 27
Leu Pro Thr Asn Gly Ser
1 5
<210> 28
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 28
Leu Pro Gly Thr Gly Ser
1 5
<210> 29
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 29
Leu Pro Gly Thr Gly His
1 5
<210> 30
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 30
Asn Pro Lys Ser Gly Asp
1 5
<210> 31
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 31
Tyr Pro Phe Gly Ser Ser Pro Asn Trp Glu Phe Asp Tyr
1 5 10
<210> 32
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 32
Tyr Tyr Phe Gly Ser Ser Pro Asn Trp Tyr Phe Asp Val
1 5 10
<210> 33
<211> 10
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 33
Gly Ser Ser Pro Asn Trp Ala Met Asp Tyr
1 5 10
<210> 34
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 34
Tyr Phe Phe Gly Ser Ser Pro Asn Trp Ala Met Asp Tyr
1 5 10
<210> 35
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 35
Tyr Phe Phe Gly Ser Thr Pro Asn Trp Tyr Phe Asp Val
1 5 10
<210> 36
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 36
Gly Trp Trp Gly Met Asp Val
1 5
<210> 37
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 37
Arg Ala Ser Gln Asn Ile Asn Asn Tyr Leu His
1 5 10
<210> 38
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 38
Gly Ala Thr Glu Asn Ile Tyr Gly Ala Leu Asn
1 5 10
<210> 39
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 39
Arg Ala Ser Glu Ser Ile Tyr Gly Ala Leu Asn
1 5 10
<210> 40
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 40
Gly Ala Ser Glu Asn Ile Tyr Gly Ala Leu His
1 5 10
<210> 41
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 41
Arg Ala Ser Glu Gly Ile Tyr Gly Ala Leu Ala
1 5 10
<210> 42
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 42
Ala Ala Ser Asn Leu Gln Gly
1 5
<210> 43
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 43
Gly Ala Ser Asn Leu Ala Asp
1 5
<210> 44
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 44
Gly Ala Ser Asn Arg Tyr Thr
1 5
<210> 45
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 45
Asp Ala Ser Asn Leu Glu Ser
1 5
<210> 46
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 46
Gly Ala Ser Thr Arg Glu Ser
1 5
<210> 47
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 47
Leu Gln Thr His Ala Tyr Pro Leu Thr
1 5
<210> 48
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 48
Gln Asn Val Leu Asn Thr Pro Leu Ser
1 5
<210> 49
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 49
Gln Gln Val Leu Asn Thr Pro Val Ser
1 5
<210> 50
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 50
Gln Asn Val Leu Ser Thr Pro Trp Thr
1 5
<210> 51
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 51
Gln Asn Val Leu Asn Thr Pro Tyr Thr
1 5
<210> 52
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 52
Gln Gln Val Leu Asn Thr Pro Leu Thr
1 5
<210> 53
<211> 1676
<212> БЕЛОК
<213> Homo sapiens
<400> 53
Met Gly Leu Leu Gly Ile Leu Cys Phe Leu Ile Phe Leu Gly Lys Thr
1 5 10 15
Trp Gly Gln Glu Gln Thr Tyr Val Ile Ser Ala Pro Lys Ile Phe Arg
20 25 30
Val Gly Ala Ser Glu Asn Ile Val Ile Gln Val Tyr Gly Tyr Thr Glu
35 40 45
Ala Phe Asp Ala Thr Ile Ser Ile Lys Ser Tyr Pro Asp Lys Lys Phe
50 55 60
Ser Tyr Ser Ser Gly His Val His Leu Ser Ser Glu Asn Lys Phe Gln
65 70 75 80
Asn Ser Ala Ile Leu Thr Ile Gln Pro Lys Gln Leu Pro Gly Gly Gln
85 90 95
Asn Pro Val Ser Tyr Val Tyr Leu Glu Val Val Ser Lys His Phe Ser
100 105 110
Lys Ser Lys Arg Met Pro Ile Thr Tyr Asp Asn Gly Phe Leu Phe Ile
115 120 125
His Thr Asp Lys Pro Val Tyr Thr Pro Asp Gln Ser Val Lys Val Arg
130 135 140
Val Tyr Ser Leu Asn Asp Asp Leu Lys Pro Ala Lys Arg Glu Thr Val
145 150 155 160
Leu Thr Phe Ile Asp Pro Glu Gly Ser Glu Val Asp Met Val Glu Glu
165 170 175
Ile Asp His Ile Gly Ile Ile Ser Phe Pro Asp Phe Lys Ile Pro Ser
180 185 190
Asn Pro Arg Tyr Gly Met Trp Thr Ile Lys Ala Lys Tyr Lys Glu Asp
195 200 205
Phe Ser Thr Thr Gly Thr Ala Tyr Phe Glu Val Lys Glu Tyr Val Leu
210 215 220
Pro His Phe Ser Val Ser Ile Glu Pro Glu Tyr Asn Phe Ile Gly Tyr
225 230 235 240
Lys Asn Phe Lys Asn Phe Glu Ile Thr Ile Lys Ala Arg Tyr Phe Tyr
245 250 255
Asn Lys Val Val Thr Glu Ala Asp Val Tyr Ile Thr Phe Gly Ile Arg
260 265 270
Glu Asp Leu Lys Asp Asp Gln Lys Glu Met Met Gln Thr Ala Met Gln
275 280 285
Asn Thr Met Leu Ile Asn Gly Ile Ala Gln Val Thr Phe Asp Ser Glu
290 295 300
Thr Ala Val Lys Glu Leu Ser Tyr Tyr Ser Leu Glu Asp Leu Asn Asn
305 310 315 320
Lys Tyr Leu Tyr Ile Ala Val Thr Val Ile Glu Ser Thr Gly Gly Phe
325 330 335
Ser Glu Glu Ala Glu Ile Pro Gly Ile Lys Tyr Val Leu Ser Pro Tyr
340 345 350
Lys Leu Asn Leu Val Ala Thr Pro Leu Phe Leu Lys Pro Gly Ile Pro
355 360 365
Tyr Pro Ile Lys Val Gln Val Lys Asp Ser Leu Asp Gln Leu Val Gly
370 375 380
Gly Val Pro Val Thr Leu Asn Ala Gln Thr Ile Asp Val Asn Gln Glu
385 390 395 400
Thr Ser Asp Leu Asp Pro Ser Lys Ser Val Thr Arg Val Asp Asp Gly
405 410 415
Val Ala Ser Phe Val Leu Asn Leu Pro Ser Gly Val Thr Val Leu Glu
420 425 430
Phe Asn Val Lys Thr Asp Ala Pro Asp Leu Pro Glu Glu Asn Gln Ala
435 440 445
Arg Glu Gly Tyr Arg Ala Ile Ala Tyr Ser Ser Leu Ser Gln Ser Tyr
450 455 460
Leu Tyr Ile Asp Trp Thr Asp Asn His Lys Ala Leu Leu Val Gly Glu
465 470 475 480
His Leu Asn Ile Ile Val Thr Pro Lys Ser Pro Tyr Ile Asp Lys Ile
485 490 495
Thr His Tyr Asn Tyr Leu Ile Leu Ser Lys Gly Lys Ile Ile His Phe
500 505 510
Gly Thr Arg Glu Lys Phe Ser Asp Ala Ser Tyr Gln Ser Ile Asn Ile
515 520 525
Pro Val Thr Gln Asn Met Val Pro Ser Ser Arg Leu Leu Val Tyr Tyr
530 535 540
Ile Val Thr Gly Glu Gln Thr Ala Glu Leu Val Ser Asp Ser Val Trp
545 550 555 560
Leu Asn Ile Glu Glu Lys Cys Gly Asn Gln Leu Gln Val His Leu Ser
565 570 575
Pro Asp Ala Asp Ala Tyr Ser Pro Gly Gln Thr Val Ser Leu Asn Met
580 585 590
Ala Thr Gly Met Asp Ser Trp Val Ala Leu Ala Ala Val Asp Ser Ala
595 600 605
Val Tyr Gly Val Gln Arg Gly Ala Lys Lys Pro Leu Glu Arg Val Phe
610 615 620
Gln Phe Leu Glu Lys Ser Asp Leu Gly Cys Gly Ala Gly Gly Gly Leu
625 630 635 640
Asn Asn Ala Asn Val Phe His Leu Ala Gly Leu Thr Phe Leu Thr Asn
645 650 655
Ala Asn Ala Asp Asp Ser Gln Glu Asn Asp Glu Pro Cys Lys Glu Ile
660 665 670
Leu Arg Pro Arg Arg Thr Leu Gln Lys Lys Ile Glu Glu Ile Ala Ala
675 680 685
Lys Tyr Lys His Ser Val Val Lys Lys Cys Cys Tyr Asp Gly Ala Cys
690 695 700
Val Asn Asn Asp Glu Thr Cys Glu Gln Arg Ala Ala Arg Ile Ser Leu
705 710 715 720
Gly Pro Arg Cys Ile Lys Ala Phe Thr Glu Cys Cys Val Val Ala Ser
725 730 735
Gln Leu Arg Ala Asn Ile Ser His Lys Asp Met Gln Leu Gly Arg Leu
740 745 750
His Met Lys Thr Leu Leu Pro Val Ser Lys Pro Glu Ile Arg Ser Tyr
755 760 765
Phe Pro Glu Ser Trp Leu Trp Glu Val His Leu Val Pro Arg Arg Lys
770 775 780
Gln Leu Gln Phe Ala Leu Pro Asp Ser Leu Thr Thr Trp Glu Ile Gln
785 790 795 800
Gly Val Gly Ile Ser Asn Thr Gly Ile Cys Val Ala Asp Thr Val Lys
805 810 815
Ala Lys Val Phe Lys Asp Val Phe Leu Glu Met Asn Ile Pro Tyr Ser
820 825 830
Val Val Arg Gly Glu Gln Ile Gln Leu Lys Gly Thr Val Tyr Asn Tyr
835 840 845
Arg Thr Ser Gly Met Gln Phe Cys Val Lys Met Ser Ala Val Glu Gly
850 855 860
Ile Cys Thr Ser Glu Ser Pro Val Ile Asp His Gln Gly Thr Lys Ser
865 870 875 880
Ser Lys Cys Val Arg Gln Lys Val Glu Gly Ser Ser Ser His Leu Val
885 890 895
Thr Phe Thr Val Leu Pro Leu Glu Ile Gly Leu His Asn Ile Asn Phe
900 905 910
Ser Leu Glu Thr Trp Phe Gly Lys Glu Ile Leu Val Lys Thr Leu Arg
915 920 925
Val Val Pro Glu Gly Val Lys Arg Glu Ser Tyr Ser Gly Val Thr Leu
930 935 940
Asp Pro Arg Gly Ile Tyr Gly Thr Ile Ser Arg Arg Lys Glu Phe Pro
945 950 955 960
Tyr Arg Ile Pro Leu Asp Leu Val Pro Lys Thr Glu Ile Lys Arg Ile
965 970 975
Leu Ser Val Lys Gly Leu Leu Val Gly Glu Ile Leu Ser Ala Val Leu
980 985 990
Ser Gln Glu Gly Ile Asn Ile Leu Thr His Leu Pro Lys Gly Ser Ala
995 1000 1005
Glu Ala Glu Leu Met Ser Val Val Pro Val Phe Tyr Val Phe His
1010 1015 1020
Tyr Leu Glu Thr Gly Asn His Trp Asn Ile Phe His Ser Asp Pro
1025 1030 1035
Leu Ile Glu Lys Gln Lys Leu Lys Lys Lys Leu Lys Glu Gly Met
1040 1045 1050
Leu Ser Ile Met Ser Tyr Arg Asn Ala Asp Tyr Ser Tyr Ser Val
1055 1060 1065
Trp Lys Gly Gly Ser Ala Ser Thr Trp Leu Thr Ala Phe Ala Leu
1070 1075 1080
Arg Val Leu Gly Gln Val Asn Lys Tyr Val Glu Gln Asn Gln Asn
1085 1090 1095
Ser Ile Cys Asn Ser Leu Leu Trp Leu Val Glu Asn Tyr Gln Leu
1100 1105 1110
Asp Asn Gly Ser Phe Lys Glu Asn Ser Gln Tyr Gln Pro Ile Lys
1115 1120 1125
Leu Gln Gly Thr Leu Pro Val Glu Ala Arg Glu Asn Ser Leu Tyr
1130 1135 1140
Leu Thr Ala Phe Thr Val Ile Gly Ile Arg Lys Ala Phe Asp Ile
1145 1150 1155
Cys Pro Leu Val Lys Ile Asp Thr Ala Leu Ile Lys Ala Asp Asn
1160 1165 1170
Phe Leu Leu Glu Asn Thr Leu Pro Ala Gln Ser Thr Phe Thr Leu
1175 1180 1185
Ala Ile Ser Ala Tyr Ala Leu Ser Leu Gly Asp Lys Thr His Pro
1190 1195 1200
Gln Phe Arg Ser Ile Val Ser Ala Leu Lys Arg Glu Ala Leu Val
1205 1210 1215
Lys Gly Asn Pro Pro Ile Tyr Arg Phe Trp Lys Asp Asn Leu Gln
1220 1225 1230
His Lys Asp Ser Ser Val Pro Asn Thr Gly Thr Ala Arg Met Val
1235 1240 1245
Glu Thr Thr Ala Tyr Ala Leu Leu Thr Ser Leu Asn Leu Lys Asp
1250 1255 1260
Ile Asn Tyr Val Asn Pro Val Ile Lys Trp Leu Ser Glu Glu Gln
1265 1270 1275
Arg Tyr Gly Gly Gly Phe Tyr Ser Thr Gln Asp Thr Ile Asn Ala
1280 1285 1290
Ile Glu Gly Leu Thr Glu Tyr Ser Leu Leu Val Lys Gln Leu Arg
1295 1300 1305
Leu Ser Met Asp Ile Asp Val Ser Tyr Lys His Lys Gly Ala Leu
1310 1315 1320
His Asn Tyr Lys Met Thr Asp Lys Asn Phe Leu Gly Arg Pro Val
1325 1330 1335
Glu Val Leu Leu Asn Asp Asp Leu Ile Val Ser Thr Gly Phe Gly
1340 1345 1350
Ser Gly Leu Ala Thr Val His Val Thr Thr Val Val His Lys Thr
1355 1360 1365
Ser Thr Ser Glu Glu Val Cys Ser Phe Tyr Leu Lys Ile Asp Thr
1370 1375 1380
Gln Asp Ile Glu Ala Ser His Tyr Arg Gly Tyr Gly Asn Ser Asp
1385 1390 1395
Tyr Lys Arg Ile Val Ala Cys Ala Ser Tyr Lys Pro Ser Arg Glu
1400 1405 1410
Glu Ser Ser Ser Gly Ser Ser His Ala Val Met Asp Ile Ser Leu
1415 1420 1425
Pro Thr Gly Ile Ser Ala Asn Glu Glu Asp Leu Lys Ala Leu Val
1430 1435 1440
Glu Gly Val Asp Gln Leu Phe Thr Asp Tyr Gln Ile Lys Asp Gly
1445 1450 1455
His Val Ile Leu Gln Leu Asn Ser Ile Pro Ser Ser Asp Phe Leu
1460 1465 1470
Cys Val Arg Phe Arg Ile Phe Glu Leu Phe Glu Val Gly Phe Leu
1475 1480 1485
Ser Pro Ala Thr Phe Thr Val Tyr Glu Tyr His Arg Pro Asp Lys
1490 1495 1500
Gln Cys Thr Met Phe Tyr Ser Thr Ser Asn Ile Lys Ile Gln Lys
1505 1510 1515
Val Cys Glu Gly Ala Ala Cys Lys Cys Val Glu Ala Asp Cys Gly
1520 1525 1530
Gln Met Gln Glu Glu Leu Asp Leu Thr Ile Ser Ala Glu Thr Arg
1535 1540 1545
Lys Gln Thr Ala Cys Lys Pro Glu Ile Ala Tyr Ala Tyr Lys Val
1550 1555 1560
Ser Ile Thr Ser Ile Thr Val Glu Asn Val Phe Val Lys Tyr Lys
1565 1570 1575
Ala Thr Leu Leu Asp Ile Tyr Lys Thr Gly Glu Ala Val Ala Glu
1580 1585 1590
Lys Asp Ser Glu Ile Thr Phe Ile Lys Lys Val Thr Cys Thr Asn
1595 1600 1605
Ala Glu Leu Val Lys Gly Arg Gln Tyr Leu Ile Met Gly Lys Glu
1610 1615 1620
Ala Leu Gln Ile Lys Tyr Asn Phe Ser Phe Arg Tyr Ile Tyr Pro
1625 1630 1635
Leu Asp Ser Leu Thr Trp Ile Glu Tyr Trp Pro Arg Asp Thr Thr
1640 1645 1650
Cys Ser Ser Cys Gln Ala Phe Leu Ala Asn Leu Asp Glu Phe Ala
1655 1660 1665
Glu Asp Ile Phe Leu Asn Gly Cys
1670 1675
<210> 54
<211> 5
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 54
Asn Tyr Trp Met Gln
1 5
<210> 55
<211> 5
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 55
Asp Phe Tyr Met Gln
1 5
<210> 56
<211> 5
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 56
Asn Tyr Trp Ile Gln
1 5
<210> 57
<211> 5
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 57
Ser Tyr Trp Ile Gln
1 5
<210> 58
<211> 5
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 58
Gly Asn Tyr Met His
1 5
<210> 59
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 59
Glu Ile Leu Pro Gly Thr Gly Ser Thr Glu Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 60
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 60
Glu Ile Leu Pro Gly Thr Gly His Thr Glu Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 61
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 61
Glu Ile Leu Ala Gly Ser Gly Ser Thr Glu Tyr Ser Gln Lys Phe Arg
1 5 10 15
Gly
<210> 62
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 62
Glu Val Leu Pro Gly Ser Gly Ser Thr Glu Tyr Ser Gln Lys Phe Arg
1 5 10 15
Gly
<210> 63
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 63
Glu Ile Leu Pro Gly Asp Gly Ser Thr Glu Tyr Ser Gln Lys Phe Arg
1 5 10 15
Gly
<210> 64
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 64
Glu Ile Leu Pro Thr Asn Gly Ser Thr Glu Tyr Ser Gln Lys Phe Arg
1 5 10 15
Gly
<210> 65
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 65
Trp Ile Asn Pro Lys Ser Gly Asp Thr Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 66
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 66
Tyr Phe Phe Gly Ser Thr Pro Asn Trp Tyr Phe Asp Val
1 5 10
<210> 67
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 67
Tyr Pro Phe Gly Ser Ser Pro Asn Trp Glu Phe Asp Tyr
1 5 10
<210> 68
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 68
Tyr Tyr Phe Gly Ser Ser Pro Asn Trp Tyr Phe Asp Val
1 5 10
<210> 69
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 69
Tyr Phe Phe Gly Ser Ser Pro Asn Trp Ala Met Asp Tyr
1 5 10
<210> 70
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 70
Gly Trp Trp Gly Met Asp Val
1 5
<210> 71
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 71
Gly Ala Thr Glu Asn Ile Tyr Gly Ala Leu Asn
1 5 10
<210> 72
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 72
Arg Ala Ser Glu Gly Ile Tyr Gly Ala Leu Ala
1 5 10
<210> 73
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 73
Arg Ala Ser Glu Ser Ile Tyr Gly Ala Leu Asn
1 5 10
<210> 74
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 74
Gly Ala Ser Glu Asn Ile Tyr Gly Ala Leu His
1 5 10
<210> 75
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 75
Arg Ala Ser Gln Asn Ile Asn Asn Tyr Leu His
1 5 10
<210> 76
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 76
Gly Ala Ser Asn Leu Ala Asp
1 5
<210> 77
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 77
Gly Ala Ser Asn Arg Tyr Thr
1 5
<210> 78
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 78
Asp Ala Ser Asn Leu Glu Ser
1 5
<210> 79
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 79
Gly Ala Ser Thr Arg Glu Ser
1 5
<210> 80
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности: Синтетический
пептид"
<400> 80
Ala Ala Ser Asn Leu Gln Gly
1 5
<210> 81
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 81
Gln Asn Val Leu Asn Thr Pro Leu Ser
1 5
<210> 82
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 82
Gln Gln Val Leu Asn Thr Pro Val Ser
1 5
<210> 83
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 83
Gln Gln Val Leu Asn Thr Pro Leu Thr
1 5
<210> 84
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 84
Gln Asn Val Leu Ser Thr Pro Trp Thr
1 5
<210> 85
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 85
Gln Asn Val Leu Asn Thr Pro Tyr Thr
1 5
<210> 86
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<400> 86
Leu Gln Thr His Ala Tyr Pro Leu Thr
1 5
<210> 87
<211> 8
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Phe" или "His"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Thr"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Thr"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Ser" или "Asp" или "Gly"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /заменить="Asn" или " "
<220>
<221> SITE
<222> (1)..(8)
<223> /примечание="ВАРИАНТ остатки предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 87
Gly Tyr Ile Phe Ser Asn Phe Tyr
1 5
<210> 88
<211> 6
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Asn"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Pro"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Thr" или "Lys"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Asp" или "Asn" или "Thr" или "Ser"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="His" или "Asp"
<220>
<221> SITE
<222> (1)..(6)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 88
Leu Ala Gly Ser Gly Ser
1 5
<210> 89
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Gly"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Tyr" или "Ser" или "Phe" или "Trp"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Ser" или "Trp"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Pro"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Asn" или "Met"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Trp" или "Thr" или "Asp"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /заменить="Ala" или "Val"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /заменить="Met" или " "
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /заменить="Asp" или " "
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /заменить="Tyr" или "Ala" или " "
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /заменить="Met" или " "
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /заменить=" "
<220>
<221> ВАРИАНТ
<222> (13)..(13)
<223> /заменить="Val" или " "
<220>
<221> SITE
<222> (1)..(13)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 89
Tyr Pro Phe Gly Ser Ser Pro Asn Trp Glu Phe Asp Tyr
1 5 10
<210> 90
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Gly"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Thr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Glu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Ser" или "Gly"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /заменить="Tyr"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /заменить="Gly"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /заменить="Ala"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /заменить="Asn" или "Ala"
<220>
<221> SITE
<222> (1)..(11)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 90
Arg Ala Ser Gln Asn Ile Asn Asn Tyr Leu His
1 5 10
<210> 91
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Gly" или "Asp"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Thr"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Arg"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Ala" или "Tyr" или "Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /заменить="Asp" или "Thr" или "Ser"
<220>
<221> SITE
<222> (1)..(7)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 91
Ala Ala Ser Asn Leu Gln Gly
1 5
<210> 92
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Gln"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Asn"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Val"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Leu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Asn" или "Ser"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Thr"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /заменить="Val" или "Trp" или "Tyr"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /заменить="Ser"
<220>
<221> SITE
<222> (1)..(9)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 92
Leu Gln Thr His Ala Tyr Pro Leu Thr
1 5
<210> 93
<211> 1685
<212> БЕЛОК
<213> Mus musculus
<400> 93
Met Pro Leu Pro Ala Met Gly Leu Trp Gly Ile Leu Cys Leu Leu Ile
1 5 10 15
Phe Leu Asp Lys Thr Trp Gly Gln Glu Gln Thr Tyr Val Ile Ser Ala
20 25 30
Pro Lys Ile Leu Arg Val Gly Ser Ser Glu Asn Val Val Ile Gln Val
35 40 45
His Gly Tyr Thr Glu Ala Phe Asp Ala Thr Leu Ser Leu Lys Ser Tyr
50 55 60
Pro Asp Lys Lys Val Thr Phe Ser Ser Gly Tyr Val Asn Leu Ser Pro
65 70 75 80
Glu Asn Lys Phe Gln Asn Ala Ala Leu Leu Thr Leu Gln Pro Asn Gln
85 90 95
Val Pro Arg Glu Glu Ser Pro Val Ser His Val Tyr Leu Glu Val Val
100 105 110
Ser Lys His Phe Ser Lys Ser Lys Lys Ile Pro Ile Thr Tyr Asn Asn
115 120 125
Gly Ile Leu Phe Ile His Thr Asp Lys Pro Val Tyr Thr Pro Asp Gln
130 135 140
Ser Val Lys Ile Arg Val Tyr Ser Leu Gly Asp Asp Leu Lys Pro Ala
145 150 155 160
Lys Arg Glu Thr Val Leu Thr Phe Ile Asp Pro Glu Gly Ser Glu Val
165 170 175
Asp Ile Val Glu Glu Asn Asp Tyr Thr Gly Ile Ile Ser Phe Pro Asp
180 185 190
Phe Lys Ile Pro Ser Asn Pro Lys Tyr Gly Val Trp Thr Ile Lys Ala
195 200 205
Asn Tyr Lys Lys Asp Phe Thr Thr Thr Gly Thr Ala Tyr Phe Glu Ile
210 215 220
Lys Glu Tyr Val Leu Pro Arg Phe Ser Val Ser Ile Glu Leu Glu Arg
225 230 235 240
Thr Phe Ile Gly Tyr Lys Asn Phe Lys Asn Phe Glu Ile Thr Val Lys
245 250 255
Ala Arg Tyr Phe Tyr Asn Lys Val Val Pro Asp Ala Glu Val Tyr Ala
260 265 270
Phe Phe Gly Leu Arg Glu Asp Ile Lys Asp Glu Glu Lys Gln Met Met
275 280 285
His Lys Ala Thr Gln Ala Ala Lys Leu Val Asp Gly Val Ala Gln Ile
290 295 300
Ser Phe Asp Ser Glu Thr Ala Val Lys Glu Leu Ser Tyr Asn Ser Leu
305 310 315 320
Glu Asp Leu Asn Asn Lys Tyr Leu Tyr Ile Ala Val Thr Val Thr Glu
325 330 335
Ser Ser Gly Gly Phe Ser Glu Glu Ala Glu Ile Pro Gly Val Lys Tyr
340 345 350
Val Leu Ser Pro Tyr Thr Leu Asn Leu Val Ala Thr Pro Leu Phe Val
355 360 365
Lys Pro Gly Ile Pro Phe Ser Ile Lys Ala Gln Val Lys Asp Ser Leu
370 375 380
Glu Gln Ala Val Gly Gly Val Pro Val Thr Leu Met Ala Gln Thr Val
385 390 395 400
Asp Val Asn Gln Glu Thr Ser Asp Leu Glu Thr Lys Arg Ser Ile Thr
405 410 415
His Asp Thr Asp Gly Val Ala Val Phe Val Leu Asn Leu Pro Ser Asn
420 425 430
Val Thr Val Leu Lys Phe Glu Ile Arg Thr Asp Asp Pro Glu Leu Pro
435 440 445
Glu Glu Asn Gln Ala Ser Lys Glu Tyr Glu Ala Val Ala Tyr Ser Ser
450 455 460
Leu Ser Gln Ser Tyr Ile Tyr Ile Ala Trp Thr Glu Asn Tyr Lys Pro
465 470 475 480
Met Leu Val Gly Glu Tyr Leu Asn Ile Met Val Thr Pro Lys Ser Pro
485 490 495
Tyr Ile Asp Lys Ile Thr His Tyr Asn Tyr Leu Ile Leu Ser Lys Gly
500 505 510
Lys Ile Val Gln Tyr Gly Thr Arg Glu Lys Leu Phe Ser Ser Thr Tyr
515 520 525
Gln Asn Ile Asn Ile Pro Val Thr Gln Asn Met Val Pro Ser Ala Arg
530 535 540
Leu Leu Val Tyr Tyr Ile Val Thr Gly Glu Gln Thr Ala Glu Leu Val
545 550 555 560
Ala Asp Ala Val Trp Ile Asn Ile Glu Glu Lys Cys Gly Asn Gln Leu
565 570 575
Gln Val His Leu Ser Pro Asp Glu Tyr Val Tyr Ser Pro Gly Gln Thr
580 585 590
Val Ser Leu Asp Met Val Thr Glu Ala Asp Ser Trp Val Ala Leu Ser
595 600 605
Ala Val Asp Arg Ala Val Tyr Lys Val Gln Gly Asn Ala Lys Arg Ala
610 615 620
Met Gln Arg Val Phe Gln Ala Leu Asp Glu Lys Ser Asp Leu Gly Cys
625 630 635 640
Gly Ala Gly Gly Gly His Asp Asn Ala Asp Val Phe His Leu Ala Gly
645 650 655
Leu Thr Phe Leu Thr Asn Ala Asn Ala Asp Asp Ser His Tyr Arg Asp
660 665 670
Asp Ser Cys Lys Glu Ile Leu Arg Ser Lys Arg Asn Leu His Leu Leu
675 680 685
Arg Gln Lys Ile Glu Glu Gln Ala Ala Lys Tyr Lys His Ser Val Pro
690 695 700
Lys Lys Cys Cys Tyr Asp Gly Ala Arg Val Asn Phe Tyr Glu Thr Cys
705 710 715 720
Glu Glu Arg Val Ala Arg Val Thr Ile Gly Pro Leu Cys Ile Arg Ala
725 730 735
Phe Asn Glu Cys Cys Thr Ile Ala Asn Lys Ile Arg Lys Glu Ser Pro
740 745 750
His Lys Pro Val Gln Leu Gly Arg Ile His Ile Lys Thr Leu Leu Pro
755 760 765
Val Met Lys Ala Asp Ile Arg Ser Tyr Phe Pro Glu Ser Trp Leu Trp
770 775 780
Glu Ile His Arg Val Pro Lys Arg Lys Gln Leu Gln Val Thr Leu Pro
785 790 795 800
Asp Ser Leu Thr Thr Trp Glu Ile Gln Gly Ile Gly Ile Ser Asp Asn
805 810 815
Gly Ile Cys Val Ala Asp Thr Leu Lys Ala Lys Val Phe Lys Glu Val
820 825 830
Phe Leu Glu Met Asn Ile Pro Tyr Ser Val Val Arg Gly Glu Gln Ile
835 840 845
Gln Leu Lys Gly Thr Val Tyr Asn Tyr Met Thr Ser Gly Thr Lys Phe
850 855 860
Cys Val Lys Met Ser Ala Val Glu Gly Ile Cys Thr Ser Gly Ser Ser
865 870 875 880
Ala Ala Ser Leu His Thr Ser Arg Pro Ser Arg Cys Val Phe Gln Arg
885 890 895
Ile Glu Gly Ser Ser Ser His Leu Val Thr Phe Thr Leu Leu Pro Leu
900 905 910
Glu Ile Gly Leu His Ser Ile Asn Phe Ser Leu Glu Thr Ser Phe Gly
915 920 925
Lys Asp Ile Leu Val Lys Thr Leu Arg Val Val Pro Glu Gly Val Lys
930 935 940
Arg Glu Ser Tyr Ala Gly Val Ile Leu Asp Pro Lys Gly Ile Arg Gly
945 950 955 960
Ile Val Asn Arg Arg Lys Glu Phe Pro Tyr Arg Ile Pro Leu Asp Leu
965 970 975
Val Pro Lys Thr Lys Val Glu Arg Ile Leu Ser Val Lys Gly Leu Leu
980 985 990
Val Gly Glu Phe Leu Ser Thr Val Leu Ser Lys Glu Gly Ile Asn Ile
995 1000 1005
Leu Thr His Leu Pro Lys Gly Ser Ala Glu Ala Glu Leu Met Ser
1010 1015 1020
Ile Ala Pro Val Phe Tyr Val Phe His Tyr Leu Glu Ala Gly Asn
1025 1030 1035
His Trp Asn Ile Phe Tyr Pro Asp Thr Leu Ser Lys Arg Gln Ser
1040 1045 1050
Leu Glu Lys Lys Ile Lys Gln Gly Val Val Ser Val Met Ser Tyr
1055 1060 1065
Arg Asn Ala Asp Tyr Ser Tyr Ser Met Trp Lys Gly Ala Ser Ala
1070 1075 1080
Ser Thr Trp Leu Thr Ala Phe Ala Leu Arg Val Leu Gly Gln Val
1085 1090 1095
Ala Lys Tyr Val Lys Gln Asp Glu Asn Ser Ile Cys Asn Ser Leu
1100 1105 1110
Leu Trp Leu Val Glu Lys Cys Gln Leu Glu Asn Gly Ser Phe Lys
1115 1120 1125
Glu Asn Ser Gln Tyr Leu Pro Ile Lys Leu Gln Gly Thr Leu Pro
1130 1135 1140
Ala Glu Ala Gln Glu Lys Thr Leu Tyr Leu Thr Ala Phe Ser Val
1145 1150 1155
Ile Gly Ile Arg Lys Ala Val Asp Ile Cys Pro Thr Met Lys Ile
1160 1165 1170
His Thr Ala Leu Asp Lys Ala Asp Ser Phe Leu Leu Glu Asn Thr
1175 1180 1185
Leu Pro Ser Lys Ser Thr Phe Thr Leu Ala Ile Val Ala Tyr Ala
1190 1195 1200
Leu Ser Leu Gly Asp Arg Thr His Pro Arg Phe Arg Leu Ile Val
1205 1210 1215
Ser Ala Leu Arg Lys Glu Ala Phe Val Lys Gly Asp Pro Pro Ile
1220 1225 1230
Tyr Arg Tyr Trp Arg Asp Thr Leu Lys Arg Pro Asp Ser Ser Val
1235 1240 1245
Pro Ser Ser Gly Thr Ala Gly Met Val Glu Thr Thr Ala Tyr Ala
1250 1255 1260
Leu Leu Ala Ser Leu Lys Leu Lys Asp Met Asn Tyr Ala Asn Pro
1265 1270 1275
Ile Ile Lys Trp Leu Ser Glu Glu Gln Arg Tyr Gly Gly Gly Phe
1280 1285 1290
Tyr Ser Thr Gln Asp Thr Ile Asn Ala Ile Glu Gly Leu Thr Glu
1295 1300 1305
Tyr Ser Leu Leu Leu Lys Gln Ile His Leu Asp Met Asp Ile Asn
1310 1315 1320
Val Ala Tyr Lys His Glu Gly Asp Phe His Lys Tyr Lys Val Thr
1325 1330 1335
Glu Lys His Phe Leu Gly Arg Pro Val Glu Val Ser Leu Asn Asp
1340 1345 1350
Asp Leu Val Val Ser Thr Gly Tyr Ser Ser Gly Leu Ala Thr Val
1355 1360 1365
Tyr Val Lys Thr Val Val His Lys Ile Ser Val Ser Glu Glu Phe
1370 1375 1380
Cys Ser Phe Tyr Leu Lys Ile Asp Thr Gln Asp Ile Glu Ala Ser
1385 1390 1395
Ser His Phe Arg Leu Ser Asp Ser Gly Phe Lys Arg Ile Ile Ala
1400 1405 1410
Cys Ala Ser Tyr Lys Pro Ser Lys Glu Glu Ser Thr Ser Gly Ser
1415 1420 1425
Ser His Ala Val Met Asp Ile Ser Leu Pro Thr Gly Ile Gly Ala
1430 1435 1440
Asn Glu Glu Asp Leu Arg Ala Leu Val Glu Gly Val Asp Gln Leu
1445 1450 1455
Leu Thr Asp Tyr Gln Ile Lys Asp Gly His Val Ile Leu Gln Leu
1460 1465 1470
Asn Ser Ile Pro Ser Arg Asp Phe Leu Cys Val Arg Phe Arg Ile
1475 1480 1485
Phe Glu Leu Phe Gln Val Gly Phe Leu Asn Pro Ala Thr Phe Thr
1490 1495 1500
Val Tyr Glu Tyr His Arg Pro Asp Lys Gln Cys Thr Met Ile Tyr
1505 1510 1515
Ser Ile Ser Asp Thr Arg Leu Gln Lys Val Cys Glu Gly Ala Ala
1520 1525 1530
Cys Thr Cys Val Glu Ala Asp Cys Ala Gln Leu Gln Ala Glu Val
1535 1540 1545
Asp Leu Ala Ile Ser Ala Asp Ser Arg Lys Glu Lys Ala Cys Lys
1550 1555 1560
Pro Glu Thr Ala Tyr Ala Tyr Lys Val Arg Ile Thr Ser Ala Thr
1565 1570 1575
Glu Glu Asn Val Phe Val Lys Tyr Thr Ala Thr Leu Leu Val Thr
1580 1585 1590
Tyr Lys Thr Gly Glu Ala Ala Asp Glu Asn Ser Glu Val Thr Phe
1595 1600 1605
Ile Lys Lys Met Ser Cys Thr Asn Ala Asn Leu Val Lys Gly Lys
1610 1615 1620
Gln Tyr Leu Ile Met Gly Lys Glu Val Leu Gln Ile Lys His Asn
1625 1630 1635
Phe Ser Phe Lys Tyr Ile Tyr Pro Leu Asp Ser Ser Thr Trp Ile
1640 1645 1650
Glu Tyr Trp Pro Thr Asp Thr Thr Cys Pro Ser Cys Gln Ala Phe
1655 1660 1665
Val Glu Asn Leu Asn Asn Phe Ala Glu Asp Leu Phe Leu Asn Ser
1670 1675 1680
Cys Glu
1685
<210> 94
<211> 5
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Asp" или "Ser" или "Gly"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Phe" или "Asn"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Tyr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Ile"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="His"
<220>
<221> SITE
<222> (1)..(5)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 94
Asn Tyr Trp Met Gln
1 5
<210> 95
<211> 17
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Trp"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Val"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Asn"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Thr" или "Lys"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Ser" или "Asp" или "Asn"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /заменить="His" или "Asp"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /заменить="Asn"
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /заменить="Ser"
<220>
<221> ВАРИАНТ
<222> (16)..(16)
<223> /заменить="Arg"
<220>
<221> SITE
<222> (1)..(17)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 95
Glu Ile Leu Pro Gly Thr Gly Ser Thr Glu Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 96
<211> 13
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Gly"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Pro" или "Tyr" или "Trp"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить=" "
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить=" "
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить=" "
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Ser" или " "
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /заменить=" "
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /заменить=" "
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /заменить="Glu" или "Ala" или "Gly"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /заменить="Met"
<220>
<221> ВАРИАНТ
<222> (13)..(13)
<223> /заменить="Tyr"
<220>
<221> SITE
<222> (1)..(13)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 96
Tyr Phe Phe Gly Ser Thr Pro Asn Trp Tyr Phe Asp Val
1 5 10
<210> 97
<211> 11
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Arg"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Ser"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Gln"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Gly" или "Ser"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /заменить="Asn"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /заменить="Asn"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /заменить="Tyr"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /заменить="Ala" или "His"
<220>
<221> SITE
<222> (1)..(11)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 97
Gly Ala Thr Glu Asn Ile Tyr Gly Ala Leu Asn
1 5 10
<210> 98
<211> 7
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Asp" или "Ala"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="Thr"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Arg"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Tyr" или "Glu" или "Gln"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /заменить="Thr" или "Ser" или "Gly"
<220>
<221> SITE
<222> (1)..(7)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 98
Gly Ala Ser Asn Leu Ala Asp
1 5
<210> 99
<211> 9
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /заменить="Leu"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /заменить="Gln"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /заменить="Thr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /заменить="His"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /заменить="Ser" или "Ala"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /заменить="Tyr"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /заменить="Val" или "Trp" или "Tyr"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /заменить="Thr"
<220>
<221> SITE
<222> (1)..(9)
<223> /примечание="ВАРИАНТ остатки, предоставленные в последовательности
не имеют преимощества в отношении таковых в аннотациях к позициям
ВАРИАНТа"
<220>
<221> источник
<223> /примечание="Для подробного описания замещений и предпочтительных
вариантов смотри поданное описание изобретения"
<400> 99
Gln Asn Val Leu Asn Thr Pro Leu Ser
1 5
<210> 100
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 100
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tatttttacc aactattgga tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcag caccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 101
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 101
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc tggcggatgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagaac gtgctgaaca ccccgctgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 102
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 102
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tatttttacc gatttttata tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcag caccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 103
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 103
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc tggcggatgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagaac gtgctgaaca ccccgctgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 104
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 104
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcca tatttttacc aactattgga tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcca taccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 105
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 105
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc tggcggatgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagaac gtgctgaaca ccccgctgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 106
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 106
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcca tatttttacc gatttttata tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcca taccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 107
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 107
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc tggcggatgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagaac gtgctgaaca ccccgctgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 108
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 108
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tatttttacc aactattgga tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcag caccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 109
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 109
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc gctataccgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagcag gtgctgaaca ccccggtgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 110
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 110
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tatttttacc gatttttata tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcag caccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 111
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 111
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc gctataccgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagcag gtgctgaaca ccccggtgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 112
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 112
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcca tatttttacc aactattgga tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcca taccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 113
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 113
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc gctataccgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagcag gtgctgaaca ccccggtgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 114
<211> 366
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 114
caggtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcca tatttttacc gatttttata tgcagtgggt gcgccaggcg 120
ccgggccagg gcctggaatg gatgggcgaa attctgccgg gcaccggcca taccgaatat 180
gcgcagaaat ttcagggccg cgtgaccatg acccgcgata ccagcattag caccgtgtat 240
atggaagtgc gccgcctgcg cagcgatgat accgcggtgt attattgcgc gcgctatttt 300
tttggcagca ccccgaactg gtattttgat gtgtggggcc agggcaccct ggtgaccgtg 360
agcagc 366
<210> 115
<211> 321
<212> DNA
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полинуклеотид"
<400> 115
gaaattgtga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcg gcgcgaccga aaacatttat ggcgcgctga actggtatca gcatgaaccg 120
ggcaaagcgc cgaaactgct gatttatggc gcgagcaacc gctataccgg cgtgaccagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcac cctgcagccg 240
gaagattttg cgacctatta ttgccagcag gtgctgaaca ccccggtgag ctttggcggc 300
ggcaccaaag tggatattaa a 321
<210> 116
<211> 326
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 116
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Leu Gly Lys
325
<210> 117
<211> 326
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 117
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Tyr Ile Thr Arg Glu Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Leu Gly Lys
325
<210> 118
<211> 326
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 118
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Leu Gly Lys
325
<210> 119
<211> 330
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 119
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 120
<211> 107
<212> БЕЛОК
<213> Искусственная Последовательность
<220>
<221> источник
<223> /примечание="Описание Искусственной Последовательности:
Синтетический полипептид"
<400> 120
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОЛЕКУЛЫ АНТИТЕЛ ПРОТИВ APRIL И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2793755C2 |
| Композиции и способы активации интегринов | 2020 |
|
RU2836262C1 |
| АНТИТЕЛА К РЕЦЕПТОРУ-1 НАТРИЙУРЕТИЧЕСКОГО ПЕПТИДА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2827871C2 |
| АНТИТЕЛА К ICOS | 2016 |
|
RU2742241C2 |
| АНТИТЕЛА К ENTPD2, ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ И СПОСОБЫ ПРИМЕНЕНИЯ АНТИТЕЛ И ВИДОВ КОМБИНИРОВАННОЙ ТЕРАПИИ | 2019 |
|
RU2790991C2 |
| СООТВЕТСТВУЮЩАЯ МИШЕНЬ ДЛЯ ЛЕЧЕНИЯ ФИБРОЗИРУЮЩИХ ЗАБОЛЕВАНИЙ И ЕЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2830698C1 |
| АНТИТЕЛА К TIGIT И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2827445C2 |
| АНТИТЕЛО, СПОСОБНОЕ СВЯЗЫВАТЬСЯ С ТИМИЧЕСКИМ СТРОМАЛЬНЫМ ЛИМФОПОЭТИНОМ, И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2825304C2 |
| АНТИТЕЛА-МИМЕТИКИ FGF21 И ПУТИ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2774368C2 |
| АНТИТЕЛО К PD-L1, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2778085C2 |

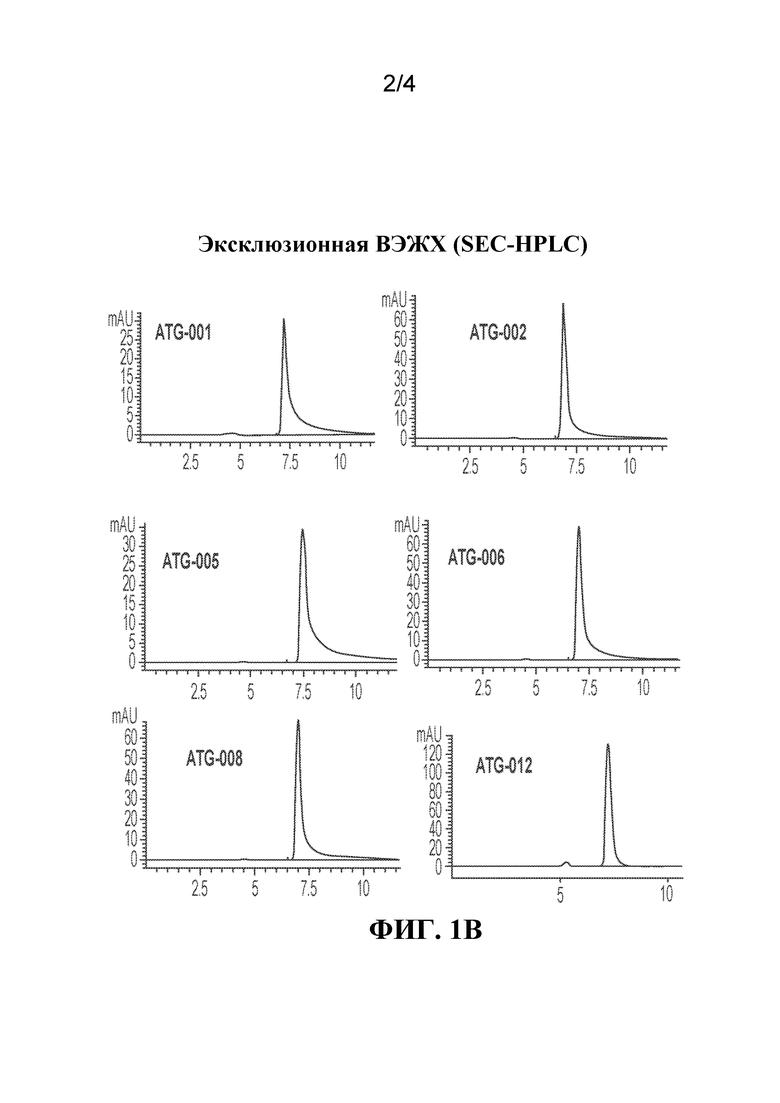
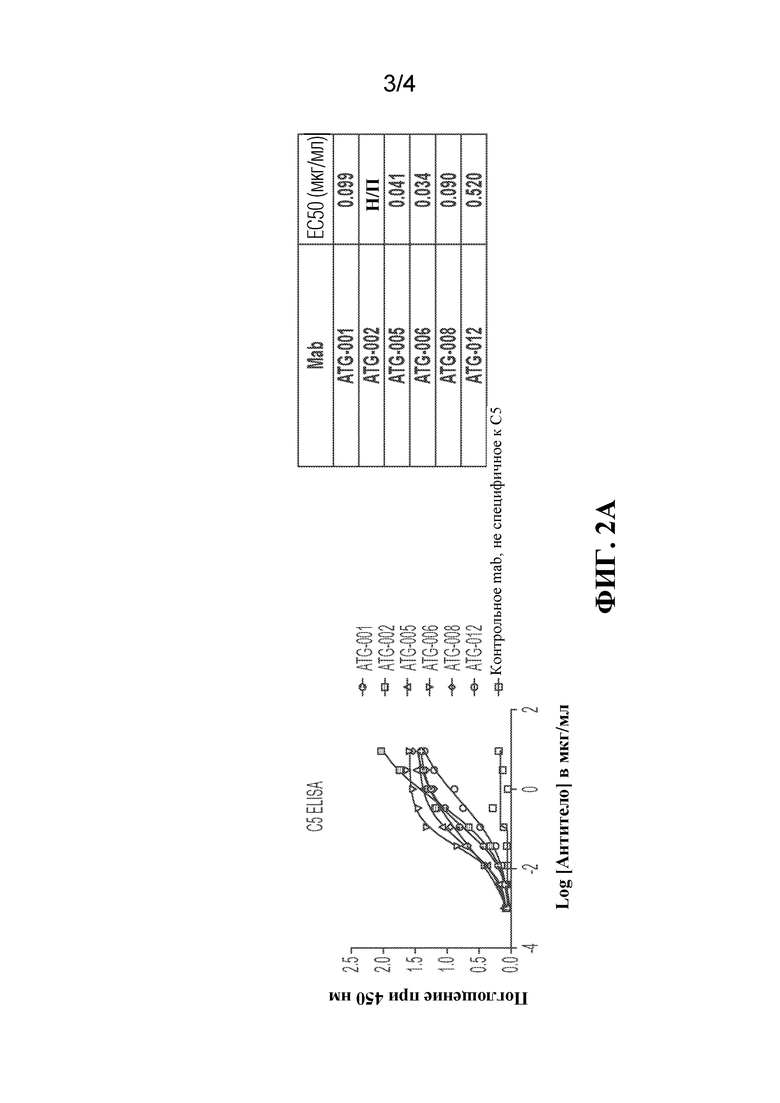
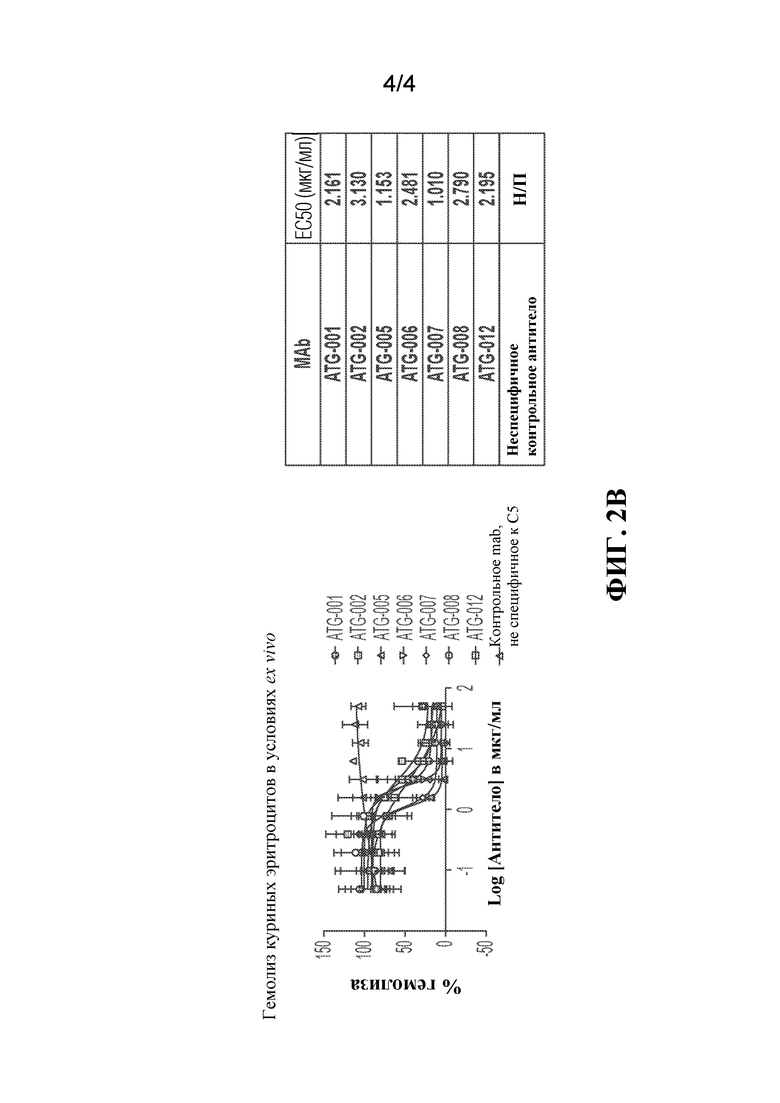
Изобретение относится к области биотехнологии. Раскрыты антитела или их антигенсвязывающие фрагменты, которые специфически связываются с C5, а также фармацевтические композиции, включающие указанные антитела или их фрагменты. Кроме того, раскрыты нуклеиновые кислоты, кодирующие указанные антитела или их фрагменты, векторы экспрессии и клетки-хозяева, содержащие указанные нуклеиновые кислоты, способ получения антител. Предложенные антитела можно применять для лечения, предотвращения и/или диагностики расстройств, таких как комплемент-опосредованные расстройства. 11 н. и 37 з.п. ф-лы, 4 ил., 6 табл., 1 пр.
1. Выделенное антитело или его антигенсвязывающий фрагмент, способные связывается с компонентом 5 комплемента (C5), содержащие:
(а) вариабельную область тяжелой цепи (VH), содержащую
HCDR1 с аминокислотной последовательностью SEQ ID NO:22,
HCDR2 с аминокислотной последовательностью SEQ ID NO:29 и
HCDR3 с аминокислотной последовательностью SEQ ID NO:35; и
(b) вариабельную область легкой цепи (VH), содержащую
LCDR1 с аминокислотной последовательностью SEQ ID NO:38,
LCDR2 с аминокислотной последовательностью SEQ ID NO:44 и
LCDR3 с аминокислотной последовательностью SEQ ID NO:49.
2. Выделенное антитело или его антигенсвязывающий фрагмент, способные связывается с компонентом 5 комплемента (C5), содержащие:
(а) VH, содержащую
HCDR1 с аминокислотной последовательностью SEQ ID NO:55,
HCDR2 с аминокислотной последовательностью SEQ ID NO:60 и
HCDR3 с аминокислотной последовательностью SEQ ID NO:66; и
(b) VL, содержащую
LCDR1 с аминокислотной последовательностью SEQ ID NO:71,
LCDR2 с аминокислотной последовательностью SEQ ID NO:77 и
LCDR3 с аминокислотной последовательностью SEQ ID NO:82.
3. Антитело или его антигенсвязывающий фрагмент по любому из пп.1 или 2, которые содержат VH, содержащую аминокислотную последовательность, которая по меньшей мере на 85%, 90% или 95% идентична SEQ ID NO:4.
4. Антитело или его антигенсвязывающий фрагмент по п.3, которые содержат VH, содержащую аминокислотную последовательность SEQ ID NO:4.
5. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат VL, содержащую аминокислотную последовательность, которая по меньшей мере на 85%, 90% или 95% идентична SEQ ID NO:11.
6. Антитело или его антигенсвязывающий фрагмент по п.5, которые содержат VL, содержащую аминокислотную последовательность SEQ ID NO:11.
7. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат
VH, содержащую аминокислотную последовательность, которая по меньшей мере на 85%, 90% или 95% идентична SEQ ID NO:4, и
VL, содержащую аминокислотную последовательность, которая по меньшей мере на 85%, 90% или 95% идентична SEQ ID NO:11.
8. Антитело или его антигенсвязывающий фрагмент по п.7, которые содержат
VH, содержащую аминокислотную последовательность SEQ ID NO:4, и
VL, содержащую аминокислотную последовательность SEQ ID NO:11.
9. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат антигенсвязывающий фрагмент.
10. Антитело или его антигенсвязывающий фрагмент по п.9, где антигенсвязывающий фрагмент содержит Fab, F(ab')2, Fv или scFv.
11. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат константную область тяжелой цепи, выбранную из константных областей тяжелой цепи IgG1, IgG2, IgG3 или IgG4, или химерные вариант из двух или более изотипов (например, IgG2/4).
12. Антитело или его антигенсвязывающий фрагмент по п.11, где константная область тяжелой цепи содержит одну или более модификаций аминокислот в шарнирном участке, CH2 или CH3 участке, как показано в IgG2/4-LS или IgG2/4-YTE.
13. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат константную область легкой цепи, выбранную из константных областей легкой цепи каппа или лямбда.
14. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат константную область тяжелой цепи, выбранную из константных областей тяжелой цепи IgG1, IgG2, IgG3, IgG4 или химерный вариант из двух или более изотипов (например, IgG2 и IgG4), и константную область легкой цепи, выбранную из константных областей легкой цепи каппа или лямбда.
15. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат Fc-участок.
16. Антитело или его антигенсвязывающий фрагмент по п.15, где Fc-участок содержит одно или оба замещения Met-429-Leu и Asn-435-Ser в остатках, соответствующих метионину 428 и аспарагину 434, соответственно, нумерация каждого представлена согласно нумерации ЕС.
17. Антитело или его антигенсвязывающий фрагмент по п.15, где Fc-участок содержит одно, два или три замещения Met-252-Tyr, Ser-254-Thr и Thr-256-Glu в остатках, соответствующих метионину 252, серину 254 и треонину 256, соответственно, нумерация каждого представлена согласно нумерации ЕС.
18. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые содержат две VH и две VL.
19. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, где указанное антитело является гуманизированным антителом.
20. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, где указанное антитело является моноклональным антителом.
21. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, где указанное антитело является синтетическим антителом.
22. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, где указанное антитело является моноспецифическим антителом.
23. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, где C5 является C5 человека.
24. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые связываются с C5 человека с KD', равной менее 0,1 мкг/мл или 0,6 нМ.
25. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые связываются с C5 человека с KD', равной 0,03-0,08 мкг/мл или 0,2-0,53 нМ.
26. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые связываются с C5 человека с EC50, равной менее 2 мкг/мл (например, менее 0,5 мкг/мл), как определено методом ELISA.
27. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые связываются с C5 человека с EC50, равной 0,01-2 мкг/мл (например, 0,02-0,2 мкг/мл), как определено методом ELISA.
28. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые связываются с C5 человека с EC50, равной 0,03-0,8 мкг/мл (например, 0,03-0,16 мкг/мл), как определено методом ELISA.
29. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые ингибируют гемолиз при IC50, равной менее 10 мкг/мл, как определено способом оценки гемолиза в условиях in vitro.
30. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые ингибируют гемолиз при IC50, равной 0,5-6 мкг/мл (например, между 2 мкг/мл и 6 мкг/мл), как определено способом оценки гемолиза в условиях in vitro.
31. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые ингибируют гемолиз при IC50, равной 0,5-3,3 мкг/мл (например, между 2,3 мкг/мл и 3,3 мкг/мл), как определено способом оценки гемолиза в условиях in vitro.
32. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, которые связываются с C5 человека, содержащим аминокислотную последовательность SEQ ID NO:53.
33. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, где:
(1) LCDR1, LCDR2, LCDR3, HCDR1 и HCDR2 принадлежат к каноническим классам 2, 1, 1, 1 и 2, соответственно, участков, определяющих комплементарность (CDR) по Chothia; и
(2) молекула антитела содержит по меньшей мере один из контактов паратоп-паратоп, представленных в Таблице 6.
34. Фармацевтическая композиция для связывания с компонентом 5 комплемента (C5), содержащая терапевтически эффективное количество выделенного антитела или его антигенсвязывающего фрагмента по п.1 или 2, и фармацевтически приемлемый носитель, вспомогательное вещество или стабилизатор.
35. Выделенная нуклеиновая кислота, кодирующая антитело или его антигенсвязывающий фрагмент по п.1 или 2.
36. Вектор экспрессии, содержащий нуклеиновую кислоту по п.35.
37. Клетка-хозяин, продуцирующая антитело или его антигенсвязывающий фрагмент по п.1 или 2, содержащая нуклеиновую кислоту по п.35.
38. Способ получения антитела или антигенсвязывающего фрагмента по п. 1 или 2, включающий культивирование клетки-хозяина по п.37 в условиях, подходящих для экспрессии гена, таким образом экспрессируя антитело или его антигенсвязывающий фрагмент по п.1 или 2.
39. Способ ингибирования C5 in vitro, включающий приведение в in vitro контакт C5 с антителом или его антигенсвязывающим фрагментом по п.1 или 2.
40. Фармацевтическая композиция для лечения расстройства, связанного с компонентом 5 комплемента (C5), у больного, содержащая выделенное антитело или его антигенсвязывающий фрагмент по п.1 или 2, способные связывается с компонентом 5 комплемента (C5), и фармацевтически приемлемый носитель, вспомогательное вещество или стабилизатор.
41. Фармацевтическая композиция по п.40, где расстройство является комплемент-опосредованным расстройством.
42. Фармацевтическая композиция по п.41, где комплемент-опосредованное расстройство выбрано из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aHUS), типичного или инфекционного гемолитико-уремического синдрома (tHUS), болезни плотных депозитов (DDD), пароксизмальной ночной гемоглобинурии (PNH), оптического нейромиелита (NMO), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (TTP); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита или тромботической микроангиопатии (ТМА).
43. Фармацевтическая композиция по п.41, где антитело вводят больному в дозе между 0,1 мг/кг и 50 мг/кг.
44. Фармацевтическая композиция для получения медицинского средства для профилактики расстройства, связанного с компонентом 5 комплемента (C5), у больного, содержащая выделенное антитело или его антигенсвязывающий фрагмент по п.1 или 2, способные связывается с компонентом 5 комплемента (C5), и фармацевтически приемлемый носитель, вспомогательное вещество или стабилизатор.
45. Фармацевтическая композиция по п.44, где расстройство является комплемент-опосредованным расстройством.
46. Фармацевтическая композиция по п.44, где расстройство является комплемент-опосредованным расстройством, причем необязательно комплемент-опосредованное расстройство выбрано из повреждения, вызванного ишемией/реперфузией, атипичного гемолитико-уремического синдрома (aHUS), типичного или инфекционного гемолитико-уремического синдрома (tHUS), болезни плотных депозитов (DDD), пароксизмальной ночной гемоглобинурии (PNH), оптического нейромиелита (NMO), макулярной дегенерации, тромботической тромбоцитопенической пурпуры (TTP); миастении гравис, болезни холодовых агглютининов, синдрома Гийена-Барре, болезни Дегоса, отторжения трансплантата, сепсиса, гломерулонефрита или тромботической микроангиопатии (ТМА).
47. Способ обнаружения C5, включающий
(i) приведение образца в контакт с антителом или его антигенсвязывающим фрагментом по п.1 или 2 в условиях, которые обеспечивают взаимодействие молекулы антитела или его антигенсвязывающего фрагмента и C5, и
(ii) обнаружение образования комплекса молекулы антитела или его антигенсвязывающего фрагмента и образца.
48. Способ по п.47, дополнительно включающий приведение референсного образца с антителом или его антигенсвязывающим фрагментом по п.1 или 2 в условиях, которые обеспечивают взаимодействие молекулы антитела и C5, и
(ii) обнаружение образования комплекса молекулы антитела и образца.
| WO 2007106585 A1, 20.09.2007 | |||
| WO 2010015608 A1, 11.02.2010 | |||
| US 7430476 B2, 30.09.2008 | |||
| US 9079949 B1, 14.07.2015 | |||
| RU 2012102021 A, 27.07.2013. |
Авторы
Даты
2024-11-12—Публикация
2019-06-19—Подача